 国家高新企业 | ISO9001认证
国家高新企业 | ISO9001认证 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com

谷禾健康

导语
微生物在在地球上无处不在,适应了几乎所有可用的生态栖息。 微生物在不同物种和个体之间差异性很大,存在着广泛的微生物多样性。
野生动物之所以能够耐受病原菌的感染和有毒食物的威胁以及抵御多种疾病,可能与其体内或体表生存的微生物密切关联。然而,与已被广泛研究的人类微生物群相比,野生动物的微生物群受到的关注较少。
当宿主有着共同的饮食或共同祖先,尤其是哺乳动物,通常肠道菌群构成也更为相似,不过这种相关性在鱼类、两栖类、鸟类和非脊椎动物中较弱。在许多情况下,肠道微生物都参与宿主的关键生理过程,包括代谢特殊的饮食化合物。
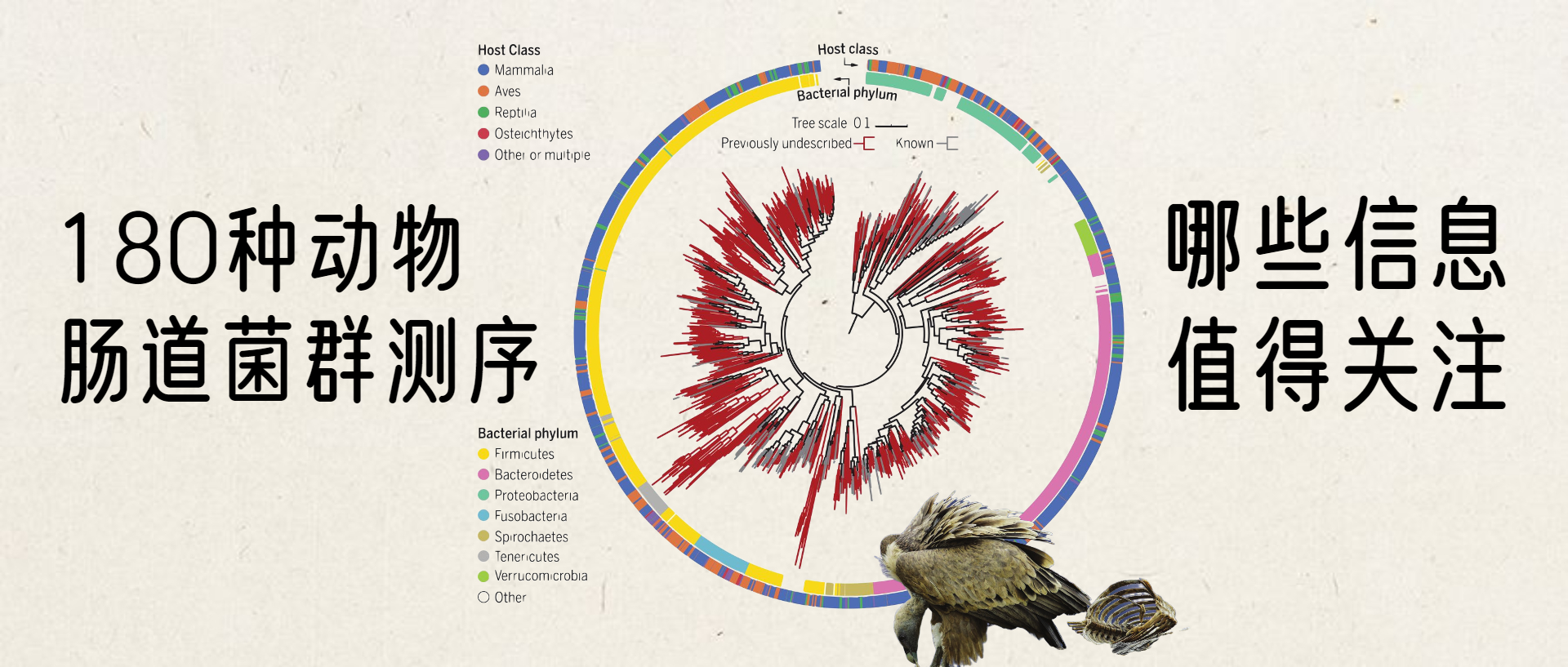
近日,以色列魏茨曼科学研究院Eran Segal团队采用一致的方法从全球四大洲采集了406份动物粪便样品,包括121份养殖样品和285份野生样品。共涉及184个动物物种,包括哺乳类、禽类、两栖类、硬骨鱼类等的物种。这些物种在分类单元、觅食/取食行为、地理分布、性状等方面具有较高的多样性。
使用宏基因组学来分析这180多个物种的肠道菌群,使用从头基因组组装,构建并在功能上注释了5000多个基因组的数据库,其中包括1209种细菌,但是其中75%未知。
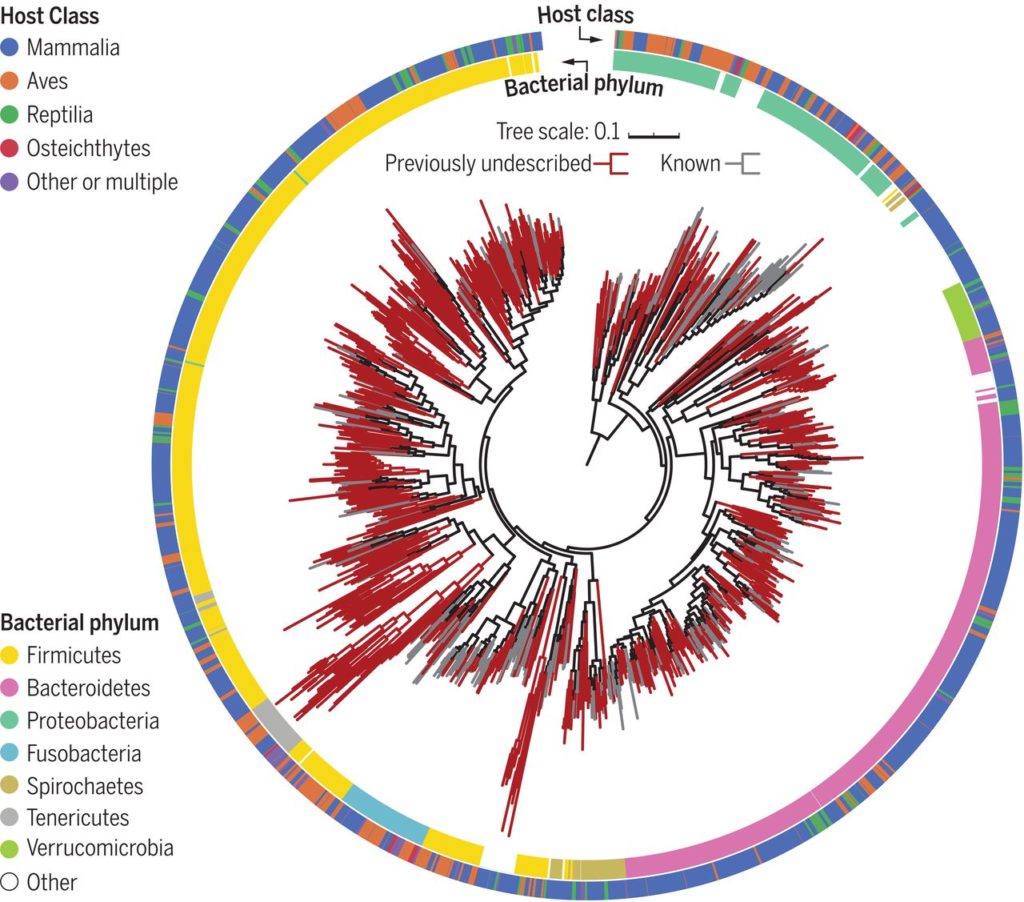
在这项研究中组装的1209个基因组的最大似然比的系统发育树。
内有色环和外有色环分别表示细菌门和宿主类别。先前未描述的基因组进化枝为深红色。
一,坚持野外采样。野外采样,尤其对于动物采样存在很多挑战,但是证据表明圈养动物会改变微生物组,而且,过往大量有关哺乳动物的研究大部分来来自于是圈养动物,包括大小鼠。这次大规模全球野外采样,可以扩大和了解动物宿主栖息微生物的机会。
二,要获得广泛的野生动物代表性,需要在全球不同的生态环境采样,并从具有不同特征和喂养方式的多种动物中取样。此外,该研究为每个物种手工制定了特质,包括饮食适应性,活动时间和社会结构,使我们能够系统地研究微生物群组成与宿主表型之间的关系。
三,为未知物种的大规模注释细菌基因组数据库,并确定了与这些动物的性状和分类相关的多种微生物模式,并强调了其潜力作为发现新的工业酶和治疗剂的主要未开发资源。
微生物的组成,多样性和功能含量与动物分类,饮食,活动,社会结构和寿命相关。动物微生物群系是生物功能的丰富来源,可能会对生物技术产生影响,包括抗生素,工业酶和免疫调节剂。
此外,野外动物表现出适应性,例如安全食用腐烂,感染病原体的肉类和有毒植物,可以产生强效毒素、生物发光以及各种疾病和微生物病原体具有特异性免疫力、再生能力并且在某些物种中具有极长的寿命。这些适应性中的某些,例如毒素产生和生物发光至少部分是由生活在动物体内/上的微生物共生体赋予的。该研究构建和功能注释从自然栖息地的野生动物中提取的微生物群的综合数据库可以对动物性状与其微生物群之间联系的进行全面了解。
例如,为了证明在动物微生物群中可以发现新的细菌功能,作者在实验中验证了细菌毒素——食用腐肉的欧亚兀鹫(Gyps fulvus)的MAG中发现的代谢蛋白酶。这些蛋白酶可用作抗菌化合物,具有抗菌活性潜在的应用包括对抗人类食物中毒。
欧亚兀鹫(学名:Gyps fulvus):体长95-105厘米,尾长24-29 厘米,翼展240-280厘米,体重6-11千克。是一种大型的褐色鹫。栖息在海拔高达2,500米的范围内。主要以山羊、鹿和瞪羚等野生动物,以及人类养殖的绵羊、山羊、牛和马为食。靠灵敏的嗅觉来找寻腐烂的动物尸体,并常常为抢一块肉而争个不停。而且习惯把头伸进动物尸体的腹腔内,啄食内脏和肌肉。分布范围非常广泛,遍布欧洲、中东和北非,也分布于印度、喜马拉雅山脉。在地中海沿岸国家最常见。
这项研究的最大贡献是其丰富的、系统生成的数据集。很容易想象,微生物保护和新出现的抗生素耐药性等不同领域的突破是由这些亚基因组的发现推动的。在欧亚兀鹫微生物群中发现的蛋白酶证明了从野生动物微生物群中进行生物勘探的原理,尽管尚不清楚该案例研究是否应被视为例外或预期的发现。


新发现的食腐肉的欧亚兀鹫(Gyps fulvus)的肠道细菌中的毒素代谢蛋白酶可能在抵抗食物中毒方面有应用。
这项研究仅仅触及了可以用这个数据集检验的假设的表面。未来方向包括:
01 微生物群如何帮助动物降解有毒的植物化学物质。
02 抵御食物中的病原体。
03 从多种食物来源中提取营养的问题。
四,丰富了许多未知物种的细菌门,并发现某些细菌进化枝相对于同一门中的其他细菌具有独特的功能特性。动物种类和已发现的动物种类(共存细菌的特定簇)之间的细菌状况有所不同。动物中这种未被探索的微生物多样性与被充分研究的人类微生物组形成了对比,而人类微生物组在参考数据库中表现得更好。未描述的物种中的富集度最高的是疣状菌属(Verrucomicrobia),这是一个存在于水、土壤和人类肠道中的门,但培养物种相对较少。
确定了多种途径和直系同源物,这些途径和直系同源物在特定的动物性状中显着丰富,并表明功能性景观与这些性状相关。这些功能中的一些功能提示了野生生物微生物群的新角色和特性。绘制野生动物的微生物群落图也可能有助于野生微生物的保护工作。
五,重述了首次通过扩增子测序发现的结果,包括食草动物微生物组比食肉动物微生物组更加多样化。这是一个比较重要的发现,是否说明植物性饮食可以提高微生物多样性?此外,不同动物群体的微生物组编码的遗传途径因宿主饮食、体型和其他特征而不同。
六,野生动物的微生物区系也是动物和人类病原体的天然库,如当前的COVID-19大流行一样,通过对野生生物微生物景观的广泛的基因组集合可以阐明其传播到人群中的时间和途径。
一,使用MAGs(宏基因组组装的基因组)限制了研究其中一些目标的拓展,即保护医学和生态上重要的细菌菌株。有些微生物物种将需要分析未组装的读取、培养或富集技术,而不是本研究中使用的全基因组测序。
二,即使是那些基因组被MAG组装捕获的细菌,这些组装体也倾向于排除“辅助”基因组,即在不同菌株间存在的基因。然而,这些基因往往在适应特定的宿主和环境中发挥作用。例如,抗菌素抗性、致病性和能量收集是经常由移动元件或其他辅助基因编码的性状。
三,Levin等人检测到的大多数非特征微生物在宿主体内的活动,以及它们是稳定地定殖在动物体内还是短暂地通过它们的胃肠道的问题仍然存在。在这个庞大的数据集上测试每个假设需要大量的计算、解释和实验验证。
参考文献:
Levin D, Raab N, Pinto Y, et al. Diversity and functional landscapes in the microbiota of animals in the wild[J]. Science, 2021, 372(6539).
Coleman M. Diagnosing nutritional stress in the oceans[J]. Science, 2021, 372(6539): 239-240.
L.-X. Chen, K. Anantharaman, A. Shaiber, A. M. Eren, J. F. Banfield, Genome Res. 30, 315 (2020)
E. C. Lindsay, N. B. Metcalfe, M. S. Llewellyn, J. Anim. Ecol. 89, 2415 (2020)

谷禾健康

我们知道,SARS-CoV-2感染引起的新型冠状病毒肺炎COVID-19,最常见的症状是发烧和呼吸道不适。也有胃肠道感染的报道,症状包括腹泻、恶心、呕吐、腹痛和食欲不振等。
胃肠道感染SARS-CoV-2或其他病毒后,部分患者可能发生胃肠道微生物群改变。此外,部分新冠肺炎患者可能会接受抗生素治疗,这也可能会扰乱胃肠道稳态。
本文就以下问题,对COVID-19,胃肠道疾病,程度菌群,营养干预之间的联系进行探讨。

腹泻患者粪便样本中病毒RNA阳性率更高?
COVID-19和胃肠道疾病有什么联系?
肠-肺轴在COVID-19的发展中发挥作用?
肠道菌群在其中扮演什么角色?
针对COVID-19不同严重程度的措施?
营养干预是否有效?如何干预?
……
SARS-CoV-2在鼻咽清除后仍能在粪便中呈阳性,并可能继续具有传染性。
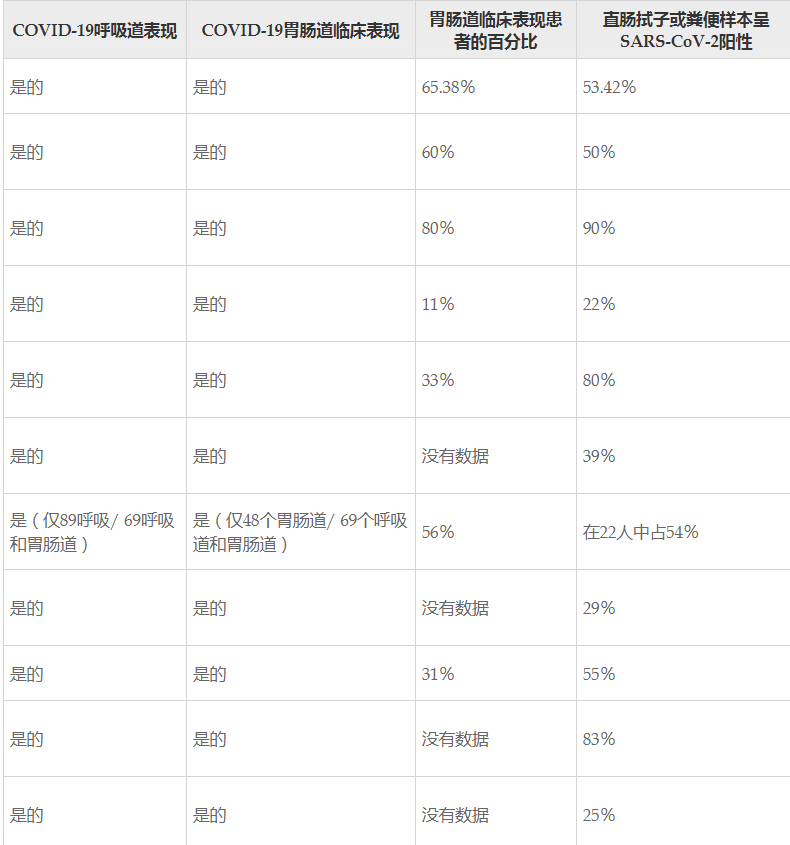
Alberca GGFet al., World J Gastroenterol. 2021
COVID-19最常见的胃肠道症状是腹泻、恶心、腹痛和食欲不振。
在病毒性胃肠道感染后,一些患者可能会出现胃肠道微生物群的改变,如变形菌增加、拟杆菌减少。
最近的一份报告确定了COVID-19住院患者肠道微生物群的改变,有益共生细菌减少,条件致病菌增加。
肠道组织和粪便也可能是一个贮存器。最近研究表明,即使鼻咽和口咽拭子检测SARS-CoV-2RNA呈阴性,患者粪便样本中仍然有可能含有SARS-CoV-2RNA.
另有研究指出,腹泻患者的COVID-19症状持续时间延长,而腹泻患者的粪便样本中病毒RNA的阳性率更高。
目前的假设是可能涉及肠道组织上的直接病毒感染和对该病毒的局部免疫反应。实际上,在粪便COVID-19患者中检测到SARS-CoV-2 RNA可能表明粪-口传播。
除了SARS-CoV-2对肠道免疫反应的影响外,COVID-19患者还可能发生细菌共感染和继发感染,也就是说必须使用抗生素。即使COVID-19患者没有细菌共感染,对其抗生素的使用也是在临床上常见的做法。这也可能会破坏胃肠道微生物组。
微生物群受环境因素,食物,药物和感染的影响。根据人体的部位不同,每个微生物群具有独特的特性。许多因素会影响微生物组的组成,例如局部pH值,温度和养分。
微生物几乎可以在人体的每个小生境中发现,但胃肠道是宿主与人体中微生物之间最大的界面。大约有1013-1014胃肠道中的微生物,其基因组含量比人类基因组中更大。
微生物与人类有共生关系。共生微生物对于人类健康,调节许多生理功能,物质降解,代谢产物的产生和免疫反应至关重要。
微生物能激活和刺激T辅助细胞(Th)1、Th2、Th17和T调节细胞(Treg)的分化,从而调节免疫应答。肠道菌群多样性低会增加对局部和肺部疾病的易感性。
微生物组的环境处于不断调节中,受到外部微生物和其他非细菌化合物(例如肠道菌群中的食物和病毒)的调节。微生物群的突然变化会导致共生细菌的失衡和/或条件致病菌增加,增加对疾病的敏感性。
微生物群对于人类免疫系统的发展至关重要,并且可以影响局部和非局部免疫反应,例如肠-肺轴。肠道菌群的改变可以调节呼吸系统疾病的发展。在患有肠道功能障碍的患者,例如已确诊的肠道炎性疾病的患者或肥胖患者中,肠道菌群可能是发生严重COVID-19的次要危险因素。
此外,患有COVID-19的患者可能会出现胃肠道菌群失调,且产短链脂肪酸的细菌减少。
肠道菌群的破坏可以触发与代谢功能障碍,肥胖症,癌症,和神经障碍相关的炎症事件。某些微生物的增加或减少可以增加对先天性免疫受体的刺激,例如核苷酸结合寡聚化域样受体和Toll样受体。该受体的刺激触发几个促炎症信号和细胞因子和趋化因子的产生,它们调节适应性免疫系统,影响局部和全身免疫反应。
微生物群激活免疫细胞上的Toll样受体可在宿主体内产生低度全身性炎症,这与代谢和免疫反应的改变有关。微生物组的改变与疾病的发展有关,例如肥胖,炎症性肠病和癌症。
因此,SARS-CoV-2胃肠道感染和肠道稳态的改变可能与疾病的发展有关,并影响对口服疫苗和药物的免疫应答以及病原体的免疫应答。
一些研究强调了营养物质在调节对SARS-CoV-2或直接抗病毒和/或抗SARS-CoV-2特性的免疫应答中的潜在作用。
营养方面如肥胖,营养不良,和微量营养素缺乏已经假定作为严重COVID-19的危险因素。然而,人类微生物群的组成受到许多因素的影响,包括饮食成分。一些细菌可以发酵不可消化的碳水化合物(益生元),例如可溶性纤维,以产生短链脂肪酸(SCFA)。
短链脂肪酸
短链脂肪酸可以刺激共生细菌的生长和/或活性,并与健康有关。短链脂肪酸可以诱导肠屏障的调节,降低氧化应激,控制腹泻,并调节肠能动性,并且还诱导局部和全身抗炎作用。
短链脂肪酸可诱导抗炎细胞因子的释放,如IL-10,促进Th细胞和炎症性疾病的调节,包括炎症性肠病。
短链脂肪酸分为乙酸,丙酸和丁酸。所有短链脂肪酸都具有潜在的抗炎作用,降低前列腺素E2和炎症因子。
乙酸盐能抑制含有3个炎症小体的NLR家族pyrin结构域的激活;
丙酸盐能抑制组蛋白脱乙酰酶,减轻脂多糖引起的炎症。
丁酸盐具有抗癌和减少肺部炎症的作用。
总的来说,研究表明短链脂肪酸有直接抗炎作用或调节微生物群在局部(肠道)和非局部炎症中具有潜在的抗炎作用。
益生菌
对于胃肠微生物的调节,另一个干预是通过益生菌。益生菌是可以被摄入并与宿主产生有益相互作用的细菌。
一些研究调查对肠道菌群益生菌的作用,但有关它们移植物于共生微生物群的能力的结果相互矛盾。
然而,益生菌产生代谢物可影响共生微生物群,肠屏障,免疫系统。益生菌还可以帮助预防或治疗细菌和病毒感染。益生菌的使用可以提高感染流感病毒的小鼠的存活率。除流感病毒外,研究还显示出对呼吸道合胞病毒感染的有益保护作用。
益生菌在呼吸道病毒感染中的健康益处是由于细胞因子的产生和氧化应激的调节; 因此,它们可能是严重COVID-19期间促炎性细胞因子,趋化因子和氧化应激异常释放的辅助治疗。
最常用的益生菌是乳杆菌,双歧杆菌和肠球菌。尽管有大量研究表明它们具有健康益处,但目前在益生菌菌株之间涉及理想剂量和菌株之间比较的知识尚存在差距。
高纤维饮食
高纤维饮食可以诱导有益菌的繁殖,比如乳酸杆菌属和双歧杆菌属在胃肠道。实际上,高纤维饮食可能增加免疫球蛋白A的生产和调节干扰素-γ和白细胞介素(IL)-10的分泌,这有助控制胃肠道感染。
益生元
益生元可以通过一种称为交叉喂养的机制改变微生物群的组成,当益生元的发酵产物可以被另一种微生物作为底物使用。
益生元可以改变微生物群的另一种机制是通过改变pH值。
发酵产物主要是酸,这可能会导致肠道pH降低,抑制酸敏感细菌(如拟杆菌)的生长并促进产生丁酸的细菌生长。
病毒感染可以改变胃肠道微生物群。一份报告确认了COVID-19患者粪便样本中乳酸杆菌和双歧杆菌的减少。同样,必要或不必要使用抗生素会干扰COVID-19患者的微生物组。
肠道微生物组的改变包括在SARS-CoV-2清除后的30天内,柔嫩梭菌群Faecalibacterium prausnitzii、Eubacterium rectale和双歧杆菌的减少。
COVID-19中的微生物群失调可能与炎症反应有关,并且可能是COVID-19解决后的一个持久性问题,这表明营养干预可能在抑制炎症反应和重建COVID-19患者胃肠道稳态方面发挥作用。
低纤维饮食增加胃肠道感染的易感性
饮食和营养干预可以调节免疫反应,增加或抑制抗病毒反应。西式饮食(低纤维含量)可增加拟杆菌和减少厚壁菌,并与肥胖的发展有关,后者是严重COVID-19的危险因素。
虽然有报告指出肥胖者粪便样本中的短链脂肪酸增加,但短链脂肪酸与控制食欲和增加能量消耗有关。
此外,非常低纤维的饮食可以降低肠粘液的产生,增加胃肠道感染的易感性。
饮食的改变可以改变微生物群的组成。微生物群落处于不断变化之中,并且还受到食物消耗的季节性影响。事实上,减少纤维的消耗可以在短短的1天内改变微生物群,减少短链脂肪酸的产生。
高纤维饮食减少肺部炎症,促进抗炎反应
相反,高纤维饮食增加了肠道微生物群中的厚壁菌和放线菌,并增加了短链脂肪酸的产生,这有助于通过肠-肺轴减少肺部炎症,并通过IL-10的产生和Treg细胞促进局部和全身的抗炎反应。
益生菌治疗减少呼吸机相关肺炎
摄入益生菌可能会稳定或改变胃肠道微生物组,特别是在微生物组受到干扰后,如抗生素使用后或胃肠道感染。
使用枯草芽孢杆菌Bacillus subtilis和粪肠球菌Enterococcus faecalis的益生菌治疗已被证明可减少呼吸机相关肺炎。
鼠李糖乳杆菌Lactobacillus rhamnosus治疗可减少机械通气患者的呼吸机相关性肺炎和艰难梭菌相关性腹泻,使其成为重症监护病房辅助机械通气患者治疗的可能补充。
使用乳酸杆菌治疗可能特别重要,因为呼吸道感染可能导致乳酸菌减少,肠杆菌科增加和肠道IL-17炎症。
调节免疫应答
靶向IL-17被认为是治疗COVID-19的一种方法,因为与中度COVID-19患者相比,重度COVID-19患者的IL-17增加。
IL-17和产生IL-17的辅助性T细胞(Th17)、三型固有淋巴细胞、不变的自然杀伤细胞和γδT细胞参与了COVID-19的免疫应答。IL-17受体表达于许多不同细胞的表面,如中性粒细胞、嗜酸性粒细胞、上皮细胞、角质形成细胞和成纤维细胞。此外,IL-17可直接影响ACE2、SARS-CoV-2入口受体的表达。
IL-17阻断剂的使用,如针对IL-17A和/或IL-17受体A的单克隆抗体,可能代表了COVID-19的一种可能的治疗选择。尽管如此,IL-17在对抗肺炎链球菌Pseudomonas aeruginosa和铜绿假单胞菌Pseudomonas aeruginosa(呼吸道和肠道感染中常见的病原体)的免疫反应中是一种重要的细胞因子。
继发性细菌感染可发生在SARS-CoV-2感染后的呼吸系统,尤其是有创机械通气患者。IL-17对肠道内稳态尤其重要。因此,抗IL-17治疗应考虑呼吸道和肠道细菌感染易感性增加的可能风险。
增加短链脂肪酸辅助治疗
COVID-19患者也可能出现细胞因子风暴综合征,这可能导致多器官衰竭,并导致死亡或长期后果。在这种情况下,益生菌或益生元治疗通过增加短链脂肪酸在呼吸道感染中的抗炎作用已经被证实。
摄入高发酵纤维饮食、益生菌、口服三丁酸甘油酯(丁酸的前药)或直接服用短链脂肪酸等药物均可增加短链脂肪酸的生产和健康效益。
在这种情况下,摄入益生元和/或益生菌可代表COVID-19患者的显著预防性干预和/或康复。
显然,SARS-CoV-2可以感染胃肠道并影响肠道免疫反应和肠道微生物组。但胃肠道的SARS-CoV-2感染以及COVID-19在胃肠道稳态中的长期后果仍需进一步研究。
目前,尚无针对COVID-19的特异性治疗方法,但已对通过调节免疫应答或通过肠道微生物群进行营养干预的影响进行了研究,这可能是对COVID-19的重要干预和/或恢复的手段。
相关阅读:
参考文献
Zuo T, Liu Q, Zhang F, et al., Depicting SARS-CoV-2 faecal viral activity in association with gut microbiota composition in patients with COVID-19. Gut. 2021;70:276-284.
Yeoh YK, Zuo T,et al., Gut microbiota composition reflects disease severity and dysfunctional immune responses in patients with COVID-19. Gut . 2021
Alberca GGF, Solis-Castro RL, Solis-Castro ME, Alberca RW. Coronavirus disease–2019 and the intestinal tract: An overview. World J Gastroenterol 2021; 27(13): 1255-1266
Vieira RS, Castoldi A, Basso PJ, et al., Butyrate Attenuates Lung Inflammation by Negatively Modulating Th9 Cells. Front Immunol. 2019;10.
Zhang N, Gong Y, Meng F et al., Comparative study on virus shedding patterns in nasopharyngeal and fecal specimens of COVID-19 patients. Sci China Life Sci. 2020

谷禾健康
《中华人民共和国生物安全法》于2021年4月15日起正式施行。

《中华人民共和国生物安全法》是生物安全领域的一部基础性、综合性、系统性、统领性法律。其颁布和实施具有里程碑意义,标志着我国生物安全进入依法治理的新阶段。
生物安全风险防控体制
防控重大新发突发传染病、动植物疫情
生物技术研究、开发与应用安全
病原微生物实验室生物安全
人类遗传资源与生物资源安全
防范生物恐怖与生物武器威胁
生物安全能力建设
此次,关于病原微生物实验室生物安全管理章节,明确以下内容:
第四十二条 严格遵守生物安全标准
国家加强对病原微生物实验室生物安全的管理,制定统一的实验室生物安全标准。病原微生物实验室应当符合生物安全国家标准和要求。
从事病原微生物实验活动,应当严格遵守有关国家标准和实验室技术规范、操作规程,采取安全防范措施。
第四十三条 具备条件,符合规范
国家根据病原微生物的传染性、感染后对人和动物的个体或者群体的危害程度,对病原微生物实行分类管理。
从事高致病性或者疑似高致病性病原微生物样本采集、保藏、运输活动,应当具备相应条件,符合生物安全管理规范。具体办法由国务院卫生健康、农业农村主管部门制定。
第四十四条 依法批准或备案
设立病原微生物实验室,应当依法取得批准或者进行备案。
个人不得设立病原微生物实验室或者从事病原微生物实验活动。
第四十五条 实验室分等级管理
国家根据对病原微生物的生物安全防护水平,对病原微生物实验室实行分等级管理。
从事病原微生物实验活动应当在相应等级的实验室进行。低等级病原微生物实验室不得从事国家病原微生物目录规定应当在高等级病原微生物实验室进行的病原微生物实验活动。
第四十六条 高致病性经有关部门批准
高等级病原微生物实验室从事高致病性或者疑似高致病性病原微生物实验活动,应当经省级以上人民政府卫生健康或者农业农村主管部门批准,并将实验活动情况向批准部门报告。
对我国尚未发现或者已经宣布消灭的病原微生物,未经批准不得从事相关实验活动。
第四十七条 加强实验动物和废弃物管理
病原微生物实验室应当采取措施,加强对实验动物的管理,防止实验动物逃逸,对使用后的实验动物按照国家规定进行无害化处理,实现实验动物可追溯。禁止将使用后的实验动物流入市场。
病原微生物实验室应当加强对实验活动废弃物的管理,依法对废水、废气以及其他废弃物进行处置,采取措施防止污染。
第四十八条 定期检查、维护、更新
病原微生物实验室的设立单位负责实验室的生物安全管理,制定科学、严格的管理制度,定期对有关生物安全规定的落实情况进行检查,对实验室设施、设备、材料等进行检查、维护和更新,确保其符合国家标准。
病原微生物实验室设立单位的法定代表人和实验室负责人对实验室的生物安全负责。
第四十九条 建立完善安全保卫制度
病原微生物实验室的设立单位应当建立和完善安全保卫制度,采取安全保卫措施,保障实验室及其病原微生物的安全。
国家加强对高等级病原微生物实验室的安全保卫。高等级病原微生物实验室应当接受公安机关等部门有关实验室安全保卫工作的监督指导,严防高致病性病原微生物泄漏、丢失和被盗、被抢。
国家建立高等级病原微生物实验室人员进入审核制度。进入高等级病原微生物实验室的人员应当经实验室负责人批准。对可能影响实验室生物安全的,不予批准;对批准进入的,应当采取安全保障措施。
第五十条 制定安全应急预案
病原微生物实验室的设立单位应当制定生物安全事件应急预案,定期组织开展人员培训和应急演练。发生高致病性病原微生物泄漏、丢失和被盗、被抢或者其他生物安全风险的,应当按照应急预案的规定及时采取控制措施,并按照国家规定报告。
第五十一条 提高医疗救治能力
病原微生物实验室所在地省级人民政府及其卫生健康主管部门应当加强实验室所在地感染性疾病医疗资源配置,提高感染性疾病医疗救治能力。
第五十二条 企业微生物车间规范管理
企业对涉及病原微生物操作的生产车间的生物安全管理,依照有关病原微生物实验室的规定和其他生物安全管理规范进行。
涉及生物毒素、植物有害生物及其他生物因子操作的生物安全实验室的建设和管理,参照有关病原微生物实验室的规定执行。
生物安全实验室主要分为2类:
病原微生物生物安全实验室和动物生物安全实验室,前者主要用于研究病原微生物,后者用于开展病原微生物感染动物的实验。
CHEN Jiejun.Journal of Biosafety.2018
6.2 BSL-1 实验室
6.2.1 应为实验室仪器设备的安装、清洁和维护、安全运行提供足够的空间。
6.2.2 实验室应有足够的空间和台柜等摆放实验室设备和物品。
6.2.3 在实验室的工作区外应当有存放外衣和私人物品的设施,应将个人服装与实验室工作服分开放置。
6.2.4 进食、饮水和休息的场所应设在实验室的工作区外。
6.2.5 实验室墙壁、顶板和地板应当光滑、易清洁、防渗漏并耐化学品和消毒剂的腐蚀。地面应防滑,不得在实验室内铺设地毯。
6.2.6 实验室台(桌)柜和座椅等应稳固和坚固,边角应圆滑。实验台面应防水,并能耐受中等程度的热、有机溶剂、酸碱、消毒剂及其他化学剂。
6.2.7 应根据工作性质和流程合理摆放实验室设备、台柜、物品等,避免相互干扰、交叉污染,并应不妨碍逃生和急救。台(桌)柜和设备之间应有足够的间距,以便于清洁。
6.2.8 实验室应设洗手池,水龙头开关宜为非手动式,宜设置在靠近出口处。
6.2.9 实验室的门应有可视窗并可锁闭,并达到适当的防火等级,门锁及门的开启方向应不妨碍室内人员逃生。
6.2.10 实验室可以利用自然通风,开启窗户应安装防蚊虫的纱窗。如果采用机械通风,应避免气流流向导致的污染和避免污染气流在实验室之间或与其他区域之间串通而造成交叉污染。
6.2.11 应保证实验室内有足够的照明,避免不必要的反光和闪光。
6.2.12 实验室涉及刺激性或腐蚀性物质的操作,应在 30 m 内设洗眼装置,风险较大时应设紧急喷淋装置。
6.2.13 若涉及使用有毒、刺激性、挥发性物质,应配备适当的排风柜(罩)。
6.2.14 若涉及使用高毒性、放射性等物质,应配备相应的安全设施设备和个体防护装备,应符合国家、地方的相关规定和要求。
6.2.15 若使用高压气体和可燃气体,应有安全措施,应符合国家、地方的相关规定和要求。
6.2.16 应有可靠和足够的电力供应,确保用电安全。
6.2.17 应设应急照明装置,同时考虑合适的安装位置,以保证人员安全离开实验室。
6.2.18 应配备足够的固定电源插座,避免多台设备使用共同的电源插座。应有可靠的接地系统,应在关键节点安装漏电保护装置或监测报警装置。
6.2.19 应满足实验室所需用水。
6.2.20 给水管道应设置倒流防止器或其他有效的防止回流污染的装置;给排水系统应不渗漏,下水应有防回流设计。
6.2.21 应配备适用的应急器材,如消防器材、意外事故处理器材、急救器材等。
6.2.22 应配备适用的通讯设备。
6.2.23 必要时,可配备适当的消毒、灭菌设备。
6.3 BSL-2 实验室
6.3.1 普通型 BSL-2 实验室
6.3.1.1 适用时,应符合 6.2 的要求。
6.3.1.2 实验室主入口的门、放置生物安全柜实验间的门应可自动关闭;实验室主入口的门应有进入控制措施。
6.3.1.3 实验室工作区域外应有存放备用物品的条件。
6.3.1.4 应在实验室或其所在的建筑内配备压力蒸汽灭菌器或其他适当的消毒、灭菌设备,所配备的消毒、灭菌设备应以风险评估为依据。
6.3.1.5 应在实验室工作区配备洗眼装置,必要时,应在每个工作间配备洗眼装置。
6.3.1.6 应在操作病原微生物及样本的实验区内配备二级生物安全柜。
6.3.1.7 应按产品的设计、使用说明书的要求安装和使用生物安全柜。
6.3.1.8 如果使用管道排风的生物安全柜,应通过独立于建筑物其他公共通风系统的管道排出。
6.3.1.9 实验室入口应有生物危害标识,出口应有逃生发光指示标识。
6.3.2 加强型 BSL-2 实验室
6.3.2.1 适用时,应符合 6.3.1 的要求。
6.3.2.2 加强型 BSL-2 实验室应包含缓冲间和核心工作间。
6.3.2.3 缓冲间可兼作防护服更换间。必要时,可设置准备间和洗消间等。
6.3.2.4 缓冲间的门宜能互锁。如果使用互锁门,应在互锁门的附近设置紧急手动互锁解除开关。
6.3.2.5 实验室应设洗手池;水龙头开关应为非手动式,宜设置在靠近出口处。
6.3.2.6 采用机械通风系统,送风口和排风口应采取防雨、防风、防杂物、防昆虫及其他动物的措施,送风口应远离污染源和排风口。排风系统应使用高效空气过滤器。
6.3.2.7 核心工作间内送风口和排风口的布置应符合定向气流的原则,利于减少房间内的涡流和气流死角。
6.3.2.8 核心工作间气压相对于相邻区域应为负压,压差宜不低于10Pa. 在核心工作间入口的显著位置,应安装显示房间负压状况的压力显示装置。
6.3.2.9 应通过自动控制措施保证实验室压力及压力梯度的稳定性,并可对异常情况报警。
6.3.2.10 实验室的排风应与送风连锁,排风先于送风开启,后于送风关闭。
6.3.2.11 实验室应有措施防止产生对人员有害的异常压力,围护结构应能承受送风机或排风机异常时导致的空气压力载荷。
6.3.2.12 核心工作间温度18 ℃~26 ℃,噪音应低于68 dB。
6.3.2.13 实验室内应配置压力蒸汽灭菌器,以及其他适用的消毒设备。

生物安全柜的排风系统中装有高效空气过滤器 (HEPA),它能有效地截留所有已知传染因子, 对于直径 0.3 μm 的颗粒它可以截留 99.97%, 对大于或小于直径0.3μm 颗粒它可以截留 99.99%,并确保从安全柜中排出的是不含微生物的空气。
因此正确使用生物安全柜可以有效地减少由于气溶胶暴露或溅出物所造成的实验室污染以及培养物等交叉污染,减少对环境和人身安全所造成的危害,有效地保护实验室人员的健康与安全,减少职业暴露的发生。
生物安全实验室的关键设备:

·生物安全柜安装位置应避开人流频繁处;
· 安全柜安装的周围和电源处要留出足够的空间;
· 操作人员要经过专业培训方可上岗;
· 操作者必须穿戴紧口长纤维易灭菌的洁净工作服、帽、口罩;
· 操作过程中,台面不能存放过多物品;
· 操作时,操作者的双臂以直线方向缓慢伸入生物安全柜,并至少静止1min,使柜内气流相对稳定后再进行操作;
· 操作者头部、身体严禁伸到操作区内,操作动作应控制在最小程度;
· 应该按照从清洁区、半污染区到污染区的方向进行,防止交叉污染;
·实验完成后,对所有从安全柜取出的器材和物品均要进行严格的消毒处理。
只有了解生物安全柜的性能、结构、防护级别及一些注意事项,正确使用生物安全柜,才能针对自己实验室选择适合本实验室使用生物安全柜,保护实验环境不受污染,有效地减少由于气溶胶暴露或有害气体扩散所造成实验室感染事件的发生,规避感染风险。


《生物安全法》为促进我国生物技术产业发展提供了法律保障,筑牢生物安全法治“防火墙”。
谷禾实验室作为二级病原微生物安全实验室,全面贯彻落实法律规定的重要制度,严格遵守管理规范,防止生物安全风险发生,做好《生物安全法》落地实施“主力军”,让用户更放心的同时,也为国家科研、健康产业的发展,人民幸福安康贡献自己的力量。
参考资料:
《中华人民共和国生物安全法》
病原微生物实验室生物安全通用准则. WS 233—2017
孟宪军, 史志旭. 加强生物安全柜正确使用规避感染风险[D]. , 2010.

谷禾健康
饮食的改变会改变人体的微生物群,对健康造成潜在的影响。根据以往的研究,饮食驱动的微生物群变化不仅可以导致失调,还可以塑造生活史特征,推动人类进化。考虑到环境、健康和进化是相互关联的,那么饮食驱动的微生物群干扰是否会产生超出其对人类健康直接影响的后果?
最近德国科学家指出,饮食结构的变化会导致微生物组宿主基因配置不匹配,从而影响人类的寿命和繁殖成功。 这些失配也可引起可遗传的全功能体(holobiont)应激反应,这促使全生命周期在变化的营养环境中重新建立平衡。
该研究介绍一个前瞻性的模型,其中的微生物组在现代人类适应环境变化中发挥作用。假设饮食变化重新配置了整合人类微生物群中表观遗传控制的平衡健康状态。这种重新配置是一把双刃剑。一方面,它可能通过调节完整生物的生命史特征(如寿命和繁殖)的表达而增加疾病的风险和严重性。另一方面,它有助于重新调整全功能体(holobiont)系统与新的营养环境,利用宿主基因和微生物组之间的不匹配产生的压力。
简单笼统的说,就是该机制框架将两个迄今联系不充分的辩论联系起来:全球气候变化对饮食的影响,以及微生物组,表观基因组和宿主之间的复杂关系。
这些假设的动态不必只与正在进行的气候变化相耦合,也不必只适用于人类全息生物。相反,微生物群-表观基因组-免疫轴中的类似动力学可能是对过去非人为气候变化的反应,并对我们和其他物种的进化轨迹作出了贡献。
气候变化可以通过多种途径影响人类健康。到目前为止,关于气候变化对人类健康的影响的公众关注和科学研究主要集中在气候灾难(例如洪水,热浪和流行病)产生的CO2排放和健康风险上。尽管仍然相对罕见,但随着气候变化,这些灾难预计会变得更加频繁和严重。
在这些事件中暴露于危险条件的风险很高,幸存者可能会遭受长期的健康危机(例如,运动功能丧失)的困扰。随着时间的推移,这些风险会积累。饮食就是其中一种途径。
气候变化和经济发展压力会影响许多影响人类饮食的因素,包括作物产量,耕作方式和饮食习惯。农作物的生产耕作以及烹饪方式可能在正在改变以适应人类的饮食习惯。 气候变化,对饮食有明显影响。 例如,对玻利维亚八个Aymara社区的案例研究发现,农民在介绍他们认为更坚固的农作物的同时,种植了他们认为更易受气候影响的作物,例如块茎旱金莲(一种不一样的土豆)。
饮食变化对人类健康和进化有何后果? 虽然气候变化与饮食之间的联系在文献中可能已经很好地确立,但饮食变化转化为健康后果并帮助产生新的表型性状的机制仍需要阐明。
饮食摄入可能通过影响寄主的表观遗传学和寄主的微生物组而影响健康。 此外,宿主与微生物组之间存在复杂的表观遗传关系,表观遗传现象可能会影响进化。
在此基础上,德国科学家Francesco Catania和Jan Baedke提出了一个模型,该模型考虑了表观遗传机制与人类微生物组之间的相互作用以及它们与宿主遗传学的串扰。 并且认为,将人类概念化为灵活的生态系统或整体生物可能有助于揭示与饮食有关的变化对人类健康的某些后果,并提供对人类后代的预测历史特征和适应能力。
在该模型中,气候变化引起的饮食变化会通过营养不良增加健康风险。 同时,这些过程促使微生物组重新配置,从而触发跨代对环境变化的适应性反应。 作为实现这些短期和长期影响的关键途径,我们确定了微生物组-表观基因组-免疫轴。
饮食、人类健康和表观遗传学饮食对人类健康有重大影响。不同的饮食和饮食模式可以调节个体间的变异性(例如,增加心血管疾病的风险)。饮食有助于出生体重,这是婴儿和儿童健康以及成人疾病易感性的主要预测因素。饮食也会影响寿命和繁殖。例如‘饮食限制’,在不饥饿的情况下减少食物摄入量可以上调应激反应和先天免疫的相关途径,下调不同物种间生长和繁殖的相关途径。
饮食也可以有长期的影响,代际后果。由于营养不良(即营养过剩或营养不足)导致免疫状态受损的父母的后代本身也经常受到免疫系统的干扰。
此外,为了应对父母饮食能量的增加,后代表现出较高的促炎性和抑制的抗炎性。然而,在某些条件下,饮食的改变也可能对后代的健康产生相反的积极影响。在一个例子中,一组瑞典北部人的孙子孙女经历了几代人的作物短缺器,他们的死亡率和心血管疾病的风险较低,与前几代人相比,这些研究中的一些暗示了饮食对人类健康影响的表观遗传机制。
近年来,微生物组群已成为环境因素(如营养模式)与人类健康之间的一个新中介。人类微生物群包括定植于人类皮肤、胎盘、子宫、精液、肺、唾液、口腔粘膜、结膜,尤其是胃肠道的所有细菌、古细菌、真菌、原生生物和病毒。如果我们将人类视为一个完整的生态系统及其微生物群。那么,微生物群提供了大量的生态系统服务。通过生态系统服务,刺激免疫系统并塑造其发育,有助于神经系统的发育和功能,微量营养素的合成,营养素的消化和吸收,以及能量调节。
这些生态系统服务的可靠性取决于宿主与其微生物组之间的有效串扰,而这种串扰受饮食模式的影响。因此,根据最近的建议,气候变化引起的饮食或生活方式的改变也可能影响宿主的健康状况。
事实上,人类健康状况的变化肠道微生物群(例如,由于在食品生产中越来越多地使用抗生素)与各种疾病的发生和发展有关,如自身免疫疾病,癌症,代谢紊乱和精神障碍,如抑郁症,通过所谓的“肠-脑轴”。然而,这种关系的分子基础以及表型与微生物组的组成和丰度之间联系的范围和强度仍然不清楚。
已经提出了微生物群建立、稳定性和跨代传播的多种进化和生态模型。人类宿主与其驻留微生物群之间的广泛串扰表明它们已经共同进化或可能已经共同适应,即人类微生物群已经与宿主共同进化,适应人类生态系统并发展互利。与此观点一致,在人类生态系统中只有一小部分已知细菌菌群存在 。整体全息图关联也可能反映了一种单方面的适应过程(例如,宿主已适应其微生物,但微生物未适应其宿主)。
但是如何实现微生物组与人类宿主之间的共同进化或单方面的适应或共同适应?
这个问题对于理解饮食对人类健康和进化的影响至关重要。共进化意味着微生物组必须世代遗传和/或忠实获得。但是这是怎么做到的呢?
微生物群的构型在生命的早期就受到很大影响。在成年人中,微生物群保持一定程度的灵活性,这种灵活性可能在一定程度上受到环境条件和因素的调节,如宿主的遗传背景、行为和生活方式、性别和年龄。因此,微生物组分的跨代复发至少在一定程度上依赖于生命早期展开的生物过程。
在人类中,母体环境似乎有助于婴儿肠道的细菌定植。然而,这种母体贡献是部分的,因此不足以保证类似于遗传信息的可靠传播。稳定的(环境遗传的)文化和行为模式可以弥补宿主-微生物群关系的跨代稳定性不足。 例如,稳定的喂养方式,分娩方式和卫生习惯中的文化模式会导致婴儿期相似的微生物连续定居。 与其他动物一样,社会互动和网络可能会打开微生物传播的渠道。
最后,宿主遗传学也可能在微生物组(尤其是肠道)的获取,维持和稳定中发挥重要作用。 基因决定的免疫特性,连同微生物细胞之间的竞争,可能有助于调节和维持给定生态位空间中微生物种群的适当组成和水平。总之,垂直和水平传播以及宿主基因有助于微生物组的跨代稳定性。
宿主表观基因组对微生物定殖的贡献与将表观遗传变化(如DNA甲基化、组蛋白修饰、非编码RNA的调控)与微生物群定殖和功能性联系起来的研究一致。这也与研究改变微生物群表观遗传修饰的报告一致与疾病的发生有关。
宿主表观基因组既可以形成,也可以由获得的微生物群形成。获得的微生物群可以影响宿主的食欲、摄食行为和食物选择,进而影响基因调节和调节免疫反应。
因此,建议微生物群不仅可以通过各种模式和渠道稳定地传播和获取。 它也可以重塑宿主表观基因组。 这种表观遗传重塑会影响后代的发育,从而有效地将当前的环境变化(如饮食变化)与宿主的发育,代谢和免疫过程的未来变化联系起来。
表观和微生物组重塑的这种相互过程可能会在各个世代之间展开,直到整个全功能系统达到平衡状态(宿主-微生物组匹配)为止。

全功能生物的微生物群-表观基因组-免疫轴。(1) 气候变化改变了人类的饮食。(2) 与气候变化相关的饮食变化会影响微生物组(例如,影响微生物多样性、成分或代谢物)、宿主的表观基因组(例如,通过摄入改变基因表达的化合物)和宿主免疫系统(例如,营养不足可延迟对病原体的免疫反应)。(3) 在人体内,微生物群、宿主表观基因组和宿主免疫系统之间的相互作用是广泛而动态的。宿主DNA和环境会影响这种串扰(例如,表观遗传因素标志着微生物定殖的宿主生态位,这一过程也由免疫系统决定)。饮食介导的效应可以使微生物组、表观基因组和免疫系统之间的关系失去平衡,并在世代内和世代间对全息生物特性产生影响。(4) 同时,人类全息生物通过潜在的下游反馈积极地改变其环境(例如,通过文化生态位构建)
扩展上述命题,假设微生物物种的优势和复发及其在人类中的功能部分反映了可以跨代传递生态信息的保守的表观遗传调控过程。这些表观遗传过程可直接(例如,通过生态位特异性基因调控)和/或间接(例如,通过免疫系统的可塑性选择性)指导宿主的微生物定殖。
进一步假设“微生物组表观基因组免疫轴”对与气候变化相关的饮食、饮食习惯和压力相关的营养变化敏感。充分的饮食改变改变了宿主的表观基因组,进而改变了宿主的微生物组。同时,它们影响微生物的定殖过程,并通过这一过程影响宿主的表观基因组。这些动态变化在宿主的基因组成和非基因成分之间产生了不同程度的不匹配,从而产生了两个关键效应和权衡。
首先,全功能体内的生态系统服务可能被破坏,有害表型可能出现。这与通常提出的异常肠道菌群组成与肥胖症、炎症性肠病、和其他疾病之间的联系一致。然而,改变常驻或定植微生物群,如抗生素使用、饮食变化和人为影响也可能产生非疾病表型。
先前的研究表明,一方面,完整生物环境(即导致微生物组分和代谢能力失衡的环境)与生命早期先天免疫系统活性降低以及生命后期适应性免疫系统(AIS)的过度刺激有关。AIS过度刺激可能会增强免疫失火,从而促进自身免疫疾病的发生。
另一方面,AIS过度刺激可能会增强全功能体生物的防御机制,这种机制通常会随着年龄的增长而恶化,从而延长生物的寿命。AIS过度刺激导致的增强的免疫失火预计会降低妊娠至足月的几率。例如,自身免疫性疾病系统性红斑狼疮增加了妊娠丢失、临产前分娩和胎盘功能不全的风险。因此,在增加疾病的风险,饮食相关的改变也可能延长寿命,降低人类的生育成功率。
其次,宿主的基因组成与其微生物组之间的不匹配可能会产生生物内部的压力,这可能会对生物的组成部分施加不同程度的压力。这种压力类似于在宿主-病原体相互作用中或在本地物种和入侵物种之间的生物入侵过程中出现的压力。例如,宿主-微生物组错配可能会触发不期望的免疫反应,从而削弱宿主,同时在本地(即共同进化的)微生物组分受到破坏后,为定植创造生态位空间。因此,这种不匹配代表了获得适应性变化的第一步。
要理解这一进化过程,首先必须注意的是,寄主的基因组成和微生物群之间的不匹配可以由后代遗传。更具体地说,完整生物的表观基因组可能通过表观遗传修饰的直接传递或表观遗传标记的从头诱导从母亲传给胎儿。这些反复出现的表观遗传模式有利于后代完整生物中亲本微生物组群的重新配置。这意味着患有自身免疫性疾病的个体的后代可能通过非基因遗传表现出相同的特征。与此相一致的是,具有适度遗传力和共同环境风险因素的自身免疫性疾病通常会跨代复发。该模型的一个含义是,人类父母和后代寿命之间的正相关部分反映了跨代表观遗传,与先前的观察和其他物种的发现一致。
与上一代相比,根据宿主基因(其中一半遗传自母亲,另一半遗传自父亲)和环境(可能相对恒定或世代不同)之间的不匹配程度,后代完整生物反复出现的生理或免疫反应可能减弱或加剧。
在一个基本不变的环境中,表型性状的代际转换可能是有方向的,并趋向于局部最优。或者,当环境不断变化时,代际转换可能是波动和不规则的。最简单的情况是,代际环境基本不变,遗传变异性很小,全生命体内的压力有助于恢复生命史特征之间的失调前关系(即,生殖成功率的增加以寿命为代价)。
更一般地说,我们假设,人口的平均适合度有一种自然趋势,即在健康平衡中断时反弹(下图)。类似的动态也与“辅助基因流”有关,通过这种做法,合适的基因型被重新定位,以帮助当地人口跟上气候变化的步伐。这种非当地基因型的重新定位可能会导致繁殖抑制,从而降低人口相对于亲本人口的平均适应度。然而,这种健康状况的下降通常是暂时的。当地人口在几代之内恢复,可能获得比引进移民基因型之前更高的平均适应值。

整体人的健康和适应饮食变化的适应能力。 饮食变化会触发宿主微生物组失配,从而扰乱整个节肢动物(例如,在宿主体内触发不良的免疫反应),同时促进其适应性反应(例如,通过为新型微生物定殖创造适当的空间)。 箭头描绘了由于气候变化引起的饮食转变而引发的人类全生命周期的进化轨迹。 在第一阶段(红色箭头)描述了与饮食变化相关的整体全息内应力。 在这里,整体人面临着疾病的易感性,例如过敏性和自身免疫性疾病,这些疾病可能是表观遗传的。 在这种不稳定的健康状态下,整体类人承受着促进获得微生物,遗传和非遗传变异的压力,最终使整体类人达到了新的平衡(绿色箭头)
影响表型状态遗传的表观遗传机制有助于在新环境中建立最佳适应度。除此之外,还可能发生重新建立宿主-微生物和谐关系的基因变化。免疫、生殖和寿命相关的宿主基因是上述许多可塑性的基础。因此,这些基因的变化有助于重建生态失调前的宿主-微生物平衡。事实上,这些基因在人类适应中起着重要作用,是最常见的候选选择目标之一。
遗传变化也可能在全功能体生物的微生物成分中积累。应激诱导的突变提高了微生物的突变率,加速了有益基因变体的出现。此外,微生物组对应激(暴露于有毒物质)的快速适应和抗性细菌的选择可能使宿主的后代产生更高的毒性耐受性。这可能通过不同的微生物传播途径遗传。最后,微生物组对新饮食的适应可能解释了人类食用海藻的原因,]奶牛的草食进化,吸血蝙蝠的嗜血性。例如,有人认为,应对吸血蝙蝠新饮食所需的形态、免疫和生理适应的很大一部分并不是由于宿主的基因组适应,而是由普通蝙蝠功能核心微生物群中基因的正选择驱动的。因此,由于微生物组的适应性变化,全功能体生物可能进化出适应营养挑战的解决方案。宿主基因组的适应性变化可能伴随也可能不伴随微生物组的重组。
总而言之,与饮食相关的生物体内应激可能会促进宿主和微生物群的遗传和非遗传变化,这些变化可能会传染给下一代。虽然这些变化可能会增加疾病易感性,但也可能有助于重新调整宿主和微生物群的利益。宿主与其微生物群之间重新建立的和谐串扰(如果实现)表明了全息生物在新环境中的最佳综合性能。
除了对全基因组方法的扩展之外,该模型还提供了“健康”或“有利”微生物组的操作定义,即微生物联合体,不仅与宿主的生活方式、社会文化和环境环境相协调,而且在很大程度上,以及它的遗传背景。这些联盟不需要由固定物种组成。由于相当多的代谢冗余,具有相同功能的基因分布在许多细菌物种中。这使得一个“健康”的肠道微生物组群能够以多种不同的方式组合起来,并允许在宿主世代间丢失或重新发现微生物类群。这一定义有助于实施“精确”肠道微生物组群调节的最佳治疗策略。
微生物组通常被认为是许多慢性疾病(如自身免疫疾病)治疗干预的有效靶点,前提是改变的微生物组与某种疾病有因果联系,目前减轻与局部疾病相关的健康挑战的医疗干预形式有可能减轻或抑制生物体内的压力。
在该模型支持下,意味着医疗干预也延迟了潜在适应性变异的出现。基于医学干预放松了对疾病相关基因变异的自然选择这一观点,先前也得出了质量上类似的结论。最后,如果模型是正确的,目前未能解释表观遗传微生物背景和代际影响阻碍了我们对许多疾病的理解。通常与癌症等风险增加相关的特定基因变异,只有在与相关(微)环境因素相结合的情况下才可能是重要的。
到目前为止,很少有生物学家认为发育中有机体的微生物群是有偏见和快速适应性变异的潜在来源,尤其是在人类中。
该研究提出的大视野,跨时空观点需要理解全功能生物体既是一个免疫个体,也是一个进化个体。
为了研究这两者之间的复杂纠缠。首先需要掌握人类微生物变异的限度和范围,了解在环境变化面前(肠道)微生物群落的重组是如何广泛和迅速的。
第二个挑战是了解人类群体之间和内部肠道微生物变异性的差异是否会导致对气候变化相关营养挑战的不同健康和进化反应。
最后,为患者量身定制的医疗应用程序的开发不应将人类个体视为与气候变化相关的健康干预措施的唯一目标。相反,全功能生物体的集体应被视为潜在患者。它复杂的内部关系、串扰和权衡需要成为人们关注的焦点。
相关阅读:
参考文献:
Tomova, A., Bukovsky, I., Rembert, E., Yonas, W., Alwarith, J., Barnard, N. D., & Kahleova, H. (2019). The effects of vegetarian and vegan diets on gut microbiota. Frontiers Nutrition 6, 47
Meldrum, G., Mijatović, D., Rojas, W., Flores, J., Pinto, M., Mamani, G., Condori, E., Hilaquita, D., Gruberg, H., & Padulosi, S. (2018). Climate change and crop diversity: Farmers’ perceptions and adaptation on the Bolivian Altiplano. Environment, Development and Sustainability, 20(2), 703– 730.
Lynch, J. B., & Hsiao, E. Y. (2019). Microbiomes as sources of emergent host phenotypes. Science, 365(6460), 1405– 1409.
Catania Francesco,Baedke Jan,Fábregas-Tejeda Alejandro et al. Global climate change, diet, and the complex relationship between human host and microbiome: Towards an integrated picture.[J] .Bioessays, 2021.
Deutsch, C. A., Tewksbury, J. J., Tigchelaar, M., Battisti, D. S., Merrill, S. C., Huey, R. B., & Naylor, R. L. (2018). Increase in crop losses to insect pests in a warming climate. Science, 361(6405), 916– 919.

谷禾健康


细 菌
单一细菌,是一种微观的单细胞微生物,生活在地球上的几乎每个角落,从深海喷口到地表以下再到人类的消化道,都存在于其中。
结核分枝杆菌
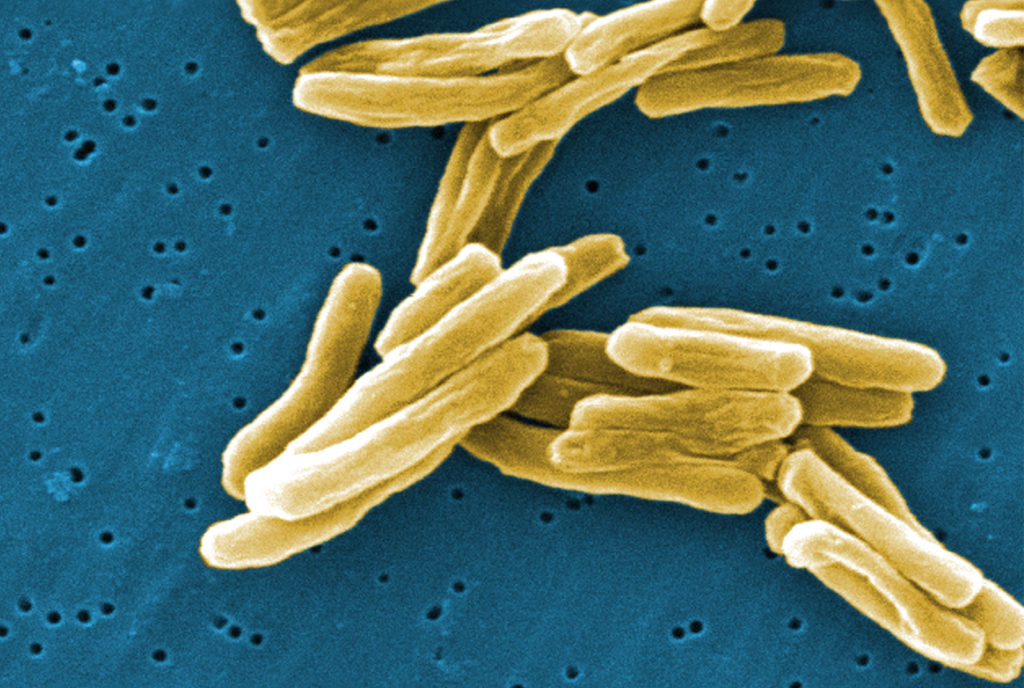
图源:Centers for Disease Control and Prevention
革兰氏阳性结核分枝杆菌细菌(结核病的原因)的扫描电子显微照片
细菌细胞
细菌缺乏与膜结合的细胞核和其他内部结构,因此被称为原核生物。原核生物是地球上占主导地位的生物,在地球历史上大约有四分之三的时间都存在,并且已经适应了几乎所有可用的生态栖息地。
作为一个群体,它们表现出极其多样化的代谢能力,几乎可以使用任何有机化合物和一些无机化合物作为食物来源。一些细菌可以引起人类、动物或植物的疾病,但大多数是无害的,是有益的生态因子,其代谢活动维持更高的生命形式。
其他细菌是植物和无脊椎动物的共生体,它们对宿主起着重要的作用,如固氮和纤维素降解。没有原核生物,土壤就不会肥沃,死去的有机物腐烂的速度也会慢得多。一些细菌被广泛用于食品、化学品和抗生素的制备。对不同细菌群之间关系的研究,不断为地球生命起源和进化机制提供新的见解。
细菌——原核生物
地球上所有的生物都是由两种基本类型的细胞中的一种组成:一种是真核细胞,其遗传物质被包裹在核膜内;另一种是原核细胞,其遗传物质不与细胞的其他部分分离。传统上,所有的原核细胞都被称为细菌,被归为原核生物界。但是,它们的分类为Monera,在分类学上与其他王国(植物界,动物界,真菌和原生生物)相当,这低估了原核细胞相对于真核细胞表现出的显着遗传和代谢多样性。
1970年代后期,美国微生物学家卡尔·沃斯(Carl Woese)率先在分类上进行了重大变革,将所有生物分为真核生物、细菌(原名真细菌)和古细菌(原名古细菌)三个领域,以反映三条古老的进化路线。原核生物以前被称为细菌,然后被分为两个领域,细菌和古细菌。细菌和古细菌在表面上是相似的;例如,它们没有细胞内的细胞器,它们有环状DNA。但是,它们在本质上是截然不同的,它们的分离是基于其古老而又独立的进化谱系的遗传证据,以及其化学和生理学的根本差异。 这两个原核域的成员彼此之间的区别与它们与真核细胞中的区别一样。
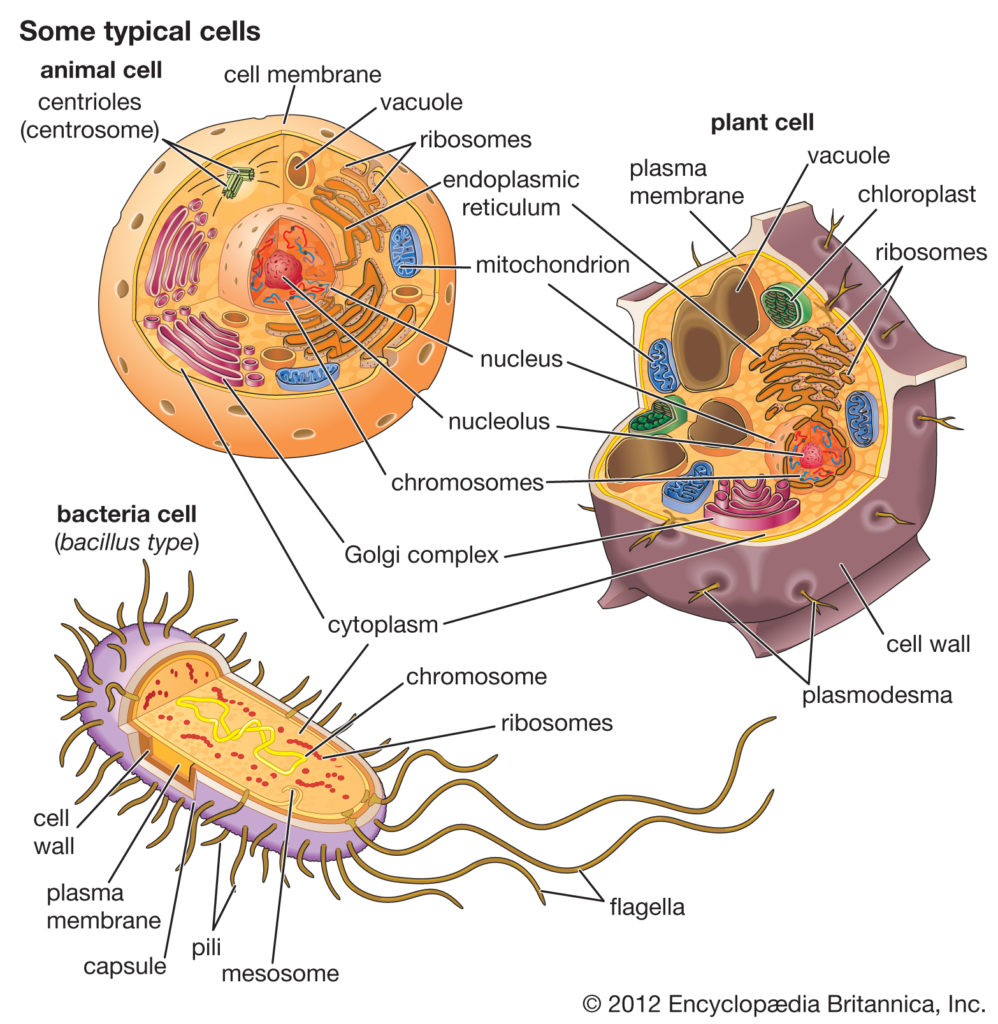
细菌,动物和植物细胞的比较
细菌细胞在几个方面不同于动物细胞和植物细胞。一个根本的区别是细菌细胞缺乏动物细胞和植物细胞中都存在的细胞内细胞器,例如线粒体,叶绿体和细胞核。
原核细胞(即细菌和古细菌)与构成其他生命形式的真核细胞有根本的不同。原核细胞的定义比真核细胞要简单得多。最明显的简化是缺乏细胞内的细胞器,这是真核细胞的特征。所有由细胞器执行的活动也发生在细菌中,但它们不是由专门的结构执行的。此外,原核细胞通常比真核细胞小得多。细菌体积小,设计简单,代谢能力强,使它们能够迅速生长和分裂,并在几乎任何环境中生存和繁衍。
杆菌型细菌细胞
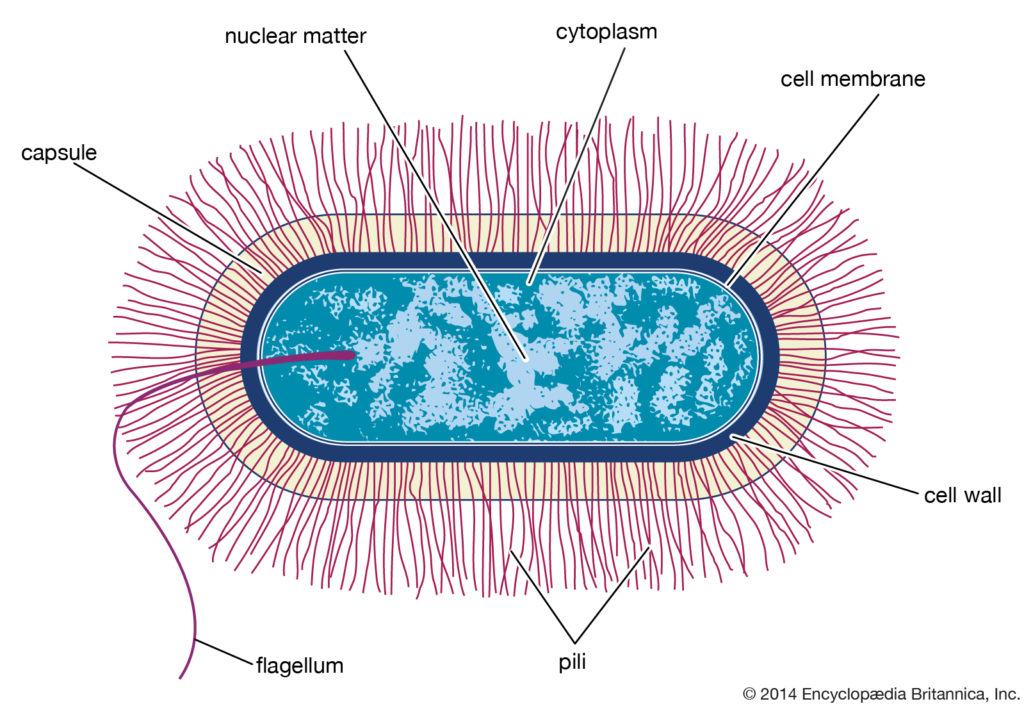
典型的芽孢杆菌属细菌细胞的结构示意图
原核和真核细胞在许多其他方面有所不同,包括脂质组成,关键代谢酶的结构,对抗生素和毒素的反应以及遗传信息的表达机制。 真核生物包含多个线性染色体,这些染色体的基因比编码蛋白质合成所需的基因大得多。 遗传信息的核糖核酸(RNA)副本(脱氧核糖核酸或DNA)的大部分被丢弃,剩余的信使RNA(mRNA)在被翻译成蛋白质之前已被充分修饰。相反,细菌具有一个包含所有遗传信息的环形染色体,它们的mRNA是其基因的精确副本,不会被修饰。
细菌结构的多样性
尽管细菌细胞在结构上比真核细胞小得多,也简单得多,但细菌是一个在大小、形状、生境和代谢上都有差异的极其多样化的有机体群体。许多关于细菌的知识来自对致病细菌的研究,这些细菌比许多自由生活的细菌更容易在纯培养中分离出来,也更容易被研究。必须注意的是,许多自由生活的细菌与适应作为动物寄生虫或共生体生活的细菌有很大的不同。因此,关于细菌的组成或结构没有绝对的规则,任何一般的说法都会许多例外。
单个细菌可以呈现三种基本形状之一:球形(球菌)、棒状(芽孢杆菌)或弧形(弧菌、螺旋体或螺旋体) 。在细菌的实际形状中可以看到相当大的变化,细胞可以在一维中拉伸或压缩。细胞分裂后不分离的细菌形成有助于鉴定的特征性簇。
例如,有些球菌主要成对出现,包括肺炎链球菌Streptococcus pneumoniae(一种引起细菌性大叶性肺炎的肺炎球菌)和淋病奈瑟菌Neisseria gonorrhoeae(一种引起性传播疾病淋病的淋病球菌)。大多数链球菌类似于一长串珠子,而葡萄球菌则形成随机的团块(“葡萄球菌”这个名字来源于希腊语staphyle,意思是“葡萄簇”)。
此外,有些球菌呈方形或立方形。杆状杆菌通常单独出现,但有些菌株形成长链,如棒状杆菌的杆状杆菌,通常以任意角度彼此相连。有些杆菌的末端是尖的,而有些杆菌的末端是方的,有些杆菌的杆弯曲成逗号形状。这些弯曲的杆状病毒通常被称为弧菌,包括霍乱弧菌,它能引起霍乱。
其他形状的细菌包括弯曲和弯曲的螺旋形螺线管和螺旋形螺线管,螺旋形螺线管类似于开瓶器,其中细胞体包裹在称为轴向细丝的中央纤维周围。
变形链球菌
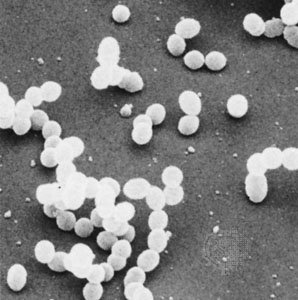
图源:David M. Phillips/Visuals Unlimited
变形链球菌细菌是球形(球菌)细菌的一个例子。这种细菌通常会聚集成对和短链。
细菌是最小的生命体。一种细菌的平均大小,如杆状大肠杆菌,是人类和动物肠道的“正常居民”,长约2微米(μm;百万分之一米),直径0.5μm,金黄色葡萄球菌的球形细胞直径可达1μm。
少数细菌种类甚至更小,如肺炎支原体是最小的细菌之一,其宽度约为0.1至0.25μm,长度约为1至1.5μm;百日咳的病原体为棒状百日咳杆菌,其直径为0.2至0.5μm,长度为0.5至1μm;梅毒病原体螺旋形梅毒螺旋体直径仅0.1~0.2μm,长度6~15μm。蓝藻聚球藻平均直径约0.5~1.6μm。有些细菌相对较大,例如固氮菌,其直径为2至5μm或更大;无色菌,其最小宽度为5μm,最大长度为100μm,视物种而定。用肉眼可以看到巨大的细菌,例如平均直径为750μm的Thiomargarita namibiensis和长度在30到600μm之间的杆状Epulopiscium fishelsoni。
细菌是单细胞微生物,因此通常不会组织起来。 每个细菌的生长和分裂都独立于其他任何细菌,尽管常会发现细菌的聚集体,有时包含不同物种的成员。许多细菌可以形成称为生物膜的聚集结构。
生物膜中的生物通常表现出与处于个体状态或浮游状态的同一生物基本不同的特性。 聚集到生物膜中的细菌可以传达有关种群大小和代谢状态的信息。 这种类型的通信称为群体感应,通过产生称为自动诱导剂或信息素的小分子来进行操作。
群体感应分子(最常见的是肽或酰化高丝氨酸内酯(AHL;特殊的信号化学物质))的浓度与生物膜中相同或不同物种的细菌数量有关,有助于协调生物膜的行为。
革兰氏染色
细菌如此之小,直到1677年才被首次发现,当时荷兰科学家安东尼·列文虎克借助原始显微镜(在设计上与现代放大镜比现代显微镜更相似)在各种物质中看到了微生物,其中一些能放大200倍以上。现在细菌通常在能放大1000倍以上的光学显微镜下进行检查;然而,只有借助更强大的透射电子显微镜才能观察到其内部结构的细节。除非使用特殊的合适的显微镜,否则细菌必须用有色染料染色,以使它们从背景中脱颖而出。
肺炎克雷伯菌
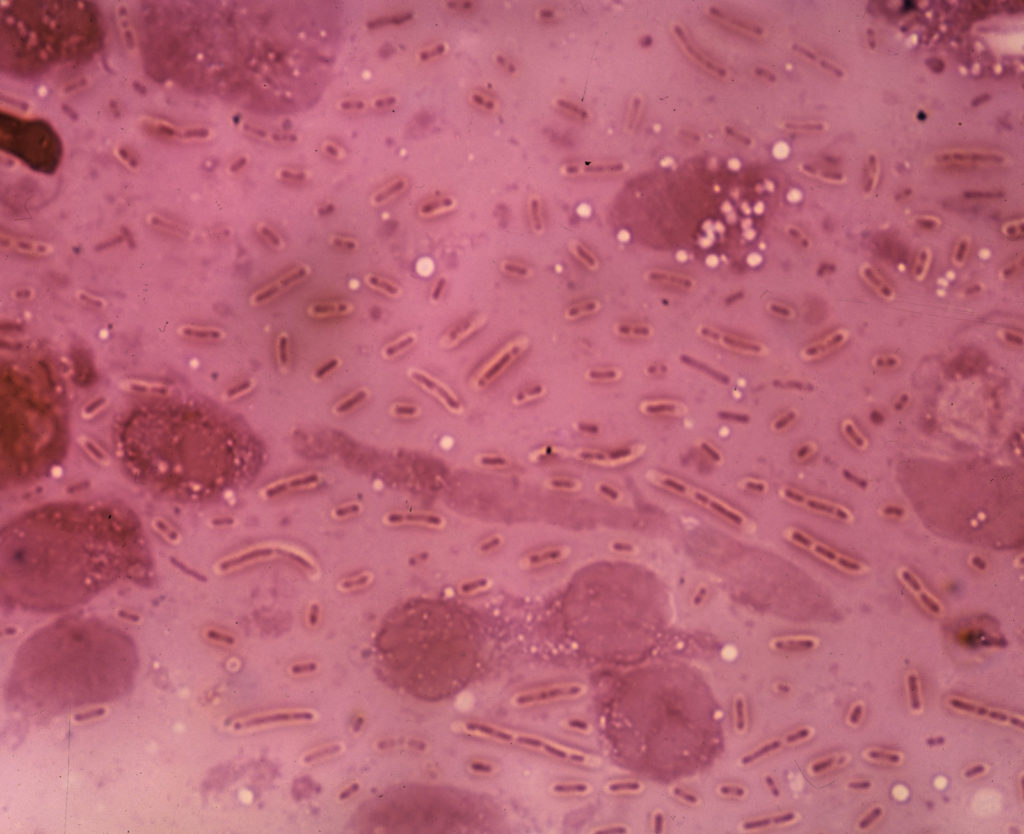
图源:AW Rakosy /Encyclopædia
从肺炎患者的肺脓肿中分离出的革兰氏阴性杆菌肺炎克雷伯菌。
对细菌最有用的染色反应之一叫革兰氏染色,由医生汉斯·克里斯蒂安·格兰姆(Hans Christian Gram)于1884年开发。
悬浮液中的细菌通过短暂加热固定在玻片上,然后暴露在两种染料中,这些染料会在每个细胞内结合形成大的蓝色染料复合物。 当用酒精溶液冲洗载玻片时,革兰氏阳性菌会保留蓝色,而革兰氏阴性菌会失去蓝色。然后用一种较弱的粉红色染料将玻片染色,这种粉红色的染料会使革兰氏阴性菌变成粉红色,而革兰氏阳性菌则保持蓝色。革兰氏染色剂对细菌细胞表面结构的差异起反应,当在电子显微镜下观察细胞时,这种差异是显而易见的。
金黄色葡萄球菌
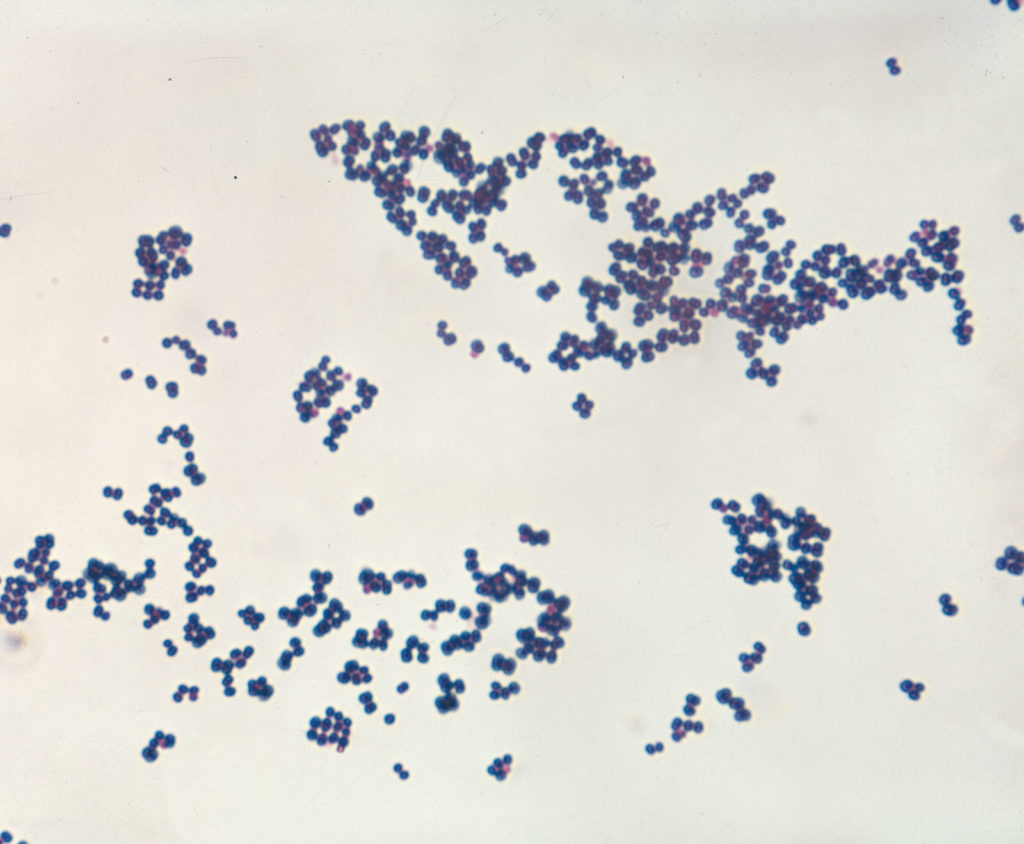
图源:AW Rakosy /Encyclopædia
实验室培养中的革兰氏阳性球菌金黄色葡萄球菌
细胞包膜
细菌细胞表面(或包膜)的结构变化很大,它在细胞的性质和能力中起着核心作用。所有细胞的一个特征是细胞质膜,它将细胞内部与外部环境分开,调节营养物质的流动,维持适当的细胞内环境,并防止细胞内容物的丢失。细胞质膜执行许多必要的细胞功能,包括能量产生、蛋白质分泌、染色体分离和有效的营养物质主动运输。它是一种典型的由蛋白质和脂类组成的单位膜,与包围所有真核细胞的膜基本相似。在电子显微照片中,它是由脂质和蛋白质组成的三层结构,完全包围细胞质。
水螺螺旋藻的肽聚糖层
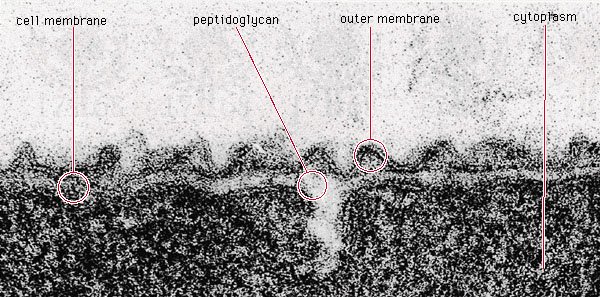
图源:AW Rakosy /Encyclopædia
革兰氏阴性细菌蛇形藻(Aquaspirillum serpens)具有薄的肽聚糖层,位于细胞膜和外膜之间。
肽聚糖只存在于细菌中(没有细胞壁的细菌除外,如支原体)。肽聚糖是两个重复糖(N-乙酰氨基葡萄糖和N-乙酰壁酸)的长链聚合物,其中相邻的糖链通过肽桥相互连接,从而提供刚性稳定性。
肽桥的性质在不同种类的细菌之间有很大差异,但一般由四种氨基酸组成:L-丙氨酸与D-谷氨酸相连,在革兰氏阴性细菌中与二氨基丙酸相连,或在革兰氏阳性细菌中与赖氨酸、L-鸟氨酸或二氨基丙酸相连,最后与D-丙氨酸相连。
在革兰氏阴性菌中,肽桥将一条链上的D-丙氨酸连接到另一条链上的二氨基丙酸。在革兰氏阳性细菌中,可以有一个额外的肽链延伸交叉连接的范围;例如,在金黄色葡萄球菌中有一个额外的五个甘氨酸桥。
肽聚糖的合成是许多有用的抗菌剂的目标,包括阻断肽桥交联的β-内酰胺类抗生素(如青霉素)。动物合成的一些蛋白质作为天然抗菌防御因子攻击细菌的细胞壁。例如,一种名为溶菌酶的酶分解肽聚糖分子的主链糖链。这些药物中的任何一种都会削弱细胞壁并破坏细菌。
在革兰氏阳性细菌中,细胞壁主要由一层厚的肽聚糖网状结构组成,该网状结构与被称为磷壁酸(来自希腊单词teichos,意思是“壁”)的其他聚合物以及一些蛋白质或脂质交织在一起。相反,革兰氏阴性菌有一个复杂的细胞壁,由多层组成,其中一个外膜层位于一个薄肽聚糖层的顶部。这种外膜由磷脂和脂多糖组成,磷脂是一种含有磷酸盐分子的复合脂质,脂多糖是一种复合脂质,通过脂质末端锚定在细胞外膜上,并有一长链糖从细胞延伸到培养基中。
脂多糖,通常被称为内毒素,对动物和人类是有毒的;它们在血液中的存在会导致发烧、休克,甚至死亡。
对于大多数革兰氏阴性细菌来说,外膜形成了一道屏障,阻碍了许多对细菌有害的化学物质的通过,例如通常溶解细胞膜的染料和洗涤剂。对油溶性化合物的不渗透性在其他生物膜中是不存在的,这是由于膜中存在脂多糖和外膜蛋白的不寻常特性造成的。作为外膜抵抗恶劣环境的能力的证据,一些革兰氏阴性细菌在浮油、喷气燃料箱、酸性矿井排水甚至是瓶装消毒剂中生长良好。
古细菌的表面结构与细菌明显不同。它们没有肽聚糖;相反,它们的膜脂是由支链类异戊二烯通过乙醚键与甘油相连组成的。一些古菌的壁材料与肽聚糖相似,只是与氨基酸桥相连的特定糖不是壁酸而是塔罗糖胺酸。许多其他古细菌使用蛋白质作为其细胞壁的基本组成部分,有些则缺乏坚硬的细胞壁。
胶囊和粘液层
许多细菌细胞以荚膜或粘液层的形式分泌一些细胞外物质。黏液层松散地与细菌结合在一起,很容易被洗掉,而胶囊则紧紧地附着在细菌上,并有明确的边界。通过将细胞置于印度墨水的悬浮液中,在光学显微镜下可以看到胶囊。胶囊排除了墨汁,在细菌细胞周围出现了清晰的光晕。
胶囊通常是单糖(多糖)的聚合物,尽管炭疽杆菌的胶囊是由聚谷氨酸制成的。大多数胶囊都是亲水的,可以通过防止水分流失帮助细菌避免干燥(脱水)。胶囊可以保护细菌细胞免受白细胞的吞噬和破坏。虽然逃避吞噬作用的确切机制尚不清楚,但可能是因为胶囊使细菌表面成分更光滑,帮助细菌逃避吞噬细胞的吞噬。肺炎链球菌中存在的胶囊是导致肺炎的最重要因素。肺炎链球菌的突变株失去了形成荚膜的能力,很容易被白细胞吸收,不会引起疾病。在许多其他种类的细菌中也发现了毒力和荚膜形成的联系。
醋酸钙不动杆菌
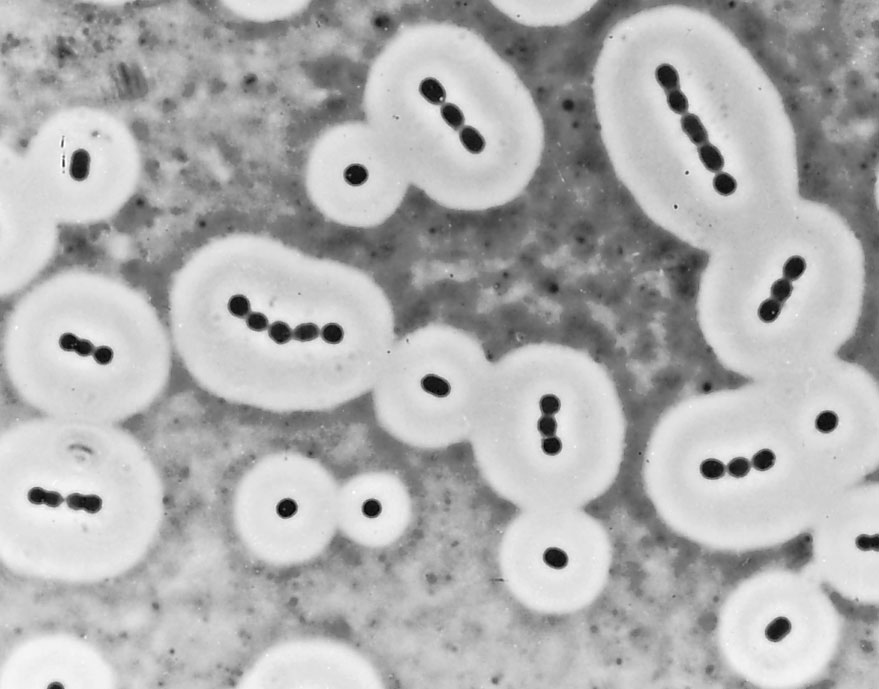
图源:T.J. Beveridge
这些细菌周围的荚膜材料(钙不动杆菌)显示在印度墨水的悬浮液中,并通过光学显微镜(放大约2500倍)观察。
胞外多糖材料的包膜层可以将许多细菌包裹成一个生物膜,并具有多种功能。引起龋齿的变形链球菌Streptococcus mutans,会分解食物中的蔗糖,并利用其中一种糖类来构建它的荚膜,使之紧紧地附着在牙齿上。被困在胶囊中的细菌利用其他糖来促进新陈代谢,并产生一种强酸(乳酸),攻击牙釉质。当铜绿假单胞菌定植于囊性纤维化患者的肺部时,它会产生一种厚的海藻酸囊膜聚合物,从而导致根除细菌的困难。Zoogloea属的细菌分泌纤维素纤维,将细菌缠绕成漂浮在液体表面的絮状物,使细菌暴露在空气中,这是该属新陈代谢的需要。一些杆状细菌,如Sphaerotilus,分泌长而复杂的管状鞘,这些鞘包围了大量的细菌。这些细菌和许多其他环境细菌的外壳会被铁或锰氧化物包裹。
变形链球菌
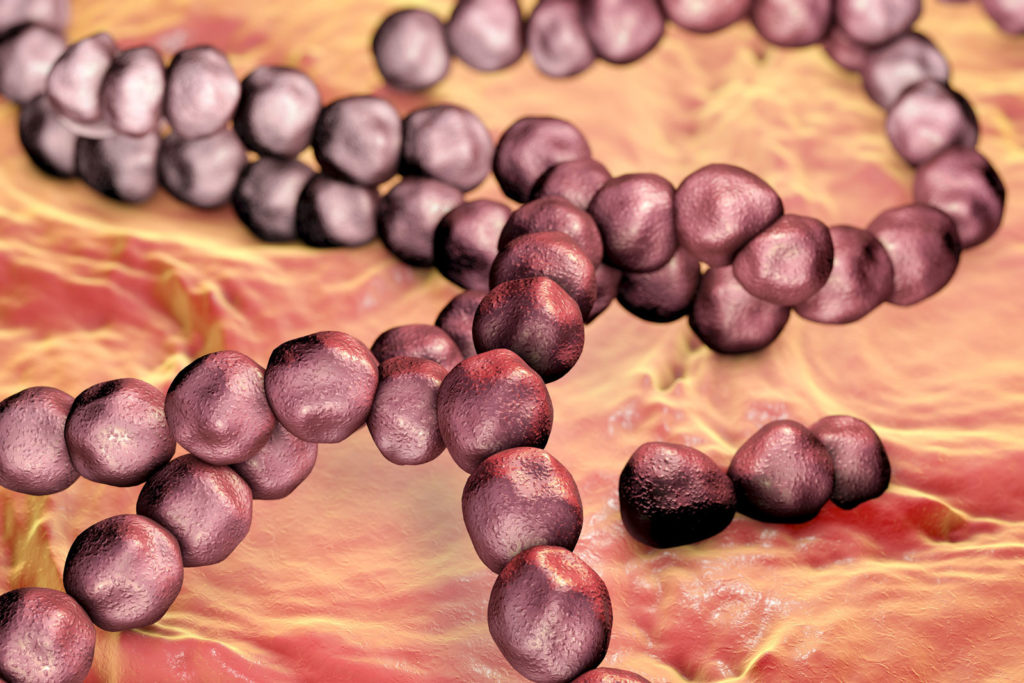
图源:Kateryna Kon / Shutterstock
变形链球菌是一种在口腔中发现的细菌,可导致蛀牙。
鞭毛、菌毛
许多细菌是运动的,能够在液体介质中游动,或在固体表面滑动或聚集。游动和成群的细菌拥有鞭毛,鞭毛是运动所需的细胞外附属物。
鞭毛是由单一类型的蛋白质组成的长而螺旋的细丝,位于杆状细胞的末端,如霍乱弧菌或铜绿假单胞菌,或遍布细胞表面,如大肠杆菌。鞭毛可以在革兰氏阳性和革兰氏阴性杆菌上找到,但在球菌上很少见,并且被困在螺旋体的轴向丝中。
鞭毛在其基部附着在细胞膜的基体上。在膜上产生的原动力被用来转动鞭毛丝,就像涡轮一样,由氢离子流通过基体进入细胞。当鞭毛以逆时针方向旋转时,细菌细胞以直线游动;顺时针方向旋转导致以相反方向游动,或者,如果每个细胞有多个鞭毛,则随机翻滚。趋化性使细菌能够调整自己的游泳行为,使其能够感觉到并向不断增加的引诱性化学物质或远离排斥性化学物质的方向迁移。
细菌不仅能够游向或滑向更有利的环境,而且它们还有附属物,使它们能够粘附在表面,防止被流动的液体冲走。有些细菌,如大肠杆菌和淋病奈瑟菌,会产生笔直、坚硬的尖刺状突起,称为菌毛,它们从细菌表面延伸出来,附着在这些菌株的其他细胞上的特定糖上,肠上皮细胞或泌尿道上皮细胞。菌毛只存在于革兰氏阴性菌中。某些菌毛是用来让一个细菌识别和坚持另一个在有性交配过程中称为接合。许多水生细菌产生一种酸性粘多糖固着物,使它们能够紧紧地附着在岩石或其他表面。
细胞质
虽然细菌在表面结构上有很大的不同,但它们的内部内容物非常相似,显示出相对较少的结构特征。
所有细胞的遗传信息都存在于DNA超长分子的含氮碱基序列中。与真核细胞中的DNA不同的是,细菌细胞中的DNA并没有被隔离在膜结合的细胞器中,而是呈长螺旋状分布在细胞质中。
在许多细菌中,DNA是以单个环状染色体的形式存在的,尽管有些细菌可能含有两条染色体,而且在某些情况下DNA是线性的而不是环状的。可变数量的较小的,通常是圆形的(虽然有时是线性的)DNA分子,称为质粒,可以携带辅助信息。
DNA中的碱基序列已经为数百种细菌所确定。细菌染色体的DNA含量从生殖支原体的580000碱基对到大肠杆菌的4700000碱基对,再到黄色粘球菌的9450000碱基对。粘液杆菌纤维素(Sorangium cellulosum),拥有最大的细菌基因组之一,包含超过1300万个碱基对。大肠杆菌染色体的长度,如果从细胞中取出并拉伸到最大限度,约为1.2毫米,考虑到细胞的长度约为0.001毫米,这蛮惊人的。
与所有生物体一样,细菌DNA含有四种含氮碱基腺嘌呤(A)、胞嘧啶(C)、鸟嘌呤(G)和胸腺嘧啶(T)。 双链DNA分子碱基配对的规则要求腺嘌呤和胸腺嘧啶碱基的数目相等,胞嘧啶和鸟嘌呤碱基的数目也相等。
G和C碱基对的数量与A和T碱基对的数量之间的关系是生物体内进化和适应性遗传变化的重要指标。
G + C的比例或摩尔比可以用G + C除以所有碱的总和(A + T + G + C)乘以100%来测量。生物体之间G + C比率的变化程度可能是相当大的。在动植物中,G + C的比例约为50%。 在原核生物中,G + C的比例范围更广,从大多数支原体的约25%到大肠杆菌中的约50%,到微球菌,放线菌和结实的粘菌中的近75%。但是,单个属中某个物种内的G + C含量非常相似。
细菌的细胞质包含高浓度的酶,代谢产物和盐。 另外,细胞的蛋白质是在分散在整个细胞质中的核糖体上制造的。 细菌核糖体与真核细胞中的核糖体不同之处在于它们更小,具有更少的成分(由三种类型的核糖体RNA和55种蛋白质组成,而真核生物中则由四种类型的rRNA和78种蛋白质组成)并且与作用于真核核糖体的抗生素相比,它们受到不同抗生素的抑制。
细菌细胞质中有许多包涵体或颗粒。这些物体从不被膜封闭,而是作为储存容器。糖原是葡萄糖的聚合物,是碳水化合物和能量的储备。 Volutin或变色颗粒含有聚合磷酸盐,是无机磷酸盐和能量的储存形式。许多细菌具有含有聚β-羟基丁酸聚合物酯或相关化合物的脂滴。这与真核生物不同,真核生物利用脂滴储存甘油三酯。在细菌中,储存颗粒是在有利的生长条件下产生的,并在营养物质从培养基中耗尽后被消耗掉。 许多水生细菌产生气体空泡(或叫气囊),这是一种蛋白质结合的结构,含有空气,其中包含空气,并使细菌能够调节其浮力。 细菌也可以有内部的膜结构,作为细胞质膜的外生物形成。
细菌的生物类型
致病细菌不断地与宿主的免疫系统搏斗,这一事实可能解释了属于同一物种但可通过血清学试验加以区分的不同菌株或类型的细菌数量之多,令人困惑。微生物学家通常通过细胞表面的特定分子来识别细菌,这些分子是用特定的抗体检测出来的。抗体是一种血清蛋白,在免疫反应中与外来分子(抗原)紧密结合,以清除或破坏抗原。抗体具有显着的特异性,蛋白质中甚至一个氨基酸的取代都可能阻止该蛋白质被抗体识别。
对于许多细菌种类,有成千上万种不同的菌株(称为血清变异体,用于血清学变异体),它们主要或仅在其脂多糖、鞭毛或荚膜的抗原特性上彼此不同。例如,肠内细菌的不同血清型,如大肠杆菌和沙门氏菌,常常被发现与栖息在不同宿主动物或引起不同疾病的能力有关。这些众多血清型的形成反映了细菌对免疫系统强烈的防御行为作出有效反应的能力。
生殖过程
二分裂法
大多数原核生物通过二分裂过程进行繁殖,细胞体积不断增大,直至分裂成两半,产生两个完全相同的子细胞。每个子细胞可以继续以与父细胞相同的速度生长。为了实现这一过程,细胞必须在其整个表面生长,直到细胞分裂时,在细胞中部的分裂隔膜处形成一个新的半球形极。
在革兰氏阳性细菌中,隔膜沿着细胞的中点从质膜向内生长;在革兰氏阴性细菌中,细胞壁更具弹性,当侧壁向内挤压时形成分裂隔膜,将细胞一分为二。为了使细胞分裂成两半,肽聚糖的结构必须在半球形帽中不同于在细胞壁的笔直部分,并且不同的壁交联酶必须在隔膜处比在其他地方更活跃。
出芽生殖
一群环境细菌通过出芽繁殖。在这个过程中,在母细胞的一端或丝上形成一个小的芽,称为前列腺癌。随着生长的进行,母细胞的大小保持不变,但芽会扩大。当芽的大小和母细胞差不多时,它就会分离。这种繁殖方式类似于萌芽真菌,如啤酒酵母(Saccharomyces cerevisiae)。分裂和出芽的一个区别是,在后者中,母细胞通常具有与后代不同的特性。在某些巴氏杆菌菌株(Pasteuria strains)中,子芽有鞭毛,并能运动,而母细胞没有鞭毛,但有长的菌毛,但在芽对面的末端具有长的菌毛和固定的附肢。在浮游生物中发现的相关浮萍菌在芽对面的末端具有长的纤维状茎。 在Hyphomicrobium中,菌丝(prostheca)从细胞的一端长出,芽从prostheca的尖端长出,与母细胞相距相对较长的距离。
多形生丝单胞菌
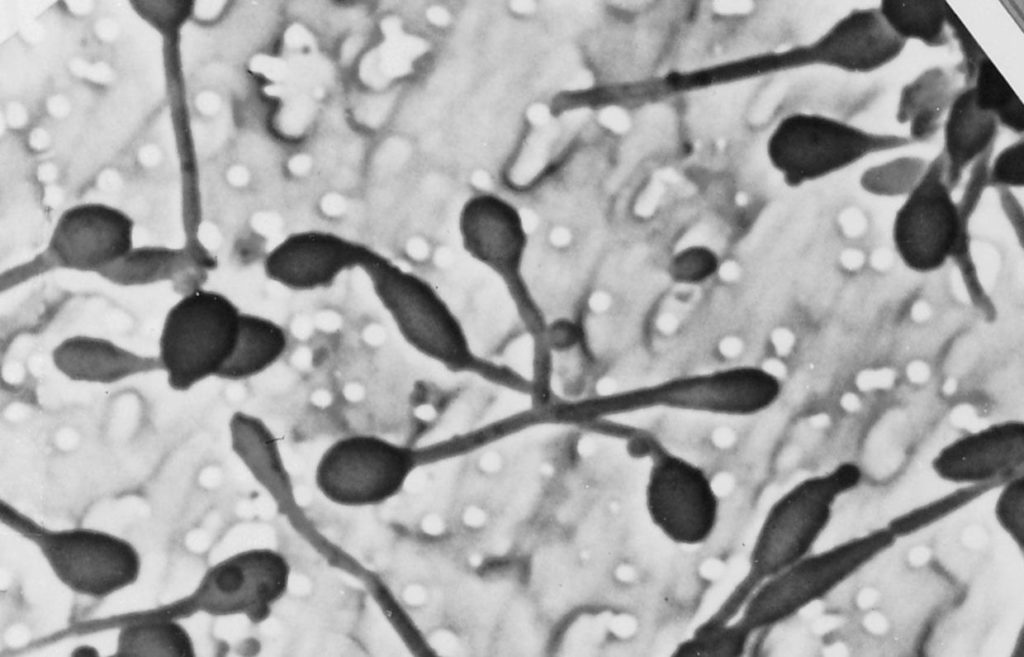
图源:Biological Photo Service
在萌芽的多形性hyphomonas细菌中,芽长在称为prostheca的细丝末端。
孢子繁殖
许多环境细菌能够产生稳定的休眠或休眠形式,作为其生命周期的一个分支,以增强其在不利条件下的生存能力。这些过程不是细胞生命周期的一个强制性阶段,而是一种中断。这种休眠形式被称为内生孢子、胞囊或异胞囊(主要见于蓝藻),这取决于孢子形成的方法,而孢子形成的方法因细菌群而异。
在许多属的细菌中都发现了形成内生孢子的能力,这些细菌主要是革兰氏阳性菌,包括需氧芽孢杆菌(aerobic rod Bacillus),微需氧菌芽孢杆菌(microaerophilic rod Sporolactobacillus),厌氧菌梭状芽孢杆菌(anaerobic rods Clostridium)和脱硫芽孢杆菌(Desulfotomaculum),球菌孢子菌(coccus Sporosarcina)和丝状嗜热放线菌(filamentous Thermoactinomyces)。
孢子的形成是对营养缺乏的反应。 因此,在营养物质可用之前,内生孢子不具有代谢活性,这时它们能够从孢子分化为营养细胞。 在孢子形成过程中,每个细菌细胞内部仅形成一个孢子。孢子的形成始于细菌染色体拷贝周围细胞质膜的内陷,从而使较小细胞的内容物与母细胞分离。
母细胞的膜吞噬了其细胞质内的较小细胞,有效地提供了两个同心的单元膜来保护正在发育的孢子。 薄的孢子膜和厚的肽聚糖皮质位于两个单元膜之间。 皮质外部形成坚硬的孢子皮,包围整个孢子结构。孢子皮具有类似于角蛋白的特性,能够抵抗热,干燥(脱水),冷冻,化学药品和辐射的致死作用。 内生孢子抵抗这些有害物质的能力可能来自于孢子内部极低的水含量。 甲基肌球菌属中的甲烷氧化细菌(Methylosinus)也会产生耐干燥性的孢子,称为外孢子。
包囊是由固氮菌(Azotobacter), 蛭弧菌(Bdellovibrio,蛭包囊)和粘球菌(Myxococcus,粘孢子)的休眠成员产生的厚壁结构。它们对干燥和其他有害条件有抵抗力,但程度低于内生孢子。在固氮固氮菌的包囊中,细胞分裂后形成一层厚厚的多层细胞壁和外壳,包围着静息细胞。
丝状放线菌产生两类生殖孢子:分生孢子,是在地上或基质菌丝体上形成的多个孢子链;孢子囊孢子,是在称为孢子囊的特殊囊中形成的。
遗传信息交流
细菌在其生命周期中没有一个专有性生殖阶段,但它们可以非常活跃地交换遗传信息。DNA中携带的遗传信息可以从一个细胞转移到另一个细胞;然而,这不是真正的交换,因为只有一个’同伴’接收到新的信息。
此外,转移的DNA量通常只是染色体的一小部分。发生这种情况有几种机制。在转化过程中,细菌吸收漂浮在培养基中的游离DNA片段。为了有效地吸收DNA,细菌细胞必须处于一种有能力的状态,这是由细菌结合DNA自由片段的能力来定义的,并且仅在有限数量的细菌中自然形成,例如嗜血杆菌(Haemophilus)、奈瑟菌(Neisseria)、链球菌(Streptococcus)和芽孢杆菌(Bacillus)。在实验室条件下,例如通过暴露于氯化钙(CaCl2)溶液,可以使许多其他细菌,包括大肠杆菌,变得人为地具有竞争力。转化是重组DNA技术中的一个主要工具,因为来自一个生物体的DNA片段可以被另一个生物体摄取,从而使第二个生物体获得新的特性。
细菌之间交换遗传物质
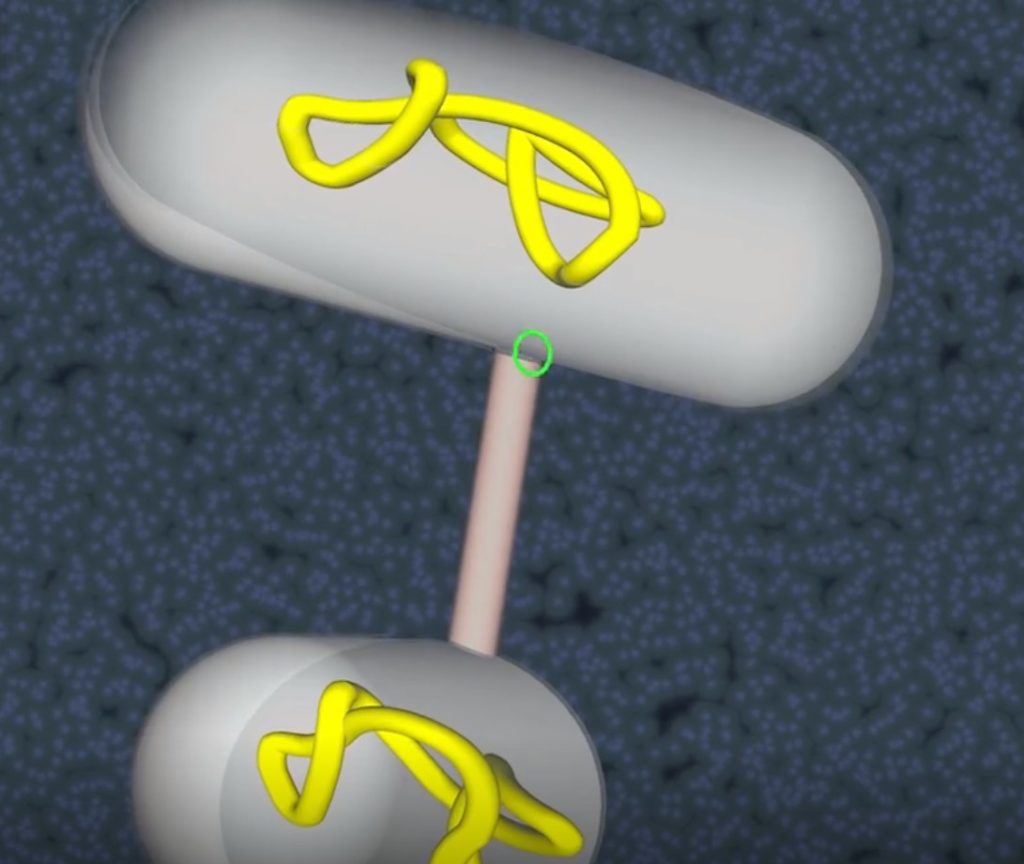
图源:Encyclopædia
细菌DNA可以通过结合和转导过程从一个细胞传递到另一个细胞。
转导是指通过一种称为噬菌体的细菌感染病毒将DNA从一种细菌转移到另一种细菌。转导是在细菌之间转移DNA的有效手段,因为封闭在噬菌体中的DNA受到保护,免受物理降解和环境中酶的攻击,并通过噬菌体直接注入细胞中。 然而,通过转导的广泛基因转移具有有限的意义,因为将细菌DNA包装到病毒中效率低下,并且噬菌体通常在它们可感染的细菌种类范围内受到高度限制。 因此,通过转导进行种间转移的DNA很少。
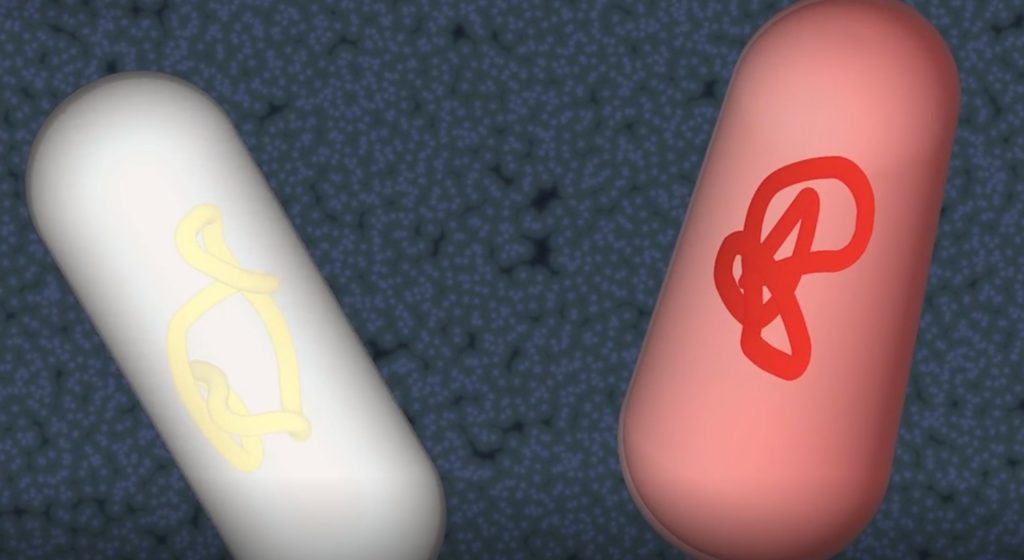
图源:Encyclopædia
接合是通过质粒(非染色体DNA分子)介导的细胞间直接接触的DNA转移。接合质粒编码一种极其有效的机制,它介导自己从供体细胞到受体细胞的转移。因为仅供体细胞包含结合质粒,所以该过程在一个方向上发生。在革兰氏阴性细菌中,供体细胞产生特定的质粒编码菌毛,称为性菌毛,该菌毛将供体细胞附着到受体细胞上。 连接后,两个细胞将直接接触,并形成一个偶联桥,DNA通过该桥从供体转移到受体。 许多接合质粒可以在大量不同的革兰氏阴性细菌之间转移,并在其中繁殖。 质粒的大小不等,从几千个到超过100,000个碱基对。 后者有时被称为巨质粒。
巴氏杀菌如何保护食物
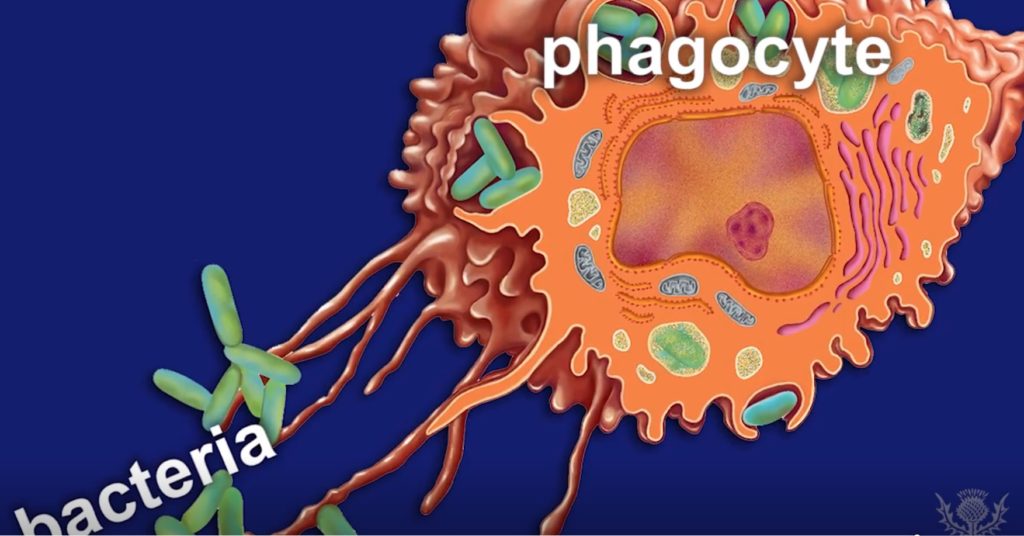
图源:Encyclopædia
细菌可能是致病的(引起疾病),并可能产生毒素,使食物变质并引起食物中毒。细菌引起的某些疾病包括肉毒杆菌中毒,伤寒和肺炎。
细菌的种群增长
细菌培养物的生长被定义为一个群体中细菌数量的增加,而不是单个细胞大小的增加。细菌种群的生长是以几何或指数方式发生的:每一个分裂周期(世代),一个细胞产生2个细胞,然后是4个细胞,然后是8个细胞,然后是16个细胞,然后是32个细胞,依此类推。生成一代所需的时间,即生成时间(G),可通过以下公式计算:
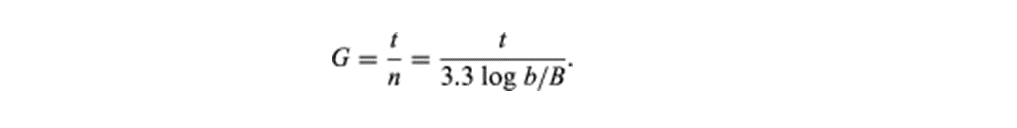
在公式中,B是观察开始时出现的细菌数量,B是时间段t后出现的细菌数量,n是世代数。这种关系表明,平均产生时间是恒定的,细菌数量增加的速度与任何给定时间的细菌数量成正比。这种关系只在种群以指数方式增长的时期有效,称为对数增长期。因此,显示细菌培养物生长的图形被绘制为细胞数的对数。
枯草芽孢杆菌生长周期
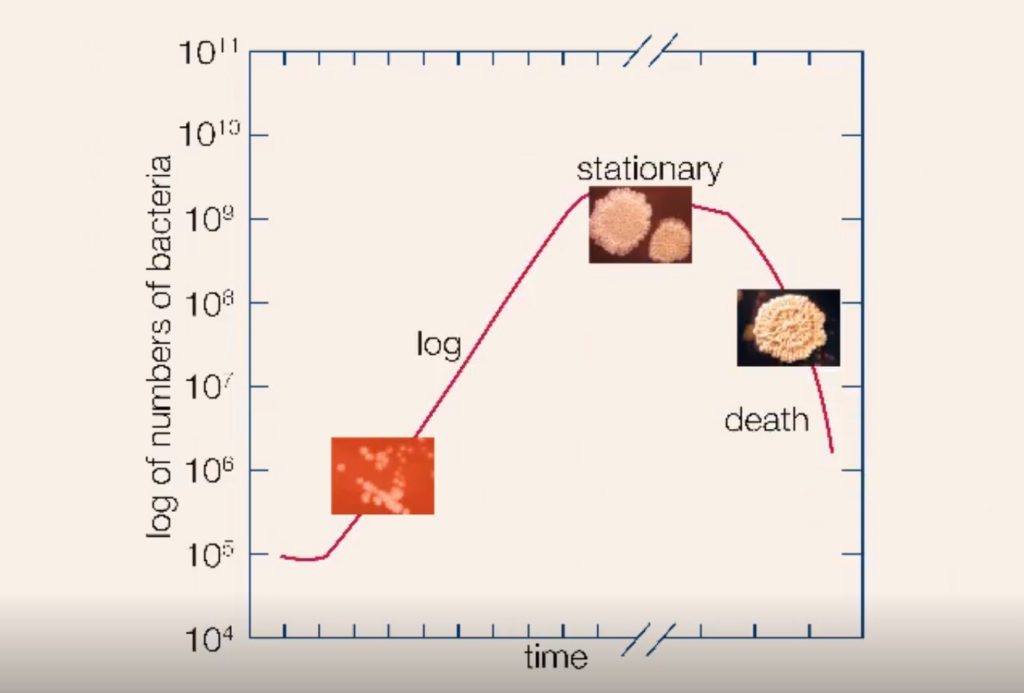
图源:AW Rakosy /Encyclopædia
细菌菌落通过生长的四个阶段进行:滞后阶段,对数阶段,静止阶段和死亡阶段。
细菌的产生时间因细菌而异,受许多环境条件和细菌种类的性质所控制。例如,生长最快的细菌之一产气荚膜梭状芽胞杆菌的最佳生成时间约为10分钟。 大肠杆菌每20分钟可以翻一倍; 生长缓慢的结核分枝杆菌的产生时间为12至16小时。 一些研究人员建议,某些生活在地球表面深处的细菌种群可能以极慢的速度生长,每隔几千年才繁殖一次。 “生长培养基” 例如摄入食物的组成是控制生长速率的主要因素。 当培养基提供更好的能源和细胞原本必须自己制造的更多生物合成中间体时,生长速率会增加到最大。
细菌生长曲线
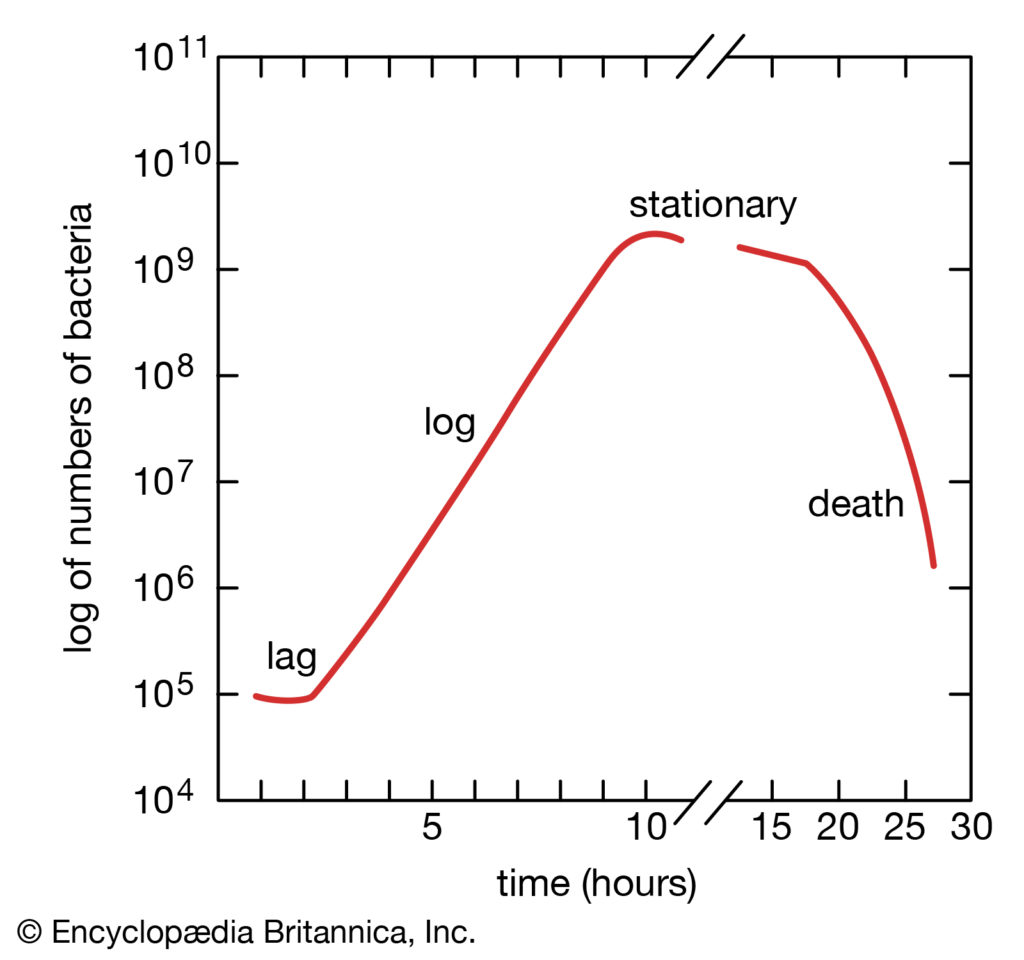
广义细菌生长曲线显示了细菌菌落生长的各个阶段。
当细菌被放置在一个能提供其生长所需的所有营养物质的培养基中时,菌群表现出四个生长阶段,这四个阶段代表了典型的细菌生长曲线。一旦接种到新的培养基中,细菌不会立即繁殖,种群大小保持不变。在这一时期,称为滞后期,细胞代谢活跃,只增加细胞大小。它们还在新的环境条件下合成细胞分裂和种群增长所需的酶和因子。
然后,种群进入对数阶段,细胞数量以对数方式增加,每一代细胞与前一代细胞在相同的时间间隔内发生,从而使每一代细胞的成分均衡增加。对数阶段一直持续到营养物质耗尽或有毒物质积累,此时细胞生长速度减慢,一些细胞可能开始死亡。在最佳条件下,对数末期某些细菌的最大种群密度可达每毫升100亿至300亿个细胞。
枯草芽孢杆菌
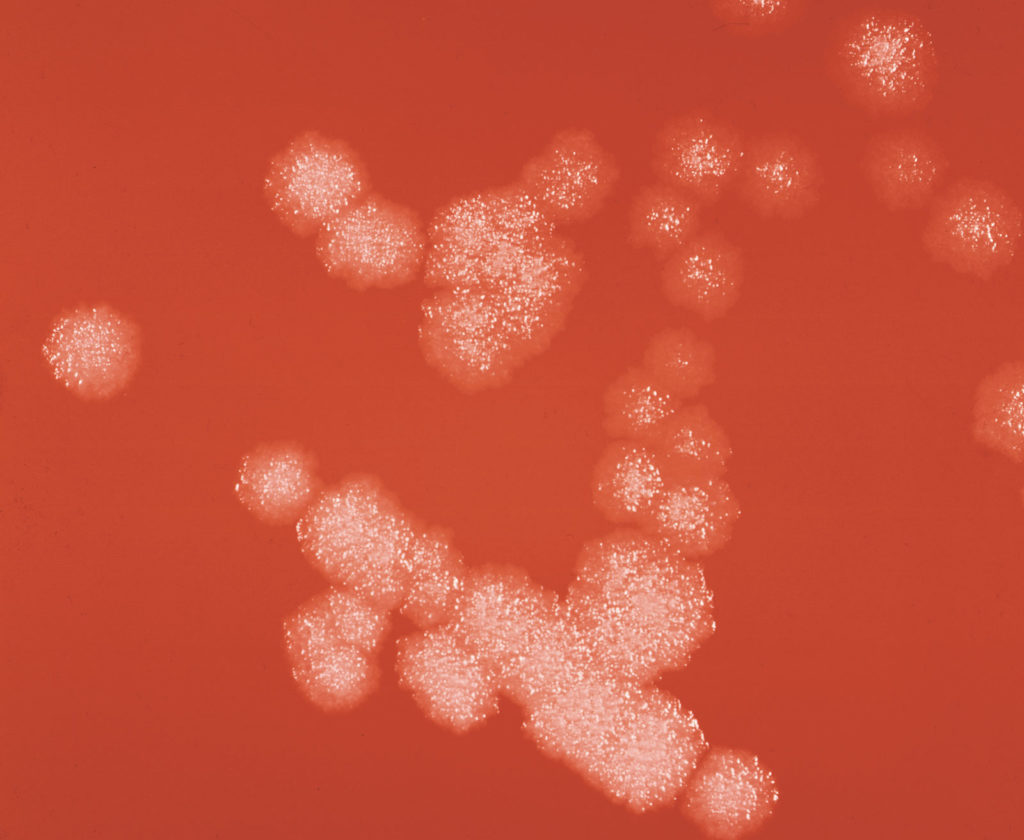
图源:AW Rakosy /Encyclopædia
枯草芽孢杆菌的细菌菌落在37℃下进入生长的对数期培养18-24小时后,(98.6°F;放大约6倍)
细菌生长的对数阶段之后是稳定阶段,在这个阶段,细菌种群的大小保持不变,即使一些细胞继续分裂,而另一些细胞开始死亡。稳定期之后是死亡期,在这一阶段,群体中细胞的死亡超过了新细胞的形成。死亡阶段开始前的时间长短取决于物种和培养介质。即使在缺乏营养的情况下,细菌也不一定会死亡,并且它们可以长期存活。
大自然中的分布
原核生物在地球表面无处不在。 从极地冰到冒泡的温泉,从山顶到海底,从动植物到森林土壤,都可以找到它们。 有些细菌可以在接近冰点的温度下在土壤或水中生长,而另一些细菌则可以在接近沸腾(100°C 的温度下繁殖。 每种细菌都适合生活在特定的环境环境中,无论是海洋表面,泥浆沉积物,土壤还是其他生物的表面。 空气中的细菌含量很低,但是当灰尘被悬浮时含量会升高。 在未受污染的自然水体中,细菌数可以是每毫升数千。 在肥沃的土壤中,细菌数可以达到每克数百万。 在粪便中,细菌数量可能超过每克数十亿。

细菌在有机分解中的作用是从垃圾填埋场和水中去除不需要的生物材料的过程的一部分。
细菌是其栖息生态系统中的重要成员。尽管它们的体积很小,但它们的数量之多意味着它们的新陈代谢在外部环境中的元素转化中起着巨大的作用,有时有益,有时有害。可能每一种自然产生的物质,以及许多人工合成的物质,都能被某些种类的细菌降解(代谢)。奶牛最大的胃——瘤胃是一个发酵室,细菌在其中消化草料和饲料中的纤维素,将其转化为脂肪酸和氨基酸,这是奶牛使用的基本营养素,也是奶牛产奶的基础。污水或堆肥堆中的有机废物被细菌转化为适合植物新陈代谢的营养物质,或转化为气态甲烷(CH4)和二氧化碳。包括动植物在内的所有有机物质的残余物最终通过细菌和其他微生物的活动转化为土壤和气体,从而可供进一步生长。
许多细菌生活在溪流和其他水源中,它们在水样中的低种群密度并不一定表明水不适合饮用。然而,含有大肠杆菌等细菌的水,是人类和动物肠道的正常居民,表明污水或粪便物质最近污染了该水源。这类大肠菌群本身可能是病原体(致病生物),它们的存在表明其他不太容易检测到的细菌和病毒病原体也可能存在。净水厂中使用的沉淀、过滤和氯化程序旨在去除这些以及任何其他可能存在于人类饮用水中的微生物和传染源。水中微生物分解有机物质消耗氧气(生化需氧量),导致氧气水平下降,这对接收废水的溪流和湖泊中的水生生物非常有害。污水处理的一个目标是在有机物排放到水系统之前尽可能地氧化它们,从而降低废水的生化需氧量。为此,污水消化池和曝气装置专门利用细菌的代谢能力。
土壤细菌通过转化土壤的各种物质、腐殖质和矿物质,在影响生物化学变化方面极为活跃。对生命至关重要的元素,如碳、氮和硫,被细菌从无机气态化合物转化为可供植物和动物使用的形式。
细菌还将动植物代谢的最终产物转化为细菌和其他微生物可以利用的形式。氮循环可以说明细菌在影响各种化学变化中的作用。氮在自然界中以几种氧化状态存在,如硝酸盐、亚硝酸盐、二氮气体、几种氮氧化物、氨和有机胺(含有一种或多种取代烃的氨化合物)。固氮是将大气中的二氮气体转化为可供生物利用的形式。一些固氮细菌,如固氮菌、巴氏梭菌和肺炎克雷伯菌,是自由生活的,而根瘤菌则与豆科植物密切相关。
土壤中的根瘤菌生物识别并侵入其特定植物宿主的根毛,进入植物组织,并形成根瘤。 这个过程导致细菌失去许多自由活动特性。 它们变得依赖于植物所提供的碳,并且作为碳的交换,它们将氮气转化为氨,氨被植物用于其蛋白质的合成和生长。 另外,当硝酸盐用作电子受体时,许多细菌可以将硝酸盐转化为胺,以合成细胞材料,或将其转化为氨。反硝化细菌将硝酸盐转化为氮气。 氨或有机胺向硝酸盐的转化是通过需氧生物硝化单胞菌和硝化细菌的联合活动来完成的,它们利用氨作为电子供体。
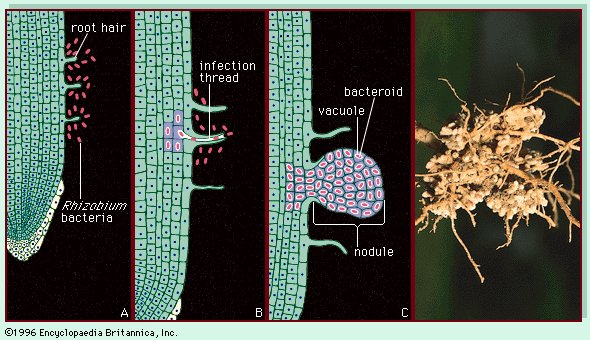
固氮细菌 (右)豌豆植物(Pisum sativum)的根部,其根瘤内藏有固氮细菌(Rhizobium)。(左)根瘤是根瘤菌与植物根毛之间共生关系的结果。细菌识别根毛并开始分裂(A),通过感染线(B)进入根部,使细菌进入根细胞,然后分裂成结节(C)
在碳循环中,二氧化碳被植物和自养原核生物转化为细胞物质,有机碳通过异养生物返回大气。 微生物分解的主要分解产物是二氧化碳,它是由呼吸需氧生物而形成的。
甲烷是碳代谢的另一种气体最终产物,是全球碳循环中相对次要的组成部分,但在当地情况下具有重要意义,是供人类使用的可再生能源。甲烷的产生是由高度专业化和专性厌氧产甲烷原核生物进行的,它们都是古细菌。产甲烷菌利用二氧化碳作为末端电子受体,从氢气(H2)中接收电子。其他一些物质可以被这些生物转化为甲烷,包括甲醇、甲酸、乙酸和甲胺。
尽管产甲烷菌可利用的物质范围极窄,但在许多有机物质(包括纤维素、淀粉、蛋白质、氨基酸、脂肪、醇和大多数其他底物)的厌氧分解过程中,甲烷的生成非常普遍。从这些物质中生成甲烷需要其他厌氧菌将这些物质降解为醋酸盐或二氧化碳和氢气,然后由产甲烷菌(methanogens)使用。产甲烷菌通过去除甲烷代谢活动中产生的氢气来支持混合物中其他厌氧菌的生长。消耗氢气会刺激其他细菌的新陈代谢。
尽管产甲烷菌的代谢能力非常有限,而且对氧非常敏感,但它们在地球上很普遍。大量的甲烷是在厌氧环境中产生的,比如沼泽和沼泽,但是土壤和反刍动物也会产生大量的甲烷。大气中至少80%的甲烷是由产甲烷菌作用产生的,其余的则是从煤层或天然气井中释放出来的。
食物中的细菌
健康奶牛的牛奶最初含有很少的细菌,这些细菌主要来自奶牛的皮肤和处理牛奶的程序。牛奶是许多细菌的极好生长介质,除非牛奶经过适当加工,否则细菌的数量会迅速增加。如果存在致病菌,细菌生长会破坏牛奶,甚至对健康造成严重危害。可以从被感染的牛传播的疾病包括结核病(结核分枝杆菌,Mycobacterium tuberculosis),不发烧的发热(流产的布鲁氏菌Brucella abortus)和发热的病原体(柯氏杆菌Coxiella burnetii)。
此外,伤寒可通过受感染的牛奶处理者的牛奶传播。 巴氏杀菌程序将牛奶的温度升高30分钟至63°C(145°F)或15秒升高至71°C(160°F),这可以杀死可能存在的任何病原菌,尽管这些程序不能杀死所有微生物。
某些细菌将牛奶转化成有用的乳制品,如酪乳、酸奶和奶酪。商业培养的酪乳是从接种了乳酸菌(Lactococcus)发酵剂(通常是乳酸乳杆菌或乳酪乳杆菌)的牛奶中制备的。酸奶和其他发酵乳制品是用不同的细菌培养物以类似的方式生产的。许多奶酪也是通过细菌的作用制成的。产酸细菌如乳乳酸杆菌在牛奶中的生长会使酪蛋白沉淀成凝乳。除去水分和加盐后,凝乳在其他微生物的作用下成熟。不同的细菌赋予食物不同的风味和特性;例如,干酪乳杆菌、嗜热链球菌和舍曼丙酸杆菌的混合物负责瑞士奶酪的成熟,并产生其特有的味道和大气泡。其他类型的细菌长期以来被用于制备和保存通过细菌发酵生产的各种食品,包括腌制产品、泡菜和橄榄。
在食物中传播的许多致病菌的毒素在摄入时会引起食物中毒。其中包括一种由金黄色葡萄球菌(Staphylococcus aureus)产生的毒素,这种毒素能引起迅速、严重但有限的胃肠道不适,或者肉毒梭菌(Clostridium botulinum)的毒素,这种毒素通常是致命的。在密封前未完全煮熟的罐装非酸性食品中可能产生肉毒杆菌毒素。肉毒梭菌形成耐热孢子,可以发芽为营养细菌细胞,在厌氧环境中茁壮成长,这有利于产生其极强的毒素。其他食源性感染实际上是由受感染的食物处理者传播的,包括伤寒、沙门氏菌病(沙门氏菌属)和志贺氏菌病(痢疾志贺氏菌属)。

图源:Encyclopædia
工业中的细菌
各种细菌的厌氧糖发酵反应会产生不同的最终产物。用酵母生产乙醇已经被酿酒工业开发了几千年,并被用于燃料生产。在醋的生产过程中,特定的细菌将酒精氧化成醋酸。其他的发酵过程可以制造出更有价值的产品。有机化合物,如丙酮、异丙醇和丁酸,是由各种梭状芽孢杆菌(Clostridium)在发酵过程中产生的,可以在工业规模上制备。在极端环境的生物中也发现了其他细菌产物和反应。 从嗜热细菌中分离出的酶引起了极大的兴趣,在这些酶中,由于可以在较高的温度下进行反应,因此可以以较高的速率进行反应。
来源:Encyclopædia
烃类氧化细菌和真菌对石油产品的微生物分解具有重要的生态学意义。石油的微生物分解是一个好氧过程,如果石油沉淀到底部的厌氧沉积物层(厌氧环境中的天然石油沉积物有数百万年的历史),那么这一过程就会被阻止。碳氢化合物氧化细菌附着在水面上漂浮的油滴上,它们的作用最终将油分解为二氧化碳。 将此类细菌及其生长因子喷洒到溢油上以提高非挥发性脂族和芳族烃的降解速度已成为一种常见的做法。
医学中的细菌
菌性疾病在人类历史上起着主导作用。 霍乱和鼠疫的广泛流行使世界上某些地区的人口减少了三分之一以上。细菌性肺炎可能是老年人死亡的主要原因。 也许有更多的军队被伤寒,痢疾和其他细菌感染击败,而不是被武力击败。 随着管道和卫生设备的现代发展,细菌疫苗的发展以及抗菌素的发现,细菌性疾病的发生率已降低。 然而,细菌没有继续作为传染因子消失,因为它们继续进化,产生了越来越强的毒株并获得了对许多抗生素的抗性。
尽管大多数细菌对地球上的生命都是有益的,甚至是生命所必需的,但少数细菌却对人类有害。 目前,没有一种古细菌被认为是病原体,但是包括人类在内的动物不断遭到大量细菌和各种细菌的轰击和居住。 与动物接触的大多数细菌都可以通过宿主的防御系统迅速消除。 口腔,肠道和皮肤被大量特定类型的细菌定殖,这些细菌适应这些栖息地的生活。 这些生物在正常情况下是无害的,并且仅在它们以某种方式穿过身体的屏障并引起感染时才变得危险。
一些细菌擅长入侵宿主,被称为病原体或疾病产生者。 一些病原体作用于人体的特定部位,例如脑膜炎球菌(Neisseria meningitidis),它会侵袭并刺激脑膜,大脑和脊髓周围的膜,并刺激脑膜。白喉细菌(Corynebacterium diphtheriae),最初感染喉咙; 以及在肠道中繁殖的霍乱细菌(霍乱弧菌),其产生的毒素导致该霍乱的大量腹泻。 其他能感染人类的细菌包括葡萄球菌(主要是金黄色葡萄球菌),它能感染皮肤引起疖子(疖子),血液引起败血症(血液中毒),心脏瓣膜引起心内膜炎,或骨头引起骨髓炎。
来源:Encyclopædia
人体中的细菌
图源:Encyclopædia
人体屏障(例如皮肤和肠道内壁)中的天然细菌在正常的人类生理过程中起着重要的作用。
侵入动物血液的病原菌可以利用多种机制中的任何一种来逃避宿主的免疫系统,包括形成长的脂多糖链,从而对一组血清免疫蛋白(称为补体)产生抵抗力,补体通常会抑制细菌的生长。细菌表面蛋白的致病性重组阻止动物产生的抗体识别病原体,在某些情况下使病原体能够在吞噬性白细胞中存活和生长。许多病原菌产生毒素,协助它们入侵宿主。这些毒素包括蛋白酶,分解组织蛋白质的酶,以及脂肪酶,分解脂质(脂肪)并通过破坏细胞膜来损伤细胞的酶。其他毒素通过在细胞膜上形成孔或通道来破坏细胞膜。一些毒素是修饰参与蛋白质合成或控制宿主细胞代谢的特定蛋白质的酶;例如白喉、霍乱和百日咳毒素。
补体激活途径
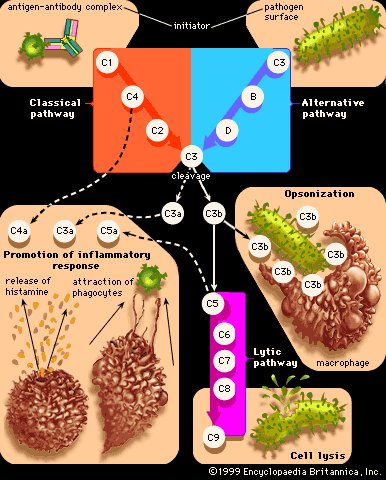
补体蛋白的主要功能是通过刺穿病原体的外膜(细胞裂解)或使它们对吞噬细胞(例如巨噬细胞)更具吸引力来帮助破坏病原体(这一过程称为调理作用)。一些补体成分还通过刺激细胞释放组胺和将吞噬细胞吸引到感染部位来促进炎症。
一些病原细菌在宿主体内形成区域,在这些区域中它们被封闭并不受免疫系统的保护,例如葡萄球菌形成的皮肤疖子和结核分枝杆菌形成的肺部空洞。脆弱拟杆菌(Bacteroides fragilis)大量存在于人体肠道中,但是一般不会对宿主造成任何困难。如果这种细菌通过损伤进入体内,细菌囊会刺激身体将细菌隔离成脓肿,从而减少细菌的传播。在许多情况下,细菌感染的症状实际上是免疫系统过度反应的结果,而不是细菌产生毒性因子的结果。
对抗致病性细菌感染的其他方法包括使用生物治疗剂或益生菌。这些无害的细菌会干扰病原菌的定殖。另一种方法是利用噬菌体,即杀死细菌的病毒,来治疗特定细菌病原体的感染。此外,20世纪80年代发展起来的重组DNA技术使细菌合成几乎任何蛋白质成为可能,大肠杆菌是这一过程中常见的宿主。重组DNA技术用于廉价、大规模生产极为稀缺和有价值的动物或人类蛋白质,如激素、凝血因子,甚至抗体。
细菌自地球生命史以来就已经存在。 在岩石中发现的细菌化石至少可以追溯到泥盆纪时期(4.192亿至3.589亿年前),并且令人信服的论点是自前寒武纪大约35亿年前就已经存在细菌。细菌至少在大约18亿年前的古元古代末期就已在地球上广泛传播,当时由于蓝细菌的作用,大气中出现了氧气。 因此,细菌有足够的时间来适应其环境,并产生了许多后代。
关于生命起源所涉及的原始祖先的性质,人们有相当多的猜测。有人认为原始细胞可能使用RNA作为其遗传物质,因为研究表明RNA分子可以具有多种催化功能。在这个时期,细菌和古菌很早就从它们共同的前体中分化出来。这两类原核生物倾向于栖息在不同类型的环境中,并以不同的速度产生新的物种。许多古菌喜欢高温生态位。古细菌树的一个主要分支仅由嗜热物种组成,而另一个主要分支中的许多产甲烷菌可以在高温下生长。相反,没有一个主要的真细菌分支仅仅由嗜热菌组成。细菌和古细菌都含有能够在高温下生长的成员,以及其他能够在低温下生长的物种。另一个显著的区别是细菌广泛地适应好氧条件,而许多古细菌是专性厌氧菌。没有古细菌是专性光合作用的。也许古细菌是一种较原始的生物体,对变化的环境条件的遗传反应受损。 适应新情况的能力有限可能会将古细菌限制在恶劣的环境中,与其他生命形式的竞争较少。
根据三域系统的生命之树
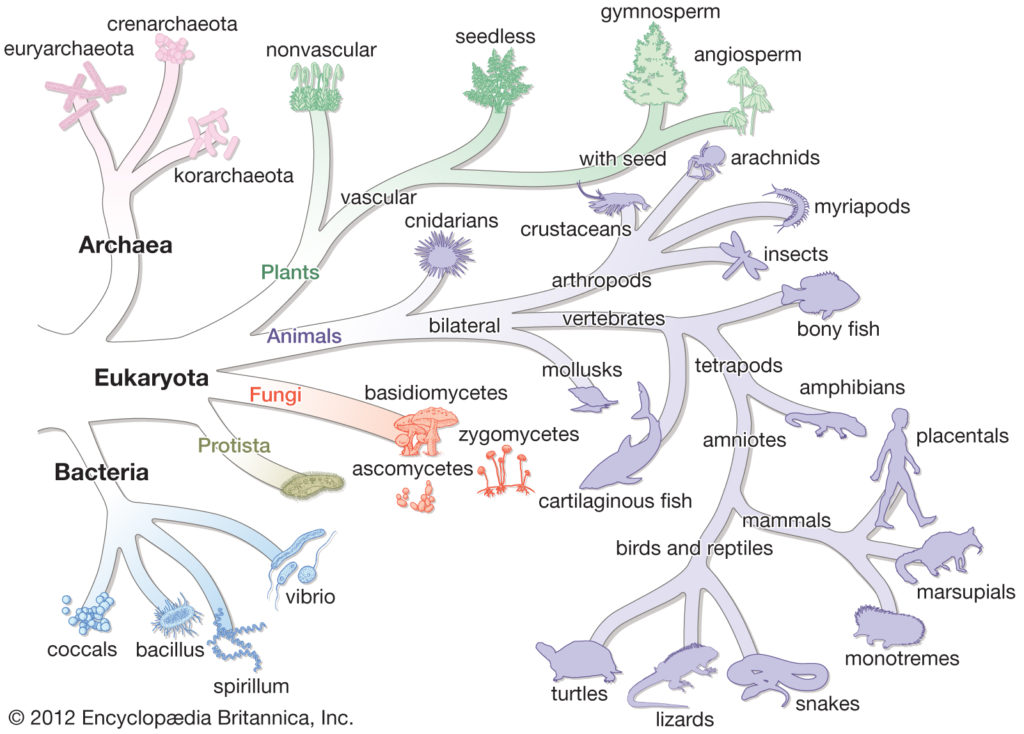
有机体必须不断进化或适应不断变化的环境,很明显,突变,即有机体DNA中核苷酸序列的变化,在所有有机体中不断发生。DNA序列的变化可能会导致该DNA片段编码的蛋白质的氨基酸序列发生变化。因此,改变后的蛋白质可能更适合或不太适合在当前条件下发挥功能。尽管DNA中可能发生的许多核苷酸变化对细胞的适应性没有影响,但如果核苷酸变化能促进细胞的生长,哪怕是很小的程度,那么突变型细胞就能够增加其在群体中的相对数量。然而,如果核苷酸的改变阻碍了细胞的生长,那么突变形式就会被其他细胞所取代而丧失。
在生物体之间传递遗传信息的能力是适应环境变化的一个主要因素。DNA交换是高等真核生物生命周期的重要组成部分,在所有真核生物中都有发生。基因交换也发生在整个细菌世界,虽然转移的DNA量很小,但这种转移可以发生在远缘生物之间。携带在质粒上的基因可以进入细菌染色体,成为细菌遗传的稳定部分。生物体通常拥有称为转座子的可移动遗传元件,可以重新排列染色体上任何基因的顺序和存在。转座子可能在帮助加快进化速度方面发挥作用。
细菌快速进化的例子很多。在20世纪40年代以前,抗生素还没有用于医疗实践。当抗生素最终投入使用时,大多数致病菌对它们很敏感。然而,从那时起,细菌对一种或多种抗生素的耐药性增加,以至于以前有效的抗生素对某些类型的细菌不再有用。大多数致病细菌对抗生素耐药的例子并不是由于突变改变了抗生素攻击的蛋白质,尽管这种机制可能发生。相反,抗生素抗性通常涉及细菌产生的酶,这些酶会改变抗生素并使之失活。抗生素耐药性传播的一个主要因素是可传播的质粒,它将药物灭活酶的基因从一个细菌携带到另一个细菌。尽管这些酶的基因的原始来源尚不清楚,但可移动的基因元件(转座子)可能在它们的出现中起了作用,也可能允许它们转移到其他细菌类型。
影响细菌生长的因素
细菌在最佳生长所需的条件上有很大的不同。就营养需求而言,所有细胞都需要碳、氮、硫、磷、多种无机盐(如钾、镁、钠、钙和铁)以及大量其他微量元素(如锌、铜、锰、硒、钨和钼)。碳是细菌最需要的元素,因为氢和氧可以从水中获得,这是细菌生长的先决条件。同时还需要一种能量来源来促进细菌的新陈代谢。组织细菌的一种方法是基于这些基本的营养需求:碳源和能源。
细胞可用于碳的来源有两种:无机化合物和有机化合物。使用无机化合物二氧化碳(CO2)作为碳源的生物称为自养生物。 需要碳的有机源(例如糖,蛋白质,脂肪或氨基酸)的细菌称为异养生物(或有机营养菌)。 许多异养生物,例如大肠杆菌或铜绿假单胞菌,都由简单的糖(例如葡萄糖)合成所有细胞成分,因为它们具有必要的生物合成途径。 其他异养生物失去了其中一些生物合成途径。 为了生长,它们要求其环境包含化学上完整的特定氨基酸,含氮碱或维生素。
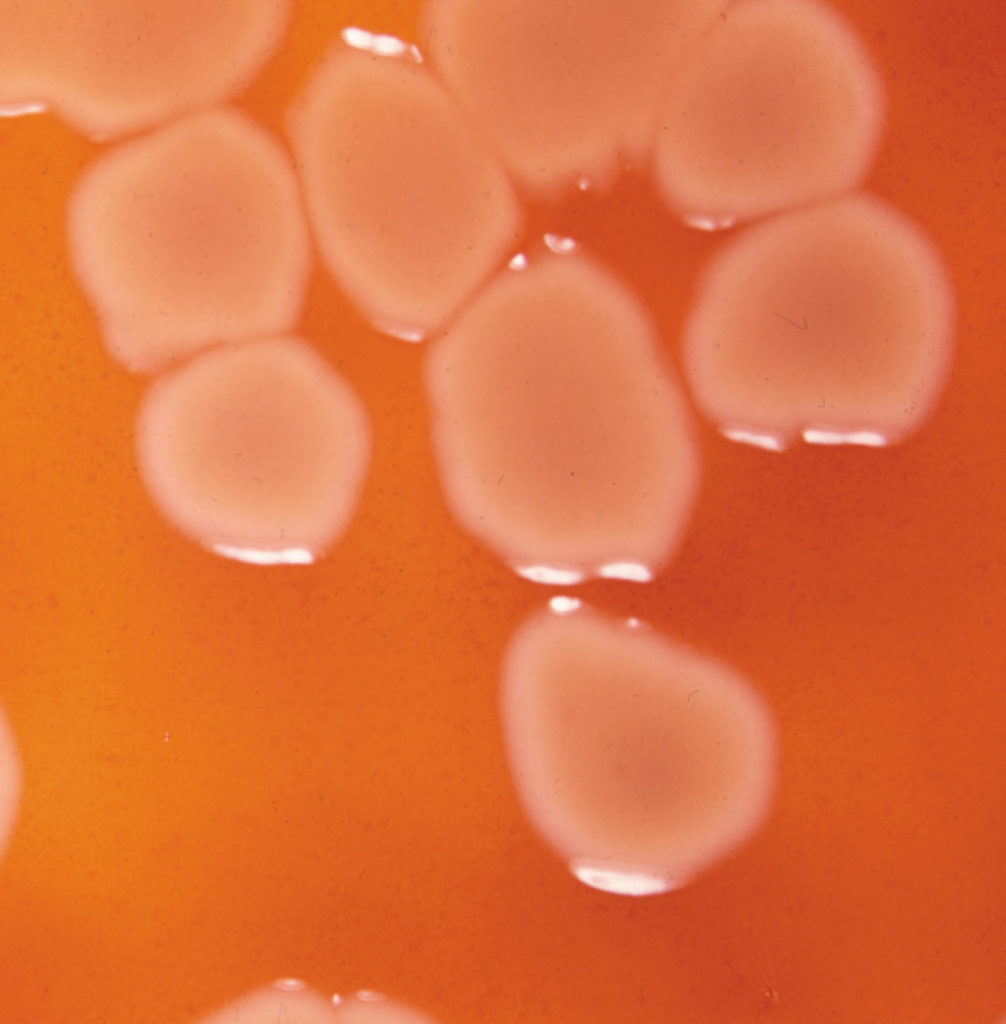
铜绿假单胞菌
除了碳,细菌还需要能量,能量几乎总是通过电子从电子供体转移到电子受体来获得的。有三种基本的能源:光、无机化合物和有机化合物。光营养细菌利用光合作用从光能中产生三磷酸腺苷(ATP)形式的细胞能量。化学营养体从化学物质(有机和无机化合物)中获取能量;化学石营养体从与无机盐的反应中获取能量;化学异养体从有机化合物中获取碳和能量(能量源也可作为这些生物体的碳源)。
在大多数情况下,细胞能量是通过电子转移反应产生的,其中电子通过一种途径从电子或有机供体分子移动到受体分子,从而保留了电子在转移过程中释放出的能量,其形式为电子俘获 细胞可用于其化学或物理工作的物质。 从电子传输中捕获的主要能量形式是ATP。 分解有机分子以产生能量的代谢过程称为分解代谢反应。 相反,合成分子的代谢过程称为合成代谢反应。
许多细菌可以使用大量的化合物作为碳和能源,而其他细菌的代谢能力受到很大限制。尽管碳水化合物是真核生物的常见能源,但是由于大多数细菌不具有代谢这些通常复杂的分子所必需的酶,因此这些分子仅通过有限数量的细菌进行代谢。 相反,许多细菌都依赖于其他能源,例如氨基酸,脂肪或其他化合物。 对细菌重要的其他化合物包括磷酸盐,硫酸盐和氮。 由于许多细菌无法合成磷酸盐,因此在许多环境中,尤其是在水中,磷酸盐含量低可能是细菌生长的限制因素。 另一方面,大多数细菌可以将硫酸盐或硫化物转化为蛋白质合成所需的有机形式。 生命有机体从氨中吸收氮的能力是广泛存在的,细菌将其他形式的氮(例如土壤中的硝酸盐或大气中的二氧化氮转化为细胞物质的能力也有所不同。
有些细菌是专性寄生虫,只在活的宿主细胞内生长。例如,立克次体(Rickettsia)和衣原体(Chlamydia), 在真核细胞中生长,蛭弧菌(Bdellovibrio)在细菌细胞中生长。梅毒螺旋体(Treponema pallidum)很难(即使不是不可能)在培养中生长,可能是因为它需要低的氧张力和低的氧化还原水平,这是由于存在动物细胞而不是任何特定的营养素所致。因为有些细菌可能只以动物或植物寄生虫的形式生长,或者只在牛奶等营养丰富的来源中生长,所以它们在自然界中不可能以游离细菌的形式生长。许多来自自然环境的细菌与其他细菌联合存在,很难从该伙伴关系的其他成员中分离和培养。
对于不同的细菌类型来说,最适合细菌生长的物理条件有很大的不同。作为一个群体,细菌在不同环境中的生存能力在所有生物中表现出最大的差异。
氧 气
细菌之间最显著的区别之一是它们对大气氧(O2)的需求和反应。实际上,所有的真核生物都需要氧气才能茁壮成长,而许多种类的细菌可以在厌氧条件下生长。需要氧气才能生长的细菌称为专性需氧细菌。在大多数情况下,这些细菌需要氧气才能生长,因为它们产生能量和呼吸的方法依赖于电子向氧气的转移,而氧气是电子传递反应中的最终电子受体。
专性需氧菌包括枯草芽孢杆菌(Bacillus subtilis)、铜绿假单胞菌(Pseudomonas aeruginosa)、结核分枝杆菌(Mycobacterium tuberculosis)和氧化亚铁硫杆菌(cidithiobacillus ferrooxidans)。
只有在缺氧条件下才能生长的细菌,如梭状芽孢杆菌、类杆菌和产甲烷的古细菌(产甲烷菌)被称为专性厌氧菌,因为它们产生能量的代谢过程与氧气的消耗相无关。事实上,氧气的存在实际上会毒害它们的一些关键酶。有些细菌(肺炎链球菌)是微需氧或耐氧厌氧菌,因为它们在低浓度的氧气中生长得更好。在这些细菌中,氧气通常会刺激微小的代谢过程,从而增强能量产生的主要途径。兼性厌氧菌可以根据氧气的存在改变其代谢过程,在氧气存在时使用更有效的呼吸过程,在缺氧时使用效率较低的发酵过程。兼性厌氧菌包括大肠杆菌和金黄色葡萄球菌。
破伤风梭状芽胞杆菌
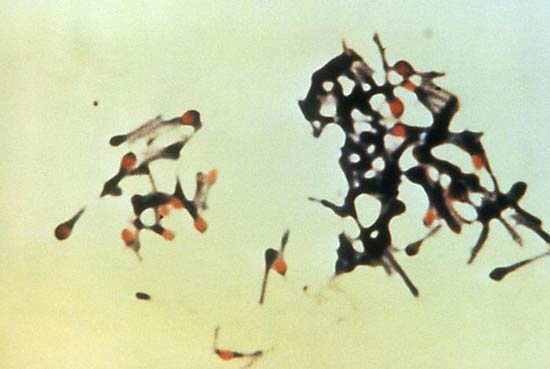
图源:Centers for Disease Control and Prevention
细菌对氧的反应不仅仅取决于它们的代谢需要。氧是一种非常活泼的分子,会形成一些有毒的副产物,如超氧物(O2-)、过氧化氢(H2O2)和羟基自由基(OH·)。有氧生物产生的酶可以使这些氧气产物解毒。
最常见的排毒酶是分解过氧化氢的过氧化氢酶和分解超氧化物的超氧化物歧化酶。 厌氧细菌通常不产生过氧化氢酶,其超氧化物歧化酶的水平随细胞对氧气的敏感性而成比例地变化。 许多厌氧菌对氧气过敏,短时间接触就会被杀死,而其他厌氧菌,包括大多数梭状芽孢杆菌,对氧的存在更具耐受性。这些酶的联合作用,以消除过氧化氢和超氧物是重要的,因为这些副产品与铁一起形成极为活跃的羟基自由基,这是能够杀死细胞。
温度
细菌已适应多种温度。 在低于约15°C(59°F)的温度下生长的细菌是嗜冷菌。细菌在低温下生长的能力并不意外,因为温带土壤的平均地下温度约为12°C(54°F),90%的海洋温度为5°C(41°F)或更低。专性嗜冷菌是从北极和南极海水和沉积物中分离出来的,其最适生长温度约为10℃(50℉),如果暴露在20℃(68℉)下,则无法存活。
大多数嗜冷细菌属于革兰氏阴性菌属假单胞菌属、黄杆菌属、无色杆菌属和产碱菌属。中温细菌是指在20至45°C(68至113°F)之间发生最佳生长的细菌,尽管它们通常可以在10至50°C(50至122°F)的温度下存活和生长。动物病原体一般是嗜中性的。
嗜热原核生物可以在高于60°C(140°F)的温度下生长。这些温度在腐烂的堆肥堆、温泉和海洋地热喷口中都会遇到。在温泉的径流中,在温度下降到70℃左右的源头附近发现了嗜热菌,如水热菌(生长的最适温度为70℃[158℉];最高温度为79℃[174℉])。
蓝藻合成球藻和光营养滑动细菌氯曲菌的厚席在径流较冷的部分发育。古生酸硫菌对酸性条件有很高的耐受性,允许在pH值约为1.0至6.0的范围内生长,最适温度为80°C(176°F)。许多细菌和古细菌适应于50至70°C(122至158°F)的温度范围,包括芽孢杆菌属、热放线菌属、甲烷杆菌属、甲基球菌属和硫菌属的一些成员。
最引人注目的是上世纪80年代中期在深海海底营养丰富、温度极高的热液喷口中发现了细菌和古细菌。焦菌属的古细菌在80到110°C(176到230°F)的温度范围内繁衍生息,在这种温度下,水只有在极高的压力下才能保持液态。
pH值
大多数细菌在中性pH值范围内(5-8之间)生长,尽管有些物种已经适应了酸性或碱性极端条件下的生活。 嗜酸细菌的一个例子是氧化铁曲霉。 当煤层通过采矿作业暴露于空气中时,黄铁矿硫化物沉积物会受到A.ferrooxidans的攻击而生成硫酸,从而将pH值降低至2.0甚至0.7。 但是,铁氧化农杆菌的耐酸性仅适用于硫酸,因为这些细菌在暴露于等浓度的其他酸(例如盐酸)时会死亡。许多细菌不能耐受酸性环境,特别是在厌氧条件下,结果,植物聚合物在酸性沼泽(pH值在3.7和5.5之间),松树林和湖泊中会缓慢降解。 与嗜酸菌相反,嗜碱菌能够在高达10至11的pH值的碱性浓度下生长。嗜碱菌已从土壤中分离出来,大多数是革兰氏阳性芽孢杆菌属。
盐和水
水是生命的基本需求。有些细菌喜欢咸的环境,因此被称为嗜盐菌。极端嗜盐菌,如嗜盐杆菌,在含盐量为20%至30%的条件下表现出最佳生长,如果盐含量降低,它们会溶解(破裂)。这种细菌存在于死海、盐水池中,有时也存在于咸鱼和兽皮上。中度嗜盐细菌在含盐量为5%至20%的条件下生长,在盐卤和泥浆中也有发现。
死海中的盐柱

图片来源:Peter Carmichael/ASPECT
细菌代谢
异养代谢
如上所述,异养(或有机营养)细菌需要有机分子来提供它们的碳和能量。产生能量的分解代谢反应可以有许多不同的类型,尽管它们都涉及电子转移反应,其中电子从一个分子到另一个分子的运动与产生ATP的能量捕获反应相耦合。一些异养细菌可以代谢糖或复杂的碳水化合物来产生能量。这些细菌必须产生许多特定的蛋白质,包括将多糖降解为其组成糖单位的酶,在细胞内积累糖的运输系统,以及将糖转化为代谢中间产物之一的酶,如葡萄糖-6-磷酸。糖酵解的Embden-Meyerhof途径和磷酸戊糖途径都存在于真核细胞中。有些细菌拥有Entner-Doudoroff途径,主要将葡萄糖转化为丙酮酸,还有一些途径可以用较少的酶催化步骤将葡萄糖转化为较小的化合物。
糖代谢通过发酵和呼吸两个不同的过程为细胞产生能量。发酵是在没有任何外部电子受体的情况下进行的厌氧过程。有机化合物,如糖或氨基酸,被分解成更小的有机分子,这些分子接受在能量源分解过程中释放的电子。
这些分解代谢反应包括几个步骤,直接形成ATP。当葡萄糖被分解成乳酸时,就像某些乳球菌和乳酸杆菌以及高等真核生物的肌肉细胞中发生的那样,每个葡萄糖分子只产生两个ATP分子,相当数量的葡萄糖必须被降解以提供足够的能量供细菌生长。由于有机分子在发酵过程中仅被部分氧化,发酵细菌的生长会产生大量的有机终产物,而消耗的每个葡萄糖分子的能量输出相对较小。
很少有细菌只产生乳酸,乳酸对细菌毒性很大,限制了菌落的生长。特定细菌利用多种额外的发酵途径分解葡萄糖;这些途径的特征性终产物有助于细菌的鉴定。这些最终产物通常比乳酸毒性小,或者是利用额外的代谢能量形成的。例如,大肠杆菌混合酸发酵的产物包括乳酸、琥珀酸、乙酸、甲酸、乙醇、二氧化碳和氢气。产气肠杆菌能产生大部分相同的发酵产物,以及大量的2,3-丁二醇,它是非酸性的,允许更多的细菌生长。
细胞可以从呼吸中获得相当多的能量,在这个过程中,糖分子的电子不是转移到另一个有机分子,而是转移到一个无机分子上。最常见的呼吸过程(有氧呼吸)使用氧气作为最终的电子受体。糖被完全分解成二氧化碳和水,每分子葡萄糖最多产生38个ATP分子。
电子通过电子传递链转移到氧中,电子传递链是位于细胞膜上的酶和辅助因子系统,其排列方式使电子沿着链的传递与质子(氢离子)穿过膜并离开细胞的运动相耦合。电子传输引起带正电荷的氢离子向细胞外移动,带负电荷的离子向细胞内移动。这种离子梯度导致外部介质的酸化和带电的质膜,其电荷为150至200毫伏。离子梯度的产生,包括质子动力(质子梯度),是所有生物能量产生和储存的一个共同方面。
质子的梯度被细胞直接用于许多过程,包括营养物质的主动运输和鞭毛的旋转。质子还可以通过一种被称为F1F0质子转位ATP酶的膜酶从细胞外部进入细胞质,该酶将质子运动与ATP合成结合,其过程与真核细胞线粒体中发生的过程相同。
能够利用呼吸作用的细菌每一个糖分子产生的能量比发酵细胞多得多,因为能量源的完全氧化(分解)可以完全提取所有可用的能量,如呼吸生物的ATP产量比发酵细菌的ATP产量大得多所示。呼吸有机体利用一定量的营养物质获得更高的细胞物质产量;它们也产生更少的有毒最终产品。然而,氧在水中的溶解度是有限的,需氧菌群的生长和存活与可用的氧供应量成正比。只有与空气接触的细菌才能获得连续的氧气供应,当细菌能够漂浮在暴露在空气中的表面上时,或者当细菌所在的介质被剧烈搅拌时,就会发生这种情况。
在厌氧条件下,呼吸也可以通过称为厌氧呼吸的过程发生,其中最终的电子受体是无机分子,如硝酸盐(NO3-)、亚硝酸盐(NO2-)、硫酸盐(SO42-)或二氧化碳(CO2)。在硫酸盐和二氧化碳的情况下,使用这些受体的细胞可获得的能量产量比氧气的呼吸低得多,但它们仍然比发酵可获得的能量产量高得多。一些细菌利用无机分子进行无氧呼吸的能力可能具有环境意义。大肠杆菌可以使用氧气,硝酸盐或亚硝酸盐作为电子受体,斯图氏假单胞菌在反硝化,硝酸盐转化为亚硝酸盐和氮气(N2)方面具有重要的全球意义。脱硫弧菌和脱硫单胞菌分别还原硫酸盐和元素硫,产生硫化物(S2-),而木醋杆菌和产甲烷古细菌,如嗜热甲烷杆菌,将二氧化碳还原为乙酸盐和甲烷。古细菌通常使用氢作为电子供体,使用二氧化碳作为电子受体以产生甲烷,或者使用硫酸盐作为电子受体以产生硫化物。
自养代谢
自养细菌以二氧化碳为碳源合成所有的细胞成分。从二氧化碳合成有机化合物的最常见途径是还原性戊糖磷酸(Calvin)循环,还原性三羧酸循环和乙酰辅酶A途径。 由美国生物化学家梅尔文·卡尔文(Melvin Calvin)阐明的卡尔文循环是这些途径中分布最广泛的途径,在植物,藻类,光合细菌和大多数需氧自养细菌中起作用。
卡尔文循环的关键步骤是核酮糖1,5-二磷酸与二氧化碳的反应,产生两个分子的3-磷酸甘油酯,葡萄糖的前体。这种循环在能量方面对细胞来说是极其昂贵的,因此一个甘油醛-3-磷酸分子的合成需要消耗九个ATP分子和六个电子供体分子的氧化,即烟酰胺腺嘌呤二核苷酸磷酸(NADPH)的还原形式。自养行为取决于细胞进行光合作用或有氧呼吸代谢的能力,这是唯一能够提供足够能量来维持碳固定的过程。
卡尔文循环
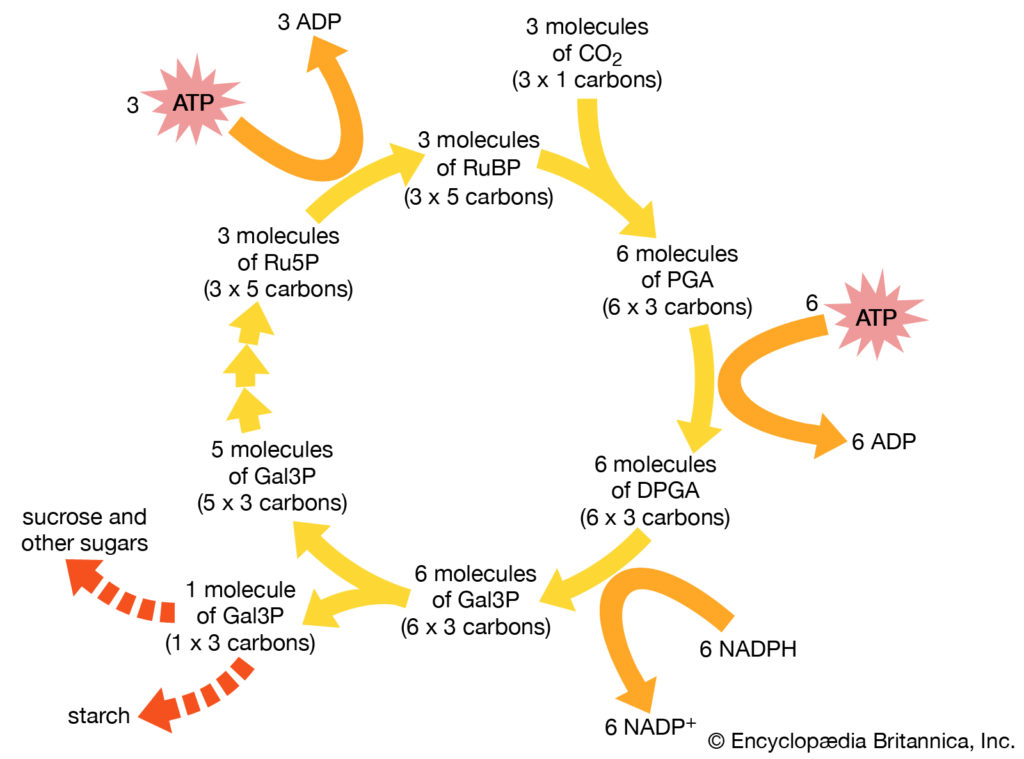
细菌使用加尔文循环来合成有机化合物。核糖1,5-二磷酸(RuBP)与二氧化碳的反应导致生成3-磷酸甘油酸酯(PGA)分子,该分子通过多次中间反应转化为一分子3-磷酸甘油醛(Gal3P)。然后可以将3-磷酸甘油醛转化为其他分子,包括糖或淀粉。
需氧非光合自养菌是指不仅以二氧化碳为唯一碳源,而且以氧为电子受体的无机化合物(电子供体)为能源的细菌。这些细菌在分类上是多样的,通常由它们使用的电子供体来定义。例如,欧洲亚硝基单胞菌将氨(NH4+)氧化为亚硝酸盐,而Nitrobacter winogradskyi将亚硝酸盐氧化为硝酸盐。 硫杆菌将硫代硫酸盐和元素硫氧化为硫酸盐,而氧化铁曲霉将亚铁离子氧化为三价铁。
这种不同的氧化能力使氧化亚铁杆菌能够耐受高浓度的许多不同离子,包括铁、铜、钴、镍和锌。所有这些类型的细菌似乎都是专性的岩性滋养菌,不能在很大程度上利用有机化合物。一氧化碳(CO)被寡糖carboxidovorans氧化成二氧化碳,而氢气(H2)被真核产碱杆菌(Alcaligenes eutrophus)氧化,在较小程度上也能被其他许多细菌氧化。
代谢能是由这些电子供体的氧化提供的,其方式基本上与呼吸异养生物相同,异养生物将电子从有机分子转移到氧气中。当电子沿着电子传递链传递到氧时,质子在细胞膜上产生梯度。这个梯度被用来产生ATP分子。岩石自养生物中存在的其他反应是用于从无机供体中去除电子和固定二氧化碳的反应。
光营养代谢
地球上的生命依靠光合作用将太阳能转化为细胞能量。光合作用的一般过程是利用叶绿素来吸收来自太阳的光能,并释放出一个能量更高的电子。这种电子通过电子传递链,通过形成质子梯度和伴随的ATP合成产生能量。电子最终返回叶绿素。这种循环反应路径可以满足电池的能量需求。
然而,为了使细胞生长,二氧化碳固定的卡尔文循环必须被激活,电子必须转移到辅助因子NADP以形成NADPH,这是循环运行所需要的大量的NADPH。因此,光营养细胞的生长需要一个电子源来取代生物合成反应中消耗的电子。
光合生物根据这些电子来源的性质分为两大类。其中一类包括高等植物、真核藻类和蓝藻(蓝绿藻);这些生物含有色素叶绿素a,在产生氧气的反应中以水为电子源。
据认为,到18亿年前,蓝藻的前身已经在全球产生了足够的氧气,开始允许更高形式的生命的发展。析氧光合作用需要两个独立的光吸收系统的作用,将水中电子的能量提高到足以转移到NADP的水平。因此,在这些生物体中存在两个不同的光反应中心,一个用于产氧反应,另一个用于能量产生的循环过程。
在蓝藻中,两个光反应中心都含有叶绿素a。它们的光合器官还含有其他光吸收色素,这些色素作为触角来捕获光能并将其转移到反应中心。蓝藻触角包括额外的叶绿素a分子和藻胆体,叶绿素a分子将能量转移到循环反应中心,藻胆体是一种蛋白质色素,它们吸收短、高能波长的光,并将能量传递到析氧反应中心。在几乎所有的蓝藻中,光合器都包含在一个广泛的细胞内扁平膜囊系统中,称为类囊体,其外表面布满规则排列的藻胆体颗粒。这种色素聚集体存在于类囊体表面的排列称为光系统。
其他光合细菌只含有一种不同色素的单一反应中心,称为细菌叶绿素,它能吸收长而低能波长的光。这些生物需要除水以外的电子供体,并且不释放氧气。绿色细菌(绿藻科)和紫色硫细菌(藻科)使用元素硫、硫化物、硫代硫酸盐或氢气作为电子供体,而紫色非硫细菌使用氢或有机基质中的电子。这些细菌需要厌氧条件才能进行光合作用。绿色细菌的光系统与高等植物的光系统Ⅰ有关,而紫色细菌的光系统Ⅱ则与光系统Ⅱ有关,后者提供了从细菌到植物的进化轨迹。
细菌的生物合成途径
许多原核生物能够将任何给定的碳源转化为生物合成的组成部分,例如氨基酸、嘌呤、嘧啶、脂类、糖和酶辅因子。在这些生物合成途径中,每种酶的数量和活性都受到严格的调节,因此细胞在任何时候只产生所需的任何化合物。
在进化过程中,一些细菌失去了编码某些生物合成反应的基因,因此可能需要营养补充。例如,支原体的DNA含量约为大肠杆菌的四分之一,它有许多营养需求,甚至丧失了形成细胞壁的能力。
支原体
图源:Centers for Disease Control and Prevention
革兰氏阴性人型支原体和在琼脂培养基上生长的常见机会性T株支原体的分离株。
细菌是肉眼看不到的单细胞微生物,是地球上最古老的生物之一,它们无处不在且数量惊人,难以逃避。由于我们看不到它们并且对它们的了解相对较少,因此细菌的世界对我们来说是神秘的,并且通常不为大众所重视。
人类每天使用细菌。细菌可用于保存食物,为农作物增添养分,制作奶酪和酸奶以及消除固体废物。这些用途有益于人类的日常生活。一些细菌在生物研究以及药物和疫苗的开发中非常有用。有的细菌帮助管理化粪池系统和清理漏油,或制作酸奶,奶酪和葡萄酒。人体中的细菌可以使身体受益,这取决于它们是细菌的类型。一些细菌有助于训练免疫系统,并有助于预防过敏。其他的则可以保护人体免受有害的致病细菌的侵害。细菌负责帮助我们消化食物,有些细菌会产生对人体非常有用的酶,激素和维生素。
细菌还会导致人患病或死亡。当人打喷嚏或咳嗽时,传染病(例如普通感冒和流感)可能会从细菌中传播。粪便中的细菌也会使人生病。如果一个人上完洗手间后没有正确洗手,他们可能会感染大肠杆菌和自己。这些特性使人类需要花更大精力来研究和重视细菌。
客观全面认识细菌,是我们正确管理和利用它们的第一步。
附录:
常见革兰氏阳性菌属:
Corynebacterium 棒杆菌属 , Propionibacterium 丙酸杆菌属, Alloiococcus 差异球菌属, Oscillospira 颤螺菌属, Enterococcus 肠球菌属, Dialister 戴阿利斯特杆菌属, Anaerostipes 丁酸弧菌属, Butyrivibrio 丁酸弧菌属, Mobiluncus 动弯杆菌属, Planomicrobium 动性杆菌属, Brevibacillus 短芽孢杆菌属, Actinomycetales 放线菌目, Actinomyces 放线菌属, Mycobacterium 分枝杆菌属, Finegoldia 芬戈尔德菌属, Faecalibacterium 粪杆菌属, Coprococcus 粪球菌属, Coprobacillus 粪芽孢菌属, Gordonia 戈登氏菌, Holdemania 霍尔德曼氏菌属, Rhodococcus 红球菌属, Arthrobacter 节杆菌属, Blautia 经黏液真杆菌属, Rubrobacter 红色杆菌属, Cetobacterium 鲸杆菌属, Catonella 卡托氏菌属, Lachnobacterium 毛螺旋菌属, Collinsella 柯林斯氏菌属, Nocardioides 类诺卡氏菌属, Paenibacillus 类芽孢杆菌属, Streptococcus 链球菌属, Ruminococcus 瘤胃球菌属, Roseburia 罗氏菌属, Rothia 罗氏菌属, Vagococcus 漫游球菌属, Lachnospira 毛螺菌属, Moryella 毛螺旋菌属, Oribacterium 毛螺旋菌属, Leuconostoc 明串珠菌属, Ureaplasma 尿枝原体属, Dermabacter 皮杆菌属, Staphylococcus 葡萄球菌属, Aerococcus 气球菌属, Carnobacterium 肉杆菌属, Lactobacillus 乳杆菌属, Lactococcus 乳球菌属, Slackia 史雷克氏菌属, Bifidobacterium 双歧杆菌属, Fusobacterium 梭杆菌属, Parvimonas 微单胞菌属, Weissella 魏斯氏菌属, Peptostreptococcus 消化链球菌属, Peptococcus 消化球菌属, Sporosarcina 芽孢八叠球菌属, Bacillus 芽孢杆菌属, Anaerococcus 厌氧球菌属, Alicyclobacillus 脂环酸杆菌属, Dactylosporangium 指孢囊菌属
常见革兰氏阴性菌属:
Escherichia 埃希氏菌属, Eikenella 艾肯氏菌属, Acidaminococcus 氨基酸球菌属, Hymenobacter 薄层菌属, Phenylobacterium 苯基杆菌属, Burkholderia 伯克霍尔德氏菌属, Acinetobacter 不动杆菌属, Filifactor 产丝菌属, Asticcacaulis 不粘柄菌属, Ochrobactrum 苍白杆菌属, Oxalobacter 草酸杆菌属, Flavobacterium 产黄菌属, Enterobacter 肠杆菌属, Comamonas 丛毛单胞菌属, Acetobacter 醋杆菌属, Brevundimonas 短波单胞菌属, Capnocytophaga 二氧化碳嗜纤维菌属, Delftia 代尔夫特菌属, Paracoccus 副球菌属, Arcobacter 弓形菌属, Devosia 德沃斯氏菌属, Mesorhizobium 根瘤菌属, Citrobacter 枸橼酸杆菌属, Azospirillum 固氮螺菌属, Stenotrophomonas 寡养单胞菌属, Marinobacter 海杆菌属, Rhodobacter 红细菌属, Rhodoplanes 红游动菌属, Porphyromonas 红棕色单胞菌属, Vibrio 弧菌属, Methylobacterium 甲基杆菌属, Pseudomonas 假单胞菌属, Succiniclasticum 解琥珀酸菌属, Chryseobacterium 金黄杆菌属, Kingella 金氏菌属, Megasphaera 巨球形菌属, Megamonas 巨单胞菌属, Klebsiella 克雷伯氏菌属, Lautropia 口动菌属, Aggregatibacter 凝聚杆菌属, Bradyrhizobium 慢生根瘤菌属, Agrobacterium 农杆菌属, Sphingomonas 鞘氨醇单胞菌属, Rikenella 理研菌属, Myroides 类香味菌属, Helicobacter 螺杆菌属, Chloronema 绿丝菌属, Erwinia 欧文氏菌属, Bilophila 嗜胆菌属, Treponema 密螺旋体属, Moraxella 莫拉氏菌属, Neisseria 奈瑟氏菌属, Sphingobacterium 鞘氨醇杆菌属, Bacteroides 拟杆菌属, Prevotella 普雷沃氏菌属, Sporocytophaga 生孢噬纤维菌属, Psychrobacter 嗜冷杆菌属, Hyphomicrobium 生丝微菌属, Prosthecobacter 突柄杆菌属, Cytophagales 嗜细胞菌目, Pectinatus 梳状菌属, Lysobacter 溶杆菌属, Sutterella 萨特氏菌属, Serratia 赛氏杆菌属, Cupriavidus 贪铜菌属, Leptotrichia 纤毛菌属, Haemophilus 嗜血杆菌属, Cytophaga 噬纤维菌属, Leptolyngbya 瘦鞘丝藻属, Campylobacter 弯曲杆菌属, Desulfobulbus 脱硫叶菌属, Enhydrobacter 水栖菌属, Pedomicrobium 土微菌属, Desulfovibrio 脱硫弧菌属, Veillonella 韦荣菌属, Shewanella 希瓦氏菌属, Gemmatimonas 牙单胞菌属, Selenomonas 月形单胞菌属, Phormidium 席蓝细菌属, Nitrospira 硝化螺菌属, Cardiobacterium 心杆菌属, Anaerovibrio 厌氧弧菌属, Halomonas 盐单胞菌属, Anaerobiospirillum 厌氧螺菌, Bdellovibrio 蛭弧菌属
以上信息整理来自谷禾健康,若需转载,请备注出处。
相关阅读:
主要参考资料:
Robert J. Kadner, Kara Rogers, Yamini Chauhan Swati, Yamini Chauhan, Swati Chopra, Aakanksha Gaur, Parul Jain, Robert Lewis, Gloria Lotha, Deepti Mahajan, Richard Pallardy, Chelsey Parrott-Sheffer, Marco Sampaolo, Veenu Setia, Shiveta Singh, Grace Young. Science Biology Archaea & Bacteria Bacteria. (1999-2020)
GEORGE M. GARRITY et al. (eds.), Bergey’s Manual of Systematic Bacteriology, 5 vol., 2nd ed. (2001–12)
MICHAEL T. MADIGAN et al., Brock Biology of Microorganisms, 14th ed. (2015)
JOANNE M. WILLEY, LINDA M. SHERWOOD, and CHRISTOPHER J. WOOLVERTON, Prescott’s Microbiology, 10th ed. (2015)
LUCY SHAPIRO and RICHARD LOSICK (eds.), Cell Biology of Bacteria (2011)
THOMAS D. BROCK, The Emergence of Bacterial Genetics (1990)
LARRY SNYDER et al., Molecular Genetics of Bacteria, 4th ed. (2013)
CLIVE EDWARDS (ed.), Microbiology of Extreme Environments (1990)
CHARLES GERDAY and NICOLAS GLANSDORFF (eds.), Physiology and Biochemistry of Extremophiles (2007)

谷禾健康


看过往期文章的小伙伴都知道,人体微生物群维持体内的共生关系,促进新陈代谢功能,抵御病原体,训练和发展免疫系统,直接或间接影响我们的大部分生理功能。
每个人都拥有属于自己的独特的微生物组,人与人之间这种显著的个体差异性是疾病易感性差异的潜在来源。
基因是从出生开始确定了,很大程度上伴随着人的一生,微生物组是否也是遗传决定的呢?
2018年的研究显示,家庭中的遗传血统或单个多态性变体在肠道微生物组组成中的作用很小(<2%),而微生物组多样性中超过20%的变异可以从共享的环境因素中推断出来,例如与饮食和生活方式。可见环境是影响微生物组的重要因素。
那么:
影响微生物组环境因素包括哪些?
环境如何对人类微生物组产生影响?
环境如何通过微生物组影响人的健康?
环境对人类微生物组的影响研究会有哪些挑战?
这对理解非传染性疾病的微生物基础带来哪些启示?
本文我们来详细阐述以上问题。
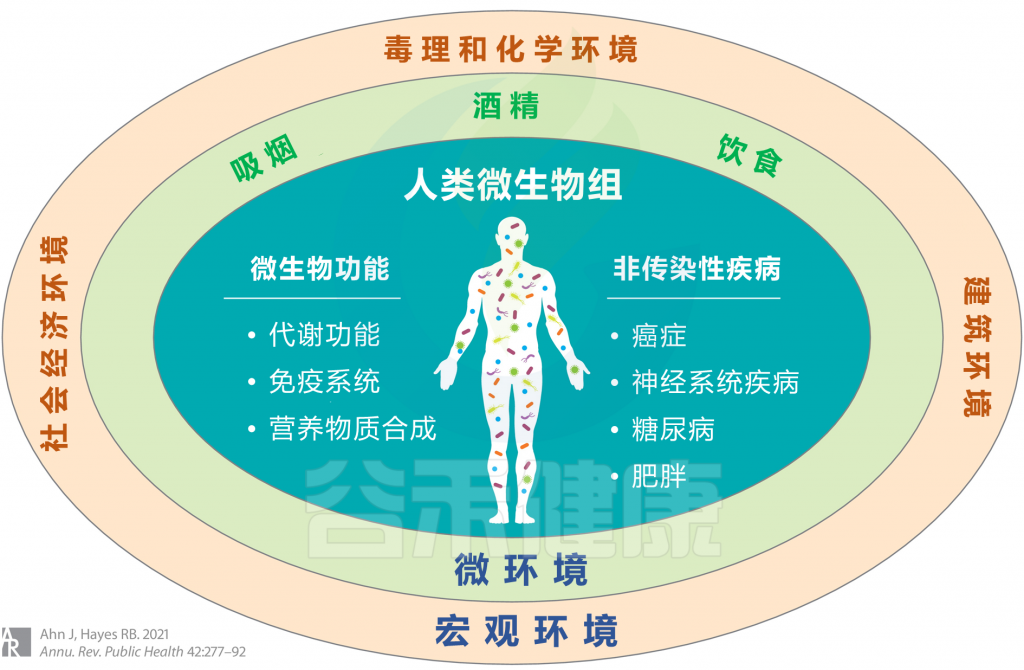
<从广义上考虑环境,涉及宏观环境和微环境,并考虑个人行为,包括吸烟,饮酒和饮食摄入等>

口腔消化道癌症
微生物诱发了至少60%的人类口腔消化道癌症,这表明控制微生物相关过程在预防和治疗口腔消化道癌症方面具有巨大的潜力。
流行病学研究一致报告口腔疾病与口腔消化道癌症(包括头颈部、食道癌、胃癌和胰腺癌)风险之间的联系。由于口腔疾病具有重要的微生物基础,这些观察导致了口腔微生物组与口消化癌的发生有关的假设。
基于大量人群的队列研究中的病例对照研究发现,用漱口水样本评估的诊断前口腔微生物组与随后发生的头颈部、食道和胰腺消化道癌症的相关。一些研究也明确指出了肠道微生物组梭菌属Fusobacterium和其他菌群与结肠癌之间的联系,以及肠道微生物组与炎症性肠病和结直肠腺瘤之间的联系。
微生物来源的信号通过不同的机制调节癌症的许多特征。一般来说,细菌不能直接诱发癌症;这一过程通常伴随着慢性炎症,并需要致癌信号通路的独立突变。
进一步的研究表明,微生物组与宿主之间的交互作用通过调节肿瘤微环境中的先天和适应性免疫功能,对口腔消化道肿瘤发生至关重要。
细菌-癌症模型提出,革兰氏阴性细菌促进致癌作用,因为脂多糖细菌外膜通过Toll样模式识别受体为先天免疫系统反应提供免疫原性刺激,导致由核转录因子NF-κB原瘤细胞因子释放、免疫细胞募集和活性氧释放引起的基因突变。
因此,微生物在形成肿瘤免疫微环境中的作用在癌症的发病机制中具有重要的潜在意义,特别是在口腔消化道。
神经系统疾病
肠道和中枢神经系统通过肠-脑轴相互作用,调节中枢神经系统功能,包括情感行为、认知表现、疲劳和睡眠。
研究表明,肠道微生物组通过影响肠-脑轴,可能在某些神经精神和神经发育障碍中发挥作用,改变行为,并可能影响神经系统障碍的发作和/或严重程度。
无菌小鼠和用抗生素治疗的小鼠表现出大量的神经免疫功能障碍和行为缺陷。主要在临床前模型中,肠道微生物组与大脑障碍有关,包括焦虑、抑郁、癫痫以及自闭症谱系障碍。
在人类中,胃肠道病理和神经精神疾病之间相互作用的证据已经在焦虑、抑郁和自闭症等情况中报告;然而,因果关系仍未得到证实。
揭示微生物组介导肠-脑连接的机制可能为靶向治疗肠道提供新的机会,以预防和治疗神经疾病。
糖尿病
大量的文献已经为肠道菌群在糖尿病前期和2型糖尿病病因学中的作用提供了证据。一份2020年的综述总结了40多项已发表的人类研究。
例如,在糖尿病前期研究中发现,基于肠道微生物群、炎症和免疫标志物的分子特征预测了2型糖尿病的发病。
两项开创性研究发现,2型糖尿病患者和非糖尿病对照组的肠道微生物组不同。
随后一项研究表明,2型糖尿病患者的肠道微生物群介导了用于控制糖尿病的二甲双胍的治疗效果。

还有研究人员开发了个性化饮食以优化2型糖尿病患者的血糖水平,同时考虑了个性化饮食习惯、体育活动和肠道微生物群。研究人员随后在一项盲法随机对照饮食干预试验中表明,应用这种算法可以改善餐后血糖反应。
目前面临的挑战是搞清楚,具体精确到哪些肠道微生物组组成部分,能驱动异质性、多因素、多器官疾病。
肥 胖
肥胖在全球范围内日益流行,导致过早死亡和许多慢性非传染性疾病。虽然肥胖的根本原因是能量摄入和输出之间的不平衡,但肠道微生物组成是导致体重增加的公认因素,当然还有其他机制,如遗传变异和表观遗传调节。


从野生型小鼠、肥胖小鼠或肥胖人类转移到无菌小鼠的肠道菌群实验表明,在该试验系统中,肠道菌群在体重增加和肥胖中起着关键作用,与肥胖表型的建立有关。这些实验结果引出了这样一个问题:
肠道的微生物组成是否会影响人类体重增加(无论是基因决定的还是饮食诱导的)?
一份早期的小规模人类样本报告与小鼠的研究结果一致,即肥胖状态与厚壁菌门(Firmicutes)的相对丰度增加和拟杆菌门(Bacteroidetes)的相对丰度减少有关。
然而,对人类的研究并没有证实这一特定模式:一些研究发现拟杆菌门(Bacteroidetes)的减少(但没有发现厚壁菌门(Firmicutes)的增加)与肥胖有关,而另一些研究则发现相反或未发现这两种门水平与体重指数(BMI)有关。
此外,研究已经确定了与BMI或肥胖相关的不同属和种水平的分类群。
点击此处查看 体重增长:目前为止我们所知道的一切
未来在动物模型和人类中的下游实验可以确定这些候选菌群是否在肥胖的病因学中起作用,如果是,建议干预肥胖的预防和治疗。
目前也有通过各种治疗方法(如益生菌、益生元、抗生素)改变菌群的潜力,微生物组是预防和治疗肥胖的一个不错的方式。


宏观环境
——毒理和化学环境
在人体中,消化道和呼吸系统是环境毒物进入和加工的主要途径。在这些器官系统中,人类微生物组丰富的代谢系统具有强大的转化外来生物化学物质的能力,有时与宿主的生物转化模式相反。
宿主代谢酶的典型特征是氧化和结合排泄,而微生物的酶反应主要是还原、水解和去甲基化,生成碳源进一步生长和分裂。
环境砷形态与心血管疾病和其他健康影响有关;证据表明,口腔消化道微生物组的甲基化能力可能会影响这些毒性。
肠道乳酸菌Lactobacillus对金属(如镉和铅)的固定化可能会影响金属毒性,降低重金属积累。
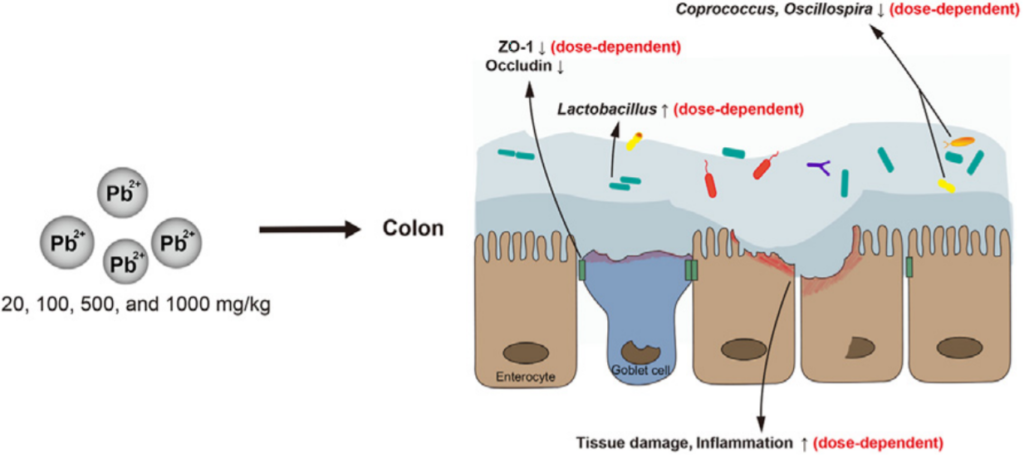
Yu.Let al., chemosphere2020
某些肠道细菌表达偶氮还原酶来代谢潜在致突变的偶氮化合物。个人护理产品中对环境具有持久性的化学物质,如三氯卡班(TCC)和三氯生(TCS)普遍存在,并与啮齿类动物微生物群的潜在变化有关。
肠道微生物群对化学物质(包括内分泌干扰物)的代谢会伴随微生物的失调:改变微生物群落结构,诱导特定细菌基因,改变微生物分子转化。此外,内分泌干扰物可以被吸收并运输到肝脏,然后被结合并通过胆汁分泌排泄回肠道,进一步进行微生物代谢。
酶如偶氮还原酶、酯酶、甲基酶、硫代还原酶、脂肪酶、硝基还原酶、β-葡萄糖醛酸苷酶、硫酸盐酶和β-裂解酶也参与环境化学物质的微生物代谢。
——建筑环境与新兴假说
建筑环境包括人类建造的所有建筑,包括家、工作场所、学校、车辆等。研究人员认识到许多微生物病原体可能存在于建筑环境中。
例如,细菌病原体,如结核分枝杆菌;真菌病原体,如烟曲霉菌Aspergillus fumigatus;致病性病毒,如鼻病毒和流感病毒,以及SARS-CoV-2冠状病毒等,均可通过在建筑环境中直接吸入传播。其他病原体,如艰难梭菌和粪肠球菌,以及诺如病毒和流感病毒,可通过皮肤或黏液接触传播给人,原因是病菌从表面传播。
除了直接的微生物传播,建筑环境中的微生物代谢产物也可能涉及人类健康,包括细菌和真菌毒素、细胞壁的致敏成分和微生物衍生的挥发性有机化合物。
室内空气和表面与灰尘和微生物化学产物有关。环境中相对湿度的增加导致灰尘和表面微生物代谢物的增加。室内潮湿和发霉条件(例如,可见的霉菌和霉菌气味)与许多不同的疾病状态有关,但建筑环境中微生物及其代谢产物的组成和浓度与疾病之间的联系仍然难以捉摸。

通过靶向细菌16S rRNA测序和宏基因组测序的应用,研究人员对建筑环境微生物生态的复杂性有了更全面的认识,包括可培养和非培养因子的多样性。认识到环境样品中微生物DNA序列的组成可能是由大量的不可活残留物组成的,环境微生物相关DNA表现出丰富的复杂性,反映了人类微生物来源,室内建造环境和人类来源的微生物来源之间的关系特别强。
卫生假说认为,卫生条件的改善可能与自身免疫性疾病的增多有关,这一概念也适用于有益菌暴露的概念。
研究人员研究了人类微生物组和建筑环境微生物组之间的相关关系,重点关注家庭环境,并绘制居住者和他们的家庭之间的细菌共享。这项调查表明,与表面有关的大多数细菌有很大的可能来自该住宅的居住者。暴露于室内灰尘中的复杂微生物群与患哮喘的可能性呈负相关。在另一项研究中,与没有接触到农业环境的儿童相比,接触到农场附近家庭灰尘并在农场积极参与工作的儿童患哮喘的风险有统计学上显著降低。

总之,越来越多的证据表明,建筑环境、微生物群和健康之间存在相互关系,但要了解建筑环境中微生物的生态和进化与人类健康之间的关系,还需要做大量的工作。
其他与建筑环境有关的著名假说也出现了。其中一个在文献中越来越流行的假说是野化假说,该假说认为,改变城市绿地使其恢复到更自然的状态,有可能改变环境中的微生物群,进而改变人类微生物群。对人和动物的研究表明,野化可能会影响微生物组和宿主的免疫反应。
除其他环境因素外,2018年的研究表明,吸入颗粒物空气污染会改变肠道微生物组的组成。
此外,日光暴露可以调节家庭灰尘细菌群落,这也可能表明阳光和紫外线辐射影响人体微生物群落组成,例如皮肤上的细菌群落。
微生物在皮肤老化中的作用模式
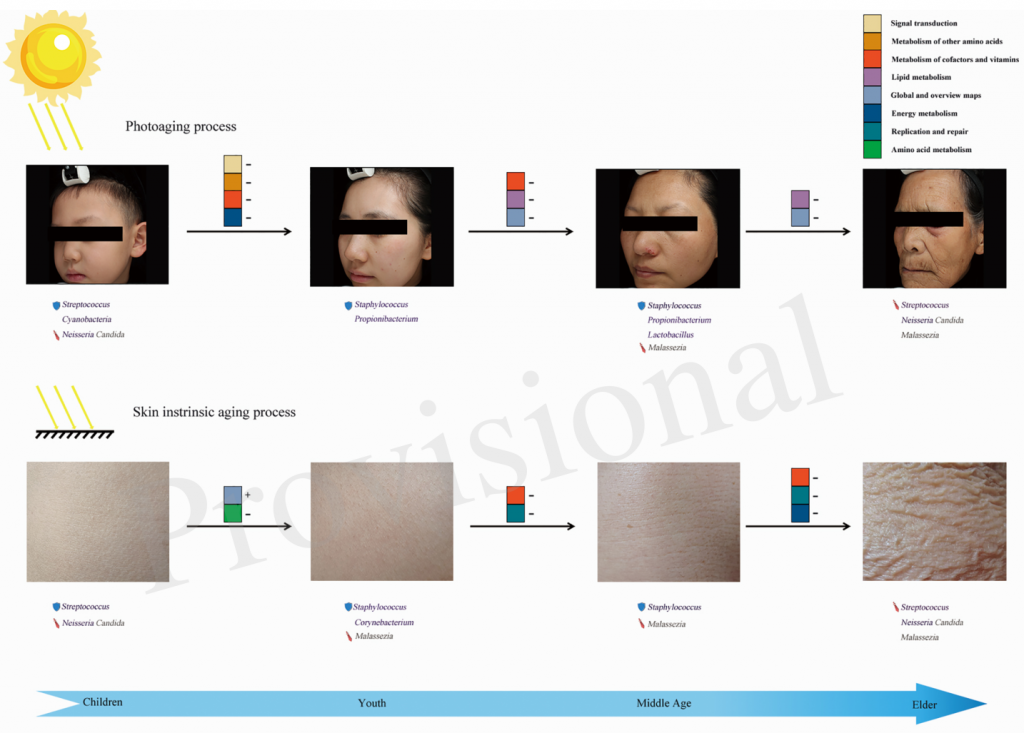

Li Zichao,et al., Front Microbiol, 2020
气候变化和极端高温也可能引发生理变化,可能有利于周围环境、食物或体内的某些微生物群。
此外,在应对将大量微生物菌群与无数已建立和新出现的暴露物结合起来的挑战时,将细菌宏基因组与环境暴露物结合起来的无针对性评估和发现可能是前瞻性研究议程的一部分。
——社会经济环境
较低的社会经济地位与多种与健康有关的行为有关,如获得医疗和牙科护理的机会减少,增加参与不健康行为(如吸烟和酒精依赖),减少对积极健康行为(如健康饮食和锻炼)的参与。低社会经济地位与较高的发病率和死亡率以及其他一些健康状况如肥胖、糖尿病和癌症的高发病率相关。
微生物群在调节社会经济地位和健康之间关系中的作用正在研究中。许多与低社会经济地位社区和生活方式相关的特征(例如,加工食品、久坐的生活方式、社会心理压力、暴露于污染物和内分泌干扰物)也与肠道微生物多样性减少有关。


研究已经检验了高社会经济地位和低社会经济地位群体之间微生物组成的差异。在美国,较高的社会经济地位与肠道微生物群中特定微生物的α多样性和种群丰度相关。
更好地理解微生物组在社会经济地位相关疾病易感性中的中介关系需要综合研究,包括调查社区和个人水平的暴露。建筑环境是考虑的一个部分。
微环境
——吸烟
香烟烟雾是大量有毒物质的来源,直接接触口腔和上呼吸道的细菌;这些毒物可以通过抗生素作用、缺氧或其他潜在机制扰乱微生物生态。由于吸烟而失去有益的口腔菌群可导致病原体定植并最终导致疾病;吸烟在微生物依赖性牙周炎的发病和发展过程中所起的既定作用有力地支持了这一论点。

实验室调查发现,与从不吸烟的人(变形菌门11.7%)相比,吸烟人群口腔微生物组的总体多样性降低,变形菌门的相对丰度降低(4.6%) (FDR q = 5.2×10−7)。
当前吸烟者体内三羧酸(TCA)循环和氧化磷酸化等微生物有氧代谢途径相关基因的丰度降低,糖酵解等非氧碳水化合物代谢途径的丰度增加。
当前吸烟者所消耗的其他途径包括与甲苯、一硝基甲苯、苯乙烯、氯环己烷和氯苯降解有关的某些外来生物降解途径以及细胞色素P450的外来生物代谢。相反,多环芳烃(PAH)和二甲苯降解在当前吸烟者中富集。这些化学物质是香烟烟雾的组成部分,因此口腔菌群降解这些物质的能力的改变可能会对宿主产生毒性后果。
除了创造一个厌氧、酸性和/或选择性有毒的环境,吸烟还被认为对人体免疫有显著的影响,这反过来可以影响宿主阻止病原体殖民的能力。
总之,越来越多的证据表明:
吸烟影响口腔微生物群的整体组成和许多种群丰度;吸烟可促进厌氧口腔环境和具有减少的异种生物降解能力的菌群。
观察性和介入性研究也提示吸烟者肠道微生物组的多样性降低,总的来说,变形菌门、拟杆菌门和梭菌属、拟杆菌属、普雷沃氏菌属呈上升趋势,放线菌门、厚壁菌门和双歧杆菌属、乳球菌属呈下降趋势。
可能解释吸烟对肠道微生物组影响的机制包括氧化应激增强、肠道紧密连接和肠道粘蛋白组成的改变以及酸碱平衡的改变。一些吸烟引起的肠道微生物组改变类似于炎症性肠病和肥胖等情况下的改变。应该进行进一步的研究来研究这种联系。吸烟会影响肠道微生物群,建议改变其组成。吸烟和肠道微生物组之间的相互作用可能有助于肠道和全身疾病的发展。
——酒精
酒精摄入可能通过几种方式影响人体口腔微生物群:
首先,口腔细菌和真菌将酒精和膳食糖代谢成致癌的乙醛,与香烟烟雾冷凝液相互作用,产生致癌的亚硝胺,并在实验上促进口腔癌变。无论是在体内还是体外,在吸烟者中,口腔微生物群有更强大的能力从乙醇中产生乙醛。
体外和动物实验也指出了口腔微生物群参与口腔癌变的可能机制,包括抑制细胞凋亡,激活细胞增殖,促进细胞侵袭,诱导慢性炎症,以及口腔多菌群中细菌和真菌的合作。
第二,酒精可能对细菌产生直接的细胞毒性作用。动物研究表明,摄入20%的酒精会增加变形链球菌Streptococcus mutans的定植,并显著减少大鼠口腔生物膜中可检测到的细菌种类。

在人类研究,饮用红酒与物种丰度降低以及龈下和龈上菌斑中某些厌氧菌的减少有关,而过量同时使用烟草和酒精与物种丰富度降低以及口腔粘膜生物膜中奈瑟菌Neisseria、Aggregatibacter和梭杆菌Fusobacteria丰度降低有关。
酒精除了直接作用外,还可能通过干扰宿主防御系统间接影响口腔微生物群,从而导致宿主介导的牙周炎。
大量以人群为基础的研究表明,每天至少喝一杯标准饮料会增加牙周炎15-27%的风险,并与糟糕的口腔健康有关。有证据表明,口腔微生物群与口腔健康状况密切相关。
酒精和肠道微生物组的研究主要是在大量饮酒的背景下进行的,酒精可能改变肠道屏障功能,导致肠道渗漏,产生促炎病原微生物产物,并扰乱肝脏代谢途径。
大量饮酒和肝硬化患者的研究表明,拟杆菌门细菌的相对丰度随着变形菌门的增加而降低,肝硬化患者中梭杆菌门的独特增加。
大量饮酒与肠道失调有关,而红酒作为膳食多酚的丰富来源,如果适量饮用,可能有利于改变胃肠道微生物群的组成。红酒多酚能显著增加变形菌门(Proteobacteria)、梭杆菌门(Fusobacteria)、厚壁菌门(Firmicutes)和拟杆菌门(Bacteroidetes)的丰度,而杜松子酒则能显著减少这些细菌门。
——饮食
西方饮食的特点是高脂肪,高糖,大量食用红肉和加工肉类,大量食用精制谷物,而纤维摄入量较低。
许多研究表明,西方饮食与炎症、糖尿病、心血管疾病、肥胖、代谢综合征和癌症有关。而西方饮食有着广泛的生理影响,影响许多不同的细胞类型,如脂肪细胞,免疫细胞和内分泌细胞。
这个饮食习惯也与肠道菌群的变化密切相关,其特征是微生物多样性和物种丰富度降低,厚壁菌门增加,拟杆菌门减少。在属水平上,西方饮食显示双歧杆菌和乳酸菌减少,而肠杆菌增加。
纤维摄入量,是一个诱人的可改变的饮食因素,因为其假定有益的生物效应。一些研究表明,纤维可以预防2型糖尿病、心血管疾病、结肠癌和肥胖等疾病。纤维加速结肠运输,并可能减少结肠上皮细胞暴露于摄入的致癌物质。


此外,纤维经过微生物群发酵,产生短链脂肪酸如丁酸,对结肠能量代谢和上皮细胞增殖至关重要,在小鼠模型中,通过抑制组蛋白去乙酰化酶,显示出肿瘤抑制活性。因此,人们越来越关注膳食纤维对肠道微生物组成的影响,这可能最终影响一个人患癌症和其他疾病的风险。
高纤维饮食与更高的胃肠道微生物丰富度和多样性有关,特别是与普氏菌Prevotella和密螺旋体Treponema的丰富度有关,还与炎症信号的减少有关,对肥胖的保护,以及可能减少结肠直肠癌的存在。尽管短期饮食干预试验已经证明,不同数量的纤维摄入量可以在几周内显著改变肠道微生物群的组成,但很少有研究在人类中评估长期摄入纤维的饮食习惯对肠道微生物群的影响。
点此查看 你吃的膳食纤维对你有帮助吗
人类微生物组、健康、环境科学的这三个要素每一个都是复杂的,整合具有挑战。环境因素往往是复杂的;要考虑的环境因素众多,更不用说对微生物组的不断深入了解,难以全面把握外部环境如何在疾病发生率和死亡率中起因果作用。在现实生活中,这些因素通常相互影响,随着时间的推移是动态变化的。
化学毒物经常在混合物中出现,例如,与化妆品和内分泌干扰物的混合物。此外,在整个生命过程中暴露的风险可能随年龄而变化,即易感性窗口。由于这种复杂性,确定直接或间接影响人类健康和疾病的微生物特征仍然具有极大的挑战性。
需要新的方法来充分评价可能影响微生物组和人类健康的现有和尚未确定的因素。前瞻性队列研究是环境和人类健康研究的支柱,特别是因为这项研究设计在建立因果关系的自然时间序列方面很重要,而这在横断面或回顾性研究中往往很难理清。
对粪便样本和人体其他部位样本进行前瞻性收集,以及连续的纵向样本收集也只是在最近才达到一定规模。需要以大量人群为基础的队列,包括不同社会经济地位和地理群体等。

此外,环境和微生物组对健康状况的多维影响,加强了整合其他组学的需要,包括代谢组学、转录组学、基因组学和免疫组学。需要开发相关的数据集成工具和流程。
结语
以上强调了环境中通过影响人类微生物群与非传染性疾病相关的许多因素。必须考虑复杂的相互作用、上游因果因素和多种因果路径。以大数据驱动的技术正为微生物组研究和临床运用带来许多便捷。
随着深入研究,不久的将来我们会对环境,微生物组,健康三者之间的关系有进一步认识,结合公共政策领域,有效地从多方面去实现健康的改善。
相关阅读:
主要参考文献:
Li Zichao,Bai Xiaozhi,Peng Tingwei et al. New Insights Into the Skin Microbial Communities and Skin Aging [J]. Front Microbiol, 2020, 11: 565-549.
Ahn Jiyoung,Hayes Richard B,Environmental Influences on the Human Microbiome and Implications for Noncommunicable Disease [J] .Annu Rev Public Health, 2021, 42: 277-292.
Yu L, Yu Y, Yin R, Duan H, Qu D, Tian F, Narbad A, Chen W, Zhai Q. Dose-dependent effects of lead induced gut injuries: An in vitro and in vivo study. Chemosphere. 2021 Mar, 266: 129-130.
Hayes RB, Ahn J, Fan X, Peters BA, Ma Y, et al. 2018. Association of oral microbiome with risk for incident head and neck squamous cell cancer. JAMA Oncol. 4:358–65
Sampson TR, Mazmanian SK. 2015. Control of brain development, function, and behavior by the microbiome. Cell Host Microbe 17:565–76
Daisley BA, Monachese M, Trinder M, Bisanz JE, Chmiel JA, et al. 2019. Immobilization of cadmium and lead by Lactobacillus rhamnosus GR-1 mitigates apical-to-basolateral heavy metal translocation in a Caco-2 model of the intestinal epithelium. Gut Microbes 10:321–33
Gilbert JA, Stephens B. 2018. Microbiology of the built environment. Nat. Rev. Microbiol. 16:661–70
Rook GAW, Raison CL, Lowry CA. 2014. Microbial ‘old friends’, immunoregulation and socioeconomic status. Clin. Exp. Immunol. 177:1–12

谷禾健康

肠道的内部环境作为外部环境和宿主之间的接口,不断受到宿主的消费习惯的挑战。在管腔一侧,微生物能够附着并定植于该空间,而在宿主一侧,胃肠道充当体内免疫细胞的最大隔室。
从解剖学上讲,肠道由不同的部分组成。十二指肠,空肠和回肠代表小肠(SI),它比由结肠和直肠组成的大肠(LI)占据更多的物理空间。与人类相比,啮齿动物的盲肠增大,盲肠囊是连接小肠和大肠的盲端囊。在小鼠中,盲肠充当了共生微生物的大贮藏库,这些微生物参与了无法通过其他方式裂解的纤维的发酵。 盲肠在小鼠中的作用很重要,因为它是短链脂肪酸(SCFA)产生的主要途径,去除盲肠会导致胃肠道远端部位炎症的增加 。在人类中,该部位微生物的体积远小于小鼠,但该隔室在兼性厌氧发酵中仍起着重要作用。
值得注意的是,共生微生物的组成和丰度在不同的胃肠道区域是不同的,例如,成年小肠中的微生物丰度低(<105个微生物/ mL),在结肠中则增加到1012。小肠和大肠具有独特的生理功能。 虽然十二指肠和空肠参与消化,营养吸收和运动过程,但大肠具有三个主要功能:吸收水和电解质,产生和吸收维生素以及形成和运输排泄的粪便。肠道不断暴露在食物颗粒和食物抗原,生理或机会性微生物群衍生的代谢产物以及其他免疫调节刺激。 胃肠道内的免疫细胞不仅对肠道内的抗原刺激作出反应,而且还显示出扩散到全身的远端器官,表明它们在全系统炎症稳态中的重要性。
微生物无处不在。 他们自我组织,在原本无法居住的生态环境中创建了复杂的生态系统,迅速适应了他们的环境。宿主依赖微生物组实现几种基本的共生功能,例如启动免疫系统和生产必需的维生素,以及从食物中获取能量。 肠道微生物群(定义为人类体内的微生物分类群)现在被认为是内分泌器官,可产生可在宿主中充当效应子的代谢产物,从而触发局部微环境或远端的靶器官系统(如心脏,肾脏,脉管系统)的反应和大脑。
肠腔内壁衬里是抵抗细菌感染的生理屏障,可以与毒素结合。此外,粘液是细菌的营养来源,因此会影响具有在粘液层中生存和扩展能力的微生物的定殖。Akkermansia muciniphila(AKK菌) 和Citrobacter rodentium (柠檬酸杆菌)能够降解粘蛋白,而后者在纤维缺乏期间会增殖。结肠粘液层完整性的丧失会增加宿主对病原体的敏感性。 在健康条件下,紧密的上皮层可防止病原微生物的入侵,而某些刺激物(如炎症性疾病或西餐)可导致肠道通透性和所谓的肠道渗漏综合征的发展。
随着高通量测序技术和代谢组学的建立以及高性能计算和人工智能的发展,人们逐渐破译生活方式,饮食,药物治疗和肠道微生物组之间的相互关系。每个人肠道微生物组随时间推移相对稳定,并与周围环境平衡共存。但是诸如抗生素,肠道感染以及饮食或生活方式变化等扰动都会引起短暂或持续的变化。
在过去的几十年中,实验和临床研究表明,先天性和适应性免疫系统的细胞在高血压,靶器官损害和心血管疾病(CVD)的发病机理中起着关键作用。促炎性效应记忆T细胞和 T辅助细胞亚型T辅助细胞17(Th17;产生IL-17)和1型辅助细胞(产生IFN-γ)促进高血压和心血管靶器官损伤,而调节性T细胞(Tregs)通常产生大量的抗炎性IL-10可以减轻血管,心脏和肾脏的损害。
此外,γδT细胞和髓样来源的抑制细胞在高血压的发病机理中也起着重要作用。 已经证明可以改变几种T细胞亚型激活状态的树突状细胞会增加盐反应性高血压,并提示其在菌群失调与血压(BP)之间的相互作用中发挥作用。
细菌可以直接或通过其产生的代谢产物与参与心血管的不同免疫细胞发生反应。例如,分段丝状细菌或Bifidobacterium adolescentis(青春双歧杆菌)可诱导Th17细胞,而Lactobacillus murinus(鼠乳杆菌)及其色氨酸代谢产物吲哚3乳酸则可抑制Th17细胞。 和SCFA丁酸盐是结肠中Treg的杰出诱导剂。
图 肠道微生物与宿主免疫相互作用

在宿主和微生物组方面均可发现肠道空间变异性。内腔和组织相关内容的相对水平在此处进行了说明,表明这两种功能的区域专业化。 已知肠道中的内腔含量在微生物负荷,微生物种群以及所产生的微生物产生的代谢产物方面有显着差异。尽管在整个胃肠道中的种群和区域规格都受到微生物的影响, 根据管腔内物质含量的变化,宿主免疫系统同样具有区域特异性。
这里显示的是免疫细胞,这些细胞在免疫稳态过程中表现出空间动态。
高血压的发病机制涉及多种因素,包括遗传、环境、激素、血液动力学和炎症等。越来越多的证据表明,肠道微生物群在高血压的发生和发病机制中起着重要作用。胃肠道是人体内最大的免疫细胞库,代表着环境和宿主的交汇点。因此,生活方式因素的形成和调节的微生物组,影响着高血压疾病形成和发生的风险。一个被广泛研究的例子是膳食纤维的消耗,能导致短链脂肪酸的产生,并有助于抗炎免疫细胞的扩张,从而防止高血压的进展。饮食干预如禁食也被证明通过微生物群影响高血压。
图 血压与肠道菌群的关系
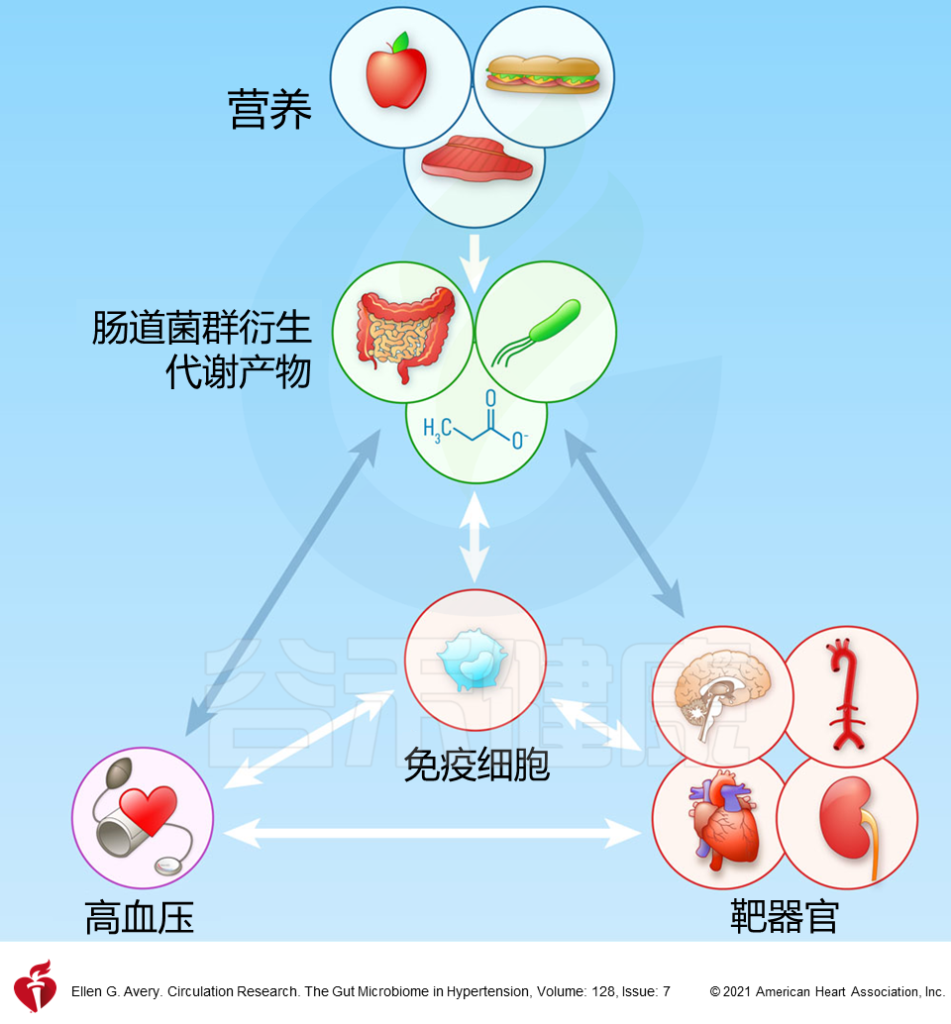
摄入的食物被肠道微生物群转化为小的代谢物。食物抗原、微生物产生的代谢物以及微生物本身都有助于免疫稳态。干扰宿主和微生物群之间的共生关系可通过免疫系统直接或间接导致血压变化和相关的心脏、血管或肾脏损害。
在过去的十年中,许多关于肠道微生物组和高血压的作用的证据已积累起来。多项针对人体的横断面研究表明,肠道微生物组与血压或高血压之间存在关联。高血压患者或血压较高的患者,α多样性降低,肥胖,高胰岛素血症和血脂异常也已观察到。 许多人类肠道微生物组研究报告了革兰氏阴性菌群较高的菌群之间的相关性,包括克雷伯菌,副细菌,脱硫弧菌和普氏菌,尽管并非所有研究都能确定这种模式。
来自HELIUS队列研究(城市环境中的健康生活)的研究表明,克雷伯菌属和链球菌属与血压呈正相关。此外,与高血压小鼠相比,从高血压人类供体接受粪菌移植的GF小鼠出现了与其供体相似的肠道菌群,以及8周后收缩压和舒张压升高。它从2个血压正常的供体那里接受了粪菌移植。
此外,还有几种有价值的啮齿动物高血压模型分析了肠道微生物组和血压的作用。自发性高血压大鼠存在失调,与正常血压WKY(Wistar-Kyoto)对照大鼠的微生物群存在显著差异。自发性高血压大鼠的肠道通透性和菌群失调也可能可通过使用降压药治疗大鼠来补救。
肠道微生物组与高血压之间的联系不是物种特异性的。 例如,在小鼠和人类中高盐处理都会减少乳酸杆菌属。 值得注意的是,未治疗的高血压患者中盐的适度降低能够降低血压并改善动脉顺应性。改善的临床结果伴随着8种循环SCFA的增加(包括2-甲基丁酸、丁酸、己酸、异戊酸和戊酸 )。此外,已证明益生菌乳酸菌处理可通过恢复吲哚3乳酸水平(抑制微生物色氨酸代谢)抑制Th17细胞并减轻盐敏感性高血压。
已显示,Lactobacillus coryniformis可以改善血管功能和胰岛素敏感性。Lactobacillus(乳杆菌)治疗不仅可以改善心血管疾病,还可以改善实验性自身免疫性疾病的结局。 对益生菌对高血压的作用进行调查的随机对照试验的系统评价表明,如果以足够高的剂量使用至少8周,含乳酸杆菌的益生菌是有效的。
在人类中,肠道中的核心微生物群落是稳定的,并且仅在响应诸如肠道感染,整体旅行或药物治疗等主要扰动时才发生变化,从而导致肠道微生物组发生短暂或持续的变化。 肠道菌群不仅对某些饮食刺激的比例具有反应性,而且还可能在时空环境中做出反应。
目前,我们对特定饮食变化影响炎症,自身免疫和心血管疾病易感性的确切机制的理解还很模糊。 使用经过微生物组组成和功能训练的机器学习算法可提供令人兴奋的机会,以促进更好地预测对营养刺激的反应。
新兴的研究表明,饮食因素(高盐或高纤维)和生活方式干预(盐分限制或热量限制)会影响微生物群落的结构和功能,这对免疫细胞活化和血压具有重要意义。西方人的生活方式通常涉及每天进食几顿主餐,并导致细菌多样性下降,某些食物喂养细菌的过度生长,以及随之而来的其他食物为底物的细菌的抑制。因此,菌群产生的代谢产物发生了转移,从而促进了炎症,最终可能导致肥胖症和动脉粥样硬化等疾病的发展。
从历史上看,餐食通常是新鲜烹制的,但如今,人们更经常食用通常含盐量更高的加工食品。这种生活方式通常会导致较高的盐摄入量 而不是医学指南或专家的建议。为减少心脏代谢疾病的风险,通常应节食健康的饮食和运动。 大多数建议的重点是将富含饱和脂肪,糖,盐和卡路里但纤维含量低的西方饮食改变为更健康的地中海式阻止高血压饮食方法,以实现最佳营养,平衡和降低盐摄入量,尽管合规性是一个重大挑战。
SCFA是最典型的微生物群代谢产物之一,它是在不易消化的纤维发酵过程中产生的。 乙酸,丙酸和丁酸是3种高丰度的SCFA。 膳食纤维是由≥3种单体组成的膳食碳水化合物的统称,如非淀粉多糖,抗性淀粉,菊粉,果胶,β-葡聚糖和低聚糖。 这些纤维状化合物中的大多数都被拟杆菌、厚壁菌和放线菌门微生物消化。Bifidobacterium adolescentis, Eubacterium rectale, Eubacterium hallii, Faecalibacterium prausnitzii ,Ruminococcus bromii 通常在大肠中定居,并具有消化纤维以生产SCFA的酶。
大肠的丙酸和丁酸水平比小肠高约4倍。SCFA在结肠中迅速吸收,而丁酸在很大程度上被用作向结肠上皮细胞提供能量的燃料。肠道SCFAs与门静脉血相比要高得多,而门静脉SCFAs较高,其次是肝脏血液,外周血最少,这表明SCFAs基本上被肝脏吸收。肝中丙酸的摄取是糖异生,脂肪生成的前体,以及蛋白质合成,而乙酸盐进入循环系统并被多个组织代谢,并且是胆固醇合成的底物。
SCFA可以与G蛋白偶联受体Gpr41(G蛋白偶联受体41),Gpr43( 小鼠中的G蛋白偶联受体43),Gpr109a(G蛋白偶联受体109 A),Olfr558(嗅觉受体558)和Olfr78(嗅觉受体78),也称为FFARs(游离脂肪酸受体)。FFARs存在于各种组织中,包括血管和肾脏,并参与调节丙酸、乙酸和丁酸的血管反应性。
Gpr41和Olfr78似乎都参与了血压的调节,尽管它们似乎促进了相反的作用。Olfr78激活后会诱导肾素分泌。与此相符的是,Gpr41敲除小鼠为高血压,有趣的是,醋酸盐以前曾用于血液透析缓冲液,但由于其降压作用而被大量废弃,这与SCFA在大多数情况下降低血压的观点一致。
纤维本身已被建议在一定程度上塑造微生物组成。
关于血压,纤维的刺激作用增加了SCFA生产者Faecalibacterium prausnitzii和Eubacterium rectale以及乳杆菌属的丰度。一项具有里程碑意义的研究表明,与传统上纤维含量高的未加工饮食的非洲儿童相比,食用西方饮食的欧洲儿童SCFA水平显着降低,Firmicutes与Bacteroidetes(F/B)比率高。自该研究以来,高F/B比率通常被用作肠道生态失调的替代指标,虽然也已知一些Firmicutes细菌产生有助于健康微生物组的微生物代谢物。
同样,实验工作通常依赖于F/B比作为疾病标志物。自发性高血压大鼠和易中风的自发性高血压大鼠显示F/B比率增加,这支持了这可以作为肠道生态失调的标志物的概念。
各种实验或临床研究已证明益生元高级纤维或后生SCFA治疗对血压的影响。研究报道丙酸在麻醉小鼠中诱导了急性的剂量依赖性降血压反应,这是由Gpr41介导的。益生元纤维不仅可以预防心血管疾病,而且这些营养素的缺乏可能是导致高血压和心血管疾病的危险因素。 还发现在低纤维饮食中添加益生元乙酸盐,丙酸盐或丁酸盐可改善血压并减少靶器官损害。
此外,GF小鼠的粪菌移植表明,与抗性淀粉相比,饮食中的肠道微生物组缺乏抗性淀粉。高纤维情况不仅在血管紧张素II攻击后导致较高的血压,而且还导致了心脏和肾脏损害的发病机制。
德国一项研究测试了在有和没有动脉粥样硬化的高血压小鼠中口服丙酸治疗的特性。在这两种模型中,丙酸治疗均能降低全身和局部炎症反应,血压以及心脏损害。丙酸的治疗作用是由Treg细胞介导的。但是该研究指出丙酸的降血压作用不是急性的,而是随着时间的推移而发生,提示SCFA的抗炎特性间接促进了血管表型的改善。Th17细胞和Th17与Treg的平衡介导SCFA在血压调节中的作用。
关于SCFA在血压中的作用的人类研究非常少见。对微生物群组成和高血压的一些研究表明,SCFA的生产者为Ruminococcaceae spp,Rothia或Roseburia spp. 与较低的血压相关。
在一项小型干预试验中,生物素丁酸酯(600 mg / d),益生素菊粉(10 g / d)以及这两者的组合均降低了代谢综合征患者的舒张压。在HELIUS队列中,将机器学习算法应用于微生物组数据可确定Roseburia spp解释对血压的最大绝对影响,甚至在调整混杂因素(包括使用药物)后,丰度也使收缩压降低4.1 mmHg。
相反,血压较高的患者的粪便SCFA水平较高。这种正相关与以前的研究一致,但似乎与血压与胃肠道内微生物SCFA生产者之间的负相关性相矛盾。 但是,粪便中的SCFA含量不一定反映肠道内的SCFA含量,而是反映肠道中产生的SCFA含量而宿主无法吸收的。
自发性高血压大鼠的实验工作支持了这一观点,表明实验性高血压会减少结肠丁酸对宿主的吸收。此外,AT1(血管紧张素II型1型)受体阻滞剂坎地沙坦(一种经常用于治疗高血压的药物) 已发现自发性高血压大鼠可以增加乳杆菌的丰度和粪便SCFA水平,改善肠道完整性并降低血压。
坎地沙坦治疗改善了重度肥胖受试者肠道中丁酸生成基因的缺失。总之,在HELIUS队列中,基于肠道微生物群组成的机器学习模型分别解释了收缩压和舒张压变异性的4.4%和4.3%。
纤维来源的SCFAs不仅影响血压,而且在其他心血管疾病和自身免疫中也起着关键作用。例如,用醋酸盐,丙酸盐或丁酸盐进行生物后处理可改善急性肾损伤。肾脏保护与局部和全身炎症反应减少,氧化性细胞应激和细胞凋亡。在多发性硬化症动物模型中,T细胞介导的中枢神经系统炎症性疾病丙酸盐增加了肠道和脾脏中抗炎Tregs的频率,这伴随着临床症状的改善。
高纤维摄入量和增加的SCFA浓度也被证明可以保护中枢神经系统。值得注意的是,多发性硬化症患者可以从丙酸盐治疗中获益。短期丙酸盐治疗导致显着和持续的富集功能正常的Tregs,同时1型辅助细胞和Th17细胞同时消耗。此外,补充SCFA或高纤维摄入对类风湿性关节炎(一种关节慢性炎症性疾病)的预后有积极影响。丙酸酯可增加骨量,并且发现SCFA通过增加Treg的数量刺激骨形成。
从机制上讲,SCFA可以影响不同的免疫细胞群。 例如,发现丙酸和丁酸处理后中性粒细胞产生的炎性细胞因子较少。丁酸还可以减少氧化应激和吞噬能力。
SCFA通过减少树突状细胞成熟并抑制CD4和CD8T细胞增殖来调节炎症过程。与乙酸盐相反,丁酸盐或丙酸盐通过HDAC(组蛋白脱乙酰基酶)抑制作用影响骨髓前体细胞的树突状细胞成熟。此外,丁酸可促使M1巨噬细胞分泌更少的炎性细胞因子,增加抗炎细胞因子IL-10的分泌。
SCFAs还引起人单核细胞和T细胞中抗炎标记的表达。 例如,丁酸抑制金黄色葡萄球菌刺激的人单核细胞中IL-12的产生并增强IL-10的分泌。
最近,研究证明了丙酸会降低Th17细胞分化的速率。还发现丁酸盐还通过Gpr43增加1型辅助细胞分化细胞中IL-10的分泌,由SCFA驱动的IL-10诱导激活STAT3(信号转导子和转录激活子3)和mTOR(雷帕霉素的机械靶标),从而上调转录因子B淋巴细胞诱导的表达成熟蛋白。
此外,SCFA最深入研究的特性之一是它们在诱导抗炎Treg中的作用。丁酸和丙酸可增加鼠和人Treg的分化并增强其抑制能力。除丁酸外,丙酸(而非乙酸)通过HDAC诱导外周新生Treg细胞形成。值得注意的是,Clostridia(梭菌)是共生微生物的主要类别,它介导了诱导性结肠Tregs,这与Clostridium butyricum(酪酸梭状芽胞杆菌)诱导Tregs并减少Th17细胞从而减轻实验性自身免疫的症状的发现是一致的。
越来越多的证据表明,禁食是控制代谢性疾病和炎性疾病的有效工具。热量限制会影响微生物组的基本原理令人兴奋。 然而,仍然缺乏关于人类的可靠数据。
一项研究关于10天定期禁食对15名健康男性的粪便微生物群的影响。禁食导致Lachnospiraceae和Ruminococcaceae菌减少。一项小型的人体试验研究表明,斋月禁食影响了健康受试者的微生物组,丰富了一些SCFA生产者。
在一项临床研究中,35名代谢综合征患者接受了5天的禁食,然后进行了3周的DASH饮食,也被译为「得舒饮食」,字面意思是防止高血压的饮食方法饮食。

对照组仅接受DASH饮食。禁食后接着DASH饮食降低血压,需要抗高血压药物和干预后3个月的体重,并改变影响SCFA生产者的肠道微生物群。队列对血压反应性的分层显示,空腹组中存在的免疫细胞变化在血压反应者中比在无反应者中更明显。
此外,禁食组的免疫移位与DASH组观察到的变化根本不同。观察到干预后禁食组中血压响应者特异性微生物组的变化(F.prausnitzii,拟杆菌和厚壁菌的富集;放线菌的消耗)。值得注意的是,丁酸盐生产者F.prausnitzii的富集甚至在禁食后3个月仍然存在。血压反应者和无反应者不仅对禁食反应不同,而且在基线时的丙酸合成能力不同。
将机器学习算法应用于基线免疫组或16S微生物组数据,预测模型通过重新分析调查禁食和血压影响队列(Mesnage数据集)证实,队列中显着的长期血压下降预计准确率约为70%,进一步支持这些发现可能是普遍化的想法。重要的是要强调,上述研究建立了微生物组和血压之间的关联,以应对禁食。禁食对许多患者来说是一项艰巨的挑战。能够操纵负责响应禁食的血压变化的机制将具有高临床效用。
禁食是热量限制的一种极端形式,在不同的文化和宗教习俗中起着重要的作用。 大量的热量限制不仅影响宿主的健康和生理,还降低了血压。生活方式和饮食引起的微生物群及其代谢产物的扰动可直接影响上皮细胞和免疫细胞的稳态。但是我们对营养,微生物群和微生物产物,免疫系统与宿主健康或疾病之间的联系仍处于‘婴儿期’。
宿主-微生物组相互作用对人类健康和疾病显然有影响。模型系统经常用于基础和临床前高血压研究,以研究疾病的发病机制和进展。小鼠和大鼠模型非常有用,可以提供人类队列研究无法获得的信息。然而,在模型系统中研究人-宿主-微生物组相互作用存在许多障碍。
差 异
01 胃肠生理学和形态学有许多方面,这在人类和啮齿动物物种之间是截然不同的。盲肠可能是人类和啮齿动物不同物种形成的最明显的例子,以及小鼠结肠粘液层的薄度。
02 小鼠和人类对炎症应激物的基因组反应是明显不同的,这可能与宿主特异性或微生物组特异性特征或两者的组合有关。
03 居住在胃肠道的微生物在小鼠和人类之间通常也是不同的。人和小鼠只有约15%的细菌谱系。虽然它们在属或门的水平上可能具有可比性,但物种特异性变化通常在高血压中具有临床重要性。
04 已知在每个微生物进化枝内,成员物种之间共享功能特性的程度例如,厚壁菌作为进化枝特别代谢不一致,当考虑到普遍使用F/B比率作为生态失调的标志物时,这再次提出了一个问题。
05 由于人类微生物组随时间的相对稳定性,实验室小鼠在这方面与人类不同。
06 小鼠和人体免疫组成和建立不同,人类免疫系统的强劲发展,需要接触各种真菌,病毒,微生物等,而GF小鼠与人或大鼠微生物的定殖不会诱导免疫成熟,只有小鼠特异性微生物能够诱导完全的免疫能力。
07 啮齿动物模型的嗜食性已被认为对微生物组具有独特的影响,这可以通过使用单一住房策略来避免,尽管这会诱发小鼠的应激反应,增加一个额外的混杂因素。
许多研究人员试图通过使用人类微生物定殖小鼠或野外捕获的小鼠来规避物种比较问题。这提出了两个重要的挑战,应该加以考虑。
一,存在宿主与其微生物之间相互作用的相互排斥的问题。事实上,这种相互作用的重要性在最近的一项研究中得到了证实,该研究表明GF小鼠与人或大鼠微生物的定殖不会诱导免疫成熟,只有小鼠特异性微生物能够诱导完全的免疫能力。有几点差异在小鼠和人体免疫组成之间注意到,这可能与免疫微生物组轴有关,例如,与小鼠(10%–25%)相比,外周血中性粒细胞的比例约为人类的两倍(50%–70%)。此外,CD8+T细胞在成年人非淋巴组织中的分布远高于无特定病原体的小鼠,这可能对细胞内感染或癌症的进展有影响。
二,尽管野外捕获的小鼠比实验室培养的无特定病原体的小鼠更准确地概括人体生理,可能与临床试验结果的一致性更高,对疾病的抵抗力更强。但是在科研研究和临床上应用大规模野外捕获老鼠的可能性会受到限制。
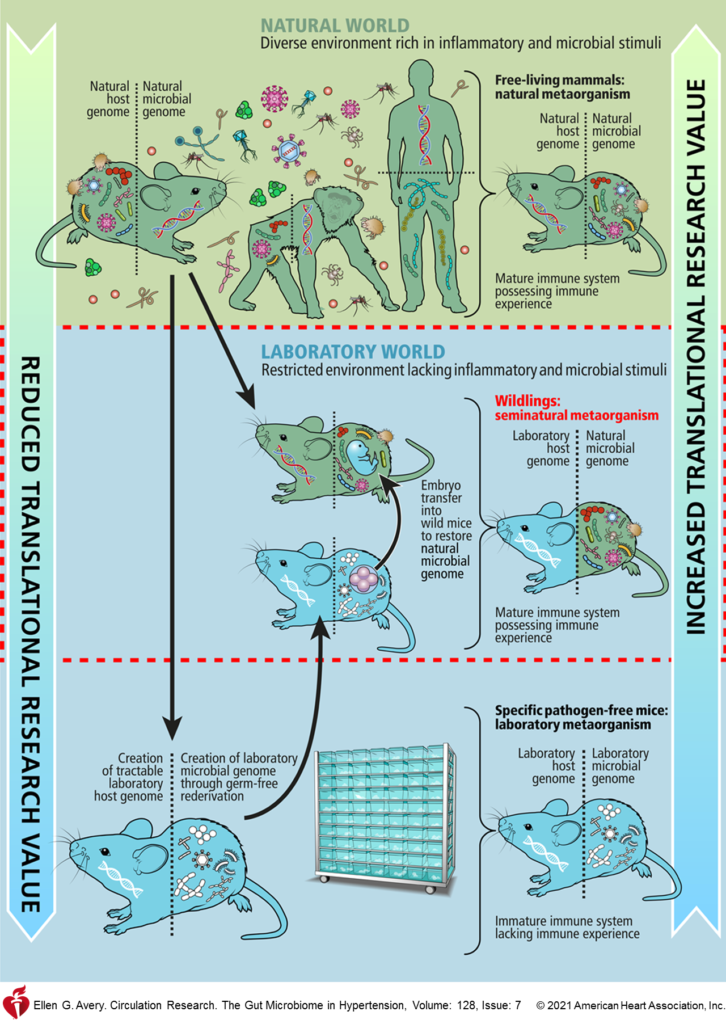
因此,在未来动物研究中,整个领域的程序标准化,例如使用同窝对照和可能影响微生物组的条件的稳健记录是必不可少的。要注意笼养,用品和饮食等因素可能会对结果产生重大影响。此外,采样时间,地点也尽量一致。
值得注意的是除了不同胃肠道区域的空间动态外,从粘膜和管腔空间取样的微生物组在小鼠和人类中是独特的。由于胃肠道是免疫细胞极化和微生物产生的代谢物吸收的作用部位,许多人质疑粪便取样是否正确研究宿主-微生物组界面的途径。粪便代表该系统的排泄产物。
然而,粪便取样是检查微生物组的最常见和实际适用的方法,特别是对于需要非侵入性方法的纵向研究。粪便的收集无疑有助于我们理解宿主-微生物组的相互作用。尽管怀疑局部产生的微生物副产物的相关性是重要的,特别是影响代谢物对循环的摄取并影响胃肠免疫细胞的活性,但是该隔室的测量是不发达的。在间质液中的作用部位鉴定微生物产生的化合物的能力可能提供对宿主-微生物组动力学的不同观点。
总之,尽管在解释微生物组数据时需要谨慎,但是,高血压中微生物组-宿主界面的研究是一个有前途且正在迅猛加速的研究领域。随着各种技术的进一步发展,针对微生物组领域的以药理学和辅助诊断方式为中心的方案可能会在不久的将来出现。
相关阅读:
参考文献:
Schluter J, Peled JU, Taylor BP, Markey KA, Smith M, Taur Y, Niehus R, Staffas A, Dai A, Fontana E, et al.. The gut microbiota is associated with immune cell dynamics in humans.Nature. 2020; 588:303–307.
Evangelou E, Warren HR, Mosen-Ansorena D, Mifsud B, Pazoki R, Gao H, Ntritsos G, Dimou N, Cabrera CP, Karaman I, et al.; Million Veteran Program. Genetic analysis of over 1 million people identifies 535 new loci associated with blood pressure traits.Nat Genet. 2018; 50:1412–1425.
Ellen G. Avery. CirculationResearch. The Gut Microbiome in Hypertension, Volume: 128, Issue: 7, Pages:934-950
Tierney BT, Yang Z, Luber JM, Beaudin M, Wibowo MC, Baek C, Mehlenbacher E, Patel CJ, Kostic AD. The landscape of genetic content in the gut and oral human microbiome.Cell Host Microbe. 2019; 26:283–295
Forslund K, Hildebrand F, Nielsen T, Falony G, Le Chatelier E, Sunagawa S, Prifti E, Vieira-Silva S, Gudmundsdottir V, Pedersen HK, et al.; MetaHIT Consortium. Disentangling type 2 diabetes and metformin treatment signatures in the human gut microbiota.Nature. 2015; 528:262–266.
Verger EO, Armstrong P, Nielsen T, Chakaroun R, Aron-Wisnewsky J, Gøbel RJ, Schütz T, Delaere F, Gausseres N, Clément K, et al.; MetaCardis Consortium. Dietary assessment in the metacardis study: development and relative validity of an online food frequency questionnaire.J Acad Nutr Diet. 2017; 117:878–888.