 国家高新企业 | ISO9001认证
国家高新企业 | ISO9001认证 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com

谷禾健康
双歧杆菌
双歧杆菌属(Bifidobacterium)是放线菌门严格厌氧的革兰氏阳性多形性杆状细菌。末端常常分叉,故名双歧杆菌。是人和动物肠道的重要核心菌群和有益生理菌群,也是母乳喂养婴儿中发现的第二大菌。
肥胖、糖尿病和过敏等各种疾病都与生命各个阶段的双歧杆菌数量减少有关。双歧杆菌有助于改善消化问题,抗菌和病毒、抗炎、改善血糖控制,降低血脂水平,提高免疫力,表现出抗氧化活性,有助于预防湿疹,缓解压力和过敏。
从代谢的角度来看,该属比较典型的特征是单糖的分解代谢(即所谓的果糖 6-磷酸途径),主要发酵葡萄糖产生乳酸和乙酸和少量乙醇。
重要的是,双歧杆菌产生硫胺素(维生素B1)、核黄素(维生素B2)、维生素 B6和维生素 K。可能还具有合成叶酸、烟酸(维生素B3)和吡哆醇(维生素B6)的能力。双歧杆菌代谢产物还包括γ-氨基丁酸 (GABA)和生物素。比如青春双歧杆菌是人体肠道微生物群中 GABA生产的关键成员。
by Kateryna Kon
食用双歧杆菌食品可以通过降低胃 pH 值(促进矿物质的电离,这是矿物质的吸收所必需的)来提高某些矿物质的生物利用度,包括钙、锌和铁。
多种因素会导致人体肠道内双歧杆菌变化
导致减少的因素包括:
增加双歧杆菌的因素包括:
补充益生菌:可以通过食物或药物的方式补充益生菌,可以增加肠道内双歧杆菌。
吃发酵食品:多吃发酵食品,如酸奶、奶酪、泡菜,适量葡萄酒等,可以增加肠道内双歧杆菌。
增加特定膳食补充剂,比如低聚果糖,抗性淀粉,白藜芦醇、镁、绿茶、水苏糖,杏仁/杏仁皮、岩藻多糖、大麦、菊芋、阿拉伯木聚糖、菊粉等
多样性饮食,摄入足够的蔬菜、水果、豆类和全谷物,定期摄入奶制品。
合理运动和良好睡眠,清洁的水源等。
存在于不同生态位的双歧杆菌物种与其宿主之间有不同的生态关系
抗生素敏感性
药敏实验显示双歧杆菌对多种抗生素敏感,如氯霉素、四环素、红霉素等,但对氨苄青霉素、庆大霉素、痢特灵、丁胺卡那霉素、新霉素、环丙沙星等抗生素耐受。
应用
目前双歧杆菌制剂已经广泛应用于保健食品、医药等领域。比如双歧杆菌药品、双歧杆菌与药成分搭配的保健药品、双歧杆菌与双歧因子搭配的保健食品以及双歧杆菌与寡糖、葡萄糖酸、精氨酸配合,对青春双歧杆菌有选择的增殖作用,发挥特有的免疫赋活功能等。
开发价值
未来还可能扩大双歧杆菌利用面,促进双歧杆菌向多元化方向发展。比如双歧杆菌富含B族维生素,该菌的代谢产物富含(L+)乳酸和一些酶类,可用来生产微生态护肤品或其他化妆品。除用于特定保健食品和医药外,在畜业、水产业和肉制品加工中也广泛应用,也大有开发价值。
通过补充益生菌或益生元调节双歧杆菌水平可以改变肠道微生物群的整体组成和代谢。但是双歧杆菌介导的健康益处是双歧杆菌、肠道微生物群的其他成员和人类宿主之间建立的复杂动态相互作用的结果。值得强调的是,某些双歧杆菌定植特征受肠道因素调节,包括其他微生物的存在。
这体现在具有不同肠道微生物群组成的个体似乎对双歧杆菌补充剂的反应不同,这一事实提供了双歧杆菌-肠道微生物群串扰存在的进一步证据。
本文主要讨论和介绍双歧杆菌的菌属特性,生态代谢特征,对人体的健康特性以及影响双歧杆菌在体内定植的主要因素。
—正文—
★
▼
双歧杆菌属于放线菌目,双歧杆菌在细胞壁类型上与其他放线菌(如链霉菌和诺卡氏菌)是分开的;双歧杆菌被指定为具有 VIII 型细胞壁(鸟氨酸浓度相对较高)。
属水平
双歧杆菌属(Bifidobacterium)于 1899 年首先由 Tissier 从母乳喂养婴儿的粪便中分离出来,并命名为Bacillus bifidus。
然而,由于它们与乳杆菌相似的形态和生理特征,在 20 世纪的大部分时间里它们被归类为乳杆菌属的成员,直到最近才被认为是和乳杆菌不同的属。
种水平
随着鉴定方案的技术改进和微生物系统学信息的扩展,该属中已定义物种的数量已经稳步增加。
Bergey 的系统细菌学手册(1986) 鉴定了 24 种不同的双歧杆菌。在这些物种中,被认为主要起源于人类的类型有以下种:
B.bifidum、B.longum、B.infantis、
B.breve、B.adolescentis、B.angulatum、B.catenulatum、B.pseudocatenulatum 、B.dentium 。
大多数这些物种在人类结肠中占主导地位,随后可以在粪便和污水中找到。
在2004共列出了 33 种双歧杆菌;大多数新添加的物种都是从动物来源中分离出来的。
截止2020年已在该菌属在分类学上已鉴定出 78 个种和 10 个亚种,而且这个数字每年都在上升。
▼
双歧杆菌是革兰氏阳性、不运动、过氧化氢酶阴性、不形成孢子和非还原细菌的多样化菌属。是厌氧菌和多形性细菌,具有单细胞、链、聚合物形、V 形或 Y 形或栅栏形等多种排列方式。
适宜生长条件
人源双歧杆菌的最适生长温度为 36 至 38 °C,而动物源双歧杆菌的最适生长温度为 41 至 43 °C。但蒙古双歧杆菌和嗜冷双歧杆菌除外,它们分别可以在 15°C 和 8°C 下生长;最高生长温度为 43–45°C,但嗜热双歧杆菌除外,其最高生长温度为 49.5°C。
双歧杆菌的最适生长 pH为 6.5–7.0。pH 值低于 4.5–5.0 或高于 8.0–8.5 时不会一般发生生长。嗜热双歧杆菌除外,它可以在 pH 4.5 下生长或 pH 8.0–8.5 下不生长。
双歧杆菌菌落与乳酸菌易混淆
在琼脂平板上,双歧杆菌的菌落与乳酸菌(尤其是乳酸杆菌)的菌落非常相似,容易混淆,经常被错误地称为乳酸菌的一员;然而,双歧杆菌与发酵食品生产中使用的传统乳酸菌都没有密切关系。
与乳酸菌相比,双歧杆菌的耐酸性较差,它们的生长不能称为“兼性厌氧”。双歧杆菌确实会通过碳水化合物的发酵产生乳酸,但通常产生的乙酸量高于乳酸,并且所使用的分解代谢途径不同于乳酸菌所采用的同源发酵和异源发酵途径。
乳杆菌的 DNA 的平均(G+C)mol%约为 37%,双歧杆菌的平均值约为 58%。
▼
它们是正常人类和动物肠道菌群的天然居民,并且已经从六个不同的生态位中分离出来,双其中三个与人类和动物肠道环境直接相关:例如人类肠道、动物肠道(牛、兔、鼠、鸡和昆虫)和口腔,而其他(污水、血液和食物)可能是胃肠道污染的结果。
从不同生态位分离出来的双歧杆菌物种表
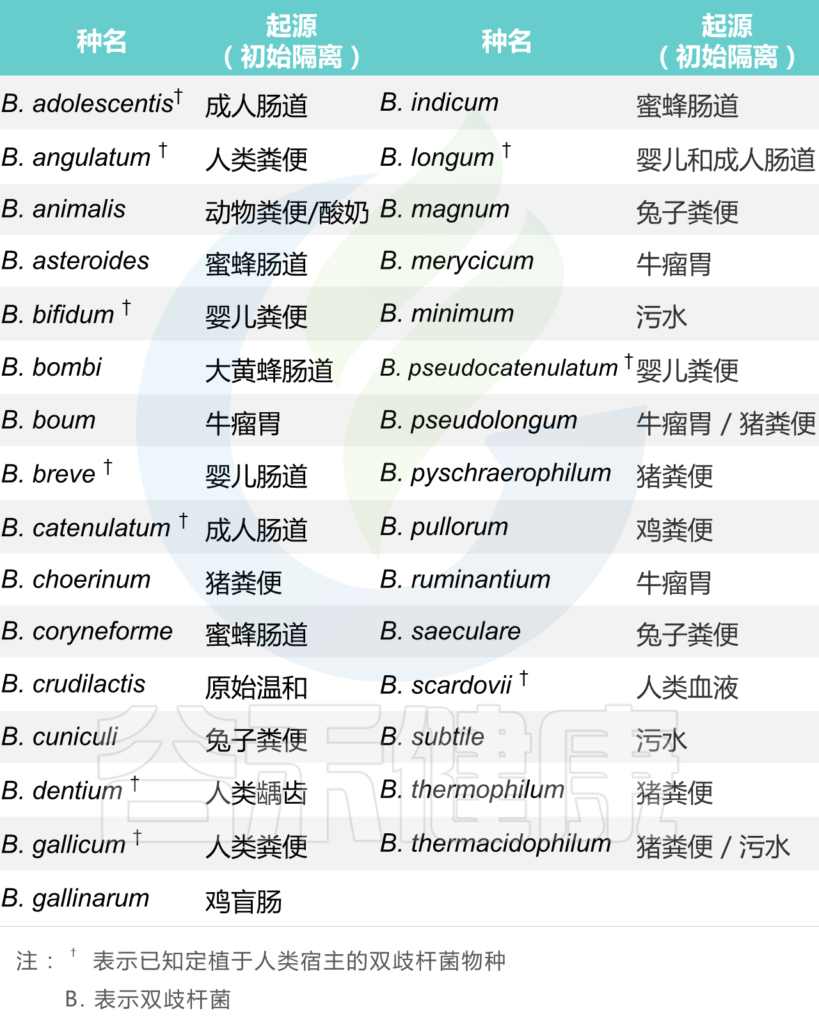
doi.org/10.2217/fon-2019-0374
▼
通常在我们的认知中,双歧杆菌是益生菌,但实际上,双歧杆菌与其宿主之间可以建立不同的生态关系,从机会性致病相互作用(例如齿双歧杆菌)到共生甚至促进健康的关系(例如双歧双歧杆菌和短双歧杆菌)。
在已知的促进健康的菌群中,双歧杆菌代表了最主要的群体之一,一些双歧杆菌物种通常被用作许多功能性食品中的益生菌成分。
动物双歧杆菌已被证明是在冷藏条件下保持活力的双歧杆菌物种中最顽强的物种之一,并且一些菌株已被证明可以为人类带来健康益处,但动物这个名称在暗示对人类有益方面并不易于使用,尤其是老鼠粪便作为原始来源。
在当前的文献中,人们越来越意识到双歧杆菌的潜在致病性。双歧杆菌的致病潜力尚不清楚;有报道称在免疫功能低下的宿主和肠道屏障受损的宿主中具有“败血症样图像”的侵袭性。
双歧杆菌的促炎作用

Lim HJ,et al., J Microbiol Biotechnol. 2020
先前的研究表明,最常见的引起双歧杆菌感染是长双歧杆菌和齿双歧杆菌。在儿科和成人菌血症病例中,无论是否使用过益生菌,公认的菌种是婴儿双歧杆菌、青春双歧杆菌、短双歧杆菌、长双歧杆菌和齿双歧杆菌(在较早的文献中称为埃里克森双歧杆菌)。
已经报道了由双歧杆菌引起的几种类型的感染。偶尔的感染发现还包括B. scardovii。
在一项研究中,从无菌场所分离出的 15 种推定的双歧杆菌分离株或大量存在的双歧杆菌被鉴定到物种水平,鉴定出四种:A. omnicolens、B. breve、B. longum、B. scardovii ,来自胃肠道或泌尿生殖道,B. breve来自血液。Scardovia wiggsiae 是一种新物种,与严重的幼儿龋齿有关。
在血培养分析中,双歧杆菌约占厌氧血培养分离株的 0.5-3%,截至 2015 年,文献中仅报道了 15 例成人双歧杆菌菌血症,因此,双歧杆菌还是相对安全的。
▼
双歧杆菌属属于放线菌门、放线菌纲(高 G+C 革兰氏阳性菌)、双歧杆菌目和双歧杆菌科。
产生B族维生素
双歧杆菌可产生硫胺素、核黄素、维生素 B6 和维生素 K。还有报道称它们具有合成叶酸、烟酸和吡哆醇的能力。这些维生素B复合物在人体中被慢慢吸收。
产生乳酸
关于含有双歧杆菌的发酵乳的营养特性的现有信息表明,与非发酵乳相比,它们的残留乳糖含量较低,游离氨基酸和维生素含量较高。它们优先含有(+)-乳酸[双歧杆菌除乙酸外还产生(+)-乳酸,而乳酸菌产生(−)-乳酸],更容易被人体代谢。这对于 1 岁以下的婴儿尤为重要,因为在这些婴儿中代谢性酸中毒可能是一个问题。
所有与人类有关的物种都可以发酵乳糖;在考虑将双歧杆菌应用于乳制品和作为益生菌培养物以缓解乳糖吸收不良不适的预期效果时,这是一个重要特征。
主要代谢途径:果糖 6-磷酸途径
双歧杆菌使用果糖 6-磷酸途径(双歧途径)作为碳水化合物代谢的主要途径,其中Xfp是该途径的主要酶,具有双底物特异性,最终代谢产物是乙酸盐、乳酸盐和乙醇。
注:Xfp——果糖 6-磷酸磷酸酮醇酶
其他代谢途径
人们认为,双歧杆菌能够与其他胃肠道细菌竞争并在胃肠道区域的细菌菌群中占据很大比例,部分原因可能是它能够利用多种分子提供能量。双歧杆菌可能还参与的其它代谢通路如下:
2-氧代羧酸代谢
ABC转运体
丙氨酸、天冬氨酸和谷氨酸代谢
氨基糖和核苷酸糖代谢
氨酰-tRNA生物合成
精氨酸和脯氨酸代谢
精氨酸生物合成
细菌分泌系统
碱基切除修复
氨基酸的生物合成
抗生素的生物合成
次级代谢物的生物合成
不饱和脂肪酸的生物合成
生物素代谢
丁酸代谢
C5-支链二元酸代谢
碳青霉烯生物合成
碳代谢
氯代烷烃和氯代烯烃降解
柠檬酸循环(TCA循环)
氰基氨基酸代谢
半胱氨酸和甲硫氨酸代谢
D-丙氨酸代谢
D-谷氨酰胺和D-谷氨酸代谢
DNA复制
芳香族化合物的降解
脂肪酸生物合成
脂肪酸降解
脂肪酸代谢
叶酸生物合成
果糖和甘露糖代谢
半乳糖代谢
谷胱甘肽代谢
甘油脂代谢
甘油磷脂代谢
甘氨酸、丝氨酸和苏氨酸代谢
糖酵解/糖异生
乙醛酸和二羧酸代谢
组氨酸代谢
同源重组
肌醇磷酸代谢
胰岛素抵抗
赖氨酸生物合成
代谢途径
甲烷代谢
不同环境中的微生物代谢
错配修复
内酰胺生物合成
萘降解
烟酸盐和烟酰胺代谢
氮代谢
非核糖体肽结构
核苷酸切除修复
一个由叶酸组成的碳库
其他聚糖降解
氧化磷酸化
泛酸和 CoA 生物合成
戊糖和葡萄糖醛酸相互转化
戊糖磷酸途径
肽聚糖生物合成
苯丙氨酸代谢
苯丙氨酸、酪氨酸和色氨酸的生物合成
磷酸转移酶系统 (PTS)
聚酮化合物糖单元生物合成
卟啉和叶绿素代谢
丙酸代谢
蛋白质输出
嘌呤代谢
嘧啶代谢
丙酮酸代谢
RNA降解
RNA聚合酶
核黄素代谢
核糖体
次级胆汁酸生物合成
硒化合物代谢
鞘脂代谢
淀粉和蔗糖代谢
链霉素生物合成
硫代谢
牛磺酸和亚牛磺酸代谢
萜类骨架生物合成
硫胺素代谢
双组分系统
酪氨酸代谢
泛醌和其他萜类醌生物合成
缬氨酸、亮氨酸和异亮氨酸的生物合成
缬氨酸、亮氨酸和异亮氨酸降解
万古霉素耐药
维生素B6代谢
β-内酰胺抗性
▼
Bifidus在拉丁语中的意思是裂开或分开(当营养受限时,细胞的特征性分叉很明显)。
双歧杆菌属的物种具有较高的 rRNA 16S 序列相似性,构成了一个连贯的系统发育单元。
2002年,来自长双歧杆菌的第一个基因组被发表,并且此后公开可用的双歧杆菌基因组数量稳步增加。截至2016年4月,共有254个公开的双歧杆菌基因组序列,其中61个代表完整的基因组序列。通过比较不同物种的基因组,揭示了该属的系统发育和进化适应性。
双歧杆菌基因组平均长度为2.2 Mb,通常编码52-58个tRNA基因和3-5个rRNA操纵子。
▼
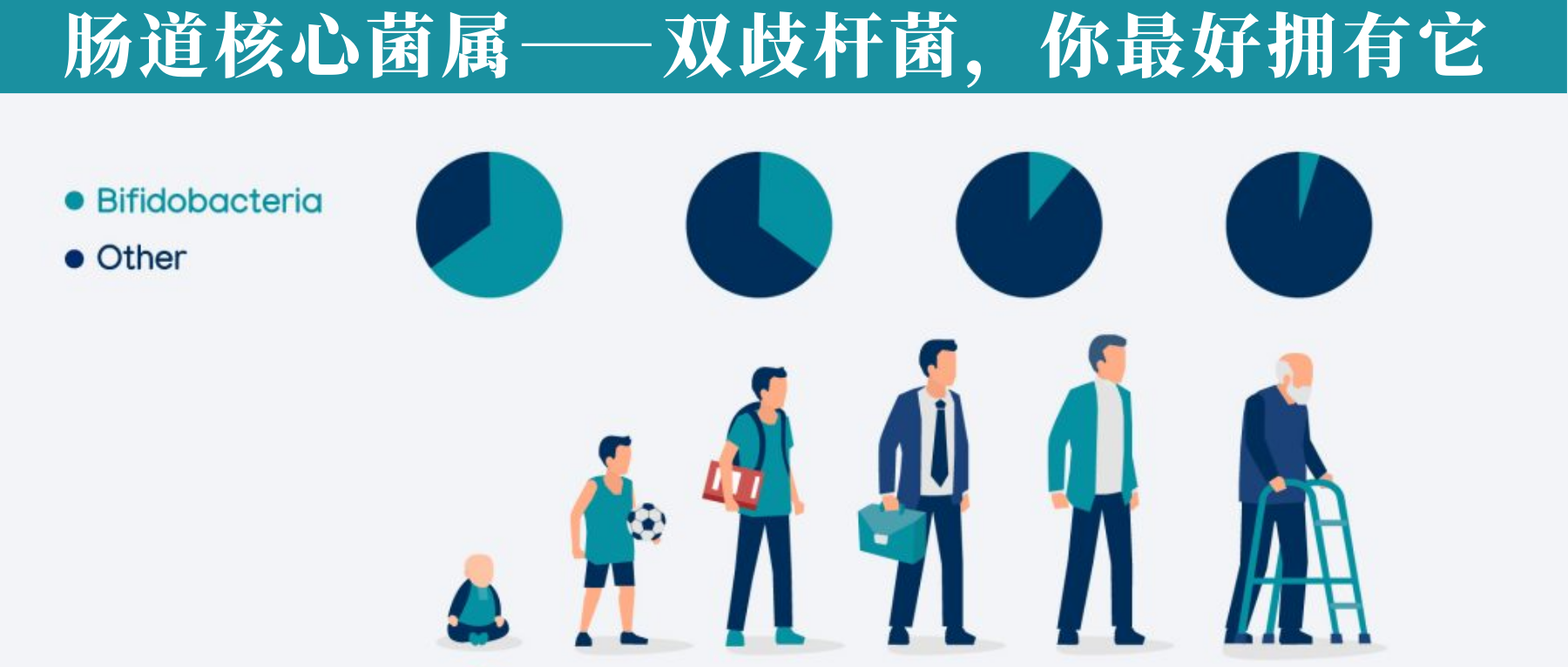
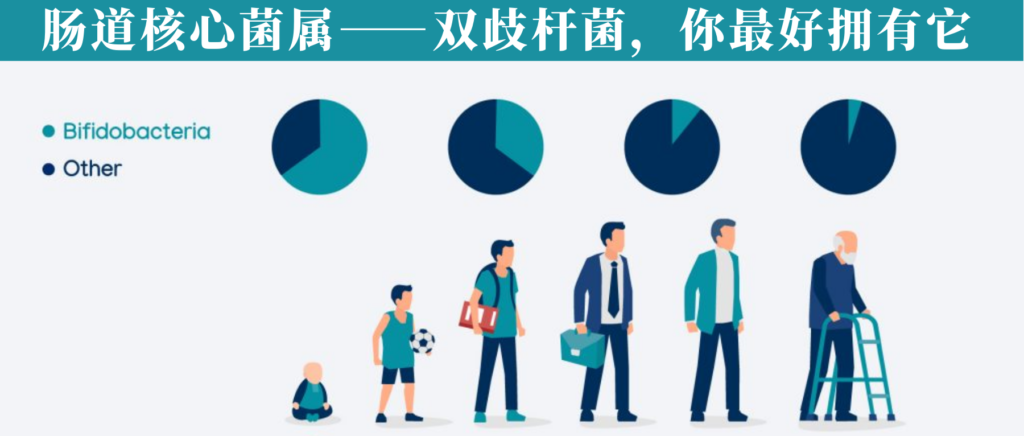
• 通常,在婴儿肠道内以婴儿双歧杆菌和短双歧杆菌为优势菌群;
• 而在成人肠道内则缺少这两种双歧杆菌,仅有少量双岐双歧杆菌、青春双歧杆菌和长双歧杆菌存在
通过使用不同的方法和技术,已经观察到双歧杆菌的数量和多样性会随着年龄的增长而减少(当然这个目前仍然不明确)。
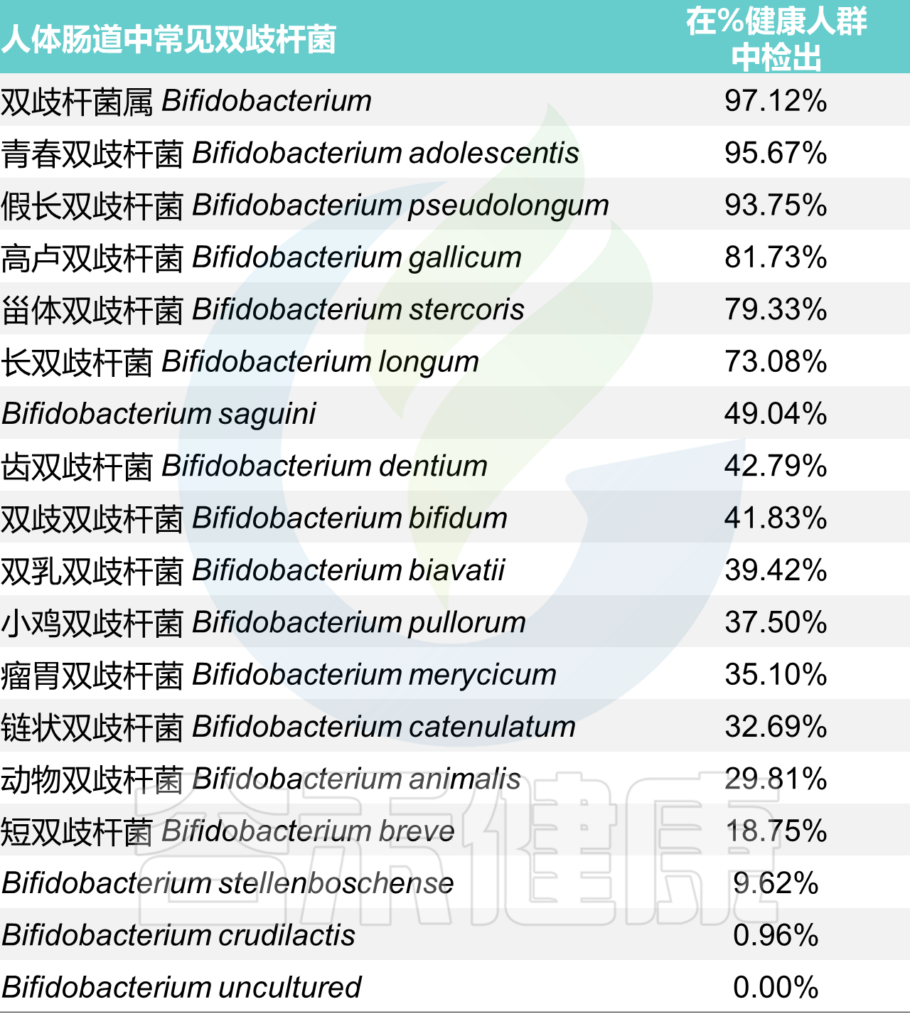
<来源:谷禾健康肠道菌群检测数据库>
其中能在人体肠道内定植并能用于制备保健食品的双歧杆菌主要有5种:
婴儿:双歧杆菌占90%,断奶后迅速下降
双歧杆菌通常是婴儿肠道微生物群中最丰富的分类群(高达 90%),其丰富性与对婴儿健康的各种有益影响有关,包括肠道中叶酸的产生、对疫苗接种的免疫反应增加和预防或减少过敏性疾病。
已知双歧杆菌产生的紧密粘附菌毛会刺激结肠上皮细胞增殖,从而可能影响新生儿肠道的成熟。富含双歧杆菌的健康肠道微生物群在母乳喂养期间继续存在,但相对丰度在断奶后迅速下降。
成人:双歧杆菌参与复杂碳水化合物的代谢
存在于成人肠道中的肠道双歧杆菌基因组,例如青春双歧杆菌,似乎并不包含与母乳成分利用相关的基因,相反,它们包含大量专门用于成人饮食中常见的复杂碳水化合物的代谢(例如,淀粉和淀粉衍生的碳水化合物)。
到目前为止,饮食类型(西方、亚洲、地中海)与特定双歧杆菌种类在肠道中的富集之间尚无明确关系,但据报道不同人群和国家之间存在差异。
老人:双歧杆菌物种水平变化
在老年人(百岁老人)中也提到了物种水平的变化。结果仍然有些争议。在某些地区,百岁老人的微生物群组成仍然与成年人相似,然而,也有些地方百岁老人的双歧杆菌比例高于年轻老人。
与衰老过程间接相关的其他外在因素也会影响双歧杆菌的组成。抗生素在老年人群中的长期使用无疑对肠道菌群组成产生巨大影响,从而减少双歧杆菌数量。
▼
双歧杆菌介导的健康益处是双歧杆菌、肠道微生物群的其他成员和人类宿主之间建立的复杂动态相互作用的结果。
这些错综复杂的相关模式尚未在分子水平上得到完全破译。因此,目前正在努力了解肠道生态系统内的代谢通量,以辨别健康和疾病中的微生物群-宿主串扰。这将为通过以微生物组为目标的方法以更精确、安全和可控的方式调节宿主健康奠定基础。
在双歧杆菌益处中,抑制肠病原体和减少轮状病毒感染是它们最确定的结果。许多体外研究表明,双歧杆菌可以通过产生有机酸、抗菌肽、群体感应抑制剂来抑制病原体, 或免疫刺激以及其他机制,为它们预防某些感染的能力提供分子线索。
双歧杆菌的抗菌作用
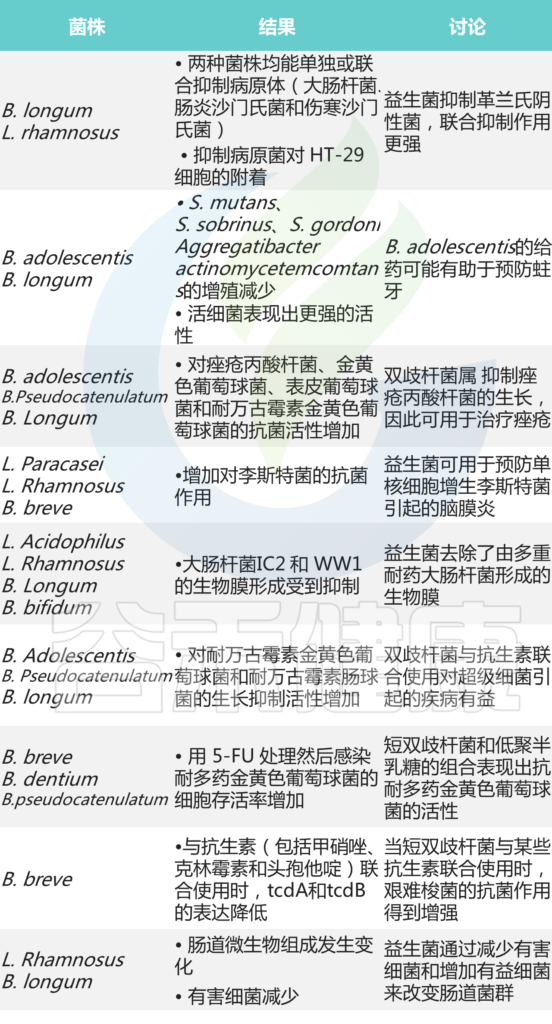
Lim HJ,et al., J Microbiol Biotechnol. 2020
另一个事实表明,存在一个关键的双歧杆菌-肠道微生物群-宿主串扰,即婴儿早期微生物群的建立似乎遵循一种精心策划和有组织的菌群演替模式。
与人类肠道菌群的串扰机制表现在:
第一批肠道定殖者,双歧杆菌占主导地位
有助于减少环境并产生代谢物,使其他细菌种群能够稳定地定植肠道。
和其他肠道细菌间存在显著的共生效应
多形拟杆菌能够在长双歧杆菌存在下,扩大其利用多糖的能力,这表明常驻肠道共生体能够调整其底物利用以响应对双歧杆菌。
通过补充益生菌调节双歧杆菌
通过补充益生菌调节双歧杆菌水平可以改变肠道微生物群的整体组成和代谢。
在源自人肠道的微生物群小鼠模型中补充长双歧杆菌菌株会增加丙酮酸、丁酸和生物素的产量。可能是由于长双歧杆菌和Bacteroides caccae的共存。
补充长双歧杆菌还与肠杆菌科的减少和直肠真杆菌的增加相关,支持双歧杆菌对其他肠道菌群的数量和功能的影响。
双歧杆菌分子调节肠道菌群
体外研究表明,在双歧杆菌胞外多糖存在的情况下,脆弱拟杆菌和Faecalibacterium prausnitzii(粪栖杆菌,又名普拉梭菌)会改变它们的代谢。
通过补充益生元调节双歧杆菌
通过益生元(包括菊粉、阿拉伯木聚糖、低聚半乳糖和低聚果糖)促进双歧杆菌生长,也与更高的乳杆菌-双歧杆菌与肠杆菌科比例相关,并调节短链脂肪酸,有机酸等的产生。
对益生元代谢分析,了解双歧杆菌与其他菌群的交叉喂养机制
B. longum NCC2705 和E. rectale ATCC 33656之间的交叉喂养机制,有利于双歧杆菌菌株和产丁酸菌在同一生态位中共存。为阿拉伯木聚糖寡糖的产双歧和产丁酸作用提供了新的见解。
理解双歧杆菌和拟杆菌属物种以及双歧杆菌和普拉梭菌之间的交叉喂养机制),这将有助于理解共培养发酵的产丁酸活性。这些结果也有助于阐明益生元发酵过程中肠道内的细菌相互作用。
双歧杆菌菌株间的潜在串扰
分析长双歧杆菌和短双歧杆菌菌株之间的相互作用,证明它们对碳水化合物利用酶的产生显著影响。
双歧双歧杆菌PRL2010和短双歧杆菌UCC2003之间存在交叉喂养机制:
短双歧杆菌UCC2003不能在体外利用唾液酸作为唯一的碳源,尽管它可以以消耗唾液酸的残留物为代价生长。
双歧双歧杆菌PRL2010 从粘蛋白上裂解。事实上,对双歧杆菌属糖苷利用能力的详细分析强调了特定物种专门针对特定碳水化合物的利用,因此表明双歧杆菌物种可能在肠道内合作利用碳水化合物。
也就是说益生菌菌株的混合物可能会产生协同效应,提高它们对肠道菌群以及宿主健康发挥作用的能力。
值得强调的是,某些双歧杆菌定植特征受肠道因素调节,包括其他微生物的存在。具有不同肠道微生物群组成的个体似乎对双歧杆菌补充剂的反应不同,这一事实提供了双歧杆菌-肠道微生物群串扰存在的进一步证据。
双歧杆菌与其他菌群可能的相互影响如下:
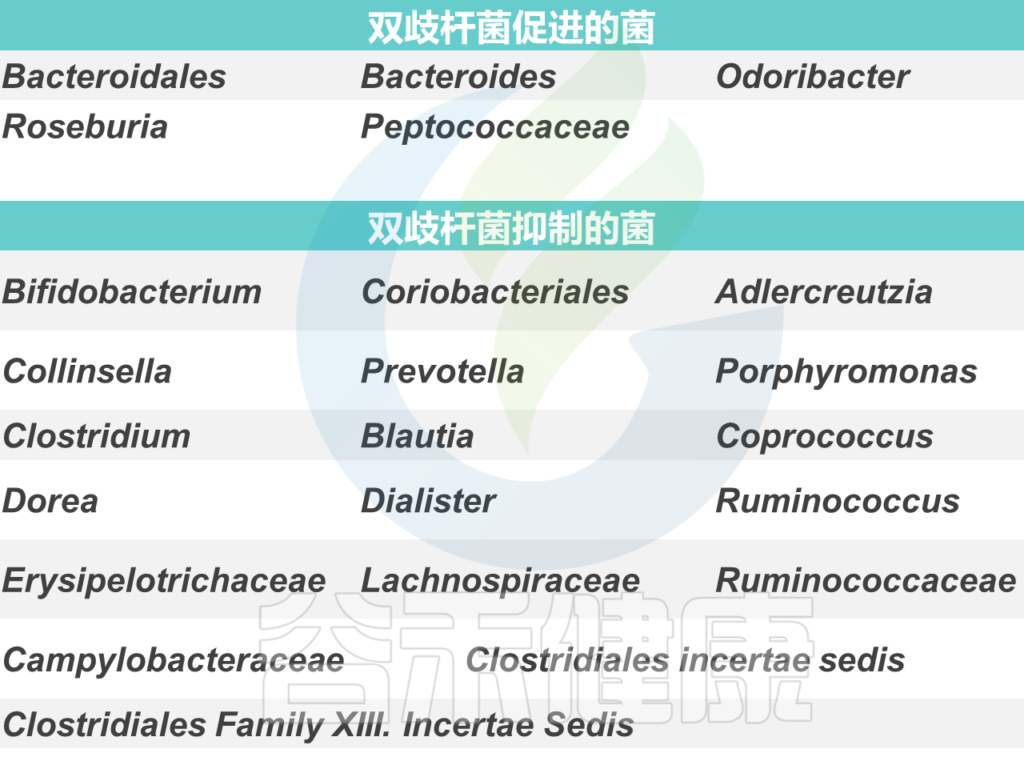
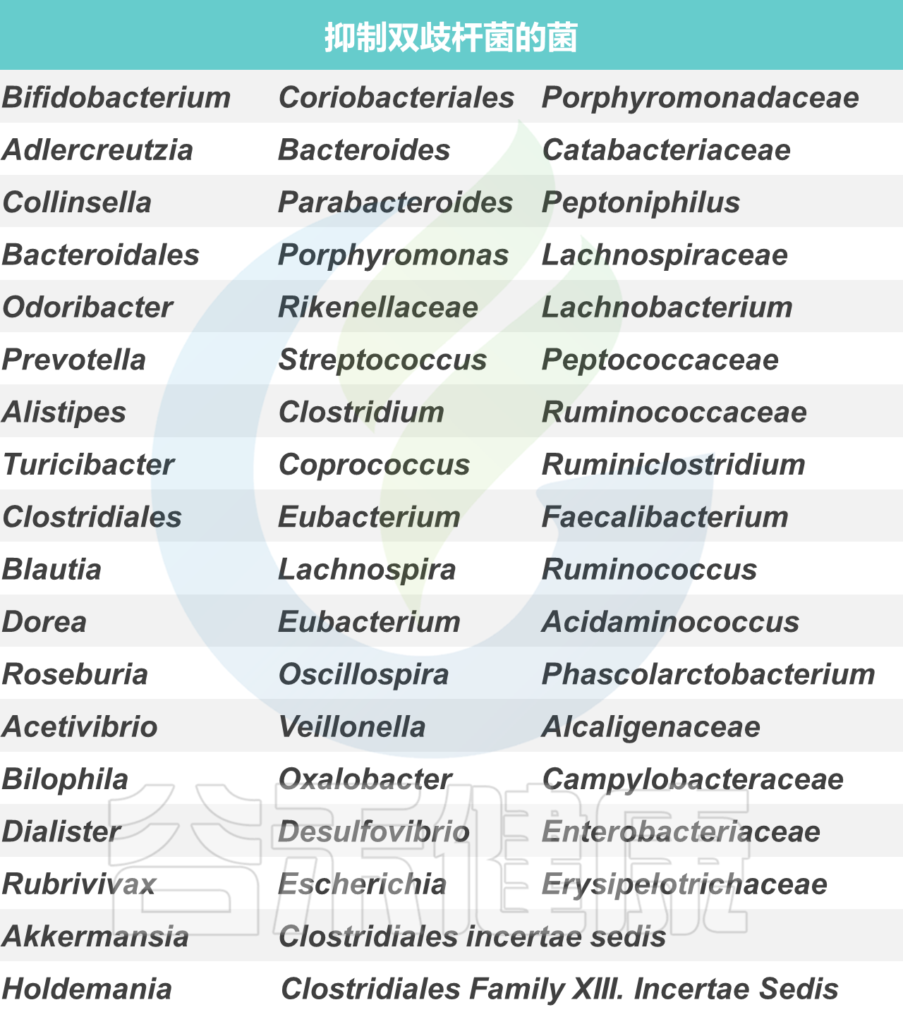
尽管这种不同行为背后的串扰的分子机制还远未被理解,但对它们的理解将极大地帮助设计基于益生菌的疗法,即使在目前在临床试验中被归类为“无反应者”的那些亚群中也能发挥作用。
★
双歧杆菌是革兰氏阳性菌,必须能够在胃肠道运输中存活下来,了解双歧杆菌对克服胃肠道应激因素的反应,对于合理选择益生菌菌株和开发分子工具箱以提高其性能至关重要。最近的发展,如表达载体和突变生成系统,以及功能基因组学和其他组学技术的巨大进步,揭示了双歧杆菌使用多种策略来适应人类肠道的特定环境条件。
▼
在通过胃肠道期间,口服益生菌会遇到各种恶劣的环境条件(下图)。这些条件危及这些有益微生物的生存,损害它们的生存能力和功能。这些包括消化酶、胃中的酸性 pH 值、防御素和肠道中高浓度的胆汁盐。
人类胃肠道的示意图和双歧杆菌对各种环境因素或生态位的反应
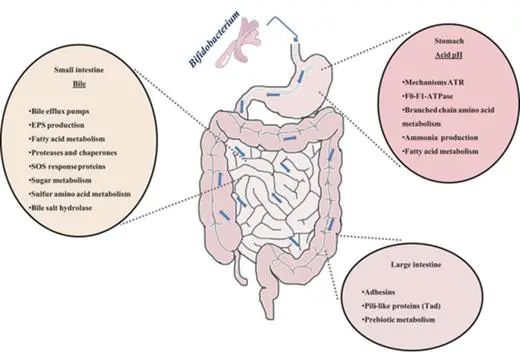
低 pH 值
胃液成分造成的强酸性条件是双歧杆菌在胃中应对的首要障碍之一。除动物双歧杆菌和嗜酸双歧杆菌外,双歧杆菌对酸的耐受性较低。因此,益生菌的使用需要分离具有良好耐酸性的菌株,这些菌株通常对其他技术和胃肠道应激因素表现出交叉抗性。
细菌可能通过一系列酸诱导机制对随后的酸胁迫产生耐受性。双歧杆菌中这种耐酸反应 (ATR) 的分子机制在部分研究中已经被报道。长双歧杆菌中的乳酸和酸适应与 F0-F1-ATP 酶亚基的过量产生有关,这通过增加的 H + 排出活性来抵消这种 H + 积累。
注:暴露于低pH值会影响质子动力,导致H+在细胞内积累。
在双歧杆菌中发现了环境条件(例如可发酵碳源的可用性或生长期)对酸耐受性的强烈影响。这突出了体外模型模拟双歧杆菌在肠道中面临的条件的局限性。
胆汁
胆汁的存在是双歧杆菌在肠道中必须面对的生理障碍之一。胆汁酸是这种生物体液的主要成分,它们具有类似洗涤剂的抗菌特性。这些酸在细胞质中的积累会影响细胞的稳态,导致离子泄漏。
双歧杆菌对这种肠道疾病的抵抗力取决于物种,尽管它们可以通过接触胆汁获得稳定的抵抗表型。这个过程经常涉及对其他压力因素的交叉抗性的出现、抗生素抗性模式的改变、碳水化合物代谢、细胞表面结构和组成,以及它们与肠道生态系统的相互作用等。
酶和抗菌肽
双歧杆菌在胃肠道中存活和功能受到多种因素的影响,其中包括消化酶(如胃蛋白酶和胰酶)、肠道抗菌肽(如防御素和导管素)以及某些益生菌的刺激。
研究表明,消化酶可能影响双歧杆菌的粘附,而肠道抗菌肽可能影响双歧杆菌的存活和功能,但其机制尚未完全了解。
某些益生菌会刺激肠道防御素的产生。B. animalis亚种lactis Bb12导致人体中 β-2-防御素的产生增加,这可能解释了双歧杆菌预防某些感染的能力。
▼
微生物对肠粘膜的粘附是定植过程中的一个重要特征,并且与菌株与宿主相互作用的能力有关。因此,对粘膜的粘附经常被用作选择益生菌菌株的标准。
菌株的粘附能力似乎对免疫调节和竞争性排斥病原体也很重要。肠粘膜的外部区域由覆盖上皮细胞的粘液层组成。这种粘液富含糖蛋白和糖脂,为细菌粘附提供了丰富的目标,包括碳水化合物部分。
竞争性排除肠道病原体
一些益生菌与肠道病原体共享碳水化合物结合特异性,这为使用益生菌对抗过度竞争的病原体以预防感染提供了明确的理由。因此,对人肠粘液和/或人肠上皮细胞系的粘附一直是评估细菌粘附的最常用模型。在这方面,某些双歧杆菌菌株具有从肠道细胞和人体肠道粘液中竞争性排除肠道病原体的能力。
细菌粘附到胃肠道粘膜的机制很复杂,涉及非特异性现象,细胞壁特性和组成以及粘附素的存在等因素,构成了菌株粘附粘膜能力的最重要决定因素。
★
双歧杆菌在预防疾病方面的作用仍在研究中,但它们的一些有益作用包括:
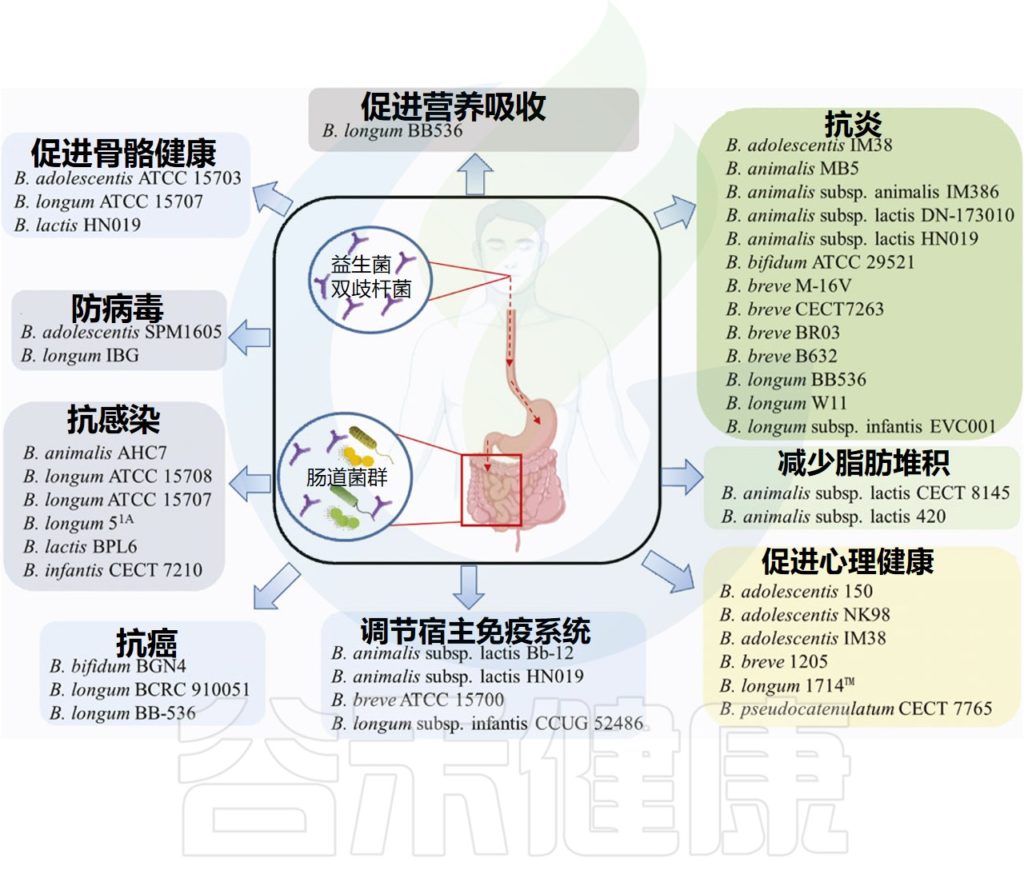
doi.org/10.3389/fbioe.2021.770248
补充双歧杆菌也被证明可以增强肠道新陈代谢,理论支持两者之间的协同相互作用双歧杆菌和其他有益的肠道菌种。
✔ 治疗消化系统疾病中发挥作用
在消化系统中可以看到双歧杆菌最流行的治疗效果之一:
在因使用抗生素而出现腹泻的婴儿中,含有双歧杆菌和嗜热链球菌的益生菌配方可显著降低腹泻的发生率。
施用婴儿双歧杆菌CECT 7210 和短双歧杆菌K-110 可成功抑制轮状病毒并治疗腹泻。
双歧杆菌的抗病毒作用

Lim HJ,et al., J Microbiol Biotechnol. 2020
动物双歧杆菌已发现发酵乳制品中的双歧杆菌可以改善结肠规律性,这引发了关于双歧杆菌是否可以帮助治疗便秘的问题。
✔ 治疗感染疾病中发挥作用
双歧杆菌已被证明对产气荚膜梭状芽孢杆菌、肠病原性大肠杆菌和轮状病毒具有作用。双歧杆菌的另一种普遍尝试的临床应用涉及粪便移植作为治疗复发性艰难梭菌结肠炎的方法。
研究进一步表明双歧杆菌在预防艰难梭菌相关性腹泻、改善幽门螺杆菌根除(与抗生素治疗相结合)以及降低结肠手术后术后感染率方面的功效。
虽然作用机制尚不清楚,但研究报告称,双歧杆菌可减轻炎症性肠病的症状,缓解溃疡性结肠炎,并降低早产儿坏死性小肠结肠炎的发生率。尽管溃疡性结肠炎症状有所改善,但益生菌在克罗恩病的治疗中没有显示出益处。
双歧杆菌属的抗炎作用

Lim HJ,et al., J Microbiol Biotechnol. 2020
✔ 治疗肝病中发挥作用
双歧双歧杆菌可能通过帮助重建肠道菌群在慢性肝病的管理中发挥作用,肠道菌群是肝硬化期间受到干扰的环境。在这些患者中,含双歧杆菌的益生菌补充剂可有效预防肝性脑病的发展,但无法确定对总体死亡率的影响。
✔ 免疫反应中发挥作用
双歧杆菌也可能在刺激宿主的免疫反应中发挥作用:给予长双歧杆菌的小鼠产生了 T 和 B 淋巴细胞的显著增加,以及巨噬细胞吞噬活性的增加。有趣的是,已发现乳糜泻患者肠道微生物组中的双歧杆菌水平较低,并且在一些研究中,益生菌给药可降低 TNF-α 水平并改善症状。
B. animalis、B. longum 和B. bifidum的某些菌株在体外和体内实验中展示的对免疫功能影响的示意图
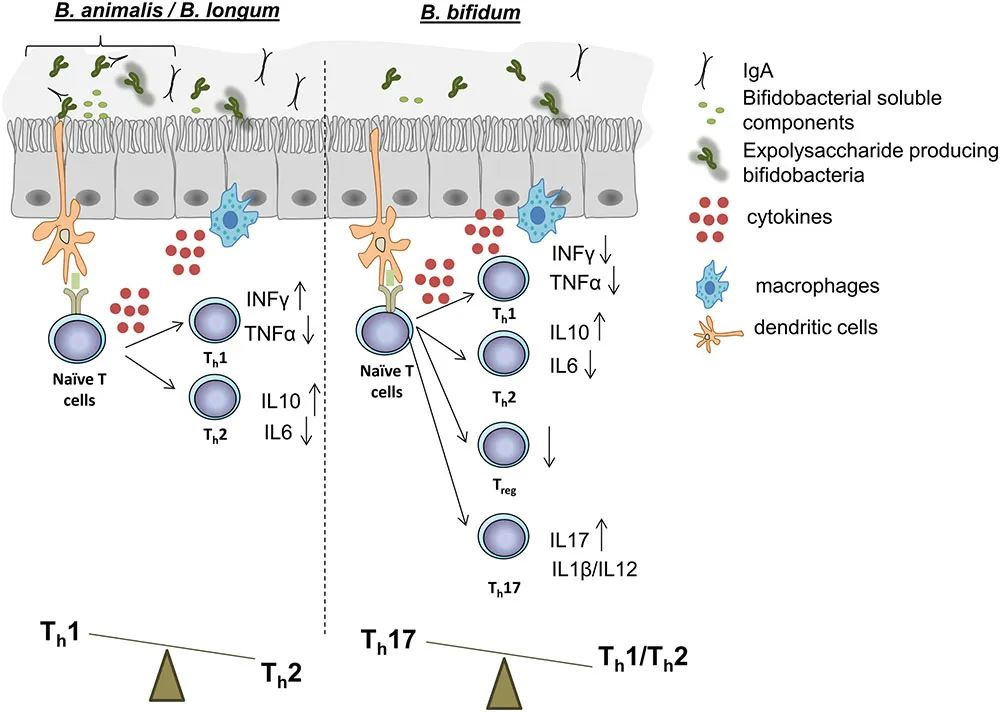
doi.org/10.3389/fmicb.2017.02345
✔ 治疗过敏性疾病中发挥作用
服用含双歧杆菌的益生菌后,患有特应性皮炎和过敏性鼻炎症状的儿童得到改善。还对高危婴儿的特应性皮炎的预防进行了研究,一些证据表明对产前或产后妇女给予益生菌有益。
✔ 治疗代谢性疾病中发挥作用
双歧杆菌对糖尿病、肥胖症和高脂血症的有益作用也得到了研究,证据显示其对普通人群的血糖水平和胰岛素抵抗具有有益作用,同时还能降低孕妇妊娠糖尿病的发病率。
一些数据也已发表,显示含有双歧杆菌的补充剂在降低胆固醇水平方面的功效,尽管更多的证据表明其他益生菌菌株的功效更大。双歧杆菌属,也显示出对减轻体重和减少体脂有益。
✔ 治疗精神类疾病中发挥作用
双歧杆菌益生菌干预在改善重度抑郁症患者的症状方面显示出显着疗效,一些数据表明,服用含双歧杆菌的益生菌补充剂的健康个体和精神分裂症患者的抑郁和焦虑水平发生率较低。
✔ 婴儿人群中发挥作用
在婴儿人群中,补充双歧杆菌可降低极低出生体重婴儿患坏死性小肠结肠炎的风险、降低全因死亡率以及迟发性败血症。
双歧杆菌菌株在人体试验中显示出有效性

编辑
doi.org/10.1128/microbiolspec.BAD-0010-2016
总之,大量证据支持双歧杆菌在治疗和预防多种人类疾病方面的安全、有益作用。
★
各种研究报道双歧杆菌通过不同的机制表现出抗肿瘤作用,包括发酵和生物转化。
不同种类的双歧杆菌通过下调和上调抗凋亡和促凋亡基因对结直肠癌细胞表现出抗癌活性。
此外,双歧杆菌可以与现有的癌症治疗手段发挥协同效应,通过调节免疫反应以帮助抗癌。越来越多的证据表明,双歧杆菌的某些物种和菌株可以改善免疫监视和抗肿瘤反应。
通过对非小细胞肺癌患者队列中癌症治疗有反应者和无反应者的肠道微生物群进行比较,作者发现,对治疗有反应的患者的粪便样本中富含双歧杆菌。
特定的双歧双歧杆菌菌株与癌症治疗协同作用
Hall, L.J, et al.,Nat Microbiol 2021
在癌症小鼠模型中测试了四种商业双歧杆菌菌株。只有那些在细胞壁中表达高水平肽聚糖的菌株在额外处理的同时,才会产生协同效应。产生协同作用的菌株诱导TLR2依赖性反应,导致IFN-γ和IL-2水平升高,并增加抗肿瘤白细胞。研究结果表明,用某些双歧杆菌菌株补充,可能会使无反应患者变得有反应。
体内和体外研究表明,长双歧杆菌和短双歧杆菌菌株能够保护 DNA 免受致癌物的侵害,并在大鼠模型中抑制两种不同致癌物的遗传毒性作用。
另一项研究表明,动物双歧杆菌对致癌物喹诺酮具有抗突变活性。在研究双歧杆菌的潜力在预防和/或治疗癌症方面,发现益生菌和细菌的组合可以减少小鼠结直肠癌模型中致癌物诱导的癌细胞。
双歧杆菌在免疫监视和刺激宿主免疫反应中的作用
一项早期研究表明,将短双歧杆菌添加到淋巴集结细胞的培养物中会导致免疫反应增强,如抗脂多糖抗体生产。
一项更近期的综合研究比较了口服或未口服双歧杆菌的小鼠黑色素瘤的生长情况。接受细菌制剂的小鼠表现出自发的抗肿瘤作用,这些作用在粪便转移后被逆转。
此外,肿瘤控制得到了与检查点封锁相同程度的改善,两者的结合几乎消除了肿瘤的生长。这些作用是通过增加树突状细胞功能、增强 CD8 + T 细胞启动和肿瘤微环境中的积累来介导的。
双歧杆菌可以作为一种运载工具,这种运载工具可以被设计用来表达感兴趣的基因/质粒。
双歧杆菌最有前途的作用,也是未来的药物输送载体。作为一种非致病性厌氧共生细菌,它成为了一种有吸引力的药物递送候选物,第一个肿瘤靶向研究表明该细菌在艾氏腹水小鼠肿瘤中高度定位。双歧杆菌对肿瘤组织的独特定位源于该细菌只能在缺氧条件下生存的厌氧特性:缺氧是恶性肿瘤的普遍现象,在肿瘤中心更为明显,从而选择性地吸引双歧杆菌生物体。
类似的后续工作证明了双歧杆菌不仅能够定位于肿瘤组织,而且能够表达lux报告基因的工程质粒。
几项研究证明了双歧杆菌作为疫苗递送载体、所需基因质粒的载体、可在无需质粒转染的情况下富集抗癌物质(如硒)的细菌的广泛用途。在不同的模式中,双歧杆菌证明有效地选择性靶向肿瘤细胞,同时表现出抗肿瘤作用。
当使用青春双歧杆菌菌株递送时,内皮抑素是一种广泛的血管生成抑制剂,可成功并选择性地抑制血管生成。
肝癌小鼠异种移植模型注射了经改造以表达内皮抑素基因的青春双歧杆菌。结果与细菌对肿瘤的选择性定位一致,因为在处死的正常组织中没有发现杆菌,并且与对照小鼠相比,血管生成受到强烈抑制,肿瘤生长减少。
考虑到双歧杆菌选择性定位于厌氧肿瘤环境的能力,及其携带转染质粒的能力,“货物”基因传递的可能性几乎是无限的。这种运载工具已被用于提供靶向分子通路调节剂。
双歧杆菌递送PTEN,抑制肿瘤生长
一个例子是使用长双歧杆菌穿梭载体递送PTEN,这是一种主要的肿瘤抑制基因,通常在癌发生的早期步骤中丢失,试图“挽救”其在小鼠实体瘤中的表达,并重建抑癌活性。 尽管结果尚未完全发表,但已描述了携带线性质粒的长双歧杆菌 L17菌株的成功改造,该质粒由pMB1和PTEN cDNA上游的HU基因启动子组成。当对小鼠实体瘤给药时,它会显着抑制肿瘤生长。
双歧杆菌递送中草药
如前所述,通过双歧杆菌载体递送药物/产品的可能性实际上是无限的,并且可能会扩展到包括递送正在临床评估的传统医学中使用的产品,比如,臭椿酮。
双歧杆菌递送生物转化剂
双歧杆菌也已被用于将生物转化剂递送至肿瘤部位。在该模型中,将无活性前药转化为其有效活性形式所需的酶通过双歧杆菌穿梭输送,确保在肿瘤内选择性地发生激活。
这种生物转化模型实现了两个目标:
此外,在有假体关节或心脏瓣膜等异物的患者中,细菌可能会脱靶到这些厌氧部位,需要高度警惕。
关于双歧杆菌属药物递送系统的可用临床前研究

doi.org/10.2217/fon-2019-0374
★
双歧杆菌是杂食“动物”,许多食物有利于促进其生长。
优质益生元:
低聚半乳糖GOS、低聚果糖FOS 和 母乳低聚糖HMO 已被用于婴儿配方奶粉,以增强婴儿肠道中的双歧杆菌。它们是经过临床验证的益生元,对促进肠道中的双歧杆菌非常有效。
含有多酚的食物:
苹果皮、红茶和绿茶、黑巧克力、咖啡、橄榄、橄榄油、姜黄和石榴、蔓越莓、蓝莓、黑莓和覆盆子等深色水果,适量葡萄酒等。
含有可溶性纤维的食物:
苹果、梨、燕麦、大麦、萝卜、西兰花、鳄梨和豆类。
含有抗性淀粉的食物:
绿色或半绿色香蕉、煮熟和冷却的土豆、煮熟和冷却的米饭、豆类和豆类。
某些发酵食品:
例如,酸奶,开菲尔,泡菜等。
其他食物:
例如:菊苣、洋葱、大蒜等。
如何知道这些吃进去的食品或补充剂对双歧杆菌产生影响?
肠道菌群检测是目前较为直观地反映补充剂和食物对肠道双歧杆菌影响的方法,使用 DNA 测序技术评估肠道中的菌群丰度。
如果通过检测发现双歧杆菌处于正常水平,则不需要额外补充,过高的双歧杆菌水平并不代表更健康;如果发现双歧杆菌缺乏,那么通过食物或益生菌补充剂等各种针对性补充方式是有利于健康的手段之一。
双歧杆菌是益生菌混合物的重要组成部分,当以适当的剂量给药时,它基本上具有各种有益健康的特性,包括抗感染、抗炎、抗癌、促进宿主心理和身体健康以及调节宿主免疫系统。
双歧杆菌通过抑制促炎细胞因子,诱导抗炎细胞因子来调节免疫系统,表明其作为感染性或炎症性疾病或癌症的潜在疗法的有效性。
当然,并非所有双歧杆菌都可以是益生菌菌株,需要正确识别益生菌干预的菌株、病理学和对应人群。深入理解双歧杆菌在宿主微生物组中的作用机制,从而了解更多未来使用这些微生物治疗疾病的影响和安全性。
此外,双歧杆菌工程可以促进增值化学品的生物产量的增加,同时消耗更少的资源。有必要进一步研究双歧杆菌作为工程宿主的可行性。
除了特定保健食品和医药行业外,双歧杆菌在微生态护肤、畜业、水产业和肉制品加工中也广泛应用,大有开发价值。
注:本账号内容仅作交流参考,不作为诊断及医疗依据。
主要参考文献:
Turroni F, van Sinderen D, Ventura M. Genomics and ecological overview of the genus Bifidobacterium. Int J Food Microbiol. 2011 Sep 1;149(1):37-44. doi: 10.1016/j.ijfoodmicro.2010.12.010. Epub 2010 Dec 28. PMID: 21276626.
Lim HJ, Shin HS. Antimicrobial and Immunomodulatory Effects of Bifidobacterium Strains: A Review. J Microbiol Biotechnol. 2020 Dec 28;30(12):1793-1800. doi: 10.4014/jmb.2007.07046. PMID: 33144551; PMCID: PMC9728261.
Chen J, Chen X, Ho CL. Recent Development of Probiotic Bifidobacteria for Treating Human Diseases. Front Bioeng Biotechnol. 2021 Dec 22;9:770248. doi: 10.3389/fbioe.2021.770248. PMID: 35004640; PMCID: PMC8727868.
Sanchez B, Ruiz L, de los Reyes-Gavilan CG, Margolles A. Proteomics of stress response in Bifidobacterium. Front Biosci. 2008 May 1;13:6905-19. doi: 10.2741/3198. PMID: 18508704.
Sánchez B, Ruiz L, Gueimonde M, Ruas-Madiedo P, Margolles A. Adaptation of bifidobacteria to the gastrointestinal tract and functional consequences. Pharmacol Res. 2013 Mar;69(1):127-36. doi: 10.1016/j.phrs.2012.11.004. Epub 2012 Nov 22. PMID: 23178557.
Luo J, Li Y, Xie J, Gao L, Liu L, Ou S, Chen L, Peng X. The primary biological network of Bifidobacterium in the gut. FEMS Microbiol Lett. 2018 Apr 1;365(8). doi: 10.1093/femsle/fny057. PMID: 29546277.
González-Rodríguez I, Ruiz L, Gueimonde M, Margolles A, Sánchez B. Factors involved in the colonization and survival of bifidobacteria in the gastrointestinal tract. FEMS Microbiol Lett. 2013 Mar;340(1):1-10. doi: 10.1111/1574-6968.12056. Epub 2012 Dec 17. PMID: 23181549.
Andriantsoanirina V, Allano S, Butel MJ, Aires J. Tolerance of Bifidobacterium human isolates to bile, acid and oxygen. Anaerobe. 2013 Jun;21:39-42. doi: 10.1016/j.anaerobe.2013.04.005. Epub 2013 Apr 15. PMID: 23598280.
Gwiazdowska D, Juś K, Jasnowska-Małecka J, Kluczyńska K. The impact of polyphenols on Bifidobacterium growth. Acta Biochim Pol. 2015;62(4):895-901. doi: 10.18388/abp.2015_1154. Epub 2015 Nov 30. PMID: 26619254.
Jung DH, Seo DH, Kim YJ, Chung WH, Nam YD, Park CS. The presence of resistant starch-degrading amylases in Bifidobacterium adolescentis of the human gut. Int J Biol Macromol. 2020 Oct 15;161:389-397. doi: 10.1016/j.ijbiomac.2020.05.235. Epub 2020 May 30. PMID: 32479932.
Ferrario C, Milani C, Mancabelli L, Lugli GA, Turroni F, Duranti S, Mangifesta M, Viappiani A, Sinderen Dv, Ventura M. A genome-based identification approach for members of the genus Bifidobacterium. FEMS Microbiol Ecol. 2015 Mar;91(3):fiv009. doi: 10.1093/femsec/fiv009. Epub 2015 Jan 27. PMID: 25764568.
Lugli GA, Milani C, Turroni F, Tremblay D, Ferrario C, Mancabelli L, Duranti S, Ward DV, Ossiprandi MC, Moineau S, van Sinderen D, Ventura M. Prophages of the genus Bifidobacterium as modulating agents of the infant gut microbiota. Environ Microbiol. 2016 Jul;18(7):2196-213. doi: 10.1111/1462-2920.13154. Epub 2016 Jan 18. PMID: 26627180.
Lugli GA, Milani C, Turroni F, Duranti S, Ferrario C, Viappiani A, Mancabelli L, Mangifesta M, Taminiau B, Delcenserie V, van Sinderen D, Ventura M. Investigation of the evolutionary development of the genus Bifidobacterium by comparative genomics. Appl Environ Microbiol. 2014 Oct;80(20):6383-94. doi: 10.1128/AEM.02004-14. Epub 2014 Aug 8. PMID: 25107967; PMCID: PMC4178631.
Collado MC, Hernández M, Sanz Y. Production of bacteriocin-like inhibitory compounds by human fecal Bifidobacterium strains. J Food Prot. 2005 May;68(5):1034-40. doi: 10.4315/0362-028x-68.5.1034. PMID: 15895738.

谷禾健康

随着一日三餐米面肉蛋菜等一些列食物的食用,数百种化学成分会进入我们的消化道。在那里,它们被肠道微生物组进一步代谢,这是数千种微生物物种的独特集合。
因此,肠道微生物组在决定营养如何影响健康方面发挥着重要作用。然而到目前为止,微生物组中的许多微生物的代谢能力仍然是未知的。这意味着我们不知道它们以什么物质为食,以及它们是如何处理这些物质的。
近期,来自普林斯顿大学的研究人员在《CELL》期刊上发表了最新的文章:
“Gut bacterial nutrient preferences quantified in vivo”,研究人员使用同位素追踪定量研究了小鼠肠道微生物群的输入和输出。

微生物碳水化合物发酵的主要输入是膳食纤维,支链脂肪酸和芳香代谢物的主要输入为膳食蛋白质。此外,循环宿主乳酸、3-羟基丁酸和尿素(但不是葡萄糖或氨基酸)为肠道微生物群提供食物。
肠道菌群拥有巨大的酶多样性,超过哺乳动物基因组的数量100多倍。这些酶的能力能使摄入的膳食营养物质加工成一些列微生物代谢物。
为了复制自身和释放代谢产物,肠道细菌需要营养输入。这些形式包括摄入的食物、宿主合成的肠道粘液和宿主循环代谢物。
//
在本文中,研究人员通过对肠道菌群及其进入宿主循环系统的代谢物进行了大规模的定量评估。
研究了膳食淀粉、纤维和蛋白质的贡献以及宿主粘液的贡献,也研究了大多数主要的循环宿主营养素,发现乳酸、3-羟基丁酸和尿素在从宿主传递到肠道微生物群中表现突出。基于对细菌特异性肽序列的测量,评估了不同细菌属的营养偏好,并表明这些偏好与响应改变饮食的微生物组分变化一致。
同位素追踪能够定量测量代谢物和生物量的输入。与质谱检测相结合的稳定同位素示踪剂,使得能够测量特定下游产物的标记。通过注入氮标记的苏氨酸来标记宿主粘液,研究人员能够比较饮食和粘液蛋白对肠道微生物群的贡献,并观察到喂食低蛋白饮食的小鼠中粘液贡献的变化。
从小鼠尾部静脉抽取血样;
使用注射器从小鼠膀胱采集尿液;
所有血清样品在没有抗凝剂的情况下置于冰上 15 分钟,并在 4°C 下以 16,000 x g 离心 15 分钟。
用预冷的Wollenberger钳在液氮中快速分离并快速冷冻(< 5秒)获得组织;夹紧前取出肠内容物;盲肠内容物取样时,先将小鼠盲肠取出并在表面切开,然后用镊子将盲肠内容物挤出。
取新鲜粪便,轻揉小鼠腹部诱导排便。将血清、组织和粪便样本保存在 -80 ºC 直至进一步分析。
为了测定血清和组织样本中的代谢物浓度,进行了同位素标配(isotope spike-in)或标准标配(standard spike-in )。
对于前者将已知浓度的同位素标记标准品加入血清或组织提取液中,通过标记与未标记代谢物的比值计算浓度。
当没有同位素标准品时,加入连续稀释的非标记标准品,测量的总离子计数与加入的标准品浓度之间产生线性拟合。然后通过拟合线的x截距确定内源代谢物的浓度;蛋白质氨基酸组成采用酸水解法测定。
首先,使用13C同位素标记的不同营养物质,通过口服管饲法对小鼠进行灌胃采集小鼠的血清、组织和粪便样本。对粪便和肠内容物进行16S rRNA测序获得细菌分类。
首先使用代谢组学方法测定盲肠内容物中游离氨基酸13C-或15N标记。
然后,对于每个肽,模拟了未标记(Iunlabeled)和由游离盲肠氨基酸(Ifree)合成的肽的同位素包膜模式。标量γ可以通过将测量的肽同位素分布(Imeasured)与Iunlabeled和Ifree的线性组合拟合来确定。
注意,当一个菌属使用的特定营养素超过该营养素对盲肠游离氨基酸的贡献时,γ将大于1。
具体来说,测量的每个肽的γ如下:
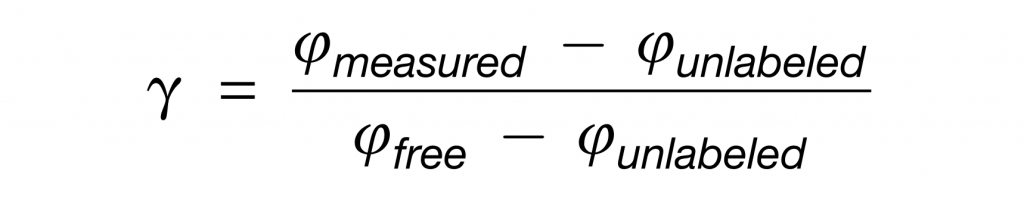

对于细菌属水平的原料贡献程度的测量,分析中只保留测量超过3个肽的属,多肽的中位数为γ-genus。
对于细菌科水平,仅分析在蛋白质组学中始终检测到的属,以及在 16S rRNA 基因扩增子测序中检测到 (> 0.5%) 的属的上一级科。
每种营养物质对菌属的贡献程度的定量公式如下:
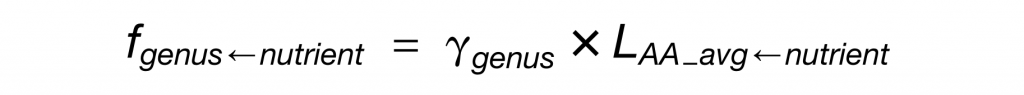

LAA_avg-nutrient为各营养物质对细菌蛋白质的贡献程度,其计算公式如下:
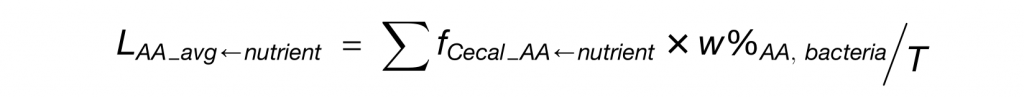

1 微生物组消耗较少的可消化膳食成分
微生物群影响宿主生理学的主要机制是通过分泌代谢产物。研究人员在门静脉和体循环以及盲肠内容物中测量了微生物衍生的50多种代谢产物的绝对浓度。
微生物群相关代谢物的绝对浓度和来源
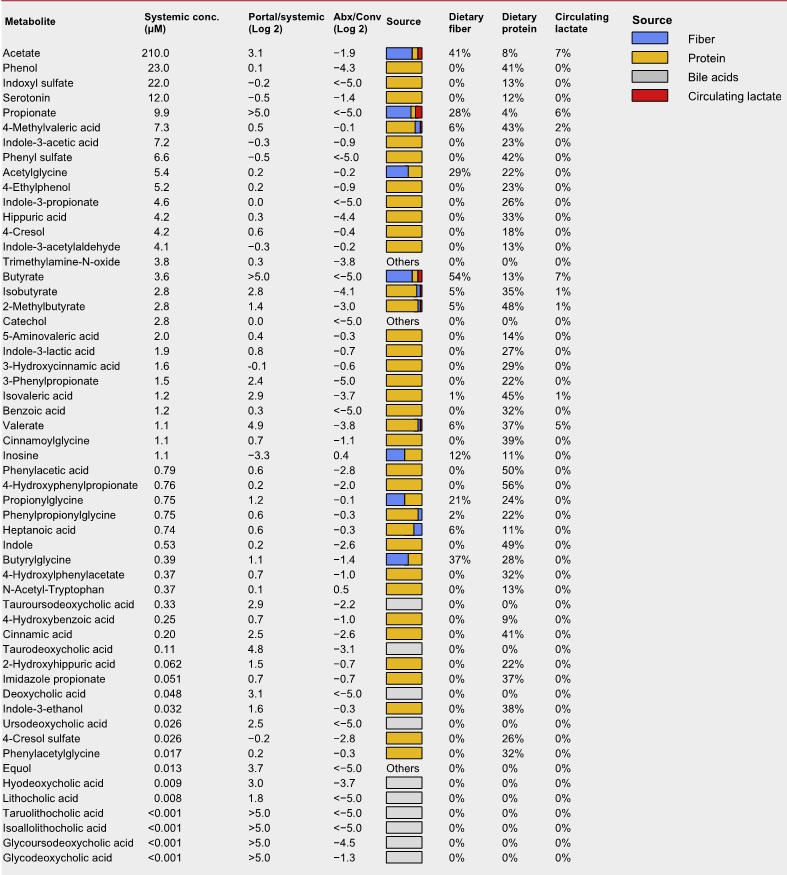
上表可以看到,与全身血液相比,大多数在门静脉循环中升高,除两种(肌苷和N-乙酰色氨酸主要来源于宿主)外,其余均被抗生素治疗耗尽。
门静脉血中主要排泄产物是短链脂肪酸。
其他相对丰富的微生物群产物是芳香族氨基酸发酵产物(苯酚、吲哚硫酸盐和3-苯丙酸盐)和支链脂肪酸(戊酸盐、异戊酸盐,4-甲基戊酸、异丁酸盐和2-甲基丁酸盐)。
探索肠道微生物产物的膳食输入:淀粉、菊粉
研究人员通过口服管饲法、淀粉(易消化葡萄糖聚合物)和菊粉(易消化果糖聚合物,即可溶性纤维)喂养小鼠:
13C淀粉灌胃后,标记的葡萄糖、乳酸和丙氨酸迅速出现在门脉循环中,并占大多数淀粉碳(约75%)。
13C菊粉和13C淀粉有什么不同?
13C菊粉灌胃后,没有观察到大量标记的果糖、葡萄糖、乳酸和丙氨酸,取而代之的是标记的门静脉代谢产物以短链脂肪酸的形式缓慢出现,约40%的菊粉碳成为短链脂肪酸,其余未消化并随粪便排出。
膳食菊粉,而不是淀粉,在盲肠内容物中广泛标记糖酵解和TCA中间体和氨基酸。
藻类蛋白大量标记了微生物群衍生的门静脉代谢物:短链脂肪酸、支链脂肪酸和芳烃(吲哚、吲哚-3-丙酸盐和3-苯丙酸盐)。
“难以消化的碳水化合物和蛋白质直接为微生物组提供营养,并通过微生物产物间接为宿主提供营养。”
研究中发现宿主循环系统中的乳酸,3-羟基丁酸以及尿素能为肠道细菌提供营养。
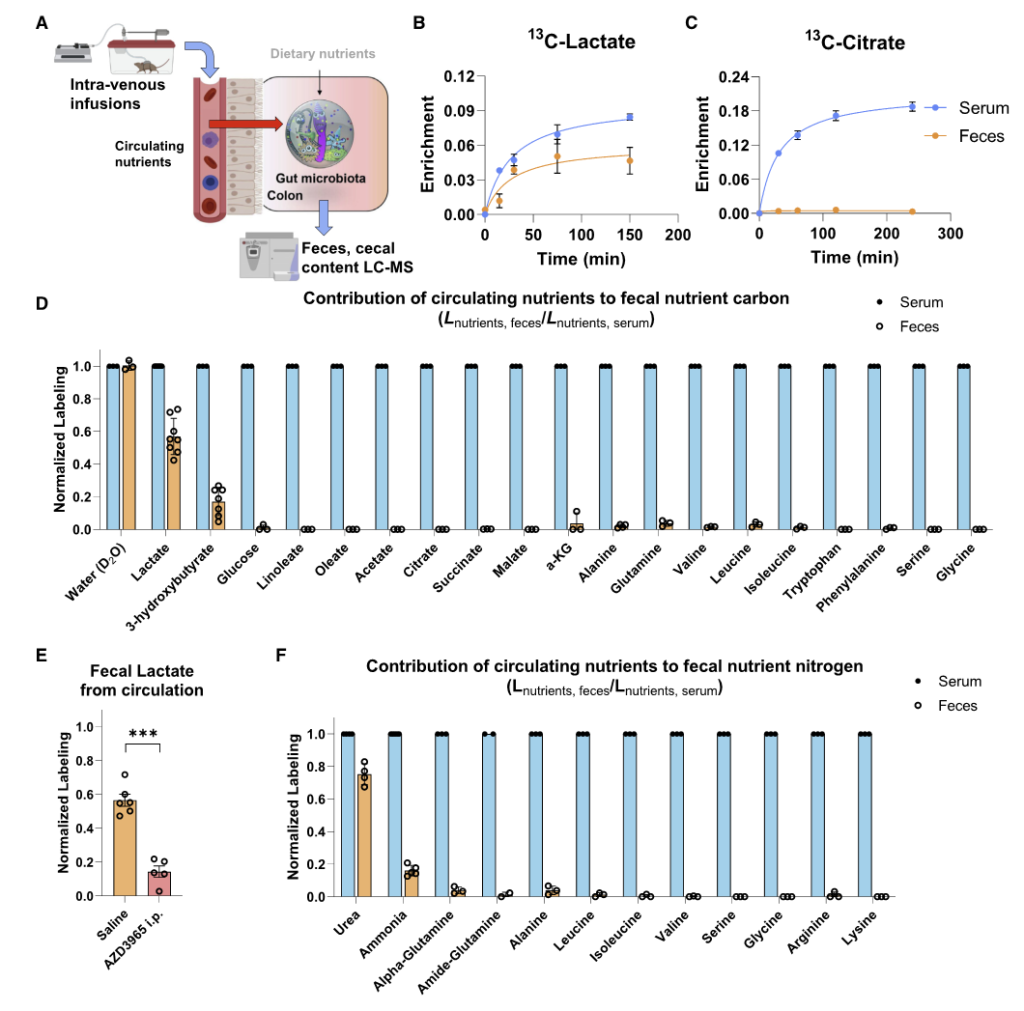
如图A,将同位素标记的营养物质通过静脉输注到小鼠的全身血液循环中。 2.5 小时后收集血清和粪便以量化每种营养物质对相应菌群代谢物的碳贡献。
图BCD表示了13C标记的各种营养物质在小鼠的血液和粪便中的含量,可见乳酸和 3-羟基丁酸有进入肠道菌群中,而其余大部分营养物质如柠檬酸盐、葡萄糖、氨基酸等都没有进入到肠道菌群中。
图F为15N标记的营养物质,可见尿素也同样被菌群大量利用。
为了定量确定微生物代谢物的来源,研究人员给小鼠喂食部分纤维、脂肪或蛋白质13C标记的标准食物,盲肠标记在12小时内达到稳定状态。
为了说明循环营养输入,研究人员还注入了13C乳酸或3-羟基丁酸。
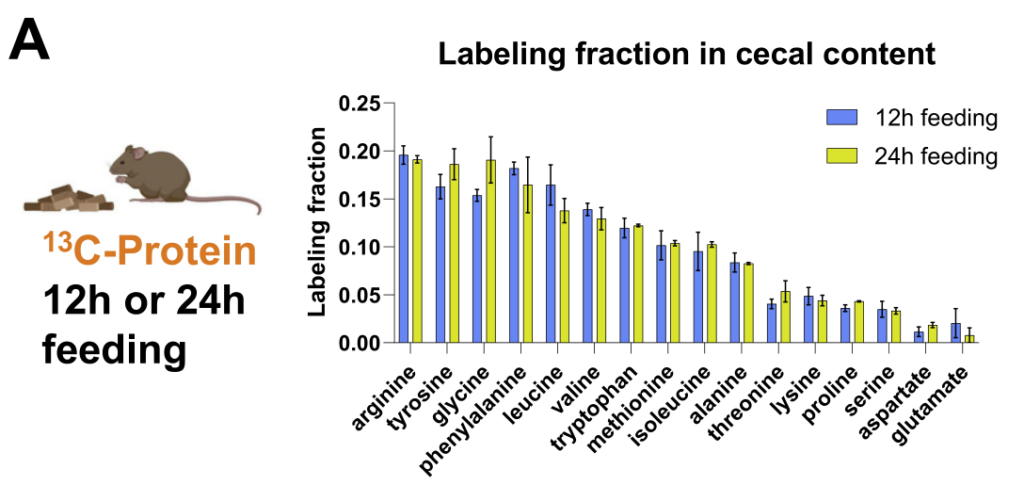
这些研究确定了大多数微生物群中心代谢物中的碳供给:
接下来,研究人员检查了微生物组游离氨基酸的输入,并用15N标记的膳食蛋白和注入的尿素进行追踪。
与哺乳动物不同,大多数肠道细菌具有合成所有20种蛋白质氨基酸的生物合成能力。
然而,研究人员观察到“必需氨基酸”主要来源于膳食蛋白质,哺乳动物无法制造,需要在细菌中表达广泛的生物合成途径。
“非必需氨基酸”主要在肠道微生物群中合成,使用膳食菊粉和循环乳酸作为碳源。
抗生素或无菌小鼠中的微生物群消耗有利于盲肠中氨基酸的积累(基于同位素追踪研究),这些氨基酸主要来自膳食蛋白质和微生物合成的氨基酸的消耗。
膳食蛋白质是必需氨基酸和非必需氨基酸的主要氮源,宿主尿素对非必需氨基酸也有很大贡献。
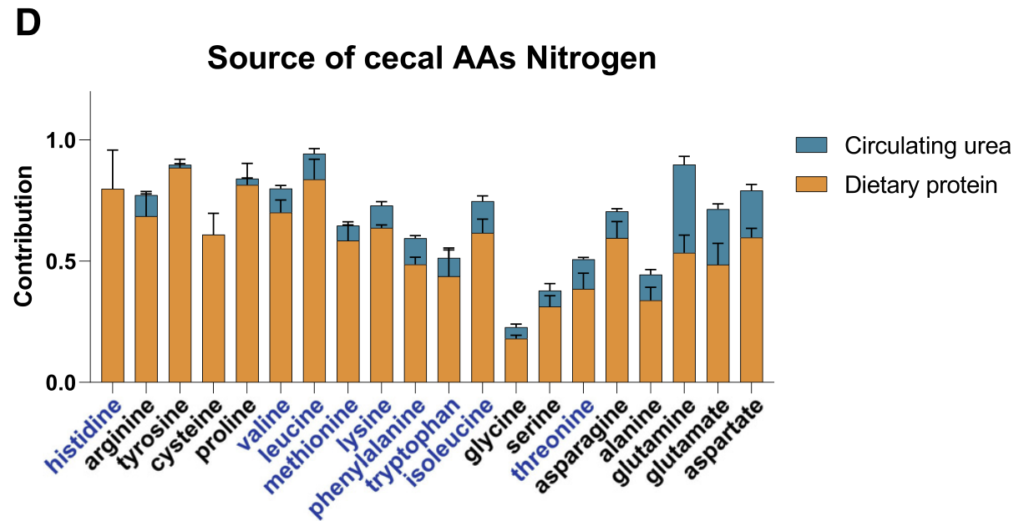
研究人员的发现如下:
【1】必需氨基酸,尽管能够由微生物群合成,但主要来自饮食,不经历任何碳重排;
【2】与TCA连接最紧密的非必需氨基酸基本上由微生物群合成,使用来自纤维的碳,通过中心代谢反应与其他碳争夺;
【3】转氨反应部分地将来自饮食衍生氨基酸的氮与来自宿主尿素的氮混合。
研究人员发现,许多微生物来源的代谢物来源于到达结肠的未吸收膳食蛋白。假设这些代谢物的循环水平将取决于膳食蛋白质到达结肠微生物群的程度。
为了控制这一点,研究人员给小鼠喂食的食物中,一部分蛋白质(酪蛋白,部分到达结肠微生物群)被游离氨基酸(基本上在小肠中完全吸收)取代。
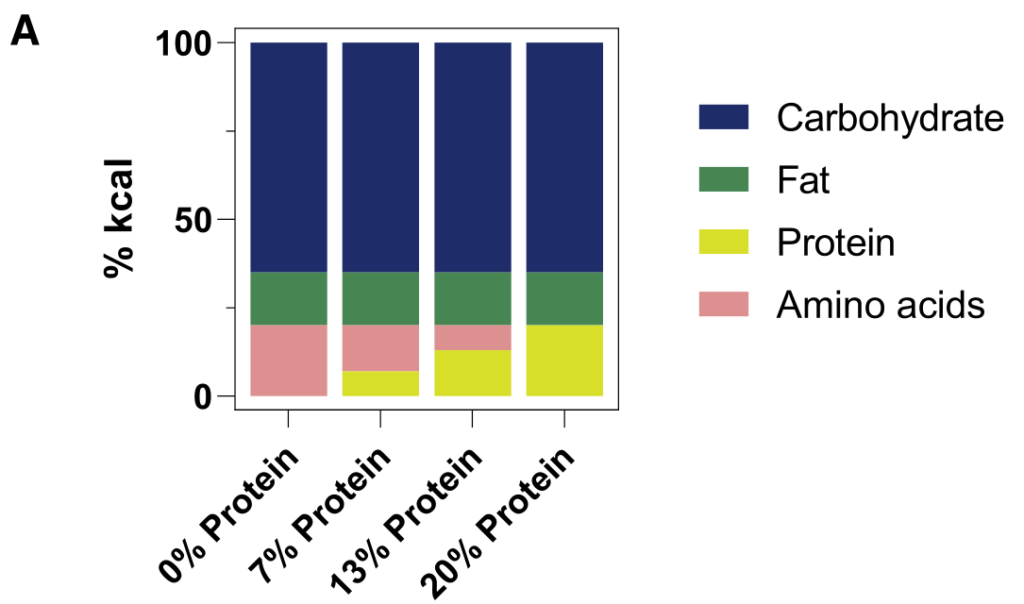
2周后对全身血液进行代谢组学研究。含有较少完整蛋白质和更多游离氨基酸的饮食往往会增加循环氨基酸水平。
重要的是,蛋白质衍生的循环微生物代谢物(酚类、吲哚类和酰基甘氨酸)串联下降。
“微生物代谢物营养来源的知识可用于操纵其系统水平。”
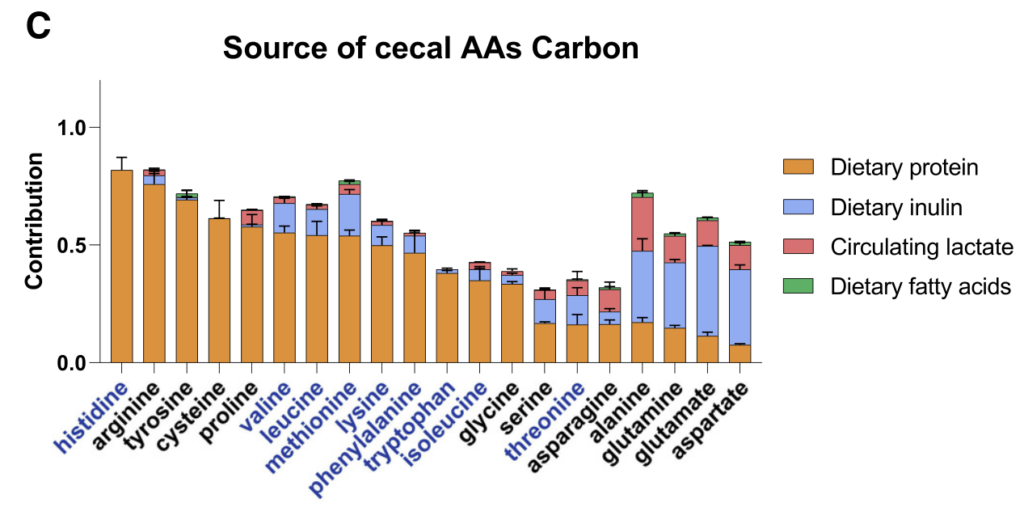
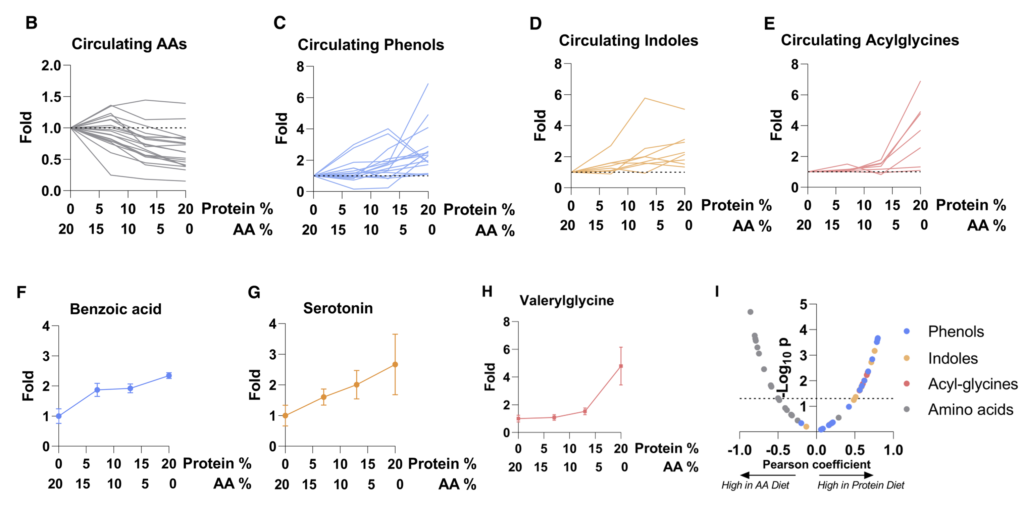
研究人员通过结合13C营养标记和蛋白质组学来定量不同微生物的碳原料。
每种13C标记的营养素(膳食菊粉、膳食藻蛋白或循环乳酸)提供24小时,这足以在肠道细菌中实现稳态标记。
如同B-D,分别计算了在膳食中使用的菊粉和蛋白质以及乳酸在各细菌内的喜好程度,这个喜好程度也就是将在细菌特异性肽上被同位素标记的程度进行了量化。
结果可见:
拟杆菌属和梭状芽胞杆菌利用菊粉的程度是 Akkermansia、Muribaculum 或 Alistipes 的 4 倍多。
总体而言,厚壁菌门下的菌属比拟杆菌门的使用膳食中的蛋白质(厚壁菌0.237±0.052;拟杆菌0.175±0.031,p=0.02)。
Akkermansia通常被认为是一种促进健康的肠道微生物,使用的菊粉和蛋白质最少。相比之下,它使用了来自宿主的循环乳酸最多。
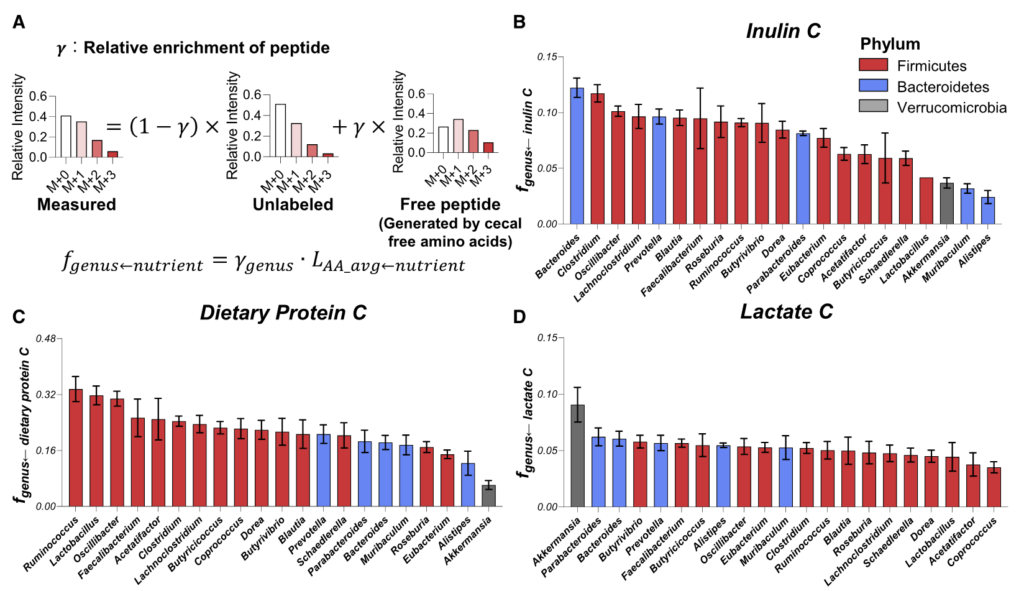
为了知晓这些细菌的营养偏好是否能预测饮食变化后的肠道菌群的组成变化。研究人员给小鼠喂食富含菊粉或藻类蛋白的饮食 2 天,并通过 16S rRNA 测序测量微生物组的组成。
结果如图F和I:
利用最多菊粉的拟杆菌属在高菊粉饮食后增加了4倍;
另一种利用较多菊粉的梭状芽胞杆菌也增加了2倍;
利用较少菊粉的菌属要么没有变化,要么略有下降;
富含藻类蛋白饮食的实验结果同理。
图G和J计算了这两种营养物与对其利用程度最高的前两名菌属相对丰度的相关性,p<0.05呈显著相关。
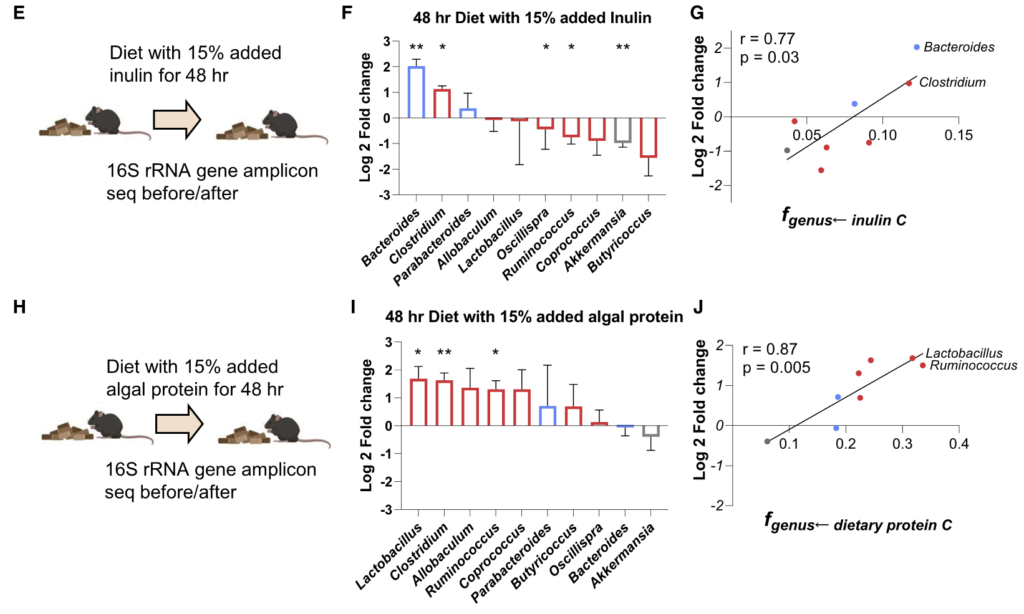
“不同肠道细菌的营养偏好有助于解释饮食操作后微生物组分的变化。”
最后,研究人员转向不同肠道细菌的氮源偏好,比较15N标记的膳食蛋白喂养和15N尿素输注。
高度利用膳食蛋白质中碳的细菌属也高度利用膳食蛋白中的氮,这与细菌蛋白质组中完整吸收的膳食蛋白质中的氨基酸一致。
厚壁菌喜欢从膳食蛋白质获取氮
在厚壁菌门成员中,偏好尿素氮的属往往是菊粉的疯狂使用者,即使用菊粉和尿素合成自己的氨基酸。这包括一些脲酶阴性菌属,它们可能通过交叉喂养获得尿素氮。
此外,在厚壁菌中也看到了一些属更喜欢从膳食蛋白质中获得氮,而其他属更喜欢循环尿素。
静脉注射尿素以提高循环尿素浓度后,偏好尿素的厚壁菌以及阿克曼菌的丰度大幅增加。
拟杆菌喜欢从宿主分泌的蛋白质中获取氮
与厚壁菌相比,拟杆菌对膳食蛋白质和循环尿素氮的利用率较低,这提出了一个关键问题:
拟杆菌如何获得氮?
肠道微生物群的一些成员(如拟杆菌和阿克曼菌)能够消化宿主分泌的蛋白质,如粘蛋白。
假设宿主分泌的蛋白质是拟杆菌氮的关键来源。为了探索这种可能性,研究人员进行了长期15N标记的赖氨酸和精氨酸输注(12、18和36小时),以标记结肠中的宿主蛋白。
尽管没有直接给微生物组喂食,但在36小时输注后,赖氨酸和精氨酸确实起作用,这与通过宿主蛋白进行的标记一致。这种标记优先发生在拟杆菌和阿克曼菌中。
膳食和分泌宿主蛋白的氮贡献呈负相关,与某些肠道细菌优先消耗膳食蛋白和其他宿主蛋白一致。
“膳食蛋白质和循环尿素是厚壁菌的主要氮原料,而分泌的宿主蛋白质为拟杆菌提供氮。”
研究人员开发了定量同位素追踪方法来测量肠道细菌的营养偏好。除了膳食纤维和分泌的宿主蛋白外,还将膳食蛋白和循环宿主乳酸、3-羟基丁酸和尿素确定为喂养肠道细菌的重要营养素。排除了其他循环宿主营养素(如葡萄糖和氨基酸)对结肠微生物群的直接贡献。
一项关键技术成就是能够从不同碳源和氮源追踪到细菌特异性肽,从而揭示复杂和竞争性肠腔环境中不同细菌的营养偏好。
厚壁菌门倾向于从膳食蛋白质获得氨基酸,而拟杆菌门更多地依赖宿主分泌蛋白。同样,一些厚壁菌门(如梭菌属)大量利用纤维(菊粉),而其他厚壁菌门则不利用纤维。
动物饮食干预实验发现,拟杆菌属和梭菌属是转化纤维最活跃的菌属。宿主循环代谢物水平也可能影响微生物组的营养获取和最终组成。
本文提供了关于哪些营养素喂养肠道微生物群以及哪些细菌更喜欢哪些营养素的基础知识。
文中所开发的方法具有广泛的应用前景,最终将有助于全面和定量地了解饮食-微生物-健康的关系。
参考文献:Zeng X, Xing X, Gupta M, Keber FC, Lopez JG, Lee YJ, Roichman A, Wang L, Neinast MD, Donia MS, Wühr M, Jang C, Rabinowitz JD. Gut bacterial nutrient preferences quantified in vivo. Cell. 2022 Sep 1;185(18):3441-3456.e19. doi: 10.1016/j.cell.2022.07.020. PMID: 36055202; PMCID: PMC9450212.

谷禾健康
热门综艺《向往的生活》第四季中,嘉宾岳云鹏的“吃了就困”,“吃了睡,睡了吃”…意外抢镜。
他说自己,吃完饭就犯困 ↓↓↓

对于 “饭后就困” 这件事,网友们表示太真实,自己也一样 ↓↓↓

生活中,我们会发现很多人吃完就会感到疲倦,想睡觉,那么,
为什么吃完饭会想睡觉?
所有人都是这样的吗?
有没有可能通过一些方法改善?
……
饭后感到疲倦的程度可能会因人而异,因为它可能取决于许多因素,包括年龄、健康状况、食物的数量和类型、一天中就餐时间等等。
本文将归纳整理“餐后疲劳”的一些原因,从而帮助预防和改善餐后疲劳。
关于人们饭后感到困倦的原因,科学家们有许多假设。
根据一项实验假设,困倦的原因之一与下丘脑有关。这个假设主要在动物身上进行了测试。
科学家认为几个下丘脑区域,例如视交叉上核 (SCN)、外侧下丘脑 (LH) 和下丘脑腹内侧核 (VMH),与睡眠、清醒和食物摄入的调节有关。
睡眠和进食之间有很强的双向互动。
我们知道,身体需要能量来运作和生存。人体从食物中获取能量,食物通过消化过程分解并转化为燃料或葡萄糖,然后大量营养素为身体提供能量。这个消化代谢过程触发体内的各种反应。
以下列举的每一种原因都可能与餐后疲倦有关,虽然每个原因都是不同的,但餐后疲劳可以由这些因素的任意组合引发。
01 糖和精制碳水化合物
单糖和精制碳水化合物会迅速分解成葡萄糖,这可能会引发更突然和明显的疲劳。
研究表明,高血糖会抑制控制清醒的食欲素。食欲素在下丘脑中最为活跃。
这里要提到orexin/hypocretin(食欲素/下丘脑分泌素)。
食欲素是一种调节清醒和食欲的神经递质。大脑在下丘脑中包含大约 10,000 到 20,000 个神经元,但这些神经元的轴突延伸到整个大脑和脊髓,那里也有食欲素的受体。
它有什么作用?
科学表明,大脑食欲素神经元刺激清醒、警觉、进食、寻求奖励和健康的葡萄糖平衡。食欲素被认为是迄今为止最重要的唤醒刺激剂。
因此,将白面包等精制碳水化合物换成高纤维(低升糖指数)碳水化合物对整体健康更好。
02 炎症和食物敏感性
研究人员认为,有些人饭后感到疲倦的另一个可能原因与炎症有关。TNF和IL-1b等炎性细胞因子似乎会抑制促进清醒的食欲素。

谷禾健康
韦荣氏球菌属(Veillonella)是革兰氏阴性厌氧性微小球菌,直径0.3~0.5μm,初期培植为革兰氏阳性,过夜转为阴性。光学显微镜下为双球状、片状和短链状,无荚膜,无鞭毛,无芽孢。最适生长温度37℃,最适pH6.5~8.0。
Veillonella该属的成员是非发酵的,它们无法使用碳水化合物或氨基酸,不发酵无法葡萄糖或任何其他碳水化合物(除了有一个种发酵果糖外)或氨基酸,但它们会积极发酵发酵丙酮酸、乳酸、苹果酸、富马酸和草酰乙酸。胰蛋白酶-葡萄糖-酵母提取物肉汤中的主要代谢终产物是乙酸和丙酸。能代谢乳酸产生丙酸、CO2和H2。一些物种产生一种缺乏卟啉的非典型过氧化氢酶。大多数菌株产生气体,如H2S。
在动物和人的自然腔道中大量存在,是分布于口腔、咽部、呼吸道、消化道的常见菌群。其粘附于表面或与其他细菌并形成生物膜的能力对于肠道和口腔微生物群组成和功能至关重要,尤其是在口咽和肠道中。 在一些严重的感染过程中,如菌血症、骨髓炎和心内膜炎,在各种混合感染中起作用。常从软组织脓肿及血液中检出。青霉素已被建议作为韦韦氏菌属病原体感染的治疗选择 。
Veillonella属最早于1898年被Veillon和Zuber分离。Prevot在1933年进一步描述了这些细菌,并提出了目前的分类法。
大多数Veillonella菌是从脓肿,吸入性肺炎,烧伤,叮咬和鼻窦中回收的。在95%例患者中感染是多菌种,但在5%例患者中,纯培养物中回收Veillonella。与该菌检出相关的诱因条件是先前的手术,恶性肿瘤,类固醇治疗,异物和免疫缺陷。。
已知的Veillonella属中已描述了超过10种。
人类样品分离出(齿状Veillonella denticariosi,Veillonella dispar,Veillonella montpellierensis,Veillonella rogosae 和 Veillonella tobetsuensis)
非人类动物样品分离出(Veillonella caviae,Veillonella criceti,Veillonella magna,Veillonella ratti和Veillonella rodentium)
Veillonella atenty 从人和其他动物来源分离出。
它们的表型特征,包括形态,主要代谢终产物,产气,硝酸盐还原和琥珀酸脱羧,这些菌株被鉴定为Veillonella属的成员。 多基因座序列分析和相应的系统发育基于16S rRNA,dnaK和rpoB基因,以及新近提出的gltA基因。
其中一个重要的菌种,小韦荣球菌(Veillonella parvula)在120年前,当Veillon和Zuber将其从阑尾炎脓肿中分离出来时被发现并被描述。六十年后,同样的微生物被用于第一次观察外膜(OM),从而证明了革兰氏阴性和革兰氏阳性细胞包膜结构之间的关键区别。目前在包括口腔、肺、胃肠道和阴道内的人体多个生态位中发现了Veillonella parvula菌。Veillonella parvula可能在许多环境中发挥重要作用,但其主要生态位是作为口腔中的第二殖民者。
与口腔疾病
Veillonella是牙周炎的重要病原体,是舌苔中的本土口腔细菌,而且Veillonella附着在舌头上的能力很高,已被确定为硫化氢(H2S)的主要生产者,H2S是口腔恶臭的主要成分之一。并且在1份报告中,它是慢性上颌窦炎中最常见的厌氧性病原体。
口腔生物膜是一个多物种的社区,敌对双方共存,以保持社区成员的生态平衡。 在早期的口腔生物膜形成的各个阶段中,Veillonella作为早期定居物种可以与许多细菌形成聚集,包括最初的定居者戈登链球菌和牙周病原体Fusobacter nucleatum。 除了为许多微生物提供结合位点外,Veillonella还能为牙周病原体的生存和生长提供营养。 这些发现表明,Veillonella在口腔生物膜的发育和人类口腔生态学中起着重要的“架桥”作用。
Veillonella和链球菌在生态系统(如口腔和结肠)中发生代谢相互作用并经常共生,共存可能部分取决于它们在代谢中的相互作用的潜力。链球菌属参与糖的发酵,产生乳酸作为其主要发酵终产物。反过来,Veillonella也以利用乳酸作为碳和能源的能力而闻名。
全世界龋齿的患病率仍然很高。 当牙齿暴露于产酸微生物通过碳水化合物代谢产生的酸(如乳酸)环境下时,就会引发龋齿。 Veillonella是主要的口腔微生物之一,由于它们具有将乳酸转化为弱酸并从NO3产生NO2的能力,而NO2可以抑制链球菌的生长和代谢。因此,Veillonella被认为对预防龋齿有好处。但是Veillonella代谢乳酸的能力受口腔环境因素(即pH和乳酸)的调节。
与免疫相关
肠道是肠道菌群与粘膜免疫系统相互作用的关键部位。近年来,人们发现Veillonella对人类微生物组,感染和免疫发育的重要影响。研究发现Veillonella parvula是细胞因子和TLR2 / 6信号转导的有效诱导。链球菌与韦永氏菌的组合似乎可以抵消IL-12p70的产生,同时增强IL-8,IL-6,IL-10和TNF-α的反应。
Veillonella的存在与疾病缓解或疾病稳定相关。这些特定的细菌属可能是免疫检查点抑制剂的生物标志物。在单抗治疗的患者中,或许它们可能成为晚期胃癌的特异性生物标志物。
一项研究指出对免疫治疗有响应的患者体内,富含屎肠球菌(Enterococcus faecium),产气柯林斯菌(Collinsella aerofaciens),青春双岐杆菌(Bifidobacterium adolescentis),肺炎克雷伯菌(Klebsiella pneumonia),小韦荣球菌(Veillonella parvula), Parabacteroides merdae, 乳酸杆菌(Lactobacillus species)和长双歧杆菌(B longum)8个菌种。
最近的数据表明,Veillonella parvula可能在儿童早期免疫系统发育中起到保护作用和帮助作用。对婴儿的流行病学研究表明,Veillonella parvula的存在与哮喘、毛细支气管炎和自闭症呈负相关。在有哮喘风险的儿童中,肠道中相对丰富的细菌属Veillonella的相对丰度显著降低。
Prevotella 作为革兰氏阴性菌,产生 LPS 进而诱发炎症反应。与此同时,该菌代谢产生的丙酸盐可以发挥抗炎症的作用。产生相互矛盾的结论背后或许是由于肠道微环境以及菌群构成的不同所导致的。当在肠道中 Veillonella 与唾液链球菌菌株 1 共培养时可降低炎性细胞因子的产生,而与菌株 2 共培养时炎性细胞因子的产生比各自单独培养时显著增加。
链球菌 和Veillonella在肠道微生物群的高丰度和种内遗传多样性,可能是这些菌对由于食物摄入量变化引起的营养物利用率变化而引起的高种群动态的主要驱动因素。这些动态的种群可能会深刻影响当地宿主与微生物之间的相互作用,从而调节肠道的生理和免疫系统功能。
与运动耐力相关
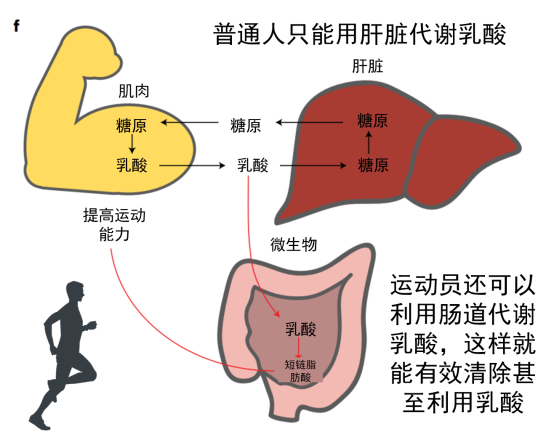
当我们跑步速度较慢时,糖和脂肪可以充分氧化分解成二氧化碳和水,并提供能量。但是,高强度运动后往往会出现肌肉酸痛现象,这是因为运动超过了有氧运动强度,导致葡萄糖通过无氧呼吸在体内代谢产生了乳酸,乳酸堆积会引起局部肌肉酸痛。
体内堆积的乳酸一部分继续分解成丙酮酸,再进一步被分解为二氧化碳和水,一部分则进入肝脏,乳酸可以再次合成糖原,这个过程称为糖异生。
Scheiman及其同事发表在《自然医学》(Nature Medicine)上文章研究了肠道微生物组对精英跑步者运动表现的影响,并确定了属于Veillonella属的一种能增强性能的微生物。比赛结束后,马拉松长跑运动员中富集了非典型的Veillonella atypica菌种。Veillonella 利用乳酸作为碳源, 分析发现乳酸到丙酸的代谢通路的运动后运动员中富集。
图片来源:慧跑
与其他厌氧菌不同,Veillonella atypica具有通过三羧酸循环的乳酸代谢的完整途径。Veillonella细菌可以将乳酸变成丙酮酸,而且体内产生的乳酸可以穿过上皮屏障进入肠腔,也就是说运动中体内积累的乳酸可以运输到肠道,肠道中的veillonella细菌就可以分解乳酸了。
在这个过程中,会产生丙酸,而丙酸可以提高小鼠心率和氧气利用率,丙酸还可以促进人体的新陈代谢。为了验证丙酸是否可以改善运动性能,研究人员给一些小鼠使用丙酸灌肠。与喂食Veillonella atypica 菌株的小鼠相同,这些使用丙酸灌肠的小鼠的运动时间也明显增加了。科学家们还给小鼠注射了可以追踪的乳酸,发现这些乳酸会进入到肠道。 而且乳酸有助于这种微生物的生长。
总的来说,葡萄糖因肌肉运动产生乳酸,一部分乳酸通过血液循环进入肝脏,在肝脏中通过糖异生作用重新合成葡萄糖;一部分乳酸通过血液循环进入肠道,肠道中的Veillonella属细菌迅速将乳酸分解成丙酸,从而降低乳酸浓度,改善运动表现。
哺乳动物肠道微生物组可能会通过肌肉衍生的乳酸代谢为丙酸酯来为其宿主提供额外的跑步耐力能力提升。 此外,由于在多个独立的人体研究中,相对于久坐的控制者,经常运动者中的Veillonella菌增加了,这增加了这些微生物通过利用独特的代谢环境(L-乳酸代谢)而在运动员的肠道中具有适应性优势的可能性。 这可能会导致积极的反馈循环,从而以较小的能力加强锻炼。 换句话说,由于预期重复运动会导致肠道L-乳酸浓度增加,L-乳酸代谢物的代谢位扩大,因此,这些L-乳酸代谢物反过来有望提高运动的耐力。
与其他疾病
原发性硬化性胆管炎
原发性硬化性胆管炎(PSC)是一种罕见的、以肝内外胆管受损为主要特征的原发疾病,易导致胆管炎症和肝纤维化的发生而原发性硬化性胆管炎。
PSC患者肠道菌群某些菌群丰富度也会产生相应变化。特别是韦荣球菌(Veillonella)、肠球菌(Enterococcus)和链球菌(Streptococcus),其丰度显著升高。Veillonella可以通过肠道淋巴细胞进入肝脏。而肠球菌则是一种对万古霉素敏感的细菌,它可以通过分泌金属蛋白酶分解上皮钙黏蛋白破坏肠屏障。
肝病
在NAFLD和NASH中有几项研究确定,随着纤维化的进展,微生物群结构和功能恶化。晚期纤维化和NASH与碳水化合物和脂质代谢的变化有关,因为他们观察到相应功能的细菌含量增加。酒精性肝炎患者或肝脏疾病患者中Veillonella和Enterococcus丰度显著增加,而Veillonella parvula的丰度与白蛋白和血小板计数呈负相关。事实上,在所有3项肝硬化研究中,患者体内的几种Veillonella species的丰度都发生了改变。
肺癌
与对照组相比,肺癌患者的口腔菌群增加,特别是Streptococcus和Veillonella。口腔菌群的增加与PI3K和ERK上调有关。在体外实验中,气道上皮细胞暴露于Veillonella,Prevotella和Streptococcus也会导致ERK和PI3K通路上调(Tsay et al,2018)。PI3K通路被认为是肺癌发生的早期事件,因此共生微生物群失调会上调该通路促进肺癌发生。
胰腺癌
结果显示患有胰腺癌的病人组中三种口腔微生物Streptococcus,Treponema和Veillonella的组分显著低于其他组别。
其他
子痫前期患者会富集 Fusobacterium, Veillonella,Clostridum 等这些细菌。剖腹产的新生儿粪便微生物群富含Veillonella dispar/V这表明皮肤、口腔微生物以及出生过程中周围环境中的细菌是第一批在这些婴儿中定殖的细菌。
与对照组相比,后发展为T2D的研究对象Veillonella dispar的丰度较低,结果表明肠道菌群中的该物种可能与参与宿主血糖调节。
在肥胖的男性中观察到韦荣氏球菌属(Veillonella)和产甲烷短杆菌属(Methanobrevibacter)高于女性。 在吸烟人群中,Veillonella dispar的脂多糖生物合成通路相关的基因出现频率较高。
口腔,捏着呼吸道的脉搏,牙好胃口好,也不是句空话。Veillonella作为口腔和肠道的重要“居民”,它的定植,丰度以及与其他菌落共存的能力决定和影响着人体的口腔和消化道甚至肝肺胃疾病。
相关阅读:
主要参考文献:
Yu Sunakawa, et al. Genomic pathway of gut microbiome to predict efficacy of nivolumab in advanced gastric cancer: DELIVER trial (JACCRO GC-08). ASCO GI. Jan 15-17, 2021. ABSTRACT 161.
Jackson, M.A., Goodrich, J.K., Maxan, M.-E., Freedberg, D.E., Abrams, J.A., Poole, A.C., Sutter, J.L., Welter, D., Ley, R.E., Bell, J.T. et al. (2015) Proton pump inhibitors alter the composition of the gut microbiota. Gut, 65, 749-756.
Shi, Y.-C., Cai, S.-T., Tian, Y.-P., Zhao, H.-J., Zhang, Y.-B., Chen, J., Ren, R.-R., Luo, X., Peng, L.-H., Sun, G. et al. (2019) Effects of Proton Pump Inhibitors on the Gastrointestinal Microbiota in Gastroesophageal Reflux Disease. Genom Proteom Bioinform, 17, 52-63.
Bajaj, J.S., Acharya, C., Fagan, A., White, M.B., Gavis, E., Heuman, D.M., Hylemon, P.B., Fuchs, M., Puri, P., Schubert, M.L. et al. (2018) Proton Pump Inhibitor Initiation and Withdrawal affects Gut Microbiota and Readmission Risk in Cirrhosis. 113, 1177-1186.
Wang L, Yu X, Xu X, Ming J, Wang Z, Gao B, Xing Y, Zhou J, Fu J, Liu T, Liu X, Garstka MA, Wang X and Ji Q (2021) The Fecal Microbiota Is Already Altered in Normoglycemic Individuals Who Go on to Have Type 2 Diabetes. Front. Cell. Infect. Microbiol. 11:598672. doi: 10.3389/fcimb.2021.598672
Wong-Rolle A, Wei HK, Zhao C, Jin C. Unexpected guests in the tumor microenvironment: microbiome in cancer. Protein Cell. 2020 Dec 9. doi: 10.1007/s13238-020-00813-8. Epub ahead of print. PMID: 33296049.
Metagenomic analysis of bacterial species in tongue microbiome of current and never smokers 03-13, doi: 10.1038/s41522-020-0121-6
Scheiman J, Luber JM, Chavkin TA, MacDonald T, Tung A, Pham LD, Wibowo MC, Wurth RC, Punthambaker S, Tierney BT, Yang Z, Hattab MW, Avila-Pacheco J, Clish CB, Lessard S, Church GM, Kostic AD. Meta-omics analysis of elite athletes identifies a performance-enhancing microbe that functions via lactate metabolism. Nat Med. 2019 Jul;25(7):1104-1109. doi: 10.1038/s41591-019-0485-4. Epub 2019 Jun 24. PMID: 31235964; PMCID: PMC7368972.
Djais AA, Theodorea CF, Mashima I, Otomo M, Saitoh M, Nakazawa F. Identification and phylogenetic analysis of oral Veillonella species isolated from the saliva of Japanese children. F1000Res. 2019 May 3;8:616. doi: 10.12688/f1000research.18506.5. PMID: 31448103; PMCID: PMC6688723.
Mashima I, Theodorea CF, Djais AA, Kunihiro T, Kawamura Y, Otomo M, Saitoh M, Tamai R, Kiyoura Y. Veillonella nakazawae sp. nov., an anaerobic Gram-negative coccus isolated from the oral cavity of Japanese children. Int J Syst Evol Microbiol. 2021 Jan;71(1). doi: 10.1099/ijsem.0.004583. Epub 2020 Dec 2. PMID: 33263509.
Rovery C, Etienne A, Foucault C, Berger P, Brouqui P. Veillonella montpellierensis endocarditis. Emerg Infect Dis. 2005 Jul;11(7):1112-4. doi: 10.3201/eid1107.041361. PMID: 16022792; PMCID: PMC3371781.
Maqsood A. Bhatti, Michael O. Frank, Veillonella parvula Meningitis: Case Report and Review of Veillonella Infections, Clinical Infectious Diseases, Volume 31, Issue 3, September 2000, Pages 839–840, 0人