 国家高新企业 | ISO9001认证
国家高新企业 | ISO9001认证 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com

谷禾健康
粪菌移植是一项近年来备受关注的医疗技术,它涉及将健康捐赠者的粪便物质转移至患有疾病或障碍患者的胃肠道。

简单来说就是选择健康合适的人粪便,通过科学方法提取出有用的微生物,去除有害与无用的部分,然后制成制剂,给病人口服或者直接注入肠道,目的是恢复健康的肠道微生物群并改善整体健康状况。
粪菌移植的历史悠久
粪菌移植在传统中医中已有数百年的应用,粪菌移植的第一个记录可以追溯到四世纪的中国,当时人类粪便被称为黄汤,用于治疗严重腹泻的患者。
15到16世纪的中国明朝,有关于将新鲜或发酵的粪便悬浮液用于治疗腹泻、便秘和腹痛等胃肠道疾病的记载。
但直到20世纪50年代晚期,它才首次用于现代医学,以治疗由抗生素耐药菌引起的严重腹泻。
在20世纪80年代和90年代,粪菌移植主要用于治疗反复发作的艰难梭菌感染。然而,随着肠道微生物群的发现及其在健康和疾病中的作用,粪菌移植开始被探索作为治疗其他疾病的潜在方法,包括炎症性肠病、肠易激综合征甚至神经系统疾病等。

粪菌移植在未来拥有巨大前景
近年来,粪菌移植受到医学界和公众越来越多的关注,许多临床试验和研究正在进行,以评估其疗效和安全性。
粪菌移植的疗效已经在多种肠道疾病中得到证实,如艰难梭菌感染、肠炎、炎症性肠病等。粪菌移植的出现,为肠道微生物失调带来了新的治疗思路和方法,也为人类健康提供了新的希望。
随着我们对肠道微生物群研究的不断发展,粪菌移植很可能成为治疗其他疾病越来越重要的工具。谷禾在本文中将为大家介绍粪菌移植。
粪便微生物群移植 (粪菌移植) 是一种医疗程序,涉及将粪便从健康供体转移到受体的胃肠道中。已发现粪菌移植可有效治疗各种胃肠道疾病,包括艰难梭菌感染、炎症性肠病和肠易激综合征。
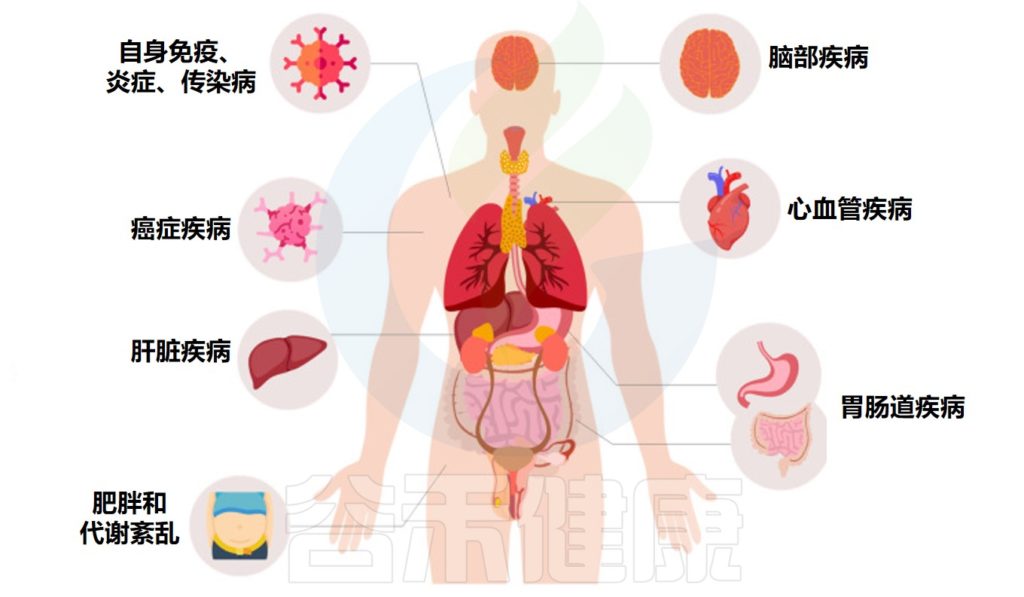
来自大量临床试验的数据表明,粪菌移植也可能对许多其他疾病具有治疗潜力,从胃肠道到肝脏疾病,神经系统疾病、自身免疫性疾病、皮肤疾病、心血管疾病、脑部疾病、肥胖和代谢综合征。
根据这些相关研究,谷禾带大家了解粪菌移植在治疗人体疾病中的作用。
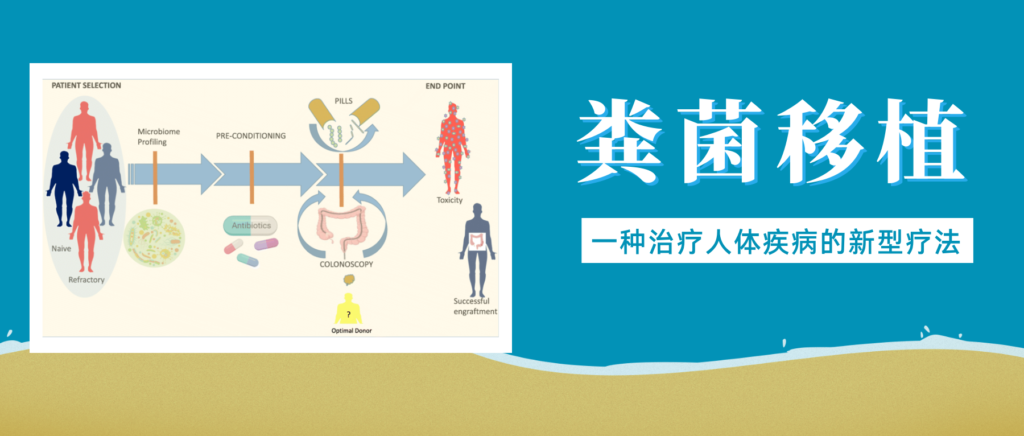
人类疾病中的粪菌移植
Biazzo M,et al.J Clin Med.2022
▼
粪菌移植主要用于治疗反复发作的艰难梭菌感染(CDI),这是一种细菌感染,会引起严重的腹泻和结肠炎症。
√粪菌移植对治疗艰难梭菌感染特别有效
研究表明,粪菌移植在治疗复发性艰难梭菌感染方面特别有效,已发现粪菌移植在治疗艰难梭菌感染方面的成功率超过90%,而且几乎没有副作用。
▼
粪菌移植已被证明是治疗多种胃肠道疾病的有效方法,包括炎症性肠病(IBD)、肠易激综合征(IBS)。
炎症性肠病是一种复杂的炎症和慢性疾病,其特征是免疫失调,最终导致消化道免疫介导的损伤,包括溃疡性结肠炎(UC)和克罗恩病(CD)。肠道微生物群失调被认为是炎症性肠病发展中的关键调节事件,因此粪菌移植代表了一种可能的治疗策略。
√缓解溃疡性结肠炎患者症状
最近一项随机对照试验的荟萃分析发现,粪菌移植可有效诱导溃疡性结肠炎患者症状缓解,缓解率为36%,而对照组仅为9%。对核糖体 16S RNA 的分析表明,粪菌移植后微生物多样性增加并持续存在。
对活动期溃疡性结肠炎的儿科患者(4至17岁)进行了随机临床试验。粪菌移植组中92%的患者在第6周实现了小儿溃疡性结肠炎活动指数的改善(与安慰剂组的50%相比)。
√短期内改善了克罗恩病患者症状
评估了25名患有腹腔内炎症性肿块的克罗恩病患者使用多种新鲜粪菌移植(初始粪菌移植随后每三个月重复粪菌移植)的疗效和安全性。
超过一半的患者在第一次粪菌移植后三个月表现出临床反应的缓解,这一比例在12个月和18个月时有所下降。
注:这表明尽管粪菌移植在短期内缓解了临床症状,但未能产生持久的临床效果。
√对肠易激综合征有积极影响
六项不同的临床试验发现粪菌移植对肠易激综合征症状有积极影响:
(1) 在一项只有10名患者入组的小型临床试验中,在粪菌移植后4周,6 名患者有所改善;有趣的是,作者发现报告改善的患者接受了来自双歧杆菌含量高于无效供体的粪菌移植,这表明富含双歧杆菌的粪便供体可能是粪菌移植成功的预测因素。
(2)观察到65%的患者在通过结肠镜检查接受粪菌移植治疗三个月后症状缓解以及粪菌移植之后微生物特征向供体特征的转变,包括增加的α和β多样性。
(3)报告了腹泻型肠易激综合征患者的症状和生活质量的改善,这些患者通过胃镜接受新鲜粪便,并且(在连续分析中)增加了短链脂肪酸。
(4)报告显示,在接受来自健康供体(同种异体移植)或来自他们自己(自体移植)的粪便材料的患者中,肠易激综合征症状出现短暂改善;接受同种异体移植的患者抑郁评分有所下降。
(5)使用仅从一名健康、特征良好的供体获得的粪便样本通过胃镜粪菌移植治疗肠易激综合征患者,发现了疲劳和生活质量的改善以及细菌微生物群概况的变化、粪便短链脂肪酸的变化。
(6)在最近的一项临床试验中,招募了难治性肠易激综合征患者,主要是腹胀,并通过鼻空肠给药接受一次粪菌移植治疗;粪菌移植一年后,56%的患者报告肠易激综合征症状和生活质量有所改善。
▼
复发性肝性脑病是肝硬化的并发症(与饮酒无关),由肝功能衰竭和肠-肝-脑轴受损引起,可导致意识障碍和昏迷 。
√粪菌移植改善肝性脑病患者认知和微生态失调
粪菌移植最近被研究为一种可能的新治疗工具。第一项试验描述,通过灌肠递送的单一粪菌移植在短期内减少了肝性脑病患者的住院时间,改善了他们的认知和微生态失调。
粪菌移植治疗后一年内,与对照组相比,降低了住院率并改善了认知功能。
√粪菌移植展现出肝病的治疗潜力
广泛的研究支持粪菌移植作为一种控制肝病的疗法。粪菌移植改善了高脂肪饮食引起的肝损伤和脂质代谢,同时增加了小鼠肠道微生物群的多样性。来自对酒精性肝病有抵抗力的供体小鼠的粪菌移植可以预防酒精性肝损伤。
此外,粪菌移植已经用于慢性肝病患者。最近一项针对严重酒精性肝炎患者的初步研究表明,粪菌移植与存活率提高和腹水消退有关。
▼
多项研究探索了粪菌移植在治疗神经系统疾病方面的潜在益处,例如帕金森病、多发性硬化症和自闭症谱系障碍。
√改善帕金森病患者症状
发表在《神经病学》杂志上的一项研究发现,粪菌移植改善了帕金森病患者的症状,如便秘和睡眠障碍。
在帕金森病小鼠模型中,来自正常小鼠的粪菌移植可以减少黑质的病理特征并减轻身体损伤。
√改善多发性硬化症患者症状
发表在《神经炎症杂志》上的另一项研究发现,粪菌移植改善了多发性硬化症患者的症状,例如疲劳和抑郁。
√影响抑郁症、阿尔兹海默症状态
此外,来自重度抑郁症患者的粪菌移植在正常小鼠中诱导了抑郁症的行为/生理特征。
最后,在阿尔茨海默病小鼠模型中,源自正常对照小鼠的粪菌移植改善了认知功能。
▼
除神经系统疾病外,粪菌移植在治疗其他非胃肠道疾病(如肥胖、糖尿病和代谢综合征)方面也显示出前景。
√改善代谢综合征患者胰岛素敏感性
几项临床试验研究了粪菌移植对代谢综合征患者的的影响,显示出改善:报告说,患有代谢综合征的男性参与者接受了来自健康人群的肠道微生物群输注六周后胰岛素敏感性增加。
研究人员概括了关于胰岛素抵抗增加的发现,并补充说它取决于粪菌移植后肠道微生物群的变化。
最后,与移植正常供体粪便的受试者相比,使用代谢综合征供体粪便移植肥胖和胰岛素抵抗的男性受试者时,胰岛素敏感性降低,从而显示代谢综合征中胰岛素敏感性和微生物群之间的因果关系。
发表在《胃肠病学》杂志上的一项研究也发现,粪菌移植改善了代谢综合征患者的胰岛素敏感性。
注:代谢综合征是糖尿病的前兆。
除了这些已经确定的应用,粪菌移植还有一些新兴的用途。例如,粪菌移植被探索作为治疗肥胖和2型糖尿病的潜在方法。
▼
在过去的几年中,肠道微生物群在致癌过程中的作用已得到越来越多的认可。肠道微生物失调和个别细菌可以通过激活致瘤途径、诱发炎症和破坏宿主DNA来诱发癌症或影响癌症进程。
细菌影响癌症的具体机制
几种细菌拥有或产生促进β-连环蛋白与E-钙粘蛋白分离的蛋白质,激活参与癌发生的β-连环蛋白信号通路。
肠道生态失调导致细菌衍生的短链脂肪酸的产生减少。肠道生态失调通过Toll 样受体 (TLR) 的微生物相关分子模式发挥促炎作用,增加细胞产生促炎因子,从而增加致癌作用。
除了诱发炎症外,许多细菌还能够通过释放特定代谢物来破坏DNA,从而促进癌症进展。
β-连环蛋白(β-catenin)是一种细胞骨架蛋白,主要位于细胞膜,在乳腺上皮中,β-catenin游离量较少,通过介导与E-cadherin的相互作用,将细胞外黏附因子与细胞质内细胞骨架相互连接,以保持质膜的完整性,并参与细胞的黏附、迁徙与转移等过程。
β-catenin异常表达时脱离细胞间连接进入细胞质或细胞核,将失去介导细胞间链接、黏附的功能,并引起某些癌基因的表达,导致细胞癌变、转移。
β-catenin还是介导Wnt信号传导的关键分子,其在细胞核中决定着Wnt信号通路的开放或关闭,通过调节基因表达过程,在乳腺发育以及肿瘤发生的调控中起到了重要的作用。
细胞膜中β-catenin的丢失以及细胞质、细胞核中β-catenin的高表达都可以经过不同的调节途径独立发生,诱导乳腺癌的发生,并影响乳腺癌的预后。
E-钙粘蛋白(E-cadherin)是钙黏蛋白家族成员,在上皮细胞中连接细胞骨架与细胞外环境,参与细胞信号传导。在正常乳腺组织中,E-cadherin在肌上皮中呈颗粒状膜阳性,在腺上皮细胞中呈细胞膜强阳性,是区分DCIS和小叶原位癌的标志物;E-cadherin几乎在所有的DCIS细胞上呈线状膜染色,而小叶原位癌的细胞膜大多不表达E-cadherin。
令人惊讶的是,特定的微生物群物种具有调节癌症治疗的功效,显著影响癌症患者的临床预后。
√粪菌移植有助于治疗黑色素瘤
黑色素瘤是一种皮肤癌,涉及产生黑色素的黑色素细胞。最近,新工具利用免疫检查点抑制剂来增强患者对肿瘤的免疫反应(这种治疗方法称为“癌症免疫疗法”),并且有趣地发现肠道微生物组调节这种反应。
注:谷禾前面的文章中也有讲过癌症免疫疗法。
在两个具有不同肠道微生物组成的小鼠中,黑色素瘤的生长及其对抗程序性死亡配体1(PD-L1)免疫疗法的反应显著不同。
如果将来自对抗PD-1治疗有积极反应的黑色素瘤患者的粪便样本移植到无菌小鼠体内,则PD-1阻断的抗肿瘤作用会得到改善。
粪菌移植似乎有望通过转移有利的肠道微生物群来增强黑色素瘤患者的抗肿瘤免疫力。
通过粪便微生物群移植治疗癌症
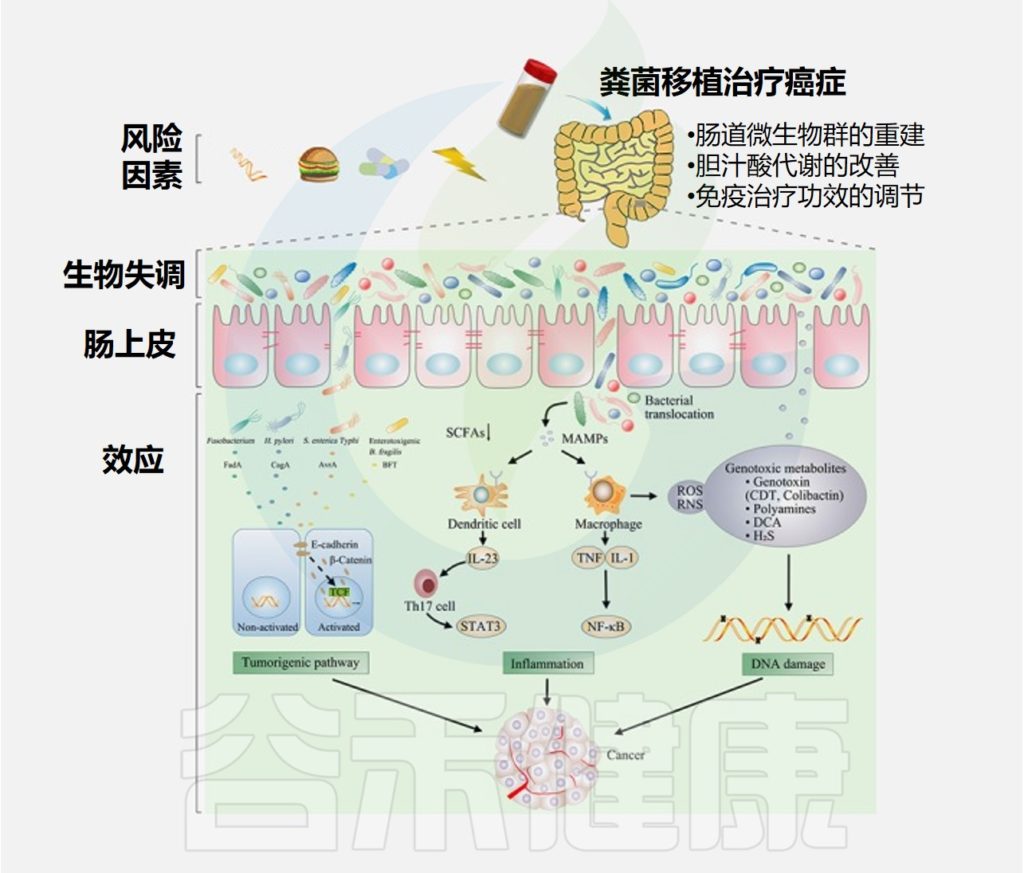
Chen D,et al.Int J Cancer.2019
▼
根据最近的研究,粪菌移植可能是治疗各种皮肤病症(包括湿疹和牛皮癣)的潜在治疗选择。人体肠道微生物群在免疫调节中起着至关重要的作用,肠道微生物群的改变与各种皮肤病有关。
一些案例报告了湿疹和牛皮癣患者经粪菌移植后成功治疗。
√改善了牛皮癣患者的严重程度
在研究皮肤病学杂志上发表的一项研究中,研究人员发现粪菌移植改善了四分之三的牛皮癣患者的严重程度。
√湿疹症状有了显著改善
此外,发表在美国皮肤病学会杂志上的一项研究报告说,粪菌移植使三分之二的患者的湿疹症状有了显著改善。
总之,粪菌移植显示出作为治疗湿疹等皮肤病的巨大潜力。同样重要的是要注意粪菌移植具有潜在的风险,包括感染和不良反应。
需要更多的研究来确定粪菌移植治疗皮肤病的最佳频率和剂量。因此,在考虑将其作为皮肤病的治疗选择之前,必须彻底评估粪菌移植的潜在益处和风险。
▼
关于微生物群和粪菌移植干预在心血管疾病中的作用,只有有限的证据可用,而且大多是在动物模型中获得的。
√菌群影响房颤的易感性
最近提出了老年人肠道菌群失调在房颤发病机制中的因果作用。研究表明,将患有心房颤动的老年大鼠粪菌移植移植到年轻大鼠体内会导致更高水平的脂多糖和更高的疾病易感性。
√菌群移植改善了心肌损伤
仍然在动物模型中,实验性自身免疫性心肌炎(EAM)小鼠模型中对照小鼠的粪菌移植增加了微生物的丰富度,包括厚壁菌门/拟杆菌门的比例增加,并且由于炎症减轻而改善了心肌损伤。
尽管科学文献中很少有证据表明粪菌移植策略在心血管疾病中有治疗价值,但在动物模型和人类中获得的这些数据肯定会为进一步研究提供坚实的基础。
本章小结
未来,粪菌移植也可能用于治疗自身免疫性疾病,如类风湿性关节炎和红斑狼疮,以及精神健康状况,如抑郁症和焦虑症。
值得注意的是,这些新兴应用仍处于研究的早期阶段,需要进一步的研究来确定它们的疗效和安全性。
总的来说,目前粪菌移植主要用于治疗反复发作的艰难梭菌感染和一部分胃肠道疾病,但它在治疗其他疾病和障碍方面具有巨大的潜力,正在进行研究探索其在各个医学领域的潜在应用。
▼
移植所需的粪菌来自经过严格筛查的供体,供体捐赠样本后,用一套全自动化的机器进行分离,经过注水、搅拌、过滤、离心、沉淀等步骤,得到纯化的细菌。
粪便菌群移植过程示意图
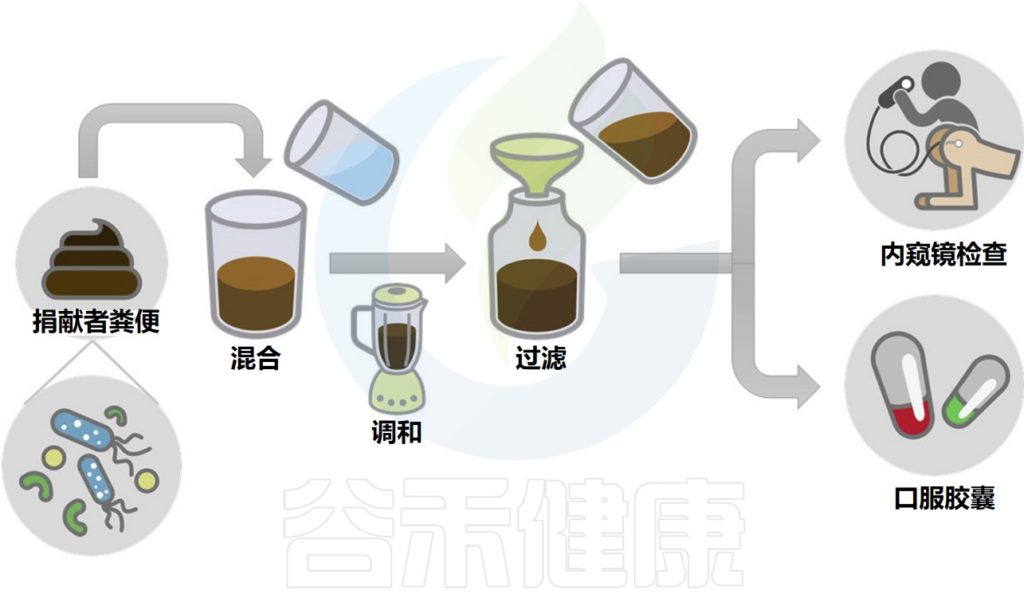
Wang JW,et al.J Formos Med Assoc.2019
其中单单过滤的步骤就要重复数次,每一道过滤用的滤网孔径都比前一道滤网的孔径更小,最后一道滤网的孔径只有0.07毫米,基本上可以把所有的杂质去除,只剩下细菌这些微生物。
分离出来的粪菌再用生理盐水制成混悬液供移植使用。
▼
“移植”过程不是简单粗暴的将一个人的粪便直接注入患者的肠道,主要是将健康供体的粪便离心纯化,获得功能菌,然后通过上消化道、中消化道和下消化道转移至受体肠道。从而重建稳定的肠道微生态环境,缓解相关症状,治疗疾病。
★ 粪菌移植的途径与治疗目的有相关性
例如,想要治疗溃疡性结肠炎可以采取经结肠镜灌肠。要治疗慢性乙型肝炎,则是经上消化道,可以采取:经麻醉胃镜、普通胃镜、经鼻饲管,或者用粪菌胶囊,经典方式是通过麻醉胃镜。
粪便微生物群移植的方法
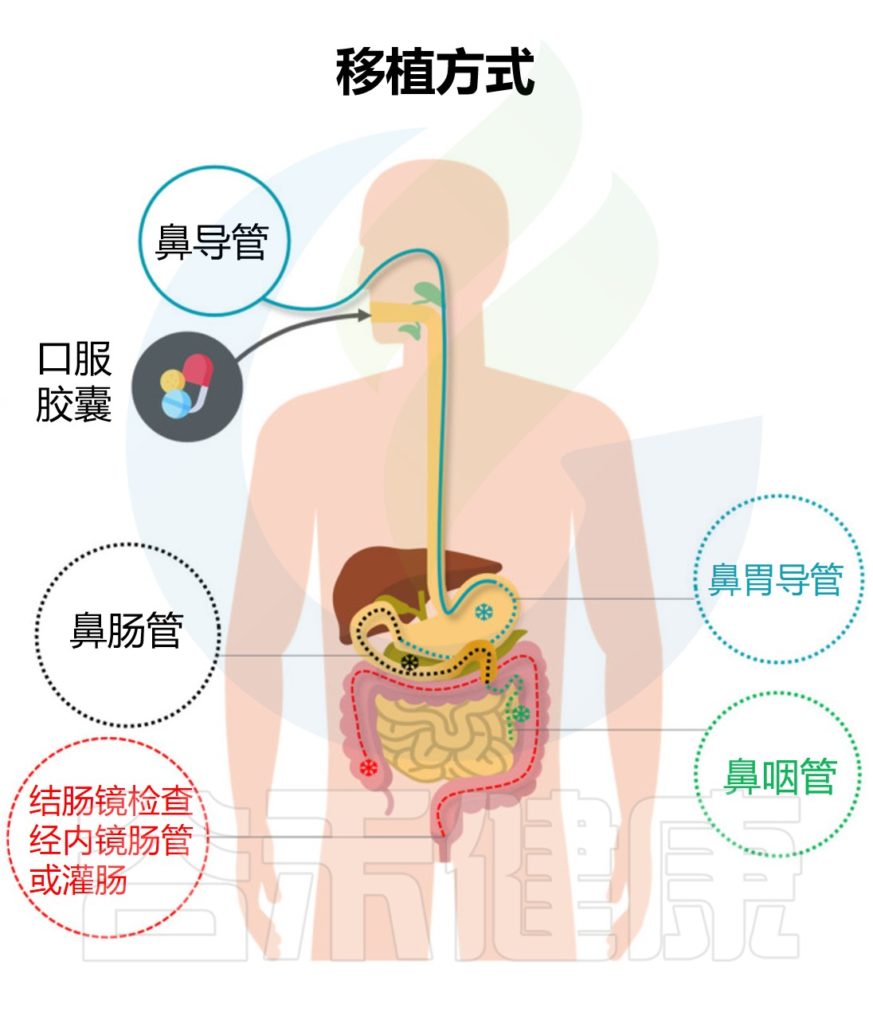
Biazzo M,et al.J Clin Med.2022
不同的粪菌移植方式具有各自的优缺点,下面谷禾具体来讲述经不同部位消化道进行粪菌移植的特点。
▸ 上消化道
操作简单,总体风险较低
上消化道途径中,口服给药和鼻胃管应用广泛,操作简单,总体风险较低。但在此过程中,可能会因菌液反流或吸出而导致窒息,如果机体本身存在梗阻,则移植的菌液可能无法准确到达肠道。
其中,口服途径主要指包封粪菌材料,通过将提取的粪菌与冷冻保护剂(主要是甘油)混合制备,然后进行多重包装以保护粪菌移植材料免受胃肠道环境的影响。同时,操作人员可以根据预期的释放位置进一步选择胶囊壳的材料。目前,市售的胶囊壳通常针对胃或结肠的释放,并被配制以确保细菌的存活率和定植。
降低潜在疾病传播的概率
此外,在制作胶囊的过程中,也可以去除无症状供体中可能存在的真菌、寄生虫、病毒和部分炎症介质,以降低潜在的疾病传播概率。
总的来说,通过上消化道途径的粪菌移植具有无需昂贵器械、重复使用对患者损伤小、患者耐受性好等优点。该途径适用于不能耐受鼻肠管和胃镜移植的患者,以及需要口服定制菌的患者。
▸ 中消化道
减少移植时的细菌位移
中消化道途径主要是指鼻肠移植和经内镜肠道植管术,能够实现全肠道给药。其中鼻肠管通过导丝拉伸拉直,在胃肠蠕动正常的情况下自动通过幽门,进一步减少粪菌移植时的细菌移位。
在一项随机对照试验中报道,通过鼻肠管的粪菌移植优于单独使用万古霉素治疗艰难梭菌感染,但粪菌移植组患者也出现了腹泻、痉挛和便秘等不良事件。
什么是经内镜肠道植管术?
经内镜肠道植管术(TET)具体指的是在内镜下辅助植入固定管并固定在肠道深处,同时外端沿肠道与外部相通。TET主要包括结肠途径介导的TET和中胃肠道途径介导TET。
结肠通路介导的TET需要应用结肠镜检查,并且使用这种途径进行重复粪菌移植是昂贵的。相比之下,中胃肠道途径介导的TET更方便,更容易维持。
由于中胃肠道介导的TET不需要在内镜手术后通过X射线或其他医疗仪器进一步确认肠道位置,对于无法进行结肠镜检查肠道准备的患者,或需要重复粪菌移植的患者,中胃肠道中介导的经内镜肠道植管术也是主要选择。
▸下消化道
下消化道通路主要指灌肠、结肠镜检查、结肠通路介导的经内镜肠道植管术等操作。
灌肠侵入性较小且相对简单
其中,灌肠是一种侵入性较小且相对简单的操作。灌肠法患者耐受性好,不需要昂贵的器械,有效降低了手术风险。但这种方法需要将输注的粪悬液保留较长时间,患者保持仰卧位以减少粪便排泄,同时反复灌肠易于被患者接受。
注意:粪菌移植的细菌是否可以通过灌肠的方式保留在肠段的命题尚不明确,而且这种方式也伴随着无法到达结肠和脾曲的风险,需要多次灌注才能获得疗效和更长的手术时间,以弥补肠道菌群保留率低的缺陷。同时,由于细菌液的滞留,这种方法可能不适用于肛门括约肌松弛或尿失禁的患者。
此外,在结肠镜检查和结肠通路介导的经内镜肠道植管术方面,它具有多种优势,主要包括:
(1)能够完整显示结肠和活检可疑组织的情况,有利于疾病的诊断、识别和分期;
(2) 允许操作人员直接评估肠道炎症,并在适当的部位注入足量的供体粪便细菌;
(3) 可将肠道菌群准确移植到受影响的肠段,并进一步将细菌保留在目标肠段;
(4)可以准确地输入足量的供体粪便菌,可以在一定程度上提高治疗效率。
然而,这些手术也伴随着部分不良事件,包括加重肠道反应。
粪菌移植的主要操作方式及优缺点


Zhang YW,et al.J Bone Miner Metab.2022
▼
粪菌移植的安全性主要与两方面因素有关,即供体的生物安全性、移植的操作安全性。
•供体的生物安全性
供体不仅要筛查排除乙肝、丙肝、梅毒、艾滋病、这些已知传染病,还要排除寄生虫、条件致病菌感染,甚至连饮食习惯、排便习惯、情绪状态、肿瘤家族史都要进行调查,不符合要求的都要排除。
供体的筛查可以说是“百里挑一”,要成为一个合格的供体是非常困难的。所有这些筛查工作都是为了保证供体的生物安全性。
•移植的操作安全性
移植的操作安全性主要与移植的方式有关。经胃镜、结肠镜的移植操作风险与常规胃镜、结肠镜检查的风险基本一致。
注:在后面的章节我们会详细讲述粪菌移植操作的具体要求。

为了评估粪菌移植的安全性,上海同济粪菌移植工作组主任等研究人员对8547名采用过粪菌移植的患者进行跟踪研究,得出以下结论:
1、回顾性分析数据表明,粪菌移植的短期和长期(从2周到5年)安全性都是比较好的,患者不要担心;
2、短期不良事件与粪菌移植给药方法有关,多为轻中度、较短暂,包括恶心、呕吐、腹泻等,只有42名(0.5%左右,很低比例)患者发生胃肠症状恶化;
3、长期随访期间的新发疾病主要是胃肠道和呼吸道疾病,发病率与一般人群无异;
4、 随访期间无粪菌移植相关感染传播事件,11例死亡与粪菌移植无关;
5、通过规范适应症和给药时机后,短期安全性和患者满意度升高。
所以,粪菌移植还是比较安全的。
粪菌移植已被证明是治疗多种胃肠道疾病的有效方法,然而,粪菌移植的潜在长期影响以及粪菌移植的最佳频率和剂量仍未得到很好的了解。
本章节旨在回顾有关粪菌移植潜在长期影响的现有文献,并为未来的研究和临床实践提供建议。
▼
虽然粪菌移植已被证明在短期内有效,但对粪菌移植长期影响的研究有限,粪菌移植对肠道微生物组和整体健康的长期影响仍不清楚。
✦可能导致抗生素抗性基因的转移
粪菌移植是一种医疗程序,它将健康捐赠者粪便中的微生物移植到受体的肠道中,以恢复或改善肠道微生物平衡。虽然粪菌移植已被证明在治疗某些疾病方面非常有效,但它的使用也存在一定争议。
一些研究表明,粪菌移植可能会产生意想不到的后果,例如抗生素抗性基因的转移或致病菌的引入。
✦病毒或其他感染因子可能通过粪菌移植传播
此外,人们还担心病毒或其他感染因子可能通过粪菌移植传播。需要更多的研究来充分了解粪菌移植的长期影响,并制定安全有效地使用该程序的指南。
▼
✦粪菌移植的监管
粪菌移植的监管因国家而异,一些国家如美国对其使用采取更为严格的方法。在美国,粪菌移植被美国食品药品监督管理局作为生物制品进行监管,只批准用于治疗未对其他治疗方法产生反应的复发性艰难梭菌感染。
在欧洲,粪菌移植通常被视为医疗程序,并由国家卫生部门进行监管。
✦粪菌移植的伦理问题
粪菌移植的伦理考虑包括知情同意、捐赠者选择以及对捐赠者和受体的潜在风险。捐赠者必须接受广泛的筛查,以确保他们健康且没有传染病,并且必须同意他们的粪便用于粪菌移植。
受体也必须提供知情同意,并且必须完全了解该程序的潜在风险和好处。粪菌移植的主要争议之一是该程序缺乏标准化。目前没有粪菌移植的标准化方案,粪便成分在捐赠者之间可能会有很大的差异。
▼
✦粪菌移植的剂量会影响其疗效
目前,粪菌移植的最佳频率和剂量仍不确定。一些研究表明,粪菌移植的剂量可能会影响其疗效,但目前还没有确定最佳剂量的标准。
✦一般需要多次粪菌移植
关于粪菌移植的频次,目前尚无明确的建议。一些研究表明,单次粪菌移植可能无法完全恢复肠道微生物群的平衡,需要多次粪菌移植才能达到最佳疗效。
单次粪菌移植可以有效治疗某些疾病,如复发性艰难梭菌感染。然而,对于其他疾病,可能需要多次粪菌移植才能获得最佳效果。
但是,多次粪菌移植也可能增加感染和其他不良反应的风险。因此,粪菌移植的频次应根据患者的具体情况和病情进行个体化的决策。
总之,粪菌移植的最佳频次和剂量应根据患者的具体情况和病情进行个体化的决策,同时应注意监测和预防不良反应的发生。
需要更多的研究来确定粪菌移植的最佳频率和剂量,以便在临床实践中更好地使用该程序。
根据《上海市菌群移植技术管理规范(2021年版)》,以下是部分粪菌移植操作要求:
▼
(一)严格遵守粪菌移植治疗操作规范和诊疗指南,严格掌握粪菌移植治疗适应证和禁忌证。
▷粪菌移植适用于治疗以下消化系统疾病
(1)艰难梭状芽胞杆菌感染:复发性/难治性艰难梭状芽胞杆菌感染。
(2)其他消化系统疾病:溃疡性结肠炎、克罗恩病、功能性便秘、肠易激综合征、菌群紊乱相关腹泻等。
▷粪菌移植治疗的其他疾病
(1)神经系统疾病:帕金森病、阿尔兹海默症、癫痫等。
(2)精神疾病:自闭症、情绪障碍、多动症、抽动症等。
(3)代谢相关疾病:代谢综合征、糖尿病等。
(4)肿瘤相关疾病:免疫治疗及放化疗所致肠炎等。
(二)除复发性/难治性艰难梭状芽胞杆菌感染外,出于其他治疗目的使用粪菌移植治疗均须以临床研究形式开展,并通过本机构伦理审查与备案。
(三)实施粪菌移植治疗前应当向患者及其家属告知治疗目的、风险、注意事项及可能发生的并发症等,并签署知情同意书。
(四)医疗机构应当建立完整的电子化临床数据库及严格的术后随访制度,在完成每例粪菌移植治疗后应当按照有关规定将治疗相关信息上报卫生健康行政部门。
▼
(1)有明确与肠道菌群紊乱有关的肠道内疾病,如肠功能障碍性疾病、肠道感染性疾病(复发性艰难梭菌感染)、肠道炎症性疾病及假性和麻痹性肠梗阻等;
(2)有明确与肠道疾病或者肠道菌群紊乱有关的肠道外疾病,如便秘合并帕金森病、便秘或腹泻合并自闭症、便秘或腹泻合并过敏性皮炎;
(3)患者需充分理解粪菌移植治疗过程及机制,并签署知情同意书。
!
出现以下情况之一不宜进行粪菌移植:
(1)肠道大面积溃疡、出血;
(2)移植通道梗阻;
(3)移植操作本身(内镜、置管、灌肠、经口饮食)的禁忌证;
(4)未通过伦理审核的临床试验或患者拒绝接受粪菌移植。
(5)生命体征(体温、心率、血压、呼吸)不稳定;
(6)严重免疫系统紊乱;
(7)孕妇或哺乳期妇女;
(8)代偿或者失代偿肝功能障碍。
▼
(1)个人情况:作息规律,饮食健康,家庭和睦,无不良性交,无吸烟、饮酒、吸毒等嗜好,无药物成瘾,近6个月未接种过疫苗或参加药物试验,近6个月未接受纹身或出现皮肤破损,近6个月无热带地区旅居史;无胃肠道病变家族史,无恶性肿瘤家族史,无传染病家族史;非孕期,非经期。
(2)开展病史和身体检查,评估供体的健康状况和是否符合粪菌移植的供体资格;选择无传染病史、无抗生素使用史、无消化系统疾病等方面的供体。
身体状态:年龄18-30周岁,体重指数(BMI)18.5-23.9 kg/m2,儿童医院开展粪菌移植,供体要求可放宽至15-30周岁。
心理状态:心理科医师或心理咨询师访谈认定心理状态良好;抑郁自评量表(SDS)、焦虑自评量表(SAS)、匹兹堡睡眠质量指数(PSQI)等评分正常。
(3)进行多项检测,如血液化验、粪便检测、病原菌检测、URTI检测等,确保找到适合的健康供体;以确保其不携带有害微生物和多重耐药菌。同时,需要考虑供体的肠道微生物组成和短链脂肪酸水平,以选择最适合的供体。
血液学检测:包括血常规、肝肾功能、电解质、C反应蛋白正常,肝炎病毒、HIV、梅毒、EB病毒、巨细胞病毒、COVID-19抗体、线虫、阿米巴等病原检测阴性;
粪便检测:粪便常规检查正常,隐血实验阴性,艰难梭菌、弯曲菌、沙门菌、志贺菌、产志贺毒素大肠杆菌及虫卵、小肠结肠耶尔森菌、致病性弧菌(副溶血弧菌、霍乱弧菌)、气单胞菌、阿米巴、孢子、诺如病毒、轮状病毒和新型冠状病毒(COVID-19)等病原学检测阴性。
(4)评估供体的肠道微生物组成,多样性和稳定性,包括菌群、真菌群和病毒群,并建立数据库;在选择供体时,除了肠道微生物群的总体多样性外,还应考虑到益生菌的丰富度,如乳酸菌、双歧杆菌等,选择粪便丁酸浓度高的供体微生物组。
(5)根据评估结果选择合适的供体,注意进行家族成员偏向,判别成熟度和完整性,同时避免与患者组群共同优势菌种重合等;一些研究表明,供体微生物组成与受体的微生物组成相似,可以提高移植成功率。
(6)移植前需对受体进行评估和准备,包括清洁肠道和停用抗生素等;为了提高移植效果,一些研究还使用抗生素预处理和肠道灌洗等方法来增强供体菌株的移植。
限食耐受性:通过限食实验完成。部分受体存在食物过敏及食物不耐受(如鸡蛋、牛奶等),根据受体要求,供体需在捐赠粪便前5天限制食物种类,如该供体不可耐受,则不可作为本次移植的捐赠者。
(7)进行移植后,对受体的微生物组成进行多次采样和分析,以评估移植效果和持续时间;
①每2个月复查以上条目,仍然符合上述要求;
②每次捐赠的粪便均留样行宏基因或者16s rDNA测序(根据各自单位检测能力),保证菌群组成及多样性稳定;
③每次捐献粪便应留样行代谢组学检测。
(8)监测受体的生理状况和不良反应,及时采取措施进行处理。
▼
(1)粪便采集:应采用无菌容器采集,粪便重量不少于100g,性状为Bristol评分标准中3-5分方为合格,立即进入菌液制作流程,或立即密封后2-8℃保存。
(2)制作流程:每次需取不少于50g粪便与无菌生理盐水以1∶3比例混合,充分搅拌混匀后过滤,从粪便排出体外至菌液制作完成应保证在2小时以内,整个处理过程应在无菌环境下操作。
注:为了避免感染窗口期的问题,菌液或胶囊制备后应待21 天后经过病毒细菌等检验合格后出库,每批产品留样至少6个月以供追溯。
(3)冻存与复融:菌液制备完成后置于-80℃保存,6个月之内使用不影响疗效;如置于-20℃保存,应在1-4周内使用。使用前置于室温复融,6小时内输注;如使用水浴锅复融,则水温不得超过37℃。
(4)质控标准:每次制作完成的菌液应随机抽样,进行致病菌监测、细胞计数及宏基因或16s rDNA菌群测序。
每50mL菌液中活细胞数应不小于2.5×10^12个,同供体同批次样本应达到菌群组成一致,6个月内同供体不同批次样本应达到菌群组成差异无统计学意义。
制作完成的菌液应有独立包装与标签。如制作胶囊,还应取胶囊内容物进行细菌活性监测与活细胞计数,其中细菌活性应不低于85%,每克内容物包含活菌数不小于10^9CFU。
▼
(1)菌液输注前需结合患者自身情况及疾病种类行肠道准备。
(2)应根据指南及操作规范选择上消化道或下消化道进行菌液输注。
(3)操作时应观察患者耐受情况,并及时处理不良反应。
▼
(1)管理原则:医疗安全(不良)事件的管理,遵循预防为主、紧急处理、合理控制、防微杜渐、持续改进的原则。
(2)上报要求:凡科室职工均有权上报医疗安全(不良)事件,可通过网络、书面、电话上报,上报时限要求在不良事件发生后24小时之内。
(3)审核、处置要求:科室负责人24小时内审核、处置科室发生的不良事件,并呈报至相关职能部门。
注意:主管职能部门自接报之日起,24小时内审核、处置不良事件;对于接报的Ⅱ级及以上不良事件,应呈报至主管院领导。
主管院领导对于接报的Ⅱ级及以上不良事件,必要时组织委员会进行讨论分析,并提交院务会。
▼
(1)每次菌液输注后密切观察患者耐受情况24小时,如有不良反应立刻处理并及时上报。
(2)1个疗程治疗结束后4周内应对患者症状学和肠道菌群改善情况进行评估,粪菌移植治疗疾病的随访及疗效判断指标主要遵循原发疾病的治疗指南。移植前后重复检测粪便及血液中传染病相关指标,有条件者可行免疫相关检测。
注意:如第1个疗程结束3周后病情无改善,可尝试更换供体,重新给予1个疗程粪菌移植,若有效可继续治疗,若仍无效则应视为粪菌移植无反应性,此时不应继续给予粪菌移植,以免耽误病情;如患者接受粪菌移植治疗后症状明显改善,可重复3-5次粪菌移植后结束治疗。
随访至末次粪菌移植结束后至少8周,有条件者应进行大于1年甚至5年以上的长期随访。
随着对微生物与宿主相互作用的了解不断加深,肠道微生物群的参与已成为一种新颖、巧妙且不可忽视的调节宿主健康的方式。
粪菌移植是一种治疗胃肠道疾病的有效方法,还有望治疗其他更多疾病。未来的研究应该重点关注粪菌移植对肠道微生物组和整体健康的长期影响,并制定安全有效地使用该程序的指南。
此外,需要进一步研究如何提高粪菌移植的改善效果,供体和受体的配型以及移植肠道菌群的定植和效果的长期性,以便在临床实践中更好地使用。
主要参考文献:
Zhang YW, Cao MM, Li YJ, Zhang RL, Wu MT, Yu Q, Rui YF. Fecal microbiota transplantation as a promising treatment option for osteoporosis. J Bone Miner Metab. 2022 Nov;40(6):874-889.
Biazzo M, Deidda G. Fecal Microbiota Transplantation as New Therapeutic Avenue for Human Diseases. J Clin Med. 2022 Jul 15;11(14):4119.
Quaranta G, Guarnaccia A, Fancello G, Agrillo C, Iannarelli F, Sanguinetti M, Masucci L. Fecal Microbiota Transplantation and Other Gut Microbiota Manipulation Strategies. Microorganisms. 2022 Dec 7;10(12):2424.
Vendrik KEW, Ooijevaar RE, de Jong PRC, Laman JD, van Oosten BW, van Hilten JJ, Ducarmon QR, Keller JJ, Kuijper EJ, Contarino MF. Fecal Microbiota Transplantation in Neurological Disorders. Front Cell Infect Microbiol. 2020 Mar 24;10:98.
Wang JW, Kuo CH, Kuo FC, Wang YK, Hsu WH, Yu FJ, Hu HM, Hsu PI, Wang JY, Wu DC. Fecal microbiota transplantation: Review and update. J Formos Med Assoc. 2019 Mar;118 Suppl 1:S23-S31.
Chen D, Wu J, Jin D, Wang B, Cao H. Fecal microbiota transplantation in cancer management: Current status and perspectives. Int J Cancer. 2019 Oct 15;145(8):2021-2031.
Stallmach A, Steube A, Stallhofer J, Grunert PC, Merkel U, Hartmann M. Fäkaler Mikrobiomtransfer – Indikationen, Risiken und Chancen [Fecal microbiota transplantation: indications, risks and opportunities]. Inn Med (Heidelb). 2022 Oct;63(10):1036-1042. German.

谷禾健康

帕金森综合征
帕金森病(Parkinson’s disease,PD)是全球增长最快的神经系统疾病之一,原因有很多,包括人口老龄化和环境影响。老年人多见,平均发病年龄为60岁左右,40岁以下起病的青年帕金森病较少见。
我国流行病学调查显示,65岁以上人群帕金森病的患病率大约是1.7%。估计全国每年新发患者数达10万以上,我国现有帕金森病患者人数近300万。大部分帕金森病患者为散发病例,仅有不到10%的患者有家族史。
帕金森病最主要的病理改变是中脑黑质多巴胺(dopamine, DA)能神经元的变性死亡,由此而引起纹状体多巴胺含量显著性减少而致病。
虽然这种神经退行性疾病目前主要由临床运动特征(运动迟缓、僵硬和静止性震颤)来定义,但非运动特征,如自主神经功能障碍、认知行为问题和睡眠障碍,大大增加了总体疾病负担。
200多年前,詹姆斯·帕金森首次正式描述帕金森病时,胃肠功能障碍被认为是帕金森病临床表现的一部分。值得注意的是,他还推测帕金森病可能起源于胃肠系统,并评论道“胃肠紊乱状态可能会导致脊髓的一部分发生病态行为”。
肠道微生物群对神经系统过程(如神经发生、髓鞘形成和小胶质细胞激活)至关重要,能够调节行为和认知,并越来越多地参与调节神经退行性疾病和神经精神疾病的易感性和进展。
帕金森发病过程中肠道和大脑之间的串扰被认为受到肠道微生物失衡(失调)以及由此引起的细菌代谢活性改变的重大影响。
本文概述了帕金森病的肠-脑轴,包括迷走神经、肠神经系统中的α-突触核蛋白、改变的肠道通透性和炎症以及肠道微生物及其代谢活动的潜在作用和相互关系。阐述了肠道相关因素(包括肠道菌群)在帕金森病治疗进展中的作用和作为治疗靶点的作用,并基于研究文献讨论了常见的一些帕金森疗法。
关键词解释
α-突触核蛋白
是一种在中枢神经系统突触前及核周表达的可溶性蛋白质,它与帕金森病的发病机制和相关功能障碍密切相关,是路易小体的主要成分。
路易小体
是以帕金森病为代表的路易体病患者脑内的特征性标志物。显微镜下为圆形粉红色均质状结构。
▸ 震颤
震颤通常始于手或手指,其他包括手臂、腿、下巴或头部都可能出现震颤。可能会来回摩擦拇指和食指,类似弹丸滚动的震颤。手在休息时可能会颤抖。
▸ 肌肉僵硬
肌肉长时间保持收缩。尤其是在疾病的早期阶段,可能被误认为关节炎或骨科问题。
▸ 运动缓慢
随着时间的推移,帕金森病可能会让人减慢运动速度,使简单的任务变得困难且耗时。走路时步数可能会变短,可能拖着脚。可能很难从椅子上站起来。
▸ 平衡和协调受损
可能会变得弯腰,或者可能因帕金森病而出现平衡问题,有时会导致跌倒。
▸ 认知变化
一项研究发现,认知障碍是帕金森病常见且进展迅速的症状。在平均患有帕金森病五年且在研究开始时认知正常的参与者中,约有一半在确诊帕金森病后的六年内(约11年)出现轻度认知障碍。
少数出现轻度认知障碍的患者在五年内发展为痴呆。帕金森痴呆症患者可能有严重的记忆和思维问题,影响日常生活。
▸ 抑郁、焦虑等
可能会经历抑郁症,有时是在非常早期的阶段。
大约 40%-50% 的帕金森患者会出现抑郁症。可能还会经历其他情绪变化,例如恐惧、焦虑或失去动力等。也包括可能出现的精神病,例如幻觉或妄想。
▸ 吞咽、咀嚼和说话困难
由于吞咽缓慢,唾液可能会积聚在口腔中,导致流口水。晚期帕金森病会影响口腔中的肌肉,使咀嚼变得困难。这会导致窒息和营养不良。
▸ 排尿问题或便秘
帕金森病可能会导致膀胱问题,包括无法控制尿液或排尿困难。许多帕金森病患者出现便秘,主要是由于消化道较慢。
▸ 睡眠问题
帕金森病患者经常有睡眠问题,包括整夜频繁醒来、早起或白天想睡觉。
▸ 其他影响
其他还包括嗅觉障碍、疲劳、皮肤问题(黑色素瘤)、性功能障碍、疼痛、头晕目眩、眼睛和视力问题、体重减轻等问题。
帕金森氏症的症状和进展速度因人而异。这种疾病的早期症状很微妙,并且逐渐发生。例如:
有时候朋友或家人可能是第一个注意到早期帕金森氏症患者的变化的人。他们可能发现患者:
当疾病发展到晚期帕金森病时,症状变得更加严重且相当复杂,行动变得局限。其中包括:
从1980年代帕金森病患者肠道神经系统(ENS)中发现α-突触核蛋白沉积开始,进行了尸检研究,提出突触核蛋白病起源于迷走神经背运动核(DMNV)和前嗅核,帕金森病病理学肠-脑传播的“上升解剖学理论”获得了广泛的关注。
根据这一理论,作用于肠道的损伤会触发α-突触核蛋白的错误折叠和聚集,α-突触核蛋白开始于肠上皮细胞,然后通过朊病毒样细胞间转移传播到大脑。
这些结果表明,需要进一步的研究才能得出α-突触核蛋白的肠-脑支持是否是帕金森病的关键致病步骤。
鉴于帕金森病的复杂性和异质性以及肠-脑相互作用的多方面性质,目前的观点是,这种相互作用可能在帕金森病中起作用,但在个别患者中的作用程度不同。
▸▸
在过去十年中,多项临床和临床前研究提供了帕金森病患者肠道通透性改变(“肠道渗漏”)和炎症的证据。
Toll样受体4(TLR4)信号通路可感知受损或坏死组织释放的革兰氏阴性细菌脂多糖和内源性分子,被认为在帕金森病的肠道和脑部炎症中起着至关重要的作用。
虽然研究普遍显示帕金森病患者存在肠道炎症的证据,但这些变化仅在一部分患者中明显,胃肠道通透性研究的结果也具有高度异质性。
肠道相关因素在某些但并非所有患者的神经退行性变中起着重要作用。已知炎症可导致肠屏障功能障碍,在炎症性肠病(IBD)患者中,抗肿瘤坏死因子(anti-TNF)治疗可抑制肠道炎症,使胃肠道通透性恢复正常。
然而,屏障缺陷有时可以作为疾病的早期事件发生,与炎症无关。
一些支持和反对肠道优先参与PD的证据
▸流行病学研究
支持证据:
• 便秘、胃食管反流和胃轻瘫等胃肠道症状可先于帕金森病运动症状几十年。
• 大量研究表明,完全切断迷走神经干与显著降低帕金森病的发病风险相关。
反对证据:
• 胃肠功能障碍等非运动特征可能比运动特征更早出现,因为副交感神经系统(PNS)和肠神经系统(ENS)对神经退行性变的补偿能力不如中枢神经系统(CNS)。
• 一项大型纵向研究发现迷走神经切断术后帕金森病风险没有显著降低。
▸神经病理学研究
支持证据:
• 尸检研究表明,几乎所有帕金森病患者的肠神经系统中都存在突触核细胞病变。
• 在帕金森病诊断前20年,在食道、胃、小肠和结肠的活检中检测到α-突触核蛋白沉积。
反对证据:
• 对老年人的尸检研究发现,在没有脑α-突触核蛋白参与的情况下,没有“仅肠道”路易病理学,尽管不能排除在胃肠道迅速传播或高度局限性病理学的可能性。
• 其他活检研究发现,神经健康个体的胃肠道中存在α-突触核蛋白积聚。
▸动物研究
支持证据:
• 在啮齿动物模型中已经证明,肠-脑α-突触核蛋白传递,伴有黑质多巴胺能神经变性和帕金森病样运动和非运动症状,可能与年龄有关。
• 在鱼藤酮帕金森病小鼠模型中,半迷走神经切断术阻止了α-突触核蛋白在迷走神经背侧运动核(DMNV)中的积聚以及与该方法同侧的黑质多巴胺能细胞死亡。
•暴露于胃肠道中的微生物淀粉样蛋白(CULLI)会增加老年大鼠肠道和大脑中的α-突触核蛋白病理学和炎症,以及转基因α-突触核蛋白过度表达的小鼠,并伴有相应的运动缺陷。
反对证据:
• 涉及将大量α-突触核蛋白注射到胃肠道的动物模型可能无法准确再现人类帕金森病。
• 中枢神经系统紊乱也会改变肠道功能;例如,大鼠的黑质病变导致肠道运动障碍、炎症和微生物组改变。
半透性肠道屏障调节营养吸收,允许免疫感应,同时限制有害物质的运输。
在帕金森病中,“渗漏”的肠道允许微生物和分子(包括细菌和毒素)通过肠道上皮细胞的流量增加。表达脂多糖(LPS)的失调的肠道微生物群可以激活上皮细胞、免疫细胞和肠胶质细胞上表达的Toll样受体,并促进肠道渗漏以及肠道和脑炎症。
正如在患者结肠活检和粪便样本中观察到的那样,肠道炎症部分通过系统机制驱动疾病发病,包括细胞因子产生增加、血脑屏障破坏、炎性细胞迁移到大脑和小胶质细胞激活,最终导致神经功能障碍或丢失。
恶性循环可能发生,生物失调、通透性增高、炎症和α-突触核蛋白聚集相互延续。
这些因素的重要性和时间顺序可能因患者而异,这取决于环境影响(如影响微生物组的饮食)、衰老和宿主遗传学,导致不同的途径更容易出现功能障碍。
α-突触核蛋白参与先天性和适应性免疫
炎症环境增强了α-突触核蛋白的表达、错误折叠和聚集,进而诱导局部促炎免疫反应,从而形成促进α-突触核蛋白扩散的反馈环。
帕金森患者肠道屏障、炎症和α-突触核蛋白聚集
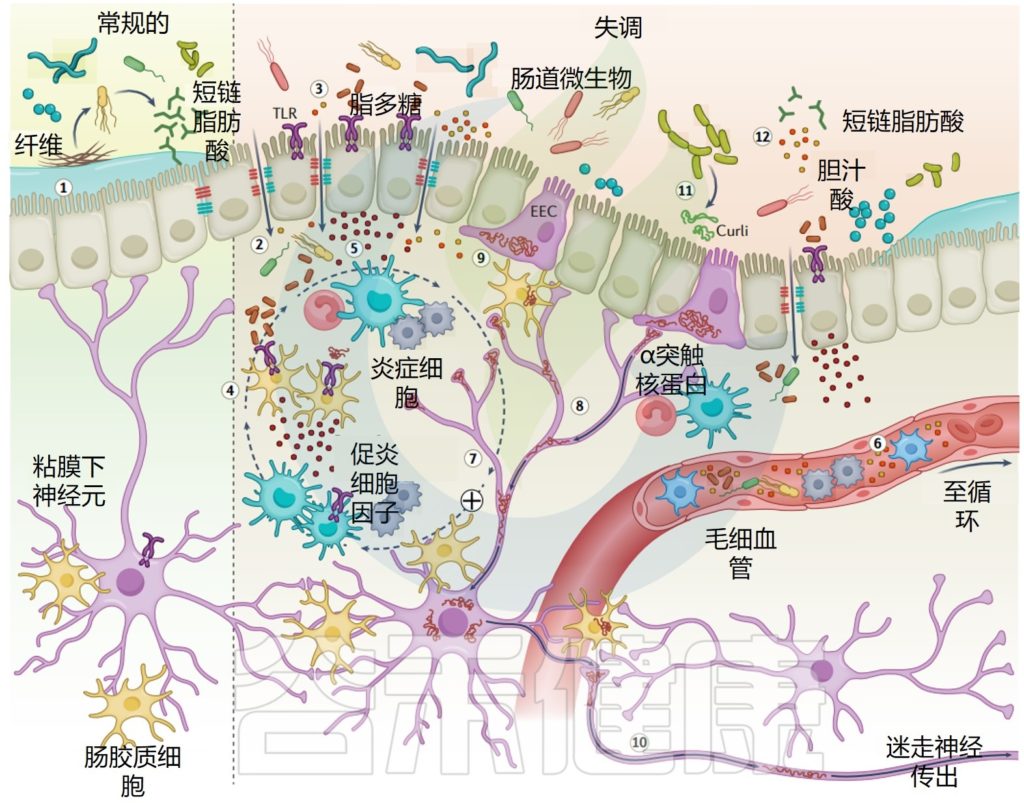
Tan AH, et al.,Nat Rev Neurol. 2022
值得注意的是,轴突终止于肠腔的粘膜下神经元和具有直接管腔和神经连接的肠内分泌细胞可以表达α-突触核蛋白,可能是α-突触核蛋白聚集的来源,并通过迷走神经扩散到大脑。微生物卷曲被建议在肠道中模板α-突触核蛋白聚集。
虽然肠道炎症和α-突触核蛋白表达可能是常见事件,但人们认为只有在存在其他促发因素(如宿主遗传脆弱性或衰老)时,帕金森才会发生。潜在有益的肠道代谢物的改变,如短链脂肪酸也可能在帕金森病发病中发挥作用。
帕金森病中微生物-肠-脑轴的示意图
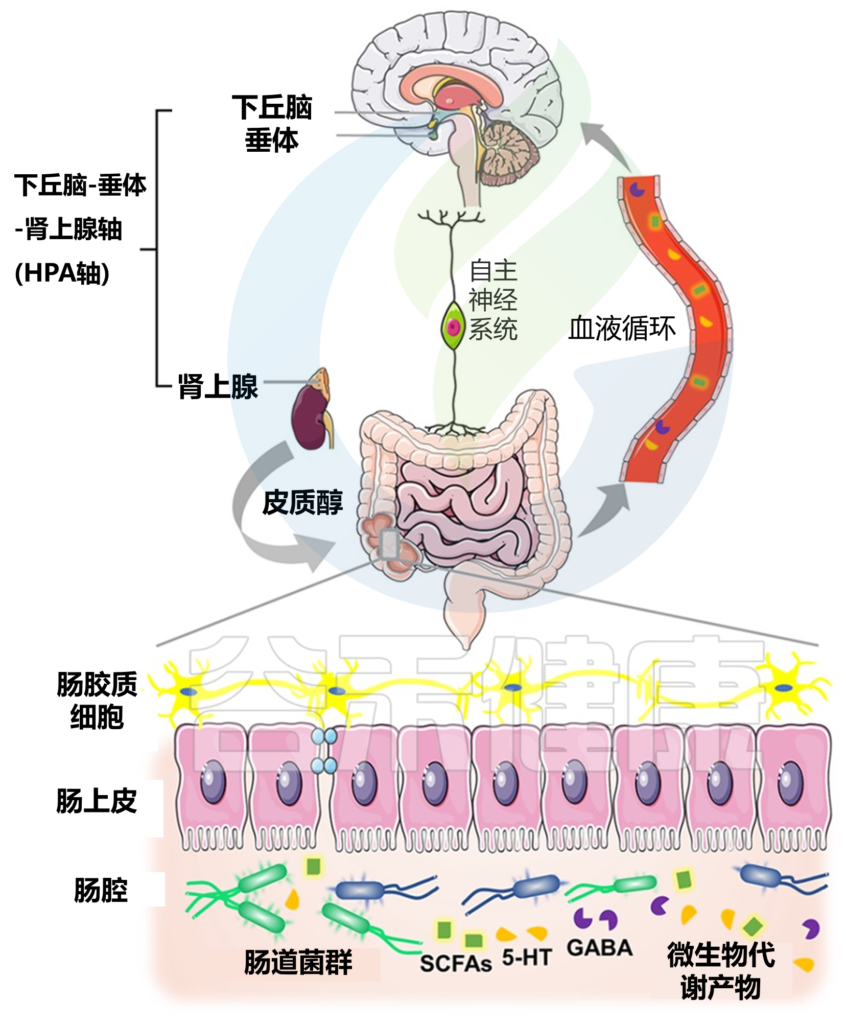
Wang Q, et al., Brain. 2021
在肠神经系统中,肠道菌群通过释放各种信号分子来调节大脑功能,这些信号分子可能进入体循环并到达目标部位。
中枢神经系统通过自主神经系统 (ANS) 下丘脑-垂体-肾上腺 (HPA) 轴在生理上支配胃肠道;反过来,肠道向大脑提供反馈以建立双向交流。
肠道微生物与宿主共同进化,形成复杂的互惠关系:胃肠道为其微生物群落提供滋养环境,而微生物群发挥着广泛的重要功能,影响宿主的生理机能。
在解释与疾病相关的肠道微生物组组成和功能改变时,宿主-微生物组相互作用的多维度和微生物组的个体变异是需要考虑的重要因素。
各种内在和外在因素改变了肠道微生物组,导致微生物组成的显著个体间差异。
影响肠道菌群的因素
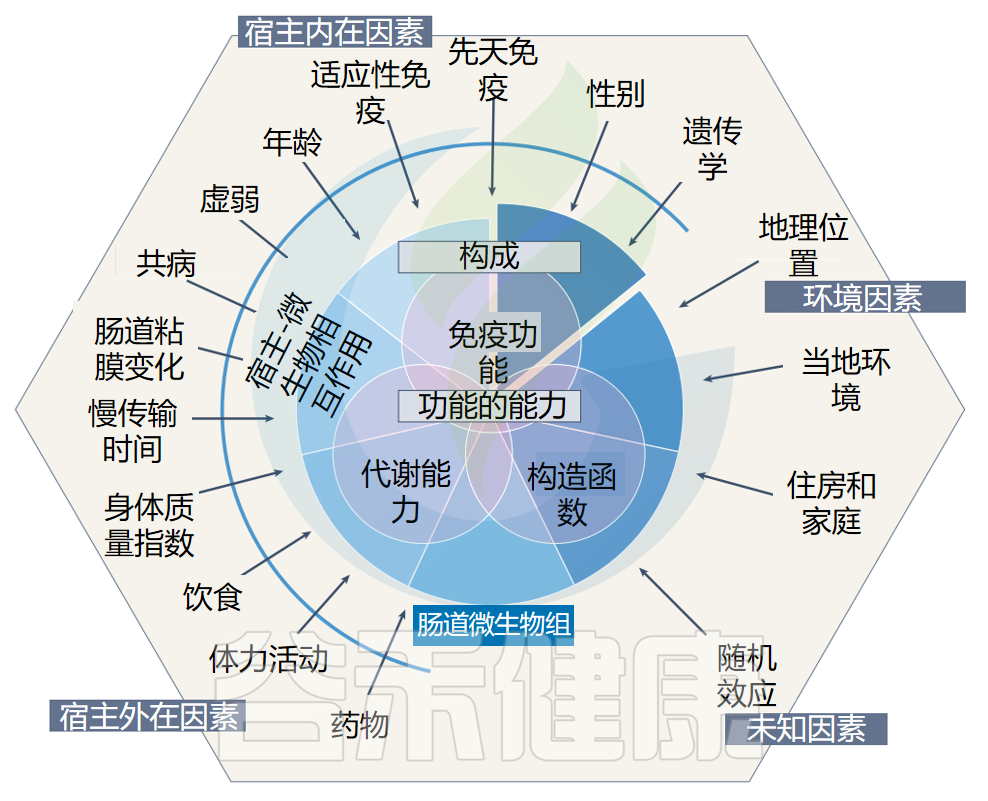
Tan AH, et al.,Nat Rev Neurol. 2022
微生物组适应环境和宿主因素的变化并不总是产生有害后果,宿主-微生物和微生物-微生物相互作用的动力学是整个肠道微生物组成和功能的重要决定因素。
事实上,健康个体之间的微生物组成可能差异很大,但仍保持着非常相似的功能能力,这为肠道健康提供了更好的衡量标准。因此,对肠道失调的研究不仅应关注与疾病相关的微生物组成变化,还应考虑影响疾病病因、发病机制、诊断、预后和治疗的功能变化。
衰老是帕金森病病理生理学的一个重要因素,并对肠道微生物生态系统有重要影响。在讨论PD相关变化之前,我们先概述与年龄相关的肠道微生物组变化。
与年龄相关的肠道菌群变化可归因于肠道生理衰老(例如,黏膜变薄、屏障破坏、肠道运动能力下降和免疫衰老)、生活方式的改变(例如,饮食、生活条件和体育活动)和健康状况(例如,共病、药物和虚弱)。
关于肠道微生物群在衰老过程中发生变化详见我们之前的文章:
肠道微生物群的老化及其对宿主免疫力的影响
健康长寿的步伐永不停歇
值得注意的是,肠道菌群具有调节炎症信号和与其他器官相互作用的能力,越来越多地认为它在“炎症”中发挥着核心作用。
来自ELDERMET联盟的开拓性研究表明,老年人肠道微生物组个体间具有高度的差异性,居住在社区的老年人与居住在长期护理机构的老年人之间存在显著差异,后者的微生物组多样性和时间稳定性较差。
长期护理患者的微生物组变化也与饮食因素、营养状况受损以及炎症和虚弱标志物的增加有关。
▸ 百岁老人的肠道菌群多样性较高,有益菌富集
在寻找健康老龄化和长寿的微生物标志的过程中,对百岁老人和超级百岁老人的研究几乎无一例外地揭示出,与其他老年人和年轻人相比,他们的微生物组多样性水平很高,不同地域不同人群研究表明长寿个体会富集例如瘤胃球菌(Ruminococcaceae)和阿克曼菌(Akkermansia)在内的几个细菌类群,同时,两组shotgun宏基因组的功能分析表明,长寿人群的微生物群具有较高的碳水水化合物和脂类代谢能力,以及外源生物降解能力。
▸ 炎症变化导致菌群变化
随着年龄的增长,可能出现相关炎症,引起肠道生理和营养环境变化,这时候,能够适应炎症的肠道环境的菌群,具有竞争优势,而其他微生物可能在炎症状态下丢失。
整合了来自 11 个国家的 30 项独立病例对照 NGS 研究,几乎所有的研究都发现,帕金森病患者和对照组之间的总体肠道微生物组组成存在显著差异。
重要的是,一些研究发现了可能影响肠道微生物组的潜在混杂因素,包括年龄、饮食因素(可能受到吞咽困难或 PD 嗅觉和味觉改变的影响)、便秘、虚弱和帕金森病药物(COMT 抑制剂和左旋多巴),虽然在控制这些因素后,帕金森病患者和对照组之间的差异仍然很大,不过这些差异的影响大小是在适度范围内的。
事实上,研究方法和地理位置可以解释微生物组组成中比PD状态更大的方差比例(在18-54%之间)。与之前关于微生物多样性减少与不健康衰老之间关系的观点相反,大多数研究发现帕金森病患者与对照组相比要么没有差异,要么总体多样性增加。
帕金森病:AKK菌、双歧杆菌、乳酸杆菌增加
据报道,帕金森病患者与对照个体之间至少有42科、102属和44种细菌存在差异。然而,只有大约四分之一的研究结果在一项或多项研究中得到了重复。
帕金森病最一致的发现是阿克曼菌(Akkermansia)的丰度增加(30项研究中的14项),该属属于疣状菌科(12项研究中也发现帕金森病增加)。
其他组成特征包括双歧杆菌(Bifidobacterium)属和乳酸杆菌(lactobacillus)属的丰度增加,丁酸生产菌(Roseburia)、粪杆菌属和布劳特氏菌(Blautia)的丰度减少。
帕金森病患者在物种或亚种水平上的研究仍然很少,在两项鸟枪式宏基因组研究和一些具有较高测序分辨率的16S rRNA研究中进行了初步探索。
Akk菌增加可能的原因
阿克曼菌(Akkermansia)、双歧杆菌(Bifidobacterium)和乳酸杆菌(lactobacillus) 被广泛视为“有益”细菌,后两个属通常包含在益生菌制剂中。
它们在帕金森病含量增加的原因尚不清楚,但可能与它们在改变的肠道环境中生存的适应性更强有关。值得注意的是,Akkermansia的增多与结肠运输缓慢和体重或脂肪量低有关,这两个特征在帕金森病患者中普遍存在。
其他神经系统疾病中也有Akkermansia丰度增加的报道,包括多系统萎缩(MSA)、进行性核上性麻痹、阿尔茨海默病和多发性硬化症,表明这一特征并非帕金森病特有。
扩展阅读:Nature | AKK菌——下一代有益菌
引人注目的是,对跨越十种疾病的28项病例对照研究进行的荟萃分析发现,与疾病相关的细菌属之间存在明显的重叠,表明某些变化代表了对健康和疾病的共同反应。
菌株特异性
细菌的功能可能具有菌株特异性,同一物种的不同菌株可能产生相反的作用。因此,根据目前在属和种水平上的知识推断细菌在帕金森病中的潜在作用可能信息不足。
此外,人类肠道微生物群中的大多数基因尚不能进行功能分配,其动态转录和翻译活动尚待阐明。
在统一的人类胃肠道基因组目录中,从超过200000个人类微生物基因中鉴定出的物种中,有70%以上仍有待培养或实验鉴定,对这些物种内的菌株和功能变异性的了解仍极为有限。
至关重要的是,单一微生物分类群的作用不能在隔离中看待,但应在社区环境中考虑,考虑到具有类似代谢功能的微生物与具有对抗作用的微生物的净效应,以及微生物-微生物和微生物-宿主相互作用。
因此,使用粪便转录组学、代谢蛋白质组学和代谢组学对代表肠道菌群集体功能输出的活性细菌代谢途径和产物进行直接测量,可能比细菌分类学描述更具相关性,以便更深入地了解肠道菌群在健康和疾病中的作用。
帕金森病患者:短链脂肪酸下降
帕金森病患者粪便短链脂肪酸的水平(乙酸盐,丙酸盐,丁酸盐)一直在下降。短链脂肪酸在微生物群-肠-脑串扰中发挥关键作用,部分通过调节肠道和血-脑屏障的完整性、炎症级联、内分泌信号和神经元存活。
除了作为结肠上皮的主要基质外,实验性帕金森模型中还发现丁酸通过组蛋白脱乙酰酶抑制发挥神经保护作用,包括减轻运动损伤和多巴胺能细胞死亡。
在MSA中也发现粪便短链脂肪酸和胆碱代谢产物水平降低,表明这种情况与帕金森病之间存在共同的微生物反应。
帕金森病患者肠道微生物组和代谢物的临床相关性在后面章节关于帕金森病风险和进展中的肠道相关因素中进行了讨论。
在几种帕金森病啮齿动物模型中已证实肠道微生物群的改变,包括:通过腹腔注射或皮下注射的神经毒素模型等,大多数研究还发现,与野生同窝鼠相比,患病啮齿动物的胃肠道(肠道运动障碍、炎症、屏障破坏和神经功能丧失)或大脑(运动功能障碍、炎症和多巴胺能细胞丧失)发生病理生理学变化。
在其中一些研究中,观察到肠道变化先于帕金森病样运动特征的出现;然而,肠道微生物对观察到的变化的贡献尚不清楚。
与帕金森病相关的菌群改变的因果关系推断
几项使用无菌小鼠(出生和饲养时未接触活微生物)、粪便微生物移植(FMT)或使用广谱抗生素治疗的研究,可以推断出与人类帕金森病相关的微生物组改变的因果关系。
与无菌ASO小鼠相比,含有复杂微生物群的ASO小鼠运动功能和便秘更差,伴有明显的神经炎症反应和脑内α-突触核蛋白沉积。
值得注意的是,帕金森病患者肠道微生物群的移植加剧了无菌ASO小鼠的运动功能障碍。有趣的是,补充短链脂肪酸(SCFA)通常被认为是有益的,与无菌ASO小鼠中的小胶质细胞激活和α-突触核蛋白聚集有关。
然而,无菌小鼠小胶质细胞缺陷的观察结果使这些发现与人类帕金森病的解释复杂化。短链脂肪酸的作用也可能取决于剂量和类型;肠道中不同短链脂肪酸浓度和比率的差异可能导致不同的健康结果。
在另一项研究中,长期口服鱼藤酮会导致常规饲养小鼠的肠道通透性增高和运动功能障碍,但在无菌小鼠中则没有。
在另外两项针对啮齿动物的研究中,抗生素治疗耗尽了肠道微生物负荷和多样性,似乎可以减轻MPTP和六羟基多巴(6-OHDA)诱导的多巴胺能神经毒性。
综上所述,这些实验模型提供了证据,证明肠道微生物的存在、组成和代谢产物在帕金森病样发病机制中具有致病或促进作用。
肠道微生物及其代谢产物的高度个人化和复杂性质使微生物组因果成分的鉴定变得复杂,这些微生物及其代谢产物可能单独发挥作用,或在微生物群中发挥增强或抵消作用。
此外,大多数研究中使用的供体数量较少,无法捕获人类肠道微生物群的广泛个体间差异。至关重要的是,未能解释宿主-微生物相互作用和内环境平衡及其在个人整个生命周期中的演变,以及饮食、生活方式、衰老和其他因素的变化,是这些实验的主要限制。
几项大型流行病学和临床研究将肠道疾病、肠道干预和饮食因素与随后的帕金森病发展和恶化风险联系起来。
便秘是帕金森病的典型前驱症状,20多年前发表了第一项基于社区的长期研究,证明患有这种疾病的个体患帕金森病的风险升高。
帕金森病的便秘是由一系列因素引起的,包括结肠传输缓慢和肛门直肠功能障碍。2021发表的一项研究表明,便秘的不同亚型与帕金森病的不同发病风险相关,慢传输比排便协同障碍的发病风险略高。
便秘也预示着帕金森病的恶化趋势
一项针对465名社区帕金森病患者的研究发现,患者在发病时便秘的存在和严重程度与痴呆更快进展之间存在关系。
这些患者从诊断开始就接受了长达8年的监测。严重便秘患者平均得痴呆症的时间为6.0年,而无便秘的患者则为7.5年。排便协同障碍是便秘患者排便过程中出现的一种反常肛门括约肌收缩障碍。
同样,使用来自帕金森病进展标志物倡议423名新诊断帕金森病患者的数据,这些患者接受了长达5年的监测发现,胃肠道症状的综合得分越高(肠蠕动、大便硬和失禁的频率越低),认知能力越差,轻度认知障碍和痴呆的发生率越高。
在这两项研究中,认知功能与非胃肠道自主症状无关,这表明这种关联是胃肠道系统特有的,而不是自主功能障碍本身。
帕金森病患者便秘的相关因素
在一个单独队列的3年随访研究中,基线便秘严重程度与体脂质量损失独立相关。反过来,帕金森病患者的体重减轻与营养不良、骨折、压疮和死亡的风险增加有关。
2021发表的一项粪便代谢组学研究发现,帕金森病患者的便秘严重程度与丁酸盐(一种潜在有益的SCFA)水平降低相关。
另一项初步研究发现,帕金森病和便秘患者外周血中辅助性T细胞的数量增加。这种具有强大炎症潜能的CD4+T辅助细胞亚群可由特定的肠道细菌诱导,并与帕金森病(以及炎症性肠病)的发病机制有关。
长期以来,人们推测结肠淤滞会导致细菌产物和其他毒素更多地转移到循环中;尽管这一点尚未得到令人信服的证明,但粪便稠度被认为对肠道微生物群组成有重大影响。
如上所述,炎症与帕金森病的发病机制有关,帕金森病患者的一些结肠活检和粪便结果与炎症性肠病患者相似。
迄今为止最大的一项研究调查了美国1.7亿多人的索赔数据,发现炎症性肠病患者的帕金森病发病率增加了28%。
荟萃分析表明,当分别分析克罗恩病患者和溃疡性结肠炎患者时,帕金森病风险的增加仍然显著。研究人员还发现,抗TNF疗法可以显著降低这种风险,这表明炎症性肠病的有效治疗可能会降低帕金森病的发病风险。
一项利用瑞典全国组织病理学数据库进行的研究还发现,显微镜下结肠炎(另一种慢性肠道炎症疾病)与帕金森病之间存在强烈的相关性。
遗传学研究表明,帕金森病和炎症性肠病患者(尤其是克罗恩病)的发生有共同的生物学机制。LRRK2基因中的突变是单基因(常染色体显性)帕金森病最常见的原因之一。
随后的几项研究确定了LRRK2变异体与散发性帕金森病和克罗恩病之间的关联,还报告了帕金森病和炎症性肠病的其他重叠风险位点。这些位点进一步暗示了免疫反应和微生物感应(例如,NOD2基因和HLA位点),以及溶酶体功能障碍,这是两种情况下的常见机制。
约有50个和10个基因分别与单基因炎症性肠病和帕金森病相关,但导致这两种疾病的单基因形式的罕见变异迄今尚未报道。
最后,在2022年发表的一项研究中,与无结肠炎的小鼠相比,患有结肠炎的小鼠的运动功能降低,多巴胺能神经元丢失加重,进一步支持LRRK2、结肠炎和帕金森病之间的联系。
肠易激综合征(IBS)症状,如腹痛和肠道习惯改变,在帕金森病患者中很常见,并与粪便微生物群的变化相关。
在肠易激综合征患者身上观察到的病理生理变化,包括失调、肠道通透性增加和轻度粘膜炎症,可能会使胃肠道更容易受到帕金森病病理的影响。
肠易激综合征与帕金森病之间的关联
在一项来自台湾的全国性注册研究中,涉及约120000人,肠易激综合征与帕金森病风险增加相关。
然而,在芬兰进行的一项类似研究中,在前2年的随访中,风险显著升高,导致作者得出结论,肠易激综合征与帕金森病之间的关联可归因于反向因果关系(即帕金森病的前驱胃肠道症状被误解为肠易激综合征症状);或检测偏差(即,对肠易激综合征症状患者进行更密切的临床监测可提高诊断帕金森病的可能性)。
韩国的一项研究包括约285000名受试者,他们接受了长达11年的监测,发现患有肠易激综合征的老年人(65岁及以上)患帕金森病的风险增加。
迄今为止最大的一项涉及瑞典170万参与者的研究发现,专家诊断肠易激综合征与帕金森病风险增加相关。
然而,在同一研究者进行的补充队列研究中,肠易激综合征的诊断基于自我报告的症状,结果没有统计学意义。因此,这种常见的肠-脑相互作用障碍(影响全球十分之一的人)与帕金森病之间的可能联系仍然没有定论。
迷走神经
迷走神经起源于延髓,在腹腔内为胃、小肠和大肠提供副交感神经支配,直至脾曲。
在两项大型研究中,完全躯干(但非选择性)迷走神经切断术与患帕金森病的风险显著降低相关。
另一项研究分析了相同的丹麦数据库,但包含了较长时间内的大量病例,并使用了不同的编码分类和统计方法,发现躯干或其他类型的迷走神经切断术没有显著降低风险。
相互矛盾的结果可能部分归因于迷走神经切断术的混合效应:虽然这种干预可能限制α-突触核蛋白病理学从肠道向大脑的传播,但由于胆碱能抗炎途径的破坏,它也可能导致免疫稳态向促炎反应的转变。
阑尾切除术
虽然阑尾以前被认为是一个退化器官,但现在人们认识到它富含多种免疫细胞,可以影响胃肠道的炎症和自身免疫,它还充当肠道微生物组的蓄水池和调节器。
研究发现,除了迷走神经背侧运动核的密集神经支配外,阑尾在帕金森病发病机制中的可能作用还表现在该器官中大量聚集的α-突触核蛋白。
在一项研究中,发现年轻人和老年人(从婴儿到84岁)的阑尾中都有大量截短形式的α-突触核蛋白,这些截短形式的α-突触核蛋白是路易小体的主要成分,在实验模型中被证明是α-突触核蛋白聚集的有效种子,包括那些没有神经系统疾病的人,表明阑尾是α-突触核蛋白致病形式的储库。
在2021发表的一项研究中,53%的帕金森病患者和8%的对照组患者的CT扫描显示有慢性阑尾炎的病变。
一小群7名患者接受了阑尾切除术,对切除组织的组织病理学分析显示,阑尾粘膜和粘膜下层存在α-突触核蛋白聚集。
在一些研究中,阑尾切除术与帕金森病风险降低相关,但在大多数研究中,未发现任何影响,甚至风险轻度升高。
有趣的是,一项针对12名帕金森病患者的小型研究采用多组学方法研究了阑尾微生物群,发现了脂质和胆汁酸代谢紊乱的证据,包括阑尾中微生物源性(次生)胆汁酸升高5.6–18.7倍。这些胆汁酸具有毒性作用,并与肠道炎症有关。
与上文所述的对帕金森病下消化道失调的理解的扩展相反,关于帕金森病上消化道失调的研究主要集中在幽门螺杆菌感染和小肠细菌过度生长(SIBO)。
有幽门螺杆菌感染史的人帕金森风险高
幽门螺杆菌感染与帕金森病之间的联系始于20世纪60年代,一项观察性研究显示,患有这种疾病的患者中消化性溃疡的发生率很高,通常在8-10年前出现帕金森症状。
一项来自台湾的研究发现,有感染史的人患帕金森病的风险增加了一倍。
来自丹麦的另一项研究发现,患者根除幽门螺杆菌的治疗史与5年或更长时间后患帕金森病的风险增加45%相关。
帕金森病患者的幽门螺杆菌感染率在不同地理区域的研究中有所不同,从呼吸和粪便抗原检测的25-33%到血清学检测的48-50%不等。这些比率与当地人口的比率相当。
帕金森患者的小肠细菌过度生长患病率范围广
小肠细菌过度生长可作为幽门螺杆菌诱导的胃酸过少的后遗症;其他原因包括使用质子泵抑制剂、小肠运动障碍和免疫反应受损。
研究发现,帕金森病患者的小肠细菌过度生长患病率范围广泛(25–67%),这可能是由于研究参与者的异质性和呼吸测试协议,这些协议提供了小肠细菌过度生长的间接评估,准确性有限。
幽门螺杆菌感染和小肠细菌过度生长均与更严重的运动严重性和更严重的运动反应并发症(延迟和缩短时间)相关。
致病原理
幽门螺杆菌感染和小肠细菌过度生长可能通过降低左旋多巴的生物利用度,或通过诱导慢性外周炎症状态来加剧神经退行性变过程,从而导致帕金森病患者的运动功能障碍。
例如,幽门螺杆菌诱导的细胞毒素可以改变宿主的免疫反应并触发大量促炎物质的释放,这可能导致血脑屏障的破坏、小胶质细胞的激活,最终导致神经元损伤和死亡。
在一项小型研究中,幽门螺杆菌阳性的帕金森病患者被发现对神经功能至关重要的蛋白质的自身抗体水平升高,包括核因子I亚型A、血小板衍生生长因子B和真核翻译起始因子4A3。
另一方面,肠道运动障碍(以及更普遍的自主神经功能障碍)可能是严重帕金森病的表现,并可能导致小肠细菌过度生长,导致观察到这些疾病之间的关联。
几项研究调查了肠道微生态系统与帕金森病风险或前驱症状之间的关系,包括睡眠行为障碍(RBD),它可能在 PD 运动诊断之前 20 年或更长时间。
肠道菌群
对来自德国和日本的队列(包括46名特发性睡眠行为障碍(RBD)患者、223名帕金森病患者和137名对照个体)进行的荟萃分析表明,睡眠行为障碍患者与帕金森病患者具有不同的微生物成分,尽管观察到一些重叠(例如,两种情况下Akkermansia的丰度增加)。
有趣的是,与对照组相比,在一小群睡眠行为障碍患者中,产生短链脂肪酸的细菌数量并没有减少,
作者认为短链脂肪酸可能在孤立性快速眼动睡眠行为障碍向帕金森病的转化中发挥作用。同时,在包括666名个体的大趋势队列研究中,一些帕金森病的风险或前驱标记物与微生物组组成的改变相关,尽管其影响很小。
如上所述,病例对照研究已经确定了帕金森患者中存在大量差异丰富的菌群。然而,在单独的研究中,只有少数与运动特征(MDS-UPDRS评分、运动反应并发症或姿势不稳定和步态困难(PIGD)表型)或非运动特征(认知、抑郁、焦虑或便秘)相关。
在一项研究中,肠杆菌科细菌的丰度与更严重的运动表型相关,这与大肠杆菌通过产生脂多糖和卷曲菌毛在帕金森病发病机制中的可能作用有关。
纵向研究的结果也不一致。在25名新发PD患者的3年随访研究中,更快的PD运动进展(使用Hoehn和Yahr评分量表或UPDRS测量)与较低的基线Roseburia丰度相关;在36名PD189患者的2年随访研究中,使用19种细菌分类群的定量PCR,与双歧杆菌和Atopobium 的基线丰度相关。
短链脂肪酸
帕金森病患者肠道微生物群衍生代谢的临床研究仍然很少。低水平的粪便丁酸盐与较差的认知功能和步态困难评分以及更早出现运动和非运动症状相关,而低水平的粪便乙酸盐与低BMI和排便频率降低相关。
帕金森病患者的血浆乙酸盐和丙酸盐水平高于对照组。一些研究人员推测,由于肠道屏障破坏和结肠上皮细胞对肠道短链脂肪酸的利用或清除减少,肠道短链脂肪酸会泄漏到体循环中。
血浆丙酸水平与运动严重程度呈负相关,这与短链脂肪酸对帕金森病有益的总体临床趋势一致。
氧化三甲胺(TMAO)
另一种对帕金森病越来越感兴趣的肠道代谢物是氧化三甲胺(TMAO),根据实验研究,氧化三甲胺可以通过促进正确的蛋白质折叠和防止病理性不溶性纤维的形成来防止神经变性。
如上所述,一些研究发现帕金森病患者粪便和血浆样本中的氧化三甲胺水平均降低,尽管其他研究发现帕金森病患者的血浆氧化三甲胺水平高于对照组。血浆氧化三甲胺水平与帕金森病进展之间的相关性也得到了相互矛盾的结果。
饮食是决定微生物组成和功能的关键因素。肠道微生物将摄入的营养物质用于基本的生物过程,反过来,它们的代谢产物被认为对人类健康有重要影响。
尽管每种主要的宏量营养素和微量营养素都能改变肠道微生物群,但为大肠微生物提供主要能量来源的不可消化碳水化合物(例如纤维和抗性淀粉)在饮食-微生物群相互作用中发挥着特别突出的作用。
这些聚糖的低消耗与微生物多样性降低、短链脂肪酸产量减少以及肠道微生物对粘液的觅食增加有关,导致肠道屏障完整性中断。
许多研究调查了帕金森病风险与饮食成分(包括大量营养素、微量营养素、特定食物和饮食模式)之间的关系。
饮食与帕金森病风险和进展

Tan AH, et al.,Nat Rev Neurol. 2022
研究结果往往相互矛盾,前瞻性研究和病例对照研究之间存在差异。虽然前瞻性研究比病例对照研究更好地确定饮食和疾病之间的因果关系,但它们不能完全消除反向因果关系,即患者因疾病早期迹象改变饮食习惯。
此外,病例对照研究受到选择和饮食回忆偏差的限制。然而,令人惊讶的是,咖啡因研究的结果具有显著的可重复性,这使得咖啡因成为最能降低帕金森病风险的环境暴露之一。
地中海饮食
近年来,地中海饮食已成为一种潜在的“健康”饮食模式,与降低慢性病(包括帕金森病)的风险相关,以及几项前瞻性研究中的总体死亡率减低。
这种饮食通常包括相对较高的水果、蔬菜、全谷物和不饱和脂肪的摄入量,相对较低的肉类(包括家禽)和乳制品的摄入量,以及适度的酒精摄入。
据推测,地中海饮食的有益健康效应部分是通过保护机体免受氧化应激和炎症的影响,以及通过肠道微生物代谢产物改善宿主代谢的调节来实现的。
与其他慢性病一样,大量研究与缺乏减少帕金森病发展或进展的决定性饮食建议之间仍存在明显差距。对饮食化合物反应的个体间差异,可能源于肠道微生物群和宿主基因组成的差异,进一步使饮食与疾病之间的关联复杂化,基于人群的研究结果可能对个别病例的普遍性有限。帕金森的饮食干预研究仍处于起步阶段,将在后面的治疗策略部分进行讨论。
前面介绍了LRRK2基因、帕金森病和炎症性肠病之间相互关系的概念。LRRK2蛋白在免疫细胞中高度表达,并在接触微生物病原体后上调。
与克罗恩病患者的非炎症结肠组织相比,炎症结肠组织中检测到更高水平的LRRK2,与匹配对照组相比,散发性帕金森病患者的外周免疫(血单个核)细胞中检测到更高水平的LRRK2。
LRRK2过度表达也显示出增加结肠炎的严重程度,因此,LRRK2被认为在一定程度上通过介导肠道中的异常炎症反应参与帕金森病的发病机制。然而,其他作者推测,通过增强肠道细菌清除和减轻肠道炎症,增加LRRK2激酶活性会产生有益的效果。
免疫细胞中高水平的LRRK2是否对帕金森病产生保护作用或有害作用,目前尚不清楚。
就动物模型而言,缺乏PTEN基因诱导的假定激酶1(PINK1)的小鼠的肠道革兰氏阴性细菌感染,该激酶参与线粒体内环境平衡,并由帕金森病的某些单基因形式突变的基因编码,触发外周和大脑中自反应性线粒体特异性细胞毒性CD8+T细胞的产生,导致纹状体多巴胺能丧失和运动障碍。
左旋多巴是帕金森病的主要治疗药物,必须到达原代小肠才能被吸收。
胃轻瘫是一种在没有机械阻塞的情况下胃排空延迟的情况,导致左旋多巴留在胃中并转化为多巴胺,而多巴胺不能穿过血脑屏障进入大脑。
反过来,胃中的多巴胺可能进一步损害胃运动。通过使用无线运动胶囊(“智能药丸”),这是一项相对较新的技术,35%患有各种胃肠道症状的帕金森病患者发现胃排空时间延长,20%有小肠传输延迟,8%有合并传输异常。
胃轻瘫通过降低左旋多巴的生物利用度,导致反应波动,如延迟开启状态,甚至剂量失效。因此,胃轻瘫的治疗,以及“绕过”胃的新疗法,可能会缓解帕金森病的运动波动和症状。
饮食蛋白质限制可以减少摄入的氨基酸和左旋多巴之间的竞争,以实现通过肠道上皮和血脑屏障的可饱和主动运输;然而,由于人们认识到体重减轻、营养不良、肌肉减少和骨质疏松症在帕金森病中已经很常见,并且可能被这种方法放大,因此现在人们往往不鼓励这种做法。
胃肠功能和左旋多巴药代动力学
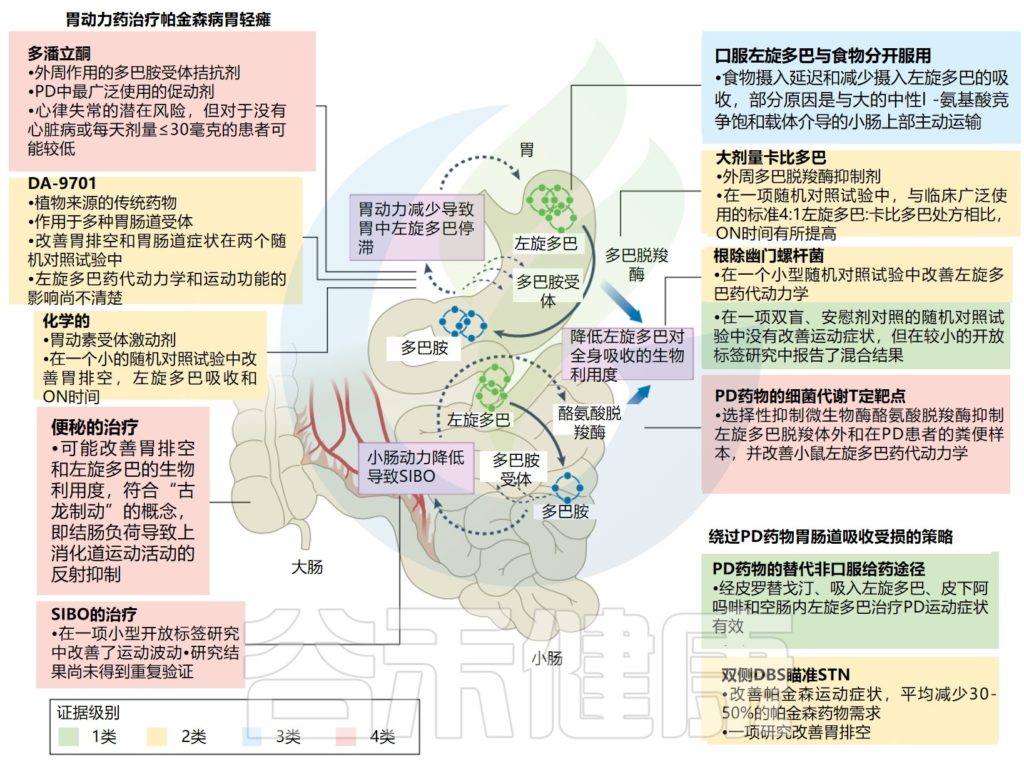
Tan AH, et al.,Nat Rev Neurol. 2022
该图说明了胃轻瘫和小肠微生物活性对帕金森病患者左旋多巴药代动力学的影响,并概述了改善胃肠功能和提高左旋多巴生物利用度的治疗策略。
促动力药物,尤其是多潘立酮,是治疗帕金森病相关胃轻瘫的主要药物,临床试验证明了DA-9701和Camicinal (胃动素受体激动剂)等新型促动力药物的潜在益处,而其他药物,如5-羟色胺5-HT4受体激动剂莫沙必利和普鲁卡因丙利、组胺激动剂尼扎替丁和胃饥饿素(ghrelin)激动剂对帕金森病的益处的证据仍然有限。
从食物中单独口服左旋多巴或与大剂量卡比多联合使用可以帮助提高左旋多巴的生物利用度。一些临床研究探讨了幽门螺杆菌感染、小肠细菌过度生长(SIBO)和便秘治疗对左旋多巴生物利用度和帕金森病运动反应并发症的影响。
肠道微生物在左旋多巴代谢中的作用也得到强调,并可能开辟新的治疗途径来改善帕金森病药物的吸收。绕过胃肠道的策略,包括非口服形式的多巴胺替代品和DBS,是治疗帕金森病运动症状的可能选择。
高度多样化的肠道微生物群及其丰富的酶库可以将许多药物转化为活性更高或活性更低的代谢物,现已被认为是药物药理、疗效和毒性个体间差异的主要因素。
在一项开创性的研究中,在271种不同的口服药物中,三分之二的药物被76种人类肠道细菌分离物中的至少一种显著耗尽,每种菌株代谢11-95种不同的药物。
细菌酪氨酸脱羧酶的发现可以在小肠中将左旋多巴转化为多巴胺,从而限制其生物利用度并可能导致外周多巴胺能不良反应,这为帕金森病患者对左旋多巴观察到的显著个体间反应提供了一种解释。
粪肠球菌(Enterococcus faecalis)是负责左旋多巴脱羧的主要微生物。考虑到小肠细菌过度生长与运动严重程度和波动之间的关联,推测小肠中的细菌过度生长会导致酪氨酸脱羧酶或其他代谢左旋多巴的细菌酶的产生增加。
值得注意的是,左旋多巴肠道细菌代谢产生的多巴胺也会损害肠道运动,可能导致恶性循环,增加小肠细菌过度生长。
然而,目前几乎没有直接证据支持这些观点,部分原因是进入小肠的技术困难。帕金森病的所有研究都使用呼吸试验评估小肠细菌过度生长,如前所述,缺乏标准化。
一项针对18名帕金森病患者的小型研究发现,使用利福昔明进行西博治疗不会影响左旋多巴的药物动力学,但会改善治疗的及时性(但6个月后复发率为43%)。
肠道微生物也可以通过间接机制与左旋多巴相互作用,包括肠道环境的变化(例如,粘膜损伤和炎症),导致细菌降解产物与左旋多巴之间的无效吸收和竞争,以在小肠中进行主动转运。
例如,幽门螺杆菌相关性胃十二指肠炎伴胃低氯酸盐被认为可减少左旋多巴的吸收,左旋多巴在酸性降低的环境中溶解性较低。然而,幽门螺杆菌感染对左旋多巴药代动力学的影响尚不清楚。
一项小型研究(n=34)发现根除幽门螺杆菌后左旋多巴药代动力学得到改善;然而,另一项较大的研究(n=73)没有发现帕金森病幽门螺杆菌阳性和阴性患者之间左旋多巴的药代动力学有任何差异。
此外,尽管几项小型开放标签研究发现根除幽门螺杆菌后运动结果显著改善,但2020年发布的一项双盲、安慰剂对照、随机临床试验(DBPC-RCT)在短(12周)或长(52周)随访后,未发现运动功能或运动波动(使用MDS-UPDRS和可穿戴传感器评估)或生活质量的改善。小肠细菌过度生长状态不影响本研究的结果。
虽然在本研究中根除幽门螺杆菌与任何临床意义的改善无关,但从长远来看或在疾病早期阶段,仍有可能改变根除幽门螺杆菌对帕金森病的影响。
各种微生物导向疗法有望在各种情况下进行症状管理或疾病治疗,但临床试验患者人数相对较少。
最好的证据来自粪菌移植(FMT)对严重梭状芽胞杆菌感染的治疗,证明了约90%的疗效,并为这些方法的临床应用提供了概念证明。
前面我们已经知道,饮食可以通过微生物群-肠-脑轴影响肠道微生物群的组成和中枢神经系统的神经活动。
★ 地中海饮食
前面已经提到,地中海饮食与帕金森的关联。
也有研究表明,坚持地中海饮食与前驱帕金森病的低发病率显着相关。
最近的一项随机临床试验调查了地中海饮食对帕金森病患者认知功能的影响,发现坚持地中海饮食可显着提高执行功能、语言、注意力、记忆力并改善认知功能。因此,地中海饮食可能是减少帕金森病发病和发展的有前景的干预策略。

地中海饮食
地中海饮食是以大量植物性食物为特征的健康饮食模式,如水果、蔬菜、谷类、豆类、坚果等,中低量的乳制品,以橄榄油为主,少量和中等量的鱼和肉,以及少量的红肉,用香料代替盐。
高膳食纤维是地中海饮食的特点之一。膳食纤维结构的细微变化可能强烈影响肠道微生物群的组成和功能。
扩展阅读:你吃的膳食纤维对你有帮助吗?
将富含抗氧化剂的食物(对整体大脑健康很重要)加入饮食中。包括颜色鲜艳的和深色的水果和蔬菜。前瞻性研究发现膳食维生素 E 和胡萝卜素的摄入可以降低患帕金森病的风险。这些抗氧化剂可以中和氧自由基的作用,减少氧化损伤。
橄榄油是地中海饮食的主要脂肪来源,主要含有单不饱和脂肪酸,具有抗氧化活性并抑制α突触核蛋白聚集。橄榄油中的酚类化合物具有抗炎、抗氧化、神经保护和免疫调节活性。
补充水分,每天至少应饮用 8 杯水。
需要限制或避免摄入的:
避免食用含有大量胆固醇或饱和脂肪的食物,少吃肉类(尤其是红肉类)也很重要。
糖、盐、饮料的摄入量也应该严格限制。
尽量限制加工食品的摄入。
★ 禁食疗法
除了我们熟悉的地中海饮食,与预防或治疗帕金森病相关的饮食疗法还包括禁食疗法。
模拟禁食的饮食可以减少 MPTP 诱导的帕金森病小鼠黑质中多巴胺能神经元的损失。
间歇性禁食可以保护疾病动物模型中的神经元,减少多巴胺能神经元的数量并改善帕金森病的运动功能。
关于间歇性禁食详见我们上一篇文章:
间歇性禁食 & 肠道菌群 & 心血管代谢疾病
药物治疗时需要注意避免混合在一起的:
在服用药物治疗帕金森氏症时最好避免饮酒,因为酒精可能会干扰药物治疗。
对于一些帕金森病患者来说,如果服药时间与蛋白质或铁(以铁补充剂的形式)的摄入时间接近,那么服药时间的安排尤其成问题。这些人对药物的吸收很敏感。
总之,饮食可以调节肠道菌群的改变,并通过抗炎、减少氧化应激和神经保护作用对大脑产生影响。饮食介导的治疗可以作为治疗和预防帕金森病的新策略。
益生元主要是不易消化的碳水化合物,短链脂肪酸是由其发酵产生的。益生元是宿主微生物(或施用的益生菌菌株)利用的基质,具有健康益处。
在一项小型开放标签研究(n=19)中,富含不溶性纤维(一种常见益生元食物来源)的饮食改善了便秘、血浆左旋多巴生物利用度和运动功能。
此外,一项有87名参与者参与的开放性研究报告称,在接受益生元干预的帕金森病患者中,使用抗药性进行益生元干预后,非运动症状评分得到改善,粪便丁酸显著增加,粪便钙卫蛋白水平降低。
在仅接受饮食指导的患者中未观察到此类变化,并且两种干预措施均未导致微生物成分或便秘严重程度的显著变化。
帕金森病肠道微生物组的治疗调节
Tan AH, et al.,Nat Rev Neurol. 2022
益生菌是活的微生物,当剂量足够时,可带来健康益处。
两项研究为多系列益生菌的价值提供了I级证据(作为添加益生元纤维的发酵乳服用(n=120)或作为每日一次的胶囊配方(n=72))用于治疗帕金森病便秘,据报道,肠道频率和粪便组成有所改善。
益生菌配方中包括各种乳酸杆菌(Lactobacillus)、双歧杆菌(Bifidobacterium)和肠球菌(enterococcus)菌株。由于这两项研究的干预持续时间仅为4周,因此需要进一步研究,以检查益生菌治疗帕金森病的长期疗效和安全性。
事实上,大多数益生菌制剂中都含有双歧杆菌和乳酸杆菌,但它们是帕金森病患者中已经普遍升高的两个属。肠球菌有时也包括在益生菌中,但已显示出强大的左旋多巴降解能力,强调在PD患者中使用这些益生菌时需要谨慎。
粪菌移植(FMT)对肠道微生物群的调节作用可能通过免疫、内分泌、代谢和神经通路对神经系统疾病的症状或进展产生影响。
粪菌移植在帕金森病患者便秘治疗中的潜在价值已在6名患者的病例系列和11名患者的开放标签研究中显示。
从供体向患者传播传染病或其他微生物介导的特征是与这种方法相关的潜在风险。
在两项研究中,供体粪便菌群均采用内窥镜管理,无重大不良事件发生。目前正在研究粪菌移植(FMT)对帕金森病运动和非运动症状的影响。
抗菌剂减少了许多肠道微生物的数量,可能无法区分有害微生物和有益微生物。此外,反复治疗(例如,反复出现的小肠细菌过度生长)也有产生抗生素耐药性的风险。
上文讨论了根除幽门螺杆菌或治疗帕金森病SIBO的抗生素。尽管在研究后1年的随访中,根除幽门螺杆菌并没有改善临床特征,但潜在的疾病改善效应仍然存在。
在几项研究中发现的安慰剂干预后小肠细菌过度生长状态的自发变化和治疗后相对较高的复发率突出了与研究和试图根除帕金森病患者小肠细菌过度生长相关的挑战。
后生元是指赋予健康益处的无生命(杀死的)微生物和/或其成分的制剂。作用于肠道相关靶点的小分子、生物制剂或代谢物可能包括抑制肿瘤坏死因子、Toll样受体或富含亮氨酸的重复激酶2信号、短链脂肪酸和肠道屏障恢复治疗,如紧密连接调节剂或粘液稳定剂。
其他有可能使帕金森病患者受益的微生物导向药物,包括小分子药物和生物制剂,尚未在临床环境中进行广泛探索。
给予短链脂肪酸和靶向抑制左旋多巴代谢细菌酶似乎具有特别的前景,但仍需在人类干预研究中进行测试。
免疫调节和肠道屏障恢复方法也值得进一步关注。抗TNF治疗可降低炎症性肠病患者的帕金森病发病率,已证明可使炎症性肠病患者的粪便微生物群组成向健康人的粪便微生物群组成转变,丁酸盐和相关底物的粪便水平与临床缓解有关。
针对肠道神经系统中帕金森病相关分子发病机制(例如,涉及α-突触核蛋白或葡萄糖脑苷酶)的策略可能代表另一个新的前沿;在一项开放性试验中,口服角鲨胺(建议以静电方式取代肠道神经元中的α-突触核蛋白聚集体)是安全的,并能显著改善帕金森病患者的便秘症状。
发表在《神经病学》杂志上的一项研究发现,患有早期帕金森病的人每周两次定期通过散步或园艺等活动进行一到两个小时的适度体育锻炼,他们的平衡、行走能力、力量和耐力可能会有所改善。
五年以上经常锻炼的早期帕金森患者,在认知测试中表现更好,症状进展较慢。
每周至少进行4小时中等强度到剧烈运动(比如走路或跳舞)的人,与没有进行那么多运动的人相比,平衡能力下降的速度要晚5年。
有规律的活动,即使是小量的活动,也会有产生影响。
不同形式的体力活动似乎有不同的效果:
研究表明,89% 的帕金森病患者会出现言语和声音障碍,包括声音轻柔、单调、呼吸沙哑和发音不确定。因此,患有帕金森的人不太能参与正常对话,或者对社交环境没有信心。
言语障碍会逐渐降低帕金森患者的生活质量。一个人越早接受基线言语评估和言语治疗,就越有可能随着疾病的进展保持沟通技巧。沟通是帕金森患者生活质量高、充满信心的关键因素。
音乐疗法作为一种发展相对成熟、安全、方便实施而又成本低廉的非药物干预方法,被广泛应用于帕金森病人的康复中。
★ 措施
根据音乐疗法的性质及其应用方式可将音乐疗法分为 3 种类型:
① 主动音乐疗法:
大多采用治疗师与病人合作的方式,通过让病人唱歌、跳舞等形式调节病人情绪,逐步提高病人适应外界的能力,是国外康复机构主要治疗方法之一。
② 被动音乐疗法:
多注重治疗师的引导作用,常在病人休息时进行,让病人在欣赏和感受音乐的过程中,通过音乐的节奏、音色等因素影响人的神经系统,从而达到治疗的作用。
③ 综合疗法:
综合疗法往往是主动、被动双管齐下,并不限于哪种方法的使用,如在绘画时听音乐以陶冶情绪,或用音乐导引练习气功等。通过综合考虑音乐风格、人格类型、文化背景 、兴趣爱好 、职业等因素开出音乐处方实行辨证施乐。
★ 效果
改善运动障碍,增加运动协调性
对11例男性帕金森病人实施音乐疗法方案,用维也纳测试系统(VTS)测量病人在听音乐前后的身体运动协调性,研究发现实施音乐疗法后病人肢体瞄准和直线追踪方面有显著改善。
从华盛顿大学医学院招募了 23 例帕金森病人进行音乐疗法实验,研究者让病人边走边唱自己熟悉且韵律感强的歌曲,结果发现当病人以与舒适的步态步调相匹配的节奏唱歌时,可以改善步态的协调性和稳定性,同时还增强了病人的语言清晰度和声音强度。
18 例帕金森病人随机分为干预组和对照组,干预组采用音乐疗法,病人根据音乐节拍做一些特定的舞蹈动作或跟着音乐唱歌,对照组则采用传统理疗方式,结果显示干预组病人在身体灵活性、步态等方面较对照组有显著改善,病人的跌倒次数也显著减少。
研究平板训练联合音乐疗法对帕金森病人冻结步态的影响,结果显示平板训练联合音乐干预能够显著缓解帕金森病人冻结步态,减少摔跤次数。
提高认知能力,改善吞咽功能和言语障碍
有研究招募了 25 例帕金森病高龄病人为研究对象,实验组病人接受音乐疗法 24 周,对照组不进行任何干预,结果发现实验组病人认知能力、处理速度、注意力、记忆能力较对照组有明显改善。
美国一项研究对 27 例帕金森病人进行音乐疗法干预后,病人吞咽功能明显改善,同时说话吐字也更加清晰,但在实验干预的过程中使用多个研究人员进行干预和评估,无法保证被测病人的 2 次评估是由相同的研究人员完成,因此不同的评估者的主观因素可能会影响评估结果。
对 4 例帕金森病人进行了为期 1 个月的音乐干预,结果显示音乐疗法提高了帕金森病人的声音强度和语言清晰度。和谐而又有节奏感的音乐能够有效改善帕金森病人的认知能力,同时也有利于病人的言语康复。
改善负面情绪,提高病人生活质量
将80 例帕金森病人随机分为对照组和实验组各 40 例,对照组接受常规治疗,实验组病人在常规治疗的基础上接受音乐干预,通过汉密尔顿抑郁量表评估干预后的效果,结果显示实验组抑郁评分明显下降,并激发了病人积极的情绪状态。
对 32 例帕金森病人进行为期 3 个月的随机对照实验发现,接受音乐干预的帕金森病人调节情绪的能力明显提高,同时病人也对音乐疗法提供的社交和创造性的交流方式表达了欣赏和喜爱,幸福指数也明显增高。
镁
矿物镁的摄入量低会使过量的重金属和毒素在大脑中沉积,从而导致帕金森和阿尔茨海默病。
当有足够的镁存在时,重金属不能在小肠中被吸收。镁在保护神经元免受铝和汞中毒的致命影响方面起着至关重要的作用。
镁也是治疗震颤最重要的自然疗法之一。研究人员发现,每天服用镁补充剂可以缓解手部震颤的症状。
富含镁的食物:
B族维生素
缺乏维生素 B9 和 B12可能导致最初表现为抑郁、焦虑甚至精神病的大脑问题。其他 B 族维生素可用于防止与年龄有关的脑萎缩,并可能防止记忆丧失。
谷胱甘肽
谷胱甘肽是抗氧化剂,能有效中和自由基损伤,并大大减少破坏神经元的氧化应激。
葡萄籽提取物
具有超强抗氧化作用,可减少大脑中的 DNA 碎片。它能够进入大脑,保护脑细胞免受自由基损伤。
帕金森病微生物组研究的当前差距和未来方向
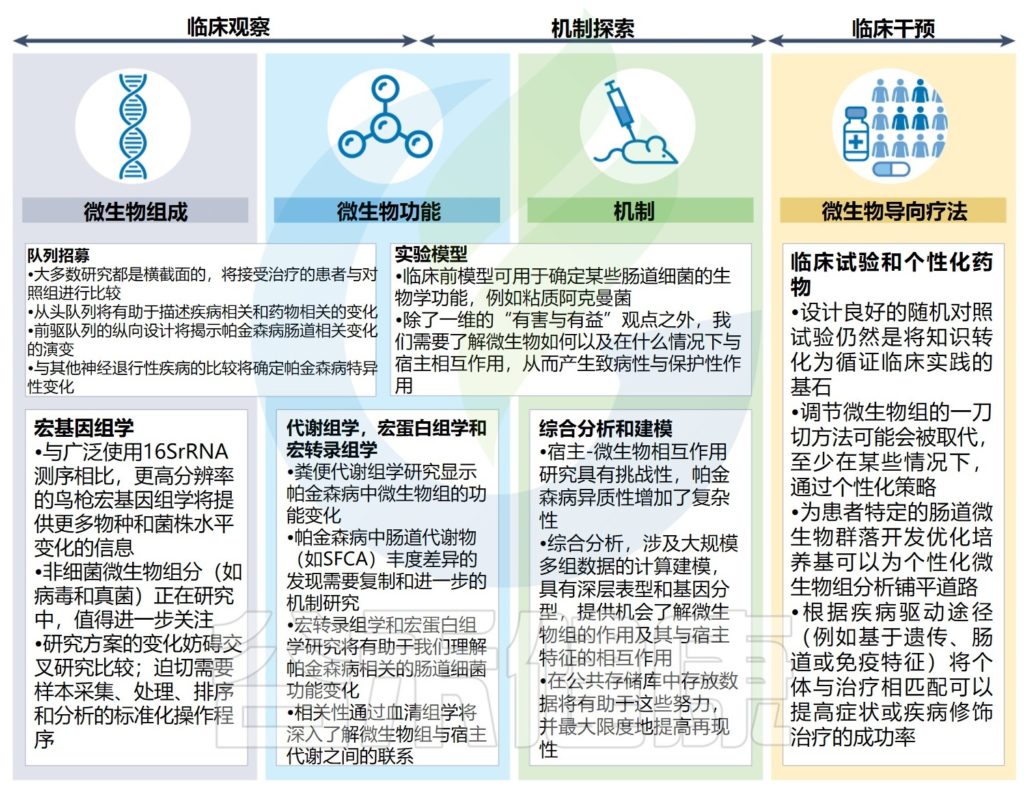
Tan AH, et al.,Nat Rev Neurol. 2022
帕金森病微生物组研究重点正在从研究微生物组结构和潜力(即肠道中存在哪些微生物及其相对丰度和代谢潜力)转向通过使用多组学平台和机理研究来了解微生物功能。
根据观察性研究和基本机制研究的结果,以回答有关肠道微生物和代谢物在帕金森病发病、维持和进展中的作用的基本问题,该领域有望发展到微生物导向疗法的临床试验,从而将微生物组学转化为这种疾病患者的临床现实。
目前,有关肠道相关因素与人类帕金森病之间关系仍然存在很大的相关性,现在需要从观察性研究设计过渡到干预性研究设计。
然而,一些问题仍然存在,确定改变是否是疾病过程的因果关系或促成因素将是至关重要的。例如,与肠道微生物组分的相关性——可能反映了对疾病因素(如转运时间改变或炎症)的次要或共同的非特异性反应。
总之,关于胃肠道参与神经退行性路径,许多疑难杂症仍有待解开。我们希望这一领域的科学进步可以给人们带来新的诊断、预后和治疗方法,最终将改善帕金森病患者及其家人的生活质量。主要参考文献:
Tan AH, Lim SY, Lang AE. The microbiome-gut-brain axis in Parkinson disease – from basic research to the clinic. Nat Rev Neurol. 2022 Jun 24. doi: 10.1038/s41582-022-00681-2. Epub ahead of print. PMID: 35750883.
Wang Q, Luo Y, Ray Chaudhuri K, Reynolds R, Tan EK, Pettersson S. The role of gut dysbiosis in Parkinson’s disease: mechanistic insights and therapeutic options. Brain. 2021 Oct 22;144(9):2571-2593. doi: 10.1093/brain/awab156. PMID: 33856024.
Menozzi, E., Macnaughtan, J. & Schapira, A. H. V. LRRK2 parkinsonism: does the response to gut bacteria mitigate the neurological picture? Mov. Disord. 36, 71–75 (2021).
Nishiwaki, H. et al. Short- chain fatty acid- producing gut microbiota is decreased in Parkinson’s disease but not in rapid- eye-movement sleep behavior disorder. mSystems 5, e00797-20 (2020).
Vascellari, S. et al. Clinical phenotypes of Parkinson’s disease associate with distinct gut microbiota and metabolome enterotypes. Biomolecules 11, 144 (2021).
马春潮.帕金森的防治[J].开卷有益-求医问药,2021(09):35.
Koutzoumis,D.N. et al. Alterations of the gut microbiota with antibiotics protects dopamine neuron loss and improve motor deficits in a pharmacological rodent model of Parkinson’s disease. Exp. Neurol. 325, 1 13159 (2020).

谷禾健康
写在前面
排便行为虽然是人类普遍存在的经历,但我们一般很少提及这个生理过程,开启“便便”这个话题并不是容易的事。如果可以抛开偏见,厌恶或者羞耻感,或许你可以尝试去了解更多这方面相关知识。如果这些知识能够普及更多人,或许世界上可以少一些胃肠道疾病患者。

排便是一个复杂而协调的过程,它整合了多个生理系统,包括神经、肌肉、激素、认知系统等。
结肠基本知识
在了解排便过程之前,我们先认识一些关于结肠结构的基本知识。
结肠和肛门直肠的神经肌肉解剖结构
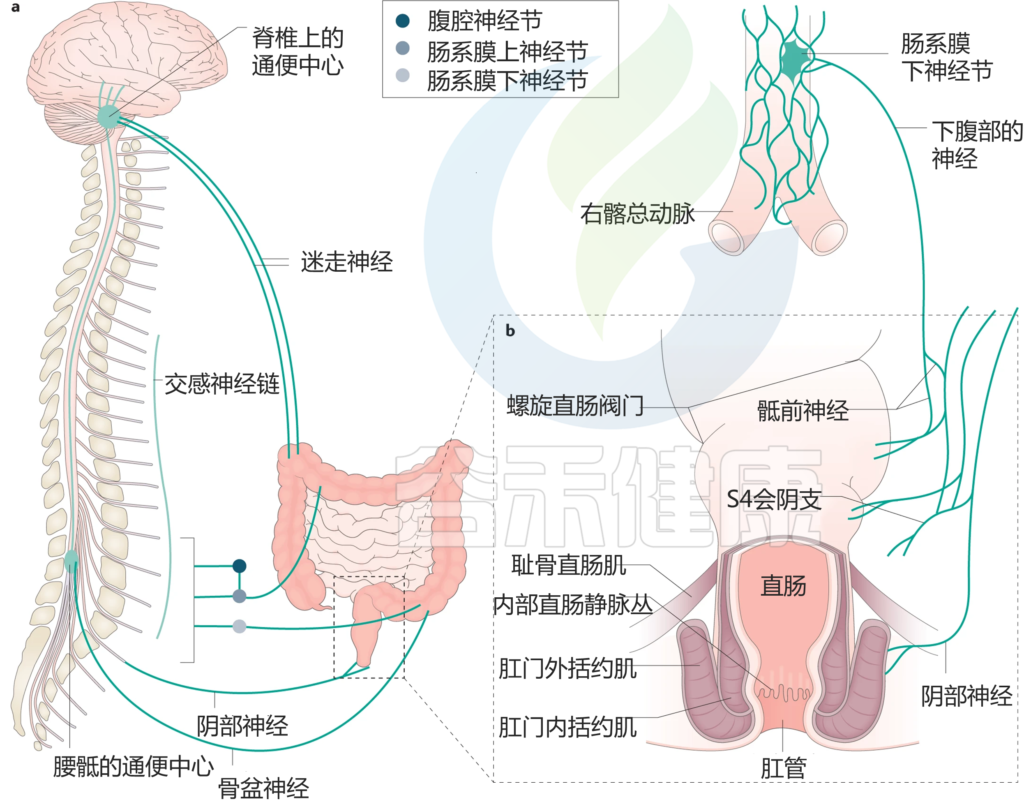
Heitmann PT, et al., Nat Rev Gastroenterol Hepatol. 2021
a| 结肠和肛门直肠与排便生理有关的外源性感觉运动神经支配。
b| 肛门直肠的冠状图,显示了克制中结构重要性的特征。
结肠是一个粘弹性管状器官,从近端回盲肠交界处开始,远端直肠乙状结肠交界处结束。成人结肠长约130厘米,盲肠的管腔直径为60-80毫米,乙状结肠的管腔逐渐狭窄至25毫米。
结肠接受来自肠神经系统的内在神经支配,来自腰神经的外在交感神经支配,以及来自迷走神经(近端结肠)和盆腔内脏神经的外在副交感神经支配,这些神经支配结肠的感觉运动功能。
便便的产生
我们吃进去的食物在体内经历了什么?是如何变成粪便排出的?
进食的时候,食物与唾液相混合,唾液浸湿食物,同时也含有消化淀粉和脂肪的酶。
随后食道将食物推向胃。胃酸、胃液、酶进一步分解,完成后食物就到了小肠。
在胰腺、胆囊、微生物群的帮助下,脂肪、蛋白质、微量营养素等进一步被分解,通过小肠吸收后到肝脏,剩下的部分则转到大肠。
大肠吸收水分、电解质后产生的粪便进入直肠。直肠积累多了就会向大脑发出信号,大脑考虑现在是否是适合排便的时间。
思考的结果如果是适合的,那么大脑就会向肛门括约肌发出信号,让它放松…
排便过程
关于排便过程,这里主要涉及四个阶段:基础阶段、排出前阶段、排出阶段、结束阶段。下图详细说明了在每个阶段中为保持自制或促进排便所发生的具体变化。
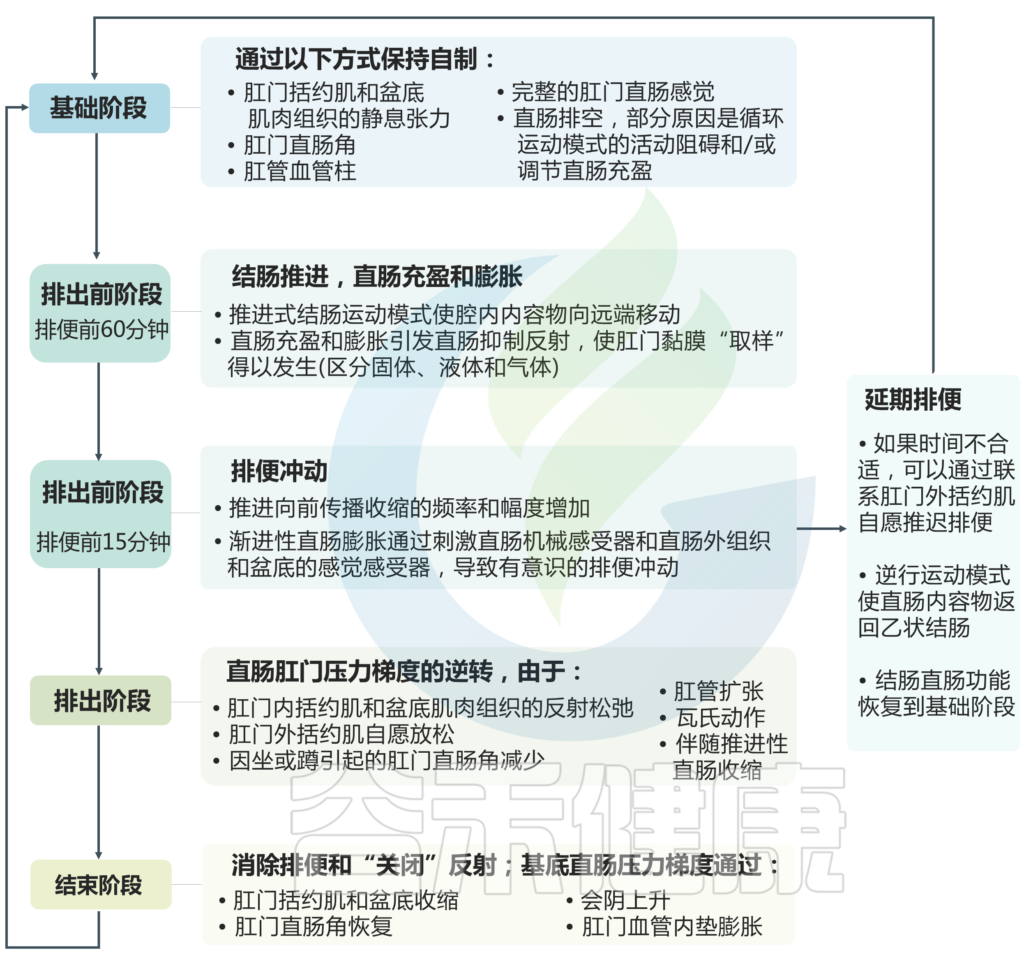
Heitmann PT, et al., Nat Rev Gastroenterol Hepatol. 2021

谷禾健康
便秘的全球患病率为14%。慢性便秘会影响生活质量。健康人相比,便秘还会导致粪便重量降低,且与结直肠癌风险增加相关。
饮食调整是治疗便秘的主要方法之一。世界胃肠病学协会建议通过饮食建议或补充来增加纤维摄入量。在英国,健康专家指南建议食用水果,包括富含山梨醇的水果,例如杏子、桃子和李子,以及相应的果汁。然而,关于水果对肠道运动和便秘的作用机制的证据有限。
本文旨在探讨水果和水果制品对肠道微生物群、肠道运动和便秘的作用机制和有效性。
关于水果中的成分,离不开以下几大成分。
▌ 膳食纤维
水果是膳食纤维的极好来源。
纤维是什么?
纤维是指三个或三个以上单体单元的聚合物碳水化合物加上木质素在小肠中不被消化或吸收的总和。纤维不是一个分子,而是一系列在溶解度、粘度和发酵性方面不同的分子。
纤维会增加粪便体积和生物量
不可发酵纤维完好无损地到达下消化道,而粘性纤维具有较高的水结合能力,因此,这两种纤维都能有效地增加粪便体积。
粪便体积的增加进一步导致管腔扩张并触发蠕动。可发酵纤维增加肠道微生物群的丰度,从而增加粪便生物量,并增加短链脂肪酸的产生。
纤维使粪便变软
这导致结肠渗透负荷增加,从而增加粪便的含水量,从而导致粪便变软。研究发现,各种高纤维食物可以缩短整个肠道的转运时间。
▌ 山梨糖醇
山梨醇是一种在植物中发现的糖醇。山梨醇在小肠内不被消化或吸收,并且能够在其分子中保持水分,从而导致肠腔中水分的增加,从而软化粪便,从而缓解排便。
在一项随机对照试验(RCT)中,与安慰剂相比,每天40克山梨醇持续6天会导致粪便水和粪便重量显著增加。此外,未被吸收的山梨醇到达结肠,在结肠中被肠道微生物群发酵,增加短链脂肪酸的产生,并可能改变微生物群。
虽然这一假设尚未在人类身上得到验证,但与低聚果糖和对照组相比,大鼠体内的山梨醇增加了粪便、结肠和盲肠乳酸杆菌AD102和粪便罗氏乳酸杆菌,并且结肠和盲肠样本中的丁酸含量高于对照组。
▌ (多)酚类
多酚是植物性食品和饮料中的一大类化合物,包括水果、蔬菜、谷物、茶、咖啡和葡萄酒。它们的结构由一个或多个与芳香烃基团结合的羟基组成。
只有一小部分低分子量(聚)酚在小肠中被吸收,而那些高分子量的酚到达结肠时不受影响,在结肠中它们可被肠道微生物群发酵,从而将较大的(聚)酚分解成较小的可吸收分子,可能对多种健康有益。
此外,现有证据表明,(多)酚有可能通过增加有益细菌(如双歧杆菌和乳酸杆菌)来积极改变肠道微生物群,或者通过抑制潜在致病菌的生长。虽然有人假设,由于其抗炎能力(多聚)酚类可能有助于治疗炎症性肠病或肠易激综合征,但目前没有足够的数据显示其对便秘的直接影响。
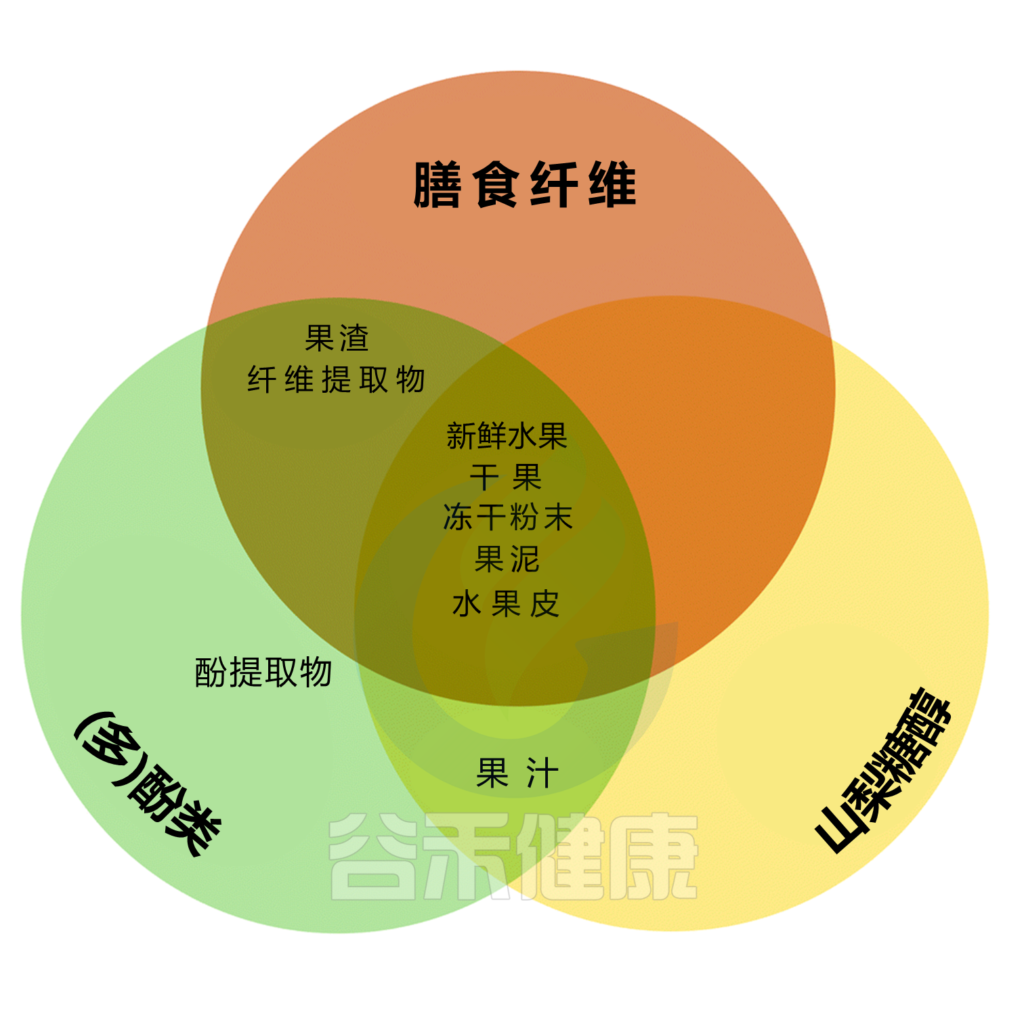
纤维、山梨醇和(多)酚是介导水果对肠道微生物群、肠道运动和肠道功能影响的主要成分,因此可能影响便秘。
不同的水果含有不同数量的纤维、山梨醇和(多)酚类物质,而水果的加工过程可能对这些物质产生重大影响。例如,新鲜或干果、果肉或全果冰沙(用新鲜、纯水果制成的饮料)可能含有大量的纤维、山梨醇和(多)酚,而浓缩果汁或浓缩果汁可能含有山梨醇和(多)酚,但纤维很少。

谷禾健康

便秘是世界范围内高度流行的功能性胃肠道疾病,患病率为 2-20%.
根据罗马 IV 标准,慢性便秘的典型症状是排便困难、不频繁或不完全排便。便秘的症状总是连续不断、反复出现,严重影响患者的身心健康和生活质量。


慢性便秘与多种因素有关,如肠道神经细胞的变化、菌群改变、肌病、神经递质和生态失调。此外,部分原因是其久坐的生活方式,情绪、饮食方式和液体摄入偏少,用药物(例如磷酸盐结合剂)和多种合并症(例如糖尿病,甲状腺疾病等),
而长期便秘会使人心情烦躁、容貌衰老,还可能造成肛肠疾患、胃肠道功能紊乱、心血管疾病和性生活障碍等,同时还会增加溃疡性结肠炎、患结肠癌等疾病的患病率。
最近的流行病学研究表明,便秘与许多不良临床结局相关,例如结直肠癌、肝性脑病、乳腺疾病、阿尔茨海默病、终末期肾脏疾病(ESRD),心血管(CV)疾病和死亡率等。
便秘严重影响生活质量,耗费大量金钱与医疗资源,但目前临床治疗效果却不尽如人意,往往停药便复发,因此寻找新的治疗方法或改进现有的治疗方法,可改善患者生活质量与减少社会医疗负担。
临床上认为一周小于3次的排便就叫便秘,尽管很多患者想力求每天一次才舒适。此外,判别便秘的其他特征和症状还包括:

谷禾健康
可能大部分人都有过:气胀、肿胀或膨胀。对许多人来说,这些可能是短暂的感觉,一般发生在进食后。然而,对于有些人来说,腹胀气和腹胀(腹部膨胀)是慢性和长期并且反复发作严重影响生活质量。
腹胀的患病率很高,在普通人群中为16%-31%,肠易激综合征(IBS)患者中为66%-90%。女性腹胀率普遍高于男性,而便秘型IBS患者(IBS-C)腹胀率高于IBS患者腹泻。
腹胀气和慢性腹胀对生活质量的影响很大。75%的腹胀(无IBS)患者的症状为中度至重度,而50%的患者报告症状导致日常活动减少。
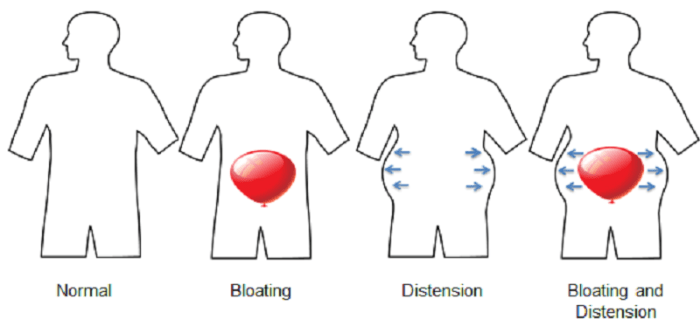
腹胀气(Abdominal bloating)是一种主观感觉,即有气体滞留,或感觉压力或膨胀没有明显可见的扩张。有些时候是一种饱腹感或压迫感,这种感觉可以发生在腹部的任何部位(上腹部、中部、下部或全身)。
腹胀(Abdominal distension)是定义为腹围可测量的增加,是腹围增大的客观表现。患者通常描述他们看起来“像气球”或“像我怀孕了”。

这些症状通常是并存的,当然也可以分别发生。
根据罗马四世的标准定义,腹胀气和腹部胀大通常与其他功能性胃肠道疾病(例如功能性消化不良,肠易激综合征和功能性便秘)同时发生。一项研究发现,只有50%-60%的腹胀患者报告腹部膨胀,从而突出了这些疾病的不同性质。
过去,腹胀气被认为直接与腹部膨胀有关,但最近的研究表明,腹胀并不总是伴有‘腹胀气’,因此腹胀气和腹部膨胀应被视为具有不同机制的独立疾病。
腹胀气和腹胀的病因很复杂,本质上常常是多因素的,而且还不完全清楚。鉴别诊断包括器质性和功能性疾病(下表)。
表 腹胀气和腹胀的常见原因

大多数患者认为,他们的症状是由于胃肠道(GI)内“气体” 数量增加所致,尽管这仅占少数患者的症状。正常的气体产生,吸收和排泄如下图所示。计算机断层扫描(CT)成像显示,只有25%的功能性胃肠疾病(FGID)患者在自发性腹胀发作期间或食用“高胀气”饮食后,管腔气体增加。
正常的气体产生,吸收和排泄
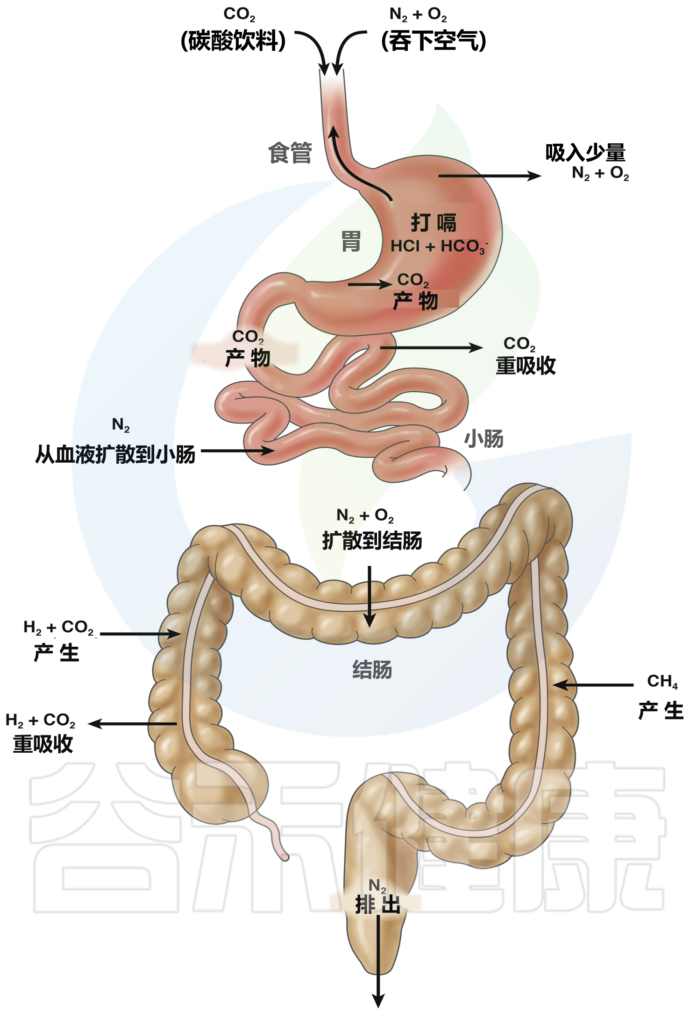
Lacy BE et al.Clin Gastroenterol Hepatol.2021
腹胀和腹部胀大的发生可能有多种原因,包括食物不耐受,先前的感染会干扰肠道菌群,内脏感觉紊乱,肠运输延迟或内脏反常等 (下图)。
腹胀气和腹胀的病理生理学
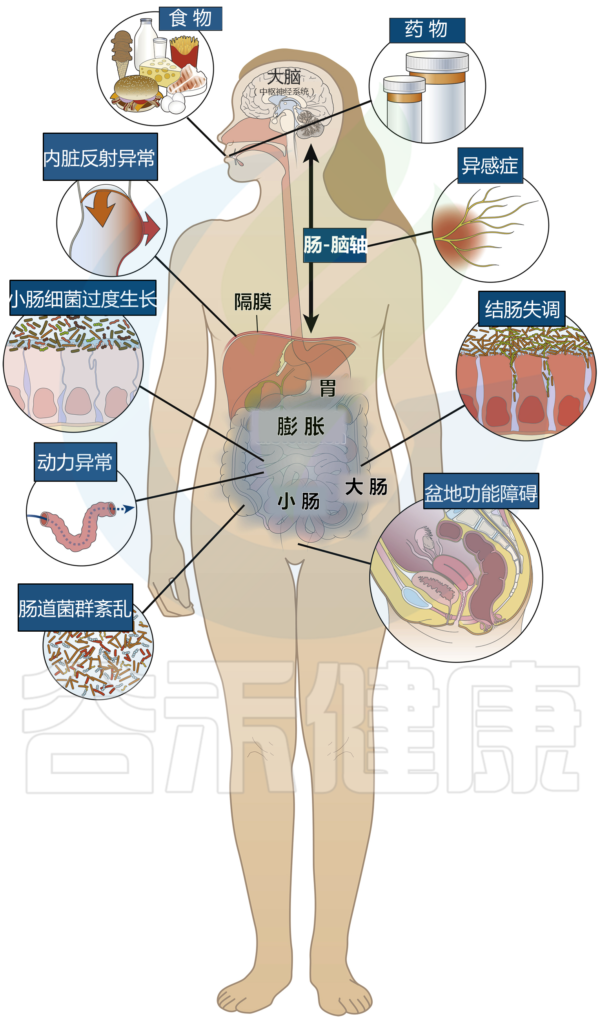
Lacy BE et al.Clin Gastroenterol Hepatol.2021
01 小肠细菌过度生长与碳水化合物不耐受
小肠细菌过度生长(SIBO)和碳水化合物(例如乳糖和果糖)不耐受是导致腹胀气和腹部胀大的常见原因。过量的小肠细菌会由于碳水化合物的发酵而导致症状,随后会产生气体,并导致小肠的拉伸和扩张。
尽管尚未对SIBO患者进行充分研究,但感觉改变和内脏反射异常也可能起作用。碳水化合物不耐受症可能会导致渗透力增加,体液过多滞留以及结肠中过度发酵,从而导致腹胀和胀大症状。
对于诊断SIBO的理想检测方法尚无共识,因此很难确定其真实患病率。 此外,没有前瞻性试验评估单纯诊断为慢性腹胀气和腹胀的患者来确定SIBO或食物不耐受的患病率,因此,大多数数据来自研究较充分的有关FGID(胃肠道功能紊乱)和 IBS数据。
一项meta分析报告SIBO在健康对照组的患病率为0%-20%,而在IBS患者中患病率为4%-78%。
众所周知,饮食习惯可能是造成腹部症状的原因,并且已在努力证明饮食与IBS症状之间的关系。
碳水化合物吸收不良如何通过增加渗透活性和增加细菌发酵产气的生理效应而引起胃肠道症状(例如腹胀)。可能有几个因素起作用,包括:
(1)摄入的碳水化合物量;
(2)进食时是否伴产气食物或其他食物;
(3)胃排空率(餐食进入小肠的速度有多快);
(4)小肠运输时间(一餐进入小肠后进大肠所花费的时间);
(5)膳食中是否含有能分解碳水化合物的酶的细菌;(6)结肠细菌对个人饮食的适应性;
(7)宿主因素,例如是否存在内脏超敏反应。
此外,乳糖不耐症可能导致IBS发生发展。在小肠中,二糖被肠酶分解成单糖,然后被吸收。如果不进行此过程,则二糖到达结肠,然后被细菌酶分解成短链碳酸和气体。因此,IBS患者乳糖吸收不良可能会产生腹胀的症状。
此外,一个新的假设,提出了,过度向小肠和结肠递送高发酵但吸收差短链碳水化合物和多元醇的(统称FODMAPs、发酵寡糖、二糖和单糖类和多元醇)可能会导致胃肠道症状的发展。
FODMAPs是小分子,具有渗透活性,并且与长链碳水化合物相比,发酵非常迅速。这些分子诱导了相对选择性的细菌增殖,尤其是双歧杆菌的增殖,并且间接证明了这些分子可导致远端小肠细菌种群的扩大。
因此,高FODMAP饮食已证明可以使肠道中的氢产生时间延长,发酵引起的结肠扩张,肠腔内渗透负荷增加导致结肠输送量增加以及胃肠道症状的产生。
FODMAP组中的碳水化合物清单以及包含这些碳水化合物的食物的示例
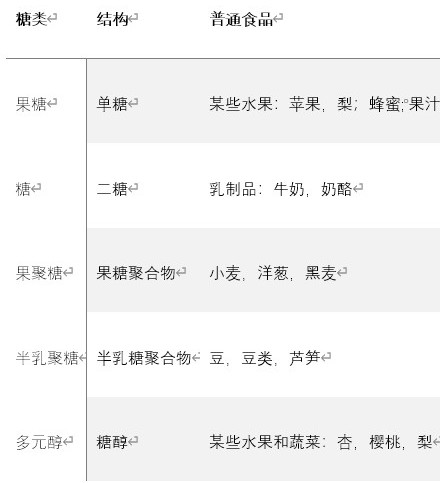
在一般人群中,食物耐受性的症状相似,其患病率约为20% 。糖耐量的真正患病率尚不清楚,因为糖耐量未必与呼气试验中的糖吸收不良有关。
乳糖酶缺乏本身并不会引起吸收不良,因为并非所有乳糖酶缺乏的个体都在摄入乳糖后出现症状。 这表明在某些患者中可能需要其他因素(例如,遗传易感性,内脏超敏性)。
02 肠道菌群异常
比较少研究仅仅关注肠道微生物群在腹胀或腹部膨胀症状发病机制中的意义。相反,许多研究描述了肠道微生物群在胃肠运动、感觉和肠道通透性紊乱中的作用。
通过比较IBS患者和健康对照受试者,确定了肠道微生物群的数量和构成差异,一项研究指出,与患有腹胀的IBS患者和健康对照者相比,没有腹胀的IBS患者中瘤胃菌科和拟杆菌科成员显著减少。
过去几十年的研究表明,在IBS患者的粪便样本中发现了结肠菌群的改变。胃肠微生物群可以分为2个生态系统:管腔细菌和黏膜相关细菌(下图)。管腔菌群构成了大部分胃肠道菌群,它们通过糖类发酵和产气在IBS的腹胀和肠胃气胀中起关键作用。
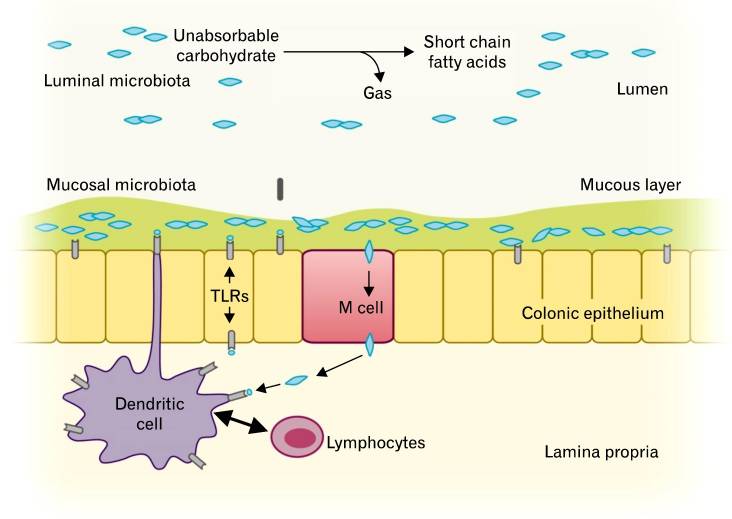
来自韩国的使用16S rRNA基因研究也表明,IBS和非IBS粪便样品之间在多样性和优势方面存在显着差异。此外,这些微生物变化改变了肠道中的蛋白质和碳水化合物的代谢。
来自日本的一项研究还显示,IBS患者的韦荣氏菌( P = 0.046)和乳杆菌(P = 0.031)的计数高于对照组。此外,他们的乙酸(P = 0.049),丙酸( P = 0.025)和总有机酸( P = 0.014)的水平明显高于对照组,这与腹痛,腹胀和肠蠕动等症状有关。
另一项研究表明,IBS患者产生的H2较多,但IBS患者和对照组的总气体排泄量相似。这可能与耗氢细菌在结肠发酵中的变化有关,这可能是IBS发病机理中的重要因素。
破坏宿主和肠道菌群之间的平衡会导致粘膜免疫系统发生从微观到明显的炎症变化,这也会导致肠道感觉运动功能和免疫活性发生变化。
此外,这些改变的微生物群可能在发酵气体类型和体积上产生差异,这可能是腹胀患者症状的原因。已经有一些报道证实结肠菌群产生的气体类型与腹胀之间的关系。
甲烷产量低的人在摄入山梨糖醇和纤维后报告腹胀和痉挛明显增加,甲烷产量高的人显示出严重的乳果糖不耐症患病率低水平。因此,产甲烷菌群的作用在腹胀的发病机理中可能很重要。
03 异常胃肠蠕动
腹胀常见于胃轻瘫患者(超过50%)和小肠运动障碍患者(如慢性假性肠梗阻和硬皮病)。一项对2000多名功能性便秘和肠易激综合征患者的前瞻性研究表明,90%以上的患者出现腹胀症状。
在肠易激综合征患者中,与正常运输的患者相比,结肠运输延长的患者腹胀更大。功能性腹胀和IBS患者近端结肠的气体清除受损,但结肠对气体输送的适应能力正常。
04 盆底功能障碍
肛门直肠运动功能障碍的患者可能会因为有效排空肠胃和大便的能力受损而出现腹胀和腹胀。在便秘患者中,气囊排出时间延长与扩张症状相关。
05 腹腔干扰 (腹肌性神经痛)
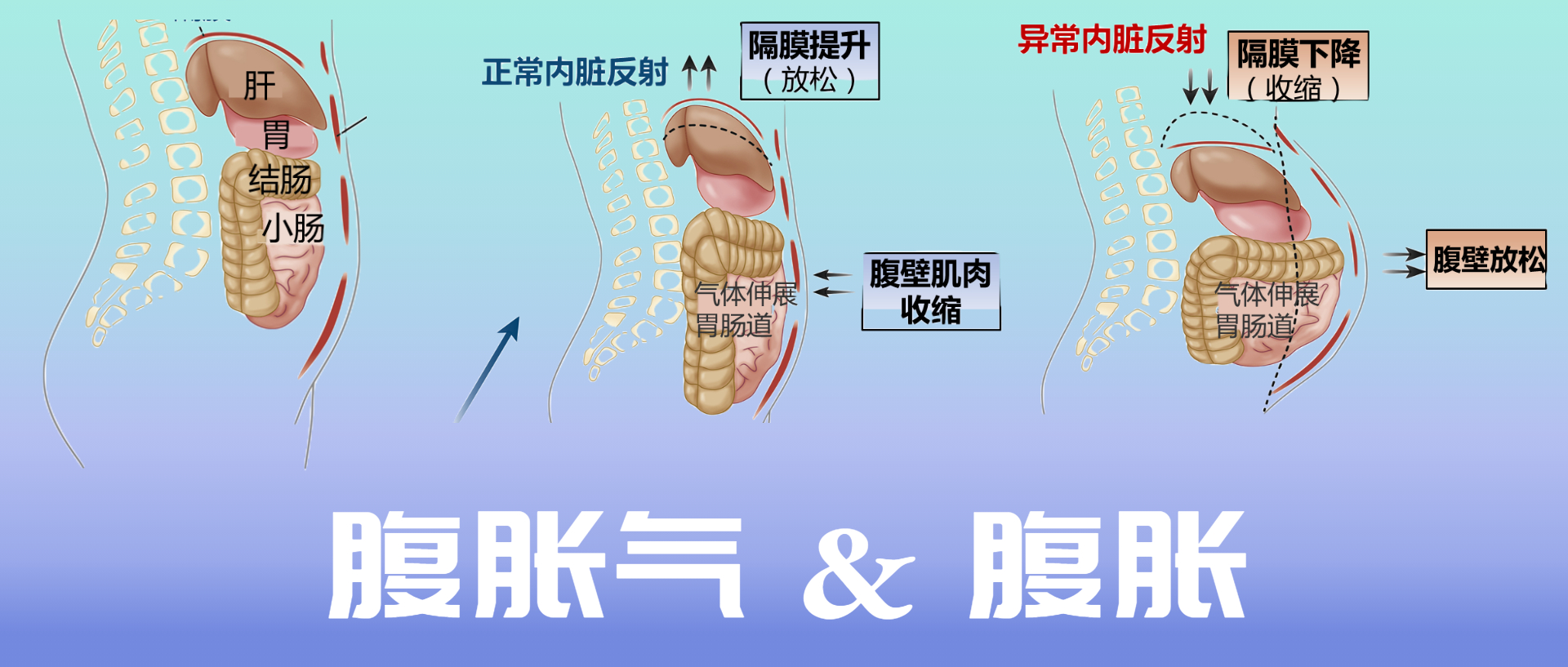
盆腔出口梗阻已被证明会延迟结肠传输。腹腔干扰在一些患有慢性腹胀气和腹胀大的患者中,出现了一种自相矛盾的腹肌反应,称为腹肌神经性神经痛。 在这个过程中膈肌收缩(下降)和前腹壁肌肉放松。这种反应与对腔内气体增加的正常生理反应相反,膈肌放松,而腹前肌收缩,以增加腹腔的颅尾容量而不突出(见下图)。
正常和异常内脏反射
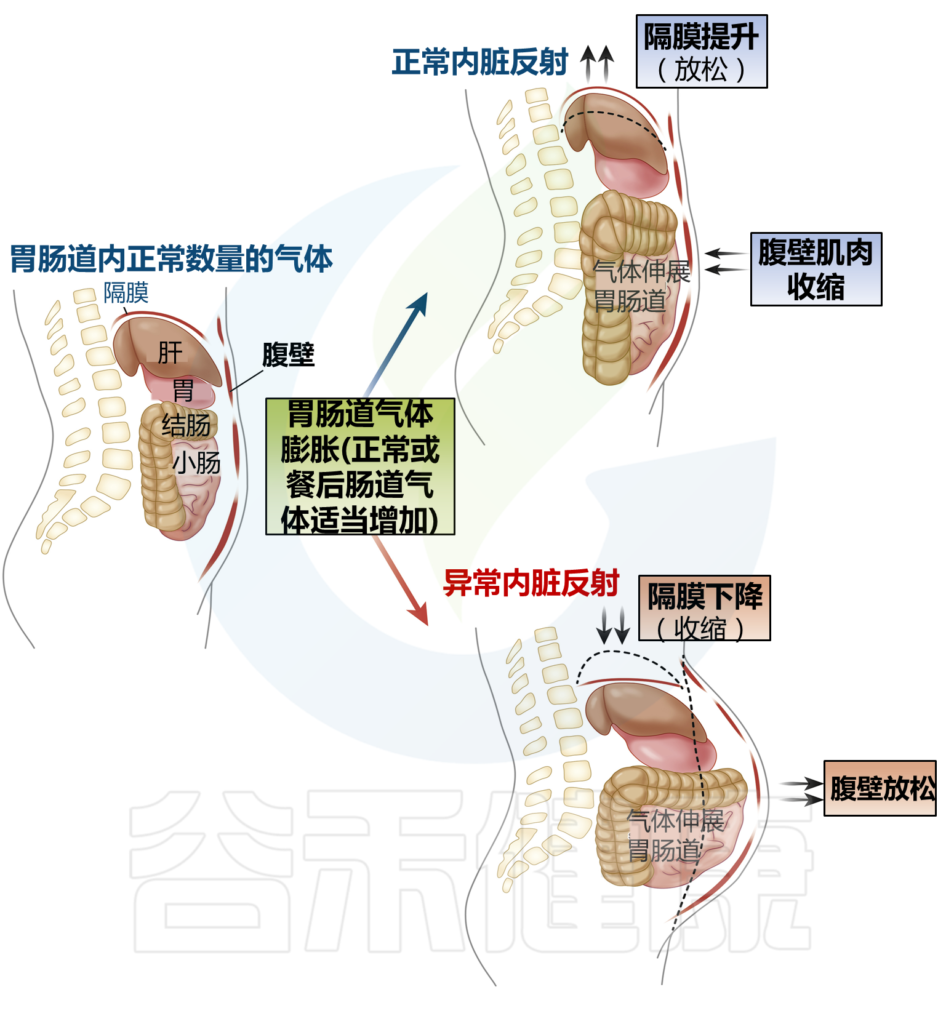
Lacy BE et al.Clin Gastroenterol Hepatol.2021
CT扫描研究表明,腹胀患者的腹壁突出明显,膈肌下降,腔内气体增加相对较小。 相比之下,发现腹胀和肠动力障碍的患者腔内气体含量显着增加,从而导致膈肌上升。在功能性消化不良(FD)和餐后腹胀的症状中,还发现了腹痛性神经痛。
06 内脏过敏
腹胀的感觉可能源自患者的腹部内脏,其中正常刺激或肠道内气体含量的微小变化可能被认为是腹胀。事实上,在一些IBS患者中,小肠收缩的感知阈值低于正常水平。另外,IBS患者中有报道称通过相继性球囊扩张评估了直肠知觉改变。与腹胀和胀气症状相比,仅具有腹胀症状的IBS患者内脏过敏性增高。
在FD患者中发现餐后对胃球囊扩张的敏感性与饭后症状(如腹胀)密切相关。管腔内内容物和腹胀可能会导致症状性腹胀,这可以通过复杂的肠胃神经通路来放大,并进一步受焦虑,抑郁,躯体化和警惕性等因素的影响。
自主神经系统也可能有助于调节内脏敏感性。众所周知,交感神经激活可增加FD患者对肠扩张的感觉。同样,自主神经功能障碍也会影响IBS患者的内脏敏感性。这个机制可以在腹胀发挥作用。
此外,已经提出内脏知觉可能受到认知机制的影响。即,腹胀的IBS患者更加注意其腹部症状,这是一种过度警惕。
另外,患有IBS的女性患者在月经期阶段腹部疼痛和腹胀加重,此时直肠敏感性增强可能会导致腹胀,但不会导致胀气。两者合计,改变的感觉阈值与改变的意识知觉组合可能解释腹胀的机制。
07 肠气积聚
在空腹状态下,健康的胃肠道仅包含约100 mL气体,几乎平均分布在6个隔室中:胃,小肠,升结肠,横结肠,降结肠和远端(骨盆)结肠。餐后气体增加约65%,主要在骨盆结肠。
肠道气体过多被认为是引起腹胀和扩张的可能原因,许多研究人员试图确定这种观点。一些使用腹部平片的研究表明,IBS患者的肠内气体量比对照组大。
但是,腹腔内气体含量与腹胀之间的相关性较差。绝大多数研究不支持过量气体引起腹胀或腹痛。一项使用氩气冲洗技术的研究表明,在腹胀患者和健康受试者之间肠道气体的积聚没有差异。最近使用CT扫描结合现代成像分析软件进行的研究还表明,大多数患者的过量气体与腹胀无关。
因此,这些观察结果表明,增加的气体量可能不是造成腹胀的主要机制,而更常见的是问题的根源是气体的运输或分配受到损害。
08 肠腔内容物
腹胀在没有气体滞留的情况下发展,而可能是由其他肠内容物引起的。通过观察健康受试者对乳果糖或2种类型的纤维(蚤草或甲基纤维素)对膳食补充剂的反应,对气态症状进行了随机,双盲,交叉研究。
乳果糖组的气体通过量,直肠气体的主观感觉和呼吸氢排泄显着增加,而纤维组则没有。但是,所有3组的腹胀感均增加。因此,已经提出,腹腔内增大而不是气态填充可能是腹胀的原因。
在另一项研究中,麸皮在不引起对照组症状的情况下加速了小肠运输并提高了结肠清除率,但IBS腹胀患者的小肠运输并没有进一步加速。因此,他们推测麸皮可能在结肠中引起增加的膨大作用,从而导致IBS患者腹胀加剧。甚至建议应重新考虑在IBS中使用麸皮,因为过量食用麸皮可能会导致IBS患者出现腹胀等症状。
尽管需要更多的研究来进一步了解它们之间的关系,但某些IBS患者的腔内膨大可能会加重腹胀。
09 便秘
许多便秘患者会伴有腹胀。还有一种趋势,即IBS-C患者(便秘型)比IBS-D(腹泻型)患者更普遍,尽管在某些研究中它在统计学上不显着。
粪便由小肠转运以及结肠直肠的运输减慢,会大概率加剧了便秘病人腹胀。另外,便秘可以与麸皮相同的方式通过腔内膨胀作用促进腹胀。
10 心理方面
腹胀是患有IBS的女性的常见症状。当腹胀更加严重时,存在一种增加心理困扰指数的趋势。而且,腹胀患者显示焦虑和抑郁增加,这提出了心理困扰可能导致感觉到的腹胀严重性的假说。
此外,在大量人口调查中,腹胀与精神功能障碍(例如重度抑郁症,恐慌症和睡眠障碍)显着相关。然而,其他研究未能证明心理困扰,要么腹胀或腹胀之间的关系。但是,目前尚不清楚腹胀与社会心理困扰之间是否存在实际关系,需要进一步研究证明这一点。
11 肠道菌群异常
在美国进行的一项基于人群的研究中,IBS中女性性别与腹胀和腹胀症状的增加显着相关,迄今为止,已有类似的发现报道。
虽然在IBS性别角色的问题已经从许多研究提出,性别差异在气胀和膨胀的机制尚不清楚。如前所述,一些研究表明,腹胀是月经的常见症状之一。
激素效果也已推测,即,生殖激素的整个月经周期和在绝经后的变化可以影响肠能动性和内脏感觉。
此外,性别的症状表达差异也被认为是一种可能的解释。尽管关于这些差异的潜在机制的更多研究仍有待确定,但似乎有可能推测,荷尔蒙波动可能导致女性IBS患者腹胀。
治疗可能对患者和提供者具有挑战性,没有任何一种疗法能够持续取得成功。成功的治疗包括确定病因,评估严重程度,教育患者并使患者放心以及设定期望值。治疗选择包括饮食变化,益生菌,抗生素,促运动剂,解痉剂,神经调节剂和生物反馈。
认识到治疗需要个体化,以临床实践中通常遵循的顺序列出治疗方法(下表)。
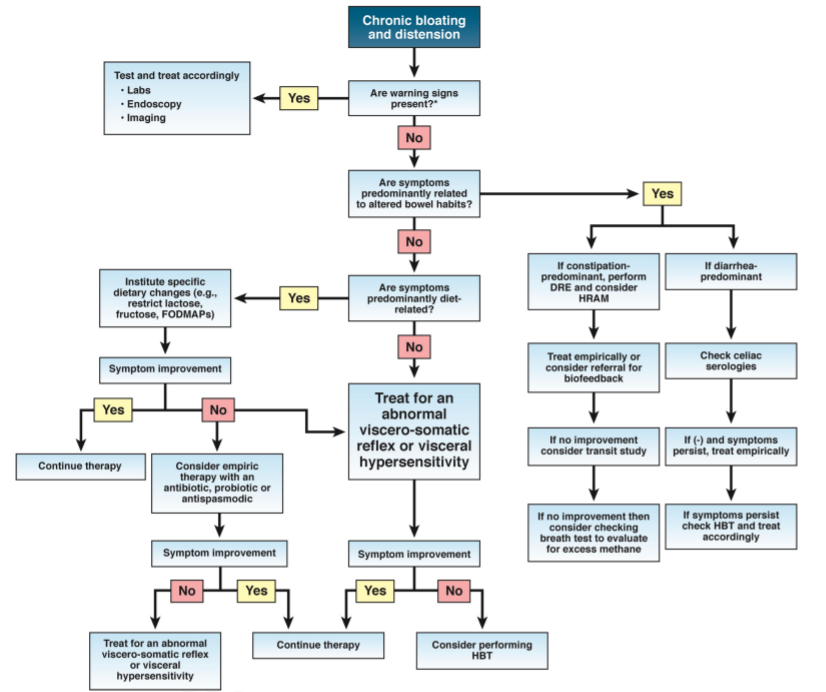
Lacy BE et al.Clin Gastroenterol Hepatol.2021
1 饮食改善
包含吸收不良的糖醇(如山梨糖醇,甘露糖醇,木糖醇和甘油)的人造甜味剂可促进气体产生。
证据表明糖吸收不良的81%的功能性腹胀患者出现症状改善。
大约70%具有非乳糜泻谷蛋白敏感性患者出现腹胀。
与安慰剂相比,以前接受无麸质饮食控制的IBS患者在接受麸质刺激1周后,腹胀明显恶化。
然而,面筋作为饮食的腹胀和其他胃肠道症状的来源的作用是有争议的。有证据表明,果聚糖和FODMAP(可发酵的寡糖,二糖和单糖)是真正的罪魁祸首。两项研究表明,低FODMAP饮食治疗的IBS患者注意到腹胀和腹胀得到改善。如果经验治疗和/或治疗测试不能缓解症状,则建议改善方案。
2 益生菌
益生菌是一种有益于宿主的活微生物,可以修饰肠道微生物组,从而有可能改善腹胀。益生菌的组合和配方很多。但是,评估益生菌腹胀改善情况的设计良好的研究很少。
对干酪乳杆菌菌株GG(Lactobacillus casei strain GG),植物乳杆菌Lactobacillus plantarum和罗伊氏乳杆菌Lactobacillus reuteri的研究表明,IBS腹胀的患者没有益处。
随机分配给L. sporogens / bacillus coagulans的IBS患者的腹胀严重程度评分有显着改善。
而双歧杆菌的研究也证明了疗效。然而,在最近的一项多中心试验中,在从普通人群中招募的受试者中,被包封的婴儿芽孢杆菌35624未能显示出腹胀分数的任何差异。
3 抗生素类
用于腹胀治疗的最常研究的抗生素是rifaximin(利福昔明)。
接受抗生素治疗的IBS患者的总体症状改善与乳果糖氢BT中的氢水平正常化相关。这表明使用抗生素的基本原理是修饰肠道微生物组并减少细菌的产气量。
与安慰剂相比,无便秘IBS的患者每天3次随机服用rifaximin 550 mg,共14天,IBS相关的腹胀缓解率更高。在另一项研究中,与安慰剂相比,每天两次×10天两次接受利福昔明400 mg治疗的IBS患者的平均累积和腹胀特异性评分显着改善(P < .05)。
4 解痉药
如果平滑肌解痉药是由于胃肠道的气体扩张引起的,则可能会改善症状。
对解痉药的两项荟萃分析着重于腹胀或扩张症状。第一个评估了6项研究,涉及885名患者和5种不同的药物。与安慰剂相比,IBS患者的平滑肌松弛剂更有可能改善腹胀症状(优势比为1.46; 95%置信区间为1.10-1.94)。
对涉及1419名患者和4种不同药物的7项研究进行了第二次荟萃分析,发现镇痉药优于安慰剂,尽管两项研究的优势比均为临界值(优势比为1.455; 95%置信区间)。
对IBS患者进行的一项前瞻性,随机,安慰剂对照试验(Rome III标准; n = 285)发现,相比安慰剂,匹维溴铵(Pinaverium bromide) 和西甲硅油(simethicone) 的组合在缓解腹痛和腹胀症状方面更有效。
Pinaverium bromide (匹维溴铵),是一种对胃肠道具有选择性的L型钙通道阻滞剂,能有效缓解疼痛、腹泻和肠道不适,对肠易激综合征 (IBS) 具有有良好的研究效果。
simethicone (西甲硅油)是一种具有表面活性的胃肠道用药,服用后不会被吸收,但是可以改变消化道中存在于食物或者黏液中的气泡的表面张力,使气泡分解。而释放出来的气体可以被肠壁和胃壁吸收,通过蠕动逐渐排出体外。在临床中,主要是用于由于肠道内产气过多引起的腹胀或者是腹部手术后卧床的病人。也可用于胃镜、X线、超声检查等作为双重对比显示造影剂的添加剂,用于消除胃肠道中的气体,使检查得更为清楚。
5 便秘药
在一项对1171例IBS-C(罗马Ⅱ标准)患者进行的随机、安慰剂对照研究中,每天两次lubiprostone(8μg) 改善整体IBS症状和腹胀(P<0.05)。
一项为期48周的lubiprostone开放性研究(24μg(每日两次)在慢性特发性便秘(CIC)患者(n=248)中发现,与基线检查时相比,腹胀有所改善(P<0.011),但安慰剂组不包括在内。
两项随机、双盲、安慰剂对照研究评估了linaclotide (145或290ug)的疗效和安全性。在为期12周的研究中,1276名CIC患者的两种剂量均改善了腹胀症状(P<0.001)。
在一项前瞻性随机研究中,483例CIC患者(罗马II标准)伴有中度至重度腹胀,每天服用一次利那洛肽(Linaclotide) 与安慰剂相比,腹胀症状显著改善。
在一项针对804名患者的3期双盲安慰剂对照试验中,利纳克罗肽除了改善腹胀的相关症状,还改善了IBS-C症状(P<0.001)。
在一项随机试验中,对1394名CIC患者进行的安慰剂对照研究(罗马III标准)与安慰剂相比,每天服用一次3毫克和6毫克剂量的普卡那肽(Plecanatide)均能改善便秘和腹胀症状。
最后,两个相同设计的随机对照组,双盲安慰剂对照研究评估了普利卡那肽治疗IBS-C的疗效和安全性(n=2189)。两种剂量(3和6毫克,每天一次)都能改善腹胀症状(P<0.001)。
Linaclotide (利那洛肽) 是一种有效和选择性的鸟苷酸环化酶C (guanylate cyclase C)激动剂;开发用于研究便秘型肠易激综合症 (IBS-C) 和慢性便秘。
普卡那肽(Plecanatide),由美国Synergy制药公司研发,是尿鸟苷蛋白(uroguanylin)的类似物,含有16个氨基酸的环状多肽,具有促尿钠排泄的鸟苷酸环化酶受体激动药的作用,能调节胃肠道中的酸碱离子,诱导液体转运进入胃肠道,增加胃肠道的蠕动,适用于治疗成人慢性特发性便秘。
6 促动剂
促动剂用于治疗FD(功能性消化不良),胃轻瘫,CIC(慢性特发性便秘)和IBS(肠易激综合征)的症状。
关于使用动力学治疗慢性腹胀和腹胀的数据是有限的。胆碱酯酶抑制剂可改善空肠输注患者的气体清除率。
在一项针对IBS患者的随机,安慰剂对照小型随机研究中,Pyridostigmine在改善腹胀症状方面优于安慰剂(n = 20)。
乙酰硫胺,一种毒蕈碱拮抗剂和胆碱酯酶抑制剂,在日本FD患者中轻微改善,但没有消除与饮食相关的腹胀症状。
对4个随机,对1596名亚裔和非亚裔妇女进行的安慰剂对照研究发现,每天服用2毫克prucalopride(5-HT4激动剂),可改善大便次数,减少腹胀症状。
对34例胃轻瘫患者进行的安慰剂对照交叉研究发现,prucalopride(2毫克,每天一次)改善了全身胃轻瘫症状,包括腹胀和腹胀症状(P<0.0005)。
prucalopride (普卡洛必利),是一种选择性血清素4型(5-HT4)受体激动剂,这是一种胃肠促动力剂,可刺激结肠蠕动,提高肠道运动机能。
7 神经调节剂
在大脑和肠道中起作用的药物已被重新标记为“神经调节剂”。
该组包括中枢和外周作用剂。迄今为止,尚无研究将腹胀作为一种单一症状。FD患者的很大的研究表明,这两种amitriptyline 和 escitalopram(10毫克,每天)与安慰剂相比显著改善餐后腹胀。
对17名FD患者的交叉研究表明,buspirone是一种5-HT 1A受体激动剂,可显着改善整体腹胀的严重程度。
在一项针对23名IBS患者的为期6周的交叉研究中, citalopram(先20 mg,然后40 mg每天四次)显着改善了腹胀的频率和严重程度,而与焦虑和抑郁无关。
8 生物反馈
在一项对45名具有各种FGID的患者的研究中,腹胀发作与内脏反射异常有关。
利用肌电信号提供的视觉指导,对26例患者进行生物反馈治疗,使所有患者都能有效地控制肌肉活动并改善扩张。这些结果在随后的一项随机,安慰剂对照试验中得到了证实,该试验在44名FGID并有餐后腹胀症状的患者中进行。
在一项对52名慢行性便秘患者的研究中,生物反馈疗法显示可显着减少骨盆功能不全和骨盆出口梗阻患者的腹胀症状。
对患有特发性便秘并伴有盆底功能障碍或结肠缓慢转移的各种患者的其他研究还显示,生物反馈疗法后,腹胀症状显着减轻。
没有研究评估使用骨盆底物理疗法来单独治疗功能性腹胀。
腹胀气和腹胀是非常普遍的症状。评估具有腹胀气和腹部胀大症状的患者时,从业者面临许多挑战。
首先,确定潜在的病因,因为这可能有助于查明所需的诊断测试。
其次,识别其他器质性或更严重疾病的警告信号。
第三,评估可能导致腹胀的饮食,药物,医学,外科和行为因素。
第四,考虑引起腹胀和腹胀的主要潜在生理过程,以期开始特定治疗(例如,碳水化合物不耐受的饮食干预与内脏反射异常的行为疗法的比较)。
基于机制的管理性腹胀和扩张应该是理想的,但阐明个别患者的关键操作机制并非总是可行的。通过评估肠蠕动的频率和粪便的稠度以及特殊的成像技术以测量胀气发作期间的腹部形状,可以通过详细的饮食史来收集一些线索。
长期严重的情况下,可能需要将患者转至专门的中心,在该中心可以测量对腔内刺激做出反应的运动性,内脏敏感性和腹肌活动。集中于推测或证明的致病机理的治疗资源包括饮食调节,微生物组调节,促进气体排出,减弱内脏知觉以及通过生物反馈控制腹壁肌肉活动。
最后,提供者应就不同疗法的风险和益处进行深入的讨论,并综合考虑涉及成本,功效和安全性的因素。
主要参考文献
Lacy BE, Cangemi D, Vazquez-Roque M. Management of Chronic Abdominal Distension and Bloating. Clin Gastroenterol Hepatol. 2021 Feb;19(2):219-231.
Malagelada JR, Accarino A, Azpiroz F. Bloating and Abdominal Distension: Old Misconceptions and Current Knowledge. Am J Gastroenterol. 2017 Aug;112(8):1221-1231.
Sandler RS, Stewart WF, Liberman JN, Ricci JA, Zorich NL. Abdominal pain, bloating, and diarrhea in the United States: prevalence and impact. Dig Dis Sci. 2000 Jun;45(6):1166-71. doi: 10.1023/a:1005554103531. PMID: 10877233.
Zuckerman MJ, Nguyen G, Ho H, Nguyen L, Gregory GG. A survey of irritable bowel syndrome in Vietnam using the Rome criteria. Dig Dis Sci. 2006 May;51(5):946-51. doi: 10.1007/s10620-005-9005-0. Epub 2006 May 3. PMID: 16670940.