 国家高新企业 | ISO9001认证
国家高新企业 | ISO9001认证 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康

心力衰竭 Heart Failure(HF)
心力衰竭是一种严重的心血管疾病,其特点是较高的发病率和死亡率,同时也会带来高昂的医疗成本。
一般都认为心力衰竭是老年人的疾病,但其实心力衰竭已经呈现年轻化趋势。


以上症状都有可能与早期心力衰竭相关。发生心力衰竭时,血液通常会回流并导致液体在肺部积聚,从而引发气短。
长期熬夜睡眠不足,不健康饮食,吸烟酗酒,压力大,过度劳累等各种因素日积月累都有可能导致心律失常,诱发突发性心衰。
越来越多的证据表明,心力衰竭与肠道微生物群变化相关。
肠道微生物群失调会导致肠道屏障功能受损,从而使肠道中的有害物质和细菌进入血液循环系统,引发炎症反应。这些炎症因子会进一步损害心脏功能,导致心力衰竭的发生和发展。
肠道微生物群还可以通过产生代谢产物,如短链脂肪酸、TMAO等,影响心血管系统的功能。
本文主要介绍有关肠道微生物群及其代谢物对心力衰竭的影响,以便更好地理解这种多层次的复杂关系。
更深入地了解人体肠道微生物组、心力衰竭和相关风险因素之间的相互作用,对于优化基于微生物群调节的治疗策略和提供个体化治疗非常重要。
本文主要内容:
01 了解心力衰竭
心力衰竭的类型
心力衰竭的症状
心力衰竭的形成
心力衰竭的发病率
心力衰竭的风险因素
02心力衰竭&肠道屏障功能受损和炎症
03心力衰竭的肠道菌群变化
04心力衰竭的风险因素和肠道菌群
西方饮食
肥胖
2型糖尿病
高血压
05与心力衰竭相关的肠道菌群代谢产物
苯丙氨酸
TMAO
短链脂肪酸
胆汁酸
06 肠道菌群与心血管药物的相互作用
强心甙类药物
血液稀释剂
β-阻断剂、ACEi和ARBs
他汀类药物
07 基于肠道菌群的干预措施
饮食方式
特定食物
益生菌
益生元
抗生素
粪菌移植
生活方式
08 结语
心力衰竭是一种心脏疾病,指心脏无法泵出足够的血液来满足身体需要,导致身体器官缺氧和水肿等症状。
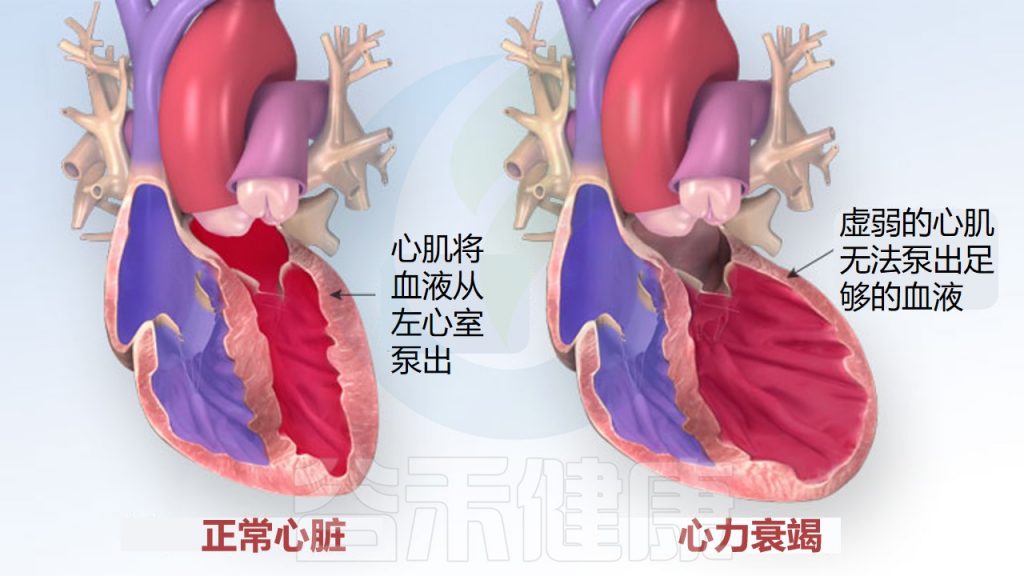

图源:American Heart Association / watchlearnlive.heart
根据急缓程度区分:
两者可以互相转变。
根据部位区分:
左侧和右侧心力衰竭不同,左侧心力衰竭比右侧心力衰竭更常见。
左侧心力衰竭可能出现的症状有:
呼吸困难;咳嗽;疲劳(即使休息后也极度疲倦);手指和嘴唇呈蓝色;嗜睡;注意力不集中;平躺无法入睡。
右侧心力衰竭可能出现的症状有:
恶心(胃部不适)和食欲不振、腹部疼痛(胃周围区域);脚踝、脚、腿、腹部和颈部静脉肿胀;需要经常小便;体重增加。
根据射血分数区分:
注:射血分数是心脏强度的指标。在临床常用于判断心功能的基本情况以及心力衰竭的诊断,射血分数越低,心脏的泵血功能就越弱。
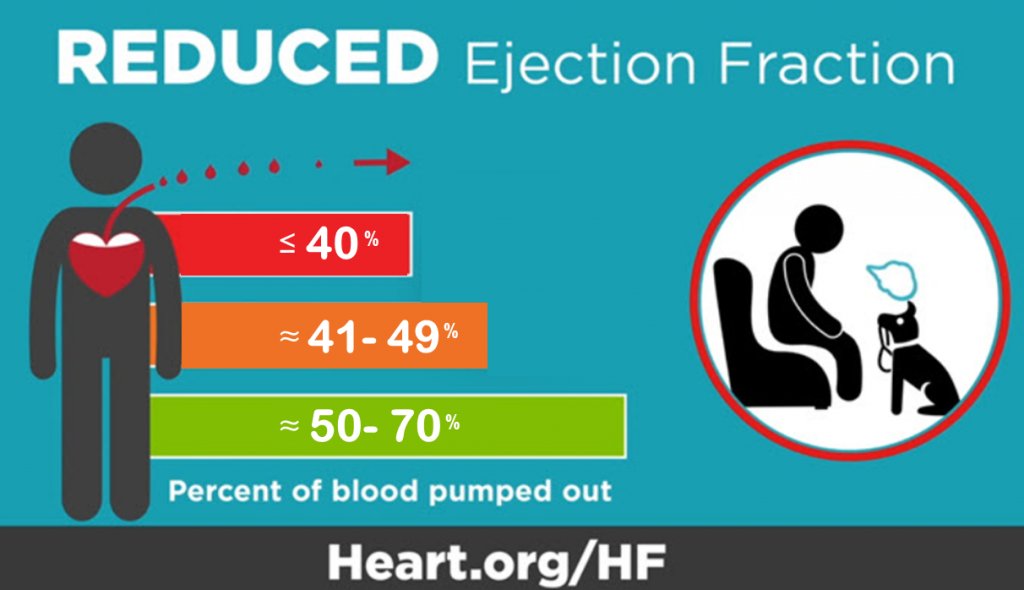

收缩性心力衰竭:心脏无法将足够的血液泵出,导致心脏收缩功能下降。
舒张性心力衰竭:心脏在舒张时无法完全放松和扩张,导致心脏无法充分填充血液,从而降低了心脏泵血的效率。
大多数情况下,心力衰竭是由另一种损害心脏的疾病引起的,比如冠心病、心脏炎症、高血压、心肌病、心律不齐等。
我们知道,心力衰竭是心肌无法泵出足够的血液来满足身体的需求,那么在心力衰竭的初始阶段,心脏会通过一些方式来弥补:
身体还会通过其他方式进行补偿:
以上是身体的补偿机制,这就可以解释为什么有些人在心脏开始衰退多年后才意识到自己的病情。
根据 Framingham 心脏研究的数据,心力衰竭的患病率随着年龄的增长而增加,该研究估计:
50 – 59 岁:
心力衰竭患病率为 8 / 1000;
80 – 89岁:
男性为66/1000,女性患病率为79/1000。
发病率随着年龄的增长而急剧增加:
在 65 岁后,男性心力衰竭的发病率每增加10岁就会翻一倍,而在同年龄段的女性中,发病率会翻三倍。
所有年龄段的血压和BMI越高,终身风险越高。
以下人群更容易患心力衰竭:
心力衰竭中的“肠道假说”表明,肠道微生物群、其代谢物与心力衰竭发病机制之间存在密切关系。
这种细菌易位出现在心力衰竭中,是导致胃肠道结构和功能改变的各种机制的结果,从内脏充血到宿主的免疫防御系统。
心力衰竭的肠-心轴
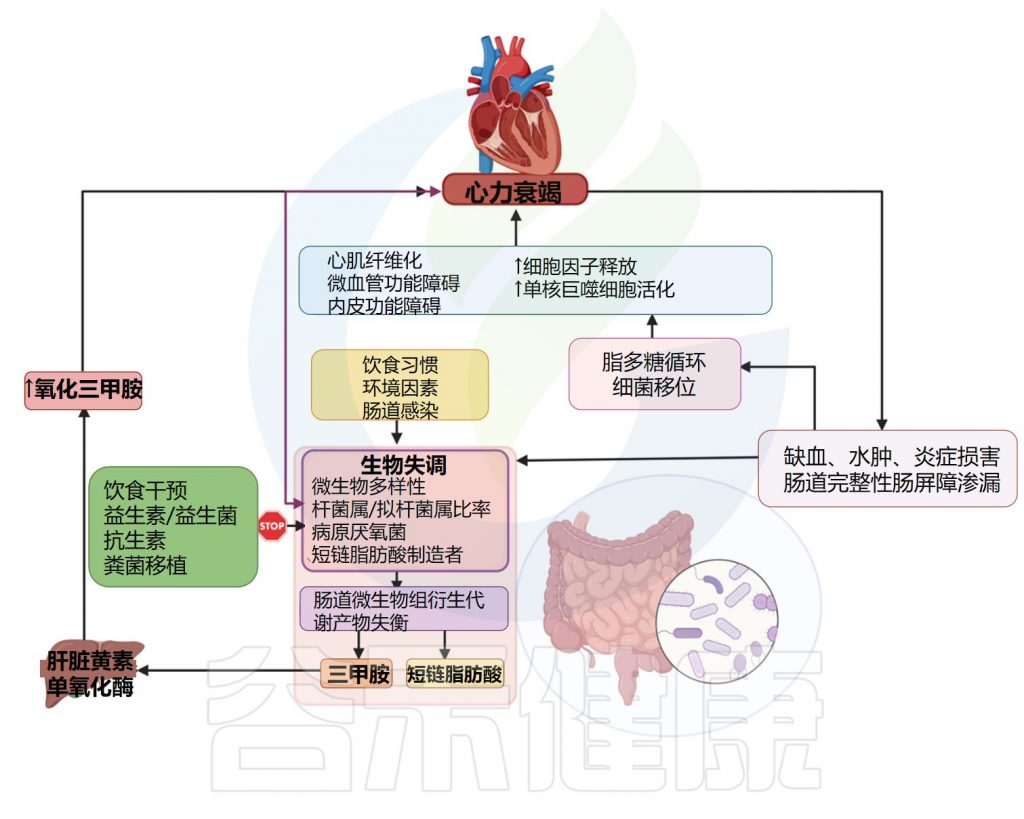

doi.org/10.3390/cells12081158
心力衰竭患者 ⇒ 肠道屏障功能受损
肠道结构和功能的改变是心力衰竭患者微循环紊乱的结果。在这些患者中,尤其是在疾病失代偿的形式中,肠道微生物群落的正常组成被打破,这是由于肠道灌注不足导致的,从而导致局部pH和肠腔缺氧。
肠壁水肿
有证据表明,与心力衰竭相关的肠道上皮功能受损:这种改变似乎是肠道灌注减少和缺血的结果。心输出量降低导致全身循环向多个终末器官的适应性再分配。因此,肠壁水肿增加,肠壁增厚与肠道通透性标志物、血液白细胞和循环C-反应蛋白水平的增加呈正相关。
肠道吸收能力降低,上皮通透性增加
除了肠壁水肿外,心力衰竭还表现为肠道吸收能力降低和上皮通透性增加,促进了多种肠道细菌和/或内毒素(如脂多糖)的通过,从肠道进入全身循环。
脂多糖黏膜屏障功能恶化
脂多糖是革兰氏阴性菌壁的生物活性成分,具有潜在的免疫刺激活性,通过使用Toll样受体4(TLR4)模式识别受体。
在心力衰竭患者中,在肝静脉中发现高浓度的脂多糖,支持肠道菌群的肠道易位过程的假设。此外,据推测,脂多糖本身可以加剧黏膜屏障功能恶化,导致心力衰竭进展。
心力衰竭患者 ⇒ 炎症
内毒素易位导致炎症因子水平升高
内毒素肠吸收刺激系统炎症因子水平的增加。根据目前的数据,心力衰竭与慢性炎症状态相关,这种微生物易位可以诱导或加速炎症,间接影响心肌细胞的正常功能。
循环细胞因子水平升高,心力衰竭患者预后不良,与脂多糖相关
循环细胞因子水平的升高对应于心力衰竭患者生存中更严重的临床症状和更差的预后。心力衰竭患者的血清TNF-α、IL-1和IL-6水平直接受到现有脂多糖数量的影响,目前认为脂多糖是高炎症性疾病的主要因素。
而在失代偿的心力衰竭患者中,脂多糖水平似乎与全身炎症标志物直接相关,并且在心力衰竭代偿后降低。治疗后血浆细胞因子水平并不一定会下降,这表明随着疾病的进展,其影响是持续的。根据两项大型随机安慰剂对照试验,使用TNF- α拮抗剂均不能降低心力衰竭患者的住院或死亡风险。
所有的心力衰竭患者炎症水平上升
另一项针对心力衰竭伴射血分数降低(HFrEF)患者的研究,该患者具有不同的疾病严重程度,或采用了先进的干预措施,如心脏移植(HT)或左心室辅助装置(LVAD),评估了他们的血液和粪便标本。从纽约心脏协会(NYHA)的I级到IV级的所有受试者,炎症标志物水平都有所增加。
治疗后水平下降,但未到正常,脂多糖仍处高位
在左心室辅助装置和心脏移植治疗后,他们的水平下降,但未能达到正常值。然而,所有NYHA级别的脂多糖水平均有所增加,并且在心脏移植和左心室辅助装置干预的患者中仍保持升高。
与脂多糖类似,血清中IL-6、IL-1β和TNF-α水平的升高也诱导肠通透性,促进炎症细胞因子增加和内毒素易位的恶性前馈循环。
肠道微生物群已被证明对心力衰竭有很大影响。心力衰竭患者有更多的致病菌和更少的有益菌。
心力衰竭肠道菌群变化
在心力衰竭中,由于射血分数降低,肠道血流量减少,氧气输送减少。这使肠道容易滋生致病性厌氧菌。
综合目前的研究来看,与对照相比,心力衰竭患者肠道菌群主要变化如下:
下列菌群丰度增加:
↑↑ Escherichia Shigella
↑↑ Streptococcus 链球菌
↑↑ Pseudomonadota 假单胞菌门
↑↑ Klebsiella 克雷伯菌
↑↑ Candida 念珠菌
↑↑ Enterococcus 肠球菌属
下列菌群丰度减少:
↓↓ Faecalibacterium 粪杆菌属
↓↓ Faecalibacterium prausnitzii 普拉梭菌
↓↓ SMB53
↓↓ Dorea longicatena
↓↓ Roseburia intestinalis
↓↓ Collinsella 柯林斯氏菌
α多样性随着疾病严重程度的增加而降低
尽管接受了LVAD或HT等治疗,但仍保持较低水平,这可能是由于持续的炎症。随着心力衰竭发展到晚期,内毒素血症和全身炎症水平增加,细菌群落的肠道多样性降低。
几项关于急性失代偿或稳定型HFrEF患者肠道细菌谱的研究报告称,与健康个体相比,心力衰竭患者的α和β多样性显著降低。
心力衰竭相关的肠道菌群失调因患者年龄而异
与已知患有心力衰竭的年轻患者相比,老年患者表现出拟杆菌门水平下降,变形菌门、假单胞菌门数量增加。
在所有已知的心力衰竭患者中,毛螺菌科的Dorea longicatena和Eubacterium rectale的数量都有所减少,而与年轻患者相比,Clostridium clostridioforme和普拉梭菌(Faecalibacterium prausnitzii)在老年心力衰竭患者中的数量更少。
下表中总结了关于心力衰竭患者肠道微生物群的研究。
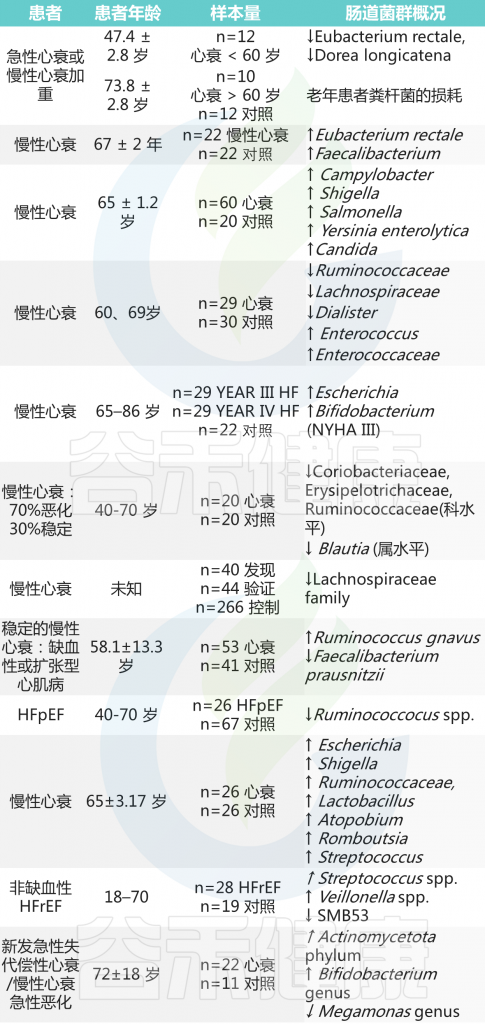

doi.org/10.3390/cells12081158
患有心力衰竭的人有各种危险因素,但他们中的大多数人患有高血压、肥胖、血脂异常、糖尿病、遗传易患心力衰竭、吸烟、久坐不动的生活方式或不健康的饮食。新证据表明,肠道微生物群及其代谢物也可能对心力衰竭危险因素产生影响。
西方饮食的特点是摄入高糖和精制碳水化合物,血糖指数高;抑制一氧化氮合酶的含量,导致心肌氧化功能障碍、心肌肥大和心肌细胞重塑,所有这些都是心力衰竭的诱发因素。
西方饮食:通过菌群代谢增加TMAO,胆固醇积累,动脉粥样硬化,心力衰竭风险增加
这种饮食富含快餐食品会导致微生态失调,其菌群特征是假单胞菌(Pseudomonadota)和Bacillota水平升高,从而增加TMAO和神经酰胺的水平,促进巨噬细胞中的胆固醇积累,并加剧动脉粥样硬化的发展。
西方饮食诱发心力衰竭
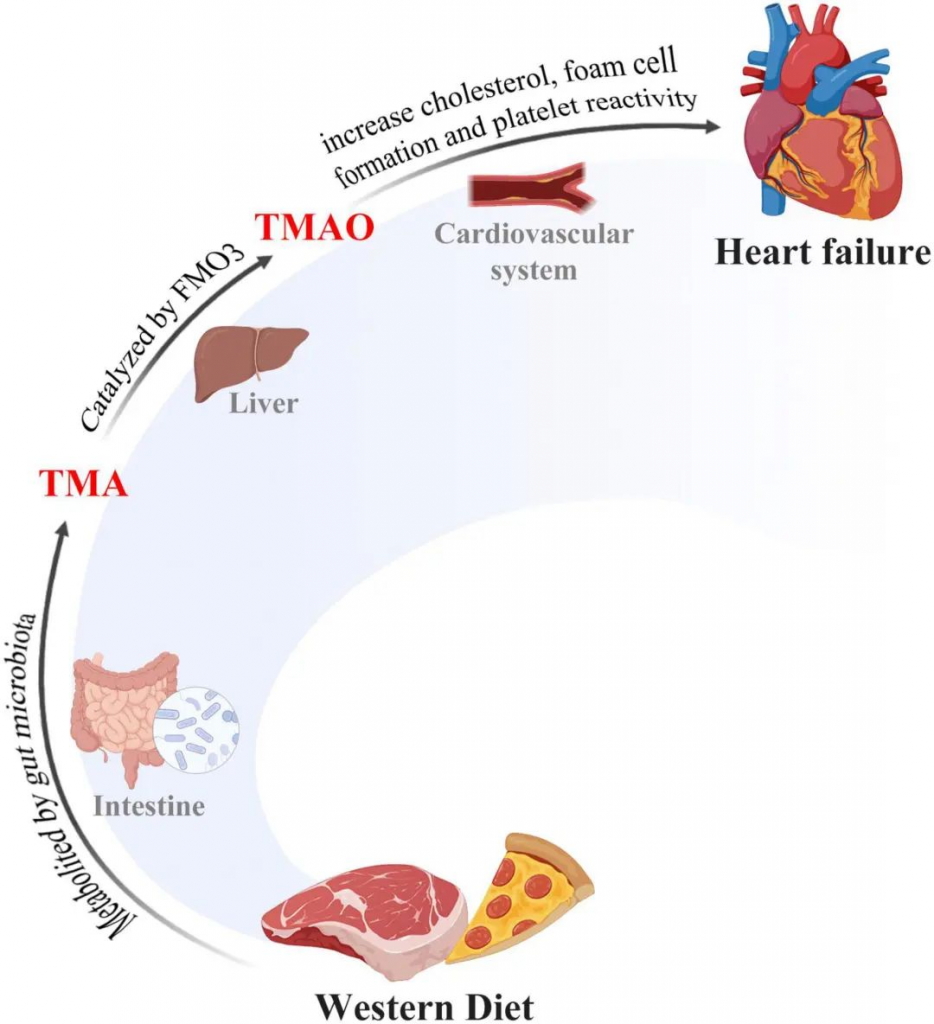

doi.org/10.3389/fmicb.2022.956516
西方饮食通过肠道微生物群代谢为 TMA,然后 TMA 在肝组织中转化为 TMAO。TMAO 积累在许多病理过程中触发胆固醇,包括运输和泡沫细胞形成,从而诱发心力衰竭。
西方饮食还会导致心肌中的脂质积聚、慢性炎症和肥胖。快餐食品加工中使用的盐和食品添加剂(包括亚硝酸盐和磷酸盐)水平的增加与心力衰竭风险的增加有关。它们改变了厚壁菌与拟杆菌的比例。
西方饮食:构建肠道屏障菌群减少,屏障破坏
西方饮食还改变了肠道屏障的通透性,其特征是拟杆菌属、双歧杆菌属、梭状芽孢杆菌属、乳酸杆菌属和Akkermansia muciniphila以及所有促进肠道屏障细菌的水平降低。此外,肠壁完整性似乎被脱硫弧菌属和Oscillibacter的增加所破坏。
扩展阅读:AKK菌——下一代有益菌
研究表明,肥胖及其相关的代谢障碍,包括高脂血症、高血糖和胰岛素抵抗,与心力衰竭密切相关。
肥胖 ⇒ 促炎
肥胖及其相关的心脏代谢因子(胰岛素抵抗、血脂异常和腹部肥胖)加剧促炎环境,也就是促炎细胞因子水平升高。
肥胖 ⇒ 血容量改变
内皮功能障碍和一氧化氮不可用,可能导致HFpEF的左心室肥大以及收缩和舒张功能障碍。此外,肥胖会导致血管系统和血容量的改变,这与氧气消耗的增加有关,导致心室肥大、平均肺动脉压增加和左心室舒张压升高。
肥胖 ⇌ 肠道菌群变化
在动物和人类研究中,在大多数研究中,肥胖似乎与厚壁菌门和拟杆菌门之间的比例改变有关,拟杆菌门减少,厚壁菌增加。肠道拟杆菌数量与肥胖有关。
限制热量饮食并减肥的肥胖者肠道微生物群中拟杆菌类的比例似乎较高。具体而言,所有产短链脂肪酸菌Clostridium bartlettii、Akkermansia muciniphila和双歧杆菌都与高脂肪饮食诱导的肥胖及其代谢并发症呈负相关。
扩展阅读:肠道菌群与肥胖
2型糖尿病是心力衰竭和其他心血管疾病的强相关危险因素。
已知2型糖尿病患者粪杆菌、双歧杆菌、Akkermansia、拟杆菌和Roseburia降低。Roseburia、拟杆菌和Akkermansia具有抗炎作用。拟杆菌和Akkermansia水平下降导致紧密连接基因表达不足,“肠漏”加剧,从而导致内毒素血症。
扩展阅读:肠道重要基石菌属——罗氏菌属(Roseburia)
此外,产丁酸菌普拉梭菌和Roseburia nestiinalis的丰度降低,会导致脂肪酸代谢失调,导致氧化应激及其相关的心脏代谢不良表现。
另一方面,2型糖尿病与梭杆菌属、瘤胃球菌属和厚壁菌门的细菌呈正相关,这些细菌都具有促炎活性。
与血压正常的对照组相比,持续升高的血压患者的厚壁菌与拟杆菌比例更高(高达5倍)。此外,高血压时,肠道菌群以产乳酸菌属(如Turicibacter、Streptococcus)为主,而产短链脂肪酸菌属(如Clostridiaceae、Bacteroides、Akkermansia)似乎减少。其中一些相关的肠道菌群稳态扰动部分与心力衰竭发病有关,并增加心衰进展的风险。
扩展阅读:认识肠道微生物及其与高血压的关系
经典的心力衰竭的生物标志物:利钠肽(NP)、脑型钠尿肽(BNP)、BNP的N-末端原激素和肌钙蛋白测量,已被欧洲心脏病学会和美国心脏协会纳入心力衰竭的诊断和治疗指南。
肠道微生物衍生的代谢物也可以在心力衰竭的发病机制中发挥重要作用。通过产生包括短链脂肪酸、三甲胺(TMA) / 三甲胺 N-氧化物 (TMAO) 和胆汁酸在内的活性生物代谢物,肠道微生物群会影响宿主生理。
影响心力衰竭的微生物代谢产物及相关治疗策略
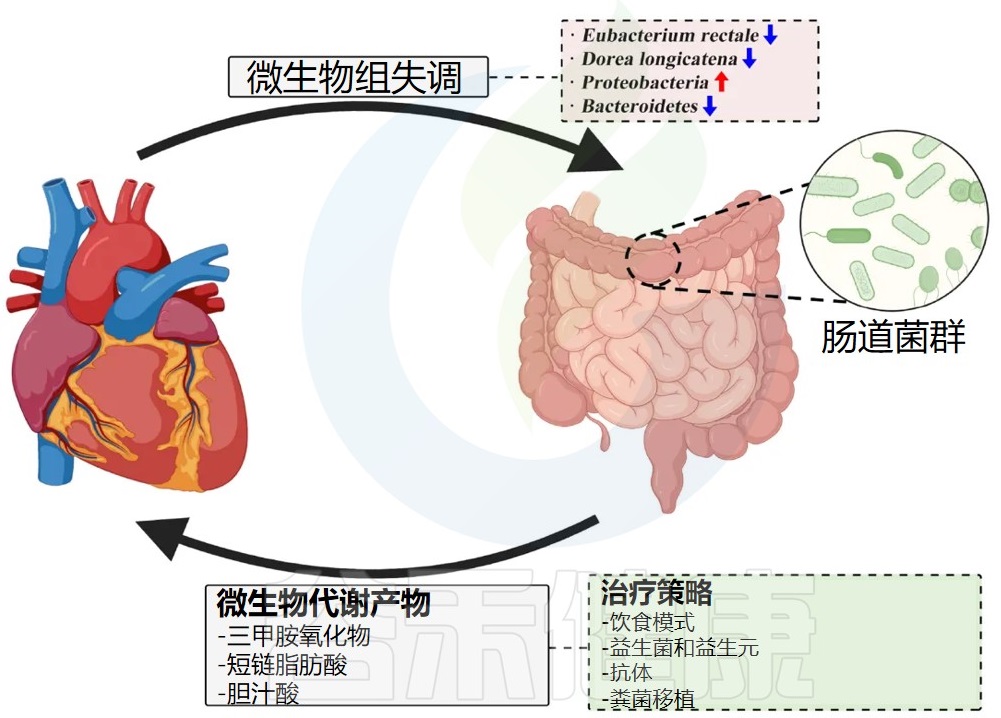

doi.org/10.3389/fmicb.2022.956516
苯丙氨酸:与炎症细胞因子呈正相关,是心力衰竭的独立预测因子
这些代谢物可被视为肠道微生态失调的生物标志物,并且可以预测已知患有心力衰竭的患者的炎症。血浆苯丙氨酸水平升高的患者表现出炎症细胞因子(IL-8、IL-10)、C反应蛋白 (CRP) 水平升高,并伴有更高的死亡率。而甘氨酸表现出抗炎作用,似乎提供保护细胞和心脏。对从 FINRISK 和 PROSPER 队列收集的数据进行的分析中,苯丙氨酸是心力衰竭的独立预测因子。
升高的TMAO水平与心力衰竭的风险相关
TMAO 是一种由包括厚壁菌和假单胞菌属在内的肠道细菌产生的代谢产物,从胆碱、磷脂酰胆碱和左旋肉碱发酵中获得。
高饱和脂肪和高糖饮食导致的 TMAO 水平升高,可导致纤维化、心肌炎症和舒张功能受损。瘤胃球菌、普雷沃氏菌和梭状芽孢杆菌属和毛螺菌科丰度增加,以及拟杆菌门水平降低,表明其血浆中的 TMAO 水平较高。
心力衰竭相关生态失调的特点是循环中高水平的TMAO,能够通过促进心肌纤维化和促炎作用来刺激心脏重塑。现有证据表明,TMAO 水平升高会刺激具有促炎作用的细胞因子(包括 IL-1β 和 TNF-α)的过度表达,以及 IL-10 和其他具有抗炎特性的细胞因子的减弱。
TMAO水平升高可作为急性和慢性心力衰竭的预后生物标志物
与健康人相比,心力衰竭患者的血浆TMAO水平升高。TMAO水平升高可作为急性和慢性心力衰竭的预后生物标志物,独立于B型钠尿肽(BNP)和传统风险因素,因为TMAO水平可预测这些患者的死亡率。
TMAO血浆值升高对应于左心室舒张功能障碍的晚期。TMAO也可被视为HFeEF的预后预测因子和这一特定类别患者的风险分层标志物。
对于住院的心力衰竭急性失代偿患者,TMAO水平升高与肾功能下降相关,可作为心力衰竭恶化死亡或再次入院风险升高的预测指标。
TMAO水平还与血红蛋白、肌酐、BUN和NT-proBNP相关。
肉碱相关代谢产物与不良预后有关
特别是L-肉碱和乙酰-L-肉碱与短期预后(急性事件后30天)有关,而TMAO与长期预后(急性事件后1年)有关。
短链脂肪酸属于胃肠道中肠道微生物产生的代谢产物。短链脂肪酸对心力衰竭具有保护作用,并在维持肠道屏障的完整性方面发挥主要作用:在粘液产生中,它们在抗炎保护中具有活性。
肠道菌群产生的短链脂肪酸对心血管系统的下游影响
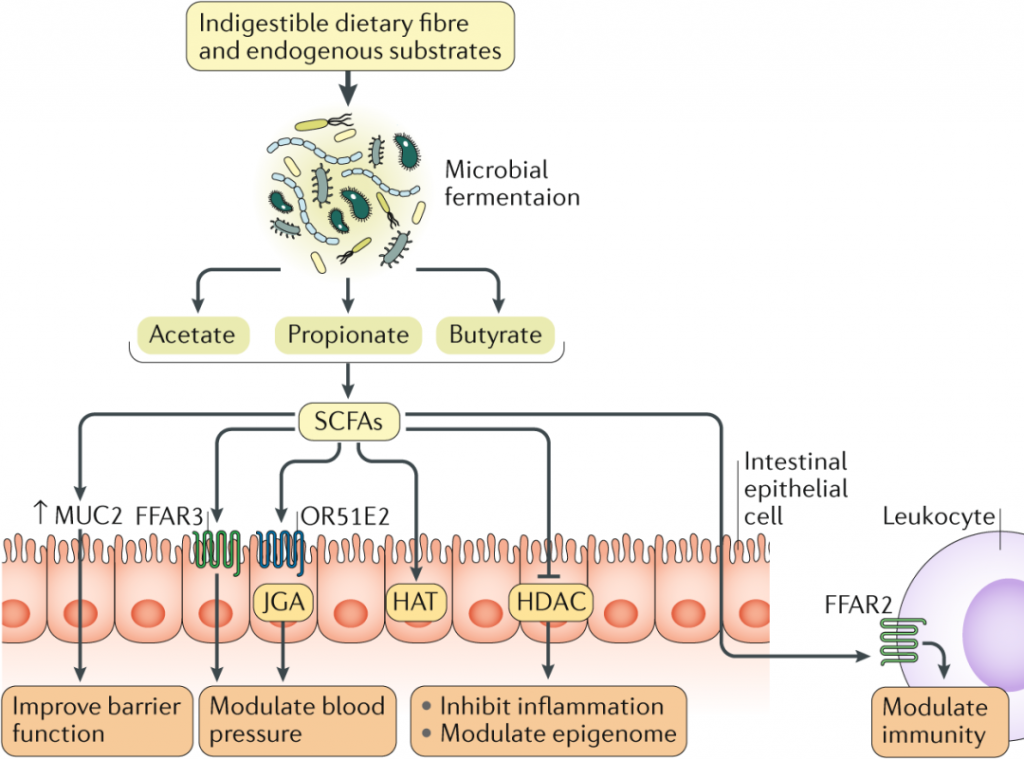

doi: 10.1038/s41569-018-0108-7.
肠道微生物群产生的短链脂肪酸通过以下方式发挥其心血管作用:
胆汁酸(BA)是由肠道微生物合成的胆汁代谢物,在脂质代谢中起着关键作用。饮食习惯、禁食和昼夜节律对胆汁酸的产生和重吸收有影响。
胆汁酸信号传导的受体,如法尼醇-X受体(FXR),在几乎所有的心血管细胞中表达,与心脏组织中的电传导和细胞力学密切相关。因此,胆汁酸信号在调节宿主的生理过程和许多心脏疾病方面非常重要。
一项前瞻性队列研究评估了慢性心力衰竭患者的原发性和继发性胆汁酸水平,然后显示原发性胆汁酸水平显着降低,继发性胆汁酸水平增加。研究人员这些发现归因于微生物群的功能,因为微生物代谢对胆汁酸合成的影响很大,尤其是次级胆汁酸。
这项工作揭示了胆汁酸和肠道菌群在调节心肌功能方面的密切相关性,但潜在的机制仍然未知。法尼类 X 受体(FXR)和 G 蛋白偶联受体 5 (TGR5)是 胆汁酸信号通路中的两个重要分子。
FXR是心力衰竭患者的潜在治疗靶点,因为FXR可以通过增加脂联素来改善心功能障碍并促进心肌重塑。此外,FXR的敲除通过抑制心脏病细胞的凋亡和纤维化促进了衰竭心脏的恢复。
年龄、性别、营养状况、疾病状态以及遗传和环境暴露是可以解释个体对药物治疗反应的因素。我们知道,微生物群参与药物代谢和药理作用,同时也存在双向交流,药物也会影响微生物群的组成。
药物吸收是一个复杂的过程,取决于许多因素,如它们在胃肠液中的溶解度和稳定性、pH值、胃肠道转运期、通过上皮膜的渗透性以及药物与宿主和微生物酶的相互作用。
人类肠道微生物群能够产生参与口服药物代谢的酶,促进其在肠道和血液中的吸收。肠道细菌群落的失调可以进一步改变药物的药代动力学;前药的激活可能加剧产生不需要的毒性代谢产物和药物的失活。
由于肠道细菌种类的个体间差异,“健康”肠道中也可能存在药物反应的变化。
心力衰竭患者粪便样本的宏基因组测序显示,他汀类药物、β受体阻滞剂、血管紧张素转换酶抑制剂、血小板聚集抑制剂等几种药物的使用对肠道微生物组成有重要影响。下表列出了微生物生物转化的例子。
肠道菌群可能影响心血管药物疗效的已知和提出的机制


doi.org/10.3390/cells12081158
地高辛,一种经常被推荐用于心力衰竭的药物,是微生物群影响药物生物利用度的一个很好的例子。
一些迟缓埃格特菌(Eggerthella lenta)菌株负责将地高辛转化为一种无活性的微生物代谢产物,限制了10%的患者吸收到系统血流中的活性药物的数量。
最近的研究证明,地高辛与抗生素或富含精氨酸的饮食共同给药,都会导致全身地高辛水平升高和药物水平的临床相关波动。
阿司匹林是一种非甾体抗炎药,通常用于降低脑血管和心血管疾病的风险。
阿司匹林破坏肠道微生物群的组成
与未使用或未使用其他类型非甾体抗炎药的患者相比,使用阿司匹林的患者的瘤胃球菌科、普雷沃氏菌、Barnesiella和拟杆菌的细菌水平存在差异。
肠道菌群的组成对阿司匹林的代谢产生影响
口服抗生素可以通过减缓肠道微生物群的降解、提高其生物利用度和延长其抗血栓作用来降低其代谢活性。
含有短双歧杆菌Bif195的益生菌可以预防阿司匹林摄入的不良反应,如肠壁损伤和阿司匹林诱导的胃溃疡。
抗生素通过改变肠道菌群影响华法林的药效
华法林是一种常用的抗凝剂,通过抑制维生素K依赖性的凝血因子II、VII、IX和X的激活来表达其作用。当与抗生素一起服用时,与华法林使用相关的出血事件增加。
两种机制:抗生素可以通过抑制或诱导CYP酶来干扰华法林的使用;还可以改变肠道细菌组成,消除产生维生素K的细菌,如拟杆菌属。
抗高血压药物的作用已经在动物和人类研究中进行了多次研究。
β受体阻滞剂、血管紧张素受体阻滞剂(ARBs)和血管紧张素转换酶抑制剂(ACE抑制剂)的使用之间的关联可以改变肠道微生物群的组成。
一项大型宏基因组学研究报告了,钙通道阻滞剂、ACE抑制剂和肠道细菌组成之间的正相关。对高血压大鼠研究发现,包括卡托普利在内的血管紧张素转换酶抑制剂带来的有益作用,是通过减轻肠道微生态失调、改善肠壁通透性和增加绒毛长度来实现。
他汀类药物是用于降低低密度脂蛋白-C(LDL-C)和胆固醇水平的药物。
他汀类药物治疗反应的存在个体间差异,与特定的他汀类药物或剂量无关。
他汀类药物在调节肠道菌群方面的作用
接受阿托伐他汀治疗的个体表现出抗炎肠道细菌水平的增加,如普拉梭菌(Faecalibacterium prausnitzii)和AKK菌(Akkermansia muciniphila)
已知患有高胆固醇血症的未经治疗的患者表现出具有促炎作用的细菌种类的增加,例如柯林斯氏菌(collinsella)和链球菌。
与LDL-C水平相关的菌群
LDL-C水平似乎与厚壁菌门和梭杆菌门呈负相关,而黏胶球形菌(Lentisphaerae)和蓝细菌门与LDL-C呈正相关。现有证据表明,LDL-C对他汀类药物治疗的反应可能受到含有胆汁盐水解酶(bsh)的细菌的影响。路氏乳杆菌是一种bsh活性升高的肠道细菌,给药后LDL-C水平显著降低。
同一项研究报告称,低密度脂蛋白胆固醇水平的个体变化与循环胆汁酸呈负相关。以前与LDL-C水平呈负相关的厚壁菌门也与bsh活性有关。几种动物模型维持了他汀类药物治疗对肠道微生物群落的有益作用。
使用瑞舒伐他汀有一种罕见的副作用
由于瑞舒伐他汀中含有一种叔胺,在肝脏水平上与TMA竞争代谢,血清TMA水平及其在尿液中的排泄量增加,导致鱼腥味综合征。
考虑到微生态失调是心力衰竭发病机制和疾病进展的关键因素,靶向破坏的肠道微生物群是一个有效的治疗目标。
表征每个患者的肠道微生物群及其与疾病相关的肠道微生态失调的可能性,需要个性化的、有针对性的治疗计划。
有各种方法可以管理和调节失调的肠道微生物群,如饮食干预(也包括使用益生元、后生元)和粪便移植,但现有文献中的几份研究将饮食调节和使用益生菌作为调节微生物群的主要干预措施。
●
饮食方式
饮食一直被认为是塑造肠道相关微生物群结构和功能的关键因素。
地中海饮食
医学文献中经常引用的地中海饮食包括高水平的多不饱和脂肪酸、膳食纤维、多酚和少量红肉。
在其对人类健康的益处中,地中海饮食提供了更丰富的益生菌、更大的生物多样性、增加的短链脂肪酸和减少的TMAO。坚持地中海饮食与心力衰竭发病率下降相关,最高可达74%。
此外,地中海饮食的高依从性似乎与心力衰竭呈负相关,并改善了HFpEF患者的长期预后,因为这是10年随访的结果。地中海饮食可能具有抗炎作用,因为有益作用与CRP水平相关。
扩展阅读:深度解析 | 炎症,肠道菌群以及抗炎饮食
得舒饮食(DASH饮食)
控制高血压的饮食方法(DASH饮食)饮食计划代表了一种摄入多不饱和脂肪、富含全谷物营养、蔬菜、水果和低脂乳制品的饮食,在降低心力衰竭发病率方面具有重要潜力。
饱和脂肪和胆固醇会导致其他心血管问题,请避免使用黄油、起酥油和人造黄油,避免奶酪、熏肉等,并食用有限量的橄榄油、亚麻籽油、山茶油等。
高纤维饮食
最近,在高血压诱导的心力衰竭实验模型中,高纤维饮食被证明可以改善肠道微生态失调(厚壁菌和拟杆菌的比例)、降低血压、改善心脏功能和使心脏肥大正常化。此外,纤维的发酵会增加短链脂肪酸的产量,对人类健康具有有益作用。
避免高钠饮食
通常建议心力衰竭患者限制饮食中的钠含量。美国心脏协会建议个人将钠摄入量限制在每天 2300 毫克以下。
管理液体量
心脏无法将血液泵送到身体其他部位时,体液就会积聚,喝太多液体可能会导致肿胀、体重增加和呼吸急促。
因此要控制饮水量,其他液体也要限制一定的量,比如说咖啡、果汁、牛奶、茶、苏打水等,还有酸奶、布丁、冰淇淋、果汁,少喝汤。


总体而言,饮食中尽可能将各种新鲜水果和蔬菜比例调大,适量食用全谷物、去皮家禽、鱼、坚果和豆类以及非热带植物油。
尽量少吃饱和脂肪、反式脂肪、胆固醇、钠、红肉、糖果、油腻甜点、含糖饮料等。
山楂
山楂有助于将心率和血压水平提高到正常水平。它还含有抗氧化剂,可以保护心脏免受自由基的侵害,山楂是心脏营养的绝佳来源,因为它含有生物类黄酮、单宁、维生素A、B族维生素、维生素C,以及铁、钙和钾等必需矿物质。
大蒜
大蒜可以降低心脏病的风险因素,包括高血压和胆固醇。它还降低了冠心病(CAD)心力衰竭患者的心率和心脏收缩力(心脏泵血的强度),冠心病是心力衰竭最常见的原因。


银杏叶
与安慰剂相比,银杏叶通过增加摄氧量、产生能量以及改善局部左心室功能,对心力衰竭有帮助。它还可以预防肾损伤。
人参
人参长期以来一直被用于中医治疗心脏病和心血管疾病。可以帮助降低血压,并降低因压力而导致的体内皮质醇水平。人参可以通过改善动脉和静脉的血液流动、增加心肌的氧合和防止动脉硬化来改善心脏功能。
生姜
生姜含有有益心脏健康的营养物质,如抗氧化剂和抗炎剂。它可以通过预防心脏病发作或心肌损伤、降低胆固醇水平和调节血压来帮助治疗心力衰竭。
水飞蓟补充剂
水飞蓟补充剂已被用于心力衰竭患者,水飞蓟含有一组黄酮类抗氧化剂水飞蓟素,可减少心力衰竭时的氧化应激。
辣椒
辣椒能增加血液循环,这意味着心力衰竭患者可以从中受益匪浅。此外,辣椒中含有辣椒素,辣椒素可以使心脏动脉放松和扩张,从而减少心脏病发作。它还可以防止血栓形成或扩大。

大多数关于益生菌治疗心力衰竭疗效的研究都是在动物模型中进行的。
大鼠模型中:益生菌促进产短链脂肪酸
口服植物乳杆菌299v和鼠李糖乳杆菌GR-1可产生有益的心脏作用。补充乳杆菌属似乎可以促进产短链脂肪酸菌,如真细菌、罗氏菌属(Roseburia)和瘤胃球菌,以促进膳食纤维发酵的副产物短链脂肪酸,在维持健康的心血管活动中发挥关键作用。
临床改善:益生菌改善心脏收缩功能
在一项针对心力衰竭患者(NYHA II级或III级,LVEF<50%)的小型双盲、安慰剂对照试点研究中,随机接受益生菌治疗,接受布拉酵母菌(Saccharomyces boulardii)(每天1000mg,持续3个月)或安慰剂。与安慰剂组相比,接受益生菌治疗的心力衰竭患者总胆固醇水平和尿酸水平降低,心脏收缩功能改善。
在人类中,一项初步研究报告称,在慢性心力衰竭患者中使用益生菌布拉酵母菌进行干预后,不仅减少了全身炎症,而且改善了左心室射血分数。不过参与者人数较少(n = 20),应谨慎解释结果。
扩展阅读:如果你要补充益生菌 ——益生菌补充、个体化、定植指南
最近的一项研究报告称,益生元低聚果糖可减少大鼠炎症细胞的浸润。益生元可以促进有益细菌的发生长,包括双歧杆菌和乳杆菌,减轻体重和炎症,改善葡萄糖和胰岛素耐受,所有这些都与更好的心力衰竭结果有关。
关于肠道微生物群对有害代谢产物产生的调节,临床前研究报告了DMB给药,饮食中TMAO的去除,胆碱TMA裂解酶抑制剂碘甲基胆碱的给药在降低血清TMAO水平、改善心脏重塑和减少促炎细胞因子表达方面的有益作用。
白藜芦醇还可以通过重建肠道菌群来刺激肠道中有益细菌的生长,从而减少TMAO的产生。
扩展阅读:如何调节肠道菌群?常见天然物质、益生菌、益生元的介绍
与抗生素在心力衰竭患者肠道微生物群调节中的应用有关,研究结果存在争议。
万古霉素
在动物模型中,与未经治疗的大鼠相比,口服万古霉素可诱导较小的左心室梗死面积,并改善缺血/再灌注实验后的心功能恢复。
利福昔明
利福昔明除了具有杀菌和抑菌作用外,还具有减少细菌移位和毒性的能力,具有抗炎作用,可以积极调节肠道微生物群的组成,促进乳酸杆菌和双歧杆菌的生长。至于人体临床试验,结果是矛盾的。
妥布霉素和多粘菌素B
在心力衰竭患者中使用妥布[拉]霉素和多粘菌素B的混合物,使肠道革兰氏阴性杆菌水平正常化,显著降低促炎细胞因子,血流介导的舒张改善:内皮功能障碍的证据。然而,结果仅限于给药治疗期间。
此外,在开具抗生素治疗处方时,必须考虑副作用,如多粘菌素B毒性和大环内酯类药物增加心肌梗死风险。
最近一项评估共生给药对慢性心衰患者左心室肥大的影响及其对血压和hsCRP作为炎症生物标志物的影响的研究报告称,与安慰剂组相比,共生给药10周后,作为左心室肥大标志物的NT-proBNP水平显著下降。hsCRP水平或血压值没有显著差异。
最近的一项研究报告称,在饮食诱导的HFpEF前啮齿动物模型中,FMT和三丁酸治疗改善了早期心脏功能障碍,并增加了支链氨基酸的分解代谢。
在人类受试者中,FMT使患有代谢综合征的肥胖个体的胰岛素敏感性正常化,但其影响是短期的。目前,还没有可用的临床研究来评估心力衰竭患者的FMT结果,但FMT具有巨大的治疗潜力,并代表了未来研究的一个有希望的方向。
戒烟
烟草烟雾中的尼古丁会暂时增加心率和血压,吸烟还会导致血管结块或粘稠。戒烟的人更有可能改善心力衰竭症状。
适当运动,维持体重稳定
体重突然增加或减少可能是正在发展为心力衰竭的迹象。适当运动,维持体重,高强度间歇训练 (HIIT)、低强度有氧运动或阻力训练等运动训练方法均能有效改善心肌功能。研究表明,高强度间歇训练在提高患者的活动水平和心脏性能方面最为有效。
注意:具体合适的运动量请根据个人情况咨询医生。
限制饮酒
如果需要饮酒,请适度。男性每天不要超过一到两杯,女性每天不超过一杯。
管理压力
每天花 15 到 20 分钟静静地坐着,深呼吸,想象一个宁静的场景,或者尝试瑜伽或冥想等方式。
涉及深横膈膜呼吸的呼吸练习,可以帮助心力衰竭患者缓解焦虑、增加血液中的氧气水平和降低压力水平,从而改善心脏功能。
充分休息
为了改善晚上的睡眠,请使用枕头支撑头部。避免睡前小睡和大餐。试着在午饭后打个盹,或者每隔几个小时把脚抬起来几分钟。
选择合适的衣服
避免穿紧身袜或袜子,例如大腿或膝盖高的袜子,它们会减慢腿部的血液流动并导致血栓。也尽可能避免极端温度。分层穿着,以便根据需要添加或脱掉衣服。
肠道相关微生物群的组成和功能及其在人类健康中的病理生理作用一直是活跃的研究领域。现代技术的不断进步进一步推动了心力衰竭研究的前沿,探索了心力衰竭的新方面。
本文总结了有关肠道菌群及其代谢产物对心力衰竭及其相关风险因素的影响。心力衰竭与肠道微生态失调、细菌多样性低、肠道潜在致病菌过度生长和产短链脂肪酸菌减少有关。肠道通透性增加,允许微生物移位和细菌衍生的代谢产物进入血液,这与心力衰竭的进展有关。
靶向被破坏的肠道微生物群可以被认为是一个有效的治疗目标。有许多方法可以用来调节失调的肠道微生物群,如饮食干预(包括益生元、益生菌)、生活方式调整、补充剂、粪菌移植等。
然而这些方式带来的效果可能各不相同,因为这在很大程度上取决于每个个体的肠道菌群特征,也包括遗传背景、肠道屏障功能等。因此,通过肠道菌群健康检测,以及基于菌群特征开发个性化的微生物组疗法,或为心力衰竭临床治疗带来新的途径。
注:本账号内容仅作交流参考,不作为诊断及医疗依据。
主要参考文献:
Tang WHW, Li DY, Hazen SL. Dietary metabolism, the gut microbiome, and heart failure. Nat Rev Cardiol. 2019 Mar;16(3):137-154. doi: 10.1038/s41569-018-0108-7. PMID: 30410105; PMCID: PMC6377322.
Lu X, Liu J, Zhou B, Wang S, Liu Z, Mei F, Luo J, Cui Y. Microbial metabolites and heart failure: Friends or enemies? Front Microbiol. 2022 Aug 15;13:956516. doi: 10.3389/fmicb.2022.956516. PMID: 36046023; PMCID: PMC9420987.
Desai D, Desai A, Jamil A, Csendes D, Gutlapalli SD, Prakash K, Swarnakari KM, Bai M, Manoharan MP, Raja R, Khan S. Re-defining the Gut Heart Axis: A Systematic Review of the Literature on the Role of Gut Microbial Dysbiosis in Patients With Heart Failure. Cureus. 2023 Feb 12;15(2):e34902. doi: 10.7759/cureus.34902. PMID: 36938237; PMCID: PMC10014482.
Malik A, Brito D, Vaqar S, Chhabra L. Congestive Heart Failure. 2022 Nov 7. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2023 Jan–. PMID: 28613623.
Lupu, V.V.; Adam Raileanu, A.; Mihai, C.M.; Morariu, I.D.; Lupu, A.; Starcea, I.M.; Frasinariu, O.E.; Mocanu, A.; Dragan, F.; Fotea, S. The Implication of the Gut Microbiome in Heart Failure. Cells 2023, 12, 1158.
Gallo A, Macerola N, Favuzzi AM, Nicolazzi MA, Gasbarrini A, Montalto M. The Gut in Heart Failure: Current Knowledge and Novel Frontiers. Med Princ Pract. 2022;31(3):203-214. doi: 10.1159/000522284. Epub 2022 Jan 28. PMID: 35093952; PMCID: PMC9275003.
Branchereau M, Burcelin R, Heymes C. The gut microbiome and heart failure: A better gut for a better heart. Rev Endocr Metab Disord. 2019 Dec;20(4):407-414. doi: 10.1007/s11154-019-09519-7. PMID: 31705258.
Chen X, Li HY, Hu XM, Zhang Y, Zhang SY. Current understanding of gut microbiota alterations and related therapeutic intervention strategies in heart failure. Chin Med J (Engl). 2019 Aug 5;132(15):1843-1855. doi: 10.1097/CM9.0000000000000330. PMID: 31306229; PMCID: PMC6759126.
Trøseid M, Andersen GØ, Broch K, Hov JR. The gut microbiome in coronary artery disease and heart failure: Current knowledge and future directions. EBioMedicine. 2020 Feb;52:102649. doi: 10.1016/j.ebiom.2020.102649. Epub 2020 Feb 12. PMID: 32062353; PMCID: PMC7016372.
谷禾健康
心血管疾病(CVD)已成为主要的健康问题,是导致发病率和死亡率高的主要原因,2型糖尿病(T2DM)患者发生CVD和重大心血管不良事件(MACE:心衰梗死、中风、死亡)风险更高,且预后较差。传统的CVD风险指标以及T2DM的血糖控制都不能很好地预测T2DM患者发生CVD的风险。

肠道菌群最近被认为是一种新型的内分泌器官,它通过产生生物活性代谢产物,在调节宿主的心脏代谢和肾脏功能中发挥关键作用。
肠道并不是第一个被用来研究心血管疾病病理生理学的器官。它不仅是处理食物消化吸收的器官,而且是体内最大的具有免疫活性的器官。
最近的研究表明,肠道菌群会产生并释放许多代谢产物和毒素,其中一些代谢产物和毒素会吸收到宿主的体循环中,作为微生物影响宿主的媒介。
我们整理汇总了这篇综述调查来自数项临床和实验研究的证据,这些证据表明肠道微生物群来源的毒素与CVD之间存在关联,包括脂多糖LPS、氧化三甲胺TMAO和苯乙酰谷氨酰胺PAGln。目前已经正在进行一些临床研究,旨在探索降低这些毒素水平以抑制心血管事件的有效性。
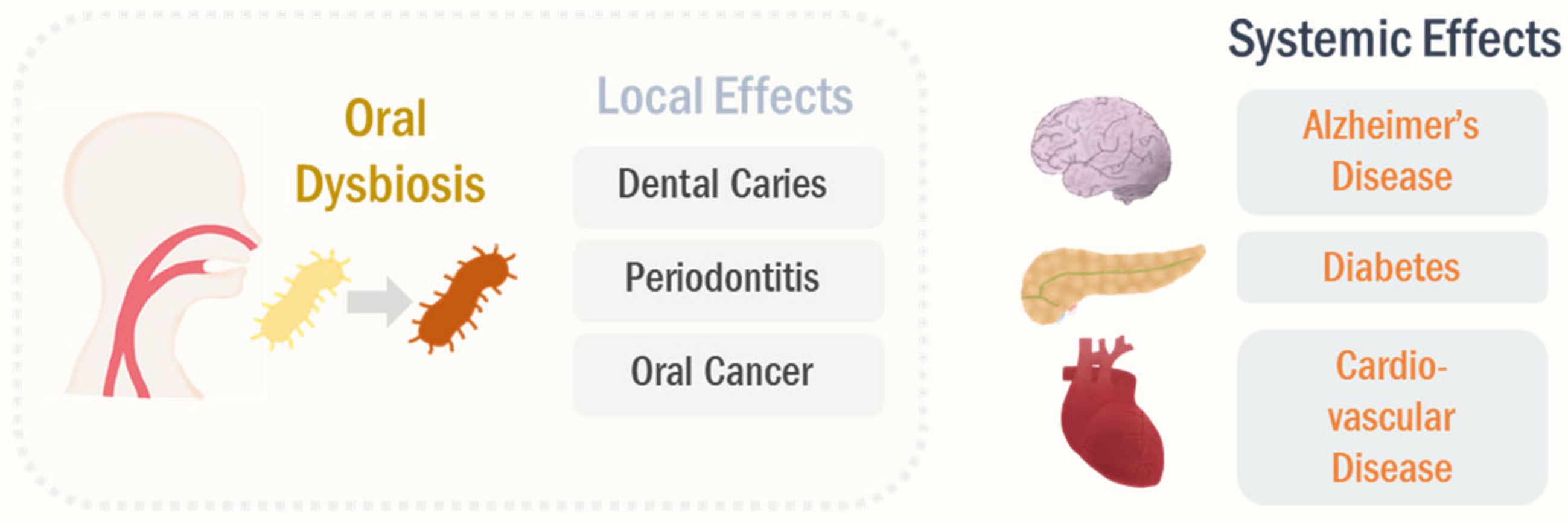
了解这些菌群相关代谢物是如何产生并如何影响心血管疾病有助于我们了解可能的风险和找到更好的生活方式来预防CVD。
缩略词:

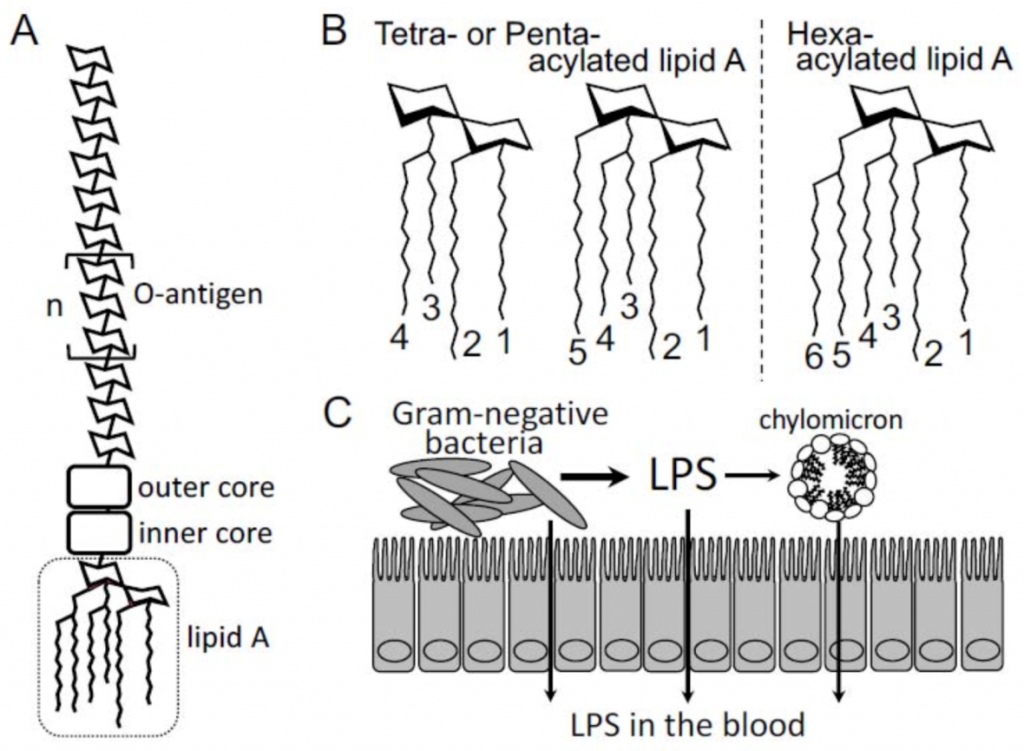

LPS的结构和特点
LPS,也称为内毒素,是革兰氏阴性细菌外膜的组成部分,主要存在于人体的肠道和口腔中。LPS的基本化学结构由亲水区和糖部分结合到疏水区组成,称为脂质A(下图A)。
LPS的亲水区域由内核和外部核以及O抗原(物种特异性重复寡糖亚基)组成,该区域对LPS的促炎活性影响最小(下图A)。
脂多糖(LPS)和脂质A的结构
Yamashita T,et al., Toxins,2021
疏水区脂质A在各种革兰氏阴性细菌中在结构上是保守的,由磷酸化的二葡萄糖胺主链组成,该主链具有4至7条相连的酰基链(上图B)。脂质A是Toll样受体4(TLR4)的配体和LPS的最关键“毒素”部分,它激活先天免疫系统,包括单核细胞和巨噬细胞,并引起宿主的炎症反应。
宿主血液中的 LPS 是从哪里来的?
——从肠道菌群中来
LPS是革兰氏阴性细菌外膜的主要成分,因此肠道微生物群可能是血液LPS的主要来源。人类胃肠道中存在数百万亿细菌,实际上,粪便LPS水平通常反映了肠道菌群衍生的LPS量,这个量因人的菌群构成和总量而异。
此外肠道通透性的提高会增强肠道菌群来源的LPS从肠道到血液的渗透。高脂饮食会增加肠道的通透性。
而Akkermansia菌可以加强肠道的紧密连接并防止代谢性内毒素血症,此外肠道菌群产生的短链脂肪酸可以保护肠屏障功能。
——从食物中来
除了肠道菌群以外,食物也是LPS的天然来源,因为食物和水总是含有少量LPS。饮食模式反映了血液中LPS的水平。
具体来说,选择健康的饮食食物(包括鱼,新鲜蔬菜和水果)可能会带来积极的健康结果,因为它们有助于减少内毒素血症。
CVD与几种传统的危险因素有关,例如高血压,血脂异常,糖尿病,吸烟和肥胖。
炎性过程已知在心血管病的发展中扮演至关重要的角色,而LPS是一种众所周知的炎症物质。LPS被认为是包括CVDs在内的炎性疾病的一种毒素,并参与CVDs发病和进展的病理生理过程。
由于LPS刺激TLR4诱导释放关键的促炎性细胞因子,而这些因子是激活有效免疫反应所必需的,大量的流行病学证据表明,内毒素血症的血液中LPS处于高水平,是动脉粥样硬化的重要危险因素,并且是LPS与动脉粥样硬化疾病之间联系的纽带。
不同的菌群,其LPS结构不同
虽然肠道菌群可以是粪便LPS的主要来源,但不同的菌群构成其LPS的炎症效应是不同的。LPS的脂质A部分的结构在不同菌群之间有所不同(上一小节图B)。这些结构差异可能是决定LPS活性的主要因素。
例如,已知拟杆菌属具有四酰基和五酰基酰化的脂质A部分,而大肠杆菌具有六酰化类脂A部分。通常,四和五酰化脂质A部分相比六酰化类脂A部分会减少TLR4反应。这表明如拟杆菌的LPS其诱导的促炎性细胞因子生成要远低于大肠杆菌的LPS。
因此肠道细菌组成和这些细菌所拥有的脂质A部分的类型可能是影响肠道微生物LPS与CVD之间关联的重要因素。
越来越多的证据表明,全身性内毒素血症和肠道菌群衍生LPS参与心血管病和许多其它流行疾病的发作和进展,如炎性肠疾病,肥胖和相关代谢性疾病,和非酒精性脂肪性肝炎。
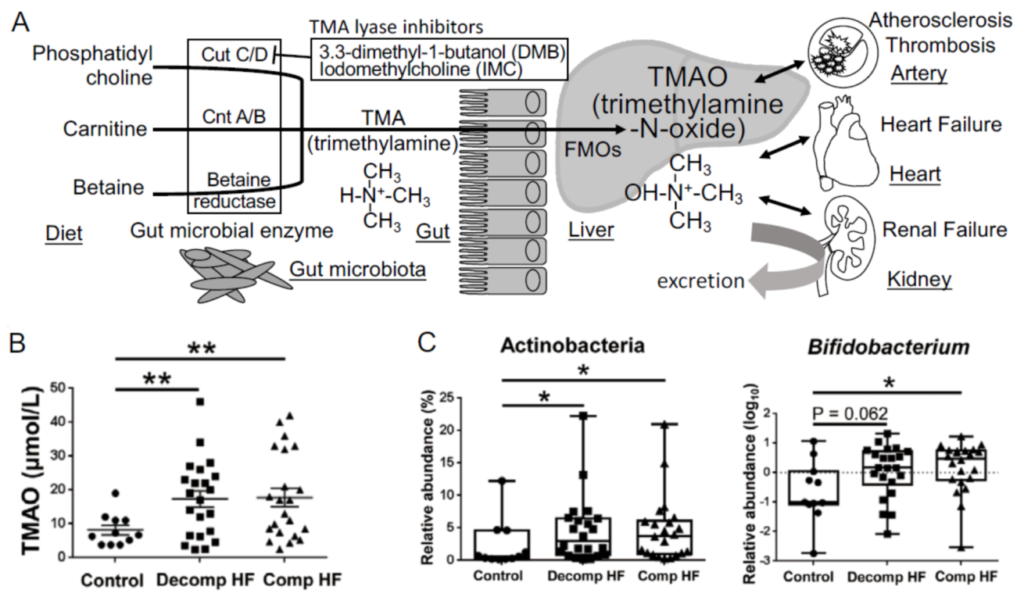
2011年,Hazen博士和他的同事使用代谢组学方法在动脉粥样硬化研究中取得了显著发现,并揭示了肠道衍生的代谢产物TMAO是心血管疾病大型临床队列中心血管事件的独立预测因子。
TMAO是心血管疾病的危险因素
TMAO在伴有冠状动脉疾病、血栓形成、慢性肾病和心力衰竭的CVD患者中升高,并与不良心血管事件和全因死亡率相关。
据报道,TMAO水平升高与慢性肾病患者的肾功能程度和全身炎症增加密切相关,而TMAO可作为该组严重慢性肾病患者死亡率的独立预测因子。可以合理地得出结论,TMAO是肠道菌群来源的尿毒症或心血管毒素,可导致全身性炎症。
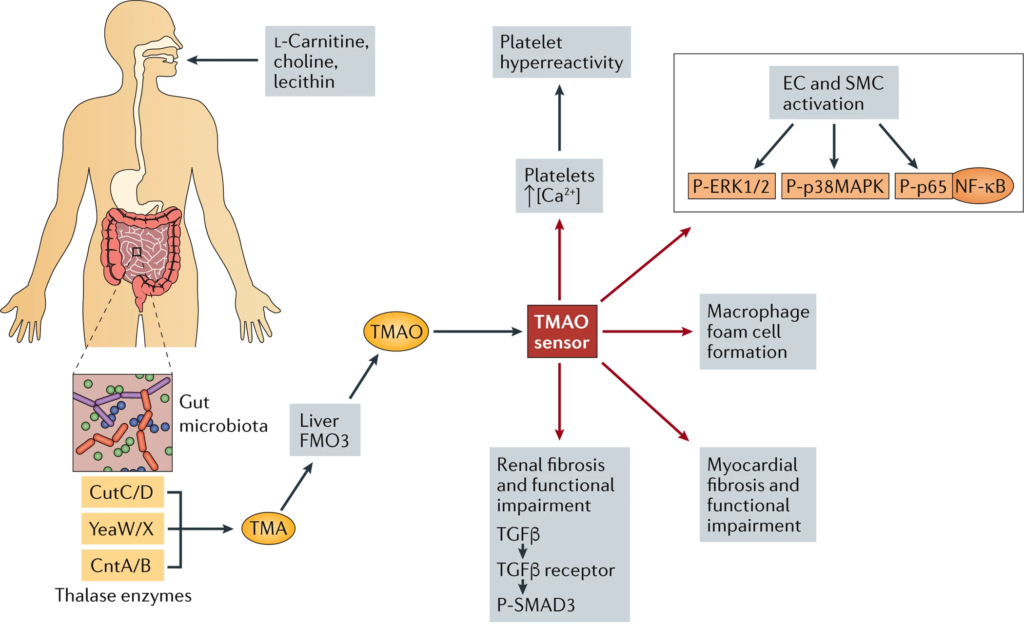
TMAO的产生
Brown J M, et al., Nature Reviews Microbiology, 2018
磷脂酰胆碱是一种在食品中发现的饮食成分,例如奶酪,蛋黄,肉和贝类,在肠道中被转化为胆碱,随后利用肠道微生物酶TMA裂解酶代谢为三甲胺(TMA)。TMA从肠道吸收进入门脉循环,然后通过肝脏中含黄素的单加氧酶(宿主酶)转化为TMAO 。
他们还证明,饮食中的左旋肉碱是红肉中的一种丰富营养物质,含有类似于胆碱的三甲胺结构,会促进血浆TMAO水平的升高并加速动脉粥样硬化。
肠道微生物衍生的TMAO代谢
Yamashita T,et al., Toxins,2021
与TMA产生有关的三个关键的微生物功能基因簇是胆碱TMA裂解酶(cutC)及其激活物(cutD)(cutC/D),一种糖基自由基酶和一种糖基自由基激活蛋白;肉碱加氧酶A/B(cntA/B),是一种由两部分组成的Riesketype加氧酶/还原酶复合物;甜菜碱还原酶途径(上图A)。
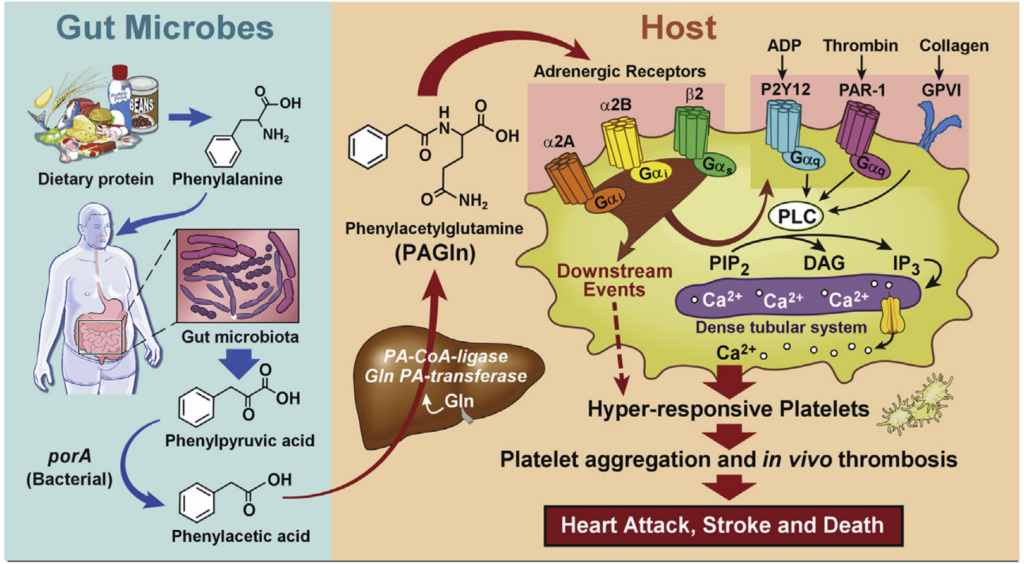
2020年Hazen团队通过代谢组学分析发现苯丙氨酸(Phe)与T2DM患者发生CVD风险升高有关,该物质被肠道微生物代谢生成苯乙酰谷氨酰胺(PAGln)。
对人群队列的代谢物检测发现,高PAGln水平与MACE高风险显著相关,较高的PAGln水平仍是MACE风险的独立预测因子。
肠道菌群影响PAGln水平
通过检测基线(Pre-Abx)、7天广谱复合抗生素处理(Abx)和3周清除期菌群重塑(Post-Abx)的血浆PAGln水平,发现PAGln水平受肠道微生物影响。
有研究表明,PAGln由苯乙酸(PAA)与谷氨酰胺(Gln)在肝酶的作用下形成,而PAA由苯丙氨酸(Phe)经菌群代谢产生。此外,PAA也可与甘氨酸(Gly)结合形成苯乙酰甘氨酸(PAGly)。
因此,在人类和小鼠体内,PAGln和PAGly都是通过肠道微生物群将饮食中的苯丙氨酸转化为PAA的元生物途径产生的,此时宿主与Gln(人类首选)或Gly(啮齿类动物首选)发生结合反应,分别产生PAGln和PAGly

Nemetet al. Cell , 2020
PAGln与血小板相互作用
根据人PAGln水平与血栓事件正相关性,提示PAGln可影响血小板功能和血管基质相互作用。研究结果显示,PAGln加速了胶原依赖性血小板粘附和扩散速度,并呈现剂量依赖性,表明PAGln可能与血小板直接相互作用,促进胞质内Ca2+浓度([Ca2+]i)呈现依赖性升高,并进行了相关验证。此外,在PAGly实验中也观察到类似结果。
因此,肠道菌群相关代谢产物PAGln和PAGly显著影响血小板功能,增强血小板与胶原基质的粘附,以及血小板刺激依赖性[Ca2+]i升高和对激动剂的聚集反应。
降低血栓形成
有研究报道Phe主要由生孢梭菌(Clostridium sporogenes)代谢为PAA(氧化途径)和苯丙酸(PPA)(还原途径),随后分别与Gln或Gly缩合形成PAGln或PAGly。其中参与反应的酶主要由porA或fldH基因编码。基因porA主要影响PAA产生,而fldH主要调节PPA产生,且敲除fldH会增加PAA水平继而影响PAGly水平从而显著降低血栓形成。
PAGln通过G蛋白偶联受体和ADRs介导细胞反应
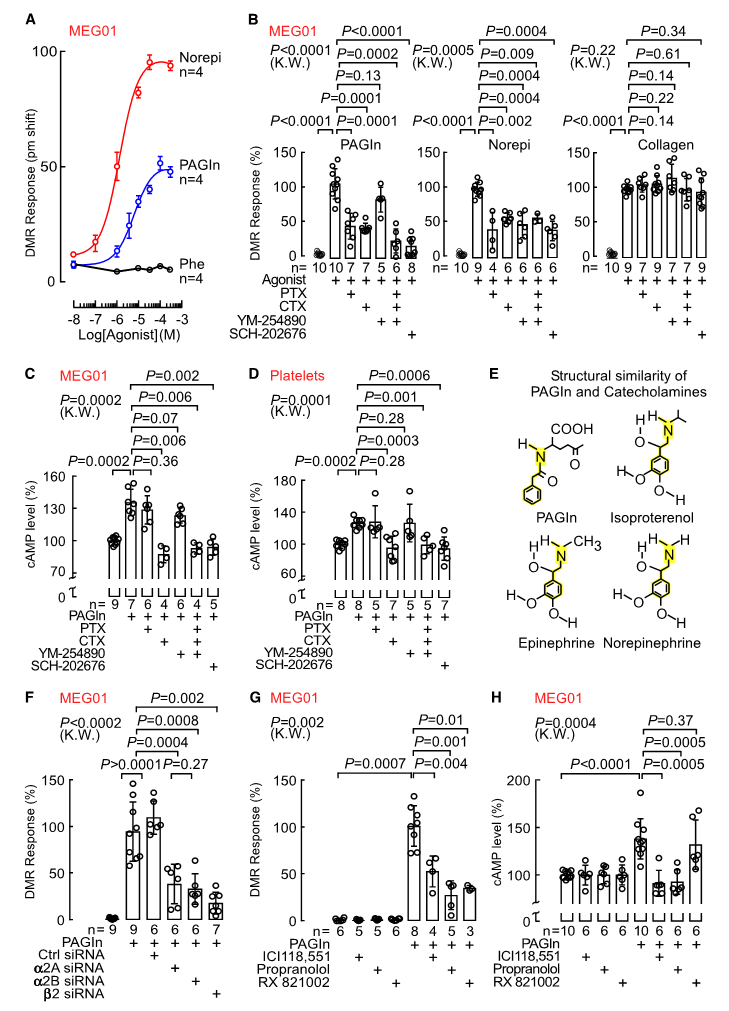
Nemetet al. Cell , 2020
研究人员发现PAGln与儿茶酚胺结构相似(上图E),暗示PAGln通过肾上腺素能受体(ADRs)发挥作用。遗传和药理学方法的功能丧失和功能获得研究证实,PAGln可通过G蛋白偶联受体(包括α2A,α2B和β2-ADRs)介导细胞反应。而β受体阻滞剂(卡维地洛)可显著降低PAGln诱导的高血栓风险。
微生物代谢产物可以调节宿主的生理和病理生理过程,这一发现开启了多种可能性,特别是证明了许多微生物途径可以作为抑制心血管病的治疗靶点。
LPS和TMAO可用于开发有效的治疗策略,然而目前还不能证明这些毒素水平是如何在宿主体内被确定和调节的。因此,需要进一步研究阐明肠道微生物源毒素与心血管疾病之间的因果关系,进一步探索肠道微生物及其代谢产物,包括毒素之间的关系,以确定心血管疾病治疗干预的最佳方法及患者的预后。
相关阅读:
主要参考文献:
Brown J M, Hazen S L. Microbial modulation of cardiovascular disease[J]. Nature Reviews Microbiology, 2018, 16(3): 171.
Yoshida, N.; Yamashita, T.; Kishino, S.; Watanabe, H.; Sasaki, K.; Sasaki, D.; Tabata, T.; Sugiyama, Y.; Kitamura, N.; Saito, Y.; et al. A possible beneficial effect of Bacteroides on faecal lipopolysaccharide activity and cardiovascular diseases. Sci. Rep. 2020, 10, 13009
Nemet et al. A Cardiovascular Disease-Linked Gut Microbial Metabolite Acts via Adrenergic Receptors. 2020, Cell 180, 862–877.
Yamashita T, Yoshida N, Emoto T, et al. Two Gut Microbiota-Derived Toxins Are Closely Associated with Cardiovascular Diseases: A Review[J]. Toxins, 2021, 13(5): 297.
Cui, X.; Ye, L.; Li, J.; Jin, L.; Wang, W.; Li, S.; Bao, M.; Wu, S.; Li, L.; Geng, B.; et al. Metagenomic and metabolomic analyses unveil dysbiosis of gut microbiota in chronic heart failure patients. Sci. Rep. 2018, 8, 635
Guo, C.J., Allen, B.M., Hiam, K.J., Dodd, D., Van Treuren, W., Higginbottom, S., Nagashima, K., Fischer, C.R., Sonnenburg, J.L., Spitzer, M.H., and Fisch-bach, M.A. (2019). Depletion of microbiome-derived molecules in the host using Clostridium genetics. Science 366, eaav1282