 国家高新企业 | ISO9001认证
国家高新企业 | ISO9001认证 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康

肠道微生物除了在肿瘤发生过程有重要作用,在抗癌治疗过程中也有着不可忽视的价值。
现有的癌症疗法很多,化疗、放疗等方式虽然有效,但副作用较多;免疫疗法有其局限性,有效率低且针对癌症类型有限。研究表明,肠道微生物群的调节不仅有助于增强机体免疫力,抑制肿瘤细胞的增殖和侵袭,还可以改善治疗的耐受性和减轻不良反应。
例如,研究发现化疗中伊立替康的毒性取决于肠道微生物群的组成;
毛螺菌科、肠球菌科通过产生短链脂肪酸减轻放疗毒性;
在晚期黑色素瘤患者中,双歧杆菌科、瘤胃球菌科、毛螺菌科等关键细菌与抗PD1治疗后的良好结果有关。
因此,如何通过将肠道微生物群结合现有的癌症治疗方式,更好地促进肿瘤患者的康复和疗效,值得深入挖掘和探讨。
本文我们就来详细了解一下,微生物群与各类癌症疗法,最主要是免疫疗法及其与免疫相关的不良反应。根据患者微生物群组成训练的机器学习方法,可以准确预测患者对免疫疗法的反应能力。
粪菌移植或饮食、益生元等干预可在临床上用于提高癌症患者免疫治疗的成功率,这里讨论了基于微生物群的癌症治疗的新策略。
理解肠道微生物群与肿瘤治疗之间的相互关系,可以为创新的治疗方法提供有力的支持,并为肿瘤治疗领域带来新的突破。
化疗是指使用药物来杀死或控制癌细胞的生长。这些药物可以通过静脉注射、口服或局部应用的方式给予患者。
缺点
由于化疗中使用的药物可能对癌症没有特异性,无法区分细胞好的坏的,会影响身体的其他健康组织,引起副作用,比如脱发、口腔溃疡、恶心、精疲力竭等。
肠道菌群影响化疗药代动力学、疗效和毒性
一个代表性的例子是:伊立替康的毒性取决于肠道微生物群的组成。
注:伊立替康用于治疗结直肠癌的拓扑异构酶 I 抑制剂。
肝脏中:
葡萄糖醛酸转移酶将活性形式的伊立替康 SN-38 解毒成无活性的 SN-38-G。
肠道中:
许多表达 β-葡萄糖醛酸酶的细菌将 SN-38-G 转化回 SN-38,从而引发腹泻。
这种毒性可以通过广谱抗生素或 β-葡萄糖醛酸酶抑制剂来预防。
肠道菌群可优化肿瘤治疗、增强免疫抗癌效果
肠道微生物群可以通过提供有利于药物对癌症细胞毒性作用的肿瘤微环境,并在药物诱导的免疫原性细胞死亡后维持抗癌适应性免疫,从而调节化疗效果。
奥沙利铂、顺铂
无菌或抗生素处理的小鼠中,铂基化合物奥沙利铂和顺铂显示出降低抗肿瘤功效。这些药物仍然可以在微生物群耗尽的小鼠的肿瘤中形成铂-DNA加合物,但没有观察到DNA损伤。肠道微生物群通过NOX2(NADPH氧化酶2)启动肿瘤中的髓细胞产生活性氧(ROS),这是铂治疗诱导的DNA损伤所需的。
肠道微生物发酵的膳食纤维产物——丁酸盐,可以通过 IL-12 信号传导调节 TME 中 CD8+ T 细胞的功能,从而增强奥沙利铂的抗癌作用。
烷化剂环磷酰胺(CTX)
同样,烷化剂环磷酰胺疗效也取决于肠道菌群。
注:烷化剂环磷酰胺既是一种化疗剂,也是一种免疫抑制剂。
CTX减少了小肠中厚壁菌门和螺旋体门,同时增加了其他细菌类群的丰度,其中一些细菌转移到肠系膜淋巴结。CTX诱导免疫原性肿瘤细胞死亡,这依赖于微生物群调节的致病性辅助T细胞17(TH17)和记忆性TH1细胞。
CTX治疗后, Enterococcus hirae移位至淋巴结和Barnesiella intestinihominis在结肠中的积聚促进了癌症免疫。
此外,接受化疗免疫治疗的癌症或卵巢癌患者的存活率与E. hirae和B. intestinihominis特异性TH1反应相关。
吉西他滨
吉西他滨是胰腺导管腺癌常用的化疗药物。肠道微生物参与化疗药物的药代动力学,吉西他滨治疗胰腺导管腺癌的疗效可能受到肠道微生物的影响。
γ-变形菌能够代谢吉西他滨并将其转化为无活性的2′,2′-二氟脱氧尿嘧啶。因此,未来有可能通过将抗γ-变形菌的抗生素与化疗相结合来提高吉西他滨的抗癌效果。
除了负面影响外,肠道微生物代谢产物丁酸盐,还可以通过诱导细胞凋亡来增强吉西他滨对抗癌症细胞的功效。
除了肠道微生物群,肿瘤内细菌促进肿瘤生长并干扰化疗效果,这表明:
肿瘤内微生物群可能是癌症治疗的靶向菌
肿瘤内微生物群已显示在人类乳腺癌、骨癌、胰腺癌、卵巢癌、肺癌、黑色素瘤、胶质母细胞瘤以及原发性和转移性结直肠癌中。肿瘤微生物群可能在肿瘤发生、肿瘤进展和治疗反应中发挥着重要作用。
肿瘤相关γ-变形菌表达细菌胞苷脱氨酶,该脱氨酶使细胞毒性药物吉西他滨失活;使用抗生素环丙沙星可以清除细菌,恢复对吉西他滨的敏感性。然而,吉西他滨治疗也通过增加变形杆菌的丰度来改变肠道微生物群。
↓↓↓
因此,抗生素治疗是否通过对肿瘤相关的γ-变形菌或其他与肠道或肿瘤相关的微生物成分的特异性影响来影响肿瘤生长,目前没有确切的证据。
*************************************************************************
小鼠乳腺癌模型:
通过循环肿瘤细胞携带的肿瘤内细菌,重组了细胞骨架,促进了宿主细胞的存活。通过肿瘤微生物群落中分离的菌株直接注入肿瘤,增强了转移形成。
在原发性人类结肠癌和远处转移中检测到:
——梭杆菌门(Fusobacteria)
使用甲硝唑抗生素治疗可以消除梭杆菌,并减小肿瘤生长速度。
肝癌和肝硬化患者:
肝脏中Stenotrophomonas maltophilia丰度的增加诱导了肝星状细胞的细胞衰老相关的分泌表型(SASP),从而促进了肝癌发生。
↓↓↓
这些数据表明,抗生素有可能靶向肿瘤微生物群,但抗生素治疗的全身效应与肿瘤局部效应可能是拮抗的,特别是考虑到抗生素对免疫检查点阻断的有害影响。
*************************************************************************
细胞内细菌可能逃避RAB11介导的吞噬作用,并寄居于稳定的含有细菌的液泡中,使其对抗生素无效。
↓↓↓
因此,使用细胞穿透肽和核酸可能会最大限度地增强抗生素对肿瘤相关细菌的效力。
肠道微生物群调节癌症治疗,可以有针对性地提高治疗效果并预防不良反应
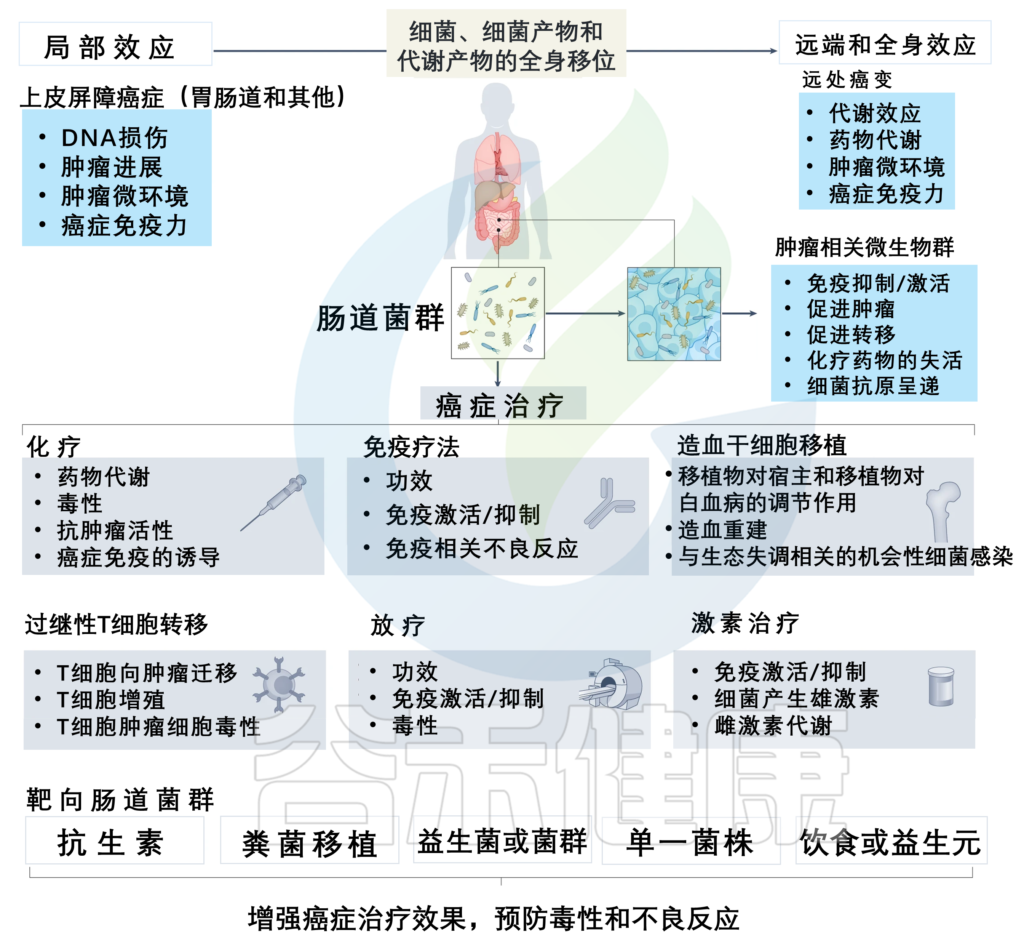
doi: 10.1038/s41568-022-00513-x
放射治疗在于缩小或破坏肿瘤,但过程不同。
辐射是一种高能不可见光波,可以针对癌细胞破坏其遗传物质,最终杀死它们。辐射波会损害癌细胞,癌细胞会随着时间的推移而死亡并被身体清除,从而导致肿瘤缩小。
与化疗不同,放疗通常是一种局部治疗,也就是说一般不会传播到全身。
缺点
如果附近的健康组织在治疗过程中受损,局部放射可能会产生副作用,比如恶心、口腔溃疡、喉咙问题导致进食困难、皮肤干燥、精疲力竭等。
不同癌症类型在毒性和敏感性方面存在差异,这是影响电离放射治疗安全性和有效性的主要障碍。
肠道微生物群的细菌和真菌成分都可能导致患者间的异质性
在实验动物中,对革兰氏阳性细菌有选择性的抗生素万古霉素通过消耗产短链脂肪酸的肠道细菌,提高RTX的有效性,并增强树突状细胞抗原呈递和癌症免疫。
向万古霉素处理的小鼠施用丁酸盐,部分通过抑制树突状细胞功能,包括它们产生IL-12的能力,消除了这种作用。
使用广谱抗生素治疗肠道微生物群会导致酵母菌类真菌肠道扩张,通过β-葡聚糖受体Dectin 1的信号传导抑制肿瘤免疫,从而降低RTX有效性。使用抗真菌药物治疗可提高未经治疗小鼠的RTX有效性,尤其在抗生素治疗的对RTX反应较差的小鼠中。
在乳腺癌患者中,肿瘤内髓细胞中Dectin1的表达与生存率呈负相关,这一观察结果表明真菌免疫抑制作用可能与临床相关。
短链脂肪酸在癌症治疗中的复杂功能:对抗毒性 与 免疫调节
传统饲养的小鼠比无菌小鼠更容易受到全身照射(TBI)毒性的影响,因为微生物群抑制ANGPTL4的表达。
注:ANGPTL4,血管生成素样4,也称为FIAF,是一种支持组织修复的脂蛋白脂肪酶抑制剂。
然而,产短链脂肪酸菌通过诱导ANGPTL4,来保护接受RTX治疗的患者免受结肠炎和粘膜炎的侵袭。
毛螺菌科、肠球菌科→产丙酸→减轻毒性
在全身照射存活的小鼠中,产生色氨酸代谢产物和短链脂肪酸(特别是丙酸盐)的细菌,毛螺菌科(Lachnospiraceae)和肠球菌科(Enterococcaceae)大量存在,并且可以将对TBI毒性的耐药性转移到其他小鼠。
在进行异基因造血干细胞移植(allo-HSCT)预处理过程中,观察到患有白血病的患者的粪便样本中存在着毛螺菌科(Lachnospiraceae)和肠球菌科(Enterococcaceae)。这些患者在接受全身放疗治疗(TBI)时出现的肠道毒性较轻。
这些发现可以解释为什么产生短链脂肪酸的益生菌,如乳酸杆菌和双歧杆菌,可以预防TBI毒性。
总体而言,几项研究表明,不同的短链脂肪酸可能对癌症免疫和治疗毒性产生复杂影响,包括粘膜保护作用,部分由ANGPTL4、IL-18和IL-22的诱导介导,以及通过Treg细胞诱导和抑制树突状细胞功能介导的对立的免疫调节效应。
因此,短链脂肪酸在放疗和其他癌症治疗中的功能似乎很复杂,需要进一步研究。
最新的癌症疗法利用宿主免疫系统来对抗癌症。免疫细胞通过识别和消灭癌细胞来抑制肿瘤的发生。
CTLA-4充当淋巴结中 T 细胞激活的“关闭”开关,而 PD-L1/PD-1降低肿瘤部位的晚期免疫反应。
免疫检查点抑制剂(ICI) 是一种单克隆阻断抗体,可以释放免疫系统的“刹车”,使免疫细胞能够更有效地识别和攻击癌细胞。
这种方法给一些难治癌症患者带来了显著的持久缓解,如晚期和转移性黑色素瘤、肾细胞癌、非小细胞肺癌等。目前用于超过25种不同的肿瘤类型。
缺点
免疫治疗(ICI)每年每个患者的费用超过10万元,成功率仅为20%-40%,同时许多患者会出现与免疫相关的不良事件。
因此,迅速发展的需求突显了将免疫疗法的有效性扩展到所有癌症患者的必要性。
微生物群维持对病原体的抵抗力和疾病耐受性,防止对无害抗原的过度炎症反应。
饮食、生活方式、抗生素和其他药物使用的变化可能会改变这种健康保护生态平衡。与对急性感染的抗原特异性耐药性不同,肿瘤通过劫持疾病耐受机制抑制癌症免疫。因此,肠道微生物群的改变,可能会影响患者对免疫疗法的反应和免疫相关不良事件(irAE)的程度。
过继性T细胞疗法(ACT):万古霉素增强ACT抗肿瘤,其他抗生素降低抗肿瘤
万古霉素的治疗增加了肠道中变形杆菌门的丰度,但耗尽了厚壁菌门和拟杆菌门的大多数物种,增强了ACT在小鼠中的抗肿瘤作用。
而其他抗生素,特别是新霉素和甲硝唑,分别消耗革兰氏阴性需氧菌和厌氧菌,降低了ACT的抗肿瘤作用。
万古霉素修饰的微生物群诱导产生刺激T细胞的IL-12,维持过继转移的细胞毒性T细胞。
Toll样受体激动剂:CpG-ODN、ICB疗法
革兰氏阴性菌与诱导坏死的CpG-ODN的有利先天反应,以及维持适应性CD8+T细胞介导的抗癌免疫的肿瘤微环境的重定向有关。
ICB 疗法增强的适应性免疫(如后面所讨论的)与几种革兰氏阳性细菌的存在相关,包括:
在这种情况下,革兰氏阴性菌与免疫抑制性局部和全身炎症状态有关。
在一项临床试验(NCT03618641)中,证明了 CpG-ODN和ICB组合的功效,抗PD1治疗下,初始CpG-ODN诱导的坏死和维持无复发生存,与革兰氏阴性细菌(变形菌门、拟杆菌门和革兰氏阴性Oscillospiraceae)的粪便丰度相关。
免疫检查点阻断
一般来说,只有20-40%的患者对ICB有反应,因此需要确定响应标志物并开发克服耐药性的治疗方法。
而肠道微生物群已成为预测ICB响应的肿瘤外部生物标志物。
CTLA4
➦ 无菌小鼠对抗CTLA4治疗反应不佳。
➥ 向微生物群耗尽的小鼠注射多形拟杆菌(Bacteroides thetaiotaomicron)或脆弱拟杆菌(Bacteroides fragilis),通过诱导肿瘤中的DC成熟和引流淋巴结中的TH1反应,恢复抗CTLA4反应。
PDL1
相反,小鼠对肿瘤生长的抵抗力和对抗PDL1的反应性与几种双歧杆菌的粪便丰度有关。
在晚期黑色素瘤患者中,放线菌门(双歧杆菌科和Coriobacteriaceae)和厚壁菌门(瘤胃球菌科和毛螺菌科)的关键细菌种类的粪便丰度与抗PD1治疗后的良好结果有关。
在肺癌、肾细胞癌或肝细胞癌患者中,粘蛋白降解的Akkermansia muciniphila在抗PD1治疗中发挥抗肿瘤作用。然而,在一些接受抗生素治疗的患者中,粪便中A. muciniphila的高丰度与抗PD1治疗的耐药性有关,这可能表明AKK菌在抗PD1疗法反应中具有双峰效应。
在抗PD1治疗无反应的患者粪便中,溶血性葡萄球菌和Corynebacterium aurimucosum的更高,在有反应的肾癌和肺癌患者中,E. hirae菌的粪便频率更高。
研究中发现的细菌种类的一致性有限,可能是由于ICB介导的免疫机制的变化。
TIM3
抗生素治疗对抗TIM3癌症治疗的损害,也表明了肠道微生物群在维持这种类型的ICB的疗效中的作用。
肠道菌群、血液相关菌群和肿瘤相关菌群的组成不同,对不同类型的癌症具有特异性,导致不同的细菌种类对免疫治疗的反应产生影响。
对相同类型肿瘤和相同ICB治疗的患者队列的研究,即使仍然受到队列内微生物群异质性的影响,也报告了更一致的结果。
事实上,复杂微生物群落中的未知变异阻碍了稳健的特征识别。未来的研究依赖于细菌亚种和菌株的新特征,并分析单个细菌基因或途径的关联,将更好地识别特定细菌与治疗反应的关联及其作用机制。
肠道菌群对抗PD1免疫检查点阻断反应的调节
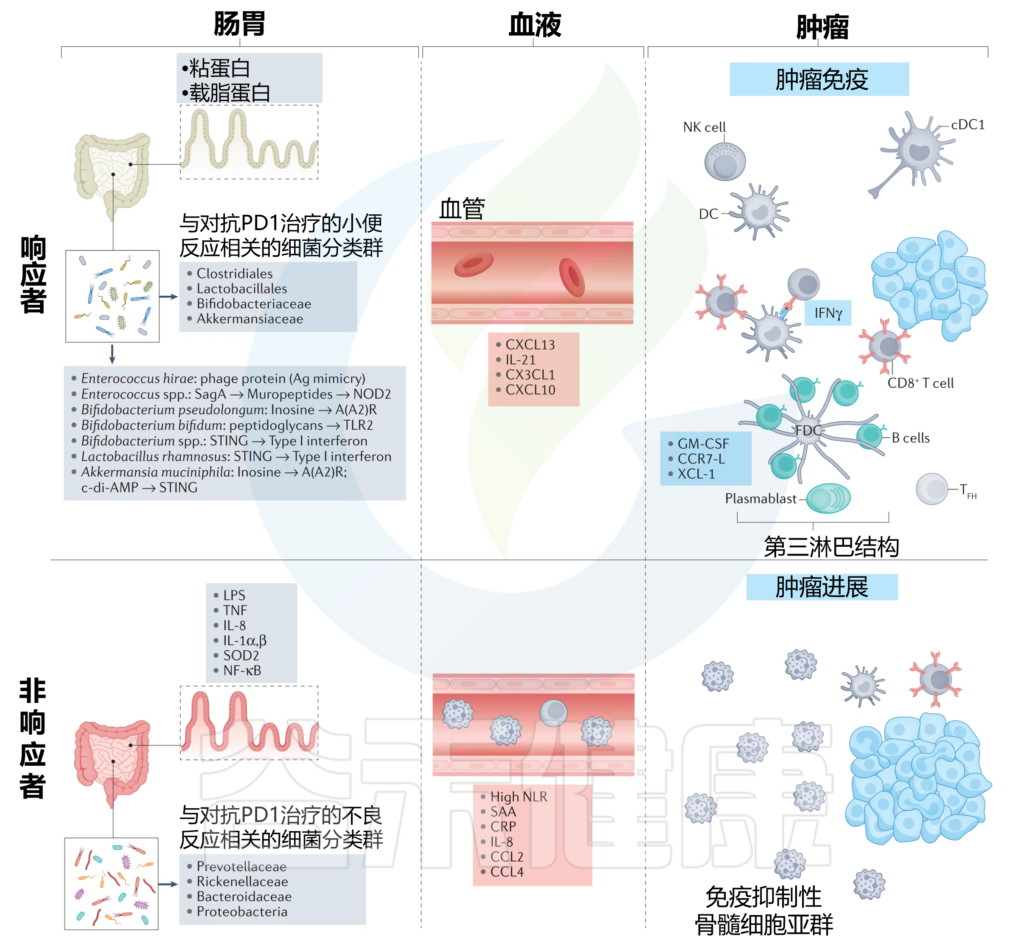
doi: 10.1038/s41568-022-00513-x
在大多数接受抗PD1治疗的癌症患者的研究和荟萃分析中,与有利或不利治疗反应普遍相关的细菌已得到一致定义。
在对抗PD1治疗有反应的患者中观察到一种健康、无炎症的肠粘膜,其特征是编码抗炎载脂蛋白和跨膜粘蛋白的转录物。在这些患者的血液中,参与T细胞和B细胞募集的细胞因子和趋化因子升高,这对抗肿瘤免疫很重要。左上角列出了与抗PD1治疗的有利反应相关的确定细菌种类及其在调节抗肿瘤免疫中的作用机制。
在对抗PD1治疗没有反应的患者中,观察到肠粘膜发炎和炎症细胞脱落,而在他们的血液中,通常存在全身炎症的生物标志物。所列的肠道革兰氏阴性菌群与抗PD1治疗的不良反应以及局部和全身炎症的生物标志物有关,可能反映了免疫抑制肿瘤微环境。
早期临床反应取决于肿瘤内在因素或宿主因素;而肠道菌群的调节作用在治疗开始约1年后更具影响力
一项针对黑色素瘤患者的抗PD1治疗研究报告称,较高的肠道微生物群α多样性与良好反应之间存在关联。但没有更多研究证实,α多样性用于区分健康个体和癌症患者,它不能预测对免疫疗法的反应性。
对已发表的接受抗PD1治疗的黑色素瘤患者队列的数据进行的荟萃分析显示,不仅在单个物种水平上,而且在更大的分类分支中,识别出的细菌之间存在共性。
大多数研究认为有利的微生物群特征,包括放线菌门的多个成员,以及在厚壁菌门中,瘤胃球菌科和Lachnospiraceae科。
而一个不利的特征包括拟杆菌门和变形菌门。
对黑色素瘤患者的免疫治疗反应进行的两项荟萃分析使用了大队列,研究发现,肠道微生物群的基线组成在3个月时进行放射学评估时,区分有反应的患者和没有反应的患者的能力有限,但它可以更好地区分在治疗开始后约1年有进展或没有进展的患者。此外,长期无进展生存期患者在开始抗PD1治疗后数年保持良好的微生物群。
为什么没有在队列中一致地识别出某些菌作为生物标志物?
一项研究的样本来自三个欧洲国家和一些公开的数据集,并包括用抗CTLA4、抗PD1或两者联合治疗的黑色素瘤患者。这里涉及到,地理和治疗类型的异质性。
即使同卵双胞胎,每个个体的肠道微生物组都是独特的,并且这种独特性的很大一部分是在单个菌株水平上编码的。需要分析方法更深入探索这种个体特异性的微生物多样性。
不同地理区域的肠道微生物类型不同,因为人类肠道微生物组受到种族和地理起源的影响。利用美国肠道项目的7000多个样本,对微生物类型进行了地理测绘,揭示了美国各地理区域的分布不均。
接受抗PD1治疗的黑色素瘤患者队列中的微生物类型代表性也不一样,并反映了他们的地理环境。此外,对抗PD1治疗有反应的概率与肠道微生物类型相关。
因此,通过微生物类型视角分析肠道微生物群与免疫疗法反应之间的关系,为先前研究的不一致性提供了可能的解释,并可作为纠正地理和临床中心特异性偏见的工具。
肠道菌群中的肽聚糖酶介导的抗癌
一些肠球菌在小鼠中维持ICB作用的能力是由一簇肽聚糖水解酶介导的,包括分泌抗原a(SagA),它产生NOD2激活的胞壁肽(muropeptides),增强抗PDL1诱导的肿瘤免疫。
当给予小鼠时,SagA转染的乳酸乳球菌抑制肿瘤生长并提高抗PD1反应性。某些与小鼠抗PD1和奥沙利铂癌症治疗协同作用的双歧双歧杆菌菌株富集了肽聚糖合成基因,通过TLR2刺激癌症免疫。
肠道菌群调控干扰素
肠道菌群维持I型干扰素表达,增强肿瘤免疫
在微生物群耗尽的小鼠中,肿瘤内先天免疫细胞中的干扰素信号减弱,改变巨噬细胞极化、树突状细胞分化和DC-自然杀伤(NK)细胞串扰,并使肿瘤微环境从抗肿瘤变为促肿瘤。
肠道微生物通过诱导免疫细胞产生干扰素,通过一系列的受体和信号通路来增强免疫应答。
注:一些列受体如TLR3、TLR4、TLR7、TLR9、Dectin 1、干扰素基因刺激因子(STING)、DDX41、RIG-I等。
微生物群诱导的细胞和基因表达特征激活了小鼠的STING-干扰素途径,并与黑色素瘤患者的良好ICB反应有关。
某些共生菌如AKK菌、双歧杆菌、鼠李糖乳杆菌,通过激活干扰素途径来抑制肿瘤进展,并增强免疫治疗的效果。
干扰素的作用也与肿瘤类型和治疗阶段有关
I型干扰素信号传导并不总是与抑制肿瘤生长有关。肝脏中持续的I型干扰素信号传导,分别通过诱导一氧化氮或改变尿素循环,诱导对抗PD1治疗的耐药性或抑制抗病毒T细胞反应。
不同刺激产生的干扰素还会对肿瘤生长和免疫反应产生不同的影响。在肿瘤治疗中,详细了解干扰素在不同时间点对不同细胞的作用,以及如何影响肿瘤环境和免疫治疗效果,还需深入研究。
肠道促炎:预测ICB疗效不佳
系统性炎症的许多外周血生物标志物,如高中性粒细胞与淋巴细胞比率(NLR)和C反应蛋白(CRP)、IL-8和血清淀粉样蛋白a(SAA)水平升高,是对ICB反应不佳的预测因素。
黑色素瘤患者粪便微生物群中,高NLR与革兰氏阴性拟杆菌门的丰度增加有关。人类粪便转录组分析显示,对抗PD1治疗没有反应的患者肠道中存在促炎特征,主要由脱落的中性粒细胞和其他髓细胞引起,这与LPS和NF-κB信号传导有关,导致产生促炎细胞因子,如TNF、IL-1和IL-8。
革兰氏阴性菌:阻碍ICB反应
总体而言,这些数据表明,肠道微生物群中的革兰氏阴性菌可能通过LPS产生和TLR4信号传导,诱导免疫抑制性局部肠道和全身炎症,从而阻碍ICB反应。
实验诱导的小鼠胆汁淤积诱导革兰氏阴性菌从肠道转移到肝脏,导致TLR4依赖性炎症反应,产生CXCL1,募集免疫抑制性中性粒细胞,抑制抗肿瘤免疫,导致胆管癌生长增强。此外,革兰氏阴性菌Fusobacterium nucleanum与原发性和转移性结直肠癌癌症的关联,通过吸引髓细胞而具有免疫抑制性。
自身抗原和微生物异种抗原之间交叉反应
自身抗原和微生物异种抗原之间的交叉反应在自身免疫性疾病中很常见,可能与癌症免疫有关。身体不仅对病原体产生免疫反应,而且对共生微生物产生免疫反应。尽管这种反应得到了很好的控制,但失调可能会引发免疫病理,并可能在接受ICB治疗的患者中被重新激活,导致免疫相关不良反应,并可能与肿瘤新抗原发生交叉反应。
ICB治疗的患者中鉴定的一些肿瘤新抗原,可能与微生物抗原具有交叉反应
在抗CTLA4处理的小鼠中,通过过继转移B.thetaiotaomin特异性或B.fragilis特异性T细胞导致其活化,进而抑制MCA-205肉瘤肿瘤生长,支持肿瘤和微生物抗原之间分子模拟的观点。
小鼠细菌共生体E.hirae与对环磷酰胺和ICB的有利反应相关的,E.hirae携带表达肽的原噬菌体,针对该肽引发主要组织相容性复合物(MHC)I类反应,并与癌症细胞中过表达的非突变蛋白酶体组分中的表位交叉反应。
在人类中,相同的原噬菌体在肠球菌属中表达。除毛滴虫外,其MHC限制性表位与甘油-3-磷酸脱氢酶1-样蛋白(GPD1L)中的表位发生交叉反应,后者也在肿瘤中过表达。
在人类黑色素瘤转移中,表达人类白细胞抗原(HLA)I类和II类限制性肽的细菌物种存在于造血细胞和肿瘤细胞中。当对表达肿瘤匹配HLA等位基因的EB病毒转化的B细胞进行脉冲时,其中一些肽能够特异性激活肿瘤浸润淋巴细胞。
因此可以推测,在患者中,这些肽通过传统抗原呈递细胞或黑色素瘤细胞的呈递,引发了可能影响抗癌免疫的T细胞免疫反应。
有望成为预测免疫疗法反应的生物标志物
前面第二章节有提到短链脂肪酸与放疗,这里我们主要看短链脂肪酸对接受 ICI 的癌症患者的预测作用。
在日本进行的一项研究中,52名接受抗PD-1抗体治疗的实体瘤患者的粪便短链脂肪酸与良好的临床结果相关。高浓度的粪便乙酸盐、丙酸盐、丁酸盐和戊酸盐以及血清异戊酸盐与PFS的延长有关。
相比之下,另有研究发现,高血清丁酸盐和丙酸盐水平与黑色素瘤患者对抗CTLA4抗体的耐药性和Treg细胞数量的增加有关。
鉴于临床前肿瘤模型也揭示了短链脂肪酸对抗CTLA4抗体或放射治疗的疗效的负面影响,在利用血液或粪便中的任何短链脂肪酸作为ICI疗效的生物标志物之前,需要进一步的研究来验证不同地理位置的大型队列中短链脂肪酸的预测价值。
不同的细菌种类,包括假长双歧杆菌、约氏乳杆菌和粘球菌,产生肌苷及其代谢产物次黄嘌呤。这些分子结合腺苷受体A2a(A2aR),激活抗肿瘤T细胞并提高小鼠的ICB效率,特别是抗CTLA4疗法。
肌苷增强抗PD1治疗效果
除了A2aR介导的T细胞活化外,肌苷是葡萄糖限制下CD8+T细胞的替代碳源,并增强了对不能利用肌苷作为能量来源的肿瘤的抗PD1治疗功效。表明肌苷活性增强了ICB疗效,并且像腺苷一样激活了A2aR,在临床癌症治疗的试验中,A2aR是一个免疫抑制的检查点,增强ICB效果。
肌苷也可能抑制自身免疫
罗伊氏乳杆菌(Lactobacillus reuteri)可以预防ICB诱导的结肠炎,但不会影响ICB在小鼠中的抗肿瘤功效,它通过增强作用于A2aR110的肌苷的产生,来抑制Treg细胞缺陷的Scurfy小鼠的自身免疫。
这些高度矛盾的结果可能可以通过肌苷对T细胞的直接刺激效应与上下文相关的事实来加以解释;在无菌动物中或在没有共生细菌提供的促炎启动的体外,肌苷需要在这些实验条件下分别由CpG-ODN或IFNγ提供的炎症刺激。由于缺乏这种炎症刺激,肌苷确实会抑制T细胞。
因此,在癌症免疫疗法中靶向肌苷依赖性途径需要更好地理解肌苷的这些对比效应,同时考虑到腺苷和肌苷通过A2aR的信号可能不相同,并且肌苷通过A2aR或A3R影响不同的全身炎症模型。
两项研究调查了接受ICIs的晚期癌症患者的犬尿氨酸与色氨酸(Kyn与Trp)比率的临床意义。
Kyn/Trp比率高,与总生存期缩短有关
第一项研究中,早期疾病进展患者(3个月内)的Kyn/Trp比率显著高于有反应者(P = 0.017)。
第二项研究中,在接受nivolumab治疗的黑色素瘤和肾细胞癌患者中,开始治疗4-6周后Kyn与Trp比率的增加(>50%)与中位总生存期的缩短密切相关(P ≤ 0.026)。
有争议的发现
鉴于代谢适应在癌症免疫疗法中的重要性,以及在黑素瘤患者中选择性IDO1抑制剂与ICI联合治疗的疗效不佳(在ECHO-301/KEYNOTE-252第三期试验中),这些发现不仅对未来试验中基于血清肾上腺素/色氨酸比率监测而进行患者分层的必要性提出了质疑,还对ICI治疗期间肠道菌群动态调节的分析提出了质疑。
事实上,色氨酸不仅由肿瘤和髓系细胞代谢,而且由肠道菌群中的不同种类代谢成吲哚和吲哚衍生物,包括吲哚乙酸、吲哚-3-醛(I3A)和吲哚丙酸等,这些物质能够与芳香烃受体结合。
可能支持富含色氨酸的饮食,或基于I3A或3-IAA 的益生元与ICI的组合
当罗伊氏乳杆菌与ICI联合给小鼠口服时,它可以从回肠转位到黑素瘤部位,释放I3A,激活CD8阳性T细胞的TCR信号通路,促进IFNγ的释放和抗肿瘤效应。
这些实验发现的临床意义已在一项涉及接受ICI治疗的黑素瘤患者的研究中得到证实,为基于色氨酸的饮食干预在癌症患者中的应用开辟了道路。
细胞内L-精氨酸浓度也直接影响T细胞的代谢适应度和存活率,从而影响它们在小鼠模型中介导有效抗肿瘤免疫反应的能力。
L-精氨酸水平升高诱导了整体代谢变化,包括活化T细胞从糖酵解向氧化磷酸化的转变,并促进了中枢记忆样T细胞的产生。
在发现组和验证组中,低血清L-精氨酸水平(<42 µM)与减少的临床获益率、无进展生存期和总生存期显著独立相关(P = 0.004)。此外,低血清L-精氨酸水平与髓系细胞中PD-L1的表达增加相关。因此,血浆L-精氨酸监测可能成为ICI疗效的适宜预测生物标志物。

doi: 10.1038/s41571-023-00785-8.
尽管广谱抗生素可能会导致真菌过度生长,从而降低放疗效率
万古霉素消耗产短链脂肪酸菌,提高放疗效果
一项正在进行的临床试验(NCT03546829),测试在接受立体定向身体放射治疗的非小细胞癌症(NSCLC)患者中,通过IFNγ的产生评估,万古霉素是否增加抗肿瘤免疫力。
万古霉素还通过增强自然杀伤T细胞(NKT)在肝脏中的迁移和IFNγ的产生,削弱小鼠原发性和转移性癌症的生长。
万古霉素耗尽革兰氏阳性菌,调控胆汁酸
万古霉素耗尽革兰氏阳性菌,特别是Clostridium scindens,它将初级胆汁酸转化为次级胆汁酸。微生物群衍生的胆汁酸影响炎症、免疫和致癌物的许多方面。初级胆汁酸,如鹅去氧胆酸,通过肝窦内皮细胞诱导趋化因子CXCL16的产生,该细胞通过CXCR6吸引NKT细胞,而次级胆汁酸,特别是ω-鼠胆酸,抑制CXCL16产生。
还计划进行临床试验(NCT03785210),测试万古霉素是否改善原发性肝癌或转移患者对抗PD1治疗的反应。然而,即使是特定的抗生素也会引起肠道微生物群组成的广泛变化,这可能会对癌症治疗产生相反的影响。
胆汁酸对免疫反应的调节也是复杂的
黑色素瘤患者FMT后,次级胆汁酸水平与抗PD1治疗的良好临床反应有关。
然而在小鼠中,拟杆菌属部分地将抑制TH17细胞的次级胆汁酸3-oxoLCA,转化为激活Treg细胞的isoalloLCA,从而限制自身免疫和癌症免疫。
万古霉素提高ADT疗效
去势抵抗性前列腺癌与促癌的肠道菌群变化有关,使用含有万古霉素的抗生素混合物来消耗小鼠体内产生雄激素的细菌,这种抗生素可以专门减少厚壁菌门的细菌,包括产生雄激素的梭菌属,从而提高ADT(雄激素剥夺疗法)的效果。因此,如果抗生素与ADT一起使用,它们的性质应该是选择性地消耗产生雄激素的细菌,而不是免疫刺激物种。
抗生素治疗仍有挑战,更特异性的方法有待探索
一般来说,在ICB期间或之前使用抗生素对临床反应产生不利影响,很可能是因为它们改变了肠道生态以及有利和不利细菌之间的平衡。尽管通过抗生素来靶向肠道菌群可能具有益处(如上面例子所述),但总体而言,这面临着大部分抗生素的广泛反应性以及可能诱导抗生素耐药性的挑战。
除了抗生素,其他更具特异性的方法,如噬菌体治疗以及更有效、更具特异性的噬菌体介导的CRISPR-Cas3抗微生物药物,可以在我们对直接影响抗肿瘤反应的细菌种类以及由其消除引起的生态变化的认识更加精确之后使用。
FMT可解决80-90%的抗生素耐药性艰难梭菌感染,其他包括各种机会性感染、炎症性肠病等也在研究中。
对免疫疗法后的结肠炎,FMT效果好
抗CTLA4治疗免疫相关不良反应中常见的有结肠炎,这类结肠炎可能比较严重,皮质类固醇或TNF拮抗剂的治疗难以治愈。
两名癌症患者在接受ICB治疗后出现结肠炎,经健康捐赠者FMT治疗后,病情迅速恢复。供体菌群确实发生了定植,厚壁菌门和变形菌门的丰度降低,拟杆菌门和Verrumicrobiae的丰度增加。随后的一份初步报告显示,在FMT治疗的15名癌症患者中,有11人从ICB诱导的结肠炎中恢复。
FMT:提高黑色素瘤患者的抗PD1治疗效果
两项临床试验证明,FMT可以靶向微生物群,以提高黑色素瘤患者的抗PD1治疗效果。由于预测微生物群组成尚不可行,这可能支持抗PD1治疗反应,以选择健康的粪便微生物群供体,两项试验都使用了黑色素瘤患者和对抗PD1疗法有持久反应的患者作为供体。
*****************************************************************************
第一项试验
10名进展中的黑色素瘤患者接受了抗生素治疗(其中6人之前对ICB有阳性反应),并通过结肠镜检查。这10个人做了FMT,供体是两名对抗PD1治疗有反应的捐赠者中的其中一人,随后重复胶囊形式的FMT和抗PD1疗法。
● 在从供体1接受移植的5名患者中,一个完全反应和两个部分反应;
● 在从供体2接受移植的五名患者没有反应。
两个供体的微生物群都包含有利于抗PD1治疗反应的菌群,供体1在梭菌属和放线菌属中更富集。FMT后,供体1受体的微生物组成变化比供体2受体更一致,人类粪便转录组中炎症和抗原呈递特征的表达增加。治疗后,三名有反应的患者表现出更显著的肿瘤排斥反应,其特征是I型干扰素反应和单核细胞、DC、NK细胞和T细胞浸润。
*****************************************
第二项试验
15名对抗PD1治疗原发性无反应的黑色素瘤患者在结肠清洗后(没有抗生素治疗),接受了来自6名抗PD1疗法有反应的供体中的1名,随后接受了持续的抗PD1治疗;1名患者完全缓解,2名患者部分缓解,3名患者病情稳定超过18个月。
这些反应良好的患者的菌群怎么样了?
在反应良好的患者中,FMT后的粪便微生物群变得更像供体,并且针对供体菌群的IgG抗体更显著诱导。有益菌的丰度增加,如毛螺菌科、瘤胃球菌科和双歧杆菌科,有害菌如拟杆菌属减少。
其他指标有什么变化?
在这些有反应的患者的血液中,IL-8水平下降,而CXCR13和IL-21水平上升,表明T卵泡辅助细胞(TFH)有反应。
初级和次级胆汁酸的水平以及苯甲酸盐降解的产物都增加了,苯甲酸盐是微生物群多样性,与抗PD1治疗反应相关的某些菌群的存在的标志。
******************************************************************************
尽管规模小且单臂试验,但这两项初步研究中的整体临床反应率为36%,高于其他联合治疗方案在难治性抗PD-1治疗患者中的反应率,且没有额外严重毒副作用。
FMT后菌群有效定植,干扰时长超1年
总的来说,即使没有抗生素调理,单次结肠镜进行FMT,也会干扰微生物群组成超过1年。宏基因组分析表明,大多数存在于供体而不在受体患者身上的菌属(和微生物基因),可以有效且持久地定植,除非受体接受了抗生素治疗。
供体菌株定植与治疗效果之间可能存在不一致?
事实上,FMT后的微生物群组成不仅反映了供体特异性菌群的定植情况,还反映了FMT引起的肠道生态变化,改变了来自供体或接受者的不同菌群的丰度。
对抗PD1治疗无效的黑色素瘤患者来说,FMT可能只有当患者存在针对肿瘤的免疫反应,但受到免疫抑制或微生物组成不利的影响,导致缺乏免疫促进的微环境时,才会产生对继续抗PD1治疗的反应。FMT可以纠正这种不利的微生物组成。
自体FMT,重建肠道微生物群
供体可以提供更健康、更多样的微生物群,能够重建受体微生物群的多样性。然而,将病原体或抗生素耐药性病原体转移到免疫抑制受体中存在风险,这也说明了患者自体微生物群的储存是合理的。
接受自体FMT的患者每种白细胞谱系的数量都更高,这表明FMT是有利的。Faecaliberium、Ruminococcus、Akkermansia与白细胞数量增加有因果关系的是通过自体FMT重建的。
癌症患者对抗PD1治疗产生抗药性的原因各不相同,可能导致FMT治疗失败
其中原因包括:
1)由于免疫抑制或肿瘤可能缺乏新抗原,无论微生物群组成如何,都无法对肿瘤做出反应
2)FMT供体可能缺乏对抗-PD4治疗做出反应所需的菌群
3)由于供体与受体微生物群的不相容性,FMT不能使微生物群扰动足够大
4)FMT模式的递送方法和频率可能不是最佳的
FMT在癌症免疫治疗中的未来发展
需要重点评估患者预处理和微生物群转移的最佳方案,确定最有可能受益于FMT的患者和合适的供体。
许多计划中以及正在进行的试验将通过评估FMT在不同肿瘤类型中的有效性,以及将FMT与其他方法(如益生菌、饮食和益生元)进行比较或结合,调节肠道微生物群的组成,来确定FMT是否成为治疗对ICB无反应患者的常规方法。
益生菌制剂含有具有抗炎和粘膜保护能力的菌群,如乳酸杆菌属和双歧杆菌属,用于预防化疗和放疗引起的毒性。
临床和小鼠研究,都确定了可能对特定机会性感染产生耐药性的细菌,以及可能纠正微生物群失衡的潜在益生菌。
乳杆菌属:抑制肿瘤生长,改善对ICIs的反应
鼠李糖乳杆菌、嗜酸乳杆菌和发酵乳杆菌对结肠癌发展的缓解作用已在小鼠模型中得到证实。
鼠李糖乳酸杆菌GG可通过cGAS/STING信号传导途径刺激I型干扰素,从而改善对ICIs的反应。
乳酸菌(LAB)可有效减少结直肠癌的发生,这可能归因于炎症因子的减少。此外,LAB还影响肠道微生物群落,其特征是拟杆菌丰度的降低。因此,LAB有利于抑制癌症的发生和发展。
罗伊氏乳杆菌能促进肠上皮的更新和修复,刺激宿主免疫。它能将上皮内CD4+T细胞转化为CD4+CD8αα双阳性上皮内淋巴细胞,从而缓解炎症性肠病,预防部分消化道癌症的发生。
罗伊氏乳杆菌抑制 ICI相关结肠炎的能力,与第 3 组先天淋巴细胞分布的减少有关。
罗伊氏乳杆菌通过产生三种色氨酸降解产物,抑制黑色素瘤、肝癌和结直肠癌的生长:
双歧杆菌属:增强抗PDL1疗效
对无特定病原体或微生物群耗尽的小鼠,给予与ICB反应相关的各种菌群可提高治疗反应。
为了验证双歧杆菌属支持小鼠抗PDL1治疗,施用含有四种双歧杆菌属菌株的非处方商业益生菌制剂可提高对抗PDL1疗法的反应。在对抗PD1治疗有反应的患者中,双歧杆菌也会增加。
只有一些双歧杆菌菌株能够在小鼠中与抗PD1治疗协同作用。这些协同菌株表达参与合成肽聚糖途径的基因,表明它们有助于产生免疫刺激分子。
Faecalibaculum rodentium: 抑制肿瘤生长
F.rodentium和Holdemanella biformis(人类同源物)在肿瘤发生过程中缺失或丢失,这两者都可以产生短链脂肪酸,通过抑制钙调神经磷酸酶和NFATc3激活来控制肿瘤细胞的增殖和蛋白质乙酰化。
当将F.rodentium应用于ApcMin/+小鼠时,80%以上的结直肠癌中会发生结肠腺瘤样息肉(APC)基因突变,或者用偶氮甲烷和右旋糖酐硫酸钠治疗可以减轻小鼠的肿瘤生长。同样,在ApcMin/+模型中,H.biformis在通过丁酸盐抑制肿瘤生长方面似乎与F.rodentium相似。因此,H.biformis可以应用于癌症治疗的设计。
嗜热链球菌:分泌β-半乳糖苷酶,释放叶酸
嗜热链球菌(Streptococcus thermophiles)是一种强大的益生菌,具有消化和免疫益处,通常在结直肠癌患者中被耗尽。更重要的是,嗜热链球菌对肿瘤发生有抑制作用。
具体而言,在结直肠癌小鼠中经口灌胃嗜热链球菌将显著减少肿瘤形成。嗜热链球菌分泌的β-半乳糖苷酶是抑制结直肠癌生长的活性成分;β-半乳糖苷酶可以增加另外两种益生菌乳酸杆菌和双歧杆菌的丰富性,这表明了协同作用。
嗜热链球菌通过释放叶酸来影响肿瘤生长。叶酸是一种主要的膳食元素,在细胞代谢和DNA复制、修复、甲基化和核苷酸合成中发挥重要作用。研究表明,叶酸缺乏在人类中相当普遍,嗜热链球菌释放的叶酸可能与肿瘤抑制有关。此外,嗜热链球菌对淋巴细胞特征、结肠炎的严重程度和调节性T细胞反应有影响。
大肠杆菌Nissle 1917: 减少并发症
大肠杆菌Nissle 1917 菌株可以调节肠道屏障上皮功能,缓解肠道菌群失调,最终减少伊立替康引起的肠道并发症。
丁酸梭菌588菌株:改善抗PD1治疗后患者生存率
相反,在一项回顾性分析中,一种单一的益生菌制剂,在日本和中国广泛用于治疗与胃肠道病理学相关的微生态失调的丁酸梭菌(CBM)588菌株,显著改善了接受抗PD1治疗的小细胞肺癌癌症患者的客观反应、PFS和总生存率。丁酸梭菌通过增加乳酸杆菌和双歧杆菌来改善微生态失调。
然而,一项对接受联合ICB治疗的肾细胞癌症患者的随机试验证实,接受丁酸梭菌治疗的患者临床反应有所改善,但未能检测到双歧杆菌的增加。
多种菌组合,效果 1+1>2
虽然单一益生菌菌株显示出前景,但细菌群落可能更好地维持肠道微生物群内的生态平衡。人类和小鼠种,某些种类的梭状芽孢杆菌与对结肠癌的耐药性有关。
小鼠口服下列四种梭菌菌株:
诱导了激活的CD8+T细胞在肿瘤内的积聚,并成功治疗了化学诱导的结肠癌和可移植结肠癌。
该联合体作为一种独立的治疗方法以及单个物种,在小鼠中比单独的抗PD1治疗更有效。所有四个菌株都产生短链脂肪酸,包括丁酸盐;然而,它们的免疫刺激作用独立于丁酸盐。
鉴定免疫激活细菌群落的另一种方法涉及鉴定罕见的人类共生菌株,该菌株可以激活小鼠肠道中产生IFNγ的CD8+T细胞。一个由11个物种组成的群落在无菌小鼠中对单核细胞增多性李斯特菌感染保持耐药性,并具有与抗PD1治疗相加的抗肿瘤作用。值得注意的是,7种本身没有抗癌活性的拟杆菌目物种确实对该群落的总活性有贡献,这支持了多物种细菌生态学在重建肠道微生物群中的重要性。因此,使用单一菌株和联合体的试验正在进行中。
免疫治疗期间,益生菌的服用也需谨慎
与不服用益生菌的患者相比,服用非处方益生菌的黑色素瘤患者对抗PD1治疗的反应并没有改善,反而有所下降。
这些结果,再加上商业益生菌的配方是异质的,缺乏严格的成分和生存能力质量标准,表明在免疫治疗期间使用这些产品时应谨慎。
饮食的变化会迅速改变肠道微生物群的组成,以及食物发酵衍生的细菌代谢产物的产生,从而产生代谢和免疫后果。
不同的饮食策略,包括热量限制、间歇性禁食、模拟禁食饮食、高纤维饮食、生酮饮食、发酵食物,都已在小鼠或患者中提出或测试,以改善癌症的治疗,至少在某些情况下,显示出通过改变肠道微生物群的组成来影响免疫力。
在T细胞过继转移模型中,小鼠的饮食热量限制促进了记忆性T细胞在骨髓中的积累,并增强了T细胞对细菌感染和肿瘤的免疫力。
发酵食品饮食持续增加了微生物组的多样性,并通过整体抗炎作用改变了其组成。
高纤维饮食对微生物组多样性和组成的影响更为温和,对免疫细胞的频率和细胞因子的表达没有显著影响,但对免疫细胞中的内源性信号传导产生了不同的影响,在一组具有高炎症指数的个体中,内源性信号传导增加,而在另外两组具有低炎症指数特征的个体中则减少炎症指数。
饮食可能通过改变菌群影响抗癌免疫
接受抗PD1治疗的黑色素瘤患者,在纤维充足的饮食超过20g/天时有更好的反应和存活率 ,每5 g纤维的增加相当于进展或死亡风险降低30%。
与另一项研究一致,不同纤维摄入量的人类肠道微生物群在组成或细菌丰富度方面没有显示出重大变化,但从小鼠食物中去除大部分纤维含量导致微生物群迅速变化,双歧杆菌属减少,AKK菌增加。低纤维饮食的小鼠对抗PD1癌症治疗反应较差,与临床结果相似。因此,在无菌小鼠中,高纤维和低纤维饮食不会影响对抗PD1治疗的反应,这表明该饮食可能通过改变微生物群影响抗癌免疫。
跨物种网络分析表明,小鼠的高纤维饮食通过扩大发酵纤维的瘤胃球菌属来维持有效的肿瘤免疫。瘤胃球菌属诱导T细胞的激活和肿瘤浸润,包括表达诱导型T细胞共刺激因子(ICOS)的CD8+和CD4+T细胞。
模拟禁食饮食(FMD)可降低癌症患者的毒性,并改善其对化疗的反应,但大多数关于这种饮食干预的研究尚未解决肠道微生物群改变的作用。
禁食对化疗的积极作用体现在四个方面:
二甲双胍、维生素 C、铂和曲美替尼与禁食联合使用可以增强化疗的效果。
对于三阴性乳腺癌,模拟禁食饮食激活癌细胞中的饥饿逃逸途径,并减少癌症干细胞的表面标志物,从而导致化疗药物的识别增加。
生酮饮食在小鼠中通过诱导由酮体3-羟基丁酸介导的T细胞癌症免疫,来增强抗PD1治疗的抗肿瘤作用。在小鼠和人类中,尽管在低碳水化合物饮食在增加Eisenbergiella massiliensis等细菌种类的丰度方面与抗癌效应相一致,但饮食对肿瘤免疫的影响是由3-羟基丁酸盐的增加介导的,并不依赖于肠道微生物群的改变。
菊粉和果胶是许多蔬菜和水果中天然存在的可溶性纤维,不能被胃肠道酶消化,但可以被细菌发酵。因此,它们通过改变肠道微生物群的组成、增强粘膜屏障、增强上皮完整性以及激活或抑制先天免疫细胞来发挥益生元的作用。
菊粉→产短链脂肪酸菌→增强抗PD1疗效
在小鼠中,菊粉凝胶的口服治疗增加了产短链脂肪酸菌的丰度,并增强了抗PD1疗法的抗肿瘤活性。
↘
果胶增强抗肿瘤免疫,有两种不同的机制。
果胶→产短链脂肪酸菌→增强抗PD1疗效
果胶喂养增强了移植有癌症患者粪便微生物群的小鼠对抗PD1治疗的反应能力,通过扩大纤维喂养和产生短链脂肪酸的Lachnospiraceae和Ruminococceae,通过丁酸盐激活肿瘤免疫。
果胶→AKK菌→激活STING→提高肿瘤免疫
果胶喂养也可以通过导致AKK菌的扩张来提高肿瘤免疫力,从而产生环状二磷酸腺苷(cyclic-di-AMP)并激活STING;由此产生的I型干扰素依赖性免疫肿瘤微环境特征,与小鼠和黑色素瘤患者的免疫介导的肿瘤抵抗相关。
卡姆果→增加多样性,有益菌→增强抗PD1疗效
小鼠研究中,从卡姆果(camu camu)中分离的多酚——栗木鞣花素(castalagin,一种可水解的单宁)的口服给药具有抗肿瘤作用,并通过增加肠道微生物群的多样性,增加有望对抗PD1治疗有益的菌(如瘤胃菌科,颤螺旋菌科Oscillospiraceae和AKK菌)来改变其组成,从而增强小鼠的抗PD1治疗效果。
栗木鞣花素通过影响肠道微生物群组成,重新编程肿瘤免疫微环境,并在一定程度上通过直接结合而不内化于共生细菌(如Ruminococcus bromii)来促进抗癌反应,这可能有助于扩大这种细菌和其他有益细菌的种类,促进抗PD1治疗反应。这表明,栗木鞣花素和其他传统食品添加剂或其成分可能是益生元的来源,通过靶向微生物群来提高免疫疗法的反应性。
人参多糖→增加戊酸→增强抗PD1疗效
人参多糖是一种来源于人参的益生元,可以通过降低犬尿氨酸/色氨酸的比例,增加微生物代谢产物戊酸来增强癌症对PD1抑制剂的反应,从而促进Teff细胞的诱导和调节T细胞的抑制。
肠道微生物群在癌症治疗中,可以通过多种机制影响肿瘤的发展和治疗效果。
研究表明,肠道微生物群可能成为多种癌症类型的预后和预测标记。肠道微生物群有望增强抗癌力,改善放疗化疗效果和增强免疫治疗效果,以降低死亡率和提高生活质量。初步临床试验表明,对抗PD1治疗有反应的患者的FMT可以克服对ICB治疗的原发性和获得性耐药性,这证明可以靶向微生物群增强治疗反应。
然而,在这些临床治疗研究的进展中存在许多障碍和局限性。个体生物学差异可能会阻碍微生物策略的应用。该领域的挑战包括需要在不同的癌症类型、分期、地理区域、年龄、遗传、性别、生活方式、伴随疾病、治疗和合并症中进行前瞻性验证。将小鼠的结果推广到人类也应该谨慎。
虽然存在挑战,但相应的解决方案也在不断研究中。目前应用机器学习方法分析,在考虑了不同群体和地理差异的患者肠道菌群的组成方面取得了进展,这可能很快使肠道菌群成为一个可靠的生物标志物,用于预测患者对治疗的反应,从而实现个性化选择最适合的治疗方法。
将肠道微生物群与独立调节 ICI 功效的其他生物标志物(例如 PD-L1、TMB、IL-8 或某些代谢物等)结合起来,预测免疫疗法效果的能力可能会提高。
未来的临床进展需要更精确地鉴定细菌分类单元对癌症治疗具有积极和负面效应的因果关系,并了解其作用机制,因此需要进行更广泛的试验。
改进的细菌或许可以作为抗癌治疗药物,甚至可以被改造成指导性的“微型机器人”用于药物传递。
总的来说,这一领域的发展为癌症患者提供了新的治疗选择和希望,但同时也需要谨慎评估和监测,确保安全性和有效性。
肠道微生物群对于开发新的抗癌策略的重要性和潜力值得强调,并且有必要探索一种将微生物调节疗法纳入当前癌症管理的整体方法系统。未来我们有望实现更加精准和个性化的肠道菌群调节策略,为癌症治疗带来更大的突破和进展。
主要参考文献
Thomas AM, Fidelle M, Routy B, Kroemer G, Wargo JA, Segata N, Zitvogel L. Gut OncoMicrobiome Signatures (GOMS) as next-generation biomarkers for cancer immunotherapy. Nat Rev Clin Oncol. 2023 Sep;20(9):583-603.
Fernandes MR, Aggarwal P, Costa RGF, Cole AM, Trinchieri G. Targeting the gut microbiota for cancer therapy. Nat Rev Cancer. 2022 Dec;22(12):703-722.
Lee KA, Thomas AM, Bolte LA, Björk JR, de Ruijter LK, Armanini F, Asnicar F, Blanco-Miguez A, Board R, Segata N et al., Cross-cohort gut microbiome associations with immune checkpoint inhibitor response in advanced melanoma. Nat Med. 2022 Mar;28(3):535-544.
Zhao LY, Mei JX, Yu G, Lei L, Zhang WH, Liu K, Chen XL, Kołat D, Yang K, Hu JK. Role of the gut microbiota in anticancer therapy: from molecular mechanisms to clinical applications. Signal Transduct Target Ther. 2023 May 13;8(1):201.
Liu L, Shah K. The Potential of the Gut Microbiome to Reshape the Cancer Therapy Paradigm: A Review. JAMA Oncol. 2022 Jul 1;8(7):1059-1067.
McCulloch JA, Davar D, Rodrigues RR, Badger JH, Fang JR, Cole AM, Balaji AK, Vetizou M, Prescott SM, Fernandes MR, Costa RGF, Yuan W, Salcedo R, Bahadiroglu E, Roy S, DeBlasio RN, Morrison RM, Chauvin JM, Ding Q, Zidi B, Lowin A, Chakka S, Gao W, Pagliano O, Ernst SJ, Rose A, Newman NK, Morgun A, Zarour HM, Trinchieri G, Dzutsev AK. Intestinal microbiota signatures of clinical response and immune-related adverse events in melanoma patients treated with anti-PD-1. Nat Med. 2022 Mar;28(3):545-556.
Guillot N, Roméo B, Manesh SS, Milano G, Brest P, Zitvogel L, Hofman P, Mograbi B. Manipulating the gut and tumor microbiota for immune checkpoint inhibitor therapy: from dream to reality. Trends Mol Med. 2023 Nov;29(11):897-911.

谷禾健康

现代化疗,放射疗法在摧毁癌细胞的同时,对健康细胞也造成了伤害,引发相关毒性,反应例如便秘,腹泻,疲劳,恶心,呕吐等。
癌症患者的营养状况可能是癌症治疗相关毒性的核心决定因素,也是癌症症状的指标。
一些临床前研究和初步临床试验表明,饮食干预可能会减轻某些癌症治疗相关的症状和毒性。可能机制包括影响炎症、氧化应激、肌肉质量、心脏健康和调节肠道菌群。
本篇涵盖了三大块内容,包括:
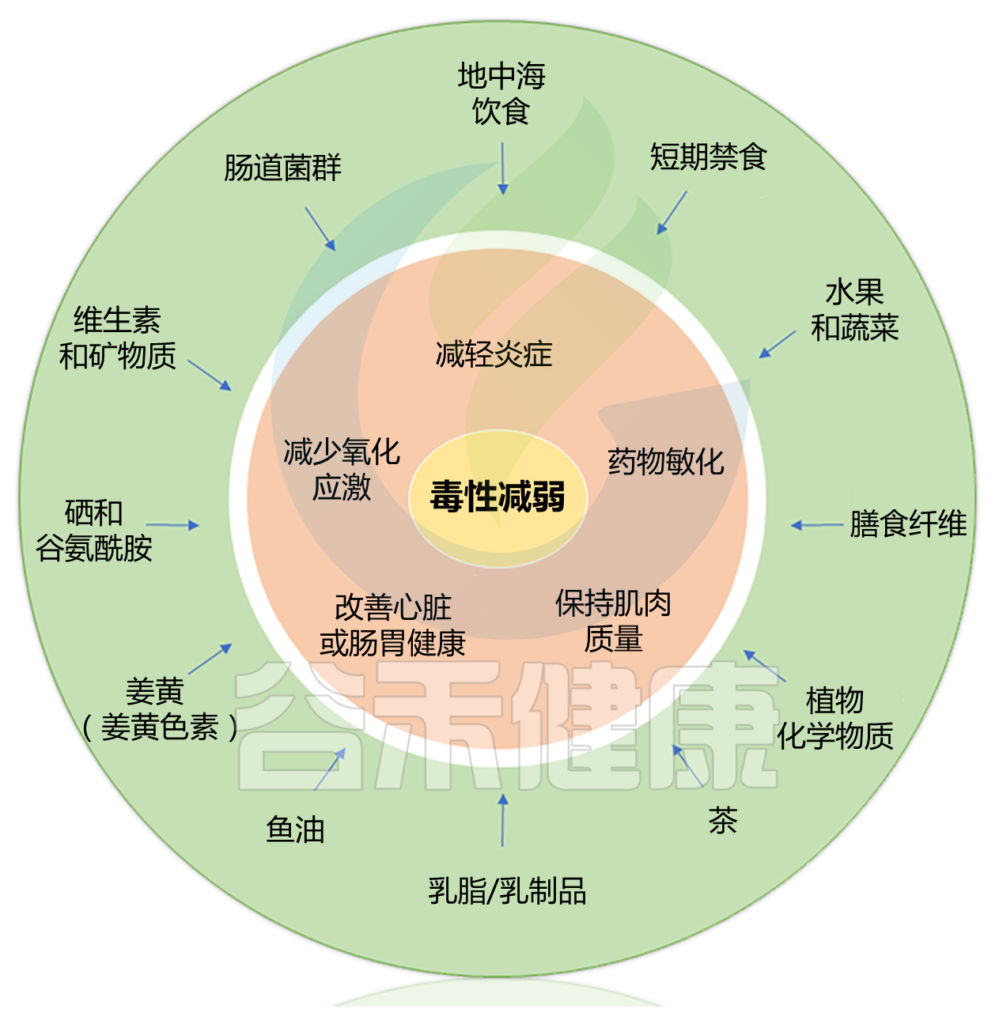
Alan J. Kim et al.,Cancer Treatment Reviews, 2022
地中海饮食模式,其特点是大量摄入水果、蔬菜、豆类、橄榄、全谷物、不饱和脂肪、坚果和鱼类;适度饮酒;减少红肉和加工肉类以及高脂肪乳制品的摄入,对减少炎症,改善心血管健康,抗肥胖,改善血脂以及对肠道菌群和免疫调节有积极作用。
↓↓ 降低心源性猝死
在一项大型前瞻性研究中,调查了激素替代疗法、钙和维生素D或饮食调整对健康绝经后妇女的影响,发现地中海饮食模式与降低心源性猝死的风险有关。
↓↓ 缓解癌症相关的疲劳
一项随机对照试验中,23名前列腺癌男性患者接受了至少3个月的雄激素剥夺治疗,被随机分成两组,一组接受12周常规治疗,另一组接受地中海饮食并同时接受六次个性化营养咨询,与常规治疗相比,坚持地中海饮食与缓解癌症相关的疲劳以及提高总体生活质量有关。
↓↓ 减轻妇科肿瘤患者症状
一项对22名接受铂类化疗的妇科肿瘤患者的观察研究表明,坚持地中海饮食的患者胃肠道毒性较小,恶心、胃痛、腹胀和干扰日常活动的频率和严重程度差异有统计学意义。
周期性禁食即在给定的时间内部分或完全不吃除水以外的食物和饮料。在动物模型和人类患者中,周期性禁食与降低癌症治疗中的毒性密切相关。
↓↓ 延缓肿瘤进展
例如,在一项临床前研究中证明,禁食条件增加了对化疗药物的敏感性,并延缓了肿瘤的进展。还有人发现,在荷尔蒙受体阳性乳腺癌的小鼠模型中,周期性禁食或类似禁食的饮食(FMD)可增强激素治疗的活性(如他莫昔芬和氟维司群),并通过降低循环中胰岛素、瘦素和IGF1的水平以及抑制AKT-mTOR信号传导来促进长期的肿瘤消退。
↓↓ 提升生活质量
在一项针对131名HER2阴性的II/III期乳腺癌患者的II期临床研究证实了4天FMD的潜在益处。在新辅助化疗前3天和新辅助化疗当天,接受了植物性、低氨基酸替代饮食(包括肉汤、汤、液体、维生素片和茶)的患者报告称,与对照组(常规饮食)相比,总体幸福感有所提高,情绪、身体、认知和社会功能都有所改善。
↓↓ 减少化疗相关毒性
在一项对照交叉初步研究中,调查了30名接受化疗的妇科癌症患者,结果表明,短期禁食的改良形式减少了化疗相关的毒性,包括口腔炎、头痛、虚弱和总体毒性。
据报道,FMD是安全可行的,可以减少脂肪量,降低循环中胰岛素生长因子1、胰岛素和瘦素的水平。禁食强烈影响新陈代谢和细胞途径,导致循环中类胰岛素一号生长因子(IGF-1)和葡萄糖水平下降。这些变化反过来影响几个癌基因,包括RAS和AKT信号通路,导致细胞生长和增殖的下调。
禁食和FMD(低卡路里、低蛋白质和低糖的饮食)可能与减少化疗副作用有关,即当营养素缺乏时,正常细胞,而不是肿瘤细胞,可以切换到抑制生长和增殖途径的保护模式,这一过程被称为差异应激抵抗。
↓↓ 增强免疫
此外,禁食和/或FMD已被证明可以增强免疫系统,减少炎症,减缓小鼠的骨密度损失,并减少HER2阴性的II期乳腺癌患者化疗引起的淋巴细胞DNA损伤。
生酮饮食的特点通常是碳水化合物消耗量低,占每日总热量摄入量的5%-10%,但其他产生能量的大量营养素,即脂肪和蛋白质的含量却不同。生酮比用来定义饮食的生酮能力,定义为脂肪克数与碳水化合物和蛋白质克数之和的比值。
在癌症中研究最多的生酮饮食包括经典生酮饮食(CKD),其特征是生酮比为4:1或3:1,每日87%-90%的热量来自脂肪)和中链甘油三酯生酮饮食[MCTKD,其中30%-60%的总热量来自中链脂肪酸,如己酸(C6)、辛酸(C8)、葵酸(C10)和月桂酸(C12)]。
↓↓ 血糖,体重更可控,生活质量高
在接受放化疗和辅助化疗的胶质母细胞瘤患者中,那些生酮饮食患者的血糖水平低于那些标准饮食的患者。有人研究发现,在接受放疗的非转移性乳腺癌患者中,以天然食物为基础的生酮饮食与未指定标准饮食相比,体重和脂肪减少得更多,生活质量水平更高。
↓↓ 降低癌症治疗相关毒性
生酮饮食降低癌症治疗相关毒性的机制可以用瓦氏效应(Warburg effect)来解释,在瓦氏效应中,癌细胞利用糖酵解而不是氧化磷酸化,能预防由活性氧引起的氧化损伤。
生酮饮食(通常是高脂肪低葡萄糖),可以利用这种代谢差异,要么让癌细胞挨饿,要么迫使它们转而利用氧化磷酸化。与正常细胞相比,癌细胞中氧化应激的增加可以使它们对化疗和放射更加敏感,从而减少治疗所需的剂量,降低与治疗相关的毒性。
↓↓ 注意高脂肪生酮饮食的副作用
有限的依据支持在临床实践中使用生酮饮食,而且,根据总含量和相对常量营养素组成,不同类型的生酮饮食可能对治疗相关的毒副作用产生不同的影响。例如,长期食用高脂肪生酮饮食可能会增加心血管或脑血管疾病的风险,特别是与特定的抗癌药物联合使用时。高脂生酮饮食还可能增加严重脂肪性肝炎的风险,促进肝纤维化的进展。此外,研究表明,高脂肪生酮饮食增加了酮体乙酰乙酯的循环水平,并促进了异种移植小鼠中表达BRAF-V600E致癌基因的人类黑色素瘤细胞的肿瘤生长潜力。
因此,根据目前对营养的理解,接受癌症治疗的患者的饮食应该包括所有的常量营养素,以降低营养不良的风险。
膳食纤维与多种肿瘤类型的胃肠道毒性和症状的预防有关。在一项随机对照试验中,在放疗期间服用高剂量膳食纤维(18克/天)的盆腔癌患者报告称辐射引起的胃肠道毒性发生率较低,证明了膳食纤维在预防放射治疗相关毒性方面存在潜在影响。
膳食纤维还可以促进健康的肠道菌群,从而降低毒性并增强治疗效果,例如纤维与促进免疫的普拉梭菌和短链脂肪酸丁酸盐的有关。有人发现在黑色素瘤患者中,膳食纤维会影响肠道菌群,并与免疫检查点阻断反应的增强有关。

Spencer CN, et al.,Science. 2021
tips
对于腹膜癌、肠癌进展或原发性胃肠癌的患者来说,可能需要低膳食纤维饮食,以降低肠梗阻的风险。
增加水果和蔬菜的摄入量与改善胃癌幸存者的身体和认知功能、减少疲劳和食欲不振有关。
水果和蔬菜含有过多的植物化学物质,并且已经检查了几种植物化学物质的影响,并在下表中进行了总结。

Alan J. Kim et al.,Cancer Treatment Reviews, 2022
例如,葡萄产品的抗氧化和抗炎作用归因于它们的植物化学物质,即芪类、花青素和原花青素,包括白藜芦醇。
其他几种水果,包括黑醋栗、李子、石榴和苹果,已经被证明具有抗癌和细胞毒性作用,这归因于植物化学物质,特别是多酚和黄酮类物质的抗氧化和抗炎作用。
tips
对于肠梗阻风险较高的患者,应避免过量摄入水果和蔬菜相关的膳食纤维。
据报道,在70多种植物中发现的一种植物化学物质白藜芦醇可以增加结直肠癌细胞系对化疗药物的敏感性,包括阿霉素、索拉非尼、5-氟尿嘧啶、依托泊苷、丝裂霉素、奥沙利铂和姜黄素。
关于白藜芦醇在该文有详细介绍:
注意:高剂量(每天>2.5克)会引起轻微的毒性(包括腹泻、胃肠道症状和前额头痛),即使在健康的人身上也是如此。
其他多酚也可能具有抗炎和抗氧化作用。
▸槲皮素是浆果中一种常见黄酮醇,它通过作用于炎症介质,包括白细胞介素6、白细胞介素8、干扰素γ、诱导型一氧化氮合酶、环氧合酶2和肿瘤坏死因子α来诱导抗炎作用,并在对促凋亡刺激敏感的癌细胞系中提供促凋亡作用。
▸非瑟素是一种存在于草莓、苹果和柿子中的类黄酮类化合物,在结构上与槲皮素相似,具有类似的抗炎和抗癌活性。
▸番茄红素是番茄和红色水果(包括木瓜和西瓜)中的一种植物化学物质,具有高抗氧化活性,并通过减少氧化应激以及染色体和膜的异常来减轻致癌损害。此外,番茄红素具有神经保护作用,并被认为可以通过减少氧化应激和神经炎症来预防神经毒性。
喝茶,尤其是绿茶,与抗癌作用、减轻药物引起的毒性以及对化疗药物的敏感性有关。
↓↓ 抑制继发性肿瘤
茶中存在的儿茶素在促进健康的作用中起着重要作用。表没食子儿茶素没食子酸酯在体外和体内乳腺癌模型中显示了抗氧化和抗炎活性(尤其是在他莫昔芬诱导的氧化应激情况下),能够抑制头颈部或盆腔癌症患者的放射性皮炎,并抑制继发性肿瘤的继发发展。
↓↓ 防止辐射带来的不良反应
据报道,表没食子儿茶素没食子酸酯还可用于预防暴露于γ辐射或以顺铂为基础的治疗后的唾液腺细胞功能障碍,防止辐射引起的不良血液学变化(如贫血、血小板减少),以及预防博莱霉素引起的肺纤维化。
↓↓ 减少药物引起的毒性
此外,表没食子儿茶素没食子酸酯可减少伊立替康治疗期间的胃肠紊乱、顺铂引起的肾毒性和耳毒性,以及阿霉素和柔红霉素治疗引起的心脏毒性。
在药物致敏方面,绿茶显示了许多与化疗的协同作用,其中一些包括与4-羟基他莫昔芬联合使用可以提高细胞毒性水平,通过降低大B细胞淋巴瘤(Bcl-xL)基因(编码抗凋亡蛋白)的表达使得MCF7细胞对5-氟尿嘧啶增敏,以及4只接种T1的Balb/c小鼠对紫杉醇的敏感性。这种致敏作用通过降低所需化学治疗药物的剂量有效地降低了药物引起的毒性的严重程度。
乳制品/奶制品与癌症治疗之间的关系一直存在争议。尽管据报道在Balb/c小鼠中,乳制品/乳脂可以增强紫杉醇治疗的有效性,并减少与该制剂相关的毒性,例如,器官损伤、腓肠肌丧失、附睾脂肪组织减少、红细胞和白细胞损失以及空肠形态、绒毛长度和肠 γ-谷氨酰转肽酶活性的破坏。
tips
有研究表明,在被诊断患有早期浸润性乳腺癌的女性中,高脂牛奶与乳腺癌、全因和非乳腺癌死亡率的增加有关,以及与绝经前妇女乳腺癌进展的风险增加有关。
鱼油富含omega-3脂肪酸,如二十碳五烯酸(EPA)和二十二碳六烯酸(DHA),在减少癌症和癌症治疗相关症状和毒性方面的作用已被广泛研究。
↓↓ 减少化疗引起的毒性
一项随机临床试验表明,在宫颈癌患者(n=40)中,补充鱼油可以减少化疗引起的毒性,如厌食、恶心、口干和味觉障碍。一项对88例癌症患者补充精氨酸、谷氨酸和鱼油的研究表明,补充精氨酸、谷氨酸和鱼油可显著减少3-4级血液毒性,并提高两年总生存率。
↓↓ 增强抗肿瘤作用
一些体外和体内研究表明,与单纯化疗相比,化疗期间给予EPA和DHA可以增强抗肿瘤作用,减少化疗对正常组织的毒性,抑制全身炎症,改善癌症患者的营养状况。同样,在紫杉醇和顺铂/卡铂治疗期间,在等卡路里饮食中添加EPA与非小细胞肺癌患者的疲劳减轻、食欲改善和化疗引起的神经病变减少有关。
↓↓ omega-3脂肪酸减少化疗毒性
omega-3脂肪酸还可以减少癌症相关的恶病质,增加免疫调节作用,从而增强结直肠癌和食道癌患者的化疗与放疗,减少食道癌患者化疗引起的毒性(如口腔炎,3/4级腹泻,以及天冬氨酸转氨酶和丙氨酸转氨酶水平的升高)。
已经提出了多种机制来解释omega-3脂肪酸在降低癌症治疗相关毒性方面的作用。其中一种假设是细胞膜的组成,这表明不饱和脂肪酸掺入癌细胞膜中,导致细胞膜组成模式与正常细胞不同。考虑到细胞膜是细胞内信号传导和基因表达调控的中心,癌细胞和正常细胞之间细胞膜上脂肪酸分布的不同可能导致信号通路的不同激活(例如,PKC激活和NF-KB 通路)。
尽管omega-3脂肪酸在临床试验中显示出了益处,但在临床前模型中,omega-3脂肪酸十六碳-4,7,10,13-四烯酸已证明可以抑制铂化合物的肿瘤导向细胞毒性,这可能会对患者造成潜在的伤害。
因此,在建议临床食用鱼油之前,有必要进一步研究普通鱼油成分与纯化的EPA/DHA对特定化疗药物的细胞毒性的影响。
姜黄是一种开花植物,可从中提取姜黄素。它们与预防和治疗化疗和放疗相关的不良事件有关。姜黄/姜黄素对癌症的有益作用归因于它们的抗氧化和抗炎特性,以及它们在抑制细胞增殖和肿瘤干细胞发展方面的作用,以及它们对肠道菌群和免疫系统的积极作用。
↓↓ 姜黄油降低化疗4级毒性发生率
姜黄油具有保肝作用,并缓解刀豆蛋白A诱导的氧化应激和炎症,从而减少人类患者的多种症状和毒性。同样,与其他草本物质:发酵大豆提取物、绿茶提取物、樟芝菌丝体、螺旋藻和葡萄籽提取物相结合,可显著降低接受亚叶酸钙/5-氟尿嘧啶化疗患者的4级毒性发生率。
↓↓ 姜黄/姜黄素减轻粘膜炎严重程度
一项评估的结论是,局部应用姜黄和姜黄素可以控制接受化疗和/或放疗的癌症患者的口腔粘膜炎,而接受姜黄/姜黄素治疗的患者报告称疼痛较轻,红斑强度较低,溃疡区域较少。一项评估32名接受放射治疗的头颈部癌症患者的临床试验也得出结论,口服纳米胶束姜黄素显著减轻了放疗引起的粘膜炎的严重程度。
↓↓ 姜黄/姜黄素有助于控制癌症相关的疼痛
一项针对绝经后乳腺癌患者的多中心临床试验(n=45)显示,联合应用羟基酪醇(一种在橄榄油中发现的具有强大抗氧化作用的酚类植物化学物质)、omega-3脂肪酸和姜黄素可以减轻患者报告的疼痛,并降低炎症生物标志物的水平。
↓↓ 姜黄与常见化疗药物的协同 / 拮抗作用
姜黄素在I期临床试验中协同增强化疗药物FOLFOX(5-氟尿嘧啶、亚叶酸钙、奥沙利铂)和达沙替尼对经FOLFOX处理的HCT116和HT-29细胞有抗增殖作用。
尽管这些结果提示了有希望的进一步研究领域,但对人乳腺癌细胞株(即MCF-7、MDA-MB-231和BT-474)的体外实验表明,姜黄素与以伊立替康或环磷酰胺为基础的化疗之间存在拮抗作用,饮食补充姜黄素可能会抑制基于化疗的肿瘤消退。这些发现表明,需要更多的研究来确定乳腺癌患者是否应该在化疗期间避免补充姜黄素。
谷氨酰胺是巨噬细胞、淋巴细胞和肠细胞的主要燃料来源,具有多种有益作用,包括改善免疫系统、减少炎症和分解应激状态。
↓↓ 化疗配合谷氨酰胺补充,降低血液学毒性发生率
一项针对接受同步放化疗的癌症患者的随机研究表明,除了常规饮食外,还接受精氨酸、谷氨酰胺和鱼油营养补充剂的患者与未接受补充剂的患者相比,发生3级或4级血液学毒性的发生率较低。
↓↓ 补硒改善免疫系统
据报道,补硒在脂质过氧化方面具有抗氧化作用,刺激自然杀伤细胞的细胞毒活性,减少肿瘤内血管生成,并在体外改善免疫系统。硒与重金属的解毒作用有关。这些影响的产生可能是因为硒是硒蛋白和酶的重要组成部分,这些硒蛋白和酶有助于抗氧化防御、减少炎症、甲状腺激素产生、DNA合成。
一项对关于硒和放射治疗的文章进行了评估,得出的结论是,每天服用300-500微克的硒,持续10天到6个月,可以减少放疗的副作用,包括腹泻、唾液腺损伤和辐射伤口,不会产生不良影响。
tips
高剂量的硒(>400微克/天)会产生严重的副作用,像指甲变脆、脱发、胃肠功能障碍、皮疹、神经紊乱等。
维生素补充剂在减少癌症和癌症治疗相关症状和毒性方面的功效研究显示出相互矛盾的结果。
例如,尽管许多研究表明维生素C补充剂具有潜在的抗癌作用和降低毒性作用,但对接受化疗的癌症患者的维生素C进行的系统审查发现,没有明确的证据表明服用维生素C补充剂可以减少毒性或改善治疗的抗癌效果。
同样,尽管维生素D补充剂已被证明可以预防癌症治疗引起的骨质流失,并恢复许多早期乳腺癌患者经历的维生素D不足,但在各种研究中报告的维生素D的抗肿瘤效果仍然很差。
tips
由于维生素补充剂在癌症治疗期间的效果尚不清楚,强烈建议患者遵守饮食建议,通过水果和蔬菜等天然食物摄入维生素,而不是依赖膳食补充剂。
一个健康人体胃肠道中的各种复杂的微生物群已显示出显著的生理益处,如增强肠道功能和消化能力、抵御病原体和调节免疫力。
虽然“健康”肠道菌群的定义并不明确,但数据表明,具有高度功能冗余度的多样化和稳定的微生物群是健康状态的关键标志。
肠道菌群对癌症患者的治疗反应有显著影响。例如,白血病或淋巴瘤患者在造血干细胞移植后具有高水平的粘液真杆菌,其复发或肿瘤进展的可能性较低。
↓↓ 肠道菌群失调影响抗PD-L1治疗效果
人类、动物和体外研究表明,肠道菌群的免疫调节影响靶向免疫治疗的疗效,如细胞毒性T淋巴细胞相关4(CTLA-4)阻断和抗PD-L1治疗。与这些发现一致的是,一部分接受抗PD-L1治疗和广谱抗生素治疗的上皮性肿瘤患者经历了失败治疗,其原因可能是导致了微生物群的失调。
进一步支持这些发现的是,从应答者和无应答者患者向有免疫活性小鼠的粪便转移导致小鼠对抗PD-L1抗体产生了与相应粪便移植供体相同的反应,从而证明了肠道菌群对抗PD-L1治疗的效果。
↓↓ 肠道菌群调节化疗的疗效和毒性
化疗药物环磷酰胺和阿霉素能诱导革兰氏阳性菌(约氏乳杆菌、鼠乳杆菌和海氏肠球菌)转移到小鼠的次级淋巴器官中。一旦转移到淋巴器官,微生物就会刺激17型和1型T辅助细胞反应的积累,从而增强免疫反应。
临床前和临床证据都表明,抗生素会降低化疗的疗效。例如,长期使用抗生素已被证明会降低环磷酰胺治疗荷瘤小鼠P815肥大细胞瘤的疗效,支持了肠道细菌易位的重要性。
一项对C57BL/6(B6)和129SvEv(129)小鼠化疗所致周围神经病变的临床前研究表明,肠道细菌在确定紫杉醇诱导的疼痛敏感性中起主导作用;在对紫杉醇诱导的疼痛敏感和抵抗的小鼠之间,观察到肠道微生物群组成的显著差异。
↓↓ 肠道菌群与胃肠道不良反应的发生率有关
一项对接受放化疗的宫颈癌患者进行的临床研究(n=35)得出结论,肠道微生物多样性与胃肠道毒性的发生率呈负相关。
同样,一项针对儿童急性淋巴细胞性白血病患者(n=51)的临床研究确定,化疗期间肠道微生物群的变化与胃肠道不良反应的发生率有关,如全身炎症和肠道粘膜炎。Toll样受体(TLRs)和肠道微生物之间的免疫调节相互作用可能调节结肠的炎症和愈合,防止甲氨蝶呤化疗的毒性。
↓↓ 肠道菌群从根本上与粘膜炎的发病机制相关
粘膜炎是一种常见的胃肠道毒性,会导致腹泻、疼痛、体重减轻和剂量限制。例如,伊立替康是一种已知会引起严重腹泻的化疗剂。这种毒性的一种机制可能是某些细菌β-葡萄糖醛酸酶的作用,这些酶已被证明通过将伊立替康的活性代谢物SN-38释放到肠腔中来诱导腹泻。
与这一假设一致,通过喹诺酮类抗生素环丙沙星抑制此类酶可抑制伊立替康治疗小鼠的腹泻,从而证明肠道微生物群的调节可以降低伊立替康的毒性。
↓↓ 肠道菌群影响癌症治疗相关的心理神经症状
一项系统评价评估了肠道微生物群与化疗之间关系的研究,得出的结论是,肠道微生物群可能会影响癌症治疗相关的心理神经症状,例如疲劳、焦虑、抑郁和睡眠障碍。
因此,相对健康的肠道微生物群可以改善癌症患者的健康,通过增强治疗效果和减少免疫疗法和化学疗法的副作用以及通过免疫调节等方式。
饮食影响肠道微生物种类的组成和多样性。膳食纤维的高摄入量有利于膳食纤维消化细菌的增加。作用机制是消化膳食纤维的细菌产生丁酸等短链脂肪酸,滋养肠道上皮细胞,从而加强肠道黏膜屏障,增强黏膜和全身免疫。
↓↓ 食品补充剂调节微生物群驱动的化学治疗毒性
由于肠道屏障和微生物群稳态的潜在损害,化疗通常与肠道菌群的改变有关。因此,预防和治疗与化疗相关的肠道菌群改变可能有助于预防与化疗相关的胃肠道毒性。
▸从鱿鱼墨汁中提取的多糖在小鼠给药环磷酰胺后可富集双歧杆菌,并减少拟杆菌,从而改善肠道微生物群功能障碍。
▸人参化合物可以增强化疗药物5-氟尿嘧啶对结直肠癌细胞系的作用,特别是当这些化合物被肠道微生物群菌群代谢时。
▸鞣花酸,一种常见于草莓、葡萄和黑莓等蔬菜和水果中的多酚,被肠道菌群代谢释放尿石素,这对人类结肠癌具有抗增殖作用。
↓↓ 益生元和益生菌在癌症治疗中发挥作用
益生元(促进有益肠道微生物生长的难消化的食物成分,例如香蕉、芦笋和朝鲜蓟)和益生菌(引入体内以发挥有益作用的微生物,例如酸奶、克非尔、酸菜、豆豉,和泡菜)与肠道菌群的组成密切相关,这些物质在癌症治疗过程中的作用很关键。
许多动物和人类研究表明,益生元、益生菌在预防化疗期间的粘膜炎方面具有强大的作用。
对于接受同步放化疗的鼻咽癌患者,益生菌与放射治疗相结合,可以通过改变肠道菌群,显着增强宿主免疫力,缓解放化疗相关的口腔黏膜炎。
VSL #3(包括Streptococcus thermophiles, Bifidobacterium breve, B. longum, B. infantis, Lactobacillus paracasei, L. delbrueckii subsp. bulgaricus, L. acidophilus, L. plantarum),在伊立替康治疗期间,减少大鼠腹泻和体重减轻。
L. casei, L. rhamnosus, B. bifidum 通过抑制肿瘤坏死因子α、白细胞介素-1b和白细胞介素-6 mRNA的表达减少化疗诱导的小鼠腹泻。
鼠李糖乳杆菌GG补充可减少人类大肠癌患者在5-氟尿嘧啶化疗期间的严重腹泻和腹部不适。
在接受化疗的儿童中使用养乐多的短双歧杆菌菌株可预防发烧并减少静脉注射抗生素的频率。
膳食补充益生元低聚果糖和菊粉可放大药物对小鼠的作用(5-氟尿嘧啶、多柔比星、长春新碱、环磷酰胺、甲氨蝶呤、阿糖胞苷),从而证明了益生元与化疗之间的协同作用。
编辑
大量临床前数据以及有限的临床证据表明,饮食因素可能在预防和/或治疗癌症以及癌症治疗相关的症状和毒性方面发挥作用,寻求特定饮食干预措施的数据仍在不断涌现。
人们对肠道菌群的性质和对癌症治疗的影响也越来越感兴趣。期待更大样本量的随机对照试验,进一步研究饮食干预措施。
最好的饮食是患者愿意并且能够坚持的饮食,因此在将这些策略引入临床时可能需要一定程度的个性化。
如果能开发出,通过调节肠道菌群来改善治疗效果的药物,其潜力是巨大的。
主要参考文献
Spencer CN, McQuade JL, Gopalakrishnan V, McCulloch JA, Vetizou M, Cogdill AP, Khan MAW, Zhang X, White MG, et al. Dietary fiber and probiotics influence the gut microbiome and melanoma immunotherapy response. Science. 2021 Dec 24;374(6575):1632-1640. doi: 10.1126/science.aaz7015. Epub 2021 Dec 23. PMID: 34941392; PMCID: PMC8970537.
Yu ZK, Xie RL, You R, et al. The role of the bacterial microbiome in the treatment of cancer. BMC Cancer. 2021;21(1):934. Published 2021 Aug 19. doi:10.1186/s12885-021-08664-0
Kim AJ, Hong DS, George GC. Dietary influences on symptomatic and non-symptomatic toxicities during cancer treatment: A narrative review. Cancer Treat Rev. 2022 May 13;108:102408. doi: 10.1016/j.ctrv.2022.102408. Epub ahead of print. PMID: 35623220.
Barrea L, Caprio M, Tuccinardi D, Moriconi E, Di Renzo L, Muscogiuri G, Colao A, Savastano S; Obesity Programs of nutrition, Education, Research and Assessment (OPERA) group. Could ketogenic diet “starve” cancer? Emerging evidence. Crit Rev Food Sci Nutr. 2022;62(7):1800-1821. doi: 10.1080/10408398.2020.1847030. Epub 2020 Dec 4. PMID: 33274644.
Baguley BJ, Skinner TL, Jenkins DG, Wright ORL. Mediterranean-style dietary pattern improves cancer-related fatigue and quality of life in men with prostate cancer treated with androgen deprivation therapy: A pilot randomised control trial. Clin Nutr. 2021 Jan;40(1):245-254. doi: 10.1016/j.clnu.2020.05.016. Epub 2020 May 25. PMID: 32534948.