 国家高新企业 | ISO9001认证
国家高新企业 | ISO9001认证 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康

抗生素耐药性是当下和未来几十年人类健康将面临的重要挑战之一。从2000年到2015年,抗菌药物的普及导致人类抗生素消耗量增加了约65%,2015年后这个数据还在增加。最明显的后果是抗生素耐药性的增多,这使得近年来常见的感染难以治疗。
最近,由于担心出现更难治疗的肠道感染和其他感染,以及耐药病原体可能传播给更脆弱的人群(如小孩和老人),人们对使用抗生素进行严格管理和开展精准用药算是迈开了第一步。
抗生素的使用经常产生脱靶效应,这意味着抗生素的使用浓度所引发的抗菌作用超出了消除影响病原菌的作用。下一代靶向测序已证明抗生素会导致肠道细菌生物量、分类多样性和功能多样性减少。
除了耐药性之外,抗生素未能清除感染的原因还有多种。感染灶中药物的药代动力学较差或生物膜(下期专门讲)等受保护的生态位中细菌的持续存在会导致治疗失败。
此外,在感染过程中,一些细菌(持续存在)可能会由于进入抗生素持久性状态而在药物治疗后达到致命的浓度。然后会引起长期和反复感染,导致最终治疗失败。
感染期间抗生素的持久性涉及持久性在宿主免疫反应和药物的联合作用下生存的能力。病原体已经进化出多种方式来击败宿主的免疫反应,并且它们的毒力因子已经被仔细研究了几十年。然而,细菌通过持久性抵抗抗生素暴露的能力仍然更加难以捉摸。
虽然抗生素暴露对病原体清除的正向影响有利于宿主健康,但抗生素暴露对肠道微生物组组成和功能的脱靶影响可能会对宿主健康产生有害或有益的影响,具体取决于初始成分和原生微生物群落的功能。
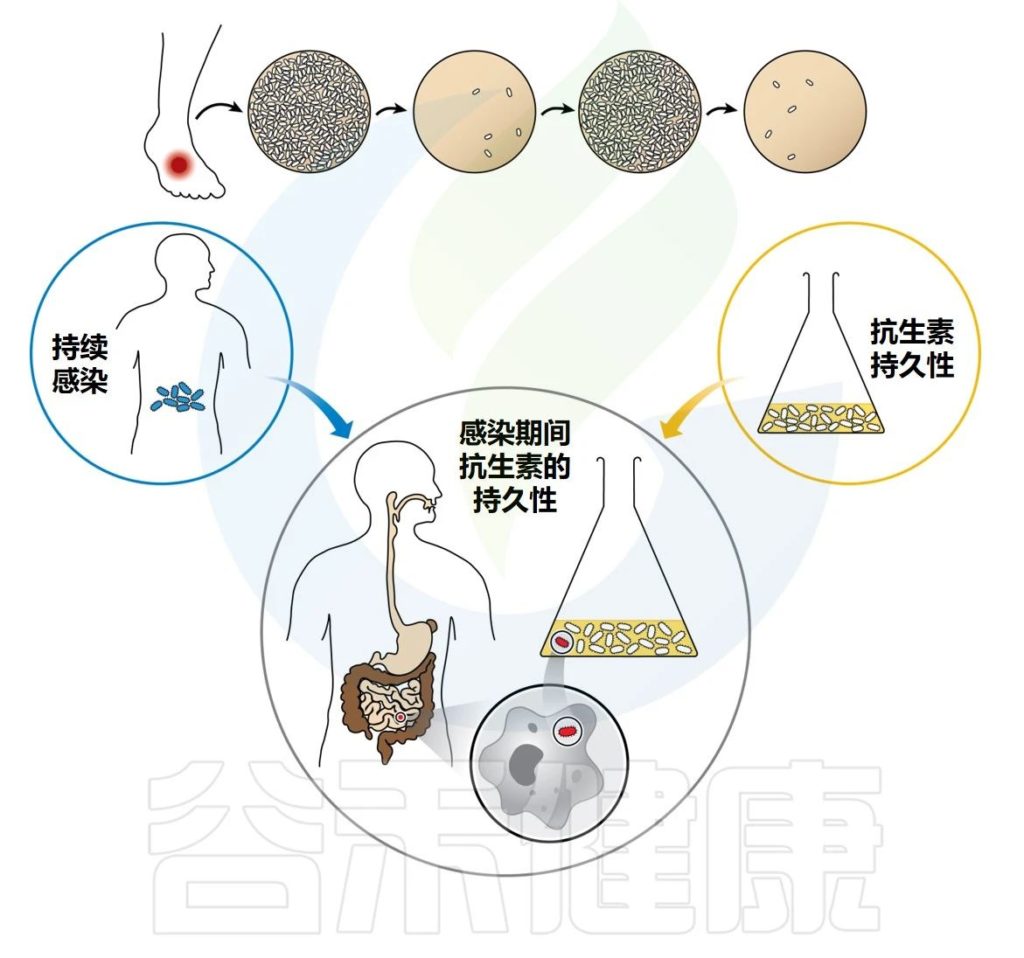
预测抗生素耐药性进化轨迹以及耐药风险的能力对于调整抗生素的给药方案以最大限度地延长其使用寿命具有重要价值。
本文将讨论抗生素持久性以及微生物持久性形成在感染中的重要性,了解肠道微生物群如何对抗生素扰动做出反应以及对特别人群的影响、影响抗生素暴露对微生物群影响的因素、抗生素引起的微生物群改变的潜在健康结果以及有可能改善这些问题的策略。
抗生素持久性领域仍处于起步阶段;然而,关于定义的争议和讨论已经模糊了关键概念及其各自的重要性。在这里,采用的定义和说明与最近几十个研究小组的文章一致。
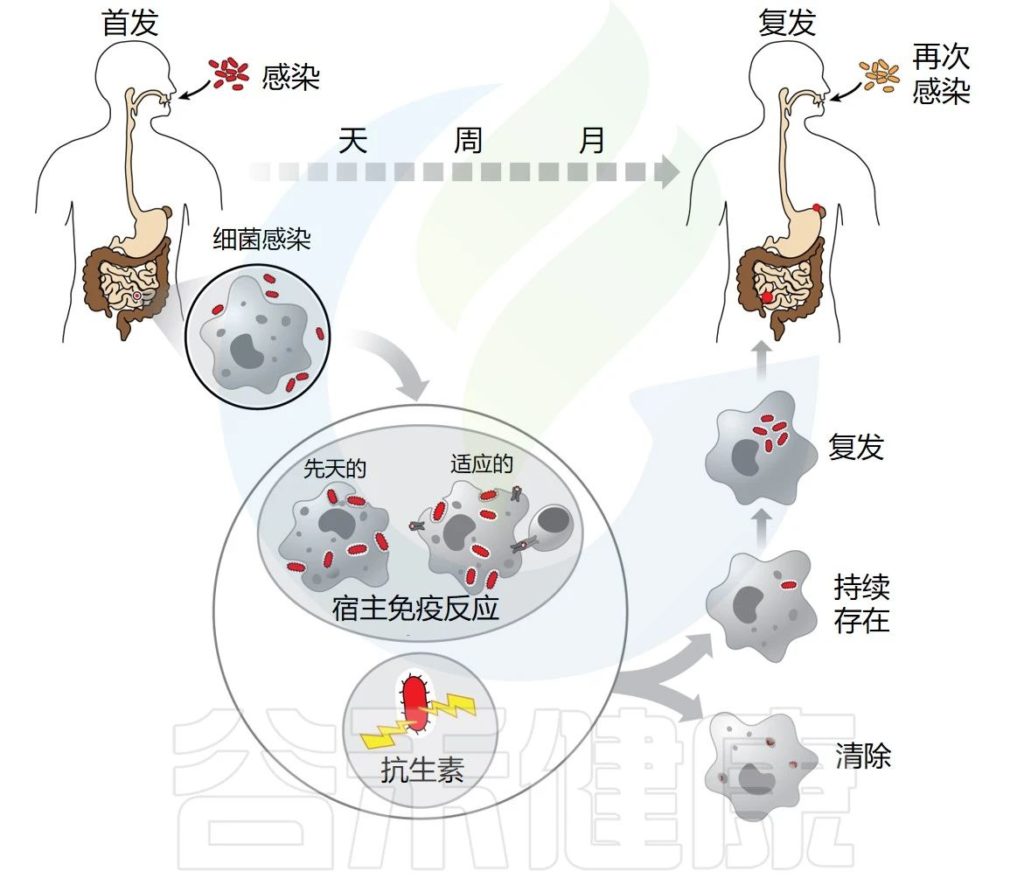
Gollan B,et al.Annu Rev Microbiol.2019
确定的定义主要集中在体外研究的细菌上,并以最小抑制浓度(MIC——明显抑制细菌生长的药物最低浓度)和杀死99%数量细菌所需的最少时间(MDK99)的测量为中心。
尽管这些测量对于区分允许细菌在实验室培养物中暴露于抗生素后存活的不同现象非常有价值,但它们在感染模型中的工作中难以进行。
因此,研究者们更多地关注不同概念的描述性定义。重要的是,一些导致抗生素暴露存活率增加的细菌行为(即抗生素持久性和表型耐药性)涉及复制群体内的表型异质性,因此最好通过群体和单细胞特征的组合来描述。
▼
▸ 细菌的耐药性
当细菌能够在对同一物种的参考菌株致死的药物浓度下增殖时,细菌被认为对抗生素具有耐药性。
耐药性通常(但并非总是)特定于一种药物或一类药物,并且是由于非耐药亲本菌株的基因修饰(从头突变或通过水平基因转移获得)造成的。
遗传性状会代代相传
一旦获得,遗传性状就会代代相传。产生耐药性的主要原因是药物或药物靶点的输出或修改。在体外,可以通过测量增加的明显抑制细菌生长的药物的最低浓度。
▸ 群体的耐受性
当暴露于杀菌药物时,整个细菌群体可能表现出较低的杀灭率,因为群体的增长率因遗传或环境因素而降低。因此,与普通菌株相比,生长缓慢的细菌表现出相对的药物冷漠,这增加了种群在抗生素暴露下存活的时间。
从理论上讲,足够长的时间接触抗生素应该可以清除整个人群。营养缺陷型突变代表了这种耐受现象的一个极端例子。当环境条件发生变化允许恢复快速生长时,种群就会恢复到易感表型。在体外,可以通过测量杀死一定比例的群体的持续时间来量化耐受性。
▼
抗生素持久性和表型耐药性代表了抗生素存活方面的异质行为。“持久性”与“耐药性”一词指的是两个不同的概念,它们被认为是有联系的,但又是不同的。因此,它们不能互换使用。
▸ 感染持续存在
当病原体有能力在宿主体内停留较长时间时,无论宿主免疫反应如何或长期抗生素治疗如何,感染都会持续存在。
据信,持续感染至少部分依赖于感染人群的耐受性(或药物冷漠)以及抗生素的持久性,但这种联系仍然很脆弱。迄今为止,抗生素持久性领域主要忽视了持久性细菌在宿主体内生存的能力。
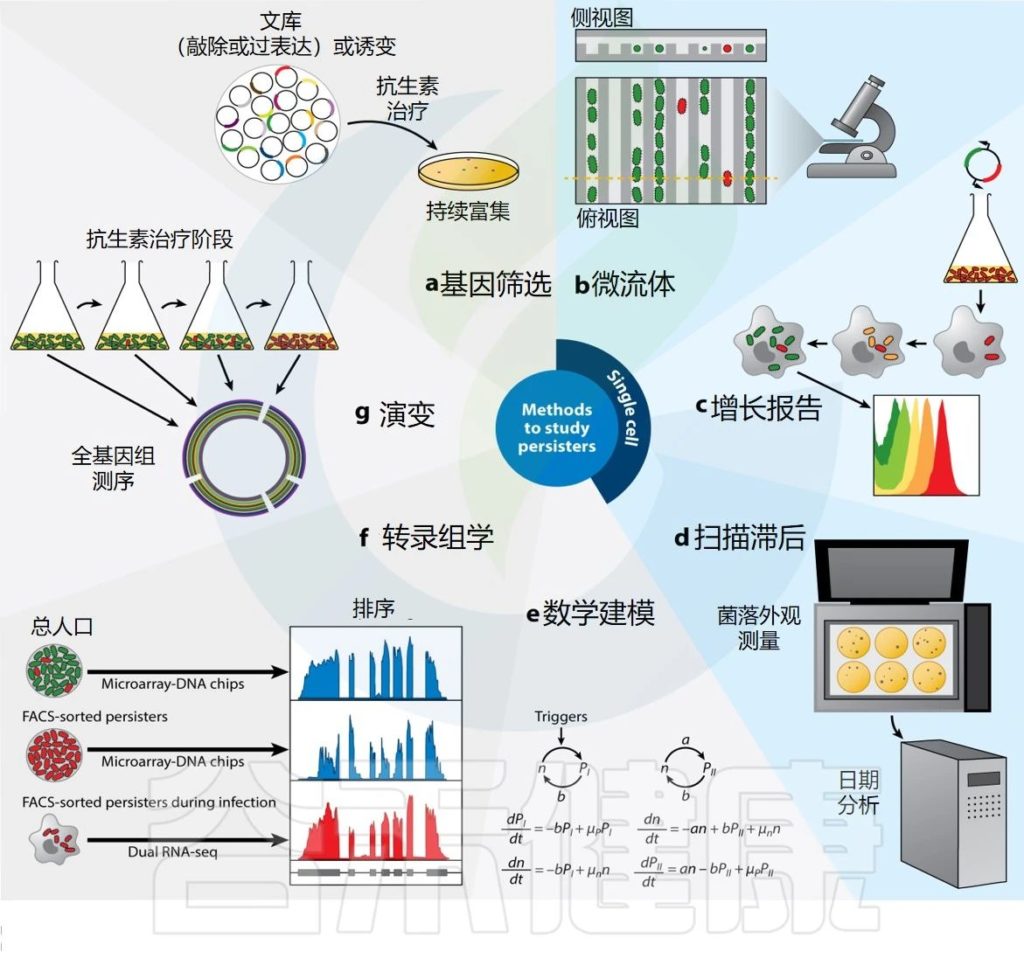
Gollan B,et al.Annu Rev Microbiol.2019
▸ 抗生素持久性
药物暴露后的这种异质群体行为是由于细菌亚群(持续存在)通过生长停滞、暴露于对其余群体致命的浓度的抗生素而得以生存的能力。
由于持续者是非定植者,因此他们的存在不会影响整个种群的MIC。在种群水平上,这种现象在几代群体中都是稳定的,这表明种群内的所有细菌都具有持续存在的遗传装备。
MIC——明显抑制细菌生长的药物最低浓度
抗生素持久性与压力有关
抗生素持久性很大程度上是由 “压力” 引发的,最好在压力缓解后进行评估,以免与耐受现象混淆。
事实上,与耐受人群相反,持久人群携带着压力暴露的记忆。由于现象的异质性,通常可能需要允许单细胞分析的工具来获取有意义的信息。
▸ 持续者
持续者是抗生素持久性种群中的个体,当暴露于对其他种群中的亲属致命的浓度的抗生素时,它们能够通过生长停滞而生存。
持久菌在药物中存活的能力是短暂的,并且持久菌后代是异质的,由易感细菌和持久菌组成。在体外,群体中存留菌的存在可以通过双相杀伤曲线来揭示,该曲线显示存活率与时间的关系,其中易感细菌被快速杀死,存留菌存活时间更长。
▼
表型耐药性是在药物暴露时可能发生的另一种异质行为,这是由于细菌亚群(耐药性)在抗生素浓度达到对其余菌群致命的情况下能够增殖的能力。
整个群体的最小抑制浓度与易感菌株相当
由于群体主要由易感细菌组成,因此整个群体的MIC(明显抑制细菌生长的药物最低浓度)与易感菌株的MIC相当。在种群水平上,这种现象在几代菌中都是稳定的,这表明种群中的所有细菌都具有抵抗力的遗传装备。
▸ 休眠
休眠是一个用于定义一系列特征的术语,从缺乏任何可测量的细胞活性到生长停滞。在这篇文章中,我们用它来表示缺乏活性。
从体内感染模型中积累的新证据强调了持续感染者在持续感染中的重要性。持续感染者在感染复发中的潜在作用是对其进行研究的重要原因。
★ 开发研究持久性的技术
由于这种生理状态的短暂性和可逆性,以及相对稀有的残留物可以产生少量的生物材料,研究抗生素残留物具有挑战性。
长期以来,最常见的方法是从基因或环境角度操纵细菌种群,并测量其对持久性水平的影响。虽然这使得能够识别涉及调节群体中持续者水平的压力和途径,但近年来通过建立能够跟踪、收集和分析持续者的方法,取得了重要突破(下图)。
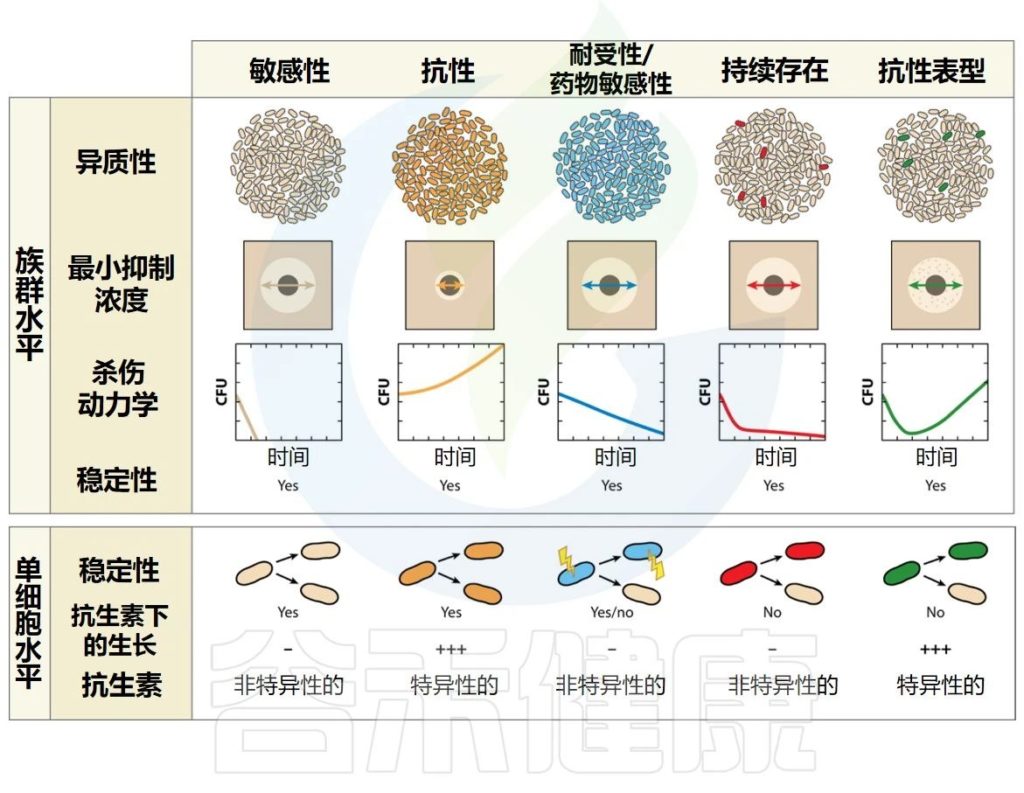
Gollan B,et al.Annu Rev Microbiol.2019
很快,人们就清楚地意识到重点应该放在单细胞研究上,因为持久性细菌只是细菌种群的一小部分。微流体装置与显微镜和流式细胞术相结合的使用成为一种选择技术。微流体背后的基本原理是分离单个细菌,以便使用延时显微镜来跟踪个体随时间的行为,以检查持久细胞的历史。
然而,微流体带来的对单个细菌的直接可视化和跟踪的能力受到可同时评估的细胞数量有限的阻碍。因此,流式细胞术提供了一种替代方法,允许以高通量方式进行单细胞分析,并通过荧光报告基因的发展,增强对感兴趣细胞进行分选的能力。
因此提出休眠(代谢活动的缺乏)对于进入持久性既不是必要的,也不是充分的。第一个开发荧光稀释技术来在单细胞水平上追踪细菌分裂的人。这种方法类似于免疫学家用来追踪T细胞增殖的羧基荧光素琥珀酰亚胺酯 (CFSE) 染色。
高通量下一代测序技术的兴起,随着生物信息学分析的改进和此类平台的可访问性的增加,也为持久化领域带来了视野。
最后,除了用于跟踪持久者的实验室技术之外,数学模型还允许对持久者行为进行计算机预测。例如,已经建立了一些模型来重点了解单细胞水平上持久物形成的分子机制。
▼
许多病原菌在宿主组织内建立持续感染,避免被免疫系统和抗生素清除。细菌感染通常会导致宿主产生先天免疫反应,然后产生适应性免疫反应,这通常足以清除感染。然而,许多病原体已经进化出复杂的生存机制来逃避免疫反应并建立持续感染。
// 急性结核感染
急性结核感染是细菌躲避免疫系统且相对难以治疗的典型例子,导致需要长时间的抗生素治疗才能治愈感染。
然而,分枝杆菌感染有时只能部分清除,并且10%的患者在其一生中会出现复发。复发不仅出现在结核病中。5%至10%的患者会出现伤寒复发。
// 其他感染
尿路致病性大肠杆菌引起的尿路感染(UTI)后,20%至30%的女性会再次出现症状;许多其他细菌感染在治疗后往往会复发。
✦许多感染会反复发作
“复发”一词用于描述这样一种现象:最初感染的症状暂时消退,直到首次感染时未清除的细菌库重新激活。
有多种原因会导致感染反复发作,例如宿主易感性增加、其他慢性合并感染以及环境和生活方式因素。
较难确定是再次感染还是复发
长期以来,无法确定感染复发是再次感染还是复发。当初次感染完全清除后,个体出现新的感染时,就会发生再感染。
▼
抗生素残留物研究中投入的许多努力都围绕着调查残留物形成的触发因素和途径。
✦持久性的形成是一种细菌应激反应
但一个总体观察结果是,持久性的形成是一种普遍的细菌应激反应。多种环境因素充当压力信号,促进持久者的产生。
此外,大多数已被确定参与持久物形成的分子途径都是应激反应元件。我们首先回顾了持续细胞形成的触发因素,然后回顾了持续细胞形成所涉及的分子途径和效应器(下图)。
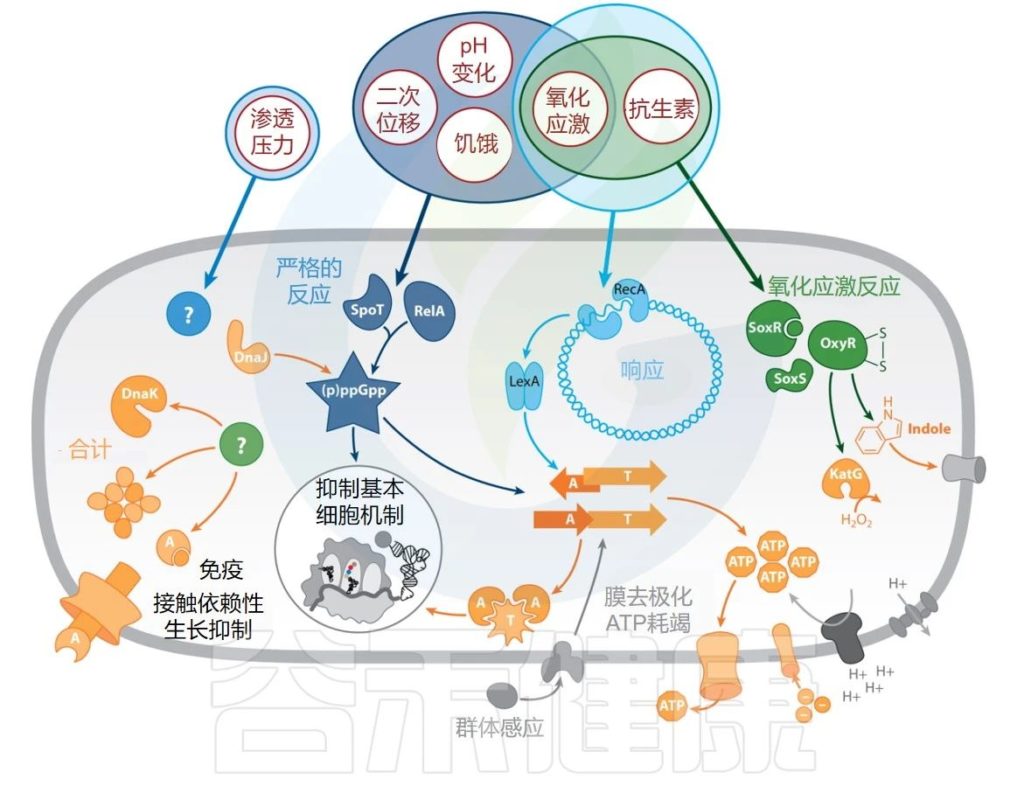
Gollan B,et al.Annu Rev Microbiol.2019
抗生素持久性的触发因素、途径和效应器。持久性的外部触发因素以红色圆圈显示。应激反应途径为蓝色或绿色(已识别的效应器为橙色,受效应器影响的细胞成分为灰色)。
缩写:A—抗毒素;T—毒素。
▼
选择压力可能是最难确定和纳入模型的因素。因此,在人类、动物和其他环境中,细菌病原体暴露于各种选择剂,这些选择剂通常存在于复杂的混合物中(例如抗生素、杀生物剂),并且其浓度可能随着时间的推移而发生很大变化。因此,在实验室环境之外通常很难确定选择的强度。
✦抗药性的选择具有较大差异
此外,抗药性的选择过程将有很大差异,具体取决于药物浓度是否足够高以(a)阻止病原体生长(如果> MIC则致命选择,如果< MIC则非致命选择)和(b)允许敏感和耐药菌同时生长。
在前一种情况下,在应用选择之前需要存在抗性突变体,富集率由群体中突变体的数量及其在特定抗生素浓度下的适应性决定。
然而,在最小抑制浓度选择过程中,可能会出现突变体,其富集率由群体中突变体的数量以及易感细胞和耐药细胞之间的适应度差异决定。因此,致死和非致死选择压力的出现率和选择的突变体类型有所不同。
高致死抗生素浓度
在高致死抗生素浓度下,在一个遗传事件中提供高水平耐药性的罕见的预先存在的大效应突变往往会被选择性富集(下图)。
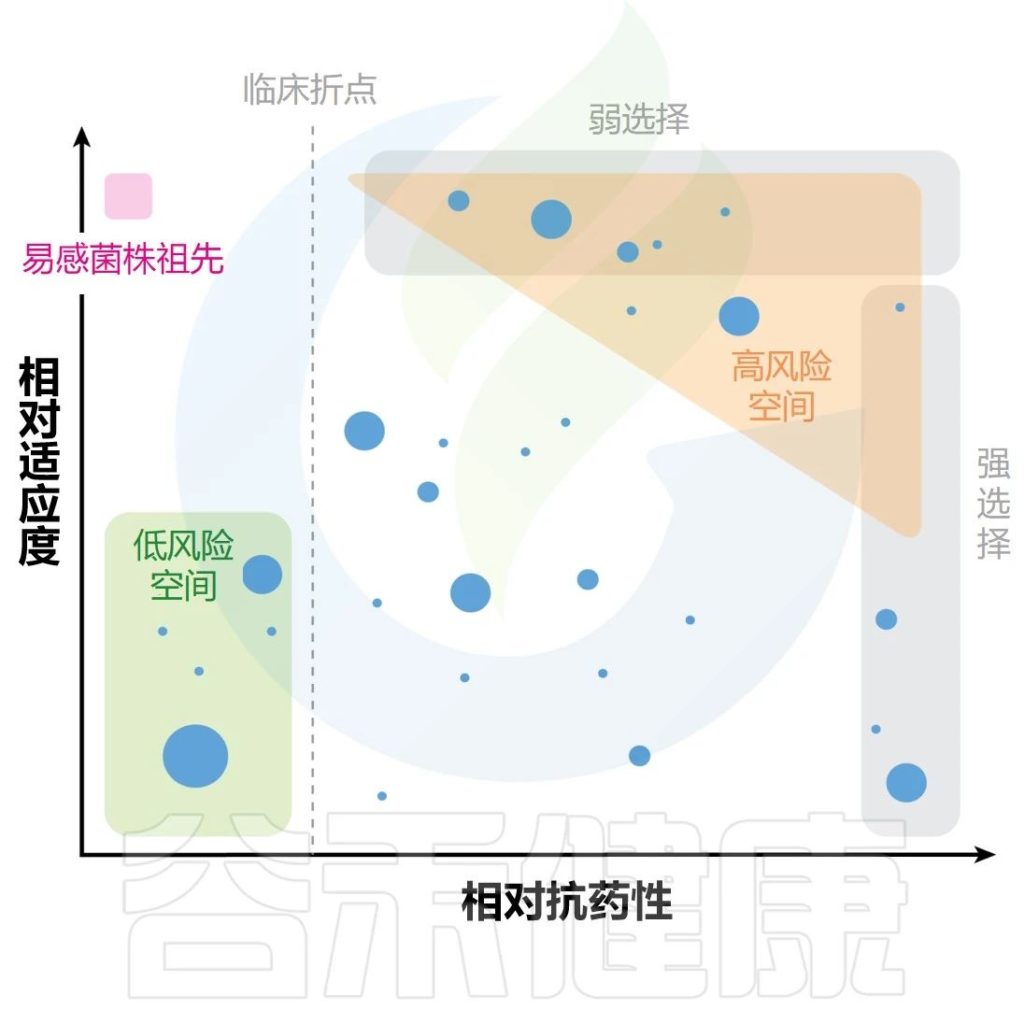
Gollan B,et al.Annu Rev Microbiol.2019
非致死性抗生素浓度
相反,在非致死性抗生素浓度下,富集的突变体通常是由许多对耐药性影响较小的突变引起的(但它们组合起来可能会产生高水平的耐药性)。
重要的是,选择越弱(即易感细菌和耐药细菌之间的适应度差异越小),对于低适应度成本的突变体(上半部分)的富集就越强。
此外,由于在弱非致死选择压力下逐步选择连续的小效应突变,通过突变或水平基因转移获得抗性的概率增加的突变菌株得到富集。
注:矛盾的是,较弱的非致死选择可能比致死选择更富集有问题的突变体(高适应度菌株和突变体)。
许多触发因素似乎都会刺激持久性的形成,从饥饿或氧化应激等营养应激再到细胞外代谢信号。
几十年来,人们都知道抗生素的杀灭率取决于细菌的生长速度,而细菌的生长速度又取决于碳源的可用性,因此控制整个细菌群体的抗生素耐受性。
✦营养缺乏是持久性形成的诱因
此外,营养缺乏似乎是持久性形成的主要诱因之一。例如,氨基酸或氮饥饿会增加铜绿假单胞菌(Pseudomonas aeruginosa)、变形链球菌(Streptococcus mutans)和大肠杆菌(Escherichia coli)等不同物种中经抗生素治疗后存活下来的细菌数量。
! 手术或抗生素治疗后患者的营养非常重要
这就涉及另外一个主题,就是手术或抗生素治疗后,患者的营养,尤其肠内营养的监测或补充非常重要。
还有充分的证据表明,细菌培养物在进入稳定期及以后往往会开始积累持续细胞,然后持续细胞的比例达到与生物膜中所见的水平一样高。事实上,研究表明,营养和氧气有限的生物膜中含有非常高比例的持久物。
除了饥饿造成的剧烈压力外,碳源的变化会破坏代谢通量(可被视为暂时饥饿),也会导致大肠杆菌的持续存在增加。
这种碳源转变伴随着严格反应关键介体四磷酸或五磷酸鸟苷 [ (p)ppGpp ] 水平的大幅增加,这可能是饮食模式改变或节食诱发的。
重要的是,通过营养转换形成的持续细胞似乎维持高 ATP 水平,从而允许非生长相关过程的继续,例如维持膜电位。
除了营养变化之外,氧化、酸性和渗透应激也被认为是持久物形成的触发因素。例如,用过氧化氢处理大肠杆菌培养物或通过向培养基中添加水杨酸盐产生活性氧会导致持久性细菌的增加。
✦吲哚促进持久细胞的形成
同样在大肠杆菌中,吲哚(一种色氨酸生物合成中间体,其产量因氧化应激而增加)被证明可以促进持久细胞的形成。
此外,无法合成海藻糖的大肠杆菌突变体产生的氧化应激与吲哚分泌增加和持久物形成同时发生。
暴露于吲哚的细菌上调了它们的oxyR调节子和噬菌体休克pspBC途径,并且这些途径的缺失降低了吲哚促进持久细胞形成的能力。
沙门氏菌也观察到对吲哚的类似反应,伴随着katG 过氧化氢酶表达的增加,有趣的是,沙门氏菌不产生吲哚。然而,这可能有利于肠道中的沙门氏菌,肠道中的沙门氏菌在感知来自其他微生物群的吲哚时升高的氧化防御反应可能会保护其免受伴随局部炎症的氧化应激。
✦pH值变化和高渗透压也促进持久性形成
pH值变化和高渗透压是促进持久物形成的其他压力。此外,抗生素本身也可能引发持久性细菌的形成,例如在大肠杆菌或金黄色葡萄球菌中,其中用亚抑制浓度的各种抗生素进行预处理显著增加了残留物水平。
✦氧化应激和抗生素诱导细菌群体的持续存在
重要的是,暴露于逐渐增加的抗生素浓度的肺炎克雷伯菌(Klebsiella Pneumoniae)临床菌株显示出持续增加的水平,以及随后出现的耐药变异体。
这一观察结果可能特别相关,因为在临床中抗生素输送和药代动力学通常会导致血液中抗生素浓度逐渐增加。这可能会增加持久菌群的规模,从而增加产生耐药性的细菌库。
同样,氧化应激和抗生素诱导的DNA损伤的结合已被证明可以诱导细菌群体的持久存在。总体而言,许多非生物胁迫导致持久细胞形成增加,大量研究充分支持了这一点,表明主要的细菌胁迫反应是这种表型的强有力的协调者。
当暴露于细菌分泌到周围环境中的细胞外代谢物时,也可以刺激持久细胞的形成。
✦细胞外代谢物也刺激持久细胞的形成
除了上面引用的吲哚的例子之外,能力刺激肽CSP(一种群体感应分子)被证明可以促进变形链球菌(Streptococcus mutans)持久细胞的形成。
这种群体感应分子似乎是一种中间体,向其他群体发出压力信号,以便其做出适当的压力反应,包括持久性形成。同样,一些假单胞菌群体感应分子不仅可以增加假单胞菌的存留细胞分数,还可以增加通常从囊性纤维化患者中分离出来的不动杆菌和伯克霍尔德氏菌的存留细胞分数。
因此,似乎不仅种内信号传导而且种间信号传导也可能促进持久物的形成。
在感染过程中,细菌会经历上述压力的组合,其强度和时间各异,可能有利于持久细胞的形成。
这提出了一种可能性,即在受感染宿主中形成的细菌持续存在可能独特地适应了它们最初形成的触发因素,并且与从生长的细菌中分离出的细菌不同,后者通常使用单一应激因子来诱导细菌持久化状态。
✦宿主巨噬细胞诱导持久化
就沙门氏菌而言,它在宿主免疫骨髓细胞中存活,其持续水平在被小鼠巨噬细胞内化后急剧增加。
结核分枝杆菌持续细胞的形成也是由与宿主巨噬细胞的相互作用触发的。
▼
鉴于刺激存留细胞形成的不同应激,看到相应的应激反应途径也在存留细胞形成中发挥作用也就不足为奇了,这可能会在细菌暴露于应激和最终导致长期生长停滞的分子效应物之间架起桥梁。
▸ 严格响应
由于饥饿是持久细胞形成的重要触发因素,因此对于严格反应和持久细胞之间的联系已经进行了大量的工作。
严格反应的关键介质是警报素 (p)ppGpp,在营养饥饿时被激活。(p)ppGpp 水平升高,与DksA协同作用,导致转录和翻译重排,使细菌能够适应稀缺资源。
当暴露于低pH值或氧化条件时,DksA会发生影响其调节功能的构象变化,因此,严格的反应不仅与饥饿有关,而且与氧化和pH应激因素有关。
影响 (p)ppGpp 合成或 DksA 的突变会显著降低革兰氏阴性和革兰氏阳性细菌中的存留细胞分数。
▸ SOS反应
SOS反应是一种DNA修复机制,在暴露于各种环境应激因素(氧化应激和抗生素暴露)时被激活,这些都是持久性的一般触发因素。
这些压力会造成损伤,产生单链DNA,而单链DNA 又会被RecA蛋白识别。RecA 随后激活LexA阻遏物的蛋白水解活性,最终导致细胞内的全局转录重排。去除这些主调节因子中的任何一个都会导致持续细胞的大量损失。
▸ ATP水平下降
在大肠杆菌和金黄色葡萄球菌中,持久性与细胞内ATP下降有关。
在这两种生物体中,处于指数期但表现出稳定期标记表达的细胞富含持久细胞。此外,用砷酸盐(一种已知能降低ATP浓度的化合物)处理呈指数增长的细菌,会导致持续细胞的大幅增加。
因此,ATP水平的降低可能是大多数细菌过程(例如翻译)关闭的普遍模式,从而导致抗生素在休眠期间持续存在。
一般来说,暴露于抗生素通常会导致微生物群落结构、物种组成和代谢能力发生重要变化。
▼
阿奇霉素是世界卫生组织消除沙眼和雅司病战略的重要组成部分。
雅司病是由雅司螺旋体引起的慢性接触性传染病,病原为雅司螺旋体,亦称纤细螺旋体。
五项随机对照试验研究了阿奇霉素预防性使用对普通人群肠道微生物群的影响。肠道微生物组的特征主要在于α多样性,它量化了单个微生物群中不同细菌类群的数量及其丰度的均匀性。
•阿奇霉素治疗后微生物群α多样性下降
据报道,12个月后微生物群α多样性下降了16%–22%。24个月的长期随访发现,阿奇霉素治疗后,乌普萨拉弯曲菌(Campylobacter upsaliensis)和人弯曲杆菌(campylobacter hominis)丰度降低,并且主要与微生物存活、生长和炎症相关的细菌代谢途径的丰度降低,这可能部分解释了所报道的对儿童死亡率的降低。
乌普萨拉弯曲菌(Campylobacter upsaliensis)在高收入环境中,特别是在农村儿童中,它是一种公认的食源性肠道病原体;而人弯曲杆菌(campylobacter hominis)与肠道炎症和菌血症有关。
三个国家的四项随机对照试验报告了短期使用的影响。与安慰剂相比,阿奇霉素治疗使微生物群α多样性降低高达32%。据报道,Akkermansia muciniphila和Proteobacteria也有所减少。
注:后一组细菌包括常见的病原体,例如大肠杆菌和弯曲杆菌属。
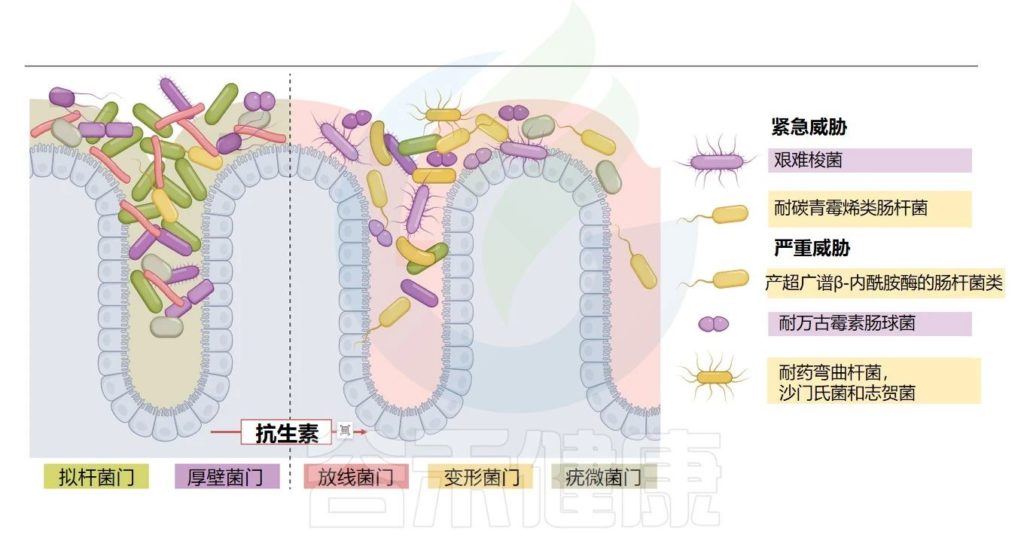
Fishbein SRS,et al.Nat Rev Microbiol.2023
总之,这些研究表明阿奇霉素引起的α多样性明显减少,同时肠杆菌科病原体也减少。
▼
抗生素与代谢或饮食元素之间的协同作用可以进一步塑造微生物组动力学并改变对抗生素的易感性,从而导致疾病的临床相关差异。
•高脂饮食下进行抗生素治疗会引起病理性炎症
对高脂肪饮食的小鼠进行抗生素治疗会引起肠道黏膜的病理性炎症,并增加肠杆菌(Enterobacteriaceae)的水平。这些小鼠表现出炎症性肠病的免疫症状。
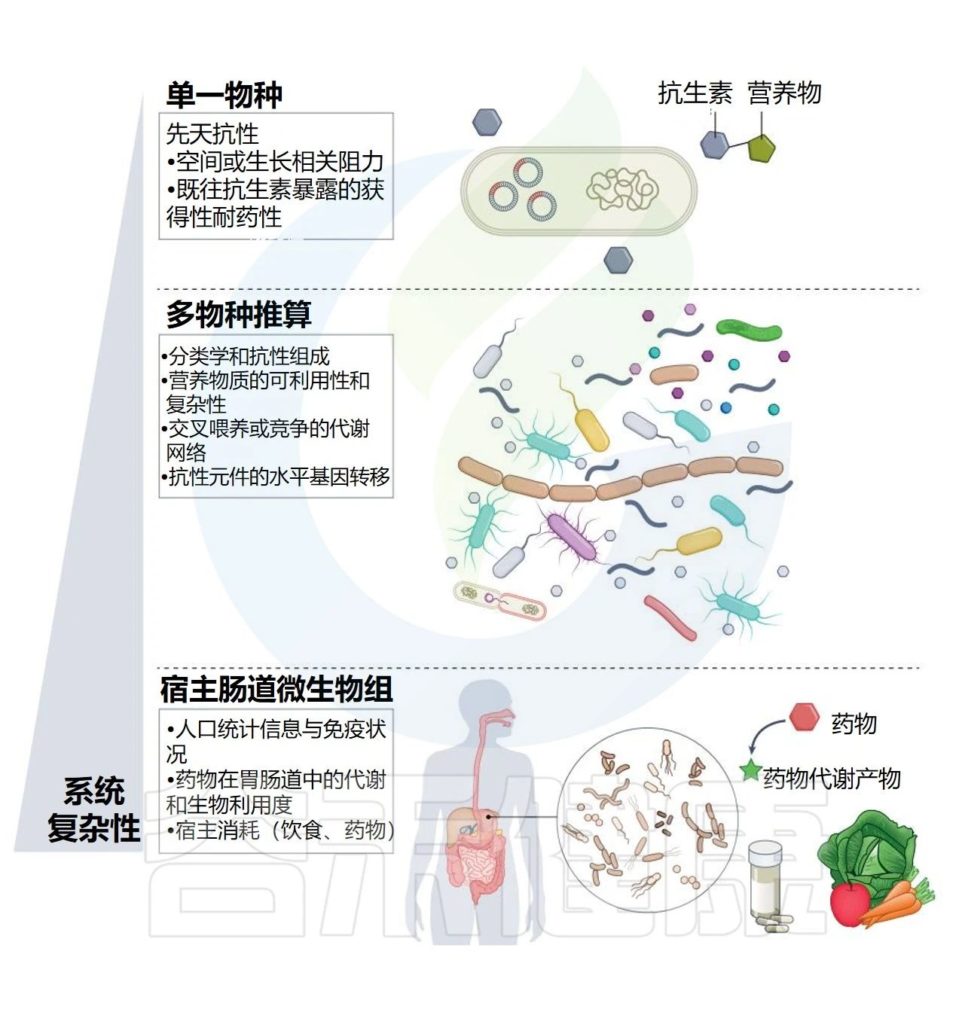
Fishbein SRS,et al.Nat Rev Microbiol.2023
•饮食和抗生素结合改变了微生物和宿主的代谢
从其他几项使用饮食和化学干预来模拟西式饮食影响的小鼠研究来看,很明显,饮食和抗生素的结合改变了微生物和宿主的代谢。
具体来说,在一个模型中,这种协同干预通过改变脂肪酸代谢释放了单糖和乙醇胺,最终增加了肠道沙门氏菌感染的易感性。
另外,饮食中多糖或微生物可及的碳水化合物水平的调节对抗生素治疗结果有很大影响。在没有纤维的情况下,使用传统微生物组或人源化微生物组的小鼠在环丙沙星治疗后α多样性恢复延迟。
•含纤维饮食促进了丁酸水平的恢复
在人类实验中,在联合抗生素治疗期间,以杂食和纯素饮食喂养的志愿者,相对于那些不含纤维的液体饮食的志愿者,表现出了更快的微生物群恢复(通过α和β多样性来衡量)。
具体来说,含纤维饮食促进了粪便丁酸水平的快速恢复和具有独特氨基酸代谢的厚壁菌门的恢复。
▼
抵抗组(resistome)是指存在于肠道微生物群中的抗生素抵抗基因的集合。抗生素对肠道抵抗组具有显著但高度可变的影响。
•抗生素通常会增强肠道抵抗组
通过抗生素暴露对肠道抵抗组的改变可能引起微生物组中耐药病原体的病理性繁殖。值得注意的是,抗生素治疗最常见的结果是肠道微生物组中抵抗组负荷急剧增加(通过相对丰度的变化来衡量)。
这些研究揭示了抗生素诱导的抵抗组变化的一些一般模式。尽管增加了总抗性组负担,但抗生素可同时导致特异性的大量丧失和抗性组多样性的减少,这可能是由于分类损失。
•水平基因转移促进抗性组富集
抗生素诱导的肠道抵抗组扩张也可能由ARG编码的MGEs驱动。
在短期内,抗生素治疗后抵抗组负担的增加主要是由染色体编码ARGs的富集(即耐药细菌谱系的扩大)驱动的。
然而,此后不久(约1个月),染色体ARGs的微生物丰度急剧下降。相反,mge编码的ARGs在治疗停止后持续更长的时间,这可能是由于mge的寄生性质。(尽管缺乏抗生素介导的生长优势或细菌宿主存在适应性缺陷,它们仍在细菌群体中持续存在)
抗生素可以增加肠道中mge编码的ARGs的丰度,并导致ARGs和MGEs在患者中更频繁和更广泛(涉及更多样化的分类群)的传播。
总体而言,在临床使用和环境抗生素暴露较高的人群中,ARGs水平转移率较高。
▼
在全球范围内,使用产时抗生素预防(IAP)是预防围产期感染和相关不良妊娠结局的最常见策略。
产时抗生素预防涉及使用广谱抗生素,这些抗生素可有效对抗最有可能引起高危母亲感染的微生物,主要是B族链球菌。
建议在剖腹产手术切开前进行抗生素预防;分娩期间,母亲B族链球菌培养呈阳性或有侵袭性GBS感染风险;或出生后立即进行,以减少与手动去除胎盘、过度宫内操作或生殖道撕裂相关的感染风险。
•经过产时抗生素预防的婴儿微生物多样性降低
七项观察性研究和一项随机对照研究调查了抗生素预防与肠道微生物群之间的关联。经过产时抗生素预防治疗的母亲所生的婴儿在6-7天时的微生物群α多样性有所降低。
暴露于产时抗生素预防还与微生物群组成的更大相似性(即β多样性减少)相关,这表明母体抗生素暴露的选择性压力对婴儿的早期婴儿微生物群组成具有一致的影响。
•产时抗生素预防组以肠杆菌为主,双歧杆菌较少
一项前瞻性队列研究发现,产时抗生素预防组10日龄时放线菌门(包括双歧杆菌)的相对丰度显著减少,厚壁菌门(包括一些值得注意的致病菌群,如葡萄球菌、李斯特菌和链球菌)显著增加。
双歧杆菌是母乳喂养的婴儿肠道微生物群的重要成员,可以通过与其他重要肠道细菌(如乳杆菌)的共生交叉喂养相互作用来驱动微生物群的持续发育。
总体而言,这些研究表明,婴儿微生物群的α多样性降低与母亲产生接触抗生素相关,包括肠杆菌科相对丰度较高和拟杆菌和双歧杆菌丰度较低。
以下讨论抗生素类别、细菌进化枝、起始微生物群组成和长期微生物群组成。
▼
√不同抗生素会影响对应的菌属丰度
最近对55项人类研究的回顾总结了微生物群组成的变化,这些变化与分为22个抗生素类别的68种不同抗生素显著相关。研究表明,每种抗生素对属于一组有限属的细菌影响最强烈。
此外,受影响的细菌属的数量在抗生素类别之间和内部都存在差异。
阿奇霉素与3个属(拟杆菌、双歧杆菌、梭菌)的丰度变化相关,而其他大环内酯类药物则与2-6个属的丰度变化相关(包括前三个属,以及粪杆菌属、普雷沃菌属、瘤胃球菌、链球菌、肠球菌、嗜血杆菌或假单胞菌)。
β-内酰胺类药物,例如氨苄西林和头孢菌素,分别与8和12个属的丰度变化相关,这些属与其他β-内酰胺类药物不同,涵盖系统发育上不同的门(放线菌门、厚壁菌门、变形菌门、疣微菌门)。
√抗生素的不同分类群具有特异性作用
培养实验证实了不同抗生素的这些分类群特异性作用。例如,甲硝唑强烈抑制拟杆菌属和双歧杆菌属的生长。在厌氧培养中,而氨苄青霉素显著减少拟杆菌属和产气荚膜梭菌的生长,但其对双歧杆菌属的影响取决于细菌的生长速度。
此外,氨基糖苷类和磺胺类药物对测试的细菌几乎没有影响。大环内酯类药物对所有测试的细菌种类均具有抑菌作用(但不会杀死),但对艰难梭菌没有影响。
注意:β-内酰胺的作用具有菌株特异性,并且因所使用的特定抗生素而异。
因此,抗生素对微生物群的影响取决于所使用的抗生素,以及细菌分支的反应以及反应方式。
然而,抑制对抗生素敏感的微生物可能会破坏定植抵抗力,并为机会致病菌打开生态位,增加宿主对抗生素后感染的易感性。另外,抗生素的使用也可以增加耐抗生素的共生细菌,这对宿主有潜在的好处。
影响这些效应的因素包括不同抗生素的药代动力学、不同细菌对每种抗生素的降解和耐药机制,这些降解和耐药机制对不主动执行这些功能的其他细菌的间接影响,以及特定耐药决定因素的局部或区域流行率。
▼
考虑到抗生素作用因抗生素类别和细菌进化枝而异,微生物群的初始组成也可能决定抗生素的短期和长期作用。
√微生物群的初始组成会影响抗生素的作用
对五个队列的数据分析确定,具有增强的降解复杂碳水化合物(特别是宿主粘蛋白)的功能能力的特定物种的丰度,准确地预测了微生物群从抗生素相关的α多样性减少中恢复。
这些细菌的基线丰度可以识别使用抗生素后α多样性减少的参与者,准确度为70%。
√粘蛋白降解能力促进细菌在肠道繁殖
研究人员提出粘蛋白降解能力可能为这些细菌在肠道中重新繁殖提供了优势。此外,这些复杂碳水化合物的降解可能会产生次生代谢物,这些代谢物反过来又可以被其他细菌用作营养源以支持其再生。
注:与恢复相关的细菌包括拟杆菌属的几种。
无菌小鼠的证据支持了这一在人类身上的发现。两组均被富含普雷沃氏菌和粪杆菌或富含拟杆菌和副拟杆菌的人类粪便微生物群定植,并且两组均接受为期7天的阿莫西林克拉维酸治疗。
18天后,拟杆菌组的α-多样性对抗生素暴露更具弹性。然而,拟杆菌属的粘蛋白消化降解可以促进肠道感染,这已在艰难梭菌、啮齿类梭菌和鼠伤寒沙门氏菌中得到证实。
▼
两项分析均使用了10个月期间纵向收集的成人数据,其中包括两个为期5天的环丙沙星疗程。
√不同菌群达到新的平衡所需时间不等
一项分析确定,对于不同的细菌亚群,微生物群达到新的稳定配置所需的时间从2到42天不等。
拟杆菌属中的一个细菌亚群在两周内以相同或更高的相对丰度建立了新的平衡。然而,其他细菌如毛螺菌科(Lachnospiraceae)和一部分细菌在治疗期间有所增加,并需要42天才能恢复到使用抗生素前的水平。
相比之下,瘤胃球菌科的一组细菌在一次治疗后减少到检测不到的水平,十个月后仍未恢复。该综述发现细菌进化枝的特异性决定了抗生素对微生物群的影响。
√更短的恢复时间可能由于暴露于环境来源的细菌
对相同数据的第二次分析表明,更短的恢复时间可能是由于更多地暴露于环境来源的细菌,这些细菌可以重新定殖受干扰的微生物组。
尽管这些研究涉及的个体很少,并且最多只能代表个体间的异质性,但他们探索了微生物群丰度数据的采样时间序列,并且他们的发现得到了实验工作的支持。
√更复杂的微生物群可以减轻抗生素暴露的影响
在一项这样的实验中,两组小鼠被分配到无特定病原体的条件或暴露于土壤的一般动物条件下,并且均接受为期两周的万古霉素和链霉素治疗。
暴露于土壤的小鼠在治疗后表现出更大的α多样性和稳定性,并且在停用抗生素后更快地恢复治疗前的α多样性。这些研究表明,更受控制的外源细菌,例如复杂的益生菌混合物,可以减轻抗生素暴露对微生物组的影响。
√抗生素暴露使婴儿α多样性降低
抗生素暴露的长期影响也在婴儿中进行了研究。α-多样性降低与出生后立即治疗有关,但在产后第一年恢复。α-多样性的减少是由于毛螺菌科和肠杆菌科被抑制所致。
尽管微生物群α多样性在一岁时基本上恢复,但由于新生儿接触抗生素而导致这些早期定植菌减少对宿主健康的影响需要仔细调查。
在另一项研究中,与在那段时间没有接触过抗生素的婴儿相比,从出生到三岁接受抗生素治疗的婴儿的物种α多样性较低,但α多样性的减少幅度不大,仅在第一年明显。然而,在细菌菌株水平上,暴露于抗生素的婴儿和未暴露于抗生素的婴儿之间的差异更大。
此外,还发现部分细菌菌株只在肠道定殖一次。这些菌株通过接触抗生素而被消除,但在未经治疗的婴儿中仍然存在。相比之下,其他菌株在随访期间多次在肠道重新定殖。这些菌株更有可能在暴露和未暴露的婴儿中持续存在,这为以下观点提供了进一步的支持:再定殖是使用抗生素后微生物群恢复的驱动力。
★ 评估菌群经过抗生素治疗恢复原有结构的能力
根据菌群的基本构成,尤其是底层代谢黏蛋白以及短链脂肪酸的菌构成情况,可以评估菌群在经过抗生素治疗后恢复原有菌群结构的能力。
该恢复能力越强菌群结构较难通过抗生素改变,越弱则易受抗生素影响,导致后续菌群构成发生较大变化。该指标可以为菌群的抗生素干预选择和菌群重建提供参考。
抗生素耐药是指病原体(细菌、病毒、真菌等)不能被抗生素及其他抗感染药物有效杀死的抵御能力。由于存在抗生素滥用的情况,导致环境中许多细菌尤其是病原菌产生对特定抗生素类型的耐药性。通过对大量抗生素耐药菌基因组和耐药基因的分析,结合肠道菌群测序数据,报告中评估了肠道菌群对主要抗生素类型可能存在的耐药风险。
注意:仅作为风险提示和参考,并不直接对应抗生素耐药,具体用药和耐药检测请谨遵医嘱和进行耐药检测。

<来自:谷禾健康肠道菌群检测数据库>
总而言之,这些分析表明,微生物群从抗生素暴露中恢复可能取决于所使用的抗生素、初始微生物群组成以及受药物影响的特定细菌分类群。
此外,纵向观察研究提供了额外的证据,表明肠道的重新定植可能在抗生素暴露后微生物组的恢复中发挥关键作用。然而,还需要更多的研究来检验这几项研究提出的具体假设。
值得注意的是,仅恢复可能无法保护宿主免受抗生素扰动对微生物组的潜在长期影响。
流行病学研究已确定抗生素使用与肥胖、哮喘,过敏特应性和结直肠癌以及其他健康疾病之间存在关联。抗生素对肠道微生物组的破坏已被认为是这些关联背后的重要机制。
▼
50%或更多中低收入国家的婴儿在3个月大时携带至少一种肠道病原体,并在24个月大时经历至少一次腹泻发作。
中度至重度腹泻的最常见原因是病毒(轮状病毒、沙波病毒、诺如病毒)或细菌(大肠杆菌致病型、志贺氏菌、弯曲杆菌属)感染。
特定病原体的流行情况因国家而异。死亡率和严重腹泻发作也因国家和病原体而异。
▷抗生素降低了腹泻和痢疾导致的死亡率
抗生素的广泛目标是减轻病原菌对宿主健康的负担和影响。使用阿奇霉素进行的随机对照试验结果表明,对弯曲杆菌属具有抑制作用。促炎微生物组代谢途径可能部分解释了在这些环境中观察到的腹泻和痢疾导致的儿童死亡率持续下降。
在另一项研究中,长双歧杆菌(Bifidobacterium longum)抑制了儿科病例中分离的轮状病毒,并缩短了病毒性胃肠炎的持续时间。
▷抗生素也会扰乱肠道微生物群促进肠道感染
抗生素扰乱肠道微生物组后可促进肠道感染,这一点已在艰难梭菌、啮齿类梭菌和鼠伤寒沙门氏菌中得到证实。
或者,用抗生素扰乱肠道微生物群已被证明可以延迟轮状病毒感染并预防小鼠的诺如病毒感染。
相比之下,在艾滋病毒感染儿童中长期使用复方新诺明,4年后仍可抑制炎性草绿色链球菌以及相关的全身性炎症,从而增加该人群的防御风险。
▼
抗生素的使用与肥胖风险增加有关。接触时间越早(6个月之前)和接触频率越高,这种关联就越大。较低的肠道微生物群α多样性也与肥胖有关。
▷抗生素促进营养不良儿童的体重增加
相比之下,抗生素可以促进营养不良儿童的体重增加,尽管其影响是异质的,并且可能是由抗生素类别以及不同人群中生长限制性合并症(例如艾滋病毒和严重急性营养不良)的不同患病率驱动的。
微生物组组成对体重增加的因果影响也已在无菌小鼠中得到证实。
如果不清楚微生物群组成变化与健康结果之间的因果机制,微生物群组成通常被定义为“生态失调”,这是基于与疾病相对于健康对照的关联。
在高收入成年人群中,α多样性下降是“生态失调”的一个共同特征,“生态失调”是根据与疾病的关联来定义的。在这种情况下,α多样性减少表明肥胖和相关代谢紊乱(例如I型和II型糖尿病)的风险增加。
▷抗生素导致α多样性下降增加肥胖风险
相比之下,在纯母乳喂养的婴儿中,肠道微生物组以双歧杆菌为主。由于母乳中存在高浓度的寡糖,导致与混合或配方奶喂养的婴儿相比,α多样性较低。
更大的α多样性与较早引入补充食品和青春期超重风险增加有关。因此,婴儿早期微生物群α多样性的增加可能表明由于婴儿早期营养不足而导致“生态失调”,抗生素相关的α多样性减少对健康的影响也可能是因情况而异的。
▷新生儿抗生素暴露于儿童生长有关
抗生素暴露的时间可能有助于进一步了解具体情况的影响。在芬兰的一个由12422名足月新生儿组成的队列中,新生儿抗生素暴露(主要是静脉注射苄青霉素和庆大霉素)与男孩生命前6年生长受损有关。
一项由1707名德国新生儿组成的独立队列证实了与男孩生长的相关性。相反,新生儿期后接受抗生素疗程的次数与男女6岁时体重指数的增加有关 。
最近的一项针对小鼠的研究表明,出生时注射的低剂量青霉素会导致肥胖增加,并加剧高脂肪饮食对体重增加的影响。生长表型是在无菌接种抗生素处理小鼠的粪便微生物群时诱导的,表明改变的微生物群起着因果作用。
然而,还需要更多的研究来表征和确认促进从抗生素暴露中恢复的微生物组的成分,以及健康新陈代谢可能需要的成分,并将这些转化为人类健康。
▼
较早和更频繁的抗生素处方也与儿童哮喘风险增加有关。较低的肠道微生物群α多样性与婴儿期和儿童期的湿疹和过敏有关。
▷婴儿抗生素使用与儿童哮喘风险存在联系
最近证明婴儿抗生素使用引起的微生物群改变与5岁时哮喘风险之间存在直接联系。在出生第一年接触抗生素的婴儿到5岁时患哮喘的可能性是正常婴儿的两倍。估计这种关联的25%可归因于抗生素引起的α多样性减少或抗生素相关的特定细菌丰度变化。
▷母亲使用抗生素会影响婴儿微生物的早期定植
尽管整个婴儿期的肠道微生物组存在巨大的变异性,但婴儿期微生物组的有意义的一部分是在出生后立即从母体肠道获得的,并保留长达3年。因此,母亲接触抗生素也可能会改变分娩过程中微生物物种向婴儿的传播,并影响早期定植。
影响新生儿微生物组组成的抗生素暴露可能会对儿童发育产生长期影响。几项使用动物模型的研究表明,新生儿期对于免疫系统的成熟至关重要,这一过程依赖于新生儿肠道微生物组的定植,并且会受到抗生素消融的干扰。
小结
抗生素在治疗细菌感染和减少疾病传播方面起着积极的作用。然而,滥用和不适当使用抗生素可能导致细菌耐药性的增加,并对肠道微生物群产生负面影响。
因此,我们应该合理使用抗生素,遵循医生的建议,并在使用抗生素期间维护肠道健康。谨慎使用抗生素有助于最大限度地减少负面影响,确保抗生素继续为我们的健康服务。
人们提出了一些有前景的方法来减轻抗生素使用对微生物组的影响。
▼
共同施用益生元以促进共生细菌的生长就是这样的策略之一。在婴儿中,母乳富含复杂的低聚糖,可作为双歧杆菌生长的底物,并促进其他物种的交叉喂养。
在一个观察队列中,母乳喂养与产时抗生素预防暴露婴儿微生物组α多样性的更快恢复有关。母乳喂养的好处也可能超出其益生元含量。
•儿童益生元和抗生素联合给药使有益菌丰度升高
在儿童中,乳果糖与阿奇霉素的联合给药有助于恢复乳果糖的相对丰度。治疗后18天内,乳杆菌属(Lactobacillus)、肠球菌(Enterococcus)、Anaerostipes、经黏液真杆菌属(Blautia)和罗氏菌属(Roseburia)出现增加,而单独使用阿奇霉素可导致治疗后60天内促炎性链球菌的丰度增加。
•成人联合使用益生菌和抗生素可减轻耐药性
在成人中联合使用益生菌和抗生素也显示出一定的潜力,可以减轻耐药性遗传决定因素的抗生素选择。
然而,口服益生菌在肠道的成功定植表现出因人、肠道区域和益生菌菌株而异的相当大的变异性,这可以通过宿主和本土微生物组特征来解释。
此外,益生菌菌株中缺乏对所施用抗生素的耐药性可能会加剧微生物组中抗生素耐药性的选择,进一步限制了益生菌的潜在保护作用。
注:使用抗生素给药前收集的自备健康粪便样本进行粪便微生物群移植可能是恢复微生物组的更有效方法,尽管这对于中低收入国家来说可能不太实用。
▼
另一种策略涉及使用抗生素药物组合来实现比单一抗生素治疗更有针对性的物种特异性效果。
例如,一项调查筛选了超过1000种药物,以确定可降低抗生素广谱活性而不损害其对抗相关病原体活性的候选药物。
•红霉素对肠道共生细菌具有强抑制作用
抗凝药物双香豆素和两种非甾体类抗炎药物托芬那酸和二氟尼柳成为红霉素对肠道共生细菌(例如普通拟杆菌和均匀拟杆菌)作用的强抑制剂。
然而,红霉素对致病菌(例如金黄色葡萄球菌、肺炎链球菌和屎肠球菌)没有显著影响。
•药物组合具有物种特异性效应
另一项研究分析了近3000种抗生素、药物和食品添加剂的组合,以确定可以减轻对微生物群的附带影响而不减少对病原体影响的候选化合物。超过70%的药物组合具有狭窄的物种特异性效应,20%显示出菌株特异性效应。
▼
另一种方法是确定窄谱抗生素替代品,尽可能选择狭谱抗生素,这些抗生素只对特定类型的细菌有效,而不是广谱抗生素,后者会杀死更多的细菌,包括有益菌。
微生物组本身可能是此类窄谱化合物的来源。例如,对人类微生物组计划中的752个细菌基因组的研究发现了共生细菌携带的一组编码硫肽的基因。
•对病原菌有很强的抑制作用,对共生菌没有抑制
乳青霉素是一种由加氏乳杆菌编码的硫肽,对金黄色葡萄球菌和阴道加德纳菌等常见病原体具有很强的抑制活性,但对共生菌没有抑制作用。
苏云金素是另一种已被鉴定的抗菌素,由苏云金芽孢杆菌(Bacillus thuringiensis)产生。它已被证明可以有效对抗艰难梭菌,而不影响人类结肠的粪便培养系统中的微生物群组成。
开发此类干预措施需要更深入地了解与抗生素结合产生健康益处或不良副作用的机制,以便窄谱替代品能够实现预期结果,同时最大限度地减少不必要的风险。
最后,环境中可能还存在重要的微生物成分,有助于防止生态失调或在关键发育时期恢复肠道微生物组的生理重要子集。识别这些成分可以指导缓解干预措施的开发和测试。
有令人信服的证据表明,即使不存在抗生素耐药性,感染也很难治疗。几项依赖于对患者分离株进行深度基因组测序的纵向研究表明,这些持续性感染的复发与宿主体内细菌库的维持有关,这些细菌在免疫防御和抗生素的联合作用下幸存下来。
用于追踪动物和细胞感染模型中细菌的细菌生长停滞报告者已经证明,尽管接受抗生素治疗,但在持续感染部位仍存在不增殖或缓慢增殖的细菌。过去几年,追踪和分析稀有非生长细菌的尖端技术的发展极大地促进了抗生素持久性的研究。在这方面,这个领域正在不断发展。
总结如下:
1.与普通菌株相比,生长缓慢的细菌表现出相对的药物冷漠,这增加了种群在抗生素暴露下存活的时间。
2.药物暴露后的这种异质群体行为是由于细菌亚群(持续存在)通过生长停滞、暴露于对其余群体致命的浓度的抗生素而得以生存的能力。
3.许多病原菌在宿主组织内建立持续感染,避免被免疫系统和抗生素清除。细菌感染通常会导致宿主产生先天免疫反应,然后产生适应性免疫反应,这通常足以清除感染。然而,许多病原体已经进化出复杂的生存机制来逃避免疫反应并建立持续感染。
4.有多种原因会导致感染反复发作,例如宿主易感性增加、其他慢性合并感染以及环境和生活方式因素。长期以来,无法确定感染复发是再次感染还是复发。
5.持久性的形成是一种普遍的细菌应激反应。多种环境因素充当压力信号,促进持久者的产生。许多触发因素似乎都会刺激持久细胞的形成,从饥饿或氧化应激等营养应激到细胞外代谢信号。
6.婴儿微生物群的α多样性降低与母亲接触抗生素相关,包括肠杆菌科相对丰度较高和拟杆菌和双歧杆菌丰度较低。
7.不同的抗生素对不同细菌菌属影响不同,肠道内菌群结构的恢复与抗生素的使用和患者基线菌群有关。
8.超重,肥胖,哮喘,过敏等人群与早期和长时间抗生素的使用引起的菌群失调以及部分关键菌属的消失或下降有关。
9.未来可以发展更综合的预防措施,例如,乳青霉素是一种由加氏乳杆菌编码的硫肽,对金黄色葡萄球菌和阴道加德纳菌等常见病原体具有很强的抑制活性,但对共生菌没有抑制作用。
相关阅读:
主要参考文献
Gollan B, Grabe G, Michaux C, Helaine S. Bacterial Persisters and Infection: Past, Present, and Progressing. Annu Rev Microbiol. 2019 Sep 8;73:359-385.
Gough EK. The impact of mass drug administration of antibiotics on the gut microbiota of target populations. Infect Dis Poverty. 2022 Jun 30;11(1):76.
Shah T, Baloch Z, Shah Z, Cui X, Xia X. The Intestinal Microbiota: Impacts of Antibiotics Therapy, Colonization Resistance, and Diseases. Int J Mol Sci. 2021 Jun 20;22(12):6597.
Vuong HE, Pronovost GN, Williams DW, Coley EJL, Siegler EL, Qiu A, Kazantsev M, Wilson CJ, Rendon T, Hsiao EY. The maternal microbiome modulates fetal neurodevelopment in mice. Nature. 2020 Oct;586(7828):281-286.
Fishbein SRS, Mahmud B, Dantas G. Antibiotic perturbations to the gut microbiome. Nat Rev Microbiol. 2023 Jul 25.
Koh E, Hwang IY, Lee HL, De Sotto R, Lee JWJ, Lee YS, March JC, Chang MW. Engineering probiotics to inhibit Clostridioides difficile infection by dynamic regulation of intestinal metabolism. Nat Commun. 2022 Jul 4;13(1):3834.
Gomaa EZ. Human gut microbiota/microbiome in health and diseases: a review. Antonie Van Leeuwenhoek. 2020 Dec;113(12):2019-2040.

谷禾健康

感染是人类面临的健康威胁之一。各种病原体,如细菌、病毒、真菌、寄生虫等,存在于我们日常接触的环境、物品、食物等中。一些常见的感染病例包括感冒、流感、腹泻、组织器官或血液感染等,在全球范围内广泛传播。这些疾病的传播方式多样,可能通过空气、水源、接触和食物等途径传播。
感染的症状包括发热、头痛、咳嗽、呕吐、腹泻等,严重感染可能导致器官衰竭、败血症等并发症。感染的原因包括接触感染源、免疫力下降、不良生活习惯等,易感人群有免疫力低下者、老年人、慢性疾病患者等。
研究发现,肠道菌群与感染也有密切关系。肠道菌群有助于消化、吸收营养物质,同时还调节人体免疫系统的功能。但如果肠道菌群失衡,会导致多种疾病,包括感染。
本文我们来了解一下关于感染的种类,症状,致病途径,易感因素,免疫系统应对病原体的三大防线,肠道菌群失衡与免疫系统的关联,以及肠道菌群检测在临床感染案例中的应用。
▼
感染可以按多种不同方式分类。
按影响部位分为局部和全身的:
按影响持续时间分为急性和慢性的:
按病原体类型划分:
病毒、细菌、真菌、寄生虫等都是导致感染的不同类型的病原体。
► 细菌感染
细菌感染是由体内过量的有害细菌引起的。正常情况下,人体的免疫系统能够通过白细胞和吞噬细胞等机制对抗细菌感染。但如果人体的免疫系统出现异常或受到外界因素干扰,细菌就可能趁虚而入,导致细菌感染的发生。
常见的细菌感染包括:肺炎、腹泻、皮肤感染、脑膜炎、膀胱炎、中耳炎等。
► 真菌感染
真菌感染多为继发性感染,由机会致病性真菌引起,特别是深部真菌感染多是由于各种诱因使机体免疫功能显著下降所致。
真菌是一类与细菌和病毒不同的微生物,它们包括霉菌、酵母菌等,常见的真菌感染有白色念珠菌感染、曲霉菌感染等。
► 病毒感染
病毒感染与细菌感染不同,因为病毒本身并不能独立存在,只有当它侵入人体细胞后才能产生病毒性病变。当病毒进入细胞时,它会留下迫使细胞复制的遗传物质。
当细胞死亡时,它会释放新的病毒感染其他细胞。并非所有的病毒都会破坏细胞——有些病毒会改变细胞的功能。
病毒会导致多种疾病,包括普通感冒、流感、登革热、水痘、艾滋病等。
► 寄生虫感染
寄生虫是需要以其他生物为食才能生存的生物。有些寄生虫不会对人产生明显影响,而有些寄生虫会生长、复制并侵入器官系统。
常见的寄生虫感染有阿米巴病、血吸虫病、肠道蠕虫感染等。
▼
无论何时发生感染,身体的一线反应都是炎症性的。
炎症是身体抵御疾病的方式,同时促进受影响组织的愈合。炎症的主要症状:红、肿、热、痛、组织功能的暂时丧失。
在感染期间,由于潜在的炎症反应,人们通常会出现非特异性的全身症状。症状和严重程度可能因受影响的器官系统而异,但可能包括:
▼
► 病史采集
询问患者或病人家属发病情况、既往病史、服药史、过敏史、流行病学史等。
► 体格检查
体温、呼吸、心率、血压、身体部位肿胀、红肿、局域性压痛、淋巴结肿大等都是感染体征,可以作为诊断和判断感染病情严重程度的参考指标。
► 实验室检查(抽血、尿检等)
通过血液、尿液、呼吸道分泌物、伤口分泌物等样本的化验检查可以更直接地确定病原体的种类和数量,以及感染程度的严重程度。
► 影像学检查(做CT等)
如X射线、CT、MRI等技术,可以帮助医生了解感染的程度以及可能受影响的部位,从而确定感染的类型和严重程度。影像学检查为临床医生在明确诊断之前的经验性治疗提供线索。
► 快速诊断测试(做核酸等)
如血清学检测、ELISA试剂盒、PCR技术等,可以在短时间内快速准确地检测出患者血清中的病原体抗体、抗原以及核酸等,提供对感染病原体的敏感性和特异性的快速诊断。
▼
呼 吸 道
普通感冒的另一个名称是上呼吸道感染。鼻病毒是引起感冒的最常见病毒。其他通过空气传播的传染病也以这种方式感染。
感冒和流感通常不会直接影响肺部,但它们可能会导致继发性细菌感染——肺炎。
消 化 道
如果不小心吃了被细菌或病毒感染的食物、饮料或水、或是农产品在种植或运输过程中接触了污染物,或者过期变质的食物等,病原体也一并被吞入,感染胃部或肠道,有时表现为腹泻和/或呕吐。一个常见的例子是细菌性肠胃炎,也称为食物中毒。
泌尿生殖系统
病原体也可以通过泌尿系统进入人体,如尿路感染,或生殖系统,如性传播疾病。传染源可能停留在局部,也可能进入血液。例如,性传播疾病最常感染生殖器,而艾滋病毒通过体液携带,也可以通过唾液、精液或血液传播。
皮 肤 接 触
皮肤的功能之一是充当抵御感染的屏障。但如果有割伤、抓伤、虫咬或任何类型的开放性伤口,皮肤阻挡不住,病原体可能会进入血液。如:蜂窝组织炎、脓疱疮等都是通过皮肤接触开始的常见感染。
▼
无论来源如何,任何人都可能感染。但有些人更容易感染,或感染并发症的风险增加,例如:
以上我们可以看到,那些免疫系统功能低下的人更容易发生感染。那么当病原体入侵时,免疫系统正常运作会发生什么呢?
下一章节我们来了解一下,默默帮助我们抵抗病原体的——免疫系统。
前面章节我们知道感染是微生物进入人体并造成伤害的结果。引起感染的生物体很多,包括病毒、细菌、真菌、寄生虫等。
当它们试图攻击的时候,免疫系统是如何运作的?
第一道防线——物理屏障
正常情况下,皮肤、呼吸道等组成的物理屏障在保护你,一般只有水分、气体等小分子物质进出,细菌、病毒难以入侵。
然而,也许你只是摔了一跤擦破了皮,也许只是水果刀不小心划伤了…皮肤作为免疫系统的第一道防线破了。
这时候细菌就开始争先恐后进入体内,不断繁殖,增强武力值。
第二道防线——先天性免疫防线
(广泛执行任务)
巨噬细胞——以吞制敌
巨噬细胞开始介入这场搏斗,它往往通过吞噬的方式以一敌百,不管三七二十一先吞下将其困在膜泡里,利用酶等物质分解杀敌,如果细菌还来不及生长繁殖就被吞完了,这场搏斗也就随之终止了。该过程可能引发局部的炎症,表现为红,肿,痛,热等。

但如果一直持续下去,巨噬细胞也可能累了,它开始发出紧急信号,召集后援团…
中性粒细胞——不分敌我直接干
中性粒细胞出现了,它离开了原本在血液中巡逻的路线,第一时间冲过来加入,武力值开始飙升,健康细胞也会被它误杀,它也会给细菌设置障碍,从而困住细菌将其干掉。
它们也会“适可而止、功成身退”,几天后自杀,不带来更多伤害。
如果这还不足以击退,发出的求救信号越来越多,当中枢神经检测到,下丘脑便会开始调节体温上升,也就是发烧。较高的体温可以抑制病原体的活性与繁殖。
以上就是人体免疫系统的第二道防线,也就是先天性免疫(非特异性免疫)。
如果第二道防线没有阻止入侵者呢?
最终对抗会发生在第三道防线,也就是后天性免疫。
第三道防线——后天性免疫防线
(形成记忆,长期保护)
后天性免疫系统是一个成长、学习和经验的累积,学习和记忆着病原体的模式,进而识别并产生特异性的免疫应答。具有极强的打击和防守能力,可以持续有效地保护我们的身体。

这时候,树突状细胞登场了。
树突状细胞——先天性免疫和后天性免疫之间的桥梁
树突状细胞开始手撕敌军,把病原体碎片暴露在自己的细胞膜上,带着病原体的信息去淋巴结,这里有很多T细胞待激活,当T细胞出生时会经过一个训练,之后会配备一个装备。
树突状细胞要寻找的正是可以和病原体表面特征蛋白结合的那个T细胞。
T细胞——等待激活,加入战斗
找到后该T细胞会被瞬间激活,然后开始分裂复制,并分化出三种T细胞,分别为:
B细胞——产生抗体,继续奋斗
当辅助T细胞过去找到B细胞识别结合之后,B细胞瞬间激活,大量复制,产生抗体。
抗体的出现意味着胜利的曙光,抗体表面有多个结合点,可以把多个病原体结合在一起,病原体捆在一起行动不便,失去活力。其他免疫细胞过来可以轻松把它们干掉。
抗体还可以拉着病原体连接杀伤细胞,将其消灭。
记忆T细胞和B细胞——学会对付,默默守护
在清除病原体后,分化出来的大量免疫细胞完成任务,会程序性自杀,防止继续占用资源。会有一小部分留下来,也就是记忆T细胞和记忆B细胞,等待病原体下次来的时候直接杀敌。
以上就是免疫系统的三大防线,它们的存在为人体提供了多重保护。正是因为它们的不懈努力,在感染发生后我们也会挺过来。
研究发现肠道菌群与人体免疫功能以及许多疾病的发生密切相关。
肠道菌群失衡如何与感染相关?肠道菌群与免疫系统之间存在怎样的关联?
下一章节我们继续来看。
肠道菌群中某些微生物和宿主的免疫系统之间存在相互作用,肠道菌群能够影响和调节上述第三大防线中B细胞和T细胞的活性,通过调节免疫细胞的行为,促进抗原递呈细胞的活化和作用,影响细胞因子及其受体的表达等。
肠道微生物代谢产物能够影响免疫平衡。例如,肠道菌群可以通过代谢产生短链脂肪酸、色氨酸胆汁酸等代谢产物,这些代谢产物能够通过激活特定的神经元和免疫细胞来调节免疫反应,从而维持肠道黏膜的免疫稳态。
短链脂肪酸可能具有抗炎和免疫调节作用,当然短链脂肪酸只是一部分,因为除了产生的酶和其他代谢物之外,细菌本身的成分,包括脂多糖、细胞囊碳水化合物和其他内毒素,也可能被释放并对宿主产生二次影响。
肠道微生物群衍生的代谢物丙酸盐(一种短链脂肪酸)水平降低可能导致 Th17/Treg 细胞分化的病理失衡。
一些菌群代谢物,如 4-甲基苯甲酸、3,4-二甲基苯甲酸、己酸和庚酸等,已被证明会加剧结肠上皮细胞的损伤,从而影响免疫。
在肠道菌群失调的情况下,某些有益菌可能会缺乏消化酶等必要的代谢产物和物质,使机体免疫系统无法及时有效地对病原体进行攻击。
许多致病菌与肠道屏障的特定元素相互作用。一些有益的菌群可以激活上皮细胞,加强它们的黏附能力和抗病原性,从而提高肠黏膜的免疫防御能力。
致病菌和抗生素的使用可能会通过增强黏液降解,或抑制正常的共生黏液生成触发器来扰乱肠道黏液层,从而破坏肠道屏障,也就是我们常说的“肠漏”。
肠道屏障的破坏也会诱发体内炎症:与微生物相关的代谢物离开肠道并进入血液。作为回应,身体会产生细胞因子和其他介质,有效地启动炎症反应。
肠道上皮组织内的细胞将细菌代谢物传递给免疫细胞,从而在局部和全身范围内促进炎症。这种情况的持续存在可能导致亚急性或慢性炎症,随后可能会导致炎症性肠病、糖尿病或心血管疾病等疾病的发展。
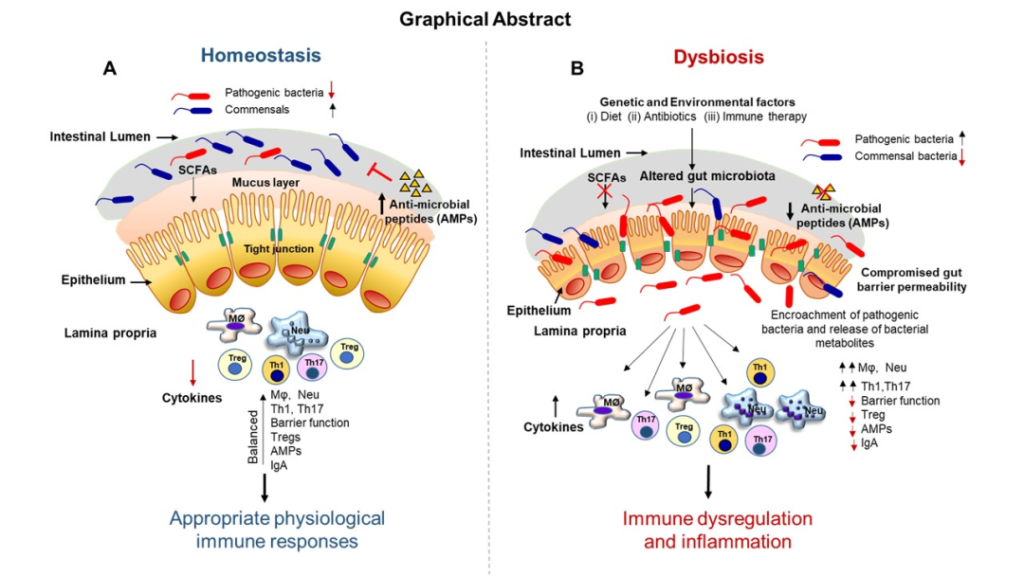
doi.org/10.3390/biomedicines11020294
C 反应蛋白 (CRP) 是一种下游炎症标志物,可以通过特定肠道微生物的抗炎代谢产物的作用下调。当巨噬细胞和 T 细胞分泌白细胞介素 IL-6 时,该分子随后以高水平释放到循环中。我们在肠道菌群检测报告中也可以用CRP来辅助判断炎症状况。
炎症标志物是复杂的双向调节机制的组成部分,并且参与多个重叠过程,与感染和体内稳态的维持有关。
由此,肠道菌群变化对于免疫功能强弱具有重要指示作用,那么我们可以结合肠道菌群检测中的实际案例,来了解更多关于肠道菌群和感染的关联。
在谷禾肠道菌群健康检测中,有许多关于感染的病例,我们选取一例来详细看一下。
年初,一名7岁女孩入院,经诊断后发现患有:
菌血症是一种严重的感染症状,通常由细菌或真菌等微生物感染引起。菌血症分为原发性和继发性。
只有大约20%病例是原发性菌血症,也就是说病原体最初进入血液系统并引起血流感染,例如创伤、手术、注射等导致血管受损直接感染。
其余大多数都是继发性菌血症,也就是在其他部位先感染,未能及时处理,致使病原菌进入血液系统引起继发性菌血症。
常见的菌血症类型包括葡萄球菌菌血症,肺炎链球菌菌血症,鲍曼不动杆菌菌血症,克雷伯菌菌血症,真菌菌血症等,都是相应的致病菌感染引起的。
入ICU后,出现腹胀问题,且愈发严重 ⇊
肠道菌群检测结果显示:
1. 患儿肠道菌群严重失调
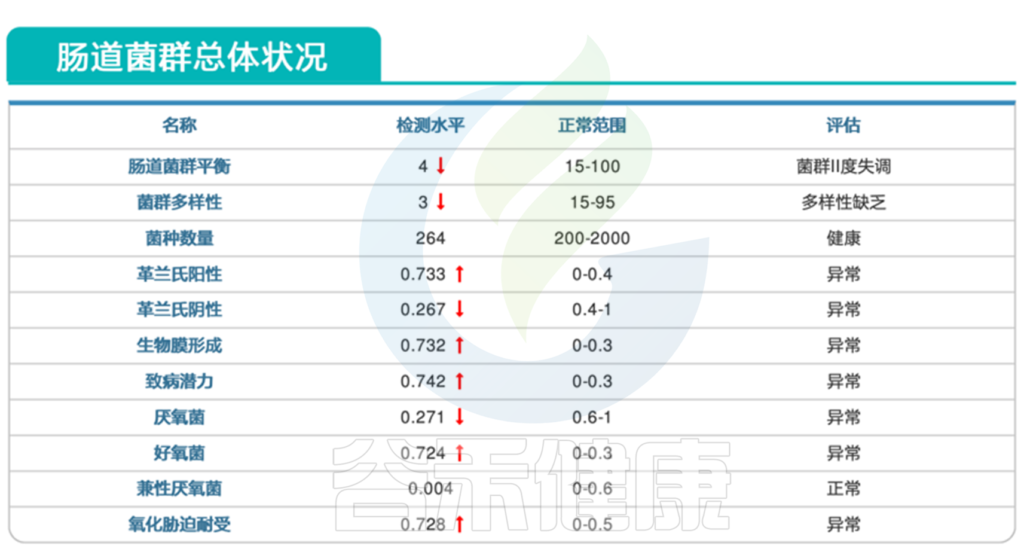
<来源:谷禾健康肠道菌群检测数据库>
显然,该患者的肠道菌群失调,多项指标均显示异常。
从报告的肠道菌群总体状况这部分,我们可以看到,菌群多样性下降,其中革兰氏阳性菌明显偏高,革兰氏阳性菌包括葡萄球菌,链球菌,梭菌等,可能与多种感染相关。同时报告中致病潜力这项指标也是大幅上升。
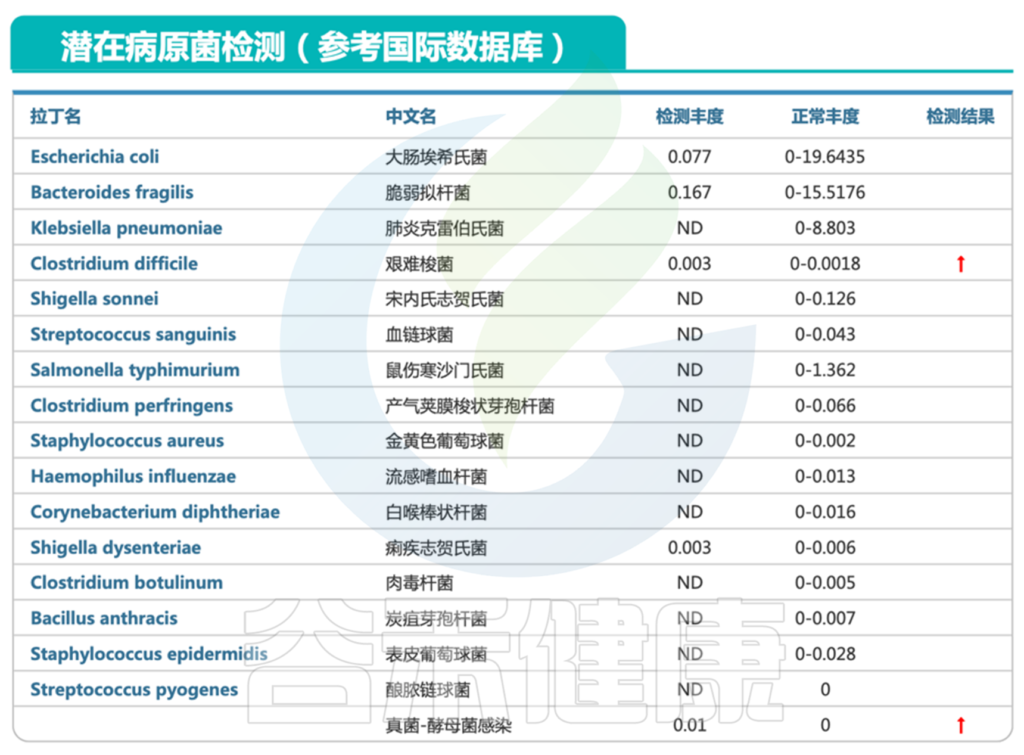
2. 存在艰难梭菌携带超标、酵母菌感染、不动杆菌超标严重(感染)情况
<来源:谷禾健康肠道菌群检测数据库>
艰难梭菌超标 ↑
艰难梭菌是一种常见的肠道病原菌。它可以引起广泛感染,症状最常见的是腹泻,伴随着腹部疼痛,刺痛,腹胀等不适,有些人还可能会出现发热,发冷,胃部压痛或疼痛,恶心呕吐的症状。
更严重的可能出现水样腹泻,心跳加快、体温升高、腹部绞痛、体重下降、腹部肿胀、肾功能衰竭等。
这与患儿的某些症状相符,从肠道菌群检测中可以发现艰难梭菌感染。
艰难梭菌感染与免疫功能有怎样的关联?
艰难梭菌毒素通过炎症小体和TLR4、TLR5和含有核苷酸结合寡聚结构域的蛋白1(NOD1)信号通路刺激先天免疫细胞,随后产生大量促炎细胞因子(如IL-12、IL-1β、IL-18、IFN-γ和TNFα)和趋化因子(MIP-1a、MIP-2、IL-8),导致粘膜通透性增加、肥大细胞脱颗粒、上皮细胞死亡和中性粒细胞浸润,引发免疫功能低下。
这与患者一开始诊断中中性粒细胞功能低下相符。
艰难梭菌感染通常与抗生素使用相关
通过某些抗生素,特别是克林霉素,可能会去除大量肠道中的有益细菌,使艰难梭菌得以繁殖,导致结肠炎和随后的腹泻。
真菌——酵母菌感染 ↑
报告中可以看到酵母菌超标,存在感染。这与入院时的粪便培养中的真菌感染相吻合。
真菌感染可能通过影响肠道微生物群和免疫反应,促进病原体的定殖和发展。
<来源:谷禾健康肠道菌群检测数据库>
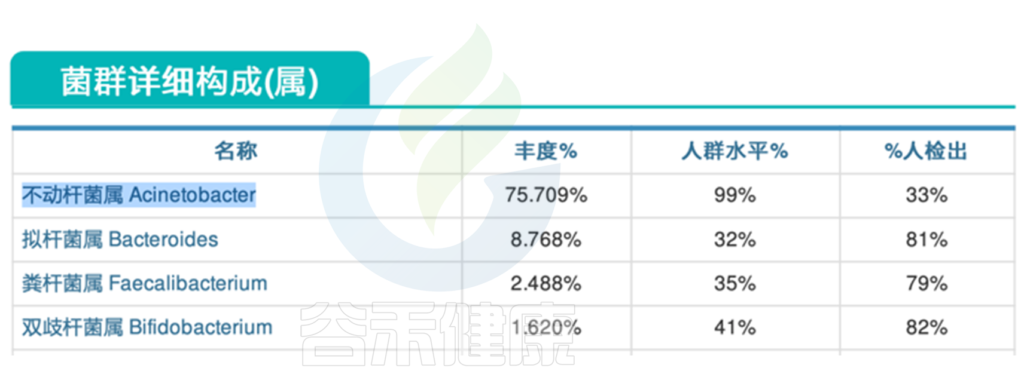
不动杆菌属(75.709%)占比过多 ↑
从报告中的菌群详细构成这部分可以看到,不动杆菌属的丰度竟然超过75%,严重超标。
这种情况下,不动杆菌属严重挤压了其他肠道核心菌属的生存空间,有益菌生长受限,菌群多样性下降,肠道菌群整体失调。
不动杆菌属Acinetobacter是一类革兰氏阴性菌,该菌属于常见的医院感染病原体之一。不动杆菌属感染常见的病症包括呼吸道感染、泌尿道感染、创伤感染等,严重情况下还可能导致败血症。
不动杆菌属对常见抗生素经常会产生抗药性。这里不动杆菌属丰度较高可能与抗生素使用较多相关。
结合该患者的情况,一开始入院时的组合抗生素一周未见好转,可能与不动杆菌属占比过多相关,对许多常见的抗生素已经产生耐药性,且免疫功能低下,因此难以好转。
针对上述情况,临床考虑口服抗生素,针对消化道微生物进行抗感染治疗。
初步选定:口服利福昔明 + 甲硝唑治疗。2天未见明显改善。
后改为:口服万古霉素 + 阿莫西林治疗。当天腹胀症状明显缓解,3天治疗腹胀明显改善。
同时辅助康复新液+B族维生素+谷氨酰胺治疗。
用药两周后,患儿整体情况平稳,仍存在轻微腹胀⇊

肠道菌群复查提示菌群结构基本恢复正常。
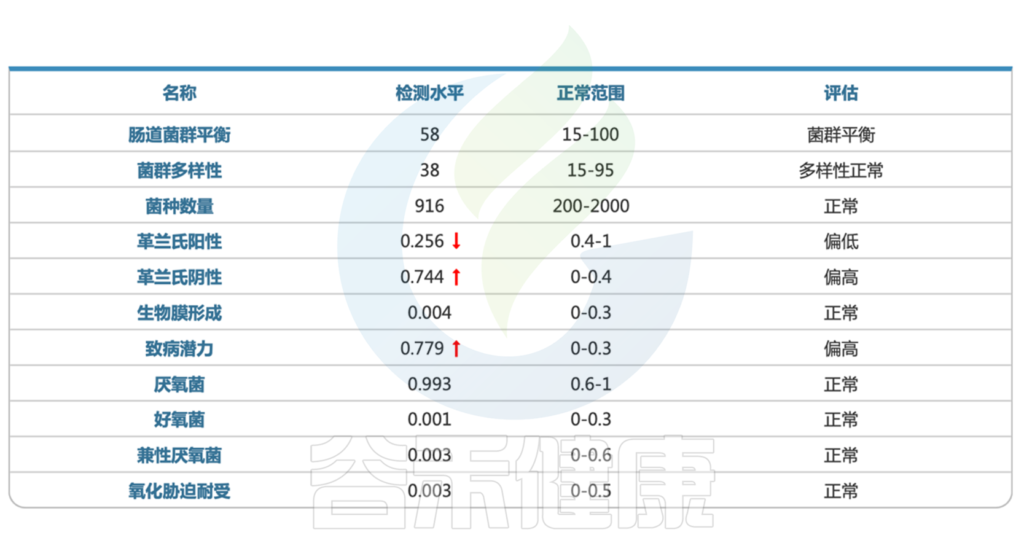
<来源:谷禾健康肠道菌群检测数据库>
一年后随访,该儿童身体已经好转,生活正常。
备注:临床中还有其它治疗药物等没有全部分享,主要分享了与菌群相关的治疗,仅做交流,不能作为治疗参考。
宿主感染与肠道菌群之间存在复杂的相互作用,免疫系统有两个分支,即先天性和适应性,它们协同工作以保护身体免受外部和内部威胁。这两个免疫系统分支都受到严格调节,肠道微生物群是其中的一个重要因素。
要揭开这其中的机制关联可能需要依靠营养学、流行病学、医学、免疫学和微生物学等多学科研究人员的共同努力。
不过从以上案例我们可以看到,肠道菌群健康检测在感染治疗中发挥重要价值。
辅助判别
在传统诊断中得知患者存在菌血症,真菌感染,但通过肠道菌群健康检测可以了解更多具体的感染信息,比如说艰难梭菌感染可能引起的腹胀等问题,不动杆菌属占比过大形成的抗生素耐药性。
除了致病菌超标等直观的信息之外,我们还可以判断整个肠道微生态的健康状况。肠道微生物群的失调可能导致肠道易感性增加,使得易感性疾病如艰难梭菌感染更容易发生。
辅助用药
针对这些具体信息可以使用药更加精确,而不是直接使用常见的组合抗生素。
用对抗生素对于恢复速度有很大提升,同时也避免了患者因使用不必要的抗生素产生耐药性。

谷禾健康
人的身体拥有数千种细菌,这些细菌在维持健康方面发挥着重要作用。当这些细菌失控繁殖并侵入身体的其他部位或将有害细菌引入身体的系统时,可能会发生细菌感染。
细菌感染的严重程度取决于所涉及的细菌类型和所感染的部位等。细菌最常感染肠道、皮肤和呼吸系统,包括肺、泌尿道和阴道。
目前应对细菌感染的主要治疗方法还是使用抗生素,但是抗生素管理,或改进抗生素的处方和使用方式,对于优化感染患者的治疗、保护患者免受伤害和对抗抗生素耐药性至关重要。
今天我们重点了解下什么是细菌感染,感染的症状、原因和类型,包括诊断测试和治疗方案,抗生素什么时候使用,什么时候不用,抗生素的耐药性如何产生以及使用抗生素的注意事项等。
了解什么是细菌感染以及如何治疗细菌感染,我们应该先了解细菌的概念。
来源:MedicineNet
地球上所有的生物都是由两种基本类型的细胞中的一种组成:
真核细胞,其遗传物质被包裹在核膜内;
原核细胞,其遗传物质与细胞的其他部分不分离。
传统上,所有的原核细胞都被称为细菌,被归为原核生物界。
1970年代后期,美国微生物学家卡尔·沃斯(Carl Woese)率先在分类上进行了重大变革,将所有生物分为真核生物、细菌(原名真细菌)和古细菌(原名古细菌)三个领域,以反映三条古老的进化路线。原核生物以前被称为细菌,然后被分为两个领域,细菌和古细菌。
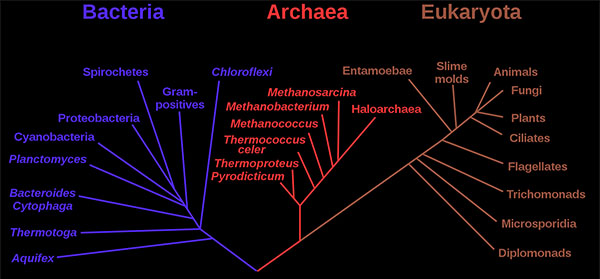

published by Woese et al.
细菌和古细菌在表面上是相似的,例如,它们没有细胞内的细胞器,它们有环状DNA。但是,它们在本质上是截然不同的,它们的分离是基于其古老而又独立的进化谱系的遗传证据,以及其化学和生理学的根本差异。这两个原核域的成员彼此之间的区别与它们和真核细胞中的区别一样。
细菌细胞在几个方面不同于动物细胞和植物细胞。一个根本的区别是细菌细胞缺乏动物细胞和植物细胞中都存在的细胞内细胞器,例如线粒体,叶绿体和细胞核。细菌体积小,设计简单,代谢能力强,使它们能够迅速生长和分裂,并在几乎任何环境中生存和繁衍。
细菌,动物和植物细胞的比较

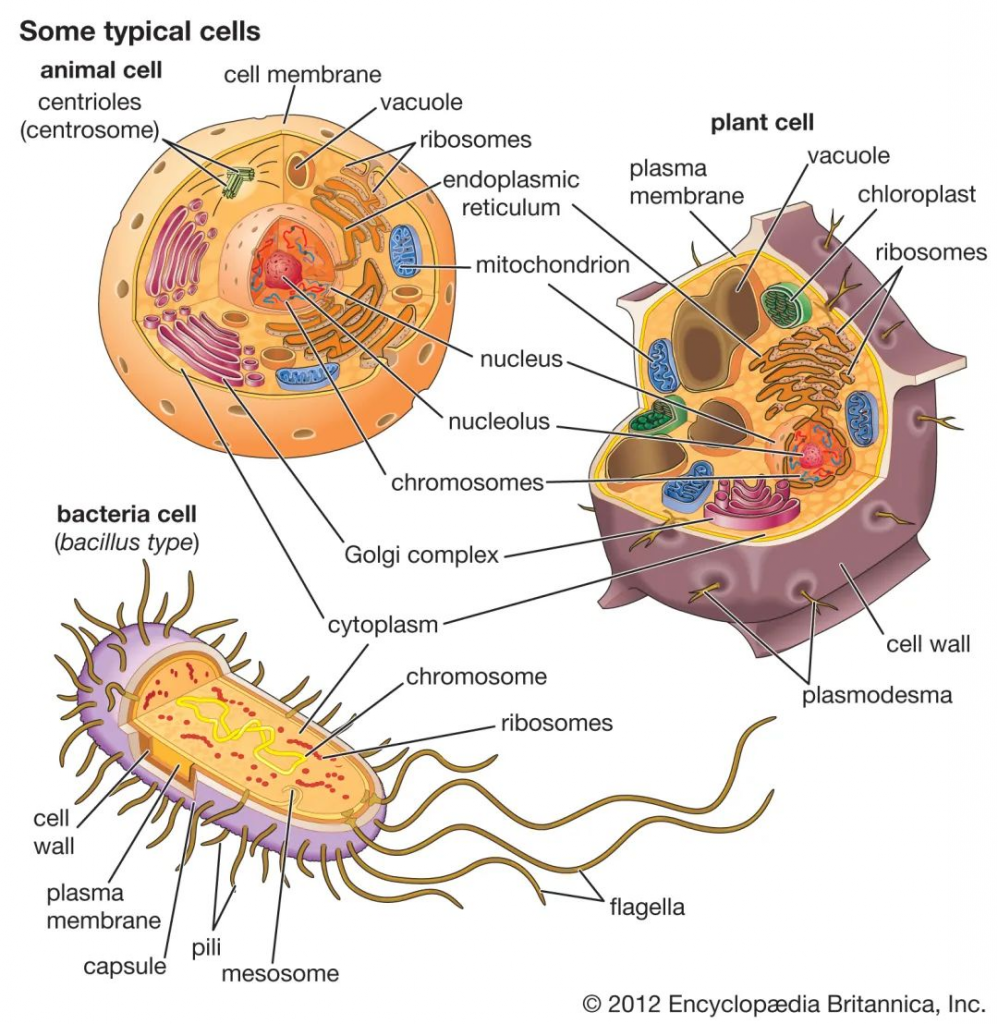
除此之外,原核和真核细胞在许多其他方面有所不同,包括脂质组成,关键代谢酶的结构,对抗生素和毒素的反应以及遗传信息的表达机制。
真核生物包含多个线性染色体,这些染色体的基因比编码蛋白质合成所需的基因大得多。遗传信息的核糖核酸(RNA)副本(脱氧核糖核酸或DNA)的大部分被丢弃,剩余的信使RNA(mRNA)在被翻译成蛋白质之前已被充分修饰。相反,细菌具有一个包含所有遗传信息的环形染色体,它们的mRNA是其基因的精确副本,不会被修饰。
细菌细胞在结构上比真核细胞小得多,也简单得多,但细菌是一个在大小、形状、生境和代谢上都有差异的极其多样化的有机体群体。
许多关于细菌的知识来自对致病细菌的研究,这些细菌比许多自由生活的细菌更容易在纯培养中分离出来,也更容易被研究。必须注意的是,许多自由生活的细菌与适应作为动物寄生虫或共生体生活的细菌有很大的不同。因此,关于细菌的组成或结构没有绝对的规则,任何说法都会有许多例外。
大多数细菌对地球上的生命都是有益的,甚至是生命所必需的,但少数细菌却对人类有害。目前,没有一种古细菌被认为是病原体,但是包括人类在内的动物不断遭到大量细菌的“轰击和居住”。
口腔,肠道和皮肤被大量特定类型的细菌定殖,这些细菌适应这些栖息地的生活。这些微生物在正常情况下是无害的,并且仅在它们以某种方式穿过身体的屏障并引起感染时才变得危险。
一些细菌擅长入侵宿主,被称为病原体或疾病产生者。一些病原体作用于人体的特定部位,例如:
在食物中传播的许多致病菌的毒素在摄入时会引起食物中毒。
由金黄色葡萄球菌(Staphylococcus aureus)产生的毒素,能引起迅速、严重但有限的胃肠道不适。
肉毒梭菌(Clostridium botulinum)的毒素,通常是致命的。在密封前未完全煮熟的罐装非酸性食品中可能产生肉毒杆菌毒素。肉毒梭菌形成耐热孢子,可以发芽为营养细菌细胞,在厌氧环境中茁壮成长,这有利于产生其极强的毒素。
其他食源性感染实际上是由受感染的食物处理者传播的,包括伤寒、沙门氏菌病(沙门氏菌属)和志贺氏菌病(痢疾志贺氏菌属)。
关于食物中毒相关细菌详见:正值夏季,警惕食源性疾病,常见的食物中毒的病原菌介绍
细菌感染是指病原菌侵入宿主组织。当有害细菌进入人体或伤口并繁殖,导致疾病、器官损伤、组织损伤或疾病时,就会发生细菌感染。细菌可以感染身体的任何部位。
细菌感染很常见,但它们并不完全相同。细菌有很多种,每种对身体都有不同的影响。广义上来讲,细菌感染也可以是由任何细菌引起的任何内部或外部疾病的广义术语。
细菌存在于与人体的各种关系中。它们在体表内定殖并提供益处,正常情况下细菌可以与人类身体共存不会产生有害的影响(在共生关系中)。但是有时候,通常无害地存在于我们体内或皮肤上,而不会造成任何异常问题的细菌会失控并导致感染。这种情况通常发生在我们的免疫系统不够强大,无法保持它们的平衡,或者我们的微生物区系的组成发生了一些变化,对某些细菌生存繁殖更有利。
细菌感染是由体内的坏细菌引起的。一些细菌感染可能危及生命。标准的医学治疗通常涉及一剂抗生素。细菌感染很容易与病毒感染混淆。但是他们并不一样,后面我们会单独解释。
当皮肤粘膜有破损或发生化脓性炎症时,细菌则容易侵入体内。
人体的免疫反应可分为非特异性免疫反应及特异性免疫反应两种,后者又可分为细胞免疫与体液免疫两方面。当机体免疫功能下降时,不能充分发挥其吞噬杀灭细菌的作用时,即使入侵的细菌量较少,致病力不强也能引起感染;条件致病菌所引起的医源性感染也逐渐增多。
人体免疫功能正常时,进入血中的细菌迅速被血中防御细胞如单核细胞、嗜中性粒细胞等所清除,而患肝硬变、糖尿病、血液病、结缔组织病等慢性病者,可因代谢紊乱、体液免疫及细胞免疫功能减低,易招致败血症发生;各种免疫抑制药物的使用、放射治疗亦是导致败血症发病率高的原因。广谱抗菌药物使用后,对药物敏感的细菌虽被抑制或杀灭,而一些耐药菌乘机繁殖,亦可酿成败血症。
细菌侵入人体后是否引起感染,除了与人的防御、免疫功能,还与细菌的毒力及数量有关。毒力强或数量多的致病菌进入机体,引起感染的可能性较大。
严重烧伤时,创面为细菌敞开门户,皮肤坏死、血浆渗出又为细菌繁殖提供了良好环境,故极易发生感染。
尿路、胆道、胃肠道、呼吸道粘膜受破坏后,若同时有内容物积滞、压力增高,细菌更易进入血中,保留导尿管、静脉等血管内留置导管、人工辅助呼吸时插管等,也使细菌易于侵入。
细菌是微观的,通常是单细胞生物,到处都可以找到(例如,在我们体内、皮肤上、空气中、水里、土壤中或我们吃的食物里)。细菌具有传染性,因此,它可以通过与患者的密切接触在人与人之间传播。接触受污染的表面、食物、水以及打喷嚏和咳嗽就是例子。
发生感染的几个条件:
此外,细菌还可以导致急性感染(快递治疗)和慢性感染(持续很长时间甚至终生),以及潜伏感染(最初可能没有任何明显迹象或症状但可以过段时间自然发展)。症状可以从轻度、中度到重度不等。在严重的情况下,导致数百万人死亡;例如,许多人死于黑死病或鼠疫。
细菌感染的常见特征:
常见的各部位细菌感染的症状

细菌性感冒
细菌性感冒(Bacterial cold)是指继发细菌感染引起的感冒。感冒在习惯上分为病毒性感冒和细菌性感冒。
病毒性感冒有:普通感冒、流行性感冒和病毒性咽炎等。其主要不同是致病因素不同,病毒性感冒是由于病毒所致,而细菌性感冒是由于细菌所致。
注:流行性感冒(流感通过病毒传播,不是细菌性感冒,注意区分),是由流感病毒引起的急性呼吸道传染病。
细菌的感染还取决于受感染细菌的类型,常见的细菌感染例如:
细菌感染具有高度传染性,因此需要特别注意避免通过洗手、打喷嚏和咳嗽时遮盖以及不共用杯子和饮料瓶来传播感染。
细菌有多种传播方式,包括:

当你忍不住咳嗽或打喷嚏时,用纸巾捂住口鼻或用手肘内侧。
在下述情况下需要洗手,至少洗20秒:
如果没有肥皂和水,可以使用酒精含量至少为 60% 的酒精类洗手液。
除此之外,其他需要注意的:
接种疫苗。如轮状病毒是一种导致婴儿和幼儿严重肠胃炎的病毒。所有婴儿都应在 6 周和 4 个月大时接种轮状病毒疫苗。
流感疫苗。当患上流感时,免疫系统会被削弱。这使细菌有机会侵入肺部并引起感染。每年注射一次流感疫苗可以防止感染肺部细菌。
肺炎球菌多糖疫苗。美国疾病控制与预防中心 (CDC) 推荐 65 岁及以上的人接种肺炎球菌多糖疫苗 (PPSV)。它也适用于免疫系统较弱或患肺炎风险较高的成年人。
治疗取决于感染的严重程度、患者的年龄、免疫系统有多强、是否存在任何并存症状以及现有的医疗条件。
治疗可能包括:
扩展阅读:
细菌素——对抗感染、保存食品、重塑肠道菌群
还在滥用抗生素?15种天然抗生素助你调节肠道菌群
这里我们主要来了解一下,用于细菌感染的药物——抗生素。
目前抗生素是对抗细菌感染的常用药物。它们通过破坏细菌细胞生长和增殖所需的过程来发挥作用。
抗生素根据抗菌谱可以分为:
广谱抗生素,中谱抗生素和窄谱抗生素。
✓ 广谱抗生素
广谱抗生素可对抗多种细菌。广谱抗生素可治疗革兰氏阳性菌和阴性菌,因此如果医生不确定有哪些细菌,他或她可能会开出其中一种抗生素。
阿莫西林、奥格门汀、头孢菌素(第 4 代和第 5 代)、四环素氨基糖苷类和氟喹诺酮类(环丙沙星)是广谱抗生素的例子。
✓ 中谱抗生素
中谱抗生素针对一组细菌。青霉素和杆菌肽是流行的中谱抗生素。
✓ 窄谱抗生素
窄谱抗生素用于治疗一种特定的细菌。多粘菌素属于这一小类抗生素。当确定患有哪种细菌感染时,治疗会更容易和更有效。
抗菌活性通常分为五种机制:
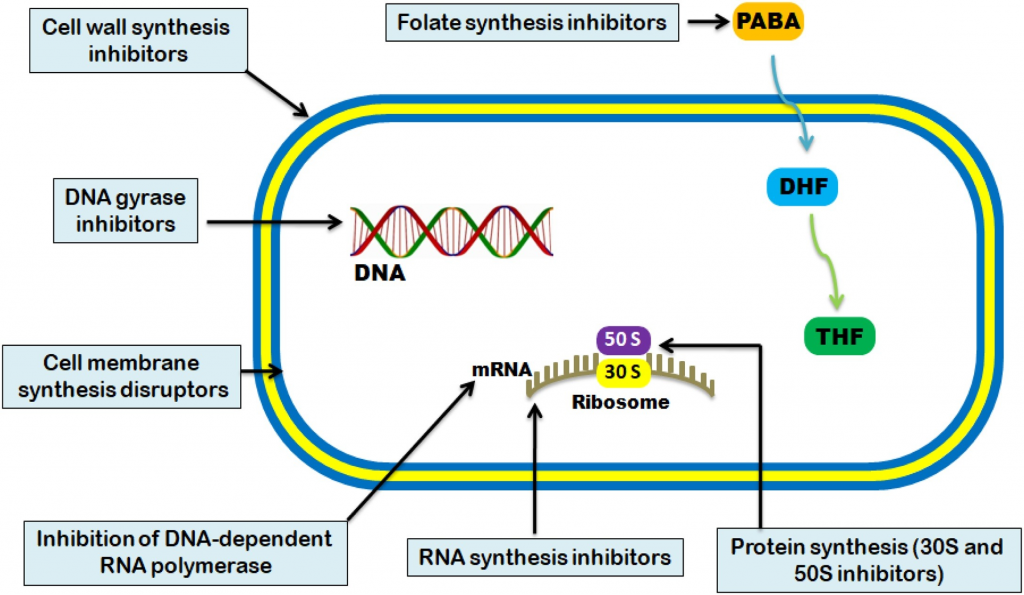

Uddin TM, et al., J Infect Public Health. 2021
不同种类抗生素作用的方式


Uddin TM, et al., J Infect Public Health. 2021
青霉素
最初的青霉素仅用于革兰阳性菌感染的治疗,由于金黄色葡萄球菌很快产生一种青霉素酶对青霉素产生了耐药,人们研制出了以甲氧西林、苯唑西林为代表的耐酶青霉素,用于产青霉素酶的葡萄球菌( 甲氧西林耐药者除外) 感染。
之后,以氨苄西林、阿莫西林为代表的广谱青霉素由仅对革兰阳性(G+) 菌有效扩展到对革兰阴性(G-) 菌( 主要为肠杆菌科细菌) 也具有抗菌活性。在广谱青霉素的基础上又发展为对铜绿假单胞菌等非发酵菌也具抗菌活性者,当前应用主要为脲基类青霉素,包括: 哌拉西林、阿洛西林、美洛西林。
代表药物: 阿莫西林(amoxicillin)
阿莫西林是一种抗细菌的青霉素抗生素。
阿莫西林用于治疗由细菌引起的多种不同类型的感染,例如扁桃体炎、支气管炎、肺炎以及耳、鼻、喉、皮肤或泌尿道感染。
阿莫西林有时还与另一种称为克拉霉素( Biaxin ) 的抗生素一起用于治疗由幽门螺杆菌感染引起的胃溃疡。这种组合有时与一种称为兰索拉唑(Prevacid)的胃酸减少剂一起使用。
四环素
四环素是一类抗生素,可用于治疗由易感微生物引起的感染,例如革兰氏阳性菌和革兰氏阴性菌、衣原体、支原体、原生动物或立克次体。
它们是在 1940 年代发现的,第一个四环素是从链霉菌中获得或衍生的。
四环素抑制微生物 RNA 中的蛋白质合成(一种重要的分子,作为 DNA 的信使)。它们主要是抑菌剂,这意味着它们可以防止细菌繁殖,但不一定会杀死它们。
四环素类药物现今应用的品种除四环素外,更常用有多西环素( 强力霉素) 和米诺环素( 二甲胺四环素) 。由于常见病原菌对本类药物耐药性普遍升高及其不良反应多见,当前本类药物临床应用已受到很大限制。
代表药物:强力霉素(doxycycline)
强力霉素是一种四环素抗生素,可以对抗体内的细菌。
强力霉素用于治疗许多不同的细菌感染,例如痤疮、尿路感染、肠道感染、呼吸道感染、眼部感染、淋病、衣原体、梅毒、牙周炎(牙龈疾病)等。
强力霉素也用于治疗由红斑痤疮引起的瑕疵、肿块和痤疮样病变。
某些形式的强力霉素用于预防疟疾、治疗炭疽或治疗由螨虫、蜱虫或虱子引起的感染。
什么是林可霉素衍生物?
林可霉素衍生物是一小类抗生素,可抑制细菌蛋白质的合成,而细菌蛋白质对细菌的生存至关重要。林可霉素衍生物保留用于治疗由肺炎球菌、葡萄球菌和链球菌的敏感菌株引起的感染。一种衍生物也可用于治疗恶性疟原虫(疟疾)。
林可霉素类包括林可霉素及克林霉素。克林霉素的体外抗菌活性优于林可霉素,主要可应用于敏感肺炎链球菌、其他链球菌属( 肠球菌属除外) 及甲氧西林敏感金葡菌所致的各种感染。该类药物对厌氧菌有良好的抗菌活性常与其他抗菌药物联合用于腹腔感染及盆腔感染,也由于其骨组织浓度较高适用于骨和关节的G + 菌感染。使用本类药物时,应注意假膜性肠炎的发生,如有可疑应及时停药。本类药物有神经肌肉阻滞作用,应避免与其他神经肌肉阻滞剂合用,应注意静脉滴注速度宜缓慢滴注,不可静脉推注。
代表药物:克林霉素(Clindamycin)
克林霉素是一种抗生素,可以对抗体内的细菌。
克林霉素用于治疗由细菌引起的严重感染。
服用此药前 如果对克林霉素或林可霉素过敏,则不应使用该药。
为确保克林霉素的安全,请告诉医生是否曾经有过:结肠炎、克罗恩病或其他肠道疾病; 湿疹或皮肤过敏反应; 肝病; 哮喘或对阿司匹林的严重过敏反应; 对黄色食用色素过敏。
什么是喹诺酮类药物?
喹诺酮类是一种抗生素。抗生素杀死或抑制细菌的生长。
有五种不同的喹诺酮类。此外,另一类抗生素,称为氟喹诺酮类,是从喹诺酮类通过氟修饰其结构衍生而来的。氟喹诺酮类抗生素可导致严重或致残的副作用,这些副作用可能不可逆。
喹诺酮类药物和氟喹诺酮类药物有许多共同点,但也有一些区别,例如它们对哪些生物有效。有些人互换使用喹诺酮和氟喹诺酮这两个词。
喹诺酮类和氟喹诺酮类对细菌产生的两种酶(拓扑异构酶 IV 和 DNA 促旋酶)的功能产生不利影响,因此它们不能再修复 DNA 或帮助其制造。
现今临床主要应用为氟喹诺酮类,常用有诺氟沙星、环丙沙星等主要用于单纯性下尿路感染或肠道感染。但应注意,现今国内尿路感染的主要病原菌大肠埃希菌中,耐药株已达半数以上。环丙沙星尚与β-内酰胺类抗生素联合用于治疗中、重度革兰阴性杆菌感染包括铜绿假单胞菌的感染。
近年来研制的新品种左氧氟沙星、莫西沙星等对肺炎链球菌、化脓性链球菌等G + 球菌的抗菌作用增强,对衣原体属、支原体属、军团菌等细胞内病原或厌氧菌的作用亦有增强,但对G-菌活性增强不明显,对铜绿假单胞菌的抗菌活性仍以环丙沙星为最强。左氧氟沙星、莫西沙星除可用于尿路感染或肠道感染外也可用于呼吸道感染,特别适合于肺炎链球菌( 包括耐青霉素肺炎链球菌) 、支原体、衣原体、军团菌等所致社区获得性肺炎的治疗,此外亦可用于皮肤软组织感染。
在治疗腹腔、胆道感染及盆腔感染时除莫西沙星外需与甲硝唑等抗厌氧菌药物合用。部分品种可与其他药物联合应用作为治疗耐药结核分枝杆菌和其他分枝杆菌感染的二线用药。
代表药物:环丙沙星(Ciprofloxacin)和左氧氟沙星(Levofloxacin)
环丙沙星和左氧氟沙星是一种氟喹诺酮抗生素,用于治疗不同类型的细菌感染。也用于治疗接触过炭疽或某些类型鼠疫的人。环丙沙星和左氧氟沙星应仅用于无法用更安全的抗生素治疗的感染。
左氧氟沙星、莫西沙星:对肺炎链球菌、A 组溶血性链球菌等革兰阳性球菌、衣原体属、支原体属、军团菌等细胞内病原或厌氧菌的作用强。
环丙沙星、左氧氟沙星:主要适用于肺炎克雷伯菌、肠杆菌属、假单胞菌属等革兰阴性杆菌所致的下呼吸道感染。
头孢霉素
头孢菌素是一大类从霉菌顶孢菌(以前称为头孢菌素)中提取的抗生素。头孢菌素具有杀菌作用(杀死细菌),其作用方式与青霉素相似。它们结合并阻断负责制造肽聚糖的酶的活性,肽聚糖是细菌细胞壁的重要组成部分。它们被称为广谱抗生素,因为它们对多种细菌有效。
自 1945 年发现第一个头孢菌素以来,科学家们一直在改进头孢菌素的结构,以使其对更广泛的细菌更有效。每次结构发生变化,都会产生新的“一代”头孢菌素。迄今为止,头孢菌素已有五代。所有头孢菌素均以 cef、ceph 或 kef 开头。请注意,该分类系统在不同国家/地区的使用并不一致。
第一代头孢菌素是指发现的第一组头孢菌素。它们的最佳活性是对抗革兰氏阳性细菌,如葡萄球菌和链球菌。它们对革兰氏阴性菌几乎没有活性。
第二代头孢菌素尚可应用于由流感嗜血杆菌、大肠埃希菌、奇异变形杆菌等中的敏感株所致的尿路感染、皮肤软组织感染、败血症、骨及关节感染和腹腔、盆腔等感染。但如用于腹腔感染和盆腔感染时需与抗厌氧菌药合用。头孢呋辛尚可用于脑膜炎球菌、流感嗜血杆菌所致脑膜炎的治疗,也可作为围术期预防用药。
第三代头孢菌素:对肠杆菌科细菌等革兰阴性杆菌具有强大抗菌作用,头孢他啶和头孢哌酮对铜绿假单胞菌亦具较强抗菌活性;注射品种有头孢噻肟、头孢曲松、头孢他啶、头孢哌酮等,口服品种有头孢克肟和头孢泊肟酯等,口服品种对铜绿假单胞菌均无作用。应注意的是,不是所有的三代头孢菌素都可用于非发酵菌( 如铜绿假单胞菌、不动杆菌等) 感染的治疗,除了头孢哌酮和头孢他啶;外,如头孢曲松和头孢噻肟不可以用于非发酵菌感染的治疗。
第四代头孢菌素:常用者为头孢吡肟,对肠杆菌科细菌作用与第三代头孢菌素大致相仿,对铜绿假单胞菌的作用与头孢他啶相仿,对革兰阳性球菌的作用较第三代头孢菌素略强。其不同于三代头孢菌素之处为对产头孢菌素酶( AmpC) 的肠杆菌属有效,其次是增强了对作用靶位细菌青霉素结合蛋白( PBP) 的亲和力以及其抗革兰阳性菌的抗菌活性亦较三代头孢菌素增强。
第五代(或下一代)头孢菌素头孢洛林( Teflaro ) 对耐甲氧西林金黄色葡萄球菌(MRSA)具有活性。Avycaz 含有β-内酰胺酶抑制剂avibactam。
代表药物:头孢氨苄(Cephalexin)
头孢氨苄是一种头孢菌素(SEF 一种低孢子)抗生素。它通过对抗体内的细菌起作用。
头孢氨苄用于治疗由细菌引起的感染,包括上呼吸道感染、耳部感染、皮肤感染、尿路感染和骨骼感染。
头孢氨苄用于治疗成人和至少 1 岁儿童的感染。
注意事项:
如果对头孢氨苄或类似抗生素(如Ceftin、Cefzil、Omnicef等)过敏,则不应使用该药。如果对任何药物(尤其是青霉素或其他抗生素)过敏,请告诉医生。
对任何药物(尤其是青霉素)过敏;
肝脏或肾脏疾病;要么肠道问题,例如结肠炎,请告诉医生。
头孢氨苄可以进入母乳。如果正在哺乳婴儿,请咨询医生。
β-内酰胺酶抑制剂
β-内酰胺酶抑制剂是一类阻断 β-内酰胺酶(也称为 β-内酰胺酶)活性,防止 β-内酰胺类抗生素降解的药物。本类药物适用于因产β-内酰胺酶的细菌感染,其抗菌谱主要依据原有抗生素的活性而酶抑制剂仅有对抗细菌产酶的作用,一般不增加抗菌活性。
β-内酰胺酶由以下细菌的某些菌株产生:拟杆菌属、肠球菌属、流感嗜血杆菌、卡他莫拉菌、淋病奈瑟菌和葡萄球菌属,无论是组成型还是暴露于抗微生物剂。
β-内酰胺酶裂解易感青霉素和头孢菌素的 β-内酰胺环,使抗生素失活。一些抗微生物药物(如头孢唑啉和氯唑西林)对某些 β-内酰胺酶具有天然耐药性。β-内酰胺类:阿莫西林、氨苄青霉素、哌拉西林和替卡西林,可以通过与β-内酰胺酶抑制剂组合来恢复和扩大其活性。
克拉维酸、舒巴坦和他唑巴坦都是β-内酰胺酶抑制剂。
大环内酯类
大环内酯类药物主要作为青霉素过敏患者的替代药物,用于治疗β-溶血性链球菌、肺炎链球菌中的敏感菌株所致的上、下呼吸道感染、敏感β-溶血性链球菌引起的猩红热及蜂窝织炎等感染。
大环内酯类是从红糖多孢菌(原名红链霉菌)中提取的一类抗生素,一种土壤传播的细菌。
红霉素是第一个发现的大环内酯类;其他大环内酯类包括阿奇霉素、克拉霉素和罗红霉素。
它们的作用主要是抑菌,但在高浓度时可能具有杀菌作用,或取决于微生物的类型。
代表药物:红霉素
红霉素为大环内酯类原型代表药物,由于其胃肠道反应大、口服吸收差使其疗效受到影响。当下在临床应用的主要为大环内酯类新品种罗红霉素、阿奇霉素和克拉霉素等,其他大环内酯类疗效多不如该三种药物。
罗红霉素主要是改善了其药代动力学,口服生物利用度明显提高、给药剂量减小、不良反应明显减少,但其抗菌谱没有明显的改善,是红霉素的替代药物。
氨基糖苷类
临床常用的氨基糖苷类药物主要有: 链霉素、卡那霉素、丁胺卡那霉素、庆大霉素、妥布霉素、奈替米星、依替米星。
其中链霉素当前主要用抗结核治疗,其次可用于治疗鼠疫及布鲁菌病; 庆大霉素、妥布霉素、奈替米星、依替米星肠杆菌科细菌和铜绿假单胞菌等G - 杆菌具强大抗菌活性,对葡萄球菌属亦有良好作用者。所有氨基糖苷类药物对肺炎链球菌、溶血性链球菌的抗菌作用均差。
链霉素、卡那霉素:对肠杆菌科和葡萄球菌属细菌有良好抗菌作用,但对铜绿假单胞菌无作用者。
庆大霉素、妥布霉素、奈替米星、阿米卡星、异帕米星、小诺米星、依替米星:对肠杆菌科细菌和铜绿假单胞菌等革兰阴性杆菌具强大抗菌活性,对葡萄球菌属亦有良好作用。
碳青霉烯类
碳青霉烯类药物是当下抗菌药物中抗菌谱最广的药物,对各种革兰氏阳性球菌、革兰氏阴性杆菌( 包括铜绿假单胞菌的非发酵菌) 和多数厌氧菌具强大抗菌活性,对大多数β-内酰胺酶高度稳定,但对甲氧西林耐药葡萄球菌和嗜麦芽窄食单胞菌等抗菌作用差。
当下在国内应用的碳青霉烯类抗生素有亚胺培南-西司他丁、美罗培南、帕尼培南-倍他米隆、比阿培南。厄他培南与上述品种不同对非发酵菌缺乏抗菌活性,而其他抗菌作用与上述药品基本相同,适合于治疗社区与医院早期特别是G-杆菌感染的重症患者。
碳青霉烯类对各种革兰阳性球菌、革兰阴性杆菌(包括铜绿假单胞菌、不动杆菌属)和多数厌氧菌具强大抗菌活性,对多数β-内酰胺酶高度稳定,但对甲氧西林耐药葡萄球菌和嗜麦芽窄食单胞菌等抗菌作用差。
现用于细菌感染的抗生素被认为是医学史上最重要的突破之一。不幸的是,细菌的适应性很强,抗生素的过度使用让许多人对抗生素产生了耐药性,造成了严重的问题,尤其是在医院的环境里。
抗生素耐药性是细菌抵抗抗生素杀伤力的能力。换句话说,以前治疗感染的抗生素没有效果了,或者说根本无法杀死细菌。
由于过度使用抗生素,抗生素耐药率持续上升,新的抗菌药物开发缓慢。感染耐药细菌可能导致住院时间更长、费用更高,并增加死于感染的风险。
抗生素耐药性是对全球健康的紧迫威胁,包括后来逐渐出现危险耐药细菌——“超级细菌”。
疾病控制和预防中心 (CDC)发布了对美国的前 18 种耐药性威胁的清单,至少包括:
注:以上这些并未全面列出所有耐药菌。抗生素耐药性模式不断演变,细菌可能并不总是对每位患者的选择抗生素表现出耐药性。在正常情况下,抗生素的选择应基于感染部位和由医疗保健专业人员评估的临床表现、培养/敏感性和其他所需的实验室结果、局部耐药性/敏感性模式以及患者的特定特征。
细菌通过以某种方式调整其结构或功能作为防御机制,从而对抗生素产生抗药性。
当细菌以某种方式发生变化时,细菌会抵抗药物。这种变化可以保护细菌免受药物的影响或限制药物接触细菌。或者这种变化可能导致细菌改变药物或破坏药物。
细菌可以用以下方式与抗生素抗争:
如果说以上列举的是抗生素产生耐药性的内因,那么除细菌本身外的因素也会导致抗生素耐药性的出现。
早前,医生有时会依赖不可靠或不准确的知识,开具抗生素“以防万一”,或在特定窄谱抗生素可能更合适时却开出广谱抗生素。这些情况加剧了选择压力并加速了抗菌素耐药性。
当医生不清楚是细菌或病毒加剧了感染时,他们可能会开抗生素。抗生素对病毒感染不起作用,可能会产生耐药性。
抗生素自我治疗(SMA)与药物使用不当的可能性有关,这会使患者面临药物不良反应的风险,掩盖潜在疾病的迹象,并在微生物中产生耐药性。
过度使用抗生素,尤其是在不正确治疗的情况下服用抗生素,会促进抗生素耐药性。根据疾病控制和预防中心的数据,人类使用大约三分之一的抗生素既不需要也不合适。
抗生素可以治疗由细菌引起的感染,但不能治疗由病毒引起的感染(病毒感染)。例如,抗生素是可以治疗由细菌引起的链球菌性咽喉炎。但对于大多数由病毒引起的喉咙痛,并不是正确的治疗方法。
每天都有成千上万的患者、工作人员和访客到达医院,每个人的衣服上和身体上/体内都有自己的一套微生物组。如果医院没有适当的程序和规程来帮助保持空间清洁,细菌就会传播。
抗生素被用作动物的生长补充剂和生长促进剂。在家畜中发现的耐抗生素细菌可能对人类致病,很容易通过食物链传播给人类,并通过动物粪便在生态系统中广泛传播。在人类中,这可能会导致复杂的、无法治疗的和长期的感染。
由于技术挑战、缺乏知识、对抗细菌生理学的重大困难,制药业对新抗生素的发明在很大程度上放缓了,当新抗生素普及时,耐药性的发展(在相对较短的时间内)几乎是不可避免的。
世界范围内抗生素的过度使用和滥用正在导致抗生素耐药性的全球医疗问题。可能会发生抗生素耐药性感染,在最坏的情况下,可能会没有有效的抗生素。这种情况在严重感染时可能会危及生命。
大多数病毒性疾病不需要特殊药物并且是“自限性”的,也就是说患者自身的免疫系统可以抵抗疾病。病毒性疾病的患者可以休息、多喝水并使用对症治疗。
由病毒引起的疾病包括:
有时,在复杂或长期的病毒感染中,细菌也可能侵入,并导致所谓的“继发感染”。在这些情况下,如果需要,可以使用抗生素。
在感染由病毒引起的疾病中,例如咳嗽、感冒或流感,患者不应要求医生开抗生素。抗生素不能治愈病毒感染,患者可能会因不必要的药物而产生副作用。医生可以用其他方法来帮助患有病毒性疾病的患者进行治疗。
如果感染没有得到正确治疗,抗生素耐药细菌也可能传播给其他人。
——有以下几个原因:
它可能不是治疗感染的正确抗生素
它可能已过时且无效
整个疗程可能没有足够的药物
如果新疾病是病毒感染,则不需要抗生素
一些疫苗可以预防细菌性疾病。抗病毒疫苗,例如流感疫苗或COVID-19 疫苗,可以帮助预防可能与继发性细菌感染(如严重的肺部肺炎)相关的原发性疾病。
在治疗的最初几天感觉好些了的时候,仍应完成整个抗生素疗程。
抗生素使用注意事项
✓ 按照指示使用抗生素
按照医生的指示治疗感染。医生会选择最能对抗导致感染的特定细菌的抗生素类型。目前市面上有许多不同种类的抗生素,大部分需要医生开出的非处方抗生素。
✓ 了解抗生素
有的抗生素需要进行皮试,比如青霉素,以防过敏,不同的抗生素杀菌的作用原理不尽相同,比如青霉素是通过能破坏细菌的细胞壁并在细菌细胞的繁殖期起杀菌作用的一类窄普抗生素,杀菌作用强,可用于敏感菌所致的严重感染,由于该类药物作用的靶位为细菌细胞壁,而人体的细胞没有细胞壁,因此毒性低,用于老年人,新生儿和孕妇时安全性相对较高。
✓ 确保清楚抗生素的使用方式
确保明确知道应该服用多少抗生素,以及何时服用。有些抗生素需要与食物一起服用,有些需要在晚上服用等。特别注意要用完整的病征疗程抗生素,有些人担心抗生素对身体有副作用,病情稍微好转就会停止服用或注射抗生素,但是这可能导致体内的致病细菌未完全清楚,再次发生感染,或引起形成抗生素抗药性,使得以后的感染治疗变得困难。
✓ 清洁伤口以防止细菌感染
通过立即正确清洁和包扎伤口来预防皮肤感染。适当的急救治疗对于帮助预防细菌感染至关重要,但不应尝试自己治疗严重的皮肉伤口。如果伤口很深、很宽或出血很多,应该立即寻求医疗帮助。
治疗伤口前先洗手。如果你用脏手治疗伤口,会增加细菌感染的机会。用温水和抗菌肥皂洗手 20 秒,然后擦干。如果有条件可以戴上手套。
细菌感染性疾病起病急、进展快,重症疑难患者病原细菌复杂,诊断及治疗困难,可危及生命。早期、准确地明确病原微生物对感染判定至关重要,有助于改善预后。
准确诊断细菌感染对于避免不必要的抗生素使用和集中适当的治疗至关重要。
细菌感染是细菌的存在与炎症或全身功能障碍的结合;因此,通常需要不止一种诊断方式进行确认,确定患者是否符合临床病例定义的病史和检查。
不同的病原微生物检测技术对感染的判定价值不同,临床上也会根据患者的病情,可能感染的部位,可供采集的标本等选择适宜的检测技术。


当前,病原微生物检测技术层出不穷,能识别的微生物种类越来越多,但如何正确利用和分析微生物检测结果仍是临床关注的难题。值得注意的是,感染首先是个临床诊断,所有的判定必须基于临床。
定植容易对感染判定产生混淆。正常生理状态下人体口腔、胃肠道、呼吸道及体表等部位均有细菌、真菌存在,患者无感染症状时称为定植菌。当定植菌的致病力改变或机体防御能力下降时,可大量繁殖或被带入机体深部引起感染成为致病菌。
临床医生应如何判断所获取的病原体为定植还是感染,是长久以来的难题,且未形成成熟统一的解决方案。
呼吸道定植菌的综合分析:
就呼吸道定植菌而言,既往认为可根据菌落数量或菌种拷贝数来判定定植与感染,但结果存在偏差。越来越多的学者认为,临床上判定是定植还是感染,需结合患者症状、体征及其他检查结果综合分析。
若患者存在与检测阳性结果相匹配的临床症状和体征,如发热、咳嗽、咳痰等,感染指标升高,肺部出现新发病灶,应考虑感染并给予相应的抗感染治疗。如仅培养阳性,患者无任何感染相关临床表现,则倾向于定植菌。
念珠菌定植的综合分析:
念珠菌可广泛定植于呼吸道、胃肠道及泌尿生殖道,正常屏障破坏、免疫功能受损或局部菌群失调时,定植的念珠菌可生长繁殖引起感染。痰和尿标本中分离出的念珠菌亦应根据临床症状和体征鉴别是定植还是感染,念珠菌血培养阳性时要高度警惕念珠菌血症。
此外,病原微生物检测结果阳性,并不意味着患者一定存在感染或感染一定由检出的病原体所致,需结合标本质量、采集部位、病史及其他检测结果综合分析。
不同部位标本检测出同一种病原体,其代表的临床意义可能并不相同。
以肺炎克雷伯氏菌为例,从肠道粪便样本中检出肺炎克雷伯氏菌,其中丰度占比超过1%的人群有3765例,占比28.2%【谷禾健康数据库】。但是当肺炎克雷伯菌进入血液并感染时,通常会发生细菌血症。症状可能包括发冷,发烧,发抖,肌肉酸痛,疲劳和嗜睡。当肺炎克雷伯菌感染肝脏时,会引起脓性病变,也被称为化脓性肝脓肿。这种类型的感染更常见于患有糖尿病一段时间或已经服用抗生素多年的人。
因病原微生物种类不同,微生物检测方法的选择也不相同;即便检测同一种微生物,因采集部位不同所选择的检测方法也有所差别。
如大肠埃希菌,血培养阳性时需考虑血流感染,怀疑致病性大肠埃希菌感染肠道时需特殊培养或者血清学、PCR,16s测序检测等。因普通大肠埃希菌可寄居在肠道中,粪便普通培养有大肠埃希菌生长并不能直接考虑大肠埃希菌肠道感染。
病原微生物检测技术快速发展,能识别的微生物种类越来越多,但感染首先是个临床诊断,所有的判定必须基于临床。随着检测技术革新带来的是临床辅助手段的进步和多样化,更快、更准确地判定感染一直都是病原学检测的挑战,不同方法各有优劣。当前,并没有一项技术可通过从标本中识别微生物来直接判定机体是否感染该病原体,甚至依靠检测的阴性结果来排除感染都很难实现。
在面对细菌感染诊疗过程中始终需要思考3个问题:患者是否存在感染?如果有感染,致病病原体是什么?如何治疗干预?
充分利用现有的病原微生物检测方法和其他实验室检查手段,综合判定,给出合适的抗菌治疗或其他综合治疗方法,是科学可持续的手段。
主要参考文献:
Uddin TM, Chakraborty AJ, Khusro A, Zidan BRM, Mitra S, Emran TB, Dhama K, Ripon MKH, Gajdács M, Sahibzada MUK, Hossain MJ, Koirala N. Antibiotic resistance in microbes: History, mechanisms, therapeutic strategies and future prospects. J Infect Public Health. 2021 Dec;14(12):1750-1766. doi: 10.1016/j.jiph.2021.10.020. Epub 2021 Oct 23. PMID: 34756812.
Cheung GYC, Bae JS, Otto M. Pathogenicity and virulence of Staphylococcus aureus. Virulence. 2021 Dec;12(1):547-569. doi: 10.1080/21505594.2021.1878688. PMID: 33522395; PMCID: PMC7872022.
Tshibangu-Kabamba E, Yamaoka Y. Helicobacter pylori infection and antibiotic resistance – from biology to clinical implications. Nat Rev Gastroenterol Hepatol. 2021 Sep;18(9):613-629. doi: 10.1038/s41575-021-00449-x. Epub 2021 May 17. PMID: 34002081.
BRM, Mitra S, Emran TB, Dhama K, Ripon MKH, Gajdács M, Sahibzada MUK, Hossain MJ, Koirala N. Antibiotic resistance in microbes: History, mechanisms, therapeutic strategies and future prospects. J Infect Public Health. 2021 Dec;14(12):1750-1766. doi: 10.1016/j.jiph.2021.10.020. Epub 2021 Oct 23. PMID: 34756812.
Carmen Fookes, BPharm, Bacterial Infection. January 13, 2020 Medicine
Spagnolo F, Trujillo M, Dennehy JJ. Why Do Antibiotics Exist? mBio. 2021 Dec 21;12(6):e0196621. doi: 10.1128/mBio.01966-21. Epub 2021 Dec 7. PMID: 34872345; PMCID: PMC8649755
Baquero F, Coque TM, Cantón R. Counteracting antibiotic resistance: breaking barriers among antibacterial strategies. Expert Opin Ther Targets. 2014 Aug;18(8):851-61. doi: 10.1517/14728222.2014.925881. Epub 2014 May 31. PMID: 24881465.
武洁, 王荃. 病原微生物检测在感染判定的意义[J]. 中国小儿急救医学, 2020, 27(3):6.
李丹鹤, 荣爱国, 马瑞芝,等. 病原微生物检验在抗感染经验治疗中的临床意义[J]. 医学理论与实践, 2019, 32(09):127-129.
谷禾健康

链球菌咽喉炎是一种细菌感染引起的呼吸道疾病,可导致喉咙痛,喉咙痒。全世界每年有超过6亿人感染链球菌性咽喉炎。
链球菌咽喉炎是由化脓性链球菌(A族乙型溶血性链球菌)引起的,通常在患者咳嗽或打喷嚏时通过飞沫传播。
链球菌性咽喉炎的症状包括如下:
喉咙痛,扁桃体肿胀、发红,喉咙后面有白斑,发热,恶心想吐,头疼,浑身疼痛,皮疹等。
这些症状中有许多与病毒感染的症状类似。有这些症状的同时流鼻涕或咳嗽,更有可能是病毒感染,如普通感冒。
与普通感冒有所区分,最常见的链球菌咽喉炎症状是:突然出现喉咙痛,吞咽困难或吞咽困难,发烧以及扁桃体上有红斑。
链球菌咽喉炎的症状也可能与COVID-19的症状类似,COVID-19是由一种冠状病毒引起的。
如果因感冒引起喉咙痛,通常会在一两天后好转或消失。对于链球菌,喉咙痛持续存在,而且往往更加严重。
2019年2月发表在《科学转化医学》杂志上的一项新研究发现,基因变异和免疫力低下可能是一部分儿童反复遭受链球菌感染的原因。
当然,任何人都有可能患链球菌咽喉炎。但在以下符合以下条件的人群更容易得:
年龄:在5到15岁之间
季节:冬天或初春
环境:一大群人在室内封闭环境
兄弟姐妹,或者是同一班级的孩子中有人感染上了,其他人就可能会被传染,出现类似症状。
成年人中虽然少见,但与儿童接触的家长或其他成年人也可能会被传染。
如果怀疑自己或孩子可能患有链球菌性喉炎,建议去医院检查。医生诊断链球菌性咽喉炎的方法是进行快速抗原测试或咽喉培养。
两者都涉及在喉咙和扁桃体的背面擦拭无菌棉签以获取分泌物样本。
通常,医生会先进行快速抗原测试。通过在喉咙中查找,在几分钟内检测出链球菌。
如果测试结果呈阴性,但医生仍怀疑是链球菌,则下一步可能是咽喉培养。有些医生会根据当地规程同时进行两项检查。
从喉咙后部收集的样品在实验室中进行培养(繁殖)以发现细菌的存在。咽喉培养时间可能需要两天。
潜伏期:2-5天;
一般人经过治疗,会在10天内恢复正常。
由于链球菌性咽喉炎是一种细菌感染,因此需要使用抗生素。不过需要注意的是,使用抗生素后,虽然症状会很快缓解,但仍需坚持服用一个疗程或遵医嘱。
另外,常规非处方药也有助于缓解症状。
补充疗法:
家庭疗法不能治愈链球菌性咽喉炎,但可以对抗不适。美国疾病控制与预防中心建议,简单的如喝蜂蜜,柠檬茶或用温盐水漱口,可以缓解症状,减轻肿胀。

也可以使用加湿器来增加空气中的水分,可以缓解干燥、喉咙痛,并缓解充血。

充足的睡眠。睡眠有助于身体抵抗感染,自主修复。

不吸烟,远离二手烟。香烟烟雾会刺激喉咙痛,并增加诸如扁桃体炎等感染的可能性。
避免油漆或灰尘刺激喉咙和肺部。
链球菌咽喉炎也会引起并发症(虽然不是很常见)。
如果细菌传播到身体的其他部位,就会导致所谓的侵入性感染。
并发症包括:
扁桃体周围有脓肿
颈部肿大的淋巴结
鼻窦感染
耳部感染
链球菌感染后肾小球肾炎
未经治疗的链球菌性咽喉炎也会引起风湿热,这是一种罕见但严重的感染,会对心脏造成损害(风湿性心脏病)。
链球菌感染和风湿热之间的联系还不清楚,但似乎是可以欺骗免疫系统。人体免疫系统转而攻击自己的组织,特别是心脏、关节、皮肤和中枢神经系统的组织,进而导致持续几周到几个月的炎症或肿胀。
其他与链球菌咽喉炎相关的病包括:
猩红热(A组溶血性链球菌感染引起的急性呼吸道传染病)
当A组链球菌产生一种毒素,导致典型的红疹时,就会发生这种疾病。猩红热的最初症状是发烧和喉咙痛。症状还包括寒战、呕吐或腹痛。
猩红热通常是一种轻微的感染。接触到A组链球菌的人通常需要两到五天的时间才会生病。
发病后一两天,颈部和胸部通常会出现红色凹凸不平的“草莓状”皮疹,然后蔓延到全身。皮疹约7天后消退。
熊猫病(与链球菌感染有关的儿童自身免疫性神经精神障碍)
根据美国国家精神健康研究所研究显示,当免疫系统对链球菌感染的反应错误地攻击大脑时,就会出现熊猫病。导致类似强迫症的症状和身体抽搐,通常是戏剧性的“一夜之间,突然发生”。
孩子们也可能变得喜怒无常或易怒,焦虑发作,或表现出与父母或所爱的人分离的担忧。
链球菌性咽喉炎具有高度传染性。当感染者咳嗽或打喷嚏时,通过空气飞沫传播细菌。
另外,接触携带细菌的表面,比如门把手,然后细菌就可能转移到其他人的眼睛、鼻子或嘴巴,其他人可能会感染链球菌咽喉炎。因此病人在咳嗽或打喷嚏时尽量遮住口鼻。

目前还没有疫苗可以预防,但可以通过一些措施减少感染。
· 建议经常洗手(可以随身携带一瓶洗手液),尤其在咳嗽或打喷嚏之后,烹饪食物或进食之前。
· 在病人用完杯子、盘子等餐具后及时清洗。
· 空调通风系统应注意清洗消毒。
· 病人在治疗期间(尤其是服用抗生素还没超过24小时的时候)尽量待在家里,不去公共场所包括学校,工作单位等地方,以免传染给其他人。
相关阅读:
主要参考资料:
Sore Throat. Centers for Disease Control and Prevention. August 30, 2019
Dan Jennifer M,Havenar-Daughton Colin,Kendric Kayla et al. StreptococcusRecurrent group A tonsillitis is an immunosusceptibility disease involving antibody deficiency and aberrant T cells.[J] .Sci Transl Med, 2019, 11: undefined.
Strep Throat: Diagnosis and Treatment. Mayo Clinic. September 28, 2018.
Vekemans J, Gouvea-Reis F, Kim JH, et al. The Path to Group A Streptococcus Vaccines: World Health Organization Research and Development Technology Roadmap and Preferred Product Characteristics. Clinical Infectious Diseases. September 1, 2019
PANDAS — Questions and Answers. National Institute of Mental Health. 2019
Strep Throat or Sore Throat? Best Ways You Can Tell. Cleveland Clinic. March 6, 2020
王亚莉, 孙丽娟, 刘桂兰. 儿童链球菌性咽炎的发病年龄、季节及诊治[J]. 人民军医, 2000(11):671-672.