 国家高新企业 | ISO9001认证
国家高新企业 | ISO9001认证 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com

谷禾健康
组胺是人体内的一种生物胺,最为人们所熟知的作用是作为过敏反应的介质,但也是神经系统、肠道、皮肤和免疫系统中重要的信号分子。
花粉之所以会引起人体过敏反应,并不是因为花粉本身,而是由于花粉颗粒携带了能引起过敏的抗原。接触过敏源后,体内的组织会释放组胺,作为一种神经递质,组胺会使毛细血管和微静脉的管壁通透性增加,导致局部组织水肿,造成皮肤发红、疹块;也会使气管平滑肌收缩,造成呼吸道狭窄,引起气喘、呼吸困难。
组胺主要由肥大细胞和嗜碱性粒细胞等免疫细胞产生和释放。一些细胞如树突状细胞或T细胞可以表达组氨酸脱羧酶,这是一种在刺激后合成组胺的酶。
尽管如此,一些食物中的微生物群和部分人体肠道微生物群也可以分泌组胺。表明组胺在肠道免疫调节中的潜在作用。事实上,最近的一项研究表明,组胺可以通过抑制肠道中白细胞介素18的产生来发挥抗炎作用。
组胺在免疫反应、神经传递和过敏反应中发挥着重要作用。在某些浓度范围内,组胺起着保护作用,对于维持健康状态至关重要。例如组胺可以刺激胃酸分泌,有助于消化;还会影响排便情况;组胺作为重要的神经递质,参与睡眠调节和体温调节。
然而,在较高浓度下,会导致包括组胺中毒和组胺不耐受或扩张血管,影响血压,导致免疫调节紊乱、胃肠道症状和神经系统疾病。组胺中毒是在食用被大量组胺污染的食物后发生的。如果个体由于基因突变而缺乏生物胺降解能力,或者正在服用单胺氧化酶抑制剂等抗抑郁药来减缓胺的降解,他们就会更容易出现组胺不耐受的症状。
组胺在体内与相应受体(H1、H2、H3、H4)结合而介导的各种症状。不同类型的组胺受体与该化合物之间的相互作用可能会引起多种影响,例如H1R主要介导过敏反应,而H2R具有抗炎作用,而H3R主要影响睡眠、认知障碍等精神健康。
肠道内的组胺对许多细胞过程的广泛影响会导致各种胃肠道疾病,包括食物过敏、肠易激综合征、炎症性肠病、结直肠癌等。谷禾将在本文带大家了解组胺在免疫及各种肠道疾病中的保护或致病作用。
组胺(C5H9N3)是一种重要的生物胺类神经递质,于20世纪初首次发现。从那时起,它的功能开始被逐渐发现并得到越来越详细的描述。
组胺存在于多种细胞类型中,是人体的关键信号分子,具有多种功能。例如作为神经递质或免疫反应调节剂。
拓展知识:组胺的发现
1903年,一位叫威廉·邓巴的医生证明了吸入花粉后的过敏反应并不是由花粉本身引起的,而是机体对花粉的反应引起的一种毒素的释放所造成的。
后来,亨利·戴尔于1910年在研究黑麦的毒性时,从麦角菌中提取出一种叫做组织胺的物质。他发现用组胺可以人工诱发荨麻疹。如果将组胺滴入气管,还会诱发哮喘发作。
★ 组胺的重要作用
介导过敏反应
组胺最被人熟知的是在过敏反应中的作用。例如在过敏性鼻炎、荨麻疹和血管神经性水肿等过敏性疾病中发挥重要的病理生理学作用。
当免疫系统对过敏原产生过度反应时,免疫细胞(如肥大细胞和嗜酸性粒细胞)会释放存储在细胞内的组胺。释放的组胺会结合到特定的受体上,引发一系列生理反应,例如瘙痒、肿胀、打喷嚏等。
扩张血管,影响血压
组胺对人心血管系统最突出的作用是扩张小血管。血管扩张使外周阻力降低,血压下降,并伴有潮红、头痛等症状。
组胺还增加毛细血管的通透性,使渗出增加,引起水肿,严重时甚至导致循环血量减少,可能引起休克。组胺对心脏的直接作用包括增强心肌收缩力、加快心率和减慢房室传导。
刺激胃酸分泌
首先,组胺可以刺激胃黏膜细胞中的H2受体,当组胺与H2受体结合时,会激活细胞内的信号转导通路,导致胃壁上的壁细胞释放胃酸。
其次,组胺还可以通过刺激嗜酸性细胞(胃窦细胞)来促进胃酸的分泌。嗜酸性细胞是胃黏膜中的一种细胞类型,它们包含大量的组胺。当胃黏膜受到刺激时,嗜酸性细胞会释放存储的组胺。释放的组胺通过与H2受体结合,刺激壁细胞分泌胃酸。
影响排便
一项研究中,发现细菌产生的组胺与小鼠结肠运动和粪便排出量增加有关,并且组胺受体拮抗剂治疗在很大程度上阻断了细菌组胺对结肠运动的影响。
收缩平滑肌
此外,组胺会诱导平滑肌细胞(包括支气管和肠道)收缩,哮喘患者对组胺比正常人敏感100~1000倍,组胺可引起支气管痉挛导致呼吸困难。组胺收缩胃肠平滑肌和子宫平滑肌还会引起痉挛性腹痛。
重要的神经递质
在中枢神经系统中,组胺作为一种神经递质,参与睡眠调节和体温调节等生理过程。组胺对感觉神经末梢有强烈的刺激作用,尤其对调节痛和痒的神经,该效应由H1受体所调节。
除此之外,有研究发现组胺还会影响伤口愈合、食欲和情绪等方面。
组氨酸是组胺的前体物质
组胺的主要细胞来源是肥大细胞和嗜碱性粒细胞。在细胞的高尔基体中,组胺是通过组氨酸脱羧酶将L-组氨酸氧化脱羧形成的,其辅助因子是吡哆醛(维生素B6)。
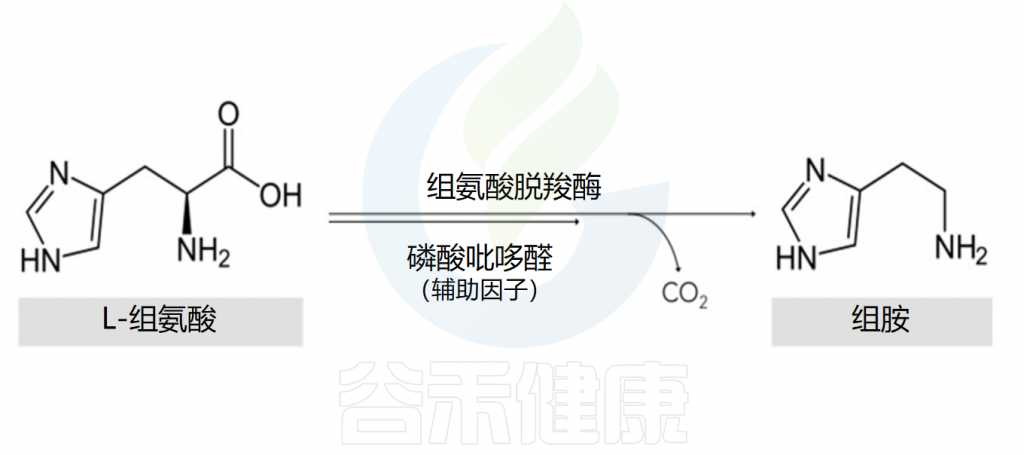
Comas-Basté O,et al.Biomolecules.2020
该反应的结果是组胺的形成,组胺随后与其他胺(如5-羟色胺)、蛋白酶、蛋白聚糖、细胞因子/趋化因子和血管生成因子一起储存在细胞质颗粒中,并在细胞致敏和脱颗粒后释放。
过敏时组胺会大量释放
肥大细胞的脱颗粒和组胺的释放主要是由于特异性抗原与FcRI受体结合以及对非免疫刺激(例如神经肽、补体系统的一部分、细胞因子、血小板活化因子)的反应。
IgE抗体是过敏性疾病期间肥大细胞脱颗粒的介质。IgE与其肥大细胞表面的高亲和力IgE受体的结合称为“致敏”。肥大细胞和嗜碱性粒细胞释放的组胺通过激活四种G蛋白偶联受体,即H1R、H2R、H3R(主要在大脑中表达)和H4R,发挥其生物活性。
细菌感染
某些细菌感染也可以引起组胺的释放。例如,胃幽门螺杆菌感染可以导致胃黏膜炎症,促使组胺释放,进而引发胃酸增多和溃疡等胃部疾病。
药物和化学物质
某些药物和化学物质也可以诱发组胺的释放。例如,非甾体抗炎药(如阿司匹林)和某些麻醉药物以及酒精可以引起组胺的释放,可能导致过敏样反应。
物理刺激
组胺释放也可由多种物理因素引起,如极端温度、创伤、摩擦等。这种情况下的组胺释放通常是局部性的,导致局部组织的充血和炎症反应。
运动和应激
剧烈运动、情绪激动和精神压力等也可以促使组胺的释放。这种情况下,组胺的释放通常是全身性的,可能导致血管扩张、心率增加和其他应激反应。
注:组胺也可以由其他细胞类型(例如胃肠嗜铬样细胞、组胺能神经元、树突状细胞、T淋巴细胞、血小板等)合成和释放。
食物和肠道微生物也是组胺的重要来源
一部分组胺通过食物进入人体或由肠道微生物产生。最受欢迎的富含组胺的食物是鱼和海鲜、发酵食品(如奶酪、葡萄酒、泡菜等)和一些蔬菜(如菠菜、茄子、番茄等)。
组氨酸主要在自溶或细菌过程中产生,因此高浓度的组胺主要存在于微生物发酵产物中。食品中生物胺形成的条件是游离氨基酸的可用性、脱羧酶阳性微生物的存在以及细菌生长和脱羧酶活性的条件。
影响细菌组氨酸脱羧酶活性的因素
细菌分泌脱羧酶受许多因素(例如,发酵碳水化合物、氧气或氯化物浓度的存在)调节。在酸性环境中,氨基酸脱羧酶活性的表达增加。
组氨酸脱羧酶活性较高的细菌种类有:
Morganella morganii,Eschericha coli, Hafnia alvei, Proteus vulgaris, Proteus milabilis, Enterobacter aerogenes, Raoultella planticola, Raoultella ornithinolytica, Citrobacter freundii, Pseudomonas fluorescens, Photobacterium damselae。其中一些细菌具有代谢组胺的能力。
我们将在下面的一个段落中展开讲述肠道中的组胺与微生物群。
在人体内,组胺降解主要有两种途径,涉及二胺氧化酶(DAO)或组胺-N-甲基转移酶(HNMT)。组胺降解酶缺失会导致组胺浓度过高甚至中毒,组胺不耐受患者就是组胺降解酶的酶活性降低或受到抑制,并且不足以灭活食物中的组胺并阻止其进入血液。
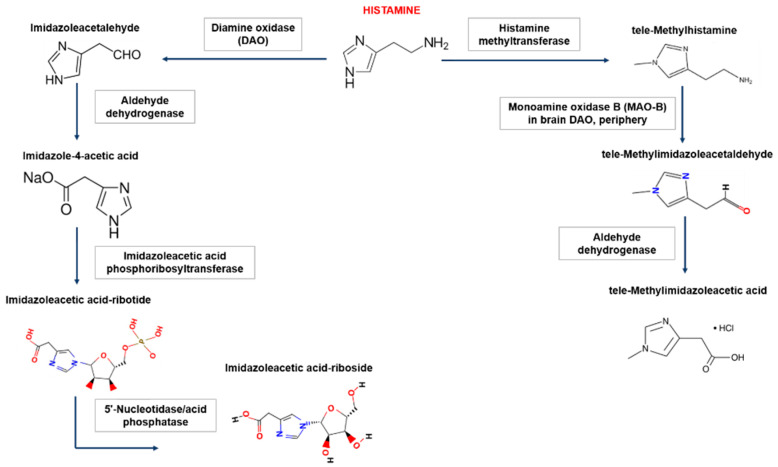
Shulpekova YO,et al.Nutrients.2021
组胺-N-甲基转移酶负责细胞内的组胺降解
组胺-N-甲基转移酶(HNMT)主要负责细胞内组胺的降解。HNMT在肾脏和肝脏以及脾脏、结肠、前列腺、卵巢、脊髓细胞、支气管和气管中的表达最高。一小部分组胺在HNMT的作用下转化为N-甲基组胺。
注:在原始形式中,约2%-3%的组胺被排泄。
二胺氧化酶负责细胞外的组胺降解
二胺氧化酶(DAO)是一种分泌蛋白,负责细胞外组胺的降解。DAO的最大活性记录在小肠、结肠、胎盘和肾脏中。DAO在细胞内囊泡中积累,然后进入细胞外空间,在那里降解组胺。绝大多数组胺通过DAO转化为咪唑乙酸。
保护身体免受组胺过高的侵害
二胺氧化酶执行“屏障功能”,从而限制组胺从肠道进入血液;组胺-N-甲基转移酶通过B族维生素和S-腺苷甲硫氨酸的参与使组胺甲基化,从而调节细胞内的组胺含量。
尽管二胺氧化酶和组胺-N-甲基转移酶这两种酶都存在于肠上皮中,但吸收组胺进入血流的主要障碍是 二胺氧化酶,组胺-N-甲基转移酶在此过程中仅发挥次要作用。在正常情况下,这种酶屏障足以防止组胺被吸收到血流中。
注:二胺氧化酶和组胺-N-甲基转移酶基因的多态性可能是组胺代谢个体差异的基础。在突触中,乙醛脱氢酶在组胺降解中发挥作用。
虽然健康人体内的组胺很快就会被二胺氧化酶降解,但即使在健康人体内,也可能会因摄入组胺含量高的食物(例如鲭鱼)导致血液中组胺浓度升高而出现严重症状——组胺中毒。
• 组胺中毒的症状
组胺中毒症状多种多样,可能包括口腔麻木、头痛、头晕、心悸、低血压、吞咽困难、脉搏微弱、荨麻疹、面部肿胀、潮红、呕吐、恶心和腹泻等。
组胺中毒的症状可能持续数小时或一天,但在极少数情况下,症状可能会持续数天。
• 组胺中毒的主要原因是食用鱼类和海鲜
不仅是鲭鱼,一些非鲭鱼(鲯鳅鱼、蓝鱼、沙丁鱼等)都含有大量组胺,此外发酵产品(奶酪、葡萄酒、罐头食品、腌制蔬菜和一些饮料)中组胺和血清素的含量也较高。
一项针对科学报告的分析显示,在98%的病例中,组胺中毒的原因是食用鱼类和海鲜,其余2%是由于食用奶酪等发酵食品。
鱼组织中的组胺是由多种细菌对游离组氨酸进行转化而产生的,这些细菌包括摩氏摩根菌(Morganellamorganii)、产气肠杆菌 (Enterobacter aerogenes), Raoultella planticola, Raoultella ornithinolytica和Photobacterium damselae。
鱼分解产生的其他物质会增强组胺的毒性并促进吸收
组胺中毒的发病机制不能仅用组胺的作用来解释。与口服等效剂量的纯组胺相比,鲭鱼毒性较高。还提出了其他机制,例如控制组胺的酶的抑制或增强、导致肥大细胞脱颗粒的物质的存在、其他组胺激动剂的存在。
鱼分解过程中产生的其他物质(尸胺和腐胺)会增强组胺的毒性,这些物质还会抑制肠道单胺氧化酶和二胺氧化酶,或从与粘膜粘蛋白的结合中释放组胺,促进其吸收。
组胺中毒后的干预及治疗
在生理值范围内。组胺中毒的病程通常是轻微的、自限性的、持续时间较短且不需要治疗。
对于严重的组胺中毒病例,需要进行治疗干预——支持性容量疗法和氧气疗法,并给予口服抗组胺药和支气管扩张剂。
组胺不耐受是由于组胺摄入量与机体清除能力不相称,导致组胺过度蓄积,并与相应的物质结合而出现症状的病理过程。
与组胺中毒不同,组胺中毒的严重程度与营养物质中组胺的含量成正比,组胺不耐受的发病机制与先天性或后天性缺乏中和组胺的酶有关。在健康患者中,肠上皮细胞具有由二胺氧化酶和组胺-N-甲基转移酶创建的酶屏障。该屏障可防止血液中外源性组胺的过度吸收。如果这些酶被抑制或减少,即使摄入少量的组胺也可能出现组胺不耐受的症状。
• 组胺不耐受的症状
组胺不耐受的神经系统症状包括头痛。除头痛外,其他重要症状包括弥漫性胃痛、绞痛、胀气和腹泻。
组胺不耐受的患者,在摄入组胺或酒精含量高的食物时或摄入后会出现流鼻涕、鼻塞等症状,极端情况下甚至会出现支气管哮喘发作、支气管收缩、咳嗽、喘息并伴有肺功能下降。
组胺不耐受患者还会出现皮肤瘙痒、发红、肿胀甚至荨麻疹。而患有组胺不耐受的女性会出现与月经周期相关的痛经和头痛。
• 影响组胺降解酶活性的因素
在胃肠道疾病(炎症性肠病、寄生虫感染、微生物菌群失调、代谢吸收不良)中,损伤的肠上皮细胞会减少二胺氧化酶的产生,或其他生物胺、酒精或药物也会抑制二胺氧化酶。
二胺氧化酶活性降低可见于慢性肾功能衰竭、病毒性肝炎、晚期肝硬化和慢性荨麻疹(一种典型的组胺相关疾病,对内源性组胺的耐受性降低)的患者。
二胺氧化酶降解能力下降还可能是由于缺乏其辅助因子、维生素B6、维生素C、铜和锌而导致的。
• 肠道微生物会影响组胺不耐受的发生
肠道微生物群也会影响组胺不耐受的发生。最近的研究表明,组胺不耐受可能是由肠道微生物群的改变引起的。肠道中大量的组胺分泌细菌可能会导致组胺不耐受。健康人体内双歧杆菌的数量较多。而在血清二胺氧化酶活性降低的人群中观察到变形菌属数量较多。
组胺不耐受人群存在肠道菌群失调
在组胺不耐受人群中观察到肠道菌群失调,与健康个体相比,与肠道健康相关的普氏菌科(Prevotellaceae)、瘤胃球菌(Ruminococcus)、粪杆菌(Faecalibacterium)和普拉梭菌(Faecablibacterium prausnitzii)的比例明显较低。组胺不耐受人群还具有显著更高丰度的组胺分泌细菌,包括葡萄球菌属和变形杆菌属、属于肠杆菌科的几个未识别属,以及产气荚膜梭菌和粪肠球菌。
需要注意的是,几项研究表明,即使在没有二胺氧化酶缺陷的个体中,大量的组胺产生细菌也会导致肠道内高水平组胺的积累、随后在血浆中的吸收以及不良反应的出现。
低组胺饮食
组胺不耐受疗法的基础是基于低组胺含量食物的消除饮食。一般来说,公认的饮食指南尚未制定;但是,建议避免食用富含组胺的食物如奶酪、油性鱼类和贝类,以及生发酵肉制品、腌菜、发酵豆制品、葡萄酒和啤酒、鸡蛋、巧克力和蘑菇。
避免食用易刺激组胺释放的蔬果
此外,应避免食用会刺激内源性组胺释放的蔬菜和水果(如菠菜、西红柿、柑橘类水果、草莓、茄子、鳄梨、木瓜、香蕉、猕猴桃、菠萝和李子)。


Kovacova-Hanuskova E,et al.Allergol Immunopathol.2015
补充二胺氧化酶
研究还发现补充二胺氧化酶可以改善组胺不耐受患者的生活质量。已开发出基于肠溶猪肾提取物的含二胺氧化酶食品添加剂。豆芽也被用作二胺氧化酶的来源,这种酶的活性是未发芽种子的250倍。
施用抗组胺药物
纠正组胺不耐受的药物方案基于使用组胺受体阻滞剂、肥大细胞膜稳定剂和其他具有抗组胺活性的药物。
在这方面,H1R拮抗剂是最有效的,特别是依巴斯汀。每天服用20毫克该药物,持续12周,46%的患者出现临床缓解。
一些生物活性物质有助于增强组胺降解
维生素C被用作纠正组胺不耐受的佐剂。每日剂量300-500毫克可增强组胺降解并抑制肥大细胞脱颗粒。
天然类黄酮(非瑟酮、山奈酚、槲皮素、芦丁和木犀草素)和活性生物碱小檗碱在体外抑制肥大细胞脱颗粒。这些都有助于减轻组胺不耐受。
虽然组胺含量过低的情况相对较少见,但也可能会对身体产生一些影响,包括:
• 伤口愈合减慢
组胺在人体中起着重要的调节作用,其能够帮助调节纤维细胞生长因子的生成,该成分可以加速局部肉芽的生长,帮助促进伤口的愈合。因此组胺含量较低时,伤口愈合能力也会减弱,速度会随之减慢。
• 消化不良
组胺可以通过刺激胃部,进而起到促进胃酸分泌的效果。若身体中没有组胺,则会导致胃酸减少,无法有效消化分解食物,进而引起消化不良的问题。
• 情绪不良
组胺还可以作为神经递质帮助调节中枢神经系统,而一旦没有组胺,则会影响中枢神经系统稳定性,引起睡眠异常、激素水平紊乱等情况,进而导致情绪不良。
• 血压升高
人体缺少组胺还会导致血压升高。因为组胺可以促进血管扩张,增加血管的通透性,所以具有降低血压的作用。若没有该成分,则血管会由于舒张能力减弱,因此出现血压升高的问题。
• 免疫力下降
组胺对免疫细胞,如吞噬细胞、T细胞、B细胞等,起到增强活性的功效,因此组胺还具有增强免疫功能的作用。若人体缺少该物质,则人体免疫力会下降,无法有效抵抗细菌、真菌等有害物质的侵入。
组胺对人体许多生理功能都可以起到积极作用,但是人体中的组胺也不能过量,否则容易导致过敏反应,出现头晕、皮肤瘙痒、胸闷等不适症状。
此种情况需及时就医,并且在医生的指导下服用抗组胺药物,例如盐酸西替利嗪片、氯雷他定片等药物,进行抗过敏治疗。
★ 组胺的免疫调节因受体的不同而存在区别
先天性和适应性免疫系统的细胞都可以被组胺调节。组胺的调节取决于它与组胺受体的四种亚型的结合,这些亚型按发现时间顺序命名——H1R-H4R,在多种细胞类型中差异表达,进而产生不同的作用。
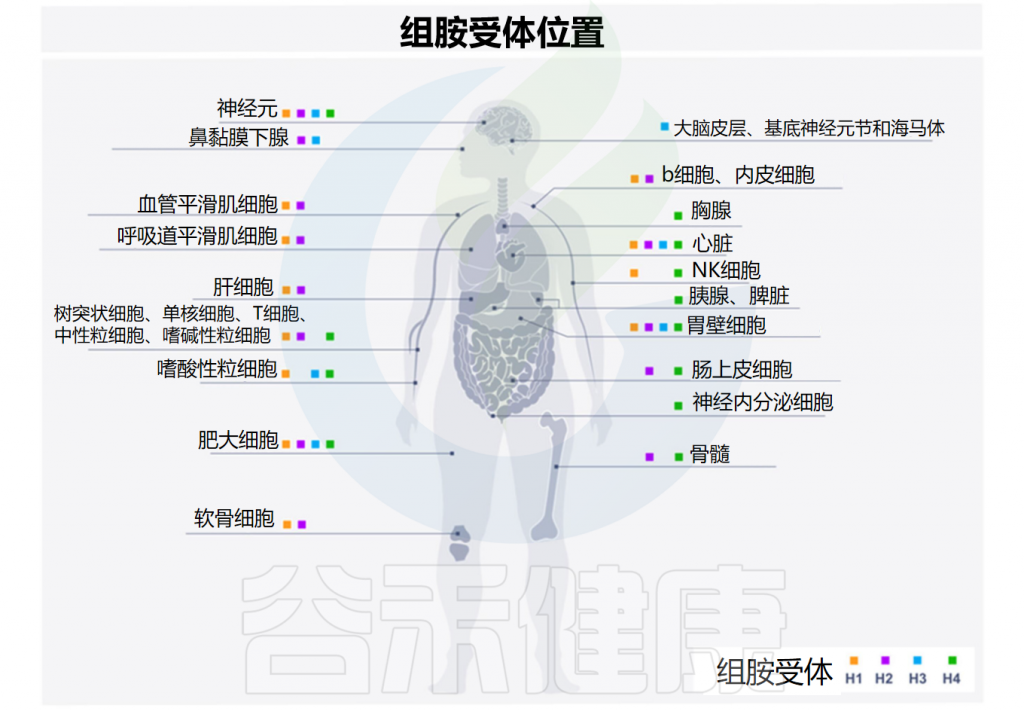
Smolinska S,et al.Metabolites.2022
1
H1R
H1R受体存在于几乎所有组织的内皮细胞和血管平滑肌细胞中(它们的密度在胃肠道中特别高),以及下丘脑、肾上腺髓质和免疫活性细胞(单核细胞、中性粒细胞、T细胞和B细胞)中。
• H1R受体介导的主要作用
H1R刺激的主要作用是炎症、全身血管舒张、血管通透性增加、支气管收缩、回肠收缩和昼夜节律周期调节。
外周H1R介导的影响包括鼻漏、支气管收缩、过敏反应、结膜炎和荨麻疹,而中枢相关的H1R影响包括食物和水摄入的调节、抽搐、注意力和睡眠调节。
• H1R是过敏反应的主要受体
IL-3、IL-4和组胺可上调H1R基因表达,而H1R激活导致许多与过敏性即时型超敏反应相关的特征,例如发红、瘙痒和肿胀。
例如小鼠模型中H1R的激活会诱导IFN(干扰素)产生增加,这与1型辅助性T细胞的增殖有关,并诱导促炎作用。
研究表明,瘙痒因子(例如神经生长因子、信号素 3A)的表达受组胺H1R的调节。在小鼠模型和特应性皮炎患者中,使用H1R拮抗剂可降低IL-31(白细胞介素-31)水平,这与瘙痒的发作有关。
2
H2R
与H1R类似,H2R的表达存在于多种组织和细胞中,包括脑、胃壁细胞、平滑肌细胞、T和B细胞、树突状细胞和心脏组织。H2R受体位于突触后,主要通过环腺苷单正膦(cAMP)传递信号并与Gαs偶联。
不同组胺受体下游的信号通路
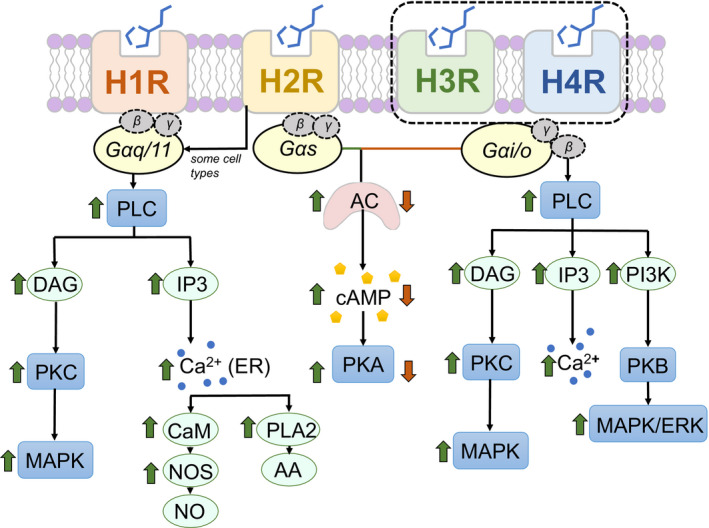
Sudarikova AV,et al.Physiol Rep.2021
H2R刺激的主要作用是外分泌(主要是盐酸)、心动过速、平滑肌细胞松弛、抗炎作用、抗体合成等免疫活动。
• H2R具有抗炎作用
在组胺与H2R结合期间,H2R刺激通过抑制单核细胞或巨噬细胞和肥大细胞产生IL-12、IFN-γ、TNF-α细胞因子,而IL-10分泌增加,从而引起抗炎作用。
• H2R影响对微生物的免疫反应
组胺(内源性和外源性)通过H2R显著改变对微生物的先天免疫反应。特别地,树突状细胞对微生物配体的反应被组胺以H2R依赖的方式显著改变。
H2R敲除的小鼠免疫系统紊乱以及胃缺陷(胃酸分泌减少),此外还观察到认知能力下降和伤害感受异常。
• 注意:不同组胺受体可能具有相反的作用!
H2R以与H1R不同的方式传输信号,H1R和H2R的激活对各种生物过程具有相反的影响。在T细胞介导的免疫反应中,H1R激活促进Th1极化,而H2R激活则抑制Th1极化。
在平滑肌收缩中也观察到H1R和H2R激活的相反作用。H1R和H2R拮抗剂分别抑制和加剧组胺引起的轻度哮喘患者的支气管痉挛。这些数据表明,组胺可能会产生相反的作用,具体取决于被激活的特定组胺受体。
3
H3R
• H3R主要存在于神经系统中
H3R受体在神经系统细胞中表达,特别是在大脑皮层,基底神经节神经元和海马体中。H3R位于含组胺神经元的突触前区域。它们的功能是调节组胺以及其他神经递质(如多巴胺、去甲肾上腺素、γ-氨基丁酸、乙酰胆碱和血清素)的合成和释放。
• H3R受体影响睡眠、认知障碍等精神健康
H3R受体表达和激活的变化在睡眠-觉醒周期障碍、注意力缺陷多动障碍、癫痫和认知障碍以及炎症的发展中发挥重要作用。
H3R缺陷小鼠表现出行为反应和运动的变化,以及伴有肥胖、食欲过盛以及瘦素和胰岛素水平升高的代谢综合征。
• H3R可能会促进炎症反应
H3R刺激可增加促炎活性以及免疫细胞呈递抗原的能力。H3R敲除也可导致神经炎症性疾病的严重程度和T细胞中IFN-诱导蛋白10的表达增加。
因此,组胺H3R拮抗剂的使用有可能用于预防或抑制炎症性疾病(例如呼吸系统疾病)的发展。
4
H4R
H4R受体是最近才发现的,它们的作用尚未完全了解。H4R主要存在于免疫细胞(嗜酸性粒细胞、嗜碱性粒细胞、肥大细胞、自然杀伤细胞、树突状细胞、单核细胞和T细胞)中,也存在于脾脏、胸腺、骨髓、胆管、胰腺、肠上皮细胞和神经内分泌细胞中。
• H4R会增强过敏和炎症反应
与其他类型的组胺受体相比,H4受体在中枢和周围神经系统中表达并不显著。H4R通过与蛋白质Gα/io相互作用介导,参与炎症和超敏反应的发展。
H4R介导的肥大细胞活化,促炎细胞因子和趋化因子IL-6、TNF-α、TGF-β1、RANTES、IL-8、MIP-1α和MCP-1均被表达。研究发现H4R激活显著增强结肠炎、放射性结肠炎、肠道缺血/再灌注损伤和过敏反应的炎症反应。
因此,选择性H4R阻滞剂的开发可能代表了治疗炎症性肠病的一种有前途的方法。
• H4R的激活还会导致瘙痒
H4R的激活已被证明会导致瘙痒。而H1R和H4R拮抗剂的联合治疗可能通过协同抑制瘙痒和皮肤炎症对慢性皮炎产生显著的治疗效果。
此外,H4R通过激活Th2细胞并产生 IL-31,可能引发过敏性皮炎的发生。H4R和H3R的激活增加了乙酰胆碱对肠道蠕动的影响。H4R受体还参与消化性溃疡的形成和癌变。
//小结
如前所述,组胺特异性受体的组织定位、功能和对组胺的亲和力不同。组胺调节广泛的代谢过程,具有促炎和抗炎作用,具体取决于受体亚型和受刺激细胞的类型。
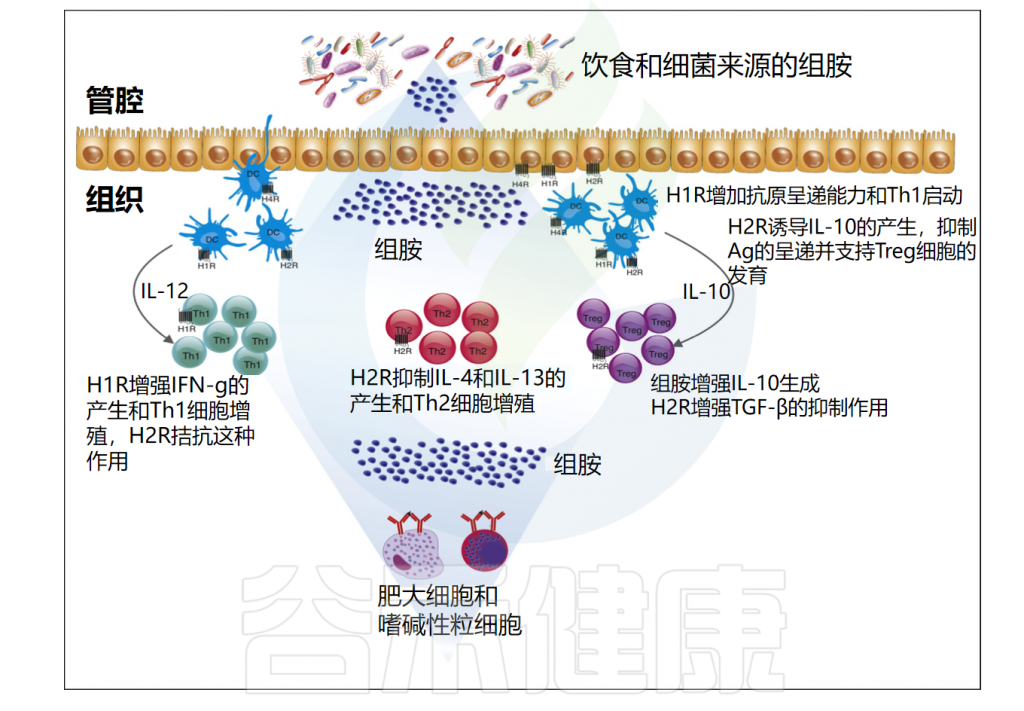
Barcik W,et al.Curr Opin Immunol.2017
组胺对免疫调节的各种作用似乎与其受体及其各自的细胞内信号的差异表达和调节有关。此外,这些受体对组胺的亲和力的差异在组胺和组胺受体药物配体的生物效应中发挥着关键作用。组胺受体在多种病理生理状况中发挥重要作用,是治疗过敏的有效靶点。
组胺因其在速发型超敏反应中的作用而广为人知。在胃肠道内,组胺以相对较高的浓度存在,特别是在炎症过程中。组胺水平的增加改变了宿主与微生物群的免疫相互作用,并导致体内平衡的破坏,导致许多难以应对的肠道疾病的发展。
★ 组胺的水平会影响肠道稳态
肠道中的组胺水平受到宿主过敏和炎症反应的影响,除了宿主微生物群的产生外,还会以某种方式改变降解或合成组胺的酶的活性及其饮食摄入量。
此外,在刺激产生组胺的免疫细胞时,可以增加内源性组胺的水平。所有这些都会影响肠道稳态,导致组胺积累,并影响特定疾病。组胺还可能对肠道寄生虫和细菌感染产生一定影响。
注:除H3R外,所有组胺受体都在人体肠道中表达。从量的角度来看,H4R表达的丰度明显低于H1R和H2R。
粘膜内的组胺
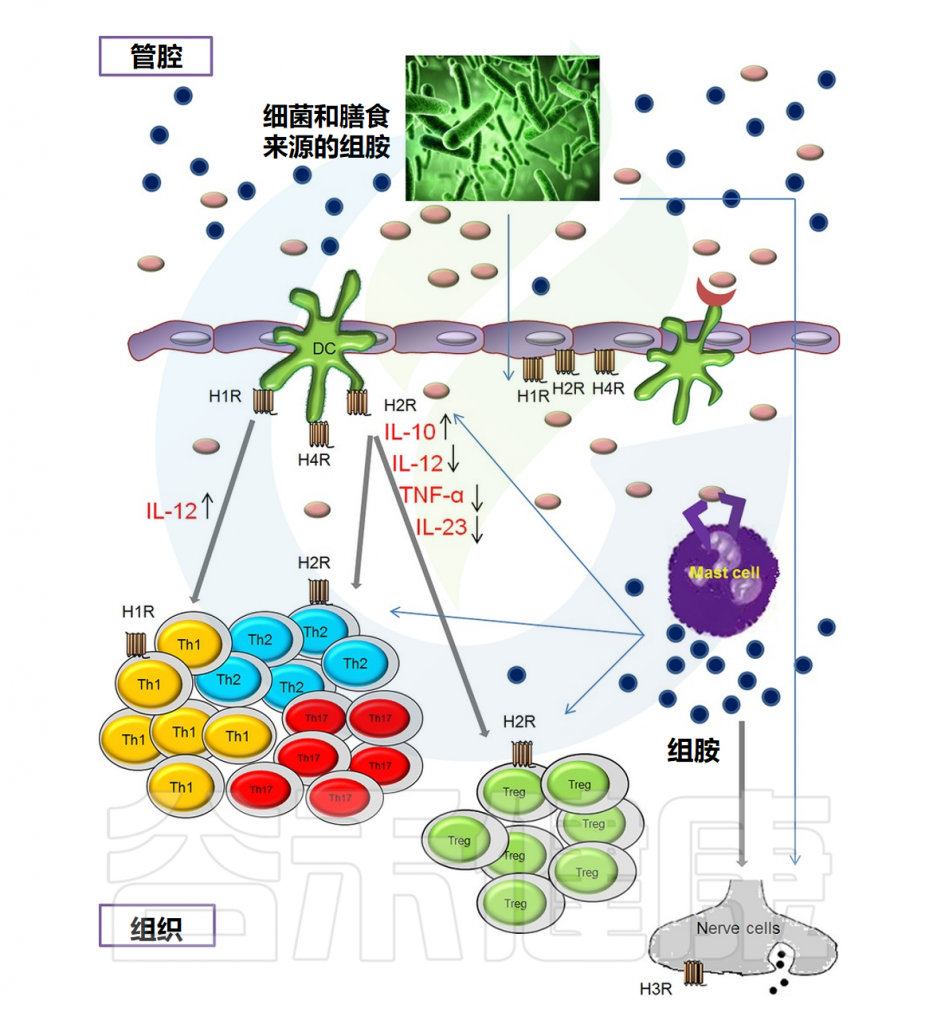
Smolinska S,et al.Allergy.2014
• 食物中的一些菌株会分泌组胺
除哺乳动物细胞外,还发现许多不同的细菌菌株能够在组氨酸通过组氨酸脱羧酶作用后分泌组胺。
最有力的证据就是那些能够在食品中分泌组胺的细菌。它们在奶酪、肉罐头、乳制品以及啤酒和葡萄酒发酵过程中产生组胺。鲭鱼中毒就是在储存或加工过程中处理不当,细菌代谢了鱼类中的组氨酸,导致组胺含量过高。
• 部分肠道微生物也会分泌组胺
迄今为止,对产生组胺细菌的研究主要集中在从食物样品中分离的菌株。肠道微生物群的组胺生成能力直到最近才被研究,数据仍然有限。
2021年发表的一项荟萃分析展示了人类肠道微生物组中具有假定组胺分泌能力的物种 ,其中许多属于广泛报道的组胺产生属,例如摩根菌属(Morganella),乳杆菌(Lactobacillus),葡萄球菌属(Staphylococcus), Photobacterium和巴氏梭菌(Clostridium)。
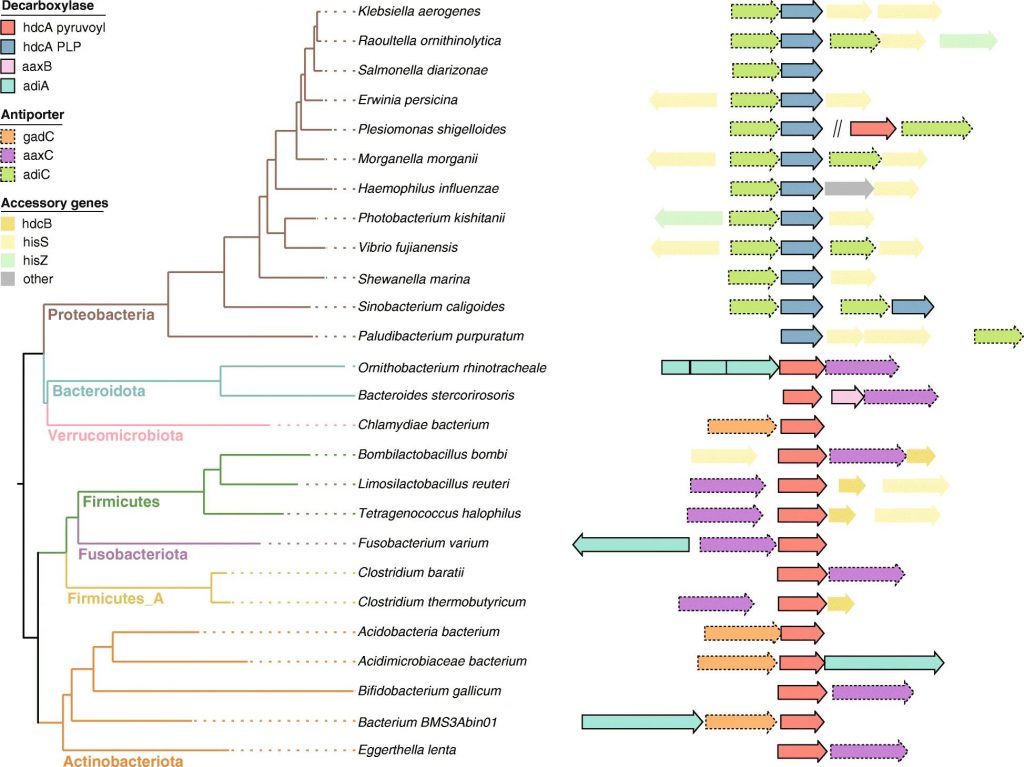
Mou Z,et al.BMC Genomics.2021
• 一些细菌具有组氨酸脱羧酶活性,也可能产生组胺
需要注意的是,一些具有组氨酸脱羧酶活性并与组胺中毒有关的细菌,可能也是潜在的组胺产生细菌。包括:Morganella morganii,
Eschericha coli,
Hafnia alvei,
Proteus vulgaris,
Proteus milabilis,
Enterobacter aerogenes,
Raoultella planticola,
Raoultella ornithinolytica,
Citrobacter freundii,
Pseudomonas fluorescens,
Photobacterium damselae。
证据表明细菌衍生的组胺具有多种影响,例如对宿主健康和食品安全。
• 抑制了促炎细胞因子的分泌
初步体外研究表明,组胺抑制人单核细胞衍生的树突状细胞中趋化因子和促炎细胞因子的分泌。
小鼠研究表明,给予分泌组胺的鼠李糖乳杆菌具有抗炎作用,各种白细胞介素和肿瘤坏死因子α的分泌减少。这种作用在缺乏组胺2受体的动物中消失,表明微生物群衍生的组胺可能具有免疫调节作用。
• 组胺的含量对于免疫效果至关重要
与鼠李糖乳杆菌相比,另一种乳杆菌能够分泌大约100倍多的组胺,服用这种乳杆菌会导致动物体重减轻和健康状况恶化。谷禾认为,微生物分泌的组胺量可能是决定其作用性质的关键。
最近的研究还表明,肠道中细菌释放的组胺不仅会引起宿主免疫系统的局部调节,而且还会在远处的粘膜部位(例如肺部)产生免疫学后果。例如成年哮喘患者肠道中分泌组胺的细菌丰度有所增加。
由于许多食物中含有组胺,一部分肠道微生物群也可以产生组胺,研究发现组胺在肠道疾病中可能发挥多种作用,下面讲述了一些与组胺相关的肠道疾病,组胺在其中发挥着有益或有害的作用。
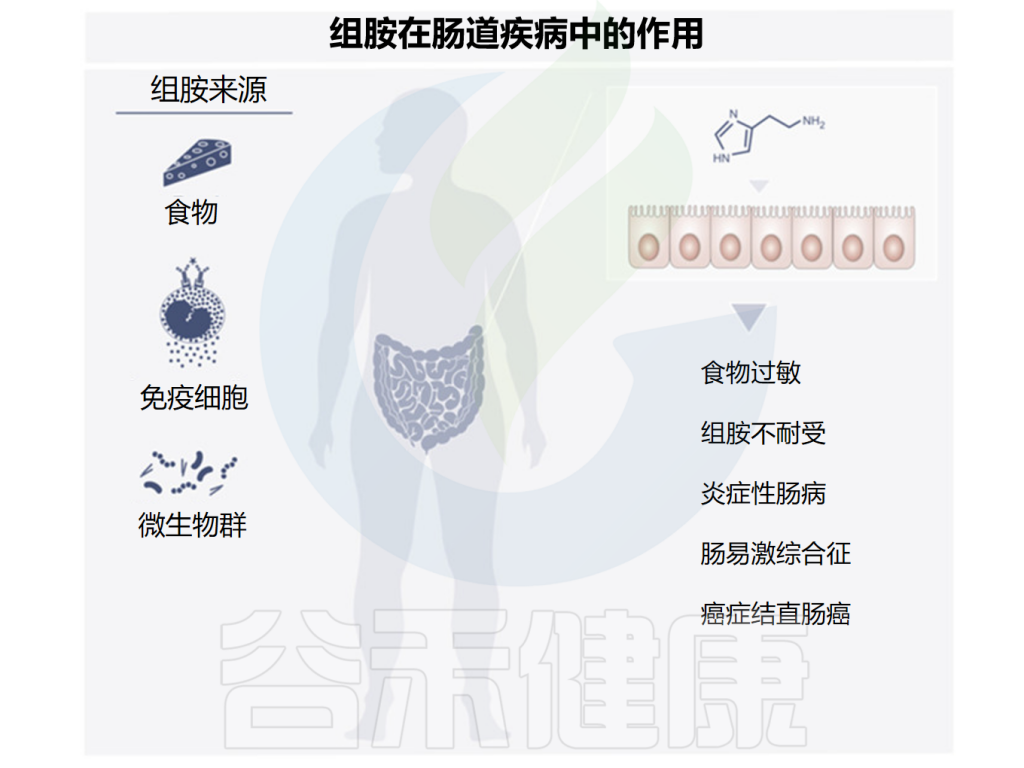
Smolinska S,et al.Metabolites.2022
消化道是接触大量不同分子的地方,这些分子中的一部分是潜在的过敏原,可能从而引起食物过敏。食物过敏可表现为轻度和重度症状,最严重的可能危及生命。
拓展:常见的食物过敏症状
食物过敏的症状表现在呼吸系统、消化系统、心血管系统和皮肤系统等。
皮肤反应:皮肤反应是最常见的食物过敏症状之一。它可以表现为皮疹、荨麻疹、瘙痒、红肿、水肿等。这些反应通常发生在口腔、面部、颈部和四肢等部位。
呼吸道症状:食物过敏还可以引起呼吸道症状,包括鼻塞、流涕、打喷嚏、喉咙痒、咳嗽、喉咙紧闭感和哮喘。严重的过敏反应可能导致呼吸困难和哮喘发作。
消化系统症状:食物过敏可以引起消化系统症状,包括腹痛、腹胀、恶心、呕吐和腹泻。这些症状还可能与肠道炎症反应、肠道收缩有关。
循环系统症状:在严重的食物过敏反应中,可能出现循环系统症状,如低血压、心悸、头晕和昏厥。这些症状是由于过敏反应导致血管扩张和血压下降。
全身症状:某些人可能出现全身性症状,如疲劳、焦虑、情绪波动和体重下降。这些症状可能与食物过敏引起的炎症反应和免疫系统的激活有关。
• 食物过敏时组胺分泌增加
IgE依赖性食物过敏是免疫系统紊乱的结果,使耐受性丧失。这导致将温和的食物抗原识别为病原体。组胺受体参与食物过敏的发展。研究表明,在人类中使用H2R拮抗剂会增加针对食物抗原的IgE的产生。在Th2细胞的刺激下,IgE与效应细胞(肥大细胞和嗜碱性粒细胞)上的Fcε受体结合。由于效应细胞的激活,组胺以及其他介质被释放。
在食物过敏受试者中,组胺分泌增加和肥大细胞数量增加已得到充分证明。嗜碱性粒细胞释放的组胺与皮肤点刺试验和食物激发呈正相关。与非过敏患者相比,食物过敏患者抗IgE介导的肥大细胞组胺释放增加。
此外,将食物过敏患者的活检与抗IgE(人类)抗体或过敏原一起孵育,会导致组胺释放增加9倍。
• 食物过敏的治疗
由于食物过敏的发生率不断增加,已经进行了大量研究以开发新的治疗和预防策略。严格避免食物过敏原是管理IgE介导的食物过敏的长期策略。
关于食物过敏发病机制的各个阶段也有许多研究,例如对Th2通路的影响、阻断IgE、抑制效应细胞和微生物治疗。长期免疫耐受应该是治疗食物过敏最理想的效果。
口服免疫疗法是食物过敏的发展治疗方法之一。它包括以每2-4周增加一次的剂量向患者施用过敏原,直到达到最大维持剂量。这个过程的结果是发展对食物的耐受性。该方法已用于对牛奶、鸡蛋、小麦、花生、坚果和贝类的食物过敏。
目前正在研究表皮和舌下免疫疗法。对牛奶和鸡蛋过敏的表皮免疫疗法也进行了临床试验。
炎症性肠病是特发性、慢性复发性肠道疾病。溃疡性结肠炎和克罗恩病是两种主要临床表现。
在克罗恩病中,炎症出现在弥漫性病变中,这些病变遍布消化道并深入穿透肠壁,可能影响所有层。相反,溃疡性结肠炎的炎性病变从直肠开始,向上但不超过结肠,并在黏膜浅表处保持。克罗恩病导致整个胃肠道的透壁性炎症,但其特征是模式不连续。与炎症为浅表的溃疡性结肠炎相比,溃疡主要局限于结肠粘膜。
• 炎症性肠病患者黏膜组胺水平升高
这两种疾病的发展都是遗传易感患者宿主免疫系统、肠道微生物群和环境因素之间复杂相互作用的结果。
炎症性肠病患者的黏膜组胺水平(而非血浆水平)升高。在患者尿液中发现与疾病活动度相关的N-甲基组胺水平升高。当受到抗原刺激时,源自活动性克罗恩病或溃疡性结肠炎切除结肠的肥大细胞能够释放比正常结肠更多的组胺。
• 炎症性肠病患者的组胺通路被破坏
克罗恩病和溃疡性结肠炎患者的组胺信号通路均被破坏,研究分析显示。炎症性肠病患者的组胺受体表达和功能活性发生改变。
在结肠炎模型中,H2R的阻断导致更严重的炎症性疾病。组胺主要抑制IFN-γ和TNF-α的分泌,这些细胞因子的基因表达与溃疡性结肠炎患者的H4R和H2R表达呈正相关。
发炎黏膜中组胺-N-甲基转移酶(HNMT)表达降低,二氨基氧化酶(DAO)多态性与炎症性肠病风险增加有关。使用H2R拮抗剂会增加克罗恩病患者的风险。
注:在小鼠结肠炎模型中,缺乏H2R或使用非莫替丁(H2R拮抗剂)抑制H2R的T细胞转移可加速体重减轻并增加疾病严重程度。
• 炎症性肠病的治疗
在许多情况下,获得缓解的唯一选择是根治性手术,切除发炎区域。潜在地,使用H1R和H4R拮抗剂同时使用H2R激动剂可能对炎症性肠病患者有益。
炎症性肠病患者还可接受抗炎药、类固醇、抗生素、氨基水杨酸盐治疗,或使用英夫利昔单抗(抗 TNF-α)进行生物疗法。
肠易激综合征是一种与腹部不适或疼痛有关的慢性疾病,其中吃的食物是更严重症状的触发因素。一些证据表明,肠易激综合征中肠道菌群发生了改变,这种改变会破坏黏膜的免疫应答。
• 内源性组胺与肠易激综合征的严重程度相关
研究显示,超过一半的患者因食用释放组胺的食物或富含生物胺的食物而出现胃肠道症状。内源性组胺的水平与肠易激综合征患者症状的严重程度绝对相关。活化的肥大细胞产生更多的组胺,这与肠易激综合征患者的腹痛相关。肠易激综合征患者的黏膜上清液的组胺含量高于健康受试者的上清液。
组胺水平更高,组胺受体表达也更高
肠易激综合征患者中组胺受体H1R和H2R的表达水平上调。我们推测:伴有组胺分泌或含组氨酸脱羧酶细菌的菌群失调可能与肠易激综合征的发生和加重有关。
给予特定微生物具有治疗作用,这也可能是微生物群变化导致疾病的原因。肠易激综合征没有特效治疗方法,减少炎症的药物正在使用中。
结直肠癌是第三常见癌症,也是癌症相关死亡的重要原因。与一般人群相比,炎症性肠病患者发生结直肠癌的终生风险会增加。
• 组胺可能具有潜在的抗肿瘤作用
肠道微生物群在结直肠癌中的作用已在谷禾之前的文章中详细描述过。而特定的肠道微生物代谢物可能与结直肠癌的病因有关。组氨酸脱羧酶缺乏已被证明通过CD11b+Gr-1+未成熟髓系细胞的积累促进炎症相关的结直肠癌,表明组胺具有潜在的抗肿瘤作用。
几种益生菌菌株,包括长双歧杆菌(Bifidobacterium longum)、嗜酸乳杆菌(Lactobacillus acidophilus NCFM)和鼠李糖乳杆菌GG,在结肠癌的小鼠模型中显示出有益作用。这些产生组胺的益生菌减少了结肠肿瘤的数量和大小。
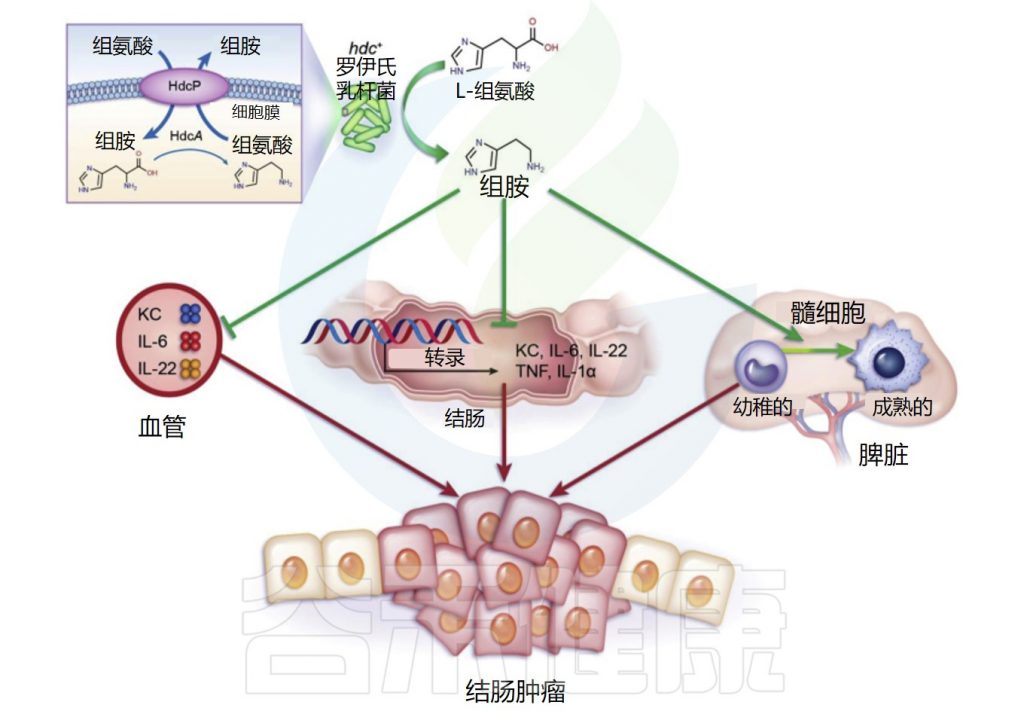
Gao C,et al.Am J Pathol.2017
罗伊氏乳杆菌(L. reuteri)抑制结肠粘膜中IL-22、IL-6、tnf-α和IL-1α 基因的表达,并减少血浆中促炎、癌症相关细胞因子、角质形成细胞趋化剂、IL-22和IL-6的数量。
此外,不能产生组胺的等基因组氨酸脱羧酶(HDC)缺陷罗伊氏乳杆菌突变体不能抑制致癌作用,这表明共代谢物组胺在抑制慢性肠道炎症和结直肠肿瘤发生中具有重要作用。
• 结直肠癌患者组胺含量和活性增加
在结直肠癌患者的结肠黏膜中,组氨酸脱羧酶活性和组胺含量均高于正常样本。在实验诱导的结直肠癌小鼠中,与野生型小鼠相比,组氨酸脱羧酶的缺失导致肿瘤发生增强,这也表明组胺具有抑制结直肠肿瘤发生的作用。
• 注意:过高的组胺含量可能对癌症不利!
需要注意的是,已发现肥大细胞在结肠癌中含量丰富,并促进小鼠化学诱导的结直肠癌的癌变,并且与人类结直肠癌患者的不良预后有关。与组胺通过H4R的促炎作用类似,H4R表达的缺失也导致小鼠化学诱导的致癌作用减少。
组胺作为一种重要信号分子,主要因其在诱导过敏症状中的作用而被识别,但它也参与非过敏性炎症反应。
组胺是肠道稳态的重要调节剂。通过增强分泌和蠕动,组胺促进潜在有毒物质的快速清除。这种生物胺对于肠道细菌的生存也至关重要。与健康个体相比,组胺不耐受患者的肠道菌群失衡或失调。
在某些浓度范围内,组胺起着保护作用,对于维持健康状态至关重要。然而,由于先天性或后天性缺乏组胺降解酶,以及肠道肥大细胞过度增生和过度活跃,使组胺浓度较高,会导致粘膜炎症性疾病,产生腹泻和腹痛。增强H2R表达或其细胞内信号,同时降低H1R和 H4R活性是提高粘膜免疫力的合理方法
组胺不耐受的现代治疗方法包括避免高组胺食物的摄入、影响组胺水平的药物(H1R阻滞剂、肥大细胞膜稳定剂和米氮平)和补充天然成分(维生素C、类黄酮、二氨基氧化酶强化补充剂和益生菌) 。
与此同时,使用具有释放组胺潜力的肠道微生物群提供了一种新的治疗视角。
主要参考文献
Smolinska S, Winiarska E, Globinska A, Jutel M. Histamine: A Mediator of Intestinal Disorders-A Review. Metabolites. 2022 Sep 23;12(10):895.
Sánchez-Pérez S, Comas-Basté O, Duelo A, Veciana-Nogués MT, Berlanga M, Latorre-Moratalla ML, Vidal-Carou MC. Intestinal Dysbiosis in Patients with Histamine Intolerance. Nutrients. 2022 Apr 23;14(9):1774.
Shulpekova YO, Nechaev VM, Popova IR, Deeva TA, Kopylov AT, Malsagova KA, Kaysheva AL, Ivashkin VT. Food Intolerance: The Role of Histamine. Nutrients. 2021 Sep 15;13(9):3207.
Krell T, Gavira JA, Velando F, Fernández M, Roca A, Monteagudo-Cascales E, Matilla MA. Histamine: A Bacterial Signal Molecule. Int J Mol Sci. 2021 Jun 12;22(12):6312.
Mou Z, Yang Y, Hall AB, Jiang X. The taxonomic distribution of histamine-secreting bacteria in the human gut microbiome. BMC Genomics. 2021 Sep 26;22(1):695.
Gao C, Ganesh BP, Shi Z, Shah RR, Fultz R, Major A, Venable S, Lugo M, Hoch K, Chen X, Haag A, Wang TC, Versalovic J. Gut Microbe-Mediated Suppression of Inflammation-Associated Colon Carcinogenesis by Luminal Histamine Production. Am J Pathol. 2017 Oct;187(10):2323-2336.
Kovacova-Hanuskova E, Buday T, Gavliakova S, Plevkova J. Histamine, histamine intoxication and intolerance. Allergol Immunopathol (Madr). 2015 Sep-Oct;43(5):498-506.
Barcik W, Wawrzyniak M, Akdis CA, O’Mahony L. Immune regulation by histamine and histamine-secreting bacteria. Curr Opin Immunol. 2017 Oct;48:108-113.
Smolinska S, Jutel M, Crameri R, O’Mahony L. Histamine and gut mucosal immune regulation. Allergy. 2014 Mar;69(3):273-81.

谷禾健康
罗氏菌属是共生细菌的一部分,在世界各地的人群中都有代表,占健康肠道细菌总数的 2-31%(谷禾数据库)。产生短链脂肪酸,特别是丁酸,影响结肠运动,具抗炎特性。


罗氏菌属(Roseburia),专性革兰氏阳性厌氧菌, 轻微弯曲,杆状,并通过多个亚末端鞭毛运动。
罗氏菌属包括5种:

罗氏菌属代谢膳食成分,刺激其增殖和代谢活动。
罗氏菌属可以分泌各种分子,与宿主和消化道的其他细菌相互作用。
罗氏菌属可以改善肠道生物多样性,提高葡萄糖耐受性,帮助减肥,使结肠细胞恢复活力。
罗氏菌属的失调(过少)可能影响多种代谢途径,并与多种疾病相关(包括肠易激综合征、肥胖、2型糖尿病、神经系统疾病、过敏、肝病等)。
Roseburia也可以作为症状性病理(如胆石形成)的生物标志物,或作为益生菌修复有益菌群。
研究人员利用16S rRNA测序技术研究早产儿肠道菌群的多样性,并对早期肠道定植模式进行了监测。在新生儿中没有发现Roseburia,但在母乳中发现了,可能通过食用母乳获得。
Roseburia在老年人中降低,提示衰老可能导致肠道菌群的改变。 相反,与较年轻的老年人相比,百岁老人的肠道菌群中有更丰富的Roseburia。
罗氏菌产生短链脂肪酸(乙酸,丙酸,丁酸),分解不可消化的碳水化合物。短链脂肪酸在碳水化合物和脂肪等重要营养素的代谢中发挥重要作用。
典型的Roseburia菌株特别喜欢生产高水平的丁酸盐。这些化合物通常参与能量产生,可以保护肠道免受病原体和疾病的侵害。
目前,发现只有Roseburia inulinivorans产生丙酸,但不是从葡萄糖中产生的。在Roseburia中,乙酸辅酶a转移酶是进行丁酸合成最后一步的主要酶。丁酸盐的形成可通过底物水平的磷酸化和质子梯度导致肠上皮能量产生和细胞反应调节。丁酸是罗氏菌属与寄主相互作用的关键因子。
前面小节我们知道,Roseburia从可发酵的膳食碳水化合物中产生了大量的丁酸盐。R. intestinalis主要寄生在粘蛋白层,并确保丁酸盐的生成。Roseburia作为一种高产丁酸菌,可能对控制炎症过程,尤其是肠道炎症过程具有重要作用。

谷禾健康

我们知道,肠道菌群在调节肠道生理中起着不可或缺的作用。最新研究发现,肠道真菌与宿主的健康和疾病有关。
细菌和真菌对免疫系统的作用非常相似,肠道细菌可以影响肠道真菌,如在某些情况下,大肠杆菌的超级感染会增强白色念珠菌的毒力。
肠道真菌不仅会影响肠道功能,还会影响其他重要肠外器官的生理功能,例如肝,肺和脑。
本文阐述了肠道真菌在肠道,肺,肝,肾,胰腺和脑功能调节中的重要性,并提出了将肠道真菌应用于减轻/治疗人类疾病的可能性。
最近,真菌在胎粪中被发现,表明肠道真菌的定植从出生时就开始了。(然而,由于缺乏直接证据和胎粪生物量低,很难忽视环境因素的影响。为了得到更有说服力的结论,迫切需要能够模拟整个妊娠过程的新模型和先进的检测技术。)
在新生儿肠道中,真菌的α多样性从出生到2岁一直持续增加,而β多样性在10天的婴儿中达到峰值。
在10日至3个月大的婴儿中,汉逊德巴利酵母Debaryomyces hansenii和胶红酵母Rhodotorula mucilaginosa是最丰富的真菌,而在1-2年后,肠道真菌群的组成发生了变化,其中酿酒酵母S. cerevisiae成为最丰富的真菌,而念珠菌属Candida spp.开始减少。
此外,在10天至3个月的婴儿中未检出青霉菌,但在1- 2岁的婴儿中可检出。
囊泡菌门Cystofilobasidium sp.子囊菌门Ascomycota sp.和单枝菌门Monographella sp. 仅在1- 2岁中检测到。之后,子囊菌门、接合菌门、担子菌门主导健康肠道真菌群。
念珠菌是人类和其他几种动物胃肠道和其他粘膜表面最普遍和丰富的真菌。
总的来说,肠道真菌的定殖和组成的研究还处于起步阶段。
肠道真菌在新生儿出生后立即在肠道内定居,其组成可能受到分娩方式、出生胎龄、婴儿喂养方式、母亲饮食、环境和宿主遗传等因素的影响。
影响肠道真菌群组成的因素

Wu X et al., Microbiome. 2021
分娩方式和孕妇的益生菌暴露
出生时健康的肠道菌群定植受分娩方式(自然分娩或剖宫产)的影响。自然分娩的婴儿更有可能从产妇生殖道获得真菌(例如白色念珠菌),而剖宫产后出生的婴儿更有可能从产妇的皮肤和周围环境获得真菌。
除了分娩方式外,胎龄和母亲的益生菌暴露量还决定了婴儿肠道菌群的组成。然而,在298对母亲-后代受试者中,婴儿抗生素或母体益生菌的递送和/或使用类型对肠道真菌的操作分类单位(OTUs)的丰度影响很小。这种差异可能源于所分析的样本,因为他们选择的都是参与同一项研究的母亲-子女对。
饮食营养
饮食是决定肠道真菌组成的决定因素之一。甚至有人提出,口腔和饮食中的真菌来源可以解释健康受试者粪便中存在的所有真菌,这表明饮食对肠道真菌组成有很大的影响。
有趣的是,由于西方饮食的脂肪和碳水化合物含量高,具有引发代谢综合症的高风险,并且已经显示出它可以诱导人肠道真菌结构的改变。例如,高脂肪饮食会降低小鼠肠道中S. cerevisiae的丰度。
猪体内梅奇酵母属Metschnikowia、革菌属Tomentella、Loreleia的丰度与短链脂肪酸相关;短链脂肪酸与人体内曲霉属真菌Aspergillus的肠道丰度呈负相关。
此外,富含碳水化合物的饮食与肠道念珠菌的丰度呈正相关。
同样,在健康志愿者中,高蛋白饮食与产甲烷短杆菌和念珠菌的丰度呈负相关。
有趣的是,酿酒酵母S. cerevisiae具有氨基酸转运蛋白,某些氨基酸如γ-氨基丁酸(GABA)和瓜氨酸,是酿酒酵母的重要氮源;因此,饮食中的氨基酸可能对肠道真菌的组成有深远的影响。
此外,亮氨酸代谢副产物2-羟基异己酸在72 mg/mL时具有较低的抑菌活性,可抑制假丝酵母菌丝的形成。
人类饮食中的特定化学物质,例如开心果和杏仁的植物化学物质,也与青霉菌和念珠菌属的含量呈负相关。
总之,检查饮食控制是否有可能减轻真菌感染是很重要的。如果该策略有效,那么对免疫抑制患者预防和控制继发感染可能特别有益。
其他因素
环境还能够触发肠道真菌的变化。
有趣的是,从杰克逊实验室的小鼠和服务部(JAX)获得的C57BL / 6J小鼠和在威尔·康奈尔医学(WCM-CE)处繁殖的小鼠的肠道真菌组成不同,分别以担子菌纲和子囊菌为主。而且,当SPF小鼠“野化”为野生状态时,它们的肠道真菌会显着增加。
季节是改变肠道真菌的另一个因素,尤其是真菌的α多样性。
性别和代谢紊乱(富营养,超重和肥胖)也会改变肠道真菌。例如,西藏猕猴的雌性与雄性有不同的菌群。
在肥胖的人类个体中观察到酵母数量增加,而富营养和超重的人类个体具有更多的丝状真菌。肠道念珠菌属仅在哺乳动物物种中发现。因此,肠道真菌可能在某种程度上因物种或基因型而异。
总体而言,肠道真菌受到内部和外部因素的影响。
这些因素不是独立的
也就是说,季节和环境与哺乳动物,特别是野生动物赖以生存的食物有关。环境也影响宿主接触潜在的致病或非致病微生物。
此外,不同物种有不同的遗传背景,更不用说它们的食物。
随着婴儿的进一步成长,他们将接受多种饮食,并暴露于复杂的环境和刺激下,例如yao物,性激素等。因此,必须系统地、相互关联地认识这些因素,不应过分强调每一个因素的单独作用。
与肠道细菌相似,肠道真菌高度多效性,调节宿主的各种生理功能。
目前对肠道真菌群对免疫反应途径和细胞网络的影响的认识:
肠道真菌对肠道免疫的影响
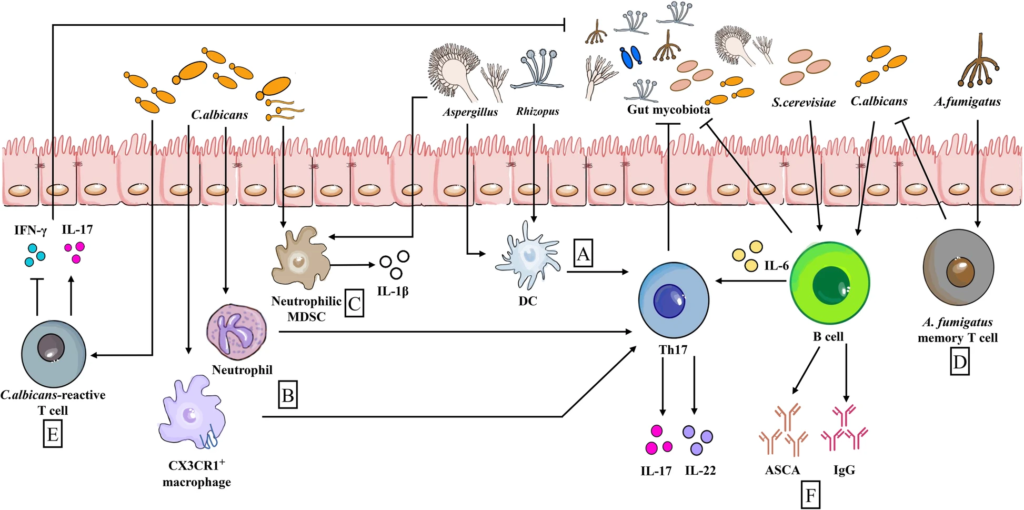
Wu X et al., Microbiome. 2021
(a) 当由曲霉属真菌Aspergillus和根霉属菌Rhizopus触发时,DCs促进Th17反应
(b) CX3CR1+巨噬细胞和中性粒细胞通过诱导Th17反应,产生高水平的IL-17和IL-22,有利于早期念珠菌控制。
(c) 同样,入侵的白色念珠菌和曲霉菌触发中性粒细胞MDSCs和IL-1β的产生。
(d)烟曲霉菌(A.fumigatus)记忆T细胞显示交叉反应白色念珠菌,因为他们有一个共享的TCR序列
(e) 同样,白色念珠菌活性T细胞通过产生IL-17与其他肠道真菌发生交叉反应
(f) 来自B细胞的抗酿酒酵母菌抗体ASCA和免疫球蛋白G(由白色念珠菌或酿酒酵母刺激)具有抗肠道真菌的作用。
除上述真菌成分和真菌代谢物,提取物和分泌物外,次生代谢物还负责影响宿主体内稳态。
表2 真菌衍生的化合物及其功能

Wu X et al., Microbiome. 2021
产生次级代谢物的各种基因簇表明,真菌通过复杂的途径产生次级代谢物,具有巨大的结构和功能多样性。
值得注意的是,真菌次生代谢产物在真菌疾病和合成生物学方面具有无限的潜力;它们也是抗生素和免疫抑制yao物的大量来源,因为它们具有靶向或干扰真菌和/或细菌的能力。
然而,真菌的一些次生代谢产物,包括黄曲霉毒素和柠檬酸,具有较强的肝毒性和/或肾毒性。
小鼠长期抗真菌治疗后肠道真菌的紊乱使结肠炎恶化,甚至使过敏性气道疾病恶化,肠道真菌组成失衡可能与肠道和肠外疾病有关。
肠内和肠外疾病与肠道真菌群的关系

Wu X et al., Microbiome. 2021
肠道真菌和肠道疾病
具体来说,健康的肠道真菌主要由几种丰富的共生真菌组成。肠道真菌可能是条件致病菌的贮存库。
炎症性肠病 IBD
炎症性肠病(IBD),包括溃疡性疾病(UC)和克罗恩氏病(CD),与肠道真菌失调有关。
与健康儿童相比,IBD儿童的粪便样本显示出较低的真菌多样性,而IBD样本(72.9%)的念珠菌属丰富度比健康对照组(32.9%)高两倍。
这些结果与溃疡性疾病和克罗恩氏病相关的人类白念珠菌肠道定植的报道一致。此外,白色念珠菌在IBD发作时比缓解时增加。
限制性马拉色菌是一种常见的皮肤常驻真菌,它与克罗恩病的发病机制有关,特别是在CARD9 (S12N)中携带IBD连锁多态性的患者中,限制性马拉色菌的定植加剧了DSS诱导的小鼠结肠炎的严重程度。
这项研究表明,除了白色念珠菌,其他鉴定出的真菌也可能参与IBD的发展,遗传因素,特别是CARD9多态性,在定义定植的炎症反应中很重要。
此外,克罗恩病样本中真菌与细菌多样性的比例增加,这表明克罗恩病患者的肠道环境可能更适合真菌的定植。
总的来说,IBD过程中肠道环境的改变与各种真菌和细菌的变化有关,并诱导真菌-细菌关系的改变。
然而,宿主IBD的最终命运不仅与影响肠道稳态的细菌和/或真菌群落有关,宿主免疫也起着决定性作用。
更重要的是,上述结果聚焦于克罗恩病和/或溃疡性疾病和克罗恩病混合患者或实验模型中的真菌群特征;溃疡性疾病患者肠道真菌群落的变化需要进一步的独立研究或实验模型。
有趣的是,酿酒酵母是有益菌,有能力改善肠胃炎,减轻CEACAM6(癌胚抗原相关细胞粘附分子6)表达小鼠的粘附性侵袭性大肠杆菌(AIEC)诱导的结肠炎,缓解人类受试者肠易激综合征(IBS)的腹痛。
因此,肠道真菌的调节可能是治疗IBD的一个潜在靶点。肠道共生真菌与IBD之间的因果关系有待进一步研究。此外,目前还不清楚肠道真菌是否通过与肠道细菌相互作用影响IBD的进展。
乳糜泻(CeD)
已发现乳糜泻(CeD)与肠道真菌群紊乱有关。乳糜泻的典型标志是可逆的小肠黏膜萎缩,临床症状不典型往往导致漏诊,疾病严重程度增加。
白色念珠菌可能是乳糜泻的潜在原因之一
念珠菌与乳糜泻的发病机制有关。具体来说,白念珠菌和乳糜泻之间的关联始于白色念珠菌毒力因子-菌丝壁蛋白1 (HWP1)的假设,它与T细胞抗原表位中乳糜泻相关的-α和γ醇溶蛋白相同或高度同源,并作为谷氨酰胺转胺酶(TG)底物,协助自身反应性抗体的产生。
随后,通过抗原抗体反应和微芯片分析,乳糜泻组和白色念珠菌感染(CI)组均表达高水平的抗HWP1、抗麦胶蛋白抗体和抗转谷氨酰胺酶(anti-TG) IgA抗体,乳糜泻组对HMP1的反应较高。然而,需要更多的证据来确定白色念珠菌参与乳糜泻。
其他
结肠癌与肠道真菌的失调有关,特别是在CARD9−/−小鼠中热带念珠菌的显著增加。
很少有研究证明肠易激综合征(IBS)和肠道真菌之间的联系。IBS的症状(如腹泻)与接受抗生素治疗或由念珠菌产物引发的念珠菌种类过度生长有关。然而,还需要更多的研究来揭示肠道真菌与这些肠道疾病之间的因果关系。
如上所述,黏膜免疫系统可能介导肠道真菌对肠道疾病发病机制的影响。特别是肠上皮细胞、其常驻免疫细胞、肠系膜淋巴系统、细胞因子、抗体以及上述真菌代谢产物,都可能在肠道疾病的发病机制中发挥重要作用。
肠脑轴和肠道真菌
肠道微生物-脑轴的证据主要包括以下几个方面:
(1) 肠道微生物通过迷走神经、细胞因子及其代谢产物如色氨酸、GABA和乙酰胆碱影响大脑
(2) 下丘脑-垂体-肾上腺(HPA)轴在肠道微生物群与大脑的交流中起核心作用
(3) 肠道-脑-微生物轴为抑郁症、自闭症和帕金森病提供了新的治疗靶点
肠道真菌在肠道-脑轴中的潜在机制

Wu X et al., Microbiome. 2021
(a) 肠道真菌以性别依赖的方式调节犬尿氨酸通路基因和海马区相关miRNAs的表达。
(b) 多发性硬化患者(MS)外周血和脑脊液中检测到念珠菌高。
(c) 精神分裂症患者(SC)的肠道真菌alpha多样性发生改变,毛壳菌属Chaetomium的丰度更高。
(d) 肠道补充乳酒假丝酵母 Candida kefyr有助于缓解实验性自身免疫性脑脊髓炎(EAE)。
念珠菌可能在介导肠道真菌-大脑相互作用中发挥重要作用。因此,肠道真菌可能在精神疾病中占有重要地位。
肠肺轴和肠道真菌
哮喘是一种典型的慢性过敏性气道疾病(AAD),被视为与Th2相关的疾病。
根据嗜酸性粒细胞和中性粒细胞的比例,哮喘已分为不同的炎症亚型。除Th2细胞外,Th1、Th9、Th17、NKT、CD8+ T、Treg细胞也参与了不同类型的哮喘。
众所周知,真菌细胞壁的许多成分是哮喘的过敏原,因此,真菌疾病与哮喘有关并不奇怪。
肠-肺轴上肠道真菌的潜在机制

Wu X et al., Microbiome. 2021
箭头表示激活,水平线表示抑制
(a) 氟康唑引起的肠道真菌失调足以恶化屋尘螨(HDM)所致的呼吸道变态反应(AAD),但对无肠道菌群的小鼠无影响。氟康唑诱导的肠道真菌失调刺激肠道CX3CR+巨噬细胞,导致Th2扩增,伴有巨噬细胞、中性粒细胞和嗜酸性粒细胞浸润肺。
(b) 肠道真菌诱导的前列腺素E2(PGE2)促进肺泡巨噬细胞M2极化,加重AAD。
(c) 肿瘤坏死因子(TNF)拮抗剂增强组织胞浆菌诱导的肺部感染的敏感性,在此过程中肠道特异性CD11b+CD103+DCs在肺内迁移和增强,从而增强肺部感染。
(d)白念珠菌C.albicans和酿酒酵母S. cerevisiae在肠道定植可触发肺中病毒特异性CD8T细胞(原因不明)和IFN-γ的产生,最终阻止流感病毒侵入呼吸道上皮细胞。
肠肝轴和肠道真菌
肝脏是一个重要的解毒器官并参与防御反应,参与肠道衍生的危险防御反应,被称为“肠-肝-轴”。
肠道微生物群的破坏是密切肝病如肝炎和肝硬化有关。例如,仔鸭口服赭曲霉毒素A (ochratoxin A,简称OTA)后,盲肠微生物多样性降低,产脂多糖拟杆菌门(LPS-producting Bacteroidetes)在盲肠和肝脏中的丰度增加,最终OTA通过TLR4-Myd88通路促进肝脏炎症。
肠道真菌可能通过肠肝轴参与肝脏疾病。也就是说,与健康对照相比,原发性硬化性胆管炎患者的真菌多样性增加了。
肝硬化患者的十二指肠真菌丰富,酒精滥用引起的肝硬化与念珠菌过度生长有关,血清酿酒酵母 S. cerevisiaeIgG抗体更高。
值得注意的是,开菲尔是一种针对肠道真菌群的抗酒精性脂肪肝的有效治疗方法。
注:开菲尔(Kefir)是以牛乳、羊乳或山羊乳为原料,添加含有乳酸菌和酵母菌的开菲尔粒发酵剂,经发酵酿制而成的一种传统酒精发酵乳饮料。
肠道真菌在肠-肝轴、胰腺疾病和肠-肾轴中的潜在机制
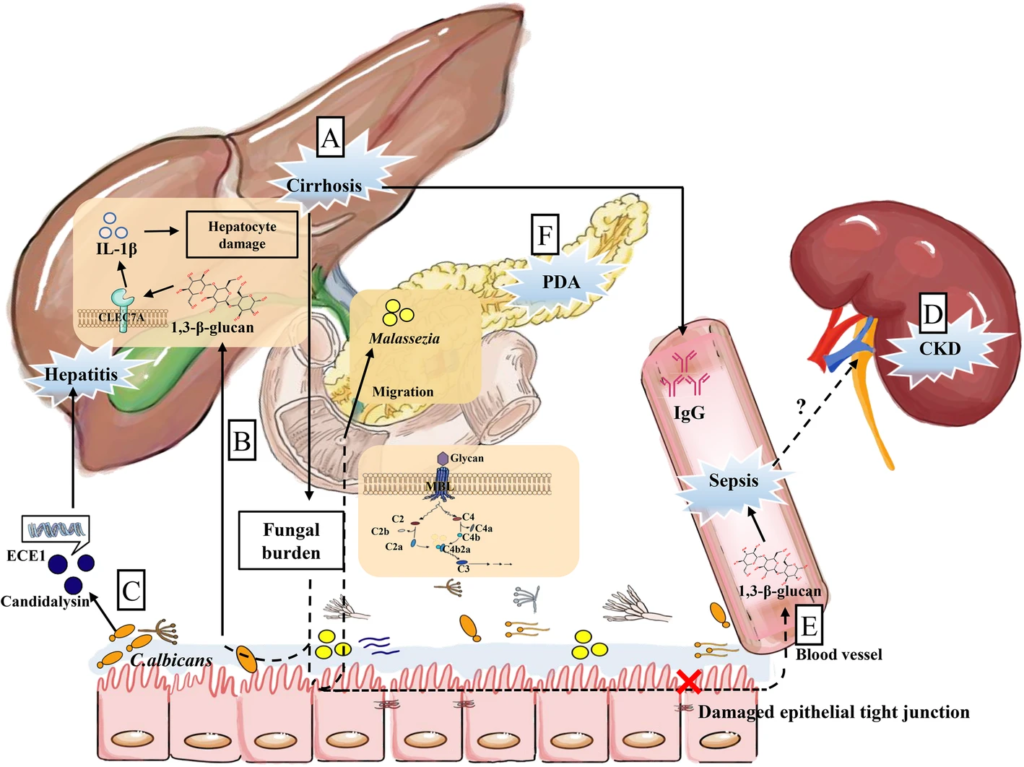
Wu X et al., Microbiome. 2021
(a)肝硬化患者肠道真菌负荷高,血清IgG水平高。
(b)随着1,3-β-D-葡聚糖(BG)的转运,肠道真菌负担增加。然后BG被C型凝集素样受体CLEC7A识别,诱导IL-1β的产生,加重肝细胞损伤。
(c)肠道定殖白色念珠菌分泌ECE1基因编码的念珠菌素,这与酒精性肝炎患者疾病加重有关。
(d)慢性肾病(CKD)小鼠肠道菌群发生改变,上皮紧密连接受损,导致细菌或真菌产物泄漏。
(e)肠漏可促进BG在血清中的迁移,加重脓毒症。
(f) PDA肿瘤在胰腺中高度富集马拉色菌,这是肠道真菌通过Oddi括约肌直接连接这两个器官而迁移的结果。此外,真菌细胞壁- MBL-补体级联途径的多糖在PDA中起重要作用。
肠肾轴和肠道真菌
肠-肾轴可能是肠道微生物的远端靶点。值得注意的是,慢性肾病(CKD)小鼠肠道微生物群的变化与上皮紧密连接受损有关,细菌产物可能通过肠道屏障泄漏,激活免疫反应。
同样,念珠菌在重症监护室患者肠道中的定植是念珠菌血症的一个易感因素。
两项研究均表明,白色念珠菌的肠道定植可能与败血症有关,肠道泄漏可能促进BG迁移,从而加重疾病进程。
在发生念珠菌播散感染的ICR小鼠中,肾脏的真菌负担最高,提示肾脏可能在循环真菌感染中发挥重要作用,但其机制仍有待研究。
然而,肾脏疾病中某些真菌的大量变化和假定的BG渗漏不能真正解释真菌肠肾轴的存在。同样,目前有关肠道真菌失衡直接影响肾脏疾病发病机制的研究还很有限,推测真菌肠道-肾脏轴是可行的。肠道真菌与肾脏之间是否还有其他联系值得探讨。
肠胰轴和肠道真菌
胰腺β细胞与1型糖尿病(T1DM)的发病机制相关。
与健康对照组相比,T1DM和2型糖尿病(T2DM)患者白色念珠菌定植率更高。T1DM患者甚至有更高的真菌种类多样性。这些发现表明,肠道真菌可能参与了糖尿病的发病机制。
然而,关于肠道真菌与胰腺细胞功能之间的直接关系的证据仍然有限。此外,肠道共生细菌衍生的Nod1配体(作为信号分子)是胰腺细胞中胰岛素转运所必需的。因此,探索肠道真菌来源的分子是否对胰腺细胞的功能有影响将很有意思。
此外,在胰腺导管腺癌(PDA)患者中,胰腺细菌和真菌明显增多。马拉色菌在人和小鼠的PDA中高度富集,肠道真菌可能通过Oddi括约肌迁移到胰腺。
然而,目前尚不清楚肠道真菌的失调是致癌进展的原因还是结果,揭示PDA的真菌特征是必要的;因此,我们仅提出Oddi和/或MBL补体级联可能作为肠-胰腺轴的连接。
总的来说,就像肠-肾轴一样,肠道真菌-胰腺相互作用的研究仍处于早期阶段。
虽然我们普遍关注肠道菌群,但值得注意的是,肠道真菌也具有许多潜在的功能。
肠道真菌参与肠道疾病或其他器官疾病可能为开发新的疾病治疗策略和提供新的诊断靶标提供新的窗口。然而,需要更多的研究来确定肠道真菌与肠道或肠道外疾病之间的因果关系。
除真菌本身外,肠道真菌化合物可能在疾病治疗中具有巨大潜力。一些真菌提取物具有抗病毒特性,因此利用真菌化合物可能为克服不可治愈的病毒性疾病提供新的突破。
相关阅读:
参考文献:
Kaźmierczak-Siedlecka K, Dvořák A, Folwarski M, Daca A, Przewłócka K,Makarewicz W. Fungal hut microbiota dysbiosis and its role in colorectal, oral, and pancreatic carcinogenesis. Cancers. 2020;12(5)
Sebaa S, Boucherit-Otmani Z, Courtois P. Effects of tyrosol and farnesol onCandida albicans biofilm. Mol Med Rep. 2019;19(4):3201–9.
Leonhardt I, Spielberg S, Weber M, Albrecht-Eckardt D, Bläss M, Claus R, BarzD, Scherlach K, Hertweck C, Löffler J, et al. The fungal quorum-sensing molecule farnesol activates innate immune cells but suppresses cellular adaptive immunity. mBio. 2015;6
Wu X, Xia Y, He F, Zhu C, Ren W. Intestinal mycobiota in health and diseases: from a disrupted equilibrium to clinical opportunities. Microbiome. 2021 Mar 14;9(1):60.
Leger T, Garcia C, Camadro JM. The Metacaspase (Mca1p) Restricts Oglycosylation during farnesol-induced apoptosis in Candida albicans. Mol Cell Proteomics. 2016;15(7):2308–23
Aaron L, Torsten M. Candida albicans in celiac disease: a wolf in sheep’sclothing. Autoimmun Rev. 2020;19(9):102621.
Enaud R, Prevel R, Ciarlo E, Beaufils F, Wieers G, Guery B, Delhaes L. The gut-lung axis in health and respiratory diseases: a place for inter-organ and inter-kingdom crosstalks. Front Cell Infect Microbiol. 2020;10:9.