 国家高新企业 | ISO9001认证
国家高新企业 | ISO9001认证 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康

营养不良的微生物 Malnourished Microbes
儿童营养不良是全球主要的健康负担,营养干预措施只能部分解决这一问题。儿童营养不良的慢性和急性形式均以多种生物系统紊乱为特征,包括新陈代谢、免疫和内分泌系统。
越来越多的证据支持肠道微生物组在调节这些影响早期生命生长的途径中的作用。观察性研究报告了营养不良儿童肠道微生物组的变化,而临床前研究表明,这可能引发肠病,改变宿主代谢,并破坏免疫介导的针对肠道病原体的抵抗力,这些都会导致早期生命生长不良。
肠道微生物组在健康和疾病中发挥着不可或缺的作用,而饮食是其组成、多样性和功能的主要驱动因素。鉴于婴儿和儿童肠道微生物组的动态发育,解决两个主要问题至关重要:
a) 饮食能否改变肠道微生物组的组成、多样性或功能
b) 这种修改是否会影响功能/临床结果,包括免疫功能、认知发展和整体健康?
本文汇编了临床前和临床研究的证据,包括生命早期肠道微生物组影响宿主代谢、免疫、肠道功能、内分泌调节和其他导致儿童营养不良的途径的新兴病理生理学途径。
我们综合了儿童青少年的营养、营养干预措施和肠道微生物群之间联系的最新研究,该年龄段儿童是一个生长阶段,对疾病的易感性各不相同。还讨论了营养素如何单独或组合如何影响肠道微生物组的机制。
同时综合并讨论了新兴的微生物组导向疗法,并考虑未来的研究方向,以确定和针对儿童营养不良的微生物组治疗目标。
2013年发表在《柳叶刀》上文章统计,儿童营养不良导致全球儿童死亡人数的 45%,并对健康产生终生影响。全世界超过五分之一的5岁以下儿童至少表现出一种形式的慢性或急性营养不良。
首先我们来了解一下发育迟缓、消瘦的定义。
发育迟缓[定义为年龄别身长 Z 得分 (LAZ) < −2],影响着全球 22% 的儿童,与认知发展较差、终身综合能力下降以及成年后慢性病风险增加有关。
消瘦[定义为身高体重 Z 得分 (WHZ) < –2] 影响着全世界近 7% 的儿童,除了长期认知和健康缺陷不佳之外,还与高死亡率相关。
▸ 目前的治疗方法无法完全解决这一问题
营养疗法不足以完全恢复生长缺陷和营养不良的相关病理生理后果。标准生命早期营养补充剂仅可将发育迟缓降低 12-14%。
而严重消瘦后会出现高死亡率、再入院和长期生长缺陷。因此,存在与儿童营养不良相关的隐藏的病理生理学负担,目前的治疗方法无法完全解决这一问题。
▸ 儿童营养不良与多个生命早期生物系统紊乱有关
发育迟缓和消瘦儿童的肠道功能受到环境肠道功能障碍(EED)的影响。这种肠道病理学损害营养吸收,并可能导致全身炎症,从而损害早期生命生长。
在营养不良的儿童中宿主免疫力广泛缺陷,导致抵抗感染能力受损,特别是病原体密集的环境。
营养良好和营养不良的儿童之间存在激素差异,尤其是与生长 [生长激素 (GH) 和胰岛素样生长因子1 (IGF-1)] 和食欲调节(瘦素和生长素释放肽)相关的荷尔蒙差异。
营养不良时宿主代谢发生改变,氨基酸、脂质和能量代谢受到干扰。这些受到干扰的生理系统表明,儿童营养不良背后存在复杂的病理生理学,涉及相互关联的生物系统。
▸ 微生物群影响生命早期的生长发育
生命早期接触微生物也可能导致儿童营养不良中这些扰动途径。肠道病原体携带量高与线性生长和体重生长下降以及 EED 相关,而腹泻和呼吸道感染也与儿童营养不良密切相关。
除了病原体之外,共生肠道微生物群也会影响早期生命的生长。生命早期复杂微生物组的组装对于免疫训练、对病原体的定植抵抗、母乳寡糖(HMO) 和其他营养物质的代谢、肠道结构和内分泌信号传导至关重要。
因此,儿童时期肠道微生物组的破坏可能会损害这些有助于儿童健康成长的途径。
▸ 儿童在出生时就获得了一些的微生物组
除了环境获得的微生物外,这些微生物组主要源自母体肠道、阴道、口腔和皮肤微生物组。
在纯母乳喂养的儿童中,最初的婴儿肠道微生物群的多样性仍然很低,主要由大肠杆菌、双歧杆菌和拟杆菌组成物种。
在接下来2-3 年里,肠道微生物群会经历一种模式化的组装,这种组装主要是由纯母乳喂养和随后的补充食品的引入所形成的,这导致肠道微生物群的快速扩张和多样化。
▸ 许多环境因素会影响微生物,从而影响生长
包括地理位置、分娩方式、抗生素暴露、胎龄以及其他母亲和家庭因素。这些微生物群在出生后在胃肠道内的积累,除了肠道结构和对病原体的定植抵抗力之外,还推动了免疫、代谢和内分泌途径的成熟,这些都有助于儿童的正常生长。
如果微生物演替因营养不足、卫生或抗生素暴露而受到干扰,这些生长决定途径可能会受到损害。很少有研究纵向研究在营养匮乏的环境中保持良好营养的儿童与消瘦或发育迟缓的儿童的肠道微生物群的演替和组装情况。
因此,这种依赖高收入环境的微生物组数据库的现象,限制了低收入和中等收入国家中个体所产生的营养不良微生物组的解释性(这也是构建本地数据库和谷禾长期追踪重点人群纵向数据的主要原因),这些国家的肠道微生物组特征不太明确。
来自中低收入国家的横断面和短期纵向研究的越来越多的证据揭示了微生物组的差异,这些差异将营养不良与健康生长区分开来。
▸ 发育迟缓——多因素驱动
“发育迟缓”是一种慢性营养不良的形式,由多种遗传和环境因素共同驱动。高达30%的发育迟缓发生在子宫内,这可以通过出生体重对发育迟缓风险的强烈影响来证明。
之后一系列环境因素有助于产后线性生长。很少有研究纵向研究健康婴儿与发育不良婴儿肠道微生物组的获取和组装情况。
▸ 横断面研究:肠道菌群特征破坏导致发育迟缓
对马拉维和孟加拉国队列的二次分析发现,微生物组多样性减少和Acidaminococcus(氨基酸球菌)丰度增加分别与发育迟缓严重程度和未来线性生长缺陷相关。
其他一些小型横断面研究已经发现,在一系列中低收入国家队列中,发育不良儿童与健康儿童的粪便微生物组组成存在不同差异。来自中非共和国和马达加斯加的一项更大规模的多点横断面分析发现,发育不良儿童的粪便微生物群中大肠杆菌/志贺氏菌和弯曲杆菌种类丰富,而产生丁酸的种类较少。
▸ 发育迟缓的儿童:小肠细菌过度生长
在发育迟缓的儿童中观察到小肠细菌过度生长的比率较高,其特征是十二指肠中口咽微生物的富集。发现一群来自孟加拉国的发育迟缓儿童的小肠细菌载量与 LAZ 之间呈负相关。韦荣球菌属、链球菌属和Rothia mucilaginosa的十二指肠丰度也与 LAZ 呈负相关。
▸ 肠道菌群的功能潜力——预测儿童生长的指标
对 335 名津巴布韦农村的 1 至 18 个月大儿童的肠道微生物组的组成和功能发育的跟踪发现,肠道微生物组的功能宏基因组组成(而非分类组成),可以预测孩子已达到的线性生长和未来的生长速度,其中 B 族维生素和核苷酸生物合成途径是最具预测性的特征之一。这些数据表明,肠道微生物组的功能潜力是儿童生长的更强大的指标。
来自马拉维的一个纵向队列发现了类似的结果,即 16S 测序无法识别成分多样性、成熟度或物种丰度与 LAZ 之间的关联。秘鲁对 6-24 个月大的儿童(作为营养不良和肠道疾病队列的一部分)进行的一项纵向研究表明,成分多样性与线性生长之间存在一定关联,仅针对出生时发育迟缓的儿童。
该研究组另外一项研究究表明,肠道微生物组可能介导腹泻和弯曲杆菌感染对线性生长的影响。除了肠道微生物组细菌成分的影响之外,发育迟缓婴儿与非发育迟缓婴儿中噬菌体(可以调节微生物组组成的病毒)的丰度也有所不同。
总的来说,发育不良儿童的肠道微生物群与营养良好的儿童不同。然而,这因地理群体而异。因此,目前不存在一致的发育迟缓的组成或功能微生物组特征。
▸ 儿童口腔微生物组与发育迟缓有关
发育迟缓的儿童在十二指肠和粪便中表现出更丰富的口咽微生物,包括唾液乳杆菌,这表明胃肠道的隔室化可能导致营养不良儿童中肠道菌群变化,并通过减少营养吸收而导致生长不良或口腔微生物在其生态位之外的炎症作用。
▸ 怀孕期间母亲的口腔微生物组预测儿童营养不良
牙周炎是一种口腔生态失调疾病,会导致局部免疫反应功能失调,并与低出生体重呈负相关。在怀孕期间的母亲口腔中,Actinomyces naeslundii(内氏放线菌)的相对丰度与出生体重和妊娠持续时间呈负相关,而Lactobacillus casei(干酪乳杆菌)则呈正相关,两者都强烈预测儿童营养不良。
▸ 早产的阴道微生物组,与新生儿低出生体重和随后的发育迟缓密切相关
高度多样化、缺乏乳杆菌的阴道微生物群与西方地区的早产以及撒哈拉以南非洲地区新生儿 LAZ 的减少密切相关。阴道微生物组的改变很可能与早产的经典感染触发因素同时发生,包括绒毛膜羊膜炎、细菌性阴道病和泌尿生殖感染,从而导致泌尿生殖环境炎症,这些共同可能限制胎儿生长或引发早产。
▸ 消瘦及其分类:营养不良形式的反映
消瘦是营养不良的一种形式,可以反映慢性营养缺乏和急性疾病,通常与发育迟缓同时发生。
消瘦可分为中度[中度急性营养不良(MAM)]或重度[严重急性营养不良(SAM)],取决于 WHZ 阈值、中上臂围 (MUAC) 和/或水肿的存在。
▸ 水肿性SAM、非水肿性SAM、复杂SAM
SAM 还以两种主要形式存在:
如果出现急性感染、食欲不振、休克或水肿(也称为复杂 SAM)。
患有水肿性和非水肿性 SAM 的儿童具有不同的临床结果,其中非水肿性 SAM 儿童在某些情况下接受 SAM 住院治疗后表现出更高的死亡率和再入院率。
尽管治疗 SAM 的营养疗法有所改进,但需要住院治疗的复杂 SAM 的死亡率在 10% 至 40% 之间,而生长缺陷可能会持续长达7年,此外,日后认知缺陷和慢性病风险也会增加。
▸ 在SAM 儿童肠道中肠道微生物组具有影响力
患有 SAM 的儿童肠道微生物多样性降低,肠杆菌科细菌增多,而与健康生长一致的双胞胎相比,SAM不一致的双胞胎肠道病毒组受到干扰。
▸ 年龄微生物群Z评分——微生物群成熟度指标
2014 年,孟加拉国的一项具有里程碑意义的研究创建了微生物群成熟度指标,称为年龄微生物群Z评分(MAZ),该评分在 SAM 儿童中显着降低,并且与术后营养恢复的人体测量指标高度相关。这项研究和最近的后续研究使得所谓的微生物组生态群得以细化,该生态群由 15 种细菌类群组成,这些细菌类群在不同地理环境中在生命的头 2 年中表现出一致的共变,可用作微生物群落的指标。
不成熟的微生物组发育并衡量MAM 或 SAM 后微生物组的恢复程度。根据 MAZ 的评估,标准治疗性往往只能暂时恢复微生物组的成熟度,表明 MAZ 可能有潜力作为未来 MAM/SAM 复发的指标,或者针对肠道微生物组的营养疗法可能有助于营养恢复。
事实上,这些微生物群成熟度指标为 MAM 中新的微生物群导向营养干预措施提供了信息,在试点研究中,与标准治疗食品相比,这些干预措施在更大程度上改善了营养恢复。
▸ 在水肿性SAM 和非水肿性 SAM 儿童差异
这可能部分解释了他们营养恢复的差异。与水肿性SAM儿童相比,非水肿性 SAM 儿童的α多样性显著降低,并且与普雷沃氏菌科(Prevotellaceae)、毛螺菌科 (Lachnospiraceae) 、瘤胃菌科(Ruminoccoaceae)相对丰度的减少有关。
总的来说,与健康成长的儿童相比,SAM 儿童的微生物组始终不成熟且多样性降低。这种失调的微生物组可能是急性营养状态以及与治疗相关的合并症和抗生素治疗的结果。
如上所述,越来越多的人类观察研究证据表明,营养良好和营养不良的儿童之间的微生物组组成存在差异。
临床前和临床研究已开始揭示,生命早期肠道微生物群紊乱可能导致儿童生长不良的病理生理机制。其中包括肠道微生物组对免疫、新陈代谢、肠道功能和内分泌信号传导等途径的影响(如下图)。
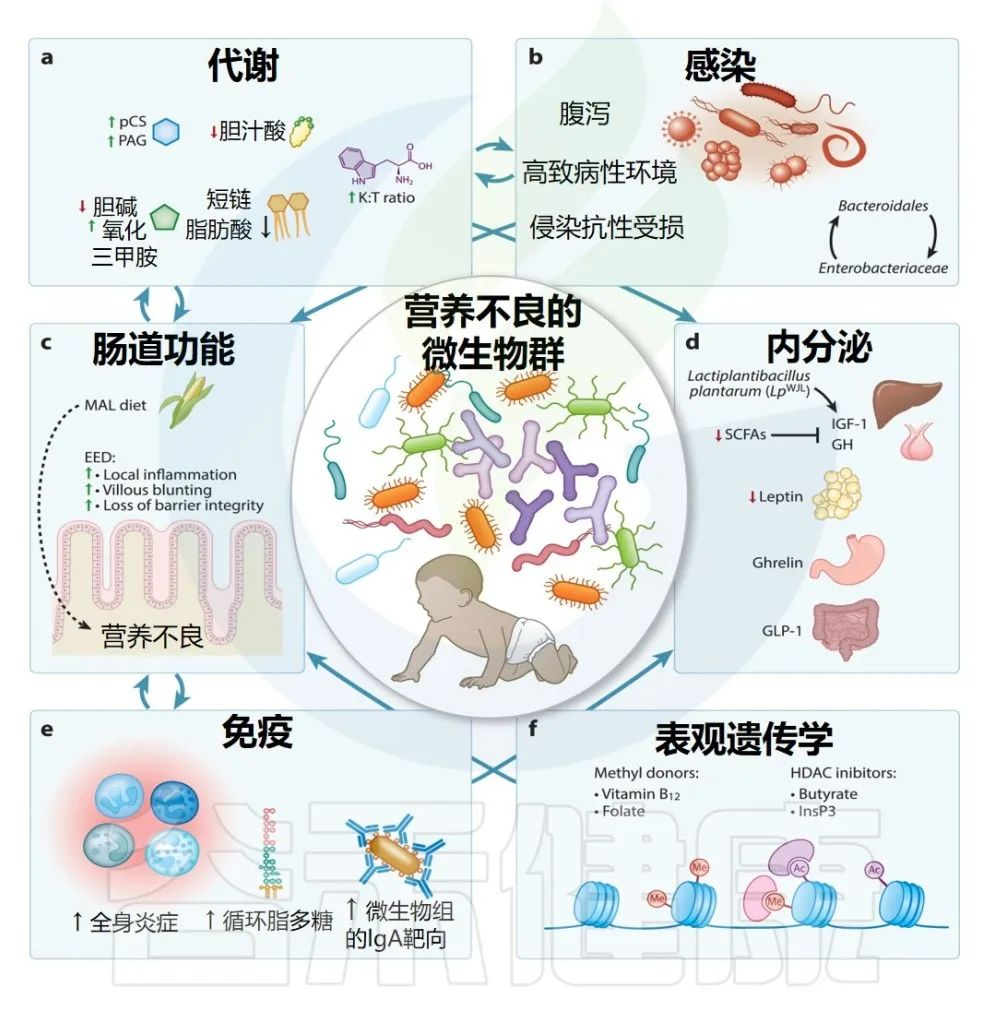
doi.org/10.1146/annurev-nutr-061121-091234
下面我们逐一来了解营养不良的微生物群带来的多方面影响。
共生肠道微生物群的存在,对于生命早期肠道屏障的正常结构、功能和转录发育至关重要。临床前研究的大量证据表明,无菌小鼠幼崽表现出肠道屏障成熟延迟,这与自发性结肠炎、更容易肠道感染和营养吸收不良有关。
生命早期长期接触肠道病原体会破坏肠道结构和功能。环境肠道功能障碍(EED)是一种胃肠道现象,在营养匮乏的环境中很常见,并且经常在营养不良的儿童中观察到(我们以前也专门写过儿童EED的文章)。
▸ 什么是环境肠道功能障碍(EED)?
EED 通常是亚临床的,局限于小肠,其特征是肠道通透性增加、绒毛萎缩和变钝、粘膜屏障变化、吸收不良、局部炎症和隐窝伸长。屏障功能的丧失还导致微生物及其产物(最常研究的是脂多糖)从肠道转移到体循环中,从而刺激全身炎症。据推测,营养吸收不良、肠道炎症和慢性全身炎症的结合会阻碍儿童的健康成长。
▸ 环境肠道功能障碍(EED)与什么相关?
EED 通常归因于在水、环境卫生和个人卫生 (WASH) 较差的环境中长期接触肠道病原体。然而,在此类环境中改善怀孕期间和早期生活中的 WASH 的大型随机试验未能减少幼儿 EED 的常见生物标志物,这可能是由于同时未能减少其肠道病原体携带。
除了病原体携带之外,共生微生物组的破坏也可能导致 EED。对611 名儿童( 6、18 和 30 个月大)大型分析发现,微生物群多样性/成熟度与 EED 的三种生物标志物之间存在负相关:
表明肠道微生物群的不成熟可能会导致肠道炎症和屏障功能障碍。特定菌群的丰度升高,包括Megasphaera、Mitsuokella、Sutterella也与 EED 有关。
注:REG1B,Regenerating family member 1 beta 是一种蛋白质,它是一种由胰腺细胞产生的蛋白质,在胰岛细胞再生和胰岛功能调节中起着重要作用。
REG1B在胰腺细胞再生过程中被表达,且参与了胰岛细胞增殖和分化,对胰岛细胞的生长和修复有促进作用,在胰岛素分泌和血糖调节中发挥一定的调节作用。
EED 动物模型有助于深入了解可能驱动该疾病表型的机制。一些模型能够通过应用低蛋白饮食和 LPS 或吲哚美辛等肠道损伤来复制 EED 的某些方面。
注:吲哚美辛:用于治疗关节炎,癌性疼痛,痛风,滑囊炎、肌腱炎及肩周炎等非关节软组织炎症;可用于高热的对症解热,恶性肿瘤引起的发热或其他难以控制的发热。
▸ 肠道微生物对 EED 的潜在贡献
利用异常微生物状态和改变的营养环境之间相互作用的新模型已经成功地概括了几种 EED 表型。例如,肠道生理学和微生物组通过血管紧张素 I 转换 2 酶 (ACE2) 的表达联系起来。
注:ACE2是一种在分化上皮细胞的管腔表面表达的蛋白质。
与野生型小鼠相比,缺乏 ACE2 的小鼠在受到DSS攻击时,表现出类似 EED 的病理学、氨基酸代谢紊乱和肠道微生物组紊乱。DSS 攻击期间的 EED 表型可以在从 ACE2 缺陷小鼠进行粪便移植后转移到野生型动物中,这表明微生物群被破坏。
注:DSS,右旋糖酐硫酸钠,一种破坏肠上皮屏障并导致结肠炎的刺激物
膳食色氨酸及其代谢物烟酰胺可以通过哺乳动物雷帕霉素靶点 (mTOR) 活性刺激抗菌肽的产生,从而挽救 ACE2 缺陷小鼠的表型,从而维持微生物组稳态。
▸ 微生物结合营养物质影响EED
低蛋白、低脂肪饮食会导致小鼠小肠微生物群遭到破坏,其特点是小肠内物种丰富度升高,此外拟杆菌门和变形菌门也会扩张。
将营养不良的饮食与拟杆菌和大肠杆菌结合起来作者产生了 EED 的表型,包括肠道通透性、绒毛和隐窝萎缩增加、空肠细胞因子 (IL-6 和 MCP-1)释放到腔内增加,以及细菌对小肠上皮细胞的粘附增加。这种表型依赖于微生物组的改变和营养不良的饮食,这表明 EED 表型是复杂的微生物与营养物质相互作用的结果。
总体表明,肠道微生物群破坏在营养不良相关肠道功能障碍的病理学中具有潜在的因果作用。
▸ 腹泻和有症状的呼吸道感染与发育迟缓和消瘦有关
关于腹泻和儿童营养不良的大型多中心研究的有力证据表明,肠道病原体的高负担与生命早期生长不良有关。
健康且多样化的肠道微生物群通过生态位排除提供针对肠道病原体的定植抵抗力。因此,受损的肠道微生物组可能为病原体定植提供了环境。
肠道微生物组也可能介导远处部位的感染易感性,包括肺部。因此,生命早期健康肠道微生物组可能有助于在卫生条件差的环境中抵抗病原体的定植,从而防止感染负担和相关的生长不良。
▸ 发育迟缓:肠道菌群多样性减少——预示腹泻发病率的增加
来自秘鲁的发育不良儿童在生命的前两年表现出肠道微生物组多样化轨迹受损。在此期间,发育迟缓的儿童的微生物多样性显着减少,腹泻后多样性的恢复也较慢。因此,肠道微生物组的组装受损可能会加剧感染-发育迟缓的循环。
来自同一队列的一项研究发现,弯曲杆菌的携带与肠道微生物群的改变有关。此外,肠道微生物组内与弯曲杆菌携带相关的物种与 LAZ 的减少独立相关,这表明肠道微生物组组成受损会促进病原体定植和并发生长缺陷。
▸ 营养不良:微生物组对病原体定植产生影响
与营养良好的小鼠相比,由营养不良饮食和肠道微生物群紊乱引起的 EED 小鼠模型对感染的敏感性更高,这表明与营养不良相关的微生物群破坏可能会导致病原体定植和感染负担。
蓝氏贾第鞭毛虫感染后生长缺陷的易感性也取决于动物模型中的肠道微生物组。人类研究报告称,贾第鞭毛虫和相关的肠侵袭性病原体,除了那些涉及粘膜破坏的病原体外,对全身炎症、肠道炎症和生长受损具有最深远的影响。
在小鼠中,贾第鞭毛虫与小肠中的肠杆菌科细菌相互作用,以限制蛋白质营养不良期间的生长,这种作用在用没有抗贾第鞭毛虫活性的抗菌药物治疗后消失,表明失调的微生物群在此过程中发挥着关键作用。
这种相互作用表明特定的病原体或病原体依赖于共生肠道微生物群的成员来定殖和增殖。这在人类发育迟缓研究中很明显,即肠杆菌科细菌和拟杆菌目细菌之间的交叉喂养与儿童发育迟缓有关。
▸ 在体外,肠杆菌科和拟杆菌目之间协同生长
特别是在蛋白质和铁含量低的营养不良条件下。在这种情况下拟杆菌属利用饮食和粘蛋白衍生的糖和肠杆菌科细菌提高铁的生物利用度,铁是特定病原体增殖所必需的微量营养素。
拟杆菌科和肠杆菌科在营养不良的儿童中具有很强的相关性,但在营养良好的儿童中则没有。另一种拟杆菌属的脆弱拟杆菌,还依赖周围的微生物群来诱导小鼠的生长效应。含有bft毒素的脆弱拟杆菌的产肠毒素菌株会导致无菌小鼠体重减轻和能量代谢受损,这些小鼠被来自发育迟缓儿童的微生物群定植,但对于那些被来自营养良好儿童的微生物群定植的小鼠则不会。
这些数据表明,病原体和感染对儿童营养不良的影响可能依赖于共生肠道微生物群的组成和功能,在儿童营养不良患病率高的环境中减少病原体负担的策略除了考虑病原体负担外,还必须考虑共生微生物群。
营养不良儿童的宿主蛋白质、脂肪和能量代谢紊乱早已有报道。然而,肠道微生物组的代谢能力大大扩展了哺乳动物宿主的生物转化能力,扩大了可加工底物的多样性,并增加了宿主接触的分子范围。
许多微生物衍生的代谢物可以在肠道和肠壁中发挥局部作用,并且在吸收后还可以影响周围组织中的宿主过程。因此,儿童早期肠道微生物组的变化可能会通过改变提供给儿童的代谢副产物和宿主代谢途径本身来影响代谢表型,从而影响生长。
▸ 成熟度与微生物代谢
与用于绘制儿童微生物组成熟度的MAZ评分类似,代谢成熟度模型,称为年龄表组 Z 评分 (PAZ),是根据秘鲁、坦桑尼亚和孟加拉国儿童的尿液样本构建的,并用于追踪生化年龄及其与生长的关系。用于计算 PAZ 的八种代谢物中的三种——对甲酚硫酸盐 (pCS)、苯乙酰谷氨酰胺 (PAG) 和马尿酸,与肠道微生物代谢相关。
有趣的是,与未生长受限的婴儿相比,生长受限的婴儿早在出生后 3 个月就出现生化不成熟(即,其生化年龄低于实际年龄)。这凸显了微生物群在宿主整体代谢能力发展及其对生长的后续影响中的重要性。
健康肠道微生物群的一个主要功能是发酵宿主无法消化的膳食底物。在母乳喂养期间,这主要涉及HMO的微生物消化。患有发育不良婴儿的母亲的母乳中 HMO 含量明显较低,结构相似的牛乳低聚糖可以恢复营养不良模型中小鼠的生长。
然而,这种效果取决于微生物群,因此补充乳寡糖后,无菌小鼠的生长不会恢复。断奶后,肠道微生物群转向不可消化的碳水化合物、抗性淀粉、粘蛋白和蛋白质的代谢。
▸ 糖分解产生短链脂肪酸,满足能量需求
糖分解活性(即碳水化合物的分解)的主要最终产物是短链脂肪酸。这些都有助于宿主日常的能量需求。丁酸盐是结肠细胞的主要能量来源,提供其所需能量的 80%,而乙酸盐在肌肉等全身区域代谢,丙酸盐在肝脏中用于产生 ATP。
这种微生物活动提供了一种从饮食中释放能量的机制,可用于支持生长。此外,短链脂肪酸还具有其他有益作用,例如降低结肠 pH 值以增强对潜在病原体的定植抵抗力并提高矿物质吸收。此外,丁酸盐已被证明可以通过增加 AMP 激活蛋白激酶 (AMPK) 活性和紧密连接蛋白的组装来促进肠道屏障的发育。
▸ 营养不良:从碳水化合物发酵和短链脂肪酸生产转向蛋白水解代谢
例如,与营养良好的儿童相比,印度尼西亚中度营养不良儿童的粪便丙酸盐和丁酸盐含量较低,粪便 pH 值较高。
在营养不良的猪模型中,肠道微生物组产生的丁酸盐较少,并且与肝脏脂肪酸代谢(β-氧化)减少有因果关系。同样,在对巴西东北部儿童进行的代谢组学研究中,发育不良的婴儿排出了更多由微生物降解氨基酸而产生的微生物-宿主共代谢物。
其中包括 pCS 和 PAG,它们分别源自酪氨酸和苯丙氨酸的微生物分解。营养不良病原体相关的EED导致肠道吸收不良可能会推动这一观察。这增加了小肠中氨基酸的可用性,从而导致发育不良儿童中的小肠细菌过度生长,并增加到达结肠进行细菌代谢的氨基酸。
▸ 营养不良:微生物群与发育中的宿主竞争氨基酸
有趣的是,虽然 SCFA 促进上皮屏障完整性,但 pCS 被发现会损害它,可能导致营养不良个体中观察到的肠漏表型。
此外,pCS由艰难梭菌和其他病原体产生,限制肠道微生物群的生物多样性。可能导致营养不良婴儿中观察到的微生物群失调。另外两种氨基酸代谢物,吲哚乳酸和N-乙酰谷氨酸,分别源自色氨酸和谷氨酸代谢,在来自孟加拉国的一组儿童中,它们与 2-24 个月龄之间的线性和体重生长指标呈正相关。长双歧杆菌也与生长呈正相关,它编码了参与这些化合物生产的大部分微生物代谢途径,这些化合物可能有助于支持早期生命的生长。
▸ 膳食胆碱的微生物分解增加还导致蛋白质营养不良和发育迟缓
在蛋白质缺乏的小鼠模型中,尿胆碱减少,而胆碱代谢的微生物产物三甲胺和二甲胺增加。
同样,在马拉维儿童中,血清中三甲胺-N-氧化物(TMAO)与胆碱的比率与线性生长障碍呈正相关。
胆碱和甜菜碱排泄量降低与巴西婴儿发育迟缓有关。胆碱的可用性不仅对于肌肉获得很重要,对于S-腺苷甲硫氨酸 (SAMe)的生成也是必要的,而 S-腺苷甲硫氨酸 (SAMe) 是 DNA 甲基化和发育的关键。
重要的是,胆碱是骨骼肌的必需营养素以及神经发育和大脑功能。胆汁酸是宿主肝脏和肠道微生物群组合代谢产生的代谢物的一个例子,在消化中发挥重要作用。
初级胆汁酸,例如胆酸和鹅去氧胆酸,在肝脏中合成,然后通常与甘氨酸或牛磺酸结合,并分泌到胆汁中。释放到肠道后,一小部分胆汁酸可以到达结肠,在那里微生物群将它们分解并转化为次级胆汁酸,例如脱氧胆酸。这些修饰的胆汁酸可以通过粪便排出或再循环回肝脏。
与没有 EED 的儿童相比,患有 EED 的儿童的血清总胆汁酸含量较低,其中牛磺鹅去氧胆酸、牛磺鼠胆酸和甘氨酰去氧胆酸存在特定差异。除了消化之外,胆汁酸在代谢调节中也发挥着重要作用。通过充当全身表达的受体(例如 FXR、PXR、VDR 和 TGR5)的配体,胆汁酸可以调节多种宿主途径和功能的表达,例如能量稳态、葡萄糖和脂质代谢。
▸ 这些细菌相关代谢物还具有抗菌特性,既能抑制又能促进特定病原体的生长
例如,胆汁酸代谢的变化,特别是细菌胆汁盐水解酶活性,被认为是隐孢子虫卵囊排泄的重要触发因素。此外,观察到未患阿米巴病的儿童粪便中次级胆汁酸、脱氧胆酸的含量较低。研究表明,给小鼠注射这种胆汁酸足以增加粒细胞-单核细胞祖细胞的数量,并提供针对阿米巴病的保护。这表明胆汁酸可能在预防营养不良环境中常见的不同肠道感染和对这些感染的易感性方面发挥潜在作用。
▸ 从微生物代谢,到宿主代谢的改变
除了微生物代谢的改变外,在营养不良的儿童中还观察到宿主代谢的改变,这可能部分是由菌群失调引起的。例如,从发育迟缓儿童的小肠中分离出的口腔微生物在体外和体内模型中会损害脂质吸收,从而提供小肠微生物组和小肠细菌过度生长在营养不良中的潜在因果作用。
肠道屏障功能的丧失会导致微生物群及其产物(包括脂多糖)从肠道进入体循环的易位增加。LPS 易位可导致慢性全身炎症,从而通过吲哚胺 2,3-双加氧酶诱导激活色氨酸-犬尿氨酸途径。事实上,秘鲁和坦桑尼亚儿童的血浆犬尿氨酸与色氨酸 (K:T) 比率与血浆 LPS 和 LPS 结合蛋白 (LBP) 相关,并且还与线性增长缺陷相关。
扩展阅读:
犬尿氨酸途径的激活可以抑制炎症并促进耐受性,但可能会失调色氨酸途径,而色氨酸途径对于血清素的产生以及 NAD +和烟酰胺的生成非常重要,而后者是生长的关键。免疫耐受性的增加也可能对增强对病原体的有效反应产生影响,这也可能受到色氨酸剥夺的影响,并可能导致此类感染在营养不良的肠道中持续存在。
儿童营养不良与内分泌信号中断有关,包括介导食欲和能量代谢的瘦素和生长素释放肽,以及共同构成生长轴的GH 和IGF-1 。
发育迟缓儿童与非发育迟缓儿童相比,在童年后期血浆 IGF-1 较低以及生命的前 18 个月,一种与慢性炎症相关的现象。
▸ 瘦素水平低可预测SAM儿童的死亡率
新数据表明,肠道微生物组直接和间接影响肠道局部激素的产生,例如胰高血糖素样肽-1 (GLP-1),并通过介导瘦素、生长素释放肽和 IGF-1 的产生来系统地进行,每一个都调节新陈代谢和营养状况。
▸ 微生物组→产生SCFA→GLP-1 的产生→抑制胰高血糖素原的表达
GLP-1 是一种肠道源性激素,负责刺激胰岛素分泌、减少胃排空和增加饱腹感,从而影响新陈代谢和营养状况。
在没有微生物组的情况下,在无菌小鼠中,GLP-1 的产生在一种假设的适应性机制中升高,当微生物组被破坏或不存在时,GLP-1 的产生会增加营养物质的吸收,而 SCFA 给药可以逆转这种效应。
▸ 微生物衍生的SCFA也会影响 IGF-1 的产生
IGF-1 在肝脏和脂肪组织中产生,影响骨形成、骨量和骨骼生长,尤其是在生命早期。当无菌小鼠被微生物定植时,血浆中血清 IGF-1 的浓度会增加。
同样,抗生素的使用会降低 IGF-1 浓度,而补充 SCFA 可恢复抗生素治疗期间 IGF-1 的浓度。不产生短链脂肪酸的细菌种类也可以通过刺激生长轴来刺激实验动物的生长。植物乳杆菌的特定菌株可恢复果蝇和小鼠的线性生长、股骨长度、IGF-1 产生和活性以及外周组织对 GH 的敏感性。
植物乳杆菌WJL ( Lp WJL ) 菌株对 IGF-1 产生和生长的活性取决于肠上皮细胞中含有核苷酸结合寡聚化结构域的蛋白 2 (NOD2) 的刺激。
▸ 肠道共生细菌还可以防止感染时的肌肉萎缩
共生大肠杆菌在骨骼肌中维持 IGF-1 信号传导,独立于宿主代谢、热量吸收或炎症,从而防止肠道或肺部感染后肌肉萎缩。
▸ 与饱腹感和新陈代谢有关的激素与特定共生菌群丰度相关
在动物模型中,双歧杆菌和乳酸菌丰度与瘦素浓度呈正相关,而生长素释放肽则与拟杆菌和普雷沃氏菌丰度呈正相关。
在营养不良模型中,生长素释放肽水平还与双歧杆菌、乳酸菌和球状球菌-直肠真杆菌呈负相关。一项针对 6 至 24 个月大的冈比亚儿童( n = 60)的横断面观察队列研究发现,严重营养不良儿童的肠道微生物群与代谢激素浓度之间存在许多密切相关性,使用网络分析模拟肠道微生物组和激素相互作用。埃希氏菌/志贺氏菌通过其与生长素释放肽和生长素释放肽受体的相互作用,在区分健康对照和营养不良患者方面具有高度预测性,而粘膜乳杆菌与瘦素/瘦素受体之间的相互作用也对营养不良和营养良好的儿童具有高度区分性。肠杆菌科细菌和 IGF-1 的相互作用也区分了 MAM 和 SAM。
这些相互作用可能是双向的,瘦素可以刺激粘蛋白的产生并改变肠道微生物组的组成,而特定的产生脂多糖的肠杆菌科细菌的炎症活性可能会损害 IGF-1 和 GH 信号传导。
微生物群在整个生命过程中与宿主免疫系统保持着相互的、动态的沟通,而这种沟通会因营养不良而被破坏。
越来越多的证据表明,营养不良的儿童在免疫学上与营养充足的同龄人不同,胸腺较小,免疫细胞组成和分布在质量和数量上不同,全身和肠道环境中的促炎介质长期升高,以及由不利因素驱动的免疫基因上的表观遗传标记。
产前和产后暴露。迄今为止,大多数营养不良儿童的免疫表型都是在感染和病原体携带的背景下进行研究的。然而,新出现的数据表明,肠道微生物组内共生和条件致病微生物的多样性可能会驱动营养不良儿童的独特免疫表型,而与病原体无关。
▸ 营养不良引起的肠道炎症的特征——EED生物标志物
例如钙卫蛋白和髓过氧化物酶,这些生物标志物是由肠道组织中微生物激活的先天免疫细胞产生的,这些细胞可能会被破坏的肠道微生物组激活。
EED 动物模型表明,营养缺乏的小鼠与营养充足的小鼠相比,肠道菌群失调会导致小肠上皮内淋巴细胞数量增加和促炎细胞因子分泌增加。尽管空肠免疫激活增加,但营养缺乏的动物在肠道内抑制鼠伤寒沙门氏菌感染的能力较差,导致细菌传播到脾脏和肝脏,并导致肝脏分泌促炎介质。
▸ 儿童营养不良还与慢性全身炎症有关
尽管反复出现症状的感染可以引发全身炎症表型,但小鼠模型表明,在没有明显感染的情况下,肠道微生物群和/或其成分系统性扩散到功能失调的肠道屏障进入循环也可能发生这种情况,如 EED 中观察到的那样。
与营养充足的幼鼠相比,断奶后采用缺乏蛋白质、铁、锌的饮食的健康小鼠出现了微生物群失调和体重减轻,这与向结肠给药时未能含有脂多糖有关;全身、盲肠和结肠(但不包括回肠)促炎细胞因子升高;在没有感染的情况下,LPS 攻击后促炎细胞因子的分泌增多。
在该模型中,通过针对革兰氏阴性(LPS 阳性)而非革兰氏阳性(LPS 阴性)共生体的抗生素治疗,使体重增加和促炎性免疫反应的差异正常化。
该模型中抗生素治疗效果的选择性支持了对革兰氏阴性微生物群成分的播散性促炎性免疫反应的作用,这些微生物群成分从肠道转移到循环系统中,从而导致营养不良的体重和身高缺陷。
由微生物易位驱动的慢性全身炎症可能影响人体测量的一种方式是通过抑制生长因子信号传导和骨/骨骼肌生长。来自动物研究的证据表明,依赖于微生物群代谢的唾液酸化HMO会增加成骨细胞驱动的骨形成,并且该过程是由 Th2 极化免疫反应介导的,即增加大肠中的嗜酸性粒细胞募集和嗜酸细胞趋化因子浓度。
中低收入国家儿科队列研究一致的证据表明,炎症介质也与IGF-1呈负相关。
注:前面讲过,营养良好和营养不良的儿童之间存在激素差异,尤其是与生长[生长激素 (GH) 和胰岛素样生长因子 1 (IGF-1)] 和食欲调节(瘦素和生长素释放肽)相关的激素差异。
包括 sCD14、补体蛋白 2、巨噬细胞炎症蛋白 1B 和 LBP 在内的炎症介质与SAM入院后康复儿童的体重和/或 MUAC 增加呈负相关。
▸ 炎症介质对生长的直接影响
无菌小鼠持续过度表达促炎细胞因子 IL-6 和循环 IGF-1 减少,生长速度较慢,并且比非无菌同窝小鼠小 30-50%,这种表型可以通过给予 IL-6 来部分挽救。
研究发现,IL-1β 和TNFα 与 IL-6 一起下调人肝细胞中生长激素受体 (GHR) 的表达、通过细胞因子信号传导抑制因子 3 (SOCS3) 产生的 GH 信号传导以及 IGF-1 的产生体外细胞系和小鼠肝脏体内细胞系。
▸ 微生物群:或将使炎症驱动的生长缺陷正常化
在一项以豆类为基础的治疗性营养的临床试验中,已经探索了将微生物群作为使炎症驱动的生长缺陷正常化的一种手段的潜力,该营养旨在增强营养不良的孟加拉国儿童肠道微生物组的多样性和成熟度。
与之前的观察结果一致,30 名 SAM 儿童在基线时可以通过血浆蛋白质组与 21 名健康儿童区分开来,该血浆蛋白质组与较低的骨化和成骨细胞分化以及较高的急性期炎症反应有关,包括 C 反应蛋白 (CRP)、IL- 6、促炎核因子 kappa B (NF-κB) 信号通路中的中间蛋白。干预后,尽管证据表明总体肠道病原体携带或绝对粪便微生物群多样性存在差异,但 WHZ 和微生物群成熟度有所增加;这些变化与血浆蛋白质组向健康生长和减少炎症特征的转变有关,表明肠道微生物组针对性的干预措施可以减少营养不良相关的炎症。
菌群失调引起肠道和全身炎症的能力也可能取决于抗体介导的肠道微生物组成的控制。肠道中的分泌性免疫球蛋白,特别是免疫球蛋白 A (IgA),选择性地结合微生物组成分,从而调节微生物组组成。
扩展阅读:
▸ 发育不良:IgA靶向的细菌比例更高
研究发现,与来自马达加斯加和中非共和国的非发育迟缓对照儿童相比,发育不良儿童的粪便中 IgA 所靶向的细菌比例更高。除了 IgA 靶向肠道微生物群的数量差异外,IgA 还靶向健康儿童与 SAM 儿童不同的肠道微生物子集。其中 IgA 倾向于靶向SAM 儿童中的肠杆菌科细菌,同时针对健康儿童中更广泛的共生生物。
从患有 SAM 的儿童身上提取的IgA +微生物群在移植到小鼠体内时会诱发类似 EED 的病理学和全身炎症,这种效应依赖于营养不良的饮食。
在另一个模型中,给小鼠喂食低蛋白、低脂肪饮食,并进行或不进行细菌灌胃来模拟 EED,这些小鼠的 IgA 对乳杆菌属的靶向作用受损。尽管空肠中乳酸杆菌的相对丰度、粪便 IgA 总量以及 IgA 目标细菌总数的百分比与营养良好的对照组相似。
这些差异是由于乳杆菌碳水化合物代谢对饮食变化的适应,而不是 IgA 丰度或亲合力的差异。总的来说,这些观察结果强调了肠道屏障处免疫-微生物群相互作用的可塑性,有证据表明,微生物群和组织驻留免疫细胞的适应可能会损害 EED 中微生物及其抗原的免疫介导遏制,从而导致生长缓慢。
▸ 营养不良儿童的口服疫苗反应受损并反映营养不良中存在的一些免疫缺陷
小鼠模型为营养不良时微生物组失调如何损害口服疫苗的免疫原性提供了一些线索。然而,这些范式需要在人类队列研究中进一步探索。
在针对产肠毒素大肠杆菌(ETEC)进行初免加强口服疫苗接种后,由于饮食缺乏和大肠杆菌粘附定植而诱导出现 EED 样表型的小鼠,其小肠中的疫苗特异性 CD4 + T 细胞较低,且疫苗水平较低-相对于饲喂营养充足饮食的小鼠和饲喂营养不足或充足饮食的未定植小鼠的特异性 IgA。这些差异取决于微生物群,因为 ETEC 定植小鼠的小肠疫苗特异性 T 细胞数量在广谱抗生素治疗 3 周后恢复正常。
EED 表型中疫苗反应受损是由于微生物群依赖性 RORγT + FOXP3 +Treg 的扩张,这些细胞能够抑制小肠中的疫苗反应;小肠中疫苗特异性 CD4 + T 细胞增殖和 IgA 丰度得到恢复,并且在有条件地消耗 Tregs 后体重增加百分比增加。
总的来说,这些研究为微生物群靶向疗法如何恢复营养不良儿童受损的免疫表型(包括受损的疫苗反应)提供了概念证明,但也强调了固有的免疫和微生物异质性,在设计转化研究和人群时应考虑到这一点。
许多研究开始探索食物或食物成分对整个童年时期肠道微生物组的影响。
纳入的试验采用了涉及天然食品的干预措施;微量营养素补充或强化;食品成分,例如牛乳脂肪球膜(MFGM);以及特殊配方食品,例如早期限量配方食品(ELF)、即用治疗食品、即用补充食品(RUSF)和脂类营养补充剂(LNS)。
母乳
纯母乳喂养的婴儿往往含有较高比例的双歧杆菌和乳酸菌属。与配方奶喂养的婴儿相比,他们的肠道微生物组往往含有更高丰度的潜在致病菌,例如变形菌门成员。
双歧杆菌属丰度更高对婴儿健康有益,而肠球菌属的比例较高与不良的健康结果相关。
从瓶子中挤出的母乳,与潜在病原体的富集和双歧杆菌的消耗相关。
▸ 母乳是一种复杂的基质,有助于双歧杆菌定植
母乳含有许多成分,包括乳糖、400 多种不同的脂肪酸、蛋白质(乳清)、核苷酸、维生素、矿物质、乳脂肪球 (MFG) 、HMO等。
HMO 可以与牛奶中的其他化合物(例如糖复合物)结合,形成母乳聚糖 (HMG),其完整地到达婴儿结肠并驱动细菌定植,特别是双歧杆菌的定植。
HMG 逃脱肠道消化并转运到结肠,进入那里常驻双歧杆菌的发酵循环,使这些物种能够增殖并在 HMO 的双歧杆菌效应的过程中占据主导地位。特别是,婴儿双歧杆菌(ATCC 15697) 、短双歧杆菌、长双歧杆菌和双歧双歧杆菌(PRL2010) 在婴儿期占主导地位,是更健康肠道微生物组的标志。
▸ 母乳本身也含有细菌
在几组哺乳期妇女中,发现母乳样本最常见有葡萄球菌、链球菌和假单胞菌,其他分类单元因女性和环境而异;这些细菌可能有助于在婴儿肠道中播种。
配方奶
▸ 配方奶与对肠道微生物群的潜在负面影响有关
a ) pH 值的变化,导致大肠杆菌和沙门氏菌等细菌过度生长,从而破坏肠道完整性,可能是由于蛋白质类型和含量的差异
b ) 牛乳中缺乏母乳中存在的游离氨基酸和某些生物活性化合物。
食用牛奶配方奶粉的婴儿往往具有较高的肠道微生物多样性和丰富的厚壁菌门、梭状芽胞杆菌、肠球菌属、肠杆菌科和拟杆菌属和双歧杆菌属的丰度较低。
在配方奶喂养的婴儿中存在的双歧杆菌属中,有更多的青春双歧杆菌和假链状双歧杆菌,这两种细菌都与成人肠道微生物群有关。
▸ MFGM 对肠道菌群的影响:嗜血杆菌水平较低
MFGM (牛乳脂肪球膜)因其在婴儿肠道成熟、免疫以及大脑结构和功能中的潜在作用而受到关注。MFGM 源自乳腺上皮,包含 60% 蛋白质和 40% 脂质,使 MFG 稳定为乳液。为了复制母乳,婴儿配方奶粉中添加了牛 MFGM。
在 2 至 6 个月龄期间,MFGM 配方奶粉组的几种氨基酸及其分解产物的含量较低,乳酸和琥珀酸的含量也较低。12 个月时,MFGM 组的婴儿嗜血杆菌水平较低与接受标准配方奶粉的婴儿相比,该属含有多种病原体。
然而,与母乳喂养(非随机)参考组相比,MFGM 配方奶粉组的微生物群与标准配方奶粉组的微生物群更相似,因此,将 MFGM 和标准组的结果汇总进行分析,并与来自 MFGM 配方奶粉组的结果进行比较。
▸ ELF:改善健康的同时,尽量不破坏肠道菌群
母乳和婴儿配方奶粉中乳清蛋白和酪蛋白的含量各不相同。婴儿配方奶粉中牛奶的比例较高,较难消化。水解牛奶可以提高其消化率,水解牛奶用于早期限量配方食品(ELF),用于纯母乳喂养的新生儿作为干预措施,以增加肠内摄入量并避免并发症,例如胆红素血症或脱水。
与纯母乳喂养相比,ELF 不会导致α 多样性或群落结构出现显着差异,也不会导致乳杆菌丰度降低或更高丰度的梭状芽胞杆菌。这些发现表明,ELF 可能有助于改善体重大幅减轻的新生儿的健康,同时不会对肠道微生物群产生不利影响。
碳水化合物
碳水化合物包括简单的单糖和二糖以及复杂的寡糖和多糖,例如淀粉和纤维素。简单的糖在小肠 (SI) 中被消化和吸收,而复杂的或非血糖碳水化合物在到达结肠之前仍未被消化。
后者已被证明可以通过聚糖的降解来调节肠道微生物群,特别是以纤维和寡糖的形式。
关于单糖对肠道微生物群影响的研究有限,因为它们通常不会到达大肠;更常见的是针对人工甜味剂影响的研究或高糖、高脂肪的西方饮食的组合对肠道微生物群的影响。
注:单糖,如葡萄糖、半乳糖和果糖;二糖,例如乳糖、蔗糖、麦芽糖和海藻糖;和糖醇(多元醇)
▸ 果糖
一项小鼠研究中,果糖可以逃避肠道吸收并到达结肠,从而降低多形拟杆菌的丰度。
在一项针对 12-19 岁青少年的队列研究中,高果糖摄入量与真杆菌和链球菌含量降低有关,而这些细菌被认为有利于碳水化合物代谢。这些研究的结果提供了一些证据,证明在随机试验中检查单糖对人类肠道微生物组的影响是有益的,这些试验尚未在儿童中进行。
▸ 复杂碳水化合物
包括寡糖、多糖和膳食纤维,可以起到益生元的作用,被定义为“被宿主微生物选择性利用并赋予健康益处的底物”。这些分子不会被人类消化,而是被完整地运送到结肠,在那里微生物可能会代谢和发酵它们。
碳水化合物益生元包括HMO、低聚果糖、低聚半乳糖、甘露低聚糖、低聚木糖和膳食纤维,例如不溶性纤维,包括纤维素和半纤维素,例如β-葡聚糖(来自燕麦)。碳水化合物益生元还包括可溶性纤维,例如果胶和菊粉,两者都是微生物发酵罐的底物,包括长双歧杆菌亚种、婴儿杆菌、拟杆菌、拟杆菌、乳杆菌和普氏粪杆菌。
▸ 益生元通过直接机制发挥作用
简而言之,结构与宿主聚糖相似的碳水化合物分子可以直接阻断与宿主细胞的粘附;β-葡聚糖可以与吞噬细胞和自然杀伤细胞上的受体结合,引发中性粒细胞的吞噬作用;
菊粉型果聚糖可以通过 Toll 样受体、C 型凝集素受体和半乳糖凝集素作为肠道树突状细胞的受体,诱导抗炎细胞因子。
▸ 益生元可以间接地选择有益共生细菌的增殖
其代谢副产物可以直接影响肠道环境或宿主基因表达。例如,与潜在致病性大肠杆菌和梭菌相比,双歧杆菌属、拟杆菌和厚壁菌门中的物种将到达结肠的未消化碳水化合物发酵成微生物副产物,宿主或其他共生细菌可以将其用作底物。
▸ 麸皮添加:微生物群的变化因基线饮食差异而异
麸皮(小麦、燕麦和大米等谷物的外皮)是益生元可溶性纤维以及其他营养素(如植物化学物质、脂肪酸和酚类物质)的主要来源。
在一项试验中,生活在尼加拉瓜 ( n = 47) 和马里 ( n = 48)的 6 个月大婴儿每天补充米糠(每天 1-5 克),添加到断奶食品中,或者不进行干预 6 个月。
不同国家的基线肠道微生物群落结构(通过非度量多维尺度(NMDS)绘制的布雷-柯蒂斯差异来测量)存在差异,这种差异导致 8 个月和 12 个月龄时微生物对米糠补充剂的反应越来越明显;例如,马里样本在两个时间点的群落结构差异(NMDS 图上的分离)更为明显。对米糠摄入量敏感的属也因国家而异:在尼加拉瓜,8 个月和 12 个月龄时,双歧杆菌属、乳杆菌和韦荣球菌的相对丰度增加,而在马里乳杆菌在 8 个月和 12 个月大时,对米糠的反应丰度有所增加。
这些反应性类群被公认为碳水化合物消化者。这项研究在比较这些人群时的一个局限性是,整个马里队列都是纯母乳喂养和阴道分娩,而尼加拉瓜样本包括配方奶喂养和大多数剖腹产婴儿;这些基线饮食差异可能导致了微生物对米糠的不同反应。
引入补充食品,包括低聚糖的植物性食物来源,例如大豆和其他豆类、水果和蔬菜,帮助婴儿肠道微生物群多样化并增加其丰富度,使其达到类似成人的组成。
▸ 蜂蜜:双歧双歧杆菌有变化
蜂蜜是单糖(即葡萄糖、果糖、蔗糖和麦芽糖)以及益生元低聚果糖的来源。
在早产儿肠道微生物群研究中,埃及早产儿 ( n = 40) 连续 14 天食用添加到牛奶配方奶粉中的 5、10、15 或 0 克医用级三叶草蜂蜜。从定量实时聚合酶链反应 (qRT-PCR) 结果来看,双歧双歧杆菌似乎以剂量依赖性方式对蜂蜜做出反应,而乳酸杆菌种不会。10g 组的计数最高,5g、15g 和 0g 组变化不大;这可能与这些细菌的底物代谢差异有关。
一些局限性包括样本量小(每组仅 10 名婴儿)、通过 qRT-PCR 定量特定细菌(相对于整个细菌群落的下一代测序)、干预持续时间短以及研究结果的适用性(考虑到不推荐蜂蜜)对于 12 个月以下的儿童,因为担心它可能含有导致婴儿肉毒杆菌中毒的细菌。
然而,作为一项试点研究,这些发现为进一步研究蜂蜜和单糖对老年人群肠道微生物组的潜在影响提供了支持。除了豆类外,没有其他试验研究过碳水化合物在天然食品中的作用,包括天然存在的益生元,对足月婴儿或年龄较大的儿童或青少年人群的作用。
脂 肪
脂肪酸,包括单不饱和脂肪酸 (MUFA)、多不饱和脂肪酸 (PUFA)(例如亚麻酸 ω-3 和亚油酸 ω-6 脂肪酸)和饱和脂肪酸 (SFA),构成脂质分子的一部分,例如甘油三酯、磷脂、胆固醇和植物甾醇。
膳食脂肪在整个胃肠道中被分解。大多数甘油三酯的消化和吸收发生在小肠(特别是十二指肠)中,并且依赖于胰脂肪酶、肝脏中的胆汁盐和胆囊中的胆汁。
初级胆汁盐,包括胆酸盐和鹅脱氧胆酸盐,是由胆固醇合成的;共生微生物群从初级胆汁盐合成次级胆汁盐、脱氧胆酸盐和石胆酸盐,这些盐进一步被细菌用作底物或被肝细胞修饰。大约 7% 的游离脂肪酸完好无损地到达结肠,它们可能会影响体内的微生物群。食物通常含有短链、中链和长链脂肪酸的混合物。
脂肪酸影响肠道微生物群的机制仍然是一个活跃的研究领域,并且关于 SFA、MUFA 和 PUFA 对人类肠道微生物组的影响存在相互矛盾的证据。
▸ 促炎:饱和脂肪酸、ω-6 多不饱和脂肪酸; 抗炎:ω-6多不饱和脂肪酸、单不饱和脂肪酸
一些研究表明,SFAs 和 ω-6 PUFA 会促进炎症和氧化应激,而 ω-3 PUFA 和 MUFA 则具有积极作用,例如增加乳酸杆菌和双歧杆菌属。由于膳食脂肪的代谢需要氧气,因此脂肪不太可能成为厌氧肠道细菌的能量来源。然而,较高的脂肪摄入量可能会取代饮食中的膳食纤维和碳水化合物;因此,对肠道微生物群的影响可能是由于饮食替代或较低的碳水化合物底物可用性,而不是较高的脂肪摄入量。膳食脂肪可能对细胞膜有杀菌作用,导致细菌丰度降低。此外,膳食脂肪可以诱导细菌增加胆汁酸代谢,以应对增加的脂肪。
一项研究旨在分析鱼和红花油的混合物对接受小肠肠造口术的早产儿(n = 16)肠道微生物群的影响(即在腹壁上开一个开口,以便在出生后进行肠内喂养)因炎症性疾病而需要进行腹部手术,例如坏死性小肠结肠炎 (NEC),与标准护理相比这是早产儿的常见病症。
与标准营养疗法相比,干预措施持续 9 周,结果增加了微生物α 多样性,降低了潜在致病菌(肠杆菌科、梭状芽胞杆菌)的丰度,并丰富了碳水化合物代谢的预测基因功能。
总之,这些研究表明,ω-3 LCPUFA 干预可能会改善婴儿肠道微生物群多样性、组成和预测功能,特别是患 NEC 的早产儿,但母亲在怀孕期间摄入 LCPUFA 不会影响婴儿肠道微生物组。
蛋白质
膳食蛋白质由形成肽的氨基酸 (AA) 组成,肽是组织的基本组成部分。氨基酸对于骨骼肌功能、生长、健康、发育和生存至关重要,可以为宿主和肠道微生物群提供能量,而肠道微生物群可以改变宿主对氨基酸的生物利用度。
膳食蛋白质的消化从胃开始,蛋白酶将蛋白质切割成大肽。小肠中的肽酶分解这些肽,以便随后由肠上皮细胞和腔细菌进行转运和分解代谢。
增加蛋白质摄入量通常会导致结肠消化率降低和可发酵底物增加。细菌将游离氨基酸转化为多肽有助于肠道中氨基酸的代谢和生物利用度,而 L-谷氨酰胺等氨基酸的可用性可以调节必需和非必需氨基酸的小肠细菌代谢。
结肠细菌,特别是拟杆菌、梭状芽胞杆菌和大肠菌,将摄入的蛋白质和来自宿主酶、粘蛋白和脱落的肠细胞的内源蛋白质转化,产生副产物,例如较短的肽、AA、脂肪酸(例如 SCFA)和气体例如氨和硫化氢。
整个肠道的蛋白水解活性各不相同:例如,体外实验发现,与回肠微生物群相比,结肠微生物群可以更有效地降解结肠中的牛血清白蛋白,具体取决于 pH 水平、碳水化合物可用性和肠道模型保留时间。
▸ 较高的蛋白质摄入量:促进潜在致病菌
较高的蛋白质摄入量(例如西方饮食中的蛋白质)被认为会增加 pH 值,从而减少双歧杆菌等严格厌氧菌的生长。并促进蛋白质发酵,潜在致病性兼性厌氧细菌。
这些细菌,例如大肠杆菌和沙门氏菌,可以通过形成降解产物(例如三甲胺氧化物以及芳香族和支链氨基酸)来破坏肠道屏障和免疫系统;这些副产品与胰岛素抵抗和 2 型糖尿病有关。除了摄入水平之外,蛋白质来源、浓度和 AA 组成也会影响肠道微生物群的组成和功能。
▸ 蛋白质来源会导致微生物组成和功能的变化
由于植物细胞壁的原因,豆类等植物蛋白不能被宿主酶完全消化,导致它们作为微生物发酵的益生元运输到结肠。
难解析出植物蛋白来源中的蛋白质、纤维或其他化学物质的个体效应,但总的来说,这些蛋白质来源往往与细菌组成的有益变化有关,包括乳酸菌的生长和更大的微生物多样性。
进行了两项试验,利用 V4 区的 16S 测序来检查植物性蛋白质来源(包括豇豆、黄豌豆和普通豆)对肠道微生物群的影响。
一项试验比较了烤豇豆粉(25% 蛋白质,21% 纤维)、烤普通豆粉(25% 蛋白质,28% 纤维)和挤压煮熟的玉米大豆混合 (CSB) 面粉(13% 蛋白质,8% 纤维) ,6 个月大的儿童每天服用 6 个月,豇豆导致双歧杆菌属的比例更高。
与普通豆和 CSB 相比, 9 至 12 个月期间普雷沃氏菌丰度较低,6 至 9 个月期间埃希氏菌/志贺氏菌丰度较低;这是出乎意料的,因为与普通豆相比,豇豆的纤维含量较低。
另一项针对儿童(6-10 岁)的研究检查了四种不同剂量的补充微量营养素的豆类蛋白质(黄豌豆)(即 6、8、10 或 12 克),连续 1 个月每天食用两次,在厚壁菌门和拟杆菌门中发现了 9 个有区别的类群,其中许多与植物多糖发酵和 SCFA 生产有关——对应于肠道微生物组的变化。
三个类群(普雷沃菌属、颤旋菌属、普氏镰刀菌)与儿童线性生长的增加显着相关,并且所有类群的相对丰度发生变化,特别是在最低蛋白质剂量组(6 g)和最高蛋白质剂量组(12 g)。这些结果强调了豆类对肠道微生物群的潜在剂量反应效应,并确定了与功能结果(例如儿童线性生长)相关的分类群以进一步研究。
与植物蛋白相比,动物来源的蛋白质在近端肠道更容易消化,因此运输到结肠的蛋白质较少,导致结肠微生物群调节减少,并可能抑制病原体。
维生素A
维生素A是一类具有全反式视黄醇生物活性的类视黄醇化合物,包括视黄醛(视黄醛)、视黄酸、视黄酯(主要是棕榈酸视黄酯)和类胡萝卜素化合物,如β-胡萝卜素、α-胡萝卜素和β-胡萝卜素。
▸ 维生素 A 的功能
维生素 A 对于维持肠道屏障的完整性和受损粘膜上皮的再生至关重要,特别是肠上皮细胞的正常增殖和产生粘液的杯状细胞分化,这会影响肠道微生物群的定植和粘附。
膳食维生素 A 可以作为植物来源的维生素 A 原(类胡萝卜素)或动物来源的预制维生素 A(视黄酯)形式食用。
▸ 维生素 A在体内的加工
消化从咀嚼开始,包括通过胆汁盐和胰脂肪酶的胃作用,胆汁盐和胰脂肪酶在肠腔中从膳食脂质形成混合胶束以供吸收。虽然预先形成的维生素 A 来源更容易被宿主肠细胞吸收以运输至储存或循环,但维生素 A 原类胡萝卜素必须进一步加工才能转化为类视黄醇并被宿主使用。
▸ β-胡萝卜素的吸收
根据食物基质的不同,大约 5-50% 的 β-胡萝卜素被吸收。例如,膳食脂质的存在会增加小肠中类胡萝卜素的吸收;如果β-胡萝卜素被纤维吸附,它可以绕过上肠的吸收并被转运到结肠。结肠微生物群可以消化纤维,释放β-胡萝卜素供结肠细胞吸收。在结肠粘膜中发现了类胡萝卜素,主要是在升结肠中。
一项研究发现,大肠杆菌表达一种与 β-胡萝卜素单加氧酶 1 同源的耐盐酶,使大肠杆菌能够积累 β-胡萝卜素;然而,没有证据表明这种β-胡萝卜素被裂解形成视网膜以供进一步使用。
▸ 维生素A与普通拟杆菌:此消彼长
在一项针对小鼠的研究中,普通拟杆菌(Bacteroides vulgatus)先前被证明是一种生长歧视类群,随维生素 A 补充而丰度降低,并因维生素 A 缺乏而丰度增加,可能与胆汁酸代谢的改变有关。作者报告说,这些变化是由于普通双歧杆菌视黄醇流出系统的破坏以及随后对视黄醇和胆汁辅助敏感性的影响造成的。
▸ 肠道共生菌与视黄酸代谢
另一项针对小鼠的研究发现,粘膜树突状细胞 (DC) 对肠道共生婴儿双歧杆菌进行摄取,导致其从维生素 A 向视黄酸的转化增加,并且具有更高数量的具有耐受性的粘膜 DC,例如抑制 1 型 T 辅助细胞(Th1) 和 Th17 细胞。这种效果也随着宿主视黄酸状态的不同而变化。然而,还需要对人类进行进一步的研究,因为啮齿类动物的类胡萝卜素代谢效率比人类高得多,并且没有其他动物模型能够完全代表人类类胡萝卜素代谢。
最近的一项研究检查了补充维生素 A 对新生儿肠道微生物群的影响,结果发现对细菌组成(包括大双歧杆菌属)有积极的以及性别特异性的影响。
与安慰剂相比,入组时单剂量 50,000 国际单位剂量不会改变α-多样性,但在 6-15 周龄时对雄性产生双歧效应,但对雌性没有影响;作者推测,这可能有助于解释本研究中男性死亡率低于女性的原因。
维生素E
维生素 E 主要通过 α-生育酚活性发挥抗氧化剂的作用。
α-生育酚可来源于坚果、植物油、乳制品、奶酪和鸡蛋,也可以作为酯化 α-生育酚的补充剂形式食用。
作为自由基清除剂,α-生育酚可破坏细胞膜和血浆脂蛋白中的自由基链,以维持 LCPUFA 的完整性。维生素E与膳食脂质一起被吸收到肠道细胞中,融入乳糜微粒中,分泌到淋巴系统中,并转运到肝脏,然后被极低密度脂蛋白吸收并分泌到与α-生育酚转移蛋白结合的血液中; 然而,其吸收和贩运的许多细节基本上不为人所知。
经过额外的代谢步骤后,未结合的维生素 E 异构体通过粪便和尿液排出体外。维生素 E 与铁一起,与氧化电位降低有关;因此,维生素 E 被认为可以改善铁相关炎症的影响,改善肠道微生物群的结果。
一项针对美国缺铁 6 个月大婴儿的研究发现,每天两次服用 18 毫克维生素 E 和 15 毫克元素铁,持续 2 个月,并不会导致细菌多样性的变化,但确实会导致相对细菌多样性的变化出现差异。随着时间的推移,维生素 E 与铁的结合导致拟杆菌门(尤其是拟杆菌科)数量减少,而厚壁菌门(尤其是毛螺菌科)和罗氏菌属(Roseburia)数量增加。Roseburia产生丁酸盐,可以刺激结肠血流。
铁
铁是人体内最丰富的微量营养素,对于人体的氧运输、氧化还原反应、新陈代谢和电子传递链机制以及许多细菌的新陈代谢和毒力功能至关重要。
膳食血红素铁 (10%) 和非血红素铁 (90%) 的摄取和吸收存在不同的机制。牛肉是血红素铁的来源;美国的一项对测序研究使用牛肉作为干预措施。从 16S测序数据来看,以牛肉作为补充食品的群体中双歧杆菌属没有下降。与基线相比,4 周后细菌种类丰富度更高;4 个月后,放线菌和 XIVa 族梭菌(丁酸盐生产者)的丰度增加,并且与铁强化婴儿谷物相比,拟杆菌门较低。
差异可能是由于肉类中铁的生物利用度较高,以及未吸收的铁进入结肠,以及铁强化谷物类中存在植酸盐。
▸ 铁的生物利用度
铁的生物利用度随着植酸盐和多酚的存在而降低,而抗坏血酸(维生素 C)则提高铁的生物利用度。胃酸和蛋白水解可能会从食物基质中释放非血红素铁,需要更多的消化才能释放血红素和铁蛋白。一些细菌可以通过特殊机制获取食物中的铁源,例如解没食子链球菌或路邓葡萄球菌降解多酚单宁酸。
营养干预措施对肠道菌群影响的潜在机制
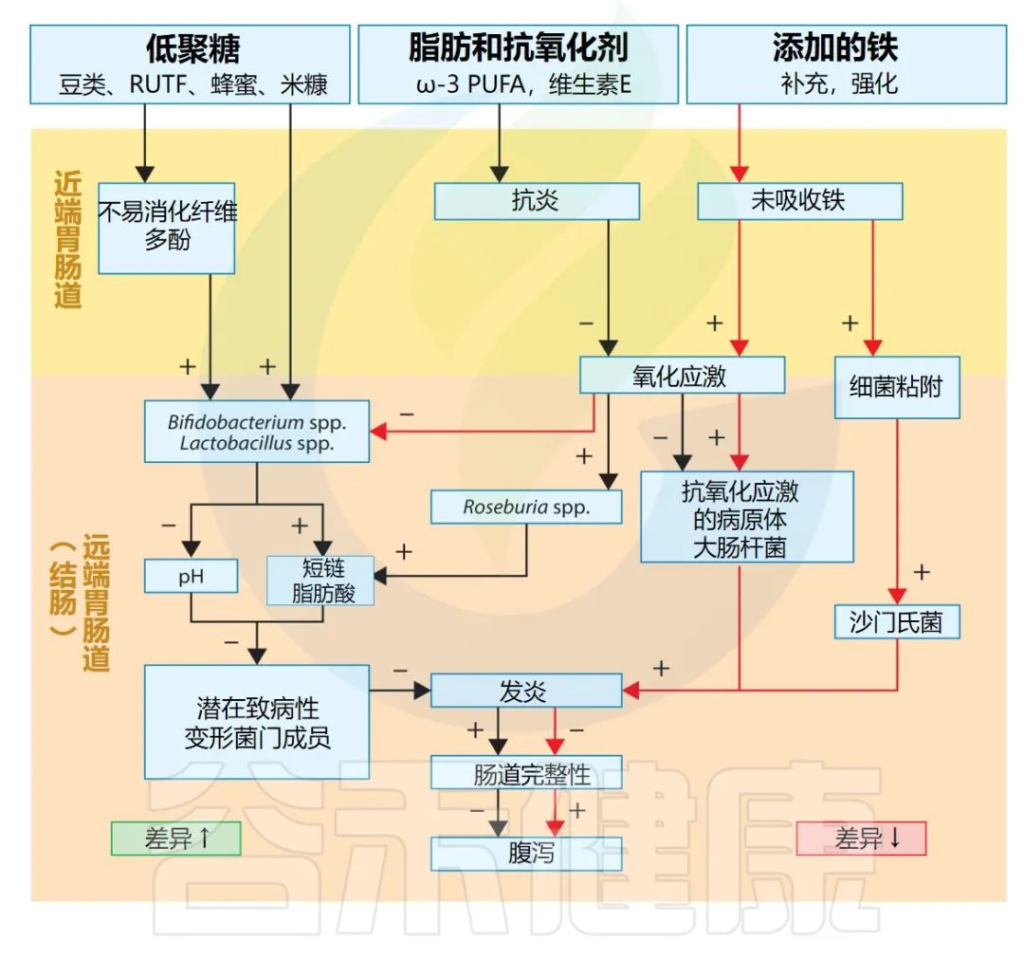
doi.org/10.1146/annurev-nutr-021020-025755
▸ 未吸收的铁被认为会刺激肠道中细菌病原体的生长和毒力
例如大肠杆菌,而宿主铁的状态会影响细菌免疫防御和宿主炎症反应,包括乳杆菌科和伯氏疏螺旋体在内的一些细菌不依赖铁生长,而是利用锰。
链球菌属可以使用铁或锰,具体取决于可用性。大肠杆菌使用 Feo 摄取系统来摄取二价铁,而三价铁在摄取之前首先被细胞外还原酶还原为二价铁,或者被摄取为柠檬酸铁或与细菌铁载体结合。
▸ 感染期间可用铁量的变化向毒力基因发送信号
低铁会导致铁载体抑制和毒素上调,而较高的铁可用性会诱导细菌粘附到肠上皮细胞,如肠沙门氏菌的情况鼠伤寒血清型。缺铁还会减少肠道细菌(包括Roseburia 、直肠真杆菌和梭状芽胞杆菌IV 族成员)等产生的短链脂肪酸。
在易缺铁的人群中,婴儿和幼儿最常需要口服铁剂治疗,例如补充剂,尽管他们的肠道微生物群仍在成熟。
▸ 铁干预措施对腹泻:负面影响
多项研究表明铁干预措施对腹泻等胃肠道症状有负面影响以及肠道微生物群的变化,例如较高的肠杆菌科和较低的乳杆菌科和双歧杆菌属。
▸ 铁补充剂,取决于基线铁或贫血状态
为了帮助抵消铁的这些影响,儿童随机试验检查了铁与维生素 E 等抗氧化剂结合使用的效果或冻干覆盆子作为抗氧化剂来源。例如,在加拿大一项研究中,与仅接受铁强化谷物的婴儿相比,接受含冻干覆盆子的电解铁强化米粉的婴儿在2 -4周后肠道微生物组的丰富度和多样性有所增加。
然而,接受冻干覆盆子的组活性氧并没有显着减少,与胃肠道中过量铁相关的炎症过程的引发剂;这可能是由于冻干覆盆子的消耗量很小,或者与新鲜覆盆子中的抗氧化剂含量相比可能较低,而新鲜覆盆子没有被任何群体食用。
在未来的研究中,考虑其他抗氧化剂来源(例如新鲜浆果或提取物)和不同剂量的这些抗氧化剂来源,以及对大量贫血婴儿的研究或铁充足,将有助于建立铁和抗氧化剂之间潜在的相互作用。
▸ 使用铁剂联合干预的随机试验
包括叶酸, 锌和多种微量营养素(MMN),无论是片剂的形式还是作为微量营养素粉(MNP)的一部分。铁的形式包括硫酸亚铁、富马酸亚铁、NaFeEDTA 和电解铁,它们可能对儿童肠道微生物群产生不同的影响;其他变量包括给药剂量、基线铁和贫血状况、抗氧化剂和其他微量营养素等辅助干预措施以及研究环境。
大多数检查 MNP 的研究都是在肯尼亚针对开始添加辅食的 6 个月大婴儿进行的;MNP 与玉米粥一起服用 3 至 4 个月。MNP 的微量营养素成分各不相同,但都含有维生素 A、叶酸和维生素 C,并且除了一种还含有 B 族维生素、维生素 D、铜、碘、硒和锌。
根据靶向 qRT-PCR 结果,MNP ( MixMe ) 加上 2.5 mg NaFeEDTA 4 个月,导致大肠杆菌/志贺氏菌丰度增加,以及肠杆菌科:双歧杆菌属比例增加。与单独使用相同MNP产生的丰度相比,10个月大时的比例增加。
在一项比较 MNP(Sprinkles)加 12.5 毫克富马酸亚铁与单独使用相同 MNP 的试验中,以及当含铁组组合并与仅使用 MNP 的组进行比较时,也观察到了类似的结果。
在另一项试验中,与单独使用相同的 MNP 相比,MNP 中的铁含量(2.5 mg NaFeEDTA 和 2.5 mg富马酸亚铁)对微生物组组成有显着影响,包括较低丰度的有益菌(如乳杆菌属和双歧杆菌属)以及较高比例的梭菌目,而拟杆菌门在各组之间保持相似。在一项辅助研究中,抗生素治疗并没有抵消铁的作用,铁仍然导致肠杆菌科细菌的增加。
最后,在另一项试验中,与单独的 MNP 相比,含铁的 MNP(12.5 毫克富马酸亚铁)在多样性或相对丰度方面没有组间差异。然而,接受含铁 MNP 的组梭状芽胞杆菌增加,双歧杆菌减少,而仅接受 MNP 的组大肠杆菌减少。
尽管 MNP 配方和 16S 测序区域存在差异,但这些研究一致发现铁会导致有益细菌减少和可能有害细菌增加,这为铁对肠道微生物组的影响提供了多种证据。需要进一步的研究来检查铁在其他环境中对肠道微生物组的影响。
▸ 铁强化和补充剂:对肠道菌群的影响
在科特迪瓦 6-14 岁儿童中(n = 60),铁强化饼干(20 毫克电解铁)不会导致微生物多样性发生变化,肠杆菌科细菌增加,乳杆菌属细菌减少,并且双歧杆菌属没有差异。6个月后这些发现与之前对婴儿进行的研究一致。
在南非进行的另一项针对 6-11 岁儿童的研究中,与安慰剂组(两组均服用维生素 C)相比,饮用含 50 毫克硫酸亚铁的饮料会导致组内相对含量存在差异;然而,尽管铁剂量较高,但没有发现组间差异。这些发现可能是由于肠道病原体负担和卫生设施的差异造成的,包括优质水和卫生设施、饮食质量和感染负担。
▸ 存在于全食物基质中的铁可能有利于铁的吸收
如LNS,不会产生与铁相关的负面影响,例如增加潜在致病菌、炎症和腹泻等胃肠道疾病症状。
LNS由植物油、花生、奶粉、糖、维生素和矿物质组成,食用量约为54g小袋,或在少量的情况下,食用量为20g(~6g脂肪),以帮助解决大量营养素和能量不足问题,并满足微量营养素需求。
已经进行了三项随机试验来检验直接给予婴儿 LNS 的影响或在怀孕期间给予母亲,然后给予婴儿。在同一队列的两项研究中,6 个月大的儿童接受基于牛奶蛋白的 LNS、基于大豆蛋白的 LNS、CSB 或 12 个月内不接受干预。通过 16S rRNA V4 区域测序评估肠道微生物群,双歧杆菌属的定植率或计数没有差异。与未接受营养补充剂的对照组相比,接受 LNS 和 CSB 补充剂的组中发现了金黄色葡萄球菌或其他肠道细菌。
在另一项试验中,将 SQ-LNS(20 克铁)给予孕妇(妊娠 <29 周),然后给予 6 至 18 个月大的婴儿;对照组包括给怀孕期间和哺乳期前 6 个月的母亲服用含有 20 毫克铁的 MMN,或者给怀孕期间的母亲服用标准护理铁和叶酸(含有 60 毫克铁)加上安慰剂哺乳期的前 6 个月。
12 个月时,与任一对照组相比,SQ-LNS 组的婴儿肠道微生物α 多样性和均匀度更高,而β 多样性没有差异或观察年龄微生物群 z 评分 (MAZ)。
然而,由于干预组之间干预的类型、数量、接受者和给药方案存在差异(只有 SQ-LNS 组中的婴儿接受直接补充),因此很难确定任何一种特定的营养素或干预类型可能会造成这些影响。总之,这些发现表明,怀孕和哺乳期间补充铁可能不会影响新生儿和婴儿的微生物组。
锌
微量矿物质锌在体内发挥催化、结构和调节作用,包括肠道健康和免疫健康,并已广泛用于治疗严重腹泻。
锌的吸收主要发生在人体的小肠中,受到食品中含锌物质是否存在以及食品加工方法的影响。例如,植物性锌来源(如种子、根和块茎)中的植酸盐会抑制锌的吸收,而铁等其他微量营养素会竞争性地抑制锌的吸收,而谷物的发酵可以提高锌的吸收。
此外,由于存在组氨酸等氨基酸增强锌的溶解度,动物源产品中的锌更容易被利用。过量的锌,包括未吸收的膳食锌和内源性锌,以受控机制通过粪便排出体外,以维持体内平衡。由于体内没有锌的储存,低锌饮食后可能会迅速出现锌缺乏症。
▸ 共生菌和病原菌在肠道中的定植和功能可能受到锌的调节
锌对于许多细菌(例如毒力因子)至关重要,并因其抗菌作用而用于动物生产。
在大肠杆菌中,锌受到严格调控,并在 300 多种蛋白质中发挥结构和催化作用,并且许多细菌拥有重金属外排系统或进行特定重金属质粒的基因转移。乳酸杆菌等细菌对膳食锌的抗性也不同。
关于锌和肠道微生物群的研究主要在动物模型中进行;这些研究的作者发现了细菌组成的差异,特别是乳杆菌属、梭菌属和肠杆菌科。
一项针对患有继发于肺炎的抗生素相关性腹泻的 2-36 个月大儿童的研究,检查了锌补充剂与益生菌的作用,为期 14 天,与单独益生菌相比,双歧杆菌属的计数没有显着差异。与基线相比,每个干预组中大肠杆菌减少。
另一项针对 6 个月大儿童食用铁和锌强化或仅铁强化谷物的研究发现,锌可以抵消铁强化对肠道微生物群的潜在不利影响。
上面的证据表明肠道微生物组在生命早期生长中的作用,为儿童营养不良的营养和药物治疗提供了新的目标。
目前预防发育迟缓和消瘦的营养策略并不能完全解决短期和长期生长缺陷或相关的临床结果。6-24 个月龄小剂量脂质营养补充剂可将发育迟缓发生率降低12%,将严重发育迟缓发生率降低 17%。
使用即用型治疗食品 (RUTF) 对 SAM 进行社区管理可显着改善营养恢复;然而,复杂的 SAM 后仍然存在高死亡率和长期生长缺陷。
总的来说,目前的治疗方法通过抗生素解决感染负担,并通过单糖、脂质和微量营养素恢复宿主营养;然而,这些治疗方法并不专门针对肠道微生物组,而肠道微生物组可能有助于改善生长。
事实上,目前对复杂 SAM 的建议(包括在所有情况下进行抗生素治疗)可能会损害肠道微生物组的恢复。而越来越多的试验报告了针对微生物群的干预措施对儿童营养不良的临床有益效果。
益生菌
少数益生菌试验报告了在营养不良负担较高的环境中益生菌对儿童生长的不同影响。对 795 名 SAM 儿童进行的一项大型随机临床试验发现,尽管观察到门诊死亡率有降低的趋势,但多物种益生菌和益生元联合治疗对营养恢复、死亡率或相关临床症状没有影响。较小规模的试验表明,其他益生菌种类对 SAM 和其他形式的营养不良具有潜在益处。
长双歧杆菌亚种由于婴儿益生菌与资源匮乏环境中的生长呈正相关,因此它具有作为促进生长的潜在益生菌的巨大潜力。在孟加拉国开展的一项 SAM 儿童试验,在临床稳定和急性期管理后,将 62 名参与者随机分为婴儿双歧杆菌益生菌(婴儿双歧杆菌 EVC001)、益生菌和纯化 HMO(乳-N-新四糖)或安慰剂,为期4周在医院。
在开始治疗 8 周后的研究终点,益生菌组的年龄别体重 Z 评分 (WAZ) 和 MUAC 显着更高。鼠李糖乳杆菌GG (LGG) 和动物双歧杆菌亚种组合的试验。SAM 治疗期间的乳酸菌和 LGG 也证明了感染发生率和门诊腹泻减少的证据。
由于患有复杂 SAM 的儿童的临床不稳定和高死亡率,特定益生菌用作 SAM 标准治疗的潜力将在很大程度上取决于成本、可持续性和安全性。
此外,需要合理选择益生菌,以确定那些能够适当定植于营养不良儿童受损肠道的益生菌,并针对可以改善生长恢复的特定途径。
来自动物研究的进一步数据可能有助于为未来合适益生菌的临床试验提供信息,例如针对内分泌生长途径的益生菌。
即食治疗性食品(RUTF)
针对肠道微生物群的改良营养疗法有潜力成为儿童营养不良的可持续且经济有效的疗法。SAM 的证据表明,RUTF 喂养后微生物组成熟度的恢复是短暂的,并且往往在治疗后 3-4 个月恢复到不成熟状态。
因此,针对 SAM 恢复中肠道微生物组和预防发育迟缓的改良补充食品可能有助于促进生长。
一项试点试验评估了在 SAM 治疗期间向 F75 和 F100 治疗奶中添加可微生物发酵的碳水化合物菊粉或豇豆粉,发现与对照组相比,对营养恢复没有改善作用;然而,补充营养可以防止住院治疗期间物种多样性的暂时丧失,这部分是由抗生素治疗引起的。
豇豆辅助喂养可以显着减少有发育迟缓风险的儿童的一些 LAZ 缺陷;然而,它仅引起肠道微生物组组成的适度变化,包括双歧杆菌增加和大肠杆菌/志贺氏菌减少,表明对生长的有益影响可能与肠道微生物组无关。
来自孟加拉国的一个队列的研究,与标准 RUTF 疗法相比,微生物群导向的补充食品 (MDCF) 对 MAM 恢复儿童生长的影响显着增强。通过合理设计由当地可用的、文化上可接受的食物组成的补充食品组合 (MDCF-2),该组合可促进人源化动物模型中早期生命肠道微生物组的成熟。
这些有希望的数据表明,与目前的疗法相比,针对微生物群的补充食品可以在更大程度上促进儿童营养不良后的生长恢复。从长远来看,这些小但显着更大的生长改善是否与持续的生长改善、认知益处或感染和慢性病风险的降低相对应,目前尚不清楚。
来自高收入环境的临床试验越来越多的证据支持针对微生物群的治疗在各种感染、胃肠道和代谢疾病中的功效。
由于世界上超过五分之一的儿童发育迟缓或消瘦,旨在进一步表征导致儿童营养不良的微生物介导的病理生理途径的研究对于为更好的治疗提供信息至关重要。
儿童营养不良涉及许多生理系统的紊乱,包括代谢、免疫和内分泌系统,其中许多系统与肠道微生物组密切相关,因此可能适合针对微生物组的干预措施。
未来潜在的微生物组靶向疗法将补充针对宿主营养需求和感染负担的现有疗法。此外,必须根据国家或地区的具体要求调整这些干预措施,以制定具有成本效益且本国或本地区上可接受的可持续干预措施。
Tips
在这篇文章中综合了营养干预试验的现有证据,这些试验测试了多种饮食干预措施对婴儿和儿童微生物组相关结果的影响,并讨论了来自实验室和动物研究的支持证据,以及来自人类研究的观察数据,旨在指导未来的研究并增强可解释性,为饮食相关政策提供信息。
可比性较差,因为纳入的研究在干预类型和持续时间上有所不同,是在有或没有既往疾病的不同儿科人群中进行的,并且是在可能影响基线微生物组成的各种环境中进行的。
虽然调查婴儿微生物群的研究发现,母亲在怀孕期间的饮食变化几乎没有影响儿童肠道微生物群。但是通过单独检查研究而不是包括整个全球背景,很难将研究偏差与真实的生物现象分开。可以使用 Qiita 等工具尝试进行此类分析,前提是研究数据与符合标准的样本元数据是公开的,以促进未来分析中的跨研究可比性。
在进行 16S rRNA 测序的 19 项研究中,只有两项对 16S V4 区域进行测序的试验可用于 Qiita 的进一步分析。作者将这两个试验人群的肠道微生物群与 2012 年具有里程碑意义的微生物组队列研究的亚组进行了比较。
在 2012 年的研究中发现,马拉维出生的婴儿和美国出生的婴儿之间存在显着的微生物分离,但在纳入最近的两项试验时,缺乏数据来深入研究营养干预措施的效果与2012年的研究对比。
尽管微生物组生物信息学取得了很大进展,并且研究的人群类型和健康状况的广度不断扩大,但在营养和肠道微生物组领域,特别是儿童,仍需要解决许多研究空白和问题。
为了解决基于发现的差距,未来的研究人员将需要:
a)识别饮食细分成分响应微生物群并确定它们是否影响宿主的生理结果;
b)与最适合现实世界应用的特定膳食成分相比,了解全食干预措施的作用;
c)提高复制性和再现性,例如在不同人群中使用相同的饮食干预措施,以及在同一人群中测试不同的饮食干预措施;
d)确定食品加工和准备的作用,了解熟食或生食如何影响肠道微生物群(烹饪的影响最近已被研究,但仍是一个研究不足的领域);
e)考虑到依从性的差异,设计和使用饮食干预措施,这需要大量的队列和长时间的随访;
f)将研究结果和序列数据整合到一个数据库中,用于对类似处理的序列进行汇总分析并了解全局现象,同时最大限度地减少研究偏差。
介入/治疗差距
未来的研究应解决以下五个介入和治疗差距。
首先,需要解决稳定性和可塑性问题。虽然短期饮食变化可以改变肠道微生物群,但长期饮食模式与更稳定的微生物群构象相关,并且很难改变。仍有待确定的是哪种饮食模式具有最大或最小的可塑性,以及这种可塑性是否也取决于基线微生物种群和过去的饮食模式。
第二个差距是干预研究中针对不同人群的营养素和食物研究不足。尽管本次综述确定了几项微量营养素粉 (MNP) 试验,而关于补充个别维生素、矿物质和天然食品的试验相对较少,但仍然需要在中国以及其他国家重复研究中对 MNP 进行调查。
第三,应进行纵向、长期的人体研究。需要对 2-18 岁婴儿、青春期、成年早期和晚年等人群进行长期喂养研究,以了解衰老微生物群的动态。
第四,解决精准营养健康问题。
第五,未来健康建议应考虑大局。建议食物和饮食(生活方式)改变需要全面的方法和来自营养师和营养科学家、心理学家、医生和生物统计学家的多方面团队的支持。
小编寄语
中国在医疗和队列研究方面的发展仍有待提升。正如首都医科大学附属北京天坛医院院长王拥军教授所指出的:“中国目前还缺乏具有全球影响力的标志性队列研究,尤其是能够改变临床指南的里程碑试验”。
举例来说,美国的弗明汉心脏研究和英国的UK Biobank人群队列都对临床研究产生了重大影响。弗明汉心脏研究自1948年开始,最初只有5200名参与者,但经过70年的发展,参与者数量增加到15000人,产生了3698篇文章。这项研究改变了几乎所有心血管疾病的临床危险因素的认知。
另外,英国的UK Biobank人群队列从2006年开始策划,至今已发表超过3000篇文章。该队列成为世界上其他国家难以逾越的临床队列研究之一。
因此,谷禾也愿意和期待与各大医疗机构合作构建大型研究队列,尤其是关于青少年儿童的。通过对这些队列进行全面多组学以及生活营养指标的调查分析,将为我国医疗研究带来新的机遇和突破,为改善人们的健康水平做出重要贡献。
主要参考文献
Jones HJ, Bourke CD, Swann JR, Robertson RC. Malnourished Microbes: Host-Microbiome Interactions in Child Undernutrition. Annu Rev Nutr. 2023 Aug 21;43:327-353.
Acosta A, De Burga R, Chavez C, Flores J, Olortegui M, et al. 2017. Relationship between growth and illness, enteropathogens and dietary intakes in the first 2 years of life: findings from the MAL-ED birth cohort study. BMJ Glob. Health 2(4):e000370
Alves da Silva AV, de Castro Oliveira SB, Di Rienzi SC, Brown-Steinke K, Dehan LM, et al. 2019. Murine methyl donor deficiency impairs early growth in association with dysmorphic small intestinal crypts and reduced gut microbial community diversity. Curr. Dev. Nutr. 3(1):nzy070
Mehta S, Huey SL, McDonald D, Knight R, Finkelstein JL. Nutritional Interventions and the Gut Microbiome in Children. Annu Rev Nutr. 2021 Oct 11;41:479-510.
Amadi B, Fagbemi AO, Kelly P, Mwiya M, Torrente F, et al. 2009. Reduced production of sulfated glycosaminoglycans occurs in Zambian children with kwashiorkor but not marasmus. Am. J. Clin. Nutr. 89(2):592–600
Amadi B, Zyambo K, Chandwe K, Besa E, Mulenga C, et al. 2021. Adaptation of the small intestine to microbial enteropathogens in Zambian children with stunting. Nat. Microbiol. 6(4):445–54
Ansaldo E, Farley TK, Belkaid Y. 2021. Control of immunity by the microbiota. Annu. Rev. Immunol. 39:449–79
Attia S, Versloot CJ, Voskuijl W, van Vliet SJ, Di Giovanni V, et al. 2016. Mortality in children with complicated severe acute malnutrition is related to intestinal and systemic inflammation: an observational cohort study. Am. J. Clin. Nutr. 104:1441–49
Barratt MJ, Nuzhat S, Ahsan K, Frese SA, Arzamasov AA, et al. 2022. Bifidobacterium infantis treatment promotes weight gain in Bangladeshi infants with severe acute malnutrition. Sci. Transl. Med. 14(640):eabk1107
Bartelt LA, Bolick DT, Mayneris-Perxachs J, Kolling GL, Medlock GL, et al. 2017. Cross-modulation of pathogen-specific pathways enhances malnutrition during enteric co-infection with Giardia lamblia and enteroaggregative Escherichia coli. PLOS Pathog. 13(7):e1006471
Bartz S, Mody A, Hornik C, Bain J, Muehlbauer M, et al. 2014. Severe acute malnutrition in childhood: hormonal and metabolic status at presentation, response to treatment, and predictors of mortality. J. Clin. Endocrinol. Metab. 99(6):2128–37
Bhattacharjee A, Burr AHP, Overacre-Delgoffe AE, Tometich JT, Yang D, et al. 2021. Environmental enteric dysfunction induces regulatory T cells that inhibit local CD4+ T cell responses and impair oral vaccine efficacy. Immunity 54(8):1745–57.e7
Black RE, Victora CG, Walker SP, Bhutta ZA, Christian P, et al. 2013. Maternal and child undernutrition and overweight in low-income and middle-income countries. Lancet 382(9890):427–51
Bourdon C, Lelijveld N, Thompson D, Dalvi PS, Gonzales GB, et al. 2019. Metabolomics in plasma of Malawian children 7 years after surviving severe acute malnutrition: “ChroSAM” a cohort study. EBioMedicine 45:464–72
Aakko J, Grzeskowiak L, Asukas T, Paivansade E, Lehto KM, et al. 2017. Lipid-based nutrient supplements do not affect gut Bifidobacterium microbiota in Malawian infants: a randomized trial. J. Pediatr. Gastroenterol. Nutr. 64:610–15
Aly H, Said RN, Wali IE, Elwakkad A, Soliman Y, et al. 2017. Medically graded honey supplementation formula to preterm infants as a prebiotic: a randomized controlled trial. J. Pediatr. Gastroenterol. Nutr. 64:966–70
Amarri S, Benatti F, Callegari ML, Shahkhalili Y, Chauffard F, et al. 2006. Changes of gut microbiota and immune markers during the complementary feeding period in healthy breast-fed infants. J. Pediatr. Gastroenterol. Nutr. 42:488–95
Andrews SC, Robinson AK, Rodriguez-Quinones F. 2003. Bacterial iron homeostasis. FEMS Microbiol. Rev. 27:215–37
Arimond M, Zeilani M, Jungjohann S, Brown KH, Ashorn P, et al. 2015. Considerations in developing lipid-based nutrient supplements for prevention of undernutrition: experience from the International Lipid-Based Nutrient Supplements (iLiNS) Project. Matern. Child Nutr. 11:31–61
Arrieta MC, Stiemsma LT, Amenyogbe N, Brown EM, Finlay B. 2014. The intestinal microbiome in early life: health and disease. Front. Immunol. 5:427
Black RE, Victora CG, Walker SP, Bhutta ZA, Christian P, de Onis M, Ezzati M, Grantham-McGregor S, Katz J, Martorell R, Uauy R; Maternal and Child Nutrition Study Group. Maternal and child undernutrition and overweight in low-income and middle-income countries. Lancet. 2013 Aug 3;382(9890):427-451.

谷禾健康

微量营养素缺乏或称之为“隐性饥饿”,是目前一个严重的公共卫生问题,会对儿童发育及成人健康造成严重后果。
传统的治疗和预防方法,有些时候并是很有效,并且可能产生不良副作用(例如补铁引起的消化问题)。
★ 肠道细菌与微量营养素间存在重要的相互作用
许多研究发现肠道中的共生细菌可以增加特定微量营养素的生物利用度,特别是通过去除抗营养化合物(例如植酸盐和多酚),或通过合成维生素。
肠道黏膜是抵御病原体的第一道防线。肠黏膜微生物群有助于增强肠上皮的完整性并更好地吸收微量营养素。
细菌代谢还依赖于从肠道环境中获取的微量营养素,常驻细菌可能会竞争或协作以维持微量营养素稳态。因此,肠道微生物群的组成可以通过微量营养素的可用性来调节。

本文汇集了有关微量营养素和肠道微生物群之间双向关系的最新知识,重点关注铁、锌、维生素A和叶酸(维生素B9),因为这些缺乏症是全球范围内的比较严重的公共卫生问题。
目录
1.微量营养素缺乏
2.微量营养素与宿主健康
3.营养素与细菌的相互作用:以铁为例
4.细菌在锌生物利用中的作用
5.微生物群与宿主叶酸间的关联
6.微生物群与维生素A的相互作用
7.改善人体微量营养素的建议
8.结语
微量营养素,包括矿物质和维生素,是每天只需要少量的物质,但对人体代谢至关重要。
▼
微量营养素缺乏在全世界范围内非常普遍,最新估计表明,3.72亿学龄前儿童和1.20亿育龄非孕妇缺乏一种或多种微量营养素。
维生素和矿物质缺乏,也被称为“隐性饥饿”,是一个严重的公共卫生问题,世界各个国家都存在,特别是低收入和中等收入国家的弱势群体。
在全球范围内,三分之二的妇女和儿童(主要来自经济不发达家庭)的饮食中至少缺乏一种微量营养素。全球最普遍的微量营养素缺乏症包括铁、锌、维生素A和叶酸。
★ 微量营养素缺乏会导致不良健康结果
微量营养素缺乏与多种不良健康结果相关,例如儿童发病率和死亡率增加、贫血、发育迟缓和认知缺陷。
虽然存在多种改善个人或人群微量营养素状况的策略,其中主食强化被认为是改善人群微量营养素状况最具成本效益的干预措施。
然而,由于多种原因,应对微量营养素缺乏症的策略并不总是有效。包括可接受性差(例如,孕妇铁补充剂)、强化水平差和质量控制不足(例如,维生素A强化食用油),强化食品未能惠及最贫困人群。
★ 不同营养素的吸收具有差异
微量营养素的吸收主要发生在小肠中,根据微量营养素的不同,具有不同的机制。
例如,锌和铁主要通过特定的运输载体在十二指肠和空肠中吸收,这些运输载体针对每种矿物质及其形式而异,而叶酸不仅在小肠中被吸收,而且在结肠中也被吸收,因为在这两个部位都鉴定出了转运蛋白。
微量营养素的吸收差异很大,例如,铁充足的男性成年人吸收的铁摄入量不到5%,而正常条件下摄入的锌吸收量大于30%。
注:大部分摄入的微量营养素会到达结肠。
★ 微生物群与微量营养素之间存在相互作用
在消化道中,有一个复杂的微生物群落,其浓度和多样性从口腔到结肠不断增加。尽管含有其他微生物(病毒、真菌),但大多数研究都重点关注细菌,其中厚壁菌门、拟杆菌门、放线菌门、变形菌门和疣微菌门是最重要的。
粪便细菌组成在个体之间存在很大差异,并且不仅取决于宿主的遗传学,还取决于包括饮食在内的许多环境因素。
注:大多数关于食物对肠道微生物群影响的研究都集中在大量营养素(脂肪、碳水化合物、蛋白质)上。
然而,细菌需要微量营养素才能生存。例如,细菌需要外部来源的铁,其中一些甚至开发出特定的机制,例如转铁蛋白来竞争铁源。
相比之下,许多细菌可以直接合成维生素,例如叶酸(维生素B9),因此不一定需要外部来源。
细菌影响微量营养素的生物利用度
常驻细菌可能对微量营养素产生直接作用,影响其对宿主的生物利用度,或者产生间接作用,例如通过产生能够改善上皮健康的代谢物,从而导致更好的吸收。
微量营养素影响肠道细菌的组成和功能
微量营养素的消耗反过来会影响肠道细菌的组成和功能。事实上,事实证明,补充铁可以导致潜在致病性肠杆菌科细菌的增加,以及被认为对健康具有积极影响的双歧杆菌科细菌和乳杆菌科细菌的减少。
微量营养素在控制人类健康的新陈代谢和组织功能维持中发挥着核心作用。
然而,尽管人们努力通过补充食品和饮食多样化来增加微量营养素的摄入量,全球微量营养素缺乏症的患病率仍然非常高,包括工业化国家。
推荐营养素摄入量和摄入上限
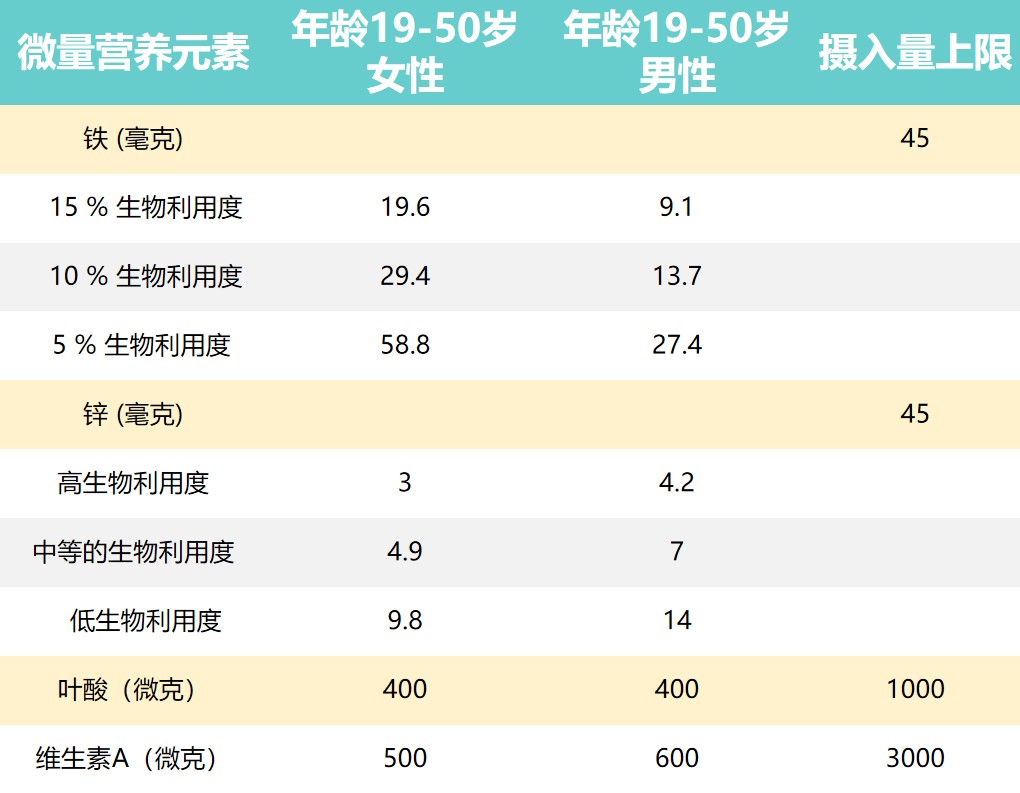
Dje Kouadio DK,et al.Crit Rev Food Sci Nutr.2023
上表提出了男性和女性一些推荐营养素摄入量和可耐受的上限摄入水平。
由于维持生长和补偿损失(例如月经)的需求更高,儿童和妇女受到的影响更大。
★ 缺乏微量营养素的症状多样且大部分在晚期
单一微量营养素缺乏的临床症状多种多样,并且通常是具有微量营养素特异性的,但一般发生在缺乏的晚期阶段。例如缺铁性贫血是缺铁的最后阶段。
▼
缺铁被认为是最常见的微量营养素缺乏症,全世界估计有超过20亿人缺铁。它会导致贫血、免疫功能受损、工作能力下降以及内分泌功能受损。
导致铁缺乏的因素包括:
(1)血红素铁摄入量低,其生物利用度高于非血红素铁
(2)富含植酸酶或酚类化合物的饮食会降低生物利用度
(3)慢性炎症,导致铁调素水平升高,下调铁吸收
▼
据估计,全球有超过10亿人缺锌,它与儿童生长迟缓相关,但也会降低免疫能力,从而增加儿童对多种疾病的易感性,包括腹泻、肺炎,也许还有疟疾。
此外,锌缺乏似乎会导致其他微量营养素缺乏。
▼
据估计,低收入和中等收入国家超过20%的育龄妇女缺乏叶酸。
怀孕期间叶酸摄入不足与胚胎最初几周的神经发育缺陷有关。在普通人群中,叶酸缺乏还会导致巨幼红细胞性贫血和神经系统症状,这些症状与维生素B12缺乏症的症状部分重叠。
▼
维生素A缺乏不仅会导致干眼症和失明,还会影响免疫功能的许多方面,导致免疫能力下降以及皮肤和上皮完整性降低。
许多低收入和中等收入国家每半年向5岁以下儿童提供高剂量维生素A补充剂,以降低儿童死亡率,但这种干预措施的有效性受到质疑。
有关铁、细菌和宿主的相互作用,参考了最近的研究,下面总结了这种复杂关系的关键要素。
铁的吸收和稳态受到严格调节
由于人类无法主动排泄铁,因此铁的吸收在十二指肠中受到严格调节。
// 血红素铁
血红素铁和非血红素铁通过两种不同的途径吸收,血红素铁被十二指肠刷膜边缘的血红素载体蛋白1(HCP1) 吸收。
// 非血红素铁
非血红素铁通常呈三价铁形式,不具有生物利用度,必须通过十二指肠细胞色素b(DCYTB) 将其还原为二价铁形式,然后再由二价金属转运蛋白 (DMT1) 转运到十二指肠刷膜上 。
注:二价金属转运蛋白的存在已被描述,铁也在回肠和结肠中被吸收,但这些吸收位点对宿主铁状态的贡献仍不清楚。
铁进入肠上皮细胞后,储存在铁蛋白中,或通过基底外侧铁转运蛋白输出到循环系统中。
铁稳态由激素铁调素调节,铁调素通过不同机制抑制铁释放到血浆中。
铁调素是由肝脏合成并分泌的富含半胱氨酸的抗菌多肽,在免疫过程中能够大量表达参与免疫反应;在机体内铁平衡的调节中起到负性调节的作用。
肠道微生物群在铁吸收中的作用示意图
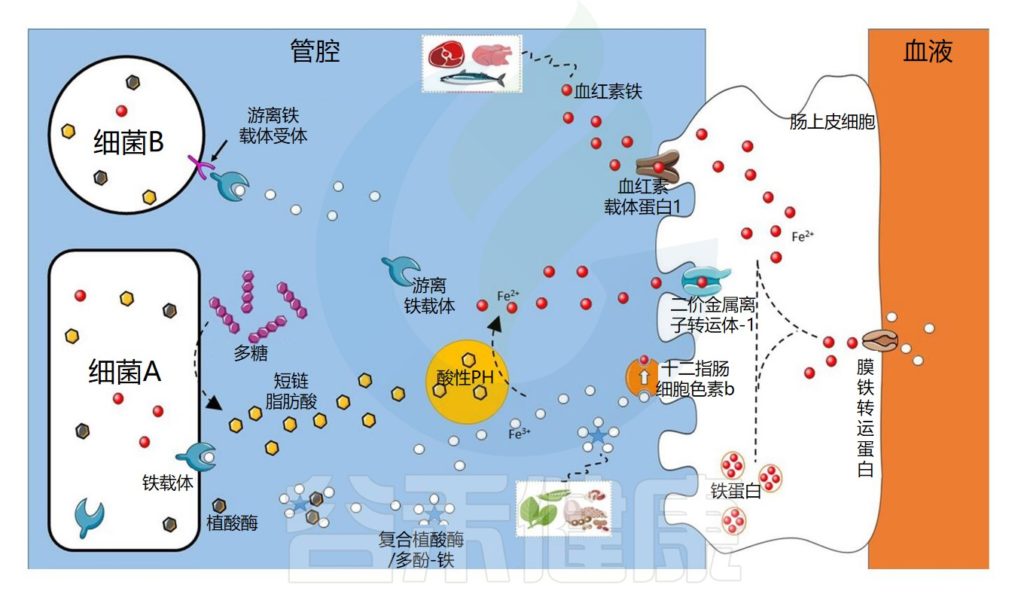
Dje Kouadio DK,et al.Crit Rev Food Sci Nutr.2023
细菌可以通过不同的机制获取铁
细菌可以通过不同的机制获取铁,例如使用称为铁载体的铁特异性螯合剂,铁载体是化学性质多样的次级代谢产物,对铁具有高亲和力。
由此产生的铁-铁载体复合物通过特定的外膜蛋白(上图中的细菌A)内化。细菌还可以通过产生具有不同配体结合位点的外膜受体来利用其他细菌产生的铁载体(上图中的细菌B)。
铁载体在细菌缺铁的情况下表达
铁载体在细菌缺铁的情况下表达,因此不在铁充足的环境中表达。在厌氧条件和低pH值下,铁主要以二价铁的形式存在,可以被细菌直接转运,主要通过专用转运系统Feo,由不同的蛋白质。
细菌可以利用宿主铁化合物
细菌还可以利用宿主铁化合物,例如血红素或转铁蛋白,它们通过特定受体转运或直接吸收。此外,尽管牛奶中存在的乳铁蛋白具有抑菌功能,但它也可以被具有特定受体的细菌利用。
铁吸收的调节对于细菌非常重要,因为铁在较高浓度下有毒。在许多细菌物种中,当铁浓度过高时,铁吸收调节蛋白 (Fur) 会抑制与铁吸收相关的基因转录。
研究细菌有助于揭示新的铁吸收途径
值得注意的是,大部分关于细菌铁吸收的知识来自对病原菌的研究。长期以来,人们一直认为一些有益菌,例如乳杆菌科的成员,不需要铁来生长。然而已经在植物乳杆菌(Lactiplantibacillus plantarum)和清酒乳杆菌(Latilactobacillus sakei)中鉴定出了特定的系统。
研究这些细菌可能会揭示新的铁吸收途径。在铁吸收的主要部位十二指肠中,大约有103 个细菌/克,低于空肠(104 个细菌/克),并且远低于结肠,结肠中的细菌数量高达1012 个细菌/克。
此外,乳杆菌科属的成员在铁吸收最多的小肠中数量众多,因此这些细菌对宿主铁吸收的作用应受到更多关注,以确定它们是否在铁的生物利用度中发挥作用。
▼
铁对于许多细菌来说是必需的,它们的生长需要铁。
据计算,结肠中的铁浓度很高,并且远远超过细菌生长的最低要求。但细菌对铁的生物利用度还取决于一系列因素(铁的形式、铁形态、pH值、氧气水平等)。
不同形式的铁可用于补充或强化,例如硫酸亚铁、富马酸亚铁或乙二胺四乙酸铁钠。由于铁补充剂中含有的铁明显多于人体可以吸收的铁,因此大量未吸收的铁会留在消化道内腔中。
•铁补充剂会导致潜在致病菌水平升高
多项人类研究表明,铁补充剂或强化铁会导致潜在致病菌水平升高,并导致通常被认为是有益细菌种类减少,例如乳杆菌科成员。
最近一项针对大鼠的研究还表明,出生后补充铁会导致肠道微生物群发生改变,这种改变会持续到成年期。此外,研究表明,抗生素治疗后服用铁剂会导致肠道细菌的组成和功能发生改变。
铁对于致病细菌至关重要,哺乳动物的免疫系统已经具备了通过表达铁结合蛋白(如脂质运载蛋白-2 或乳铁蛋白)来控制细菌对铁的可用性的能力,这种现象称为“营养免疫”。
研究了补充铁对肠道微生物群的作用,总的来说,根据所使用的模型(体外、动物或人类),结果似乎有很大不同。
事实上,在补充铁期间,乳杆菌科总是减少,这在体外、小鼠和婴儿中均观察到。所用铁的化学形式似乎对细菌组成有不同的影响。此外,出乎意料的是,补充铁的效果与缺铁的效果并不直接相反。
▼
对于细菌和人体来说,非血红素铁的生物利用度低于血红素铁的生物利用度,因为它受到食物基质的成分和管腔的物理化学成分的影响。
•肠道细菌有助于更好地吸收铁
事实上,许多食物基质中的非血红素铁与抑制剂(例如多酚、纤维或植酸盐)相连,这些抑制剂可以被专用细菌酶降解,从而导致更好的铁吸收。
细菌还可以通过发酵饮食中的不可消化碳水化合物来产生短链脂肪酸,这会降低管腔pH值,从而将三价铁还原为二价铁,从而提高其被细菌和宿主的吸收。
其他一些有机酸(例如乳酸)是由许多细菌产生的,存在于整个消化道中。酸化的肠道环境还可以降解螯合微量营养素的复合物并促进铁的吸收。
扩展阅读:
▼
考虑到补铁的依从性低以及腹泻或便秘等副作用,很多研究已经测试和发现其他改善铁状态的策略。
它们包括使用益生菌、益生元和后生元等。
•使用益生菌改善铁状况
例如,将益生菌植物乳杆菌(Lactiplantibacillus plantarum 299v)与铁、抗坏血酸和叶酸一起食用,对健康、非贫血的瑞典孕妇的铁状况是安全的,可减少铁储备的损失并改善铁状况。
在另一项研究中,将果胶组装成铁纳米颗粒作为基质,用于植物乳杆菌(Lactiplantibacillus plantarum CIDCA 83114)的递送。益生菌没有毒性,生存能力没有减弱,这为用替代的铁输送策略对抗缺铁提供了新的视角。
•使用益生元帮助铁的吸收
在大鼠模型中,食用益生元寡糖通过调节肠道微生物群来增强铁吸收。摄入益生元后肠道pH值的降低可以帮助铁的吸收,此外还能以有益的方式改变肠道微生物组成。因此,益生元可以成为改善宿主铁状况的良好选择。
•食用乳铁蛋白增加铁的吸收
在肯尼亚婴儿中,研究表明,与单独服用硫酸亚铁相比,同时食用无铁乳铁蛋白(脱铁乳铁蛋白)和硫酸亚铁能够显著增加铁的吸收。
注:考虑到乳铁蛋白对肠道微生物群的影响,一些学者认为乳铁蛋白可能在婴儿铁配方中有用,因为它可以增加铁的吸收,同时可能减轻未吸收的铁对肠道微生物群的不利影响。
•使用富铁微生物
这些预防和治疗缺铁的新策略可能包括使用富铁微生物,除了从益生菌摄入中获益之外,它还可以为宿主提供大量矿物质。
在贫血小鼠中已显示,食用在铁存在下生长的酵母能够提高小鼠的血红蛋白浓度。在人类中只进行了一些尝试,其中含有富铁酵母的奶酪的吸收效率不如单独含有硫酸铁的奶酪。
注:还应该进行补充研究来评估富铁微生物在人类中的应用的全部潜力。
小结
从上面可以明显看出,肠道细菌在调节宿主铁的生物利用度方面发挥着重要作用。然而,宿主因素可以调节细菌对铁的吸收,例如,在炎症的情况下,脂质运载蛋白将与铁载体结合,从而对抗肠道细菌对铁的捕获。
最近,有人提出,共生细菌不仅使用不同的机制来释放和捕获铁,而且还在它们自己和它们的宿主之间共享铁。事实上,细菌扩散性铁载体生产的例子可以捕获铁,但不能保证这些铁将被生产细菌利用,这表明对可用铁的共同管理。
迄今为止,人类对锌、宿主和肠道微生物群之间相互作用的研究远少于铁。
★ 人体需要每日摄入锌
每日摄入锌补充剂,成人 40 毫克/天,通常被认为是安全的。
锌参与DNA合成、转录和翻译等重要过程。锌的吸收发生在十二指肠,涉及跨膜锌转运蛋白Zip4。然后,锌通过锌调节蛋白ZnT2-10转运至金属蛋白合成位点,或通过锌转运蛋白ZnT1输出至循环系统。
与铁相反,哺乳动物缺乏锌储存机制,每日摄入是必不可少的。如果过量,锌也可以主动排泄,锌通过基底外侧的 Zip5/Zip14 蛋白从循环分配到肠上皮细胞,并通过ZnT5从肠上皮细胞流出到管腔。
肠道微生物群在锌吸收中的作用示意图
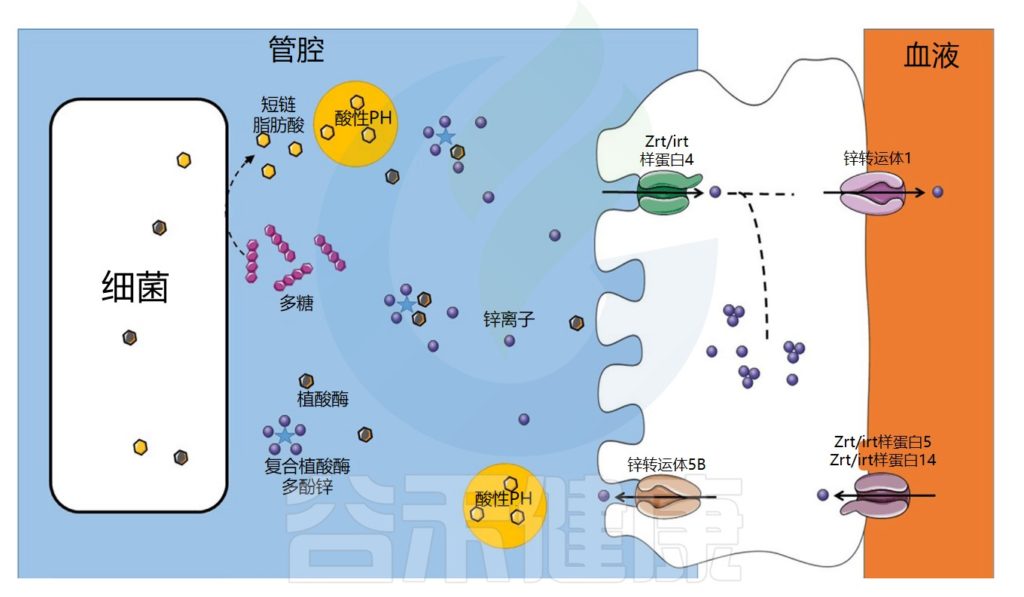
Dje Kouadio DK,et al.Crit Rev Food Sci Nutr.2023
锌的转运与吸收过程
在食物中,锌可以与抗营养因子如植酸盐或多酚络合,从而减少其吸收。未被小肠吸收的锌会到达结肠,并可能被结肠细胞吸收,因为锌转运蛋白也在结肠中表达。
在细菌中,锌通过锌伴侣蛋白转运至金属蛋白合成位点。细菌对锌的吸收受锌吸收抑制因子Zur和锌流出抑制因子CzrA的调节。一些病原菌可以通过表达高亲和力转运蛋白(ZnuABC)来克服锌限制条件。
锌浓度过高可能对某些病原菌有毒。与铁的情况一样,宿主和病原微生物之间也存在竞争。事实上,宿主还利用营养免疫来通过产生钙卫蛋白来限制锌的生物利用度。
例如,钙卫蛋白在消化道中结合锌。
▼
锌缺乏与慢性腹泻相关。补锌对肠道微生物群的影响主要在动物模型中进行研究。它已在家禽和养猪业中以药物剂量用于减少胃肠道感染和腹泻。
√锌具有抗菌活性,能够减少腹泻
锌具有抗菌活性,不同的研究强调了高剂量的锌会引起肠道不同部位(从胃到结肠)细菌组成的变化。
在断奶仔猪中,使用低剂量的锌可以通过改善小肠形态和通透性、增强屏障功能,有效促进生长性能并减少腹泻。
此外,锌还能丰富肠道微生物群中的链球菌科(Streptococcaceae)和乳杆菌科(Lactobacillaceae),并减少芽孢杆菌和肠道疾病相关病原体,包括回肠腔中的梭状芽胞杆菌和克罗诺杆菌。
注:如果缺锌小鼠补充锌是有益的,那么过量的锌饮食摄入会改变肠道微生物群并降低对艰难梭菌感染的抵抗力。
√一些菌属可以预测锌的充足性
但研究结果并不一致。事实上,一项针对鸡的研究表明,瘤胃球菌属(Ruminococcus)可以预测宿主体内锌的充足性。但在一项针对小鼠的研究中,黑色素杆菌(Melainabacteria)和脱硫弧菌属(Desulfovibrio)被确定为锌状态的潜在标志物。
▼
尽管许多代谢过程都需要锌,但关于锌状态或补充剂对肠道微生物群影响的研究却很少。
√一些细菌可以作为锌缺乏的生物标志物
最近的研究表明,尽管缺锌和锌充足的学龄儿童之间的细菌多样性相似,但缺锌儿童的个体多样性更高。特别是,粪杆菌(Coprobacter)、醋酸弧菌(Acetivibrio)、副普雷沃氏菌(Paraprevotella)和梭状芽胞杆菌在缺锌组中更为丰富。它们可以用作进一步临床诊断锌缺乏的生物标志物,但需要更多的工作来推广这一结果。
锌的摄入量也会显著增加儿童粪便细菌。在同一项研究中还鉴定出了纳米颗粒抗性细菌的一些代表。
▼
由于补锌会改变肠道微生物群的组成和功能,因此许多研究已经研究了锌与益生菌一起服用的效果。
√锌与益生菌一起补充
例如,在大鼠中,施用在富锌培养基中生长的长双歧杆菌(Bifidobacterium longum CCFM1195)比单独补充锌更能有效地增加血浆锌浓度。
此外,一些细菌群(如乳杆菌科)的丰度随着富含锌的双歧杆菌的消耗而增加。使用富含硒和锌的植物乳杆菌对小鼠进行类似的设计,与对照组或补充硒锌的组相比,能够增加循环锌浓度。这种增加伴随着肠道细菌组成的改变,乳杆菌科(Lactobacillaceae)的比例增加。
√儿童单独补充锌可能更有效
最近总结了研究中获得的数据,对于24个月以下儿童的治疗,单独补充锌可能比益生菌更有效;在学龄前儿童中同时补充锌和植物乳杆菌并不比单独补充益生菌更有效。因此,锌和益生菌联合给药的有效性需要更多的人体研究。
使用益生元似乎效率较低,因为给猪施用锌和马铃薯纤维对大多数分析指标没有显示出任何交互作用。
注:锌源和纤维补充对微生物群生态的影响是独立的。
小结
与铁的情况一样,对锌状态和宿主微生物群的研究主要集中在致病条件上,而对细菌在正常情况下的作用知之甚少。
肠道细菌、锌和宿主之间的关系值得更深入地研究,尤其是在人类中。事实上,富锌益生菌等有前途的工具正在出现,它们代表了治疗锌缺乏症的替代方案。特别是大剂量、长期补锌可能会干扰铁和铜的吸收,导致铁和铜的缺乏。
叶酸,也可以称之为维生素B9,是一种水溶性维生素。叶酸在蛋白质合成及细胞分裂与生长过程中具有重要作用,对正常红细胞的形成有促进作用。
一些共生细菌已被证明可以合成某些维生素,细菌也可以成为宿主叶酸的来源,即使整体贡献的程度不清楚。同时,叶酸的摄入会影响肠道微生物群。
叶酸的转运与吸收过程
饮食中的叶酸以单谷氨酸盐和聚谷氨酸盐形式存在,它们被肠道结合物分解为单谷氨酸盐形式,然后通过特定的转运蛋白偶联叶酸转运蛋白(PCFT)在回肠中吸收。
在肠上皮细胞中,叶酸单谷氨酸转化为活性形式5-甲基四氢叶酸(5-MTHF),它可以被运输到循环系统。
注:细胞叶酸外排可能由多个耐药蛋白(MRPs)家族介导。在结肠中,已经发现了相同的一种受体。
肠道微生物群在叶酸吸收中的作用示意图
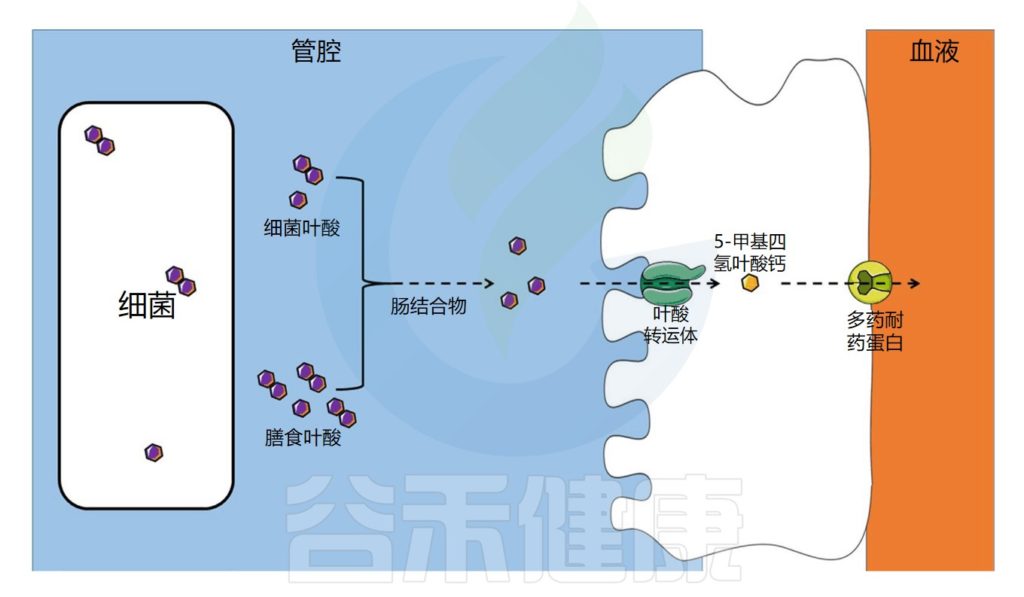
Dje Kouadio DK,et al.Crit Rev Food Sci Nutr.2023
▼
细菌的生长需要叶酸,一些细菌是原养型细菌,可以从环境中存在的前体合成叶酸,而营养缺陷型细菌必须从环境中获取叶酸。
✦肠道细菌合成叶酸
大量文献支持细菌叶酸合成对宿主叶酸状态的重要贡献。早期研究报告称,人类粪便样本中的叶酸浓度为300-500µg/天,而饮食摄入量低于100µg/天,表明肠道细菌可以合成叶酸。
事实上,512个细菌基因组的叶酸生物合成能力预测表明,其中13%的细菌基因组包含所有叶酸生物合成相关基因,而39%的细菌基因组可以在外部来源提供额外的对氨基苯甲酸的情况下合成叶酸。
总而言之,这些数据表明肠道微生物群是叶酸的重要来源,并且饮食等不同因素导致的肠道微生物群组成的变化可能会影响叶酸的需求。
✦肠道细菌可以转化叶酸以便更好地利用
由于纤维消耗而改变肠道微生物群组成可能导致结肠内容物或循环中叶酸浓度增加。此外,尽管结肠中的叶酸吸收比小肠中的叶酸吸收慢100倍,但标记的叶酸被专门包裹在结肠中并在结肠中分解,并被纳入宿主组织。
肠道细菌不仅合成可供宿主使用的叶酸,还可以将叶酸转化为更好地被宿主吸收的维生素体,正如秀丽隐杆线虫(Caenorabditis Elegans)模型所证明的那样,其中细菌可以将叶酸转化为四氢叶酸。
✦微生物代谢叶酸的能力与宿主生理状况相关
肠道微生物群的代谢能力不仅取决于其组成,还取决于宿主的生理特征。例如,与成人相比,婴儿和幼儿肠道微生物群中更频繁地发现编码参与叶酸生物合成的酶的基因。
有趣的是,受营养不良影响的儿童的微生物组显示,参与B族维生素代谢的多个途径中的基因丰度显著降低。此外,在肥胖女性中观察到叶酸水平较低,同时产生B族维生素的细菌也减少。
▼
许多产生叶酸的细菌被鉴定并成功用于增加发酵食品的叶酸含量。其中一些细菌还能够改善缺乏叶酸饮食的啮齿动物的叶酸状况。
✦产生叶酸的益生菌改善叶酸状态并调节微生物组成
使用产生叶酸的益生菌可能是改善叶酸状态并调节肠道微生物群的一种方法。在体外发现了有希望的结果,其中产生叶酸的清酒乳杆菌(Latilactobacillus sakei)被证明可以增加短链脂肪酸并改变粪便细菌组成。
在大鼠中,食用使用产生叶酸的植物乳杆菌制备的发酵奶能够恢复正常的叶酸状态,同时广泛改变肠道细菌组成。
▼
叶酸摄入量对肠道细菌的影响并不一致。
✦叶酸缺乏可能影响部分动物的肠道细菌组成
在小鼠身上发现膳食叶酸缺乏不会影响肠道细菌组成,可能是一些细菌可以在缺乏时产生叶酸,叶酸摄入量的波动对肠道微生物群的影响较小。
然而,在其他动物模型中,叶酸摄入改变了肠道微生物群的组成,例如鸡和小猪。
✦叶酸缺乏影响微生物多样性
叶酸缺乏也会影响微生物多样性,因为在限生小鼠中发现,与微量营养素充足的饮食相比,叶酸缺乏的饮食在21天后增加了β多样性,但随后的14天全饮食治疗并没有改变这一趋势。
小结
宿主的叶酸状态、食物或肠道中的叶酸产生细菌之间存在多种关联。这种关联通常是矛盾的,但有利于宿主和细菌区室之间的密切相互作用,这表明需要进行大规模人类研究,以更好地了解与叶酸可用性和改善人群叶酸状态的策略相关的宿主-微生物群相互作用。
叶酸重要天然来源有:
花生(246微克/100克)、葵花籽(238微克/100克)、芦笋(149微克/100克)、生菜(136微克/100克)、一些绿叶蔬菜和柑橘类水果等。
扩展阅读:维生素B9(叶酸)
维生素A在免疫调节中发挥着至关重要的作用,包括调节细胞因子的产生和淋巴细胞归巢至粘膜表面。它通过调节肠上皮中免疫细胞的增殖和分化,直接有助于维持肠道屏障,并在抵抗肠道病原体入侵方面发挥着至关重要的作用。
膳食维生素A以视黄醇和类胡萝卜素的形式存在,分别存在于动物和蔬菜中。
肠道微生物群在维生素A吸收中的作用示意图
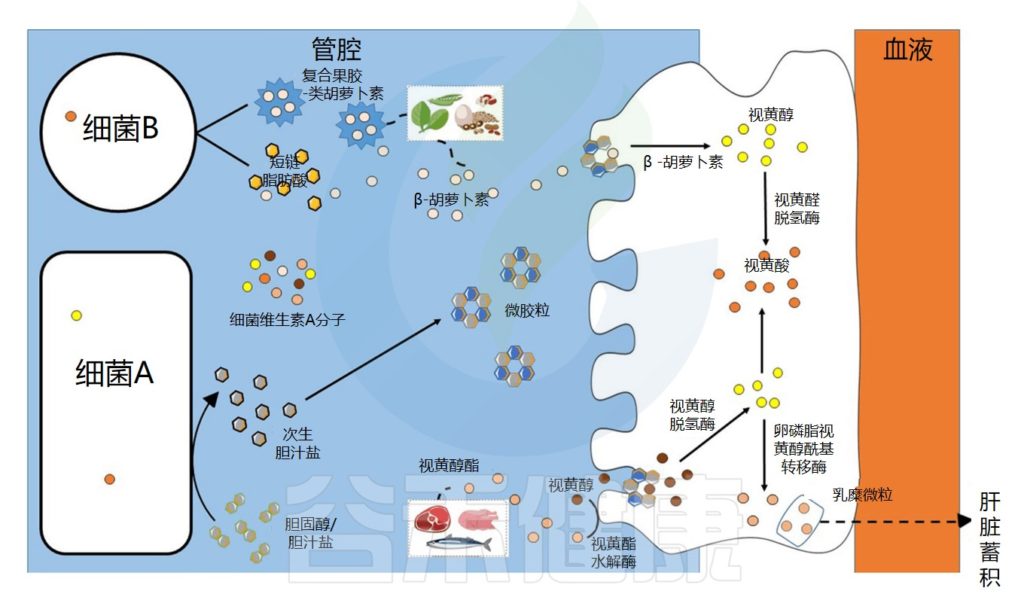
Dje Kouadio DK,et al.Crit Rev Food Sci Nutr.2023
维生素A的吸收过程
视黄醇和类胡萝卜素是膳食脂溶性成分,在被肠上皮细胞吸收之前需要通过胶束溶解 。在胃和十二指肠中发生乳化成液滴的阶段,类胡萝卜素和视黄醇的摄取发生在小肠的上半部。
在肠上皮细胞中,类胡萝卜素通过胡萝卜素-15,15′-双加氧酶直接转化为全反式视黄醛。视黄醛可被视黄醛脱氢酶不可逆地转化为具有生物活性的视黄酸分子,或被转化为视黄醇酯,储存在肝脏中。
▼
肠道微生物群在维生素A代谢中的作用可能依赖于特定酶、脂多糖的产生,脂多糖可能有助于胶束形成或直接吸收,以及胆汁稳态。
•微生物通过调节胆汁酸有利于维生素A的溶解和吸收
一项以绵羊为模型的研究表明,宿主微生物群通过调节胆汁酸分泌对维生素A吸收产生影响。在该模型中,胆汁酸水平降低与维生素A吸收减少相关,并与瘤胃球菌科丰度密切相关。
由乳杆菌(Lactobacillaceae)、双歧杆菌(Bifidobacterium)、拟杆菌(Bacteroides)或梭菌属等细菌产生的二级或三级胆汁盐的分泌可能有利于维生素A的溶解并改善其吸收,因为胆汁盐对于胶束化过程至关重要。
•肠道微生物可以直接和间接影响维生素A代谢
肠道细菌的基因组具有在动物和植物中发现的不同酶的类似物,这些酶允许乙酰辅酶A通过甲羟戊酸途径合成类胡萝卜素和类维生素A。
此外,来自拟杆菌(Bacteroides)、肠球菌(Enterococcus)和链球菌(Streptococcus)的细菌具有与宿主BCMO基因相似的brp/blh基因,可以将β-胡萝卜素转化为全反式视黄醇。
因此,肠道微生物组对维生素A代谢的影响既包括直接影响(如类胡萝卜素的合成),也包括间接影响(如调节其生物利用度)。
•肠道微生物合成相关蛋白有助于维生素A转运
类胡萝卜素的生物利用度会受到各种食物成分的影响,其中食物基质中蔬菜的细胞壁结构和组成形成物理屏障,从而限制消化酶的作用。
果胶和一些多酚(例如柚皮素)已被证明可以通过结合管腔中的胆固醇和胆汁盐来降低类胡萝卜素的体外生物利用度,从而抑制胶束的形成。
相反,果胶可以被许多共生细菌降解,并且肠道中的这种降解可能会增加类胡萝卜素的生物利用度。
此外,肠道微生物群合成酶或补体蛋白,例如细菌脂质运载蛋白,这可能有助于将类维生素A转运到肠上皮细胞中。
•肠道细菌调节宿主视黄醇的代谢
肠道微生物群可以消化膳食纤维,从而释放 β-胡萝卜素或其他结合态的微量营养素。
此外,肠道细菌群还可以调节宿主视黄醇的代谢,调节驱动免疫反应的视黄酸的产生。梭状芽胞杆菌类细菌可以通过抑制基因Rdh7的表达来调节肠道上皮中的视黄酸浓度,从而启动视黄醇向视黄酸的转化。
此外,这项研究表明,共生细菌群落降低了视黄酸的产生,视黄酸的产生通过肝脏储存形式的增加来平衡,并有利于视黄酯途径,而潜在致病菌则促进视黄酸的产生。
▼
肠道中维生素A的状态和类视黄醇的可用性可以调节肠道微生物的组成。
•维生素A调节免疫球蛋白的产生帮助保持细菌稳态
类胡萝卜素摄入、免疫功能和肠道细菌稳态之间相互作用的模型,表明维生素A可以通过调节IgA的产生来有助于保持细菌稳态。
在动物中,与未缺乏维生素A的小鼠相比,缺乏维生素A的小鼠的肠道微生物组成中,以下菌属的丰度较低:
另一项研究表明,拟杆菌在维生素A缺乏小鼠中的比例较低,维生素A缺乏组和维生素A充足组之间的几个细菌比例不同。在小鼠模型中,维生素A被证明可以调节分段丝状细菌(SFB)的丰度。
分段丝状细菌是一组能够诱导Th17细胞分化的细菌。
▼
•维生素A的摄入与微生物群多样性相关
类胡萝卜素的摄入量和状态与更大的微生物群多样性和有益细菌丰度的增加有关。
例如,在孕妇中,类胡萝卜素的摄入量和血浆浓度与肠道微生物群的α多样性呈正相关。
•维生素A影响免疫反应
维生素A对肠道微生物群组成的调节可能作为调节肠道免疫反应的间接途径。
例如,维生素A在体外和体内均被证明可以抑制诺如病毒(急性胃肠炎最常见的病毒因子)的复制,并且这种抑制似乎是通过微生物组变化直接或间接发生的,特别是肠道中的乳杆菌科。
•改善疾病患者的微生物组成
在溃疡性结肠炎患者中,摄入维生素A有益,可导致微生物群组成发生显著变化。
在自闭症儿童中,维生素A补充剂增加了拟杆菌目细菌的比例,并减少了双歧杆菌属的细菌比例。
有趣的是,一项针对306名孟加拉国新生儿的研究表明,与安慰剂相比,补充维生素A增加了男孩双歧杆菌的丰度,而这种差异在女孩中并未观察到。
对这些婴儿直至2岁的随访表明,女孩中放线菌相对丰度与血浆视黄醇呈浓度依赖性正相关,但男孩中则不然。
此外,阿克曼菌(一种与粘膜相关的细菌)的相对丰度也与女孩的血浆视黄醇呈正相关。
微生物群在肠道中参与了微量营养素的代谢和吸收,并且可以影响宿主的微量营养素状态。在这方面,给出以下一些建议:
➤ 1
摄入多样化的食物可以为肠道微生物提供更广泛的营养来源,从而促进微生物群的多样性和稳定性。
建议摄入富含膳食纤维的水果、发酵食物、蔬菜、全谷类食物以及富含微量营养素的食物,如坚果和海鲜等。
例如,香蕉钾含量高,还含有大量维生素 B6 和维生素 C。西兰花不仅富含维生素 C,还富含维生素 K、铁、钙和钾。
确保摄入足够的每种维生素和矿物质的一个简单方法就是“彩虹饮食”,彩虹饮食顾名思义就是色彩缤纷的蔬菜和水果,它们含有丰富的微量营养素,是一种健康趋势。每餐可以注意一下,是否有至少三到四种不同颜色的植物性食物,对于孩子,也可以鼓励他们去寻找不同的颜色。

下表列出了常见的维生素的食物来源,可供参考。

➤2
维生素D可以增加肠道对钙的吸收能力,并促进钙的转运到骨骼和其他组织中。
维生素 C 有助于改善植物中铁的吸收,这对于素食者来说尤其重要,可以在菠菜沙拉中添加柠檬汁。维生素C通过提高铁的溶解度或作为十二指肠细胞色素B将铁从铁还原为铁的辅助因子,有助于非血红素铁的生物利用度。
维生素B12和叶酸之间存在相互依赖的关系。维生素B12参与叶酸的代谢和激活,而叶酸则有助于维生素B12的合成和利用。
其他如,维生素E是一种脂溶性维生素,需要脂肪的存在来促进其吸收。摄入适量的脂肪可以提高维生素E的吸收率。
微量营养素之间的相互作用是复杂的,并且还受到其他因素的影响,最好的方式是通过均衡的饮食来获取各种微量营养素,因为食物中的微量营养素通常以复杂的组合形式存在,相互之间的相互作用更加协调和自然。
➤3
益生菌和益生元是一些有益的微生物和它们的营养物质,可以促进肠道的健康和微生物群的平衡。
建议摄入含有益生菌的酸奶、发酵食品、益生元的食物如洋葱、大蒜和麦麸等,以支持肠道微生物的生长和活动。
益生菌和益生元可能有助于微量营养素的最佳生物利用度,减少负面影响
例如,益生元低聚半乳糖减轻了补铁对婴儿肠道的不利影响,而罗伊氏乳杆菌与泻药氧化镁结合使用可以改善儿童的慢性便秘,而不会导致微生物组失衡。
益生元可以改变肠道微生物群,促进产短链脂肪酸的菌产生(如双歧杆菌、乳酸杆菌、真杆菌等),与钙吸收(在人类和动物模型中)、骨密度和强度(在动物模型中)增加相关。
扩展阅读:
肠道微生物群与健康:探究发酵食品、饮食方式、益生菌和后生元的影响
➤4
一般来说,在小谷物食品的自然发酵中,B族维生素的利用率可能会增加,并且可能会产生一些氨基酸,虽然说谷物含有一些维生素,但在小谷物食品发酵过程中添加乳酸菌或酵母可能会提高维生素水平。
例如,添加乳酸乳球菌N8 和布拉酵母菌Saccharomyces boulardii SAA655可将 idli 面糊中核黄素和叶酸的浓度提高 40-90%。
注:Idli 是印度的一种传统发酵面包,是一种由大米和脱壳黑豆原料的混合物,经过湿磨和传统发酵制成的糕点。
尽管小米主要用于制造面粉,但其加工(发芽和发酵)会增加谷物的铁含量。
➤5
抗生素的滥用可能破坏肠道微生物群的平衡,影响微量营养素的代谢和吸收。
抗生素还可能导致肠道黏膜的炎症反应,进一步干扰微量营养素的吸收和利用。
在使用抗生素时,建议按照医生的指导使用,并且在必要时采取预防措施,如同时摄入益生菌和益生元,以减少对肠道微生物的不良影响。
扩展阅读:
➤6
过度摄入糖或长期的压力和焦虑会对肠道微生物和宿主营养吸收产生不良后果。
深加工食品通常经过多道工序,其中许多有益的营养物质可能被去除或破坏。这些食品通常富含添加剂、防腐剂和高糖分,而这些成分可能会对微量营养素的吸收和利用产生负面影响。
通过减少摄入加工食品、管理压力等干预措施,可以帮助改善营养吸收和维持良好的微量营养素水平。
扩展阅读:
你的焦虑可能与食品添加剂有关,警惕食品添加剂引起的微生物群变化
➤7
运动可以改善血液循环,增加血液流向肠道和其他组织,从而提高微量营养素的输送和吸收。
运动还可以提高新陈代谢,提高能量消耗和细胞代谢的速度。这可能会导致对微量营养素的需求增加,从而促进其吸收和利用。
➤8
定期体检可以帮助发现潜在的营养和健康问题,及早采取措施。
定期进行体检是监测体内微量营养素的一种方法,但它可能无法提供详细的微量营养素水平信息。常规体检通常包括血液检查,可以检测一些关键的营养素水平,如铁、维生素B12、维生素D等。对于有些微量营养素,可能需要进行特殊的检测。
➤9
由于每个人的肠道微生物群和微量营养素状态可能存在差异,个体化的营养咨询和评估可以帮助确定针对个体需求的饮食和营养。
肠道菌群和微量营养素之间存在着紧密的关系和相互作用。肠道菌群中的某些菌种可以帮助合成和吸收微量营养素。这些菌种通过代谢和转化,将食物中的原始形式的微量营养素转化为人体可以吸收和利用的活性形式,提供给宿主机体所需。
同时,适当的微量营养素摄取也对肠道菌群的平衡和健康至关重要。一些微量营养素,如锌、铁等,不仅是肠道菌群的生长和代谢所必需,还能影响菌群的结构和功能。缺乏这些微量营养素可能导致菌群紊乱,而菌群紊乱又可能影响微量营养素的吸收和利用。
肠道细菌对宿主微量营养素状态的影响是一个急需关注的研究领域。同时对微量营养素代谢的研究应该扩大到包括一般肠道微生物组成,而不仅仅是病原菌。
相关阅读:
主要参考文献
Dje Kouadio DK, Wieringa F, Greffeuille V, Humblot C. Bacteria from the gut influence the host micronutrient status. Crit Rev Food Sci Nutr. 2023 Jun 27:1-16.
Amimo, J., H. Michael, J. Chepngeno, S. Raev, L. Saif, and A. Vlasova. 2022. Immune impairment associated with vitamin A deficiency: Insights from clinical studies and animal model research. Nutrients 14 (23):5038.
Baldi, A. J., L. M. Larson, and S.-R. Pasricha. 2020. Balancing safety and potential for impact in universal iron interventions. Global Landscape of Nutrition Challenges in Infants and Children 93:51–62.
Cuisiniere, T., A. Calve, G. Fragoso, M. Oliero, R. Hajjar, E. Gonzalez, and M. Santos. 2021. Oral iron supplementation after antibiotic exposure induces a deleterious recovery of the gut microbiota. BMC Microbiology 21 (1):1–15.
Kang, S., R. Li, H. Jin, H. Y ou, and G. Ji. 2020. Effects of selenium and zinc-enriched Lactobacillus plantarum SeZi on antioxidant capacities and gut microbiome in an ICR mouse model. Antioxidants 9 (10):1028.
Kramer, J., Ö. Özkaya, and R. Kümmerli. 2020. Bacterial siderophores in community and host interactions. Nature Reviews. Microbiology 18 (3):152–63.
McMillen, S., S. Thomas, E. Liang, E. Nonnecke, C. Slupsky, and B. Lonnerdal. 2022. Gut microbiome alterations following postnatal iron supplementation depend on iron form and persist into adulthood. Nutrients 14 (3):412.
Qin H, Wu H, Shen K, Liu Y, Li M, Wang H, Qiao Z, Mu Z. Fermented Minor Grain Foods: Classification, Functional Components, and Probiotic Potential. Foods. 2022 Oct 11;11(20):3155. doi: 10.3390/foods11203155. PMID: 37430904; PMCID: PMC9601907.

谷禾健康

我们之前几篇文章都讲过关于抑郁,焦虑和肠道菌群的关系。
最新研究速递 | 柳叶刀:肠道微生物群在神经系统疾病中的作用
不仅如此,还和微量元素、维生素缺乏有关。
1. 微 量 元 素 篇
锌是帮助调节许多生物过程(包括我们的情绪)的核心营养素之一。锌的饮食来源多种多样,尤其是在红肉,家禽和鱼类中。当人的锌水平低时,可能会出现焦虑,抑郁,失眠和情绪失调等状况。
Petrilli 等人研究发现抑郁症和精神病患者的锌含量低。在患有帕金森氏病,阿尔茨海默氏病,唐氏综合症和多动症的患者中也发现了锌缺乏。
对于缺锌的患者,补锌已被证明有助于改善抑郁症状,是 “自然的抗抑郁药”。


一项研究表明,与仅接受SSRI治疗的患者相比,补充锌和SSRI可以更有效地改善重度抑郁症。对实验动物进行锌的长期治疗具有与抗抑郁药相同的作用。
注:SSRI是一类新型的抗抑郁药
当然,在评估锌水平和补充需求时,还需要考虑许多其他因素(例如炎症,其他微量元素的吸收等)。
碘缺乏,特别是在早年间缺乏,会阻碍身体和大脑的发育。碘是甲状腺激素必不可少的组成部分,这对大脑的发育和维持至关重要。碘缺乏症困扰着非常多人,但实际上因碘缺乏引起的智力障碍是可预防的。
大多数植物性食品的碘含量都非常低。素食主义者通常相对容易缺碘。
大脑非常需要铁。铁是产生神经递质(血清素,多巴胺和去甲肾上腺素),脑能量生成,海马功能(记忆),细胞信号传导和婴儿大脑发育所必需的。
许多植物性食物中的铁含量低于动物性食物,且更难吸收。素食者血液中铁的含量与杂食者差不多,但是他们体内的总铁存储量(储备量)较低。


2. 维 生 素 篇
维生素B在调节我们的心理健康方面也起着重要作用。
“B族维生素” 是指有助于人体细胞正常运作的八种必需营养素。B族维生素们既可以一起协同工作,又可以发挥各自的独特功能。


B维生素的八种类型包括:
B1,B2,B3,B5,B6,B7,B9,B12
某些与心理健康有关的疾病也可能与维生素B缺乏症并存。例如,早期研究表明,自闭症儿童的B6偏低,补充B6后,有些儿童表现出明显的改善,并且是第一次开始说话。
维生素B1,B3,B6
已成功用于治疗许多患有焦虑症和其他心理疾病的患者。在小鼠研究中,实际上发现VB3与苯二氮卓类和巴比妥类具有共同的特性。
维生素B12
有抑郁症患者存在B12缺乏症,而B12缺乏症的人比非缺乏症的人更容易患严重抑郁症。B12缺乏的其他症状可包括疲劳,嗜睡,躁狂等。
素食主义者饮食中几乎不含维生素B12,长期严重缺乏B12会致命。素食主义者可以服用补品或食用强化酵母(未经强化的天然酵母不包含维生素B12)。


维生素B12缺乏很普遍。一些研究发现,多达86%的成年人(无论选择哪种饮食)都缺乏。研究人员报告说,其价值范围很广,总的来说,素食主义者的B12含量往往较低。
B类维生素包括B2,B6,B9,B12也已被证明有助于治疗精神分裂症的症状。
维生素D——“阳光”维生素,对我们的心理健康也至关重要。大约50-90%的维生素D是由阳光照射产生的,其余的来自饮食。
维生素D缺乏症的人数众多,一些专家认为维生素D缺乏症是“全球健康问题”。
目前还不清楚维生素D与精神障碍之间的确切关系,但发现存在维生素D缺乏症风险的人群患抑郁症的风险增加,而维生素D含量较低可能会导致或加剧抑郁症状。
神经退行性疾病,肥胖,糖尿病,高血压,纤维肌痛,慢性疲劳综合症和骨质疏松症也与维生素D缺乏症有关。
关于神经退行性疾病与菌群详见文章 最新研究进展 | 行为和神经退行性疾病中的肠道微生物分子
维生素D3


维生素D3是我们身体需要的维生素D形式。在大脑的生长和发育中很重要,调节大脑中的钙水平,帮助保护脑细胞免受有害的氧化作用,并支持海马体(大脑记忆中心)的健康。
大多数研究发现,纯素食者的血液中维生素D3含量较低,并且在冬季,素食者更有可能出现维生素D3不足。
维生素K1在许多植物性食品中都丰富,但是维生素K2同样重要,而且常常被忽略。


维生素K2有多种形式,但我们需要的基本形式称为MK-4。在大脑中,需要MK-4来构建鞘脂的关键细胞膜成分,以及维持脑细胞的整体健康和功能。
维生素K2的MK-4形式仅存在于动物性食品中。
那么,是不是这些微量营养素补充越多越好呢?
国际自闭症研究会议上,约翰·霍普金斯大学研究人员提出:怀孕期间叶酸和维生素B12含量过高的女性,孩子患自闭症风险较高。
我们看看研究人员是如何得出这样的结论:
样本量及来源
研究人员分析了1391名母亲及其子女的数据。在孩子出生时招募志愿者,然后追踪长达15年。
检测指标及相关调查
在分娩的头几天检查母亲的血液中叶酸和维生素B12的水平。所有母亲均在怀孕期间进行了有关产前维生素和其他补充剂使用情况的调查。
发 现
在1391名儿童中有107名被诊断出患有自闭症谱系障碍,但这种自闭症的风险并不是在所有母婴中平均分布的。
· 每周服用三至五次产前复合维生素的母亲,孩子患自闭症的可能性较小。
·在头三个月服用这些补充剂的母亲生自闭症孩子的可能性要低67%
·在中晚期服用,其孩子自闭症可能性要低62%
·在妊娠中期服用,孩子患病的可能性要低57%
至此,服用产前维生素听起来很不错吧,问题来了:
在1391名母亲中,有95名母亲的VB12血液水平被世界卫生组织认为过高。在这些母亲中,有15个孩子被诊断出患有自闭症谱系障碍,这一风险是其他母亲的三倍。
同样,140名母亲的血液中叶酸水平“过高”,其中16名儿童患有自闭症谱系障碍。
而这其中有21位母亲两种维生素都“过量”。
更夸张的是,这21位母亲,有10个孩子被诊断出患有自闭症。换句话说,维生素水平过高的人中有将近一半有自闭症儿童。


当然,此研究也存在缺陷。
缺点之一是血样是在孩子出生后立即采集的,而不是在怀孕期间采集的。
此外也有猜测,是否因为她们知道正在接受研究而服用较大剂量的维生素?这些不得而知。
综上,如果您或者您家人现在正在孕育新的生命,需要考虑维生素服用的剂量以及评估相应风险。
换句话说,可以服用,但不宜过量。
相关阅读:
主要参考文献:
Naeem Z. (2010). Vitamin d deficiency- an ignored epidemic. International journal of health sciences, 4(1), V–VI.
Penckofer, S., Kouba, J., Byrn, M., & Estwing Ferrans, C. (2010). Vitamin D and depression: where is all the sunshine?. Issues in mental health nursing, 31(6), 385–393. doi:10.3109/01612840903437657
Ranjbar, E., Kasaei, M. S., Mohammad-Shirazi, et al., (2013). Effects of zinc supplementation in patients with major depression: a randomized clinical trial. Iranian journal of psychiatry, 8(2), 73–79.
Petrilli, M. A., Kranz, T. M., Kleinhaus, K., Joe, P., Getz, , et al., (2017). The Emerging Role for Zinc in Depression and Psychosis. Frontiers in pharmacology, 8, 414. doi:10.3389/fphar.2017.00414
Grabrucker A. M., Rowan M., Garner C. C. (2011). Brain-delivery of zinc-ions as potential treatment for neurological diseases: mini review. Drug Deliv. Lett. 1, 13–23.
免责声明:本公众号内容仅作交流参考,不作为诊断及医疗依据,身体问题请及时就医。
图片来自网络,侵删