-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com

谷禾健康
儿童呼吸系统疾病,包括呼吸道感染、反复喘息和哮喘,是儿童及其以后年龄发病和死亡的重要原因。
而哮喘是其中比较典型的一种,哮喘是全球最常见的慢性疾病之一,是一种复杂的、异质性的免疫介导的紊乱集合,以气道重塑和慢性气道炎症为特征。
▸ 哮喘的危险因素
哮喘的发病机制仍不清楚,但该疾病与多种遗传、环境、感染和营养因素有关。
哮喘的许多危险因素,包括生命早期的抗菌素暴露、配方奶喂养、以及母体接触抗生素怀孕期间,集中在产前和产后早期,儿童过敏性哮喘的发生可能与微生物和免疫发育关键时期的早期肠道微生物群落有关。
动物模型提供的证据表明,生命早期肠道微生物群的组成可能会影响呼吸道免疫以及对哮喘和呼吸道感染的易感性。
在这里我们总结了婴儿(0-12 个月大)肠道微生物群组成与儿童(0-18 岁)呼吸道疾病(即呼吸道感染、喘息或哮喘)之间的关联。
谷禾健康希望通过研究数据,找到更利于儿童健康的菌群数量与种类,有助于为未来的干预研究提供信息和构建更好的健康。
本文主要内容
●生命早期的肠道微生物
●生命早期肠道微生物群对儿童呼吸道疾病的影响
●早期肠道微生物的调理方法
●青少年哮喘的预防与治疗
每个人都可以被视为一个岛屿,由各种栖息地组成,这些栖息地被微生物群落定殖,并遵循创造和塑造当地组合多样性的规则。
不同婴儿身体部位的微生物群组成
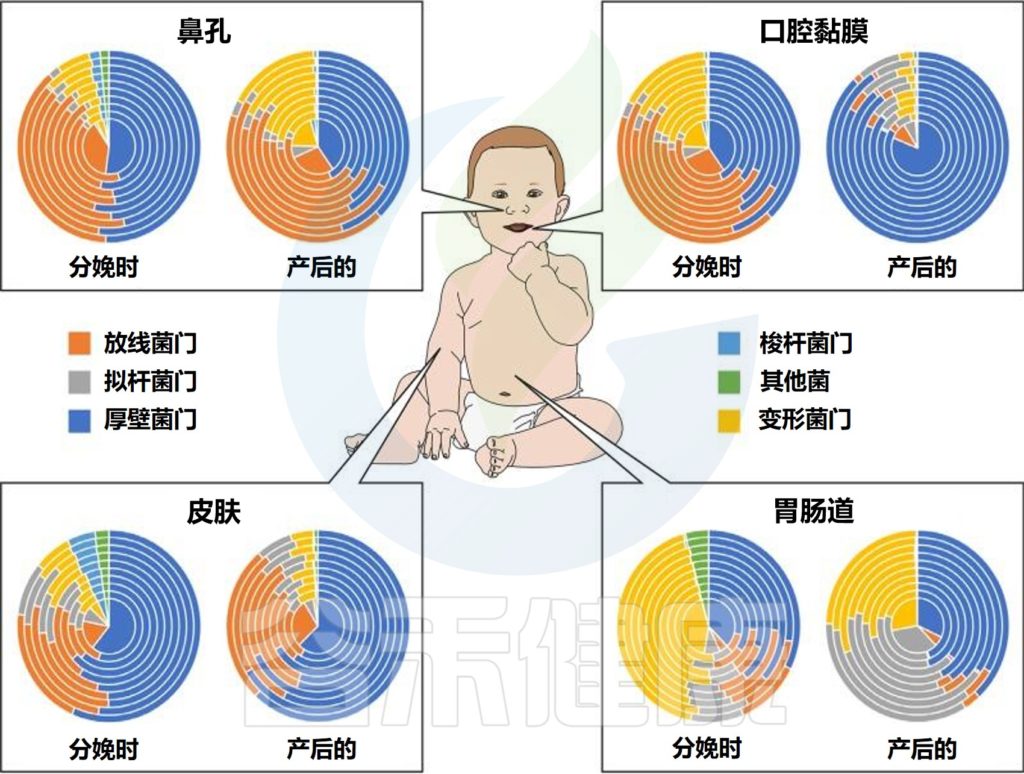
Milani C,et al.Microbiol Mol Biol Rev.2017
该图显示了婴儿微生物群组成的关键门在不同身体部位和生命早期不同阶段的相对丰度的全局概览。同心饼图示意性地表示个体间的可变性。
肠道微生物群是体内最大和最多样化的微生物群,包含数十亿细菌(主要生物)、古细菌、真核生物和病毒。
肠道菌群定植从出生时就开始了,在生命的最初几年是高度动态的,在1-3年后趋于稳定。
婴儿肠道核心微生物群
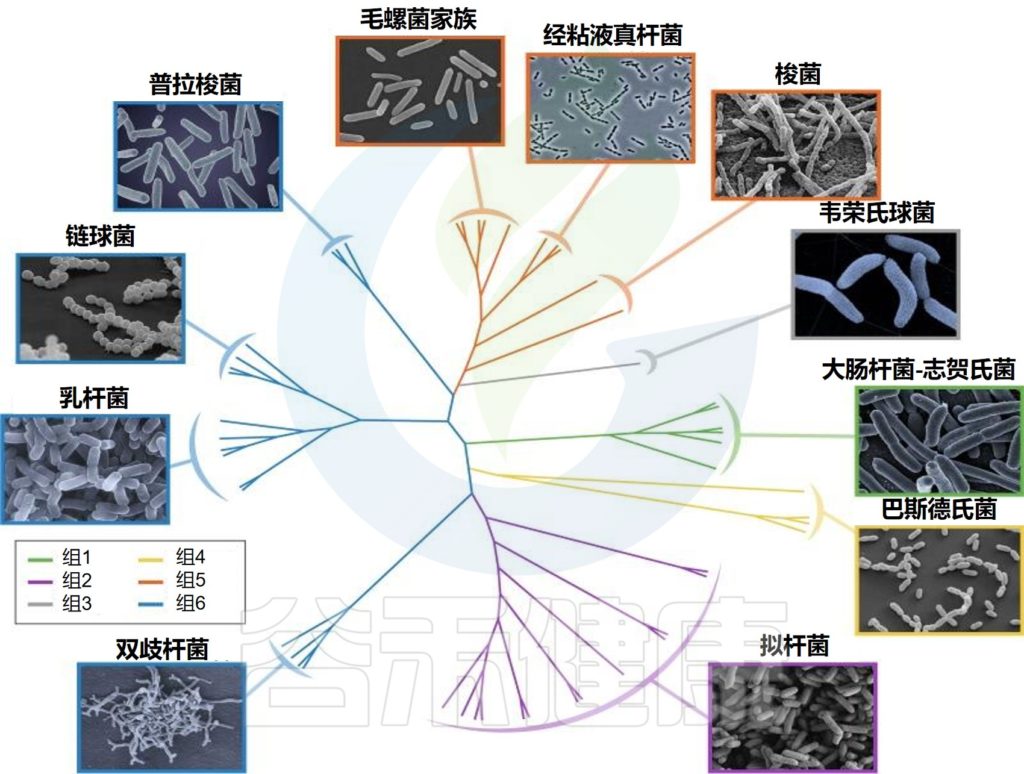
Milani C,et al.Microbiol Mol Biol Rev.2017
该图显示了涉及婴儿细菌核心微生物群的基于 16S rRNA 基因的树。树枝的颜色表示婴儿肠道微生物群的六个主要系统发育组。显示树的每个分支的关键婴儿肠道细菌分类群的电子显微镜图像。
相对于成人或年龄较大的儿童(>1岁)的肠道菌群,婴儿肠道菌群的多样性较低,菌群结构通常不稳定且高度动态。
双歧杆菌通常大量存在于婴儿,特别是母乳喂养的婴儿中,因此被认为是婴儿肠道微生物群的关键成员 。
尽管从婴儿肠道微生物群的初始组合到成人肠道微生物群的建立期间,个体水平的差异很大,但婴儿肠道微生物群可分为六种主要类型。
这种婴儿肠道微生物群的类型是根据肠道微生物群的组成和优势菌群的出现来确定的。详细地说,这些主要群体包括以下:
第1类,由肠杆菌目组成;
第2类,由拟杆菌目和疣微菌目组成;
第3 类,包括Selenomonadales以及梭菌目Pseudoflavonifractor、Subdoligranum和Desulfovibrio的成员;
第4类,包括所有巴斯德氏菌目;
第5类,包括大多数梭菌目;
第6类,包括梭状芽孢杆菌属、厌氧菌属和粪杆菌属、乳酸杆菌属和双歧杆菌属。
Bifidobacterium, Veillonella,
Streptococcus, Citrobacter,
Escherichia, Bacteroides, Clostridium
以上这些菌群在不同个体中主导婴儿肠道微生物群,它们在成人肠道微生物群中也很丰富。
▸ 梭状芽孢杆菌
梭状芽胞杆菌属的成员最近被重新分类为几个属,它们都属于梭状芽胞杆菌纲。这些物种通常存在于婴儿肠道微生物群中的微生物类群中。
▸ 拟杆菌
拟杆菌属。拟杆菌属的成员是成人肠道微生物群的主要成分,尽管它们也可能存在于婴儿肠道微生物群中,它们的存在似乎受到母乳低聚糖(HMO)的调节,其方式类似于双歧杆菌。
母乳低聚糖(HMO)——是母乳中第三丰富的固体成分(仅次于脂肪和乳糖),含量为5~15g/L,具有调节免疫,帮助大脑发育及调节肠道菌群等功能,有助于婴幼儿成长发育。
在小鼠实验中,已显示拟杆菌属的肠道定植。是宿主免疫系统识别和选择的结果,通过Toll样受体 (TLR) 和其他特定微生物-宿主相互作用。该属的成员被归类为能够代谢宿主产生的聚糖(例如HMO和粘蛋白)以及复杂的植物多糖(例如淀粉、纤维素、木聚糖和果胶)的糖破碎细菌。
●拟杆菌的作用
由于细胞外蛋白酶的作用,拟杆菌属物种通常具有蛋白水解活性。拟杆菌属成员利用的其他关键代谢功能包括胆汁酸的去结合。
在拟杆菌属中,脆弱拟杆菌被描述为可以产生多种荚膜多糖的成员,称为多糖A(PSA),是肠道菌群定植、宿主-微生物串扰或免疫调节的重要介质。
在各种拟杆菌属物种中,预计荚膜多糖会改变细胞表面的物理特性,并在宿主细菌共生中发挥关键作用。
▸ 韦荣氏球菌和链球菌
韦荣氏球菌和链球菌是婴儿肠道微生物群的一个次要成分。
这些细菌具有糖分解作用,利用其他婴儿肠道细菌(如链球菌和双歧杆菌)的碳水化合物发酵的最终产物(如乳酸)产生丙酸,形成重要的营养链。
这种短链脂肪酸被认为是肠道菌群的有益产物,因为它表现出抗炎特征,影响葡萄糖和能量稳态,增加胰岛素敏感性。
链球菌属的特定成员也构成婴儿肠道核心微生物群的一部分,并且是婴儿肠道中最早建立的细菌之一,可以在出生后的最初24小时内被识别出来。
▸ 乳酸杆菌
已知乳酸杆菌存在于婴儿肠道微生物群中,尽管它们在大肠中的数量低于上述细菌属,但在分娩后不久就存在。
乳酸杆菌的后续研究表明,与阴道分娩婴儿相比,剖腹产婴儿在生命的前6个月内的不同时间点的乳酸菌属检出率显著降低。
▸ 阿克曼氏菌
阿克曼氏菌自生命早期就存在于人类肠道中,但是水平非常低,阿克曼氏菌的存在与肠道完整性相关,已知其相对丰度和绝对数量会随着年龄的增长而迅速增加,特别是在断奶后。
小鼠实验证实了阿克曼氏菌对肠道屏障功能的影响,并证明其给药可防止饮食引起的肥胖。最近,还提供了涉及通过特定菌毛相关蛋白的TLR信号传导的机制解释。
临床、母体、喂养方式和环境因素共同塑造了生命早期的肠道微生物群。 对身体更方面都产生了一定影响。
考虑了生命早期肠道微生物群与儿童呼吸道疾病(包括呼吸道感染)之间的关联,在这里汇总了一些之前对肠道菌群与呼吸道疾病直接关联的研究。
肠道微生物的测量:通常通过收集粪便样本来测量,并且可以从多样性和丰度方面进行广泛描述。多样性描述了社区内不同分类群的数量。
探索哮喘或特应性喘息的研究
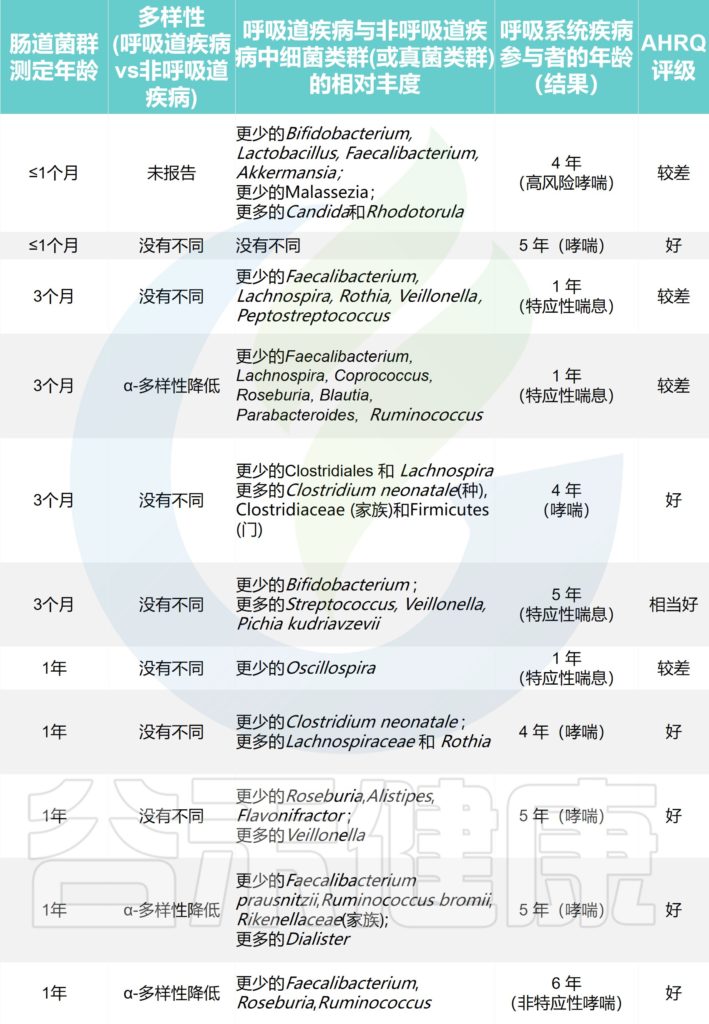
Alcazar CG,et al.Lancet Microbe.2022
探索呼吸道感染的研究

Alcazar CG,et al.Lancet Microbe.2022
喘息是与感染、过敏或后来的哮喘诊断相关的呼吸道症状。我们发现较高的α多样性与的喘息之间存在关联,这主要发生在阴道分娩的婴儿中。
α-多样性是指每个样本检测到的分类群数量,而β-多样性表示样本之间的组成差异。更细微的比较确定了不同分类水平下细菌或真菌的特定相对丰度。
大型研究(>700 名参与者)报告说,高 α 多样性对哮喘和喘息有保护作用。
探索了α-多样性与哮喘或特应性喘息之间的直接关联:与较低的α-多样性相比,生命第一年较高的肠道微生物群α-多样性与1岁时没有特应性喘息显著相关,并且在5岁和6岁时没有哮喘。
一项研究报告称,5周龄时肠道微生物群成熟度增加,肠道微生物群成熟度下降与6-11岁的哮喘高风险相关;还有两项研究报告了12个月时未成熟的肠道微生物群与5-6岁时哮喘风险增加之间存在一定关联。
基于细菌类群组成随时间的变化探索了健康参与者肠道微生物成熟度,并将该微生物群成熟度与儿童呼吸道疾病参与者的微生物群成熟度进行了比较。
总体而言,有证据表明双歧杆菌在3个月前婴儿的粪便中的相对丰度较低,与1岁时的呼吸道感染和4-5岁时的哮喘有关。
在3-12个月时的粪便样本中粪杆菌属、罗氏菌属和瘤胃球菌的丰度较低,与1-6岁时的哮喘和特应性喘息有关。
注意
然而,存在重要的研究限制,包括异质的结果定义和随访时间、残余混杂、小样本量以及异质的生物信息学和统计方法,大多数研究没有报告效果估计。
还有一些研究报告说,在1周龄时,非共生肠道细菌(如克雷伯氏菌和肠球菌)的相对丰度较高与1岁时的呼吸道感染有关; 3 个月时链球菌的相对丰度与 5 岁时的特应性喘息有关;1岁时Rothia或Dialister的高相对丰度与4-5岁时哮喘相关。但是具体作用机制目前还不清楚。
▸ 双歧杆菌增强呼吸道的免疫
双歧杆菌属(Bifidobacterium)是出生后4个月内儿童肠道中最丰富的细菌之一。并且已被证明通过体外和体内的表面相关分子和微生物群衍生代谢物调节个体的全身免疫反应。
在哮喘和呼吸道感染小鼠模型中,特定的双歧杆菌已被证明会影响呼吸道疾病的易感性。
一项研究表明,婴儿双歧杆菌的肠道定植可调节Th1和Th2反应之间的平衡,从而减少诱导小鼠模型中特应性哮喘的症状。
Th1(辅助型T淋巴细胞1)主要是增强吞噬细胞介导的抗感染免疫,特别是抗胞内病原体的感染。
Th2(辅助型T淋巴细胞2)Th2细胞的主要效应是辅助B细胞活化,其分泌的细胞因子可以促进B细胞增殖、分化和抗体的生成。
另一项研究报告称,当受到流感病毒的攻击时,与肠道丰度较低的小鼠相比,肠道丰度较高的双歧杆菌和拟杆菌的小鼠通过增强的CD8 T细胞和调节良好的巨噬细胞反应来提高流感存活率,从而防止过多的气道中性粒细胞流入。
▸ 梭状芽胞杆菌降低呼吸道炎症
Faecalibacterium、Ruminococcus、Lachnospira、Roseburia和Veillonella属于梭状芽孢杆菌类,在4-6个月大的儿童肠道中丰度较高。
已经描述了Roseburia和Faecalibacterium的潜在免疫调节机制,它们产生丁酸盐。
丁酸盐——一种在动物和体外模型中具有抗炎特性的细菌代谢物。
研究发现上呼吸道感染与婴儿粪便样本中丁酸梭菌的丰度降低有关。梭状芽胞杆菌可促进调节性T细胞产生并抑制炎症细胞因子,其中一些与人类全身感染有关。因此,丁酸梭菌对婴儿对感染的免疫反应的潜在抑制作用需要进一步研究。
另一项研究表明,给无菌小鼠接种毛螺菌属、韦荣氏菌属、粪杆菌属和罗氏菌可改善这些小鼠成年后代的气道炎症,但是这些细菌在呼吸系统疾病中的机制作用了解还是较少。
▸ 韦荣氏球菌刺激免疫分化
在我们的研究中,韦荣氏球菌,特别是小韦荣氏球菌(Veillonella parvula),与上呼吸道感染呈正相关,尤其是剖宫产婴儿。Veillonella parvula常见于口腔菌群中,它在口腔和肠道生态系统中都可以观察到。
一项针对120名荷兰婴儿的前瞻性研究发现,在1周大的婴儿中使用 16S V4 rRNA 测序发现了大量的韦荣氏菌操作分类单位,这与出生后第一年的呼吸道感染数量增加有关。
在研究中,Veillonella parvula在人体肠道中产生丙酸盐,这可能会刺激产生IL10的调节性T细胞分化;在小肠中,它会诱导产生IL-8、IL-1β、IL-10和 TNF- α37来影响呼吸道以至于全身的免疫。
▸ 棒状杆菌为呼吸道的致病菌
在剖宫产婴儿中,较高的棒状杆菌属(Corynebacterium)物种相对丰度与较高的上呼吸道感染风险相关。
棒状杆菌属物种通常被列为呼吸道中的致病菌。病例系列表明,痰中的假白喉棒状杆菌是肺部感染的驱动因素,一项来自法国的鼻咽微生物组病例对照研究发现,与健康对照组相比,病毒性呼吸道感染患者的假白喉棒状杆菌富集。
在3个月和1岁收集的粪便中,Faecalibacterium、 Roseburia和Ruminococcus相对丰度较低,与1-6岁的哮喘和特应性喘息相关。
3个月时Lachnospira的相对丰度较低,但1岁时的相对丰度增加也与1-6岁时哮喘和特应性喘息相关。
一项研究显示3个月时Veillonella的相对丰度较低与1岁时的特应性喘息相关,而两项研究报告称3个月和1岁时Veillonella的相对丰度较高与5岁时的哮喘和特应性喘息相关。
✦真菌与哮喘的关系
三项研究探索了真菌和哮喘之间的关系。
在一项研究中,在 1 个月大时测量的念珠菌和红酵母菌的相对丰度较高,而马拉色菌类群的丰度较低。
在另一项研究中,3月龄时Pichia kudriavzevii的相对丰度增加,与4-5岁时的哮喘和特应性喘息相关。
第三项研究却发现真菌成熟度与6岁儿童哮喘之间没有关联。
肠道菌群对哮喘的影响至少部分是由细菌代谢物介导的,这些代谢物可能会影响身体远端的免疫反应。
✦短链脂肪酸降低哮喘致敏性
在人类气道炎症中具有保护作用的最知名代谢物是 短链脂肪酸。1岁时粪便中含有大量丁酸盐和丙酸盐的儿童的特应性致敏性显著降低,并且在3至6岁之间不太可能患哮喘。
✦组胺和氧化脂质影响肺部炎症
与非哮喘志愿者相比,哮喘患者粪便样本中分泌组胺的细菌数量显著高于非哮喘志愿者。
此外,分泌组胺的细菌数量与疾病严重程度相关。然而,在过敏性气道炎症模型中,细菌来源的组胺降低了支气管肺泡液中的总细胞数和肺匀浆中IL-4、IL-5和IL-13的量。
相反,在蟑螂抗原小鼠气道炎症模型中,用12,13-diHOME(一种氧化脂质)对小鼠进行腹腔内治疗会减少肺部调节性T细胞的数量并增加肺部炎症。
建议
越来越多的证据表明细菌在哮喘中的作用,但需要进一步的研究来更清楚地定义所涉及的最重要的物种,并了解哮喘背景下的细菌生态失调是否是疾病的原因或影响。
有必要进行更详细的机制研究,以充分了解生命不同阶段肺和肠道微生物群组成和代谢与特定类型的哮喘炎症之间的复杂关联。
最后,未来的工作应该集中在继续详细描述在哮喘中介导细菌与宿主之间交流的细胞和分子机制。
通常用于预防或治疗不一定由特定病原体引起的感染的抗生素可以有效地消耗肠道微生物群。患有 NEC的新生儿感染肠道微生物的风险很高,抗生素通常用于预防或治疗这些感染。
NEC——新生儿坏死性小肠结肠炎(NEC)为一种获得性疾病,是多种原因引起的肠黏膜损害,使之缺血、缺氧,导致小肠、结肠发生弥漫性或局部坏死的一种疾病。
对于儿童炎症性肠病的治疗,使用单一抗生素对有并发症的患者有益,例如瘘管和脓肿,而广泛的抗生素组合可能会改善临床结果。
注意
在幼儿中使用抗生素存在很大风险。大量证据表明,抗生素会影响我们抵抗感染的能力、免疫系统的功能以及我们加工食物的能力。
肠道微生物群的破坏可能导致长期的健康后果,包括维生素产量减少、营养吸收减少以及糖尿病、哮喘、肥胖和感染风险增加。
口服益生元和益生菌是影响生命早期肠道微生物群发育的最常见方法。
益生元被定义为“选择性刺激肠道微生物群中一种或多种微生物属或物种的生长和活性,从而为宿主带来健康益处”的化合物,而益生菌被定义为“赋予宿主健康益处的活微生物”。摄入足量时会对宿主产生健康影响。
目前可用的益生元包括人乳低聚糖、菊粉、低聚果糖和低聚半乳糖;可用的益生菌包括双歧杆菌和乳酸杆菌属。
✦益生元和益生菌的作用
通过调节肠道微生物群,益生元对宿主产生健康影响。益生菌通过对粘膜和上皮的竞争性粘附、粘膜 IgA反应、抗菌物质的分泌、促炎途径的下调、抗炎细胞因子的产生和免疫系统的调节来增强肠道上皮屏障。
最近的研究表明,益生菌可以预防儿科疾病和障碍的进展,包括过敏、胃肠道感染、肥胖,甚至上呼吸道感染。
干预研究进一步表明,益生菌可以减轻某些疾病的严重程度,但对每种疾病的最佳干预仍然知之甚少。
虽然益生菌在某些情况下可以缓解过敏症状,但它们通常不能有效调节肠道微生物的组成。有证据表明,嗜热链球菌和双歧杆菌的组合可有效预防儿童抗生素相关性腹泻。
此外,合成生物学使益生菌和共生微生物的工程具有新的治疗功能。例如,融合蛋白HSP65-6P277的表达减少了非肥胖糖尿病小鼠中1型糖尿病的发病,而在非肥胖糖尿病鼠中口服重组乳酸乳球菌可改善糖耐量并显著减少胰岛素炎。
建议
尽管益生元和益生菌的应用前景不错,但在未来的研究中,应讨论益生菌和益生素的施用时间、不同菌株和菌株组合的效果、工程、安全性以及这些益生菌与益生素组合是否更有效的确定。
营养素可以通过塑造微生物菌群的组成,对婴儿肠道微生物的定植模式产生短期和长期影响。
越来越多的证据表明,摄入的膳食成分与炎症性肠病、2型糖尿病和动脉粥样硬化的发展有关。肠道菌群的最大变化发生在固体食物的引入,这表明饮食应被视为肠道菌群的核心决定因素。
✦饮食疗法
有趣的是,在中医中,早就有“药食同源”的概念。该概念的一个方面是食物是一种药物,适当的饮食或某些食物可以维持身体的平衡和健康,并预防或减轻某些疾病的发展。
在现代医学中,饮食改变越来越被认为是一种通过改变肠道微生物群来改变全身炎症的相对简单的方法。
早期肠内营养 (EEN) 是一种饮食疗法,已被用作儿童克罗恩病的一线疗法,通过用仅由液体营养素组成的配方代替正常饮食成分,旨在使炎症标志物正常化并诱导临床缓解。
✦高膳食纤维可以减轻呼吸道疾病
此外,另一项研究报告称,喂食高纤维饮食的小鼠可以产生独特的肠道微生物群,从而导致短链脂肪酸乙酸酯水平升高。
高纤维或醋酸盐喂养通过减少与人类哮喘和小鼠哮喘模型相关的某些基因在小鼠胎肺中的表达,显著抑制过敏性气道疾病。
此外,发现肠道微生物不仅与哮喘有关,而且还降低了与哮喘严重程度和炎症表型相关的气道微生物群的多样性和群落组成。
抗炎特性
此外,最近的一些研究证明,膳食纤维具有抗炎特性,这可以部分解释纤维对肠道微生物菌群的影响。 使用临床前模型的几项研究表明,可发酵纤维补充剂通过微生物群诱导的特定抗炎代谢物产生的变化来改变疾病结果。
然而,还需要更多的研究来增加我们对不同饮食如何塑造微生物群和改变健康结果的理解。
粪便微生物群移植(FMT)被定义为将健康供体的粪便悬浮液输注到受体患者的胃肠道中,以恢复肠道微生物群的正常多样性和功能。
粪菌移植的方式:粪便微生物群可通过结肠镜检查、鼻胃管或鼻十二指肠管、灌肠剂或口服胶囊置于患者体内。
由于肠道微生物群宏基因组测序的技术进步以及对其组成和功能的日益了解,粪菌移植近年来引起了越来越多的兴趣和关注。尽管粪菌移植仍然知之甚少,但它不再被认为是一种“替代”和最后的医疗实践,现在作为一种具有生物学合理性的有价值的疗法正在获得主流接受。
此外,这种疗法已被证明能够重建正常运作的微生物群落。通过为患者提供来自合适供体的平衡微生物群,纠正了在艰难梭菌感染 (CDI)发病机制中起重要作用的不平衡肠道微生物菌群。
在一系列关于复发性CDI的研究中,85%接受粪菌移植的患者出现症状缓解。此外,考虑到肠脑轴和肠道微生物之间的相互作用,粪菌移植被认为是治疗某些精神疾病的可能方法,例如自闭症谱系障碍。
建议
然而,粪菌移植的微生物组成尚未完全确定。因此,需要澄清与改善临床结果相关的微生物结构或功能特征,以确定优选的组合。
未来的研究应侧重于确定“健康”微生物菌群的范围以及制定评估最佳组成的标准。
5岁至14岁的哮喘患病率约为10%,使其成为全球儿童时期最普遍的慢性病。尽管下呼吸道感染带来了巨大的健康负担,但目前还没有专门针对它们或儿童哮喘被广泛许可的预防策略,所以暂时只能用一般呼吸道疾病的方法来预防。
✦注意空气卫生
注意室内的清洁和空气流通,因为空气中的灰尘和细菌是哮喘病发的主要致敏原,所以应该勤加打扫,减少空气中的尘埃。尽量减少暴露于空气污染的室内和室外。
✦良好饮食习惯
坚持每天喝水,喝水是排出身体毒素的最佳的方法。在日常生活中注意饮食习惯,一日三餐要按时就餐,少吃油腻。
✦良好生活,避免螨虫
哮喘病人要在日常生活中每天要保持良好的生活态度,放松心情。不要在家里养猫、狗、花、鸟等。经常晾晒被褥、换洗床单,避免螨虫孳生。
✦加强自我管理
对于5岁及以上被诊断为哮喘的儿童或青少年,提供哮喘自我管理计划,包括书面的个性化行动计划和教育。
说明污染会引发或加剧哮喘,并在个性化的行动计划中包含尽量减少暴露于室内和室外空气污染的方法。
注:哮喘好发于青少年和儿童,一旦患病,如防治不当,很容易反复发病,随着发病频度的增加,病情会逐渐加重,必将严重影响生活质量和学习工作能力,给个人家庭和社会造成沉重负担。
我们结合当前的研究与认知,提出了一些适用于儿童和青少年新诊断哮喘或当前治疗无法控制哮喘的治疗建议。
✦药物治疗
•SABA
β2受体激动剂(SABA)是一类能够分布在气道平滑肌上的β2受体产生支气管扩张作用的哮喘治疗药物。这类药物属于支气管扩张药,是哮喘急性发作(气道痉挛)的首选药物,能够迅速改善哮喘急性发作时的呼吸困难、咳嗽等的症状。
对新诊断为哮喘的儿童和年轻人(5至16岁),可以提供SABA作为缓解疗法。
对于患有哮喘的儿童和青少年(5至16岁),他们很少出现短暂的喘息和正常的肺功能,也可以考虑单独使用SABA缓解疗法进行治疗。
•ICS
吸入性糖皮质激素(ICS)是目前控制哮喘病的气道炎症最有效的药物,以定量气雾剂、干粉剂或溶液吸入。
在哮喘炎症表型中,通常接受高剂量吸入性皮质类固醇 (ICS) 的中性粒细胞性哮喘患者表现出较少的细菌负荷,其中嗜血杆菌和莫拉菌属、变形杆菌门的成员相对富集,而链球菌的相对丰度降低。
ICS已经成为目前哮喘治疗的第一线治疗,对病人是最为重要的治疗,任何哮喘患者,只要诊断正确,都应该接受ICS的治疗,这是一个长期维持治疗,可以起到气管局部抗炎的效果,改善病情,预防哮喘急性发作。
为儿童和青少年(5至16岁)提供儿科低剂量ICS作为一线维持治疗。
就诊时出现明显表明需要维持治疗的症状(如导致夜间醒来)或单独使用SABA无法控制的哮喘也应使用ICS治疗。
✦风险分层
同时使用风险分层来识别预后不良风险增加的哮喘患者,并使用此信息优化他们的护理。
根据诸如不依从哮喘药物、心理社会问题和反复发作的哮喘计划外护理等因素进行风险分层。
总体而言,有观察证据表明,在生命的第一年,肠道共生细菌属的低α多样性和相对丰度与随后的呼吸系统疾病,尤其是哮喘有关。因此在婴儿早期关注和了解肠道菌群状况对于后面哮喘发生和预防非常重要,进一步研究哮喘患者的肠道和下呼吸道微生物群可能有助于开发更有效的方法来预防和治疗哮喘。
主要参考文献
Alcazar CG, Paes VM, Shao Y, Oesser C, Miltz A, Lawley TD, Brocklehurst P, Rodger A, Field N. The association between early-life gut microbiota and childhood respiratory diseases: a systematic review. Lancet Microbe. 2022 Aug 18:S2666-5247(22)00184-7. doi: 10.1016/S2666-5247(22)00184-7. Epub ahead of print. PMID: 35988549.
Milani C, Duranti S, Bottacini F, Casey E, Turroni F, Mahony J, Belzer C, Delgado Palacio S, Arboleya Montes S, Mancabelli L, Lugli GA, Rodriguez JM, Bode L, de Vos W, Gueimonde M, Margolles A, van Sinderen D, Ventura M. The First Microbial Colonizers of the Human Gut: Composition, Activities, and Health Implications of the Infant Gut Microbiota. Microbiol Mol Biol Rev. 2017 Nov 8;81(4):e00036-17. doi: 10.1128/MMBR.00036-17. PMID: 29118049; PMCID: PMC5706746.
Zhuang L, Chen H, Zhang S, Zhuang J, Li Q, Feng Z. Intestinal Microbiota in Early Life and Its Implications on Childhood Health. Genomics Proteomics Bioinformatics. 2019 Feb;17(1):13-25. doi: 10.1016/j.gpb.2018.10.002. Epub 2019 Apr 12. PMID: 30986482; PMCID: PMC6522475.
Barcik W, Boutin RCT, Sokolowska M, Finlay BB. The Role of Lung and Gut Microbiota in the Pathology of Asthma. Immunity. 2020 Feb 18;52(2):241-255. doi: 10.1016/j.immuni.2020.01.007. PMID: 32075727; PMCID: PMC7128389.
Ver Heul A, Planer J, Kau AL. The Human Microbiota and Asthma. Clin Rev Allergy Immunol. 2019 Dec;57(3):350-363. doi: 10.1007/s12016-018-8719-7. PMID: 30426401; PMCID: PMC7449604.
Moroishi Y, Gui J, Hoen AG, Morrison HG, Baker ER, Nadeau KC, Li H, Li Z, Madan JC, Karagas MR. The relationship between the gut microbiome and the risk of respiratory infections among newborns. Commun Med (Lond). 2022 Jul 14;2:87. doi: 10.1038/s43856-022-00152-1. PMID: 35847562; PMCID: PMC9283516.

谷禾健康

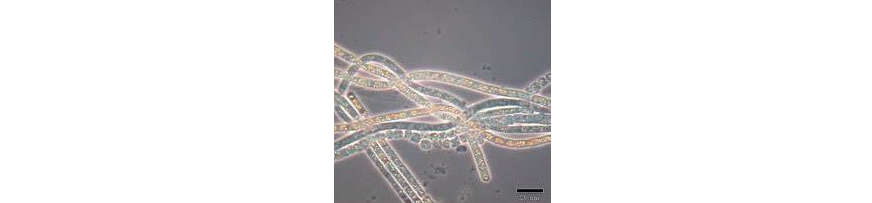
毛螺菌属(Lachnospira),属于厚壁菌门,毛螺菌科(Lachnospiraceae),该菌属存在于大多数健康人的肠道里,可能是一种潜在的有益菌,参与多种碳水化合物的代谢,尤其水果蔬菜中的果胶(一种复杂的膳食纤维和益生元)的能力很强,发酵导致乙酸和丁酸的产生为宿主提供能量的主要来源。
图片来源:microbiomology
毛螺菌科(Lachnospiraceae)目前在NCBI中被描述为包括 58 个属和几个未分类的菌。毛螺菌属(Lachnospira)是毛螺菌科的一个重要组成成员。
认识毛螺菌属之间先了解下毛螺菌科。
人类结肠微生物群可以处理多种底物,包括蛋白质、寡肽、膳食多糖、内源性粘蛋白和逃避宿主消化的糖蛋白 。肠道菌群对碳水化合物的代谢是向宿主提供营养和能量的关键过程。
在厚壁菌门中,毛螺菌科、乳杆菌科和瘤胃球菌科水解淀粉和其他糖以产生丁酸盐和其他短链脂肪酸。
毛螺菌科(Lachnospiraceae)的基因组分析揭示了其组内成员利用饮食衍生的多糖(包括淀粉、菊粉和阿拉伯木聚糖)的相当大的能力,但是在菌种和菌株之间存在很大差异。
毛螺菌科是一个系统发育和形态异质的分类群,属于厚壁菌门的梭菌簇 XIVa,毛螺菌科的所有成员都是厌氧的、发酵的和化学有机营养的,并且一些表现出强水解活性,例如通过果胶甲酯酶、果胶酸裂合酶、木聚糖酶、α-L-阿拉伯呋喃糖苷酶、β-木糖苷酶α-和β-半乳糖苷酶的活性、α-和β-葡萄糖苷酶、N-乙酰-β-氨基葡萄糖苷酶或α-淀粉酶。
毛螺菌科存在于早期婴儿中,甚至在胎粪中也有发现。然而,毛螺菌科丰度的增加与衰老有关。毛螺菌科的丰度在患有不同疾病的受试者的肠腔中也增加了,尽管该科的分类群一再显示出它们为宿主产生有益代谢物的能力。
★ 形态和代谢
Lachnospira细胞形态呈直的或略微弯曲的棒状细胞,有的可能呈螺旋状。单细胞尺寸为 0.35–0.6×2.0–4.0 µm,DNA G + C 含量( mol %):38–45。细胞成对出现,有时呈长链状。细胞具有革兰氏阳性超微结构,严格厌氧。
在 30–45 °C 下生长,在含有瘤胃液或酵母提取物、无机盐、果胶或聚半乳糖醛酸的厌氧培养基中生长。
化能有机营养,发酵代谢;发酵果胶、聚半乳糖醛酸、果糖和纤维二糖等。乙酸盐、甲酸盐、乙醇和 CO2是聚半乳糖醛酸和果胶发酵的主要最终产物。也可能产生少量的H2 。果胶发酵时也会产生甲醇,不产生琥珀酸盐、丁酸盐和丙酸盐。
不产生吲哚、过氧化氢酶或 H2S,不还原硝酸盐。不水解明胶或淀粉。主要存在于哺乳动物肠道,从牛瘤胃内容物和猪粪便和盲肠内容物中分离。
在肠道中,抗性淀粉和低聚半乳糖可以通过结合胆盐直接降低胆汁酸的浓度。Lachnospira等产生丁酸盐细菌的增加都间接导致胆汁盐浓度降低。
★ 分类和物种
Lachnospira(毛螺菌属)主要有以下结果物种:
Lachnospira rogosae
Lachnospira eligens
Lachnospira multipara
Lachnospira multiparis
Lachnospira pectinoschiza
模式种是多对毛螺菌(Lachnospira multiparus)。
以前的16S 的测试,可能会错误地将Lachnospira rogosae识别为乳酸杆菌。后来纠正这一错误并更新了数据库,重新正确重命名为Lachnospira rogosae。
Lachnospira pectinoschiza 是从猪的结肠内容物中分离的能分解果胶的菌。但是该菌物种无法从羊的瘤胃内容物中分离出来,即使这些动物被喂食高果胶饮食。实验中果胶、聚半乳糖醛酸和葡萄糖酸盐是支持该菌快速生长的唯一底物。
不同的是,Lachnospira multiparus 是瘤胃内主要的果胶分解菌。它的碳水化合物代谢在实验室发酵罐的生长实验中进行的研究。
★ 哪些因素影响毛螺菌属
增加
食用富含纤维的植物性饮食与Roseburia、Lachnospira和Prevotella属的丰度增加以及短链脂肪酸产量增加相关。
用全谷物代替六周的饮食习惯精制谷物增加了 Lachnospira和Roseburia,减少了肠杆菌科的成员,总体上产生了更有利的微生物景观。
全谷物:是指完整、碾碎、破碎或压片的谷物,其基本组成包括淀粉质胚乳、胚芽与皮层,各组成部分的相对比例与完整颖果一样。
全谷物不仅含有丰富的B族维生素、镁、铁和膳食纤维,还含有多酚、维生素E、单宁、类胡萝卜素、植酸、木质素和木脂素等常见抗氧化成分,而且还含有一些果蔬食品中少见但具有很高营养价值的抗氧化成分,如γ-谷维素、烷基间苯二酚、燕麦蒽酰胺等。比如:全燕麦,荞麦,黑米,小米,全麦等。
果胶是一种水果蔬菜中发现的复杂的膳食纤维和益生元。研究表明水果中纤维的消耗与健康成人肠道中大量的果胶分解细菌属Lachnospira 密切相关。果胶摄入增加梭菌属簇 XIV(Lachnospira、Dorea和Clostridium),其中Lachnospira的增幅最大。
最近的一项研究发现Lachnospira与 β-胡萝卜素、维生素 E 和植物脂肪的摄入量呈正相关,而与肉类、总蛋白和胆固醇的摄入量呈负相关 。
洋车前子是一种广泛用于治疗便秘的药物。它将水分困在肠道中,增加粪便中的水分,缓解排便并改变结肠环境。研究显示洋车前子处理可以增加Lachnospira,Roseburia 和 Faecalibacterium.
茶多糖维持了肠道微生物群的多样性,恢复了一些因糖尿病而减少的细菌属(毛螺菌属、罗斯氏菌和Fluviicola)的相对丰度。
茶多糖主要由葡萄糖、阿拉伯糖、木糖、岩藻糖、核糖、半乳糖等组成。
葡萄不仅含有各种植物化学物质,如儿茶素,原花青素,花青素,亮氨酸花青素,槲皮素,山奈酚,二苯乙烯,鞣花酸和羟基肉桂酸酯,而且也是膳食纤维的良好来源。与基线相比,4周的葡萄粉摄入量显着增加三个属Akkermansia,Flavonifractor和毛螺菌属的相对丰度。
减少
将117名超重成年人随机均分为食用4次/周炸肉组和不食用炸肉组,干预4周,发现食用炸肉组的菌群多样性降低,Lachnospira和Flavonifractor丰度降低,Dialister、Dorea、韦荣球菌属丰度增加。
越来越多的证据表明,众所周知的致癌驱动因素吸烟会影响肠道微生物组。一项研究针对 803 名成年人子集的吸烟和肠道微生物组使用16s测序进行了分析。
发现以前和现在吸烟者的粪便微生物组的整体组成与从不吸烟者有显着差异。相对于从不吸烟者而言, Lachnospira 和Tenericutes菌则被耗尽。这些变化在种族和族裔亚群中是一致的,表明吸烟会导致Lachnospira消失或减少。
★ 与其他菌的相互作用(仅供参考)
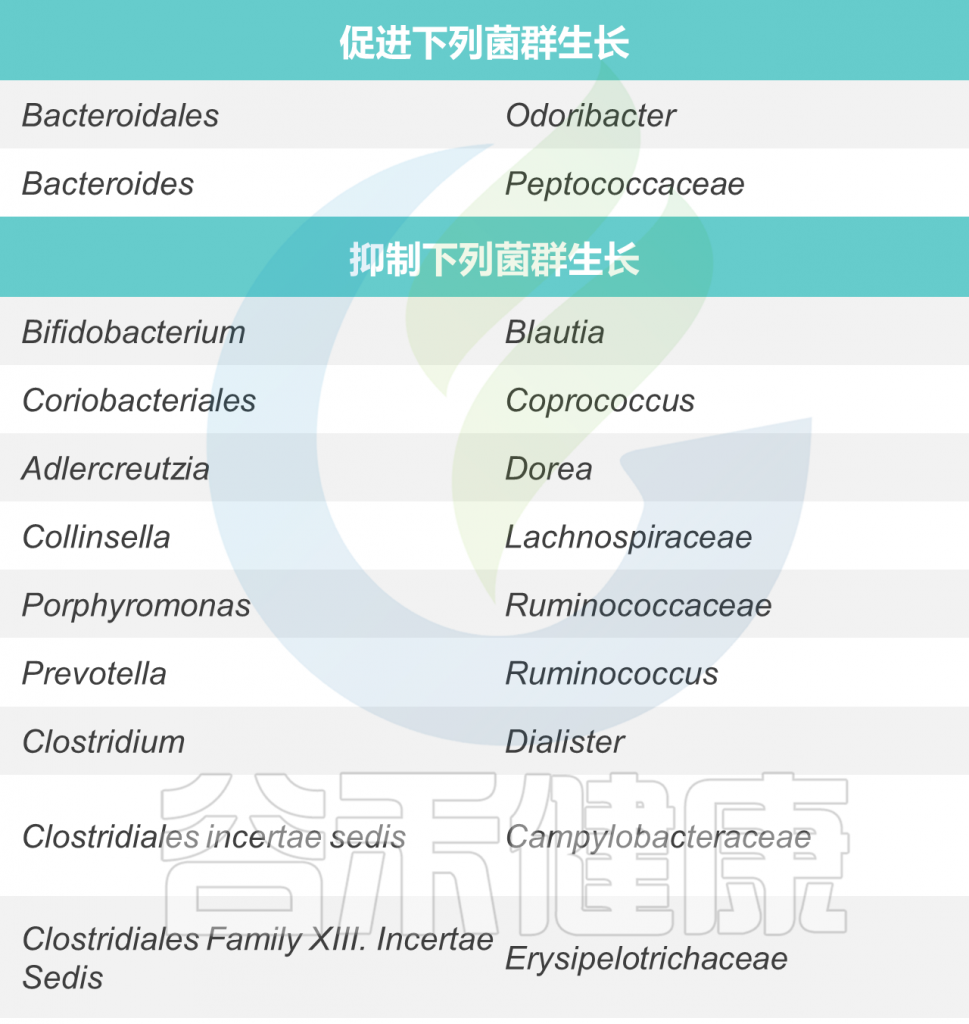
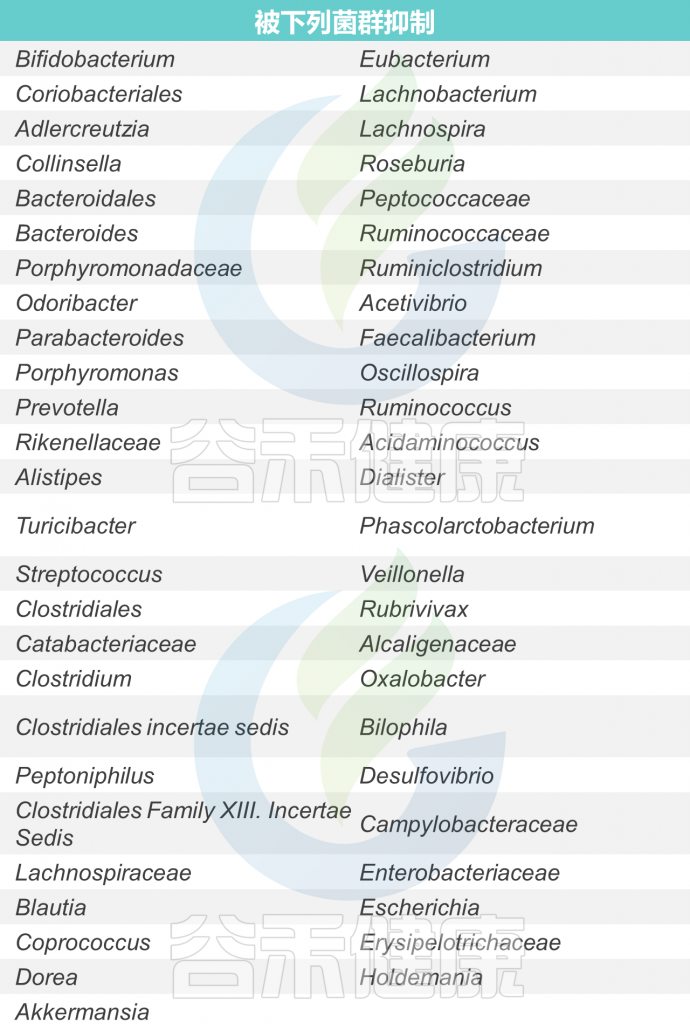


睡眠(夜猫子)
海法大学和以色列理工学院的合作研究项目发现,“早起的人”和“夜猫子”的肠道微生物组(寄居在消化道的细菌群)彼此不同。该研究将人们分为三种不同的‘时型’:
“云雀”——早起的晨型人,在早晨活力最好;
“猫头鹰”——晚睡的夜猫子,在早晨运作困难;
“中间群体”——大部分人属于这种。
研究结果指出了“云雀”和“猫头鹰”的微生物组之间的差异;在“云雀”中,细菌属Alistipes 的百分比更高,而在“猫头鹰”中,属于Lachnospira属的细菌更高,该细菌为产生丁酸盐的细菌,是一种短链脂肪酸,是睡眠和觉醒相关信号的来源。
其他研究也陆续发现包括毛螺菌属Lachnospira、棒状杆菌属Corynebacterium 和 布劳特氏菌属Blautia 在内的几种微生物与睡眠质量呈负相关。
调节肠道菌群是改善睡眠的可行路径之一,好好睡觉也可以帮助我们维护肠道微生态健康,好眠养好菌,好菌助好眠。
肝病
非酒精性肝脂肪变性疾病中毛螺菌属的丰度相对对照较高,同样在非酒精性脂肪肝中也发现毛螺菌属的富集。
哮喘
哮喘是一种气道慢性疾病,尤其对于儿童。生命早期的特定细菌属与 1 岁儿童的特应性和喘息有关。越来越多的证据表明,其中一个原因可能是儿童在生命早期获得的健康微生物受到破坏。
加拿大健康婴儿纵向发育 (CHILD) 研究中发现,在生命的前 3 个月内,毛螺菌相对丰度的的下降与学龄前哮喘有关,并且 Lachnospira/Clostridium 比率可作为预测哮喘发展的潜在生命早期生物标志物。
《Science Translational Medicine》上刊登了加拿大温哥华的不列颠哥伦比亚大学(UBC)Brett Finlay 等科学家的文章,他们采集了300多个婴儿在3个月和1岁时的便便和尿液样本,结果显示,粪便样品中缺乏四种细菌(Lachnospira,Veillonella,Faecalibacterium,Rothia)的3个月的婴儿,后来在1岁时都显示出了早期哮喘的症状(喘息和皮肤过敏)。
而那些在1岁时没有这些症状的孩子,无一例外在其3个月的粪便样本中含有大量的这四种微生物。检测这些肠道微生物即可预测这些孩子日后患哮喘的风险,通过控制这些肠道细菌的组成还有可能找到预防儿童哮喘的方法。
抑郁症
研究发现,Lachnospira、Roseburia和Faecalibacterium与抑郁症状的严重程度呈负相关。
自闭症
南医大刘星吟团队揭示在属水平上,Lachnospira 和Megamonas 在对照组内的2-3岁和7-11岁亚组中丰度较高,而自闭症组不存在此趋势。
阿尔兹海默症
与健康对照组相比,阿尔茨海默病 (AD) 患者的肠道微生物组发生了改变。然而,以前的研究经常评估一直在服用药物或其他疾病干预措施的 AD 患者。此外,在一项研究中同时测定轻度认知障碍 (MCI) 或 AD 患者的肠道微生物组是罕见的。
与健康对照组相比,阿尔茨海默病患者的拟杆菌属、毛螺菌属和瘤胃梭菌减少,普氏菌属水平增加。而轻度认知障碍患者中这些属的变化方向与AD患者相同。然而,Lachnospira是唯一一个在轻度认知障碍患者中的丰度在统计学上显着低于健康对照组的属,表明该菌属的关键作用。
慢性肾病
研究表明,与健康人群相比,慢性肾脏病人群的肠道菌群组成不同,Lachnospira 和Ruminocococus gnavus 是很好的微生物标志物。
食管鳞状细胞癌
口腔健康以及口腔微生物不佳与食管鳞状细胞癌(ESCC)的发生有很大的关系。中国淮安市第一人民医院的 23 名食管癌患者身上采集的粪便样本中含有丰富的厚壁菌门和放线菌门。根据这项研究, Lachnospira可用作食管鳞状细胞癌潜在的生物标志物。
系统性红斑狼疮
肠道微生物组与系统性红斑狼疮 (SLE) 之间相关性被越来越多的研究关注。研究表明Lachnospira与SLE风险呈负相关。
慢性自发性荨麻疹
慢性自发性荨麻疹(CSU)是一种肥大细胞驱动的疾病,在过去几年中其病因和发病机制取得了许多进展。CSU的主要治疗方法是口服第二代抗组胺药。
然而,只有平均 50% 的 CSU 患者对常规或四倍剂量的非镇静抗组胺药有充分反应。同时,肠道菌群会影响药物的疗效。研究发现毛螺菌科及其下属分类群被发现是响应者和非响应者之间肠道微生物群的主要差异。而且Lachnospira是预测抗组胺药对 CSU 患者疗效的标志物。
格雷夫斯病(GD)
格雷夫斯病(GD)是一种以甲状腺功能亢进为特征的全身性自身免疫性疾病。有证据表明,肠道菌群的改变可能与自身免疫性疾病的发展有关。研究发现GD患者中Lachnospira 相较于对照减少。
肠癌
根据已有报道发现,两个丁酸盐生产者Lachnospira multipara和Eubacterium eligens在结直肠癌中含量降低,生成硫化物的细菌Desulfovibrio vietnamensis、D.longreachensis和Bilophila wadsworthia 增加。
大肠癌是由大肠息肉(腺瘤)和粘膜内癌一步步演变而来的(多阶段癌变)。研究表明,双歧杆菌属(Bifidobacterium)的细菌群会在粘膜内癌阶段减少。另外,作为丁酸产生菌的多毛毛螺菌(Lachnospira multipara)和挑剔真杆菌(Eubacterium eligens)从粘膜内癌阶段到晚期大肠癌阶段一直持续减少。
胃癌
胃癌患者肠道菌群的特点是物种丰富度增加,丁酸产生菌减少,以及其他共生细菌的富集,尤其是乳酸杆菌、埃希氏菌和克雷伯氏菌。据报道乳杆菌属和毛螺菌属是胃癌相关细菌属网络中的关键物种。毛螺菌属、乳杆菌属、链球菌属、韦荣氏菌属的组合在区分胃癌患者和健康对照方面表现出良好的表现。
2 型糖尿病 (T2D)
肠道微生物组可能在与 2 型糖尿病 (T2D) 发展相关的炎症中发挥作用。横断面研究发现 2 型糖尿病患者中毛螺菌属和消化链球菌科较少。
与对照大鼠相比,糖尿病大鼠肠道菌群中厚壁菌属的比例增加而拟杆菌属的丰度降低,菊粉治疗可使糖尿病大鼠的肠道菌群组成恢复正常。
与未治疗的糖尿病大鼠相比,接受菊粉治疗的糖尿病大鼠的益生菌乳杆菌及可产生短链脂肪酸的细菌(如毛螺菌属、考拉杆菌属及拟杆菌属)丰度会明显增加,可产生脂多糖的脱硫弧菌属丰度会降低。进一步分析发现,毛螺菌属的丰度与葡萄糖负荷后的血糖反应呈负相关。
白塞病
在白塞病 (BD) 中,一种自身炎症性血管炎,不平衡的肠道微生物群可导致促炎反应。与对照相比,Barnesiellaceae和Lachnospira属的显着减少与 BD 患者有关。

尽管毛螺菌属是一个重要的肠道菌属,但是目前关于该菌的研究和证据还不是很多,还仅限于关联性研究,在机制方面研究较少,以上文中主要的健康相关性证据支持还不充足,需要更大队列来探讨。
总的来说,该菌是一个对健康有益的菌,更深入地了解其与宿主相互作用的机制将有利于我们干预肠道菌群,最终目标是将其用于预防和治疗肠内外疾病。
主要参考文献:
Carasso S, Fishman B, Lask LS, Shochat T, Geva-Zatorsky N, Tauber E. Metagenomic analysis reveals the signature of gut microbiota associated with human chronotypes. FASEB J. 2021 Nov;35(11):e22011. doi: 10.1096/fj.202100857RR. PMID: 34695305.
Liu R, Peng C, Jing D, Xiao Y, Zhu W, Zhao S, Zhang J, Chen X, Li J. Lachnospira is a signature of antihistamine efficacy in chronic spontaneous urticaria. Exp Dermatol. 2022 Feb;31(2):242-247. doi: 10.1111/exd.14460. Epub 2021 Sep 30. PMID: 34558729.
Xiang K, Wang P, Xu Z, Hu YQ, He YS, Chen Y, Feng YT, Yin KJ, Huang JX, Wang J, Wu ZD, Yang XK, Wang DG, Ye DQ, Pan HF. Causal Effects of Gut Microbiome on Systemic Lupus Erythematosus: A Two-Sample Mendelian Randomization Study. Front Immunol. 2021 Sep 7;12:667097. doi: 10.3389/fimmu.2021.667097. PMID: 34557183; PMCID: PMC8453215.
Saladrigas-García M, D’Angelo M, Ko HL, Nolis P, Ramayo-Caldas Y, Folch JM, Llonch P, Solà-Oriol D, Pérez JF, Martín-Orúe SM. Understanding host-microbiota interactions in the commercial piglet around weaning. Sci Rep. 2021 Dec 6;11(1):23488. doi: 10.1038/s41598-021-02754-6. PMID: 34873196; PMCID: PMC8648723.
Maskarinec G, Raquinio P, Kristal BS, Setiawan VW, Wilkens LR, Franke AA, Lim U, Le Marchand L, Randolph TW, Lampe JW, Hullar MAJ. The gut microbiome and type 2 diabetes status in the Multiethnic Cohort. PLoS One. 2021 Jun 23;16(6):e0250855. doi: 10.1371/journal.pone.0250855. PMID: 34161346; PMCID: PMC8221508.
Prakash A, Peters BA, Cobbs E, Beggs D, Choi H, Li H, Hayes RB, Ahn J. Tobacco Smoking and the Fecal Microbiome in a Large, Multi-ethnic Cohort. Cancer Epidemiol Biomarkers Prev. 2021 Jul;30(7):1328-1335. doi: 10.1158/1055-9965.EPI-20-1417. Epub 2021 May 21. PMID: 34020999; PMCID: PMC8254769.
Ye X, Wang D, Zhu H, Wang D, Li J, Tang Y, Wu J. Gut Microbiota Changes in Patients With Major Depressive Disorder Treated With Vortioxetine. Front Psychiatry. 2021 May 7;12:641491. doi: 10.3389/fpsyt.2021.641491. PMID: 34025474; PMCID: PMC8138160.
Chen W, Bi Z, Zhu Q, Gao H, Fan Y, Zhang C, Liu X, Ye M. An analysis of the characteristics of the intestinal flora in patients with Parkinson’s disease complicated with constipation. Am J Transl Res. 2021 Dec 15;13(12):13710-13722. PMID: 35035709; PMCID: PMC8748098.


大多数外行人没有听到过一个词——过敏级联反应,要深度了解过敏,非常有必要知道和了解过敏级联反应,在了解这个概念之前,我们先了解回顾下免疫系统的工作原理。
免疫系统是非常具体和目标导向的。虽然你可能对多种物质过敏,但过敏反应是针对特定过敏原的。例如,你可能对花生过敏,但一般对海鲜不过敏。
然而有时,两种或多种外来物质可能对于免疫系统而言,在性质上看起来相似,这可能会使免疫系统误认为另一种并对两者都产生反应。

例如,本来你是对桃树花粉过敏,但你的免疫系统也可能会对苹果或其他水果产生反应,免疫系统会误认为它们是桃树花粉。好比一个多层次的瀑布,水从一个壁到另一个壁越来越强。
这些交叉反应的发生是由于多种植物产生的类似过敏原。不幸的是,这会导致细胞和化学相互作用的有害序列,有时针对无害的物质。最终结果是由“过敏级联”产生的一系列明确的体征和症状。
身体的免疫系统旨在不断寻找入侵者。它能区分“我”和“非我”(它保护我们免受外来物质的侵害)。
来看看这个复杂的过程:
有些人接触到花粉过敏。一旦花粉进入体内,就会被免疫系统的侦察兵[称为抗原呈递细胞(APC)]吞噬。这些 APC 将花粉切成小碎片,然后与细胞中的特殊蛋白质结合,称为人类白细胞抗原 (HLA)。
HLA 的功能就像一个指南,帮助身体区分“自我”和“非我”。当与 HLA 结合时,这些碎片对于过敏级联反应中的关键参与者淋巴细胞变得可见,淋巴细胞将它们识别为外来物。这种花粉片段-HLA 组合暴露在 APC 的表面,这些特化的白细胞完全可见。
基本概念:免疫反应重要细胞类型和信使蛋白
术语白细胞源自希腊语单词“leukos”,意思是白色,“cytes”意思是细胞。白细胞对免疫系统至关重要,包括:单核细胞、巨噬细胞、中性粒细胞和淋巴细胞。
淋巴细胞是白细胞,在免疫和过敏中都起着关键作用。它们分为两种类型:T淋巴细胞和B淋巴细胞。每种类型负责免疫系统的特定分支。
T 淋巴细胞的职责是准备好直接转变为攻击外来物质的行动(细胞介导的免疫)。一些 T 淋巴细胞是“杀伤”(细胞毒性或杀伤性 T 细胞)专家。
而另一些则有助于免疫反应,被称为“辅助”细胞(TH 细胞)。根据它们释放的蛋白质,TH 细胞进一步分为 TH1(抗感染)和 TH2(过敏促进剂)。

T 淋巴细胞的伙伴是 B 淋巴细胞。B 淋巴细胞是微小的抗体工厂,当受到 TH 细胞的刺激时,它们会产生抗体以帮助破坏外来物质。
嗜碱性粒细胞和嗜酸性粒细胞是其他在过敏反应中起重要作用的白细胞。
T 细胞通常会在过敏条件下调用这些细胞。患有哮喘和其他过敏性疾病的人的血液嗜酸性粒细胞水平通常会升高。
细胞因子是一组多样化的蛋白质,由淋巴细胞和巨噬细胞在损伤或激活(例如过敏原)时释放。它们充当“加强”或“降低”免疫反应的化学信号。
淋巴细胞 — T & B
淋巴细胞 — T & B:淋巴细胞是白细胞家族的一部分,由 T 和 B 两种类型组成。每个 T 淋巴细胞或 T 细胞就像一个受过专门训练的侦探。T 细胞检查 APC 暴露的证据。
当特定 T 细胞与 APC 上的、花粉片段接触并将其识别为外来物时,就会触发“辅助”细胞(实际上是 TH2 细胞)的特化 T 细胞大军,从而释放刺激 B 淋巴细胞的化学物质(细胞因子)。
B 淋巴细胞产生与过敏原(如花粉片段)结合的 IgE 抗体。一旦 IgE 产生,它就会特异性识别花粉,并在未来暴露时识别它。
已发现促进过敏的 TH2 细胞和抗感染的 TH1 细胞之间的平衡是我们免疫系统的关键组成部分。过敏反应涉及大量 TH2 细胞,而感染会产生大量 TH1 细胞,然后释放出有助于消灭微生物的化学物质。
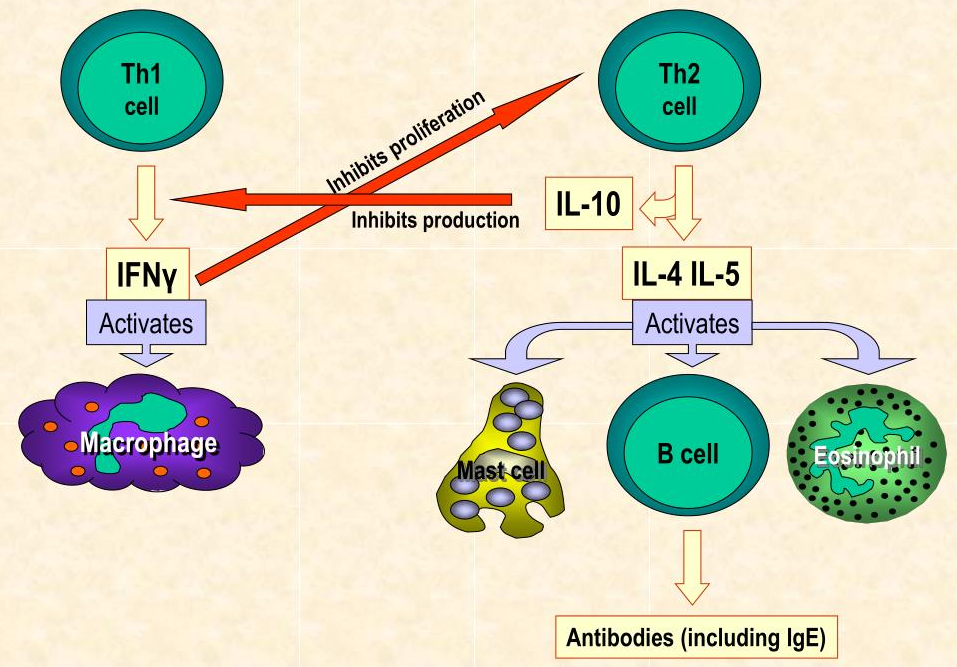
近几十年来,过敏和哮喘发病率一直在上升。一种“卫生假说”的理论解释了这种增加是由于现代人相对无菌的环境(可能是由于抗生素和疫苗接种)导致的人类免疫系统“装备不足”的结果。
这个概念意味着暴露于足够微生物的个体的免疫系统在受到刺激时会产生 TH1 细胞。但是,如果一个人的免疫系统因接触微生物而没有得到充分刺激以产生 TH1 细胞,它反而会倾向于产生过敏反应的系统并产生 TH2 细胞,结果就是过敏反应的倾向。
虽然这看起来很复杂,但了解不同的淋巴细胞反应对于治疗过敏很重要。理想情况下,我们希望用 TH1 淋巴细胞而不是 TH2 淋巴细胞对花粉作出反应,后者会促进过敏反应并大量产生 IgE。过敏者会召唤大量 TH2 细胞来响应过敏原,而非过敏者则不会。
最后,发生过敏性疾病的倾向(例如,对过敏原产生强烈的TH2反应)被认为部分遗传自父母。出生时,抗感染的 TH1 细胞和促进过敏的 TH2 细胞之间似乎存在平衡。
目前的看法是,当孩子暴露于环境中的某些物质时,过敏会在出生后发展。免疫系统受到这些暴露的刺激,因此倾向于产生促进过敏的 TH2 细胞。他们特别倾向于在继承父母遗传倾向的个体中促进过敏。
肥大细胞和嗜碱性粒细胞
如果你患有任何形式的肥大细胞增多症,重要的是要了解过敏级联反应链中每个环节的工作原理,以及肥大细胞以外的那些细胞与过敏反应以及每一步在身体中的发生。
肥大细胞和嗜碱性粒细胞是过敏级联反应中的下一个关键参与者。它们是具有潜在爆炸行为的“挥发性电池”。肥大细胞存在于组织中,而嗜碱性粒细胞存在于血液中。这些细胞中的每一个都有超过 100,000 个 IgE 受体位点,可以使 IgE 结合在这些细胞表面。
IgE 与这些细胞的结合就像炸弹上的保险丝。细胞现在用 IgE 致敏或引发。当这个过敏或致敏的个体再次接触花粉时,IgE 已准备好与这种花粉结合。当这种情况发生时,肥大细胞和嗜碱性粒细胞被激活并释放出许多化学物质,最终产生我们可以看到和感觉到的过敏反应。
这些化学物质在体内释放的任何地方都会显示过敏症状。以花粉为例,当鼻中的肥大细胞因接触花粉而被激活时,释放出的化学物质可能会导致打喷嚏、鼻塞和流鼻涕——这是花粉热的典型症状。一旦致敏,肥大细胞和嗜碱性粒细胞可以在数月甚至数年内保持准备好用 IgE 点燃。
化学介质
每个肥大细胞和嗜碱性粒细胞可能含有 1000 多个小包(颗粒)。这些颗粒中的每一个都含有 30 多种过敏化学物质,称为化学介质。许多这些化学介质已经准备好并在颗粒发生过敏反应时从颗粒中释放出来。这些化学介质中最重要的是组胺。一旦释放到组织或血流中,组胺就会附着在大多数细胞表面存在的组胺受体(H1 受体)上。
这种附着会对血管、粘液腺和支气管产生某些影响。这些影响会导致典型的过敏症状,例如鼻子、喉咙和上颚肿胀、打喷嚏和瘙痒。
一些化学介质直到肥大细胞或嗜碱性粒细胞活化 5 到 30 分钟后才会形成。其中最突出的是白三烯。白三烯 D4 的效力是组胺的 10 倍。其作用与组胺相似,但白三烯D4还会吸引其他细胞到该区域,从而加重炎症。
白三烯最初于 1938 年被发现,被称为“过敏反应的慢反应物质(SRS-A)”。四十年后,瑞典的 Samuelsen 发现它们在过敏性炎症中起着重要作用。
最近,发现一种白三烯调节剂的新药物家族有助于治疗哮喘。例如孟鲁司特( Singulair ) 和扎鲁司特( Accolate )。
在肥大细胞刺激后形成的另一组引起炎症的化学介质是前列腺素。特别是前列腺素 D2,是过敏性哮喘患者肺气道(支气管)炎症的一个重要因素。
回到过敏级联的概念,当医生使用这个术语时,他们指的是对过敏原的渐进致敏和反应。
有3个阶段:
致敏或诱导——早期阶段——后期
在这三个阶段中,每个阶段都有不同的身体细胞和激素或化学物质在起作用。例如,如上所述,最初 IgE 会引发过敏反应。后来,嗜酸性粒细胞发挥更大的作用。在这些阶段,化学介质也会与这些免疫系统细胞相互作用。
★ 致敏
我们每天都会接触到环境中的数百种物质。但是对于某些人来说,第一次接触其中的一些东西,例如花粉,会导致免疫系统反应过度并从此对这种物质变得“敏感”。
当这种情况发生时,免疫细胞之间会发生级联反应,例如:
T 辅助细胞因子刺激B细胞
B 细胞变成浆细胞,开始制造 IgE 抗体
IgE 抗体与肥大细胞结合
在大多数情况下,这一切都在悄无声息地发生。
这意味着虽然过敏过程已在体内触发,但你第一次可能不会有任何明显的症状。可能有些人仅与过敏原接触一次就发生完全致敏;但某些人,可能需要接触几次才能完全致敏。
★ 早期阶段
一旦完全敏感,到再次接触该过敏原时,身体就会知道这是一种(假定的)威胁,并准备好应对它。
从本质上讲,免疫系统的反应方式与它对抗引起感染的细菌和病毒等细菌的方式类似。
想想那些在致敏阶段形成的 IgE 抗体和肥大细胞的组合,就像士兵一样。它们会释放调解器,在全身上下移动并击退入侵者(如花粉)。最常见的介质之一是组胺。
早期阶段反应可以在暴露后几分钟内开始于变应原,然后可以持续3-4小时。
★ 后期
在花粉引起强烈过敏和哮喘发作后,症状在几个小时后开始消退。但随后又变得更糟了。级联的后期阶段是发生这种情况的原因。
晚期阶段的免疫系统反应与早期阶段同时开始。然而,它引起的变化实际上并不会立即引起症状。在这个阶段,早期动员的“士兵”招募帮手。
炎症细胞包括:
嗜酸性粒细胞、中性粒细胞、嗜碱性粒细胞、单核细胞、淋巴细胞
这些细胞导致气道进一步和持续的炎症。因此,该阶段的症状会在接触过敏原 4 小时后开始出现,然后会持续 6-12 小时。
总结下过敏级联过程:
1. 首次接触过敏原
2. 抗原呈递细胞向 T 细胞提供过敏原
3. T 细胞激活 B 细胞
4. B 细胞释放“Y”形 IgE 过敏原抗体(IgE – 免疫球蛋白 E)
5. IgE 抗体附着于肥大细胞和嗜碱性粒细胞表面的 FC 受体,等待下一次接触
6. 第二次接触过敏原(有时几年后)
7. 过敏原附着在从肥大细胞 / 嗜碱性粒细胞表面伸出的 IgE
8. 免疫反应细胞脱颗粒,释放介质或化学物质
9. 介质/化学品引起全身效应,例如血管舒张、粘液分泌、神经刺激和平滑肌收缩
10. 全身效应导致个体化过敏反应(从鼻子痒、哮喘、湿疹到过敏反应)
虽然一些过敏反应是轻微的,可能仅限于身体的某些部位,但有些过敏反应是严重的,会影响整个身体的健康。
// 黑眼圈
黑眼圈除了是熬夜,另外一个可能是过敏的一个迹象。当你总是揉眼睛发痒时,可能是过敏。服用抗组胺药可以缓解眼睛发痒、流泪、打喷嚏和流鼻涕等症状。

// 堵塞
感冒或流感,鼻塞应该在一两周内消失。如果充血一直持续下去,则更可能归咎于过敏。在过敏反应期间,鼻腔内壁会膨胀并产生额外的粘液,感到鼻窦压力和头痛。鼻用类固醇用于减少由过敏引起的鼻腔粘膜炎症。用药请咨询过敏症专科医生。
// 喘息
喘息通常与哮喘有关,但也可能与季节性过敏或严重的过敏反应有关。当你必须通过狭窄的气道呼吸时,就会发出口哨声。在严重的情况下,可能需要紧急护理。
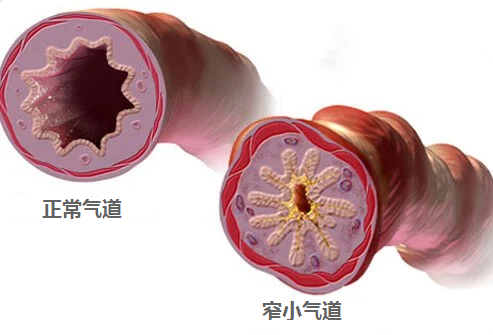
图源:medicinenet
// 呕吐腹泻
进食某种食物后造成呕吐,腹泻及腹痛等不良反应。轻度食物过敏会慢慢好转,严重的食物过敏能引起喉咙水肿而造成窒息。食物过敏最常涉及的是消化系统,症状呈非特异,容易漏诊。
// 发痒
不停瘙痒或变成皮疹,则可能患有湿疹。这种皮肤反应在过敏人群中很常见。触发因素包括肥皂或洗涤剂、织物柔软剂中的化学物质、宠物皮屑和粗糙的织物。可以使用抗组胺药、保湿剂和氢化可的松乳膏治疗。
// 荨麻疹
伤口苍白、发痒、发红,可持续数小时到数天不等。它们是对食物、药物或昆虫叮咬等事物的过敏反应。抗组胺药通常可以立即缓解,也可能需要类固醇。最好的防御是找到过敏源避免触发。
// 失眠
皮肤和眼睛发痒、头痛不舒服、鼻窦疼痛和其他过敏症状会让人难以入睡。咳嗽或喘息也可能导致难以入睡。
希望每个人都远离过敏。请注意,本文信息仅供学习参考交流,不参与提供医疗建议。

谷禾健康
疾病表现、进展和治疗反应的可变性一直是医学的核心挑战。尽管宿主因素和遗传学的变异性很重要,但很明显,在迈向个性化治疗的过程中,必须考虑肠道微生物组具有巨大的遗传和代谢多样性。
疾病表现、治疗反应和治疗不良反应的个体差异是有效管理疾病和患者安全的主要挑战。这种认知是精准医学的基础,其最简单的形式可以这么说,用个性化方法为合适的患者确定合适的治疗方法,无需反复试验。
将肠道微生物组与人类遗传学区分开来的一个方面是它代表了我们健康的动态组成部分,通过复杂的网络不断与宿主和环境因素相互作用。虽然存在潜在挑战,肠道微生物组的可塑性也提供了一个独特的机会,使其成为精准医学的一个有吸引力的目标。
本文支持使用肠道微生物组作为精准医学工具的当前证据,并建议未来需要将微生物组作为个体化治疗或干预工具的工作。
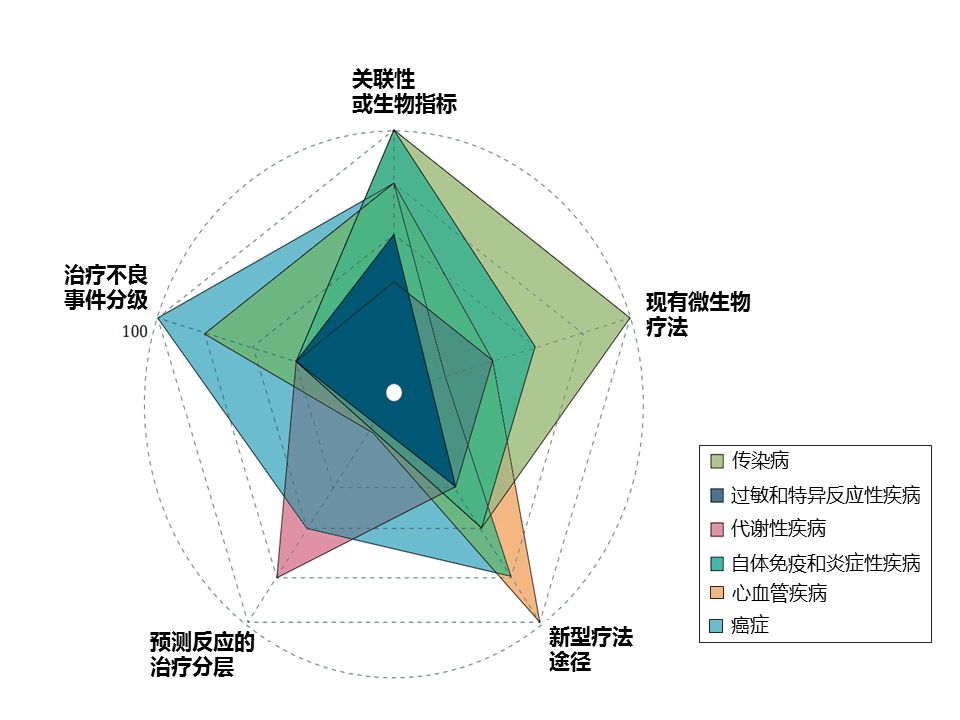
该研究团队选择了六个广泛的疾病组,这些组具有相对较强的证据表明肠道微生物组的作用。 尽管每个疾病组都有不错的发展,但在考虑临床影响时,不同疾病组的前景和成熟度各不相同(下图)。
抗生素诱导的肠道微生物组破坏会促进机会性和医院感染的机制。最常见的院内腹泻感染艰难梭菌为例,强调可能解释临床结果的个体差异的微生物组和病原体特异性特征。
复发性艰难梭菌感染 (CDI) 一直是微生物组研究的中心焦点。CDI 出现最常见的原因是使用抗生素,但矛盾的是,CDI 的一线治疗也包括抗生素。
抗生素对一般人相当有效,但为什么部分患者出现治疗失败,或是成功治疗后复发?
这可能与宿主特征(例如高龄)或药物的使用(例如质子泵抑制剂)有关, 以及肠道微生物组中特定病原体的特征有关。
除了宿主因素外,肠道微生物群的破坏也是 CDI 的关键因素。
· 与健康对照个体相比,CDI患者的肠球菌、韦永氏菌、乳杆菌、γ-变形菌属的相对丰度较高,而拟杆菌属、毛螺菌科、瘤胃球菌科的含量较低。
谷禾健康

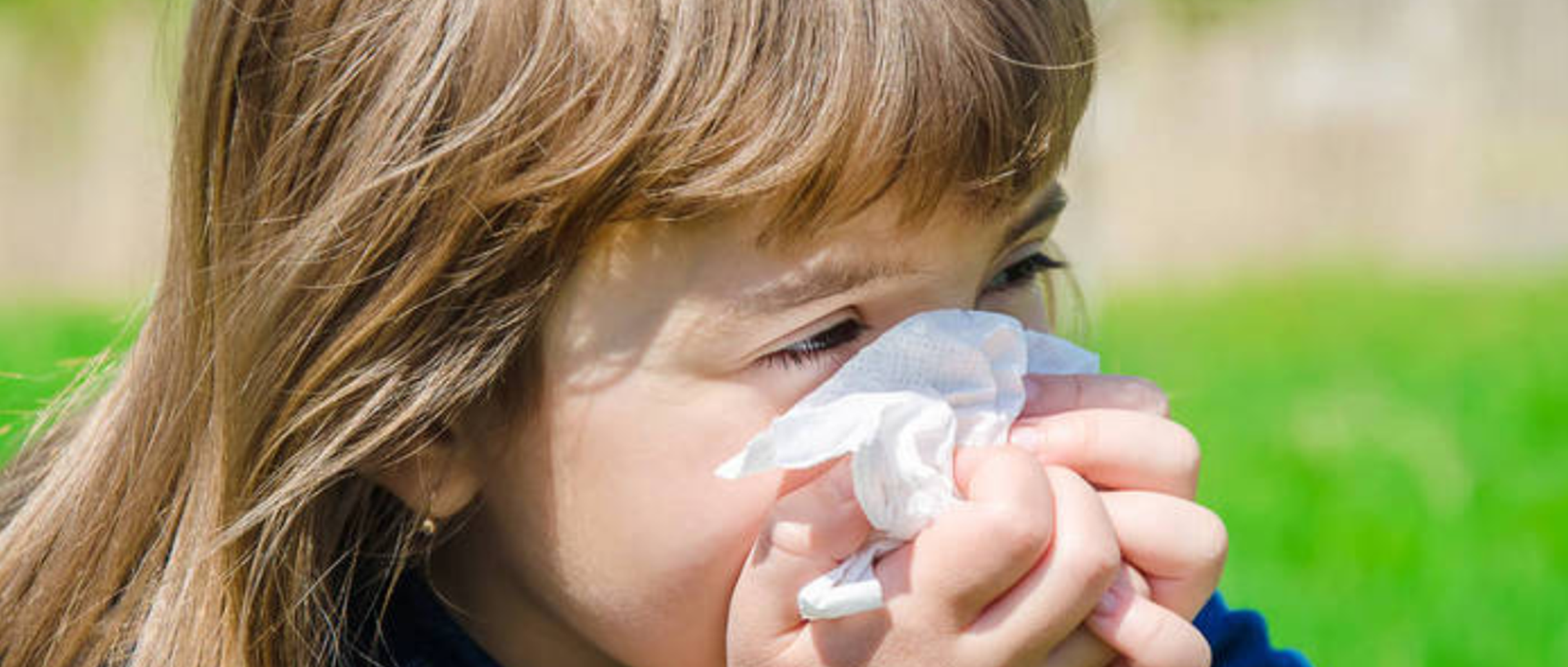
现如今,有过敏症状的宝宝越来越多,如何防治孩子过敏成了颇受关注的公共健康问题之一。
过敏的原因除了遗传因素外,还与宝宝肠道菌群失调,自身的免疫系统发育不成熟,环境因素等息息相关。
本文列举的最新研究进展,从过敏早期识别干预,耐药基因,食物过敏及其因果关联等方面,展示了微生物群如何在其中发挥作用,为儿童过敏的防治提供新思路。
新生儿的第一次大便可能揭示发生过敏的风险
微生物群的成熟与免疫系统的发育同时发生,两者都与一系列疾病有关,包括过敏、花粉热、哮喘和湿疹。
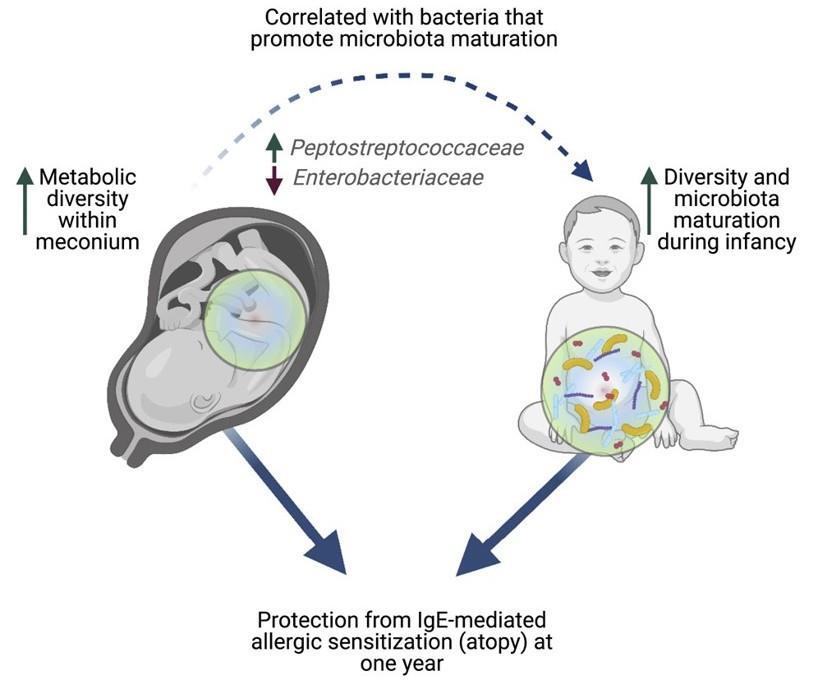
发表在Cell Reports Medicine 通过分析 100 名新生儿的粪便,研究人员发现婴儿第一次粪便的成分可以决定儿童在以后的生活中是否有可能患上过敏症和其他疾病。研究小组发现,缺乏特定分子与一年后过敏的风险增加有关。这些化学物质的减少与在微生物群成熟中起关键作用的细菌的变化有关。
Petersen Cet al., Cell Rep Med. 2021
新生儿的第一次粪便,称为胎粪。胎粪是一种粘稠的深绿色物质,在怀孕 16 周左右开始在胎儿肠道中形成,含有羊水、皮肤细胞以及婴儿摄入的其他物质和分子。
胎粪也是出生后在肠道中定殖的第一批微生物的最初“食物来源”。胎粪就像一个时间胶囊,揭示了婴儿在出生前接触过的东西。
过 敏
为了评估胎粪成分是否会影响以后发生过敏的风险,研究人员研究了新生儿第一次粪便中存在的代谢物。然后,当孩子们满一岁时,该团队进行了一项皮肤测试,以测量免疫系统的反应性。
分析表明,婴儿胎粪中不同类型的分子越少,孩子在出生后第一年内发生过敏的风险就越高。
一些代谢途径,包括那些涉及氨基酸代谢的途径,在后来出现过敏性疾病的婴儿的胎粪中最少。
与没有发生过敏反应的新生儿相比,在一岁时发生过敏反应的新生儿在出生时的胎粪代谢多样性降低。
早 期 干 预
接下来,研究人员分析了胎粪成分是否会影响肠道微生物群的成熟。胎粪“代谢组”较少的婴儿的细菌丰度平较水平低,如肠杆菌科,这在微生物群的成熟中起着关键作用。
最后,研究人员将有关胎粪和微生物群组成的信息与新生儿及其母亲的临床数据相结合,以准确预测婴儿是否会在 1 岁时出现过敏反应。
这项工作表明,健康的免疫系统和微生物群的发展实际上可能在孩子出生之前就开始了——这表明婴儿在子宫内接触的微小分子对未来的健康起着至关重要的作用。
研究人员说,调节子宫内关键代谢物的早期干预措施有助于促进微生物群和免疫系统的健康发育,从而预防过敏性疾病的症状。
这些发现可能有助于识别有患过敏症或哮喘风险的婴儿,并制定有助于预防这些疾病的早期干预措施。
参考文献:
Petersen C, Dai DLY, Boutin RCT, Sbihi H, Sears MR, Moraes TJ, Becker AB, Azad MB, Mandhane PJ, Subbarao P, Turvey SE, Finlay BB. A rich meconium metabolome in human infants is associated with early-life gut microbiota composition and reduced allergic sensitization. Cell Rep Med. 2021 Apr 29;2(5):100260.
婴儿的肠道微生物群包含数百个抗生素抗性基因
人类肠道微生物群已成为细菌的储存库,这些细菌含有帮助它们抵抗抗生素的基因。
发表在Cell Host & Microbe的一项研究通过分析丹麦 650 多名一岁儿童的粪便样本,发现婴儿的肠道细菌有数百个抗生素抗性基因。