-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康


You are what you eat
国庆放假除了玩玩玩,当然少不了吃吃吃,把各种一直想吃的都提上日程,应该是对假期最起码的尊重了…
有时候我们喜欢吃的并不是食材本身,而是喜欢融入食材中的“味道”,不知从什么时候开始,我们对“重口味食物”越来越上瘾,而“重口味食物”往往意味着过甜、过咸、过辣……
我们知道饮食可以影响肠道菌群,在之前的文章里也多次提到,诸如食物种类,饮食方式,饮食习惯等对肠道菌群的影响。
之前写过关于饮食对肠道菌群的文章:
间歇性禁食 & 肠道菌群 & 心血管疾病
利用饮食精准干预肠道微生物群
饮食-肠道菌群对心血管疾病的相互作用
正视暴饮暴食、厌食症等饮食失调问题
深度解析 | 炎症,肠道菌群以及抗炎饮食
饮食习惯或将引领新的健康革命
深度解读 | 饮食、肠道菌群与健康
本文试着从不同饮食口味的角度「包括甜、咸、辣」,来了解一下糖、盐、辣椒等对肠道菌群的影响,对健康的潜在影响机制,以及相关食用小妙招。
如果说厨房里只能有一款调料,那一定是盐。盐,号称”百味之王”,同时也是一把”双刃剑”。身体缺不了它,食用不当也会给身体带来很多伤害,例如体重增加,高血压,慢性肾病等。

氯化钠,“盐”,是日常食物的重要组成部分,对身体的体内平衡起着至关重要的作用。
盐参与调节人体内水分的均衡分布,增强神经肌肉兴奋性,为使机体内酸碱平衡和血压正常功能,保证体液的正常循环,参与胃酸的形成,促使消化液的分泌,能增进食欲。
一般成人每天摄入3克食盐就可以维持基本生理需求。2022年颁布的《中国居民膳食指南》中也将食盐摄入量再次严格限制,每人每日食盐摄入量从原先的6克以内改为不高于5克。
过多的盐摄入量,可能给健康带来危害。
饮食中高盐含量会导致肠道免疫系统的变化。血液中含有过多的钠会导致体内免疫细胞产生较少的能量,还会影响机体正常代谢和细胞的渗透压等,引发心脑血管疾病和代谢性疾病,业已知道盐摄入过量是心脑血管疾病的主要风险因素之一。
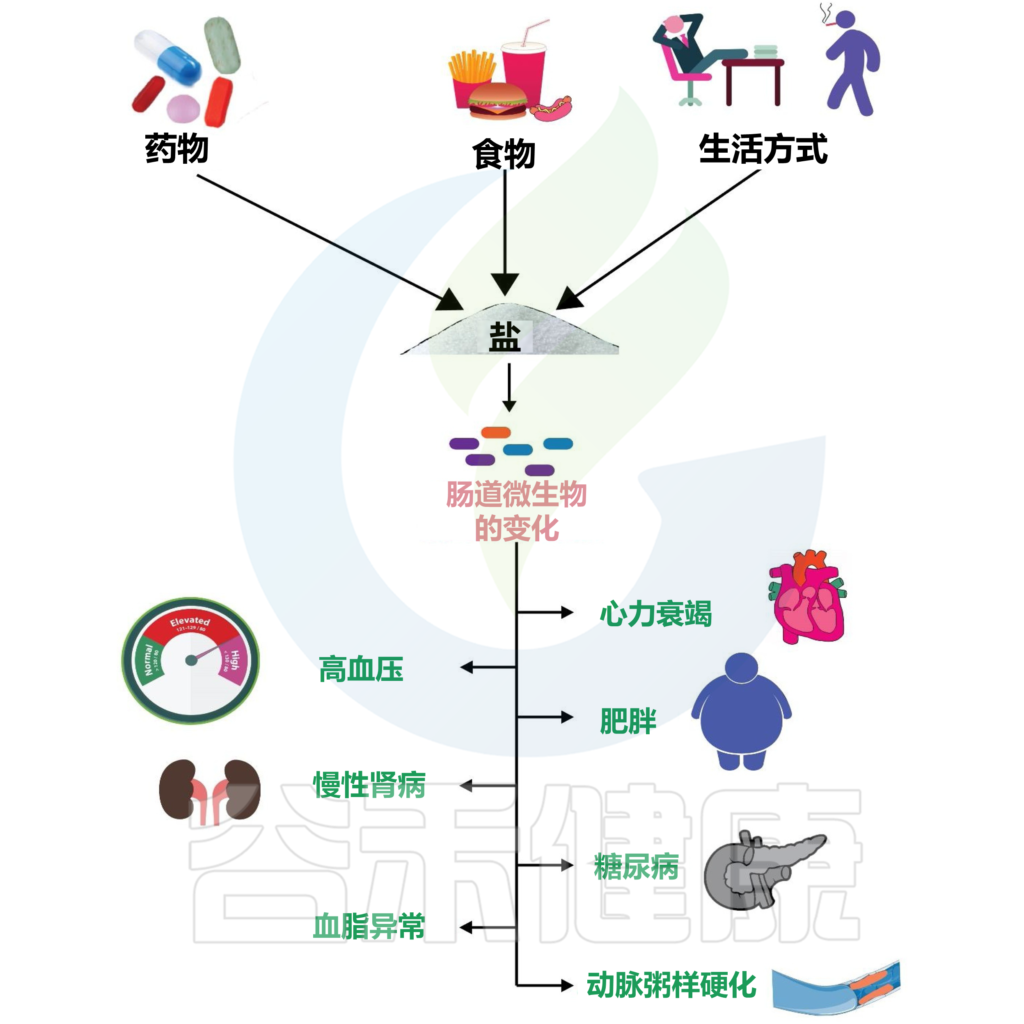
doi.org/10.1016/j.biopha.2020.111156
◣ 高盐饮食和体重增加相关
或许会有这样的疑惑,盐含的热量极少,为什么会与体重增加有关?
这个问题不在于热量,确实盐一点热量都没有。然而摄入大量的盐会导致体重暂时增加,是因为它会导致身体保留水分。
盐摄入过多会增加口渴感。身体消耗的额外液体被用来稀释身体无法足够快速排出的多余钠。
小鼠研究表明,高盐饮食也可能使身体对瘦素产生抵抗力。
注:瘦素是一种激素,负责防止饥饿,让你感到充实和满足。
高盐饮食也可能间接导致体重增加,因为它们通常与大量的超加工食品有关。高度加工的食物导致摄入更多的热量并增加体重。
当热量相等时,高盐饮食不会比低盐饮食增加或减少更多的体脂。
含盐量较高的食物:零食、薯条、西式快餐、披萨、油炸食品、加工食品、调味品,甚至面包,也含有较高的热量。
因此,如果你的饮食中含有大量这些经过高度加工的食物,那么胃很可能会感觉不到满足感和饱腹感,最终导致摄入更多的热量并增加体重。
◣ 高盐饮食和夜尿症相关
如果你有夜尿症,钠摄入量可能是罪魁祸首。
在一项研究中,当那些夜间排尿频繁且饮食中摄入高钠的人减少了钠的摄入量时,他们报告说夜间上厕所的次数减少了,而良好的睡眠习惯提高了生活质量。
在用餐期间和白天大量喝水可以帮助排出体内的钠,导致夜间小便减少。
◣ 高盐饮食和心血管疾病的关系
说到高盐饮食,就会联想到高血压。
有些人可以吃含钠量很高的食物,但血压水平不会有任何有意义的变化。其他人吃同样的饮食可能会导致高血压,这是为什么呢?
可能与“盐敏感性”有关。“盐敏感性”的人,如果从低钠饮食转向高钠饮食,血压会增加。盐敏感性的潜在原因很多,从遗传到环境。
研究表明,对盐敏感的人比中度敏感的人患高血压的可能性至少高40%.
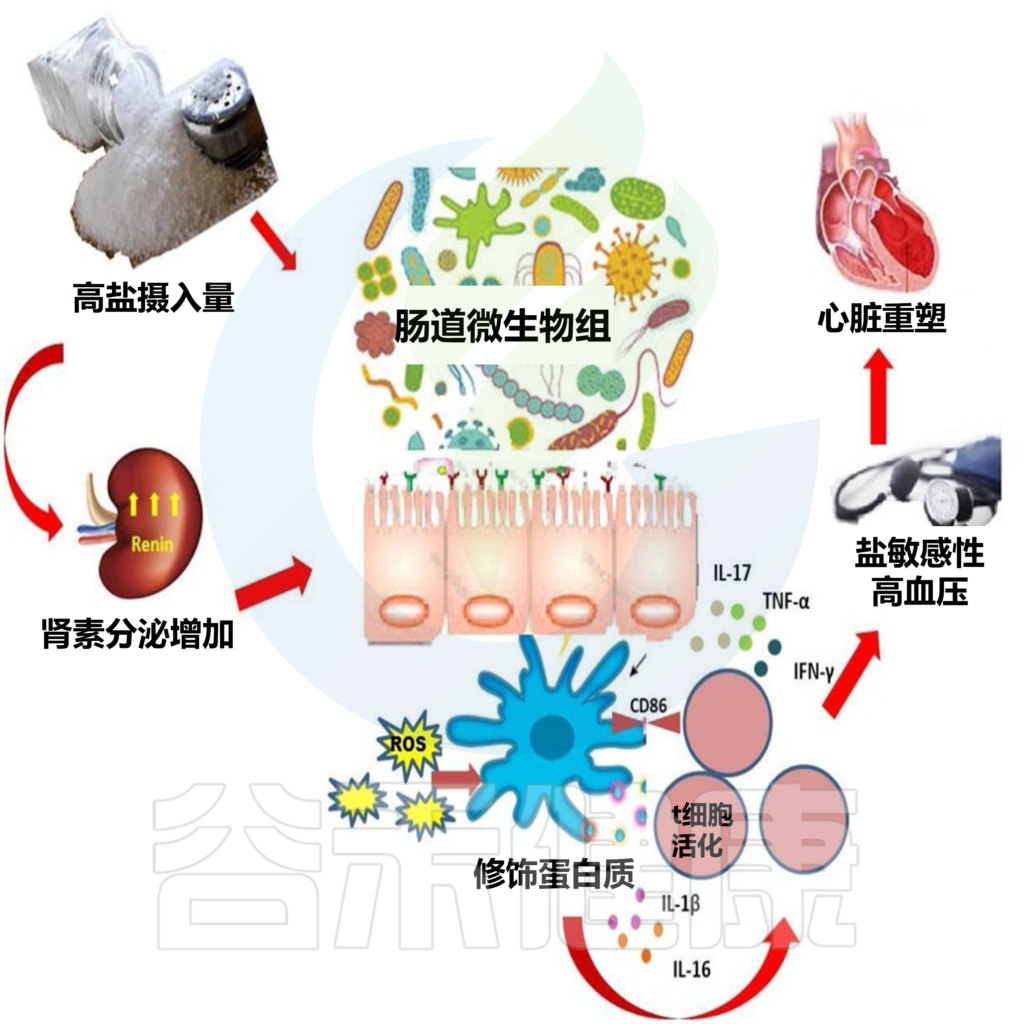
doi.org/10.1016/j.biopha.2020.111156
临床研究发现,较高的钠摄入量与心血管疾病和相关死亡有关。以下是重点研究:
研究人员测量了来自 32 个国家/地区的 10,000 多名成年人在 24 小时内排泄的钠量(这是盐摄入量的良好替代品)。平均每天接近 4,000 毫克钠。然而,范围很大,从巴西亚诺马莫人的每天 200 毫克到日本北部的 10,300 毫克。盐摄入量较高的人群平均血压较高,并且随着年龄的增长血压升高幅度较大。
两项预防高血压试验 (TOHP) 于 1987 年至 1995 年进行。他们测试了生活方式改变对血压的影响,例如减肥、压力管理、营养补充剂和摄入更少的钠。在每项研究中,在 18-36 个月内减少钠摄入后,血压略有下降。试验结束多年后,研究人员对参与者进行了调查,发现:
平均 10-15 年后,减钠组的 TOHP 参与者心脏病发作或中风的可能性降低 25%。需要手术打开或绕过胆固醇阻塞的冠状动脉,或死于心血管疾病的可能性降低。
参与者饮食中钾与钠的比例越高,患心血管疾病的机会就越低。这表明包括增加钾和降低钠的策略可能是对抗高血压的最有效方法。
◣ 高盐饮食与慢性肾病进展有关
对诊断为慢性肾病的患者进行的一项系统评价发现,每天摄入超过 4600 毫克的高钠盐与慢性肾病的进展有关。
与每天 2300 毫克的适度钠摄入量相比,每天摄入少于 2300 毫克的低钠盐没有显着影响。
一般来说,指南通常建议适度而不是低钠限制以防止慢性肾病的发展。
对于慢性肾病的整体管理,建议每日钠摄入量少于 4000 mg,对于伴有体液潴留或蛋白尿症状的慢性肾病,建议每日钠摄入量少于 3000 mg.
◣ 高盐饮食与骨质疏松症有关
身体通过排尿流失的钙量随着你摄入的盐量而增加。如果血液中钙供应不足,它会从骨骼中流失。因此,高钠饮食可能会产生额外的不良影响,即骨质疏松症。
一项对绝经后妇女的研究表明,两年内髋骨密度的下降与研究开始时24小时尿钠排泄有关,而且与骨质流失的联系与钙摄入量的联系一样强烈。
其他研究表明,减少盐的摄入量会导致钙的正平衡,这表明减少盐的摄入可以减缓随着年龄增长而发生的骨骼中钙的流失。
◣ 高盐饮食可能和胃癌相关
世界癌症研究基金会和美国癌症研究所的结论是,盐和咸的食物都是“胃癌的可能病因”。
高盐饮食通过肠道菌群影响健康
我们吃的东西和其中的盐,在某个阶段到达我们的肠道,是否会影响肠道微生物?
肠道菌群最有可能参与体内盐分的吸收,钠通过钠质子交换剂 3 (NHE3) 在结肠中被高度吸收。在小鼠 NHE-3 缺失时观察到肠道微生物环境的改变和血压的降低。
高盐消耗会影响蛋白质的消化并改变肠道菌群的多样性,菌群变化例如:棒状杆菌科的增加,乳酸杆菌的减少,详见下表:
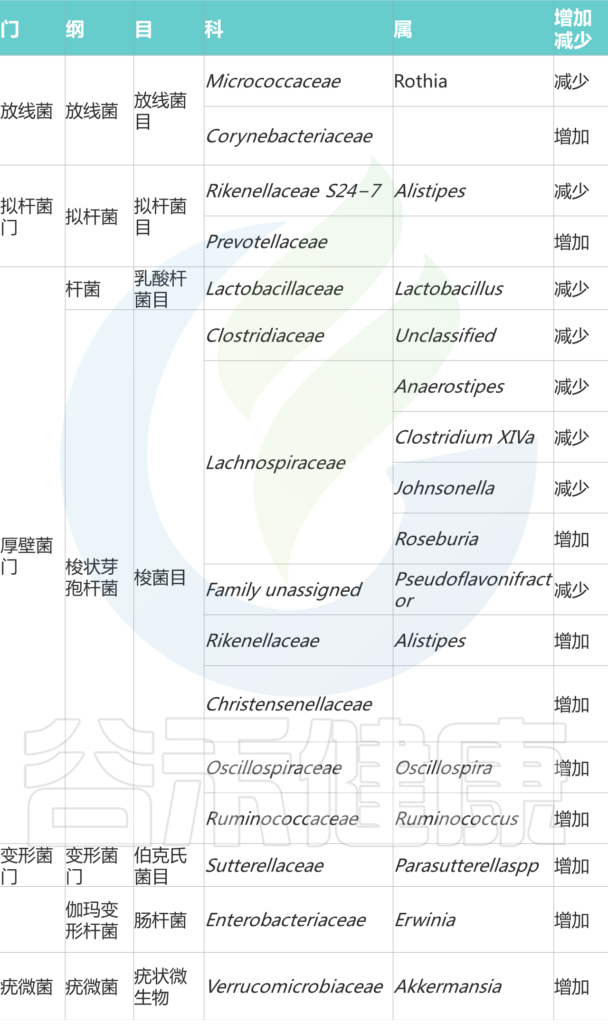
doi.org/10.1016/j.biopha.2020.111156
在大鼠模型中,食盐摄入降低了鼠乳杆菌的丰度,并增加了促炎性脾Th17细胞数量。
反过来想,作为一种益生菌疗法,每天服用鼠乳杆菌可显著减少治疗大鼠的Th17细胞并改善血压。
另一项研究发现,8周的高盐摄入显著改变了小鼠的肠道微生物组成。结果显示,拟杆菌和变形杆菌分别显著减少50.53%和2.96%,厚壁菌显著增加42.77%。
同时,在高盐饮食喂养的小鼠中,发现下肠中的短链脂肪酸水平显著降低,这归因于细菌发酵受到抑制。
饮食中钠的适度减少可以增加循环中的短链脂肪酸,从而增加肠道微生物群。短链脂肪酸水平的增加反过来降低血压并改善动脉顺应性。
以上是高盐饮食带来的危害,然而最近的研究表明高盐饮食也有可能带来某些益处。
▸ 高盐饮食:介导NK细胞和肠道微生物群之间的相互作用,诱导有效的肿瘤免疫
发表在《Science Advances》的一项研究报道了高盐饮食通过抑制PD-1表达,同时增强IFNγ和血清马尿酸水平,诱导自然杀伤(NK)细胞介导的肿瘤免疫。盐与次优剂量的抗PD1抗体联合使用可增强肿瘤免疫。
虽然高盐饮食诱导的肿瘤免疫随着肠道微生物群的减少而减弱,但高盐饮食小鼠的粪便微生物群移植恢复了与NK细胞功能相关的肿瘤免疫。
高盐饮食增加了双歧杆菌的数量,并导致肠道通透性增加,导致双歧杆菌在肿瘤内定位,从而增强NK细胞功能和肿瘤消退。瘤内注射双歧杆菌激活NK细胞,抑制肿瘤生长。
这些结果表明,高盐饮食通过潜在的平移作用调节肠道微生物组,诱导NK细胞依赖性肿瘤免疫。
▸ 高盐饮食:抵消高米饭饮食带来的肥胖影响
一项研究发现,高盐摄入可改善与大米饮食相关的代谢变化,包括粪便微生物群组成的变化。
研究将小鼠分为三组(n = 9),分别喂食正常饮食(ND)、高米饭饮食(HRD)、补充高盐(HRS)的高米饭饮食12周。
与正常饮食的小鼠相比,喂食高米饭饮食的小鼠厚壁菌门与拟杆菌门的比率(p < 0.01)和变形菌门与拟杆菌门的比率(p <0.001)显着增加。然而,高盐摄入减弱了这些影响,尽管变形杆菌的比例没有减少。
高盐摄入降低了高米饭饮食引起的体质量和白色脂肪组织重量的增加。另外,高盐饮食并没有逆转葡萄糖耐量和胰岛素抵抗的增加。
高盐饮食改变了高米饭诱导的微生物组成,高盐饮食调节高米饭饮食诱导的PPAR-γ和脂质代谢相关蛋白表达的增加。
注:PPAR-γ——过氧化物酶体增殖物激活受体-γ
此外,在白色脂肪组织中,高盐饮食可以逆转高米饭饮食诱导的脂联素的减少和PPAR-γ表达的增加。在体外,高氯化钠浓度也显著降低了3T3-L1细胞的分化和调节脂质代谢,而不会引起细胞毒性。
▸ 适度增加盐摄入量对中枢神经系统自身免疫病具有多方面和潜在的有益影响
研究人员用自发 EAE 小鼠模型评估了高盐饮食对启动中枢神经系统自身免疫所必需的早期致病事件的影响。
高盐饮食消耗增加了糖皮质激素皮质酮的循环血清水平。皮质酮增强了脑内皮细胞上紧密连接分子的表达,促进了血脑屏障 (BBB) 的收紧,从而控制了炎症性 T 细胞进入中枢神经系统。
注:需要进一步的研究来证实以上结果,以确保高盐摄入不会加剧高碳水化合物饮食引起的代谢紊乱。
以上高盐饮食带来的益处尚处于动物模型研究阶段,不宜擅自应用在个人健康。
调整烹调方法减少食盐摄入量应当注意烹饪时少放盐 , 控制烹调时和餐桌上的用盐,一家3口每日用盐不宜超过 250 克 , 也就是全家每日总共用一小汤勺(约8克 )。
大多数新鲜水果和蔬菜天然含钠量低。鲜肉比午餐肉、培根、热狗、香肠和火腿含钠量低。
习惯咸味的人, 为满足口感的需要,可在烹制菜肴肘放少许醋,提高菜肴的鲜香味,帮助自己适应少盐食物。
或者可以考虑有些时候用无盐香草和香料代替,例如迷迭香、百里香、大蒜粉,辣椒粉等。
还要注意减少酱菜 、 腌制食品以及其他咸食品的摄入量。
从燕麦粥到汤面到土豆,一切都可以以“速食”的形式获得。通常,这些速食食品比非速食食品含盐量高得多。例如,普通即食燕麦片含有近200毫克的盐。
例如,添加了盐的冷冻蔬菜可以在蒸或煮之前用漏勺冲洗一下。这个简单的步骤可以减少高达23%的盐量。
糖或甜味食物无处不在,很多人喜欢吃糖或者甜味食物,它在许多人心中占据重要的位置,甜食可能会唤起我们的舒适和美好的回忆。
然而需要注意的是,它让人上瘾的同时,可能会喂养有害菌,有害菌大量增殖的同时有益菌也在减少……
糖,正在悄悄地破坏着肠道菌群原有的平衡。

研究表明腹泻和某些糖的消化不良有关,患有乳糜泻、克罗恩病和慢性腹泻的人在肠道中产生异常高量的粘液,这阻碍了消化,阻止了这些淀粉和二糖的吸收。
糖摄入可能会扰乱微生物群的平衡,增加促炎性,降低调节上皮完整性和粘膜免疫的能力。
大量摄入添加糖和加工食品,包括典型的西方饮食,都会损害有益菌,使我们更容易受到有害物质的影响。
肠道内层很薄,没有肠道内有益菌产生的保护性粘膜层,一些东西会渗入血液中,这就会导致炎症。
也就是说,持续摄入过量糖可能会带来肠漏、慢性炎症增加和各种健康问题的风险。
身体无法分解和吸收的多余糖分将留在肠道中发酵。这种糖通过大肠的速度更慢,喂养了有害细菌和酵母,并导致气体的积累。这种气体会导致抽筋、痉挛和疼痛。
乳糖是牛奶中的糖分。当身体不能产生分解乳糖所需的酶时,就会发生乳糖不耐症,导致胀气、腹胀和其他消化不适。
同样,高果糖玉米糖浆会抑制消化,因为身体也不能分解它。果糖停留在肠道中,导致胃肠胀气和不适。
虽然吸收水分是大肠的主要工作,但糖可以将水分吸入大肠,或者至少阻止水分被正常吸收。这可能会导致腹胀或肠道沉重。
消化是由肝脏刺激的。果糖只能由肝脏处理,所以摄入的所有果糖都被一次性送到肝脏,使其超载并造成潜在的损害,进而损害消化。
果糖无法刺激胰岛素,而胰岛素又无法抑制“饥饿激素”。结果,饱腹荷尔蒙瘦素也没有被刺激,这导致吃得更多。
这就容易导致体重增加、腹部肥胖、胆固醇升高、血糖升高等各种代谢疾病。
而这些代谢疾病的发生离不开肠道菌群的运作,接下来我们来了解一下,糖是如何通过影响肠道菌群,从而引发代谢疾病的?
糖通过影响肠道菌群引发代谢疾病的机制
一项新的研究发表在8月29日在线出版的《细胞》杂志上,科学家们发现:
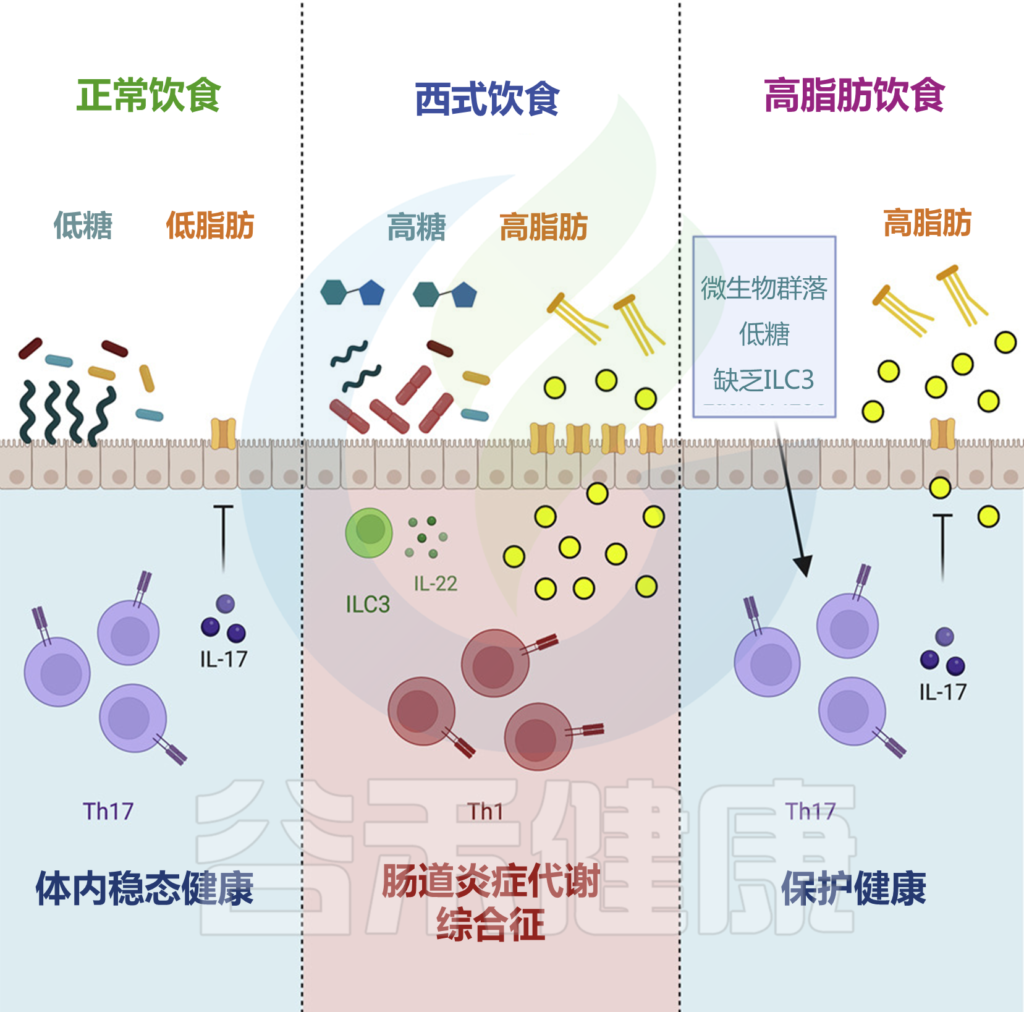
糖可能会破坏肠道菌群,从而耗尽关键的免疫细胞,导致肥胖等代谢综合征。
简单来说高糖饮食带来的影响如下:
高糖饮食
↓↓↓
刺激Faecalibaculum rodentium 的生长
↓↓↓
挤走了特定菌群SFB, SFB丢失
↓↓↓
改变了吸收膳食脂肪的方式
↓↓↓
出现“代谢综合征”的特征
注:SFB是小鼠肠道中的特定细菌,即分段丝状细菌。
我们来看下研究过程:
研究人员给小鼠喂食含蔗糖和麦芽糊精的高糖饮食,高糖饮食刺激了Faecalibaculum rodentium的生长,这种细菌基本上挤走了SFB。SFB的突然丢失在小鼠肠道内引发了连锁反应,最终改变了动物吸收膳食脂肪的方式。
吸收脂肪的改变导致小鼠肥胖,并出现“代谢综合征”的特征。代谢综合征如高血压、高血糖和胰岛素抵抗,共同增加了患心脏病、中风和2型糖尿病的风险。
也就是说:SFB在某种程度上可以防止代谢综合征和过度体重增加。那么,SFB是如何发挥作用的?
研究发现,随着小鼠逐渐失去SFB,它们的Th17细胞总数也下降,体重增加,出现胰岛素抵抗和葡萄糖不耐症等代谢综合征的症状。
这里不得不提一下,该过程中重要的细胞——Th17.
SFB会与免疫系统进行“对话”,促进产生一种特定类型的免疫细胞——Th17。
可以这么说,Th17细胞是一种保护小鼠免受代谢疾病影响的“盔甲”。
这些免疫细胞释放影响肠壁的蛋白质,防止多余脂肪被组织吸收进入血液。这些免疫细胞产生的分子可以减缓肠道对‘坏’脂质的吸收,并减少肠道炎症。也就是说,它们保持肠道健康,保护身体不吸收致病的脂质。
当喂食高脂肪、高糖饮食时,小鼠肠道中的Th17细胞发生了什么变化?
小鼠迅速发展出代谢疾病的几个特征(体重增加、葡萄糖不耐受),并显示出肠道Th17细胞的减少。
更具体地说,研究人员发现Th17水平的下降是由于饮食诱导的肠道微生物群的变化。已知促进Th17的细菌被其他种类的肠道细菌所取代。尤其是糖似乎增加了有害菌的数量,最终降低了Th17的水平。
也就是说,糖通过干扰微生物组分间接破坏了这种盔甲。
研究人员认为,只要动物保持高水平的诱导Th17的肠道细菌,高脂饮食就不会导致负面的代谢效应。
doi.org/10.1016/j.cell.2022.08.005
如果没有健康的肠道菌群,减糖也不能避免疾病
在另一个实验中,研究小组从一组小鼠中去除了SFB,然后喂它们无糖、高脂肪的饮食,发现这些小鼠尽管没有吃糖,但体重也增加了,并患有代谢疾病。那么,是什么导致体重增加呢?
本质上,如果没有健康的肠道菌群,小鼠就不会产生足够的Th17细胞,因此也就缺乏前面所说的“盔甲”。
研究小组发现可以通过两种方式提供这种盔甲:
这表明,如果小鼠的肠道中已经耗尽了SFB,那么减少糖的摄入并不能帮助小鼠避免代谢疾病。
如果把这一发现放到人类身上,那就意味着如果一个人的肠道微生物群已经被破坏,那么减少摄入糖不一定会有帮助。
我们可以想象,一些流行的饮食干预,如尽量减少糖,可能只对微生物群中有某些细菌种群的人有效。
研究人员说,可能需要额外的干预措施来恢复这些人的肠道细菌或Th17细胞。
当然也需要更多的研究来了解类似的机制是否在人体肠道中起作用。
通过以上研究,我们可以大致了解糖对肠道菌群的影响,及带来的危害,因此,一定程度上减少糖的摄入会带来好处。
重新控制饮食习惯,试着对糖说不
当对糖强烈的渴望袭来时,试着忽略它,深呼吸几次,然后问自己:

意识到微生物只是利用你来喂养它自己,是很好的第一步,也就是重新控制饮食习惯。
当你减少糖的摄入量时,这些以糖为食的微生物会进入饥饿模式,与此同时,你对糖的渴望会变得更加强烈,可能会“说服自己”去得到它。

编辑
识别糖的触发因素
有时候会在特定的情况下渴望吃糖。
想想上一次吃甜食是什么时候,是感到有压力吗?疲劳?抑郁?焦虑?压抑?紧张?……
可以把这些糖分触发因素想象成某个按钮。这个按钮一触碰就想吃甜食类食物,每个人的按钮可能不一样,有些人是焦虑,有些人是疲劳…
了解属于你自己的糖分触发因素,会帮助你在渴望到来时安然度过。有意识地关注你的渴望,是减少 对甜食不受控的一个强有力的方法。
喂养健康的肠道细菌
相对较为健康的做法是多吃真正的食物,并在饮食中加入更多的植物,来自植物的益生元可以喂养我们的微生物群,例如:
菊苣、朝鲜蓟、蒲公英嫩叶、芦笋、大蒜、洋葱、苹果、浆果类、香蕉、菠菜、羽衣甘蓝、胡萝卜、番茄、山药、黄瓜、芝麻菜等。
酸奶、泡菜、味噌、开菲尔、康普茶等。
尽可能避免加工和包装食品、含糖食物、酗酒等。
养成良好的生活方式
研究表明,如果你在吃饭时看电视或刷手机看各类小视频等,可能会吃得更快,嚼得更少,吃得更多。
吃饭时,试着把手机放在一边,关掉电视,有意识地彻底咀嚼每一口食物,并真正品尝味道,可能会吃的更少,消化更好。
看到一些新闻或对即将截止的工作任务感到压力,你会很难从膳食中吸收营养。因此,坐下来吃饭之前,试着深呼吸让自己平静下来。
其他还包括:适当运动、规律作息、保持充足的睡眠、适量沐浴阳光,保持良好的心情等方式。
扩展阅读:
菌群多样性是如何形成的,与健康的关系,如何改善?
20种有效改善肠道健康的科学方法
此外,减少糖的摄入并不意味着转向人工甜味剂。经常食用人工甜味剂可能会对微生物群产生负面影响,导致代谢紊乱和肥胖。
扩展阅读:
你的焦虑可能与食品添加剂有关,警惕食品添加剂引起的微生物群变化
现代人的嗜辣程度日益走高,很多人已经到了无辣不欢的境界。
「辣」准确地说并不是一种味觉,可以说是痛觉,是舌、口腔和鼻腔粘膜受到刺激产生的辛辣、刺痛、灼热的感觉。
「辣」让人一边痛不欲生,一边欲罢不能。
「辣」对身体的影响褒贬不一。有人说吃辣上火,腹泻,长痘痘;有人说吃辣抗氧化,助消化,降胆固醇…

辣椒素的吸收部位:
辣椒素在胃和小肠上部被被动吸收的效率超过80%。
吃辣的健康益处
• 支持正常的血液循环,有利于心血管健康,以及降低患心脏病的风险。
• 促进新陈代谢和脂肪燃烧。一些研究表明,随着时间的推移,食用辛辣食物与体重增加较少之间存在联系,因为辛辣香料可能会增加卡路里燃烧。
• 增强消化健康,支持肠道微生物群中的有益菌生长。
• 提供抗氧化剂,包括抗氧化应激的酚类化合物。
• 减少炎症,包括胃肠道,以及影响关节和动脉的炎症。
• 通过表现出抗菌活性来支持免疫功能。
• 可能降低慢性病风险,包括高血压、高低密度脂蛋白胆固醇、二型糖尿病、心脏病和中风。
• 降低某些癌症的风险,包括食道癌和直肠癌等。
• 潜在地降低了过早死亡的风险。在一项研究中,与每周吃少于一次辛辣食物的成年人相比,那些每周吃六到七天辛辣食物的人受益于降低14%的风险总死亡率。
……
看到这里全是吃辣的益处,是不是想赶紧吃吃吃,先别急,这也要看辣的程度。
辣椒素(CAP)是辣椒的主要辛辣成分。
接下来我们来了解一下,不同剂量的辣椒素引起的肠道菌群变化,以及肠道菌群在辣椒素对抗疾病(肥胖,糖尿病等)中的作用。
一项研究评估了辣椒素对胃肠道健康的影响,并研究辣椒素是否调节短链脂肪酸和肠道微生物群的组成。
以40、60和80 mg/kg的剂量给小鼠施用辣椒素。
高剂量的辣椒素会损害胃肠道组织
对照组小鼠的结肠组织显示出丰富的杯状细胞和具有整齐绒毛的健康隐窝结构;
而辣椒素干预组小鼠显示出炎性细胞浸润,以及隐窝和杯状细胞的丧失。
与对照组中的小鼠相比,用60 mg/kg 辣椒素处理的小鼠显示出产生粘液的杯状细胞的损失;
在80 mg/kg 辣椒素处理的小鼠中,炎症细胞浸润明显。
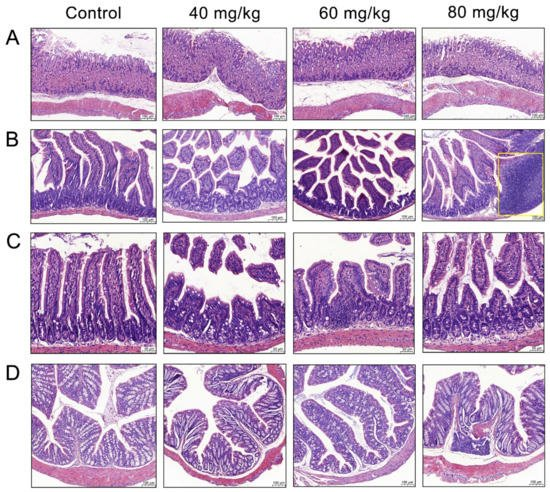
doi.org/10.3390/foods11050686
辣椒素引起的炎症反应,与剂量有关
辣椒素影响胃和回肠中的抗炎细胞因子水平,但不会导致严重的炎症损伤
炎症反应与胃肠道损伤密切相关。研究表明,辣椒素诱导小鼠胃肠道炎症的主要特征是炎症细胞因子水平升高,尤其是IL-10、IL-1β和TNF-α。
注:IL-10是一种关键的细胞因子,可以减少炎症介质的释放,并显示抗炎特性。
IL-1β和TNF-α是引起粘膜炎症和肠屏障损伤的重要促炎细胞因子。
高剂量辣椒素可能导致空肠和结肠的炎症损伤
结果表明,80 mg/kg 辣椒素干预组可导致所有胃肠组织中IL-10水平降低,空肠和结肠中IL-1β和TNF-α水平升高。
多样性下降
与对照组相比,40 mg/kg 辣椒素组的香浓指数显著下降(p<0.001),Chao1指数略有下降。同时,与对照组相比,60 mg/kg辣椒素组显著降低了Chao1指数。
使用加权UniFrac距离的PCoA测量β多样性,揭示了对照组和不同剂量辣椒素组之间的不同菌群。
在门的水平上,对照组小鼠中:
与对照组相比,40 mg/kg 辣椒素干预显著降低了拟杆菌的丰度至34.17%,但增加了厚壁菌的丰度(56.64%)(p<0.0001)。
80 mg/kg的辣椒素干预显著降低了拟杆菌的相对丰度,增加了放线菌和变形杆菌的丰度。
变形杆菌的存在是肠道微生物群稳态失衡的标志,与腹泻症状和炎症密切相关。
辣椒组的优势细菌标记物
对照组、40、60和 80mg/kg 辣椒素干预组中分别发现了优势细菌标记物。
差异最大的属包括丁酸杆菌属、乳杆菌属、粪杆菌属、科氏杆菌属_UCG_002、双歧杆菌属、Rikenellaceae_RC9_肠组、拟杆菌属、Alistites属和Dubosiella属。
高剂量增加了:双歧杆菌和粪杆菌的比例
对具有显著差异的选定属的相对丰度进行了分析,表明辣椒素处理以剂量依赖的方式增加了双歧杆菌和粪杆菌的比例,但仅在80 mg/kg 辣椒素干预组中显示出显著变化。
Faecalibacterium被认为是胃肠道疾病的生物指示剂,并与丁酸生成呈正相关。这可能是60和80 mg/kg 辣椒素组小鼠盲肠丁酸水平显著升高的原因。
在辣椒素干预组中,尤其是在40 mg/kg 辣椒素干预的组中,乳酸杆菌和Alistites的相对丰度显著降低。
与对照组相比,40 mg/kg 辣椒素干预显著提高了Dubosiella的比例,但减少了拟杆菌、丁酸单胞菌和Rikenellaceae_RC9_gut_group的丰度。
注:有研究曾报道,Dubosiella可以抑制小鼠的肥胖。
80 mg/kg 辣椒素干预后:Coriobacteriaceae_UCG_002的丰度增加。
注:Coriobacteriaceae_UCG_002可以通过产生必需氨基酸和发酵膳食蛋白而对宿主有利。
辣椒素的抗肥胖作用
辣椒素已被证明能够引起饱腹感,减少热量摄入,增加能量消耗,并增强脂肪氧化,这反过来可能导致体重减轻。
厚壁菌/拟杆菌 ↑↑↑↑
大量研究表明,在以辣椒素作为补充的高脂肪诱导小鼠模型中,厚壁菌/拟杆菌的比率会更高。
发现肠道菌群失调可减少拟杆菌,并增强在肥胖人类和动物肠道中观察到的分泌革兰氏阴性病原体的厚壁菌和脂多糖。
AKK菌 ↑↑↑
最近,还研究了辣椒素的抗肥胖作用,与肠道微生物群的变化、喂食高脂肪辣椒素小鼠中变形菌门的减少以及对宿主新陈代谢有益的粘液降解细菌Akkermansia muciniphila 的高丰度有关。
Faecalibacteria ↑↑↑
辣椒素对肠道和微生物群有消炎作用。辣椒素可以增加Faecalibacteria,从而有助于防止肥胖,调节血糖水平,防止肠道炎症。
产丁酸菌 ↑↑↑
此外,饮食中的辣椒素可以诱导产生丁酸盐的瘤胃球菌科和拉氏螺旋菌科的水平增加,但也可以刺激盲肠产丁酸细菌和丁酸盐水平的升高,以抑制结肠CB1受体,并减少LPS的生物合成。
注:丁酸盐的好处:保护肠道内壁,有助于肠漏的愈合,保护大脑和神经系统,它能增强免疫系统,更有效地对抗感染。
刺激微生物群减少饥饿激素——饥饿素
胃内产生的一种肽被称为“饥饿激素”.它是肠道在肠道微生物的帮助下产生的一种激素。它不仅能影响食欲,还能促进身体储存脂肪的能力。
辣椒素通过刺激微生物群向身体发送信号,告诉它减少饥饿素,从而帮助你控制饥饿。
综上所述,辣椒素是一种有效的抗肥胖化合物。补充后,它会激活肠道内的某些受体,称为TRPV1受体。一旦打开,这些受体向身体发送信号,告诉身体增加肠道菌群Akkermansia muciniphila。更高比例的Akk菌促进减肥和调节血糖水平,因此有助于控制糖尿病和肥胖症。
辣椒素抗糖尿病作用
大量体内和体外研究表明,辣椒素在改善葡萄糖代谢方面发挥着重要作用。早些时候已经证明,在糖尿病大鼠中,系统性辣椒素激活可导致辣椒素敏感细胞变性和葡萄糖诱发胰岛素分泌的长期变化。
补充辣椒素(100 mg/kg)的雄性肥胖Zucker大鼠的血浆CGRP水平升高,同时通过辣椒素诱导的感觉神经脱敏改善糖耐量。
新生辣椒素治疗SD大鼠(50 mg/kg)胰岛素介导的糖代谢增加,通过辣椒素诱导的含有神经肽的感觉神经增强体内胰岛素敏感性。
患有糖尿病的雄性Wistar大鼠以1 mg/kg·天的剂量长期服用辣椒素8周,表明辣椒素具有利尿作用,并增加了尿液表皮生长因子水平。含有高酚和辣椒素含量的红辣椒茎(9.7 mg/g,DW)具有较强的α-淀粉酶和α-葡萄糖苷酶抑制作用。
所有这些发现表明,辣椒素敏感结构一定参与了调节胰岛素分泌和血糖。
一项随机双盲临床试验表明,含有辣椒素的辣椒补充剂(5 mg/d辣椒素)定期改善妊娠期糖尿病妇女的餐后高血糖和高胰岛素血症以及空腹脂代谢紊乱。
膳食辣椒素通过对肠道微生物群的调节作用影响葡萄糖稳态和肥胖的拟议途径
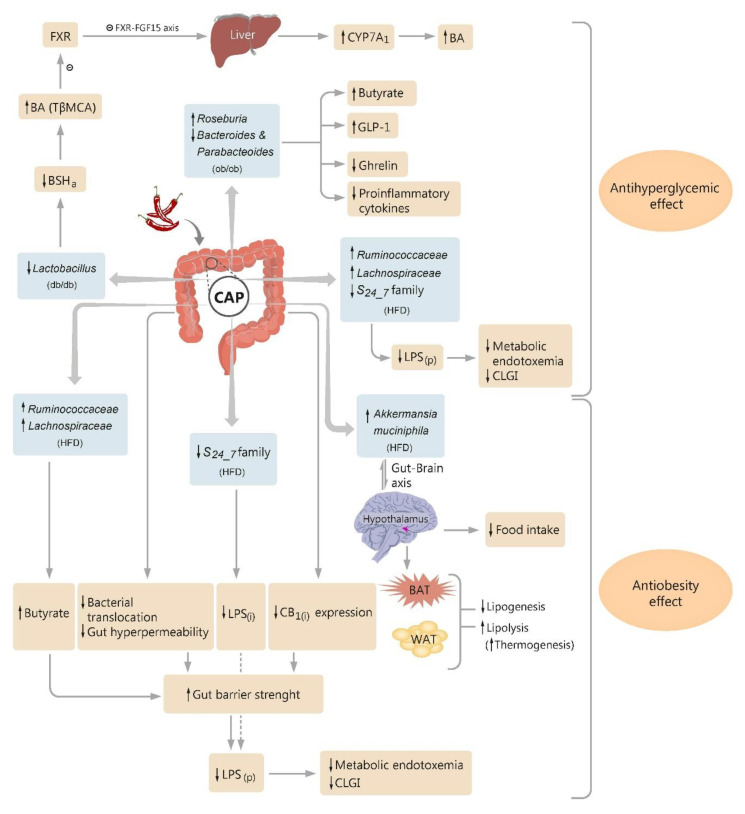
doi: 10.3390/molecules25235681
辣椒素可降低2型糖尿病小鼠体内乳酸杆菌的丰度(db/db),从而降低胆汁盐水解酶活性(BSHa),增加肠道中结合胆汁酸(BA)的水平,尤其是法尼样X受体(FXR)拮抗剂牛磺酸-β-鼠胆酸(TβMCA)。FXR信号发生改变,肠肝FXR-FGF15轴(FGF15成纤维细胞生长因子15)也受到抑制,导致胆固醇7α-羟化酶(CYP7A1)表达上调,肝BA合成增强。在肥胖糖尿病小鼠中,辣椒素增加Roseburia并抑制拟杆菌和副杆菌的丰度,随后粪便丁酸水平和血浆胰高血糖素样肽-1(GLP-1)增加,血浆总ghrelin和促炎细胞因子减少。
辣椒素通过调节肠-脑(下丘脑)轴,最终针对棕色脂肪组织、白色脂肪组织和小鼠食物摄入量,在高脂饮食喂养的小鼠中发挥抗肥胖作用。辣椒素减少了能够分泌LPS(i)(肠道细菌脂多糖)的革兰氏阴性病原体的数量,如S24_7科成员,并增加了高脂饮食小鼠中产丁酸菌的数量(例如,瘤胃球菌科和Lachnospiraceae),从而增加了粪便丁酸盐。辣椒素可减弱高脂饮食小鼠肠道通透性增加和细菌移位,并抑制肠道大麻素受体1型(CB1(i))的表达。
通过这些途径,辣椒素增加了这些肥胖小鼠的肠道屏障强度,同时减少了肠道菌群改变所产生的高水平LPS(i),从而降低了高水平血浆循环LPS.
TRPV1通道在感觉异常中起着核心作用,并在糖尿病动物模型中显示出高表达水平。
“恶性循环假说”指出,肥胖期间TRPV1对感觉神经的激活可能导致持续的神经肽物质P(SP)和CGRP释放,从而阻止胰岛素介导的葡萄糖摄取,最终导致代偿性高胰岛素血症(下图)。因为CGRP可以减少胰岛素分泌,而SP可以诱导胰岛素抵抗,它们会引发一个恶性循环,从而导致2型糖尿病发病。
而辣椒素作为一种TRPV1激动剂,可能会打破这种恶性循环,并有可能改善胰岛素分泌和胰岛素敏感性。
辣椒素抗肥胖、抗糖尿病和抗高血压的可能机制
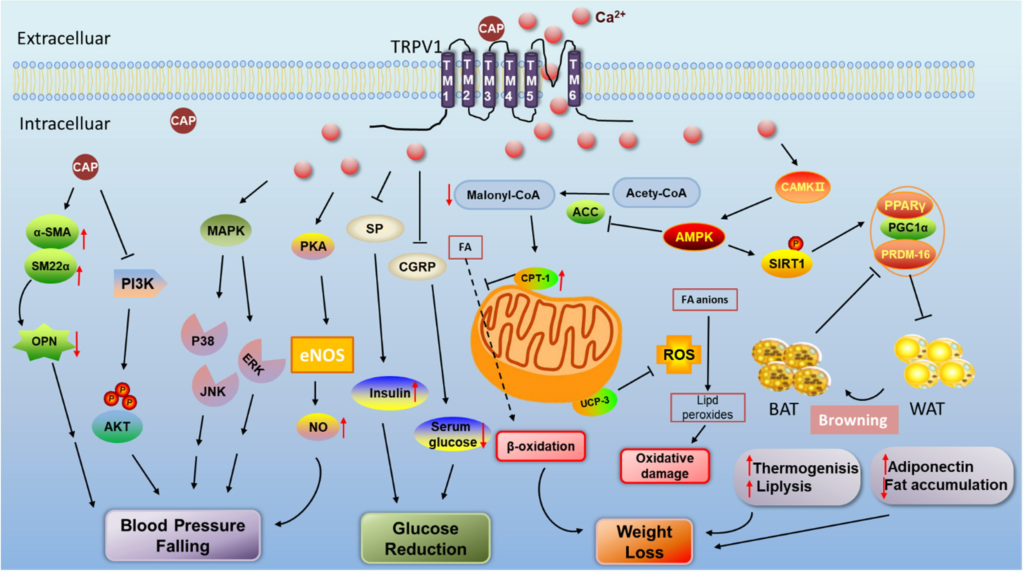
doi.org/10.1080/10408398.2021.1884840
抗肥胖机制:
通过磷酸化激活AMPK抑制ACC,抑制ACC降低丙二酰辅酶a浓度,导致CPT-1抑制解除,脂肪酸(FA)氧化增加,减少肌肉内脂质堆积。此外,辣椒素(CAP)没有增加HFD喂养的动物中UCP3的表达,但增加了正常肌肉细胞中的表达,因此影响产热。此外,CAP可能增加PRDM-16的表达,并促进其与PPARγ的相互作用,以及增加PGC-1α的表达来触发BAT分化和WAT褐变,从而增加产热和能量消耗来对抗肥胖。
抗糖尿病机制:
TRPV1在感觉神经上的激活可能导致神经肽P物质(SP)和降钙素基因相关肽(CGRP)的持续释放,从而阻断胰岛素介导的葡萄糖摄取。
抗高血压机制:
CAP诱导TRPV1激活Ca2+内流和PKA介导的内皮一氧化氮合酶(eNOS)磷酸化。此外,通过CAP激活TRPV1,通过增加α-平滑肌肌动蛋白(α-SMA)和SM22α的表达,减少骨桥蛋白(OPN)的表达,抑制PI3K/Akt信号通路,抑制高血压期间血管平滑肌细胞(VSMC)的表型转化,从而减轻颅内小动脉重塑。
辣椒素抗高血压作用
几项动物研究显示了辣椒素或辣椒摄入量与高血压之间的密切关系。
辣椒素对体内血压影响的关键研究综述

doi.org/10.1080/10408398.2021.1884840
一项包含9273名健康成年人的横断面研究表明,女性参与者中高频率的辛辣食物消费与高血压的低风险显著相关,但男性参与者中没有。
在1991年至2011年的中国健康与营养调查中,一项对13670名20-75岁成年人的队列研究表明,每1000人中不食用辣椒或每天食用1-20、20.1-50、> 50.1克辣椒的高血压发病率分别为30.5、33.4、31.9和24.0,表明辣椒食用量与高血压风险呈负相关。
辣椒素抑制高血压的机制可能涉及一些关键酶和不同的信号通路。
包括通过TRPV1激活、PKA活性激活和eNOS磷酸化增加以及p38/MAPK途径释放血管舒张神经肽。此外,抑制PI3K/AKT途径,刺激尿钠排泄和利尿,ACE抑制活性和L型钙2+平滑肌细胞中的通道抑制也涉及抗高血压机制。
因此,食用辣椒素可能是一种潜在的抗高血压干预手段。
辣椒素在炎症性肠病中的作用
克罗恩病患者的回肠粘膜碎片显示,Faecalibacterium prausnitzii的丰度较低,这与6个月后内镜下复发有关。众所周知,Faecalibacterium prausnitzii具有抗炎特性,在外周血单核细胞培养物和结肠炎动物模型中,分别减少促炎细胞因子的产生,并增加抗炎细胞因子IL-10的分泌。
扩展阅读:
肠道核心菌属——普拉梭菌(F. Prausnitzii),预防炎症的下一代益生菌
富含 CAP 的饮食可能对克罗恩病产生有益的影响,因为它们会增加厚壁菌门/拟杆菌门的比例和粪杆菌的丰度,从而将免疫平衡改变为对食物抗原和共生细菌更具耐受性的状态。
辣椒素抗癌症作用
体外和体内研究表明辣椒素对不同种类的癌症具有抗癌作用,如胃癌、结肠癌、前列腺癌、胰腺癌、肺癌、乳腺癌、膀胱癌等。
辣椒素潜在的抗癌机制可能与其对肿瘤细胞凋亡、自噬和转移的影响有关。
辣椒素通过诱导凋亡和抑制血管生成来抑制各种永生化或恶性细胞系的生长。
辣椒素可以通过调节其广泛的分子靶标来调节细胞增殖和凋亡,这些分子靶标包括转录因子、生长因子及其受体、细胞因子、酶和基因。
除了细胞凋亡之外,辣椒素在防止体液细胞转移方面也起着重要的作用。
体内研究评估辣椒素在各种癌症中的抗癌机制

doi.org/10.1080/10408398.2021.1884840
总之,辣椒素的抗癌机制如下图,包括细胞凋亡的激活、细胞生长停滞、细胞自噬以及血管生成和转移的抑制。
辣椒素可能的抗癌作用机制:
因此,辣椒素有可能成为一种预防和治疗癌症的新疗法。
辣椒素抗癌的关键机制
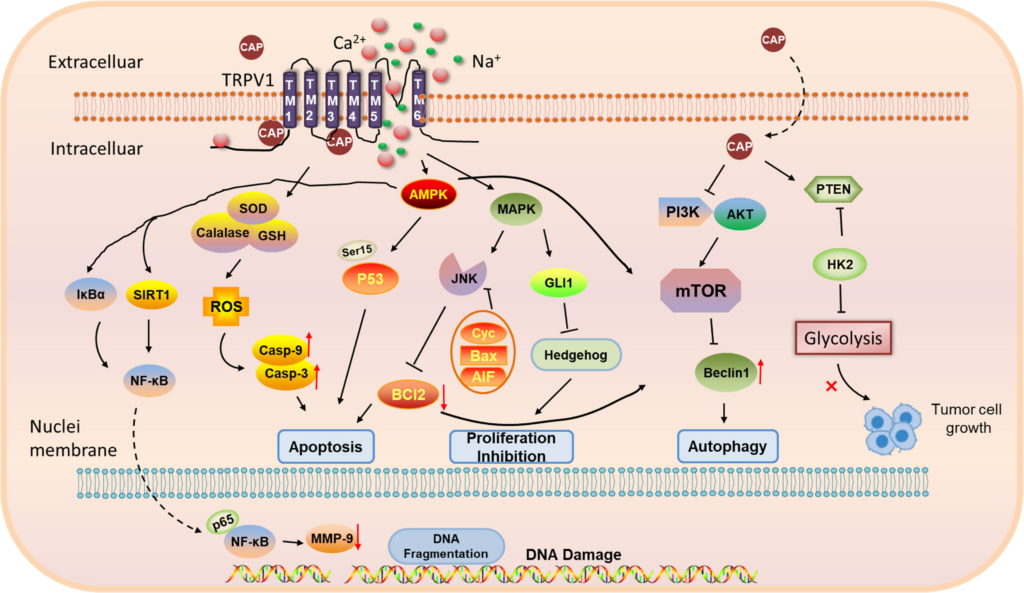
doi.org/10.1080/10408398.2021.1884840
CAP通过抑制Akt/mTOR途径抑制Akt磷酸化并诱导自噬。此外,CAP可以增加磷酸酶和张力蛋白同源物(PTEN)的表达,导致己糖激酶-2(hk2)表达的减少,从而抑制肿瘤细胞糖酵解。此外,TPPV1激活了Ca2+内流可以激活MAPK,进而阻断Hedgehog通路,抑制细胞增殖。此外,细胞内GSH水平的降低可能导致ROS的增加,进而激活线粒体死亡途径。CAP可能上调促凋亡基因,包括Cyc、AIF、Bax和裂解的caspase-3和-9,同时下调抗凋亡基因BCl2。P38和JNK MAPK通路以及AMPK/p53通路的激活也参与诱导细胞周期阻滞和凋亡。此外,CAP通过AMPK-SIRT1和AMPK-IκBα信号通路抑制NF-κB p65,从而抑制肿瘤细胞的迁移和侵袭,并引起基质金属蛋白酶-9 (MMP-9)的下调。
辣椒素的认知干预作用
在动物研究中,辣椒素在认知功能中的作用是有争议的。一些研究表明辣椒素具有神经毒性。
然而,辣椒素也被证明对认知功能或老年痴呆症有积极作用。例如,已经证明辣椒素对大鼠大脑中应激诱导的阿尔茨海默样变化具有预防作用。
具体而言,辣椒素可以部分减轻冷水应激诱导的大鼠空间记忆保留缺陷、LTP抑制、树突形态异常和突触相关蛋白丢失。
此外,辣椒素可以降低含辣椒素的高脂饮食喂养的SD大鼠患阿尔茨海默的风险。
关于食用辣椒与认知功能之间关系的流行病学研究有限。
目前,一项针对338名40岁以上参与者的调查表明,高水平的辣椒素饮食可能对中老年人的认知功能和AD血清Aβ水平产生有利影响,中国健康与营养调查(CHNS)在4582名中国成年人中收集了15年的数据,这些数据支持辣椒摄入量与认知功能之间存在正相关。
研究表明,与非消费者相比,那些累积平均辣椒摄入量超过50克/天的人,其总体认知功能的回归系数(和95%CI)为−1.13 (−1.71至0.54),自报记忆力差和自报记忆能力下降的比值比(和95%CI)分别为2.12(1.63–2.77)和1.56(1.23–1.97).
与食物一起摄入的辣椒素可以通过胃肠道中的非主动过程被迅速吸收。在被运输到门静脉,然后进入人和啮齿动物的全身后,约5%的未改变的辣椒素穿过血脑屏障并进入脑组织。
辣椒素受体TRPV1被证实可增加海马胰岛素信号通路,从而抑制GSK-3β,防止ad相关的tau蛋白过度磷酸化。
此外,自噬在β-淀粉样蛋白的生成和代谢中也起着重要作用,tau的组装及其功能障碍可能导致阿尔茨海默病的进展。
总之,辣椒素可以通过抑制tau蛋白过度磷酸化来减轻阿尔茨海默样神经病理改变和认知障碍,这表明它可能是一种有前途的阿尔茨海默治疗干预方法。
扩展阅读:
阿尔茨海默病de饮食-微生物-脑轴
辣椒素抗抑郁作用
膳食辣椒素可改善LPS诱导的抑郁样行为小鼠的抑郁样行为,如厌恶刺激、快感缺失和绝望等得到缓解。
辣椒素可以恢复抑郁症相关微生物群的异常变化。特别是在属水平上,辣椒素增加了某些关键微生物的相对丰度,如瘤胃球菌、普雷沃菌、 Allobaculum, Sutterella, Oscillospira.
相关分析显示,微生物群落组成的变化与抑郁行为改善、5-HT下降和TNF-α水平密切相关。
注:5-HT是一种代表性的单胺类神经递质,涉及调节几种生理活动和行为,包括与情绪和焦虑有关的活动和行为,并且低水平的5-HT已被证明与抑郁有关。
这些结果表明,膳食辣椒素可以调节肠道菌群的结构和数量,并在预防抑郁方面发挥重要作用。
▸ 健康的辛辣食物有哪些?
▸ 什么人群不适合吃辣?
虽然辛辣食物不会引起溃疡,但在部分人中也会引发腹痛。
一项研究特别强调,经常食用辛辣食物会引发一些消化不良患者的上消化道症状。对于肠易激综合征(IBS)患者,辛辣食物也会引发症状。
对于炎症性肠病(或IBD-克罗恩病或溃疡性结肠炎)患者,辛辣食物也会引发一些症状。
如果患有肛裂,可能会感觉到烧灼感。一项研究表明,辛辣食物会加重与肛裂相关的症状。
其他患胃酸倒流、胃灼热、腹泻、胃痛、怀孕期间的晨吐或恶心等人群,则需注意谨慎吃辣。
▸ 准备辣椒食物要注意什么?
准备辣椒时要戴手套,或者至少处理完后要彻底洗手。
保护眼睛和其他敏感区域。切辣椒时考虑戴眼镜。洗手前不要揉眼睛、鼻子或嘴巴等部位。
▸ 如何适应辛辣食物?
从微辣的食物开始,每周吃点辣的,舌头会慢慢习惯这种感觉,身体就像对酒精和咖啡因产生耐受性一样,慢慢也会对辣椒素产生耐受性。
▸ 一不小心吃太多辣如何缓解?
——牛奶或酸性饮料中和辣
辣的受不了的时候,可以喝点牛奶缓解,牛奶中的脂肪和蛋白质会中和食物中的香料,如果没有牛奶,可以喝冰水或酸性饮料。
普通的一杯水不会对解辣有帮助,因为水会将辣椒素扩散到嘴里,而柠檬水、橙汁或葡萄汁之类的酸性饮品都可以。
——不同质地的食物分散注意力
不同食物的质地可能会分散你对辣的注意力,吃口卷饼、饼干、面包丁之类的固体食物,它们本身其实并不能对抗辣椒素,但会给舌头一些不同的东西来关注。
——碳水化合物有助于吸收辣椒素
淀粉类碳水化合物会形成一道屏障,使辣椒素更难进入味蕾。
——吃饭的时候用嘴呼吸
每一口之间,慢慢呼气,把辣吹走,让嘴冷却下来。如果真的很痛,想象自己真的把辣椒片吹向空中,可能有助于减轻压力。
——提前吃点抗酸剂来防止胃不舒服
可以提前吃点抗酸剂或吃点小零食,比如三明治或土豆泥来填饱肚子,让辣椒素进入肠道后有所保留。注意不要过量使用抗酸剂,吃太多会扰乱胃产生酸的方式。
——记住熬过15分钟
辛辣食物的辣劲儿只需要15分钟就可以消散。如果感觉嘴巴着火一样,只要提醒自己这种感觉不会永远持续下去,不用害怕。
主要参考文献:
Naqvi S, Asar TO, Kumar V, Al-Abbasi FA, Alhayyani S, Kamal MA, Anwar F. A cross-talk between gut microbiome, salt and hypertension. Biomed Pharmacother. 2021 Feb;134:111156. doi: 10.1016/j.biopha.2020.111156. Epub 2021 Jan 2. PMID: 33401080.
Do MH, Lee HB, Oh MJ, Jhun H, Ha SK, Park HY. Consumption of salt leads to ameliorate symptoms of metabolic disorder and change of gut microbiota. Eur J Nutr. 2020 Dec;59(8):3779-3790. doi: 10.1007/s00394-020-02209-0. Epub 2020 Mar 3. PMID: 32125529.
Czesnikiewicz-Guzik M, Müller DN. Scientists on the Spot: Salt, the microbiome, and cardiovascular diseases. Cardiovasc Res. 2018 Aug 1;114(10):e72-e73. doi: 10.1093/cvr/cvy171. PMID: 30052920.
Na SY, Janakiraman M, Leliavski A, Krishnamoorthy G. High-salt diet suppresses autoimmune demyelination by regulating the blood-brain barrier permeability. Proc Natl Acad Sci U S A. 2021 Mar 23;118(12):e2025944118. doi: 10.1073/pnas.2025944118. PMID: 33723078; PMCID: PMC7999868.
National Academies of Sciences, Engineering, and Medicine; Health and Medicine Division; Food and Nutrition Board; Committee to Review the Dietary Reference Intakes for Sodium and Potassium. Dietary Reference Intakes for Sodium and Potassium. Oria M, Harrison M, Stallings VA, editors. Washington (DC): National Academies Press (US); 2019 Mar 5. PMID: 30844154.
Ma Y, He FJ, Sun Q, Yuan C, Kieneker LM, Curhan GC, MacGregor GA, Bakker SJL, Campbell NRC, Wang M, Rimm EB, Manson JE, Willett WC, Hofman A, Gansevoort RT, Cook NR, Hu FB. 24-Hour Urinary Sodium and Potassium Excretion and Cardiovascular Risk. N Engl J Med. 2022 Jan 20;386(3):252-263. doi: 10.1056/NEJMoa2109794. Epub 2021 Nov 13. PMID: 34767706; PMCID: PMC9153854.
Rizvi ZA, Dalal R, Sadhu S, Kumar Y, Kumar S, Gupta SK, Tripathy MR, Rathore DK, Awasthi A. High-salt diet mediates interplay between NK cells and gut microbiota to induce potent tumor immunity. Sci Adv. 2021 Sep 10;7(37):eabg5016. doi: 10.1126/sciadv.abg5016. Epub 2021 Sep 10. PMID: 34516769; PMCID: PMC8442882.
Kawano Y, Edwards M, Huang Y, Bilate AM, Araujo LP, Tanoue T, Atarashi K, Ladinsky MS, Reiner SL, Wang HH, Mucida D, Honda K, Ivanov II. Microbiota imbalance induced by dietary sugar disrupts immune-mediated protection from metabolic syndrome. Cell. 2022 Sep 15;185(19):3501-3519.e20. doi: 10.1016/j.cell.2022.08.005. Epub 2022 Aug 29. PMID: 36041436.
Xia J, Gu L, Guo Y, Feng H, Chen S, Jurat J, Fu W, Zhang D. Gut Microbiota Mediates the Preventive Effects of Dietary Capsaicin Against Depression-Like Behavior Induced by Lipopolysaccharide in Mice. Front Cell Infect Microbiol. 2021 Apr 27;11:627608. doi: 10.3389/fcimb.2021.627608. PMID: 33987106; PMCID: PMC8110911.
Wang F, Xue Y, Fu L, Wang Y, He M, Zhao L, Liao X. Extraction, purification, bioactivity and pharmacological effects of capsaicin: a review. Crit Rev Food Sci Nutr. 2022;62(19):5322-5348. doi: 10.1080/10408398.2021.1884840. Epub 2021 Feb 16. PMID: 33591238.
Xiang Q, Tang X, Cui S, Zhang Q, Liu X, Zhao J, Zhang H, Mao B, Chen W. Capsaicin, the Spicy Ingredient of Chili Peppers: Effects on Gastrointestinal Tract and Composition of Gut Microbiota at Various Dosages. Foods. 2022 Feb 25;11(5):686. doi: 10.3390/foods11050686. PMID: 35267319; PMCID: PMC8909049.

谷禾健康
在过去几十年中,人类的饮食行为发生了巨大的变化。传统的早餐-午餐-晚餐模式已被频繁的小吃、夜间大餐和不吃早餐所取代。这种不规律的饮食模式可能对心血管代谢疾病风险产生不利影响,如肥胖、胰岛素抵抗、高血糖症、2型糖尿病等。
间歇性禁食已被越来越多的人认为是一种有前途的治疗心血管代谢疾病(CMD)的方法。一些神经科学家认为,我们的身体已经进化到能够不吃东西几个小时,甚至几天。
进食时机和频率可以一定程度上改善生活方式和心血管代谢,防止2型糖尿病和心血管疾病的发生。
间歇性禁食(IF),包括周期性禁食和限时饮食(TRF)等开始越来越流行。

本文讨论肠道微生物组的组成和功能改变,对代谢、高血压、2型糖尿病、肥胖症及其长期微血管和大血管并发症发展的风险之间潜在联系的新证据,同时也包括间歇性禁食的安全性,将间歇性禁食融入日常生活的建议等。
本文关键词

间歇性禁食在进食和禁食之间循环,通常是只能在特定时间进食,比如通过每周12小时至几天的限制进食。它关注的不是吃什么,而是在什么时间段内可以吃。
在食物缺乏的时间内,人体新陈代谢通过产生和利用脂肪酸衍生的酮,以及通过自噬增加细胞水平的营养循环,将脂肪从储存转换到动员。
注:脂肪动员是指储存在脂肪细胞中的脂肪,被脂肪酶逐步水解为游离脂酸(FFA)及甘油并释放入血液,被其他组织氧化利用的过程。
目前已有许多研究表明,间歇性禁食在减轻体重、改善葡萄糖稳态和血脂以及抗炎作用等方面都带来益处。
间歇性禁食包括以下几种常见的方式:
隔日禁食(ADF)
在某一天规律进食和第二天不进食之间进行交替。
周期性禁食(5:2天)
5:2天的进食也称为周期性禁食,其特征是一周两天极度限制或完全禁食,而一周其他五天可以不受限制地进食。
模拟禁食的饮食(FMD)
定期禁食的一种变体,特点是连续几天低热量摄入周期,然后每一到四个月或每隔一周进行一次正常的饮食循环。
限时饮食(TRF)
不那么极端的饮食,将每天的食物摄入量限制在4-12小时内,例如,分别在12:12小时或16:8小时(禁食:进食),包括斋月期间的禁食。
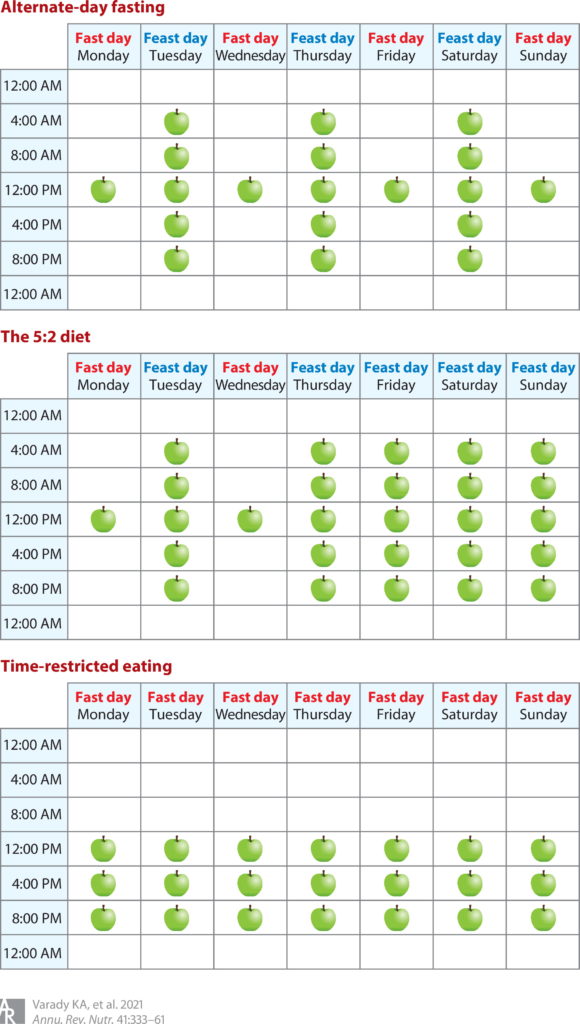
此图概述了一周中每一天的隔日禁食、5:2 饮食和限时进食 (TRE)(此处显示 8 小时 TRE)期间的食物摄入时间。食物摄入时间用苹果图标表示。
临床上对间歇性禁食的研究结果不一致:
几项临床研究表明,间歇性禁食可延长预期寿命并提供广泛的益处,包括减轻肥胖、高血压、2型糖尿病和心血管疾病。
然而,其他研究发现,特定时间的饮食在改善心血管和代谢结果方面并不优于控制能量的饮食。
因此,禁食和进食期间代谢转换的机制值得进一步研究。
最近,间歇性禁食已被证明会影响肠道菌群,几乎涉及宿主生理学的所有方面,这表明间歇性禁食生理影响的全新机制。
人类研究中,关于禁食对肠道菌群的影响

Angoorani P, et al.,Nutr Metab (Lond). 2021
本小节重点介绍一些关于肠道微生物组在间歇性禁食中作用的显著发现,肠道微生物组反过来影响心血管疾病相关的代谢表现,如肥胖、高血糖、高血压等。
我们知道,体重增加是由于过多的能量摄入加上较低的能量消耗,这通常是由体内脂肪的积累造成的。脂肪积累会对心血管系统造成严重的威胁。
关于肥胖与菌群的关系详见我们之前的文章:
体重增长:目前为止我们所知道的一切(更新你的减肥工具箱)
对人体随机对照试验的Meta分析表明,每周定期禁食2-3天的间歇性能量限制可改善超重和肥胖使体重减轻,降低体脂。这些改善的重要贡献可归因于肠道微生物群对脂质代谢和能量平衡的影响。
其中一种机制涉及脂肪组织,这是一种对营养刺激敏感并在间歇性禁食期间经历动态重塑的异质器官。
在哺乳动物中发现了两种不同形式的脂肪组织:
▸ 肠道菌群在隔日禁食介导的代谢改善中具有因果作用
喂食高脂肪食物并接受隔日禁食方案的肥胖小鼠在WAT中表现出白色脂肪积累增加,同时伴有体重减轻和肠道微生物组组成改变。
值得注意的是,向接受隔日禁食的肥胖小鼠补充抗生素消除了隔日禁食的有益代谢作用,并且将 隔日禁食小鼠的粪便移植到抗生素治疗的肥胖小鼠的粪便改善了代谢健康,表明肠道微生物组在隔日禁食介导的代谢改善中具有因果作用。
间歇性禁食介导的肠道微生物群调节宿主能量代谢的积极作用
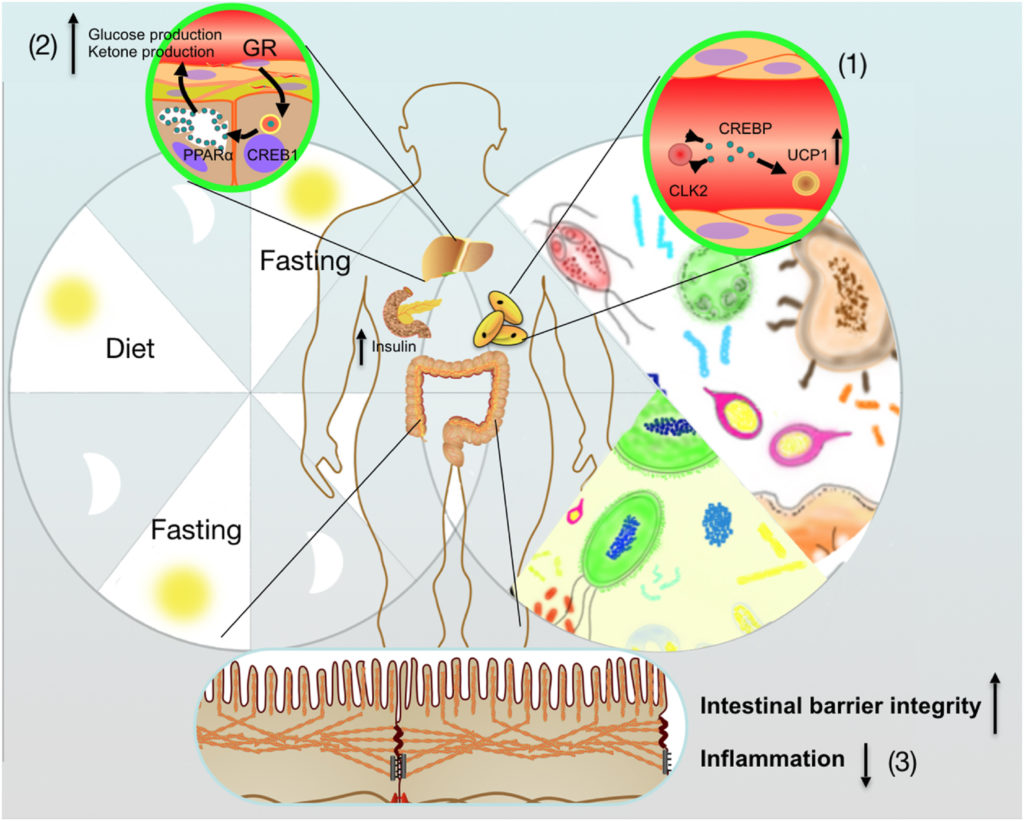
Rong B, et al.,Anim Nutr. 2021
(1) 间歇性禁食通过改善肠道菌群,促进WAT米色脂肪组织
(2) 在不摄入营养期间,肠道微生物群参与增加肝酮的产生
(3) 间歇性禁食优化的微生物群还负责保护宿主肠道屏障
▸ 隔日禁食诱导多种肠道细菌产生乙酸和乳酸
将盲肠代谢组学与Shotgun宏基因组学相结合,发现隔日禁食会导致肠道微生物群的组成发生变化,从而导致产生乳酸和乙酸的细菌(如罗伊氏乳杆菌)发生变化,进而导致血清乳酸和乙酸的积累。
关于罗伊氏乳杆菌详见:认识罗伊氏乳杆菌(Lactobacillus reuteri)
隔日禁食还通过促进米色脂肪生成来增加能量消耗,并改善体重增加和其他代谢紊乱。
在另一项研究中,仅在喂食正常饲料的小鼠中,乳酸杆菌水平在隔日禁食喂养的小鼠身上重复升高,而Allobaculum属则只在隔日禁食和高脂肪饲料的小鼠中富集。Allobaculum属是一种活性的葡萄糖代谢产物,能产生丁酸盐和乳酸盐。
这些结果表明,隔日禁食诱导多种肠道细菌产生乙酸和乳酸。然而,还需要更多的研究来确定乳酸和短链脂肪酸对WAT褐变以及对宿主产热和能量消耗的影响。
肠道微生物群的变化除了影响脂肪细胞产热之外,也可能影响适时进食过程中的脂质摄取。
控制宿主昼夜脂质吸收可能通过以下几种机制发生:
▸核因子白细胞介素-3 (NFIL3)的调节
核因子白细胞介素-3是一种受昼夜节律控制的转录因子,调节参与肠上皮细胞中脂质的摄取、加工和储存的基因的节律性表达。
NFIL3中的节律振荡由肠道微生物组通过激活先天免疫细胞反应驱动。
▸组蛋白脱乙酰酶3(HDAC3)的调节
刺激HDAC3的节律性表达和向染色质招募导致肠上皮组蛋白乙酰化的同步昼夜振荡,这反过来调节营养转运蛋白的基因表达,从而影响营养物质摄取和脂质吸收。
总的来说,肠道微生物群通过调节控制脂质和营养摄入的基因,以及通过产生影响脂肪组织的微生物代谢物来影响能量代谢。
间歇性禁食导致肠道微生物组分和功能的改变,这反过来可能影响心血管代谢健康
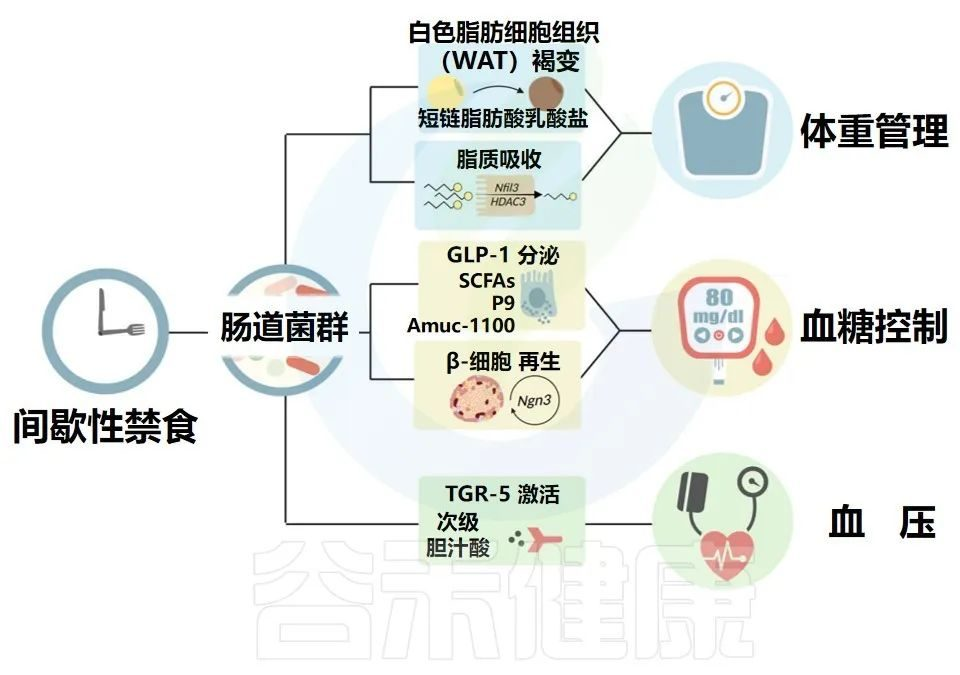
Karina R,et al.Rev Art Jou of Dia.2022
肠道微生物群驱动的WAT褐变和脂质吸收有助于体重管理。微生物通过GLP-1分泌和β细胞再生对血糖控制的影响。
微生物衍生的次级胆汁酸激活TGR-5以控制血压。
对啮齿动物和猴子的研究表明,间歇性禁食对血糖控制具有持续的有益作用。
肠道微生物组分与血糖水平相关,并适应日常生活中的禁食和再喂养期,包括昼夜饮食模式和限时饮食(例如,作为宗教禁食的一部分)。
在小鼠中,乳酸杆菌属在禁食期间高度富集,而Akkermansia muciniphila在喂养期间高度富集。除了昼夜变化外,A. muciniphila在接受限时饮食的人和小鼠体内都显著扩增。
▸A. muciniphila的增加如何在血糖控制中发挥作用?
这些成分的变化很有趣,因为A. muciniphila 与啮齿动物和人类的血糖水平呈负相关。
此外,A. muciniphila的增加与GLP-1的分泌增强有关,GLP-1是一种促胰岛素激素,由肠内分泌L细胞分泌,对膳食作出反应,并在全身血糖控制中发挥关键作用。
▸ 微生物群的昼夜变化 & GLP-1的昼夜分泌
GLP-1的分泌遵循昼夜节律,在活动期葡萄糖负荷后,餐后GLP-1水平较高,而在静息期,GLP-1水平较低,此外还受L细胞时钟机制的调节。
在喂食西方饮食的肥胖小鼠和缺乏微生物组的小鼠中,GLP-1的波动性分泌减弱。这项研究表明,通过将食用正常食物的常规小鼠的粪便微生物群转移到肥胖小鼠中,可以恢复无菌小鼠GLP-1的昼夜节律。
间歇性禁食、肠道微生物群和昼夜节律之间的多向关系
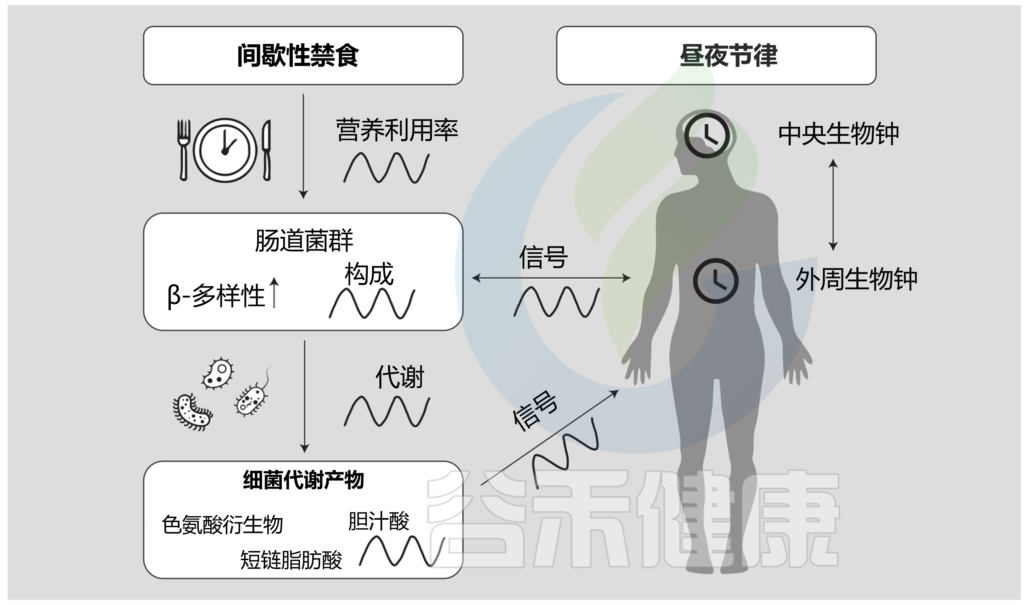
Daas MC, et al.,Benef Microbes. 2021
这些结果表明,微生物群的昼夜变化可能在GLP-1的昼夜分泌及其对葡萄糖稳态的后续影响中起着核心作用。至于机制,最近的研究已经确定了由A. muciniphila产生的几个假定的生物分子,它们可以触发肠L细胞分泌GLP-1。其中,丙酸盐和蛋白P9和Amuc-1100可刺激L细胞分泌GLP-1。
▸ 间歇性禁食改善血糖调节和2型糖尿病
给予肥胖和高血糖小鼠或缺乏瘦素受体的糖尿病db/db小鼠间歇性禁食或模拟禁食的饮食(FMD),可分别改善血糖控制和2型糖尿病。
模拟禁食的饮食有益于葡萄糖稳态的一个主要潜在机制包括神经生长素3(Ngn3)的激活,Ngn3是产生胰岛素的β细胞发育所必需的转录因子。β细胞的再生发生在暴露于间歇性模拟禁食的饮食后,并表明其遵循肠道微生物群的重组,这与db/db小鼠的血糖水平相关。
根据粪便微生物群的16S rRNA测序,
模拟禁食的饮食增加了下列菌的丰度:
模拟禁食的饮食降低了下列菌的丰度:
这与低血糖水平相关。
在此背景下,发现在模拟禁食饮食中具有较高丰度的Blautia,在糖尿病大鼠经2型糖尿病药物治疗后相对增加。
总之,营养时间对肠道微生物群、GLP-1分泌以及β细胞增殖的影响可能有助于改善血糖控制和胰岛素敏感性,从而为基于饮食和微生物群的2型糖尿病治疗潜力提供理论基础。与间歇性禁食对啮齿动物β细胞再生的影响一致,人类随机临床试验表明,与每日热量限制的匹配组相比,定期禁食(5:2饮食)对空腹胰岛素的影响更为显著。
有几个迹象表明,间歇性禁食和进餐时间可能有助于改善小鼠和人类的高血压。
不过间歇性禁食的有效性仍有争议,但DASH饮食(阻止高血压的饮食方法)提供了一种可以降低高血压的低钠饮食。
最近的一项研究表明,在高血压代谢综合征患者中,五天禁食后进行改良DASH饮食可以降低收缩压。
▸ 五天禁食通过改变肠道菌群影响血压
这种禁食还改变了肠道微生物群,包括一些与短链脂肪酸产生相关的菌群和基因。
使用对基线微生物组数据的机器学习分析来预测持续的收缩压反应,确定以下菌群为控制高血压的潜在贡献菌:
在大鼠中,五周的隔日禁食治疗可显著降低易患高血压卒中动物的血压。这种表型变化伴随着微生物组结构的改变,包括下列菌升高:
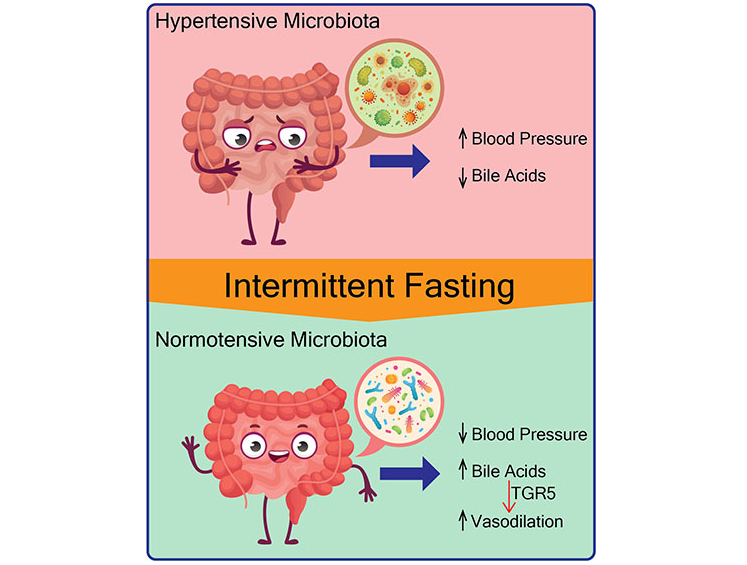
Shi H, et al.,Circ Res. 2021
▸ 隔日禁食饮食的调节血压机制
从机理上讲,隔日禁食饮食与微生物向产生次级胆汁酸的细菌转移有关,包括共轭和非共轭的二级胆汁酸(如牛磺胆酸、牛磺脱氧胆酸、牛磺脱氧胆酸[TUDCA]、LCA、甘鹅脱氧胆酸等),以及胆汁酸受体TGR5的激活。
此外,用胆酸或TGR5激动剂治疗这些高血压大鼠可降低血压,从而超过隔日禁食的需要。
从隔日禁食喂养的大鼠到无菌大鼠的粪菌移植可防止收缩压升高,表明肠道微生物群在降低血压方面的因果作用。
进一步的研究需要确定对次级胆汁酸产生反应的靶组织和细胞类型,以及这些胆汁酸诱导的导致血压下降的细胞途径。此外,还需要更多的试验来确定不同的间歇性禁食在降低各种心血管代谢紊乱患者血压方面的疗效和可持续性。
心血管代谢疾病是一种进行性疾病,具有长期和毁灭性的后果。
2型糖尿病患者的常见表现是微血管并发症,包括视网膜病和肾病以及心血管疾病。作为营养疗法的一部分,间歇性禁食已经成为治疗2型糖尿病几种长期并发症的潜在干预措施,包括视网膜病、认知能力下降、心力衰竭和肾病。
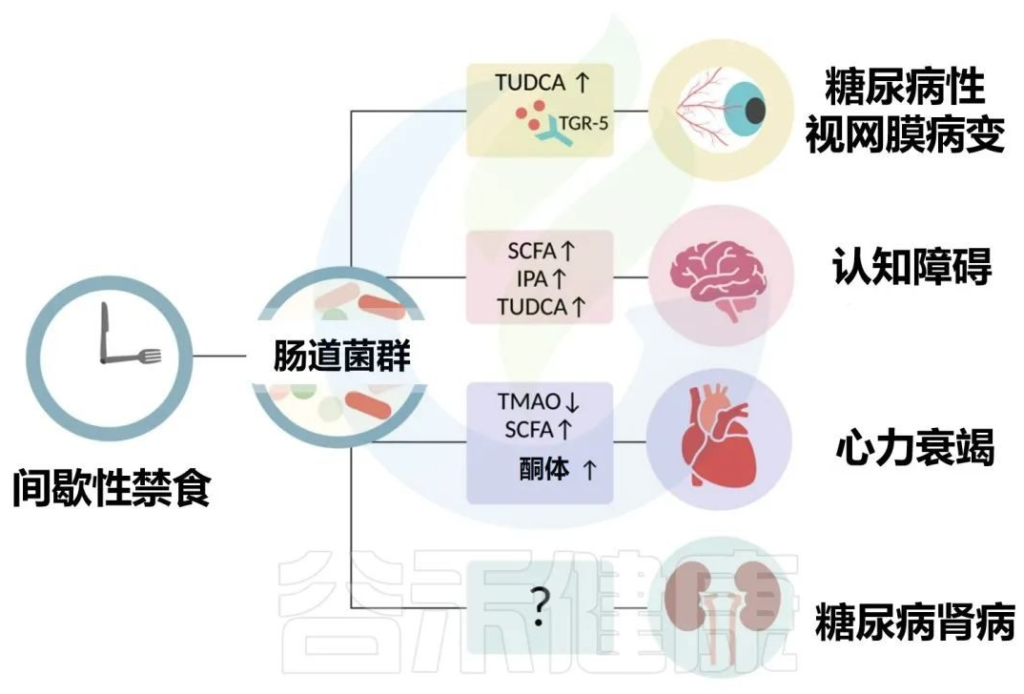
Karina R,et al.Rev Art Jou of Dia.2022
糖尿病性视网膜病变是2型糖尿病的一种并发症,它会影响视网膜的血管,并可能导致未经治疗的个体失明。
幸运的是,通过早期检测和及时治疗可以控制血糖水平和血压,可以降低糖尿病性视网膜病变导致的失明风险。
▸ 糖尿病性视网膜病变的菌群变化
以下三者之间的肠道微生物群存在显著差异:
比如说,研究人员Das等人发现,糖尿病视网膜病变患者中菌群变化:
在这项观察性研究之后,其他研究人员提出了肠道微生物组作为糖尿病视网膜病变鉴别生物标志物的潜在用途,并发现以下细菌是区分2型糖尿病患者和糖尿病视网膜病变患者的主要生物标志物:
这可能有助于视网膜病变的诊断。
其中,巴氏杆菌科在患有视网膜病的2型糖尿病患者中特别减少,这种细菌的减少可以作为该疾病的预测生物标志物。
▸ 隔日禁食干预后,糖尿病小鼠的菌群变化
研究人员使用糖尿病小鼠(db/db)比较了隔日禁食喂养的小鼠与随意喂养的小鼠糖尿病视网膜病变的经典标志物,发现隔日禁食方案阻止了无细胞视网膜毛细血管数量的增加,并减少了炎性细胞对视网膜的浸润。
隔日禁食的糖尿病小鼠具有厚壁菌门显著扩张的特征,更具体地说,在属的水平上,下列菌群丰度增加:
下列菌群减少:
随着肠道微生物组组成的变化, 作者观察到,与非糖尿病小鼠相比,糖尿病小鼠表现出昼夜微生物模式的差异,这种差异也在对隔日禁食的反应中发生了改变。
▸ 隔日禁食引起的代谢变化,有助于改善及诊断视网膜病变
值得注意的是,隔日禁食仅在糖尿病小鼠中增强了初级至次级胆汁酸的代谢,如TUDCA。
TUDCA的受体TGR5在视网膜神经节细胞中表达,这表明TUDCA的微生物生产可能会潜在地影响视网膜。
给糖尿病小鼠补充TGR5的强效激动剂导致糖尿病视网膜病变减少,其特征是视网膜炎症减少和无细胞毛细血管减少。
因此,隔日禁食可能导致次级胆汁酸的肠道细菌生产发生改变,激活视网膜TGR5,防止视网膜变性。
综上所述,这些结果表明,如果隔日禁食等干预措施可能导致肠道微生物群和代谢物的独特改变,这可能有助于视网膜病的诊断,并可能潜在地改善糖尿病视网膜病变。
▸ 2型糖尿病 → 认知障碍
2型糖尿病可引起明显的中枢神经系统并发症,包括结构改变或脑萎缩、脑微血管损伤、神经炎症以及最终导致认知缺陷的脑电生理特性改变。
随着时间的推移,这些认知和大脑结构的改变可能会导致认知能力的加速下降,并增加老年痴呆症等与年龄相关的神经退行性变的风险。
多项因素会导致糖尿病认知障碍,包括大脑胰岛素抵抗和葡萄糖摄取降低以及神经递质代谢紊乱。在动物模型中,各种类型的间歇性禁食有益于大脑健康,延缓神经退行性疾病的发展。
▸ 肠道菌群在调节隔日禁食诱导的认知功能中发挥作用
在隔日禁食治疗糖尿病db/db小鼠期间,肠道微生物组与认知功能之间存在联系。
糖尿病小鼠表现出认知能力下降,但28天的隔日禁食方案改善了焦虑行为、运动活动和突触结构,同时保护了海马中的胰岛素信号和线粒体生物生成。
隔日禁食干预小鼠组脑功能的改善伴随着下列菌群增加:
下列菌群减少:
抗生素治疗后,隔日禁食对糖尿病小鼠认知功能的保护作用被部分消除。学者发现隔日禁食组的初级和次级胆汁酸生物合成途径丰富。
▸ 菌群代谢物在调节隔日禁食诱导的认知功能中发挥作用
此外,db/db隔日禁食小鼠组的粪便和血浆中几种微生物相关代谢物的水平升高,其中包括短链脂肪酸、TUDCA(也可预防视网膜病变的次生胆汁酸)、吲哚-3-丙酸(IPA)和血清素。
补充这些代谢物可改善db/db小鼠的认知功能和胰岛素敏感性。
总的来说,隔日禁食诱导的肠道细菌种类和代谢物可能有助于减轻糖尿病诱导的认知障碍,并表明即使在没有隔日禁食的情况下,细菌代谢物也可能调节大脑功能的特征。
胰岛素抵抗的小鼠模型表明,如TRF和FMD等饮食方式可以改善高血压、血脂异常、高血糖和高胰岛素血症,所有这些都是心血管健康的一般指标。
▸心力衰竭与肠道菌群联系的证据
多项研究表明,心力衰竭患者肠道微生物群的组成发生了改变。对Dahl盐敏感大鼠进行的一项研究表明,补充益生菌植物乳杆菌可降低其对心力衰竭的易感性,并可在心肌梗死后更好地恢复。
已经提出了几种机制来解释肠道微生物组与心力衰竭之间的潜在联系,包括微生物组诱导的炎症调节、肠道通透性以及与细菌过度生长和细菌生物膜形成的关联。
▸肠道菌群影响心血管健康的机制:增加短链脂肪酸产生菌,为心脏提供能量
在几项研究中,在心力衰竭患者中也检测到几种病原菌的扩增。一项研究揭示了间歇性禁食对心脏的益处,提出肠道微生物群可以产生短链脂肪酸,在禁食期间为心脏提供充足的能量。
与常规小鼠相比,无菌小鼠的肝脏酮体生成量减少。根据这项研究,禁食与更高丰度的拟杆菌有关,这些拟杆菌可能负责产生短链脂肪酸,尤其是乙酸盐,可用于肝脏生酮,从而为心脏提供能量来源。
▸肠道菌群影响心血管健康的机制:TMAO降低
一项开创性研究表明,肠道微生物代谢膳食胆碱和左旋肉碱产生TMA,TMA被宿主肝脏转化为 TMAO.
研究发现,TMA-TMAO通路与动脉粥样硬化、血小板过度活跃和血栓形成有关,并用于预测心血管疾病风险的增加。
禁食影响肝脏代谢,与TMAO降低有关。此前有研究表明,维持低水平的TMAO可能对预防2型糖尿病相关的心肌病特别有帮助。
最近,在白天和夜间的db/db小鼠中发现TMAO水平升高,这与各种肠道细菌的昼夜振荡消失有关。作者建议,可以通过限制活跃期的摄食来恢复失去的细菌的昼夜振荡。
根据啮齿类动物的研究结果,间歇性禁食是否能够利用肠道微生物群,调节氧化三甲胺水平,并导致2型糖尿病患者心血管预后的有效改善,仍有待确定。
糖尿病可能导致肾功能障碍或肾病。在糖尿病患者中,血糖控制不良和高血压可导致肾小球滤过、蛋白尿、肾病性蛋白尿,并发展为终末期肾脏疾病。
多项研究表明,糖尿病肾病患者的肠道细菌丰度发生改变,总体上较低的细菌多样性与疾病进展相关。
在啮齿类动物中,糖尿病肾病与菌群及其代谢物(如苯基硫酸盐)的改变有关,并与肾素-血管紧张素系统的激活相关。
已有多项观察性研究测试了斋月禁食对糖尿病肾病严重程度的影响,但没有一项研究显示肾功能有显著变化。这些报告不是随机对照研究,样本量小,并且包含使用不同药物或透析治疗的患者。
目前,间歇性禁食对肾功能和糖尿病肾病的疗效以及肠道菌群在这一过程中的作用尚未阐明。
间歇性禁食除了前面章节提到的,通过脂质代谢来调节能量平衡从而减轻肥胖之外,还可以改善食欲调节,促进减肥。
▸ 三项短期研究评估:间歇性禁食增加饱腹感
在为期8周的ADF试验中,从基线检查到治疗后,主观饥饿感保持不变,饱腹感水平增加。这些饱腹感的增加与肽YY(PYY)的增加平行,肽YY是一种有效的饱腹激素。然而在任何时间点,饱腹感和PYY的变化与体重减轻或静息代谢率无关。
其他研究也有类似的发现。12周ADF后,肥胖受试者的饥饿感未受影响,饱腹感显著增加。饱腹感增加与体重减轻之间没有显著关系。
研究人员比较了ADF和每日卡路里限制对体重减轻后食欲的影响(比基线降低5%)。饥饿感在两组中都有类似的下降,但饱足指数保持不变。
▸ 一项长期研究评估:间歇性禁食对食欲调节没有长期有益影响
Kroeger等人进行的一项为期12个月的试验表明,ADF期间体重下降不理想和饮食依从性差与食欲没有任何有益变化有关。
总之,对ADF的短期研究表明,主观食欲有所改善(最常见的是饱腹感增加),而对ADF的长期研究表明,在食欲调节方面没有长期的益处。这方面还需要更多的研究。
目前似乎还没有任何人体试验检测ADF或5:2饮食对睡眠的影响,但有几项研究测试了限时进食对睡眠的影响。
▸三个限时进食试验:限时进食期间睡眠质量无变化
研究一:经过8周的4小时或6小时限时进食后,睡眠质量没有改变。
研究二:观察到8小时限时进食治疗12周后对睡眠质量没有影响。
研究三:10周10小时限时进食后,睡眠质量没有变化。
虽然这一初步证据表明,限时进食不会影响睡眠质量,但应该注意的是,这些研究的参与者基本上都是良好的睡眠者。因此,通过干预,他们的睡眠质量没有进一步改善,这并不奇怪。
▸限时进食不会影响睡眠时间
限时进食是否会改变睡眠时间也已得到评估。
前面的研究指出,4小时或6小时限时进食的睡眠时间没有变化。同样,8小时和9小时限时进食的睡眠时间保持不变。
然而,大多数参与者的平均睡眠时间为每晚约7小时,这符合国家睡眠基金会规定的最低7小时。这些受试者已经有足够的睡眠时间,这可以解释为什么限时进食不会影响睡眠时间。
▸限时进食可能改善睡眠
研究还评估了限时进食对失眠严重程度的影响。
研究人员推测,睡前禁食2-3小时可能会改善睡眠。更具体地说,睡前不吃脂肪和酸性食物可以减少胃酸反流和夜间胃灼热,这可能有助于降低失眠率。
在6小时限时进食研究中,受试者在基线检查时表现出阈下失眠症,到8周试验结束时,没有出现具有临床意义的失眠症。
相比之下,对于基线检查时无临床意义失眠的受试者,4小时和8小时限时进食对失眠严重程度没有影响。
综上所述,这些发现表明,对于已经显示出健康睡眠习惯的受试者来说,使用限时进食进行轻度减肥不会影响睡眠质量或睡眠时间。相比之下,限时进食可能有助于减轻受这种情况困扰的人的失眠严重程度。需要更多的研究来证实这些初步发现。
间歇性禁食虽然带来以上种种益处,但其安全性一直受到质疑。有些人对胃肠道问题、能量水平紊乱、饮食失调症状和激素紊乱的发生率增加表示担忧。这些饮食是否会对饮食质量产生负面影响也是一个问题。
人体试验的结果表明,禁食通常不会产生任何长期的胃肠道不良反应,例如便秘、腹泻、恶心、口干或口臭。不过早期的 6 小时限时进食导致了一些轻微的呕吐和腹泻病例。
最近的几项试验证明了,间歇性禁食也不会导致易怒、疲劳或头晕的程度增加。因此,迄今为止的研究结果表明,间歇性禁食几乎不会产生胃肠道问题或能量水平紊乱。
禁食因可能增加饮食失调风险而受到质疑。
来自 ADF 和限时进食研究的最新数据表明,这类饮食不会增加抑郁、暴饮暴食、通便行为或对肥胖的恐惧的发生率。
事实上,一项研究表明,ADF 可能对身体形象感知产生很小的有益影响。ADF 的这些发现与每日卡路里限制的发现相当。
在减少能量摄入的长期影响综合评估 (CALERIE) 试验中,将能量限制 25% 不会增加饮食失调症状,也没有其他有害的心理影响。
因此,间歇性禁食,也和卡路里限制一样,不会增加饮食失调症状,并且对身体形象感知具有良性或有益的影响。
然而,应该指出的是,这些研究排除了有饮食失调史的参与者。对于诊断为饮食失调的人来说,间歇性禁食是否安全仍然未知。
▸甲状腺激素
在健康人群和亚临床甲状腺功能减退人群中,研究了禁食期间甲状腺激素水平的变化。
招募年轻男性运动员参加8小时限时进食与阻力训练相结合的试验。8周后,血浆总三碘甲状腺原氨酸(T3)略有下降,但促甲状腺激素(TSH)无明显变化。在这些受试者中未观察到体重变化。游离甲状腺素(fT4)的变化没有报道,因此很难确定限时进食是否破坏这些甲状腺功能正常受试者的T3:fT4比率。
其他研究人员比较了ADF和每日卡路里限制对肥胖和亚临床甲状腺功能减退患者甲状腺水平的影响。24周后,ADF和卡路里限制(8%)同样降低体重,循环fT4、T3和TSH保持不变。这些试点数据表明,在间歇性禁食期间,瘦人的T3水平可能会略有降低,但这些影响不会发生在肥胖和亚临床甲状腺功能减退的人身上。
▸ 生殖激素
在 5:2 禁食 24 周后,绝经前妇女的睾酮、雄烯二酮、脱氢表雄酮硫酸盐、性激素结合球蛋白或催乳素没有变化。
相比之下,在 8 小时限时进食 8 周后,年轻男性的游离和总睾酮浓度降低。合成代谢激素睾酮的减少并没有导致身体成分的任何有害变化或肌肉力量的损害。
由于缺乏这方面的数据,因此很难就禁食对生殖健康的影响得出结论。此外,这些变化如何影响生育能力仍然未知,因为没有研究测试过这些饮食对男性和女性怀孕能力的影响。
据推测,在限时进食期间限制进食时间窗口期会导致高能量食物的消耗增加和补偿性地多喝(即,增加无糖苏打水和咖啡因的摄入)。
研究人员评估了4小时和6小时限时进食期间饮食质量的变化。
▸ 纤维摄入量偏少
8周后,4小时和6小时限时进食组的糖、饱和脂肪、胆固醇和钠摄入量与对照组相比没有显著差异。然而,限时进食受试者纤维摄入量远远低于(∼10-15克/天)在基线检查和治疗后的推荐量[25-38克/天]。ADF和5:2饮食试验中也经常报告纤维摄入不足。
▸ 饮料、酒等摄入量没有变化
至于饮料摄入,8周后,4小时限时进食、6小时限时进食和对照组的饮食苏打水、含咖啡因饮料(即咖啡、茶和能量饮料)和酒精的摄入没有差异。
作为这些发现的补充,一项为期一年的ADF试验报告称,饮料摄入量没有变化。
这些初步发现表明,间歇性禁食不会对饮食质量或饮料摄入产生不利影响。然而,应在间歇禁食期间向受试者提供膳食咨询以增加纤维摄入量,以确保肠道健康。
▸ 间歇性禁食并不代表胡吃海喝
重要的是,个人应注意间歇禁食期间的饮食质量。诚然,这些方案要求个人更多地关注用餐时间,而不是所摄入的营养素类型。虽然如此,临床医生应该向患者明确指出,进食窗口时间并不能让患者完全不考虑健康影响,彻底放纵自己乱吃。
为了使这些方案成为改善健康的可持续解决方案,应鼓励间歇性禁食的人食用水果、蔬菜和全谷物含量高、加工食品含量低的饮食。
本章节总结了一些关于如何开始禁食方案,以及如何将这些方法融入日常生活的实用建议。同时,就哪些人不应该使用间歇性禁食来控制体重提供建议。
对于大多数人来说,大约需要1-2周才能完全适应这种新的饮食模式。
据报道,在初期可能会出现头晕,头痛和便秘,但这些不良反应通常在禁食第二周后消退。
头痛通常是由于水分摄入不足导致脱水,当食物受到限制时可能会发生脱水。增加饮水量(每天增加1.5升)可能有助于个人在禁食期间缓解头痛。
与普遍的看法相反,禁食时锻炼确实是可能的。已经进行了几项将禁食与运动相结合的人体试验。
这些研究中的受试者可以在12-36小时的禁食期内进行中等强度到高强度的耐力或阻力训练。
有趣的是,在研究中,受试者在快节奏的日子里感觉到能量的增强,这对那些希望锻炼的人来说是有利的。
然而ADF期间,建议个人在运动后食用禁食日餐。一些人在运动后会出现能量摄入的代偿性增加。因此,把饭留到运动后吃,可能有助于个人保持在禁食日卡路里目标的范围内。
虽然对于间歇性禁食期间摄入的食物类型没有具体的建议,但始终建议强调多吃水果、蔬菜和全谷类食物。
这些食物可以帮助禁食参与者增加纤维摄入量,从而有助于缓解禁食期间偶尔出现的便秘。
避免超加工食品也很重要。与富含能量相匹配的未加工食品的饮食相比,富含加工食品的饮食会导致自由摄入的能量增加和体重增加。
间歇性禁食期间允许饮酒。然而不建议在ADF和5:2禁食模式中的禁食日饮酒。
禁食日的能量摄入非常有限(∼500千卡),因此建议将这些卡路里花在能提供营养的健康食品上,而不是酒精上,因为酒精会消耗营养。
无论是在禁食期间还是在进食窗口,都允许喝含咖啡因的饮料。越来越多的证据表明,与基线相比,个体在禁食期间的含咖啡因饮料消费模式没有显著改变。
不过,将咖啡因的摄入限制在上午和下午可能是值得的,这样它就不会干扰一个人晚上的入睡能力。
除以上人群之外,一般都可以安全地进行间歇性禁食,这可能是一种生活方式的改变。
如果尝试间歇性禁食后持续发现,异常焦虑、头痛、恶心或其他症状,不要勉强继续,说明暂时还不适合这种方式,可暂停。
间歇性禁食导致肠道菌群结构改变,以及细菌产生特定的代谢物发生变化,如次级胆汁酸和酮体,可能会潜在地影响正常宿主生理,及心血管代谢异常的临床结果。这些发现可以作为治疗干预的潜在基础。
当相同的膳食在不同的时间提供时,餐后对食物的反应因人而异。由于肠道微生物群参与了个人对食物的反应,因此有理由假设个人对间歇性禁食的反应也与肠道微生物群有关。这也是将间歇性禁食方案转化为临床实践的一个挑战。
需要更多控制良好的、前瞻性的、纵向的临床研究,来确定不同饮食带来的微生物变化,以便进一步转化为临床实践。同时包括肠道菌群健康检测在内的对个体肠道微生物组的进一步了解,或将为最终的临床实践带来益处。
注:本账号内容仅作交流参考,不作为诊断及医疗依据。
主要参考文献:
Ratiner K, Shapiro H, Goldenberg K, Elinav E. Time-limited diets and the gut microbiota in cardiometabolic disease. J Diabetes. 2022 Jun;14(6):377-393. doi: 10.1111/1753-0407.13288. Epub 2022 Jun 13. PMID: 35698246.
Angoorani P, Ejtahed HS, Hasani-Ranjbar S, Siadat SD, Soroush AR, Larijani B. Gut microbiota modulation as a possible mediating mechanism for fasting-induced alleviation of metabolic complications: a systematic review. Nutr Metab (Lond). 2021 Dec 14;18(1):105. doi: 10.1186/s12986-021-00635-3. PMID: 34906176; PMCID: PMC8670288.
Varady KA, Cienfuegos S, Ezpeleta M, Gabel K. Cardiometabolic Benefits of Intermittent Fasting. Annu Rev Nutr. 2021 Oct 11;41:333-361. doi: 10.1146/annurev-nutr-052020-041327. PMID: 34633860.
Shi H, Zhang B, Abo-Hamzy T, Nelson JW, Ambati CSR, Petrosino JF, Bryan RM Jr, Durgan DJ. Restructuring the Gut Microbiota by Intermittent Fasting Lowers Blood Pressure. Circ Res. 2021 Apr 30;128(9):1240-1254. doi: 10.1161/CIRCRESAHA.120.318155. Epub 2021 Feb 18. Erratum in: Circ Res. 2022 Mar 4;130(5):e18. PMID: 33596669; PMCID: PMC8085162.
Aron-Wisnewsky J,Clément K.The gut microbiome, diet,and links to cardiometabolic and chronic disorders. Nat RevNephrol. 2016;12(3):169-181.
Di Francesco A, Di Germanio C, Bernier M, de Cabo R. A time to fast. Science. 2018;362(6416):770-775.
Daas MC, de Roos NM. Intermittent fasting contributes to aligned circadian rhythms through interactions with the gut microbiome. Benef Microbes. 2021 Apr 12;12(2):147-161. doi: 10.3920/BM2020.0149. Epub 2021 Feb 3. PMID: 33530881.
Rong B, Wu Q, Saeed M, Sun C. Gut microbiota-a positive contributor in the process of intermittent fasting-mediated obesity control. Anim Nutr. 2021 Dec;7(4):1283-1295. doi: 10.1016/j.aninu.2021.09.009. Epub 2021 Oct 9. PMID: 34786501; PMCID: PMC8567329.

谷禾健康
神经免疫,菌群,心血管疾病
最新的《中国心血管病健康和疾病报告2019》数据显示,中国居民心血管病现患人数已达3.30亿,拐点尚未到来,且7-17岁儿童青少年高血压患病率呈现上升趋势。
心血管疾病(CVD)仍然是全世界发达国家死亡和残疾的主要原因。此外,广泛存在的心血管危险因素,如代谢综合征、糖尿病、肥胖和性类固醇激素代谢紊乱,有效预防策略已成功减少急性心血管事件和死亡的影响。
大脑和其他器官系统之间的双向通信对于大脑健康和生物体的整体健康至关重要。曾经被认为具有免疫特权的大脑现在被认为是一个高度免疫特化的器官,拥有自己的大脑驻留免疫细胞。这些细胞形成神经元回路和淋巴系统,这些系统调节免疫细胞的复杂流出,以及从脑脊髓空间与循环的其余部分交换的液体。
而共生微生物群是个体间异质性的重要来源,可以通过调节宿主免疫来影响人类健康。人们越来越认识到 CVD 的许多潜在原因,包括免疫和肠道菌群失调可能是 CVD 的致病因素,提出了对新的免疫调节治疗策略的需求。
本文总结了免疫、炎症的神经调节以及肠道菌群如何参与 CVD 的发病和进展,并探索菌群-神经免疫通讯是否为 CVD 的潜在治疗靶点。
本文缩略词:
CVD: 心血管疾病 (cardiovascular disease )
心血管疾病,又称为循环系统疾病,是一系列涉及循环系统的疾病,循环系统指人体内运送血液的器官和组织,主要包括心脏、血管(动脉、静脉、微血管),可以细分为急性和慢性,一般指心脑血管疾病。
ANS: 自主神经系统 (autonomic nervous system)
自主神经系统是脊椎动物的末梢神经系统,由躯体神经分化、发展,形成机能上独立的神经系统,是外周传出神经系统的一部分,能调节内脏和血管平滑肌、心肌和腺体的活动,又称植物性神经系统、不随意神经系统,故名自主神经系统(参考自:百度百科)。
SFO: 穹窿下器神经元 (Neurons of the subfornical organ )
穹窿下器官,室周器官,位于第三脑室前背侧壁、海马连合腹侧穹窿柱分歧处、适平室间孑L平面。
OVLT: 下丘脑终板血管区(Organum vasculosum laminae terminalis)
终板就是第三脑室前缘的隔膜。下丘脑终板血管区,内生致热原作用于血脑屏障外的脑血管区,即下丘脑终板血管区,该区位于第三脑室壁的视上隐窝处。
PVN: 下丘脑室旁核 (paraventricular nucleus)
下丘脑室旁核 位于第三脑室下丘脑部的上端两侧,呈长楔形轮廓,是下丘脑前区最显著的核团之一,与神经内分泌活动和植物性功能等有关的复合体结构,参与体内电解质与体液平衡,心血管活动调节及其它多项生理功能的调控。
NTS: 孤束核 (nucleus tractus solitarius)
孤束核为延髓内重要内脏感觉性核团,为一般内脏感觉和味觉传导通路上的第一级中继站。随着神经解剖学和神经生理学研究方法的不断发展,人们对孤束核的认识日趋深入,近年来HRP和ARG技术有关孤束核的大量的研究证实了孤束核不但与低级中枢(脊髓、脑干)具有传入、传出神经联系,而且与高位中枢(前脑、小脑)也具有复杂的往返联系。
DMV:迷走神经运动背核 (dorsal nucleus of vagus nerve)
迷走神经背核是2014年经全国科学技术名词审定委员会审定发布的人体解剖学名词。位于延髓室底灰质内,迷走神经三角深面的神经核。属一般内脏运动核,支配颈部、胸部所有内脏器官和腹腔大部分内脏器官的平滑肌、心肌的活动和腺体的分泌。
神经和免疫系统通常通过特定的大脑区域、传入和传出周围神经以及神经激素通路进行交流(下图)。
大脑和周围器官之间的通讯途径
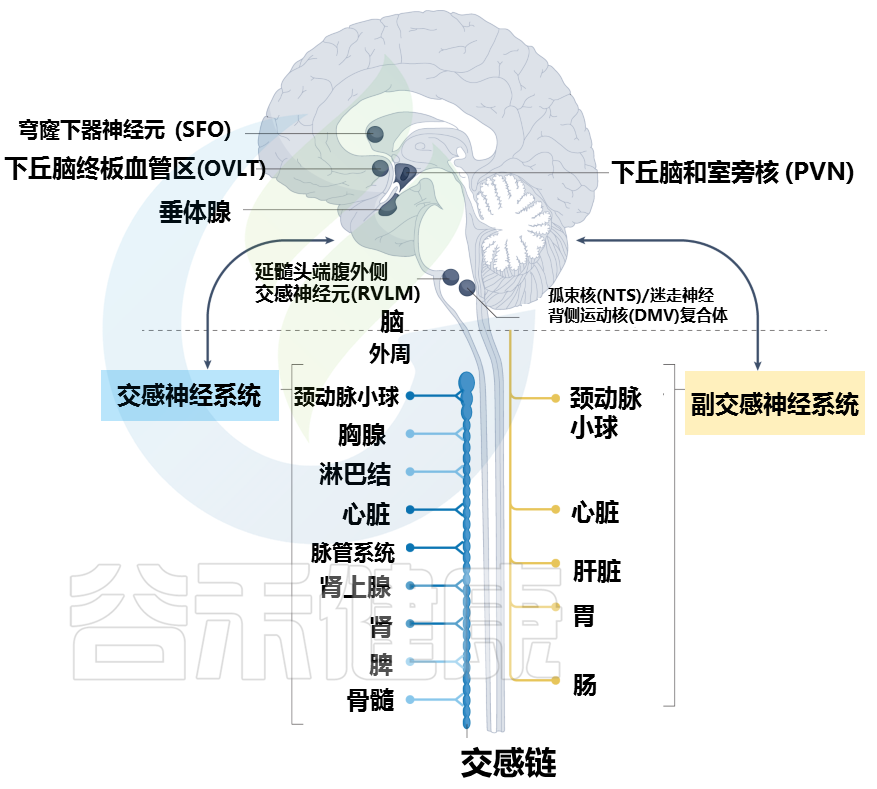
Carnevale D. Nat Rev Cardiol. 2022
大脑通过不同的途径与周围器官和组织相连。特定的大脑区域,统称为脑室周围器官,与周围形成自然的大脑界面,内衬有渗漏的血脑屏障。神经网络从脑室器官延伸到周围神经系统,并建立重要的神经解剖学连接。
穹窿下器官 (SFO) 和终板血管器官 (OVLT) 的神经元密集表达 1 型血管紧张素 II 受体和渗透压感受器,并为下丘脑的室旁核 (PVN) 提供神经支配。反过来,PVN 与延髓腹外侧 (RVLM) 的交感神经元相连,RVLM 具有调节外周交感神经活动的重要功能。
PVN 的其他神经元连接到孤束核 (NTS) 和迷走神经背运动核 (DMV) 的复合体,它们负责通过迷走神经传递的外周胆碱能神经支配。
所有主要的外周器官通常都有交感神经支配(包括心脏、脉管系统、肾脏和颈动脉体)和副交感神经支配(包括心脏、颈动脉体、肝脏、胃和肠)。
交感神经支配是免疫器官(以浅蓝色显示)和内脏组织的神经控制的主要途径。大脑、心血管系统和免疫器官之间的进一步整合轴是由神经内分泌系统通过下丘脑-垂体-肾上腺轴形成的。
循环物质,如细菌源性肽、宿主源性细胞因子和组织代谢物,向特定的大脑区域发出信号,这些区域的特点是存在渗漏的血脑屏障。
脑室周围器官由穹窿下器官(SFO)、终板血管器(OVLT)和末梢区组成,是监测周围组织并在神经免疫过程中发挥关键功能的大脑区域。同时,脑室周围器官在心血管疾病中起着至关重要的作用。
穹窿下器官富含血管紧张素II受体1型,它是肾素-血管紧张素-醛固酮系统的关键介质。
OVLT的神经元同时表达血管紧张素II受体1型和渗透压感受器,它们对感知细胞外钠/盐负荷浓度至关重要。
它们共同传递有关血容量、血压和细胞外液渗透压的外围信息。
有趣的是,从穹窿下器和OVLT投射到下丘脑室旁核(PVN)的神经元也被描述过,脑室旁核也接受后脑的投射,这表明它具有整合功能。虽然它们位于脑室周围器官之外,但孤束核(NTS)和迷走神经背侧运动核(DMV;心血管功能最有效的调节器之一)接收来自末梢区的输入。
大脑通过在脑室旁核和脊髓中间外侧细胞柱之间建立直接投射,或通过延髓头端腹外侧间接连接,来控制周围交感神经反射反应。外周的稳态扰动由延髓头端腹外侧感觉到,并通过蓝斑的去甲肾上腺素能神经元以反射反应传递。
作为补充,神经元表达细胞因子受体,这有助于神经免疫串扰和脑与身体的相互作用。
当细胞因子在各种生理和病理生理环境中的外周组织中分泌时,神经元活动就会改变。虽然神经元细胞因子受体的生理功能仍在研究中,但细胞因子在脑发育、外周组织损伤和动物行为方面的作用已被证明。这些观察表明存在由细胞因子介导的脑-体双向轴。
接下来进一步的讨论这些信号是如何在心血管疾病中启动、传播和转移到大脑的。
投射到中枢神经系统之外的神经被称为外周神经系统,它双向连接大脑和外周器官和组织。
外周神经系统分为两个部分:
躯体神经系统和自主神经系统(ANS)
躯体神经系统与中枢神经系统交换感觉和运动信息,而ANS调节非自愿功能,并在神经免疫和心血管相互作用中起决定作用。
ANS由传入和传出神经元组成,将大脑与周围内脏器官和组织连接起来。历史上,ANS被定义为平行的交感和副交感臂,分别负责所谓的“逃跑或战斗”和“休息和消化”反应。
ANS作为大脑与外周沟通的关键途径的概念不断发展,有证据表明,ANS也发挥了神经免疫调停者的作用。生理和心血管反应的改变都受到ANS的深度影响,ANS的失衡是许多心血管疾病的典型特征。
我们对ANS如何调节心血管功能的理解有了实质性的进步,这得益于实验方法的发展,使直接分析神经系统活动成为可能。
实验性和临床性的显微神经学被用来测量指向心血管系统的节后交感神经传出的电活动。例如,骨骼肌血管的显微神经造影术成为评估人类区域交感神经活动的金标准方法。
应用于动物实验的类似程序有助于确定ANS调节心血管功能的解剖路线和分子机制。在过去5年中,已经制定了直接评估调节免疫系统的ANS臂的实验方案,从而能够定义神经免疫机制如何促进心血管疾病的发病和进展。
神经系统和免疫系统之间的进一步相互作用是通过神经内分泌系统进行的,主要通过下丘脑-垂体-肾上腺轴进行调节。下丘脑-垂体-肾上腺轴通常对心理压力敏感,是免疫反应和心血管功能的有效调节剂。
神经元顺行和逆行追踪技术已被用于通过周围神经系统的传入和传出臂绘制大脑和免疫器官之间的连接(下图)。
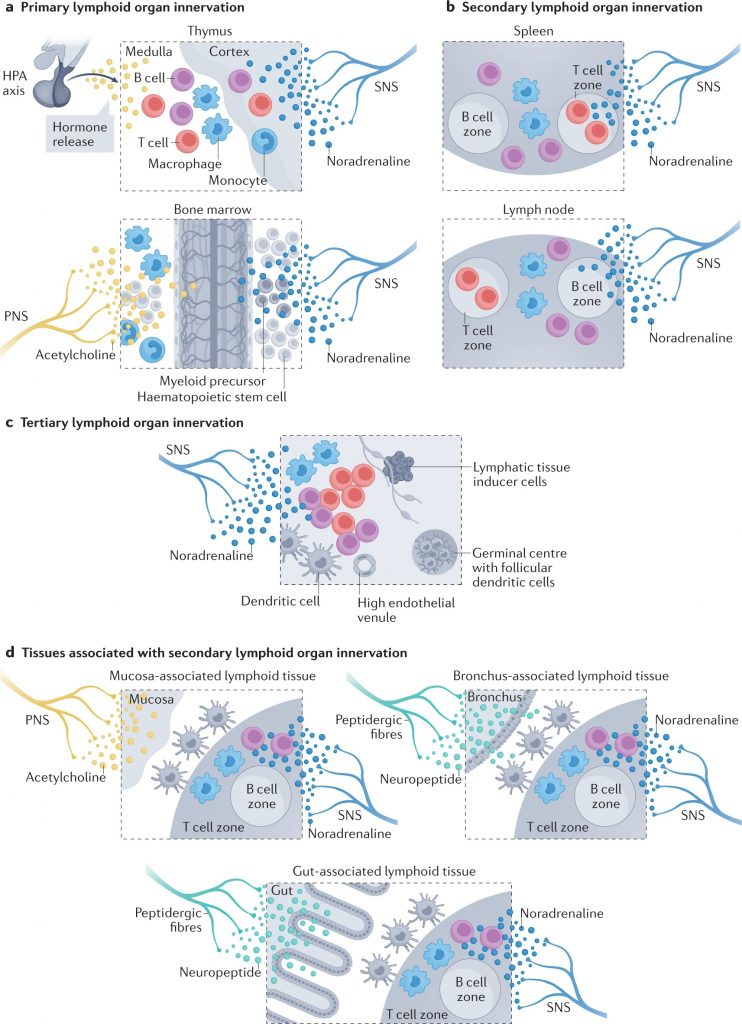

Carnevale D. Nat Rev Cardiol. 2022
a |初级淋巴器官神经支配。胸腺主要由去甲肾上腺素能纤维支配。虽然不存在直接的胆碱能神经支配,但交感神经与下丘脑-垂体-肾上腺(HPA)轴之间的相互作用已被证实。相反,骨髓神经支配更为复杂,包括交感神经系统(SNS)、副交感神经系统(PNS)和与大脑建立双向通讯的感觉纤维。骨髓的造血和免疫功能受到这种神经网络的严格调节。
b |次级淋巴器官包括脾脏和淋巴结,由去甲肾上腺素能纤维密集支配,其起源于大脑,已通过神经调节研究确定。淋巴结也有一个明显的感觉神经网络,可以严密监测外周免疫状态。
c |三级淋巴器官是为了应对非淋巴器官的病理挑战而形成的,具有独特的组织特异性组织。控制第三淋巴器官神经支配的神经纤维仅在少数解剖部位被发现。
d |粘膜相关淋巴组织在粘膜组织(如支气管或肠道)中形成,以响应稳态的扰动,并由神经网络严格控制,包括SNS、PNS和肽能感觉纤维。
神经元追踪确定外周器官神经支配路线
神经元连接性的研究需要对轴突进行双向追踪,包括从神经元细胞体到轴突终末的顺行追踪,以及从终末到胞体的逆行追踪。神经解剖学追踪是一种通过追踪神经元在突触前或突触后水平的连接来识别神经元的常用方法。神经解剖学追踪技术在确定包括免疫器官在内的外周器官的神经支配途径方面变得特别有用。
原始追踪研究的基础是将氟金注射到免疫器官中,使研究人员能够逆行识别节前神经元,或注射生物素化葡聚糖胺以顺行识别神经元连接。几十年来,这些单独使用或联合使用的示踪剂使研究人员能够研究连接大脑和周围器官的神经回路。
随后的技术进步利用伪狂犬病病毒(一种高度传染性的神经营养性α疱疹病毒,Pseudorabies virus,PRV)的能力来定义中枢神经系统中的多突触回路。病毒的逆行扩散只发生在突触相连的神经元链中。在将伪狂犬病病毒注射到感兴趣的器官或组织后,更高阶的神经系统结构在稍后的时间点被标记。通过这种方式,可以定义神经元连接的精确路径,从外周器官开始,追溯到大脑。此外,伪狂犬病病毒在神经元细胞体中复制的过程具有自我放大的能力,这使得在受感染动物的大脑中识别二级、三级甚至四级神经元成为可能。
初级免疫器官包括胸腺和骨髓,它们参与淋巴细胞的产生和初始选择。胸腺在新生儿和青春期前发育阶段活跃,逐渐退化,只有残留的淋巴细胞生成持续到成年期。骨髓包含在骨腔中,从未成熟的造血祖细胞开始产生红细胞和免疫细胞。
胸腺神经支配和神经元调节
不同类型的细胞参与胸腺器官发生,这需要神经嵴细胞的协调相互作用。基于旧追踪技术的初步研究显示,交感神经纤维错综复杂,主要释放去甲肾上腺素,并在胸腺中形成血管周围神经网络。使用经典单突触逆行和顺行示踪剂的类似方法并没有识别胸腺的副交感神经支配。
后续的研究使用伪狂犬病病毒(PRV)的逆行跨神经元多突触追踪,来确定负责交感神经流出到胸腺的中枢神经系统区域。PRV感染的神经元分布在脊髓、延髓、脑桥、下丘脑室旁核、去甲肾上腺素能细胞A5组、延髓头端腹外侧核和中缝尾侧核。
值得注意的是,PRV感染的动物在DMV中没有PRV阳性细胞核,这与之前的观察结果一致,之前的观察排除了支配该区域胸腺的迷走神经纤维的存在。
虽然连接胸腺和大脑的硬连线路径的证明来自动物研究,追踪技术是可行的,但报告显示人类存在类似的胸腺神经支配模式,为这些发现提供了转化相关性。
神经样纤维和垂体激素通过人胸腺的免疫组织进行化学鉴定。胸腺糖皮质激素通过调节儿茶酚胺释放和肾上腺素受体表达,对胸腺细胞的存活和分化以及交感神经系统功能都很重要。相反,接受肾上腺切除术的动物胸腺去甲肾上腺素水平显著降低。
典型的感觉神经肽,如P物质和降钙素基因相关肽(CGRP),已在胸腺中被发现,但没有明确的报告表明,这些神经肽可以为大脑提供感觉通路,这意味着交感神经支配可能是调节胸腺免疫功能的唯一神经通路。
骨髓神经支配和神经元调节
骨髓神经支配沿着主动脉传导,并通过血管丛穿透骨髓。实质以神经纤维树枝状排列为特征,末端靠近造血细胞和淋巴细胞。大多数纤维支配骨髓血管系统,但其他一些神经末梢支配实质性和血窦元素以调节造血和细胞迁移。
酪氨酸羟化酶是去甲肾上腺素合成的限速酶,存在于大动脉周围的所有神经中,并延伸至骨髓实质。除了主要的去甲肾上腺素能神经支配外,还确定了神经肽Y的免疫反应性,从而表明骨髓的去甲肾上腺素能神经支配和肽能神经支配是混合的。
在很久以前发表的研究中也检测到对 P 物质和 CGRP 呈阳性的神经纤维,但感觉神经元的功能直到最近才被发现。CGRP感觉纤维与去甲肾上腺素能神经一起延伸到骨髓,在那里它们与酪氨酸羟化酶神经元合作,控制造血干细胞的动员。这些发现表明大脑通过硬连接的交感神经和感觉连接控制骨髓的免疫和稳态功能。
随后的研究还发现了支配骨骼和骨髓的副交感神经纤维。尽管在造血生态位附近检测到合成乙酰胆碱的胆碱乙酰转移酶的免疫反应性,但仅在骨中发现了明显的功能性副交感神经支配,其中胆碱乙酰转移酶调节骨重塑。
后来的研究表明,骨髓神经支配与昼夜节律密切相关。骨髓中去甲肾上腺素的释放依赖于昼夜振荡,进而调节与控制白细胞和造血干细胞的保留和排出过程相关的基因表达。尽管这种构成过程在生理上是相关的,但神经介导的白细胞和造血干细胞转运的节律过程在疾病背景下可能特别重要。
未来的研究将有必要澄清清晨急性心血管事件的高发病率是否与神经调节白细胞和造血干细胞运输的影响有关。
次级淋巴器官包括淋巴结、脾脏和与粘膜相关的淋巴组织,通常由交感神经和感觉神经支配。
淋巴结神经支配和神经调节
淋巴结的结构包括血管系统和淋巴管,它们穿透髓质实质,在 T 细胞区域中被复杂的去甲肾上腺素能纤维网络缠绕。相比之下,富含B细胞的生发中心缺乏神经支配。
在稳定状态下,去甲肾上腺素的释放依赖于昼夜节律的激活,进而通过β2-肾上腺素受体信号调节淋巴细胞的生理日常再循环。
通过使用各种技术,从整体免疫标记到逆行神经元追踪、单细胞基因组学和光遗传学,研究人员发现了支配淋巴结的独特感觉神经元阵列。将腺相关病毒注射到淋巴结后,四种类型的神经元被追溯到背根神经节。对这些不同的神经元群体进行的单细胞RNA测序确定了肽能伤害感受器的密集表达,形成了与大脑的双向通讯途径,并持续监测周围免疫环境。
脾神经支配和神经调节
脾脏是最大的次级淋巴器官,监测血液传播的物质和抗原。脾脏主要由去甲肾上腺素能脾神经支配,通常通过神经信号调节免疫功能。
脾神经从腹腔神经节分支,从脾门进入脾脏,沿着脾动脉外侧走行。去甲肾上腺素能神经分布穿过边缘区,伸入白髓,在白髓中,T细胞、B细胞和树突状细胞附近可以发现神经末梢。相反,红髓的神经支配似乎稀疏而分散。通过组织学和追踪的方法,在脾脏中没有发现直接的胆碱能神经支配。
白髓,位于脾脏内部,包含着一种特殊的白细胞,这些细胞聚集在血管周围,当血液流过脾脏的时候,白髓中的淋巴细胞辨认并吞噬掉任何侵入的细菌和病毒,以此方式过滤人体血液,防止机体被病菌感染。
红髓,动物体内最大的淋巴器官。位于左上腹胃的背面,胃与膈之间,呈内侧向内凹陷的扁椭圆形或条索状等。
一项使用完整全组织3D成像的研究提供了有关脾脏神经支配的额外信息。实质内交感神经支配的结构被揭示为圆锥状结构,这在其他免疫器官中是不存在的,这表明独特的神经调节功能发生在脾脏中。
在脾脏中发现了具有独特特征的神经胶质细胞,这又增加了复杂性。自主神经支配通常包含非髓鞘神经胶质细胞。虽然神经胶质细胞在由周围神经系统支配的内脏器官中的特定功能尚未得到充分研究,但它们在免疫器官中的存在可能在神经细胞和免疫细胞之间起着中介作用,这需要进一步研究。
使用逆行示踪剂和后来的跨神经元多突触PRV追踪的研究明确证明,脾脏神经支配完全是去甲肾上腺素能的,起源于腹腔神经节。
通过对脾脏注射PRV后较长时间点的分析,确定了脑干、桥脑和下丘脑的运动前脑核团。随后,光遗传学领域出现了一种追踪神经元回路的完全创新工具,它在功能上映射直接投射到腹腔神经节的DMV胆碱能神经元。
当DMV神经元被光激活时,会诱发脾神经放电,从而直接证明腹腔迷走神经和脾神经之间的解剖联系。
粘膜相关淋巴组织神经支配
身体内的粘膜,如呼吸道和胃肠道的粘膜,有分散的粘膜淋巴组织区域,这些区域共同构成了最广泛的淋巴组织,这些区域统称为粘膜相关淋巴组织,保护机体免受各种挑战。
虽然传统的次级淋巴器官是在胚胎发生过程中发育起来的,但淋巴滤泡,如支气管相关淋巴组织或肠道相关淋巴组织,在出生后会因炎症或感染而聚集。尽管如此,这些异位淋巴组织与传统淋巴组织在结构上有许多相似之处。
粘膜相关淋巴组织的一个典型特征是广泛的神经支配。早期研究描述了支气管相关淋巴组织和肠道相关淋巴组织的交感神经和肽能神经支配,这些淋巴组织含有大量神经肽,如P物质、血管活性肠肽和生长抑素。通常情况下,神经纤维沿着小血管排列,然后在与淋巴细胞接触的粘膜组织的实质中分支,在含有T细胞的区域,神经占优势。
随后的研究通过专门检测和解码各种有害外周刺激的伤害感受器,确定了粘膜相关淋巴组织神经支配的感觉通路。
支配肠道相关淋巴组织的伤害感受器感知胃肠道的扰动,并建立具有保护功能的神经反射。虽然肠道相关淋巴组织的感觉神经支配在抵御微生物方面的作用越来越明显,但对心血管疾病中肠道神经系统的影响仍不清楚。
支气管相关淋巴组织的神经支配作用研究较少,但交感神经、胆碱能神经和感觉神经纤维已被确定。
三级淋巴样器官是指在成年期由淋巴样新生在随机、典型的非淋巴样和非粘膜部位形成的淋巴样组织,以应对慢性炎症。这些组织在自身免疫性疾病、微生物感染、慢性同种异体移植排斥反应、癌症甚至动脉粥样硬化中都被观察到。
在几种转基因小鼠模型中诱导第三淋巴器官,可以表征炎症细胞因子和淋巴趋化因子的模式,这些细胞因子和趋化因子是其发育和调节所必需的。
虽然已经描述了三级淋巴器官的形态、细胞和血管成分,与第二淋巴器官(如B细胞和T细胞室的独特组织、含有滤泡树突状细胞的B细胞滤泡和生发中心)有相当大的相似性,他们在疾病进展中的参与是有争议的,并且仍然是研究的主题。
例如,在微生物感染期间,三级淋巴样器官会在局部保留病原体,从而阻碍它们进入生物体的其他部位。相反,自身免疫性疾病的进展可能因同时存在三级淋巴器官而加剧。通过选择性地去神经支配肠道交感神经或胆碱能神经,迷走神经在三级淋巴器官形成中的重要作用已在实验性结肠炎中得到证实。目前还尚不清楚ANS是否有助于其他器官中第三淋巴器官的发育、组织和功能。
神经免疫相互作用是对挑战体内平衡的应激源做出快速反应的基本适应机制。这一概念首次出现时,脾脏神经支配在细菌内毒素血症(对身体最危险的疾病之一)期间被观察到具有保护功能。
去甲肾上腺素能纤维和淋巴细胞之间的直接神经免疫相互作用被描述,同时确定在脾脏中引起去甲肾上腺素能放电的神经回路,该回路在抑制脂多糖诱导的细胞因子负荷和对抗感染性休克方面有效。
神经免疫相互作用已被确定为心血管危险因素和心血管疾病病理生理学的潜在机制。
神经免疫相互作用促进心血管危险因素的发生及进展
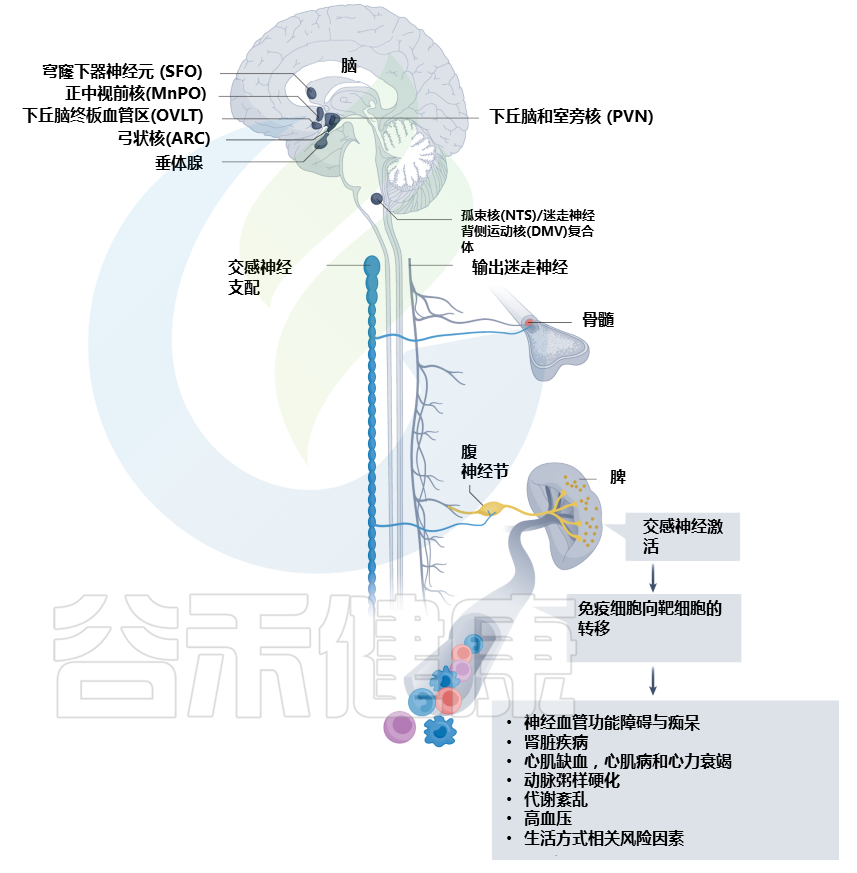
Carnevale D. Nat Rev Cardiol. 2022
大脑中的环室器官被心血管系统的挑战激活。通过一系列中枢和周围神经系统的解剖连接,大脑在免疫器官中建立神经反射来控制和调节免疫功能。心血管危险因素,如高血压、代谢紊乱和动脉粥样硬化,是常见的神经免疫机制改变的基础。心血管疾病,例如心肌缺血、压力过载心肌病、心力衰竭、肾脏疾病和神经血管功能障碍,其特征在于受影响的心血管组织中局部和免疫器官中的神经免疫改变。ARC,弓状核;DMV,迷走神经背运动核;MnPO,正中视前核;NTS,孤束核;OVLT, 终板的血管器官;PVN,下丘脑室旁核;SFO,穹窿下器官。
高血压
与高血压相关的炎症和免疫反应最早出现在20世纪70年代。然而,这些过程大多被认为是高血压导致靶器官损害的结果。
免疫系统在高血压中的机制作用的第一个证据,来自缺乏 T 细胞和 B 细胞且典型的高血压刺激不会增加血压的Rag1 -/-小鼠的研究。通过过继转移重建Rag1 -/-小鼠中的 B 细胞或 T 细胞池,这项研究表明,血管紧张素II或脱氧皮质酮醋酸盐(DOCA)仅在小鼠具有成熟 T 细胞时才会诱发高血压。
随后大量研究调查了特定的T细胞亚群是否对高血压的发展至关重要,发现血管紧张素II给药不会增加Cd8 -/-小鼠的血压,但会增加Cd4 -/-小鼠的血压。免疫系统在血压升高中所起作用的细胞和分子机制仍有待研究。
与血压稳态有关的基本生理变量,如血管张力和肾脏钠排泄,依赖于严格的神经控制。因此,神经调节系统、免疫器官和心血管功能之间建立的关系值得研究。
重要的研究揭示了大脑和免疫系统之间的联系可能对高血压至关重要。首先,在动物模型中,脑室内注射血管紧张素II可通过交感神经系统诱导外周细胞因子的释放。此外,选择性的脑室周围器官损伤阻碍了小鼠对血管紧张素II的典型血压升高反应。
有趣的是,脑室周围器官受损的小鼠无法激发T细胞并促进T细胞在血管系统中的浸润,这表明高血压患者的神经系统和免疫系统之间存在关系。
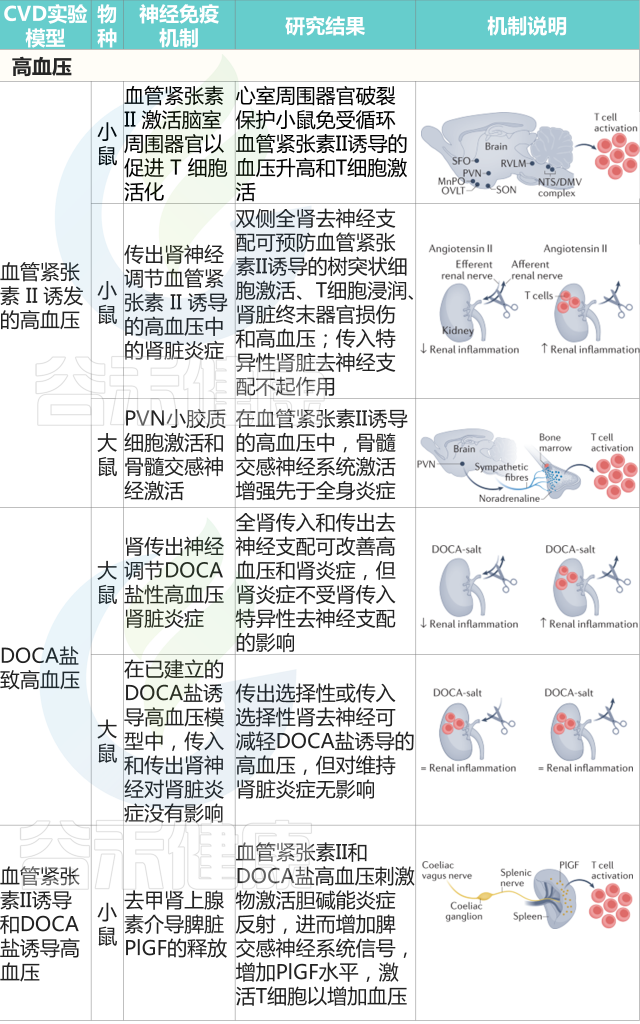

Carnevale D. Nat Rev Cardiol. 2022
高血压患者免疫系统的直接神经控制随后被证实。利用小鼠脾神经的显微神经学检查,血管紧张素II和DOCA盐均能增加神经放电,促进脾脏中去甲肾上腺素的释放。选择性脾脏去神经可防止血压升高以应对任何一种高血压刺激,脾切除术也重现了这一效应。
逆行追踪法,加上在测量脾神经放电时进行的选择性去神经手术,阐明了腹腔迷走神经输出是由高血压刺激激活的节前神经元。
在分子水平上,脾脏中的去甲肾上腺素释放是促进胎盘生长因子激活所必需的,胎盘生长因子是一种血管内皮生长因子家族的血管生成生长因子,也具有对血压升高至关重要的免疫调节功能。
高血压患者的神经免疫另一个相互作用的水平被称为双向脑-骨髓轴,即骨髓中交感神经流出增加先于全身炎症。
有关高血压患者肠道失调的证据正在迅速积累,来自小肠的激活免疫细胞已被证明与血压升高和大脑靶器官损伤有关。目前还不清楚是否存在相反的途径,即神经信号控制与高血压发病和进展相关的肠道和免疫机制。
动脉粥样硬化
脂质在动脉壁的积聚是动脉粥样硬化的一个典型特征,并伴随着免疫细胞的进行性浸润,导致斑块的形成。这一过程以慢性低度炎症为特征,逐渐增加动脉粥样硬化斑块的大小并导致动脉阻塞。
尽管有很多工作研究了导致斑块形成和决定斑块稳定性的机制,但神经免疫通讯的潜在作用才刚刚开始研究。
动脉粥样硬化斑块没有神经支配,但在斑块形成和进展过程中调节免疫反应的神经线索已被确定。Netrin 1首先被确定为指导轴突生长锥的神经信号,在人和小鼠动脉粥样硬化动脉的巨噬细胞中也发现了Netrin 1,它通过趋化因子驱动的迁移过程抑制巨噬细胞的排出。
巨噬细胞中的Ntn1缺失阻碍了小鼠的动脉粥样硬化过程,促进巨噬细胞从斑块中流出。
另一种蛋白质通常存在于神经元中,与胆碱能途径有关,可调节高胆固醇血症Ldlr–/–小鼠的动脉粥样硬化过程。在骨髓来源的细胞中,编码α7烟碱型乙酰胆碱受体(α7-nAChR)的Chrna7被切除会恶化小鼠动脉粥样硬化的进展。值得注意的是,人类动脉粥样硬化病变的特征是存在α7-nAChR+免疫细胞,表明该受体的通用相关性。
对受动脉粥样硬化影响的动脉周围三级淋巴器官的鉴定表明,神经机制可能与这些淋巴聚集相互作用,以控制和/或调节动脉粥样硬化疾病的进展。
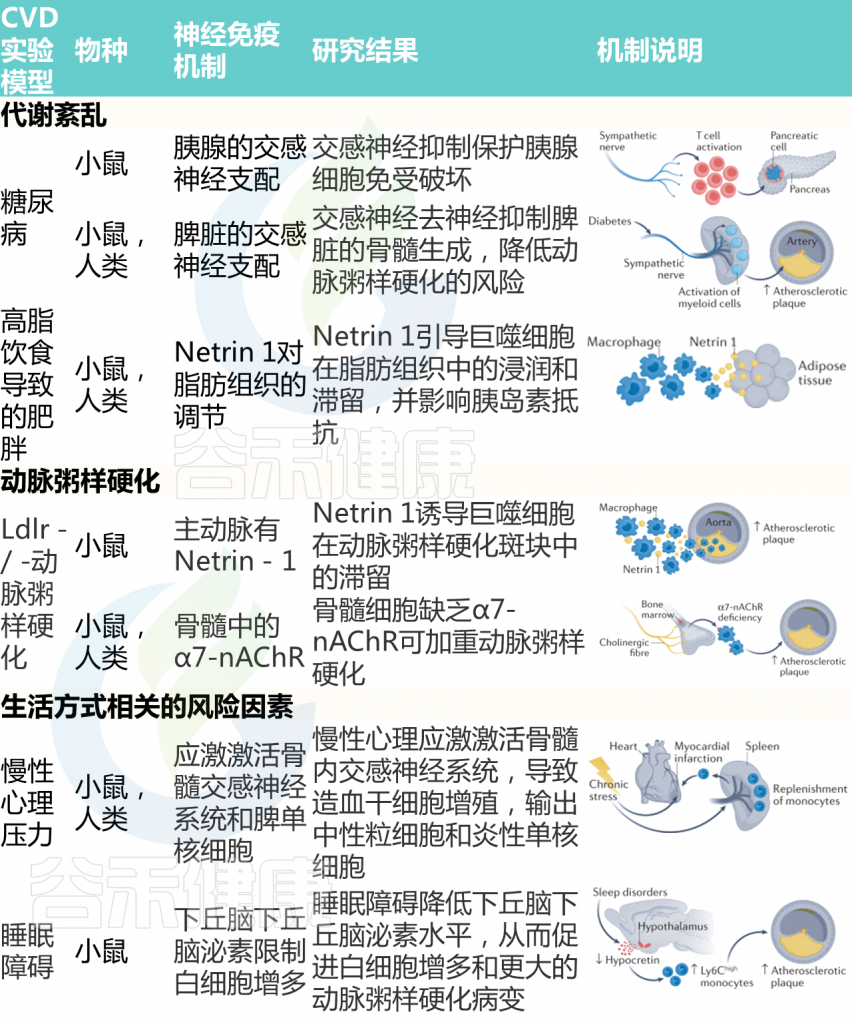

Carnevale D. Nat Rev Cardiol. 2022
代谢紊乱和肥胖
代谢综合征通常指可能单独或合并发生的一系列疾病,总体上增加了CVD的风险。除了血压升高,通常还包括高血糖和肥胖。
已知ANS失衡和免疫系统激活是代谢综合征的特征。在小鼠中发现了自身免疫性糖尿病的神经免疫机制。由CD8+T细胞介导的对胰腺β细胞的攻击诱导,糖尿病的发病取决于完整的胰腺神经支配的存在。
事实上,6-羟基多巴胺的化学消融或去甲肾上腺素能胰腺纤维的手术去神经支配阻碍了这些小鼠糖尿病的发病。在分子水平上,这种效应是由α1-肾上腺素能受体信号诱导的,因为使用哌唑嗪而不是普萘洛尔可以重现胰腺去神经支配的保护作用。
神经信号还可以控制与高脂饮食诱发的肥胖相关的糖尿病。患有肥胖症的小鼠和人类的脂肪组织被免疫细胞密集浸润,这些细胞导致脂肪组织炎症和胰岛素抵抗。
值得注意的是,脂肪组织中存在神经免疫指导线索netrin 1,这表明netrin 1可能调节巨噬细胞向脂肪组织的动员。此外,选择性缺失小鼠造血细胞中的Ntn1可有效促进巨噬细胞从脂肪组织中排出,减少炎症,并改善胰岛素敏感性。
这些发现确定了靶组织中的神经免疫相互作用,但免疫器官的神经控制也参与了疾病相关炎症状态的系统调节。例如,由脾交感神经驱动的神经通路已被确定为糖尿病的关键。通过手术或使用6-羟基多巴胺实现的选择性脾脏去神经支配,阻碍了糖尿病小鼠的过度脾脏骨髓生成。
一种连接大脑和脂肪组织的新型神经免疫途径已经被描述。在小鼠的脂肪间充质细胞附近发现了交感神经,交感神经控制着一个特定免疫细胞亚群的活动:2型固有淋巴细胞。
反过来,2型固有淋巴细胞通过释放神经营养因子来调节脂肪组织的稳态和肥胖。重要的是,通过在小鼠身上使用逆行追踪技术,结合外科手术和化学遗传学操作,定义了一个新的神经回路,通过交感主动脉-肾回路将脂肪组织中的2型固有淋巴细胞连接到高阶脑区,如室旁核。未来的研究应该调查这种新发现的神经免疫回路是否与肥胖和胰岛素抵抗的心血管并发症有关。
生活方式相关的危险因素
众所周知,生活方式相关的风险因素对CVD的发病率有着深远的影响,同时也对免疫系统构成挑战。此外,心理或身体上的应激状态与ANS的紊乱有关。对生活方式相关风险因素对心血管系统有害影响的潜在相关神经免疫相互作用的研究可以揭示创新的治疗机会。
正如在人类身上经常观察到的那样,慢性应激状态会增加小鼠的血压。值得注意的是,Rag1–/–小鼠对应激诱导的高血压具有抵抗力,并能减轻靶器官损伤。
除了血压升高,慢性应激还会增加动脉粥样硬化和心肌梗死的易感性。经过反复和各种应激性挑战的小鼠显示出造血干细胞增殖增加,导致产生高水平的促进疾病的炎性白细胞。这种效应是由骨髓交感神经纤维释放的去甲肾上腺素增加介导的,而去甲肾上腺素又反过来调节造血干细胞增殖、中性粒细胞和炎性单核细胞的排出。
睡眠障碍对心血管健康构成了重大挑战。小鼠正常睡眠节律的改变会增加动脉粥样硬化,与过度造血和促炎性单核细胞积聚有关。
在分子水平上,研究发现,睡眠碎片化可下调小鼠130的下视黄醇水平。下视黄醇是一种下丘脑神经激素,在控制睡眠、觉醒和觉醒方面具有重要功能。鉴于下视黄醇通过减少巨噬细胞集落刺激因子1的产生来限制骨髓生成,睡眠不良引起的下视黄醇水平降低与白细胞增多有关。
流行病学数据显示,健康的生活方式,如定期的体育活动,可以降低患CVD的风险。尽管许多观察分析都支持这种关联,但很少有机制研究调查这种有益关系的根本原因。有趣的是,习惯性自愿性跑步会降低小鼠的造血活动。在动脉粥样硬化小鼠中,运动抑制了慢性白细胞增多,但不影响紧急造血。通过降低脂肪-瘦素水平,这种效应促进造血生态位静止,改善心血管炎症和预后。
心肌缺血、心肌病和心力衰竭
ANS通过控制血管张力和各种心肌细胞特性,如收缩力、传导和频率,调节心脏功能。交感神经流出增加是慢性心力衰竭不良后果的最强预测因子之一。此外,非心肌细胞,尤其是常驻和非常驻免疫细胞,在应对各种挑战的心脏重塑中起着至关重要的作用。神经、免疫和心脏机制之间的相互作用值得研究。
急性缺血性心脏损伤通过增加骨髓中的交感神经信号与脾髓样细胞的生成增加有关。从脾脏部署的一部分单核细胞积聚在缺血心肌中,并参与心脏重塑。心-脾轴也被发现参与慢性心肌缺血的长期免疫反应,这总体上有助于不良的心脏重塑。脾脏的神经控制是否与这些表型有关仍有待阐明。
慢性高血压和肾功能衰竭会对心肌造成压力或容量过载,如果没有得到充分补偿,最终会导致心力衰竭。
在舒张功能不全的小鼠中,由于单核细胞募集和骨髓和脾脏造血增加,心脏巨噬细胞的数量增加。当巨噬细胞进入心肌时,会产生促纤维化细胞因子IL-10,进而促进胶原沉积和心肌僵硬,进一步加重舒张功能损害。
然而,其他巨噬细胞群体可以通过依赖于多器官相互作用的机制,促进慢性压力超负荷的适应性重塑。受到横向主动脉收缩以诱导心脏压力超负荷的小鼠增加了肾交感神经流出,由此去甲肾上腺素刺激粒细胞-巨噬细胞集落刺激因子的分泌,并对心脏巨噬细胞产生旁分泌作用。这项研究表明,心肌对慢性压力超负荷的适应取决于肾脏和心脏的神经和免疫反应之间的整合。
随后的研究阐明,心肌在稳定状态下含有大量不同的免疫细胞,对挑战的反应取决于常驻和招募的免疫细胞群体之间的整合。
鉴于ANS通过从颈上神经节、星状神经节和胸上神经节分支的纤维直接支配心肌,可以想象,参与心脏重塑的免疫反应的神经调节可能发生在心脏局部。
值得注意的是,尽管颈上神经节的去神经支配对心肌缺血引起的急性心脏重构没有影响,但从长远来看,这一过程减少了炎症浸润,减轻了心力衰竭。
肾脏疾病
肾钠处理、肾素分泌和肾血管张力受ANS的严格调节。肾传入和传出神经支配构成了最广为人知和研究最广泛的心血管反射系统之一。此外,炎症和免疫浸润通常伴随肾脏疾病。
急性肾损伤或慢性肾脏疾病均可导致肾功能衰竭,总的来说会增加心血管疾病的风险。促炎症环境和ANS平衡改变是肾病的特征,但神经系统和免疫系统之间的相互作用才刚刚开始澄清。
已经证实神经免疫调节在急性缺血再灌注反应中对肾损伤的重要作用。当用能引起胆碱能炎症反射的胆碱能激动剂进行预处理时,患有双侧肾缺血-再灌注或细菌内毒素血症的啮齿类动物对肾损伤的敏感性较低,这意味着神经反射调节由不同原因引起的肾损伤引起的炎症过程。
鉴于在类似的肾缺血再灌注损伤小鼠模型中,通过超声激活胆碱能炎症反射通过抑制炎症减轻了结构和功能损伤,该发现具有转化相关性。
2021发表的一项研究确定在小鼠急性肾损伤期间连接肾脏、大脑和脾脏的神经通路。通过光遗传学,迷走神经的传出或传入纤维被选择性地刺激,表明两者都对肾脏损伤有保护作用。通过激活传入的顺行感觉纤维,可以描绘出从肾脏追溯到延髓头端腹外侧的神经回路,以补充迷走神经-脾反射。
肾脏也是高血压损害的主要目标,这是心血管疾病不良后果的一个强有力的独立风险因素。浸润肾脏的活化免疫细胞和ANS失衡是高血压性慢性肾病的特征。
在动物模型中,肾脏去神经支配可有效对抗过度的肾交感神经流出和血压升高,并抑制T细胞聚集和由此引起的炎症反应、肾纤维化和蛋白尿。
在分析传入和传出肾神经支配的差异贡献时,在DOCA盐大鼠中,传入特异性肾去神经支配降低动脉血压和交感神经活动的程度与总(传入+传出)肾去神经支配的程度相同,但对血管紧张素II诱导的高血压没有影响。
有趣的是,在随后的一项研究中,同样的研究人员对已建立高血压和肾炎症的DOCA盐大鼠进行了传入特异性或全肾去神经支配。在这些动物中,虽然传入特异性和全肾去神经支配在降低血压方面仍然轻微有效,但两种治疗均未显着改变已确立的肾脏炎症。
总之,这些研究表明,肾神经(传入神经和传出神经)和炎症在高血压和肾脏炎症的发病机制中存在密切联系,但是,在确定高血压后,去肾神经支配不是抑制炎症过程的有效治疗,是通过其他机制维持的。
内脏器官炎症由ANS调节的观察可以追溯到之前研究肾传入和传出神经支配的作用。
一项初步研究表明,肾脏去神经支配可有效预防大鼠实验性肾小球肾炎,从而减少蛋白尿、系膜血管溶解、肾小球胶原沉积和转化生长因子-β的表达。这些数据表明,来自肾脏神经输入的信号分子可能在各种疾病环境下引发肾脏炎症和纤维化,进一步导致终末器官肾损伤。
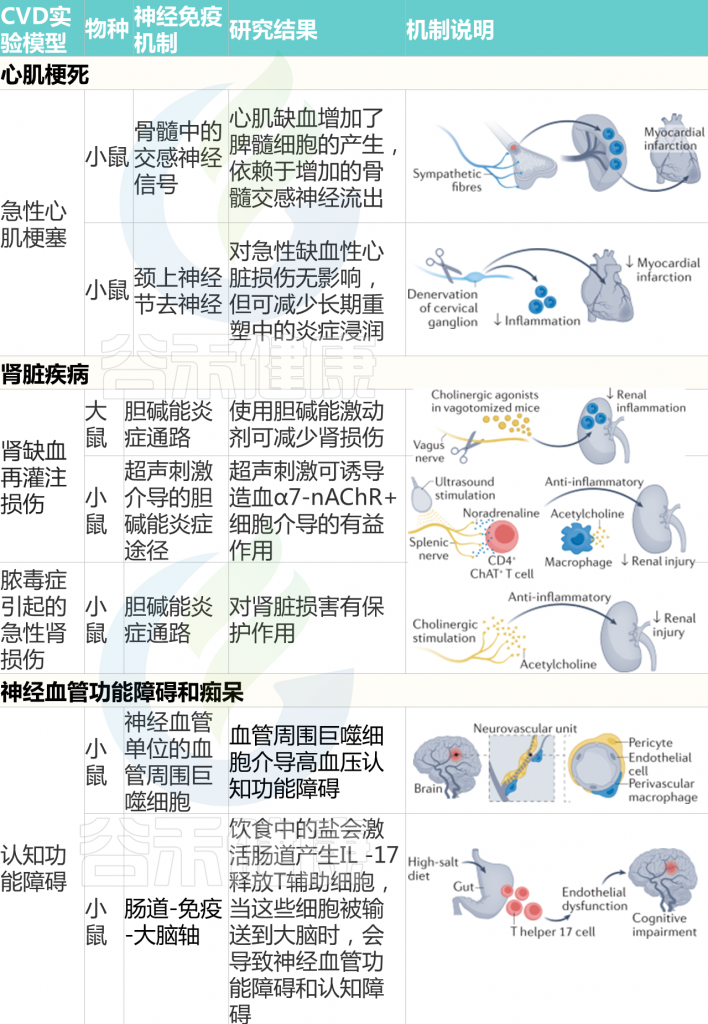

Carnevale D. Nat Rev Cardiol. 2022
神经血管功能障碍和痴呆
大脑由于没有能量储备,一直依赖于通过循环提供的营养,必须根据动态区域激活来适应其需求。因此,大脑对循环系统的改变特别敏感。
多种细胞类型构成脑实质和血管周围组织,包括免疫细胞。正如在其他器官和组织中观察到的那样,大脑中含有常驻免疫细胞(主要是小胶质细胞和血管周围巨噬细胞),当挑战干扰血脑屏障通透性时,这些细胞可以与招募的免疫细胞相互作用。
心血管风险因素会影响血脑屏障的完整性,改变脑血管内稳态,增加患痴呆症的风险。在小鼠和人类中,高血压会导致进行性脑血管损伤,并伴有典型的认知障碍症状。
免疫系统在高血压发病中的作用已得到明确证明,但免疫细胞如何参与高血压诱导的脑损伤才刚刚开始研究。
血管紧张素II诱导的高血压小鼠脑血管周围巨噬细胞的耗竭抵消了血管氧化应激和神经血管损伤,表明免疫的关键作用。
相反,在小鼠中,募集的免疫细胞会导致由血管危险因素(例如过度盐摄入)引起的脑损伤。脑血流、内皮功能和认知能力的损害取决于T淋巴细胞产生的IL-17,而IL-17是通过摄入肠道中的盐激活的。随后的一项研究还阐明了辅助性T淋巴细胞17对大脑有害影响的机制,表明肠道免疫轴对神经的调节非常关键。
外周神经系统的解剖结构和组织结构对轴突亚群的选择性和精确治疗提出了挑战,轴突亚群在特定器官中发挥独特的调节功能。因此,研究人员试图开发出越来越复杂的电极,以刺激更靠近目标组织的较小神经。这种方法有助于获得有关生理学和疾病中免疫神经调节的病理生理学基础的信息。
值得注意的是,靶向脾神经并直接测量其活性的技术的发展,使我们能够确定该免疫器官是神经系统和心血管系统之间串扰的中枢介质。相反,选择性去神经提供了有关该通路在CVD发病和进展中的相关性的机制信息。
研究表明,ANS调节免疫功能的功能障碍是心血管风险和CVD进展的重要组成部分。免疫器官自主神经外流的靶向调节是将这些发现转化为患者治疗的一种可能性。
值得注意的是,神经免疫通讯的机制研究被认为与一系列临床条件有关,如克罗恩病、类风湿性关节炎和原发性干燥综合征,所有这些都涉及免疫和炎症过程的失调。在临床前模型以及随后的炎症和自身免疫性疾病的人类临床试验中进行了探索,以非侵入性方式针对神经免疫机制的可能性也可能成为CVD的一种可能性。
对心血管疾病中调节免疫反应的神经通路的分子和电生理成分的临床前和临床研究为创新疗法提供了理论基础。能够对涉及心血管疾病的神经免疫反射进行精细调节的工具将有助于设计针对组织靶向免疫调节作用的策略,而不会增加感染风险或导致其他不良反应的普遍免疫抑制。根据特定疾病的特定背景和炎症环境,可以通过设计对腹腔迷走神经传出神经的生物电子刺激的选择性模式来微调脾脏的迷走交感神经激活。迄今为止,只有临床前工具已被开发并证明可有效调节免疫细胞从脾脏排出的过程。相反,通过手术切除腹腔神经节或热消融脾动脉周围的交感神经纤维,可以减弱脾交感神经流出的过度激活。
到目前为止,迷走神经刺激的研究主要集中在使用颈部植入装置,这些装置会触发传出和传入神经通路的混合,并产生潜在的不良影响。因此,尽管在自身免疫性疾病的临床试验中取得了有希望的结果,但迷走神经刺激方案具有引起脱靶刺激的局限性。
为了克服这一缺点,已经实施了改进的实验性迷走神经刺激方案,以选择性地刺激腹腔传出迷走神经并诱发脾神经流出。有趣的是,一系列研究提供了交感神经介导的脾神经控制的证据。特别是,通过腹腔神经节与脾神经相连的内脏神经已被证明可调节脾介导的炎症反应。具体作用是整合的还是单独作用的,取决于具体的病理生理学背景。
对腹腔迷走神经刺激后的脾脏免疫细胞的分析显示,特定的生物电子调节模式促进选择性T细胞亚型的排出,这表明可能会发展出靶向免疫调节。
使用活体和离体制剂对小鼠、大鼠、猪和人脾神经进行神经解剖学和功能比较,表明将临床前发现转化为临床相关工具的可行性。然而,尽管这种方法需要在实验模型中进行进一步研究,以揭示CVD中神经免疫通讯的病理生理学基础,但临床应用可能会受到该过程侵入性的限制。
肠道微生物群决定下丘脑-垂体系统的激活水平。特别是,肠道微生物群是心血管疾病发病机制中神经免疫介质的重要来源。
心肌缺血、心肌病和心力衰竭
与 CVD 相关的压力通过激活 ANS 的交感神经分裂来影响整个生物体,包括胃肠道。在 ANS 的影响下,肠道内微生物群的血液供应减少,从而降低了消化腺的活动,胃肠道的肠道蠕动减慢。上述机制决定了由于 CVD 相关应激导致的肠上皮细胞的进一步紊乱。
CVD相关应激期间肠道上皮损伤的机制

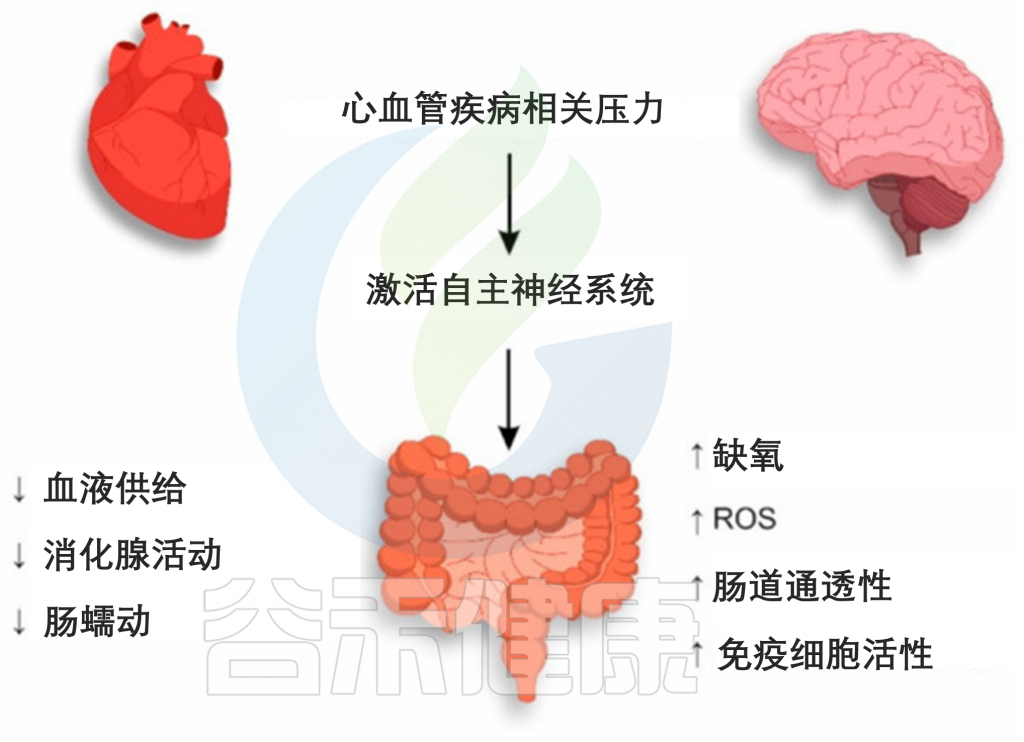
Suslov, Andrey V,, et al. J Clin Med. 2021
肠壁由肾上腺素能交感神经纤维支配,在刺激期间增加水和钠的吸收,伴随着肠道通透性的增加。同时,在大肠迷走神经的影响下,肠上皮杯状细胞产生的粘液减少。
值得注意的是,一方面,粘液为肠道上皮细胞提供保护,使其免受共生体及其代谢产物的影响,另一方面,粘液阻止免疫细胞的过早激活。因此,粘液层的减少和肠壁通透性的增加可导致肠道细菌的紊乱和肠上皮细胞的空间分离。
在Wistar大鼠中显示,出生后早期有限的筑巢压力会导致高皮质类固醇激素血症,增加肠道通透性,减少粪便微生物多样性,导致肠道微生物群组成失衡。肠道血供减少不仅是由于ANS交感分裂的影响,也是由于CVD的致病影响。
几项研究表明,肠道供血衰竭伴随着多种类型的CVD:心肌梗死、严重动脉粥样硬化、慢性心力衰竭、糖尿病和肥胖。因此,CVD期间肠道内的血供衰竭是由多种机制同时决定的。
肠血供减少伴有组织缺氧,而肠粘膜对缺氧最为敏感。
肠粘膜是一种支持粘液层以及微生物群与上皮下组织空间分离的解剖结构。在缺氧期间,有氧和无氧分解代谢循环中的葡萄糖转化会在中间阶段损害能量的生物合成。这导致活性氧(ROS)的释放。
由于活化免疫细胞的积累和 ROS 的产生,再灌注会增加缺血性损伤的破坏性影响。活性氧对蛋白质、脂质、碳水化合物和核酸具有高反应性,导致肠上皮完整性受损。至于肠道菌群与缺血性肠道损伤之间的关系,在大鼠模型中显示,肠道缺血-再灌注损伤导致肠道菌群发生显著变化,大肠杆菌和口腔普氏杆菌数量增加,随后在愈合阶段乳酸杆菌数量增加。
同时,在急性心肌梗死大鼠模型中证明,肠道微生物群的改变会导致肠道炎症和细胞凋亡的发展,也就是说,肠道缺血不仅会导致肠道微生物群失衡,反之亦然,肠道微生物群的变化会导致肠道损伤。
除粘液层外,肠上皮层在提供肠屏障功能方面也起着重要作用。肠上皮层由与紧密连接蛋白连接的上皮细胞组成,特别是紧密连接蛋白、封闭蛋白、钙粘蛋白和粘附分子。
紧密连接蛋白作为肠-脑轴结构中肠屏障的重要元素。研究表明,脑肠肽ghrelin可以减轻动物模型脑出血后激活紧密连接蛋白 zonula occludens-1 和 claudin-5 的肠道屏障功能障碍。
一些研究通过改变紧密连接蛋白证明了肠道微生物组变化与肠道屏障损伤的关系。例如,植物乳杆菌增强上皮屏障刺激基因的表达,这些基因参与紧密连接zonula occludens-1、zonula occludens-2 和 occludin 的信号通路。
在小鼠模型的另一项研究中也证明了相同的效果,其中用乳酸杆菌、双歧杆菌和链球菌的混合物治疗增加了紧密连接 zonula occludens-1 和紧密蛋白的表达。紧密连接完整性的改变可导致与代谢宿主状态受损相关的细菌或细菌代谢物的流入增加,表现为心脏代谢疾病。
肠上皮和粘液屏障位于肠道环境、肠道细菌和免疫系统之间。
众所周知,肠上皮层包括不同类型的细胞:
肠细胞
杯状细胞
肠内分泌细胞
潘氏细胞
簇状细胞
M细胞
以及多种专业免疫细胞,如
淋巴细胞
树突状细胞
巨噬细胞
均位于肠粘膜表面附近
上皮内淋巴细胞是第一个对致病因素做出反应的免疫细胞,它侵入上皮并传播树突以检测肠腔抗原。
其他细胞位于有组织的淋巴结构中,如派尔斑和隐斑,或分散在固有层内。
与巨噬细胞和树突状细胞等专业免疫细胞类似,肠上皮细胞表达先天免疫受体,如模式识别受体,包括 Toll 样受体 (TLR) 和核苷酸结合蛋白,含有寡聚化结构域 (NOD)。
潘氏细胞合成抗菌分子受 TLR4/MyD88 和 NOD2 信号传递的调节,这些信号传递受肠道微生物的控制。
TLR 通过激活促炎信号通路以响应微生物抗原,在先天免疫系统中发挥着重要作用。
肠道免疫细胞通过细胞因子或直接的细胞连接支持肠道黏膜的屏障功能。因此,由 Th17 细胞或 3 型先天性淋巴细胞 (ILC3) 产生的 IL-17 和 IL-22 会增加肠上皮细胞分泌的 AMP 和 Reg3 家族蛋白 。
此外,上皮内淋巴细胞产生的 IL-6 可增强肠上皮细胞增殖并促进损伤后黏膜的修复。然而,其他促炎细胞因子,如 TNF-α 和 IFN-γ,通过抑制 β-连环蛋白/T 细胞因子 (TCF) 信号传递来抑制上皮细胞增殖 。
肠上皮细胞还通过分泌细胞因子和趋化因子来调节宿主免疫反应。
在用革兰氏阴性细菌大肠杆菌和变形杆菌的鞭毛蛋白刺激肠内皮期间,TLR5 / MyD88 信号促进 IL-8 的产生,IL-8 将中性粒细胞募集到固有层中。
前面CVD中提到的胆囊收缩素、胰高血糖素样肽 (GLP) 和血清素由肠道内分泌细胞分泌,影响肠道免疫系统的活动。
胆囊收缩素通过 CD4+ 细胞和 B 细胞调节细胞因子的分化和产生。值得注意的是,交感神经系统调节的消化腺活性的降低间接影响免疫细胞的活性。
有趣的是,微生物群对上皮肠屏障的影响不仅取决于免疫成分,还取决于其他影响。特别是,由肠道微生物群合成的短链脂肪酸被用作上皮细胞的能量来源,并间接增强上皮屏障。微生物代谢产物吲哚通过激活孕烷-X 受体具有防御屏障作用,并增加胰高血糖素样肽-1 的分泌。
无法保存肠上皮的复杂解剖和功能特征会降低上皮屏障的抗菌、免疫调节和再生能力。粘膜的破坏导致共生细菌及其代谢物从肠腔转移到上皮下组织,导致促炎细胞因子的分泌。反过来,这会导致器官功能障碍,并伴有肠粘膜炎症。
现在越来越多的证据表明,肠道细菌的代谢物在炎症过程中通过被破坏的肠道屏障进入循环。
微生物组介导疾病的三个因素:
首先,肠道细菌的代谢物是慢性免疫反应的永久激活剂,会在肠道以及整个生物体中引起持续性炎症。
其次,先天免疫系统成熟期肠道微生态失调导致免疫耐受性受损,随后表现为自身免疫和自身炎症性疾病。
第三,微生物组可以影响控制肠道远处组织特异性免疫的免疫因素。
考虑到肠道微生物群在神经免疫网络形成中的作用。脑源性神经营养因子 (BDNF) 是一种应激蛋白,是神经营养因子家族的成员,可增加大脑中神经元对功能障碍的抵抗力,并提供神经系统的可塑性。
BDNF 控制了广泛的过程,包括微生物群-肠-脑轴参与心脏代谢疾病的发病机制。研究表明,BDNF 信号可能介导间歇性禁食对血糖调节和心血管功能的影响 。此外,研究表明,用高剂量益生菌治疗可以调节斑马鱼的行为,导致一些大脑相关基因的表达发生显着变化,例如 BDNF。因此,BDNF 可能代表了微生物-肠-脑轴的分子机制。
神经免疫轴:微生物群-肠-脑-CVD
肠道粘液膜的缺氧损伤、微生物群转移到上皮下组织、肠上皮屏障功能的破坏、肠道细菌代谢产物和炎症细胞因子的合成使肠道成为最大的内毒素源。炎症介质通过全身血液和淋巴循环到达神经系统中心。
血脑屏障
血脑屏障 (BBB) 在妊娠期间形成,充当大脑和血液循环系统之间的选择性过滤器。肠道微生物群和微生物代谢物在血脑屏障形成中的重要性已在不可知菌小鼠身上得到证实。在没有肠道微生物的情况下,与正常动物的血脑屏障相比,小鼠的血脑屏障变得具有渗透性。
研究发现,大脑的淋巴系统流入脑脊液,进入蛛网膜下腔,并进一步进入颈深淋巴结。脂质的溶解度、蛋白质的三级结构、浓度、分子质量和化合物的电荷决定了介质从外周血供应和淋巴系统到大脑的通道。
外周血中的细胞因子主要是亲水性的,可以调节神经系统的免疫功能。研究还表明,静脉注射吲哚(类似于色氨酸的细菌代谢产物)可以克服BBB。
LPS(脂多糖)的神经炎症效应通过外周组织中的TLR激活发挥作用,通过血脑屏障阳性的促炎细胞因子在神经系统中引起继发效应。
血脑屏障和淋巴血管系统被认为是信号进入大脑的入口。例如,循环免疫细胞和炎症介质(包括宿主和细菌的激素和神经递质)以及迷走神经刺激代表了有助于直接或间接微生物信号从肠道传输到大脑的机制 。
炎性细胞因子也是激活中枢神经系统的一个重要因素,作为对各种刺激的反应,包括在肠道病理过程中激活下丘脑-垂体-肾上腺轴的促炎性细胞因子。
肠易激综合征患者的皮质醇和促炎细胞因子白细胞介素IL-6和IL-8显著升高。IL-1α细胞因子在中枢神经系统水平上刺激机体的整个葡萄糖代谢;IL-6、IL-1、TNF-α和IFN细胞因子相互独立地刺激下丘脑-垂体-肾上腺轴(HPA轴)。
除了炎性细胞因子外,炎症期间环氧合酶系统合成的前列腺素也参与HPA轴的激活。多项研究发现炎性细胞因子(TNF-α、IL-1和IL-6)在HPA轴激活中的作用。任何炎性细胞因子的注射都会刺激HPA轴,并导致循环皮质酮水平升高。值得注意的是,在LPS穿透后,任何细胞因子的阻断都不会阻断HPA轴的激活,也就是说,如果肠上皮屏障功能停止,LPS进入血液,那么细胞因子激活HPA轴的复制效应就会实现。那么接下来就是神经免疫性疾病和靶器官损伤了。
因此,所有炎症介质都会促进HPA轴的激活,而阻断任何一种细胞因子都不能减少HPA轴的刺激,因为它们之间存在重复效应。
因此,下丘脑-垂体-肾上腺轴的激活是大脑介导的对疾病的基本反应之一。HPA 轴被认为是神经内分泌系统的基础,它在心理和生理压力(包括感染)的影响下调节机体的稳态,促进对压力的充分反应。
所考虑的机制在慢性应激中非常重要。由于情绪唤醒的阈值不足以在CVD期间形成压力,因此神经系统中形成全值压力反应,随后通过肠内炎症介质持续激活HPA,激活ANS的交感分裂。
值得注意的是,机体的整个复杂病理变化是通过急性应激途径发展起来的,而情绪成分(情绪刺激)与慢性应激阈值相对应或完全缺失。这个问题需要进一步研究。因此,综述的机制对神经系统中心(包括ANS中心)有激活作用,ANS中心反过来又支配内脏器官,包括微生物群居住的肠道。
结合有关肠道微生物群的机制及其与神经系统通过肠-脑轴发育紊乱的关系,可以初步得出结论,在CVD期间,来自肠道的介质通过血流和淋巴进入大脑,并激活下丘脑核团。然后,只要下丘脑是ANS的节段上整体中心,ANS的交感神经分裂就会被激活。
因此,来自肠道的介质到达ANS的节段上中心,并激活交感和副交感分裂的工作,从而关闭肠道微生物群参与CVD发病机制的病理循环。许多发表的研究报告表明,微生物群介导的炎症介质的增加会加重CVD的病程和预后。
研究还发现,恢复CVD患者的肠道菌群可以改善疾病的预后。使用增加阿克曼菌属、双歧杆菌、乳酸杆菌、拟杆菌和普氏杆菌的细菌数量的复合治疗制剂可改善CVD的病程。
众所周知,双歧杆菌和乳酸杆菌属的细菌对肠壁具有局部抗炎作用。肠上皮屏障功能的恢复是因为肠壁炎症的减少,这意味着炎症介质在体循环中的水平降低,因此它们对神经系统的激活作用降低。
尤其是,高血压与肠道微生物群紊乱和肠脑轴失调有关。在高血压大鼠模型中证明,长期开菲尔治疗可降低IL-6和TNF-α蛋白密度,并消除在下丘脑室旁核和延髓头端腹外侧区观察到的小胶质细胞激活,保护心脏调节核免受肠道介导炎症的影响,从而提供开菲尔的降压作用。在小鼠缺血性中风或脑缺血模型中进行的一些研究表明,缺血性中风脑损伤通过增加促炎反应和细胞因子、趋化因子和免疫细胞浸润大脑结构,促进肠道失调的发展,这与不良预后有关。
CVD患者肠道菌群与神经系统的相互作用
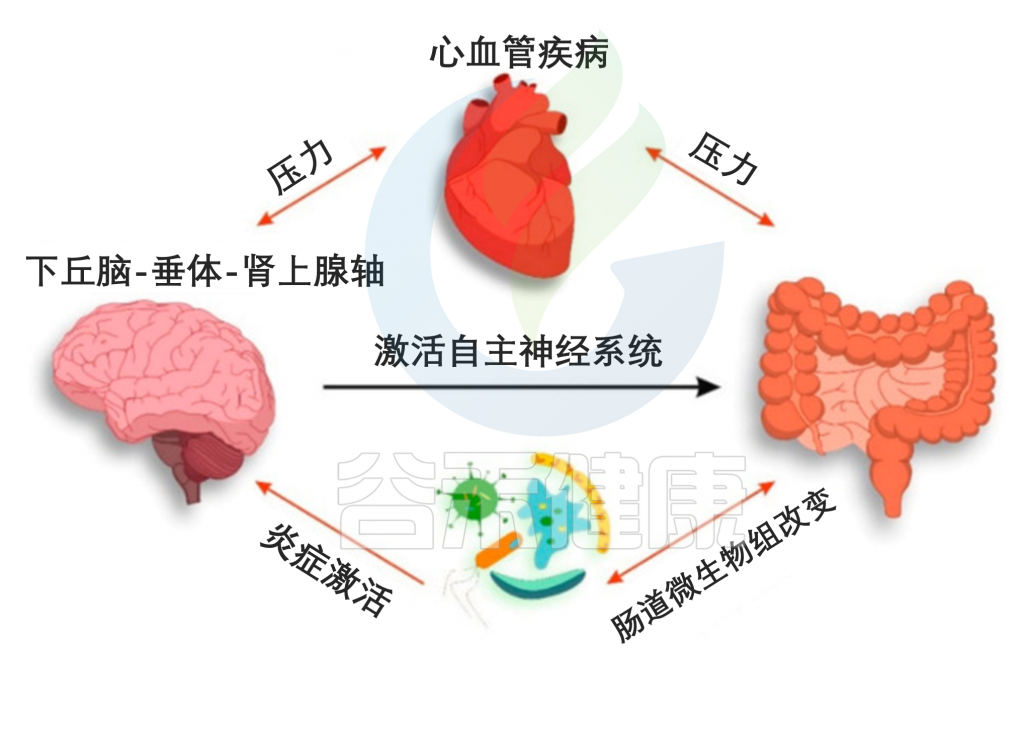

Suslov, Andrey V,, et al. J Clin Med. 2021
肠道微生物群参与了 CVD 的发病机制并决定了 HPA 轴的炎症激活。
一些研究调查了微生物组靶向制剂可改善 CVD 病程,减少动脉粥样硬化的进展和主要 CVD 并发症的风险 。
在这里,我们可以假设基于微生物组治疗的有益心脏保护机制是由于其对微生物组-肠道-脑轴的影响。
通过阻断左前冠状动脉诱发心肌梗死的大鼠中显示,与安慰剂组相比,使用基于瑞士乳杆菌和长双歧杆菌组合的益生菌可降低与心肌梗死相关的不同脑区的凋亡倾向。
另一项针对小鼠的研究表明,在实验性中风后,抗生素调节肠道微生物群可降低缺血脑内的LPS水平和神经炎症。一项针对冠心病患者的研究发现,益生菌鼠李糖乳杆菌与益生元菊糖复合物对抑郁、焦虑和炎症生物标志物具有有益作用。
建议所有成年人每周至少进行150-300分钟的中等强度或75-150分钟的高强度有氧运动,或两者的同等组合。当然要视身体状况而定,如果自身基础不太好,在能力和条件允许的情况下尽可能保持一些低强度活动。
减少久坐时间,适当进行轻度体力活动是有益的。
饮食对人类健康的多个方面都有重大影响,不健康的饮食模式(例如高脂肪的西式饮食)与动脉粥样硬化、代谢综合征和肥胖症等一系列慢性疾病的风险增加有关。免疫系统正在成为这种关系的关键中介,通过食物诱导调节与慢性炎症相关的促炎/抗炎因子以及增加/减少各种病理结果的风险。
支持这一观点的大型流行病学研究表明,以高摄入饱和脂肪和低纤维为特征的饮食模式与促炎生物标志物水平升高有关,例如 C 反应蛋白 (CRP) 和白细胞介素 IL- 6。相反,摄入大量水果和蔬菜和/或经常食用鱼类的饮食模式与较高的脂联素血清浓度相关,脂联素具有抗炎特性。
这些观察性研究得到了干预试验的进一步支持,干预试验表明饮食可能会影响血清炎症生物标志物谱。例如,高胆固醇食物的饮食干预增加了对胰岛素敏感的参与者的 CRP 和血清淀粉样蛋白 A 浓度。
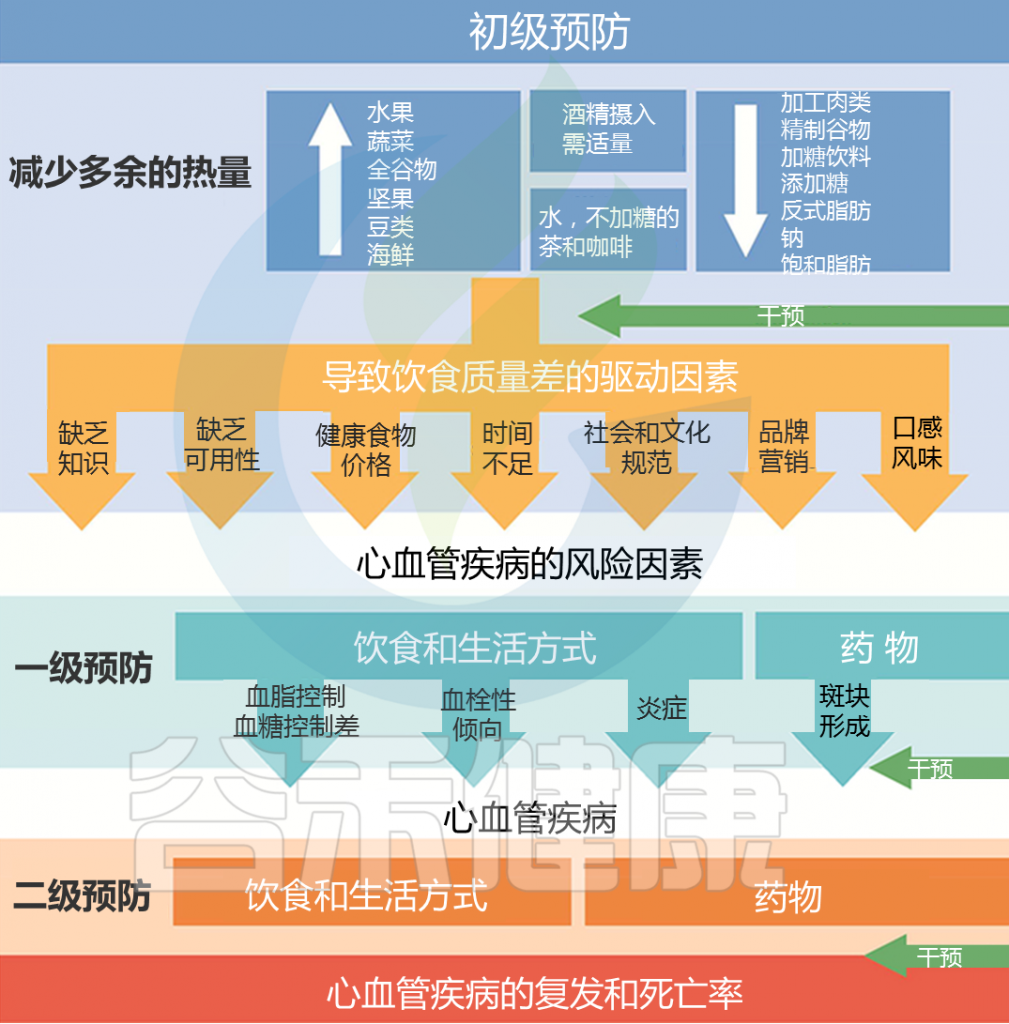

Yu E, et al.,J Am Coll Cardiol. 2018
健康的饮食可以降低心血管疾病和其他慢性疾病的风险。从更多荤食(以动物为基础的)饮食模式转变为素食(以植物为基础的)饮食模式,可能会减少心血管疾病。
建议饮食中多吃水果、蔬菜、坚果等;少量食用低脂乳制品和海鲜;而且尽可能少摄入加工肉类、含糖饮料、精制谷物、盐等。
戒烟可迅速降低心血管疾病风险,是预防动脉粥样硬化性心血管疾病最具成本效益的策略。
建议限制饮酒或戒酒,每周最多饮酒100g。
通过改变生活方式来达到和保持健康体重,对这些指标可产生有利影响(如血压、血脂、血糖等),并降低CVD风险。
当饮食和体力活动改变以及其他常规的非侵入性干预措施效果不佳时,应考虑对高危人群行减重手术;也可以考虑使用具有心血管保护作用的抗肥胖药物。
新指南提出心理压力与动脉粥样硬化性心血管疾病风险相关,需要加强对心理障碍患者的关注和支持,对其进行生活方式和药物干预,方式包括呼吸练习、冥想、写日记、适当锻炼、与大自然接触、与他人建立联系等,尽可能改善压力症状和生活质量,可改善心血管疾病。
通过对血压,血糖,血脂等指标的日常监测来了解健康状况,也可以通过肠道菌群健康检测等方式来了解慢病风险,阻断这类慢病的进程,预防控制代谢紊乱,从根本上预防心血管疾病的发生。
本文主要基于研究阐述免疫、炎症的神经调节以及肠道菌群如何参与 CVD 的发病和进展。
在CVD的初始阶段,肠道微生物群在其发病机制中的作用是次要的,这意味着细菌的定性和定量变化不像在随后的阶段那么重要。
然而,后来,当肠道微生物群决定了下丘脑-垂体-肾上腺轴的炎症激活水平时,肠道微生物群的变化对CVD的发展具有重要意义。
在CVD进展过程中,肠道细菌与肠壁的病理过程密切相关,成为CVD发病机制中的关键因素之一。在这方面,试图确定与CVD进展过程最相关的肠道细菌,可能是开发CVD诊断、预防和治疗新相关方法的重要一步。
此外,注意通过饮食衍生的微生物代谢物、炎症反应转变、校准神经免疫从而影响CVD干预和治疗反应。
·
具体基于肠道菌群的饮食调节,以及CVD 进展中的饮食-微生物群串扰的机制,菌群代谢产物的作用等详见本次推文的第二篇:
《 饮食-肠道微生物群对心血管疾病的相互作用 》主要参考文献:
Carnevale D. Neuroimmune axis of cardiovascular control: mechanisms and therapeutic implications. Nat Rev Cardiol. 2022 Mar 17. doi: 10.1038/s41569-022-00678-w. Epub ahead of print. PMID: 35301456.
Yu E, Malik VS, Hu FB. Cardiovascular Disease Prevention by Diet Modification: JACC Health Promotion Series. J Am Coll Cardiol. 2018;72(8):914-926. doi:10.1016/j.jacc.2018.02.085
Suslov, Andrey V et al. “The Neuroimmune Role of Intestinal Microbiota in the Pathogenesis of Cardiovascular Disease.” Journal of clinical medicine vol. 10,9 1995. 6 May. 2021, doi:10.3390/jcm10091995
Thaiss CA, Zmora N, Levy M, Elinav E. The microbiome and innate immunity. Nature. 2016 Jul 7;535(7610):65-74. doi: 10.1038/nature18847. PMID: 27383981.
Huh JR, Veiga-Fernandes H. Neuroimmune circuits in inter-organ communication. Nat Rev Immunol. 2020 Apr;20(4):217-228. doi: 10.1038/s41577-019-0247-z. Epub 2019 Dec 17. PMID: 31848462.
Frank L J Visseren, François Mach, Bryan Williams,et al., ESC Scientific Document Group, 2021 ESC Guidelines on cardiovascular disease prevention in clinical practice: Developed by the Task Force for cardiovascular disease prevention in clinical practice with representatives of the European Society of Cardiology and 12 medical societies With the special contribution of the European Association of Preventive Cardiology (EAPC), European Heart Journal, Volume 42, Issue 34, 7 September 2021, Pages 3227–3337
谷禾健康

最近的Nature 和 Nature Medicine 连发表了好几篇关于肠道菌群的文章,包括肠道菌群与神经互作,和基于这个原理的针对自闭症的临床治疗方案。心血管疾病的微生物组和代谢特征等。
今天我们主要介绍心血管疾病中冠状动脉疾病的相关重要研究发现和意义。
复杂的疾病,如冠状动脉疾病(CAD),往往是多因素的,由多种潜在的病理机制引起。尽管冠状动脉疾病在预防、诊断和治疗方面取得了巨大进展,但仍然是世界范围内发病率和死亡率的主要原因。目前对冠状动脉疾病的治疗基于传统的和可控制的冠状动脉疾病风险因素,只能取得部分成功。
冠状动脉疾病的发展包括血管壁上动脉粥样硬化斑块的逐渐生长,这通常与代谢状态受损有关。人体接触环境分子的主要部位是胃肠道,其中膳食成分被微生物群转化,利用产生代谢物传播到全身器官。
血液充当体内分子的液体输送器, 特别是数以千计的循环代谢小分子,它们可以帮助我们了解体内生物过程状况,并且是研究冠状动脉疾病多因素性质疾病的宝贵来源。肠道微生物组积极参与血液代谢物的代谢。
几种肠道微生物群衍生的循环代谢物与心血管疾病相关:
三甲胺 N-氧化物
三甲胺 N-氧化物被确定为人类心血管疾病的标志物,进一步的证据表明在小鼠模型中具有促动脉粥样硬化性和促血栓形成。
硫酸吲哚酚
硫酸吲哚酚在细菌色氨酸酶降解色氨酸后在肝脏中产生,并被证明与动脉僵硬和外周血管疾病有关。
对甲酚
对甲酚是苯丙氨酸和酪氨酸的结肠细菌发酵产物,显示与心血管事件增加相关。
近期,以色列科学家招募了下列人群,采集其粪便和血清样本进行了全面的多组学分析,同时调查详细的医疗、生活方式和营养问卷等。
通过对粪便样本宏基因组测序(每个样本1000万 reads,约3G/样本)和对血清样本的进行非靶向质谱LC-MS测量了 961 种代谢物的水平,包括脂质、氨基酸、异生物质、碳水化合物、肽、核苷酸和大约 30% 的未命名化合物。
通过 Nightingale Health 的质子核磁共振 ( 1 H-NMR) 平台测量了另外 228 种血浆代谢物和比率,并使用了一个独立宏基因组数据集MetaCardis进行验证(该数据集样本来自于北欧血统队列,在地里区域上与该研究样本来源不同,这样可以分析遗传,饮食差异变量)。
MetaCardis数据集主要由四个主要群体组成:缺血性心脏病、健康对照组、代谢匹配的对照组和未经治疗的代谢受损对照组(详细数据集描述可以参看原文)
一、ACS的肠道微生物组特征
1. ACS 患者的变形杆菌丰度更高
这与之前的大多数研究结果一致,变形菌增多会导致处于炎症状态,是生态失调的标志。
20个在 ACS 或对照个体中显着富集的细菌,包括产丁酸盐的细菌如:梭菌属(Clostridium)、Anaerostipes hadrus嗜热链球菌(Streptococcus thermophilus)和Blautia菌属,以及Odoribacter splanchnicus 和大肠杆菌。
2. ACS患者队列中一种梭菌科的细菌物种 SGB 4712缺乏
在20 个显着富集的基因组中,鉴定到了一种以前未知的梭菌科细菌物种,索引为 SGB 4712。为了进一步验证该结果稳定和实用性,使用另外一个来自北欧血统地理上分布不同的队列,MetaCardis宏基因组数据集进行验证,与该研究结果一致,该物种的相对丰度随着具有 CAD 传统风险因素的种群逐渐减少。
3. SGB 4712关联15种显著差异的代谢物,其中包括降低心血管疾病风险的独立标志物——麦角硫因(ergothioneine,天然氨基酸)
对照组相比, 鉴定到SGB 4712 菌种与15 种循环代谢物的水平显着相关,在 MetaCardis 研究中,所有 15 种代谢物与 SGB 4712 的相关系数均可以重复,其中 10 种相关性仍然显著。
值得注意的是,SGB 4712与麦角硫因呈正相关,麦角硫因是一种天然存在的氨基酸,在体外显示对细胞应激源具有抗氧化和细胞保护能力,最近被证明是降低心血管疾病和人类死亡率风险的独立标志物。
此外,SGB 4712 与七种化学结构未知的化合物有关。其中包括 X-11315 和 X-24473,预测它们来自饮食,并与 SGB 4712 呈正相关。
图一 ACS 的微生物组和血清代谢组学特征
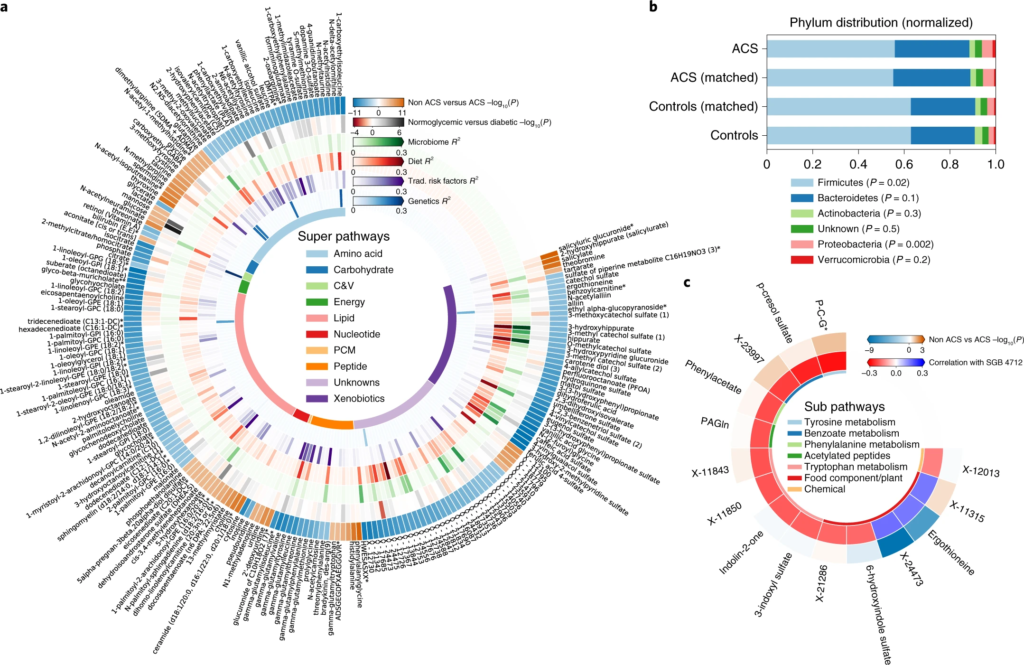
圆形热图显示 ACS 和非 ACS 对照组之间显着差异的前 200 种代谢物,与年龄、性别、BMI、吸烟状况和 DM 相匹配(方法)。每个切片代表一个代谢物,其名称显示在图表的外层周围。
这些结果突出了SGB 4712菌种在 CAD 发展中具有潜在的保护作用,由一系列循环血液代谢物介导,其中一些以前被证明在元生物途径中发挥核心作用,而另一些则未知。
因此,在实验研究中进一步验证后,这些代谢物可能会形成降低 CAD 风险的新目标。
二、ACS 的代谢特征因人而异
1. ACS 患者的血清代谢物水平个体化差异较大
虽然 CAD 患者具有共同的内表型,但他们通常表现出生物学上不同的疾病特征。为了更好地了解 ACS 的个体水平变异性,作者试图检查与非 ACS 对照的代谢偏差,并询问它们是否是个体特异性的。
计算了他们的个体偏差,并根据之前根据饮食、微生物组、传统风险因素和遗传学估计的 EV 对每个个体的前 100 个偏差代谢物进行加权。最后发现ACS 患者与其匹配对照的代谢偏差是因人而异的。
急性冠脉综合征患者的血清谱在血清代谢物水平上表现出广泛的扰动,包括533种显著改变的代谢物。
ACS的血清代谢组遵循一种主要的消耗模式,因为在对照组参与者中,358种代谢物(67%)的平均测量值较高。然而,这一趋势在主要的生物途径中并不一致。但是,与富含 ACS 的代谢物相比,饮食和微生物组在与 ACS 耗尽代谢物的偏差相关联方面更为显着(双尾 Mann–Whitney U-检验,P-value小于10 -20),这表明微生物组对 CAD 起保护作用。
值得注意的是,超过 90% 的显着扰动的代谢物无法用血糖状态来解释,这表明这种变化背后还有其他机制。所以进一步分析了其他系列综合因素(包括宿主遗传学、微生物组和饮食),得到一个重要发现就是:饮食和微生物组可以更好地解释 ACS 缺乏或含量低的代谢物,而传统的风险因素可以更好地解释 ACS 富集的代谢物。
图2 代谢偏差由潜在决定因素解释,并与临床参数相关
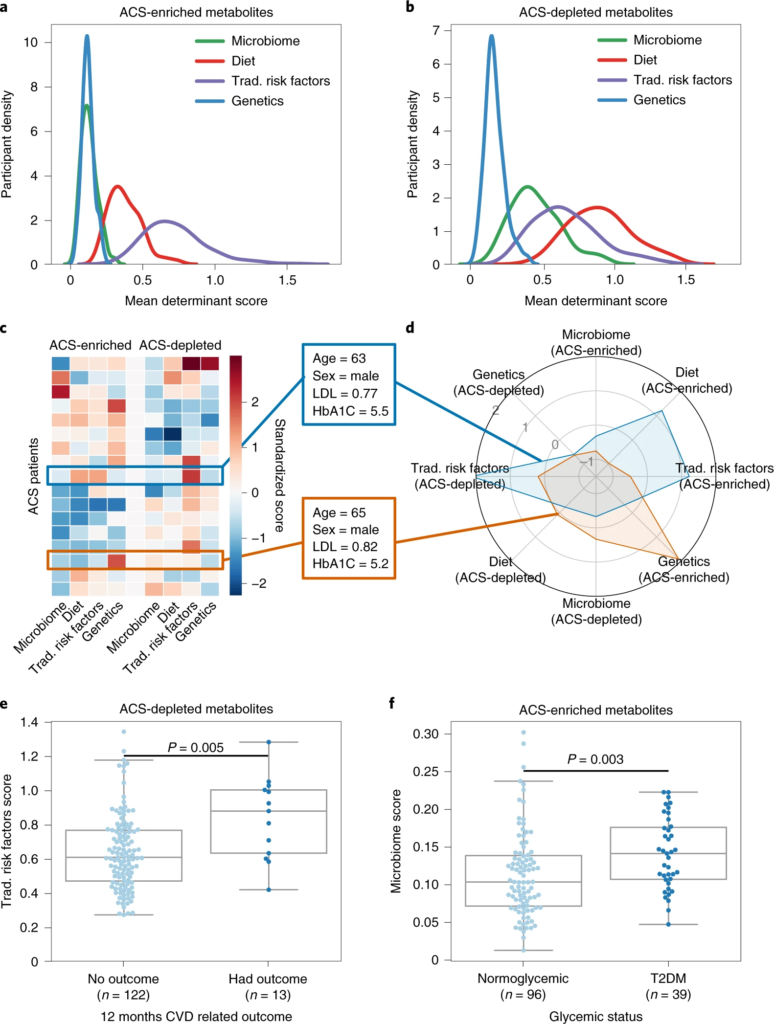
a、b、密度图显示 ACS 参与者的分布(y轴)与代谢物的潜在决定因素(微生物组、饮食、传统风险因素或遗传学)的平均加权R 2 ( x轴);富含 ACS 的代谢物。
2. 相似的临床特征,但其动脉粥样硬化负担的代谢机制却不同
虽然一些患者可能具有相似的临床特征,但他们的潜在生理状态和疾病轨迹可能不同。为了强调这种 CAD 患者的变异性,作者选择了 ACS 患者的常规危险因素的同质亚组。其中包括 17 名 60 至 70 岁的男性患者,低密度脂蛋白 (LDL) 在 0.70–1.30 mg ml -1范围内,糖化血红蛋白 (HbA1C) 低于 6%。尽管具有相似的临床特征,但该 ACS 患者亚组在代谢偏差方面表现出异质性。
三、微生物组在CAD早期阶段发挥作用
动脉粥样硬化是一种经过多年发展的进行性疾病,其中动脉粥样硬化斑块形成的每个阶段的特点是不同的病理过程。在早期阶段,血管壁上的动脉粥样硬化斑块的生长通常与代谢状态的损害有关。
为了解释每个代谢成分在 CAD 发展的时间轴上的参与,作者将个体代谢偏差的分析应用于代谢受损的对照(定义为 T2DM、高血压或血脂异常的诊断,或 BMI > 35),以及到非 ACS 个体的随机子集。
在比较这三组的分数时,我们发现分数分布存在一致的差异。与微生物组和饮食相关的代谢异常呈现出渐进的趋势,与对照组的随机子集相比,代谢受损的对照参与者的代谢物存在显着偏差。
这表明,微生物组和饮食对ACS的贡献可能是通过受损的代谢状态介导的,而不是代谢受损个体中尚未表现出的与传统风险因素和遗传学相关的代谢物异常。
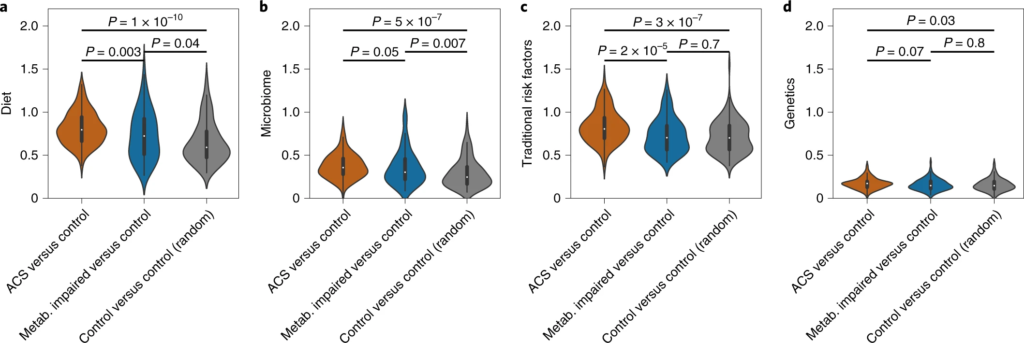
a – d,归因于饮食 ( a )、微生物组 ( b )、传统风险因素 ( c ) 和遗传学 ( d ) 的代谢偏差分数计算三个亚组:(1) ACS 个体 ( n = 135) 与非 ACS 对照与年龄、性别和 BMI 相匹配(橙色);(2) 患有代谢障碍的非 ACS 对照(定义为:诊断为 T2DM、高血压或血脂异常,或 BMI > 35;n = 102)与其他年龄、性别和 BMI 匹配的非 ACS 对照(蓝色);(3) 一组随机的非 ACS 个体 ( n = 132) 与其他匹配年龄、性别和 BMI(灰色)的非 ACS 对照。
四、血清代谢组学预测ACS患者 BMI 更高
肥胖是 CAD 的主要独立危险因素,影响已知的危险因素,如血脂异常、高血压、葡萄糖耐受不良和炎症状态,以及可能尚未认识到的机制。BMI 测量被用作肥胖的标志和代谢健康的指标。
为了研究肥胖作为 CAD 的独立危险因素,该研究设计并彻底验证了基于血清代谢组学的 BMI 模型,并表明较高的预测 ΔBMI 对应于更广泛的动脉粥样硬化疾病。
作者分析了CAD 患者的 BMI-代谢组平衡是否以及如何被破坏。使用了梯度提升决策树 (GBDT) 算法预测 BMI,结果表明在非ACS受试者中发现的代谢组-BMI模式在ACS患者中受到干扰。
为了研究这些扰动,作者测试了对照组和 ACS 测试集中预测和测量 BMI 之间的差异,这里称为 ΔBMI。结果发现,与非 ACS 受试者相比,该研究的模型预测 ACS 的 ΔBMI 更高。
为了验证这些结果的稳健性,作者试图根据其他类型的代谢组学数据和独立队列来复制这些发现。将相同的预测程序应用于基于 NMR 的代谢组学数据,并观察到ACS 和对照之间 ΔBMI 的更大差异,应用于为发表的MetaCardis 队列数据中得出在所有 BMI 范围内,与血糖正常的缺血性心脏病患者相比,患有糖尿病的缺血性心脏病患者的 ΔBMI 显着更高。
进一步分析推断哪些特定代谢物是 ACS 患者高 ΔBMI 的主要驱动因素,发现两种脂质在对照组中与 BMI 呈负相关,后者在患有更广泛疾病的患者中也显着减少,这两种脂质分别是:
1-(1-enyl-palmitoyl)-2-oleoyl-GPC (P-16:0/18:1)
1-(1-enyl-palmitoyl)-2-linoleoyl-GPC (P-16:0/18:2)
最近的研究表明,脂质1-linoleoyl-GPC (18:2) 与肥胖和 T2DM呈负相关,并且脂质水平的增加显着降低了T2DM的风险。该研究发现 1-linoleoyl-GPC (18:2) 和 1-(1-enyl-palmitoyl)-2-linoleoyl-GPC (P-16:0/18:2) 在对照组中与 BMI 呈负相关,并且在患有更广泛 CAD 的患者中显着耗尽,这表明这些代谢物可能作为降低 CAD 风险的潜在靶点。
此外,两种代谢物都含有一条亚油酸链,一种必需脂肪酸,与 T2DM 风险呈负相关。然而,这些假设应在干预性研究中进一步检验。
迄今为止,大多数研究都集中在寻找在 CAD 患者中增加的新代谢物,而该研究对 199 名 ACS 患者进行了全面的多组学分析结果强调, ACS 的代谢组学特征是缺乏多种血清代谢物,其中许多与饮食和微生物组有关。
其中一个重要的发现是以前未知的细菌物种 SGB 4712,它在 ACS 患者和独立验证队列中都显着缺乏或偏低。通过进一步将这种细菌与心脏毒性和心脏保护代谢物的水平联系起来,证明了特定细菌基因组的缺失可能与 CAD 风险增加相对应,并提出在后续干预研究中评估的具体目标。总体而言,这些发现因此为 CAD 患者的预测甚至治疗提供了一种新方法。
迄今为止,大多数研究都对 CAD 患者进行了批量分析,寻找人群水平的风险因素,而不是关注个体水平的生物变异性。在这项研究中,作者使用全面的代谢组学和微生物组分析,呈现了 CAD 内部变异性的深度映射。总之,结果揭示了新的范式和治疗方向。
参考文献:Talmor-Barkan Y, Bar N, Shaul AA, Shahaf N, Godneva A, Bussi Y, Lotan-Pompan M, Weinberger A, Shechter A, Chezar-Azerrad C, Arow Z, Hammer Y, Chechi K, Forslund SK, Fromentin S, Dumas ME, Ehrlich SD, Pedersen O, Kornowski R, Segal E. Metabolomic and microbiome profiling reveals personalized risk factors for coronary artery disease. Nat Med. 2022 Feb;28(2):295-302. doi: 10.1038/s41591-022-01686-6. Epub 2022 Feb 17. PMID: 35177859.

谷禾健康

Alistipes是拟杆菌门的一种革兰氏阴性细菌,也是相对新的细菌属,主要从医学临床样本中分离出来。该菌的生态失调,可能是有益的也可能是有害的。
Alistipes可能对某些疾病有保护作用,包括肝纤维化、癌症免疫治疗和心血管疾病。相比之下,其他研究表明Alistipes在结直肠癌中具有致病性,并且与抑郁症有关。
该菌避开富含植物性食物的饮食,可以在高脂肪饮食中茁壮成长,并且在肥胖患者的肠道微生物群中生长得特别好,表明与肥胖相关。
Alistipes 是拟杆菌门中的一个属,革兰氏阴性,专性厌氧,是肠道共生的细菌,G+C 含量为55–58%,直径为 0.2–0.9 µm,长度为 0.5–4 µm 的直或略微弯曲的棒状,末端为圆形。不会形成孢子。细胞通常单独或成对出现,偶尔以较长的细丝出现。
不运动,可产生吲哚。不能还原硝酸盐,不水解精氨酸和尿素,葡萄糖代谢终产物是琥珀酸和少量的乙酸,丙酸。
microbiomology
在分类学上,Alistipes 是在 2003 年在患有阑尾炎的儿童的组织样本中发现后描述的一个属。第一个被发现的Alistipes物种是Alistipes Finegoldii,它是以美国厌氧细菌学和传染病临床研究学家Sydney M. Finegold 的名字命名,极大地促进了我们对厌氧菌的理解。
根据NCBI分类数据库,目前Alistipes由13个物种组成:
2017 年从肠易激综合征患者的结肠中分离出来一种名为Tidjanibacter massiliensis Marseille-P3084 的新物种,与A. putredinis具有 92.1% 的序列同源性,不过该菌株尚未被官方认可或存放在公共菌株生物储存库中。
此外,三个较新的亚种:
从生态学角度来看,Alistipes主要存在于健康人的肠道中。然而,Alistipes也从其他液体中分离出来、如尿液、阑尾、腹部、直肠周围和脑脓肿中分离出来,突出了它们在人类疾病中潜在的机会致病作用。
A. putredinis(ATCC 29800 T型菌株)已从各种标本中分离出来,例如粪便、急性阑尾炎患者的阑尾组织、腹部和直肠脓肿、甚至农场土壤。该菌株对克林霉素、头孢西丁、氯霉素、红霉素和甲硝唑敏感,对四环素和强力霉素有中度耐药。
Alistipes finegoldii 已被认为是肉鸡的生长促进剂,并且已观察到在人类中,A. putredinis随着十字花科蔬菜摄入量的增加而增加,因此可以合理假设不同的Alistipes物种在营养和健康方面可能具有不同的作用。
A. onderdonkii和 A. shahii 分别从腹部脓肿和阑尾组织以及尿液中分离出来。它们具有圆形菌落。这两个种都对 20% 的胆汁具有抗性,并将色氨酸水解为吲哚。它们是过氧化氢酶、氮还原酶和脲酶阴性。琥珀酸是主要的代谢终产物,少量产生乙酸和丙酸。
其他两个种,A. senegalensis 和 A. timonensis 最初是从健康患者的粪便菌群中分离出来的。它们有圆形菌落并产生色素,可以将色氨酸水解为吲哚。A. senegalensis会发酵甘露糖,而A. timonensis 不会。这些细菌菌株对青霉素、阿莫西林加克拉维酸、亚胺培南和克林霉素敏感。此外,A. senegalensis菌株对甲硝唑耐药,A. timonensis 菌株对甲硝唑敏感。
Alistipes inops从人类粪便中分离出物种。它对吲哚产生呈阳性,对过氧化氢酶、硝酸还原酶和脲酶呈阴性。这种细菌是非发酵的,主要代谢终产物是琥珀酸和乙酸。
A. megaguti (Marseille-P5997 T型菌株)是从一名年轻健康女性的新鲜粪便样本中分离出来的。
A. megaguti是过氧化氢酶、脲酶和氧化酶阴性。
A. provencensis (Marseille-P2431 T型菌株) 分离自一名患有高血压和糖尿病的男性患者。该种属氧化酶和脲酶阴性,而过氧化氢酶阳性。
A.ihumii 已从患有神经性厌食症的患者的粪便中分离出来,而A.obesi则从患有病态肥胖症的患者中分离出来。
该菌属大部分耐胆汁,因此,有必要确定对胆汁酸的抗性是否确实决定了Alistipes胃肠道内的区域性富集,或临床上以胆汁改变为特征的疾病,其与Alistipes菌的关系。
肝病和短链脂肪酸中的 Alistipes
肝细胞癌 (HCC) 是全球第二大致命癌症。HCC 通常是由肝硬化、非酒精性脂肪肝病 (NAFLD) 或非酒精性脂肪性肝炎 (NASH) 引起的晚期肝纤维化发展而来的。这些肝脏疾病与“微生物-肝轴”有关,表明生态失调是潜在原因之一。
肝纤维化中Alistipes减少
在对微生物群组成和肝纤维化进行的研究中可以看出,在纤维化的整个进展过程中,Alistipes减少。
例如,在代偿性和失代偿性肝硬化 (LC) 患者中,来自健康志愿者和各种类型 LC 患者的新鲜粪便宏基因组序列表明,与健康对照组相比,A. shahii和A. putredinis菌减少。
针对 LC 患者粪便和活检的研究中,与 LC 患者相比,健康对照患者的Alistipes丰度增加。
代偿发展到失代偿,Alistipes减少
随着疾病从代偿发展到失代偿,观察到Alistipes indistinctus 的减少。一旦个体出现失代偿性肝硬化,患者就会开始产生多种严重并发症,例如肝性脑病。
另一项研究表明,在比较失代偿性肝硬化和急性肝性脑病患者的粪便微生物群时,Alistipes具有保护作用,其丰度的降低与肝性脑病复发的增加相关。因此,Alistipes的减少与肝硬化进展为失代偿状态有关。
NASH 和 NAFLD中 Alistipes 降低
在NASH 和 NAFLD 等其他纤维化疾病中可以看到肝纤维化患者的Alistipes丰度降低。有实质性纤维化的 NAFLD 患者粪便中乙酸盐和丙酸盐浓度降低,丁酸盐浓度无显着差异。当将健康对照与 NASH 患者进行比较时,A. finegoldii 显着减少,标准化计数平均值从 542 减少到 19。在具有显着纤维化的 NAFLD 患者中,观察到 A. onderdonkii 的显着减少从 285 到 31。
Alistipes生产短链脂肪酸
值得注意的是,这些晚期纤维化患者的粪便乙酸盐和丙酸盐水平降低。
Alistipes是一种丙酸生产者,表达甲基丙二酰辅酶A差向异构酶,其中该酶的基因位于具有乙酰辅酶A羧化酶基因的操纵子上。
此外,Alistipes是乙酸盐生产者,由于先前的研究表明短链脂肪酸具有抗炎机制,因此可以表明Alistipes 减少促使短链脂肪酸减少,可能加剧这些 NAFLD 患者中的晚期纤维化。
心血管疾病、高血压和上皮中的 Alistipes
心血管疾病 (CVD) 是发展中国家和发达国家死亡和发病的主要原因。随着全球人口老龄化,预计心血管疾病在未来会上升,因此对与肠道微生物群关系的评估进行了更广泛的研究。
Alistipes与高血压等心血管疾病风险因素以及心房颤动 (AF)、充血性心力衰竭 (CHF) 和动脉粥样硬化性心血管疾病 (ACVD) 等多种心血管疾病相关。
各种研究表明,Alistipes在心血管疾病中起保护作用。
心房颤动患者Alistipes减少
Alistipes与心房颤动 (AF) 等心血管疾病直接相关。心房颤动是最常见的心律失常,在高血压、心力衰竭和肥胖患者中普遍存在。
为了量化肠道微生物组和心房颤动之间的关系,对来自中国参与者的 100 个粪便样本全基因组鸟枪序列进行分析,显示在心房颤动患者肠道中Alistipes急剧减少。
Alistipes和链球菌的拮抗作用
然而,研究中提出在心房颤动期间急剧增加的细菌,如链球菌,可能是导致Alistipes下降的原因,这表明Alistipes和链球菌之间存在潜在的拮抗作用。这种趋势在其他心脏病中很常见,例如 ACVD和 CHF。
但是Alistipes在心血管疾病中证据是矛盾的,尚不清楚关联是保护性的、有益的还是致病的。因为大多数心血管疾病具有共同的病理生理特征,例如内皮功能障碍 ,Alistipes的作用可能取决于多个心血管疾病共享的疾病机制。因此,更多关于肠心轴的研究可能会导致未来对微生物组相关疾病和潜在疗法的理解。
高血压中Alistipes有助于炎症和上皮细胞的改变
宏基因组分析研究了 22 名高血压患者和 18 名对照患者的粪便样本。数据显示A. finegoldii和A. indistinctus的增加与收缩压呈正相关,表明该物种是高血压患者肠道屏障功能障碍和炎症的潜在驱动因素,但是该研究样本量较少,证据力度不大。
肠道炎症和结直肠癌中不一样的 Alistipes
由于胃肠道中微生物群的多样性,菌群失调与炎症性肠病(IBD)之间存在很强的相关性。
人群中最常见的炎症性肠病是克罗恩病 (CD) 和溃疡性结肠炎 (UC)。溃疡性结肠炎是一种主要针对结肠的慢性炎症性疾病。有人提出A. Finegoldii是一种针对结肠炎的保护性物种,因为A. Finegoldii在患有结肠炎的小鼠中减少。
基于这个事实,进行了一项研究,其中微生物群耗竭的小鼠用口服 DSS 治疗以诱发结肠炎。当用 A. finegoldii 灌胃时,结肠炎的严重程度与野生小鼠相似。当给患上结肠炎小鼠添加了A. finegoldii和 Bacteroides Eggerthii (一种结肠炎诱导细菌)时,与单独添加B. Eggerthii 或添加其他细菌(如Parabacteroides distasonis或Prevotella falsenii)的小鼠相比,结肠炎的严重程度显着降低,这进一步表明A. Finegoldii是一种减轻结肠炎的细菌。
具有对比临床意义的是,已从严重克罗恩病的肠壁海绵状瘘管 (CavFT) 微病变中分离出与其他拟杆菌有关的 A. finegoldii. 对自发性克罗恩病回肠炎小鼠模型粪便样本的宏基因组研究显示,与亲代 AKR/J 小鼠群体相比,Alistipes 富集。
8 周龄 NOD2 敲除小鼠富含Alistipes、抗炎细胞因子(TGF-β 和 IL-10)和 CD4 + LAP + FoxP3 –调节性 T 细胞。这些观察结果的一个可能联系来自对姜黄素的研究,姜黄素是一种已被证明可通过 IL-10增加 CD4 + LAP + FoxP3 -细胞来调节肠道炎症的香料。
有趣的是,有炎症的患者服用益生菌后,Alistipes增加了。迄今为止,尚不清楚该属与肠道中的其他微生物(包括食物和益生菌菌株)之间存在哪些相互作用机制。
诱发结直肠癌
已发现Alistipes作为潜在的病原体可能会诱发结直肠癌。A. Finegoldii 通过 IL-6/STAT 3 途径促进右侧结直肠癌。报告指出Alistipes能产生磺脂,已知磺脂类药物可作为血管性血友病因子受体的拮抗剂并抑制肿瘤坏死因子-α (TNF-a),这些物质与微炎症和血管内皮功能障碍有关。
Lipocalin 2 (LCN 2) 是一种与铁载体结合的抗微生物蛋白,最终会降低铁的利用率。
在 IBD 患者中,LCN 2 在黏膜和粪便样本中的浓度很高。从本质上讲,这可以减少Alistipes的繁殖,因为铁是A. finegoldii 生长的调节因子。
小鼠研究表明A. finegoldii在 WT、LCN 2 KO 和 IL-10 KO C57BL/6J 小鼠中口服给药 1 周后引起肠道炎症。因此,该论文得出结论,Alistipes在缺乏 LCN 2 并促进炎症和肿瘤形成的发炎环境中茁壮成长。此外,他们发现在盲肠中发现Alistipes finegoldii的丰度高于大肠内的其他位置。
癌症免疫疗法中的Alistipes
该属已被证明可以通过调节肿瘤微环境在癌症免疫治疗中发挥有益作用。癌症的主要标志之一是逃避免疫系统。因此,一种形式的抗癌治疗是操纵肿瘤微环境。
免疫疗法的一个例子是通过诱导肿瘤相关骨髓细胞产生肿瘤坏死因子 (TNF) 来操纵微环境,最终导致肿瘤根除。
一种方法是使用肿瘤内 CpG-寡脱氧核苷酸 (ODN) 的组合来激活 TLR9 和抑制性 IL-10R 抗体。这种免疫疗法通常会阻止肿瘤生长并通过肿瘤相关的骨髓细胞诱导肿瘤坏死因子依赖性出血性坏死,从而导致肿瘤抑制。
免疫疗法效果依赖微生物群的存在
由于 TNF 产生减少,抗生素导致肿瘤根除效率降低。然后,研究人员怀疑这是否取决于肠道中的细菌负荷。因此,具有 MC38 肿瘤的无菌 (GF) 小鼠接受了抗 IL-10R/CpG-ODN 治疗。与无特定病原体 (SPF) 小鼠相比,经处理的 GF 小鼠产生的 TNF 量显着降低。
这表明肿瘤相关的先天性骨髓细胞由微生物群引发,以响应抗 IL-10R/CpG-ODN 产生炎性细胞因子,并且抗生素治疗或无菌状态导致的细菌负荷减少会降低这种反应,并且TNF依赖的早期肿瘤坏死。
为了更好地了解抗生素的作用和肠道微生物群的作用,用 LPS 灌胃 MC38 荷瘤小鼠并重建 TNF 表达。Alistipes属和 TLR4 引发/TNF 产生的作用,两者之间存在正相关。
TNF 恢复是由于促炎性革兰氏阴性菌A. shahii与 TLR4 结合,启动 TNF 产生表达的作用。
为了进一步证明他们的假设,作者随后显示了抗生素治疗后A. shahii恢复的延迟,这也与抗生素给药后约 4 周的 TNF 恢复阶段平行。
此外,他们表明,当用抗生素预处理并用A. shahii灌胃的小鼠时,与肿瘤相关的骨髓细胞产生 TNF 的功能得到恢复。临床相关,该研究表明,当Alistipes减少,对癌症免疫疗法的最佳反应平行减少 。陆续其他人也确定了Alistipes在癌症免疫治疗中的作用。
精神健康中的 Alistipes
虽然Alistipes常见于肠道,但它已被证明对定位于肠道外的疾病有显着影响,例如抑郁症、焦虑症、慢性疲劳综合征、自闭症、肝硬化和衰老。肠道内的生态失调会影响肠脑轴,并用于解释肠道微生物群、抑郁症和其他情绪障碍(如焦虑)之间的关系。
抑郁患者中Alistipes增加
与健康对照组相比,重度抑郁症患者的粪便中肠杆菌科和Alistipes水平升高,粪杆菌水平降低。Alistipes属吲哚阳性,影响血清素前体色氨酸,而Faecalibacterium具有抗炎特性。
在一项对 BALB/c 小鼠进行的研究中,该小鼠置于压力环境中,Alistipes丰度显着增加。此外,还发现挪威患有慢性疲劳综合症的患者的Alistipes浓度增加了近 4 倍。这些发现与抑郁症患者Alistipes增加的证据相关,因为抑郁症患者通常与疲劳和压力作斗争 。
Aistipes丰度的增加可能与GABA增加有关
研究指出,Alistipes的增加扰乱了肠-脑轴,因为Alistipes是一种吲哚阳性生物体,因此会降低血清素的可用性。色氨酸是血清素的前体,血清素的减少与抑郁症有关。此外,Alistipes已被证明可表达谷氨酸脱羧酶,这是一种在鸡体内将谷氨酸代谢为 γ-氨基丁酸 (GABA) 的酶。因此Alistipes丰度的增加也可能与 GABA 的增加有关。然而,应该进行研究以证明 GABA 是否被分泌到肠腔中。
自闭症患者中Alistipes研究不一致
此外,自闭症谱系障碍患者的大脑和肠道之间存在关联。研究发现自闭症谱系障碍患者的Alistipes减少。然而,另一项针对不同形式的自闭症 PDD-NOS 的研究表明,儿童中存在大量Alistipes。据推测,这可能来自丙酸的产生,丙酸已被证明对大鼠具有神经生物学作用。需要对Alistipes进行更多研究及其对肠脑轴的影响,因为关于其在两个系统中的保护/致病作用存在矛盾的证据。
磺胺类和生化标志物
Alistipes是一种细菌,具有许多与上述疾病相关的免疫和生化途径。一个重要的意义是Alistipes通过 IL-6/STAT 3 途径促进结直肠癌。
因此,未来的研究可以考虑使用Alistipes物种作为结直肠癌的潜在生物标志物,利用我们基于微生物组 DNA 数据的理解以及对疾病发病机制的生化概念的整合。
实现这一目标的一种潜在方法是寻找磺基脂,这是一类独特的鞘脂,在鞘氨醇碱基中具有磺酸基团。
Alistipes产生磺基脂
研究表明,当 C57BL/6N 小鼠喂食含有红花油或猪油脂肪的高脂肪饮食 3 周时,与喂食正常食物的小鼠相比,磺胺脂以及体重都会增加。进行了宏基因组分析并筛选了这些小鼠盲肠中参与磺胺脂生物合成的细菌基因。发现除A. inops外的所有Alistipes物种都产生磺基脂(关于最新物种 A. megaguti、A.provencensis和磺基脂生产的信息仍然未知)。
为了进一步证明磺基脂是细菌的产物和Alistipes的标志物,科学家们对带有Alistipes的无菌 (GF) 小鼠进行了单定殖研究并检测到单定殖小鼠盲肠中明显出现了以前在无菌小鼠中不存在的磺基脂。
因此,由于结直肠癌的常见风险因素是高脂肪饮食、肥胖和年龄,除了这些结肠疾病中Alistipes的丰度增加外,还有一个有趣的提议是使用磺基脂类作为结直肠癌患者风险的标志物。此外,应进行研究以验证Alistipes丰度是否在息肉中增加,癌前与癌性,息肉是结直肠癌的另一个危险因素。
有害代谢产物与结直肠癌相关
此外,Alistipes在共生细菌中具有最多的腐败途径。腐败是肠道微生物群在胃肠道中发酵未消化的蛋白质,通常会导致细菌产生有害代谢物。据报道,这些产物有害并与结直肠癌相关。此类产品包括氨、H2S、甲酚、吲哚和苯酚。
在一项旨在确定肠道细菌使用的主要腐败途径的研究中,发现Alistipes有助于组氨酸降解/四氢呋喃产生、吲哚产生和苯酚产生。已发现组氨酸降解/THF 产生会释放过量的氨,当吸收时会损害结肠细胞。还发现氨会增加肠细胞增殖并有助于结直肠癌中癌细胞的生长。当患者有结直肠癌风险时,发现过量氨和其他Alistipes产生的腐败产物可能对临床医生有用。
Alistipes是一种从临床样本中分离出来的相对较新的细菌属,尽管与拟杆菌门中的其他细菌相比,其分离率较低。全基因组蛋白质系统发育分析表明,与拟杆菌门中的其他成员相比,该属可能具有独特的功能特性。
一般,超过一定量的Alistipes在临床和临床前研究中已被认为是导致疾病的原因。有趣的是,其他研究表明它们的存在与促进健康表型相关,例如Alistipes在结肠炎、自闭症谱系障碍以及各种肝脏和心血管纤维化疾病等疾病中的保护作用。
尽管Alistipes在健康表型中发挥作用,但与之形成鲜明对比的是,Alistipes在焦虑、肌痛性脑脊髓炎/慢性疲劳综合征、抑郁症、PDD-NOS 和 CRC 等疾病中具有致病作用。
根据相关研究的结论,该属可能在疾病的调节中起主导作用,或者可能只是具有辅助作用或共同诱导作用。将进一步需要动物研究来破译其复杂多模式疾病机制,以及亚型表型的有针对性研究。
使用无菌动物和模型将有助于了解该属在疾病和健康中的作用以及与宿主免疫防御耐受性的相互作用,例如应该有研究调查Alistipes及其生产的 SCFAs 的作用对各种肝病的影响和Alistipes对T细胞分化的直接作用。
主要参考文献
Parker BJ, Wearsch PA, Veloo ACM, Rodriguez-Palacios A. The Genus Alistipes: Gut Bacteria With Emerging Implications to Inflammation, Cancer, and Mental Health. Front Immunol. 2020 Jun 9;11:906. doi: 10.3389/fimmu.2020.00906. PMID: 32582143; PMCID: PMC7296073.
Sakamoto M, Ikeyama N, Ogata Y, Suda W, Iino T, Hattori M, et al. . Alistipes communis sp. nov., Alistipes dispar sp. nov. and Alistipes onderdonkii subsp. vulgaris subsp. nov., isolated from human faeces, and creation of Alistipes onderdonkii subsp. onderdonkii subsp. nov. Int J Syst Evol Microbiol. (2020) 70:473–80.
Rau M, Rehman A, Dittrich M, Groen AK, Hermanns HM, Seyfried F, et al. . Fecal SCFAs and SCFA-producing bacteria in gut microbiome of human NAFLD as a putative link to systemic T-cell activation and advanced disease. United Euro. Gastroenterol J. (2018) 6:1496–1507. 10.1177/2050640618804444
Song Y, Könönen E, Rautio M, Liu C, Bryk A, Eerola E, et al. . Alistipes onderdonkii sp. nov. and Alistipes shahii sp. nov., of human origin. Int J Syst Evol Microbiol. (2006) 56:1985–90. 10.1099/ijs.0.64318-0
Kim S, Goel R, Kumar A, Qi Y, Lobaton G, Hosaka K, et al. . Imbalance of gut microbiome and intestinal epithelial barrier dysfunction in patients with high blood pressure. Clin Sci. (2018) 132:701–18. 10.1042/CS20180087
Shen L, Liu L, Ji HF. Regulative effects of curcumin spice administration on gut microbiota and its pharmacological implications. Food Nutr Res. (2017) 61:1361780. 10.1080/16546628.2017.1361780
Merrill AH. Sphingolipid and glycosphingolipid metabolic pathways in the era of sphingolipidomics. Chem Rev. (2011) 111:6387–422. 10.1021/cr2002917
Parker BJ, Wearsch PA, Veloo ACM, Rodriguez-Palacios A. The Genus Alistipes: Gut Bacteria With Emerging Implications to Inflammation, Cancer, and Mental Health. Front Immunol. 2020 Jun 9;11:906. doi: 10.3389/fimmu.2020.00906. PMID: 32582143; PMCID: PMC7296073.
Sakamoto M, Ikeyama N, Ogata Y, Suda W, Iino T, Hattori M, et al. . Alistipes communis sp. nov., Alistipes dispar sp. nov. and Alistipes onderdonkii subsp. vulgaris subsp. nov., isolated from human faeces, and creation of Alistipes onderdonkii subsp. onderdonkii subsp. nov. Int J Syst Evol Microbiol. (2020) 70:473–80.
Rau M, Rehman A, Dittrich M, Groen AK, Hermanns HM, Seyfried F, et al. . Fecal SCFAs and SCFA-producing bacteria in gut microbiome of human NAFLD as a putative link to systemic T-cell activation and advanced disease. United Euro. Gastroenterol J. (2018) 6:1496–1507. 10.1177/2050640618804444
Song Y, Könönen E, Rautio M, Liu C, Bryk A, Eerola E, et al. . Alistipes onderdonkii sp. nov. and Alistipes shahii sp. nov., of human origin. Int J Syst Evol Microbiol. (2006) 56:1985–90. 10.1099/ijs.0.64318-0
Kim S, Goel R, Kumar A, Qi Y, Lobaton G, Hosaka K, et al. . Imbalance of gut microbiome and intestinal epithelial barrier dysfunction in patients with high blood pressure. Clin Sci. (2018) 132:701–18. 10.1042/CS20180087
Shen L, Liu L, Ji HF. Regulative effects of curcumin spice administration on gut microbiota and its pharmacological implications. Food Nutr Res. (2017) 61:1361780. 10.1080/16546628.2017.1361780
Merrill AH. Sphingolipid and glycosphingolipid metabolic pathways in the era of sphingolipidomics. Chem Rev. (2011) 111:6387–422. 10.1021/cr2002917

谷禾健康

肠道的内部环境作为外部环境和宿主之间的接口,不断受到宿主的消费习惯的挑战。在管腔一侧,微生物能够附着并定植于该空间,而在宿主一侧,胃肠道充当体内免疫细胞的最大隔室。
从解剖学上讲,肠道由不同的部分组成。十二指肠,空肠和回肠代表小肠(SI),它比由结肠和直肠组成的大肠(LI)占据更多的物理空间。与人类相比,啮齿动物的盲肠增大,盲肠囊是连接小肠和大肠的盲端囊。在小鼠中,盲肠充当了共生微生物的大贮藏库,这些微生物参与了无法通过其他方式裂解的纤维的发酵。 盲肠在小鼠中的作用很重要,因为它是短链脂肪酸(SCFA)产生的主要途径,去除盲肠会导致胃肠道远端部位炎症的增加 。在人类中,该部位微生物的体积远小于小鼠,但该隔室在兼性厌氧发酵中仍起着重要作用。
值得注意的是,共生微生物的组成和丰度在不同的胃肠道区域是不同的,例如,成年小肠中的微生物丰度低(<105个微生物/ mL),在结肠中则增加到1012。小肠和大肠具有独特的生理功能。 虽然十二指肠和空肠参与消化,营养吸收和运动过程,但大肠具有三个主要功能:吸收水和电解质,产生和吸收维生素以及形成和运输排泄的粪便。肠道不断暴露在食物颗粒和食物抗原,生理或机会性微生物群衍生的代谢产物以及其他免疫调节刺激。 胃肠道内的免疫细胞不仅对肠道内的抗原刺激作出反应,而且还显示出扩散到全身的远端器官,表明它们在全系统炎症稳态中的重要性。
微生物无处不在。 他们自我组织,在原本无法居住的生态环境中创建了复杂的生态系统,迅速适应了他们的环境。宿主依赖微生物组实现几种基本的共生功能,例如启动免疫系统和生产必需的维生素,以及从食物中获取能量。 肠道微生物群(定义为人类体内的微生物分类群)现在被认为是内分泌器官,可产生可在宿主中充当效应子的代谢产物,从而触发局部微环境或远端的靶器官系统(如心脏,肾脏,脉管系统)的反应和大脑。
肠腔内壁衬里是抵抗细菌感染的生理屏障,可以与毒素结合。此外,粘液是细菌的营养来源,因此会影响具有在粘液层中生存和扩展能力的微生物的定殖。Akkermansia muciniphila(AKK菌) 和Citrobacter rodentium (柠檬酸杆菌)能够降解粘蛋白,而后者在纤维缺乏期间会增殖。结肠粘液层完整性的丧失会增加宿主对病原体的敏感性。 在健康条件下,紧密的上皮层可防止病原微生物的入侵,而某些刺激物(如炎症性疾病或西餐)可导致肠道通透性和所谓的肠道渗漏综合征的发展。
随着高通量测序技术和代谢组学的建立以及高性能计算和人工智能的发展,人们逐渐破译生活方式,饮食,药物治疗和肠道微生物组之间的相互关系。每个人肠道微生物组随时间推移相对稳定,并与周围环境平衡共存。但是诸如抗生素,肠道感染以及饮食或生活方式变化等扰动都会引起短暂或持续的变化。
在过去的几十年中,实验和临床研究表明,先天性和适应性免疫系统的细胞在高血压,靶器官损害和心血管疾病(CVD)的发病机理中起着关键作用。促炎性效应记忆T细胞和 T辅助细胞亚型T辅助细胞17(Th17;产生IL-17)和1型辅助细胞(产生IFN-γ)促进高血压和心血管靶器官损伤,而调节性T细胞(Tregs)通常产生大量的抗炎性IL-10可以减轻血管,心脏和肾脏的损害。
此外,γδT细胞和髓样来源的抑制细胞在高血压的发病机理中也起着重要作用。 已经证明可以改变几种T细胞亚型激活状态的树突状细胞会增加盐反应性高血压,并提示其在菌群失调与血压(BP)之间的相互作用中发挥作用。
细菌可以直接或通过其产生的代谢产物与参与心血管的不同免疫细胞发生反应。例如,分段丝状细菌或Bifidobacterium adolescentis(青春双歧杆菌)可诱导Th17细胞,而Lactobacillus murinus(鼠乳杆菌)及其色氨酸代谢产物吲哚3乳酸则可抑制Th17细胞。 和SCFA丁酸盐是结肠中Treg的杰出诱导剂。
图 肠道微生物与宿主免疫相互作用

在宿主和微生物组方面均可发现肠道空间变异性。内腔和组织相关内容的相对水平在此处进行了说明,表明这两种功能的区域专业化。 已知肠道中的内腔含量在微生物负荷,微生物种群以及所产生的微生物产生的代谢产物方面有显着差异。尽管在整个胃肠道中的种群和区域规格都受到微生物的影响, 根据管腔内物质含量的变化,宿主免疫系统同样具有区域特异性。
这里显示的是免疫细胞,这些细胞在免疫稳态过程中表现出空间动态。
高血压的发病机制涉及多种因素,包括遗传、环境、激素、血液动力学和炎症等。越来越多的证据表明,肠道微生物群在高血压的发生和发病机制中起着重要作用。胃肠道是人体内最大的免疫细胞库,代表着环境和宿主的交汇点。因此,生活方式因素的形成和调节的微生物组,影响着高血压疾病形成和发生的风险。一个被广泛研究的例子是膳食纤维的消耗,能导致短链脂肪酸的产生,并有助于抗炎免疫细胞的扩张,从而防止高血压的进展。饮食干预如禁食也被证明通过微生物群影响高血压。
图 血压与肠道菌群的关系
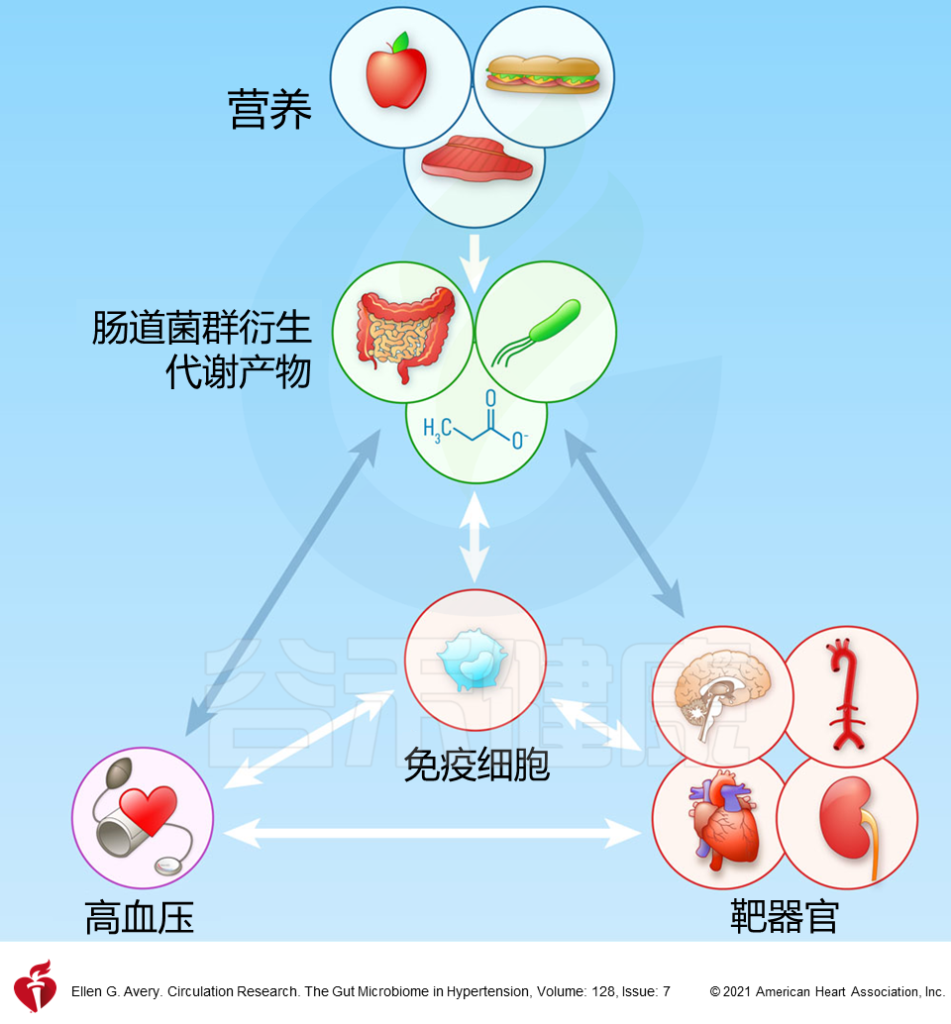
摄入的食物被肠道微生物群转化为小的代谢物。食物抗原、微生物产生的代谢物以及微生物本身都有助于免疫稳态。干扰宿主和微生物群之间的共生关系可通过免疫系统直接或间接导致血压变化和相关的心脏、血管或肾脏损害。
在过去的十年中,许多关于肠道微生物组和高血压的作用的证据已积累起来。多项针对人体的横断面研究表明,肠道微生物组与血压或高血压之间存在关联。高血压患者或血压较高的患者,α多样性降低,肥胖,高胰岛素血症和血脂异常也已观察到。 许多人类肠道微生物组研究报告了革兰氏阴性菌群较高的菌群之间的相关性,包括克雷伯菌,副细菌,脱硫弧菌和普氏菌,尽管并非所有研究都能确定这种模式。
来自HELIUS队列研究(城市环境中的健康生活)的研究表明,克雷伯菌属和链球菌属与血压呈正相关。此外,与高血压小鼠相比,从高血压人类供体接受粪菌移植的GF小鼠出现了与其供体相似的肠道菌群,以及8周后收缩压和舒张压升高。它从2个血压正常的供体那里接受了粪菌移植。
此外,还有几种有价值的啮齿动物高血压模型分析了肠道微生物组和血压的作用。自发性高血压大鼠存在失调,与正常血压WKY(Wistar-Kyoto)对照大鼠的微生物群存在显著差异。自发性高血压大鼠的肠道通透性和菌群失调也可能可通过使用降压药治疗大鼠来补救。
肠道微生物组与高血压之间的联系不是物种特异性的。 例如,在小鼠和人类中高盐处理都会减少乳酸杆菌属。 值得注意的是,未治疗的高血压患者中盐的适度降低能够降低血压并改善动脉顺应性。改善的临床结果伴随着8种循环SCFA的增加(包括2-甲基丁酸、丁酸、己酸、异戊酸和戊酸 )。此外,已证明益生菌乳酸菌处理可通过恢复吲哚3乳酸水平(抑制微生物色氨酸代谢)抑制Th17细胞并减轻盐敏感性高血压。
已显示,Lactobacillus coryniformis可以改善血管功能和胰岛素敏感性。Lactobacillus(乳杆菌)治疗不仅可以改善心血管疾病,还可以改善实验性自身免疫性疾病的结局。 对益生菌对高血压的作用进行调查的随机对照试验的系统评价表明,如果以足够高的剂量使用至少8周,含乳酸杆菌的益生菌是有效的。
在人类中,肠道中的核心微生物群落是稳定的,并且仅在响应诸如肠道感染,整体旅行或药物治疗等主要扰动时才发生变化,从而导致肠道微生物组发生短暂或持续的变化。 肠道菌群不仅对某些饮食刺激的比例具有反应性,而且还可能在时空环境中做出反应。
目前,我们对特定饮食变化影响炎症,自身免疫和心血管疾病易感性的确切机制的理解还很模糊。 使用经过微生物组组成和功能训练的机器学习算法可提供令人兴奋的机会,以促进更好地预测对营养刺激的反应。
新兴的研究表明,饮食因素(高盐或高纤维)和生活方式干预(盐分限制或热量限制)会影响微生物群落的结构和功能,这对免疫细胞活化和血压具有重要意义。西方人的生活方式通常涉及每天进食几顿主餐,并导致细菌多样性下降,某些食物喂养细菌的过度生长,以及随之而来的其他食物为底物的细菌的抑制。因此,菌群产生的代谢产物发生了转移,从而促进了炎症,最终可能导致肥胖症和动脉粥样硬化等疾病的发展。
从历史上看,餐食通常是新鲜烹制的,但如今,人们更经常食用通常含盐量更高的加工食品。这种生活方式通常会导致较高的盐摄入量 而不是医学指南或专家的建议。为减少心脏代谢疾病的风险,通常应节食健康的饮食和运动。 大多数建议的重点是将富含饱和脂肪,糖,盐和卡路里但纤维含量低的西方饮食改变为更健康的地中海式阻止高血压饮食方法,以实现最佳营养,平衡和降低盐摄入量,尽管合规性是一个重大挑战。
SCFA是最典型的微生物群代谢产物之一,它是在不易消化的纤维发酵过程中产生的。 乙酸,丙酸和丁酸是3种高丰度的SCFA。 膳食纤维是由≥3种单体组成的膳食碳水化合物的统称,如非淀粉多糖,抗性淀粉,菊粉,果胶,β-葡聚糖和低聚糖。 这些纤维状化合物中的大多数都被拟杆菌、厚壁菌和放线菌门微生物消化。Bifidobacterium adolescentis, Eubacterium rectale, Eubacterium hallii, Faecalibacterium prausnitzii ,Ruminococcus bromii 通常在大肠中定居,并具有消化纤维以生产SCFA的酶。
大肠的丙酸和丁酸水平比小肠高约4倍。SCFA在结肠中迅速吸收,而丁酸在很大程度上被用作向结肠上皮细胞提供能量的燃料。肠道SCFAs与门静脉血相比要高得多,而门静脉SCFAs较高,其次是肝脏血液,外周血最少,这表明SCFAs基本上被肝脏吸收。肝中丙酸的摄取是糖异生,脂肪生成的前体,以及蛋白质合成,而乙酸盐进入循环系统并被多个组织代谢,并且是胆固醇合成的底物。
SCFA可以与G蛋白偶联受体Gpr41(G蛋白偶联受体41),Gpr43( 小鼠中的G蛋白偶联受体43),Gpr109a(G蛋白偶联受体109 A),Olfr558(嗅觉受体558)和Olfr78(嗅觉受体78),也称为FFARs(游离脂肪酸受体)。FFARs存在于各种组织中,包括血管和肾脏,并参与调节丙酸、乙酸和丁酸的血管反应性。
Gpr41和Olfr78似乎都参与了血压的调节,尽管它们似乎促进了相反的作用。Olfr78激活后会诱导肾素分泌。与此相符的是,Gpr41敲除小鼠为高血压,有趣的是,醋酸盐以前曾用于血液透析缓冲液,但由于其降压作用而被大量废弃,这与SCFA在大多数情况下降低血压的观点一致。
纤维本身已被建议在一定程度上塑造微生物组成。
关于血压,纤维的刺激作用增加了SCFA生产者Faecalibacterium prausnitzii和Eubacterium rectale以及乳杆菌属的丰度。一项具有里程碑意义的研究表明,与传统上纤维含量高的未加工饮食的非洲儿童相比,食用西方饮食的欧洲儿童SCFA水平显着降低,Firmicutes与Bacteroidetes(F/B)比率高。自该研究以来,高F/B比率通常被用作肠道生态失调的替代指标,虽然也已知一些Firmicutes细菌产生有助于健康微生物组的微生物代谢物。
同样,实验工作通常依赖于F/B比作为疾病标志物。自发性高血压大鼠和易中风的自发性高血压大鼠显示F/B比率增加,这支持了这可以作为肠道生态失调的标志物的概念。
各种实验或临床研究已证明益生元高级纤维或后生SCFA治疗对血压的影响。研究报道丙酸在麻醉小鼠中诱导了急性的剂量依赖性降血压反应,这是由Gpr41介导的。益生元纤维不仅可以预防心血管疾病,而且这些营养素的缺乏可能是导致高血压和心血管疾病的危险因素。 还发现在低纤维饮食中添加益生元乙酸盐,丙酸盐或丁酸盐可改善血压并减少靶器官损害。
此外,GF小鼠的粪菌移植表明,与抗性淀粉相比,饮食中的肠道微生物组缺乏抗性淀粉。高纤维情况不仅在血管紧张素II攻击后导致较高的血压,而且还导致了心脏和肾脏损害的发病机制。
德国一项研究测试了在有和没有动脉粥样硬化的高血压小鼠中口服丙酸治疗的特性。在这两种模型中,丙酸治疗均能降低全身和局部炎症反应,血压以及心脏损害。丙酸的治疗作用是由Treg细胞介导的。但是该研究指出丙酸的降血压作用不是急性的,而是随着时间的推移而发生,提示SCFA的抗炎特性间接促进了血管表型的改善。Th17细胞和Th17与Treg的平衡介导SCFA在血压调节中的作用。
关于SCFA在血压中的作用的人类研究非常少见。对微生物群组成和高血压的一些研究表明,SCFA的生产者为Ruminococcaceae spp,Rothia或Roseburia spp. 与较低的血压相关。
在一项小型干预试验中,生物素丁酸酯(600 mg / d),益生素菊粉(10 g / d)以及这两者的组合均降低了代谢综合征患者的舒张压。在HELIUS队列中,将机器学习算法应用于微生物组数据可确定Roseburia spp解释对血压的最大绝对影响,甚至在调整混杂因素(包括使用药物)后,丰度也使收缩压降低4.1 mmHg。
相反,血压较高的患者的粪便SCFA水平较高。这种正相关与以前的研究一致,但似乎与血压与胃肠道内微生物SCFA生产者之间的负相关性相矛盾。 但是,粪便中的SCFA含量不一定反映肠道内的SCFA含量,而是反映肠道中产生的SCFA含量而宿主无法吸收的。
自发性高血压大鼠的实验工作支持了这一观点,表明实验性高血压会减少结肠丁酸对宿主的吸收。此外,AT1(血管紧张素II型1型)受体阻滞剂坎地沙坦(一种经常用于治疗高血压的药物) 已发现自发性高血压大鼠可以增加乳杆菌的丰度和粪便SCFA水平,改善肠道完整性并降低血压。
坎地沙坦治疗改善了重度肥胖受试者肠道中丁酸生成基因的缺失。总之,在HELIUS队列中,基于肠道微生物群组成的机器学习模型分别解释了收缩压和舒张压变异性的4.4%和4.3%。
纤维来源的SCFAs不仅影响血压,而且在其他心血管疾病和自身免疫中也起着关键作用。例如,用醋酸盐,丙酸盐或丁酸盐进行生物后处理可改善急性肾损伤。肾脏保护与局部和全身炎症反应减少,氧化性细胞应激和细胞凋亡。在多发性硬化症动物模型中,T细胞介导的中枢神经系统炎症性疾病丙酸盐增加了肠道和脾脏中抗炎Tregs的频率,这伴随着临床症状的改善。
高纤维摄入量和增加的SCFA浓度也被证明可以保护中枢神经系统。值得注意的是,多发性硬化症患者可以从丙酸盐治疗中获益。短期丙酸盐治疗导致显着和持续的富集功能正常的Tregs,同时1型辅助细胞和Th17细胞同时消耗。此外,补充SCFA或高纤维摄入对类风湿性关节炎(一种关节慢性炎症性疾病)的预后有积极影响。丙酸酯可增加骨量,并且发现SCFA通过增加Treg的数量刺激骨形成。
从机制上讲,SCFA可以影响不同的免疫细胞群。 例如,发现丙酸和丁酸处理后中性粒细胞产生的炎性细胞因子较少。丁酸还可以减少氧化应激和吞噬能力。
SCFA通过减少树突状细胞成熟并抑制CD4和CD8T细胞增殖来调节炎症过程。与乙酸盐相反,丁酸盐或丙酸盐通过HDAC(组蛋白脱乙酰基酶)抑制作用影响骨髓前体细胞的树突状细胞成熟。此外,丁酸可促使M1巨噬细胞分泌更少的炎性细胞因子,增加抗炎细胞因子IL-10的分泌。
SCFAs还引起人单核细胞和T细胞中抗炎标记的表达。 例如,丁酸抑制金黄色葡萄球菌刺激的人单核细胞中IL-12的产生并增强IL-10的分泌。
最近,研究证明了丙酸会降低Th17细胞分化的速率。还发现丁酸盐还通过Gpr43增加1型辅助细胞分化细胞中IL-10的分泌,由SCFA驱动的IL-10诱导激活STAT3(信号转导子和转录激活子3)和mTOR(雷帕霉素的机械靶标),从而上调转录因子B淋巴细胞诱导的表达成熟蛋白。
此外,SCFA最深入研究的特性之一是它们在诱导抗炎Treg中的作用。丁酸和丙酸可增加鼠和人Treg的分化并增强其抑制能力。除丁酸外,丙酸(而非乙酸)通过HDAC诱导外周新生Treg细胞形成。值得注意的是,Clostridia(梭菌)是共生微生物的主要类别,它介导了诱导性结肠Tregs,这与Clostridium butyricum(酪酸梭状芽胞杆菌)诱导Tregs并减少Th17细胞从而减轻实验性自身免疫的症状的发现是一致的。
越来越多的证据表明,禁食是控制代谢性疾病和炎性疾病的有效工具。热量限制会影响微生物组的基本原理令人兴奋。 然而,仍然缺乏关于人类的可靠数据。
一项研究关于10天定期禁食对15名健康男性的粪便微生物群的影响。禁食导致Lachnospiraceae和Ruminococcaceae菌减少。一项小型的人体试验研究表明,斋月禁食影响了健康受试者的微生物组,丰富了一些SCFA生产者。
在一项临床研究中,35名代谢综合征患者接受了5天的禁食,然后进行了3周的DASH饮食,也被译为「得舒饮食」,字面意思是防止高血压的饮食方法饮食。

对照组仅接受DASH饮食。禁食后接着DASH饮食降低血压,需要抗高血压药物和干预后3个月的体重,并改变影响SCFA生产者的肠道微生物群。队列对血压反应性的分层显示,空腹组中存在的免疫细胞变化在血压反应者中比在无反应者中更明显。
此外,禁食组的免疫移位与DASH组观察到的变化根本不同。观察到干预后禁食组中血压响应者特异性微生物组的变化(F.prausnitzii,拟杆菌和厚壁菌的富集;放线菌的消耗)。值得注意的是,丁酸盐生产者F.prausnitzii的富集甚至在禁食后3个月仍然存在。血压反应者和无反应者不仅对禁食反应不同,而且在基线时的丙酸合成能力不同。
将机器学习算法应用于基线免疫组或16S微生物组数据,预测模型通过重新分析调查禁食和血压影响队列(Mesnage数据集)证实,队列中显着的长期血压下降预计准确率约为70%,进一步支持这些发现可能是普遍化的想法。重要的是要强调,上述研究建立了微生物组和血压之间的关联,以应对禁食。禁食对许多患者来说是一项艰巨的挑战。能够操纵负责响应禁食的血压变化的机制将具有高临床效用。
禁食是热量限制的一种极端形式,在不同的文化和宗教习俗中起着重要的作用。 大量的热量限制不仅影响宿主的健康和生理,还降低了血压。生活方式和饮食引起的微生物群及其代谢产物的扰动可直接影响上皮细胞和免疫细胞的稳态。但是我们对营养,微生物群和微生物产物,免疫系统与宿主健康或疾病之间的联系仍处于‘婴儿期’。
宿主-微生物组相互作用对人类健康和疾病显然有影响。模型系统经常用于基础和临床前高血压研究,以研究疾病的发病机制和进展。小鼠和大鼠模型非常有用,可以提供人类队列研究无法获得的信息。然而,在模型系统中研究人-宿主-微生物组相互作用存在许多障碍。
差 异
01 胃肠生理学和形态学有许多方面,这在人类和啮齿动物物种之间是截然不同的。盲肠可能是人类和啮齿动物不同物种形成的最明显的例子,以及小鼠结肠粘液层的薄度。
02 小鼠和人类对炎症应激物的基因组反应是明显不同的,这可能与宿主特异性或微生物组特异性特征或两者的组合有关。
03 居住在胃肠道的微生物在小鼠和人类之间通常也是不同的。人和小鼠只有约15%的细菌谱系。虽然它们在属或门的水平上可能具有可比性,但物种特异性变化通常在高血压中具有临床重要性。
04 已知在每个微生物进化枝内,成员物种之间共享功能特性的程度例如,厚壁菌作为进化枝特别代谢不一致,当考虑到普遍使用F/B比率作为生态失调的标志物时,这再次提出了一个问题。
05 由于人类微生物组随时间的相对稳定性,实验室小鼠在这方面与人类不同。
06 小鼠和人体免疫组成和建立不同,人类免疫系统的强劲发展,需要接触各种真菌,病毒,微生物等,而GF小鼠与人或大鼠微生物的定殖不会诱导免疫成熟,只有小鼠特异性微生物能够诱导完全的免疫能力。
07 啮齿动物模型的嗜食性已被认为对微生物组具有独特的影响,这可以通过使用单一住房策略来避免,尽管这会诱发小鼠的应激反应,增加一个额外的混杂因素。
许多研究人员试图通过使用人类微生物定殖小鼠或野外捕获的小鼠来规避物种比较问题。这提出了两个重要的挑战,应该加以考虑。
一,存在宿主与其微生物之间相互作用的相互排斥的问题。事实上,这种相互作用的重要性在最近的一项研究中得到了证实,该研究表明GF小鼠与人或大鼠微生物的定殖不会诱导免疫成熟,只有小鼠特异性微生物能够诱导完全的免疫能力。有几点差异在小鼠和人体免疫组成之间注意到,这可能与免疫微生物组轴有关,例如,与小鼠(10%–25%)相比,外周血中性粒细胞的比例约为人类的两倍(50%–70%)。此外,CD8+T细胞在成年人非淋巴组织中的分布远高于无特定病原体的小鼠,这可能对细胞内感染或癌症的进展有影响。
二,尽管野外捕获的小鼠比实验室培养的无特定病原体的小鼠更准确地概括人体生理,可能与临床试验结果的一致性更高,对疾病的抵抗力更强。但是在科研研究和临床上应用大规模野外捕获老鼠的可能性会受到限制。
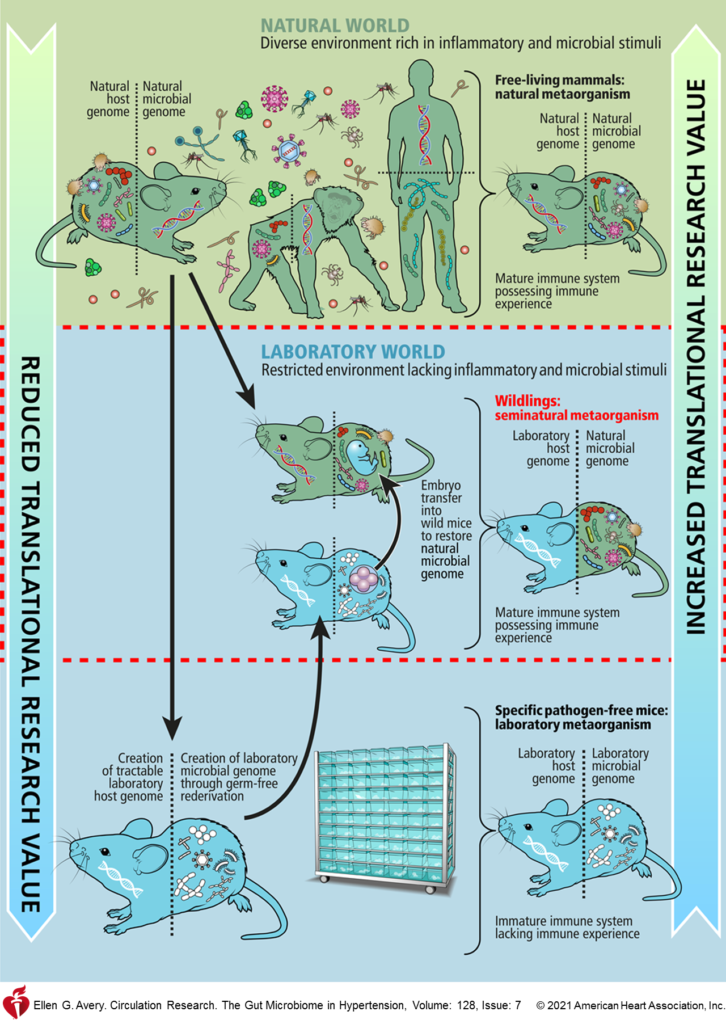
因此,在未来动物研究中,整个领域的程序标准化,例如使用同窝对照和可能影响微生物组的条件的稳健记录是必不可少的。要注意笼养,用品和饮食等因素可能会对结果产生重大影响。此外,采样时间,地点也尽量一致。
值得注意的是除了不同胃肠道区域的空间动态外,从粘膜和管腔空间取样的微生物组在小鼠和人类中是独特的。由于胃肠道是免疫细胞极化和微生物产生的代谢物吸收的作用部位,许多人质疑粪便取样是否正确研究宿主-微生物组界面的途径。粪便代表该系统的排泄产物。
然而,粪便取样是检查微生物组的最常见和实际适用的方法,特别是对于需要非侵入性方法的纵向研究。粪便的收集无疑有助于我们理解宿主-微生物组的相互作用。尽管怀疑局部产生的微生物副产物的相关性是重要的,特别是影响代谢物对循环的摄取并影响胃肠免疫细胞的活性,但是该隔室的测量是不发达的。在间质液中的作用部位鉴定微生物产生的化合物的能力可能提供对宿主-微生物组动力学的不同观点。
总之,尽管在解释微生物组数据时需要谨慎,但是,高血压中微生物组-宿主界面的研究是一个有前途且正在迅猛加速的研究领域。随着各种技术的进一步发展,针对微生物组领域的以药理学和辅助诊断方式为中心的方案可能会在不久的将来出现。
相关阅读:
参考文献:
Schluter J, Peled JU, Taylor BP, Markey KA, Smith M, Taur Y, Niehus R, Staffas A, Dai A, Fontana E, et al.. The gut microbiota is associated with immune cell dynamics in humans.Nature. 2020; 588:303–307.
Evangelou E, Warren HR, Mosen-Ansorena D, Mifsud B, Pazoki R, Gao H, Ntritsos G, Dimou N, Cabrera CP, Karaman I, et al.; Million Veteran Program. Genetic analysis of over 1 million people identifies 535 new loci associated with blood pressure traits.Nat Genet. 2018; 50:1412–1425.
Ellen G. Avery. CirculationResearch. The Gut Microbiome in Hypertension, Volume: 128, Issue: 7, Pages:934-950
Tierney BT, Yang Z, Luber JM, Beaudin M, Wibowo MC, Baek C, Mehlenbacher E, Patel CJ, Kostic AD. The landscape of genetic content in the gut and oral human microbiome.Cell Host Microbe. 2019; 26:283–295
Forslund K, Hildebrand F, Nielsen T, Falony G, Le Chatelier E, Sunagawa S, Prifti E, Vieira-Silva S, Gudmundsdottir V, Pedersen HK, et al.; MetaHIT Consortium. Disentangling type 2 diabetes and metformin treatment signatures in the human gut microbiota.Nature. 2015; 528:262–266.
Verger EO, Armstrong P, Nielsen T, Chakaroun R, Aron-Wisnewsky J, Gøbel RJ, Schütz T, Delaere F, Gausseres N, Clément K, et al.; MetaCardis Consortium. Dietary assessment in the metacardis study: development and relative validity of an online food frequency questionnaire.J Acad Nutr Diet. 2017; 117:878–888.