-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com

谷禾健康
2024年6月19日,广东省人民医院儿科杨敏团队取得了一项备受瞩目的成果。该团队关于“肠道菌群失调通过糖原贮积病中的 CCL4L2-VSIR 轴引发炎症性肠病”,在国际著名期刊《Advanced Science》(影响因子IF=15.1)发表,针对这一通路不仅可以为 GSD 患者提供有益的治疗,还可以为结肠炎和其他形式的 IBD 患者提供有益的治疗。
谷禾健康技术团队参与并支持本研究的菌群测序和分析部分。
这一突破性研究为糖原贮积病及其相关并发症的治疗提供了新的视角,这也是我国儿科在罕见病领域的研究中取得的重大突破。

糖原贮积病(GSD),是一类由于先天性酶缺陷所造成的糖原代谢障碍疾病,多数属常染色体隐性遗传,发病因种族而异。该病类型多样,其中GSD-Ib型患者常伴有炎症性肠病。
在GSD-Ib型患者中,肠道菌群失调通过CCL4L2-VSIR轴影响炎症性肠病(IBD)。研究发现,与典型IBD不同,GSD-Ib患者展现出独特的消化道症状和肠道菌群特征。
肠道菌群失调主要由特定病原菌引起,导致肠道巨噬细胞过度激活,CCL4L2-VSIR轴的过度激活促进上皮细胞特定基因的表达,从而推动IBD的进展。
研究结果表明,靶向肠道菌群失调或CCL4L2-VSIR轴可能成为治疗GSD相关IBD的潜在策略。
糖原是肝脏和骨骼肌中储存的葡萄糖形式,其分解提供稳定的葡萄糖供应。当特定酶的活性缺失时,会导致糖原积累,进而影响组织的功能,导致一系列健康问题,包括低血糖、肌肉痉挛、疲劳、肝脏肿大等。
糖原贮积病的类型多样,根据受影响的酶和组织不同,可以分为几种主要类型。例如:
糖原贮积病的治疗主要是通过调节血糖水平和预防低血糖来管理。对于GSD-Ia和GSD-Ib,过去十多年的治疗方法包括间歇性未煮玉米淀粉或通过胃管给予夜间葡萄糖输注。给GSD-III患者高蛋白饮食,以增加儿童的生长速率。
GSD不仅影响儿童,成人也可能受到影响。未经最佳终身饮食葡萄糖治疗的成人GSD患者的长期预后不佳,可能会出现多种并发症,成人GSD患者常见的并发症包括骨质疏松症和骨折、肾结石、肾盂肾炎等。
▼
正常情况下,人体摄入的碳水化合物会被转化为葡萄糖,一部分葡萄糖会被立即利用以提供能量,而多余的葡萄糖则会在肝脏和肌肉等组织中合成糖原储存起来。当身体需要能量时,糖原又会分解为葡萄糖以供使用。
然而,在糖原贮积病患者中,由于参与糖原合成或分解的某些酶存在缺陷,导致糖原的合成、分解或储存出现异常,从而引起一系列的健康问题,包括低血糖、肌肉痉挛、疲劳、肝脏肿大等。
这类疾病有一个共同的生化特征,即是糖原贮存异常,绝大多数是糖原在肝脏、肌肉、肾脏等组织中贮积量增加。
▼
糖原贮积病是一种罕见病,总体发病率相对较低,但具体的发病率因不同类型的糖原贮积病而有所差异。
《世界胃肠病学杂志》资料显示,发病率约为20000-43000名新生儿中的1人。
由于其症状的多样性和隐匿性,一些病例可能未被准确诊断,实际的发病率可能被低估。
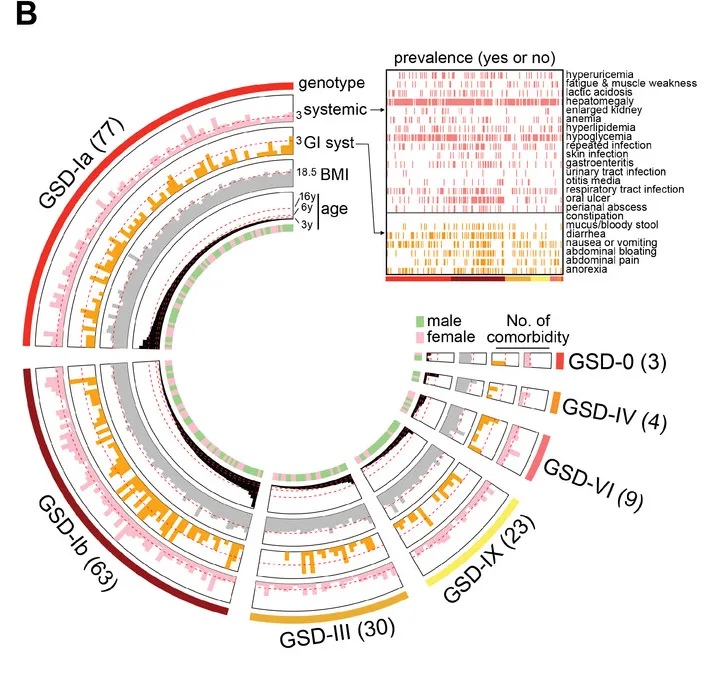
为了调查中国大陆GSD的流行病学和临床特征,杨敏及其团队进行了两项大型多中心研究,并通过问卷调查报告了2020年10月至2021年6月的209例GSD病例(如图)。
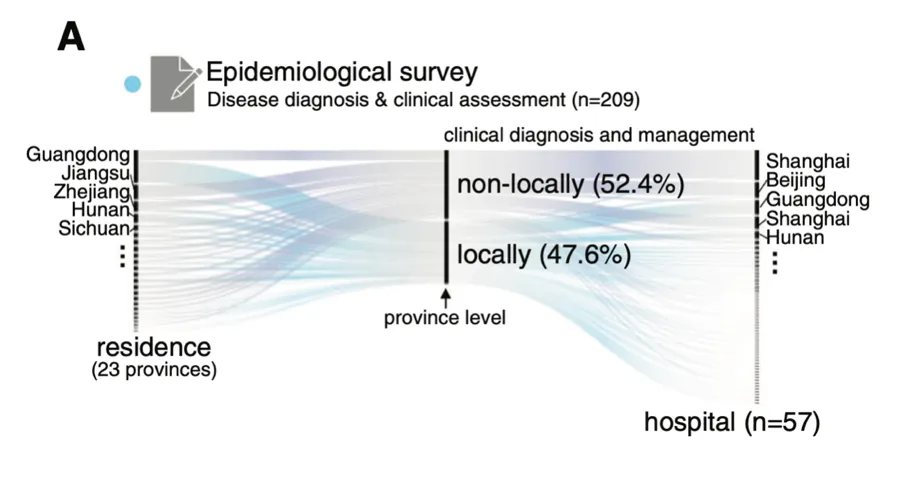
关于患者的就医情况,其中最显著的一个特点是超半数家庭(52.4%)为“省级”外来病例,就医的医院主要来自相对发达地区。且就诊地主要集中在上海、北京、广东等医疗资源相对发达的城市。
▼
糖原合成和分解代谢中所必需的各种酶至少有8种,由于这些酶缺陷所造成的临床疾病有15型,其中:
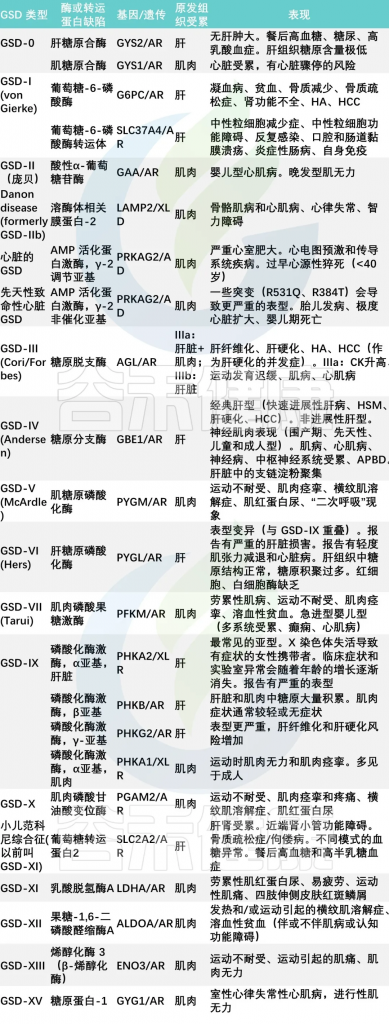
doi: 10.3748/wjg.v29.i25.3932
杨敏团队的调查研究中,主要包括6种类型的GSD,即:
其中最常见的是I型(66.9%)。
▼
不同类型的糖原贮积病临床表现各异,但常见的症状包括:
低血糖、肝肿大、酸中毒(乳酸性酸中毒)、高脂血症、高尿酸血症、疲劳、肌肉无力等。
由于糖原无法正常分解为葡萄糖,患者在空腹或长时间运动后容易出现低血糖症状,如头晕、乏力、出汗、心慌等。
糖原在肝脏中过度积累,导致肝脏体积增大。
长期的低血糖和代谢紊乱可能影响儿童的生长发育,导致身高、体重增长缓慢。
某些类型的糖原贮积病会影响肌肉功能,表现为肌肉无力、疼痛、痉挛等。
如Ⅱ型糖原贮积病可能导致心脏肥大、呼吸肌无力等,严重影响心肺功能。
其中:
口疮性口炎、肛周病变、胃肠炎、呼吸道感染和皮肤感染等症状在I型GSD中更常见;
厌食、呕吐、腹泻、粘液/血便、腹痛和腹胀是 GSD 患者常见的胃肠道并发症,尤其是在 GSD-Ib 组(77.8%)。
造成患者家庭问诊困难的一个主要原因是该疾病表型的复杂,例如下图:
一种奇怪的糖原贮积病亚型:许多GSD-lb患者也患有慢性 IBD
杨敏教授表示,他们关注 GSD相关IBD 已有近10年了。多中心内镜监测研究中,他们招募了 32 名 GSD 患者。这些患者在内镜检查期间表现出活动性胃肠道症状。在这 32 名患者中,27 名患有 GSD-Ib,25 名最初诊断为 IBD。
其中GSD-Ib型患儿消化道症状比例最高(77.8%)且最为特殊,表现为单个或多发散在深圆形溃疡、炎性假息肉、梗阻和狭窄(如下图)。
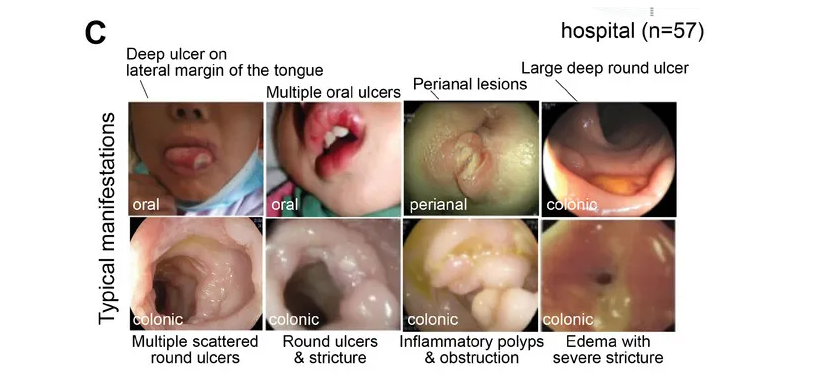
目前人们对 GSD-lb 中 IBD 的发病机制和发病原因知之甚少,超过 70% 的病例会出现严重的消化道症状,而这种症状在其他疾病亚型中偶尔才会出现。
如果不具体了解这些机制以及免疫系统与肠道微生物群之间的关系,科学家将无法开发出针对与 GSD 相关的 IBD 症状的有效治疗方法或干预措施。杨敏及其团队希望改变这一现状,开始了他们的实验探索过程。
▼
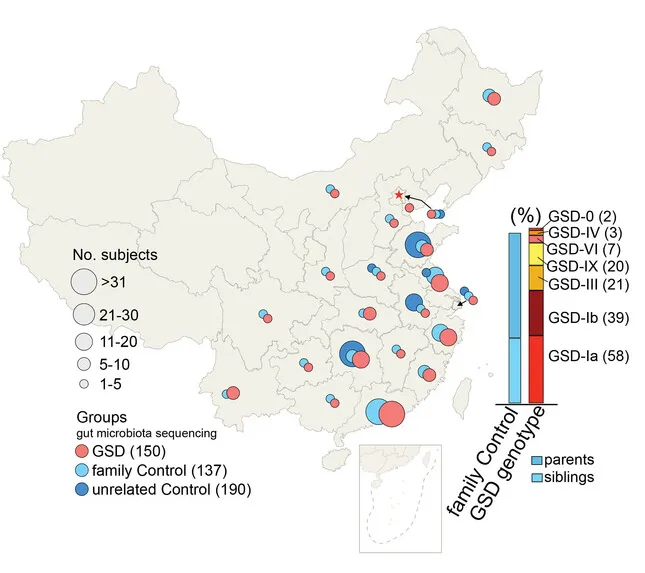
为了探究GSD群体消化系统异常,特别是IBD高发的原因,杨敏及其团队在全国23个省份招募了150名GSD患者(共涵盖Ia、Ib、III、IX、VI、IV及0型共7种类型)采集粪便样本, 327个健康对照者的粪便样本。
注:这327个对照样本包括:137 名家庭对照者和 190 名在山东、浙江、湖南等地收集的无关健康对照者。
GSD基因型是肠道菌群的主要影响因素
肠道菌群受多种因素影响,包括饮食、地域和医疗条件等。
通过结合个人临床信息与肠道菌群数据的EnvFit分析发现(如下图),共有45个个人因素与肠道菌群的变异显著相关,如疾病情况(基因型)、家庭因素、年龄、身高体重、共患病等等。
值得注意的是,在这个队列中,GSD基因型主要影响肠道菌群组成。总体而言,家庭因素(家庭组配对比较)和居住地区是影响肠道菌群组成的第二和第三重要因素。
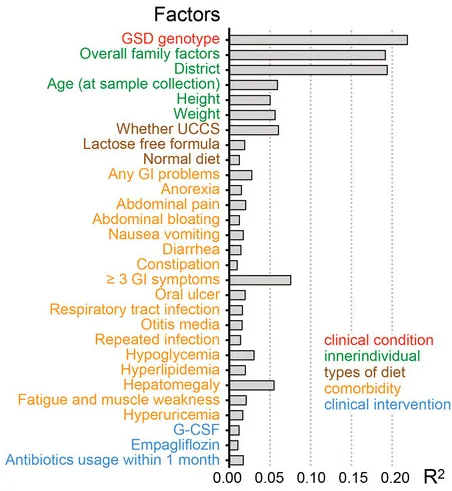
这在肠道菌群研究中颇为少见,因为多数研究认为地域因素极大且显著地影响个体菌群构成。这说明,特殊的基因型对于塑造个体肠道菌群构成起到决定性作用。
具体而言,研究人员将患者分为三组:
GSD-Ia、GSD-Ib、GSD-no IaIb
▼
GSD引起了个体肠道菌群多样性显著降低(下图H)及潜在致病菌显著升高(下图G),特别是GSD-Ia和GSD-Ib。这些肠道菌群的变化在校正性别、年龄、BMI和地域等因素后,仍然存在。
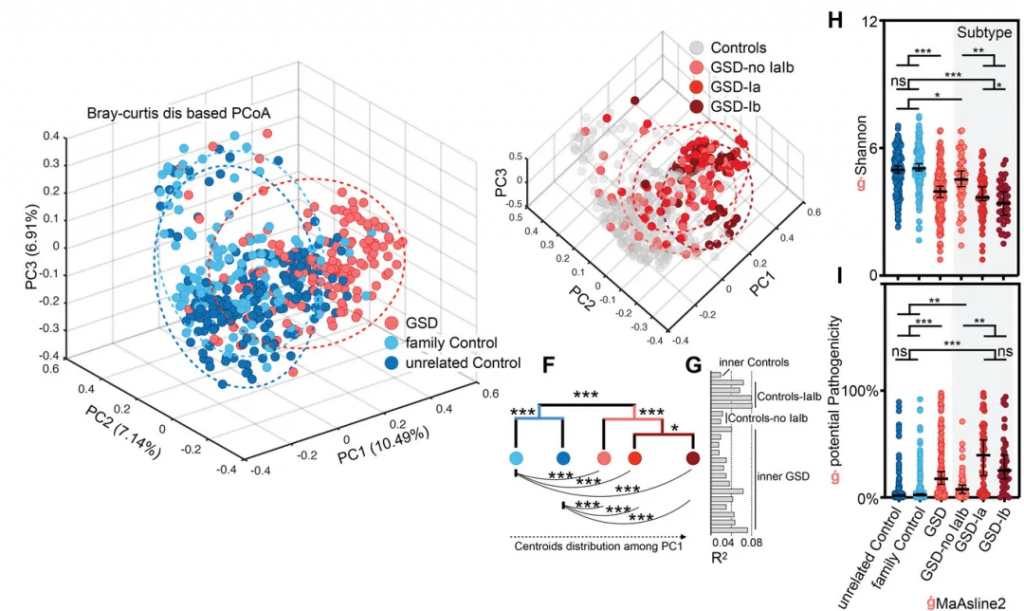
厚壁菌门和拟杆菌门仍是主要菌群;但变形菌门和放线菌门的比例显著增加。
GSD 患者共有31个属发生显著改变。其中18个属减少,而其余13个增加。这31个属中28个属在校正掉性别、年龄、BMI和地域等因素影响后,仍与GSD显著相关(下图D)。
有22物种的丰度和GSD显著关联(下图E),其中10 个增加和12个降低。
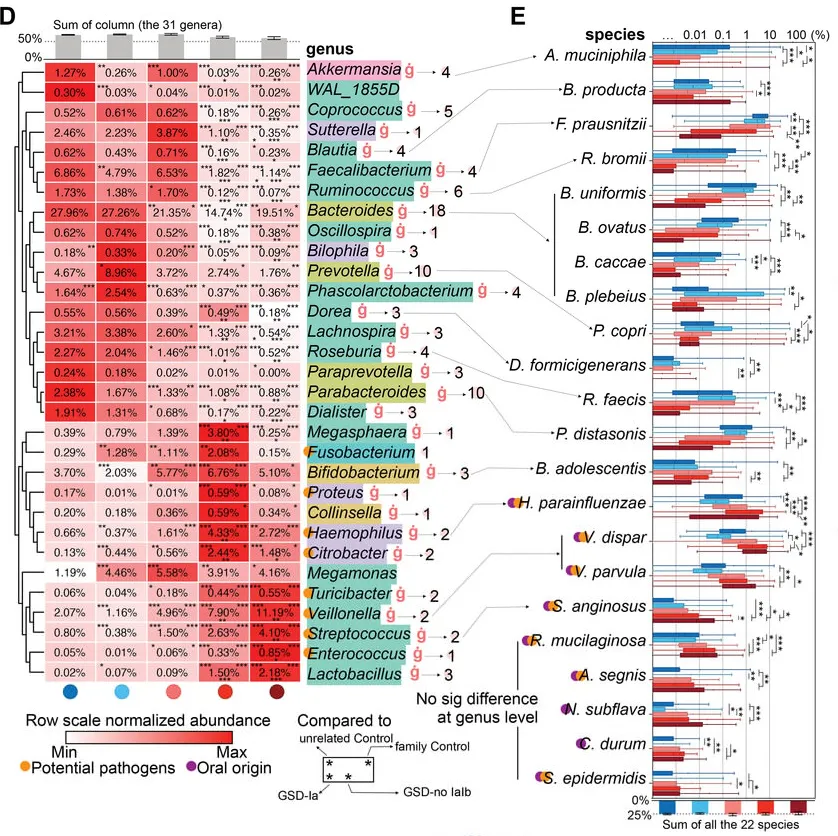
这31个显著改变的属的总丰度在不同分组人群中的总占比达到60-70%,种水平则为~25%,表明这些GSD相关的属种变化,是肠道菌群构成主体的紊乱。
▼
GSD-Ia和GSD-Ib患者表现出更严重的菌群紊乱,特别是那些最常见、功能性的微生物类群在其肠道内丢失,例如下列菌群在GSD-Ia和-Ib几乎完全耗尽:
丁酸可增强上皮氧合,有利于结肠中的低氧微环境并抑制病原体定植。然而,主要丁酸生产菌,如拟杆菌属、粪杆菌属和瘤胃球菌,以及相关代谢途径在GSD中显著降低,这可能导致兼性厌氧病原菌的延伸。
具体到每个菌来说:
AKK菌与肠道屏障的维持和抗炎作用有关,其减少可能会削弱肠道屏障,增加肠道炎症的风险,从而可能与IBD症状的出现有关。
粪杆菌参与肠道内的发酵过程,对维持肠道健康和免疫功能有重要作用。在糖原贮积病患者中,由于糖原代谢异常可能影响了肠道环境,进而影响了粪杆菌的定殖和功能,导致其数量减少。这可能会减少短链脂肪酸的产生,影响肠道健康。
拟杆菌在肠道内参与碳水化合物的分解,产生短链脂肪酸,糖原贮积病患者拟杆菌的减少可能导致肠道炎症反应加剧,与IBD症状的出现有关。
瘤胃球菌是产生短链脂肪酸的重要菌群,对肠道健康和宿主能量代谢有重要作用。瘤胃球菌的减少可能会导致短链脂肪酸的产生下降,影响肠道屏障功能和抗炎作用,从而可能与IBD症状的出现有关。以动物为基础的饮食会增加有害菌Ruminococcus gnavus。
GSD患者中存在口腔源的潜在病原体激增,例如:
口腔中的致病菌可以在肠道中定植和繁殖,说明肠道为这些菌群的生长繁殖提供了条件和环境。
链球菌,已被证明可通过GasderminA依赖性细胞焦亡诱导肠道损伤;可能通过产生超抗原等物质激活宿主T细胞免疫反应进而引发肠道炎症。
肠球菌的成员已显示出促炎作用;肠球菌可以通过分泌金属蛋白酶分解上皮钙黏蛋白破坏肠屏障。
韦荣氏球菌属在IBD中延伸,细小病毒通过产生硝酸盐诱导炎症。韦荣氏球菌属和链球菌的组合抑制了IL-12p70的生物合成,随后增强了IL-8、IL-6和TNFα的炎症反应。
菌群该定植时未定植,该退出时却长期占据
值得注意的是,双歧杆菌、韦荣球菌和乳杆菌这些本应该在健康儿童生命早期保持较高比例的细菌,在GSD患者的肠道中扩张,并且这些细菌在 GSD 患者的整个童年和成年期都会扩增,这可能抑制了其他正常菌群的定植。
▼
GSD患者肠道菌群发育落后于实际年龄
使用微生物组年龄Z分数(MAZ)评估菌群发育状态,随机森林回归和调整的深度神经网络分析均显示GSD患者的MAZ显著降低,特别是在GSD-Ia和Ib患者中。
这表明GSD患者的肠道菌群发育落后于实际年龄,呈现发育延迟状态。
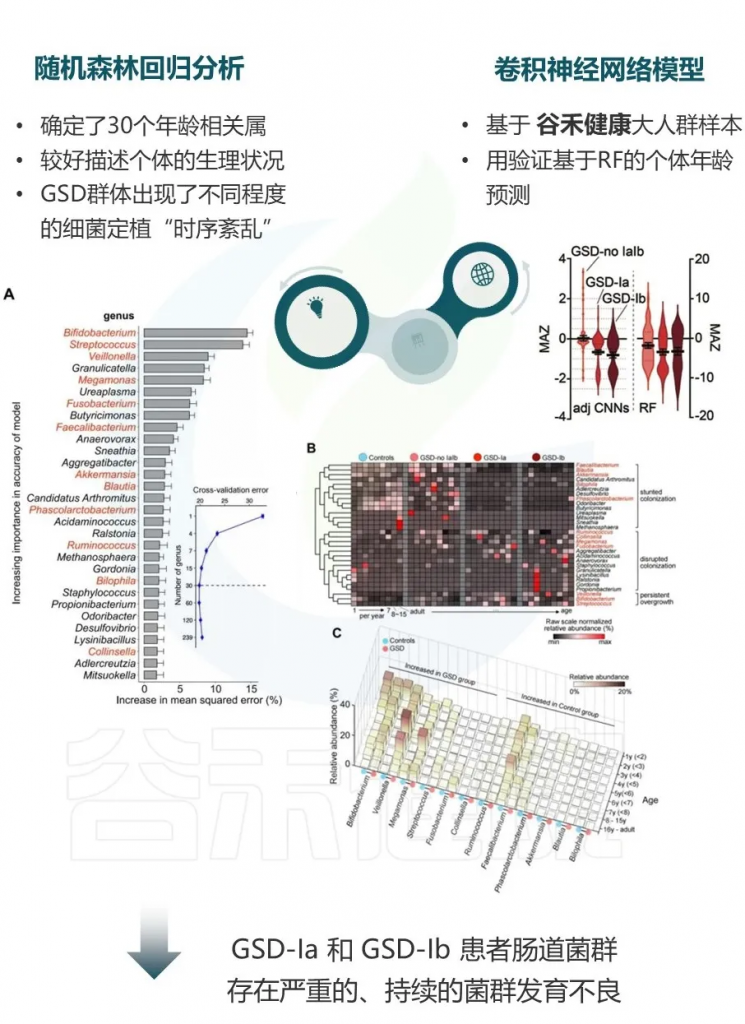
▼
从数据分析的角度,研究团队进一步分析了GSD患病情况、共患病与肠道菌群紊乱的中介关系。
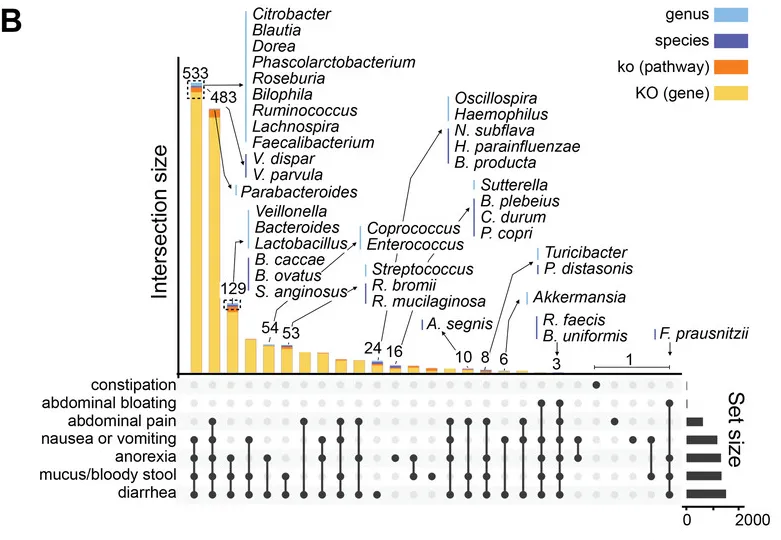
他们用最具代表性的肠道微生物特征和临床元数据构建了一个中介模型,在校正年龄、性别、BMI、地域及特殊治疗性饮食(生玉米淀粉)的影响后,肠道菌群仍然是GSD背景下,患者消化道异常的显著中介因子(下图)。说明GSD会通过影响肠道菌群构成最终造成消化道异常。
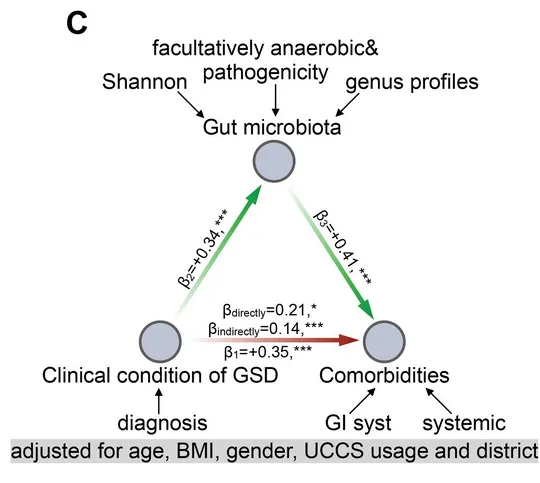
GSD 中这些细菌可能相互依赖资源和生存,形成一个复杂的相互支持网络,肠道菌群失调可能通过细菌的“群体犯罪”引起 GSD 患者的肠道上皮功能障碍。
下面我们来看一下该研究的另一个重要内容——肠道微生物群和免疫细胞之间的“串扰”。
▼
为了明确GSD相关的肠道菌群紊乱,如何引起个体IBD表性的产生。研究者们采集3名GSD-Ib患者的结肠粘膜组织(下图G),并使用单细胞测序技术分析患者结肠粘膜单细胞层面的转录水平变化。通过转录水平注释发现,相较于健康人、典型IBD和结肠炎的肠粘膜组织,GSD-Ib患者肠粘膜上有非常高的巨噬细胞聚集(下图H)。
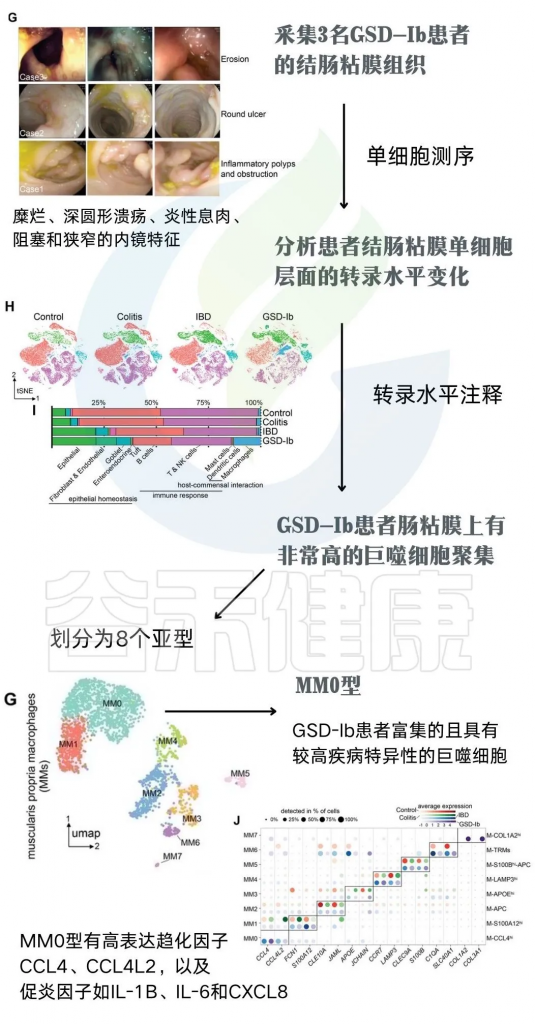
注:巨噬细胞中差异表达基因的KEGG通路注释显示,GSD-Ib中调节抗菌体液免疫反应和趋化因子介导的信号通路的基因集显著富集。GSD-Ib组中上调的基因主要参与环境信息处理和人类疾病。
“
更深入的分析确定了一种巨噬细胞亚型(MM0)的重要性,这种亚型产生一种名为CCL4L2的趋化因子,负责激活其他免疫细胞对抗有害细菌的生长。
虽然CCL4L2的自然功能通常是保护性的,但杨敏及团队怀疑,由于GSD-Ib患者相关肠道细菌的存在,CCL4L2的过度或失调刺激可能是他们出现IBD症状的可能原因。
这一点最初在实验室中得到了支持,其中用有害细菌感染的细胞获得的细胞培养基处理的巨噬细胞,比用对照培养基处理的巨噬细胞更加“激活”。
下面我们来看一下他们选用了哪些菌群进行相关实验,来刺激巨噬细胞:
▼
研究人员选择了三种GSD相关菌群来刺激巨噬细胞,即:
暴露于粪肠球菌、小弧菌和咽峡炎链球菌以及混合感染 (EVS) 的巨噬细胞中 CCL4L2 的表达在 mRNA 和蛋白质水平上显著增加,但不影响 IL-1 β和 IL-6 的表达。
来自EVS感染的条件培养基(CM)与对照组相比,诱导了显著的巨噬细胞迁移趋化性,而这种趋化性部分被CCL4L2中和所减弱。
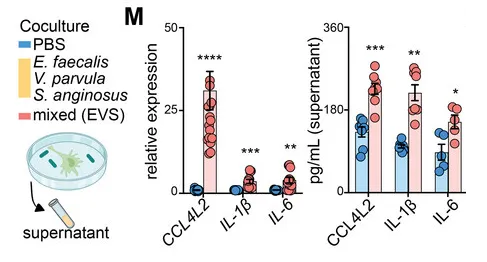
因此,是特定的肠道病原菌(如E. faecalis、V. parvula、S. anginosus)引发了CCL4L2的高表达,那么具体是如何影响炎症性肠病的进展?我们接着看。
“
然后,团队在从GSD-Ib患者取得的活检样本中寻找CCL4L2,并发现CCL4L2蛋白与一种叫做VSIR的受体结合,这种受体存在于肠道细胞壁中。
在IBD的小鼠模型中也发现了类似的结果,科学家们发现与健康对照组相比,巨噬细胞的水平更高,并且在用一种旨在抑制VSIR的抗体处理后,他们发现小鼠的症状加重了。
巨噬细胞通过CCL4L2-VSIR配体-受体信号与肠道上皮细胞相互作用,以促进损伤修复。
具体研究如下:
调节核糖体、氧化磷酸化途径和抗病原体反应的基因集在GSD-Ib上皮细胞中特异性富集。
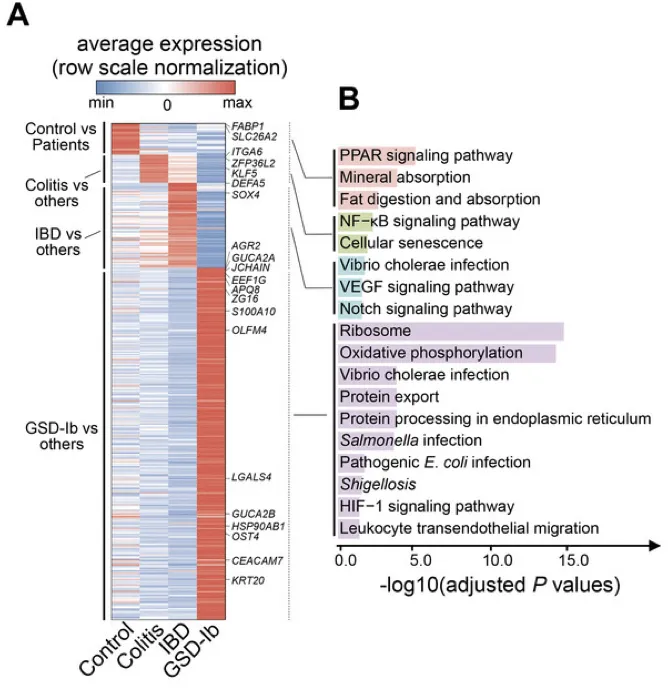
上皮细胞中典型的差异表达基因是AQP8、ZG16、GUCA2C、SLC26A3、AGR2,它们负责吸收、分泌、代谢、上皮屏障完整性、pH稳态、粘液屏障功能。
▼
免疫荧光染色显示GSD-Ib患者肠道组织中CCL4L2和VSIR的显著共定位,进一步验证了CCL4L2在巨噬细胞中的高表达及其与VSIR的相互作用。
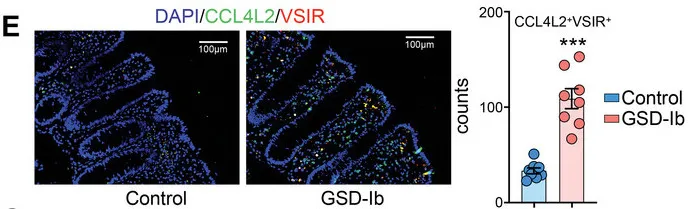
CCL4L2与其受体VSIR形成的CCL4L2-VSIR轴主导参与了MM0型巨噬细胞与其他类型细胞交互,特别是OLFM4+上皮细胞(这类细胞是GSD特异性增加的,同时也被报道在克罗恩病中较高)。
预测MM0巨噬细胞与其他细胞类型之间的相互作用
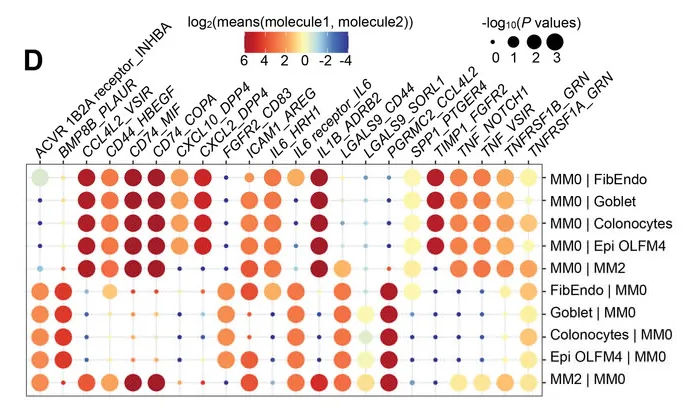
而这些受体细胞的基因表达情况,决定了患者肠道组织的疾病发展方向,如AGR2、ZG16、MUC2等。
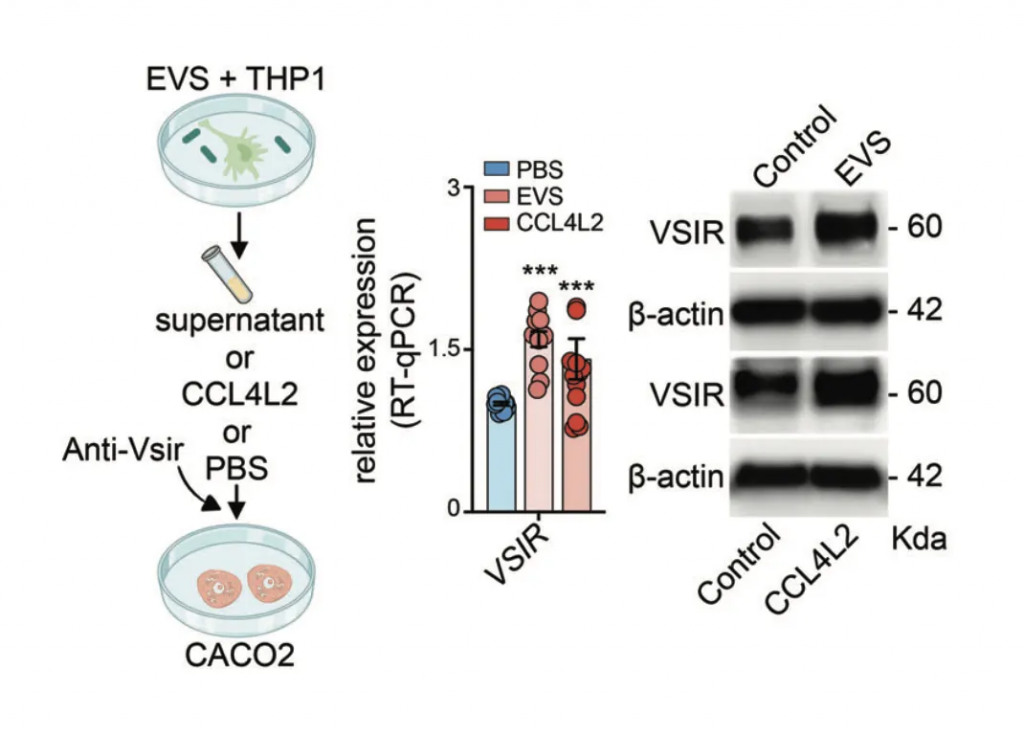
表明GSD相关的肠道菌群紊乱,通过引起肠上皮巨噬细胞高表达趋化因子CCL4L2,激活其他下游细胞膜蛋白VSIR表达,从而引起了GSD独有的消化系统IBD表型。这个现象进一步在C57BL/6小鼠中得到验证。
▼
研究人员在C57BL / 6小鼠中进行了选择性细菌移植,通过口服灌胃的方式将EVS移植到小鼠体内,并用DSS诱导结肠炎。研究发现,抗生素治疗显著降低了EVS灌胃诱导的小鼠血清CCL4L2水平,而抗VSIR则显示出完全相反的趋势。
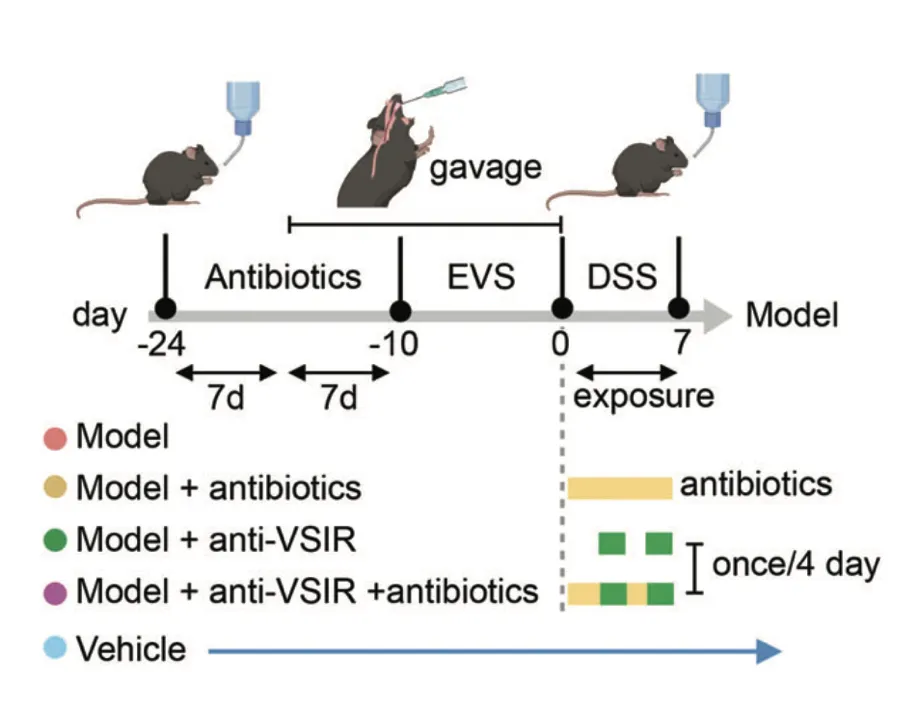
免疫荧光染色显示,模型组中MM0巨噬细胞增强,但在给予抗生素或抗VSIR注射后减少,这进一步导致模型组中肠上皮细胞的MUC2、AGR2和ZG16表达显著下调,引发粘膜损伤。
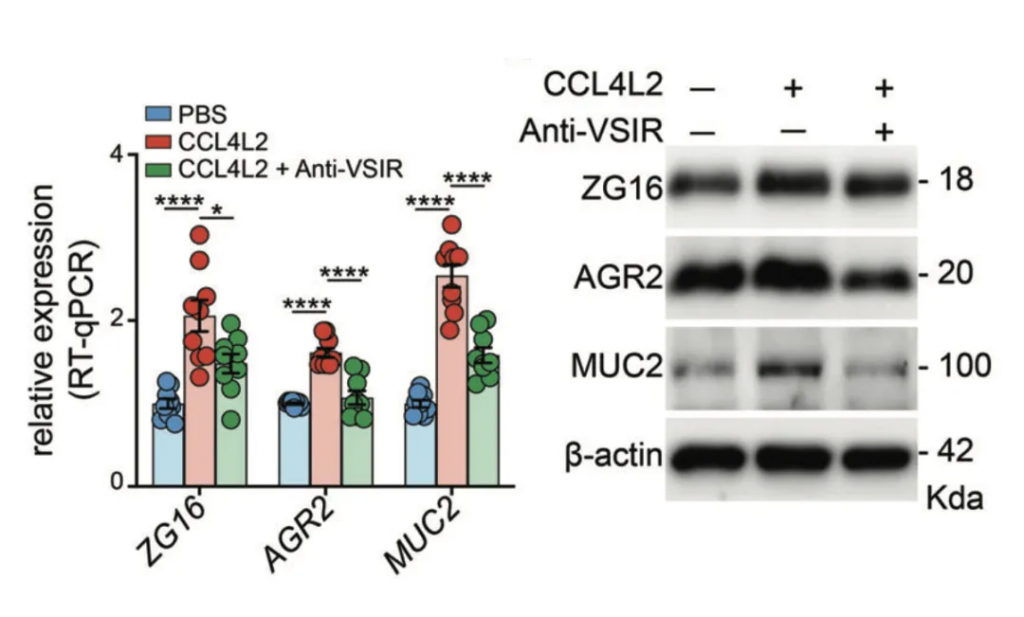
研究结果表明,EVS 增强的 MM0 巨噬细胞可以通过调节 CCL4L2-VSIR 轴来介导结肠肠上皮稳态。因此,靶向CCL4L2-VSIR通路可用于结肠炎和IBD的广泛应用。
肠道驻留免疫细胞和上皮之间的串扰,对于胃肠道稳态、抗原致敏调节、预防感染和 IBD 发展至关重要。在该研究中 GSD相关IBD 与典型的 IBD 相比具有不同的特征,特别是复杂的内镜表现及其特殊的解构:大量巨噬细胞积聚和上皮细胞增殖。
从病因上讲,肠道致病菌激活粘膜巨噬细胞导致胃肠道内形成炎症环境。在 GSD-Ib 中,一群独特的巨噬细胞由致病菌诱导,并表达高水平的趋化因子CCL4L2。
关于CCL4L2的有益方面:
潜在有害方面:
值得注意的是,CCL4L2-VIR通路的激活可能促进严重细胞因子风暴中的T细胞耗竭,这与新冠肺炎的不良预后有关。
靶向CCL4L2-VSIR可以抑制各种炎症性疾病、自身免疫性疾病和肿瘤转移。在这里,研究人员揭示了胃肠道中CCL4L2-VSIR轴的异常激活,最终驱动GSD-Ib中的非典型IBD。该发现为诊断和治疗GSD-Ib以及潜在的GSD相关IBD引入了一个新的靶点,并为VSIR相关研究提供了证据。
总的来说,这项研究证实了在糖原贮积病群体中独有的肠道菌群紊乱,即:
而这样的肠道菌群紊乱会引起个体结肠巨噬细胞高表达CCL4L2,并通过其受体蛋白VSIR介导上皮细胞的异常基因表达,最终造成GSD相关的IBD表型。
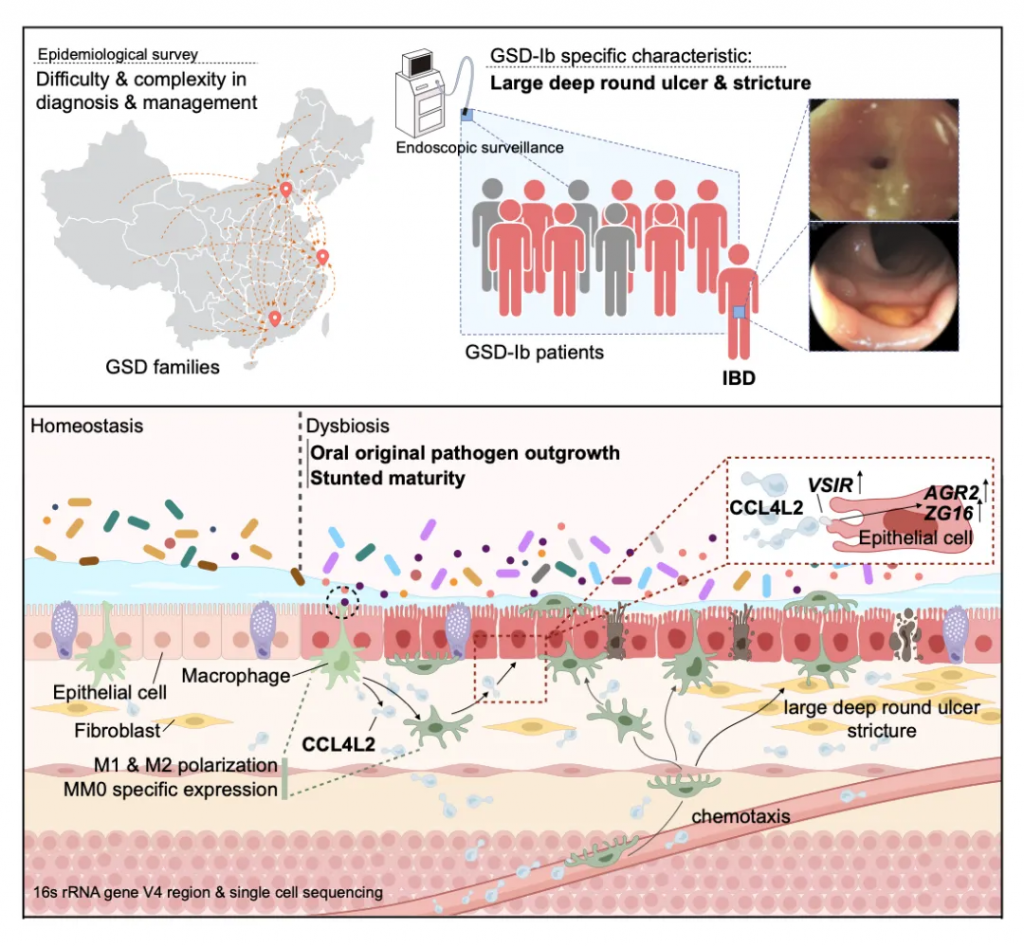
该研究的意义及未来方向:
该研究通过识别GSD-Ib与IBD之间的特定生物学联系,推动了精准医疗在代谢性疾病和消化系统疾病中的应用。
目前杨敏团队正在研究 CCL4L2-VSIR 通路的作用机制,并将探索其在患者治疗中的潜力。该团队预计,针对这一通路不仅可以为 GSD 患者提供有益的治疗,还可以为结肠炎和其他形式的 IBD 患者提供有益的治疗。
CCL4L2-VSIR轴的发现也可能促进新药开发,特别是针对GSD-Ib相关IBD的治疗。
这些研究结果也可应用于个性化治疗方案(基于肠道菌群特征),为患者提供更有效的治疗选择,有助于改善GSD-Ib患者及更广泛消化系统疾病患者的生活质量。
主要参考文献
Lan J, Zhang Y, Jin C, Yang M et al., Gut Dysbiosis Drives Inflammatory Bowel Disease Through the CCL4L2-VSIR Axis in Glycogen Storage Disease. Adv Sci (Weinh). 2024 Jun 18:e2309471.
Gümüş E, Özen H. Glycogen storage diseases: An update. World J Gastroenterol. 2023 Jul 7;29(25):3932-3963.
Hannah WB, Derks TGJ, Drumm ML, Grünert SC, Kishnani PS, Vissing J. Glycogen storage diseases. Nat Rev Dis Primers. 2023 Sep 7;9(1):46.
Zhong J, Gou Y, Zhao P, Dong X, Guo M, Li A, Hao A, Luu HH, He TC, Reid RR, Fan J. Glycogen storage disease type I: Genetic etiology, clinical manifestations, and conventional and gene therapies. Pediatr Discov. 2023;1(2):e3.
Wang Y, Liu H, Dong F, Xiao Y, Xiao F, Ge T, Li D, Yu G, Zhang T. Altered gut microbiota and microbial metabolism in children with hepatic glycogen storage disease: a case-control study. Transl Pediatr. 2023 Apr 29;12(4):572-586.

谷禾健康

细菌耐药性
抗生素耐药性细菌感染的发生率正在上升,而新抗生素的开发由于种种原因在制药行业受重视程度下降。
最新在《柳叶刀-微生物》(The Lancet Microbe)上,科学家提出了基于细菌适应性、竞争和传播的生态原则的跨学科研究方法,可能开辟新途径来对抗抗生素耐药性感染。
许多兼性细菌病原体使用人类粘膜表面作为其主要储藏库,并在微生物组和宿主的某些病理状态下诱发传染病,以帮助其横向传播到新的宿主生物体。
有益的细菌共生体可以战胜特定的病原体,从而降低病原体传播和引起严重感染的能力。然而,尽管具有临床相关性,但对其自然栖息地中的共生-病原体相互作用的了解仍然很少。
本文将在人类微生物组和宿主生物学背景下讨论细菌病原体和共生体之间相互作用的研究最新内容,为预防和治疗传染病提供一些新视角。
The Gut Microbiome
对人类微生物组完整性作为健康需求的日益认可,正在极大地改变人们对细菌微生物组成员及其相互作用的评价,无论是微生物之间的互动还是与宿主的互动。这种理解的变化使得微生物生态学的原则成为了预防和治疗主要人类疾病的创新方法的核心。
从海量数据中分析推断出的微生物组特征正被考虑作为不同疾病诊断中的生物标志物,这些疾病包括各种类型的癌症,如结肠癌或乳腺癌,以及自身免疫性疾病,如类风湿性关节炎或银屑病。
粪便微生物移植在治疗艰难梭菌感染方面已被有效使用,而补充微生物组成员(例如AKK菌)或微生物组产品(例如短链脂肪酸),已显示出在改善代谢紊乱和癌症的健康结果方面的潜力。
然而,环境与人类相关的微生物生态系统之间存在根本性差异。许多环境微生物组代表了广阔、不受限制的生态系统,通常具有无限的生命周期,对微生物扩散几乎没有障碍。相比之下,与宿主相关的微生物组,如人类肠道中的微生物组,是受限的生态系统,具有较短的生命周期。
与宿主相关的微生物组需要特定的细菌机制来在个体和世代之间传播,并在其首选的生活条件之外暂时持续存在。
此外,宿主将微生物定殖者暴露于环境栖息地以外的压力源中,特别是通过其粘膜免疫系统。
Microbial Symbiosis and Pathogenicity
▸ 过去,对共生体和病原体的理解不全面
从历史上看,对与宿主相关的微生物生态系统的研究,曾局限于不同研究团队分别对中性或共生的细菌共生体和有害病原体进行的独立调查。因此,对这些不同组的与宿主相关细菌的当前理解高度不对称,且存在对病原体的强烈偏见,这阻碍了对人类微生物组生态的全面理解。
虽然这些细菌组在自然栖息地中有广泛的相互作用,但关于共生菌和病原体相互作用的实验研究却很少。例如,典型的病原体可以被发现几乎是人类微生物组的驯化成员,而共生菌则可以与病原体勾结,这会像多重微生物感染中那样。
▸ 共生菌和致病菌的区分较复杂
尽管在感染医学中,共生菌和致病菌之间的传统区分仍然是一个重要标准,但在生态学上下文中,这两组微生物固有的属性重叠使得这种区分变得不够充分。
有益的共生现象和对立的致病性代表了细菌行为范围的两个极端(下图),尽管很少有细菌微生物组成员表现出真正的致病行为。多细菌物种或菌株可以根据其环境背景和宿主生理状态动态改变其作为共生体或病原体的能力,这进一步使区别变得复杂。
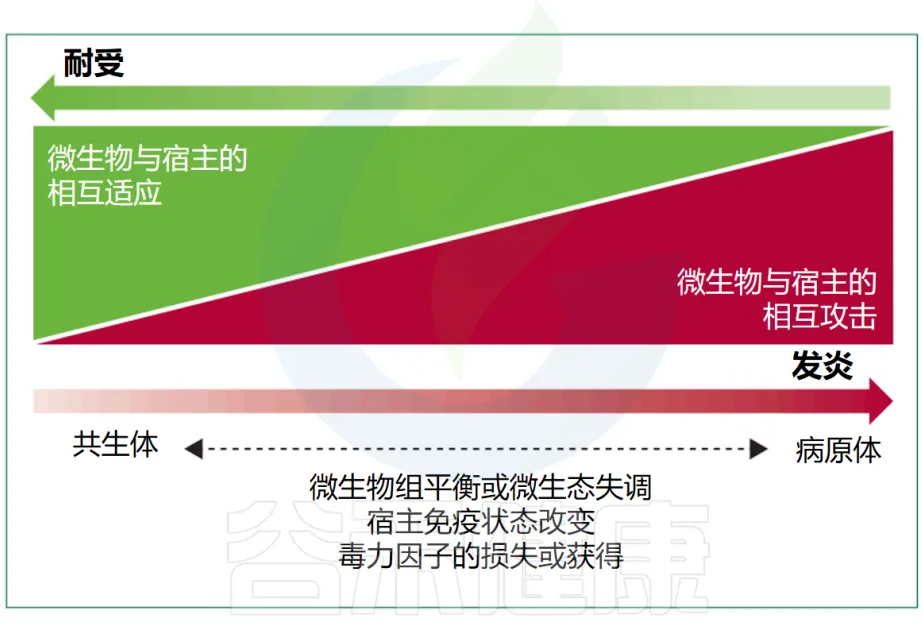
Maier L, et al. Lancet Microbe. 2024
例如,微生物组失调和宿主免疫缺陷,可以将肠球菌(Enterococcus faecium)从一个几乎无害的肠道微生物组成员转变为血流感染的原因。
单个水平基因转移事件可以改变共生生活方式和致病生活方式之间的平衡,例如,当预测的编码毒素成为肠出血性大肠杆菌或皮肤定植和口咽定植的白喉杆菌的主要毒力因子时。这意味着,原本可能是相对无害的微生物,在获得某些特定基因后,其生物学性质和行为可能发生显著变化,从而增加了其致病潜力。这种基因的转移和表达可以使这些微生物在宿主体内表现出更强的侵袭性和病原性,从而对宿主健康构成更大的威胁。
Redefining “Infection”
条件性细菌病原体之间的共生与致病性的动态变化,这挑战了当前对“感染”一词的使用,这种使用往往不一致。
《柳叶刀-微生物》全体作者建议仅将“感染”这个术语,保留用于由特定器官组织中出现的细菌菌株引起的病理状态。例如下列情况:
因此,在这篇个人观点文章中,我们也建议将常规引起感染的细菌称为病原体,而不常引起感染的细菌称为共生菌,尽管这些术语有其局限性,并不能适当描述所有类型的微生物与宿主之间的对抗关系。
目前病原体与共生菌之间的界限模糊,也挑战了科赫的假说,该假说提出了特定微生物与相应疾病之间的单一因果关系。然而,实际上,有些疾病是由多种细菌种类的间接效应引起的,当微生物群落失衡而不仅仅是这些种类的存在,导致了一种特定的病理状态,而这种状态目前并不被视为典型的感染。
Understanding of Bacterial Pathogens and Symbiotic Bacteria
微生物组科学,尤其测序技术的快速进展以及新技术的出现,为微生物学开启了一个新阶段,这一阶段的研究将细菌病原体和共生菌整合在一起,超越了简化的研究方法。
为了探究环境变化如何影响细菌微生物组成员的动态行为变化,来自不同背景的微生物学家应当合作,并结合系统生物学、天然产物化学、粘膜免疫学和临床传染病等互补学科的专业知识。这些新方法可能有助于回答一些最相关和明显的问题:
Future Research on Commensal Bacteria
由于其高度的临床相关性以及培养和操控相对容易,像S. flexneri(志贺氏菌)、S. aureus(金黄色葡萄球菌)和 S. pneumoniae(肺炎链球菌)这样的主要细菌病原体已经被研究了几十年,远超过典型的宿主相关共生菌。相比之下,主要的人类相关共生菌,例如来自属如拟杆菌属、梭菌属(Clostridium)、Cutibacterium,仅被少数实验室研究。
实际上,大多数人类微生物组成员仍然难以培养,并且在遗传上不易处理。在特定情况下可以成为偶发性病原体的一些共生菌,如医院获得性大肠杆菌、粪肠球菌(E.faecium)或表皮葡萄球菌(Staphylococcus epidermidis),已经在一定程度上被研究。但为什么这些特定的细菌比其他更无害的共生菌更频繁地引起侵袭性感染,这一点仍然不清楚(如下表)。


Maier L, et al. Lancet Microbe. 2024
The Important Role of Symbiotic Bacteria in Human Health
越来越多的证据表明,一些共生细菌对人类健康至关重要。
▸ Blautia producta 抑制粪肠球菌
例如,Blautia producta 的共生菌株通过产生特定的抗菌化合物,可以抑制并排除粪肠球菌(E.faecium),而Staphylococcus lugdunensis的共生菌则可以抑制并排除金黄色葡萄球菌。
▸ 枯草芽孢杆菌阻止金黄色葡萄球菌
肠道中的枯草芽孢杆菌(Bacillus subtilis)释放一种抑制性化合物,可以阻止金黄色葡萄球菌的定植能力,或抑制肠球菌(Enterococcus faecalis)的毒力因子表达。
一些共生菌还能产生对宿主有直接益处的化合物,例如促进肿瘤疗法的成功。病原体的研究可以帮助理解这些有益共生菌的生物学特性,并利用它们来对抗细菌感染。
共生菌的许多重要特性在不同菌株间可能会有所不同,这取决于例如获得或丢失移动遗传元素,如编码抗性或适应性特征的基因岛。用于病原体菌株特异性分类的现有方法,如序列分型方案,也可以应用于共生菌。这些方法可以帮助提升当前的诊断策略,达到个性化感染医学的新水平,不仅监测特定有害病原体的存在,还监测如那些保护免受潜在病原体定植的特定有益共生菌的缺失。
bacterial pathogens and symbiotes
▸ 共生菌的宿主特异性适应
与许多主要的细菌病原体一样,很多共生菌也特定于特定的宿主物种。这种适应过程导致宿主特异性,可能作为一种策略来增加细菌在与其他适应性较差的微生物竞争中的生存能力。这些基础机制对于病原体来说理解得很少,对于非致病性共生菌来说则基本上是不清楚的。
▸ 共生菌的粘附与持续定殖机制
特定宿主的持续定殖往往依赖于有效地粘附到上皮细胞的结合基序,如表面蛋白、蛋白多糖或糖脂。尽管在许多主要病原体中已经在一定程度上研究了相应的细菌粘附素,但现在才开始探索共生微生物中的这些机制。
▸ 共生菌与宿主免疫系统的相互作用
细菌在上皮表面的生存受到粘膜宿主防御机制的限制,这些机制包括IgA、抗菌肽和脂质以及活性氧和氮化合物的产生。先天和适应性免疫机制,通过感知与微生物相关的分子模式分子或通过粘膜白细胞检测微生物抗原来启动,有助于粘膜免疫过程,导致促炎或抗炎信号和效应分子的释放。
宿主的持续定殖依赖于细菌耐受抗菌免疫效应分子的能力或通过诱导免疫耐受来减少它们的表达。具有对抗菌宿主效应分子增强耐受性的细菌甚至可以诱导和利用抗菌宿主反应来消除更易感的竞争者。
根据宿主免疫反应,与微生物群其他成员的拮抗干扰已在表皮葡萄球菌和鼠伤寒沙门氏菌中得到记录。广泛的研究揭示了主要病原体的免疫逃避机制,但共生菌是否使用类似或不同的策略仍然未知。
▸ 共生菌免疫调节的复杂性及其潜在影响
例如,一些肠道共生菌通过产生非炎症性鞭毛蛋白来钝化先天免疫反应,这些蛋白抑制人类的Toll样受体5,或产生可以在粘膜表面诱导调节性T细胞的短链脂肪酸,以促进免疫耐受。然而,这些潜在的控制机制可能会被干扰,并可能在宿主无法启动耐受并以炎症反应的情况下导致疾病,例如当口腔共生菌异位定殖在肠道时。
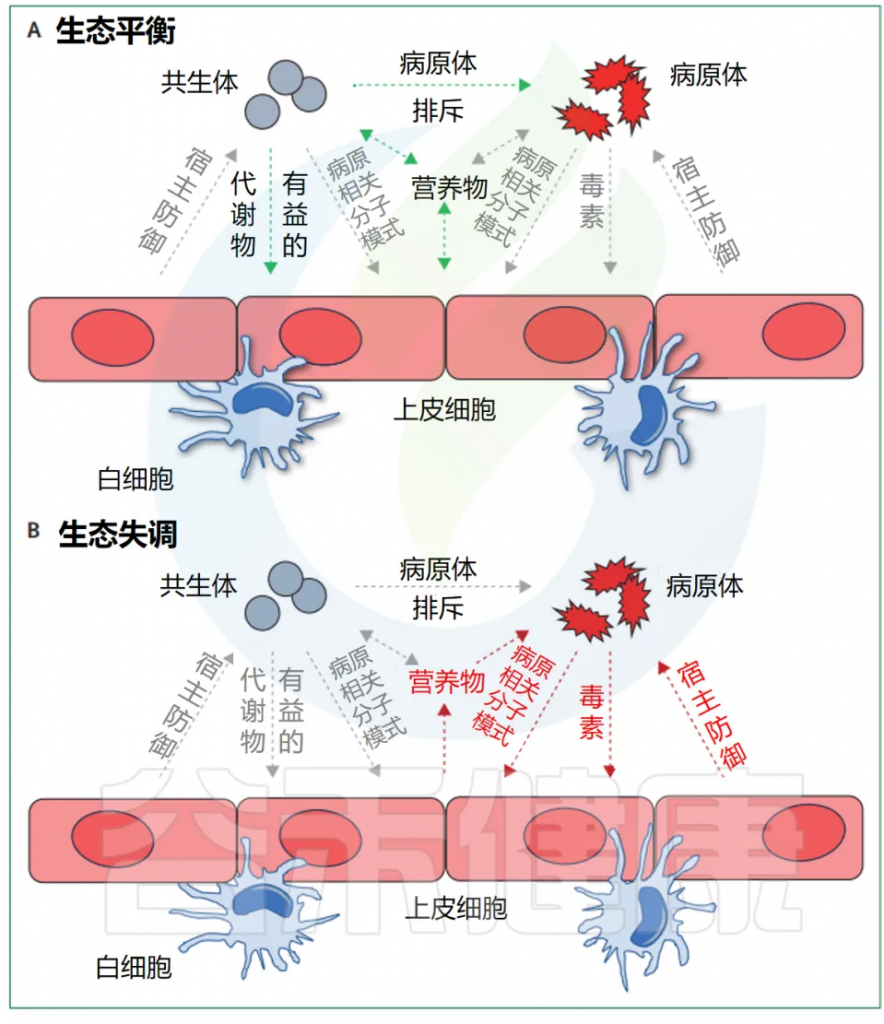
doi.org/10.1016/S2666-5247(24)00049-1
总的来说,宿主相关生态系统中的细菌间的相互作用很大程度上依赖于分泌的因子,这些因子可以通过专门的分泌系统以单独的可溶性分子的形式释放出来,或者作为膜囊泡的组成部分释放出来(上图)。
因此,细菌病原体的分泌毒力因子已经被广泛研究。相比之下,共生菌分泌的初级或次级代谢产物或蛋白质介质如何调节与病原体和宿主的相互作用的研究较少。这些研究显示,例如一些共生菌可以释放杀菌素等分子,消灭金黄色葡萄球菌等病原体,或产生营养物促进艰难梭菌等病原体的扩展,由此凸显了宿主相关微生物生态系统中的一个新的复杂层面。
Fitness mechanisms of facultative human pathogens
许多主要的人类细菌病原体不是专性病原体,而是作为常见微生物组成员定植于人类或动物体表面,但不会引起疾病(下表)。

doi.org/10.1016/S2666-5247(24)00049-1
事实上,在大多数兼性病原体的共生生活方式中,急性感染是罕见的。然而,研究主要集中在S.flexneri、金黄色葡萄球菌、肺炎链球菌等病原体的毒力机制上,而在共生行为期间引导这些生物体与其他微生物组成员竞争的适应性的机制仍然被忽视。
从微生物的角度来看,感染是否以及哪些类型确实对细菌有利,或者应该被视为偶然事件,而不利于它们在几代宿主中的长期进化成功,目前尚不清楚。
Importance of a Deep Understanding of Bacterial Infections
现在比以往任何时候都更需要深入理解细菌感染,因为全球抗菌药物抗性和细菌感染的负担日益增加。目前对细菌感染的了解主要限于少数模型病原体,如金黄色葡萄球菌和肺炎链球菌。相比之下,一些臭名昭著的抗生素抗性细菌种类,根据以下病原体种属的首字母被命名为ESKAPE病原体,包括粪肠球菌、金黄色葡萄球菌、肺炎克雷伯菌、鲍曼不动杆菌、假单胞菌和肠杆菌,这些病原体的研究细节远不够充分。
▸ ESKAPE病原体的持久抗性与适应性进化
抗生素抗性机制在某些情况下可能会给细菌带来适应性的负担,即抗性可能会影响细菌的其他生存能力,但在没有抗生素的环境中,这种抗性通常会消失。然而,一些被称为ESKAPE病原体的细菌已经进化出了一种能力,使它们能够在医疗环境之外保持这种抗性特征。补偿性突变可以帮助这些细菌克服由于抗性而带来的适应性负担,从而促进抗性菌的成功和抗性的传播。
▸ 社区相关的抗性细菌扩散
这就是为什么社区相关的甲氧西林抗性金黄色葡萄球菌(MRSA)和万古霉素抗性屎肠球菌(VRE)等细菌,能够如此有效地在社区中扩散和扩张,甚至以牺牲它们对抗生素敏感的同类为代价,这一现象仍然是科学界未解之谜。这表明这些细菌可能已经发展出了一些未知的机制来维持和增强其抗性,即使在抗生素使用减少的环境中也是如此。这种现象需要进一步的研究来解明其背后的具体机制和因素。
The Relationship Between Bacterial and Ecological Success
生态学概念在普通微生物学和环境微生物学领域很常见,但尚未广泛应用于对病原菌的理解。
细菌在与其他微生物组成员的竞争中的成功依赖于多种机制,包括利用生长限制性营养物质的能力,从其他细菌那里获取促进生长的共同物质如聚合物水解酶或微量金属捕获剂,抵抗由微生物群体成员释放的抗菌分子,或者附着在少数上皮细胞附着点上。
一个细菌种类或菌株的长期生态成功来自于该种类在特定宿主体内的增殖和向新宿主体传播的综合效应。为了研究一个种类在特定宿主体内的增殖,应采用一系列研究策略,从共生菌的研究到对主要专业和偶发病原体的调查。
细菌有两种主要的传播方式:垂直传播和横向传播。
每个人体内都有大量细菌,它们组成了独特的微生物组。这些细菌有的倾向于垂直传播,有的倾向于横向传播,不同细菌的传播方式和速度是不一样的。
2022年的一项研究就发现,微生物组中的细菌在这两种传播方式的偏好上有所不同。我们已经对一些常见的致病细菌的横向传播有了较多了解,比如幽门螺杆菌、肺炎链球菌、金黄色葡萄球菌等。它们能在人群中快速传播,传播过程也被很好地监测和记录。但目前对这些细菌是如何在人体外存活,又是如何进入新的人体的,还不太清楚。
The association between the epidemic spread of pathogens
主要病原体的流行扩散很可能与它们引起的感染类型和严重程度有关(下图)。
▸ 感染类型
疾病特性对细菌传播的贡献在引起腹泻的病原体(如志贺氏菌)中最为明显,这类病原体通过污染的污水传播而获益。
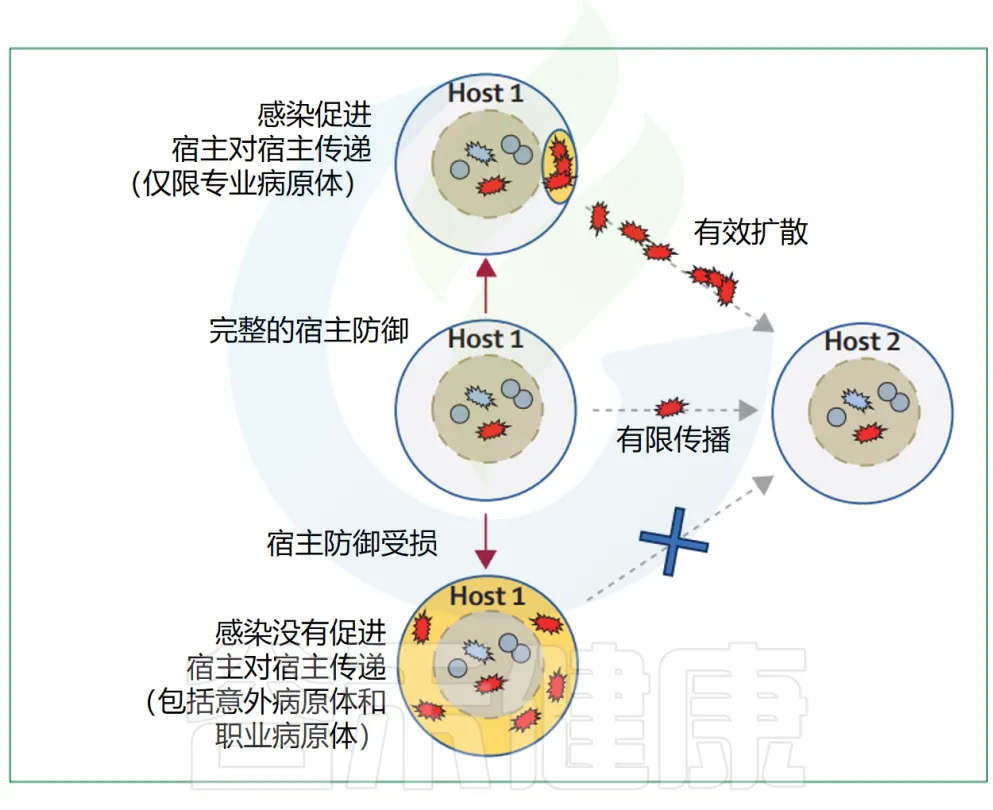
其他常见的感染表现可能也具有类似的作用。例如,金黄色葡萄球菌引起的典型感染——化脓性皮肤和伤口感染,会导致大量的S.aureus细胞在体表出现,从而支持通过皮肤接触的宿主间传播。
类似的机制也可以使尿生殖道病原体,如淋病奈瑟菌Neisseria gonorrhoeae在宿主间迅速传播。引起呼吸道感染的病原体,如百日咳博德特氏菌Bordetella pertussis、化脓性链球菌Streptococcus pyogenes或肺炎链球菌S pneumoniae则通过咳嗽或打喷嚏的个体释放的气溶胶传播。
▸ 严重程度
关于疾病的严重程度如何通过支持传播来增强病原体的适应性已有讨论,例如在SARS-CoV-2的背景下,但尚未对细菌病原体进行系统性评估。值得注意的是,大多数专业化的细菌病原体并非人类微生物组的核心成员,它们只是暂时性地定植在人类体内(见表1),这就需要它们具备有效的横向传播机制。
专业人类病原体(如志贺氏菌和淋病奈瑟菌N.gonorrhoeae)的持续定植在人群中较为罕见,或仅在人群的一小部分(如金黄色葡萄球菌)或特定年龄组(如化脓性链球菌或肺炎链球菌)中发现,这表明维持广泛的致病力涉及与其他微生物组成员竞争时的重大适应性负担。
诸如粪肠球菌(E.faecium)和表皮葡萄球菌( S.epidermidis )等偶然病原体表达的因子有助于其免疫逃避能力,但几乎不表达任何侵袭性毒素,这可能导致这些病原体在人类微生物组中比大多数专业病原体具有更高的患病率和持久性。
由于偶发性病原体主要在免疫力低下的个体中引起感染,它们也常被称为机会性病原体。然而,这一术语也经常用于诸如金黄色葡萄球菌和肺炎链球菌等专业病原体,这些病原体在免疫力低下的个体中引起的感染类型不同且更为严重(通常是血流感染),而在免疫力正常的个体中则不然。因此,专业病原体有时也可能引起偶发性感染,这种感染并不促进病原体的传播。偶发性人类感染也可以由适应于非人类宿主的病原体如军团菌(Legionella pneumophila)或霍乱弧菌引起,这些病原体只在特定的环境条件下感染人类。
The association between the epidemic spread of pathogens
在自然环境中同时研究共生菌和病原体,可以帮助我们更好地控制微生物,对抗感染以及其他与微生物组相关的疾病。
共生细菌对传染病的影响远比先前假设的要复杂得多。一些共生菌种采用主动防御策略,如释放抗菌肽或通过依赖接触的V型、VI型或VII型分泌系统消除其他细菌,这些系统在针对特定目标物种的特异性上可能有很大差异。此外,共生菌还可以使用更微妙的抑制策略来增加其在抗击病原体定植方面的生态成功,这基于代谢干扰。
共生细菌群落可以以依赖于群落多样性及其与病原体的代谢重叠的协作方式,阻止诸如克雷伯肺炎菌和鼠伤寒沙门氏菌等病原体获取营养物。
病原体的排除可能是由于共生菌释放的金属载体螯合必需的微量金属,或产生抑制性代谢产物而产生的。例如,一些肠道共生菌可以将原生胆酸转化为抑制肠道病原体艰难梭菌C difficile孢子生长的次生胆酸代谢产物。
Challenges in Fecal Microbiome Transplantation Treatment
粪便微生物组移植(FMT)是治疗艰难梭菌感染的一种有效策略。粪便微生物组移植成功至少部分是由于恢复了有益细菌群及其代谢产物,这些代谢产物能抑制艰难梭菌的生长。然而,粪便微生物组移植难以标准化,其对抗其他病原体的效果仍不明确。
目前,临床前和临床试验正在评估使用基于共生菌的生命治疗产品来预防处于风险中的个体被抗生素耐药病原体定植。然而,那些防止病原体定植的共生菌往往比目标病原体更易受抗生素影响,这可能会消除共生菌的有益效果,并在抗生素治疗期间加剧与菌群失调相关的疾病。
因此,研究人员需要平衡使用共生菌治疗产品的风险和好处。深入了解不同共生菌菌株对抗生素的敏感性,以及这些菌株如何与目标病原体相互作用。只有通过深入的研究和严格的监测,才能确保共生菌的治疗潜力得到充分发挥,同时避免不良后果的发生。
系统评估关键共生菌群的抗生素敏感性,并将这些知识纳入个性化的、基于微生物组的抗生素管理方案中,对于最小化广谱抗生素对微生物组的附带伤害至关重要。
除了我们通常使用的抗生素之外,许多针对人类的其他药物也可能意外地影响到人体肠道中的有益细菌。这种药物的副作用在未来的医疗实践中需要被特别注意,特别是对于那些需要同时使用多种药物治疗多种疾病的患者。此外,人体内的微生物群体本身可能是一种新型抗菌剂的重要来源。通过系统地研究和描述这些微生物产生的创新化合物,我们可能会发现新的药物,这些药物有望用于预防或消除病原体在人体内的定植。
Antibiotic Resistance Issues in Treatment
在现代医疗中,我们常用的广谱抗生素不仅攻击病原体(引起病症的微生物),还会影响到人体内的有益共生细菌。这种广泛的攻击会导致细菌之间的抗药性基因传递,特别是通过一些可以在不同细菌间转移的元素,如质粒和噬菌体。这种基因的传递可能导致抗生素更难以消灭病原体。
由于这种抗药性基因的传递,需要更好地监控不仅是病原体的抗药性发展,也要监控那些可能是抗药性传播者的共生菌。这样可以更有效地控制病原体的传播和抗药性的发展。
此外,通过理解这些微生物之间的生态关系,可以更好地发现病原体的弱点,从而开发出新的治疗方法。
这些方法不仅限于传统的抗生素,还包括能够利用有益共生菌或宿主防御机制的新型药物。这些新药物的开发需要在模拟真实生态环境的实验模型中进行,比如使用人类挑战模型,这种模型允许我们在受控的环境中测试病原体和治疗方法。
总之,通过更好地理解微生物之间的相互作用和生态平衡,可以开发出更有效的策略来对抗病原体,同时减少对有益共生菌的损害。这种方法有助于限制病原体的传播和疾病的爆发。
主要参考文献:
Maier L, Stein-Thoeringer C, Ley RE, Brötz-Oesterhelt H, Link H, Ziemert N, Wagner S, Peschel A. Integrating research on bacterial pathogens and commensals to fight infections-an ecological perspective. Lancet Microbe. 2024 Apr 9:S2666-5247(24)00049-1. doi: 10.1016/S2666-5247(24)00049-1. Epub ahead of print. PMID: 38608681.

谷禾健康

大多数细菌对我们的生活是有帮助和必要的,某些细菌可以帮助消化,为身体提供能量,分解毒素,保护肠道,增强免疫力等,从而有益健康;也有一些细菌会给我们的健康带来一些危害。
然而有些菌并不是天生注定就是致病菌,也许正常状况下,它只是体内默默地存在着,但可能在某种特定条件下突然变身,彰显其致病威力。
事实上,许多严重的疾病是由健康个体的皮肤、粘膜或肠道中常见的细菌引起的。在这些情况下,致病菌根本不是专性病原体,而是遵循新的生态轨迹的共生体,通常会迁移到与宿主不再和谐相处的侵入性生态位。
细菌从共生到致病的转变在肺炎、脑膜炎、全身感染和医院获得性感染等疾病中发挥重要作用。当然,宿主环境扰动可能会提供感染机会。
因此,我们需要对致病菌的个性、不同环境下的状态有个基本的了解。
在谷禾肠道菌群健康检测报告中,我们会看到关于有益菌,有害菌,致病菌的检测:
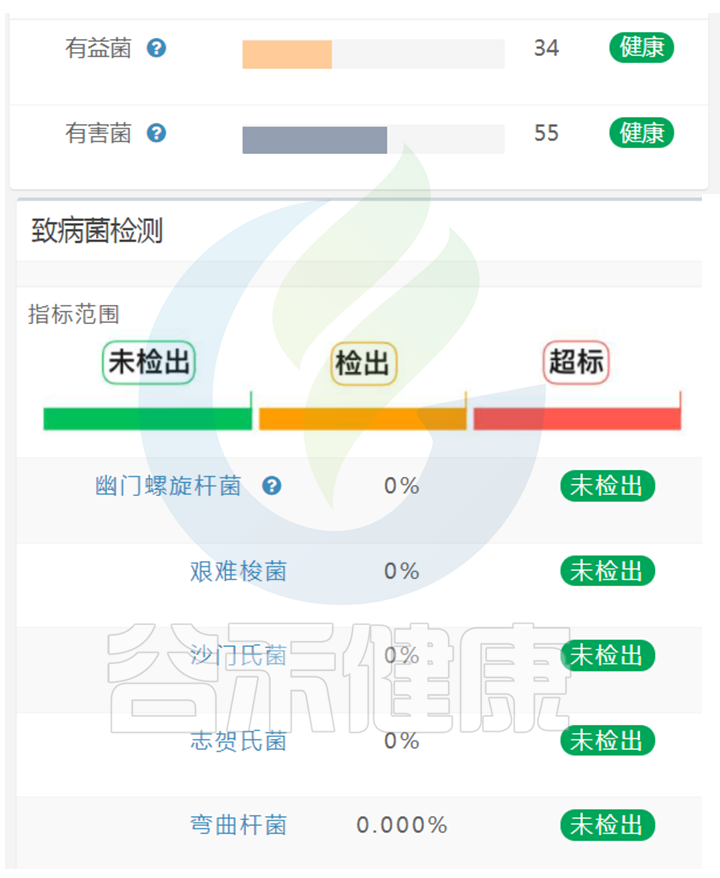
有小伙伴有疑问,这里既显示有害菌又有致病菌,有害菌不是致病菌吗?
携带致病菌就一定会生病吗?
条件致病菌是如何引起感染的?
有害菌很多,该如何改善?
…
本文也将围绕着这些问题,展开一些讨论。
致病菌是引起疾病的细菌,也称为病原菌。当它进入身体时,就会破坏细胞或干扰身体的正常活动,人可能会患上轻微疾病或致命疾病。
✦ +
致病菌通过多种方式导致宿主生病。最明显的方法是在复制过程中直接破坏组织或细胞,通常是通过产生毒素,使病原体到达新组织或离开它复制的细胞。细菌毒素是已知的最致命的毒物之一,包括著名的例子,如破伤风、炭疽等。
然而,对宿主的损害通常是通过强烈的或有时是过度的免疫反应自行造成的,这种免疫反应会不加选择地杀死受感染和未感染的细胞并损害宿主组织。免疫系统过度反应的典型例子包括乙型肝炎中的肝硬化和肝癌。
一些病原体受益于宿主的免疫反应,可以在受感染的宿主内传播或增加它们向未感染宿主的传播。
流感主要通过它引起的打喷嚏和咳嗽产生的气溶胶传播。
霍乱弧菌在肠道粘膜中引发强烈的炎症反应,导致水样腹泻,并确保其在环境中的释放,从而感染更多的宿主。
✦ +
从概念上来讲,致病菌和病原菌意思差不多。需要注意的是,这里我们报告用的两个词分别是:
肠道致病菌,病原菌。
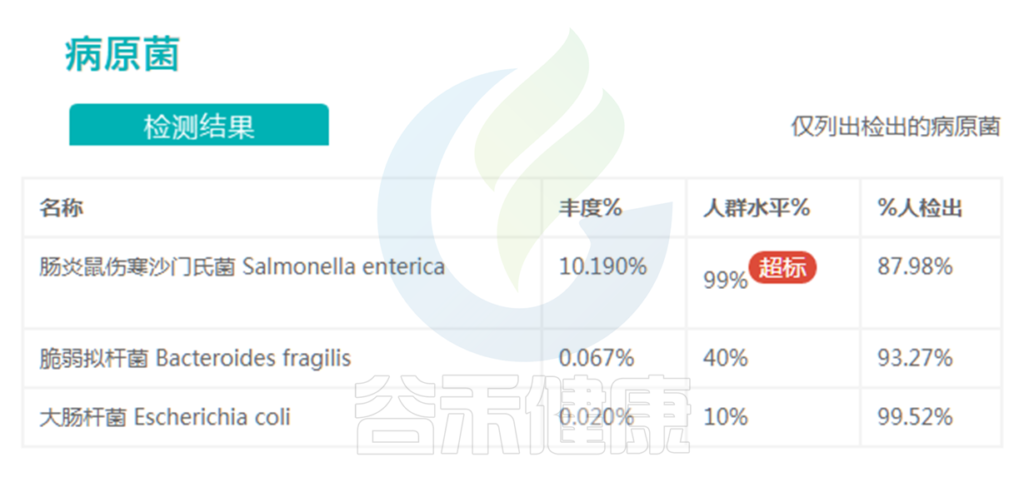
✦ +
正常情况下,肠道内是存在少量的病原菌,但是其丰度相对较低,丰度低于健康人群98%以下,不一定会导致疾病的发生。
这里我们可以了解一下关于“细菌感染”:
细菌感染:
病原菌侵入宿主体内并引起病理变化称为“感染”。
也就是说,如果报告中只是检出极少的病原菌,同时并没有症状,那么可能只是表面有病原菌摄入,需要注意饮食和生活卫生,这并不能称之为病原菌感染,因此不需要过于恐慌。
如果报告中病原菌检出已经超过98%人群,则代表可能存在感染的风险,需要结合相应症状和具体菌群丰度比例综合进行判断。
此外,如果出现多种病原菌或病原菌丰度水平很高,则需要引起注意。
✦ +
需要注意的是,谷禾肠道菌群检测报告中的疾病风险,是综合了多项指标判别的,并不只是考虑了致病菌。
慢病是每一种病单独构建模型,不一定和有害菌或菌群平衡指标直接有关。
下面我们来看一些致病菌,这些致病菌一旦感染可能会给人体带来较大危害。
✦ +
★ 炭疽杆菌 Bacillus anthracis
炭疽杆菌是革兰氏阳性、非运动、兼性厌氧、孢子形成和杆状细菌。
炭疽杆菌是一种人畜共患病的病原体,是一种专性病原体,因为细菌的繁殖周期只发生在合适的宿主中。
编辑
图源:tvmdl.tamu.edu . by Mallory Pfeifer
炭疽杆菌的发病机制主要由两种毒力因子引起:三方外毒素和聚γ-d-谷氨酸(γ-DPGA)。
人类可以通过四种不同的方式感染炭疽:吸入、摄入、通过皮肤和注射。
吸入性炭疽被认为是最致命的炭疽形式。如果不进行治疗,病死率接近95%,而立即干预可以将病死率降至50%。
胃肠道炭疽的发生是由于食用了来自感染炭疽的动物制备不当的肉类或肉制品。死亡率是可变的,通过适当的抗生素治疗可以达到≤40%.
皮肤炭疽通常通过皮肤接触受感染的动物或动物产品而发生。这种形式的炭疽病占全球人类病例的 95%。治疗后病死率<1%。潜伏期为 3-7 天。临床表现从轻度到重度不等。
抗生素疗法用于治疗炭疽感染。青霉素、强力霉素、环丙沙星。抗生素治疗必须在接触后立即开始,因为其有效性会随着毒血症的进展而降低。炭疽疫苗在治疗中也很重要。在确诊或疑似接触炭疽孢子的情况下,建议进行 60 天抗生素治疗。
★ 鼠疫耶尔森菌 Yersinia pestis
鼠疫耶尔森菌是一种小型、非运动的革兰氏阴性细菌,属于肠杆菌科。鼠疫耶尔森氏菌是鼠疫的病原体,鼠疫是一种罕见但高度致命的人畜共患病。
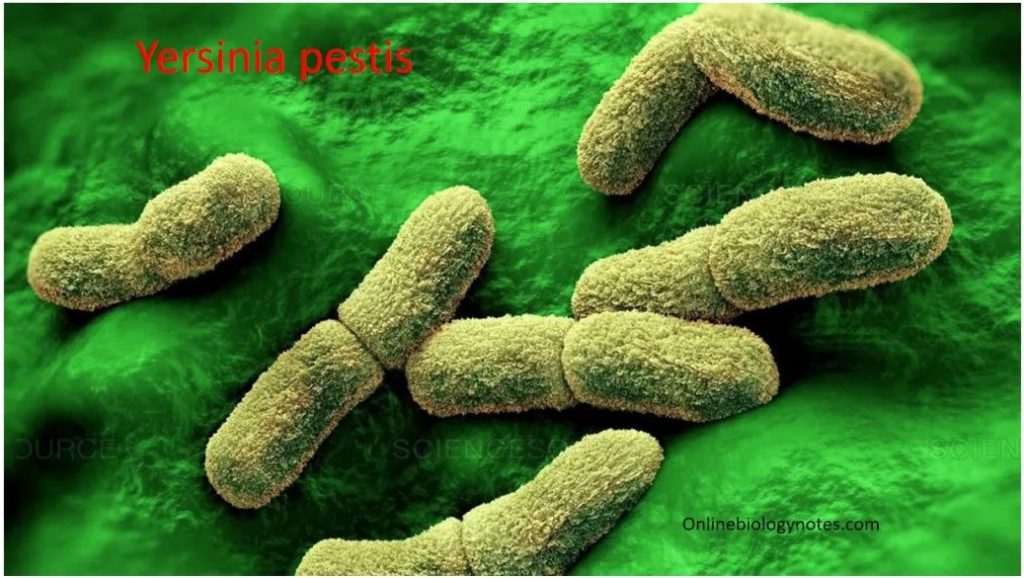
图源:onlinebiologynotes
大多数人类感染是由于与受感染的动物接触或被受感染的跳蚤叮咬造成的。
鼠疫在全球超过 25 个国家流行。尽管有有效的抗生素治疗,流行地区的死亡率仍超过 10%,这主要是由于发病机制的快速发展。
鼠疫主要以三种形式发生:肺鼠疫、腺鼠疫和败血症鼠疫。
鼠疫最严重的表现,发展最快的是肺鼠疫,在没有治疗的情况下死亡率接近100%.
肺鼠疫通过呼吸道飞沫在人与人之间传播。经过 2-4 天的潜伏期后,疾病的各种症状包括发烧、头痛、恶心、不适、呕吐、咳痰带血、呼吸困难和胸痛。如果在症状出现后 24 小时内给予适当的抗生素治疗,死亡率可降低高达 50%。
腺泡形式是最常见的,腺鼠疫是鼠疫的主要形式,占病例的 80-95%。死亡率为 10–20%。腺鼠疫由受感染的跳蚤叮咬引起。腺鼠疫的特点是形成淋巴结(淋巴结肿大)。通常的潜伏期从 2 到 6 天不等,有时更长。
如果腺鼠疫没有在适当的时间得到诊断和治疗,它会通过血液传播细菌而发展成败血性鼠疫。这种形式的瘟疫也可能是由传染性跳蚤叮咬通过受损的皮肤或粘膜直接进入鼠疫耶尔森氏菌引起的。通常的潜伏期为 2-7 天,但这种类型的鼠疫甚至在临床表现出现之前就可能导致死亡。
败血性鼠疫的症状包括腹痛、皮肤和其他器官出血。皮肤和其他组织可能会坏死,尤其是鼻子、手指和脚趾。此外,可以观察到发烧、腹泻、呕吐和虚弱。败血症性鼠疫以高菌血症为特征,并伴有危险的内毒素血症。
★ 土拉弗朗西斯菌 Francisella tularensis
土拉弗朗西斯菌是一种革兰氏阴性、非运动、非产孢球杆菌。它是一种小的细胞内病原体,具有高毒力和低感染剂量(1-10 个细胞)的特点。
细菌可以通过接触受污染的水进一步传播。吸入受感染的气溶胶,或直接接触受感染动物的组织和液体,也可用作细菌传播的途径。
细菌进入体内后,在局部繁殖,引起溃疡和坏死,然后侵入血液和淋巴管,扩散至肝、脾、肺、肾、浆膜、骨髓等淋巴结和器官,引起多发性凝固性坏死灶。
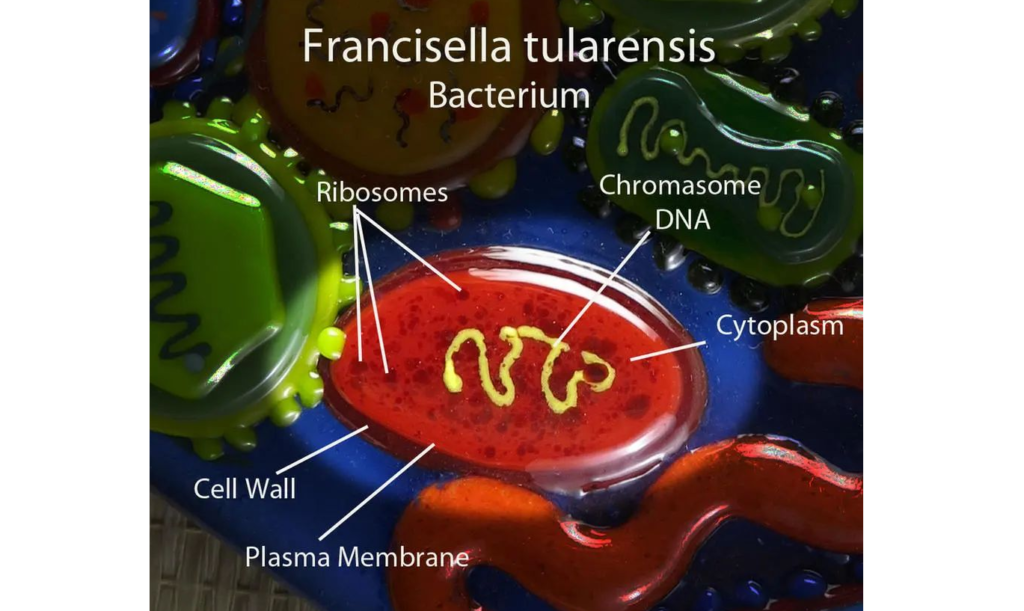
图源:DeviantArt
土拉弗朗西斯菌不仅容易在巨噬细胞中生长,而且还可以感染许多其他细胞类型,如上皮细胞、肝细胞、肌肉细胞和中性粒细胞。
有六种主要形式的土拉菌病,根据症状分类:肺病、腺病、溃疡腺病、口咽病、伤寒病和眼腺病。
该病的潜伏期通常为暴露后3-5天。
溃疡腺形式是最常见的,是节肢动物媒介叮咬或在与受感染动物接触期间通过皮肤获得感染的结果。
细菌通过磨损进入生物体后,可能会发生腺体形式的土拉菌病。
食用未煮熟、受感染的食物或受污染的水后,可能会形成口咽形式,之后细菌会感染咽部。患者常出现发热、咽痛、颈淋巴结肿大伴耳下淋巴结受累。
在疾病的严重形式中,可能会出现由于肠溃疡导致的胃肠道出血。
当细菌进入循环系统并从另一个感染部位扩散到肺部时,就会出现继发性肺炎性土拉菌病。症状包括高烧、干咳、胸痛和肺门淋巴结肿大;也可能出现肺部浸润或胸腔积液。
伤寒形式的主要症状是发烧、发冷和严重疲劳。然后出现呕吐、腹泻、谵妄和腹痛。临床表现还包括全身疲劳、败血症和死亡。伤寒形式是最难诊断的,因为它的一般症状没有明显的外部病变或区域淋巴结肿胀。
★ 肉毒杆菌 Clostridium botulinum
革兰氏阳性菌,厌氧菌,可运动,致病菌。
它会引起一种罕见但严重的疾病。产生一种特殊类型的外毒素,通过抑制神经肌肉连接的活动来影响神经系统。因此,肉毒杆菌毒素表现为一种神经毒素,它会阻止神经递质的释放。
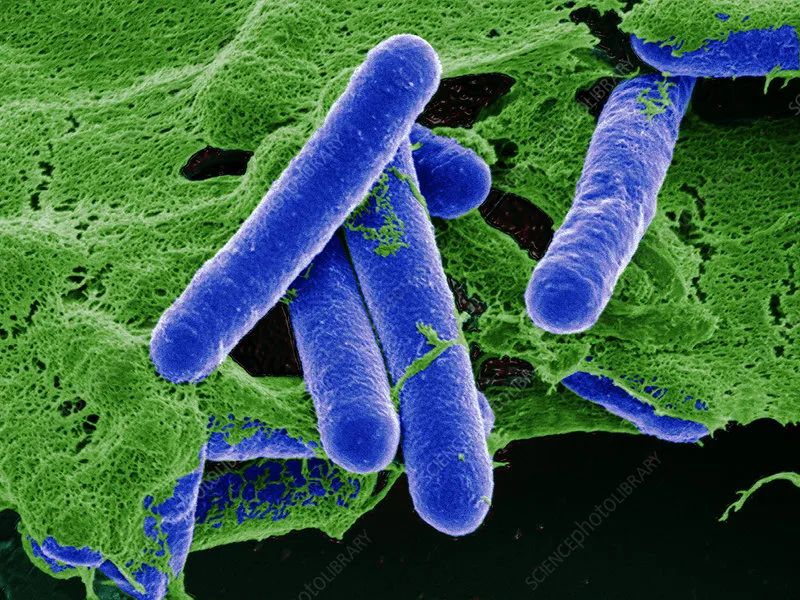
图源:Science Photo Library
肉毒中毒的症状通常始于控制眼睛,面部,嘴巴和喉咙的肌肉无力。
这种无力可能会蔓延到脖子,手臂,躯干和腿部。肉毒杆菌中毒还会削弱呼吸所涉及的肌肉,从而导致呼吸困难甚至死亡。
分为五种传播类型:
预防:
包括减少微生物污染水平,酸化,减少水分水平,以及尽可能破坏食物中所有肉毒杆菌孢子。
易感食物包括罐装芦笋、绿豆、油蒜、玉米、汤、熟橄榄、金枪鱼、香肠、午餐肉、发酵肉、沙拉酱和熏鱼。食用前,考虑将这些食物煮沸10分钟。
以上列举了一些常见的致病菌。致病菌与非致病菌并不是绝对的,是一个动态作用的过程。我们知道肠道中还有大量其他菌群,这些菌群在特定条件下,也可能转为致病菌,我们把这类细菌称为条件致病菌,接下来章节我们来详细了解一下条件致病菌的特点。
正常菌群与宿主、其他菌群之间,通过营养竞争、代谢产物的相互制约等因素,维持着良好的生存平衡。
然而,在一定条件下这种平衡关系被打破,一部分平时看起来正常的细菌就开始“作妖”,变成可以致病的细菌,这就是所谓的 “条件致病菌”。
条件致病菌包括引起肺炎、血流感染、脑膜炎和其他疾病的细菌。它们存在于环境中,可以通过皮肤上的伤口或吸入含有细菌的灰尘进入人体。
健康的免疫系统可以对抗许多病原体,但如果它受损,条件致病菌通常会引起感染。
与免疫系统受损相关的因素有:
遗传易感性;
癌症化疗;
给予免疫抑制药物以防止移植后排斥反应;
艾滋病感染;
严重营养不良;
长期抗生素治疗;
天生免疫系统较弱的婴儿和老年人;
导致白细胞生成减少的骨髓疾病;
怀孕;
正所谓 “橘生淮南则为橘,生于淮北则为枳”。某些细菌在肠道内是乖乖成长的,可一旦冲破束缚,例如在肠漏的情况下,细菌或其代谢物泄露到循环中,可能会变身“有害菌”,可以通过诱导慢性或急性炎症反应,导致疾病发生,包括损害肝脏和胰腺等重要器官,肝癌和胰腺癌可能与细菌易位有关。
如果没有健康的器官和器官系统来适当调节正常的身体功能,条件致病菌就有下手的机会,利用此环境推动疾病的发生。
手术通常涉及切口和伤口,这些切口和伤口为病原体进入身体创造了入口。这也为条件致病菌创造了有利条件。
长期使用会破坏体内正常的微生物群,杀死有益细菌,并导致条件致病菌增殖。
其实细菌(即便是致病菌),它们要生存下来并没有我们想象的容易,生活在复杂的群落中,多个物种和菌株存在相互竞争。
例如,在共生葡萄球菌中,分泌蛋白酶的表皮葡萄球菌菌株,会抑制金黄色葡萄球菌的生物膜形成和鼻腔定植。此外,生物膜破坏介导与其他物种的相互作用,并增加金黄色葡萄球菌对宿主免疫反应成分的易感性。可以看到宿主和共生细菌发出协同反应以排除其他物种。
然而你以为只有宿主和其他菌会带来威胁吗?不,另一种威胁来自与它们同居的同一物种的另一个谱系,同种内部也会互相竞争。这种种内争夺优势的斗争在金黄色葡萄球菌中得到了例证。
关于细菌之间如何交流详见:
金黄色葡萄球菌
Staphylococcus aureus
金黄色葡萄球菌是一种需氧的革兰氏阳性细菌,通常在健康人的鼻腔和皮肤上定植。
但当存在于假体关节和静脉输液管等内部装置中时,可能会导致感染,感染可能导致严重的败血症。
铜绿假单胞菌
Pseudomonas aeruginosa
铜绿假单胞菌是一种需氧、不发酵、高度运动的革兰氏阴性菌。
当感染宿主时,铜绿假单胞菌需要铁。因此铜绿假单胞菌合成了两种铁载体:pyochelin和pyoverdin。铜绿假单胞菌随后将这些嗜铁细胞秘密地存在于细胞的外部,与铁紧密结合并将铁带回细胞。铜绿假单胞菌还可以利用肠杆菌素中的铁来满足其铁需求。
其优先代谢是呼吸,通过将电子从葡萄糖(还原的底物)转移到氧(最终的电子受体)来获得能量。当处于厌氧状态时,铜绿假单胞菌使用硝酸盐作为末端电子受体。
形成生物膜,附着在金属,塑料,医疗植入材料和组织表面。
症状:
肺部感染:发烧和发冷、呼吸困难、胸痛、疲倦、咳嗽
尿路感染:强烈尿频冲动、小便疼痛、尿液中难闻的气味、尿液混浊或带血、骨盆区域疼痛
伤口感染:伤口发炎、漏液
耳部感染:耳痛、听力下降、外耳发红或肿胀、发热
也可能是囊性纤维化患者或机械呼吸机患者呼吸道感染的重要原因。
传播:
当暴露于受该菌污染的水或土壤中时,可以传播到医院患者。还可以在医院中通过被污染的手,设备或表面从一个人传播到另一个人。
治疗:
抗生素治疗
注:铜绿假单胞菌感染通常难以治疗,因为该细菌对许多抗生素具有抗性,并且具有形成生物膜的非凡能力。
易感人群:
免疫力低下人群
使用呼吸机患者、使用导管等装置、有手术或烧伤的伤口患者
预防:
患者和护理人员应保持双手清洁,避免感染。尤其是在护理伤口或触摸医疗设备之前和之后要彻底洗净双手。每天打扫房间。避免共享个人物品。
艰难梭菌
Clostridium difficile
革兰氏阳性,厌氧菌。经过氨基酸发酵,以产生ATP作为能量来源,并且还可以利用糖。
产生两种毒力因子:在70%的菌株中发现肠毒素(毒素A)和在所有菌株中发现的细胞毒素(毒素B)。毒素通过糖基化使Rho-gtpase失活,破坏肠上皮细胞的紧密连接,导致细胞旁通透性增加,从而导致体液分泌(腹泻)、粘膜损伤和炎症。
艰难梭菌存在于整个环境中,包括土壤,空气,水,人类和动物的粪便以及食品(例如加工肉)中。
疾病症状:
艰难梭菌通常影响住院的老年人。
常见症状有:严重腹泻、发热、排便频繁、胃部压痛或疼痛、食欲不振、恶心。
更严重的症状可能包括:
水样腹泻,每天10至15次;
脱水、心跳加快、体温升高、食欲不振、严重的腹部绞痛和疼痛、粪便中有脓液或血、体重下降、腹部肿胀、肾功能衰竭等。
传播:
通过粪-口途径在人与人之间转移。感染通常在医院发生。
该菌可以从粪便传播到食物,然后传播到其他物体表面,如果不洗手或者不正确洗手,就容易感染。
治疗:
抗生素(万古霉素,非达霉素)治疗。患有艰难梭菌感染的人容易脱水,可能需要住院治疗。但是,使用抗生素治疗可能会攻击体内有益细菌。
其他治疗感染的方法,包括:
脆弱拟杆菌
bacteroides fragilis
无芽孢,专性厌氧革兰氏阴性杆菌,人类结肠正常菌群的一部分。
BF毒素引起剧烈的炎症和“细胞间附着物的丧失”,从而引起典型的腹痛和腹泻。
某些脆弱类芽孢杆菌菌株无毒,甚至对其宿主生物有益。
疾病症状:
菌血症、阑尾炎、褥疮、化脓性关节炎、脑膜炎、喉咙发炎、上呼吸道感染、皮肤感染、心内膜炎、软组织感染、心包炎
该菌是正常肠道菌群成员,但是如果转移到周围组织中也会引起腹腔内感染。
这些感染包括产后子宫内膜炎,盆腔脓肿,会阴切开后软组织感染,微管卵巢脓肿和盆腔炎。
菌血症定义为血液中细菌的存在。脆弱拟杆菌是血液培养后最常见的厌氧菌。细菌在腹部,软组织和女性生殖道中的存在是最常见的菌血症来源。
该菌不是人体皮肤微生物菌群的一部分。如果这种细菌进入任何组织,则会引起皮肤感染,例如坏疽和坏死。糖尿病患者还容易受到该菌引起的皮肤感染的影响。
该菌还与引起心包炎,心内膜炎,脑膜炎,阑尾炎和咽喉发炎有关。
传播:
如果细菌被转移到任何其他人体组织,则可能导致该组织的疾病;可能由于外伤,割伤,烧伤,异物侵入或由于不当的外科手术做法造成感染。
治疗:
单一药物治疗或组合治疗
易感人群:
患有腹腔内感染的患者,糖尿病患者易感染
预防:
产气荚膜梭状芽胞杆菌
Clostridium perfringens
革兰氏阳性细菌,是嗜温菌,最适生长温度为37℃,产生内生孢子的非运动性菌。
通过无氧呼吸产生能量,使用硝酸盐作为其电子受体。可能导致许多胃肠道疾病,严重程度从轻微的肠毒血症到致命的气性坏疽。
还具有进行糖酵解和糖原代谢所需的所有酶,利用各种糖酵解酶将糖化合物分解为更简单的形式。
可以在人体肠道,污水和土壤中正常发现。
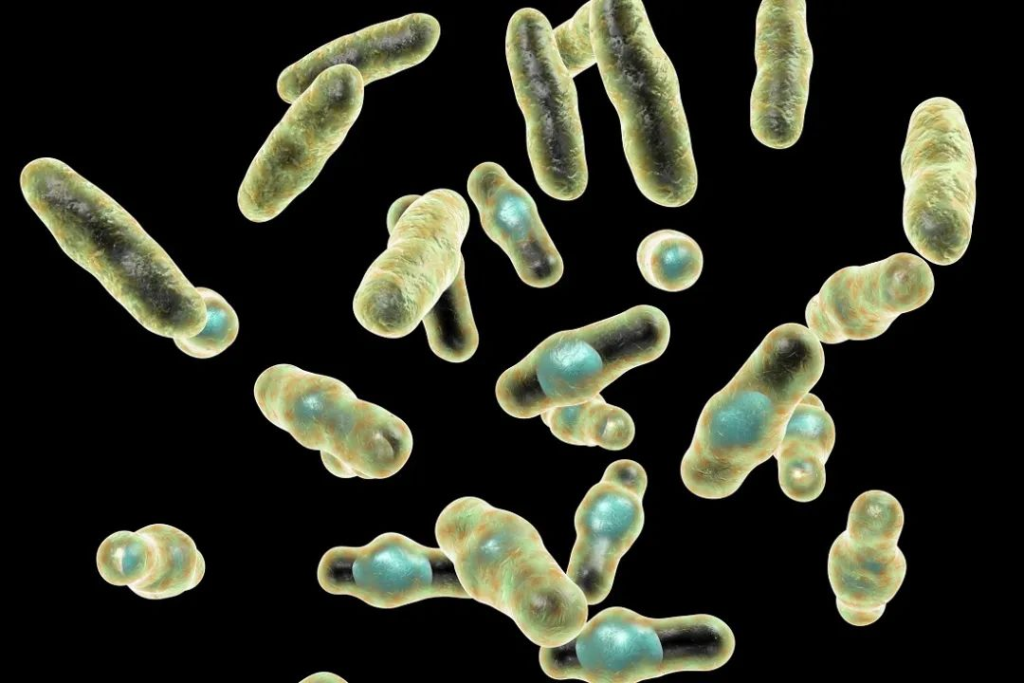
图源:Food Safety News
疾病症状:
食源性疾病(食物中毒)的最常见原因之一。
关于食源性疾病详见:正值夏季,警惕食源性疾病,常见的食物中毒的病原菌介绍
大多数感染了产气荚膜梭菌的人在食用受污染的食物后6-24小时内会出现腹泻和胃痉挛。这种疾病通常突然发作,持续不到24小时。
这种感染通常不会引起发烧或呕吐。
传播:
营养和食品卫生状况较差的地区人群;
糖尿病和动脉粥样硬化等患者;
产气荚膜梭菌感染也与多发性硬化症有关
危险因素:
常见感染来源包括肉类,禽类,肉汁和其他不安全温度下的食物。
爆发往往发生在医院,学校食堂,监狱和疗养院,以及带有餐饮的活动。最常发生在11月和12月。
治疗:
大多数人未经抗生素治疗即可恢复。
如持续腹泻应多喝水,多休息。
对于源自深层伤口的感染, 必须尽可能清洁该区域,并应使用抗生素。
预防:
将食物煮至安全温度;
食物煮熟后应保持在大于60度或低于4度
可以将热食直接放入冰箱,从冰箱拿出来后加热食用。
结核分枝杆菌
Mycobacterium tuberculosis
革兰氏阳性,专性需氧菌,无运动能力,无孢子形成,细胞内生长的细菌。
通常感染单核吞噬细胞。
在感染的潜伏期,结核分枝杆菌利用一系列效应蛋白将宿主免疫系统弄混,并使其生活方式驻留在肉芽肿中,肉芽肿是宿主为应对持续感染而建立的复杂和有组织的免疫细胞结构。肉芽肿中的结核分枝杆菌通常被限制在具有免疫能力的宿主中,但是当宿主免疫力受损时,它可能导致结核病复发。
常见的症状:
低烧、盗汗、疲劳、厌食(食欲不振)、体重下降。肺结核患者通常会产生咳嗽,并伴有低烧发冷,肌痛(疼痛)和出汗。
潜伏期没有症状。
引发疾病:
传播:
吸入飞沫(咳嗽或打喷嚏)
治疗:
抗生素治疗
预防:
肺炎链球菌
Streptococcus pneumoniae
柳叶刀形,革兰氏阳性,兼性厌氧菌,α-溶血性,条件致病菌。
该菌通过胞外酶系统获得大量的碳和氮,胞外酶系统允许多糖和己糖胺的代谢,并对宿主组织造成损害并使其定植。
荚膜多糖的组成和数量在毒力中起主要作用。产生最大量多糖的菌株可能是最强毒的。
图源:Science Photo Library
疾病症状:
从无症状的咽部定植到粘膜疾病(中耳炎,鼻窦炎,肺炎)再到侵袭性疾病(通常在无菌部位的细菌;菌血症,脑膜炎,脓胸,心内膜炎,关节炎)
传播:
通过呼吸道飞沫直接进行人与人接触,上呼吸道携带细菌的人自动接种。
易感人群:
治疗:
抗生素;静脉注射疗法
预防:
无乳链球菌
Streptococcus agalactiae
革兰氏阳性双球菌,不耐酸,不形成孢子,不易动,兼性厌氧的条件致病菌。
通常称为B组链球菌(GBS),是四种Beta-溶血性链球菌之一,可导致血琼脂上细菌菌落周围宽阔清晰区域显示的血细胞完全破裂。
使用葡萄糖作为能源。该细菌能够通过氧化磷酸化合成ATP。
是一种异养菌,能够导入多种碳源。能够将不同的碳源发酵成多种副产物,如乳酸,乙酸盐,乙醇,甲酸盐或乙酰丙酮。
需要许多氨基酸才能生长,因为它不存在任何TCA循环来合成氨基酸。
毒力因子: 多糖胶囊, β溶血素毒素
属于生殖道的正常菌群。5-20%的女性阴道定植。
疾病症状:
尿路感染, 新生儿和幼儿败血症,脑膜炎
患有基础疾病的成年人:肺炎,心内膜炎,皮肤和软组织感染等。
传播:
GBS阴道或直肠定植的母亲所生的婴儿中,有1%至2%的婴儿发生早发感染。
通过孕妇在怀孕或分娩期间的生殖器官和/或肠道,以及来自其他新生儿或妇产医院的医院工作人员。
治疗:
抗生素治疗
易感人群:
预防:
流感嗜血杆菌
Haemophilus influenzae
革兰氏阴性杆菌。有6种囊化血清型(指定为a至f)具有不同的囊化多糖。
该菌在人的鼻子和喉咙中,通常不会造成伤害。但有时会移动到身体的其他部位并引起感染:
肺炎(肺部感染),菌血症,脑膜炎,喉咙肿胀,蜂窝织炎(皮肤感染);
引起儿童耳部感染和成人支气管炎;
较不常见的感染包括心内膜炎和骨髓炎。

图源:ecdc.europa.eu
易感人群:
5岁以下和65岁以上感染风险增加,免疫力低下的(如艾滋病患者,癌症患者)感染风险增加。
传播方式:
咳嗽或打喷嚏;新生儿可以通过吸入羊水或与含有该菌的生殖道分泌物接触而感染。
治疗:
服用抗生素
预防:
婴儿接种Hib疫苗
衣氏放线菌
Actinomyces israelii
直径为1μm的革兰氏阳性杆菌,厌氧细菌,它是肠道正常菌群的一部分,条件致病菌。
浸润性,组织渗透/破裂;可引起慢性化脓性感染,放线菌病。
通过在各种手术(牙科,胃肠道),抽吸或病理性疾病(例如憩室炎)过程中破坏粘膜屏障来建立感染。
感染部位:
口腔,宫颈,面部疾病是最常见形式,有时感染可能发生在胸部(肺放线菌病),腹部,骨盆或身体其他部位。
当细菌进入人体时,它可以在软组织上形成脓肿。随着脓肿随着时间的流逝而扩大,它会穿透皮肤表面,引起皮肤溃疡。这些脓肿或肿块通常会影响头和颈部,并且会引起肌肉痉挛,阻止下巴正常运动。
其他常见症状包括:
发烧,体重减轻,咳嗽,胸痛和窦腔过度引流。症状可能发展缓慢,但是早期治疗是迅速康复的关键。
易感人群:
治疗:
抗生素;如果与宫内节育器有关,则须卸下
预防:
良好的口腔卫生和定期看牙医可能有助于预防某种形式的放线菌病。
嗜肺军团菌
Legionella pneumophila
具有一定铁含量的细胞内多形革兰氏阴性细菌,条件致病菌。
普遍存在于水环境中,例如饮用水系统、温泉、冷却水,可引起人类感染军团菌肺炎。
通过抽吸或直接吸入到达肺部后,会附着在呼吸道粘膜上。

图源:apotheekteirlinck.be
症状:
高烧(可能到40℃或更高),发冷,咳嗽,肌肉酸痛和头痛。
传播:
可以在人类制造的水系统(例如空调)中繁殖。大多数人吸入含有军团菌细菌的微小水滴时会被感染。这可能来自淋浴,水龙头或漩涡浴池中的喷雾,或者来自大型建筑物中通风系统中的水。
如何避免致病菌感染?
尽快恢复免疫力,减少致病菌感染的发生率。
个人应通过煮熟鸡蛋和肉类来避免传染源,饮用巴氏杀菌乳制品,避免感染个人和医院的潜在感染源,避免与粪便、灰尘或农场动物接触,这些是主要的感染源。
不要饮用未经处理的水,例如直接来自湖泊或河流的水。避免在国外饮用自来水。使用瓶装水或滤水器。
不要共用针头、注射器或其他药物注射设备。
有害菌和肠道内的其他共生菌共同构成菌群微生态,也是大部分人群肠道内常见的菌群。
有害菌是相对而言的。正常肠道菌群也包含许多有害菌,但有害菌比例或个别菌属丰度超标可能预示着肠道菌群的健康状况受到破坏。
有害菌过多会影响肠道内环境,如pH值,含氧量以及肠道内毒素等,可能会导致出现一些机会感染和机会致病菌入侵,进而诱发炎症和疾病。
谷禾肠道菌群检测报告中的有害菌包含了原发致病菌和条件致病菌,以及属内主要菌种为致病菌的属。
为便于统计,我们在计算的时候统一按照属层级进行计算比例。
报告中的有害菌包括了以下的菌属:韦荣氏球菌属、葡萄球菌科、变形菌属、弓形菌属、弯曲菌属、螺杆菌属、厌氧螺菌属以及弧菌属等。
具体每个菌相关介绍详见:
全面认识——肺炎克雷伯菌 (Klebsiella pneumoniae)
慢病是每一种病单独构建模型,不一定和有害菌或菌群平衡指标直接有关。
肠道菌群中的有害菌过多,也就是说肠道菌群趋向于失衡,这会给身体带来诸多麻烦。
当肠道内的有害菌增多时,起初可能会有些症状出现,例如:
随着时间的推移,如果没有采取相应的干预措施,有害菌变得过多,则可能会对身体方方面面产生影响:
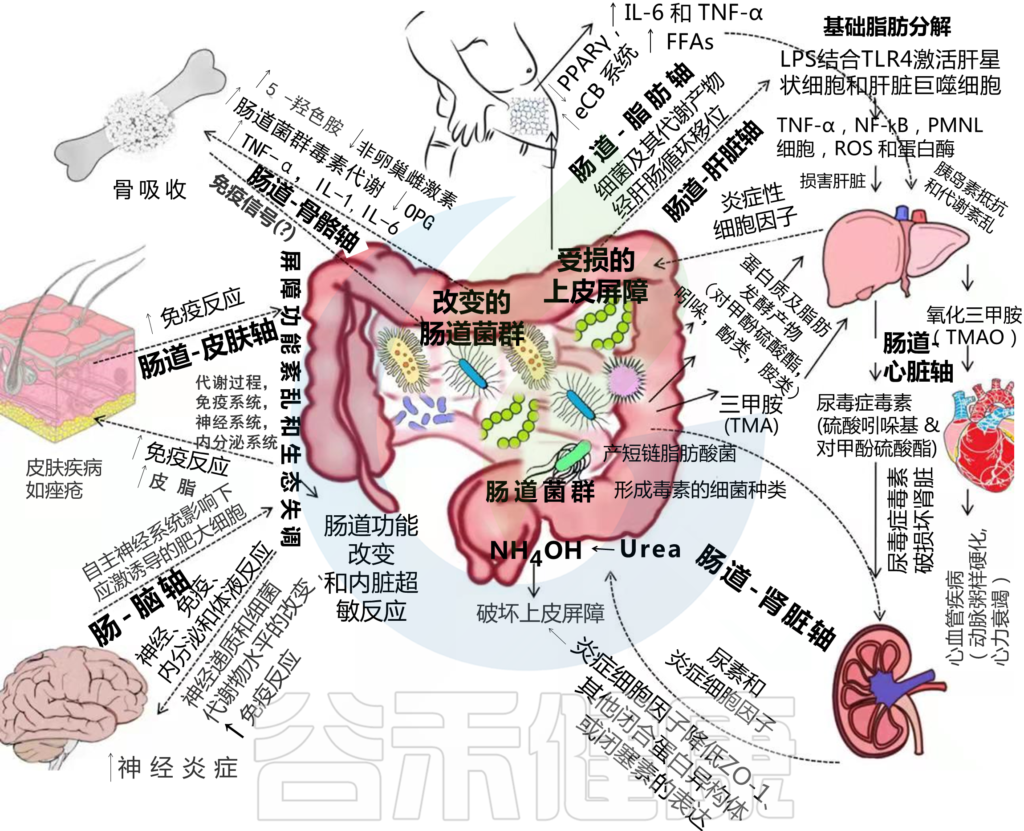
特殊类型的细菌会产生一种化学物质,肝脏会将其转化为三甲胺- n -氧化物(TMAO)。
TMAO产生的增加会导致血管中胆固醇的积聚,从而可能导致心脏病。
详见:
TMAO产生的增加也与慢性肾脏疾病有关。也会导致肾结石的发展。
与健康对照组相比,终末期肾病患者体内的TMAO浓度可高出20倍。
对终末期肾病患者的类似研究表明,从普雷沃氏菌向拟杆菌转变,产丁酸菌减少。

有害细菌将纤维转化为脂肪酸。身体可能会把它们沉积在肝脏中,如果不及时治疗,可能导致代谢综合征的发展。
肝硬化患者中韦荣球菌属和链球菌增多。
肝细胞癌与肠道大肠杆菌过度生长有关,患者微生物群多样性增加,与产丁酸菌属(如Alistipes)减少有关,而致病性产脂多糖菌(如克雷伯氏菌)增加。
研究表明,肠道菌群在宿主的代谢和疾病状态中起着重要的作用。特别是2型糖尿病,其病因复杂,包括肥胖、慢性低度炎症,受肠道微生物群和微生物代谢产物的调节。
在2型糖尿病患者普遍具有相对高丰度的特定属:
Blautia、Coprococcus、Sporobacter、Abiotrophia、Peptostreptococcus、Parasutterella、Collinsella
2型糖尿病患者肠道菌群详见:
谷禾数据库统计发现,在有害菌属的丰度水平分布上,肥胖人群要高于对照人群。进一步对具体菌属进行分析,发现肺炎克雷伯氏菌的丰度水平肥胖人群更高。
肥胖患者肠道菌群详见:
肠道有许多直接与大脑沟通的神经末梢,称为肠脑轴。肠道炎症和菌群失调与心理健康不良有关。过多的有害肠道细菌会导致:
详见:
不良的肠道细菌会影响你的整体健康。它会增加消化问题的风险,这些症状通常伴有体重减轻和腹痛。比如:
肠道上皮、免疫系统和共生细菌之间的串扰是启动全身炎症反应的关键。有益菌和有害菌的失衡,抗炎和促炎细胞因子之间的失衡,包括白细胞介素(IL)-1β、肿瘤坏死因子、干扰素(IFN)-γ、白细胞介素-6、白细胞介素-12和白细胞介素-17,在参与RA发病机制的炎症过程中起着核心作用。
为了支持肠道菌群成分变化在类风湿性关节炎发病和进展中起重要作用的假说,已经提出了肠道菌群与关节炎相关的几种机制。
这些包括调节宿主免疫系统(触发T细胞分化)、通过作用Toll样受体(TLR)或NOD样受体(NLR)激活抗原呈递细胞(APC)、通过酶促作用促进肽的瓜氨酸化、抗原模拟和增加肠粘膜通透性。关于对APCs TLRs表达的影响,这可能导致Th17/Treg细胞比率失衡,这种局部免疫反应可能导致系统性自身免疫。
有害菌过多会导致肠道通透性和肠道屏障破坏。肠黏膜屏障功能障碍可能导致血清脂多糖 (LPS) 水平升高,从而导致代谢性内毒素血症。早期研究表明,LPS 可促进体内股骨的骨质流失和体外破骨细胞的。
与骨骼疾病相关的肠道菌群变化如下:

编辑
详见:
鉴于具有高度稳定性的平衡肠道微生物群与宿主的免疫系统具有共生相互作用,能够抑制有害菌增长。然而不稳定的状态例如肠道紊乱,慢性疾病,由遗传易感性、化学物质或肠道病原体感染引起的肠道炎症会导致有害菌增加。
其他包括饮食、生活方式、环境等因素也会影响肠道微生物群的分类和功能组成。例如,西方饮食、高糖饮食,饮食结构过于单一,加工食品过多摄入等不健康的饮食方式,睡眠不足,作息不规律,不运动等不良生活习惯,压力过大,服用药物等因素都会导致有害菌增多。
有害菌和肠道内的其他共生菌共同构成菌群微生态,如果有害菌过多,通常我们可以通过服用益生菌或益生元的方式首先增加有益菌的比例,相应的有害菌比例就会降低。
双歧杆菌和乳酸杆菌有助于发酵碳水化合物,同时会产短链脂肪酸,有助于维持良好的消化系统。
乳酸杆菌
乳酸杆菌菌株产生乳糖酶。它有助于分解乳制品中的乳糖,有助于维持肠道的酸度水平,对于吸收关键矿物质至关重要。
双歧杆菌
保护肠壁;维持肠道的酸度;限制产生硝酸盐菌的生长;生产 B 族维生素和维生素 K 等。
益生菌抑制其他菌群的生长:
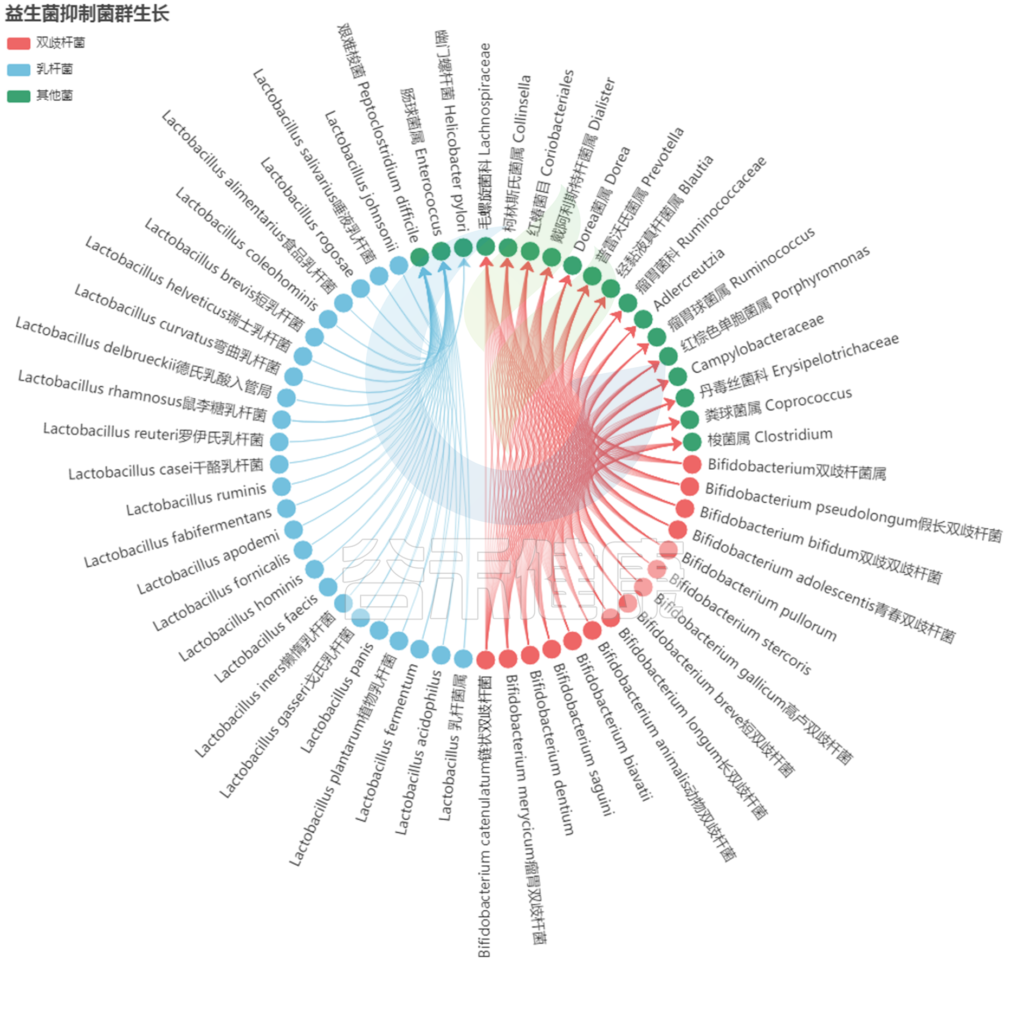
编辑
<来自谷禾健康数据库>
除了直接服用益生菌这种方式之外,有些食物中也富含益生菌,如:
乳制品:酸奶、牛奶、开菲尔等
发酵食品:泡菜、酸菜、味噌汤、豆豉等
益生元是一种可溶于水的可溶性纤维,可以作为益生菌的“食物”。
最广泛认可的益生元包括低聚果糖 (FOS)、菊粉和低聚半乳糖 (GOS) 等。
此外还包括抗性淀粉、果胶寡糖 (POS)、多酚等。
含益生元的食物包括:菊芋、青香蕉或青香蕉粉、大麦和燕麦、魔芋根、菊苣根、牛蒡根、亚麻籽、海藻、苹果、土豆等。
关于益生菌,益生元的补充详见:
想要持久的改善菌群结构降低有害菌水平就需要改善生活方式,适当增加抗性淀粉等膳食纤维并规律饮食和睡眠,增加运动等。
下面介绍一些日常生活中可以自行调整的饮食及生活方式。
尝试食用多种食物,避免每天食物一样
饮食多样性更有利于菌群维持健康平衡。体内的微生物群就好比一群挑剔的孩子,每个孩子都会去吃自己喜欢的食物。当你吃下各种食物时,就相当于喂食了各种微生物。
如果可以的话,一个星期的饮食中可以摄入 40 种及以上不同类型的天然食物,尽可能地提高肠道多样性。
减少西方饮食
西方饮食(其特点是大量摄入脂肪、蛋白质、糖、盐和加工食品),可能增加有害菌,与伴随的导致自身免疫疾病发展的微生物变化之间的联系越来越明显。
尝试地中海饮食
其他可以参考地中海饮食结构摄入,适量食用纤维,多吃各种颜色的水果和蔬菜。将红肉的摄入限制在每月两三次,可以将其视为一种“奢侈品”,每周食用两到三次家禽。它的饱和脂肪和胆固醇比红肉少得多,选择健康的脂肪,每周可以食用两次三文鱼等,做菜选择橄榄油,适量食用坚果(杏仁、巴西坚果、榛子、松子、开心果和核桃都是非常健康的坚果类型),它们是单不饱和脂肪的重要来源。
尝试抗炎饮食
很多种食物均具有抗炎特性,其中包括抗氧化剂和多酚含量高的食物。肠道抗炎饮食推荐的食物包括:浆果类,西兰花,牛油果,辣椒,姜黄,洋葱,大蒜等。
详见:
避免膳食纤维过多或过少
膳食纤维细菌发酵的产物(短链脂肪酸、乙醇和乳酸)过多会破坏细菌。纤维也会让人“上瘾”,其发展方式:随着发酵破坏细菌,需要越来越多的纤维来形成粪便。
但是膳食纤维摄入不足或突然停止所有纤维摄入,也会发生菌群失衡,导致便秘或其他肠道问题,从而导致有害菌增加。
减少摄入加工和包装食品
食用的加工食品越多,饮食越无菌,加工食品会减少我们体内有益细菌的数量,相应的有害菌会逐渐增多,破坏肠道菌群原有的平衡。
具体来说,防腐剂,比如聚山梨酯80和羧甲基纤维素(CMPF),它们是许多加工食品中常见的乳化剂,直接改变了肠道微生物群的组成。
食品添加剂对菌群的影响详见:
你的焦虑可能与食品添加剂有关,警惕食品添加剂引起的微生物群变化
尽量避免含糖饮食
对于我们大多数人来说,糖在我们的饮食中太普遍了。
在现代饮食中,糖无处不在,而且形式多种多样。我们大多数人现在都知道,过度消费“游离糖”的精制糖并不健康。糖也是造成菌群失调的主要因素。然而在忙碌的现代生活中,很难不过度摄入糖分。
高糖食物的常见罪魁祸首包括碳酸饮料、能量饮料、糖果、饼干、甜点、蛋糕、果汁和谷物等,它们都会导致菌群失调。
还有一些食物,含有的糖分更加隐蔽。这些包括:即食食品、腌泡汁、酸辣酱和泡菜、一些酒精饮料、调味酱、白面包、白米饭和土豆。
糖对菌群的影响详见:
吃八分饱
少吃多餐,每三到四个小时吃一顿小餐或吃零食,以补充精力。
间歇性禁食
间歇性禁食是一种越来越流行的健康实践,研究发现间歇性禁食导致肠道菌群结构改变,进食时机和频率可以一定程度上改善生活方式和心血管代谢,防止2型糖尿病和心血管疾病的发生。
关于间歇性禁食详见:
维生素维持肠道菌群稳态和减少肠道炎症以预防癌症的机制;肠道菌群帮助吸收营养,并参与维生素代谢。几项观察表明,微生物群失调和维生素缺乏是相互关联的。
例如:
补充维生素 C 可减少肠杆菌科细菌的数量,增加乳酸杆菌的丰度,抑制有害菌的生长,促进有益菌的增加。
维生素 D 的缺乏会增加拟杆菌门、变形杆菌门和螺杆菌科的丰度。
维生素E对变形菌有抑制作用,而维生素E(和纤维)的摄入量较低与Sutterella水平较高相关。


详见维生素的文章:
当肠道渗漏也就是屏障受损时,大量的有害菌及微生物代谢毒素、食物中的有毒物质逃离肠道,涌入血液循环,这可能会产生炎症并导致组织损伤,器官从感染到炎症再到功能缺失,甚至是到癌症。
关于什么情况会导致肠漏,肠漏带来的危害详见:
即使是很小的压力也会触发体内激素和化合物的释放。压力会慢慢积累,如果你是一个压力大的人,经常烦躁,愤怒,那么会对微生物群产生负面影响,扰乱 HPA 轴。不过这是双向的,肠道中的某些细菌菌株也会影响体内神经递质的方式。
适当给自己减压,可以帮助菌群恢复平衡。减压的方式包括:
农村环境和微生物群与过敏患病率的降低有关。通过暴露于农村室内灰尘来调节肠道微生物群可以改善过敏预防。
城市儿童和小鼠暴露在城市灰尘提取物中,肠道菌群向拟杆菌类的变化是明显的。相比之下,农村儿童和接触农村粉尘提取物的小鼠肠道菌群分别富含普雷沃氏菌属和梭状芽孢杆菌属。
环境对菌群的文章详见:
环境污染物通过肠脑轴影响心理健康,精神益生菌或将发挥重要作用
睡眠质量与肠道菌群组成之间存在双向关系。

编辑
拟杆菌门和厚壁菌门的丰度与睡眠质量呈正相关,而毛螺菌科(Lachnospiraceae)、棒状杆菌(Corynebacterium)、Blautia等几种菌与睡眠质量测量值呈负相关。
睡眠不足或者其他因素如受伤、食物摄入、压力、昼夜节律和运动等,可致肠屏障损伤和细菌移位,增加感染易感性,激活HPA轴从而影响菌群。
详见睡眠对肠道菌群的影响的文章:
抗生素
正常情况下,强大的免疫系统会追捕并消灭病原体,但在系统较弱的情况下,人体的免疫防御系统无法控制病原菌的生长。
服用抗生素会杀死体内的许多好细菌和坏细菌。在瑞典的一项临床试验中,研究人员发现,在服用抗生素仅一周后,一些参与者在一整年后就破坏了微生物组。
抗生素使用对肠道菌群变化的不同影响

Yang L, et al., AMB Express. 2021
我们之前写过抗生素对菌群的影响文章,详见:
其他包括非甾体抗炎药、质子泵抑制剂 (PPI)等也会影响肠道菌群的组成。
限制饮酒量
酒精诱导的胃肠道菌群组成和代谢功能的变化可能有助于建立酒精诱导的氧化应激、肠道对菌群产物的高通透性和随后发展的酒精性肝病和其他疾病之间建立明确联系。如果体内酒精过多,肝酶可能没有足够的能力对其进行处理。过量的酒精会在身体的其余部分循环,产生负面影响。
坚持适量运动
运动锻炼与肠道微生物群组成之间可能存在密切关联。经常中等强度的耐力运动对肠道微生物产生最有益的影响,促进健康和抗炎细菌增加;长期运动的人菌群多样性更高。
运动改善菌群多样性,增加菌群种类,有益于提高菌群稳定性,降低有害菌的相对比例。
运动对菌群的影响详见:
肠道微生物组如何影响运动能力,所谓的“精英肠道微生物组”真的存在吗?
在我们的检测实践中,以上的这些干预调节方式可以有效的定向改善特定有害菌和致病菌的超标,并最终带来整体健康状况的改善。
主要参考文献:
Janik E, Ceremuga M, Niemcewicz M, Bijak M. Dangerous Pathogens as a Potential Problem for Public Health. Medicina (Kaunas). 2020 Nov 6;56(11):591. doi: 10.3390/medicina56110591. PMID: 33172013; PMCID: PMC7694656.
Sheppard SK. Strain wars and the evolution of opportunistic pathogens. Curr Opin Microbiol. 2022 Jun;67:102138. doi: 10.1016/j.mib.2022.01.009. Epub 2022 Feb 12. PMID: 35168173.
Balloux F, van Dorp L. Q&A: What are pathogens, and what have they done to and for us? BMC Biol. 2017 Oct 19;15(1):91. doi: 10.1186/s12915-017-0433-z. PMID: 29052511; PMCID: PMC5648414.
Kinnula H, Mappes J, Sundberg LR. Coinfection outcome in an opportunistic pathogen depends on the inter-strain interactions. BMC Evol Biol. 2017 Mar 14;17(1):77. doi: 10.1186/s12862-017-0922-2. PMID: 28288561; PMCID: PMC5348763.
Engen PA, Green SJ, Voigt RM, Forsyth CB, Keshavarzian A. The Gastrointestinal Microbiome: Alcohol Effects on the Composition of Intestinal Microbiota. Alcohol Res. 2015;37(2):223-36. PMID: 26695747; PMCID: PMC4590619.
Kouzu K, Tsujimoto H, Kishi Y, Ueno H, Shinomiya N. Bacterial Translocation in Gastrointestinal Cancers and Cancer Treatment. Biomedicines. 2022 Feb 4;10(2):380. doi: 10.3390/biomedicines10020380. PMID: 35203589; PMCID: PMC8962358.

谷禾健康
人的身体拥有数千种细菌,这些细菌在维持健康方面发挥着重要作用。当这些细菌失控繁殖并侵入身体的其他部位或将有害细菌引入身体的系统时,可能会发生细菌感染。
细菌感染的严重程度取决于所涉及的细菌类型和所感染的部位等。细菌最常感染肠道、皮肤和呼吸系统,包括肺、泌尿道和阴道。
目前应对细菌感染的主要治疗方法还是使用抗生素,但是抗生素管理,或改进抗生素的处方和使用方式,对于优化感染患者的治疗、保护患者免受伤害和对抗抗生素耐药性至关重要。
今天我们重点了解下什么是细菌感染,感染的症状、原因和类型,包括诊断测试和治疗方案,抗生素什么时候使用,什么时候不用,抗生素的耐药性如何产生以及使用抗生素的注意事项等。
了解什么是细菌感染以及如何治疗细菌感染,我们应该先了解细菌的概念。
来源:MedicineNet
地球上所有的生物都是由两种基本类型的细胞中的一种组成:
真核细胞,其遗传物质被包裹在核膜内;
原核细胞,其遗传物质与细胞的其他部分不分离。
传统上,所有的原核细胞都被称为细菌,被归为原核生物界。
1970年代后期,美国微生物学家卡尔·沃斯(Carl Woese)率先在分类上进行了重大变革,将所有生物分为真核生物、细菌(原名真细菌)和古细菌(原名古细菌)三个领域,以反映三条古老的进化路线。原核生物以前被称为细菌,然后被分为两个领域,细菌和古细菌。
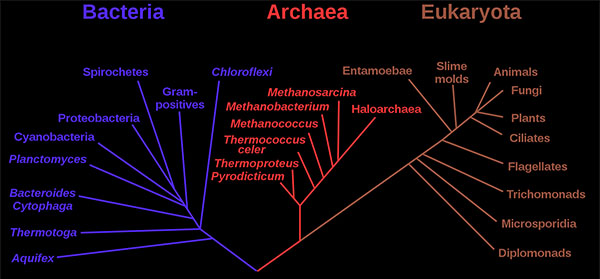

published by Woese et al.
细菌和古细菌在表面上是相似的,例如,它们没有细胞内的细胞器,它们有环状DNA。但是,它们在本质上是截然不同的,它们的分离是基于其古老而又独立的进化谱系的遗传证据,以及其化学和生理学的根本差异。这两个原核域的成员彼此之间的区别与它们和真核细胞中的区别一样。
细菌细胞在几个方面不同于动物细胞和植物细胞。一个根本的区别是细菌细胞缺乏动物细胞和植物细胞中都存在的细胞内细胞器,例如线粒体,叶绿体和细胞核。细菌体积小,设计简单,代谢能力强,使它们能够迅速生长和分裂,并在几乎任何环境中生存和繁衍。
细菌,动物和植物细胞的比较

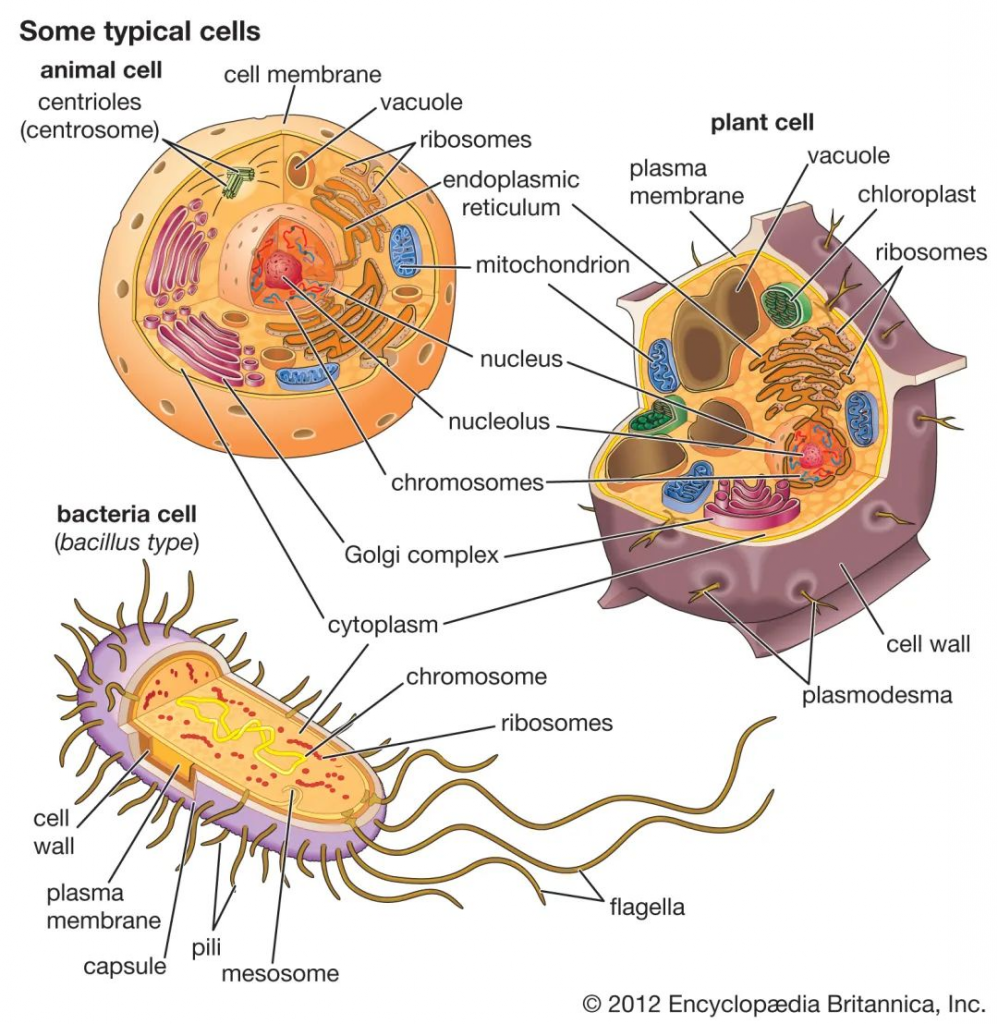
除此之外,原核和真核细胞在许多其他方面有所不同,包括脂质组成,关键代谢酶的结构,对抗生素和毒素的反应以及遗传信息的表达机制。
真核生物包含多个线性染色体,这些染色体的基因比编码蛋白质合成所需的基因大得多。遗传信息的核糖核酸(RNA)副本(脱氧核糖核酸或DNA)的大部分被丢弃,剩余的信使RNA(mRNA)在被翻译成蛋白质之前已被充分修饰。相反,细菌具有一个包含所有遗传信息的环形染色体,它们的mRNA是其基因的精确副本,不会被修饰。
细菌细胞在结构上比真核细胞小得多,也简单得多,但细菌是一个在大小、形状、生境和代谢上都有差异的极其多样化的有机体群体。
许多关于细菌的知识来自对致病细菌的研究,这些细菌比许多自由生活的细菌更容易在纯培养中分离出来,也更容易被研究。必须注意的是,许多自由生活的细菌与适应作为动物寄生虫或共生体生活的细菌有很大的不同。因此,关于细菌的组成或结构没有绝对的规则,任何说法都会有许多例外。
大多数细菌对地球上的生命都是有益的,甚至是生命所必需的,但少数细菌却对人类有害。目前,没有一种古细菌被认为是病原体,但是包括人类在内的动物不断遭到大量细菌的“轰击和居住”。
口腔,肠道和皮肤被大量特定类型的细菌定殖,这些细菌适应这些栖息地的生活。这些微生物在正常情况下是无害的,并且仅在它们以某种方式穿过身体的屏障并引起感染时才变得危险。
一些细菌擅长入侵宿主,被称为病原体或疾病产生者。一些病原体作用于人体的特定部位,例如:
在食物中传播的许多致病菌的毒素在摄入时会引起食物中毒。
由金黄色葡萄球菌(Staphylococcus aureus)产生的毒素,能引起迅速、严重但有限的胃肠道不适。
肉毒梭菌(Clostridium botulinum)的毒素,通常是致命的。在密封前未完全煮熟的罐装非酸性食品中可能产生肉毒杆菌毒素。肉毒梭菌形成耐热孢子,可以发芽为营养细菌细胞,在厌氧环境中茁壮成长,这有利于产生其极强的毒素。
其他食源性感染实际上是由受感染的食物处理者传播的,包括伤寒、沙门氏菌病(沙门氏菌属)和志贺氏菌病(痢疾志贺氏菌属)。
关于食物中毒相关细菌详见:正值夏季,警惕食源性疾病,常见的食物中毒的病原菌介绍
细菌感染是指病原菌侵入宿主组织。当有害细菌进入人体或伤口并繁殖,导致疾病、器官损伤、组织损伤或疾病时,就会发生细菌感染。细菌可以感染身体的任何部位。
细菌感染很常见,但它们并不完全相同。细菌有很多种,每种对身体都有不同的影响。广义上来讲,细菌感染也可以是由任何细菌引起的任何内部或外部疾病的广义术语。
细菌存在于与人体的各种关系中。它们在体表内定殖并提供益处,正常情况下细菌可以与人类身体共存不会产生有害的影响(在共生关系中)。但是有时候,通常无害地存在于我们体内或皮肤上,而不会造成任何异常问题的细菌会失控并导致感染。这种情况通常发生在我们的免疫系统不够强大,无法保持它们的平衡,或者我们的微生物区系的组成发生了一些变化,对某些细菌生存繁殖更有利。
细菌感染是由体内的坏细菌引起的。一些细菌感染可能危及生命。标准的医学治疗通常涉及一剂抗生素。细菌感染很容易与病毒感染混淆。但是他们并不一样,后面我们会单独解释。
当皮肤粘膜有破损或发生化脓性炎症时,细菌则容易侵入体内。
人体的免疫反应可分为非特异性免疫反应及特异性免疫反应两种,后者又可分为细胞免疫与体液免疫两方面。当机体免疫功能下降时,不能充分发挥其吞噬杀灭细菌的作用时,即使入侵的细菌量较少,致病力不强也能引起感染;条件致病菌所引起的医源性感染也逐渐增多。
人体免疫功能正常时,进入血中的细菌迅速被血中防御细胞如单核细胞、嗜中性粒细胞等所清除,而患肝硬变、糖尿病、血液病、结缔组织病等慢性病者,可因代谢紊乱、体液免疫及细胞免疫功能减低,易招致败血症发生;各种免疫抑制药物的使用、放射治疗亦是导致败血症发病率高的原因。广谱抗菌药物使用后,对药物敏感的细菌虽被抑制或杀灭,而一些耐药菌乘机繁殖,亦可酿成败血症。
细菌侵入人体后是否引起感染,除了与人的防御、免疫功能,还与细菌的毒力及数量有关。毒力强或数量多的致病菌进入机体,引起感染的可能性较大。
严重烧伤时,创面为细菌敞开门户,皮肤坏死、血浆渗出又为细菌繁殖提供了良好环境,故极易发生感染。
尿路、胆道、胃肠道、呼吸道粘膜受破坏后,若同时有内容物积滞、压力增高,细菌更易进入血中,保留导尿管、静脉等血管内留置导管、人工辅助呼吸时插管等,也使细菌易于侵入。
细菌是微观的,通常是单细胞生物,到处都可以找到(例如,在我们体内、皮肤上、空气中、水里、土壤中或我们吃的食物里)。细菌具有传染性,因此,它可以通过与患者的密切接触在人与人之间传播。接触受污染的表面、食物、水以及打喷嚏和咳嗽就是例子。
发生感染的几个条件:
此外,细菌还可以导致急性感染(快递治疗)和慢性感染(持续很长时间甚至终生),以及潜伏感染(最初可能没有任何明显迹象或症状但可以过段时间自然发展)。症状可以从轻度、中度到重度不等。在严重的情况下,导致数百万人死亡;例如,许多人死于黑死病或鼠疫。
细菌感染的常见特征:
常见的各部位细菌感染的症状

细菌性感冒
细菌性感冒(Bacterial cold)是指继发细菌感染引起的感冒。感冒在习惯上分为病毒性感冒和细菌性感冒。
病毒性感冒有:普通感冒、流行性感冒和病毒性咽炎等。其主要不同是致病因素不同,病毒性感冒是由于病毒所致,而细菌性感冒是由于细菌所致。
注:流行性感冒(流感通过病毒传播,不是细菌性感冒,注意区分),是由流感病毒引起的急性呼吸道传染病。
细菌的感染还取决于受感染细菌的类型,常见的细菌感染例如:
细菌感染具有高度传染性,因此需要特别注意避免通过洗手、打喷嚏和咳嗽时遮盖以及不共用杯子和饮料瓶来传播感染。
细菌有多种传播方式,包括:

当你忍不住咳嗽或打喷嚏时,用纸巾捂住口鼻或用手肘内侧。
在下述情况下需要洗手,至少洗20秒:
如果没有肥皂和水,可以使用酒精含量至少为 60% 的酒精类洗手液。
除此之外,其他需要注意的:
接种疫苗。如轮状病毒是一种导致婴儿和幼儿严重肠胃炎的病毒。所有婴儿都应在 6 周和 4 个月大时接种轮状病毒疫苗。
流感疫苗。当患上流感时,免疫系统会被削弱。这使细菌有机会侵入肺部并引起感染。每年注射一次流感疫苗可以防止感染肺部细菌。
肺炎球菌多糖疫苗。美国疾病控制与预防中心 (CDC) 推荐 65 岁及以上的人接种肺炎球菌多糖疫苗 (PPSV)。它也适用于免疫系统较弱或患肺炎风险较高的成年人。
治疗取决于感染的严重程度、患者的年龄、免疫系统有多强、是否存在任何并存症状以及现有的医疗条件。
治疗可能包括:
扩展阅读:
细菌素——对抗感染、保存食品、重塑肠道菌群
还在滥用抗生素?15种天然抗生素助你调节肠道菌群
这里我们主要来了解一下,用于细菌感染的药物——抗生素。
目前抗生素是对抗细菌感染的常用药物。它们通过破坏细菌细胞生长和增殖所需的过程来发挥作用。
抗生素根据抗菌谱可以分为:
广谱抗生素,中谱抗生素和窄谱抗生素。
✓ 广谱抗生素
广谱抗生素可对抗多种细菌。广谱抗生素可治疗革兰氏阳性菌和阴性菌,因此如果医生不确定有哪些细菌,他或她可能会开出其中一种抗生素。
阿莫西林、奥格门汀、头孢菌素(第 4 代和第 5 代)、四环素氨基糖苷类和氟喹诺酮类(环丙沙星)是广谱抗生素的例子。
✓ 中谱抗生素
中谱抗生素针对一组细菌。青霉素和杆菌肽是流行的中谱抗生素。
✓ 窄谱抗生素
窄谱抗生素用于治疗一种特定的细菌。多粘菌素属于这一小类抗生素。当确定患有哪种细菌感染时,治疗会更容易和更有效。
抗菌活性通常分为五种机制:
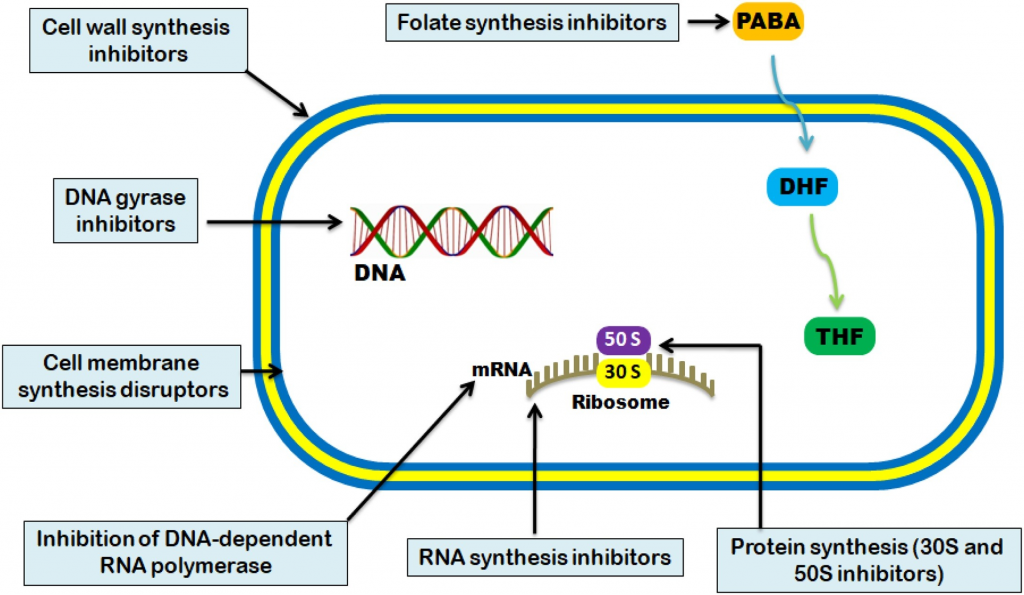

Uddin TM, et al., J Infect Public Health. 2021
不同种类抗生素作用的方式


Uddin TM, et al., J Infect Public Health. 2021
青霉素
最初的青霉素仅用于革兰阳性菌感染的治疗,由于金黄色葡萄球菌很快产生一种青霉素酶对青霉素产生了耐药,人们研制出了以甲氧西林、苯唑西林为代表的耐酶青霉素,用于产青霉素酶的葡萄球菌( 甲氧西林耐药者除外) 感染。
之后,以氨苄西林、阿莫西林为代表的广谱青霉素由仅对革兰阳性(G+) 菌有效扩展到对革兰阴性(G-) 菌( 主要为肠杆菌科细菌) 也具有抗菌活性。在广谱青霉素的基础上又发展为对铜绿假单胞菌等非发酵菌也具抗菌活性者,当前应用主要为脲基类青霉素,包括: 哌拉西林、阿洛西林、美洛西林。
代表药物: 阿莫西林(amoxicillin)
阿莫西林是一种抗细菌的青霉素抗生素。
阿莫西林用于治疗由细菌引起的多种不同类型的感染,例如扁桃体炎、支气管炎、肺炎以及耳、鼻、喉、皮肤或泌尿道感染。
阿莫西林有时还与另一种称为克拉霉素( Biaxin ) 的抗生素一起用于治疗由幽门螺杆菌感染引起的胃溃疡。这种组合有时与一种称为兰索拉唑(Prevacid)的胃酸减少剂一起使用。
四环素
四环素是一类抗生素,可用于治疗由易感微生物引起的感染,例如革兰氏阳性菌和革兰氏阴性菌、衣原体、支原体、原生动物或立克次体。
它们是在 1940 年代发现的,第一个四环素是从链霉菌中获得或衍生的。
四环素抑制微生物 RNA 中的蛋白质合成(一种重要的分子,作为 DNA 的信使)。它们主要是抑菌剂,这意味着它们可以防止细菌繁殖,但不一定会杀死它们。
四环素类药物现今应用的品种除四环素外,更常用有多西环素( 强力霉素) 和米诺环素( 二甲胺四环素) 。由于常见病原菌对本类药物耐药性普遍升高及其不良反应多见,当前本类药物临床应用已受到很大限制。
代表药物:强力霉素(doxycycline)
强力霉素是一种四环素抗生素,可以对抗体内的细菌。
强力霉素用于治疗许多不同的细菌感染,例如痤疮、尿路感染、肠道感染、呼吸道感染、眼部感染、淋病、衣原体、梅毒、牙周炎(牙龈疾病)等。
强力霉素也用于治疗由红斑痤疮引起的瑕疵、肿块和痤疮样病变。
某些形式的强力霉素用于预防疟疾、治疗炭疽或治疗由螨虫、蜱虫或虱子引起的感染。
什么是林可霉素衍生物?
林可霉素衍生物是一小类抗生素,可抑制细菌蛋白质的合成,而细菌蛋白质对细菌的生存至关重要。林可霉素衍生物保留用于治疗由肺炎球菌、葡萄球菌和链球菌的敏感菌株引起的感染。一种衍生物也可用于治疗恶性疟原虫(疟疾)。
林可霉素类包括林可霉素及克林霉素。克林霉素的体外抗菌活性优于林可霉素,主要可应用于敏感肺炎链球菌、其他链球菌属( 肠球菌属除外) 及甲氧西林敏感金葡菌所致的各种感染。该类药物对厌氧菌有良好的抗菌活性常与其他抗菌药物联合用于腹腔感染及盆腔感染,也由于其骨组织浓度较高适用于骨和关节的G + 菌感染。使用本类药物时,应注意假膜性肠炎的发生,如有可疑应及时停药。本类药物有神经肌肉阻滞作用,应避免与其他神经肌肉阻滞剂合用,应注意静脉滴注速度宜缓慢滴注,不可静脉推注。
代表药物:克林霉素(Clindamycin)
克林霉素是一种抗生素,可以对抗体内的细菌。
克林霉素用于治疗由细菌引起的严重感染。
服用此药前 如果对克林霉素或林可霉素过敏,则不应使用该药。
为确保克林霉素的安全,请告诉医生是否曾经有过:结肠炎、克罗恩病或其他肠道疾病; 湿疹或皮肤过敏反应; 肝病; 哮喘或对阿司匹林的严重过敏反应; 对黄色食用色素过敏。
什么是喹诺酮类药物?
喹诺酮类是一种抗生素。抗生素杀死或抑制细菌的生长。
有五种不同的喹诺酮类。此外,另一类抗生素,称为氟喹诺酮类,是从喹诺酮类通过氟修饰其结构衍生而来的。氟喹诺酮类抗生素可导致严重或致残的副作用,这些副作用可能不可逆。
喹诺酮类药物和氟喹诺酮类药物有许多共同点,但也有一些区别,例如它们对哪些生物有效。有些人互换使用喹诺酮和氟喹诺酮这两个词。
喹诺酮类和氟喹诺酮类对细菌产生的两种酶(拓扑异构酶 IV 和 DNA 促旋酶)的功能产生不利影响,因此它们不能再修复 DNA 或帮助其制造。
现今临床主要应用为氟喹诺酮类,常用有诺氟沙星、环丙沙星等主要用于单纯性下尿路感染或肠道感染。但应注意,现今国内尿路感染的主要病原菌大肠埃希菌中,耐药株已达半数以上。环丙沙星尚与β-内酰胺类抗生素联合用于治疗中、重度革兰阴性杆菌感染包括铜绿假单胞菌的感染。
近年来研制的新品种左氧氟沙星、莫西沙星等对肺炎链球菌、化脓性链球菌等G + 球菌的抗菌作用增强,对衣原体属、支原体属、军团菌等细胞内病原或厌氧菌的作用亦有增强,但对G-菌活性增强不明显,对铜绿假单胞菌的抗菌活性仍以环丙沙星为最强。左氧氟沙星、莫西沙星除可用于尿路感染或肠道感染外也可用于呼吸道感染,特别适合于肺炎链球菌( 包括耐青霉素肺炎链球菌) 、支原体、衣原体、军团菌等所致社区获得性肺炎的治疗,此外亦可用于皮肤软组织感染。
在治疗腹腔、胆道感染及盆腔感染时除莫西沙星外需与甲硝唑等抗厌氧菌药物合用。部分品种可与其他药物联合应用作为治疗耐药结核分枝杆菌和其他分枝杆菌感染的二线用药。
代表药物:环丙沙星(Ciprofloxacin)和左氧氟沙星(Levofloxacin)
环丙沙星和左氧氟沙星是一种氟喹诺酮抗生素,用于治疗不同类型的细菌感染。也用于治疗接触过炭疽或某些类型鼠疫的人。环丙沙星和左氧氟沙星应仅用于无法用更安全的抗生素治疗的感染。
左氧氟沙星、莫西沙星:对肺炎链球菌、A 组溶血性链球菌等革兰阳性球菌、衣原体属、支原体属、军团菌等细胞内病原或厌氧菌的作用强。
环丙沙星、左氧氟沙星:主要适用于肺炎克雷伯菌、肠杆菌属、假单胞菌属等革兰阴性杆菌所致的下呼吸道感染。
头孢霉素
头孢菌素是一大类从霉菌顶孢菌(以前称为头孢菌素)中提取的抗生素。头孢菌素具有杀菌作用(杀死细菌),其作用方式与青霉素相似。它们结合并阻断负责制造肽聚糖的酶的活性,肽聚糖是细菌细胞壁的重要组成部分。它们被称为广谱抗生素,因为它们对多种细菌有效。
自 1945 年发现第一个头孢菌素以来,科学家们一直在改进头孢菌素的结构,以使其对更广泛的细菌更有效。每次结构发生变化,都会产生新的“一代”头孢菌素。迄今为止,头孢菌素已有五代。所有头孢菌素均以 cef、ceph 或 kef 开头。请注意,该分类系统在不同国家/地区的使用并不一致。
第一代头孢菌素是指发现的第一组头孢菌素。它们的最佳活性是对抗革兰氏阳性细菌,如葡萄球菌和链球菌。它们对革兰氏阴性菌几乎没有活性。
第二代头孢菌素尚可应用于由流感嗜血杆菌、大肠埃希菌、奇异变形杆菌等中的敏感株所致的尿路感染、皮肤软组织感染、败血症、骨及关节感染和腹腔、盆腔等感染。但如用于腹腔感染和盆腔感染时需与抗厌氧菌药合用。头孢呋辛尚可用于脑膜炎球菌、流感嗜血杆菌所致脑膜炎的治疗,也可作为围术期预防用药。
第三代头孢菌素:对肠杆菌科细菌等革兰阴性杆菌具有强大抗菌作用,头孢他啶和头孢哌酮对铜绿假单胞菌亦具较强抗菌活性;注射品种有头孢噻肟、头孢曲松、头孢他啶、头孢哌酮等,口服品种有头孢克肟和头孢泊肟酯等,口服品种对铜绿假单胞菌均无作用。应注意的是,不是所有的三代头孢菌素都可用于非发酵菌( 如铜绿假单胞菌、不动杆菌等) 感染的治疗,除了头孢哌酮和头孢他啶;外,如头孢曲松和头孢噻肟不可以用于非发酵菌感染的治疗。
第四代头孢菌素:常用者为头孢吡肟,对肠杆菌科细菌作用与第三代头孢菌素大致相仿,对铜绿假单胞菌的作用与头孢他啶相仿,对革兰阳性球菌的作用较第三代头孢菌素略强。其不同于三代头孢菌素之处为对产头孢菌素酶( AmpC) 的肠杆菌属有效,其次是增强了对作用靶位细菌青霉素结合蛋白( PBP) 的亲和力以及其抗革兰阳性菌的抗菌活性亦较三代头孢菌素增强。
第五代(或下一代)头孢菌素头孢洛林( Teflaro ) 对耐甲氧西林金黄色葡萄球菌(MRSA)具有活性。Avycaz 含有β-内酰胺酶抑制剂avibactam。
代表药物:头孢氨苄(Cephalexin)
头孢氨苄是一种头孢菌素(SEF 一种低孢子)抗生素。它通过对抗体内的细菌起作用。
头孢氨苄用于治疗由细菌引起的感染,包括上呼吸道感染、耳部感染、皮肤感染、尿路感染和骨骼感染。
头孢氨苄用于治疗成人和至少 1 岁儿童的感染。
注意事项:
如果对头孢氨苄或类似抗生素(如Ceftin、Cefzil、Omnicef等)过敏,则不应使用该药。如果对任何药物(尤其是青霉素或其他抗生素)过敏,请告诉医生。
对任何药物(尤其是青霉素)过敏;
肝脏或肾脏疾病;要么肠道问题,例如结肠炎,请告诉医生。
头孢氨苄可以进入母乳。如果正在哺乳婴儿,请咨询医生。
β-内酰胺酶抑制剂
β-内酰胺酶抑制剂是一类阻断 β-内酰胺酶(也称为 β-内酰胺酶)活性,防止 β-内酰胺类抗生素降解的药物。本类药物适用于因产β-内酰胺酶的细菌感染,其抗菌谱主要依据原有抗生素的活性而酶抑制剂仅有对抗细菌产酶的作用,一般不增加抗菌活性。
β-内酰胺酶由以下细菌的某些菌株产生:拟杆菌属、肠球菌属、流感嗜血杆菌、卡他莫拉菌、淋病奈瑟菌和葡萄球菌属,无论是组成型还是暴露于抗微生物剂。
β-内酰胺酶裂解易感青霉素和头孢菌素的 β-内酰胺环,使抗生素失活。一些抗微生物药物(如头孢唑啉和氯唑西林)对某些 β-内酰胺酶具有天然耐药性。β-内酰胺类:阿莫西林、氨苄青霉素、哌拉西林和替卡西林,可以通过与β-内酰胺酶抑制剂组合来恢复和扩大其活性。
克拉维酸、舒巴坦和他唑巴坦都是β-内酰胺酶抑制剂。
大环内酯类
大环内酯类药物主要作为青霉素过敏患者的替代药物,用于治疗β-溶血性链球菌、肺炎链球菌中的敏感菌株所致的上、下呼吸道感染、敏感β-溶血性链球菌引起的猩红热及蜂窝织炎等感染。
大环内酯类是从红糖多孢菌(原名红链霉菌)中提取的一类抗生素,一种土壤传播的细菌。
红霉素是第一个发现的大环内酯类;其他大环内酯类包括阿奇霉素、克拉霉素和罗红霉素。
它们的作用主要是抑菌,但在高浓度时可能具有杀菌作用,或取决于微生物的类型。
代表药物:红霉素
红霉素为大环内酯类原型代表药物,由于其胃肠道反应大、口服吸收差使其疗效受到影响。当下在临床应用的主要为大环内酯类新品种罗红霉素、阿奇霉素和克拉霉素等,其他大环内酯类疗效多不如该三种药物。
罗红霉素主要是改善了其药代动力学,口服生物利用度明显提高、给药剂量减小、不良反应明显减少,但其抗菌谱没有明显的改善,是红霉素的替代药物。
氨基糖苷类
临床常用的氨基糖苷类药物主要有: 链霉素、卡那霉素、丁胺卡那霉素、庆大霉素、妥布霉素、奈替米星、依替米星。
其中链霉素当前主要用抗结核治疗,其次可用于治疗鼠疫及布鲁菌病; 庆大霉素、妥布霉素、奈替米星、依替米星肠杆菌科细菌和铜绿假单胞菌等G - 杆菌具强大抗菌活性,对葡萄球菌属亦有良好作用者。所有氨基糖苷类药物对肺炎链球菌、溶血性链球菌的抗菌作用均差。
链霉素、卡那霉素:对肠杆菌科和葡萄球菌属细菌有良好抗菌作用,但对铜绿假单胞菌无作用者。
庆大霉素、妥布霉素、奈替米星、阿米卡星、异帕米星、小诺米星、依替米星:对肠杆菌科细菌和铜绿假单胞菌等革兰阴性杆菌具强大抗菌活性,对葡萄球菌属亦有良好作用。
碳青霉烯类
碳青霉烯类药物是当下抗菌药物中抗菌谱最广的药物,对各种革兰氏阳性球菌、革兰氏阴性杆菌( 包括铜绿假单胞菌的非发酵菌) 和多数厌氧菌具强大抗菌活性,对大多数β-内酰胺酶高度稳定,但对甲氧西林耐药葡萄球菌和嗜麦芽窄食单胞菌等抗菌作用差。
当下在国内应用的碳青霉烯类抗生素有亚胺培南-西司他丁、美罗培南、帕尼培南-倍他米隆、比阿培南。厄他培南与上述品种不同对非发酵菌缺乏抗菌活性,而其他抗菌作用与上述药品基本相同,适合于治疗社区与医院早期特别是G-杆菌感染的重症患者。
碳青霉烯类对各种革兰阳性球菌、革兰阴性杆菌(包括铜绿假单胞菌、不动杆菌属)和多数厌氧菌具强大抗菌活性,对多数β-内酰胺酶高度稳定,但对甲氧西林耐药葡萄球菌和嗜麦芽窄食单胞菌等抗菌作用差。
现用于细菌感染的抗生素被认为是医学史上最重要的突破之一。不幸的是,细菌的适应性很强,抗生素的过度使用让许多人对抗生素产生了耐药性,造成了严重的问题,尤其是在医院的环境里。
抗生素耐药性是细菌抵抗抗生素杀伤力的能力。换句话说,以前治疗感染的抗生素没有效果了,或者说根本无法杀死细菌。
由于过度使用抗生素,抗生素耐药率持续上升,新的抗菌药物开发缓慢。感染耐药细菌可能导致住院时间更长、费用更高,并增加死于感染的风险。
抗生素耐药性是对全球健康的紧迫威胁,包括后来逐渐出现危险耐药细菌——“超级细菌”。
疾病控制和预防中心 (CDC)发布了对美国的前 18 种耐药性威胁的清单,至少包括:
注:以上这些并未全面列出所有耐药菌。抗生素耐药性模式不断演变,细菌可能并不总是对每位患者的选择抗生素表现出耐药性。在正常情况下,抗生素的选择应基于感染部位和由医疗保健专业人员评估的临床表现、培养/敏感性和其他所需的实验室结果、局部耐药性/敏感性模式以及患者的特定特征。
细菌通过以某种方式调整其结构或功能作为防御机制,从而对抗生素产生抗药性。
当细菌以某种方式发生变化时,细菌会抵抗药物。这种变化可以保护细菌免受药物的影响或限制药物接触细菌。或者这种变化可能导致细菌改变药物或破坏药物。
细菌可以用以下方式与抗生素抗争:
如果说以上列举的是抗生素产生耐药性的内因,那么除细菌本身外的因素也会导致抗生素耐药性的出现。
早前,医生有时会依赖不可靠或不准确的知识,开具抗生素“以防万一”,或在特定窄谱抗生素可能更合适时却开出广谱抗生素。这些情况加剧了选择压力并加速了抗菌素耐药性。
当医生不清楚是细菌或病毒加剧了感染时,他们可能会开抗生素。抗生素对病毒感染不起作用,可能会产生耐药性。
抗生素自我治疗(SMA)与药物使用不当的可能性有关,这会使患者面临药物不良反应的风险,掩盖潜在疾病的迹象,并在微生物中产生耐药性。
过度使用抗生素,尤其是在不正确治疗的情况下服用抗生素,会促进抗生素耐药性。根据疾病控制和预防中心的数据,人类使用大约三分之一的抗生素既不需要也不合适。
抗生素可以治疗由细菌引起的感染,但不能治疗由病毒引起的感染(病毒感染)。例如,抗生素是可以治疗由细菌引起的链球菌性咽喉炎。但对于大多数由病毒引起的喉咙痛,并不是正确的治疗方法。
每天都有成千上万的患者、工作人员和访客到达医院,每个人的衣服上和身体上/体内都有自己的一套微生物组。如果医院没有适当的程序和规程来帮助保持空间清洁,细菌就会传播。
抗生素被用作动物的生长补充剂和生长促进剂。在家畜中发现的耐抗生素细菌可能对人类致病,很容易通过食物链传播给人类,并通过动物粪便在生态系统中广泛传播。在人类中,这可能会导致复杂的、无法治疗的和长期的感染。
由于技术挑战、缺乏知识、对抗细菌生理学的重大困难,制药业对新抗生素的发明在很大程度上放缓了,当新抗生素普及时,耐药性的发展(在相对较短的时间内)几乎是不可避免的。
世界范围内抗生素的过度使用和滥用正在导致抗生素耐药性的全球医疗问题。可能会发生抗生素耐药性感染,在最坏的情况下,可能会没有有效的抗生素。这种情况在严重感染时可能会危及生命。
大多数病毒性疾病不需要特殊药物并且是“自限性”的,也就是说患者自身的免疫系统可以抵抗疾病。病毒性疾病的患者可以休息、多喝水并使用对症治疗。
由病毒引起的疾病包括:
有时,在复杂或长期的病毒感染中,细菌也可能侵入,并导致所谓的“继发感染”。在这些情况下,如果需要,可以使用抗生素。
在感染由病毒引起的疾病中,例如咳嗽、感冒或流感,患者不应要求医生开抗生素。抗生素不能治愈病毒感染,患者可能会因不必要的药物而产生副作用。医生可以用其他方法来帮助患有病毒性疾病的患者进行治疗。
如果感染没有得到正确治疗,抗生素耐药细菌也可能传播给其他人。
——有以下几个原因:
它可能不是治疗感染的正确抗生素
它可能已过时且无效
整个疗程可能没有足够的药物
如果新疾病是病毒感染,则不需要抗生素
一些疫苗可以预防细菌性疾病。抗病毒疫苗,例如流感疫苗或COVID-19 疫苗,可以帮助预防可能与继发性细菌感染(如严重的肺部肺炎)相关的原发性疾病。
在治疗的最初几天感觉好些了的时候,仍应完成整个抗生素疗程。
抗生素使用注意事项
✓ 按照指示使用抗生素
按照医生的指示治疗感染。医生会选择最能对抗导致感染的特定细菌的抗生素类型。目前市面上有许多不同种类的抗生素,大部分需要医生开出的非处方抗生素。
✓ 了解抗生素
有的抗生素需要进行皮试,比如青霉素,以防过敏,不同的抗生素杀菌的作用原理不尽相同,比如青霉素是通过能破坏细菌的细胞壁并在细菌细胞的繁殖期起杀菌作用的一类窄普抗生素,杀菌作用强,可用于敏感菌所致的严重感染,由于该类药物作用的靶位为细菌细胞壁,而人体的细胞没有细胞壁,因此毒性低,用于老年人,新生儿和孕妇时安全性相对较高。
✓ 确保清楚抗生素的使用方式
确保明确知道应该服用多少抗生素,以及何时服用。有些抗生素需要与食物一起服用,有些需要在晚上服用等。特别注意要用完整的病征疗程抗生素,有些人担心抗生素对身体有副作用,病情稍微好转就会停止服用或注射抗生素,但是这可能导致体内的致病细菌未完全清楚,再次发生感染,或引起形成抗生素抗药性,使得以后的感染治疗变得困难。
✓ 清洁伤口以防止细菌感染
通过立即正确清洁和包扎伤口来预防皮肤感染。适当的急救治疗对于帮助预防细菌感染至关重要,但不应尝试自己治疗严重的皮肉伤口。如果伤口很深、很宽或出血很多,应该立即寻求医疗帮助。
治疗伤口前先洗手。如果你用脏手治疗伤口,会增加细菌感染的机会。用温水和抗菌肥皂洗手 20 秒,然后擦干。如果有条件可以戴上手套。
细菌感染性疾病起病急、进展快,重症疑难患者病原细菌复杂,诊断及治疗困难,可危及生命。早期、准确地明确病原微生物对感染判定至关重要,有助于改善预后。
准确诊断细菌感染对于避免不必要的抗生素使用和集中适当的治疗至关重要。
细菌感染是细菌的存在与炎症或全身功能障碍的结合;因此,通常需要不止一种诊断方式进行确认,确定患者是否符合临床病例定义的病史和检查。
不同的病原微生物检测技术对感染的判定价值不同,临床上也会根据患者的病情,可能感染的部位,可供采集的标本等选择适宜的检测技术。


当前,病原微生物检测技术层出不穷,能识别的微生物种类越来越多,但如何正确利用和分析微生物检测结果仍是临床关注的难题。值得注意的是,感染首先是个临床诊断,所有的判定必须基于临床。
定植容易对感染判定产生混淆。正常生理状态下人体口腔、胃肠道、呼吸道及体表等部位均有细菌、真菌存在,患者无感染症状时称为定植菌。当定植菌的致病力改变或机体防御能力下降时,可大量繁殖或被带入机体深部引起感染成为致病菌。
临床医生应如何判断所获取的病原体为定植还是感染,是长久以来的难题,且未形成成熟统一的解决方案。
呼吸道定植菌的综合分析:
就呼吸道定植菌而言,既往认为可根据菌落数量或菌种拷贝数来判定定植与感染,但结果存在偏差。越来越多的学者认为,临床上判定是定植还是感染,需结合患者症状、体征及其他检查结果综合分析。
若患者存在与检测阳性结果相匹配的临床症状和体征,如发热、咳嗽、咳痰等,感染指标升高,肺部出现新发病灶,应考虑感染并给予相应的抗感染治疗。如仅培养阳性,患者无任何感染相关临床表现,则倾向于定植菌。
念珠菌定植的综合分析:
念珠菌可广泛定植于呼吸道、胃肠道及泌尿生殖道,正常屏障破坏、免疫功能受损或局部菌群失调时,定植的念珠菌可生长繁殖引起感染。痰和尿标本中分离出的念珠菌亦应根据临床症状和体征鉴别是定植还是感染,念珠菌血培养阳性时要高度警惕念珠菌血症。
此外,病原微生物检测结果阳性,并不意味着患者一定存在感染或感染一定由检出的病原体所致,需结合标本质量、采集部位、病史及其他检测结果综合分析。
不同部位标本检测出同一种病原体,其代表的临床意义可能并不相同。
以肺炎克雷伯氏菌为例,从肠道粪便样本中检出肺炎克雷伯氏菌,其中丰度占比超过1%的人群有3765例,占比28.2%【谷禾健康数据库】。但是当肺炎克雷伯菌进入血液并感染时,通常会发生细菌血症。症状可能包括发冷,发烧,发抖,肌肉酸痛,疲劳和嗜睡。当肺炎克雷伯菌感染肝脏时,会引起脓性病变,也被称为化脓性肝脓肿。这种类型的感染更常见于患有糖尿病一段时间或已经服用抗生素多年的人。
因病原微生物种类不同,微生物检测方法的选择也不相同;即便检测同一种微生物,因采集部位不同所选择的检测方法也有所差别。
如大肠埃希菌,血培养阳性时需考虑血流感染,怀疑致病性大肠埃希菌感染肠道时需特殊培养或者血清学、PCR,16s测序检测等。因普通大肠埃希菌可寄居在肠道中,粪便普通培养有大肠埃希菌生长并不能直接考虑大肠埃希菌肠道感染。
病原微生物检测技术快速发展,能识别的微生物种类越来越多,但感染首先是个临床诊断,所有的判定必须基于临床。随着检测技术革新带来的是临床辅助手段的进步和多样化,更快、更准确地判定感染一直都是病原学检测的挑战,不同方法各有优劣。当前,并没有一项技术可通过从标本中识别微生物来直接判定机体是否感染该病原体,甚至依靠检测的阴性结果来排除感染都很难实现。
在面对细菌感染诊疗过程中始终需要思考3个问题:患者是否存在感染?如果有感染,致病病原体是什么?如何治疗干预?
充分利用现有的病原微生物检测方法和其他实验室检查手段,综合判定,给出合适的抗菌治疗或其他综合治疗方法,是科学可持续的手段。
主要参考文献:
Uddin TM, Chakraborty AJ, Khusro A, Zidan BRM, Mitra S, Emran TB, Dhama K, Ripon MKH, Gajdács M, Sahibzada MUK, Hossain MJ, Koirala N. Antibiotic resistance in microbes: History, mechanisms, therapeutic strategies and future prospects. J Infect Public Health. 2021 Dec;14(12):1750-1766. doi: 10.1016/j.jiph.2021.10.020. Epub 2021 Oct 23. PMID: 34756812.
Cheung GYC, Bae JS, Otto M. Pathogenicity and virulence of Staphylococcus aureus. Virulence. 2021 Dec;12(1):547-569. doi: 10.1080/21505594.2021.1878688. PMID: 33522395; PMCID: PMC7872022.
Tshibangu-Kabamba E, Yamaoka Y. Helicobacter pylori infection and antibiotic resistance – from biology to clinical implications. Nat Rev Gastroenterol Hepatol. 2021 Sep;18(9):613-629. doi: 10.1038/s41575-021-00449-x. Epub 2021 May 17. PMID: 34002081.
BRM, Mitra S, Emran TB, Dhama K, Ripon MKH, Gajdács M, Sahibzada MUK, Hossain MJ, Koirala N. Antibiotic resistance in microbes: History, mechanisms, therapeutic strategies and future prospects. J Infect Public Health. 2021 Dec;14(12):1750-1766. doi: 10.1016/j.jiph.2021.10.020. Epub 2021 Oct 23. PMID: 34756812.
Carmen Fookes, BPharm, Bacterial Infection. January 13, 2020 Medicine
Spagnolo F, Trujillo M, Dennehy JJ. Why Do Antibiotics Exist? mBio. 2021 Dec 21;12(6):e0196621. doi: 10.1128/mBio.01966-21. Epub 2021 Dec 7. PMID: 34872345; PMCID: PMC8649755
Baquero F, Coque TM, Cantón R. Counteracting antibiotic resistance: breaking barriers among antibacterial strategies. Expert Opin Ther Targets. 2014 Aug;18(8):851-61. doi: 10.1517/14728222.2014.925881. Epub 2014 May 31. PMID: 24881465.
武洁, 王荃. 病原微生物检测在感染判定的意义[J]. 中国小儿急救医学, 2020, 27(3):6.
李丹鹤, 荣爱国, 马瑞芝,等. 病原微生物检验在抗感染经验治疗中的临床意义[J]. 医学理论与实践, 2019, 32(09):127-129.

谷禾健康

在持续的肠道菌群检测实践过程中,我们收到很多新的问题反馈和对肠道菌群检测在具体问题中的疑问。在此谷禾基于长期和大规模样本群的经验以及实验分析,对部分常见问题进行汇总和整理。

一次肠道菌群检测好比一场健康考试,你拿到报告的那一刻,等同于拿到了你考的那张卷子,那么你首先会关心自己考了多少分。
在肠道菌群检测报告中,同样也有基于肠道菌群的健康评估分数,即健康总分。
基于大数据和整体性评估,报告中会给出健康总分这项指标。这个健康总分是如何计算得出的?
还是拿我们最熟悉不过的考试举例,一场语文考试可能包括了拼音词语、阅读理解、写作等模块,所以最后你的总分是综合各个模块的测试之后得到的(比如说拼音写错了扣1分,阅读理解错了一题扣5分……),通过各模块测评后得到的总分反映的是你的综合能力。
健康总分也是一样,综合计算了三个部分:肠道菌群健康状况、疾病风险情况和营养饮食均衡情况综合评估计算。总分100分,采取扣分制,疾病风险和营养不均衡以及菌群失衡都会相应的减分。
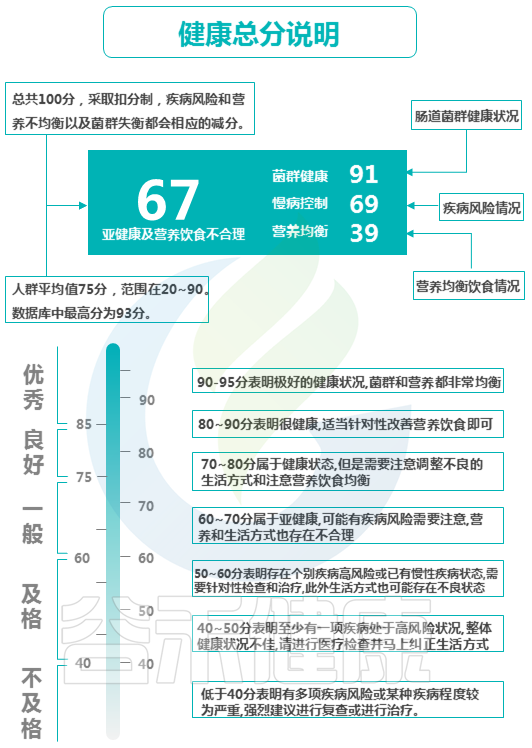
以上是具体的评分标准。
健康总分可以说是非常直观的一个指标,除此之外,整体性评估指标还有一个:肠道预测年龄。
生理年龄是指人达到某一时序年龄时生理和其功能所反映出来的水平,是从医学、生物学角度来衡量的。
谷禾肠道预测年龄是基于超过6万人群队列的深度学习模型构建的,对健康人群的肠道年龄预测与真实生理年龄吻合度很好。
肠道预测年龄和生理年龄就像齿轮运作,井井有条匹配状态,身体这个系统运作起来相对健康轻松。
疾病人群或菌群紊乱人群,肠道年龄会较大偏离真实年龄,也就是这个齿轮系统出现一些偏差问题。
如果肠道菌群多样性下降,且以大肠杆菌为主,可能会被预测为10岁以下儿童,也就是预测年龄远小于真实年龄。
如果存在较多病原菌,则预测年龄会偏向远大于真实年龄。
如果菌群预测年龄和实际生理学年龄相差很大,如何解读?
还是用考试来说,每个年龄段都应具备该年龄段的能力。如果你是一个初中学生,那么就应该答出初中阶段学生该会的题,这时候给你做个测评,发现还停留在幼儿园水平或者已经到了大学生水平,要么太幼稚要么太早熟,都不符合健康的身心发展规律。
肠道预测年龄同样,如果肠道预测年龄偏离实际年龄很大,两种情况,一种是偏大,另一种是偏小。
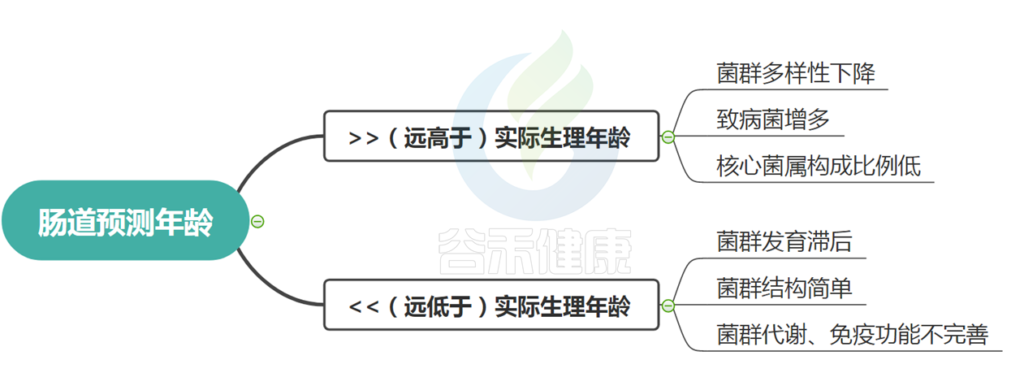
这两种情况均表明菌群发育成熟偏离了实际生长发育,我们均认为其代表菌群状况不太好,存在菌群异常或不健康状况。
如果偏小,即肠道年龄远小于生理学年龄,一般菌群发育滞后或者偏幼龄,菌群构成简单,代谢以及免疫功能不完善。
如果偏大,即肠道年龄远大于生理学年龄,一般菌群多样性下降,变形菌、肠杆菌等致病菌增多,核心菌属构成比例低等。
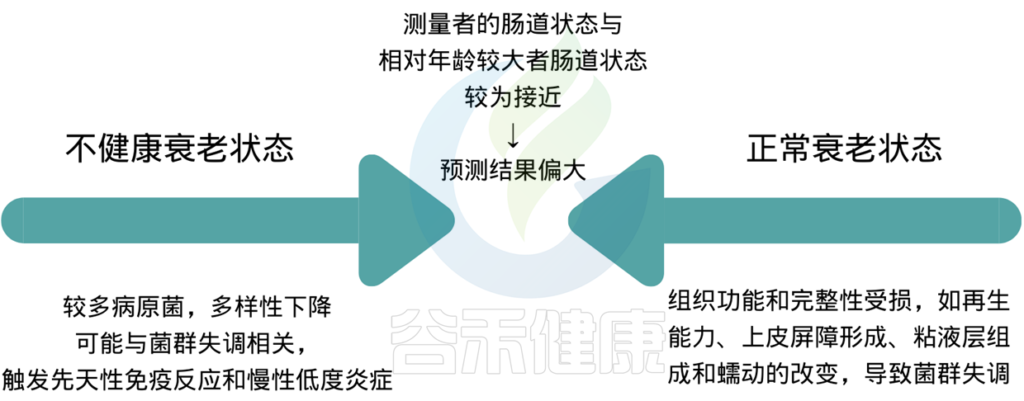
而在正常范围内,肠道预测年龄小于生理学年龄,那么表示菌群发育正常,菌群构成和代谢偏向于更年轻,比较好。那么什么是正常范围呢?
谷禾肠道年龄预测如下范围内表示正常:
0~2岁:偏差小于3个月
3~5岁:偏差在6个月以内
6~15岁:偏差在1岁左右
16~50岁:偏差在3岁以内
50岁以上:偏差在5岁以内
真实年龄与肠道预测年龄在范围内的差异可以反映其肠道菌群的发育和衰老状况。以下情况可能会导致肠道预测年龄完全偏离真实年龄,包括:
▪ 肠道菌群紊乱
▪ 菌群结构过于单一
▪ 近期服用可能严重干扰菌群的药物(如抗生素)
▪ 病原菌感染或者处于疾病状态
▪ 长期补充益生菌
由于肠道年龄考虑了整体的肠道菌群结构,如果肠道年龄严重偏离真实年龄,通过干预调整或去除上述干扰因素肠道年龄是能够恢复正常范围,但该干预周期一般需要1个月以上。
有益菌
有益菌包括益生菌,益生菌主要来自两个菌属:
分别是双歧杆菌属和乳杆菌属,目前已获得批准的有效益生菌菌株均来自这两个细菌属。
其中双歧杆菌可有效改善肠道状况,而特定的乳杆菌菌株可以改善精神健康,包括焦虑和情绪,也能改善肠道健康。双歧杆菌和乳杆菌也是人体肠道菌群中常见的菌。
虽然说是常见菌,却不见得它们数量多。在成年人肠道菌群中,双歧杆菌的比例较低,在1%左右,乳杆菌更是低于1%,甚至很多人(20~40%)的肠道菌群中比例低至万分之一。
下表是谷禾检测的益生菌列表,列出了主要的常见益生菌。

除了上述益生菌,有益菌还包括下列种属,这些菌属是构建肠道菌群的核心菌属,在评估有益菌水平时根据菌属对肠道菌群结构的重要性会给予不同的权重。
Faecalibacterium、Ruminococcus、Roseburia
Phascolarctobacterium、Prevotella、Parabacteroides
Oscillospira、Megamonas、Lachnospira
Lachnoclostridium、Gemmiger、Eubacterium
Coprococcus、Dorea、Dialister
Clostridium、Blautia、Bacteroides
Akkermansia、Alistipes、Agathobacter
通常益生菌的检出率比较低,一般在益生菌补充一周左右在报告中可以体现。从大数据来看,益生菌检出的同时,菌群的相关指标也会有所提升,比如说有害菌降低,改善菌群平衡状况。
有害菌
有害菌和肠道内的其他共生菌共同构成菌群微生态,也是大部分人群肠道内常见的菌群。
有害菌是相对而言的,正常肠道菌群也包含许多这些菌属的菌,但有害菌比例或个别菌属丰度超标可能预示着肠道菌群的健康状况受到破坏。这些菌过多会影响肠道内环境,如pH值,含氧量以及肠道内毒素等,可能会导致出现一些机会感染和机会致病菌入侵,进而诱发炎症和疾病。
我们报告中的有害菌包含了致病菌和条件致病菌,以及属内主要菌种为致病菌的属。为便于统计,我们在计算的时候统一按照属层级进行计算比例。
报告中的有害菌包括了以下的菌属:韦荣氏球菌属、葡萄球菌科、变形菌属、弓形菌属、弯曲菌属、螺杆菌属、厌氧螺菌属以及弧菌属等。
在肠道菌群检测报告中会有对有益菌,有害菌的整体评估。
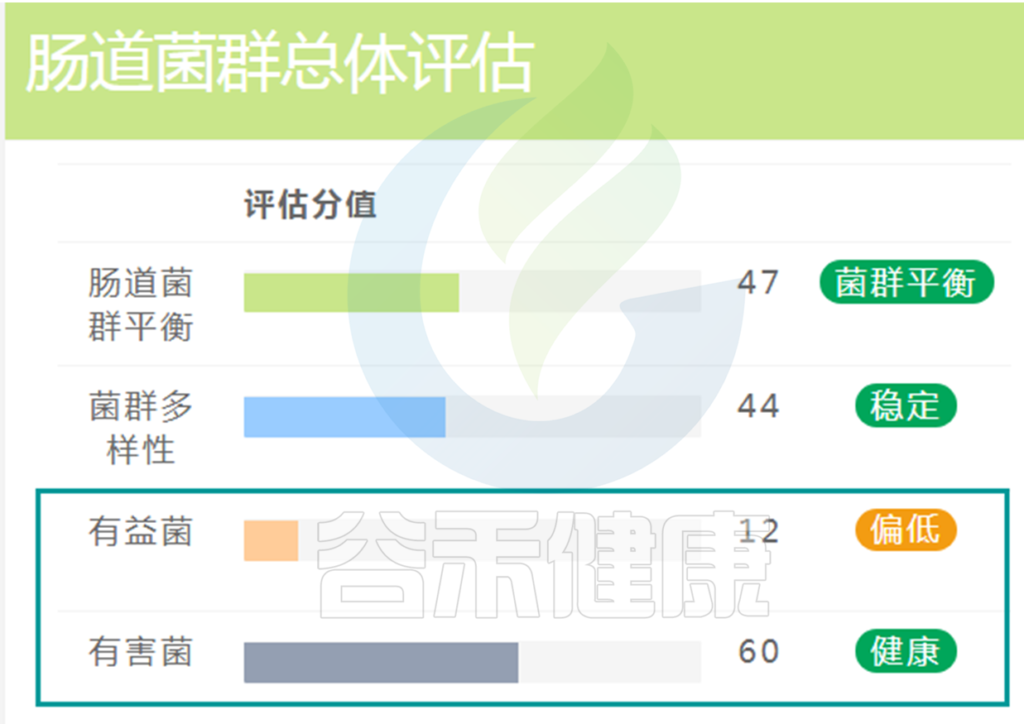
如果有害菌过多,通常建议服用益生菌或益生元的方式首先增加有益菌的比例,相应的有害菌比例就会降低。想要持久的改善菌群结构降低有害菌水平就需要改善生活方式,适当增加抗性淀粉等膳食纤维并规律饮食和睡眠,增加运动等。
整个生态系统平衡对于地球而言十分重要,同理,肠道菌群平衡对于我们人体健康也很重要。健康的肠道菌群丰富且多样性高。
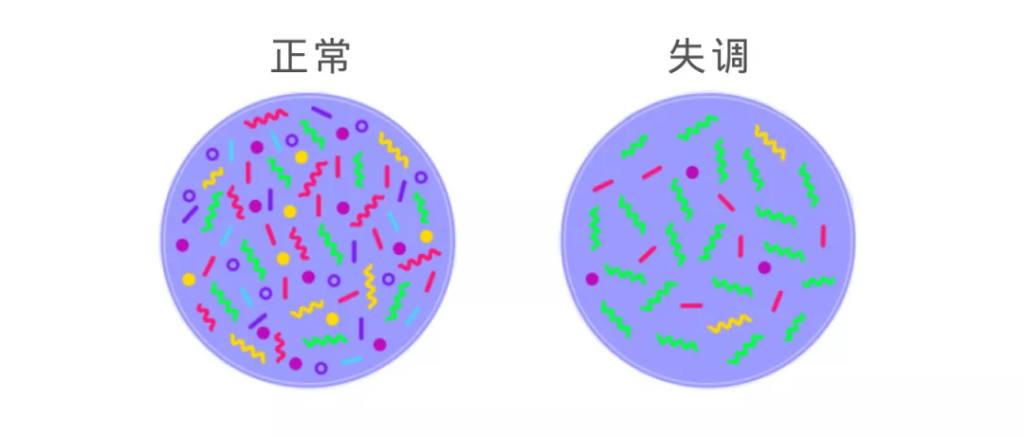
菌群失调是指体内微生物群不平衡,这可以表现为某些细菌的出现率较高,细菌的出现率较低,细菌的多样性不足,有害菌,有益菌比例失调等。
通常临床上采用大便常规检查,通过显微镜下观察统计染色细菌中杆菌和球菌以及革兰氏阴性和阳性菌的比值是否超标来判别的。
其中致病菌多为球菌和革兰氏阴性菌,而肠道有益菌多为杆菌和阳性菌,因而在传统临床上简单比较两者的比值评估是否菌群紊乱,是相对比较粗放的。
谷禾菌群检测报告中的菌群失调:
基于高通量测序可以精准的检测低至万分之一水平的菌,甚至可以分类到种水平,因此可以更加精细化评估菌群是否出现紊乱和异常。
基于谷禾超过30万人群的菌群数据库分析结果,我们将在90%的人群都有检出,且人群平均丰度1%以上的菌属做为核心菌属。这些核心菌属通过长期与人类共生,在帮助消化复杂碳水化合物和产生短链脂肪酸外还影响整个肠道环境,抑制病原微生物的定植生长。因此当这些核心菌属占总肠道菌群比例低于60%时,肠道菌群很可能处于紊乱状态。
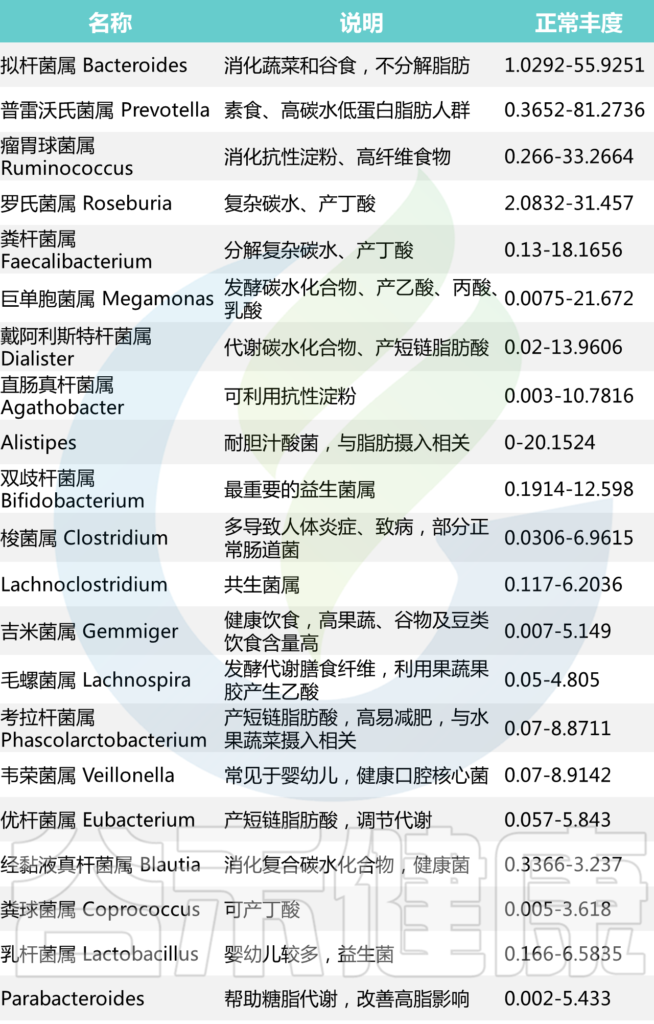
【谷禾健康菌群数据库】
如果出现菌群严重失衡,例如致病菌占了相当大比例,那么首先应考虑针对致病菌使用相应的抗生素治疗,然后再通过益生菌补充及饮食、生活方式的改变进行调理,直到菌群恢复平衡。
多样性包含两个维度。
一个是肠道菌群种类,人群中肠道菌群的种类参考范围在100~2000种,种类数量越多多样性越高。
另一个维度是均匀性,即各个菌种的含量丰度较为均一没有出现单一菌种占据绝大部分的情况。
多样性的评估一般通过一个叫做香农-维纳多样性指数的指标来进行评估,计算公式为:
H=-∑(Pi)(log2Pi)
其中Pi为每个菌的占比例,值越大代表物种种类越多,均匀性也更好相应的多样性也越高。正常人群中香浓指数在2~9之间,一般大于3以上表明具有一定多样性。
换句话说,肠道菌群多样性表现在:微生态系统的稳定性,以及面对外界致病菌等入侵的抵御能力。
在一定范围内,更高的多样性通常代表饮食更加丰富多样,同时也意味着更健康的身体状况。
菌群多样性高可能与下列情况有关:
环境,农村儿童比城市儿童菌群多样性高;
饮食,低脂饮食与菌群多样性较高有关;
年龄,长寿老人的菌群多样性较高;
……
多样性低不代表一定有疾病,但是更容易受到饮食,环境或疾病的影响,包括更易发生水土不服或更容易因饮食不洁导致腹泻等。
多样性低可能与下列情况有关:
分娩方式,剖腹产宝宝菌群多样性较低;
饮食营养,营养不良的孩子菌群多样性会下降;
药物,抗生素的使用会大幅降低菌群多样性,并且需要一段时间才能恢复。其他药物也会降低菌群多样性,如治疗胃溃疡和反酸的质子泵类药物也会导致菌群多样性降低;
环境,医院的ICU病房、更衣室等消毒严格,可能导致环境菌群多样性下降。
此外,神经系统、代谢、免疫等慢性疾病也与多样性下降有关。
你可以通过在饮食中增加纤维素,从高脂饮食逐渐转为低脂饮食来提高菌群多样性,另外规律运动也可增加多样性。
另外,我们在实际检测中会发现有这样一种情况:
多样性指标虽然很高,但是整体看起来健康总分并不理想。甚至还有很多慢性疾病风险,这是为什么呢?
这种情况可能是核心菌群丰度不够,核心菌群在代谢、免疫等方面都发挥重要作用,一旦核心菌群丰度下降,则可能造成外源物质侵入。感染、旅行等可能会出现这种情况。
看过我们检测报告的可能会发现,报告里有包括肠道致病菌和病原菌,分别代表什么?

<篇幅关系,此处仅展示部分>
肠道致病菌列出了最主要和常见的感染类肠道致病菌。(注意这里重点是肠道)

病原菌中给出的包括几十种人体的致病菌,不仅仅是肠道的。<如果没有检出就没有列出>
病原菌和条件致病菌的区别是什么?
病原菌一般极少存在于健康人的肠道菌群,正常范围很小,条件致病菌一般会在正常人群的肠道内存在,丰度较高或菌群结构单一到一定程度会引发疾病。如大肠杆菌和肺炎克雷伯氏菌正常人群中都会有检出,但当丰度较高是就会导致肠道菌群紊乱或疾病。
报告中如果出现病原菌超标的情况,不一定直接认为有病,需要结合症状。
如果出现相应的腹泻等症状,需要考虑是不是因为这些病原菌导致的。单纯超标如果没有症状只是表面有病原菌摄入,注意一下饮食和生活卫生,无须过于担心。
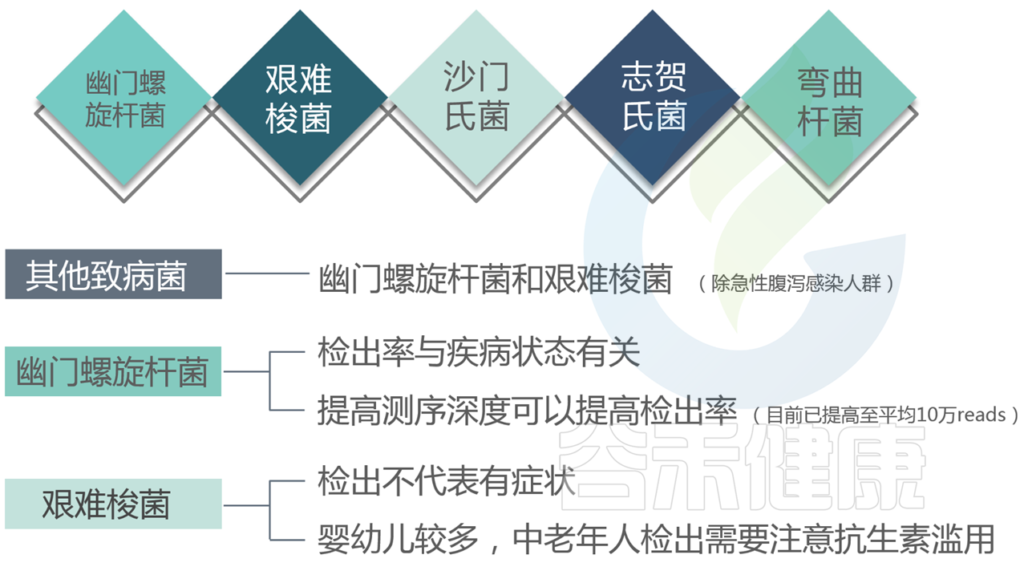
★ 幽门螺杆菌
为什么在医院检查出幽门螺杆菌感染,而报告中并未显示?
注意:本检测未检出并不代表完全不存在该致病菌感染,可能由于比例或其他因素未能达到检测丰度或未检出。
如果肠道菌群检测报告中检出幽门螺杆菌,是否需要去医院进行幽门螺杆菌呼气检测?
如果肠道菌群检测报告显示该项为超标,且同时存在胃部不适或其他胃酸、胃胀等症状,建议前往医院进行幽门螺旋杆菌检测,及早发现治疗。
★ 沙门氏菌
在食物中毒案例中,通常伴随着沙门氏菌,沙门氏菌粘附到肠上皮表面是发病机制中重要的第一步,并且是其在肠道定植的核心。
关于沙门氏菌的治疗及预防详见:食物中毒一文
扩展阅读:细菌大盘点(二) | 葡萄球菌、沙门氏菌、弯曲杆菌
通过以上部分,我们大概了解了菌群的构成及其扮演的角色,那么我们能利用检测到的这些菌的信息,给我们的健康带来什么帮助呢?
很重要的几个点:
第一,也就是前面所述的,菌群的构成本身就可以反映你的肠道内的环境是不是健康菌群,如果紊乱,它会带来很多的问题,比如说儿童菌群紊乱,可能会营养不良,因为菌群紊乱本身会影响营养吸收。
第二,对病原物的抵抗,也就是说身体是不是比较容易出一些状况,比如说腹泻,感染等问题。
第三,它还会诱发一些长期的慢性疾病,比如说糖尿病,实际上当然饮食是一个问题,但是有一些炎症相关的菌群,会诱发慢性的持续的炎症,从而导致慢性疾病的发展。
这就是我们接来下要讲的,疾病风险这块内容。
目前我们疾病风险检测部分包括16类主要疾病,根据疾病检测准确度和稳定性,我们将检测疾病的水平分为三个等级:低风险、中风险和高风险。
根据每种病的分值,0~0.3归为低风险,0.3~0.5评估为注意,0.5~0.7为中等风险,超过0.7为高风险。
目前报告中提供的疾病均经过大量病例样本检验并且准确率超过90%,虽然不作为疾病的诊断依据,但是其分值的高低仍然具有很强的指示作用。
0-0.3
如果某种疾病的风险值低于0.3以下表明菌群状态提示疾病风险较低,不同身体条件和生活方式下会有0.05的波动。
0.3-0.5
如果某种疾病的风险值位于0.3~0.5之间我们认为属于疾病前期阶段,通过饮食调理和相应的注意就可以降低风险。
0.5-0.7
如果某种疾病的风险值位于0.5~0.7之间表明可能患有该疾病或处于疾病风险阶段,这时候我们建议最好前往医院相关科室进行检查,如果不便前往医院也可根据建议先进行饮食调理和相应的注意,一般一个月后再进行一次检测查看疾病风险是否下降到正常范围,如果仍然较高甚至升高建议最好前往医院复查。
0.7- 1
如果某种疾病的风险值超过0.7表明有很大可能已患有该疾病,且分值越高表明风险越高。因此我们强烈建议去医院进行相应检查并听从医生建议。
注意:本检测目前尚不属于医疗诊断,疾病分值作为提示,低分值不代表完全没有疾病,只表示风险较低,也可能存在一定的未检出。高分值只表示存在很大疾病风险,疾病的确诊和精确诊断需要通过进一步的医疗检查确认。
说到这里,可能有人对以上这个0.3,0.5…这些风险值有所不解,风险值是你们自己确定的吗?如何计算得出这个值的呢?有参考依据吗?
这里我们来了解一下风险值的计算。
通过模型的构建和大规模人群队列的测试和学习,现在大概已经有几十种病,我们可以比较好的通过菌的构成,来预测到底有没有这个疾病。虽然现在它还做不到直接确诊,但它可以起到一个很好的提示作用,以及对病程进展的评估。
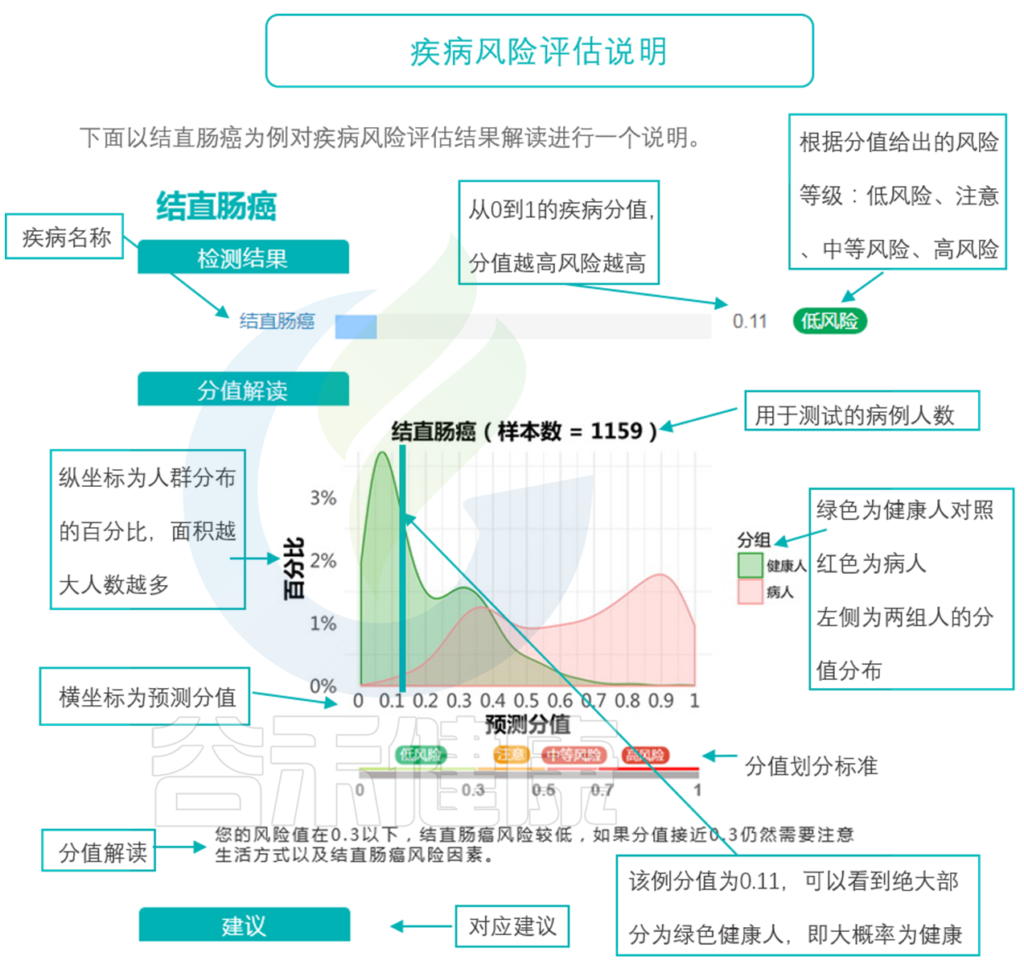
那么,具体哪些方面的疾病跟菌群有重要的关系,并且能够用菌群来预测和评估呢?
消化系统疾病
首先当然是消化道疾病,这很好理解,因为菌群本身就在消化道环境内。像肠炎,就包括克罗恩病,溃疡性结肠炎之类的,还有消化性的腹痛、腹胀这些问题,可能是由于菌群的特征变化造成。
炎症性肠病中的菌群失调
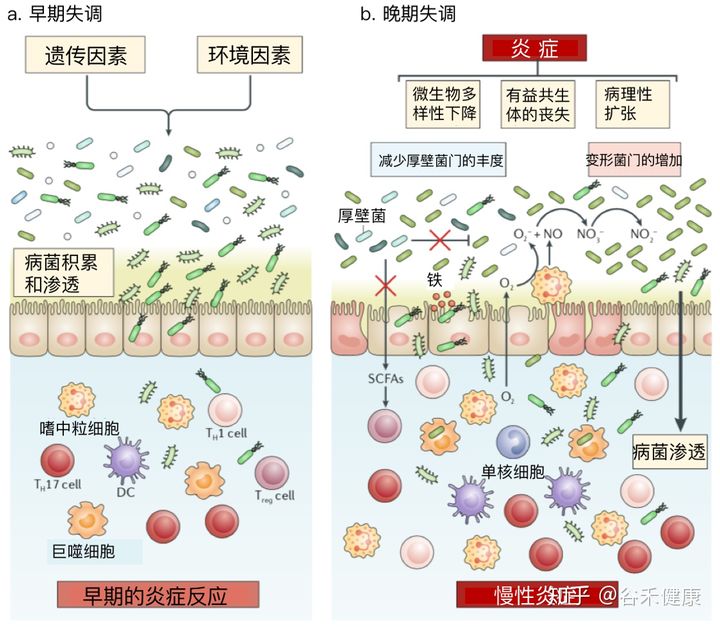
详见:炎症性肠病一文
还有过敏性腹泻,有人可能对一些食物过敏,吃完之后会导致一些腹泻,菌群特征变化很明显,包括甚至一些肠道病毒的感染,比如说诺如病毒、轮状病毒的感染。它也会体现出非常特定的菌群变化特征。
在肠道菌群检测报告中,这类疾病风险呈现如下:
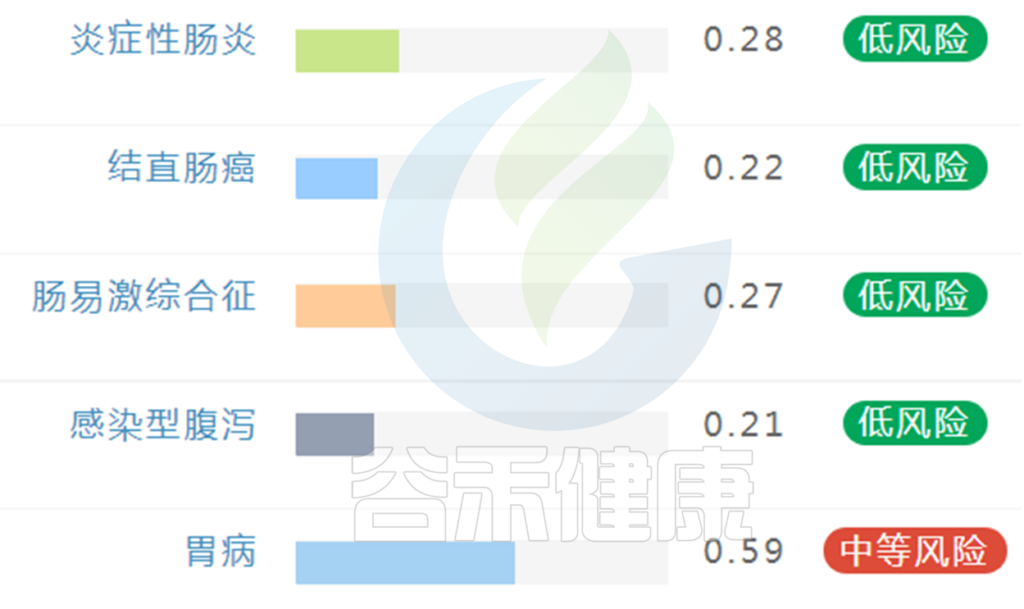
上图样本可以看到胃病有中等发现,其备注信息里有填:胃痛,可能要开始注意这方面的疾病隐患,通过饮食等调理一段时间,或前往医院就诊。
★ 胃癌
胃部更严重一点的疾病就是胃癌,胃癌与肠道菌群之间也有很大关系,最近,在“谷禾开放基金项目”中,也有相关论文也已发表。
肠道菌群在区分胃癌患者和健康人方面具有高度的敏感性和特异性,表明肠道微生物群是胃癌诊断的潜在无创工具。
胃炎与胃癌具有某些微生物群特征,化疗降低了胃癌患者的微生物丰度和多样性。乳酸杆菌Lactobacillus和巨球菌Megasphaera,是胃癌的预测标志物。
★ 结直肠癌
现在已经有多项研究表明,通过菌群可以做一个很好的标志物。虽然做不到所有的结直肠癌患者都能够被检出,但是最终的准确率相对来说还是挺高的,甚至比一些,包括肿瘤标注可能还要更高一些。
我们现在大概能做到70%多的肿瘤患者是能被筛查出来。并且准确度其实能够到90%,作为普筛或者健康评估来说,已经是一个比较有效的标志物了。
化疗与手术会大幅降低风险分值,但仍比健康人高。
此外,结直肠癌会经历从息肉到腺瘤到癌症多个阶段,应结合年龄和家族史判断息肉和结直肠癌。
肝胆类疾病
肝脏类疾病,比如说非酒精性脂肪肝跟肠道菌群有相当大的关系。
不同肝病有不同的菌群特征,尤其是脂肪肝的严重程度,肝功能异常的严重程度。
扩展阅读:深度解析 | 肠道菌群与慢性肝病,肝癌
因为菌群会产生大量的刺激代谢物,这些代谢物本身可能会加重肝脏的负担,并且诱发一些肝脏的疾病,但反过来肝脏的代谢能力的减弱和一些慢性肝脏疾病进展又会反映在菌群的构成上,所以它们是相互的。当然也可以用菌群的构成来反映具体肝病的特征。

由于不同阶段肝功能异常,脂肪肝等情况都统一归类在肝病这个大类,因此目前还无法判断确切的疾病分类,后续如果有更多细分疾病的样本用于建模,报告也会随之迭代更新。
代谢类疾病
代谢类疾病,比如糖尿病,肥胖等,都与肠道菌群有密切关联。
★ 2型糖尿病
2型糖尿病的发病率越来越高,也有更多人开始关注菌群与2型糖尿病的关系。很多文献都有报道它们之间的关联性。
2型糖尿病人群中个体微生物群的差异
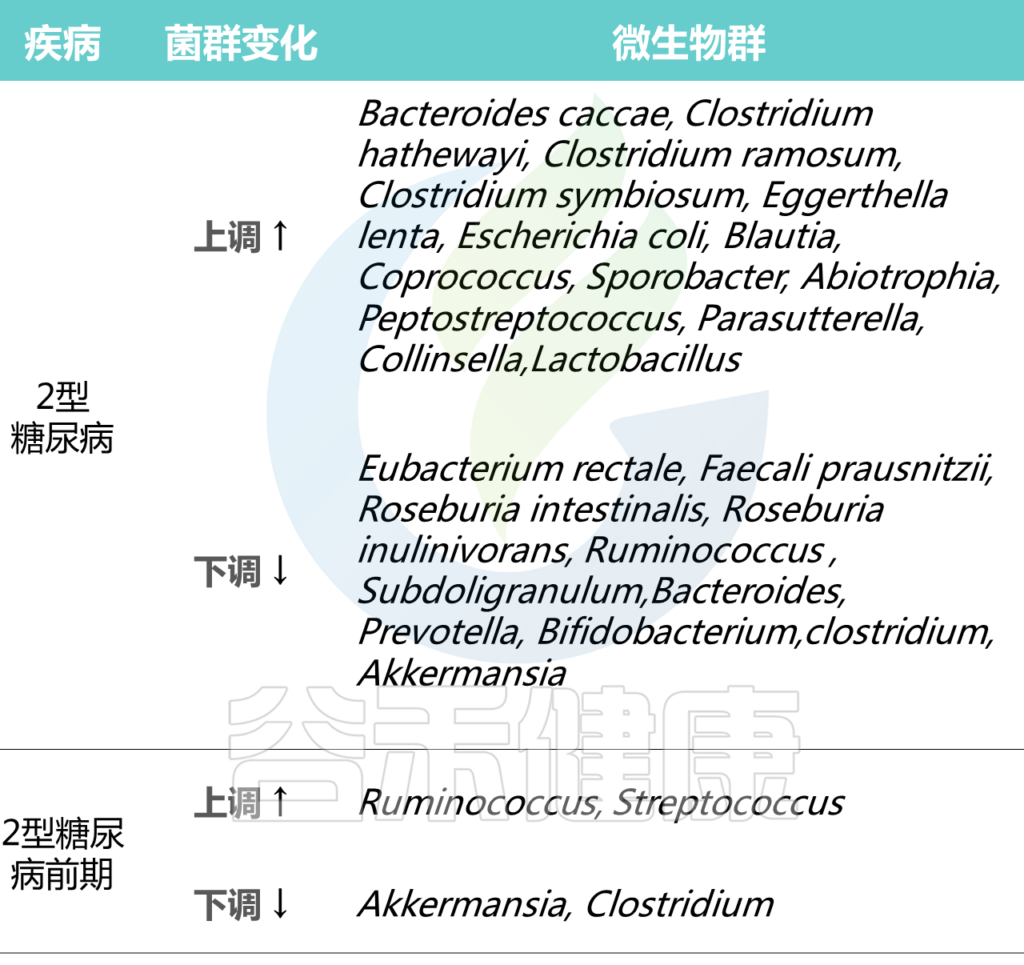
Cunningham A L et al., Gut Pathog, 2021
在2型糖尿病患者普遍具有相对高丰度的特定属:Blautia、Coprococcus、Sporobacter、Abiotrophia、Peptostreptococcus、Parasutterella、Collinsella。
2型糖尿病患者中,产生丁酸菌特别缺乏,特别是梭菌目,包括:
Ruminococcus、Subdoligranulum,Eubacterium rectale、Faecali prausnitzii、Roseburia intestinalis 、
Roseburia inulinivorans
通过肠道菌群检测,一方面健康人群可以查看是否有患病风险,另一方面如果已经患病人群,也可以查看菌群是否异常,推测是否是因菌群显著变化导致的,从而能进行更有针对性的干预。
肠道菌群检测报告中疾病风险预测如下:
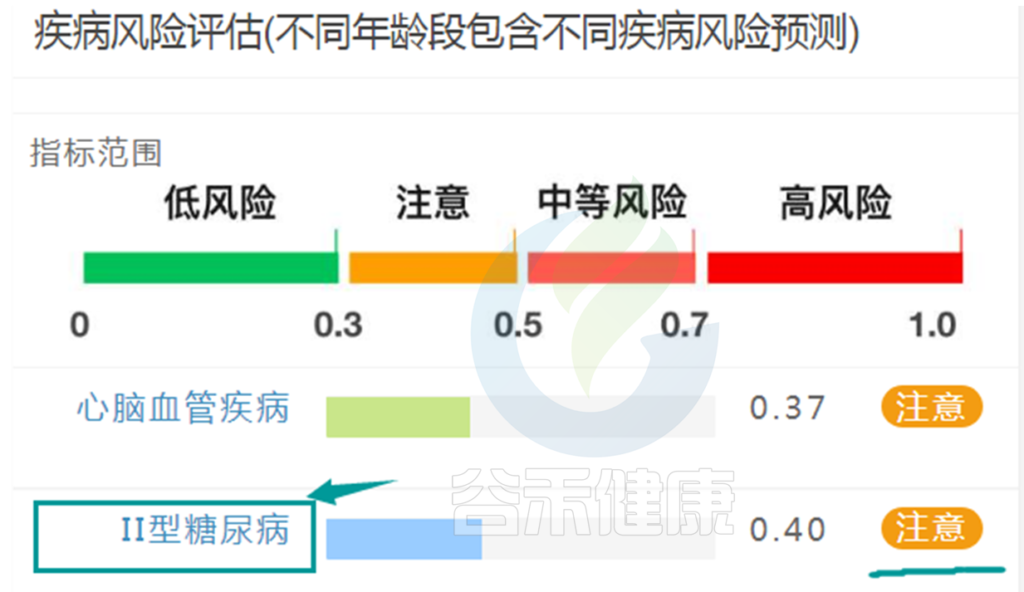
2型糖尿病的检出率相对较高,可以达到95%以上,准确的也较高,可以预测早期糖尿病风险。
★ 肥胖
目前已有很多关于肠道菌群和肥胖之间关系的研究。
人体摄入大量营养素、肠道菌群与肥胖的关系
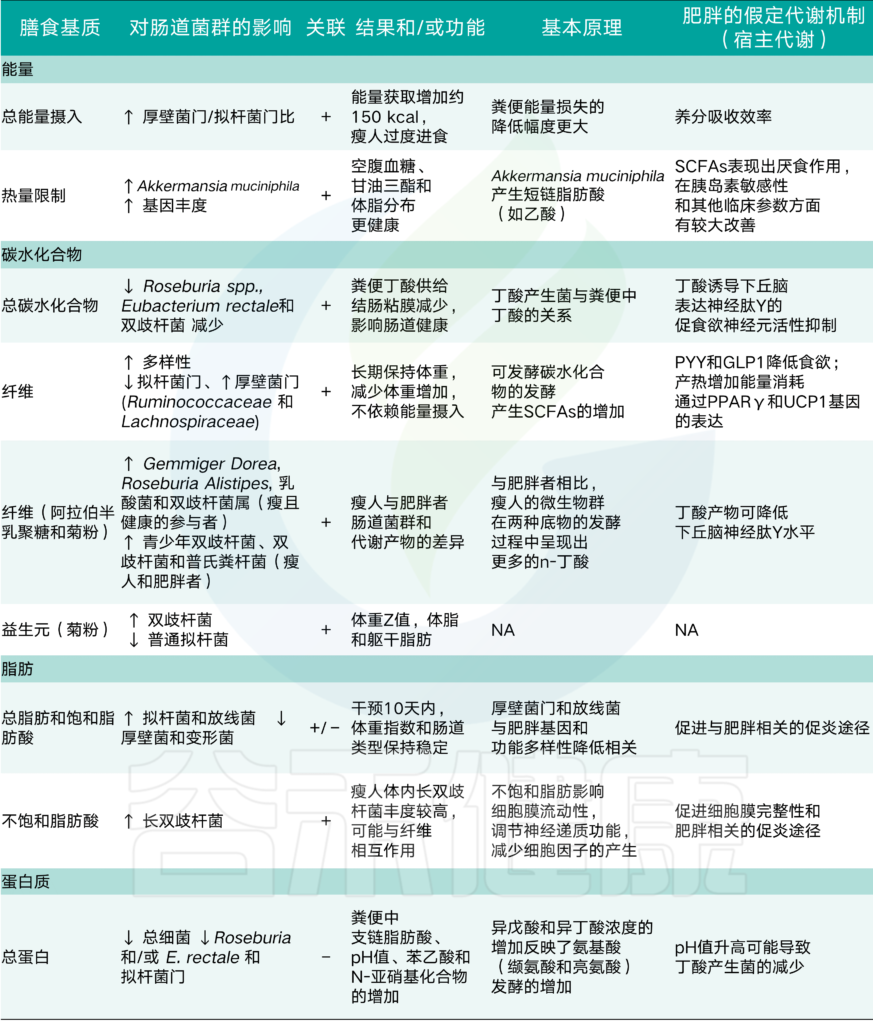
↑, 增加;↓,减少;NA,不可用;第三列:营养物质和/或饮食基质与肠道微生物群之间的关系
有人说,为什么我们的肠道菌群报告没有判别测试者是否肥胖?
首先,肥胖不肥胖这个症状是肉眼可见的,也就是说测试者自身已经了解,这种情况下用模型来判别没有意义。
而我们更希望通过肠道菌群检测来可以告诉你,可能是什么因素造成的肥胖,饮食结构的,还是某些菌属代谢问题。
通过菌群知道营养构成,以及是否存在一些特定代谢菌的异常,比如说Akk菌,它是一种在一定程度上帮助减肥的菌群。
如果在你的肠道内该菌特别少,那么可能同样减肥,控制饮食,别人一个月假设瘦十斤,你就不一定能达到这个效果。这些都是菌群可以提供的一些信息。
在肠道菌群检测报告中,会列出肥胖正负相关菌群,及其是否超标。
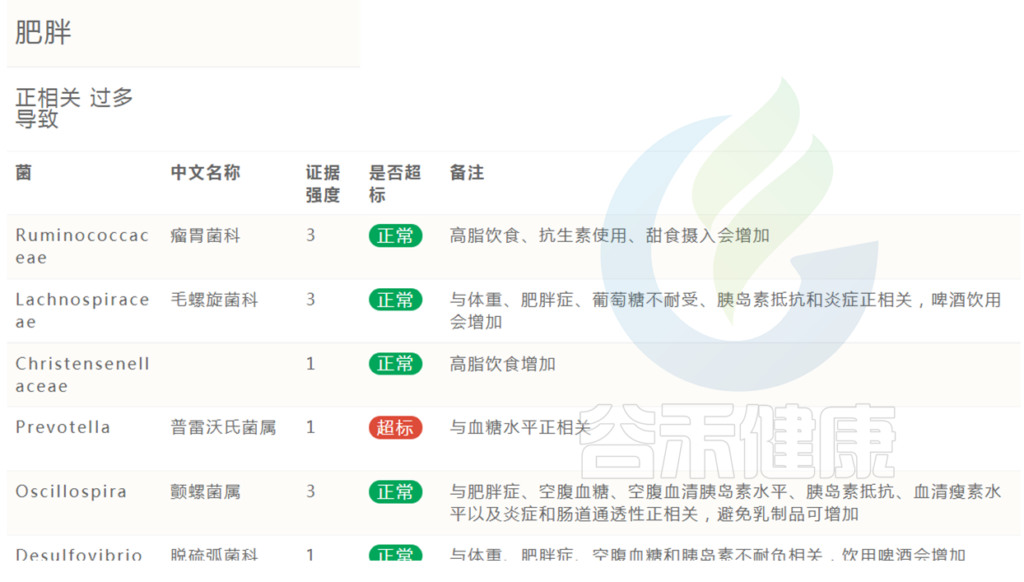
同理,其他各类肉眼可见的症状(包括腹泻、便秘、腹胀、过敏、皮肤状况等)正负相关菌群都会在报告中呈现,此处就不一一列举。
神经系统疾病
听起来神经系统好像没什么关系,但实际上很多肠道菌群能代谢产生大量神经递质及其他代谢产物。
肠道菌群会影响HPA轴的发育,该轴调节压力反应并参与皮质醇的释放。在抑郁和长期处于压力下的人中,HPA轴可能失调,导致过量的皮质醇(一种压力激素)被循环。
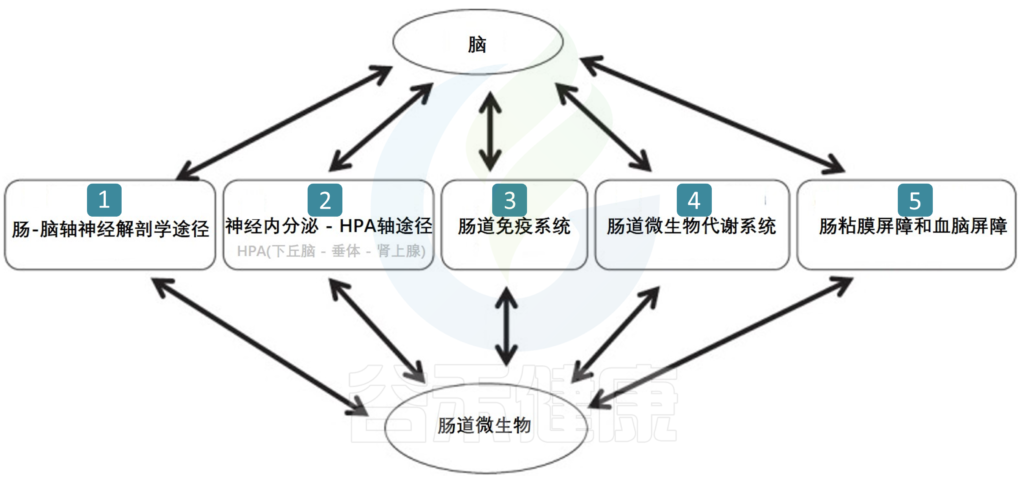
肠道菌群的部分代谢物质也会通过免疫系统影响神经系统。促炎性细胞因子的失衡可导致慢性炎症和自身免疫性疾病,通常与抑郁症同时发生。
通过肠道菌群检测,可以了解体内血清素水平及激素水平,同时也可以了解神经系统相关疾病风险,包括自闭症,抑郁症,阿尔兹海默症等。

肺部疾病
宿主,微生物组和环境之间的三重相互作用在健康功能中维持了肺稳态。
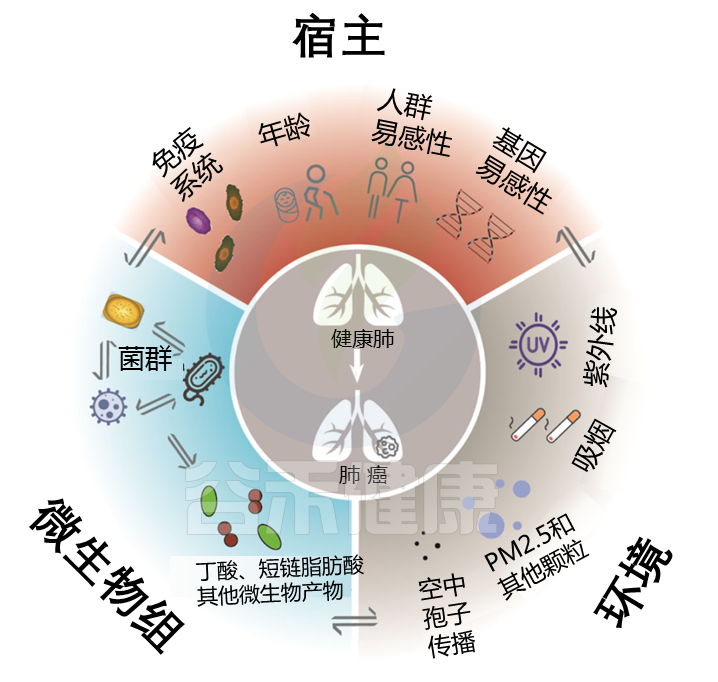
Liu NN, et al., NPJ Precis Oncol. 2020
在大量的临床样本数据当中可以发现,肺部感染,包括社区性肺炎,慢性阻塞性肺疾病,通过血氧浓度和全身的免疫反应,一定程度上是可以反映在肠道菌群上。
另外像肺部的感染,比如说在肺炎链球菌之类的感染中,肺部的病原菌可以通过痰或者是呼吸进入到肠道,所以我们在肠道当中是能检测到这些肺部的感染菌,并且随着其严重程度和感染进程,菌群的丰度会越来越高。
肠道菌群检测报告中也有对肺部相关疾病风险提示。

免疫疾病
肺部感染会出现咳嗽等症状,但咳嗽不一定仅是肺部感染,也可能是哮喘。
★ 哮喘
在哮喘中,微生物群是导致肺和肠道之间相互作用的重要因素。肠道微生物可以影响肺部的免疫反应,而肺部刺激可以导致肠道反应。
在一项研究中,来自加拿大的三个月大婴儿哮喘高风险的粪便样本中观察到 Lachnospira, Veillonella, Faecalibacterium, Rothia显著下降。这种菌群特征在1岁时不再明显,同时伴随着粪便乙酸的减少和肝肠代谢物失调。
肠道微生物对哮喘的影响部分是由细菌代谢物介导的,1岁时粪便中含有大量丁酸和丙酸的儿童,其特应性敏感性明显降低,3至6岁之间哮喘的可能性较小。此外,哮喘患者的粪便中Akkermansia muciniphila 菌水平均有所降低。
★ 过敏
已知的婴儿期与过敏性疾病相关的微生物群改变如下:
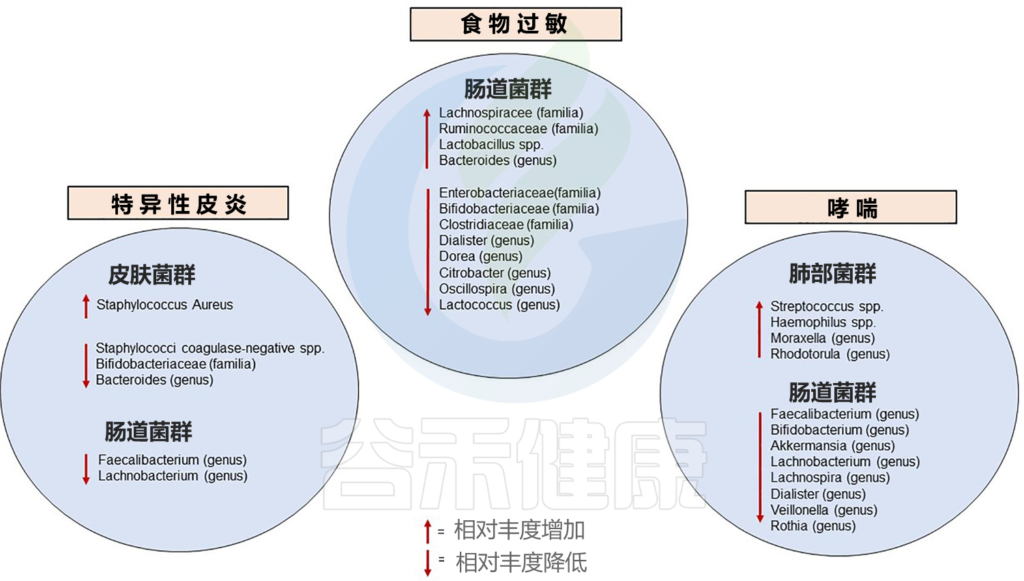
Diego G. Peroni et al, Front.Immunol. 2020
肠道菌群检测报告中有列出与过敏正负相关菌群,及是否超标。
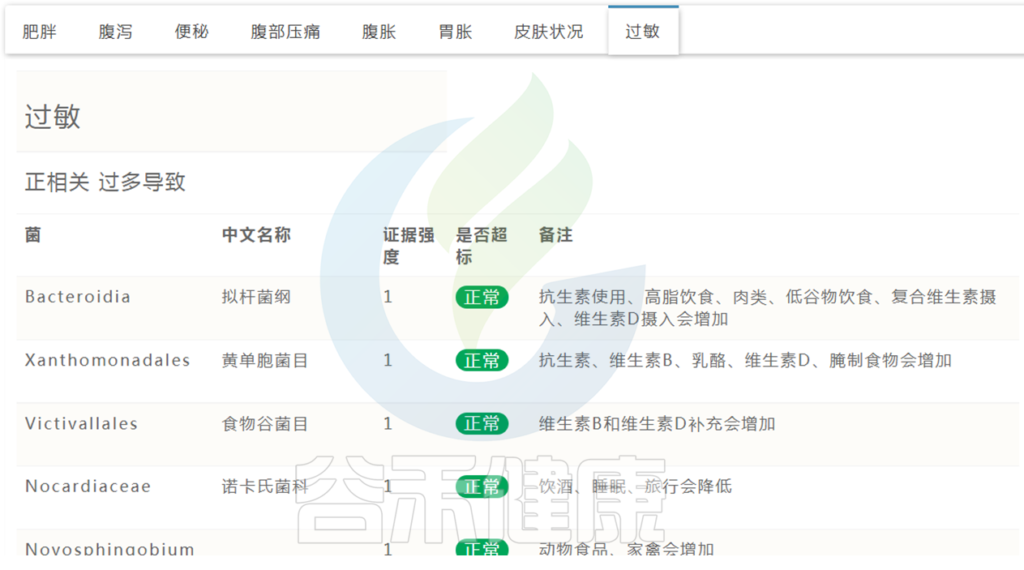
< 篇幅关系,此处仅展示部分 >
菌群生长需要养分,它的食物来源取决于你的肠道,有句话叫:you are what you eat (在我们这篇文章中有详细解释它们之间的关系 深度解读 | 饮食、肠道菌群与健康)。
也就是说,你吃的食物会帮助构建你的专属菌群。有的菌擅长代谢碳水化合物,有些菌擅长代谢脂肪,所以饮食结构不同,也就是食物来源比例不同,最后会塑造不同的菌。
那反过来,如果知道你的菌群的构成,就可以相对数量化的去了解你的饮食构成,包括营养摄入具体是什么样子,所以菌群很大的另外一个作用就可以反映你的营养饮食摄入状况。
这部分内容在我们报告中的呈现如下:
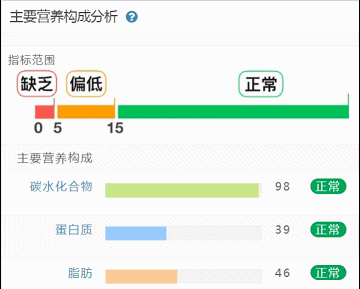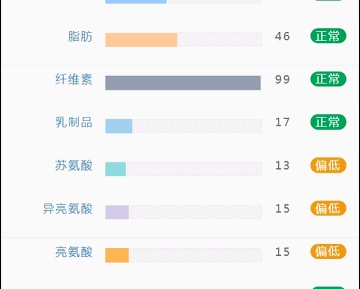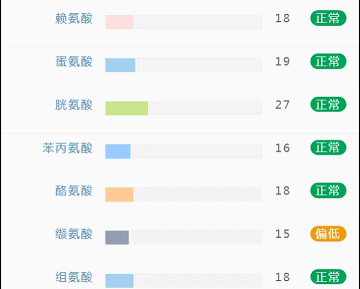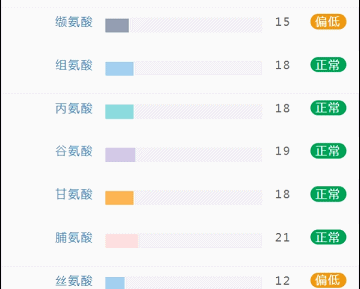
那么这里可能又会有疑惑,以上这些数值是什么意思,如何计算的呢?
不同的细菌有不同的代谢能力,需要不同的营养物质进行繁殖。通过评估特定营养供给下的偏好菌群的比例,即可反映不同营养物质的摄入比例。所以报告中的主要营养代谢分值评估的是主要营养物质摄入的比例在人群中的分布水平。
因此不会出现所有主要营养物质均高或均低的情况,也因此主要营养指标的最佳分值在70,且更关注不同营养物质的均衡性。
单项营养物质的分值低于5,表明摄入比例在人群中属于最低的5%,评估为缺乏,低于15评估为偏低。
而如果某项指标达到或超过95,则表明该项可能摄入比例偏高,通常对应会有其他营养成分较低。只需要针对性的增加缺乏或偏低的营养成分摄入,维持不同营养成分相对一致即达到营养均衡的目标。
为什么会出现所有的营养指标都很低?
这可能是菌群失调引起的。营养指标的评估是基于菌群构成特征和菌群代谢生成特定营养素的途径来评估的,如果菌群结构异常,将导致后续的预测失常,例如大量氨基酸都评估缺乏的情况。
这时候需要先调节菌群,等菌群指标恢复到一定水平后再次检测,评估营养指标。
我们日常摄入的除了上一小节提到的宏量营养素之外,还包括微量元素和维生素等。有些维生素比如说B族维生素中有相当一部分,甚至百分之六七十需要通过肠道菌群对初始原料进行代谢之后才会产生,也就是说有些细菌会代谢我们食物中的一些成分,转换成B族维生素。
而你的菌群构成和代谢B族维生素的能力,会直接决定是否缺乏该类维生素。当然也有部分受基因影响,因此肠道菌群相应的基因和代谢途径的丰度水平也会直接反映这些维生素的摄入水平。
总的来说,菌群在这其中起重要作用。在我们报告中呈现如下:

微量营养元素和维生素的评估分值与主要营养物质不同,是通过调查人群的单项营养成分水平,然后寻找与该项成分异常相关的菌群,并基于这些菌群和代谢途径计算丰度并转换为人群分布后的值。
简单来说,报告中的微量营养元素的分值即代表该营养元素的摄入水平。
菌群检测营养状况与血液检测有什么区别吗?
通过肠道菌群评估的维生素一般反映一段周期内的维生素状况,因为肠道菌群在没有突发疾病的情况下相对稳定,受一段周期的饮食影响为主,一般是2周。B族维生素是水溶性维生素,每日摄入后会通过尿液代谢排出,通过血液检测,不同时间检测波动较大。
菌群评估营养和血液检测营养趋势是一样的,在极端缺乏和极端过量是吻合的,中间档可能在数值上不是完全吻合,血液反映的营养水平比较及时。
★
当了解了体内的营养素和维生素是否缺乏,以及哪方面的缺乏,就可以进行有针对性地补充。菌群也是需要营养物质的,这就离不开我们的日常饮食,那么该如何补充呢?
我们的肠道菌群检测报告中有个体化饮食推荐表。

<篇幅关系,此处仅展示部分>
以上食物推荐表是怎么来的?
这是经过综合考虑疾病风险和营养缺乏状况计算得到的。主要是计算每种食物的营养构成与目前营养状况的匹配度,以及特定疾病需要避免的食物。
该表推荐的食物分数从-100~100,排序为不推荐到强烈推荐,日常饮食可以参考这个推荐表。推荐分值,表示基于目前的菌群和营养状况对食物的推荐指数,正数分值越大,建议优先选择,同时也是对改善最有帮助;负数分值越大,并不表示不能吃,而是目前状况下不优先推荐或尽量少吃。
p.s. 如果有特殊疾病需要忌口的,优先遵医嘱。
该表包括几百种日常食物,如下图。

<个体化饮食推荐,建议用电脑查看,目前手机端展示不太美观>
对于长期调理菌群而言,饮食无疑是最主要的驱动因素之一。
下一步我们将利用更全和详细的菌群结构,食物营养,人群膳食构成以及营养数据库推出个性化膳食营养升级方案,特别会针对个别菌属的异常和失衡状况以及营养元素异常和缺乏问题。
前面章节我们知道,通过菌群可以反映你的饮食状况,那么反过来,如果你吃了一个东西,会对菌群检测造成影响吗?是不是菌群就变了,那检测就不准了?
这也是比较重要的一部分,也就是肠道菌群检测的准确性,它能允许多大范围内的变化?什么因素会影响?
其实,菌群变化算快,也不算快。饮食对菌群是有一定影响没错,但这种影响呢,一般来说是前一天的饮食会影响第二天的菌群结构的百分之十几,也就是说,假设你昨天吃大餐,大量吃肉,蛋白摄入非常高,而你之前是以碳水化合物为主的,那么第二天饮食当中,你的蛋白质相关的这部分菌的比例可能会有15%,最高到20%可能会有,但一般来说是在15%以内,会有一个波动。
然而,总体的核心菌群构成,不会因为你今天一顿大餐,就直接从素食的变成肉食的菌群结构,核心菌是相对稳定的,那么多久会发生变化呢?
一般来说坚持两周,饮食结构的变化,核心菌群就会发生一个迁移改变。但两周只是一个短暂的周期,如果你两周后又换回先前的那种饮食方式,菌群也会随之改变到之前的状态。那要怎么样才能持久改变菌群呢?
这个时间线可能要拉长到两个月。
这是在我们的菌群干预中,很多人会遇到的一个周期性的问题。也就是如果你想有效改善菌群,至少需要两周会见到相对明显的菌群结构变化,那如果把干预延伸到持续两个月的周期,甚至是持续干预周期更长,那效果会更好。
取样前饮食会不会造成影响?
前面我们知道,菌群会受检测前一天饮食的影响,造成15~30%的菌群改变,同样也会反映在营养状况的评估上,因此建议检测前一天尽量保持近期正常饮食,这样能更好的反映真实的营养饮食状态。
此外,如果你是在调理一段时间后再次检测,想要和上次比较的话,最好在检测前保持饮食大体相似(意思是不要突然吃和平时不一样的食物或者吃完大餐后取样)。
取样过少会怎么样?
取样不能太少,如果太少的话,可能会影响DNA提取,另外会导致一些低丰度的菌检测不到。
取样过多会怎么样?
如果说取样太少导致样本不合格可以理解,那么取样过多为什么也会有问题呢?
我们的采样管中有保存液,可以将菌群固定在采样的瞬间,但是如果取样过多的话,可能导致部分粪便无法完全溶解于粪便,这部分样不能正常保存可能会使其中的大肠杆菌等兼性厌氧菌开始在管内繁殖。
正确合格取样量(黄豆大小,约200mg,如果是稀便,反复沾取)

只需棉签沾取少量,混匀于保存液,固体粪便取样不能超过管子1/5体积(右图刻度线)。且保存液带有粪便颜色即可。(右图所示)

详见:肠道菌群取样方法
注 意 事 项
如3天内使用过抗生素类、质子泵类胃药、阿片类精神药物请停药3天后进行检测(如果长期服用某种药物,如降压、降血糖药等,不建议停药,检测反映的是用药控制的菌群和身体状况)。
感冒、腹泻或其他症状期间不影响取样,拉稀或稀便可以用棉签反复沾取粪便至取样管。
★
总的来说,取样虽然很重要,但也只是其中一个环节。每一个样本的结果呈现都凝聚了我们与你共同的努力。那么,从取样到结果报告呈现的那一刻,中间经历了什么?
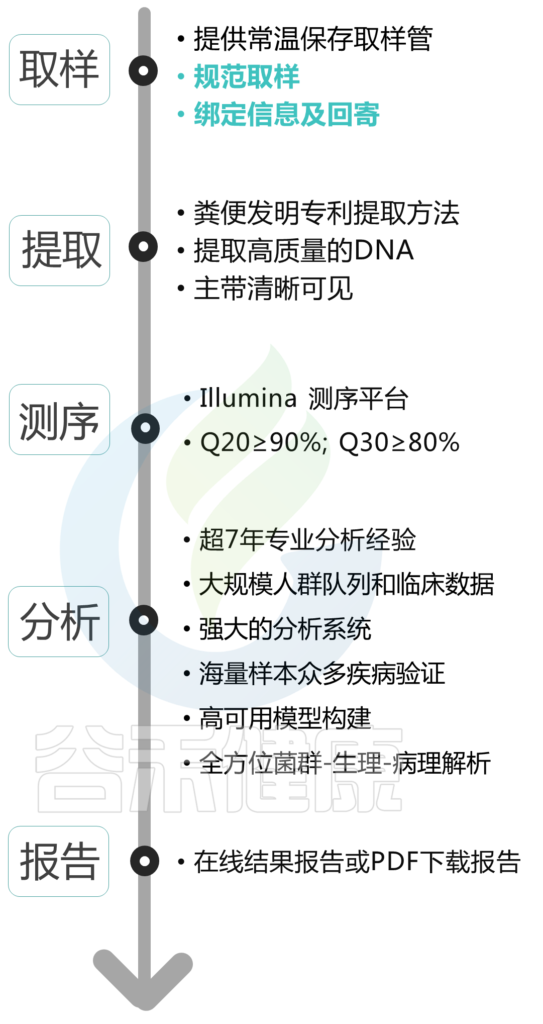
在你取完样之后,把样本用快递寄到我们这里之后,它会经历提取->测序->分析->报告到你手上。下图绿色标注部分是你需要完成的。

近年来,我国将全面健康和预防作为国家重点领域。我们致力于将信息技术(IT)与生物技术(BT)相融合,发展推动肠道菌群基因检测进入成为精准和预防医学时代下的“生命健康新基建”,尽管目前的菌群检测,包括疾病关系,算法,数据库,后端干预均在成长积累阶段,但是菌群检测正在进入大数据时代,菌群基因中蕴藏海量对人体生命和健康的重要数据,我们致力于将这些数据和实际应用相结合,最终转化为疾病预防、改善健康的有效方案。
前沿技术正在不断创新发展,报告也在迭代更新中,谷禾肠道菌群健康检测在辅助判别慢病风险、精准营养、亚健康管理、临床治疗干预中显示出其广泛的社会需求和指导价值。
你问我答
不同部位间的样本(如前段/中段/后段),检测结果差异性有多大?
答:会有不同的,不过主要反映在具体的菌种丰度上,有无这种菌的差异不大。另外慢病的评估也影响不大慢病模型中使用了高维特征,丰度的变化波动对结果的影响没那么大。营养和代谢部分受菌群丰度影响相对大一些,同一个人的前后两天的取样最大可能有15%左右的差异。
肠道菌群在肠道内不同部位以及粪便的不同部分其实都存在差异,含水量、连续几餐的饮食构成和排便周期的长度都会对菌群各个菌种的丰度造成影响。单纯从绝对丰度上来看是一个动态变化的过程,各个菌属在继承之前的构成比例的情况下因各种因素的变化增长或降低。因此并不存在一个绝对的菌群构成以及完全准确的单一指标。肠道菌群检测获取的丰度含量本身信息量很大,但是稳定性和一致性并不很高。
更高层级的菌群相对比例顺序则相对稳定一些,之后具体包含的菌种也相对稳定。目前我们使用的疾病预测模型主要通过高维的菌群结构特征,并不单纯依靠每个菌的绝对丰度来评估,稳定性很高。针对一些特定的病原菌或问题菌,需要通过与人群范围比较,在正常范围内并无问题。
日常多添加有益菌或益生菌的酸奶,可以改善肠道菌群状况吗?
答: 大范围人群调查显示添加益生菌的酸奶可以改善肠道健康,但效应因人和状态而定。总体而言我们支持服用益生菌酸奶有益,但需要注意酸奶饮料可能包含果糖,游离糖等,其作用仍然非常有限。
同一份样本,不同批次的实验环节如上机测序,差异有多大?这种差异率是否有一个范围呢?
答:不同批次上机影响很小,菌群数据相关性不低于98%。我们会在每轮设置一个阳性对照,一个上轮检测样本对照,一个阴性对照。评估污染,轮次比对。理论上不同的实验室,扩增引物,方法都会带来对不同菌丰度的系统误差,我们尽力保证本实验体系下各个轮次之间最小化的实验误差。另外使用的引物是经过大量验证的标准化引物。
实际患者建不建议送检,我们这个产品主要针对健康体检,还是也可以辅助诊断和预后治疗呢?
答:产品主要针对健康体检,如果临床诊断判断可能菌群异常或疾病症状与菌群相关,产品可以通过菌群检测提供临床参考,用于辅助诊断和治疗方案的评估。产品关于疾病和菌群相关指标的评估仅限于菌群相关方面,以临床诊断为准,不适用于单独使用产品进行疾病诊断。
抗生素是如何影响菌群的,菌群的敏感性和抗性基因是什么?
答:广谱抗生素会杀死细菌,但是部分细菌在抗生素选择或滥用的情况下会在抗生素靶点基因产生突变或携带耐药基因,从而对特定抗生素产生耐药。不同菌目前的耐药菌比例以及携带的耐药基因水平不同,对应的抗生素耐药水平和种类也有不同。
有在吃富含某种事物或者相关营养素,为什么报告显示缺乏?
答:营养指标的评估是基于菌群构成特征和菌群代谢生成特定营养素的途径来评估的,直接的营养素补充会反映在相关菌群构成上,但部分营养素因为吸收部位不同以及菌群代谢途径上下游的影响,预测可能有一定差异。另外菌群构成异常的情况也会导致营养指标预测失常,如大量氨基酸都评估缺乏的情况。
有人说长期服用益生菌,会让肠道自己产生的益生菌的能力减弱或者可以说是肠道自主平衡的能力减弱,不能长期服用。这种说法是否有依据?长期服用一种益生菌,也容易产生耐药性,那么是否建议定期更换或者调整益生菌的菌种和数量呢?
答:持续服用单一或特定组合的益生菌确实会存在效力减退的情况,主要是菌群具有适应性,如果不配合生活方式和饮食结构的改变,会较快失效。可以根据菌群检测结果来调整益生菌的方案。
样品的稳定性对于那些数据的影响是比较大的哪些是影响比较小的?
答:越是直接和具体菌相关的指标变化越快越大,和菌群结构相关的指标,比如一些慢病风险还有总体饮食结构一类的变化较稳定。
从波动性排序来看,具体菌丰度>多样性>微量营养(锌 铁 氨基酸 维生素)>消化道疾病风险评估 (受当前状态影响较大)>肠龄>宏量营养素(碳水 蛋白 脂肪 纤维素 乳制品)>抗生素水平 >菌属是否出现>其他慢病风险
中大龄儿童小孩检测到自闭症风险高,如何解读?
答:肠道菌群在1-3岁期间主要是菌群发育滞后会影响神经发育和营养,3~6岁左右菌群参与的神经递质代谢异常会加剧自闭症的程度,但这个年龄段已有的神经发育滞后不光靠菌群改善就能解决了。
所以如果是0~2岁的如果这个风险值较高,不管有没有症状都建议改善菌群。如果是3~6岁甚至6岁以上,如果就风险值高没有相应的神经或行为异常,就问题不大,可能是菌群代谢构成不太好,不会导致自闭症的。如果有症状那改善菌群有助于改善症状。
肠道菌群平衡,为何多样性指数是低的?
答:菌群平衡和多样性指数是2个不同指标;
多样性仅仅评估肠道菌群的种类数量和丰度分布,与具体是有益和有害无关。多样性主要与饮食摄入,药物如抗生素类以及疾病状态有关。
菌群平衡对应的异常称为肠道菌群失调,临床上有I度失调和更严重的II度失调。大便常规检查是通过显微镜下观察统计染色细菌中杆菌和球菌以及革兰氏阴性和阳性菌的比值是否超标来判别的。本报告同时提供了另一评估算法,通过有益菌/有害菌的总体情况来评估菌群平衡状态,低于2为重度失衡,低于5为失衡,同时分值也提示菌群平衡水平,越高越正常。
菌群失衡如何调整?
从菌群失衡的评估角度来看,首先就是快速增加有益菌特别是双歧杆菌的丰度可有效改善该项指标。因此临床上通常提供多联的益生菌制剂来快速补充益生菌,可以短期有效改善菌群平衡比例。
菌群平衡和多样性分值都高的,但是肠道年龄预测比实际大,年龄预测模型是不参考多样性和平衡性参数的?
答:肠道年龄是靠机器学习和人群大队列做的,不是只根据菌群平衡和多样性,每个年龄段都有核心和标致的菌群特征,比如婴儿的双歧杆菌,老年人瘤胃球菌等,这几个指标都是表征菌群的状态和健康的。
END
声明
谷禾专注于提供肠道菌群基因检测和基于此的健康评估咨询,肠道菌群对人体健康的影响和关联性已被广泛研究和认可,但基于对健康的慎重和法规,谷禾重申其提供的肠道菌群基因检测目前不用于临床疾病诊断,仅作为菌群状况构成检测和健康评估以及基于菌群的科研。分析报告中疾病风险和健康相关评估来自于公开研究数据和谷禾构建的大人群队列数据分析的预测评估结果,涉及临床诊断和医疗建议请遵照临床诊断和医生的医嘱。由于技术进步和样本数据不断积累,报告中可能存在尚未完全涵盖的因素或状况,不可避免的存在一定概率部分风险未被完全检出的情况。

谷禾健康
一般在肠道菌群健康检测报告中,会有主要菌属构成比例,类似下图:
图源:谷禾肠道菌群健康检测报告我们可以看到图中列举了拟杆菌门,厚壁菌门…等。很多小伙伴拿到报告之后,对于这些细菌门表示困惑。
这些细菌门都代表了什么意思?
某个细菌门比例高了会怎么样?
某个细菌门比例高,是好是坏?
是不是与某些疾病相关?
…….
实际上,这几大类门的丰度和构成比例变化与人类健康和疾病发生息息相关。
两个主要门类,拟杆菌门和厚壁菌门,构成人类肠道细菌的大部分。七岁以后,拟杆菌和厚壁菌之间的比例相对稳定,而它们比例紊乱可能会导致肥胖和糖尿病等代谢综合征。
本文,我们就给大家详细介绍一下这其中最常见的几大细菌门:
拟杆菌门、厚壁菌门、变形菌门、放线菌门。
为什么选这四大细菌门?
依据自然属性分类,人类肠道菌群已经鉴定出细菌的几十个门,包括:拟杆菌门、厚壁菌门、变形菌门、放线菌门、疣微球菌门、梭杆菌门、蓝藻菌门、螺旋体门等。 但是其中98%的肠道菌可以归属为前四类,拟杆菌门、厚壁菌门、变形菌门和放线菌门,大多数人这4个门的菌占据肠道细菌数量的99%。 了解这四大细菌门,可以说你对大部分人体内肠道菌群的有了一定的了解。
▲ 拟杆菌 :革兰氏阴性菌
不形成孢子 厌氧菌 杆菌 ▲
它们具有外膜、肽聚糖层和细胞质膜。它们无氧呼吸的主要副产物是乙酸、异戊酸和琥珀酸。
包括碳水化合物的发酵、含氮物质的利用以及胆汁酸和其他类固醇的生物转化。大多数肠道细菌是糖酵解的,这意味着它们通过碳水化合物分子的水解获得碳和能量。
据估计,只有约 2% 的单糖通过上消化道到达结肠。因此,单糖可能不是拟杆菌的主要能量来源。然而,来自植物纤维的多糖,如纤维素、木聚糖、阿拉伯半乳聚糖和果胶,以及植物淀粉,如直链淀粉和支链淀粉,在结肠中更为普遍。
多糖还被证明可以诱导来自拟杆菌的多种葡糖苷酶活性,包括负责海带多糖降解的 β-1,3-葡糖苷酶活性以及多种 α、β-1,4 和 α、β–1,6 木糖苷酶和葡糖苷酶活性。大部分拟杆菌成员蛋白质组包括水解这些多糖的蛋白质。
表现出相当大的营养灵活性和对宿主和肠道环境施加的压力做出反应的能力。很难说肠道拟杆菌是否对宿主产生负面或正面影响。拟杆菌能够通过预防可能定植和感染肠道的潜在病原体感染来使宿主受益。由但是,在短链脂肪酸存在下,弱酸性 pH 值会抑制生长。诸如脆弱拟杆菌之类的致病物种已经开发出逃避宿主免疫系统的策略。
作为多糖降解联盟的成员,它们有助于从膳食纤维和淀粉中释放能量,它们很可能是丙酸盐的主要来源;然而,它们也参与了蛋白质分解过程中有毒产物的释放,这个群体的成员有一些可能有助于抑制炎症的活动,但他们也有可能促进炎症,有些是已知的机会性病原体。

谷禾健康
S. pneumoniae (or pneumococcus,肺炎链球菌)是中耳炎、细菌性脑膜炎、败血症和社区获得性肺炎的主要病因。世卫组织将肺炎链球菌列为一种抗生素耐药的“优先病原体”。
肺炎链球菌是下呼吸道感染的主要原因之一,每年在全世界造成近100万儿童死亡。肺炎链球菌在人类宿主中占据不同的生态位,导致共生和致病性存在。侵袭性肺炎链球菌疾病是一个多步骤的过程。它是通过肺炎链球菌渗透进入富含糖的粘液层,然后粘附到人鼻咽的上皮细胞层而引发的。通常,微生物在鼻咽中定殖较长时间而不会引起疾病。
另外,由于未知的原因,它可以扩散到中耳,肺,大脑或血液中。直接从鼻咽或最经常通过肺部进入血液,可以进入中枢神经系统,心脏和脾脏。在所有这些组织中,肺炎链球菌都受到免疫系统和各种环境条件的攻击。

刚刚,来自美国宾夕法尼亚州匹兹堡卡内基梅隆大学生物科学系的一篇综合评论文章题为:“The pneumococcal social network” 综合阐述了人类致病菌肺炎链球菌分泌肽的机制和功能特点。讨论了三大类小肽的序列特征、转运机制和受体:双甘氨酸肽、Rap、RGG、NprR、PlcR和PRGX(RRNPP)结合肽,以及含羊毛硫氨酸的小肽。强调影响携带和致病的因素,特别是遗传多样性、微生物竞争、生物膜发育和环境适应。
注:羊毛硫氨酸是一类结构独特的肽类,因其序列中含有羊毛硫类非常规氨基酸而得名。
革兰氏阳性细菌使用一系列分泌肽来控制种群水平的行为,以响应环境提示。最近肺炎链球菌多肽研究的扩展揭示了一个相互作用的信号系统的复杂网络,其中多个多肽被整合到同一信号通路中,允许多个进入该通路的点,并向新的方向扩展信息内容。
此外,由于多肽存在于细胞外环境中,因此存在串扰、群体感应(QS)以及株内、株间和种间相互作用的机会。关于人群行为导致疾病的方式的知识为设计和开发抗感染策略提供了一条途径。
社会行为在生物体内广泛存在。蚁群的形成、蝗虫的协调运动和鱼类的浅水化都是复杂的社会行为例子。这些行为通过保护人们免受捕食、增加食物供应或比竞争对手具有战略优势而受益。细菌也不例外。
细菌执行群体感应(QS):细胞密度相关的信号传导,导致群体水平的反应。QS的早期证明是在海洋细菌fischeri弧菌中,高细胞密度诱导生物发光,这是细菌与鱿鱼共生关系的一部分。从那时起,细菌群的行为就被牵涉到细胞过程中,比如基因转移、运动、抗生素的产生和生物膜的形成。
细胞-细胞间的通讯是由供体细胞分泌到细胞外环境中的信号分子来协调的,并由产生细胞和邻近细胞感应到。感知导致基因表达的变化,最终触发同步的群体行为。这种细胞-细胞通讯的核心是通过自体诱导剂-2(AI-2)和肽发出信号。
肺炎链球菌细胞-细胞通信系统可根据肽序列、转运蛋白和受体分为3大类(图1)。这些是(1)双甘氨酸肽,(2)与QS蛋白RRNPP超家族相关的肽,(3)含羊毛硫氨酸肽。从它们的作用来看,肽介导的细胞-细胞通信系统至少履行了三个主要功能:确保遗传多样性、微生物竞争和环境适应。
图1 肺炎链球菌分泌肽的三大类示意图
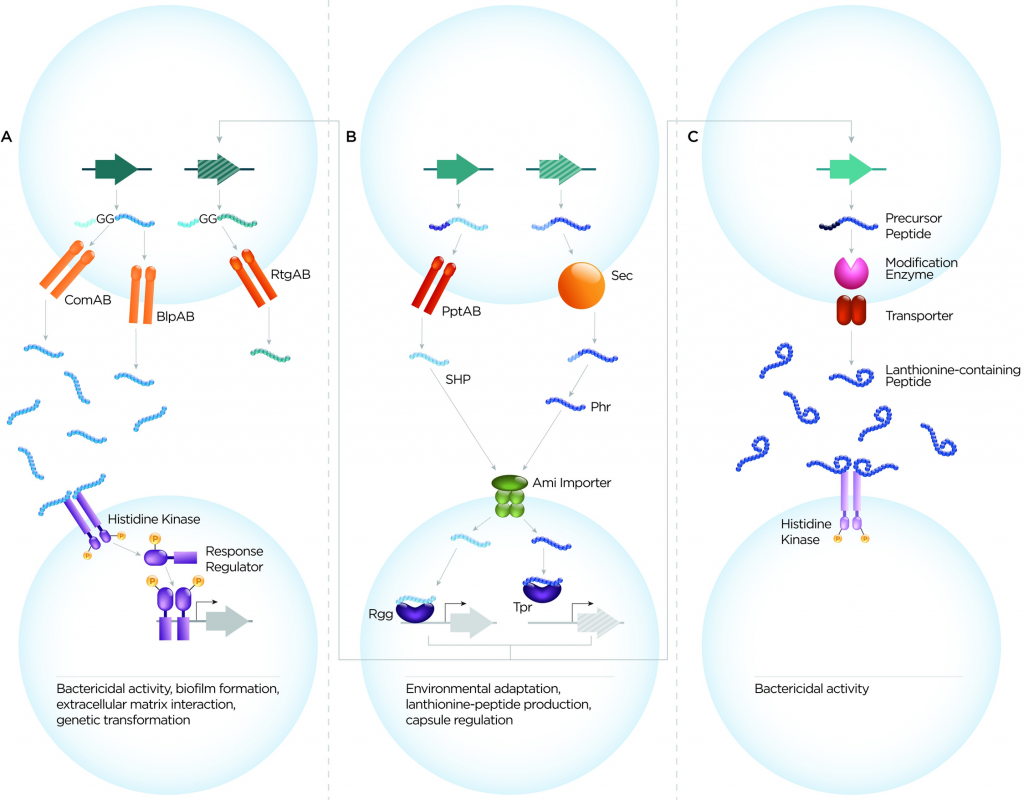

双甘氨酸肽
最具特征的肺炎链球菌双甘氨酸肽是能力刺激肽(CSP)。其他例子包括细菌素诱导肽(BIP)、感受态诱导细菌素(Ciba和CibB)、细菌素免疫区的肽(BIR)、毒力肽1(VP1)、感受态诱导的生物膜调节肽(BRIC)、RTG位点的肽和LANA(表1)。此外,比较基因组学方法已经揭示了额外的双甘氨酸肽,这些多肽还有待鉴定。
表1:核糖体合成肽在肺炎链球菌中的实验研究
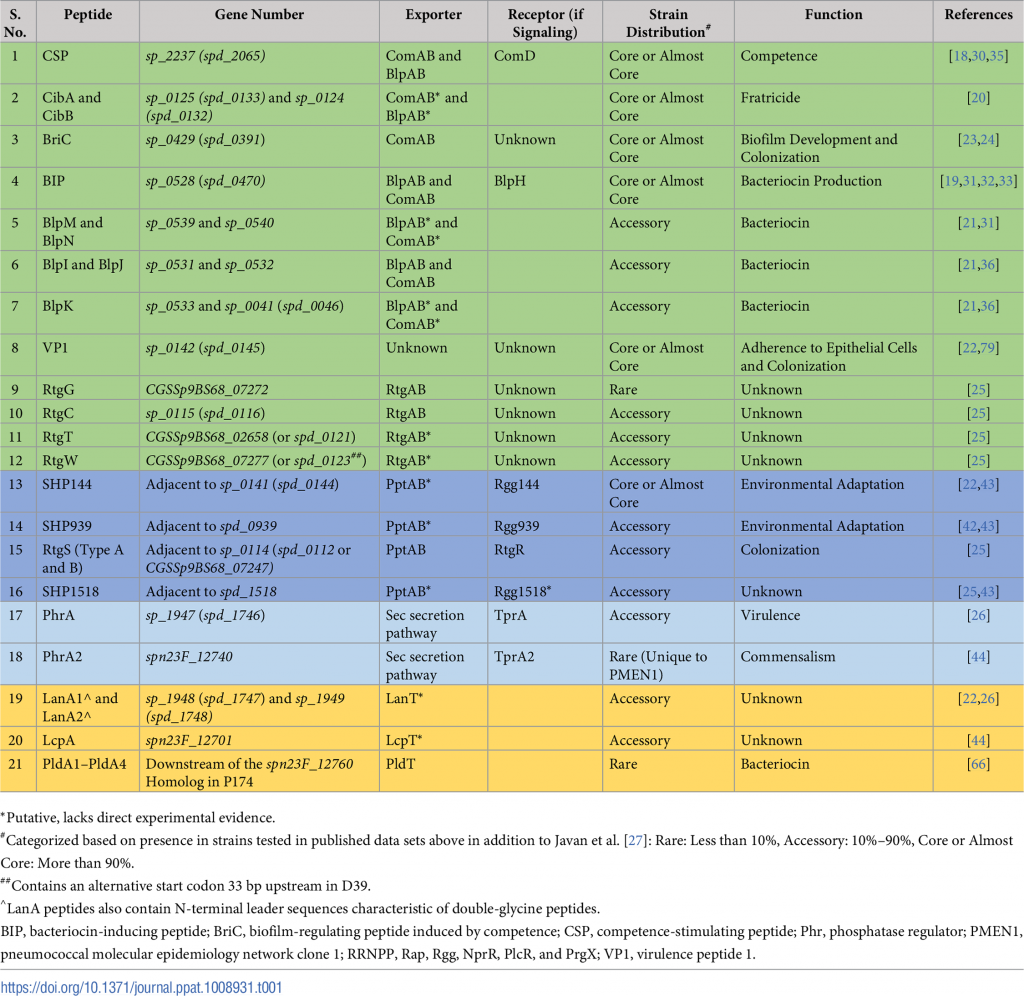

双甘氨酸肽的特征是保守的N末端前导序列,该序列终止于Gly–Gly残基(或更常见于Gly–Ala或Gly–Ser)。前导将这些肽引导至含有肽酶的ATP结合盒(ABC)转运蛋白(具有C39肽酶结构域),其可切割前导序列并将肽输出到细胞外。 CSP和BIP的基因座分别编码同源的输出蛋白ComAB和BlpAB。移码突变使BlpAB在大约60%的菌株中失去功能。
QS蛋白的RRNPP超家族的肽
该组中的肽通过与它们的同源细胞质转录因子直接相互作用而发出信号,它们是RRNPP超家族的成员(图1B)。如前所述,这些肽可以基于多种序列特征进行分类。在肺炎链球菌中,已经鉴定了短疏水肽(SHP)SHP144,SHP939,SHP1518和RtgS,以及磷酸酶调节剂(Phr)肽PhrA和PhrA2。
在整个链球菌中,糖基转移酶(Rgg)蛋白质的调节基因与它们的同源SHP结合后被激活,后者通常在rgg基因附近编码。 SHP仅在出口后才有活性,这是由通常短于35个残基的前体多肽加工而成的。尚未在肺炎链球菌中研究加工蛋白酶,但在其他链球菌物种中,膜结合金属蛋白酶(Eep)有助于加工。
多种链球菌物种通过ABC转运蛋白PptAB出口SHP,其粪便肠球菌的同源物出口性信息素。在缺乏已知靶序列的情况下,将SHP引导至其转运蛋白的机制仍不清楚。成熟的肽通过寡肽渗透酶系统重新导入细胞,在那里它们与同源的Rgg调节剂相互作用,从而改变细胞的转录状态。
在肺炎链球菌中,RtgS是唯一显示其前体肽由PptAB出口并由Ami寡肽进口商AmiACDEF内化的SHP。鉴于PptAB在物种间的广泛功能,其他肺炎链球菌SHP可能利用相同的机制进行进出口。
含羊毛硫氨酸肽类
这是由革兰氏阳性细菌产生的一族小肽(19-38个氨基酸),具有各种结构和功能。这些是环状肽,其特征是翻译后修饰,导致硫醚氨基酸、羊毛硫氨酸和甲基羊毛硫氨酸的引入(图1C)。当前肽中的丝氨酸或苏氨酸残基脱水并与半胱氨酸硫醇连接时,它们的特征结构由LanM修饰酶形成。该肽通过专用的LanT转运蛋白输出。许多含羊毛硫氨酸的肽形成细菌素的两大类中的一种。
这些肽被称为羊毛硫氨酸抗生素或羊毛硫氨酸的抗生素。用于加工羊毛硫氨酸的肽,修饰酶,免疫蛋白和转运蛋白的基因通常以簇的形式组织。肺炎链球菌中有许多这样的簇。其中,已经研究了与Tpr / Phr和肺炎链球菌素簇相关的瘦肽。
肺炎链球菌肽介导的细胞-细胞通讯系统提供多种功能,而不是相互排斥。细胞-细胞通信系统可以被概念化为控制种群水平结构和行为的电路。
许多细胞-细胞通讯回路对不同的环境刺激作出反应,如菌群密度、营养状况、pH值、氧气供应和抗生素压力。来自细胞-细胞通讯系统的信号在群体水平的变化中表现为聚合。这些可能会影响生物膜的发育或与细胞表面成分的改变有关,如膜成分和胶囊表达。
细胞-细胞通讯系统的行为也可能伴随着DNA摄取、自残或杀菌能力的改变。这些生理变化可能改变细胞获得抗生素抗性基因的倾向,并影响疫苗逃逸株的出现。
此外,细胞间通讯系统还可以调节宿主基质的降解、生物膜的发育和营养吸收能力。因此,这些特性共同影响致病潜能、抗生素耐药性和对疫苗的反应。
调节群体反应的能力为肺炎链球菌细胞提供了相对于居住在鼻咽的其他微生物物种的竞争优势。细胞间的通讯系统使微生物能够改变其转录模式,以获得合适的表型,从而优化种群水平的适应性。它能在DNA水平和转录水平上引入多样性,从而能够长期维持鼻咽部的共生生活方式,在无症状时期,肺炎链球菌在高度可变的生物膜中被发现。
此外,一般来说,“转录适应”不仅有助于在动态的鼻咽中存活,而且在感染期间微生物从一个宿主生态位迁移到另一个宿主生态位时也能促进存活。
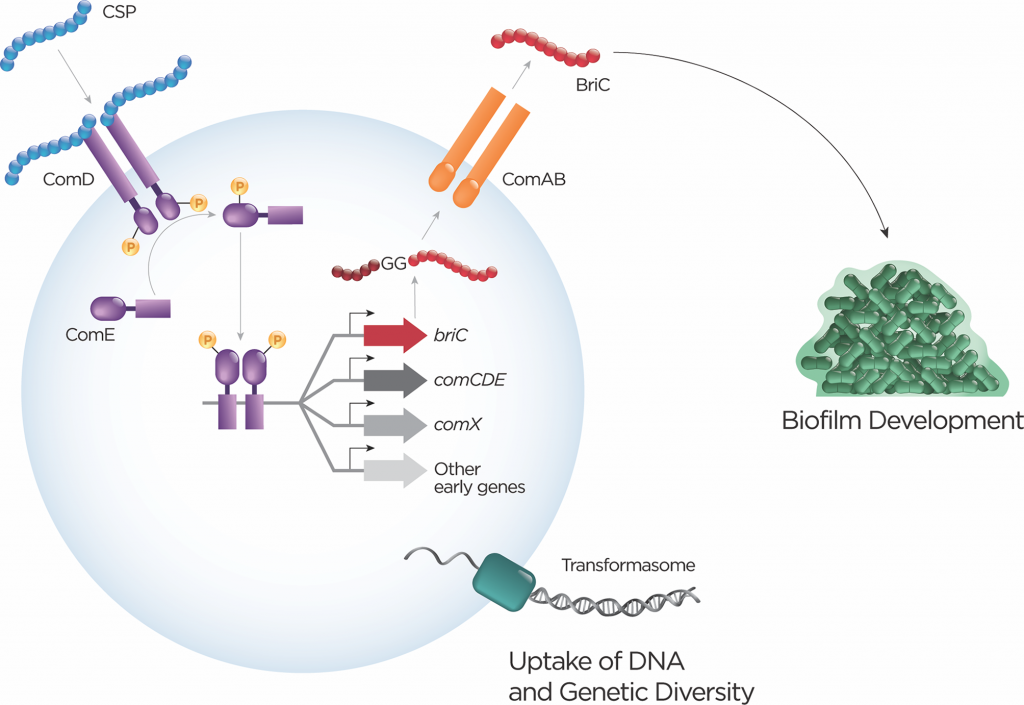
当检测到CSP,双甘氨酸肽家族的典型代表就会被激活。肺炎链球菌泛基因组拥有comC的6个不同等位基因,其中大多数菌株编码2个等位基因变体中的1个。在混合种群中,能力不仅在空间上局限于生物膜内的某个区域;信号可能局限于单个的信息类型(框1)。CSP是由高细胞密度、pH值增加、氧利用率和抗生素压力等因素引起的。
除了在环境中扩散外,CSP还通过其他机制(包括自分泌信号和细胞-细胞接触)向邻近细胞发出信号。激活会导致一个菌株的10%的基因发生转录变化。最典型的反应是激活转化机制,允许通过重组将外源DNA纳入,并且在这样做的过程中,通过等位基因的交换和基因拥有量的变化来促进遗传多样性的产生(图2)。
全基因组内遗传物质的交换测试了新颖的遗传组合,其中单个等位基因或基因片段已经克服了通过选择修剪的问题。
图2 多个双甘氨酸肽的分级活化

种内和种间竞争是呼吸道肺炎链球菌生活方式的一部分。杀菌活性通过双甘氨酸和羊毛硫氨酸的肽家族中的小分子产生。限制竞争者生长的能力对于细菌定殖很重要。此外,受害者可能成为DNA的来源,增加了进化的可能性。
能力激活导致许多这些效应分子的产生,包括CibAB和BIR基因座。双甘氨酸肽CibAB引发异源分解或反式裂解,并以细胞接触依赖性方式负责非功能细胞的裂解。与乳酸乳球菌IFPL105相似,据信这种杀微生物剂是通过将细菌素插入敏感细胞的膜中而导致其细胞能量消耗而产生的。
此后,细胞壁水解酶(包括自溶素LytA,溶菌酶LytC和莫林蛋白酶水解酶CbpD)的作用引起裂解。跨膜肽CibC保护细胞免受CibAB的同素分解作用。 CibAB从非感受态细胞释放的营养物质和DNA可能会使攻击细胞受益。在定殖的鼠模型中,CibAB诱导的同素分解作用使常驻菌株具有通过入侵菌株抵抗竞争和定殖的能力。
IR编码多种效应基因,赋予其抑菌作用或抑制作用的免疫力。 BIR基因座是同系的,但细菌素(假定的和特征的)和免疫蛋白在不同菌株之间差异很大。blpIJ,blpMN和blpK的产品已证实具有杀菌活性。这些是双甘氨酸肽,由BlpAB输出,并与同源免疫蛋白共转录。所有这些肽都显示出菌株间的活性,并且在体内,BlpMN和BlpIJ细菌素在定植过程中提供了比免疫缺陷型菌株更具竞争优势的菌株。
除肺炎链球菌外,细菌素基因座的表达还抑制了一些其他革兰氏阳性细菌,包括化脓性链球菌,链球菌性微生物,口腔链球菌和乳酸乳球菌,但不抑制其他细菌,例如变形链球菌,粪肠球菌或单核细胞增生李斯特菌。
BIR基因座的表达是由BIP诱导的,BIP由blpC和BIR的上游编码。与CSP相似,BIP结合膜结合的组氨酸激酶(B1pH),并且在肽及其受体之间具有特异性。这种特异性限制了竞争性表型之间的串扰。与能力途径的激活相似,BIP的表达是由抗生素诱导的,并且会增加pH值。而且,在能力和细菌素系统之间存在串扰,其中BIP的产生是在CSP刺激后诱导的。
另一类细菌素是羊毛硫氨酸的肽,其特征是肺炎链球菌素(pld)。pld基因座在肺炎链球菌分离株中很少见,其特征是有4个串联推定的短肽同源物(PldA1-PldA4)。这4种肽中的3种PldA1-3对细胞的杀菌活性是必需的,而第4种肽PldA4对于该表型是必不可少的。
除具有杀菌特性外,肺炎链球菌素(PldA1-3)还可作为自动诱导信号肽,通过位点(pldK)中编码的组氨酸激酶进行信号传导,从而激活pld位点。免疫是由邻近的ABC运输商PldFE授予的。这些肽的信号传导和杀菌作用是相互联系的:当Pld肽的信号传导低时,PldA2不会诱导细菌抑制作用。另外,肺炎链球菌素在小鼠定植过程中为肺炎链球菌菌株提供了竞争优势。
最后,全面的比较基因组筛选揭示了许多其他肽,它们在肺炎链球菌菌株之间分布不同(从稀有到核心),而且是肺炎链球菌特有的或在链球菌种之间共有。许多细胞与推定的转运蛋白,修饰蛋白或免疫蛋白一起组织成操纵子。肺炎链球菌菌株和相关物种内的多样性分布与种内和种间微生物竞争中的作用一致。
肺炎链球菌有一个细胞间通信系统网络,可调节其对宿主环境的适应性。肺炎链球菌只能使用糖来产生其代谢能。此外,糖被用于胶囊生产和信号传递。此外,通过磷酸转移酶系统(PTS)转运糖可以触发磷酸化依赖性信号通路。此外,宿主糖的降解不仅是营养的来源,而且还是宿主粘附,定植和致病性的主要因素。
几种细胞间通讯肽的表达对宿主碳水化合物的水平有反应:甘露糖和半乳糖诱导SHP144和SHP939,半乳糖诱导PhrA。另外,这些肽以及PhrA2和VP1在丰富的培养基中被阻遏。Rgg144 / SHP144系统是核心。当自诱导肽SHP144导入细胞并结合Rgg144时,它被激活。Rgg144受主要营养调节剂CodY和谷氨酰胺/谷氨酸代谢的负面控制。
SHP939是一种正向调节Rgg939的自诱导肽。该系统是辅助基因组的一部分。 Rgg939 / SHP939调控的基因多样性随环境条件的变化而变化,当在甘露糖上生长时具有广泛的调节子,而在半乳糖中则具有有限的调节子。
Rgg系统并非孤立运行,而是看起来形成了一个连接的网络。因此,为了最大程度地诱导SHP144和SHP939,需要存在非同源Rgg调节剂。此外,Rgg1518控制其邻近基因座(SPD_1513–1517),这些基因也受Rgg144和Rgg939调控。这种串扰可能会超出物种的范围。 SHP939的序列与化脓性链球菌中发现的SHP3的序列相同,无乳链球菌和米氏链球菌中的SHP序列相差1个残基。SHP序列的相似性可能使肺炎链球菌Rgg系统受到其他常驻细菌的影响。
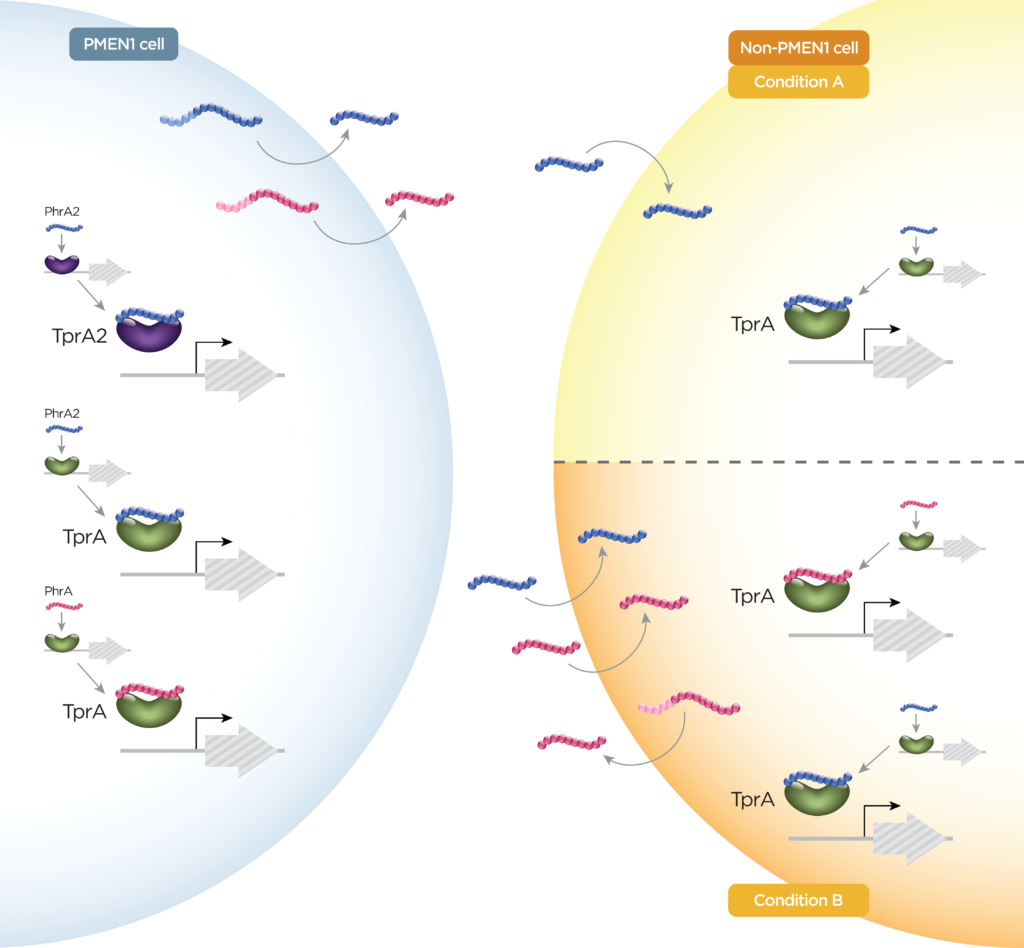
类似于TprA / PhrA,PhrA2与TprA2相互作用,导致TprA2调节子的阻遏并诱导紧靠下游的羊毛硫氨酸肽(LcpA)的表达。有证据表明TprA2 / PhrA2与TprA / PhrA系统之间存在单向串扰(图3)。
图3 如PhrA和PhrA2所示的肽串扰示例
肺炎链球菌所编码肽的多样性凸显了群落水平表型在引入遗传多样性、微生物竞争和环境适应方面的重要性。一些研究证实了细胞间通讯在肺炎链球菌毒力中的作用。需要更多的研究来绘制这些系统在感染过程中的时空表达。
上呼吸道是许多细菌物种的常住栖息地。为了在宿主环境中立足,肺炎链球菌细胞必须在竞争中生存并抵抗住其他寄居物种的挑战。肺炎链球菌产生大量的肽,直接或间接地通过激活下游分子(例如,由CSP激活CibAB或CbpD)介导杀菌活性。虽然其中一些细菌素已被鉴定,但许多假定细菌素有待功能鉴定,尤其是在目标菌株/物种和刺激其合成的环境条件下。
多种肺炎链球菌肽与生物膜形成有关,包括CSP、BriC和VP1。生物膜在运输和疾病中起着关键作用。载体包括一种生物膜生长模式,它本身能够实现局部细胞-细胞通讯(通过肽和AI-2)和吸收生物膜基质中提供的DNA。
此外,生物膜为表型异质性提供了一个平台,这是一个未被充分研究的课题,可能有助于肺炎链球菌适应慢性感染和适应宿主生态位。生物膜促进发病。它们不仅是细菌传播的场所,而且从生物膜中传播的细菌比它们的生物膜或浮游生物具有更强的毒性。
综上所述,肺炎链球菌信号肽和生物膜紧密相连:生物膜中的局部环境可能促进细胞-细胞通讯的条件,而肽会影响生物膜的发育和向其他组织和新宿主的扩散。
肽对调控网络的控制使肺炎链球菌不仅在单个细胞水平上,而且在整个群体水平上对其环境作出快速反应。系统间的串扰和由多个肽对一条通路的调节使不同的信号得以整合,可能会增加反应的动态性和复杂性。研究表明,多链肺炎链球菌共定植是一种相对常见的现象,突出了跨菌株肽交换的重要性。PhrA2和PhrA存在串扰(图3)。
来自同一家族或不同家族的肽可以在同一途径中发出信号。例如,通过CSP的信号转导可诱导多个双甘氨酸蛋白,而SHP144诱导VP1(一种双甘氨酸肽)的水平。这种肽激活的层次结构描述了生物途径激活的多个入口点的存在。这表明这些途径的激活是严格控制的,代表了相关但不同的可能性。
一种可能性是,不同的信号组合允许诱导整个通路或通路的一部分,提供与反应相关的类型、幅度和代谢成本的粒度。或者,当遇到合适的条件时,细胞可以激活肽信号,为诱导下游通路做好准备。
抗生素耐药性是一个全球性的公共卫生问题,因此迫切需要开发有效的抗感染药物。非抗生素抗感染药物有望减少抗生素耐药性的出现。开发破坏细胞-细胞通讯的化合物的不同策略包括抑制信号产生、信号降解或阻断信号转导。在化脓链球菌和其他一些链球菌中,化合物的使用会破坏Rgg/SHP信号传导,从而破坏生物膜的形成。在肺炎链球菌中,使用竞争性类似物可以抑制能力发展和水平基因转移。此外,以可溶性LMIP形式靶向PhrA肽的抗感染药物可降低肺炎链球菌介导的小鼠发病率。不同的抗感染药物是如何影响细菌适应度和促进耐药性发展的,还有待检验。肺炎链球菌细胞间通讯系统的多样性为探索不同的可能性提供了许多机会。对肺炎链球菌群体水平表型的研究为开发新的抗感染靶向肽介导系统以及这些系统调控的途径提供了机会。
参考文献:
Aggarwal SD, Yesilkaya H, Dawid S, Hiller NL (2020) Thepneumococcal social network. PLoS Pathog 16(10): e1008931.
Bassler BL. Small talk: Cell-to-cell communication in bacteria.Cell. 2002;109:421–424. pmid:12086599
Slager J, Kjos M, Attaiech L, Veening JW. Antibiotic-inducedreplication stress triggers bacterial competence by increasing gene dosage nearthe origin. Cell. 2014;157:395–406. pmid:24725406
Miller EL, Evans BA, Cornejo OE, Roberts IS, Rozen DE. Pherotypepolymorphism in Streptococcus pneumoniae has no obvious effects on populationstructure and recombination. Genome Biol Evol. 2017;9:2546–2559. pmid:28992304
Junges R, Sturød K, Salvadori G, Åmdal HA, Chen T, Petersen FC.Characterization of a signaling system in Streptococcus mitis that mediatesinterspecies communication with Streptococcus pneumoniae. Appl EnvironMicrobiol Microbiol. 2019;85:e02297–e02218. pmid:30389765