-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康
凌晨两点外卖订单又刷新了记录
刚下单的芝士炸鸡、烤串、肥宅快乐水…
这些号称“当代青年续命神器”的食物
在不知不觉中消耗着我们的情绪健康
越来越多人有这样的感觉
“吃饱” ≠ “快乐”
超加工食品,就是那些经过复杂工业加工的食物,主要由食物和添加剂制成的配方,几乎不含完整的天然食物,比如方便面、薯片、汉堡、冷冻披萨、各种包装零食等,与较差的身心健康结果相关。
一份涵盖15,262人的国际ALIMENTAL研究刚报道了一篇文章,发现女性/年轻人食用超加工食品后抑郁风险更高。
本文我们为大家介绍一下这项涉及15,262名参与者的大规模国际ALIMENTAL研究的核心发现,系统阐述了不同饮食模式与重度抑郁症风险之间的量化关联,了解不同饮食习惯可能会如何影响他们的抑郁症风险。基于研究结果,本文还提供了具有循证医学依据的饮食调整策略,为通过营养干预预防和辅助治疗抑郁症提供了科学指导。
研究采用横断面设计,通过在线问卷收集数据,使用主成分分析识别饮食模式,并通过多变量分析评估其与抑郁症的关联。
ALIMENTAL研究是一项模断面在线国际调查,在2021年11月~2023年6月期间进行。
研究获得了法国、德国和加拿大伦理委员会的批准,通过社交媒体、心理健康协会和医疗机构招募参与者。
为了确保研究结果的可靠性,研究团队设置了严格的筛选标准,这样做的目的是避免这些因素对结果造成干扰,确保观察到的关联确实来自饮食本身。
采用 Benjamini-Hochberg 法校正多重检验,以优势比(OR)和 95% 置信区间(CI)评估膳食模式与抑郁的关联强度。
然后用统计学方法,比如运用主成分分析(PCA)提取 13 种膳食模式,把复杂的饮食数据简化成几种主流的饮食模式,再分析这些模式跟抑郁症的关系。
主成分分析简单说,就是把一大堆食物信息压缩成几个关键的饮食模式因子,他们最终识别出了13个因子。
其中最引人注目的两个是:
其他的因子还包括了:
每个因子代表一类具有相似营养特征或加工程度的食物组合。这些因子就像是给我们的饮食习惯贴标签,方便后续分析。
1. 超加工食品增加抑郁风险,性别差异显著
核心发现:女性和年轻人最脆弱。
换句话说就是:
这个发现并不孤立,实际上是证实了之前科学界在2021年和2022年,研究人员发表的两项荟萃分析:
说完坏消息,再来说说好消息。
2.健康饮食可降低抑郁风险(仅女性有效)
健康饮食包括水果、坚果(杏仁或榛子)、绿色蔬菜(如四季豆、西兰花、芦笋)、橄榄油、菜籽油或大豆油、绿叶沙拉或苦苣、茶饮、全麦面包等。
3. 其他重要发现
除了超加工饮食和健康饮食之外,其他的饮食也值得关注,比如吃罐头食品、喝含糖饮料,似乎和女性抑郁症风险增加有关。
关于膳食补充剂和女性抑郁风险增加有关,这可能是因为,吃这些补充剂的人本身就可能已经有抑郁倾向,或者存在其他健康问题,所以才去补充。
不能排除这些食物的摄入与其他食物的排除呈负相关,这也可能有助于解释观察到的关联。
吃高血糖指数食物、乳制品等,反而和抑郁风险降低有关,这可能是因为这些食物提供了一些必要的营养素,比如说在营养不良或能量不足群体中(如老年/慢性病患者),高GI食物提供快速能量,短期改善情绪低落。
也可能是因为存在人与人之间本身存在代谢差异,某些体质对糖代谢更适应,这要根据个人肠道菌群结构来看,肠道菌群检测报告中也有相关指标,可以看出个体对于碳水、糖类的代谢能力。
混杂因素影响
该研究还发现,某些混杂因素在某些群体中与抑郁症风险降低相关,如更高的成就、营养知识、有在家居住的伴侣、在家居住的儿童;
而另一些混杂因素则与抑郁症风险增加相关,如当前每日吸烟、肥胖、失业、肤色等。
科学家们提出了几种可能的解释:
◆ 女性的身体构造不同
女性和男性的激素水平、新陈代谢方式都不一样,女性的激素水平在月经周期、怀孕、更年期等不同生理阶段会发生显著变化。超加工食品通常高糖、高盐、高脂肪,可能干扰女性体内激素的正常平衡。
比如说,雌激素会放大乳化剂对肠道紧密连接蛋白ZO-1表达的抑制作用,增加肠道通透性,肠漏则进一步影响免疫系统功能,体内炎症因子水平上升更明显。
女性的身体脂肪分布与男性不同,通常更容易在腹部、臀部和大腿堆积脂肪。超加工食品的高热量和高脂肪含量,会加剧这种脂肪堆积,这可能与心血管疾病、糖尿病等慢性疾病相关。
◆ 男女吃的不一样
男性和女性可能偏爱不同类型的垃圾食品,吃的量也不同。比如女性可能更爱吃甜食和零食,男性可能更偏爱油炸或肉类食品。这些”口味偏好”的差异,可能导致对心理健康的影响也不同。
女性可能更容易受到情绪的影响,而出现情绪性进食行为。超加工食品往往具有浓郁的口感和香气,能够快速满足情绪上的需求,但长期来看,这种饮食习惯会导致营养不均衡和体重增加。
比如说,膳食乳化剂可能对肠-脑轴产生影响,并通过微生物群依赖机制诱导暴露者的心理/行为障碍。
乳化剂中羧甲基纤维素和聚山梨酯80过量食用会导致微生态失调,粘液降解细菌过度生长,以及IL-10或Toll样受体5进一步缺乏。
乳化剂可能还会增加肠上皮屏障中病原微生物的易位,引起肠道炎症。
乳化剂和相关微生物代谢对大脑的影响
Tan H,Nie S.FEMS Microbiol Rev.2021
比如说一些冰淇淋、奶昔、预包装蛋糕里面都含有乳化剂,而女生相对更爱吃这类超加工食品,因此可能带来更高的抑郁症风险。
可以详见谷禾之前写过的文章:
抑郁症与肠道微生物群有何关联
抑郁、焦虑、压力的肠道故事——精神健康的改善新途径
食品添加剂:健康还是危险?——从肠道微生物角度分析
◆ 对健康信息的处理方式不同
** 需要坦诚地说,这项研究的参与者中女性比男性多很多。这在抑郁症研究中很常见,可能是因为:女性本来就更关注健康话题,而且研究主要通过医疗机构和社交媒体传播,这些地方本身可能女性用户更多。不过研究者认为,这种”男女比例不均”不太可能影响他们观察到的性别差异。
◆ 各年龄段的吃法本来就不一样
想想看,爷爷奶奶那一代和现在的年轻人,饮食习惯都不一样。最近的科学调查发现了一个很有意思的现象:
越年轻、住在大城市、单身或离异的人,
越爱吃超加工食品。
这背后有很现实的原因:年轻人可能工作忙、不会或不愿意做饭,单身的人懒得准备精致丰盛的食物,大城市生活节奏快、外卖方便——这些都让方便面、冷冻食品、各种包装零食成了救命稻草。
◆ “从小就被喂坏了”
现在的年轻人可以说是垃圾食品的原住民——从幼儿园开始就接触各种包装饮料、膨化食品、快餐。这种从小培养的饮食习惯,可能让年轻男性比老年男性更容易受到超加工食品的情绪攻击。
就像抽烟一样,越早开始接触,成瘾性和伤害性往往越大。
这里有个更可怕的发现:超加工食品不只是让人心情不好,它还会引发一连串的健康问题——糖尿病、高血压、心脏病、肥胖等等。而这些慢性病本身就容易让人患抑郁症,形成一个”恶性循环“。
吃垃圾食品→身体发炎、代谢乱套→得慢病→心情更差→可能更依赖安慰性食物→恶性循环
具体来说:
◆ 影响菌群
高糖、高脂、防腐剂、缺乏纤维等超加工食品,不利于有益菌的生长,人工添加剂改变肠道环境的酸碱度,当坏细菌占上风时,它们会产生有毒物质(如脂多糖),破坏肠道屏障,让本来不该进入血液的东西跑进去,触发炎症反应。
抑郁症个体与健康对照组相比,微生物群变化如下:
Basiji K, et al., Metab Brain Dis. 2023
◆ 肠-脑轴
迷走神经直接连接肠道和大脑;肠道菌群能产生血清素、多巴胺等代谢产物(我们90%的血清素其实是在肠道产生的)。
血清素,参与调节情绪、食欲、睡眠和其他身体功能,比如说:
这些代谢产物通过血液循环或直接通过迷走神经传递到大脑,影响我们的情绪和行为。肠道炎症也会激活大脑中的炎症反应。
微生物群-肠-脑异常导致抑郁症
DOI: 10.1007/978-981-19-7376-5_10
◆ 其他微生物代谢产物
超加工食品通过双重途径加剧抑郁症风险:
◆ 炎症反应
超加工食品会让身体产生慢性炎症,当大脑接收到来自肠道的炎症信号时,负责情绪调节的区域(如海马体、杏仁核)开始罢工,压力激素皮质醇飙升,可能带来焦虑、抑郁、注意力不集中等情况。
抑郁症患者的炎症标志物包括:血清 IL-6、IL-1β、C反应蛋白升高。
◆ 代谢紊乱
超加工食品中的高糖、高脂肪成分会导致血糖快速上升后迅速下降,这种波动会引起情绪的起伏。长期食用会干扰胰岛素敏感性,导致能量代谢紊乱,使人容易感到疲劳、注意力不集中。
◆ 心血管负担
超加工食品中的反式脂肪酸和高钠含量会增加心血管疾病风险,血管健康受损时,大脑供血也会受到影响,可能导致认知功能下降。
◆ 恶性循环启动
心情不好的人往往会更渴望高糖、高脂的”安慰性食物”(这是大脑的本能反应),更没有动力去准备健康食物,从而选择一些方便快捷的垃圾食品。
这种本能的自我安慰机制却可能成为抑郁发展的催化剂——当不健康的饮食选择形成恶性循环时,科学干预的价值就凸显出来。
这正是研究食物与抑郁关系的关键意义:揭示这些现象背后的生理机制,才能为精准的健康干预指明方向。
健康的饮食习惯会帮助摄入许多营养成分,可以减轻炎症。其中,蓝莓,姜黄素等存在的植物化学物质(例如多酚)具有很强的抗炎特性,可能有助于治疗多种精神疾病。
益生菌,单独乳酸菌或与双歧杆菌联合使用——可能会改善抑郁和焦虑。
益生元,每天 5 克的低聚半乳糖和 1 克或以下的二十碳五烯酸可以有效缓解抑郁症状。
Omega-3脂肪酸、多不饱和脂肪酸在鲑鱼等海洋食品中含量很高,具有抗炎特性,可以改善并延缓细胞因子诱发的抑郁症的发作。
维生素,例如抗坏血酸(维生素C)和α-生育酚(维生素E)具有直接清除自由基的特性。
营养素(例如硒,锌和半胱氨酸)是抗氧化剂系统(例如谷胱甘肽过氧化物酶和超氧化物歧化酶)的辅助因子。初步证据表明,补充抗氧化剂如n-乙酰半胱氨酸可以改善抑郁症状。
当心理健康成为
全社会关注的焦点时
答案或许就藏在
我们每一餐的选择里
主要参考文献:
Achour, Y.; Lucas, G.; Iceta, S.; Boucekine, M.; Rahmati, M.; Berk, M.; Akbaraly, T.; Aouizerate, B.; Capuron, L.; Marx, W.; et al. Dietary Patterns and Major Depression: Results from 15,262 Participants (International ALIMENTAL Study). Nutrients 2025, 17, 1583.
谷禾健康

有这样一些病人:经常性的腹痛、拉肚子、甚至便血、人也日渐消瘦,这很有可能是患有炎症性肠病。
炎症性肠病是一种慢性、非特异性的肠道炎症性疾病,因其顽固无法治愈且需要终身治疗的特点,又称为“绿色癌症”。目前全世界有超过1000万人患炎症性肠病。
在我国炎症性肠病的发病率也呈上升趋势,已经成为常见的肠道疾病,预计2025年患病人数将达到150万,且发病人群偏年轻化。如何预防和治疗炎症性肠病,成为了许多病友和大众关注的重点。
肠道微生物群是一个复杂而独特的实体,在宿主免疫、获取营养物质和强化肠道上皮方面发挥着重要的生理作用。与常见胃肠道疾病的预防、发病机制和进展有关。
虽然肠道微生物群主要由细菌主导,但先进的测序技术已经确定了共生真菌群落,统称为真菌群。大量研究和谷禾的检测数据发现,肠道炎症与微生物组成改变有关,称为肠道菌群失调。微生物群落改变与各种病理疾病有关,例如炎症性肠病(IBD),但它们作为炎症的原因或后果的作用仍是正在进行的研究主题。
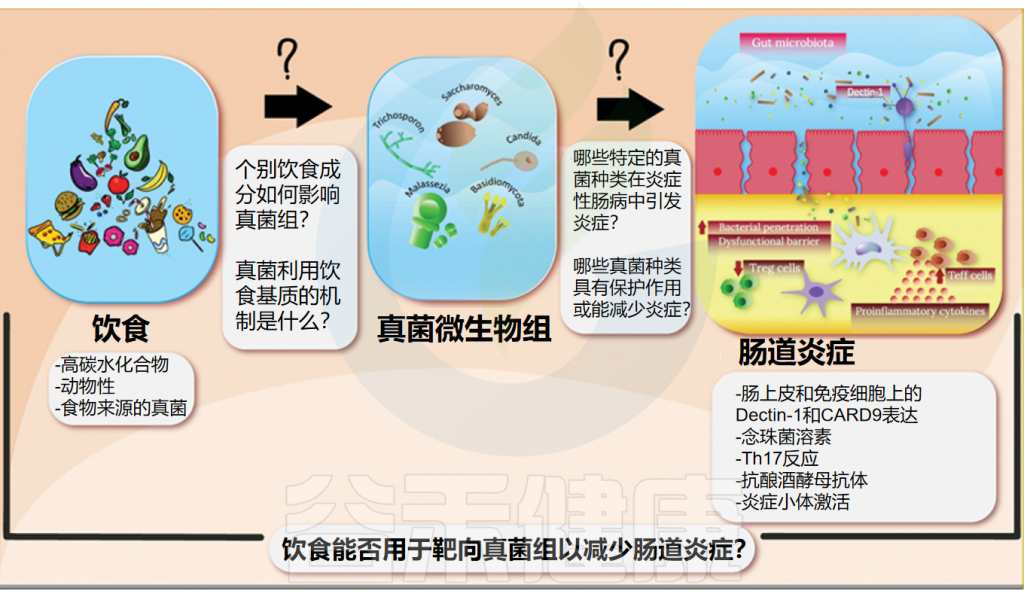
而饮食在预防和管理各种疾病方面起着至关重要的作用,被认为是全身炎症的重要调节剂。近年来,随着饮食与肠道微生物关系的深入研究,我们逐渐认识到饮食不仅塑造了肠道细菌的组成,同样也在悄然影响着肠道真菌群落的结构和功能,包括真菌发酵中涉及的代谢途径和酶。
本文将探讨饮食如何调节肠道真菌群,并分析这一过程与炎症性肠病(IBD)之间的潜在联系,为未来饮食疗法在IBD治疗中的应用提供新的视角和研究方向。
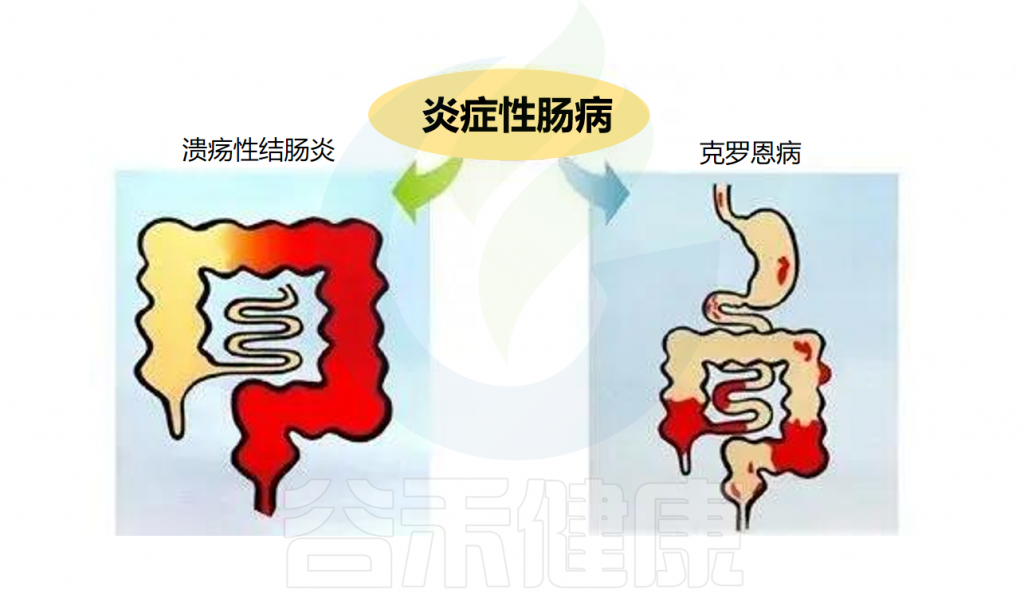
☆ 什么是炎症性肠病?
炎症性肠病(IBD)是一种慢性、非特异性的肠道炎症性疾病。包括溃疡性结肠炎(UC)和克罗恩病(CD)。克罗恩病涉及所有粘膜层,可在胃肠道的任何区域发现,并被细分为穿透性或狭窄性表型。溃疡性结肠炎累及直肠并向近端延伸,涉及粘膜和粘膜下层。
克罗恩病
-主要表现:腹泻、腹痛、大便带血、消瘦、乏力。
-可能还会出现:发烧 、关节痛、关节僵硬、眼睛红肿及疼痛、儿童生长或性发育延迟、皮肤红肿及发痛、口腔溃疡。
–并发症包括:瘘管、狭窄、脓肿、肠穿孔。
溃疡性结肠炎
主要表现:腹泻,多见黏液血便,常常伴发下腹部疼痛尤其以左下腹部疼痛多见。
可能还会出现:腹痛、腹胀、食欲不振、恶心、呕吐、发热、营养不良、关节炎、口腔溃疡。
并发症包括:下消化道大出血,肠穿孔、中毒性巨结肠及癌变。
☆ 炎症性肠病患病率有多高?
近几十年来,炎症性肠病(IBD)发病率逐年上升,目前已成为全球性疾病,具有显著的患者发病率和卫生保健负担。
在全球范围内,IBD的患病人数从1990年的332万例增加到2010年的490万例,增加了47%。据相关数据推测,预计到2025年,全球超过1000万人受到炎症性肠病的影响,我国炎症性肠病患者将达到150万,且以青壮年居多,发病高峰年龄为15至40岁。
注:在欧洲和北美,IBD已经逐步发展为常见疾病。比如在患病率最高的国家,UC和CD的患病率都已高达823/10万。在美国,目前大约有160万UC或CD患者,每年约7万人确诊为IBD。目前中国地区IBD发病率为1.96/10万-3.14/10万左右。
☆ 为什么会得炎症性肠病?
目前暂未明确炎症性肠病的发病机制,可能与多种因素有关:包括遗传因素、感染因素、过度反应的T细胞介导的免疫因素、环境触发因素、生活饮食因素和肠内微生物群因素。
炎症性肠病的日益流行引发了基础科学和临床研究的广泛关注,促使研究者们致力于开发有效的短期和长期治疗方案。这些研究的统一目标是显著减少患者的住院率,并同时提高患者的生活质量,以应对这一日益严重的健康问题。通过不断探索和创新,找到了一些有效的治疗方法,以改善患者的整体健康状况和生活体验。
▸ 药物治疗
抗炎药物短期效果好
炎症性肠病(IBD)的药物治疗是双管齐下的,旨在诱导或维持缓解。包括皮质类固醇和5-氨基水杨酸在内的抗炎药物可以通过多种方式给药,并且在及时诱导活动期病情缓解方面最为有效。
生物制剂可改善长期预后并提高疗效
相比之下,免疫调节剂和生物制剂起效较慢,但可以通过实现长期缓解维持来改变疾病轨迹。生物制剂是基于蛋白质的分子,可以阻断促炎细胞因子。
近年来,生物制剂已成为IBD治疗的基石,有证据表明,在IBD病程早期应用生物制剂可改善长期预后并提高疗效。此外,鉴于生物源化合物耗尽其开放性,生物疗法变得更具成本效益。
注:目前批准了四种不同类别的生物制剂:抗TNF制剂、抗整合素制剂、抗白介素12/23 IgG 1κ制剂和鞘氨醇-1-磷酸(S1P)抑制剂。
生物疗法的出现减少了炎症性肠病(IBD)相关的住院和腹部手术,然而,与IBD相关的总体发病率仍然很高。
▸ 饮食疗法
炎症性肠病(IBD)患者经常询问饮食策略来控制他们的胃肠道症状。饮食调节作为一种非药物疗法,具有显著的益处,其可以调节炎症和促进粘膜愈合并且基本没有副作用。
肠内营养
纯肠内营养(EEN)是一种通过消化道提供全面营养的方法,包括营养全面的流质饮食。在儿科克罗恩病患者中使用纯肠内营养(EEN)显示出与类固醇相似的功效,促进黏膜生长而无相关副作用。
部分肠内营养(PEN),允许一些食物摄入,比EEN耐受性更好,以克罗恩病排除饮食(CDED)为例。避免或减少动物/乳制品脂肪/蛋白质、小麦和食品添加剂的饮食相结合,允许逐渐重新引入水果、蔬菜和豆类以提高食物的灵活性。
特定碳水化合物饮食
一些针对成年IBD患者的饮食,如特定碳水化合物饮食(SCD),已经显示出减轻胃肠道症状的前景。SCD限制IBD患者难以吸收的复合碳水化合物,避免食用谷物、淀粉类蔬菜、乳制品、糖和甜味剂以及某些食品添加剂。
地中海饮食
地中海式饮食最近受到了关注,因为它限制较少,但却和SCD一样有效。这种饮食强调水果、蔬菜、坚果、鱼、全谷物、油性鱼和橄榄油,可以减少炎症,同时限制具有促炎症特性的动物脂肪/蛋白质和食品添加剂。
高膳食纤维并不总是有益
虽然膳食纤维通常被认为对健康有益,但一些炎症性肠病患者,尤其是在疾病活动期,对高纤维食物的耐受性降低。
在活动期疾病患者中证明,某些纤维,特别是低聚果糖(FOS),触发了促炎细胞因子IL-1β。而用来自非IBD或轻度感染患者的微生物群发酵FOS减少了IL-1β的分泌。但这种减少在大多数患有中度或重度IBD患者的微生物群中并不存在,这表明共生微生物群对FOS的发酵不足可能导致异常的免疫反应。
尽管饮食在炎症性肠病(IBD)发病机制中的作用已被认可,但我们对其对IBD进展的影响仍不够深入。目前尚未定义一种能够促进活动性疾病成年患者病情缓解的“IBD饮食”。需要加强对饮食对人类肠道影响的理解,特别是饮食与肠道微生物之间的关系及其在炎症中的作用。
最近的研究表明,肠道微生物群对不同纤维的反应存在相当大的个体间差异。菊粉和欧车前纤维的微生物群组成和功能差异很大,一些个体具有纤维抗性微生物群,而另一些个体具有纤维敏感性微生物群。这强调了个性化饮食建议的必要性,特别是在管理肠道健康和炎症方面。
人类肠道内居住着超过100万亿个微生物,包括细菌、古菌、病毒和真菌。这些微生物统称为肠道微生物群。肠道微生物群是一个复杂而独特的实体,与常见胃肠道疾病的预防、发病机制和进展有重要联系。
☆ 真菌虽然只占肠道微生物群的一小部分,但与多种疾病相关
然而,肠道中超过99%的微生物基因属于细菌,真菌只构成了常驻微生物群的一小部分,在不同的身体部位,包括皮肤、泌尿生殖系统、呼吸道和胃肠道,已经鉴定出390多种真菌。
尽管与细菌相比,真菌的多样性和丰度较低,但真菌的组成和功能与多种疾病有关,包括炎症性肠病、结直肠癌和代谢综合征。
☆ 肠道核心真菌群
然而,微生物组的研究主要集中在细菌上,而对真菌等其他重要的微生物组关注不够。真菌是单细胞或多细胞的异养真核生物,具有惊人的分解和获取营养物质的能力。
早期的研究集中在真菌对肠道健康的潜在危害上,随着人类微生物组项目的出现,真菌物种作为具有共生和互利关系的微生物组的必要组成部分获得了证明。
人体肠道内真菌的多样性和丰度较低,但个体之间存在相当大的可变性,然而,一些真菌物种在个体之间是共享的,这表明可能存在肠道核心真菌群落。
为了描述哪些真菌物种是本地的并有助于肠道健康,真菌群落被分为常驻和非常驻物种。常驻物种具有在缺氧的肠道环境中生长的内在能力,包括子囊菌门、担子菌门和接合菌门中的属,例如假丝酵母菌属(Candida)、马拉色菌属(Malassezia)和枝孢菌属(Cladosporium)。
相比之下,非常驻物种是通过非培养技术在肠道中分离出来的,常见的非常驻物种包括酵母属(Saccharomyces),曲霉属(Aspergillus),以及青霉菌属(Penicillium)等。非常驻物种通常是外部影响的产物,如短期饮食暴露或环境触发因素。这个亚群占分离真菌种类的三分之二。
念珠菌
常驻真菌中最常报道的是假丝酵母菌(Candida),假丝酵母菌又称念珠菌。包括白色念珠菌(C.albicans)、热带念珠菌(C.tropicalis)、近平滑念珠菌(C.parapsilosis),以及光滑念珠菌(C.glabrata)。
具有共生和致病双重特性
白色念珠菌是一种具有共生和致病双重特性,最广为人知的是作为肠道、口腔粘膜、阴道和血液的条件致病菌。它是每年数百万阴道和口腔感染病例的原因,当感染免疫低下的宿主时,导致显著的死亡率。
经历肠道诱导的转变更适合营养吸收
白色念珠菌当暴露于哺乳动物肠道时,会经历“胃肠诱导的转变”,这被认为部分是由于WOR1转录因子,导致更适合短链脂肪酸(SCFA)和N-乙酰氨基葡萄糖营养吸收的表型变化。
白色念珠菌的形态转变机制尚未完全了解,初步研究认为宿主上皮细胞在其中起调节作用。
马拉色菌
马拉色菌属主要以皮肤的定植者和病原体而闻名,也是肠道内第二普遍的真菌种类。其中,M.globosa、M.restricta、M.sympodalis和M.pachydermatis是肠道中最普遍的物种。
马拉色菌经常定植于富含皮脂的区域
几乎所有种类的马拉色菌属不合成脂肪酸,而是依赖外部来源的脂质,这解释了它们在人类皮肤富含皮脂的区域增殖。
在肠道内,脂质可从胆汁盐中获得,胆汁盐由胆汁酸通过肝细胞合成。人们对马拉色菌如何在人类肠道中定植仍然知之甚少,相互竞争的假设包括从人体皮肤间接暴露或由于婴儿期摄入母乳。
在炎症性肠病患者中更多,并可能导致黏膜炎
无论机制如何,马拉色菌都是真菌定植的主要参与者,最近的研究表明它与肠道共生有关。然而,在某些情况下,马拉色菌具有致病潜力,会诱发有害的、异常的免疫反应。
在皮肤上,它与脂溢性皮炎和花斑癣的发病机理有关。与肠道相比,马拉色菌在胰腺导管腺癌组织中的相对丰度更高,通过刺激模式识别受体甘露糖结合凝集素(MBL)与肿瘤发生有关。与健康对照者相比,在炎症性肠病患者中发现的马拉色菌相对比例更高,并且被认为会导致粘膜炎。
酵母菌
酵母菌被认为是人类肠道的非常驻真菌,通常是短暂的定植者和饮食习惯的结果。其中最主要的物种是酿酒酵母。它有助于面包发酵、啤酒酿造,可用作食品添加剂。它在肠道微生物组稳态中的作用经常被忽视。
有助于减轻胃肠道疾病引起的腹泻
最近的研究表明,酵母菌确实可以在肠道中茁壮成长,代谢被称为粘蛋白的高度糖基化蛋白质。布拉氏酵母菌(S.cerevisiae var. boulardii),为酿酒酵母变种,是一种众所周知的益生菌酵母物种,已知有助于解决各种胃肠道疾病,包括旅行者腹泻和抗生素相关性腹泻。研究表明克罗恩病(CD)患者的结肠通透性降低之后,使用布拉氏酵母菌有助于治疗CD。
胃肠道承载着一系列微生物,它们共同形成复杂而动态的生态系统。最近,人们开始关注细菌-真菌的相互作用,因为它们与疾病有关。
细菌-真菌存在互惠共生和竞争
细菌-真菌相互作用可能是互利的,然而,建立特定生态位或营养的竞争可能导致细菌和真菌的失衡。有各种各样的机制参与细菌-真菌的相互作用和拮抗作用。
一项研究表明,纤维发酵过程中细菌产生的短链脂肪酸本身具有抗真菌的特性。另一项研究发现细菌细胞壁合成过程中分泌的肽聚糖片段直接结合并灭活白色念珠菌,阻止其从出芽酵母转变为细长的菌丝。
稳定的肠道细菌群有助于抵抗病原真菌
一个稳定多样的肠道细菌群落调节其真菌对应物。在肠道炎症或长期使用抗生素期间,肠道中的细菌数量减少,使其容易受到侵袭性真菌物种的影响。这在一项涉及用万古霉素治疗的小鼠研究中得到强调,该研究显示在没有细菌种类的情况下存在播散性白色念珠菌感染。因此,病原真菌不仅受宿主免疫的调节,还受各种共生细菌的调节。
真菌和细菌相互作用以优化它们的微环境。肠道微生物产生一种称为生物膜的细胞外基质,以防止抗菌因子。体外研究表明,热带念珠菌(C.tropicalis)、大肠杆菌(E.coli)和粘质沙雷氏菌(Serratia marcescens)共生作用,形成比它们单独产生的能力要厚得多的生物膜。
扫描电子显微镜揭示了这三种生物体之间的密切相互作用,粘质沙雷氏菌使用菌毛将大肠杆菌和热带念珠菌连接在一起。
众所周知,炎症性肠病(IBD)患者体内的微生物群发生了改变,以往的研究主要集中在细菌的相对失衡上。IBD患者的细菌生物多样性降低,来自厚壁菌门的细菌相对减少,来自变形杆菌门的细菌相对增加。
炎症性肠病患者的真菌群落主要由子囊菌门和担子菌门的真菌组成,最常见的属包括酵母属、德巴利酵母(Debaryomyces)、青霉属、曲霉属,以及念珠菌属。
☆ 不同IBD表型真菌群落存在差异
炎症性肠病涉及疾病表型的异质性集合。疾病的表型和炎症的程度与独特的菌群特征有关。在克罗恩病(CD)中,与仅发生在结肠的疾病相比,霉菌种群因累及回肠的疾病而异。特别是,保留回肠的CD显示出较高的念珠菌和德巴利酵母菌,而曲霉菌属(Aspergillus)和毕赤酵母菌(Pichia)在回肠受累的CD中的丰度较高。
在疾病发作期间,与对照组相比,担子菌门与子囊菌门的比率增加。在物种水平上,处于活动发作期的克罗恩病患者显示出念珠菌属、Gibberella moniliformis、Alternaria brassicicola和新型隐球菌(Cryptococcus neoformans)的相对丰度更高。
当根据疾病程度分类时,菌群组成的变化在溃疡性结肠炎(UC)中最为突出。直肠炎患者的青霉菌相对丰度最高,随着疾病程度向近端进展呈负相关。与直肠炎患者相比,毕赤酵母菌(Pichia)在左侧结肠炎患者中的比例过高。
☆ 白色念珠菌增加,导致促炎细胞因子释放
随着与炎症性肠病发作相关的独特微生物组特征得到进一步验证,真菌致病因子在促炎状态中的作用逐渐被认可。
与健康对照相比,炎症性肠病(IBD)患者肠道中白色念珠菌的丰度增加。在菌丝形式中,白色念珠菌上调内皮转化酶1(ECE1)基因,导致ECE1蛋白的丰度更高。这种蛋白质经过蛋白水解加工以释放其活性形式,称为念珠菌溶血素。
念珠菌溶血素是一种31个氨基酸的溶细胞肽,以破坏上皮细胞质膜和刺激编码促炎细胞因子的转录因子而闻名。念珠菌溶血素还损害巨噬细胞的功能,对其抗真菌能力产生负面影响。与健康对照相比,一组克罗恩病患者表现出对念珠菌溶血素特异性的IgA介导的反应水平较低。这表明炎症性肠病患者的高免疫原性真菌病原体没有得到充分控制,并可能导致其促炎状态。
☆ 可作为炎症的替代标志物
作为炎症性肠病中真菌分析的副产品,某些物种已被确定为炎症的替代标志物。与同一克罗恩病(CD)患者体内的发炎组织相比,发现酿酒酵母在非发炎组织中的相对丰度更高。活跃发作的克罗恩病患者表现出更高水平的抗酿酒酵母抗体(ASCA)。
抗酿酒酵母抗体(ASCA)也被用于疾病预测,与对照组相比,在后来诊断为CD的患者中发现的ASCA 水平更高。此外,ASCA已被推断为疾病严重程度的预测指标,与ASCA IgG阴性的CD患者相比,ASCA IgG阳性患者的手术干预率更高。
对患有克罗恩病患者进行定期筛查抗酿酒酵母抗体(ASCA)尚未渗透到临床医学的常规实践中,但它作为一种辅助的、无创的疾病活动和严重程度的衡量方法继续显示出前景。
肠道真菌通过先天和适应性免疫系统影响宿主免疫,这是由真菌细胞壁成分和肠道免疫细胞的模式识别受体(PRR)之间的相互作用引发的。
真菌激活先天免疫和适应性免疫
真菌的吞噬作用导致各种免疫反应的激活,以努力控制真菌的定居。当这些调节机制功能障碍或缺失时,真菌定植不受抑制,导致肠道微生物结构紊乱和肠道炎症。
通过几个检查点,先天和适应性免疫系统可以区分共生真菌或致病真菌。鉴于白色念珠菌可作为共生因子或致病因子,通常用于免疫学分析,以帮助区分这些不同的免疫反应。蛋白质相关分子模式(PAMPs)白色念珠菌和其他真菌与肠道单核吞噬细胞(MNPs)上的toll样受体(TLRs)、C型凝集素受体(CLRs)和NOD样受体(NLRs)相互作用。
例如,巨噬细胞甘露糖受体1(MMR)、树突细胞特异性ICAM3抓取非整合素(DC-SIGN)和巨噬细胞诱导型C-型凝集素(MINCLE)识别某些真菌细胞壁上富含甘露糖的结构。常见的MNPs C型凝集素受体包括dectin-1和dectin-2。dectin-1与真菌β-葡聚糖结合后刺激构象变化,暴露其尾部的免疫受体基于酪氨酸的激活基序(ITAM),随后被SRC家族激酶磷酸化。这一过程使得磷酸化的ITAMs能够与脾酪氨酸激酶(Syk)的SH2结构域结合,激活含有胱天蛋白酶募集结构域的CARD9,并引导Th-17细胞的诱导,动员中性粒细胞进入肠道。
共生和致病形态分别通过不同的免疫途径影响肠道炎症
dectin-1与白色念珠菌或曲霉菌上的β-葡聚糖结合,促进生物活性IL-1β从非活性形式pro-IL-1β通过非经典caspase-8炎性小体激活。重要的是,caspase-8炎性小体的激活不依赖于真菌物质的内化。因此,dectin-1能够在识别外部真菌细胞壁成分后,通过激活IL-1β产生快速有效的反应。IL-1β是IL-1家族的一员,以诱导全身炎症而闻名,同时也能防御外来抗原。作为对真菌识别的反应,IL-1β刺激辅助性T细胞,动员中性粒细胞,并增强吞噬作用,以改善肠道中真菌病原体的清除。
当白色念珠菌处于共生酵母形态时,其负责炎症小体和IL-17通路的PAMPs被隐藏。当它转变为致病菌丝形式时,炎症小体通路和IL-17信号通路被激活。特别是,TLR会分泌细胞因子,如IL-1β、IL-23和IL-6,促进CD4+ T细胞激活进入Th17谱系。Th17细胞则分泌IL-17,招募巨噬细胞、中性粒细胞和抗菌肽,产生有效的抗真菌反应。因此,致病真菌上的PAMPs与宿主树突状细胞上的PRR之间的独特相互作用决定了炎症反应。
共生真菌通过训练免疫系统增加对病原体的抵抗
真菌群在宿主免疫中发挥重要作用。参与真菌识别的巨噬细胞和单核细胞在接触共生真菌(如酿酒酵母)后会获得训练,进一步接触细菌或真菌时,TNF-α和IL-6的产生会增加。
真菌共生菌直接参与稳定肠道稳态,白色念珠菌能够在宿主应激时脱落其致病菌株,保护宿主免受细菌和真菌病原体的侵害。
此外,真菌共生对结肠炎相关的致癌作用也有保护作用。与野生型小鼠相比,真菌耗尽的小鼠在施用氧化偶氮甲烷-葡聚糖硫酸钠(AOM/DSS)后结肠肿瘤发生率更高,而补充外源性IL-18则显著降低肿瘤发生率。因此,真菌共生通过炎症小体途径在预防结肠炎及其相关癌症中发挥重要作用。
鉴于肠道微生物组的广泛多样性及其对人类健康的独特、多模式影响,优化肠道微生物组以改善健康的机制已成为许多新兴研究的焦点。饮食不仅是胃肠道内许多微生物成分的载体,也是其主要营养来源。因此,饮食调节可以通过微生物群组成和功能的变化间接传播起到促炎或抗炎作用。
例如,以植物为基础的饮食与肠道细菌向更具抗炎性的转变有关,其特征是更高的普拉梭菌(Faecalibacterium prausnitzii),直肠真杆菌(E.rectale)和两形真杆菌(Eubacterium biforme),均为丁酸盐生产者。
注:丁酸盐对人体健康的重要性已经在谷禾之前的多篇文章中有过具体讲述。
相反,以肉类为基础的饮食与更易引发炎症的特征相关,这些特征包括活泼瘤胃球菌属(Ruminococcus gnavus)和柯林斯氏菌物种(Collinsella species)的增加。
然而迄今为止,大多数饮食微生物组研究关注点主要集中在细菌种群的组成和功能变化上。鉴于真菌群落在肠道健康中的重要性,有必要进一步研究饮食调节对这一重要群落的影响。这一更广阔的视角会增强我们对饮食如何针对微生物群的所有关键成员的理解,为它们对肠道健康和疾病的影响提供更全面的见解。
可消化的碳水化合物,如单糖、二糖和淀粉多糖,在被身体消化分解为能量并吸收。相比之下,大多数不易消化的碳水化合物或纤维与胃肠道微生物群相互作用,主要在结肠中进行发酵。这个发酵过程产生气体、短链脂肪酸和其他代谢物。
• 念珠菌与近期摄入的碳水化合物呈正相关
研究表明念珠菌与最近的碳水化合物摄入呈正相关。此外,发现高果糖、葡萄糖、麦芽糖和蔗糖的摄入增加了内皮细胞的粘附假丝酵母物种(白色念珠菌,热带念珠菌,以及克柔念珠菌)到上皮细胞。此外,减少饮食中的单糖和淀粉已被证明可以减少肠道中念珠菌的慢性过度生长。
• 高碳水化合物饮食的真菌变化
观察到,与健康的日本人相比,健康的印度成年人的粪便微生物群中含有更高比例的念珠菌和普雷沃氏菌,这可能是由于印度成年人对膳食植物多糖的摄入量较高。
高碳水化合物饮食增加了五个真菌属:
Pleurotus ↑↑↑
Kazachstania ↑↑↑
Auricularia ↑↑↑
Paraphaeosphaeria ↑↑↑
Ustilaginaceae ↑↑↑
并降低了布氏白粉菌属(Blumeria)。
相反,低碳水化合物饮食导致了肠道真菌群落的显著变化,减少了:
Blumeria ↓↓↓
Agaricomycetes ↓↓↓
Malassezia ↓↓↓
Rhizopus ↓↓↓
Penicillium ↓↓↓
增加了Ustilaginaceae。
一些真菌群也可以产生短链脂肪酸,并呈正相关
多项研究表明念珠菌有助于将复杂的碳水化合物发酵成单糖,单糖是其他微生物的能量来源。对猪的研究发现,饮食中碳水化合物含量的差异与不同的真菌种群和短链脂肪酸(SCFA)产量有关。具体来说,低碳水化合物饮食的猪具有较低水平的乙酸盐、丁酸盐和总短链脂肪酸,一些真菌属与这些短链脂肪酸正相关,包括Tomentella,Metschnikowia和Loreleia。
人类研究中膳食碳水化合物调节对肠道真菌的影响


Buttar J,et al.Gut Microbes.2024
因此,膳食碳水化合物的摄入可能会影响肠道真菌种群及其代谢活动,未来的研究应侧重于阐明不同碳水化合物影响真菌群落的确切机制。
肠道微生物群高度参与蛋白水解发酵,产生短链脂肪酸、支链脂肪酸(BCFA)、气体和有害的腐败代谢物,如氨、胺和硫化氢。
• 真菌对氨基酸的高利用率提高其在肠道中的存活率
一项体外研究发现,氨基酸利用率与真菌生长呈正相关。氨基酸可以作为白色念珠菌的碳源,因为这种真菌物种产生蛋白酶并具有寡肽转运蛋白,使白色念珠菌能够通过代谢途径调节适应不同的环境。
在另一项研究中,发现酿酒酵母(S.cerevisiae)和无冠构巢曲霉(Aspergillus nidulans)使用转运蛋白,如氨基酸-多胺-有机阳离子(APC)超家族和主要促进剂超家族(MFS)来利用氨基酸,这可以提高真菌在肠道中的存活率。
• 高蛋白饮食与念珠菌丰度呈负相关,与酵母菌呈正相关
很少有研究评估富含蛋白质的饮食对人类的影响。研究了影响肠道真菌群落稳态的因素,发现乳制品消费是一种高蛋白食物来源,与念珠菌呈负相关,与酵母菌呈正相关。
膳食脂肪主要在小肠中被消化和吸收,并在小肠中代谢,为身体提供能量和各种脂肪酸。一项人类研究表明,脂肪会影响肠道真菌群落。具体来说,证明了念珠菌与总饱和脂肪消耗量呈负相关。
• 脂肪酸可能抑制真菌的生长
体外研究表明,不同真菌物种将脂肪酸和脂肪醇代谢为碳源和能源的效率差异很大。脂肪酸可以抑制真菌的生长。在专注于食品防腐的研究中,发现饱和脂肪酸、不饱和脂肪酸和氧化脂质具有抗真菌特性。
由于缺乏研究调查脂肪对人类肠道真菌群落的影响,这些饮食成分对肠道真菌群落的影响仍然不清楚。然而,在一项小鼠研究中,与喂食标准食物的小鼠相比,喂食高脂肪饮食的小鼠几种真菌类群有所增加,包括Alternaria, Saccharomyces, Septoriella和Tilletiopsis。
动物模型中饮食调节对肠道菌群的影响

Buttar J,et al.Gut Microbes.2024
虽然膳食脂肪对能量代谢至关重要,但它们对肠道真菌群落的影响还不太清楚。未来的研究还需要深入研究膳食脂肪在塑造肠道真菌群落中的作用。
已经发现某些饮食习惯和模式显著影响肠道真菌群落的组成。城市化和饮食习惯的变化会导致中国不同地区人群真菌组成的差异。

这项研究确定了食用酪乳和蓝莓茶与Tetrapissipora blattae、Sugiyamaella lignohabitans、Kazachstania naganishii等的存在之间的相关性。
此外,红茶和猪肉的消费与镰刀真菌属(Fusarium spp.)的四个物种的组成有关。
在另一项研究中,发现杏仁和开心果的摄入与念珠菌和青霉菌属呈负相关。此外,对动物性饮食和植物性饮食进行了比较分析,结果显示动物性饮食组中Neosartorya fischeri(一种源自青霉属的真菌)的丰度更高。
• 素食者体内易出现食源性真菌
研究表明,超过60%的素食者粪便样本中存在食源性真菌,如青霉菌和曲霉菌,以及潜在的致病真菌,如镰刀菌和马拉色菌,但这些真菌类群在食用西方饮食的个体中很少发现。小鼠研究进一步支持饮食调节对真菌群落特征的影响。与标准食物相比,喂食加工饮食的小鼠的总体真菌多样性降低。
• 酵母菌可能随饮食来源进入体内
另一个值得注意的方面是我们的食品中普遍存在常见的肠道真菌,例如酿酒酵母(S.cerevisiae)和汉斯德巴氏酵母菌(Debaryomyces Hansenii)。这些真菌常见于乳制品、面包、果皮(包括葡萄)、普洱茶和奶酪中,因此很难确定这些真菌物种是真的存在于肠道中,还是在自然界中更短暂。
研究发现,食用不含酿酒酵母的饮食导致酿酒酵母水平从基线时的86%大幅降低到无酿酒酵母饮食2天后ITS读数的 0.1%。这表明酿酒酵母的丰度高度依赖于这种真菌物种的饮食来源。
因此,探索特定真菌物种对疾病潜在影响的研究应考虑食物来源的真菌分类群的潜在短暂性。这种考虑很重要,因为它可能会影响这些物种在健康和疾病中的重要性。
• 利于真菌群落稳态和健康的饮食
最近的营养学研究利用Mycobiome 饮食来选择性地改变肠道中真菌的组成。Mycobiome 饮食的特点是消耗瘦肉或植物蛋白、单不饱和脂肪或多不饱和脂肪、富含纤维和抗性淀粉的食物,同时避免加工的高糖食物。
遵循Mycobiome饮食28天导致念珠菌的丰度下降了72.4%,尤其是白色念珠菌和热带念珠菌。此外,Mycobiome饮食增加了一些有益真菌物种的浓度,包括Pichia kluyveri和Galactomyces geotrichum。
这种饮食除了对肠道菌群的有益影响外,还使小肠细菌过度生长患者的细菌过度生长减少,并改善了所有参与者的疲劳、睡眠、腹胀、便秘和腹泻。
尽管研究表明,真菌群落随着饮食而变化,但我们对饮食对这些微生物功能潜在影响的了解仍然有限。据了解,细菌和真菌群落都产生代谢物,这些代谢物不仅形成它们自己的群体,而且对其他群落成员和各种宿主细胞群体施加影响。
作为对高纤维饮食的响应,肠道细菌上调功能途径和酶,使纤维发酵产生短链脂肪酸,特别是丁酸。
真菌作为真核生物,表现出与细菌等原核生物不同的代谢特征。真菌具有发酵植物细胞壁的代谢途径和酶,一些真菌种类在食品工业中用于乙醇生产,并通过发酵果胶、纤维素和木质素等纤维产生乳酸和气体。
真菌在降解纤维素纤维方面优于细菌。真菌产生更多的甲烷、乙酸盐和甲酸盐,而细菌产生更多的丁酸盐和丙酸盐。
重要的是要考虑代谢物在调节肠道细菌和真菌之间的作用。代谢物,如胆汁酸,可以影响微生物的相互作用,因为真菌有能力通过胆汁酸的转化对细菌的生存力产生不利影响。
!
小贴士
饮食对改变真菌群落组成的影响可能不直接归因于饮食成分对肠道真菌的影响。相反,这些影响可能是间接的,源于肠道细菌的调节,进而影响真菌的组成。
由于阐明饮食如何调节肠道真菌群落背后的机制的证据有限,有必要进行进一步的研究来辨别饮食对肠道真菌群落的直接和间接影响。
肠道微生物组是一个复杂而独特的实体,能对环境、饮食和疾病的变化做出反应。它充满了来自各个种群的微生物,通过复杂而动态的关系相互作用。虽然细菌是微生物组稳态中最重要的部分,但真菌在其中也起着不容忽视的作用,参与机会性病原体的调节和原本无法获得的营养物质的发酵。
菌群结构的改变与菌群失调有关,菌群失调是一种与包括炎症性肠病(IBD)在内的各种慢性疾病有关的发炎免疫状态。菌群概况因IBD表型和严重程度而异,菌群标志物有望作为疾病进展的指标。
还需研究饮食对非细菌微生物群的调节作用,以及参与真菌发酵和膳食成分利用的代谢途径和酶的机制。深入了解饮食如何影响肠道菌群的组成和功能至关重要。这些知识将帮助确定饮食疗法是否应该专门针对肠道真菌,从而可能减轻炎症并改善炎症性肠病患者的预后。
主要参考文献
Buttar J, Kon E, Lee A, Kaur G, Lunken G. Effect of diet on the gut mycobiome and potential implications in inflammatory bowel disease. Gut Microbes. 2024 Jan-Dec;16(1):2399360.
Rinninella E, Raoul P, Cintoni M, Franceschi F, Miggiano GAD, Gasbarrini A, Mele MC. What is the healthy gut microbiota composition? A changing ecosystem across age, environment, diet, and diseases. Microorganisms. 2019. Jan 10;7(1):14.
Liang G, Cobián-Güemes AG, Albenberg L, Bushman F. The gut virome in inflammatory bowel diseases. Curr Opin Virol. 2021. Dec;51:190–198.
Nacer S, Haddad F, Tahiri M, Hliwa W, Badre W, Choukri EM, Jai SR, Erguibi D, Boufettal R, Chehab F. P51 predictive factors of surgery in crohn’s disease. Gut. 2022.
Wang R, Li Z, Liu S, Zhang D. Global, regional and national burden of inflammatory bowel disease in 204 countries and territories from 1990 to 2019: a systematic analysis based on the global burden of disease study 2019. BMJ Open. 2023. Mar. 13(3):e065186.
Sigall-Boneh R, Levine A, Lomer M, Wierdsma N, Allan P, Fiorino G, Gatti S, Jonkers D, Kierkuś J, Katsanos KH, et al. Research gaps in diet and nutrition in inflammatory bowel disease. A topical review by D-ECCO working group [dietitians of ECCO]. J Crohns Colitis. 2017.
Raimondi S, Amaretti A, Gozzoli C, Simone M, Righini L, Candeliere F, Brun P, Ardizzoni A, Colombari B, Paulone S, et al. Longitudinal survey of fungi in the human gut: ITS profiling, phenotyping, and colonization. Front Microbiol. 2019. Jul 10;10:1575.
Dalle F, Wächtler B, L’Ollivier C, Holland G, Bannert N, Wilson D, Labruère C, Bonnin A, Hube B. Cellular interactions of Candida albicans with human oral epithelial cells and enterocytes. Cell Microbiol;2010;12(2):248–271. doi: 10.1111/j.1462-5822.2009.01394.x.