-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康

随着高通量多组学技术的快速创新推动,微生物群,尤其是肠道菌群失调已被明确与许多人类疾病有关,包括 2 型糖尿病和炎症性肠病。
多组学数据的综合分析,包括宏基因组学和代谢组学以及宿主指标的检测和细菌物种的分类,已经确定了许多与疾病相关的细菌和细菌产物。然而,深入了解微生物影响肠道健康的机制需要从关联拓展到因果关系。
目前对肠道微生物群对疾病因果关系的贡献的理解仍然有限,这主要是由于微生物群落结构的异质性、疾病进化的个体差异以及对将微生物群衍生信号整合到宿主信号通路中的机制的不完全理解。
最近,德国慕尼黑工业大学从事肠道菌群和营养研究的Haller 教授团队在《Nature reviews gastroenterology & hepatology》 (自然评论胃肠病学和肝病学)发表评论文章,系统讨论了目前已知的炎症和代谢紊乱相关微生物组的特征和认知,并讨论提高对其作用机制理解的困难所在。
在这里我们将文章整理与大家分享。


关键信息
1、肠道菌群组成的改变和细菌衍生代谢物经宿主加工后的变化与 IBD 和 T2DM 相关,并提供了共同的潜在致病机制。
2、益生菌与 IBD 或 T2DM 之间的因果关系已通过无菌小鼠实验和综合多组学研究明确。
3、对于疾病特异性生物标志物发现的挑战,包括确定观察到的变化的因果关系,了解它们在疾病机制中的功能以及肠道微生物群的地理和种族差异。
4、特定细菌菌株、其编码基因和代谢副产物的大数据细化、测试和验证对于识别疾病生物标志物是必要的。
文章内容
人体消化道含有一系列复杂的微生物,包括细菌、古细菌、病毒和真菌。由于消化道及其微生物组被认为位于免疫和代谢过程的交叉点,本文重点关注炎症性肠病 (IBD) 和 2 型糖尿病 (T2DM) 作为微生物群相关疾病的范例。
IBD 和 T2DM 都被认为是多因素疾病,随着工业化的进展其发病率在全球范围内呈上升趋势。病因涉及遗传易感性、环境诱因和城市生活方式相关因素的复杂相互作用。
在这种共同的背景下,代谢疾病(如 T2DM)的另外特征是肝脏、脂肪组织、肌肉、胰腺和肠道的慢性亚临床炎症,而炎症性胃肠道疾病,如克罗恩病(CD)和溃疡性结肠炎(UC) ,也与炎症驱动的代谢改变有关。
环境触发因素的重要性(肠道菌群)
全基因组关联研究已经确定了大量的遗传变异与 T2DM (143 位点) 或 IBD (>240 位点)的易感性增加相关。然而,这些变异共同解释了这些疾病的一小部分遗传性:T2DM < 10 %,UC < 15 % 和 CD < 50 % 。这种情况表明环境触发因素的重要性,特别是肠道微生物组,作为这些疾病病因的主要贡献者。对大型人群研究和 IBD 或 T2DM 患者队列的多项分析已经确定了与特定疾病表型、复发风险和治疗反应相关的微生物组特征。
IBD 和 T2DM 都与特征性微生物改变有关,特别是随着有益微生物的减少和病原菌的增加而降低群落多样性。尽管它们的病理学不同,IBD 和 T2DM 有几个共同的机制特征。T2DM 的代谢特征伴随着慢性低度炎症和肠道屏障的破坏,IBD 患者的复发性炎症发作与细胞和全身水平的代谢改变共同发生。
这些复杂疾病的治疗仍然具有挑战性,但粪便微生物群移植(FMT) 的对照试验已显示出对T2DM和IBD的临床疗效,包括UC以及较轻的 CD。
FMT对炎症、免疫和代谢疾病有效果但存在差异
FMT 的临床试验还提供了肠道菌群与其他炎症、免疫或代谢疾病之间存在因果关系的证据。例如,FMT 在治疗大约 90% 的艰难梭菌(以前的艰难梭菌)感染患者方面非常有效并已被评估为治疗肥胖和移植物抗宿主病。
在四项随机临床试验中,FMT 在 28% 的 UC 患者中诱导了临床缓解。但很少有临床试验检查过 FMT 在 CD 患者中的疗效,而且结果相当不同。
在一项对 174 名接受 FMT 治疗的 CD 患者进行的研究中,20% 的患者获得了临床缓解,总体而言,43% 的患者获得了临床缓解。
一项单独的随机对照试验发现 FMT 对 CD 患者的临床缓解率没有影响,但供体微生物群的植入增加与维持缓解有关。相反(尽管大量研究表明,特定的菌群失调或特定的微生物群谱与代谢紊乱有关),FMT 对代谢性疾病患者有益的证据尚不明确。具有里程碑意义的研究表明,从较瘦、健康的捐赠者那里接受 FMT 的代谢综合征患者的代谢改善以及肠道微生物组的有益变化。然而,这些影响是不一致和短暂的,这可以通过供体微生物群的有限移植或基线时供体粪便微生物多样性的变化来解释。
有趣的是,口服 FMT 后补充低发酵性纤维可改善肥胖和代谢综合征患者的胰岛素敏感性、增加微生物多样性,并延长供体微生物定植。这些数据强调了微生物调节疗法在逆转代谢功能障碍中的价值。
与这些发现一致,来自代谢受损的肥胖供体的 FMT 会暂时恶化代谢综合征受体的胰岛素敏感性,而胃旁路术后健康供体的 FMT 会导致代谢综合征受体的胰岛素敏感性略有增加。
几项大型队列研究(表 1、表2)通过分析 IBD 患者的肠腔和黏膜微生物群落,研究了肠道微生物群的改变。
总体而言,活跃期IBD 与某些菌群的数量过多有关,如:
肠杆菌科Enterobacteriaceae
梭杆菌属Fusobacterium
咽峡炎链球菌Streptococcus anginosus
肠球菌Enterococcus
巨球菌Megasphaera
弯曲杆菌Campylobacter
Gammaproteobacteria
Deltaproteobacteria
相反,IBD 与有益菌群的缺失有关,例如:
Faecalibacterium prausnitzii
Christensenellaceae
Collinsella
Roseburia
Ruminococcus
其他产丁酸盐的细菌
在我们检测的炎症性肠病的菌群报告中也发现,炎症性肠病风险高的人群中,炎症水平很高,肠杆菌科Enterobacteriaceae,梭杆菌属Ruminococcus gnavus偏高,而Faecalibacterium prausnitzii和Roseburia丰度普遍降低或者缺乏。


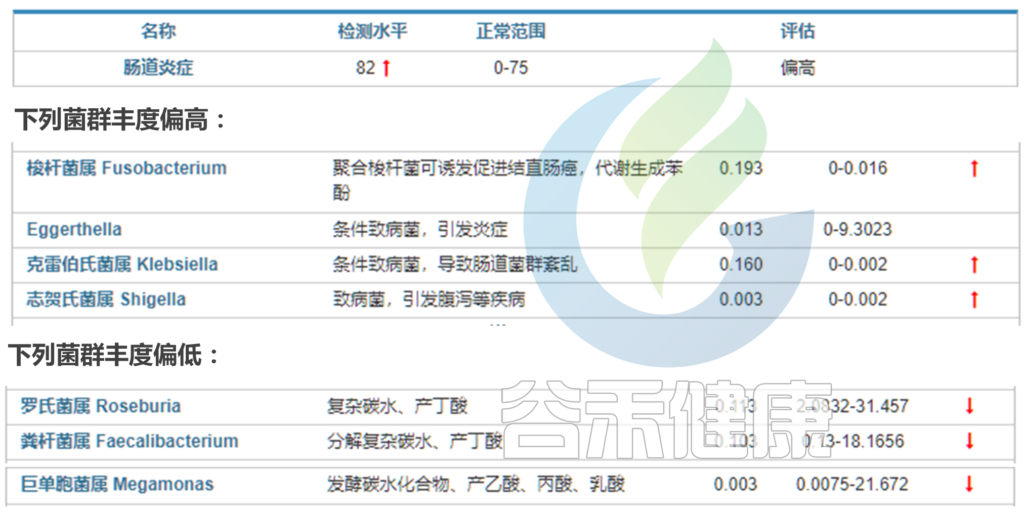
< 选自:谷禾肠道菌群健康检测报告 >
菌群代谢功能
粪便样本的宏基因组学为 IBD 中发生的功能失调和代谢途径的扰动提供了更全面的观点。这些研究表明,参与含硫氨基酸合成、核黄素代谢、谷胱甘肽转运蛋白、氧化应激和营养转运的代谢途径均被上调。
一项能够将微生物群落分解到物种内单个菌株水平的研究显示,与健康对照相比,IBD 或肠易激综合征 (IBS) 患者粪便样本中致病菌的菌株多样性增加,而有益微生物的菌株多样性降低。深入分析表明,219个类群(包括152种)与CD相关,102个类群(包括93种)与UC相关。
CD的主要特征是属于毛螺菌科和瘤胃球菌科的分类群减少和属于肠杆菌科的分类群增加,而对于UC观察到属于拟杆菌科的分类群减少和属于毛螺菌科的分类群增加。与这种异质性一致,在不同的 IBD 研究中仅存在少数物种的共同变化,这表明尽管疾病表型和病程相似,但在 CD 患者群体中仍存在个体间差异。
IBD和肠道菌群的因果关系探究
肠道微生物群在 IBD 中的致病作用的首批临床证据之一源于实验表明,从 CD 患者的小肠发炎段转移粪便流可改善疾病症状。粪便流的恢复和新末端回肠术后暴露于肠腔内容物会诱发炎症,这表明肠道微生物群会引发 CD的术后复发。此外,抗生素治疗对活动性 CD 患者亚群的疗效强调了肠道细菌和 IBD 之间的因果关系。
急性和慢性肠道炎症小鼠模型的机制研究为微生物失调与 IBD 之间因果关系的提供了进一步证据。例如,将IBD 患者的菌群移植到无菌受体小鼠,会将IBD 表型转移到无菌小鼠中。而具有 IBD 遗传易感性的小鼠在无菌条件下不会发生自发性炎症。
免疫响应
IBD 发病的遗传易感小鼠的失调菌群,能够将这种疾病症状转移到无菌受体小鼠。将 IBD 微生物群转移到无菌的野生型小鼠体内会导致肠道 T 细胞反应失衡,肠道 T 辅助 17 (TH17) 细胞和 TH2 细胞数量增加,RORγt +数量减少。同样,肠道微生物群的人类共生细菌脆弱拟杆菌对无菌小鼠的定植诱导CD4 + T 细胞转化为产生IL-10的FOXP3 + T reg细胞,这表明微生物群驱动的存在IBD 的发病机制。
在 T2DM 中也发现了几种细菌类群的丰度变化很大。
例如,据报道,2型糖尿病患者中下列菌相对丰度增加:
大肠杆菌E. coli、
韦荣氏菌属Veillonella、
布劳氏菌属Blautia、
厌氧菌属Anaerostipes、
乳杆菌属Lactobacillus、
粪杆菌属Faecalibacterium、
梭状芽胞杆菌属Clostridiales(等)
相反,下列菌丰度降低:
拟杆菌属Bacteroides
双歧杆菌属Bifidobacterium、
副拟杆菌属Parabacteroides、
颤螺菌属Oscillospira
可降解粘蛋白的阿克曼菌Akkermansia muciniphila
2019 年发表的一项宏基因组和宏蛋白质组学研究分析了来自 254 名中国个体的粪便样本中的肠道微生物群组成和功能,其中包括 77 名未接受治疗的 T2DM 患者、80 名糖尿病前期患者和 97 名葡萄糖耐量正常的对照个体。与代谢健康的对照组相比,T2DM 患者和前驱糖尿病患者的梭菌目Clostridiales细菌丰度较低,而埃氏巨球形菌Megasphaera elsdenii的丰度较高。
菌群代谢功能
在 T2DM 患者和糖尿病前期患者的微生物组中观察到功能差异。与对照个体相比,糖尿病前期个体的肠道微生物群显示出与糖磷酸转移酶系统、细菌分泌系统和氨基酸的 ATP 结合盒 (ABC) 转运蛋白有关的途径富集。这些发现表明,在糖尿病前期患者转变为 T2DM 之前,可以检测到肠道微生物组的疾病特异性变化。
环境因素影响
细菌种类和代谢基因簇谱的差异已被用于确定一组具有正常葡萄糖耐量或 T2DM 的个体的糖尿病状态。然而,包括地理位置、种族、健康状况和用药史在内的混杂因素导致在识别与 T2DM 相关的微生物变化方面不同研究存在不一致。
因果关系研究
几项研究提供了肠道微生物群特定成员与 T2DM 发病机制之间因果关系的证据。例如,A. muciniphila属于在人类和小鼠研究中显示对代谢紊乱具有保护作用的分类群。有趣的是,补充益生元使A. muciniphila的丰度正常化并改善了人类的代谢健康。同样,对喂食高脂肪饮食的小鼠施用A. muciniphila可逆转其增加的脂肪量、代谢性内毒素血症、脂肪组织炎症和胰岛素抵抗。
此外,产生丁酸盐的细菌Anaerobutyricum soehngenii(以前称为Eubacterium hallii菌株 L2-7)显示出丰度增加,这与来自瘦供体的FMT受体的外周胰岛素敏感性改善相关。
对T2DM 患者A. soehngenii菌水平进行管理,在治疗 4 周后改善了外周胰岛素敏感性,这些益处伴随着微生物群组成的改变和胆汁酸代谢的变化。
奇怪的是,特定的细菌分类群在 IBD 和 T2DM 中表现出相似的变化,这表明免疫介导和代谢疾病的共同特征导致微生物群的相似适应。
下列菌丰度下降:
梭状芽孢杆菌属 Clostridium spp.
粪杆菌属 Faecalibacterium
瘤胃球菌属 Ruminococcus
阿克曼氏菌属 Akkermansia
柯林斯氏菌属 Collinsella
罗斯氏菌属 Roseburia
下列菌丰度增加:
肠杆菌科 Enterobacteriaceae
大肠杆菌 E. coli
具核梭杆菌 Fusobacterium nucleatum spp.
这为定义疾病特异性标志物提出了挑战(下图)


Metwaly et al.,Nat Rev Gastroenterol Hepatol. 2022.
例如,一项针对 2,045 名 IBD 患者的研究的作者确定了 8 个分类群的特征,包括克里斯滕森菌科Christensenellaceae和梭杆菌属Fusobacterium的未知成员,它们可以区分 CD 患者和健康个体。
然而,Christensenellaceae 的丰度增加与低 BMI 和体重减轻有关,这是一种在 IBD 患者中经常观察到的分解代谢状况。同样,梭杆菌的富集被认为是转移性结直肠癌患者预后不良的标志。鉴于 IBD 患者患结直肠癌的风险增加,这一提议的微生物组特征可能是一种附带现象,与潜在的疾病机制没有因果关系。
对来自 132 名个体的微生物组、代谢组和转录组数据集的综合网络分析确定了连接关键细菌分类群(即F. prausnitzii 、未分类的Subdoligranulum、Alistipes、大肠杆菌、Roseburia)的某些代谢物(短链脂肪酸、辛酰肉碱和几种脂质)。有趣的是,有和没有 IBD 的研究参与者之间的差异在粪便代谢组中,比在粪便宏基因组、粪便宏转录组或粪便蛋白质组中更明显。
在综合个人组学分析研究 (iPOP) 中,血浆代谢物与来自 106 名个体的纵向样本中的胰岛素抵抗密切相关,这表明宿主代谢组和肠道微生物组之间的相互作用在胰岛素抵抗个体中受到干扰。
许多研究调查了微生物改变作为疾病生物标志物的效用,特别是在 CD 或 UC 患者中。最初试图定义可以作为疾病活动指标的单一细菌分类群。
例如,F. prausnitzii (一种产生丁酸盐的厚壁菌)在 CD患者中被耗尽。CD 患者回肠黏膜活检样本中这种细菌丰度的降低与回肠切除术后内镜下复发风险的增加密切相关。相反,粘附的侵袭性大肠杆菌丰度增加与回肠 CD相关。
然而,由于大多数细菌物种由许多个体菌株组成,这些菌株可以表现出相当大的基因组和蛋白质组变异,因此菌株多样性具有重要的功能,特别是在确定致病性方面。
例如,R. gnavus和大肠杆菌的亚种都与 IBD 的严重程度增加有关。此外, R. gnavus的一个特定亚种表明,来自 IBD 患者的粪便样本中丰度增加含有菌株特异性基因(与改善的细菌定植有关)。这些基因涉及诸如氧化应激反应、细菌粘附、铁获取和宿主粘液利用等功能。同样,不同的脆弱拟杆菌菌株表现出功能差异,导致 IBD 相关小鼠模型中 IgA 诱导水平不同。这些遗传上不同的脆弱拟杆菌菌株在接种到受体小鼠时也表现出不同的致结肠和免疫调节作用。在一项旨在定义用于监测 IBD 患者疾病活动的关键菌群失调的研究中,使用定量 PCR 计算了F. prausnitzii和大肠杆菌的绝对丰度比(也称为 F-E 指数)。F-E 指数的使用提高了 UC 和 IBS 患者与 CD 患者的区分,并有助于区分结直肠癌与其他肠道疾病。然而, F-E 指数无法区分 IBD亚型,这表明单一分类群指标在分类疾病亚型方面的效用有限。
大规模生物标志物分析
基于微生物特征的判别模型
几项研究已经使用机器学习算法来验证横截面和纵向患者队列中复杂的微生物组特征。
例如,2017 年发表的一项研究使用 16S rRNA 微生物群来分析来自大量 IBD 患者和没有 IBD 的对照个体的粪便样本。研究人员使用序列聚类算法根据八种细菌类群的丰度来识别 CD 特异性微生物特征。
此外,另一组研究表明,基线肠道微生物组组成的特征可以预测 IBD 患者在治疗开始后14周对抗整合素治疗的反应。由深度神经网络生成的微生物组特征的受试者工作特征曲线 (AUC) 下面积为 0.87,而基于临床协变量的模型的 AUC 为 0.62。研究小组还评估了微生物组特征作为 IBD 和 T2DM 生物标志物的效用。
在一项研究中,检查了 29 名接受过自体造血干细胞移植的 CD 患者的独特队列中的疾病活动性和对治疗的反应。来自人类供体和人源化小鼠的微生物组和代谢组风险概况的整合将疾病结果的预测模型的性能从 AUC 0.79 提高到 0.96,并确定了与硫代谢相关的疾病相关细菌和代谢物网络。
这些发现听起来很有前景,但重要的是要承认微生物组风险概况是基于来自前瞻性队列研究中的人群或患者组的预测模型,因此比起对于个人的预测结果,对于相似患者组(人群或队列)可能更准确。重要的是记住,预测的风险可能不会直接转化为个体患者,这可能是由于在异质环境中风险概况的普遍性有限。
不忽略混杂变量
另一项研究调查了以德国人群为基础的 1,976 人队列中的代谢健康和肠道微生物群的昼夜节律性。粪便微生物群分析确定了 13 个微生物分类群的风险特征,这些分类群显示 T2DM 患者的昼夜节律性受到破坏。基于这种心律失常风险特征的预测模型成功识别出有患 T2DM 风险的个体,当模型中包含 BMI 时,AUC 为 0.78。
这些例子为微生物组特征在用于诊断和治疗目的的生物标志物发现中的作用提供了证据。然而要注意,生态失调指数不是独立的测量值,需要整合到额外的宿主衍生数据和临床数据中。这些指标的标准化和验证需要大规模究研,包括对潜在生物标志物的纵向评估,并考虑可能的混杂变量,例如饮食、年龄、种族、病史和最后的排便时间,所有这些因素都会影响微生物组的改变。
在寻找疾病生物标志物时,代谢物作为疾病活动的最接近指标,并且与作为疾病机制基础和调节疾病机制的调节信号密切相关。事实上,代谢组和微生物组都随着饮食、环境、衰老和整体健康状况等内源性和外源性因素而波动。
许多研究报告了 IBD或 T2DM患者的肠道代谢物谱的显着变化。
例如,已在 IBD 患者的粪便代谢组中发现中链脂肪酸(如戊酸和己酸水平降低)和 B 族维生素水平降低。相反,据报道,成人和儿童 IBD 患者的粪便和血清中氨基酸、胺和肉碱的含量分别增加。
一项具有里程碑意义的研究结果表明,代谢物分析可以区分 IBD 患者和健康个体。该报告之后有许多其他人一致表明 IBD 患者的代谢物表型与健康个体的不同。有趣的是,代谢物分析还可以区分不同形式的 IBD,例如 CD 和 UC,并且可以进一步将 CD 患者分类为患有回肠或结肠炎症。同样,T2DM 患者的代谢物分析表明代谢途径的活性发生了改变。
在多份报告中,支链和芳香族氨基酸(如亮氨酸、异亮氨酸、缬氨酸、苯丙氨酸、酪氨酸和色氨酸)的血清水平与胰岛素抵抗、肥胖和发生 T2DM的风险相关。
T2DM 患者的代谢物分析还揭示了特定细菌代谢物水平与疾病发作之间的强关联。
例如,色氨酸代谢途径包括几个候选代谢物生物标志物,这些生物标志物由于与人类和小鼠研究中炎症和代谢疾病的发展相关而引起了研究关注。色氨酸是一种从饮食中获得的必需氨基酸,主要在小肠中吸收,尽管一小部分在结肠中分解代谢为吲哚代谢物。
一项纵向队列研究证实,在 213 名中国个体(包括 51 名继续发展为 2 型糖尿病和 162 名保持代谢健康的个体)中,高基线空腹血清色氨酸浓度与患 T2DM 的风险增加有关。此外,色氨酸水平作为生物标志物的预测能力与五种现有氨基酸在区分患有和未患 T2DM 的个体方面的预测能力相当 。
值得注意的是,先前的报告表明,几种氨基酸的血清水平可以以不同的准确性识别来自不同人群的 T2DM 患者。例如,苯丙氨酸和缬氨酸在美国人群中表现最好,而酪氨酸在南亚人群中最准确。这些发现指出了识别区域特异性生物标志物在实现最佳诊断准确性方面的重要性。
有价值的生物标志物必须为从临床信息中获得的分类能力提供额外的分类能力。因此,粪便生物标志物是粘膜疾病诊断标志物的明显来源,因为粪便流与肠粘膜直接接触。
钙卫蛋白
粪便钙卫蛋白是一种可在粪便中检测到的粒细胞衍生的细胞溶质蛋白,由于炎症严重程度与粪便钙卫蛋白水平之间的相关性强,它是最广泛使用的用于炎症性疾病的粪便生物标志物。
两份报告证实了粪便钙卫蛋白水平检测内窥镜炎症的能力,报告的敏感性为70-100% ,特异性为44-100%。这些值的广泛范围可以通过每项研究中应用的截止阈值的变化来解释。
然而,粪便钙卫蛋白水平升高并不是 IBD 特有的,而是反映了肠道炎症状况,这也与其他肠道和代谢疾病(包括 IBS、胃肠道恶性肿瘤、肥胖和 T2DM)有关。
例如,对来自 1,792 个人的粪便样本中肠道微生物群的鸟枪宏基因组分析能够区分 IBD 和 IBS,与单独的粪便钙卫蛋白水平 (AUC) 相比,机器学习算法显着提高了这些预测模型的准确性 (AUC 0.91>0.80)。
重要的是,具有最高预测准确度 (AUC 0.93) 的模型包括粪便钙卫蛋白水平以及前 20 个选定分类群的宏基因组分析。这些结果表明,临床和微生物生物标志物的整合提高了诊断的准确性。这种综合方法已被用于预测 IBD 患者对治疗的反应。
在这项研究中,基线临床数据(包括血清学、内窥镜和临床生物标志物)不足以预测缓解(AUC 0.62),而添加分类学和代谢谱将诊断能力分别提高到 AUC 0.72 和 AUC 0.74。
此外,仅粪便钙卫蛋白水平就能够区分储袋炎患者和无储袋炎患者 (AUC 0.63)。相比之下,微生物组物种模型(有或没有粪便钙卫蛋白水平作为额外的预测因子)实现了 0.78 的 AUC,证实微生物分析在识别储袋炎方面具有优于仅粪便钙卫蛋白水平的诊断性能。
用于诊断 T2DM 的葡萄糖代谢受损的血清学生物标志物包括空腹血糖水平、75g口服葡萄糖激发后 2 小时血糖水平(口服葡萄糖耐量试验)和糖化血红蛋白水平。
一项使用来自两个瑞典队列136数据的研究确定了预测 T2DM 进展的血清学和微生物组生物标志物的组合。
在这项研究中,多变量分析表明胰岛素抵抗程度与微生物组变异之间存在很强的相关性。
有趣的是,使用基于微生物组的机器学习模型来区分验证队列中胰岛素抵抗程度最低和最高的个体的 AUC 为 0.78,这表明肠道微生物群是 T2DM 进展的重要调节因子。
事实上,尽管已经为 T2DM 提出了广泛的诊断生物标志物,但它们中的大多数未能捕捉到这种疾病的复杂性或掌握微生物和代谢的变化。在这方面,已将代谢物生物标志物与已确定的临床风险因素结合使用,以显着改善疾病分类。
微生物特征
了解单个细菌类群(病原菌)和/或复杂微生物群落(生态失调)变化的功能作用和特异性对于解决IBD或T2DM中微生物-宿主相互作用的发病机制至关重要。在这种情况下,肠道微生物组的功能改变可能代表宿主适应的结果。

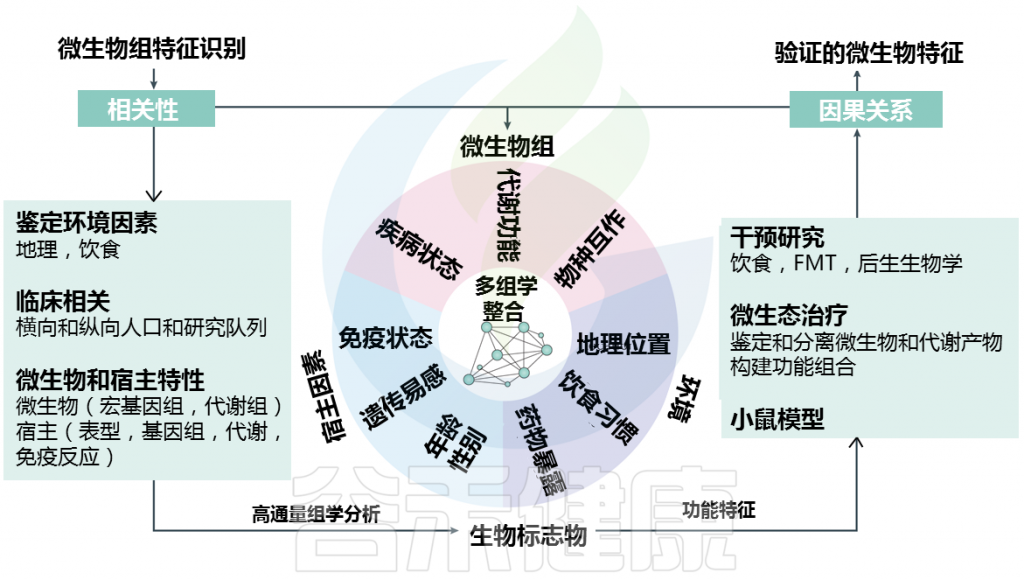
Metwaly et al.,Nat Rev Gastroenterol Hepatol. 2022.
肠道微生物群与多种疾病之间存在因果关系,已在小鼠实验中得到证实。无菌小鼠模型可以选择性地用单一细菌菌株、最小细菌聚生体或来自人类粪便或其他供体材料的定义复杂的肠道微生物生态系统进行定植,以研究它们对宿主表型的影响。在 IBD 中,无菌小鼠模型的单菌株定植有多种共生细菌,包括大肠杆菌、粪肠球菌、普通拟杆菌和Bilophila wadsworthia使我们能够了解疾病引发或保护的一些潜在机制。已有的研究工作表明,肠道菌群是驱动结肠炎小鼠模型炎症所必需的,而这些细菌与 CD患者的复发风险相关。肠道微生物群移植到无菌小鼠体内导致了几种疾病状态,从而揭示了与炎症有关的共享功能代谢途径。同样,以前的工作表明葡萄糖耐量和胰岛素抵抗受肠道微生物组组成的影响,已通过一系列 FMT 研究得到证实。
在过去的二十年里,人类和小鼠研究的证据揭示了肠道微生物组在炎症和代谢疾病(如 IBD 和 T2DM)的发病机制中的基本作用。肠道微生物生态系统结构和功能的变化(失调),与这些疾病患者的疾病活动、复发风险或对治疗的反应有关。然而,大多数这些疾病的复杂性和多因素发病机制,以及人类研究中存在多种混杂因素,依然对微生物组特征在诊断、预测预后和治疗决策中的临床应用提出重大挑战。
当前的微生物组研究不仅仅局限于描述微生物群落结构和疾病关联,还在了解肠道菌群在复杂慢性病发病机制中的致病作用方面取得进展。预计这些努力将增强微生物组建模,并推进可用于临床环境的基于菌群特征和/或疾病风险的模型开发。
参考文献:
Metwaly A, Reitmeier S, Haller D. Microbiome risk profiles as biomarkers for inflammatory and metabolic disorders. Nat Rev Gastroenterol Hepatol. 2022 Feb 21. doi: 10.1038/s41575-022-00581-2. Epub ahead of print. PMID: 35190727.
谷禾健康
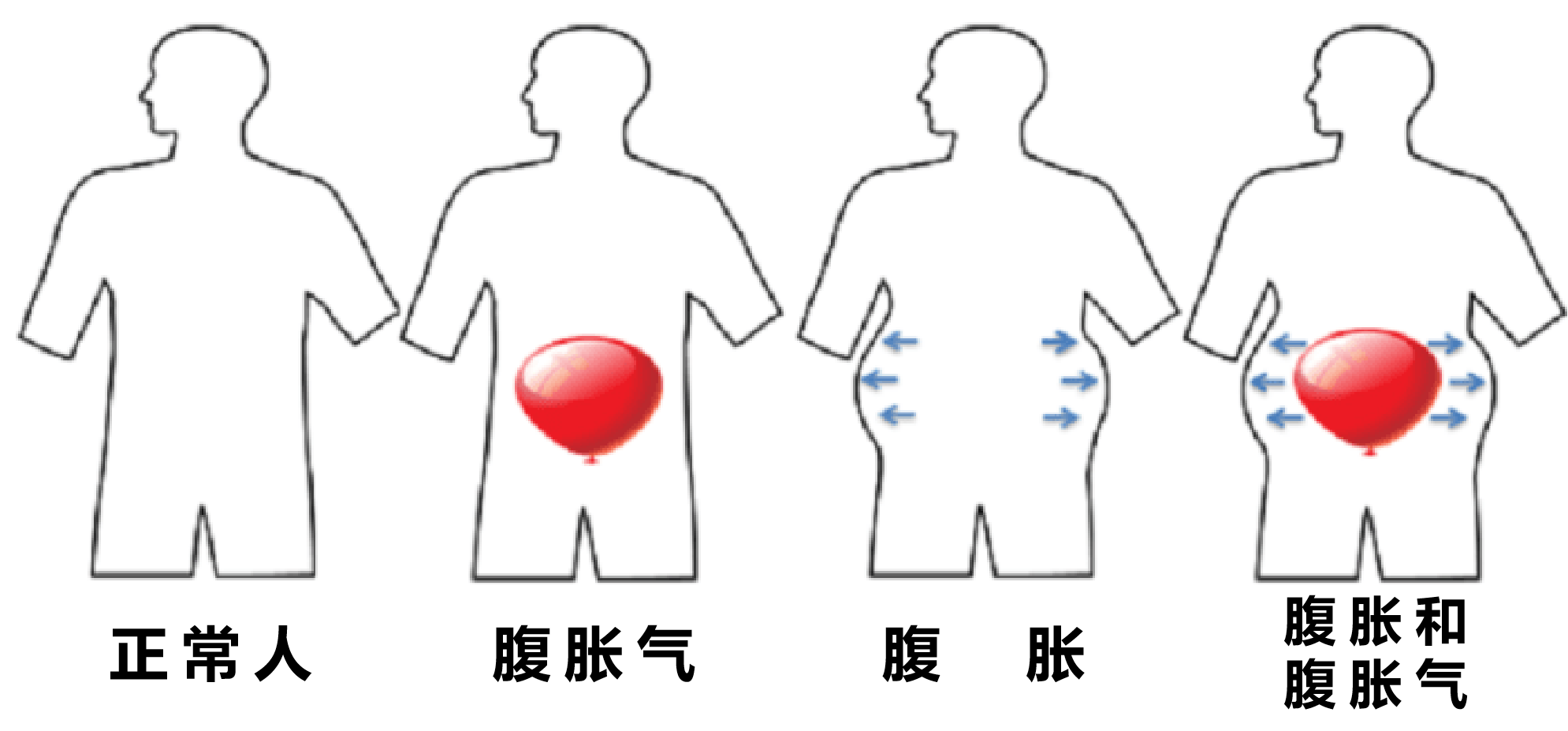
可能大部分人都有过:气胀、肿胀或膨胀。对许多人来说,这些可能是短暂的感觉,一般发生在进食后。然而,对于有些人来说,腹胀气和腹胀(腹部膨胀)是慢性和长期并且反复发作严重影响生活质量。
腹胀的患病率很高,在普通人群中为16%-31%,肠易激综合征(IBS)患者中为66%-90%。女性腹胀率普遍高于男性,而便秘型IBS患者(IBS-C)腹胀率高于IBS患者腹泻。
腹胀气和慢性腹胀对生活质量的影响很大。75%的腹胀(无IBS)患者的症状为中度至重度,而50%的患者报告症状导致日常活动减少。
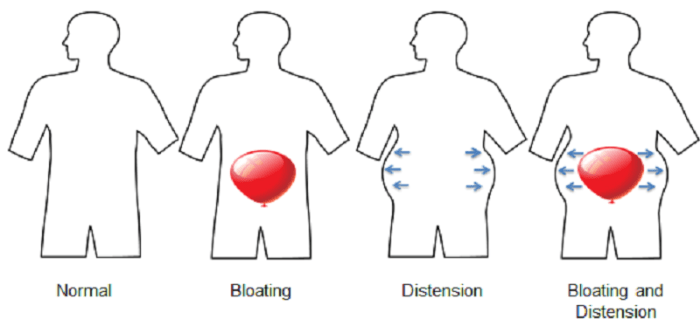
腹胀气(Abdominal bloating)是一种主观感觉,即有气体滞留,或感觉压力或膨胀没有明显可见的扩张。有些时候是一种饱腹感或压迫感,这种感觉可以发生在腹部的任何部位(上腹部、中部、下部或全身)。
腹胀(Abdominal distension)是定义为腹围可测量的增加,是腹围增大的客观表现。患者通常描述他们看起来“像气球”或“像我怀孕了”。
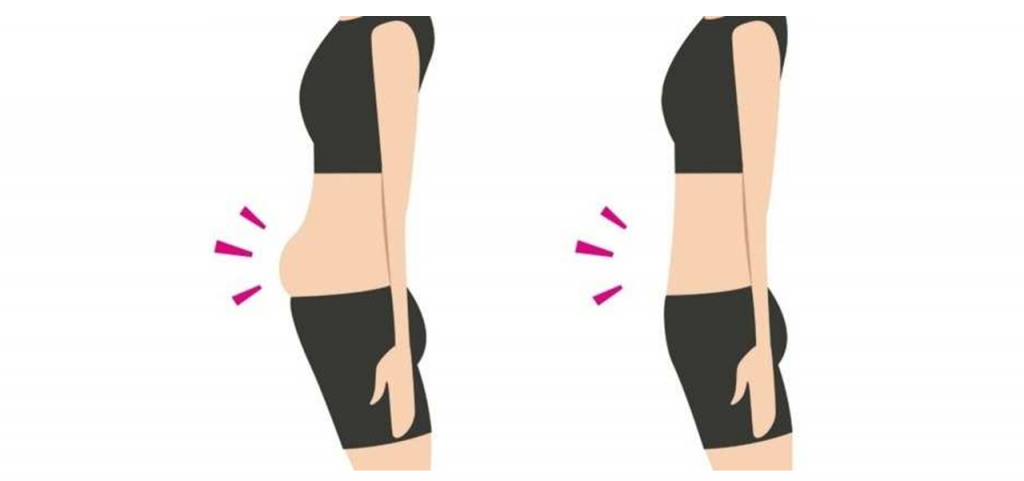

这些症状通常是并存的,当然也可以分别发生。
根据罗马四世的标准定义,腹胀气和腹部胀大通常与其他功能性胃肠道疾病(例如功能性消化不良,肠易激综合征和功能性便秘)同时发生。一项研究发现,只有50%-60%的腹胀患者报告腹部膨胀,从而突出了这些疾病的不同性质。
过去,腹胀气被认为直接与腹部膨胀有关,但最近的研究表明,腹胀并不总是伴有‘腹胀气’,因此腹胀气和腹部膨胀应被视为具有不同机制的独立疾病。
腹胀气和腹胀的病因很复杂,本质上常常是多因素的,而且还不完全清楚。鉴别诊断包括器质性和功能性疾病(下表)。
表 腹胀气和腹胀的常见原因

大多数患者认为,他们的症状是由于胃肠道(GI)内“气体” 数量增加所致,尽管这仅占少数患者的症状。正常的气体产生,吸收和排泄如下图所示。计算机断层扫描(CT)成像显示,只有25%的功能性胃肠疾病(FGID)患者在自发性腹胀发作期间或食用“高胀气”饮食后,管腔气体增加。
正常的气体产生,吸收和排泄
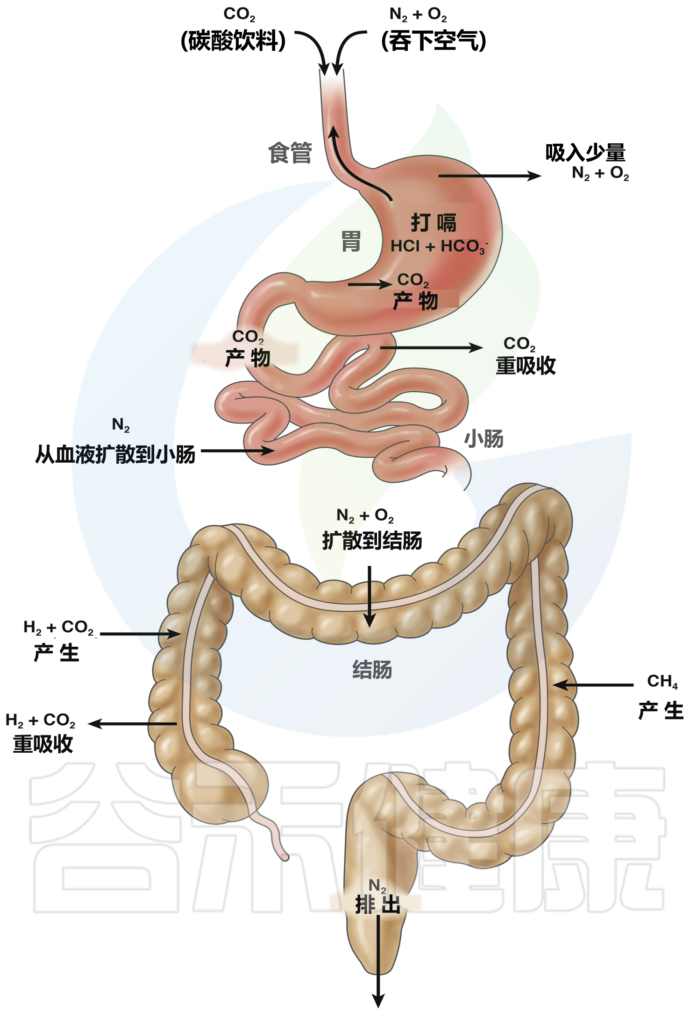
Lacy BE et al.Clin Gastroenterol Hepatol.2021
腹胀和腹部胀大的发生可能有多种原因,包括食物不耐受,先前的感染会干扰肠道菌群,内脏感觉紊乱,肠运输延迟或内脏反常等 (下图)。
腹胀气和腹胀的病理生理学
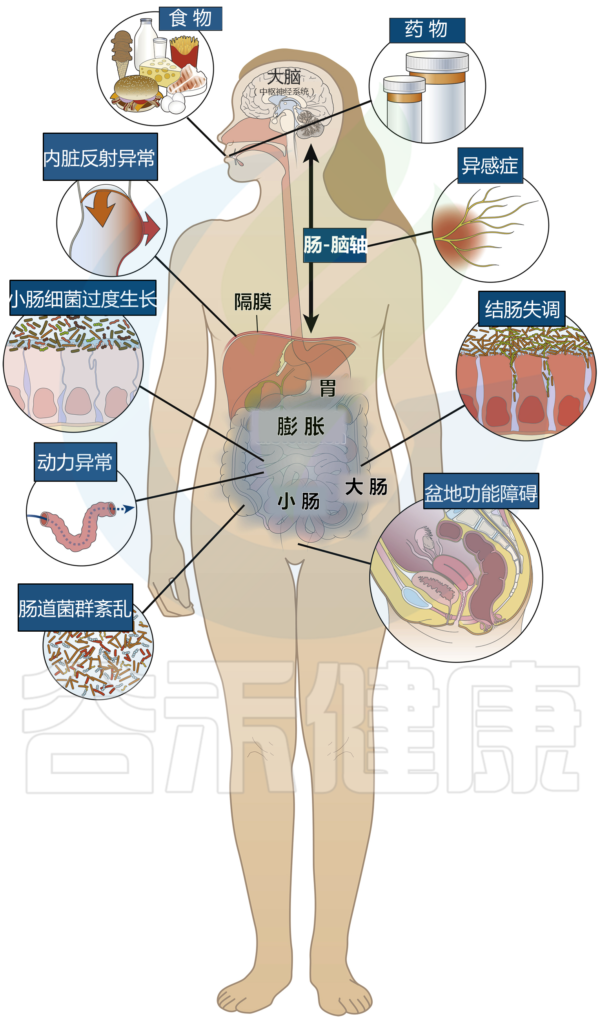
Lacy BE et al.Clin Gastroenterol Hepatol.2021
01 小肠细菌过度生长与碳水化合物不耐受
小肠细菌过度生长(SIBO)和碳水化合物(例如乳糖和果糖)不耐受是导致腹胀气和腹部胀大的常见原因。过量的小肠细菌会由于碳水化合物的发酵而导致症状,随后会产生气体,并导致小肠的拉伸和扩张。
尽管尚未对SIBO患者进行充分研究,但感觉改变和内脏反射异常也可能起作用。碳水化合物不耐受症可能会导致渗透力增加,体液过多滞留以及结肠中过度发酵,从而导致腹胀和胀大症状。
对于诊断SIBO的理想检测方法尚无共识,因此很难确定其真实患病率。 此外,没有前瞻性试验评估单纯诊断为慢性腹胀气和腹胀的患者来确定SIBO或食物不耐受的患病率,因此,大多数数据来自研究较充分的有关FGID(胃肠道功能紊乱)和 IBS数据。
一项meta分析报告SIBO在健康对照组的患病率为0%-20%,而在IBS患者中患病率为4%-78%。
众所周知,饮食习惯可能是造成腹部症状的原因,并且已在努力证明饮食与IBS症状之间的关系。
碳水化合物吸收不良如何通过增加渗透活性和增加细菌发酵产气的生理效应而引起胃肠道症状(例如腹胀)。可能有几个因素起作用,包括:
(1)摄入的碳水化合物量;
(2)进食时是否伴产气食物或其他食物;
(3)胃排空率(餐食进入小肠的速度有多快);
(4)小肠运输时间(一餐进入小肠后进大肠所花费的时间);
(5)膳食中是否含有能分解碳水化合物的酶的细菌;(6)结肠细菌对个人饮食的适应性;
(7)宿主因素,例如是否存在内脏超敏反应。
此外,乳糖不耐症可能导致IBS发生发展。在小肠中,二糖被肠酶分解成单糖,然后被吸收。如果不进行此过程,则二糖到达结肠,然后被细菌酶分解成短链碳酸和气体。因此,IBS患者乳糖吸收不良可能会产生腹胀的症状。
此外,一个新的假设,提出了,过度向小肠和结肠递送高发酵但吸收差短链碳水化合物和多元醇的(统称FODMAPs、发酵寡糖、二糖和单糖类和多元醇)可能会导致胃肠道症状的发展。
FODMAPs是小分子,具有渗透活性,并且与长链碳水化合物相比,发酵非常迅速。这些分子诱导了相对选择性的细菌增殖,尤其是双歧杆菌的增殖,并且间接证明了这些分子可导致远端小肠细菌种群的扩大。
因此,高FODMAP饮食已证明可以使肠道中的氢产生时间延长,发酵引起的结肠扩张,肠腔内渗透负荷增加导致结肠输送量增加以及胃肠道症状的产生。
FODMAP组中的碳水化合物清单以及包含这些碳水化合物的食物的示例
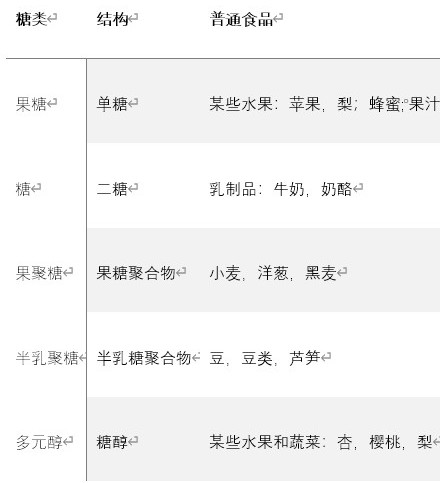
在一般人群中,食物耐受性的症状相似,其患病率约为20% 。糖耐量的真正患病率尚不清楚,因为糖耐量未必与呼气试验中的糖吸收不良有关。
乳糖酶缺乏本身并不会引起吸收不良,因为并非所有乳糖酶缺乏的个体都在摄入乳糖后出现症状。 这表明在某些患者中可能需要其他因素(例如,遗传易感性,内脏超敏性)。
02 肠道菌群异常
比较少研究仅仅关注肠道微生物群在腹胀或腹部膨胀症状发病机制中的意义。相反,许多研究描述了肠道微生物群在胃肠运动、感觉和肠道通透性紊乱中的作用。
通过比较IBS患者和健康对照受试者,确定了肠道微生物群的数量和构成差异,一项研究指出,与患有腹胀的IBS患者和健康对照者相比,没有腹胀的IBS患者中瘤胃菌科和拟杆菌科成员显著减少。
过去几十年的研究表明,在IBS患者的粪便样本中发现了结肠菌群的改变。胃肠微生物群可以分为2个生态系统:管腔细菌和黏膜相关细菌(下图)。管腔菌群构成了大部分胃肠道菌群,它们通过糖类发酵和产气在IBS的腹胀和肠胃气胀中起关键作用。
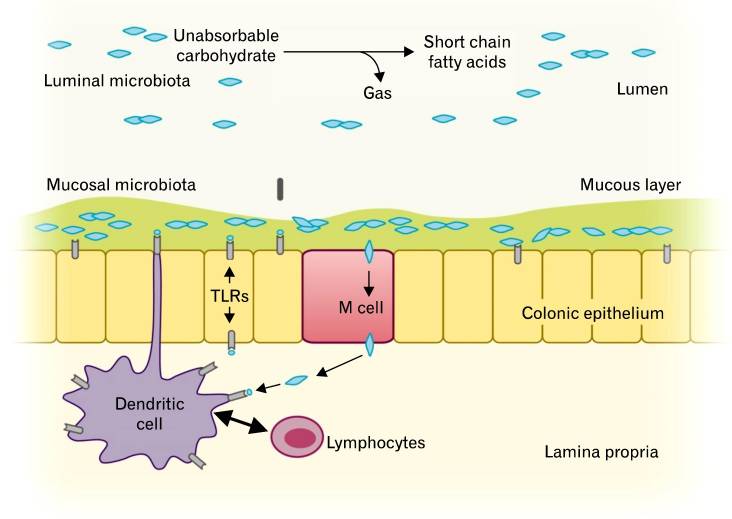
来自韩国的使用16S rRNA基因研究也表明,IBS和非IBS粪便样品之间在多样性和优势方面存在显着差异。此外,这些微生物变化改变了肠道中的蛋白质和碳水化合物的代谢。
来自日本的一项研究还显示,IBS患者的韦荣氏菌( P = 0.046)和乳杆菌(P = 0.031)的计数高于对照组。此外,他们的乙酸(P = 0.049),丙酸( P = 0.025)和总有机酸( P = 0.014)的水平明显高于对照组,这与腹痛,腹胀和肠蠕动等症状有关。
另一项研究表明,IBS患者产生的H2较多,但IBS患者和对照组的总气体排泄量相似。这可能与耗氢细菌在结肠发酵中的变化有关,这可能是IBS发病机理中的重要因素。
破坏宿主和肠道菌群之间的平衡会导致粘膜免疫系统发生从微观到明显的炎症变化,这也会导致肠道感觉运动功能和免疫活性发生变化。
此外,这些改变的微生物群可能在发酵气体类型和体积上产生差异,这可能是腹胀患者症状的原因。已经有一些报道证实结肠菌群产生的气体类型与腹胀之间的关系。
甲烷产量低的人在摄入山梨糖醇和纤维后报告腹胀和痉挛明显增加,甲烷产量高的人显示出严重的乳果糖不耐症患病率低水平。因此,产甲烷菌群的作用在腹胀的发病机理中可能很重要。
03 异常胃肠蠕动
腹胀常见于胃轻瘫患者(超过50%)和小肠运动障碍患者(如慢性假性肠梗阻和硬皮病)。一项对2000多名功能性便秘和肠易激综合征患者的前瞻性研究表明,90%以上的患者出现腹胀症状。
在肠易激综合征患者中,与正常运输的患者相比,结肠运输延长的患者腹胀更大。功能性腹胀和IBS患者近端结肠的气体清除受损,但结肠对气体输送的适应能力正常。
04 盆底功能障碍
肛门直肠运动功能障碍的患者可能会因为有效排空肠胃和大便的能力受损而出现腹胀和腹胀。在便秘患者中,气囊排出时间延长与扩张症状相关。
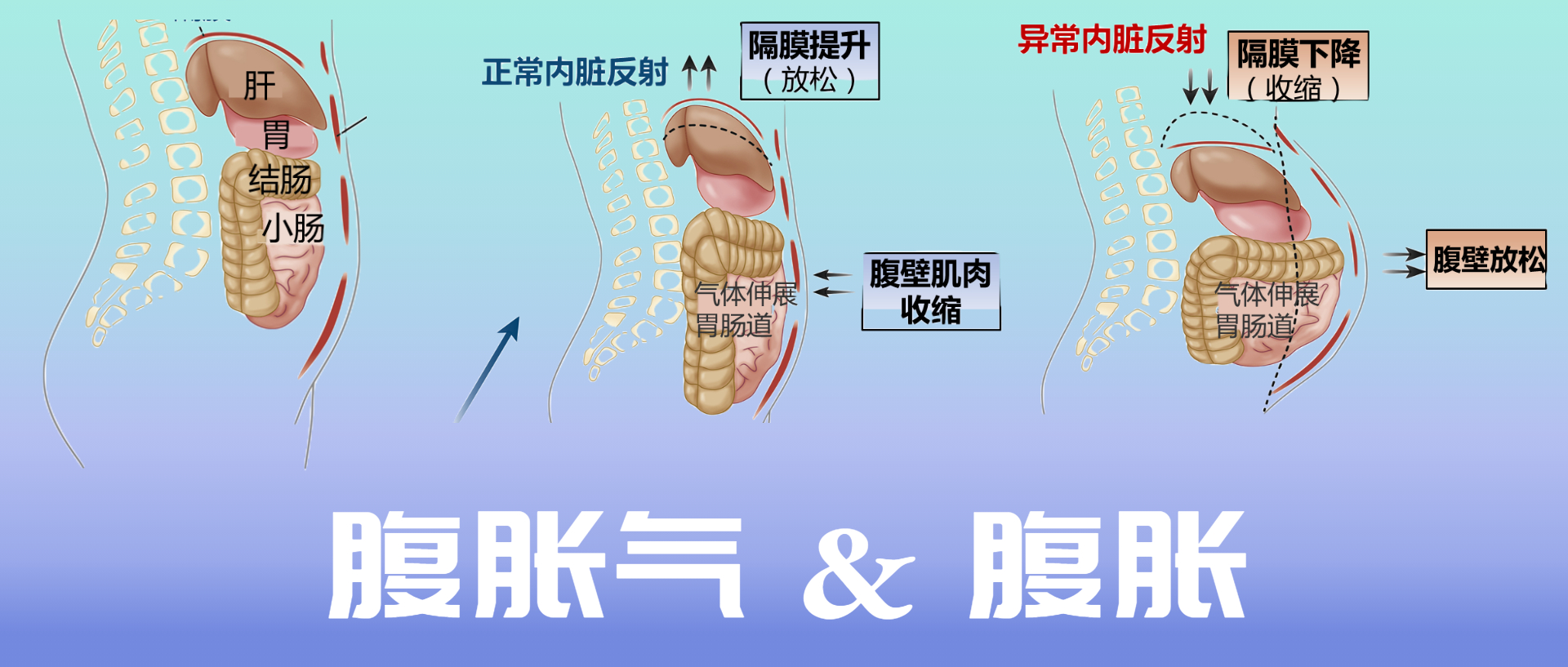
05 腹腔干扰 (腹肌性神经痛)
盆腔出口梗阻已被证明会延迟结肠传输。腹腔干扰在一些患有慢性腹胀气和腹胀大的患者中,出现了一种自相矛盾的腹肌反应,称为腹肌神经性神经痛。 在这个过程中膈肌收缩(下降)和前腹壁肌肉放松。这种反应与对腔内气体增加的正常生理反应相反,膈肌放松,而腹前肌收缩,以增加腹腔的颅尾容量而不突出(见下图)。
正常和异常内脏反射
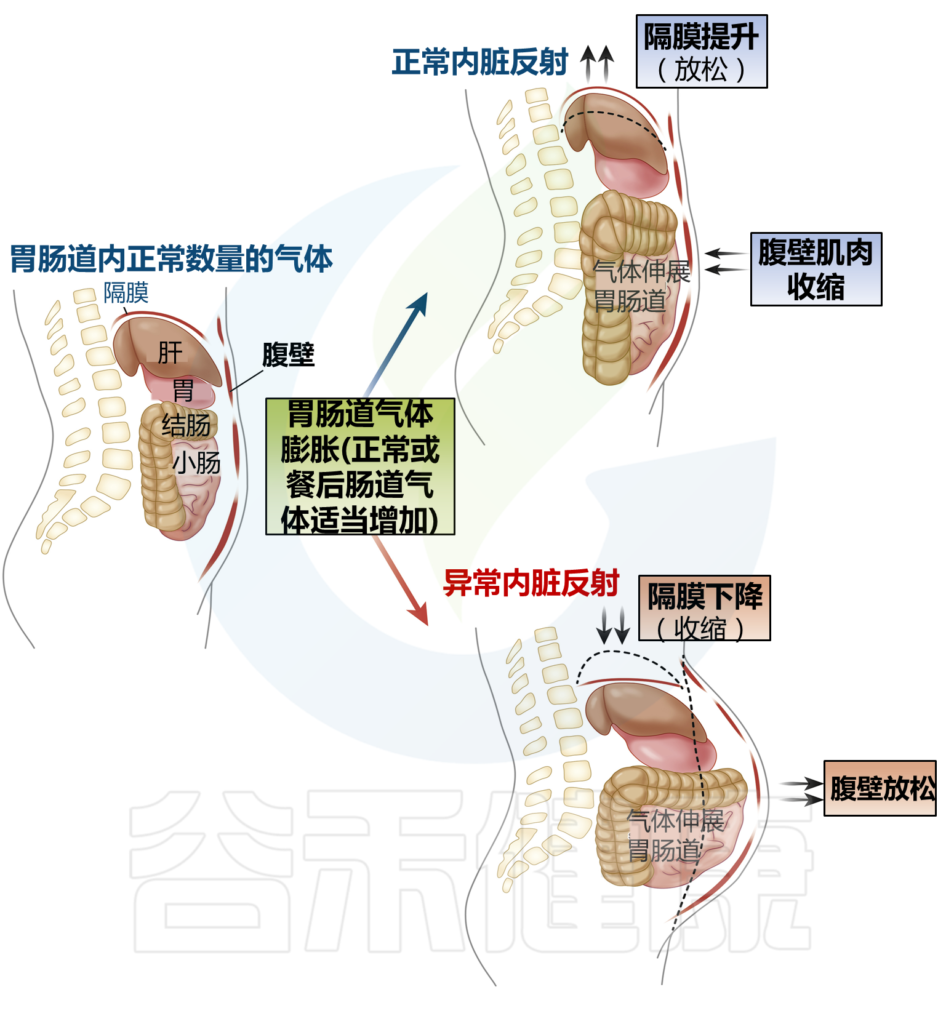
Lacy BE et al.Clin Gastroenterol Hepatol.2021
CT扫描研究表明,腹胀患者的腹壁突出明显,膈肌下降,腔内气体增加相对较小。 相比之下,发现腹胀和肠动力障碍的患者腔内气体含量显着增加,从而导致膈肌上升。在功能性消化不良(FD)和餐后腹胀的症状中,还发现了腹痛性神经痛。
06 内脏过敏
腹胀的感觉可能源自患者的腹部内脏,其中正常刺激或肠道内气体含量的微小变化可能被认为是腹胀。事实上,在一些IBS患者中,小肠收缩的感知阈值低于正常水平。另外,IBS患者中有报道称通过相继性球囊扩张评估了直肠知觉改变。与腹胀和胀气症状相比,仅具有腹胀症状的IBS患者内脏过敏性增高。
在FD患者中发现餐后对胃球囊扩张的敏感性与饭后症状(如腹胀)密切相关。管腔内内容物和腹胀可能会导致症状性腹胀,这可以通过复杂的肠胃神经通路来放大,并进一步受焦虑,抑郁,躯体化和警惕性等因素的影响。
自主神经系统也可能有助于调节内脏敏感性。众所周知,交感神经激活可增加FD患者对肠扩张的感觉。同样,自主神经功能障碍也会影响IBS患者的内脏敏感性。这个机制可以在腹胀发挥作用。
此外,已经提出内脏知觉可能受到认知机制的影响。即,腹胀的IBS患者更加注意其腹部症状,这是一种过度警惕。
另外,患有IBS的女性患者在月经期阶段腹部疼痛和腹胀加重,此时直肠敏感性增强可能会导致腹胀,但不会导致胀气。两者合计,改变的感觉阈值与改变的意识知觉组合可能解释腹胀的机制。
07 肠气积聚
在空腹状态下,健康的胃肠道仅包含约100 mL气体,几乎平均分布在6个隔室中:胃,小肠,升结肠,横结肠,降结肠和远端(骨盆)结肠。餐后气体增加约65%,主要在骨盆结肠。
肠道气体过多被认为是引起腹胀和扩张的可能原因,许多研究人员试图确定这种观点。一些使用腹部平片的研究表明,IBS患者的肠内气体量比对照组大。
但是,腹腔内气体含量与腹胀之间的相关性较差。绝大多数研究不支持过量气体引起腹胀或腹痛。一项使用氩气冲洗技术的研究表明,在腹胀患者和健康受试者之间肠道气体的积聚没有差异。最近使用CT扫描结合现代成像分析软件进行的研究还表明,大多数患者的过量气体与腹胀无关。
因此,这些观察结果表明,增加的气体量可能不是造成腹胀的主要机制,而更常见的是问题的根源是气体的运输或分配受到损害。
08 肠腔内容物
腹胀在没有气体滞留的情况下发展,而可能是由其他肠内容物引起的。通过观察健康受试者对乳果糖或2种类型的纤维(蚤草或甲基纤维素)对膳食补充剂的反应,对气态症状进行了随机,双盲,交叉研究。
乳果糖组的气体通过量,直肠气体的主观感觉和呼吸氢排泄显着增加,而纤维组则没有。但是,所有3组的腹胀感均增加。因此,已经提出,腹腔内增大而不是气态填充可能是腹胀的原因。
在另一项研究中,麸皮在不引起对照组症状的情况下加速了小肠运输并提高了结肠清除率,但IBS腹胀患者的小肠运输并没有进一步加速。因此,他们推测麸皮可能在结肠中引起增加的膨大作用,从而导致IBS患者腹胀加剧。甚至建议应重新考虑在IBS中使用麸皮,因为过量食用麸皮可能会导致IBS患者出现腹胀等症状。
尽管需要更多的研究来进一步了解它们之间的关系,但某些IBS患者的腔内膨大可能会加重腹胀。
09 便秘
许多便秘患者会伴有腹胀。还有一种趋势,即IBS-C患者(便秘型)比IBS-D(腹泻型)患者更普遍,尽管在某些研究中它在统计学上不显着。
粪便由小肠转运以及结肠直肠的运输减慢,会大概率加剧了便秘病人腹胀。另外,便秘可以与麸皮相同的方式通过腔内膨胀作用促进腹胀。
10 心理方面
腹胀是患有IBS的女性的常见症状。当腹胀更加严重时,存在一种增加心理困扰指数的趋势。而且,腹胀患者显示焦虑和抑郁增加,这提出了心理困扰可能导致感觉到的腹胀严重性的假说。
此外,在大量人口调查中,腹胀与精神功能障碍(例如重度抑郁症,恐慌症和睡眠障碍)显着相关。然而,其他研究未能证明心理困扰,要么腹胀或腹胀之间的关系。但是,目前尚不清楚腹胀与社会心理困扰之间是否存在实际关系,需要进一步研究证明这一点。
11 肠道菌群异常
在美国进行的一项基于人群的研究中,IBS中女性性别与腹胀和腹胀症状的增加显着相关,迄今为止,已有类似的发现报道。
虽然在IBS性别角色的问题已经从许多研究提出,性别差异在气胀和膨胀的机制尚不清楚。如前所述,一些研究表明,腹胀是月经的常见症状之一。
激素效果也已推测,即,生殖激素的整个月经周期和在绝经后的变化可以影响肠能动性和内脏感觉。
此外,性别的症状表达差异也被认为是一种可能的解释。尽管关于这些差异的潜在机制的更多研究仍有待确定,但似乎有可能推测,荷尔蒙波动可能导致女性IBS患者腹胀。
治疗可能对患者和提供者具有挑战性,没有任何一种疗法能够持续取得成功。成功的治疗包括确定病因,评估严重程度,教育患者并使患者放心以及设定期望值。治疗选择包括饮食变化,益生菌,抗生素,促运动剂,解痉剂,神经调节剂和生物反馈。
认识到治疗需要个体化,以临床实践中通常遵循的顺序列出治疗方法(下表)。
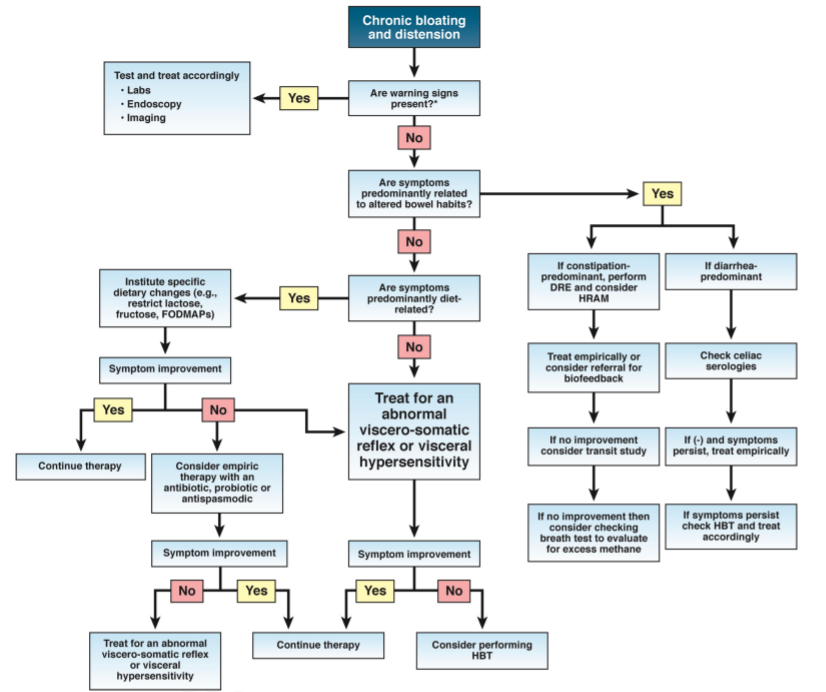
Lacy BE et al.Clin Gastroenterol Hepatol.2021
1 饮食改善
包含吸收不良的糖醇(如山梨糖醇,甘露糖醇,木糖醇和甘油)的人造甜味剂可促进气体产生。
证据表明糖吸收不良的81%的功能性腹胀患者出现症状改善。
大约70%具有非乳糜泻谷蛋白敏感性患者出现腹胀。
与安慰剂相比,以前接受无麸质饮食控制的IBS患者在接受麸质刺激1周后,腹胀明显恶化。
然而,面筋作为饮食的腹胀和其他胃肠道症状的来源的作用是有争议的。有证据表明,果聚糖和FODMAP(可发酵的寡糖,二糖和单糖)是真正的罪魁祸首。两项研究表明,低FODMAP饮食治疗的IBS患者注意到腹胀和腹胀得到改善。如果经验治疗和/或治疗测试不能缓解症状,则建议改善方案。
2 益生菌
益生菌是一种有益于宿主的活微生物,可以修饰肠道微生物组,从而有可能改善腹胀。益生菌的组合和配方很多。但是,评估益生菌腹胀改善情况的设计良好的研究很少。
对干酪乳杆菌菌株GG(Lactobacillus casei strain GG),植物乳杆菌Lactobacillus plantarum和罗伊氏乳杆菌Lactobacillus reuteri的研究表明,IBS腹胀的患者没有益处。
随机分配给L. sporogens / bacillus coagulans的IBS患者的腹胀严重程度评分有显着改善。
而双歧杆菌的研究也证明了疗效。然而,在最近的一项多中心试验中,在从普通人群中招募的受试者中,被包封的婴儿芽孢杆菌35624未能显示出腹胀分数的任何差异。
3 抗生素类
用于腹胀治疗的最常研究的抗生素是rifaximin(利福昔明)。
接受抗生素治疗的IBS患者的总体症状改善与乳果糖氢BT中的氢水平正常化相关。这表明使用抗生素的基本原理是修饰肠道微生物组并减少细菌的产气量。
与安慰剂相比,无便秘IBS的患者每天3次随机服用rifaximin 550 mg,共14天,IBS相关的腹胀缓解率更高。在另一项研究中,与安慰剂相比,每天两次×10天两次接受利福昔明400 mg治疗的IBS患者的平均累积和腹胀特异性评分显着改善(P < .05)。
4 解痉药
如果平滑肌解痉药是由于胃肠道的气体扩张引起的,则可能会改善症状。
对解痉药的两项荟萃分析着重于腹胀或扩张症状。第一个评估了6项研究,涉及885名患者和5种不同的药物。与安慰剂相比,IBS患者的平滑肌松弛剂更有可能改善腹胀症状(优势比为1.46; 95%置信区间为1.10-1.94)。
对涉及1419名患者和4种不同药物的7项研究进行了第二次荟萃分析,发现镇痉药优于安慰剂,尽管两项研究的优势比均为临界值(优势比为1.455; 95%置信区间)。
对IBS患者进行的一项前瞻性,随机,安慰剂对照试验(Rome III标准; n = 285)发现,相比安慰剂,匹维溴铵(Pinaverium bromide) 和西甲硅油(simethicone) 的组合在缓解腹痛和腹胀症状方面更有效。
Pinaverium bromide (匹维溴铵),是一种对胃肠道具有选择性的L型钙通道阻滞剂,能有效缓解疼痛、腹泻和肠道不适,对肠易激综合征 (IBS) 具有有良好的研究效果。
simethicone (西甲硅油)是一种具有表面活性的胃肠道用药,服用后不会被吸收,但是可以改变消化道中存在于食物或者黏液中的气泡的表面张力,使气泡分解。而释放出来的气体可以被肠壁和胃壁吸收,通过蠕动逐渐排出体外。在临床中,主要是用于由于肠道内产气过多引起的腹胀或者是腹部手术后卧床的病人。也可用于胃镜、X线、超声检查等作为双重对比显示造影剂的添加剂,用于消除胃肠道中的气体,使检查得更为清楚。
5 便秘药
在一项对1171例IBS-C(罗马Ⅱ标准)患者进行的随机、安慰剂对照研究中,每天两次lubiprostone(8μg) 改善整体IBS症状和腹胀(P<0.05)。
一项为期48周的lubiprostone开放性研究(24μg(每日两次)在慢性特发性便秘(CIC)患者(n=248)中发现,与基线检查时相比,腹胀有所改善(P<0.011),但安慰剂组不包括在内。
两项随机、双盲、安慰剂对照研究评估了linaclotide (145或290ug)的疗效和安全性。在为期12周的研究中,1276名CIC患者的两种剂量均改善了腹胀症状(P<0.001)。
在一项前瞻性随机研究中,483例CIC患者(罗马II标准)伴有中度至重度腹胀,每天服用一次利那洛肽(Linaclotide) 与安慰剂相比,腹胀症状显著改善。
在一项针对804名患者的3期双盲安慰剂对照试验中,利纳克罗肽除了改善腹胀的相关症状,还改善了IBS-C症状(P<0.001)。
在一项随机试验中,对1394名CIC患者进行的安慰剂对照研究(罗马III标准)与安慰剂相比,每天服用一次3毫克和6毫克剂量的普卡那肽(Plecanatide)均能改善便秘和腹胀症状。
最后,两个相同设计的随机对照组,双盲安慰剂对照研究评估了普利卡那肽治疗IBS-C的疗效和安全性(n=2189)。两种剂量(3和6毫克,每天一次)都能改善腹胀症状(P<0.001)。
Linaclotide (利那洛肽) 是一种有效和选择性的鸟苷酸环化酶C (guanylate cyclase C)激动剂;开发用于研究便秘型肠易激综合症 (IBS-C) 和慢性便秘。
普卡那肽(Plecanatide),由美国Synergy制药公司研发,是尿鸟苷蛋白(uroguanylin)的类似物,含有16个氨基酸的环状多肽,具有促尿钠排泄的鸟苷酸环化酶受体激动药的作用,能调节胃肠道中的酸碱离子,诱导液体转运进入胃肠道,增加胃肠道的蠕动,适用于治疗成人慢性特发性便秘。
6 促动剂
促动剂用于治疗FD(功能性消化不良),胃轻瘫,CIC(慢性特发性便秘)和IBS(肠易激综合征)的症状。
关于使用动力学治疗慢性腹胀和腹胀的数据是有限的。胆碱酯酶抑制剂可改善空肠输注患者的气体清除率。
在一项针对IBS患者的随机,安慰剂对照小型随机研究中,Pyridostigmine在改善腹胀症状方面优于安慰剂(n = 20)。
乙酰硫胺,一种毒蕈碱拮抗剂和胆碱酯酶抑制剂,在日本FD患者中轻微改善,但没有消除与饮食相关的腹胀症状。
对4个随机,对1596名亚裔和非亚裔妇女进行的安慰剂对照研究发现,每天服用2毫克prucalopride(5-HT4激动剂),可改善大便次数,减少腹胀症状。
对34例胃轻瘫患者进行的安慰剂对照交叉研究发现,prucalopride(2毫克,每天一次)改善了全身胃轻瘫症状,包括腹胀和腹胀症状(P<0.0005)。
prucalopride (普卡洛必利),是一种选择性血清素4型(5-HT4)受体激动剂,这是一种胃肠促动力剂,可刺激结肠蠕动,提高肠道运动机能。
7 神经调节剂
在大脑和肠道中起作用的药物已被重新标记为“神经调节剂”。
该组包括中枢和外周作用剂。迄今为止,尚无研究将腹胀作为一种单一症状。FD患者的很大的研究表明,这两种amitriptyline 和 escitalopram(10毫克,每天)与安慰剂相比显著改善餐后腹胀。
对17名FD患者的交叉研究表明,buspirone是一种5-HT 1A受体激动剂,可显着改善整体腹胀的严重程度。
在一项针对23名IBS患者的为期6周的交叉研究中, citalopram(先20 mg,然后40 mg每天四次)显着改善了腹胀的频率和严重程度,而与焦虑和抑郁无关。
8 生物反馈
在一项对45名具有各种FGID的患者的研究中,腹胀发作与内脏反射异常有关。
利用肌电信号提供的视觉指导,对26例患者进行生物反馈治疗,使所有患者都能有效地控制肌肉活动并改善扩张。这些结果在随后的一项随机,安慰剂对照试验中得到了证实,该试验在44名FGID并有餐后腹胀症状的患者中进行。
在一项对52名慢行性便秘患者的研究中,生物反馈疗法显示可显着减少骨盆功能不全和骨盆出口梗阻患者的腹胀症状。
对患有特发性便秘并伴有盆底功能障碍或结肠缓慢转移的各种患者的其他研究还显示,生物反馈疗法后,腹胀症状显着减轻。
没有研究评估使用骨盆底物理疗法来单独治疗功能性腹胀。
腹胀气和腹胀是非常普遍的症状。评估具有腹胀气和腹部胀大症状的患者时,从业者面临许多挑战。
首先,确定潜在的病因,因为这可能有助于查明所需的诊断测试。
其次,识别其他器质性或更严重疾病的警告信号。
第三,评估可能导致腹胀的饮食,药物,医学,外科和行为因素。
第四,考虑引起腹胀和腹胀的主要潜在生理过程,以期开始特定治疗(例如,碳水化合物不耐受的饮食干预与内脏反射异常的行为疗法的比较)。
基于机制的管理性腹胀和扩张应该是理想的,但阐明个别患者的关键操作机制并非总是可行的。通过评估肠蠕动的频率和粪便的稠度以及特殊的成像技术以测量胀气发作期间的腹部形状,可以通过详细的饮食史来收集一些线索。
长期严重的情况下,可能需要将患者转至专门的中心,在该中心可以测量对腔内刺激做出反应的运动性,内脏敏感性和腹肌活动。集中于推测或证明的致病机理的治疗资源包括饮食调节,微生物组调节,促进气体排出,减弱内脏知觉以及通过生物反馈控制腹壁肌肉活动。
最后,提供者应就不同疗法的风险和益处进行深入的讨论,并综合考虑涉及成本,功效和安全性的因素。
主要参考文献
Lacy BE, Cangemi D, Vazquez-Roque M. Management of Chronic Abdominal Distension and Bloating. Clin Gastroenterol Hepatol. 2021 Feb;19(2):219-231.
Malagelada JR, Accarino A, Azpiroz F. Bloating and Abdominal Distension: Old Misconceptions and Current Knowledge. Am J Gastroenterol. 2017 Aug;112(8):1221-1231.
Sandler RS, Stewart WF, Liberman JN, Ricci JA, Zorich NL. Abdominal pain, bloating, and diarrhea in the United States: prevalence and impact. Dig Dis Sci. 2000 Jun;45(6):1166-71. doi: 10.1023/a:1005554103531. PMID: 10877233.
Zuckerman MJ, Nguyen G, Ho H, Nguyen L, Gregory GG. A survey of irritable bowel syndrome in Vietnam using the Rome criteria. Dig Dis Sci. 2006 May;51(5):946-51. doi: 10.1007/s10620-005-9005-0. Epub 2006 May 3. PMID: 16670940.
谷禾健康
克罗恩病(CD)是一种慢性消化系统疾病,会引起消化道炎症和损害。
该疾病属于称为炎症性肠病(IBD)的一组病症,是一种慢性、免疫介导的肠道炎症疾病,其特征是反复发作的肠道炎症和不可逆的消化道损伤累积。
据Meta分析估计 ,中国克罗恩患病率为每10万人2.29例,发病率为每10万人0.848例,在美国约有780,000人患有克罗恩氏病近年来呈快速上升趋势。目前,在临床上,克罗恩病无法治愈,需要创新的治疗方法和药物控制疾病的进展,减少并发症,提高患者生活质量。
克罗恩氏病无法治愈,但有许多治疗方法可帮助治疗其症状,包括症状缓解和黏膜愈合。但是,很多患者对当前可用的治疗方案效果欠佳。克罗恩病的治疗仍存在巨大的未满足需求。
克罗恩病有几种不同类型,按受影响的消化道面积分类。
结肠结肠炎是克罗恩病最常见的形式,它影响小肠(回肠)和大肠(结肠)的末端。
回肠炎这种克罗恩病仅影响回肠。
克罗恩氏结肠炎又称肉芽肿性结肠炎,这种疾病仅影响结肠。
胃十二指肠克罗恩氏病这种形式的疾病会影响胃部和小肠的始端(十二指肠)。
空肠回肠炎这种克罗恩氏病涉及小肠(空肠)上半部分的炎症。
没有两个人会以完全相同的方式经历克罗恩病。
不同人的症状将取决于肠的哪些部位受到影响,疾病的进展程度以及治疗的效果如何。
大多数患有克罗恩氏病的人在小肠和大肠(结肠)都会发炎,这通常会引起腹泻,腹痛或绞痛。
其他常见的消化系统症状包括直肠出血,恶心或食欲不振,急需排便和便秘。
克罗恩氏病还可能导致体重减轻,疲劳和消化系统以外的症状,例如关节痛,眼睛发红或发痒,以及皮肤发红或起伏不定。
定义克罗恩病的持续炎症和肠壁损伤可导致许多并发症。这些并发症大多数会影响消化系统,但有些可能发生在身体的其他部位。
一种常见的消化系统并发症是肠梗阻,当炎症导致疤痕组织积聚并缩小肠道区域时,会发生肠梗阻。
其他消化系统并发症可能包括肛门撕裂,感染袋,营养不良,甚至结肠癌。
患有克罗恩病的人罹患某些轻度肝病的风险较高,包括脂肪肝疾病,肝炎和原发性硬化性胆管炎(PSC),这种疾病的特征是肝脏的胆管系统发炎。
不太常见的克罗恩氏病会引起身体其他部位的并发症,例如口腔,关节,皮肤和眼睛问题。它也可能在怀孕期间引起问题。
克罗恩氏病是肠易激症的一种形式,这是一个总括性术语,用于描述涉及消化道慢性炎症的疾病。IBD的另一种主要类型是溃疡性结肠炎,其特征在于慢性炎症和结肠和直肠内壁的溃疡。
同样重要的是不要将克罗恩氏病或溃疡性结肠炎等肠易激病与肠易激综合症(IBS)混淆。这两种情况听起来相似,甚至有一些相同的症状,但有很大的不同。
截止目前,克罗恩病的发病机制仍然不明。目前主流的观点认为,肠道上皮细胞,IgA以及肠道菌群为代表的 三大因素是导致克罗恩病发病的主要因素之一。例如中国科学院微生物研究所张福萍课题组发现,致病菌感染对该小鼠的影响要比野生型明显,其炎症性肠病(包括克罗恩病)的表现更加强烈,说明这一敏感基因的突变导致宿主中肠道菌群的平衡被破坏,肠道内环境的稳态发生改变。
诊断克罗恩氏病的第一步是完整的病史,体格检查以及一系列测试以诊断克罗恩氏病并排除可能引起类似症状的其他疾病。这些包括肠易激综合症(IBS),乳糖不耐症和溃疡性结肠炎。
在体格检查期间,医生还可能会检查您的腹部是否有腹胀,肿胀以及疼痛或触痛的斑点。
诊断克罗恩氏病通常需要进行其他检查,其中包括:血液检查,粪便检查,结肠镜检查,上消化道(胃肠道)内窥镜检查,无线胶囊内窥镜检查以及X射线和CT(计算机断层扫描)扫描等影像学检查。
粘膜愈合是治疗克罗恩病的主要目标,但有些病人无法进行整个小肠的内窥镜评估。目前越来越多的科学研究表明克罗恩病与肠道菌群密切相关,且肠道菌群或可用于预测克罗恩病患者的小肠粘膜愈合。
接下来我们分享一下谷禾肠健康道菌群检测在克罗恩病患者预测和治疗用药康复评估方面的案例:


男,46岁 , 2020年确诊为克罗恩病
2003年怀疑克罗恩,未确诊,经治疗后得到改善,后持续肠镜检查未显示溃疡平时感觉良好,吃多了肚子容易不舒服。2020年因肠道出血住院,肠镜检查发现回盲瓣溃疡,病理检查确诊为克罗恩病,阿达木单抗治疗。治疗前后分别留取粪便进行肠道菌群检查。检测结果如下所示。
治疗前肠道菌群检测评估
治疗前肠道菌群健康总体状况:


总体健康评分:23分(总分100分),其中菌群,慢病和营养状况份值菌比较低
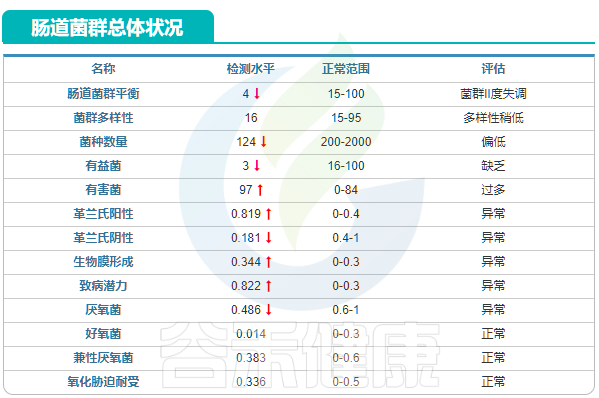

治疗前肠道菌群结果显示肠道菌群II度失调,菌种数量少,只检测124种,远低于这个年龄段人群的菌种数量(造成菌种数量少原因可能是饮食单一,用药或者长期的疾病状态),有益菌不足,有害菌过多,致病潜力高。此外多个菌群评估指标均显示欠佳。
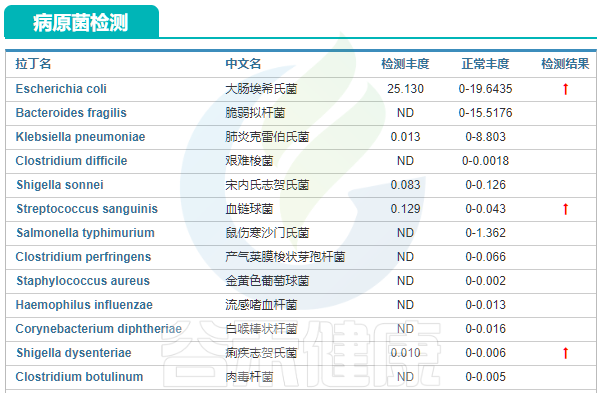

多项病原菌超标,如:
大肠埃希氏菌Escherichia coli、血链球菌Streptococcus sanguinis和痢疾志贺氏菌Shigella dysenteriae超标。
接下来,我们逐一来看这些超标菌的作用。
1. 大肠埃希氏菌
革兰氏阴性菌,于 1885 年首次被发现。
大肠杆菌是条件致病菌,在一定条件下可以引起多种疾病,如腹泻,肠炎,尿路感染,呼吸道感染、菌血症和其他临床感染(如新生儿脑膜炎)。
致病机制
克罗恩病中,粘附侵袭性大肠杆菌对宿主细胞的侵袭作用(下图)。回肠粘膜的异常定植是由粘附侵袭性大肠杆菌与肠上皮细胞相互作用引起的。
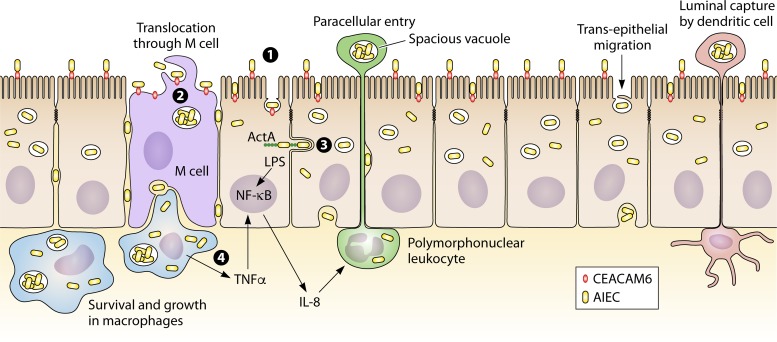
Mirsepasi-Lauridsen HC,et al., Clin Microbiol Rev.2019
溃疡性结肠炎中,弥散粘附性大肠杆菌感染(下图)。弥散粘附性大肠杆菌通过细菌识别衰变/加速因子(DAF),癌胚抗原相关细胞黏附分子CEACAM1或CEACAM6(通过Afa / Dr CEA粘附素)来启动其与完全分化的上皮细胞的相互作用。
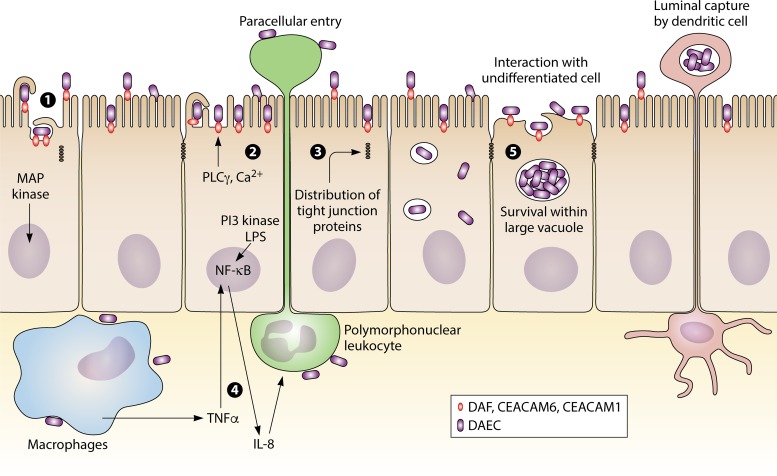
Mirsepasi-Lauridsen HC, et al., Clin Microbiol Rev. 2019
2. 血链球菌
属革兰氏阳性,无孢子形成的兼性厌氧菌。像其他链球菌一样,血红链球菌的细胞分裂沿单个轴发生,从而形成链球或成对链球菌。血红链球菌是一种共生细菌,广泛分布在口腔中,主要是牙齿表面,口腔粘膜的表面和人唾液。
致病机制
血链球菌最初的附着是由它的毛和粘附素促成的,葡聚糖和eDNA的产生促进血链球菌生物膜的成熟。流行病学研究表明,血链球菌可能抑制龋齿的产生。体外研究表明血链球菌和变形链球菌之间存在竞争,变形链球菌是最常见的致龋物种。
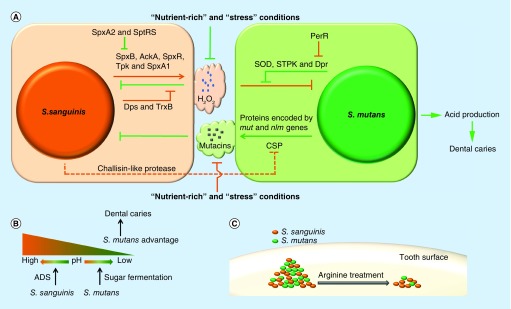
Zhu B,et al., Future Microbiol. 2018
16S rRNA测序结果表明,血链球菌可能与牙周健康有关。与患病的龈下微生物组相比,健康人的血链球菌的丰度显著增加。
然而,体外研究表明,血链球菌也可能促进后续与牙周炎相关的病原体附着。血链球菌与牙周炎相关病原体的相互作用。
这里提示我们“病从口入,牙好身体好”,并不是空话,多数的慢病患者均有口腔或牙周病问题。
3.痢疾志贺氏菌
革兰氏阴性细菌,兼性厌氧,不运动。
痢疾志贺氏菌产生志贺毒素,引起细菌性痢疾或志贺氏痢疾。接触细菌后1至2天开始出现症状。志贺菌病的症状包括:
腹泻(有时带血),发热,肚子痛,粪便稀少,含有粘液,脓液和血液。即使排空也感觉需要排便。与患者描述的症状接近。
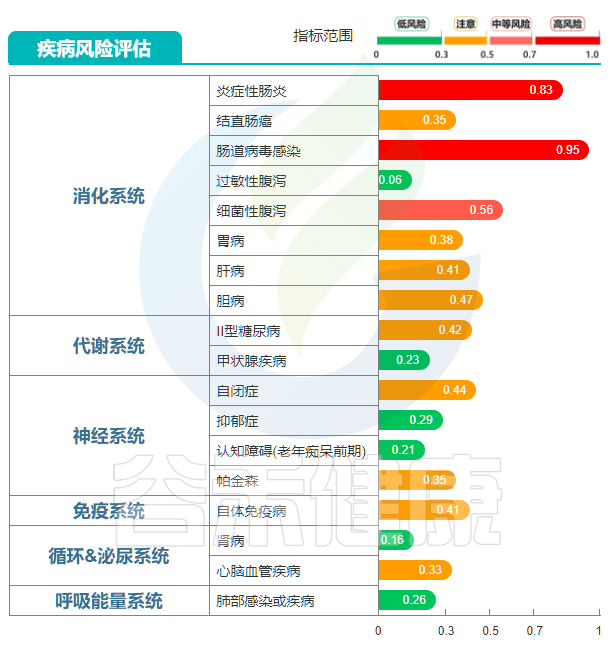

炎症性肠炎以及肠道病毒感染在内的多项疾病风险评估显示中高风险,炎症性肠炎分值为0.83
治疗方式
阿达木单抗治疗,同时结合肠道菌群检测结果补充益生菌,调整饮食结构和生活习惯。
|修美乐(阿达木单抗注射液)是目前中国首个可以用于治疗克罗恩病的全人源抗肿瘤坏死因子(TNFi)单克隆抗体。
治疗6个月后肠道菌群检测评估
健康总体评估和肠道年龄:


治疗后肠道菌群总体情况:
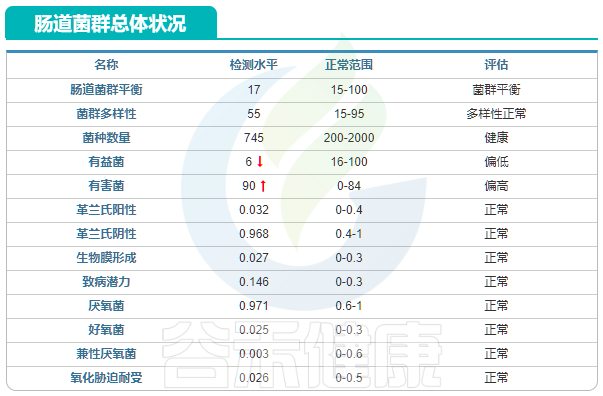

治疗后病原菌检测:
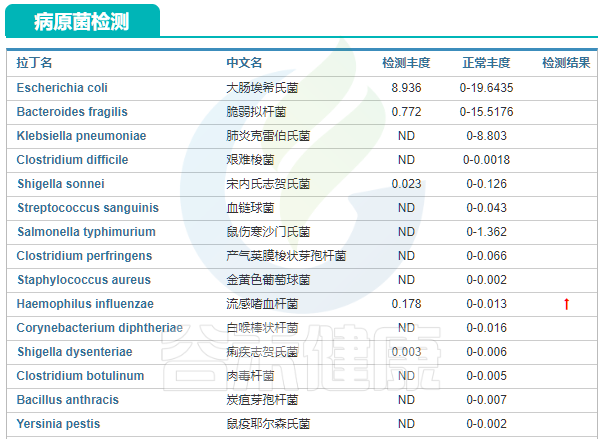

治疗6个月后患者无再次出血情况,感觉良好,肠道菌群结果显示肠道菌群基本恢复平衡,有益菌虽仍偏少,但较治疗前增加,有害菌数量较治疗前减少,原来超标的病原降低或者消失。

包括炎症性肠炎在内的多项疾病风险较之前显著下降,炎症性肠炎分值仅为0.38。
其中炎症相关指标显示(治疗后):炎症指标,白介素6,钙卫蛋白和高敏C反应蛋白均恢复正常。
炎症相关指标前后对比
治疗前:


治疗后:

可以看到明显改善。
我们再看,这些炎症指标发挥什么作用。
白介素6
白介素6 ( IL-6) 是细胞因子网络中的重要成员,是一种功能广泛的多效性细胞因子,炎症反应发生后,IL-6率先生成,产生后诱导产生CRP和降钙素原(PCT)生成。如在发生感染、内外伤、外科手术、应激反应、脑死亡、肿瘤产生以及其他情况的急性炎症反应过程中会快速产生。IL-6参与许多疾病的发生和发展,其血液水平与炎症、病毒感染、自身免疫疾病密切相关,它的变化比高敏C反应蛋白更早。
IL-6分泌或基因表达异常往往可导致一系列疾病的发生,在病理状态下IL-6可大量分泌进入血液循环,检测IL-6对于了解病情、判断预后都有非常重要的意义。
钙卫蛋白
钙卫蛋白是钙卫蛋白是一种来自于中性粒细胞分泌的钙和锌结合蛋白,广泛分布于人体细胞、组织和体液中。
钙卫蛋白是一个相当稳定的蛋白,随着钙的出现而出现,在粪便中不易被酶降解,从而使其可能成为一个方便的肠道炎症监测指标。
目前越来越多的临床和研究认可将钙卫蛋白则体现了黏膜的病变程度,肯定其在炎症性肠病的治疗中具有重要的指导作用。
此外,粪钙卫蛋白目前已经越来越多地用于预测IBD维持治疗期间的疾病复发。内镜检查可以提供客观的黏膜炎症改善结果,但内镜是一种侵入性检查,频繁进行患者难以耐受。粪钙卫蛋白是一种可以准确反映肠道黏膜炎症病变的非侵入性生标志物。
但是注意对于腹泻患者而言,粪便钙卫蛋白正常不能排除药物性腹泻(例如,二甲双胍,质子泵抑制剂引起的腹泻)、胆盐吸收不良或其它腹腔疾病。轻微的结肠炎也可能使钙卫蛋白的检测值升高。
高敏C反应蛋白
阿达木单抗克罗恩病的获批是基于两项关键性临床研究的结果,其中包括一项2期、随机、双盲、多中心研究,评价两组阿达木单抗剂量方案在高敏C反应蛋白升高的中重度活动性克罗恩病中国受试者中的药代动力学、安全性和有效性。
有效性结果证实:与阿达木单抗80/40 mg治疗方案相比,存在中度至重度活动性克罗恩病和hs-CRP水平升高的中国受试者采用阿达木单抗160/80 mg治疗方案治疗后可更快获得临床缓解和临床应答,而且客观疾病指标(hs-CRP和粪便钙卫蛋白)的改善更快。
1. 克罗恩病的早期征兆是什么?
虽然没有两个人会以相同的方式经历克罗恩氏病,但大多数人会出现腹泻和腹痛或绞痛。其他常见症状包括直肠出血,恶心,食欲不振,急需使用洗手间和便秘。
体重减轻,疲劳,关节痛,眼睛发红或发痒以及皮肤发红或起伏也可能发生。
2. 哪些饮食变化帮助控制克罗恩病?
没有克罗恩氏病的单一饮食。但是,您可能要避免的常见诱因包括全谷类,坚果和种子,未加工的水果和蔬菜,辛辣食物,高脂或油腻食物以及含咖啡因和酒精的饮料。
在爆发期间,当症状最严重时,坚持温和,流食类的食物可能会有所帮助。
3. 如果不治疗,会发生什么?
克罗恩病伴发的持续炎症会导致许多并发症。一个常见的消化问题是肠道阻塞,当炎症导致疤痕组织积聚并缩小肠道区域时,就会发生肠道阻塞。其他并发症包括肛门撕裂,感染袋,营养不良和结肠癌。
Tips
不同克罗恩病患者之间的疾病表现和肠道微生物组均不同,治疗结果差异可能也很大,但是本案例让我们看到了菌群监测对于克罗恩病的辅助判别和治疗疗效潜在的应用价值。
肠道菌群真正应用于临床并造福病人需要扎实的临床数据和更多的临床积累。我们会积极探索和与更多临床科室合作,将谷禾多年的菌群检测与临床需求相结合,科学和精准的推进肠道微生态临床应用。
相关阅读:
主要参考文献:
Allocati N, Masulli M, Alexeyev MF, Di Ilio C. Escherichia coli in Europe: an overview. Int J Environ Res Public Health. 2013;10(12):6235-6254. Published 2013 Nov 25. doi:10.3390/ijerph10126235
Mirsepasi-Lauridsen HC, Vallance BA, Krogfelt KA, Petersen AM. Escherichia coli Pathobionts Associated with Inflammatory Bowel Disease. Clin Microbiol Rev. 2019;32(2):e00060-18. Published 2019 Jan 30. doi:10.1128/CMR.00060-18
Haffajee AD, Teles RP, Patel MR, Song X, Yaskell T, Socransky SS, Factors affecting human supragingival biofilm composition. II. Tooth position. J Periodontal Res. 2009 Aug; 44(4):520-8.
Zhu B, Macleod LC, Kitten T, Xu P. Streptococcus sanguinis biofilm formation & interaction with oral pathogens. Future Microbiol. 2018 Jun 1;13(8):915-932. doi: 10.2217/fmb-2018-0043. Epub 2018 Jun 8.
Lindsey KonkelMedically, Kareem Sassi, MD.
What Is Crohn’s Disease? Symptoms, Causes, Diagnosis, Treatment, and Prevention, 2020.5.29
修美乐®用于治疗中至重度成人克罗恩病的关键临床研
《中国大陆克罗恩病的患病率和发病率:55年研究的荟萃分析》2010;11(3):161-6.