-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com

谷禾健康
Blautia (经黏液真杆菌属)
Blautia 是一种最近发现的细菌属,是将几种丰富的胃肠道细菌归类,这些细菌以前属于 Ruminococcus 属。基于表型和系统发育分析,梭菌属和瘤胃球菌属中的一些物种也已被重新归类为Blautia.
Blautia 作为毛螺菌科的一个属,自成立以来,因其对缓解炎症性疾病和代谢疾病的贡献以及对特定微生物的抗菌活性而备受关注。最近的几份报告表明,肠道中Blautia菌的组成和变化与宿主年龄、地理、饮食、基因型、健康状况、疾病状态和其他生理状态等因素有关。
研究人员发现:该属中的物种水平在老年患者中经常减少,在结直肠癌患者的黏膜样本中水平降低,在肠易激综合征 (IBS) 患者中水平升高。
此外,Blautia与内脏脂肪面积负相关,内脏脂肪面积被认为是心血管和代谢疾病风险的肥胖生物标志物。研究还确定了Blautia luti 和Blautia wexlerae 的减少与肥胖个体的胰岛素抵抗有关。Blautia菌通过产生细菌素来防止病原体的定植,并通过上调调节性 T 细胞和 SCFA 的产生而表现出抗炎特性和维持葡萄糖稳态作用。
Blautia. 图片来源:microbiomology
Blautia 属严格厌氧,不能运动,是哺乳动物肠道内重要的核心菌属。Blautia 能够使用氢气和二氧化碳来制造乙酸盐。乙酸是肠上皮细胞的次要能力来源,也是肌肉和脑组织的能量来源,可以抑制病原菌,有抗炎作用。
Blautia菌通常为球形或椭圆形,成对或成股出现,大多数菌株无孢子。Blautia广泛分布于哺乳动物的粪便和肠道中。大多数Blautia菌株的最适温度和 pH 值分别为 37°C 和 7.0。DNA的GC含量约为 37-47 mol%。
培养实验表明,所有Blautia菌株都可以利用葡萄糖,但不同菌株对蔗糖、果糖、乳糖、麦芽糖、鼠李糖和棉子糖的利用能力不同。Blautia发酵葡萄糖的最终产物是乙酸、琥珀酸、乳酸和乙醇,主要生化试验显示卵磷脂、脂肪酶、过氧化氢酶和吲哚的阴性结果。
Blautia菌株的碳水化合物利用特性
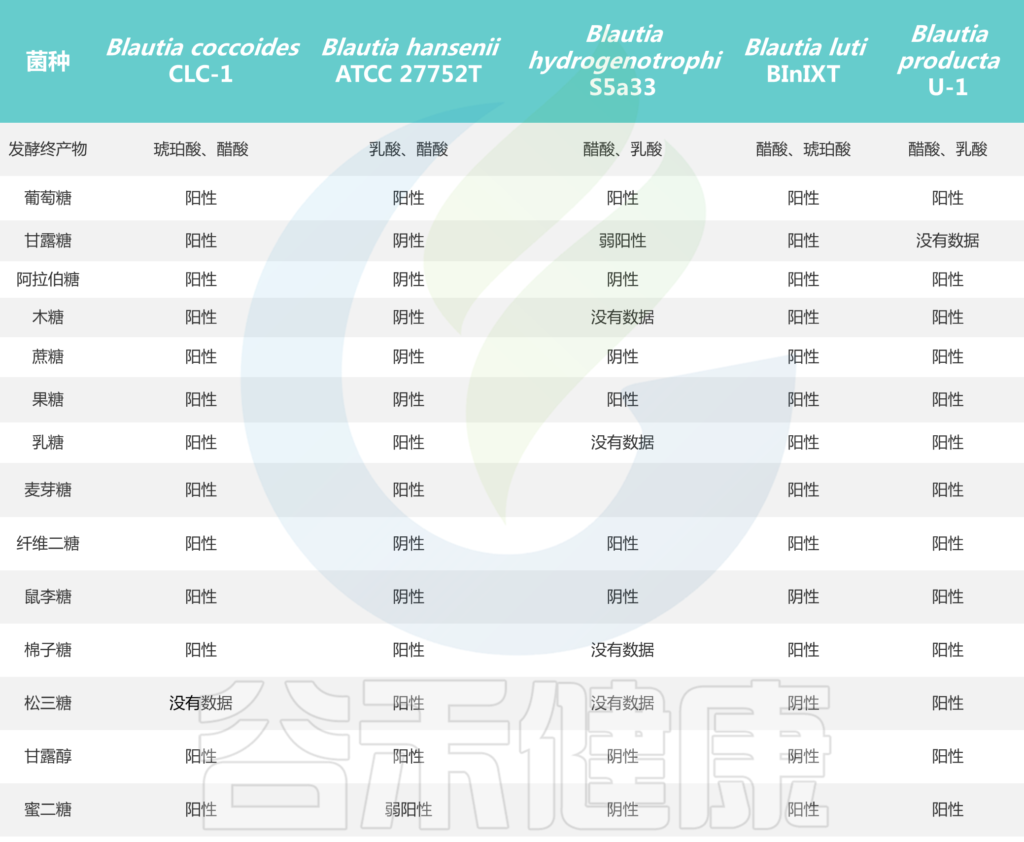

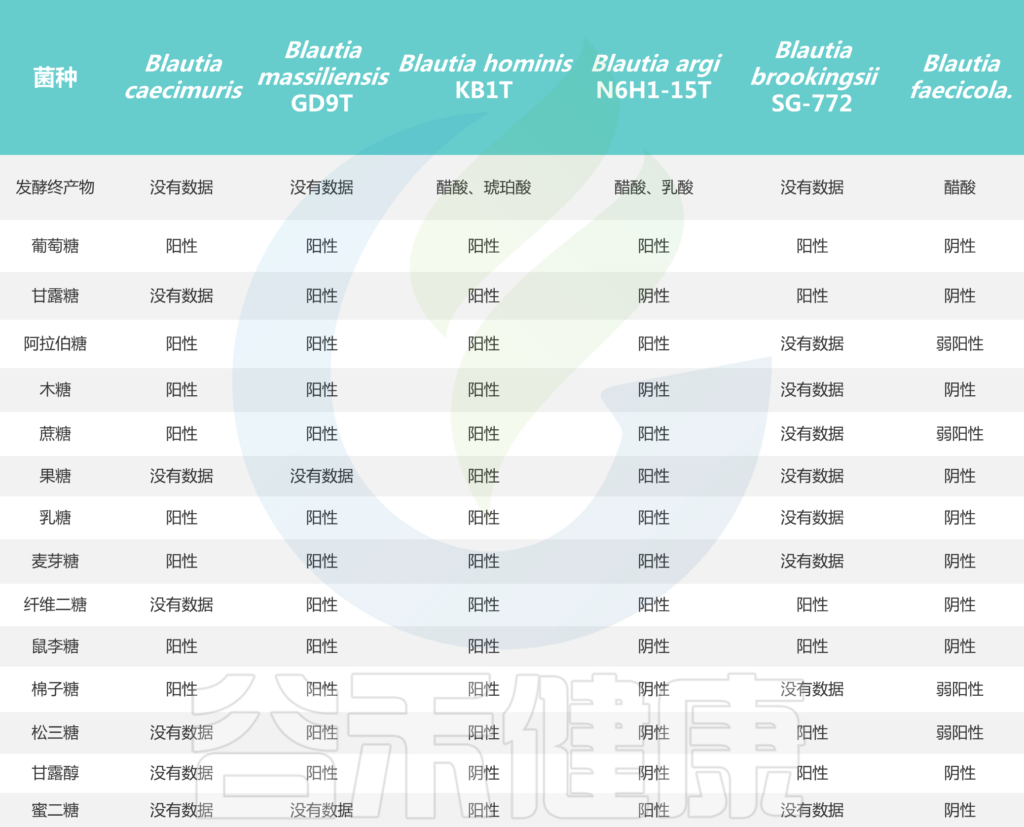
Liu X, et al., Gut Microbes. 2021
Blautia属目前根据公布的有效名称物种共计20个,包括:
它们最初被错误分类为Ruminococcus、梭菌属或瘤胃球菌属。
文献中报道的Blautia的所有种
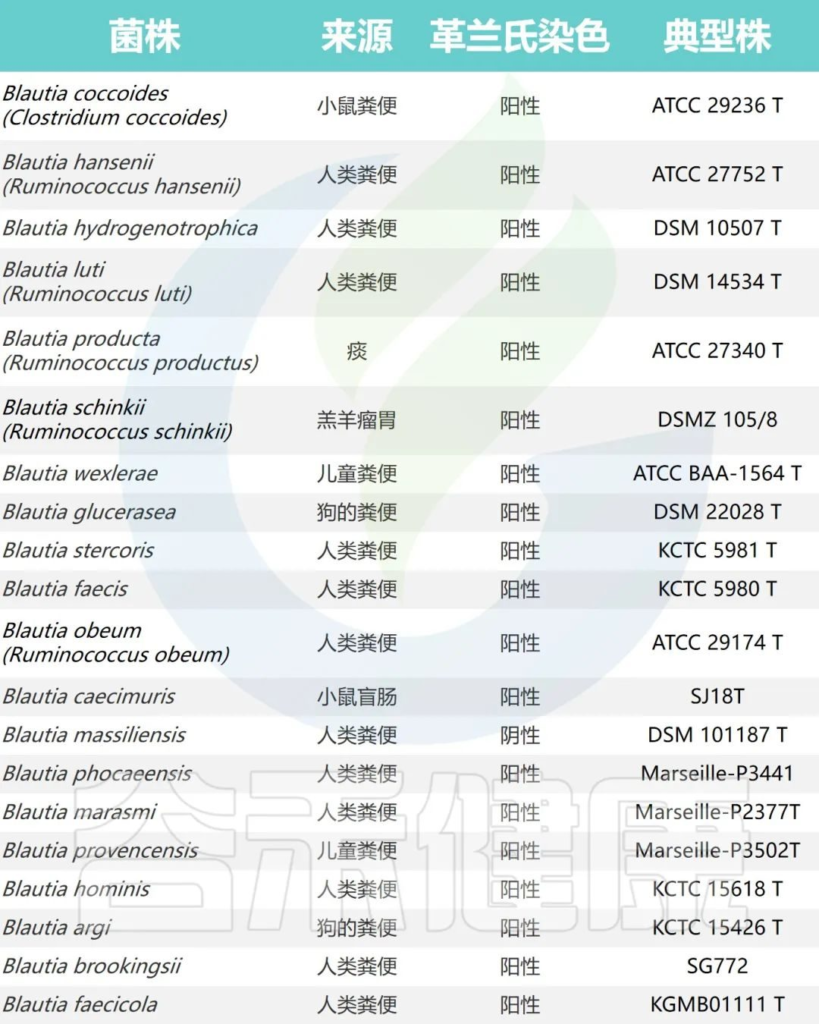
Liu X, et al., Gut Microbes. 2021
该属的组成通过增加新的种和品系而不断更新,但总的来说,Blautia中的种仍形成一个相对稳定和连贯的单系分支。
不同物种首次发现的来源不同,但是主要物种都是从人粪便分离出来的。
例如:Blautia hydrotrophica (B.hydrotrophica)和Blautia stercoris (B. stercoris) 首先是从人类粪便中分离出来的。
B.hydrotrophica 的代谢途径
Blautia hydrotrophica 是革兰氏阳性、无芽孢、球杆菌状细菌,平均大小为 0.7-0.6 毫米。Hydrogenotrophica,意为以氢为食,是指生物体利用 H2 和 CO2 作为生长能源的能力。它将 H2 和 CO2 代谢形成乙酸盐作为唯一代谢物自养生长。该生物体还能够使用几种不同的有机化合物作为底物异养生长。通过葡萄糖和果糖的发酵,乙酸是主要产物,但也可以形成乙醇、乳酸以及较小程度的异丁酸和异戊酸。
B.hydrotrophica的生存环境
B.hydrotrophica的最佳栖息地pH范围为6.0-7.0,温度为35-37˚C。B.hydrotrophica也可能是一种重要的微生物,可替代反刍家畜体内的产甲烷菌,以限制释放的甲烷量。
B.hydrotrophica栖息在哺乳动物的内脏中,有助于分解宿主饮食中原本难以消化的部分,主要是植物材料。膳食多糖和蛋白质的分解是通过微生物群在厌氧肠道环境中发酵完成的。这些微生物群是共生的,这意味着它们的相互作用创造了一个相互关联的食物网。这种代谢食物网的产物是短链脂肪酸,例如乙酸盐、其他有机酸以及 H2 和 CO2 气体。H2 气体的积累实际上可以抑制 NADH 的再氧化,从而减少 ATP 和短链脂肪酸的产生量。据估计,这些短链脂肪酸的代谢产生了人类所需能量的 5%-10% 。Blautia hydrotrophica在宿主新陈代谢中发挥重要作用,因此更好地了解这些微生物可能会导致能够操纵人体能量平衡。
B. wexlerae和B. luti 是Blautia中最丰富的物种,是人类肠道的主要物种之一。
B. wexlerae 治疗代谢疾病
Blautia wexlerae ( B. wexlerae ) 是主要的丁酸盐生产者。动物实验表明,丁酸盐可以改善胰岛素抵抗,减少脂肪堆积。因此,这可能是B. wexlerae抗肥胖的机制之一。B. wexlerae在治疗代谢疾病方面具有发展潜力。
B. faecis DSM33383 菌株预防管理呼吸道疾病
Blautia faecis也是从人粪便分离出来的,细胞染色呈革兰氏阳性、严格厌氧。研究人员已经确定了B. faecis DSM33383 菌株,该菌株降低了 TNF 诱导的肠上皮细胞系 HT-29 产生的 IL-8。在流感后的两个临床前模型中进一步研究了该菌株的作用表明该菌株胃内给药可保护感染了肺炎链球菌的小鼠,并在较小程度上保护鼠伤寒沙门氏菌继发感染。该研究表明,粪杆菌DSM33383 可能是预防和管理呼吸道传染病的有希望的候选者。
B. coccoides参与促炎途径
B. coccoides最初是从喂食高乳糖饮食的小鼠的粪便中分离出来的;Blautia coccoides已通过免疫调节和促炎途径参与多发性硬化,包括与抗原呈递、B 和 T 细胞活化以及补体活化相关的基因的上调。
B. hydrogenotrophica,以前称为 Ruminococcus hydrogenotrophicus,是一种在哺乳动物(人类和反刍动物)的肠道内发现的物种。
B. glucerasei从狗的粪便中分离出来。
另外的物种如B. producta和B. schinkii甚至从痰液、污水和瘤胃中分离出来。
这些发现表明Blautia在肠道和其他微环境中的生存和进化的重要性。
当细菌从膳食成分中产生的代谢物作为底物支持其他物种的生长时,称为交叉喂养。交叉喂养是肠道微生物群中厌氧菌之间的重要相互作用,可影响其代谢途径并有助于其稳定性和生产力。
作为厌氧菌的一个属,Blautia与其他细菌的交叉喂养也在一定程度上有助于代谢调节。
Blautia & R. bromii
一项研究发现,通过使用 0.2% 的抗性淀粉作为能量来源,布氏瘤胃球菌(R. bromii)在 RUM-RS 培养基上可以产生大致相等摩尔比的甲酸、乙醇和乙酸。
注:布氏瘤胃球菌(R. bromii)是存在于人类肠道中的降解抗性淀粉的细菌,富含抗性淀粉的饮食可以增加它的丰度。
然而,在淀粉上与产乙酸细菌B. hydrotrophica进行批量共培养导致甲酸消失,乙酸水平增加。产生甲酸的物种和产生乙酸的物种之间的交叉喂养可能在结肠中短链脂肪酸的形成中起重要作用,并有助于大量产生乙酸。
Blautia & Dorea
在肠易激综合征 (IBS) 患者中观察到 Blautia 菌种水平升高,研究人员推测可能由于由高丰度的Dorea菌产生的较高气体水平,Dorea 是一种可以被 Blautia 使用的细菌。
Blautia & B. bifidum
Blautia hydrotrophica消耗 H2和 CO2通过 Wood-Ljungdahl 途径产生乙酸——当与双歧双歧杆菌共存时,该途径显着激活。B. bifidum (双歧双歧杆菌)作为一种特殊的碳水化合物发酵物种并产生 CO2,它是 Wood-Ljungdahl 途径中的固定底物。因此,在 Blautia hydrotrophica 中观察到的 Wood-Ljungdahl 途径的变化可能是B. bifidum交叉喂养的结果。
备注:Wood-Ljungdahl 途径又称为厌氧乙酰辅酶 A 途径,存在于产甲烷菌、硫酸盐还原菌和产乙酸菌等化能自养的厌氧细菌和古生菌中。
饮食是驱动肠道菌群组成和代谢活动的主要因素,不同种类和数量的饮食以及主要营养素之间的平衡对肠道微生物有显着影响。
酒曲通过糖基神经酰胺作为 Blautia coccoides 的益生元
传统的日本烹饪方法和食,其中包含用非致病性真菌酒曲制备的发酵食品,与日本人的长寿密切相关。一项研究报道,酒曲中含有大量的糖基神经酰胺,并表明在小鼠饮食中添加 1% 纯化的糖基神经酰胺作为益生元1周可以提高小鼠肠道中球状芽孢杆菌的丰度,减少其血液糖水平,并上调其肾腺激素水平。同时发现Blautia coccoides可以将糖基神经酰胺降解为神经酰胺,然后将神经酰胺代谢为脂肪酸和鞘氨醇碱,它们被肠道吸收并产生有益作用。
玉米中提取的膳食纤维F-FOP增加Blautia
将从玉米中提取的膳食纤维 (F-FOP) 添加到喂食高脂肪 (HF) 饮食的小鼠的饮食中,显着增加了小鼠粪便中Blautia的丰度。与 HF 饮食的小鼠相比,F-FOPs + HF 饮食的小鼠表现出体重和组织重量的损失,结果显示Blautia的丰度与肥胖相关代谢紊乱的标志物呈负相关。
低聚果糖、冻干豆浆增加Blautia
在喂食高脂饮食的大鼠中添加 20% 的冻干豆浆会导致大鼠粪便中的Blautia含量增加。
在一项研究中,将 30 只雌性大鼠分为六组,分别喂食酪蛋白或大豆分离蛋白,每组都含有纤维素、棉子糖或低聚果糖 (FOS)。结果表明,两种来源的日粮蛋白质都可以改变大鼠粪便中乙酸浓度和乳酸杆菌的丰度,但无论膳食蛋白质来源如何, FOS都会增加Blautia的丰度。
研究还表明,大鼠肠道酸化可能会抑制次级胆汁酸的形成。
omega-3增加Blautia
在另一项研究中,一名 45 岁的男性志愿者每天摄入 600 毫克 omega-3,持续 14 天,该志愿者的整体肠道微生物多样性下降,尤其伴随着粪杆菌丰度的降低和Blautia丰度的显着增加。
交替饮食和自助饮食增加Blautia
除了食物,人们的饮食方式也会塑造肠道菌群。与普通饮食相比,交替饮食和自助饮食可以提高肠道菌群中Blautia菌属和瘤胃球菌的丰度,此外还会引起一些宿主代谢相关参数的变化。随着全基因组测序的发展,未来的研究可以检验各种饮食如何调节Blautia的代谢活动并改善宿主健康。
在生命的不同阶段(即从童年到成年再到老年)的过渡期间,肠道微生物群会发生显着变化。使用高通量测序对 367 名 0-104 岁健康日本受试者的粪便样本进行的横断面研究报告称,日本成年人(21-69 岁)的肠道微生物群含有高丰度的Blautia和Bifidobacterium和低丰度Bacteroides。此外,与成年人相比,老年人的微生物组多样性和个体微生物丰度降低,包括Blautia丰度降低。这种现象可能与年龄相关的免疫功能下降(称为免疫衰老)有关,并伴有许多与年龄相关的疾病,包括慢性低水平炎症。
Blautia wexlerae和Bifidobacterium pseudocatenulatum的丰度在成人型肠道微生物群中显着更高,而在老年型肠道微生物群中观察到兼性厌氧菌(如大肠杆菌)的丰度更高。这些发现表明,通过增加会随着年龄增长而减少的菌群,将肠道微生物群从老年人型转变为成人型,可以预防与年龄相关的疾病的风险。
最近的一项研究分析了来自亚洲温带和热带地区五个国家的城市或农村地区的 303 名学龄儿童粪便样本中的微生物群落特征。儿童肠道菌群分为普氏菌属(P型)和双歧杆菌/拟杆菌属(BB型)两组。中国(包括台湾地区)、日本等温带地区儿童肠道菌群多为BB型,泰国、印度尼西亚等热带地区儿童肠道菌群多为P型。值得注意的是,Blautia 在 BB 型肠道菌群中显着富集,占总 BB 型细菌组成的 10%,但仅占总P的 5%。
一项研究指出,日本人的主要肠道菌属是双歧杆菌和梭状芽孢杆菌。在美国人、中国人、法国人和西班牙人中存在拟杆菌属;在澳大利亚人中是Blautia。据报道,地理位置之间人类肠道微生物多样性的差异在很大程度上与遗传、生活方式和饮食有关。
有趣的是,据报道Blautia在双胞胎遗传中具有很强的分类关联。一项研究收集了七种宿主的粪便样本,包括人类、猪、牛、鹿、狗、猫和鸡,并对 16S rRNA 基因的 V6 区域进行了测序。发现Blautiaoligotypes可以准确识别不同的宿主来源,表明该属具有宿主特异性和宿主偏好。
近年来,Blautia对草本植物和功能性食品的生物转化和代谢的研究引起了研究关注。
多甲氧基黄酮 (PMF) 是从山奈和柑橘类水果中分离出来的黄酮类化合物,具有抗癌、抗炎、抗病毒和抗凝血等生物学功能。
研究表明,Blautia菌属通过将 5,7-二甲氧基黄酮 (5,7-DMF) 和 5,7,4-三甲氧基黄酮 (5,7,4-TMF)分别转化为具有生物活性的白杨素和芹菜素,对芳基甲基醚官能团具有水解作用。该菌还具有去糖基化能力,它可以将异黄酮、黄酮和类黄酮代谢成相应的苷元。
作为黄酮类化合物的另一个例子,姜黄素在治疗某些疾病,包括癌症、心血管疾病、糖尿病、肝病和神经退行性疾病方面表现出抗氧化、抗炎、抗病毒、抗菌的有益作用,受到了广泛的关注。
由于姜黄素结构中含有β-二酮,该化合物具有高的疏水性、低的溶解性和“生物利用度”,因此,每天大量摄入姜黄素,可以观察到对健康的促进作用。不幸的是,大量摄入姜黄素可能会产生有害影响并降低疗效,这会导致限制了姜黄素在疾病预防中的应用。
由肠道细菌产生的姜黄素代谢物具有生物效应,而不是姜黄素的原始形式。
据报道,姜黄素是由人肠道细菌Blautia 菌株MRG-PMF1通过甲基芳醚裂解,转化为去甲基姜黄素和双去甲基姜黄素的。有证据表明,未被吸收的姜黄素可以间接调节结肠微生物群,通过产生额外的生物可利用和生物活性分子(如二氧去甲基姜黄素和二甲氧基姜黄素)对多种疾病产生有益的影响。
此外,Blautia sp AUH-JLD56 菌株已被证明可特异性且有效地将牛蒡子苷或牛蒡子苷元生物转化为具有良好自由基清除活性的 (-)-3′-去甲基牛蒡子苷元。 B. glucerasei sp. 产生一种特定的细胞外葡萄糖神经酰胺酶,将葡萄糖神经酰胺水解成功能性物质,对结肠癌具有特定的预防作用。
但是值得提醒的是,Blautia的某些生物转化可能无益,甚至可能有害。某些Blautia物种可以对初级胆汁酸进行 7-α-脱羟基化,并将其转化为次级胆汁酸,如石胆酸和脱氧胆酸。这些物质是诱发结肠癌的致癌物,在溃疡性结肠炎、发育不良或癌症患者的粪便中发现这些物质浓度高。
一般来说,肠道中的细菌代谢不涉及氧气,而是还原和水解,导致形成非极性低分子量产物。在类黄酮转化过程中,Blautia菌种催化的反应包括去甲基化、脱羟基化、O-和 C-去糖基化和 C-环裂解,这可能是由于其相应的酶,如 β-葡萄糖苷酶和 O-糖苷酶。因此,深入开发Blautia对生物转化的探索对于开发用于食品补充剂的新酶和生物活性代谢物至关重要,并为人体肠道微生物组的代谢组学研究提供有价值的视角。
次级代谢产物是微生物在生长代谢过程中产生的具有生物活性的化合物,广泛用于抗菌抗癌药物、除草剂、杀虫剂等,也是微生物药物开发的重要来源。如双歧杆菌产生的细菌素对单核细胞增生李斯特菌、产气荚膜梭菌和大肠杆菌等病原微生物具有抗菌活性。
Blautia通常具有生产细菌素的能力。通过antiSMASH数据库对次生代谢物的注释,将74株Blautia菌株注释为7类共261个次生代谢生物合成基因簇(BGCs),包括NRPS、sactipeptide、lanthipeptide、bacteriocin、lassopeptide、betalactone、transat-pks。
NRP、sactipeptide、lanthipeptide 通常分布在所有菌株中。NRP 和 PK 是具有多种功能的最丰富的次级代谢产物家族之一,包括参与铁清除的铁载体、提供针对一系列压力因素的保护的色素,以及营养获取、化学通讯和防御反应。
备注:antiSMASH数据库可实现基因组与基因组之间的相关天然产物合成基因簇的查询和预测。临床上使用的大部分抗生素和药物均来自植物或微生物的天然产物。近二十年来,基因组数据的不断增加,使通过基因组挖掘来获取化合物的生物合成簇成为可能。antiSMASH是该领域最流行的工具之一。自2011年首次发布以来,antiSMASH已成为次级代谢产物基因组挖掘的标准工具,antiSMASH数据库为许多公开可用的微生物基因组提供预先计算的antiSMASH结果,并允许进行高级跨基因组搜索。
Blautia产生的细菌群具有抑制肠道内病原菌定植的潜力,并且它还可以影响肠道微生物群的组成。研究显示B. obeum和B. producta可以抑制产气荚膜梭菌和耐万古霉素肠球菌的增殖,使其成为潜在的益生菌,发挥益生菌功能。
肠道微生物群是一个复杂的生态系统,与宿主疾病的发展、药物代谢、免疫系统调节和其他过程有关。Blautia 作为肠道微生物群中的优势菌属,与宿主生理功能障碍具有显着相关性,例如肥胖、糖尿病、癌症和各种炎症性疾病。
一项研究观察到连续 3 周食用低热量和高蛋白饮食的超重/肥胖非酒精性脂肪肝患者的肠道微生物群组成发生变化和Blautia丰度增加。在另一项研究中,无论是否存在非酒精性脂肪性肝炎,肥胖儿童的肠道拟杆菌属丰度较高,同时Blautia和粪杆菌丰度较低。
在一项基于人群的横断面研究中,研究人员调查了 20-76 岁日本男性和女性的内脏脂肪积累和体重指数与按性别分层的肠道微生物群的关系。发现Blautia是唯一一个其丰度与日本人的内脏脂肪积累呈显着负相关的属,无论性别如何。
Blautia是肠道中常见的乙酸生产者,可通过激活 G 蛋白偶联受体 GPR41 和 GPR43 来抑制脂肪细胞中的胰岛素信号传导和脂肪积累,进而促进其他组织中未结合的脂质和葡萄糖的代谢,从而减轻肥胖相关疾病。
Blautia是有效减肥组女性肠道菌群中的优势菌属,但在减肥无效组中则不然。在另一项研究中,与健康儿童相比,糖尿病儿童的Blautia丰度显着下降。一项横断面研究表明,Blautia,特别是B. luti和B. wexlerae,可能有助于减少与肥胖相关并发症相关的炎症。
肥胖组的Prevotella、巨型单胞菌(Megamonas)、梭杆菌属和Blautia显著增加。
Blautia作为共生的专性厌氧菌属,通过上调肠道调节性T细胞和产生短链脂肪酸,在维持肠道生态平衡和预防炎症方面发挥着重要作用。
IBD患者和健康人的粪便和黏膜菌群分析表明,CD患者盲肠黏膜菌群中Blautia的丰度显着降低。在结直肠癌患者的黏膜粘连菌群中,同样报道了Blautia的丰度降低。
霍乱弧菌通常会导致人类腹泻,但人们对病原体的易感性不同,这可能是由人际微生物组变异驱动的。
发现霍乱患者的肠道菌群与健康个体存在显着差异,其中Blautia obeum与霍乱弧菌的定植呈显着负相关。进一步研究表明,B. obeum基因组中编码胆汁盐水解酶(BSH)的基因可以降低霍乱弧菌tcpA基因的表达,抑制其定植,缓解腹泻。
一项生物标志物分析研究表明,接受异体 BMT 的患者肠道微生物群多样性增加,特别是Blautia属共生细菌的丰度增加,与致死性移植抗宿主病的减少和总生存期的增加有关。
少数研究也报道了Blautia丰度降低与回肠袋-肛门吻合和肝硬化的关系。Blautia作为共生的专性厌氧菌属,通过上调肠道调节性 T 细胞和产生短链脂肪酸,在维持肠道环境平衡和预防炎症方面发挥重要作用。
上述研究表明,Blautia的丰度与某些疾病呈负相关。然而,与健康个体相比,在肠易激综合征和溃疡性结肠炎患者的粪便微生物群中发现了更高丰度的Blautia.
尽管Blautia在各种疾病中的潜在机制尚不明确,但 Blautia丰度仍可作为相关疾病早期诊断或治疗的潜在工具。
老年人特别容易出现食欲不振和营养不良。这可能部分是由于肠道微生物群老化。Blautia属的较低丰度可能与营养不良有关,而来自毛螺菌科、瘤胃球菌科 UCG-002、Parabacteroides merdae和Dorea formicigenerans 的分类群丰度较高与食欲不振相关。食欲不振或营养不良的参与者的粪便乙酸水平降低。
Blautia丰度减少可能会增加慢性低度炎症,并降低通过发酵从饮食中摄取的能量。该结论需要进一步的研究支持。
与对照组相比,来自虚弱组的粪便样本下列菌群具有较高的水平:
Akkermansia, Parabacteroides, Klebsiella
而共生属较低水平菌群如下:
Blautia, Megamonas, Faecalibacterium, Prevotella, Roseburia
在自闭症谱系障碍患有功能性肠胃疾病的儿童中观察到几种与粘膜相关的梭菌显着增加,而 Dorea 和Blautia以及 Sutterella的显着减少。
此外,帕金森病患者子中发现在属的分类水平上,来自 Blautia、Coprococcus 和 Roseburia 属的推定“抗炎” 丁酸盐产生菌在对照组的粪便中明显多于帕金森病患者。
肌肉减少症是一种症状性病症,其特征是由于骨骼肌质量随着年龄的增长而过度损失,导致肌肉力量和身体机能下降。
肌肉减少症伴随着身体平衡差、步态障碍、使用拐杖和跌倒。研究发现与附肢骨骼肌质量/体重 (ASM/BW)与 ASM/BW 呈正相关的Blautia、Bifidobacterium可能有助于增加骨骼肌质量。
Blautia coccoides可能会通过免疫调节和促炎途径参与多发性硬化,包括与抗原呈递、B 和 T 细胞活化以及补体活化相关的基因的上调。与其他疾病一样,在多发性硬化中,肠道菌群失调会增加肠道通透性,从而促进 LPS 的进入。
如何增加(来自文献,证据不是很充分)
食物:
富含 Omega-3 的食物
糙米
大麦
迷迭香
黄酮类
高谷物饮食
益生元或药物:
二甲双胍
黄连素
小檗碱
红花油
丁酸钠
抗性淀粉(II、IV型)
橙子(果胶/黄烷酮)
葡萄籽多酚/酒
亚麻籽
维生素 D3
益生菌:
枯草芽孢杆菌
布拉酵母菌
德氏乳杆菌
鼠李糖乳杆菌GG
长双歧杆菌 BB
例如:一项研究指出富含阿拉伯木聚糖的麦麸提取物会提高Blautia物种的比例 ,这表明有可能设计基于饮食的干预措施,以增加肥胖儿童体内耗尽的这些细菌物种的肠道生态系统。需要对B. luti和B. wexlerae菌株进行临床前和临床干预试验,以明确证明它们对肥胖和糖尿病前期状态的潜在保护作用。
减少Blautia
人类肠道微生物研究的不能忽略的关注之一是研究核心微生物群。拟杆菌、普雷沃氏菌、瘤胃球菌、经黏液真杆菌属(Blautia)、考拉杆菌、罗伊氏菌、吉米菌、粪杆菌、毛螺菌以及梭菌等是世界代表性人群的核心肠道菌群。在目前谷禾健康超过60万的肠道菌群数据库中,肠道微生物群的几个核心肠道细菌普遍存在于超过90%人群粪便中。
Blautia作为一个重要的核心菌属,在肠道中占比丰度,是短链脂肪酸尤其乙酸的主要生产者,对于减肥和抗炎均有重要的积极作用。此外,其属下某些菌株分泌的细菌素可以抑制特定病原菌,这对于当下耐药性问题无疑看到了新方向。
但是经黏液真杆菌属(Blautia)作为一种严格厌氧的细菌,需要苛刻的培养条件和严格的操作程序。因此,将属于该属的细菌用作商业益生菌并不容易。相反,Blautia的益生元底物可以用于健康维护。一些食物成分,例如低聚果糖、乳果糖和日本酒曲糖基神经酰胺,均表明可以增加小鼠体内的Blautia丰度。然而,需要注意的是粪便微生物群的益生元作用也会因人而异。
主要参考文献:
Liu X, Mao B, Gu J, Wu J, Cui S, Wang G, Zhao J, Zhang H, Chen W. Blautia-a new functional genus with potential probiotic properties? Gut Microbes. 2021 Jan-Dec;13(1):1-21.
Benítez-Páez A, Gómez Del Pugar EM, López-Almela I, Moya-Pérez Á, Codoñer-Franch P, Sanz Y. Depletion of Blautia Species in the Microbiota of Obese Children Relates to Intestinal Inflammation and Metabolic Phenotype Worsening. mSystems. 2020 Mar 24;5(2):e00857-19.
Stanley D, MS G, SE D, VR H, TM C, RJ H, RJ M. Identification of chicken intestinal microbiota correlated with the efficiency of energy extraction from feed. Vet Microbiol. 2013;164(1–2):85–21.
Biddle A, Stewart L, Blanchard J, Leschine S. Untangling the genetic basis of fibrolytic specialization by lachnospiraceae and ruminococcaceae in diverse gut communities. Diversity. 2013;5(3):627–640.
Chakravarthy SK, Jayasudha R, Prashanthi GS, Ali MH, Sharma S, Tyagi M, Shivaji S. Dysbiosis in the gut bacterial microbiome of patients with uveitis, an inflammatory disease of the eye. Indian J Microbiol. 2018;58(4):457–469.
Milani, C.; et al. The first microbial colonizers of the human gut: composition, activities, and health implications of the infant gut microbiota. Microbiology and molecular biology reviews. 2017, 81(4): e00036-17.
Luu TH, Michel C, Bard JM, Dravet F, Nazih H, Bobin-Dubigeon C. Intestinal Proportion of Blautia sp. is Associated with Clinical Stage and Histoprognostic Grade in Patients with Early-Stage Breast Cancer. Nutr Cancer. 2017 Feb-Mar;69(2):267-275
Chen, W., Liu, F., Ling, Z. et al. “Human Intestinal Lumen and Mucosa-Associated Microbiota in Patients with Colorectal Cancer.” PloS ONE. 7(6): e39743; doi: 10.1371/journal.pone.0039743
Grisham, J. “Bacteria May Hold the Key to Preventing Dangerous Side Effect of Transplants.” Memorial Sloan Kettering Cancer Center. (2014). Memorial Sloan Kettering Cancer Center
Jenq, R.R., Taur, T., Devlin, S.M. et al. “Intestinal Blautia is Associated with Reduced Death from Graft-versus-Host Disease.” Biology of Blood and Marrow Transplantation. (2015). 21(8) 1373-83; doi: http://dx.doi.org/10.1016/j.bbmt.2015.04.016,/p>
Murat Eren, A., Sogin, M.L., Morrison, H.G. et al. “A single genus in the gut microbiome reflects host preference and specificity.” The ISME Journal. (2015). 9: 90-100; doi: 10.1038/ismej.2014.97
Rajilić-Stojanović, M., de Vos W.M. “The first 1000 cultured species of the human gastrointestinal microbiota.” FEMS Microbiology Reviews. (2014). 38(5) 996-1047; doi: 10.1111/1574-6976.12075
Horigome A, Hashikura N, Yoshida K, Xiao JZ, Odamaki T. 2′-Fucosyllactose Increases the Abundance of Blautia in the Presence of Extracellular Fucosidase-Possessing Bacteria. Front Microbiol. 2022 Jun 2;13:913624.

谷禾健康

膀胱癌主要是老年人的疾病,约75%的新诊断发生在65岁以上的患者,约45%发生在75岁以上的患者。膀胱癌对男性和女性的影响比例为3:1,但随着年龄的增长,男性和女性的发病率都显著增加。
年龄增长与膀胱癌的发病率和死亡率升高有关。高龄还与慢性炎症标志物升高以及肠道和尿液微生物群紊乱有关。
老年人膀胱癌发病率和死亡率增加的一个原因可能是,微生物组中与年龄相关各种变化,引起全身代谢变化,导致免疫失调,具有潜在的致癌作用。
膀胱癌患者的肠道和尿道微生物群可能失调,尽管这些变化的影响尚不清楚。
提高对免疫系统、肠道和尿液微生物群的年龄相关改变的理解,可能有助于深入了解老年人膀胱癌发生和发展的风险。在膀胱癌患者中,提高对微生物群的认识也可能为治疗干预提供潜在的靶点。
目前的数据支持炎症、免疫和微生物失调可能是已知的与衰老相关的膀胱癌发病率增加的原因,但需要在这一领域开展工作,以直接检验这一假设,以及更好地了解肠道中微生物成分的组成,膀胱癌期间膀胱和膀胱肿瘤微生物组及其对免疫系统的影响。
从这个角度出发,本文讨论了炎症、免疫、衰老和癌症之间的复杂联系。研究了表明老龄化和炎症可促进膀胱癌发展的数据,老龄化如何导致或促进多个区域的菌群失调,以及菌群失调如何影响对膀胱癌治疗的反应。
本文主要从以下几个方面讲述
本文出现的专业名词缩写
非肌肉浸润性膀胱癌——NMIBC
肌肉浸润性膀胱癌——MIBC
肿瘤坏死因子——TNF
损伤相关的分子模式——DAMPs
病原相关的分子模式——MAMPs
血清中性粒细胞:淋巴细胞比值——NLR
免疫组织化学——IHC
肠血管屏障——GVB
高龄不仅与患膀胱癌的风险增加有关,还与发生侵袭性肿瘤有关,这些肿瘤复发和发展为侵袭性疾病的可能性增加。
这些数据很复杂,因为“年轻”和“老年”的定义在研究中高度可变,可以作为连续或分类报告变量。此外,癌症特异性生存率增加背后的原因可能是多因素的,但仍然包括这样的事实:年轻患者通常比老年患者的肿瘤侵袭性更小、级别更低。
✦ 非肌肉浸润性膀胱癌:年轻患者肿瘤侵袭性更小,级别低,不易复发
年轻患者,如年龄小于30岁的患者,其乳头状、低级别Ta、非肌肉浸润性膀胱癌(NMIBC)的发病率高于年龄大于30岁的患者,其肿瘤通常较小、单发且不太可能复发。
尽管数据表明年轻患者和老年患者的肿瘤分期相似,即使按年龄<30岁或>30岁分组。膀胱癌基因表达数据的荟萃分析结果表明,在多个肿瘤亚型中,年轻化与激活成纤维细胞生长因子受体(FGFR)突变率增加相关,这一发现与Ta肿瘤相关,Ta肿瘤比高级别肿瘤具有更有利的预后。
在晚期膀胱癌中,与FGFR激活突变相关的有利结果丢失,因为FGFR3在化疗背景下可能与较差的结果相关。
在对肿瘤亚型的同一荟萃分析中,与老年患者相比,年轻患者的肿瘤中claudin的表达水平比老年患者高,claudin是一种肿瘤转移的反向标记物。
✦ 肌肉浸润性膀胱癌:发病率随年龄增长而增加
相比之下,在普通人群中,肌肉浸润性膀胱癌(MIBC)的发病率随着年龄的增长而增加。85岁以上的患者中有30%以上发生MIBC,而10岁以下的患者中有23%发生MIBC。
随着年龄的增长,肿瘤抑制因子TP53、APC和PTEN12突变的可能性增加,这在MIBC中很常见,并与不良预后相关。
最后,随着人类年龄的增长,他们通常会累积共病和虚弱指数增加,这导致了与年轻患者的总体预后差异,特别是与使用根治性膀胱切除术的手术干预有关。
有证据表明,当仔细选择时,许多老年患者是手术治疗的合适人选,但老年患者较不积极的治疗也会影响预后。
所有这些数据都广泛支持这样一种观点,即年轻患者的膀胱癌出现在疾病的较低阶段,临床上侵袭性较低,最终,年轻患者比他们的老年对手更有可能存活。
膀胱癌中与年龄和微生物组相关的变化
在衰老过程中,炎症系统和肠道和尿道中的微生物都发生了大量的变化。
✦ 膀胱癌
•老年患者的膀胱癌预后比年轻患者差,年轻患者通常表现为低级肿瘤。
•在膀胱癌亚型中,年轻患者比老年患者表达FGFR3突变的比例更高,连接蛋白水平也更高
•在膀胱癌亚型中,老年患者更有可能发生肿瘤,肿瘤抑制蛋白p53, APC和PTEN突变
•在24个月的随访点,老年患者(80岁以上)的非肌肉浸润性膀胱癌患者对卡介苗的反应低于年轻患者(61-70岁) (39%对61%的绝对反应率)
✦ 肠道微生物组
• 老年个体(90岁以上)β-多样性较年轻个体减少,α-多样性没有变化
• 老年个体(90岁以上)与年轻个体相比肠道中以下菌群丰度增加:
Akkermansia ↑↑↑
Escherichia ↑↑↑
Bifidobacterium ↑↑↑
Christensenellaceae ↑↑↑
• 老年个体(90岁以上)与年轻个体相比肠道中以下菌群丰度降低:
Faecalibacterium ↓↓↓
Bacteroides ↓↓↓
Lachnospiracae ↓↓↓
• 百岁老人(100岁)比非百岁老人群体有的Akkermansia,通常与改善健康状况有关。
关于AKK菌详见:AKK菌——下一代有益菌
✦ 尿液微生物群
• 70岁及以上的个体与年轻个体相比尿道中:
saccharofermentans ↑↑↑
Proteiniphilum ↑↑↑
Jonquetella ↑↑↑
Parvimonas ↑↑↑
• 70岁及以上的男性比年轻男性有的细菌属
• 70岁及以上的男性比年轻男性体内的细菌总数要少
• 与年轻女性相比,70岁以上的女性在细菌种类或数量上没有差异
✦ 肠道上皮屏障
• 与4或12月龄小鼠相比,21月龄小鼠血清脂多糖增加与肠道通透性增加相关
• 在老年小鼠模型中,IL-6和肿瘤坏死因子随肠道通透性线性增加
• 与10岁及以下的狒狒相比,18岁及以上的狒狒IL-6、IL-1β和IFNγ水平显著升高
• 18岁及以上的狒狒与10岁及以下的狒狒相比,occludin、claudin和紧密连接分子减少
• 与年轻人相比,老年人的短链脂肪酸(如丁酸、丙酸、乙酸)水平较低,这些脂肪酸被认为可以保持粪便中的肠道-上皮完整性
先天和适应性免疫系统在衰老过程中都出现失调。
衰老主要通过两种途径导致免疫系统失调事件:
在膀胱癌患者中,先天免疫活性的血清和组织标志物升高预后较差,可能与肿瘤生长有关。
适应性免疫系统在膀胱癌中的作用尚不清楚,基于所研究免疫细胞的差异、其相对丰度和抗原肿瘤标记物的存在,结果相互矛盾。
先天免疫系统和适应性免疫系统都可能影响膀胱癌的进展,与衰老相关的免疫系统变化会对肿瘤清除产生有害影响。
衰老:免疫系统逐渐破坏、炎症增加
随着年龄的增长,细胞分解的无菌产物的积累,包括代谢废物,如细胞游离DNA或错误折叠或氧化的蛋白质,以及异常分布的病原相关的分子模式(MAMPs),如脂多糖(LPS),长期激活先天免疫系统。
当衰老伴随着其他对人类健康有害的问题,如营养过剩、慢性惰性感染、癌症或肠道失调时损伤相关的分子模式(DAMPs)和错误折叠蛋白的积累会加速,并导致免疫系统中与衰老相关的破坏。
这种破坏至少部分是由巨噬细胞和中性粒细胞中的细胞信号传导介导的:巨噬细胞上进化保守的toll样受体(TLRs)识别升高的内源性MAMPs和DAMPs。
在衰老过程中,MAMPs和DAMPs在组织中积累,检测它们诱导IL-6、IL-8和tnf等细胞因子的表达,导致先天免疫活性升高,并从常驻免疫细胞向组织释放活性氧(ROS)。
临床前癌症模型支持这一观点,即局部炎症的增加会导致细胞因子的产生和导致DNA损伤的局部活性氧水平的增加,并可能会在某些肿瘤中刺激肿瘤生长和进展。
异常的DNA修复和增强的炎症也与老年小鼠中与肿瘤形成增加相关的DNA损伤有关。
先天免疫信号升高——膀胱癌不良预后
临床上,先天免疫信号升高似乎与NMIBC和MIBC患者的不良预后相关。这种作用不仅限于膀胱癌,因为肿瘤相关的巨噬细胞(TAMs)和肿瘤浸润性中性粒细胞(TINs)可能促进结直肠癌和肺癌的发生。
在膀胱癌中,使用免疫组织化学(IHC)对296个肿瘤的泛巨噬细胞标志物CD68和泛T细胞标志物CD3的组织芯片分析表明,巨噬细胞与T细胞的比例是不良生存的最大预测因子。
CD163+TAMs的存在:复发率增加
一项对13项来自人类膀胱组织的meta分析结果显示,CD163+TAMs的存在与复发率增加相关,而CD68+TAMs的存在与复发率无关。
值得注意的是,这一发现可能与这些巨噬细胞的炎症状态有关,因为CD163是抗炎巨噬细胞的标志,与肿瘤免疫逃逸相关。相比之下,CD68并不能描述巨噬细胞的炎症状态,并由大多数巨噬细胞亚型表达。
TINs水平升高:预后不良,生存率较差
对102个人膀胱癌肿瘤的免疫组化分析表明,TINs水平的升高与NMIBC复发率的升高和较差的总生存率呈正相关。
此外,在MIBC患者中,TIN水平升高与总生存期降低和化疗反应不良相关。然而,所有这些研究都使用了免疫组化相关分析,限制了推断因果关系的程度。
由于肿瘤浸润免疫细胞的测量需要在组织中进行评估,因此确定系统性炎症标志物是否可以作为组织相关炎症蛋白或细胞的替代物是有用的。
NLR高分与无复发和无进展生存期相关
系统性炎症的一个指标,血清中性粒细胞:淋巴细胞比率(NLR),可以预测NMIBC和MIBC的疾病复发和进展。
在MIBC中,两项回顾性研究结果显示,NLR评分大于3.0和2.5的患者5年无复发较差(HR 1.49;95% CI 1.12-2.0),总体(危险比1.67;95% CI 1.17-2.39)和无病生存期(危险比1.946;95% CI 1.03-3.66)高于NLR评分较低的患者。
在NMIBC中,对6项回顾性研究的荟萃分析结果显示,NLR高分与无复发和无进展生存期相关。
在一项对899例NLR分界点为2.7的MIBC患者的大型回顾性研究中,年龄的增加与NLR评分的增加相关,年龄的增加与免疫功能障碍的增加有关。
免疫变化在 NMIBC 中任何年龄都可能很重要
NMIBC的研究结果大部分显示膀胱癌患者的年龄与NLR评分之间没有显著的相关性,但仍显示NLR可以预测结果,这表明在NMIBC中,无论年龄如何,免疫改变可能都是重要的,年龄、NLR和预后之间的联系在MIBC中比在NMIBC中更强。
一项针对NMIBC患者的单一前瞻性研究发现,校正年龄后,NLR与无复发和无进展生存期之间的差异消失,这表明年龄是主要决定因素,应与NLR状态一起测量和校正,这进一步复杂化了高龄、NLR和膀胱癌预后之间的潜在关系。
当考虑到先天免疫系统在肿瘤微环境中的潜在致瘤作用时,显然,需要进一步的研究来确定膀胱局部先天免疫信号是否与系统性免疫失调相关,这可以很容易地测量和潜在地用于预后。
年龄、NLR和预后在MIBC中的相关性似乎比NMIBC更强,这并不奇怪,因为MIBC由于侵袭组织而被认为是更具有炎症性的疾病。
先天免疫调节膀胱癌:活性氧产生,增强致癌性
来自小鼠模型的数据支持先天免疫调节膀胱癌的观点。在膀胱癌模型中,与仅用亚硝胺(BBN)治疗的小鼠相比,致癌物n-丁基-n(4-羟基丁基)亚硝胺(BBN)和膀胱内脂多糖治疗的小鼠体内活性氧浓度与肿瘤发生增加呈正相关。
脂多糖注射促进了大鼠模型膀胱癌的形成,支持了先天免疫激活增加有助于肿瘤发展的观点。
脂多糖激活的中性粒细胞增强大鼠尿路上皮细胞系的恶性转化,这与脂多糖在其他肿瘤中的致瘤作用的数据一致,表明先天免疫系统产生的活性氧可以通过氧化应激和基因突变促进肿瘤的形成。
在缺乏铜/锌超氧化物歧化酶的老年小鼠中进行的研究结果表明,与年龄匹配的对照组相比,这些小鼠在肝癌模型中活性氧水平和致癌性增加,这支持了先天免疫系统不受控制的活性氧产生可增强致癌性的观点。
先天免疫系统与免疫疗法的复杂作用
在治疗上,炎症抑制剂,如塞来昔布,可以阻断促炎前列腺素的形成,减少大鼠膀胱癌模型中的肿瘤数量和体积,并减少体外细胞系中的细胞增殖。
在膀胱癌小鼠模型中,先天免疫系统似乎也调节了卡介苗的反应;在膀胱癌小鼠原位模型中,中性粒细胞减少消除了卡介苗介导的免疫治疗的反应。
这些数据表明,先天免疫系统的作用可能是复杂的,因为它可能需要通过启动免疫反应对卡介苗免疫疗法作出适当反应,但如果不加以检查,也会促进癌症的进展,这取决于肿瘤微环境和肿瘤的状态。
值得注意的是,这种效应在本研究中归因于中性粒细胞,但这一结论是在发现用于消耗中性粒细胞的抗体也会消耗单核细胞之前得出的,因为该抗体识别单核细胞上的LY6C和中性粒细胞上的LY6C和LY6G。
因此,单核细胞也可能影响模型中免疫治疗的疗效,突出了改善治疗结果的另一个潜在调控靶点。事实上,区分中性粒细胞和单核细胞在膀胱癌中的作用可能是增强患者免疫治疗和了解疾病进展的一种手段。
总之,这些数据支持这样一种观点:
在多种实体肿瘤类型中,与衰老相关的异常先天免疫导致了致瘤前表型。
然而,目前还缺乏利用解决潜在机制的转化模型来理解浸润肿瘤的先天免疫细胞在膀胱癌中的作用。这些模型是有根据的,因为阻断中性粒细胞募集也可以减少肿瘤的生长和其他肿瘤的转移进展,如乳腺、结肠和肝脏。
通过使先天免疫系统的慢性激活正常化,减少老年先天免疫过度刺激的新方法可能是减缓膀胱肿瘤发病率和复发的潜在手段,特别是在炎症指数自然增加的老年患者中。
先天免疫反应可以在老年时被长期激活,但适应性免疫的组成部分,如初始CD4和CD8 T细胞,由于免疫衰老而数量下降,这是由细胞衰老引起的免疫细胞随时间的变化,整体多样性下降。
随着年龄增长,老年人适应性免疫反应受损,肿瘤的感知和清除能力下降
随着个体年龄的增长,他们的初始T细胞逐渐减少,T细胞受体多样性减少,T细胞上的共刺激效应分子CD28的水平也比年轻的T细胞上的CD28低。这些变化损害了老年人的适应性免疫反应。
随着适应性免疫反应的下降,肿瘤的感知和清除能力也在下降。这些改变在很大程度上导致了观察到的免疫差异。
将适应性免疫细胞蛋白(如CD3和CD8)和肿瘤浸润淋巴细胞(TILs)浓度与临床结果相关联的尝试产生了相互矛盾的结果。
免疫组化分析显示,肿瘤突变负担增加的膀胱肿瘤CD8效应因子评分相应增加,T细胞浸润增强。对膀胱切除术后MIBC肿瘤的研究结果,支持CD3+或CD8+ TILs的增加与生存率的提高相关的观点。
MIBC中TILs的存在是否受年龄的影响尚不清楚。在一项对>50岁患者的MIBC膀胱切除术样本的研究中,没有发现患者的年龄、性别或T细胞标记CD4、CD8或CD56存在相关性。
然而,从更广泛的免疫衰老和衰老意义上来说,所使用队列中的患者的年龄范围相当有限,并没有在特定年龄组之间进行比较。
在更有针对性的比较队列(<40岁和>80岁)中,需要了解免疫衰老的变化如何影响免疫治疗,以提高对膀胱癌中衰老对适应性免疫的影响的理解。
衰老与基础先天免疫活动的增加有关,数据表明,在人类组织和小鼠模型中,先天免疫细胞(如中性粒细胞)的增加是肿瘤形成的促进剂。
然而,尽管T细胞在肿瘤免疫中的非常重要,但是适应性免疫反应在衰老和肿瘤发生中的作用仍不清楚。还需要确定炎症如何促进膀胱癌的决定性实验。
肠道微生物群
人体的肠道微生物组估计有超过1000种不同的细菌和100万亿个单独的细菌细胞。
这些不同菌群的代谢产物通过一层肠细胞、肠道粘液和微折叠免疫细胞与全身循环分离。肠道微生物的产物被腔细胞摄取后,运输到全身,对全身免疫系统产生广泛影响。
由肠道菌群组成的变化引起的宿主和肠道菌群间稳态的破坏,是菌群失调,会导致炎症、肿瘤进展和肿瘤对乳腺癌、肺癌和结直肠癌治疗的反应。
菌群失调如何影响免疫
菌群失调破坏肠道屏障,导致释放促炎症的MAMPs,如脂多糖和未甲基化的CpG DNA,加速年龄相关的免疫系统失调。
肠道物质的泄漏也发生在肠道血管屏障(GVB)。对肝脏疾病的研究表明,酒精性和非酒精性脂肪性肝炎等情况可破坏肠血管屏障,导致微生物物种的全身传播。
我们知道,衰老会导致上皮完整性屏障的破坏,因此,除了肠道-上皮完整性的丧失外,肠血管屏障的完整性的丧失可能是肠道功能障碍中微生物或微生物组分系统性传播的一个尚未被充分研究的方面。据推测,这些物质的泄漏会以对人体健康有害的方式广泛影响免疫力。
膀胱癌中的微生物群及其的潜在联系
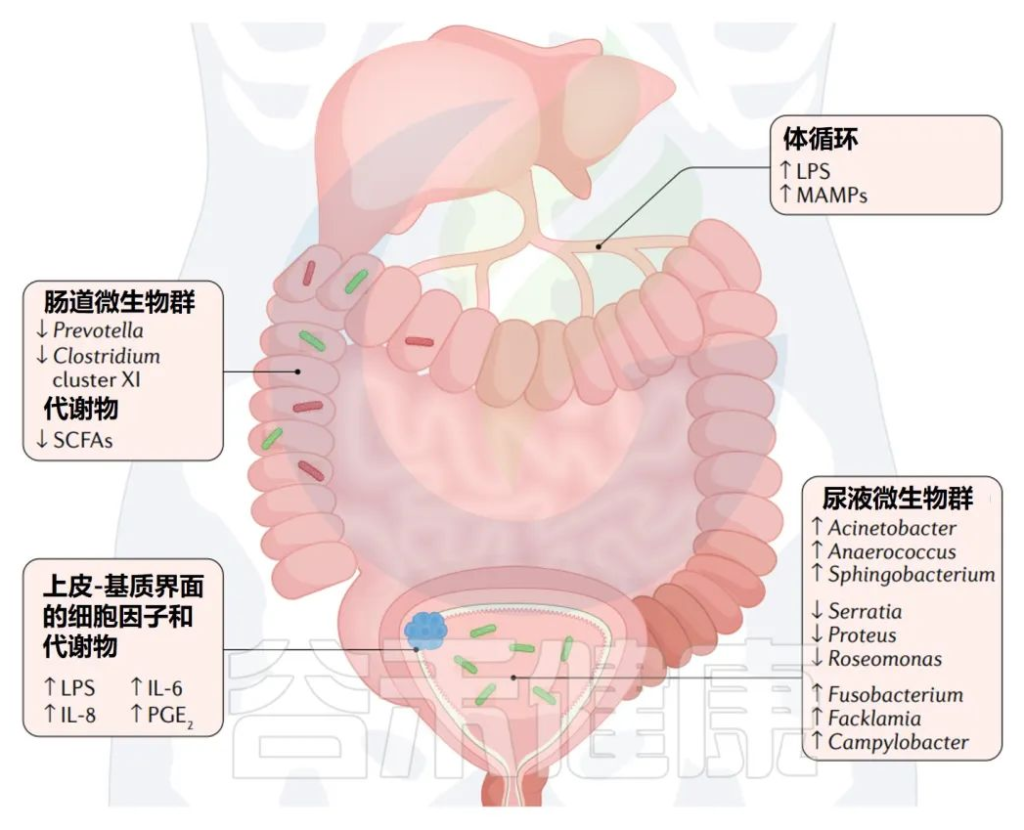
Martin A,et al.Nat Rev Urol.2022
多种微生物群可能会影响或被膀胱癌的形成所改变,包括肠道微生物群的改变、尿液微生物群的改变和上皮基质界面的改变。
与健康人相比,膀胱癌肠道微生物群的变化包括Prevotella和Clostridium的丰度降低。
膀胱癌患者尿微生物组中以下菌群的丰度高于健康人群:
同时以下三个菌群的丰度较健康人群偏低:
肠道失衡与结直肠癌之间的正相关已经得到了很好的证实,但是肠道失衡在多大程度上影响其他肿瘤的进展,包括膀胱癌,还不清楚。
此外,肠上皮完整性的破坏在多大程度上是由肠道菌群的非共生变化驱动的,反之亦然,这一点也存在争论。
膀胱癌患者:普雷沃氏菌、梭菌属减少,丁酸水平降低
一项研究包括26名膀胱癌患者和16名年龄匹配的健康参与者通过定量PCR分析证明,普雷沃氏菌和梭状菌群显著减少 。
在同一研究中,膀胱癌患者粪便中的丁酸盐(一种短链脂肪酸)水平降低,而血清中的脂多糖水平升高。鉴于丁盐酸的抗肿瘤作用以及脂多糖和其他与肠道功能障碍相关的MAMPs的促肿瘤作用,这些数据表明微生物群的变化可能是疾病发生的相关因素。
迄今为止只进行了这种单一的、小规模的试验。这些发现是否代表肠道失衡、炎症和膀胱癌发生之间的潜在因果联系,或仅是相关的,还需要进一步的研究来确定。
需要在临床前模型中采用直接介入方法来了解短链脂肪酸在肠道失衡和膀胱癌中的作用,更重要的是,需要进行更大规模的试验,在膀胱癌患者的分子水平上调查肠道功能障碍,以验证任何发现。
需要进一步调查来确定,这些发现是否代表肠道菌群失调、炎症和膀胱癌肿瘤发生之间的潜在因果关系。
年龄相关的失调机制和对系统性炎症标志物的影响
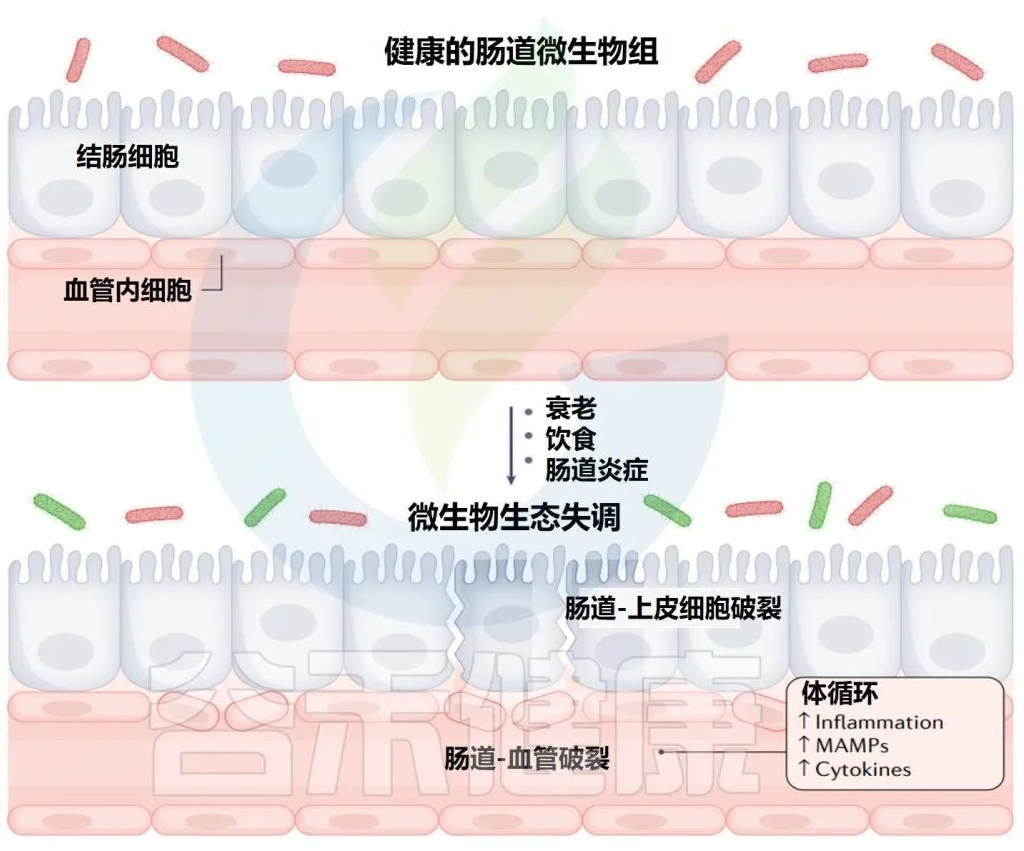
Martin A,et al.Nat Rev Urol.2022
衰老和饮食都可以影响肠道微生物群,导致微生物失调和肠道上皮细胞的破坏。
这种分解导致微生物相关分子模式(MAMPs)的释放增加和短链脂肪酸(SCFAs)的产生减少,并可导致体循环中MAMP和细胞因子的炎症增加。
大多数研究的结果都认为,当肠道菌群失调发生时,肠上皮细胞的分解通常与之相关,尽管特定细菌亚群的变化及其与肠上皮细胞的相互作用并不完全清楚。了解这些变化对于确定哪些菌群可能对免疫系统产生负面的全身影响非常重要。
首先出现的问题是菌群失调或上皮破裂,这一点很复杂,因为它们之间可能有着不可分割的联系,因此,一个或另一个的刺激可能会促成这两个事件。
对健康百岁老人肠道菌群的研究,为通过恢复肠道健康进行治疗干预提供了潜在的途径。这一观点得到了一项研究的支持,该研究显示,健康状况良好的30-100岁人群的微生物含量具有很强的相似性,这表明存在健康的微生物组,并可能对不符合这一类别的患者进行调节。
到目前为止,结果还没有表明任何特定细菌种类的丰度与长寿是绝对相关的。
相反,尽管老年人有效对抗感染的能力明显下降,但长寿的人会形成促炎和抗炎细菌的平衡。
对27项研究的系统综述结果表明,长寿个体在β-多样性(微生物环境间的多样性程度)方面与年轻个体存在差异;然而,通常不会观察到 α 多样性的差异,即每个微生物系统的多样性程度。
总的来说,8项研究涉及百岁老人,4项研究比较了高龄人群和59-85岁人群,4项研究中有2项报告了高龄人群和低龄人群微生物环境多样性程度的差异,而没有研究发现α-多样性的差异。
▸ 老年人的菌群丰度
与年轻个体相比,老年人至少有两个菌群的丰度更高:
与此同时下列菌群的丰度更低:
然而,研究设计存在相当大的差异,关于哪些菌群构成良好的健康,以及老年人存在哪些变化仍未确定的一致意见。
▸ 长寿老人:AKK菌丰度高
值得注意的是,在系统综述中,Akkermansia在高龄人群(99岁以上)中最常见,这可能与此相关,因为该菌在适当水平时与肠道通透性降低、内毒素血症减少和对癌症治疗的免疫反应改善有关。
阿克曼菌(Akkermansia,简称AKK菌)还促进Treg分化,限制肠道功能障碍高脂饮食模型中细胞因子的产生,并通过类似机制预防衰老相关炎症。没有保留阿克曼菌的患者可能会增加疾病发展的风险,包括膀胱癌,或者可能对化疗反应不好。
▸可能存在:AKK菌促进健康的“正确”水平或必要的平衡
抗生素的使用与免疫治疗的不良结果相关,矛盾的是,与不使用抗生素的患者相比,许多服用抗生素的患者AKK菌增加,而且,AKK菌高水平的存在与总生存率呈负相关(使用抗生素的患者P = 0.011,不使用抗生素的患者P = 0.018)。
然而,AKK菌只是可能对微生物功能至关重要的许多不同实体之一,单一实体治疗不太可能像基于平衡微生物组的更强大的改变(如粪菌移植)那样有效。
肠道菌群随年龄或并发疾病的变化可能是膀胱癌的危险因素,可通过直接给予益生元和益生菌或通过粪菌移植减轻。
▸ 短链脂肪酸
短链脂肪酸(SFCAs)由肠道细菌产生,是肠细胞的主要能量来源,是G蛋白偶联的游离脂肪酸受体配体。作为组蛋白去乙酰化酶抑制剂,可通过预防致瘤前表观遗传变化直接限制肿瘤生长。
短链脂肪酸主要存在于肠道中,但它们也可能对治疗膀胱癌有用。在体外,短链脂肪酸在很大程度上抑制先天免疫系统。
由于它们的多种作用和潜在的抗肿瘤活性,产生有益的短链脂肪酸可能是肠道维持健康环境的一种手段,也可能有助于预防结肠癌。
丁酸盐减少癌细胞生长,帮助维持健康的上皮屏障
由于癌细胞与非恶性细胞之间代谢的Warburg效应型变化(有氧糖酵解),丁酸盐通过氧化代谢和能量产生促进非恶性细胞的生长,但减少了癌细胞的生长,因为癌细胞不能有效代谢丁酸盐,丁酸盐在细胞核中积累,在细胞核中发挥组蛋白去乙酰化酶抑制剂的作用。因此,丁酸盐可以帮助维持健康的上皮屏障。
百岁老人肠道菌群中的短链脂肪酸水平上调
在一项研究中,80-99岁的老年人群中健康的老人总短链脂肪酸浓度升高;另一项研究结果显示,与老年患者相比,百岁老人的肠道菌群中产生短链脂肪酸的代谢途径(如乙酸和丙酸)表达水平上调。
除了存在一些与短链脂肪酸产生相关的细菌外,与小于80岁的人群相比,老年人粪便中的细菌数量通常减少。短链脂肪酸水平随着年龄的增长逐渐下降,而百岁老人开始恢复Akkermansia水平。
粪菌移植期间补充Akk菌可能有助于短链脂肪酸的保留
另一项研究的结果表明,在粪菌移植期间用巴氏消毒Akkermansia治疗小鼠,会导致肠道中短链脂肪酸的形成短暂增加,因此,如果这项技术能够完善,在粪菌移植期间补充Akkermansia或其他产生短链脂肪酸的细菌可能有助于改善短链脂肪酸的保留,并预防或治疗癌症。
在脂多糖处理的骨髓源性巨噬细胞中,丁酸、丙酸和乙酸均以剂量依赖的方式降低IL-6和IL-12的产生。丁酸和丙酸也会降低脂多糖处理单核细胞中单核细胞趋化蛋白-1的表达。
通过这些作用,短链脂肪酸可能缓和过度的免疫激活,促进免疫调节。
短链脂肪酸体外作用似乎具有抗炎作用,但其对膀胱癌适应性免疫系统的作用尚不清楚。
特别是丁酸盐,通过诱导调节性T细胞产生IL-10和激活 FAS 介导的T细胞凋亡,下调适应性免疫反应。
短链脂肪酸高可能影响免疫治疗效果
丁酸盐和丙酸盐均通过抑制抗原呈递细胞产生IL-12来抑制CD8+T细胞活化,全身水平的短链脂肪酸高与转移性黑色素瘤细胞毒性T淋巴细胞抗原4(CTLA4)免疫治疗的不良结果有关。
直接通过短链脂肪酸或间接通过前列腺素E2下调T细胞对免疫治疗和顺铂化疗均有不利影响,因为传统的肌肉浸润性膀胱癌新辅助顺铂化疗会刺激效应T细胞。因此,降低T细胞的疗效也可能改变化疗。
这些观察结果可以部分解释在肿瘤床上升高的前列腺素E2表达与不适当抑制的免疫反应和化学耐药性有关。
总之,这些发现表明短链脂肪酸在宿主免疫功能中参与发挥抗炎作用,尽管这一假设可能过于简单化,短链脂肪酸还可以刺激中性粒细胞趋化,因此可能有其他重要的调节作用。
然而,文献强烈支持短链脂肪酸的抗肿瘤作用,尤其在结直肠癌中,可能是因为短链脂肪酸在结肠中的浓度增加,以及介导丁酸差异效应的代谢变化,对癌细胞具有直接作用。
在衰老过程中,维持体内稳态需要抗炎和促炎信号,而短链脂肪酸除了自身具有抗肿瘤作用外,还可能是调节这一系统的一种手段。这些发现已经在体外和体内观察到,但迄今为止没有研究将人类短链脂肪酸水平与膀胱癌结果直接相关。
鉴于与肠道和全身短链脂肪酸水平相关的多种影响,短链脂肪酸可能充当免疫调节剂,因此,塑造使短链脂肪酸产生正常化的微生物含量,是增强或促进免疫治疗的潜在手段。
肠道微生物群的变化可能成为膀胱癌和其他癌症的治疗靶点。应该在这些群体和其他群体之间进行更广泛的比较,以了解哪些类型的微生物生态系统对人类的健康和寿命最有益。
当前的数据支持这样一种观点,即与年龄相关的微生物群变化可能最终影响疾病进展、结果或治疗反应等因素。
衰老在肠道微生物变化中的作用尚不清楚;此外,一些证据表明,环境因素对肠道微生物群有实质性的影响。
一项包括来自中国同一小区域的1000多名极健康个体的研究结果表明,当研究人员试图控制总体健康时,30至100岁的个体粪便微生物群组成几乎没有变化,虽然在30岁以下的个体和30岁以上的个体中发现了相当大的差异。
通过主成分分析评估,30-100岁非常健康的个体的粪便微生物群高度一致,支持了其他研究的结果,这些研究表明环境,而不是年龄或遗传,是微生物组的主要影响者。
值得注意的是,该研究的入选标准具有极高的选择性,通过严格的生活方式分析,几乎99%的患者被拒绝入选;选择标准包括吸烟状况、饮酒、饮食和其他与肠道功能障碍相关的因素。
因此,尽管这些数据表明年龄是肠道微生物群变化的促成因素,但这一观察结果可能仅与这些高选择性标准所代表的一小部分人有关。然而,本文提出了一个假设,即衰老本身可能不如与衰老相关的饮食变化或生活方式变化重要。
在小鼠、狒狒和果蝇模型中,肠道菌群的变化与年龄有关,并与肠道屏障完整性的破坏有关。
在小鼠中,用荧光素异硫氰酸酯(FITC)标记的葡聚糖测量肠道通透性,其血清水平与IL-6和肿瘤坏死因子(TNF)水平一起随年龄线性增加。
肠道菌群组成——肠道屏障功能障碍
在果蝇中,观察到老年果蝇肠道中细菌组成的改变和细菌总负荷的增加,与年轻果蝇相比,肠道中不可吸收蓝色染料(肠道屏障功能障碍的替代品)浓度也相应增加。
结肠完整性的破坏——年龄
在狒狒中,结肠完整性的破坏与年龄有关,与10岁以下的狒狒相比,年长的狒狒(年龄≥18岁)结肠组织的免疫组化分析显示封闭蛋白(occludin)、连接蛋白(claudin)和紧密连接粘附分子减少,同时大分子辣根过氧化物酶(肠通透性的另一标志)在结肠上皮的通量增加。
此外,18岁狒狒的结肠活检中IL-6、IL-1β和IFNγ水平高于10岁灵长类动物。
肠道功能障碍——细菌成分的全身释放
另一项比较21月龄小鼠与4或12月龄小鼠肠道通透性的研究结果显示,老年小鼠血清FITC-右旋糖酐水平的增加与体循环中脂多糖水平的增加相关,将肠道功能障碍和细菌成分的全身释放联系起来。
LPS 和其他 MAMP 与 IL-1β、IL-6 和 TNF 等细胞因子的增加密切相关,提供了肠道菌群失调、慢性炎症和肿瘤发生之间可能的机制联系。
所有这些数据都支持这样的观点,即肠道功能障碍随着年龄的增长而增加,与其他哺乳动物的饮食或生活方式的变化无关,但由于适当控制人类饮食的复杂性,尚未在人类中进行评估。
免疫功能障碍——衰老——微生物群
衰老过程中,循环细胞因子的增加在具有14个月或以上老年动物的微生物群的小鼠模型中加剧,将免疫功能障碍与衰老和微生物群联系起来。
相比之下,无菌小鼠在衰老过程中通常不会表现出,老年特异性无病原体小鼠所表现出的循环细胞因子的增加,并且在很大程度上可以防止衰老相关炎症和巨噬细胞功能障碍,除非它们再次暴露于微生物群。
衰老——肠道通透性——炎症——菌群
将无菌小鼠暴露于14月龄动物的菌群中,比无菌小鼠暴露于幼龄小鼠的菌群中更能促进肠道通透性和细胞因子释放。
这一机制依赖于肿瘤坏死因子,使用抗肿瘤坏死因子拮抗剂治疗可以改善衰老引起的微生物群的变化。因此,由肠道功能障碍介导的MAMP或DAMP释放与老年炎症表型之间发生了实质性的相互作用,从而导致炎症系统的慢性全身激活。
为了将这些发现转化为膀胱癌,除了了解局部微生物群(包括尿液微生物群和肿瘤本身)之间的联系外,还需要进一步了解膀胱癌背景下的肠道微生物群。
到目前为止,对尿液微生物群的研究还缺乏一个关于什么是正常尿液微生物群的明确共识:由于收集方法的差异和相对较小的样本量,目前关于健康尿液微生物群的定义存在很大差异。
目前对尿液和膀胱微生物群及其改变的了解有限。局部微生物环境的失衡与多种上皮性癌症的肿瘤进展有关,包括乳腺癌、宫颈癌和子宫内膜癌。
健康的尿液微生物群
目前的初步研究一致认为,健康成年志愿者的尿液微生物中至少包含四种细菌种群:乳酸菌和链球菌是尿液微生物中最稳定存在的属,与年龄和采样方法有关,而厚壁菌门和不动杆菌门是两性尿液微生物中最丰富的门。表明这些是该人群中最有可能构成健康尿液微生物组的成分。
女性尿液中乳酸杆菌种类的含量高于男性
根据对健康志愿者进行的两项独立研究的结果,尿液微生物群的性别差异很明显。研究表明,女性尿液中乳酸杆菌种类的含量高于男性尿液中的含量。
我们还不清楚这一观察结果与癌症的关系,但这一发现的一个潜在的重要方面是,男性与女性泌尿系统微生物群的差异或女性泌尿系统微生物群的个体间差异可能与女性泌尿系统感染的流行有关,或她们膀胱癌发病率的降低,因此可能会影响膀胱的整体微环境。
菌群在不同年龄的差异
在同一项包括23名健康成年人的研究中,下列四种菌群仅在>70岁的个体中发现:
此外,在男性中,属的数量会随着年龄的增长而增加,而细菌总数减少。性别或年龄差异会影响尿液微生物群。
尿液微生物:个体间差异极高
研究结果还表明,个体间差异极高,限制了更深入的分析。由于这种高变异性,对泌尿系统微生物的调查缺乏类似的大型多种族和多种族肠道微生物群研究的力量,因此饮食、基因、男性和女性短期或长期激素变化的重要性,以及泌尿系统微生物的卫生还没有确定。
需要大型的、多中心的、多种族的、具有共识方法论和清晰统一的分析管道的研究来完善该领域的假设并产生共识。
多项研究报道尿失禁、间质性膀胱炎和泌尿生殖系统癌患者尿液微生物群落的物种多样性和相对丰度存在差异。
健康人群与膀胱癌人群的微生物组差异
在膀胱癌方面,一项包括12例膀胱癌患者和11名年龄匹配的志愿者的研究结果显示,与健康成年人相比,膀胱癌患者富集了以下四种菌群:
与间质性膀胱炎和慢性前列腺炎等疾病相比,使用Simpson指数测量的健康成人和膀胱癌患者之间的物种多样性(α-多样性)在种或科水平上没有总体差异,这表明膀胱癌的尿液微生物群可能不像其他炎症性疾病状态那样受影响,尽管这一观察结果可能是因为该研究力量不足。
然而,在特异性操作分类单元(OTUs)水平上进行差异分析,可以减少测量参数的数量,从而识别差异,表明相互关联的物种可能在肿瘤发生中发挥作用。
一项针对31名膀胱癌男性的研究结果显示,与18岁匹配的健康个体相比,下列三种菌群的丰度增加:
同时下列几种菌群降低:
由于个体数量少,这些研究不足以完全确定特定细菌种群的变化。对于尿液微生物菌群研究在多大程度上反映了膀胱内的微生物群也知之甚少。
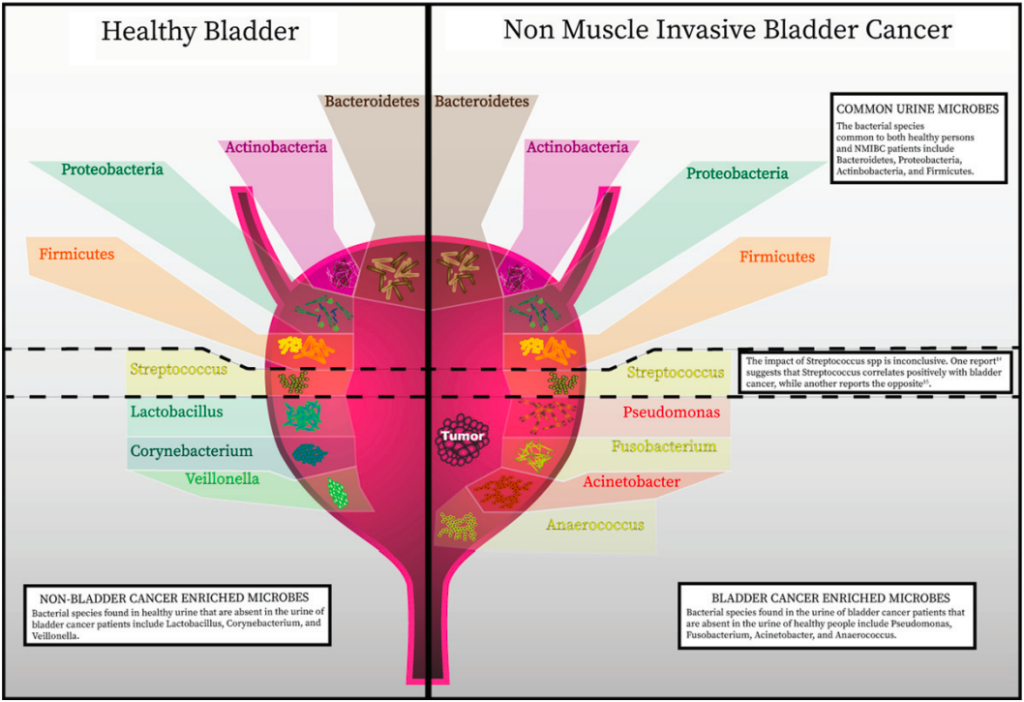
Andolfi C, et al., Bladder Cancer. 2020
关于膀胱肿瘤微生物组的研究仅限于两项研究。两者的结果都表明,肿瘤与非恶性组织中的 α 多样性导致物种丰富度相对降低。一项研究发现,膀胱微生物组的门(如厚壁菌门和放线菌门)的相对丰度与之前在其他研究中报道的尿液微生物组值相似。
联合测量来自同一患者尿液和膀胱肿瘤样本的微生物群目前在文献中还没有。这些因素支持了对肿瘤分级或分期与泌尿系统微生物组之间差异的调查,以及使用更大的患者队列进行明确的、多机构的、控制良好的研究的必要性。
尿液微生物群的影响尚不完全清楚,衰老和肠道生态失调导致的免疫失调的直接影响可能会增加膀胱癌的发病风险。
然而,没有研究直接比较同一患者的尿液微生物群和肠道微生物群的变化。需要进行研究来评估与衰老和炎症相关的肠道生态失调是否也发生在泌尿系统的微生物群水平上,或任何其他含有微生物的解剖部位。
如果存在潜在的机制,尿液微生物的失调可能是衰老、炎症、失调和膀胱癌风险之间的联系。
系统性炎症、尿路上皮增生与膀胱癌之间的假设联系

Martin A,et al.Nat Rev Urol.2022
衰老引起的炎症变化以及肠道上皮完整性的降低可导致循环促炎介质水平的增加,例如细胞因子和微生物激活分子模式 (MAMP).
LPS介导的toll样受体4 (TLR4)激活可导致骨形态发生蛋白4 (BMP4)、音猬因子 (SHH)、WNT -β-catenin和STAT3通路的激活,促进尿路上皮的增殖。BMP4、SHH、WNT -β-catenin和STAT3通路在膀胱癌中调控异常,但还没有研究直接将LPS或MAMP介导的BMP4、SHH、WNT -β-catenin和STAT-3的激活与膀胱癌的发生联系起来。当转化发生时,带有肿瘤相关巨噬细胞(TAMs)和肿瘤浸润性中性粒细胞(TINs)的尿路上皮的慢性炎症阻止了适当的免疫反应和肿瘤清除,并可能通过释放细胞因子、生成活性氧(ROS)和促进免疫抑制环境进一步加剧肿瘤的形成。PGE2,前列腺素E2.
由尿路上皮细胞和局部感染性细菌引起病原相关分子模式(MAMPs)驱动和损伤相关分子模式驱动炎症可能是年龄、肠道上皮破坏和在许多膀胱肿瘤中发现的先天免疫信号之间的一种机制联系。
脂多糖增加炎症因子的释放
在体外人类和小鼠模型中,来自尿路致病性大肠杆菌的脂多糖通过TLR4信号通路增加尿路上皮细胞中IL-6、IL-8和PGE2细胞因子的释放。
此外,脂多糖激活尿路上皮细胞上的电压门控钾通道,介导IL-6释放。脂多糖通过磷酸化途径激活巨噬细胞和泌尿黏膜中的TLR4,这与膀胱癌的发展和化疗耐药有关。
STAT3促肿瘤
免疫组织化学(IHC)分析发现,与非侵袭性发光型肿瘤相比,局部侵袭性肿瘤中STAT3磷酸化水平升高,抑制STAT3可降低膀胱癌细胞系的增殖。在小鼠中,阻断尿路上皮细胞中的 STAT3 可降低膀胱癌的发生和侵袭性。
IL-8和PGE2促肿瘤
脂多糖介导的尿路上皮IL-8和PGE2的增加在膀胱癌中也具有促肿瘤作用。在经尿道膀胱肿瘤标本切除的新鲜冷冻组织中,与非侵入性肿瘤相比,浸润性肿瘤中IL-8和基质金属蛋白酶9水平升高。
前列腺素E2促肿瘤
此外,前列腺素E2增加高级别膀胱癌细胞系的增殖,在接受吉西他滨和顺铂标准化疗方案治疗的小鼠中使用塞来昔布抑制前列腺素E2,产生了持续的治疗反应,并通过消除患者来源的肿瘤异种移植模型中CK14+细胞的形成克服了化疗耐药性。
这些研究表明尿路感染期间脂多糖相关炎症与膀胱癌进展之间存在多种趋同途径。
尿路感染后信号通路的改变
重要的是,对尿路感染的生理尿路上皮反应受到音猬因子重组蛋白(SHH)、骨形态发生蛋白4 (BMP4)和WNT -β-catenin信号通路的高度调控,这些信号通路在恶性转化过程中经常发生改变。
尿路感染后的尿路上皮再生是由尿路上皮基底层分泌SHH的干细胞增殖驱动的。感染后,下游SHH信号通路通过BMP4和WNT-β-catenin信号通路诱导尿路上皮和基质细胞增殖和终末分化。
这种作用在前列腺素合成抑制剂治疗后被逆转。
这些再生途径中的每一个的丧失或改变都与膀胱癌发生有关。在 BBN 小鼠模型中,SHH 阳性基底细胞是膀胱癌的主要祖细胞。SHH 的丧失和进展为膀胱癌可能是通过 BMP 基质信号传导的丧失而发生的。
免疫组化分析显示,与非恶性尿路上皮黏膜相比,在人膀胱癌肿瘤中观察到WNT糖蛋白活性升高。这一发现在小鼠模型中得到了进一步的支持,在功能获得突变体中β-连环蛋白的构成性激活导致了12周后30%的小鼠发生低级别膀胱肿瘤。
有趣的是,在具有构成型活性β-连环蛋白的小鼠中,肿瘤的发生是性别依赖的,45%的雄性小鼠发生肿瘤,而雌性小鼠只有3%,这最终与雄激素受体(AR)信号有关。
在人类和普通小鼠模型中都发现了膀胱癌的性别二态,但其原因是多因素的,也与表观遗传机制中的染色体差异有关。
这些发现呈现了尿路上皮在响应急性脂多糖介导的炎症反应和尿路上皮癌的发展之间呈现出许多重叠特征。
年龄相关的肠屏障破坏,诱发炎症;免疫系统变化,增加肿瘤风险
然而,尿路感染与膀胱癌风险的增加并没有特别的关联。当与衰老和肠上皮完整性丧失相结合时,由于与年龄相关的肠屏障破坏,长期暴露于基底尿路上皮层的脂多糖或其他损伤相关分子可能会诱发慢性膀胱炎症,并增加细胞周转,以及与年龄相关的免疫系统变化,增加肿瘤转化的可能性。
慢性膀胱炎症诱导的肿瘤转化可能是女性特有的一种机制,因为尿路感染在女性中更为突出,而膀胱癌在男性中更为常见。
关于衰老相关炎症、微生物群和膀胱癌发生的研究仍然不完整,需要更多的假设检验来确定这些不同实体(衰老、微生物功能障碍、炎症改变)在这一过程中导致的具体变化和肿瘤相关结果。
研究肠道和尿液微生物群对浅表性癌症治疗反应的影响,可能为微生物群和膀胱癌进展提供额外的见解。
新的证据表明,浅表膀胱癌治疗受到肠道和尿道微生物群的影响。
目前,高级别非肌肉浸润性膀胱癌的一线治疗是细菌疫苗株卡介苗。卡介苗的疗效随着年龄的增长而降低,早期数据表明,疗效还受尿微生物中变形菌群丰度的影响。
一项包括1106例患者的卡介苗干扰素膀胱内治疗的II期多中心试验的数据表明,年龄在61-70岁的患者在卡介苗干扰素治疗后的无癌生存期优于80岁或以上的患者(3 年无癌生存率为 65%对 47% ,P = 0.036)或卡介苗单药治疗(3 年无癌生存率 55% 对 32%,P < 0.003)。
令人惊讶的是,在这项研究中,小于50岁的患者的预后较差;然而,在多变量分析中,年龄仍然是反应的独立危险因素。
在一项包括805名Ta、T1或CIS高分级患者的独立研究中,年龄为>70岁的患者的无癌生存期低于年龄<70岁患者(37% 对 27%,P = 0.005)。
在接受益生元或益生菌治疗的个体中,非肌肉浸润性膀胱癌复发减少。最后,肠道菌群介导了实体肿瘤(如黑色素瘤)中对PD1治疗的反应,这可能与晚期膀胱癌中免疫治疗具有共同机制。
关于卡介苗抑制肿瘤复发的机制尚不清楚,一种假设是卡介苗诱导膀胱内的局部促炎性先天免疫反应,进而刺激对卡介苗和肿瘤抗原的适应性免疫反应。
在治疗后的前3年,由于未知的原因,卡介苗未能阻止肿瘤复发的患者占30%,年龄可能是无反应的原因之一。
年龄越大,卡介苗疗效越差
接受卡介苗治疗后,61-70岁的患者中有61%在24个月时无复发,而>80岁的患者中有39%无复发。
这些结果得到了另一项研究的支持,该研究表明70岁以下(27%)和70岁以上(37%)患者5年后无病生存率的绝对差异为10%;然而,这两个年龄组中与年龄相关的死亡风险没有报道。
因此,年龄可能是非肌肉浸润性膀胱癌复发的独立危险因素,但与年龄相关的免疫系统衰退是否相关尚不清楚。
卡介苗应答取决于多种因素,不止年龄
在一项小型研究中,31名卡介苗应答者与32名卡介苗无应答者进行了比较,结果表明,肿瘤PDL1状态而不是T细胞PD1状态是卡介苗应答的决定因素,这表明卡介苗的总体应答可能取决于许多不同的因素,而不仅仅是年龄。
尿液微生物群也可能在卡介苗反应中起作用
在一项包括31例接受卡介苗治疗的高危非肌肉浸润性膀胱癌患者的研究中,观察到卡介苗应答者和无应答者在OTU水平上的尿液微生物群差异。
卡介苗治疗6个月后无病的患者比复发患者尿厚壁菌门(如乳杆菌和变形杆菌)丰度更高。
鉴于非肌肉浸润性膀胱癌中益生菌和饮食的潜在保护作用,对卡介苗有反应的人群中乳酸杆菌丰度的增加尤其引人注目。
年龄、免疫状态和尿液微生物组与卡介苗反应之间的确切联系尚未确定。
考虑到有相当多的非肌肉浸润性膀胱癌患者最终会进行膀胱切除术,对年龄相关卡介苗反应降低的机制进行更好的了解,将对评估复发风险和改善对现有治疗的反应非常有益。
在日本,肠道微生物组长期以来一直是浸润性膀胱癌治疗的目标,部分原因是发酵乳制品中广泛使用的乳酸菌,以及报道的小鼠口服乳酸菌制剂的抗肿瘤特性。
★ 乳酸杆菌
乳酸杆菌与膀胱癌复发减少或低发病率相关
一项包括138名患者的双盲随机对照试验结果显示,口服干酪乳杆菌制剂与安慰剂相比,男性和女性浸润性膀胱癌复发减少。
这些结果得到了一项病例对照研究的支持,该研究包括180名膀胱癌患者和445名年龄和性别匹配的健康志愿者,他们有10-15年的发酵牛奶的习惯摄入史(发酵奶是高脂肪的天然来源),每周1-2次乳酸杆菌(OR 0.46,95 % CI 0.27–0.79)或3-4次乳酸杆菌(OR 0.61,95% CI 0.38–0.99)与膀胱癌发病风险的降低有关。
这些发现得到了一项前瞻性试验结果的进一步支持,该试验包括202例经尿道膀胱肿瘤切除术后的浸润性膀胱癌患者,他们被随机分为两组,一组接受六次膀胱内表阿霉素治疗,另一组接受六次膀胱内表阿霉素治疗,外加每日3克干酪乳杆菌口服制剂,为期1年。
接受表阿霉素加每日制剂乳酸杆菌的患者3年无复发生存率为74.6%,而单独表阿霉素组仅为59.9% 。
这些研究没有调查粪便微生物组是否发生了变化,因此可以推断因果关系的程度有限。需要通过研究确定益生菌相关的变化,以及这些变化如何影响膀胱癌相关结果,来验证这些发现。
乳酸杆菌与肠道黏膜炎症减少有关
然而,在葡聚糖硫酸钠诱导的小鼠结肠炎症模型中,乳酸杆菌种类与肠道黏膜炎症减少有关。
在体外实验中,唾液乳杆菌降低肠上皮细胞系中TLR受体的激活,导致上皮细胞之间紧密连接的组装增加,可能减少系统性脂多糖和慢性炎症。
还需要在膀胱癌动物模型中进行更多的研究,以直接确定全身的病原相关分子模式水平是否也与全身炎症相关。
扩展阅读:如何调节肠道菌群?常见天然物质、益生菌、益生元的介绍
★ 萝卜硫素
除了乳酸菌,萝卜硫素也可能在恢复肠道屏障健康和降低膀胱癌发展风险方面发挥保护作用。
萝卜硫素饮食的小鼠丁酸水平增加
用亚硝基胺(BBN)治疗的小鼠和喂食高萝卜硫素饮食的小鼠丁酸水平增加,但与单独用亚硝基胺治疗的小鼠相比没有表现出增加的存活率。
肿瘤发生时间延长,发病率降低
然而,有趣的是,饲喂西兰花提取物(萝卜硫素的主要来源)的大鼠在暴露于亚硝基胺8周后,与未接受西兰花提取物的大鼠相比,肿瘤的发生时间延长了24周,其膀胱肿瘤发病率降低了58%.
重要的是,口服西兰花提取物导致小鼠在喂食12小时后尿液中生物活性异硫氰酸盐(包括萝卜硫素)的浓度比血清中高70% 。
这些化合物也会干扰亚硝基胺的代谢,由于它们在尿液中积累,其功能主要是通过改善肠道健康还是直接作用于尿路上皮细胞的其他机制尚不清楚。需要新的研究来调查它们对肠道健康、随后的炎症和微生物差异的影响,以改进对确切机制的定义。
总之,这些研究的结果表明,改变饮食,无论是口服乳酸杆菌或萝卜硫素,都可以降低膀胱癌的风险。这两种方法都与血清中细菌脂多糖浓度的降低相关,脂多糖是小鼠模型中肠道炎症的系统性标记物。
然而,关于乳酸杆菌或萝卜硫素在多大程度上诱导与治疗反应相关的肠道或尿液微生物组的积极改变,目前还缺乏数据。
菌群失调对PDL1-PD1轴的影响是一个有趣的话题。2016年首次批准PD1抑制剂用于顺铂难治性晚期膀胱癌。
总的来说,阿克曼菌Akkermansia、肠球菌、梭状芽孢杆菌、瘤胃球菌、粪杆菌和双歧杆菌的丰度增加与肺癌、肾癌和黑色素瘤等癌症对PDL1治疗的反应改善有关。
在转移性黑色素瘤患者中,研究中定义的患者粪便中“有益”与“无益”OTU数量的增加与抗PD1治疗反应的改善呈正相关。
PD1响应者粪菌移植的小鼠有更强的抗肿瘤反应
在对肠道微生物组和免疫治疗反应的三项独立研究中,从PD1治疗反应者到无菌小鼠的粪便移植产生了比无菌小鼠更强的抗肿瘤反应。
在一项研究中,研究了转移性黑色素瘤患者肠道微生物组和肿瘤微环境之间的相关性,以评估肿瘤微环境的发现是否可以预测对PD1免疫疗法的治疗反应。
对肿瘤活检的免疫组化分析显示,对PD1免疫治疗反应良好的患者,其肿瘤床上的CD8+ T细胞密度更大,调节性T细胞更少。
此外,响应者的物种多样性和瘤胃球菌科细菌的相对丰度高于无响应者。考虑到准确定义和匹配供体材料的重要性,必须了解粪菌移植如何改善抗免疫抑制分子或抗PDL1治疗的反应。
鉴于这些变化,作者得出结论,为 FMT 和其他微生物疗法准确匹配和定义微生物群可能需要额外的匹配,如年龄和性别,并准确定义理想的供体-宿主关系。
总之,这些发现强烈表明,在PD1免疫治疗的情况下,肠道微生物群可能会影响对癌症的全身免疫反应。
所有关于肠道微生物组和对PD1抑制剂的反应的初步研究都比较了相对物种丰度和处理反应。这种方法不能解释细菌总负荷的变化以及体循环中代谢物浓度的潜在差异。
微生物组是否通过直接的抗原相互作用对免疫系统产生影响,或者微生物组的代谢产物,包括潜在的有益成分和潜在的有害成分,是否间接地影响免疫系统,目前尚不清楚。
这种区别很重要,因为如果微生物组的主导作用是通过体循环中的代谢物间接发生的,那么微生物组可以被广泛地认为是一个更大的代谢产物网络的代表。
在这个模型中,许多不同的细菌组合有可能创造一个治疗性代谢网络,这与结果一致,表明促炎和抗炎成分对健康的老龄化都是必要的。
如果微生物组主要通过直接的免疫原性相互作用发挥作用,使免疫细胞对抗特定抗原,那么某些细菌种群的丰度是至关重要的。
膀胱癌的发病率与衰老密切相关。在老年患者中常见的炎症导致先天免疫系统失调,持续激活与活性氧表达和细胞因子释放相关的细胞。
与年龄相关的肠道微生物组变化可能有助于防止老年患者肿瘤的发生和肿瘤的治疗,但这些变化是否在功能上与老年患者的致瘤性炎症特征有关还有待确定。
许多膀胱癌患者以及其他尿道疾病患者与健康人群相比,尿液微生物群出现紊乱。需要更多大样本的基础研究,来确定膀胱癌或尿道疾病相关的菌群变化机制,从而更好地帮助治疗疾病。
没有确定的方法可以预防膀胱癌。但可以做一些有助于降低风险的措施。
虽然说没有一种食物本身可以绝对防止患癌症。但研究表明 ,富含各种水果、蔬菜、豆类、全谷物和其他植物性食物的饮食可以降低患多种癌症的风险,包括膀胱癌。
绿叶蔬菜
根据BCAN的数据,研究人员将每份蔬菜与膀胱癌风险减少10%联系起来。绿叶蔬菜含有抗氧化剂,抗氧化剂修复细胞损伤,同时还具有抗炎特性,甚至可以帮助预防癌症。例如:西兰花、卷心菜、南瓜、小麦胚芽、菠菜、羽衣甘蓝等
水果
研究人员还认为水果可以降低10%的膀胱癌风险。柠檬、橙子、葡萄柚和酸橙等柑橘类水果具有抗氧化特性,可以起到保护作用。其他还包括浆果,梨,苹果等。
茶
BCAN 表示,每天喝一杯茶,患膀胱癌的风险降低 6%,对动物的研究表明,多酚化合物会阻碍膀胱肿瘤的生长。绿茶中含有表没食子儿茶素-3-没食子酸酯,具有抗癌特性。
注意:红肉等加工食品中的化学物质会加剧膀胱癌的病情,此外还应避免酒精,零食等。尽可能均衡、健康地饮食。
西兰花芽丸、绿茶或姜黄素补充剂已经成为接受膀胱癌治疗的流行天然补充剂。然而,研究未能提供它们对人类有益的结论性证据。
在膀胱癌治疗期间服用姜黄素补充剂似乎可以使小鼠的肿瘤减小。
西兰花芽提取物对膀胱癌细胞的体外生长有抑制作用。
维生素E
据MayoClinic称,大量摄入富含维生素E的食物可以降低膀胱癌恶化的风险。
硒
硒是指一种具有抗氧化特性以防止细胞损伤的矿物质。因此,专家认为通过食用富含硒的食物可能帮助控制膀胱癌。如巴西坚果、核桃和燕麦片等。
限制场所
化工场所包括橡胶、皮革、印刷材料、纺织,油漆,铝,芳香胺、砷,染料,地毯,美发,打印等行业,接触时间过长可能患膀胱癌的风险更高,如在这些行业工作,尽可能遵守安全规则,做好防护措施。
尽可能减少吸烟
吸烟的人患膀胱癌的可能性至少是不吸烟的人的 3 倍。
多喝水
多喝水可能降低患膀胱癌的风险。如果喝白开水有困难,可以在水中加入新鲜柠檬片等来保持水分。
注:本账号内容仅作交流参考,不作为诊断及医疗依据。
主要参考文献:
Martin A, Woolbright BL, Umar S, Ingersoll MA, Taylor JA 3rd. Bladder cancer, inflammageing and microbiomes. Nat Rev Urol. 2022 Jul 7. doi: 10.1038/s41585-022-00611-3. Epub ahead of print. PMID: 35798831.
Babjuk M. Bladder Cancer in the Elderly. Eur Urol. 2018 Jan;73(1):51-52. doi: 10.1016/j.eururo.2017.04.018. Epub 2017 May 4. PMID: 28478044.
Andolfi C, Bloodworth JC, Papachristos A, Sweis RF. The Urinary Microbiome and Bladder Cancer: Susceptibility and Immune Responsiveness. Bladder Cancer. 2020 Sep 21;6(3):225-235. doi: 10.3233/BLC-200277. PMID: 33195783; PMCID: PMC7605348.
Kacew A, Sweis RF. FGFR3 Alterations in the Era of Immunotherapy for Urothelial Bladder Cancer. Front Immunol. 2020 Nov 5;11:575258. doi: 10.3389/fimmu.2020.575258. PMID: 33224141; PMCID: PMC7674585.
Palumbo C, Knipper S, Pecoraro A, Rosiello G, Luzzago S, Deuker M, Tian Z, Shariat SF, Simeone C, Briganti A, Saad F, Berruti A, Antonelli A, Karakiewicz PI. Patient frailty predicts worse perioperative outcomes and higher cost after radical cystectomy. Surg Oncol. 2020 Mar;32:8-13. doi: 10.1016/j.suronc.2019.10.014. Epub 2019 Oct 25. PMID: 31683158.
Zhang Y, Hou Q, Ma C, Zhao J, Xu H, Li W, Wang Y, Ma H, Zhang H, Sun Z. Lactobacillus casei protects dextran sodium sulfate- or rapamycin-induced colonic inflammation in the mouse. Eur J Nutr. 2020 Jun;59(4):1443-1451. doi: 10.1007/s00394-019-02001-9. Epub 2019 May 23. PMID: 31123864.

谷禾健康

现代化疗,放射疗法在摧毁癌细胞的同时,对健康细胞也造成了伤害,引发相关毒性,反应例如便秘,腹泻,疲劳,恶心,呕吐等。
癌症患者的营养状况可能是癌症治疗相关毒性的核心决定因素,也是癌症症状的指标。
一些临床前研究和初步临床试验表明,饮食干预可能会减轻某些癌症治疗相关的症状和毒性。可能机制包括影响炎症、氧化应激、肌肉质量、心脏健康和调节肠道菌群。
本篇涵盖了三大块内容,包括:
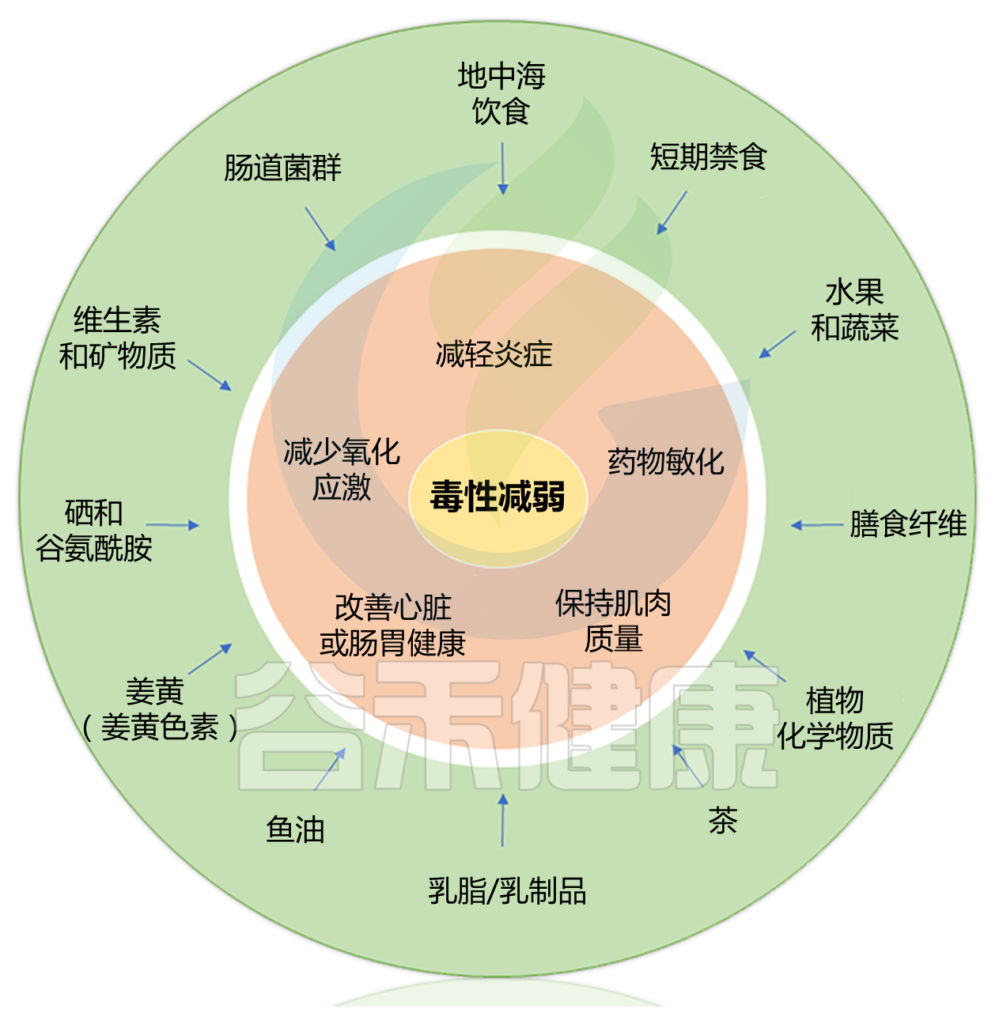
Alan J. Kim et al.,Cancer Treatment Reviews, 2022
地中海饮食模式,其特点是大量摄入水果、蔬菜、豆类、橄榄、全谷物、不饱和脂肪、坚果和鱼类;适度饮酒;减少红肉和加工肉类以及高脂肪乳制品的摄入,对减少炎症,改善心血管健康,抗肥胖,改善血脂以及对肠道菌群和免疫调节有积极作用。
↓↓ 降低心源性猝死
在一项大型前瞻性研究中,调查了激素替代疗法、钙和维生素D或饮食调整对健康绝经后妇女的影响,发现地中海饮食模式与降低心源性猝死的风险有关。
↓↓ 缓解癌症相关的疲劳
一项随机对照试验中,23名前列腺癌男性患者接受了至少3个月的雄激素剥夺治疗,被随机分成两组,一组接受12周常规治疗,另一组接受地中海饮食并同时接受六次个性化营养咨询,与常规治疗相比,坚持地中海饮食与缓解癌症相关的疲劳以及提高总体生活质量有关。
↓↓ 减轻妇科肿瘤患者症状
一项对22名接受铂类化疗的妇科肿瘤患者的观察研究表明,坚持地中海饮食的患者胃肠道毒性较小,恶心、胃痛、腹胀和干扰日常活动的频率和严重程度差异有统计学意义。
周期性禁食即在给定的时间内部分或完全不吃除水以外的食物和饮料。在动物模型和人类患者中,周期性禁食与降低癌症治疗中的毒性密切相关。
↓↓ 延缓肿瘤进展
例如,在一项临床前研究中证明,禁食条件增加了对化疗药物的敏感性,并延缓了肿瘤的进展。还有人发现,在荷尔蒙受体阳性乳腺癌的小鼠模型中,周期性禁食或类似禁食的饮食(FMD)可增强激素治疗的活性(如他莫昔芬和氟维司群),并通过降低循环中胰岛素、瘦素和IGF1的水平以及抑制AKT-mTOR信号传导来促进长期的肿瘤消退。
↓↓ 提升生活质量
在一项针对131名HER2阴性的II/III期乳腺癌患者的II期临床研究证实了4天FMD的潜在益处。在新辅助化疗前3天和新辅助化疗当天,接受了植物性、低氨基酸替代饮食(包括肉汤、汤、液体、维生素片和茶)的患者报告称,与对照组(常规饮食)相比,总体幸福感有所提高,情绪、身体、认知和社会功能都有所改善。
↓↓ 减少化疗相关毒性
在一项对照交叉初步研究中,调查了30名接受化疗的妇科癌症患者,结果表明,短期禁食的改良形式减少了化疗相关的毒性,包括口腔炎、头痛、虚弱和总体毒性。
据报道,FMD是安全可行的,可以减少脂肪量,降低循环中胰岛素生长因子1、胰岛素和瘦素的水平。禁食强烈影响新陈代谢和细胞途径,导致循环中类胰岛素一号生长因子(IGF-1)和葡萄糖水平下降。这些变化反过来影响几个癌基因,包括RAS和AKT信号通路,导致细胞生长和增殖的下调。
禁食和FMD(低卡路里、低蛋白质和低糖的饮食)可能与减少化疗副作用有关,即当营养素缺乏时,正常细胞,而不是肿瘤细胞,可以切换到抑制生长和增殖途径的保护模式,这一过程被称为差异应激抵抗。
↓↓ 增强免疫
此外,禁食和/或FMD已被证明可以增强免疫系统,减少炎症,减缓小鼠的骨密度损失,并减少HER2阴性的II期乳腺癌患者化疗引起的淋巴细胞DNA损伤。
生酮饮食的特点通常是碳水化合物消耗量低,占每日总热量摄入量的5%-10%,但其他产生能量的大量营养素,即脂肪和蛋白质的含量却不同。生酮比用来定义饮食的生酮能力,定义为脂肪克数与碳水化合物和蛋白质克数之和的比值。
在癌症中研究最多的生酮饮食包括经典生酮饮食(CKD),其特征是生酮比为4:1或3:1,每日87%-90%的热量来自脂肪)和中链甘油三酯生酮饮食[MCTKD,其中30%-60%的总热量来自中链脂肪酸,如己酸(C6)、辛酸(C8)、葵酸(C10)和月桂酸(C12)]。
↓↓ 血糖,体重更可控,生活质量高
在接受放化疗和辅助化疗的胶质母细胞瘤患者中,那些生酮饮食患者的血糖水平低于那些标准饮食的患者。有人研究发现,在接受放疗的非转移性乳腺癌患者中,以天然食物为基础的生酮饮食与未指定标准饮食相比,体重和脂肪减少得更多,生活质量水平更高。
↓↓ 降低癌症治疗相关毒性
生酮饮食降低癌症治疗相关毒性的机制可以用瓦氏效应(Warburg effect)来解释,在瓦氏效应中,癌细胞利用糖酵解而不是氧化磷酸化,能预防由活性氧引起的氧化损伤。
生酮饮食(通常是高脂肪低葡萄糖),可以利用这种代谢差异,要么让癌细胞挨饿,要么迫使它们转而利用氧化磷酸化。与正常细胞相比,癌细胞中氧化应激的增加可以使它们对化疗和放射更加敏感,从而减少治疗所需的剂量,降低与治疗相关的毒性。
↓↓ 注意高脂肪生酮饮食的副作用
有限的依据支持在临床实践中使用生酮饮食,而且,根据总含量和相对常量营养素组成,不同类型的生酮饮食可能对治疗相关的毒副作用产生不同的影响。例如,长期食用高脂肪生酮饮食可能会增加心血管或脑血管疾病的风险,特别是与特定的抗癌药物联合使用时。高脂生酮饮食还可能增加严重脂肪性肝炎的风险,促进肝纤维化的进展。此外,研究表明,高脂肪生酮饮食增加了酮体乙酰乙酯的循环水平,并促进了异种移植小鼠中表达BRAF-V600E致癌基因的人类黑色素瘤细胞的肿瘤生长潜力。
因此,根据目前对营养的理解,接受癌症治疗的患者的饮食应该包括所有的常量营养素,以降低营养不良的风险。
膳食纤维与多种肿瘤类型的胃肠道毒性和症状的预防有关。在一项随机对照试验中,在放疗期间服用高剂量膳食纤维(18克/天)的盆腔癌患者报告称辐射引起的胃肠道毒性发生率较低,证明了膳食纤维在预防放射治疗相关毒性方面存在潜在影响。
膳食纤维还可以促进健康的肠道菌群,从而降低毒性并增强治疗效果,例如纤维与促进免疫的普拉梭菌和短链脂肪酸丁酸盐的有关。有人发现在黑色素瘤患者中,膳食纤维会影响肠道菌群,并与免疫检查点阻断反应的增强有关。

Spencer CN, et al.,Science. 2021
tips
对于腹膜癌、肠癌进展或原发性胃肠癌的患者来说,可能需要低膳食纤维饮食,以降低肠梗阻的风险。
增加水果和蔬菜的摄入量与改善胃癌幸存者的身体和认知功能、减少疲劳和食欲不振有关。
水果和蔬菜含有过多的植物化学物质,并且已经检查了几种植物化学物质的影响,并在下表中进行了总结。

Alan J. Kim et al.,Cancer Treatment Reviews, 2022
例如,葡萄产品的抗氧化和抗炎作用归因于它们的植物化学物质,即芪类、花青素和原花青素,包括白藜芦醇。
其他几种水果,包括黑醋栗、李子、石榴和苹果,已经被证明具有抗癌和细胞毒性作用,这归因于植物化学物质,特别是多酚和黄酮类物质的抗氧化和抗炎作用。
tips
对于肠梗阻风险较高的患者,应避免过量摄入水果和蔬菜相关的膳食纤维。
据报道,在70多种植物中发现的一种植物化学物质白藜芦醇可以增加结直肠癌细胞系对化疗药物的敏感性,包括阿霉素、索拉非尼、5-氟尿嘧啶、依托泊苷、丝裂霉素、奥沙利铂和姜黄素。
关于白藜芦醇在该文有详细介绍:
注意:高剂量(每天>2.5克)会引起轻微的毒性(包括腹泻、胃肠道症状和前额头痛),即使在健康的人身上也是如此。
其他多酚也可能具有抗炎和抗氧化作用。
▸槲皮素是浆果中一种常见黄酮醇,它通过作用于炎症介质,包括白细胞介素6、白细胞介素8、干扰素γ、诱导型一氧化氮合酶、环氧合酶2和肿瘤坏死因子α来诱导抗炎作用,并在对促凋亡刺激敏感的癌细胞系中提供促凋亡作用。
▸非瑟素是一种存在于草莓、苹果和柿子中的类黄酮类化合物,在结构上与槲皮素相似,具有类似的抗炎和抗癌活性。
▸番茄红素是番茄和红色水果(包括木瓜和西瓜)中的一种植物化学物质,具有高抗氧化活性,并通过减少氧化应激以及染色体和膜的异常来减轻致癌损害。此外,番茄红素具有神经保护作用,并被认为可以通过减少氧化应激和神经炎症来预防神经毒性。
喝茶,尤其是绿茶,与抗癌作用、减轻药物引起的毒性以及对化疗药物的敏感性有关。
↓↓ 抑制继发性肿瘤
茶中存在的儿茶素在促进健康的作用中起着重要作用。表没食子儿茶素没食子酸酯在体外和体内乳腺癌模型中显示了抗氧化和抗炎活性(尤其是在他莫昔芬诱导的氧化应激情况下),能够抑制头颈部或盆腔癌症患者的放射性皮炎,并抑制继发性肿瘤的继发发展。
↓↓ 防止辐射带来的不良反应
据报道,表没食子儿茶素没食子酸酯还可用于预防暴露于γ辐射或以顺铂为基础的治疗后的唾液腺细胞功能障碍,防止辐射引起的不良血液学变化(如贫血、血小板减少),以及预防博莱霉素引起的肺纤维化。
↓↓ 减少药物引起的毒性
此外,表没食子儿茶素没食子酸酯可减少伊立替康治疗期间的胃肠紊乱、顺铂引起的肾毒性和耳毒性,以及阿霉素和柔红霉素治疗引起的心脏毒性。
在药物致敏方面,绿茶显示了许多与化疗的协同作用,其中一些包括与4-羟基他莫昔芬联合使用可以提高细胞毒性水平,通过降低大B细胞淋巴瘤(Bcl-xL)基因(编码抗凋亡蛋白)的表达使得MCF7细胞对5-氟尿嘧啶增敏,以及4只接种T1的Balb/c小鼠对紫杉醇的敏感性。这种致敏作用通过降低所需化学治疗药物的剂量有效地降低了药物引起的毒性的严重程度。
乳制品/奶制品与癌症治疗之间的关系一直存在争议。尽管据报道在Balb/c小鼠中,乳制品/乳脂可以增强紫杉醇治疗的有效性,并减少与该制剂相关的毒性,例如,器官损伤、腓肠肌丧失、附睾脂肪组织减少、红细胞和白细胞损失以及空肠形态、绒毛长度和肠 γ-谷氨酰转肽酶活性的破坏。
tips
有研究表明,在被诊断患有早期浸润性乳腺癌的女性中,高脂牛奶与乳腺癌、全因和非乳腺癌死亡率的增加有关,以及与绝经前妇女乳腺癌进展的风险增加有关。
鱼油富含omega-3脂肪酸,如二十碳五烯酸(EPA)和二十二碳六烯酸(DHA),在减少癌症和癌症治疗相关症状和毒性方面的作用已被广泛研究。
↓↓ 减少化疗引起的毒性
一项随机临床试验表明,在宫颈癌患者(n=40)中,补充鱼油可以减少化疗引起的毒性,如厌食、恶心、口干和味觉障碍。一项对88例癌症患者补充精氨酸、谷氨酸和鱼油的研究表明,补充精氨酸、谷氨酸和鱼油可显著减少3-4级血液毒性,并提高两年总生存率。
↓↓ 增强抗肿瘤作用
一些体外和体内研究表明,与单纯化疗相比,化疗期间给予EPA和DHA可以增强抗肿瘤作用,减少化疗对正常组织的毒性,抑制全身炎症,改善癌症患者的营养状况。同样,在紫杉醇和顺铂/卡铂治疗期间,在等卡路里饮食中添加EPA与非小细胞肺癌患者的疲劳减轻、食欲改善和化疗引起的神经病变减少有关。
↓↓ omega-3脂肪酸减少化疗毒性
omega-3脂肪酸还可以减少癌症相关的恶病质,增加免疫调节作用,从而增强结直肠癌和食道癌患者的化疗与放疗,减少食道癌患者化疗引起的毒性(如口腔炎,3/4级腹泻,以及天冬氨酸转氨酶和丙氨酸转氨酶水平的升高)。
已经提出了多种机制来解释omega-3脂肪酸在降低癌症治疗相关毒性方面的作用。其中一种假设是细胞膜的组成,这表明不饱和脂肪酸掺入癌细胞膜中,导致细胞膜组成模式与正常细胞不同。考虑到细胞膜是细胞内信号传导和基因表达调控的中心,癌细胞和正常细胞之间细胞膜上脂肪酸分布的不同可能导致信号通路的不同激活(例如,PKC激活和NF-KB 通路)。
尽管omega-3脂肪酸在临床试验中显示出了益处,但在临床前模型中,omega-3脂肪酸十六碳-4,7,10,13-四烯酸已证明可以抑制铂化合物的肿瘤导向细胞毒性,这可能会对患者造成潜在的伤害。
因此,在建议临床食用鱼油之前,有必要进一步研究普通鱼油成分与纯化的EPA/DHA对特定化疗药物的细胞毒性的影响。
姜黄是一种开花植物,可从中提取姜黄素。它们与预防和治疗化疗和放疗相关的不良事件有关。姜黄/姜黄素对癌症的有益作用归因于它们的抗氧化和抗炎特性,以及它们在抑制细胞增殖和肿瘤干细胞发展方面的作用,以及它们对肠道菌群和免疫系统的积极作用。
↓↓ 姜黄油降低化疗4级毒性发生率
姜黄油具有保肝作用,并缓解刀豆蛋白A诱导的氧化应激和炎症,从而减少人类患者的多种症状和毒性。同样,与其他草本物质:发酵大豆提取物、绿茶提取物、樟芝菌丝体、螺旋藻和葡萄籽提取物相结合,可显著降低接受亚叶酸钙/5-氟尿嘧啶化疗患者的4级毒性发生率。
↓↓ 姜黄/姜黄素减轻粘膜炎严重程度
一项评估的结论是,局部应用姜黄和姜黄素可以控制接受化疗和/或放疗的癌症患者的口腔粘膜炎,而接受姜黄/姜黄素治疗的患者报告称疼痛较轻,红斑强度较低,溃疡区域较少。一项评估32名接受放射治疗的头颈部癌症患者的临床试验也得出结论,口服纳米胶束姜黄素显著减轻了放疗引起的粘膜炎的严重程度。
↓↓ 姜黄/姜黄素有助于控制癌症相关的疼痛
一项针对绝经后乳腺癌患者的多中心临床试验(n=45)显示,联合应用羟基酪醇(一种在橄榄油中发现的具有强大抗氧化作用的酚类植物化学物质)、omega-3脂肪酸和姜黄素可以减轻患者报告的疼痛,并降低炎症生物标志物的水平。
↓↓ 姜黄与常见化疗药物的协同 / 拮抗作用
姜黄素在I期临床试验中协同增强化疗药物FOLFOX(5-氟尿嘧啶、亚叶酸钙、奥沙利铂)和达沙替尼对经FOLFOX处理的HCT116和HT-29细胞有抗增殖作用。
尽管这些结果提示了有希望的进一步研究领域,但对人乳腺癌细胞株(即MCF-7、MDA-MB-231和BT-474)的体外实验表明,姜黄素与以伊立替康或环磷酰胺为基础的化疗之间存在拮抗作用,饮食补充姜黄素可能会抑制基于化疗的肿瘤消退。这些发现表明,需要更多的研究来确定乳腺癌患者是否应该在化疗期间避免补充姜黄素。
谷氨酰胺是巨噬细胞、淋巴细胞和肠细胞的主要燃料来源,具有多种有益作用,包括改善免疫系统、减少炎症和分解应激状态。
↓↓ 化疗配合谷氨酰胺补充,降低血液学毒性发生率
一项针对接受同步放化疗的癌症患者的随机研究表明,除了常规饮食外,还接受精氨酸、谷氨酰胺和鱼油营养补充剂的患者与未接受补充剂的患者相比,发生3级或4级血液学毒性的发生率较低。
↓↓ 补硒改善免疫系统
据报道,补硒在脂质过氧化方面具有抗氧化作用,刺激自然杀伤细胞的细胞毒活性,减少肿瘤内血管生成,并在体外改善免疫系统。硒与重金属的解毒作用有关。这些影响的产生可能是因为硒是硒蛋白和酶的重要组成部分,这些硒蛋白和酶有助于抗氧化防御、减少炎症、甲状腺激素产生、DNA合成。
一项对关于硒和放射治疗的文章进行了评估,得出的结论是,每天服用300-500微克的硒,持续10天到6个月,可以减少放疗的副作用,包括腹泻、唾液腺损伤和辐射伤口,不会产生不良影响。
tips
高剂量的硒(>400微克/天)会产生严重的副作用,像指甲变脆、脱发、胃肠功能障碍、皮疹、神经紊乱等。
维生素补充剂在减少癌症和癌症治疗相关症状和毒性方面的功效研究显示出相互矛盾的结果。
例如,尽管许多研究表明维生素C补充剂具有潜在的抗癌作用和降低毒性作用,但对接受化疗的癌症患者的维生素C进行的系统审查发现,没有明确的证据表明服用维生素C补充剂可以减少毒性或改善治疗的抗癌效果。
同样,尽管维生素D补充剂已被证明可以预防癌症治疗引起的骨质流失,并恢复许多早期乳腺癌患者经历的维生素D不足,但在各种研究中报告的维生素D的抗肿瘤效果仍然很差。
tips
由于维生素补充剂在癌症治疗期间的效果尚不清楚,强烈建议患者遵守饮食建议,通过水果和蔬菜等天然食物摄入维生素,而不是依赖膳食补充剂。
一个健康人体胃肠道中的各种复杂的微生物群已显示出显著的生理益处,如增强肠道功能和消化能力、抵御病原体和调节免疫力。
虽然“健康”肠道菌群的定义并不明确,但数据表明,具有高度功能冗余度的多样化和稳定的微生物群是健康状态的关键标志。
肠道菌群对癌症患者的治疗反应有显著影响。例如,白血病或淋巴瘤患者在造血干细胞移植后具有高水平的粘液真杆菌,其复发或肿瘤进展的可能性较低。
↓↓ 肠道菌群失调影响抗PD-L1治疗效果
人类、动物和体外研究表明,肠道菌群的免疫调节影响靶向免疫治疗的疗效,如细胞毒性T淋巴细胞相关4(CTLA-4)阻断和抗PD-L1治疗。与这些发现一致的是,一部分接受抗PD-L1治疗和广谱抗生素治疗的上皮性肿瘤患者经历了失败治疗,其原因可能是导致了微生物群的失调。
进一步支持这些发现的是,从应答者和无应答者患者向有免疫活性小鼠的粪便转移导致小鼠对抗PD-L1抗体产生了与相应粪便移植供体相同的反应,从而证明了肠道菌群对抗PD-L1治疗的效果。
↓↓ 肠道菌群调节化疗的疗效和毒性
化疗药物环磷酰胺和阿霉素能诱导革兰氏阳性菌(约氏乳杆菌、鼠乳杆菌和海氏肠球菌)转移到小鼠的次级淋巴器官中。一旦转移到淋巴器官,微生物就会刺激17型和1型T辅助细胞反应的积累,从而增强免疫反应。
临床前和临床证据都表明,抗生素会降低化疗的疗效。例如,长期使用抗生素已被证明会降低环磷酰胺治疗荷瘤小鼠P815肥大细胞瘤的疗效,支持了肠道细菌易位的重要性。
一项对C57BL/6(B6)和129SvEv(129)小鼠化疗所致周围神经病变的临床前研究表明,肠道细菌在确定紫杉醇诱导的疼痛敏感性中起主导作用;在对紫杉醇诱导的疼痛敏感和抵抗的小鼠之间,观察到肠道微生物群组成的显著差异。
↓↓ 肠道菌群与胃肠道不良反应的发生率有关
一项对接受放化疗的宫颈癌患者进行的临床研究(n=35)得出结论,肠道微生物多样性与胃肠道毒性的发生率呈负相关。
同样,一项针对儿童急性淋巴细胞性白血病患者(n=51)的临床研究确定,化疗期间肠道微生物群的变化与胃肠道不良反应的发生率有关,如全身炎症和肠道粘膜炎。Toll样受体(TLRs)和肠道微生物之间的免疫调节相互作用可能调节结肠的炎症和愈合,防止甲氨蝶呤化疗的毒性。
↓↓ 肠道菌群从根本上与粘膜炎的发病机制相关
粘膜炎是一种常见的胃肠道毒性,会导致腹泻、疼痛、体重减轻和剂量限制。例如,伊立替康是一种已知会引起严重腹泻的化疗剂。这种毒性的一种机制可能是某些细菌β-葡萄糖醛酸酶的作用,这些酶已被证明通过将伊立替康的活性代谢物SN-38释放到肠腔中来诱导腹泻。
与这一假设一致,通过喹诺酮类抗生素环丙沙星抑制此类酶可抑制伊立替康治疗小鼠的腹泻,从而证明肠道微生物群的调节可以降低伊立替康的毒性。
↓↓ 肠道菌群影响癌症治疗相关的心理神经症状
一项系统评价评估了肠道微生物群与化疗之间关系的研究,得出的结论是,肠道微生物群可能会影响癌症治疗相关的心理神经症状,例如疲劳、焦虑、抑郁和睡眠障碍。
因此,相对健康的肠道微生物群可以改善癌症患者的健康,通过增强治疗效果和减少免疫疗法和化学疗法的副作用以及通过免疫调节等方式。
饮食影响肠道微生物种类的组成和多样性。膳食纤维的高摄入量有利于膳食纤维消化细菌的增加。作用机制是消化膳食纤维的细菌产生丁酸等短链脂肪酸,滋养肠道上皮细胞,从而加强肠道黏膜屏障,增强黏膜和全身免疫。
↓↓ 食品补充剂调节微生物群驱动的化学治疗毒性
由于肠道屏障和微生物群稳态的潜在损害,化疗通常与肠道菌群的改变有关。因此,预防和治疗与化疗相关的肠道菌群改变可能有助于预防与化疗相关的胃肠道毒性。
▸从鱿鱼墨汁中提取的多糖在小鼠给药环磷酰胺后可富集双歧杆菌,并减少拟杆菌,从而改善肠道微生物群功能障碍。
▸人参化合物可以增强化疗药物5-氟尿嘧啶对结直肠癌细胞系的作用,特别是当这些化合物被肠道微生物群菌群代谢时。
▸鞣花酸,一种常见于草莓、葡萄和黑莓等蔬菜和水果中的多酚,被肠道菌群代谢释放尿石素,这对人类结肠癌具有抗增殖作用。
↓↓ 益生元和益生菌在癌症治疗中发挥作用
益生元(促进有益肠道微生物生长的难消化的食物成分,例如香蕉、芦笋和朝鲜蓟)和益生菌(引入体内以发挥有益作用的微生物,例如酸奶、克非尔、酸菜、豆豉,和泡菜)与肠道菌群的组成密切相关,这些物质在癌症治疗过程中的作用很关键。
许多动物和人类研究表明,益生元、益生菌在预防化疗期间的粘膜炎方面具有强大的作用。
对于接受同步放化疗的鼻咽癌患者,益生菌与放射治疗相结合,可以通过改变肠道菌群,显着增强宿主免疫力,缓解放化疗相关的口腔黏膜炎。
VSL #3(包括Streptococcus thermophiles, Bifidobacterium breve, B. longum, B. infantis, Lactobacillus paracasei, L. delbrueckii subsp. bulgaricus, L. acidophilus, L. plantarum),在伊立替康治疗期间,减少大鼠腹泻和体重减轻。
L. casei, L. rhamnosus, B. bifidum 通过抑制肿瘤坏死因子α、白细胞介素-1b和白细胞介素-6 mRNA的表达减少化疗诱导的小鼠腹泻。
鼠李糖乳杆菌GG补充可减少人类大肠癌患者在5-氟尿嘧啶化疗期间的严重腹泻和腹部不适。
在接受化疗的儿童中使用养乐多的短双歧杆菌菌株可预防发烧并减少静脉注射抗生素的频率。
膳食补充益生元低聚果糖和菊粉可放大药物对小鼠的作用(5-氟尿嘧啶、多柔比星、长春新碱、环磷酰胺、甲氨蝶呤、阿糖胞苷),从而证明了益生元与化疗之间的协同作用。
编辑
大量临床前数据以及有限的临床证据表明,饮食因素可能在预防和/或治疗癌症以及癌症治疗相关的症状和毒性方面发挥作用,寻求特定饮食干预措施的数据仍在不断涌现。
人们对肠道菌群的性质和对癌症治疗的影响也越来越感兴趣。期待更大样本量的随机对照试验,进一步研究饮食干预措施。
最好的饮食是患者愿意并且能够坚持的饮食,因此在将这些策略引入临床时可能需要一定程度的个性化。
如果能开发出,通过调节肠道菌群来改善治疗效果的药物,其潜力是巨大的。
主要参考文献
Spencer CN, McQuade JL, Gopalakrishnan V, McCulloch JA, Vetizou M, Cogdill AP, Khan MAW, Zhang X, White MG, et al. Dietary fiber and probiotics influence the gut microbiome and melanoma immunotherapy response. Science. 2021 Dec 24;374(6575):1632-1640. doi: 10.1126/science.aaz7015. Epub 2021 Dec 23. PMID: 34941392; PMCID: PMC8970537.
Yu ZK, Xie RL, You R, et al. The role of the bacterial microbiome in the treatment of cancer. BMC Cancer. 2021;21(1):934. Published 2021 Aug 19. doi:10.1186/s12885-021-08664-0
Kim AJ, Hong DS, George GC. Dietary influences on symptomatic and non-symptomatic toxicities during cancer treatment: A narrative review. Cancer Treat Rev. 2022 May 13;108:102408. doi: 10.1016/j.ctrv.2022.102408. Epub ahead of print. PMID: 35623220.
Barrea L, Caprio M, Tuccinardi D, Moriconi E, Di Renzo L, Muscogiuri G, Colao A, Savastano S; Obesity Programs of nutrition, Education, Research and Assessment (OPERA) group. Could ketogenic diet “starve” cancer? Emerging evidence. Crit Rev Food Sci Nutr. 2022;62(7):1800-1821. doi: 10.1080/10408398.2020.1847030. Epub 2020 Dec 4. PMID: 33274644.
Baguley BJ, Skinner TL, Jenkins DG, Wright ORL. Mediterranean-style dietary pattern improves cancer-related fatigue and quality of life in men with prostate cancer treated with androgen deprivation therapy: A pilot randomised control trial. Clin Nutr. 2021 Jan;40(1):245-254. doi: 10.1016/j.clnu.2020.05.016. Epub 2020 May 25. PMID: 32534948.

谷禾健康
神经免疫,菌群,心血管疾病
最新的《中国心血管病健康和疾病报告2019》数据显示,中国居民心血管病现患人数已达3.30亿,拐点尚未到来,且7-17岁儿童青少年高血压患病率呈现上升趋势。
心血管疾病(CVD)仍然是全世界发达国家死亡和残疾的主要原因。此外,广泛存在的心血管危险因素,如代谢综合征、糖尿病、肥胖和性类固醇激素代谢紊乱,有效预防策略已成功减少急性心血管事件和死亡的影响。
大脑和其他器官系统之间的双向通信对于大脑健康和生物体的整体健康至关重要。曾经被认为具有免疫特权的大脑现在被认为是一个高度免疫特化的器官,拥有自己的大脑驻留免疫细胞。这些细胞形成神经元回路和淋巴系统,这些系统调节免疫细胞的复杂流出,以及从脑脊髓空间与循环的其余部分交换的液体。
而共生微生物群是个体间异质性的重要来源,可以通过调节宿主免疫来影响人类健康。人们越来越认识到 CVD 的许多潜在原因,包括免疫和肠道菌群失调可能是 CVD 的致病因素,提出了对新的免疫调节治疗策略的需求。
本文总结了免疫、炎症的神经调节以及肠道菌群如何参与 CVD 的发病和进展,并探索菌群-神经免疫通讯是否为 CVD 的潜在治疗靶点。
本文缩略词:
CVD: 心血管疾病 (cardiovascular disease )
心血管疾病,又称为循环系统疾病,是一系列涉及循环系统的疾病,循环系统指人体内运送血液的器官和组织,主要包括心脏、血管(动脉、静脉、微血管),可以细分为急性和慢性,一般指心脑血管疾病。
ANS: 自主神经系统 (autonomic nervous system)
自主神经系统是脊椎动物的末梢神经系统,由躯体神经分化、发展,形成机能上独立的神经系统,是外周传出神经系统的一部分,能调节内脏和血管平滑肌、心肌和腺体的活动,又称植物性神经系统、不随意神经系统,故名自主神经系统(参考自:百度百科)。
SFO: 穹窿下器神经元 (Neurons of the subfornical organ )
穹窿下器官,室周器官,位于第三脑室前背侧壁、海马连合腹侧穹窿柱分歧处、适平室间孑L平面。
OVLT: 下丘脑终板血管区(Organum vasculosum laminae terminalis)
终板就是第三脑室前缘的隔膜。下丘脑终板血管区,内生致热原作用于血脑屏障外的脑血管区,即下丘脑终板血管区,该区位于第三脑室壁的视上隐窝处。
PVN: 下丘脑室旁核 (paraventricular nucleus)
下丘脑室旁核 位于第三脑室下丘脑部的上端两侧,呈长楔形轮廓,是下丘脑前区最显著的核团之一,与神经内分泌活动和植物性功能等有关的复合体结构,参与体内电解质与体液平衡,心血管活动调节及其它多项生理功能的调控。
NTS: 孤束核 (nucleus tractus solitarius)
孤束核为延髓内重要内脏感觉性核团,为一般内脏感觉和味觉传导通路上的第一级中继站。随着神经解剖学和神经生理学研究方法的不断发展,人们对孤束核的认识日趋深入,近年来HRP和ARG技术有关孤束核的大量的研究证实了孤束核不但与低级中枢(脊髓、脑干)具有传入、传出神经联系,而且与高位中枢(前脑、小脑)也具有复杂的往返联系。
DMV:迷走神经运动背核 (dorsal nucleus of vagus nerve)
迷走神经背核是2014年经全国科学技术名词审定委员会审定发布的人体解剖学名词。位于延髓室底灰质内,迷走神经三角深面的神经核。属一般内脏运动核,支配颈部、胸部所有内脏器官和腹腔大部分内脏器官的平滑肌、心肌的活动和腺体的分泌。
神经和免疫系统通常通过特定的大脑区域、传入和传出周围神经以及神经激素通路进行交流(下图)。
大脑和周围器官之间的通讯途径
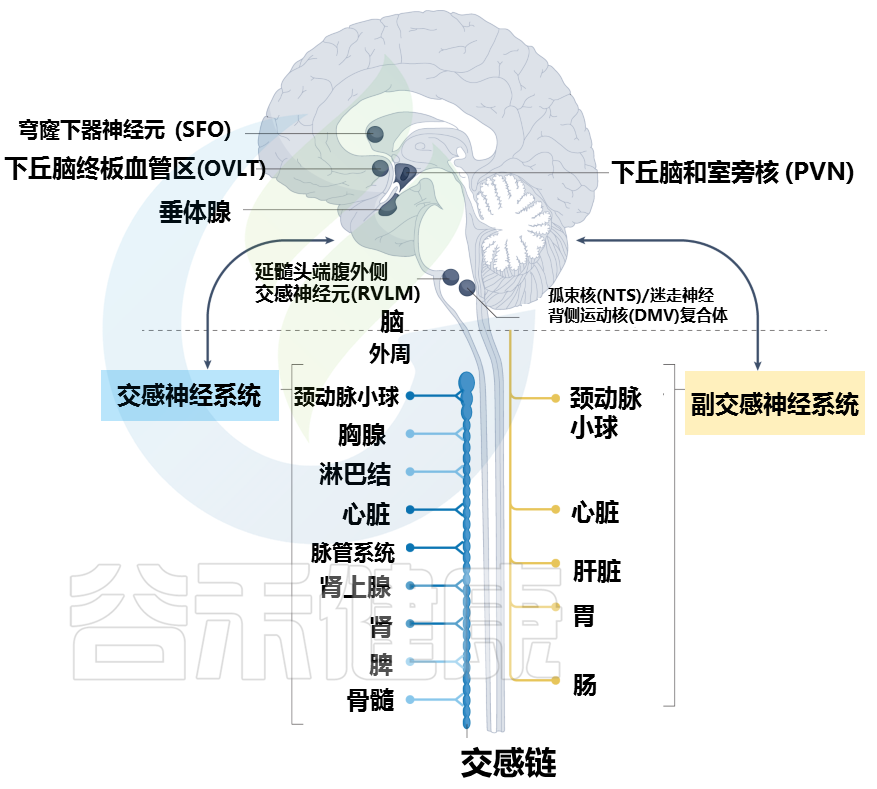
Carnevale D. Nat Rev Cardiol. 2022
大脑通过不同的途径与周围器官和组织相连。特定的大脑区域,统称为脑室周围器官,与周围形成自然的大脑界面,内衬有渗漏的血脑屏障。神经网络从脑室器官延伸到周围神经系统,并建立重要的神经解剖学连接。
穹窿下器官 (SFO) 和终板血管器官 (OVLT) 的神经元密集表达 1 型血管紧张素 II 受体和渗透压感受器,并为下丘脑的室旁核 (PVN) 提供神经支配。反过来,PVN 与延髓腹外侧 (RVLM) 的交感神经元相连,RVLM 具有调节外周交感神经活动的重要功能。
PVN 的其他神经元连接到孤束核 (NTS) 和迷走神经背运动核 (DMV) 的复合体,它们负责通过迷走神经传递的外周胆碱能神经支配。
所有主要的外周器官通常都有交感神经支配(包括心脏、脉管系统、肾脏和颈动脉体)和副交感神经支配(包括心脏、颈动脉体、肝脏、胃和肠)。
交感神经支配是免疫器官(以浅蓝色显示)和内脏组织的神经控制的主要途径。大脑、心血管系统和免疫器官之间的进一步整合轴是由神经内分泌系统通过下丘脑-垂体-肾上腺轴形成的。
循环物质,如细菌源性肽、宿主源性细胞因子和组织代谢物,向特定的大脑区域发出信号,这些区域的特点是存在渗漏的血脑屏障。
脑室周围器官由穹窿下器官(SFO)、终板血管器(OVLT)和末梢区组成,是监测周围组织并在神经免疫过程中发挥关键功能的大脑区域。同时,脑室周围器官在心血管疾病中起着至关重要的作用。
穹窿下器官富含血管紧张素II受体1型,它是肾素-血管紧张素-醛固酮系统的关键介质。
OVLT的神经元同时表达血管紧张素II受体1型和渗透压感受器,它们对感知细胞外钠/盐负荷浓度至关重要。
它们共同传递有关血容量、血压和细胞外液渗透压的外围信息。
有趣的是,从穹窿下器和OVLT投射到下丘脑室旁核(PVN)的神经元也被描述过,脑室旁核也接受后脑的投射,这表明它具有整合功能。虽然它们位于脑室周围器官之外,但孤束核(NTS)和迷走神经背侧运动核(DMV;心血管功能最有效的调节器之一)接收来自末梢区的输入。
大脑通过在脑室旁核和脊髓中间外侧细胞柱之间建立直接投射,或通过延髓头端腹外侧间接连接,来控制周围交感神经反射反应。外周的稳态扰动由延髓头端腹外侧感觉到,并通过蓝斑的去甲肾上腺素能神经元以反射反应传递。
作为补充,神经元表达细胞因子受体,这有助于神经免疫串扰和脑与身体的相互作用。
当细胞因子在各种生理和病理生理环境中的外周组织中分泌时,神经元活动就会改变。虽然神经元细胞因子受体的生理功能仍在研究中,但细胞因子在脑发育、外周组织损伤和动物行为方面的作用已被证明。这些观察表明存在由细胞因子介导的脑-体双向轴。
接下来进一步的讨论这些信号是如何在心血管疾病中启动、传播和转移到大脑的。
投射到中枢神经系统之外的神经被称为外周神经系统,它双向连接大脑和外周器官和组织。
外周神经系统分为两个部分:
躯体神经系统和自主神经系统(ANS)
躯体神经系统与中枢神经系统交换感觉和运动信息,而ANS调节非自愿功能,并在神经免疫和心血管相互作用中起决定作用。
ANS由传入和传出神经元组成,将大脑与周围内脏器官和组织连接起来。历史上,ANS被定义为平行的交感和副交感臂,分别负责所谓的“逃跑或战斗”和“休息和消化”反应。
ANS作为大脑与外周沟通的关键途径的概念不断发展,有证据表明,ANS也发挥了神经免疫调停者的作用。生理和心血管反应的改变都受到ANS的深度影响,ANS的失衡是许多心血管疾病的典型特征。
我们对ANS如何调节心血管功能的理解有了实质性的进步,这得益于实验方法的发展,使直接分析神经系统活动成为可能。
实验性和临床性的显微神经学被用来测量指向心血管系统的节后交感神经传出的电活动。例如,骨骼肌血管的显微神经造影术成为评估人类区域交感神经活动的金标准方法。
应用于动物实验的类似程序有助于确定ANS调节心血管功能的解剖路线和分子机制。在过去5年中,已经制定了直接评估调节免疫系统的ANS臂的实验方案,从而能够定义神经免疫机制如何促进心血管疾病的发病和进展。
神经系统和免疫系统之间的进一步相互作用是通过神经内分泌系统进行的,主要通过下丘脑-垂体-肾上腺轴进行调节。下丘脑-垂体-肾上腺轴通常对心理压力敏感,是免疫反应和心血管功能的有效调节剂。
神经元顺行和逆行追踪技术已被用于通过周围神经系统的传入和传出臂绘制大脑和免疫器官之间的连接(下图)。
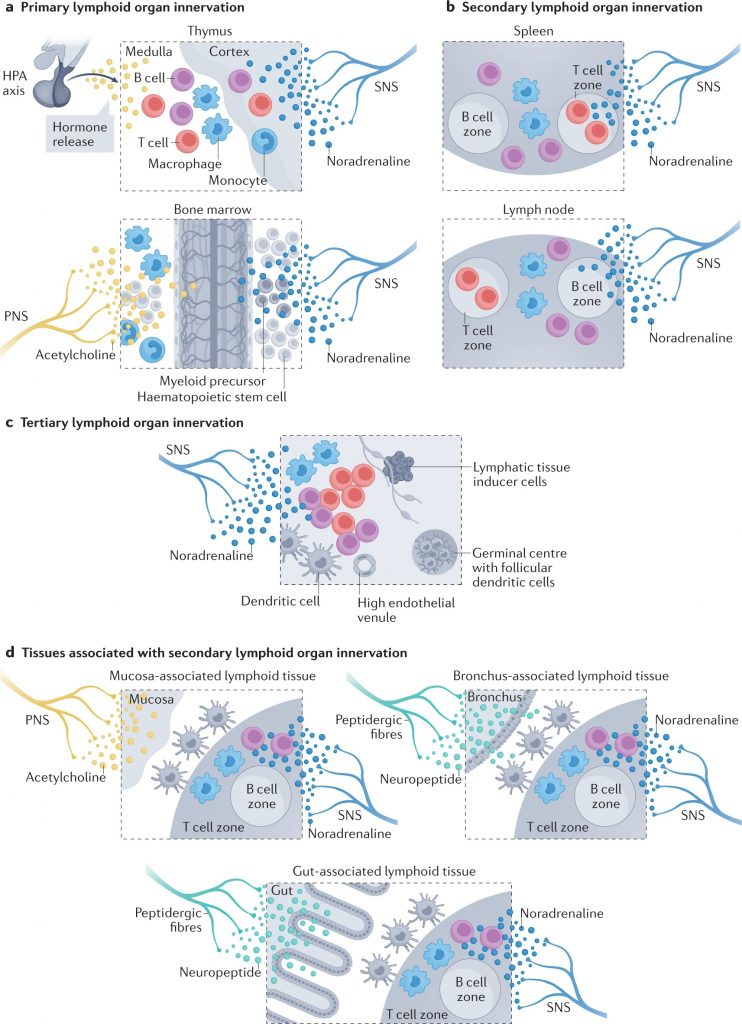

Carnevale D. Nat Rev Cardiol. 2022
a |初级淋巴器官神经支配。胸腺主要由去甲肾上腺素能纤维支配。虽然不存在直接的胆碱能神经支配,但交感神经与下丘脑-垂体-肾上腺(HPA)轴之间的相互作用已被证实。相反,骨髓神经支配更为复杂,包括交感神经系统(SNS)、副交感神经系统(PNS)和与大脑建立双向通讯的感觉纤维。骨髓的造血和免疫功能受到这种神经网络的严格调节。
b |次级淋巴器官包括脾脏和淋巴结,由去甲肾上腺素能纤维密集支配,其起源于大脑,已通过神经调节研究确定。淋巴结也有一个明显的感觉神经网络,可以严密监测外周免疫状态。
c |三级淋巴器官是为了应对非淋巴器官的病理挑战而形成的,具有独特的组织特异性组织。控制第三淋巴器官神经支配的神经纤维仅在少数解剖部位被发现。
d |粘膜相关淋巴组织在粘膜组织(如支气管或肠道)中形成,以响应稳态的扰动,并由神经网络严格控制,包括SNS、PNS和肽能感觉纤维。
神经元追踪确定外周器官神经支配路线
神经元连接性的研究需要对轴突进行双向追踪,包括从神经元细胞体到轴突终末的顺行追踪,以及从终末到胞体的逆行追踪。神经解剖学追踪是一种通过追踪神经元在突触前或突触后水平的连接来识别神经元的常用方法。神经解剖学追踪技术在确定包括免疫器官在内的外周器官的神经支配途径方面变得特别有用。
原始追踪研究的基础是将氟金注射到免疫器官中,使研究人员能够逆行识别节前神经元,或注射生物素化葡聚糖胺以顺行识别神经元连接。几十年来,这些单独使用或联合使用的示踪剂使研究人员能够研究连接大脑和周围器官的神经回路。
随后的技术进步利用伪狂犬病病毒(一种高度传染性的神经营养性α疱疹病毒,Pseudorabies virus,PRV)的能力来定义中枢神经系统中的多突触回路。病毒的逆行扩散只发生在突触相连的神经元链中。在将伪狂犬病病毒注射到感兴趣的器官或组织后,更高阶的神经系统结构在稍后的时间点被标记。通过这种方式,可以定义神经元连接的精确路径,从外周器官开始,追溯到大脑。此外,伪狂犬病病毒在神经元细胞体中复制的过程具有自我放大的能力,这使得在受感染动物的大脑中识别二级、三级甚至四级神经元成为可能。
初级免疫器官包括胸腺和骨髓,它们参与淋巴细胞的产生和初始选择。胸腺在新生儿和青春期前发育阶段活跃,逐渐退化,只有残留的淋巴细胞生成持续到成年期。骨髓包含在骨腔中,从未成熟的造血祖细胞开始产生红细胞和免疫细胞。
胸腺神经支配和神经元调节
不同类型的细胞参与胸腺器官发生,这需要神经嵴细胞的协调相互作用。基于旧追踪技术的初步研究显示,交感神经纤维错综复杂,主要释放去甲肾上腺素,并在胸腺中形成血管周围神经网络。使用经典单突触逆行和顺行示踪剂的类似方法并没有识别胸腺的副交感神经支配。
后续的研究使用伪狂犬病病毒(PRV)的逆行跨神经元多突触追踪,来确定负责交感神经流出到胸腺的中枢神经系统区域。PRV感染的神经元分布在脊髓、延髓、脑桥、下丘脑室旁核、去甲肾上腺素能细胞A5组、延髓头端腹外侧核和中缝尾侧核。
值得注意的是,PRV感染的动物在DMV中没有PRV阳性细胞核,这与之前的观察结果一致,之前的观察排除了支配该区域胸腺的迷走神经纤维的存在。
虽然连接胸腺和大脑的硬连线路径的证明来自动物研究,追踪技术是可行的,但报告显示人类存在类似的胸腺神经支配模式,为这些发现提供了转化相关性。
神经样纤维和垂体激素通过人胸腺的免疫组织进行化学鉴定。胸腺糖皮质激素通过调节儿茶酚胺释放和肾上腺素受体表达,对胸腺细胞的存活和分化以及交感神经系统功能都很重要。相反,接受肾上腺切除术的动物胸腺去甲肾上腺素水平显著降低。
典型的感觉神经肽,如P物质和降钙素基因相关肽(CGRP),已在胸腺中被发现,但没有明确的报告表明,这些神经肽可以为大脑提供感觉通路,这意味着交感神经支配可能是调节胸腺免疫功能的唯一神经通路。
骨髓神经支配和神经元调节
骨髓神经支配沿着主动脉传导,并通过血管丛穿透骨髓。实质以神经纤维树枝状排列为特征,末端靠近造血细胞和淋巴细胞。大多数纤维支配骨髓血管系统,但其他一些神经末梢支配实质性和血窦元素以调节造血和细胞迁移。
酪氨酸羟化酶是去甲肾上腺素合成的限速酶,存在于大动脉周围的所有神经中,并延伸至骨髓实质。除了主要的去甲肾上腺素能神经支配外,还确定了神经肽Y的免疫反应性,从而表明骨髓的去甲肾上腺素能神经支配和肽能神经支配是混合的。
在很久以前发表的研究中也检测到对 P 物质和 CGRP 呈阳性的神经纤维,但感觉神经元的功能直到最近才被发现。CGRP感觉纤维与去甲肾上腺素能神经一起延伸到骨髓,在那里它们与酪氨酸羟化酶神经元合作,控制造血干细胞的动员。这些发现表明大脑通过硬连接的交感神经和感觉连接控制骨髓的免疫和稳态功能。
随后的研究还发现了支配骨骼和骨髓的副交感神经纤维。尽管在造血生态位附近检测到合成乙酰胆碱的胆碱乙酰转移酶的免疫反应性,但仅在骨中发现了明显的功能性副交感神经支配,其中胆碱乙酰转移酶调节骨重塑。
后来的研究表明,骨髓神经支配与昼夜节律密切相关。骨髓中去甲肾上腺素的释放依赖于昼夜振荡,进而调节与控制白细胞和造血干细胞的保留和排出过程相关的基因表达。尽管这种构成过程在生理上是相关的,但神经介导的白细胞和造血干细胞转运的节律过程在疾病背景下可能特别重要。
未来的研究将有必要澄清清晨急性心血管事件的高发病率是否与神经调节白细胞和造血干细胞运输的影响有关。
次级淋巴器官包括淋巴结、脾脏和与粘膜相关的淋巴组织,通常由交感神经和感觉神经支配。
淋巴结神经支配和神经调节
淋巴结的结构包括血管系统和淋巴管,它们穿透髓质实质,在 T 细胞区域中被复杂的去甲肾上腺素能纤维网络缠绕。相比之下,富含B细胞的生发中心缺乏神经支配。
在稳定状态下,去甲肾上腺素的释放依赖于昼夜节律的激活,进而通过β2-肾上腺素受体信号调节淋巴细胞的生理日常再循环。
通过使用各种技术,从整体免疫标记到逆行神经元追踪、单细胞基因组学和光遗传学,研究人员发现了支配淋巴结的独特感觉神经元阵列。将腺相关病毒注射到淋巴结后,四种类型的神经元被追溯到背根神经节。对这些不同的神经元群体进行的单细胞RNA测序确定了肽能伤害感受器的密集表达,形成了与大脑的双向通讯途径,并持续监测周围免疫环境。
脾神经支配和神经调节
脾脏是最大的次级淋巴器官,监测血液传播的物质和抗原。脾脏主要由去甲肾上腺素能脾神经支配,通常通过神经信号调节免疫功能。
脾神经从腹腔神经节分支,从脾门进入脾脏,沿着脾动脉外侧走行。去甲肾上腺素能神经分布穿过边缘区,伸入白髓,在白髓中,T细胞、B细胞和树突状细胞附近可以发现神经末梢。相反,红髓的神经支配似乎稀疏而分散。通过组织学和追踪的方法,在脾脏中没有发现直接的胆碱能神经支配。
白髓,位于脾脏内部,包含着一种特殊的白细胞,这些细胞聚集在血管周围,当血液流过脾脏的时候,白髓中的淋巴细胞辨认并吞噬掉任何侵入的细菌和病毒,以此方式过滤人体血液,防止机体被病菌感染。
红髓,动物体内最大的淋巴器官。位于左上腹胃的背面,胃与膈之间,呈内侧向内凹陷的扁椭圆形或条索状等。
一项使用完整全组织3D成像的研究提供了有关脾脏神经支配的额外信息。实质内交感神经支配的结构被揭示为圆锥状结构,这在其他免疫器官中是不存在的,这表明独特的神经调节功能发生在脾脏中。
在脾脏中发现了具有独特特征的神经胶质细胞,这又增加了复杂性。自主神经支配通常包含非髓鞘神经胶质细胞。虽然神经胶质细胞在由周围神经系统支配的内脏器官中的特定功能尚未得到充分研究,但它们在免疫器官中的存在可能在神经细胞和免疫细胞之间起着中介作用,这需要进一步研究。
使用逆行示踪剂和后来的跨神经元多突触PRV追踪的研究明确证明,脾脏神经支配完全是去甲肾上腺素能的,起源于腹腔神经节。
通过对脾脏注射PRV后较长时间点的分析,确定了脑干、桥脑和下丘脑的运动前脑核团。随后,光遗传学领域出现了一种追踪神经元回路的完全创新工具,它在功能上映射直接投射到腹腔神经节的DMV胆碱能神经元。
当DMV神经元被光激活时,会诱发脾神经放电,从而直接证明腹腔迷走神经和脾神经之间的解剖联系。
粘膜相关淋巴组织神经支配
身体内的粘膜,如呼吸道和胃肠道的粘膜,有分散的粘膜淋巴组织区域,这些区域共同构成了最广泛的淋巴组织,这些区域统称为粘膜相关淋巴组织,保护机体免受各种挑战。
虽然传统的次级淋巴器官是在胚胎发生过程中发育起来的,但淋巴滤泡,如支气管相关淋巴组织或肠道相关淋巴组织,在出生后会因炎症或感染而聚集。尽管如此,这些异位淋巴组织与传统淋巴组织在结构上有许多相似之处。
粘膜相关淋巴组织的一个典型特征是广泛的神经支配。早期研究描述了支气管相关淋巴组织和肠道相关淋巴组织的交感神经和肽能神经支配,这些淋巴组织含有大量神经肽,如P物质、血管活性肠肽和生长抑素。通常情况下,神经纤维沿着小血管排列,然后在与淋巴细胞接触的粘膜组织的实质中分支,在含有T细胞的区域,神经占优势。
随后的研究通过专门检测和解码各种有害外周刺激的伤害感受器,确定了粘膜相关淋巴组织神经支配的感觉通路。
支配肠道相关淋巴组织的伤害感受器感知胃肠道的扰动,并建立具有保护功能的神经反射。虽然肠道相关淋巴组织的感觉神经支配在抵御微生物方面的作用越来越明显,但对心血管疾病中肠道神经系统的影响仍不清楚。
支气管相关淋巴组织的神经支配作用研究较少,但交感神经、胆碱能神经和感觉神经纤维已被确定。
三级淋巴样器官是指在成年期由淋巴样新生在随机、典型的非淋巴样和非粘膜部位形成的淋巴样组织,以应对慢性炎症。这些组织在自身免疫性疾病、微生物感染、慢性同种异体移植排斥反应、癌症甚至动脉粥样硬化中都被观察到。
在几种转基因小鼠模型中诱导第三淋巴器官,可以表征炎症细胞因子和淋巴趋化因子的模式,这些细胞因子和趋化因子是其发育和调节所必需的。
虽然已经描述了三级淋巴器官的形态、细胞和血管成分,与第二淋巴器官(如B细胞和T细胞室的独特组织、含有滤泡树突状细胞的B细胞滤泡和生发中心)有相当大的相似性,他们在疾病进展中的参与是有争议的,并且仍然是研究的主题。
例如,在微生物感染期间,三级淋巴样器官会在局部保留病原体,从而阻碍它们进入生物体的其他部位。相反,自身免疫性疾病的进展可能因同时存在三级淋巴器官而加剧。通过选择性地去神经支配肠道交感神经或胆碱能神经,迷走神经在三级淋巴器官形成中的重要作用已在实验性结肠炎中得到证实。目前还尚不清楚ANS是否有助于其他器官中第三淋巴器官的发育、组织和功能。
神经免疫相互作用是对挑战体内平衡的应激源做出快速反应的基本适应机制。这一概念首次出现时,脾脏神经支配在细菌内毒素血症(对身体最危险的疾病之一)期间被观察到具有保护功能。
去甲肾上腺素能纤维和淋巴细胞之间的直接神经免疫相互作用被描述,同时确定在脾脏中引起去甲肾上腺素能放电的神经回路,该回路在抑制脂多糖诱导的细胞因子负荷和对抗感染性休克方面有效。
神经免疫相互作用已被确定为心血管危险因素和心血管疾病病理生理学的潜在机制。
神经免疫相互作用促进心血管危险因素的发生及进展
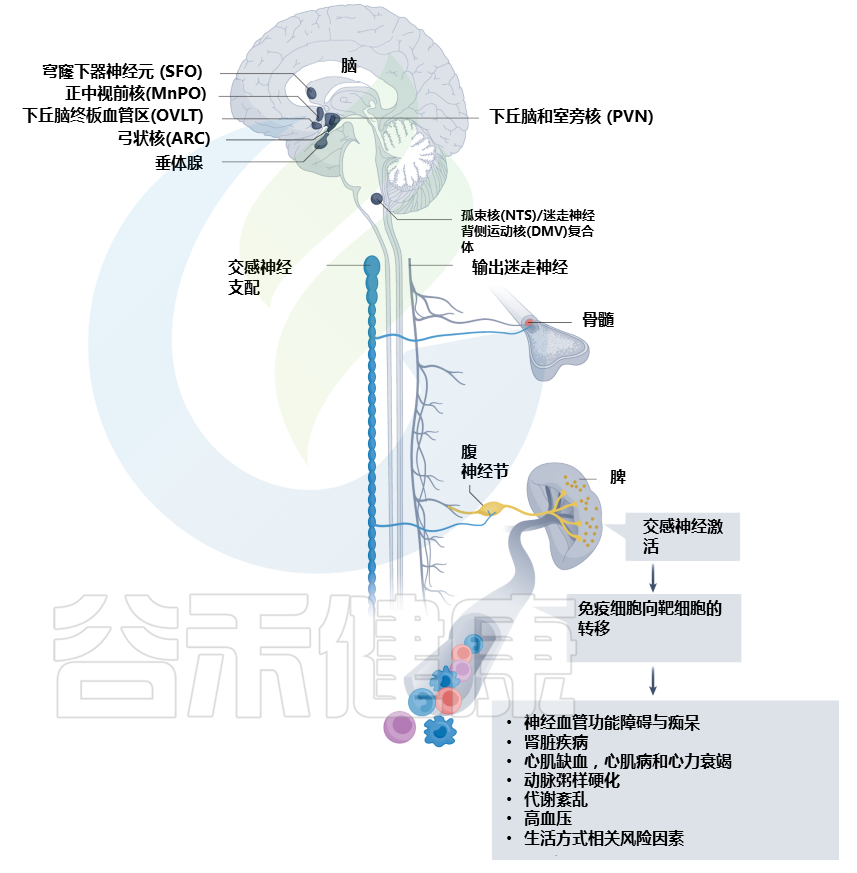
Carnevale D. Nat Rev Cardiol. 2022
大脑中的环室器官被心血管系统的挑战激活。通过一系列中枢和周围神经系统的解剖连接,大脑在免疫器官中建立神经反射来控制和调节免疫功能。心血管危险因素,如高血压、代谢紊乱和动脉粥样硬化,是常见的神经免疫机制改变的基础。心血管疾病,例如心肌缺血、压力过载心肌病、心力衰竭、肾脏疾病和神经血管功能障碍,其特征在于受影响的心血管组织中局部和免疫器官中的神经免疫改变。ARC,弓状核;DMV,迷走神经背运动核;MnPO,正中视前核;NTS,孤束核;OVLT, 终板的血管器官;PVN,下丘脑室旁核;SFO,穹窿下器官。
高血压
与高血压相关的炎症和免疫反应最早出现在20世纪70年代。然而,这些过程大多被认为是高血压导致靶器官损害的结果。
免疫系统在高血压中的机制作用的第一个证据,来自缺乏 T 细胞和 B 细胞且典型的高血压刺激不会增加血压的Rag1 -/-小鼠的研究。通过过继转移重建Rag1 -/-小鼠中的 B 细胞或 T 细胞池,这项研究表明,血管紧张素II或脱氧皮质酮醋酸盐(DOCA)仅在小鼠具有成熟 T 细胞时才会诱发高血压。
随后大量研究调查了特定的T细胞亚群是否对高血压的发展至关重要,发现血管紧张素II给药不会增加Cd8 -/-小鼠的血压,但会增加Cd4 -/-小鼠的血压。免疫系统在血压升高中所起作用的细胞和分子机制仍有待研究。
与血压稳态有关的基本生理变量,如血管张力和肾脏钠排泄,依赖于严格的神经控制。因此,神经调节系统、免疫器官和心血管功能之间建立的关系值得研究。
重要的研究揭示了大脑和免疫系统之间的联系可能对高血压至关重要。首先,在动物模型中,脑室内注射血管紧张素II可通过交感神经系统诱导外周细胞因子的释放。此外,选择性的脑室周围器官损伤阻碍了小鼠对血管紧张素II的典型血压升高反应。
有趣的是,脑室周围器官受损的小鼠无法激发T细胞并促进T细胞在血管系统中的浸润,这表明高血压患者的神经系统和免疫系统之间存在关系。
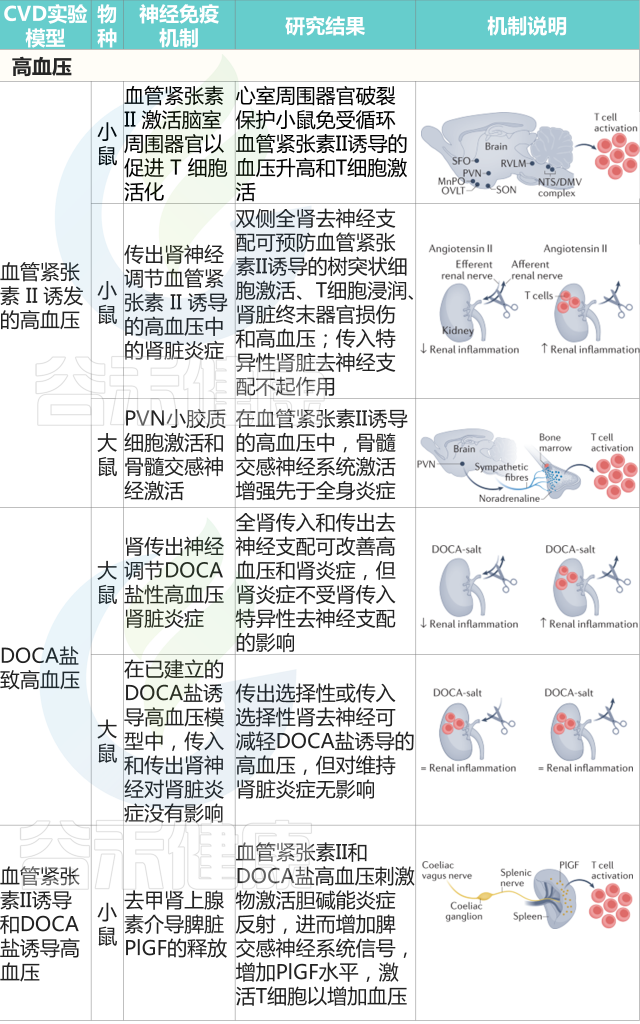

Carnevale D. Nat Rev Cardiol. 2022
高血压患者免疫系统的直接神经控制随后被证实。利用小鼠脾神经的显微神经学检查,血管紧张素II和DOCA盐均能增加神经放电,促进脾脏中去甲肾上腺素的释放。选择性脾脏去神经可防止血压升高以应对任何一种高血压刺激,脾切除术也重现了这一效应。
逆行追踪法,加上在测量脾神经放电时进行的选择性去神经手术,阐明了腹腔迷走神经输出是由高血压刺激激活的节前神经元。
在分子水平上,脾脏中的去甲肾上腺素释放是促进胎盘生长因子激活所必需的,胎盘生长因子是一种血管内皮生长因子家族的血管生成生长因子,也具有对血压升高至关重要的免疫调节功能。
高血压患者的神经免疫另一个相互作用的水平被称为双向脑-骨髓轴,即骨髓中交感神经流出增加先于全身炎症。
有关高血压患者肠道失调的证据正在迅速积累,来自小肠的激活免疫细胞已被证明与血压升高和大脑靶器官损伤有关。目前还不清楚是否存在相反的途径,即神经信号控制与高血压发病和进展相关的肠道和免疫机制。
动脉粥样硬化
脂质在动脉壁的积聚是动脉粥样硬化的一个典型特征,并伴随着免疫细胞的进行性浸润,导致斑块的形成。这一过程以慢性低度炎症为特征,逐渐增加动脉粥样硬化斑块的大小并导致动脉阻塞。
尽管有很多工作研究了导致斑块形成和决定斑块稳定性的机制,但神经免疫通讯的潜在作用才刚刚开始研究。
动脉粥样硬化斑块没有神经支配,但在斑块形成和进展过程中调节免疫反应的神经线索已被确定。Netrin 1首先被确定为指导轴突生长锥的神经信号,在人和小鼠动脉粥样硬化动脉的巨噬细胞中也发现了Netrin 1,它通过趋化因子驱动的迁移过程抑制巨噬细胞的排出。
巨噬细胞中的Ntn1缺失阻碍了小鼠的动脉粥样硬化过程,促进巨噬细胞从斑块中流出。
另一种蛋白质通常存在于神经元中,与胆碱能途径有关,可调节高胆固醇血症Ldlr–/–小鼠的动脉粥样硬化过程。在骨髓来源的细胞中,编码α7烟碱型乙酰胆碱受体(α7-nAChR)的Chrna7被切除会恶化小鼠动脉粥样硬化的进展。值得注意的是,人类动脉粥样硬化病变的特征是存在α7-nAChR+免疫细胞,表明该受体的通用相关性。
对受动脉粥样硬化影响的动脉周围三级淋巴器官的鉴定表明,神经机制可能与这些淋巴聚集相互作用,以控制和/或调节动脉粥样硬化疾病的进展。
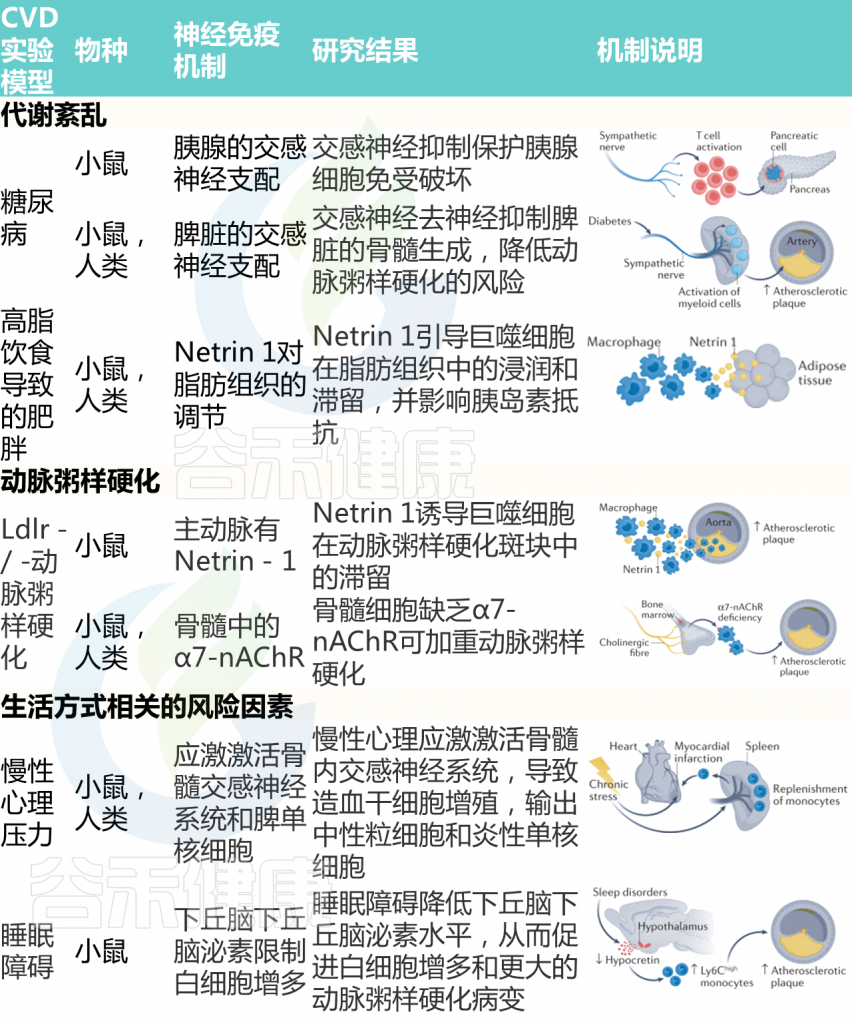

Carnevale D. Nat Rev Cardiol. 2022
代谢紊乱和肥胖
代谢综合征通常指可能单独或合并发生的一系列疾病,总体上增加了CVD的风险。除了血压升高,通常还包括高血糖和肥胖。
已知ANS失衡和免疫系统激活是代谢综合征的特征。在小鼠中发现了自身免疫性糖尿病的神经免疫机制。由CD8+T细胞介导的对胰腺β细胞的攻击诱导,糖尿病的发病取决于完整的胰腺神经支配的存在。
事实上,6-羟基多巴胺的化学消融或去甲肾上腺素能胰腺纤维的手术去神经支配阻碍了这些小鼠糖尿病的发病。在分子水平上,这种效应是由α1-肾上腺素能受体信号诱导的,因为使用哌唑嗪而不是普萘洛尔可以重现胰腺去神经支配的保护作用。
神经信号还可以控制与高脂饮食诱发的肥胖相关的糖尿病。患有肥胖症的小鼠和人类的脂肪组织被免疫细胞密集浸润,这些细胞导致脂肪组织炎症和胰岛素抵抗。
值得注意的是,脂肪组织中存在神经免疫指导线索netrin 1,这表明netrin 1可能调节巨噬细胞向脂肪组织的动员。此外,选择性缺失小鼠造血细胞中的Ntn1可有效促进巨噬细胞从脂肪组织中排出,减少炎症,并改善胰岛素敏感性。
这些发现确定了靶组织中的神经免疫相互作用,但免疫器官的神经控制也参与了疾病相关炎症状态的系统调节。例如,由脾交感神经驱动的神经通路已被确定为糖尿病的关键。通过手术或使用6-羟基多巴胺实现的选择性脾脏去神经支配,阻碍了糖尿病小鼠的过度脾脏骨髓生成。
一种连接大脑和脂肪组织的新型神经免疫途径已经被描述。在小鼠的脂肪间充质细胞附近发现了交感神经,交感神经控制着一个特定免疫细胞亚群的活动:2型固有淋巴细胞。
反过来,2型固有淋巴细胞通过释放神经营养因子来调节脂肪组织的稳态和肥胖。重要的是,通过在小鼠身上使用逆行追踪技术,结合外科手术和化学遗传学操作,定义了一个新的神经回路,通过交感主动脉-肾回路将脂肪组织中的2型固有淋巴细胞连接到高阶脑区,如室旁核。未来的研究应该调查这种新发现的神经免疫回路是否与肥胖和胰岛素抵抗的心血管并发症有关。
生活方式相关的危险因素
众所周知,生活方式相关的风险因素对CVD的发病率有着深远的影响,同时也对免疫系统构成挑战。此外,心理或身体上的应激状态与ANS的紊乱有关。对生活方式相关风险因素对心血管系统有害影响的潜在相关神经免疫相互作用的研究可以揭示创新的治疗机会。
正如在人类身上经常观察到的那样,慢性应激状态会增加小鼠的血压。值得注意的是,Rag1–/–小鼠对应激诱导的高血压具有抵抗力,并能减轻靶器官损伤。
除了血压升高,慢性应激还会增加动脉粥样硬化和心肌梗死的易感性。经过反复和各种应激性挑战的小鼠显示出造血干细胞增殖增加,导致产生高水平的促进疾病的炎性白细胞。这种效应是由骨髓交感神经纤维释放的去甲肾上腺素增加介导的,而去甲肾上腺素又反过来调节造血干细胞增殖、中性粒细胞和炎性单核细胞的排出。
睡眠障碍对心血管健康构成了重大挑战。小鼠正常睡眠节律的改变会增加动脉粥样硬化,与过度造血和促炎性单核细胞积聚有关。
在分子水平上,研究发现,睡眠碎片化可下调小鼠130的下视黄醇水平。下视黄醇是一种下丘脑神经激素,在控制睡眠、觉醒和觉醒方面具有重要功能。鉴于下视黄醇通过减少巨噬细胞集落刺激因子1的产生来限制骨髓生成,睡眠不良引起的下视黄醇水平降低与白细胞增多有关。
流行病学数据显示,健康的生活方式,如定期的体育活动,可以降低患CVD的风险。尽管许多观察分析都支持这种关联,但很少有机制研究调查这种有益关系的根本原因。有趣的是,习惯性自愿性跑步会降低小鼠的造血活动。在动脉粥样硬化小鼠中,运动抑制了慢性白细胞增多,但不影响紧急造血。通过降低脂肪-瘦素水平,这种效应促进造血生态位静止,改善心血管炎症和预后。
心肌缺血、心肌病和心力衰竭
ANS通过控制血管张力和各种心肌细胞特性,如收缩力、传导和频率,调节心脏功能。交感神经流出增加是慢性心力衰竭不良后果的最强预测因子之一。此外,非心肌细胞,尤其是常驻和非常驻免疫细胞,在应对各种挑战的心脏重塑中起着至关重要的作用。神经、免疫和心脏机制之间的相互作用值得研究。
急性缺血性心脏损伤通过增加骨髓中的交感神经信号与脾髓样细胞的生成增加有关。从脾脏部署的一部分单核细胞积聚在缺血心肌中,并参与心脏重塑。心-脾轴也被发现参与慢性心肌缺血的长期免疫反应,这总体上有助于不良的心脏重塑。脾脏的神经控制是否与这些表型有关仍有待阐明。
慢性高血压和肾功能衰竭会对心肌造成压力或容量过载,如果没有得到充分补偿,最终会导致心力衰竭。
在舒张功能不全的小鼠中,由于单核细胞募集和骨髓和脾脏造血增加,心脏巨噬细胞的数量增加。当巨噬细胞进入心肌时,会产生促纤维化细胞因子IL-10,进而促进胶原沉积和心肌僵硬,进一步加重舒张功能损害。
然而,其他巨噬细胞群体可以通过依赖于多器官相互作用的机制,促进慢性压力超负荷的适应性重塑。受到横向主动脉收缩以诱导心脏压力超负荷的小鼠增加了肾交感神经流出,由此去甲肾上腺素刺激粒细胞-巨噬细胞集落刺激因子的分泌,并对心脏巨噬细胞产生旁分泌作用。这项研究表明,心肌对慢性压力超负荷的适应取决于肾脏和心脏的神经和免疫反应之间的整合。
随后的研究阐明,心肌在稳定状态下含有大量不同的免疫细胞,对挑战的反应取决于常驻和招募的免疫细胞群体之间的整合。
鉴于ANS通过从颈上神经节、星状神经节和胸上神经节分支的纤维直接支配心肌,可以想象,参与心脏重塑的免疫反应的神经调节可能发生在心脏局部。
值得注意的是,尽管颈上神经节的去神经支配对心肌缺血引起的急性心脏重构没有影响,但从长远来看,这一过程减少了炎症浸润,减轻了心力衰竭。
肾脏疾病
肾钠处理、肾素分泌和肾血管张力受ANS的严格调节。肾传入和传出神经支配构成了最广为人知和研究最广泛的心血管反射系统之一。此外,炎症和免疫浸润通常伴随肾脏疾病。
急性肾损伤或慢性肾脏疾病均可导致肾功能衰竭,总的来说会增加心血管疾病的风险。促炎症环境和ANS平衡改变是肾病的特征,但神经系统和免疫系统之间的相互作用才刚刚开始澄清。
已经证实神经免疫调节在急性缺血再灌注反应中对肾损伤的重要作用。当用能引起胆碱能炎症反射的胆碱能激动剂进行预处理时,患有双侧肾缺血-再灌注或细菌内毒素血症的啮齿类动物对肾损伤的敏感性较低,这意味着神经反射调节由不同原因引起的肾损伤引起的炎症过程。
鉴于在类似的肾缺血再灌注损伤小鼠模型中,通过超声激活胆碱能炎症反射通过抑制炎症减轻了结构和功能损伤,该发现具有转化相关性。
2021发表的一项研究确定在小鼠急性肾损伤期间连接肾脏、大脑和脾脏的神经通路。通过光遗传学,迷走神经的传出或传入纤维被选择性地刺激,表明两者都对肾脏损伤有保护作用。通过激活传入的顺行感觉纤维,可以描绘出从肾脏追溯到延髓头端腹外侧的神经回路,以补充迷走神经-脾反射。
肾脏也是高血压损害的主要目标,这是心血管疾病不良后果的一个强有力的独立风险因素。浸润肾脏的活化免疫细胞和ANS失衡是高血压性慢性肾病的特征。
在动物模型中,肾脏去神经支配可有效对抗过度的肾交感神经流出和血压升高,并抑制T细胞聚集和由此引起的炎症反应、肾纤维化和蛋白尿。
在分析传入和传出肾神经支配的差异贡献时,在DOCA盐大鼠中,传入特异性肾去神经支配降低动脉血压和交感神经活动的程度与总(传入+传出)肾去神经支配的程度相同,但对血管紧张素II诱导的高血压没有影响。
有趣的是,在随后的一项研究中,同样的研究人员对已建立高血压和肾炎症的DOCA盐大鼠进行了传入特异性或全肾去神经支配。在这些动物中,虽然传入特异性和全肾去神经支配在降低血压方面仍然轻微有效,但两种治疗均未显着改变已确立的肾脏炎症。
总之,这些研究表明,肾神经(传入神经和传出神经)和炎症在高血压和肾脏炎症的发病机制中存在密切联系,但是,在确定高血压后,去肾神经支配不是抑制炎症过程的有效治疗,是通过其他机制维持的。
内脏器官炎症由ANS调节的观察可以追溯到之前研究肾传入和传出神经支配的作用。
一项初步研究表明,肾脏去神经支配可有效预防大鼠实验性肾小球肾炎,从而减少蛋白尿、系膜血管溶解、肾小球胶原沉积和转化生长因子-β的表达。这些数据表明,来自肾脏神经输入的信号分子可能在各种疾病环境下引发肾脏炎症和纤维化,进一步导致终末器官肾损伤。
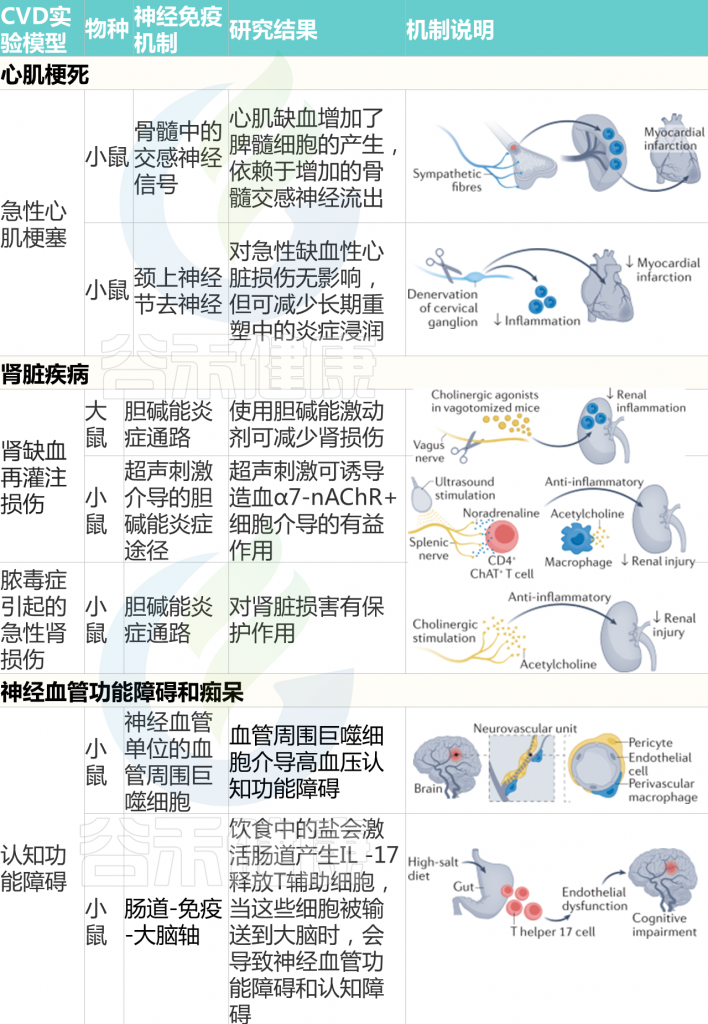

Carnevale D. Nat Rev Cardiol. 2022
神经血管功能障碍和痴呆
大脑由于没有能量储备,一直依赖于通过循环提供的营养,必须根据动态区域激活来适应其需求。因此,大脑对循环系统的改变特别敏感。
多种细胞类型构成脑实质和血管周围组织,包括免疫细胞。正如在其他器官和组织中观察到的那样,大脑中含有常驻免疫细胞(主要是小胶质细胞和血管周围巨噬细胞),当挑战干扰血脑屏障通透性时,这些细胞可以与招募的免疫细胞相互作用。
心血管风险因素会影响血脑屏障的完整性,改变脑血管内稳态,增加患痴呆症的风险。在小鼠和人类中,高血压会导致进行性脑血管损伤,并伴有典型的认知障碍症状。
免疫系统在高血压发病中的作用已得到明确证明,但免疫细胞如何参与高血压诱导的脑损伤才刚刚开始研究。
血管紧张素II诱导的高血压小鼠脑血管周围巨噬细胞的耗竭抵消了血管氧化应激和神经血管损伤,表明免疫的关键作用。
相反,在小鼠中,募集的免疫细胞会导致由血管危险因素(例如过度盐摄入)引起的脑损伤。脑血流、内皮功能和认知能力的损害取决于T淋巴细胞产生的IL-17,而IL-17是通过摄入肠道中的盐激活的。随后的一项研究还阐明了辅助性T淋巴细胞17对大脑有害影响的机制,表明肠道免疫轴对神经的调节非常关键。
外周神经系统的解剖结构和组织结构对轴突亚群的选择性和精确治疗提出了挑战,轴突亚群在特定器官中发挥独特的调节功能。因此,研究人员试图开发出越来越复杂的电极,以刺激更靠近目标组织的较小神经。这种方法有助于获得有关生理学和疾病中免疫神经调节的病理生理学基础的信息。
值得注意的是,靶向脾神经并直接测量其活性的技术的发展,使我们能够确定该免疫器官是神经系统和心血管系统之间串扰的中枢介质。相反,选择性去神经提供了有关该通路在CVD发病和进展中的相关性的机制信息。
研究表明,ANS调节免疫功能的功能障碍是心血管风险和CVD进展的重要组成部分。免疫器官自主神经外流的靶向调节是将这些发现转化为患者治疗的一种可能性。
值得注意的是,神经免疫通讯的机制研究被认为与一系列临床条件有关,如克罗恩病、类风湿性关节炎和原发性干燥综合征,所有这些都涉及免疫和炎症过程的失调。在临床前模型以及随后的炎症和自身免疫性疾病的人类临床试验中进行了探索,以非侵入性方式针对神经免疫机制的可能性也可能成为CVD的一种可能性。
对心血管疾病中调节免疫反应的神经通路的分子和电生理成分的临床前和临床研究为创新疗法提供了理论基础。能够对涉及心血管疾病的神经免疫反射进行精细调节的工具将有助于设计针对组织靶向免疫调节作用的策略,而不会增加感染风险或导致其他不良反应的普遍免疫抑制。根据特定疾病的特定背景和炎症环境,可以通过设计对腹腔迷走神经传出神经的生物电子刺激的选择性模式来微调脾脏的迷走交感神经激活。迄今为止,只有临床前工具已被开发并证明可有效调节免疫细胞从脾脏排出的过程。相反,通过手术切除腹腔神经节或热消融脾动脉周围的交感神经纤维,可以减弱脾交感神经流出的过度激活。
到目前为止,迷走神经刺激的研究主要集中在使用颈部植入装置,这些装置会触发传出和传入神经通路的混合,并产生潜在的不良影响。因此,尽管在自身免疫性疾病的临床试验中取得了有希望的结果,但迷走神经刺激方案具有引起脱靶刺激的局限性。
为了克服这一缺点,已经实施了改进的实验性迷走神经刺激方案,以选择性地刺激腹腔传出迷走神经并诱发脾神经流出。有趣的是,一系列研究提供了交感神经介导的脾神经控制的证据。特别是,通过腹腔神经节与脾神经相连的内脏神经已被证明可调节脾介导的炎症反应。具体作用是整合的还是单独作用的,取决于具体的病理生理学背景。
对腹腔迷走神经刺激后的脾脏免疫细胞的分析显示,特定的生物电子调节模式促进选择性T细胞亚型的排出,这表明可能会发展出靶向免疫调节。
使用活体和离体制剂对小鼠、大鼠、猪和人脾神经进行神经解剖学和功能比较,表明将临床前发现转化为临床相关工具的可行性。然而,尽管这种方法需要在实验模型中进行进一步研究,以揭示CVD中神经免疫通讯的病理生理学基础,但临床应用可能会受到该过程侵入性的限制。
肠道微生物群决定下丘脑-垂体系统的激活水平。特别是,肠道微生物群是心血管疾病发病机制中神经免疫介质的重要来源。
心肌缺血、心肌病和心力衰竭
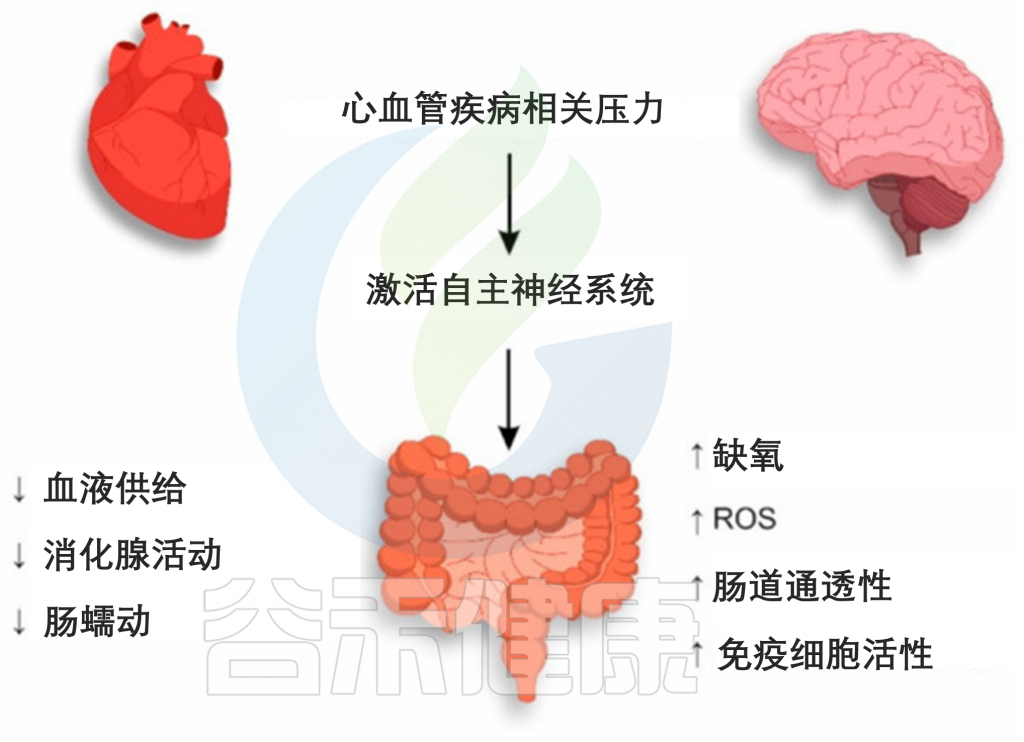
与 CVD 相关的压力通过激活 ANS 的交感神经分裂来影响整个生物体,包括胃肠道。在 ANS 的影响下,肠道内微生物群的血液供应减少,从而降低了消化腺的活动,胃肠道的肠道蠕动减慢。上述机制决定了由于 CVD 相关应激导致的肠上皮细胞的进一步紊乱。
CVD相关应激期间肠道上皮损伤的机制

Suslov, Andrey V,, et al. J Clin Med. 2021
肠壁由肾上腺素能交感神经纤维支配,在刺激期间增加水和钠的吸收,伴随着肠道通透性的增加。同时,在大肠迷走神经的影响下,肠上皮杯状细胞产生的粘液减少。
值得注意的是,一方面,粘液为肠道上皮细胞提供保护,使其免受共生体及其代谢产物的影响,另一方面,粘液阻止免疫细胞的过早激活。因此,粘液层的减少和肠壁通透性的增加可导致肠道细菌的紊乱和肠上皮细胞的空间分离。
在Wistar大鼠中显示,出生后早期有限的筑巢压力会导致高皮质类固醇激素血症,增加肠道通透性,减少粪便微生物多样性,导致肠道微生物群组成失衡。肠道血供减少不仅是由于ANS交感分裂的影响,也是由于CVD的致病影响。
几项研究表明,肠道供血衰竭伴随着多种类型的CVD:心肌梗死、严重动脉粥样硬化、慢性心力衰竭、糖尿病和肥胖。因此,CVD期间肠道内的血供衰竭是由多种机制同时决定的。
肠血供减少伴有组织缺氧,而肠粘膜对缺氧最为敏感。
肠粘膜是一种支持粘液层以及微生物群与上皮下组织空间分离的解剖结构。在缺氧期间,有氧和无氧分解代谢循环中的葡萄糖转化会在中间阶段损害能量的生物合成。这导致活性氧(ROS)的释放。
由于活化免疫细胞的积累和 ROS 的产生,再灌注会增加缺血性损伤的破坏性影响。活性氧对蛋白质、脂质、碳水化合物和核酸具有高反应性,导致肠上皮完整性受损。至于肠道菌群与缺血性肠道损伤之间的关系,在大鼠模型中显示,肠道缺血-再灌注损伤导致肠道菌群发生显著变化,大肠杆菌和口腔普氏杆菌数量增加,随后在愈合阶段乳酸杆菌数量增加。
同时,在急性心肌梗死大鼠模型中证明,肠道微生物群的改变会导致肠道炎症和细胞凋亡的发展,也就是说,肠道缺血不仅会导致肠道微生物群失衡,反之亦然,肠道微生物群的变化会导致肠道损伤。
除粘液层外,肠上皮层在提供肠屏障功能方面也起着重要作用。肠上皮层由与紧密连接蛋白连接的上皮细胞组成,特别是紧密连接蛋白、封闭蛋白、钙粘蛋白和粘附分子。
紧密连接蛋白作为肠-脑轴结构中肠屏障的重要元素。研究表明,脑肠肽ghrelin可以减轻动物模型脑出血后激活紧密连接蛋白 zonula occludens-1 和 claudin-5 的肠道屏障功能障碍。
一些研究通过改变紧密连接蛋白证明了肠道微生物组变化与肠道屏障损伤的关系。例如,植物乳杆菌增强上皮屏障刺激基因的表达,这些基因参与紧密连接zonula occludens-1、zonula occludens-2 和 occludin 的信号通路。
在小鼠模型的另一项研究中也证明了相同的效果,其中用乳酸杆菌、双歧杆菌和链球菌的混合物治疗增加了紧密连接 zonula occludens-1 和紧密蛋白的表达。紧密连接完整性的改变可导致与代谢宿主状态受损相关的细菌或细菌代谢物的流入增加,表现为心脏代谢疾病。
肠上皮和粘液屏障位于肠道环境、肠道细菌和免疫系统之间。
众所周知,肠上皮层包括不同类型的细胞:
肠细胞
杯状细胞
肠内分泌细胞
潘氏细胞
簇状细胞
M细胞
以及多种专业免疫细胞,如
淋巴细胞
树突状细胞
巨噬细胞
均位于肠粘膜表面附近
上皮内淋巴细胞是第一个对致病因素做出反应的免疫细胞,它侵入上皮并传播树突以检测肠腔抗原。
其他细胞位于有组织的淋巴结构中,如派尔斑和隐斑,或分散在固有层内。
与巨噬细胞和树突状细胞等专业免疫细胞类似,肠上皮细胞表达先天免疫受体,如模式识别受体,包括 Toll 样受体 (TLR) 和核苷酸结合蛋白,含有寡聚化结构域 (NOD)。
潘氏细胞合成抗菌分子受 TLR4/MyD88 和 NOD2 信号传递的调节,这些信号传递受肠道微生物的控制。
TLR 通过激活促炎信号通路以响应微生物抗原,在先天免疫系统中发挥着重要作用。
肠道免疫细胞通过细胞因子或直接的细胞连接支持肠道黏膜的屏障功能。因此,由 Th17 细胞或 3 型先天性淋巴细胞 (ILC3) 产生的 IL-17 和 IL-22 会增加肠上皮细胞分泌的 AMP 和 Reg3 家族蛋白 。
此外,上皮内淋巴细胞产生的 IL-6 可增强肠上皮细胞增殖并促进损伤后黏膜的修复。然而,其他促炎细胞因子,如 TNF-α 和 IFN-γ,通过抑制 β-连环蛋白/T 细胞因子 (TCF) 信号传递来抑制上皮细胞增殖 。
肠上皮细胞还通过分泌细胞因子和趋化因子来调节宿主免疫反应。
在用革兰氏阴性细菌大肠杆菌和变形杆菌的鞭毛蛋白刺激肠内皮期间,TLR5 / MyD88 信号促进 IL-8 的产生,IL-8 将中性粒细胞募集到固有层中。
前面CVD中提到的胆囊收缩素、胰高血糖素样肽 (GLP) 和血清素由肠道内分泌细胞分泌,影响肠道免疫系统的活动。
胆囊收缩素通过 CD4+ 细胞和 B 细胞调节细胞因子的分化和产生。值得注意的是,交感神经系统调节的消化腺活性的降低间接影响免疫细胞的活性。
有趣的是,微生物群对上皮肠屏障的影响不仅取决于免疫成分,还取决于其他影响。特别是,由肠道微生物群合成的短链脂肪酸被用作上皮细胞的能量来源,并间接增强上皮屏障。微生物代谢产物吲哚通过激活孕烷-X 受体具有防御屏障作用,并增加胰高血糖素样肽-1 的分泌。
无法保存肠上皮的复杂解剖和功能特征会降低上皮屏障的抗菌、免疫调节和再生能力。粘膜的破坏导致共生细菌及其代谢物从肠腔转移到上皮下组织,导致促炎细胞因子的分泌。反过来,这会导致器官功能障碍,并伴有肠粘膜炎症。
现在越来越多的证据表明,肠道细菌的代谢物在炎症过程中通过被破坏的肠道屏障进入循环。
微生物组介导疾病的三个因素:
首先,肠道细菌的代谢物是慢性免疫反应的永久激活剂,会在肠道以及整个生物体中引起持续性炎症。
其次,先天免疫系统成熟期肠道微生态失调导致免疫耐受性受损,随后表现为自身免疫和自身炎症性疾病。
第三,微生物组可以影响控制肠道远处组织特异性免疫的免疫因素。
考虑到肠道微生物群在神经免疫网络形成中的作用。脑源性神经营养因子 (BDNF) 是一种应激蛋白,是神经营养因子家族的成员,可增加大脑中神经元对功能障碍的抵抗力,并提供神经系统的可塑性。
BDNF 控制了广泛的过程,包括微生物群-肠-脑轴参与心脏代谢疾病的发病机制。研究表明,BDNF 信号可能介导间歇性禁食对血糖调节和心血管功能的影响 。此外,研究表明,用高剂量益生菌治疗可以调节斑马鱼的行为,导致一些大脑相关基因的表达发生显着变化,例如 BDNF。因此,BDNF 可能代表了微生物-肠-脑轴的分子机制。
神经免疫轴:微生物群-肠-脑-CVD
肠道粘液膜的缺氧损伤、微生物群转移到上皮下组织、肠上皮屏障功能的破坏、肠道细菌代谢产物和炎症细胞因子的合成使肠道成为最大的内毒素源。炎症介质通过全身血液和淋巴循环到达神经系统中心。
血脑屏障
血脑屏障 (BBB) 在妊娠期间形成,充当大脑和血液循环系统之间的选择性过滤器。肠道微生物群和微生物代谢物在血脑屏障形成中的重要性已在不可知菌小鼠身上得到证实。在没有肠道微生物的情况下,与正常动物的血脑屏障相比,小鼠的血脑屏障变得具有渗透性。
研究发现,大脑的淋巴系统流入脑脊液,进入蛛网膜下腔,并进一步进入颈深淋巴结。脂质的溶解度、蛋白质的三级结构、浓度、分子质量和化合物的电荷决定了介质从外周血供应和淋巴系统到大脑的通道。
外周血中的细胞因子主要是亲水性的,可以调节神经系统的免疫功能。研究还表明,静脉注射吲哚(类似于色氨酸的细菌代谢产物)可以克服BBB。
LPS(脂多糖)的神经炎症效应通过外周组织中的TLR激活发挥作用,通过血脑屏障阳性的促炎细胞因子在神经系统中引起继发效应。
血脑屏障和淋巴血管系统被认为是信号进入大脑的入口。例如,循环免疫细胞和炎症介质(包括宿主和细菌的激素和神经递质)以及迷走神经刺激代表了有助于直接或间接微生物信号从肠道传输到大脑的机制 。
炎性细胞因子也是激活中枢神经系统的一个重要因素,作为对各种刺激的反应,包括在肠道病理过程中激活下丘脑-垂体-肾上腺轴的促炎性细胞因子。
肠易激综合征患者的皮质醇和促炎细胞因子白细胞介素IL-6和IL-8显著升高。IL-1α细胞因子在中枢神经系统水平上刺激机体的整个葡萄糖代谢;IL-6、IL-1、TNF-α和IFN细胞因子相互独立地刺激下丘脑-垂体-肾上腺轴(HPA轴)。
除了炎性细胞因子外,炎症期间环氧合酶系统合成的前列腺素也参与HPA轴的激活。多项研究发现炎性细胞因子(TNF-α、IL-1和IL-6)在HPA轴激活中的作用。任何炎性细胞因子的注射都会刺激HPA轴,并导致循环皮质酮水平升高。值得注意的是,在LPS穿透后,任何细胞因子的阻断都不会阻断HPA轴的激活,也就是说,如果肠上皮屏障功能停止,LPS进入血液,那么细胞因子激活HPA轴的复制效应就会实现。那么接下来就是神经免疫性疾病和靶器官损伤了。
因此,所有炎症介质都会促进HPA轴的激活,而阻断任何一种细胞因子都不能减少HPA轴的刺激,因为它们之间存在重复效应。
因此,下丘脑-垂体-肾上腺轴的激活是大脑介导的对疾病的基本反应之一。HPA 轴被认为是神经内分泌系统的基础,它在心理和生理压力(包括感染)的影响下调节机体的稳态,促进对压力的充分反应。
所考虑的机制在慢性应激中非常重要。由于情绪唤醒的阈值不足以在CVD期间形成压力,因此神经系统中形成全值压力反应,随后通过肠内炎症介质持续激活HPA,激活ANS的交感分裂。
值得注意的是,机体的整个复杂病理变化是通过急性应激途径发展起来的,而情绪成分(情绪刺激)与慢性应激阈值相对应或完全缺失。这个问题需要进一步研究。因此,综述的机制对神经系统中心(包括ANS中心)有激活作用,ANS中心反过来又支配内脏器官,包括微生物群居住的肠道。
结合有关肠道微生物群的机制及其与神经系统通过肠-脑轴发育紊乱的关系,可以初步得出结论,在CVD期间,来自肠道的介质通过血流和淋巴进入大脑,并激活下丘脑核团。然后,只要下丘脑是ANS的节段上整体中心,ANS的交感神经分裂就会被激活。
因此,来自肠道的介质到达ANS的节段上中心,并激活交感和副交感分裂的工作,从而关闭肠道微生物群参与CVD发病机制的病理循环。许多发表的研究报告表明,微生物群介导的炎症介质的增加会加重CVD的病程和预后。
研究还发现,恢复CVD患者的肠道菌群可以改善疾病的预后。使用增加阿克曼菌属、双歧杆菌、乳酸杆菌、拟杆菌和普氏杆菌的细菌数量的复合治疗制剂可改善CVD的病程。
众所周知,双歧杆菌和乳酸杆菌属的细菌对肠壁具有局部抗炎作用。肠上皮屏障功能的恢复是因为肠壁炎症的减少,这意味着炎症介质在体循环中的水平降低,因此它们对神经系统的激活作用降低。
尤其是,高血压与肠道微生物群紊乱和肠脑轴失调有关。在高血压大鼠模型中证明,长期开菲尔治疗可降低IL-6和TNF-α蛋白密度,并消除在下丘脑室旁核和延髓头端腹外侧区观察到的小胶质细胞激活,保护心脏调节核免受肠道介导炎症的影响,从而提供开菲尔的降压作用。在小鼠缺血性中风或脑缺血模型中进行的一些研究表明,缺血性中风脑损伤通过增加促炎反应和细胞因子、趋化因子和免疫细胞浸润大脑结构,促进肠道失调的发展,这与不良预后有关。
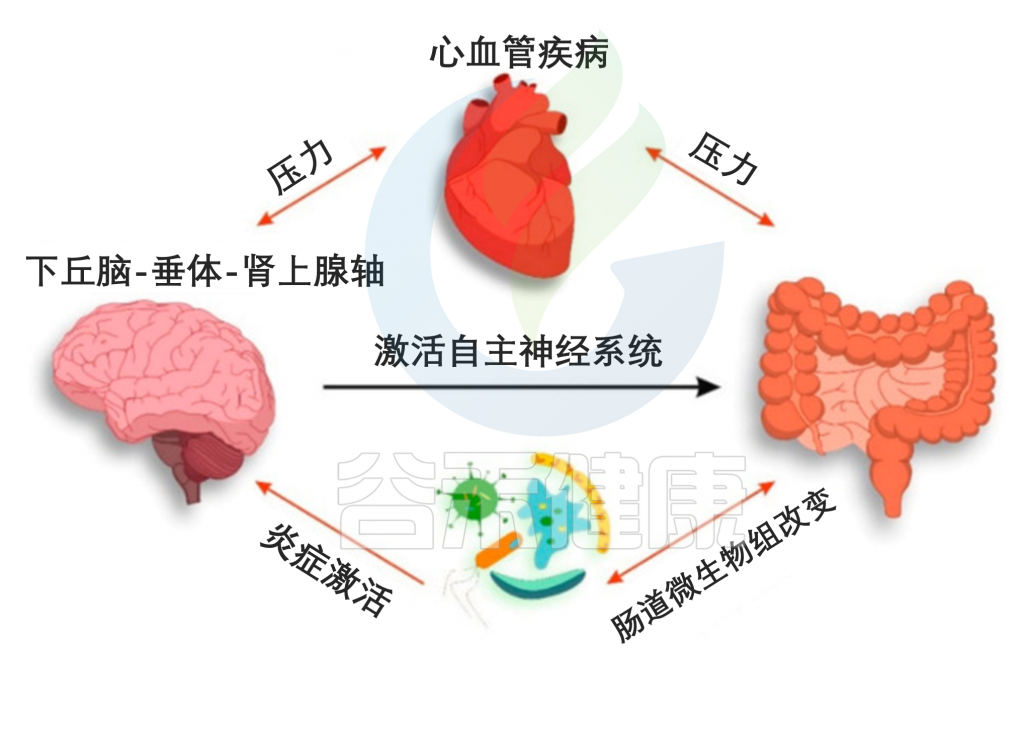
CVD患者肠道菌群与神经系统的相互作用

Suslov, Andrey V,, et al. J Clin Med. 2021
肠道微生物群参与了 CVD 的发病机制并决定了 HPA 轴的炎症激活。
一些研究调查了微生物组靶向制剂可改善 CVD 病程,减少动脉粥样硬化的进展和主要 CVD 并发症的风险 。
在这里,我们可以假设基于微生物组治疗的有益心脏保护机制是由于其对微生物组-肠道-脑轴的影响。
通过阻断左前冠状动脉诱发心肌梗死的大鼠中显示,与安慰剂组相比,使用基于瑞士乳杆菌和长双歧杆菌组合的益生菌可降低与心肌梗死相关的不同脑区的凋亡倾向。
另一项针对小鼠的研究表明,在实验性中风后,抗生素调节肠道微生物群可降低缺血脑内的LPS水平和神经炎症。一项针对冠心病患者的研究发现,益生菌鼠李糖乳杆菌与益生元菊糖复合物对抑郁、焦虑和炎症生物标志物具有有益作用。
建议所有成年人每周至少进行150-300分钟的中等强度或75-150分钟的高强度有氧运动,或两者的同等组合。当然要视身体状况而定,如果自身基础不太好,在能力和条件允许的情况下尽可能保持一些低强度活动。
减少久坐时间,适当进行轻度体力活动是有益的。
饮食对人类健康的多个方面都有重大影响,不健康的饮食模式(例如高脂肪的西式饮食)与动脉粥样硬化、代谢综合征和肥胖症等一系列慢性疾病的风险增加有关。免疫系统正在成为这种关系的关键中介,通过食物诱导调节与慢性炎症相关的促炎/抗炎因子以及增加/减少各种病理结果的风险。
支持这一观点的大型流行病学研究表明,以高摄入饱和脂肪和低纤维为特征的饮食模式与促炎生物标志物水平升高有关,例如 C 反应蛋白 (CRP) 和白细胞介素 IL- 6。相反,摄入大量水果和蔬菜和/或经常食用鱼类的饮食模式与较高的脂联素血清浓度相关,脂联素具有抗炎特性。
这些观察性研究得到了干预试验的进一步支持,干预试验表明饮食可能会影响血清炎症生物标志物谱。例如,高胆固醇食物的饮食干预增加了对胰岛素敏感的参与者的 CRP 和血清淀粉样蛋白 A 浓度。
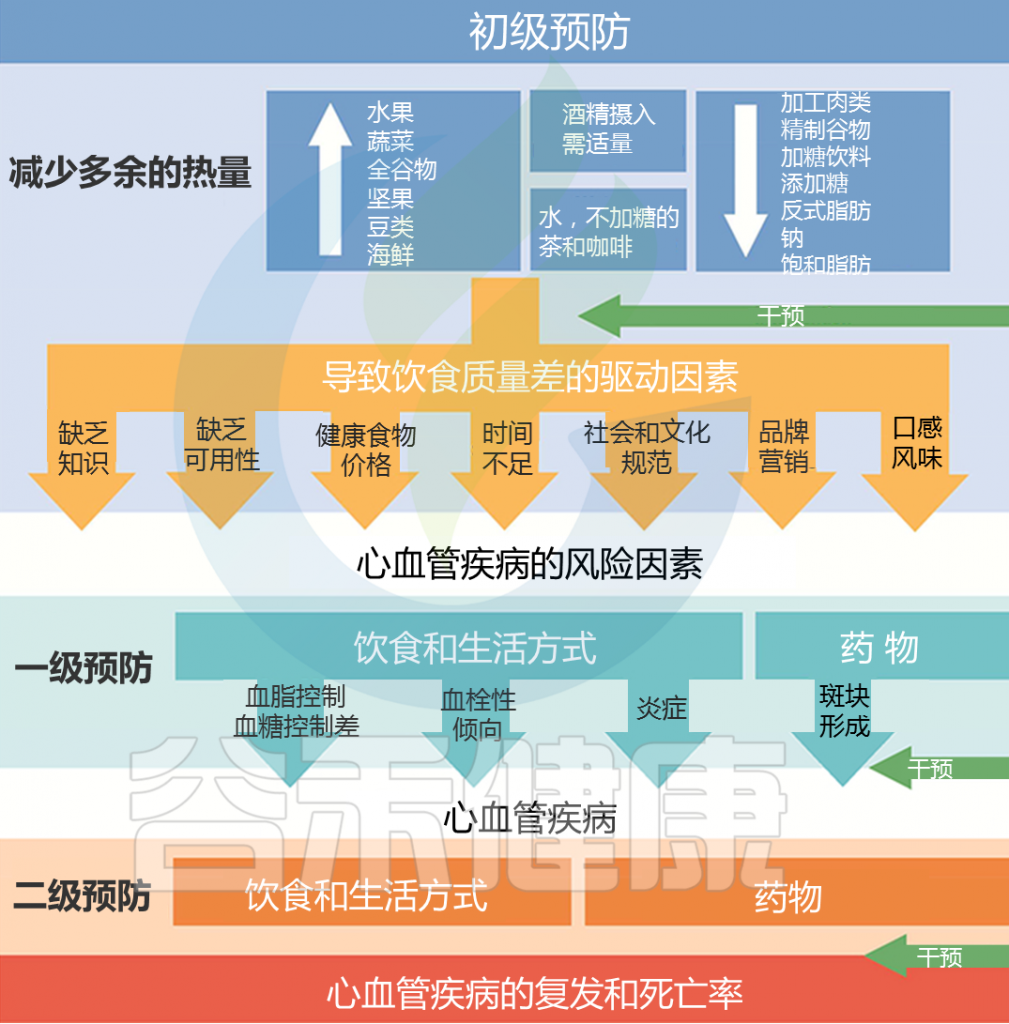

Yu E, et al.,J Am Coll Cardiol. 2018
健康的饮食可以降低心血管疾病和其他慢性疾病的风险。从更多荤食(以动物为基础的)饮食模式转变为素食(以植物为基础的)饮食模式,可能会减少心血管疾病。
建议饮食中多吃水果、蔬菜、坚果等;少量食用低脂乳制品和海鲜;而且尽可能少摄入加工肉类、含糖饮料、精制谷物、盐等。
戒烟可迅速降低心血管疾病风险,是预防动脉粥样硬化性心血管疾病最具成本效益的策略。
建议限制饮酒或戒酒,每周最多饮酒100g。
通过改变生活方式来达到和保持健康体重,对这些指标可产生有利影响(如血压、血脂、血糖等),并降低CVD风险。
当饮食和体力活动改变以及其他常规的非侵入性干预措施效果不佳时,应考虑对高危人群行减重手术;也可以考虑使用具有心血管保护作用的抗肥胖药物。
新指南提出心理压力与动脉粥样硬化性心血管疾病风险相关,需要加强对心理障碍患者的关注和支持,对其进行生活方式和药物干预,方式包括呼吸练习、冥想、写日记、适当锻炼、与大自然接触、与他人建立联系等,尽可能改善压力症状和生活质量,可改善心血管疾病。
通过对血压,血糖,血脂等指标的日常监测来了解健康状况,也可以通过肠道菌群健康检测等方式来了解慢病风险,阻断这类慢病的进程,预防控制代谢紊乱,从根本上预防心血管疾病的发生。
本文主要基于研究阐述免疫、炎症的神经调节以及肠道菌群如何参与 CVD 的发病和进展。
在CVD的初始阶段,肠道微生物群在其发病机制中的作用是次要的,这意味着细菌的定性和定量变化不像在随后的阶段那么重要。
然而,后来,当肠道微生物群决定了下丘脑-垂体-肾上腺轴的炎症激活水平时,肠道微生物群的变化对CVD的发展具有重要意义。
在CVD进展过程中,肠道细菌与肠壁的病理过程密切相关,成为CVD发病机制中的关键因素之一。在这方面,试图确定与CVD进展过程最相关的肠道细菌,可能是开发CVD诊断、预防和治疗新相关方法的重要一步。
此外,注意通过饮食衍生的微生物代谢物、炎症反应转变、校准神经免疫从而影响CVD干预和治疗反应。
·
具体基于肠道菌群的饮食调节,以及CVD 进展中的饮食-微生物群串扰的机制,菌群代谢产物的作用等详见本次推文的第二篇:
《 饮食-肠道微生物群对心血管疾病的相互作用 》主要参考文献:
Carnevale D. Neuroimmune axis of cardiovascular control: mechanisms and therapeutic implications. Nat Rev Cardiol. 2022 Mar 17. doi: 10.1038/s41569-022-00678-w. Epub ahead of print. PMID: 35301456.
Yu E, Malik VS, Hu FB. Cardiovascular Disease Prevention by Diet Modification: JACC Health Promotion Series. J Am Coll Cardiol. 2018;72(8):914-926. doi:10.1016/j.jacc.2018.02.085
Suslov, Andrey V et al. “The Neuroimmune Role of Intestinal Microbiota in the Pathogenesis of Cardiovascular Disease.” Journal of clinical medicine vol. 10,9 1995. 6 May. 2021, doi:10.3390/jcm10091995
Thaiss CA, Zmora N, Levy M, Elinav E. The microbiome and innate immunity. Nature. 2016 Jul 7;535(7610):65-74. doi: 10.1038/nature18847. PMID: 27383981.
Huh JR, Veiga-Fernandes H. Neuroimmune circuits in inter-organ communication. Nat Rev Immunol. 2020 Apr;20(4):217-228. doi: 10.1038/s41577-019-0247-z. Epub 2019 Dec 17. PMID: 31848462.
Frank L J Visseren, François Mach, Bryan Williams,et al., ESC Scientific Document Group, 2021 ESC Guidelines on cardiovascular disease prevention in clinical practice: Developed by the Task Force for cardiovascular disease prevention in clinical practice with representatives of the European Society of Cardiology and 12 medical societies With the special contribution of the European Association of Preventive Cardiology (EAPC), European Heart Journal, Volume 42, Issue 34, 7 September 2021, Pages 3227–3337

谷禾健康

铁 (Iron)作为人体不可或缺的元素之一,在氧气运输,新陈代谢和免疫防御中起着基本作用。铁元素的良好调控是人体健康的保障,过多过少都会对人体产生不利影响。铁稳态的失调与各种疾病的发生和发展息息相关:铁缺乏会导致宿主发育迟缓,免疫低下,而铁过载更易引发炎性反应和代谢问题, 还可能与癌症的发生发展密切相关。
在人类中,小肠作为宿主体内铁的主要吸收场所,大约每天吸收2-3mg铁,但是在一些病理条件下,小肠并不能完全将食物中的铁吸收,而相当一部分铁进入结肠中与肠道菌群发生密切的交互作用,并影响肠道菌群的“生态系统”,从而进一步调节宿主的健康和代谢。
自法国国家农业研究院与法国国家健康与医学研究院(INSERM)的研究人员首次发现肠道菌群如何影响肠道内铁元素的转运与储备成果后,多项研究表明,铁失衡会导致肠道菌群的改变,进而改变微生物多样性,增加病原体丰度并诱导肠道炎症的发生发展。
谷禾在多年的肠道菌群研究和检测实践中,也发现饮食中的铁水平是导致肠道菌群改变的重要因素。我们基于机器学习算法,建立了预测模型,可以预测评估膳食摄入和铁的菌群代谢的总体水平,这有助于避免缺铁和铁过量引起的肠道菌群失调及其可能导致的宿主健康损害和疾病风险。
铁和微生物组之间相互作用
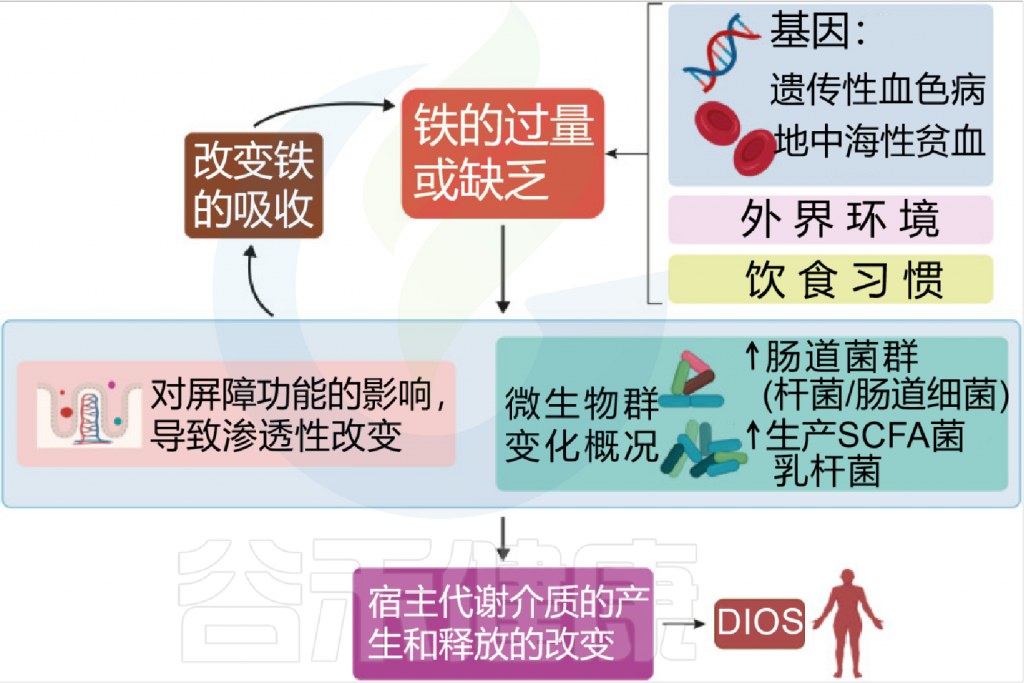

Botta A, et al., J Lipid Atheroscler. 2021
铁是人类必需的营养素,在环境中含量非常丰富,并参与了许多生物过程,如氢气的产生、呼吸和DNA 生物合成。它还在宿主细胞内的许多代谢途径中起到辅助因子的作用。
在人类中,由于没有排泄铁的途径,小肠上皮细胞对铁的吸收是一个非常严格的调节过程。
吸收效率取决于饮食中铁的潜在可用性,并受生理铁需求的调节,包括体内铁储存,铁调素在控制吸收中起核心作用。
膳食铁大致分为两种类型,非血红素铁和血红素铁。两种形式的膳食铁都有单独的肠细胞吸收途径:


这里主要关注的是非血红素铁(口服铁通常以非血红素铁的形式给予)。
肠上皮细胞对非血红素铁的吸收
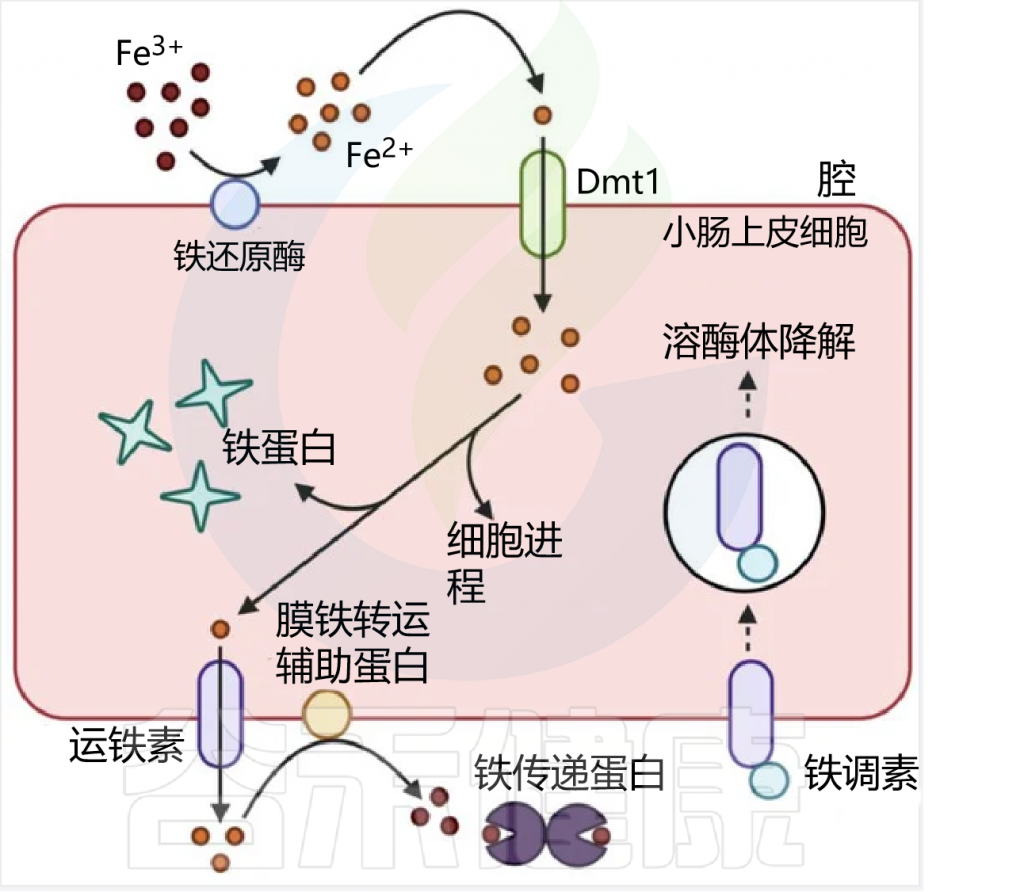

日常生活中,缺铁的常见症状包括:
一般我们常见的缺铁,主要是以下几个原因:
这很好理解。我们的身体不能制造铁,需要从食物中获取。如果你每天摄入的铁量没有达到身体需要的量,就会出现缺铁。
快速生长会增加铁需求,因此儿童、孕妇和哺乳期女性更可能缺铁。此外,进行耐力锻炼的人更容易患低铁症。
出血和失血会增加铁的流失,包括:月经出血、分娩、溃疡、痔疮、因受伤或手术而出血、献血等。长期使用消炎药(布洛芬、萘普生、双氯芬酸)会增加肠道出血的可能性。
需要注意的是,缺铁性贫血的一个常见且常被忽视的原因是月经过多。随着时间的推移,这种缓慢的血液流失通常会导致铁流失过多。
在慢性炎症性疾病中也会出现缺铁,例如自身免疫性疾病、慢性感染、慢性肾病或癌症。这被称为慢性病性贫血。
因为铁对病原体和癌细胞的生长很重要,所以当发生感染或炎症时,身体会试图通过锁定铁来抑制病原体或恶性细胞的生长。
受感染或炎症影响的组织会释放降低铁血水平的细胞因子,从而导致贫血的发展。
消化系统的疾病会降低铁的吸收,包括:
乳糜泻、炎症性肠病、胃炎、幽门螺杆菌感染、小肠细菌生长过度等,此外,减肥手术也会减少营养吸收,包括铁。
铁吸收不足的其他原因包括大量摄入抑制铁吸收的食物或药物,包括:植酸盐(全谷物、豆类)、多酚(茶、咖啡、葡萄酒)、抗酸药、H2受体阻滞剂、四环素或消胆胺等药物等。还有一个很重要的我们可能会忽略的环节,就是菌群。
细胞铁浓度是感染性的关键决定因素之一。肠道病原体在宿主细胞中的存活可能部分取决于宿主铁的状态。铁也可以促进肠道病原体的复制和毒力,例如沙门氏菌属、志贺氏菌属和弯曲杆菌属。
利用铁载体获取铁的一些细菌还包括如:
大肠杆菌、铜绿假单胞菌、肺炎克雷伯菌、金黄色葡萄球菌和结核分枝杆菌。
这些病原菌的定植会与宿主进行铁的竞争吸收,同时诱发肠道炎症,改变肠腔环境,影响菌群构成,进一步导致缺铁加剧。


大多数细菌都依赖于铁的存在来进行呼吸和各种代谢过程。在细菌内部,铁在生长和增殖中起着至关重要的作用,例如,某些细菌蛋白质和酶的正常功能需要铁。此外,铁还可以调节某些毒力因子的表达。
铁浓度的波动会产生病理影响,对肠道微生物群组成产生负面影响。铁的波动有两种情况,过多或者缺乏,接下来我们逐一来看铁过量和缺乏会对菌群造成什么影响。
宿主铁稳态的改变可能会影响肠道的管腔铁含量,从而影响肠道菌群的组成。在无菌小鼠中,铁转运蛋白表达减少两倍,细胞铁含量较低,在移植肠道细菌定植后,上皮细胞利于铁的能力增加,细胞内铁含量增加。
铁过量
肠道中富含铁的环境有利于变形菌。对儿童的研究表明,过量的铁会导致炎症和病原菌的生长。这些病原菌可能会诱发炎症性肠病或结直肠癌。铁的强化增加了粪便钙卫蛋白的水平,显示了肠道的炎症。
患有铁过载综合征(包括血色素沉着症和难治性贫血)的人更容易受到细菌感染,包括:
耶尔森菌属Yersinia
单核细胞增生李斯特菌Listeria monocytogenes
创伤弧菌Vibrio vulnificus
膳食铁过量摄入可影响大鼠正常的生长发育,并引起小肠粘膜炎性损伤。过量铁摄入可引起大鼠肠道菌群失调,肠道菌群丰度有所降低,其中乳酸杆菌、双歧杆菌降低,血清中肿瘤坏死因子和内毒素水平升高可能与肠道菌群紊乱有关。
铁缺乏
当铁水平下降时,也会对肠道微生物群组成产生影响,诱发肠道感染。缺铁会抑制细菌细胞繁殖过程,从而损害细菌生长。
在啮齿类动物模型中,缺铁导致微生物群组成的显著重组,微生物多样性降低。
在铁含量非常低的条件下(0.9 mg Fe/L),Roseburia,肠杆菌减少,丁酸盐水平也降低,而Lactobacillus增加。此外,低铁条件下生长的Roseburia gutis优先产生乳酸而不是丁酸盐。
图 铁和炎症之间相互作用
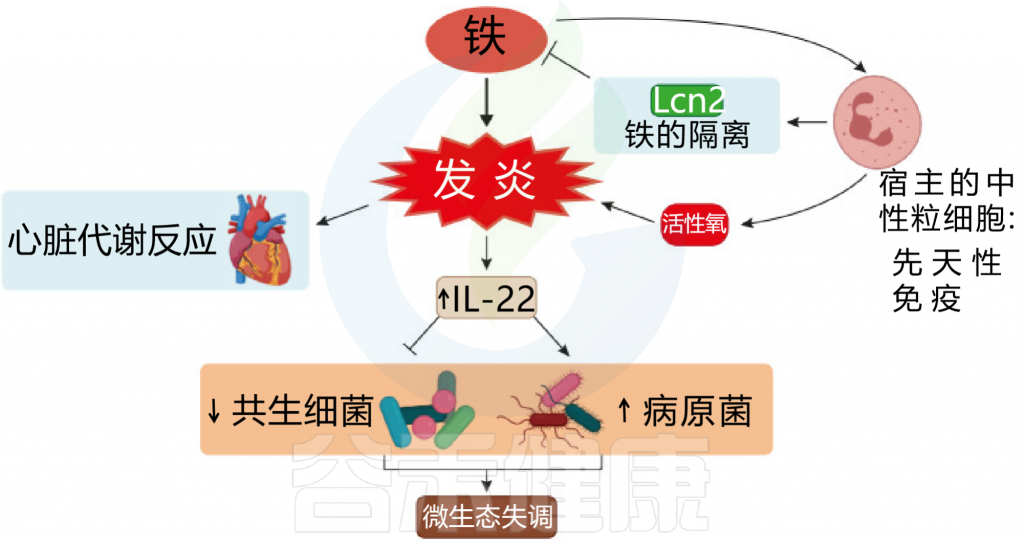

Botta A, et al., J Lipid Atheroscler. 2021
铁补充
铁的补充和强化对人体肠道细菌组成有不同的影响。
接受低剂量(0-10 mg Fe/天)或高剂量(大于60 mg Fe/天)铁补充剂的孕妇在肠道菌群任何分类水平上均没有显著差异。
接受含铁微量营养素粉(12.5 mg/天)的肯尼亚婴儿的病原体丰度增加。在健康、非贫血的瑞典婴儿中,食用高铁配方奶粉(6.6 mg Fe/天)45天不会增加病原菌的生长;然而,双歧杆菌的相对丰度降低。
但是,值得注意的是在同一项研究中,与服用高铁配方奶粉的婴儿相比,服用铁滴剂(6.6 mg Fe/天)的婴儿的乳酸菌种类相对丰度较低。尽管剂量相当,但这项研究表明,给药形式(即配方奶粉与滴剂)对肠道微生物组成的影响存在差异。
此外,由于铁滴剂会导致乳酸杆菌的减少,乳酸杆菌是重要的共生细菌,因此铁滴剂可能会增加感染的易感性。
在疟疾流行地区补充铁被证明会增加严重不良事件的发生率,包括因疟疾和其他感染而住院。疟疾感染恶化的潜在机制被认为是过量铁抑制铁转运蛋白(ferroportin,防止红细胞中铁过量,防止感染)。
口服铁补充剂和强化对 4-59 个月儿童腹泻发病率的影响。在19项研究中发现,12项研究中铁不会影响腹泻发病率,在其余的研究中,四项记录的腹泻发病率显着增加,三项记录在特定亚群中的增加。
为什么有些研究表明补铁导致腹泻增加?
有两个主要假设可以解释有时观察到的效果。
首先,铁可以在肠道内产生活性氧,从而导致肠道损伤,并导致炎症性腹泻。这一假设得到了体外实验的支持,在体外实验中,铁暴露后,肠上皮细胞失去了完整性。
其次,铁可以改变肠道细菌的组成,创造一个更具炎症性的环境。
口服铁剂后结肠腔内的微生物和代谢变化
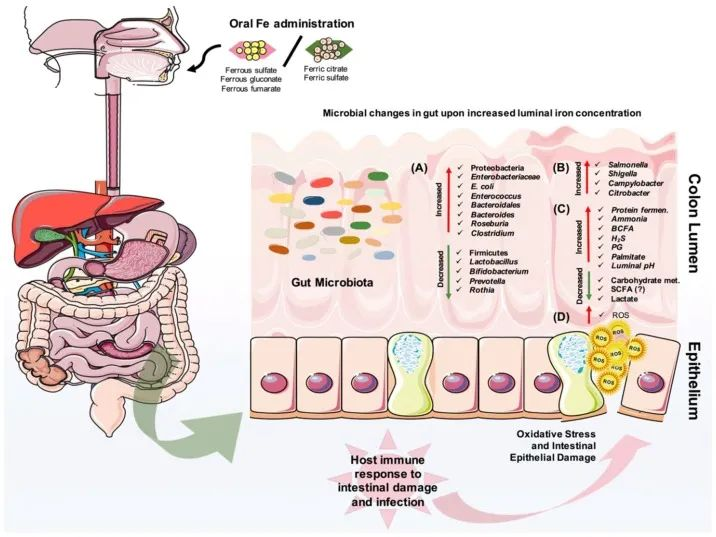
Yilmaz B, Li H. Pharmaceuticals (Basel). 2018
口服铁对肠道微生物组成的改变有直接影响。
(A)它可以导致有益微生物群的减少和致病菌的扩张,
(B)也可以为肠道病原体的扩张提供机会。
(C)此外,蛋白质发酵的增加和碳水化合物代谢的减少也会影响宿主的代谢。
(D)重要的是,铁可以在肠道中诱导活性氧(ROS)的产生,从而导致氧化应激,从而导致肠上皮损伤。
· 反过来,宿主的肠道免疫系统会对炎症、肠道损伤和可能的感染做出反应。
对于缺铁个体的补铁,可以改善肠道微生物的组成,降低致病菌的数量。但是在一些研究中,缺铁性贫血的个体口服补铁常会伴随胃肠道症状和肠道感染等副作用。在非洲的研究中,接受了铁强化剂饼干的儿童,铁补充并未改善机体贫血状况,反而增加了肠道致病菌肠杆菌数量,减少了乳酸菌和双歧杆菌数量,这些现象的发生可能与宿主的肠道高炎症水平密切相关,受到肠道内铁含量和微生物的影响。
当人体存在低肠道病原体负担时,补充铁剂对于肠道优势菌群或肠道炎症没有明显的影响;当人体不存在肠道病原负担的时候,补充铁剂可恢复肠道菌群,显著增加粪便中抗炎短链脂肪酸浓度并且降低肠道炎症,改善肠道微环境。
铁与病原菌
在哺乳动物中,大多数铁在血红素的卟啉结构中被螯合。由于病原菌生长需要铁,有的病原菌如霍乱包含的基因使霍乱弧菌能够从血红素中获取铁。霍乱毒素通过堵塞末端的毛细血管增加管腔血红素的生物利用度,导致宿主铁利用降低。
图 铁和代谢功能之间联系
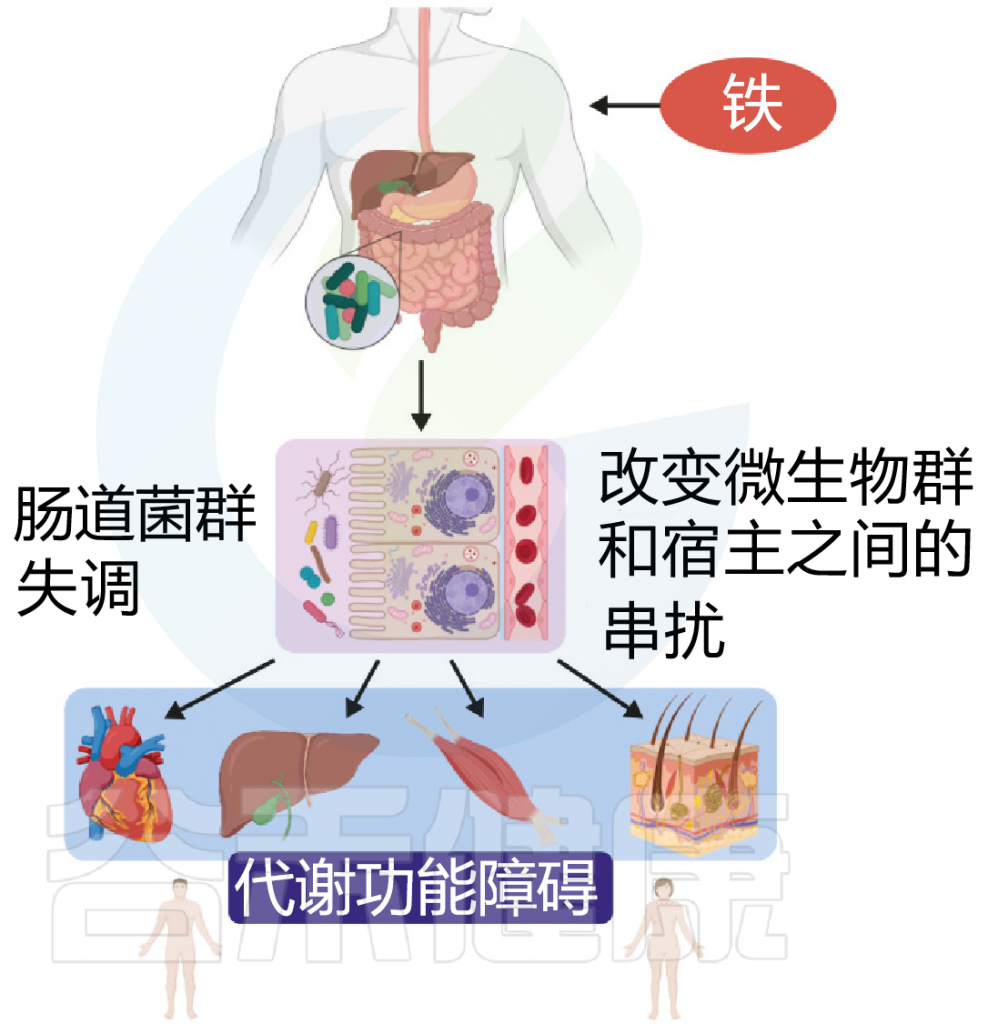

Botta A, et al., J Lipid Atheroscler. 2021
此外,霍乱弧菌产生一种称为弧菌素的铁载体。与肠杆菌素等其他儿茶酚酸酯铁载体不同,这种独特的协同作用有助于逃避宿主免疫系统。霍乱毒素还会增加管腔内的长链脂肪酸和L-乳酸代谢产物,从而导致编码TCA循环含铁硫簇酶的霍乱弧菌基因上调。
因此,霍乱和霍乱毒素的产生在肠道中创造了一个缺铁代谢生态位,通过获得宿主来源的血红素和脂肪酸,选择性地促进霍乱弧菌的生长。
空肠弯曲菌也能捕获宿主铁并在宿主内引起感染。空肠弯曲菌感染是通过食用生的或未煮熟的家禽、海鲜、肉类和未经处理的饮用水发生的,当空肠弯曲菌通过胃时,它必须首先在极端酸性环境中存活。铁的存在增强了它在酸胁迫环境中的生存能力,因此它含有与铁介导的酸保护有关的基因,包括鞭毛生物发生基因、细胞膜生物发生基因、热休克蛋白(GroEL、GroES),这些基因有助于它的生存。
膳食铁可抑制肠道病原体柠檬酸杆菌的生长,并促使选择无症状的柠檬酸杆菌菌株;这些反应与胰岛素抵抗和抑制病原体毒力的葡萄糖水平升高有关。
除了促进胰岛素抵抗外,膳食铁还增加了肠道葡萄糖水平,这是抑制病原体毒力的关键肠道环境变化,并推动了无症状柠檬酸杆菌菌株的选择。然而,相比之下,其他研究表明,铁可用性的降低是有益的,因为它可以减少潜在致病性肠道细菌的生长。
铁对促、健康的 SCFAs 产生的影响
细菌代谢对我们的肠道健康很重要。短链脂肪酸是结肠中的主要代谢物,对肠道健康非常有益,并且是肠细胞和更远距离组织的能量来源。
铁与短链脂肪酸
两项研究首次描述了铁和短链脂肪酸产生之间的联系。
具体来说,体内大鼠管腔缺铁期间丁酸盐和丙酸盐水平较低,并通过补铁恢复。尽管不能排除饮食干预会改变肠道对短链脂肪酸的摄取,但这些结果表明,补铁可以通过增加短链脂肪酸的产生对肠道健康产生有益的影响。
然而,相比之下,高铁条件下似乎没有太大刺激体外短链脂肪酸的产生,而在极低铁条件下丁酸盐和丙酸盐的产生最明显受到损害。这种产量下降伴随着产生短链脂肪酸的菌Roseburia spp./ E. rectale和Clostridium Cluster IV 成员的减少。
体外发酵研究表明,补充铁会略微增加丙酸盐水平,但总短链脂肪酸水平没有显着变化。
与补充铁饮食的大鼠相比,缺铁饮食大鼠的盲肠乙酸盐、丙酸盐和丁酸盐水平降低。他们还表明,与对照组饮食(并且没有首先耗尽铁)的大鼠相比,补充铁饮食的大鼠的丙酸盐和丁酸盐水平更高。因此可以假设,缺铁饮食(与缺铁相结合)可能对肠道健康无益,因为在这些条件下,腔内短链脂肪酸水平会降低。相反,铁补充剂可能会增加促进健康的肠腔短链脂肪酸水平。
值得注意的是,短链脂肪酸可能会影响肠道病原体的毒力。丁酸盐的减少也可能会降低肠内 AMP 导管素的表达,从而削弱宿主的防御能力。
铁与支链氨基酸(BCFA)
与碳水化合物发酵相比,肠道细菌的蛋白质发酵会产生有毒或潜在有毒的代谢物,例如氨、H2S、BCFA(例如异丁酸和异戊酸)、吲哚和酚类化合物。
在体外,低铁条件下 BCFAs 的产生减少,也就是说:铁增加了成人粪便微生物群的 BCFA 的产生以及有毒氨的产生。
值得注意的是,BCFAs 和氨被认为是蛋白质发酵的指标。研究表明铁会刺激蛋白质发酵,这可能会导致更腐败、潜在有毒或致癌的环境。相比之下,在体外发酵研究中发现乳酸(主要来自碳水化合物)水平会随着铁的反应而降低。
虽然在多项体外研究中显示了源自蛋白质发酵的产品毒性的证据,但体内毒性是有限的,最近的一项试验不支持蛋白质发酵在人体肠道毒性中的作用。
另一方面,蛋白质发酵通常与病原菌的生长有关。因此,有必要在体内研究铁对蛋白质发酵和毒性的影响。
重要的是要认识到微生物代谢物的影响不仅限于肠道,因为它们被吸收,并且可能对远处部位和全身宿主代谢产生影响。目前我们还不知道这如何影响人类健康和疾病,但研究暗示铁诱导的肠道微生物活性变化也可能具有全身性影响。
在稳态条件下,肠道内的微生物必须相互竞争,并与宿主竞争可用铁。因此,细菌发展了不同的吸收系统,如铁运输系统和铁载体(铁螯合分子),以便在铁有限的环境中更有利地竞争。
前面我们知道,铁对于细菌的生长繁殖至关重要,但过量的铁也会产生毒性,因此,细菌对铁离子的摄取必须受到精确严格的调控。
细菌已经进化出了铁源的摄取系统。
细菌获取铁的机制
细菌可以通过分泌铁载体摄取Fe3+。铁载体是一种Fe3+特异性的螯合剂,对Fe3+具有超强的络合力。
铁载体能够与宿主体内的转铁蛋白、乳铁蛋白等铁结合蛋白竞争Fe3+,从而形成可溶性的Fe3+-铁载体复合体,这种复合体可以特异性地与细菌细胞外膜上的铁载体受体蛋白(OMRs)相结合,最终被转运至细胞周质中,转运过程通过TonB系统提供能量。
细胞周质中的Fe3+-铁载体复合体与周质结合蛋白(PBPs)相结合,形成Fe3+-铁载体-PBPs复合物。最后Fe3+-铁载体-PBPs复合物由ABC转运蛋白介导,通过内膜进入胞浆。进入细胞后,Fe3+-铁载体-PBPs复合物中的Fe3+被铁还原酶还原为Fe2+,Fe2+与铁载体的亲和力低,从而被释放。
除了分泌高亲和力的铁载体竞争Fe3+外,一些细菌还进化出直接利用转铁蛋白或乳铁蛋白中Fe3+的机制。
大多数革兰氏阳性菌存在直接吸收血红素而获得铁元素的转运系统。
细菌外膜上的血红素受体可以直接与血红素或血红蛋白结合,并将血红素或血红蛋白转运至周质,通过ABC转运蛋白转运至胞质降解或利用,整个过程由TonB系统提供能量。
金黄色葡萄球菌铁依赖性表面决定系统(Isd)可从血红蛋白中获取Fe2+。
除直接的血红素转运系统外,还存在间接的血红素转运系统。如革兰氏阴性菌中存在的Hemophore蛋白介导的血红素转运系统。
除此之外,细菌也可以产生分泌的或位于膜上的铁还原酶,将Fe3+还原成更容易溶解的Fe2+形式,并通过Feo、Yfe、Efe等转运系统来摄取Fe2+。其中Feo转运系统最为重要,大约80%的革兰氏阴性菌都存在Feo转运系统。
调节铁稳态
铁储存蛋白通过以可溶且无毒的形式储存细胞内游离铁来降低其浓度。在铁缺乏时,例如当存在于哺乳动物宿主细胞内或血液中时,铁可以从这些细菌储存中释放出来。
例如,大肠杆菌可以通过FieF输出铁,而且已经描述了一种用于伤寒杆菌的柠檬酸铁外排转运体(IceT);这些铁外流系统的目的是防止细胞内高水平的游离铁造成的压力。此外,血红素输出机制(HrtAB或同源蛋白)已被证明可以缓解某些细菌中血红素的铁胁迫。
最后,双歧杆菌科能够将铁结合到其表面,从而减少周围环境中自由基的形成,并可能在结肠腔中起到铁螯合的作用,以防止病原菌吸收铁。
铁的形态、可用性和结肠腔中的铁之争

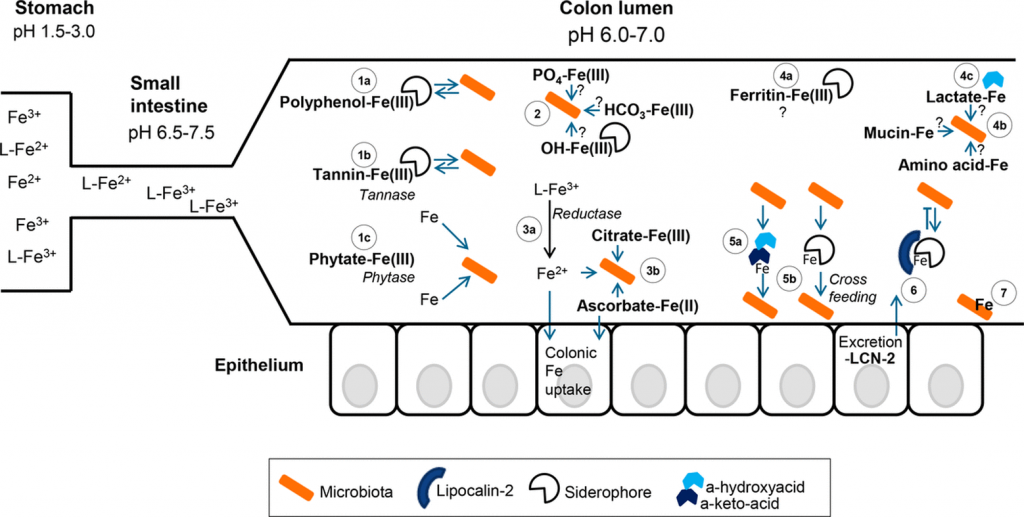
Kortman GA, et al., FEMS Microbiol Rev. 2014
胃肠道中的铁形态可能对肠道微生物群获取铁起着重要作用。
低pH值有利于铁和亚铁的溶解性,不一定需要配体(L)来溶解。
当小肠内的pH值升高时,主要是三价铁的溶解度降低,并与食物成分和宿主排泄物形成更多的络合物。
在结肠内,由于微生物群产生乳酸和短链脂肪酸等,pH值略有下降。图中结肠部分的微生物群以橙色表示(有益的)常驻物种和致病物种。
铁调素(Hepcidin)是一种由肝脏产生的肽激素,是全身铁稳态的主要调节剂。铁调素结合并降解铁转运蛋白,从而影响铁被巨噬细胞回收、被肠上皮细胞吸收以及被肝细胞储存的过程。
当体内缺铁时,铁调素浓度较低,从而有利于铁的吸收和从储存部位输送到血浆;
但当体内铁含量充足时,较高的铁调素浓度会降低铁的吸收,并损害铁的释放。
体内“铁稳态”
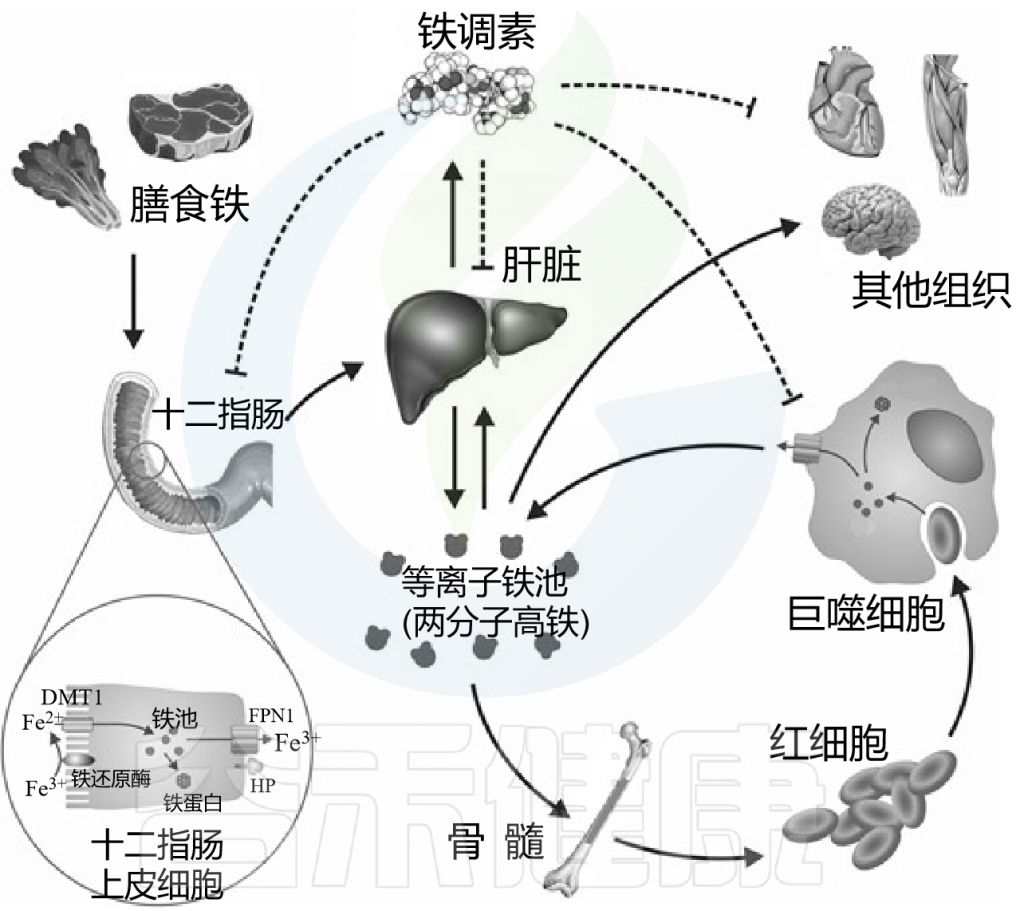

Anderson GJ, et al., Am J Clin Nutr. 2017
铁在饮食中以血红素和非血红素形式存在。非血红素铁通过DMT1穿过肠上皮细胞的根尖膜,通过FPN1穿过基底外侧膜后进入血液循环。铁与血浆TF结合,分布到全身组织。
菌群会通过代谢物信号传导途径调控系统铁稳态平衡。美国密西根大学研究人员在《Cell-Metabolism》上发表的研究证明了,细菌具有铁依赖性机制,可以抑制宿主铁的运输和储存。肠道菌群产生的代谢物能抑制肠道铁吸收主要转录因子低氧诱导因子 2α (HIF-2α),并增加铁存储蛋白铁蛋白 (Ferritin),从而抑制宿主的铁吸收。
两种菌群代谢物——1,3-二氨基丙烷 (DAP) 和 Reuterin,通过抑制异二聚化作用作为 HIF-2α 抑制剂,可以有效缓解全身铁超负荷。
与铁摄取相关的抗菌治疗
针对细菌生存繁殖对铁稳态的严重依赖,可将病原菌的铁获取系统作为抗菌治疗的靶点,开发针对病原菌铁稳态的化合物治疗细菌感染,同时可基于该系统研发疫苗。
大鼠和家兔服用抗生素后,铁的吸收也减少了。然而,小鼠研究发现,抗生素治疗后,铁的吸收增加了。这些发现表明,抗生素的使用可能改善铁缺乏症患者的铁吸收。
铁是饮食变化、微生物组改变和代谢功能障碍之间串扰的关键节点。
代谢综合征指的是一组异常,包括肥胖、血脂异常、胰岛素抵抗和2型糖尿病,这些疾病共同增加了心血管疾病的风险,包括心力衰竭(HF)和非酒精性脂肪性肝病。
通过血清中非转铁蛋白结合铁的存在、高铁蛋白血症、肝铁超载与胰岛素抵抗的相关性,明确了代谢综合征患者中轻度铁过量的患病率。
铁过量与胰岛素抵抗的结合通常被称为代谢异常铁过量综合征,15%-30%的代谢综合征患者会出现这种情况。因此,目前铁过量与代谢当量的关系已被充分认识,但导致代谢功能障碍的机制尚不完全清楚。
降低代谢疾病中铁的效果
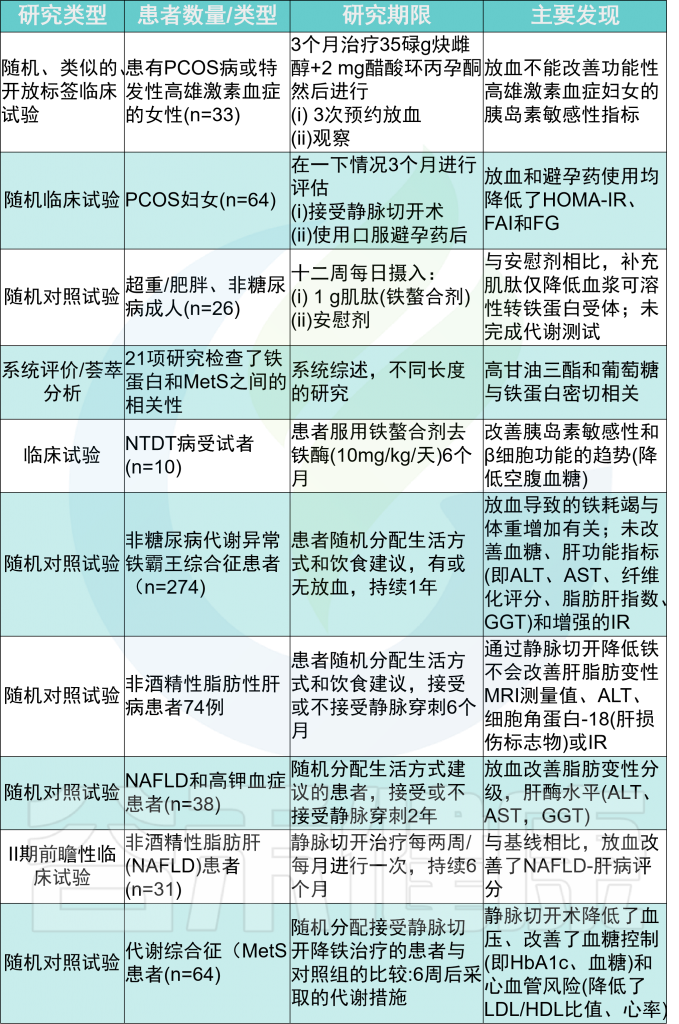

在铁储量较高的MetS患者中,男性对心脏和肝脏疾病的易感性较高。
通过静脉切开或使用螯合剂等降低铁含量的干预措施,在某些情况下可以提高胰岛素敏感性,延缓2型糖尿病(T2DM)和心力衰竭的发病,但并不总是成功的。
在长期病态肥胖后,缺铁是一种常见现象,同样也可导致2型糖尿病和心力衰竭。因此,之前的研究表明铁和葡萄糖稳态或心肌病之间存在双向关系,表明最佳铁水平的平衡至关重要。
可能铁在代谢综合征发病机制及其并发症中的作用仍未得到充分重视,而微生物群的修饰是铁代谢影响的一种重要且相对未被探索的中介物。特别是,肠道内饮食中的铁水平改变了微生物群的组成。预计随后会影响微生物组的代谢组谱功能,包括短链脂肪酸和支链氨基酸。这种改变的后果将是宿主的外周胰岛素抵抗和代谢功能障碍。
炎症性肠病 (IBD) 的特征是胃肠道的慢性炎症。炎症与溃疡性结肠炎 (UC) 和克罗恩病 (CD) 中的肠道溃疡有关。IBD 也可能出现出血和吸收不良,三分之一的患者会出现缺铁性贫血。
一项IBD小鼠模型的研究发现,铁含量的改变显着影响 DSS 在小鼠中诱导的结肠炎的严重程度,铁含量的过多或过少都会加剧结肠炎的严重程度。
DSS治疗的高铁饮食小鼠的体重减轻程度不如低铁饮食小鼠,但粪便钙卫蛋白测定的肠道炎症更严重。这些喂食高铁饮食的小鼠经历了变形菌的增加,同时厚壁菌和拟杆菌的减少。
膳食铁水平与结肠炎症的 DSS 治疗和粪便钙卫蛋白水平之间似乎存在协同作用。
摄入两倍于标准水平铁(400 ppm)的饮食会导致微生物组的关键变化,这意味着观察到的这些变化不仅仅是由炎症的严重程度驱动的,还有管腔游离铁也会导致导致IBD中经常观察到的异源状态发展的复杂因素相互作用。
还需要更多了解的是,管腔铁如何影响IBD。此外,还需要研究管腔铁的增加对肠道微生物群的生理影响,以及这可能如何影响菌群多样性。未来也需要更多人体干预研究,进一步确定不同剂量的治疗性口服铁对人体肠道微生物群的复杂影响,尤其是代谢后果。
研究表明,缺铁和铁过量都与结直肠癌的发病机制有关,这表明必须谨慎平衡最佳铁摄入量。
在 965 名 50-75 岁的人群研究中,发现铁摄入量与结直肠息肉之间存在 U 型关系,铁摄入量高(>27.3 毫克/天)或低量(<11.6 毫克/天)的人更容易患上结直肠息肉,这是结直肠癌的前兆病变。
缺铁
由于铁在维持免疫功能中至关重要,铁的可用性不足可能会通过削弱对肿瘤变化的免疫监测,并潜在地改变肿瘤免疫微环境而增强致癌性。来自临床研究的数据表明,在结直肠癌患者中,缺铁与较差的预后和较低的治疗反应相关。
铁过量
大多数强有力的研究证实,膳食铁和铁储存过量都会增加结直肠癌的风险。
五项前瞻性人类队列研究,包括566607名个体和4734例结肠癌患者的数据,表明高血红素铁摄入量与结肠癌风险增加有关(虽然有一个队列没有发现任何关联)。
在防御方面,长双歧杆菌和嗜酸乳杆菌是肠道保护性共生菌。它们形成了一道保护屏障,防止病原菌定植,并产生丁酸盐,作为一种抗癌剂。双歧杆菌科可通过将铁结合到其表面来影响自由基的形成,并促进结肠上皮的日常更新,而乳酸杆菌菌株可降低胆汁酸的诱变效应。
大多数致病菌都具有增强的铁获取机制,因此往往比保护性细菌更容易获得游离铁。也就是说,铁可以促进致病菌和肠道共生菌之间比例的变化,增加肠道中的特定代谢物和炎症。
研究显示,拟杆菌/普氏杆菌、梭状芽孢杆菌、牛链球菌和粪肠球菌可产生遗传毒性代谢物,如硫化氢和次生胆盐,这可能会促进炎症和致癌。
基于抗生素的肠道致病菌清除降低了结肠癌的发病率,并改变了小鼠的肠道微生物群。这些发现得到了人体研究的支持。
可见,针对肠道微生物群的饮食干预有望治疗结直肠癌,但这些方法仍需要进一步研究。
过量的铁对身体会带来不良影响,因此如果体内铁过量则需要采取相应措施。
多酚-铁:结合牢固,防止铁被吸收
饮食中通常含有单宁和儿茶酚等多酚,它们大量存在于茶和咖啡中。这些化合物可以非常牢固地结合铁,从而防止宿主吸收铁,但也防止细菌吸收铁。
然而,在铁缺乏的环境中,致病菌可以产生和/或占用含铁细胞可能受益于铁多酚提取机制,很可能通过清除铁绑定到多酚。
目前尚不清楚这种机制是否在肠腔中发挥重要作用,但可能与此有关,因为肠环境中可能同时存在多酚和铁载体。
此外,某些细菌,如甘蓝链球菌或卢格敦葡萄球菌,可以降解多酚鞣酸盐,并通过这种方式暂时将铁从这种有效的铁粘合剂中释放出来。
可以通过在用餐后一小时内饮用以下饮料来减少铁的吸收:


植酸盐-铁:结合物通过菌群降解,释放铁
另一种具有强铁结合活性的化合物是植酸盐,在食用谷物和豆类为主的饮食后,其肠道可利用性很高。
与单宁酸类似,某些肠道微生物(如大肠菌和双歧杆菌科)可以降解植酸盐,这可能是一种特殊的释放铁的方式,铁可能被降解生物体或其他细菌物种利用。因此,与植酸盐结合的铁可能是结肠肠道微生物群的相关铁源。
然而,应该注意的是,铁与植酸盐的复合物到达结肠时大多是不溶性的,因此不易被降解。然而,之前在常规大鼠的结肠中发现了只能通过微生物作用产生的植酸盐降解产物,但在无菌大鼠中却没有发现。这些发现表明微生物降解的植酸发生在结肠。
在每餐 2-10mg 植酸盐的极低浓度下,植酸盐会降低铁的吸收。
大豆蛋白(存在于豆腐、组织化植物蛋白和一些加工肉制品中)可以减少铁的吸收,因为它含有植酸盐。
钙
钙对骨骼很重要,但它也可能抑制铁的吸收。为了更好地吸收铁,避免在吃富含铁的食物的同时服用钙补充剂。
牛奶和鸡蛋中的蛋白质
虽然动物肉中的蛋白质会增加铁的吸收,但牛奶和鸡蛋中的蛋白质(卵清蛋白除外)在与低铁食物一起食用时会减少铁的吸收。
锌
过量摄入锌(由于过度使用锌补充剂)也会损害铁的吸收。
考虑到缺铁对人体健康影响重大,因此实施适当的策略来解决这一问题至关重要。
最常见的策略是食物中的铁补充、益生菌、益生元、铁药物补充剂等方法。
富含铁的食物
前面我们知道,膳食铁有两种形式:血红素和非血红素。血红素铁具有较高的生物利用度,膳食因素对其吸收的影响最小,而非血红素铁的吸收要低得多,并受到其他食物类型的强烈影响。
大多数对年轻女性的研究发现铁状态(铁蛋白和铁)与肉类和其他血红素铁的消耗量之间存在正相关关系。
增加富含铁的食物的摄入量,以补充铁储备,确保饮食健康均衡。
其中常见的富含铁元素的食物包括:
红肉、家禽(包括肝脏类)、鱼、豆类、扁豆、豆腐、豆豉、坚果、种子等
非血红素形式的铁含量高的植物性食物(但也可能含有高含量的阻止铁吸收的物质)包括:
● 豆类,包括鹰嘴豆、豆类、豌豆和小扁豆
● 种子,包括芝麻和南瓜子
● 绿叶蔬菜,包括西兰花和羽衣甘蓝
以上是富含铁元素的食物,同时其他富含维生素的食物也能辅助铁的吸收,例如,维生素A,维生素C.
维生素C:促进铁的吸收
如果膳食中含有大量维生素C,那么蔬菜膳食的吸收量可能会增加六倍。维生素C和柠檬酸以剂量依赖的方式促进铁的吸收,部分是通过充当弱螯合剂来帮助溶解小肠中的铁。
一项研究发现,维生素 C 的摄入量与女性的铁含量呈正相关。
在存在抑制铁吸收的物质(包括植酸盐、多酚、钙和蛋白质)的情况下,维生素 C 还有助于铁的吸收。
如果同时服用,维生素 C可将植物性食物中的非血红素铁的吸收提高 2 至 3 倍。因此,为了提高铁的摄入量,可以将富含铁的植物性食物与富含维生素 C 的食物结合起来。
水果或蔬菜中都会包含维生素 C,包括:
● 柑橘类水果
● 奇异果
● 草莓
● 番茄
● 辣椒
● 西兰花
● 卷心菜
● 菠菜


维生素A:克服植酸盐的影响促进铁的吸收
维生素 A直接影响铁转运和红细胞生成。
全谷物和豆类中的植酸盐会降低铁的吸收,但如果加入富含维生素A和β-胡萝卜素的食物可以增加铁的吸收,并可以克服植酸盐的影响。
维生素A(视黄醇)有助于治疗缺铁性贫血,并能改善儿童和孕妇的铁状况。
常见的富含维生素A和β-胡萝卜素的食物:
● 胡萝卜
● 红薯
● 鱼
● 哈密瓜
● 甜椒
● 南瓜
● 葡萄柚
益生菌
大多数益生菌产生乳酸,这可能会降低 pH 值,从而增加铁的溶解度,帮助其吸收。
例如,植物乳杆菌 299v 有助于预防缺铁性贫血。这种益生菌可以改善活跃的高加索欧洲人的膳食非血红素铁吸收。
发酵乳杆菌是人类微生物群中的一种主要益生菌,具有显著的铁还原活性。对羟基苯乳酸是该菌株产生的代谢物,通过DMT1转运体将Fe3+还原为Fe2+来增加肠细胞对铁的吸收。
与益生菌菌株给药相关的铁吸收
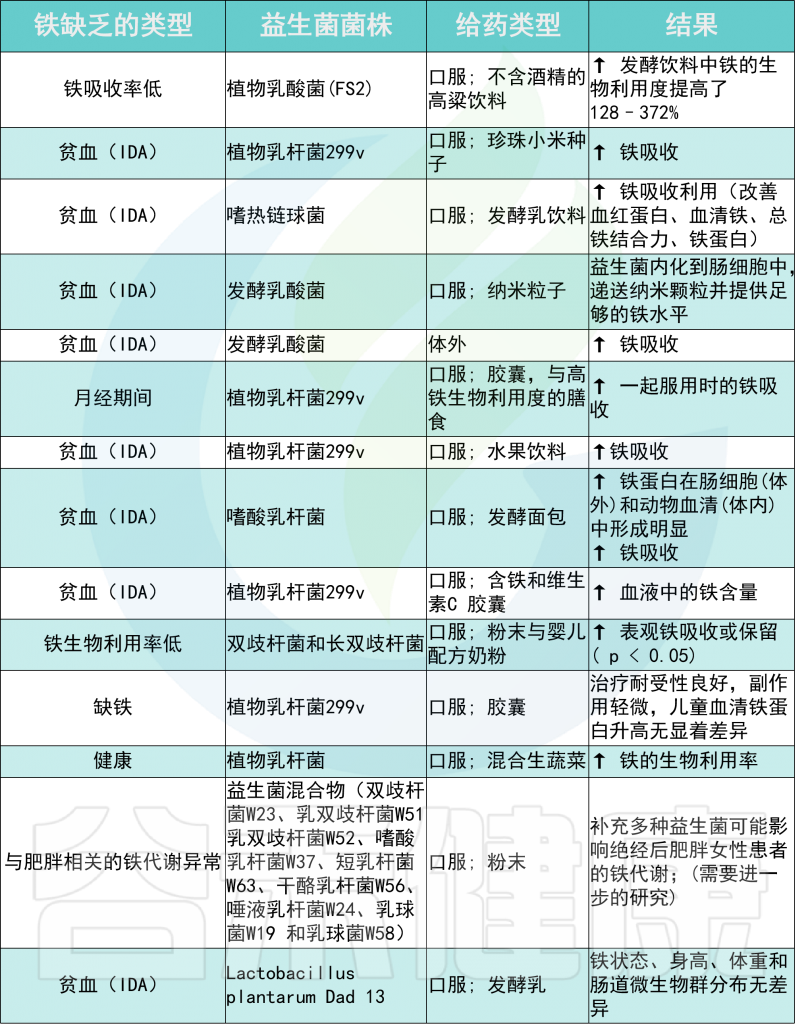

Rusu IG,et al., Nutrients. 2020
益生元
益生元是功能性食品成分,可刺激肠道中有益细菌的生长和定植,最终改善身体健康。肠道微生物群定植在肠道生理学中起着重要作用。
几项研究将益生元和/或合生元的摄入与铁可用性的增加联系起来,主要是通过将 Fe 3+转化为 Fe 2+(由于它们的铁还原活性),并促进肠细胞对铁的吸收。
例如,在肯尼亚儿童中进行的一项补铁试验报告称,在服用益生元期间铁吸收更高半乳糖寡糖 (GOS)底物。
不同类型铁缺乏症的益生元和合生元摄入量及其对机体铁水平的影响
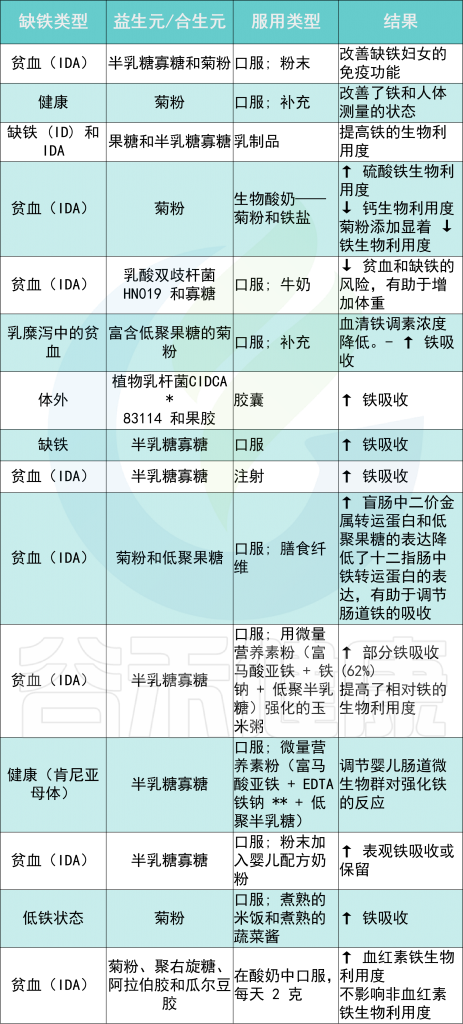

Rusu IG,et al., Nutrients. 2020
* CIDCA——食品冷冻技术研发中心
** EDTA——乙二胺四乙酸
补充剂
不同形式的铁补充剂补充铁以亚铁(+2)和铁(+3)的形式存在。由于铁形态必须在体内转化为亚铁形态以供吸收,因此亚铁形态更具生物利用度。
常用的口服亚铁补充剂包括:
● 柠檬酸亚铁
● 硫酸亚铁
● 葡萄糖酸亚铁
● 铁琥珀酸亚铁
● 氨基酸螯合物(如双甘氨酸铁、天冬氨酸铁)
● 血红素铁
虽然最常研究的铁补充剂是硫酸亚铁,但食品强化和补充剂研究表明,氨基酸螯合形式的铁(如甘氨酸)更好或同样好地被吸收。
例如,在一项针对孕妇的研究中,25mg甘氨酸亚铁能够将铁水平提高到与50mg硫酸亚铁相同的水平。
较新配方的铁补充剂可能比亚铁盐更容易耐受,胃肠道副作用更少,如:
然而,在提高产品螯合率、安全性,降低产品成本等方面有待进一步研究。
铁注射需要医疗监督。当口服铁补充剂不能耐受时,可以注射,这通常适用于患有腹腔疾病和炎症性肠病的患者。在手术或输血后血红蛋白必须迅速增加的情况下,也建议使用。注射铁剂比口服疗法更昂贵,而且不能在怀孕的前三个月用。
建议注射羧麦芽糖铁和异麦芽糖铁,因为它们能够以更大剂量给药,且安全性好。


另外,特殊人群对铁的需求量不同:
健身人群补铁
运动会加快铁在机体中的代谢,长期的运动使组织内储存铁的含量明显下降,是红细胞的更新速度加快,运动还导致机体对铁的吸收率降低,这些都增加了健身人群对铁的需要量。
我国对健身人群每日膳食的推荐的摄入量为:男性20毫克/天,女性25毫克/天。
妊娠期补铁
孕妇对铁的需求量比一般人群更高,每天 27 毫克。
妊娠期间,受母体铁状态调节的铁调素血清浓度极低。由于铁调素是肠道铁吸收的负调节剂,低水平表明对铁的需求高。
妊娠早期和中期缺铁与孕产妇发病率增加和不良妊娠结局风险增加有关,包括低出生体重、早产或宫内生长受限。
大多数产前维生素都含有足够的铁来弥补这种增加,但由于对血液产生的需求增加,缺铁性贫血在怀孕期间很常见。因此需要合理补铁。
具体补铁方式可参考上面列出的形式。
铁对于维持宿主肠道菌群稳态和肠道微生物的生长定植有重要作用。一些菌群,尤其是致病菌的生存,必须依靠铁的存在,因此形成了多种摄取铁的机制,并且参与调节宿主的肠道铁吸收。同时,铁与宿主的肠道微生物和微生物代谢产物共同作用,可对肠道乃至整体健康产生影响。
在补铁的同时,需要防止补铁带来的代谢紊乱和炎症损伤,也就是说铁的补充要在允许的条件下适度补充。那么怎么知道是否在合理范围内?目前对铁的监测以血液检测较常见,但血液检测波动较大。
此外,既已发现了铁与肠道菌群相关性,肠道菌群检测也是一个可行方向。谷禾肠道菌群健康检测报告中包含铁的水平,这是基于菌群代谢计算得到的,与血液检测有所不同,肠道菌群检测反映的是一段时间(2周左右)的长期状态。
未来需要更多的研究来证明铁、宿主与肠道菌群的相互作用机制,以及其与肠道炎症疾病等多种慢性疾病发生发展之间的因果关系,为铁补充的个性化策略提供更多支持。
各类人群的铁需求量


►►►
铁补充的副作用及相关禁忌
► 可能出现的副作用
► 禁忌症
铁补充剂不应用于以下人群:
声明:本账号发表的内容用于信息的分享,仅供学习参考使用。在采取任何预防、治疗措施之前,请先咨询临床医生。
主要参考文献:
Yilmaz B, Li H. Gut Microbiota and Iron: The Crucial Actors in Health and Disease. Pharmaceuticals (Basel). 2018;11(4):98. Published 2018 Oct 5. doi:10.3390/ph11040098
Botta A, Barra NG, Lam NH, et al. Iron Reshapes the Gut Microbiome and Host Metabolism. J Lipid Atheroscler. 2021;10(2):160-183. doi:10.12997/jla.2021.10.2.160
Finlaysontrick E C , Fischer J A , Goldfarb D M , et al. The Effects of Iron Supplementation and Fortification on the Gut Microbiota: A Review[J]. Gastrointestinal Disorders, 2020, 2(4):327-340.
Yilmaz B, Li H. Gut Microbiota and Iron: The Crucial Actors in Health and Disease. Pharmaceuticals (Basel). 2018 Oct 5;11(4):98. doi: 10.3390/ph11040098. PMID: 30301142; PMCID: PMC6315993.
Kortman GA, Raffatellu M, Swinkels DW, Tjalsma H. Nutritional iron turned inside out: intestinal stress from a gut microbial perspective. FEMS Microbiol Rev. 2014 Nov;38(6):1202-34. doi: 10.1111/1574-6976.12086. Epub 2014 Sep 29. PMID: 25205464.
Georgieff MK. Iron deficiency in pregnancy. Am J Obstet Gynecol. 2020;223(4):516-524. doi:10.1016/j.ajog.2020.03.006
Rusu IG, Suharoschi R, Vodnar DC, et al. Iron Supplementation Influence on the Gut Microbiota and Probiotic Intake Effect in Iron Deficiency-A Literature-Based Review. Nutrients. 2020;12(7):1993. Published 2020 Jul 4. doi:10.3390/nu12071993
Anderson GJ, Frazer DM. Current understanding of iron homeostasis. Am J Clin Nutr. 2017 Dec;106(Suppl 6):1559S-1566S. doi: 10.3945/ajcn.117.155804. Epub 2017 Oct 25. PMID: 29070551; PMCID: PMC5701707.
LIU Fang-Tong, FAN Hao-Nan, SHEN Li-Xin, LI Bo. Iron acquisition by bacterial and adaptive immune responses[J]. Microbiology China, 2019, 46(12): 3432-3439.
Tolkien Z, Stecher L, Mander AP, Pereira DI, Powell JJ. Ferrous sulfate supplementation causes significant gastrointestinal side-effects in adults: a systematic review and meta-analysis. PLoS One. 2015;10(2):e0117383. Published 2015 Feb 20. doi:10.1371/journal.pone.0117383
GUAN Lingjuan,CAO Congcong,TU Piaohan,et al. Research progress of the effect of iron deficiency on intestinal immune function and new iron supplements[J]. Food and Fermentation Industries,2020,46(19):264 -270
高鹤, 杨浕滢, 应晓玲,等. 铁,宿主和肠道菌群相互作用的研究进展[J]. 现代预防医学, 2020, 47(20):4.

谷禾健康
说起抗生素,可能会觉得有些抽象,那如果说阿莫西林、头孢、红霉素、阿奇霉素等等这些日常生活经常使用的药物,会不会有一些熟悉的感觉。当我们发现身体有一些小炎症(如头痛发热、喉咙痒疼、咳嗽)的时候,首先会想到要使用这类药物(抗生素) 进行消炎。
在现实生活中,抗生素被许多人当作是包治百病的妙药,一遇到头痛发热或喉痒咳嗽,首先想到的就是使用抗生素,而对滥用抗生素产生耐药性的危害却知之甚少。
世界卫生组织在1996年时就向全世界发出了警告,因为人们对抗生素的滥用,产生了一些严重的后果。其中之一就是导致了细菌的耐药性增强,其结果直接提高了人类对感染类疾病的治疗的难度,增加治疗所需的成本,甚至患病人群的死亡率剧增。
在人类和其他哺乳动物中,所有暴露于环境的表面都是无数古细菌、细菌、病毒和真核微生物的家园,这些定殖微生物被称为微生物群。
微生物群的定植为我们抵御病原微生物感染提供了最有效的屏障之一。微生物群通过启动免疫防御、通过代谢将病原体排除在其首选的生态位中以及通过直接的抗微生物拮抗作用来防止感染。微生物群的破坏,尤其是抗生素的破坏,是细菌病原体定植的主要风险因素。
研究表明,常见的革兰氏阴性菌感染包括由克雷伯氏菌、铜绿假单胞菌和大肠杆菌以及革兰阳性菌感染如艰难梭菌感染,最初的定植与治疗复发均与抗生素的使用和被破坏的肠道菌群有关。
例如,肺炎克雷伯菌是属于肠杆菌科的革兰氏阴性变形菌。它是包括人类在内的几种哺乳动物的胃肠道和上呼吸道共生的,估计人类携带率约为 3-8%。在住院患者中,胃肠道定植的发生率可能会显着升高(高达 38%)。在一部分宿主中,肺炎克雷伯菌会引起呼吸道、泌尿道、伤口和血流感染 。
胃肠道定植是肺炎克雷伯菌的关键步骤发病机制。住院时间和抗生素的使用会增加肺炎克雷伯菌的定植率。住院时间可能会增加患者通过医护人员和污染物接触细菌的可能性。抗生素的使用导致微生物群失调,为肺炎克雷伯菌提供了有利条件。抗生素耐药性的发展也放大了肺炎克雷伯菌的感染几率。
此外,革兰氏阳性菌感染中艰难梭菌感染可能是最广为人知且临床上最常见的感染。艰难梭菌感染的主要危险因素之一是之前的抗生素治疗 。感染的初始治疗通常依赖抗生素甲硝唑和万古霉素;然而,高达 35% 的患者会出现感染复发,并且与免疫抑制和进一步的抗生素治疗有关 。 此外,临床研究认为氟喹诺酮类、克林霉素和头孢菌素也是使患者对艰难梭菌易感的主要抗生素。
本文主要探讨抗生素究竟对人体肠道菌群有哪些影响,以及对人体健康的主要影响。
抗生素
抗生素是指由微生物(包括细菌、真菌、放线菌属) 或高等动植物在生活过程中所产生的具有抗病原体或其他活性的一类次级代谢产物,能干扰其他生活细胞发育功能的化学物质。简单来说就是在非常低浓度下对所有的生命物质有抑制和杀灭作用的药物。临床常用的抗生素有微生物培养液中的提取物以及用化学方法合成或半合成的化合物。
自人们发现抗生素的使用大大的降低了传染病导致的死亡率后,抗生素就开始被广泛的应用于疾病的治疗中,并在全球范围内彻底改变了传染病的治疗方法。在20世纪更是一度被称为 “预期寿命延长” 的一大促成因素。
抗生素的本质作用其实就是把感染我们的微生物消灭,清除掉病原体,控制住疾病的发展,最终得以将病症治疗康复。但因为人类、兽医学以及畜牧业中过度使用、误用等情况的发生,导致了当前出现了抗生素耐药性的危机。
抗生素的种类很多,目前国内在医学和兽医日常应用的抗生素不少于几十种。不同的抗生素对病菌的作用原理不尽相同:
1. 有的抗生素是干扰细菌的细胞壁的合成,使细菌因缺乏完整的细胞壁,抵挡不了水份的侵入,发生膨胀、破裂而死亡。
2. 有的抗生素是使细菌的细胞膜发生损伤,细菌因内部物质流失而死亡。
3. 有的抗生素能阻碍细菌的蛋白质合成,使细菌的繁殖终止。
4. 有的抗生素是通过改变细菌内部的代谢,影响它的脱氧核糖核酸的合成,使细菌(还有肿瘤细胞)不能重新复制新的细胞物质而死亡。
在日常生活以及医疗当中所指的抗生素主要是针对细菌、病毒微生物的药物,种类是相当多的,大概可以分成十余种大类。在临床上常见的更是有百余种之多。
在此简单的对其抗菌谱、化学结构、用途等方面进行分类。
◾ 按抗菌的范围(抗菌谱),分为:
◆ 广谱抗生素
指的是抗菌谱比较宽的药物,简单说就是能够抵抗大部分细菌的药物;
如. 氯霉素、金霉素、土霉素、四环素、甲砜霉素等
◆ 窄谱抗生素
是专门杀灭某一种或一类细菌的药物。
如. 青霉素G
◾ 按照化学结构,分为:
◆ 喹诺酮类抗生素
◆ β-内酰胺类抗生素
◆ 大环内酯类抗生素
◆ 氨基糖苷类抗生素
……
◾ 按照用途,分为:
◆ 抗细菌抗生素
◆ 抗真菌抗生素
◆ 抗肿瘤抗生素
◆ 抗病毒抗生素
◆ 畜用抗生素
◆ 农用抗生素
◆ 其他微生物药物(如麦角菌产生的具有药理活性的麦角碱类,有收缩子宫的作用) 等。
列举常用的各类抗生素及其作用、对应的病症等:
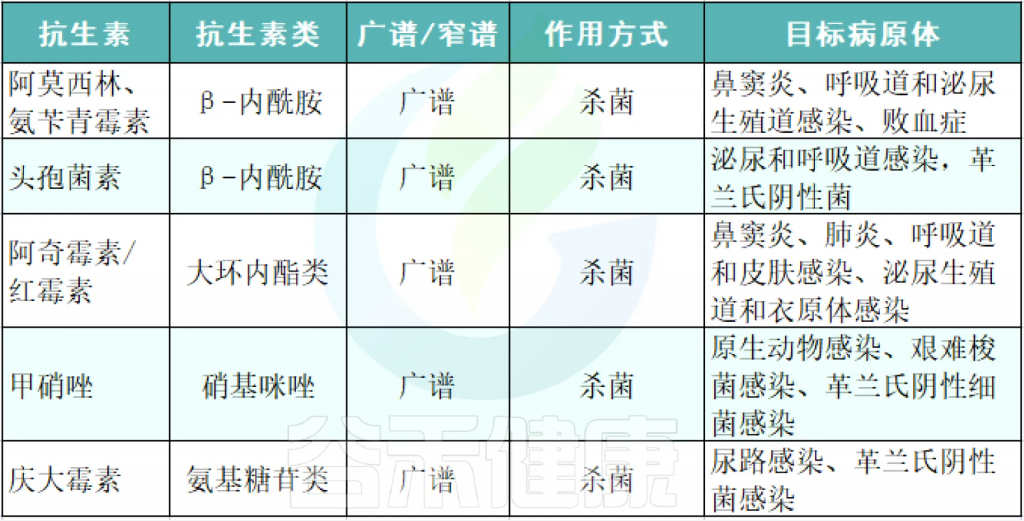

Patangia DV, et al., Microbiologyopen. 2022
肠道微生物群的组成
肠道微生物群对于宿主的健康起着重要的作用 —— 可以防止病原体的定植,调节肠道免疫,提供必需的营养物质、生物活性代谢物、参与能量稳态等。
肠道微生物群是由细菌、古细菌、微真核生物和病毒组成,且根据迄今为止的多项研究可以得出,平衡且稳定的微生物群组成和丰富的菌群多样性对于机体功能等至关重要。健康成人的肠道微生物群主要由厚壁菌门和拟杆菌门组成,其次是放线菌门、变形菌门和疣微菌门。人们普遍认为,肠道微生物群是在婴儿出生时就获得的,其母体是婴儿肠道微生物群最重要的来源,此后在肠道免疫力的发展中发挥着重要作用。婴儿肠道中菌群的多样性减少、微生物群组出现不平衡与肠道疾病和晚年易患的某些疾病有关。而健康婴儿肠道微生物群的建立以及其后续的持续发展是一个长久的过程,并受诸多因素的影响发生变化。
微生物群的变化随多种因素的影响而改变。其中对于婴儿来说,大部分的肠道菌群受其母体的影响最为严重,主要是与分娩方式、胎龄以及产后喂养习惯等方面有关;对于抗生素的使用同样是影响肠道菌群的一大常见因素。
◾ 分娩方式是影响婴儿肠道菌群的首要因素之一。通过对比发现,阴道分娩婴儿的微生物群明显更加的多样化,与其母亲的阴道微生物群相似度更高;而剖宫产出生的婴儿则因为被缺乏了部分相应的生产过程以及母体的接触,因此具有肠道微生物群仅与其母亲的皮肤和医院环境所类似。其中,
在剖宫产出生的婴儿中 ——
丰度增加的包含:
丙酸杆菌(Propionibacterium)
棒状杆菌(Corynebacterium)
葡萄球菌(Staphylococcus)
艰难梭菌(C.difficile)
链球菌(Streptococcus)
丰度降低的包含:
双歧杆菌(Bifidobacteria)
拟杆菌(Bacteroides)
在阴道分娩的婴儿中发现了 ——
乳酸杆菌(Lactobacillus)
普雷沃氏菌(Prevotella)
斯奈斯菌属(Sneathia spp.)
◾ 胎龄也是改变肠道菌群的因素。早产儿明显比足月新生儿的肠道菌群多样低,其中 ——
变形菌(Proteobacteria)的丰度较高;
专性厌氧菌(如. 双歧杆Bifidobacterium)、拟杆菌(Bacteroides)、Atopobium的水平较低。
◾ 喂养习惯是影响婴儿肠道菌群的另一个关键因素。由于母乳中存在大量的低聚糖(母乳低聚糖) 用来产生双歧杆菌(Bifidobacteria)。与配方奶喂养的婴儿相比:
母乳喂养的婴儿 ——
双歧杆菌的水平更高,且在断奶后的比例仍然很高;
检测出的菌群包含:
拟杆菌(Bacteroides)
链球菌(Streptococcus)
乳酸杆菌(Lactobacillus)
……
配方奶喂养的婴儿 ——
丰度较高的菌包含:
大肠杆菌(Escherichia coli)
艰难梭菌(C. difficile)
脆弱拟杆菌群(Bacteroides fragilis group)
乳酸杆菌(Lactobacilli)
以下,为各种抗生素对人体肠道微生物群影响:

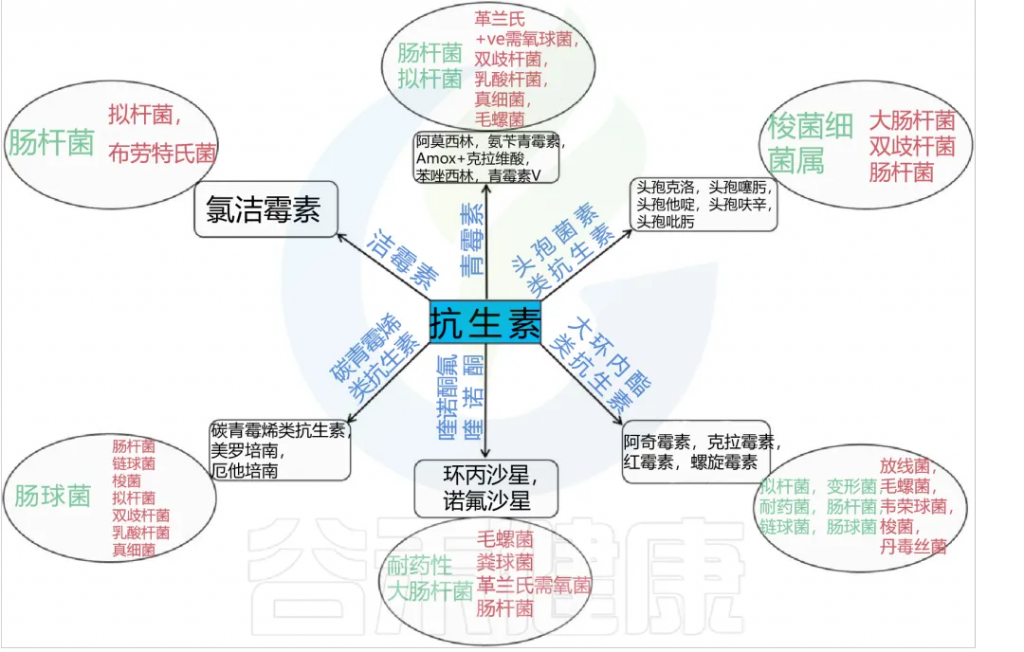
Patangia DV, et al., Microbiologyopen. 2022
怀孕期间的阴道微生物群发生了特定的变化。有研究报道,与未怀孕女性的阴道微生物群相比,怀孕期间的阴道微生物群的变化重点表现在高细菌负荷、高乳酸菌丰度、低丰富度和菌群多样性的降低等。在整个怀孕期,表示机体健康的特有特征包括了细菌的负荷增加以及肠道微生物群组成发生的明显变化。在妊娠的前三个月至妊娠晚期,随着生理的变化,会出现诸如变形菌和放线菌总含量的明显增加以及其丰富度下降的现象。
抗生素所引起微生物组成的变化会对宿主的健康产生直接或间接的负面影响。
其中包括 ——
微生物多样性下降
微生物群功能属性发生变化
抗生素抗性菌株的形成和选择
这些变化会使宿主更容易感染艰难梭菌等病原体。
以下,是过度使用和滥用抗生素可能对宿主健康产生负面影响:
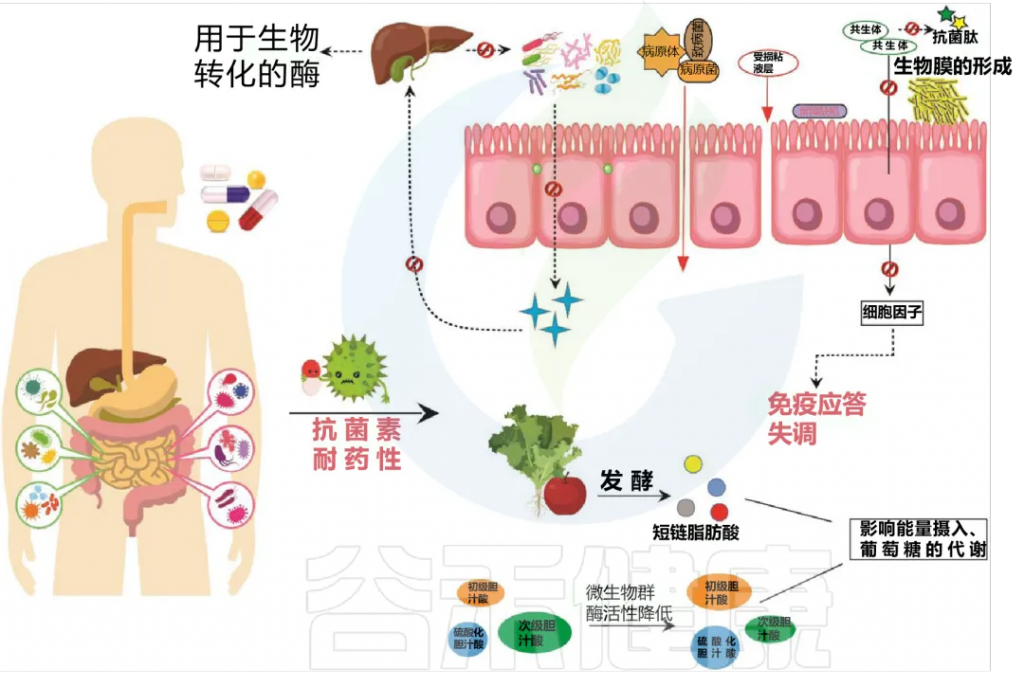

Patangia DV, et al., Microbiologyopen. 2022
◾ 母体&婴儿常使用的抗生素及原因 ——
◆ 怀孕期间 最常用的一些抗生素包含:
β-内酰胺类抗生素
磺胺类
甲氧苄啶
大环内酯类
林可酰胺
链霉素
其他规定的抗生素类
◆ 分娩期间 经常给母体服用抗生素,目的:
防止 B 群链球菌的传播
减少并预防子宫内膜感染的风险
以及预防伤口感染的产生
◆ 婴儿 最常用的抗生素包括:
阿莫西林
苄青霉素
头孢菌素
庆大霉素
万古霉素
克林霉素
阿奇霉素
……
这些抗生素适用于呼吸道和耳部的感染、支气管炎、咽炎和高温。
对于孕妇和幼儿来说要尤其注意,上肠道微生物群可能会因受到短期或低剂量抗生素的干扰,而对健康造成了长期深远的严重影响。希望人们可以警戒,不过度滥用抗生素。
◾ 广谱抗生素对肠道微生物群有害影响 ——
广谱抗生素会降低肠道微生物群的多样性,以杀死相关病原体,并根除有益微生物,其结果对宿主是有害的。
在西方国家,高达 35% 的女性在怀孕和分娩期间都会接触抗生素,并经常使用预防性抗生素来预防和治疗感染。女性在怀孕期间抗生素的使用就占了接触药物总量的 80%左右。
◾免疫性疾病
接触过产时抗生素预防(IAP) 的婴儿肠道菌群的多样性会发生改变。如果在儿童早期或发育阶段所接触到的微生物群种类较少或不足,则可能导致免疫相关疾病的产生。为此,世界卫生组织曾提出建议表示尽量不要在分娩后预防性的使用抗生素。
◆ 对于新生儿尤其是早产儿来说
由于其健康状况以及感染的高度敏感性和免疫力较低,导致经常性的要接受抗生素的相关治疗。
经常接触抗生素,会导致 ——
微生物群发生改变
增加患感染性疾病的可能性
常见如. 哮喘和过敏性致敏、NEC 和侵袭性真菌感染。
若延长使用抗生素进行治疗,则可能会 ——
增加发生迟发性败血症(主要由 B 组链球菌引起)
坏死性小肠结肠炎(NEC)
机体性死亡率增加的风险
◆ 在婴儿期使用抗生素,也会产生类似的影响。在哺乳期间,母体所使用抗生素会影响乳汁微生物群的变化,这又将会影响到婴儿肠道菌群的组成。抗生素等一些外在因素会对母体微生物群的多样性进行改变,从而直接或间接地影响到婴儿肠道微生物群的多样性、免疫力的增减以及疾病的发生。过早期的使用抗生素增加了儿童期患哮喘过敏、特应性皮炎和 IBD 等疾病的风险。
◆ 围产期(怀孕28 周到产后一周) 和围产期抗生素的使用会影响肠道菌群的定植以及婴儿的耐药性。
为了了解妊娠期间抗生素给药对后代的潜在影响,科学家们在白细胞介素 10(IL-10) 缺乏的结肠炎小鼠模型 (Miyoshi) 中研究了,在围产期给药头孢哌酮对母体及其后代微生物群随着给药时间的改变所带来的影响。暴露于头孢哌酮的后代在成年后显现出发生改变的肠道微生物群落,并且对自发性和化学性诱发的结肠炎的易感性增加。且用抗生素改变的微生物群落接种无菌怀孕小鼠后,观察到,改变的微生物群落被传播给缺乏 IL-10 的后代,此变化会导致结肠炎的显着增加。另一项研究表明,怀孕期间服用抗生素会导致出生前阴道微生物的组成发生变化;这可能会影响婴儿出生时所会接触的微生物组成。据报道,孕期母体抗生素摄入与微生物组成的改变有关,具体的改变趋势取决于抗生素类型。
对于抗生素会增加婴儿患哮喘和过敏的风险度、免疫学的改变和后代糖尿病的发生几率以及发育和认知功能的障碍等的相应结论,现阶段还存在争议和不确定性。
◾ 免疫发育
婴儿期,免疫系统就进行了对抗病原体的练习,而此时正是微生物定植的重要时期。这种共同生长发育的过程体系导致了对微生物定植的任何干扰都会影响免疫系统的成熟稳定。
通过对无菌小鼠的研究证实,如果肠道中没有微生物群则会影响肠道环境的生理结构和免疫特性,这些变化主要包括了粘液厚度和成分的改变、胃动力的降低、肠细胞和免疫细胞的非正常发育和功能缺失以及免疫系统发育不当。实验显示,抗生素治疗会减少结肠粘液层的厚度,从而增加小鼠(8-10 周龄) 病原体入侵和肠道炎症的风险。
另一项针对小鼠的研究报告称,抗生素诱导的微生物群改变将 TH1/TH2 平衡转变为 TH2 的主导免疫——伴随着淋巴细胞数量的减少,将导致特应性的发生。
在新生大鼠的相关治疗中观察到,微生物组成和基因成熟谱的改变,例如编码MHC 1b类和II类蛋白质和潘氏细胞产物(如防御素) 的基因下调,这可能会影响粘膜屏障的发育。一项研究表明,肠道菌群产生的某些分子与免疫系统的成熟发育有关。相关研究还发现了,用产生细菌多糖的脆弱拟杆菌来定殖无菌小鼠,可以纠正其T细胞的缺陷、改善 T(H)1/T(H)2 失衡同时促进淋巴器官的发育;然而在不产生多糖的突变体脆弱拟杆菌中并没有观察到该现象。
肠上皮细胞分泌抗菌肽受微环境中微生物群的调节。用常规或人类微生物群或特定益生菌物种或 LPS 定植的无菌小鼠表现出增加的抗微生物肽(如 REGIII-γ) 的产生,增强了先天免疫反应。一项针对小鼠的研究表明,产前抗生素不仅改变了新生小鼠的微生物群定植模式,而且还对影响其免疫反应的病毒感染的 CD8+ T 淋巴细胞的活性产生了负面影响。此外,还观察到,在更加严格的卫生环境下的新生小鼠更容易受到感染。另一种细菌多样性低的小鼠模型在抗生素治疗后有类似的结果产生,同时发现了 CD4+ T 淋巴细胞产生的细胞因子减少以及干扰素-γ 的产生减少。在一项涉及流感患者的研究中发现,感染滴度低并接受抗生素治疗的受试者的免疫反应较低,并会伴有微生物群的丢失以及免疫球蛋白(Ig) G1、IgA 和抗感染的次级胆汁酸水平的降低。这些研究证明了微生物群与宿主免疫反应之间的复杂关系,以及抗生素对其相互作用的影响,部分影响需要进一步相关研究证明。可能还会影响到使用抗生素疫苗治疗的有效性。
◾ 先天性异常
妊娠期间抗生素使用与新生儿和先天性异常之间存在关联。研究报告称,在怀孕期间接受大环内酯类药物治疗的母亲所生的婴儿患脑性麻痹、癫痫、心脏和生殖器畸形的风险增加,在孕早期服用这些药物的有害影响更大。
在少数病例中发现,在孕早期使用阿莫西林与婴儿的唇裂和腭裂的形成有关联,其有利证实了怀孕期间使用抗生素的不利影响。
妊娠前三个月使用磺胺类药物和呋喃妥因与小眼症、左心发育不全综合征、房间隔缺损和唇裂伴腭裂等出生缺陷也有关连;孕期使用甲氧苄啶-磺胺类药物与心血管畸形的高风险相关;可能是由于在子宫内器官发生和早期发育阶段对新生儿产生了影响。
虽然相关的病例还不能总结出确切的关系,但是对于妊娠期间抗生素的使用应该重新进行评估。
◾ 肥 胖
由于肠道微生物群在饮食代谢中的作用,肥胖与早期菌群的定植有着广泛的关联。早期使用抗生素对体重指数的增加、超重以及引起中心性肥胖症有潜在的关联。对此现象在男性中的影响大于女性,所以此类影响可能是具有性别特异性的。
在一项针对 96 人的研究中(其中抗生素组和对照组各 48 人),研究人员发现使用万古霉素和庆大霉素治疗的患者在感染性心内膜炎发作后的体重显着且持续增加。
在对动物的进一步研究后得出,如果早期使用低剂量或亚治疗浓度的抗生素会扰乱微生物组成,影响参与免疫和碳水化合物代谢基因的表达,并可能会破坏代谢的稳态,使宿主在后期更容易出现肥胖的症状。
婴儿期以及儿童期使用抗生素可能会与微生物组成以及代谢功能的改变、晚年的肥胖有关。
在功能水平上,无论是静态的还是灭活的抗生素,不同的类型都会对肠道微生物群产生不同的影响。抗生素可以影响原微生物群并导致耐药菌株的生长,这些菌株在使用治疗后可以持续保留数年。
◾对个体微生物影响
◆ 某种抑菌药物导致了革兰氏阴性菌增多,其影响了 ——
脂多糖(LPS)合成的基因数量的增加
杀菌药物与革兰氏阳性菌的增加有关
其现象还伴有内生孢子形成的基因过度表达
◆ 母体使用了产时抗生素是会影响到婴儿口腔微生物群,其中母体使用了抗生素治疗的婴儿中 —— 放线菌门、拟杆菌门、变形杆菌门更为丰富。氨苄青霉素在母体用于产时预防性药物对抗 B 组链球菌,其结果同样降低了婴儿双歧杆菌的水平含量。
◆ 产前暴露于抗生素的婴儿中拟杆菌和双歧杆菌有所降低,并且发现改变的微生物群类似于同期新生儿重症监护室中的耐药菌。许多相关的影响与产后服用抗生素观察到的结果相似。
◆ 接触 IAP 的婴儿特别是新生儿出生后的最初几周内 ——
放线菌、拟杆菌的比例较低
口腔变形杆菌属水平较高
双歧杆菌的水平较低
◆ 出生后3个月,使用抗生素的婴儿 ——
含量较低的菌属包含:
拟杆菌属
副杆菌属
高等肠球菌属
梭菌属
丰度较高的菌属包含:
而肠杆菌科
◆ 在早产儿中观察到——
双歧杆菌丰度下降
拟杆菌丰度下降
肠球菌丰度增加
早产儿短期和长期接触抗生素都会对其肠道菌群有所改变,包括细菌种群的多样性减少、肠道中物种丰富度降低、抗生素抗性基因增多等方面。
◾相关疾病的微生物
由于微生物群在宿主代谢和生理学中所起到的作用,大量研究提出了“缺失的微生物”(即.假设微生物失衡) 可能会与肥胖、糖尿病和哮喘等疾病具有一定的关联性。
通过微生物群的组成和饮食习惯等可控因素来控制来调控多因素条件,从而尽可能的防止疾病发生。
◆ 研究抗生素使用与肥胖之间的关联发现——
厚壁菌门与拟杆菌门的比例增加(不确定性)
短链脂肪酸(SCFA) 含量更高
◆ 重复性的使用广谱抗生素与糖尿病之间存在着联系。在易患糖尿病的动物中,部分原因是特异性抗原负荷的降低或耐受性 APC 的生长。微生物组成的变化与Ⅱ型糖尿病之间的关联更为明显,Ⅱ型糖尿病患者中产生丁酸盐的细菌水平有所下降。在研究了 121 名糖耐量正常、糖尿病前期以及新诊断为糖尿病的受试者得出,在糖尿病前期阶段肠道微生物组成受到调节,这可以作为糖尿病的一个状态发展标志。
抗生素所引起的微生物的定植变化与Ⅰ型糖尿病之间同样存在着关联性。对自身免疫性Ⅰ型糖尿病的新生非肥胖糖尿病小鼠,给予单独的广谱抗生素或与万古霉素的组合使用会发现——
大肠杆菌的种类增加
乳酸杆菌的种类增加
梭菌目减少
其微生物群发生了显着的变化
回肠和结肠固有层中IL-17 细胞产生大量减少
这会影响到宿主的防御机制。此外,葡萄糖稳态和胰岛素抵抗相关的代谢变化,也与糖尿病的患病有关。
◆ 抗生素导致抗生素相关性腹泻(AAD) ,克林霉素可导致微生物群发生改变,从而促进艰难梭菌等潜在病原体的定植,进而导致腹泻和结肠炎的发生。抗生素治疗导致 ——
α和β多样性下降
导致水平下降的包含:
血清素
色氨酸水解酶
次级胆汁酸
进一步影响肠道的蠕动和代谢问题。NEC 和 AAD 还与生命早期延长或预防性抗生素摄取有关。
◆ 许多抗生素通常用于牙科手术。这些抗生素可以增加口服耐药菌株的数量,还可以增加最低抑菌浓度,以及消除非致病菌株——这些菌株会导致全身感染和炎症。
Patangia DV, et al., Microbiologyopen. 2022
◾代谢物
通过影响微生物群落的组成,抗生素还会改变微生物群的功能,从而改变产生的代谢物。
◆ 肠道微生物群负责产生许多必需代谢物,包括 SCFA 和氨基酸,所产生的丁酸盐和丙酸盐具有抗炎作用,促进调节性 T 细胞的产生和分化,在能量代谢中发挥作用。抗生素的摄取会导致微生物群中的蛋白质表达、能量代谢发生变化。
抗生素治疗后,分析代谢的变化——
氨基酸代谢相关代谢产物浓度较高;
氨基酸浓度降低;
丁酸盐和丙酸盐水平降低;
SCFA产量下降;
脂肪酸氧化分解代谢;
氨基酸生物合成发生下降;
影响激素的合成途径(各类细胞因子的基因表达上调);
在微生物群的恢复中,抗生素治疗改变了细菌代谢产物,其中包括——
SCFAs、氨基酸水平的降低;
以及胆汁酸和寡糖等前体增加;
提高胰岛素敏感性;
改变了全身葡萄糖代谢;
肝脏和回肠中参与葡萄糖和胆汁酸代谢的基因表达;
可能会导致屏障功能受损,其作为溃疡性结肠炎和沙门氏菌感染的致病因素。
◆ 抗生素对宿主代谢具有性别依赖性,已研究发现万古霉素和环丙沙星-甲硝唑治疗仅导致雌性小鼠厚壁菌门和 SCFAs 显着减少;两种抗生素暴露都显着降低了雌性小鼠结肠内容物中丙氨酸、支链氨基酸(亮氨酸、异亮氨酸和缬氨酸)和芳香族氨基酸的水平,但雄性小鼠中没有发现。
◾异生素的积累
肠道微生物群可以影响宿主的异生物质半衰期、到达靶受体的程度,以及宿主代谢异生物质的能力。
◆ 异生素(包括抗生素、重金属和环境化学品) 对肠道微生物组成的影响是周期性的,因微生物群是外源生物转化所必需的,所以异生素在到达其靶器官部位之前的代谢很大程度上取决于微生物群。
◆ 通过体内和体外研究都表明了,肠道微生物群参与了异生物质的生物转化,其中缺乏肠道微生物群会影响许多肝酶基因的表达。缺乏代谢特定化合物所必需的微生物会导致其在宿主中的累积,从而导致产生毒性。
对 SPF 和无菌小鼠使用环丙沙星后,显示 —— 肝脏 Cyp3a11 表达降低,这与肠道微生物群的改变有关。由于抗生素给药后产生 LCA 的细菌减少从而导致较的低石胆酸 (LCA) 水平,这可能是Cyp3a11 表达减少的原因。对人类的类似影响可导致多种 CYP3A4(Cyp3a11 的人体类似物) 依赖性药物的清除及减少。
◆ 使用抗生素对肠道微生物组成的改变,会产生的影响 ——
肝脏脂质积累水平增加
甘油三酯(TG) 水平升高
唾液酸和琥珀酸盐的水平增加
对沙门氏菌和艰难梭菌的易感性增加
导致某些仅由细菌产生的代谢物或维生素缺乏
导致铜 (Cu) 代谢发生变化
由于铜在一些功能中所发挥的作用,这可能会对免疫和肠道屏障产生影响。
◾细菌的相关影响
抗生素可以改变几个主要功能基因的转录,其中主要包括 —— 编码转运蛋白的基因;参与碳水化合物代谢的基因和蛋白质合成。
◆ 交叉喂养是肠道微生物群的一个重要特征,常见如 利用低聚果糖和淀粉产生乳酸和乙酸;而产生丁酸盐的厌氧菌不能利用低聚果糖和淀粉,而是依赖乳酸和乙酸作为生长底物。在许多细菌群中,通过交叉喂养间接促进了产丁酸盐物种的增殖和扩张。对此进行的相关研究发现万古霉素是一种革兰氏阳性靶向抗生素,可减少肠道中革兰氏阴性细菌的丰度,这可能是由于其细菌中的相互依赖性所导致的。相互依赖可能会因使用抗生素而受到干扰,从而导致某些代谢物/化合物的积累增加或缺乏。
◆ 细菌使用模式识别受体 (PRR) 通过产生胆汁酸、SCFA、脂肪酸、氨基酸、LPS、脂磷壁酸、鞭毛蛋白、CpG DNA 和肽聚糖的信号与其宿主相互作用,这些信号分子既可以作为其他细胞的能量来源,也可以通过 G 蛋白偶联受体和核受体家族、游离脂肪酸受体调节或调节免疫细胞(如单核细胞、巨噬细胞、T 细胞)的功能。
抗生素的使用导致这些细菌的减少,从而减少了 PRR,产生如 TLR 信号传导和先天防御的下游调节。对其研究发现,抗生素介导的丁酸盐产生细菌减少会导致通过细胞内的丁酸盐传感器的过氧化物酶体增殖物其激活受体 γ 的上皮信号传导减少。
同样,由于产生 IL-22 的淋巴样细胞的迁移中断,共生微生物群的抗生素破坏,增加了其肺炎的易感性;这种效应可以通过在出生时将共生微生物群转移给小鼠来逆转。共生菌还在防止结肠损伤和维持肠道稳态方面具有重要作用,共生体通过 TLR 诱导保护因子的释放,然而这些因子在缺乏共生细菌的抗生素治疗的小鼠中没有得到释放;因此,由于微生物群落组成的变化,抗生素可以影响复杂的宿主-微生物相互作用。
◾ 抗生素抗性基因
肠道已被确定为抗生素耐药性的中心,人体也是抗生素抗性基因(antibiotic resistance genes; ARGs)的储存库。在肠道中,细菌可以通过移动遗传元件将基因水平垂直传递给其他相关或不相关的细菌。
◆ 抗生素抗性基因存在于环境中,包括海洋和淡水体、土壤、冰川、食物链以及内部人类;除细菌外,病毒也是抗生素抗性基因的携带者。有些ARG的传播是历史遗留性的,例如在一些未受污染/未受污染的环境中;但其中大部分是因为人类广泛使用抗生素所传播的,除了用于治疗人类感染外,抗生素还被广泛用作动物体重增加的生长促进剂以及治疗和控制感染的使用,甚至应用于水产养殖。
其中一些抗生素与治疗人类感染的抗生素相同或结构相似,例如红霉素、庆大霉素、恩诺沙星、新霉素、链霉素。农业和水产养殖中抗生素抗性细菌的发展是一个严重的问题,因为这些细菌可以通过食物链进入人体,促进交叉耐药性,并降低传染性细菌对抗生素治疗的敏感性。
◆ 有研究发现来自偏远地区的人类中存在抗生素抗性基因,然而这些人对抗生素的接触使用非常有限;其中 —— 四环素、氨苄青霉素、甲氧苄啶/磺胺甲恶唑、链霉素和氯霉素等抗生素的高水平获得性耐药。
进而研究发现,尽管没有使用过抗生素,但健康的人体内也有抗生素抗性基因——对从未接触过抗生素的健康婴儿和儿童进行的研究表明,存在对 β-内酰胺类、氟喹诺酮类、四环素类、大环内酯类、磺胺类药物或多种药物产生耐药性的基因。
该研究发现其肠球菌属、葡萄球菌属、克雷伯氏菌属、链球菌属和大肠杆菌/志贺氏菌属是 ARGs 的主要携带者。
以下,列举出可用于 ARGs 转移的各种可移动遗传元件:
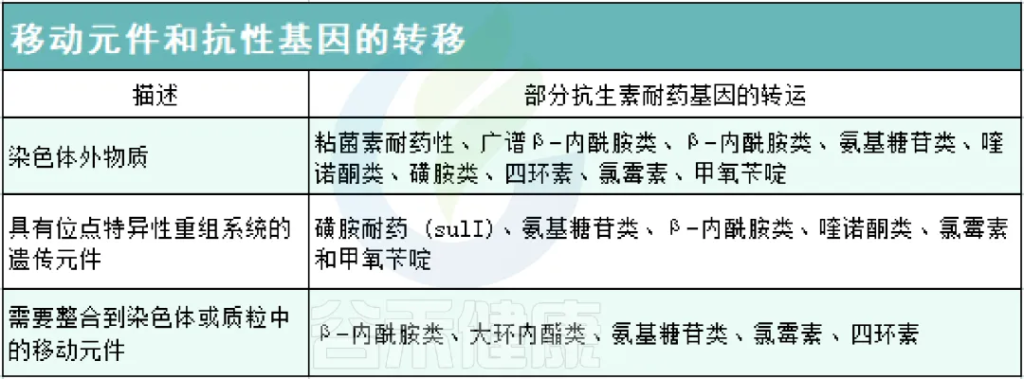
Patangia DV, et al., Microbiologyopen. 2022
抗生素可对宿主组织产生直接毒性作用,如 ——
线粒体损伤
抑制核糖体基因表达
哺乳动物细胞中的氧化组织损伤
该结论现今依旧存在一些争议。抗生素有时会使原本要治疗的病情变得恶化。许多 β-内酰胺类抗生素的杀菌作用会增加毒素的产生,例如 —— 从肠出血性大肠杆菌中释放的志贺毒素,使宿主更容易患溶血性尿毒症综合征。
抗生素还有可能直接影响宿主的代谢,无需微生物作为介质,同时会使目标病原体对抗生素的敏感性降低;宿主代谢物的这些变化大多发生在感染部位,其中包括高水平的 AMP,这会降低抗生素的功效并增加吞噬的活性。由于抗生素对免疫细胞呼吸活动的抑制作用,这可能会导致免疫功能的损伤。
以下,列举出可单独使用或在某些情况下与抗生素治疗联合使用的各种抗生素替代品:
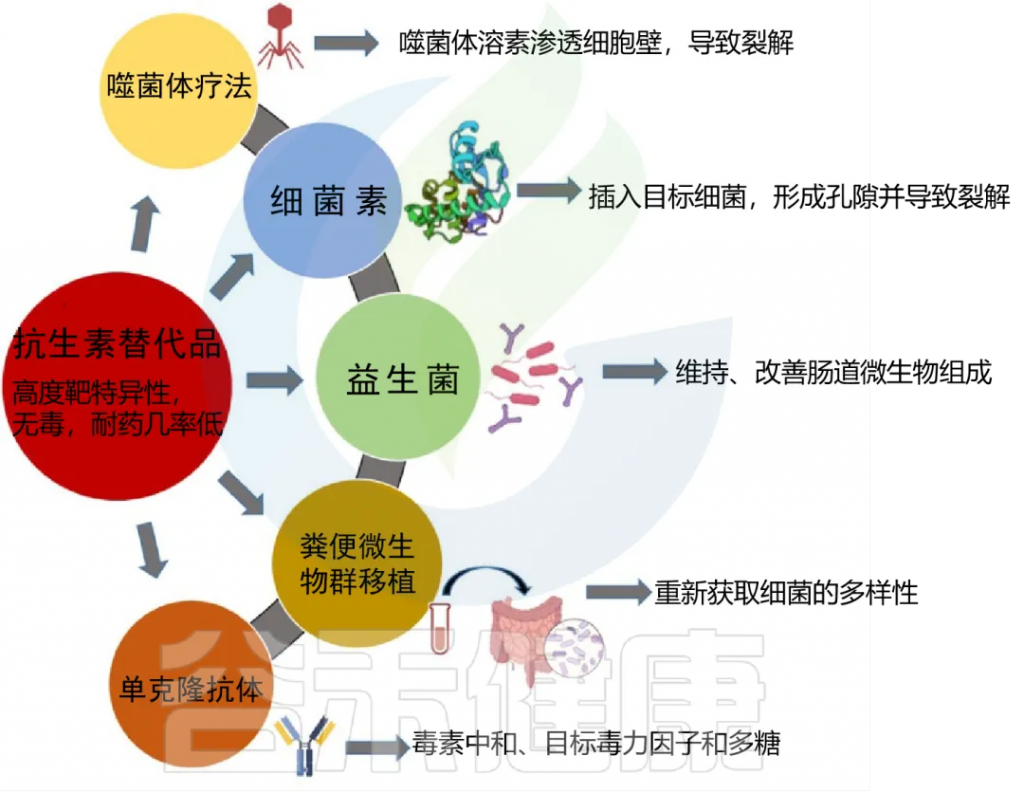

Patangia DV, et al., Microbiologyopen. 2022
因为抗生素的使用会导致微生物组成发生变化,很可能会对宿主产生有害的影响。为减少其影响,使用一些方法在使用抗生素后或与抗生素一起进行调节使用,得以更快地恢复其微生物群。
抗生素的使用其主要问题之一就是对于细菌耐药性的产生。目前正在研究诸如噬菌体(噬菌体) 疗法和细菌素等替代物作为抗生素的替代品或抗生素的补充疗法,以克服耐药性问题。
◆ 噬菌体疗法在1900年代初首次被提出和使用,但由于抗生素的引入,噬菌体疗法在西方医学中逐渐被摒弃,但在国外有部分国家仍旧使用着。随着抗生素耐药性危机的日益严重,需要对噬菌体疗法进行重新审视。
如今已经证明噬菌体疗法可以成功地治疗呼吸道铜绿假单胞菌的感染。随着使用特异性噬菌体疗法,逐步实现了对多重耐药鲍曼不动杆菌患者的感染进行了清除和成功治疗;以及对细菌性前列腺炎、败血症和急性肾损伤患者的病原体实现了临床症状的减轻以及根除。
对96名患者的伤口和溃疡的实验中有 67 名在噬菌体治疗后愈合,其愈合与病原体的减少有关;还在使用工程化噬菌体治疗耐药性脓肿分枝杆菌中显示了囊性纤维化患者的临床改善。对其进行深入研究后,发现使用噬菌体溶解蛋白作为抗菌化合物的方法,可以使噬菌体成为抗生素的强大抗菌竞争者。
◆ 细菌素 —— 另一类潜在的抗生素替代品,是由细菌产生的核糖体产生的抗菌肽,由于特定的免疫机制,细菌本身对杀伤肽免疫。迄今为止,细菌素在食品工业中主要用作食品安全剂和防腐剂;在动物研究中,细菌素作为抗菌剂已逐渐展示出期望的结果。
在小鼠模型的研究中,成功使用绿脓杆菌治疗铜绿假单胞菌肺部感染,其疗效并高无任何副作用;在给予产乳链菌肽和片球菌素的乳酸乳球菌和乳酸乳酸菌菌株有助于减少肠道内耐万古霉素的肠球菌定植。
细菌素已成功应用于治疗和预防牛乳腺炎,且其疗效与抗生素相当。此外,对由葡萄球菌引起乳腺炎的8名哺乳期女性的研究中,已经证明了乳酸链球菌肽可有效的对其进行治疗。
◆ 单克隆抗体作为替代品或与抗生素结合使用,也可以解决抗生素耐药性的问题。单克隆抗体绕过了毒性、耐药性发展和免疫系统早期清除的并发症,这在抗生素的情况下是可见的。使用单克隆抗体治疗细菌感染是近几年兴起的,在此之前,单克隆抗体主要用于治疗癌症、自身免疫性疾病或病毒感染。
在兔子身上进行实验研究表明,使用单克隆抗体bezlotoxumab对抗炭疽保护性抗原是成功的。奥比妥昔单抗的使用提高了接受致死剂量的炭疽芽孢杆菌孢子兔子的存活率;在一项 2655 名参与者的临床试验中,使用bezlotoxumab(抗艰难梭菌毒素的单克隆抗体) 治疗艰难梭菌感染可降低感染的复发率。进一步研究发现,从患者的 B 细胞中产生了一种单克隆抗体,用于对抗小鼠结核分枝杆菌的感染。
单克隆抗体比生产抗生素虽然成本更高,但有很许多好处 —— 相比较细菌素、噬菌体及其内溶素、单克隆抗体的主要优点之一是可以具有高度的靶标特异性,因此对微生物群的附带损害最小。对于这方面的研究,更多的是将用于改变医学上的使用。
◆ 益生菌被广泛的应用于此方面,如今已被证明其可以增加有益微生物的丰度,稳定微生物群落,从而减轻抗生素的影响。
益生菌是通过促进抗菌肽的产生、从而产生细菌素,通过争夺肠道黏膜上的营养物质和受体来抑制非共生菌的生长、增强肠道屏障功能和调节免疫力来发挥作用的,但使用益生菌可能不能够让肠道微生物群完全恢复如初。
◆ FMT更有利于恢复肠道中的微生物平衡。FMT已被广泛用于医疗性的重平衡艰难梭菌感染患者的微生物群,恢复其微生物群和代谢活性。
FMT还可以在抗生素治疗前利用患者自身的供体粪便,称为自体FMT。由于如疗效、成本和适用性等多种因素,使选择FMT成为了一个极具发展性的选择,但具体的使用还需要详细的研究来进行优化,并对其进一步进行肠道疾病以外的其他应用可能性的研发。
人体还可以通过合理的饮食调节和健康的作息安排来控制自身的微生物群,从长远来看,自身的调控会保持机体持续的健康,且对预防炎症疾病起到很好的作用。
以上对于肠道菌群在宿主代谢和免疫功能(如免疫发育、定植抗性、细胞信号传导) 中的重要性;抗生素在单个细菌细胞水平上的影响,其使用和滥用会导致耐药性的发生以及抗生素治疗的替代方法进行了说明。
在先进的组学技术的帮助下,宿主和微生物群之间复杂的相互作用现在变得清晰起来。抗生素会破坏微生物平衡,从而破坏细菌群落内相互关系,以及影响其与宿主之间的关联,并因此产生的耐药菌使临床治疗变得困难。
由于宿主和微生物群之间的这种复杂联系,目前对抗生素需要遵循严谨的使用规范,而;另一方面,对抗生素替代品的研究以及应用是重点,要同时满足限制替代品所附带的损害。研究出可以维持和改善宿主健康并在使用时尽量减少抗生素影响的治疗方法。
主要参考文献:
Abrams, G. D., & Bishop, J. E. (1967). Effect of the normal microbial flora on gastrointestinal motility. Proceedings of the Society for Experimental Biology and Medicine, 126(1), 301– 304.
Adedeji, W. A. (2016). The treasure called antibiotics. Annals of Ibadan Postgraduate Medicine, 14(2), 56– 57.
Adriaenssens, N., Coenen, S., Versporten, A., Muller, A., Minalu, G., Faes, C., Vankerckhoven, V., Aerts, M., Hens, N., Molenberghs, G., & Goossens, H., ESAC Project Group. (2011). European surveillance of antimicrobial consumption (ESAC): Outpatient antibiotic use in Europe (1997-2009). Journal of Antimicrobial Chemotherapy, 66(Suppl. 6), 3– 12.
Akhavan, B. J., Khanna, N. R., & Vijhani, P. (2020). Amoxicillin, StatPearls [Internet]. StatPearls Publishing.
Allegretti, J. R., Mullish, B. H., Kelly, C., & Fischer, M. (2019). The evolution of the use of faecal microbiota transplantation and emerging therapeutic indications. The Lancet, 394(10196), 420– 431.
Aagaard, K., Ma, J., Antony, K. M., Ganu, R., Petrosino, J., & Versalovic, J. (2014). The placenta harbors a unique microbiome. Science Translational Medicine, 6(237), 237ra65.
Blaser, M. (2011). Stop the killing of beneficial bacteria. Nature, 476(7361), 393– 394.
Brestoff, J., & Artis, D. (2013). Population genetic tools to dissect innate immunity in humans. Nature Immunology, 14(7), 676– 684.
Brugman, S., Klatter, F. A., Visser, J. T., Wildeboer-Veloo, A. C., Harmsen, H. J., Rozing, J., & Bos, N. A. (2006). Antibiotic treatment partially protects against type 1 diabetes in the bio-breeding diabetes-prone rat. Is the gut flora involved in the development of type 1 diabetes? Diabetologia, 49(9), 2105– 2108.
Bui, T., & Preuss, C. V. (2021). Cephalosporins, StatPearls [Internet]. StatPearls Publishing.
Cahenzli, J., Köller, Y., Wyss, M., Geuking, M. B., & McCoy, K. D. (2013). Intestinal microbial diversity during early-life colonization shapes long-term IgE levels. Cell Host and Microbe, 14(5), 559– 570.
Cao, F., Wang, X., Wang, L., Li, Z., Che, J., Wang, L., Li, X., Cao, Z., Zhang, J., Jin, L., & Xu, Y. (2015). Evaluation of the efficacy of a bacteriophage in the treatment of pneumonia induced by multidrug resistance Klebsiella pneumoniae in mice. BioMed Research International, 2015, 2015– 2019.
Cao, L. T., Wu, J. Q., Xie, F., Hu, S. H., & Mo, Y. (2007). Efficacy of nisin in treatment of clinical mastitis in lactating dairy cows. Journal of Dairy Science, 90(8), 3980– 3985.
Cash, H. L., Whitham, C. V., Behrendt, C. L., & Hooper, L. V. (2006). ‘Symbiotic bacteria direct expression of an intestinal bactericidal lectin’. Science, 313(5790), 1126– 1130.
Chaves, B. J., & Tadi, P. (2021). Gentamicin, StatPearls [Internet]. StatPearls Publishing.
Centre for Disease Control (CDC). (2017). Pediatric treatment recommendations.
Aloisio, I., Quagliariello, A., De Fanti, S., Luiselli, D., De Filippo, C., Albanese, D., Corvaglia, L. T., Faldella, G., & Di Gioia, D. (2016). Evaluation of the effects of intrapartum antibiotic prophylaxis on newborn intestinal microbiota using a sequencing approach targeted to multi hypervariable 16S rDNA regions. Applied Microbiology and Biotechnology, 100(12), 5537– 5546.
Arboleya, S., Binetti, A., Salazar, N., Fernández, N., Solís, G., Hernández-Barranco, A., Margolles, A., los Reyes-Gavilán, C. G., & Gueimonde, M. (2012). Establishment and development of intestinal microbiota in preterm neonates. FEMS Microbiology Ecology, 79(3), 763– 772.

谷禾健康

随着工业革命的发展,城市化进程的加快和经济的发展导致能源消耗和废物排放激增,在过去的几十年里,环境污染物已成为一种日益普遍的健康危害。
最近的研究还表明,人类微生物组可以代谢环境化学物质,进而可能会受到化学物质暴露的影响。
这种直接相互作用表明,在风险评估中可能需要考虑微生物组。
目前越来越多的证据表明,接触这些环境化学物质是导致多种健康障碍发展的重要因素之一。例如,体外、体内和流行病学研究已将人类暴露于内分泌干扰的化学物质与肥胖、代谢综合征和 2 型糖尿病联系起来。
此外,接触环境污染物与产前缺陷、呼吸系统疾病、心脏病和精神障碍以及患癌可能性增加和预期寿命缩短有关,而胃肠道微生物群对各种宿主代谢和免疫功能起着至关重要的作用。
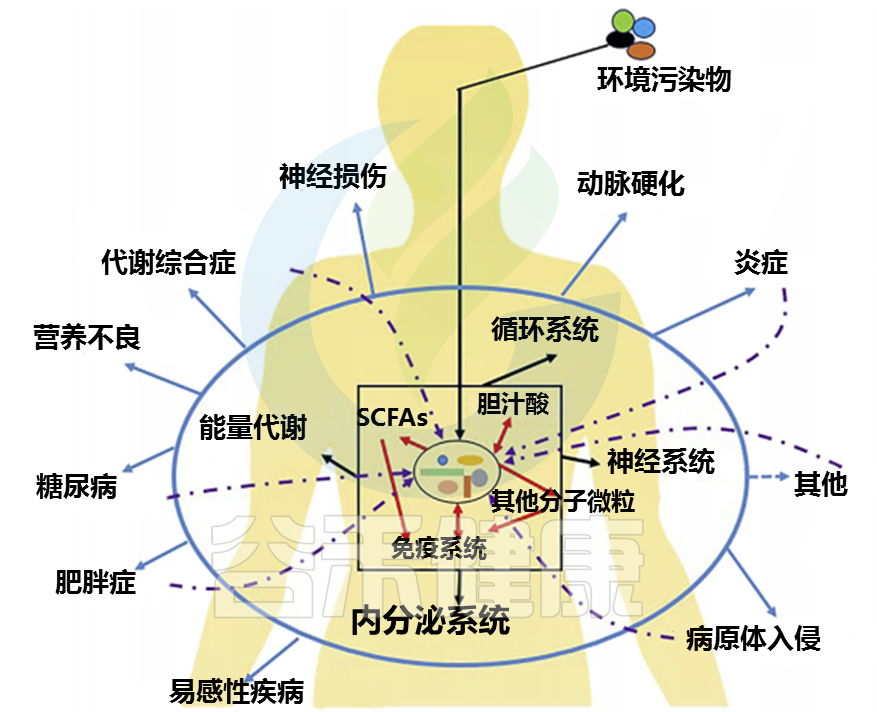
Jin Y et al. Environ Pollut. 2017.
尽管大多数环境污染物并不直接针对肠道微生物群,但一些污染物可以通过不同途径进入人体并与肠道微生物群相互作用。
先前的多项研究表明,暴露于环境污染物会改变肠道微生物群的组成,导致能量代谢、营养吸收和免疫系统功能障碍或产生其他毒性症状。有人提出胃肠道微生物可能通过改变环境化学物质的吸收、处置、代谢和排泄来影响肥胖和糖尿病等疾病。
肠道微生物群对药物、饮食以及环境污染物都非常敏感,包括抗生素、重金属、持久性有机污染物、杀虫剂、纳米材料和食品添加剂等。
环境污染物可能对肠道微生物群的影响及其对健康的产生后续影响。
我们每个人的肠道中都携带着数千种细菌以及一些其他类型的微生物。虽然说所有人都具有非常相似的微生物群,但没有两个人的肠道中细菌种类的组成完全相同,换句话说,每个人的微生物群可能会像指纹一样独特。
不过,不同的细菌物种在人与人之间可能存在很大差异,但这些物种往往编码相同的代谢途径。
通过查阅文献得出肠道微生物具有广泛的代谢环境化学物质的能力,污染物的细菌依赖性代谢会调节宿主的毒性。相反,来自各种化学家族的环境污染物已被证明会改变胃肠道细菌的组成和/或代谢活动,这可能是影响个体微生物群的重要因素。
直接代谢排出
几十年来,人们已经知道胃肠道微生物参与异生物质的生物转化。
注:异生物质,是指由人工合成的化学物质。如农药、洗涤剂及化工原料等,其中各种合成农药占绝大多数。异生物质是对身体来说是异物的物质。
早在 1973 年,Scheline 就提出,胃肠道微生物群代谢外来化合物的潜力与肝脏不差上下。此后已为胃肠道微生物群鉴定了 40 多种药物底物,并强调肠道微生物对药物进行多种化学转化的能力,包括:
还原、水解、琥珀酸基团的去除、脱羟基、乙酰化、脱乙酰、N-氧化物键的裂解、蛋白水解、脱硝、解偶联、噻唑开环、去糖基化、去甲基化
胃肠道是异生物质进入人体的主要途径。细菌代谢的速率和程度受到达远端肠道的异生物质数量的影响,在那里细菌丰度最高。环境化学物质在摄入后可能吸收不良,随后被蠕动扫到远端小肠和盲肠,或者,它们及其代谢物可能会穿过肠壁从血液中分离出来。因此,许多化学物质可以被胃肠道微生物群直接代谢。
环境化学物质(或其代谢物)也可能从胆汁中排出。大多数外源性物质是非极性的,因此在胃肠道中被吸收并通过门静脉血输送到肝脏进行解毒。肝脏通常氧化异生素并产生葡萄糖醛酸、硫酸盐或谷胱甘肽结合物。在大多数情况下,结合反应促进排泄,结合物从尿液中消除。
然而,结合物也可以在胆汁中排泄。决定一种化学物质是否排泄到胆汁中的因素尚不完全清楚,一般规则是低分子量化合物 (<325 kDa) 很少排泄到胆汁中,而较高分子量 (>325) 的化合物可以显着排出。分泌到胆汁中的结合物进入小肠,那些未被吸收的向下移动到大肠,在那里它们可能被微生物群代谢。
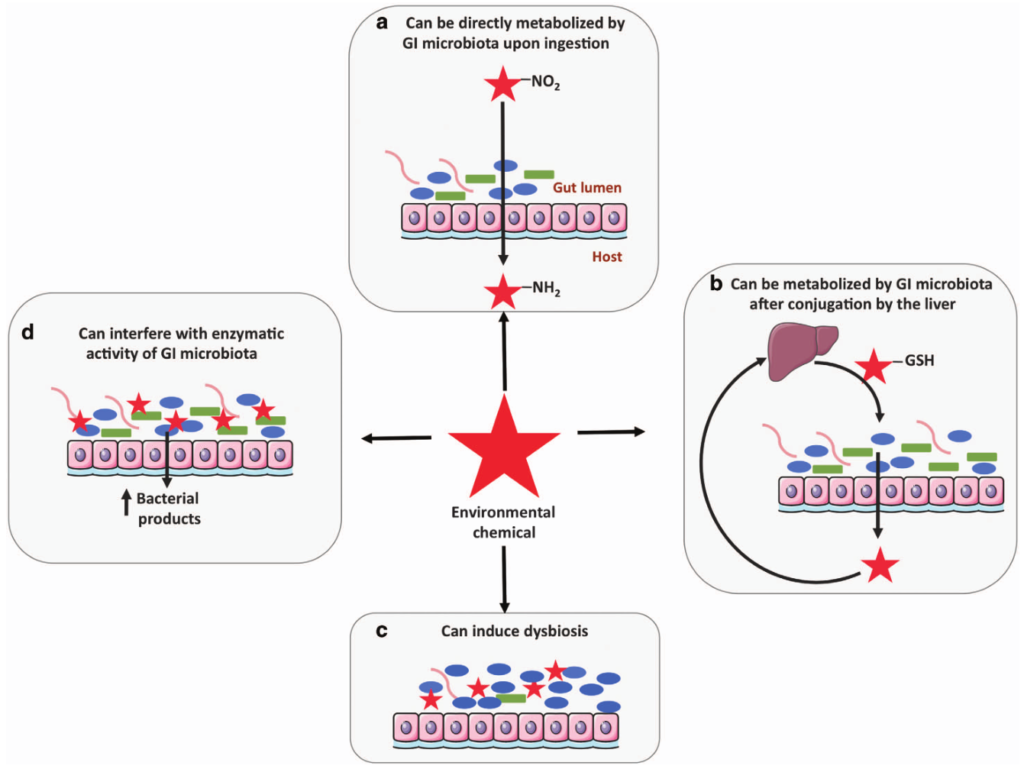
Claus SP et al. NPJ Biofilms Microbiomes, 2016
解偶联,形成肝脏循环
胃肠道微生物群可以通过解偶联并减少肝脏异生物质代谢物,导致形成低分子量的非极性分子,这些分子很容易被重吸收。这些非极性分子的重吸收和它们返回肝脏被称为“肠肝循环”。肝肠循环控制着体内内源性底物(如胆汁酸和类固醇)的储存和再利用。然而,它也延迟了体内环境化学物质的消除。
胃肠道细菌介导的环境异生物质转化的例子, 如下:
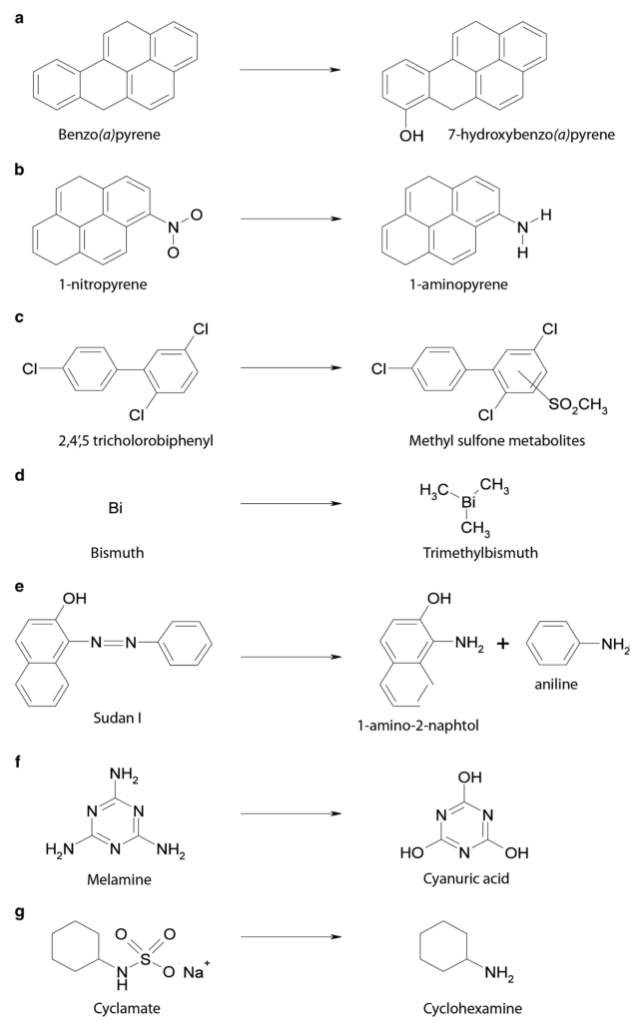
Claus SP et al., NPJ Biofilms Microbiomes, 2016
胃肠道微生物群的异生物质代谢酶
尽管已经将各种化学反应归因于胃肠道微生物,但只有少数酶家族被确定为胃肠道微生物异生物质代谢。
主要偶氮还原酶、nitroreductases、β-葡糖醛酸酶、硫酸酯酶和β-裂解酶。
胃肠道微生物群的异生物质代谢酶,如下:
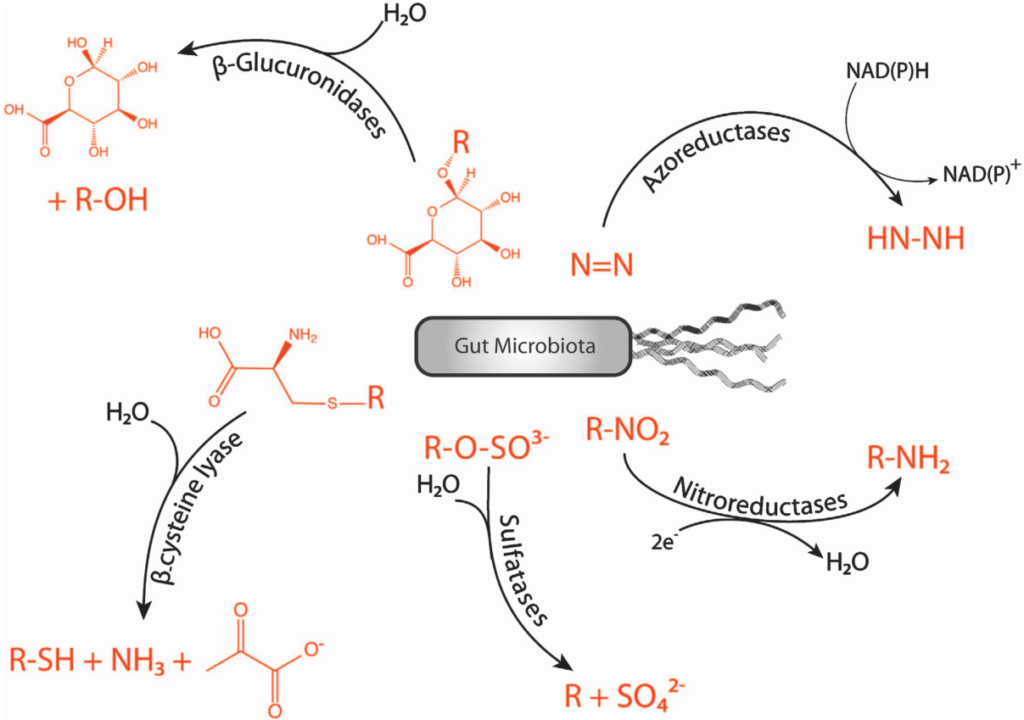
(i) 偶氮 (N=N) 键的还原裂解由细菌偶氮还原酶进行。
(ii) 细菌硝基还原酶还原硝基 (–NO2) 官能团到相应的胺。
(iii) 内源性硫酸酯在胃肠道中被细菌来源的硫酸酯酶水解。
(iv) 异生素的谷胱甘肽结合物也大量排泄在胆汁中。它们被各种哺乳动物酶(γ-谷氨酰转肽酶和羧肽酶)降解,形成半胱氨酸结合物。这些半胱氨酸结合物可能会到达含有 ß-裂解酶活性的胃肠道的一部分,并转化为相应的硫醇。
(v) β-葡糖醛酸酶存在于整个胃肠道中,并在异生物质葡糖醛酸苷的水解中发挥作用,异生物质葡糖苷酸是胆汁中排泄的最大一类异生物质结合物。肠道微生物被认为是 ß-葡萄糖醛酸酶的主要来源。
肠道细菌和人体细胞合作,制造生命所需的酶
据 NIEHS 科学家领导的一个团队称,人类肠道中的细菌与人体细胞合作,制造出一种生命必不可少的分子。烟酰胺腺嘌呤二核苷酸 (NAD) 分子是细胞生存必须完成的数百个生化反应所必需的。
研究人员还发现,一些肿瘤内的细菌保护肿瘤免受靶向 NAD 的抗癌药物的侵害。研究结果于2020年3 月 3 日在线发表在 Cell Metabolism 上。
该研究的主要作者指出,NAD 水平会随着哺乳动物的年龄增长而降低。他说有些人服用补充剂来促进 NAD 的产生。Shats 解释说,他的小组的最新研究表明,这些化合物的功效取决于肠道微生物群。
“如果你的肠道细菌没有发现负责促进 NAD 合成的酶,那么补充剂的效率就会低得多”。
内分泌干扰化学物质 (EDC) 由一大类化学物质组成,这些化学物质会改变内分泌系统并影响人类的发育和繁殖。EDC 的来源包括工业化学品、药品和个人护理产品、除草剂、有机氯杀虫剂和添加剂等。
EDC 被美国环境保护署描述为外源性因素,因为它可以干扰内源性激素,从而解除对发育过程的管制。由于内分泌系统对器官的影响,EDCs对身体具有深远的全身影响。EDC 已通过消化道对动物和人类健康产生不利影响,例如炎症、代谢紊乱、先天性异常,菌群失调。
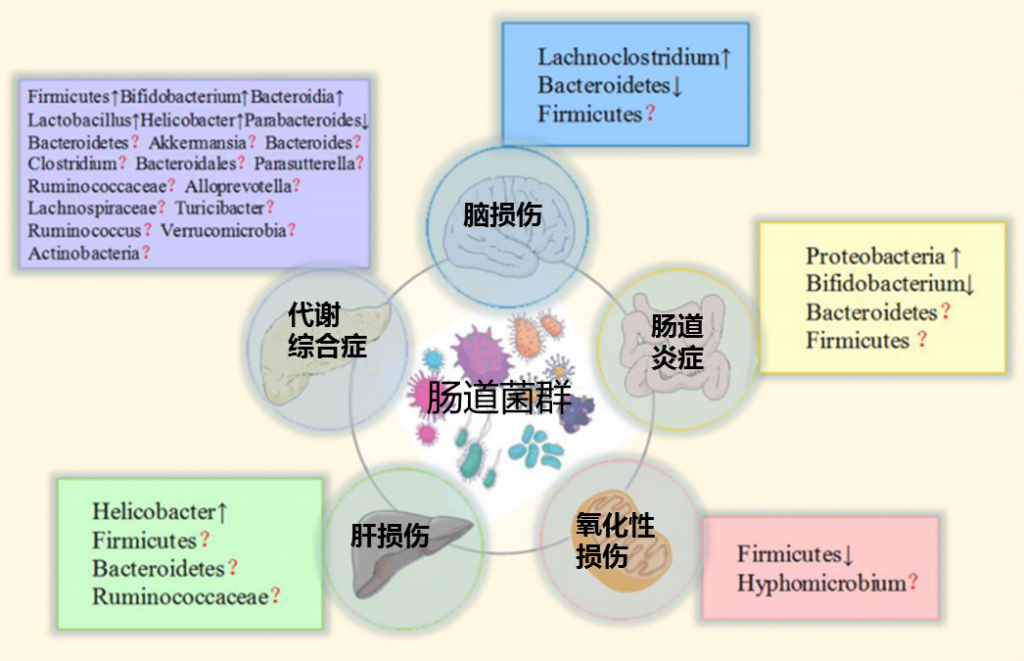
Li N, et al. Environ Pollut. 2021
抗生素:直接改变或者杀死微生物
我们现在知道人类和动物除了故意给药外,还可以通过多种途径被动摄入抗生素。通常,抗生素可以对微生物造成直接的影响。因此,即使某些抗生素的浓度非常低,动物肠道微生物群的组成也可能发生变化。人们越来越注意到,环境抗生素引起的肠道菌群失调与人类健康密切相关。
在过去的 50 年中,全世界开发了大量抗生素用于人类和兽医学。由于它们在人和动物体内的吸收不完全,部分摄入的抗生素通过粪便或尿液排出到环境中。
越来越多的研究发现,在中国和其他国家的河流和湖泊沉积物、地表水、农业土壤和废水等自然环境中发现了高浓度的各种抗生素。

先前的研究发现,抗生素治疗并没有减少肠道微生物群的总数,而是改变了人类和动物中某些物种的相对数量。此外,抗生素暴露通常会通过增加或减少多样性来改变微生物组的多样性。
更重要的是,抗生素对人类肠道微生物群的影响可持续数年。如克拉霉素和甲硝唑治疗持续改变肠道微生物群组成长达 4 年。婴儿完成抗生素治疗后,虽然微生物群组成的某些方面恢复到治疗前的水平,但某些细菌种类的丰度发生了永久性改变。这种变化对婴儿有害,扰乱他们的早期发育。值得注意的是,不同的环丙沙星治疗对个体微生物群影响也略有不同。
在生命早期向小鼠施用低剂量的青霉素,可通过降低乳酸菌Lactobacillus, Candidatus, Arthromitus, Allobaculum的水平来增强代谢表型并促进脂质积累。另一份报告显示,给小鼠服用青霉素 G、红霉素或两者结合可以增加脂质积累并诱导炎症反应。所有这些处理都降低了拟杆菌属/厚壁菌门的比率。
接触某些抗生素可能会加重某些疾病的严重程度。例如,艰难梭菌是抗生素引起的腹泻的主要原因,它会大大增加住院患者的发病率和死亡率。
用克林霉素和氨苄青霉素这两种最常用的抗生素进行治疗,通过减少 Clostridium scindens菌(胆汁酸代谢的二级调节剂)来增加患者对艰难梭菌感染的易感性。
链霉素治疗可以增加Porphyromonadaceae 和 Bacteroidaceae 两个科的水平,它们的存在与小鼠对肺炎和结肠炎的易感性或超敏性呈正相关。
甲硝唑治疗减少了小鼠结肠的内部粘液层,从而通过减少厌氧拟杆菌的组成,以及增加包括乳酸杆菌在内的耐氧细菌的组成来增加对柠檬酸杆菌引起的结肠炎的易感性。
抗生素治疗还增加了大肠杆菌等病原菌的入侵,抗生素治疗后肠道微生物群中富集了抗生素抗性基因,造成抗生素抗性。
由于使用抗生素治疗,一些非微生物驱动的疾病会更频繁地发生。

在生命早期给小鼠施用万古霉素会通过增加乳杆菌科和疣微菌科的丰度来增强过敏性哮喘,并且这些微生物群的变化与 Treg 细胞减少有关。
最近,一项研究报告称,口服链霉素、粘菌素和氨苄青霉素的组合或单独使用万古霉素治疗会增加小鼠胰腺 b 细胞死亡和 I 型糖尿病的发病率。
万古霉素处理小鼠在属水平上增加了埃希氏菌、乳杆菌和 Sutterella 的水平,并减少了属于梭菌目和毛螺菌科、普氏菌科和 Rikenellaceae 科的细菌。联合抗生素治疗导致肠道微生物群几乎完全消失。这些微生物组结构变化与回肠和结肠固有层中产生白细胞介素 (IL)17 的细胞的出现密切相关,表明肠道微生物群在免疫稳态中发挥着非常重要的作用。
然而,抗生素引起的肠道微生物群的改变有时对疾病有益。囊性纤维化是一种常染色体隐性疾病,可导致肠道细菌过度生长。链霉素治疗小鼠 9 周通过减少肠道细菌过度生长、通过降低乳酸杆菌丰度来调节 T 细胞谱以及增加肺和肠系膜淋巴结中的免疫细胞水平来改善这种疾病。
对肝硬化患者施用利福昔明可降低韦荣球菌科的丰度并增加真杆菌科的丰度。这些微生物组成的变化改变了患者的代谢特征并降低了疾病的严重程度。诺氟沙星可以减少肝硬化患者的细菌移位,改善肠道屏障功能,从而降低自发性细菌性腹膜炎的风险。
总之,抗生素很容易引起肠道微生物群失调,并对健康产生不利影响。人类和动物可能会长期被动地暴露于环境中低浓度的抗生素中。因此,环境衍生的抗生素对人和动物的健康风险不容忽视。
重金属:导致肠道微生物群失调
近年来,环境中的重金属已成为严重的健康风险。作为一种常见的环境污染形式,重金属与多种毒性作用有关,包括致癌作用、氧化应激和 DNA 损伤,以及对免疫系统的影响。最近,几项研究表明,重金属暴露也可能导致肠道微生物群失调。
砷 (As) 是一种已知的致癌物质,是一种常见的有毒污染物,广泛分布在我们的环境中。砷通常以砷酸盐 [As(V)] 的形式附着在固体表面上。摄入 As(V) 后,肠道微生物群暴露于砷会诱导 As 硫醇化和甲基化。

据此前报道,砷暴露与多种疾病有关,如皮肤癌、膀胱癌、肺癌和肝癌;糖尿病; 和心血管疾病。此外,暴露于 10 mg/L 砷 4 周会显着扰乱小鼠的微生物组组成和代谢组学特征。一般而言,As 暴露后厚壁菌门的丰度显着下降,而拟杆菌门的丰度显着增加。
还观察到这些变化与脂质代谢物、含吲哚的代谢物、异黄酮代谢物和胆汁酸代谢物密切相关。长期接触砷会导致结肠微生物组的结构和组成发生变化,并促进雄性小鼠宿主的氮和氨基酸代谢。
镉 (Cd) 经常且广泛地用于制造许多产品,例如电池、金属电镀、颜料和塑料。在一些国家,尤其是中国等发展中国家,在水生系统、沉积物和土壤中观察到高浓度的 Cd。
据报道,镉毒性与致癌作用、肝毒性、氧化应激和免疫毒性有关。最近,研究报告雄性小鼠亚慢性暴露于低剂量 Cd(饮用水中 10 毫克/升)10 周会降低厚壁菌门和变形菌门的相对丰度,并增加盲肠和粪便中拟杆菌门的相对丰度。肠道微生物组组成的这些变化与雄性小鼠血清中脂多糖 (LPS) 水平升高、肝脏炎症甚至能量代谢失调有关。
铅 (Pb) 也是一种剧毒金属,疾病控制和预防中心非常重视。事实上,环境铅是一种普遍存在的全球健康危害,因为它广泛用于各种消费品,例如汽油中的四乙基铅。由于它在空气、土壤、水、旧油漆和食物中的持久性,人类和动物可以通过摄入、吸入和皮肤吸收吸收铅。铅中毒还通过其能量产生和其他代谢过程的中断而与肥胖的发展有关。
最近的一份报告显示,围产期铅暴露(饮用水中 32 毫克/升)持续 40 周会导致成年雄性小鼠体重增加,但不会导致雌性小鼠体重增加。接触铅后微生物组中没有观察到拟杆菌/厚壁菌的比例下降; Desulfovibrionaceae、Barnesiella 和 Clostridium XIVb的丰度在科水平上有所增加;接触铅后,乳球菌、肠杆菌和柄杆菌Caulobacterales的丰度下降。此外,Akkermansia nuciniphila在暴露于铅的小鼠中。
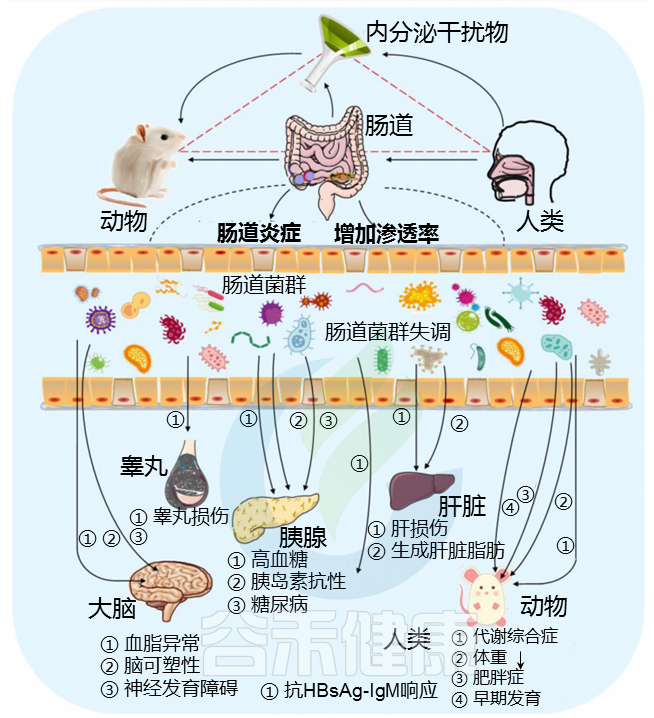
Li N, et al. Environ Pollut. 2021
持久性有机污染物:改变微生物组成,导致炎症
持久性有机污染物 (POPs) 包括有机氯农药、多氯联苯 (PCBs)、多溴联苯醚和多环芳烃 (PAHs) 是合成化合物,具有持久性、半挥发性和高毒性,可在生物组织中积累。
持久性有机污染物受到了特别关注,因为它们是导致近年来全球肥胖、糖尿病、自身免疫疾病和一些发育障碍发病率上升的众多因素之一。摄入食物和水被认为是主要的 POP 接触途径。
PCB 是一种致癌物质,因其介电特性和化学稳定性而被用于制造电容器、变压器、冷却液、液压油和润滑剂。PCBs 可以在小鼠暴露后 2 天内显着改变肠道微生物群的组成。
肠道中的产气荚膜梭菌(Clostridium perfringens)和拜氏梭菌(Clostridium beijerinckii )可以通过去除氯原子和打开苯环来降解多氯联苯。
暴露于一种 PCB,2, 3, 7, 8 四氯二苯并呋喃 (TCDF),以 24 毫克/公斤体重的剂量连续 5 天会降低厚壁菌门/拟杆菌门的比率,增加黄杆菌(Flavobacteria)的水平,并降低盲肠中的梭菌。
这些微生物群组成的变化与胆汁酸代谢的改变有关。此外,在分子水平上,TCDF 还可以抑制法尼醇 X 受体 (FXR) 信号通路,由于细菌发酵而引发宿主体内显着的炎症和代谢紊乱。此外,TCDF 诱导的变化以芳烃受体 (AHR) 依赖性方式发生。
PAH 被认为是高度优先的环境污染物,因为它们对人类具有毒性、致癌性和假定的雌激素或抗雌激素特性。人类接触高分子量多环芳烃的途径主要是通过口服炭烤、烤和熏肉或摄入未清洁干净的蔬菜。
摄入的多环芳烃到达小肠肠细胞和肝脏肝细胞并作为 AHR 配体。此外,结肠中的微生物群可以催化多环芳烃转化为雌激素。这种生物活化可能是 PAH 毒性的潜在机制。另一种 AHR 调节剂二恶英也有可能影响小鼠肠道微生物组的组成。
最近, 据报道,2, 3, 7, 8-四氯二苯-对-二恶英 (TCDD) 给药(6 毫克/千克体重)26 周显着增加厚壁菌门的丰度并降低拟杆菌门的丰度。在科水平上,TCDD暴露后粪便中乳酸杆菌科和脱硫弧菌科的含量显着增加,普氏菌科的含量下降。这些肠道微生物组的变化与链脲佐菌素诱导的高血糖小鼠的肝脏和免疫毒性相关。
农药/杀虫剂:改变微生物组成
农药残留是一个长期存在且严重的环境问题,因为在食品材料、水和土壤中检测到了大量农药。近年来,关于农药对动物影响的健康问题也有所增加。由于某些杀虫剂的抗菌活性,杀虫剂有可能改变肠道微生物组并诱发动物的其他症状。
氯菊酯 (PEM) 是最具代表性的拟除虫菊酯化合物之一,在低剂量和长期治疗的情况下(Nasuti 等人,2016)可以降低拟杆菌、普氏菌和卟啉单胞菌的丰度,并增加肠杆菌科和乳杆菌的丰度。肠道微生物群的这些变化可能导致 PEM 的神经毒性。
五氯苯酚 (PCP) 是世界范围内广泛使用的农药。即使在非常低的浓度下,五氯苯酚暴露也会导致水生动物的遗传和生殖毒性。PCP可在鱼类肝脏和肠道内蓄积,抑制鱼类生长,引起肝脏氧化和组织病理学损伤。此外,在金鱼中,接触五氯苯酚 (100 毫克/升) 28 天也通过降低厚壁菌门/拟杆菌门的比率来改变微生物组的组成。拟杆菌的相对丰度增加,金黄色杆菌、微杆菌、节杆菌和军团菌的相对丰度在属水平上下降。
环氧环唑 (EPO) 是一种广谱唑类杀菌剂,可有效防治小麦叶斑病 (Septoria tritici) 和锈病 (Puccinia triticina),被广泛用作农业抗真菌剂。据报道,EPO 对大鼠具有胎儿毒性作用,这与母体血浆中睾酮增加和雌二醇减少密切相关。
当大鼠以高剂量 EPO饮食喂养 90 天时,粪便中厚壁菌门的相对丰度下降,拟杆菌门和变形菌门的相对丰度增加。此外,毛螺菌科和肠杆菌科的相对数量被选择性地富集。作者进一步指出这些由 EPO 引起的微生物群组成的改变与肝功能受损有关。
毒死蜱 (CPF) 是一种有机磷杀虫剂,常用于处理水果、蔬菜作物和葡萄园。
CPF 可以被肝脏和肠道中的细胞色素 P450 酶代谢。围产期 CPF 暴露降低了幼鼠的体重和身长,并抑制了它们的肠道发育。
此外,CPF 诱导较高水平的拟杆菌、肠球菌和梭状芽孢杆菌,同时导致较低水平的乳杆菌属和双歧杆菌属。CPF 诱导的微生物群失调会破坏粘膜屏障,增加细菌易位,并刺激先天免疫系统。
多菌灵(CBZ;2-苯并咪唑氨基甲酸甲酯)是一种内吸性广谱苯并咪唑杀菌剂,被广泛用于防治真菌病害。 CBZ 对健康有多种不利影响,例如肝脏氧化应激和水肿、生殖毒性和内分泌紊乱。
在最近的一项研究中,我们观察到,以高剂量向小鼠口服 CBZ 28 天会增加肝脏脂质积累和体重,此外还会增加血清中促炎细胞因子 IL-1b 和 IL-6 的水平。
这些变化与 CBZ 诱导的肠道微生物群失调有关,包括在门水平上拟杆菌的相对水平降低和厚壁菌、变形菌和放线菌的相对水平增加。在科水平上,脱硫弧菌科、瘤胃球菌科、毛螺菌科和去铁杆菌科的相对丰度增加,而S24-7、副普雷沃氏菌科、瑞肯菌科、普雷沃氏菌科、拟杆菌科、卟啉单胞菌科、金银藻科(Christensencealae)的相对丰度减少。
最近,口服暴露(100 毫克/公斤体重)至 IMZ 28 天可导致小鼠肠道微生物群失调和结肠炎症。在盲肠中,49.3% 的细菌在 IMZ 暴露后发生了变化。在门水平上,拟杆菌、变形菌和蓝藻的丰度下降,而绿弯菌Chloroflexi、厚壁菌、放线菌和酸杆菌的丰度增加。在属水平上,梭菌、毛螺菌科、螺杆菌科和螺杆菌的丰度显着增加,而S24-7、理肯菌科、普氏菌、厌氧菌和柠檬酸杆菌的丰度显着降低。
微塑料:诱发肠道菌群失调和炎症
全球塑料污染问题太普遍了,因为塑料的大规模生产在过去 70 年左右的时间里呈爆炸式增长,从每年约 200 万吨增加到约 3.8 亿吨。每年约有 800 万吨塑料到海洋中,塑料碎片为水生环境中的微生物提供了稳定的基质和新的生态位,被称为“塑料圈”。

塑料降解的自然过程非常缓慢。例如,一个 PET 瓶的寿命可能长达数百年。这为环境中存在的各种微生物对这些化合物做出反应提供了足够的进化时间,并且在之前的研究中发现了许多不同的酶,它们具有降解不同塑料的能力。
在塑料污染严重的地方,更多的微生物可以降解塑料。具有降解塑料能力的微生物酶的数量正在增加,这与当地塑料污染水平有关。
最近发表在科学杂志mBIO 上的这项新研究分析了来自世界各地数百个地点的环境 DNA 样本。研究人员使用计算机建模来搜索具有塑料降解潜力的微生物酶,在污染最严重的地区增加酶的数量增加,换句话说,塑料降解酶的数量和多样性正在增加,直接响应当地的塑料污染水平。
总共发现了超过 30,000 种酶“同源物”,它们有可能降解 10 种不同类型的常用塑料。同源物是具有相似特性的蛋白质序列的成员。一些含量最高的地点是众所周知的高污染地区,例如来自地中海和南太平洋的样本。
这么多不同的微生物和环境栖息地中发现如此多的酶。这是一个令人惊讶的发现,真正说明了问题的严重性,这也说明对抗全球塑料危机的潜在途径。
塑料造成的环境污染已成为公共卫生问题。然而,微塑料对肠道微生物群、炎症发展及其潜在机制的影响尚未得到很好的表征。
用高浓度的微塑料处理增加了肠道微生物种类的数量、细菌丰度和菌群多样性。喂养组显示葡萄球菌丰度显着增加,同时副杆菌属显着减少丰度,与空白(未处理)组相比。此外,所有喂养组血清白细胞介素1α水平均显着高于空白组。
值得注意的是,微塑料处理降低了 CD4 +细胞中 Th17 和 Treg 细胞的百分比,而在 Th17/Treg 细胞比率方面,空白组和处理组之间没有观察到显着差异。喂食高浓度微塑料的小鼠的肠道(结肠和十二指肠)表现出明显的炎症和较高的 TLR4、AP-1 和 IRF5 表达。因此,聚乙烯微塑料可诱发肠道菌群失调和炎症,为微塑料相关疾病的防治提供了理论依据。
大多数塑料碎片上定植的细菌多样性高于周围水域。塑料碎片也可能比周围的水积累更多的潜在病原体。源头追踪结果表明,下游塑料圈从上游继承的细菌类群比例远高于浮游细菌。下游水中约 92.3-99.7% 的细菌群落不是来自上游,而是来自下游人类活动的输入。相反,下游塑料圈中高比例的细菌分类群与上游密切相关。塑料圈比浮游细菌具有更高的生态功能多样性。
城市和下游农业和水产养殖业的密集人类活动对乌鲁木齐河微生物群结构和功能群有很大影响。Pastisphere 群落比浮游细菌更能抵抗人类干扰。与周围的水相比,塑料圈增加了上游微生物结构和功能的遗传,也增加了下游水中病原体的存活和繁殖,其中含有高浓度的抗生素。
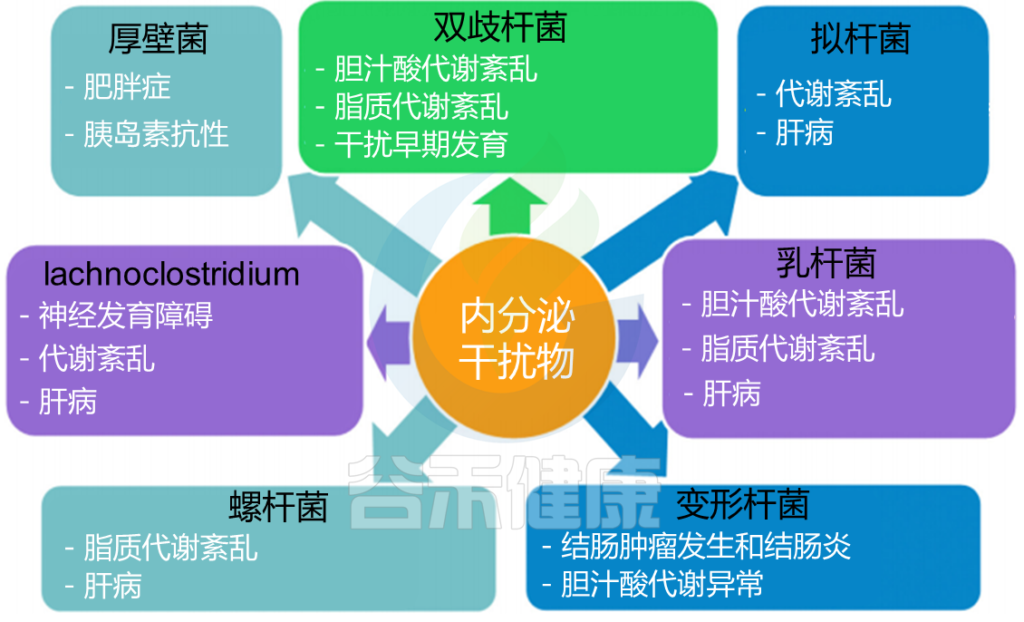
Li N, et al. Environ Pollut. 2021
空气污染物:增加肠道通透性
空气污染是指空气中可能由自然和人类活动导致的有害物质的存在。空气污染是一种复杂的气体混合物(包括臭氧、二氧化碳、二氧化硫、一氧化碳和二氧化氮)、颗粒物,包括化石燃料/汽车尾气的燃烧、多环芳烃/PAHS、花粉、孢子、微生物颗粒、矿物粉尘、有机碳、硝酸盐和硫酸盐。
大气颗粒物,尤其是空气污染是世界性的环境问题,会引发多种健康问题。颗粒物质其直径范围为2.5 μM-10 μM。
事实上,世界不同地区的几项基于队列的研究已经解决了长期暴露于空气污染与死亡率之间的相关性。他们已经证明长期暴露于细颗粒物与心血管和肺部疾病风险增加以及肺癌风险增加之间存在关联。空气污染可能与炎症性肠病的病理生理有关,从而与胃肠道疾病相关。

作为空气污染成分的颗粒物和臭氧现在被认为具有严重的健康问题,因为臭氧和颗粒物会增加肠道通透性,而且它们可能会破坏肠道细胞壁中存在的紧密连接。由于空气污染对肠道微生物群的影响而发生的变化知之甚少。当颗粒物被摄入时,它会被肠道微生物群代谢成其他一些对整个肠道有害的有毒代谢物,如果这种代谢物进入循环,那么它可能会引起其他一些影响。
生物学研究的最新进展表明,空气污染正在导致肠道微生物群的组成和生理发生改变。人类中,吸入的 PM 会迅速从肺部清除并运输到肠道,在那里它可能会导致菌群发生改变。
在炎症性肠病 (IBD) 的小鼠模型中,口服环境 PM10的浓度代表了在高水平空气污染期间可能发生的剂量,已被证明会显着影响肠道微生物群。厚壁菌门的比例增加,而拟杆菌门减少,炎症反应和肠道通透性得到提高。
肠道微生物群相对浓度的这种显着变化导致支链脂肪酸(异丁酸和异戊酸)的形成,从而导致丁酸浓度降低。丁酸是结肠细胞和肠黏膜细胞必需的脂肪酸,丁酸的减少会导致肠道屏障受损,也会导致黏膜炎症。
另一项研究表明,当小鼠暴露于另一种污染物,即多氯联苯 (PCB) 时,与肠道微生物群相关的组成和代谢过程也会发生改变。
流行病学证据表明,空气污染物也与人类 IBD 风险增加有关。有人提出,一般而言,空气污染和 PM 可能会促进人类的胃肠道疾病。
除了 IBD 外,暴露于空气污染与 2 型糖尿病和肥胖症有关,这可能是由于对肠道微生物群的影响。与 NOX暴露相关的特定肠道细菌家族,Bacteroidetes增加,而 Coriobacteriaceae减少。这些变化与发展为 2 型糖尿病的空腹血糖水平升高有关。
纳米材料和食品添加剂:直接改变或者杀死微生物
纳米粒子 (NP)被广泛用于制造许多产品,例如电子元件、无刮痕涂料、药品、运动器材、化妆品、食品容器和膳食补充剂。
由于它们的体积非常小,NPs 能够通过吸入、摄入、皮肤渗透或注射进入人体。作为一种新的环境污染物,NPs 会诱导氧化应激,这被认为是最具毒性的细胞内和体内机制。一些纳米颗粒在体外显示出抗菌特性。例如,银纳米颗粒 (Ag NPs) 对细菌、病毒和真菌生物体具有明显的细胞毒性。摄入后,Ag NPs 可以被小肠吸收并被回肠组织内的派尔氏斑吸收。碳纳米管与细胞壁结合,破坏细胞膜,并对球状或杆状形态的革兰氏阳性菌和革兰氏阴性菌具有抗菌活性。
考虑到 NPs 的生物分布和抗菌活性的潜力,NPs 有可能通过口服和非口服途径影响肠道微生物群。然而,关于纳米颗粒对肠道微生物群的影响的研究很少。
银纳米颗粒(Ag NPs): 最近的一项研究报告称,给予 Ag NPs(1 mg/mL 在 2 mM 柠檬酸盐缓冲液中或在 100 mg/mL 聚乙烯吡咯烷酮水溶液中持续 28 天)不会改变小鼠肠道微生物组的组成、结构或多样性。然而,另一项研究表明,暴露于 Ag NPs13 周会降低门水平厚壁菌的丰度,并扰乱大鼠回肠中免疫调节基因的表达。
此外,Ag NPs 对果蝇幼虫有毒,因为它们会降低幼虫肠道微生物群的多样性。需要更多证据确定 NPs 是否具有抗菌活性或对肠道微生物群的其他影响。
无热量人造甜味剂 (NAS)可为不含高热量糖分的食物提供甜味,是无糖汽水、谷物和无糖甜点中的常见成分,推荐用于减肥和患有葡萄糖耐受不良的人 或 2 型糖尿病。
最近的一份研究表明,长期给小鼠喂食 NAS(包括糖精、三氯蔗糖和阿斯巴甜)会导致更高的葡萄糖耐受性,并且与肠道中拟杆菌属和梭菌属细菌的丰度增加有关。这种葡萄糖耐受不良的增加依赖于肠道微生物群;NAS 在无菌小鼠或抗生素治疗小鼠中均未引起葡萄糖耐受不良;然而,将肠道微生物群从 NAS 处理的小鼠或体外暴露于 NAS 的细菌转移到无菌小鼠或抗生素处理的小鼠,会损害葡萄糖稳态。
乳化剂是食品添加剂,通常存在于加工食品(如面包)中,以延长保质期和新鲜度。

最近的一项研究表明,乳化剂的类似洗涤剂的特性可能会对肠道微生物群和肠道组织的完整性产生负面影响。给小鼠喂食羧甲基纤维素或聚山梨醇酯-80(乳化剂)12 周,增加了粘液溶解细菌(如瘤胃球菌)的丰度,并降低了粪便中拟杆菌的丰度。微生物群的这些变化伴随着肠道粘液厚度的减少、轻度炎症和代谢综合征的症状,包括肥胖增加和葡萄糖失调。有趣的是,乳化剂对无菌小鼠没有影响。
此外,这些变化可以通过从乳化剂处理的小鼠身上转移微生物群来转移到无菌小鼠身上。此外,作者观察到乳化剂在 IL-10 缺陷和 Toll 样受体 5 (TLR5) 缺陷小鼠中促进了强烈的结肠炎,这表明乳化剂可能会促进易感宿主的强烈结肠炎,并诱发低度炎症。
大规模的环境污染和由此产生的抗健康问题是当前主要的公共卫生问题。
当环境污染物改变肠道微生物群组成时,微生物群代谢物,包括短链脂肪酸和胆汁酸,将首先受到影响。这些特性支持短链脂肪酸影响能量代谢、肠道免疫、癌症甚至神经系统功能。
环境污染物会直接影响肠道微生物群并导致代谢物和免疫系统发生变化。生物多样性的丧失和污染物的暴露最终会导致免疫系统失衡,并增加威胁公众健康的炎症性疾病。
环境污染对肠道微生物群的影响及其后续影响
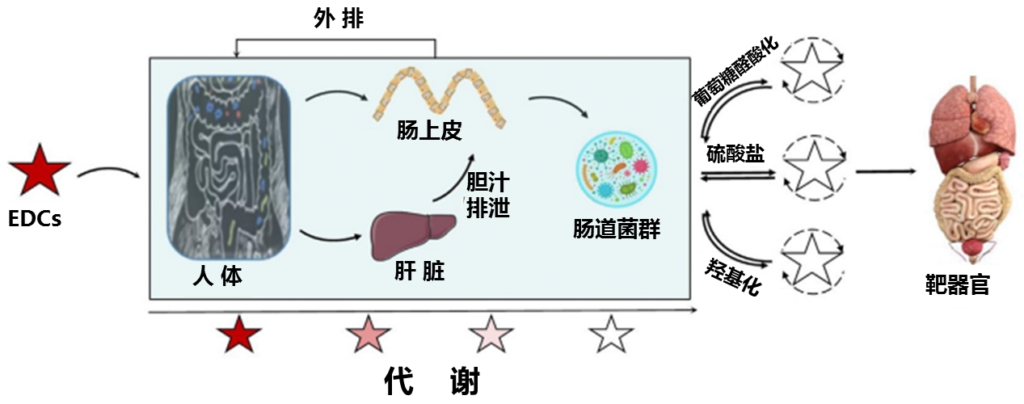
Li N, et al. Environ Pollut. 2021
需要注意的是,环境毒理性研究大多数来自动物模型,主要是大小鼠。确定动物结果对推测人类的重要性并不容易,因为它们没有相同的环境暴露以及物种差异。没有人能排除环境污染物可能对人类肠道菌群和表型产生长期影响的可能性,而这些影响迄今为止在动物身上不存在,短期使用是规则。
总之,动物实验和流行病学研究并不完全平行。因此,即使有足够的证据支持基于动物模型结果的“三向相互作用”理论,仍需要更多的流行病学证据来验证。
几十年来,评估环境化学品健康风险的核心要素保持不变(参见相关报道)。迄今为止,还没有研究方法明确考虑人类微生物组的潜在影响。因此,微生物组在改变人类对环境相关暴露的毒性易感性方面的作用在很大程度上仍不确定。
值得庆幸的是,许多已知的微生物转化必须与酶和基因相关联,为临床研究中的诊断标志物提供特定目标。对肠道菌群异物代谢的分子理解将为毒理学风险评估提供信息,并为环境污染中毒的治疗提供新的靶点。
建议今后应该确定以下几方面:
许多微生物在人类存在之前就已经存活在大自然中,它们也在不断进化从而适应环境。微生物群与人类、环境和它们自身相互作用或许远超出我们想象。
微生物群检测是我们人类得以了解它们的一个通道,对于环境微生物群的深入了解,或许能成为我们了解微生物群与人体关系的一块重要拼图。
主要参考文献
Claus SP, Guillou H, Ellero-Simatos S. The gut microbiota: a major player in the toxicity of environmental pollutants? [published correction appears in NPJ Biofilms Microbiomes. 2017 Jun 22;3:17001]. NPJ Biofilms Microbiomes. 2016;2:16003. Published 2016 May 4. doi:10.1038/npjbiofilms.2016.3
Li N, Li J, Zhang Q, Gao S, Quan X, Liu P, Xu C. Effects of endocrine disrupting chemicals in host health: Three-way interactions between environmental exposure, host phenotypic responses, and gut microbiota. Environ Pollut. 2021 Feb 15;271:116387. doi: 10.1016/j.envpol.2020.116387. Epub 2020 Dec 24. PMID: 33401209.
Jin Y, Wu S, Zeng Z, Fu Z. Effects of environmental pollutants on gut microbiota. Environ Pollut. 2017 Mar;222:1-9. doi: 10.1016/j.envpol.2016.11.045. Epub 2017 Jan 11. PMID: 28086130.
Anwar H, Iftikhar A, Muzaffar H, Almatroudi A, Allemailem KS, Navaid S, Saleem S, Khurshid M. Biodiversity of Gut Microbiota: Impact of Various Host and Environmental Factors. Biomed Res Int. 2021 May 12;2021:5575245. doi: 10.1155/2021/5575245. PMID: 34055983; PMCID: PMC8133857.

谷禾健康

我们知道肠道菌群代谢产生短链脂肪酸,丁酸是短链脂肪酸之一,它支持消化系统健康和疾病预防,地位不容小觑。
丁酸作为一种有效的调节因子,是宿主-微生物串扰的关键介体。本文整理了丁酸盐的特性,探讨其健康益处及改善健康的潜力。
肠道菌群消化膳食纤维,并将它们转化为多种有机化合物,这些化合物对人体健康有益,包括氨基酸、短链脂肪酸等。内源性丁酸主要是肠道内产丁酸细菌利用糖类发酵产生一类短链脂肪酸。
丁酸在体内可以通过脂肪酸氧化为机体供应能量,是肠道上皮细胞的主要供能物质。丁酸与机体健康密切相关,对调节肠道健康、抑制炎症及癌症等病症意义重大。在养殖业中常添加丁酸盐保护动物健康生长,如预防断奶仔猪腹泻、调节鸡肠道菌群并增强其免疫力等。
1、 为肠道细胞提供燃料
丁酸盐是结肠细胞的主要能量来源,结肠细胞是构成肠道内壁的细胞。
与身体中使用糖(葡萄糖)作为主要能量来源的大多数其他细胞不同,肠道内壁细胞(结肠细胞)主要使用丁酸盐。如果没有丁酸盐,这些细胞就无法正确执行其功能。
厚壁菌属的成员以产生丁酸盐而闻名,像Roseburia,Faecalibacterium prausnitzii,直肠真杆菌 E.rectale 等。
这种关系是相互的。丁酸盐为结肠细胞提供燃料,作为回报,这些细胞有助于提供一个无氧环境,有益的肠道微生物在其中茁壮成长。这可以控制炎症,保持肠道细胞健康,并使肠道细菌保持健康。
2、 促进肠道运动
丁酸盐还可以穿过上皮屏障,通过连接胃肠道、脾脏和肝脏的肝门静脉进入循环。肝脏似乎是内脏产生的SCFA的主要库,它们可能通过β-氧化代谢,用于合成酮体或转化为AcCoA。
最近的研究发现,外周血短链脂肪酸水平与膳食中溴的摄入量相关,这表明丁酸盐是通过循环运输的,其他器官可能会受到丁酸盐浓度变化的影响。
短链脂肪酸转运体的表达受到短链脂肪酸存在的调控,未在结肠中代谢的短链脂肪酸通过门静脉进入肝脏,作为肝细胞的能量底物,因此在体循环中只留下极少的丁酸。
实验室研究表明,丁酸盐通过作为SCFA受体的配体和激活剂,诱导肠道激素肽YY24或介导肠嗜铬细胞释放5-羟色胺来促进肠道运动。
★ 增强电解质吸收
丁酸盐通过上调Na+-H+交换器和诱导ATPase离子交换器基因来增强水和电解质的吸收。并且可能有益于预防某些类型的腹泻。
3、 激活AMPK
丁酸盐激活AMPK (AMP-activated protein kinase, AMPK)。AMPK的作用是促进细胞内的平衡。它在我们的新陈代谢功能中也扮演着重要的角色。一些科学家把减肥归功于AMPK的激活。
在有和没有NAFLD的小鼠中,当AMPK被激活时,肝脏中的脂肪水平下降,也就是说,新的脂肪产生减慢,现有的脂肪被代谢。此外,在喂食高脂肪食物的小鼠中当AMPK被激活时,小鼠的体重增加和肥胖缓解,肝脏炎症的迹象也更少。
AMPK对食欲调节至关重要。它在减肥方面也有重要作用。
刺激AMPK促进自噬。这个自然过程是细胞破坏和消耗老细胞。最后,肠道内的细胞变得更强壮。由于激活AMPK,丁酸盐帮助结肠细胞维持其4 – 5天的生命周期。有了健康细胞的存在,小肠的紧密连接变得更加强健。
反过来,来自器官的颗粒和毒素不会渗透导致肠漏的问题。因此,丁酸盐可以帮助修复肠道内壁。
4、 抗氧化能力
丁酸盐保护细胞免受有害物质的侵害,以维持肠道健康。
说起抗氧化,我们先了解一下自由基。它基本上是体内化学反应产生的废物。另一方面,抗氧化剂是身体抵御它们的防御措施。大量自由基会造成损害并压倒身体的修复系统。我们称之为氧化应激。氧化应激被认为是导致衰老和疾病的一个重要因素。
丁酸增加谷胱甘肽,可以中和自由基
结肠或大肠是身体产生的废物的储存容器。较高的丁酸盐水平已被证明会增加谷胱甘肽的水平,谷胱甘肽是一种在人体细胞中产生的抗氧化剂,可以中和肠道中的自由基(自由基与炎症和许多疾病有关)。
5、 防止肠漏
肠道内壁需要丁酸盐来保持健康和正常运作。
肠道内壁是肠道屏障。它促进绒毛的生长,微小的手指状挤压物排列在肠道内,并增加粘蛋白的产生,粘蛋白是一种覆盖肠道内部的凝胶状物质。它选择性地让维生素和矿物质等物质离开肠道,进入血液,并到达需要它们的地方。同样,它可以阻止毒素、病原体和食物化合物进入血液。
当屏障健康时,称为紧密连接的小孔会放松,让水和营养物质通过。
一些习惯,比如频繁吃零食,会阻止这些紧密连接在两餐之间的关闭,因此细菌和不需要的物质会进入血液,于是肠漏就发生了。
肠道微生物从膳食纤维中产生的丁酸盐提供了肠道内壁细胞所需的燃料。通过这样做,它可以保持肠道内壁的完整性,防止发生肠漏。
6、 抗炎、抗癌特性
丁酸盐对肠道具有抗炎和抗癌功能。
肠道内壁会保持低水平的炎症,以防与微生物群接触的粘膜表面发生任何变化。低水平的炎症受到严格控制,但如果它被破坏,会导致氧化损伤,并在很长一段时间内导致癌症。
丁酸盐会阻止体内的一些促炎物质发挥作用。丁酸盐的抗炎作用可减少氧化应激并控制自由基造成的损害。
丁酸盐的抗炎特性,部分原因是其抑制转录因子核因子-κB (NF-κB)的激活,通过下调NF-κB信号通路,丁酸盐可以调节促炎细胞因子的产生。
丁酸盐对免疫功能的调节作用
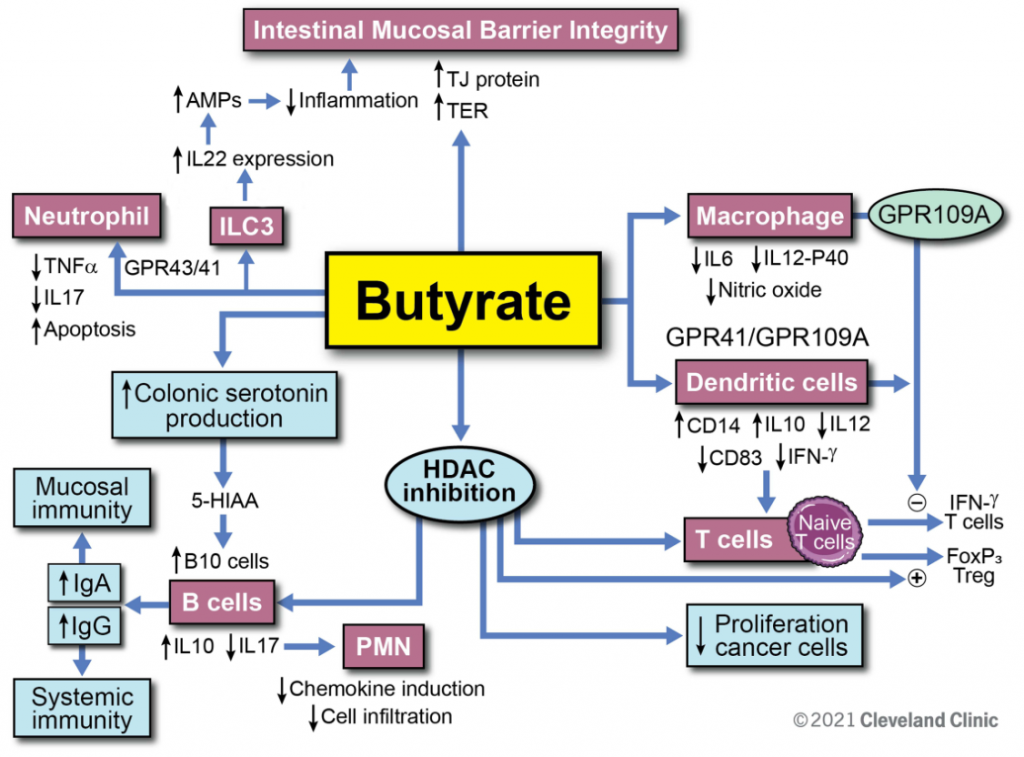

前面我们知道,丁酸盐通过直接诱导上皮中的紧密连接蛋白来增强肠粘膜屏障。此外,丁酸盐诱导ILC3细胞分泌IL-22进一步增强了这种作用。通过与GPCR 43和41的相互作用,丁酸抑制中性粒细胞的促炎细胞因子分泌。丁酸通过GPCR直接作用于巨噬细胞和树突状细胞,并通过增加Foxp3 T细胞调节T细胞功能,同时抑制产生IFN-ɣ的T细胞。丁酸增加5-羟色胺的产生,也是HDAC的抑制剂。它通过这些途径调节B细胞功能,增加抗炎细胞因子IL-10,同时降低IL-17。丁酸盐通过增加B细胞的IgA和IgG抗体反应,增强特异性免疫和抑制自身免疫。
抗炎 -> 抗癌
丁酸盐也是一种组蛋白脱乙酰酶(HDAC)抑制剂。组蛋白脱乙酰酶是大多数癌症中产生的酶。因为丁酸盐是一种抑制剂,它实际上会改变基因表达,抑制细胞增殖,诱导细胞分化或凋亡。因此,它可以阻止癌细胞的发展。
炎症性肠病
炎症性肠病(IBD)是一种慢性肠道炎症性疾病,有两种主要亚型:克罗恩病和溃疡性结肠炎。
虽然IBD的确切发病机制尚不完全清楚,但IBD涉及遗传、肠道微生物群和粘膜免疫等多种影响因素之间的复杂相互作用,包括先天性和适应性免疫反应。
据报道,在这两种IBD亚型中,产生丁酸的肠道微生物减少。丁酸对肠道防御机制具有多阶段调节作用,包括通过促进肠上皮中的紧密连接蛋白保护肠粘膜屏障,支持先天性和适应性免疫反应,以及通过降低环氧合酶-2(COX-2)水平抑制氧化应激,并通过诱导过氧化氢酶,改善过氧化氢(H2O2)的解毒作用。
肠粘膜溃疡是IBD的主要表现之一,丁酸对肠上皮细胞生长和细胞死亡过程的影响已被充分证明。
根据整体稳态条件,丁酸酯已被证明对人类结肠上皮细胞具有生长刺激或凋亡特性。此外,在人和大鼠来源的结肠细胞培养物中,丁酸已被证明能减少氧化应激引起的DNA损伤。
母乳通过丁酸保护宝宝的抗炎环境
据报道,母乳喂养等早期接触对IBD的发展和发病机制具有保护作用。母乳通过其代谢物丁酸诱导紧密连接蛋白和粘液产生基因的表达,从而诱导新生儿胃肠道的抗炎环境。
前面章节我们了解到,当肠道屏障完整时,炎性体具有保护作用,但一旦屏障被肠道失调破坏,炎性体的激活和免疫细胞的募集与粘膜炎症相关——这是IBD持续炎症的另一个主要病理生理机制。
在肠炎症的体外共培养模型中,丁酸已被证明可调节促炎症信号并抑制几种核苷酸结合寡聚化结构域样受体-3(NLRP3)炎症体标记物。
丁酸盐结合其他疗法
一项研究报告称,当IL-1β被其他IBD疗法(如5-ASA)抑制时,丁酸盐显著降低IL-8分泌,从而降低IL-8介导的趋化性,突出了单独丁酸盐不一致临床反应背后的机制,以及丁酸盐与IBD其他治疗方式相结合的可能性。
通过添加产丁酸菌改善屏障完整性
通过添加产丁酸菌(prausnitzii杆菌、白痢丁酸球菌和六种丁酸产生菌的混合物)来增加克罗恩病患者的微生物群中的产丁酸菌,从而改善体外上皮屏障完整性。
丁酸治疗潜力
由于丁酸治疗的反应不一致,可能在某种程度上由于剂量、持续时间和配方标准化的变化,目前丁酸在IBD中的适用性最多被视为补充治疗。
丁酸盐显示出更一致有效性的一个领域是转移性结肠炎,这是一种术后表现,当结肠的一部分失去连续性时,丁酸盐消耗被认为是导致炎症的主要因素。虽然手术治疗或结肠再连接或切除转移是一种更确切的治疗方法,但在考虑医疗管理时,丁酸灌肠已被证明具有治疗价值。
癌症
丁酸盐使肠道环境保持稳定,并且是膳食纤维对某些癌症的保护作用的一部分。
肠癌,是西方世界的主要健康负担,主要归咎于饮食。膳食纤维含量低的饮食会影响肠道中的细菌。结肠细胞需要丁酸盐作为能量,如果它们没有能量,就无法工作。
低膳食纤维 -> 丁酸盐↓ -> 肠癌
丁酸盐是由肠道细菌从植物性食物中的益生元纤维中产生的。如果肠道内的细胞无法工作,与肿瘤进展相关的细胞就会茁壮成长,接着会发出炎症信号并导致肿瘤发展。因此,低膳食纤维会使丁酸盐的产生减少,是肠癌的危险因素。
结直肠癌
据报道,结直肠癌患者包括丁酸盐在内的短链脂肪酸水平较低。
丁酸盐对肠上皮细胞的增殖具有双面作用,一方面支持健康细胞处于稳态,但另一方面抑制癌症诱导的过度增殖。丁酸钠已被证明以p-53非依赖性途径诱导人结肠癌细胞系凋亡。丁酸盐还可以防止氧化应激和DNA损伤。
据报道,丁酸盐还通过多种途径具有癌症保护作用,包括抑制神经纤毛蛋白-1(NRP-1)、抑制丝裂原活化蛋白激酶(MAPK)信号通路、差异调节Wnt-β-连环蛋白信号通路、上调microRNA miR-203和促进细胞凋亡,和促增殖miR-92a的抑制。
由于饮食模式在结直肠癌发病中的作用已得到充分证实,大多数人体试验研究了通过改变膳食纤维摄入量进行干预的方法,并报告了结直肠癌复发风险的降低。
代谢相关疾病
越来越多的证据表明饮食、肠道微生物群和代谢紊乱之间存在复杂的相互作用。
★ 肥胖
对人类的研究表明,肥胖和瘦人群的肠道细菌存在差异,微生物多样性的减少与胰岛素抵抗和血脂异常有关。
包括丁酸盐在内的SCFA可通过激活肠细胞内的FFAR来降低食欲和体重。这促进胰高血糖素样肽1(GLP-1)和肽YY(PYY)的释放,前者促进胰岛素分泌并抑制胰高血糖素分泌,后者降低食欲并减缓胃排空。
SCFA还能减少所谓的“饥饿激素”——ghrelin的分泌;FFAR2存在于ghrelin分泌细胞上,包括乙酸盐和丙酸盐在内的FFAR2激动剂可减少ghrelin分泌。
也有证据表明短链脂肪酸作用于交感神经系统,交感神经节中FFAR3的激活导致能量消耗增加。
然而,关于丁酸盐对食物摄入的影响,有相互矛盾的结果报道。
食物摄入量减少 -> 抗肥胖
有研究发现,丁酸盐在9天内使喂食HFD的小鼠的食物摄入量减少了22%。这与直接服用丁酸后GLP-1和PYY分泌增加有关。FFAR3基因敲除小鼠减少了丁酸刺激的GLP-1分泌,尽管丁酸减少了体重增加和食物摄入的程度与野生型小鼠相似,这表明FFAR3和GLP-1对于丁酸的抗肥胖作用不是必需的。
另一研究发现类似的结果,在HFD喂养的小鼠中,急性口服(而非静脉注射)丁酸盐在24小时内减少了21%的食物摄入量,而丁酸盐的慢性补充在9周内减少了相似量的摄入量。
在迷走神经切断术后,丁酸盐并没有改变小鼠的食物摄入量,因此作者认为丁酸盐通过肠-脑神经回路诱导饱腹感。这可能与GLP-1有关,因为GLP-1作用于迷走神经。
食物摄入量增加,体重不变 -> 抗肥胖
相反,有研究表明,在1-10周的四个测量时间点,补充丁酸盐可增加HFD喂养小鼠的食物摄入量。尽管增加了食物摄入量,但补充丁酸盐的小鼠体重并未显著增加,而对照组小鼠的平均体重增加了17克。相反,补充丁酸盐的小鼠在暴露于低温时,其能量消耗增加,产热增加,这一点可以从较高的体温中看出。
在小鼠中,丁酸增加棕色脂肪组织(UCP1)和骨骼肌(UCP2和UCP3)中解偶联蛋白、促进热量生成的线粒体蛋白的表达。在丁酸盐处理的小鼠骨骼肌中Ucp2和Ucp3基因的启动子处发现组蛋白乙酰化增加,这表明丁酸盐可能通过HDAC抑制增加解偶联蛋白表达来增加产热,从而增加能量消耗。
★ 糖尿病
研究发现,糖尿病患者和糖尿病前期受试者中丁酸盐水平降低。
丁酸盐通过多种途径影响糖代谢的调节
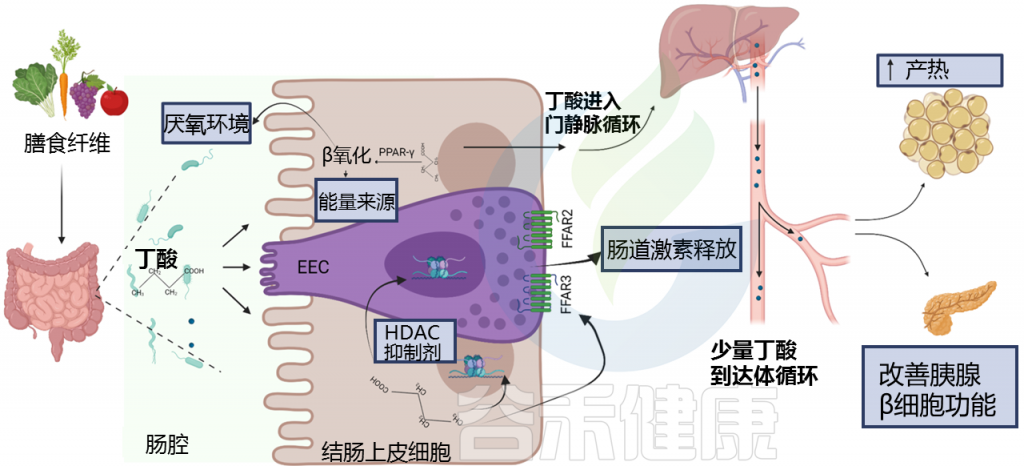

Arora T,et al., Front Endocrinol (Lausanne). 2021
膳食纤维经肠道菌群发酵产生短链脂肪酸,包括丁酸盐。丁酸盐介导的PPAR-γ的激活,诱导β-氧化和氧的消耗,从而促进厌氧条件的建立,这是几种厌氧肠道共生体生长和功能所需的条件。
丁酸在肠内分泌细胞(EEC)中与游离脂肪酸受体(FFAR) FFAR2和FFAR3结合,调节肠道激素释放,如胰高血糖素样肽 1 (GLP-1) 和肽 YY (PYY)。
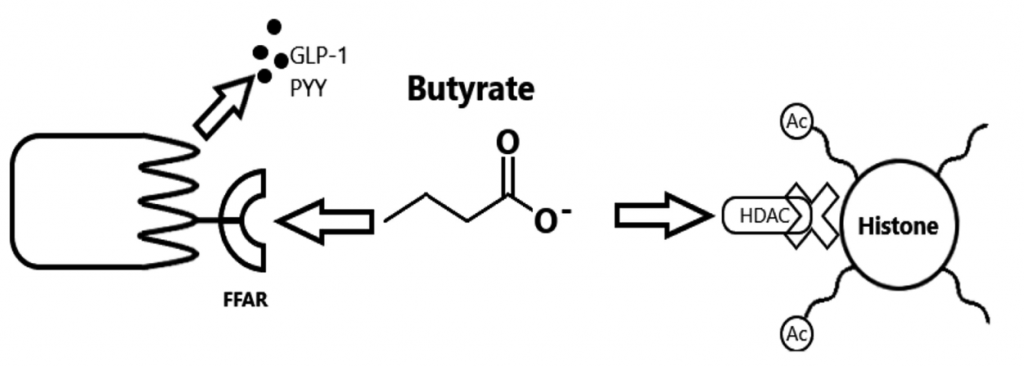

S.C. Bridgeman et al. Pharmacological Research,2020
GLP-1 增加胰岛素的产生并减少胰腺中胰高血糖素的产生。
PYY 会增加肌肉和脂肪组织对葡萄糖的吸收。
这些激素共同作用以保持血糖水平稳定。当血糖过高时,胰岛素会告诉身体的肌肉和脂肪细胞吸收多余的葡萄糖,所以说这些激素对肥胖和糖尿病很重要。丁酸盐增加这些肠道激素的释放,表明对控制血糖水平和防止体重增加有潜在的好处。
丁酸还可作为组蛋白去乙酰酶(HDAC)抑制剂,调节EEC和肠上皮细胞的基因表达。残余丁酸被结肠细胞吸收利用后,先排入门静脉循环,再排入外周体循环。在体循环中,丁酸可能调节棕色脂肪组织的产热和胰腺β细胞的功能。
增加丁酸水平的临床研究
一项随机临床研究中,对T2D患者补充混合膳食纤维可改善血糖参数,同时增加产生乙酸和丁酸的细菌丰度,并增加粪便中乙酸和丁酸水平。
在另一项研究中,将产丁酸菌(E.hallii,Clostridium beijerinckii,C.butyricum)与其他肠道细菌(A.muciniphila,婴儿双歧杆菌)和菊粉作为可发酵纤维混合,适度增加了T2D患者的丁酸水平,改善了口服葡萄糖耐量和糖化血红蛋白水平。
最后,添加菊粉和丁酸钠胶囊45天可改善T2D个体的空腹血糖和腰臀比。
这些研究清楚地表明,膳食纤维本身或与ngp或丁酸盐联合可以改善T2D的葡萄糖控制。
然而,维持患者依从性的策略和对这些补充剂的长期影响的调查仍然是值得的。此外,显然基线肠道菌群是饮食干预、益生菌注射和微生物移植成功的一个强有力的预测因素,基于微生物群对个体进行T2D分层可能有助于实现更好的代谢结果。
神经系统疾病
除了在肠道中的作用外,丁酸盐还具有支持大脑健康的巨大潜力。
由结肠中的细菌产生的丁酸盐具有一系列生物学功能。这些功能还与神经保护作用有关(有益于大脑和中枢神经系统)。
丁酸盐也是一种大脑助推器,因为它对大脑和中枢神经系统有保护作用。例如,它与许多与帕金森氏症、阿尔茨海默氏症甚至中风等疾病相关的通路有关。
丁酸盐对宿主生理和脑功能影响的示意图
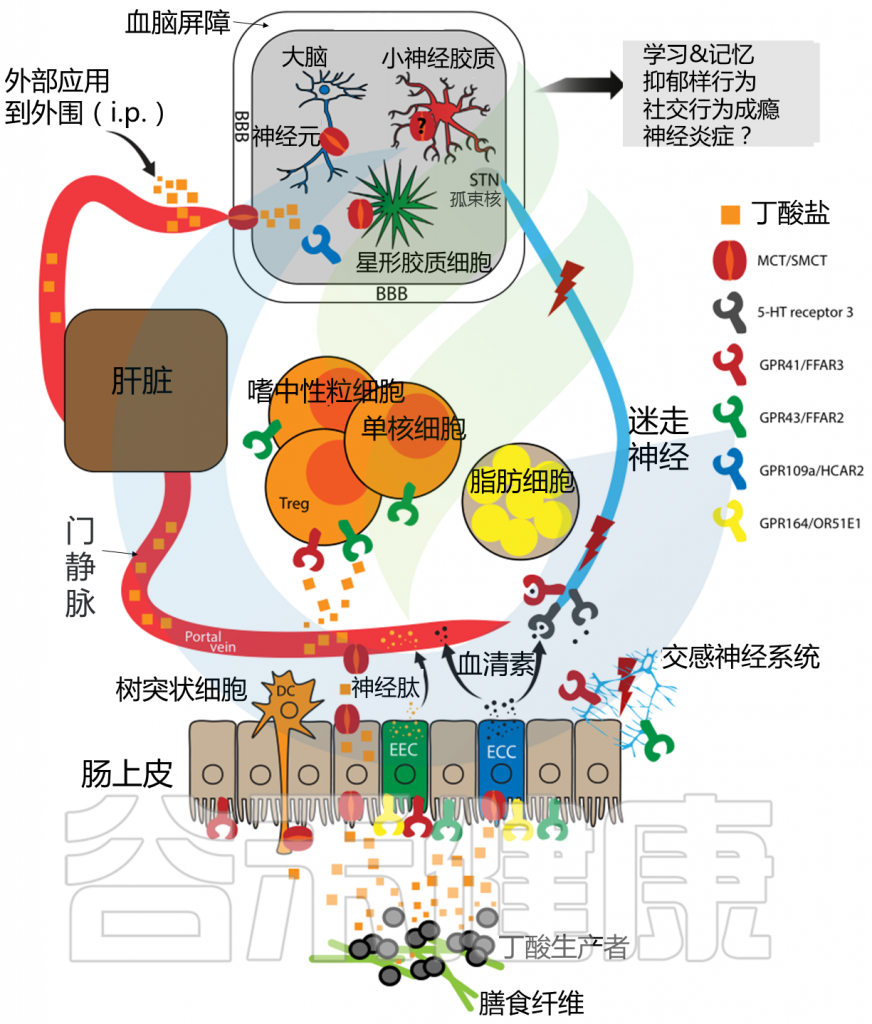

R.M. Stilling et al. / Neurochemistry International, 2016
由于抑郁症和其他神经精神疾病具有促炎症表型,反之亦然,丁酸盐在这些情况下也可能活跃。重要的是,丁酸盐的抗炎特性也对宿主(大脑)衰老具有根本意义,特别是考虑到许多组织(包括大脑)都会发生炎症衰老的慢性炎症状态。具体而言,丁酸盐通过减少NF-kB信号传导和诱导凋亡,从而促进神经保护,在脑内巨噬细胞(小胶质细胞)中显示出抗炎作用。
因此,丁酸盐会影响大脑健康,而饮食可能是改善疾病结果的一种简单方法。
压力、焦虑、抑郁等情绪都涉及肠道微生物群。
通过饮食提高丁酸盐的产量既简单又风险低。研究发现在加速老化的SAMP8小鼠模型中,长期喂养益生元纤维可改善认知能力下降,并具有抗炎、延缓衰老的作用。
未来有一天,它甚至可能成为脑部疾病的潜在治疗选择。


睡眠
新证据表明,肠道微生物群是促进睡眠信号的来源。细菌代谢产物和细菌细胞壁的成分可能在肠道共生菌群和大脑中的睡眠生成机制之间提供重要联系。
丁酸是一种短链脂肪酸,由肠道细菌通过不易消化的多糖发酵产生。研究人员验证了丁酸可能作为细菌源性促睡眠信号的假设。经口灌胃给予丁酸酯前药三丁酸甘油酯,在治疗后4小时内使小鼠非快速眼动睡眠(NREMS)增加近50%。
类似地,门脉内注射丁酸盐导致大鼠NREMS迅速而强劲地增加。在丁酸盐注射后6小时内,NREMS增加了70%。口服和门静脉注射丁酸盐都会导致体温显著下降。全身皮下或腹腔注射丁酸对睡眠或体温没有任何显著影响。
结果表明,丁酸盐的睡眠诱导作用是由位于肝脏和/或门静脉壁的感觉机制介导的。肝门丁酸盐敏感机制可能在肠道微生物群的睡眠调节中发挥作用。
扩展阅读:睡眠与肠道菌群
社交行为
微生物群可能会影响你的社交行为,虽然听起来可能有点夸张。
简而言之,丁酸盐很臭。
“butyrate”这个词实际上源自拉丁语butyrum,意思是黄油。你可能熟悉牛奶变质或变质黄油的气味,丁酸盐就是那个味儿。丁酸是哺乳动物最强烈的气味之一,人类可以通过嗅觉受体OR51E1检测到它的浓度约为亿分之240。


哺乳动物鼻子对丁酸酯气味敏感的一个合理原因是,丁酸酯是一种仅在厌氧条件下发生的细菌产物,如生物分解、腐败或发酵,也可能产生有害毒素。对丁酸盐高度敏感的另一种非互斥解释可能是其存在于体味中。
因此,它可以作为一种社会线索,携带有关微生物群组成和活动的信息,从而间接承载宿主免疫系统特征,类似于主要组织相容性复合体(MHC)中遗传变异性的公认社会信号功能。
存在于尿液和汗液中的MHC分子的肽配体被认为是携带遗传相关性和个体性信息的社会识别信号,并且可以被嗅觉上皮或犁鼻器官中的专门嗅觉受体神经元感知。
“气味相投”——可能是ta的气味在“撩”你
对包括人类在内的许多脊椎动物的研究表明,MHC基因座的变异影响社会行为,最显著的是配偶选择,但也影响社会群体的合作行为。也有人认为MHC依赖的嗅觉信号并不是携带个体和遗传变异信息的唯一线索,“嗅觉指纹”更为复杂。
化学通讯的发酵假说
一些科学家认为,它也是体味的一个组成部分。我们会使用丁酸盐等有气味的短链脂肪酸来(无意识地)相互交流。
事实上,这些微生物群是由产生挥发性脂肪酸、酯类、醇类和醛类的发酵厚壁菌门细菌主导的,这一事实促使作者提出了“化学通讯的发酵假说”,即共生细菌的变异驱动了物种、性别和个体特定气味的变化,从而促进了社会交流。
在雄性叉角羚(Antilocapra americana)的耳下气味中也发现了异戊酸和丁酸酯,用于标记其领地。此外,戊酸的潜意识气味已被证明能够引导社会偏好,例如降低人类受试者的面部受欢迎程度。
因此,丁酸盐和其他微生物发酵挥发性产物等短链脂肪酸似乎有可能不仅存在于专门的气味腺中,而且也存在于其他栖息地,如人类的腋窝,可能有助于化学交流,并传递有关微生物群组成的信息,从而也将遗传信息传递给感兴趣的接受者。
除食源性丁酸,动物体内丁酸主要是由盲肠和结肠的厌氧型细菌发酵产生,而由胃和小肠产生的丁酸含量极低。大肠产丁酸的菌种主要是梭菌属XIVa和IV族,以及真杆菌属和梭杆菌属。盲肠和结肠中丁酸的产生速度和数量主要取决于肠道微生物组成、日常膳食中可利用发酵成分组成等。
其中厚壁菌门的成员以其产生丁酸盐的能力而闻名。
在结肠中特别流行的产丁酸的细菌包括:
粪杆菌、直肠真杆菌E.rectale、Roseburia
双歧杆菌等常见益生菌配方中的微生物与丁酸盐生产者之间的交叉喂养相互作用已被证明是可以产丁酸盐的。
在消化道中发现的已知丁酸盐生产者中,大多数似乎属于毛螺菌科和瘤胃球菌科。
Faecalibacterium prausnitzii (FP) 是瘤胃球菌科的一部分,值得特别一提,因为它是消化道中最丰富的微生物之一,也是主要的丁酸盐生产者之一。FP 的特征包括通过丁酸盐产生和其他复杂途径的抗微生物活性和抗炎/免疫调节活性。
关于FP菌,详见:肠道核心菌属——普拉梭菌(Faecalibacterium Prausnitzii),预防炎症的下一代益生菌
Anerostipes、Roseburia和 Coprococcus都是属于毛螺菌科,它们也是人类肠道中的主要丁酸盐生产者。
产生丁酸盐的细菌被认为在生命的第一年内定植于宿主,并且在成年时占总细菌群落的 20% 以上。
然而各种疾病状态都表明产生丁酸盐的肠道细菌相对缺乏。
有趣的是,现如今益生菌补充剂中常用的细菌菌株很多都不是丁酸盐生产者,因为丁酸盐生产者很多是高度厌氧的,这意味着它们在氧气存在的情况下会很快死亡,所以要补充产丁酸菌就比较具有挑战性。
或许我们可以转换个思路来考虑,既然不能直接补充菌,那是不是可以补充产菌的食物呢?
所以哪些食物可以喂养产丁酸菌?
饮食对人体微生物组有显著影响,通过饮食干预可显著改变细菌数量并增加微生物多样性。
富含纤维的饮食对丁酸盐的产生特别有益,因为它可以滋养产生丁酸盐的细菌。
网上还有很多关于如何增加肠道丁酸盐的建议,比如多吃黄油或服用丁酸盐补充剂。然而,补充丁酸盐不一定对肠道有益,因为如果摄入丁酸盐,它会被胃吸收,也就是说它不会到达肠道为其细胞提供燃料。
记住,丁酸盐是微生物群产生的代谢物。
益生元是直接滋养微生物群的食物,包括蔬菜、水果、豆类和全谷物。它们含有膳食纤维,可被肠道细菌发酵成丁酸盐等有机化合物。通过食物增强微生物群是促进消化系统健康和丁酸盐生成的有效且安全的方法。
肠道细菌以膳食纤维为食,而不是动物蛋白。因此,优化丁酸盐产量的最佳方法是通过高纤维饮食。
高蛋白、高脂肪、低碳水化合物的饮食已被证明会破坏微生物组中丁酸盐的产生。在一项研究中,研究人员分析了短期饮食限制碳水化合物摄入量的肥胖参与者的微生物组,从而限制了他们对植物性膳食纤维的消耗。
在低碳水化合物饮食(每天 24 克)和中等碳水化合物饮食(每天 164 克)4 周后,短链脂肪酸的浓度低于高碳水化合物饮食(每天 399 克)。具体来说,当碳水化合物摄入量减少时,丁酸盐浓度会降低。同一项研究还发现,厚壁菌门细菌种类 Roseburia 和 E. Rectale 的密度与丁酸盐浓度之间存在联系,两者都随着碳水化合物摄入量的减少而降低。
然而,以上所谓的“膳食纤维”并不能完全解决这个问题,为什么呢?
理解以下几点很重要:
1、即使是来自同一物种的细菌菌株,对不同底物的反应也非常不同,甚至是属于同一类碳水化合物的底物。
2、某些细菌能够消化果聚糖,有些则不能。而那些可以消化的里面又有不一样的情况,其中一些能够消化短链的果聚糖,但不能消化更长链菊糖的果聚糖。
3、以上只是细菌消化不同底物能力的一个例子。由于这种变化的存在,不能一概而论。
而我们最需要的,更应该是寻找特定类型的纤维。
一项研究表明,不同类型碳水化合物的SCFA产量(单位:kJ)如下所示:
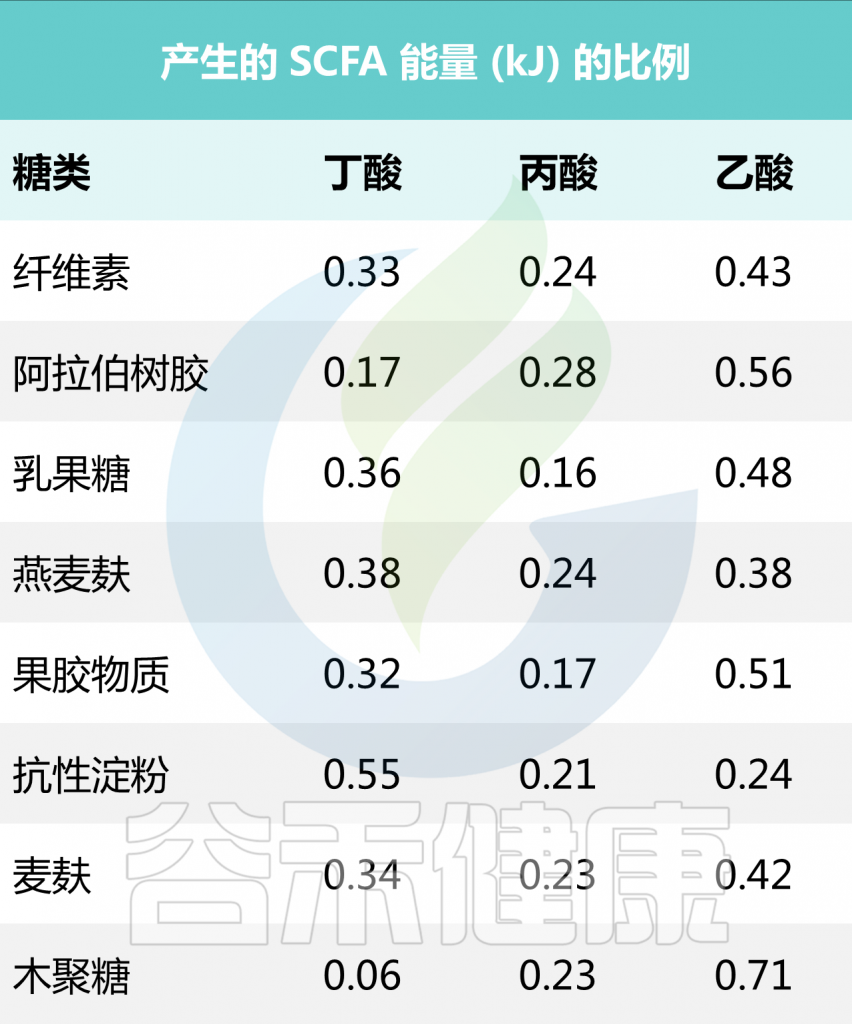

Bourassa MW, et al., Neurosci Lett. 2016
在该研究中,低聚果糖(FOS)的类型是洋葱、芦笋和香蕉等食物,而抗性淀粉(RS)则是全谷物和豆类。
另一项研究表明,补充特定猕猴桃中发现的低聚果糖可在4周内使F.prausnitzii菌增加100%。这是一项重大发现,因为目前有大量研究报告,F.prausnitzii 的相对缺乏与几种主要肠道疾病有关——最显著的是炎症性肠病、溃疡性结肠炎和克罗恩病。
抗性淀粉2型和3型,哪种更好?
这项研究表明,从生马铃薯和高直链淀粉玉米淀粉以及全谷物中发现的阿拉伯木聚糖中提取的2型抗性淀粉含量高的日粮中丁酸产量显著增加。
在174名健康年轻人的饮食中添加马铃薯抗性淀粉后,丁酸盐产量增加。玉米、菊苣和玉米中的抗性淀粉也进行了测试,但只有当食用土豆中的抗性淀粉时,粪便中的丁酸总量才会显著增加。
在该研究中,使用的是Bob’s Red Mill(品牌)未改性马铃薯淀粉。对于这种类型的抗性淀粉(RS2)是否对人类“有益”存在不同的观点,有多个来源表明RS3是一种更好的来源,因为RS2似乎可以喂养有害细菌,而RS3可以喂养有益细菌。
此外,鳄梨增加了能够产生短链脂肪酸的微生物数量,以及产生的总短链脂肪酸。
果聚糖(菊粉)
许多研究表明,菊粉可以增加短链脂肪酸的产量,包括丁酸盐。这可能解释了香蕉在溃疡性结肠炎和克罗恩病患者的饮食中如此有效的原因之一。然而,链长较短的果聚糖通常比链长的果聚糖(如菊粉)更容易喂养产丁酸菌。
补充菊粉虽然能够改变宿主的微生物群,但不会增加粪便丁酸水平。尽管这一结果似乎与谷物相反,但许多研究证明了补充菊粉在增加肠道短链脂肪酸生成方面的功效。


也就说,抗性淀粉和果聚糖(短链低聚果糖 和长链菊粉)在肠道中发酵时会产生丁酸盐。
对于抗性淀粉,似乎大多数研究都集中在 RS2 上。然而,在许多情况下,据报道 RS3 会产生更高水平的丁酸盐,对人类更健康。
抗性淀粉:
煮熟后冷却:土豆、红薯、米饭、意大利面、燕麦、豆类、豆类、全谷物。
原料:青香蕉、马铃薯、马铃薯淀粉、青香蕉粉。
果聚糖:
洋葱、菊苣、香蕉、朝鲜蓟、芦笋、大蒜、韭菜、西兰花、开心果和各种提取物。
由于人与人之间的常驻微生物存在显著差异,并且它们消化某些底物的能力不同,因此比较明智的选择是食用包含多种抗性淀粉和果聚糖的饮食。例如以马铃薯抗性淀粉、燕麦麸皮纤维或车前草种子或短链低聚半乳糖、长链低聚果糖和谷氨酰胺的混合物的形式短期补充,增加丁酸盐水平。
丁酸是不是越多越好?
丁酸并不总是越多越好,低浓度丁酸促进细胞增殖和生长,高浓度丁酸反而抑制细胞增殖和生长,增加肠道的通透性。
胃肠道不同部位对丁酸的耐受阈值也存在一定差异,胃和小肠对丁酸的耐受阈值低,结肠和盲肠耐受阈值高。
添加普通丁酸钠制剂(主要在肠道前端被吸收利用),反而造成肠道炎症、菌群失调。
更有意思的是,轻微炎症或者轻度溃疡部位添加丁酸盐可以促进肠道损伤的修复,在严重溃疡肠道部位添加,不利于溃疡的恢复,甚至加剧整个溃疡。
有学者发现溃疡部位的粘膜组织对丁酸的代谢降低,甚至只有正常粘膜组织的一半,主要是由于其转运载体和氧化相关的酶活降低。
p.s. 进行干预之前需要了解现有肠道丁酸盐的水平状况,可以更好地进行干预治疗前后对比
Tips
如果你正在被一些肠道疾病困扰,需要注意其中几种食物的凝集素含量:土豆、燕麦、豆类、豆类和全谷物。如果你打算吃这些食物,建议先浸泡和加压烹饪,然后从很少量开始。也可以排除生食。
如果你患有自身免疫性疾病,不推荐豆类和大多数全谷物。
此外,许多患有肠道疾病和/或自身免疫性疾病的人难以食用果糖,这可能是果糖不耐受的迹象。症状包括胀气、腹胀等。
相关阅读:
肠道菌群健康检测报告——常见问题解析
主要参考文献:
Arora T, Tremaroli V. Therapeutic Potential of Butyrate for Treatment of Type 2 Diabetes. Front Endocrinol (Lausanne). 2021;12:761834. Published 2021 Oct 19. doi:10.3389/fendo.2021.761834
Siddiqui MT, Cresci GAM. The Immunomodulatory Functions of Butyrate. J Inflamm Res. 2021 Nov 18;14:6025-6041. doi: 10.2147/JIR.S300989. PMID: 34819742; PMCID: PMC8608412.
Bourassa MW, Alim I, Bultman SJ, Ratan RR. Butyrate, neuroepigenetics and the gut microbiome: Can a high fiber diet improve brain health?. Neurosci Lett. 2016;625:56-63. doi:10.1016/j.neulet.2016.02.009
Hu Liu, Ji Wang, Ting He, Sage Becker, Guolong Zhang, Defa Li, Xi Ma, Butyrate: A Double-Edged Sword for Health?, Advances in Nutrition, Volume 9, Issue 1, January 2018
Bridgeman SC, Northrop W, Melton PE, Ellison GC, Newsholme P, Mamotte CDS. Butyrate generated by gut microbiota and its therapeutic role in metabolic syndrome. Pharmacol Res. 2020 Oct;160:105174. doi: 10.1016/j.phrs.2020.105174. Epub 2020 Aug 27. PMID: 32860943.
Rivière, A., Selak, M., Lantin, D., Leroy, F., & De Vuyst, L. (2016). Bifidobacteria and Butyrate-Producing Colon Bacteria: Importance and Strategies for Their Stimulation in the Human Gut. Frontiers in microbiology, 7, 979.
LeBlanc JG, Chain F, Martín R, Bermúdez-Humarán LG, Courau S, Langella P. Beneficial effects on host energy metabolism of short-chain fatty acids and vitamins produced by commensal and probiotic bacteria. Microb Cell Fact. 2017 May 8;16(1):79. doi: 10.1186/s12934-017-0691-z. PMID: 28482838; PMCID: PMC5423028.
Stilling RM, van de Wouw M, Clarke G, Stanton C, Dinan TG, Cryan JF. The neuropharmacology of butyrate: The bread and butter of the microbiota-gut-brain axis? Neurochem Int. 2016 Oct;99:110-132. doi: 10.1016/j.neuint.2016.06.011. Epub 2016 Jun 23. PMID: 27346602.
Szentirmai É, Millican NS, Massie AR, Kapás L. Butyrate, a metabolite of intestinal bacteria, enhances sleep. Sci Rep. 2019 May 7;9(1):7035. doi: 10.1038/s41598-019-43502-1. PMID: 31065013; PMCID: PMC6504874.

谷禾健康

有没有发现我们吃的食品正在变得越来越鲜艳,让人有食欲,“低脂”、“无糖”等字眼出现的频率越来越高,然而这其中必然会用到各类食品添加剂,如防腐剂,甜味剂,乳化剂,着色剂,香料等等。
可以看到孩子们喝的牛奶都是纯白无瑕的,事实上天然牛奶往往没有那么白;孩子们吃的五颜六色的糖果,糕点等也会结合一些人工色素,因此儿童比成人更容易接触到食用色素。

食品添加剂会诱发菌群失调,通过微生物群肠脑轴导致肠道疾病,代谢性疾病等各类问题的发生。这个过程是如何发生的?各类添加剂有什么不同的作用?为什么儿童学习、记忆受到影响?为什么与情绪也有关系?…
本文为大家解答相关疑惑。
首先,我们先来看看:食品添加剂都有哪些种类,它们起到什么样的作用,以及如何查看食品中是否存在添加剂。
工业界使用合成色素使其产品更有吸引力,使用防腐剂有助于保持其功能,适当pH值等特性,因此在大多数情况下,食品添加剂是不可或缺的存在。常见的食品添加剂及其功能用途见下表。


IFIC & FDA

谷禾健康

肠道菌群是居住在肠道中各种微生物。微生物群的建立甚至在个体出生之前就开始了,随着时间的推移而改变,并在体内持续存在,直到个体死亡。这些微生物群的组成是宿主特定的,在个体的一生中不断进化,并且容易受到各种因素的影响。
胎龄、分娩方式、饮食(母乳与配方奶)、卫生、抗生素,激素、疾病、衰老等都会影响并塑造肠道菌群。肠道菌群的定植、发育、成熟、稳定,老化与我们人类发育以及免疫成熟等高度吻合,不同阶段不同部位的菌群的构成以及丰度有不同特征。
肠道细菌是免疫系统发育和功能的重要组成部分。肠道菌群的变化可能是许多炎症性疾病发生的重要因素。而生活方式的改变可能改变了肠道菌群的初始发育或稳定维持。
本文从肠道菌群的功能,初始构建,到菌群健康/失衡的状态,以及相应的改善措施等进行全面阐述。
肠道菌群,居住在肠道(宿主)内的所有本土细菌的总和,被视为一个器官,执行着一系列重要的、对健康至关重要的功能,而这些功能无法通过任何其他方式复制。
研究人员通过比较无菌实验动物(没有任何肠道菌群)和正常菌群对照动物来确定这些功能。这些发现也在人群中得到了证实。
以下是肠道菌群最重要功能的简要概述:
◥ 粪便中的水分滞留
粪便主要是由水组成(平均水含量75%;各项研究的平均范围为63-86%)。单细胞生物,如细菌,主要含有水,被无法穿透的膜包围。
◥ 形成正常粪便
由于细菌是正常粪便中最主要的成分,它们的缺失可能会导致持续性慢性腹泻。
◥ 生产必需维生素
细菌会合成各种物质,包括某些复合维生素 B、维生素 B12 和维生素 K,这些物质对血液正常凝固至关重要。
◥ 保护肠道上皮(粘膜)免受病原体侵害
正常的肠道菌群控制着不良细菌的数量,例如白色念珠菌(酵母)或大肠杆菌的感染性菌株。保护机制有很多种,食物供应的竞争、对肠粘膜的粘附、维持所需的 pH 值平衡以及产生过氧化物和酶,从而杀死外来细菌。
◥ 组织发育和再生
与健康动物相比,无菌实验动物的肠粘膜(上皮)和淋巴组织(派尔氏斑)发育不良,肠道健康黏膜薄弱、免疫淋巴组织不发达等存在许多缺点。
◥ 免疫
正常肠道细菌负责实现吞噬作用:吞噬细胞在全身范围内破坏致病细菌、病毒、过敏原和其他异物,吞噬细胞是负责非特异性(抗体前)免疫系统防御的专门血细胞。
生命的前三年是可塑性增强的时期,肠道微生物群的发育很容易受到环境因素的影响。在婴儿期人与人之间的肠道微生物组差异变化最大,在成年期变得更加相似。
★ 婴幼儿
当婴儿出生后,在几口初乳后,大肠得到“培养”,初乳是一种淡黄色的液体,包含母亲的细菌,富含必需的营养。初乳先于富含脂肪和蛋白质的母乳流出。这个过程在母乳中继续,新生儿的肠道菌群在第6个月开始逐渐成熟,直到“成人”状态。
肠道微生物群的发育及主要影响环境因素
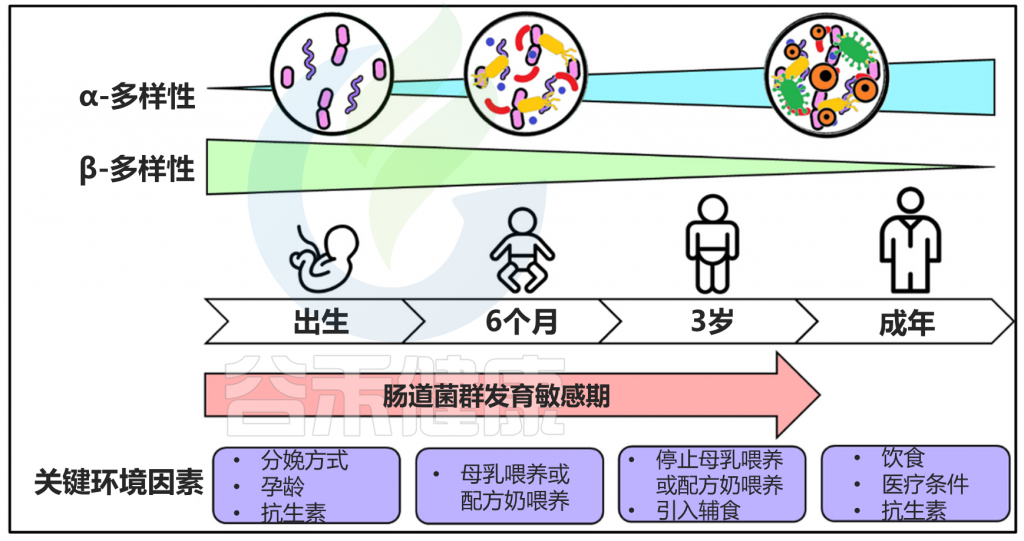

Parkin K et al., Microorganisms,2021