-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康
围产期营养是健康生长和长期发育轨迹的早期决定因素。关键发育时期的营养不良可以显著、持续地改变许多身体系统的发育过程,包括神经系统。
营养不良 是指热量、大量营养素或微量营养素的缺乏、过量或差异比例的改变。
研究表明,肠道微生物组可以调节饮食对宿主生理的影响,且调节神经系统的发育和功能。
本文围绕营养不良、肠道微生物群和神经发育三者之间的关系,讨论了围产期营养不良改变孩子大脑发育的证据,并研究了母体和新生儿微生物群作为一个潜在的促成因素,介导营养不良和大脑发育之间的关系。
常量营养素
生命早期蛋白摄入:与运动,智商,抑郁等都有关
营养不良的幼儿在社会行为上有缺陷。尤其是出生后早期蛋白质摄入与早产儿的运动和认知评分以及总脑容量呈正相关,与髓鞘形成相关缺陷、脑萎缩和心室扩张、皮质树突发育不良以及枕大池扩大和室周白质异常呈负相关。
出生后第一年低蛋白摄入的青少年表现出认知功能下降,包括儿童时期的智商和注意力下降,青春期抑郁症状增加。
生命早期脂肪摄入:影响大脑发育,甚至持续到成年
其他常量营养素也同样至关重要:在早产儿中,出生后早期脂肪摄入与更大的小脑、基底神经节、丘脑和全脑有关,此外还有内囊、辐射状晕、丘脑放射、后纵束和皮质脊髓束的分数各向异性增加。重要的是,大脑发育与后来的精神运动功能有关。
一些神经缺陷可能会持续到成年:在荷兰饥荒出生队列的118名成员中,暴露于产前营养不良与成年后期脑白质灌注减少,男性扣带皮层血流量减少,与男性衰老相关的大脑特征相关。
来自巴巴多斯的成年人在出生后第一年受到蛋白质限制,有持续的注意力缺陷,执行功能下降,包括认知灵活性、工作记忆和视觉空间整合。
微量营养素
出生后早期缺乏微量营养素,如维生素B12、叶酸和维生素K,也与脑萎缩和胼胝体变薄、精神疾病和颅内出血风险增加有关。
营养过剩
母亲营养过剩(怀孕前和/或怀孕期间的高BMI)与婴儿在认知和语言发展领域得分下降、视觉运动技能受损、社交和学习能力下降(尤其是男孩)、胎儿丘脑和皮质连接性改变有关。
实际上,营养需求以及这些需求得不到满足的后果可能比以前的模型所显示的更加复杂和相互依存,可能构成一个连续体,而不是营养不足和营养过剩的二元对立现象。
为了进一步了解营养不良作为一个连续体,研究产前营养不良的特定亚型破坏大脑和行为发育的基本机制至关重要。
肠道微生物群是饮食对宿主生理影响的关键决定因素,具有调节大脑发育和行为的能力。
饮食和营养的变化,改变了肠道微生物群的结构和功能,尤其是在发育的关键时期。
营养不良——α多样性下降:
孟加拉国2岁以下儿童出生后严重急性营养不良与微生物α多样性(物种丰富度和均匀度)下降相关,表明菌群不成熟的情况即使在饮食干预后也持续存在。在一个类似的队列中,α多样性降低的原因是发育迟缓和非发育迟缓儿童之间噬菌体(细菌病毒)的差异。
营养不良不同亚型,α多样性下降程度不同:
在塞内加尔和尼日尔的幼儿中,出生后营养不良亚型之间的微生物多样性差异显著:
不同亚型之间的菌群构成差异:
出生后严重急性营养不良儿童体内的微生物群减少,代谢和营养吸收相关的功能途径减少,毒力相关基因增加。还显示肠道氧化还原电位增加,这可能是微生物群落组成改变的功能结果。
营养不良——α多样性升高:
相比之下,与对照组和不同营养不良亚型相比,乌干达2岁以下儿童出生后夸希奥科病表现出α多样性升高,β多样性略有差异,相对分类丰度发生变化。
营养过剩:
关于营养过剩,人类妊娠期母体高脂肪饮食与婴儿微生物群的改变相关,如肠球菌增加和拟杆菌减少。
这些发现强调了营养不良对肠道微生物群的关键特定环境影响,并进一步强调了考虑干预措施时同样需要特定环境的方法。
有意思的是,仅仅改变饮食组成并不能决定营养不良;相反,宿主和微生物群对饮食的反应是营养不良表型表现的关键因素。
与相同饮食的未受影响的双胞胎相比,出生后营养不良的马拉维双胞胎改变了微生物群。与从未受影响的双胞胎中移植微生物组相比,将与营养不良相关的微生物组移植到小鼠体内,除了体重显著减轻(类似于人类营养不良的生长限制特征)之外,还产生了微生物分类特征和代谢物水平改变。
这些发现提供了强有力的概念证明,肠道微生物群因营养不良而改变,并可能导致早期营养不良对生长和发育的有害影响。
其他研究强调了开发基于微生物的治疗早期营养不良核心症状的潜力。
在一项对出生后营养不良的5岁以下儿童进行的人体研究中,这些儿童的特征是体重和身高较低,与单独给予充足饮食的儿童相比,补充充足饮食的鼠李糖乳杆菌GG减少了感染,增加了BMI,并提高了蛋白质水平。
此外,为支持肠道微生物群的健康成熟和发展而配制的“微生物群导向食品”被证明可以改变肠道微生物群,改善出生后中度急性营养不良(MAM)儿童的骨骼和免疫发育。
然而,干预可能不是普遍有效的。
在对来自尼加拉瓜和马里的婴儿进行的米糠补充剂比较中,来自不同地理区域的婴儿表现出不同的结果:尼加拉瓜婴儿的身高分数有所提高,但马里婴儿没有,每个婴儿都有不同的微生物分类特征和代谢物水平。
这些研究强调了营养不良对肠道微生物群的不同影响,并将其作为机械研究和治疗干预的潜在目标。

越来越多证据表明,微生物群影响营养不良后代生长的能力,这提出了一个重要问题,即微生物群是否也会促使与营养不良相关的神经发育异常?
在一个来自孟加拉国的出生后严重急性营养不良儿童队列中,以微生物群为目标的饮食治疗不仅改善了生长受限和微生物不成熟,还改变了血浆激素、代谢物的水平和与神经发育相关的关键蛋白的表达,如轴突导向线索和神经营养蛋白受体。这些变化还与短链脂肪酸、特定氨基酸、羟基邻氨基苯甲酸和吲哚-3-乳酸的变化有关,表明饮食干预对微生物和神经发育有依赖反应。
同样,孟加拉国产后MAM儿童在接受同样的饮食干预后显示出年龄体重和长度体重增加,后者也与轴突引导和神经营养因子相关的血浆蛋白以及23种肠道分类群呈正相关,包括Prevotella copri、Faecalibacterium prausnitzii。
低体重早产儿显示头围和微生物α多样性减少,葡萄球菌科和肠杆菌科相对丰度增加,与脂肪酸氧化和脂解相关的代谢物增加。而在出生后第一周接受益生菌/益生元补充剂的低体重早产儿体重增加更好,头围更大,仅肠道喂养的时间更短。
在动物模型中,营养不良、微生物群和大脑发育之间存在类似的联系。
在怀孕和哺乳期间喂食高脂肪食物的小鼠所生的后代表现出认知缺陷和不同的微生物群,这些微生物群基于母体饮食而聚集在一起。研究人员确定了后代中的特定分类群,包括梭状芽孢杆菌、Parabacteroide和变形杆菌,它们与母体肥胖和后代认知缺陷相关。
在一项独立的小鼠研究中,母亲在妊娠期和哺乳期食用高脂肪饮食改变了母亲和后代微生物群的组成,并产生了室旁核催产素阳性神经元减少、腹侧被盖区多巴胺能长时程增强中断和社交行为受损的后代。重要的是,微生物组的变化被证明是因果关系:用高脂肪食物喂养的母鼠后代与对照后代共同饲养,纠正了微生物组和社会缺陷。
此外,补充在高脂肪饮食相关微生物群中显著减少的罗伊乳酸杆菌Limosilactobacillus reuteri,足以挽救喂养高脂肪饮食的母鼠后代的社交行为、中枢催产素表达和长时程增强的缺陷。
总的来说,这些研究提供了证据,表明肠道微生物群可能有助于营养对神经发育和行为的影响。
直接信号机制:与神经发育相关的微生物依赖代谢物
由肠道微生物群产生或调节的代谢物因其在调节包括中枢神经系统在内的各种生理系统功能中的作用而受到关注。在产前营养不良的情况下,母体微生物组调节的代谢物亚群能够穿过胎盘,并在出生前与胎儿相互作用。
母体肠道微生物群如何介导营养不良对早期神经发育影响的概念模型
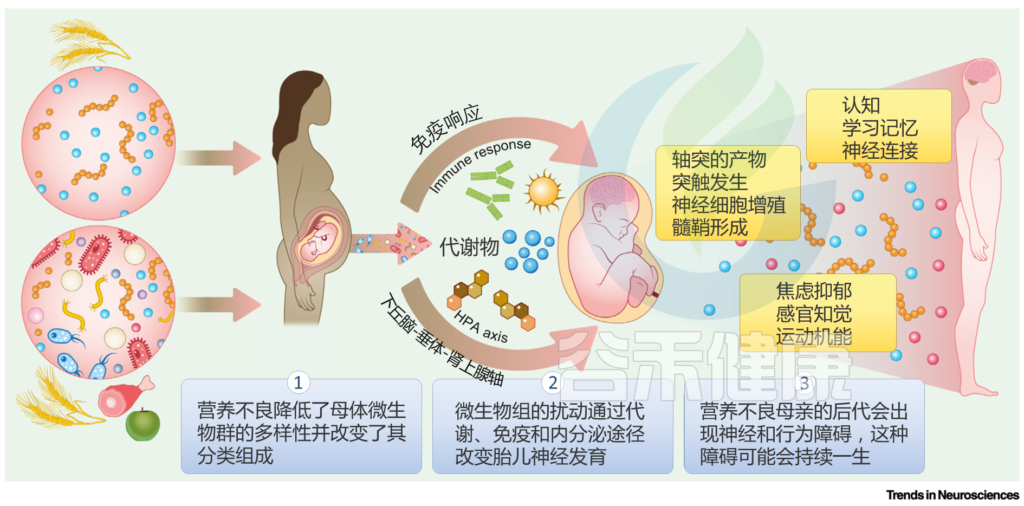
1:营养过剩和不足,以及宏量或微量营养素比例的变化,都会导致妊娠期母体微生物群的紊乱。这些扰动包括特定分类群的多样性和相对丰度的变化。
2:母体营养的变化影响循环生物分子、免疫稳态和内分泌功能。这些变化可能是由观察到的母体微生物群的变化介导的。
3:母体生物学的这些变化会反过来直接或间接影响胎儿,包括发育中的胎儿大脑。出生前或出生后早期营养不良的后代在关键的神经发育过程中表现出损伤,这可能导致大脑功能和行为的持续异常,并且可能由微生物过程介导,直接或间接机制。
短链脂肪酸在神经发育中发挥作用
短链脂肪酸如乙酸盐、丙酸盐和丁酸盐尤其重要,因为它们是复杂碳水化合物微生物发酵的直接最终产物,被认为在神经发育过程(如小胶质细胞的早期成熟)中起关键作用。
人类营养不良与全身短链脂肪酸、氨基酸和各种微生物群依赖性代谢物的改变有关,表明微生物群影响对饮食营养不良的代谢反应。
在一项人类队列研究中,母体血清中丙酸盐和丁酸盐的水平与脐带血中相同分子的水平相关,这突出表明了母体对短链脂肪酸的生物利用度对发育中的后代产生影响的潜力。
妊娠期喂食低纤维饮食的小鼠的后代表现出运动和学习/记忆行为受损,焦虑样行为增加,海马谷氨酸受体亚单位表达和兴奋性突触后电位降低,这支持了短链脂肪酸在神经发育中的作用。
此外,低纤维饮食的母鼠具有不同的微生物群,包括较高的厚壁菌门和较低的拟杆菌门,以及母鼠血清、子代血清和脑中较低水平的丁酸盐和丙酸盐。
重要的是,妊娠期补充丁酸盐减轻了后代的异常,似乎是通过降低海马中组蛋白去乙酰化酶(HDAC) 4的表达。
碳水化合物代谢
此外,在尤卡坦迷你猪妊娠和哺乳期间的营养过剩模型(使用高果糖、高脂肪和高能量饲粮)中,高脂肪饲粮的母猪妊娠期间粪便短链脂肪酸减少,血浆游离脂肪酸增加,后代在出生后1-3个月表现出相似的表型。仔猪的这种表型与海马神经发生减少相一致,特别是在颗粒细胞层,但工作记忆和参考记忆的增加是矛盾的,这可能可以用对含糖食物奖励的动机差异来解释。
类似地,在妊娠期和哺乳期喂食高脂肪食物的小鼠后代表现出长期和工作记忆受损,社交能力和社交新鲜感偏好降低,乙酸盐、丁酸盐和丙酸盐水平降低,SCFA受体Olfr78以及与小胶质细胞成熟、谷氨酸能信号传导、神经发育和前额皮质和海马突触可塑性相关的基因表达降低。
此外,微生物组被母亲的饮食改变,包括特定的类群,如S24-7,双歧杆菌,普雷沃氏菌,梭状芽孢杆菌,瘤胃球菌,并被证明与神经系统有因果关系,如共住,粪便微生物移植,不同饮食的交叉培养,在改善后代的缺陷方面是有效的。
有趣的是,行为、神经生理和细菌干扰通过母体或断奶后后代的高纤维饮食以及断奶后后代的乙酸盐和丙酸盐补充得以挽救。这表明短链脂肪酸在调节饮食对肠道微生物群和大脑的影响中发挥了作用,而且这些干预超越了传统理解的关键期。
这些研究表明微生物碳水化合物代谢在大脑发育中发挥作用。
蛋白质代谢
除了碳水化合物代谢产物,主要由蛋白质代谢产生的微生物依赖代谢物也与早期营养不良与神经系统的改变有关。
在来自赞比亚和巴西的出生后2.5岁以下急性营养不良儿童的队列中,在尿液中测得的各种肠道微生物相关代谢物(如硫酸3-吲哚酚和三甲胺,它们分别是响应L-色氨酸和膳食肉碱的微生物代谢而产生的)与肠病和生长的测量值呈负相关。
尤其是硫酸3-吲哚酚,因为它还被证明能促进小鼠感觉行为基础上的胎儿丘脑皮层回路的发育。
来自乌干达的患有产后严重急性营养不良的儿童在治疗前显示出高水平的偶链酰基肉碱。在妊娠中期的猪胆碱缺乏模型中,产前缺乏的小猪的大脑比对照组小,并且后代显示出微生物群依赖性代谢物的出生后变化,例如增加的脱氧肉碱。
此外,一项针对35对母婴的前瞻性研究报告称,肥胖母亲的母乳与瘦母亲相比代谢物水平不同,包括各种酰基肉碱和人乳低聚糖(HMOs),这对婴儿微生物群的发展至关重要。诸如此类的研究展示了微生物蛋白质代谢与神经发育相关的潜力。
脂质代谢
脂质相关代谢物也与婴儿微生物群和大脑发育有关,并且可能类似地被母体营养不良所改变。
唾液酸寡糖影响神经系统发育,依赖微生物的存在
在马拉维的一个队列中,观察到严重发育迟缓婴儿的母亲中,唾液酸化HMOs显著减少。当将唾液酸寡糖添加到有发育不良婴儿菌群的无菌小鼠和仔猪,并喂食马拉维饮食时,与对照组相比,动物表现出生长加快和血清、肝脏、肌肉和大脑中的代谢物改变。
特别受影响的是N-乙酰神经氨酸(神经节苷脂的一种成分,对突触发育和功能很重要),在神经免疫系统中起作用的腺苷,以及肌苷(一种具有神经保护特性的嘌呤核苷)。 这些变化被证明是依赖微生物的,因为无菌动物缺乏同样的积极影响。
肠道菌群影响神经酰胺变化,与大脑发育有关
在一项纵向研究中,妊娠中期检查的产前超重/肥胖母亲及其4年随访检查的后代显著降低了血浆神经酰胺,这是一类受肠道微生物群广泛调节的鞘脂。
有意思的是,鞘脂在神经发育中起着至关重要的作用:它们是形成髓鞘的主要成分,它们的表达支持关键的发育过程,包括神经元分化,它们的耗竭导致不正常的轴突生长和突触形成。这些结果表明,脂质代谢物中的微生物依赖变化可能与发育中的大脑相互作用。
总之,这些研究支持了微生物调节的营养分解代谢产物影响神经发育过程的潜力。
间接信号机制:微生物对影响神经发育的次级系统的潜在影响
除了调节在神经发育中具有直接作用的饮食代谢物之外,微生物组还可以通过间接改变神经发育轨迹的方式与宿主生理学相互作用。
例如,微生物组调节免疫发育和功能,早期神经免疫相互作用是健康围产期神经发育的组成部分。营养不良模型与免疫受损和炎症增加有关,与母体或发育中微生物群的改变有关。
促进炎症反应
在啮齿类动物中研究了怀孕期间通过感染或抗原暴露激活母体免疫系统的情况,通常显示会诱发神经发育和行为异常。这些异常与肠道微生物组组成的广泛改变有关,这种改变是由母体与肠道微生物组中促炎的分段丝状细菌定植介导的。脆弱拟杆菌治疗,一种促使免疫抑制的共生细菌,被证明可以改善由母体炎症引起的异常。
此外,由肠道细菌诱导的T辅助细胞17产生的IL-17a,对于传递母体炎症的神经和行为影响是必须的。
总的来说,这些研究提供了一个概念证明,即母体微生物组的变化可以通过促进炎症反应来改变神经发育,并进一步提出了一个问题,即母体营养不良是否可以通过免疫介导的途径影响神经发育来类似地塑造微生物组。
调节应激系统
营养不良引起的微生物组改变可能影响神经发育的另一个潜在途径是通过调节应激系统。
许多将微生物群与神经系统联系起来的研究都集中在焦虑系统和行为上,这些研究确立了微生物群在调节下丘脑-垂体-肾上腺轴功能中的可复制作用。
此外,营养不良可在人类和啮齿动物中诱发应激反应,应激是一种已知的发育扰乱因素:母体皮质酮治疗(水平类似于内源性应激源)减少了胎盘灌注和向胎儿的氨基酸转移。
微生物对环境应激反应的调节可以间接影响神经发育,如在产前应激小鼠模型中,母体阴道和婴儿肠道微生物群中乳酸杆菌种类的减少与婴儿代谢物和脑氨基酸的改变相关。
此外,母体阴道微生物群的移植有助于产前应激对下丘脑基因表达的影响。鉴于微生物组与压力信号和压力性疾病有关,可能是营养不良引起的压力与微生物组相互作用,导致后代神经发育变化。
影响早期表观遗传编程
最后,一个新兴的研究领域集中在微生物组影响早期表观遗传编程的潜力上。
微生物组被认为是营养代谢和表观遗传调节的关键介质。微生物依赖的短链脂肪酸,如丁酸盐,作为HDAC抑制剂起着关键作用,在无菌小鼠中,长非编码RNA以组织特异性方式差异表达。
营养不良中的表观遗传调节也有证据:在一项对168名人类受试者出生后第一年的蛋白质-能量营养不良的多代研究中,134个区域根据营养状况差异甲基化,包括特定的神经精神风险基因,如COMT、ABCF1、SYNGAP1、IFNG,它们与注意力和/或智商的测量相关。
与这些表型一致,妊娠期蛋白质限制的大鼠表现出注意力缺陷,大脑皮层葡萄糖代谢减少,前额叶皮层干扰素γ表达减少。此外,在怀孕期间,营养胆碱与其他物质如维生素B12和叶酸一起,通过提供甲基并作为辅助因子来修饰DNA和组蛋白甲基化。
基于这些研究,微生物组可能通过直接或间接的信号通路介导母体营养不良对胎儿神经发育的影响。
围产期营养不良及其与肠道微生物群和神经发育的关系日益成为研究的焦点,需要进一步的流行病学和机制研究。
需要对营养不良研究的当前范式进行批判性审查:
营养不良的亚型(大量营养素过量与不足、微量营养素缺乏等)真的应被视为具有特定机制和表型的独特条件?
还是应该将营养不良视为一个连续体,即一种营养素的缺乏可能会内在地改变其他营养素的相对丰度,并且可能存在共同的潜在途径和/或表型?
由于不同营养物质的交互作用,很难将营养不良的单个方面的影响与其他方面分开。虽然在简化主义实验设计中易被忽略,但实际可能会构成一系列营养需求和影响。
此外,也需要准确理解营养不良期间肠道微生物群如何影响神经发育,以及它们之间的关系如何与其他身体系统相互作用,如免疫和压力反应。
随着对于微生物群的了解不断深入,将微生物组作为营养不良的一个促成因素,为潜在的临床诊断和干预措施提供思路。
参考文献:
Neves P.A.R. et al., Poor maternal nutritional status before and during pregnancy is associated with suspected child developmental delay in 2-year old Brazilian children. Sci. Rep. 2020; 10: 1851
Coley Elena J L,Hsiao Elaine Y,Malnutrition and the microbiome as modifiers of early neurodevelopment.[J] .Trends Neurosci, 2021
Mirzaei M.K. et al., Bacteriophages isolated from stunted children can regulate gut bacterial communities in an age-specific manner. Cell Host Microbe. 2020; 27: 199-212
Gehrig J.L. et al., Effects of microbiota-directed foods in gnotobiotic animals and undernourished children. Science. 2019; 365: 139
Sanguinetti E. et al., Microbiota signatures relating to reduced memory and exploratory behaviour in the offspring of overweight mothers in a murine model. Sci. Rep. 2019; 9: 12609
Jasarevic E. et al., The maternal vaginal microbiome partially mediates the effects of prenatal stress on offspring gut and hypothalamus. Nat. Neurosci. 2018; 21: 1061-1071