-

 国家认可委 CNAS L23010 认可项目:微生物宏基因组 | 16S rRNA扩增子
国家认可委 CNAS L23010 认可项目:微生物宏基因组 | 16S rRNA扩增子

 二级病原微生物安全实验室
二级病原微生物安全实验室 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康
下一代益生菌
传统益生菌在维持肠道稳定性方面具有一定优势,但其作用效果受宿主遗传背景、菌株生物学特性以及个体肠道微生态环境等因素的制约,这也使得其在临床应用中呈现出多样化的效果,且在调控全身性疾病方面仍需进一步探索其潜在机制。
与传统益生菌不同,下一代益生菌(NGPs)采用基因工程和下一代测序技术来识别具有特定功能特性的细菌菌株。一些研究者认为,下一代益生菌可能在微生物治疗领域具有发展前景,为某些健康问题的管理提供新的思路。
下一代益生菌(NGPs)通过筛选具备特定功能的菌株,不仅在肠道内发挥作用,还通过其他途径影响全身的免疫系统、代谢过程和神经调控机制。相较于传统益生菌,NGPs在以下方面具有显著优势:
①多系统靶向性——不仅修复肠道屏障,还可通过肠脑轴、口腔、皮肤、呼吸道等通道调控局部与全身免疫反应;
②精准性与个体化潜力——结合基因组学与代谢组学,可实现更精准的宿主-微生物互动干预;
③作用机制的扩展性——不仅抑制病原体、抗炎,还能通过代谢产物和免疫调控网络实现更广泛的治疗效应。
当前,NGPs的主要种类包括但不限于:
嗜黏蛋白阿克曼菌(Akkermansia muciniphila)、普拉梭菌(Faecalibacterium prausnitzii)、丁酸梭菌(Clostridium butyricum)、Eubacterium hallii及若干经基因改造或筛选的菌株,它们在慢性炎症、胃肠道疾病、代谢综合征、皮肤健康、口腔健康、免疫相关疾病以及精神疾病等多种疾病的治疗与缓解中展现出潜在价值。
随着基因组学、代谢组学、表观遗传学及循证临床研究的迅速发展,新型益生菌有望成为个体化干预的新载体,将疾病管理从“治疗反应”转向“精准预测与预防”。
什么是益生菌?
“益生菌(probiotics)”一词源自希腊语/拉丁词根
oro(意为’为了’)与bios(意为’生命”),这主要体现了这些生物体在确保生命健康方面的作用。
益生菌是具有活性的微生物,主要是细菌和酵母,在给予足够剂量时具有健康益处, 益生菌已被证明能改善消化健康、免疫系统功能,甚至心理健康。
有效益生菌微生物的特征
doi: 10.1007/s11033-024-09398-5.
◮ 益生菌发挥效果的条件
同时益生菌要发挥效果,必须:
-忍受胃的酸性环境;
-活着抵达肠道;
-附着在肠道细胞上以发挥其益处;
-与有害细菌竞争;
-以及在肠道内定植到一定程度。
益生菌的发展历史
益生菌的概念源远流长,我们在这里简要梳理益生菌的起源及其随时间的演变。以下为历代发展要点的回顾。
◮ 古代起源
中东和中亚:两千多年来,发酵乳制品已被证明是一个值得关注的问题。中东和中亚被视为大约1万年前处于原始发酵状态的文明的摇篮。
亚洲:在古代中国和日本,也有纳豆和味噌等富含益生菌的食物,分别是发酵大豆和大豆酱。
◮ 19世纪及20世纪初:科学发现
益生菌一词直到19世纪末才进入科学界。随着微生物学的兴起,巴斯德揭示了发酵由微生物所驱动,从而解释了为何某些菌类存在是为了发酵。
1907年,梅契尼科夫被誉为“益生菌之父”,指出保加利亚农民的长寿与牛奶发酵有关,乳酸菌能阻止细菌损害宿主肠道,防止自毒与衰老。1908年,梅契尼科夫因在免疫学领域的研究荣获诺贝尔奖,进一步提升了公众对乳酸菌的认知。
◮ 20世纪中叶:益生菌产品的发展
在20世纪40–50年代,仿制食品成为益生菌引入的关键因素。自1935年起,日本率先开展商业益生菌饮料“养乐多”的生产;1939年,通过干酪乳杆菌(Lactobacillus casei)展示了益生菌在胃肠治疗中的潜力。
随后,研究扩展至其他菌株,甚至酵母菌也被探索,其中Saccharomyces boulardii已用于腹泻治疗。
◮ 现代科学中的益生菌
益生菌研究广泛开展,尤其关注其在医学上的潜在益处。自1970年代初起,益生菌的活性逐步增强,医学与微生物学的结合揭示了其积极影响的机制。此间,益生菌不再仅是传统发酵食品的成分,而是逐渐被视为可用于治疗特定健康问题的药物。
▸ 益生菌如何与微生物群相互作用
益生菌的作用机制错综复杂,涵盖众多对消化系统有益并增强免疫力的作用过程:
益生菌的作用机制
编辑
doi: 10.1007/s12602-025-10606-2.
1) 病原体的竞争排斥
益生菌通过竞争排斥来抑制病原微生物的生长:利用可用资源并争夺肠道受体位点,限制入侵生物的扩张。
此外,某些益生菌还能分泌抑制物(如细菌素),抑制致病菌增殖,从而提升整个细菌群落的健康水平。
2) 免疫反应的调节
益生菌还能通过诱导调节性T细胞来调控免疫反应,这些T细胞维持免疫平衡,避免对无害物产生过度反应。因此,益生菌在炎症并发症如炎症性肠病和自身免疫性过敏的管理中具有关键作用。
它们还支持健康的免疫反应,帮助抵抗感染、在必要时抑制过度炎症,并整体促进免疫健康。
3) 强化肠道屏障
益生菌的重要性在于提升黏膜质量与细胞间紧密连接的完整性,从而预防肠漏综合征。肠漏指肠壁的病理生理改变,导致有毒物质进入循环并引发炎症。Faecalibacterium prausnitzii和Akkermansia muciniphila这两种菌株被公认有助于维持肠道屏障功能,前者对黏膜覆盖也有保护作用。
4) 有益代谢产物的生成
益生菌能合成重要代谢产物,如短链脂肪酸(SCFAs)—丁酸、乙酸、丙酸等。证据显示SCFAs具有抗炎作用,促进肠道稳态、保护细胞完整性并缓解炎症,滋养结肠上皮,帮助维持健康的肠道黏膜。此外,SCFAs在调节与健康微生物群相关的免疫与代谢方面也发挥重要作用。
益生菌的作用机制
编辑
doi: 10.1007/s12602-025-10582-7.
5) 对肠-脑轴的影响
近期研究显示,益生菌通过肠脑轴影响心理状态的潜力。某些菌株能产生神经递质,如血清素与GABA,调节情绪与压力水平。
瑞士乳杆菌和长双歧杆菌已被证实可缓解焦虑、改善情绪,从而将健康微生物群与心理健康联系起来。
随着对人类微生物群落的深入了解,益生菌及其产品开发的研究日益广泛。借助现代微生物学工具,如PCR的16S rRNA检测、下一代测序(NGS)和生物信息学,我们能够更精准地识别和检测肠道细菌菌株。
最近,基因组测序与培养技术的进步促使从人类微生物组中分离出多种新型微生物,显示出良好的健康益处和益生菌潜力,因而有望发展成为下一代益生菌(NGPs)。
下一代益生菌(NGPs)的定义
下一代益生菌(NGPs)是指基于宏基因组学或16S rRNA测序等比较微生物组研究,遴选或工程改造的特定菌株。这些菌株在适当摄入量下,通过调节宿主肠道微生物群落结构或功能,对特定疾病状态的改善具有潜在的生物学效应和科学证据支持。与传统益生菌相比,NGPs针对性更强,而且有的已经累积了更多相关临床研究数据。
这类非传统益生菌包括嗜黏蛋白阿克曼菌(Akkermansia muciniphila)和普拉梭菌(Faecalibacterium prausnitzii)等,它们可改善肠道健康、降低炎症并增强肠道屏障。
下表总结了传统益生菌与下一代益生菌(NGPs)之间的主要区别。
▸ 对下一代益生菌(NGPs)的需求
益生菌的修复与预防作用已广泛被认可和应用,不仅有助于消化健康,也提升免疫与整体健康。传统定义多聚焦于含发酵菌株的产品,如乳杆菌和双歧杆菌,在大量应用中发挥作用。然而,随着人类微生物组的日益复杂与深入了解,经典益生菌未必能满足所有健康需求,因此出现了新型益生菌(NGPs),旨在更精准地解决更多健康问题。
下一代益生菌可能的治疗作用
编辑
doi: 10.1007/s11033-024-09398-5.
1) 针对复杂疾病
全球慢性疾病如肥胖、糖尿病、自身免疫性疾病和精神健康障碍的患病率持续上升,促使科学界逐步揭示微生物组在这些疾病中的作用。这为非处方的下一代益生菌(NGPs)提供了更有针对性的治疗潜力。
例如,Akkermansia muciniphila与健康个体的优良新陈代谢活性相关,并有助于维持黏膜屏障;而屏障的降解与代谢性疾病密切相关。Faecalibacterium prausnitzii 被视为抗炎菌株,突显了其在炎症性肠病(IBD)治疗中的潜力。
2) 个性化医疗与精准健康
下一代益生菌(NGPs)正与日益增长的个性化医疗需求融合:根据患者的基因、代谢或微生物组特征来治疗个体疾病。
与此同时,益生菌研究持续推进,致力于深入理解肠道微生物组,以实现精准、定制的益生菌处方。
3) 通过调节微生物群落提高疗效
下一代益生菌(NGPs)更接近于益生元,研究显示,一些NGPs能释放代谢产物,调控群落结构与活性,长期有助于健康。例如,它们可产生短链脂肪酸(SCFAs)如丁酸,具有显著的抗炎作用,对肠道环境至关重要。相比之下,传统益生菌尽管可提高SCFA水平,但由于功能特性,其贡献可能不及NGPs。
4) 心理健康与肠-脑轴
近期肠-脑轴研究显示,肠道微生物组的状态显著影响心理健康、情绪、应激反应与高级认知功能。传统益生菌在此领域的作用有限,新型益生菌则具更大治疗潜力。
例如,脆弱拟杆菌与植物乳杆菌可能影响脑功能。新型益生菌能合成多种功能性代谢产物,用于调节脑活动,治疗焦虑、抑郁及其他精神障碍等问题。
5) 肠道屏障完整性与免疫调节
对于慢性疾病与自身免疫过程,肠道病变引发的免疫过度激活会使有毒物质从肠道扩散入血。新型益生菌,如嗜粘蛋白阿克曼菌,通过增强肠道黏液层提升屏障防御,进而减轻全身炎症。
此外,NGPs 还可调控免疫细胞功能与促炎/抗炎反应的平衡,可能有助于治疗免疫相关疾病。
6) 在癌症治疗中的潜在应用
下一代益生菌(NGPs)在癌症管理领域的应用备受关注。研究表明,某些微生物组变体可增强免疫疗法的效果。通过使用特定菌株,可提升宿主免疫系统对肿瘤细胞的杀伤力,从而为癌症治疗中的益生菌辅助治疗提供新的可能性。
▸ 下一代益生菌的标准
与传统益生菌相比,下一代益生菌(NGPs)能更有效、更精确地解决复杂的健康问题。考虑到功能性、特异性和安全性,已提出了一些标准来界定新型益生菌。关键标准如下:
1) 菌株特异性和选择
下一代益生菌(NGPs)通常源自非传统菌株,相较于乳杆菌和双歧杆菌等传统益生菌,它们在特定健康领域具更大潜力。每种菌株的选择都以实现精确的健康目标为导向,如代谢、免疫或认知健康,以提升针对性治疗效果。
2) 作用理解
就NGPs而言,核心在于菌株对免疫反应的调控、益生代谢物的产生、肠道通透性的改变,以及与宿主微生物组的相互作用机制。多数NGP已被筛选或改造以产生代谢物(如SCFA、神经活性物质)并执行支持其健康益处的功能。
3) 临床疗效和针对性健康益处
应通过一致的前临床与临床研究证明NGPs在健康状况下的病情调节功效。在某些情境下,可能表现为提升胰岛素敏感性以改善代谢健康,或通过调控炎症来治疗自身免疫性疾病。这种功效使NGPs从一般肠道健康支持,扩展到糖尿病、炎症性肠病和精神疾病等特定疾病的治疗。
4) 生存能力和定植潜力
要让NGPs菌株成功定植,关键在于其能耐受胃肠道恶劣环境,并在可能的情况下实现内腔幼体的稳定定植,以确保长期的遗留效应。其在宿主微生物组中的建设性相互作用以及在胃酸环境中的存活能力,对疗效至关重要。
5) 安全性和最小不良反应
安全性备受关注,部分原因在于许多新型益生菌来自非传统来源,且人类使用的历史证据稀少。因此需进行严格的综合安全评估,包括毒性和长期安全性研究。应尽量减少并密切监测可能引发不良反应的机制,如免疫紊乱或对自然微生物群的破坏。
6) 个性化应用的潜力
随着个体微生物组的多样性,开发下一代益生菌(NGPs)时已将个性化纳入考量。这意味着选取或设计符合特定微生物组特征或个人健康状况的菌株。
个性化的NGP应用通过识别微生物失衡与健康风险,提供更定制化的干预,因此产生了在健康益处上更具针对性的NGP,成为个性化与精准医疗领域的宝贵资产。
小结
传统益生菌和新型益生菌之间的主要区别
编辑
总得来说,新一代益生菌(NGPs)相对于传统益生菌的科学、具体优势主要有以下几点:
•更广的靶向健康作用谱;
•更强的肠道微生态调控能力;
•更精准的作用机制与靶点;
•先进的制备与设计策略;
•改善药品监管与可控性前景
•增强个体化干预潜力;
•安全性与耐受性改进方向。
传统益生菌和新型益生菌的特征比较
编辑
doi: 10.1007/s12602-025-10582-7.
下一代益生菌(NGPs)中具有潜力的候选株正在逐步浮出水面,其中一些已在代谢调控、炎症抑制和跨系统健康影响方面显示出特别的潜力。如Akkermansia muciniphila、Faecalibacterium prausnitzii、Clostridium butyricum、Christensenella minuta等,初步研究显示它们在代谢调控、炎症抑制和肠-全身轴的潜在影响方面具有积极信号。
但这类证据尚处于早期阶段,且个体差异、长期安全性、给药策略与潜在不良反应尚需进一步验证。此外,NGP 需要经过严格的毒理学评估、长期随访与可重复的生产质量控制,才能避免潜在风险并确保可追溯性。因此,在扩展NGP候选池时,必须遵循安全优先、证据驱动、标准化与伦理法规合规的原则,强调并非所有物种都具备成为下一代益生菌的潜力,也不应过早推广到临床应用。
Akkermansia muciniphila
极具潜力
嗜黏蛋白阿克曼菌(Akkermansia muciniphila,Akk)是一种定居肠道黏膜的共生菌,作为下一代益生菌的有力候选。它在增强代谢与免疫反应方面发挥关键作用,并可能改善癌症治疗效果。
◮ 能利用黏蛋白,促进肠道屏障完整性
A. muciniphila能够利用肠道黏膜层的黏蛋白与糖蛋白作为唯一的氮碳来源,促进肠道屏障完整性并附着于黏膜,是一种有益的益生菌特征。
肠道黏膜中该菌含量下降会削弱屏障,增加毒素侵袭风险。它不仅参与葡萄糖、脂质和蛋白质代谢,还影响黏膜层的完整性与黏膜免疫反应,因此对肠道健康具有支持作用。
◮ 在肥胖、炎症性肠病、自闭症中都发挥作用
近年研究表明A.muciniphila在机体稳态与疾病中具有重要作用。其丰度与多种疾病相关,水平下降与肥胖、炎症性肠病、自闭症和2型糖尿病等相关。
它通过调节神经系统控制葡萄糖代谢,帮助抵御肥胖与糖尿病。研究还发现经巴氏杀菌的A.muciniphila可显著延长结肠长度、增强对肥胖与胰岛素抵抗的抵抗力,且炎症性肠病与代谢疾病患者常见其水平降低,提示潜在抗炎作用。此外,A.muciniphila还能增强某些抗癌治疗在动物模型中的效果。
总体而言,益生菌领域的最新证据支持A.muciniphila作为可行治疗靶点,其水平变化可作为疾病进展的潜在生物标志物。因此,A.muciniphila在癌症、代谢综合征、炎症性肠病及免疫相关疾病等领域具有广阔的临床潜力。
肠道重要菌属——Akkermansia Muciniphila,它如何保护肠道健康
Faecalibacterium prausnitzii
具有较高潜力
普拉梭菌(Faecalibacterium prausnitzii)是一种极具前景的下一代益生菌。
F.prausnitzii在肠道中的下降与微生物群失调及多种代谢疾病和慢性免疫介导疾病(如炎症性疾病和肥胖)相关,并常作为衡量年轻肥胖者是否患溃疡性结肠炎的生物标志物,这可能源于其促进黏蛋白与紧密连接蛋白合成、修复受损肠黏膜的能力。此外,它还能调控粘液分泌、肠道杯状细胞分化和糖基化,并维持黏液屏障完整性,因此被视为有益的益生菌,对肠道具有关键保护作用,其枯竭会削弱肠道免疫调控与抗炎能力。
◮ 重要的产丁酸菌、具有抗炎活性
F.prausnitzii被认定为肠道中最重要的丁酸生产者之一。丁酸是肠道上皮细胞的主要能量来源,调节肠道T细胞的活性,抑制病原体入侵,促进结肠癌细胞凋亡,预防肠道炎症,调节免疫系统,并帮助代谢综合征恢复。
此外,F. prausnitzii还会产生来自微生物抗炎分子(MAM)的肽,抑制宿主激活NF-κB通路。这些活性代谢物的优点包括抗炎活性、维持肠道屏障功能、肠道免疫稳态以及在结直肠癌细胞中诱导凋亡。
◮ 可作为癌症免疫治疗中的调节因子
目前,从健康人群中分离出的F. prausnitzii已被证明具有体外抗炎和免疫调节活性。此外,Faecalibacterium属候选物种已被研究为癌症免疫治疗中的调节因子。研究人员发现肠道中Faecalibacterium的浓度与癌症患者的存活率之间存在关联。
此外,科学家们发现,黑色素瘤转移期间,调控T细胞数量和促炎细胞因子IL-2、IL-8和IL-6的血液水平与肠道中Faecalibacterium的数量呈负相关。因此,F. prausnitzii被认为是黑色素瘤患者的关键治疗靶点和预后标志物。
肠道核心菌属——普拉梭菌(Faecalibacterium Prausnitzii),预防炎症的下一代益生菌
Clostridium butyricum
具有较高潜力
丁酸梭菌(Clostridium butyricum)是一种嗜氧、形成孢子的革兰氏阳性细菌,因其发酵非碳水化合物并高产丁酸而得名。
◮ 对肠道健康、免疫调节有益,甚至改善抑郁
丁酸梭菌,被认为对炎症性肠病有益,并起到免疫调节作用。它已被用于肠道健康支持、免疫调节和感染预防。丁酸梭菌还对肠上皮增殖和维持结肠健康至关重要。
有研究报道了丁酸梭菌的抗癌潜力,观察到其可显著抑制小鼠肠道肿瘤形成、减少肠道癌细胞增殖并诱导凋亡。此外,丁酸梭菌的益生菌株与抗抑郁药联合使用,可显著改善抑郁症状。
Christensenella minuta
具有较高潜力
Christensenella minuta已成为下一代益生菌(NGPs)候选者中的重要一员,显示出在代谢调控与炎症抑制方面的潜力。
◮ 改善能量平衡、降低炎症水平
C. minuta在肠道微环境中能够促进有益代谢产物如乙酸和丁酸的产生,改善能量平衡与脂质代谢,同时通过调节炎性介质和免疫途径,降低慢性炎症的水平。这些作用不仅局限于肠道,还通过肠-全身轴、代谢网络和免疫调控网络对全身健康产生潜在影响。
C.minuta可能通过以下途径发挥作用:增强肠道屏障功能、改变宿主基因表达与信号传导、促进短链脂肪酸等有益代谢产物的产生、以及调节脂肪组织与肝脏的炎症反应。
◮ 临床层面
研究表明,Christensenella minuta在2型糖尿病和肥胖等代谢紊乱以及炎症性肠病中的丰度显著下降。其相对丰度与低 BMI 指数相关的瘦表型呈正相关。
除此之外,支气管哮喘和过敏性疾病、肾结石、情感障碍、甲状腺癌、粘膜类天疱疮、多囊卵巢综合征和复发性口疮性口炎等疾病中C. minuta的丰度也较低。
总体而言,C. minuta 的证据虽仍处于初步阶段,但其在代谢健康与炎症控制方面展现的多维潜力使其成为有希望的下一代益生菌候选株。未来需要更多高质量的人体研究来确认其安全性、最优给药策略、长期效果及与其他干预的协同作用,以便将这一候选菌株尽快转化为可用于临床的干预工具。
Christensenella minuta——下一代益生菌候选者:改善代谢、减轻炎症
Eubacterium hallii
有潜力
Eubacterium hallii是另一种潜在的益生菌生物治疗制剂(NGP)。能利用多种碳源(包括糖和有机酸)并产生两种关键的短链脂肪酸(SCFAs):丙酸和丁酸。SCFAs对肠道健康至关重要,促进黏液生成、刺激肠上皮细胞增殖分化并维持上皮健康;SCFA不足会引发炎症。
注:据报道,E.hallii是新生儿肠道中丁酸的主要来源之一。
◮ 能与肠道其他细菌协作产生短链脂肪酸
某些E.hallii能发酵复杂碳水化合物,但也有依赖其他肠道微生物产物的情况。多项研究证实了这种交叉摄食机制在Eubacterium属SCFA生成中的重要性。
相关研究多在含复杂碳水化合物的培养基中将Eubacterium属与双歧杆菌共培养,能降解复杂碳水化合物的双歧杆菌株可产生1,2-丙二醇、乙酸酯与乳酸盐,随后被Eubacterium属吸收并转化为丁酸与丙酸。
这一交叉摄食模式明确揭示了肠道微生物与复杂碳水化合物的丁酸化协同及其在肠道生态系统中的作用。
◮ 可能改善肥胖和糖尿病
研究了E.hallii在肥胖和糖尿病中的作用。发现E.hallii能够代谢丁酸以激活G蛋白联结受体信号通路,改善GLP1和GLP2的产生,强化肠道屏障功能,同时不影响体重或食物摄入,并提升胰岛素敏感性和能量代谢率。因此,它在胰岛素敏感性方面可能安全且有效。
◮ 在体内对一些物质进行关键转化
最新研究表明,Eubacterium属在肠道中进行关键的代谢转化,对人体健康有积极影响。在这些效果中,有毒化合物解毒为更良性的形态似乎具有价值。
例如,观察到E.hallii将极为丰富的食品来源杂环芳香胺致癌物——2-氨基-1-甲基-6-苯基咪达唑(4,5-b)吡啶(PhIP)转化为生物学上无法获得的7-羟基-5-甲基-3-苯基-6,7,8,9-四氢吡啶(3′,2′:4,5 咪唑(1,2-α)嘧啶-5-m氯化物(PhIP-M1)。此外,PhIP在模拟远端和近端结肠微生物群存在下被E.hallii转化,导致其丰度分别增加了120倍和300倍。这表明它作为一种保护性治疗具有极佳的视角。
此外,在同一研究中,检测到了E.hallii的抗菌活性。作者证明,E.hallii能够将甘油分解为3-羟基丙烯醛(3-HPA),这种甘油以水溶液中的榘蛋白形式存在。
研究还发现Eubacterium属通过调节胆汁酸代谢谱,有助于肠道和肝脏健康。近年来,胆汁酸代谢或肠道微生物群的调节正被研究为肝细胞癌(HCC)和结直肠癌(CRC)的创新治疗策略。
Roseburia
有潜力
罗氏菌属(Roseburia)是一种革兰氏阳性、厌氧、弯曲杆状细菌。Roseburia物种能使用复杂多糖,产生短链脂肪酸(丙酸盐、丁酸盐、醋酸盐)。它对炎症、帕金森病和炎症性肠病(IBD)有益,并且被充分考虑为下一代益生菌(NGPs)。
◮ 降低动脉粥样硬化、改善肠道、肝脏健康
令人瞩目的是,最新研究显示,食用Roseburia和富含纤维的饮食的小鼠,其动脉粥样硬化的发生率降低了。这归因于高纤维饮食,介导了Roseburia丁酸的形成以减少动脉粥样硬化。
此外,最新研究显示 Roseburia intestinalis(细菌鞭毛的关键结构成分)在治疗酒精性脂肪肝和溃疡性结肠炎方面具有潜力。口服 Roseburia 肠源性鞭毛蛋白在酒精性脂肪肝模型中显著改善了肠道上皮完整性并抑制了肠道损伤风险。然而,关于 Roseburia 的临床证据仍然有限,需要进一步研究以明确其在多种人类疾病中的应用价值。
Bacteroides fragilis
有潜力,但同时存在安全隐患
脆弱拟杆菌(Bacteroides fragilis)是机会性病原体,然而,近期研究证实了非致毒性脆弱拟杆菌的益生菌特性。脆弱拟杆菌可以刺激宿主适应性免疫,抑制炎症,激活免疫系统的成熟,调节肠道微生物群,并通过多糖A(PsA)及该NGP的其他外膜囊泡维持肠道健康和稳态。
◮ 抑制其他致病微生物
先前研究显示,脆弱拟杆菌通过抑制其他致病微生物的生长与定居来抑制它们。在动物模型中,该菌能抑制艰难梭菌感染,且治疗后肠道微生物多样性提升、AKK菌丰度增加。
研究还表明,B.fragilis通过抑制凋亡、维持ZO-1和MUC-2完整性,从而提高肠道屏障功能,降低艰难梭菌的黏附性和定植性。因此,脆弱拟杆菌有助于维护肠道屏障的完整性。
其他研究还发现脆弱拟杆菌对沙门氏菌的易位具有竞争性抑制作用,机制包括抗菌蛋白 BSAP-1 的生成。BSAP-1 含有 MACPF 结构域,能裂解侵染宿主细胞的细菌。除了 BSAP-1 外,泛素样蛋白(BfUbb)及 VI 型分泌系统(T6SSs)等因素可能也在该竞争中发挥重要作用。
◮ 产生的荚膜多糖具有免疫调节作用
最新研究显示脆弱拟杆菌在结肠内代谢多种碳水化合物,生成八种荚膜多糖,其中多糖A(PSA)是一种独特的两性多糖,具免疫调节作用。
PSA被抗原呈递细胞内吞并处理后被T细胞识别,持续增强宿主免疫。PSA通过调节树突状细胞,促使初始T细胞分化为Treg,提升Foxp3和CD39表达,抑制IL-17并诱导IL-10产生,帮助治疗肠道炎症性疾病。
近期研究还报道脆弱拟杆菌通过增强免疫功能、抑制脂多糖信号、改善肠道微生物群活性并维持肠道屏障稳态来预防肠漏,对癌症患者有潜在益处。
SK08活细菌粉末是一种以脆弱拟杆菌为基础的活体生物药,已获中国食品药品监督管理局认可,目前处于临床试验阶段,属于治疗性生物药范畴。
Prevotella copri
有潜力
P. copri是拟杆菌门中的另一种新型益生菌,据报道可改善葡萄糖耐量和肝糖原水平。它被视为2型糖尿病、肥胖等代谢疾病的潜在靶点。
◮ 微生物组学基础
P. copri在健康人群和特定疾病患者(如类风湿关节炎、2型糖尿病)的肠道微生物群落中存在明显差异,已通过宏基因组学研究识别。
◮ 功能特性研究
•能产生短链脂肪酸(SCFAs),特别是丙酸;
•参与多糖代谢,具有特定的代谢功能;
•与肠屏障完整性和免疫调节相关;
◮ 临床相关性
•在类风湿关节炎(RA)中丰度降低,补充可能改善症状;
•与代谢相关疾病的关联有一定研究基础。
广泛存在于人群的双面使者——Prevotella copri与疾病和健康
Parabacteroides goldsteinii
有潜力
研究表明,P.goldsteinii也有望成为下一代益生菌。中山大学的程芳/陈红波教授团队探讨了肠道共生细菌P.goldsteinii衍生的外膜囊泡(OMVs)通过传递关键的抗炎分子(例如十五烷酸)来调节宿主的免疫系统。这些OMVs能够在炎症皮肤区域积聚,有效抑制IL-23/Th17轴,改善全身免疫稳态,从而显著缓解银屑病症状。
编辑
Su D,et al.J Control Release.2025
P.goldsteinii已被证实能够显著改善肠道和肺部炎症。强烈推荐用于肥胖改善。此外,P.goldsteinii也表现出显著的抗炎和胰岛素刺激特性。
Propionibacterium freudenreichii
有争议
费氏丙酸杆菌(Propionibacterium freudenreichii)主要用于乳制品行业,作为生产瑞士奶酪的食品级微生物。研究者正探索其特定的益生菌特性以实现新的健康益处。该菌已能产生丙酸,具有抗菌活性并可降低胆固醇。
另一项研究则显示,P.freudenreichii 对肠道屏障完整性与炎症状态的影响提示其在胃肠道健康方面的潜在应用。
工程菌株
具有较高潜力
工程菌株是尖端的下一代益生菌代表。经过改造的乳酸乳球菌和大肠杆菌等菌株通过产生外源蛋白或分子,可用于治疗结直肠癌、炎症性肠病甚至精神健康问题等疾病。
注:益生菌还通过CRISPR技术进行基因改造,这扩大了接种疫苗的治疗选择,并增强了免疫反应。
编辑
doi: 10.1007/s12602-025-10606-2.
小结
无论来自天然还是合成来源,这些新一代菌株都代表益生菌的未来前沿。特定有益代谢物如丁酸、抗菌肽和免疫调节化合物可作为复杂疾病的治疗干预,提供传统益生菌难以实现的疾病特异性与个性化策略。因此,研究将聚焦新一代益生菌的关键点,推动医学在预防与治疗上的新前景。
下一代益生菌(NGP)在治疗领域的前景日益广阔,标志着其不再局限于传统的肠道健康维护,而是在疾病预防、诊断与治疗中发挥更为精准和多样的作用。通过基因改造或天然/合成菌株的多样化开发,NGP 能在人体内定向表达有益代谢物、抗微生物肽以及免疫调节因子,为难治性炎症、代谢疾病、免疫相关疾病等提供新的干预路径。
临床应用将持续扩展,覆盖免疫、神经、泌尿生殖、心脏、代谢、呼吸、皮肤、口腔及体重管理等领域。下面是当前新型益生菌已涉足的方向:
下一代益生菌在各种健康疾病中的应用
编辑
doi: 10.1007/s12602-025-10606-2.
胃肠道健康
下一代益生菌可能聚焦于已被证实对特定胃肠道问题有益的单一菌株,而非传统益生菌组合的多菌株混合,从而实现更个性化、针对性的治疗。
随着DNA测序技术的发展,下一代测序能够对肠道微生物群进行更为细致的分析,帮助理解胃肠道疾病患者的微生物组结构,并识别潜在的治疗重点菌群或菌株。
•炎症性肠病(IBD):包括Akkermansia muciniphila和Faecalibacterium prausnitzii,两者都与减轻肠道炎症和促进粘膜修复有关。抗炎分解代谢物(如SCFA)的合成有助于调节与IBD相关的炎症,包括克罗恩病和溃疡性结肠炎。
•肠易激综合征(IBS):某些益生菌可以缓解腹胀、疼痛和排便异常等症状。其中一些包括婴儿双歧杆菌和丁酸梭菌(Clostridium butyricum),它们可以对抗炎症并提高肠道内的健康运动能力,在这种情况下,它们在治疗IBS相关疾病方面非常有用。
•抗生素相关性腹泻:非致病性细菌大肠杆菌Nissle 1917通过引入有益细菌来缓解抗生素相关性腹泻和其他胃肠道问题,从而恢复肠道健康。
代谢健康
代谢综合征(MS)是一组特征性疾病,包含胰岛素抵抗、血脂异常、肝肾功能异常、高血压、血糖稳态紊乱等。如今,益生菌正被视为潜在的代谢疾病生物治疗药物,作为具有健康促进作用的功能性食品成分,并具备对抗特定疾病的潜力。
小鼠研究显示,A. muciniphila 与体重、脂肪量变化相关,新型益生菌菌株能够有效调节葡萄糖、脂质和体重的平衡。其改变必需代谢物谱,包括短链脂肪酸、维生素、 多种脂肪酸、氨基酸及胆汁酸代谢物等。
•肥胖和体重管理:肠道菌群的一些调节剂会影响促进脂肪储存、脂肪燃烧和饱腹感的因素。如前所述,使用Akkermansia muciniphila已被证明可以改善胰岛素反应,缓解脂肪堆积,从而治疗肥胖。
•2型糖尿病:新型益生菌可能有助于血糖控制,因为它们会产生SCFA,SCFA已被证明可以降低血糖水平并增强胰岛素敏感性。两种有益的微生物,Akkermansia muciniphila和鼠李糖乳杆菌,抑制胰岛素抵抗,已被推荐用于控制2型糖尿病。
免疫系统调节
健康的微生物群通过迷走神经直接或间接调节免疫系统。由于肠道微态的稳定性,益生菌可调节免疫环境,有助于自身免疫疾病的治疗。
•自身免疫调节:如脆弱拟杆菌通过产生多糖A调节促炎与抗炎反应,从而为治疗类风湿性关节炎和多发性硬化症等自身免疫疾病提供干预,目标是调节免疫与减轻自身免疫。
•过敏与哮喘:部分新型益生菌能调节免疫耐受,降低过敏反应。鼠李糖乳杆菌在给药后表现出抗过敏、抗哮喘特性,透过增强调节性T细胞并降低过度免疫反应来发挥作用。
•感染:部分新型益生菌具抗感染作用,如丁酸梭菌具有抗菌特性,能够增强对感染的免疫防御,但需在宿主体补偿机制恢复后方能实现。
心理健康
•抑郁与焦虑:仍有被称为“心理益生菌”(psychobiotics)的新型益生菌(NGP)与情绪和认知改善相关”。瑞士乳杆菌和长双歧杆菌已显示抗焦虑与抗抑郁效应,可能通过产生血清素和GABA等神经递质、以及降低全身炎症来实现。
•压力管理:与GBA(脑-肠-轴)相互作用的NGP 能通过维持微生物群平衡、调节 HPA 轴来减轻生理压力对身心的影响,关联情绪与压力相关的精神状态。
新型益生菌的治疗益处
编辑
doi: 10.1007/s12602-025-10582-7.
皮肤健康
健康的皮肤微生物群通过调节免疫细胞与炎症维持体内平衡。湿度、pH、温度、脂质、营养、运动、药物、手术以及身心压力等变量共同影响皮肤微生物组的日常波动。
表皮屏障缺陷与免疫失调与特应性皮炎(AD)密切相关,且具有遗传易感性和环境影响的个体更易发病,体现了 AD 的复杂病理生理。最新研究显示局部治疗可改善 AD 患者的微生物群,帮助清除有害菌、促进有益菌生长,从而平衡微生物群。
•湿疹与皮炎:益生菌已逐步用于炎症性皮肤病的治疗。鼠李糖乳杆菌与长双歧杆菌能改善屏障功能、降低炎症,可能对湿疹与皮炎患者有益。
•痤疮与牛皮癣:部分新型益生菌具抑炎特性、可抑制免疫活动,有助于治疗痤疮及银屑病等疾病;有助于控炎、保护屏障功能,对皮肤健康有益,减少炎症发作。
口腔健康
根据既有文献,口腔内约有700多种细菌构成口腔微生物群。免疫抑制、激素治疗及不良饮食等因素可引发牙釉质侵蚀与牙周疾病。
益生菌作为一种新兴且具成本效益的微生物疗法,能抑制口腔病原体并降低粘附,延长假体装置的使用寿命。
•牙龈疾病与龋齿:最新口腔研究显示,某些益生菌通过重新定植口腔菌群来预防口腔疾病,抑制有害生物。例如,唾液链球菌与罗伊氏乳杆菌通过抗炎、维持口腔菌群平衡及抑制致病生物膜,对牙龈疾病与龋齿具有积极作用。
变形链球菌在龋齿形成中扮演重要角色,能产生胞外多糖并在酸性条件下存活。研究了鼠李糖乳杆菌GG与发酵乳杆菌KU200060对变形链球菌KCTC 5316的最小抑菌浓度(MIC),抗菌效果分别为25%与12.5%。唾液链球菌DB-B5为从健康成年女性龈上牙菌斑分离的菌株,具备产生新型细菌素等益生菌特性。
•口臭:部分益生菌能降低挥发性硫化合物,这是口臭的主要成因。通过平衡口腔微生物群,可维持口腔健康环境,减少口臭发生。
呼吸健康
•上呼吸道感染:鼠李糖乳杆菌GG及其他新型益生菌在预防肺部感染方面已显示有效。它们可通过调节免疫反应来增强上皮黏膜对呼吸道病原体的防御,具备免疫抑制潜力。这些益生菌已用于预防普通感冒与流感等疾病。
•哮喘管理:一些NGP可通过降低全身炎症、促进免疫耐受来缓解哮喘,并帮助调节在寒冷天气下的异常免疫反应,通常用于慢性呼吸道疾病的治疗。
肝脏健康
•非酒精性脂肪肝(NAFLD):新型益生菌(NGPs)通过调整肠道脂质代谢相关微生物群,促进肝脏健康,抑制脂肪积聚。像Akkermansia muciniphila等菌株能减少肝脏氧化应激与炎症的证据正在积累,但仍需更多临床试验验证。
•肝脏排毒与健康维护:某些菌株通过改善肠道环境、降低进入肝脏的微生物内毒素,提升肝脏排毒能力,从而增强肝功能并降低全身炎症。
癌症预防与治疗
•癌症预防:特异性NGPs可通过产生抗氧化与抗炎应激因子来抑制癌症诱导效应,具有抗癌潜力。研究显示,干酪乳杆菌通过调节肠道菌群和免疫监测,减少结直肠癌风险。
•癌症治疗支持:NGPs可减轻化疗相关副作用(如黏膜炎)并支持免疫功能。据报道,益生菌通过增强免疫反应与改善肠道健康,抑制肿瘤细胞增殖,或作为标准肿瘤治疗的辅助手段。
新型益生菌(NGPs)已从单纯的肠道守卫者发展为多系统、多靶点的免疫与代谢调控工具。基于对肠道微生物组及其代谢产物的深入理解,NGPs显示出在慢性炎症、代谢疾病、免疫性疾病、皮肤与神经系统疾病等领域的广阔应用前景。它们不仅能够改善局部屏障功能与炎症状态,还可能通过肠脑轴、肠-皮肤轴等通路实现对远端器官的调控,从而带来更全面、个体化的健康管理方案。
尽管前景光明,NGPs的临床转化仍面临若干挑战:菌株的稳定性与可控性、个体微生环境差异、长期安全性评估、以及标准化的制备、给药剂量与疗效评估体系尚需完善。
未来发展的关键方向包括:
总之,NGPs具备成为下一代个体化健康管理核心元素的潜力。通过持续的基础研究与循证临床探索,未来的益生菌干预有望实现更高的治疗精准度、更广的适应证和更持久的健康收益。
主要参考文献
Gupta MK, Srivastava R. Gut Microbiome Interventions: From Dysbiosis to Next-Generation Probiotics (NGPs) for Disease Management. Probiotics Antimicrob Proteins. 2025 Aug;17(4):2629-2652.
Vijayaganapathi A, Mohanasrinivasan V. A Review of Next-Generation Probiotics-As a Gateway to Biotherapeutics. Probiotics Antimicrob Proteins. 2025 Aug;17(4):1985-1997.
Al-Fakhrany OM, Elekhnawy E. Next-generation probiotics: the upcoming biotherapeutics. Mol Biol Rep. 2024 Apr 15;51(1):505.
Maftei NM, Raileanu CR, Balta AA, Ambrose L, Boev M, Marin DB, Lisa EL. The Potential Impact of Probiotics on Human Health: An Update on Their Health-Promoting Properties. Microorganisms. 2024 Jan 23;12(2):234.
Santacroce L, Charitos IA, Bottalico L. A successful history: probiotics and their potential as antimicrobials. Expert Rev Anti Infect Ther. 2019 Aug;17(8):635-645.
Meng N, Liu Q, Dong Q, Gu J, Yang Y. Effects of probiotics on preventing caries in preschool children: a systematic review and meta-analysis. J Clin Pediatr Dent. 2023 Mar;47(2):85-100.
Evivie SE, Huo GC, Igene JO, Bian X. Some current applications, limitations and future perspectives of lactic acid bacteria as probiotics. Food Nutr Res. 2017 May 3;61(1):1318034.
Haghshenas B, Kiani A, Mansoori S, Mohammadi-Noori E, Nami Y. Probiotic properties and antimicrobial evaluation of silymarin-enriched Lactobacillus bacteria isolated from traditional curd. Sci Rep. 2023 Jul 5;13(1):10916.
Silva DR, Sardi JdCO, de Souza Pitangui N, Roque SM, da Silva ACB, Rosalen PL (2020) Probiotics as an alternative antimicrobial therapy: current reality and future directions. J Funct Foods 73:104080.
Mejía-Caballero A, Salas-Villagrán VA, Jiménez-Serna A, Farrés A (2021) Challenges in the production and use of probiotics as therapeuticals in cancer treatment or prevention. J Ind Microbiol Biotechnol 48(9–10):kuab052.

谷禾健康
宝宝湿疹反复瘙痒总难根治,季节交替时喷嚏不断,擦不完的鼻涕,整晚咳嗽甚至发展为哮喘,到了学龄期孩子仍无法专注听讲…
如今约40%中国儿童在成长过程中会出现至少一种过敏症状(尤其是过敏性鼻炎),神经发育问题发生率也逐年上升。
多中心流行病学调查和系统综述显示:
神经发育障碍整体患病率呈上升趋势,已从 0.5 %‑1 % 逐步提升至约 5 %‑10 %,包括所有子类的累计比例。
中国儿童常见过敏性疾病的患病率总体呈上升趋势,哮喘约 3%–7%,过敏性鼻炎约 20%–25%,湿疹/特应性皮炎约 8%–20%,食物过敏约 3%–8%,且城市和经济发达地区患病率更高。
而这些看似独立的健康难题,都指向了肠道微生物群。
从出生开始,我们的肠道微生物群便陆续完成定植,在大约三年的时间里,从几乎一片空白,逐步演变为一个多样、稳定且高度复杂的微生态系统。这一阶段被认为是影响儿童健康的关键窗口期,而现代生活方式导致的环境污染、抗生素滥用、高加工食品摄入过多等问题,都在悄悄破坏着孩子娇嫩的肠道环境。
大量研究提示,生命早期一旦出现肠道菌群失衡,不仅会增加炎症性肠病、过敏性疾病(如哮喘、湿疹、过敏性鼻炎等)、自闭症、注意力缺陷多动障碍、儿童肥胖、糖尿病等多种儿科疾病的风险,其影响还可能延续至成年。相反,如果在这一时期通过合理的方式塑造一个平衡的肠道菌群,则有机会改善儿童免疫与代谢反应,甚至为一生的健康打下基础。
基于此,本文将围绕“早期肠道菌群与常见儿科疾病”这一主题,回顾当前研究进展,解析早期肠道菌群在疾病发生发展中的作用机制,并探讨可能的干预思路与临床应用前景。
我们知道肠道菌群不仅仅帮助我们消化食物,它还在免疫、营养吸收、抵御病菌、维护肠道屏障的完整性中扮演着关键角色。
尤其是在生命早期,肠道菌群会建立起连接大脑、肺、皮肤等远处器官的沟通轴线。这个关键发育窗口期建立的菌群平衡,就给未来打下了扎实的基础。如果这时候建立的菌群平衡被打破,就可能对儿童健康产生深远的不利影响,甚至引发多种疾病。
肠道与各大器官的交流
肠道菌群通过复杂的免疫、代谢和神经内分泌途径,与身体多个器官进行着持续的双向沟通。
这是最有名的这一条,大脑和肠道菌群,其实从宝宝还很小的时候就一起长大。
肠道菌群会产生影响情绪和行为的神经递质(如GABA),通过迷走神经和血液循环传递给大脑。
反过来,我们一紧张、焦虑,脑子里的压力信号会改变肠道里的环境,比如让酸碱度、激素水平发生变化,进而影响肠道菌群。这条轴线的失调与自闭症谱系障碍和注意力缺陷多动障碍有关。
再来看肠道和皮肤的关系。很多人都说“脸就是肠道的镜子”,其实还真有点道理。
肠道如果不太健康、菌群有点失衡,就很容易引发一些慢慢的、低度的炎症,还有一些代谢产物。这些东西会跟着血液到皮肤那儿去,影响皮肤表面的菌群平衡和局部免疫状态。
结果就是,像婴儿湿疹之类的问题,可能就会变得更严重或者更难治愈。
听起来好像肠道和肺离得挺远的,但它们之间也在悄悄互相影响。肠道菌群产生的代谢物,还有各种免疫信号,也可以通过血液到达肺部,帮忙调整呼吸道的免疫反应。肠道菌群失衡会增加儿童患哮喘和过敏的风险。
其他重要轴线: 研究还揭示了 肠-胰腺轴、肠-脂肪轴 等通路的存在。
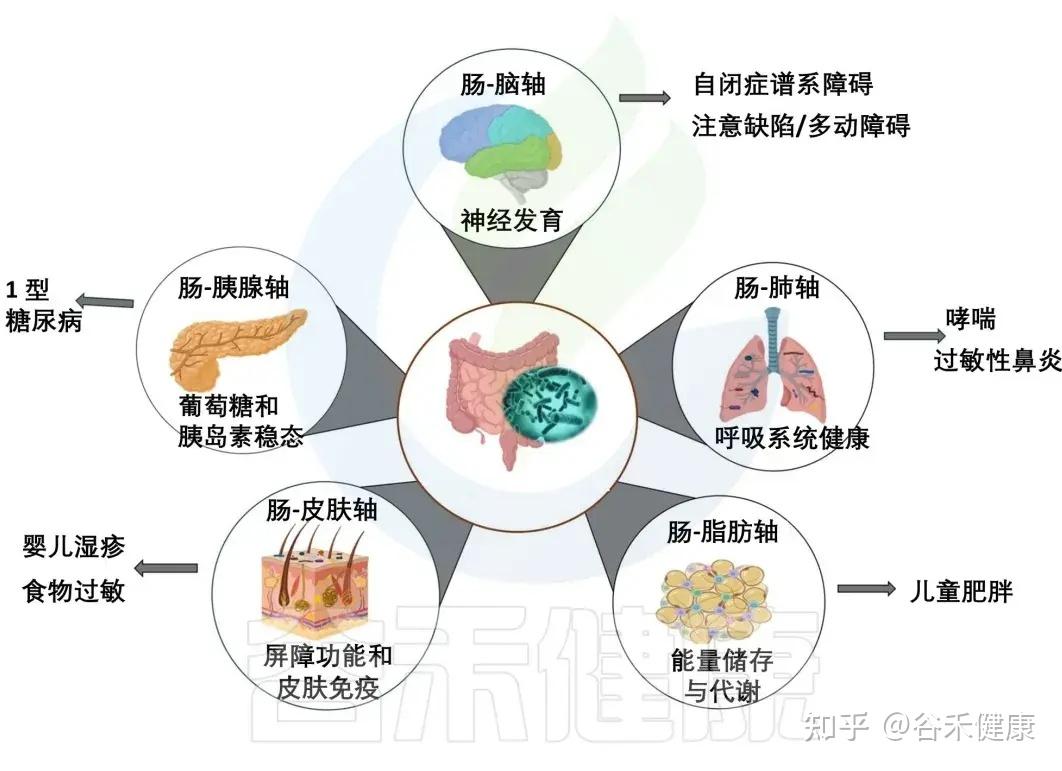
总之,肠道菌群通过这些复杂的代谢和信号通路,构建了一个覆盖全身的通讯网络,成为调节人体从免疫到神经系统等多个方面健康的核心枢纽。
母亲围产期营养状态
婴儿肠道菌群的初始状态,很大程度上继承自母亲。母亲在围产期保持均衡、健康的饮食,是为后代肠道菌群打下良好基础的第一步,也是至关重要的一步。
失衡的风险
如果母亲在孕期偏爱高热量、高脂肪的西式饮食,可能导致自身肠道菌群的失调。这种失调会通过胎盘、产道或母乳传递给婴儿,影响宝宝肠道健康。同样,营养不良也会导致菌群失调,可能增加如γ-变形菌门这类潜在致病菌群的出现。
▸细菌的入住,在出生前就开始了
与传统的“子宫无菌”理论不同,新的证据显示,细菌定植其实早在胎儿的宫内阶段便已开始。研究发现,非致病菌在妊娠期间能从母体肠道转移至胎儿,并存在于胎盘、羊水、脐带、胎儿组织及胎粪中。
而这个宫内微环境的菌群构成,又会受到母亲的健康状况、饮食习惯以及孕期菌群变化的影响,这为婴儿早期肠道菌群形成奠定了最初的基础。
分娩方式:顺产 or 剖腹产?
分娩方式,主要是顺产(即阴道分娩)与剖宫产,是显著影响新生儿肠道菌群组成和发育的关键因素。
▸出生方式决定了宝宝的第一批肠道居民
-顺产
顺产新生儿会接触到母体阴道与肠道来源的多样菌群,包括乳酸杆菌和双歧杆菌等优势菌株,这些菌群构成了初始肠道定植的核心。
顺产宝宝的菌群不仅更稳定、多样性也更高,而且他们的粪便菌群构成与母亲相似。
-剖宫产
与顺产儿相比,剖宫产儿的肠道菌群表现为双歧杆菌和乳酸杆菌的定植延迟、拟杆菌门的多样性较低,而主导菌群则通常是医院环境中常见的肠球菌属。
剖宫产宝宝的肠道里的菌群种类更少,而且这些菌群更像是来自妈妈皮肤和口腔里的。
注:
刚出生那段时间,两种分娩方式带来的菌群差别很大,这个差别会随着时间推移而慢慢变小。
有研究发现剖宫产宝宝的这种菌群特点,可能会让他们以后更容易得一些慢性病(比如哮喘、1型糖尿病、肥胖,但这个说法目前还有争议,不是所有研究结果都一样。
▸如何为剖腹产宝宝补回有益菌?
母体的阴道和粪便菌群是新生儿获得初始微生物的最主要、最丰富的来源。
——第一个办法:阴道菌群移植
为了弥补剖宫产宝宝在这方面的缺失,一些研究探索了“阴道菌群移植”的效果,就是说把母亲的阴道分泌物涂抹给新生儿。
部分研究显示,这种方法有助于部分恢复菌群定植;然而,另一些研究却得出相反结论,认为没什么影响。这种结果上的分歧,很可能是因为阴道菌群难以在婴儿肠道内实现长期定植。
——第二个办法:粪便菌群移植(仅科研探索阶段)
相对来说,母体消化道的菌群多样性要高得多,对宝宝肠道菌群定植的影响可能更深远。
基于这一理念,有些研究认为,母体粪便菌群移植是一种更有效的方法。它能近乎完全地恢复母婴间的微生物垂直传播,有效重塑新生儿的早期肠道菌群。
注:在我们看来,当前有关粪菌移植在儿童中的应用,仍主要停留在科研探索层面,且存在不少限制。成人与儿童的肠道菌群在组成和功能上存在显著差异,而目前临床检测和数据库中可用于精准匹配的儿童菌群数据仍相对有限。因此,现阶段粪便菌群移植更多作为研究工具和小范围、慎重的学术交流内容,并不适合作为常规干预手段。
喂养方式:母乳 or 配方奶?
▸母乳:不仅仅是食物
母乳 (HBM) 不仅为婴儿提供必需的营养,更在生命早期肠道菌群的成熟过程中扮演着至关重要的角色。
母乳富含多种生物活性成分,如免疫细胞、细胞因子、乳铁蛋白、抗菌蛋白和肽、抗体以及母乳低聚糖(HMOs)。这些成分能够对婴儿的肠道菌群进行正向调节,帮助宝宝抵抗感染。
与牛奶相比,母乳含有超过250种不同类型的母乳低聚糖。这些母乳低聚糖对于调节婴儿肠道微生物和影响免疫系统至关重要。
▸菌群差异:母乳 v.s. 配方奶
先前的研究已证实,母乳喂养和配方奶喂养的婴儿,其肠道菌群存在显著差异。
基于母乳喂养带来的整体健康益处,世界卫生组织推荐在婴儿出生后一小时内即开始母乳喂养,纯母乳喂养至六个月,并持续到至少一岁。
▸配方奶粉:添加母乳低聚糖
母乳喂养好处多多,但很多母亲会因乳腺炎、奶水不足或产后抑郁等原因而无法实现。为了弥补这一差距,现代高端婴幼儿配方奶粉开始添加在母乳中发现的关键成分——母乳低聚糖(HMOs),如2-岩藻糖基乳糖和乳糖-N-新四糖,这些有可能促进健康早期肠道微生物群的发展。
有研究发现,添加了HMOs的配方奶粉确实能带来积极效果:
▸生命早期,母婴间菌群如何传递?
母乳里的有益菌从何而来?研究人员认为,存在一个“肠道-乳腺通路”:
母亲肠道中的一些有益菌株可以被自身的免疫细胞(如树突状细胞)捕获。
这些免疫细胞随后通过淋巴系统,将这些细菌穿透肠上皮运送到乳腺。
最终,这些来自母亲肠道的有益菌就进入了母乳,并在喂养时传递给宝宝。
此外,母亲肠道细菌分泌的一些含有生物活性物质的小包裹(即细菌外囊泡,BEV),也可能通过同样的方式进入母乳,影响宝宝的肠道菌群建立。
总而言之,母亲自身的肠道健康状况,会直接影响母乳的微生物构成,进而深刻地影响着宝宝早期的肠道健康。
辅食添加:菌群发展的分水岭
当婴儿长到6个月左右开始添加辅食时,其肠道菌群会经历一次重大的转变。菌群会从以双歧杆菌为主的相对简单的状态,演变为一个相对更多样化的菌群。
-时机很关键
辅食添加太早或太晚,都会干扰菌群的正常成熟过程。因此,推荐在6个月左右开始添加营养丰富的辅食。
营养成分
不同的营养成分对肠道菌群有不同的影响。
▸宏量营养素(碳水、蛋白质等)
-碳水化合物
高纤维和低升糖指数的食物是肠道有益菌的“优质口粮”,有助于促进普雷沃氏菌属、双歧杆菌、毛螺菌属(Lachnoclostridium)和罗斯氏菌属(Roseburia)的生长。
一项研究表明,在婴儿的补充喂养阶段,食用来自各种全谷物、豆类、水果和蔬菜的膳食纤维会导致大量产丁细菌,如粪杆菌、粪球菌、Dorea、Oscillospira。
-蛋白质
相比动物蛋白,植物蛋白如扁豆,豆类,植物性饮食通常富含膳食纤维,含有足够量的多不饱和脂肪酸,通常更有利于结肠细菌的健康。
当然,为了维持肠道稳态,均衡摄入两种蛋白是最佳选择。
▸微量营养素(维生素与矿物质)
-维生素
多数维生素都能促进有益菌的生长,例如双歧杆菌和Akkermansia菌,同时抑制像艰难梭菌这样的致病菌。
例如,维生素A、B2、D、E、β-胡萝卜素可以增加有益共生菌的丰度。
维生素B2、E可以增加有益的SCFA产生菌。
-矿物质
它们的作用比较复杂。镁、钙、硒等有益于菌群。但需要特别注意的是,给婴儿补充铁剂可能是一把双刃剑,过量时可能会抑制双歧杆菌和乳杆菌科等有益菌,反而为一些有害菌的繁殖提供机会。
▸植物营养素(特别是多酚)
这是一类广泛存在于水果、蔬菜中的强大活性成分,能直接调节菌群。例如,生命早期服用葡萄多酚可以促进有益的Akkermansia和乳酸杆菌的生长。
更重要的是,母亲在孕期和哺乳期摄入的植物营养素可以传递益处。例如,母亲饮食中:
生命早期是一个塑造肠道菌群的黄金窗口期。在此期间,通过科学合理的营养干预来优化菌群构成,是预防多种儿童期乃至成年期疾病的有效策略。
运 动
除了我们吃什么,我们的“动与不动”也是影响肠道菌群的另一个关键因素。
▸运动如何优化肠道菌群?
规律的运动被证明可以从多个方面积极地重塑肠道微生态。
-增加有益菌和多样性
运动能显著增加肠道中有益菌的种类和数量,特别是那些能产生短链脂肪酸(SCFAs)的好菌。
宏基因组分析显示,运动量与罗斯氏菌属(Roseburia)和Akkermansia菌丰度呈正相关。
-久坐的危害
相反,久坐不动的生活方式则会破坏这种平衡。研究表明,久坐会导致肠道菌群多样性降低,并使得那些能更高效捕获食物能量的厚壁菌门增多,而放线菌门细菌减少。
▸生命早期的运动
在正确的时间运动,效果可能事半功倍,生命早期或许就是这样一个黄金窗口期。
-早期锻炼效果更佳
一项动物研究发现,如果在还很年幼的时候就开始运动,相比长大成年后才动起来,更能明显、积极地改变肠道菌群。
-具体的菌群变化
研究显示,幼年期的运动能显著增加拟杆菌门的比例,同时降低厚壁菌门的比例,这种菌群构成上的变化与增加瘦体重)直接相关。
基于这些益处,世界卫生组织建议,5岁以下的孩子,每天应累积进行至少180分钟的各类身体活动。
▸母亲的运动:给宝宝的第一份健康礼物
运动的影响力甚至可以追溯到生命开始之前。过去我们认为,父母传给孩子的是基因。现在我们知道母亲还可以传递一个健康的微生态系统。
-孕期运动的益处
母亲在孕前和孕期的规律运动,可以帮助宝宝的肠道减少有害菌,同时富集能产生短链脂肪酸的有益菌,从而改善宝宝整体的代谢健康。
-可能的机制
科学家推测,这其中的一个可能机制是,运动改变了母亲体内的代谢环境,如激素水平、血液循环和能量利用。这些生理变化信号传递到乳腺,影响了母乳的生产过程。
母乳中母乳低聚糖(HMOs)的种类和数量发生了改变。HMOs是母乳中仅次于乳糖和脂肪的第三大固体成分,但宝宝自己无法消化它。它不是给宝宝吃的,而是专门给宝宝肠道里的有益菌吃的。这样一来,宝宝的有益菌在菌群建立的早期就占据主导地位,抑制了有害菌的生长。
均衡的营养加上规律的身体活动,能最大程度地对早期肠道菌群的健康发展产生积极和深远的影响。
在生命早期操纵微生物发育的因素
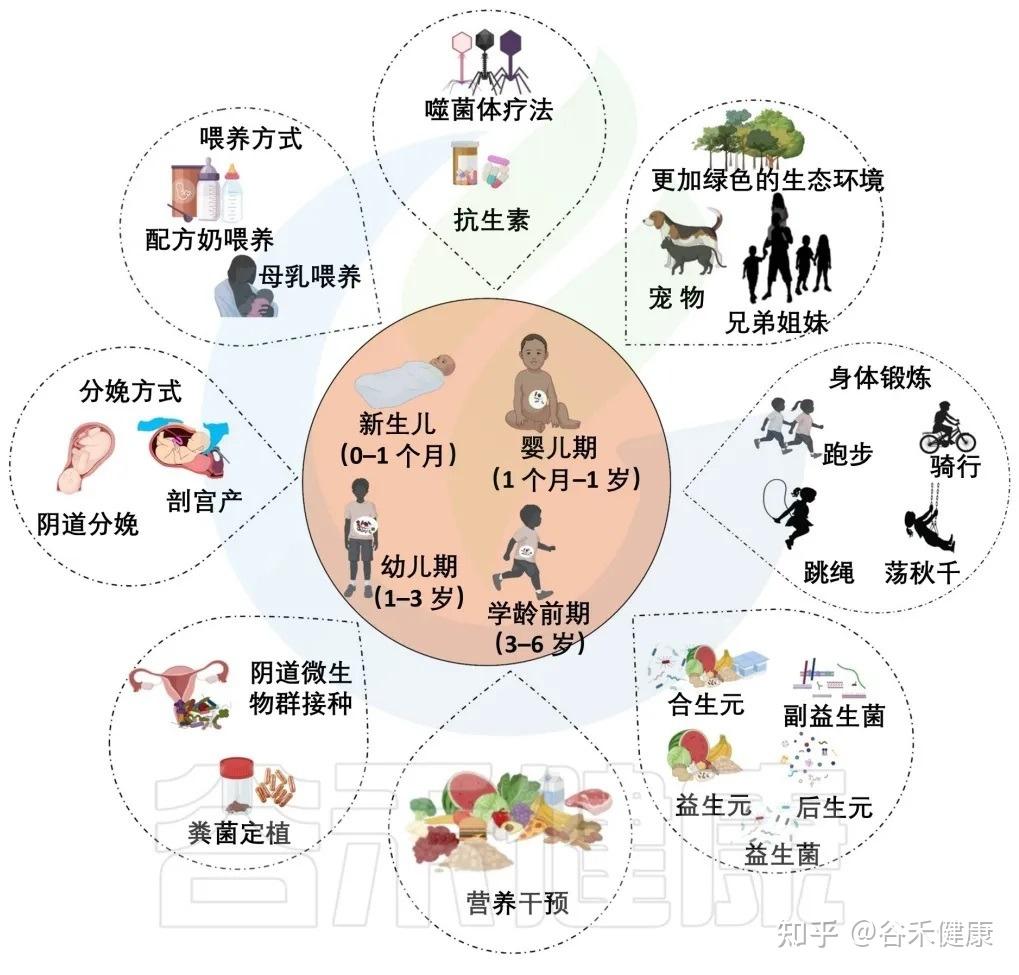
抗生素的使用:有利有弊
有些家长有过这种经历,带孩子看了一次病,用了抗生素,当时觉得病总算好了,松了口气,结果没过几天,新的问题又来了:孩子就开始拉肚子,或者突然吃一些东西开始食物不耐受了,甚至之前控制得好好的湿疹也加重了。这其实也跟肠道菌群有关。
关于抗生素,它确实对付细菌感染特别管用,不过呢,凡事都有两面,尤其是在生命早期,在宝宝身体各种系统都还在搭建的时候使用它,可能需要付出一些看不见的代价。
抗生素最大的问题在于其“不分敌我”的特性,它们不仅杀死了致病菌,也对肠道内大量的有益菌造成了连带伤害,导致肠道菌群失调。这种早期的菌群失调与日后的多种健康问题,如肥胖、哮喘以及抗生素耐药性等都有可能相关联。
婴儿接触到抗生素主要有两种途径:
▸母亲用药:穿越屏障的连锁反应
即使是母亲使用抗生素,其影响也能传递给宝宝。
-影响机制
在分娩期间,抗生素不仅会通过脐带传递给胎儿,还会改变母亲产道和粪便中的菌群,这些都是婴儿在出生时获得初始菌群的来源。
-对婴儿菌群的直接冲击
研究发现,经历过母亲产时抗生素暴露的婴儿,其粪便菌群表现出:
整体多样性降低;
放线菌门和拟杆菌门丰度显著减少;
变形菌门占据了主导地位。
-对母乳的影响
母亲使用的抗生素还会改变母乳中的微生物,这会直接阻碍双歧杆菌和乳酸杆菌等健康菌株在婴儿肠道的正常定植。
▸婴儿用药:艰难梭菌感染风险增高
当婴儿自己直接使用抗生素时,对肠道菌群的影响更为直接。
研究证实,这会导致婴儿肠道菌群构成发生剧变,主要表现为:有益的双歧杆菌数量锐减,而肠球菌属和克雷伯氏菌属等机会性致病菌的数量则会升高。
有些儿童在使用抗生素之后会发现,艰难梭菌(Clostridioides difficile)感染的风险会显著升高,艰难梭菌感染可能会引起严重的腹泻和结肠炎症。
除艰难梭菌外,抗生素使用还可能导致耐药菌株的选择性增长。例如,耐甲氧西林金黄色葡萄球菌(MRSA)和产超广谱β-内酰胺酶(ESBL)的肠杆菌科细菌,这些在抗生素治疗后更容易定植。
长远来看,可能会让宝宝更容易反复出现肠胃不适、拉肚子,或小病不断。因此,在抗生素用药之后,需要格外关注宝宝的饮食,排便,以及肠道菌群状态。
环 境
除了饮食和运动,我们生活于其中的物理和社会环境,也对生命早期的肠道菌群发展有着深刻而直接的影响。从家里的宠物到社区的公园,都在悄无声息地参与塑造这个微小的生态系统。
▸ “不干不净,吃了没病”
过度干净的环境,有时反而不利于建立一个强大的免疫系统和健康的肠道菌群。适度地接触来自外界的微生物,对婴儿来说是一种有益的早期训练。
-宠物带来的益处
宠物猫狗陪伴着孩子长大,像家人一般为孩子带来情感上的安慰与支持,也为孩子性格带来温暖的影响,让孩子感受更多无条件的爱与接纳。
从肠道菌群的角度来说,研究发现,与宠物(如猫狗)一起长大的婴儿,其肠道菌群的丰富度和多样性通常更高。具体来说,他们的肠道中比如双歧杆菌、颤螺菌属(Oscillospira)和瘤胃球菌属(Ruminococcus)这些有益菌的丰度会更丰富。

有趣的是,养猫的人肠道里的双歧杆菌水平也比不养猫的人要高。这就意味着,和猫咪一起生活,可能会通过菌群的交流,悄悄地帮我们补充有益菌,提升肠道健康水平。
注:然而也存在一些需要注意的潜在风险。研究指出,猫肠道里的抗生素耐药基因(ARG)丰度显著高于人类。这些耐药基因可能会通过猫咪在家里的活动(比如它走过地板、沙发),转移到环境中,进而有机会进入人体。简单说,就是猫可能会把它携带的耐药基因传递给主人,这增加了我们体内细菌变得耐药的可能性。
-兄弟姐妹的菌群共享
同样,有哥哥姐姐的孩子,其肠道菌群的多样性也更高。
道理其实很简单。宠物和哥哥姐姐会将更多来自室外(如土壤)或他们自身的微生物带入环境中,让婴儿有机会接触到更多样的细菌,这就像是给婴儿的肠道菌群进行了一次自然接种,有助于其发展得更加健全和有韧性。
▸新冠的意外发现:社交隔离对菌群的影响
新冠为我们提供了一个独特视角,观察环境剧变如何影响肠道菌群。
-菌群多样性下降
研究人员发现,在疫情期间出生的婴儿,其粪便样本中的微生物多样性显著低于疫情之前的同龄婴儿。
-可能的原因
这种变化被认为与疫情期间的特殊生活方式有关,包括:社交活动大幅减少,以及消毒剂、洗手液等清洁产品的使用频率急剧增加。这使得婴儿接触外界微生物的机会大大减少。
▸ 环境的力量:来自大自然的馈赠
我们与自然环境的接触,也能产生意想不到的健康关联。
-母亲接触绿色环境的益处
最近的一项研究指出,如果母亲在孕期更多地接触住宅区周围的公园、绿地等绿色环境,其母乳中母乳低聚糖(HMOs)的多样性和浓度都会更高。

我们已经知道,HMOs是婴儿肠道有益菌的超级食物。因此,通过提升母乳的质量,母亲接触绿色环境的益处最终能够传递给婴儿,积极地影响其肠道菌群的健康发育。
因此,生命早期丰富的环境暴露至关重要。一个不过分无菌、能适度接触来自他人、宠物和大自然的微生物的环境,是帮助孩子建立一个多样、稳定且有韧性的肠道菌群的关键因素之一。
生命从出生到3-6岁的这段时间,是肠道菌群发育的“关键窗口期”。这个阶段的任何干扰,都可能让菌群的健康发展偏离轨道,从而为日后儿童期的各种疾病埋下隐患。
儿童过敏
儿童过敏性疾病,包括湿疹、哮喘、过敏性鼻炎、食物过敏等,是一组以免疫系统对无害物质产生过度反应为特征的常见慢性病。它们的发病,往往与遗传和环境因素共同相关。
从临床分型上看,这些疾病都属于特应性疾病,其核心是身体产生了过度的IgE抗体来对抗那些本应无害的环境物质(如花粉、尘螨、某些食物等)。并且,患有其中一种过敏的孩子,往往更容易患上另一种,这被称为过敏进程。
▸肠道菌群:过敏病程中的关键调控者
这几年,无论是基础研究还是临床队列,都越来越一致地指向一个关键环节,肠道菌群在过敏的发生发展中扮演着关键的调控角色。
在我们对过敏儿童样本的菌群数据分析中,可以看到一种具有代表信的肠道菌群失调。
具体来说,过敏儿童的菌群通常具备几个共性:
更细分到食物过敏的时候会发现,不同食物过敏原(比如牛奶蛋白、鸡蛋蛋白、花生等)相关的菌群变化还可能各有其特异性的模式,不同分型这也是我们正在关注的方向。
▸失控的免疫反应:当前主流的菌群-免疫假说
那肠道菌群究竟是通过什么路径去影响免疫系统,进而推动过敏的呢?目前在学术界相对被广泛接受的,是围绕短链脂肪酸,尤其是丁酸盐的一条核心假说:
丁酸盐的缺失:菌群失调导致关键的代谢产物——丁酸盐浓度下降。
刹车失灵:丁酸盐是促进初始T细胞分化为调节性T细胞(Tregs)的关键信号。Tregs在免疫系统中可以理解为一个刹车装置,负责抑制过度的免疫反应,维持免疫平衡。
免疫过度激活:丁酸盐减少导致Tregs数量不足或功能受损,刹车失灵,免疫系统便会对无害物质反应过度。
典型免疫表型:在这种菌群失调的背景下,我们在过敏儿童身上通常可以看到这样一组特征性变化:
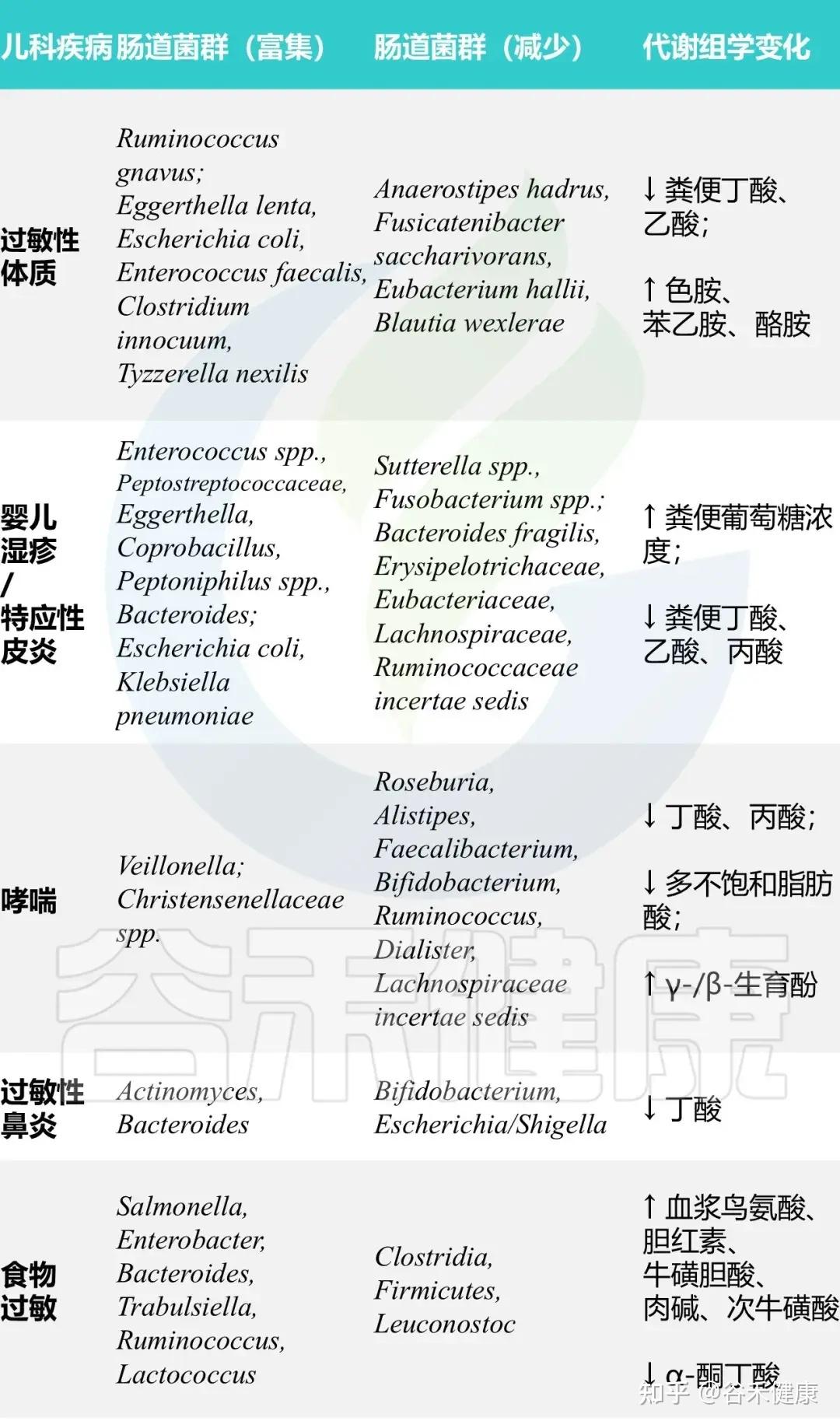
总而言之,生命早期的肠道菌群失调,通过影响免疫系统的正常教育过程,为日后一系列过敏性疾病的发生埋下了伏笔。而具体的菌群和代谢物变化,则在不同的过敏性疾病中呈现出各自的特征。
肠道菌群检测就是力求精准地捕捉到这些早期的菌群和代谢物特征,在实际应用中,我们并不会仅看哪个菌高了或者低了,而是会把菌群特征与已有的临床和免疫学指标放在一起综合判断。
例如,结合谷禾肠道菌群检测报告中的过敏相关菌群模块、肠道屏障评分,以及部分炎症相关因子和免疫调节指标(如 IL‑6 等),我们可以更准确地判断一个孩子的肠道生态,是不是已经处在一个更偏向炎症和过敏反应的状态,尽可能实现对高风险儿童的早期识别,从而为临床的早期预警和干预提供思路。
IBS 与 IBD
在儿童常见的胃肠道疾病中,炎症性肠病(IBD)和肠易激综合征(IBS)是两个重要的类别,它们都与肠道菌群的失衡密切相关。
虽然生命早期的肠道菌群构成与这两种疾病的确切因果关系仍在研究中,但科学家们已经在年龄较大的患病儿童中发现了明确的菌群改变。
▸失衡的菌群
IBS患儿的菌群特征:
IBD患儿的菌群特征:
▸代谢物的变化(化学信号的紊乱)
在IBD患儿体内,色氨酸、琥珀酸盐和3-羟基异丁酸等关键微生物代谢产物的水平较低。
在IBS患儿体内,则观察到葡萄糖、甾醇、乳酸水平升高,而有益的丁酸盐水平下降。
尽管如此,与生命早期相关的特定代谢组学特征,目前仍是一个有待深入探索的领域。
▸失控的免疫反应:炎症
在这两种疾病的背后,一个共同的核心病理机制是:由肠道屏障缺陷和微生物失调共同驱动的、失控的黏膜免疫反应。
IBD:
某些能够降解肠道黏液保护层的致病共生菌,例如黏附侵袭性大肠杆菌(adherent-invasive Escherichia coli),能够诱导巨噬细胞等免疫细胞分泌IL-1β,这会直接促进Th17细胞的分化,点燃肠道炎症。
从口腔跑到肠道的克雷伯氏菌属,也能促进树突状细胞和巨噬细胞产生促炎因子,从而推动初始T细胞分化为Th1和Th17细胞,加剧炎症。
此外,大量能产生IgG抗体的浆细胞被招募到肠道,也参与了IBD的疾病进展。
IBS:
虽然炎症程度不如IBD剧烈,但在IBS患儿的结肠黏膜和血液中,也观察到了先天免疫的过度活跃,特别是来自肥大细胞和单核细胞的活动增强。
适应性免疫同样参与其中,表现为肠道内T细胞数量增加、B细胞活性改变以及抗体的产生。
简而言之,IBD和IBS的发生,是肠道菌群失衡与免疫系统功能紊乱相互作用、相互放大的恶性循环。然而,上述这些复杂的免疫机制,在那些具有高患病风险的婴幼儿身上是如何运作的,仍需要更多未来的研究来进一步验证和阐明。
常见儿科疾病中的早期肠道生态失调
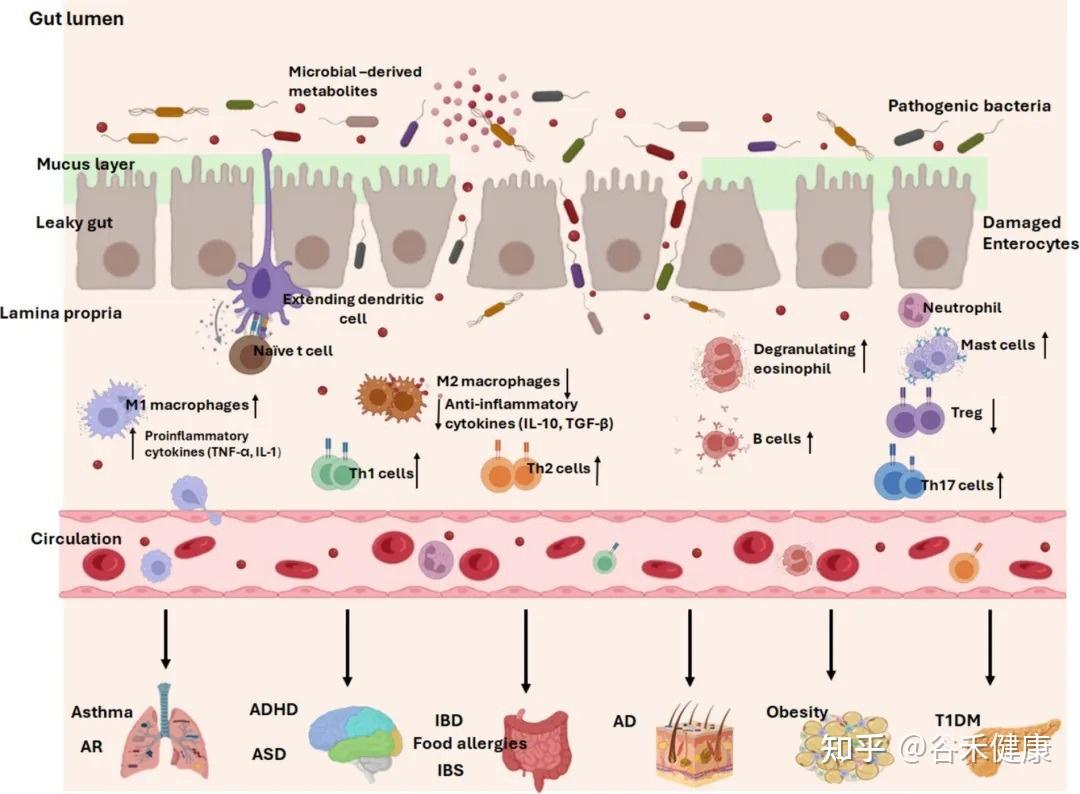
神 经 发 育
生命最初的几年,不仅是肠道菌群建立的关键窗口,也恰好与中枢神经系统发育的关键阶段,如神经突触的形成和髓鞘化高度重叠。这并非巧合。一条被称为肠-脑轴的复杂通讯网络,将肠道和大脑紧密地联系在一起,使得肠道菌群的状况能够深刻影响神经发育,甚至可能参与了自闭症谱系障碍(ASD)和注意力缺陷多动障碍(ADHD)等疾病的发生。
这两种情况有时会同时出现在一个孩子身上。
▸失衡的菌群,失调的化学信号
由于肠道微生物能通过其代谢产物和影响免疫通路来调控神经系统的发育和功能,科学家们将其视为自闭症和多动症发病的一个潜在贡献者。研究发现,与正常儿童相比,具有高患病风险的幼儿,其肠道菌群的构成和产生的生物活性代谢物均存在显著差异。
-菌群失衡
-关键神经递质的缺失
一个尤为引人注目的发现是,这些高风险儿童体内由细菌产生的、具有神经活性的分子——γ-氨基丁酸(GABA)的水平显著降低。
这些发现清晰地揭示了在生命早期,肠道菌群-代谢产物-神经系统之间存在的深刻联系。
▸从肠道炎症到大脑炎症
GABA的减少可能不仅仅是一个孤立的现象,它或许是连接肠道失衡与大脑功能异常的关键一环。GABA是大脑中主要的抑制性神经递质(负责让大脑冷静下来),它还在调节焦虑、改善睡眠、缓解疼痛以及帮助维持神经系统的整体平衡方面发挥着关键作用。
-连锁反应的启动
菌群失调导致GABA等代谢产物水平改变。
GABA水平的改变,加上菌群本身的失调,引发了不正常的免疫反应和全身性炎症(表现为血浆中细胞因子水平的异常)。
这种慢性的全身性炎症会逐渐破坏精密的血脑屏障的完整性。血脑屏障一旦受损,炎症细胞和炎症因子便更容易进入大脑,最终引发神经炎症,从而影响大脑的正常发育和功能。

简而言之,ASD和ADHD的发生,可能部分源于肠道开始,经由免疫系统,最终波及大脑。然而,这其中的具体机制非常复杂。尤其是在菌群发育的关键窗口期,究竟哪些早期的免疫学特征能够预示ASD和ADHD的发生,仍然是未来研究需要迫切解答的重要问题。
肥胖及1型糖尿病
在儿童期,最常见的代谢性疾病莫过于肥胖和1型糖尿病(T1DM),而这两者的发生,都与生命早期的肠道菌群失调有着千丝万缕的联系。
▸肠道菌群:调节新陈代谢
我们的肠道菌群在宿主的新陈代谢中扮演着至关重要的“总调度师”角色,其影响力涵盖了脂质与葡萄糖代谢、能量消耗与脂肪储存,乃至胰岛素信号的传导等多个方面。
更关键的是,T1DM的发病高峰期通常在生命最初的5-6年,这与肠道菌群发育的关键窗口期完全重合,这暗示了两者之间强烈的内在联系。
▸失衡的菌群
与健康儿童相比,患有或高风险患有这两种代谢病的儿童,其肠道菌群构成显示出特定的指纹。
-T1DM高风险儿童的预警信号
研究发现,在T1DM高风险儿童体内出现自身抗体(血清学转换)之前,他们的肠道中多形拟杆菌(Bacteroides dorei)和普通拟杆菌(B. vulgatus)的数量就已经显著增加。值得警惕的是,这两种拟杆菌属细菌均与肠道炎症有关。
-肥胖儿童的菌群
从婴儿早期开始,肥胖儿童的肠道中就表现出脆弱拟杆菌(Bacteroides fragilis)丰度更高,而有益的双歧杆菌属(Bifidobacteria)和柯林斯菌属(Collinsella)数量更少。这种菌群模式与日后过度的体重增加直接相关。
▸代谢紊乱:疾病发生前的信号
在疾病真正显现之前,身体的化学信号——代谢产物,可能已经发出了警报。
-肥胖儿童的代谢特征
他们的体内GABA(一种能调节食欲和体重的神经递质)水平显著较低。
同时,血液中对称性二甲基精氨酸和不对称性二甲基精氨酸的水平升高,这两种物质被认为与全身性炎症有关。
-代谢综合征儿童的发现
另一项研究观察到,在5岁的代谢综合征儿童体内,参与糖异生、氨基酸和脂肪酸代谢的循环代谢产物显著增加,这些代谢通路的变化与他们的BMI、腰围和空腹血糖水平密切相关。

▸免疫与炎症:连接菌群与疾病
早期肠道菌群与免疫系统之间的相互作用,是驱动这些代谢疾病的关键。
-肥胖与炎症
在3-5岁的重度肥胖儿童中,可以观察到C反应蛋白(一种全身性炎症标志物)的水平升高。
失调的肠道细菌及其代谢产物(分解代谢物)会损害脂肪组织的稳态,并诱发慢性低度炎症,从而助长儿童肥胖的发生。
-T1DM与炎症
儿童T1DM患者体内常常同时存在肠道菌群失调和全身性及组织特异性的炎症反应升高,这清晰地表明,肠道微生物在维持宿主代谢健康中扮演着不可或缺的角色。
因此,无论是儿童肥胖还是1型糖尿病,其背后都涉及生命早期的肠道菌群失调,通过扰乱宿主正常的新陈代谢通路和触发不当的免疫炎症反应,为这些慢性代谢疾病的发生和发展铺平了道路。
在生命早期干预和重塑肠道微生物群,是促进长期健康的有效方法。儿童的肠道菌群比成人更容易被环境因素改变,且该时期是免疫系统成熟的关键窗口,而免疫系统又受到肠道菌群的调节。
这里我们来了解一下在常见儿童疾病中,通过操纵早期肠道微生物组进行干预的前沿研究。
儿 童 过 敏
既然我们知道了肠道菌群失调是儿童过敏的关键推手,那么,我们是否能主动出击,通过调整菌群来拨乱反正,预防或缓解过敏呢?
答案是肯定的,现有研究已经为我们指明了几个有希望的方向。
▸抗生素的阴影与警示
在讨论干预之前,必须再次强调预防的重要性。大量证据表明,无论是母亲在孕期还是孩子在生命早期使用抗生素,都会增加儿童患过敏性疾病的风险。
剂量效应: 一项研究发现,母亲孕期使用抗生素的剂量越大,孩子日后患过敏病的风险就越高。
菌群变化: 生命早期使用大环内酯类抗生素,会导致肠道菌群发生剧烈变化,表现为放线菌门数量锐减,而拟杆菌门和变形菌门的数量则会增加。这种菌群的偏移,与哮喘风险和高BMI直接相关。
▸益生菌与益生元
直接补充益生菌及益生元,是最直接的干预手段之一,并且已经展现出不错的效果。
-针对湿疹
一项研究测试了一种含有两歧双歧杆菌(Bifidobacterium bifidum)和短双歧杆菌(B. breve)的特殊婴儿配方。结果显示,使用该配方的湿疹儿童肠道中,短双歧杆菌的丰度显著增加,同时 与乙酸盐合成相关的代谢通路被激活,这与湿疹症状的缓解显著相关。
-预防湿疹
另一项类似的研究也证明,补充益生菌和低聚半乳糖能够丰富肠道中的乳酸杆菌和双歧杆菌,从而有效预防了湿疹的发生。
-针对过敏性鼻炎
在一项芬兰的研究中,研究人员给孕晚期的母亲和她们出生后6个月内的婴儿补充四种益生菌菌株和低聚半乳糖(GOS)。在后来患上鼻炎的孩子组中,这种干预显著提升了双歧杆菌的数量,并减少了拟杆菌的数量。
▸母乳喂养与运动:有争议
-母乳喂养
理论上,母乳是建立婴儿免疫耐受的核心。但关于母乳喂养与预防过敏之间的关系,证据却并不完全一致。一些研究报告了其保护作用,而另一些则认为延长母乳喂养并没有预防效果。这说明其中的机制可能比我们想象的更为复杂。
-体育锻炼
在菌群可塑性最强的童年期,运动也可能扮演着重要角色。有研究显示,3-6岁时体育活动水平低的孩子,在儿童后期患哮喘的风险更高。然而,一个关键的不足是,这些研究并未分析运动究竟是如何影响肠道菌群的。
▸饮食:塑造菌群的日常选择
饮食是影响肠道菌群最基础、也最持久的因素。
PASTURE的一项研究发现,1岁时粪便中丁酸盐和丙酸盐水平高的婴儿,未来患上哮喘和发生过敏性致敏的风险更低。而这些短链脂肪酸的水平,又与婴儿饮食中摄入的酸奶、鱼、水果、蔬菜显著相关。
另一个代谢组学研究则指出,富含油炸和加工肉类的饮食习惯,与哮喘风险以及肠道中克里斯滕森菌科(Christensenellaceae)细菌的增多呈正相关。

「哮喘」最新研究已逐步渗透到更精细层面28 赞同 · 3 评论 文章
IBD 和 IBS
面对由菌群失调驱动的炎症性肠病(IBD)和肠易激综合征(IBS),研究人员正在积极探索一系列干预措施,试图通过调控肠道菌群,来调节肠道内的紊乱。
▸抗生素与噬菌体
越来越多的证据将矛头指向了抗生素。
一项涵盖22项研究的系统性回顾发现,生命最初两年内使用抗生素,与日后患上IBD的风险存在强烈关联。
另一项荟萃分析也指出,母亲在孕期接触抗生素和烟草烟雾,都会增加后代患IBD的风险。
噬菌体疗法:作为抗生素的潜在替代方案,噬菌体疗法(利用病毒去攻击特定的有害细菌)已在人体中显示出良好的安全性。它或许能成为治疗儿童胃肠道疾病的一种新方法,但要真正应用于临床,还需要大量深入的研究。
▸压力
早期生活压力的破坏力:肠道不仅感受生理刺激,也感受心理压力。一项动物研究利用母婴分离模型来模拟早期生活压力,结果发现,这种压力能够诱导小鼠从童年到成年持续出现类似IBS的症状,其肠道菌群也发生了改变,表现为乳酸杆菌、肠杆菌属等有益菌的减少。
▸饮食:塑造肠道的终极力量
在所有干预手段中,饮食调整可能是最基础、也最有效的方法之一。
-需要警惕的饮食
研究表明,高脂肪饮食以及富含可发酵寡糖、双糖、单糖和多元醇(FODMAPs)的饮食,会加剧IBD和IBS的症状。而在一项大型研究(斯堪的纳维亚出生队列的汇总研究数据)中,1岁时大量摄入含糖饮料也与日后更高的IBD风险相关。
-值得推荐的饮食
富含多酚、矿物质和高纤维的饮食则被证实有助于缓解症状。同一项研究发现,1岁时鱼类和蔬菜摄入量高的孩子,未来患IBD的风险更低。
-草本的力量
一些草本植物也显示出潜力。例如,在一项针对103名IBS患儿的随机双盲试验中,服用洋车前子(一种富含纤维的草本)长达6周的儿童,其腹痛发作的次数显著少于服用安慰剂的儿童。
但有趣的是,尽管症状得到了改善,两组儿童的肠道菌群构成却没有观察到显著差异,这提示其作用机制可能不仅仅是通过改变菌群。
肥胖和糖尿病
通过干预和调控生命早期的肠道菌群,我们或许能找到重置儿童新陈代谢的关键,从而预防这些疾病的发生。
▸抗生素
来自母亲的影响:现在的人群数据已经给了比较一致的信号。比如有研究发现,妈妈在备孕阶段频繁使用某些抗生素(像青霉素、喹诺酮类),和孩子日后T1DM 风险上升是相关的。
宫内暴露的后果:胎儿在子宫内接触到抗生素(如青霉素),与宝宝出生后的生长迟缓相关。这种暴露会导致婴儿肠道菌群多样性降低,并引发一系列菌群结构的改变:厚壁菌门和乳杆菌目减少,而变形菌门和拟杆菌门等则相对增多。
▸母乳喂养的黄金标准
在生命最初的几个月里,母乳是主要的营养来源,塑造早期肠道微生物群,促进双歧杆菌主导的肠道,这一点和我们日常检测到的健康婴幼儿菌群特征也是一致的。
明确的保护作用:来自两个基于人群的队列的数据显示,非母乳喂养的婴儿,其日后患T1DM的风险翻了一倍。同时,一项涵盖25项研究的荟萃分析也明确指出,母乳喂养是预防儿童肥胖的显著保护因素。
然而,大多数此类研究未能建立起从“母乳喂养”到“特定菌群改变”再到“代谢改善”之间的完整证据链。
▸益生菌
针对T1DM:研究显示,在生命最初的27天内进行益生菌干预,与T1DM高风险儿童的自身免疫风险降低相关。
针对肥胖:母亲在孕期及产后补充特定的益生菌(如鼠李糖乳杆菌HN001),能有效降低婴儿在2岁时过度肥胖的风险,这提示“母亲补充,婴儿受益”的策略或许能预防儿童肥胖。
▸运动的悖论:明确的效果与未解之谜
在肥胖儿童中的效果:研究证实,在肥胖儿童中,体育锻炼能够降低血糖和促炎通路,同时改善菌群(降低γ-变形杆菌,增加罗斯氏菌属Roseburia等),并提升有益的短链脂肪酸水平。
然而,这些研究几乎都是在年龄较大、菌群已趋于成熟的儿童或青少年中进行的。体育锻炼对于菌群可塑性最强的婴幼儿时期会产生怎样的影响,亟待未来的研究来解答。
▸营养:从母亲到孩子的饮食智慧
-母亲饮食的深远影响
母亲在孕期的饮食可以直接影响其自身的菌群,这种状态又能通过传递来重塑婴儿的早期菌群,从而为孩子未来的代谢健康打下基础。
-植物化学物质
多酚:如葡萄多酚,在动物实验中被证明能促进有益的Akkermansia菌和乳酸杆菌的定植,增加短链脂肪酸的产生。
实验室的研究也表明,无论是来自西兰花的萝卜硫苷,还是来自大豆的染料木黄酮,在生命早期摄入,都能有效减少后代的过度肥胖,改善其整体代谢健康。
这些发现揭示了巨大的潜力,但下一步需要通过转化研究来验证这些营养成分在人类儿童身上是否同样有效,以及它们是如何通过影响肠道菌群来发挥作用的。

膳食纤维对代谢健康和肥胖的影响8 赞同 · 1 评论 文章
儿 童 神 经 发 育
一切始于源头,生命最初的经历深刻地影响着大脑的发育轨迹。
-母乳喂养的保护
一项研究表明,更长时间的纯母乳喂养能够降低儿童患ASD和ADHD的风险。
-需要警惕的风险因素
相反,母亲吸烟、压力大、母乳喂养时间过短(< 4个月)则与更高的ADHD风险显著相关。而孕期感染和母亲患有自身免疫性疾病,也与ASD的发生呈正相关。
-补偿剖腹产的损失
对于剖腹产导致菌群未能正常传递的问题,一种名为阴道菌群移植(VMT)的新技术显示出潜力。研究发现,接受了VMT的新生儿,其肠道菌群和代谢物状况更优(如乳酸杆菌、双歧杆菌增多,克雷伯氏菌减少),并且在6个月大时,其神经发育评分也显著更高。
▸益生菌
直接补充特定的益生菌,为预防神经精神障碍提供了新的思路。
一项长达13年的里程碑式的研究中,科学家们给75名婴儿在生命最初的6个月里补充了鼠李糖乳杆菌GG。结果发现,这一干预引发了长期的、有益的菌群变化。更令人震撼的是,追踪到13岁时,这些接受了益生菌干预的孩子,其患上ADHD的风险显著降低了。
真实世界研究显示,植物乳杆菌PS128 服用者在注意力、沟通技能上有显著改善,且副作用小。
▸体育锻炼
体育锻炼不仅强健身体,更能健脑。
研究证实,让患有ASD的幼儿在进行课堂活动前进行体育锻炼(尤其是有氧运动),能够显著改善他们的学业反应能力。
▸母亲的饮食习惯
母亲通过塑造自身的肠道菌群,能将其影响传递给下一代,深刻影响孩子的行为和大脑功能。
母亲菌群多样性重要:一项大型队列研究发现,母亲孕期肠道菌群的α-多样性越高,其孩子在2岁时表现出的行为问题就越少。
有益菌的传承:在行为正常的孩子组中,他们的母亲肠道中富含能产生丁酸盐的菌科(如毛螺菌科Lachnospiraceae、瘤胃球菌科)。
健康的孕期饮食,与更高的母亲菌群多样性和更少的儿童内化行为问题直接相关,这清晰地表明,母亲的饮食是支持婴儿早期大脑发育的关键一环。
▸营养
研究报告称,ω-3脂肪酸、维生素、锌、镁、植物化学物质可能在管理与自闭症和多动症相关的生态失调方面发挥有益作用。
基于微生物的可改变因素对儿童疾病发展的影响
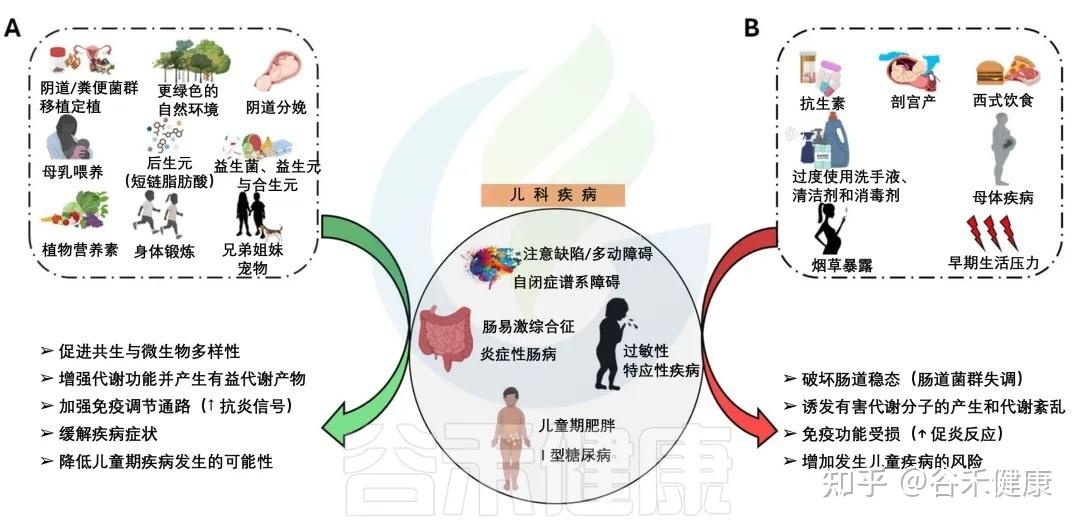

儿童神经发育异常的脑肠轴视角 – 自闭症早期风险判别和干预新路径6 赞同 · 0 评论 文章

探索大脑健康的宝藏:神经营养素、肠道菌群与我们的思维宇宙8 赞同 · 0 评论 文章
甲状腺功能障碍
甲状腺,这个位于颈部的蝴蝶状腺体,是身体新陈代谢的总开关。而它的功能状态与远在腹部的肠道菌群息息相关,形成了一条“肠道-甲状腺轴”。
肠道菌群失调和肠道屏障通透性增加(肠漏),与自身免疫性甲状腺疾病的风险增加有关,这是导致儿童甲状腺功能亢进或减退的主要原因。
▸肠道 ⇌ 甲状腺
肠道对甲状腺的影响:肠道细菌能影响甲状腺合成激素所必需的矿物质(如碘、硒、锌)的吸收和利用。同时,它们也参与甲状腺激素的代谢和激活。甲状腺免疫也受肠道微生物及其代谢产物的调节,从而导致自身免疫性甲状腺疾病的发病机制。
肠道对甲状腺的影响
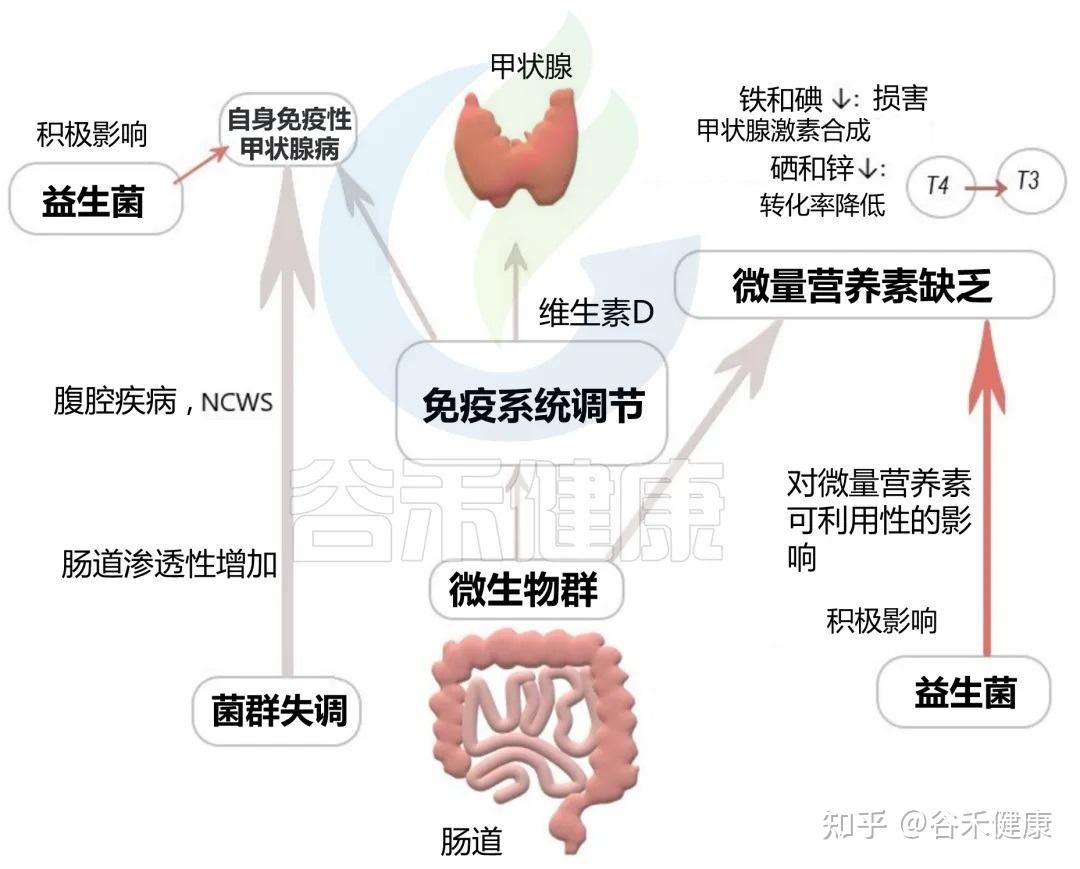
甲状腺对肠道的影响:甲状腺激素反过来也能影响胃肠道的蠕动,并可能直接调控肠道菌群的构成。
▸甲状腺相关疾病患者肠道菌群变化
在成人中:
甲亢患者的双歧杆菌和乳杆菌减少;
而桥本氏甲状腺炎患者则有Akkermansia菌和双歧杆菌的富集。
在儿童中,尤其是在菌群发育的关键窗口期,这方面的研究仍然非常稀少。
▸潜在的干预策略
研究提示,高纤维饮食、补充甲状腺相关的微量营养素、益生菌/益生元、体育锻炼甚至粪菌移植(FMT)都可能对保护甲状腺功能有益。相反,环境中的内分泌干扰物则是一个明确的风险因素。


慢性自身免疫性疾病——桥本甲状腺炎,改变认知和抓住关键16 赞同 · 1 评论 文章
性 早 熟
性早熟(PP),即第二性征过早出现,是儿童中一种日益普遍的内分泌紊乱,尤其在女孩中更为常见。最新的研究将目光投向了肠道菌群,认为它可能在“性激素-肠道菌群轴”上扮演了催化剂的角色。
▸菌群如何催熟?
影响雌激素代谢:某些肠道细菌,如瘤胃球菌属和拟杆菌属,能够通过产生β-葡萄糖醛酸酶来影响雌激素的代谢和循环,从而影响青春期的启动。
通过“肠-脑轴”通讯:菌群产生的短链脂肪酸(SCFAs)和神经递质,也能通过“肠-脑轴”向大脑发送信号,间接调控青春期的启动时机。
一项研究发现,与健康女孩相比,患有中枢性性早熟的女孩肠道中,多种特定细菌显著增加,如:
而这些细菌恰恰与肥胖、短链脂肪酸产生和雌激素代谢有关。
代谢组学分析进一步发现,这些女孩粪便中的代谢物发生了改变,与促进性腺激素分泌的通路(如类固醇生物合成)被激活有关。
性激素和肠道菌群之间的相互关系
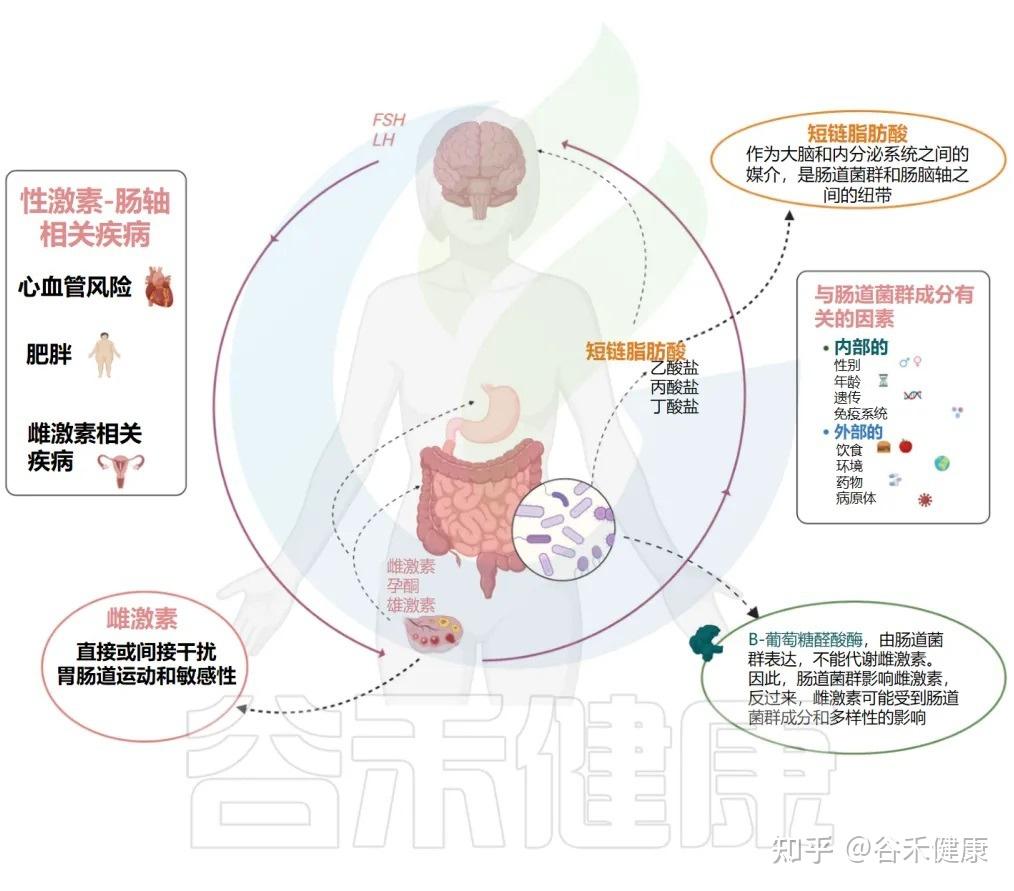
▸干预与警示
有益的干预:动物实验表明,益生菌治疗可以逆转由早期压力或环境物质诱导的性早熟。在人类中,维生素D补充、复杂的碳水化合物和高蛋白饮食(如坚果、蔬菜、海鲜等)被认为可能对预防性早熟有益。
有害的暴露:生命早期接触内分泌干扰化学物质和环境污染物,会扰乱肠道菌群,从而增加性早熟的风险。
无论是甲状腺功能还是青春期的启动,这些看似与肠道无关的生命过程,都可能受到肠道菌群的深刻调控。这为我们理解和干预儿童内分泌疾病打开了一扇全新的大门。

性早熟和微生物群:性激素-肠道菌群轴的作用3 赞同 · 0 评论 文章
综上所述,我们看到许多儿童常见的健康问题,从反复过敏到体重管理,再到消化不适,似乎都与肠道这位“看不见的伙伴”——肠道菌群息息相关。生命早期是肠道菌群蓬勃发展并奠定基础的关键时期,它像一片微型森林,受到出生方式、母乳、饮食、环境等多种因素的影响。
案例一:
肠道整体健康的宝宝,可以看到他的菌群健康、慢病控制、营养均衡三个维度都处在良好水平,有益菌充足、有害菌处于正常低水平,核心菌属完善。
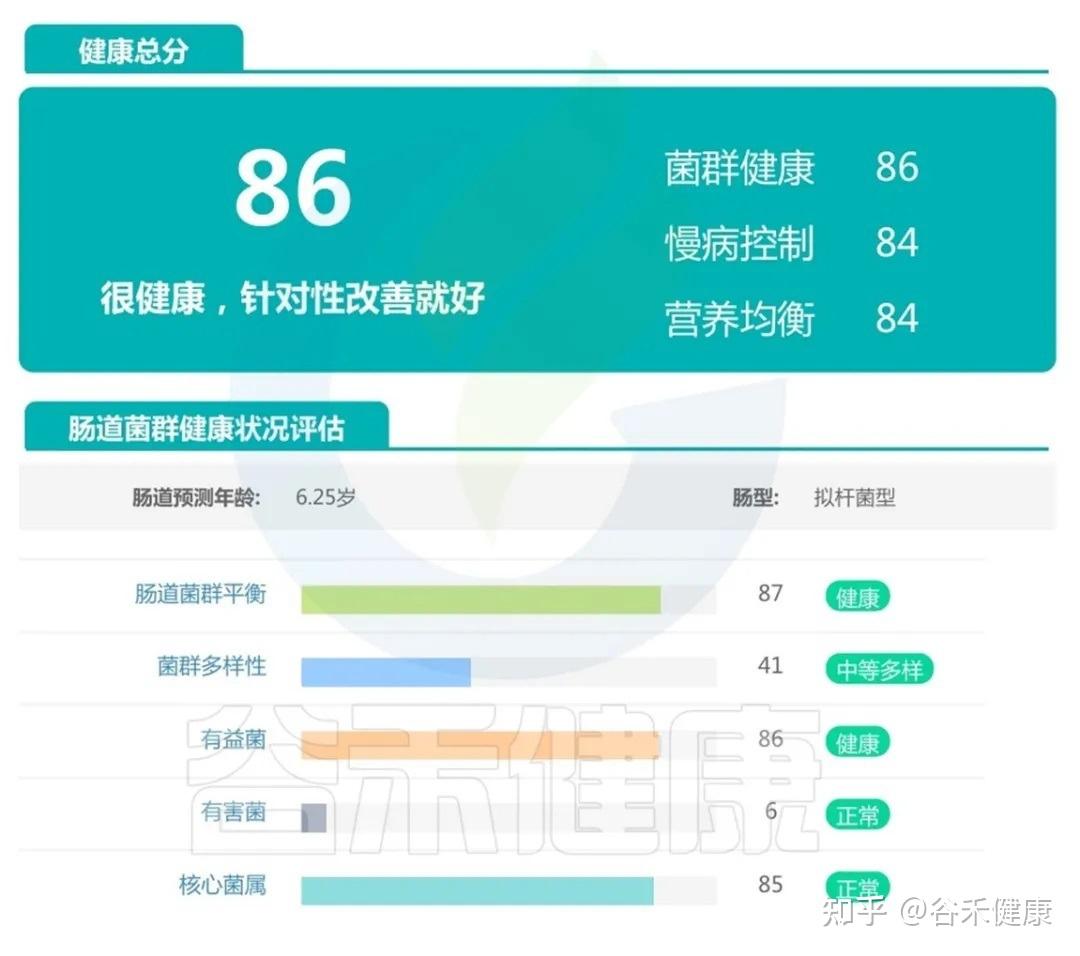
案例二:
这个宝宝处于中等平衡状态,菌群健康指标较前一位儿童有所减弱,核心菌属开始出现缺乏,提示他可能已经携带了某些代谢问题的风险信号。
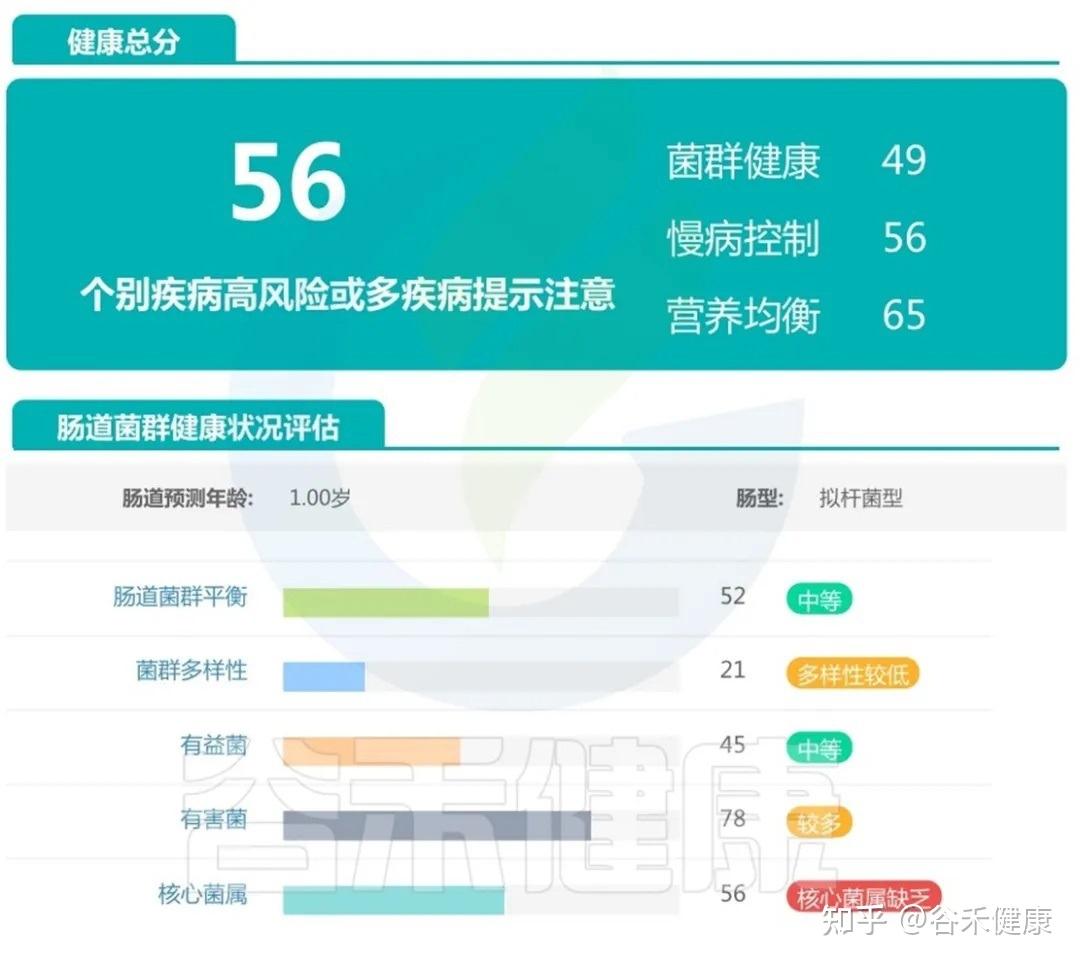
菌群多样性不足,有益菌占比下降,有害菌及产气相关菌群相对偏高。
这种菌群构成,容易让孩子陷入功能性消化不适的恶性循环:肠道动力紊乱、气体产生过多、肠腔内压波动增大,最终就表现为便秘与腹泻交替,夜间睡眠不安等问题。
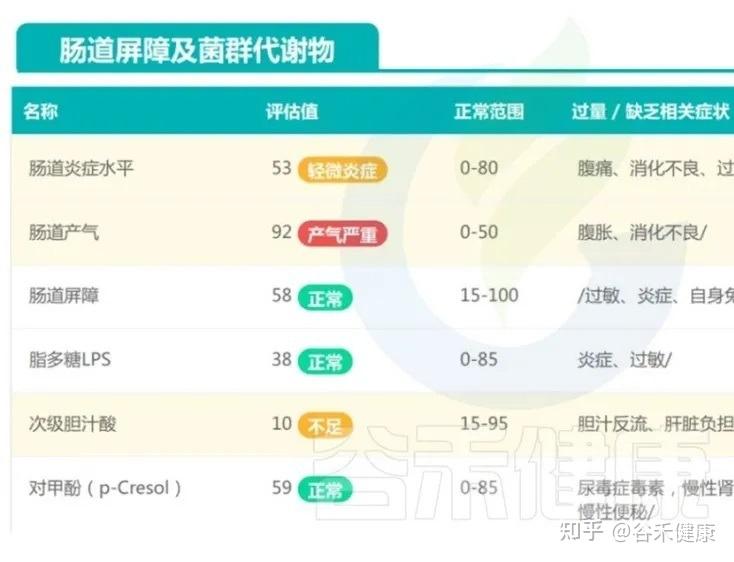
换句话说,这个孩子目前并不是存在明确器质性病变,更符合“肠道微生态已经出现早期失衡、但整体仍具有可逆性”的状态。
在这个阶段,如果能通过规范的饮食结构调整(例如逐步优化配方、增加优质膳食纤维、合理控制脂肪比例)、改善作息和生活方式,适当进行微生态干预(如针对性的益生菌/益生元支持),再配合后续的复查,就有较大机会把他的肠道环境拉回一个更平衡、更稳定的轨道。
案例三:
这个孩子目前看上去发育基本正常,仅社交能力稍不佳,从传统角度看,这样的孩子很容易被归为“现在没什么大问题”。但肠道菌群检测报告给出的信息却更加细腻:
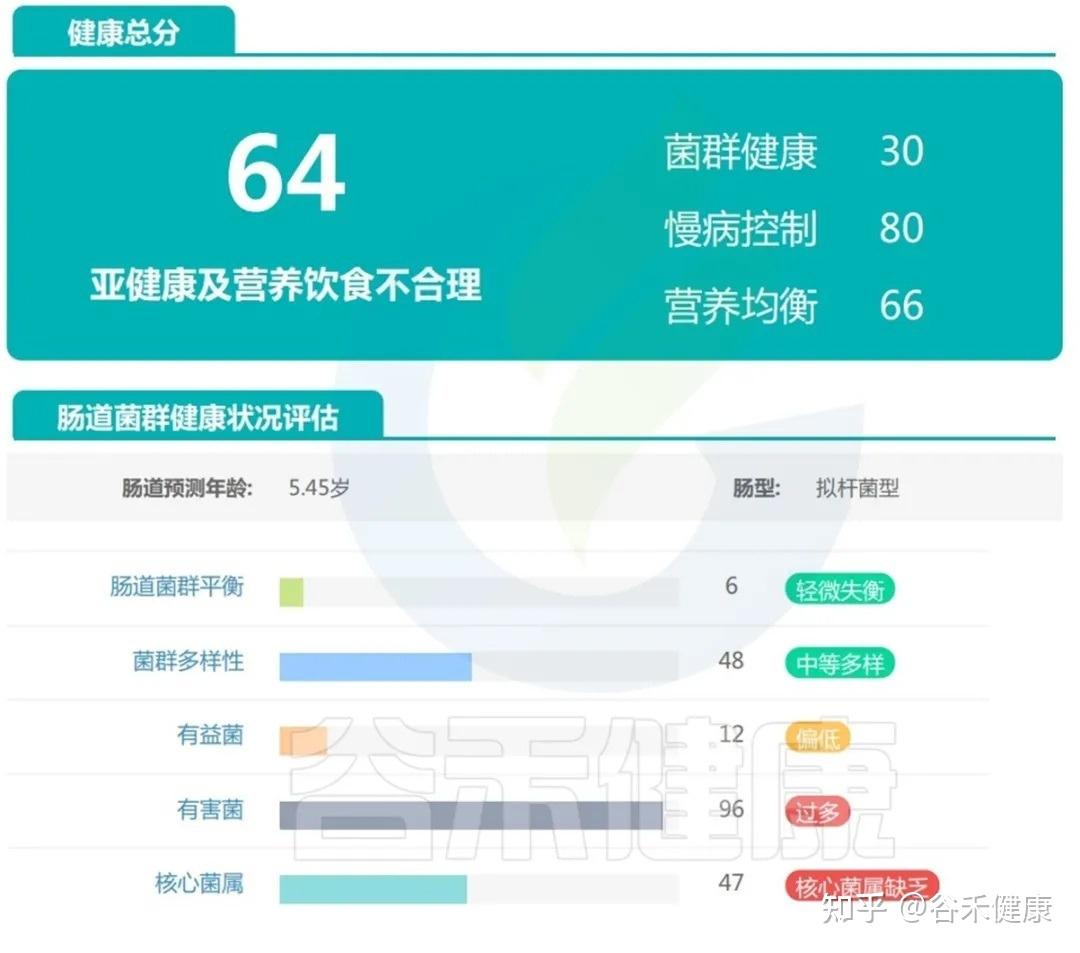
可以看到总体评分落在“轻微失衡”,已偏离理想健康状态。
有益菌丰度不足,有害菌比例偏高,核心菌属缺乏,这意味着肠道微生态的“稳定性”和“恢复力”都打了折扣。
结合该宝宝早期多次抗生素使用,很可能在肠道菌群发育的关键窗口期打断了原本的自然演化轨迹,走向一个“有益菌不足、有害菌偏多”的模式;这样的菌群背景,会让孩子在后续几年中更容易出现:反复上呼吸道感染、皮炎/湿疹、过敏性鼻炎等问题,这也与这与大量关于早期菌群失调和过敏性疾病风险上升的研究结果是吻合的。
同时,在肠–脑轴的影响下,肠道微生态的轻度失衡,过度增殖有害菌及超标代谢物(如对甲酚、硫化氢)会通过“肠脑轴”影响神经递质稳定性(如DOPAC升高提示多巴胺代谢素乱),影响孩子的情绪调节和社交意愿。
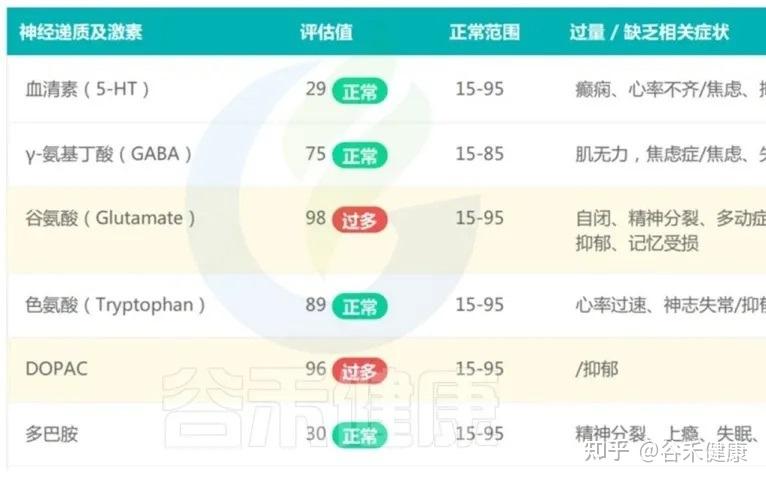
对于这种情况,肠道菌群检测不在于发现一个明确的器质性疾病,而是帮助家长在孩子看起来挺正常的当下,就开始有意识地保护和重建他的肠道微生态——包括减少不必要的抗生素使用、优化饮食结构、增加天然膳食纤维摄入、合理安排户外活动和环境暴露。

通过定期菌群监测,观察肠道菌群、有无新的过敏发作、呼吸道感染频次以及情绪和社交状态的变化,形成一个“早识别—早管理—可追踪”的长期支持路径。
因此,持续关注理解并监测儿童肠道菌群的发育与动态变化,不仅能帮助我们更全面地认识这些健康挑战,还能为未来的干预提供新的思路。通过科学的探索,我们期待能更好地守护儿童肠道微生态的健康成长,为他们一生的健康打下坚实而有力的根基。
主要参考文献
Bankole T, Li Y. The early-life gut microbiome in common pediatric diseases: roles and therapeutic implications. Front Nutr. 2025 May 29;12:1597206.
Shulhai AM, Rotondo R, Petraroli M, Patianna V, Predieri B, Iughetti L, Esposito S, Street ME. The Role of Nutrition on Thyroid Function. Nutrients. 2024 Jul 31;16(15):2496.
Yue M, Zhang L. Exploring the Mechanistic Interplay between Gut Microbiota and Precocious Puberty: A Narrative Review. Microorganisms. 2024 Feb 4;12(2):323.
Stokholm J, Blaser MJ, Thorsen J, Rasmussen MA, Waage J, Vinding RK, Schoos AM, Kunøe A, Fink NR, Chawes BL, Bønnelykke K, Brejnrod AD, Mortensen MS, Al-Soud WA, Sørensen SJ, Bisgaard H. Maturation of the gut microbiome and risk of asthma in childhood. Nat Commun. 2018 Jan 10;9(1):141.
Knezevic J, Starchl C, Tmava Berisha A, Amrein K. Thyroid-Gut-Axis: How Does the Microbiota Influence Thyroid Function? Nutrients. 2020 Jun 12;12(6):1769.
Ma T, Wu Z, Lin J, Shan C, Abasijiang A, Zhao J. Characterization of the oral and gut microbiome in children with obesity aged 3 to 5 years. Front Cell Infect Microbiol. 2023 Mar 29;13:1102650.
Tian X, Liu X, Wang Y, Liu Y, Ma J, Sun H, Li J, Tang X, Guo Z, Sun W, Zhang J, Song W. Urinary Metabolomic Study in a Healthy Children Population and Metabolic Biomarker Discovery of Attention-Deficit/Hyperactivity Disorder (ADHD). Front Psychiatry. 2022 May 20;13:819498.
Agrawal M, Sabino J, Frias-Gomes C, Hillenbrand CM, Soudant C, Axelrad JE, Shah SC, Ribeiro-Mourão F, Lambin T, Peter I, Colombel JF, Narula N, Torres J. Early life exposures and the risk of inflammatory bowel disease: Systematic review and meta-analyses. EClinicalMedicine. 2021 May 15;36:100884.

谷禾健康

菌群.营养.炎症.免疫
营养在整个生命周期中对免疫和炎症以及最终的健康有深远影响。最新研究表明,饮食对肠道微生物组成和代谢产物具有显著影响,从而对宿主免疫和炎症产生重要影响。
研究发现,我们日常饮食中的特定食物成分和代谢产物在感染、慢性炎症和癌症过程中可能表现为促炎或抗炎,这突显了饮食与微生物代谢产物对免炎调节的重要影响。这将对精准营养和治疗干预方法产生重要影响。
小鼠研究表明,饮食-微生物轴对免疫介导性疾病(包括炎症性肠病和过敏)产生影响,同时在感染、疫苗接种和癌症免疫治疗等情况下优化免疫功能。例如,人类中,膳食纤维摄入量增加与黑色素瘤免疫检查点阻断治疗反应改善相关,而长期服用抗生素可能会损害微生物群,从而降低流感疫苗的效果。
这重新激发了科学界和公众的兴趣,健康饮食意味着什么,它到底如何通过微生物群影响健康免疫系统?
本文我们就来了解一下,饮食与微生物相互作用对免疫应答调节的影响,以及对感染、慢性炎症、代谢健康和抗肿瘤免疫背景下微生物代谢产物的机制作用的新见解。
膳食成分既有直接作用,又有依赖于微生物的影响,本文侧重于后者。这也为我们提供了一个“精准营养”的新视角,根据遗传、饮食习惯、社会经济地位、微生物群等多种因素为个体或人群提供营养建议,可作为传染性、炎症性、代谢性疾病和癌症整体治疗方法的一部分。
哺乳动物与驻留在屏障部位(包括肠道)的微生物群共同演化。宿主与微生物之间的相互作用塑造了多种生理过程,包括哺乳动物的免疫应答。屏障组织及其相关微生物群暴露于各种外部因素,包括膳食摄入、药物、感染和环境污染物,统称为“暴露组”。
人类饮食的历史变化
膳食是塑造我们进化、社会和文化的最具影响力的外部因素之一。值得注意的是,在过去一个世纪,人类饮食与历史上逐渐变化的膳食相比发生了急剧而显著的变化。
这些主要变化包括:
1)植物、蔬菜和复杂碳水化合物(包括未加工的全谷物)的减少;
2)精制碳水化合物、植物脂肪、简单糖、盐和加工食品摄入量的增加;
3)广泛使用人工甜味剂、乳化剂、增稠剂、胶凝剂、稳定剂以及色素和防腐剂等化学物质。
这些变化在工业化国家更为明显,并且在与全球化增长相关的较不工业化国家中迅速发展。
饮食与肠道菌群、炎症的关联
一系列比较了世界各地人群的饮食和微生物群的人口研究表明,我们的饮食模式深刻影响肠道微生物群。例如,西方饮食改变了细菌组成并降低了微生物群的多样性或丰富度。相反,微生物群也可以改变饮食对宿主生理的影响。
人类研究表明,膳食纤维干预可以降低血液中炎症标志物;然而,在微生物多样性降低的个体中,它却会增加炎症。值得注意的是,过去100年中,炎症性疾病,包括炎症性肠病、过敏和糖尿病也一直在增加,研究揭示了与饮食和炎症相关的多样免疫调节途径。
动物来源的食物是许多营养素的高效(有时是唯一的)来源,包括铁、钙、锌、牛磺酸、肌酸、肉碱、维生素A、维生素B12、维生素D3和包括 EPA 和 DHA 在内的omega-3 脂肪酸,农业的工业化提高了这些食物的全球可获得性。
不同饮食结构影响肠道微生物组成
然而,基于动物的西方饮食会促进一种与植物为基础的饮食所促进的微生物组成不同的肠道微生物群。在小鼠和人类中,拟杆菌门(Bacteroidota)和厚壁菌门(Firmicutes)是两大微生物门,往往覆盖总微生物组的90%以上。
传统植物为基础饮食:普雷沃氏菌属主导
西方动物为基础的高脂饮食:拟杆菌属主导
通过饮食干预或由于迁徙至西方风格国家而从植物为基础的饮食转变为动物为基础的饮食,会导致拟杆菌属取代普雷沃氏菌属成为主导。因此,普雷沃氏菌属和拟杆菌属被认为是传统植物为基础饮食高纤维和西方动物为基础饮食高脂肪的生物标志物。高脂肪、高糖饮食及与之相关的肥胖在小鼠和人类中已被证明会降低拟杆菌属的总体相对丰度并增加Bacillota的丰度。
肠道菌群及其代谢产物如何影响宿主免疫反应和生理过程
饮食中的组分可以直接调节小鼠的免疫系统,然而最近的研究表明,饮食引起的微生物群变化也深刻影响宿主的免疫反应。在屏障表面的免疫系统可以检测微生物群及其结构成分,这种直接的相互作用建立了一种免疫反应的耐受状态。
然而,肠道微生物群产生成千上万种代谢产物,这些产物被吸收到我们的体内,并通过血液循环。许多这些代谢产物是由微生物群特异性产生的,而不是宿主产生的。它们属于不同的化学类别,包括短链脂肪酸(SCFAs)、非结合和结合的胆酸、酚类化合物、吲哚、胺类、黄酮类和气态化合物。
迄今为止已经确定的许多代谢产物是通过微生物群对饮食组分的直接转化而生成的,这些微生物群表达了能够消化特定膳食物质的专门酶。例如,短链脂肪酸是由膳食纤维的微生物发酵产生的。因此,微生物群从我们的饮食中提取和产生必需营养素,包括宿主无法产生的维生素。微生物群产生的代谢产物也是通过微生物将宿主代谢产物转化而生成的。
例如,初级结合胆酸被微生物群转化为初级非结合胆酸,进一步转化为次级胆酸或额外的结合胆酸。这些代谢产物可以在宿主的整个身体中循环,作为细胞表面或胞核受体的配体,并调节多种生物过程,包括新陈代谢、认知、组织稳态和免疫反应。
饮食可以迅速改变微生物群的组成
已经证明,饮食变化,例如从植物为基础的饮食转向动物为基础的饮食,可以在暴露于新饮食后的第一天就改变人类微生物群的组成。小鼠研究表明,饮食变化也会影响微生物群的代谢活动,因此可能会改变微生物群产生的代谢产物的浓度。
虽然某些饮食成分,包括特定类型的膳食纤维,可以促进有益菌的扩张,但其他成分可能导致菌群失调,即微生物群组成异常或微生物群产生的代谢产物失调的状态。
对于饮食对一些微生物群依赖的免疫调节效应,微生物群物种、微生物组分和宿主受体尚未完全表征。未来,揭示这些元素对于开发基于饮食和微生物群的精准营养和个性化医学将至关重要。
小鼠研究表明,在稳态条件下,黏膜免疫系统建立了对肠道微生物的耐受状态。参与这种耐受性反应的免疫细胞包括调节性T细胞(Treg细胞)和第3组固有淋巴细胞(ILC3s)等。然而,微生物群失调或异常免疫激活可能会破坏耐受性并引发慢性炎症病症。在这里以炎症性肠病为例来讨论。
饮食和微生物群在膳食纤维和炎症性疾病的背景下的作用是最受关注的。
膳食纤维是一种复杂的碳水化合物,哺乳动物无法消化,而是被肠道微生物群发酵。微生物群利用膳食纤维作为营养源,并将其转化为包括乙酸、丙酸和丁酸在内的短链脂肪酸(SCFAs)。
短链脂肪酸激活几种G蛋白偶联受体,包括GPR41和GPR43,并抑制组蛋白去乙酰化酶(HDACs)。最近的研究表明,在各种炎症性疾病背景下,这些受体配体相互作用通过不同机制有助于抑制炎症。
短链脂肪酸对免疫细胞的影响
2009年一项开创性研究表明,乙酸能够通过GPR43依赖的方式促进小鼠肠道损伤和炎症模型中炎症的缓解。调节性T细胞在抑制炎症中起着关键作用,并且在维持免疫稳态和自身耐受性方面至关重要。Treg细胞对于控制自身免疫疾病和包括炎症性肠病在内的慢性炎症病症至关重要。
饮食对慢性炎症性疾病的影响
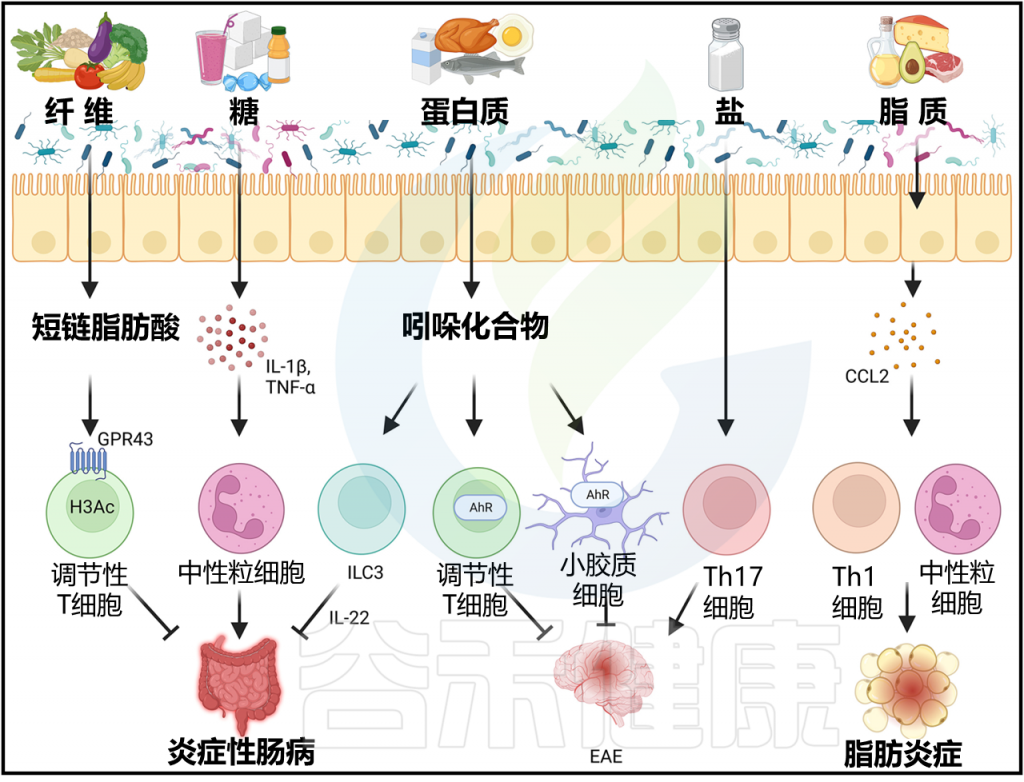
Arifuzzaman M et al., Immunity. 2024 57(1):14-27.
2013年,微生物群研究取得了重要里程碑,发现短链脂肪酸通过激活GPR43和抑制HDACs促进小鼠Treg细胞的分化和扩张。此外,无菌小鼠或饲养低纤维饮食的特定无特定病原体(SPF)小鼠显示短链脂肪酸和结肠Treg细胞减少。
最后,研究表明短链脂肪酸对小鼠T细胞转移结肠炎模型具有保护作用。这些研究是早期揭示微生物代谢产物直接调节免疫细胞的一些报告之一。从那时起,已经证明短链脂肪酸在小鼠各种炎症性疾病模型中具有抗炎作用,包括哮喘、关节炎和实验性自身免疫性脑脊髓炎(EAE)。
值得注意的是,短链脂肪酸介导的抑制HDACs的作用不仅限于促进Treg细胞,因为乙酸和丙酸也可以在适当细胞因子的预处理下促进Th1或Th17细胞的产生。
短链脂肪酸调节肠道微生物群
罗伊氏乳杆菌(Lactobacillus reuteri)是一种与人体共生的细菌物种,在系统性红斑狼疮(SLE)小鼠模型中,可以通过促进外周树突状细胞的聚集和在肠道和脾脏中提高Ⅰ型干扰素基因表达,来加重疾病结果。
通过饮食中的抗性淀粉,可以逆转罗伊氏乳杆菌(Lactobacillus reuteri)加重SLE的效应。从机制上讲,抗性淀粉诱导的短链脂肪酸通过直接抑制罗伊氏乳杆菌的生长来改善疾病。
注:抗性淀粉,一种被认为是膳食纤维的淀粉形式,因为它逃避了消化并被微生物群发酵。
膳食纤维还发挥着独立于短链脂肪酸的重要抗炎作用
膳食纤维可以保护肠壁的粘液层。如果小鼠缺乏膳食纤维,肠道微生物群就会利用宿主上皮细胞分泌的粘液糖蛋白,导致粘液层降解。这种保护性结肠粘液屏障的侵蚀,会导致肠道病原体Citrobacter rodentium(啮齿类柠檬酸杆菌)进入上皮的机会增加,从而促进结肠炎。
总的来说,这些研究突出了膳食纤维和短链脂肪酸通过多样化的免疫调节途径发挥抗炎作用。
值得注意的是,除了膳食纤维外,发酵食品(包括泡菜、酸菜、乳酪、开菲尔等)也改变了肠道微生物组成和代谢产物,这与人体中炎症标志物的降低相关。这些食物可以作为益生菌,通过提供特定的微生物种群(例如乳杆菌属)以及作为益生元,促进其他微生物种群(例如梭菌和拟杆菌属),从而改善微生物多样性。然而,发酵食品和涉及的微生物种群和代谢产物的抗炎作用机制尚未完全理解,需要进一步研究。
膳食蛋白质,特别是富含色氨酸的食物,如鸡肉、牛奶,也可以影响具有抗炎特性的微生物代谢产物。色氨酸是一种必需氨基酸,存在于富含蛋白质的食物中,人体利用它来产生神经递质5-羟色胺,稳定情绪,褪黑素,调节睡眠的激素,以及维生素B3,作为辅酶。
然而,微生物群也将色氨酸代谢为色胺和吲哚衍生物,包括吲哚-3-醛、吲哚乙酸、吲哚-3-丙酸和吲哚磺酸酯。这些代谢产物可以作为芳香烃受体(AhR)的激动剂,AhR是一个转录因子,在许多哺乳动物细胞类型中调节关键基因表达。
微生物来源的色氨酸代谢产物吲哚、吲哚-3-磺酸盐、吲哚-3-丙酸和吲哚-3-醛在小胶质细胞中的AhR信号传导改变了星形胶质细胞的免疫信号,并减轻了实验性自身免疫性脑脊髓炎的疾病严重程度。
值得注意的是,AhR还可以被各种植物来源、外源化合物和内源配体激活。通过芥蓝科蔬菜(例如西兰花和抱子甘蓝的代谢物)产生的一种代谢产物吲哚-3-甲醇(indole-3-carbinol)激活AhR已被证明促进ILC3s的扩增及其产生组织保护性IL-22,有助于增强多种结肠炎实验模型中的组织保护作用。
通过外源配体2,3,7,8-四氯二苯并二恶英(TCDD)激活AhR可以促进T调节细胞的扩增并抑制实验性自身免疫性脑脊髓炎。相反,内源配体6-甲醛吲哚[3,2-b]咔唑(FICZ)抑制T调节细胞的发育并促进T辅助17细胞的分化,导致实验性自身免疫性脑脊髓炎加重。这些研究表明,AhR在免疫细胞中的功能通常是配体特异的。
关于芳香烃受体(AhR)和色氨酸的详细代谢可以关注下谷禾以前发表的文章:
西方饮食逐渐缺乏膳食纤维,脂肪含量增加,添加盐和糖的浓度也增加,包括蔗糖和高果糖玉米糖浆。尽管西方饮食常常与动物脂肪摄入增加有关,但增加的脂肪含量主要来自全球范围内变得更加普遍的植物油和脂肪。
高脂饮食导致微生物群失调与炎症关联
与高脂饮食或肥胖相关的微生物群组成变化已与小鼠和人类的炎症联系在一起论。高脂饮食会导致小鼠和人类肠道微生物群失调,降低微生物多样性或“丰富度”。在小鼠中,这种微生物群失调已与肠道通透性增加相关联。这导致小鼠在四周内出现低级别肠道炎症。这种初始的炎症反应最终发展成涉及脂肪组织和肝脏炎症的全身性炎症状态,导致胰岛素抵抗。
Ccl2介导的炎症反应在代谢紊乱中的作用
肠道中增加上皮趋化因子Ccl2的表达引发了炎症反应,导致结肠粘膜下层的促炎性巨噬细胞的招募。随后CCL2的全身性升高导致促炎性巨噬细胞渗入脂肪组织,随后是其他炎症免疫细胞类型的积累,包括Th1细胞、CD8+T细胞、自然杀伤细胞(NK细胞)和中性粒细胞。
敲除Ccl2或其受体(Ccr2)可以改善脂肪组织炎症、肝脂肪变性和葡萄糖耐量。在人类肥胖的情况下,胰岛素抵抗主要是由肌肉内炎症驱动的,其特征是肌肉和肌周脂肪组织内免疫细胞的大量浸润。在肥胖的人类中,炎症和胰岛素抵抗与微生物群丰富度降低有关。
此外,减重会降低各种炎症标志物的浓度,包括肿瘤坏死因子α(TNF-α)、IL-6和C-反应蛋白。综上所述,这些数据突出了微生物群在促进炎症和相关代谢紊乱方面在高脂饮食和肥胖背景下的影响。
膳食脂肪促进硫还原致病菌增殖,导致慢性肠道炎症
除了微生物群失调和相关的低级别肠道炎症外,已经显示膳食脂肪可以促进特定微生物物种的积累,这些微生物可以直接导致慢性肠道炎症。例如,高脂饮食会促进牛磺胆酸(TCA)的产生,TCA被释放到肠道中溶解脂肪。研究表明,TCA的高浓度增加了肠道中有机硫的可用性,导致硫还原致病菌(Bilophila wadsworthia)的大量增殖,从而促进Il10−/−小鼠的结肠炎。这些研究需要进一步调查,以更好地表征膳食脂肪相关微生物群与炎症性肠病之间的关联。
扩展阅读:
肠道重要菌属——嗜胆菌属 (Bilophila)喜欢脂肪、耐胆汁的促炎菌
除了膳食脂肪外,添加的糖和盐也以微生物群依赖的方式促进肠道和其他器官的炎症。
高浓度简单糖改变肠道菌群,加重炎症
高浓度的简单糖(如葡萄糖、蔗糖和果糖)改变小鼠的微生物群组成,并与粘蛋白降解致病菌的增加、粘液层侵蚀和肠道通透性增加相关。这导致结肠中IL-1β、IL-6和TNF-α的表达增加,中性粒细胞浸润,并在多种实验性结肠炎模型中以微生物群依赖的方式加重疾病严重程度。
高量的食用食盐(氯化钠)也以微生物群依赖的方式加重化学诱导的结肠炎
高量的食用食盐还通过改变微生物群促进致病性Th17细胞的产生,并加重EAE中的炎症和疾病结果。此外,高量的食用食盐会减少人类和小鼠中的几种乳酸菌菌株。值得注意的是,补充乳酸菌菌株可以预防食盐诱导的EAE加重,表明乳酸菌在神经炎症中具有保护作用。
膳食成分对感染免疫力的影响
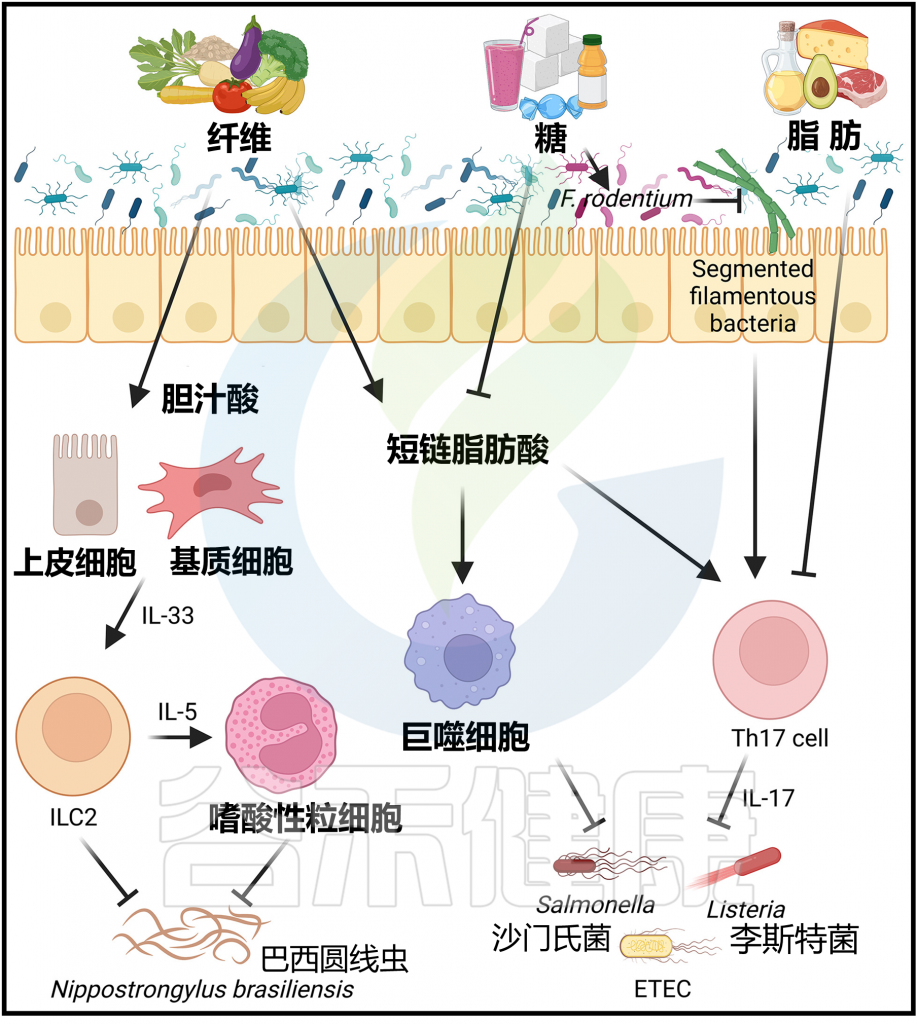
Arifuzzaman M et al., Immunity. 2024 57(1):14-27.
膳食纤维在结肠炎中的作用存在争议
尽管膳食纤维来源的短链脂肪酸(SCFAs)在多种结肠炎小鼠模型中减少肠道炎症,如前文所述,但使用各种高纤维饮食进行的类似研究报道了矛盾的结果。
例如,基于阿拉伯木聚糖的车前子、基于半乳糖的果胶和瓜尔胶具有抗炎或组织保护作用,而基于果糖的菊粉则加重炎症。已进行了多项临床试验来调节IBD患者的膳食纤维,尽管效果不一。此外,通常建议IBD患者避免富含纤维的饮食,因为膳食纤维可能加重疾病。然而,膳食纤维介导疾病恶化的机制尚不清楚。因此,在IBD背景下膳食纤维的作用仍存在争议。值得注意的是,最近的一项研究发现,低聚果糖,即菊粉纤维的结构单位,可以激活人类巨噬细胞产生与结肠炎相关的促炎细胞因子,包括IL-1β和IL-23。
此外,一项随机对照试验表明,给溃疡性结肠炎(UC)患者服用菊粉会增加结肠中的炎症细胞因子,包括IL-1β、IL-23和IL-5,并导致部分患者症状复发。在小鼠中,基于菊粉的高纤维饮食上调微生物群来源的胆酸代谢产物,促进IL-33的产生。这导致自然淋巴细胞群2(ILC2s)的激活和IL-5的产生,导致结肠中的嗜酸性粒细胞炎症。
菊粉纤维饮食还会触发肺部嗜酸性粒细胞增多,并加重小鼠过敏性气道炎症模型的疾病结果,而果胶纤维具有保护作用。
这些研究强调了假设膳食纤维的作用与SCFAs相同是误导性的。
但是以上数据表明饮食-微生物群轴对免疫细胞稳态和炎症性疾病具有深远影响。
除了影响各种炎症性疾病外,饮食和微生物群也被证明能够塑造对抗各种感染的免疫反应。尽管膳食纤维大多能够保护免受感染,但膳食脂肪和糖分却可能促成病原体发病过程。
正如前面所讨论的,膳食纤维通过维持肠道屏障完整性来保护免受肠道感染的影响,因为膳食纤维不足会促使以粘蛋白为食的微生物群破坏小鼠肠道的保护性黏液层。
丁酸对肠道病原体的多种抗菌机制
来源于纤维的丁酸盐有助于体外维持结肠上皮细胞的紧密连接完整性。丁酸也可以通过HDAC3抑制促进单核细胞向巨噬细胞的分化。因此,丁酸增强了小鼠巨噬细胞对一系列肠道病原体(包括沙门氏菌伤寒沙门氏菌和粘附侵袭性肠毒素产生大肠埃希菌)的抗菌活性,这与增强的抗菌肽产生和吞噬能力有关。丁酸还降低了上皮细胞的氧化程度,从而限制了沙门氏菌的需氧生长。
丙酸,另一种SCFA,可以通过破坏细胞内pH稳态直接抑制伤寒沙门氏菌的生长。最后,对口服感染的小鼠进行丁酸补充可以促进细菌清除,并防止这些病原体的全身传播。
微生物群对抗病毒免疫的重要性
微生物群在天然和适应性抗病毒免疫中也发挥着至关重要的作用。涉及微生物群消耗或改变的小鼠研究表明,微生物群对包括诺如病毒、黄病毒和流感病毒在内的病毒感染的保护性免疫反应至关重要。
已经证明微生物群对于最佳激活不同抗病毒机制是必不可少的,包括干扰素反应、CD4+和CD8+ T细胞反应以及抗体产生。虽然膳食纤维和SCFA通过增强效应细胞CD8+ T细胞功能在抗病毒免疫中发挥着关键作用,但饮食和微生物群来源的代谢产物在许多微生物群调节的抗病毒免疫机制中的作用仍需要进一步研究。
膳食纤维在蠕虫感染免疫中的保护作用
膳食纤维还通过其他代谢产物在小鼠中提供对蠕虫感染的保护性免疫。富含菊粉的高纤维饮食促进了细菌去共轭胆酸,提高了体内各种未共轭胆酸的浓度,包括胆酸。这些微生物群来源的胆酸增加了肺上皮细胞和肠间质基质细胞产生IL-33,导致ILC2s的激活。
当小鼠感染蠕虫寄生虫巴西圆线虫(Nippostrongylus brasiliensis),这种寄生虫会感染肺部,然后迁移到肠道,与对照组饮食喂养的小鼠相比,富含菊粉的饮食会增加肺部的杯状细胞和肠系膜淋巴结中的嗜酸性粒细胞。
这些由菊粉纤维诱导的2型免疫反应导致了肠道中蠕虫的加速排出,表明了膳食纤维在抵御寄生性蠕虫方面的益处。这些研究可能有助于增加全球对食物和补品的了解,特别是在那些细菌性肠道感染和蠕虫感染仍然地方性流行的地区。
肠道微生物群对传染性疾病疫苗效果的调节
肠道微生物群及其相关代谢产物在小鼠对传染性疾病疫苗的有效性中也发挥着重要作用。例如,小鼠巨噬细胞通过检测肠道微生物群菌株产生的鞭毛蛋白,促进巨噬细胞内固有产生浆细胞生长因子,直接促进浆细胞产生抗体。
此外,B淋巴细胞可以利用来源于膳食纤维衍生的SCFA产生的乙酰辅酶A作为细胞代谢的燃料,从而支持抗体的产生。
在人类中,许多研究将微生物群与对各种传染性疾病的疫苗反应联系起来。例如,已经证明抗生素介导的微生物群失调会损害那些预先抗体滴度较低的受试者对季节性流感的抗体反应,并且与抗生素治疗导致次生胆酸系统浓度降低有关。然而,各种饮食在微生物调节疫苗反应中的作用仍未得到充分探讨。
高脂饮食快速影响微生物群组成和免疫反应
正如前面讨论的那样,高脂饮食会增加小鼠肠道微生物群中Bacillota的数量,并以微生物群依赖的方式促进肠道通透性和炎症。尽管高脂饮食诱导的小鼠肥胖需要数月的膳食干预,但微生物群组成的转变和相关的免疫反应变化是迅速的,可以在几天内检测到。相关研究表明,进行为期两周的高脂饮食干预足以加重小鼠对病原细菌感染的情况。例如,口服李斯特菌单胞菌感染的小鼠,高脂饮食组的盲肠、肠系膜淋巴结和脾脏中细菌负荷增加,比饲喂常规饮食组高。
在人类中,饮食引起的微生物群变化也会在饮食发生重大改变后立即开始。一个典型的饮食变化例子是从以植物为基础的饮食转变为以动物为基础的饮食,这在社交活动期间的宴会中经常发生,比如参加宴会。这些宴会饮食通常富含脂肪和糖分,而纤维含量较低。
饮食改变对抗肿瘤免疫和癌症免疫疗法的影响
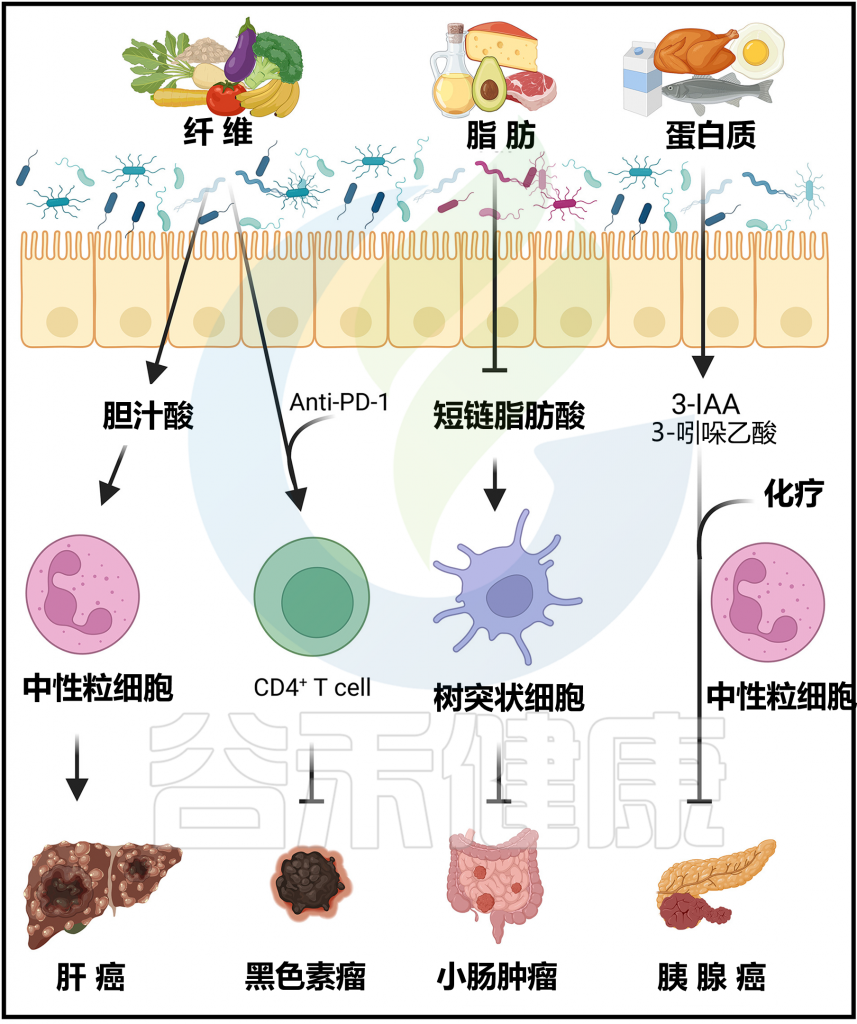
Arifuzzaman M et al., Immunity. 2024 57(1):14-27.
短期宴会饮食通过影响微生物群和Th17细胞抑制小鼠肠道免疫
一项研究使用了一种高脂肪、富含糖分(双糖和寡糖)、富含胆固醇、低纤维的饮食,因此模拟了“宴会饮食”。
研究发现,短暂接触这种宴会饮食会改变小鼠的微生物群组成,并抑制对细菌感染的黏膜免疫。在小鼠的回肠内容物中观察到了微生物群的快速和可逆性变化,宴会饮食3天后微生物群多样性减少,但在停止宴会饮食3天后迅速恢复到基线组成。
值得注意的是,这种为期3天的宴会饮食足以降低小肠Peyer氏板中Th17细胞的数量,降低回肠中Il17a、Il17f和Il22等3型细胞因 子的表达,这些细胞因子在维持肠道上皮屏障和抵御细菌病原体方面起着关键作用。
因此,这种饮食转变可能导致对沙门氏菌和李斯特菌感染的更高敏感性。与接受常规饮食小鼠回肠内容物的无菌小鼠相比,接受宴会饮食小鼠回肠内容物的无菌小鼠Il17a和Il17f的表达也减少,表明这种饮食介导的免疫抑制依赖于并可通过肠道微生物群传播。
高脂饮食(其中≥90%的热量来自脂肪)也会降低小鼠肠道中的Th17细胞,这与酮体介导的双歧杆菌耗竭有关。
值得注意的是,在不添加任何脂肪的低纤维、高糖饮食中,小鼠Th17细胞和细胞因子的减少情况也相似,这表明免疫表型的变化不取决于膳食脂肪,而是取决于饮食的能量密度和缺乏纤维。
宴会饮食降低SCFA,蔗糖促进Faecalibaculum rodentium 扩增,影响Th17细胞水平
宴会饮食会降低盲肠内容物中的乙酸和丁酸浓度,给予这两种短链脂肪酸(SCFA)的补充可以恢复Th17细胞数量并增强对沙门氏菌的保护。此外,另一项研究表明,向以普通饲料为基础的小鼠提供蔗糖饮水足以减少Th17细胞数量,这意味着小肠Th17细胞的减少也可能是由于高量的膳食糖引起的。
蔗糖会促使Faecalibaculum rodentium(该菌属于芽孢杆菌门下的Erysipelotrichaceae家族)的扩张。Faecalibaculum rodentium的扩增导致分段丝状细菌的替代,而后者已知能诱导和维持Th17细胞。
综合这些数据表明,虽然膳食纤维通过微生物群来源的短链脂肪酸和胆酸代谢产物对抗感染具有益处,但缺乏膳食纤维同时高量的脂肪和糖可能会削弱对各种肠道细菌病原体的肠道免疫力。
过去的十年里,许多临床前和临床研究报告指出,微生物群的组成在免疫系统对肿瘤的控制中起着重要作用,并可以促进对治疗的反应。
无菌小鼠或接受抗生素治疗的小鼠对化疗和免疫疗法表现出增强的抗药性。相比之下,口服具有益生菌Bacteroides fragilis有助于提高SPF小鼠对黑色素瘤的抗CTLA-4或抗PD-L1反应。
另外,缺乏膳食纤维的小鼠对黑色素瘤的抗PD1免疫检查点疗法没有反应,这与Ruminococcaceae的减少有关。这些小鼠中膳食纤维的抗肿瘤效果与CD4+T细胞增加有关。
在黑色素瘤和上皮癌患者中,对抗PD-1疗法的反应者和非反应者之间微生物组成存在显著差异。治疗反应与肿瘤中CD4+和CD8+T细胞的浸润增加有关,这与肠道微生物多样性高的几种菌,包括Akkermansia muciniphila、粪杆菌属(Faecalibacterium)、毛螺菌科(Lachnospiraceae) 等有关。这些菌谷禾专门科普过,详见:
肠道核心菌属——普拉梭菌(Faecalibacterium Prausnitzii),预防炎症的下一代益生菌
膳食纤维增强抗肿瘤效果,瘤胃球菌、粪杆菌属等与癌症免疫治疗反应有关
抗生素治疗可能降低上皮癌患者抗PD-1疗法的临床益处。黑色素瘤患者对免疫检查点抑制剂疗法的反应不佳与膳食纤维摄入不足(<20克/天)有关。
与无反应者相比,反应者的微生物群显示出瘤胃球菌科(Ruminococcaceae)和粪杆菌属(Faecalibacterium)的富集。值得注意的是,发挥抗肿瘤作用的有益微生物群是可传播的。
与无反应患者的粪便微生物群移植 (FMT) 相比,来自有反应患者的无菌或抗生素治疗小鼠,对抗 PD-1 和抗 PD-L1 治疗黑色素瘤和肉瘤的反应更好。
此外,来自应答患者的 FMT 可以促进免疫细胞(包括 CD8 + T 细胞)的数量和激活状态,并提高黑色素瘤患者抗 PD-1 治疗的临床获益。
这些发现表明,膳食纤维通过维持微生物群分类群(包括瘤胃球菌科和粪杆菌属)来促进癌症免疫治疗,从而改善治疗结果。然而,需要进一步的研究来确定微生物菌株和相关代谢物在这些疗法的有效性中的具体作用。
吲哚-3-乙酸增强胰腺癌化疗效果
微生物群来源的代谢产物已被证明可以调节多种癌症小鼠模型的临床结果。从膳食色氨酸的微生物代谢中产生的吲哚-3-乙酸可以以中性粒细胞依赖的方式增强小鼠对胰腺癌的化疗效果。从理论上讲,中性粒细胞来源的髓过氧化物酶氧化吲哚-3-乙酸,氧化产物可以阻止癌细胞的增殖。
除了上述关于饮食和微生物群在抗肿瘤疗法中的作用的研究外,还有几项研究强调了饮食和微生物群在肿瘤发生中的作用。
高脂饮食降低短链脂肪酸,促癌
高脂饮食会降低小鼠粪便中的短链脂肪酸浓度,并以微生物群依赖的方式促进易感基因小鼠肠道肿瘤的发展。通过丁酸的给药可以减轻高脂饮食介导的肿瘤进展,丁酸可以促进树突状细胞的招募。
菊粉纤维可能促癌
尽管膳食纤维通常被认为对抗肿瘤疗法有益,但特定类型的纤维可能会以依赖环境的方式发挥促肿瘤作用。例如,菊粉纤维通过改变与升高的胆酸代谢物和肝内中性粒细胞炎症相关的微生物群,促进小鼠肝细胞癌的发展。
综合这些研究表明,通过膳食调节微生物群来源的代谢产物影响肿瘤发生和治疗结果,这可以用于精准营养学以预防和治疗癌症。
肠道微生物群与免疫系统之间的相互作用形成了两者的组成和功能,从而在外周组织中维持稳态平衡。
关键是,饮食可以维持或扰乱这种平衡,导致有益或有害的影响。饮食可以调节微生物组成和菌群失调,取决于微生物群的状态和膳食暴露的类型。
挑战
剖析特定菌株与识别微生物来源代谢产物
虽然膳食纤维的抗炎作用以及膳食糖和脂肪的促炎后果已被充分确立,但我们对其他膳食成分如何影响免疫系统的了解仍然有限。此外,剖析调节这些过程的特定微生物菌株和代谢产物是具有挑战性的。基于代谢组学的最新进展已经允许在各种宿主组织部位检测和定量低丰度代谢产物。
最近可用的公共数据库和生物信息学工具有助于在质谱数据中识别微生物来源的代谢产物。此外,基于CRISPR的细菌遗传学正在使得难以培养或操作的微生物菌株的操纵成为可能。
新兴工具和技术
研究免疫介导性疾病中微生物群和代谢产物
通常,一个蛋白质的合成由一个基因介导,而一种代谢产物的合成涉及多个代谢酶(因此,多个基因),这增加了微生物群介导的宿主代谢产物生产的复杂性。据统计,在非靶向代谢组学分析中,只有不到2%的光谱被注释;即98%的光谱与现有数据库中的化合物不匹配。据推测,这些“暗物质”的相当一部分具有微生物起源。
额外的计算工具,如CSI:FingerID,将有助于通过质谱观察到的这些光谱的注释。
在微生物群的基因操纵中,可以确认微生物菌株及其代谢途径在微生物驱动的表型中的作用。然而,以往,由于许多非模式菌株的遗传可操作性存在限制,这种策略是难以实现的。
基于CRISPR-Cas9的技术的最新发展已经允许针对非模式微生物进行遗传研究。这些遗传工具还可以有助于因果关系或干预研究以及未来基于代谢产物的治疗。外部提供的代谢产物的剂量和数量可能无法准确模拟微生物来源的剂量和数量。因此,一种精确地探究微生物群衍生分子在其产生环境中的方法是通过删除负责基因,从而“切断”各种共生微生物来源的代谢产物的产生。这些额外的遗传和生物信息学工具将有助于推动机制研究,并确定特定微生物菌株和微生物来源的代谢产物在调节各种免疫途径中的不可替代作用。
潜力
微生物群与个性化治疗性饮食
我们目前对营养调节炎症的了解仅限于个别营养素或食物类别。饮食模式和摄食行为也可以影响肠道微生物群和人体健康。我们通过神经元和化学感受味觉受体感知饮食方式,可以影响与饮食相关疾病的病理生理学。
然而,对微生物群在这些过程中的作用的理解仍然不完整。通过个性化治疗性饮食和营养干预的精准营养的当前愿景需要更深入的机制理解饮食-微生物群相互作用和摄食行为,并将其与年龄、性别和疾病相关参数相结合。
对饮食-微生物群-代谢物三者之间关系的更好理解为在三个层面开发有针对性的治疗提供了潜力:
1)益生元,促进特定微生物群的饮食
2)益生菌,特定野生型或基因工程微生物群
3)后生元,特定微生物群衍生代谢产物或具有更好疗效的合成类似物。
结合我们对微生物代谢产物在基因、细胞、分子和化学生物学水平的了解,可以更好地理解它们在调节宿主炎症和免疫中的作用,并通过操纵饮食-微生物群轴促进健康。
主要参考文献:
Arifuzzaman M, Collins N, Guo CJ, Artis D. Nutritional regulation of microbiota-derived metabolites: Implications for immunity and inflammation. Immunity. 2024 Jan 9;57(1):14-27.
Akagbosu B, Tayyebi Z, Shibu G, et al. Novel antigen-presenting cell imparts Treg-dependent tolerance to gut microbiota[J]. Nature, 2022, 610(7933): 752-760.
Montrose D C, Nishiguchi R, Basu S, et al. Dietary fructose alters the composition, localization, and metabolism of gut microbiota in association with worsening colitis[J]. Cellular and molecular gastroenterology and hepatology, 2021, 11(2): 525-550.
Bisanz J E, Upadhyay V, Turnbaugh J A, et al. Meta-analysis reveals reproducible gut microbiome alterations in response to a high-fat diet[J]. Cell host & microbe, 2019, 26(2): 265-272. e4.
Alexander M, Turnbaugh P J. Deconstructing mechanisms of diet-microbiome-immune interactions[J]. Immunity, 2020, 53(2): 264-276.