-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com

谷禾健康
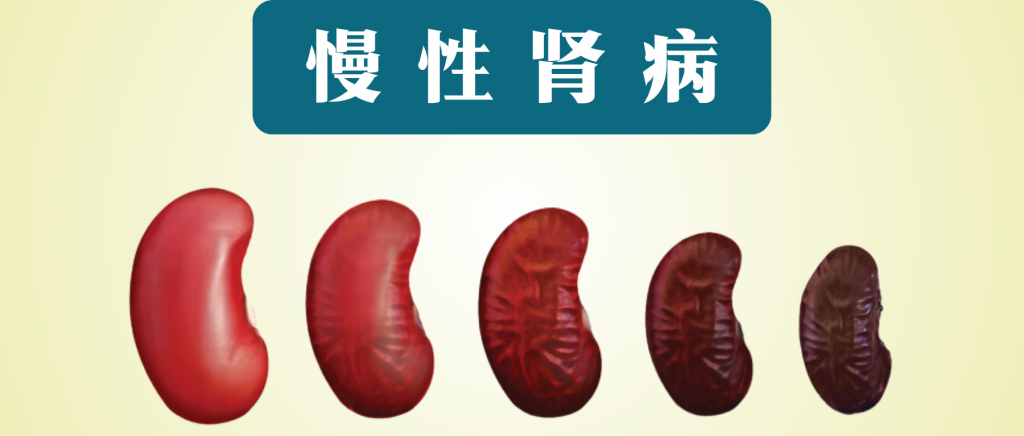
慢性肾病(CKD)被称为“隐形的杀手”,“无形的病”,因为该病在早期大多数人没有明显的症状,直到后期肾脏失去过滤血液中废物和多余液体能力时,已经可能导致肾功能衰竭,需要透析或肾移植来维持生命。
慢性肾病特征是肾脏结构异常或因肾脏损伤导致的肾功能逐渐下降,持续时间至少为 3 个月,并伴有相关的健康后果。全球慢性肾病患病率不断上升,影响全球 10% 以上的人口,全球有超过 8.436 亿人患有慢性肾病。
根据美国疾病控制与预防中心 (CDC) 的数据,美国约有 3700 万人(约占成年人的 15%)患慢性肾病。
慢性肾病的发生通常是一个非常缓慢的过程,最初症状很少。根据 CDC 的数据,90% 患有慢性肾病的成年人并不知道自己患有慢性肾病,而每 2 名肾功能极低且未接受透析治疗的人中,就有 1 名不知道自己患有慢性肾病。
慢性肾病的发生与高血压、糖尿病和肥胖等多种风险因素的持续暴露密切相关,导致肾脏排泄功能不可逆地逐渐衰退。尿毒症毒素在血液循环中的积累,对肾脏造成巨大损害,还会影响其他器官和组织,增加心力衰竭和死亡的风险。
遗憾的是,慢性肾病目前尚无法治愈,现有的治疗方法如生活方式的改变、药物治疗和透析只能缓解症状,延缓病情进展。肾移植虽然是终末期肾病患者的治疗选择,但受限于供体数量和漫长的等待期,其可及性有限。因此,迫切需要新的、有效的干预策略来改善慢性肾病患者的预后。
近年来,研究者们将目光投向了肠道微生物群。肠道菌群失调已被证实与慢性肾病的发生和进展密切相关。肠道微生物的多样性和平衡对维持宿主的代谢、免疫和炎症等功能至关重要。在慢性肾病患者中,肠道屏障功能受损,导致肠黏膜通透性增加,有害物质如内毒素和尿毒症毒素更容易进入血液循环,加重肾脏负担。
具体而言,慢性肾病患者的肠道菌群中有害菌如变形菌门和放线菌门比例增加,而有益菌如拟杆菌门和厚壁菌门减少。这种菌群失调导致短链脂肪酸等有益代谢物的产生减少,而有害代谢物如三甲胺和吲哚硫酸盐的产生增加。这些有害代谢物进入血液循环后,可诱发炎症和氧化应激,加速肾脏纤维化过程。
本文我们来了解一下慢性肾病的发生发展,症状,发病率,病因等,随着对肠-肾轴的深入了解,有助于我们制定优化的干预策略,改善慢性肾病患者的临床结局。
我们的肾脏主要功能是过滤血液中的多余水分和废物,产生尿液排出体外。为了保持身体正常运转,肾脏会平衡血液中循环的盐分和矿物质(如钙、磷、钠和钾)。肾脏还会分泌激素,帮助控制血压、制造红细胞并强健骨骼。
晚期慢性肾病可能导致液体、电解质和废物在体内积聚至危险水平。
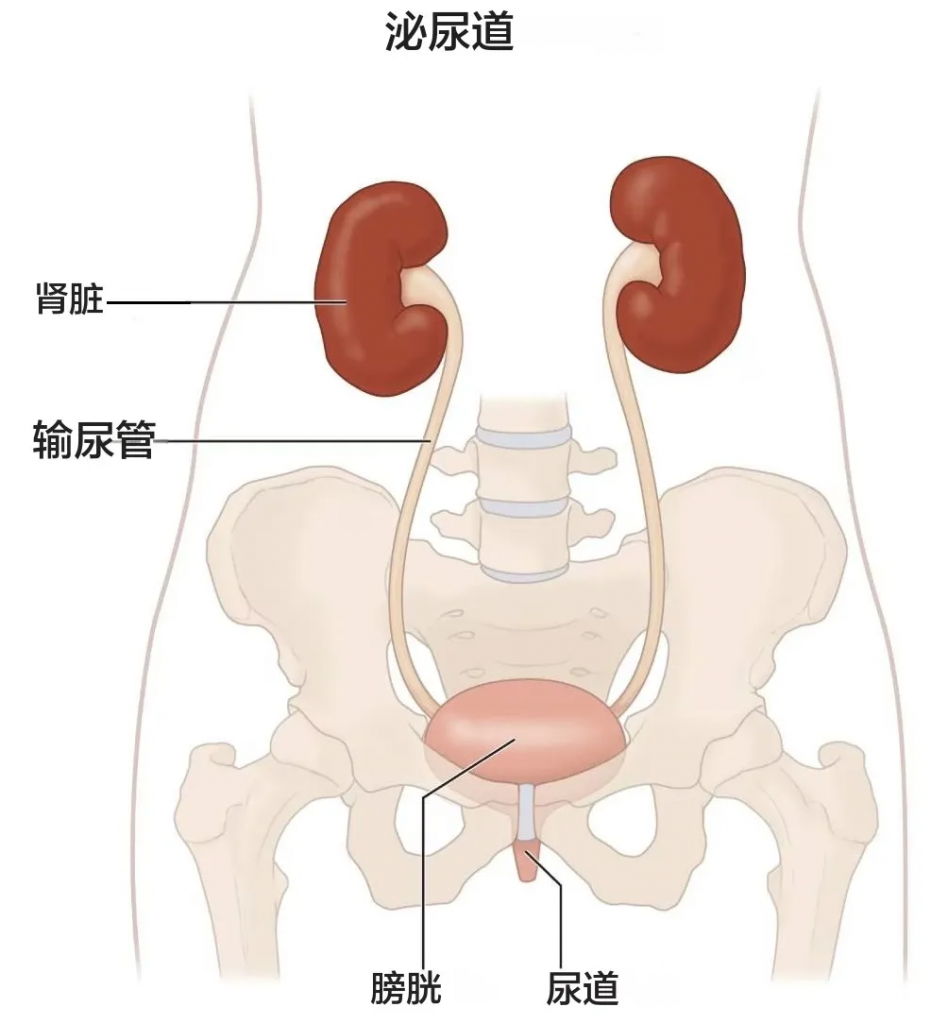
图源:NIDDK
慢性肾病的发展取决于个人的年龄、合并症、反复急性肾损伤、蛋白尿水平等。肾功能下降超过三个月称为慢性。
大多数患有慢性肾病的人会出现高滤过、肾肥大、小管间质纤维化、肾素-血管紧张素-醛固酮系统激活和内皮屏障破坏,导致肾小球滤过率和肾脏排泄效率降低。
具体如何定义慢性肾病?
根据“改善全球肾脏病预后”组织 (KDIGO) 的定义,慢性肾病目前定义为肾小球滤过率 (GFR) 降低,<60 mL/min/1.73 m 2(GFR 分类 G3a–G5),或以肾脏损害形式出现的其他肾脏结构或功能异常,对健康有影响,持续至少 3 个月。
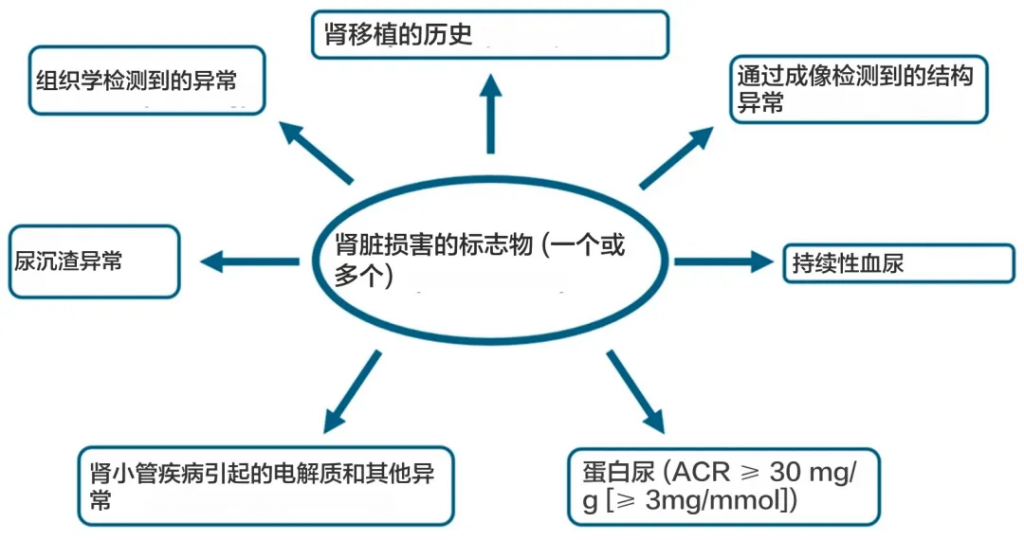
doi.org/10.3390/ijms251910429
慢性肾病的特点是病情进展缓慢,不可逆,发病相对隐匿。该病的显著特点是并发症风险增加,死亡主要与血管疾病有关。
◑ 根据肾功能分级分类
按照肾小球滤过率(GFR)进行分级,慢性肾病通常分为五个阶段,阶段越高,肾功能越差,对患者生活质量和预期寿命的影响越大:
1
GFR ≥ 90 mL/min
通常肾功能正常,可能存在其他肾脏病理改变。
2
GFR 60-89 mL/min
轻微肾功能减退,肾功能异常的早期迹象。
3
GFR 30-59 mL/min
中度肾功能减退,有可能出现明显的临床症状。
4
GFR 15-29 mL/min
重度肾功能减退,需进行透析或等待肾移植。
5
GFR < 15 mL/min
终末期肾病(ESRD),需进行透析或肾脏移植。
随着肾功能的降低,患者面临更高的并发症风险,包括心血管疾病、贫血和电解质紊乱等。
◑ 根据病因分类
慢性肾病还可以依据病因进行分类:
◑ 依据临床表现分类
根据临床症状和生化指标的不同,慢性肾病可以进一步分为:
维持肾脏健康的策略,尤其是在早期阶段,将是预防慢性肾病发展的关键因素。
根据统计,慢性肾病的全球流行率约为13%。
对于高危人群,如糖尿病患者,其慢性肾病的发病率可高达35%以上。
据欧洲肾脏健康联盟统计,慢性肾病的发病率在老年人群中较高:
其中大多数 (10.6%) 处于疾病晚期(3-5 期),0.1% 处于 5 期。当然这个百分比可能不准确,因为1-2 期慢性肾病的人群可能并不知道自己的病情,这可能导致上述数据被低估和扭曲。
5 期患者数量较少,是因为慢性肾病患者过早死亡的可能性比患肾衰竭的可能性高出五到十倍。
慢性肾病(CKD)是一种长期进行性肾脏疾病,随着病情的进展,患者可能会出现多种临床症状和体征。以下是慢性肾病的一些主要表现:
早期无症状阶段
慢性肾病的早期阶段,患者常常无明显症状,可能仅在常规体检时通过血液或尿液检查发现肾功能异常。因此定期监测高危人群(如糖尿病或高血压患者)是至关重要的。
水钠潴留
随着肾功能的逐渐下降,患者可能会出现水钠潴留,这可能导致:
尿液变化
代谢性酸中毒
慢性肾病患者由于肾脏排除酸的能力下降,会出现代谢性酸中毒,其典型症状包括:
疲劳与虚弱
随着肾功能下降,患者常常感到持续的疲乏和虚弱。部分患者可能出现贫血(通常与肾脏无法生成足够的红细胞生成素有关),导致:
肾性骨病
随着肾功能的下降,钙、磷代谢失衡可能会导致肾性骨病。相应的临床表现包括:
神经系统症状
心血管相关症状
皮肤和其他系统表现
任何人任何年龄都可能患上慢性肾病。但有些人的风险比其他人更高。最常见的风险因素是:
高血压和糖尿病:高血压和糖尿病是慢性肾病最常见的病因之一。这两种疾病通过引起肾脏血管的损伤,导致肾小球硬化和肾功能下降。
脱水:脱水,尤其是与高温相关的反复脱水,可能导致永久性的肾脏损伤。这可能通过激活血管加压素、醛固酮-果糖激酶途径和慢性高尿酸血症等机制实现。
年龄:随着年龄的增长,肾脏的质量和功能会逐渐下降,这是慢性肾病的一个重要风险因素。衰老过程中细胞衰老,特别是肾小管上皮细胞的衰老,会导致慢性炎症,进而推动慢性肾病的进展。
遗传因素:某些单基因疾病也是成人慢性肾病的原因之一。
肾小球疾病和肾小管疾病:肾小球疾病(如糖尿病肾病和肾淀粉样变性)和肾小管疾病(如急性肾衰竭后发展为慢性状态)是导致慢性肾病的重要原因。
缺氧:肾脏组织的缺氧是推动慢性肾病进展的一个重要因素。缺氧条件下,肾脏组织的持续炎症攻击是通过诱导白细胞获得粘附表型来实现的。
氧化应激和免疫系统的作用:氧化应激、免疫系统的异常活动、中性粒细胞弹性蛋白酶相关脂ocalin和基质金属蛋白酶的活动在慢性肾病的发展和进展中起着重要作用。
肠道菌群失调:这也在正常稳态的维持和慢性肾病中的失调中起着关键作用。这在接下来的章节我们会详细阐述。
共病条件:除了高血压和糖尿病外,其他共病条件,如肥胖、吸烟和性别(在男性中更为显著),也与慢性肾病的发展有关。
环境毒素和农药暴露:在低收入和中等收入国家或地区,环境毒素(如重金属暴露、农药使用、真菌毒素、水污染和蛇咬)被认为是慢性肾病未知病因的潜在原因。
其他因素:包括但不限于心血管疾病、HIV感染、代谢综合征、药物引起的肾病(如非甾体抗炎药引起的肾病)等也是慢性肾病的潜在病因。
这种进行性的疾病不仅影响患者的肾功能,而且与多种并发症有关,包括心血管疾病、贫血、骨代谢紊乱等。随着病情的发展,慢性肾病患者的症状可能包括尿量改变、水肿、疲劳、恶心和认知功能下降等。
随着对慢性肾病的理解不断深入,研究人员开始关注肠道微生物群在慢性肾病进展中的作用。肠道微生物群的组成和功能在慢性肾病患者中可能会发生显著变化,这些变化可能会通过多种机制影响慢性肾病的进展,包括影响宿主的免疫系统、代谢途径和炎症反应等。接下来我们具体来了解这其中的机制,这对于开发新的治疗策略和管理慢性肾病患者的病情具有重要意义。
近年来,随着医学研究的深入,人们逐渐认识到肠道菌群与慢性肾病之间存在着密切的联系。
一方面,慢性肾病患者的肾功能下降导致体内毒素积累,这些毒素可通过血液循环影响肠道环境,进而破坏肠道菌群的平衡;另一方面,肠道菌群失调会产生更多的有害代谢物,尿毒症毒素如吲哚硫酸盐和对甲苯磺酸盐,这些物质通过肠-肾轴加重肾脏的损伤。此外,肠道菌群失调还可能导致肠道屏障功能下降,使得细菌和内毒素更易进入血液,引发全身性炎症反应,进一步加剧慢性肾病的进展。
下面我们来详细了解一下慢性肾病患者的具体肠道菌群变化特征:
慢性肾病患者的肠道菌群组成有何特点?与健康人群相比有何不同?
慢性肾病肠道菌群基本特征
慢性肾病患者肠道菌群失调,主要表现为:
有害菌增多,有益菌减少。
有害菌增多:
有益菌减少:
肠道菌群失调如何影响慢性肾病进展?
这种菌群失调会导致:
因此,调节肠道菌群、增加有益菌、减少有害菌是改善慢性肾病患者预后的一个重要策略。
肠道菌群生物标志物
肠道菌群有潜力成为慢性肾病早期诊断和预后监测的生物标志物。
早期诊断标志物:
这些细菌属可以较准确地区分慢性肾病患者和健康对照。
疾病进展标志物:
Escherichia-Shigella和Prevotella9(AUC = 0.86)可以准确区分糖尿病肾病患者和年龄/性别匹配的糖尿病患者。
随着慢性肾病的进展,一些特定菌种的变化:
增加的菌种:
减少的菌种:
特定慢性肾病阶段的标志菌:
编辑
肾移植患者的特征菌群:
与健康对照相比,肾移植患者的肠道菌群特征类似于慢性肾病3-4期患者,表现为:
这些菌群变化与慢性肾病进展相关,可能通过以下机制影响疾病:
首先,失调的肠道菌群导致肠道屏障功能受损,使得内源性和外源性毒素(如脂多糖,LPS)进入血液。这些毒素通过激活全身性炎症反应,增强肾脏的负担,进而导致肾功能损害。脂多糖可以与Toll样受体4(TLR4)结合,诱导炎症介质的释放,如肿瘤坏死因子α(TNF-α)和白细胞介素-6(IL-6),这些介质加重肾脏的炎症反应。
其次,肠道微生物产生的代谢物,尤其是短链脂肪酸,在维持肾脏健康中发挥着关键作用。短链脂肪酸生成减少与肠道菌群失调相关,导致的肠道屏障功能进一步减弱,使肾脏暴露于更高的毒素水平和炎症状态。
慢性肾病与肠道菌群失调之间的恶性循环
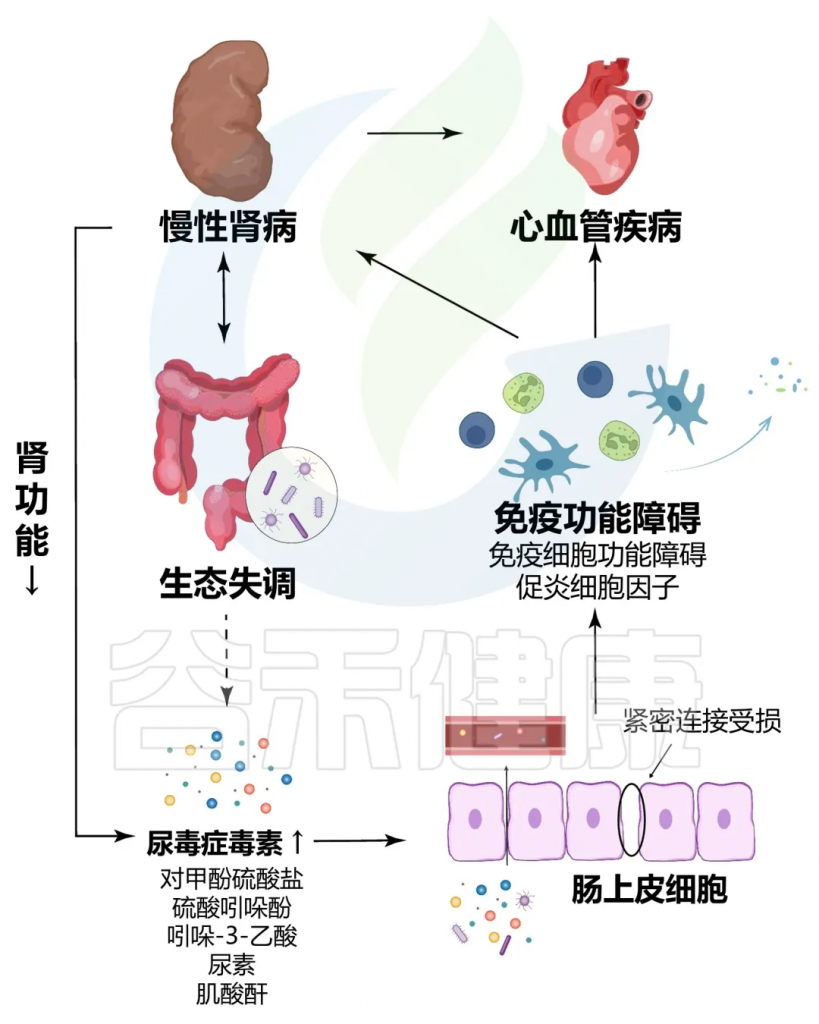
doi.org/10.1186/s12967-023-04455-2
菌群代谢物
短链脂肪酸
SCFAs(短链脂肪酸)主要通过以下几个方面影响慢性肾病:
• 通过抑制NF-κB活性和MAPK信号通路来减少促炎因子的产生
• 激活Nrf2通路,增强抗氧化防御能力。
• 通过AMPK/mTOR信号通路调节自噬,延缓CKD进展
• 改善CKD患者胰岛素敏感性和葡萄糖稳态。
• 调节T细胞和B细胞分化,参与免疫调节。
吲哚硫酸盐(IS)
•IS是一种强效的尿毒症毒素,对肾脏和血管系统有负面影响。
•IS可以促进内皮功能障碍和炎症。
•它增加氧化应激,上调转录因子NF-κB的表达(与炎症有关),并下调转录因子Nrf2(与抗氧化防御有关)。
•IS可以通过影响调节骨化血管平滑肌细胞(VSMCs)转分化的microRNAs来促进血管钙化。
•它可以下调miR-29b,这是一种血管钙化的抑制因子。
•IS可以激活肾素-血管紧张素-醛固酮系统,上调血管紧张素II 1型(AT1)受体,下调2型(AT2)受体。
•在慢性肾病(CKD)患者中观察到的浓度下,IS可以增强血管紧张素II对VSMCs的有害作用。
对甲酚硫酸盐(PCS)
• PCS与心血管损伤有关,随着肾小球滤过率(GFR)下降而在血清中累积。
•它可以促进VSMCs的迁移和增殖,这是血管钙化发展的关键细胞事件。
•PCS可以触发内皮细胞和VSMCs中氧化应激。
•它可以诱导主动脉壁平滑肌收缩,导致主动脉壁向内的共性重塑。
•PCS与动脉僵硬度、血管钙化和颈-股脉搏波速度有关。
•它可以促进主动脉炎症和钙化,通过急性期反应和凝血信号通路。
•PCS与内皮功能障碍、动脉僵硬度、血管钙化、心血管事件和全因死亡率有关。
三甲胺N-氧化物(TMAO)
•TMAO可以剂量依赖性地增加VSMCs中的钙含量,促进血管钙化。
•它刺激与VSMCs骨化分化相关的基因(如Runx2和BMP2)的表达。
•TMAO可以增加矿物质含量,上调负责VSMCs向骨样细胞转分化的基因。
•它可以激活NLRP3炎症小体和上调NF-κB,这些都与IL-1β的转录有关。
•TMAO与主要不良心血管事件的发生有关。
•它可以加速肾功能障碍的进展,影响肾小管间质纤维化和胶原沉积的发展。
•TMAO与高血压风险增加、不良心血管事件和全因死亡率有关。
铁死亡
铁死亡是一种新型的铁依赖性、脂质过氧化驱动的细胞死亡形式。
肠道菌群与多种器官、组织和疾病中的铁死亡有关
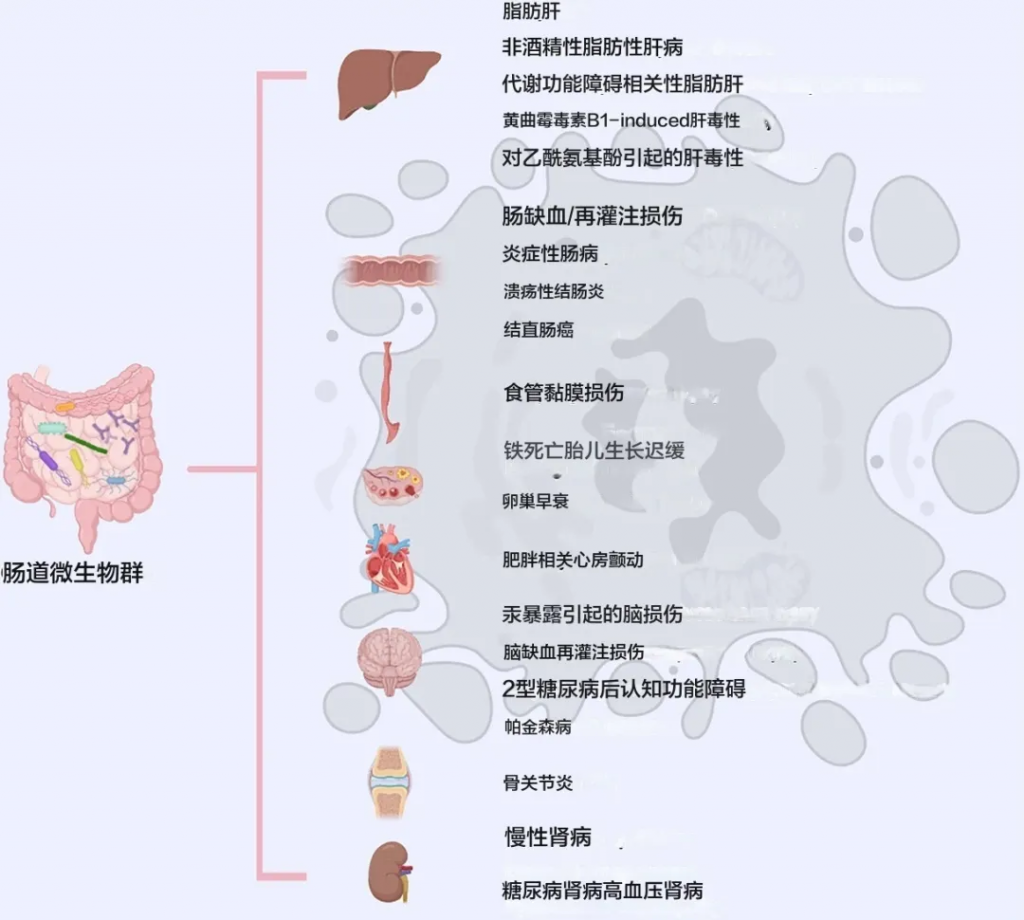
doi.org/10.1038/s41420-024-02000-8
铁死亡影响慢性肾病的方式主要如下:
○ 氧化应激和炎症反应:
铁死亡导致活性氧(ROS)积累,这会加剧氧化应激,进而引发炎症反应,对肾脏细胞造成损伤。
注:谷氨酰胺和支链氨基酸的代谢与铁死亡密切相关,它们可以通过不同机制影响谷胱甘肽合成、ROS生成和铁死亡过程。
○ 脂质代谢紊乱和脂质积聚:
铁死亡涉及多不饱和脂肪酸(PUFAs)的过氧化,这些物质在脂质代谢中起着重要作用。慢性肾病与脂质代谢紊乱和脂质积聚有关。脂质的积聚可激活先天免疫系统,促进炎症纤维化,引发线粒体和肾细胞损伤,并驱动慢性肾病进展。
○ 肾脏细胞损伤:
铁死亡导致的细胞死亡,如果发生在肾脏,将直接导致肾脏细胞的丧失,影响肾脏功能。
肠道菌群与铁死亡的关系主要表现在:
○ 代谢物的影响:
肠道菌群通过其代谢产物,如短链脂肪酸、胆汁酸、色氨酸代谢物等,影响宿主的代谢平衡和免疫状态,进而可能影响铁死亡的过程。
肠道菌群代谢物,如丁酸盐通过Nrf2/GPX4信号通路改善溃疡性结肠炎中的铁死亡,保护肠道粘膜屏障的完整性。
○ 免疫调节:
肠道菌群在维持宿主免疫平衡中起着关键作用。肠道菌群失衡可能导致系统性炎症,影响铁死亡的调节。
○ 铁代谢调节:
肠道菌群参与宿主肠道中铁的吸收和储存,影响铁代谢,进而可能影响铁死亡。
与铁死亡相关的肠道菌群有:
通过球形红杆菌(Rhodobacter sphaeroides)发酵获得的富含辅酶Q10的南瓜汁不仅具有抗氧化能力,尤其是铁离子还原抗氧化能力,而且还能调节哺乳动物的肠道菌群,保护肠道屏障。
总的来说,铁死亡在慢性肾病中的作用和肠道菌群的联系是一个复杂的过程,涉及多种代谢途径和细胞信号传导机制。慢性肾病患者应多食用富含膳食纤维的食物,避免食用高胆碱食物,如 L-肉碱和磷脂酰胆碱,因为肠道菌群代谢胆碱产生的三甲胺-N-氧化物会促进慢性肾病进展和死亡风险。
流行病学研究表明,慢性肾病患者很容易患上多种口腔疾病。
肾功能障碍会导致血清和唾液中尿素浓度升高,导致患者(尤其是晚期慢性肾病患者)因尿毒症而反复出现口臭。在口腔中,过量的尿素会被尿素酶阳性的口腔微生物群转化为氨,从而减少唾液流量并导致口干,这通常在终末期肾衰竭患者中常见。
慢性肾病患者在摄入食物后常常会感觉到不舒服的金属味道,这会导致食欲下降、营养摄入不良和蛋白质能量消耗综合征。
除了这些机制之外,其他因素,包括唾液 pH 值改变、口腔卫生不良、菌群失调、使用多种药物以及免疫反应改变,都可能大大增加患牙周病的风险。
某些因素同时增加了慢性肾病和牙周疾病的风险,如糖尿病、高血压、吸烟等。这些共同的风险因素进一步强化了两种疾病之间的联系。
两者之间也存在很大关联,慢性肾病患者的全身状况可能会加剧牙周炎症,而牙周炎症通过促进全身性炎症反应,又可能进一步损害肾脏健康。
慢性肾病对牙周疾病的影响
慢性肾病的营养不良状况、代谢性酸中毒、氧化应激、低度炎症会对口腔健康和牙周产生影响。
a) 免疫功能下降:
慢性肾病患者的免疫系统通常受到抑制,这使得他们更容易受到口腔感染和牙周疾病的影响。
b) 尿素浓度升高:
慢性肾病晚期患者体内尿素浓度升高,导致唾液中尿素浓度也随之升高。口腔中的细菌将尿素转化为氨,这可能改变口腔pH值,影响口腔微生态平衡。
c) 矿物质代谢紊乱:
慢性肾病患者常见钙磷代谢紊乱,这可能影响牙齿和牙槽骨的健康,增加牙周疾病的风险。
d) 药物副作用:
一些用于治疗慢性肾病的药物可能有口腔副作用,如口干,增加了口腔感染的风险。
e) 营养不良:
慢性肾病患者常见的营养不良状态可能影响口腔组织的修复能力,加重牙周疾病。
慢性肾病与牙周炎的直接关联机制
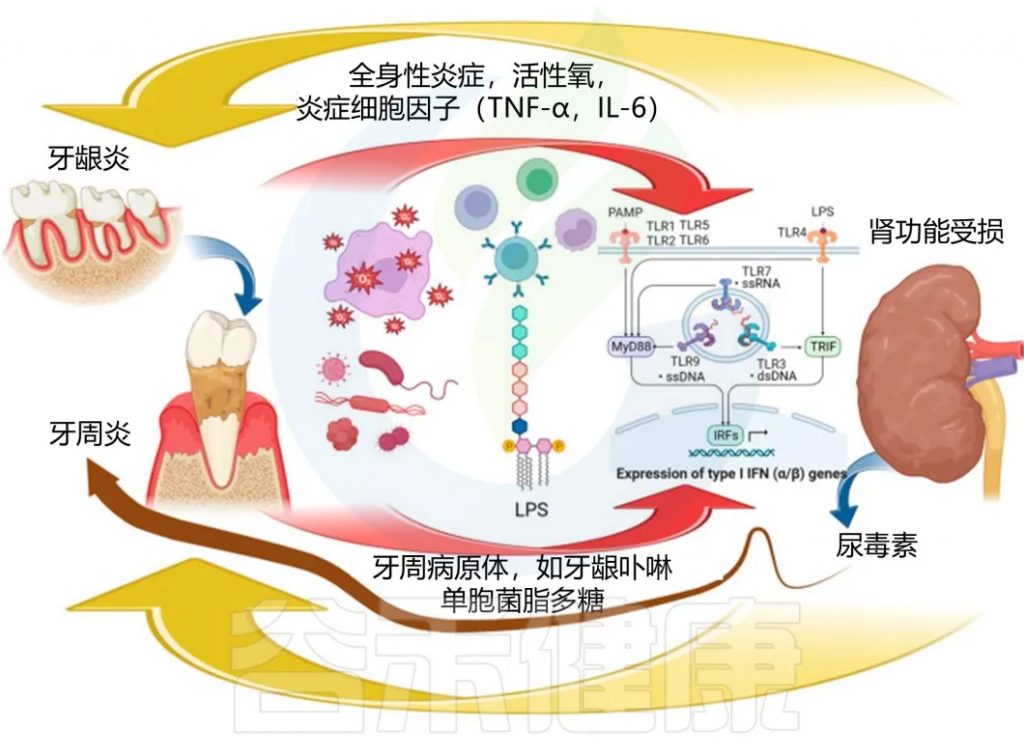
doi:10.3390/biomedicines11113033
牙周疾病对慢性肾病的影响
a) 系统性炎症:
牙周疾病是一种慢性炎症性疾病,可导致口腔内细菌和炎症因子进入血液循环。这些炎症因子(如IL-6、TNF-α、CRP、IL-8、IL-1β)可以引起全身性的低度炎症反应,进而影响肾脏功能。
b) 内皮功能障碍:
牙周病原体可以附着并侵入冠状动脉内皮细胞,导致动脉粥样硬化和血管功能障碍。这种机制同样可能影响肾脏血管,导致肾功能下降。
c) 氧化应激:
牙周疾病会增加体内的氧化应激水平,这可能导致肾脏组织的损伤和纤维化。
d)基质金属蛋白酶
基质金属蛋白酶(MMP)是一组参与组织修复和细胞凋亡的酶,它们在牙周炎症期间上调,并在肾脏中参与调节炎症反应和慢性纤维化,牙周病诱导的全身性MMP过度表达可能导致肾脏损害。
e) 微生物群相关:
菌群失调:如牙龈卟啉单胞菌、T. denticola, S. noxia, A.actinomycetemcomitans, V. parvula,导致IgG水平升高,这与肾功能受损有关。
菌群易位:口腔中的致病菌可能通过血液循环到达肾脏,直接或间接地影响肾脏功能。
口腔-肠道-肾脏轴的概念为我们提供了一个全新的视角,来理解慢性肾病与牙周病之间的联系。口腔中的微生物可以通过血液循环到达肠道,影响肠道微生物群的平衡,进而通过肠道-肾脏轴影响肾脏健康。
口腔-肠道-肾脏轴是一个复杂的动态系统,在慢性肾脏病中发挥着重要作用。这个系统的各个组成部分之间存在着密切的相互作用,形成了一个复杂的网络。以下是这个系统如何动态互作的详细解释:
牙周病与慢性肾病之间的间接关联机制
口腔-肠-肾轴
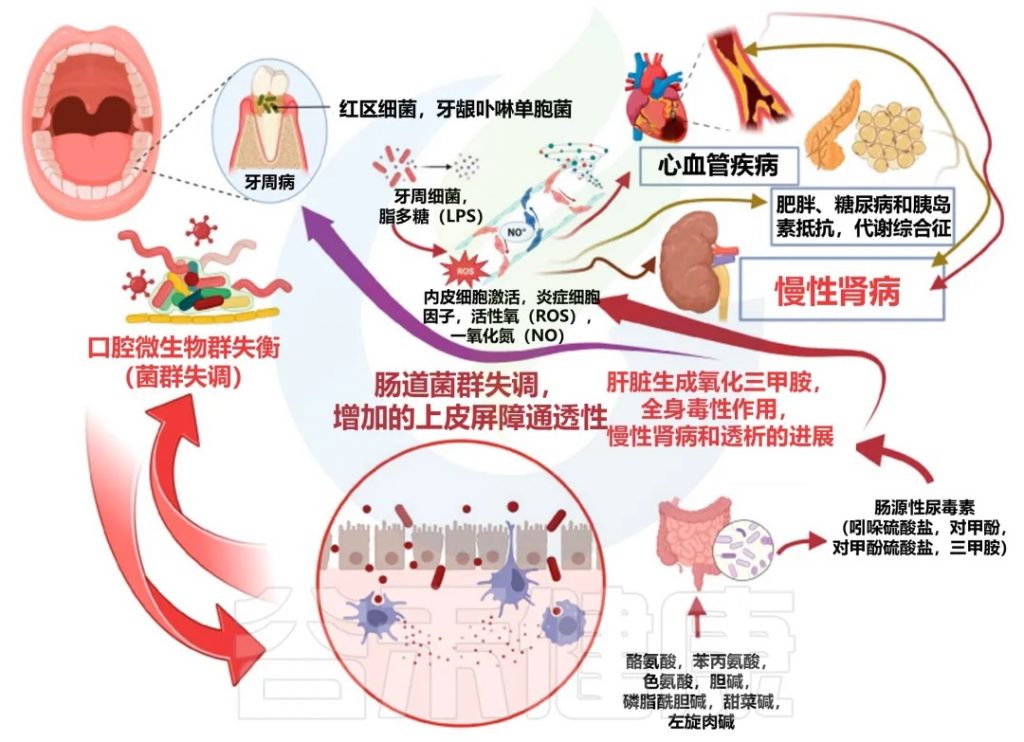
doi:10.3390/biomedicines11113033
口腔 ⇋ 肠道
● 口腔微生物群落影响肠道微生物组成
口腔中的细菌可以随唾液进入消化道,影响肠道微生物的组成。特别是在牙周病患者中,口腔病原体可能会定植在肠道中。
● 共同的炎症通路
口腔和肠道炎症可能共享一些共同的炎症通路,如NF-κB和NLRP3炎症小体的激活。
● 细菌转位
口腔病原体可能通过肠道进入血液循环,影响全身健康。
肠道 ⇋ 肾脏
● 肠道微生物代谢物影响肾功能
肠道微生物产生的代谢物,如短链脂肪酸、三甲胺N-氧化物(TMAO)等,可直接影响肾功能。
● 尿毒症毒素的产生和吸收
肠道微生物参与尿毒症毒素的产生,而这些毒素会进一步损害肾功能。
● 肠道通透性增加
慢性肾病可导致肠道屏障功能受损,增加细菌和内毒素的转位,加重全身炎症。
肾脏 ⇋ 口腔
● 尿毒症对口腔健康的影响
慢性肾病患者体内尿素浓度升高,可导致口腔pH值改变,影响口腔微生物环境。
● 免疫功能改变
慢性肾病导致的免疫功能障碍可能增加口腔感染的风险。
● 矿物质代谢紊乱
慢性肾病患者常见的钙磷代谢紊乱可能影响牙齿和骨骼健康。
牙周治疗
牙周治疗通过改善 eGFR 和肌酐水平,并降低炎症标志物(如 IL-6、CRP、ROS)对终末期肾病患者的肾功能产生积极影响。
强化牙周治疗还与接受腹膜治疗和血液透析患者的营养参数和铁利用率改善有关。3 个月牙周治疗显著降低了慢性肾病患者的全身 TNF-α 水平和其他炎症参数(IL-6、hs-CRP 和正五聚蛋白-3)。
牙周治疗可改善 ESRD 腹膜透析患者的全身炎症、营养状况和促红细胞生成素反应性。
一项为期 6 个月的随机对照临床试验旨在评估非手术牙周治疗对ESRD患者临床反应和全身状态的影响,结果表明,牙周临床参数以及 IL-6、铁蛋白、白蛋白、肌酐、血尿素氮和转铁蛋白水平均有显著改善。
一项全国性队列研究报告称,非手术性牙周治疗(尤其洁牙)效果与慢性肾病患者进展至ESRD、重大不良心血管事件、感染和全因死亡风险降低显著相关。
口腔预防措施
预防措施中,改善口腔卫生与慢性肾病发病率下降相关。
一项回顾性纵向研究报告称,刷牙频率对eGFR下降或透析需求有积极影响。
一项初步研究作者指出,强化牙科预防可能是减少全身炎症并随后降低慢性肾病儿科患者过早发生心血管疾病的一种有前途的方法。
多项研究的结果,提醒临床医生和患者注意口腔健康在控制肾功能方面的关键作用。
糖尿病肾病 (DKD) 是 1 型和 2 型糖尿病的严重并发症,是终末期肾病的主要原因。
糖尿病肾病的患病率和发病率逐年增加,大约30%~40%糖尿病患者会患上糖尿病肾病。
这种慢性肾病的标志是:
除了传统代谢因素,即高血糖和高血压外,肠道菌群的变化被认为是新型的重要影响因素之一。
肾功能下降导致尿素、尿酸等代谢废物在血液中积聚。这些代谢废物通过肠道分泌入肠腔,改变肠道环境。肠道环境改变引起肠道菌群失调。
糖尿病肾病患者的肠道菌群与健康人有明显差异,双歧杆菌、乳酸杆菌等有益菌减少,肠杆菌等致病菌增加。
关于糖尿病肾病肠道菌群变化的研究

doi.org/10.3389/fcimb.2024.1359432
肠道菌群:辅助判别的生物标志物
糖尿病肾病患者肠道菌群组成发生显著变化,可作为临床鉴别诊断或活检确诊糖尿病肾病的生物标志物。对于有肾活检禁忌症的患者,肠道菌群检测可能是一个重要的替代方案。
在四川省经活检确诊的14例糖尿病肾病患者中,Prevotella_9属可准确区分糖尿病患者与健康对照,受试者AUC为 0.900。
大肠杆菌-志贺氏菌和Prevotella_9也可准确区分经活检确诊的糖尿病肾病患者与糖尿病患者,AUC为0.860,有助于诊断糖尿病肾病。
山西地区 35 例经穿刺活检确诊的糖尿病肾病患者研究发现结果存在差异,其中Flavonifractor(AUC=0.909)或Eisenbergiella(AUC=0.886)可准确鉴别糖尿病肾病与糖尿病患者,可能与南北地区及饮食习惯差异有关。
下列可有效区分糖尿病肾病患者与健康对照组:
• Colatridium sp. CAG_768 (AUC=0.941)
• Bacteroides propionicifaciens (AUC= 0.905)
• Colatridium sp. CAG_715(AUC=0.908)
多元线性回归分析显示,Fusobacterium varium、Pseudomonadales、Prevotella sp. 3 联合检测对 糖尿病肾病患者具有较高的鉴别价值。
这些结果提示,肠道菌群可能是诊断糖尿病肾病的有效方式。但目前研究表明,用于诊断糖尿病肾病的肠道菌群生物标志物在不同地区和种族之间存在差异。因此,还需要更多临床研究来探讨其应用价值。
氨基酸代谢:
N-乙酰天门冬氨酸、L-缬氨酸、甜菜碱、异亮氨酸、天门冬酰胺和L-蛋氨酸水平升高
在糖尿病肾病中,肾脏对氨基酸的重吸收和代谢能力下降,导致这些物质在血液中积累。
L-亮氨酸和异亮氨酸水平与肾小球滤过率快速下降显著相关
这两种分支链氨基酸的水平升高可能是肾功能下降的早期标志。它们可能参与胰岛素抵抗和炎症过程,加速肾功能恶化。
谷氨酰胺水平升高
谷氨酰胺是一种重要的氨基酸,参与多种代谢过程。其水平升高可能反映了氮代谢的紊乱和肾脏对氨的处理能力下降。
脂肪酸代谢
硬脂酸水平升高
硬脂酸是一种饱和脂肪酸,其水平升高可能与脂质代谢紊乱和胰岛素抵抗有关。
亚油酸水平降低
亚油酸是一种必需脂肪酸,具有抗炎作用。其水平降低可能加剧糖尿病肾病相关的炎症反应。
其他代谢物:
短链脂肪酸(SCFAs):
尿毒症毒素:
苯硫酸盐可以直接损害肾脏,增加氧化应激,促进肾脏纤维化,从而加速糖尿病肾病的进展。
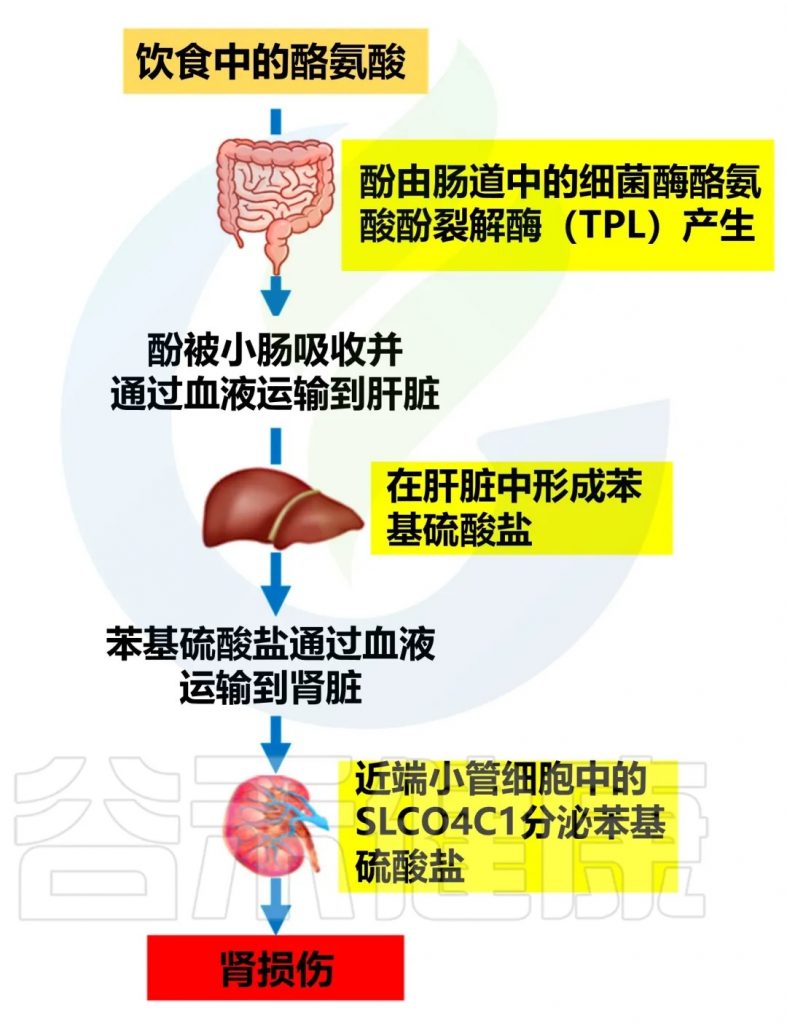
doi.org/10.3390/biom14091153
减轻苯硫酸盐对肾脏有害影响的策略:
慢性肾病相关认知障碍和抑郁风险
慢性肾病患者中16-38%存在认知障碍,肾功能与认知障碍和痴呆的发展相关。
肠道微生物失调和尿毒症毒素积累确实会影响血脑屏障(BBB)完整性,可能导致认知功能障碍。同时,慢性肾病患者更容易出现抑郁和认知障碍,这与肠道微生物改变和炎症有关。
肠道微生物失调和尿毒症毒素对血脑屏障的影响
认知功能障碍与肠道微生物和尿毒症毒素的关系
慢性肾病患者抑郁和认知障碍与肠道微生物和炎症的关系
总之,肠道微生物失调和尿毒症毒素积累通过影响血脑屏障完整性、改变神经递质和神经营养因子水平、促进炎症和氧化应激等多种机制,增加了慢性肾病患者出现认知功能障碍和抑郁的风险。这强调了维持健康肠道菌群和控制尿毒症毒素水平,对慢性肾病患者神经健康的重要性。
慢性肾脏病患者中肌肉减少症的发病机制是多方面的。
慢性炎症
首先,慢性炎症状态是导致肌肉减少症的一个重要因素。在慢性肾病患者中,系统性炎症反应指数(SIRI)与疾病的发生呈正相关,炎症因子如TNF-α、IL-6、IL-8等水平升高,这些炎症因子可以促进肌肉蛋白的降解并抑制肌肉生长。
炎症介质参与了导致肌肉减少症发生的多种机制
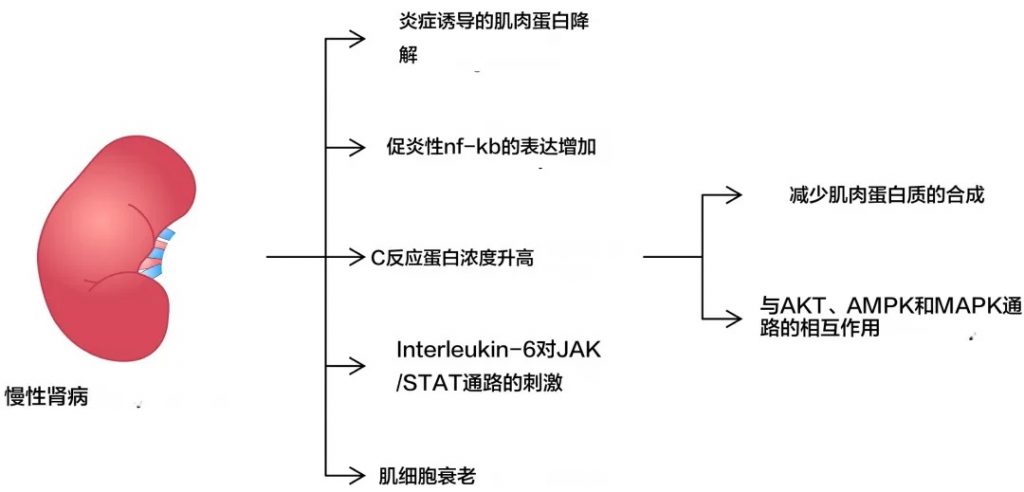
doi.org/10.3390/ijms25158474
代谢毒素积累
其次,代谢和激素调节障碍也与肌肉减少症的发展有关。慢性肾病患者常伴有代谢性酸中毒和尿毒症毒素的积累,这些因素可以导致胰岛素抵抗、线粒体功能下降,进而影响肌肉功能和肌肉质量的维持。
肠道菌群失调
慢性肾病患者的肠道菌群失调也是一个不可忽视的因素。研究发现,慢性肾病患者的肠道菌群组成发生了显著变化,如拟杆菌门和变形菌门的增加,厚壁菌门的减少。
肠道失调与肌少症之间潜在联系
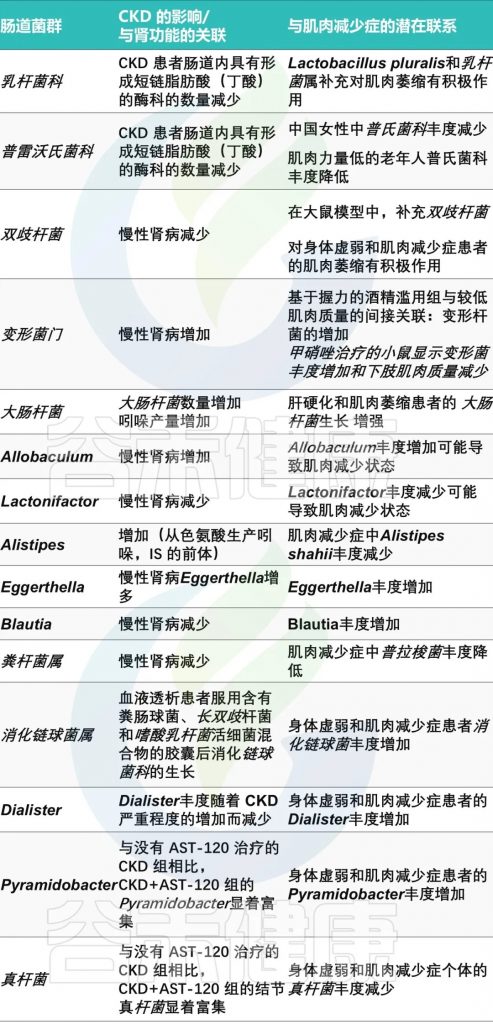
doi.org/10.3390/ijms25158474
慢性肾病状态减少了乳酸杆菌的存在,这与抑制其与肌肉健康相关的有益作用有关:
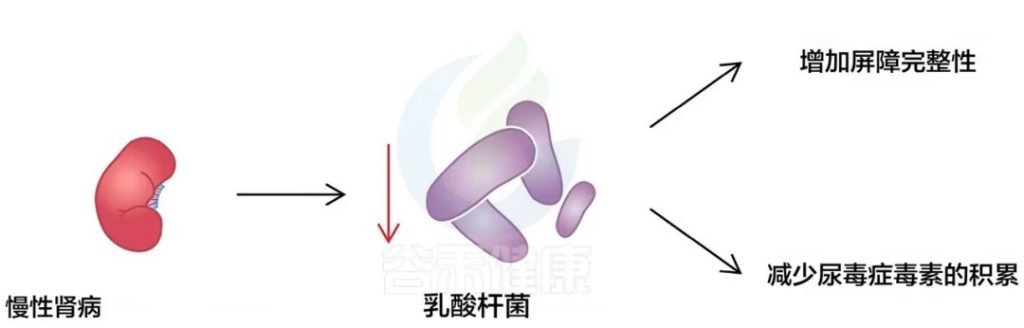
doi.org/10.3390/ijms25158474
代谢产物:硫酸吲哚酚和色氨酸
肠道菌群代谢产物硫酸吲哚酚(IS)在慢性肾病和肌肉减少症中起重要作用。
IS通过以下机制影响健康:
IS抑制肠上皮细胞的线粒体自噬,损害肠道屏障,可能通过IRF1-DRP1轴影响线粒体功能。
IS作为AhR的激动剂,激活AhR/NF-κB通路,促进炎症和纤维化,这与慢性肾病和肌肉减少症的发展有关。
IS在肌肉中激活NRF2,过度激活抗氧化反应,导致TCA循环减缓和ATP产生不足,进而引起肌肉无力和萎缩。
肠道微生物群产生的另一种代谢物是色氨酸,一种具有吲哚结构的氨基酸,色氨酸可以作为 AhR 的配体,AhR激活增加会导致线粒体损伤,从而导致肌肉损伤和萎缩。
miRNA表达异常
微小RNA(miRNA)的异常表达也参与了慢性肾病相关肌肉减少症的发病机制。例如,miR-29a和miR-29b的表达降低与肌肉减少症有关,它们通过影响YY1蛋白的表达来调节肌肉细胞的分化和凋亡。
总的来说,慢性肾脏病相关肌肉减少症的发病机制涉及炎症、代谢紊乱、肠道菌群失调和miRNA表达异常等多个方面。针对这些机制的治疗策略,如抗炎治疗、调节代谢、改善肠道菌群和miRNA治疗等,可能是未来治疗慢性肾病相关肌肉减少症的潜在方法。
泌尿系统结石是全球主要的健康问题,全球约 10-15% 的人一生中至少会经历一次。
泌尿系统结石的起因复杂且多方面,涉及遗传倾向、饮食习惯、液体摄入以及肥胖、糖尿病和高血压等潜在健康状况。结石的形成主要是由于尿液中含有钙、草酸盐、磷酸盐、尿酸盐、胱氨酸等矿物质过饱和,这个过程受尿液 pH 值以及结晶抑制剂和促进剂之间的平衡影响。
肠源性高草酸尿症
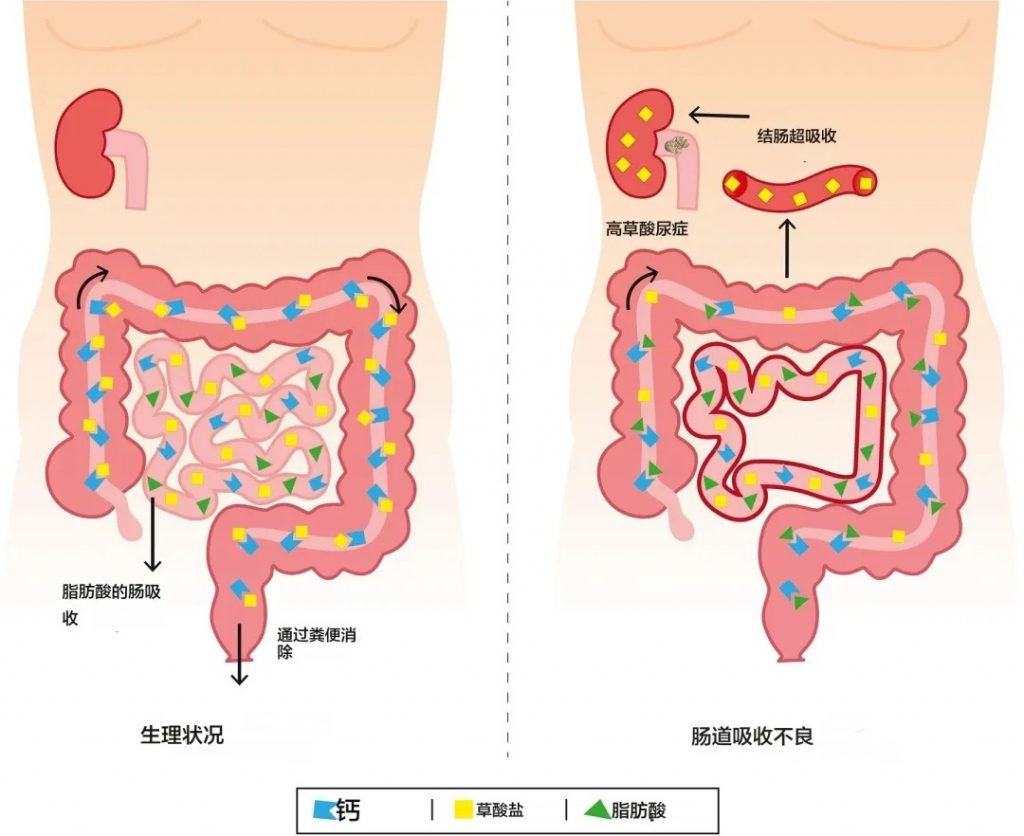
doi.org/10.1016/j.clinre.2024.102322
在生理条件下(左图),草酸的吸收受到限制,因为草酸钙复合物在结肠中不被吸收。在吸收不良状态下,例如短肠综合征或其他引起吸收不良的疾病(右图),结肠中的脂肪酸会导致钙螯合(皂化)。草酸不再与钙结合,可能会被结肠吸收,导致高草酸尿症。
新兴研究表明,肠道菌群失调可能通过调节尿液代谢物、肠道草酸代谢变化和全身炎症反应等机制,显著影响肾结石的风险和发展。
肠道菌群可降解草酸
特别是草酸杆菌属Oxalobacter等细菌,尤其是O. formigenes,以其降解草酸的能力而闻名,这种细菌通过表达草酸脱羧酶等与草酸代谢相关的蛋白来降解草酸,将其转化为甲酸盐和二氧化碳,从而减少肠道对草酸盐的吸收,并降低结石形成的风险。
Klimesova等(2015)和Mogna等(2014)的研究比较了不同菌株降解草酸的效率。
Suryavanshi等(2016)发现肾结石患者肠道微生物群中的O. formigenes 减少,但其他草酸代谢酶表达增加。
动物实验显示给予草酸降解菌可降低血草酸水平和肾钙化风险,但对尿草酸无影响。
肠道菌群调节草酸转运蛋白表达
此外,肠道微生物群可以通过调节草酸转运蛋白的表达来影响草酸的吸收和分泌。例如,SLC26A3和SLC26A6等转运蛋白在肠道草酸的吸收和分泌中起着关键作用。肠道微生物群的组成变化可能会影响这些转运蛋白的表达和活性,进而影响草酸的代谢。
菌群产生的短链脂肪酸影响草酸转运蛋白表达
微生物产生的短链脂肪酸也可以影响草酸转运蛋白的表达,这可能是通过改变肠道环境的酸碱度或通过直接与宿主细胞的信号传导途径相互作用来实现的。
肠道菌群降低胆固醇
多项研究证实了脂肪吸收不良与高草酸尿症之间的关联。
Moreland等(2017)的研究发现,胃旁路手术后患者出现脂肪吸收不良和高草酸尿症。
Chambers等(2022)和de Martines等(2019)的研究表明,慢性胰腺炎和胰腺功能不全患者也存在脂肪吸收不良、高草酸尿症和肾脏草酸钙结晶沉积。
Agrawal等(2014)报告,减肥手术后患者在术后两个月就可能出现显著的尿液草酸水平升高。
肠道微生物群的其他作用也不容忽视。例如,某些微生物如双歧杆菌、乳杆菌属等可降低胆固醇,这可能间接降低草酸的吸收。
一项研究发现,肾结石患者的乳杆菌和双歧杆菌的丰度显著低于健康个体,这与肾结石的风险增加相关。
Bordoni等(2013)和Zanotti等(2015)发现口服双歧杆菌可降低小鼠血清LDL和总胆固醇水平。
Costabile等(2017)报告Lactiplantibacillus plantarum治疗可显著降低轻度高胆固醇血症患者的血清LDL和总胆固醇水平。
益生菌治疗肾结石的潜力与挑战
在治疗肾结石方面,益生菌显示出了潜力,但也面临着定植和存活的挑战。例如,Oxalobacter formigenes是一种有潜力的益生菌,它能够降低原发性高草酸尿症患者的血浆和尿液草酸水平,但这种效果在停止治疗后会消失。乳杆菌属和双歧杆菌属的某些菌株也显示出降低尿液草酸水平的能力。然而,这些益生菌在定植和存活方面面临挑战,需要进一步研究来解决这些问题。
其他方法可以参考:
系统性红斑狼疮 (SLE) 是一种众所周知的系统性自身免疫性疾病,以产生致病性自身抗体和免疫复合物为特征,从而导致多种器官和组织的损害。大约 50% 的系统性红斑狼疮患者会出现肾脏损害,其特征是血尿、蛋白尿、水肿或肾功能减退等症状,称为狼疮性肾炎 (LN) 。在亚洲,系统性红斑狼疮患者的狼疮性肾炎患病率为 33%-82%。
狼疮性肾炎的治疗主要依赖类固醇和非选择性免疫抑制药物,但仅有50%~70%的狼疮性肾炎患者可获得临床缓解,10%~20%的患者在初次诊断后5年内进展为终末期肾病,预后不佳提示狼疮性肾炎的发病机制和治疗仍是一个尚未解决的难题。
越来越多的证据表明,肠道菌群失调可能与狼疮性肾炎相关,因为它会导致免疫失调,而这是其潜在发病机制之一。
狼疮性肾炎患者肠道菌群特征
菌群多样性降低:
临床和动物研究中狼疮性肾炎肠道菌群变化
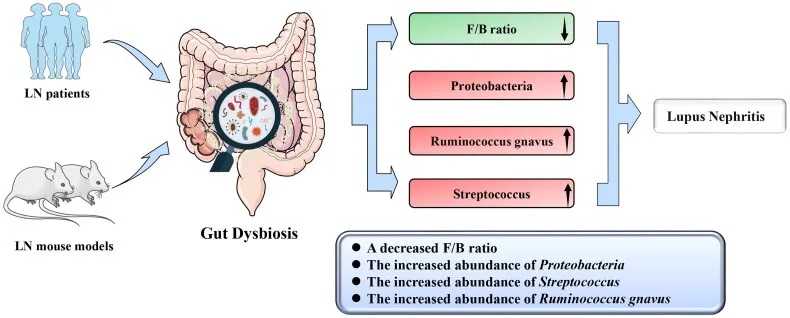
doi : 10.1080/0886022X.2023.2285877
菌群组成改变:
Firmicutes/Bacteroidetes (F/B)比例降低
这被认为是病理状态的一个标志。F/B 比率降低可导致Treg细胞和Th17细胞失衡,这可能会加剧先前存在的肠道炎症。狼疮患者 F/B 比率降低引起的菌群失调会导致 ILC3 功能障碍,而 ILC3 是屏障免疫的关键因素。
此外,F/B 比率失衡与系统性红斑狼疮患者血浆脂多糖水平升高相一致;从而增强 B 细胞的活化并促进小鼠模型中的系统性红斑狼疮进展。研究人员认为,多形拟杆菌可能是导致狼疮性肾炎患者 F/B 比降低的关键肠道菌群。
变形菌门、链球菌属、乳杆菌属↑↑
肠道菌群中变形菌增多可能是狼疮性肾炎发病机制中的一个重要因素,或许是基于自身免疫和炎症反应。
变形菌可能在以下两个方面对狼疮性肾炎的发病机制产生重大影响:
首先,从变形菌门成员大肠杆菌中获得的LPS可通过 TLR4–NF-κB和TLR4–p38MAPK通路刺激IL-6的产生,从而引发炎症反应。巧合的是,动物研究表明 IL-6在促进狼疮性肾炎中起着重要作用。
其次,变形菌门成员肠杆菌科的丰度与T细胞有关,而 T 细胞在免疫反应中至关重要。这表明,肠杆菌科丰度的变化可能促使狼疮性肾炎的发病机制和进展。
因此,变形菌的增加可作为肠道菌群改变的特异性标志,并可能通过调节IL-6和T细胞的水平促进狼疮性肾炎的发展。
链球菌属(Streptococcus)丰度增加,可能通过增强自身免疫反应促进狼疮性肾炎发展。
3项临床研究发现,狼疮性肾炎患者的链球菌属丰度高于健康对照组。
链球菌与韦荣球菌(Veillonella)的组合可增加IL-6、IL-10、IL-8和TNF-α的产生,同时抑制IL-12p70的产生。
肺炎链球菌的多糖与抗dsDNA抗体中的五肽具有相同的表位。
某些链球菌种可能通过抗原呈递触发特定CD4+ T细胞和初始B细胞刺激。
细菌同源物与人类自身抗原的分子模拟可能触发T和B淋巴细胞的交叉反应,激活自身免疫。
Ruminococcus gnavus、Lactobacillus reuteri ↑↑
Ruminococcus gnavus(简称RG)的丰度与狼疮疾病活动性和狼疮性肾炎相关,并与C3和C4补体水平呈负相关。
RG2菌株细胞壁脂聚糖具有抗原性,可诱导抗dsDNA抗体的产生。
这些抗体可与狼疮抗dsDNA抗体发生交叉反应,导致不适当的免疫反应。
活动性狼疮性肾炎患者血清中IgG抗RG2抗体浓度较高。
乳杆菌属和鼠李糖乳杆菌(L. reuteri)在狼疮性肾炎发病中存在争议
正面作用:
乳酸杆菌治疗可以促进无炎症的肠道环境,增加血清IL-10水平,恢复肾脏内Treg和Th17细胞的平衡。
负面作用:
罗伊氏乳杆菌灌胃增加了脾脏肿大和浆细胞样树突状细胞(pDCs)在脾脏和派氏结积累,加剧了白细胞向肾脏募集。
罗伊氏乳杆菌单菌定植的小鼠显示pDCs在脾脏和肠系膜淋巴结中积累增加,狼疮性肾炎症状恶化。
这些矛盾的发现表明乳酸杆菌属和鼠李糖乳杆菌在狼疮性肾炎中可能扮演复杂的角色,其作用可能取决于具体的遗传或环境条件。
特定菌群链的富集:
从系统发育图中观察到,肠道分类链拟杆菌-拟杆菌-多形拟杆菌(Bacteroides thetaiotaomicron)在狼疮性肾炎中显著富集。
肠道菌群失调与狼疮性肾炎的可能机制
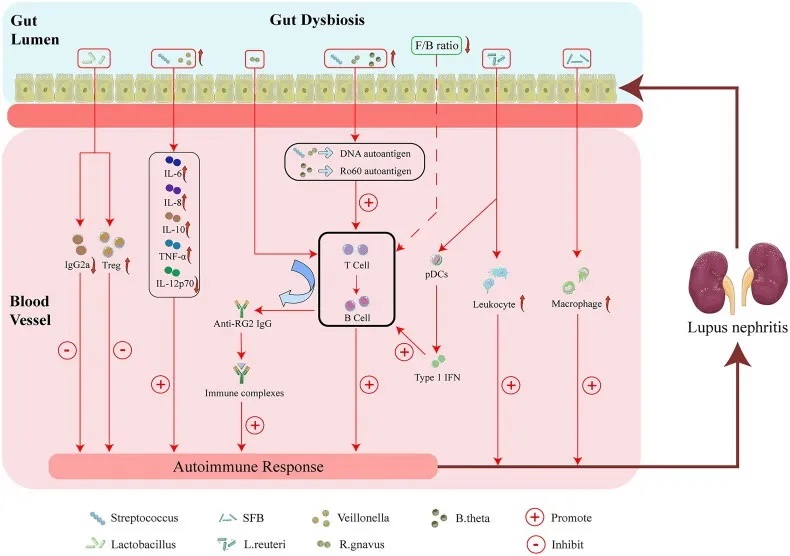
doi : 10.1080/0886022X.2023.2285877
特定微生物类群的改变可能通过以下四个因素促进狼疮性肾炎的发病和进展:
首先,特定微生物类群的改变可通过促进肾脏 M2 样巨噬细胞浸润和白细胞募集而诱发狼疮性肾炎。
其次,肠道菌群可能通过增强自身免疫反应导致狼疮性肾炎。
第三,链球菌与韦荣球菌结合可增强自身免疫反应,包括通过增加IL-6、IL-8、IL-10、TNF-α水平,而 IL-12p70 降低可能会诱发狼疮性肾炎。
第四,特定微生物类群的改变可以增加Treg的丰度,而IgG2a沉积减少可能会减轻狼疮性肾炎。
细菌代谢物:短链脂肪酸的作用
短链脂肪酸是最常被提及的细菌代谢物,对许多肾病具有有益作用。短链脂肪酸产生的变化与 系统性红斑狼疮患者的肠道菌群失调有关,而粪便 短链脂肪酸水平的升高与 F/B 比降低有关。SLE 动物模型显示,补充 SCFA 可以减轻狼疮表型。
此外,短链脂肪酸可能抑制B细胞活化诱导的胞苷脱氨酶和 Blimp1 的表达,限制浆细胞和系统性类型转换自身抗体的分化,并防止 IgG1/IgG2a 在肾脏中的沉积。
基于菌群对狼疮性肾炎的干预措施
通过饮食、益生菌和粪菌移植 (FMT) 成功治疗狼疮性肾炎可能为理解狼疮性肾炎与肠道菌群之间的关系提供新的证据。
首先,营养干预可以改善小鼠模型中的狼疮性肾炎。
其次,益生菌疗法是狼疮性肾炎的另一种治疗选择。口服脆弱拟杆菌可有效缓解狼疮性肾炎。该机制包括降低狼疮性肾炎患者的自身抗体水平、更新 B 淋巴细胞的免疫反应、缓解肠道炎症以及恢复狼疮性肾炎小鼠模型中 Treg 和 Th17 细胞的平衡。
第三,目前,FMT在治疗系统性红斑狼疮和 CKD 方面的安全性和有效性已得到证实。在系统性红斑狼疮治疗中,经过 12 周的 FMT 干预后,血清抗 dsDNA 抗体水平、炎症相关肠道微生物群和外周血中 IL-6 水平降低,同时产生 SCFA 的菌群和 SCFA 的产量增加。
总的来说,F/B 比值降低可能是狼疮性肾炎患者肠道菌群的一个特殊标志,这与 IFN-γ 水平降低、Treg 和 Th17 细胞失衡以及 B 细胞激活有关。变形菌门丰度增加,这可能与 IL-6 和 T 细胞水平有关,链球菌属和R. gnavus的富集也可能通过增强自身免疫和分子模拟在狼疮性肾炎的发病机制中发挥作用。这些发现有助于更好地了解肠道菌群如何影响狼疮性肾炎及其在预防和治疗狼疮性肾炎中未被认识到的作用。
慢性肾病患者更易发生抗菌药物相关神经毒性,主要表现为抗生素相关性脑(AAE)。
慢性肾病是抗生素相关性脑的已知风险因素。AAE被认为是慢性肾病患者中最常见的抗生素引起的不良反应之一。
在接受静脉抗生素治疗的住院终末期肾病患者中,AAE的总体患病率估计为4.4%,但可能被低估。
慢性肾病患者更容易发生抗生素相关神经毒性的原因包括:
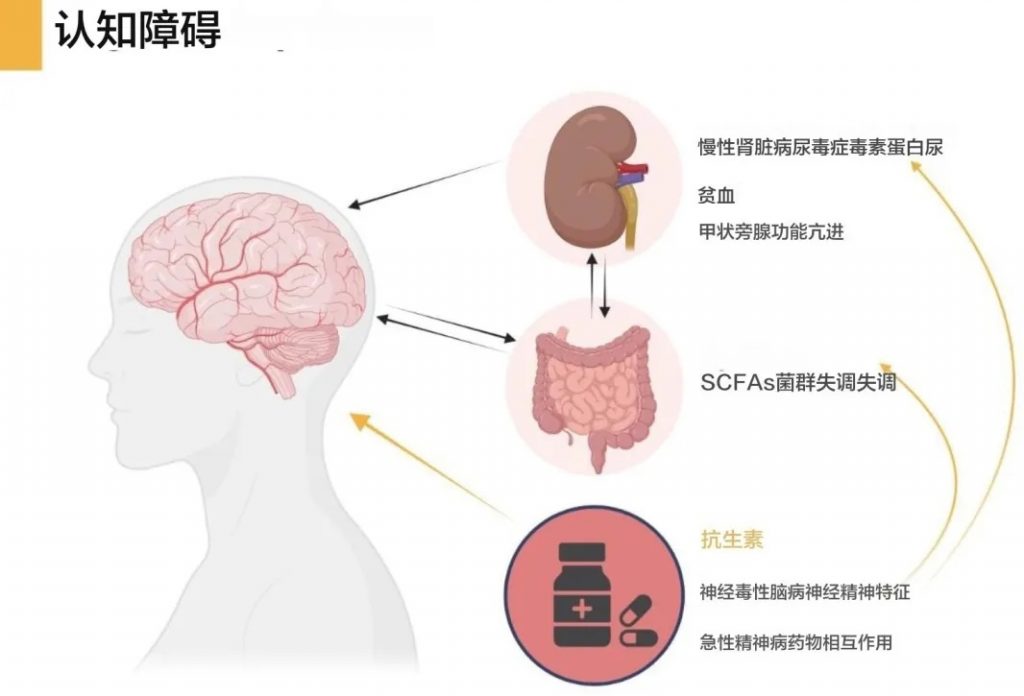
doi.org/10.1093/ckj/sfae174
以下列举的是一些CKD患者可能会用到的抗生素药物及其带来的影响。
◆β-内酰胺类抗生素(如青霉素、头孢菌素和碳青霉烯类)
◆ 氟喹诺酮类(如环丙沙星、左氧氟沙星、莫西沙星)
◆ 氨基糖苷类(如庆大霉素和妥布霉素)
氨基糖苷类抗生素以其强大的杀菌作用著称,但其肾毒性是导致CKD患者使用时的主要顾虑,其毒性作用与药物的血药浓度和使用时间密切相关。
◆ 大环内酯类(如红霉素和阿奇霉素)
大环内酯类抗生素的肾毒性相对较低,但部分药物如红霉素可能通过与肾脏药物转运体相互作用,影响其他药物的排泄,从而间接影响肾功能。
◆ 磺胺类(如磺胺甲噁唑、磺胺嘧啶)
磺胺类抗生素在慢性肾病患者中使用需谨慎,这类药物可能引起晶体性肾尿,特别在尿液酸性时更易形成药物结晶,导致肾小管堵塞和急性肾损伤。
◆ 硝基咪唑类(如甲硝唑和替硝唑):
磺胺类抗生素在CKD患者中使用需谨慎,这类药物可能引起晶体性肾尿,特别在尿液酸性时更易形成药物结晶,导致肾小管堵塞和急性肾损伤。
◆ 糖肽类(如万古霉素)
◆ 多粘菌素类(如多粘菌素B和粘菌素)
◆ 抗结核药物(如异烟肼、利福平、吡嗪酰胺和乙胺丁醇)
症状通常在开始治疗后数天内出现,停药后可逆。但某些抗生素(如甲硝唑)症状出现和恢复可能需要更长时间。
对于血液透析患者,有报道显示血液透析可能有助于清除某些抗生素并改善症状。
CKD患者使用抗菌药物时应进行治疗药物监测,调整剂量
对于慢性肾病(CKD)患者使用抗菌药物时,进行治疗药物监测(TDM)和剂量调整是非常重要的。
剂量调整原则:
监测频率:
总之,对慢性肾病患者使用抗菌药物时,进行治疗药物监测和适当的剂量调整是至关重要的。这不仅可以确保治疗的有效性,还可以显著降低药物不良反应的风险,特别是神经毒性。医生应熟悉治疗药物监测的原则和方法,并根据患者个体情况制定个性化的给药方案。
饮 食
选择健康的饮食方式
✘ 红肉摄入增加和人工甜味剂使用改变了肠道微生物组成,增加了尿毒症毒素的产生。
✘ 富含胆碱和 L-claritin(TAMO 的前体)的食物(如蛋黄、肾脏、肝脏、牛奶和肉类)可能会增加尿毒症毒素并降低肾小球滤过率,尽量避免。
✔ 一系列饮食指南已被研究作为 CKD 的潜在治疗策略,包括地中海饮食(富含蔬菜、坚果、豆类、水果和全谷物)、植物性饮食和低蛋白饮食(LPD;减少饮食蛋白质摄入但避免完全不摄入蛋白质)。
这些饮食旨在通过减少与西方饮食相关的高蛋白质消耗来减少细菌蛋白水解发酵。因此,预计炎症反应和尿毒症毒素的产生会减少,肾功能衰退可能会减缓,心血管风险可能会降低。
选择含盐和钠较少的食物
关键词:
无钠、无盐;或低盐、低钠;无盐或微咸
经常购买新鲜食物。超市或餐厅出售的许多预制或包装食品中都添加了钠(盐的一部分)。
自己烹饪食物,而不是吃预制食品、“快餐”食品、冷冻食品和钠含量较高的罐头食品。当你自己做饭时,你可以控制食物的成分。
使用香料、草药和不含钠的调味料代替盐。
检查食品包装上的营养成分标签上是否有钠。每日摄入量为 20% 或更高意味着食物中钠含量高。
尝试低钠版本的冷冻晚餐和其他方便食品。
食用前请用水冲洗罐装蔬菜、豆类、肉类和鱼类。
摄入适量、合适类型的食物
✔ 摄入超过需要的蛋白质可能会使你的肾脏更加辛苦地工作,因此,吃少量的蛋白质食物更合适。
✔ 防止脂肪在血管、心脏和肾脏中堆积:
烧烤、炙烤、烘培、烘烤或炒制食物,而不是油炸。
使用不粘烹饪喷雾或少量橄榄油代替黄油来烹饪。
食用前,应去掉肉中的脂肪,去掉家禽的皮。
尽量限制饱和脂肪和反式脂肪的摄入。阅读食品标签。
少吃这些食物
饱和脂肪、黄油、猪油、红肉、全脂牛奶、反式脂肪、商业烘焙食品,例如饼干和蛋糕、甜甜圈、炸薯条、氢化植物油、人造黄油等。
可以选择这些食物
单不饱和脂肪和多不饱和脂肪、菜籽油、坚果、麦片、橄榄油、三文鱼、香油。
✔ 随着肾功能下降,可能需要食用磷和钾含量较低的食物。
患有慢性肾病时,磷会在血液中积聚。血液中过多的磷会从骨骼中吸收钙,使骨骼变薄、变弱,更容易断裂。血液中磷含量过高还会导致皮肤瘙痒以及骨骼和关节疼痛。

来源:NIDDK
✔ 选择含适量钾的食物
当血钾水平过高或过低时,就会出现问题。受损的肾脏会导致血液中钾积聚,从而导致严重的心脏问题。
盐替代品的钾含量可能非常高,阅读成分标签。
食用前将罐装水果和蔬菜沥干。

来源:NIDDK
多酚和omega-3脂肪酸等植物成分具有抗氧化和抗炎作用,可能有助于缓解CKD。
✔ 多酚
多酚是植物中广泛存在的次生代谢物,主要包括黄酮类和酚酸类化合物。它们具有以下作用:
✔ Omega-3脂肪酸
Omega-3脂肪酸,特别是α-亚麻酸(ALA)、二十碳五烯酸(EPA)和二十二碳六烯酸(DHA),可以抗血栓形成、降低甘油三酯、还有抗炎作用。
研究表明,CKD患者体内Omega-3脂肪酸水平较低。补充Omega-3脂肪酸可能通过以下机制缓解CKD:
其他植物成分
这些植物成分通过抗氧化、抗炎、调节肠道菌群等多种机制,可能有助于减轻氧化应激和炎症,从而缓解慢性肾病的进展。然而,还需要更多的研究来确定这些成分在慢性肾病患者中的具体作用和适当剂量。
更多抗炎食物可以参考我们之前的文章:
增加维生素D的摄入量
维生素 D对肾脏的正常功能起着重要作用,
维生素D在肌肉生长、调节肌肉收缩和舒张周期、提供能量、维持葡萄糖平衡以及修复肌肉损伤方面起重要作用。
缺乏维生素 D 会导致进一步的肾功能障碍。对CKD患者而言,PTH水平升高和维生素D缺乏共同影响钙磷代谢,可能导致骨矿物质代谢紊乱。这些变化可能影响肌肉功能和生长,参与肌肉减少症的发生。
可以适当吃鲑鱼、鲭鱼、金枪鱼,乳制品和谷物产品等。多晒太阳补充。
其他饮食小Tips:
选择新鲜或冷冻的蔬菜而不是罐装的。
选择糙米或大麦而不是速食米饭或预先包装的调味谷物。
选择吃鸡胸肉等瘦肉蛋白质来源,而不是红肉。
在你的饮食中加入更多鱼。
用低盐鹰嘴豆泥蔬菜条代替薯条作为零食。
吃新鲜水果而不是烘焙食品。
中草药提取物
五层龙(Salacia chinensis)
研究:30名稳定的糖尿病CKD患者,每天两次服1000mg
结果:降低同型半胱氨酸和IL-6水平
西藏苦草(Hygrophila spinosa)
研究:分析植物化学成分,对多重耐药Pandoraea sputorum的杀菌活性,以及对HepG2和HEK 293细胞系的肝肾保护作用
结果:甲醇提取物对CCl4和顺铂诱导的细胞毒性显示肝肾保护作用
蕨麻 (Potentilla anserine L.)
研究:调查rosamultin对顺铂诱导的肾毒性的保护作用
结果:
降低血尿素氮(BUN)
提高HEK293细胞的体外活力
抑制顺铂诱导的细胞凋亡
改善肾功能障碍
减少肾小管损伤
洋甘草 (Glycyrrhiza glabra L.)
研究:分析植物化学成分,研究甘草根提取物对顺铂诱导的体内外肾毒性的保护作用
结果:通过抗氧化、抗炎和抗凋亡活性发挥肾脏保护作用
长梗黄花棯 (Sida cordata)
研究:评估乙酸乙酯提取物对CCL4诱导的肾毒性的抗氧化活性
结果:显示对CCl4诱导的大鼠肾毒性有保护作用,与其含有的抗氧化化合物有关
菝葜 (Smilax cordifolia) 和刺芹属植物(Eryngium carlinae)
研究:评估两种植物煎剂对大鼠肾功能障碍的影响
结果:
降低血清尿酸、白蛋白和尿素浓度
减少与肾小球硬化和肾小管纤维化相关蛋白的积累
增加肌酐清除率
增加促炎和保护性蛋白的浓度
中药大黄 (Rheum L.)
大黄是一种具有泻下作用的传统中药,常用于治疗CKD。
大黄与血管紧张素转换酶抑制剂(ACEI)或血管紧张素受体阻滞剂(ARB)具有协同作用。
大黄灌肠可以调节肠道菌群的丰度和组成,增加短链脂肪酸(SCFA)水平,改善肠道屏障损伤,减少炎症水平,改善肾脏病理,降低血肌酐水平。
这些研究结果表明,这些中草药提取物通过不同的机制(如抗氧化、抗炎、抗凋亡等)展现出肾脏保护作用,有望用于CKD的辅助治疗。然而,还需要进行更多的研究来确定这些植物提取物在CKD患者中的具体作用和适当剂量。
益生菌 和 益生元
给8名血液透析患者口服嗜酸乳杆菌,结果显示血清二甲胺(DMA)减少。
注:DMA这种物质会损害器官血管。
口服胶囊形式的长双歧杆菌可以降低血清IS水平。
干酪乳杆菌L. casei Zhang通过提高血清短链脂肪酸水平改善局部巨噬细胞和肾小管上皮细胞的炎症反应。研究还观察到在服用张氏乳杆菌后,CKD3-5期患者的肾功能下降速度变慢。
约翰逊乳杆菌(Lactobacillus johnsonii)治疗通过增加血清IAld水平来抑制AHR信号通路,从而减轻肾脏病变。
Lactiplantibacillus plantarum N-1在乙二醇诱导的肾结石大鼠模型中,降低了尿液草酸水平和肾脏草酸钙结晶沉积。
初步证据表明,富含益生元低聚果糖的菊粉(p-菊粉) 可促进双歧杆菌的生长、介导减肥、减轻炎症并改善代谢功能。
高膳食纤维摄入量与 CKD 患者炎症风险降低和死亡率降低相关。
益生菌对CKD患者的影响研究



doi: 10.1021/acs.jafc.4c00263
益生菌调节肠道菌群对 CKD 的缓解作用包括:
通过肠肾轴探索益生菌防治慢性肾脏病的机制
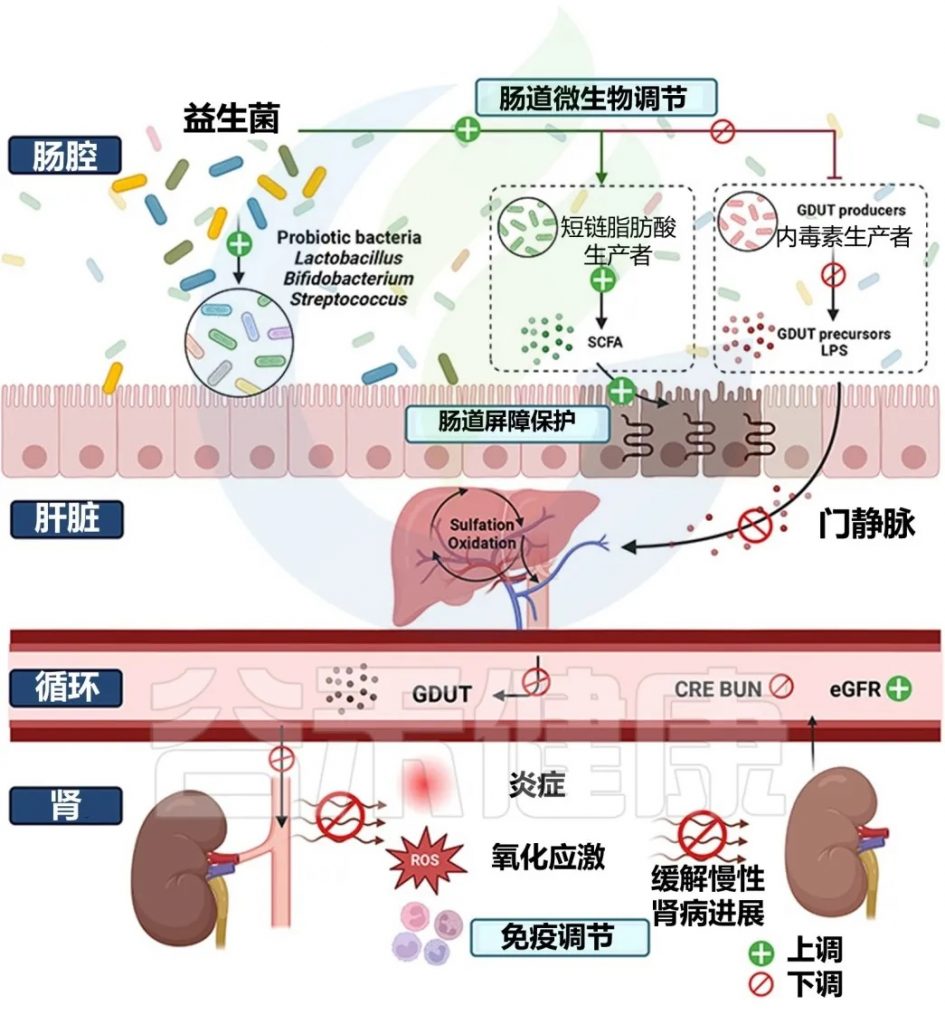
doi: 10.1021/acs.jafc.4c00263
由于饮食、疾病状况和个体年龄的广泛差异,需要充分考虑益生菌的治疗精确性。
粪 菌 移 植
多项 FMT 研究已证实,FMT 已成为一种有用工具,有助于证明肠道菌群的调节可能是 CKD 治疗干预措施发挥肾脏保护作用的关键机制之一。FMT 也已在临床病例研究中用于改善肾功能:
在一份临床病例报告中,从一名健康男性合格供体中提取的 FMT 通过内镜应用于治疗一名膜性肾病患者。经过两次治疗后,FMT 改善了相关的肾病综合征,改善了肾功能,总血清蛋白和白蛋白水平增加,血清肌酐和 24 小时尿蛋白降低。
两例 IgAN 患者通过内镜肠内插管定期接受 FMT 6-7 个月。FMT 治疗降低了两名患者的 24 小时尿蛋白,增加了血清白蛋白,并恢复了肠道菌群。
FMT 通过调节肠道菌群失调来改善肾功能并防止肾损伤,其机制包括恢复宿主的免疫力、调节肠道菌群代谢物、肾素-血管紧张素系统和改善肠道上皮屏障完整性。
FMT 治疗慢性肾病的潜在机制
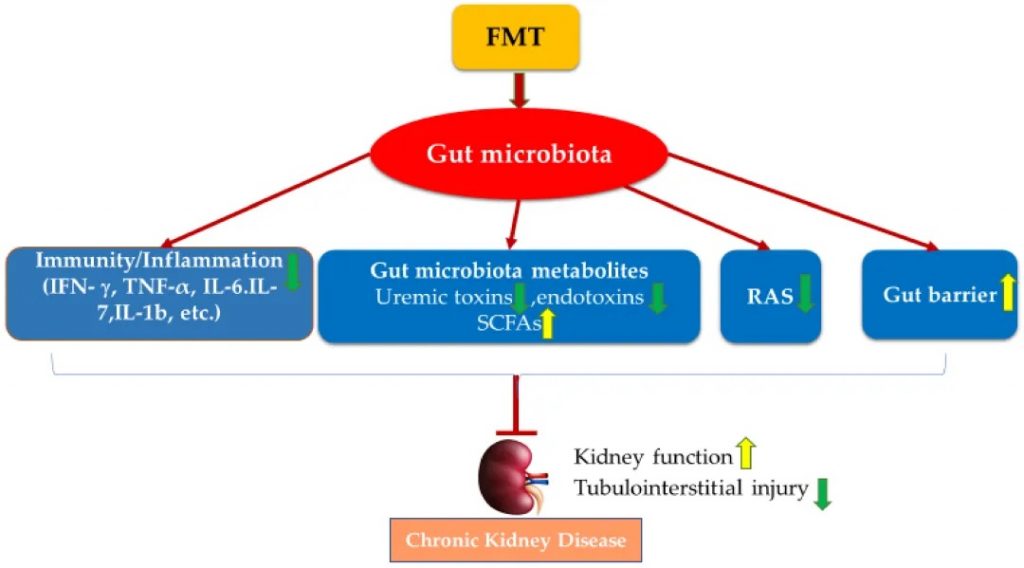
doi.org/10.3390/nu14122528
“一刀切”并不能解决所有问题。因此,特定疾病的供体选择和给药方法是 FMT 成功率的主要决定因素。
FMT 策略需要依靠人工智能、先进的生物信息学技术和机器学习算法的优势,例如多组学相关性分析。需要将肠道菌群检测、血浆、尿毒症毒素、粪便代谢物和肾功能的一组参数联系起来并进行系统分析,这将有力地支持研究人员了解FMT。
生 活 方 式
管理压力水平
重大生活事件带来的巨大压力,会增加急性肾损伤和慢性肾病进展的风险。可以通过听音乐,冥想,瑜伽等方式让身体放松。
定期锻炼
运动锻炼有助于降低血压和改善心脏健康,这两者都是肾脏疾病的风险因素。运动还有助于控制血糖水平和体重,这对糖尿病和肾病患者来说都是重要的因素。CDC建议,每周进行150分钟中等强度的锻炼。两天的肌肉强化活动。
慢性运动对CKD可能的治疗效果
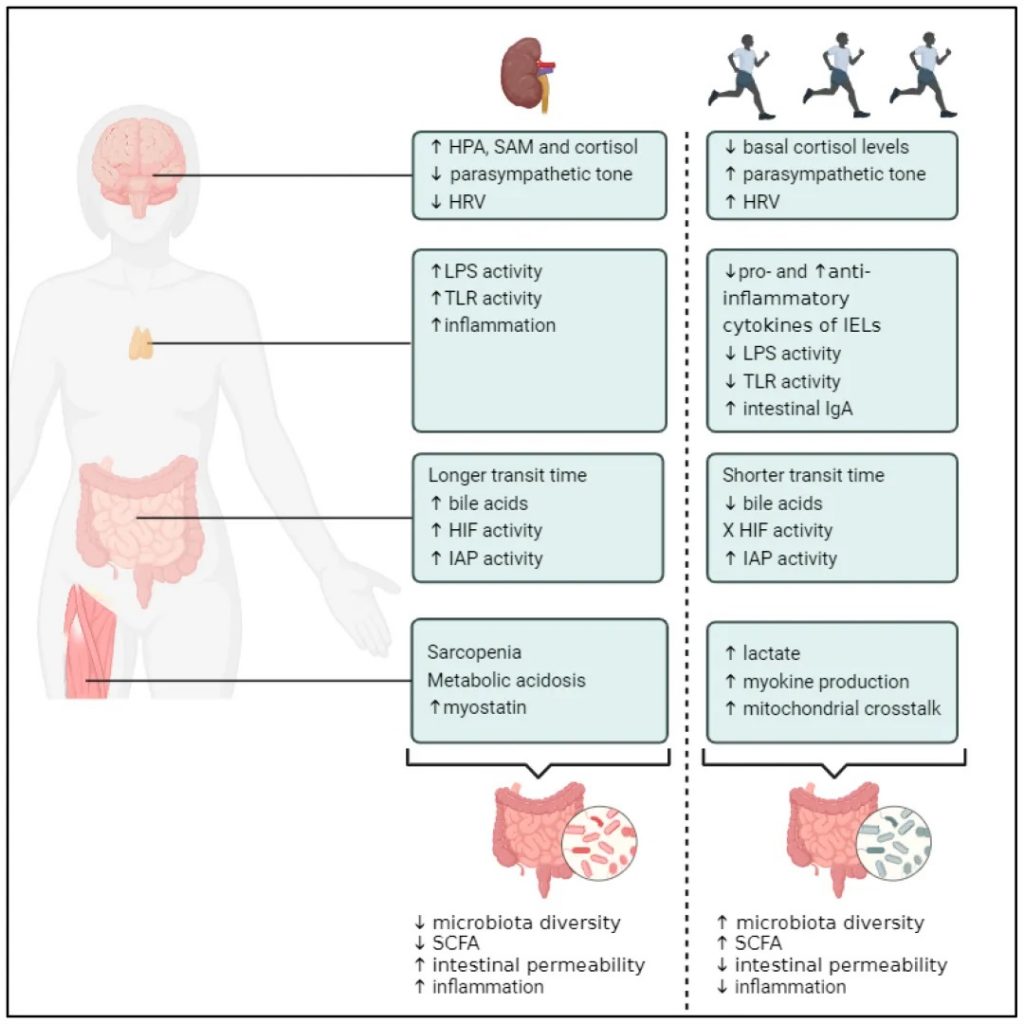
doi.org/10.3390/toxins16060242
保证充足的睡眠
一项研究发现,肾功能正常的中老年人如果每晚睡眠时间不足6小时,患慢性肾病的风险更高。
建立规律的睡眠时间表:每天在同一时间上床睡觉和起床,以调节身体的生物钟。
营造宁静的环境:让卧室安静、黑暗、凉爽。考虑使用遮光窗帘、耳塞或白噪音机。
睡前限制屏幕时间:睡前至少一小时关闭电子设备。
练习放松的睡前习惯:从事一些令人平静的活动,例如阅读、洗个温水澡或完成放松的伸展运动。
限制酒精摄入量
一些研究表明,少量至适量的酒精摄入可能对肾功能有益。
然而,他们并不建议不喝酒的人为了获得潜在的健康益处而开始饮酒。
其他研究警告称,饮酒可能会增加其他疾病的风险,例如通常与肾脏疾病有关的心血管疾病。
避免吸烟
香烟烟雾中含有有害物质,会减少流向肾脏的血液,从而降低肾脏正常工作的能力。
吸烟也是导致高血压和2 型糖尿病的风险因素,这两者都是导致肾脏疾病的主要原因。
据统计,慢性肾病(CKD)的发病率高达10%,其致残和死亡率在所有慢性疾病中增幅最快,防治面临严峻挑战。尽管通过尿液检查、血液检测、核素显像和肾脏超声等方法可以早期发现肾脏损害,但由于缺乏明显症状,许多人忽视定期检查。此外,这些检测的费用较高,增加了筛查的难度。
肾脏病种类繁多,病理类型复杂,临床症状相似,单靠临床判断诊断慢性肾病具有挑战性。患者最关心的是疾病是否会进展到尿毒症阶段。肾活检虽然是诊断的“金标准”,但在病情严重时,其适用性受到限制。治疗方案如激素和免疫抑制剂也存在副作用和风险。
近年来,研究发现慢性肾病与肠道菌群密切相关,调节肠道菌群有助于延缓疾病进展并改善生活质量。然而,个体差异、饮食模式和补充剂等因素使得研究结论难以统一。
为解决这些问题,建议扩大研究范围,利用人工智能和生物信息学技术评估肠道菌群在慢性肾病中的作用。通过肠道菌群检测技术评估干预效果,将更多基于菌群的干预手段推向临床实践。
随着研究的深入,肠道菌群有望成为慢性肾病治疗的重要方向,为患者带来新的希望。
主要参考文献
Mao ZH, Gao ZX, Pan SK, Liu DW, Liu ZS, Wu P. Ferroptosis: a potential bridge linking gut microbiota and chronic kidney disease. Cell Death Discov. 2024 May 15;10(1):234.
Krukowski H, Valkenburg S, Madella AM, Garssen J, van Bergenhenegouwen J, Overbeek SA, Huys GRB, Raes J, Glorieux G. Gut microbiome studies in CKD: opportunities, pitfalls and therapeutic potential. Nat Rev Nephrol. 2023 Feb;19(2):87-101.
Liu, H.; Diep, T.N.; Wang, Y.; Wang, Y.; Yan, L.-J. Diabetic Kidney Disease: Contribution of Phenyl Sulfate Derived from Dietary Tyrosine upon Gut Microbiota Catabolism. Biomolecules 2024, 14, 1153.
Bian, J.; Liebert, A.; Bicknell, B.; Chen, X.-M.; Huang, C.; Pollock, C.A. Faecal Microbiota Transplantation and Chronic Kidney Disease. Nutrients 2022, 14, 2528.
Młynarska, E.; Budny, E.; Saar, M.; Wojtanowska, E.; Jankowska, J.; Marciszuk, S.; Mazur, M.; Rysz, J.; Franczyk, B. Does the Composition of Gut Microbiota Affect Chronic Kidney Disease? Molecular Mechanisms Contributed to Decreasing Glomerular Filtration Rate. Int. J. Mol. Sci. 2024, 25, 10429.
Ramezani A, Raj DS. The gut microbiome, kidney disease, and targeted interventions. J Am Soc Nephrol. 2014 Apr;25(4):657-70.
Vandecruys, M.; De Smet, S.; De Beir, J.; Renier, M.; Leunis, S.; Van Criekinge, H.; Glorieux, G.; Raes, J.; Vanden Wyngaert, K.; Nagler, E.; et al. Revitalizing the Gut Microbiome in Chronic Kidney Disease: A Comprehensive Exploration of the Therapeutic Potential of Physical Activity. Toxins 2024, 16, 242.
Bakinowska E, Olejnik-Wojciechowska J, Kiełbowski K, Skoryk A, Pawlik A. Pathogenesis of Sarcopenia in Chronic Kidney Disease-The Role of Inflammation, Metabolic Dysregulation, Gut Dysbiosis, and microRNA. Int J Mol Sci. 2024 Aug 3;25(15):8474.
Joly PF. Pathophysiology and management of enteric hyperoxaluria. Clin Res Hepatol Gastroenterol. 2024 Jun;48(6):102359.
Tang Z, Yu S, Pan Y. The gut microbiome tango in the progression of chronic kidney disease and potential therapeutic strategies. J Transl Med. 2023 Oct 3;21(1):689.
Wilson S, Mone P, Jankauskas SS, Gambardella J, Santulli G. Chronic kidney disease: Definition, updated epidemiology, staging, and mechanisms of increased cardiovascular risk. J Clin Hypertens (Greenwich). 2021 Apr;23(4):831-834.
Huang HW, Chen MJ. Exploring the Preventive and Therapeutic Mechanisms of Probiotics in Chronic Kidney Disease through the Gut-Kidney Axis. J Agric Food Chem. 2024 Apr 17;72(15):8347-8364.
Liabeuf S, Hafez G, Pešić V, Spasovski G, Bobot M, Mačiulaitis R, Bumblyte IA, Ferreira AC, Farinha A, Malyszko J, Pépin M, Massy ZA, Unwin R, Capasso G, Mani LY; CONNECT Action (Cognitive Decline in Nephro-Neurology European Cooperative Target). Drugs with a negative impact on cognitive functions (part 3): antibacterial agents in patients with chronic kidney disease. Clin Kidney J. 2024 Jun 14;17(8):sfae174.
Liu X, Mo J, Yang X, Peng L, Zeng Y, Zheng Y, Song G. Causal relationship between gut microbiota and chronic renal failure: a two-sample Mendelian randomization study. Front Microbiol. 2024 Apr 3;15:1356478.
Tang Z, Yu S, Pan Y. The gut microbiome tango in the progression of chronic kidney disease and potential therapeutic strategies. J Transl Med. 2023 Oct 3;21(1):689.
Khan MA, Kassianos AJ, Hoy WE, Alam AK, Healy HG, Gobe GC. Promoting Plant-Based Therapies for Chronic Kidney Disease. J Evid Based Integr Med. 2022 Jan-Dec;27:2515690X221079688.
谷禾健康
糖尿病是一种复杂的多系统代谢紊乱,其特征是高血糖,它还会导致并发症,降低生活质量并增加死亡率。糖尿病病理生理学包括β细胞、脂肪组织、骨骼肌和肝脏功能障碍。
1型糖尿病(T1D)是由免疫介导的β细胞破坏引起的。更常见的2型糖尿病(T2D)是一种异质性疾病,其特征是不同程度的β细胞功能障碍与胰岛素抵抗共同作用。
肥胖和2型糖尿病之间的密切关联涉及由中枢神经系统调节的通路,这些通路控制食物摄入和能量消耗,并整合来自外周器官和环境的输入。
患糖尿病或其并发症的风险代表了遗传易感性和环境因素之间的相互作用,包括营养食品的可用性和其他健康的社会决定因素。
糖尿病已经困扰人类数千年。从对这一疾病的“早期”描述到现代,目前人们对全球日益增多的糖尿病病人的流行病学、病理生理学、并发症和治疗选择的理解已经大大加深。
在过去的 50 年里,我们共同目睹了有关1型糖尿病和2型糖尿病病理生理学的知识爆炸式增长,而这种知识正在彻底改变糖尿病的治疗和预防方法。因此,任何关于糖尿病病理生理学和治疗进展的观点都不可能详尽无遗,或完全统一。
本文根据顶级期刊《Cell》近期发布的关于近50年有关糖尿病研究进展总结内容,与大家分享。
◮ 关于糖尿病的基础知识
糖尿病是由于胰岛素不足以刺激生理性葡萄糖处理,从而促进能量在脂肪组织、肌肉和肝脏中的储存而发展起来的。
糖尿病的表现范围从几乎完全的胰岛素缺乏症,如1型糖尿病(T1D)中出现的情况,到在胰岛素抵抗的情况下胰岛素相对缺乏的情况——2型糖尿病(T2D)的特征。
虽然糖尿病的诊断是基于测量血糖或糖化血红蛋白,但这种疾病应该被视为一个与多种合并症相关的多系统疾病。
◮ 糖尿病的大致分类
•1型糖尿病:由免疫介导的胰岛细胞破坏引起;
•2型糖尿病:与胰岛素抵抗和相对胰岛细胞功能不全相关;
•特定单基因疾病、药物毒性或胰腺功能不全引起的糖尿病综合征;
•妊娠期糖尿病
◮ 糖尿病的患病情况
2型糖尿病患者人数最多,1型糖尿病则不到所有病例的5%。2021年,全球糖尿病的患病率估计为6.1%,相当于5.29亿人,某些地区的患病率甚至高达12.3%。2型糖尿病占96%的病例,其中超过50%与肥胖有关。
糖尿病流行的趋势令人担忧,预计到2050年,将有13.1亿人患糖尿病。其他分析指出,2021年全球患病率已经超过10%。此外,2021年估计还有4.64亿人有糖耐量受损,2.98亿人有空腹血糖受损,总体上代表了糖尿病前期。
◮ 糖尿病大大增加了患其他病的风险
糖尿病大大增加了由心血管疾病和肾脏病造成的全因死亡率,且导致多种其他病症,包括失明、肢体丧失、慢性疼痛和残疾。
尽管升高的循环葡萄糖是任何原因引起的糖尿病的特征,但2型糖尿病是一种异质性疾病,不同人群亚群的结果存在差异。
鉴于肥胖与2型糖尿病之间的关联,有人认为,只要更加注重改善营养、增加身体活动和减少肥胖的政策,这种负担的大部分是可以预防的。然而,糖尿病的异质性表明,预防和治疗策略最好量身定制,以最大限度地发挥其在特定人群中的功效。
◮ 1型糖尿病概况
1型糖尿病(T1D)占所有糖尿病病例的5%–10%,由自身免疫介导的胰腺β细胞破坏导致。
胰岛素的发现使1型糖尿病从曾经的致命诊断变为可管理的慢性病。尽管取得了管理进步和新疗法的问世,只有约20%的患者能实现最佳血糖控制,且预期寿命较短。
◮ 遗传研究和疾病进展
全基因组关联研究(GWAS)鉴定了60多个与1型糖尿病相关的基因位点,显示出该病的高度遗传性。
对自然史的研究通过新生儿筛查和自身抗体筛查提供了对环境因素、疾病触发因素、胰岛自身免疫轨迹及代谢和免疫表型的见解。
重要观察之一是综合分析显示,有两种或更多胰岛自身抗体的人在15年内发展为临床1型糖尿病的风险超过80%。
◮ 疾病分期
1期T1D:存在两种或两种以上自身抗体
2期T1D:多种自身抗体阳性和血糖紊乱
3期T1D:明显的高血糖症
历史背景
在上世纪末,关于2型糖尿病的遗传学理解主要集中在少数几个基因座上,这些基因座与环境因素共同影响个体患病风险。
现代研究进展
随着全基因组关联研究(GWAS)的发展,现在已发现数百种与2型糖尿病相关的遗传变异。这些变异大多对患病风险的影响很小。
变异的作用机制
大多数与2型糖尿病相关的变异并不直接改变蛋白质功能,而是通过影响非编码基因组序列中的调控元件来改变基因表达的丰度。这些调控元件在特定的细胞类型和发育时间点发挥作用。
挑战与机遇
当前的挑战是将这些调控信号与具体的效应基因(转录本)关联起来,以了解其对糖尿病风险的影响。识别这些基因有助于理解糖尿病的机制,并可能发现新的治疗靶点。
单细胞多组学数据的应用
单细胞分辨率多组学数据集的出现为研究人员提供了工具,以更好地将遗传变异与其效应基因关联起来。这些数据结合高通量细胞表型分析,有助于评估变异相关的基因表达改变与疾病的关系。
临床应用的局限性
尽管这些研究提供了对糖尿病潜在病理生理学的生物学洞察,但目前尚无直接的精准诊断或治疗方法。
多样性研究的需求
大多数遗传学研究是在欧洲人群中进行的,因此需要在更广泛和多样化的人群中开展类似研究,以避免因缺乏多样性导致的健康差异,尤其是在糖尿病护理方面。
未来研究方向
研究人员对将心脏代谢和血糖特征的基因数据与2型糖尿病风险的基因数据结合起来很感兴趣。这些共享信号可能揭示潜在的组织和机制,通过这些机制,变异体会影响糖尿病或其并发症的风险。
聚类分析
通过不同聚类方法,研究人员正在识别2型糖尿病中常见的缺陷过程(如胰岛素作用、β细胞功能、血脂异常),并评估其临床效用。
20世纪90年代初,通过识别单基因糖尿病的突变,揭示了葡萄糖代谢与胰岛素分泌偶联机制的重要性。这些研究表明,关键的糖酵解酶如葡萄糖激酶的功能丧失突变影响胰岛素分泌。
转录因子HNF1A/HNF4A对内分泌胰腺的发育和维持至关重要,其发现为进一步研究胰腺和内分泌细胞发育的重要步骤奠定了基础。
基因变异的影响
罕见的完全渗透性突变在生命早期表现为糖尿病,而影响较小的等位基因也会增加2型糖尿病的风险。
胰腺功能的复杂性
研究发现外分泌和内分泌胰腺之间存在意想不到的联系。罕见的消化酶基因突变和与糖尿病相关的常见变异揭示了胰腺疾病(如胰腺炎和囊性纤维化)与内分泌细胞功能障碍之间的联系。
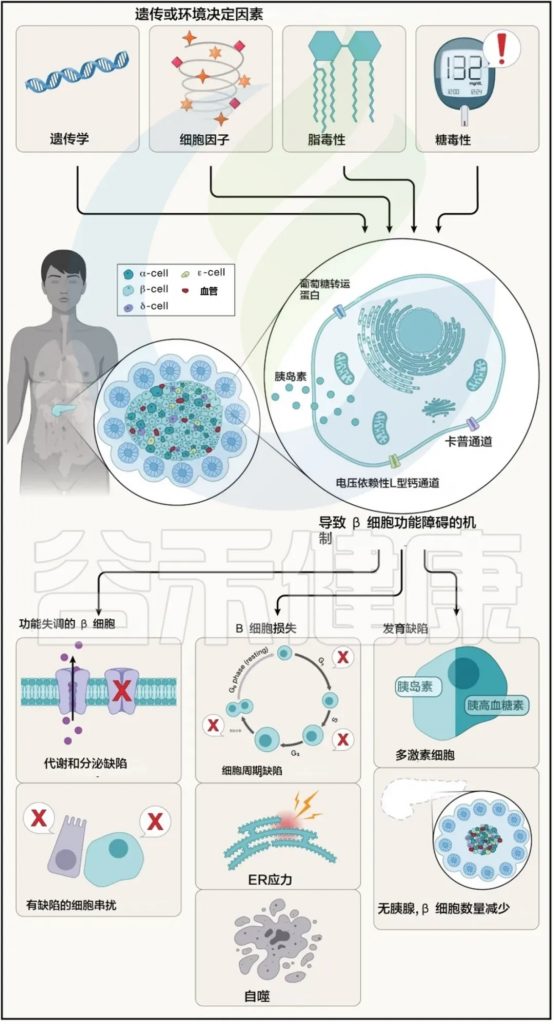
对β细胞功能受损的各种方式的机制理解得益于人类基因发现(下图)。
胰腺β细胞因环境和遗传因素受损的潜在方式示意图
Abel ED,et al.Cell.2024
提升β细胞功能的兴趣
由于β细胞在维持正常葡萄糖耐受性中的关键作用,提高“功能性β细胞质量”被视为治疗1型和2型糖尿病的重要策略。
潜在治疗靶点
人类遗传学研究支持K-ATP通道和葡萄糖激酶为改善胰岛素分泌的潜在靶点。
SLC30A8基因中的特定蛋白质变体(ZnT8的锌转运蛋白)主要在胰腺β细胞中表达,并被证明可保护个体免受2型糖尿病的侵袭,因此相关药物的开发在进行中。
GLP-1受体(GLP-1R)
虽然在GWAS证实其作为治疗靶点的有效性之前人们就已经对它进行了广泛研究,但人类遗传学为其在降低血糖和改善心脏代谢健康方面的作用提供了有力证据。
GLP-1R激动剂不仅有效控制血糖,还具有减肥和降低心血管死亡率的积极作用。
开发新疗法的挑战
GLP-1类药物的多重成功显示了从多个角度治疗疾病生物学的巨大潜力,但也增加了专注于改善β细胞功能新疗法开发的难度。
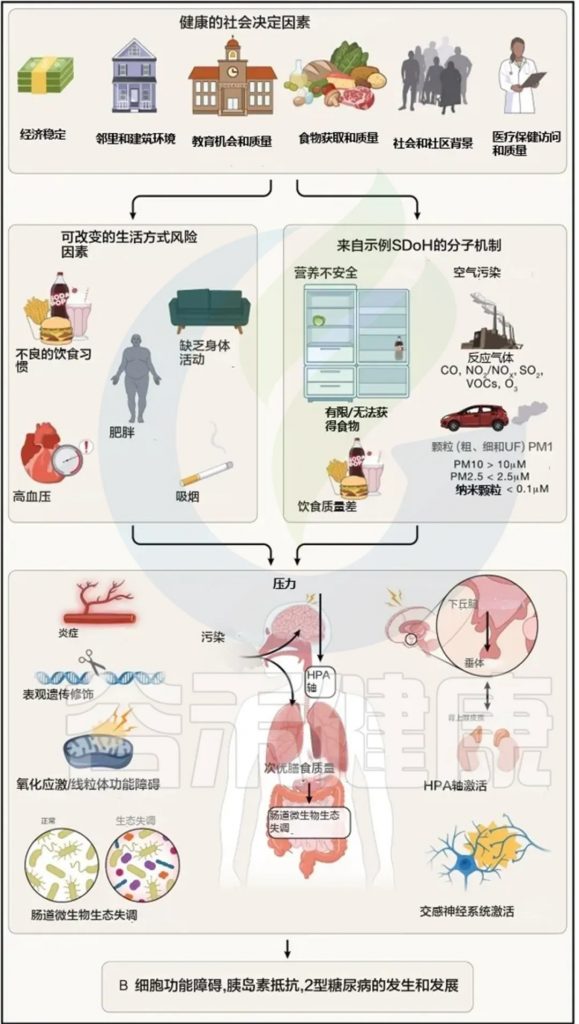
社会健康决定因素(SDoH)指的是影响健康的社会条件,包括经济、教育、食品安全、医疗保健等因素。它们对包括2型糖尿病在内的多种疾病的发病和进展有深远影响。
SDoH通过复杂的途径影响2型糖尿病的发展,从生活方式行为到分子机制(例如HPA轴激活、微生物群失调)。粮食不安全和空气污染等具体因素已经被证明与糖尿病有关,表明需要多层次的干预策略。
粮食和营养不安全
粮食安全被定义为“所有人在任何时候都能获得足够的食物以过上积极和健康的生活”。
营养安全进一步扩展为“能够公平、稳定地获取、负担得起和利用促进健康、预防和治疗疾病的食品和饮料的状态”,包括饮食质量和社会健康决定因素(SDoH)。
粮食不安全的影响:粮食不安全导致水果和蔬菜摄入减少,精制碳水化合物、饱和脂肪和添加糖摄入增加,整体饮食质量下降。长期不良饮食习惯导致氧化应激、炎症和脂肪组织扩张。
粮食不安全与增加的炎症、生物荷负和肠道微生物多样性降低有关。社会经济压力则加剧了这种状态,影响补偿行为,并激活炎症途径。
空气污染
空气污染是重大环境健康风险,社会经济地位较低的人群受影响更大。关键污染物包括臭氧 (O₃)、二氧化氮 (NO₂) 和各种颗粒物 (PM),如PM2.5。
对糖尿病的影响:空气污染与胰岛素抵抗、血糖紊乱、高脂血症和2型糖尿病的发病率增加有关。观察性研究与孟德尔随机化研究支持其因果关系。
机制:初级启动途径:包括氧化应激、淋巴细胞活化、组织内DAMP产生及直接影响胰腺β细胞等。
次级效应途径:涉及全身炎症、神经内分泌失调、肝脂肪变性以及肠道微生物群失调等。
共同的病理生理影响:无论是营养不良还是空气污染,均通过氧化应激、炎症反应、HPA轴激活等机制影响糖尿病的发展。
粮食不安全和空气污染等因素可能在从胚胎到婴儿期影响后代未来的糖尿病风险。饥荒和空气污染对母体的营养和污染暴露都有证据表明会影响后代的代谢健康。
研究和政策发展:需跨学科团队的合作来深度研究SDoH的病理生理影响,指导新的干预策略和政策制定,以提高糖尿病预防和管理的公平性。
总之,粮食不安全和空气污染通过复杂的生物和环境机制显著影响2型糖尿病的进程。理解这些机制将有助于开发更有效的公共卫生政策和临床干预措施。
Abel ED,et al.Cell.2024
大量临床前数据强调了大脑在控制体重以及易感人群中胰岛素抵抗和肥胖发展中的重要作用。尤其中枢神经系统(CNS)在控制血糖和2型糖尿病病理生理学中的重要性。
◮ 重要性与作用
大量临床前数据显示,大脑在体重控制、胰岛素抵抗(IR)、肥胖及2型糖尿病发病机制中扮演关键角色。其中肥胖是2型糖尿病的重要风险因素。
食欲和能量消耗的调节对于肥胖的发生至关重要,受中枢系统全面调控。
肠道激素如生长素释放肽和瘦素,以及肠道微生物群的变化,在调节过程中起重要作用。
已在下丘脑和脑干中对这些调控神经回路的了解取得显著进展。
临床研究
人类研究重点关注中枢及自主神经系统如何整合体重调节及葡萄糖代谢,尤其在维持循环葡萄糖浓度中的作用。
动物模型研究
动物模型研究提供了许多见解,显示迷走神经及中枢神经系统回路对营养感知的重要性。
研究表明脂肪或糖摄入与多巴胺释放及暴饮暴食行为之间存在关联。
大脑与外周之间相互作用的示意图
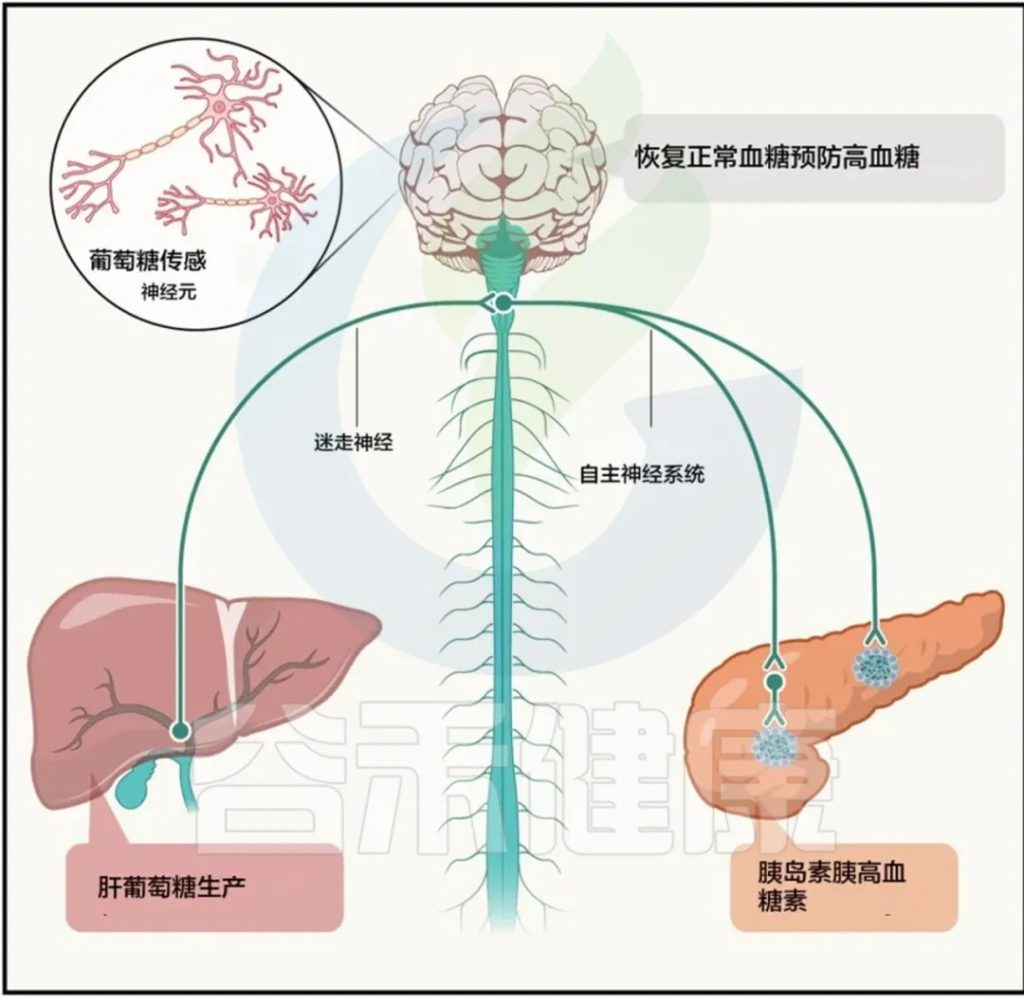
Abel ED,et al.Cell.2024
注:这些见解大多来自动物模型研究
为了更好地科普中枢神经系统(CNS)在糖尿病和代谢调节中的作用,可以从以下几个方面进一步理解:
基本概念
中枢神经系统(CNS)不仅仅是控制思维和行为的中心,它还在调节身体的代谢功能中发挥重要作用。特别是在血糖调节方面,CNS通过调控肝脏的葡萄糖生成和分解来维持血糖的稳定。
机制
下丘脑是CNS中一个关键区域,它通过神经信号影响胰腺的功能,调节胰岛素的分泌。胰岛素是降低血糖的主要激素,因此下丘脑的调控对于维持正常血糖水平至关重要。
胰岛素的作用
胰岛素不仅在外周组织中发挥作用,它在大脑中也有重要功能。研究表明,胰岛素可以通过鼻内给药直接作用于大脑,影响胰岛素的分泌和全身的胰岛素敏感性。
个体差异
不同个体对大脑胰岛素的反应存在差异,这种差异可能影响到胰岛素的分泌和代谢功能。这种差异也与肥胖和胰岛素抵抗(IR)有关。
FGF的潜力
成纤维细胞生长因子(FGF)在动物实验中显示出通过作用于大脑来缓解糖尿病的潜力。这种方法不依赖于体重减轻,而是直接改善葡萄糖代谢。
药物的CNS作用
一些用于治疗2型糖尿病的药物,如GLP-1受体激动剂,通过中枢神经系统发挥作用,影响食欲、体重和胰岛素分泌。
关联性
2型糖尿病与认知功能受损和神经退行性疾病(如阿尔茨海默病)之间存在关联。研究发现,糖尿病患者的大脑胰岛素反应性可能受损,这与认知功能下降有关。
潜在治疗
鼻内胰岛素和GLP-1受体激动剂在临床研究中显示出神经保护作用,可能降低痴呆症的发病率。
更具脑渗透性的药物
开发能够更好地穿透血脑屏障的药物,可能增强其神经保护作用,同时减少不良反应。
共同途径的探索
由于糖尿病和神经退行性疾病的发病率随着年龄增长而增加,研究共同的病理机制可能带来同时治疗这两种疾病的新方法。
胰岛素抵抗(IR)
当胰岛素无法有效地降低血糖时,称为胰岛素抵抗。这种情况不仅影响糖代谢,还导致脂肪组织释放更多的游离脂肪酸(FFA)进入血液。
脂解作用增加
在IR条件下,脂肪组织经历脂肪分解增加,产生更多的FFA。这些游离脂肪酸流入血液并扩散到其他组织,如肝脏和骨骼肌,进一步导致这些组织的发展胰岛素抵抗。
二酰甘油的作用
二酰甘油(DAG)是一种重要的信号分子。研究表明,在胰岛素抵抗的状态下,血浆中DAG水平升高。DAG可以与细胞膜上的蛋白激酶Cε (PKCε)结合,从而使胰岛素受体发生抑制性磷酸化。这一过程会限制胰岛素受体的激酶活性,削弱胰岛素的信号传导,导致细胞对胰岛素的反应降低。
特异性结合:DAG的不同立体异构体对作用靶点的结合亲和力不同,其中sn-1,2 DAG与PKCε结合最强,定位在质膜上,而其他异构体如sn-1,3 DAG和sn-2,3 DAG倾向于定位在脂滴和内质网(ER)。
神经酰胺的作用
神经酰胺是另一种导致胰岛素抵抗的脂质。高FFA水平促进长链神经酰胺(如C16和C18)的产生。神经酰胺通过激活特定的激酶,如蛋白激酶C ζ (PKCζ)和蛋白磷酸酶2A (PP2A),抑制关键信号分子Akt的磷酸化。这种抑制作用破坏了正常的胰岛素信号传导。
选择性影响:神经酰胺特异性地促进胰岛素抵抗,这是因为其他类似脂类(如二氢神经酰胺和鞘磷脂)未能在实验模型中表现出同样的效果。
异位脂质沉积
骨骼肌和肝脏中DAG和神经酰胺的积累会加剧胰岛素抵抗。这些组织的『选择性胰岛素抵抗』意味着通常应该增加葡萄糖吸收的组织变得不再敏感,反而可能继续将葡萄糖转化为脂质储存。
加速糖尿病的进展
当骨骼肌和肝脏对胰岛素的敏感性降低时,会加速糖尿病的进展。这些脂质代谢产物的积累不仅影响胰岛素信号传导,还可能引发脂质毒性,损伤细胞功能并加重代谢紊乱。
以上细节描述展示了脂质介质如何在分子水平上影响胰岛素信号通路,从而推动全身性胰岛素抵抗的发展。这些见解为开发针对性更强的干预措施和治疗策略提供了依据,以改善代谢健康并减缓或逆转糖尿病。
下面是肥胖和脂肪组织通过多种机制驱动胰岛素抵抗(IR)的详细总结:
1.脂肪酸羟基脂肪酸酯与胰岛素敏感性
脂肪酸羟基脂肪酸酯(FAHFA)的角色:FAHFA是一类由两个脂肪酸通过酯键结合形成的复合脂质。研究表明,FAHFA可以改善胰岛素敏感性,其水平在肥胖状态下和2型糖尿病中会降低。
机制:FAHFA通过与某些代谢重要组织中的G蛋白偶联受体结合,起到调节小鼠胰岛素敏感性、脂肪生成和能量消耗的作用。此作用途径表明FAHFA可能通过影响受体来调控广泛的代谢过程。
2.脂肪甘油三酯脂肪酶与FAHFA
脂肪甘油三酯脂肪酶(ATGL)的双重角色:ATGL是一种负责脂肪分解的酶,被认为可能在FAHFA代谢中也发挥作用。
ATGL可能充当FAHFA的合酶,通过改变ATGL功能,提供了FAHFA与2型糖尿病中的脂肪分解之间的潜在联系。调节ATGL功能的变化可能影响FAHFA的合成和分解。
3.前馈循环与全身性胰岛素抵抗
前馈循环:肥胖状态下,脂肪组织中多种信号分子的变化(包括FAHFA的减少)会驱动一种前馈的代谢循环。这种循环会进一步加剧全身胰岛素抵抗。
注释:代谢生理学中,”前馈循环” (feed-forward loop) 指的是一种生物学过程,其中某一信号或变化会增强或放大某一响应,而这种响应又会使初始信号或变化更加显著。上文中前馈循环是指肥胖状态下脂肪组织中多种信号分子的变化(例如 FAHFA 的减少)导致的一系列代谢事件。这些变化不仅直接影响机体的代谢状况,还通过促进某些过程或信号的放大,进一步加剧全身胰岛素抵抗。
具体来说,脂肪组织中信号分子的变化作为初始刺激,会引发代谢反应或变化,这些代谢反应可能通过各自的信号机制,反过来进一步促进初始信号或加大初始变化。如果这种循环不被打断,就可能导致长期的代谢失调,比如全身性的胰岛素抵抗,从而增加糖尿病等代谢疾病的风险。
4. 脂肪组织在全身性胰岛素抵抗中的作用
脂肪组织重塑:肥胖引起的脂肪组织重塑是全身性胰岛素抵抗、炎症以及葡萄糖和脂质代谢异常的关键驱动因素。
5. 高血糖与胰岛素抵抗的恶性循环
高血糖的影响:高血糖本身会通过增加己糖胺生物合成途径的通量,加剧胰岛素抵抗。这一途径生成尿苷二磷酸-N-乙酰葡萄糖胺 (UDP-GlcNAc),是N和O连接糖基化的前体。
O连接糖基化:包括Akt在内的胰岛素信号蛋白的O连接糖基化会进一步诱导胰岛素抵抗,形成恶性循环。
在胰岛素抵抗状态下,脂肪细胞的葡萄糖摄取功能受损。这种情况与脂肪细胞释放的胰岛素敏感因子和复合脂质的变化有关,这些变化会影响其他组织对胰岛素的响应。
肝脏和骨骼肌是胰岛素作用的主要目标组织,在胰岛素抵抗状态下,其糖代谢功能受损,尤其是肝脏的葡萄糖输出增加和骨骼肌的葡萄糖摄取减少。这些机制是糖尿病患者血糖水平升高的主要驱动因素。
糖原合成减少
在胰岛素抵抗的早期阶段,骨骼肌中胰岛素介导的糖原合成减少。这是因为胰岛素信号传导受损,影响了糖原合成酶的活性。
GLUT4易位受损
胰岛素通常促进葡萄糖转运蛋白4(GLUT4)从胞内储存池转移到质膜,以增加葡萄糖摄取。然而,在胰岛素抵抗状态下,这一过程受损,导致葡萄糖摄取减少。
葡萄糖氧化减少
由于胰岛素信号传导的缺陷,骨骼肌中葡萄糖的氧化能力降低,这进一步影响能量代谢。
长期影响
随着时间推移,骨骼肌胰岛素抵抗会导致肌肉萎缩、运动能力下降以及线粒体功能和质量的下降。
肝糖输出(HGP)增加
肝脏胰岛素抵抗的主要表现是肝糖输出增加。这是因为胰岛素对糖异生基因的抑制作用受损,导致肝脏中糖异生增加。
脂质积累
胰岛素抵抗还促进肝脏中脂质的积累,进一步影响肝脏功能。
组织间通讯的理解
未来的研究需要深入了解不同组织间的通讯机制,包括外泌体等新型介质在内的作用。
脂质动员机制
研究控制组织和细胞器之间脂质动员的机制,以及未表征脂质的功能,将有助于揭示2型糖尿病中的脂质失调。
复杂病理生理学的探索
进一步探索这些途径在持续胰岛素抵抗中的复杂病理生理学影响,将有助于开发新的治疗策略,改善代谢稳态。
综上所述,理解骨骼肌和肝脏的胰岛素抵抗机制及其与脂肪组织的相互作用,对于揭示2型糖尿病的发病机制和寻找新的治疗靶点至关重要。
近年来,越来越多的研究揭示了2型糖尿病与代谢功能障碍相关脂肪肝病(MASLD)之间的紧密联系,除了影响血糖稳态外,还对心血管并发症以及其他健康问题有显著的影响。
病理生理学背景
糖尿病患者常伴有肝脏代谢功能障碍,这是血糖稳态受损和糖尿病心血管并发症的主要因素之一。肥胖引发这些患者肝脏葡萄糖和脂质的异常增加。
MASLD的演变
MASLD从单纯脂肪变性(最初是可逆且普遍的状态)到代谢功能障碍相关脂肪性肝炎(MASH),可以进展至纤维化,这在严重情况下是主要的死亡原因。
下面是对2型糖尿病和MASLD相互作用的总结:
1.多重打击假说
这一理论解释不同患者发展严重并发症的原因,重点在于脂质蓄积后非实质细胞(NPC)的异常激活。对于早期疾病,GLP-1 基药物疗法可能有效,但对晚期纤维化无明显效果。
2.过量从头脂肪生成(DNL)
过量从头脂肪生成(DNL)在2型糖尿病患者中明显增加。健康人群中,胰岛素通过Akt信号通路抑制肝糖输出(HGP),同时激活脂肪生成的促进元素,如SREBP-1c。但在胰岛素抵抗状态下,FoxO1抑制失效增加葡萄糖生成,然而胰岛素仍然能推动DNL。
尽管胰岛素信号转导的某些功能失效,DNL却仍然活跃。这可能由于糖尿病患者CHREBP诱导Akt磷酸化调控机制存在异常,尤其是PHLPP2磷酸酶水平降低,导致了过量DNL。
3.胰岛素信号转导的动力学变化
在慢性高胰岛素血症背景下,正常的胰岛素信号分叉模型可能发生变化,影响胰岛素在早期和晚期阶段的作用。
早期阶段:胰岛素的快速作用通过抑制FoxO1来减少葡萄糖生成。
晚期阶段:延长的Akt活性则促进了DNL和脂质合成,潜在机制包括细胞自主信号、自主脂肪信号以及肠道介导的信号。
4.双向风险与相互促进
2型糖尿病和MASLD不仅拥有共同的风险因素,还可能通过如上机制双向增加各自的风险。研究显示,肝脏脂肪过多与2型糖尿病高度相关,即便在调整了BMI和其他潜在混杂因素后,二者之间的联系依然显著。
5.临床与研究启示
由于代谢功能障碍相关脂肪肝病(MASLD)在肥胖率较高的人群中表现为一种日益增长的健康挑战,当前的研究重点在于理清组织间通讯的复杂网络、揭示潜在的细胞机制、探索治疗新策略以及更好地管理代谢性肝病。
通过全面的机制研究和临床分析,我们可以更好地理解2型糖尿病与MASLD的复杂交互机制,为治疗和预防这些相关病理状态带来新的希望。
在2型糖尿病与代谢功能障碍相关脂肪肝病(MASLD)的研究中,理解肝脏脂质堆积及其进展至肝脏病变的过程尤为重要。以下是详细汇总和对当前研究状况的总结:
1.肝脂质过量与疾病进展
影像学发现:许多2型糖尿病患者在影像学检查中展示了肝脂质过量。然而,哪些患者将发展为有临床意义的肝脏疾病,以及进展的时间和诱导因素,仍不明确。
遗传因素:基因组广泛关联研究(GWAS)揭示了一些与体重和肝脏脂质积累相关的常见风险等位基因(如FTO、PNPLA3、TM6SF2和APOB)。然而,这些基因标记在预测疾病进展为代谢功能障碍相关脂肪性肝炎(MASH)方面的效能有限。
2.脂质管理障碍
2型糖尿病和MASLD患者的肝细胞可能有储存脂质的倾向,但难以在不损伤细胞的情况下管理过量的脂质。这导致了细胞的炎症反应和纤维化。
3.肝细胞的信号贡献
肝细胞在疾病中的作用:研究表明肝细胞不仅在血糖调节中起作用,还通过分泌促进NPC浸润和活化的趋化性和纤维化细胞因子,直接参与肝脏炎症和纤维化过程。
Notch信号的再激活:这是2型糖尿病和MASLD患者肝细胞炎症的一部分,影响HGP和DNL的增加。
4.临床研究和治疗前景
治疗性干预:使用如GalNAc修饰的反义寡核苷酸或siRNA,可以靶向性调制肝细胞信号通路,有可能改善病情。
5.当前研究的主要方向和挑战
高胰岛素血症的作用:2型糖尿病患者IR导致的高胰岛素血症,与肝脏DNL正相关,可能是MASLD病理机制之一。现有研究正在探讨抑制胰岛素分泌的策略,但其在糖尿病患者中的适用性仍需验证。
其他激素和营养因素:胰高血糖素、果糖和胆固醇也可能对肝脏脂质生成有影响。此外,肝交感神经系统的参与是否在脂质生成功能中有重要贡献,需要进一步探索。
通过这些研究,肝脏的代谢调节能力、遗传和环境因素的交互作用构成了2型糖尿病和MASLD在病理进程中的复杂图景。理解这些机制对于开发有效的治疗方案和风险评估方法至关重要。
尽管最近取得了进展,但许多问题依然存在,包括一下几点。
1.高胰岛素血症和非激素因素的作用
2型糖尿病的胰岛素抵抗(IR)显示出代偿性高胰岛素血症。人类数据表明血浆胰岛素水平与肝脏DNL正相关,动物研究证实胰岛素作用时机不当可能导致MASLD。有趣的是,奥曲肽通过阻断胰岛素分泌降低了大鼠的DNL标记物和肝脏甘油三酯。
目前,这一概念正在非糖尿病个体中使用二氮嗪(NCT05729282)进行测试,其结果是否适用于T2D患者尚不明确。其他激素如胰高血糖素也通过促进糖原分解和降低肝脏脂质起作用。
此外,果糖和胆固醇可能影响肝脏脂质生产。最后,非营养和非激素的肝糖输出(HGP)决定因素,如交感神经对肝脏的影响及其对脂质生产的共调节作用,仍不清楚。
2.脂肪性肝炎的空间决定因素
组织异质性:肝脏作为一种异质性组织,由于不同区域的氧张力和营养状态,产生了肝内糖异生和脂肪生成功能的分区。这种分区影响了MASH的区域特异性,表现为中枢周围或门管周围类型,后者尤为常见于儿童患者。
区域性亚型:代谢综合征和2型糖尿病患者倾向于发生门管周围类型的疾病。这种区域亚型与代谢和肝脏病理的发展程度相关,但其机制尚不清楚。针对肝脏区域特定通路(例如Notch、法呢醇X受体[FXR]、甲状腺激素受体[TR]和过氧化物酶体增殖激活受体[PPAR])的治疗可能提供新的干预策略。
3.纤维化消退的途径
尽管对肝脏促炎和纤维化途径的理解有所增加,但对纤维化清除及肝细胞途径影响纤维化消退的研究较少。我们推测,所有肝细胞决定的“纤维化开启”信号都有相应的“纤维化关闭”信号。
系统研究回归途径对肝纤维化的影响,类似于动脉粥样硬化病变的解决,可能带来重要的影响。对于部分对肠促胰岛素治疗抵抗的T2D患者,新的治疗靶点可能特别有价值。
4.双向肝细胞-非实质细胞串扰
虽然肝细胞在脂质过载中的作用被强调,但非实质细胞(NPC)对肝细胞功能也有显著影响。例如,肝星状细胞不仅是肝细胞再生的决定因素,还是一个潜在的调节因子。在2型糖尿病中,免疫细胞增加从而改变胰岛素敏感性。
6.对脂质超载的遗传适应
近来的研究揭示了MASLD/MASH患者肝细胞中FOX01的体细胞突变,这些突变可能是一种保护机制,减轻脂质超载的损伤。这种基因适应可能说明MASLD与2型糖尿病的关联。
7.与心血管疾病的关系
肝脏脂质过多增加了肝病相关死亡率的风险,但与2型糖尿病患者类似,MASLD/MASH患者的主要死因是心血管疾病(CVD)。鉴于直接加速CVD的常见并发症,需在临床前动物模型和人类中进行进一步机制研究以揭示其潜在机制。
糖尿病是一种影响全身的慢性疾病,会对多种系统造成广泛且复杂的影响,显著增加患病率和死亡率。以下是对糖尿病相关代谢异常和其主要并发症的详细分析。
增高的风险:糖尿病患者患动脉粥样硬化性心血管疾病(ASCVD)的风险增加2至5倍。
其他风险因素:包括高血压、血脂异常、肥胖和代谢综合征。
糖尿病性心肌病:糖尿病导致特有的心脏结构和功能异常,不完全依赖于冠状动脉疾病(CAD),而与异常代谢环境直接相关。
综合风险:没有单一机制可以解释CVD风险的增加,糖尿病引起的多种风险因素复杂相互作用导致CVD。
机制:与内皮细胞(EC)和血管平滑肌细胞(VSMC)功能障碍有关。
糖尿病影响:特征是内皮功能障碍,包括一氧化氮合酶功能下降和NO缺乏。
动脉粥样硬化驱动因素:糖尿病通过激活髓系细胞和炎症细胞(如单核细胞、巨噬细胞)的生成,直接加剧动脉粥样硬化。
风险因子和生物标志物:LDL胆固醇、血脂异常、HbA1c、肾功能和身体活动为疾病预测因子。新型生物标志物(如线粒体代谢物)可能用于风险分层。
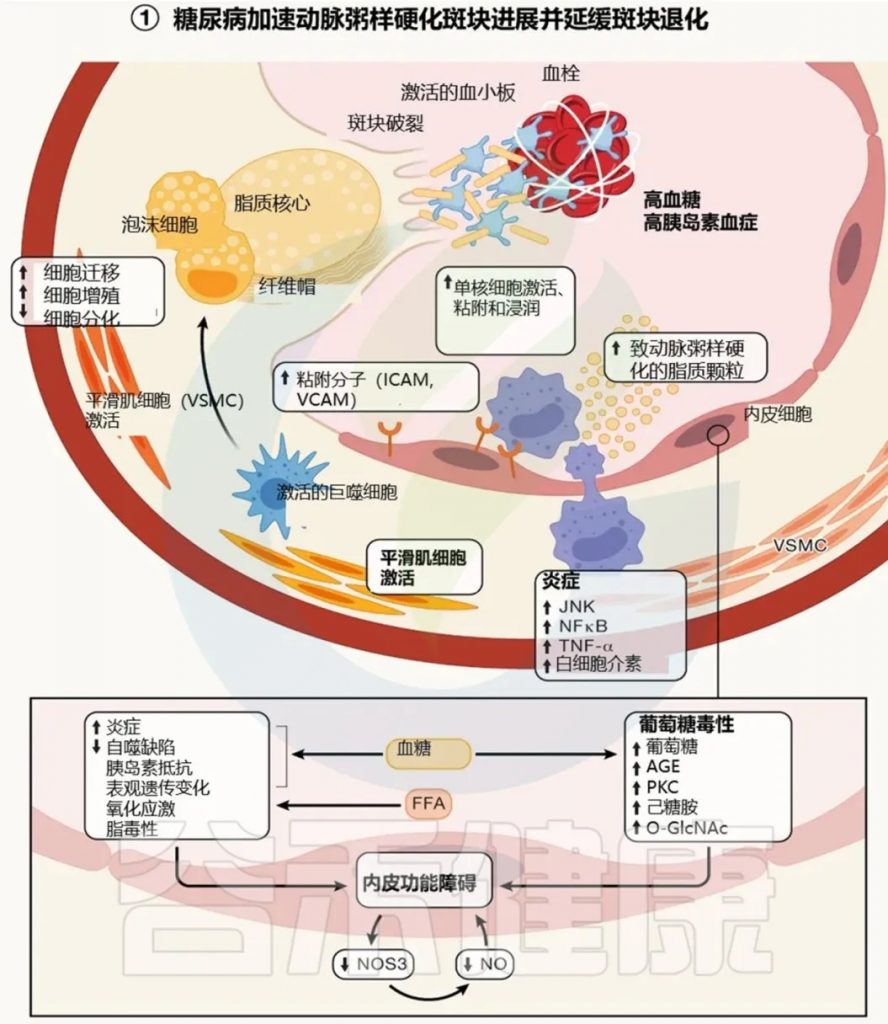
Abel ED,et al.Cell.2024
风险增加:糖尿病增加心力衰竭风险,这与冠状动脉疾病(CAD)风险增加无关。
机制:碳毒性(脂毒性和糖毒性)
氧化应激
线粒体生物能量学受损
线粒体解偶联
心肌兴奋-收缩偶联受损
促纤维化途径激活
选择性胰岛素抵抗引起的肥大性信号通路激活
人类研究证据:心脏移植研究显示,正常供体心脏在移植到糖尿病患者体内后数月内出现代谢异常。
观察到甘油三酯超载、神经酰胺等有毒脂质积聚、线粒体呼吸功能不全、氧化应激和炎症。
注:前驱糖尿病患者也观察到线粒体氧化缺陷,二甲双胍治疗可能减轻这些变化。
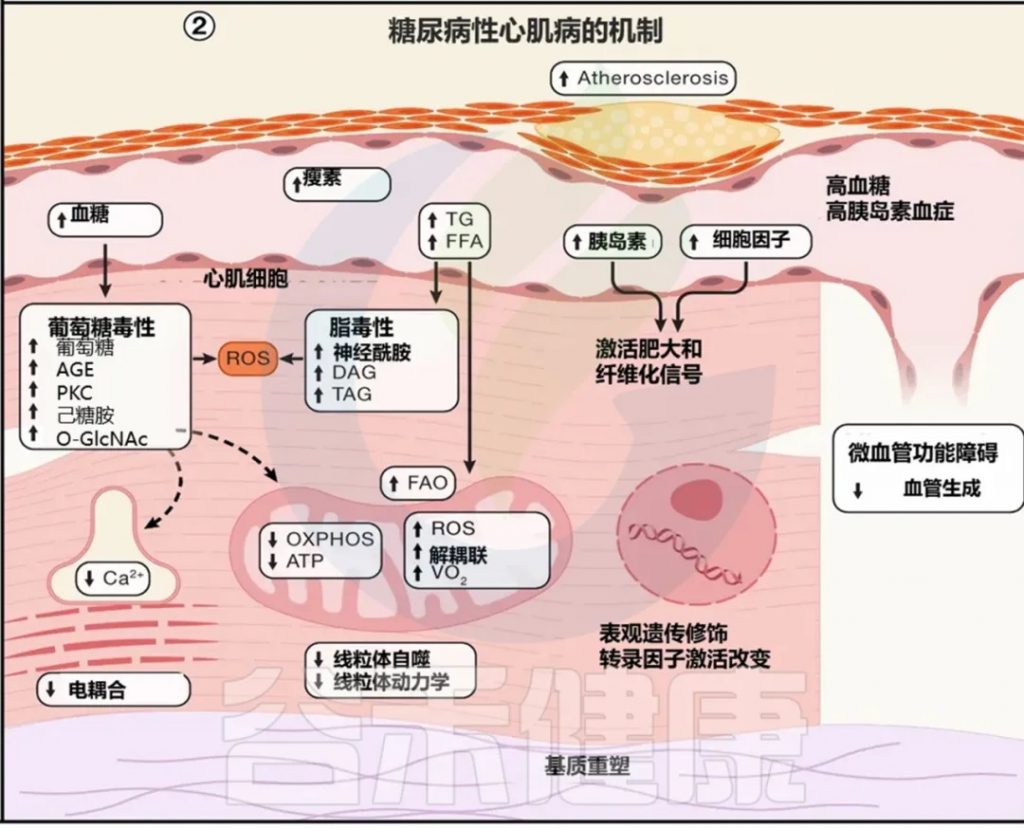
Abel ED,et al.Cell.2024
特征:糖尿病降低多种促血管生成因子的表达,导致血管生成信号通路紊乱。
影响:增加外周血管疾病和严重肢体缺血的风险。
机制:VEGF抵抗
一氧化氮信号受损
血管生成干细胞前体水平降低
周细胞丢失
微小RNA和长链非编码RNA的失调
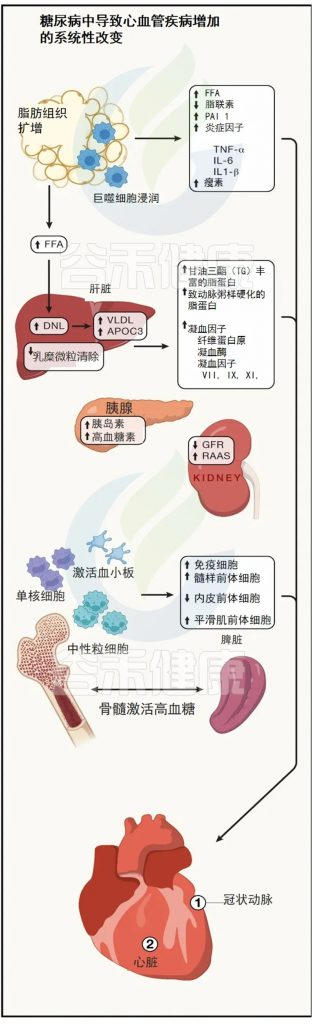
Abel ED,et al.Cell.2024
特征:白蛋白尿和估计肾小球滤过率(eGFR)降低。
患病率:约40%的糖尿病患者会发展为DKD。
肾血管功能障碍:肾小球高滤过是早期特征之一;
肾小管肾小球反馈机制导致肾小球传出动脉收缩。
肾小球和肾小管上皮细胞变化:
足细胞代谢改变,氧化应激增加。
RhoA/Rac1通路导致足突消失。
mTOR和生长因子信号改变导致足细胞增大。
足细胞丢失是疾病进展的关键步骤。
近端小管(PT)细胞:
高代谢活性,负责大量水和盐的重吸收。
初期细胞大小和数量增加,后期出现能量耗竭和细胞身份丧失。
线粒体损伤激活炎症途径。
小结
总的来说,糖尿病通过多种复杂的机制影响心血管系统和肾脏,涉及代谢异常、血管功能障碍、炎症反应和表观遗传变化等多个方面。
这些发现为理解糖尿病并发症的发生机制和开发新的治疗策略提供了重要的科学基础。
传统疗法的局限:早期治疗通常在T1D的3期开始,对于改变疾病进展的效果有限。
新进展:创新的分期系统为早期干预提供了框架,报告聚合抗CD3单克隆抗体teplizumab治疗延迟T1D进展的结果。这一研究促使FDA批准teplizumab作为首个T1D疾病改良疗法。
病毒传播与诊断挑战:目前缺乏统一的筛查指导方针,正测试多种自身抗体筛查策略。
胰岛素管理技术(如优化的药物动力学胰岛素、胰岛素泵和持续血糖监测设施)不断革新。
β细胞替代疗法:胰腺或供体胰岛移植显示出β细胞替代的可行性,但供体资源有限。
干细胞技术:通过多能干细胞分化得到的β细胞有望克服移植局限性,Vertex制药公司正在测试相关疗法(VX-880)。
异质性挑战:T2D患者的疾病表现由于遗传和环境因素而异,例如,非洲-加勒比和亚洲人群的T2D表现差异明显。
◮ 精准医疗的方法
临床分层工具:如BMI和eGFR用于HbA1c反应的预测,最新的研究表明此类因子可以指导选择更有效的治疗方法。
复杂数据整合:利用机器学习分类法如集群分析,识别糖尿病亚型,与特定并发症风险相关。
◮ 临床实施与研究挑战
标准化的必要性:研究需要一致的方法来评估精准治疗的优劣及其经济性。
证据差距:精准糖尿病治疗需要更多随机对照试验来证明其临床优势和成本效益。
精准医疗成功的例子:例如葡萄糖激酶突变的单基因糖尿病无需药物治疗,而HNF1A突变可用磺酰脲类药物有效管理。
综合来看,1型糖尿病的治疗正在向提前预防和细胞治疗方向发展,而2型糖尿病的精准医疗方法强调对不同人群亚型的特定管理。
随着研究的深入和技术的进步,这些策略有望显著改善糖尿病患者的治疗效果和生活质量。
在2型糖尿病的精准医疗和全球健康公平领域,取得了许多令人瞩目的成就,但仍面临资源可及性不均与种族多样性不足等挑战,并且新型疗法不断涌现,进一步推动病情管理和并发症预防。
◮ 资源限制与成本效益
2型糖尿病精准医疗是否能在不同资源环境中实施仍不明确,当前诊断和治疗的费用较高,尤其在中低收入国家。
如果精准医疗能提高治疗精度,减少资源浪费,则可能长期节约成本,但这些长期获益难以精准量化。
◮ 全球资源差异
许多中低收入国家患者难以获得基本药物,更复杂的精准医疗诊断尚难普及。简便的分层方法和决策支持工具可能在这些地区更具实用性。
糖尿病护理的差距往往影响社会经济地位低、少数民族群体。未经过周密计划和执行的精准医疗可能导致不平等加剧。
◮ 种群多样性的影响
研究多样性不足:大多数精准医疗研究在欧洲白人群体中进行,跨种族的应用性受限。需在不同种族背景下进行更多研究,以开发具有全球代表性的解决方案,适应不同遗传机制。
基因组研究局限:多样性缺乏的基因组研究可能导致偏见。例如,某些族群的2型糖尿病特征存在重大差异。开发跨祖先适用的基因风险评分,不同族群的参与和持续研究至关重要。
总体来看,精准医疗已经在2型糖尿病领域取得长足进步,但其广泛和公平实施受到资源、技术和种族多样性等多个因素的限制。未来的研究应致力于开发合适的工具和管理策略,以改善全球范围内的健康结果。
药物创新
GLP-1受体激动剂、DPP-4抑制剂和SGLT-2抑制剂在改善血糖及心血管、肾脏健康方面展现无与伦比的效果。
GLP-1RA的增强版本显示出非凡的减肥和心血管保护作用。SGLT-2抑制剂同样有助于不同心肾健康目标。
开发多激动剂如Tirzepatide(GIP受体-GLP-1R共激动剂),有效性超越单一疗法。此类疗法在减重和改善心血管风险方面效果显著,开创了治疗新方向。
基于GLP-1的治疗心脏代谢和神经退行性疾病
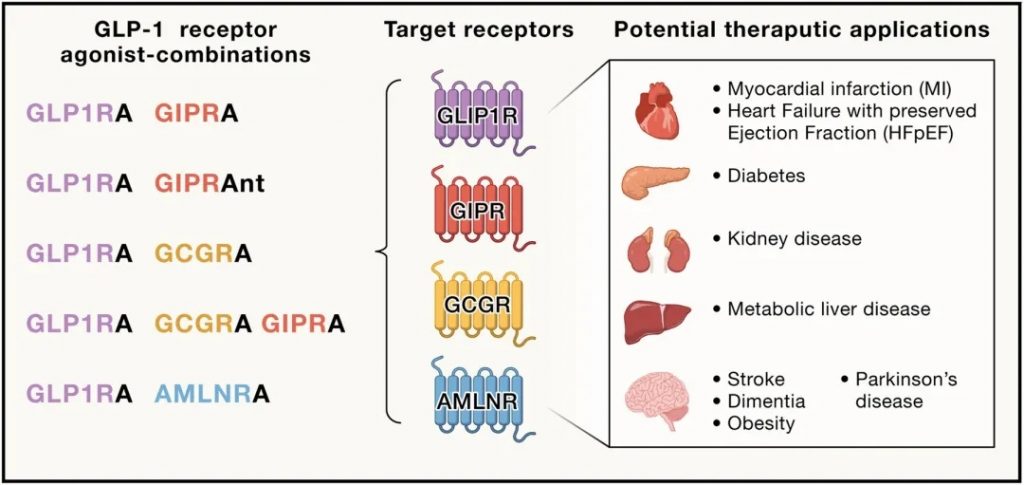
Abel ED,et al.Cell.2024
针对不同疾病机制的新疗法和联合疗法的临床试验持续进行,探索能够提供更高效、个性化处理方案的创新疗法。
多种基于GLP-1的联合疗法目前正处于临床后期开发阶段,期待它们在提高血糖控制和体重减轻效果的同时,继续展现心血管益处。这些治疗选项包括:
合成及联合应用疗法
-卡格列肽与索马鲁肽每周一次联合使用;
-胰高血糖素受体GLP-1R共激动剂如survodutide;
-GIP受体拮抗剂—GLP-1R激动剂抗体;
-三联胰高血糖素-GIP-GLP-1R多激动剂。
注:卡格列肽是一种肠促胰岛素激素,用于治疗2型糖尿病。
索马鲁肽,英文名称 “Semeglutide”,是一种新型的,长效的,每周皮下注射一次的 GLP-1 类似物,是基于利拉鲁肽基本结构而开发的长效剂型,其治疗2型糖尿病的效果更好。
新兴口服疗法
-包括danuglipron和orforglipron在内的小分子口服GLP-1R激动剂,以及ECC5004和GSBR-1290等其他小分子GLP-1RA。
-高剂量口服索马鲁肽(每天高达50毫克)与新配方吸收促进剂的应用。
这些创新药物不仅可能增强降糖和减重效果,还可能在外周动脉疾病、代谢性肝病、神经退行性疾病等领域拓展GLP-1药物的应用。
此外,对成瘾相关行为、遗传性肥胖、多囊卵巢综合征、1型糖尿病等多种适应症的研究也在进行之中。未来十年有望出现更为便捷和有效的GLP-1药物,这些药物的广泛适应症及安全性将通过更大规模临床试验的验证,为更多患者提供治疗选项。
随着糖尿病大流行的发展,我们对病理生理学以及治疗和预防方法的理解也呈指数级增长。目前的知识为提高识别增加β细胞功能障碍易感性标志物的特异性奠定了基础,特别是在肥胖环境中。
我们对大脑在体重调节中的作用以及脂肪组织分泌的新因子的理解可能有助于改进治疗或预防肥胖的方法。增加对肝功能障碍对胰岛素抵抗(IR)贡献的理解以及增加对代谢功能障碍相关肝病的理解代表了进一步研究的重要领域,以避免可能成为日益流行的肝功能衰竭。
心血管和肾脏疾病仍是糖尿病的主要死亡和发病因素,复杂的病理生理学涉及多器官系统和全身环境的交互作用。
糖尿病大流行由环境和社会因素推动,需综合管理。治疗进展为预防或治愈1型糖尿病和治疗2型糖尿病带来希望,不仅改善代谢稳态,还降低心肾疾病风险。
最后,随着我们了解和开发出识别导致糖尿病及其并发症的潜在异质性的工具,我们将为有针对性的治疗和预防策略奠定基础,以优化其在不同人群和医疗资源中的应用。
参考文献:
Abel ED, Gloyn AL, Evans-Molina C, Joseph JJ, Misra S, Pajvani UB, Simcox J, Susztak K, Drucker DJ. Diabetes mellitus-Progress and opportunities in the evolving epidemic. Cell. 2024 Jul 25;187(15):3789-3820.