-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康

当地时间12月19日,微软联合创始人、亿万富翁比尔·盖茨发布了对来年的年度预测,称 2024 年将是一个“转折点”。
在这封长达 10 页的信中他展示了对人工智能领域的更多创新、婴儿营养不良问题的突破、气候变化谈判的进展等多方面的期待。
人工智能可以让世界变得更加公平。盖茨对人工智能的预测超越了去年的超声波预测,他断言人工智能的进步将广泛改善全球健康,同时促进创新。
人工智能可以帮助世界各地对抗抗生素耐药性疾病,识别高风险妊娠并估计孕龄等,他预计人工智能在开发新药、诊断疾病和增强教育资源方面将发挥至关重要的作用。
盖茨表示,世界在利用肠道微生物补充剂来解决儿童营养不良方面即将取得突破。
本文我们来看看盖茨眼中的儿童营养不良问题及解法,盖茨预计,随着对微生物组的深入研究,人们将能够开发出以微生物为基础的新型营养治疗方案,这将给解决全球儿童营养危机带来重要进展。
期待已久的营养不良问题的突破即将到来
在盖茨基金会,我们愿意下大赌注。我们知道每一次冒险都可能没有回报,但这没关系。我们的目标不仅仅是逐步取得进展。我们的目标是将我们的努力和资源投入到重大项目中,这些项目一旦成功,就能拯救和改善生命。
当你下一个大赌注时,你往往要等待很长时间才能看到它是否有回报。当你终于意识到它会成功时,那种感觉是难以置信的。我最兴奋的一次豪赌就接近了这一时刻:利用我们对肠道微生物群的了解来预防和治疗营养不良。
经常有人问我,如果只能解决一个问题,我会选择什么。我的答案不变:营养不良。这是世界上最严重的健康不平等现象,大约每四个儿童中就有一个受到影响。如果在生命的头两年得不到足够的营养,身体和智力都无法正常发育。通过解决营养不良问题,我们可以减少导致儿童死亡的最大因素之一。
营养不良的原因远比没有得到足够的食物要复杂得多。大约15年前,研究人员注意到脊髓灰质炎等口服儿童疫苗在营养不良率高的地区效果不佳,他们开始怀疑生活在肠道中的微生物群可能在其中发挥了作用。很明显,有什么东西妨碍了它们被正常吸收。
这种怀疑在2013年得到了证实,当时生物学家杰夫·戈登(Jeff Gordon)发表了一项有里程碑意义的研究,关于马拉维一对双胞胎婴儿的微生物群。微生物群不仅是健康的副产物,还是健康的决定因素。这是第一条重要线索,表明我们或许可以通过改变肠道微生物群来减少营养不良问题。
经常有人问我,如果只能解决一个问题,我会选择什么。我的答案不变:营养不良
在过去的十年里,我们对肠道微生物群的了解比之前的1000年还要多。我们发现,生活在肠道中的细菌可能处于功能失调状态,从而导致炎症,使人无法吸收营养。我们发现,如果及早干预,就能最大程度地改善肠道微生物群。
在人类发育过程中最先出现的肠道细菌之一叫做婴儿双歧杆菌。它能帮助将母乳中的糖分分解成人体生长所需的营养物质。反过来,母乳又为婴儿双歧杆菌和整个肠道微生物群提供食物。这是一个良性循环。但是,如果婴儿一开始没有足够的婴儿双歧杆菌,他们就可能无法从母乳中吸收足够的营养来支持其他必要的肠道细菌的生长。
要克服这种缺陷几乎是不可能的。你可以获得世界上所有富含营养的食物,但这并不管用。如果你的肠道生长路径过早被打乱,你可能永远无法吸收到所需的全部营养。
但是,如果我们能给高危婴儿服用婴儿双歧杆菌作为益生菌补充剂呢?我们能否及早干预,让他们正常发育?
这正是基金会合作伙伴多年来一直在研究的问题——我们终于找到了答案。我们正在对一种可添加到母乳中的婴儿双歧杆菌粉末补充剂进行三期临床。来自5个国家的16000名婴儿参与了试验,研究人员正在对每个婴儿进行跟踪,以确保益生菌既安全又有效。
目前的研究结果令人惊叹:通过给婴儿喂食这种益生菌,可以帮助他们的微生物群进入积极状态,从而使他们能够长大并充分发挥潜力。这对预防营养不良大有裨益。
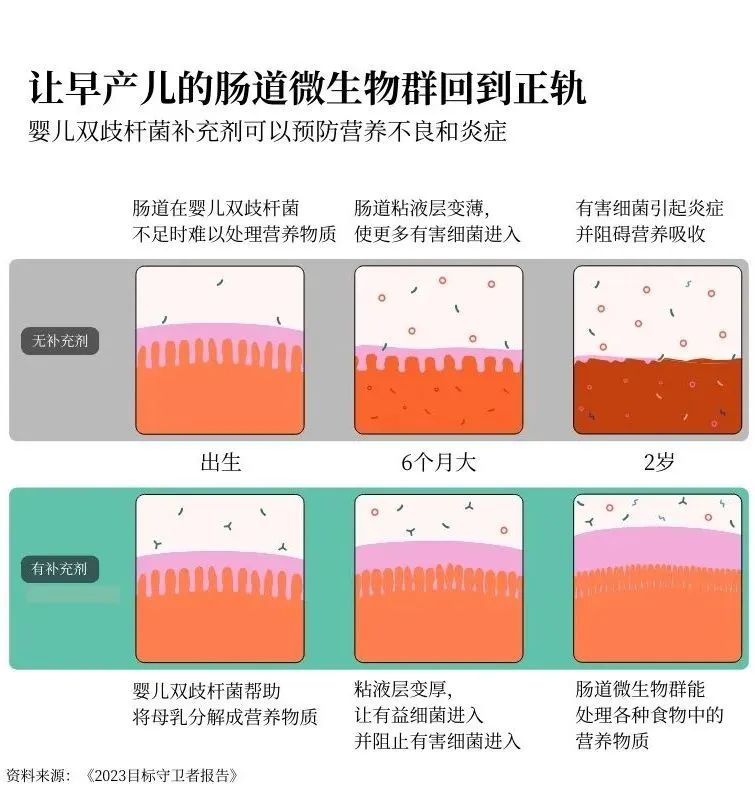
在婴儿出生前就能改善肠道微生物群,这也让我感到兴奋。新的研究发现,婴儿的微生物群与母亲的微生物群息息相关。解决子宫内的炎症问题会给产妇、胎盘和发育中的胎儿带来更多益处。
如果我们能给准妈妈提供一种益生菌补充剂,让她的孩子从出生第一天起肠道就正常发育,那会怎么样呢?目前还不清楚这些活体生物药到底是什么样的,也不清楚如何给药,这还只是非常早期的研究。但研究表明,健康的微生物群可帮助婴儿在妊娠晚期每天增加5克体重。
在过去十年里,儿童健康领域发展速度超出了我一生中的预期。看到微生物群从一个完全看不见的东西变成解决世界上最大健康不平等之一的关键策略,真是令人惊叹。我迫不及待地期待在接下来一年里我们将学到多少新知识,以及我们将如何运用这些知识来拯救生命…
——比尔·盖茨
儿童营养不良问题的现状如何?带来什么问题?
儿童营养不良问题给全球健康带来巨大挑战,据世界卫生组织和联合国儿童基金会的数据统计,到 2020 年,估计有1.49亿 5岁以下儿童生长发育迟缓(年龄身高低),而 4500万儿童出现消瘦(WLZ 低)。
营养不良及其长期后遗症是该年龄段人群发病和死亡的主要原因。后遗症包括线性生长、免疫和代谢功能以及神经发育的持续损害——所有这些都对当前的干预措施有很大的抵抗力。
从比尔·盖茨的年度总结我们也可以看到,他十分重视肠道微生物对健康的影响,总的来说,微生物方面的研究给儿童健康带来了很大希望。
从肠道微生物组的角度入手,对营养不良儿童进行基于微生物群的相关干预措施,比尔及梅琳达·盖茨基金会已支持多项相关研究。我们来看近期得到该基金会支持的两篇研究文献。
在健康儿童中,肠道微生物组在分类和功能多样性方面稳步增长,直到3岁,其中最明显的变化发生在断奶期间。相比之下,营养不良儿童的肠道微生物组是年龄倒退的,即肠道微生物组与年幼儿童相似。
抗生素是严重急性营养不良的标准治疗方法,因为即使儿童没有出现明显的疾病,他们也可能因急性感染而突然恶化。
在马拉维和尼日尔,与安慰剂相比,短期(即7天)阿莫西林给药已被证明在降低全因死亡率、住院率、腹泻病和改善人体测量方面具有益处。
然而,抗生素治疗对严重急性营养不良儿童的潜在后果(如抗生素耐药性的发展和微生物组破坏)仍存在不确定性。
研究设计
研究人员想要确定 7 天的阿莫西林治疗,对接受严重急性营养不良治疗的儿童肠道微生物组和抗生素耐药组的急性和长期变化的影响。该成果发表在《Lancet Microbe》。

研究人员对尼日尔门诊治疗的严重急性营养不良儿童(6-59 个月)的阿莫西林随机、双盲、安慰剂对照试验 (NCT01613547) 进行了二次分析。从2013年9月23日至2014年2月3日从整个队列中随机选择了161名儿童(n = 2399)进行最初12周的随访。
根据人体测量结果从这161名儿童中选择了一个方便样本,2年后(2015年9月28日至10月27日)进行随访。儿童在基线、第 1 周、第 4 周、第 8 周、第 12 周以及 2 年随访队列中的第 104 周提供了粪便样本。研究人员进行了宏基因组测序,然后对粪便样本进行了微生物组和耐药组分析。38 名无严重急性营养不良的儿童和 6 名与原始队列基线年龄相匹配的严重急性营养不良儿童被用作参考对照。
研究结果
结果表明,营养不良的尼日尔儿童在接受抗生素治疗后,虽然发现克雷伯氏菌属、埃希氏菌属等增加,这些菌可能与更严重的感染相关,但是,微生物组和耐药组扰动的负面影响似乎是短暂的,在三周内完全消失。
进一步观察到阿莫西林治疗的一些意想不到的长期益处,包括改善长期微生物组丰富度,多样性和成熟度。
阿莫西林对长期微生物组成熟的影响
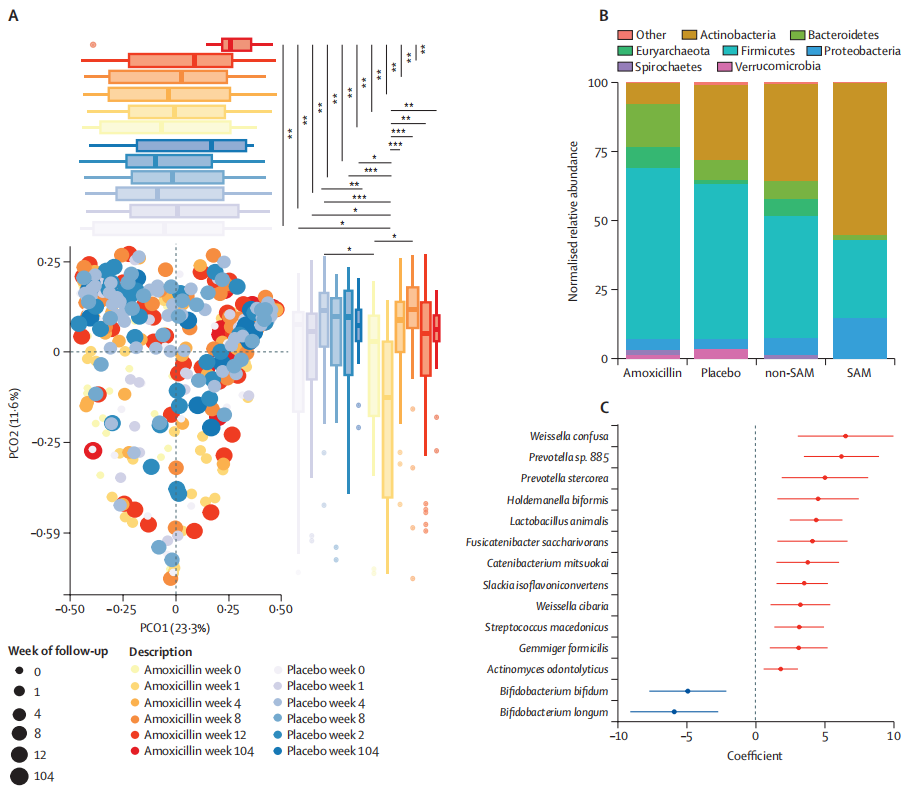
doi.org/10.1016/S2666-5247(23)00213-6
生命头三年肠道微生物组急剧成熟的一些关键驱动因素包括婴儿在出生期间和出生后接触母体微生物、加入牛奶、奶粉以及向固体食物的过渡。在营养不良的儿童中,肠道微生物组的成熟过程和生长都受到阻碍。但在治疗计划中加入抗生素改善了他们的身体测量和微生物组发育。
抗生素可能起到重置的作用,使有助于固体食物消化的微生物群在肠道生态系统中繁衍生息。
“
接受抗生素治疗的效果,对严重营养不良儿童来说算是个好消息,对于这一特定人群,抗生素治疗的益处似乎大于风险,但风险确实存在。研究人员警告说,儿童中已知的耐药细菌和耐药基因的增加不应被忽视。
营养干预措施,如即食治疗性食品,已被证明可以暂时改善肠道微生物组的成熟度和人体测量得分;然而,这种改善并不总是持续的。
在过去的5年里,合理设计的以微生物群为导向的治疗性食品在中度和重度急性营养不良儿童的微生物组恢复和人体测量得分方面显示出了希望。
接下来我们来看对于微生物群为导向的治疗性食品研究的最新进展。
生命头两年,肠道微生物群的发育需要与身体其他部分、其他器官系统的发育同步。当这个微生物群不完全形成时,仅仅增加热量是无法修复的。研究人员试图寻找特定的食物成分,以滋养健康的肠道微生物群,希望修复营养不良儿童肠道微生物群的功能失调。
使用传统食疗食品治疗可减少死亡,但并不能实质性改善营养不良的其他长期影响,包括新陈代谢、骨骼生长、免疫功能和大脑发育问题。
近日,来自华盛顿大学医学院的一项研究,已经确定了一种新型治疗食品中天然存在的关键生化成分,以及处理这些成分的重要细菌菌株。
该研究表明,识别这些成分以及作为其治疗靶标的关键促生长肠道细菌菌株,研究强调了了解细菌菌株如何加工特定食物成分的重要性,可以帮助指导当前食品配方的治疗,并可以在未来创造新的、更有效的配方。该研究成果于2023年12月13日发表在《Nature》杂志。
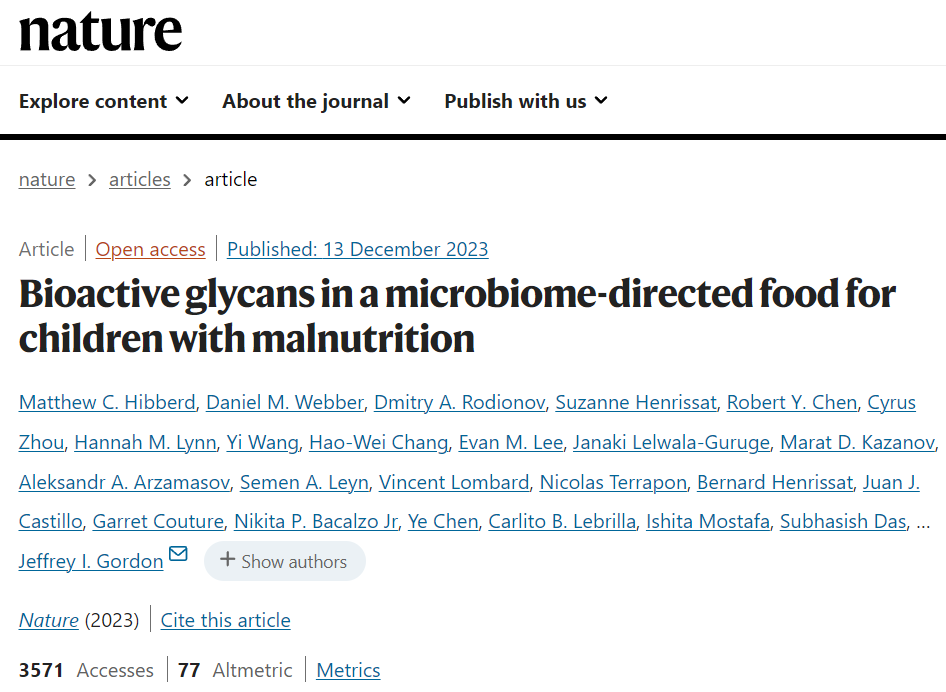
研究人员从试验参与者的粪便微生物群中重建了1000个细菌基因组(宏基因组组装基因组,简称MAG),确定了75个丰度与体重生长(体重长度Z评分变化,简称WLZ)正相关的MAGs。将MAG基因表达的变化表征为治疗类型和WLZ反应的函数,并定量MDCF-2和粪便中的碳水化合物结构。
结果表明,两个与WLZ呈正相关的普雷沃氏菌MAG是MDCF-2诱导的代谢途径表达的主要贡献者,这些代谢途径涉及利用MDCF-2的组分聚糖。
结果强调了微生物组反应的显著菌株特异性,并指出两种普氏菌菌株(MAG Bg0018 和 MAG Bg0019)是 MDCF-2 聚糖代谢和宿主体重生长反应的关键介质。
在生长相关细菌分类群代谢的MDCF中鉴定生物活性聚糖结构,有助于指导关于其在急性营养不良儿童中使用的建议,并有助于开发其他制剂。
在这项工作的基础上,世界卫生组织与比尔及梅琳达·盖茨基金会正在支持一项大型多站点临床试验,研究这种新的治疗性食品——MDCF-2,或微生物组导向的补充食品。
MDCF-2 治疗性食品包括哪些食物成分?
在 2021 年的临床试验中,MDCF-2 治疗性食品作为膳食补充剂提供,以提供儿童每日能量需求的约 20%。
Prevotella copri 两个菌株对MDCF-2干预改善营养不良的关键作用
研究人员发现:普雷沃氏菌Prevotella copri与儿童的生长发育呈正相关。
P. copri是拟杆菌门的成员,该门的成员含有一组叫多糖利用基因座(PUL)的基因,这些基因介导特定聚糖或一组聚糖的检测、导入和代谢。
它们在利用MDCF-2治疗食品中有益的生物活性碳水化合物结构的代谢途径中表现出活性的增加。
与接受传统治疗性食物的儿童相比,接受MDCF-2的儿童血液中支持肌肉骨骼生长和神经发育的某些蛋白质水平较高,与炎症有关的蛋白质水平较低。也表明,微生物群修复的作用远不止于肠道。
研究人员对这些儿童的粪便样本进行了广泛的基因组分析,了解对这些食物成分有反应的细菌,以及这些细菌对治疗的反应所具有和表达的代谢能力。事实证明,许多与儿童生长密切相关的细菌富含碳水化合物代谢的途径。
分析不同食物中的关键有效成分
在该研究中,通过质谱分析MDCF-2和RUSF两类食品,确定其组成成分。
MDCF-2、RUSF 及其食品成分中的多糖
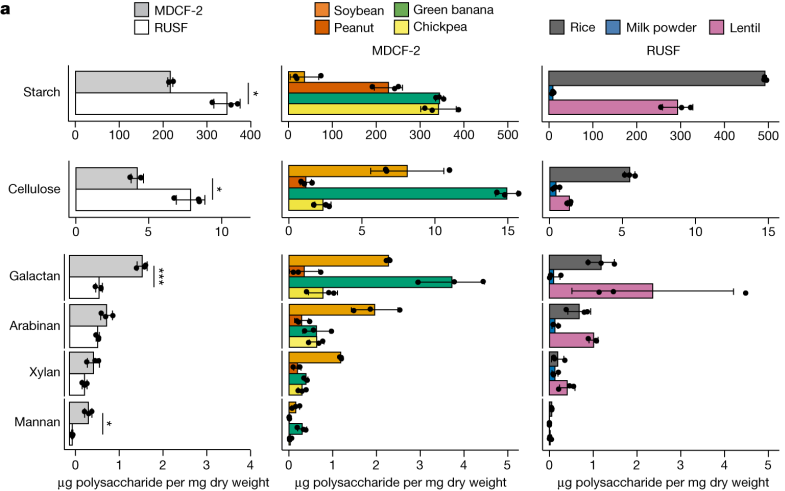
DOI: 10.1038/s41586-023-06838-3
对这些食物详细分析表明,MDCF-2食物中L-阿拉伯糖、D-木糖、L-岩藻糖、D-甘露糖和D-半乳糖醛酸 (GalA) 显著更丰富(P < 0.05)。
也就是说,MDCF-2含有更多的多糖,即半乳聚糖和甘露聚糖。而传统的治疗性食物RUSF含有更多的淀粉和纤维素。
MDCF-2 有效提高营养不良儿童生长
尽管MDCF-2的热量密度比高热量食物低15%,但与接受传统补充食物的儿童相比,接受MDCF-2治疗的儿童表现出更高的生长速度。
与MDCF-2治疗相关的生长增加与儿童微生物群中某些普氏菌菌株中存在的代谢途径的表达增加有关,这些途径与生物体利用MDCF-2中存在的多糖有关。
“来自食物频率问卷的信息表明,对MDCF-2反应最大的儿童也食用了更多的坚果和豆类作为他们日常饮食的一部分” ,研究人员表示,“这些坚果和豆类具有一些与MDCF-2相同的多糖。这表明可能有机会调整MDCF-2的成分和剂量,以进一步增强其治疗效果”。
营养不良儿童“微生物组修复”的一个定义是,重新平衡有益菌的表现和表达功能,使其呈现出更有利于健康微生物组-宿主共同发育的构型。
以这种方式将膳食聚糖和微生物代谢联系起来,为基于培养的计划提供了一个起点,这些计划旨在检索这些“效应”类群的分离物,用作潜在的益生菌制剂,或者如果与他们渴望的关键营养素相结合,修复对单独基于食物的干预反应不足紊乱的微生物群,提供合生元配方。
当然,P.copri菌株和MDCF-2聚糖之间的关系并不排除其他宏量或微量营养素对MDCF-2在增重方面优于RUSF的贡献。
总之,为改善微生物群的营养干预提供了一种新的见解。
这些和其他研究的结果有助于加深我们对微生物如何与人类细胞和器官合作,从而影响发育生物学的理解,帮助相关产业科研人员开发微生物组导向疗法的方法,帮助开发构建儿童营养健康的新策略,以确保在出生后的头几年形成健康的微生物组,尽可能规避儿童营养不良风险。
同时,随着人工智能技术及高通量测序等先进技术的不断发展,整合食物-微生物-人体交互作用研究,通过对婴幼儿的肠道菌群进行定期检测,可以帮助家长更好地监测儿童肠道菌群的变化,及时发现异常,采取相应的纠正措施,有利于促进儿童的身心健康发育。
谷禾健康

“唉,昨晚又没睡好!”
失眠已经严重影响着一部分人们的生活。失眠后会引起烦躁、白天嗜睡、精力不足、内分泌系统紊乱、认知功能受损、免疫力下降甚至易得心脑血管疾病。
据中国睡眠研究会等机构统计,中国有超3亿人存在睡眠障碍。其中,19—25岁年轻人经常熬夜至零点以后;19—35岁青壮年是睡眠问题高发年龄段。 并且由于当代社会压力增加,失眠率还在不断攀升。


影响睡眠质量的因素有很多:包括人体的生物钟,环境因素如光照、噪音、温度,还有心理状况,饮食状况及疾病状况。而近年来的研究发现体内有一种物质与睡眠紧密相关——它就是褪黑素。
褪黑素于20世纪50年代首次被发现并表征,从那时起,广泛的研究揭示了它的生产、功能和潜在的治疗应用。
褪黑素作为改善睡眠质量和调节昼夜节律紊乱的补充剂已广受欢迎。除了在睡眠调节中的作用外,褪黑素还被发现具有抗氧化、抗炎、免疫调节和神经保护特性。它影响生殖过程、心血管健康、胃肠功能以及其他生理系统。
近年来,褪黑素和肠道微生物群之间的关系已成为一个令人着迷的研究领域。研究表明褪黑素和肠道微生物之间存在双向作用,强调了肠道微生物群对褪黑激素产生和代谢的潜在影响,以及褪黑激素对肠道微生物组成和功能的影响。
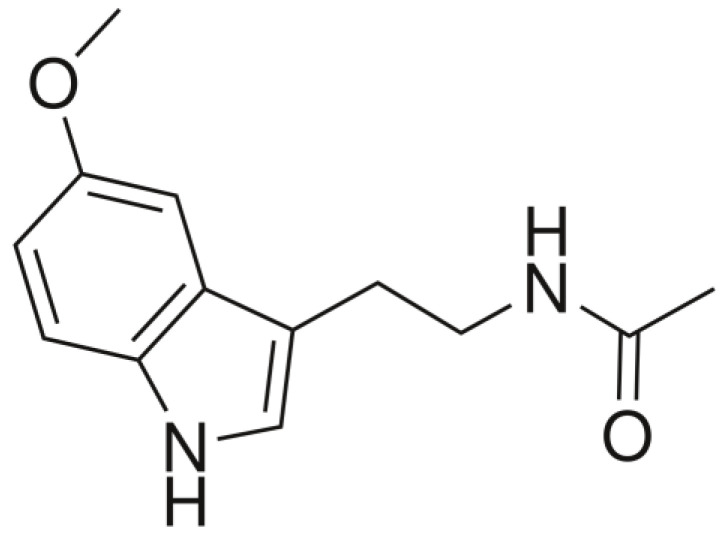
褪黑素(N-乙酰基-5-甲氧基色胺)最早于1958年在牛松果体中发现并分离出来,因其能够美白青蛙皮肤,研究人员一开始认为作为一种“美白因子”,并将其命名为“褪黑素”。
后续的研究才证明了其在调节生物节律和睡眠模式中的作用。
注:褪黑素是一种具有3-胺基和5-甲氧基的吲哚胺,因此具有两亲特性(同时具有亲水性和亲脂性)。
褪黑素的化学结构
Minich DM,et al.Nutrients.2022
✦ 色氨酸是合成褪黑素的原料
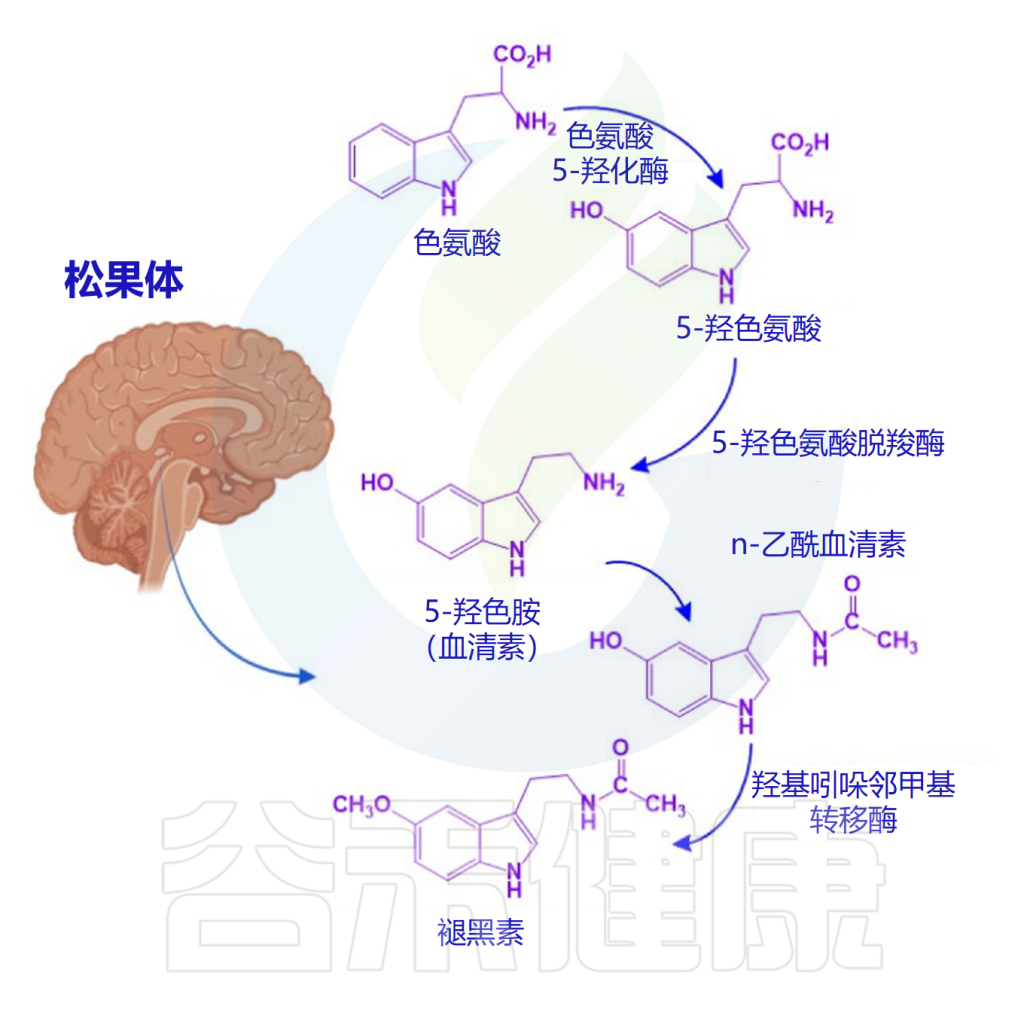
松果体通常在黑暗环境中产生褪黑素,褪黑素生物合成从色氨酸开始,接着色氨酸转化为血清素(5-羟色胺)。5-羟色胺会经历两个酶促反应:首先,N-乙酰基转移酶进行N-乙酰化,产生N-乙酰-5-羟色胺。
然后,通过羟基吲哚-氧-甲基转移酶的作用,甲基从S-腺苷甲硫氨酸转移到N-乙酰血清素的5-羟基。N-乙酰基转移酶是褪黑素合成的限制步骤,它具有昼夜节律,夜间活动是日间活动的50到100倍。
褪黑素的生物合成途径

Miranda-Riestra A,et al.Molecules.2022
✦ 其他部位也可以产生褪黑素
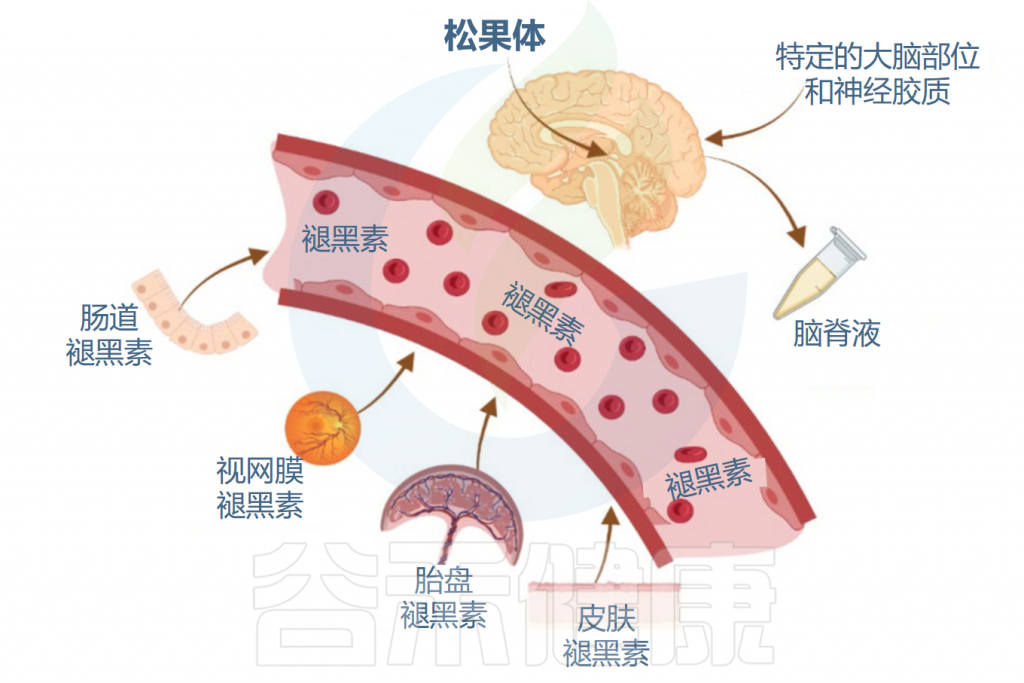
值得注意的是,其他组织和器官也会产生褪黑激素,包括视网膜、胃肠道、皮肤和免疫细胞。其在胃肠道中的浓度比血清中的浓度高10至400倍。
注:胃肠道中的褪黑素主要由肠嗜铬细胞、某些类型的免疫细胞和肠道共生细胞产生。肝脏几乎会降解所有褪黑素,这表明胃肠道褪黑素仅限于肠-肝轴,而不是循环到其他器官,并且它在局部发挥作用。
在这些外周组织中,褪黑素的产生可能不会直接受光暗周期调节,但可能受到其他因素(例如饮食和局部信号)的影响。
褪黑素在体内的合成

Miranda-Riestra A,et al.Molecules.2022
平均而言,松果体每天产生0.1至0.9毫克褪黑素。但一些因素会影响褪黑素的分泌。
✦光照
光照对于调节褪黑素的产生起着至关重要的作用。视网膜中称为本质光敏视网膜神经节细胞(ipRGC)的特殊细胞可检测光并向下丘脑视交叉上核 (SCN)发送信号。
当暴露于光,特别是蓝光时,这些细胞会抑制褪黑素的产生。这是因为光照会抑制血清素N-乙酰转移酶和N-乙酰血清素O-甲基转移酶的活性,这些酶参与褪黑素合成。

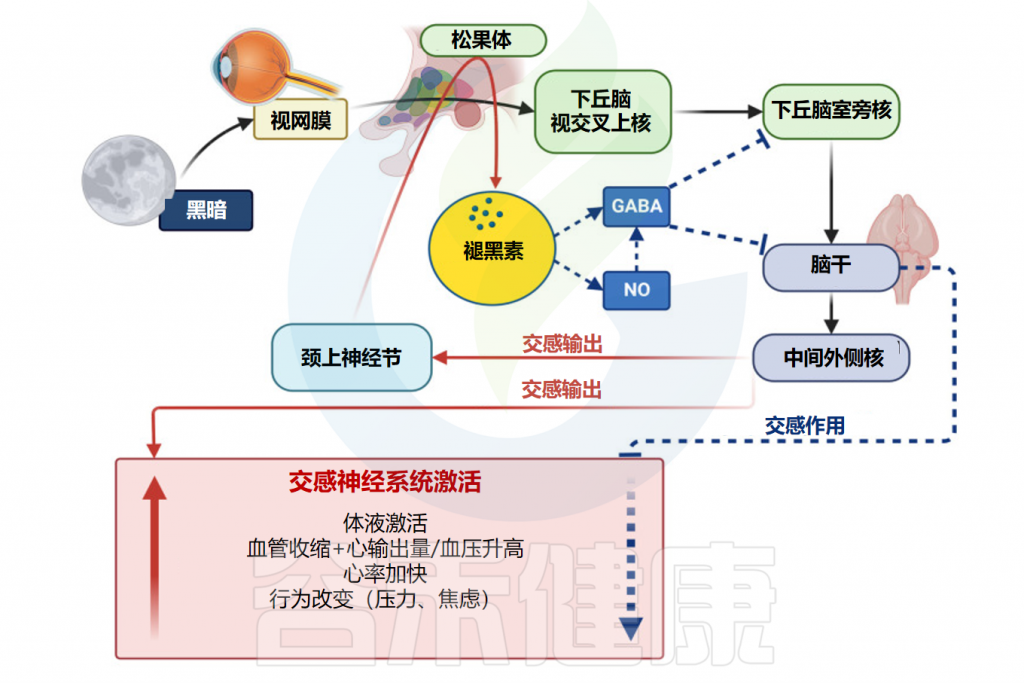
Repova K,et al.Int J Mol Sci.2022
在没有光的情况下,例如在夜间,褪黑素合成的抑制被消除。SCN向松果体发出信号,以增加褪黑素的产生。因此,褪黑素水平上升,促进困倦并帮助调节睡眠-觉醒周期。
✦生物钟
褪黑素的分泌与人体的生物钟密切相关。人体的生物钟是一种内在的生物节律,调节睡眠和其他生理过程。
褪黑素的分泌通常在晚上增加,帮助人们入睡。保持规律的作息时间和良好的睡眠习惯有助于维持正常的褪黑素分泌。

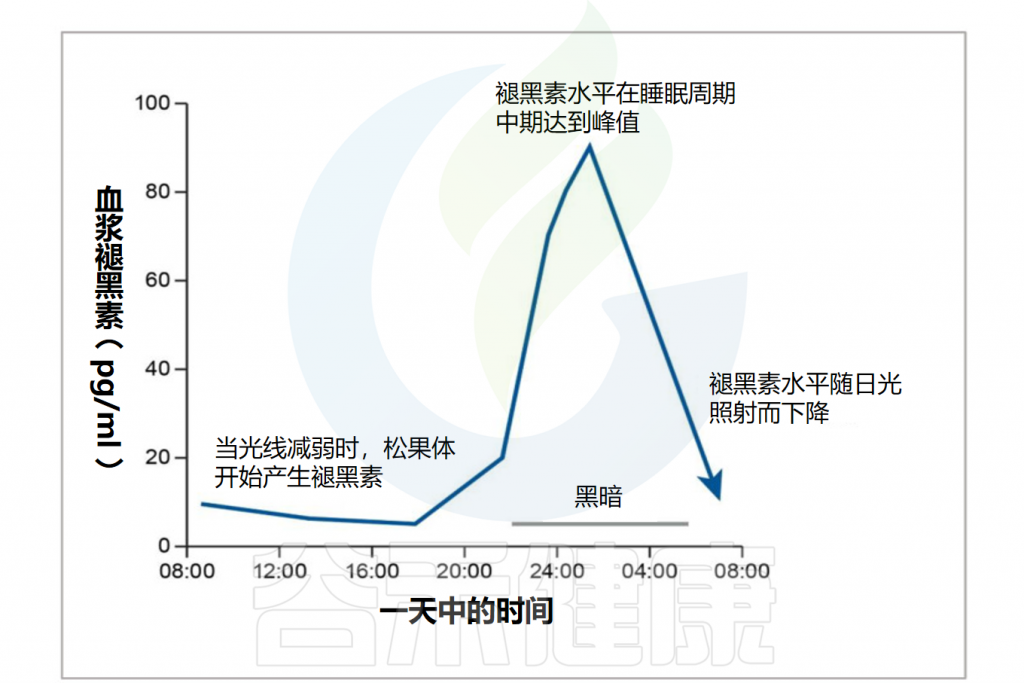
Minich DM,et al.Nutrients.2022
✦年龄
婴儿的褪黑素分泌和昼夜节律要到三个月左右才会发育。母乳喂养的婴儿可以从母乳中获得褪黑素。
从婴儿期到青春期,褪黑素的分泌水平随着年龄增长并达到稳定水平,然后从二十多岁开始随着年龄的增长而缓慢下降。儿童通常比成人产生更多的褪黑素。这也是为什么年长者常常会有睡眠质量下降的问题。

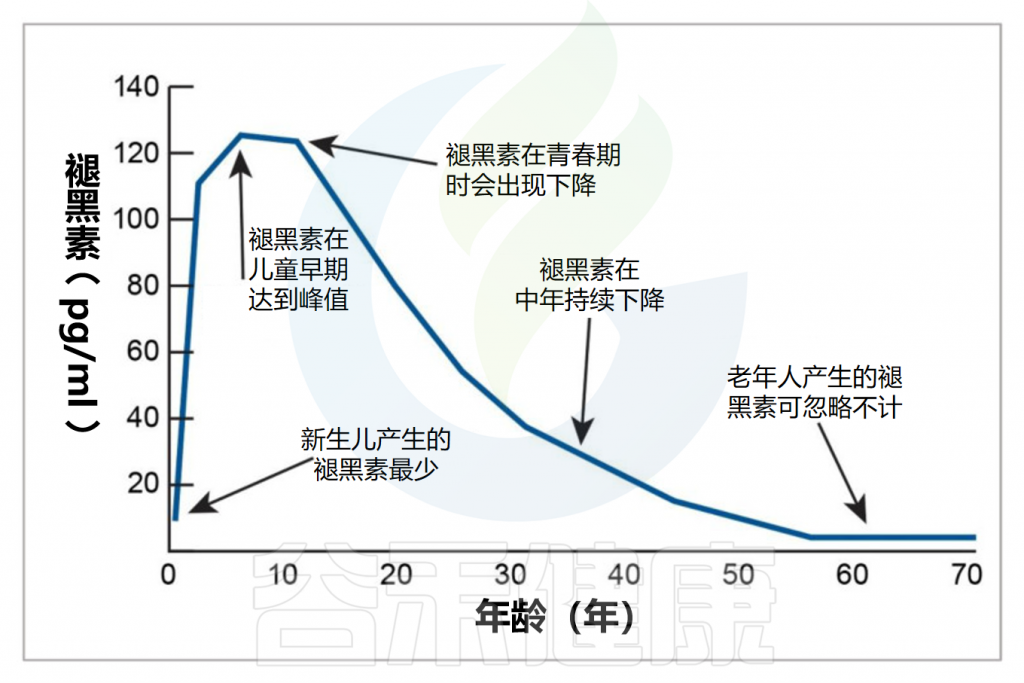
Minich DM,et al.Nutrients.2022
✦色氨酸可用性
色氨酸(褪黑素合成的前体)的可用性也会影响褪黑激素的产生。色氨酸是通过饮食来源获得的,并且可能受到饮食和新陈代谢等因素的影响。
充足的色氨酸对于合成血清素是必要的,血清素进一步转化为褪黑素。
✦药物和化学物质
某些药物和化学物质可能会影响褪黑素的分泌。例如,一些抗抑郁药物、抗高血压药物和咖啡因都可能抑制褪黑素的产生。
✦疾病和身体状况
一些疾病和身体状况也会影响褪黑素的分泌。例如,睡眠障碍、抑郁症、焦虑症和肾脏疾病等都可能干扰褪黑素的正常分泌。
值得注意的是,褪黑素产生的调节是复杂的,涉及多种因素之间的相互作用。昼夜节律紊乱,例如轮班工作、时差反应或夜间暴露在人造光下,可能会影响褪黑素的产生并扰乱睡眠模式。
总体而言,褪黑素的产生主要受到昼夜节律的调节,其中光照在抑制褪黑素合成中起着关键作用。黑暗和色氨酸的可用性促进褪黑激素的产生,有助于调节睡眠-觉醒周期并促进健康的睡眠模式。
褪黑素是一种多功能分子,在人体内具有多种生物学作用。在本节中,将介绍褪黑素对生理活动及人体健康的相关影响。

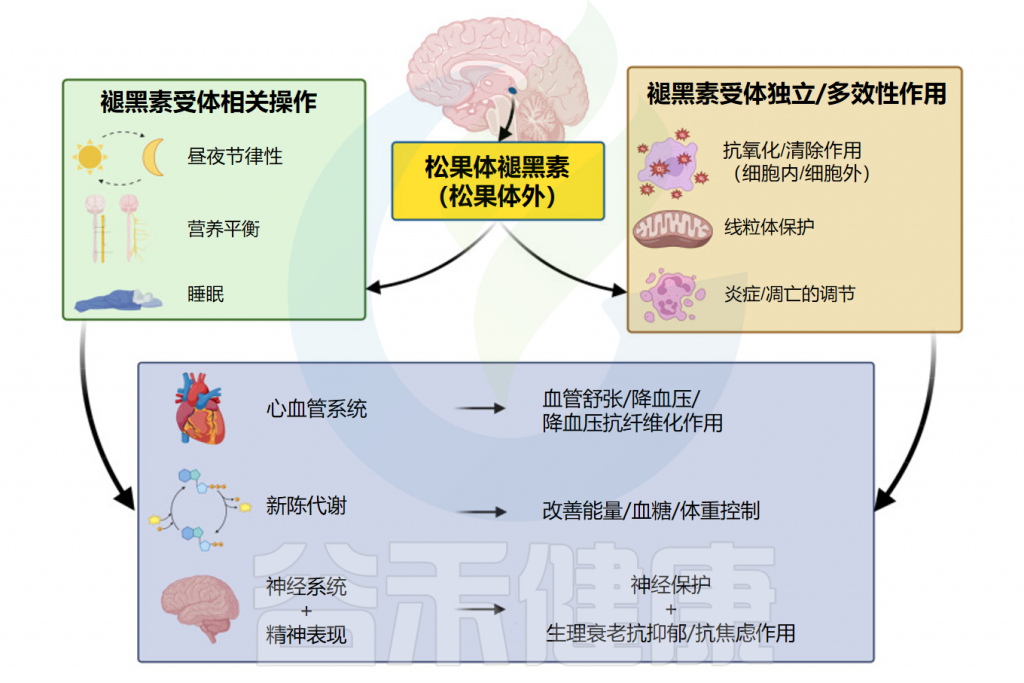
Repova K,et al.Int J Mol Sci.2022
▼
抗氧化、抗炎作用
许多研究已确定褪黑素是一种强大的自由基清除剂,甚至可能是迄今发现的最强的内源性自由基清除剂。体外和体内研究证明了褪黑素在抗氧化防御、减少氧化应激和抗炎过程中的作用。
• 褪黑素具有非常强的抗氧化作用
褪黑素是一种高效的抗氧化剂,因为一个褪黑素分子可以通过与其二级、三级甚至四级代谢物相关的级联机制清除多种活性氧和氮。
褪黑素的双重作用可以抑制促氧化酶(例如黄嘌呤氧化酶),同时还可以增强关键的抗氧化酶,例如超氧化物歧化酶、谷胱甘肽过氧化物酶和过氧化氢酶,有助于人体的第一道免疫防御和代谢解毒。
• 褪黑素可以抑制促炎性细胞因子
此外,褪黑素可以阻断作用于环加氧酶(COX-2)的促炎过程,并抑制炎症介质如肿瘤坏死因子-α(TNF-α)、白细胞介素-1β(IL-1β)和白细胞介素-6(IL-6)。
褪黑素还可以增强异常细胞的程序性细胞死亡(细胞凋亡),这在理论上使其成为一种理想的疾病治疗方法。
▼
调节昼夜节律,改善睡眠质量
人类的昼夜节律主要是由光照引起的,生活方式因素可能导致外在的昼夜节律障碍,如轮班工作或时差障碍,补充褪黑素可以通过提前或延迟来调节昼夜节律。
褪黑素对具有睡眠和昼夜节律紊乱人群的影响已得到充分证实。在失眠患者中,外源性褪黑素对一些睡眠参数有显著影响,如入睡潜伏期、总睡眠时间、早晨警觉性和睡眠质量。

• 缩短了入睡潜伏期
一项针对失眠患者的荟萃分析包含5项原始研究,结果表明睡前2小时服用褪黑素2mg显著缩短入睡潜伏期。
在其他一些目标群体中,也提供了褪黑素在纠正昼夜节律方面的证据。一项针对睡眠觉醒时相延迟障碍(DSWPD)患者的荟萃分析得出的结论是,外源性褪黑激素可提前内源性褪黑激素的发作并缩短入睡潜伏期。
在有时差症状的受试者、轮班工人和非24小时睡眠-觉醒节律障碍中也观察到褪黑素对睡眠参数的改善作用。
• 减少早醒时间,增加深度睡眠时间
最近的一项随机对照试验检查了97名中年失眠患者服用较高剂量的褪黑素(3毫克)4周对睡眠障碍的影响。研究显示褪黑素对睡眠参数有积极影响,例如减少早醒时间和增加深度睡眠百分比。
注:这些是睡眠的重要阶段,对于身体和大脑的恢复和健康至关重要。
▼
缓解焦虑
褪黑素除了对肠道炎症有一定的缓解作用外,多项研究表明,服用褪黑素还能发挥抗焦虑作用。
褪黑素的抗焦虑作用机制尚不完全清楚,可能与直接或间接作用有关。直接作用与大脑中褪黑素受体有关,间接作用与褪黑素调节各种神经体液系统(包括交感神经系统、糖皮质激素和神经递质)的能力有关,从而可能干扰应激反应和昼夜节律,并改变氧化和和炎症。
• 褪黑素用于预防术前和术后焦虑
在人类中,褪黑素已被测试为预防术前和术后焦虑的药物,作为麻醉药和止痛药辅助药物,以及用于预防术后谵妄。
临床研究表明,在接受腹部子宫切除术、静脉局部麻醉期间的手部手术或其他选择性手术的患者中,作为术前用药给予褪黑素可以减少术前焦虑,并且与苯二氮卓类药物的抗焦虑治疗同样有效。
在接受小型择期手术的儿童中,褪黑素与咪达唑仑一样,可以减轻术前分离焦虑和与引入麻醉面罩相关的焦虑。
• 褪黑素可能比一些精神药物更安全
此外,一些临床研究观察到褪黑素在降低术后兴奋、苏醒性谵妄和睡眠障碍发生率方面优于咪达唑仑。褪黑素还可以减轻结直肠手术和腹部子宫切除术患者的术后疼痛,同时减少吗啡用量。
值得注意的是,褪黑素可以有效抵消精神药物引起的代谢副作用。褪黑素可降低抗精神病药物治疗引起的血压、体重增加或胆固醇水平。
褪黑素似乎是苯二氮卓类药物的一种安全替代品,可以缓解儿童和成人与外科手术相关的焦虑,同时被认为是一种安全且耐受性良好的药物。苯二氮卓类药物会损害麻醉后的精神运动和认知功能,但褪黑激素却不会。
此外,褪黑素在人体内还有一些非常重要的功能:
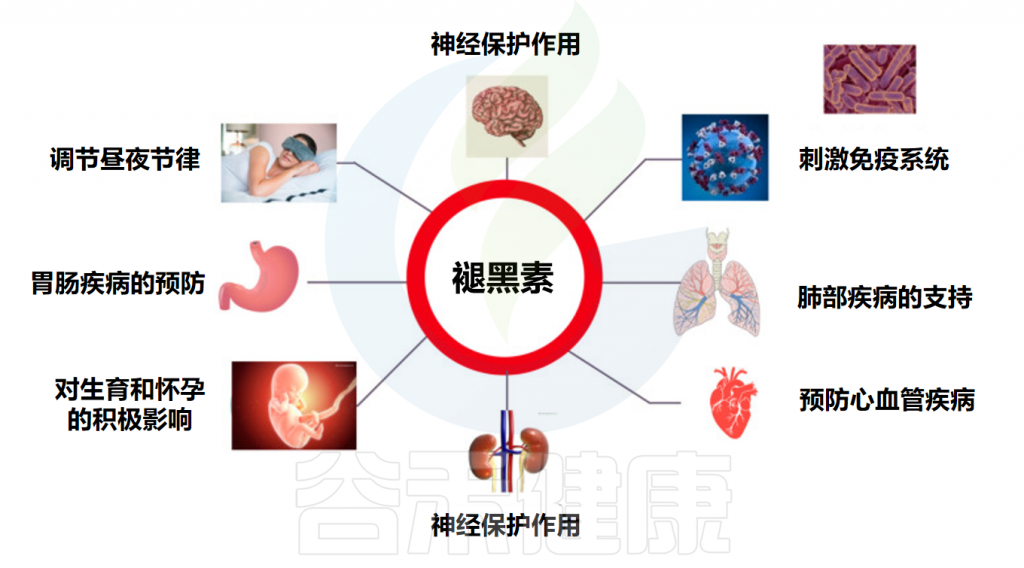

Markowska M,et al.Cells.2023
褪黑素对人体功能具有多种影响




Minich DM,et al.Nutrients.2022
▼
神经保护和神经再生作用
褪黑素的浓度变化与睡眠-觉醒周期紊乱、情绪紊乱、认知能力障碍、神经系统保护等有关。
• 对神经系统具有保护作用
由于其抗氧化特性,褪黑素可作为自由基的清除剂,在分子水平上调节多种反应,包括氧化应激、炎症和细胞凋亡。
它会影响神经营养素或神经递质的浓度。还有文献记载,褪黑素是钙蛋白酶的抑制剂,其活性在许多中枢神经系统疾病的发病机制中具有重要意义。
神经退行性疾病的发病机制与线粒体功能障碍有关。线粒体作为细胞能量来源,也是氧化损伤的目标。线粒体膜的敏感性会受到多种因素的损害,口服褪黑素可能会得到保护。线粒体膜选择性地吸收褪黑素,这是其他抗氧化剂不具备的功能。
初步研究还表明,它可能是淋巴液中的活性成分,有助于清除代谢废物,例如淀粉样蛋白的堆积。理论上,基于这一发现,从治疗角度来看,服用褪黑素可能是值得的,这样患有神经退行性疾病的老年人可以增加脑脊液和类淋巴液的水平。然而,这个概念仍处于起步阶段。
▼
免疫调节和加强监视
褪黑素另一个重要作用是其免疫调节和加强免疫监视的能力。它刺激参与体液免疫和细胞免疫的不同细胞系的产生,例如巨噬细胞、自然杀伤细胞和CD4+细胞,并影响多种细胞因子的合成。
• 褪黑素可以加强免疫调节和免疫监视
褪黑素的直接抗病毒和抗菌作用已被记录。在严重感染期间,服用褪黑激素已被发现具有免疫调节和细胞保护功能,可以降低病毒和细菌炎症的死亡率。
• 褪黑素还曾用于新冠期间的辅助治疗
考虑褪黑素在氧化应激、炎症过程以及免疫反应管理中的作用,对严重急性呼吸综合征冠状病毒2(SARS-CoV-2)引起的病毒感染患者进行了检查。
研究表明,使用褪黑素作为辅助治疗可能是有益的,在2019年新冠状病毒(COVID-19)期间也使用了褪黑激素。
▼
预防胃肠道疾病
消化系统中的褪黑素除了具有抗氧化作用和刺激免疫系统的能力外,还可以减少盐酸的分泌,增强上皮的再生,并增加微循环。
• 褪黑素有助于预防胃肠道疾病
所有这些功能使褪黑素成为预防不同胃肠道疾病的治疗选择之一,例如结直肠癌、溃疡性结肠炎、胃溃疡和肠易激综合症。
据记载,补充褪黑素可以使胃食管反流病完全缓解。它对影响食道和胃的急性和慢性刺激物具有保护作用。
一些研究还证实,褪黑素在预防非酒精性脂肪性肝炎方面对肝细胞具有很强的支持作用。
▼
改善血压、血糖
• 褪黑素可以降低胆固醇和改善血压
在30名患有代谢综合征的患者中,使用褪黑素(每天5毫克,睡前两小时)短短两个月后,低密度脂蛋白胆固醇和血压就得到了改善,而这些患者三个月的生活方式没有改变。
此外,褪黑素已被证明可以降低夜间高血压,改善收缩压和舒张压,降低颈内动脉搏动指数,减少血小板聚集,并降低血清儿茶酚胺水平。
香港中文大学研究人员最近进行的一项荟萃分析和系统评价得出结论,口服褪黑素补充剂可将睡眠收缩压降低3.57毫米汞柱。
其他研究表明,褪黑素可以改善心力衰竭患者的预后,并被认为是这些患者的预防和辅助治疗措施。
• 褪黑素可能有助于血糖控制
关于褪黑素是否有助于血糖控制的疾病(例如非胰岛素依赖型2型糖尿病)存在一些讨论。最近一项针对男性糖尿病患者的相对小型安慰剂对照研究表明,服用10毫克褪黑素三个月后,胰岛素敏感性降低了12%。
褪黑素对糖尿病人群口服葡萄糖耐量的影响差异可能与褪黑素受体1B基因(MTNR1B)中2型糖尿病相关G等位基因的多态性有关。
▼
对生育的影响
• 褪黑素有助于提高生育能力
已经在动物和人类群体中进行了褪黑素给药对生育影响的研究。研究发现,褪黑素可以提高生育能力、卵母细胞质量、成熟度和胚胎数量。
此外,还提出了在怀孕期间的积极作用。神经发生的保护、对胎盘的支持性影响以及氧化应激的减少是提高生育率和改善胚胎-胎儿发育的关键。
活性氧会在怀孕期间引起干扰,它们也是围产期并发症的罪魁祸首。褪黑素是自由基的清除剂,具有抗氧化和细胞保护能力,这可能对成功怀孕至关重要。
• 褪黑素影响新生儿的健康状况
褪黑素不仅在怀孕期间发挥着重要作用,而且在新生儿病理发生时也需要其支持。褪黑素是脱氧核糖核酸(DNA)甲基化和组蛋白改变过程中的监管者。这样可以避免基因表达的根本性变化。使胎儿受到保护,免受一些疾病的影响。
怀孕期间褪黑素浓度不足可能会在个体发育早期的遗传密码中留下内分泌紊乱,随后在儿童期发生。
▼
对骨骼健康的影响
根据细胞和临床前数据,有人认为褪黑素作用于骨代谢的合成代谢和分解代谢方面。
• 褪黑素增加了绝经后妇女的骨密度
一些临床试验证明了褪黑素在重新平衡围绝经期妇女骨重塑中的作用和增加绝经后骨质减少妇女的骨密度。
具体研究
在这些研究中,使用了多达3毫克的补充褪黑素。根据名为褪黑素微量营养素骨质减少治疗研究的为期一年的临床试验的结果,褪黑素(5毫克)、柠檬酸盐(450毫克)、维生素D3(2000IU/50微克) 的组合与安慰剂相比,能够对绝经后骨质疏松女性的骨标志物(例如骨矿物质密度)产生有利影响。
除了有益地改变骨标志物之外,干预措施还改善了情绪和睡眠质量等生活质量指标。当然,不能因此推断褪黑素是造成这些影响。
研究人员认为褪黑素是与年龄相关的骨骼肌疾病的关键化合物,因为它通过其抗氧化潜力参与线粒体功能。这方面的研究结果可能对恶病质或肌肉减少症患者有帮助。
除了上述的影响外,褪黑素与肠道微生物组之间的相互作用也很有趣。肠道中包含着大量的微生物,其与人体健康密切相关,褪黑素已被发现与肠道微生物存在复杂且多样的联系,并可能因此影响人体健康。让我们一起来了解下。
褪黑素主要由两种细胞产生:松果体细胞和肠嗜铬细胞。松果体细胞位于大脑内的松果体中。肠嗜铬细胞位于整个胃肠道的表面,在胃肠道的粘膜内层浓度很高。
与松果体细胞不同,肠嗜铬细胞不受光和暗的调节,但似乎受到食物摄入和消化的影响。
注:肠嗜铬细胞是神经内分泌免疫细胞,对肠道稳态至关重要。
★ 肠道中的褪黑素浓度比血清中高很多
据估计,肠道内的肠嗜铬细胞所含的褪黑素含量是松果体细胞产生的褪黑激素的400倍。肠道褪黑素水平可能比血清中褪黑激素水平高10至100倍。
肠嗜铬细胞中褪黑素的生物合成
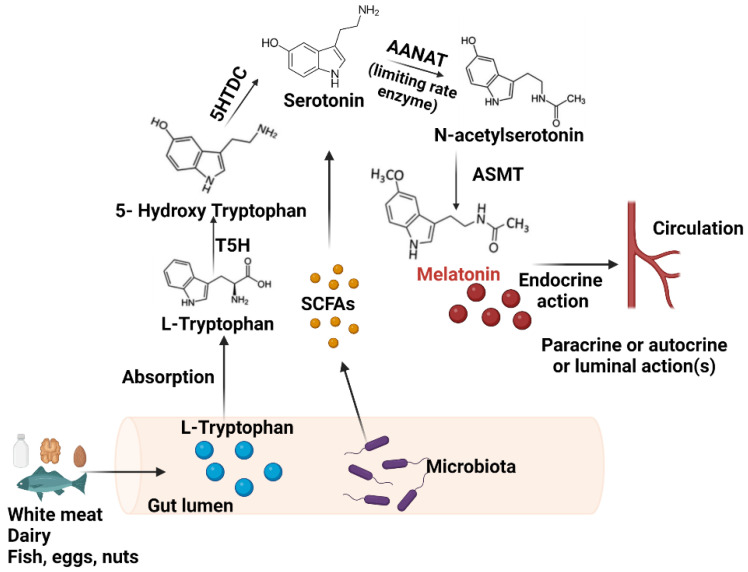
Iesanu MI,et al.Antioxidants (Basel).2022
肠道中褪黑素的释放以旁分泌方式发挥作用,增加胃粘膜的活动和循环,并增强胃肠道运动。此外,褪黑素在肠道中具有抗兴奋特性。它可以刺激上皮细胞的再生,并且还被证明对胃肠道内壁具有保护性抗氧化作用。
旁分泌——通过扩散而作用于邻近细胞的激素传递方式。

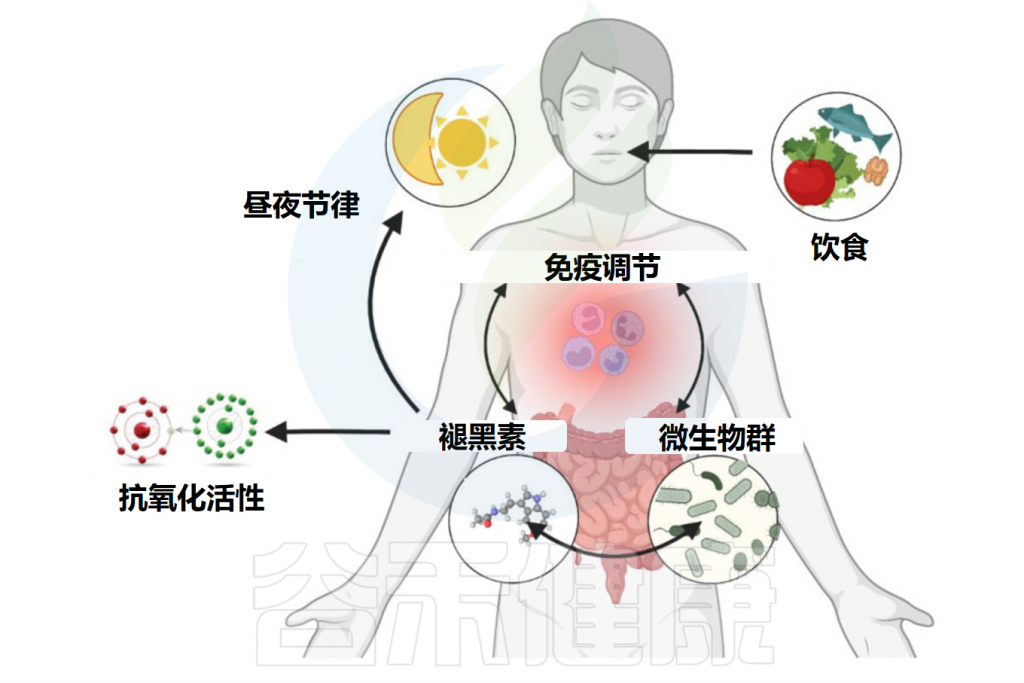
Iesanu MI,et al.Antioxidants (Basel).2022
值得注意的是,关于松果体产生的褪黑素和肠道来源的褪黑素如何相互关联,是否存在肠道-松果体轴串扰,以及不同的饮食模式甚至特定食物、禁食方案或进餐时间可能相互影响,仍然是推测性的。改变全身褪黑素水平与饮食和肠道产生的褪黑素这一领域还需要通过更多的研究来回答。
褪黑素和肠道细菌之间似乎具有复杂的相互关系。如下所述,微生物可以调节胃肠道中褪黑素的合成;相反,褪黑素与肠道微生物群的组成和动态有关。它们共同形成一个复杂的系统,在多个层面上发挥作用,以维持宿主的体内平衡。
• 肠道菌群影响褪黑素的前体进而影响其水平
肠道菌群可以通过调节其必需的前体色氨酸和5-羟色胺来影响褪黑素水平。色氨酸的可用性可以通过饮食改变或通过改变肠道微生物群组成来改变。
肠道中色氨酸代谢的三种途径都可以受到肠道细菌的调节。关于吲哚途径,微生物组特征决定了吲哚衍生物的类型。这些吲哚衍生物具有广泛的作用,从对肠粘膜和免疫系统的有益结果到肾毒性。
此外,炎症刺激激活的Toll样受体和肠道细菌释放的病原体相关分子模式分子会刺激犬尿氨酸途径。
肠腔中产生的短链脂肪酸刺激肠嗜铬细胞释放血清素并增强褪黑素的产生。内源性孢子形成细菌产生的其他代谢物可以激活肠嗜铬细胞并促进结肠中5-羟色胺的生物合成。
此外,抗生素引起的生态失调会增强吲哚途径,抑制犬尿氨酸途径,并降低动物模型中的结肠5-羟色胺。
• 病原菌感染后褪黑素的分泌减少
多种细菌对肠道合成褪黑素有影响。例如,胃粘膜幽门螺杆菌感染会下调褪黑激素生成酶的表达,并减少胃肠道中褪黑素的产生。感染清除后,褪黑素产量恢复到正常水平。
• 益生菌可能刺激褪黑素的产生
益生菌,对各种与菌群失调相关的疾病有效。研究还表明益生菌在刺激褪黑素产生方面发挥有益作用。
短期施用益生菌鼠李糖乳杆菌可以增加斑马鱼中褪黑素受体基因的丰度,与光周期转变为持续黑暗的结果相似。因此,益生菌似乎有可能影响褪黑素的产生,从而缓解各种疾病状态。
相反,生态失调和随后的肠道损伤可能会降低局部肠道和全身褪黑素水平。
越来越多的证据表明,褪黑素可以调节肠道微生物的组成和丰度,尤其是在各种病理状态下。
如下所述,褪黑素通过其作为抗氧化剂、免疫调节剂和昼夜节律调节剂的特性间接影响肠道微生物群,研究发现其还可能直接影响肠道微生物群。
• 褪黑素影响肠道微生物的昼夜节律
在人类中,褪黑素分泌主要以昼夜节律方式在夜间发生,血浆中最高水平出现在凌晨2至4点左右。
褪黑素的节律性释放由下丘脑前部的视交叉上核调节,代表中枢昼夜节律发生器。视交叉上核神经元的轴突投射到邻近的下丘脑核、丘脑和脑干,并使昼夜节律的一些组成部分同步,例如睡眠/觉醒节律、进食时间表和垂体/肾上腺轴的活动。
胃肠道和微生物群表现出与昼夜节律相关的变化,体外研究表明,多种肠道细菌受光暗循环影响,并与参与生物节律的分子密切相关。昼夜节律失调会引起并加剧炎症性肠病的炎症。
褪黑素含量高时,产气肠杆菌增殖的更快
产气肠杆菌(Enterobacter aerogenes)是人类肠道中普遍存在的细菌,具有昼夜节律,并对白天的褪黑素波动做出反应。
当褪黑素存在时,产气肠杆菌以剂量依赖性方式增殖得更快。此外,当暴露于色氨酸、5-羟色胺或N-乙酰血清素时,没有观察到相同的效果,这突显了褪黑素的重要性和敏感性。
产气肠杆菌主要生存于人类和动物的肠道,为人体内的正常菌群,在人体虚弱的特殊情况下才偶尔引起疾病。
此外,大肠杆菌和肺炎克雷伯菌对褪黑素的敏感性不同。另一项研究表明,高脂肪饮食会损害肠道细菌的日常波动,而褪黑素可以使这些波动正常化,这表明这种重新同步可能具有治疗意义 。
微生物代谢物(例如丁酸盐)的昼夜变化会影响宿主的生物钟。鉴于细菌代谢物的产生是周期性的,微生物功能与宿主的昼夜节律和代谢之间存在隐含的联系。
• 通过氧化还原平衡影响肠道微生物组成
褪黑素的抗氧化活性存在于多种功能中,直接作用是中和自由基,间接作用是通过增加抗氧化酶的水平来发挥作用。
健康的肠道微生物群也具有相当大的抗氧化作用。共生细菌直接参与活性氧的代谢,因为产生乳酸的细菌(例如乳杆菌属)具有乳酸氧化酶、超氧化物歧化酶和丙酮酸氧化酶,这些酶可以去除活性氧,减少氧化应激。
在较高浓度下,活性氧具有潜在毒性并导致生物分子损伤,例如蛋白质、脂质和DNA的氧化,这可能导致多种细胞功能障碍,包括细胞死亡。
结肠健康很大程度上受到肠道抑制过量活性氧产生的能力的影响。值得注意的是,肠道微生物群的组成根据氧化还原平衡而变化。在暴露于氧化应激的小鼠中,肠道微生物群经历了拟杆菌门的增加和厚壁菌门、梭菌目、瘤胃球菌属(Ruminococcus)和颤螺菌属(Oscillospira)的减少。
在衰老模型中,小鼠年龄越大,活性氧产生量越高,梭菌目数量减少,拟杆菌门丰度增加。当肠道损伤和生态失调时,胃肠道的抗氧化活性会受到抑制。例如,在炎症性肠病患者中,共生细菌多样性的减少和微生物群组成的变化与活性氧产生增加和肠粘膜防御系统受损有关。在这些情况下,褪黑素可以发挥其抗氧化活性并重建氧化还原平衡,从而改善肠道微生物群组成。
与其他器官类似,在肠道中,褪黑素不仅清除活性氧,还上调不同的抗氧化酶(GSH-Px、CAT、SOD)并下调促氧化酶。褪黑素可以通过与活性氧相互作用直接发挥其活性,或通过膜和核受体发挥其活性,膜和核受体作为其间接抗氧化作用的介质。
褪黑素激活该通路中的多个应激反应基因(例如AMPK、HIFa、Sirt),进而导致多种抗氧化酶的增加。
因此,通过所有这些褪黑素介导的途径减少肠道微生物群的氧化应激对肠道微环境具有显著影响。
越来越多的证据表明,褪黑素可以调节肠道特性和常驻微生物,以应对压力(例如睡眠障碍)。
当评估褪黑素、睡眠障碍和肠道微生物组之间的相互作用时,在有明显肠道损伤的临床前研究中,血浆和肠道褪黑素水平会降低。
总体而言,在睡眠障碍患者中补充褪黑素可以重建肠道微生物群平衡和肠道屏障的完整性,恢复了肠道微生物群的丰富性和多样性。

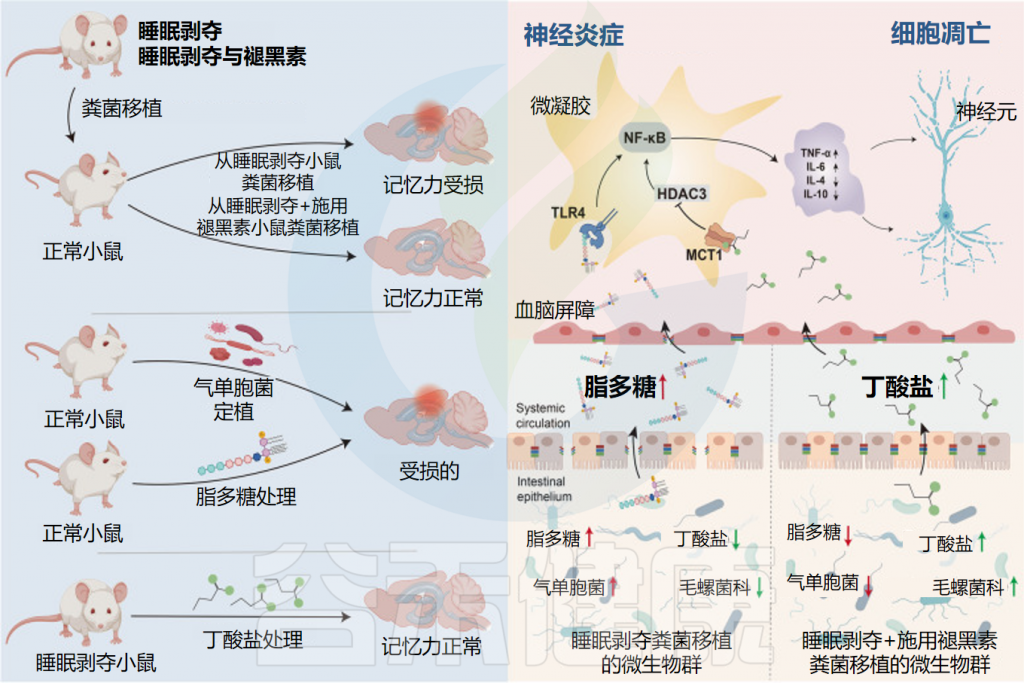
Wang X,et al.Microbiome.2023
• 增加了有益菌的丰度
在属水平上,补充褪黑素增加了阿克曼氏菌、乳杆菌、拟杆菌和粪杆菌(这些已知的有益细菌可以降低炎症),并减少了影响结肠炎的气单胞菌。
显著增加了阿克曼氏菌的丰度
褪黑素显著增加了阿克曼氏菌(Akkermansia muciniphila)的丰度,这种细菌以其在肠道中的有益作用而闻名(例如,增加粘蛋白产生,保持屏障完整性)。
提高了产丁酸盐细菌的丰度
此外,褪黑素通过增加拟杆菌属、乳杆菌属、阿克曼氏菌属和粪杆菌属的丰度,提高了丁酸盐的水平,丁酸盐是肠道微生物群的重要有益代谢物之一。
• 重建肠道屏障完整性
褪黑素还通过恢复因睡眠障碍受损的杯状细胞数量、粘液产生和肠上皮细胞增殖,增加紧密连接蛋白(claudin-1、occludin、ZO-1)和含有半胱天冬酶募集结构域的蛋白9(CARD9)的表达来重建肠道屏障的完整性。
• 降低促炎细胞因子,增加抗炎物质
睡眠障碍也会导致全身产生促炎症状态。褪黑素通过降低促炎细胞因子水平(IL-1β、IL-6、IL-17、TNF-α)同时增加抗炎标志物(IL-5、IL-10、IFN-α、IL-22)来抵消这种影响。
作为一种假定的机制,褪黑素还会下调睡眠剥夺小鼠的TLR4,从而降低长期炎症反应的可能性。
褪黑素在减轻粘膜损伤和生态失调方面发挥着至关重要的作用。这些发现表明,褪黑素可以作为益生元来治疗睡眠障碍相关的肠道损伤,并帮助保持肠道微生物群的平衡。
需要注意的是,褪黑素抑制可能是导致肠道损伤和生态失调的罪魁祸首,而不是睡眠障碍本身造成的应激。
总之,外源性给予褪黑素可恢复由睡眠障碍引起的全身和肠道微生物群改变,这意味着褪黑素在根据健康状况调节微生物群落方面发挥着作用。

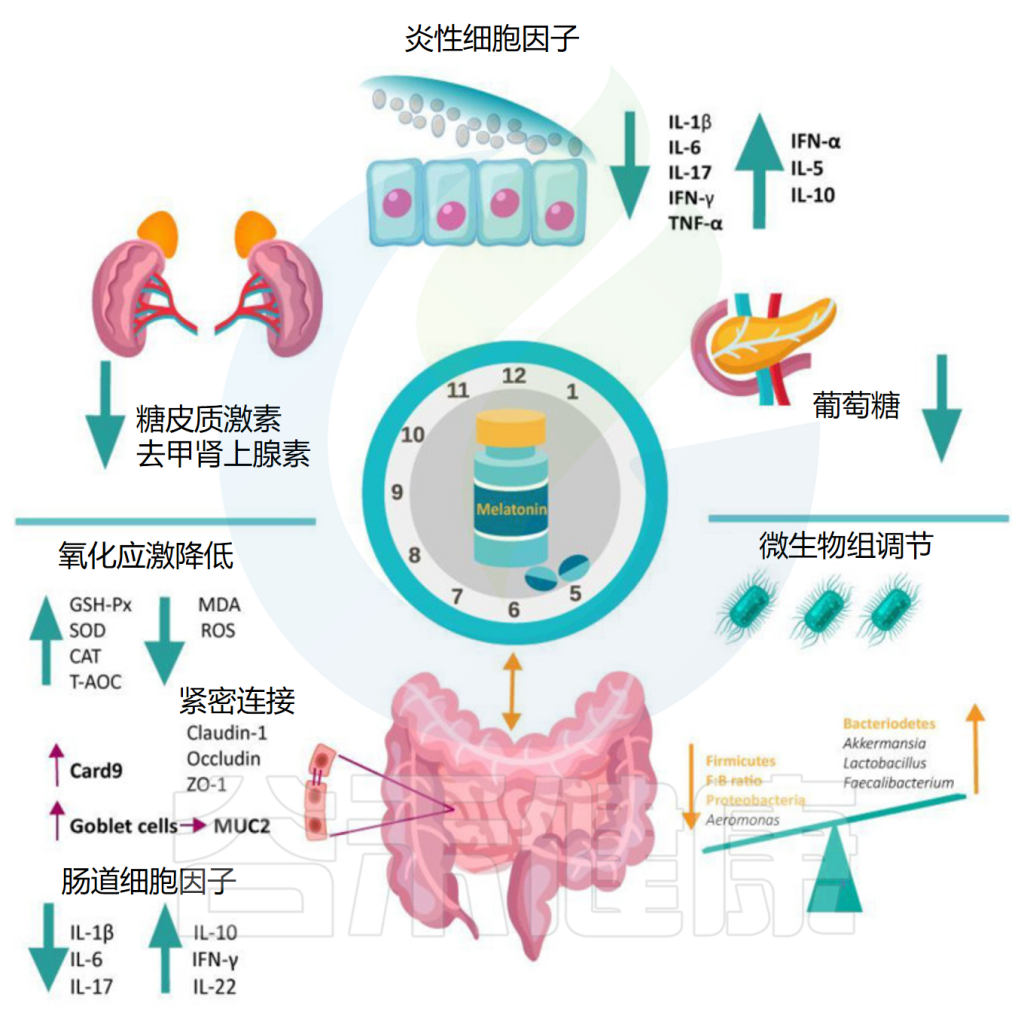
Iesanu MI,et al.Antioxidants (Basel).2022
褪黑素和肠道微生物群之间的相互作用对健康和疾病的各个方面都有潜在影响。大量临床和临床前研究证明了褪黑素对结肠炎的保护作用。
• 结肠炎患者体内褪黑素水平下降
测量了溃疡性结肠炎患者和健康对照的降结肠和乙状结肠中褪黑素的浓度。
与健康对照相比,溃疡性结肠炎患者的褪黑素水平急剧下降。值得注意的是,褪黑素浓度与组织学严重程度之间出现负相关。此外,溃疡性结肠炎患者中褪黑素生物合成途径中的关键酶AANAT和HIOMT的mRNA 水平显著低于健康对照。
这些数据表明溃疡性结肠炎患者的褪黑素水平下降,并且与疾病严重程度呈负相关,表明褪黑素可能参与溃疡性结肠炎的进展。
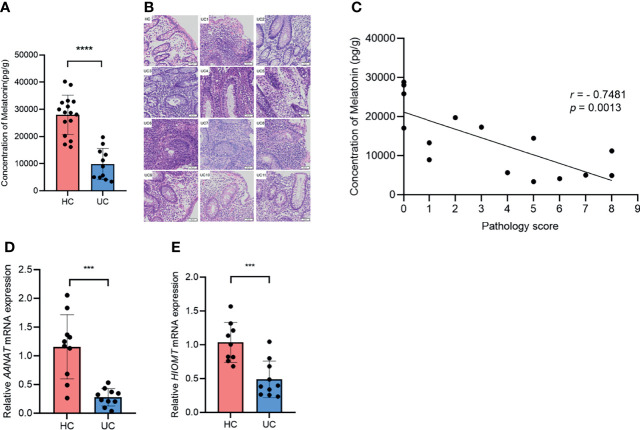
Zhao ZX,et al.Front Immunol.2022
(A)通过ELISA检测健康对照和溃疡性结肠炎患者中的褪黑素浓度;(B)结肠切片的代表性H&E染色(×20);(C)所有溃疡性结肠炎患者和健康对照的褪黑素浓度与组织学严重程度评分的相关性。
• 服用褪黑素可以减轻结肠炎
发现每日服用50毫克/公斤剂量的褪黑素治疗7天可显著改善恶唑酮诱发的小鼠结肠炎,体重减轻较少,结肠长度较长。
H&E染色显示,褪黑素治疗可预防肠道炎症,与对照组相比,褪黑素治疗导致CD11b+ Ly6G +中性粒细胞显著减少,并且炎症细胞因子的产生减少,例如TNF-α和Il-1β。
这些结果表明,褪黑素可以减轻恶唑酮诱发的结肠炎,炎症反应减少,肠道完整性提高。
• 服用褪黑素调节炎症性肠病的微生物组成
褪黑素改变微生物群组成的α和β多样性
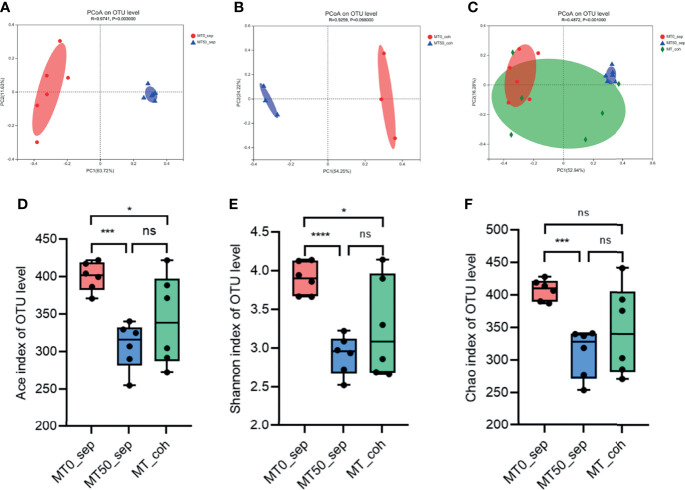
Zhao ZX,et al.Front Immunol.2022
特定的变化与有益菌株的增加和有害菌株的减少有关。例如,褪黑素增加了瘤胃球菌科(Ruminococcaceae)和粪球菌属(Coprococcus)的水平,这两种细菌都是短链脂肪酸产生菌。
它还增加了双歧杆菌的含量,双歧杆菌作为益生菌在炎症性肠病中产生了积极的结果,以及乳杆菌的含量,乳杆菌是该疾病的另一种有前途的辅助疗法。
减少了条件性致病菌
相反,褪黑素给药后,肠道菌群显示出变形菌门显着减少,该门在炎症性肠病发病机制中发挥着重要作用。
链球菌属(Streptococcus)可能代表另一种被褪黑素下调的微生物并与疾病活动相关。另一项研究报告了脱硫弧菌、消化球菌科和毛螺菌科的减少。发现脱硫弧菌和溃疡性结肠炎之间存在明显关联。尽管消化球菌科在炎症性肠病中的研究较少,但在一些研究中与肠道炎症相关。
重要的是,所有这些细菌组成的变化都伴随着明显的临床症状增强——通过多种组织学方法和症状学评估进行量化。这可能表明至少在一定程度上通过微生物群调节来影响褪黑素的效果。
褪黑素在属水平上调节一些微生物群
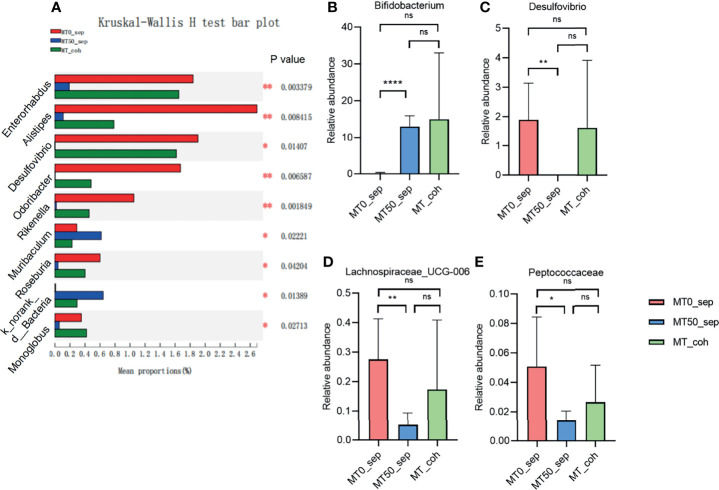
Zhao ZX,et al.Front Immunol.2022
• 褪黑素有利于肠道屏障完整性
总的来说,就肠道微生物群而言,褪黑素不仅具有改变细菌种类组成的能力,而且还能够减少肠道细菌移位。事实上,在结肠炎模型中,褪黑素诱导紧密连接蛋白和闭合蛋白的上调,这些蛋白是肠道屏障的关键组成部分。
细菌易位是一种有害过程,可导致内毒素血症,与炎症性肠病活动呈正相关。
褪黑素对肠道微生物群的调节可能对于缓解结肠炎至关重要。
除此之外,褪黑素还可以逆转高脂肪饮食产生的大多数代谢、形态和肠道微生物组成变化。
• 褪黑素恢复高脂饮食导致的微生物变化
首先,褪黑素成功恢复了因高脂饮食而减少的微生物群多样性,改变了肠道微生物结构,使其类似于正常饮食的小鼠。与对照组相比,褪黑素增加了细菌数量,但它阻止了高脂饮食引起的细菌突然过度生长。
有趣的是,与仅接受高脂饮食的小鼠相比,接受褪黑素的高脂饮食小鼠和对照组的不同类群每日振荡之间存在相似性,证明褪黑素也可以恢复细菌节律性。
它还刺激疣微菌门,包括阿克曼氏菌——一种治疗代谢紊乱的有效益生菌。脱硫弧菌科(产生内毒素的细菌)、Alistipes和Anaerotruncus中的表达下调,这些细菌与肥胖相关。
• 褪黑素改善代谢紊乱,降低脂肪比例
在影响这些微生物组相关的同时,褪黑素显著改善了高脂饮食啮齿动物的代谢紊乱。褪黑素还降低总体重和内脏脂肪比例,促进棕色脂肪组织的产生和产热作用。它还降低炎症、脂肪生成基因表达以及胆固醇和甘油三酯水平。
此外,它重建了时钟基因表达和血清甘油三酯的正常昼夜节律变化,而这些变化被高脂饮食破坏了。它还通过降低血糖和增强胰岛素敏感性来增强葡萄糖代谢。对于肝脏,它可以对抗脂肪变性并抑制 NF-κB信号,该通路与非酒精性脂肪肝病有关。
褪黑素缓解脂质代谢异常的一个特殊机制与抑制大肠杆菌有关。研究人员在时差小鼠模型中研究了与代谢综合征相关的变化,这些小鼠表现出体重增加、回肠脂质摄取增加以及血管生成素样4(脂质代谢调节剂)的减少。同时,观察到大肠杆菌和脂多糖产量增加。褪黑素逆转了所有这些修饰,并且通过下调大肠杆菌和脂多糖的合成,抑制了LPS/TLR4/STAT3等通路,使脂质摄取减少。
肠道微生物群在肥胖和代谢综合征的发展中起着关键作用。褪黑素恢复这种复杂结构正常组成和功能的能力证明了其作为药物治疗这些病症的合理性。
!
注意
需要进一步的研究来充分了解褪黑素–肠道微生物轴对健康和疾病的机制和影响。
然而,它强调了考虑肠道微生物群和褪黑素相互作用在维持肠道健康和整体健康方面的重要性。
褪黑素作为体内最重要的激素之一,过低或过高的含量都会对人体产生一些不利影响。
▸ 褪黑素过低
失眠:褪黑素是调节睡眠的重要激素,过低的褪黑素水平会导致失眠和睡眠质量下降。
生物钟紊乱:褪黑素水平过低可能导致生物钟紊乱,影响日常作息和生理节律。
免疫功能下降:褪黑素具有免疫调节作用,过低的褪黑素水平会导致免疫功能下降,增加感染和疾病的风险。
心理健康问题:褪黑素与神经系统密切相关,低褪黑素含量可能与焦虑、抑郁等心理健康问题有关。
其他健康问题:一些研究表明,褪黑素含量过低可能与肥胖、糖尿病、心血管疾病相关。
▸ 褪黑素过高
通常情况下,人体不会出现褪黑素过高。一般都是在补充了外源性褪黑素的情况下导致体内褪黑素水平过高。

一项研究对2130名患者进行了随机对照试验,发现过量服用褪黑素导致褪黑素水平过高引起的不良事件很少。其中最常报告的不良事件是日间嗜睡、头痛、头晕和体温过低。
除此之外,有一小部分研究发现过高的褪黑素水平可能对性欲和性功能产生负面影响。
由于褪黑素的代谢率较高,补充外源性褪黑素通常被认为是安全且耐受性良好的,大多数负面影响要么在几天内自然消退,要么在停药后立即消退。
褪黑素的分解代谢很快
循环中的褪黑素主要在肝脏和大脑中分解代谢。一般来说,褪黑素的半衰期(即分解一半所需的时间)约为30-50分钟。这意味着褪黑素在体内的浓度会在数小时内迅速降低。
在肝细胞中,褪黑素通过细胞色素P4501A2 (CYP1A2) 进行80%的羟基化;然后,在肾脏中,它被磺基结合(占总分解代谢的70%至80%)或与葡萄糖醛酸结合(占总分解代谢的5%)。
CYP1A2确保肝脏分解代谢。即使在肝脏水平,也存在脱乙酰化和脱甲基化途径。脱乙酰后,褪黑素转化为5-甲氧基色胺,氧化后转化为5-甲氧基吲哚乙酸。
褪黑素对人体如此重要,但经常会因一些外部环境、生活作息或疾病状态导致内源性褪黑素分泌不足,这个时候就需要一些外源性褪黑素来补充。
补充外源性褪黑素也有一些注意事项,包括可用的剂量、最佳服用时间、禁忌症。
除了人体自身会分泌褪黑素外,许多食物中也存在一些天然褪黑素,尤其是植物性食品。
✦ 许多植物性食品中含有褪黑素
自从20世纪90年代中期在植物中首次发现褪黑素(“植物褪黑素”)以来,各种食用植物和草药中的褪黑含量不断被提及。
然而,其浓度范围广泛且不一致,取决于许多因素,例如品种、生长条件、发芽、收获和加工(例如烘烤、干燥)等。
尽管褪黑素存在于大多数植物部位,但植物的生殖器官中的含量通常较高,尤其是种子,可能有助于确保植物的生存并抵御环境压力。
值得注意的是,褪黑素在植物中的众多作用之一是刺激促进健康的植物营养素(如芥子油苷和多酚)产生。
褪黑素已被记录在下列植物性食品和饮料中:


Minich DM,et al.Nutrients.2022
✦ 动物食品中的色氨酸有助于转化成褪黑素
虽然有几个变量需要考虑,但一般来说,动物性食品中的褪黑激素含量相对植物性食品中较少。根据已发表的文献,牛奶和乳制品、鸡蛋、鱼和肉类(牛肉、羊肉、猪肉)含有一定水平的褪黑素。
相反,动物食品往往是比植物食品更好的膳食色氨酸来源,因此可能需要考虑将这些食物最终转化为大量的褪黑素。
如前所述,虽然一些天然食物含有褪黑素,但其含量较低,因此很难获得足够的治疗剂量褪黑素。必须强调的是,几乎所有褪黑素产品都涉及工业加工,因此可能导致一些潜在毒性。
褪黑激素补充剂有多种形式,包括片剂、胶囊、舌下片和液体制剂。
• 褪黑素可能产生副作用和依赖性
在临床应用中,据记录,过多的褪黑素或各种缓释剂型会产生副作用,例如第二天健忘症或“褪黑素宿醉”,发现睡了三到四个小时就睡不好,醒来后无法再入睡。长期高剂量服用褪黑素随着时间的推移,个人可能会产生依赖性。
注:具有某些基因型的人,例如褪黑激素受体1B(MTNR1B)基因多态性,如果补充褪黑素,可能需要监测糖化血红蛋白。
• 补充高剂量的褪黑素会导致体温过低
一项关键研究中,比较了多个剂量:生理剂量(0.3mg)、药理剂量(3mg)和0.1mg的低生理剂量。
研究发现补充0.3毫克/天褪黑素的数据最佳客观。生理剂量(0.3 毫克)可恢复睡眠效率,并将血浆褪黑素水平提高至成年早期的正常水平。药理剂量(3毫克)也能改善睡眠;然而,它会导致体温过低,并导致血浆褪黑素在白天一直保持升高状态。
• 一般补充0.5-3毫克/天为宜
临床上补充褪黑素的剂量通常为每日0.5-3毫克;然而,发现剂量取决于产品类型,在某些情况下较低剂量也同样有效。
剂量参数可能会根据健康状况、睡眠问题类型或相关神经病理学等因素而有所不同,因此还需要根据每位患者提供适当的、个性化的剂量。
• 睡前一小时服用效果较好
从时间角度来看,许多与睡眠相关的研究都表明在睡前三十到六十分钟补充褪黑素效果较好;然而,一些研究表明,提前四个小时服用即可有效。
建议在黑暗环境或较弱光刺激下服用褪黑激素,从而模拟基于明暗模式的生理动力学和昼夜节律。
根据已发表的报告,口服褪黑素大多被认为是安全的,然而,在某些特定情况下可能需要进一步的临床监督。
• 一些药物会影响褪黑素的代谢
早期研究已发现,大部分褪黑素通过细胞色素CYP1A2代谢,小部分通过CYP1A1、CYP1B1和CYP2C19进行较少的代谢活动。
因此,影响这些酶途径的药物将影响褪黑素的代谢。褪黑素与一种或多种药物同时服用时应谨慎;否则,可能会导致不良副作用(如极度镇静)。
例如,最著名的相互作用之一是褪黑素与抗抑郁药物氟伏沙明的相互作用。该药物是一种已知的CYP1A2抑制剂,可通过减少褪黑素的降解来增强褪黑激素水平。同样,咖啡因也通过CYP1A2代谢,并可增加褪黑素水平。
总之,虽然还不全面,但褪黑素可以与具有血液稀释、降血糖、降血压、抗惊厥、镇静、抗抑郁或免疫抑制活性的药物、营养素或草药相互作用或受到影响。
褪黑素的代谢和活性可能会受到许多饮食、补充剂和药物的潜在影响,所有这些都说明了这样一个事实:每个人对褪黑素的个性化反应存在差异,具体取决于他们的饮食和医疗背景。
由于缺乏安全性数据,不建议怀孕或哺乳期的女性补充褪黑素。然而,有一些迹象表明褪黑素在这两个阶段可能都有好处。因此,让这些女性咨询了解患者个性化需求的健康专业人士是关键。同样,被诊断患有任何疾病的人应咨询其健康专业人员并接受医疗监督。
温馨提醒
调查发现,有的褪黑素产品月销已超过3万件,说明需要使用褪黑素来帮助改善睡眠的人已不在少数。需要注意的是,虽然补充外源性褪黑素可以在一定程度上改善睡眠质量、代谢健康或降低焦虑,但服用褪黑素存在的副作用使其不能成为长久的选择。
而且补充褪黑素主要是针对一些因工作昼夜颠倒导致的内源性褪黑素分泌不足造成的睡眠障碍,对于其他原因造成的失眠可能效果一般。我们额外补充的这些褪黑素,并不能促进身体去分泌更多的褪黑素。如果停用褪黑素,可能睡眠情况还会回到原样,并不会解决本质问题。
重点还是要从自身生活习惯出发,改善饮食,调节作息规律,增加体育锻炼并定期体检,及时了解自身健康状况。肠道菌群与很多影响睡眠的因素相关,例如压力、消化等,调节肠道菌群可以更全面地从根本上改善睡眠障碍。
改善内源性褪黑素的措施
除此之外,调节内源褪黑素的措施有以下几种:
•控制光照暴露,睡前半小时不玩手机
光线会影响褪黑素的分泌,晚上避免暴露于强烈的蓝光,尤其是来自电子设备的蓝光。蓝光会抑制褪黑素的分泌,影响睡眠质量。
•维持规律的睡眠时间
建立健康的睡眠习惯,如果不是因为工作导致的昼夜颠倒,尽量每天保持规律的睡眠时间,避免熬夜或睡眠不足。
•营造舒适的睡眠环境
保持安静、黑暗和凉爽的睡眠环境,可以使用遮光窗帘、耳塞或眼罩等辅助工具,有助于提高睡眠质量。
•避免过度应激
减少压力和焦虑,通过放松技巧如深呼吸、冥想和瑜伽等来缓解压力,有助于促进褪黑素的分泌。
•适度运动
进行适度的有氧运动,如散步、跑步或游泳等,可以提高睡眠质量和褪黑素的分泌。
•饮食调整
摄入富含色氨酸的食物,如禽肉、鱼类、坚果和豆类,色氨酸是合成褪黑素的必需物质。此外,可以适量摄入富含维生素B6、钙和镁的食物,这些营养素有助于褪黑素的合成和释放。
褪黑素在临床上有多种应用,以下是一些常见的褪黑素临床应用。
•睡眠障碍
褪黑素补充剂通常用于治疗睡眠障碍,如失眠、睡眠时相延迟综合征和非24小时睡眠觉醒障碍。它可以帮助调节睡眠-觉醒周期并提高睡眠质量。治疗睡眠障碍的剂量通常为0.3毫克至10毫克,睡前30分钟至2小时服用。
•时差反应
褪黑素可用于缓解时差反应症状,时差反应是因跨越多个时区旅行而导致的睡眠-觉醒周期暂时中断的症状。
在睡前适当的时间服用褪黑激素,可以帮助调整人体的生物钟,有利于更快地适应新的时区。
•轮班工作睡眠障碍
夜班或轮班工作的人经常会遇到睡眠困难和昼夜节律紊乱。褪黑素补充剂可用于帮助调节睡眠模式并改善白天的睡眠质量。
•神经退行性疾病
褪黑素已被研究其对阿尔茨海默病、帕金森病和亨廷顿舞蹈病等神经退行性疾病的潜在治疗作用。它具有抗氧化和抗炎的特性,可能有助于保护神经元并减轻神经退行性过程。然而,需要进一步研究以确定其功效和最佳剂量。
•情绪障碍
褪黑素补充剂在治疗重度抑郁症和季节性情感障碍等情绪障碍方面显示出良好的前景。它可能有助于调节昼夜节律、改善睡眠并缓解抑郁症状。
治疗情绪障碍的剂量可能会有所不同,咨询医疗保健专业人士很重要。
•癌症
褪黑素已被研究其潜在的抗癌特性。它具有抗氧化、抗炎和免疫调节作用,可能可以抑制肿瘤生长并增强癌症治疗的有效性。然而,需要更多的研究来确定其在癌症治疗中的功效和最佳用途。
关于褪黑素与肠道微生物群相互作用的新兴研究具有重要的临床意义,并为治疗干预带来了希望。
通过益生菌、益生元或粪菌移植调节肠道微生物群组成和功能可能与补充褪黑素在促进肠道健康和治疗炎症性肠病、肠易激综合征和代谢紊乱等疾病方面具有协同作用。
以下是有关褪黑素-肠道微生物轴未来前景的一些要点。
•时间生物学和个性化医疗
褪黑素和肠道微生物群之间的相互作用为个性化医疗增加了时间生物学的维度。考虑褪黑素产生的昼夜节律以及肠道微生物群组成和功能的昼夜变化,有助于优化针对褪黑激素-肠道微生物群轴的干预措施的时间和剂量。
•微生物代谢物和褪黑激素衍生物
肠道微生物群可以将褪黑素代谢成各种代谢物,其中一些可能具有不同的生物活性。探索这些褪黑激素代谢物的作用及其与肠道微生物群的相互作用可以发现新的治疗途径。
•营养干预
饮食在塑造肠道微生物群组成和功能方面起着至关重要的作用。未来的研究可以调查特定饮食成分,例如色氨酸(褪黑激素的前体)和多酚对褪黑激素-肠道微生物群轴的影响。
了解影响褪黑素产生和肠道微生物群的饮食因素可以为肠道健康的营养干预提供信息。
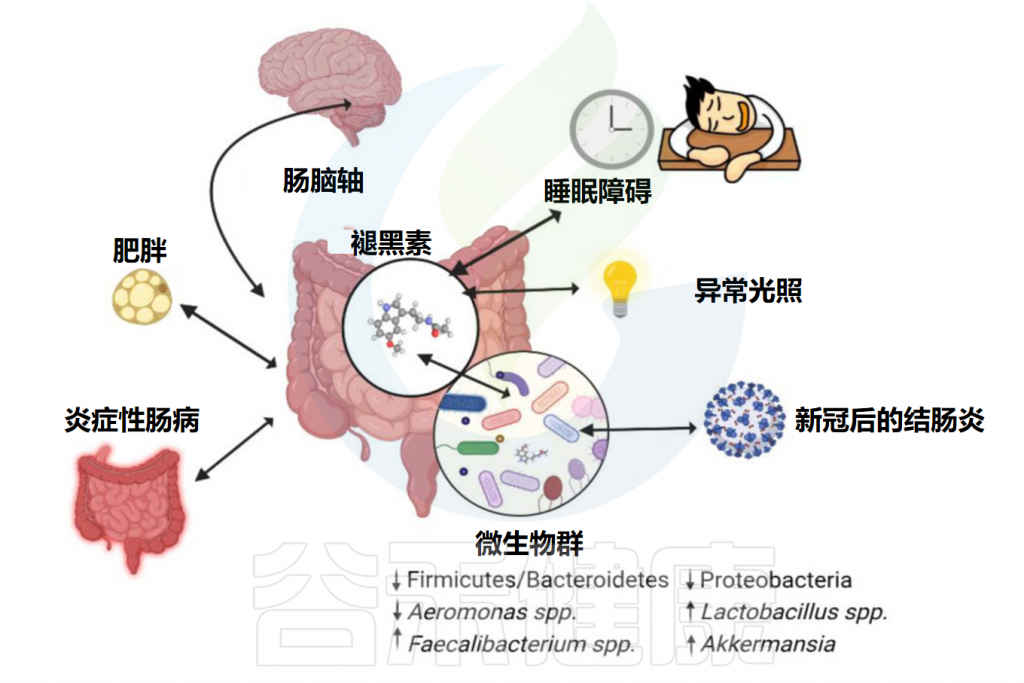

Iesanu MI,et al.Antioxidants (Basel).2022
•挑战和未来方向
尽管研究数量不断增加,但该领域仍存在一些挑战和未来方向。需要对肠道微生物群和褪黑素测量的研究方法进行标准化,以确保研究之间的一致性和可比性。
需要进行长期临床试验来评估针对褪黑激素-肠道微生物轴的干预措施的安全性、有效性和最佳剂量。
主要参考文献
Iesanu MI, Zahiu CDM, Dogaru IA, Chitimus DM, Pircalabioru GG, Voiculescu SE, Isac S, Galos F, Pavel B, O’Mahony SM, Zagrean AM. Melatonin-Microbiome Two-Sided Interaction in Dysbiosis-Associated Conditions. Antioxidants (Basel). 2022 Nov 14;11(11):2244.
Markowska M, Niemczyk S, Romejko K. Melatonin Treatment in Kidney Diseases. Cells. 2023 Mar 8;12(6):838.
Minich DM, Henning M, Darley C, Fahoum M, Schuler CB, Frame J. Is Melatonin the “Next Vitamin D”?: A Review of Emerging Science, Clinical Uses, Safety, and Dietary Supplements. Nutrients. 2022 Sep 22;14(19):3934.
Repova K, Baka T, Krajcirovicova K, Stanko P, Aziriova S, Reiter RJ, Simko F. Melatonin as a Potential Approach to Anxiety Treatment. Int J Mol Sci. 2022 Dec 19;23(24):16187.
Moon E, Kim K, Partonen T, Linnaranta O. Role of Melatonin in the Management of Sleep and Circadian Disorders in the Context of Psychiatric Illness. Curr Psychiatry Rep. 2022 Nov;24(11):623-634.
Zhao ZX, Yuan X, Cui YY, Liu J, Shen J, Jin BY, Feng BC, Zhai YJ, Zheng MQ, Kou GJ, Zhou RC, Li LX, Zuo XL, Li SY, Li YQ. Melatonin Mitigates Oxazolone-Induced Colitis in Microbiota-Dependent Manner. Front Immunol. 2022 Jan 18;12:783806.
Wang X, Wang Z, Cao J, Dong Y, Chen Y. Gut microbiota-derived metabolites mediate the neuroprotective effect of melatonin in cognitive impairment induced by sleep deprivation. Microbiome. 2023 Jan 31;11(1):17.
Miranda-Riestra A, Estrada-Reyes R, Torres-Sanchez ED, Carreño-García S, Ortiz GG, Benítez-King G. Melatonin: A Neurotrophic Factor? Molecules. 2022 Nov 10;27(22):7742.
Zhang B, Chen T, Cao M, Yuan C, Reiter RJ, Zhao Z, Zhao Y, Chen L, Fan W, Wang X, Zhou X, Li C. Gut Microbiota Dysbiosis Induced by Decreasing Endogenous Melatonin Mediates the Pathogenesis of Alzheimer’s Disease and Obesity. Front Immunol. 2022 May 10;13:900132.

谷禾健康

现代的生活工作方式大多是久坐,户外运动少,导致与骨骼肌肉相关的亚健康症状越来越普遍,覆盖人群越来越广。
例如长时间的低头垂肩的姿势会让竖脊肌处在伸展的位置,进而导致竖脊肌的无力,产生受伤的状况。长时间久坐使得臀大肌萎缩无力,无力松弛的臀肌再结合无力的竖脊肌,导致腰背疼痛等症状。

老年人的肌肉骨骼疼痛,在我们生活的每一个角落悄然出现。这无声的挑战,让他们在岁月的长河中饱受苦楚。
随着全球老龄化的日益严重,与衰老相关的疾病,包括肌肉减少症、骨质疏松症和骨关节炎,变得越来越突出,影响着至少7-27%的世界人口。
肌肉减少症的发生率为 10% 至 27%。50岁以上女性骨质疏松患病率不低于20%,骨关节炎的患病率约为7%。
肌肉骨骼系统对于平衡代谢活动和保持健康非常重要。骨骼肌是机体最大的器官之一,其质量和功能的丧失或减退会导致一系列疾病。虽然临床上用了很多方式来治疗缓解这类疾病,但有效的治疗方法却较少。
最近的研究表明,肠道微生物群稳态的破坏与肌肉骨骼系统功能异常相关,甚至可能导致肌肉骨骼系统功能异常。生活中也发现,肠道菌群与骨质疏松症的发病相关。如果你肠胃不好,时不时就腹泻腹胀、消化不良,当心了,骨质疏松也可能已经“盯”上了。
研究还表明,肠道菌群及其次级代谢产物可以通过调节炎症、免疫和蛋白质合成代谢、能量、脂质、神经肌肉接头、氧化应激、线粒体功能、内分泌和胰岛素抵抗等多种机制来影响肌肉骨骼系统。
现有文献大多支持合理的营养干预有助于改善和维持肠道菌群的稳态,并可能对肌肉骨骼健康产生积极影响。即使已提出“肠道菌群-肌肉轴”,但其因果联系仍然是未知的。
本文对现有文献进行整理、总结和讨论的目的是探讨营养补充、适度运动等干预方法能否通过调节肠道菌群微生态来影响肌肉和骨骼健康。未来更深入的功效验证实验将有助于临床应用。
骨 骼 肌
无菌小鼠:肠道菌群存在对骨骼肌健康很重要
基于无菌 (GF) 小鼠的实验揭示了体内肠道微生物群的存在或缺失,通过调节营养和能量代谢途径对骨骼肌的健康至关重要。缺乏肠道微生物群的小鼠的骨骼肌质量显著降低,无菌 (GF) 小鼠中肌球蛋白重组基因和骨骼肌分化调节基因的表达显着低于正常携带细菌的小鼠,而肌肉的表达萎缩标志物明显升高。
肠道菌群→蛋白质合成/能量代谢→骨骼肌营养
蛋白质合成和降解是影响骨骼肌质量的重要因素。胰岛素样生长因子1(IGF-1)是促进蛋白质合成和增强肌肉功能的重要物质,无菌小鼠体内的IGF-1水平显着下降。此外,无菌小鼠中糖皮质激素诱导的支链氨基酸分解代谢显着增加。
肠道菌群还可以通过改变能量代谢模式来影响骨骼肌。无菌小鼠葡萄糖和胰岛素含量较低,线粒体功能明显扰乱,影响骨骼肌对葡萄糖的利用,减少肌肉合成的能量供应,最终影响骨骼肌的氧化代谢能力。
肠道菌群调控神经肌肉接头
无菌小鼠的胆碱水平下降,导致神经肌肉接头传递受损。肌钙蛋白与骨骼肌中的肌纤维收缩性和运动功能有关。
无菌小鼠骨骼肌中肌钙蛋白编码基因的表达显着降低,表明肌纤维收缩力可能受损。更重要的是,将肠道微生物群移植到无菌小鼠体内后,结果显示骨骼肌质量增加,肌肉萎缩标记物减少,肌肉氧化代谢改善,神经肌肉接头组装基因表达增加。证据表明肠道微生物群在维持正常骨骼肌功能方面发挥着关键作用。
骨
骨骼通过骨成骨细胞(OB)和破骨细胞(OCL)不断重建。这个过程的不平衡会导致骨质疏松症。
早期研究发现,肠道微生物群也是骨量的主要调节者,其对骨量的影响是通过其对免疫系统的影响来介导的,免疫系统反过来又调节破骨细胞的生成。
肠道微生物群缺失对维持骨量有负面影响
无菌小鼠骨髓中破骨细胞前体细胞和破骨细胞的数量减少。此外,无菌小鼠肠道来源的 5-羟色胺和炎症细胞因子的水平降低。值得注意的是,肠道微生物群定植可以恢复无菌小鼠损失的骨量。当然,不排除其他机制也可能参与其中。
然而,最近的一项研究表明,成年雄性 GF BALB/c 小鼠的骨骼生长速度比正常饲养的小鼠慢。粪便微生物群对无菌小鼠的长期定植会导致股骨长度惊人的增加和骨小梁微结构的改善。
维生素D改善肠道钙吸收促进骨代谢
无菌小鼠的维生素D 代谢存在缺陷,而被微生物群定植的无菌小鼠则表明 1, 25-二羟基维生素 D 和钙水平得到恢复。因此,肠道微生物群也对骨骼产生有益影响。
骨 关 节
越来越多的证据表明肠道微生物组在骨关节炎(OA)的病理学中发挥着关键作用。早期研究表明,在无菌条件下, 在TLR4(Toll 样受体 4)缺陷小鼠中,类风湿性关节炎(RA) 表现也受到显着抑制,肠道微生物群可作为抗原或佐剂来诱导或促进类风湿性关节炎产生。
注:Toll样受体(TLR)是参与非特异性免疫(天然免疫)的一类重要蛋白质分子,也是连接非特异性免疫和特异性免疫的桥梁。当微生物突破机体的物理屏障,如皮肤、粘膜等时,TLR可以识别它们并激活机体产生免疫细胞应答(参考自百度百科)。
肠道微生物群对创伤性骨关节炎的发展产生影响
研究发现,无菌小鼠中内侧半月板不稳定手术引起的骨关节炎显着减少,表明肠道菌群促进了骨关节炎的发生。还发现肠道微生物组对小鼠模型中损伤引起的骨关节炎的严重程度有显着影响。
关节损伤后,无菌小鼠仅有轻微的骨关节炎症状,病理表现的严重程度最低。小鼠体内微生物组丰度与炎症生物标志物浓度、肠道通透性和骨关节炎严重程度呈正相关。这可能是因为在存在关节损伤的情况下,肠道微生物群(由更多的梭杆菌和粪球菌,以及更少的瘤胃球菌科)引起的免疫激活可能会加剧骨关节炎的病理过程。
以上无菌动物实验,主要是小鼠结果表明,肠道菌群的“存在与否”确实是影响和维持小鼠肌肉骨骼系统的关键因素。
无菌小鼠是通过无菌技术培育得到的。这里无菌小鼠既没有共生菌群,也没有致病菌等情况下,表现出不良的病理特征。这表明致病菌并非唯一的因素导致疾病发生。
疾病的发生通常是由多种因素共同作用引起的,包括宿主的遗传因素、环境因素和微生物因素等。致病菌可能需要与其他共生微生物或宿主因素相互作用才能引发疾病。在无菌小鼠中,缺乏这些相互作用,可能导致致病菌无法发挥其病原性。这刚好强调了微生物群落的复杂性和其与宿主的相互作用的重要性。
无菌小鼠试验的结果也需要与其他研究方法和模型相结合,例如体内试验、体外试验和临床研究,以获得更全面和准确的结论。综合多种研究方法的结果可以提供更可靠的科学依据,并有助于我们理解和解释无菌小鼠试验结果的适用性。
肠道微生物群失调一般主要指致病生物的大量繁殖、正常菌群的减少和微生物群组成多样性的减少。代谢、自身免疫、炎症和神经退行性疾病等多种因素与肠道菌群失调有关。微生物群失调对肌肉骨骼系统的影响引起了越来越多的关注。
扩展阅读:
骨 骼 肌
许多因素与肌少症的病理学相关,包括衰老、炎症、线粒体损伤和/或胰岛素抵抗。
注:肌少症是指因持续骨骼肌量流失、强度和功能下降而引起的综合症。患有肌肉减少症的老年人站立困难、步履缓慢、容易跌倒骨折。
几乎所有病理过程都会引发肠道微生物群的失调。反过来,微生物群失调也在骨骼肌质量和功能下降中发挥着至关重要的作用。由于肠道微生物组是导致肥胖或胰岛素抵抗等代谢失调表型的发生和加剧的原因,因此骨骼肌质量和功能可以部分受到肠道微生物组的调节。
老年人肠道菌群:促炎菌增多
健康肠道微生物群的主要门是厚壁菌门、拟杆菌门、放线菌门和疣微菌门,变形菌门的数量较少。在老年人和营养不良者中,都显示促炎症的变形计门增加,而产丁酸菌普拉梭菌,罗氏菌属减少。肠道菌群失调引起的循环促炎细胞因子的增加可以通过不同的机制(胰岛素抵抗、炎症和相关的氧化应激)诱导肌肉萎缩。
肠道菌群失调的两个最典型的例子:
炎症性肠病(IBD)和衰老引起的肌肉功能衰竭
接下来我们用这两个例子来具体阐述肠道菌群失调引起肌肉减少症的内在机制。
➤ IBD
IBD→肠道菌群失调→炎症→肌肉萎缩
IBD 的典型特征是肠道微生物群失调,肠道菌群失调往往伴随着肠道屏障损伤和肠道屏障通透性增加,内毒素和其他细菌代谢产物容易进入循环系统,从而增加LPS(脂多糖) 和其他炎症因子的水平,诱发体内的炎症反应。LPS 诱导的炎症的一个特征性表现是由于蛋白水解降解增加和蛋白质合成减少引起的严重肌肉萎缩。
肠道菌群失调→氧化应激→肌肉无力
肠道菌群的失调还可能导致肠道氧化应激、肠粘膜炎症和屏障功能障碍,从而引起免疫功能障碍。高水平的活性氧 (ROS) 引起的氧化应激可导致骨骼肌收缩障碍,导致肌肉无力和疲劳。因此,肠道微生物群失衡引起的炎症反应和氧化应激会对肌肉功能产生负面调节。
在结肠炎小鼠模型中,股四头肌和腓肠肌的骨骼肌质量和肌纤维横截面积减少,肌肉蛋白质含量减少。与此同时,肌肉功能障碍恶化,肌肉生长标志物 IGF-1 R(胰岛素样生长因子 1 受体) 和雷帕霉素磷酸化哺乳动物靶标 (mTOR) 下调。
研究人员认为,肠道微生物群失调引起的炎症可能是骨骼肌萎缩的触发因素。与肌原纤维分解相关的肌肉萎缩F-box(atrogin-1)和肌肉环指蛋白1(Murf-1)表达增强,介导肌原纤维加速分解。
IBD→炎症→肌肉合成和分解代谢→肌肉损伤
临床研究还发现,肌肉损伤是 IBD 等慢性胃肠道疾病的常见病理特征。42% 的 IBD 患者会出现肌肉减少症。
肠道微生物群刺激粘膜免疫细胞,促进促炎细胞因子(IL-6、IL-10、TNF-α等)的产生,产生一般状态慢性低度炎症,激活氧化应激损伤,进一步影响胰岛素敏感性、氨基酸生物合成、线粒体、生物生成、肌肉合成和分解代谢以及增加肌肉衰减相关分子途径。这可能导致肌肉骨骼损伤和虚弱。
➤ 衰 老
同样,体弱或活动能力差的老年人肠道微生物群的复杂组成也表现出不同程度的失调,物种丰富度降低以及机会性病原体和抗炎菌群之间的不平衡。
衰老→菌群多样性↓↓→代谢↓↓→炎症↑↑
肠道微生物群失调可能与肌肉萎缩的复杂机制有关。具体而言,肠道微生物群多样性因衰老而降低。同时,调节肠道环境的代谢能力也会下降,肠道屏障功能减弱,肠道粘膜通透性增加,从而导致包括脂多糖在内的细菌产物的吸收增加,并激活体内炎症反应。
与衰老相关的肠道微生物组会促进炎症,从而导致循环炎症介质的水平增加,而逆转这些与年龄相关的微生物组变化是减少与年龄相关的炎症和伴随发病率的潜在策略。
脂多糖促炎→代谢综合征→诱发骨骼肌衰老
脂多糖促进炎症信号传导,诱发骨骼肌炎症和胰岛素抵抗,从而促进代谢综合征的过程,进而诱发骨骼肌衰老。
研究表明,脂多糖相关细胞因子对蛋白质平衡(即合成和分解)的能力有决定性影响,并且随着衰老而增加的细胞因子可能会导致肌肉质量减少。
炎症反应增强会加剧骨骼肌质量损失
例如,在肌肉减少症患者中,IL-6 和 TNF-α 等促炎因子水平升高会导致肌肉质量减少。抗 TNF 治疗可以逆转微生物群中与年龄相关的变化,因此具有潜在的抗肌肉衰老作用。
肠道菌群变化与衰老中免疫稳态的紊乱有关
移植了年老小鼠肠道微生物群的年轻无菌小鼠的小肠,发现了与免疫相关的差异遗传特征,包括抗原呈递减少以及细胞因子和趋化因子产生的改变。这些基因可能在肠道微生物组老化过程中作为免疫紊乱的标志物发挥潜在作用。
肠道菌群失衡→肠漏→LPS释放到外周血
由于上述各种原因(炎症、营养不良、恶病质、衰老等)引起的肠道微生物生态系统组成的变化,可能导致肠漏和细菌内毒素(例如LPS)释放到外周血中。LPS可以通过TLR4受体触发巨噬细胞产生炎症细胞因子和ROS。
限制蛋白质合成,促进肌肉生长蛋白水解,肌肉萎缩
在骨骼肌中,TNF-α 激活参与NF-κB通路的基因表达,从而通过抑制肌细胞生成素和 myoD 来减少肌细胞分化和增殖。IL-6和IκB激酶可以抑制与诱导胰岛素抵抗相关的胰岛素受体底物1,限制mTORC1(雷帕霉素复合物1)肌肉靶标的激活,从而限制肌肉细胞中的蛋白质合成。
此外,由于蛋白激酶B受到抑制,叉头盒O的抑制作用不再发挥,导致泛素E3连接酶Atrogin-1和MuRF1表达增加,促进肌肉生长蛋白水解。
同样,不受 mTORC1 抑制的自噬激活激酶 1 进一步诱导骨骼肌细胞自噬。当肠道菌群失调引起的这些调节机制被激活时,蛋白质分解/合成之间就会出现不平衡,并最终导致肌肉萎缩。
其他机制:细菌群体感应,短链脂肪酸,胆汁酸
其他机制包括粪肠杆菌在细菌失调过程中产生的群体感应肽iAM373,下调了大多数骨骼肌发育和分化基因,降低了成肌细胞的代谢活性,并上调了肌管中的蛋白酶体降解途径,这是一种肌肉减少症新的诱导剂。
队列研究表明,肌肉减少症还与产生短链脂肪酸 的菌减少相关,从而导致肠道菌群失衡。
肠道菌群失调可能通过上调初级胆汁酸-法尼醇 X 受体途径导致骨骼肌萎缩。
骨
随着肠道微生物群在骨代谢稳态中的关键作用得到更好的了解,人们对肠道微生物群在调节骨骼健康中的重要作用越来越感兴趣(以前我们的文章专门介绍过肠道菌群与骨骼生长于骨代谢的关系,详见:肠道微生物如何影响骨骼发育和代谢 )。
肠道菌群失调与骨骼之间存在密切关系
研究发现,TLR5缺陷小鼠的肠道微生物群受损和微生物多样性较差会引起整体骨强度的变化;另外,长期使用抗菌药物引起的肠道菌群损伤(主要表现为拟杆菌、变形菌显著上调)导致小鼠骨性能受损,尤其是总骨量减少。卵巢切除术会导致小鼠肠道微生物群失调并导致骨质流失,这是由微生物依赖性 T 淋巴细胞(例如 Th17细胞)介导的。
骨密度低:
罗氏菌属、双歧杆菌属↓↓ 合成LPS的菌↑↑
在骨骼疾病患者中观察到肠道微生物群的变化。横断面研究表明,肠道微生物群与骨矿物质密度积累之间存在关联。最近,一项全基因组研究确定了与骨量变异相关的梭菌目和毛螺菌科。研究发现,与健康人相比,有害细菌过度生长的患者骨量较低,骨质流失率较高。
注:骨质流失加剧是 IBD 的常见并发症,肠道菌群失调也是IBD 的重要表现。
临床研究表明,骨矿物质密度低的个体肠道微生物群的组成和丰度显着下降。罗氏菌属(Roseburia)、双歧杆菌属和乳酸菌属等细菌群与骨密度呈正相关。然而,在骨矿物质密度较低的人群中,与LPS合成相关的微生物群更为丰富。
骨质疏松患者:多样性与骨密度呈负相关
研究发现,厚壁菌门/拟杆菌门的比例与骨量呈负相关,而放线菌和双歧杆菌与骨量呈正相关。使用 16sRNA 测序对骨质疏松症(OP)的肠道微生物群进行分析表明,肠道微生物群多样性估计值与骨矿物质密度呈负相关。
在骨质疏松患者中,如下菌属的丰度增加:
其他研究发现骨质疏松症患者Dialister和Faecalibacter显著增加。
菌群失调→营养素吸收能力下降→影响骨骼健康
微生物群对骨骼健康所需的营养素(例如钙和维生素 D)的运输和吸收具有必要的影响。肠道微生物群失调可能会损害营养物质和钙通过肠道进入循环系统的运输。随着年龄的增长,肠道对1, 25(OH) 2的吸收能力下降,这与肠道菌群失调密切相关。这也是微生物群失调影响骨骼健康的主要原因之一。
免疫系统干预肠道微生物群和骨代谢
生物多样性的变化和机会性病原体的定殖导致细菌内毒素的增加,例如脂多糖(LPS)、这与肠道炎症反应的增加有关,而炎症的增加与破骨细胞的激活有关。
肠道菌群失调会介导炎症
尤其是IL-1、TNF-α 和 IL-6,它们与骨质疏松症一样在破骨细胞激活中发挥着关键作用。
肠道微生物组依赖性Th17细胞和产生 TNF-α 的 T 细胞增殖产生大量促炎细胞因子(IL-17、TNF-α)、NF-κB 配体受体激活剂 (RANKL)、并减少RANKL拮抗剂的分泌(RANKL诱导破骨细胞功能,IL-17减少骨形成;TNF-α增强RANKL活性,诱导Th17细胞增殖和活化,是该过程中潜在的免疫调节机制。
注:Th17细胞是一类免疫细胞,主要参与调节免疫系统的炎症反应,并在自身免疫性疾病和炎症性疾病中发挥重要作用。
新生成的破骨细胞诱导了 Treg 细胞的生成。它抑制免疫反应,诱导和维持免疫耐受,通过多种途径减少炎症,并产生免疫抑制细胞因子,例如 TGF-β 和 IL-10。 Treg 细胞和 Th17 细胞之间微妙而复杂的关系会影响骨骼健康。重要的是,肠道细菌是控制这种平衡的关键。
注:破骨细胞是一种骨髓源性巨核细胞系的细胞,主要功能是吸收和降解骨组织。
Treg细胞是调节性T细胞(Regulatory T cells)的简称。它们是一类免疫细胞,主要功能是抑制免疫系统的活性,以维持免疫平衡和自身耐受。
肠道菌群→血清素下调→调节骨代谢
5-HT是5-羟色胺的缩写。它是一种神经递质,也称为血清素。根据合成部位分为两类:脑源性5-HT和肠源性5-HT。
有趣的是,这两种 5-HT 具有不同的功能:肠道来源的血清素对骨形成有负面影响,而大脑来源的血清素则具有相反的影响。近年来研究发现,肠道菌群不仅诱导细胞因子调节骨代谢,还通过减少血清素生物合成酶、增加血清素转运蛋白,下调肠源性血清素水平,从而调节骨代谢。
肠道菌群→改变 IGF-1→调节骨质量
IGF-1 在骨形成和生长的调节中也起着至关重要的作用。肠道微生物群可能通过改变 IGF-1 水平来调节整体骨质量。例如,传统特定肠道微生物群对成年 GF 小鼠的定植可以增加循环 IGF-1 并增加骨的形成和吸收。
菌群多样性↓↓→循环雌激素↓↓→影响骨钙沉积
肠道微生物群多样性减少也可能导致循环雌激素减少,进而影响正常骨钙沉积,因为肠道微生物群通过β-葡萄糖苷酶分泌调节雌激素,β-葡萄糖苷酶将雌激素分解为其活性形式。
注:IGF-1是胰岛素样生长因子-1(Insulin-like Growth Factor 1)的缩写。它是一种蛋白质激素,由肝脏和其他组织产生,并受到生长激素的调控。IGF-1促进细胞增殖和分化,对于骨骼和肌肉的生长和修复具有重要作用;也与肿瘤生长和代谢相关;较高的IGF-1水平与较长的寿命和较少的年龄相关疾病风险有关。
▸▹小结
根据上述研究结果提示,与肌肉健康类似,骨骼健康相关的肠道菌群紊乱主要表现为肠道优势菌群消失或减少,有害菌或衰老菌群的增殖导致LPS等产生过多或引起更多的炎症反应。机制主要涉及细胞因子以及Treg和Th17细胞的成骨/破骨平衡的微妙控制。
与肌肉健康不同,肠道菌群失调对钙离子有效吸收的影响以及肠道来源的 5-HT、IGF-1 和雌激素的调节作用也在此强调。这些机制是否也对肌肉健康发挥作用,可能是个有意义的探索方向。
骨 关 节
近年来,越来越多的证据表明肠道菌群失调与类风湿关节炎(RA)的发生和发展密切相关。在人类和动物研究中也观察到类风湿关节炎中肠道微生物群失调。
类风湿关节炎:拟杆菌↓↓,乳杆菌属、普雷沃氏菌属↑↑
在类风湿关节炎模型小鼠中,拟杆菌门减少、厚壁菌门和变形菌门增加。该模型还导致 14 种肠道细菌失衡,并对色氨酸、脂肪酸和次级胆汁酸等代谢物产生相当大的干扰。
在类风湿关节炎患者中,各种乳杆菌属(Lactobacillus)和普雷沃氏菌属( Prevotella)更加丰富;因此,普氏菌数量增加和肠道菌群失衡是 类风湿关节炎发展的潜在资源。
广古菌门(Euryarchaeota)与类风湿关节炎的严重程度直接相关,成为类风湿关节炎发病的独立危险因素。
拟杆菌丢失,普雷沃氏菌存在
在未经治疗的新发类风湿关节炎患者的粪便微生物群中,普雷沃氏菌(Prevotella)的存在同时拟杆菌的丧失(拟杆菌与普雷沃氏菌一般认为是拮抗菌)存在强烈相关性。
从类风湿关节炎患者的滑膜组织中分离出细菌 rRNA。类风湿关节炎患者肠道菌群中乳杆菌的数量和多样性显著增加,与报道胶原蛋白诱导性关节炎小鼠体内乳酸杆菌增加的数据一致。矛盾的是,嗜酸乳杆菌(Lactobacillus acidophilus)和干酪乳杆菌( Lactobacillus casei)似乎有利于类风湿关节炎的改善。
致病菌破坏屏障,促炎,诱导关节炎发生和维持
肠道机会致病菌,如普雷沃氏菌,可能通过增强细胞凋亡机制、破坏肠道屏障完整性,参与促炎免疫状态的形成,从而诱导关节病炎症的发生和维持。此外,Th17 细胞通过产生一系列炎症因子来促进破骨细胞分化,这些炎症因子是导致类风湿关节炎骨质破坏期的原因。拟杆菌的减少可能通过减少 Treg 细胞分化来促进局部炎症环境。
骨关节炎的发生可能是由于肠道菌群组成发生特异性变化,尤其是机会性促炎菌增多,具有抗炎特性的共生菌显著减少,肠道通透性增加,然后LPS引起炎症和免疫反应,诱导级联信号通路激活,导致关节病变甚至疼痛,但相关证据有限。而类风湿性关节炎与免疫炎症相关的研究相对深入,肠道菌群多样性较为丰富,但也导致机制更加复杂,需要进一步探索。
这里主要总结了益生菌及其次级代谢产物对肌肉骨骼系统的影响和机制。
骨 骼 肌
由于肠道微生物组的活性,肠道与骨骼肌相关,并通过调节全身/组织炎症、胰岛素敏感性等来调节肌肉功能。
益生菌通过改善肠道微生物群的多样性,来对抗肌肉质量和功能的损失。
➤小鼠模型
在小鼠癌症模型中,罗伊氏乳杆菌能够抑制恶病质的发展,并与肌肉质量的保存有关。
植物乳杆菌HY7715通过改善老年 Balb/c 小鼠的骨骼肌质量和功能来改善肌肉减少症。
补充植物乳杆菌TWK10 可改善小鼠的运动表现并增加肌肉质量。
副干酪乳杆菌PS23 通过确保 SAMP8 小鼠的线粒体功能来减缓与年龄相关的肌肉损失。恢复特定乳酸杆菌水平可减少急性白血病小鼠模型中的炎症和肌肉萎缩标志物。
其他实验还表明,至少有七种益生菌对小鼠骨骼肌质量和强度有益:
其中,使用最广泛的菌株是乳杆菌和双歧杆菌,它们可以改善肌肉质量、力量和耐力损失。
益生菌有助于肌肉健康,提高蛋白质合成和力量,但益生菌的作用可能针对不同的信号或代谢途径和组织,例如降低炎症和压力、维持肌肉蛋白质合成、并提高了肌肉力量。然而也有研究表明,对肌肉质量和功能的影响几乎很小,仅观察到一定的抗炎作用。
➤人类
年轻人:益生菌可以改善运动耐力、增肌
在人类中,已经发现摄入特定的益生菌可以改变肠道微生物群,有利于增加骨骼肌质量。例如,摄入植物乳杆菌TWK10 六周可以提高年轻人在跑步测试中的耐力表现。补充植物乳杆菌表明,益生菌可以改善运动表现、耐力以及身体成分,减少脂肪量并增加肌肉量。
老年人:需进一步探索益生菌对肌肉的影响
不过,也有报道称,老年人补充益生菌在一定程度上可以导致肠道菌群发生有益变化,减少病原体,改善便秘,但对宿主健康的影响相对较小。
含有乳酸菌和双歧杆菌菌株以及干酪乳杆菌的对老年人的肌肉状况没有影响。这些发现表明益生菌的作用机制很复杂,需要进一步研究。
最近的一项荟萃分析表明,补充益生菌可以增强肌肉质量和力量,但在总去脂体重方面没有观察到有益效果。该研究表明,探索不同老龄化人群生理机制的差异,并探索补充合适的益生菌菌株以获得最佳肌肉质量和力量非常重要。
上述发现,研究的稀缺性、人群的变异性和重复性低,导致很难找到优化肌肉质量和功能的特定益生菌菌株,需要在更明确的人群中进行进一步研究设计个性化的益生菌干预措施。
— 改善血糖,提高肌肉质量和功能
益生菌可降低厚壁菌门与拟杆菌门的比例,从而提高小鼠的肌肉质量、耐力和力量。添加 植物乳杆菌 TWK10和 CP2998 可通过抑制糖皮质激素受体激活、改善血糖对肌肉发挥积极作用。
扩展阅读:
— 抑制炎症反应,改善肌肉合成
补充干酪乳杆菌LC122 和 长双歧杆菌BL986可降低炎症细胞因子 TNF-α、IL-6 和 IL-1β 的表达,并改善肌肉蛋白合成。
口服短双歧杆菌和鼠李糖乳杆菌可显着降低小鼠促炎细胞因子 IL-2、IL-4、IL-6 和 TNF-α 的水平,从而抑制炎症反应。还通过增加 IL-10 水平来减轻肌肉炎症。
还发现含有植物乳杆菌 TWK10 和罗伊氏乳杆菌的可以改善小鼠的肌肉质量,这与减少炎症和肌肉萎缩标记物表达有关。
— 抗氧化,或增加蛋白质吸收的方式
服用副干酪乳杆菌PS23的老年小鼠肌肉中抗氧化应激因子(例如超氧化物歧化酶和谷胱甘肽过氧化物酶)的表达较高。
罗伊氏乳杆菌可提高乳清蛋白中亮氨酸的吸收比例,从而增强蛋白质吸收,提高蛋白质利用率,最终促进肌肉合成,增加肌肉质量。
— 其他作用机制
益生菌的有益作用还通过多种机制产生,包括诱导免疫调节、抵抗生理应激、抑制病原体和改善肠上皮细胞的屏障功能。益生菌调节肌肉的潜在机制主要包括:
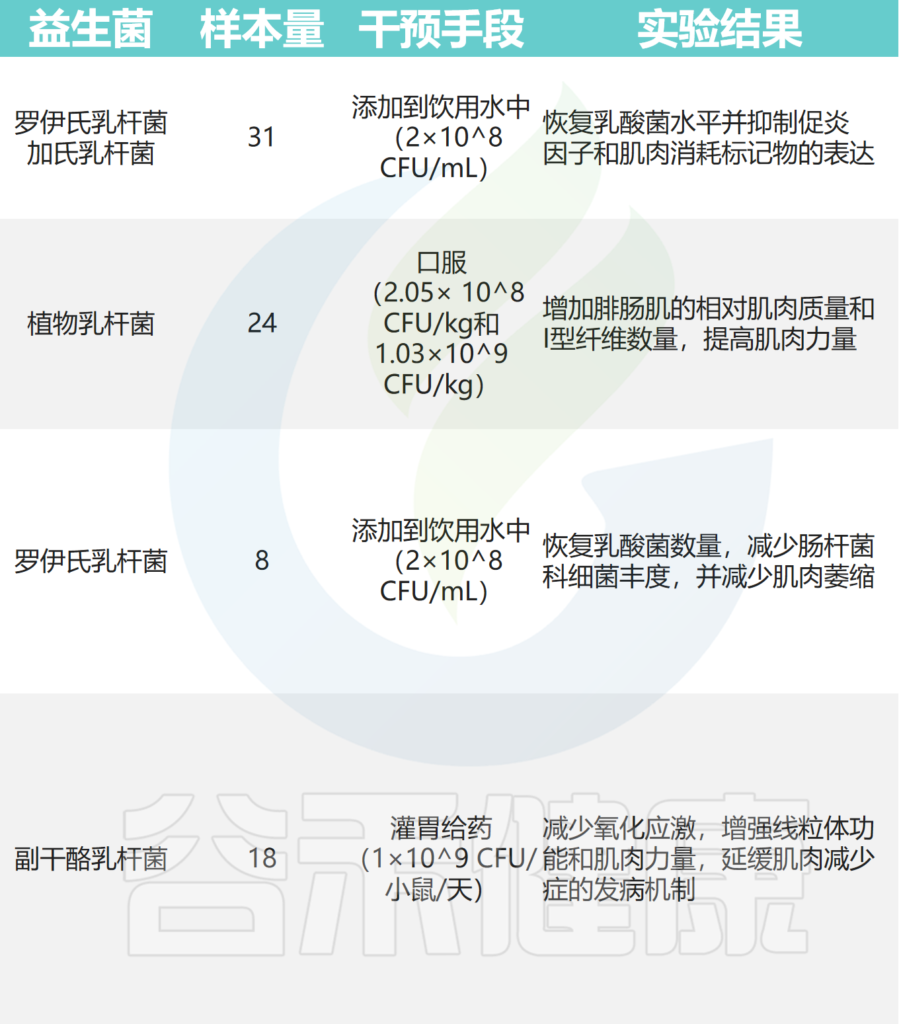
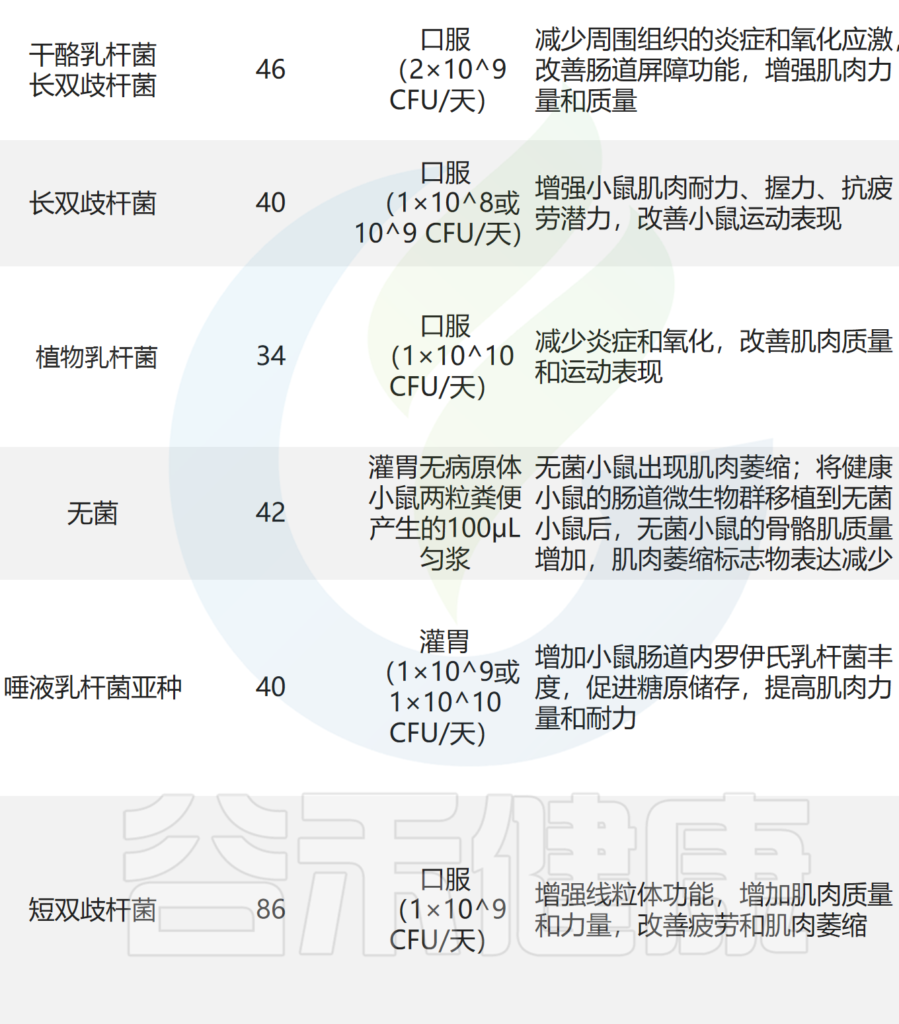
doi: 10.1080/19490976.2023.2263207
肠道益生菌限制胰岛素抵抗、调节代谢途径或抑制氧化应激和炎症。肠道菌群还可以通过不同的代谢途径将营养物质分解为次级代谢产物,调节肠道免疫和代谢稳态,维持宿主与肠道菌群之间的共生和寄生关系。
下面讨论这些代谢产物对骨骼肌代谢的主要影响和作用机制。
短链脂肪酸(SCFA)是肠道菌群对膳食纤维发酵产生的代谢产物,主要包括丁酸盐、丙酸盐和乙酸盐。SCFA 在葡萄糖和脂质稳态、炎症调节以及肠道与其他远端组织之间的连接中发挥着重要作用。
SCFA在调节肠道环境稳态、改善糖代谢、促进钙磷吸收、缓解氧化应激和炎症反应等方面发挥着重要作用,对调节骨骼肌功能具有重要意义。
无菌小鼠接受 SCFA 治疗后,骨骼肌损伤得到部分逆转(SCFA 降低了 atrogin-1 表达,增加了 MyoD 以及肌肉质量和功能),表明肠道菌群产生的 SCFA 在调节骨骼肌功能中发挥着关键作用。
丁酸盐:保持肌肉质量
在一项针对雌性 C57BL/6 小鼠的研究中,丁酸盐治疗后后肢肌肉萎缩得到完全或部分改善,而常规饮食喂养的老年 C57BL/6 雌性小鼠后肢肌肉质量显着降低。丁酸盐不仅能保持肌肉质量,还能改善小鼠的葡萄糖耐量,但对胰岛素耐量没有显着影响。
丁酸盐:改善线粒体功能,减少氧化应激,防止骨骼肌损伤
丁酸盐还能增加线粒体蛋白孔蛋白和线粒体转录因子 A 的水平,并显着改善骨骼肌细胞中的线粒体功能。
此外,丁酸盐治疗可减少小鼠氧化应激表达和细胞凋亡标记物,并改变抗氧化酶的活性,从而防止氧化应激引起的骨骼肌损伤。
丁酸盐:改善与年龄相关的肌肉损失
丁酸盐是一种重要的 SCFA 和组蛋白脱乙酰酶抑制剂,可调节与年龄相关的肌肉损失。丁酸盐已可以通过抑制组蛋白脱乙酰酶表达并改善老年小鼠的肌肉质量和横截面积来促进肌肉合成。
乙酸盐:促进葡萄糖吸收,减少肌内脂质生成
添加乙酸盐可以促进兔骨骼肌中的葡萄糖吸收和糖原生成,并通过增加脂肪酸和氧化来减少肌内脂质生成。
此外,SCFA 还可诱导 IGF-1 产生,从而促进肌肉合成代谢。SCFA 的这些代谢影响可能直接作用于骨骼肌,也可能通过刺激胰高血糖素样肽 1 (GLP-1) 分泌而间接产生。SCFA 对肌肉的其他间接影响包括加速血流效应。
分解色氨酸,产生吲哚代谢物:抗炎,增强肌肉蛋白合成
色氨酸是人体不可缺少的芳香氨基酸。肠道菌群分解色氨酸过程中产生的富含吲哚和吲哚衍生物的代谢物在维持肠道环境稳态和肠道菌群多样性方面发挥着关键作用。
来自肠道微生物群的吲哚代谢物可以增强体内IL-10水平,而IL-10在调节宿主炎症状态方面具有抗炎作用。
其他研究的证据表明,色氨酸代谢物吲哚丙烯酸可通过下调炎症和氧化应激相关基因表达来促进肠道屏障功能并抑制炎症反应。当机体处于慢性炎症状态、肌肉蛋白合成受到限制时,色氨酸代谢物的抗炎作用尤其重要。
肠道菌群→影响胆汁酸代谢→影响骨骼肌代谢
胆汁酸是肝脏产生并分泌到肠道的小代谢分子,参与膳食脂质吸收。肠道菌群可以改变胆汁酸的结构、生物利用度和生物活性,从而影响胆汁酸代谢和宿主代谢稳态。
肠道厌氧菌已被证明可以将初级胆汁酸转化为次级胆汁酸。毛螺菌科也可以产生 SCFA 并从初级胆汁酸转变为次级胆汁酸。
肠道菌群可能参与胆汁酸代谢和 FXR-FGF19 信号通路(有证据表明 FGF19 激活可以抑制肌肉萎缩标志物的蛋白表达,增强与生肌分化相关的分子,调节骨骼肌蛋白平衡,这反过来又影响骨骼肌代谢。次级胆汁酸还可以通过促进脂质和葡萄糖代谢来增强肌肉功能。
益生菌→促进维生素合成→影响骨骼肌功能
维生素是人体必需的微量营养素,大部分是人体无法合成的。实验证据证实,肠道益生菌促进体内维生素的合成,对骨骼肌功能有显著影响。例如,双歧杆菌和乳酸杆菌可以合成B族维生素 (包括叶酸、核黄素、维生素 B12)。B族维生素是直接参与能量代谢的水溶性维生素,它们的缺乏会导致心肌损伤和心力衰竭。维生素 B12缺乏会增加同型半胱氨酸水平并导致肌肉损伤。
骨
先前的研究表明,益生菌有利于肠道稳态,并在预防和治疗骨质流失中发挥关键作用。
益生菌
胃肠道中乳杆菌的上调可以产生有效的杀菌剂和有机酸,从而抑制致病性大肠杆菌。肠道菌群中乳酸杆菌和乳球菌丰度的增加。
罗伊氏乳杆菌补充剂可以显着改善肠道微生物群的不平衡,增强肠道屏障功能以防止骨质流失。
在一项随机对照试验中,75-80 岁骨量低的绝经后妇女每天服用罗伊氏乳杆菌,12个月后骨密度下降的比例明显低于对照组,这表明益生菌补充可以减少骨质流失。
补充普通双歧杆菌还可以降低 LPS 浓度,从而抑制炎症反应并防止骨质流失。
嗜酸乳杆菌和克劳氏芽孢杆菌(Bacillus Clausii)可以通过平衡炎症细胞因子的水平来维持骨稳态。
长双歧杆菌还可以预防和治疗骨质疏松症,通过增强成骨细胞活性和抑制破骨细胞形成来改善骨质流失。
此外,益生菌可以通过调节矿物质吸收来改善骨骼健康。例如,长双歧杆菌可以通过改善钙、磷酸盐和镁等矿物质的吸收来增强骨密度。罗伊氏乳杆菌可以通过抑制破骨细胞来减轻骨质流失。
益生菌促进维生素B12、维生素D、钙等吸收
维生素B12水平低还会抑制成骨细胞活性,从而增加骨质疏松风险,甚至诱发骨折。
益生菌如乳酸菌和双歧杆菌,在促进核黄素和叶酸的形成方面发挥着关键作用。核黄素和叶酸对于促进维生素合成和调节炎症反应很重要。研究表明,核黄素在一定程度上具有抗炎作用,其摄入可抑制大鼠白细胞中TNF-α的释放。
核黄素还作为抗氧化酶的辅助因子调节氧化应激。叶酸与调节胰岛素抵抗和抑制促炎细胞因子 IL-6、IL-8 和 TNF-α 有关。
不难发现,B族维生素的抗炎、抗氧化、参与能量代谢等功能对于维持骨骼健康是不可或缺的。钙和维生素 D 的吸收对于健康的骨骼维护尤为重要,益生菌可降低肠道PH值并改善钙吸收,从而增强骨骼功能。
多联益生菌→抗炎→减轻骨关节炎
在骨关节炎(OA)大鼠模型中,益生菌复合物通过抑制促炎细胞因子和软骨破坏来减轻骨关节炎的发展。
在一项人体试验中,537 名 骨关节炎(OA) 患者随机分配到干酪乳杆菌或安慰剂组,6 个月后,与对照组相比,干酪乳杆菌组的全身炎症显着降低。口服嗜热链球菌可改善骨关节炎变性。
口服丁酸梭菌(Clostridium butyricum)可有效保存 骨关节炎大鼠膝关节软骨和滑膜,显着减少纤维组织量,并显着降低骨和软骨各种炎症和代谢标志物的血清浓度。
干酪乳杆菌通过下调促炎细胞因子来减轻关节炎症损伤。益生菌最近添加到治疗关节炎症的药物清单中,因为干酪乳杆菌可以抑制关节肿胀、减少类风湿性关节炎,并防止关节炎症大鼠的骨质破坏。
嗜酸乳杆菌和干酪乳杆菌也常用于治疗类风湿性关节炎的缓解剂。还有人提出,用于缓解类风湿性关节炎相关后果的益生菌补充剂的可用性仍然很弱,而且益生菌对类风湿性关节炎的影响似乎是菌群特异性的。
肠道菌群代谢产物
短链脂肪酸:参与骨代谢,抑制骨吸收
短链脂肪酸(SCFA)参与骨代谢并影响骨形成和吸收。SCFA 对骨量的保护作用与抑制骨吸收有关。从潜在机制来看,丁酸盐和丙酸盐诱导破骨细胞代谢重编,增强糖酵解,下调关键破骨细胞基因,显着减少破骨细胞数量,从而抑制骨吸收。
因此,SCFAs是破骨细胞代谢和骨稳态的有效调节剂,在促进骨形成中发挥重要作用。
丁酸盐:促进骨合成代谢,维持骨代谢平衡
在一项小鼠研究中,发现丁酸盐可以通过调动成骨细胞中的 Wnt 信号通路来促进骨合成代谢并增加骨量。
此外,丁酸盐可以保护成骨细胞前体细胞免受过氧化氢诱导的损伤,并促进成骨细胞的矿化和分化。它主要通过增强细胞抗氧化酶的活性、促进ATP的产生、降低ROS水平来维持骨代谢的平衡。
短链脂肪酸还可诱导 IGF-1 的产生
IGF-1除了促进骨骼肌功能外,在骨代谢中起着至关重要的作用。IGF-1参与骨形成和吸收,调节骨代谢平衡。因此,SCFA 在维持骨代谢过程中的体内平衡中发挥着关键作用。
短链脂肪酸→调节IL-10→减轻关节炎
乳酸菌产生的丁酸通过控制软骨细胞自噬和炎症细胞死亡来抑制骨关节炎。益生菌衍生的丁酸盐可以通过影响 T 和 B 细胞的进展来抑制小鼠关节炎。
色氨酸代谢与骨代谢密切相关
犬尿氨酸是一种色氨酸代谢物,是色氨酸酶降解后形成的第一个稳定代谢物。
犬尿氨酸在骨代谢中的关键功能似乎是加速骨质流失并介导对骨骼的不利影响。犬尿氨酸含量随着衰老而增加,其对骨骼的不利影响可能是由于其对破骨细胞活化的影响,导致骨骼脆性增加和骨重塑失衡。
其他研究表明,犬尿氨酸水平升高会损害成骨细胞分化并增加破骨细胞吸收,从而加速骨骼老化。
次级胆汁酸调节骨稳态
次级胆汁酸还通过调节成骨细胞和破骨细胞之间的信号转导来调节骨稳态。此外,次级胆汁酸诱导 GLP-1 的产生,GLP-1 调节葡萄糖稳态并刺激成骨细胞分化并能进一步增强骨骼系统的功能。
对于益生菌及其次级代谢产物,其抗炎和免疫调节特性值得进一步研究,以确定其在肌肉骨骼系统中的作用和生物学机制。
小结
常见肠道微生物群对肌肉骨骼系统的影响
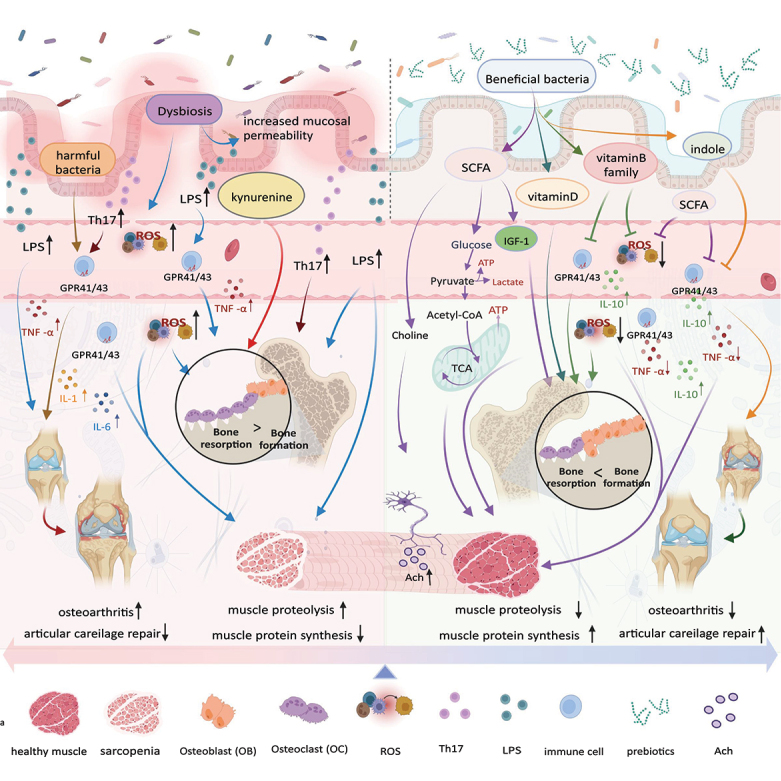
doi: 10.1080/19490976.2023.2263207
肠道微生物群及其产生的代谢物的重要作用:
然而,肠道微生物群的失衡还会引发一系列负面影响:
肠道菌群与肌肉骨骼系统的正常代谢密切相关。可以采取适当的干预措施,促进肠道益生菌发挥最佳调节作用。
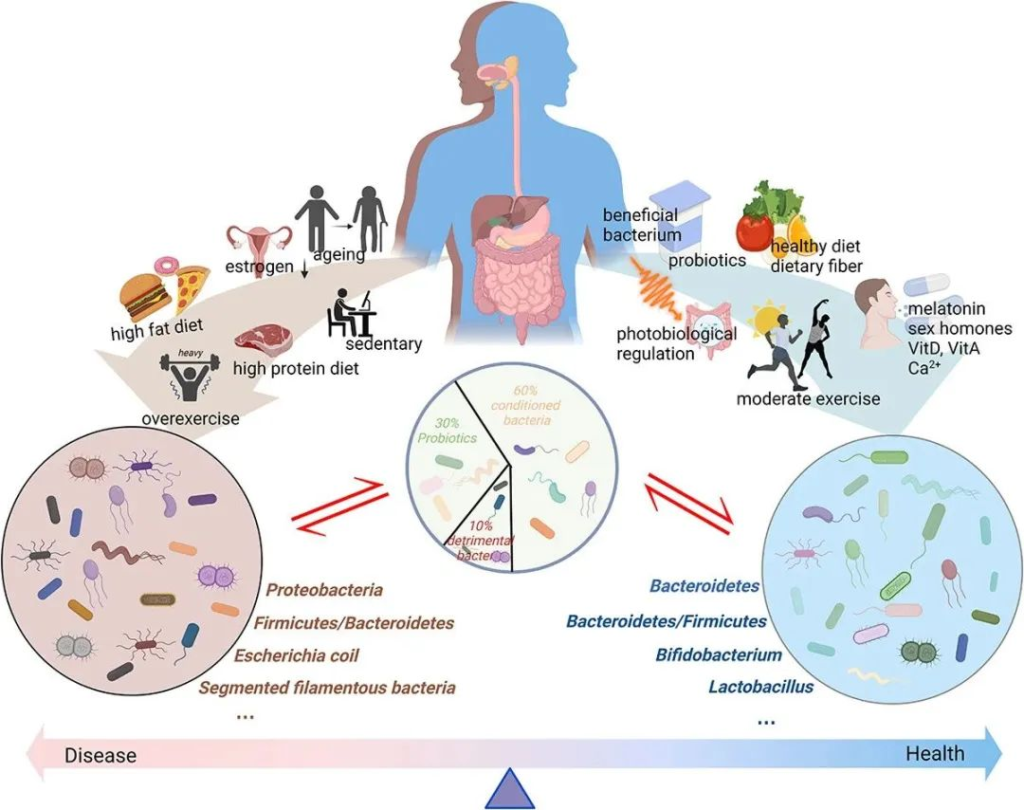
doi: 10.1080/19490976.2023.2263207
肠道微生物群一般分为三类:益生菌、有害菌和条件菌。
不同的生活方式对肠道微生物群产生不同的影响。衰老、性激素分泌减少、高脂肪饮食、高蛋白饮食以及久坐的生活方式或过度运动会对肠道微生物群产生负面影响。这些都会导致有害细菌比例增加,诱导粘膜通透性并引发一系列负面反应。同时,健康饮食、适度运动、光生物调节、补充益生元和益生菌、维生素、钙、性激素、褪黑素等可以促进肠道菌群的积极变化,从而增强肌肉骨骼系统功能。
促进肌肉骨骼系统健康
益生元通过选择性刺激某些肠道菌群的活性或生长,对宿主肌肉骨骼系统产生有益的生理作用。益生元有助于有益菌生长,比如乳杆菌和双歧杆菌等,常见的益生元有菊粉、低聚糖等。
益生元可改善肠道屏障功能和宿主免疫力,并减少梭菌等潜在致病菌的丰度。
益生元→炎症↓↓→肌肉质量↑↑
结果表明,喂食益生元纤维寡糖的小鼠的循环 LPS 水平和炎症降低,肌肉质量增加。此外,补充益生元可提高双歧杆菌、乳杆菌、拟杆菌门/厚壁菌门的比例。
同时,益生元作为膳食纤维的一种,也可以促进 短链脂肪酸的生成。
维生素D:有利于钙吸收、维持肠道屏障
维生素 D 是增加骨量的关键因素。除了直接影响钙吸收外,维生素 D 还通过维持肠道屏障的完整性来调节肠粘膜稳态,从而影响免疫系统功能和炎症反应。维生素D可以抑制促炎因子的水平,促进体内抗炎因子的分泌。
维生素D:改善肠道微生物稳态、促进肌肉合成
具体研究结果表明,维生素 D 补充剂可以调节女性肠道菌群并增加其多样性。维生素D补充后,AKK菌和双歧杆菌的相对丰度增加。
争议:维生素D能否改善肌少症,需要更多研究
维生素 A 在维持肠道屏障功能、调节免疫反应和细菌多样性以维持肠道稳态方面表现出类似的功能。但是同时有报道称,补充维生素 D 并不能改善社区老年人的任何肌肉减少症指数,并且可能会损害身体功能的某些方面。需要更多的实验证据来阐明维生素 D 的作用。
钙:菌群多样性↑↑ 有益菌↑↑ 保护肠道屏障
钙是体内最常见的矿物质,其摄入量关系到骨骼的健康发育。钙也是维持骨骼肌正常兴奋和收缩功能的最重要元素。膳食钙摄入量会引起肠道微生物群的变化。例如,用膳食钙喂养的小鼠肠道微生物群多样性显著增加,双歧杆菌、拟杆菌、瘤胃球菌科(Ruminococcaceae)和阿克曼氏菌(Akkermansia)丰度更高。
此外,膳食钙似乎对肠道屏障具有保护作用,通过增加宿主体内膳食钙的吸收来增加缓冲能力并促进骨量。总之,膳食钙可调节肠道微生物群,与宿主建立交叉对话,促进新陈代谢,并促进肌肉骨骼健康。
促进肌肉骨骼系统健康
肠道微生物群最近被定义为宿主营养信号的“传感器”。所消耗食物的类型和多样性与肠道微生物群的组成密切相关。
动物性饮食:拟杆菌门↑↑ 乙酸盐、丁酸盐↓↓
先前研究的证据表明,饮食模式的长期变化会引起肠道菌群的变化。短期饮食改变也会导致肠道微生物群的变化。例如,从植物性饮食转变为动物性饮食后,肠道中乙酸盐和丁酸盐的浓度显着降低。此外,以动物为基础的饮食增加了拟杆菌门的数量,并减少了厚壁菌门数量。
富含蛋白质的饮食:菌群多样性↑↑ 拟杆菌↑↑
骨骼肌质量受到肌肉蛋白质合成和分解的影响,肠道微生物群随年龄的变化也受到膳食蛋白质摄入量的影响。此外,摄入富含蛋白质的饮食与肠道微生物群的多样性呈正相关,可以提高肠道微生物群中拟杆菌。
长期高蛋白饮食:并不总是对肌肉产生积极影响
耐力运动员长期服用牛肉蛋白补充剂会减少双歧杆菌等有益肠道细菌的丰度。此外,结肠中未消化的蛋白质残留物发酵产生的化合物对肠道、免疫和代谢功能具有潜在的负面影响。
高脂肪饮食:炎症↑↑ 氧化应激、 变形菌↑↑
对高脂肪饮食小鼠的研究表明,这种饮食会增加体重和炎症标记物的表达,并降低葡萄糖耐量;更重要的是,高脂肪饮食喂养的小鼠体内LPS的循环水平增加了两到三倍,这导致肠道通透性增加,从而引发损害肌肉质量的炎症反应。
高脂饮食摄入引起的肥胖还可能导致体内 ROS 过量产生和氧化应激反应,并随之增加脂肪因子群和 TNF-α 表达,从而加重体内慢性炎症反应并影响骨骼肌肉功能。此外,高脂肪饮食可以减少 SCFA 的产生,并增加变形菌的比例。
地中海饮食:均衡蛋白质、碳水化合物、多酚,有益菌↑↑ 炎症↓↓
较高的碳水化合物摄入量与肠道菌群多样性下降密切相关。虽然双歧杆菌含量增加,但乳酸菌和链球菌含量减少。
咖啡、茶和红酒富含多酚,多酚与益生元丰度和双歧杆菌活性有关。膳食多酚可以增加产短链脂肪酸菌的繁殖并抑制产LPS菌的生长,从而调节肠道微生物群并影响肌肉骨骼系统健康。
地中海饮食的摄入有助于维持健康的肠道菌群,因为该饮食均衡摄入优质蛋白质和复合碳水化合物以及较高水平的纤维和多酚。因此,健康的饮食可以提高益生菌的相对比例并调节炎症,而不健康的饮食会导致肠道菌群失调、氧化应激、炎症等不良反应,最终损害肌肉骨骼系统的健康。
促进肌肉骨骼系统健康
运动改善效果大于营养补充剂
适度的运动可以改善肌肉、骨骼和关节。研究结果表明,运动干预可以有效改善60岁以上老年人的肌肉质量和功能,并且运动的效果明显大于营养补充剂。
运动还可以有效增加骨矿物质密度,提高骨强度,降低骨质流失风险以及跌倒和骨折的发生率。同样,运动可以缓解骨关节炎患者的疼痛、增强关节功能并提高生活质量。
运动:改善肠道菌群、改善肌肉骨骼健康(动物)
在人类和动物实验中,运动可以促进肠道微生物群的积极变化,从而改善肌肉骨骼功能。高强度训练可以防止高脂肪饮食诱导的肥胖小鼠中与肥胖相关的肠道微生物群失调,并维持肠道微生物群的多样性。非肥胖小鼠的拟杆菌与厚壁菌门的比例在运动后也会发生变化,并且拟杆菌的丰度在运动后显着增加。
在一项针对肥胖大鼠的运动和饮食研究中,随着时间的推移,运动对肠道微生物群产生更强、更稳定的影响,并能更有效地促进肠粘膜完整性和代谢功能。
运动员多样性高,肠道菌群有助于运动中乳酸转化为丙酸
关于运动与肠道微生物群之间关系的人体研究也获得了类似的结果。接受强化训练的精英运动员肠道微生物群的相对丰度明显高于久坐的成年人。
职业橄榄球运动员的肠道微生物群多样性高于非职业运动员。职业运动员的炎症细胞因子水平也低于非职业运动员。此外,研究表明,肠道微生物群菌群还可以通过将运动过程中产生的乳酸转化为丙酸,从而延长跑步时间,提高运动成绩。
扩展阅读:
肠道微生物组如何影响运动能力,所谓的“精英肠道微生物组”真的存在吗?
有氧运动:拟杆菌↑↑ 改善心肺健康
有氧运动期间人体中拟杆菌门和厚壁菌门之间的平衡对于维持健康至关重要,肠道细菌定植平衡的破坏可能导致炎症和代谢或神经系统疾病。
日本一项关于有氧运动干预老年女性肠道微生物群的研究表明,为期 12 周的有氧运动计划不仅增加了拟杆菌,而且还改善了心肺健康。同时,快走时间增加超过 20 分钟的受试者中拟杆菌的丰度。
因此,适度运动可以通过改善肠道菌群组成、增强肠道粘膜功能、抑制炎症反应、维持多种肠道菌群来增强肌肉骨骼功能。
有氧运动+益生元:改善代谢紊乱,预防膝关节损伤
运动对肠道微生物群的潜在影响介导了骨关节炎的过程。在一项动物研究中,研究人员给高糖、高脂肪饮食的小鼠,同时进行有氧运动、益生元或两者的结合,发现两种干预措施的结合完全可以预防肥胖老鼠的膝关节损伤。
有趣的是,另一项研究表明,有氧运动和益生元的结合可以改善肥胖大鼠的代谢紊乱,但不能改善膝关节先前存在的骨关节炎损伤。因此,需要进一步研究进行更大样本的临床调查。
过度运动:促炎,限制肌肉形成、微生态失衡
过度运动可能会促进炎症、营养限制以及氧化和代谢应激,从而限制肌肉形成。过度训练的其他负面影响包括肠道缺血、肠道屏障通透性增加和氧化应激,从而导致肠道微生态失衡、炎症反应增加、分解代谢增加和肌肉功能恶化。
定期训练与更好的生物多样性和对肠道微生物群的有益影响有关。某些研究的证据支持这样的观点,即疲劳训练可能与有害的微生物后果有关。因此,运动对肠道菌群的影响可能取决于运动的强度和持续时间。
促进肌肉骨骼系统健康
肠道细菌与人体细胞的比例因性别而异,女性的比例高于男性。细菌与人体细胞的比例男性为1.3,女性为2.2 。
绝经后女性:厚壁菌门 / 拟杆菌门比例 ↓↓
女性肠道微生物的多样性也更高。Akkermansia muciniphila在女性中尤其丰富。绝经前女性的厚壁菌门/拟杆菌门比例高于绝经后女性。
绝经前女性中普雷沃菌属、毛螺菌属(Lachnospira)、嗜胆菌属( Bilophila)的相对丰度低于绝经后女性,同时炎症水平的 IL-6 和单核细胞趋化蛋白-1 血浆水平也较低。
这表明雌激素可能影响肠道微生物稳态和免疫的调节。与此同时,肠道菌群失衡也会影响雌激素活性。
绝经后雌激素水平下降,对肠道屏障和骨骼健康造成损害
如前所述,肠道微生物群通过分泌 β-葡萄糖苷酶来调节雌激素,当这一过程因肠道菌群失调(其特点是微生物多样性减少)而受到损害时,会导致循环雌激素减少,从而影响骨骼代谢。
非卵巢雌激素更多地受到肠道微生物组的影响,这可能是绝经后妇女更容易患骨质疏松的原因之一。因此,维持肠道稳态对于雌激素的正常分泌和骨代谢的平衡至关重要。
老年人睡眠障碍:与肠道菌群,肌少症相关
人们认为肌肉骨骼健康的丧失与睡眠障碍有关。同时,在老年人中,较短的睡眠时间与促炎细菌的增加有关,而睡眠质量的改善与Warts microbacteria、Flatcoccus有关。
年轻人睡眠中断:肠道菌群变化介导促炎状态
在年轻人中,睡眠中断对肠道微生物组成的影响,特别是有益的厚壁菌门与拟杆菌门的比例,仍然是矛盾且不清楚的。这项研究不仅将加深对肌肉减少症的多种影响因素的理解,而且还可以对这种复杂的情况提供更全面的看法。
当睡眠不佳时,肠道微生物群经常发生变化,这可能介导睡眠障碍和肌肉减少症之间的促炎症状态。
这些发现不仅表明肠道微生物群在睡眠质量和肌肉减少症之间的相关性中发挥着重要作用,而且还暗示调节睡眠的激素(例如褪黑激素)可能是有效的干预目标之一。
褪黑素:调节睡眠、抗炎抗氧化、保护骨骼肌
褪黑素是另一种调节睡眠和昼夜节律的内源性激素,具有抗衰老、抗炎和抗氧化特性,是一种用于疾病治疗和骨骼肌质量改善的安全膳食补充剂。褪黑素可减少氧化应激和炎症,并保护骨骼肌免受氧化损伤。
此外,它还可以改善衰老过程中的肌肉线粒体功能。对老年人的研究也表明褪黑激素水平与肌肉力量之间存在显著相关性。
褪黑素:逆转睡眠剥夺小鼠的肠道菌群失衡
有趣的是,睡眠剥夺小鼠的肠道菌群减弱,益生菌种类有限。有趣的是,褪黑素治疗逆转了这种异常的微生物组组成。褪黑激素可以改善动物和人类的肠道微生物群。口服褪黑激素补充剂可以减少脂质积累,逆转肠道微生物群失衡,并改善肠道菌群的多样性。
褪黑素:改善肠道生态失衡,恢复SCFA水平
高脂肪饮食喂养的小鼠肠道中SCFA水平显著降低,但在补充褪黑激素后恢复。此外,高脂饲料喂养的小鼠补充褪黑素可以有效改善肠道生态失衡,褪黑素可以改变厚壁菌门与拟杆菌门的比例,增强肥胖小鼠的肠粘膜功能。
褪黑素:减轻胰岛素抵抗,参与骨代谢
同时,补充褪黑激素减轻了小鼠因低度炎症和高脂肪饮食摄入引起的胰岛素抵抗。褪黑激素可以调节胰岛素敏感性,因此在维持葡萄糖稳态和调节葡萄糖代谢方面具有关键作用。
褪黑素还可通过激活核因子红细胞 2 相关因子 2 (Nrf2)/过氧化氢酶信号通路抑制破骨细胞形成,从而治疗炎症性骨溶解。
因此,我们可以推断,褪黑激素可以增强肠道粘膜功能,改善脂质和糖代谢,并通过调节肠道微生物群失调促进 SCFA 的产生,从而最终增强肌肉骨骼系统的功能。
促进肌肉骨骼系统健康
作为一种局部治疗,光生物调节在临床上用于治疗各种病症,包括肌肉疲劳、关节和肌腱炎症以及伤口和骨折愈合。
光生物调节:肠道菌群多样性↑↑
对健康小鼠腹部照射PBM后,小鼠肠道菌群发生显着变化,肠道菌群多样性也显着增加。这种效果在每周接受 3 次红光治疗的小鼠中最为明显,但在接受单次红光治疗的小鼠中则不明显。
近红外光比红光发挥更显着的效果
近红外照射后,小鼠肠道菌群中益生菌的比例显着增加,并且治疗还调节了与肠道菌群失衡相关的细菌丰度;这种作用可能归因于 PBM 对肠道微生物群的抗炎和氧化还原信号作用。
紫外线辐射:影响肠道菌群,维生素D和钙吸收,促进骨骼健康
紫外线辐射也会影响骨质流失大鼠模型中的肠道微生物群结构和功能。除了抗炎作用外,紫外线辐射还可以通过诱导维生素D合成和肠道钙吸收来调节骨代谢,从而促进骨形成、减少骨吸收、增强骨矿物质密度。该证据表明,尽管没有太多直接证据,但 PBM 仍然显示出通过调节肠道菌群失衡维持肌肉骨骼系统稳态的潜在作用。PBM 有潜力作为辅助疗法(与饮食和运动一起)来平衡微生物组并促进肌肉骨骼健康。
包括运动、电针和补充益生菌在内的生活方式干预措施对肠道微生物群有直接影响,改变其组成和功能,改善疼痛和生活质量,这为患有多种慢性疾病的患者开辟了新的治疗机会的创新途径。
肠道和骨骼之间的跨学科作用越来越引起骨生物学领域的关注。肠道菌群调节肌肉骨骼健康的潜在机制包括蛋白质、能量、血脂、糖代谢、炎症水平、神经肌肉连接性和线粒体功能。
肠道菌群的组成和代谢变化可能会影响肌肉骨骼系统的功能。肠道菌群失衡增加促炎因子水平,激活氧化应激途径,减少肌肉质量,影响骨形成和吸收。
肠道菌群调节的个性化治疗对于肌肉骨骼系统疾病的治疗来说既困难又充满希望。
临床应用,还需深入研究
在粪便移植的临床研究中,现有的荟萃分析对粪便移植对85种疾病的治疗效果进行综述发现,大多数研究是在传染病和肠道疾病方面进行的,而与肌肉骨骼健康直接相关的研究很少。
不同人群的年龄、遗传背景、生活方式等背景下,肠道微生物群变化可能会汇聚成不同的病理微生物群模式,这些复杂的相互作用需要进行大规模的纵向研究才能解决。
临床应用刚刚开始,考虑到微生物菌群的复杂性和个体差异,是否适合筛选促进肌肉骨骼健康的细菌,或者基于人类粪便细菌移植的个体化治疗;无论是肠道微生态干预的手段和方法,还是肠道微生态干预的效果,都还需要大量的临床证据来支持,需要共同努力才能实现。
多种干预措施,组合探索
基于肠道菌群在肌肉骨骼系统中的作用机制,可以采用不同的干预措施,如益生菌、益生元、维生素和膳食钙等,改善肠道菌群的组成和代谢,增强肌肉骨骼系统功能。
此外补充雌激素和褪黑激素以及光生物调节等新兴方法已显示出调节肠道微生物群和促进肌肉骨骼健康的潜力,特别是联合使用时。各种合理干预方法的组合应用也是一种有意义的探索。
包括运动在内的生活方式干预措施对肠道微生物群有直接影响,改变其组成和功能,这为患有多种慢性疾病的患者开辟了新的治疗机会的创新途径。
主要参考文献:
Wang Y, Li Y, Bo L, Zhou E, Chen Y, Naranmandakh S, Xie W, Ru Q, Chen L, Zhu Z, Ding C, Wu Y. Progress of linking gut microbiota and musculoskeletal health: casualty, mechanisms, and translational values. Gut Microbes. 2023 Dec;15(2):2263207.
Sender R, Fuchs S, Milo R. Revised estimates for the number of human and bacteria cells in the body. PLoS Biol.2016;14(8):e1002533.
Petermann-Rocha F, Balntzi V, Gray SR, Lara J, Ho FK, Pell JP, Celis‐Morales C. Global prevalence of sarcopenia and severe sarcopenia: a systematic review and meta-analysis. J Cachexia Sarcopenia Muscle. 2022;13(1):86–35.
Ayers C, Kansagara D, Lazur B, Fu R, Kwon A, Harrod C. Effectiveness and safety of treatments to prevent fractures in people with low bone mass or primary osteoporosis: a living systematic review and network meta-analysis for the American college of physicians. Ann Intern Med. 2023;176(2):182–195.
Wei J, Zhang Y, Hunter D, Zeng C, Lei G. The gut microbiome-joint axis in osteoarthritis. Sci Bull (Beijing). 2023;68(8):759–762.
Dey P, Chaudhuri SR, Efferth T, Pal S. The intestinal 3M (microbiota, metabolism, metabolome) zeitgeist – from fundamentals to future challenges. Free Radic Biol Med. 2021;176:265–285.
Gilbert JA, Blaser MJ, Caporaso JG, Jansson JK, Lynch SV, Knight R. Current understanding of the human microbiome. Nat Med. 2018;24(4):392–400.
Turnbaugh PJ, Ley RE, Hamady M, Fraser-Liggett CM, Knight R, Gordon JI. The human microbiome project. Nature. 2007;449(7164):804–810.
Fan Y, Pedersen O. Gut microbiota in human metabolic health and disease. Nat Rev Microbiol. 2021;19(1):55–71.
Delzenne NM, Neyrinck AM, Backhed F, Cani PD. Targeting gut microbiota in obesity: effects of prebiotics and probiotics. Nat Rev Endocrinol. 2011;7(11):639–646.
Ma Q, Li Y, Li P, Wang M, Wang J, Tang Z, Wang T, Luo L, Wang C, Wang T, et al. Research progress in the relationship between type 2 diabetes mellitus and intestinal flora. Biomed Pharmacother. 2019;117:109138.
Lynch SV, Pedersen O, Phimister EG. The human intestinal microbiome in health and disease. N Engl J Med. 2016;375(24):2369–2379.
Ridaura V, Belkaid Y. Gut microbiota: the link to your second brain. Cell. 2015;161(2):193–194.
Chen Y, Zhou J, Wang L. Role and mechanism of gut microbiota in human disease. Front Cell Infect Microbiol. 2021;11:625913.
Dinan TG, Cryan JF. Brain-gut-microbiota axis and mental health. Psychosom Med. 2017;79(8):920–926.
Hu X, Wang T, Jin F. Alzheimer’s disease and gut microbiota. Sci China Life Sci. 2016;59(10):1006–1023.
Witkowski M, Weeks TL, Hazen SL. Gut microbiota and cardiovascular disease. Circ Res. 2020;127(4):553–570.
Qin J, Li Y, Cai Z, Li S, Zhu J, Zhang F, Liang S, Zhang W, Guan Y, Shen D, et al. A metagenome-wide association study of gut microbiota in type 2 diabetes. Nature. 2012;490(7418):55–60.
Moludi J, Maleki V, Jafari-Vayghyan H, Vaghef-Mehrabany E, Alizadeh M. Metabolic endotoxemia and cardiovascular disease: a systematic review about potential roles of prebiotics and probiotics. Clin Exp Pharmacol Physiol. 2020;47(6):927–939.
Koh A, De Vadder F, Kovatcheva-Datchary P, Backhed F. From dietary fiber to host physiology: short-chain fatty acids as key bacterial metabolites. Cell. 2016;165(6):1332–1345.
Bana B, Cabreiro F. The microbiome and aging. Annu Rev Genet. 2019;53(1):239–261.
Strasser B, Wolters M, Weyh C, Kruger K, Ticinesi A. The effects of lifestyle and diet on gut microbiota composition, inflammation and muscle performance in our aging society. Nutrients. 2021;13(6):2045.
谷禾健康
偏头痛
偏头痛是一种常见且使人衰弱的神经系统疾病,也是世界经济的重大负担。大约14%的成年人患有偏头痛。其特点是反复出现一侧或两侧严重头痛(抽痛),并伴有独特的相关症状,包括畏光、恐声、恶心、呕吐等。
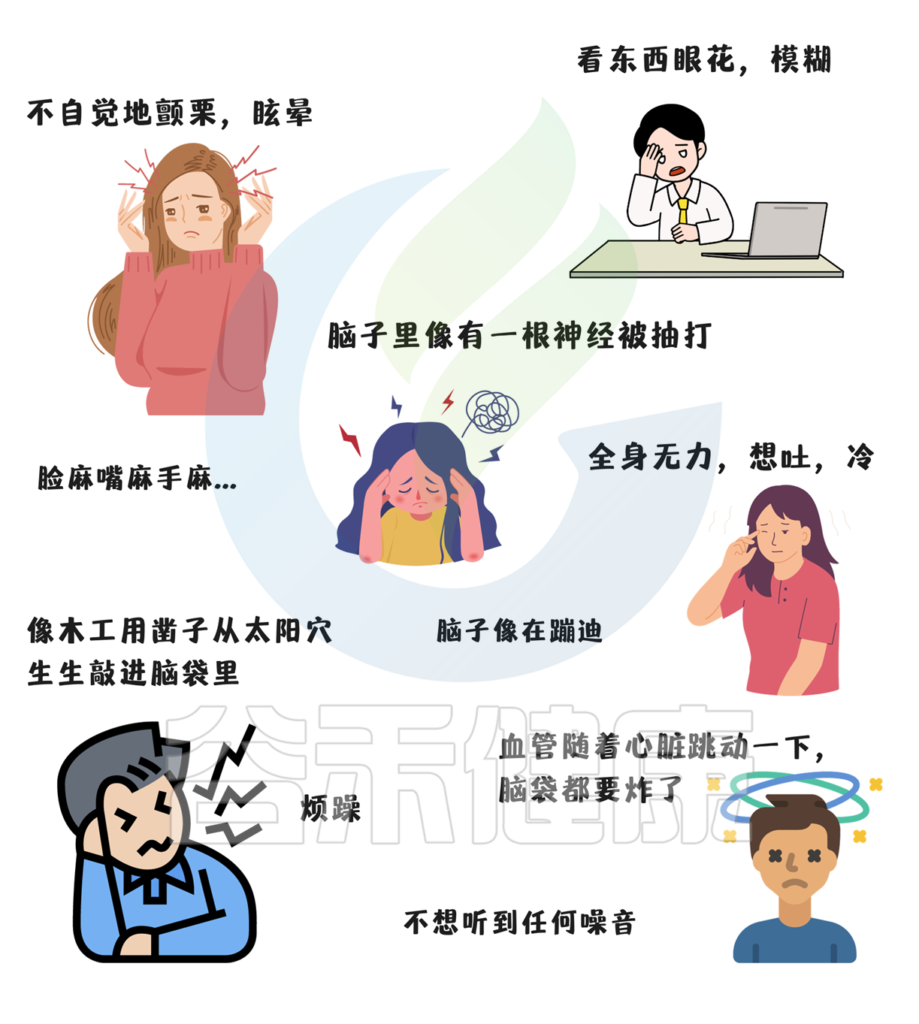
偏头痛在儿童晚期/青春期早期发病,在 40 多岁的人群中发病率最高,此后发病率下降。在所有年龄段中,女性偏头痛的发病率始终高于男性。
潜在危险因素包括压力、饮食、急性药物过量、激素波动、睡眠、环境、天气等。
对偏头痛根本原因的研究已经跨越了几个世纪,涉及外周和中枢机制等,但其根本机制仍未完全了解。已经确定三叉神经系统的激活和敏化在偏头痛发作期间至关重要。
胃肠道系统和中枢神经系统之间存在双向关系。多项研究表明偏头痛与某些胃肠道疾病有关,例如幽门螺杆菌感染、肠易激综合征(IBS)、胃轻瘫、乳糜泻等。
越来越多的证据表明微生物介导的肠-脑串扰可能导致偏头痛的发病机制。在偏头痛患者中,肠道微生物群的组成发生了改变,包括肠道菌群多样性下降,产丁酸菌减少,梭状芽孢杆菌增加等。
偏头痛患者肠道和大脑之间的相互作用,可能受到多种因素的影响,如炎症介质(IL-1β、IL-6、IL-8 和 TNF-α)、肠道微生物群、肠道菌群代谢产物、血清素途径、谷氨酸途径、神经肽(包括 CGRP、P物质、PACAP、NPY)等。
本文主要介绍了偏头痛相关症状、发病人群、四个阶段,基于偏头痛的发病机制,阐述肠道微生物群如何通过各个途径参与偏头痛的病理生理学,并探讨了潜在的干预策略。

很多人在听到偏头痛这个词的时候,会想到严重的头痛,但头痛并不直接等于偏头痛,头痛只是偏头痛的一种症状。
偏头痛是一种常见的神经系统疾病,会引起多种症状,最明显的是头部一侧的搏动性头痛,伴随着头部不适感和其他一些症状。
偏头痛是原发性头痛,这意味着它不是由其他疾病引起的。偏头痛的发作通常会对患者的日常生活和工作造成较大的干扰,那么偏头痛发作时,具体会有什么表现?
偏头痛可能会有以下症状:
日常体力活动、运动,甚至咳嗽或打喷嚏都会加剧头痛。
偏头痛最常发生在早晨,尤其是刚醒来时。有些人会在可预测的时间出现偏头痛,例如月经前或一周紧张工作后的周末。许多人在偏头痛后感到疲惫或虚弱,但在两次发作之间通常没有症状。
偏头痛的频率可以是每年一次、每周一次、或介于两者之间的任意时间。
每月发生两到四次偏头痛是最常见的。
未经治疗的发作持续 4~72 小时。
大多数偏头痛持续约 4 小时,但严重的可能会持续 3 天以上。
偏头痛的两种主要类型是:
先兆偏头痛
以前称为经典偏头痛,包括视觉障碍和其他神经系统症状,这些症状在实际头痛前约10-60分钟出现,通常持续不超过一小时。个人可能会暂时失去部分或全部视力。这种先兆可能会在没有头痛的情况下出现,并且随时可能发作。
其他典型症状包括:
说话困难;身体一侧感觉异常、麻木或肌肉无力;手或脸有刺痛感,意识混乱。头痛之前可能会出现恶心、食欲不振以及对光、声音或噪音的敏感性增加。
无先兆偏头痛
或普通偏头痛是更常见的偏头痛形式。症状包括毫无征兆地出现头痛,通常在头部的一侧感觉到,并伴有恶心、意识模糊、视力模糊、情绪变化、疲劳以及对光、声音或噪音的敏感性增加。
其他类型包括:
经期偏头痛
这些通常发生在经期开始前 2 天,并持续到经期后 3 天。可能还会在每月其他时间出现其他类型的偏头痛,但月经前后的偏头痛通常没有先兆。
沉默偏头痛
会出现前兆症状,但没有头痛。事实上,前兆通常是这种类型偏头痛的主要警告信号。但可能还会出现恶心和其他偏头痛症状。它通常只持续约20-30分钟。
前庭偏头痛
有平衡问题、眩晕、恶心、呕吐,伴或不伴头痛。这种情况通常发生在有晕车病史的人身上。
腹部偏头痛
可能会导致胃痛、恶心和呕吐。它经常发生在儿童身上,随着时间的推移可能会变成典型的偏头痛。
偏瘫偏头痛
身体一侧出现短暂瘫痪 (偏瘫)或无力。可能还会感到麻木、头晕或视力变化。这些症状也可能是中风的征兆,因此请立即寻求医疗帮助。
眼部偏头痛
也称为眼部或视网膜偏头痛。它会导致一只眼睛短暂、部分或完全丧失视力,并伴有眼睛后面的钝痛,这种疼痛可能会扩散到头部的其他部位。请立即就医检查这些症状。
带脑干先兆的偏头痛
头痛之前可能会出现头晕、意识混乱或失去平衡。疼痛可能会影响头后部。这些症状通常突然出现,并可能伴有说话困难、耳鸣和呕吐。这种类型的偏头痛与激素变化密切相关,主要影响年轻的成年女性。请立即就医检查这些症状。
持续偏头痛
这种严重类型的偏头痛可持续超过 72 小时。疼痛和恶心非常严重需要去医院。有时,药物或停药可能会导致它们出现。
眼肌麻痹性偏头痛
这会导致眼睛周围疼痛,包括周围肌肉麻痹。这是医疗紧急情况,因为这些症状也可能是由眼睛后面的神经受压或动脉瘤引起的。其他症状包括眼睑下垂、复视或其他视力变化。
活动性偏头痛的高峰发病年龄为 40 岁左右,其中 35%左右的女性和15%左右的男性受到影响。
doi: 10.1038/s41572-021-00328-4.
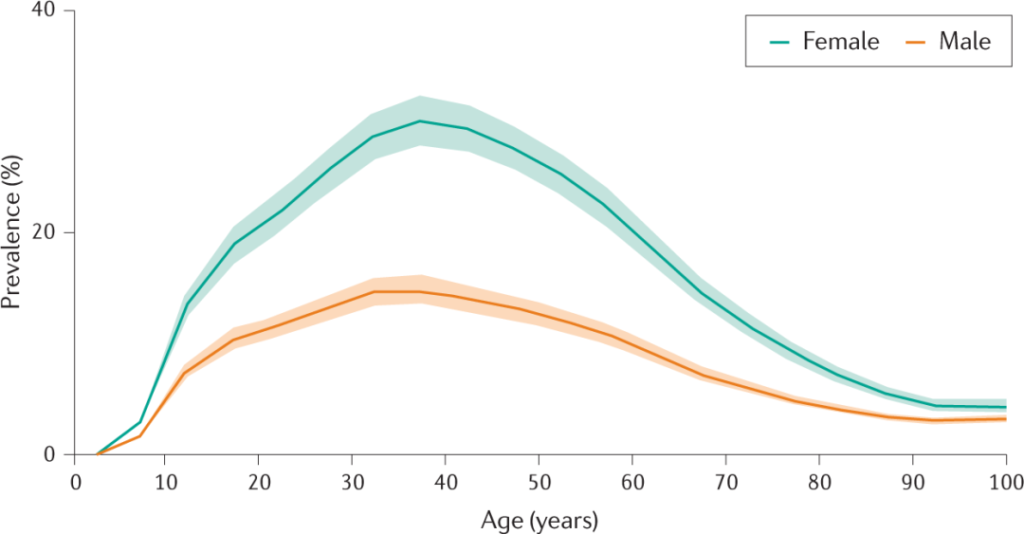
一些常见的偏头痛诱因包括:
许多女性注意到她们在月经期间、怀孕期间或排卵期间会感到头痛。症状也可能与更年期、使用激素避孕或激素替代疗法有关。
当感到压力时,大脑会释放化学物质,这些化学物质会导致血管变化,从而可能导致偏头痛。
某些食物和饮料,例如陈年奶酪、酒精、硝酸盐(意大利辣香肠、热狗和午餐肉中的硝酸盐)、味精等食品添加剂,高盐和加工食物,可能对部分人造成影响。
摄入过多或未达到习惯的摄入量都会导致头痛。咖啡因本身可以治疗急性偏头痛。
风暴锋、气压变化、强风或海拔变化都可能引发偏头痛。
大声的噪音、明亮的灯光和强烈的气味都会引发偏头痛。
口服避孕药、血管扩张剂可以扩张血管,从而引发这些症状。
这包括体育锻炼和性生活等。
当睡眠过多或不足时,可能会感到头痛。
不良习惯包括不吃饭(或推迟进餐),吸烟,酗酒等,还有晕车也都可能引发偏头痛。
doi.org/10.1016/j.biopha.2021.111557
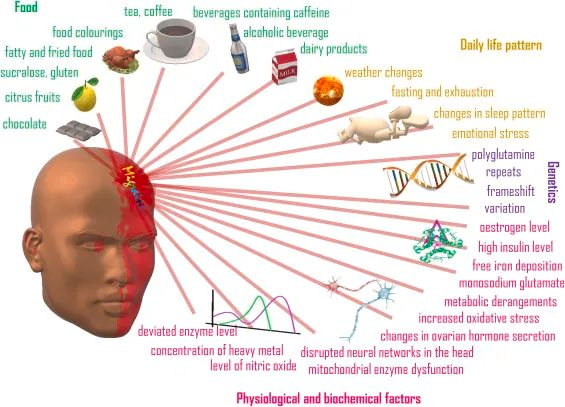
前驱症状阶段
有时称为头痛前阶段,此阶段的特点是在偏头痛出现前数小时或数天出现,特点是没有疼痛的症状。这些包括情绪波动、对食物的渴望、颈部僵硬、严重口渴、腹胀、便秘或腹泻、注意力不集中、排尿增多等。
先兆阶段
先兆是指偏头痛之前或期间发生的感觉障碍。这些障碍会影响一个人的视力、触觉或言语,但并不是每个偏头痛患者都会出现视觉异常期。例子包括:
视力模糊、看到黑点、波浪线、闪光或不存在的东西、渐渐扩大的盲点、手臂麻木、手臂和腿部有沉重感、口齿不清或语句混乱。
头痛阶段
这是通常出现疼痛的阶段,疼痛程度可能从轻微到无法忍受。
偏头痛通常以钝痛开始,然后发展为抽痛,有时候是钻孔感。也可能出现颈部疼痛、僵硬、鼻塞、恶心、呕吐、失眠等。
体力活动以及接触光、声音和气味可能会加剧疼痛。然而,有些人在发作偏头痛时并不会出现头痛。
恢复阶段
最后阶段是疼痛消退时。在此阶段,人们可能会感到疲惫、困惑或总体不适。
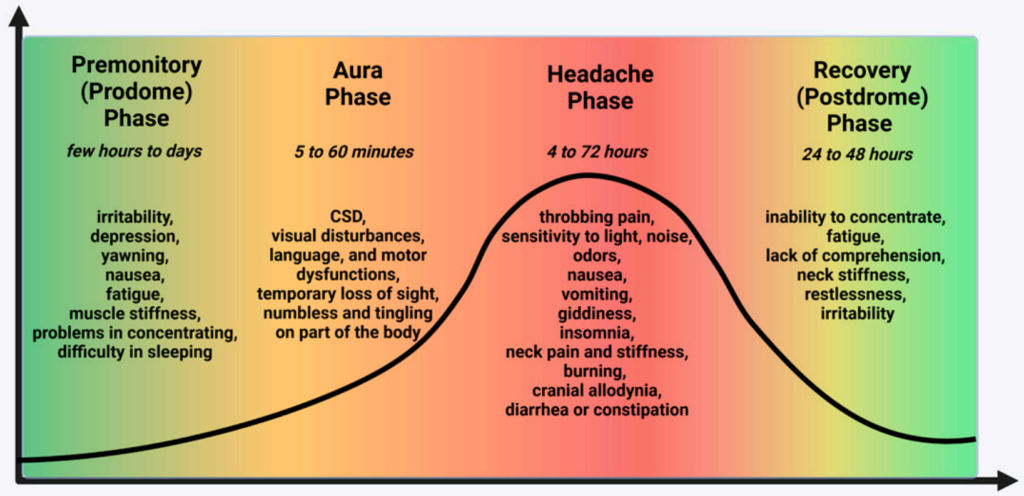
doi.org/10.3390/neurolint15030073
简单来说,在偏头痛发作之前几天,可能会感到疲劳,情绪变化,打哈欠,出现睡眠问题,恶心等情况,对光和声音敏感,这些预警信号与大脑中某个特殊的区域——下丘脑有关。下丘脑通常控制体内激素平衡,昼夜节律等,偏头痛发作之前下丘脑很活跃。
偏头痛还有常见的症状,视觉变化,刺痛感,言语困难等,这些感觉与细胞膜电位变化相关,导致脑活动和血流变化在大脑中扩散,电位变化快速在大脑表面传播,它传向哪里,哪里就出问题(*>﹏<*) …当它侵入视觉皮层,可能出现视觉盲点。
在头痛阶段,三叉神经起到关键作用,三叉神经会传递来自脸部皮肤,头皮,覆盖大脑皮层的血管和膜层的触觉,温度等,一旦被激活,三叉神经会传递痛觉信号,当偏头痛发作时,这个痛觉通路会变得敏感化,也就是说能触发痛觉的阈值下降了,那么平时不太会引起疼痛的也变得容易痛了,比如说,咳嗽,弯腰,一些强光,噪声等都会引起疼痛。
具体来说,关于偏头痛的发病机制,目前主要有以下几种理论。
I) 血管学说
该学说认为由血管舒缩功能障碍引起。基于先兆期间大脑血管收缩引起的三叉神经过度兴奋,随后产生炎症神经肽释放引起血管舒张,导致偏头痛。
II)神经学说 (皮层扩散性抑制)
该学说认为偏头痛是原发性神经功能紊乱疾病。其中通过皮层-三叉神经通路,大脑皮层的过度神经兴奋(异常的神经放电)会增加细胞外谷氨酸、钙离子、钠离子和钾离子的释放,从而引发去极化作用,造成皮质扩散性抑制(CSD)。
皮质扩散抑制是什么意思呢?
它其实是一种缓慢传播的大脑活动改变波,涉及神经、血管功能的巨大变化,皮质扩散抑制可能是偏头痛先兆的原因。这些慢电波可以激活负责感知大脑周围覆盖物(“脑膜”)疼痛的神经,并改变血管功能,这两者都可能导致偏头痛。
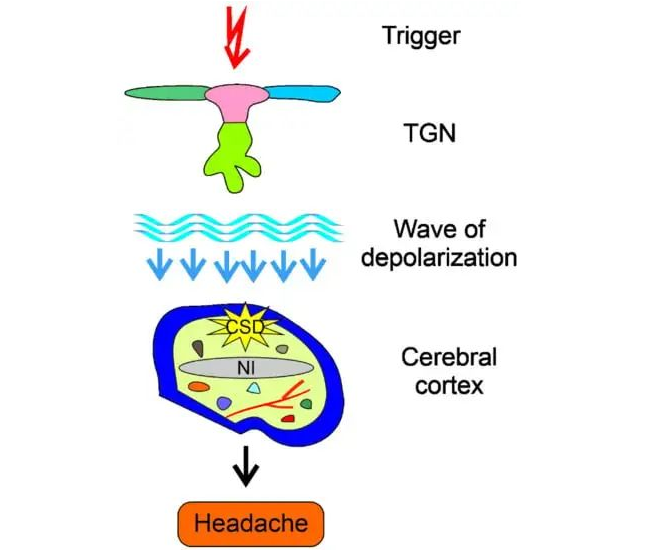
doi.org/10.3390/ijms221810134
III)三叉神经血管学说 (近年流传较广)
三叉神经感觉纤维的激活(传递疼痛信号),导致脑膜血管(硬脑膜)发生痛性神经源性炎症,此过程通过炎症神经肽(CGRP、SP、NK-A)的释放介导,这表明CGRP释放与神经源性硬脑膜血管舒张有关,这可能在偏头痛的发生中很重要。
注:关于CGRP在第四章节会详细介绍。
简单来说,激活三叉神经血管通路:
激活三叉神经元 → 释放P物质、CGRP等血管活性神经肽 → 血管扩张和促炎分子(组胺、缓激肽)的释放 → 神经源性炎症 → 激活脑膜痛觉受体
偏头痛中的 CGRP 和三叉血管系统
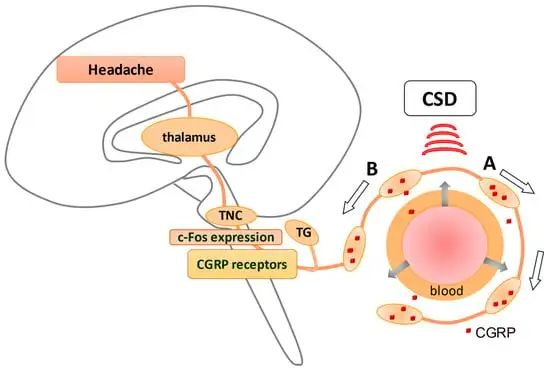
doi.org/10.3390/ijms22168929
三叉血管系统是一组感知面部和大脑覆盖层疼痛的神经细胞。三叉血管系统的反复激活会导致神经系统过敏和持续疼痛。
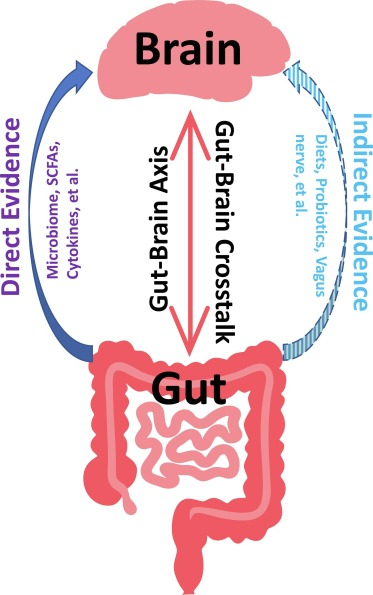
IV)肠脑轴(GBA)理论
肠-脑轴作为肠道功能和维护的协调系统,将大脑的情绪中心与肠外周机制连接起来,包括肠反射、肠道通透性、免疫反应和肠内分泌信号传导等。
肠道微生物群组成的改变可能会影响肠脑轴并引起炎症,从而可能导致偏头痛。
通过肠-脑轴影响偏头痛
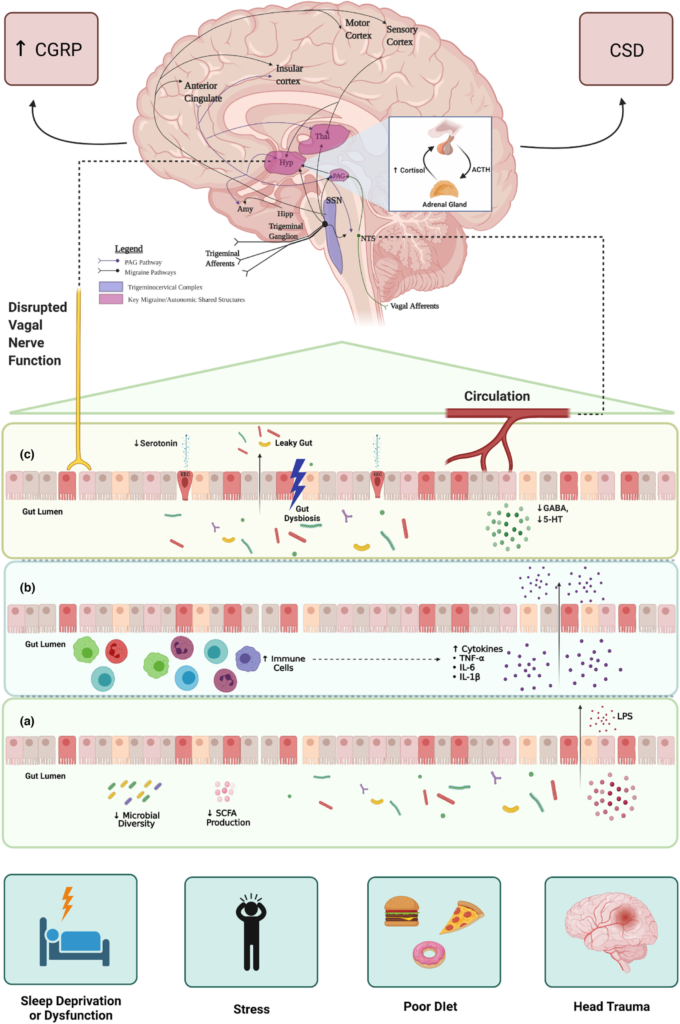
doi.org/10.1111/ene.15934
众所周知,睡眠不足和压力是原发性头痛障碍的常见诱因,不良饮食会增加偏头痛的严重程度和频率。
a) 上述因素导致肠道微生物组多样性和组成的改变,导致肠道细菌产生的短链脂肪酸减少,LPS转移到系统循环中。
b) 此外,这些因子激活免疫细胞,产生的促炎细胞因子也进入系统循环。
c) 这反过来又促进了肠道微生态失调,增加了肠道上皮的通透性,并将分子转移到系统循环中。
肠道微生物组的功能障碍,会导致与头痛病理生理学有关的必需神经递质GABA和血清素的耗竭。这反过来又改变了迷走神经功能。
而系统性促炎细胞因子和LPS,改变了HPA轴的功能,并激活了孤束核,孤束核介导了大脑中的疼痛处理途径,包括前扣带、岛叶皮层、运动皮层和感觉皮层,导致疼痛感知的改变。
神经炎症刺激三叉神经纤维释放CGRP,并驱动皮层扩散性抑郁(CSD),改变兴奋性和抑制性传递,激活三叉神经-颈复合体,加剧头痛严重程度并介导头痛频率。
接下来,我们主要就以上肠脑轴理论展开讨论一下,这其中涉及到的肠道菌群及其代谢产物与偏头痛有什么样的关联。
偏头痛常伴随一些胃肠道症状,包括恶心、呕吐、腹泻、便秘和消化不良。一些研究表明,肠道微生物群失调,可能会下调免疫系统功能,改变宿主代谢,破坏肠-脑轴,导致代谢和神经疾病的发生。胃肠道中的炎症和神经免疫调节可能在偏头痛的发病机制中发挥重要作用。
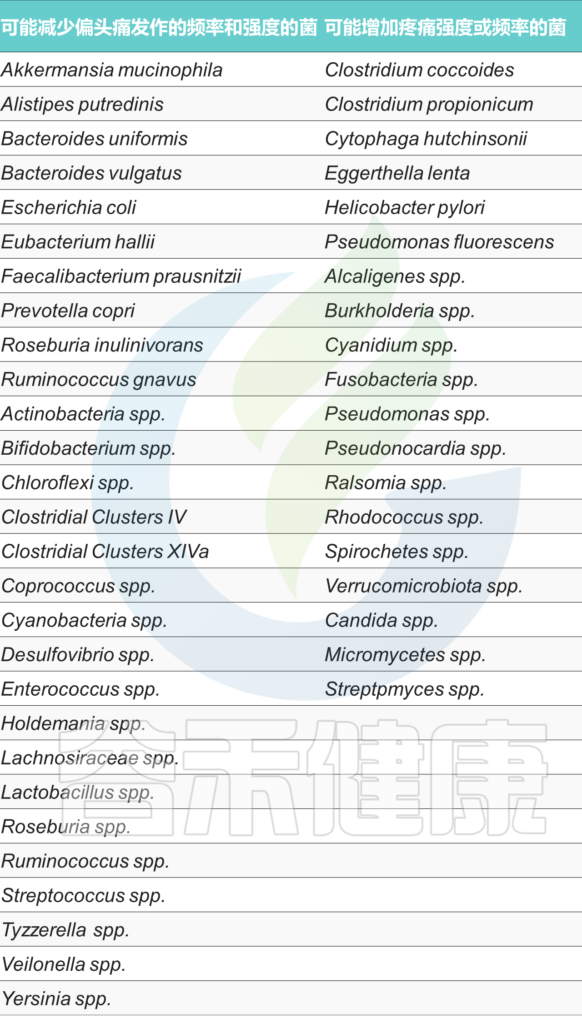
偏头痛患者的肠道微生物群的物种多样性(α多样性)和代谢功能降低,产丁酸菌减少。
而梭状芽孢杆菌增加,如:
硝酸盐已被确定为一种普遍的偏头痛诱因。
与没有偏头痛的人相比,在偏头痛患者的口腔和粪便样本中观察到能够减少硝酸盐、亚硝酸盐和一氧化氮的细菌丰度更高,如嗜血杆菌属和Rothia属。
编辑
doi.org/10.3390/microorganisms11082083
特殊年龄段的偏头痛研究队列:
儿童和青少年
偏头痛在儿童和青少年中表现出多种形式,估计全世界儿童和青少年的总患病率为 10%。儿童双侧偏头痛更为常见,且持续时间较短。偏头痛儿童会出现多种胃肠道症状,包括腹痛、恶心、呕吐、腹泻、便秘。
在381名 7-18 岁儿童的队列中(40 名患有偏头痛,341 名没有偏头痛,平均年龄 11.5 岁),在偏头痛儿童和健康对照儿童有明显的菌群差异。
与健康对照相比,偏头痛儿童下列菌群升高:
老年患者

一项针对108位老年女性(54 名偏头痛患者、 54 名健康受试者)的宏基因组关联研究发现偏头痛患者的细菌特征如下:
厚壁菌门,尤其是梭菌属显著增加。
在健康对照中有更多有益菌,例如:
普氏粪杆菌、青春双歧杆菌、史密斯甲烷杆菌。
同时,该研究发现犬尿氨酸降解、谷氨酸降解和γ-氨基丁酸(GABA)合成途径较多,提示神经传递和代谢可能发生转变。
接下来我们看这些肠道菌群代谢产物会怎样参与到偏头痛的发病机制中。
谷氨酸和γ-氨基丁酸(GABA)等都参与疼痛感知。肠道中的这些神经递质参与了几种信号通路,这些信号通路除了调节疼痛外,还调节促炎细胞因子的释放。
★ 谷 氨 酸
谷氨酸作为一种兴奋性神经递质,通过不同的作用,包括皮质扩散抑制、中枢敏化和刺激三叉血管系统,在偏头痛病理生理学中发挥作用。
研究证实,各种细菌菌株,包括在环境中发现的或用于食品发酵的菌株,都能够产生谷氨酸。
偏头痛患者谷氨酸水平升高
由于谷氨酸可以沿着三叉神经血管通路对伤害性神经元产生刺激作用,因此它可能在偏头痛和偏头痛相关的中枢敏化的病理生理学中至关重要。这一理论得到了进一步的证明,偏头痛患者的血液谷氨酸水平在间歇期和发作期都有升高,在血浆和脑脊液中均升高。
有研究表明,血浆谷氨酸水平可能是慢性偏头痛和阵发性偏头痛的潜在指标。

此外,有证据表明谷氨酸在皮质扩散性抑制中起主要作用,皮质扩散性抑制被假设为偏头痛先兆的生理底物。基于这些,谷氨酸能神经传递可能是偏头痛和微生物组之间的联系。
扩展阅读:
★ 血 清 素
血清素存在于大脑、肠道和血液的组织中,其中肠道含有~95%的人体总血清素。血清素能神经元存在于中缝背核和整个疼痛通路中。
它在体内有很多作用,例如在神经细胞之间发送信号并帮助身体控制血管收缩的方式。它还在控制情绪、睡眠、饮食和消化方面发挥作用。
血清素从血小板释放到血浆中可能与偏头痛先兆期的病理生理学有关。偏头痛发作期间储存在血小板中的血清素被耗尽;血清素血浆水平降低,而相应代谢物羟基吲哚乙酸 (5-HIAA) 水平升高。
血清素既是血管扩张剂又是血管收缩剂,可作为伤害性疼痛的调节剂
偏头痛患者经常报告说,呕吐后头痛就会停止,呕吐会刺激肠道蠕动并提高血液血清素水平。而血清素的合成与肠道菌群有关,例如肠球菌、链球菌、大肠杆菌等。
血清素可能具有促伤害感受和抗伤害感受特性,具体取决于亚型
现在估计至少有七种不同的受体家族(5-HT1-7),其中许多具有亚型,偏头痛的发生涉及不止一种亚型。由于色氨酸是血清素的前体并且可以穿过血脑屏障,因此大脑中血清素的量取决于色氨酸的水平。
接下来我们看看关于色氨酸的代谢。
★ 色 氨 酸
色氨酸在人体内以三种主要途径代谢:血清素(5-HT),犬尿氨酸(l-kyn)和微生物群相关的吲哚途径。
一些报告表明,增加膳食色氨酸的摄入量可预防偏头痛的发生或减轻其胃肠道相关症状,如恶心、呕吐以及畏光。
色氨酸的代谢途径在五个肠道门中最有效:放线菌门、厚壁菌门、拟杆菌门、变形菌门、梭杆菌门。梭菌属、Burkholderia、链霉菌属、假单胞菌属、芽孢杆菌属5个属也具有较大的肠道内色氨酸代谢潜力。
色氨酸代谢的犬尿氨酸途径,可能对偏头痛具有治疗潜力
色氨酸代谢产物可能作用于谷氨酸能系统,该系统参与疼痛传递、中枢敏化和皮质扩散性抑制,谷氨酸能离子型和代谢型受体参与偏头痛的发病机制,KYNA(犬尿喹啉酸)是NMDA受体的竞争性拮抗剂,其抑制作用可防止谷氨酸诱导的兴奋性毒性,因此有理由推测色氨酸代谢的犬尿氨酸途径可能对偏头痛具有治疗潜力。
注:NMDA受体是离子型谷氨酸受体的一个亚型
犬尿氨酸途径是色氨酸转化的主要途径,因为它在正常情况下约占色氨酸代谢的95%,并且与神经系统疾病的行为和认知症状有关。
犬尿氨酸(l-kyn)途径(KP)将l-色氨酸转化为几种神经活性化合物。犬尿氨酸和喹啉酸的产生,耗尽了作为血清素前体的色氨酸和色胺的供应。

doi.org/10.3390/ijms221810134
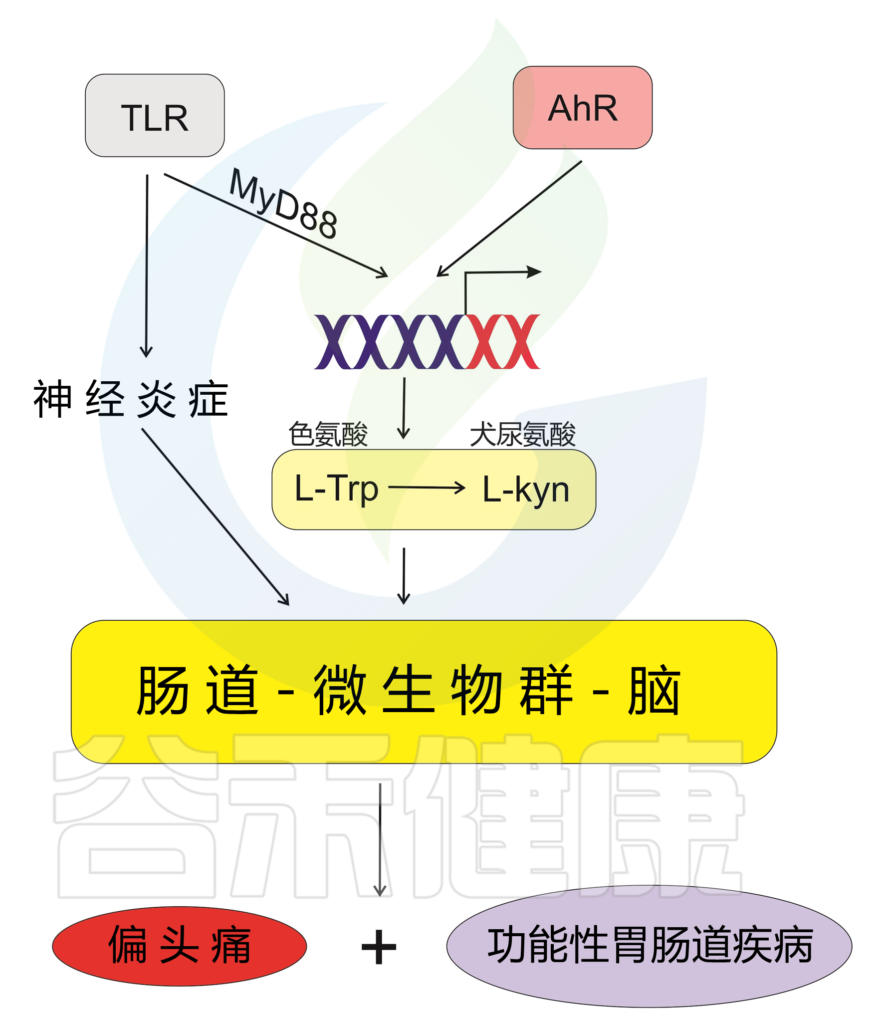
犬尿氨酸衍生物具有有效的镇痛作用,其机制包括抑制CGRP。犬尿氨酸途径产物是芳烃受体(AhR)的重要配体,其激活与胃肠道炎症和偏头痛的发病机制有关。
AhR、TLR 和 MyD888 激活可能强调犬尿氨酸参与偏头痛和功能性胃肠道疾病。
扩展阅读:
★ 短 链 脂 肪 酸
短链脂肪酸 (SCFA) 是胃肠道细菌的代谢产物,对葡萄糖稳态、饱腹感、抗炎作用和大脑信号传导有许多局部和全身影响。
通过调节免疫细胞和细胞因子→影响神经炎症
如短链脂肪酸的施用可以减少硝酸甘油诱导引起的痛觉过敏,并导致肠道促炎细胞因子如 TNF-α 和 IL-1β 的释放减少。
丙酸可以保护血脑屏障免受氧化应激
一些菌群如:普通拟杆菌、B.uniformis、Alistipes putredinis、Prevotella copri、Roseburia inulinivorans、Veilonella、Akkermansia mucinophila等,具有很高的丙酸盐生产能力。
丁酸和丙酸等短链脂肪酸通过迷走神经,穿过血脑屏障,然后激活可能改变多巴胺能和血清素能信号传导的受体。
神经保护特性:如丁酸盐
丁酸盐影响肠嗜铬细胞释放血清素,前面我们已经了解到血清素在偏头痛发病中的重要性。
与产丁酸相关的菌群,例如:
快速和极端的饮食变化直接影响肠道微生物群,影响肠道微生物群的β多样性。在高脂肪饮食中添加益生元(可发酵纤维)可以恢复产丁酸菌和双歧杆菌水平,这也突出了饮食对肠道微生物群组成的关键影响。
丁酸盐刺激齿状回的细胞增殖和分化,并增强脑源性神经营养因子(BDNF)和胶质源性神经营养因子(GDNF)的表达。丁酸盐还通过抑制 TNF-α 的合成而在大脑中显示出抗炎作用,TNF-α 是由内毒素脂多糖 (LPS) 通过抑制NF-κB 诱导的。
下面我们来看看炎症因子在偏头痛发病中扮演怎样的角色。
炎症介质
在炎症性疾病和偏头痛中都观察到炎症免疫反应增强。促炎性免疫反应的主要触发因素是由于肠道通透性增加而导致脂多糖进入循环,那么,炎症反应可能出现在身体的各个部位,当三叉神经上伤害感受器的激活时,偏头痛就出现了。
研究表明偏头痛发作期间,下列炎症因子升高:
这些炎症因子是如何在偏头痛发病中发挥作用的呢?
IL-1β 是一种主要细胞因子,可驱动大脑和全身炎症,激活普遍存在的细胞表面受体 IL-1R1。
IL-1β/IL-1R1 轴激活一系列炎症分子,包括其他细胞因子和趋化因子。IL-1β 激活脑膜伤害感受器并使之敏感,是皮质扩散性抑制后三叉神经激活的关键介质。也就是说,IL-1β/IL-1R1 轴在外周TG和中枢神经系统的三叉血管通路中尤其发挥着至关重要的作用。
IL-1和IL-6 是由调节性B细胞响应微生物群的紊乱而释放的。
研究表明,肠道微生物群失调通过三叉神经伤害感受系统中的TNF-α水平上调,促进了类似偏头痛疼痛的持续性。
肠道菌群通过间接信号传导维持肠脑轴正常平衡的作用机制
doi: 10.1186/s10194-020-1078-9
IL-8的表达,涉及到神经肽,与P物质有关,P物质可以帮助调节免疫细胞及其产生的各种细胞因子。
接下来,我们来看偏头痛中重要的——神经肽。
★ CGRP(降钙素基因相关肽)
对于患有慢性偏头痛的患者,CGRP 水平在偏头痛发作期间持续升高,并且在两次发作之间继续升高。CGRP是我们反复提到的词,我们来看看它在偏头痛疾病中发挥什么样的作用。
CGRP,降钙素基因相关肽 ,一种由37个氨基酸组成的肽,可能通过胃肠道免疫细胞和肠道运动与肠道微生物有关。在偏头痛的情况下,它在三叉神经节、三叉神经尾核、杏仁核、丘脑和皮质中浓度很高。
CGRP有两种形式:
CGRP升高如何与偏头痛关联起来:
星形胶质细胞和神经元参与了CGRP合成释放过程的正反馈循环,并维持了增加的炎症和致敏状态。
CGRP 可以作为一种有价值的治疗标志物
目前,许多用于治疗和预防偏头痛药物的原理,就是针对这个CGRP或其受体的,抑制 CGRP 转录并减少其释放,从而缓解偏头痛。
★ P 物 质
P物质(substance P),是一种广泛分布于细神经纤维内的神经肽,主要作用是传递痛觉信息。
呕吐是最常见的胃肠道反应之一,受P物质的控制
在中枢神经系统中,延髓有面突区和孤束核的区域,这两个区域控制呕吐反射并含有高水平的P物质。P物质释放结合到NK1R上会触发呕吐反应。
P物质的一个功能是通过改变细胞信号通路作为神经递质和疼痛感知调节剂
有一个假说是P物质有助于突触后神经元对谷氨酸的敏感性,有助于将疼痛信号传递到大脑的体感区域。在许多其他中枢神经系统病理中通过神经源性炎症引起早期血脑屏障的破坏。
P物质的关键作用是双向调节免疫细胞及其产生的各种细胞因子
IL-1、IL-4和IFN-γ可以诱导巨噬细胞表达NK1R。诱导细胞因子释放会导致巨噬细胞和树突状细胞的招募,这有助于刺激IL-8的表达。P物质间接参与了免疫细胞的招募和迁移。P物质能刺激和诱导肥大细胞脱颗粒化。
★ PACAP
在与偏头痛病因机制相关的几个结构中发现了PACAP(垂体腺苷酸环化酶激活肽)的存在,包括硬脑膜、脑血管、三叉神经节、三叉神经原球和颈椎脊髓。
PACAP在神经调节、神经源性炎症和痛觉中起着重要作用。PACAP在感觉神经元炎症后上调。PACAP与CGRP在一些硬膜神经纤维中共同表达,也与疼痛的中枢敏化和情绪负荷有关。
PACAP对革兰氏阳性菌、革兰氏阴性菌和真菌具有抗菌活性,因此它可以直接影响膜的杀菌功能。有效的防御能力和较低的细菌耐药性使抗微生物神经肽成为一类有吸引力的新型抗生素。
★ NPY(神经肽Y)
NPY是去甲肾上腺素能系统功能的可能指标,通过脑循环调节影响脑血流量。值得一提的是,在偏头痛发作期检测到较高水平的NPY。
NPY已经在肠-脑轴的各个层面上被检测到。NPY通路也有助于改变胃肠道功能及其血流、免疫系统和炎症状态、疼痛、能量稳态、情绪、情绪以及行为和大脑认知功能等。
★ 胆囊收缩素 (CCK)
胆囊收缩素(CCK)由小肠粘膜内层(I 细胞)、哺乳动物大脑(例如皮质、丘脑、中脑边缘、导水管周围灰质和中脑)和脊髓的肠内分泌细胞合成。这种肽抑制胃排空和胃酸分泌,刺激胆囊收缩和胰腺分泌,并通过 CCK1 受体在大脑中激发饱腹感。
CCK在导水管周围灰质中产生,可能是偏头痛内源性疼痛信号系统及其水平升高的原因。CCK也存在于三叉神经节中,因此刺激三叉神经节会导致局部CCK增加。
CCK——肥胖和偏头痛之间的桥梁之一
肥胖患者偏头痛发作的频率和严重程度明显更高。偏头痛和肥胖之间联系的一种可能解释是,是高脂饮食引起的CCK分泌,因为十二指肠内游离脂肪酸会刺激CCK的分泌。
关于CCK可以详见我们之前肠道激素的文章:
当考虑到性激素时,我们知道偏头痛在女性中的发病率是男性的2-3倍,女性的发作时间更长、更严重,恢复时间也更长。
无先兆偏头痛的风险在月经前 2 天和月经期间最高,这也是生殖道微生物群多样性最低的时候。周期中期雌激素和孕酮水平高与无先兆偏头痛的风险较低以及生殖道内微生物群落的稳定性较高有关。
众所周知,雌激素会改变肠道内的紧密连接和粘蛋白保护,改变肠道通透性。
雌激素受体广泛表达于中枢神经系统,有证据表明雌激素调节痛觉传导,雌激素敲除模型在脊髓背角水平导致CGRP升高,从而改变了发起偏头痛攻击所需的阈值。临床上支持这一点的是黄体晚期偏头痛发作的可能性增加。虽然孕酮撤退似乎不会触发偏头痛发作,但它可能在疼痛敏感性和病程演化中起作用。
关于雌激素与肠道菌群详见我们之前的文章:
睾酮降低了对CSD的易感性,增加了血清素能调,并具有抗炎特性。较高水平的睾酮与肠道微生物群多样性增加有关,研究表明,患有偏头痛的男性存在雄激素缺乏和雌二醇水平增加。
因此,肠-脑轴可能介导性激素和头痛疾病之间的关系。
以上我们阐述了肠道菌群及其代谢产物等参与偏头痛发病机制,包括炎症介质、肠道微生物群、神经肽、血清素途径等。有证据表明偏头痛和胃肠道疾病之间存在共同的病理生理学,下面我们来了解一下它们之间的关联。
偏头痛和胃肠道合并症的病理生理学都很复杂,尚未完全阐明;然而,科学证据确实表明这些复杂疾病之间的病理生理学重叠。研究这种重叠有助于阐明常见的病理生理异常或生物学机制。
特别是,自主神经系统(ANS)被认为在偏头痛和胃肠道功能障碍之间的关联中起重要作用,因为它们的症状特征相似,包括恶心,呕吐,消化不良和胃轻瘫。
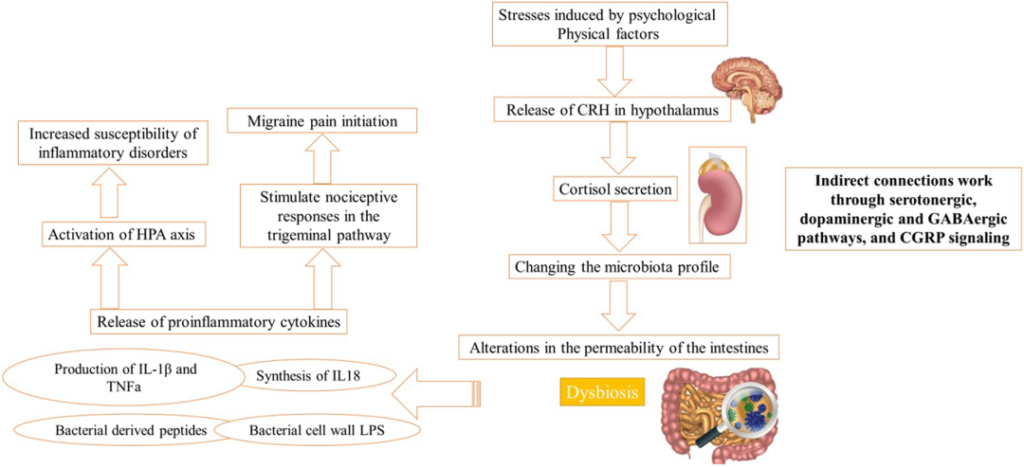
doi: 10.1111/head.14099
肠易激综合征(IBS)和炎症性肠病(IBD)的患者中,偏头痛的发生率增加。两者都是严重的肠道疾病,与肠道通透性增加和微生物引起的炎症有关。此外,中枢性、内脏性和热性皮肤过敏在IBS和偏头痛中很常见。患有长期和更频繁头痛的偏头痛患者更有可能被诊断为IBS。
偏头痛与IBS有一些共同的重要特征,这两种疾病都是慢性疼痛相关疾病,在女性中比男性更普遍,并且在纤维肌痛、慢性疲劳综合征、间质性膀胱炎、失眠、抑郁等方面与心理合并症有关。据估计,约60%的偏头痛患者患有异常性疼痛,除内脏超敏反应外,大多数IBS患者还报告异常性疼痛。
在IBS患者的粪便微生物群中评估出偏头痛的严重程度与肠道菌群失调之间存在强正相关。约一半没有先兆的年轻女性偏头痛患者患有肠道微生物群失调。
美国肠道计划队列研究发现,偏头痛与口腔微生物中具有还原硝酸盐、亚硝酸盐和一氧化氮功能活性的菌群水平呈正相关关系。
IBD是一种慢性复发-缓解炎症性疾病,由克罗恩病和溃疡性结肠炎组成。关于偏头痛和IBD之间可能关系的数据很少。
虽然机制不明确,IBD中存在的自身免疫性炎症反应、吸收不良、内皮功能障碍以及为该疾病开具的免疫抑制治疗可能参与了炎症性肠病和偏头痛之间的病理生理关联。
扩展阅读:
根据罗马IV标准,功能性消化不良分为餐后不适综合征(PDS)和上腹疼痛综合征(EPS)。
偏头痛是功能性消化不良和餐后症状患者的常见合并症。
扩展阅读:
基于人群的研究,个体主要是女性,最常见的症状(无论是持续性还是偶发性)是恶心和呕吐,但也可能包括腹痛、腹胀、体重减轻、餐后饱腹感和早饱感。
在患有特发性胃轻瘫和腹痛的个体中,腹痛严重的人比症状较轻的人更有可能患有重叠偏头痛。
在胃轻瘫中,观察到胃排空时间与偏头痛发作患者头痛、恶心和对光敏感的严重程度显著相关。多潘立酮是一种多巴胺受体拮抗剂,可用于治疗胃轻瘫,并已被证明在早期高剂量给药时可预防大多数偏头痛发作。另一种多巴胺受体拮抗剂甲氧氯普胺可用于治疗胃轻瘫和恶心,作为偏头痛的急性静脉注射治疗是有效的。
根据 5 项病例对照研究的荟萃分析结果,约 45% 的偏头痛患者患有幽门螺杆菌感染,而健康对照组的患病率估计约为 33% 。有证据表明根除幽门螺杆菌可能与缓解偏头痛症状有关。
幽门螺杆菌感染与持续的慢性炎症状态有关,这反过来可能导致炎症介质和血管活性化合物的产生增加。因此,偏头痛和幽门螺杆菌感染之间的关联机制可能包括诱导免疫、炎症和血管反应,以及随后免疫细胞、炎症和血管活性物质释放到胃粘膜中,最终可能导致大脑疼痛敏感结构的超敏反应。
扩展阅读:
正确认识幽门螺杆菌
乳糜泻具有多种神经系统表现,如癫痫、共济失调、小脑性共济失调、情绪障碍、脑炎、周围神经病变、神经肌肉疾病、痴呆、学习障碍、发育迟缓和偏头痛。
与没有这种疾病的人相比,被诊断患有乳糜泻(一种由谷蛋白肽引发的自身免疫性疾病)的人表现出更高的偏头痛发生率,据估计,大约 21-28% 的乳糜泻患者患有偏头痛。
相反,患有偏头痛的人乳糜泻的患病率更高。临床医生可能会考虑在存在此类改变的偏头痛受试者中寻找乳糜泻,特别是如果存在其他提示乳糜泻的症状。
偏头痛和乳糜泻之间的联系可归因于几种同时存在的机制,包括面筋引起的促炎细胞因子的激活、吸收不良导致的重要维生素和必需元素的缺乏、血管张力的紊乱、神经系统敏感性的增加、脑灌注不足、血管周围炎症等。
✔ 消除饮食
消除饮食需要先确定首先引发头痛的饮食成分,然后从常规饮食中排除这些成分。这是一种个人方法,个人可以识别引发或加剧头痛的成分。
如果某种食物在接触后 1 天内引起头痛,则可将其视为触发因素。大多数患者存在多种触发因素;因此,很难识别单一成分。况且有些食物含有不止一种成分,因此要完全识别出来并不简单。
✔ 综合饮食
富含ω-3和ω-6脂肪酸的低脂、高叶酸和生酮饮食对偏头痛患者有益。
改良的阿特金斯饮食提供神经保护,改善血清素能功能障碍,抑制神经炎症,改善线粒体功能。
生酮饮食会增加产生的酮体浓度,这对头痛患者有帮助。
低血糖饮食也能改善炎症状态。保持ω-6脂肪酸和ω-3摄入之间的微妙平衡可以减少炎症,维持血管张力,增强血小板功能。
偏头痛发作频率与坚持“健康”饮食模式(大量食用水果、蔬菜、鱼类、豆类、发酵食物等)成反比(P=0.04)。与坚持“西方”饮食方式(大量食用可乐、咸坚果、加工肉和快餐)成正比(P=0.02).
生姜、薄荷和辣椒都具有天然的止痛功效。生姜和薄荷有助于减少与偏头痛相关的恶心。
薰衣草可以减少血管炎症,通常是治疗焦虑、压力和压力引发的偏头痛有效的草药。
✔ 低钠饮食 / 高钠饮食
对脑脊液的分析显示,与对照组相比,偏头痛患者的钠含量较高,尤其是在头痛发作时。然而,低钠饮食的效果取决于许多因素,因此在考虑低钠饮食之前应详细评估其效果。
低钠饮食可以有效减少老年高血压患者头痛的发生。除了控制血压之外,低钠饮食还可以降低头痛的发生率。
相比之下,在没有高血压的低至正常体重指数的年轻女性人群中,高钠饮食有助于降低偏头痛发作的频率。
因此,低/高钠饮食应该根据患者群体进行调整。
低热量饮食 or 生酮饮食?
有研究认为,生酮饮食对偏头痛患者更有益,低热量饮食对偏头痛患者不利 (n = 108) 。在另一项研究中,生酮饮食显着改善了这些患者的头痛特征,并减少了发作频率和药物使用。停止生酮饮食后 2 个月观察到持续改善。
虽然看起来生酮饮食患者的头痛频率有所减少,但过渡期的头痛频率更严重。然而,经过3个月和6个月的随访后,低热量饮食组的头痛频率显著改善。
✔ 低血糖饮食(LGD)
通常从碳水化合物中获取总热量的 50-55% 是安全饮食。饮食转向低血糖指数碳水化合物已被证明可以增加短链脂肪酸水平。在某些情况下,LGD 是一种重要的替代方案,例如高脂血症、糖尿病、癫痫和体重管理。
罗马进行的一项队列研究中报告称,增加全麦面包(P = 0.04)和全麦面食(P = 0.004)的消费,以及减少白面包(P = .004)的消费,与偏头痛发作频率和每月使用药物救治的统计显著减少有关。
✔ 低脂饮食
一项研究调查了54名成年人减少脂肪饮食对偏头痛治疗的影响。患者被告知他们的脂肪消耗量将降至<20 g/天(12周)。发现头痛药物的发生率、严重程度和需求显著降低。
在一项为期 12 周的试验中,患有慢性偏头痛的成年人被随机分配接受高omega-3 / 低omega-6 饮食或低 omega-6 饮食。与采用低omega-6 饮食的偏头痛患者相比,采用高omega-3/低 omega-6 饮食的人的头痛改善程度更高。
可能与此相关:omega-6 和 omega-3 之间的平衡有助于炎症控制。omega-6 脂肪酸促进血管舒张。
谨慎选择下列食物
▸
味精在高浓度和溶解在液体中可能会引发偏头痛。并不是说引发每个患者的偏头痛发作,不能一概而论。
▸
咖啡因可能缓解偏头痛或者引发偏头痛。与阿司匹林和对乙酰氨基酚结合,咖啡因是一种高效的止痛药。咖啡因戒断会引发咖啡因使用者的偏头痛发作。需要注意自己的剂量。
咖啡因与偏头痛频率之间的联系没有定论。一些研究数据表明,不同的偏头痛和慢性日常头痛在咖啡因使用者中比不摄入这种物质的人更常见。也有研究认为偏头痛频率和咖啡因摄入之间没有关联。
▸
饮酒是偏头痛发作最常见的原因之一。酒精可以刺激三叉神经节中的脑膜伤害感受器,触发疼痛信号,然后在三叉神经脊核传递到丘脑核,最后传递到体感皮层。也可能涉及其他机制,例如血管舒张作用、脱水、毒性等。除了酒精,酒精饮料还含有某些化合物(酒精发酵的副产品),这些化合物都可能会引发偏头痛。
▸
许多研究提出了巧克力摄入与头痛之间的联系,但其确切的生理机制尚不清楚。可能是巧克力中的黄烷醇刺激内皮一氧化氮合酶(eNOS)活性,这可以通过增加一氧化氮(NO)的产生导致血管舒张。
也有研究认为巧克力含有许多维生素和矿物质(例如镁和核黄素),用于预防偏头痛。富含可可的饮食通过抑制CGRP的表达来预防三叉神经节神经元的炎症反应。
▸
酪胺(Tyramine),是一种衍生自酪氨酸的胺化合物,存在于各种食品中,包括陈奶酪、腌肉、熏鱼、啤酒、发酵食品和酵母提取物等。酪胺有可能通过促进去甲肾上腺素的释放并对α-肾上腺素受体产生激动作用而引发头痛。
▸
阿斯巴甜是一种人造甜味剂。几项研究表明,它会引起各种神经或行为症状;也会引起头痛,尤其是对于长期使用中等或高剂量(900–3000 mg/天)的人。
基于以上所述,识别和避免饮食中的偏头痛诱因至关重要,因为这有助于降低偏头痛的频率,让偏头痛患者能够控制让他们感到疲惫和无助的情况。
B族维生素
维生素B2对氧化代谢至关重要,可以降低偏头痛的风险。根据随机对照试验,服用维生素B2可以显著减少每月偏头痛天数1-3天。通过增加产短链脂肪酸菌丰度,维生素B2和其他B族维生素有助于对肠道微生物组产生正面影响。
扩展阅读:
维生素C
水溶性维生素C是最重要的非酶抗氧化剂之一,参与神经代谢。维生素C的膳食来源是水果和蔬菜。
维生素C可能调节偏头痛过程中的神经炎症和氧化应激活性的影响。
一项开放标签研究中,患者接受了含有120 mg粉红树皮提取物、60 mg维生素C和30 IU维生素E的胶囊(每粒胶囊)。在完成治疗期的患者中,得到了改善,包括头痛频率和头痛严重程度的降低。该研究人员还进行了一项开放标签研究,以检查维生素C(150 mg)和辐射松树皮提取物对偏头痛症状的影响。患者服用上述剂量的维生素C和辐射松树皮提取物3个月。治疗后,患者表现出显著改善:头痛频率和头痛严重程度减轻。
扩展阅读:
维生素D3
补充维生素D3会影响肠道微生物群的组成。为健康人补充8周维生素D3也显著减少了幽门螺杆菌的数量。几项研究报告称,血清维生素D水平可能与偏头痛/头痛风险增加有关。
偏头痛患者中这种维生素缺乏/不足的患病率可能更高。补充维生素D对偏头痛发作的强度和频率也有良好的影响。
镁
镁参与多种酶促反应,还维持细胞膜的平衡,影响其通透性并减少自发去极化的可能性。它影响外周和中枢神经系统的兴奋性和神经传导,因此在偏头痛病程中起着重要作用。
镁缺乏导致皮质扩散抑制或谷氨酸能神经传递异常是镁与偏头痛关系的一个可能机制。镁不足可能会影响 NMDA 受体阻断、钙通道、谷氨酸和 NO 活性,以及血清素受体的亲和力。
许多临床医生认为,以正确的剂量和形式补充镁可以成为预防偏头痛发作的治疗方法。补充镁也可以配合其他药物。
益生菌是偏头痛的另一种潜在疗法,它与饮食干预一样能够改变肠道微生物群。
在 NTG 诱导的偏头痛小鼠模型中,发现口服益生菌混合物显著抑制抗生素治疗引起的偏头痛样疼痛延长。
在一项随机双盲对照试验中观察到,与安慰剂对照相比,在 40 名发作性偏头痛患者和 39 名慢性偏头痛患者中,为期 8 周的益生菌试验显著降低了偏头痛的严重程度、频率和药物使用量。
其中含有14种益生菌菌株:
益生菌组偏头痛发作的平均频率显著降低(平均变化:-9.67 与 -0.22;p ≤ 0.001)。补充益生菌显著降低了严重程度(平均变化为-2.69;p≤0.001.),降低慢性偏头痛患者的发作持续时间(平均变化:-0.59;p≤0.034),减少每天服用药物数量(平均变化为-1.02;p<0.001)。
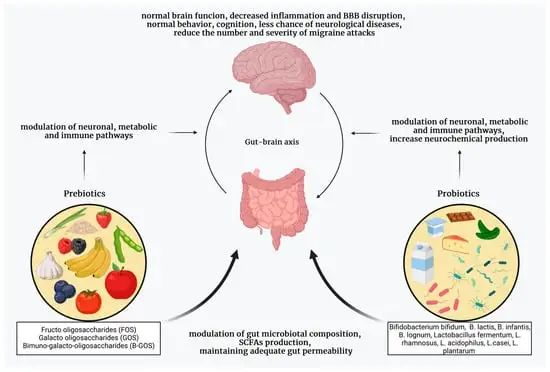
doi.org/10.3390/neurolint15030073
将芽孢杆菌、双歧杆菌、乳酸杆菌和链球菌菌株的混合物应用8-10周,可以降低发作性偏头痛患者的发作严重程度和频率,并降低慢性偏头痛患者的频率、严重程度、持续时间和每天服用的药物数量。
姜黄素
姜黄素是从姜黄根茎中提取的主要姜黄素,也是最著名的植物多酚之一。姜黄素具有许多有益的特性,如抗氧化、抗动脉粥样硬化、抗菌、免疫调节、抗衰等特性。
姜黄素可以显著抑制 IL-1β 和 TNF-α 表达、氧化应激和蛋白质积累。
对偏头痛治疗进行了一项研究,比较了单独使用舒米曲普坦(ST)和与姜黄素一起使用的效果,采用了硝酸甘油诱导的偏头痛大鼠模型。
姜黄素以下面两种形式静脉注射,因为姜黄素的肠道吸收较低:
a)酒精溶液(用生理盐水稀释)
b)脂质体的形式
当姜黄素以脂质体的形式进行注射时,其抗氧化作用更为显著。作者将所得结果归因于姜黄素能够清除羟基或过氧自由基、直接与过氧化物自由基相互作用以及抑制参与炎症性因子NF-κBs的活性。
偏头痛发病机制的一个考虑的机制涉及肿瘤坏死因子α(TNF-α)的参与,通过引发神经元超兴奋性、刺激伤害感受器和前列腺素的产生,从而引发神经炎症。
一项研究,旨在确定姜黄素和ω-3脂肪酸对TNF-α基因表达的协同作用。接受两种物质治疗的患者在血浆中显示出TNF-α mRNA水平的降低(反映了TNF-α表达的减少)。在只接受其中一种分析物的患者中,没有发现这种情况。
辅酶Q10
除了抗氧化特性外,辅酶Q10还表现出抗炎特性,参与嘧啶合成(作为辅因子),进而参与DNA复制和RNA修复过程。由于其潜在的积极作用,是许多神经系统疾病的膳食补充剂。
酶Q10被列为预防偏头痛最常用的治疗方法之一。给予偏头痛患者辅酶Q10会导致CGRP的降低。
儿童和青少年中研究了补充辅酶Q10与偏头痛发生之间的关系。患者每天服用100毫克辅酶Q10,为期4个月。结果显示,在主要结果方面,两组之间没有统计学上的显著差异。然而,与对照组相比,偏头痛患者的研究组头痛发作频率呈下降趋势。此外,在补充辅酶Q10的前四周,观察到发作性偏头痛患者头痛的严重程度降低。
在辅酶Q10的抗氧化特性中有以下方面,即超氧化物歧化酶活性的调节(导致细胞抗氧化防御的改善)、氧化应激OS的减少或增加谷胱甘肽还原形式(用作抗氧化剂)浓度的能力。上述机制可缓解偏头痛,降低偏头痛发作的频率,缩短偏头痛发作的持续时间。
银杏内酯B
银杏内酯B是从银杏叶中提取的一种草药成分。银杏叶提取物具有神经保护特性,对记忆有有益作用,也有抗氧化剂的某些特性。
一项为期六个月的开放标签多中心研究,证明了银杏内酯B对每月至少发作一次的偏头痛患者治疗先兆偏头痛的有效性。
槲皮素和银杏内酯B对减轻偏头痛症状有特殊作用。银杏叶提取物成分可降低氧化应激,抑制血小板活化因子,并影响谷氨酸能传递。
所有生物学机制都会增加神经保护作用,从而降低偏头痛的频率,减轻偏头痛,缓解先兆症状。
小白菊
小白菊(Tanacetum parthenium)属菊科植物,广泛分布于南美洲。其特征是具有抑制醛糖还原酶活性的高潜力,并显示出必要的抗氧化特性。
小白菊用于治疗多种疾病,不仅可以缓解偏头痛的症状,还可以缓解另一种来源的疼痛,如炎症、恶心和呕吐。
一项双盲、多中心、安慰剂对照研究,以确定小白菊稳定提取物(MIG-99)在降低偏头痛发作频率方面的有效性。最显著的效果记录为6.25mg剂量的MIG-99。三年后,同一作者发表了剂量为6.25 mg的MIG-99制剂的有效性和安全性结果。在服用该制剂的组中,偏头痛发作频率每月减少1.9次(安慰剂组每月减少1.3次)。
粪菌移植可以通过改变肠道菌群,帮助恢复肠道微生物平衡,使肠道微生物恢复更加有效和持久,理论上可减轻偏头痛发作和偏头痛严重程度,超过340项临床试验正在进行中。肠道菌群的改变可导致炎症介质和血清素途径的正常化,从而缓解偏头痛的频率和强度。
扩展阅读:
吴茱萸汤是一种临床用于治疗和预防偏头痛的配方,可anaerostipes和acidifaciens丰度,以恢复细菌的比例。由于5-HT合成与微生物群、功能和代谢紊乱相关,吴茱萸汤可以通过影响中枢和外周5-HT来缓解痛觉过敏。研究表明,在基因敲除小鼠和豚鼠中,5-HT1D受体具有抑制神经肽释放的作用,从而改变硬脑膜神经源性炎症反应。
良好的生活习惯
建立规律的睡眠时间。每天同一时间起床和上床睡觉,甚至周末也是如此。一天结束时放松一下。
减少吸烟。偏头痛患病率与每日吸烟的相关性为正相关(Spearman系数,rs=0.49)。
定期运动
身体活动期间,身体会释放某些化学物质来阻隔脑部疼痛信号。这些化学物质还有助于缓解焦虑和抑郁症,这两种状况都可能加剧偏头痛。
肥胖也会增加慢性头痛的风险。通过运动和饮食维持健康体重可能也有助于管理偏头痛。
值得尝试的有氧运动可能包括快走或慢跑、骑自行车、瑜伽、游泳等。
缓解压力
简化生活,明确管理时间,适当休息,可以选择接触大自然,做深呼吸(专注且缓慢),冥想,瑜伽等放松的方式,保持积极心态,享受乐趣,每天抽出至少 15 分钟做自己喜欢的事。
写偏头痛日记
记下偏头痛发作时周围的环境条件。写下感官刺激(明亮的灯光、响亮的音乐、奇怪的气味等)、压力的原因、饮食习惯和睡眠习惯。几次发作后,回顾一下日记,找出偏头痛发作前通常存在的常见情况。这些情况可能是“触发因素”,下次尽量避免。
当偏头痛发作时的缓解小方法:
关灯、静音
光线和声音会使偏头痛加剧,尽量在昏暗且安静的房间里放松,闭目休息,能睡就睡吧,让眼睛和大脑得到放松,帮助缓解头痛的不适感。
找一个安静的环境,避免嘈杂的声音,减轻对偏头痛的刺激。
如果不能马上找到这样的地方,可以考虑戴上太阳镜和耳塞。或者尝试舒缓的音乐。
试试温度疗法
热敷或冷敷头部或颈部。
按摩、放松
用双手的食指和中指,以小幅度打圈的方式轻轻按摩太阳穴、颈侧、颈后。
通过深呼吸放松身体和心理,减轻紧张和疼痛感。适量饮水,保持身体水分平衡,有助于缓解头痛。
偏头痛是由多种因素共同引起的,由遗传、内分泌、代谢和/或环境因素相互交织促成的。基于各种初始因素,广泛接受的观点是皮质扩散抑制假说和三叉神经血管假说。前者指出了大脑与神经炎症之间的相互关系,后者指出神经和血管是发生的关键因素。偏头痛复杂的机制和病理生理学仍在广泛研究中。
本文我们了解到,肠道微生物群通过参与肠-脑轴各个途径,肠道微生物群和大脑通过各种途径相互作用,包括免疫系统、色氨酸代谢、迷走神经和肠神经系统等,可能发挥着关键作用,或将作为偏头痛的有前途的生物标志物和治疗靶点。了解这种疾病的多系统联系,极大地扩展了对偏头痛机制的理解,并提供了更广泛的治疗蓝图。
偏头痛本身会产生一些诊断问题,这些问题可能会因合并症而加剧,包括功能性胃肠道疾病等。同时,复杂的疼痛通路,食物和药物代谢、免疫反应等造成的个体差异,会给在偏头痛的临床管理治疗过程中带来难度,目前药物并不能完全缓解症状或满足要求。
考虑以互补的方式将临床前和临床研究结合起来,同时包括科研人员、临床医生、健康管理以及其他相关机构的成员之间的相互交流、协作,在此过程中纳入肠道菌群健康检测,集结众多力量的合作,从预防偏头痛辅助判别其潜在风险,到偏头痛发作的疾病管理,再到预后减少发病次数等多个阶段,帮助降低偏头痛和偏头痛合并的各种胃肠道疾病的风险,改善偏头痛患者的生活质量,为他们带来更多希望。
注:本账号内容仅作交流参考,不作为诊断及医疗依据。
主要参考文献
Ferrari MD, Goadsby PJ, Burstein R, Kurth T, Ayata C, Charles A, Ashina M, van den Maagdenberg AMJM, Dodick DW. Migraine. Nat Rev Dis Primers. 2022 Jan 13;8(1):2.
Khan J, Asoom LIA, Sunni AA, Rafique N, Latif R, Saif SA, Almandil NB, Almohazey D, AbdulAzeez S, Borgio JF. Genetics, pathophysiology, diagnosis, treatment, management, and prevention of migraine. Biomed Pharmacother. 2021 Jul;139:111557.
Arzani M, Jahromi SR, Ghorbani Z, Vahabizad F, Martelletti P, Ghaemi A, Sacco S, Togha M; School of Advanced Studies of the European Headache Federation (EHF-SAS). Gut-brain Axis and migraine headache: a comprehensive review. J Headache Pain. 2020 Feb 13;21(1):15.
Aurora SK, Shrewsbury SB, Ray S, Hindiyeh N, Nguyen L. A link between gastrointestinal disorders and migraine: Insights into the gut-brain connection. Headache. 2021 Apr;61(4):576-589.
Zhou Y, Pang M, Ma Y, Lu L, Zhang J, Wang P, Li Q, Yang F. Cellular and Molecular Roles of Immune Cells in the Gut-Brain Axis in Migraine. Mol Neurobiol. 2023 Sep 11.
He Q, Wang W, Xiong Y, Tao C, Ma L, Ma J, You C; International Headache Genetics Consortium. A causal effects of gut microbiota in the development of migraine. J Headache Pain. 2023 Jul 17;24(1):90.
Kim JH, Lee Y, Kwon YS, Sohn JH. Clinical Implications of the Association between Respiratory and Gastrointestinal Disorders in Migraine and Non-Migraine Headache Patients. J Clin Med. 2023 May 12;12(10):3434.
Cámara-Lemarroy CR, Rodriguez-Gutierrez R, Monreal-Robles R, Marfil-Rivera A. Gastrointestinal disorders associated with migraine: A comprehensive review. World J Gastroenterol. 2016 Sep 28;22(36):8149-60.
Slavin M, Li HA, Frankenfeld C, Cheskin LJ. What is Needed for Evidence-Based Dietary Recommendations for Migraine: A Call to Action for Nutrition and Microbiome Research. Headache. 2019 Oct;59(9):1566-1581.
Park CG, Chu MK. Interictal plasma glutamate levels are elevated in individuals with episodic and chronic migraine. Sci Rep. 2022 Apr 28;12(1):6921.
Sgro M, Ray J, Foster E, Mychasiuk R. Making migraine easier to stomach: the role of the gut-brain-immune axis in headache disorders. Eur J Neurol. 2023 Jun 17.
Do TP, Hougaard A, Dussor G, Brennan KC, Amin FM. Migraine attacks are of peripheral origin: the debate goes on. J Headache Pain. 2023 Jan 10;24(1):3.
Pleș, H.; Florian, I.-A.; Timis, T.-L.; Covache-Busuioc, R.-A.; Glavan, L.-A.; Dumitrascu, D.-I.; Popa, A.A.; Bordeianu, A.; Ciurea, A.V. Migraine: Advances in the Pathogenesis and Treatment. Neurol. Int. 2023, 15, 1052-1105.
Kappéter, Á.; Sipos, D.; Varga, A.; Vigvári, S.; Halda-Kiss, B.; Péterfi, Z. Migraine as a Disease Associated with Dysbiosis and Possible Therapy with Fecal Microbiota Transplantation. Microorganisms 2023, 11, 2083.
Yamanaka, G.; Suzuki, S.; Morishita, N.; Takeshita, M.; Kanou, K.; Takamatsu, T.; Suzuki, S.; Morichi, S.; Watanabe, Y.; Ishida, Y.; et al. Role of Neuroinflammation and Blood-Brain Barrier Permutability on Migraine. Int. J. Mol. Sci. 2021, 22, 8929.
Martami F, Togha M, Seifishahpar M, Ghorbani Z, Ansari H, Karimi T, Jahromi SR. The effects of a multispecies probiotic supplement on inflammatory markers and episodic and chronic migraine characteristics: A randomized double-blind controlled trial. Cephalalgia. 2019 Jun;39(7):841-853.
Fila, M.; Chojnacki, J.; Pawlowska, E.; Szczepanska, J.; Chojnacki, C.; Blasiak, J. Kynurenine Pathway of Tryptophan Metabolism in Migraine and Functional Gastrointestinal Disorders. Int. J. Mol. Sci. 2021, 22, 10134.
Goschorska, M.; Gutowska, I.; Baranowska-Bosiacka, I.; Barczak, K.; Chlubek, D. The Use of Antioxidants in the Treatment of Migraine. Antioxidants 2020, 9, 116.
Spekker, E.; Nagy-Grócz, G. All Roads Lead to the Gut: The Importance of the Microbiota and Diet in Migraine. Neurol. Int. 2023, 15, 1174-1190

谷禾健康
不知道大家有没有这样的体验:紧张时会想上厕所,伤心时会食欲不振。任何情绪变化,好像都会反映在消化系统。
与此同时,你相不相信一个人的肠道微生物可以影响其认知、性格、气质、社交情况、甚至是责任心。
有大量证据表明神经系统与肠道微生物的组成和功能有关。目前,已经描述了各种肠-脑串扰途径,包括通过迷走神经途径的免疫、内分泌和神经回路。此外,中枢神经系统控制肠道菌群的失衡,构成双向通讯系统。
肠道菌群失衡,也许是导致精神问题的潜在原因。一些研究发现,肠道菌群改变(生态失调)与阿尔茨海默病、自闭症和帕金森病等神经精神疾病以及焦虑、抑郁和认知功能障碍等其他心理疾病有关。
肠道菌群可以分泌神经递质,例如乙酰胆碱、γ-氨基丁酸(GABA)和色氨酸;此外肠道中有数百万个神经元,可以通过神经递质向大脑发送信号。
肠脑轴功能障碍被认为是精神障碍的病理生理学;因此,恢复受干扰的微生物生态系统为管理或预防这些神经系统疾病提供了一种新颖且有前途的方法。
本文对人类肠道微生物群失调与几种精神和心理疾病之间联系进行了概述。此外,还展示了一些使用精神药物与调节肠道微生物相结合的方式以改善精神疾病或心理障碍的干预措施。肠道微生物群在未来可能成为缓解压力与治疗精神疾病的新工具。
人类肠道含有多样化的微生物群落,据估计,肠道中的微生物数量可以达到数万亿个。微生物群的密度在肠道不同部位也有所不同,结肠和直肠的微生物密度较高,而小肠的微生物密度较低。
肠道微生物由多种微生物类群组成,包括细菌、病毒、真菌、古细菌和原生动物,其中最主要的是细菌。
•古细菌
在健康的人类肠道中,古细菌的数量很少,其中史密斯产甲烷短杆菌(Methanobrevibactersmithii)是最常见的物种。
•真菌
肠道中最常检测到的真核微生物是真菌,例如念珠菌(Candida)和酵母菌(Saccharomyces)。这些真菌维持生态和免疫肠道微生物组的平衡。
•病毒
人体病毒组主要由噬菌体组成,它们在肠道中的作用是作为细菌组的调节剂。
•原生生物
一些原生动物,例如芽囊原虫属(Blastocystis),已在人类肠道微生物群中检测到,它们的存在通常与胃肠道疾病有关。
✦细菌是人类肠道中最常见的微生物
细菌是人体肠道中最常见的微生物,一般属于以下8个门:放线菌门 (Actinobacteria)、芽孢杆菌门 (Bacillota)(又名厚壁菌门)、拟杆菌门 (Bacteroidetes)、弯曲菌门 (Campylobacterota)、梭杆菌门(Fusobacteria)、变形菌门(Proteobacteria)、热脱硫杆菌门(Thermodesulfobacteriota)和疣微菌门(Verrucomicrobia)。
下图显示了健康人肠道微生物群中主要的门、科和属。
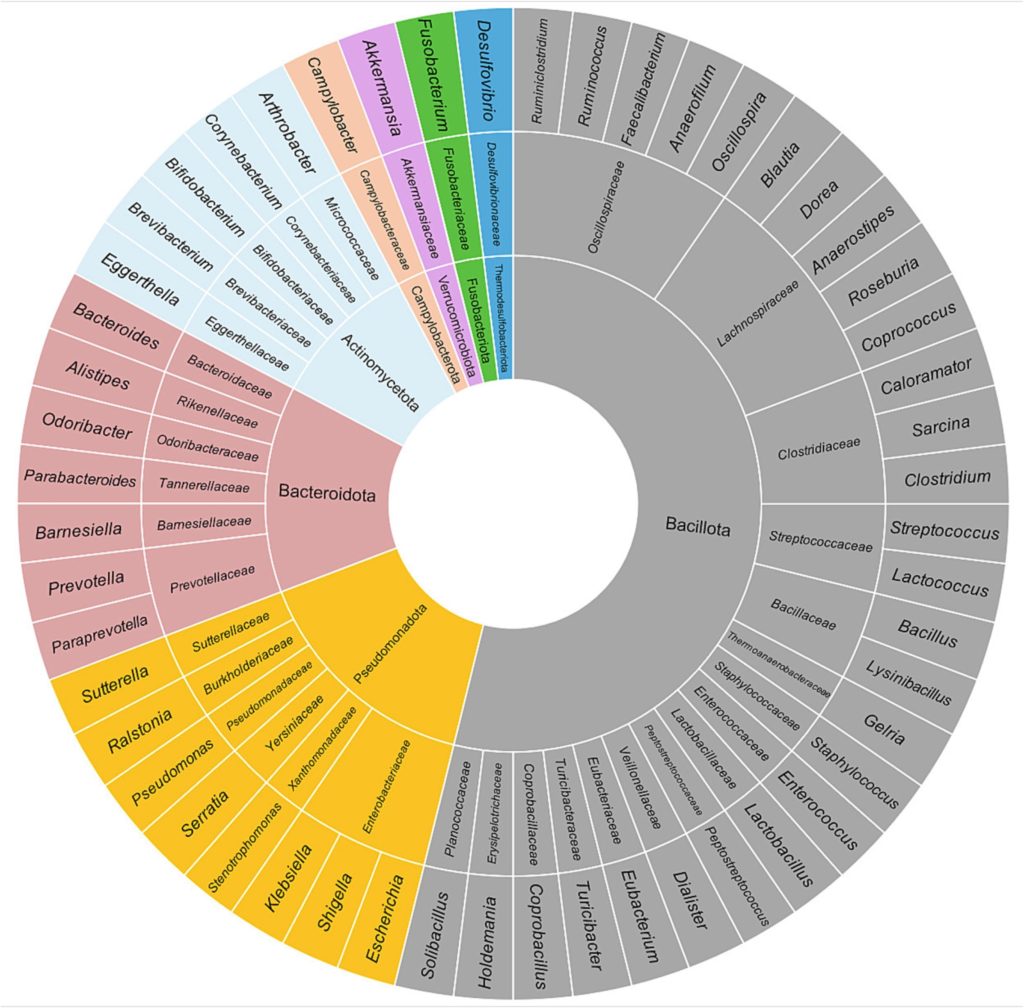
Borrego-Ruiz A,et al.Prog Neuropsychopharmacol Biol Psychiatry.2023
✦肠道不同部位的微生物群组成具有差异
肠道区室中的微生物有特定的空间分布。上消化道中最主要的是孪生球菌属(Gemella)、韦荣氏球菌属(Veillonella)、奈瑟菌属(Neisseria)、梭杆菌属(Fusobacterium)、链球菌属(Streptococcus)、普雷沃氏菌属(Prevotella)、假单胞菌属(Pseudomonas)和放线菌属(Actinomyces)。
而在下消化道中则有粪杆菌属(Faecalibacterium)、拟杆菌属(Bacteroides)和瘤胃球菌属(Ruminococcus)。
十二指肠
研究发现人类十二指肠粘膜富含芽孢杆菌(Bacillus)、Solibacillus、赖氨酸芽孢杆菌(Lysinibacillus)、微小杆菌属(Exiguobacterium)、海洋芽胞杆菌属(Oceanobacillus)和类芽孢杆菌(Paenibacillus)。
空肠
在空肠中,变形菌门和厚壁菌门是最常见的门,而埃希氏菌属、乳杆菌属和肠球菌属是空肠中最常见的属。
回肠
链球菌属(Streptococcus spp.)、大肠杆菌(Escherichia coli)和梭菌属(Clostridium spp.),是回肠中最常见的物种。
结肠
结肠是一个厌氧环境,以拟杆菌门、放线菌门和厚壁菌门以及毛螺菌科(Lachnospiraceae)、瘤胃球菌科(Ruminococcaceae)、普雷沃氏菌科(Prevotellaceae)、拟杆菌科(Bacteroidaceae)和理研菌科(Rikenellaceae)为主,以及已鉴定的主要细菌属乳杆菌属、双歧杆菌属和粪杆菌属。
研究了不同结肠区域的细菌属优势,他们发现乙状结肠中存在拟杆菌属、肠球菌属。近端结肠和远端结肠为粪杆菌和大肠杆菌。
阑尾中微生物多样性较高,以放线菌门、梭杆菌门、变形菌门、拟杆菌门和厚壁菌门为主;以及毛螺菌科、肠杆菌科、拟杆菌科、梭杆菌科和双歧杆菌科。
尽管人类肠道微生物群的组成因年龄、营养和抗生素使用等因素而在分类学和功能上存在差异,但人类肠道微生物群主要是由乳杆菌属、芽孢杆菌属、梭菌属、肠球菌属、瘤胃球菌属、粪杆菌属、罗氏菌属(Roseburia)、经黏液真杆菌属(Blautia)、Dorea属、拟杆菌属、普雷沃氏菌属、双歧杆菌属和埃希氏菌属。
✦肠道微生物对于消化非常重要
肠道微生物群为人类宿主提供了多种积极影响,包括免疫和代谢功能。肠道微生物是消化的关键调节者,通过营养物质的吸收以及多种代谢物的合成,包括脂质、氨基酸、维生素和短链脂肪酸。
✦肠道微生物有助于预防病原体感染
此外,肠道微生物群通过多种竞争过程在预防病原菌感染方面发挥着关键作用,并且还有助于维持肠上皮的完整性。
✦肠道微生物产生的化合物可作为信号分子
肠道微生物群从未消化的食物中产生多种分泌化合物。其中一些可以作为细菌间通讯的信号分子,影响细菌调节、稳态、生长、毒力和生物膜形成等。
色氨酸代谢物
细菌还可能分泌其他生物活性化合物,包括色氨酸分解代谢物、短链脂肪酸、多胺和组胺。色氨酸的代谢产物[5-羟色胺(血清素)、犬尿氨酸和吲哚]与生理和神经元活动有关。
吲哚
吲哚调节肠促胰岛素的分泌,调节肠道屏障通透性,并且可以作为微生物和宿主细胞之间细胞间通讯的信号分子。此外,吲哚及其衍生物被描述为神经炎症的抑制化合物。
短链脂肪酸
最重要的定量代谢物是由微生物降解不可消化的膳食纤维、蛋白质和糖蛋白产生的短链脂肪酸。如丁酸盐、乙酸盐和丙酸盐,可以作为信号分子,局部调节从十二指肠到结肠的肠道功能,并且通过肠内分泌细胞,它们还可以控制肝脏、肌肉和大脑的代谢,影响肠道功能及宿主能量稳态。
此外,短链脂肪酸通过诱导神经炎症反应呈现神经活性特性。短链脂肪酸是强大的表观遗传调节剂,控制DNA甲基化遗传物质的可及性并抑制组蛋白脱乙酰化。
该机制依赖于10-11易位 (TET) 蛋白,该蛋白催化胞嘧啶残基羟基化为5-羟甲基胞嘧啶,介导主动DNA去甲基化。确定丁酸盐诱导前额皮质中许多行为相关基因的变化,特别是影响涉及神经元兴奋或抑制的基因。几种兴奋性神经递质和神经元激活标记基因的减少,以及抑制性神经递质基因的增加表明丁酸盐促进抑制途径转录物的转录。
✦细菌代谢产物会影响神经发育
最近的研究表明,细菌代谢产物会影响神经发育。一些研究人员还报道了短链脂肪酸影响神经发生基因的表达。
使用无微生物的斑马鱼模型,观察到无微生物培养的胚胎中神经基因表达显著下降,并通过添加斑马鱼代谢物重新建立了该模型,识别出超过300个下调的基因。
基因分析表明,这些基因参与重要的神经发育途径,包括转录调控和Wnt信号传导。事实上,Wnt信号通路在发育和疾病中发挥着重要作用,可以推测其调控与多细胞真核生物的细菌定植共同进化。
下图展示了肠道微生物群合成的一些关键神经递质及其与心理和精神疾病的关联。这些神经活性化合物通过内在或外在传入神经通路将信息从肠腔传输到肠神经系统、肠神经胶质细胞和中枢神经系统。
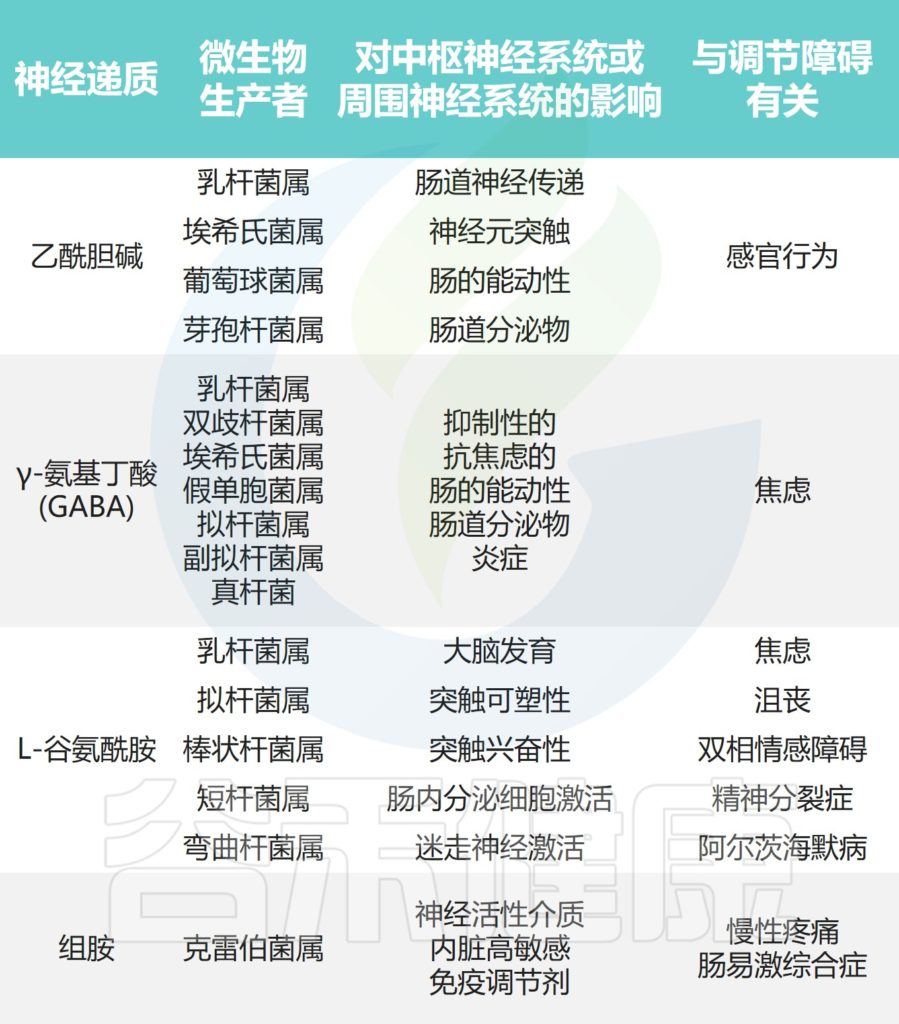

Borrego-Ruiz A,et al.Prog Neuropsychopharmacol Biol Psychiatry.2023
阿尔茨海默病(AD)是一种慢性神经退行性疾病,其中记忆和执行功能进行性丧失,与突触损伤和神经损失有关,主要发生在海马体和大脑皮层。
多项研究已明确β-淀粉样肽(Aβ)在阿尔茨海默病中的作用。最近的研究表明,细菌来源的淀粉样蛋白,例如curli、Csg A、tau、TasA、FapC和酚溶性调节蛋白,在Aβ寡聚体的聚集和促进错误折叠中发挥作用。
细菌淀粉样蛋白通过与Toll样受体2相互作用激活宿主免疫系统,诱导促炎介质刺激大脑中神经元淀粉样蛋白的产生。
•肠道微生物失调与阿尔兹海默病存在关联
其他证据表明肠道微生物群失调与阿尔茨海默病的早期阶段有关,导致细胞因子分泌增强、免疫衰老、神经炎症和氧化应激。
此外,肠道微生物失调会诱导脂多糖的分泌,从而破坏胃肠道通透性和血脑屏障,调节炎症途径,促进神经炎症和认知能力下降,并导致阿尔茨海默病中的神经元死亡。
在大鼠中,腹膜脂多糖给药导致炎症因子(例如IL-1、IL-6和TNF-α)水平升高,表明微生物组在阿尔茨海默病先天免疫反应的启动中发挥作用。
•阿尔兹海默病中短链脂肪酸水平降低
研究表明,阿尔茨海默病小鼠的微生物群组成和多样性受到干扰,短链脂肪酸水平降低,这预示着30多种代谢途径的改变,这可能与淀粉样蛋白沉积有关。
肠道菌群失调可能会增加氧化三甲胺(TMAO)浓度,这与不同的功能有关,例如β-淀粉样蛋白的形成、外周免疫反应的激活和氧化应激。此外,还与肠粘膜屏障功能障碍、血脑屏障通透性以及胆汁酸和胆固醇进入大脑的通道增加有关。
•阿尔茨海默病患者体内促炎菌群比例增加
研究发现阿尔茨海默病患者中大肠杆菌/志贺氏菌等促炎菌群的比例增加,而直肠真杆菌(eubacterium rectale)、霍氏大肠杆菌(E.hallii)、普拉梭菌(F. prausnitzii)和脆弱拟杆菌等产生丁酸的细菌则减少。
这些细菌与外周炎症状态有关,这是轻度认知障碍(MCI)和脑淀粉样变性患者的典型症状。
注:淀粉样脑血管病主要是由淀粉样物质在软脑膜以及大脑皮质小动脉中层沉积所导致的疾病,多见于80岁以上的老年人,可能会导致血管壁受损。
•阿尔茨海默病患者肠道微生物多样性较低
据报道阿尔茨海默病患者肠道菌群的微生物多样性较低,厚壁菌门和双歧杆菌种类减少。
此外,发现门水平上拟杆菌门细菌成员增加,放线菌门减少,以及科水平上瘤胃球菌科、肠球菌科和乳杆菌科增加,毛螺菌科、拟杆菌科和韦荣氏菌减少。
促炎细菌类群增加,同时产生丁酸盐的细菌减少,例如丁酸弧菌(B.proteoclasticus和B.Hungatei)、梭菌属、真杆菌属(E.Hallii、E.rectal和E.eligens)、普拉梭菌和罗斯拜瑞氏菌 (R.hominis)。
几种精神障碍疾病中的肠道菌群失调
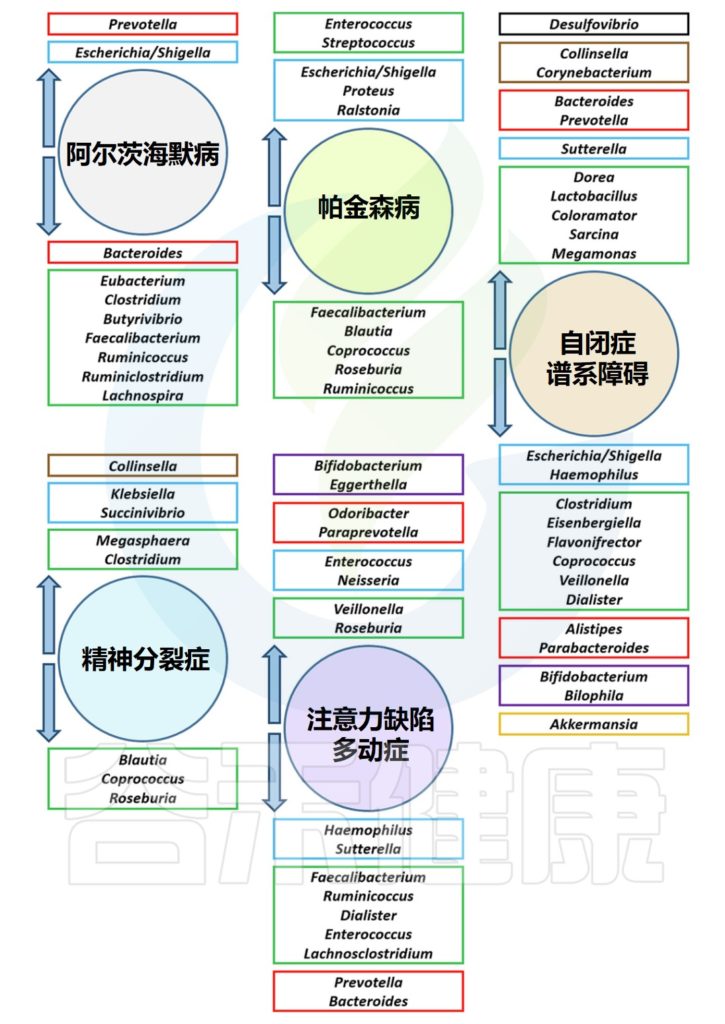
Borrego-Ruiz A,et al.Prog Neuropsychopharmacol Biol Psychiatry.2023
自闭症谱系障碍(ASD)是一种大脑发育障碍,其特征是刻板行为以及沟通和社交互动缺陷。
注:儿童自闭症是儿童精神类疾病当中最为严重的一种。
自闭症谱系障碍的确切病理学和病因很难确定,研究重点是调查遗传原因、免疫系统失调、环境毒物暴露以及肠道微生物群的改变。
•自闭症儿童的肠道微生物多样性较高
据报道自闭症儿童的肠道微生物多样性较高。自闭症谱系障碍样本中最常见的属如下:
拟杆菌属(Bacteroides),
脱硫弧菌属(Desulfovibrio),
柯林斯氏菌属(collinsella),
棒状杆菌属 (Corynebacterium),
乳杆菌属(Lactobacillus),
普雷沃氏菌属(Prevotella),
萨特氏菌属(Sutterella),
八叠球菌(Sarcina),
罗氏菌属(Roseburia),
粪杆菌属(Faecalibacterium),
巨单胞菌(Megamonas),
Caloramator,
Dorea;
此外以下属的存在减少:
双歧杆菌(Bifidobacterium) ↓↓↓
另枝菌属(Alistipes) ↓↓↓
嗜胆菌属(Bilophila) ↓↓↓
韦荣氏球菌属(Veillonella) ↓↓↓
阿克曼菌(Akkermansia) ↓↓↓
粪球菌属(Coprococcus) ↓↓↓
埃希氏杆菌属-志贺氏杆菌 ↓↓↓
梭菌属(Clostridium) ↓↓↓
艾森伯格氏菌(Eisenbergiella) ↓↓↓
嗜血杆菌属(Haemophilus)↓↓↓
Dialister ↓↓↓
Parabacteroides ↓↓↓
Flavonifractor ↓↓↓
这些发现强烈表明肠道微生物群失调与自闭症行为表现之间存在联系。
•有害菌会产生神经毒素影响自闭症
在自闭症行为表现患者中发现双歧杆菌丰度较低,而双歧杆菌是产生GABA神经递质的关键,双歧杆菌丰度过低会导致焦虑、认知缺陷和行为障碍。
产生神经毒素的艰难梭菌和溶组织梭菌的积累与自闭症谱系障碍症状相关。这些释放的有毒分子会影响血清素信号传导,可能导致自闭症谱系障碍行为模式,例如社交能力下降、对疼痛的反应减弱、语言异常以及自虐或重复行为。
受自闭症行为表现影响的个体表现出其他潜在有毒化合物水平的改变,例如抑制多巴胺-β-羟化酶的对甲酚和对甲酚硫酸盐。此外,在受自闭症谱系障碍影响的个体中检测到梭菌衍生的代谢物3-(3-羟基苯基)-3-羟基丙酸增加,这可能反映了儿茶酚胺代谢的改变。
•短链脂肪酸对自闭症的作用存在矛盾结果
短链脂肪酸在自闭症谱系障碍中的作用存在矛盾的结果。丙酸盐会诱导小胶质细胞激活、神经毒性细胞因子产生、基因表达改变、海马组织学异常和神经行为异常,例如重复动作和社交互动受损。
然而,丁酸盐对一种自闭症谱系障碍样小鼠模型的社交和重复行为具有有益影响。丁酸盐改善血脑屏障的不渗透性可能是丁酸盐可以恢复丙酸盐诱发的自闭症样疾病异常的另一种机制。
帕金森病(PD)是老年人中常见的一种痴呆症,其主要疾病症状包括神经炎症、中脑多巴胺能神经元丧失以及伴有非运动症状的异常运动。
•微生物失调引起的炎症可能导致帕金森病发展
一些研究人员认为,微生物群失调引起的炎症反应可能会导致帕金森病病理学的发展或恶化。这些反应可以促进脂多糖和α-突触核蛋白在肠道和大脑中的积累,并且由于促炎细菌活性导致氧化应激增加,从而促进α-突触核蛋白病理学通过迷走神经从头侧向尾侧区域扩散。
•帕金森病患者体内短链脂肪酸显著减少
另一方面,微生物短链脂肪酸可以防止肠粘膜通透性增加,从而减少细菌移位。帕金森病中短链脂肪酸显著减少。
短链脂肪酸在帕金森病病理学中的作用尚未完全阐明,报道短链脂肪酸的消耗导致肠神经系统中路易体的形成;相反,有研究表明短链脂肪酸能够降低血脑屏障的通透性。
注:路易体主要是以帕金森病为代表的脑门特征性标志物,患者常常会出现功能障碍。
考虑到短链脂肪酸缺乏与神经炎症和小胶质细胞激活以及便秘、肠漏和结肠炎症等胃肠道特征有关,这些研究结果支持了这样的假设:短链脂肪酸缺乏可能是帕金森病的病因。
•帕金森病患者有抗炎作用的菌群减少
帕金森病患者经常出现属于乳杆菌科、巴氏杆菌科和肠球菌科的某些细菌种类水平升高。
此外发现,帕金森病患者粪便和粘膜中产生抗炎丁酸的细菌水平显著降低(普雷沃氏菌、布氏菌、粪球菌属和罗氏菌属),以及粪杆菌属的水平显著降低。
此外,像罗尔斯通氏菌(Ralstonia)这样的促炎细菌在帕金森病患者的肠粘膜中更为丰富。
拓展
基于肠杆菌科细菌滴度与帕金森病症状严重程度之间的正相关性,这些作者认为肠道微生物群可能与帕金森病表型有关。
相关分析显示疾病严重程度和帕金森病持续时间与纤维素降解剂呈负相关,但与致病生物呈正相关,可能导致短链脂肪酸产生减少以及神经毒素和内毒素增加,可能与帕金森病病理学的发展有关。
此外,普雷沃菌科丰度的降低和乳杆菌科丰度的增加与胃饥饿素浓度的降低有关,胃饥饿素是一种与维持正常多巴胺功能有关的肠道激素,帕金森病患者的胃饥饿素分泌发生了改变。
精神分裂症是一种复杂的精神障碍,患者对现实的理解异常,经常出现焦虑和严重抑郁症状。
这种疾病的起源是有争议的,表明是遗传起源。然而,值得注意的是,通过表观遗传学机制,如神经传递基因甲基化、核苷酸修饰或非编码RNA的作用,一些环境因素可能在其易感性和疾病的发展中发挥作用。
•肠道菌群代谢物影响精神分裂症风险
短链脂肪酸、色氨酸分解代谢物和神经递质(GABA、谷氨酸)的差异被称为精神分裂症相关的肠脑模块。
微生物产生的多巴胺与精神分裂症有关,而与精神分裂症相关的胃肠道炎症增加强烈表明肠道微生物群可能在患精神分裂症或其表现的风险中发挥作用。
•精神分裂症患者肠道微生物群显著改变
研究表明抗生素治疗引起的肠道微生物群失调与精神分裂症的发病率之间存在直接关系。精神分裂症患者中巨球型菌属、琥珀酸弧菌属、梭菌属、柯林斯氏菌属、甲烷短杆菌属和克雷伯菌属的丰度显著增加,而与健康人相比,精神分裂症患者中经黏液真杆菌属、粪球菌属和罗氏菌属的滴度下降。
•抗精神病药物治疗后肠道微生物群发生改变
几项研究已经确定抗精神病药物治疗与肠道微生物群之间的联系。精神分裂症患者在接受抗精神病药物治疗后发现微生物群丰度发生了显著变化。
在其他研究中,接受抗精神病药物治疗的患者的厚壁菌门与拟杆菌门的比例逐渐增加,与体重指数的上升相关。此外,接受治疗的个体的肠道微生物群富含短链脂肪酸和血清素代谢的基因。
注意缺陷与多动障碍(ADHD)是一种神经发育障碍,其特征是高度多动冲动和注意力问题。尽管可能涉及环境和遗传因素,一些证据表明注意缺陷与多动障碍的发展或症状可能与饮食成分对肠道微生物组的调节有关。
•ADHD儿童体内有害菌丰度较高,有益菌较少
最近发现,食用加工饮食的注意缺陷与多动障碍儿童体内有害细菌(如肠杆菌、大肠杆菌和梭菌菌株)的丰度明显较高,而有益细菌(如双歧杆菌和瘤胃球菌菌株)的丰度明显较低。
食用加工食品的注意缺陷与多动障碍患者的肠道微生物群α多样性和短链脂肪酸水平显著低于对照组,研究人员认为不平衡的饮食会扰乱结肠微生物平衡,并可能成为多动症患病的潜在风险因素。
•患者肠道菌群失衡影响激素和神经递质水平
宿主-微生物组的相互作用对激素和神经递质水平产生影响,被认为与注意缺陷与多动障碍的病理生理学有关。肠道菌群失调加上持续接触微生物病原体引起的免疫功能障碍可能会导致受影响的多动症患者出现过度活跃的行为。
肠道菌群提供多巴胺和去甲肾上腺素的前体
注意缺陷与多动障碍与预测的多巴胺和去甲肾上腺素合成异常有关,其前体由肠道细菌(主要是双歧杆菌)提供。
压力被定义为由困难情况或环境压力源引起的非特定情绪或身体反应。这种反应与心理和生物因素有关,例如性激素、高情绪反应性、被动应对技巧、糖皮质激素抵抗以及中枢和外周免疫激活。
✦压力会影响肠道微生物组成与活动
不同类型的心理和社会压力源已被证明可以通过神经元、免疫细胞和结肠嗜铬细胞释放信号分子、激素或神经递质来调节肠道微生物群的组成和活动。
压力对肠道微生物群的影响可能直接通过宿主肠道微生物群信号传导介导,也可能间接通过肠道生态系统的变化介导,并涉及炎症反应、微生物栖息地的改变、肠道运动和粘蛋白分泌。
✦产生短链脂肪酸的细菌减少可能是导致焦虑的关键
暴露于压力会导致肠道微生物群组成的实质性变化,肠杆菌科细菌的增加,而乳杆菌属的细菌减少。拟杆菌属减少,梭菌属增加。以及大肠杆菌和假单胞菌属的增加。
某些微生物群可能参与应激性焦虑和一般性焦虑症,其特征是社交和职业功能下降。研究人员报道,在一般性焦虑症患者中,粪杆菌(Faecalibacterium)、直肠真杆菌(E.rectale)、毛螺菌属(Lachnospira)、丁酸球菌(Butyricicoccus)和萨特氏菌(Sutterella)较低。这些都是短链脂肪酸的重要生产者。
应激性焦虑是指在强烈的精神或躯体应激事件的刺激下,产生的过度焦虑、恐惧等情绪。患者可出现紧张、坐立不安、心慌、呼吸急促等症状,还可伴有睡眠障碍、食欲改变等表现。
大胆猜想
短链脂肪酸产生菌的减少是焦虑和抑郁单胺类假说的关键。
单胺假说——指科学家在抗抑郁药领域提出的假说,即抑郁患者神经突触间隙可有效利用的单胺类神经递质浓度明显下降,而升高突触间隙单胺递质浓度(主要是血清素)能发挥抗抑郁作用。
抑郁症是一种与压力相关的情绪障碍,涉及神经免疫-神经内分泌失调,与促炎细胞因子水平升高相关。
促炎细胞因子与高水平的皮质醇有关,通过抑制四氢生物蝶呤酶发挥重要作用,四氢生物蝶呤对于合成多巴胺、血清素和去甲肾上腺素至关重要。
多巴胺、血清素和去甲肾上腺素是人体内重要的神经递质,它们在神经系统中发挥着重要的作用。
✦肠道微生物的多样性与抑郁严重程度负相关
几项研究报告称,不同抑郁症患者的肠道微生物群组成差异较大,粪便微生物多样性的增加与抑郁症症状的严重程度呈负相关。
研究人员发现,Gelria、Turicibacter、Anaerofilum、Paraprevotella、Holdemania和Eggerthella属在抑郁症患者中普遍存在,而普雷沃氏菌(Prevotella)和戴阿利斯特杆菌(Dialiste)的存在减少。
抑郁症患者体内有益菌大量减少
后来的研究还发现,与对照组相比,抑郁症患者肠道微生物总体减少。肠道微生物群中的双歧杆菌和乳酸菌减少。Dorea、瘤胃球菌属和阿克曼氏菌属的显著减少,以及副拟杆菌属(Parabacteroides)、普雷沃氏菌属(Prevotella)和放线菌属(Actinobacteria)的增加与抑郁个体相关。
✦短链脂肪酸有助于释放神经递质和调节血脑屏障
几项研究表明,重度抑郁症患者的丁酸盐、乙酸盐和丙酸盐减少,表明短链脂肪酸可能通过直接刺激神经通路或通过神经内分泌和免疫激活的间接中枢效应改变行为。
短链脂肪酸也有助于结肠嗜铬细胞合成和释放外周神经递质(血清素和乙酰胆碱),并有助于交感神经元合成和释放去甲肾上腺素。
除了局部作用外,短链脂肪酸还可以直接作用于血脑屏障的中心受体。此外,体外研究表明,丙酸盐和丁酸盐,而不是乙酸盐,都可以调节血脑屏障的通透性,防止脂多糖引起的通透性增加。
强迫症是一种慢性且持久的疾病,会被迫出现侵入性、自我张力障碍的想法或冲动或重复行为。
尽管只有少数研究涉及肠道微生物群与强迫症的关系,但压力和抗生素治疗都会影响微生物群组成,已被认为是与强迫症症状同时发生的因素。
✦强迫症患者肠道微生物丰富度较低
据报道,患有强迫症的个体肠道微生物群的物种丰富度较低,产生丁酸盐的属(颤旋菌属、Odoribacter和Anaerostipes)的相对丰度较低。
最近还报道强迫症患者粪便样本显示文肯菌科(Rikenellaceae)(另枝菌属)丰度增加,而普雷沃氏菌和毛螺菌科(Lachnospiraceae)丰度降低。
几种心理障碍中的肠道菌群失调
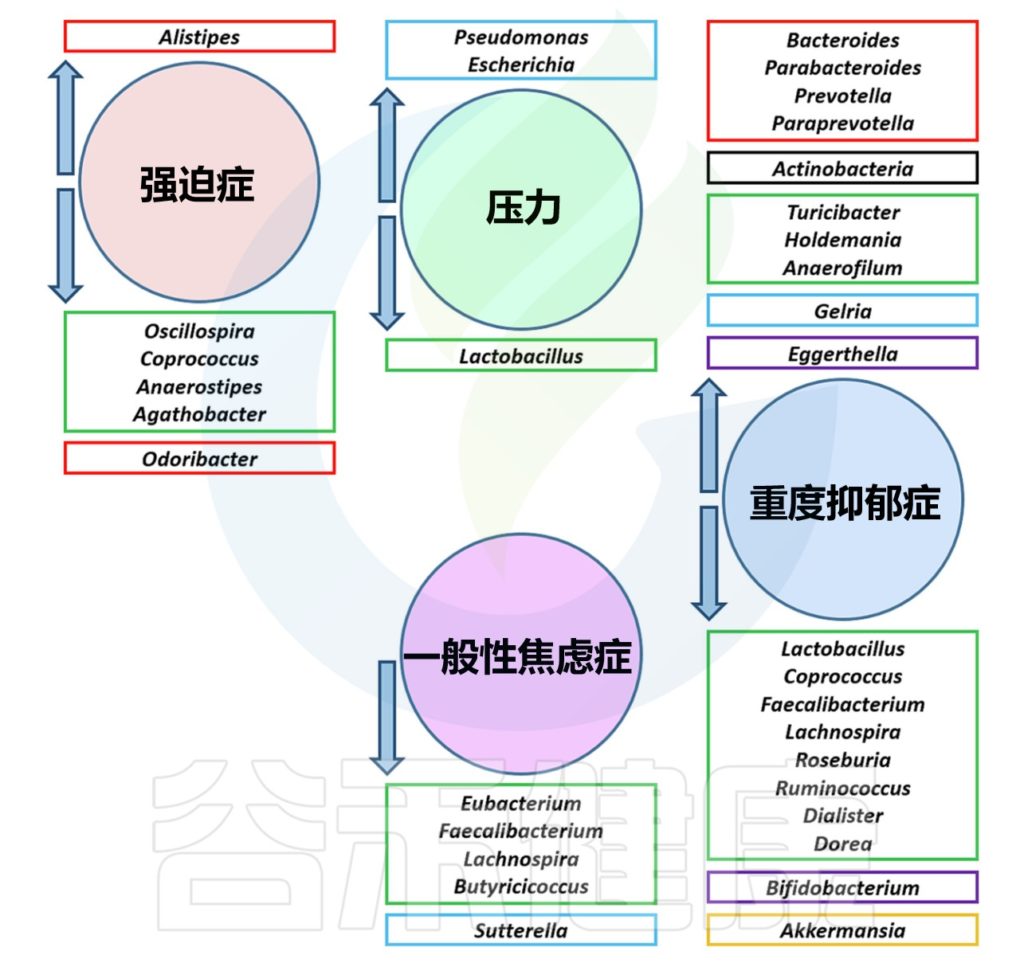
Borrego-Ruiz A,et al.Prog Neuropsychopharmacol Biol Psychiatry.2023
杏仁核在与压力相关的情绪、行为反应和情绪调节中发挥着关键作用,它显著受到肠道微生物群的影响。
杏仁核,又名杏仁体,呈杏仁状,是边缘系统的一部分。
√肠道微生物的变化可以调节认知功能
在动物模型中,有一些证据支持肠道微生物群组成的变化可以影响调节认知功能,尽管只有少数研究关注人类认知。
拟杆菌水平较高的人群拥有较好的认知表现
最近,根据粪杆菌(Faecalibacterium)、拟杆菌(Bacteroides)和瘤胃球菌科(Ruminococcaceae)的丰度建立了三组受试者,并得出结论,较好的认知表现与较高水平的拟杆菌相对应。
使用抗生素会影响认知功能,故不可滥用
用抗生素治疗剥夺或破坏肠道微生物群也会影响认知功能,包括语言学习能力以及工作和空间记忆。
√肠道微生物会影响一个人的气质和性格
由于人格特征和行为模式以及生理和心理健康结果之间存在很强的关联,一些研究已经证明肠道微生物群与气质和性格之间存在关联,这些特征甚至可以通过粪菌移植在受试者之间传播。
研究了肠道微生物的组成与儿童气质之间的关系,发现更大的暴躁/外向和恐惧与系统发育多样性呈正相关,包括戴阿利斯特杆菌属 (Dialister)、文肯菌科(Rikenellaceae)、瘤胃球菌科(Ruminococcaceae)和约氏副拟杆菌(Parabacteroides)的丰度变化。
产丁酸细菌更丰富的人可能有更高的责任心
发现高度神经质和低外向性与γ-变形菌纲丰度增加有关。低责任性与变形菌丰度增加和毛螺菌科丰度减少有关,而开放程度高的人与更大的系统发育多样性和丰富度相关。
另一方面,高度的责任心与产生丁酸的细菌滴度的增加有关,这些细菌主要属于毛螺菌科。
√多样化的肠道微生物有助于社交和好心情
最近有研究表明,特定细菌属的丰度与人格特征显著相关。对肠道微生物组多样性的分析表明,具有较高社交网络的个体呈现出多样化的肠道微生物组,而焦虑和压力与肠道微生物组的组成改变和多样性降低有关。
研究还发现某些细菌属,包括阿克曼氏菌、脱硫弧菌、乳球菌、颤螺菌和萨特氏菌可能与行为密切相关。
已经使用了几种方法来确定肠道微生物群对中枢神经系统功能的作用,包括抗生素治疗、无菌动物模型和粪菌移植。
此外,精神抗生素和益生元已被用作精神和心理疾病的辅助治疗。精神抗生素的类别可以定义为“一种活的有机体,通过与共生肠道细菌相互作用,为患有精神疾病的患者带来心理健康益处”。这些药物通过调节和改善肠道微生物群发挥作用。
为了让大家有更清晰的认识,谷禾在下表整理了使用益生菌或益生元治疗对心理或精神疾病的影响。





Borrego-Ruiz A,et al.Prog Neuropsychopharmacol Biol Psychiatry.2023
•基因集富集分析展示下肠道菌群与精神疾病的关联
使用基因集富集分析 (GSEA) 能够检测肠道微生物群与精神疾病之间的以下显著关联:注意力缺陷与多动障碍常伴有脱硫弧菌和梭状芽孢杆菌富集;自闭症谱系障碍与拟杆菌属和脱硫弧菌有关;对于重度抑郁障碍,观察到脱硫弧菌、梭状芽孢杆菌目、钩端螺旋菌科和拟杆菌类的关联。
最近报道了普雷沃氏菌与自闭症谱系障碍以及放线菌属与精神分裂症之间的特定关联。还有一组研究人员提出了放线菌和假单胞菌与重度抑郁障碍之间的关系。
肠道微生物群和中枢神经系统通过两条途径进行交流:
(1)通过迷走神经途径的神经免疫和代谢回路;
(2)通过微生物群合成的代谢产物、肠道激素和内分泌肽。
先前的研究表明,肠道微生物群的失调是几种精神疾病的病理生理学。因此,恢复受干扰的微生物生态平衡可能为管理或预防神经系统疾病提供一种新的、有前景的方法。
另一方面,心理干预已证明在治疗功能性胃肠道疾病如肠易激综合征方面是有效的;然而还需要进一步的研究来确定心理干预对肠道微生物群变化的具体影响。
通过粪菌移植、健康的饮食和生活方式或使用心理生物药物等干预措施重建失调的肠道微生物群,可能在未来调节微生物群肠脑轴功能和促进心理精神健康方面具有重大潜力。
特别是,心理干预可能对某些神经系统疾病具有潜在的治疗作用。然而,这些干预措施的有效性并不相同,取决于给药方法、干预时间、使用的微生物菌株的数量和具体类型以及宿主的生理状况等因素。
在未来,单独或与抗精神病药物联合的个性化精神微生物干预可能成为临床患者的一种新的治疗策略。
主要参考文献
Borrego-Ruiz A, Borrego JJ. An updated overview on the relationship between human gut microbiome dysbiosis and psychiatric and psychological disorders. Prog Neuropsychopharmacol Biol Psychiatry. 2023 Sep 8:110861.
Abuaish S, Al-Otaibi NM, Abujamel TS, Alzahrani SA, Alotaibi SM, AlShawakir YA, Aabed K, El-Ansary A. Fecal Transplant and Bifidobacterium Treatments Modulate Gut Clostridium Bacteria and Rescue Social Impairment and Hippocampal BDNF Expression in a Rodent Model of Autism. Brain Sci. 2021 Aug 5;11(8):1038.
Bear T, Dalziel J, Coad J, Roy N, Butts C, Gopal P. The Microbiome-Gut-Brain Axis and Resilience to Developing Anxiety or Depression under Stress. Microorganisms. 2021 Mar 31;9(4):723.
Ansari F, Pourjafar H, Tabrizi A, Homayouni A. The Effects of Probiotics and Prebiotics on Mental Disorders: A Review on Depression, Anxiety, Alzheimer, and Autism Spectrum Disorders. Curr Pharm Biotechnol. 2020;21(7):555-565.
Bharwani A, Mian MF, Foster JA, Surette MG, Bienenstock J, Forsythe P. Structural & functional consequences of chronic psychosocial stress on the microbiome & host. Psychoneuroendocrinology. 2016 Jan;63:217-27.
Cerovic M, Forloni G, Balducci C. Neuroinflammation and the Gut Microbiota: Possible Alternative Therapeutic Targets to Counteract Alzheimer’s Disease? Front Aging Neurosci. 2019 Oct 18;11:284.
Cryan JF, O’Riordan KJ, Sandhu K, Peterson V, Dinan TG. The gut microbiome in neurological disorders. Lancet Neurol. 2020 Feb;19(2):179-194.

谷禾健康
抑郁症·肠道菌群
当一个人面临抑郁症时,一切看似平常的事都会变得很有挑战性。上班、与朋友社交,甚至只是起床都感觉很困难。
抑郁症是如今已是世界上最普遍的精神障碍之一,一直是心理学和医学领域的研究热点。抑郁症是一种需要预防和治疗的疾病——它并不是软弱或失败的表现。
抑郁症影响着数百万计的人们,造成抑郁症的因素有很多,包括创伤、生活压力事件、遗传基因、环境因素、药物滥用和其他心理健康问题。
虽然我们目前仍然不完全了解导致抑郁症的原因,一个新的研究领域涉及微生物群-肠-脑轴,证明可以控制认知功能。微生物组通过内分泌、免疫和神经活性途径影响肠脑通讯。后者包括微生物源性神经递质(例如,γ-氨基丁酸、血清素)和代谢物(短链脂肪酸和胆汁酸),以及脑源性神经营养因子。

本文我们主要来了解一下关于抑郁症与肠道菌群之间的关系,它们之间的相互作用机制可能涉及肠脑轴、免疫调节、代谢途径、肠漏、神经炎症、HPA轴等多种途径,同时也列举了较多关于抑郁症的干预措施,希望为抑郁症的治疗和预防提供新的视角和方法。

-正文-
抑郁症是一种复杂的疾病,有许多影响因素,包括多种生活方式、饮食、遗传和环境因素。
据估计,全世界有超过3亿人至少经历过一次重度抑郁症。18-25 岁人群中重度抑郁发作的患病率最高。
一开始,抑郁发作的症状可能只是感觉忧郁、疲劳或“陷入困境”。因此,学习如何辨别平常的低落一天或只是感到忧郁和抑郁对于知道何时寻求帮助非常重要。
要符合抑郁发作的症状,个人必须在两周内几乎每天、全天经历抑郁情绪或兴趣丧失,以及同时经历其他四到五种症状。
▼
某些类型的抑郁症还可能出现以下症状:
▼
抑郁症的主要诊断标准包括:
然而,请注意,并非所有症状都必须出现才能被诊断为抑郁症:大多数患者仅具有完整“核心”症状的一部分。
▼
包括情绪低落或失去兴趣的症状,大多数情况持续至少两周,影响日常活动。
也称为心境恶劣或心境恶劣障碍,是指持续时间较长(通常至少 2 年)的不太严重的抑郁症状。
指怀孕期间或怀孕后发生的抑郁症。在怀孕期间开始的抑郁症是产前抑郁症,在婴儿出生后开始的抑郁症是产后抑郁症。
是一种随季节变化而出现和消失的抑郁症,症状通常在秋末冬初开始,在春季和夏季消失。
是抑郁症的一种严重形式,患者会出现精神病症状,例如妄想(令人不安的、错误的固定信念)或幻觉(听到或看到别人没有听到或看到的东西)。
其他还有:
以前称为躁狂抑郁症或躁狂抑郁症患者,也会经历抑郁发作,在此期间他们感到悲伤、冷漠或绝望,并且活动水平非常低。但双相情感障碍患者也会经历躁狂(或不太严重的轻躁狂)发作,或情绪异常升高,他们可能会感到非常高兴、烦躁或“兴奋”,活动水平显着增加。
▼
一些可能增加一个人患抑郁症风险的已知因素包括:
▼
神经递质是神经元用来将信号从一个细胞传递到另一个细胞的化学物质。神经递质有 100 多种不同类型,其中最著名的包括血清素、多巴胺和去甲肾上腺素等。
大多数最常见或广泛使用的抗抑郁药物(例如西酞普兰和许多其他药物)通常通过增加大脑中可用的神经递质血清素和去甲肾上腺素的量来发挥作用(即选择性血清素再摄取抑制剂或血清素-去甲肾上腺素再摄取抑制剂,或分别为“SSRI”和“SNRI”)。
注:西酞普兰是一种抗抑郁药,属于选择性血清素再摄取抑制剂(SSRI)类药物。是一种流行且用途广泛的处方药,用于治疗许多精神健康状况,包括抑郁、焦虑和创伤后应激障碍 (PTSD)。它于 2002 年获得 FDA 批准用于治疗抑郁症(成人和青少年)和广泛性焦虑症(成人)。
然而,其他一些抗抑郁药——例如安非他酮(Wellbutrin)——主要作用于多巴胺和去甲肾上腺素(即去甲肾上腺素-多巴胺再摄取抑制剂,或“NDRIs”)。
尽管如此,低水平的血清素或去甲肾上腺素是否直接导致抑郁症仍然是一个悬而未决的问题。许多科学尝试证实抑郁症患者实际上具有异常低水平的这些神经递质,但有时未能完全验证其中的联系。
我们理解的抑郁症的另一个主要方法学局限性是,尽管抗抑郁药已经建立了生化机制(例如抑制单胺氧化酶(MAO),或抑制特定神经递质的再摄取),但抑郁症的诊断和治疗很大程度上基于主观报告症状,而不是特定生化标志物或其他“客观”生物指标的任何离散测量。
换句话说,这并不是通过测量一个人这些化合物的水平,然后得出他们是否“患有”抑郁症那么简单。此外,虽然大多数 SSRI 会立即增加大脑中的血清素水平和活动,但许多患者在服用药物数周或数月后才报告情绪有显著改善。
诸如此类的发现表明血清素水平可能只是与抑郁症共同相关的更为复杂的机制和生物变化链中的一个部分。
虽然抑郁症的“血清素缺乏”假说仍然存在争议,并且并非 100% 被所有研究人员普遍接受,但目前根据迄今为止可获得的总体证据和数据,它通常被认为是最佳的工作假说。也就是说与调节情绪、思维和行为的大脑回路故障有关,大脑化学物质对于健康的神经细胞连接非常重要。
▼
正如识别抑郁症特定生化“标记”的尝试都失败了一样,许多识别导致抑郁症的特定基因或基因突变的尝试也只取得了有限的成功——可能是因为不同的抑郁症病例可能是由许多不同基因的突变以及独特的环境因素综合的。
几项综合研究(包括全基因组关联研究以及家族和双胞胎研究)报告的证据表明,对于某些情况或类型的抑郁症来说,大量个体基因之间的相互作用,以及这些基因与某些环境因素的复杂相互作用,可能只是部分原因。
例如,一项系统性全基因组关联研究(GWAS)报告称,许多与免疫系统功能和炎症相关的基因可能是影响一个人患抑郁症风险的可能遗传因素之一。
据报道,另一项全面的 GWAS 研究确定了许多与血清素功能、昼夜节律和其他神经递质相关的基因可能是抑郁症的遗传风险因素,如下表:
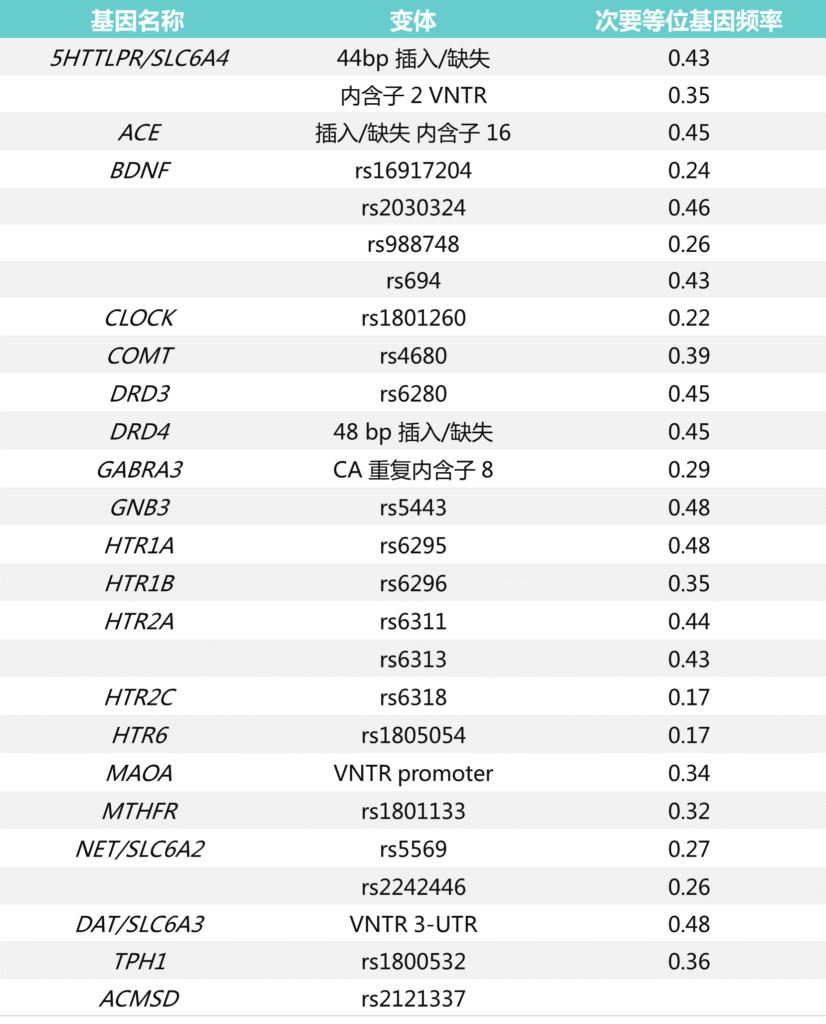
doi.org/10.1016/j.neuron.2014.01.027
对复发性/单相型重度抑郁症(“MDD-RU”)的家庭研究报告称,抑郁症诊断患者的一级亲属可能面临特别高的风险。
血清素转运蛋白基因( SLC6A4 ) 也与重度抑郁症相关。SLC6A4和其他参与大脑血清素能系统的基因现在被认为是抑郁症易感性的“候选基因”,这也符合许多最常见的抗抑郁药物被认为主要作用于该系统的事实。
其他五个与抑郁症风险相关的“候选基因”包括:
▼
肠道菌群与抑郁症之间存在一定的关联。肠道菌群是指人体消化道中的微生物群落,包括细菌、真菌、病毒等。它们与人体的健康和免疫系统密切相关。
微生物群-肠-脑轴
肠道和大脑之间存在着肠脑轴,通过神经、免疫和内分泌系统的相互作用进行沟通。肠道菌群可以通过产生代谢产物、神经递质和炎症因子等影响大脑功能和情绪调节。
炎症反应
肠道菌群失衡可能导致肠道黏膜的炎症反应,释放炎症因子进入血液循环,进而影响大脑功能。慢性炎症反应与抑郁症的发生和发展有关。
神经递质
肠道菌群可以影响神经递质的合成和代谢,如血清素、多巴胺和γ-氨基丁酸等,这些神经递质与情绪调节密切相关。
营养吸收
肠道菌群参与食物的消化和营养的吸收,它们可以合成维生素和其他有益物质,这些物质对大脑和情绪调节有影响。
而肠道菌群又受到多种因素的影响,比如:饮食、抗生素使用、生活方式、环境因素等。接下来章节,我们就肠道菌群与抑郁症展开了解它们之间密不可分的关联。
▼
一些研究发现,中度和重度抑郁症患者的肠道菌群特征是拟杆菌门富集,而重度患者中瘤胃球菌和真杆菌则减少。
抑郁症个体与健康对照组相比,微生物群变化的总结如下:
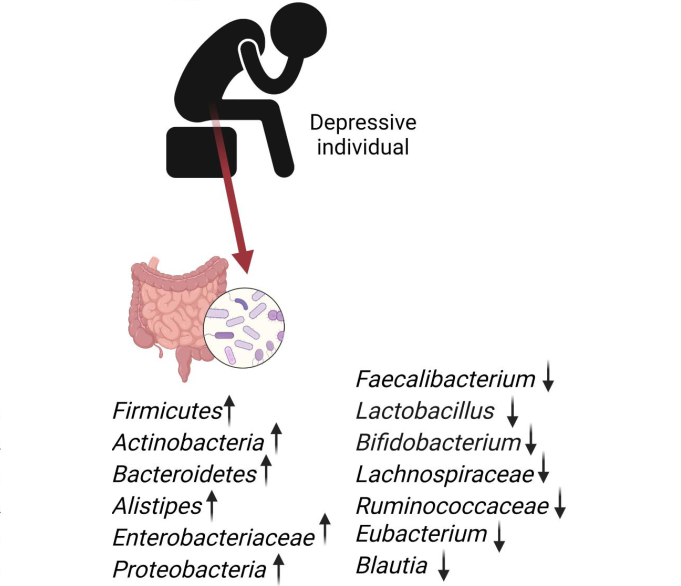
Basiji K, et al., Metab Brain Dis. 2023
▼
根据一项早期的动物研究,在没有肠道细菌的情况下生长的啮齿动物(无菌大鼠和小鼠)缺乏成熟的肠内分泌系统(胃肠道的激素产生系统)。
与具有更典型肠道细菌水平的对应物相比,它们的几种不同主要神经递质的水平和活性也有所不同。
一项初步的动物研究称,没有肠道细菌的小鼠可能会表现出自发运动的增加,该研究的作者将其解释为表明更加焦虑。他们进一步假设,这些行为差异可能是由于某些神经递质,包括血清素、多巴胺和去甲肾上腺素(去甲肾上腺素),在整个大脑中合成和代谢方式的差异造成的。
另一项研究着眼于肠道微生物与早期生活压力之间的潜在关系。在这项研究中,由于早年与母亲分离而经历压力和抑郁样症状的新生大鼠,当在其饮食中添加特定种类的细菌(双歧杆菌)时,其中一些症状会减轻。尽管抑郁相关行为的减少程度小于传统抗抑郁药物西酞普兰造成的减少,但这一初步发现仍然表明,理论上可以通过改变肠道微生物群的组成来“治疗”抑郁症。
其他一些来自动物研究的早期但有趣的证据表明,即使是复杂的行为也可以通过“粪菌移植”从一组小鼠“复制”到另一组小鼠。
一项动物研究报告称,抗生素(通过杀死肠道微生物组中的一些细菌种类来改变肠道微生物组)可能会影响小鼠表现出的“探索行为”的数量,甚至可能会改变大脑中某些重要化合物的水平,如脑源性神经营养因子(BDNF)。
▼
您以前可能听说过“益生菌”——这是指将特定菌株(菌种)引入胃肠道的食品或膳食补充剂。
一些初步证据表明,使用益生菌“修改”人类肠道微生物组可能会产生一些心理影响。例如,据报道,某些益生菌补充剂可以降低健康非老年个体以及诊断为重度抑郁症(MDD)的非老年患者的抑郁症状严重程度评分。
同样,另一项早期研究报告称,定期服用含有瑞士乳杆菌和长双歧杆菌菌株的益生菌可能有助于减少健康志愿者的抑郁症。
最后,另一项初步研究报告称,嗜酸乳杆菌、干酪乳杆菌和两歧双歧杆菌的组合可能有助于部分减轻抑郁症状。
虽然这些作用背后的潜在机制尚不清楚或不明白,但一些研究人员指出,这些“益生菌治疗”可能会导致胰岛素水平降低、胰岛素抵抗和 hs- CRP水平降低,以及谷胱甘肽(一种主要天然物质)水平升高。抗氧化化合物用于重度抑郁症患者。
总的来说,虽然这项早期研究充满希望且令人兴奋,但还需要更多的研究来充分证实这些效应,并找出哪些机制可能导致这些有趣的效应。
▼
“肠-脑轴”是指肠道微生物群与大脑之间假设的“双向”连接。
肠-脑轴可能包括许多不同的潜在机制,包括在许多不同的器官系统和所涉及的单个细菌物种之间产生的各种神经、化学、体液和免疫信号。
虽然许多不同的疾病和健康状况可能受到肠-脑轴的影响,但一些研究人员特别关注肠-脑相互作用在抑郁症发展中可能发挥的作用。
微生物群-肠-脑异常导致抑郁症
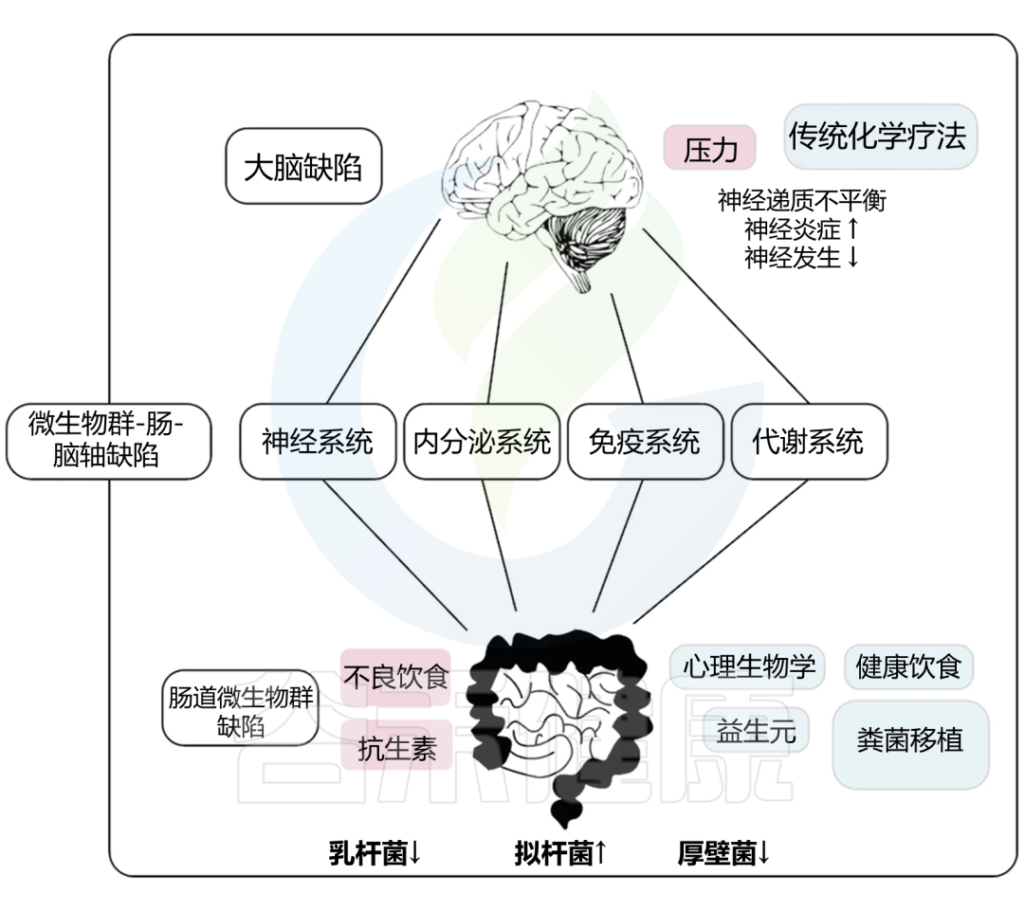
DOI: 10.1007/978-981-19-7376-5_10
▼
微生物群-肠道-免疫-神经胶质轴
微生物群对小胶质细胞稳态的重大贡献,无菌小鼠表现出小胶质细胞的整体缺陷,细胞比例改变和不成熟的表型,导致先天免疫特性受损。
值得注意的是,复杂微生物群的重新定殖,部分恢复了小胶质细胞的特征,而微生物群衍生的短链脂肪酸调节了小胶质细胞的稳态。
神经胶质细胞,包括小胶质细胞、星形胶质细胞、少突胶质细胞和室管膜细胞,与神经元相互作用,影响大脑健康和疾病(如抑郁症)。
神经胶质功能可能由肠道微生物群通过神经和化学信号途径驱动。肠道微生物群对小胶质细胞从促炎到抗炎的激活状态具有重要意义,小胶质细胞功能障碍可以触发抑郁症中神经炎症的信号级联反应。
脑功能、脑小胶质细胞(Iba1)和外周炎症细胞因子的改变(如TNF-α、IL− 1β 、IFN-γ,IL-12)。通过肠-脑轴调节小胶质细胞激活状态(M1、M2)可能是治疗抑郁症的一种有前途的治疗方法。
脑神经炎症中脑-肠-微生物轴(Th17/Treg)
许多临床前和临床研究表明,Th17 和 Treg 细胞对抑郁症有显著影响。
注:
TH17细胞是一种产生促炎细胞因子的T细胞亚群,TH17细胞的异常活化和功能异常与多种炎症性和自身免疫疾病的发生和发展有关,Treg细胞主要通过产生抑制性细胞因子和细胞接触来抑制免疫反应。
TH17细胞和Treg细胞之间的平衡是免疫系统正常功能的重要组成部分。当TH17细胞过度活化或Treg细胞功能受损时,可能导致免疫系统失衡,从而引发炎症性和自身免疫疾病。
肠道 Th17 和 Treg 细胞受到肠道微生物群的调节,而大脑相关的 Th17 和 Treg 细胞则维持免疫稳态,以控制怀孕期间的神经炎症、小胶质细胞激活、星形胶质细胞激活和大脑发育。
值得注意的是,Th17 和 Treg 细胞之间的不平衡,或 Th17/Treg 细胞的比例异常,在抑郁症中发挥着关键作用。
Th17/Treg 细胞是脑神经炎症中脑-肠-微生物轴调节所特别需要的。受肠道微生物群调节的 Th17 和 Treg 细胞之间的不平衡可能会赋予机体抵抗力和对压力的敏感性。
特定的肠道微生物群,如分节丝状菌、梭状芽胞杆菌、脆弱拟杆菌、罗伊氏乳杆菌和双歧杆菌,及其代谢产物如短链脂肪酸和ATP,也参与 Th17/Treg 活性,从而形成 Th17 和 Treg 细胞之间的不平衡。
除了脑神经炎症之外,炎症还可以发生在身体其他部位和系统,比如周围炎症,胃肠道炎症等。
▼
抑郁症和炎症的相互作用就像一个互相助长的恶性循环。炎症是抑郁症发展的主导力量之一。长期的神经炎症会影响大脑功能,这可能会决定个人的情绪和行为。
抑郁症的细胞因子假说来自于观察,即抑郁症的几种症状类似于“疾病行为”,例如嗜睡、发烧、食欲下降、对探索行为或性活动的兴趣下降等。
一些研究人员提出,从进化的角度来看,疾病行为可能是有意义的,因为其中许多行为可能有助于治愈或减少疾病的传播。例如,隔离病人可能会降低他们传播感染的几率。
抑郁症相关炎症因子变化
周围炎症与抑郁症密切相关。抑郁症患者的炎症标志物包括:
血清 IL-6、IL-1β、C反应蛋白升高。
肠道炎症性疾病患者抑郁行为的并发率很高
根据一些报告,患有胃肠道炎症等健康问题的人抑郁和焦虑症状的发生率在统计上有所增加。一些研究人员估计,高达 50-90% 的 IBS患者还同时患有某种精神疾病。
根据最近的《自然》杂志评论,尽管存在明显的异质性,但 IBD 抑郁症状(包括克罗恩病和溃疡性结肠炎)的总体患病率超过 20%。随着时间的推移,抑郁症状加剧与活动性IBD的几率增加有关。
前扣带皮层(ACC)可能是大脑中的一个交叉点,它会感知肠道炎症和不适当的反应,从而增加患抑郁症的风险。
用促炎细胞因子引发炎症的同时诱发抑郁
对人类或动物施用促炎细胞因子进行治疗会诱发抑郁症状。虽然 SSRIs(选择性血清素再摄取抑制剂)通常不会直接减轻“疾病行为”,但据报道,它们可以减少促炎细胞因子,并增加抗炎细胞因子,这一机制也与抑郁症的细胞因子假说一致。
给予脂多糖 LPS 会增加细胞因子的血浆浓度,同时诱发抑郁症状。
然而,抑郁症的正式诊断标准(由 DSM 定义)和“疾病行为”本身之间存在一些细微差别,并且关于炎症是否真的导致抑郁症的证据是相互矛盾的。
并非所有炎症患者都患有抑郁症,也并非所有抑郁症患者都具有高炎症标志物,炎症(可能与血清素缺乏相似)可能只是抑郁症的一个诱因,而不是唯一的直接原因。换句话说,炎症细胞因子的异常调节可能只是一个更加复杂的谜题的一部分,并且需要更多的研究来充分探索这些潜在联系所涉及的机制。
▼
肠粘膜屏障和粘膜免疫系统是帮助防止肠腔内的肠道微生物直接与肠道免疫系统相互作用的两个主要机制。如果这些屏障受到损害,细菌可能会易位,激活免疫系统,从而引发炎症。
注:这些屏障受到损害的情况有时非正式地被称为“肠漏”。
一项动物研究报告称,肠道屏障受损的小鼠表现出与焦虑相关的行为增加,并且一旦肠道屏障恢复或引入益生菌后,这些行为就会消退。
根据一项针对人类的初步研究的作者,IgA 和IgM等血清抗体通常会被激活以对抗有害的肠道细菌。因此,这些抗体的存在是肠道屏障受损的一种潜在生物指标,一项研究甚至报告称,这些抗体水平升高可用于识别抑郁症患者,准确率高达 90%。
尽管这种现象背后的机,但一些研究人员认为“坏”肠道细菌可能通过 TLR4 受体引发炎症。
诱发炎症
LPS 与 TLR4 结合激活免疫细胞,激活NF-κB(一种细胞内信号分子),进而促进促炎细胞因子的产生,包括 TNF-α 和 IL-1 以及环加氧酶-2。
加剧炎症
相同的过程还诱导氧化和亚硝化应激途径,通过进一步激活烟酰胺腺嘌呤二核苷酸磷酸氧化酶来增加诱导型一氧化氮的表达和活性氧 (ROS) 的产生。ROS 超载不仅会激活 NF-κB,还会导致 DNA 损伤和细胞死亡,这两个过程都会加剧炎症状态。
促炎循环——抑郁症
包括干扰素-α、IL-6、IL-1β 和 TNF-α 在内的细胞因子以及氧化和亚硝化应激途径可能会导致紧密连接屏障松动,从而在肠道通透性过高和宿主免疫反应之间形成促炎循环。
这个循环至少部分解释了抑郁症患者慢性低度但持续的炎症状态。
总的来说,这些机制及其影响复杂,值得更多的研究来验证这些初步发现。
▼
激素影响我们身体功能的许多方面,包括新陈代谢、生长、性健康和生殖系统功能。我们的心理健康受到激素的强烈影响,因为激素在情绪的调节中发挥着重要作用。这里我们来了解几种常见的和抑郁症相关的激素。
皮质醇
皮质醇是一种压力激素,由肾上腺分泌。这种激素负责通过选择使用哪种底物以及应消耗多少底物来调节能量。如果皮质醇水平过高或过低,可能会开始出现抑郁症。皮质醇水平低与过度疲劳、难以处理压力情况、不可预测和不稳定的情绪以及性欲下降有关。
雌激素
雌激素在大脑中扮演着重要的角色,它们参与调节神经递质的活动,如血清素、多巴胺和去甲肾上腺素等。这些神经递质与情绪调节密切相关,因此,雌激素的变化可能会对情绪产生影响。
女性患抑郁症的风险要高于男性,这与雌激素和孕激素变化有关。在月经周期、孕期和更年期等生理状态的激素波动可能影响情绪和抑郁症发病风险。
使用雌激素治疗抑郁症的疗效和安全性仍存在争议,因此,使用雌激素治疗抑郁症需要谨慎。
黄体酮
黄体酮有助于平衡体内雌激素水平。它还有助于改善睡眠模式,使人感到更平静。如果黄体酮水平不平衡,可能会变得烦躁或晚上无法入睡,这可能影响抑郁症。
▼
// 短 链 脂 肪 酸
短链脂肪酸在肠腔中具有多种功能,如氧化还原平衡、维持肠屏障完整性、肠道激素产生和表观遗传调节。然而研究表明,短链脂肪酸与抑郁症等精神疾病有关。
短链脂肪酸由肠道微生物群合成,主要由AKK菌、双歧杆菌、粪杆菌、毛螺菌科、乳酸杆菌和瘤胃球菌等物种合成。
短链脂肪酸与抑郁症的关联
已知短链脂肪酸调节神经反应的不同途径,如:
短链脂肪酸诱导肠道神经肽的释放,例如YY肽(YYP)和胰高血糖素样肽2(GLP-2)肽,以及参与维持肠道屏障、细胞代谢和饱腹感的激素。
戊酸与抑郁症有关,主要由Oscillibacter产生。缬草酸的结构与GABA,并可与其受体结合,这可能在严重抑郁障碍中发挥重要作用。
在抑郁症患者的粪便中发现了更高量的异戊酸,这表明微生物群和异戊酸与抑郁症有关。
在一项针对有抑郁症状患者的研究中,粪便中的乙酸盐水平与这些患者呈正相关,而丁酸盐和丙酸盐水平则呈负相关。
在一项针对患有抑郁症的波兰妇女的类似研究中,与非抑郁症患者相比,抑郁症患者粪便中的乙酸盐和丙酸盐水平降低,而异己酸含量增加。这些发现表明,为了保持心理健康,特定的短链脂肪酸水平和微生物群之间必须保持平衡。
// 胆 汁 酸
胆汁中的一种重要成分——胆汁酸,是由肝脏中的胆固醇产生的,它们与肠道菌群协同调节胆固醇代谢,帮助脂质消化和吸收。胆固醇通过肝细胞代谢为原代胆汁酸;之后被输送到胆囊,最终在十二指肠中被释放。到达肠道后,肠道细菌从初级胆汁酸中产生次级胆汁酸(脱氧胆酸和石胆酸)。只有一些细菌,主要是梭菌和真细菌,负责次级胆汁酸的合成。
胆汁酸改变了神经递质受体的功能,如M2和M3毒蕈碱乙酰胆碱、GABA和N-甲基-D-天冬氨酸(NMDA)受体。在对培养的下丘脑神经元的体外研究中,鹅去氧胆酸抑制GABA和NMDA受体。
胆汁酸与抑郁症的关联
中国的一项研究表明,与健康对照组相比,重度抑郁症患者的2,3-脱氧胆酸水平较高,而牛磺酸(TLCA)、甘胆酸(GLCA)和3-硫酸胆酸水平较低,这与汉密尔顿抑郁量表(HAM-D)评分呈负相关。
同样在这项研究中,这些菌Turicibacteraceae、Turicibacteriales和Turicibacter与TLCA和GLCA水平呈正相关。
在美国的另一项研究中,与不太严重的抑郁症患者相比,严重抑郁症患者的原发胆汁酸鹅去氧胆酸水平降低。因此,肠道菌群可以通过胆汁酸改变诱导中枢神经系统疾病,如重度抑郁症。
次级胆汁酸合成的减少会导致微生态失调,并改变肠道屏障的通透性,诱导促炎性基调,从而导致抑郁症的发病机制。
▼
肠道细菌是血液中化学物质(代谢物)的主要调节剂。其中一些是在大脑中制造神经递质的“成分”或“构件”(代谢前体)。
换句话说,这意味着肠道细菌可能能够对某些神经递质的水平和活动产生一些影响,这反过来又可能使它们能够影响大脑活动和行为(尽管是间接的)。
肠道细菌可以通过多种方式调节神经递质的产生
首先,肠道细菌可以合成和分解多种神经递质,如γ-氨基丁酸(GABA)、多巴胺、血清素等。这些神经递质可以通过门脉循环影响迷走神经的传入通路,它们在大脑中起到调节情绪、认知和行为的重要作用。
GABA是大脑中的主要抑制性神经递质。
谷氨酸是大脑中最丰富的兴奋性神经递质,负责在神经细胞之间发送信号,其在大脑中的合成取决于神经元和星形胶质细胞之间的合作,肠道中的肠内分泌细胞亚群能够合成谷氨酸,并利用它通过迷走神经将快速信号传输到大脑。关于谷氨酸详见我们之前的文章:
去甲肾上腺素在中枢神经系统内发挥作用,同时充当应激激素。它有助于“战斗或逃跑”反应,并与唤醒、注意力和聚焦机制相关。
多巴胺参与奖励处理和动机以及运动控制。
肠道微生物群对多巴胺代谢副产物的影响
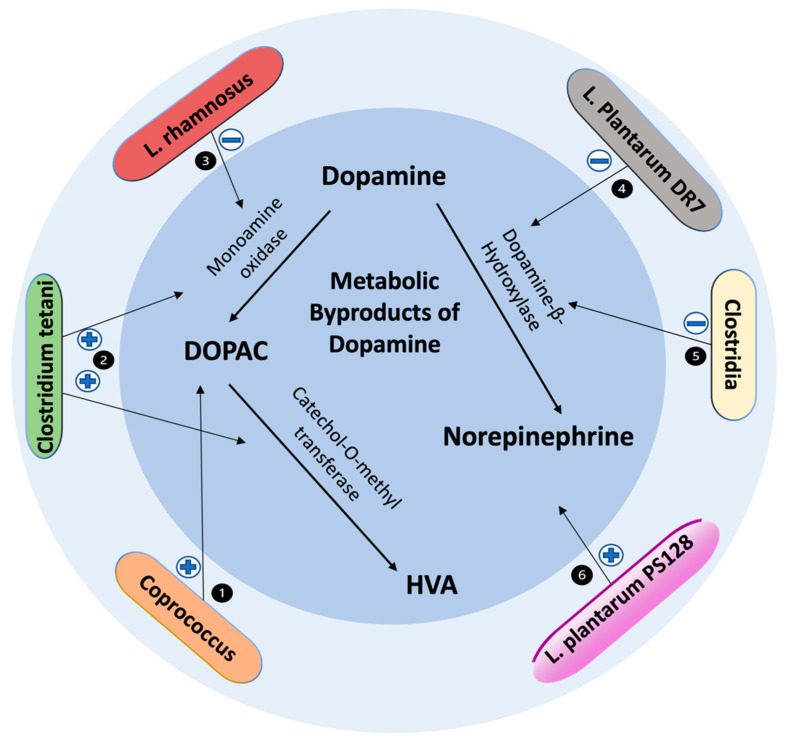
doi: 10.3390/biomedicines10020436
1) 粪球菌属Coprococcus comes和Coprococcus catus与多巴胺合成潜力密切相关
2) 破伤风梭菌对多巴胺具有降解作用,通过多巴胺中间体促进降解为高香草酸
3) 鼠李糖乳杆菌下调MAO
4) 植物乳杆菌DR7下调多巴胺β-羟化酶
5) 梭状芽孢杆菌显示下调多巴胺β-羟化酶
6) 植物乳杆菌PS128给药改善多巴胺代谢并增加去甲肾上腺素水平
血清素,也称为 5-羟色胺 (5-HT),参与调节情绪、食欲、睡眠和其他身体功能。
其次,肠道细菌可以影响神经递质的合成和代谢途径。例如,某些细菌可以产生短链脂肪酸,如丙酸、丁酸和乙酸,这些短链脂肪酸可以促进神经递质的合成和释放。
肠道细菌还可以通过与肠道上皮细胞和免疫系统的相互作用,间接影响神经递质的产生。肠道细菌可以调节免疫系统的活性,影响免疫细胞的分泌和反应,从而影响神经递质的合成和释放。
▼
氨基酸色氨酸是大脑用来产生神经递质血清素的主要“构件”(代谢前体)之一。虽然色氨酸消耗并不总是导致抑郁症,但一些研究人员认为,血清色氨酸偏低有时可能会导致易感人群抑郁症。根据前面,我们可以看出高血清脯氨酸和低血清色氨酸与抑郁症的发展有一定关系。
一些研究表明,某些促炎细胞因子(例如 IFN-α、IFN-γ和TNF-α)水平的增加可能会刺激吲哚胺-2,3-双加氧酶( IDO )的活性,从而在转刺激色氨酸转化为神经毒性化合物,包括犬尿氨酸和喹啉酸。
基于此,一些研究人员认为,可能是这些神经毒性物质,而不是色氨酸消耗本身,可能导致抑郁症的发生。
肠道细菌和炎症可能会影响血清素代谢:
色氨酸代谢途径的犬尿氨酸
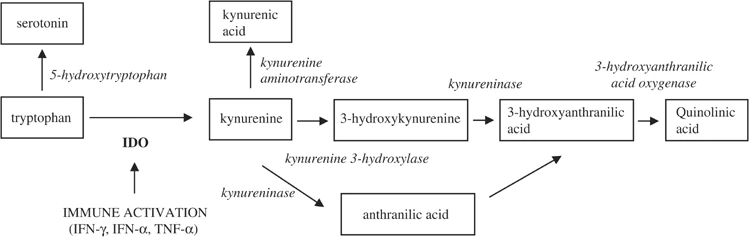
DOI: 10.1038/sj.mp.4001600
扩展阅读:
▼
重度抑郁症患者表现出应激反应系统(例如HPA 轴)过度活跃。它主要表现为腺体反应性增加、激素分泌破坏和负反馈失调。这些疾病可能进一步导致肠道炎症、神经元损伤和皮质醇过度产生,所有这些都与抑郁症相关。
此外,HPA 轴功能障碍的解决与抑郁症的缓解(“治愈”)密切相关,表明它们之间存在某种相互联系。
早期生活压力—肠道菌群—应激反应形成
一项针对大鼠的动物研究报告称,将新生儿从母亲身边带走所产生的压力(母亲分离压力)可能会导致后代肠道微生物组发生巨大的长期变化。母亲分离是早期生活压力的一种模式,它通过改变 HPA 轴、免疫系统和氨基酸代谢以及影响微生物群组成来诱发焦虑和抑郁。
早期生活压力可能使人以后对压力更加敏感。
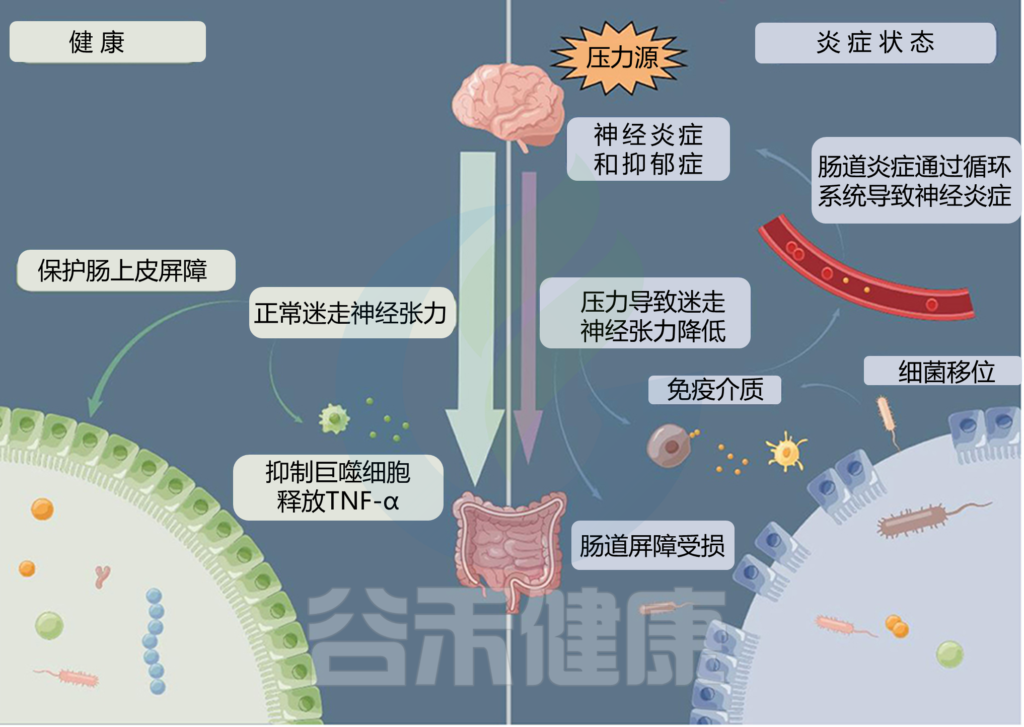
doi.org/10.3389/fneur.2022.1015175
▼
虽然迷走神经无法到达管腔内容物,但它可以通过与肠内分泌细胞的通信间接感知肠道信息。
迷走神经传入将信号从肠道菌群传递到中枢神经系统
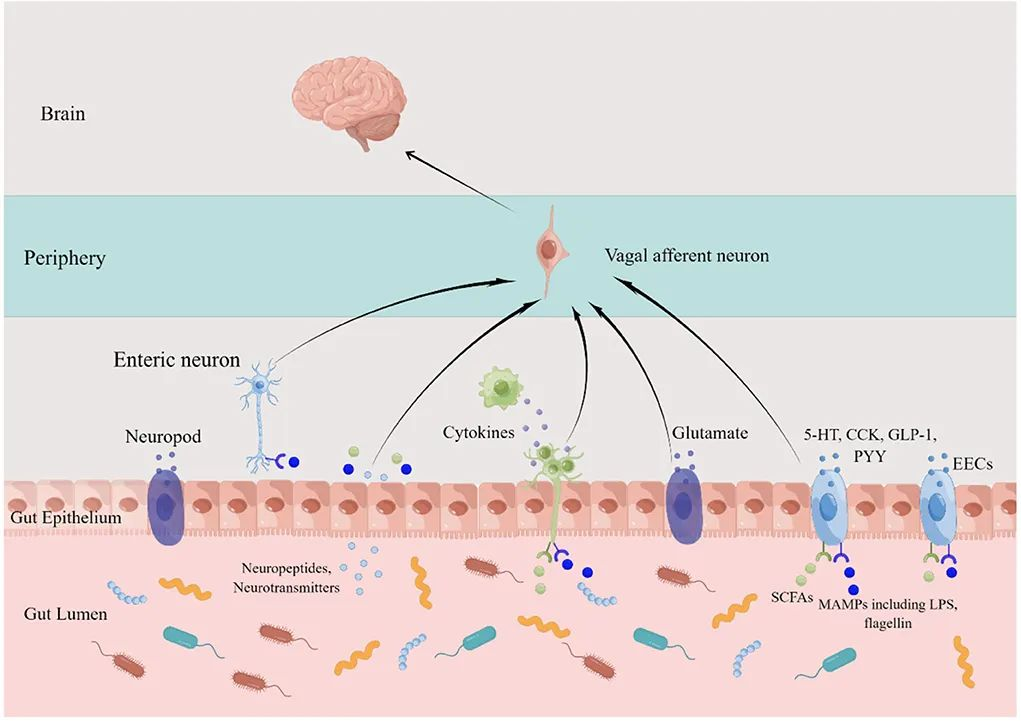
doi.org/10.3389/fneur.2022.1015175
▼
肠道微生物组可能用来与中枢神经系统沟通的其他机制之一是通过肠嗜铬细胞(ECC)和迷走神经。
例如,一些研究人员目前认为肠嗜铬细胞和迷走神经可能参与肠道细菌和大脑之间的通讯,尽管我们仍然不完全了解如何进行。
肠嗜铬细胞感知肠道细菌并分泌血清素
肠嗜铬细胞(ECC) 遍布整个消化道
▼
HPA轴是指下丘脑-垂体-肾上腺轴。HPA轴的功能紊乱可能导致患者出现情绪失调和应激反应的异常。
肠道菌群如何影响 HPA 轴?
肠道菌群失调与炎症之间存在密切关系。这些细胞因子也是 HPA 轴非常有效的激活剂。促炎细胞因子可以干扰皮质醇循环的负反馈,刺激HPA轴的活性。
肠道菌群还可以通过其他能够穿过血脑屏障的介质(例如微生物抗原和前列腺素)刺激 HPA 轴。
除了依赖这些介质之外,细菌还可以直接参与干预过程。例如,LPS和肽聚糖可以通过激活先天免疫系统来激活HPA轴,最终诱发抑郁症)。
还有证据表明,肠道菌群可以直接调节肠道和肾上腺中的类固醇生成,从而增强 HPA 轴反应。
肠道菌群衍生的代谢物也通过体液途径参与调节 HPA 轴。例如,慢性吲哚(拟杆菌属、乳杆菌属和梭菌属)可诱导肾上腺髓质 Pnmt 基因过度表达。它可以与去甲肾上腺素一起增加肾上腺素能系统中儿茶酚胺的生物合成途径。这样,吲哚可以增加小鼠在慢性轻度应激下的脆弱性,最终导致抑郁行为。
除此之外,肠道菌群还可以通过调节 HPA 轴在抑郁症中发挥积极作用。例如,其下游代谢物短链脂肪酸可以降低HPA轴中一些编码蛋白的基因表达,从而减弱HPA轴的应激反应。
最后,肠道菌群还可以影响膈下迷走神经的信号输入。孤束核通过去甲肾上腺素能神经元激活 HPA 轴。
据报道,单胺再摄取抑制剂(MAO-Is) 可以降低糖皮质激素受体抵抗,从而减少 HPA 轴功能障碍。这使得一些研究人员提出,针对大脑 HPA 轴的药物可能是治疗重度抑郁症的潜在有效方法。
▼
如果发现抑郁症的迹象,请及时进行身体检查,帮助确定症状是否可能与抑郁有关,并寻求专业医疗帮助进行抑郁症的诊断和治疗干预。
诊断抑郁症是一个多步骤的过程,通常当有人注意到自己感觉不太像自己时就开始了。在某些情况下,一个人的朋友和家人可能会首先注意到抑郁症的微妙迹象。相关判别方式有:
// 量表
医疗和心理健康专业人员使用既定的、研究支持的指南、筛查工具、检查表和其他标准来帮助他们诊断抑郁症。
DSM-5
心理健康专家可能使用美国精神病学协会出版的《精神障碍诊断与统计手册》(DSM-5) 中列出的抑郁症诊断标准。
注:《精神疾病诊断和统计手册》(DSM)是一本为诊断精神疾病的临床医生提供指南的手册。对每种情况进行分类,并给出一套明确的标准,必须满足这些标准才能做出诊断。
DSM-5 包含了评估自杀风险的新量表:一种针对成人,另一种针对青少年。
要诊断为重度抑郁症,一个人的症状必须符合 DSM-5 中概述的标准。悲伤、情绪低落和对日常活动失去兴趣的感觉必定标志着一个人以前的状态发生了变化,并且持续了至少两周。
这些感觉还必须伴有至少五种其他常见的抑郁症状,包括:
这些症状必定会导致个体出现临床上显著的痛苦或社交、职业或其他重要功能领域的损害。
这些症状不能归因于药物或物质滥用,也不能是由其他身体疾病引起的。
除了DSM-5,还有一些常用的抑郁症量表,用于评估抑郁症的严重程度和症状表现。常见的抑郁症量表包括:
用于评估抑郁症状的程度。
临床评估工具,用于评估抑郁症状的严重程度。
用于评估双相情感障碍,包括抑郁症和躁狂症。
这些量表可以帮助医生更全面地评估抑郁症的症状和严重程度,以指导治疗计划的制定。
抑郁症的诊断主要是基于临床评估和心理评估,其他也包括一些实验室测试来辅助判别。
// 实验室测试
用于识别生物标志物并应用于诊断重度抑郁症的基因组、蛋白质组和代谢分析仍处于起步阶段。
炎症标志物
严重抑郁症与细胞因子或其可溶性受体升高有关,包括:白细胞介素IL-2、可溶性 IL-2 受体 (sIL-2R)、IL-1b、IL-1 受体拮抗剂 (IL-1Ra)、IL -6、可溶性 IL-6 受体 (sIL-6R) 和 γ-干扰素。
一项病例对照研究发现,血清抵抗素(一种细胞因子和代谢标志物)水平与非典型抑郁症症状相关,抑郁症受试者的脂联素水平低于对照组。
BDNF(脑源性神经营养因子)
与对照组相比,抑郁症受试者的血清水平通常较低,并且血清BDNF水平在抗抑郁治疗后升高。血清BDNF可以作为区分单极性和双极性抑郁症的生物标志物。
皮质醇
HPA轴功能障碍已在抑郁症的病因中得到观察。抑郁症患者的高皮质醇血症表现为24小时平均血清皮质醇浓度升高和24小时尿液皮质醇排泄增加。
新型血液测试
一种新的血液测试被描述用于重度抑郁症的诊断。该测试由9种生物标志物组成,包括α-1抗胰蛋白酶、载脂蛋白CIII、BDNF、皮质醇、表皮生长因子、髓过氧化物酶、催乳素、抵抗素、可溶性肿瘤坏死因子αII型,均通过标准免疫测定进行测量。
促甲状腺激素
促甲状腺激素(TSH)被纳入并单独报道,用于评估抑郁症的总体评估中的甲状腺功能减退或甲状腺功能亢进。内源性抑郁症患者的基础血清TSH水平通常较低,从基线到峰值的TSH变化也较低。抑郁症可能与亚临床甲状腺功能减退或轻度甲状腺功能衰竭有关。
肠道菌群健康检测
某些菌群的异常与抑郁症之间可能存在相关性。肠道菌群检测可以在抑郁症的早期进行风险提示,当临床症状不明显或存在疑难病例时,结合肠道菌群检测结果,可以提供更加全面的信息,辅助医生进行准确的诊断。
▼
有时候,我们口头说的“抑郁症”很多情况是短暂的抑郁情绪,还不是重度抑郁症,可以趁抑郁症在早期阶段,通过改变生活方式对其进行干预和管理。
// 饮 食
饮食选择显著影响其他身体系统,例如内分泌、免疫和胃肠道系统。
避免不健康饮食
限制摄入食品添加剂、糖、饱和脂肪酸和精制碳水化合物等。
近年来,研究表明,西方饮食中富含加工或油炸食品、糖、精制谷物和酒精,与抑郁和焦虑症状呈正相关。2020 年的一项研究发现,食用加工食品会引发体内炎症,并对免疫系统产生连锁反应,可能会增加出现抑郁症状的风险。
富含脂肪的饮食可能促进焦虑和抑郁的发展或持续。高脂肪摄入不仅会导致肥胖,还会引起身体系统广泛的炎症。肠道微生物组可能会改变高脂肪饮食的有害影响,改善情绪和行为。
通过避免受污染的食物,改善饮食质量,增强身体的免疫力,并有助于抑郁症的治疗和康复。环境重金属污染的食物可能会含有铅、汞、镉等有害物质,海鲜也是需要格外关注的食物类型,因为海产品往往容易受到汞等重金属的污染。抑郁症患者需要特别留意,避免摄入这些污染物。
高脯氨酸食物与抑郁症相关
来自西班牙巴塞罗那赫罗纳生物医学研究所 (IDIBGI) 和庞培法布拉大学 (UPF) 的研究人员发现,较高的脯氨酸摄入量与抑郁症的发展有关。这项研究的结果发表在《细胞代谢》杂志上。
为了更多地了解饮食是否会导致抑郁症的发生,IDIBGI 研究人员将大约 100 名受试者分为三类:非抑郁症、轻度抑郁症和重度抑郁症。从那里,他们分析了抑郁症诊断与肠道微生物组组成之间是否存在关系。
通过对氨基酸的代谢物分析,研究人员能够将体内脯氨酸与抑郁症评分最紧密地联系起来。
为了了解这种脯氨酸从何而来,研究人员依靠包含参与者饮食信息的调查问卷。脯氨酸再次成为对抑郁症影响最大的饮食因素。
在健康的受试者中,脯氨酸的摄入量是与抑郁评分最相关的项目。在进一步确定小鼠体内脯氨酸/抑郁症的联系后,研究人员试图通过将人类受试者的肠道细菌移植到小鼠体内来证实他们的发现。接受脯氨酸含量最高的细菌的小鼠表现出更多的抑郁症状。
什么是脯氨酸?
我们体内的蛋白质由 20 种特定氨基酸的各种组合组成,其中 9 种被认为是“必需的”。身体无法自行制造这九种氨基酸,我们需要通过饮食摄入它们。
脯氨酸是一种非必需氨基酸,这意味着我们的身体在生命的大多数阶段都可以产生足够的量。然而,在压力、康复或成长时期,这种氨基酸变得至关重要,因为我们的需求量超过了我们身体的制造量。
富含脯氨酸的食物
脯氨酸主要存在于许多动物源食品中。“脯氨酸最重要的来源是明胶和动物皮,这些食物富含胶原蛋白,是这种氨基酸的天然来源。
事实上,脯氨酸约占胶原蛋白总氨基酸的 10%。因此,含有胶原蛋白的食物,如骨头汤、鸡翅(带皮)、猪皮和明胶,是这种氨基酸的丰富来源。
大多数肉类、鱼类和乳制品也含有脯氨酸。
需要避免脯氨酸来降低抑郁风险吗?
根据这些结果,看起来有必要从饮食中去除任何含有脯氨酸的食物,以降低患抑郁症的风险。
根据研究作者和我们经验还是不要那么绝对。毕竟许多富含脯氨酸的食物,包括肉类、鱼类和奶制品,都富含对正常生长、发育和免疫支持至关重要的营养素。
在建议减少饮食中这部分食物之前,我们认为需要进行更多的研究。
当然,关于抑郁症的饮食干预不只是避免某些食物的摄入,而是要建立一个全面健康的饮食习惯。
健康饮食
2019 年的一项研究发现,富含水果、蔬菜、鱼类和瘦肉的健康饮食有助于降低抑郁症的临床水平。
有研究发现西班牙护理学生坚持地中海饮食与心理健康问题之间存在很强的相关性。坚持地中海饮食的参与者比没有坚持的人的焦虑和抑郁分数要低得多。
地中海饮食(主要是纤维、鱼和全谷物),已被证明可以通过增加产短链脂肪酸菌丰度来调节肠道菌群组成,从而减少抑郁症的发作。
也有研究发现强有力的证据表明,适度限制热量的健康饮食有助于改善抑郁症状。
多酚还被证明可以通过抑制参与氧化应激和炎症的丝裂原激活蛋白激酶途径来改善抑郁症状。多酚还作为益生元为微生物提供营养,两者相辅相成。
一项干预性随机临床试验表明,富含类黄酮的橙汁可以通过增加BDNF和毛癣菌科Trichophyton来缓解抑郁症。
总的来说,富含 omega-3 多不饱和脂肪酸 (PUFA) 的食物,大量摄入蔬菜、水果、鱼、橄榄油、大豆、全谷物的健康饮食模式可能与降低抑郁风险相关。
相关阅读:
// 动起来
缺乏身体活动是抑郁和焦虑的常见危险因素。在治疗重度抑郁症方面有大量研究表明,体育锻炼已被证明有助于预防、缓解和治疗症状。
定期锻炼对身体有好处,有助于增强力量和健康,而且对大脑和神经系统也有帮助。在剧烈运动期间,身体会释放内啡肽和多巴胺等神经递质,这有助于增加愉悦感和幸福感。
// 注重睡眠质量
睡眠质量是幸福感的重要指标。80% 的抑郁症患者自我报告存在睡眠障碍。晚上适当的休息(不要太多或太少)是控制抑郁症和保持精力充沛的好方法。为了达到最佳健康状态,建议七到八小时。
除了适当的休息之外,充足的睡眠还有助于注意力、认知、记忆形成和情绪调节。
如果有睡眠问题,请持续保持良好的睡眠习惯。比如收起电子产品,睡前写日记,并制定一个轻松的睡前习惯来放松身心。
如果睡眠无法改善,请寻求医生的帮助。
// 冥想正念
当您处于抑郁状态时,很容易陷入消极的想法和情绪中。正念、冥想和呼吸练习可以成为抵御压力和焦虑、让你的大脑专注于当下的一种方法。还可以将正念应用于创造性追求,其中可能涉及日记、绘画、唱歌、玩耍、跳舞等活动。
从生物学角度来看,冥想对某些生理功能具有积极、显著的影响。练习冥想可以影响大脑结构、大脑网络,保持自主神经系统的稳态,甚至影响我们基因的运作方式。
练习正念也可以导致知觉转变。你的想法和情绪不再被视为压倒性的事件,而是一个有助于洞察和平静的时刻。
// 走出去,感受新鲜空气
抑郁症的症状之一是很难起床,完成基本任务可能需要付出巨大的努力。如果忽视户外活动而更多地待在室内,可能会扰乱睡眠和昼夜节律,并导致维生素D 不足。
维生素D 水平下降与抑郁症之间可能存在关联。尽管研究仍然很少,但越来越多的研究表明维生素D 可以在缓解抑郁症方面发挥治疗作用。然而,它在促进免疫功能健康、细胞生长和维持骨骼健康方面的益处是众所周知的。
为了摆脱抑郁症,充足的自然阳光照射有助于满足每日维生素D。拥抱自然疗法,感受皮肤上的阳光,并在街区周围散步以改变环境。
// 依靠爱的人
当你感到沮丧时,你很容易孤立并拒绝与人交往的尝试。或者你可能在人群中却仍然感到孤独。然而,人类天生就是社会性动物。如果你的社会支持质量下降,它可能会加剧抑郁症状,并产生更多的孤独、内疚、羞耻和疏远感。
建议适当社交,是提高自尊、适应力、爱的途径——所有这些都有助于产生积极的心理健康结果。数十年的研究证明,与社区的较高社会关系质量与降低压力水平和抑郁症状有关。
哈佛大学成人发展研究对幸福进行了一项长期研究,发现人际关系可以产生精神和情感刺激(情绪助推器),并有助于抵消孤立感。哈佛大学的研究人员指出,人际关系是幸福和生活满意度的有力预测因素。
// 尽可能寻找感激之情和欢笑
有可靠的科学证据表明,感恩可以改善认知和情感健康。研究的一项感恩干预措施是使用感恩情,在其中列出几周内每天让你感激的三到五件事。感恩练习有助于增加积极情绪、主观幸福感、生活满意度,并减少抑郁症状。
研究发现幽默可以成为对抗抑郁症状和焦虑的重要应对机制。当你沮丧时,很难从任何事情中找到乐趣。即便如此,寻找令人愉快的活动仍然是件好事,比如观看搞笑的单口喜剧、拥抱宠物、沉迷于一部让人感觉良好的电影、听音乐、犒赏自己一个热水澡,或者点你最喜欢的饭菜。做任何你喜欢做的事都可以带来快乐。
// 尝试摆脱情绪低落的小技巧
-简化生活,管理时间
列出日常任务清单,使用提醒便签,或者使用计划表有助于保持生活有条不紊。尽可能减少责任,为自己设定合理的目标。当感觉情绪低落时,允许自己少做一些事情。当感到沮丧时避免做出重大决定。
-写日记
作为治疗的一部分,可以通过表达痛苦、愤怒、恐惧或其他情绪来改善心情。
-阅读
阅读知名的自助书籍和网站。医生或治疗师会推荐书籍或网站以供阅读。
-战胜拖延
抑郁症的症状,例如疲劳和注意力不集中,很容易拖延。拖延事情会加剧抑郁。它会导致增加内疚、担忧和压力。制定短期目标并努力首先完成最重要的事情。成功完成的每一项任务都会帮你打破拖延的习惯。
-尝试社交或找到有用的团体
尝试参加社交活动,定期与家人或朋友聚会。许多组织支持联盟,提供教育、互助组、咨询和其他资源来帮助治疗抑郁症。参加各种心理小组也可以为心理健康问题提供帮助。抑郁症患者互助组可以与其他面临类似问题的患者建立联系并分享经验。
-避免酗酒
酒精似乎可以减轻抑郁症状,但从长远来看,它们通常会加重症状,使抑郁更难治疗。
▼
可以通过肠道菌群检测,了解整体菌群结构和异常指标,进行个性化干预。
如果发现核心菌属丰度低,有害菌丰度高,菌群结构紊乱,那么可以配合使用抗生素或益生元等抑制过多有害菌,加以改善。
或者通过粪菌移植的方式适当改变菌群结构,从而有效改善。
发现异常菌群,可以针对缺乏菌群,通过补充益生菌,功能性补充剂等方式加以改善。
// 益生菌 & 益生元
益生菌
最近的荟萃分析和系统综述证实了益生菌在临床研究中的抗抑郁功效。相关动物研究也表明,这种作用与肠道菌群结构的调节有关。
研究人员使用罗伊氏乳杆菌(Lactobacillus reuteri )干预CUMS小鼠,发现只有恢复乳杆菌水平才足以改善与应激相关的代谢变化和行为异常。
在另一项研究中,热灭菌的短双歧杆菌可以调节肠道菌群成分,从而预防慢性社交失败压力引起的抑郁症状。这种具有功能性食物成分的菌株可以用作新的疗法。


编辑
doi: 10.7759/cureus.40293
益生元
每天 5 克的低聚半乳糖和 1 克或以下的二十碳五烯酸可以有效缓解抑郁症状。虽然 EGCG 具有潜在的抗抑郁特性,但可能需要 3 克/天的较高剂量才能产生显着效果。
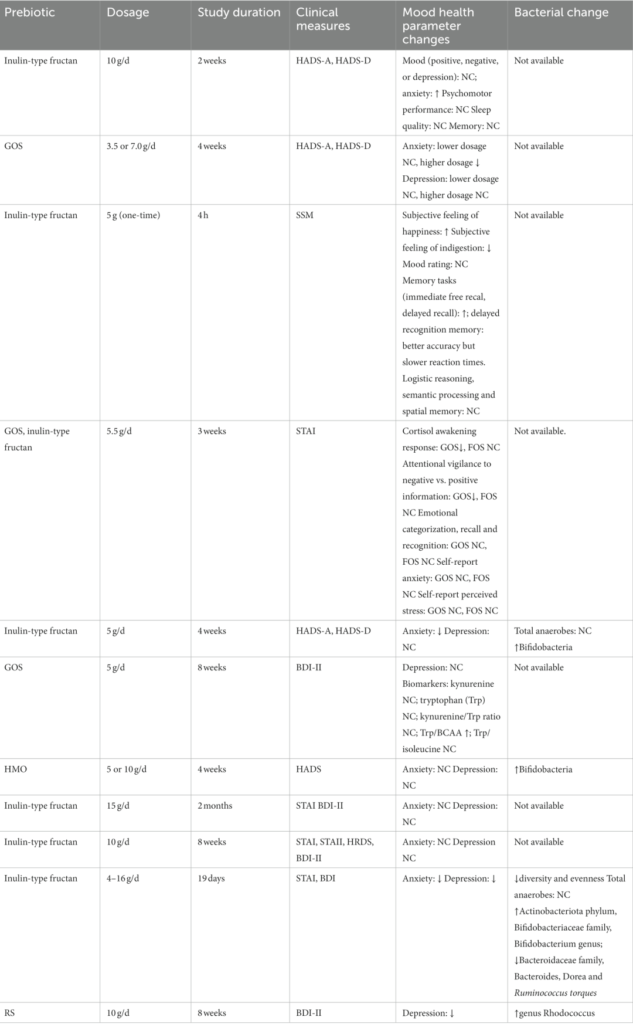
doi.org/10.3389/fnut.2023.1206468
益生菌和益生元联合给药
研究表明,益生菌和益生元的联合给药可以达到更大的抗抑郁效果。益生元的显著营养作用可能会提高益生菌的存活率,从而增强益生菌的抗抑郁能力。
没有相关研究报告益生菌引起的戒断反应和副作用等问题,这似乎是一种很有前途的抑郁症干预措施。益生菌菌株、剂量和方法的最佳组合尚不精确。为了解决这些问题,还需要更多的随机、双盲、安慰剂对照试验来解开这个谜题。
// 粪菌移植
一种直接干扰肠道菌群的方法是粪便微生物群移植(FMT)。它在抑郁症和微生物结构紊乱方面的优异表现使我们看到了新的治疗方向。
在一项动物研究中,NLRP3 KO菌群移植显著改善了受体小鼠的抑郁样行为。在他们的研究中,FMT机制主要依赖于抑制抑郁小鼠中circHIPK2的表达。
在人类受试者中,FMT也显示出类似的效果。在一份FMT作为抑郁症辅助治疗的病例报告中,入选的患者表现出抑郁症状的改善、肠道菌群多样性的增加以及胃肠道症状的缓解。
然而,这种影响并不持久,他们推测FMT的疗效与供体和受体的微生物相似性有关。FMT面临的主要挑战是提高成功率、最佳交付途径、捐赠者选择和其他需要探索的问题。
▼
// 药物
N-乙酰半胱氨酸(NAC)
NAC 通过其抗氧化、抗炎和谷氨酸调节活性,可能在多种精神疾病的治疗中发挥作用。
身体使用N-乙酰半胱氨酸(NAC)来制造自身的抗氧化剂。医学上,NAC用于治疗对乙酰氨基酚中毒;只要在服药过量后的前 8 小时内服用,几乎 100% 有效。
根据对多项单独研究数据(包括 574 名抑郁症患者和健康参与者的数据)的一项审查,据报道,NAC 在使用 3-6 个月内有可能改善抑郁症状和整体日常功能。此外,据报道,抑郁症患者的情绪在 3-4 个月后得到改善。
NAC 还可以通过减少大脑的氧化应激来平衡情绪。例如,一项针对 76 名抑郁症患者的研究报告称,服用 NAC 的患者大脑抗氧化水平较高。
以上益处仅得到有限的小规模临床研究的支持。在 NAC 推荐临床之前需要进行更长时间、更有力度的研究。
选择性血清素再摄取抑制剂(SSRI)
医生通常会先开一种 SSRI 药物。通常认为这些药物更安全,所产生的不适副作用一般少于其他类型的抗抑郁药。SSRI 药物包括西酞普兰(Celexa)、艾司西酞普兰(Lexapro)、氟西汀(Prozac)、帕罗西汀(Paxil、Pexeva)、舍曲林(Zoloft)、维拉佐酮(Viibryd)
血清素-去甲肾上腺素再摄取抑制剂(SNRI)
SNRI 药物包括度洛西汀(Cymbalta)、文拉法辛(Effexor XR)、地文拉法辛(Pristiq、Khedezla)和左米那普仑(Fetzima)
非典型抗抑郁药
这些药物不太适合归入其他任何抗抑郁药类别。这些药物包括安非他酮(Wellbutrin XL、Wellbutrin SR、Aplenzin、Forfivo XL)、米氮平(Remeron)、奈法唑酮、曲唑酮和伏硫西汀(Trintellix)。
三环类抗抑郁药
例如丙米嗪(Tofranil)、去甲替林(Pamelor)、阿米替林、多塞平、曲米帕明(Surmontil)、地昔帕明(Norpramin)和普罗替林(Vivactil)等这些药物可能都很有效,但是副作用往往比新型的抗抑郁药更严重。因此通常不会开三环类药物,除非您已经用过 SSRI,却没有起色。
单胺氧化酶抑制剂(MAOI)
反苯环丙胺(Parnate)、苯乙肼(Nardil)和异卡波肼(Marplan)等 MAOI 药物会产生严重的副作用,因此,一般在其他药物没有疗效的情况下才会开这些药物。使用 MAOI 时需要严格控制饮食,因为这类药物会和某些奶酪、泡菜、葡萄酒等食物以及某些药物和草本补充剂发生相互作用,危险甚至致命。司来吉兰(Emsam)是一种新型 MAOI,可以作为垫片贴在皮肤上,副作用少于其他 MAOI 药物。这类药物不能和 SSRI 药物联合使用。
鼻内艾氯胺酮
新药物,例如鼻内艾氯胺酮,可以快速发挥抗抑郁作用,特别是对于难治性抑郁症患者。以鼻喷雾剂的形式提供,通常在几个小时内迅速起效,缓解抑郁症状。使用艾氯胺酮的人通常会继续服用口服抗抑郁药以维持症状的改善。
多种药物
有时候可能需要尝试几种药物或联合用药,然后才能找到有效的药物。这需要耐心,因为对有些药物而言,完全起效及其副作用随着身体调整而缓解,需要数周或更长时间。
突然停药的风险
抗抑郁药需要一段时间(通常需要 4-8 周)才能发挥作用,睡眠、食欲和注意力问题通常会在情绪好转之前得到改善。
咨询医生前,请不要停止服用抗抑郁药。抗抑郁药一般不会上瘾,但有时会产生身体依赖性(这与上瘾不同)。突然停止治疗或多次漏服药物可能导致类似戒断的症状,突然放弃治疗可能导致抑郁症恶化。配合医生,逐渐安全减小剂量。
// 中药类
早在中国汉代,张仲景就记载了治疗抑郁症的经典方剂,但其具体药理机制尚不清楚。在最近的研究中,一些中药的抗抑郁作用已被证明与肠道菌群相关。
例如,舒肝颗粒可以显著改善慢性约束应激小鼠的异常行为和海马炎症。后续的机制研究表明,其给药丰富了小鼠肠道中的丁酸单胞菌和节疣念珠菌,降低了拟杆菌的丰度,并与PI3K/Akt/mTOR途径密切相关。
五味子可以通过抑制TLR4/NF-κB信号通路来减轻抑郁小鼠的肠道微生态失调。
除了调节炎症,中药还在调节神经递质水平方面发挥作用。
莲心碱治疗可以缩短抑郁小鼠的不动时间,增加海马中的DA、5-HT和NE等神经递质。同时,小鼠结肠中乳酸杆菌的相对丰度也有所增加。
在另一项研究中,特异性抗抑郁药中药的靶点可以集中在嘌呤代谢的调节上。与中药相关的动物研究,如肉苁蓉和藏红花酸,表明它们的抗抑郁作用与肠道菌群的调节密切相关。
除了动物研究,临床研究也提供了相应的证据。对患有抑郁症的癌症患者使用中药复方小柴胡汤进行干预。给药后,受试者的抑郁症状减轻,肠道微生态失调得到部分逆转(特别是减少了副拟杆菌、Blautia和瘤胃球菌科细菌的丰度)。有趣的是,这种抗抑郁的草药也表现出一些抗肿瘤作用,其潜在机制涉及TLR4/MyD88/NF-κB信号传导。
值得注意的是,这些途径在涉及微生物群的抑郁症发病机制中也发挥着重要作用。最近的系统综述和荟萃分析也表明,与抗抑郁药相比,中药可以减少不良事件。鉴于目前的研究数量有限,准确总结中药治疗抑郁症的益处和风险还为时过早。
// 专业治疗
一旦注意到抑郁症的迹象或症状,与心理健康专家交谈将是至关重要的一步。值得信赖的治疗师可以识别模式,帮助情绪调节。
心理治疗
几种类型的心理治疗(也称为谈话疗法或咨询),可以通过教抑郁症患者新的思维和行为方式以及如何改变导致抑郁的习惯来帮助他们。
治疗抑郁症的循证方法包括:
一种谈话疗法,旨在帮助改变任何可能导致或恶化抑郁症的消极思想或行为模式。这种疗法通常也是短期的,重点是解决当前的问题并学习新的应对技巧。
治疗师通过帮助个体识别和处理与人际关系有关的困难,以及改善与他人的交流方式,来促进情绪上的积极变化。 解决几个常见的人际问题,包括失去、冲突、角色变化和人际孤立感。个体可以增强情感的稳定性和归属感,提高应对人际问题的能力。
心理健康服务远程医疗的发展提供了面对面治疗的替代方案,在某些情况下使人们更容易、更方便地获得帮助。对于过去可能对寻求心理健康护理犹豫不决的人来说,远程心理健康服务可能是比传统心理健康服务更容易的第一步。
脑刺激疗法
如果药物或心理治疗不能减轻抑郁症状,脑刺激疗法可能是一种值得探索的选择。
拥有最多证据的脑刺激疗法包括:
ECT 和 rTMS 是使用最广泛的脑刺激疗法,其中 ECT 的使用历史最长。
替代疗法
每日晨光疗法是季节性情感障碍患者的常见治疗选择。光疗设备比普通室内照明明亮得多,被认为是安全的,但患有某些眼病或服用增加对阳光敏感性的药物的人不建议。
抑郁症不仅仅是一种精神疾病,还具有生理和解剖学改变,本文我们了解了抑郁症相关的基本知识,以及肠道菌群在抑郁症发展和症状表现中的重要性。深入了解抑郁症和肠道菌群之间的相互影响将有助于未来开发更有效的治疗策略,并提高患者的生活质量。
我们应该全面认识抑郁症,意识到其不仅仅是一种心理问题,而是一个涉及多个身体系统的综合性障碍。除了对心理状态的影响外,抑郁症还可以引起神经系统、免疫系统、心血管系统以及睡眠障碍等多方面的变化。
目前对于微生物组在口腔-肠道-脑轴中的作用已经有了一定的认识,这是一个重要的研究方向,从病理生理学到调节肠道微生物组对精神疾病产生影响。关于口腔微生物群与精神疾病的关联详见本次推文第二篇:
这些身体系统的紊乱可能进一步加剧抑郁症的症状,并对患者的整体健康状况产生负面影响。
在临床实践中,针对抑郁症的治疗需要不同科室的医生共同合作。未来更多需要整合心理治疗、药物治疗、营养治疗和包括菌群检测在内的综合性健康管理等多个领域的专业知识与技术,实施多学科联合治疗,为抑郁症的治疗提供全新的视角,并为未来研究和改进抑郁症治疗策略提供宝贵的经验。
吾日三省吾身:
每天给予自己足够的关怀和爱吗?
对自己的身心健康变化是否警觉并感兴趣?
是否意识到自己的情绪,并且能够充分处理和接纳它们?
…
希望大家都能健康快乐,远离抑郁。
注:本账号内容仅作交流参考,不作为诊断及医疗依据。
相关阅读:
环境污染物通过肠脑轴影响心理健康,精神益生菌或将发挥重要作用
主要参考文献:
Basiji K, Sendani AA, Ghavami SB, Farmani M, Kazemifard N, Sadeghi A, Lotfali E, Aghdaei HA. The critical role of gut-brain axis microbiome in mental disorders. Metab Brain Dis. 2023 Jul 12. doi: 10.1007/s11011-023-01248-w. Epub ahead of print. PMID: 37436588.
Chang L, Wei Y, Hashimoto K. Brain-gut-microbiota axis in depression: A historical overview and future directions. Brain Res Bull. 2022 May;182:44-56. doi: 10.1016/j.brainresbull.2022.02.004. Epub 2022 Feb 11. PMID: 35151796.
Bradlow RCJ, Berk M, Kalivas PW, Back SE, Kanaan RA. The Potential of N-Acetyl-L-Cysteine (NAC) in the Treatment of Psychiatric Disorders. CNS Drugs. 2022 May;36(5):451-482.
Chen Y, Xu J, Chen Y. Regulation of Neurotransmitters by the Gut Microbiota and Effects on Cognition in Neurological Disorders. Nutrients. 2021 Jun 19;13(6):2099. doi: 10.3390/nu13062099. PMID: 34205336; PMCID: PMC8234057.
Smith KM, Renshaw PF, Bilello J. The diagnosis of depression: current and emerging methods. Compr Psychiatry. 2013 Jan;54(1):1-6. doi: 10.1016/j.comppsych.2012.06.006. Epub 2012 Aug 15. PMID: 22901834; PMCID: PMC5502713.
Joe Cohen, BS. How Depression May Be Linked To Gut Microbes. 2022.12.selfhacked.
Major Depressive Disorder Working Group of the Psychiatric GWAS Consortium; Ripke S, Wray NR, Lewis CM, Hamilton SP, Weissman MM, et al., A mega-analysis of genome-wide association studies for major depressive disorder. Mol Psychiatry. 2013 Apr;18(4):497-511.
Zeng Y, Navarro P, Xia C, Amador C, Fernandez-Pujals AM, Thomson PA, Campbell A, Nagy R, Clarke TK, Hafferty JD, Smith BH, Hocking LJ, Padmanabhan S, Hayward C, MacIntyre DJ, Porteous DJ, Haley CS, McIntosh AM. Shared Genetics and Couple-Associated Environment Are Major Contributors to the Risk of Both Clinical and Self-Declared Depression. EBioMedicine. 2016 Dec;14:161-167.
Sharma A. Systems Genomics Support for Immune and Inflammation Hypothesis of Depression. Curr Neuropharmacol. 2016;14(7):749-58.
Flint J, Kendler KS. The genetics of major depression. Neuron. 2014 Feb 5;81(3):484-503. doi: 10.1016/j.neuron.2014.01.027. Erratum in: Neuron. 2014 Mar 5;81(5):1214.
Brundin L, Sellgren CM, Lim CK, Grit J, Pålsson E, Landén M, Samuelsson M, Lundgren K, Brundin P, Fuchs D, Postolache TT, Traskman-Bendz L, Guillemin GJ, Erhardt S. An enzyme in the kynurenine pathway that governs vulnerability to suicidal behavior by regulating excitotoxicity and neuroinflammation. Transl Psychiatry. 2016 Aug 2;6(8):e865.
Lohoff FW. Overview of the genetics of major depressive disorder. Curr Psychiatry Rep. 2010 Dec;12(6):539-46.
González-Arancibia C, Urrutia-Piñones J, Illanes-González J, Martinez-Pinto J, Sotomayor-Zárate R, Julio-Pieper M, Bravo JA. Do your gut microbes affect your brain dopamine? Psychopharmacology (Berl). 2019 May;236(5):1611-1622. doi: 10.1007/s00213-019-05265-5. Epub 2019 May 17. PMID: 31098656.
Qin J, Li R, Raes J, Arumugam M, Burgdorf KS, Manichanh C, Nielsen T, Pons N, Levenez F, Yamada T, Mende DR, Li J, Xu J, Li S, Li D, Cao J, Wang B, Liang H, Zheng H, Xie Y, Tap J, Lepage P, Bertalan M, Batto JM, Hansen T, Le Paslier D, Linneberg A, Nielsen HB, Pelletier E, Renault P, Sicheritz-Ponten T, Turner K, Zhu H, Yu C, Li S, Jian M, Zhou Y, Li Y, Zhang X, Li S, Qin N, Yang H, Wang J, Brunak S, Doré J, Guarner F, Kristiansen K, Pedersen O, Parkhill J, Weissenbach J; MetaHIT Consortium; Bork P, Ehrlich SD, Wang J. A human gut microbial gene catalogue established by metagenomic sequencing. Nature. 2010 Mar 4;464(7285):59-65.
Bercik P, Collins SM, Verdu EF. Microbes and the gut-brain axis. Neurogastroenterol Motil. 2012 May;24(5):405-13.
Mayneris-Perxachs J, Castells-Nobau A, Arnoriaga-Rodríguez M, Martin M, de la Vega-Correa L, Zapata C, Burokas A, Blasco G, Coll C, Escrichs A, Biarnés C, Moreno-Navarrete JM, Puig J, Garre-Olmo J, Ramos R, Pedraza S, Brugada R, Vilanova JC, Serena J, Gich J, Ramió-Torrentà L, Pérez-Brocal V, Moya A, Pamplona R, Sol J, Jové M, Ricart W, Portero-Otin M, Deco G, Maldonado R, Fernández-Real JM. Microbiota alterations in proline metabolism impact depression. Cell Metab. 2022 May 3;34(5):681-701.e10.
David LA, Maurice CF, Carmody RN, Gootenberg DB, Button JE, Wolfe BE, Ling AV, Devlin AS, Varma Y, Fischbach MA, Biddinger SB, Dutton RJ, Turnbaugh PJ. Diet rapidly and reproducibly alters the human gut microbiome. Nature. 2014 Jan 23;505(7484):559-63.
Bailey MT, Dowd SE, Galley JD, Hufnagle AR, Allen RG, Lyte M. Exposure to a social stressor alters the structure of the intestinal microbiota: implications for stressor-induced immunomodulation. Brain Behav Immun. 2011 Mar;25(3):397-407.
Diaz Heijtz R, Wang S, Anuar F, Qian Y, Björkholm B, Samuelsson A, Hibberd ML, Forssberg H, Pettersson S. Normal gut microbiota modulates brain development and behavior. Proc Natl Acad Sci U S A. 2011 Feb 15;108(7):3047-52.
Desbonnet L, Garrett L, Clarke G, Kiely B, Cryan JF, Dinan TG. Effects of the probiotic Bifidobacterium infantis in the maternal separation model of depression. Neuroscience 170: 1179-1188
Bercik P, Denou E, Collins J, Jackson W, Lu J, Jury J, Deng Y, Blennerhassett P, Macri J, McCoy KD, Verdu EF, Collins SM. The intestinal microbiota affect central levels of brain-derived neurotropic factor and behavior in mice. Gastroenterology. 2011 Aug;141(2):599-609, 609.e1-3.
Huang R, Wang K, Hu J. Effect of Probiotics on Depression: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. Nutrients. 2016 Aug 6;8(8):483.
Akkasheh G, Kashani-Poor Z, Tajabadi-Ebrahimi M, Jafari P, Akbari H, Taghizadeh M, Memarzadeh MR, Asemi Z, Esmaillzadeh A. Clinical and metabolic response to probiotic administration in patients with major depressive disorder: A randomized, double-blind, placebo-controlled trial. Nutrition. 2016 Mar;32(3):315-20.
Macpherson AJ, Harris NL.. Interactions between commensal intestinal bacteria and the immune system. Nat Rev Immunol 4: 478-485
Bailey MT. Influence of stressor-induced nervous system activation on the intestinal microbiota and the importance for immunomodulation. Adv Exp Med Biol. 2014;817:255-76.
García Bueno B, Caso JR, Madrigal JL, Leza JC. Innate immune receptor Toll-like receptor 4 signalling in neuropsychiatric diseases. Neurosci Biobehav Rev. 2016 May;64:134-47.
Nugent NR, Tyrka AR, Carpenter LL, Price LH. Gene-environment interactions: early life stress and risk for depressive and anxiety disorders. Psychopharmacology (Berl). 2011 Mar;214(1):175-96.
Ait-Belgnaoui A, Durand H, Cartier C, Chaumaz G, Eutamene H, Ferrier L, Houdeau E, Fioramonti J, Bueno L, Theodorou V. Prevention of gut leakiness by a probiotic treatment leads to attenuated HPA response to an acute psychological stress in rats. Psychoneuroendocrinology. 2012 Nov;37(11):1885-95.
Cryan JF, Dinan TG. Mind-altering microorganisms: the impact of the gut microbiota on brain and behaviour. Nat Rev Neurosci. 2012 Oct;13(10):701-12.
Bercik P, Verdu EF, Foster JA, Macri J, Potter M, Huang X, Malinowski P, Jackson W, Blennerhassett P, Neufeld KA, Lu J, Khan WI, Corthesy-Theulaz I, Cherbut C, Bergonzelli GE, Collins SM. Chronic gastrointestinal inflammation induces anxiety-like behavior and alters central nervous system biochemistry in mice. Gastroenterology. 2010 Dec;139(6):2102-2112.e1.
Bravo JA, Forsythe P, Chew MV, Escaravage E, Savignac HM, Dinan TG, Bienenstock J, Cryan JF. Ingestion of Lactobacillus strain regulates emotional behavior and central GABA receptor expression in a mouse via the vagus nerve. Proc Natl Acad Sci U S A. 2011 Sep 20;108(38):16050-5. doi: 10.1073/pnas.1102999108.
Bercik P, Denou E, Collins J, Jackson W, Lu J, Jury J, Deng Y, Blennerhassett P, Macri J, McCoy KD, Verdu EF, Collins SM. The intestinal microbiota affect central levels of brain-derived neurotropic factor and behavior in mice. Gastroenterology. 2011 Aug;141(2):599-609, 609.e1-3.
Mayneris-Perxachs J, Castells-Nobau A, Arnoriaga-Rodríguez M, Martin M, de la Vega-Correa L, Zapata C, Burokas A, Blasco G, Coll C, Escrichs A, Biarnés C, Moreno-Navarrete JM, Puig J, Garre-Olmo J, Ramos R, Pedraza S, Brugada R, Vilanova JC, Serena J, Gich J, Ramió-Torrentà L, Pérez-Brocal V, Moya A, Pamplona R, Sol J, Jové M, Ricart W, Portero-Otin M, Deco G, Maldonado R, Fernández-Real JM. Microbiota alterations in proline metabolism impact depression. Cell Metab. 2022 May 3;34(5):681-701.e10.
Lopez MJ, Mohiuddin SS. Biochemistry, Essential Amino Acids. 2023 Mar 13. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2023 Jan–.
Mokhtari V, Afsharian P, Shahhoseini M, Kalantar SM, Moini A. A Review on Various Uses of N-Acetyl Cysteine. Cell J. 2017 Apr-Jun;19(1):11-17.
Ershad M, Naji A, Vearrier D. N-Acetylcysteine. [Updated 2023 Feb 19]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2023 Jan-.
Fernandes BS, Dean OM, Dodd S, Malhi GS, Berk M. N-Acetylcysteine in depressive symptoms and functionality: a systematic review and meta-analysis. J Clin Psychiatry. 2016 Apr;77(4):e457-66.
Berk M, Dean OM, Cotton SM, Jeavons S, Tanious M, Kohlmann K, Hewitt K, Moss K, Allwang C, Schapkaitz I, Robbins J, Cobb H, Ng F, Dodd S, Bush AI, Malhi GS. The efficacy of adjunctive N-acetylcysteine in major depressive disorder: a double-blind, randomized, placebo-controlled trial. J Clin Psychiatry. 2014 Jun;75(6):628-36.
Fernandes BS, Dean OM, Dodd S, Malhi GS, Berk M. N-Acetylcysteine in depressive symptoms and functionality: a systematic review and meta-analysis. J Clin Psychiatry. 2016 Apr;77(4):e457-66.
Hasebe K, Gray L, Bortolasci C, Panizzutti B, Mohebbi M, Kidnapillai S, Spolding B, Walder K, Berk M, Malhi G, Dodd S, Dean OM. Adjunctive N-acetylcysteine in depression: exploration of interleukin-6, C-reactive protein and brain-derived neurotrophic factor. Acta Neuropsychiatr. 2017 Dec;29(6):337-346.
Das P, Tanious M, Fritz K, Dodd S, Dean OM, Berk M, Malhi GS. Metabolite profiles in the anterior cingulate cortex of depressed patients differentiate those taking N-acetyl-cysteine versus placebo. Aust N Z J Psychiatry. 2013 Apr;47(4):347-54.
Fekadu A, Demissie M, Birhane R, Medhin G, Bitew T, Hailemariam M, Minaye A, Habtamu K, Milkias B, Petersen I, Patel V, Cleare AJ, Mayston R, Thornicroft G, Alem A, Hanlon C, Prince M. Under detection of depression in primary care settings in low and middle-income countries: a systematic review and meta-analysis. Syst Rev. 2022 Feb 5;11(1):21.
Wickham SR, Amarasekara NA, Bartonicek A, Conner TS. The Big Three Health Behaviors and Mental Health and Well-Being Among Young Adults: A Cross-Sectional Investigation of Sleep, Exercise, and Diet. Front Psychol. 2020 Dec 10;11:579205.
Yates BE, DeLetter MC, Parrish EM. Prescribed exercise for the treatment of depression in a college population: An interprofessional approach. Perspect Psychiatr Care. 2020 Oct;56(4):894-899.
Belvederi Murri M, Ekkekakis P, Magagnoli M, Zampogna D, Cattedra S, Capobianco L, Serafini G, Calcagno P, Zanetidou S, Amore M. Physical Exercise in Major Depression: Reducing the Mortality Gap While Improving Clinical Outcomes. Front Psychiatry. 2019 Jan 10;9:762.
Peirce JM, Alviña K. The role of inflammation and the gut microbiome in depression and anxiety. J Neurosci Res. 2019 Oct;97(10):1223-1241. doi: 10.1002/jnr.24476. Epub 2019 May 29. PMID: 31144383.
Basso JC, Suzuki WA. The Effects of Acute Exercise on Mood, Cognition, Neurophysiology, and Neurochemical Pathways: A Review. Brain Plast. 2017 Mar 28;2(2):127-152.
Worley SL. The Extraordinary Importance of Sleep: The Detrimental Effects of Inadequate Sleep on Health and Public Safety Drive an Explosion of Sleep Research. P T. 2018 Dec;43(12):758-763.
Shen H, Chen M, Cui D. Biological mechanism study of meditation and its application in mental disorders. Gen Psychiatr. 2020 Jul 13;33(4):e100214.
Hölzel BK, Carmody J, Vangel M, Congleton C, Yerramsetti SM, Gard T, Lazar SW. Mindfulness practice leads to increases in regional brain gray matter density. Psychiatry Res. 2011 Jan 30;191(1):36-43.
Ljungberg T, Bondza E, Lethin C. Evidence of the Importance of Dietary Habits Regarding Depressive Symptoms and Depression. Int J Environ Res Public Health. 2020 Mar 2;17(5):1616.
Francis HM, Stevenson RJ, Chambers JR, Gupta D, Newey B, Lim CK. A brief diet intervention can reduce symptoms of depression in young adults – A randomised controlled trial. PLoS One. 2019 Oct 9;14(10):e0222768.
Wong SK, Chin KY, Ima-Nirwana S. Vitamin D and Depression: The Evidence from an Indirect Clue to Treatment Strategy. Curr Drug Targets. 2018;19(8):888-897.
Kaveladze B, Diamond Altman A, Niederhausen M, Loftis JM, Teo AR. Social relationship quality, depression and inflammation: A cross-cultural longitudinal study in the United States and Tokyo, Japan. Int J Soc Psychiatry. 2022 Mar;68(2):253-263.
Matthew Solan.The secret to happiness? Here’s some advice from the longest-running study on happiness.Harvard Health.
Cunha LF, Pellanda LC, Reppold CT. Positive Psychology and Gratitude Interventions: A Randomized Clinical Trial. Front Psychol. 2019 Mar 21;10:584.
Menéndez-Aller Á, Postigo Á, Montes-Álvarez P, González-Primo FJ, García-Cueto E. Humor as a protective factor against anxiety and depression. Int J Clin Health Psychol. 2020 Jan-Apr;20(1):38-45.
Reyes-Martínez S, Segura-Real L, Gómez-García AP, Tesoro-Cruz E, Constantino-Jonapa LA, Amedei A, Aguirre-García MM. Neuroinflammation, Microbiota-Gut-Brain Axis, and Depression: The Vicious Circle. J Integr Neurosci. 2023 May 8;22(3):65. doi: 10.31083/j.jin2203065. PMID: 37258450.
谷禾健康
运动可以说是最有效和可行的生活方式因素,个人可以利用它来保护自己免受各种疾病的侵害,包括代谢性、心血管、神经退行性和肿瘤性疾病。
世界卫生组织建议,每周进行150-300分钟的中等强度运动。
运动的好处具体不用多说了,我们大家都知道,但你有没有想过,为什么只有一小部分人能坚持呢?

让我们挪不开腿的除了以上理由之外,有没有可能存在什么生理瓶颈,阻止了我们进行定期的体育活动呢?
由Lenka Dohnalová领导的宾夕法尼亚大学的研究团队,开始使用一大群基因多样性的野生小鼠来回答这个问题。
结果发现,肠道微生物组占据了很大的因素,也就是说,“不想运动”这个想法很可能不是因为懒,而是与肠道微生物群相关。
肠道微生物群是如何影响到我们的神经系统,促进运动的进行呢?
本文我们来详细了解一下。
研究人员观察到,个体间运动能力的显著差异,表现最好的动物比最弱的动物快10倍以上。
为了探索这些差异的原因,研究人员对这些小鼠进行了深入的分子和生理学分析。神奇的是,研究人员发现:
我们来看一下研究人员的探索过程。
– 研究人员首先关注基因组,发现遗传对运动能力个体间变异的贡献很小。
– 转向非遗传参数并评估它们对运动表现的影响。动物队列中的血清代谢组、肠道微生物组组成和代谢参数差异很大。
– 使用机器学习方法来识别对运动表现有很强预测作用的变量。
– 发现 仅基于肠道微生物群 16S rDNA 测序结果的预测所达到的准确度与血清代谢组或所有测量参数组合所实现的准确度几乎一样高。
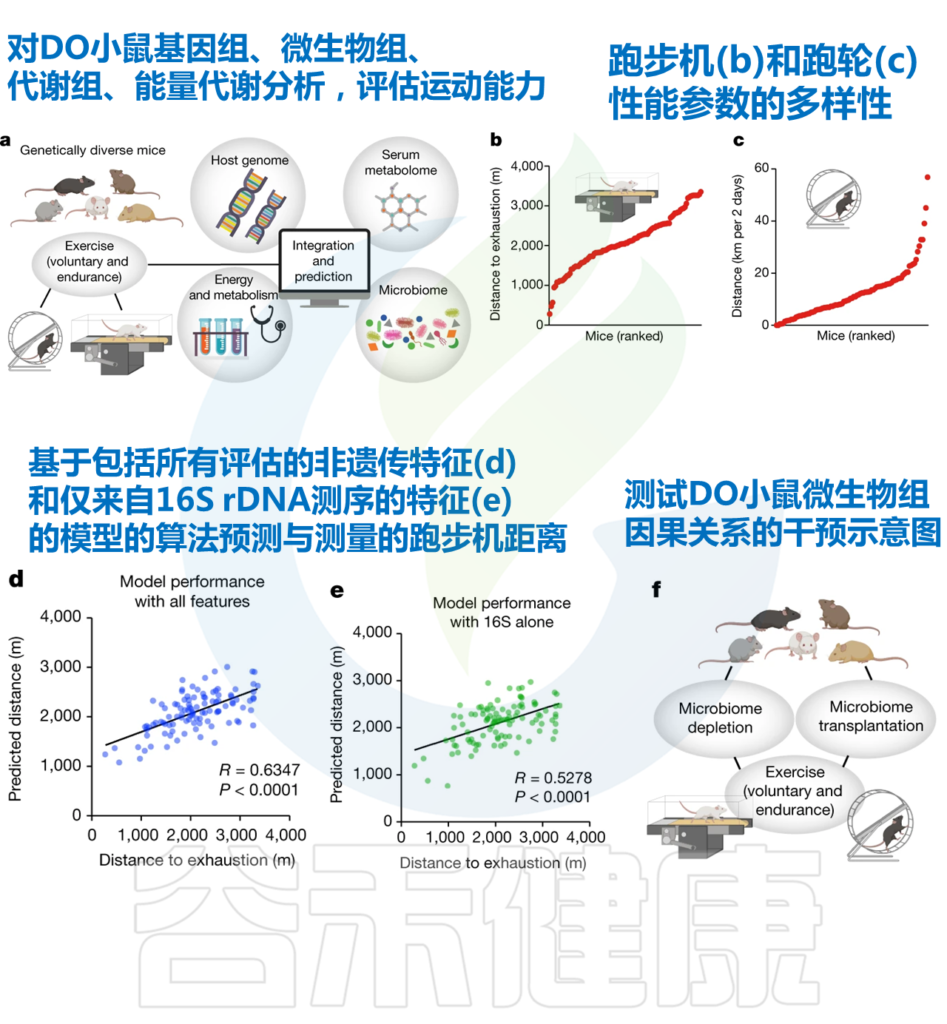
Dohnalová L, et al., Nature. 2022
研究人员探究了肠道菌群在运动表现中的功能重要性,并在无菌或接受抗生素治疗的小鼠中进行了运动测量实验(即在确定的微生物群落环境下)。
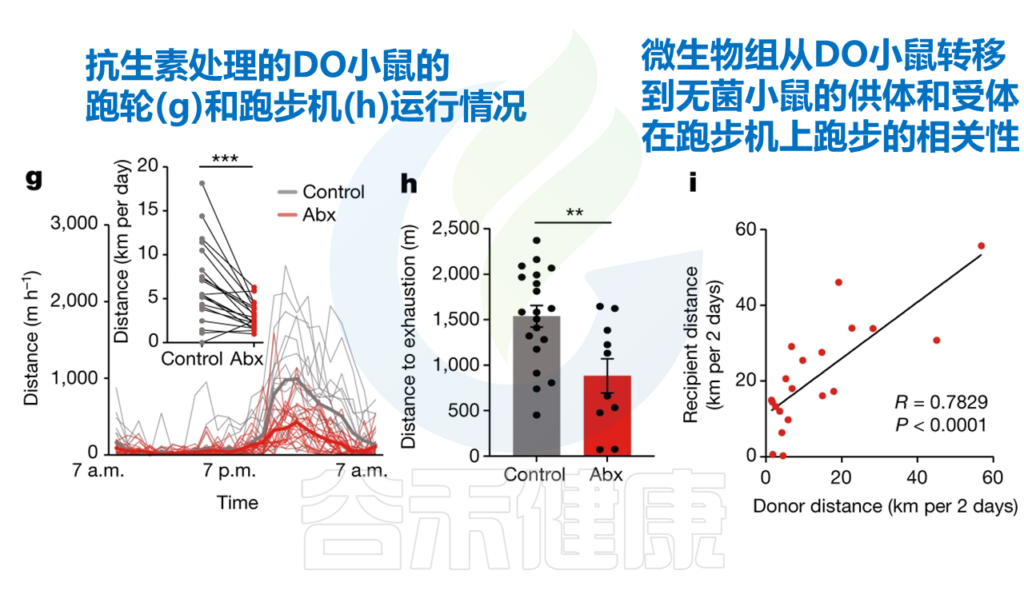
Dohnalová L, et al., Nature. 2022
发现在无菌或接受抗生素治疗的小鼠中(也就是缺乏微生物群的小鼠),自愿运动和耐力运动能力降低了50%左右。
与特定菌群相关——丹毒丝菌科和毛螺菌科
研究人员使用 SHapley Additive exPlanation (SHAP)评估了预测模型中各个微生物组特征的贡献。
所有微生物群特征的SHAP值排序有助于预测DO小鼠的运动表现
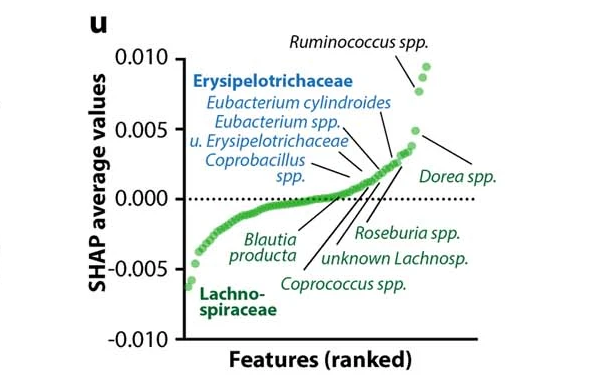
Dohnalová L, et al., Nature. 2022
研究人员确定,这一影响是由特定菌群引起的,包括毛螺菌科(Lachnospiraceae)和丹毒丝菌科(Erysipelotrichaceae)的成员。
这些实验证明,肠道菌群可能是个体运动能力差异的一个重要影响因素。
与研究人员的预期不同,肠道菌群对身体活动的影响并不是通过与运动经典相关的组织,如骨骼肌来介导的。相反,肠道菌群似乎根本上影响了运动对大脑的影响。
剧烈的体育活动会在大脑中引起多种神经化学反应,包括纹状体中多巴胺释放的激增。有趣的是,在没有肠道菌群的情况下,这种激增严重减弱了。
我们知道,多巴胺的释放会导致愉悦、动力和奖励感,这也是为什么有些人在剧烈运动后所经历的“跑步快感”现象。
基于这些发现,推测:
微生物群通过调节运动诱导的多巴胺反应来增强运动能力。
通过一系列药理学和化学遗传学的介入实验,发现多巴胺缺乏确实是导致微生物群消失动物运动能力降低的原因。与此一致的是,恢复多巴胺信号完全恢复了它们的运动能力。
微生物群与大脑之间的通信可以通过微生物分子进入全身循环,或者通过肠道和大脑之间的直接神经连接进行。
研究人员没有找到证据表明微生物群通过全身介质影响运动能力。相反,抑制与肠道神经传导相关的感觉神经元,可以重现微生物群消失对运动的影响,而刺激感觉神经元则可以在没有微生物群的情况下恢复运动能力。
为了确定微生物群在运动过程中如何影响感觉神经元的活动,研究人员结合了微生物遗传学、代谢组学和神经元记录技术。
结果发现,微生物通过合成脂肪酸酰胺,增强感觉神经元的活动,通过内源性大麻素受体CB1介导。这种神经元活动的增加进而增强了运动过程中的多巴胺信号(见下图)。
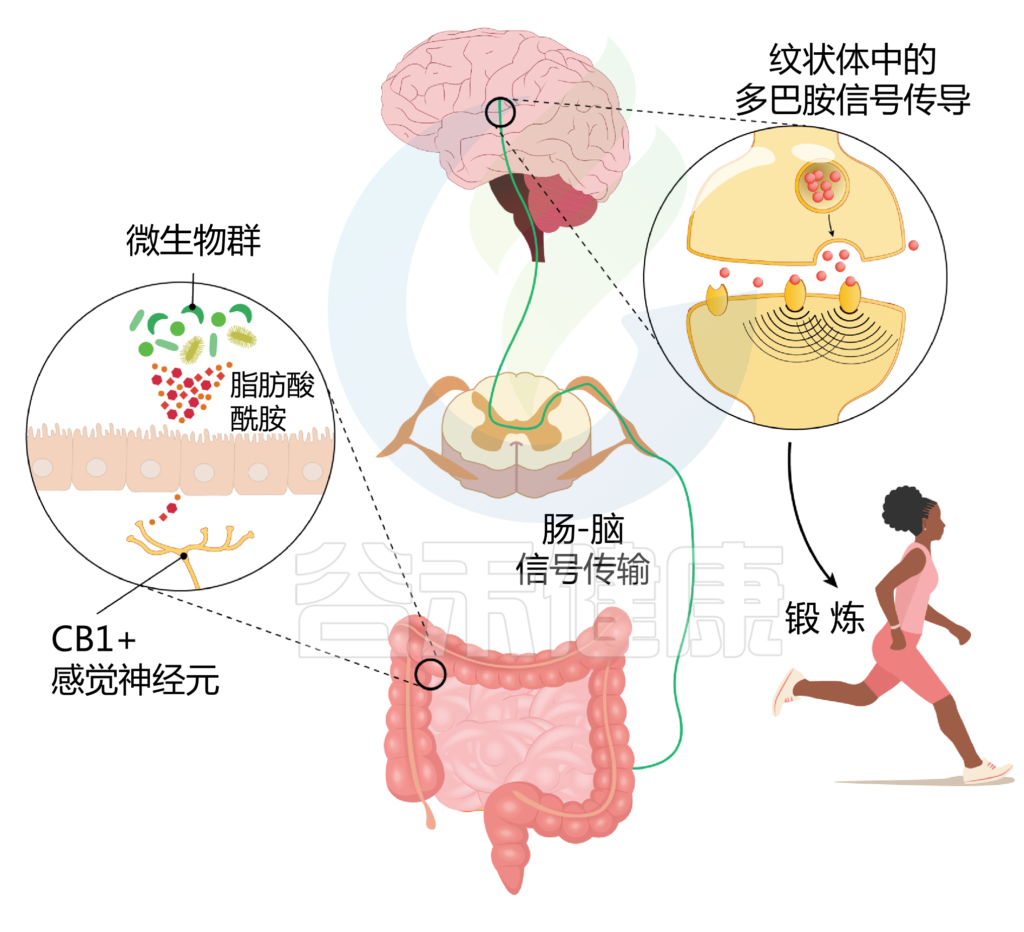
Thaiss CA. Science. 2023
这种途径可以通过胃肠道干预来调节运动表现
例如,用基因工程产生脂肪酸酰胺的细菌定植无菌小鼠,或用含有脂肪酸酰胺的饮食喂养抗生素治疗的小鼠,可以恢复它们的运动能力。
然而,使用外周CB1抑制剂或中枢多巴胺受体阻断剂时,这些干预的积极效果就会被取消掉。
该研究的重要发现:
微生物群代谢产生脂肪酸酰胺,由肠道神经支配神经元上的内源性大麻素受体CB1感知,这增强了它们在运动中的活性。感觉神经元的激活,反过来增强了纹状体中的多巴胺信号,从而推动了运动表现。
这项发现有几个重要的启示:
– 胃肠道信号作为大脑中运动反应神经元活动的调节因子,有可能促进“跑步快感”的产生
这种肠-脑途径的进化目的尚待确定,推测它可能将动物决定长期进行体育活动与胃肠道的营养状况联系起来。无论是精英运动员还是业余跑步者,心理状态在运动参与和表现中都起着至关重要的作用。
– 微生物组依赖性途径,可能有助于更好地理解促使某些个体达到巅峰表现的因素
微生物组及其代谢产物的可塑性,为在全球范围内增加运动参与及其健康益处提供了一条潜在途径。
– 纹状体多巴胺是运动以外的动机行为的关键介质
这项发现开启了利用这一途径影响其他多巴胺依赖性大脑功能的可能性,如学习、情绪、成瘾等领域都可能应用。
总的来说,这项研究为我们打开了一扇了解肠道微生物与运动之间关系的窗户,为相关领域的深入研究提供了新的启示。对影响神经元活动的微生物组衍生分子的广阔宇宙的进一步探索,将为胃肠道塑造思维的潜力提供有价值的见解。
当然,这也让我们看到了肠道菌群检测在个体运动能力评估中具有巨大潜力,通过微生物群干预,为提升运动积极性,发展个性化的运动方案和训练策略提供了新的思路和可能性。
参考文献:
Dohnalová L, Lundgren P, Carty JRE, et al., A microbiome-dependent gut-brain pathway regulates motivation for exercise. Nature. 2022 Dec;612(7941):739-747. doi: 10.1038/s41586-022-05525-z

谷禾健康

人类微生物组包含约 1000多 个常见物种,微生物细胞数量达 10-100 万亿个。微生物大多数遗传库分布在人类胃肠道内,与许多生理过程的发育和功能有内在联系,例如,肠道屏障完整性和稳态、营养、免疫和神经心理行为等。
人类肠道的菌群失调(即共生肠道微生物群的变化对宿主健康产生影响)通常与一系列疾病相关,其中许多疾病无法使用完善的医疗方案进行治疗。
在这种情况下,将健康捐赠者的粪便物质直接移植到受体的胃肠道中(称为粪便微生物群移植,简称粪菌移植,FMT)代表了一种操纵受体微生物群并赋予健康益处的治疗方法。许多国家食品和药物管理局最近的批准表明,粪菌移植和治疗性益生菌鸡尾酒疗法目前正在扩大研究和应用领域。
这种方法成功的关键是能够在患病患者的胃肠道内重建并将肠道微生物群恢复到理想的健康状态。据报道,粪菌移植在临床中治疗艰难梭菌感染成功率接近 90%。
最近发表了几项通过粪便微生物移植(FMT)来治疗炎症性肠病(IBD),特别是溃疡性结肠炎的随机临床试验,但是研究设计存在重大差异。这些包括给药剂量、给药途径和频率、安慰剂类型和评估终点的差异。总体结果看起来很有前景,但它们高度依赖于捐赠者和接受者因素。
近日,来自意大利、法国、英国、美国等 25 名IBD、免疫学和微生物学领域专家多次召开会议,通过对当前可用和/或已发布的数据进行深入评估来制定基于IBD 中与 FMT 相关证据的指南。所有成员对声明进行评估和投票,最终形成全体共识会议并生成拟议指南。
声明包括:
这份共识目的是为使用 FMT 评估、管理和潜在治疗 IBD 制定基于共识的声明和建议,以实现标准化实践。
今天谷禾与大家分享该共识或指南内容,并结合以往研究结果和相关经验阐述说明。我们也相信,在临床研究中明确考虑供体和受体的原有肠道微生物生态原则可以更好地指导FMT试验的设计并有助于提高 FMT 的疗效。
★
生态学是一门核心学科,研究集中构建生物群落的过程和机制,并调节其在空间和时间上的变化。
虽然说,生态学和微生物学在研究复杂群落的方向经常会有交叉部分,但两者在历史上都是作为独立的科学学科发展起来的,在概念、术语、综合和理论的使用上往往有所不同。
临床研究中的 FMT,个体之间粪便物质的移植符合社区合并的概念。这个概念指的是:
整个生物群落及其环境的大规模混合
虽然在宏观生物生态学(即植物和动物)中构成罕见事件,但群落合并在微生物系统中很常见,实际上,群落经常作为一个单元迁移。
这一原则与 FMT 治疗相一致,尽管该术语似乎尚未在临床研究中得到很好的确立。然而,合并后群落重新排列的结果(即植入)更常用于跟踪 FMT 功效。
基于来自供体、FMT前、FMT后接受者的粪便微生物组的微生物菌群监测,才能更好的确定与较高供体菌株植入相关的最重要的临床变量,通过不同的上消化道和下消化道引入的混合途径(即通过胶囊、肠镜检查、鼻胃管、鼻十二指肠管或上内窥镜检查和结肠镜检查),单独或结合进行 FMT 给药,会导致 FMT 后供体菌株植入率更高。
这一发现支持了繁殖压力(即引入的个体数量与独立引入的数量的组合)对于在新环境中成功引入非本地物种的重要性。
发生这种情况主要是因为:
i)初始微生物物种种群的大小可以直接影响其在非本地环境中持续存在的能力
ii)即使是短暂的入侵者也会对微生物组产生影响,有时会促进其在后续环境中的引入入侵尝试(例如,重复入侵尝试的重要性)
其次,在 FMT 给药前接受抗生素的患者中,可能供体菌株植入率更高。已知抗生素的使用会导致肠道微生物群失衡(即非生物紊乱)。这种干扰降低了受体胃肠道微生物群的生物抗性,有利于随后的供体群落植入。重要的是,这个个别研究结果,在推广这一原则时需要谨慎,因为 FMT 之前的抗生素剂量、类型和时间都会导致与 FMT 最终结果的差异。
第三,患有传染病的患者在接受单途径 FMT 给药后,微生物组植入量更大。这与以下观点一致:驻留微生物组的先前不稳定(即,在这种情况下,生物干扰)也会对肠道生物抵抗力产生负面影响。特别是,胃肠道中非本地物种(例如感染期间的致病菌)的存在可以促进其他非本地物种的后续入侵。
★
粪便微生物群移植(FMT)被定义为将健康捐赠者的粪便输注到受体的胃肠道中,以治疗与疾病相关的肠道菌群失调。
根据几项随机对照试验和荟萃分析的报告,FMT是治疗复发性艰难梭菌感染的一种既定且高效的治疗选择,最终制定了国际指南,以标准化其使用艰难梭菌感染的可行治疗方式。
继成功治疗艰难梭菌感染后,FMT 也在炎症性肠病 (IBD) 患者中进行了研究,首先是在非随机研究中,随后在随机对照试验中,尽管 FMT 方案和程序存在显着差异,但两者均显示出有希望的结果。
然而,采用 FMT 治疗 IBD 受到一些限制,包括招募捐赠者、准备粪便材料、确定最佳给药途径以及缺乏明确和既定的监管框架。
解决这些问题的潜在策略包括识别和使用可持续、可重复和标准化的方案,最终目标是改变肠道微生物组的组成。因此,建立最佳的FMT整体框架对于IBD的未来管理具有重要意义。
▼
共识过程是按照以下步骤制定的:
确定成员
确定了 25 名共识成员,他们在微生物学、免疫学、FMT 和 IBD 领域拥有公认的专业知识,并全部参加了专家小组。
注:德尔菲法是在20世纪40年代由O.赫尔姆和N.达尔克首创,经过T.J.戈尔登和兰德公司进一步发展而成的。
德尔菲法作为一种主观、定性的方法,不仅可以用于预测领域,而且可以广泛应用于各种评价指标体系的建立和具体指标的确定过程。
分工作小组
根据个人专业知识,每位成员被分配到四个工作组之一:
每个工作组提出了一份关键问题清单,并制定了与指定主题相关的声明。对于每个关键问题,最佳现有证据是通过对相关文献进行系统审查而获得的。声明以专家意见 (EO) 的形式发布。
详细陈述已上传至在线投票系统(http://scott.armstrong.delphi.stlouisintegration.com/delphi2/),并分发给专家组。
专家评分
每轮审查后,都会收集、处理并与专家小组分享专家的答复。
对于每项陈述,专家们被要求对他们的同意程度进行评分:
如果至少 80% 的受访者对每项陈述表示强烈同意或同意保留意见,则达成共识。
未通过此门槛的声明将在后续轮次投票中进行修改和再次评级,直至达成共识。小组专家于 2022 年 6 月 25 日齐聚罗马,对总体声明进行完善和最终批准。
最终达成共识
经过三轮投票,最终的累积声明达成共识。第一轮和第二轮后,分别有67%和79%的陈述通过了80%的同意门槛,而第三轮后100%的陈述达到了目标水平。
★
声明 A1
IBD 的确切病因目前尚不清楚;然而,其发病机制是多因素的,受遗传易感性、宿主粘膜免疫反应和环境(包括饮食和肠道微生物群)的影响。
评论:
IBD,如克罗恩病 (CD) 和溃疡性结肠炎 (UC),是一种慢性、复发性消化道炎症性疾病,是由于遗传易感个体肠道免疫系统和肠道微生物群之间失去稳态而导致的。由于对肠道微生物群的耐受性失调或将微生物与底层组织分开的上皮屏障破坏,导致不适当的粘膜免疫反应,可能会导致 IBD 的发展或持续。
声明 A2
肠道微生物群的组成、相对丰度、多样性和功能的改变(即菌群失调)促进IBD的发生和进展。
评论:
越来越多的证据表明,肠道微生物组组成的不平衡或“生态失调”是促进 IBD 发展影响最大的环境因素之一,因为改变的微生物群与宿主的相互作用可以触发和促进免疫与 IBD 相关的改变。大量证据表明,IBD 患者肠道微生物组存在特定的共同改变,这些改变与许多功能受损相关,包括短链脂肪酸代谢、氨基酸生物合成、氧化应激调节和毒素,可以单独或共同促进 IBD 的发展。
声明 A3
溃疡性结肠炎和克罗恩病患者的肠道微生物组特别缺乏普拉梭菌,这种细菌因其潜在的抗炎特性而被认可。
关于普拉梭菌详见:
肠道核心菌属——普拉梭菌(F. Prausnitzii),预防炎症的下一代益生菌
评论:
越来越多的临床和实验数据表明,共生微生物群在维持人类和实验性 IBD 的炎症过程中发挥着关键作用。
一些报告显示,IBD 期间微生物多样性下降,尤其是厚壁菌门和拟杆菌门。有趣的是,厚壁菌门的成员普拉梭菌显着减少,并且具有公认的抗炎活性。
相反,活动性 IBD 中的变形菌和放线菌通常升高,以及特定的大肠杆菌菌株也如此。在这种情况下,肠道微生物组的成分在炎症性肠病中发挥着至关重要的作用,这可能代表了一种与细菌加工相关的疾病。因此,肠道微生物组和宿主免疫反应之间存在功能失调的关系,从而引发和维持 IBD 的慢性炎症。
声明 A4
IBD 患者感染艰难梭菌的风险高于一般人群。
评论:
IBD 特异性危险因素,例如免疫抑制、炎症的严重程度和扩展以及 IBD 中观察到的肠道菌群失调,被认为是IBD 患者艰难梭菌感染高风险的主要原因。
IBD 患者并发艰难梭菌感染会导致住院时间延长以及结肠切除率和死亡率增加。鉴于这种情况可能会危及生命的并发症,建议在 IBD 发作期间和早期治疗干预期间筛查艰难梭菌。
艰难梭菌的选择较高毒力、抗生素耐药性和反复感染率增加的菌株使得IBD 中艰难梭菌感染的治疗更具挑战性。因此,建议采用个体化治疗方法来控制IBD 发作期间的艰难梭菌感染。
★
声明 B1
适合 IBD 实验性 FMT 的供体应接受血液和粪便检测,测试符合目前通过 FMT 治疗艰难梭菌感染的国家和国际指南,并且一般用于临床实践。
评论:
以 FMT 为目的的供体筛查的主要原则是避免潜在的传染病传播。用于筛查艰难梭菌感染 FMT 的指定血液和粪便参数已在溃疡性结肠炎患者的多项随机对照试验中被证明是安全的。应提供包含待测试的强制性国际参数的列表,而其他参数则应取决于地理区域(例如,热带地区)、患者的医疗状况或捐赠者的病史(例如,粪便钙卫蛋白增加史)。
除了血液和粪便检测外,还应通过多项调查问卷监测总体健康状况、饮食和心理状态,以避免任何潜在的非传染性不良事件。
声明 B2
粪便捐赠应该是自愿的,并且应告知捐赠者捐赠的潜在风险和/或好处。此外,每位患者必须提供书面知情同意书。
评论:
由于粪便采集程序是非侵入性的,并且可以在不受控制的环境中进行,因此不应允许捐赠者直接从粪便捐赠中受益,以避免样本欺诈。然而,根据国家规定,捐赠者可以获得时间和旅行费用的补偿。此外,捐赠者应了解捐赠的风险和益处,因为筛查过程可能会发现以前未知的疾病(例如艾滋病毒、结直肠癌)的诊断结果或其他疾病的易感性(例如与微生物群改变相关的疾病) 。此外,捐赠者应该知道他们可以随时撤回同意。
声明 B3
可以通过粪便库对供体进行管理,以供实验使用,符合适用于艰难梭菌感染的国家和国际指南和法规,并且一般用于临床实践。
评论:
粪便库能够以标准化方式处理粪便捐赠,这适合 IBD 的进一步临床和实验程序。在粪便库中,捐献者在给患者施用粪便之前经过严格筛选,FMT 制备是标准化的,与临床环境相比,制备 FMT 样本所需的成本和时间都可能减少。此外,粪便库拥有专业知识,因此总体上可能有助于优化 FMT 样本的质量。最后,粪便库可以为无法提供此项服务的 IBD 中心提供 FMT 样本。
声明 B4
捐赠者的粪便最好在粪便库现场或进行实验程序的地点收集,遵循国家和国际指南和法规。
评论:
捐赠者应收到有关如何收集粪便的明确说明,最好是在现场或粪便库收集。如果无法做到这一点,收集的粪便应储存在 4°C 下,并在收集后 6 小时内运送到临床地点或粪便库,由经过培训的人员进行处理。
声明 B5
根据实验方案,每个捐赠者都可以参与捐赠不同的 FMT 制剂。
评论:
供体粪便可用于制备不同的 FMT 制剂(例如,新鲜样品与冷冻样品,以及每个制剂的单个供体与多个供体)。到目前为止,建议使用冷冻 FMT 样品而不是新鲜制剂,主要是因为安全性。冷冻 FMT 样本可以被隔离,直到捐赠期结束时完成全面的捐赠者筛查。对于新鲜的 FMT,在完成完整的筛选过程之前对材料进行管理。因此,对于新鲜的 FMT,建议进行更定期的供体常规筛查和菌群评估。
声明 B6
应根据国家和国际准则和法规维护和存储捐助者信息登记册。
评论:
与 FMT 流程相关的捐赠者信息登记应由国家和国际医疗保健机构监管。来自捐赠者和接受者的信息应保存至少 10 年,或符合国家和国际法规。这些数据应提供给粪便库以获得长期安全数据。
声明 B7
患者不应直接使用粪便库来治疗 IBD。FMT 样本的提供应始终在治疗医疗保健提供者的指导下进行,并符合国家和国际指南和法规。
评论:
粪便库的使用应仅限于医疗保健提供者,因为 FMT 管理需要记录和适当的后续行动,以应对任何潜在的不良事件,而这些不良事件只能在医生的监督下安全地发生。因此,患者直接使用粪便库是不合适的。
声明 B8
FMT 的整个过程(从捐赠者筛选到粪便收集和 FMT 样本管理)应具有清晰的可追溯性。因此,应保留每个 FMT 样品的等分试样以进行测试,以防发生意外的不良事件。
评论:
FMT 过程的所有步骤都应进行登记,捐赠者样本的等分试样应保留并储存在 -80°C 下,以便在发生任何意外不良事件(例如病原体感染)时进行回溯。
据报道,FMT 后出现耐药大肠杆菌传播,这表明保留供体粪便以便在可能的不良事件发生后进行进一步分析的重要性,并保证在此类情况下及时干预。
声明 B9
关于供体 FMT 制备技术方面的共同协议,将有助于在全球范围内提供程序标准化和优化,从而促进结果的解释。
评论:
尽管研究设计不同,FMT 已显示出有希望的结果,尤其是在溃疡性结肠炎中。方案的变化包括不同的 FMT 输注途径(例如,鼻十二指肠、直肠、口服)、给药频率、对照安慰剂(例如,水、自体粪便材料)和终点测量。关于冷冻粪便材料制备、储存和给药量的剂量标准化将有助于未来 FMT 研究的解释和比较,包括结果。
声明 B10
需要进行研究,来确定与粪菌移植作为治疗炎症性肠病选择的临床疗效和整体治疗效果更好相关联的供体特征。
评论:
必须进行研究来确定供体标志物,以实现 FMT 在 IBD 中的最佳治疗效果和总体成功。因此,应该对微生物群、饮食模式(问卷)和其他方面(如药物使用、家族病史、心理状态和遗传背景)进行表征,以确定改善临床结果的潜在趋势。除了特定的供体标记外,还应该研究供体-受体的植入情况。
★
声明 C1
以前进行的随机对照试验一般规模较小,且方法学上存在异质性;因此,目前还不能得出明确的结论。
评论:
在成功用于治疗艰难梭菌感染后,FMT 也在溃疡性结肠炎患者中进行了研究,首先是在非随机研究中,然后在随机对照试验中,均取得了有希望的结果,尽管存在FMT 程序和测量结果存在显着差异。事实上,尽管这些研究和随后的荟萃分析强调供体 FMT 施用后令人满意的缓解率,已发表和/或可用的随机临床试验通常规模较小且方法学上异质,因为它们在粪便输注的时间、数量和途径、FMT 供体粪便与对照(假冒)的特征方面存在差异,使得结果难以从整体上解释结果,无法得出明确的结论。
声明 C2
对于患有IBD的轻度和重度复发或难治性难免性艰难梭菌感染,建议采用FMT作为治疗选择。
评论:
FMT 对于治疗无 IBD 患者的复发性艰难梭菌感染有效, 以及患有溃疡性结肠炎和克罗恩病的患者。然而,针对溃疡性结肠炎患者的研究报告称,单剂量 FMT 无法预防溃疡性结肠炎发作。没有足够的证据推荐 FMT 作为IBD首次艰难梭菌感染的治疗方法。
声明C3
FMT 可有效诱导轻度至中度溃疡性结肠炎的缓解;然而,没有足够的证据推荐 FMT 作为常规临床实践中溃疡性结肠炎的治疗方法,其使用通常应仅限于研究环境。
评论:
迄今为止,FMT 在诱导轻度至中度溃疡性结肠炎患者缓解方面显示出有希望的结果。然而,这些研究是在溃疡性结肠炎患者队列中进行的,样本量相对较小,而且研究设计之间存在差异,使得研究之间的比较难以协调。因此,没有足够的数据支持临床常规使用 FMT 来诱导溃疡性结肠炎患者缓解。但专家们一致认为,FMT可在特定情况下使用,应具体情况具体考虑,并与有关各方详细讨论。
声明C4
随机对照试验表明,在 FMT 后获得缓解的溃疡性结肠炎患者通常在 FMT 治疗后不会持续缓解超过 1 年。
评论:
溃疡性结肠炎中的 FMT 研究缺乏有关治疗效果和持久性的长期随访数据。因此,需要对治疗后的时间进行更持续的疾病监测随访。现有数据表明,复发是可能的,为了实现长期疗效,维持治疗可能是强制性的。然而,诱导治疗和维持治疗的输注次数和剂量均应进一步研究。
声明C5
反复输注和供体-受体移植可能对于 FMT 治疗溃疡性结肠炎的成功非常重要。
评论:
来自对溃疡性结肠炎进行 FMT 的现有随机对照试验的数据表明,重复输注很重要;然而,目前对于 FMT 成功所需的最少管理次数尚未达成共识。此外,FMT 在溃疡性结肠炎中的疗效似乎也依赖于受体,表明供体-受体移植至关重要。除了鉴定对 FMT 成功可能重要的供体标记外,还应研究受体标记及其与供体粪便物质/粪便抗原相互作用的重要性。
声明C6
FMT 后肠道微生物组组成多样性的增加,可能是 溃疡性结肠炎反应的标志。
评论:
除了临床和内镜缓解等临床结果外,还应评估微生物标志物,包括微生物组多样性的改变(即增加),并将其与未来研究中 FMT 的成功或失败相关联。这些标记物可用于预测患者的反应,这有可能实现精准医疗方法的个性化治疗。
声明C7
现有数据表明,FMT 对于轻度至中度溃疡性结肠炎诱导缓解的风险较低;然而,在使用 FMT 治疗 IBD 时已有严重不良事件的报道,包括疾病恶化。
评论:
已进行的随机对照试验中对患者安全性的评估显示出良好的结果,不良事件非常有限,其中大部分与给药方式有关。一般来说,鼻十二指肠给药比直肠给药灌肠产生的不良事件相对较多;因此,后者已被普遍认为是更安全的递送途径。然而,迄今为止,尚缺乏溃疡性结肠炎患者的长期 FMT 安全性数据。
事实上,在随机对照试验中,在有限数量的患者(<10%)中观察到了严重的不良事件。这些包括当通过上消化道给药进行 FMT 时误吸和疑似小肠穿孔。与 FMT 手术相关的最常见的严重不良事件是疾病恶化,需要住院治疗,在少数情况下需要结肠切除术。
在 Costello等人的试验中,观察到 43 名接受自体 FMT 的患者中有 2 名病情恶化,而 38 名接受捐赠者 FMT 的患者中有 1 名病情恶化。
在 Moayyedi 的试验中,38 名患者中有 2 名出现斑片状炎症和脓肿。其他显着的严重不良事件包括肺炎、艰难梭菌感染或其他形式的小肠结肠炎。
声明C8
随机对照试验尚未证明 FMT 和对照组在疾病恶化或轻微或严重不良事件引起的症状方面存在显着差异。
评论:
溃疡性结肠炎中的 FMT 试验对不良事件进行了评论;然而,由于对照组和治疗组之间没有发现显着差异,因此这些不良事件被认为是给药程序的结果,而不是加工后的供体粪便材料本身。
声明 C9
溃疡性结肠炎中 FMT 后,常见的不良事件是短暂的轻微胃肠道症状,如腹胀、腹泻和肠胃气胀。
评论:
FMT 试验中高达 83% 的患者观察到轻微不良事件,包括胃肠道症状,如短暂性腹泻、肠鸣、腹痛、腹胀和肠胃气胀。也有短暂发烧的报道。大多数不良事件在手术后几天内自然消失。
声明 C10
在临床实践中,没有足够的证据推荐 FMT 作为克罗恩病的治疗方法。迄今为止,其使用应仅限于研究环境。
评论:
克罗恩病中 FMT 的可用数据非常有限,主要包括病例报告和试点研究,而不是大型随机对照试验。这些研究显示不良事件,主要包括胃肠道症状,疾病发作报告为与 FMT 相关的严重不良事件。
Vermeire等人的一项初步研究显示,六名难治性 克罗恩病患者在 FMT 后第 8 周没有差异。
在评估 FMT 在维持克罗恩病缓解方面的效果时,Sokol等人报告称,与假手术组相比,FMT 组的急性发作发生率没有显着降低。
进一步的研究应包括优化该患者群体的缓解诱导和维持。大型随机对照试验必须推荐 FMT 作为克罗恩病患者的可行治疗方法。
声明 C11
在临床实践中,没有足够的证据推荐 FMT 作为贮袋炎(Pouchitis)的治疗方法。迄今为止,其使用应仅限于研究环境。
注:贮袋炎(Pouchitis)是保留肛门的大肠全切除术(或次全切除术)术后发生在患者回肠贮袋的非特异性炎症,是溃疡性结肠炎行回肠贮袋-肛管吻合术后最为常见的并发症。
本病病因不明。大约有1/3的患者在术后5年内可能出现这种难以解释的炎症,其中2/3的患者有复发的可能性。
评论:
据信,患有贮袋炎的患者也会出现菌群失调。目前,只有有限的研究使用 FMT 来治疗贮袋炎。然而,在已发表的文献和病例报告中,该手术大多被报道是安全的,但并不有效。
与溃疡性结肠炎中 FMT 的随机对照试验类似,所进行的研究也具有异质性,并评估了不同的结果测量。因此,需要进一步研究和优化方案来确定 FMT 在贮袋炎中的潜在用途。
声明 C12
关于 FMT 在克罗恩病和贮袋炎中的安全性数据不足。
评论:
基于缺乏大型随机对照试验和长期随访数据,目前无法得出FMT治疗克罗恩病和储袋炎的安全性结论。
声明 C13
需要进一步的研究来确定 FMT 在克罗恩病和贮袋炎中的有效性和安全性。
评论:
需要对克罗恩病和储袋炎的 FMT 进行进一步研究和优化,以评估疗效并生成(长期)安全性数据,以便将 FMT 引入临床环境。
★
展望D1
未来的研究需要确定精准的 FMT 供体和受体用于治疗 IBD 的最佳特征。
评论:
FMT 已被证明是一种有前景的溃疡性结肠炎治疗策略。然而,有效率似乎受到供体特异性、受体特异性和手术特异性特征的影响。此外,供体-患者移植获得了更多支持,有利于确定通用的“超级供体”。因此,需要进一步的研究来定义理想的患者和捐赠者特征及其最佳移植。
展望D2
有必要进行对照FMT试验,以优化IBD特定表型的疗效。
评论:
未来的研究在考虑 IBD 中 FMT 的结果时应考虑严格定义的患者表型。这些研究有可能确定 FMT 给药后与阳性反应或缺乏反应相关的特定表型。
展望D3
需要确定预测 IBD 中 FMT 反应的生物标志物。
评论:
除了确定供体和受体以及患者表型可能的最佳特征外,还需要确定免疫学和微生物生物标志物来预测对治疗的反应,以避免因 FMT 治疗无反应而造成时间、成本和不良事件的损失。
此类生物标志物可以通过 16S rRNA 扩增子测序、鸟枪法宏基因组测序、蛋白质组学和/或转录组分析来检测。通过识别此类生物标志物,有可能为 IBD 的 FMT 治疗设计更有针对性的策略,从而朝着更加精确、个性化的医疗方法发展。
展望D4
未来的研究需要确定基于 FMT 的 IBD 治疗的最佳配方和给药途径。
评论:
提高 FMT 功效的最佳剂量尚未确定。迄今为止,鼻十二指肠管输送以及通过结肠镜检查或直肠灌肠进行 FMT 输注已成为 IBD 研究最多的给药途径。
然而,最近的一项研究利用含有冻干粪便微生物群的口服胶囊作为其递送系统。这种给药途径侵入性较小,因此可能更受患者青睐。需要更多的随机对照试验来优化剂量和给药途径。
展望D5
需要进行研究来积累有关使用补充策略来提高 FMT 疗效的循证信息。
评论:
通过 FMT 调节肠道微生物组成的成功率可以通过补充策略来提高,例如捐赠者和接受者的支持性抗炎饮食, 通过优化FMT前的肠道准备,也可以通过抗生素预处理。如益生菌、益生元、合生元和后生元补充。
扩展阅读:
展望 D6
需要进行研究来评估 FMT 作为 IBD 的独立治疗方法或与当前可用的治疗方式相结合的作用。
评论:
除了评估补充策略(D5)之外,还需要进一步研究 FMT 与目前使用的 IBD 联合疗法(从皮质类固醇到生物制剂和 JAK 抑制剂)的组合。
这种针对免疫反应和肠道微生物组成的组合方法可能比单独的每种策略带来更高的缓解率。此外,应研究预防发病和/或术后复发,以及 FMT 对癌症治疗的影响,反之亦然。
★
本手稿的作者代表 IBD 各个方面的国际专家组,他们一致认为,在将 FMT 推广为公认的 IBD 治疗策略之前,有必要进行进一步的研究。人们普遍认为 FMT对于 IBD 患者是安全的,特别是对于溃疡性结肠炎患者。
文献中报道的大多数并发症主要与粪便输注的给药途径有关,而不是与感染传播有关。然而,为了避免不良事件的负担,应遵循针对艰难梭菌感染的 FMT 治疗现有的国际指南,来严格筛选捐赠者。
IBD 中的粪便微生物群移植 (FMT) 途径:从健康供体到恢复疾病患者的肠道微生物群
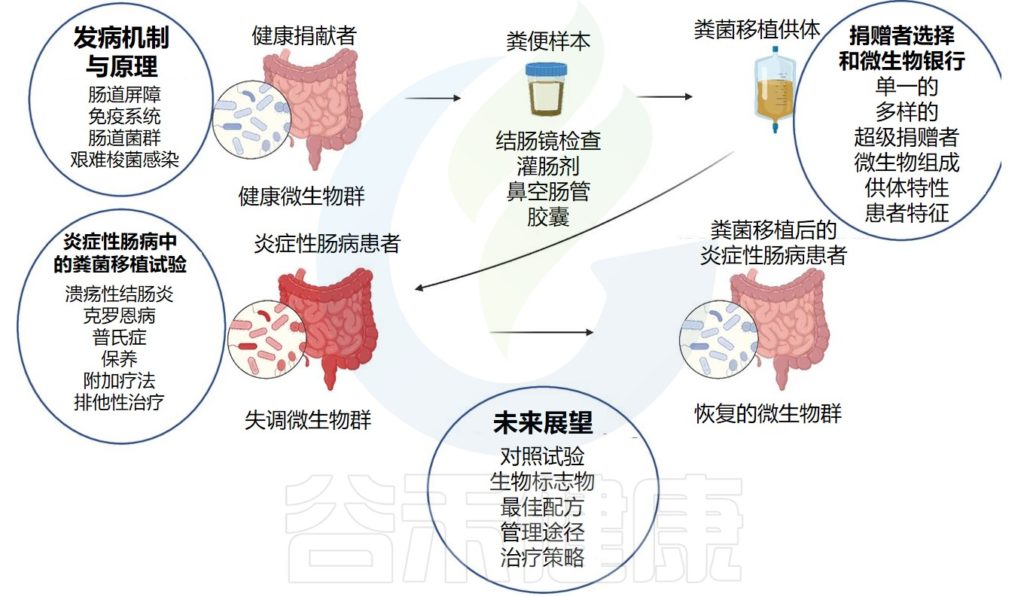
doi: 10.1136/gutjnl-2023-329948.
应投入粪便库以促进FMT研究,并应考虑通过实施永久捐赠者登记、通过微生物群特征和捐赠者健康状况筛选捐赠者粪便材料以及优化捐赠者粪便材料、粪便样本的储存,来治疗IBD的可能性。
粪便库应登记所有捐献者和患者数据,以便有效追踪并监测 FMT 施用后健康状况的变化(例如缓解/发作、心理状态)。
已经进行了几项 FMT 试点研究和随机对照试验来治疗 IBD,但使用的是异质研究设计。现有的结果,特别是在溃疡性结肠炎方面,是有希望的,但似乎依赖于供体和患者。然而,要将 FMT 纳入日常胃肠道实践中,还需要进一步研究来优化短期和长期成功率,并进一步评估安全性。
该方法应确定:最佳给药途径、剂量、频率、供体-受体植入、患者表型,以及 FMT 反应的免疫学和微生物组生物标志物的识别。
总而言之,这样将有助于 FMT 的标准化及其治疗溃疡性结肠炎的临床应用。对于克罗恩病和储袋炎,必须进行进一步的研究来评估其使用的(长期)安全性和有效性。尽管如此,这一系列研究可能会从优化其在溃疡性结肠炎中的使用所采取的措施中受益匪浅。
未来的工作包括对供体微生物群进行严格表征,以及调查 FMT 前后对 IBD 接受者的影响,这可用于最大限度地提高 FMT 功效并阐明作用机制。
通过研究供者和受者的支持性饮食、肠道准备、抗生素预处理、益生菌、益生元、合生元和生元后支持,以及与 IBD 治疗同时进行的联合治疗,进一步提高 FMT 的疗效至关重要。此外,识别与 FMT 成功预测相关的特定微生物菌株,可能会开发出明确的单菌株或多菌株益生菌。
参考文献:
Dini-Andreote F, Custer GF. Ecological principles of fecal microbiota transplantation. Trends Microbiol. 2023 Jun 8:S0966-842X(23)00162-2.
Lopetuso LR, Deleu S, Godny L, Petito V, Puca P, Facciotti F, Sokol H, Ianiro G, Masucci L, Abreu M, Dotan I, Costello SP, Hart A, Iqbal TH, Paramsothy S, Sanguinetti M, Danese S, Tilg H, Cominelli F, Pizarro TT, Armuzzi A, Cammarota G, Gasbarrini A, Vermeire S, Scaldaferri F. The first international Rome consensus conference on gut microbiota and faecal microbiota transplantation in inflammatory bowel disease. Gut. 2023 Jun 20:gutjnl-2023-329948.

谷禾健康

维生素C是一种广泛存在于自然界中的水溶性维生素。维生素C在人体新陈代谢中具有多种重要功能,包括抗氧化、参与胶原蛋白合成、增强铁的吸收等。由于其众多生理益处,维生素C被广泛地应用于修复伤口、治疗感冒、癌症等多种疾病。
人体无法自行合成维生素C,需要从膳食来源(如水果、蔬菜)中获取。维生素C的代谢过程涉及多个酶和转运蛋白。肠道微生物群可能通过影响这些酶和蛋白的活性或表达,来影响维生素C的代谢吸收过程。
维生素C也可以直接调节肠道微生物群,或通过修复肠道屏障、改变氧化还原电位等方式间接对肠道微生物群的平衡起到调节作用。
个体之间的差异、饮食习惯和生活方式等因素各不相同,这些都可能对维生素C与肠道菌群的相互作用产生影响。
本文将从维生素C的结构、功能、吸收和代谢、与肠道菌群的关联等多角度,全面探讨维生素C的作用及其对人体健康的影响,同时介绍了一些维生素C的食物来源、人体需要的剂量、如何补充、注意事项等。
▼
本文主要内容:

编辑
维生素C,也称为抗坏血酸,是一种水溶性维生素,对人体健康非常重要。它在许多身体功能中起着关键作用,包括增强免疫力、抗氧化、胶原蛋白的合成等。
▼
维生素C的化学名称是L-抗坏血酸,它是一种有机化合物。无臭,味酸,易溶于水,微溶于乙醇,不溶于乙醚。
维生素C结构简单,化学式为C6H8O6:
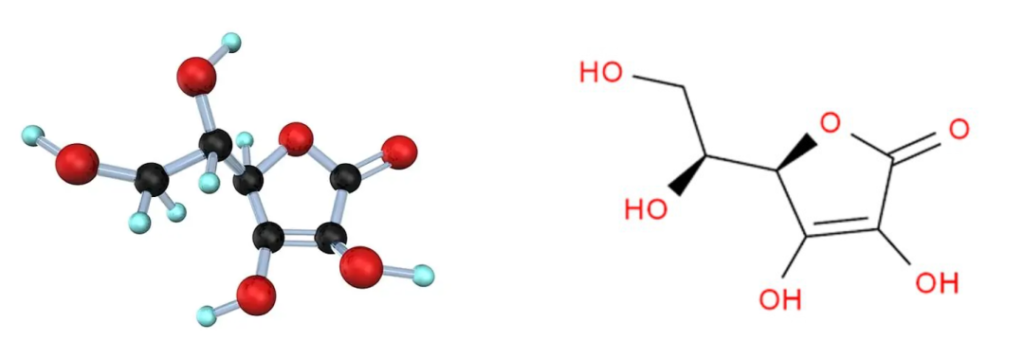
这种结构使维生素C具有抗氧化性质,能够捕捉自由基,并保护细胞免受氧化损伤。
注:体内的分子暴露于环境污染物、吸烟和慢性炎症等情况时,它们会变成自由基。自由基是不稳定的分子,会破坏细胞并导致疾病,维生素C可以通过中和自由基来减缓或预防某些健康问题。
由于其与葡萄糖的结构相似,维生素C可以在许多化学反应中取代葡萄糖,并且可以防止蛋白质的非酶糖基化。
▼
维生素C参与胶原蛋白、激素、肉碱的合成,促进铁离子的吸收,此外,它在免疫系统的功能和调节中发挥着重要作用,对维持内部环境的平衡和中枢神经系统的正常功能极为重要。
维生素C的大部分功能是由于其作为抗氧化剂和辅助因子的能力。由于人类缺乏L-gulono-1, 4-lactone氧化酶,无法自行合成维生素C,因此完全依赖于维生素C的饮食摄入。
▼
从食物中获取营养总是最好的。大约90%的日常需求来自蔬菜和水果,它们是这种维生素的极好来源,例如奇异果、橙子、芒果、草莓、红椒、青椒等。
一些维生素C含量较高的食物

注:单位“杯”是一个常见的非正式计量单位,美规和英规略有区别,大约是237毫升-250毫升左右,涉及到果蔬的份量时,一杯通常是指将果蔬切碎后填满一杯容器的量。
▼
维生素 C 对大脑健康非常重要。大脑在长期缺乏维生素 C 的情况下以牺牲其他组织为代价来保留维生素 C,并且可以维持比其他器官(例如肝脏和肾脏)高很多倍的浓度,如下图。
维生素C的分布在身体各器官之间差异很大
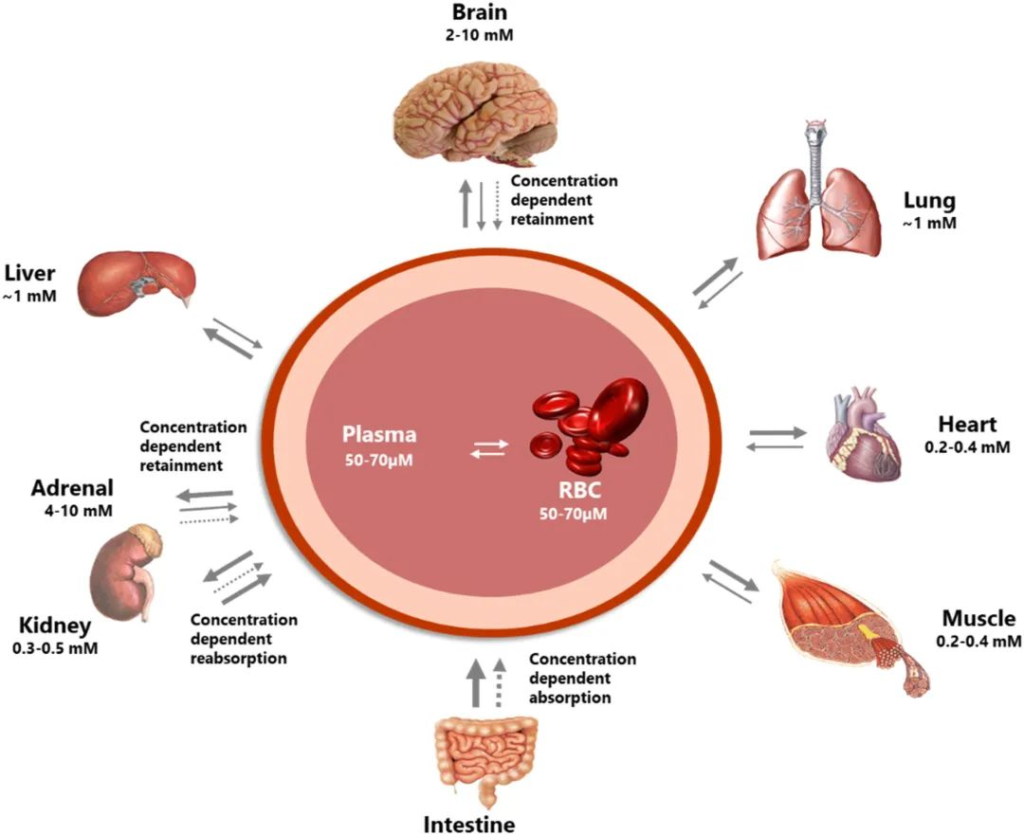
doi.org/10.1016/j.redox.2020.101532
维生素C供应不足时,首先保证大脑里的浓度,那么维生素C对于大脑而言有什么作用?
▼
维生素 C 对胶原蛋白的稳定作用对于形成整个身体的结缔组织框架至关重要;包括皮肤、骨骼、软骨、肌腱、韧带、血管等。
胶原蛋白生产的最后步骤取决于维生素 C,维生素 C 在前胶原脯氨酰和赖氨酰残基的羟基化中充当电子供体。
▼
维生素 C 可增强其他营养素的生物利用度,例如维生素 E 和非血红素铁,这可能会增强含维生素 C 的食物的健康效果。
维生素C经常添加到含铁的口服制剂中,以增加铁的吸收。
▼
维生素 C 是否可以预防或减轻包括普通感冒在内的感染的严重程度是一个有争议的话题。大多数证据都支持其好处。
▼
维生素C对正常骨骼发育至关重要。维生素C水平与骨骼健康之间存在正相关关系,如骨密度、骨折概率、骨转换标志物等。
▼
维生素 C 有助于维持健康的皮肤。
▼
肺部的维生素C水平是血液中的30倍。
维生素C在抵御氧化剂的同时也会被消耗,这表明即使是单剂量的维生素C,也能有效抵御肺部氧化应激的急性增加。
▼
根据现有证据,摄入足够的维生素 C 可能有助于保持健康的情绪。
焦虑
抑郁
▼
人类慢性低维生素 C 状态与神经退行性疾病有关。但是,尚未确定因果关系。
▼
维生素 C 可以通过抑制炎性细胞因子来减轻炎症。
▼
除上述主要的功能之外,在部分小型研究中提到的关于维生素C的功能如下:
助孕育:
助减肥:
降血压、防中风:
降血糖:
助排毒:
助抗癌:
牙周健康:
水溶性维生素在人体内储存较少,从肠道吸收后进入人体的多余的水溶性维生素大多从尿中排出。因此,摄入较多的水溶性维生素一般不会引起中毒现象,但是若摄入量过少,则会很快出现缺乏症状。
▼
刚缺乏的时候症状不明显,饮食中缺乏VC需要大约一个月的时间才会出现症状。
体内维生素C总含量低于300-400mg会出现明显症状。
维生素C的缺乏会出现什么症状?
由于维生素C功能的复杂性及其被不同还原剂的部分替代性,维生素C与坏血病症状的直接联系不容易确定。
如果发展为坏血病,典型症状是:
肌肉无力、牙龈肿胀和出血、牙齿脱落、瘀点出血、自发性瘀斑、贫血、愈合障碍、角化过度、虚弱、肌痛、关节痛和体重减轻(也可能因肿胀而出现矛盾的体重增加),而早期表现包括嗜睡、倦怠、易激惹,甚至呼吸困难等。
在生化上,维生素C血浆水平低于11μM被认为与坏血病的临床症状一致。
在专业医疗人员的指导下,补充维生素C可以轻松有效地逆转坏血病。许多症状可以在几周内轻松解决。富含维生素C的饮食将防止坏血病的发展。
什么人群更容易发生维生素C缺乏?
▼
NIH 认为,成人可耐受的上限是每天 2000 毫克,仅仅靠含有维生素 C 的食物几乎不可能达到这一上限,所以食物可以放心吃。服用补充剂则需注意剂量,可能存在过量的风险。
更高的剂量更有可能导致副作用。
维生素C过量可能会出现什么症状?
单次口服5-10克维生素C会产生短暂的渗透性腹泻和/或腹胀伴疼痛,不建议这样做。
随食物一起摄入可减少这些不良反应。
每天超过 2000 毫克的剂量可能会增加腹泻和肾结石的风险。如果有肾结石病史,每天摄入超过 1000 毫克可能会增加患结石的几率。
那么到底应该怎么补充?每日摄取多少维生素C 合适呢?
▼
科学界对维生素C的最佳剂量方案(摄入量和频率)最健康存在持续争论。
对于大多数健康人来说,通过食物可以获得足量的维生素 C。
维生素C摄入量标准在不同地区有所不同:
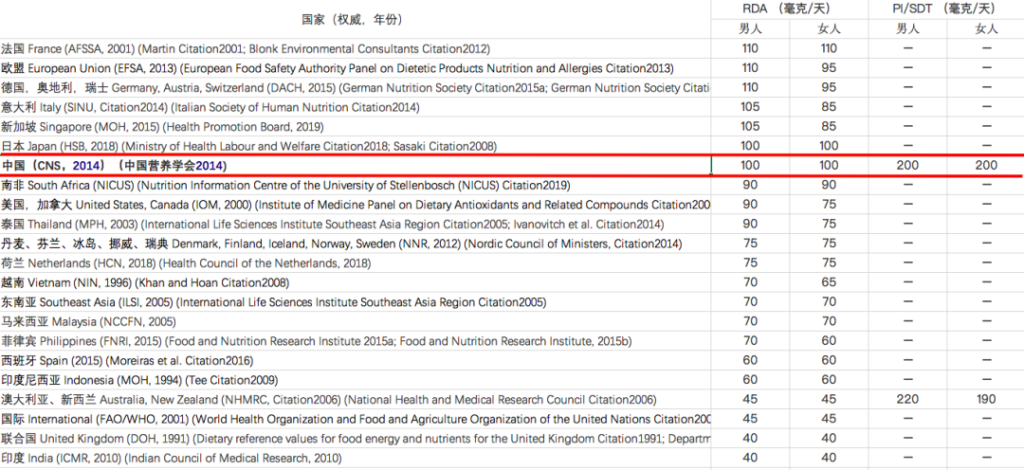
注:RDA – 推荐膳食摄入量,
PI – 建议摄入量,SDT – 建议膳食目标
在中国营养学会编著的《中国居民膳食指南》2022版中对维生素C的推荐摄入量:
中国居民膳食指南2022版
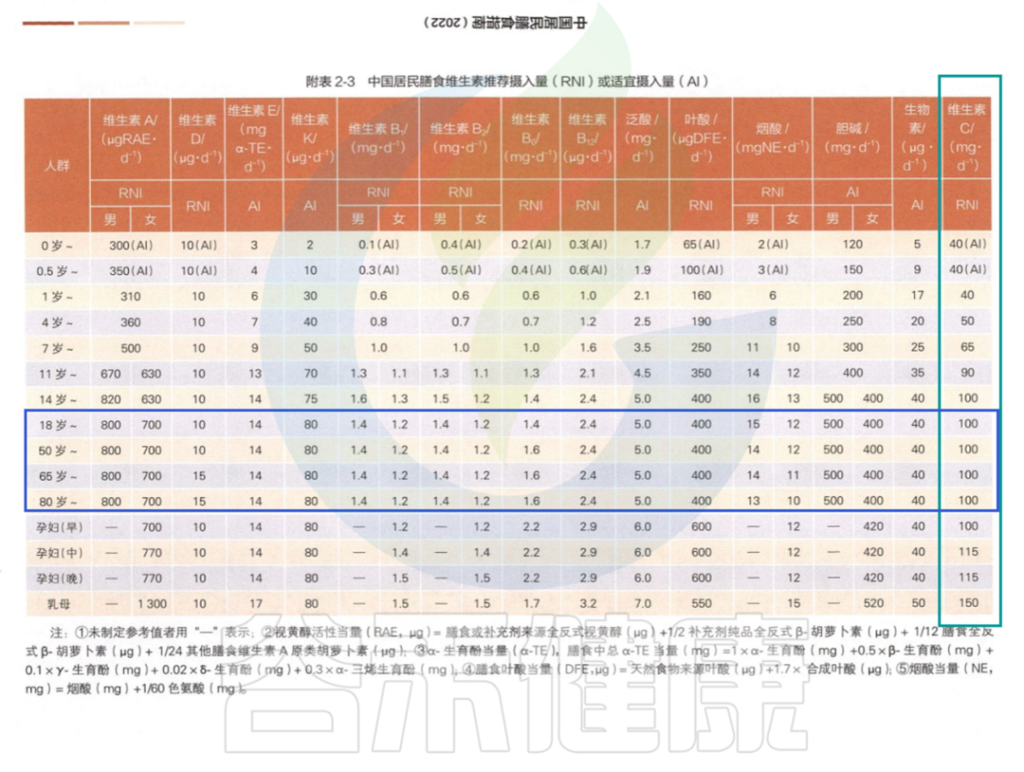
为什么不同地区的标准不一样呢?
这主要是由于RDA标准的基本前提从预防坏血病(~45 mg/d)至健康优化(~200 mg/d)。许多权威机构建议使用最低量的维生素C,但这可能无法满足不同亚群的健康需求。
例如,吸烟者和肥胖者比普通人群有更高的要求。一些国家的吸烟率继续上升,有证据表明,吸烟者每天至少摄入200 mg的维生素C。
随着全球肥胖率的增加,以及与肥胖相关的合并症,如代谢综合征、糖尿病和心血管疾病,需要更多地考虑适当的建议,以优化快速增加的亚健康人群中的维生素C状态。
以上是维生素C的摄入量标准,具体该如何补充,应该注意什么?详见下一章节。
▼
食物:如何才能最大程度地保留其维生素C?
——烹饪方式
长时间烹饪,特别是用大量水煮沸会导致维生素C浸出到水中,显著降低食物中的维生素C含量。
在少量水中蒸或煮,且持续时间较短,是保存维生素C的更温和的方法。
即使将所有外部因素消除到最低限度,也会发生损失,因为由于抗坏血酸氧化酶的存在,材料内部会发生氧化反应。因此,理想的加工方法是用最少量的水快速热灭活酶,然后快速冷却。
——长期保存条件
温度对储存稳定性也有很大影响。随着温度的升高,会出现更显著的损失。然而,在长期储存期间,即使维持短期储存期间仅发生少量损失的条件,维生素C的量也会显著减少。
损失主要是由于酶催化的氧化反应,其程度尤其取决于pH、材料完整性和温度。
总之,为了使水果和蔬菜的维生素C含量保持更长时间,最温和的方法是深度冷冻。
补充剂:一天中分几次服用
食物和许多补充剂中的维生素 C 是一种抗坏血酸的形式。
当肠道面临较低水平的抗坏血酸(即低于约 400 毫克)时,主动运输系统会吸收维生素 C(即,将营养物质通过肠道并进入血液,到身体需要的地方)。
一旦这些主动运输变得不堪重负,被动扩散就会接管吸收其余的维生素 C(这是一个相当低效的过程)。吸收并不像听起来那么容易,事实上抗坏血酸有吸收上限。
身体一次可以处理大约 300 – 400 毫克的纯抗坏血酸形式的维生素 C,更多量一下子难吸收。
所以如果能记得的话,一天中分几次服用比较合适。
▼
维生素C补充剂并非适合所有人。如果遇到以下任何情况,请首先与医生联系:
也不要认为维生素C服用越多越好,每天服用 1000 毫克或更多,实际上会使吸收率降低约 50%。
▼
维生素C可以增加某些药物的吸收,例如:
服用维生素C可以增加含铝药物(如磷酸盐粘合剂)对铝的吸收。这可能对有肾脏问题的人有害。抗酸剂中含铝:不要同时服用维生素C和抗酸剂。服用维生素C后至少等待两个小时,然后再服用抗酸剂。服用抗酸剂后等待四个小时服用维生素C。
维生素C可能会增加左旋甲状腺素的吸收。
补充维生素C会降低一些药物的疗效:
口服维生素C可能会降低这些抗病毒药物的作用。
当与维生素C一起服用时,烟酸和他汀类药物的影响可能会降低,这可能有益于高胆固醇的人。
高剂量的维生素C可能会降低人体对这种抗凝剂的反应。
其他还包括:
维生素C增加或减少药物副作用的风险
如果服用雌激素或基于雌激素的避孕药,维生素C可能会增加激素副作用的风险。这是因为维生素C可能会减缓雌激素离开身体的速度。
一些早期的研究认为, 维生素C可能有助于预防阿司匹林和非甾体抗炎药引起的胃部不适。
▼
维生素 C 和益生菌对肠道健康和免疫力有不同的好处,它们可以很好地互补,这意味着它们可以安全地一起服用。
一项针对学龄前儿童的双盲、随机、安慰剂对照初步研究中,发现益生菌与维生素 C 联合预防呼吸道感染的功效(URTI;33%,P =0.002)。
Lab4 益生菌和维生素 C 组合补充 6 个月的儿童显示,上呼吸道感染症状的发生率和持续时间有所减少,降低感染的严重程度。
注:Lab4 益生菌包含:嗜酸乳杆菌CUL21(NCIMB 30156)和CUL60(NCIMM 30157),双歧杆菌CUL20(NCIMB 30153)和动物双歧杆菌乳亚种CUL34(NCIMM 30172)。
注意:根据说明书剂量服用或遵医嘱。
以上并不是维生素C可能发生的相互作用的完整列表。在开始补充维生素C或调整摄入量之前,请与医生或药剂师沟通,让医生知道你正在服用的所有药物,包括处方药和非处方药、其他维生素或微量营养素、草药补充剂等。
▼
静脉注射和口服给药,这两者可能具有不同的药代动力学特征。
药理学模型显示,口服维生素C,即使是在非常大和频繁的剂量下,也只能适度地增加血浆浓度,从0.07 mM增加到最大0.22 mM。
而静脉注射剂量预计会导致血浆维生素C峰值水平比口服剂量高60倍以上,尿液浓度比口服剂量低140倍。
分子的实际生物利用度由许多因素控制,包括肠道和其他组织的吸收、肾脏的吸收和排泄以及其他患者特异性因素。
除了通过静脉给药和口服给药的浓度差异外,口服给药将维生素C直接输送到肠道微生物组,而不是通过血液;因此,它对肠道微生物的影响可能与动力学和浓度有关,这与影响血浆水平的动力学和浓度完全不同。
静脉注射维生素C常用于临床医疗环境中,用于治疗某些疾病或特殊情况下的高剂量补充,如感染、外伤、手术恢复等。专业医生会给予相应的建议。
口服给药适用于一般的日常维生素C补充,维持正常的维生素C水平。
有几种方法可以评估人体中的维生素C状态。这些包括测量血浆、尿液、组织、粪便中维生素 C 的浓度。
▼
检测血浆维生素C,血浆样品中维生素C的定量测定常见的有两种方法:酶法和色谱法。
酶促维生素C测定
有几种基于维生素C的酶促转化的商业试剂盒,产生可以用光光谱法检测的信号。通常,抗坏血酸氧化酶用于这种类型的测定。这些测定的常见方法是酶联免疫吸附测定(ELISA),它非常适合分批处理样品,但不太方便立即测定少数样品中的值。
根据欧洲外部质量评估计划(Instand EQAS)中报告的方法,基于酶的分析方法在医院中并不常规使用。如果临床对立即测定维生素C的需求增加,由于其直接的技术性质,这些基于酶的测定可用于护理点或集中平台。
色谱法测定维生素C
抗坏血酸和DHA的定量测量目前是通过高效液相色谱(HPLC)方法进行的。如果必须分析具有相似性质的多种化合物,或者如果存在许多可能干扰感兴趣化合物定量的物质,则HPLC方法是优越的。
将酸化样品注射到HPLC仪器中后,通过通过基于化合物的物理性质不同地保留化合物的柱来分离化合物。结果,在分离柱的末端,可以选择性地检测抗坏血酸和DHA,而不受其他化合物的干扰。
目前有两种方法可以检测分离后的抗坏血酸和DHA,一种是电化学检测,另一种是紫外线检测。这两种检测方法给出的结果相同,但由于相对技术简单,紫外线检测更广泛地用于日常检测。
其他检测技术,如荧光检测,需要在柱前对抗坏血酸和DHA进行化学改性,但使用较少。比色/荧光法可能会产生更高的DHA浓度,因为该方法缺乏特异性。
▼
可以查看近期体内维生素状况。
肠道菌群可以影响食物中的营养物质的吸收和利用。肠道菌群的失调可能会影响维生素C吸收,从而出现维生素C缺乏,引发一系列健康问题。因此,检测肠道菌群的状况,可以帮助我们更好地了解维生素C的吸收和利用情况。
与抽血检测不同,肠道菌群的评估更加反映一段时间 ( 一般2周左右 ) 的长期状态,如部分维生素无法在体内留存,需要每日补充,血液检测波动较大。
肠道菌群与维生素C的水平之间存在怎样的关联?
为什么肠道菌群检测报告可以了解维生素情况?
我们来看下一章节。
我们在日常生活会看到,同样吃食物,有些人的维生素吸收状况比较好,有些人就容易缺乏,这是为什么呢?
为什么大剂量补充对一些人的身体有益,而少数人因为过量出现了肾结石呢?
这其实都与肠道微生物群相关。
这里我们分为两个方面来讨论:
一个是肠道微生物群对维生素C的影响,
一个是维生素C的补充对肠道微生物群的影响。
维生素C在人体代谢过程中的吸收和利用,与肠道微生物群相关。了解肠道微生物群对维生素C的吸收和利用的影响,可以帮助我们更好地理解其与人体健康之间的关系。
▼
微量营养素使用各种特定的吸收途径和机制,既可以是被动的,也可以是主动的。
膳食维生素 C 很容易通过钠依赖性维生素 C 转运蛋白(SVCT1 和 SVCT2)在肠道中吸收,其他比如维生素A 、维生素D 的吸收通过小肠中的被动扩散发生。
肠道微生物群是人体肠道中的有效生物反应器,可将各种化合物转化为有益或有害的代谢物,因此对其生物利用度起着至关重要的作用。
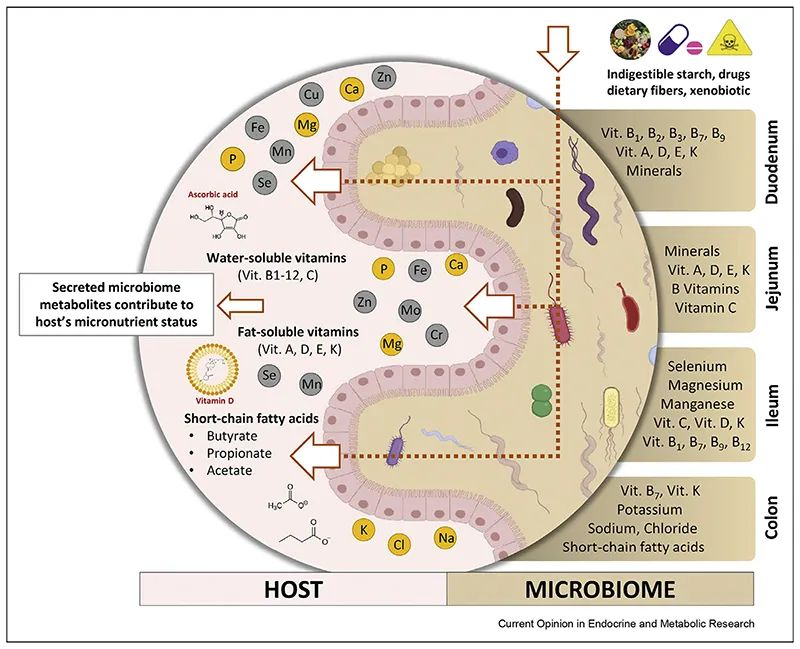
doi: 10.1016/j.coemr.2021.100285
胃肠道各部分理化特性的差异,以及位点特异性受体的存在,使得不同的维生素和矿物质能够沿胃肠道吸收。不同微生物在每个不同部分的定殖会影响当地环境,从而对微量营养素的生物利用度产生积极或消极的影响。
微生物可以干扰维生素C的吸收
微生物可以通过干预生物合成过程和调节吸收,来调节微量营养素的水平,包括维生素C。
来自革兰氏阴性菌的脂多糖降低SVCT-1的表达,进而降低SVCT-1-介导的维生素C的摄取。
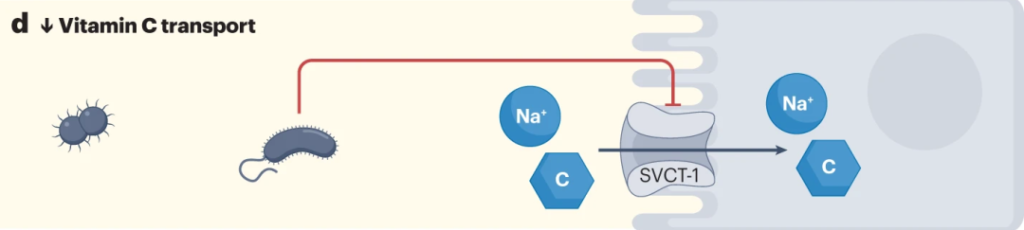
Chmiel JA, et al.,Nat Rev Urol. 2023
大肠杆菌可以通过释放脂多糖来减少宿主对抗坏血酸的摄取,从而增加NF-κB依赖性TNF的产生,其进而通过抑制SLC23A1和SLC23A2启动子(分别编码SVCT1和SVCT2),来降低钠依赖性维生素C转运蛋白SVCT1与SVCT2的表达。从而对维生素C的吸收率产生负面影响。
细菌可以与宿主竞争维生素C
大肠杆菌抗坏血酸转运蛋白对抗坏血酸的亲和力高于哺乳动物SVCT1,这表明细菌可以与宿主竞争维生素C。
因此,肠道菌群中大肠杆菌等革兰氏阴性菌占比较多的情况,可能不利于维生素C的吸收,这在谷禾肠道菌群检测报告中也是可以反映的。
▼
肠道细菌如大肠杆菌和乳酸杆菌代谢维生素C。
利用ula基因簇,大肠杆菌等细菌可以将抗坏血酸代谢为D-木酮糖,宿主细胞可以进一步加工木酮糖以产生草酸盐。
在肺炎链球菌、沙门氏菌、福氏志贺菌、粪肠球菌、肺炎克雷伯菌等病原菌中,也发现了相同的ula基因簇。
带ula的致病菌与草酸盐:携手制造结石
结石形成者(比如肾结石患者)微生物群更常见地富含携带ula基因簇的致病菌,并且这些患者在接受口服维生素C时,草酸盐增加的水平比非结石者增加得更多。高草酸盐水平增加了结石的风险。
因此,如果在肠道菌群检测报告中发现以上提到的致病菌占比较多,则有可能在代谢维生素C的时候产生的草酸盐过多,增加了结石的风险。
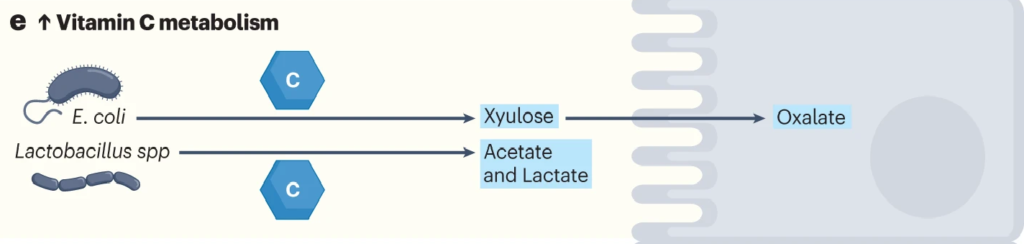
Chmiel JA, et al.,Nat Rev Urol. 2023
“
以上通过微生物群代谢维生素的机制,有助于我们更好地理解结石形成的机制。
既然有促进结石的细菌,自然也有降解的细菌:
一些乳酸杆菌可以将维生素C转化为乙酸盐和乳酸盐,这是一种无毒的代谢产物,通过生物能量途径增加微生物组的功能,并可能促进这些草酸降解细菌的定植。
Oxalobacter formigenes是一种革兰氏阴性厌氧细菌,可降解肠道草酸盐并促进原发性高草酸条件下肠道草酸盐的分泌。该菌在肠道定植可降低尿液或血浆中的草酸盐浓度。
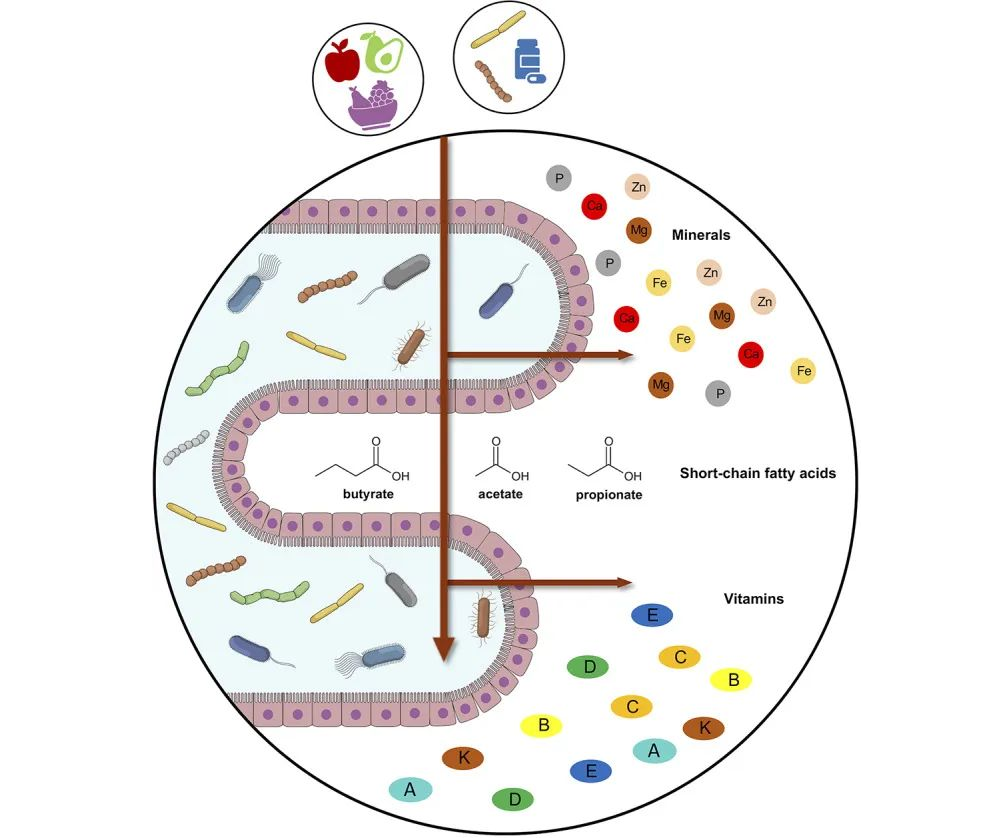
Barone M, et al., Biofactors. 2022
我们看到生活中有人认为不能吃生菠菜,会得肾结石,但有些人每天吃生菠菜也没事…其实可能是因为人家的肠道菌群中致病菌较少,而降解草酸的菌群又在拼命干活…
因此,健康的肠道菌群结构非常重要,菌群在该干活的时候各司其职,井井有条,那么你的身体抵抗疾病的能力也随之提升。
以上是肠道菌群对维生素代谢吸收的影响,反过来,维生素C的补充也可以影响肠道菌群的组成。
二、
补充维生素C可以直接调节肠道微生物群,也可以通过改变氧化还原电位、修复肠道屏障,改善肠道条件,支持部分有益菌生长,防止有害菌泄漏到身体其他部位。
▼
维生素C直接调节肠道菌群
与安慰剂组相比,补充维生素C已被证明可以显着增加微生物生态系统的多样性,以及Collinsella的相对丰度和粪便水平的短链脂肪酸,特别是丁酸盐和丙酸盐。
在健康受试者中,每日高剂量维生素C补充(1000 mg/天):
下列菌群的相对丰度升高
下列菌群的相对丰度下降
一项观察性研究探讨了微量营养素维生素C对肠道微生物组组成和多样性的影响。结果表明,维生素C增加了肠道中双歧杆菌属的丰度,在科水平上,毛螺菌科和双歧杆菌科显著增加。
双歧杆菌属的成员是有益菌,例如增加ATP生成、调节免疫系统、黏膜屏障完整性、短链脂肪酸的产生,对健康有益,维生素C通过增加肠道有益菌促进健康。
研究发现,囊性纤维化患者维生素C摄入量的增加与厚壁菌门的丰度呈正相关,与拟杆菌门的丰度呈负相关。
▼
改变氧化还原电位
调节微生物组的机制类似于维生素B2:通过改变氧化还原电位,改善消化道中的厌氧/耐氧平衡,从而选择性地支持微生物生长,改善肠道条件。
与安慰剂相比,维生素C组粪便样本中的粪便pH值和氧化还原平衡降低。
▼
修复肠道屏障
我们知道,肠道屏障受损,细菌和有害物质有可能会穿过屏障进入血液循环,对人体产生各种负面影响,导致诸如过敏、炎症、自身免疫疾病等多种反应。
关于肠漏可以详见我们之前的文章:
而维生素 C 具有维持肠粘膜屏障完整性和修复粘膜屏障的作用。
这里介绍两种修复肠屏障机制。
——通过激活Notch 信号
Notch 信号影响细胞正常形态发生的多个过程,与许多人类疾病有关,包括IBD,因此被认为是癌症治疗的潜在靶点。Notch 信号通路的激活会改变紧密连接蛋白的表达并影响其分布的连续性,从而降低细胞屏障通透性。
豚鼠结肠组织相关基因检测表明,低剂量的维生素C可强烈激活Notch/Hes-1信号通路,对DSS诱导的结肠炎豚鼠的肠粘膜具有一定的保护作用。肠上皮受损时,Notch-1表达增加可促进上皮细胞增殖,有利于损伤部位的修复和重建。
——通过增加肠道胶原蛋白合成
增加维生素 C 摄入量的另一个潜在好处是肠道胶原蛋白合成增加,从而改善屏障功能。这一提出的机制与抗坏血酸的辅酶功能一致,即羟基化脯氨酸和赖氨酸以交联胶原蛋白。
例如,对具有吲哚美辛诱导的屏障功能障碍的 T84 人隐窝样上皮细胞系的研究表明,细菌通过跨细胞途径穿过上皮细胞,维生素 C 治疗可消除该途径。因此,肠道中抗坏血酸状态不佳可能会加剧屏障功能障碍,从而增加 LPS 衍生的革兰氏阴性菌的易位,从而加剧炎症。
维生素C修复肠道屏障后,肠道屏障可以正常发挥吸收、分解和转换营养物质等功能,同时可以帮助促进健康微生物群栖息和生长,从而促进整体健康。
以上我们了解到,维生素C可以通过多种方式影响肠道菌群,从而促进整体健康。那么当我们看到肠道菌群报告中菌群多样性较低,部分菌群失调,尤其是上面提到的毛螺菌科、肠球菌属、Collinsella、Gemmiger formicilis等,可以考虑通过补充维生素C来调节。
我们首先可以考虑通过食物补充,如卡姆果、针叶樱桃等维生素C含量很高的食物,或者一些常见的蔬菜水果例如:猕猴桃、番石榴(芭乐)、青椒、羽衣甘蓝等。也可以考虑通过维生素C补充剂调节。
人体维生素研究面临着许多挑战,维生素通常是通过食物摄入的,而食物中同时存在多种营养素,这使得难以研究单一维生素的作用;某些高剂量维生素的使用可能存在潜在的风险,进行研究时涉及到人体试验和干预,需要遵循伦理准则,并确保研究的安全性;不同人对维生素的需求和代谢能力存在个体差异,基因、环境和生活方式等因素都可能影响维生素的吸收、利用和代谢。
肠道菌群研究可以揭示不同个体之间菌群组成的差异,这有助于理解个体差异对维生素代谢和利用的影响。可以通过检测肠道菌群的组成和丰度,了解维生素的代谢情况,从而辅助评估维生素水平。
综合运用多种研究方法和技术,结合肠道菌群检测,可以考虑多个因素对维生素代谢和利用的综合影响,进一步理解维生素的作用机制,对人体健康具有重要意义。
注:本账号内容仅作交流参考,不作为诊断及医疗依据。
主要参考文献
Barone M, D’Amico F, Brigidi P, Turroni S. Gut microbiome-micronutrient interaction: The key to controlling the bioavailability of minerals and vitamins? Biofactors. 2022 Mar;48(2):307-314.
Chmiel JA, Stuivenberg GA, Al KF, Akouris PP, Razvi H, Burton JP, Bjazevic J. Vitamins as regulators of calcium-containing kidney stones – new perspectives on the role of the gut microbiome. Nat Rev Urol. 2023 May 9:1–23.
Pham VT, Dold S, Rehman A, Bird JK, Steinert RE. Vitamins, the gut microbiome and gastrointestinal health in humans. Nutr Res. 2021 Nov;95:35-53.
Li XY, Meng L, Shen L, Ji HF. Regulation of gut microbiota by vitamin C, vitamin E and β-carotene. Food Res Int. 2023 Jul;169:112749.
Yang Q, Liang Q, Balakrishnan B, Belobrajdic DP, Feng QJ, Zhang W. Role of Dietary Nutrients in the Modulation of Gut Microbiota: A Narrative Review. Nutrients. 2020 Jan 31;12(2):381.
Steinert RE, Lee YK, Sybesma W. Vitamins for the Gut Microbiome. Trends Mol Med. 2020 Feb;26(2):137-140.
Gomes-Neto JC, Round JL. Gut microbiota: a new way to take your vitamins. Nat Rev Gastroenterol Hepatol. 2018 Sep;15(9):521-522.
Rowland I, Gibson G, Heinken A, Scott K, Swann J, Thiele I, Tuohy K. Gut microbiota functions: metabolism of nutrients and other food components. Eur J Nutr. 2018 Feb;57(1):1-24. doi: 10.1007/s00394-017-1445-8. Epub 2017 Apr 9. PMID: 28393285; PMCID: PMC5847071.
Traber MG, Buettner GR, Bruno RS. The relationship between vitamin C status, the gut-liver axis, and metabolic syndrome. Redox Biol. 2019 Feb;21:101091.
Rozemeijer S, Spoelstra-de Man AME, Coenen S, Smit B, Elbers PWG, de Grooth HJ, Girbes ARJ, Oudemans-van Straaten HM. Estimating Vitamin C Status in Critically Ill Patients with a Novel Point-of-Care Oxidation-Reduction Potential Measurement. Nutrients. 2019 May 8;11(5):1031.
Otten AT, Bourgonje AR, Peters V, Alizadeh BZ, Dijkstra G, Harmsen HJM. Vitamin C Supplementation in Healthy Individuals Leads to Shifts of Bacterial Populations in the Gut-A Pilot Study. Antioxidants (Basel). 2021 Aug 12;10(8):1278.

谷禾健康
花青素-肠道微生物群-健康轴
经常听到一些专家在介绍食品或保健品时说富含花青素,那么究竟什么是花青素?对我们的健康又有何益处?
花青素是在植物组织中发现的天然水溶性色素,水果、蔬菜、花卉中的呈色物质大部分与之有关,是类黄酮的一个亚类,迄今为止已鉴定出700多种结构不同的花青素。
花青素是一种重要的营养素,具有多种生物活性和保健作用,如抗氧化、抗炎、抗癌、降血压、降血糖、保护视力及心血管健康。
花青素在消化过程中还会影响肠道中的细菌代谢。花青素及其衍生物还通过调节肠道屏障功能和有益细菌的定植来促进肠道健康,从而更好地抵御病原体,改善营养代谢和整体免疫反应。
在本文中,谷禾简要介绍了不同类型的花青素,它们常见的饮食来源和通过胃肠道(包括胃、小肠和结肠)的吸收和代谢。
本文还总结了膳食花青素对健康的直接影响,以及肠道微生物群作为“媒介”时的影响。花青素-微生物的相互作用可能成为肥胖、2型糖尿病、心血管疾病、神经退行性疾病、炎症性肠病、癌症、慢性肾脏病和骨关节炎等疾病的治疗新途径。
目录
1.常见的花青素及膳食来源
2.膳食花青素在人体内的吸收和代谢
3.花青素对肠道微生物群的影响
4.花青素-微生物群对肥胖的改善作用
5.花青素-肠道菌群对糖尿病的影响
6.花青素改善心血管疾病
7.花青素降低神经退行性疾病风险
8.花青素对其他疾病的影响
9.日常补充膳食花青素的一些建议
花青素又称花色素,是自然界一类广泛存在于植物中的水溶性天然色素,是花色苷水解而得的有颜色的苷元。
水果、蔬菜、花卉中的主要呈色物质大部分与之有关。在植物细胞液泡不同的PH值条件下,花青素使花瓣呈现五彩缤纷的颜色。
▼
已知现有的花青素多达几百种,食物中重要的有6种,即天竺葵色素、矢车菊色素、飞燕草色素、芍药色素、牵牛花色素和锦葵色素。
花青素具有2-苯基苯并吡喃结构,具有完全不饱和的C环和3位的羟基。
植物性食物中主要花青素的结构
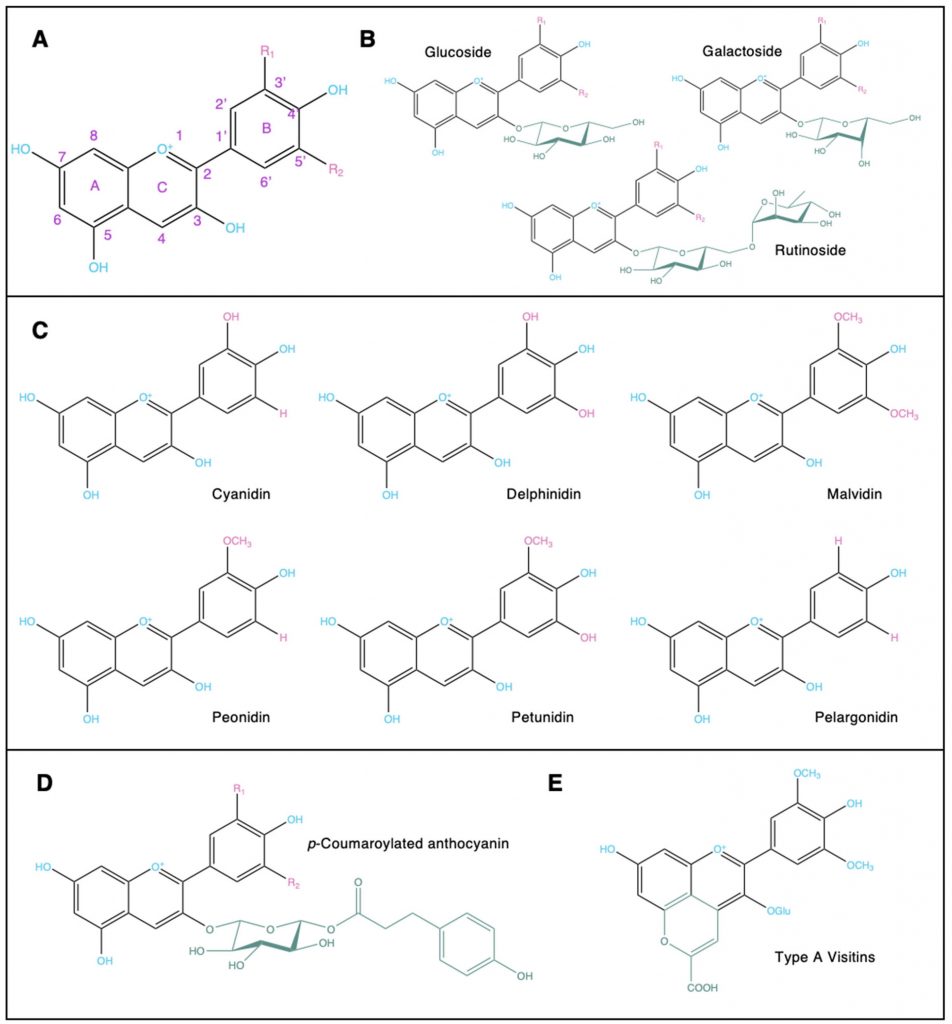

Liang A,et al.Crit Rev Food Sci Nutr.2023
(A)花青素中的2-苯基苯并吡喃骨架 (B)附着在糖基化花青素上的常见糖部分 (C)植物性食物中常见的花青素 (D)酰化花青素 (E)吡喃花青素
▼
植物性食品中花青素的浓度和组成高度依赖于植物品种、生长区域、植物部位、加工方法和测量方法。
花青素在各种红色、紫色和蓝色水果(如浆果、石榴、血橙和红梅)中含量丰富,这些水果代表了人类饮食中花青素的主要摄入。
常见水果中的花青素
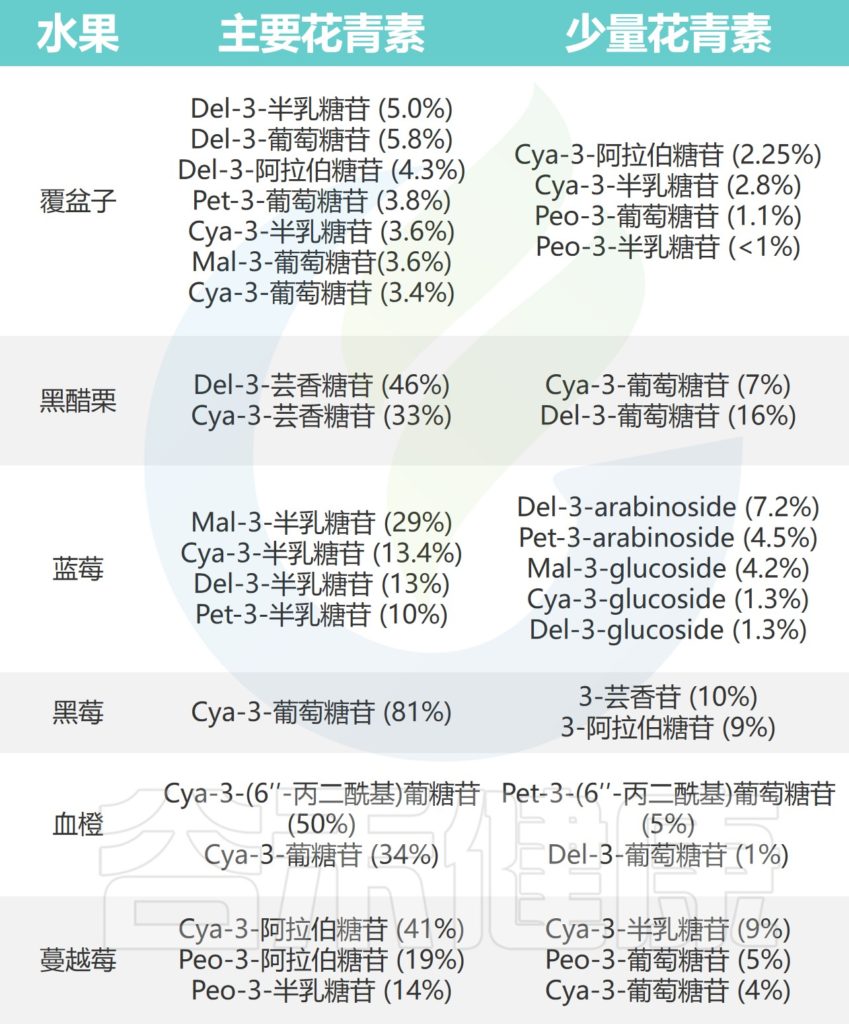
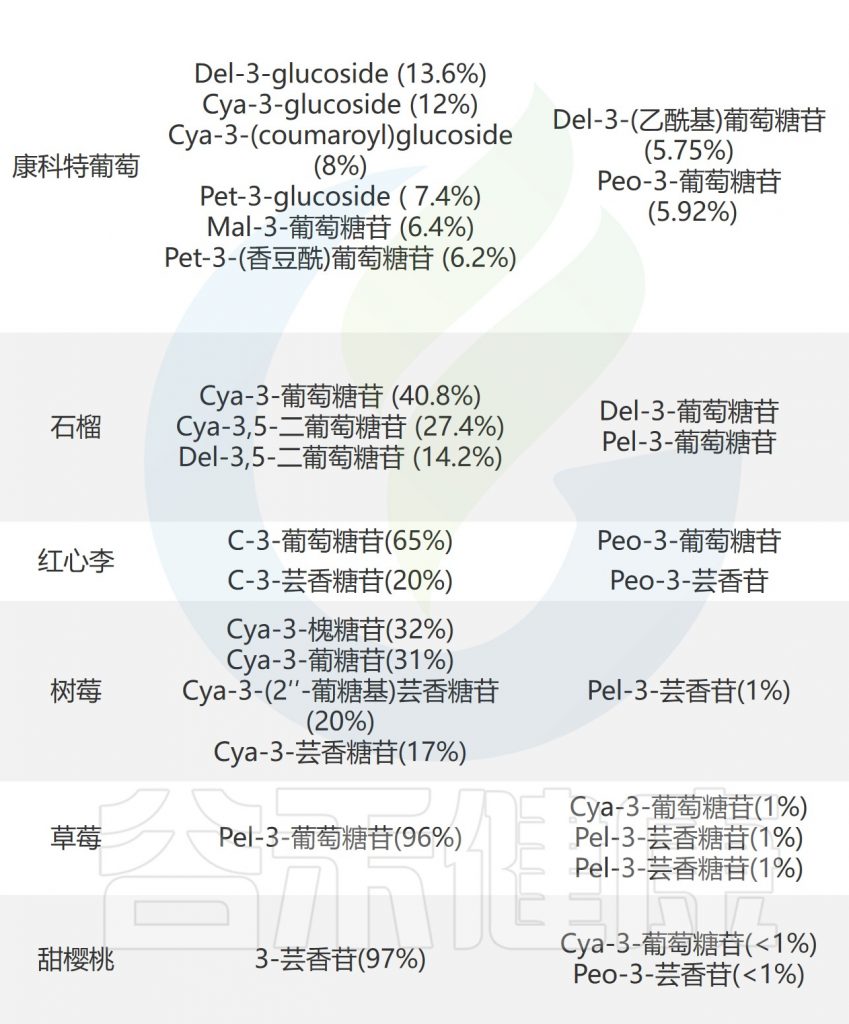

Liang A,et al.Crit Rev Food Sci Nutr.2023
•花青素在不同酸碱度下颜色不同
花青素在水果中根据pH条件,它会显示红色(pH<3)、紫色(pH=7-8)及蓝色(pH>11)。
例如飞燕草色素通常存在于花朵和葡萄中,它们提供蓝紫色,而天竺葵色素为许多浆果和水果提供橙色和红色,包括树莓、草莓和石榴。
•酰化花青素具有更强的耐热性和耐光性
酰化花青素是通过糖基和有机酸的乙酰化酯键得到的,进一步扩大了食品中花青素的多样性。常见的酰化酸包括脂肪酸(乙酸、丙二酸、苹果酸、草酸和琥珀酸)和环状酸(对香豆酸、咖啡酸、芥子酸、没食子酸和阿魏酸)。
在葡萄中鉴定出酰化花青素,在黑胡萝卜、红薯和红甘蓝中发现了肉桂酸酰化的花青素。在红萝卜中发现了多达12种酰化花青素。
酰化花青素在加工过程中表现出更强的耐热性和耐光性,因此被广泛用作食品工业中的着色剂。
•吡喃花青素具有更强的抗氧化能力
吡喃花青素是另一组具有额外吡喃环的花青素,主要在红酒的酒精发酵和陈酿过程中产生。少量吡喃花青素天然存在于血橙、草莓和黑加仑等水果中。
吡喃花青素的主要类别包括A型和B型视黄素、甲基吡喃花青素、羟基苯基吡喃花青素和黄烷基吡喃花青素。
相较于单体花青素,吡喃花青素,在更大范围的pH条件下保持其颜色,这是因为额外的吡喃环可以防止亲核攻击和无色甲醇碱的形成。
吡喃花青素在二氧化硫漂白和热降解过程中也具有更大的稳定性,并且相对于单体花青素具有更强的抗氧化能力。
由于这些原因,吡喃花青素作为颜料和生物活性剂广泛用于食品加工。
膳食花青素是指可以通过饮食摄入的一类花青素,广泛存在于深红色、紫色或蓝色蔬菜水果中,如葡萄、蓝莓、紫甘蓝、紫薯、黑枸杞等。
膳食花青素的代谢和治疗活性取决于其生物可及性(可从食物基质中获得的量)和生物利用度(在人体肠道中的吸收)。这受到许多因素的影响,包括化学结构、与食物基质的相互作用、其他膳食化合物的存在以及个体遗传学和生理学差异。
★ 不同结构的花青素消化率存在差异
例如,具有双糖部分的糖基化花青素相对于单葡萄糖苷和苷元更耐消化。酰化花青素的消化率低于非酰化化合物,主要是因为极性降低和酰基的阻碍。吡喃花青素和聚合物花青素在刺激消化过程中更稳定。
花青素及其衍生物在人体内的消化吸收发生在胃、小肠和大肠中。
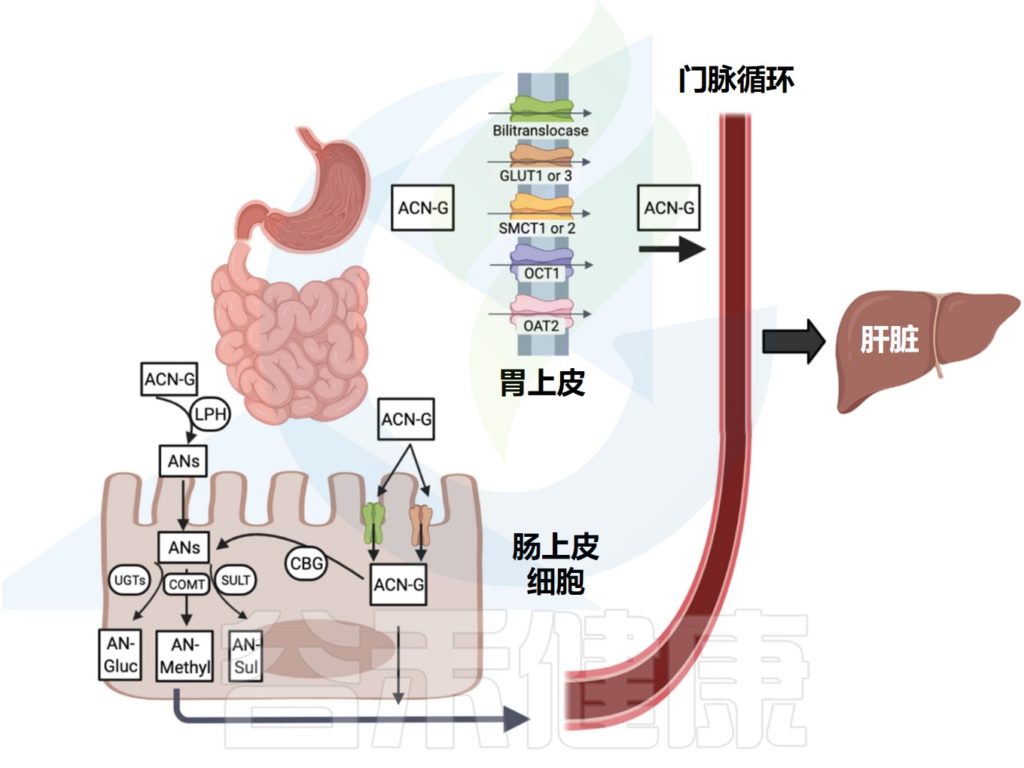
Liang A,et al.Crit Rev Food Sci Nutr.2023
▼
食用食物后第一个吸收花青素的部位是胃,在胃中,一小部分花青素穿过胃细胞屏障(大部分以完整的糖基化形式),并在血浆中检测到。
在胃内,花青素保持相对稳定,在大鼠胃肠道研究期间,从流出物中可回收总摄入花青素的75-79%,在体外研究期间可回收75-88%。
✦胃吸收效率受膳食成分影响
胃吸收效率也受到膳食成分的影响,在高葡萄糖 (>40mM)存在的情况下,花青素通过胃细胞屏障的摄取速率显著降低。
✦参与胃中花青素代谢的蛋白
胃胆转位酶是一种膜蛋白载体,可将完整的花青素转运穿过胃屏障。花青素的糖苷部分优先满足双转位酶提供的结构规格,因此无需去糖基化即可被吸收。
后来,葡萄糖转运蛋白GLUT1和GLUT3也参与了胃对花青素的摄取。花青素中的A环和C环以及葡萄糖部分在与人类GLUT1和GLUT3载体的跨膜结合中起重要作用。
其他参与花青素在胃中吸收的转运蛋白包括单羧酸转运蛋白(SMCT1和SMCT2)和有机阳离子/阴离子转运蛋白(OCT1和OAT2)。
胃以前被认为是花青素吸收而非代谢的部位,直到最近在胃上皮细胞中发现结合酶活性才证实了胃的代谢功能。
此外,红酒中花青素在体外消化(使用胃MKN-28和肠道Caco-2细胞)过程中代谢物malvidin-3-O-葡糖苷酸的存在提供了花青素在胃内代谢的证据。
▼
空肠(小肠中部)是花青素吸收的主要部位。花青素在小肠内的吸收通过膜转运蛋白促进的被动扩散或主动转运发生。
✦花青素的主动转运吸收
与胃吸收类似,完整的糖基化花青素被肠上皮细胞内的转位酶和葡萄糖转运蛋白(SGLT1和GLUT2)吸收。
SGLT1转运蛋白是一种在肠细胞顶端表面发现的钠-葡萄糖共转运蛋白1,而GLUT2转运蛋白是主要在上皮细胞基底外侧膜上发现的促进载体。这两种转运蛋白都与花青素的葡萄糖部分相互作用,并负责基于葡萄糖的花青素的肠道吸收。
除了己糖转运(糖、葡萄糖、果糖等简单碳水化合物的转运系统)外,最近发现有机阴离子转运多肽转运体(OATP)也参与了大鼠空肠上皮对完整β型酰化花青素的吸收,但其吸收率很低,仅为0.2%~2.2%。
✦花青素的被动扩散吸收
另一方面,当花青素被乳糖酶-根皮苷水解酶、β-葡萄糖苷酶、α-鼠李糖苷酶和β-葡萄糖醛酸酶等水解为其苷元形式时,花青素通过肠上皮的被动扩散吸收。
✦花青素的转运速率
最近使用Caco-2细胞(人类结直肠腺癌细胞)作为人类肠道屏障功能的模型,可以评估花青素的运输,并表明运输效率取决于附着在花青素骨架上的苷元或糖的类型,以及花青素是否为聚合物。
Caco-2细胞模型还估计,达到系统循环的花青素比例约为总膳食摄入量的1%。
✦肠道内花青素的代谢
在肠道内吸收的花青素经历第一阶段代谢,包括氧化、还原和水解,但它们发生的频率较低,在多酚代谢中也不太重要。
第二阶段的生物转化更加密集和快速,它们首先发生在小肠,然后发生在肝脏和肾脏。一旦被肠细胞吸收,花青素及其分解代谢物就会发生结合反应。
包括分别由UDP葡萄糖醛酸基转移酶(UGTs)、硫转移酶(SULT)和邻苯二酚-O甲基转移酶(COMT)催化的葡萄糖醛酸化、硫酸化和甲基化。
这些生物转化产生葡萄糖醛酸、硫酸盐和甲基化代谢产物,这些代谢产物由活性ATP结合盒蛋白转运,因为它们过于亲水,无法被动扩散到细胞中。
活性ATP结合盒蛋白——一个膜内在蛋白质超家族。将ATP水解释出的能量提供给各种分子进行穿膜转运。
花青素进入血液后,通过门静脉分布到肝组织,进行进一步的偶联反应,增加其在水中的溶解度,并最终促进其在尿液中的排泄。
▼
膳食中花青素的低生物利用度以及粪便和尿液样本中花青素的低回收率表明,花青素在结肠中会被降解。
例如,食用覆盆子后,总膳食花青素的40%从回肠液中回收。这些来自小肠的未被吸收的花青素通过细菌或化学降解进行生物转化,潜在地提高了它们的生物利用度,并允许通过结肠上皮壁吸收。
花青素的微生物降解需要多种细菌,如拟杆菌、Enterococcus casseliflavus、优/真杆菌属(Eubacterium)和梭状芽胞杆菌(Clostridium)等,它们产生各种酶,如β-葡萄糖苷酶、α-半乳糖苷酶和α-鼠李糖苷酶,用于微生物分解代谢。
✦原儿茶酸是最丰富的代谢物
由于这些相互作用,通过肠道微生物降解产生了各种代谢产物。代谢物原儿茶酸占花青素摄入量的73%,是花青素消耗后最丰富的人体代谢物。
桑椹的矢车菊素-3-O-葡萄糖苷和矢车菊苷-3-O-芸香糖苷的体外粪便发酵产生了原儿茶酸、对香豆酸和间苯三酚醛,而飞燕草素-3-O-芸香糖苷的发酵产生了没食子酸、丁香酸和间苯三酚醛。
✦其他花青素的代谢产物
桑椹的矢车菊素-3-O-葡萄糖苷和矢车菊苷-3-O-芸香糖苷的体外粪便发酵产生了原儿茶酸、对香豆酸和间苯三酚醛,而飞燕草素-3-O-芸香糖苷的发酵产生了没食子酸、丁香酸和间苯三酚醛。
在与结肠细菌孵育24小时后,Malvidin-3-O-葡萄糖苷会完全代谢为丁香酸。
如体内人体研究和体外研究所示,天竺葵素-3-O-葡糖苷被代谢为4-羟基苯甲酸。
六种主要花青素及其结肠代谢物


Liang A,et al.Crit Rev Food Sci Nutr.2023
★ 花青素的主要代谢物对人体健康有益
原儿茶酸
原儿茶酸是一种水溶性酚酸成分,并且是很多中药中的活性物质,其不仅具有抗血小板凝集、降低心肌耗氧量、提高心肌耐氧能力、减慢心率、抑菌、镇痛等药理活性,还具有抗氧化、抗肿瘤和神经保护作用。
没食子酸
没食子酸具有抗炎、抗突变、抗氧化、抗自由基等多种生物学活性;同时没食子酸具有抗肿瘤作用,可以抑制肥大细胞瘤的转移, 从而延长生存期;对肝脏具有保护作用。
丁香酸
丁香酸可以抑制炎症反应,减轻炎症症状;同时丁香酸具有抗菌作用,可以抑制多种细菌和真菌的生长;丁香酸还能够降血糖、降血脂。
✦肠道微生物在花青素的去酰化起重要作用
此外,人体肠道微生物组在花青素的去酰化过程中发挥重要作用,释放出具有更高生物利用度的酚酸。
花青素衍生的代谢物可能比母体花青素表现出更强的稳定性和生物活性,并可能调节人体肠道微生物组成。
肠道微生物群受年龄、体重、饮食模式、抗生素治疗和宿主遗传的影响,并且个体之间(以及个体内部)存在差异。这种变化可能会影响膳食花青素的生物利用度和代谢。
花青素及其结肠代谢物通过其生物活性直接改善健康,并通过重塑肠道微生物组的组成和操纵短链脂肪酸的产生间接改善健康。
在宿主的一生中,肠道微生物组的组成随着时间的推移而变化,以响应内部和外部刺激。因此,肠道微生物组成的动态平衡和多样性是正常肠道功能所必需的,包括维生素和短链脂肪酸的产生、脂质代谢、免疫防御和肠-脑轴相互作用等。
▼
花青素及其代谢物目前被认为是改变肠道微生物群的调节剂,主要是通过促进有益菌的增殖和抑制有害菌的生长,许多不同模型的研究都观察到这一点。
✦促进了有益菌的增殖
研究发现黑米中分离的矢车菊素-3-葡萄糖苷在体外发酵条件下对青春双歧杆菌(B. adolescentis)、婴儿双歧杆菌(B. infantis)、双歧双歧杆菌(B.bifidum)和嗜酸乳酸杆菌(L.acidophilus)的增殖具有促进作用。
培养48小时后还观察到生长培养基pH值的降低,这归因于由酚酸和短链脂肪酸组成的有机酸的产生。双歧杆菌和乳杆菌的数量增加。它们通过竞争底物和粘附位点以及降低结肠腔内pH值来对病原体产生抗菌作用。
研究发现,降低结肠内pH值可抑制肠杆菌科(Enterobacteriaceae)和梭状芽胞杆菌(Clostridia)等pH敏感有害菌群的过度增殖,并通过抑制前致癌物的形成来降低结直肠癌的风险。
✦抑制有害菌的生长
与上述发现一致,紫甘薯中提取的花青素增加了最知名的益生菌之一双歧杆菌(Bifidobacterium)和乳杆菌(Lactobacillus)的种群数量,但减少了溶组织梭状芽胞杆菌(C. histolyticum)和拟杆菌/普雷沃氏菌的种群数量。
溶组织梭状芽胞杆菌是与感染和炎症性肠病相关的最常见致病性物种之一。
▼
虽然许多研究表明花青素及其代谢产物促进有益菌群生长,抑制有害菌群生长,但对结肠细菌的促进作用存在差异。
对微生物群的不同影响可能是由于源自花青素的代谢物的差异。
花青素(单独和混合物)和没食子酸的孵育被证明可以增加双歧杆菌和乳酸杆菌的数量。而混合花青素和没食子酸显著诱导奇异菌属(Atopobium)的生长,并减少了潜在致病性溶组织梭菌。
没食子酸似乎是本研究中的关键代谢物,可抑制溶组织梭菌增殖。
在其他研究中,研究了没食子酸对梭菌、大肠杆菌和金黄色葡萄球菌等有害微生物的抗菌活性。
花青素对肠道菌群的调节作用



Liang A,et al.Crit Rev Food Sci Nutr.2023
▼
花青素的发酵有助于短链脂肪酸的产生,主要是乳酸、乙酸、丙酸和丁酸。短链脂肪酸通过调节细菌毒力基因表达和降低结肠中管腔pH值来抑制肠道病原体如沙门氏菌(Salmonella spp.)、大肠杆菌(E. coli)和李斯特菌(Listeria spp.)的入侵。
此外,短链脂肪酸在肠道生理事件中发挥着重要作用,如获取能量、调节pH、参与肠脑轴和保护肠道屏障功能。
花青素与肠道菌群作用的研究证据
花青素与肠道微生物的相互作用已经通过动物模型得到了广泛的研究。用黑甜樱桃对小鼠进行饮食干预发现,除了双歧杆菌和乳杆菌外,樱桃花青素的补充还促进了结肠中阿克曼氏菌(Akkermansia)的增殖。
阿克曼氏菌的丰富度被认为可以刺激粘液分泌,改善肠道屏障功能,从而降低炎症风险和免疫介导的疾病,如乳糜泻。
促进Coriobacteriaceae有助于健康
对小鼠进行为期六周的多种浆果饮食干预,结果发现放线菌(Actinobacteria)数量有所改善,这与补充蓝莓的研究结果一致。
放线菌门下的一些科,如双歧杆菌和Coriobacteriaceae,已被证明对健康有益。特别是,有人认为,在高脂肪饮食存在的情况下, Coriobacteriaceae在降低肥胖和肝脏相关疾病的风险方面发挥作用。
双歧杆菌和乳酸杆菌的丰度增加
与体内试验的结果一致,在参加为期六周的25克蓝莓能量饮料的健康男性中发现双歧杆菌和乳酸杆菌的丰度增加。
花青素、其代谢物和肠道微生物群间的相互作用
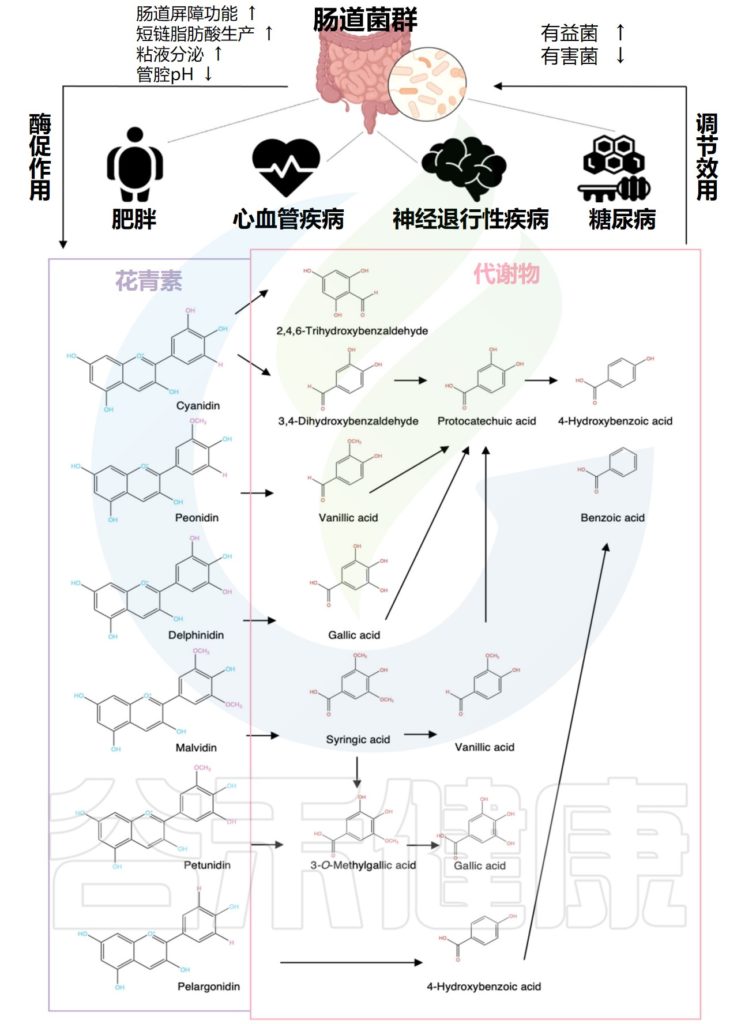
Liang A,et al.Crit Rev Food Sci Nutr.2023
小结
体外、动物和人体研究一致认为,花青素及其代谢物能够调节肠道微生物群。花青素会促进益生菌的生长,特别是双歧杆菌、乳杆菌和阿克曼氏菌,它们通过产生短链脂肪酸或通过竞争底物和定植位点来对抗有害和致病性菌株,从而有利于宿主健康。
然而,花青素对肠道微生物群的调节也可能依赖于其他相关的化学物质,如葡萄糖,因为与那些喂食高葡萄糖对照饮食的大鼠相比,在蓝莓补充后,在肠道中发现了较低水平的乳酸杆菌。
此外,不同的动物模型和志愿者群体在微生物组成方面存在较大差异,这是这些研究的另一个挑战。
因此,未来的临床研究重点应放在不同年龄和生理阶段的男性和女性不同亚类人群上,这可能会更深入地了解花青素在微生物群调节中的作用及其对特定人群的健康益处。
前面讲述了花青素对肠道菌群的调节作用,下面谷禾来具体讲讲花青素和肠道微生物群相互作用下对一些疾病的影响
肥胖和超重被定义为对健康构成威胁的脂肪组织的过度积累。脂肪组织中的代谢紊乱,如炎症、脂肪因子释放失调和脂肪生成增加,是肥胖和其他肥胖相关疾病的一些常见潜在特征。
有证据表明,与肥胖相关的疾病可能部分由肠道生态失调引起,包括微生物组成及其代谢物的变化。
最近,花青素与肠道微生物的相互作用被证明具有改善肥胖的作用。主要通过调节脂肪生成和脂肪分解,炎症反应的介导以及通过肠脑通讯控制食欲。
1
肠道微生物组影响脂质代谢,肠道菌群失调与血脂异常和肥胖等有关。
最近的一项体内研究显示,对高脂喂养的小鼠补充了200毫克/公斤体重的紫甘薯花青素(花青素和芍药苷酰基糖苷),改善了高脂饮食引起的体重增加和肝脏总脂肪积累。
√调节AMPK通路减少脂肪积累
他们认为,花青素抑制脂肪堆积的作用需要激活小鼠肝脏细胞AMPK通路。此外,在摄入花青素后,AMPK途径下游靶点乙酰辅酶a羧化酶、脂肪酸合成酶、甾醇调节元件结合蛋白也被下调,以减少小鼠肝细胞中的脂肪积累。
已知AMPK通路的上调在抑制脂肪生成中发挥重要作用,例如抑制脂蛋白脂肪酶 (LPL),这是一种可受肠道微生物群调节的酶。肠道菌群通过影响抑制脂蛋白脂肪酶,以相反的方式促进脂肪细胞中甘油三酯的储存。而活化的AMPK及其下游信号通路至少部分抵消了肠道微生物群促进的能量储存。
√操纵法尼醇X受体信号减轻代谢受损
此外,已知肠道菌群产生的次生胆汁酸通过胆汁酸受体法尼醇X受体(FXR)改变肝脏脂质代谢。胆汁酸-结肠微生物群相互作用的破坏可能导致肥胖易感性。
花青素被证明可以操纵肠道微生物群/法尼醇X受体信号,从而减轻高脂肪诱导的肝脏脂肪积累和脂质代谢受损。
黑米花青素(0.48g/kg)喂养12周使血清乳酸脱氢酶(LDH)、丙氨酸转氨酶(ALT)和天冬氨酸转氨酶(AST)含量正常化,这些指标是肝脏脂肪过度积累影响肝损伤的指标。
这些发现表明,膳食花青素可能通过改变肠道菌群来减轻高脂饮食引起的脂质代谢紊乱。
2
肠道微生物群参与调节炎症,在肥胖患者的脂肪组织中通常观察到系统性的低级别炎症并发症。
√经常摄入花青素的肥胖患者炎症标志物含量下降
在一项研究中,代谢综合征患者每天食用400克新鲜越桔,持续12周后,血清脂多糖、IL-6、IL-12和高敏C反应蛋白(hsCPR)浓度下降。
hsCPR是一种与肥胖相关的炎症标志物。
另一项动物研究显示,花青素的干预通过抑制21天大的小鼠白色脂肪组织中TLR4介导的NF-κB信号通路,降低了高脂肪诱导的促炎标志物IL-6和肿瘤坏死因子的表达。
此外,高脂肪喂养诱导下的粪便双歧杆菌减少,在妊娠期和哺乳期用花青素处理后恢复。
3
肠道微生物在调节涉及能量稳态的神经激素活动中发挥作用。由微生物群产生的花青素和短链脂肪酸会影响促食欲激素和厌食激素的释放。
√刺激肠促胰岛素激素分泌减少食物摄入量
飞燕草素3-芸香糖苷被证明可刺激释放胰高血糖素样肽-1,这是一种肠促胰岛素激素,可促进胰岛素分泌和饱腹感,从而减少食物摄入量。
√减轻肥胖引起的神经激素紊乱
肥胖会通过表观遗传修饰相关基因表达导致参与能量平衡的神经激素活动紊乱。食用花青素可能会恢复肥胖引起的这些不利影响。
在肥胖大鼠中,连续8周食用额外的樱桃和桑葚花青素可以减少体重增加,降低血清瘦素水平,增加脂联素。
与先前的研究一致,肥胖患者在食用富含花青素的水果6周后,发现瘦素受体表达增加,这表明补充花青素后瘦素敏感性有所改善。
此外,高脂饮食诱导的肥胖大鼠大脑皮层和海马体中的γ-氨基丁酸(GABA)水平下降。研究报道,与对照组相比,40天摄入黑大豆花青素减少了成年大鼠的体重增加。高剂量花青素可降低促氧神经肽Y (NPY)的表达,提高下丘脑GABA受体B (GABAB1R)的表达。
GABA是中枢神经系统中的一种抑制性神经递质,通过控制神经元的兴奋性、可塑性和额叶皮质的同步性,在摄食反应中起关键作用。
综上所述,花青素似乎通过多种方式与肠道微生物群相互作用,包括调节脂质代谢、炎症反应和参与能量平衡的神经激素活动,从而具有改善肥胖的作用。
注:关于健康和肥胖个体肠道中花青素代谢的差异,人们的理解有限。因此,未来的研究重点应放在花青素结肠代谢物及其对健康和肥胖受试者的健康影响上。
2型糖尿病是一种以高血糖为特征的代谢性疾病,由胰岛素抵抗逐渐发展而来。
许多研究已经报道了花青素及其代谢物的抗糖尿病潜力,这可能归因于以下单一或同时的作用,包括增强胰岛素敏感性,改善β细胞功能和延迟餐后血糖反应。
1
花青素可以通过自身或其微生物代谢物改善胰岛素敏感性。
脂肪组织能够分泌脂联素等脂肪细胞因子来调节葡萄糖稳态。
√花青素可以诱导脂肪细胞摄取葡萄糖
花青素及其微生物代谢物原儿茶酸已被证明可以通过上调葡萄糖转运蛋白4来增加人类脂肪细胞去除血浆葡萄糖的能力。
PPARγ的敲除消除了花青素的胰岛素增敏特性,这表明PPARγ可能在增加花青素诱导的脂肪细胞葡萄糖摄取中发挥作用。
PPARγ是一种参与葡萄糖处理和葡萄糖转运蛋白调节的核转录因子
√花青素还可以介导骨骼肌中的葡萄糖摄取
除了脂肪细胞外,骨骼肌中的葡萄糖摄取也可由花青素介导。
糖尿病小鼠口服紫玉米花青素提取物8周后,骨骼肌对葡萄糖的摄取增加,因为在肌肉细胞中发现葡萄糖转运蛋白4表达增加,并伴随AMPK通路的激活。增加AMPK活性是刺激葡萄糖转运蛋白4从细胞内囊泡转移到细胞膜的重要途径,从而促进葡萄糖流入细胞。
此外,在摄入原儿茶酸后大鼠肝脏中发现胰岛素受体底物1/磷脂酰肌醇3-激酶/蛋白激酶B-2 (IRS1/PI3K/AKT2) 信号通路的活性增加,表明肝脏胰岛素敏感性得到改善。
证据表明,花青素及其降解产物改善了脂肪细胞和肌肉细胞的胰岛素敏感性。
2
花青素还可以通过消除高血糖引起的氧化应激来保护胰腺β细胞的功能。
√改善高糖影响下的胰岛β细胞损伤
发现富含花青素的提取物可减轻高糖诱导的β细胞损伤,保护其分泌功能,并导致血清胰岛素水平升高。
一项体外研究(对与桑椹花青素孵育的高糖培养的β细胞)发现,花青素能够通过抑制β细胞中的凋亡相关蛋白,包括丝裂原活化蛋白激酶、细胞色素c和Bcl-2家族蛋白,消除高糖诱导的细胞内活性氧水平升高,并将β细胞活力恢复到84%。
除了完整的花青素外,丁香酸是花青素的主要微生物代谢产物之一,口服30天可改善四氧嘧啶诱导的糖尿病大鼠的胰岛素释放功能异常、血糖和糖蛋白水平升高。
丁香酸的抗糖尿病作用可能与保持β细胞的活力和功能有关。
3
在人体试验中也观察到了膳食花青素和微生物代谢物在调节餐前和餐后血糖中的作用,从而降低了患2型糖尿病的风险。
众所周知,血糖水平是动态的,全天都在变化。空腹和餐后血糖水平是诊断糖尿病的两个重要指标。空腹血糖值代表身体在一夜禁食后如何管理血浆葡萄糖,而餐后血糖则代表餐后的血糖反应。
√多摄入花青素表现出延迟的血糖反应
与未补充花青素的人相比,额外摄入150克混合浆果泥的参与者表现出延迟的血糖反应。
研究人员解释:餐后血糖降低至少部分是由于花青素对α-葡萄糖苷酶的抑制作用,α-葡萄糖苷酶是一种释放α-葡萄糖的酶。
该研究结果支持以下机制:花青素通过抑制胰腺α-淀粉酶和α-葡萄糖苷酶的活性,以及干扰葡萄糖转运蛋白(SGLT1和GLUT2),因为这些转运蛋白存在竞争关系,从而降低餐后血糖。
√降低了空腹血糖浓度
血清马尿酸是一种花青素的结肠代谢产物,在成年人食用越橘8周(200克/天)后显著增加。8周越桔 干预也降低了空腹血糖浓度。
然而,没有观察到血浆马尿酸与餐后血糖浓度之间存在任何相关性。
花青素可能通过抑制α-淀粉酶和α-葡萄糖苷酶活性以及与葡萄糖载体相互作用来调节餐后血糖,而花青素代谢产物马尿酸则由于微生物降解物的延迟出现而与改善空腹血糖控制有关。
小结
花青素及其代谢物的抗糖尿病作用已经在体外和体内研究中得到阐明。主要通过调节葡萄糖转运蛋白表达和易位来改善胰岛素抵抗,对胰岛β细胞及其分泌功能的保护作用,以及调节空腹和餐后血糖水平。
因此,由富含花青素的食物或补充剂组成的饮食干预可能是更好地控制患有2型糖尿病高风险个体和糖尿病患者血糖的替代途径。
心血管疾病是一类影响心脏和血管的疾病,最常见的形式包括动脉粥样硬化、冠心病、心律失常、心力衰竭和中风。
流行病学研究表明,高花青素摄入量与心血管疾病风险降低有关。花青素及其代谢物发挥保护作用,主要归因于抑制血小板过度活跃,缓解内皮功能障碍,改善脂质谱和逆转胆固醇转运。
1
花青素和原儿茶酸已被证明稳定血小板活性,从而防止血栓形成。
√摄入花青素抑制了血小板的过度聚集
一项研究发现,100μM和500μM没食子酸可以减少刺激物(二磷酸腺苷和血栓素A2激动剂U46619)诱导的血小板聚集、血小板-白细胞聚集和P-选择素表达。
P-选择素(一种参与细胞表面粘附的糖蛋白)的表达减少,表明血小板稳定性提高,血栓形成风险降低。
没食子酸抗血小板聚集的潜在机制是通过降低细胞内钙水平和下调蛋白激酶c-α(PKCα)/p38丝裂原活化蛋白激酶(p38MAPK)和Akt/糖原合成酶激酶3β (GSK3β)通路的活性。
另一项临床试验也支持了这种抗血栓作用,该试验发现,在健康志愿者中,200mL富含花青素和芸香苷的李子汁干预28天,可有效抑制人工刺激的血小板聚集,并降低P-选择素的表达。
此外,补充花青素28天后还观察到氧化应激生物标志物丙二醛水平降低,这表明血小板的抗机能亢进至少部分归因于花青素及其代谢物的抗氧化能力。
2
花青素及其代谢物具有血管内皮保护作用,内皮功能障碍被认为是动脉粥样硬化发展的早期指标。内皮功能受损可破坏血管收缩和血管舒张的止血作用,引发一系列生理事件,如促炎因子分泌、白细胞粘附等,从而引发动脉粥样硬化。
√减缓动脉粥样硬化
研究了花青素代谢物原儿茶酸对载脂蛋白e缺乏小鼠的内皮保护作用。原儿茶酸(0.03g/kg)喂养20周小鼠,动脉粥样硬化形成延迟,血管细胞粘附分子1 (VCAM-1)和细胞间粘附分子1(ICAM-1)表达显著降低。
这些粘附分子的减少可以减少单核细胞对血管内皮的附着,从而减缓动脉粥样硬化的早期发展。
√改善血管舒张情况
蓝莓花青素的血管保护特性已在临床试验中得到证实。健康志愿者在摄入蓝莓花青素(766-1791毫克)1至2小时和6小时后,内皮依赖性血管舒张得到改善。
3
许多研究也报道了富含花青素的饮食对血脂的有益影响。
√直接补充花青素缓解高脂血症
在高脂饮食诱导的肥胖小鼠中,每天补充150 mg/kg黑加仑花青素12周后,高脂血症得到缓解,相应的血清总胆固醇、甘油三酯和低密度脂蛋白水平降低。
另一项研究报告,50mg/kg原儿茶酸干预10周后,降低了先前由脂肪和果糖丰富的饮食引起的高脂血症雄性大鼠的血清甘油三酯、总胆固醇和低密度脂蛋白水平。
三项新指标,即血浆动脉粥样硬化指数(AIP)、动脉粥样硬化指数(AI)和冠状动脉危险指数(CRI),在50mg/kg原儿茶酸治疗后分别显著降低33%、52%和36%。
√通过调节菌群降低血脂
此外,花青素干预后观察到嗜黏蛋白阿克曼菌(Akkermansia muciniphila)和狄氏副拟杆菌(Parabacteroides distasonis)的富集,其与循环甘油三酯和低密度脂蛋白水平呈负相关。已知阿克曼菌可以积极调节肠道屏障完整性,防止脂多糖易位诱导炎症。
低密度脂蛋白(LDL)及其氧化修饰(oxLDL)通过刺激泡沫细胞的形成与动脉粥样硬化的发病机制有关。
最近发现狄氏副拟杆菌(Parabacteroides distasonis)通过产生琥珀酸和次生胆汁酸,如石胆酸和熊去氧胆酸,具有降血脂作用。
综上所述,花青素及其代谢物可能通过改善血脂来预防动脉粥样硬化和冠状动脉疾病。
小结
综上所述,花青素及其代谢物通过维持血小板稳定、保护血管内皮功能、改善血脂等发挥心血管保护作用。
然而,关于花青素心血管保护作用的人类和动物研究之间存在差距。因为动物中使用的浓度可能无法在人体中达到生理水平。
此外,临床研究的实验持续时间通常在4至12周之间,这可能无法捕捉到长期补充的影响。因此,未来可能需要进行长达一年的长期饮食干预研究。
帕金森病、阿尔茨海默病和肌萎缩侧索硬化症等神经退行性疾病是发生在神经系统中的疾病,导致日常活动协调困难、认知障碍和记忆丧失。
这些疾病的病因可能多种多样,但它们有一系列共同的潜在因素。这些因素包括但不限于长时间的氧化应激、中枢神经系统炎症、神经元钙信号失调和兴奋性毒性(即神经毒性)。
有证据表明,一些花青素代谢物,如原儿茶酸、香草酸、没食子酸和其他简单的酚酸,可以通过血脑屏障进入中枢神经系统,这表明这些物质可能直接在发生神经系统疾病的中枢神经系统中发挥作用。
1
花青素肠道代谢物与防止神经毒性和维持Ca2+体内平衡有关。
√没食子酸可以减轻谷氨酸诱导的神经毒性
谷氨酸是一种兴奋性神经递质,有助于大脑正常功能,而谷氨酸水平异常升高可引起谷氨酸兴奋性毒性。谷氨酸兴奋性毒性被认为是神经退行性疾病的主要原因之一。
没食子酸是能够穿透血脑屏障的代谢物之一。报道,25和50μg/ml 没食子酸预处理2小时可导致大鼠皮层神经元细胞中N-乙酰天冬氨酸(NAA)水平和微管相关蛋白2(MAP-2)表达增加,表明没食子酸处理减轻了谷氨酸诱导的大鼠神经元神经毒性。
在缺乏没食子酸的细胞中观察到的NAA和MAP-2的下调被认为是神经元损伤和丧失的直接指标。
此外,在没食子酸处理的细胞中也观察到钙结合蛋白(一种能够缓冲Ca2+内流的钙结合蛋白)的上调,表明没食子酸在保护神经元免受谷氨酸引发的钙失衡方面的作用。
√天竺葵素代谢物减轻神经兴奋性毒性
观察到4-羟基苯甲酸(HBA)是一种天竺葵素的代谢物,可在体外保护大鼠小脑颗粒神经元免受谷氨酸兴奋性毒性。当仅用谷氨酸处理的大鼠小脑颗粒神经元导致近50%的细胞损失时,4-羟基苯甲酸处理保留了细胞并且只有13%的细胞死亡得到证实,揭示了4-羟基苯甲酸在谷氨酸兴奋性毒性缓解中的作用。
注:原儿茶酸和4-羟基苯甲酸似乎发挥互补作用,表明它们的共同治疗可能比单一代谢物更有效。然而,本研究并未提供原儿茶酸和4-羟基苯甲酸的联合治疗,因此其最佳效果的混合比例值得进一步研究。
2
花青素及其代谢物的神经保护作用与它们在防止蛋白质聚集和促进自噬中的潜在作用有关。
蛋白质聚集被认为刺激神经元变性,与许多神经退行性疾病有关。例如,由聚集的淀粉样蛋白(Aβ)形成的斑块和由tau蛋白形成的神经原纤维缠结是阿尔茨海默病的标志。导致路易体形成的α-突触核蛋白(αS)的异常组装与帕金森病有关。
√原儿茶酸防止蛋白质异常聚集
48小时原儿茶酸处理(10至100 μM)对Aβ和αS原纤维聚集的抑制率分别为30–79%和70–80%。原儿茶酸治疗6天(100μM)也使预先形成的Aβ原纤维和αS原纤维不稳定65%和80%。
这些结果表明,原儿茶酸不仅能抑制Aβ和αS纤颤,还能逆转预先形成的纤颤,它们共同调节蛋白质相互作用,防止蛋白质异常聚集导致的细胞死亡
√香草酸的干预有助于治疗阿尔兹海默病
香草酸是黑芝麻色素释放的主要代谢物,它显示出对β-淀粉样蛋白的抑制活性。在用6μM香草酸处理24小时后发现一半(50%)的抑制,在50μM香草酸孵育时达到90%的抑制。
此外,较高浓度的香草酸(60μM)可使β-分泌酶活性降低60%。β-分泌酶是一种在神经元中催化淀粉样前体蛋白合成淀粉样肽的第一步酶,促进蛋白质聚集。抑制β-分泌酶活性被认为是治疗阿尔茨海默病的另一种方法。
3
花青素微生物降解产物的有益作用已通过调节神经元细胞凋亡信号通路被发现。诱导细胞死亡是神经退行性疾病的最终病理活动。
√花青素代谢物调控细胞凋亡信号
原儿茶酸在最近的动物研究中显示出抗凋亡能力。原儿茶酸通过上调大脑皮层中参与抗氧化活性的基因,如Sod2、Cat、Gpx1和Gsr,来阻止镉诱导的细胞凋亡。
原儿茶酸处理可以减轻镉引起的促炎生物标志物肿瘤坏死因子和IL-1β的表达增加,这表明原儿茶酸通过介导促凋亡蛋白和抗凋亡蛋白,增强抗氧化防御系统和减少炎症细胞因子的产生来保护皮质组织免受镉损伤。
总之,这些发现表明花青素代谢物不仅可以减轻导致神经元死亡的各种诱导剂,还可以调节凋亡信号,从而在多个层面上降低神经退行性病变的风险。
√花青素介导的肠道菌群变化减少了神经退行性疾病的风险
除了花青素及其代谢物有助于神经保护作用外,花青素介导的肠道微生物群变化间接减少了神经退行性疾病的发生。
研究表明,由于脂多糖诱导的神经炎症反应、血脑屏障渗漏增加和β-淀粉样蛋白错误折叠的发生率,肠道生态失调可能增加神经退行性疾病的易感性。
在高脂喂养大鼠中补充黑莓花青素(25mg/kg)17天可以抵消高脂饮食引起的部分生态失调,例如孢杆菌属(sporobacter)数量增加和瘤胃球菌(Rumminococcus)数量减少。
花青素相关的肠道菌群调节通过犬尿氨酸途径改变色氨酸代谢,从而与抗神经炎症活性相关。这种改变被证明可以增加犬尿氨酸的产生,犬尿酸是一种抗兴奋毒性分子,可以减轻神经退行性病变。
尽管花青素介导的色氨酸代谢对神经保护的证据有限,但肠道微生物群对色氨酸代谢的操纵很可能会影响肠-脑轴。
建议
花青素及其微生物代谢产物可能是治疗神经退行性疾病的有效分子。然而,由于大多数研究结果都是基于体外或动物模型,因此在未来的研究中需要进行大量的临床前和临床研究。
由于衰老是神经退行性变的主要危险因素,因此有必要以老年人为重点补充花青素,以探索其在认知改善中的作用和肠道微生物群。
▼
•花青素抑制了炎性细胞因子的产生
花青素可以通过调节微生物群来预防肠道疾病。在葡聚糖硫酸钠(DSS)诱导的结肠炎小鼠中,用枸杞中的花青素提取物(200 mg/kg/天)喂养持续至少一周,恢复了紧密连接蛋白的表达,抑制炎症细胞因子(如TNF-α,IL-6)的产生。
同样,食用富含花青素的马铃薯持续9周喂养结肠炎小鼠,缓解了结肠长度的缩短,降低了髓过氧化物酶(炎性粘膜标志物)水平和炎性细胞因子。
•微生物群是花青素调节炎症性肠病的介质
然而,这种作用在抗生素治疗的小鼠身上消失了,强烈表明微生物群作为花青素对炎症性肠病介质的作用。
▼
摄入花青素可通过多种潜在机制降低患非酒精性脂肪性肝病的风险,例如其固有的抗炎作用、脂质代谢和葡萄糖代谢的管理以及改变微生物群特性。
•改变了脂肪肝小鼠体内的微生物群
其他研究也证明了花青素改变微生物群的作用,但花青素来源的多样性可能导致不同的微生物种群发生改变。在高脂饮食诱导的非酒精性脂肪肝变性小鼠中,摄入桑树水提取物(0.2-0.6%)可减少促炎的Turicibacteres,并提高拟杆菌(Bacteroidales)与梭菌(Clostridiales)的比例。
总的来说,花青素的摄入可能会改变肠道微生物群的组成,从而改善肠道屏障功能和能量消耗,降低肥胖、炎症、胰岛素抵抗,并最终降低非酒精性脂肪性肝病及其代谢并发症的风险。
▼
先前的动物研究已经证明了花青素通过微生物群调节途径抑制肿瘤生长和癌症进展的潜力。
•花青素治疗后肿瘤计数显著降低
在结直肠癌小鼠模型中,用覆盆子花青素治疗可显著削弱结肠癌的发生,每只动物的肿瘤计数减少约90%,肿瘤发病率降低(从100%降至72%左右)。
肠道生态失调可能与结直肠癌的增加有关,而花青素似乎可以恢复这种平衡,并通过促进乳酸菌的生长、抑制肠球菌和脱硫弧菌来调节微生物群。
此外,口服越桔花青素可能通过微生物群加速免疫检查点抑制剂(即程序性死亡配体1,可以限制T免疫细胞反应激活的蛋白质)的肿瘤抑制特性。
研究人员提出,补充花青素可改善肠道物种多样性,诱导梭状芽孢杆菌、约氏乳杆菌和毛螺菌科的丰度增加。
▼
花青素有可能降低慢性肾脏疾病的风险。慢性肾脏疾病的特点是肠道生态失调和由此产生的尿毒症毒素。
在一项研究中,花青素显示出通过AMPK磷酸化减轻培养细胞中糖尿病肾病的能力,并在腺嘌呤诱导的慢性肾病小鼠模型中减轻症状。
▼
花青素和富含花青素的食品的抗炎作用也与减缓骨关节炎和骨修复的进展有关,主要是通过抑制MAPK信号通路和NF-kB信号通路。
认识了花青素对人体健康的重要性,那么我们在日常生活中应该如何去补充呢,谷禾在这里列出了一些建议。
水果:存在于葡萄、蓝莓、桑葚、血橙、草莓、樱桃、红心火龙果、山楂等水果中,与水果色泽有一定的关系,在外观上有所体现,水果是补充花青素的较好选择;
蔬菜:如紫甘蓝、紫薯、紫玉米、紫土豆、黑枸杞、茄子、紫苏、甜菜、萝卜、紫洋葱等蔬菜中,也含有较多的花青素;
谷物:大麦、高粱、黑米,以及豆类如绿豆、红豆、黑豆、黄豆、赤小豆等,其中也含有较多的花青素。
花青素易受热、光、氧等因素的影响而降解,因此建议选择新鲜的食物食用,以保证花青素的含量。
花青素在高温下易被破坏,因此建议采用轻微加热的烹饪方式,如蒸、煮、炖等,以尽可能保留花青素的含量。
花青素与其他营养素的搭配可以增强其吸收和利用效果。例如,与维生素C搭配可以增强花青素的抗氧化作用。
如果日常饮食中花青素的摄入量不足,可以考虑适当补充花青素保健品。但是,需要注意选择正规品牌和适量摄入。
虽然花青素对人体健康具有多种保护作用,但过量摄入也可能对健康造成负面影响。
因此,建议适量摄入花青素,不要过度依赖花青素保健品等补充剂。
总之,通过日常饮食摄入富含花青素的食物,可以有效补充花青素,发挥其保健作用。同时,需要注意花青素的摄入量和搭配方式,以充分发挥其保健作用。
总的来说,花青素的健康益处已被广泛研究,它们被认为可以有效减轻或预防一些疾病。
通过与肠道微生物相互作用了解花青素及其健康益处是很重要的。肠道菌群在花青素降解过程中发挥重要作用,并介导多种生理活动。
花青素也会改变肠道微生物组成,维持微生态平衡,操纵短链脂肪酸的产生、脂肪代谢、肠道上皮功能、与中枢神经系统的联系和免疫反应。
因此,花青素的潜在益处可能间接归因于其对肠道微生物群的调节作用及其随之而来的生理影响。由于这些原因,研究花青素和肠道微生物群的相互作用在慢性疾病预防和治疗中是很重要的。
主要参考文献
Liang A, Leonard W, Beasley JT, Fang Z, Zhang P, Ranadheera CS. Anthocyanins-gut microbiota-health axis: A review. Crit Rev Food Sci Nutr. 2023 Mar 17:1-26.
Akbari, G. 2020. Molecular mechanisms underlying gallic acid effects against cardiovascular diseases: An update review. Avicenna Journal of Phytomedicine 10 (1):11–23.
Agustí, A., M. P. García-Pardo, I. López-Almela, I. Campillo, M. Maes, M. Romaní-Pérez, and Y. Sanz. 2018. Interplay between the gut-brain axis, obesity and cognitive function. Frontiers in Neuroscience 12:155.
Cortés‐Martín, A., C. E. Iglesias‐Aguirre, A. Meoro, M. V. Selma, and J. C. Espín. 2021. Pharmacological therapy determines the gut microbiota modulation by a pomegranate extract nutraceutical in metabolic syndrome: A randomized clinical trial. Molecular Nutrition & Food Research 65 (6):2001048. 2001048.
Drago, L. 2019. Probiotics and colon cancer. Microorganisms 7 (3):66.
Foley, M. H., S. O’Flaherty, R. Barrangou, and C. M. Theriot. 2019. Bile salt hydrolases: Gatekeepers of bile acid metabolism and host-microbiome crosstalk in the gastrointestinal tract. PLOS Pathogens 15 (3):e1007581.
Hampel, H., R. Vassar, B. De Strooper, J. Hardy, M. Willem, N. Singh, … A. De Vos. 2020. The β-secretase BACE1 in Alzheimer’s disease. Biological Psychiatry 89 (8):745–756.