-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com



人体内有宏量营养素(脂肪,蛋白质和碳水化合物),还有微量营养素。虽然称为“微量”,但它很强大,是维持正常生理活动的必需品。
微量营养素的发现:
1912年,波兰生物化学家卡西米尔·芬克发现了第一种微量营养素。他开始假设我们的食物中一定有其他“必需营养素”是维持健康所必需的。他把这些神秘的化合物称为“vital amines”,最终简称为“vitamins”(维生素)。
一百多年后,科学家们进行了大量的研究,列出了人体正常功能所需的近30种维生素和矿物质。饮食中哪怕只有一种微量营养素是缺乏的,其后果也可能是严重的。
对于每一种维生素或矿物质缺乏症,身体会迅速开始出现严重的功能失调。
例如,维生素A在维持机体正常的视力、基因表达、生殖、胚胎发育、生长和免疫功能等方面发挥着重要的作用。

维生素A缺乏可能会出现眼部疾病,儿童缺乏维生素A也会出现生长发育迟滞、血细胞生成障碍等问题。
<其他营养物质缺乏可详见本文末章节>
总之,每种微量营养素都在体内发挥作用。而每种缺陷都与疾病状况密切相关。
因此,在饮食中获取足够的必需微量营养素是维持健康的必要条件。
现代营养倡导“多样化”,食用各种类型的食物,以确保能够摄入身体所需的所有维生素和矿物质。
可能你吃到的大多数谷物,面包和其他加工谷物都已添加了各种B族维生素(和其他矿物质)。此外,很多人都会在饮食中加入水果,蔬菜,谷物和蛋白质等,尽可能地去满足大部分营养素所需的摄入量。
但问题来了,并不是你吃了什么就有什么,也得看身体的吸收能力。
有时候虽然吃的多,但并不代表消化系统已经为吸收做好了充分的准备。
为了更好地吸收营养,身体需要做好准备。这里涉及几个因素,例如健康的肠壁和肠道菌群,还取决于微量营养素的吸收方式和吸收位置。
消化过程:
消化系统的首要作用是摄取食物,并将其分解为更小,更有用的成分。
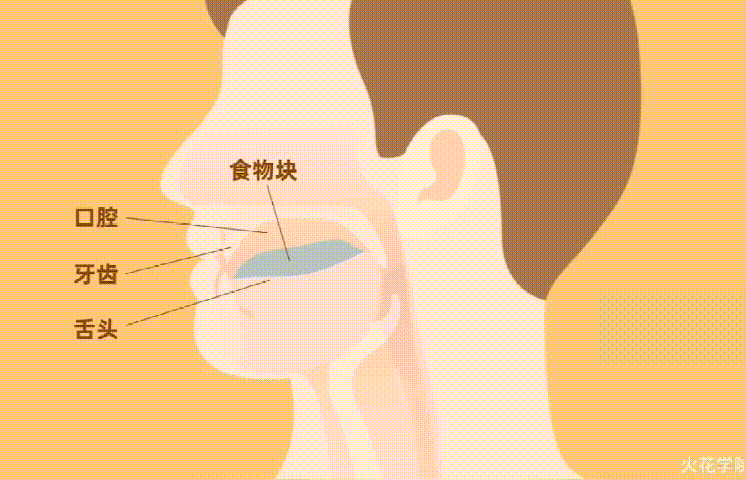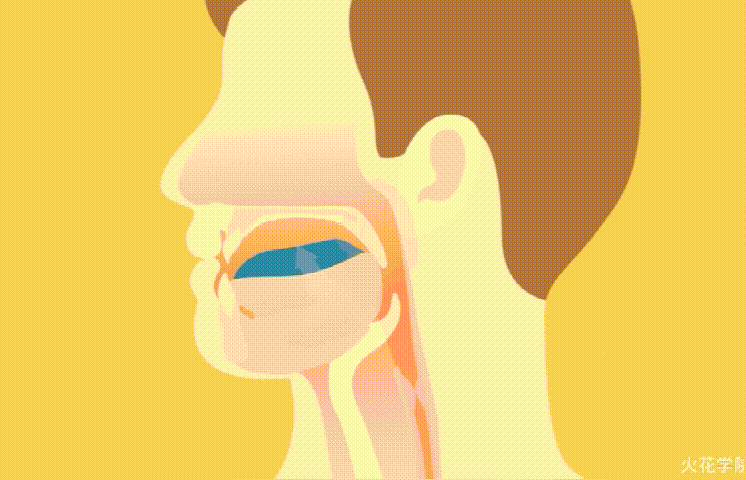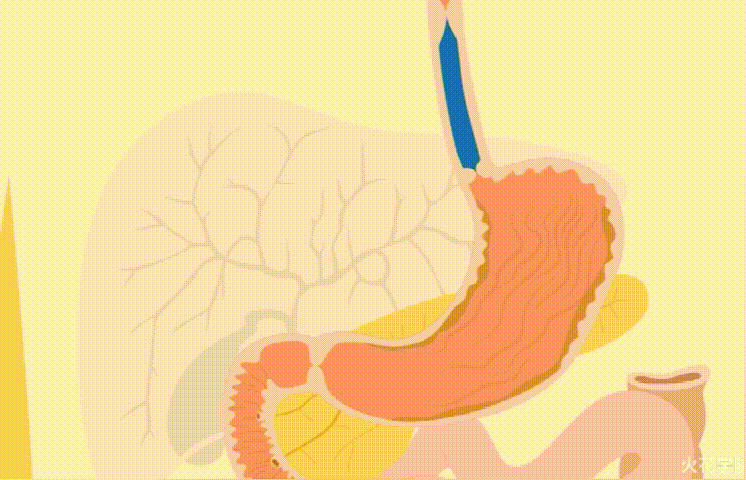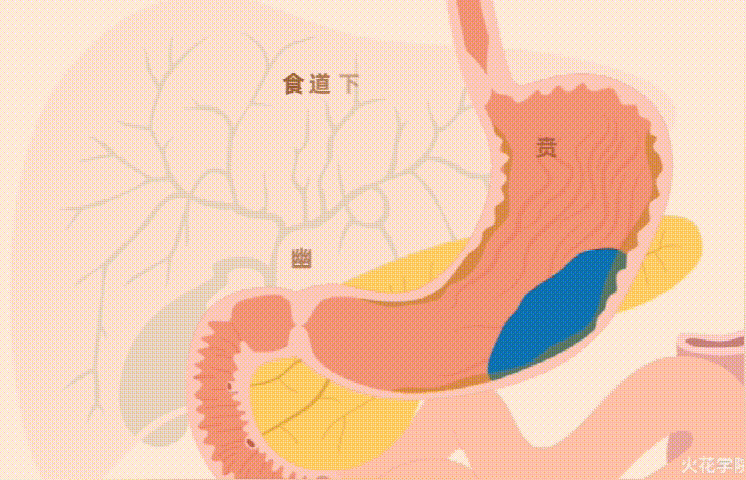
将食物放入嘴后立即开始第一步。当牙齿将食物粉碎成较小的碎片时,唾液腺开始分泌酶,其唯一目的是分解碳水化合物。
一旦被吞咽,食物就会进入食道并进入胃,暴露于强酸性胃液中,进一步降解碳水化合物,蛋白质和脂肪。
然后,消化后的食物被释放到小肠,接着,肝脏,胆囊和胰腺会分泌更多的消化酶,从而为营养吸收做好准备。
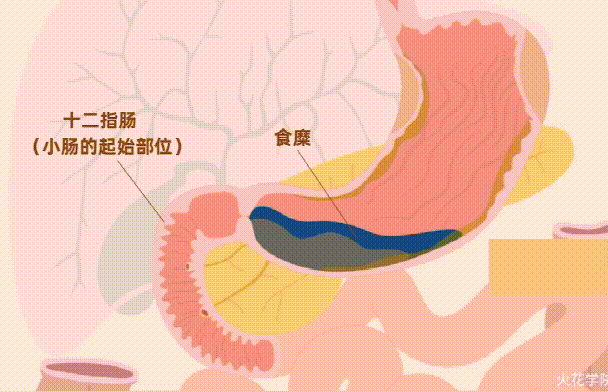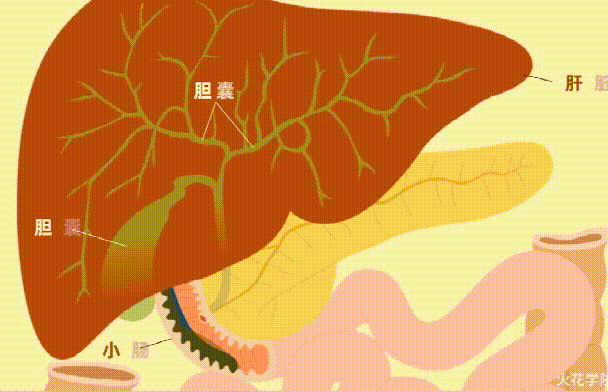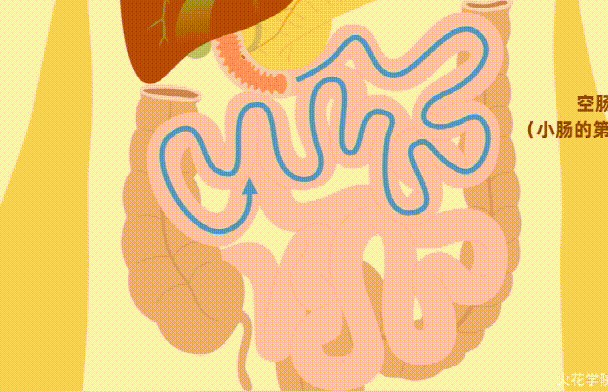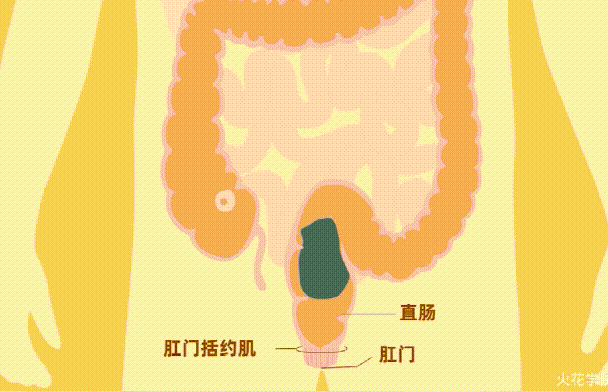
小 肠
小肠由三个不同的部分组成:十二指肠、空肠和回肠。大部分的营养吸收过程都在这里。
小肠吸收了食物中的成分,包括单糖、氨基酸、脂肪酸,微量营养素。大部分维生素和矿物质会在小肠中被吸收,但每种维生素和矿物质都需要独特的机制才能穿过肠道细胞壁。
当消化后的食物通过小肠并经历吸收营养过程后,最终进入大肠,然后被排出。
大 肠
大肠在消化中的作用相当直接。当食物的剩余成分进入大肠时,大部分营养物质已经被消化吸收了,它的主要功能是去除多余的水分和盐分,为排泄做好准备。残余物通常被分解成难以消化的残余物,如不易消化的纤维等。
现在我们知道这个领域有很多其他的关键功能。随着对肠道微生物群的更广泛了解,我们知道大多数肠道细菌在这一区域定居,吸收我们身体无法消化的东西,并将其分解,转化为对身体有益的许多必须营养素,从而给人体带来好处。
了解不同微量营养素的差异
了解不同类型的微量营养素之间的差异是改善吸收的一种方法。
例如有两类维生素:水溶性(各种维生素B和C)和脂溶性(如A、D、E和K)。
水溶性维生素需要水来运输。多喝水可以提高身体吸收和运输这些营养物质的能力。
脂溶性维生素需要脂肪来帮助吸收。改善脂肪转运的最好方法之一就是用脂溶性维生素丰富的食物来摄取健康的脂肪,确保身体能适当地吸收。
此外,水溶性维生素和矿物质都需要肠细胞内壁的特殊“转运体”来穿过细胞膜进入血液。功能越专业,保护性就越强。这种复杂而特殊的吸收过程确保只有正确的成分才能进入血液。
肠道菌群 ——营养吸收的低调英雄
微生物不仅有助于吸收营养,甚至可以提高必需营养素的水平。健康的肠道生态系统有助于维持肠道黏膜的完整。
为了真正优化吸收过程,身体需要健康的肠道细胞来吸收营养。
肠道菌群失衡可导致肠道细胞衰亡,破坏营养吸收。这大大降低了消化系统吸收修复和维持健康细胞所必需营养的能力。
肠道菌群被证明是许多必需营养素的来源。维生素K就是一个例子。
虽然我们的饮食中含有维生素K,但实际上,人体每天所需维生素K的一半以上是由肠道中的细菌产生的。
如果你的肠道生态系统不平衡,缺乏某些菌群,可能导致身体缺乏某些维生素。
因此,调理改善肠道菌群是一种可行的方式。
当然,每个人对营养物质的需求是独一无二的。归根结底,这取决于你的身体运作方式,基于生活方式、饮食、个人需求,以及肠道健康状况等多方面因素。
了解饮食中的差距可能是改善营养吸收的第一步。另外,肠道菌群检测有助于对身体健康状况的把握,知道补充哪些营养素,有助于什么类型的菌群生长,结合自身的症状,有针对性地改善菌群,从而真正改善健康状况。
随着对肠道菌群,营养饮食的研究深入,现在越来越倾向于个性化的干预方式,更加精准地选择适合自己的营养素,而不是盲目补充维生素。
1. 缺钙
麻木,手指发麻和心律异常
钙对于维持强壮的骨骼以及控制肌肉和神经功能非常重要 。严重低钙的迹象包括麻木,手指刺痛和心律异常等。
日需求量
大多数成年人每天需要1000毫克(mg)的钙,而50岁以上的女性和70岁以上的男性则需要1200毫克 。
补充钙
牛奶,酸奶,奶酪等乳制品是钙的良好来源,但如果不喜欢乳制品,可以在钙强化的橙汁或早餐麦片中获得。

2. 缺维生素D
疲劳,骨痛,情绪变化等
维生素D对骨骼健康至关重要,不过,维生素D缺乏的症状可能是模糊的,有可能出现疲劳、骨痛、情绪变化、肌肉疼痛、虚弱等。
维生素D长期缺乏会导致骨骼软化,还可能与癌症和自身免疫性疾病有关。
日需求量
大多数成年人每天需要15微克(mcg)的维生素D,而70岁以上的成年人则需要20 mcg。
补充维生素D
食物:牛奶或酸奶,金枪鱼等。
晒太阳:每周几次晒太阳,每次在10到30分钟内,对补充维生素D有帮助。

3. 缺 钾
肌肉无力,便秘,心律不齐等
钾可以帮助心脏、神经和肌肉正常工作,并在清除废物的同时向细胞输送营养物质。
此外,它还是一种有用的营养素,有助于抵消钠对血压的负面影响,对维持健康的血压很重要。
由于腹泻或呕吐;出汗过多;抗生素、泻药或利尿剂;过量饮酒;或肾脏疾病等慢性疾病,短期可能会出现低钾的情况。
缺乏的症状
包括肌肉无力、抽搐或痉挛;便秘;刺痛和麻木;以及心律异常或心悸。
天然钾的来源
香蕉、牛奶、南瓜、扁豆、芸豆和其他豆类。

4. 缺 铁
疲劳,呼吸急促,手脚冰冷,指甲脆等
铁是产生红细胞的必要物质,红细胞将氧气输送到全身。当铁含量过低时,可能会导致红细胞缺乏,从而导致贫血。
高风险的人群
包括经期妇女、成长中的人(如儿童和孕妇)和纯素食或半素食人群。
症状
包括虚弱和疲劳、呼吸短促、心跳加快、皮肤苍白、头痛、手脚冰冷、舌头肿痛、指甲脆裂以及对灰尘等奇怪事物的渴望。
刚开始的时候,这些症状可能很轻微,以至于你没有注意到有什么不对劲,但随着铁的储备越来越少,这些症状会变得更严重。
日需求量
50岁以上的成年男女每天需要8毫克
50岁以下的成年女性每天需要18毫克
富含铁的食物
牛肉、牡蛎、豆类(尤其是利马、海军和芸豆)、扁豆和菠菜等。

5. 缺维生素B12
麻木,疲劳,舌头肿胀等
维生素B12有助于红细胞和DNA的生成,还能改善神经递质功能。
半素食者和纯素食者可能特别容易缺乏维生素B12,因为植物不能产生维生素B12,而做过减肥手术的人也可能缺乏B12,因为手术后身体难以从食物中提取营养。
严重缺乏B12的症状
腿、手或脚麻木;行走和平衡方面的问题;贫血;疲劳;弱点;舌头肿胀发炎;记忆力差和思考困难,食欲不振。
这些症状可能会很快出现,也可能逐渐出现,而且由于症状的范围很广,有可能在一段时间内都没有注意到。
日需求量
成年人每天只需要:2.4微克(mcg)
怀孕或哺乳期需要更多:每天2.6至2.8 mcg
富含维生素B12食物
牛肉、猪肉、鸡肉、鱼类、内脏类、蛋类、蛤类、牛奶乳酪等。

6. 缺叶酸
疲劳,腹泻,舌苔光滑等
叶酸是一种B族维生素,对育龄女性尤其重要,叶酸支持健康的生长和功能,并能降低出生缺陷的风险,特别是那些涉及神经管(大脑和脊柱)的缺陷。
叶酸缺乏可能会使未出生婴儿的细胞总数和大红细胞数量减少,并导致神经管畸形。
叶酸缺乏的症状
包括疲劳、易怒、腹泻、生长缓慢和舌头光滑、触痛。
怀孕的女性应该确保她们每天摄入400微克的叶酸,此外还要食用含有叶酸的食物。
叶酸最好以补充剂的形式被人体吸收,其中85%是从补充剂中吸收的,50%是从食物中吸收的 。
从食物中获取叶酸
可以选择强化谷物,豆类,花生,葵花籽,全谷类,鸡蛋,深色绿叶蔬菜等。

7. 缺 镁
食欲不振,恶心,疲劳等
镁有助于骨骼健康,能量生成。
虽然缺乏镁在健康人群中并不常见,但某些药物(包括一些抗生素和利尿剂)或慢病(如2型糖尿病和克罗恩病)可能会限制镁的吸收,也可能加速镁在体内的流失。
日需求量
根据性别和年龄的不同,成年人需要310-420毫克镁。
镁缺乏症状
会导致食欲不振、恶心呕吐、疲劳,虚弱等。
在更严重的情况下,它也可能导致麻木和刺痛,肌肉痉挛或收缩,癫痫发作,心律失常,性格改变,或冠状动脉痉挛。
富含镁的食物
如杏仁、腰果、花生、菠菜、黑豆、毛豆等。

相关阅读:
参考文献:
Committee to Review Dietary Reference Intakes for Vitamin D and Calcium, Food and Nutrition Board, Institute of Medicine. Dietary Reference Intakes for Calcium and Vitamin D. Washington, DC: National Academy Press, 2010.
Burt LA, Billington EO, Rose MS, Raymond DA, Hanley DA, Boyd SK. Effect of High-Dose Vitamin D Supplementation on Volumetric Bone Density and Bone Strength: A Randomized Clinical Trial. JAMA. 2019;322(8):736–745.
Mason JB. Vitamins, trace minerals, and other micronutrients. In: Goldman L, Schafer AI, eds. Goldman-Cecil Medicine. 25th ed. Philadelphia, PA: Elsevier Saunders; 2016:chap 218.
Williams J, Mai CT, Mulinare J, et al. Updated estimates of neural tube defects prevented by mandatory folic acid fortification – United States, 1995–2011. MMWR Morb Mortal Wkly Rep. 2015;64(1):1–5.
Qin J, Pei X. Isolation of Human Gastric Epithelial Cells from Gastric Surgical Tissue and Gastric Biopsies for Primary Culture. Methods Mol Biol. 2018;1817:115-121.
Fieker A, Philpott J, Armand M. Enzyme replacement therapy for pancreatic insufficiency: present and future. Clin Exp Gastroenterol. 2011;4:55-73.
Koppel BS. Nutritional and alcohol-related neurologic disorders. In: Goldman L, Schafer AI, eds. Goldman-Cecil Medicine. 26th ed. Philadelphia, PA: Elsevier; 2020:chap 388.
Nutrient Recommendations: Dietary Reference Intakes (DRI) .National Institutes of Health.
Antony AC. Megaloblastic anemias. In: Hoffman R, Benz EJ, Silberstein LE, et al, eds. Hematology: Basic Principles and Practice. 7th ed. Philadelphia, PA: Elsevier; 2018:chap 39.
Veronese N, Stubbs B, Solmi M, et al. Dietary Magnesium Intake and Fracture Risk: Data From a Large Prospective Study. British Journal of Nutrition. June 2017.
Portincasa P, Di Ciaula A, Wang HH, Palasciano G, van Erpecum KJ, Moschetta A, Wang DQ. Coordinate regulation of gallbladder motor function in the gut-liver axis. Hepatology. 2008 Jun;47(6):2112-26.
Vegesna AK, Chuang KY, Besetty R, Phillips SJ, Braverman AS, Barbe MF, Ruggieri MR, Miller LS. Circular smooth muscle contributes to esophageal shortening during peristalsis. World J Gastroenterol. 2012 Aug 28;18(32):4317-22.

谷禾健康
肥胖与许多疾病的风险增加有关,包括糖尿病、心血管疾病和癌症。越来越多的证据也表明肠道菌群失衡与疾病有关。通过调节肠道菌群或许能逆转或干预这些现象。
本期介绍两篇,分别以饮食控制和维生素给予为变量,同时都研究了基线时和干预后肠道菌群的变化。又是新的思路,新的挑战。
第一篇文章研究了基线肠道菌群在饮食控制的前提下是否能预测减肥轨迹?
答案是可以的,研究结论表示作为节食前个人体重减轻轨迹的预测指标,基线肠道微生物的作用超过了其他因素。
研究中对83名受试者(男47人,女36人,年龄20~45岁)进行了为期6个月的在营养师指导下的饮食干预计划。受试人群以以下标准排除:
(1)重大疾病;
(2)怀孕或哺乳;
(3)高血糖或低血糖;
(4)胃肠疾病;
(5)自身免疫性疾病;
(6)甲状腺疾病;
(7)在纳入前1个月内使用抗生素或激素;
(8)预计在研究过程中经常旅行。这也排除了服用上述条件下处方药物(如二甲双胍)的受试者。
按照中国人民解放军总医院营养科的医生设计的膳食计划,即碳水化合物含量为60%-65%,蛋白质含量为24%-26%,脂肪含量为12%-14%(能量百分比)。也包括400-500克蔬菜和100-200克低血糖指数水果,严格遵循饮食建议,卡路里控制在男性1200-1680千卡/天,女性1050-1470千卡/天。
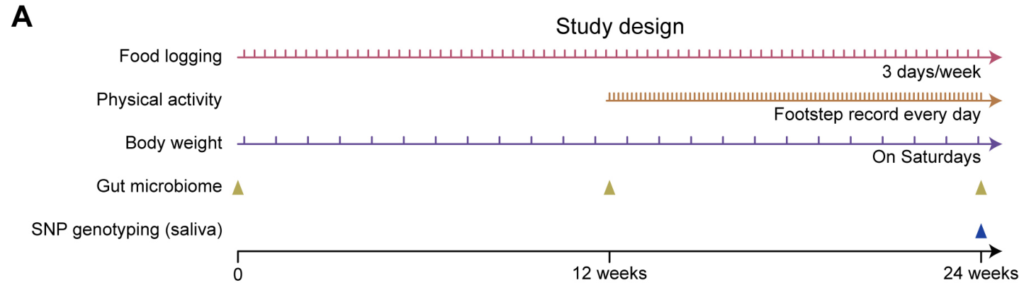
如图,结合电子秤与智能手机应用程序,纵向收集饮食、体力活动、体重和粪便微生物组数据以及SNP基因型,然后整合成高维数据用于后续分析。对采集的粪便样本进行宏基因组鸟枪法测序,得到的序列数据进行物种注释及KEGG功能注释。
1. 饮食因素与体重变化之间的联系因个体不同而不同。
首先确定有哪些饮食因素与所有个体的体重下降有关。使用GLMMLASSO模型,结果如图,当coef为非零时被认为是显著的。发现,在所有受试者中,体重下降与卡路里摄入量(系数=-0.153)、膳食中大量营养素组成(脂肪,系数=-0.161;碳水化合物,系数=-0.055;蛋白质,系数=0.084;纤维,系数=0.1)、膳食微量营养素含量和体力活动之间的具有弱相关。
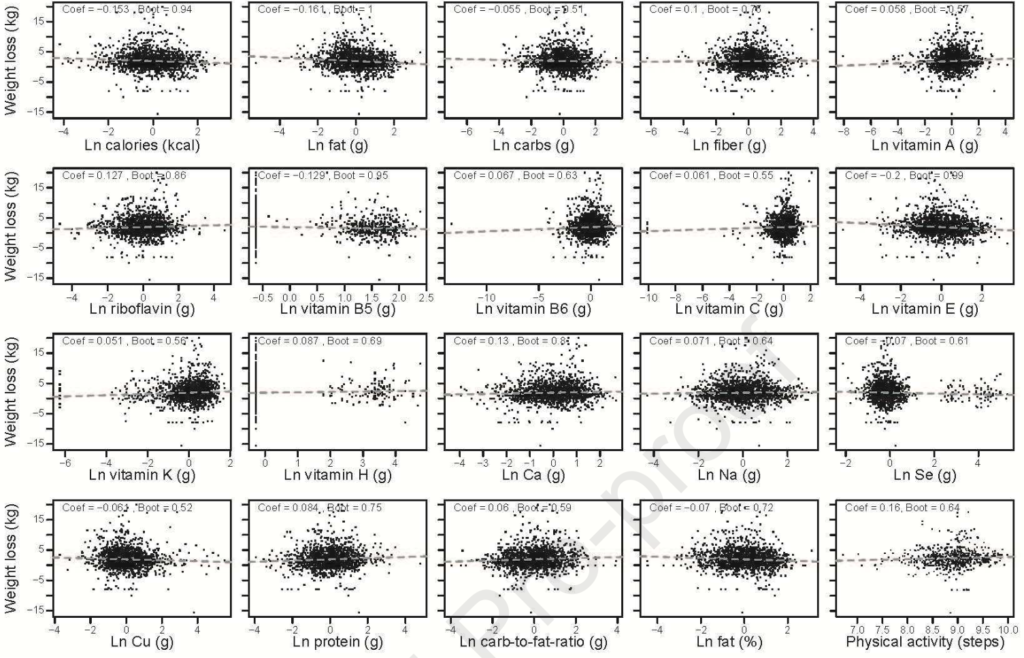
但是在个体间有很大差异。例如在受试者F00161中,纤维摄入量的增加与减肥之间存在正相关关系,而在F00147中,受试者的脂肪摄入量增加与体重减轻之间存在负相关关系。相反,尽管纤维或脂肪摄入量发生变化,F00203人仍然对体重变化不敏感(图G)。所以,即使是相似的膳食大量营养素,体重反应也是高度个性化的。蓝色,coef> 0;红色,coef< 0
2. 作为节食前减肥轨迹的预测指标,基线肠道菌群表现更好。
为了从饮食控制前的基线数据中建立预测体重下降的模型,开发了基于梯度增强回归的机器学习算法,并保留一个受试者进行交叉验证。为了识别除了饮食数据之外最相关的变量,这些模型分别在五组输入上进行了训练:
(1)膳食数据(包括卡路里摄入量、大量营养素组成、食物种类和饮食排序的前三个特征向量);
(2)膳食数据和肥胖相关SNPs;
(3)膳食数据和个人特征(年龄、性别和基线体重指数);
(4)膳食数据和基线肠道微生物群(包括细菌种类丰度和功能模块);
(5)膳食数据、个人特征、SNPs和基线肠道微生物群。

与不包含基线微生物群数据的模型相比,包含基线微生物群数据的模型的预测精度大大提高,而包括个人特征或肥胖相关的宿主基因组SNP对预测精度的贡献很小[(1)r=0.137;(2)r=0.073;(3)r=0.159;(4)r=0.523;(5)r=0.509]。因此,基线肠道菌群数据在预测6个月饮食控制计划期间体重变化方面优于其他因素(P <1e-14)。
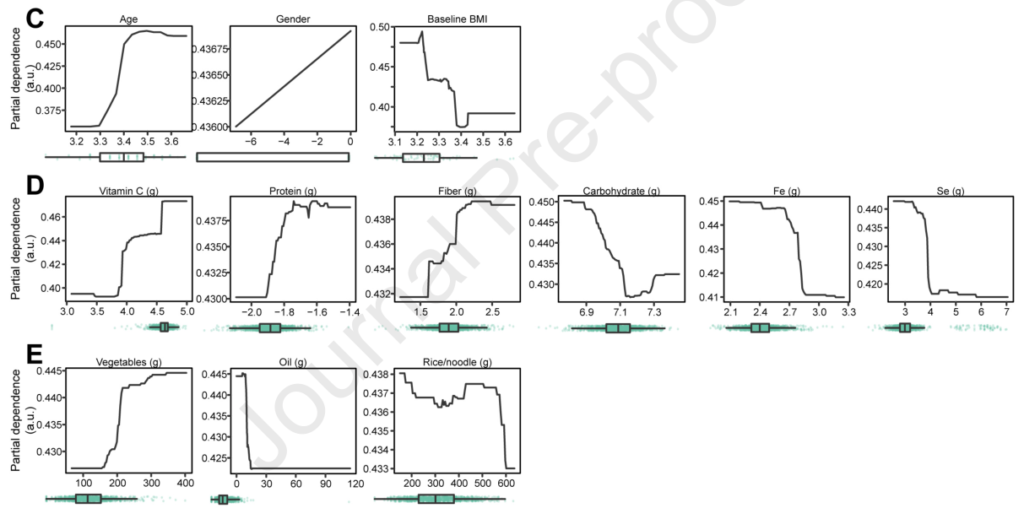
之后,研究人员进行了更细致的模型训练,发现了对体重下降模型影响最大的几个物种:

在功能分析中,发现涉及赖氨酸生物合成(M00030)和多糖运输系统(M00216)的模块对预测模型的影响最大

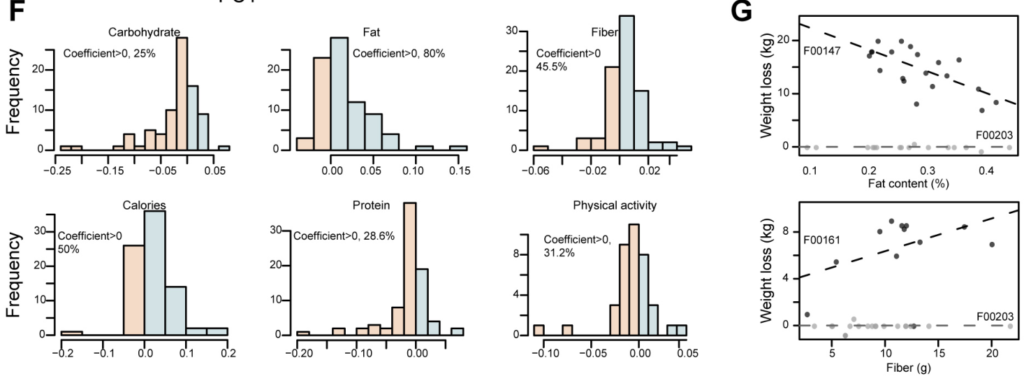
以及其他影响不那么显著的变量:年龄增加对模型产生积极影响,而基线BMI则相反;增加维生素C、蛋白质和纤维的摄入量对模型产生积极影响,而增加碳水化合物、铁和硒的摄入量则相反;剩下的几种维生素和矿物质、蔬菜、油、米和面条的摄入量以及与肥胖相关的6个SNP的基因型也对该模型产生了微弱的影响。以上这些变量都是重要的因素,可能有助于或阻止普通人群在长期节食期间的减肥轨迹。
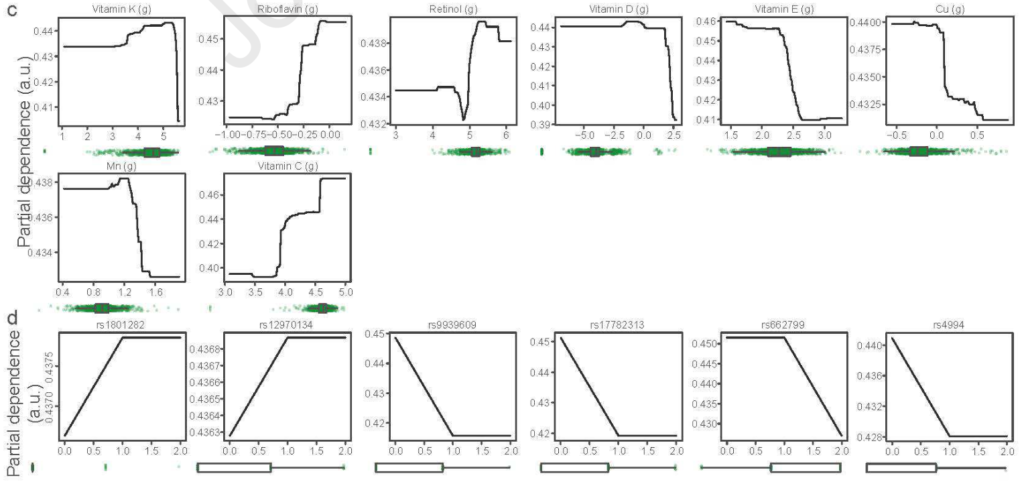
3. 饮食控制期间肠道菌群的组成变化是否会影响减肥轨迹。
研究发现许多参与者的肠道菌群组成发生了实质性的变化,0-3个月的微生物群的变化幅度与体重下降的程度呈正相关,有15个个体肠型被改变了,体重变化范围从20公斤到+7公斤。这两个时间段都是一致的。这一发现表明,在饮食控制计划中,饮食和肠道菌群之间存在着持续的相互作用。如图:
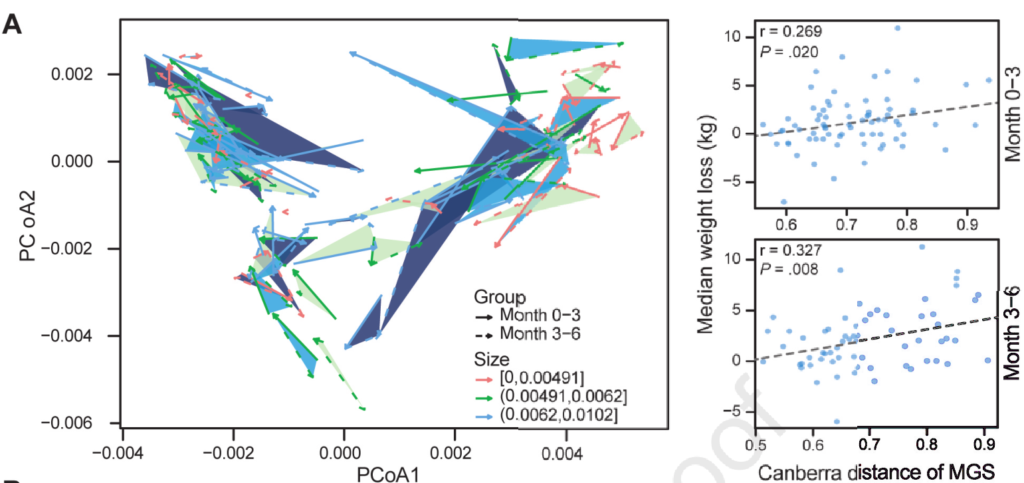
同时使用随机森林算法,基于相对于基线的种水平物种变化来预测体重下降,预测精度R=0.271,发现R. gnavus (MGS0160), Bacteroides massiliensis (MGS1424)和Bacteroides finegoldii (MGS0729)这三个物种在模型中贡献度最大。

继续统计了一些在肥胖个体中丰富或减少的物种和功能以及那些与体重变化共同变化的细菌种类。其中,粪球菌属Coprococcus sp. (MGS0232)、Holdemanellabiformis (MGS1464)、Solobacterium moorei (MGS0945)、活泼瘤胃球菌R. gnavus (MGS0160)和Clostridium (MGS0558) 在肥胖个体中显著富集,且它们的减少与体重下降显著相关;Coprobacter (MGS1138)、Bacteroides intestinalis (MGS0117和MGS1302)、阿克曼菌Akkermansia muciniphila (MGS0120)、Alistipes obesi (MGS0342)和坦纳菌属Tannerella sp. (MGS0276)在瘦人个体中显著富集,且其在饮食控制过程中的增加与体重下降显著相关;在瘦人个体中,编码脂肪酸生物合成(M00085)的基因在基线时显著富集,且其增加与体重减轻相关。如下图:
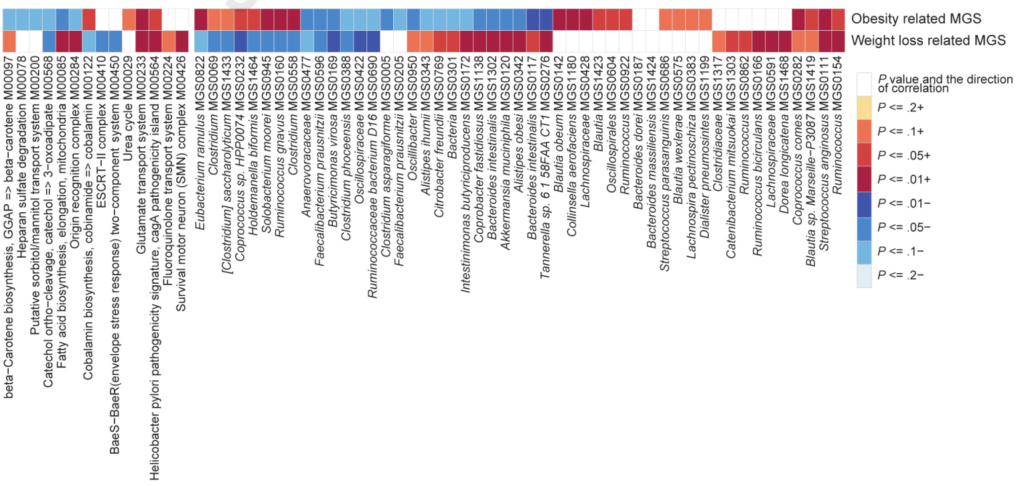
这些结果表明可以基于基线肠道菌群组成和饮食数据建立个性化的体重预测模型。我们可以利用肠道菌群的分布做个性化的饮食推荐,以此调节体重,进而促进宿主健康。文章中发现的R. gnavus (MGS0160)、B. massiliensis(MGS1424)和B. finegoldii (MGS0729)这三种物种与体重下降显著相关,它们的减少有利于体重下降。这可以记一下,要是有机会做肠道菌群检测,可以参考参考。
第二篇文章,主要研究对结肠靶向给维生素对人体肠道菌群的组成和代谢活性的影响。通过人类临床研究和体外的批量发酵实验,结合评估屏障和免疫功能的细胞模型,研究了结肠输送的维生素A、B2、C、D和E对肠道菌群的影响。大家都比较熟知益生元或一些益生元成分如低聚果糖(FOS)、低聚半乳糖(GOS)和菊粉对肠道的影响。
最近一篇使用高剂量维生素或结肠靶向配方的干预研究表示,维生素会影响肠道菌群。补充100 mg核黄素14d可以增加健康受试者每克粪便中丁酸产生菌(Faecalibacterium prausnitzii和Roseburia)的数量,并减少炎症性肠病(IBD)患者的肠杆菌科细菌数量。
一共96名健康志愿者参与了这项研究,其中12人分成6组不同的维生素组(维生素A、维生素B2、维生素C、维生素B2+C、维生素D3和维生素E),安慰剂组有24人参与。
排除标准如下:严重急性或慢性疾病;吸烟;怀孕;在过去3个月内使用抗生素;药物和/或酒精滥用史(每天2份以上);过去3个月的主要饮食变化;饮食障碍;素食或纯素食;灌肠;膳食补充剂,包括基线访问前4周内和干预期间的益生元、益生菌或富含纤维的补充剂;高纤维饮食(即>30克);治疗活动性胃肠道疾病的慢性药物(除非该产品在筛查前服用至少2个月,并在整个研究期间保持相同的剂量);最近排便习惯的改变(<3个月);以及腹痛。
所有受试者在为期4周的时间里每天服用维生素补充剂或安慰剂,一共三次数据采集:筛查,基线(筛查后1周),基线后4周。每次都采集空腹静脉血样本,填写问卷,并在基线时和干预4周后,从每个受试者身上收集两份粪便样本。用于获知粪便微生物组成、粪便短链脂肪酸水平、粪便氨含量、血浆和粪便维生素B2浓度、粪便氧化还原和pH值、生活质量和胃肠道症状问卷等信息。
对肠道菌群组成分析,比较了结肠注射维生素干预前后的多样性指数。
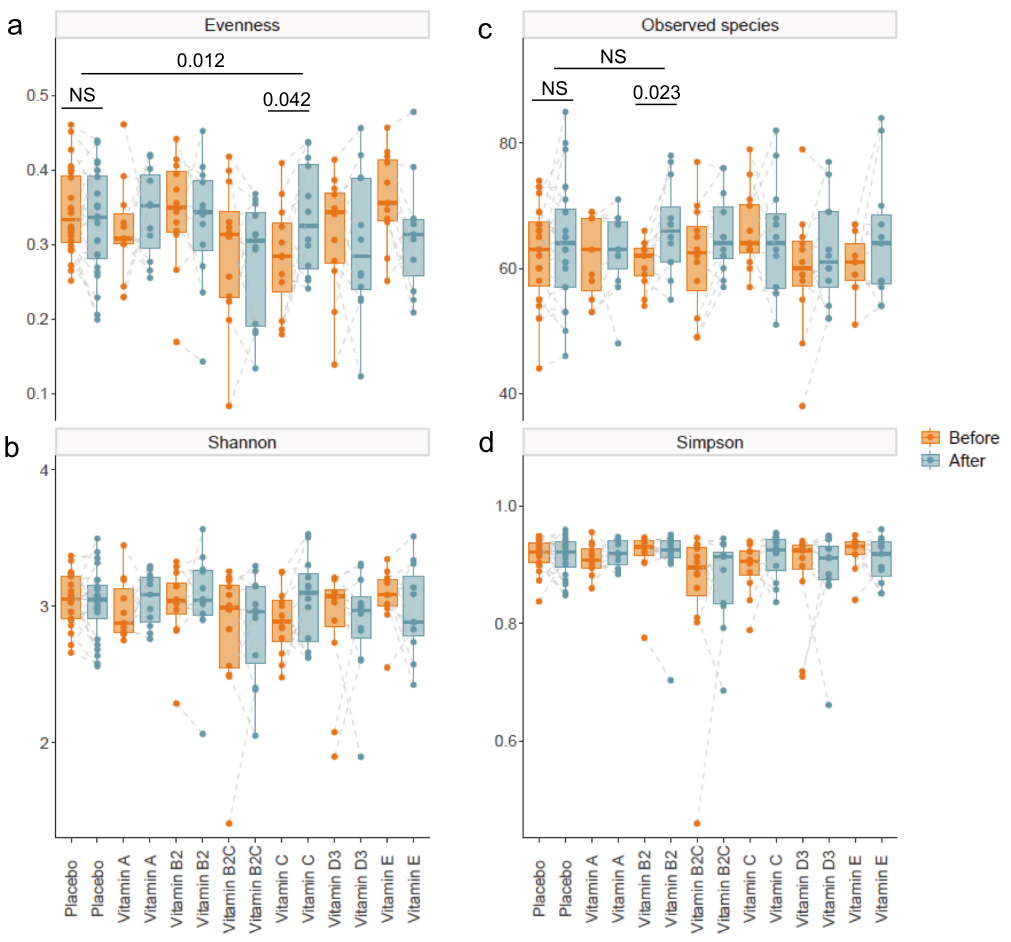
结果表明,与基线组(p=0.042)和安慰剂组(p=0.012)相比,维生素C在第四周显著提高了肠道微生物群落的均匀性。此外,与基线相比,维生素B2显著增加了观察到的物种数量(p=0.023)。
Bray-Curtis距离的置换多变量方差分析(PERMANOVA)表明,肠道微生物beta多样性的总体变化在组间或组内与基线相比没有显著差异。
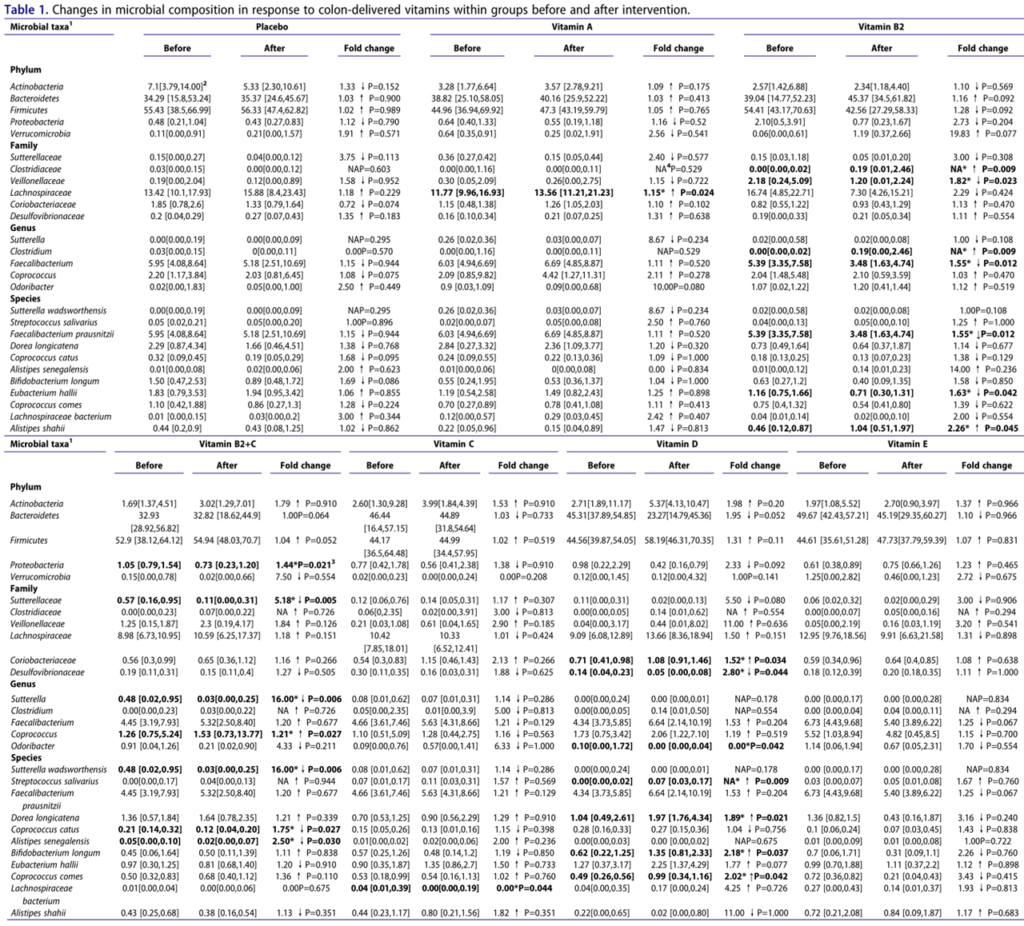
不同的维生素引起组内以及治疗组和安慰剂组在门、科、属和种水平上肠道微生物组成的变化。

门水平:维生素B2+C导致变形杆菌显著减少(p=.021),与基线相比菌落数量增加和拟杆菌数量减少。此外,服用维生素D后,与基线相比,拟杆菌有减少的趋势(p=.052),与安慰剂相比有显著差异(p=.038)。最后,与安慰剂相比,维生素D和维生素A显著增加了放线杆菌的数量(p=.033和p=.041)。
通过测量粪便中的SCFA浓度来评估肠道微生物群的代谢活性(下图)。
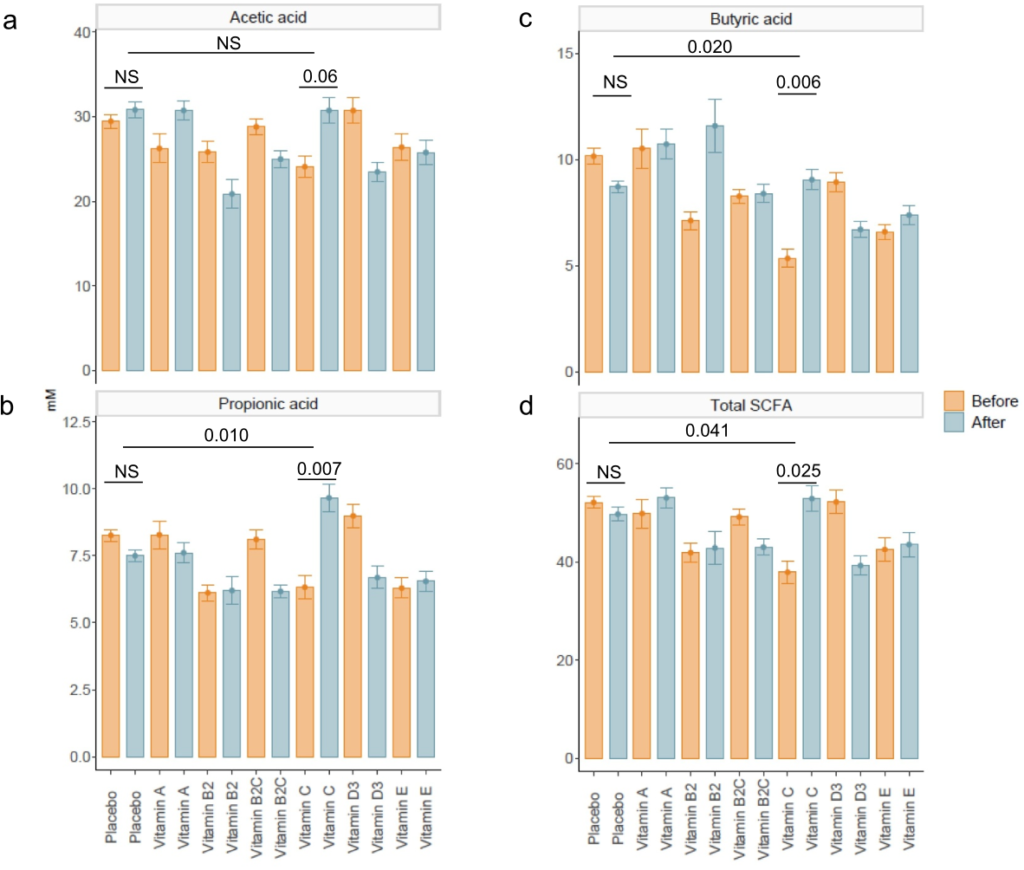
我们发现,与基线相比,维生素C显著增加了总SCFA(p=.025)、丙酸(p=.007)和丁酸(p=.006)浓度。与安慰剂相比,这些效果也很明显(分别为p=.041,p=.010和p=.020)。与安慰剂相比,服用维生素C对粪便pH值的降低更明显,但是,两组之间没有显著差异。
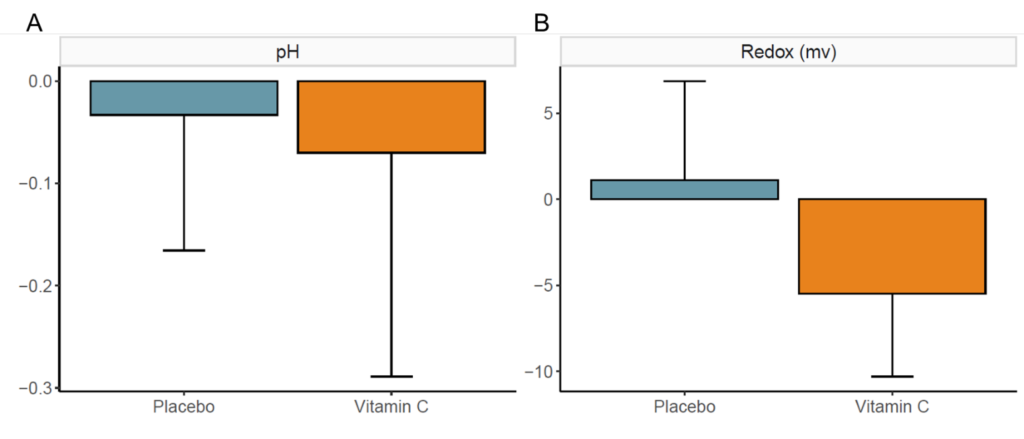
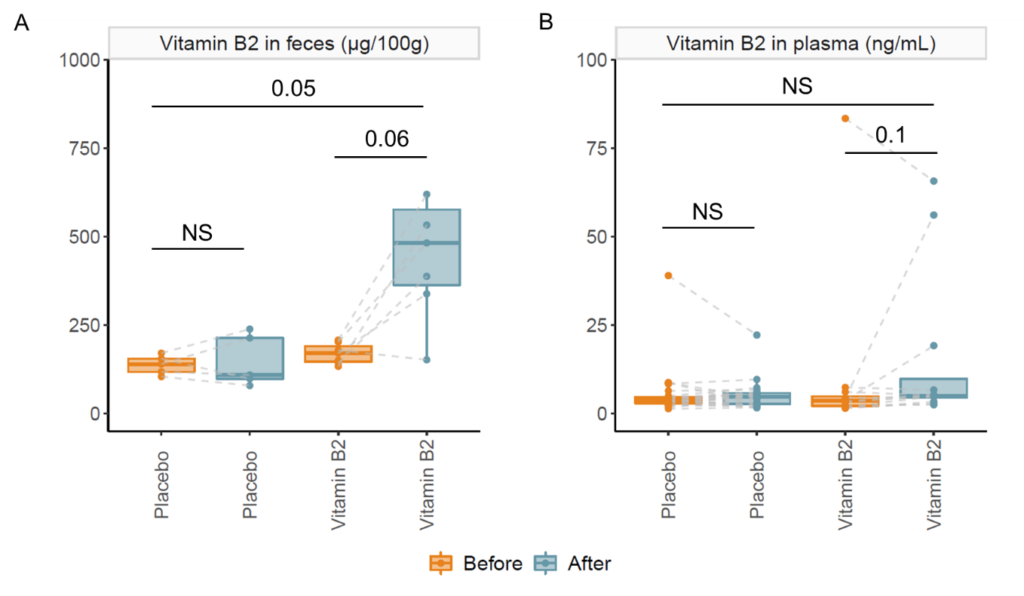
在服用维生素C后,粪便氧化还原电位降低,而服用安慰剂后,粪便氧化还原电位升高;然而,两组间也没有显著差异。最后为了确认维生素是否被输送到结肠,测量了干预前后粪便和血浆中维生素B2的浓度,并与安慰剂进行了比较。与基线(p=0.06)和安慰剂(p=0.05)相比,粪便中的维生素B2增加了。但是,这对血浆维生素B2浓度没有显著影响。
体外研究:
对3名粪便样本供体(男性,26岁;女性,35岁;女性,29岁)进行了短期结肠发酵实验,选出一名SCFA产量平衡的供体进入最终发酵实验。在发酵前(0h)和发酵后(48h)分别从每个发酵瓶采集出水样品,用0.22µm滤器过滤灭菌。样品用来分析粪便微生物组成、微生物体外代谢活性、Caco-2和HT29-MTX-E12细胞培养及屏障功能、HT29细胞培养和免疫功能。
加权UniFrac距离的主坐标分析(PCoA)显示发酵前(0h)和发酵后(24h)样品之间的分离,表明发酵随时间的影响(图a)。大多数维生素处理24 h的微生物群与24 h对照样品聚集在一起,表明维生素和对照样品之间的beta多样性没有变化。
然而,经维生素E(1x和5x)、维生素C(0.2x和5x)、维生素D(1x)和维生素B2+C(5x)处理24h的样品与对照样品明显分离,表明维生素处理对发酵过程中微生物群落的组成有一定的影响。此外,添加不同浓度的维生素C、E、B2+C、B2、A和叶酸,与24小时的对照相比,观察到的物种数量增加,表明对α多样性有影响。
同时,经维生素处理后,所有分类水平都有了些许变化,在门水平上变化最明显的是放线菌门(Actinobacteria)、厚壁菌门(Firmicutes)和Verrucomicrobia的增加以及拟杆菌门(Bacteroidetes)的减少,特别是维生素E、B2、B2 + C和C的添加。
在属水平上,除维生素B2以外,所有维生素都使Roseburia增加,而维生素C、B2、B2 + C、D和E增加了Akkermansia、Bifidobacterium和Faecalibacterium的相对丰度。
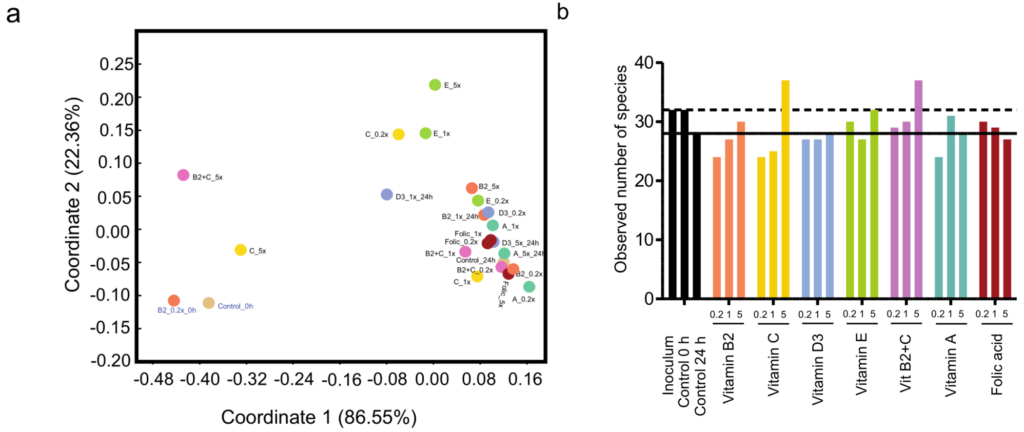
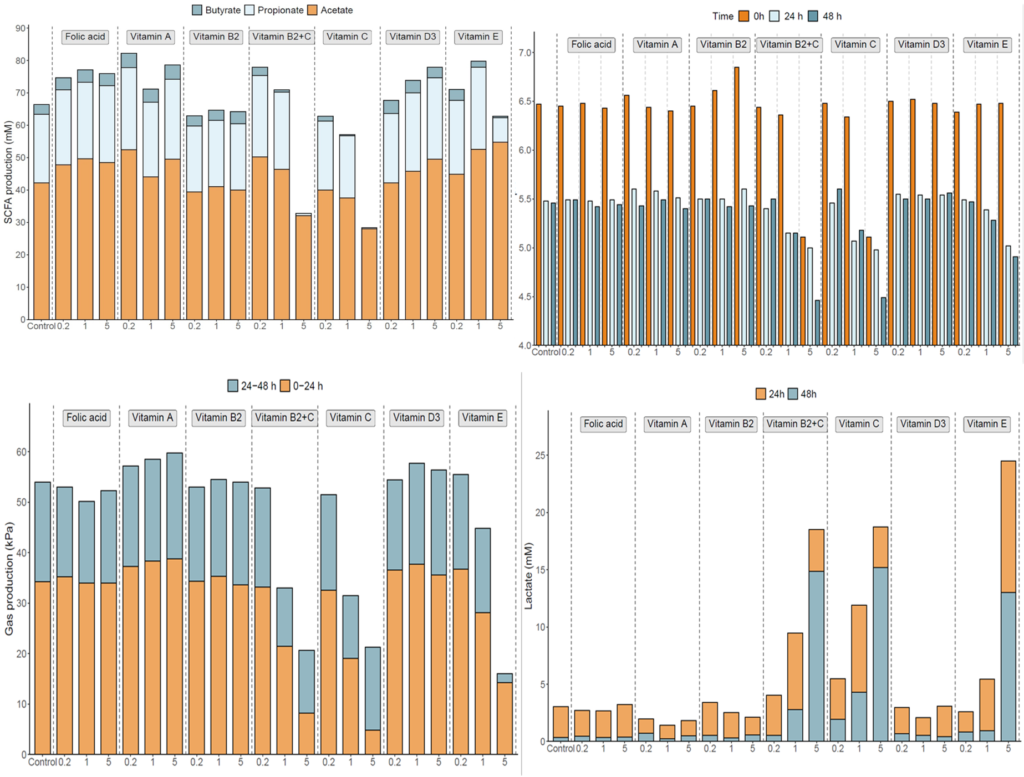
与对照相比,大多数维生素对SCFA的产生有明显的影响。维生素A处理的总SCFA浓度最高(0.2倍),而所有浓度的叶酸都持续增加总SCFA浓度。乳酸浓度、产气量和pH值为体外发酵系统的代谢活性提供了额外的衡量标准。在添加维生素C(1x和5x)和维生素E(5x)后,pH、产气量和乳酸积累量显著降低。
当HT29细胞与经维生素处理的微生物群的发酵样品孵育时,观察到IL8-CXCL8的分泌发生了变化。在所有浓度的维生素E中,IL8-CXCL8(956.67 pg/mL、1010.00 pg/mL、1544.00 pg/mL)与对照组(590.00 pg/mL)相比有轻微但一致的上调(p<0.05)。使用细胞肠道模型研究维生素C和维生素E对肠道屏障完整性的影响,发现在发酵之前,大多数维生素以剂量依赖的方式增加TEER。
此外,在发酵后用对照(水)上清液处理的细胞中,TEER显著增加,这一效果在所有实验中都是一致的(文章中只显示维生素C和E;其他维生素未显示)。橙色,发酵前;蓝色,发酵后。
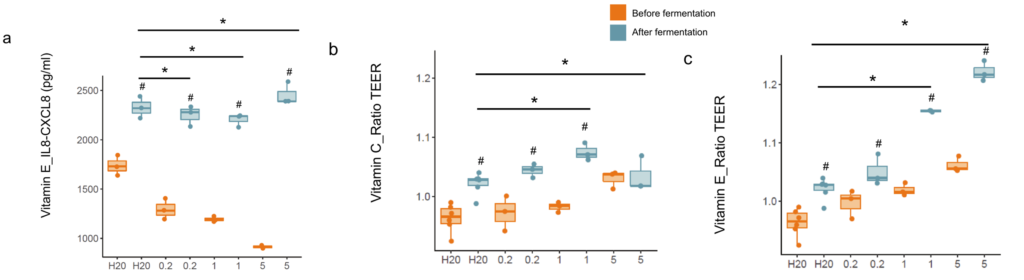
这只是一项初步研究,文章中的研究人员也提到了有些许不足需要进一步验证的地方。但是这些图表数据也实打实的给出了一些结果。
经结肠传递的维生素对人体肠道菌群和相关代谢活动起了调节作用,根据在人体和体外观察到的效果,维生素C、B2和D似乎是被测试的维生素中影响最显著的。
在人类中,维生素C的效果最为明显,与安慰剂相比,维生素C显著增加了微生物α多样性和粪便SCFA。
在肠道菌群领域研究的科研人员从未停止脚步,如果肠道菌群是通往健康的其中一把钥匙,那么在大家的打磨之下,终将可以打开更加精准的个体化医疗技术大门。
参考文献:
Jie Zhuye,Yu Xinlei,Liu Yinghua et al.The Baseline Gut Microbiota Directs Dieting-Induced Weight LossTrajectories.[J] .Gastroenterology, 2021.
Pham Van T,Fehlbaum Sophie,SeifertNicole et al. Effects of colon-targeted vitamins on the composition and metabolicactivity of the human gut microbiome- a pilot study.[J] .Gut Microbes, 2021,13: 1-20.
相关阅读:

谷禾健康
幽门螺杆菌(helicobacterpylori,H.pylori)是一种独特的,能持续定植于人类胃粘膜并能引起胃感染的细菌。
幽门螺杆菌是革兰氏阴性,螺旋形,微需氧细菌,定居于人类胃粘膜中。世界上有超过一半的人感染了幽门螺杆菌,但很多没有临床症状。幽门螺杆菌及其患病率在某些人群中高达80%。
据推测,幽门螺杆菌可能是人类土著微生物组的一部分,它与人类宿主之间有着很复杂的关系。
本文主要讨论幽门螺杆菌是如何与人类共同进化的,可能的机制可以解释基于人群的研究中幽门螺杆菌感染与几种疾病的发展之间的正相关性和负相关性,以及炎症和/或微生物组的变化是如何联系的各自的结果。
大多数幽门螺杆菌感染者并没有明显症状,但当症状出现时,一般是以下几种:
恶心,胃痛或胃灼热,空腹时腹部疼痛加剧。
怎样的情况有可能感染此菌?
幽门螺杆菌可能通过接触感染者的唾液、呕吐物或粪便传播,食用受污染的食物或水也会感染。
大多数感染幽门螺杆菌的人都是在儿童时期感染的。
有些因素可能会增加感染幽门螺杆菌的风险:
比如在拥挤的空间生活,没有干净的水,和患有幽门螺杆菌的人一起生活等。
什么情况下需要看医生?
当感觉有不寻常的胃痛或不适时,尤其是持续或反复发作的胃痛;
吞咽困难;
血腥,黑色或柏油样的粪便;
呕吐物带血或看起来像咖啡渣;
…
以上情况,最好去看医生。
( 如自行随意服用抗生素,效果不好的同时很可能带来抗生素耐药 )
如何诊断幽门螺杆菌?
目前最常见也实惠的方法是呼气检测,从分析到出结果只需数分钟,简单准确。
胃镜检查:做胃镜检查也包括幽门螺杆菌检测,因为可以取到胃里活性组织做病理切片检查。
抗体检查:通过抽血检查,以确定是否感染过幽门螺杆菌以及目前处于感染状态。
幽门螺杆菌会导致并发症?
包括溃疡,胃炎和胃癌。
溃疡约有10%的幽门螺杆菌患者会发展为胃溃疡(疼痛)。当幽门螺杆菌破坏保护胃和小肠内壁的粘膜时,就会发生这种情况,胃酸会渗透到衬里并造成伤害。
幽门螺杆菌可导致90%以上的肠道溃疡和80%的胃溃疡。
溃疡本身也会导致严重的并发症:
• 内部出血胃酸或溃疡渗入血管可能导致出血。
•阻塞溃疡会阻止食物离开您的胃。
•穿孔溃疡可能会深入并穿透胃或肠壁。
•腹膜炎 当溃疡引起感染或发炎时,可能发生腹膜炎症(腹膜)。
胃炎胃炎是胃黏膜炎症。幽门螺杆菌是处于患有这种病症的风险增加。
如果不治疗胃炎,可能会导致严重失血,并可能增加患胃癌的风险。胃癌是世界上与癌症相关的死亡的第二大最常见原因。
此外,幽门螺杆菌感染还与其他疾病有关,例如缺血性心脏病,2型糖尿病,贫血,肥胖受试者的不良代谢特征和胰岛素抵抗等。
幽门螺杆菌(Hp)感染会在胃微环境中产生剧烈变化,进而影响胃微生物群组成,并可能与肠道微生物群变化有关。可能会触发肠道共生稳态的重大改变,从而出现新的胃肠道平衡。
同时,用于根除幽门螺杆菌的治疗策略可以调节这种生理共生,但也可能相反,受到其特性的影响。感染,饮食,抗生素和/或生活方式会干扰这种共生关系。
幽门螺杆菌感染对胃微生物群的干扰
下一代测序对胃液和活检标本中的人体胃微生物群进行了研究,结果表明胃中存在多种细菌类群,主要由五个门组成,包括放线菌门、拟杆菌门、厚壁菌门、梭菌门和变形菌门。幽门螺杆菌感染极大地改变了胃微生物群的特征。
一项初步研究报道,幽门螺杆菌定植改变了胃微生物群,降低了微生物多样性,根除幽门螺杆菌可以恢复微生物多样性。
幽门螺杆菌可以利用几种机制来调节胃微环境。通过干扰质子泵的表达,幽门螺杆菌可以调节胃腔的酸度,从而使微环境与通常不能在胃中生长的微生物相容。
评估幽门螺杆菌感染对胃微生物群影响的研究
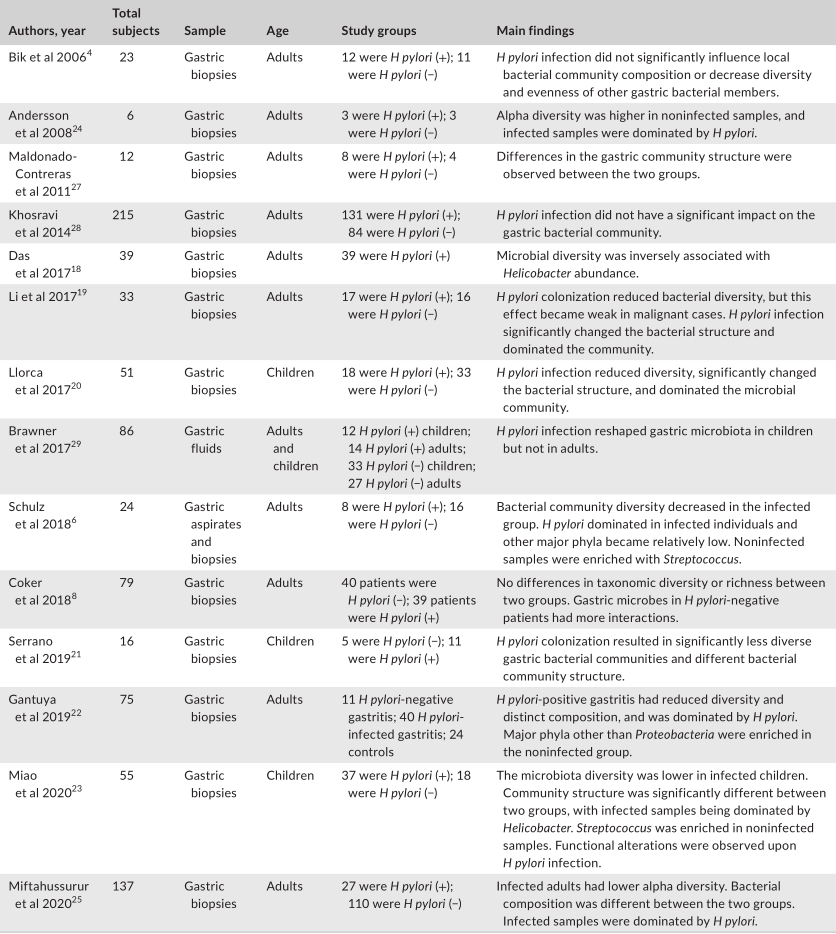
Tao et al., Helicobacter, 2020
此外,由于幽门螺杆菌的存在而改变的免疫反应可能会影响其他微生物群。幽门螺杆菌还可能通过动员抗菌肽或通过营养竞争来改变其他微生物群的生长。一般来说,研究人员表明,幽门螺杆菌的定植与α多样性的显著降低有关。微生物多样性和幽门螺杆菌丰度之间存在反比关系。
幽门螺杆菌感染对肠道微生物群的影响
与幽门螺杆菌阴性对照组相比,胃内有大量幽门螺杆菌的个体具有不同的肠道菌群,这表明胃肠段之间存在相互作用。
大多数研究表明,幽门螺杆菌感染与肠道微生物多样性之间的呈正相关。由于较高的微生物多样性通常与总体较好的健康状况有关,因此,探讨幽门螺杆菌感染后肠道微生物多样性的增加是否对宿主有一些有益的影响将是一个有趣的问题。
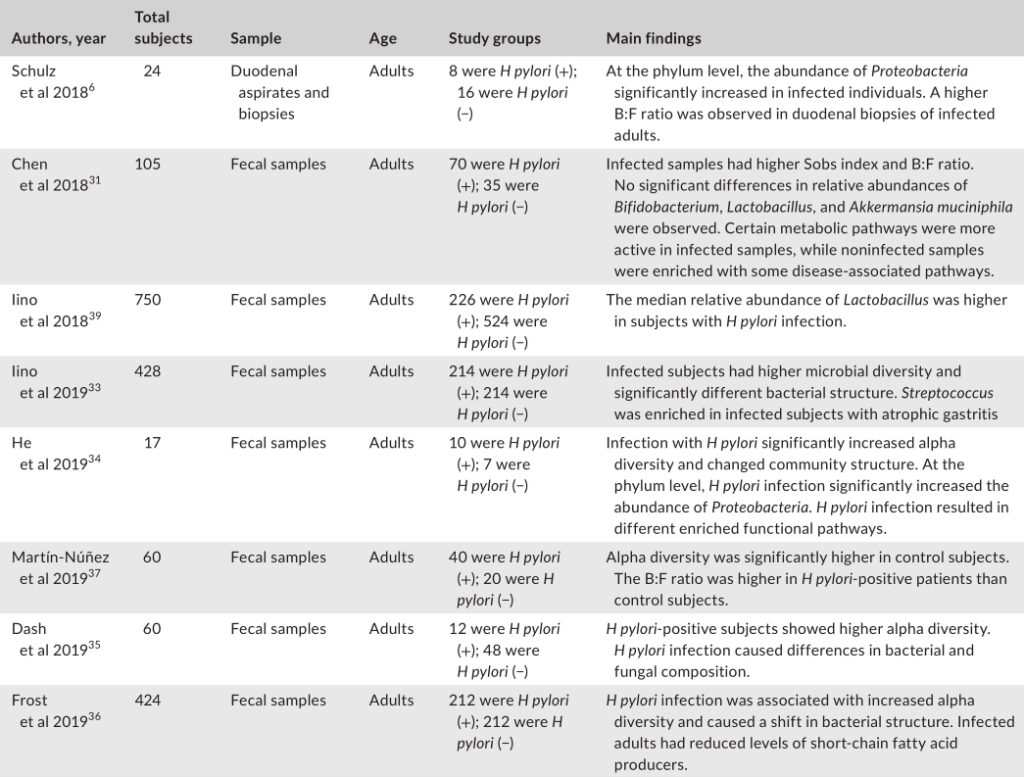
幽门螺杆菌感染对肠道微生物群影响的研究分析
Tao et al., Helicobacter, 2020
幽门螺杆菌感染组和阴性对照组的微生物群落结构存在显著差异。
在门水平上的成分分析发现,受感染个体中变形菌的丰度显著增加,这可能是由于幽门螺杆菌从胃转移到肠腔所致。值得注意的是,拟杆菌与厚壁菌(B:F)的比率在幽门螺杆菌阳性组中更高。改变的B:F比值与临床相关,因为发现厚壁菌和拟杆菌与宿主的脂质代谢和能量平衡有关。
受感染与没感染组相比,双歧杆菌、乳酸杆菌和嗜粘液阿克曼菌的丰度没有显著差异。其他研究人员发现,幽门螺杆菌感染者体内乳酸杆菌的丰度更高。
一项研究发现,在幽门螺杆菌感染的患者中,萎缩性胃炎患者的肠道微生物群中链球菌更为丰富。
另一项研究发现,幽门螺杆菌感染的个体表现出短链脂肪酸(SCFA)产生者(如丁酸盐)水平的下降,SCFA对宿主产生有益的代谢作用。
此外,鉴于SCFAs受体在免疫细胞中的普遍表达,这些代谢物被认为在调节肠道内稳态中发挥重要作用。因此,幽门螺杆菌感染时抑制SCFAs的输出可能对人类健康有害。
有功能分析指出,在幽门螺杆菌阴性人群中,疾病相关途径更活跃。相比之下,许多代谢途径在感染的患者中的比例过高。因此,微生物群中的功能变化可能是特定于部位的,因为在肠道中观察到的变化与在胃中观察到的变化呈现不同的趋势。
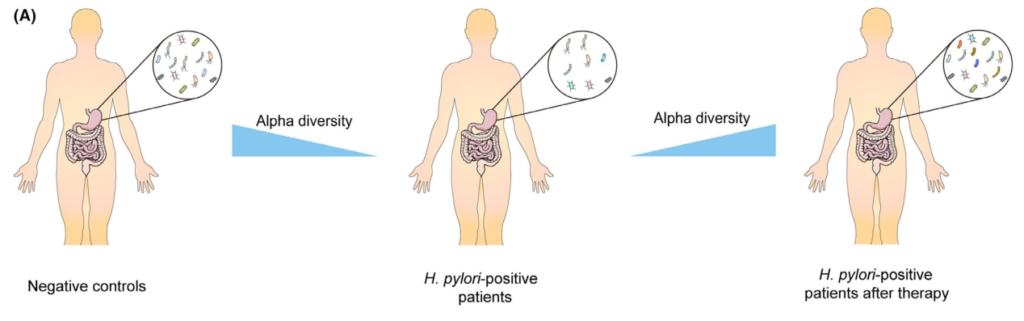
根除疗法对胃微生物群的影响
Tao et al., Helicobacter, 2020
充分的证据表明,成功清除幽门螺杆菌后,胃微生物多样性显著增加,但显示治疗失败后没有改善。研究人员认为恢复可能需要一定的时间,因为他们认为多样性从第0周到第6周和第26周逐渐增加。
此外,研究表明,成功根除幽门螺杆菌后,α多样性可以完全恢复到未感染对照组的水平。相反,尽管在清除幽门螺杆菌后,群落结构也可以部分恢复,但对于是否仍存在显著差异存在争议在根除后组和阴性对照组之间。
一些研究人员发现,接受抗幽门螺杆菌治疗的患者在治疗2个月后,胃微生物群落的组成恢复到未感染儿童的水平,然而,其他研究确定,成功治疗6个月后的成人样本仍显示出不同的菌群结构,阴性对照组则不同。
纳入分析的不同年龄组可能解释了相反的结论,因为另一项招募儿童的研究也发现根除组的菌群结构在治疗4周后与幽门螺杆菌阴性组的菌群结构接近。
根除治疗后评估胃微生物群变化的研究

Tao et al., Helicobacter, 2020
成分分析揭示了幽门螺杆菌的相对丰度治疗后幽门螺杆菌显著下降,而其他主要菌门,包括放线杆菌、拟杆菌、厚壁菌和梭杆菌,则增加。
在属水平上,治疗后乳酸杆菌和双歧杆菌(两种公认的益生菌)的数量显著增加。
两项研究的功能分析表明,成功治疗后,蛋白质和碳水化合物代谢途径上调。因此幽门螺杆菌感染期间,胃微生物群营养代谢功能受损,根除治疗可部分恢复。然而,预测的功能改变还需要进一步的验证。
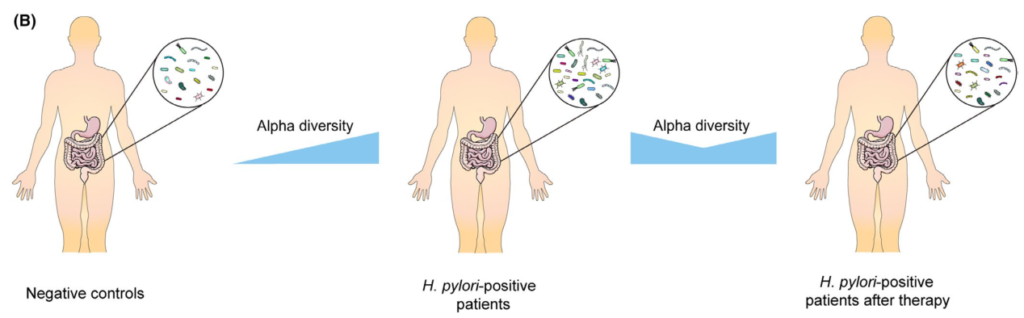
根除治疗后肠道微生物群的变化
通过降低酸度,质子泵抑制剂(PPIs)已被证明对肠道微生物群产生显著影响。因此,抗幽门螺杆菌治疗对肠道微生物群的影响是PPIs、抗生素、铋联合应用的共同结果。总的趋势是,α多样性在根除后立即下降,随后又恢复。

Tao et al., Helicobacter, 2020
具体来说,恢复需要多长时间仍有待阐明。大多数研究收集了随访2个月内的信息显示α多样性降低,而此后报告与基线无显著差异。
然而,一项研究报告,从第0周到第6周和第26周,Sobs指数和Chao指数都在下降没有达到统计学意义。值得注意的是,另一项研究发现,不同的治疗方案对肠道微生物群的影响可能不同。
在临床试验中,三种不同的治疗方案,包括三联疗法、联合疗法和铋四联疗法。结果表明,所有组的α多样性在第2周时都有所下降,但只有接受三联疗法的患者在第8周时才具有基本α多样性,而其他两组的α多样性在治疗后1年也无法恢复。
希望将来的研究验证根除疗法是否会导致肠道菌群的持续紊乱,以及不同的治疗方案如何影响可逆性。
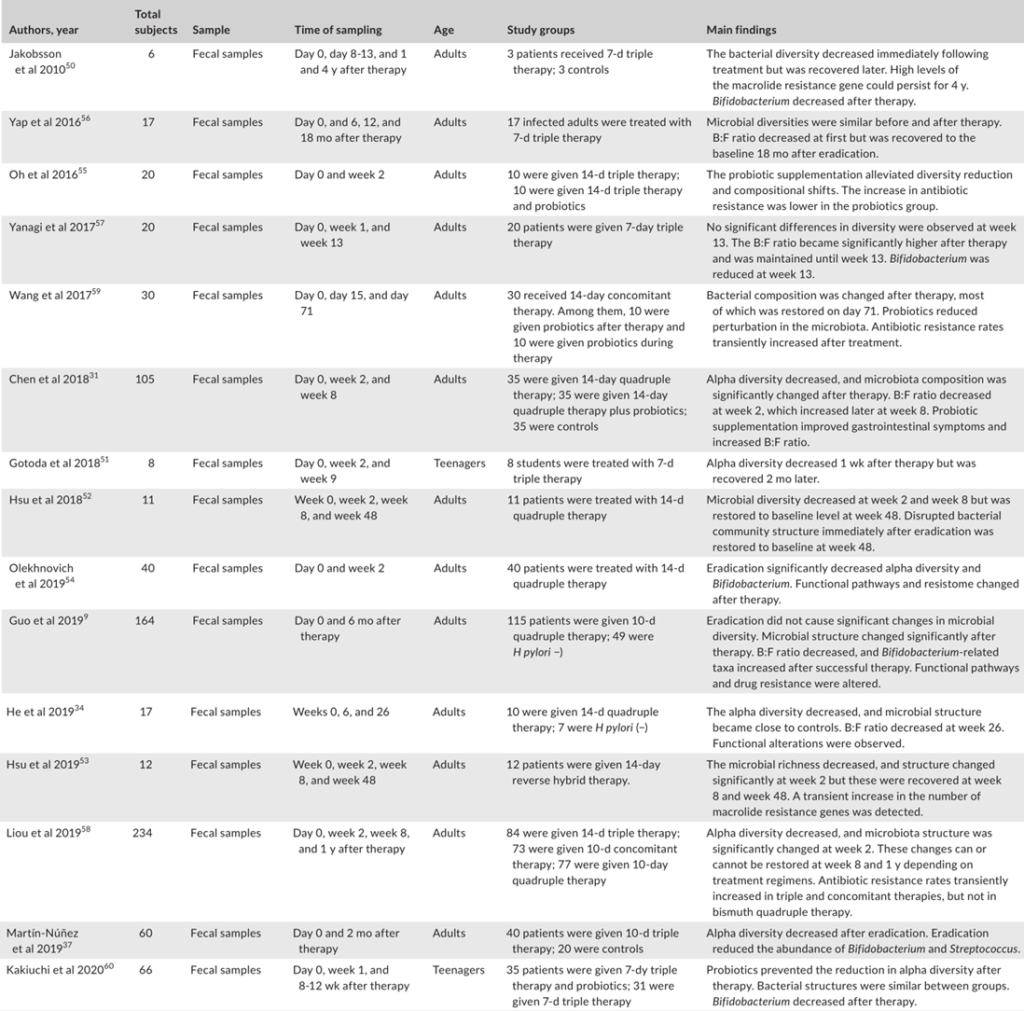
分析根除疗法对肠道微生物群影响的研究

Tao et al., Helicobacter, 2020
益生菌的补充可以缓解抗生素引起的多样性和结构紊乱
益生菌,已被证明可稳定微生物群并改善胃肠道症状。在门水平上,治疗6个月后观察到厚壁菌群增加和拟杆菌减少,表明在幽门螺杆菌感染的个体中观察到的高B:F比率逆转。在另一项研究中报告了9个类似的结果。
临床证据支持肥胖与B:F比率降低相关。因此,这些研究中检测到的B:F比率降低可能为根除治疗后体重增加提供了一种可能的解释。然而,一些研究人员说明,在根除18个月后,降低的B:F比率可以逆转。有趣的是,益生菌补充被证明与根除治疗后较高的B:F比率相关。值得注意的是,报告的结果不一致。
一项研究表明,治疗后B:F比率立即增加,并在第13周保持高于基线水平。宏基因组研究的分类图谱显示,治疗后双歧杆菌的相对丰度下降。然而,另一项研究表明,双歧杆菌在成功根除6个月后增加。
在幽门螺杆菌阳性萎缩性胃炎的肠道微生物群中富集的链球菌在根除治疗后显著减少。
尽管不同研究中肠道微生物群的长期变化不同,但根除引起肠道内稳态的短期紊乱似乎是一致的。
根除疗法对肠道菌群抗生素耐药性的影响
随着根除疗法的广泛应用,抗生素耐药性的出现已成为临床实践中的一个重要问题。
根除幽门螺杆菌感染后,抗生素耐药性的上升以及根除治疗后的长期安全性是重要的问题。
通过药敏试验指导的个性化治疗可以在一线治疗中提供可靠的优异根除率,但贵且无法广泛获得。根据局部地区的抗生素耐药性,针对特定人群的经验疗法可能是一种替代策略。
已证明会改变幽门螺杆菌相关疾病风险的宿主因素包括宿主的年龄、在幽门螺杆菌的获得和幽门螺杆菌感染之间的持续时间,但更重要的是宿主免疫介质(多态性)和酸分泌状态。
除宿主因素外,吸烟和饮食等环境因素还会影响幽门螺杆菌定植的生态位,因此可能会影响疾病风险。

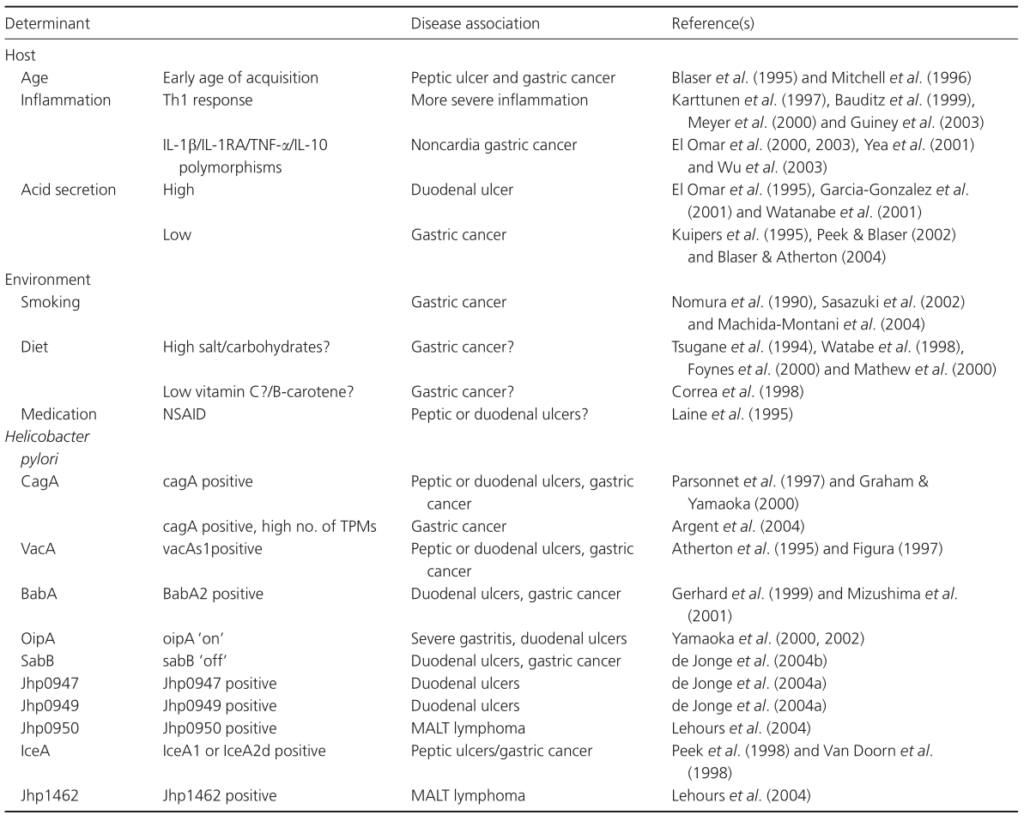
Karin et al., FEMS Microbiol Rev. 2006
在年幼时期感染幽门螺杆菌会增加患胃溃疡和胃癌的风险。 胃溃疡和胃癌的发展需要幽门螺杆菌的长期感染,因此,推测这些疾病是在慢性感染幽门螺杆菌的患者中更为常见。
此外,这种关联被认为是由不同年龄组的宿主免疫反应的差异所决定的。
感染幽门螺杆菌后,宿主胃上皮细胞释放细胞因子IL-8。这种细胞因子参与了巨噬细胞、中性粒细胞、肥大细胞、B细胞和T细胞募集到炎症部位。这些细胞通过分泌其他炎症介质,如干扰素(IFN-g)、肿瘤坏死因子(TNF-a)和白细胞介素(IL-1b),进一步增强免疫反应。
幽门螺杆菌相关发病机制的示意图

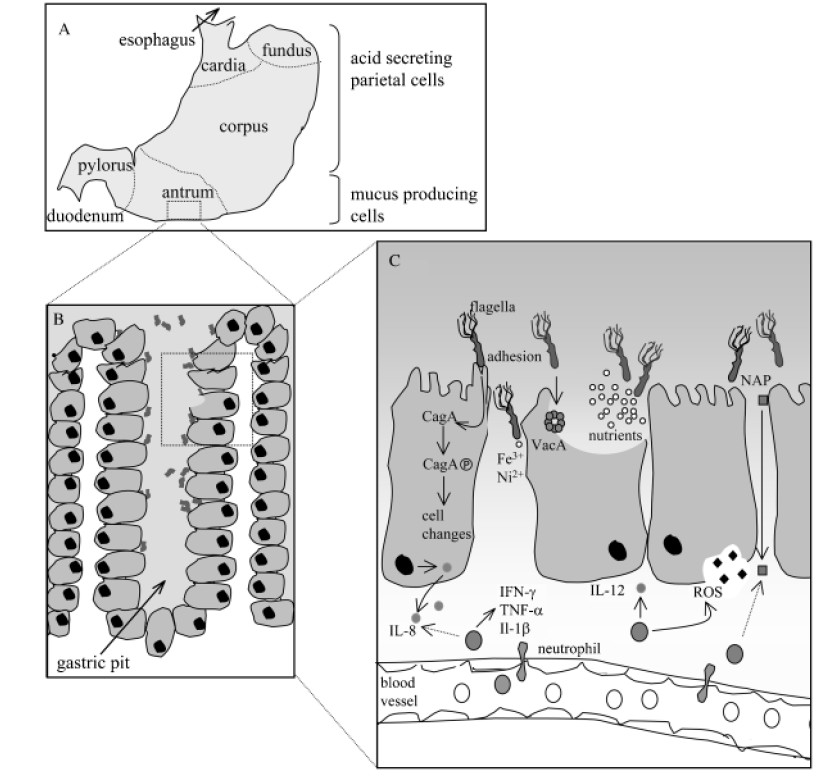
Karin et al., FEMS Microbiol Rev. 2006
A)在人类胃中,幽门螺杆菌主要定植于缺乏胃酸分泌壁细胞的胃窦中;
B)在胃小凹中,幽门螺杆菌尤其在上皮细胞紧密连接处附近增殖;
C)幽门螺杆菌对定植、持续和疾病发展具有重要作用的因子。
针对幽门螺杆菌的免疫反应进一步表现为活化的人类中性粒细胞中的氧化爆发。这种爆发会导致活性氧(ROS)的释放,活性氧是一种低分子量的代谢物,可破坏包括核酸在内的重要生物分。ROS可能损伤控制细胞生长的基因;并刺激癌症的发展。因此,免疫介质的存在会导致胃上皮的完整性受损。这种损伤是引起大多数与幽门螺杆菌感染相关的病理学,而不是直接的幽门螺杆菌活动。
幽门螺杆菌感染期间存在的免疫细胞主要是促炎细胞,而不是抗炎细胞。促炎介质由辅助性T细胞1(Th1)分泌。原始T细胞受多种因素驱动分化为Th1细胞,如TNF-a和IL-12。
在幽门螺杆菌刺激下,单核细胞大量产生细胞因子IL-12。因此,通过刺激IL-12的释放,幽门螺杆菌增强了促炎反应。这导致更多的损伤胃上皮,这容易发展胃萎缩。
一些编码免疫调节因子的宿主基因含有多态区域。这些基因的多态性将改变它们的转录,从而影响炎症过程。因此,幽门螺杆菌相关疾病的风险可能会改变。到目前为止,IL-1b、IL-1受体拮抗剂、IL-10和TNF-a基因的多态性已被证明与远端胃癌显著相关。
人类白细胞抗原(HLA)通过将病原体衍生的肽片段呈递给适当的T细胞,有助于消除病原体。HLA基因具有高度多态性,某些HLA等位基因与胃腺癌的发生有关。幽门螺杆菌感染也与胃腺癌的发生有关,但其存在与这些HLA等位基因的存在无关。因此,HLA等位基因在幽门螺杆菌介导的腺癌中的重要性仍然存在争议。
因此,遗传上预定的显性促炎性Th1反应与幽门螺旋杆菌疾病相关。
另一方面,Th1反应的强度可能受到抗炎Th2细胞因子IL10的产生的限制,从而延长感染时间。Th2型反应是由寄生虫引起的。因此,感染幽门螺杆菌的人的炎症反应和病理改变逐渐减弱。这可能导致这些个体慢性胃炎进展为胃癌的时间延迟。另外,不同的促炎反应可能直接导致幽门螺杆菌相关病理学的不同途径。
前面提到Th1反应导致胃壁细胞抑制其酸分泌。酸性较低的环境可能促进幽门螺杆菌的传播和持续。此外,当胃酸水平较低时,幽门螺杆菌以外的微生物可能在人体胃中生长,从而增强局部炎症反应。促炎细胞因子和胃酸分泌减少的联合作用增加了患消化性溃疡病和胃癌的风险。
另一方面,当酸的分泌减少时,十二指肠溃疡就不太可能发生。当酸的分泌增强时,十二指肠溃疡发生的风险增加。然而,同样在低酸性条件下,幽门螺杆菌感染后十二指肠溃疡的风险可能会增加。
胃壁细胞控制其产酸的能力在幽门螺杆菌相关疾病的发展中是重要的。幽门螺杆菌感染主要发生在人类胃中酸性较弱的部位,如胃窦。因此,胃酸分泌量高的宿主胃窦内幽门螺杆菌密度高,且主要发展为胃窦性胃炎。随后,胃体中完整的壁细胞被刺激分泌酸,从而诱导十二指肠的胃化生。幽门螺杆菌定植于这种胃化生,这可能导致十二指肠溃疡。
另一方面,胃酸分泌量低的宿主不仅胃窦易受幽门螺杆菌感染,而且胃体也易受幽门螺杆菌感染。感染的幽门螺杆菌可进一步抑制胃壁细胞的酸分泌。这可刺激胃上皮细胞持续增殖,导致胃腺进行性丧失,最终导致胃萎缩和癌症。
吸烟
一些环境因素与幽门螺杆菌相关的发病机制有关。吸烟是胃癌发展的主要因素。烟草烟雾含有致癌的亚硝胺,引发癌症的发展。
高盐饮食
一些饮食因素与幽门螺杆菌疾病有关。高盐饮食与幽门菌定植率、胃炎和胃癌风险增加。高盐浓度导致壁细胞萎缩,粘膜屏障破坏。然而,只有长期高盐摄入才会增加幽门螺杆菌相关疾病的风险。
高米饭摄入量
高米饭摄入量与胃癌之间存在正相关关系。米饭含有碳水化合物,可能会刺激胃粘膜。
水果和蔬菜摄入量低
水果和蔬菜摄入量低可能会增加胃癌的风险。水果和蔬菜含有抗氧化剂维生素C和β-胡萝卜素,通过中和活性氧来防止致癌。
因此,尽管有几个环境因素被认为与幽门螺杆菌相关疾病的发生有关,但它们的作用往往是有争议的。据推测,不同环境因素以及宿主和细菌因素之间的复杂相互作用妨碍了对研究结果的解释。
幽门螺杆菌因素在疾病发展中的总体影响是复杂的。到目前为止,已经描述了几种与幽门螺杆菌相关疾病的发生有关的幽门螺杆菌特异性蛋白。这些蛋白质被认为是导致幽门螺杆菌持续存在的原因。作为副作用,这些幽门螺杆菌蛋白诱导和改变炎症过程,损伤胃上皮,从而决定幽门螺杆菌感染后的结局。
CagA
与感染cagA阴性幽门螺杆菌分离株的患者相比,携带细胞毒素相关基因A(cagA)的幽门螺杆菌分离株的定植与严重胃炎、消化性溃疡病和远端胃腺癌的风险增加有关。
幽门螺杆菌cagA基因的存在或不存在经常被用作幽门螺杆菌中致病岛(PAI)存在或不存在的标记。 cag PAI由大约30个基因组成,并且在所有幽门螺杆菌分离株中占50%–70%。 位于cag PAI侧翼的两个31 bp重复序列之间的重组可能导致整个cag区域的缺失或获得。
cag PAI上的18个基因对于产生IV型分泌系统至关重要。 IV型分泌系统将细菌细胞中的蛋白(与毒力相关)转运到宿主细胞的胞质溶胶中。 这通常导致上皮细胞反应的级联反应的启动,例如细胞骨架的变化和细胞因子IL-8的分泌。
在幽门螺杆菌中,IV型分泌系统的成分将CagA蛋白转运到胃上皮细胞中。 随后,CagA蛋白被磷酸化。 然后,这种磷酸化的CagA与宿主磷酸酶SHP-2相互作用,引起细胞骨架的重排。 这导致宿主细胞形态发生变化,也称为“蜂鸟”表型。该表型的特征在于细胞扩散,上皮细胞的延长生长以及片状脂蛋白和丝状伪足的存在。
作为抵消事件,磷酸化的CagA与宿主Src激酶相互作用,从而减弱宿主SHP-2磷酸酶的信号传导。 这个过程减少了细胞骨架的重排,并阻止了CagA的进一步磷酸化。
最近,已经证明幽门螺杆菌菌株在体内诱导较高水平的CagA磷酸化。上皮细胞诱导更多的细胞骨架变化,并且更可能与胃癌有关。CagA磷酸化水平的差异是由cagA基因的30个区域内酪氨酸磷酸化基序(TPM)数量的差异引起的。
幽门螺杆菌人群,需要最低限度的免疫识别。因此,在萎缩的生态位中,这些TPM数量减少的亚克隆诱导了较弱的宿主免疫反应。
另一方面,较高水平的CagA磷酸化可引起强烈的炎症反应。 这种炎症会导致萎缩,并可能在限制高酸输出的生态位酸应激中发挥作用。
通过观察发现,缺乏cagA基因的幽门螺杆菌菌株是从消化性溃疡或胃癌患者中分离出来的,尽管其频率比cagA阳性幽门螺杆菌菌株的频率更低。
cagA和幽门螺杆菌相关疾病之间的关联在不同的地理区域中有所不同。 这种变异可能与CagA表达的差异有关。
然而,CagA并不是唯一的。幽门螺杆菌蛋白负责屏障功能障碍,而这一过程并没有随着CagA的清除而丢失。下一节讨论的VacA蛋白也很重要。
VacA
最初显示真核细胞在带有幽门螺杆菌的体外测试系统中经历空泡化和连续变性。 后来证明这种现象是由幽门螺杆菌毒素诱导的,现在被称为空泡细胞毒素A(VacA)。
VacA或CagA不能单独用作临床结果的决定因素。
VacA如何发挥作用,导致细胞死亡?
幽门螺杆菌VacA是一种高度免疫原性的95-kDa蛋白。VacA结合上皮细胞的顶端部分,形成阴离子选择性孔。
通过这些孔,碳酸氢盐,氯化物和尿素从细胞质中释放出来,然后,VacA被内吞进入晚期的内体区室,并改变这些区室的通透性。
在弱碱(例如氨)的存在下,这会导致水涌入,从而导致囊泡肿胀和液泡形成。 细胞内内吞途径的损伤最终导致细胞死亡。
这导致了上皮细胞抗性的降低,因此低分子量分子如Fe3+和Ni2+可以很容易地穿过上皮细胞层。Fe3+和Ni2+分子分别是幽门螺杆菌生长和脲酶活性的关键因子。
因此,推测通过降解上皮细胞屏障,幽门螺杆菌可以更容易地获得这些关键因子。
幽门螺杆菌VacA也与壁细胞的降解有关,这导致酸分泌减少,使宿主容易患上胃癌。 持续感染过程中VacA表达水平的差异导致毒性改变。 因此,溃疡的消长可以通过随时间变化的VacA表达变化来解释。
在体外在胃上皮细胞附近诱导vacA基因的转录。 这一发现证实了VacA与宿主细胞相互作用的重要性。 此外,VacA可以逃避适应性免疫反应,从而增强幽门螺杆菌在胃粘液层中的持久性。
幽门螺杆菌外膜蛋白(HOPs)
在革兰氏阴性细菌中,外膜介导与其周围环境的相互作用。 在感染期间,假定存在于幽门螺杆菌外膜上的蛋白质被改变,使得宿主免疫系统的识别作用降至最低。
幽门螺杆菌分离物含有约30种不同的外膜蛋白(HOP)。 其中几种是粘附素。 在革兰氏阴性细菌中,粘附素最常形成聚合菌毛结构。 但是,在幽门螺杆菌中,这些粘附素已经适应了胃环境,其中酸性条件可能会使这种聚合物菌毛结构解聚。
岩藻糖基化的糖蛋白和唾液酸化的糖脂都已被证明是胃上皮中幽门螺杆菌的结合位点。
与宿主细胞的粘附可保护幽门螺杆菌免受蠕动和粘膜脱落。
此外,推测粘附力可以使幽门螺杆菌更好地获取从胃上皮释放的营养物质,并更有效地将细菌毒素传递至宿主细胞。
另一方面,在剧烈炎症的部位,粘附特性的丧失可能使幽门螺杆菌逃脱宿主免疫细胞的杀伤。目前为止,一些HOP与疾病的发展有关。
幽门螺杆菌BabA (HopS)介导幽门螺杆菌粘附于人Leb血型抗原,这些抗原存在于胃上皮细胞上。BabA黏附促进幽门螺杆菌定植,增加上皮细胞分泌IL-8,导致粘膜炎症增强。
BabA调节的两种机制都有助于促进慢性感染的动态反应。
在慢性炎症期间,选择增加或减少粘附的周期可在所有血型的人群中获得所有类型的Leb结合。
宿主粘膜糖基化模式导致BabA进化,使幽门螺杆菌菌株适应其个体宿主,这有助于避免宿主反应,并在全世界范围内造成幽门螺杆菌感染的异常长期性。
幽门螺杆菌可塑性区域毒力因子
两个单独菌株基因组序列的比较表明,一个菌株中存在的幽门螺杆菌基因中约有6%-7%不存在于另一个菌株中,反之亦然。
大约一半的菌株特异性基因存在于高变区;可塑性区。 位于这种可塑性区域的基因通常与毒力增加相关。
在幽门螺杆菌中,可塑性区确实编码了与IV型分泌有关的Vir型ATP酶。 在幽门螺杆菌中,该分泌系统在例如分泌CagA细胞毒素中很重要。目前为止,一些位于可塑性区的幽门螺杆菌基因与幽门螺杆菌相关的疾病有关。
幽门螺杆菌Jhp0947和Jhp0949与十二指肠溃疡疾病相关。这两个基因均位于幽门螺杆菌菌株J99可塑性区,在幽门螺杆菌介导的IL-12释放中很重要。
在体外测试系统中从单核细胞中提取。 细胞因子IL-12对于使免疫反应偏向促炎性Th1应答是必不可少的,并且与十二指肠溃疡的形成密切相关。
由jhp0947和jhp0949编码的蛋白质的功能未知。 然而,已经假设这些蛋白通过与单核细胞的相互作用诱导促炎细胞因子IL-12的产生。
IL-12水平升高会导致幼稚T细胞分化为活化的Th1细胞,从而导致炎症反应增强和组织损伤增加。
幽门螺杆菌Jhp0950,编码一种未知功能的蛋白质,也是J99可塑性区的一部分。该基因的存在与cagA、cagE、vacA s1m1、babA2、hopQ T1、oipA有关。
在幽门螺杆菌J99基因组中,Jhp0950与Jhp0949相邻。与Jhp0949不同,Jhp0950与十二指肠溃疡风险增加无关。然而,它与疾病的关联支持了位于可塑性区域的幽门螺杆菌基因可能与毒性相关的观点。
其他幽门螺杆菌毒力因子
在美国和荷兰,幽门螺杆菌iceA1基因(iceA基因的两个等位基因变体之一)在幽门螺杆菌感染的消化性溃疡患者中比仅在幽门螺杆菌感染的胃炎患者中更为普遍。
与许多其他与毒力相关的基因相似,IceA表达与幽门螺杆菌相关疾病之间的联系是群体依赖性的。
在东南亚,未发现iceA1与幽门螺杆菌相关疾病之间的关联。 有趣的是,对iceA1呈阳性的南非幽门螺杆菌分离株在幽门螺杆菌感染的胃癌患者中比仅在幽门螺杆菌感染的胃炎患者中更普遍。
注:幽门螺杆菌iceA1最初是在与胃上皮细胞接触后转录上调后被鉴定的,iceA1基因编码的核酸内切酶与乳球菌中的限制性核酸内切酶NlaIIIR非常相似,伴随的高度保守的脱氧核糖核酸腺嘌呤甲基转移酶的活性,由幽门螺杆菌编码,似乎与控制幽门螺杆菌的基因表达有关。
幽门螺杆菌Jhp1462与MAL T淋巴瘤、十二指肠溃疡和胃腺癌的风险增加相关。由Jhp1462编码的蛋白质的功能是未知的,其在严重胃十二指肠疾病发展中的重要性仍有待阐明。
以上,我们看到幽门螺杆菌通过各种方式给人体带来种种不利影响,它似乎不应该在人体中长期生存,然而,幽门螺杆菌在人体内存在有着的悠久的历史,那么幽门螺杆菌是如何保护自己在人体中安稳生存下来?
幽门螺杆菌在疾病发生之前会长期感染人胃粘膜。 因此,导致幽门螺杆菌定植和持续存在的因素与幽门螺杆菌相关的发病机理具有内在联系。 在胃腔进入后,幽门螺杆菌必须应付胃酸。
幽门螺杆菌通过其耐酸性在这种酸性条件下得以生存:然后穿过粘液层到达其接近胃上皮细胞的位置。趋化性,运动性和粘附性是胃上皮细胞定殖的重要过程。
为了在人胃粘膜中长期持久存在,幽门螺杆菌还不断需要宿主提供营养。 这是通过降解粘液层和下面的胃上皮细胞的完整性来实现的。 此外,通过抑制宿主免疫系统,抗原变异和抗原拟态避免了幽门螺杆菌的清除。
耐酸性
幽门螺杆菌生长的下限pH值是5.0-5.5,具体取决于测试的分离物。在胃粘膜层中,pH也是酸性的,大约在4-6.5之间变化。而且,当粘液层被破坏时,pH值可能会偶尔下降。
酸冲击(pH<3)后幽门螺杆菌的存活取决于幽门螺杆菌蛋白脲酶的活性,该酶将尿素转化为氨和碳酸氢盐。这导致幽门螺杆菌的周质或细胞质被中和。幽门螺杆菌尿素酶活性对于在酸性pH下体外存活以及在动物模型中胃粘膜定植至关重要,这证明了尿素酶在幽门螺杆菌感染中的重要性。
在中性pH下高度活跃的脲酶和酸调节的尿素通道的结合解释了为什么幽门螺旋菌在人类胃部的生存能力是独特的。有效抑制UreI蛋白,将提供一种从正常的,分泌酸的胃中根除幽门螺杆菌的方法。
除耐酸性外,脲酶还具有与胃定植有关的其他基本功能
尽管尿素酶对于酸休克的生存是必不可少的,但是幽门螺杆菌尿素酶在处理胃上皮细胞附近的慢性酸性环境时还是不够的。 用酸抑制剂治疗不能恢复尿素酶阴性突变体定殖在生侏儒仔猪胃中的能力。
脲酶参与幽门螺杆菌的氮代谢,脲酶活性产生的氨和碳酸氢盐被认为会影响宿主的许多细胞过程,包括细胞裂解。
除脲酶外,非脲酶基因也有助于耐酸,并且在酸性pH下的存活和生长与脲酶无关。 在这些非脲酶基因中,已显示三种调节蛋白(Fur,NikR和HP0166)对幽门螺杆菌的适应性有贡献。 这表明严格调节耐酸机理的重要性。
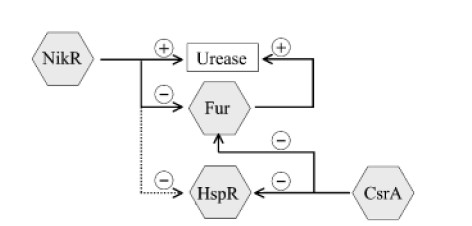
Karin et al., FEMS Microbiol Rev. 2006
NikR通过Fur调节系统直接和间接调节脲酶的表达。CsrA调节Fur和HspR调节系统的表达。通过不同基因调节蛋白的相互作用,幽门螺杆菌能够感知和响应多种信号。
细胞的趋化作用与运动
胃上皮细胞层覆盖着一层厚厚的粘液。假定该层甚至对于小分子也相对不可渗透。幽门螺杆菌的能动性和趋化性是有效穿透这一粘液层的关键。
在小鼠感染模型中,几乎任何运动和趋化性系统基因的诱变都消除了幽门螺杆菌感染胃粘膜的能力,强调了这些因素对定殖的重要性。
运动性
幽门螺杆菌的运动性是通过存在两到六个极性的带鞘鞭毛而实现的。鞭毛由三个结构元素组成:基体,钩子和细丝。迄今为止,超过50种蛋白质与鞭毛的结构或调控组织有关。
鞭毛丝由两个亚基FlaA和FlaB组成。幽门螺杆菌flaA和flaB突变体无法在感染仔猪的模型中定植,表明幽门螺杆菌鞭毛对定殖是必需的,幽门螺杆菌的毒力也因此而增加。
幽门螺杆菌motB基因编码鞭毛运动旋转蛋白。 幽门螺杆菌motB基因敲除突变体仍包含鞭毛,但不能运动。该突变体在小鼠中定植的能力降低,证实了运动性是完全传染性所必需的。
鞭毛基因转录的调控不同于许多其他细菌。与许多其他带鞭毛的革兰氏阴性细菌相反,幽门螺杆菌没有转录调控因子来调控鞭毛基因的转录。
据推测,幽门螺杆菌的运动不需要严格的调节,因为它在任何时候都是不可或缺的。然而,在幽门螺杆菌中仍然可以看到一些转录调控。例如,蛋白质FlhA和FlhF,基体的组成部分,需要在中后期鞭毛基因转录之前出现。
趋化性
除了运动性,趋化性对于幽门螺杆菌的定植也是必不可少的。趋化性允许幽门螺杆菌将其运动导向胃上皮细胞层。
由HP0099编码的幽门螺杆菌趋化性受体传感器识别碳酸氢盐和精氨酸作为引诱剂。幽门螺杆菌外膜上这种传感器蛋白与反应调节剂CheY偶联。
反应调节剂CheY调节鞭毛运动蛋白的表达,使幽门螺杆菌游向其生态位。
应答调节因子CheY的一个敲除突变体未能在非生物小猪体内定殖,强调了趋化性在最初定殖中的重要性。
反应调节因子CheY及其组氨酸激酶的敲除突变体显示出对粘蛋白的趋化性反应减弱。
免疫逃避
在长期的定殖过程中,宿主对多种幽门螺杆菌抗原产生强大的免疫反应。然而,这些抗原通常没有表面暴露。
另一方面,表面暴露的抗原通常高度多样化,使宿主清除幽门螺杆菌变得更加困难。幽门螺杆菌感染极少产生足够的免疫反应,能够清除细菌。 实际上,幽门螺杆菌能够有效规避先天性和适应性免疫反应。
先天的免疫反应不能实质上识别幽门螺杆菌。大肠杆菌脂多糖(LPS)通过TLR4激活先天免疫应答。然而,幽门螺杆菌LPS远不是TLR4介导的基因表达的有效诱导剂。
在幽门螺杆菌中,TLR5介导的免疫应答激活效率也较低。 与肠沙门氏菌血清型鼠伤寒鞭毛蛋白相比,幽门螺杆菌鞭毛蛋白没有被释放,并且在通过TLR5激活IL-8分泌中也没有那么强。
先天性免疫反应未能识别幽门螺杆菌可能导致适应性免疫反应失败以随后清除感染。
自适应免疫系统的逃避至少由两个重要机制介导:抗原模拟和免疫抑制。抗原模拟导致宿主免疫系统无法正确识别幽门螺杆菌。例如,幽门螺杆菌LPS上的Le血型抗原也在人类上皮细胞上表达。结果,幽门螺杆菌LPS免疫原性差,从而支持幽门螺杆菌的持久性。在其LPS上缺少O抗原的幽门螺杆菌菌株在小鼠中定殖的能力显着降低。因此,幽门螺杆菌LPS的典型结构在定植中很重要。
除了通过抗原模拟来逃避免疫外,免疫抑制也有助于幽门螺杆菌感染的慢性化。
免疫应答可能偏向更抗炎的应答,或者下调(VacA)。幽门螺杆菌VacA可以阻断巨噬细胞中的吞噬体-溶酶体融合,导致巨噬细胞无法杀死幽门螺杆菌。
此外,VacA表达阻断T细胞活化并因此增殖,活化T细胞凋亡,并抑制T细胞中的抗原呈递。
B淋巴细胞的抗原加工可能被阻止,可能是通过将内体的成熟限制在发生抗原加载的MHC II类区室中。因此,VacA限制了针对幽门螺杆菌的T细胞和B细胞应答。
幽门螺杆菌的存在可以预防某些疾病?
通过以上各种方式,幽门螺杆菌得以在人体中生存下来,从某种程度上来说,幽门螺杆菌并不总是对人类宿主有害。
研究表明,幽门螺杆菌的存在可能抑制引起结核的细菌(结核分枝杆菌),预防哮喘,克罗恩病,食管反流,腹泻病以及食道癌。 幽门螺杆菌的发病率下降与儿童过敏性疾病和自身免疫性疾病,多发性硬化,腹腔疾病的发病率上升相关。
因此,从某种程度上来说,幽门螺杆菌有其存在的价值。这引起了关于是否需要根除幽门螺杆菌的讨论。
需要明确的是,幽门螺杆菌感染后不会立即对人体产生致死性危害和严重后果,所导致的慢性胃炎、消化道溃疡和胃癌等疾病是长期存在并慢性与其他因素共同作用的结果。
第五次全国幽门螺杆菌感染处理共识报告中有如下陈述:
根除幽门螺杆菌的获益在不同个体之间存在差异
根除幽门螺杆菌促进消化性溃疡愈合和降低溃疡并发症发生率,根除幽门螺杆菌可使约80%早期胃 MALT 淋巴瘤获得缓解。与无症状和并发症的 幽门螺杆菌感染者相比,上述患者根除幽门螺杆菌的获益显然更大。胃癌发生高风险个体有胃癌家族史、早期胃癌内镜下切除术后和胃黏膜萎缩和(或)肠化生等。根除幽门螺杆菌预防胃癌的获益高于低风险个体。

在做出可靠的功能性消化不良诊断前,必须排除幽门螺杆菌相关消化不良。
幽门螺杆菌胃炎伴消化不良症状的患者,根除幽门螺杆菌后可使部分患者的症状获得长期缓解,是优选选择。
幽门螺杆菌感染是消化性溃疡主要病因,不管溃疡是否活动和是否有并发症史,均应该检测和根除幽门螺杆菌。
…
总的来说,对于无抗衡因素 ( 高龄、伴存疾病、社区再感染率、卫生经济因素等 ) 的个体,根除幽门螺杆菌治疗利大于弊。
儿童:
不推荐对 14 岁以下儿童行常规检测幽门螺杆菌。推荐对消化性溃疡儿童进行幽门螺杆菌检测和治疗,因消化不良行内镜检查的儿童建议行幽门螺杆菌检测与治疗。
与成人相比,儿童根除治疗不利因素较多,包括抗菌素选择余地小,对药物不良反应耐受性低。此外,儿童幽门螺杆菌感染有一定自发清除率,根除后再感染率也可能高于成人。
老年人:
老年人根除幽门螺杆菌治疗药物不良反应风险增加,因此对老年人根除幽门螺杆菌治疗应该进行获益-风险综合评估,个体化处理。
问卷调查显示,多数临床医生对老年人根除幽门螺杆菌治疗的态度趋向保守。一般而言,老年人(年龄>70 岁)对根除幽门螺杆菌治疗药物的耐受性和依从性降低,发生抗生素不良反应的风险增加;另一方面,非萎缩性胃炎或轻度萎缩性胃炎患者根除幽门螺杆菌预防胃癌的潜在获益下降。
合理看待幽门螺杆菌感染后果至关重要,对自然人群中幽门螺杆菌感染是否需要进行干预,需要综合权衡利弊。对于有根除治疗指征的患者,需要给予规范治疗,提高首次根除率,减少耐药性发生。
在慢性感染过程中,多株菌株同时定植于一个宿主,并且幽门螺杆菌分离株的遗传变异使幽门螺杆菌相关的发病机理难以从单个因素中预测。 幽门螺杆菌与其宿主的共同进化使它得以终生定居。
随着现代卫生环境改善及抗生素的大量使用,幽门螺杆菌的生长和传播越来越难,年轻一代中感染率较低,在未来几十年中幽门螺杆菌感染率将进一步下降。
更好地理解幽门螺杆菌和其他胃肠道微生物群之间的对话可能为预防或治疗其感染提供新的方向。如在肠道菌群健康检测报告中发现幽门螺杆菌感染,则应引起重视。当需要治疗时,应评估新的治疗策略和药物,或者应该制定替代策略来控制细菌的毒力,从而避免出现溃疡和胃癌而不消除其积极影响。
附录: 幽门螺杆菌的发现史
在1980年代初,幽门螺杆菌首次被发现是引起胃部疾病的原因。该发现帮助研究人员将幽门螺杆菌感染与胃炎,溃疡和胃癌等联系起来。
1982年,两名澳大利亚研究人员巴里·马歇尔和罗宾·沃伦描述了幽门螺杆菌感染的作用。
然而,沃伦和马歇尔关于幽门螺杆菌功能的理论并未立即被医学界接受。当时,大多数科学家都不相信细菌可以在人的胃中生活。
马歇尔无法在实验室小鼠中进一步测试他的工作,也不允许在人身上进行实验。马歇尔这位勇敢的科研工作者想到了一个办法。
他决定亲自吃下幽门螺杆菌。他从病人的肠道中提取该菌,将其放入肉汤中,然后饮用。
几天后,马歇尔出现了肠道症状,例如恶心,呕吐,口臭和疲劳。他做了胃活检,且能够培养幽门螺杆菌,证明是细菌引起了他的症状。
医学界最终接受了幽门螺杆菌引起溃疡和其他肠道问题的观念,但是接受的道阻且长。
1994年,美国国立卫生研究院共识发展会议正式承认幽门螺杆菌与溃疡之间的紧密联系。该小组建议对溃疡患者进行抗生素治疗。
1996年,FDA批准了首个针对幽门螺杆菌引起的溃疡的抗生素疗法。
一年后,疾控中心(CDC)与其他政府机构和学术机构合作发起了一项全国运动,为医患相关人员提供有关幽门螺杆菌与溃疡之间的联系。
2005年,马歇尔和沃伦获得了诺贝尔生理学或医学奖。溃疡不再被视为无法治愈的慢病,而是一种可以通过短期的抗生素和酸分泌抑制剂治疗的疾病。
【参考文献】
Burucoa C, Axon A. Epidemiology of Helicobacter pylori infection. Helicobacter. 2017 Sep;22 Suppl 1. doi: 10.1111/hel.12403. PMID: 28891138.
Camilo V, Sugiyama T, Touati E. Pathogenesis of Helicobacter pylori infection. Helicobacter. 2017 Sep;22 Suppl 1. doi: 10.1111/hel.12405. PMID: 28891130.
Eusebi LH, Zagari RM, Bazzoli F. Epidemiology of Helicobacter pylori infection. Helicobacter. 2014 Sep;19 Suppl 1:1-5. doi: 10.1111/hel.12165. PMID: 25167938.
Mentis A, Lehours P, Mégraud F. Epidemiology and Diagnosis of Helicobacter pylori infection. Helicobacter. 2015 Sep;20 Suppl 1:1-7. doi: 10.1111/hel.12250. PMID: 26372818.
Thorell K, Lehours P, Vale FF. Genomics of Helicobacter pylori. Helicobacter. 2017 Sep;22 Suppl 1. doi: 10.1111/hel.12409. PMID: 28891132.
Julie Marks.Robert Jasmer, MD What Is H. Pylori? Symptoms, Causes, Diagnosis, Treatment, and Prevention. 2020.9
History of H. Pylori: What We Do and Don’t Know Before the discovery of the bacterium, doctors thought stomach ulcers were due to stress and spicy foods.
Burucoa C, Axon A. Epidemiology of Helicobacter pylori infection. Helicobacter. 2017 Sep;22 Suppl 1. doi: 10.1111/hel.12403. PMID: 28891138.
Kamboj AK, Cotter TG, Oxentenko AS. Helicobacter pylori: The Past, Present, and Future in Management. Mayo Clin Proc. 2017 Apr;92(4):599-604. doi: 10.1016/j.mayocp.2016.11.017.
Eusebi LH, Zagari RM, Bazzoli F. Epidemiology of Helicobacter pylori infection. Helicobacter. 2014 Sep;19 Suppl 1:1-5. doi: 10.1111/hel.12165. PMID: 25167938.
Yang JC, Lu CW, Lin CJ. Treatment of Helicobacter pylori infection: current status and future concepts. World J Gastroenterol. 2014 May 14;20(18):5283-93. doi: 10.3748/wjg.v20.i18.5283.
Sun Y, Zhang J. Helicobacter pylori recrudescence and its influencing factors. J Cell Mol Med. 2019 Dec;23(12):7919-7925. doi: 10.1111/jcmm.14682. Epub 2019 Sep 19.
Tao Zhi-Hang,Han Ji-Xuan,Fang Jing-Yuan,Helicobacter pylori infection and eradication: Exploring their impacts on the gastrointestinal microbiota.[J] .Helicobacter, 2020, 25: e12754.
Algood HM, Cover TL. Helicobacter pylori persistence: an overview of interactions between H. pylori and host immune defenses. Clin Microbiol Rev. 2006 Oct;19(4):597-613. doi: 10.1128/CMR.00006-06.
Kori M, Daugule I, Urbonas V. Helicobacter pylori and some aspects of gut microbiota in children. Helicobacter. 2018 Sep;23 Suppl 1:e12524. doi: 10.1111/hel.12524. PMID: 30203591.
van Amsterdam K, van Vliet AH, Kusters JG, van der Ende A. Of microbe and man: determinants of Helicobacter pylori-related diseases. FEMS Microbiol Rev. 2006 Jan;30(1):131-56.
Waskito LA, Yamaoka Y. The Story of Helicobacter pylori: Depicting Human Migrations from the Phylogeography. Adv Exp Med Biol. 2019;1149:1-16. doi: 10.1007/5584_2019_356. PMID: 31016625.
Pereira-Marques J, Ferreira RM, Pinto-Ribeiro I, Figueiredo C. Helicobacter pylori Infection, the Gastric Microbiome and Gastric Cancer. Adv Exp Med Biol. 2019;1149:195-210.
RU Nan, DU Yi-qi, LI Zhao-shen. 幽门螺杆菌根除指征的演变[J]. 中国实用内科杂志, 2019, 39(006):515-519.
中华医学会消化病学分会幽门螺杆菌和消化性溃疡学组, 全国幽门螺杆菌研究协作组, 刘文忠,等. 第五次全国幽门螺杆菌感染处理共识报告[J]. 胃肠病学, 2017(6).