-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康
《血糖,微生物,胰岛素》
2型糖尿病(T2D)是一种全球性慢性代谢性疾病,目前已影响超过 4.6亿人,其社会经济负担巨大,迫切需要寻求有效的治疗方法。
根据中华医学会糖尿病学分会发布的《中国2型糖尿病防治指南》,我国2型糖尿病的管理路径清晰而规范:以生活方式干预为基石,以二甲双胍为一线首选,后续根据情况采取阶梯式的强化治疗。
然而,尽管指南明确,临床上仍然面临治疗反应个体差异大这一核心难题,这导致我国仍有近半数患者血糖控制不达标。为何同样的“金标准”方案,效果却天差地别?
多项研究发现,2型糖尿病的肠道菌群组成与健康人存在明显差异,菌群失衡可能通过影响短链脂肪酸合成、胆汁酸代谢及胰岛素敏感性等途径促进代谢紊乱。
甚至连二甲双胍这些药物的降糖效应,竟有相当一部分是依赖其对患者肠道微生物群的重塑和调节。
本文将介绍当前有关肠道微生物群调控葡萄糖稳态的潜在机制,并重点探讨近年来通过靶向肠道菌群改善糖代谢的研究进展。其中包括粪菌移植、益生元、益生菌、合生元与外源性代谢调节物质等多种策略在动物模型中的应用及其转化潜力。这些非侵入性干预手段有望为2型糖尿病带来新的、有效的治疗或至少是辅助选择。
要揭示肠道菌群与个体糖尿病的关系,需要谨慎和长期的队列研究
肠道菌群:一个多因素互动的复杂网络
然而,事情并非绝对“好细菌”与“坏细菌”的简单对抗。肠道菌群是一个复杂的生态系统,这个复杂的网络包括:
所有这些因素交织在一起,共同决定了我们的代谢健康状况。
因此,要真正揭示肠道菌群在糖代谢中的作用机制,就需要做到:
这类研究不仅能为糖尿病的早期预测和个体化干预提供坚实证据,也将为利用肠道菌群进行精准营养调控和代谢重塑奠定科学基础。
谷禾已经通过14,846例2型糖尿病患者(包括妊娠糖尿病)构建了早期糖尿病预测模型,但该模型仍面临若干挑战。
未来谷禾会继续推进研究结合代谢组,药理学等多组学数据,并通过多中心、纵向的设计来控制药物等潜在混杂因素,以实现更高精度、更具普适性的肠道菌群早期糖尿病预测模型。
通过深入探索这些微生物是通过哪些机制影响血糖平衡和代谢功能的,也许会为糖尿病治疗带来新的突破。
肠道屏障受损:免疫与糖代谢的微妙联系
肠道屏障是先天性免疫系统的重要组成部分,它的主要工作就是筑起一道坚固的墙,将肠道内的细菌、病原体及其代谢产物牢牢地限制在肠道内,防止进入血液循环。
▸当肠道屏障出现漏洞
然而,高脂饮食(HFD)会破坏肠道微生物群平调,诱发肠漏,这使得细菌内毒素,特别是革兰阴性菌产生的脂多糖(LPS),更容易进入血液循环,形成“代谢性内毒素血症”。
▸炎症的触发机制
—警报响起
泄漏到血液中的LPS会激活免疫细胞表面的Toll样受体4 (TLR4)。
—信号传导
TLR4被激活后,会启动一个信号级联反应,导致细胞核内的 NF-κB激活。NF-κB是调控炎症反应的总开关。
—促炎因子
被激活的NF-κB会命令细胞大量生产和释放促炎细胞因子,如肿瘤坏死因子-α (TNF-α)、白介素-6(IL-6)等。在全身造成低度慢性炎症。
值得注意的是,近期研究发现,不同菌种来源的LPS在影响葡萄糖代谢、炎症反应及肠屏障完整性方面存在差异,说明仅以LPS总量评价肠漏程度可能并不准确。
▸ 慢性炎症:导致胰岛素抵抗的元凶
这种炎症状态是导致代谢紊乱的关键因素之一,例如,TNF-α会直接干扰肌肉细胞对胰岛素的响应,阻碍血糖的正常利用,最终引发胰岛素抵抗、高血糖及高胰岛素血症。
▸免疫系统与菌群的双向互动
免疫系统和肠道菌群的关系并非单向的,而是一个复杂的双向互动。
关键免疫细胞:Th17细胞
这是一种特殊的T细胞,它在正常情况下分泌IL-17和IL-22等因子,对于维持肠道屏障的完整性和抵御病原体至关重要。可以看作是城墙的守护者。
➦ 菌群 → 免疫系统
证据1(生酮饮食):生酮饮食会减少肠道中Th17细胞的数量。但如果给无菌小鼠移植了采用生酮饮食的人的粪菌,小鼠的Th17细胞也会减少。而补充双歧杆菌则可以恢复Th17细胞的水平。
证据2(高糖高脂饮食):高糖高脂饮食会减少那些能够诱导Th17细胞发育的特定细菌。如果给高糖高脂饮食喂养的小鼠补充这些特定的细菌,它们的Th17细胞水平得以恢复,血糖也得到改善。
➦ 免疫系统 → 菌群
证据(过继转移):将Th17细胞直接移植到肥胖小鼠体内,这些小鼠的肠道菌群结构发生了有益的改变,葡萄糖耐量也得到了改善。
doi.org/10.1146/annurev-physiol-051524-094728
►▷
不良饮食 → 菌群失调 → 肠漏 → LPS进入血液 → 激活免疫系统(TLR4)→ 慢性炎症(TNF-α)→ 胰岛素抵抗。
菌群的改变会影响关键免疫细胞(如Th17)的数量,而免疫系统的状态反过来又能重塑肠道菌群的构成。
这种菌群与肠道免疫之间错综复杂的相互作用,是理解代谢性疾病病理生理的核心,也为未来的治疗提供了新的靶点。
短链脂肪酸:菌群送给你的控糖礼物
短链脂肪酸(SCFAs)包括丁酸、丙酸、乙酸,它们是由肠道细菌通过碳水化合物发酵产生。
它们不仅仅是代谢产物,更是重要的信号分子,是肠道菌群与我们身体对话的语言。
▸ 短链脂肪酸如何调控血糖?
▸ 动物研究,直接补充SCFA改善血糖
多项动物实验表明,外源性补充SCFAs可改善能量代谢与血糖稳态,表现为体重下降、葡萄糖耐受性提升及胰岛素抵抗减轻。
▸ 人体研究,效果不一致
例如,口服丁酸仅在健康受试者中改善血糖控制,而对代谢综合征患者无显著效应,提示代谢紊乱本身,可能就损害了人体对SCFA信号的响应能力。
▸ 口服补充为何会失效?
口服补充SCFA是不符合生理规律的。
在自然状态下,绝大多数SCFA是在远端肠道(结肠)中由细菌产生的。
口服的缺陷:口服的SCFAs在到达结肠之前,可能早已在胃或小肠中被吸收或代谢掉,无法到达它们应该发挥主要作用的地方。
有力的证据: 一项巧妙的研究解决了这个问题。科学家设计了一种“菊粉-丙酸酯”,这种特殊结构可以保护丙酸不被提前吸收,精准地将其运送到结肠释放。结果发现,这种精准投放的丙酸,确实能够有效改善超重和肥胖人群的能量代谢和胰岛素敏感性。
这说明,SCFA在哪里释放,比释放了多少,可能更为重要。
▸ 为何病人的粪便里SCFA反而更高?
库存 ≠ 产量
一些研究发现,代谢疾病患者粪便中的SCFA含量反而更高。这似乎与“SCFA是有益的”这一观点相矛盾?
合理解释:粪便中的SCFA含量,仅仅是未被肠道吸收和利用的“剩余物资”。
▸ 肠道菌群-短链脂肪酸-肠道激素轴
短链脂肪酸通过与肠内分泌细胞(EECs)上的受体结合,刺激激素的释放,比如说,GLP-1(胰高糖素样肽-1)、PYY(肽YY)、GIP(胃抑制肽)、CCK(胆囊收缩素)等。GLP-1与GIP为主要的“促胰素”,能够在摄食后迅速加强胰岛素分泌反应,是控制餐后血糖的关键。
doi.org/10.1146/annurev-physiol-051524-094728
近年来的新发现进一步揭示,微生物群可通过调控宿主营养感知机制影响肝脏糖异生,形成由GLP-1介导的“肠–脑–肝”信号轴。
►▷
由于肠道菌群与上皮层密切接触,它可能通过改变肠内分泌细胞的营养感知机制,并利用短链脂肪酸及其他微生物代谢物作为信号分子,调控肠激素分泌和葡萄糖平衡。这种微生物与宿主的相互作用网络为解析肠源信号调控代谢疾病提供了新的理论框架。
菌群把胆汁酸变成影响血糖的信号
肠道是一个高度复杂的生态系统,如同一个动态的生物反应器,在这个反应器里,无数的微生物与我们吃进去的食物、以及我们身体自己分泌的物质(如胆汁)发生反应,生成了大量独特的代谢产物。
关于肠源性代谢产物我们前面已经讨论过短链脂肪酸,现在焦点转向另一位主角:胆汁酸。
★ 胆 汁 酸
▸ 初级胆汁酸
出生地: 肝脏。 原料: 胆固醇。
初始形态:在肝脏合成后,它们会与牛磺酸(主要在小鼠中)或甘氨酸(主要在人类中)结合,形成结合型初级胆汁酸。
主要工作:进入肠道,帮助我们消化和吸收脂肪。
▸ 次级胆汁酸
一旦初级胆汁酸完成了消化任务并进入肠道后段,肠道菌群就接管了,对胆汁酸进行两步关键的改造:
这种从初级到次级的转变至关重要,因为不同形态的胆汁酸,会像不同的钥匙一样,激活不同的细胞受体“锁”,从而触发完全不同的生理效应。
doi.org/10.1146/annurev-physiol-051524-094728
▸ 两大关键受体:TGR5 与 FXR
次级胆汁酸主要通过激活两个著名的受体来发挥信号作用:
—— TGR5受体 (明确益处)
激活机制:菌群将初级胆汁酸(如鹅去氧胆酸)转化为次级胆汁酸(如石胆酸),后者是TGR5受体的强效激动剂。
明确的益处:激活肠道细胞上的TGR5受体,能够促进GLP-1的分泌,从而改善高脂饮食动物的血糖稳态。
—— FXR受体 (更具争议)
FXR受体则要复杂得多,它的作用似乎取决于它在哪个器官被激活。
在肝脏中(作用清晰):
激活肝脏的FXR受体,可以改善健康和糖尿病小鼠的胰岛素敏感性。
在肠道中(作用矛盾):
一些研究报告称,使用激动剂激活肠道FXR能改善胰岛素抵抗和葡萄糖耐量。
而另一些研究(包括我们之前讨论的产乳酸菌的研究)则发现,使用拮抗剂抑制肠道FXR,或者直接把肠道FXR基因敲除掉,反而能改善血糖稳态。
这说明,FXR在肠道中的作用远非简单的“开”或“关”,而是受到多种因素调控的复杂网络。
★ 其他代谢产物
这些肠源性代谢产物通过影响能量代谢、免疫反应以及宿主信号通路,构成肠道微生物–代谢–宿主疾病之间的重要生物学纽带。
既然我们已经明确,肠道菌群是糖尿病发生发展的关键一环,那么一个问题随之而来:我们目前广泛使用的那些经典降糖疗法,比如二甲双胍等,它们的疗效背后,是否也隐藏着菌群的秘密?下面我们就来看看,常见的治疗方式是如何通过影响肠道菌群来帮助我们控制血糖的。
二甲双胍
二甲双胍是最常见的降糖药之一。它降低血糖的传统机制是减少肝脏制造葡萄糖的能力。但近些年,人们发现——它在肠道里也发挥着巨大作用。
研究发现,口服二甲双胍比注射更能有效降糖,提示它在消化道内可能有额外的作用通路。科学家进一步发现,二甲双胍能改变肠道菌群结构:
更有趣的是,如果把“吃过二甲双胍的小鼠”的小肠菌群移植到其他糖尿病老鼠体内,这些受体小鼠体内的营养感知通路得以恢复,进而抑制了肝脏的葡萄糖生成——也就是说,药效可以通过菌群“传递”出来。
这说明,二甲双胍不仅是“肝药”,更是“肠药”。它同时通过肠道菌群、胆汁酸,以及“肠–脑–肝”信号网络,共同调控血糖代谢。
GLP-1受体激动剂
GLP-1受体激动剂(胰高糖素样肽-1受体激动剂,GLP-1RAs)是一类降糖药物,GLP-1受体激动剂通过多靶点机制发挥作用:
▸肠道菌群对GLP-1的双重影响
促进分泌:肠道菌群能够促进肠道内GLP-1激素的分泌,这是一种有益的代谢效应。
限制作用:分泌的GLP-1在体内极易被二肽基肽酶-IV(DPP-IV)快速降解,导致其对血糖和食欲的系统性调节作用受限,仅产生局部、短暂的代谢效应。
注:DPP-IV 是 Dipeptidyl Peptidase-IV 的缩写,中文名称为 二肽基肽酶-4。它是一种丝氨酸蛋白酶(serine protease),广泛存在于人体的多种组织中,包括肠道上皮、肝脏、肾脏、免疫细胞以及血浆中。
因此,肠道菌群在介导GLP-1药物系统性效应中的具体角色仍不明确。
▸动物与人体研究中的差异
关于GLP-1RAs对肠道菌群的影响,现有研究结果存在不一致。
动物研究:在高脂饮食或糖尿病动物模型中,GLP-1RAs治疗能够增加肠道菌群的多样性,并提升有益菌(如Akkermansia muciniphila、乳酸杆菌)的丰度。
🧍♀️人类研究:也有观察到双歧杆菌数量增加。但大多数人类临床研究报告称,在接受GLP-1RAs治疗后,患者的肠道菌群组成并无显著变化。
▸给药途径:可能是造成差异的关键因素之一
大部分GLP-1RAs均经皮下注射给药,因此菌群改变或许是药物通过影响肠道生理功能(如延缓胃排空、降低肠蠕动等)所致的间接效应,而非药物直接作用于菌群。
目前,虽然口服剂型司美格鲁肽已获批准,但其对肠道菌群的直接影响尚缺乏系统性评估。
▸新视角:来自肠道菌群的DPP-IV
近期的一项关键研究为理解这一复杂关系提供了重要的新视角:
部分肠道微生物自身能够产生并分泌DPP-IV酶。这种细菌源性的DPP-IV同样会降解宿主的GLP-1,从而削弱其生理活性。
临床关联: 研究发现,在对DPP-IV抑制剂药物西他列汀反应不佳的个体中,其肠道微生物的DPP-IV活性显著更高。
干预潜力: 基于此,研究人员已鉴定出一种能特异性抑制微生物DPP-IV的抑制剂,并在动物模型中证实其能改善葡萄糖耐受性,并降低粪便DPP-IV活性。
►▷
这一发现为2型糖尿病(T2D)的治疗开辟了新思路。未来可能开发出一种联合干预策略,即同时靶向宿主和菌群来源的DPP-IV。这种策略有望更有效地保护内源性GLP-1,从而实现更优的血糖控制效果。
减重手术
两种常见的减重手术——Roux-en-Y胃旁路术(RYGB)和 袖状胃切除术(VSG),在胃肠道生理结构上的改变机制不同,但它们在治疗肥胖和糖尿病方面的效果及益处相当。
起初,人们认为手术后的机械性限制,也就说胃容量变小减少食物摄入,是体重下降与代谢改善的主要原因。然而,后续研究发现,减重手术会引发一系列深远的胃肠道生理适应,包括肠道激素分泌、胆汁酸代谢及 肠道微生物群的显著变化,这些因素彼此关联,共同促进体重下降与血糖耐受性改善。
▸ 肠道菌群的核心作用与证据
——菌群持久且独立的变化
研究表明,减肥手术后,肠道菌群会发生显著且持久的变化(至少维持十年)。这种改变似乎是独立于体重减轻或热量限制本身。
证据:与仅节食减肥个体相比,RYGB手术患者的菌群多样性增加;并且,RYGB手术的肥胖大鼠菌群,与体重相当的假手术组大鼠(未真正手术但体重通过节食控制)的菌群显著不同。
——因果关系的探索 (动物、人类)
动物实验:将接受了RYGB手术小鼠的肠道菌群移植到无菌小鼠体内,能够复制体重下降的效果,这强烈暗示了由手术介导的菌群改变在驱动体重减轻中可能具有部分因果作用。
人类研究:然而,在人类研究中结果更为复杂。将术后一年且体重下降30%的供体的菌群移植给代谢综合征患者,并未能改善其葡萄糖稳态。但值得注意的是,这种移植确实阻止了受体胰岛素敏感性的进一步恶化(相比之下,接受其他代谢综合征患者菌群移植的对照组则出现了恶化)。
这说明,肠道微生物群在RYGB的代谢改善中虽起到一定作用,但更可能是与其他机制协同发挥效应,而非单一决定因素。
▸ 菌群发挥作用的关键途径
近期的证据揭示了菌群影响代谢的具体机制,主要涉及以下两个方面:
——胆汁酸信号通路
垂直袖状胃切除术的降糖效果依赖于肠道菌群,并且需要功能正常的FXR和TGR5受体(两者均为胆汁酸受体)。
手术后的菌群改变会增加肠道中胆汁酸转运体的表达,从而促进石胆酸 (lithocholic acid) 的吸收并将其运输至肝脏。
在肝脏,石胆酸被转化为CA7S,这种物质可以直接激活TGR5受体,从而增加GLP-1的分泌,最终改善血糖控制。
——短链脂肪酸信号通路
减肥手术后,肥胖个体循环系统中的丁酸和丙酸水平显著增加,而乙酸水平则降低。
这些短链脂肪酸的变化,同样被认为有助于改善体重和葡萄糖稳态。
减肥手术带来的全面健康益处(体重减轻和葡萄糖稳态改善)不能归因于任何单一机制。它很可能是多种因素,包括肠道菌群的深远影响、胆汁酸信号的改变和短链脂肪酸的产生等共同作用的结果。
总结来说,不同的减重手术(如胃旁路术和袖状胃切除术)虽然操作方式差别很大,但减重与控糖效果相近。关键并非只是吃得少、吸收少,而是对肠道—代谢轴的系统性重启。
肠道菌群、胆汁酸、激素信号和神经代谢网络共同协作,把机体从易胖、胰岛素抵抗的状态,切换回更健康、更稳定的能量代谢模式。
以上这些发现让我们意识到,我们可能一直在间接利用菌群的力量。这自然而然地将我们引向了糖尿病治疗的下一个前沿:与其依赖药物对菌群的附带效应,不如直接将肠道菌群作为干预的核心。接下来,我们将探索那些专门为此设计的创新途径。
FMT 是目前临床上应用最广泛且成功率最高的治疗方法之一,特别是在治疗艰难梭菌感染以及其他多种胃肠道疾病中表现突出。近年来,FMT 也被探索作为一种新型的神经系统、免疫系统及代谢性疾病(包括肥胖与2型糖尿病)替代疗法。
▸ 动物研究中,FMT显著成效
糖尿病小鼠实验:持续为糖尿病模型小鼠(db/db小鼠)移植健康人类的粪便菌群,能够改善它们的葡萄糖耐量和新陈代谢。
运动与饮食实验:从健康饮食并坚持运动的小鼠身上获取菌群,并将其移植给久坐不动的高脂饮食小鼠,可以改善后者的葡萄糖耐量并减少其脂肪堆积。
肠道内容物移植:将健康大鼠的小肠内容物移植到高脂饮食的大鼠体内,可以迅速改善其对葡萄糖的耐受能力,并减少葡萄糖的生成。
动物研究普遍表明,移植健康的肠道菌群能够有效改善代谢问题。
▸ 🧍♀️人体临床研究的:效果有限且短暂
关键研究案例: 在两项人类研究中,患有代谢综合征的男性受试者,接受了来自瘦型的健康捐赠者的FMT。
短期效果(6周后): 受试者的胰岛素介导的葡萄糖摄取能力得到改善,糖化血红蛋白(HbA1c)水平也下降了。这是一个积极的信号。
长期效果(18周后):然而,之前观察到的有益效果不再显著。
▸ 为什么在人类身上效果不佳?
▸ 未来的改进方向
为了让FMT成为治疗代谢疾病的可行方案,需要更精细化的策略:
优化方案:需要调整FMT的时间、重复和剂量。
联合疗法:将FMT与生活方式干预(如改变饮食、补充膳食纤维)相结合。
近期的两项临床试验证明,当FMT与饮食改变或膳食纤维补充相结合时,这种联合策略确实能改善肥胖或2型糖尿病患者的代谢结果。
个性化FMT:类似于个性化医疗,未来可能需要发展“个性化粪菌移植”。即根据每个患者的具体情况,精心挑选或设计最适合他们的菌群来进行移植。
谷禾也会根据肠道菌群检测报告为合作方提供相关指标,便于更好地筛选与匹配。
多项研究表明,在代谢性疾病(包括肥胖与2型糖尿病)的动物和人类模型中,补充益生菌可在急性及长期阶段均显著改善多项代谢指标。
在这里,介绍用产乳酸菌、产丁酸菌和特定物种Akkermansia muciniphila治疗2型糖尿病和其他代谢疾病状态的效果。
AKK菌|Akkermansia muciniphila
Akkermansia muciniphila(简称AKK菌)是一种革兰氏阴性菌,具有降解黏蛋白的能力,主要定植于肠道黏液层,并可在粪便样本中检测到。
肠道粘液层的主要成分是粘蛋白(Mucins),粘蛋白是一种富含糖基的结构蛋白,是肠道黏液层的重要组成部分,这也是Akk菌的“主食”。
AKK菌与健康的关系:绝大多数证据指向有益
大量研究发现,在啮齿动物与人类中,肥胖或2型糖尿病患者体内的Akk菌丰度都显著偏低;当其丰度减少时,常伴随炎症水平上升、肝脏脂肪变性以及胰岛素抗性增强。
有一项宏基因组学研究报告指出,AKK菌的增加与2型糖尿病相关,理由是它降解粘蛋白会破坏肠道粘液层的完整性。
更多的研究表明,AKK菌的丰度与更厚的粘液层和更低的肠道通透性(即更少的“肠漏”)正相关。它似乎能通过一种尚不完全明确的机制,刺激肠道中负责生产粘蛋白的杯状细胞数量增加,从而实现“越吃越有”的良性循环。
Akk菌如何发挥作用?
Akk菌的益处主要通过其菌体上的特定成分和它分泌的蛋白质来实现。
Akk菌外膜上的一种叫 Amuc_1100 的蛋白质。
作用过程: 这种蛋白质可以激活肠道细胞上的TLR2受体,进而调节一系列负责细胞连接的紧密连接蛋白(如Claudin 3,Occludin等)的表达。
最终效果: 这大大增强了肠道细胞间的连接,加固了肠道屏障。屏障加固后,肠道中的有害物质(如内毒素LPS)就难以泄漏到血液中,从而减轻了全身的低度炎症,最终改善胰岛素抵抗和血糖控制。
最近,科学家发现Akk菌还能分泌一种名为 P9 的新型蛋白质。
作用效果: 在小鼠实验中,P9被证实能够促进GLP-1(一种重要的降糖激素)的分泌,从而改善葡萄糖耐量。
研究发现,活的Akk菌和巴氏杀菌的Akk菌都有效,但高温彻底灭活(Heat-killed/Autoclaved)的Akk菌则无效。
原因在于:巴氏杀菌的温度(约70°C)足以杀死细菌,但不会破坏关键蛋白Amuc_1100的结构和活性。而更高的灭菌温度则会使其变性失效。这为开发安全的菌剂产品提供了重要依据。
🧍♀️人体临床证据
Akk菌的益处已经在人体上得到初步验证。
安全性:早期的临床研究证实,无论是活菌还是巴氏杀菌的Akk菌,对人体都是安全且耐受性良好的。
有效性: 在一项针对代谢综合征患者的研究中,与安慰剂组相比,服用巴氏杀菌Akk菌的患者出现了显著的积极变化:
►▷
综合来看,上述动物与早期临床研究一致显示:
AKK菌的干预可重建肠道屏障完整性、降低代谢炎症并改善血糖稳态,提示该菌株具有成为治疗肥胖与2型糖尿病的潜在候选益生菌的巨大应用前景。
产丁酸菌
产丁酸菌并非单一菌种,而是一个庞大的功能性菌群。产丁酸菌是一类能够在厌氧环境下、通过发酵多种底物产生丁酸的肠道共生菌群。
★ Faecalibacterium prausnitzii
F. prausnitzii 是一种严格厌氧、产丁酸的共生菌,在小鼠与人类结肠中含量丰富。
为什么它如此重要?(关联性证据)
研究发现,2型糖尿病患者体内 F. prausnitzii 的丰度显著降低,而在接受减重手术后,该菌丰度显著增加,且与炎症标志物水平呈显著负相关。
这一系列发现表明,F. prausnitzii 可能通过减少肠道炎症、增强肠屏障完整性、改善代谢性内毒症,从而发挥潜在益生作用。
它如何发挥作用?
在结肠炎小鼠模型中,给予 F. prausnitzii 或其上清液,可显著增加肠上皮紧密连接蛋白表达,并降低炎症性细胞因子水平。
一个关键的发现是:单独使用丁酸,其抗炎效果远不如用F. prausnitzii的培养上清液。这说明,F. prausnitzii的益处并不仅仅来自于丁酸,它还分泌其他抗炎的有益物质。
研究人员后来确实鉴定出了一种由F. prausnitzii产生的“微生物抗炎分子”(microbial anti-inflammatory molecule, MAM),这种分子能够修复糖尿病小鼠的肠道屏障功能,并上调紧密连接蛋白表达。
给予F.prausnitzii可以改善啮齿动物的葡萄糖稳态,并且对2型糖尿病患者进行GLP-1RA治疗可以增加粪便中F.prausnilzii的丰度,这与空腹血糖呈负相关。
虽然目前尚无直接临床试验验证F. prausnitzii 在血糖调节中的疗效,但近期一项研究已证实,其长期补充在人体中是安全且可耐受的,并已启动相关的临床试验以进一步评估其作为下一代益生菌的潜力。
★ Anaerobutyricum soehngenii
这个菌它最初是在一项粪菌移植临床试验中引起关注的。研究者观察到,Anaerobutyricum属增加与受试者胰岛素敏感性改善密切相关。
动物实验:给糖尿病小鼠补充 A. soehngenii 可显著提高粪便中丁酸及次级胆汁酸水平,增强胰岛素敏感性,提升能量消耗。
🧍♀️人体临床试验:两项针对代谢综合征人群的临床试验表明,A. soehngenii 的口服或十二指肠输注均安全且耐受良好;单次十二指肠灌注实验显著提升GLP-1水平,并改善胰岛素分泌与敏感性。
►▷
无论是F. prausnitzii还是A. soehngenii,它们的益处是多方面的,不仅仅是生产丁酸,还包括分泌其他抗炎分子和调节宿主激素(如GLP-1)。这些产丁酸菌的研究都凸显了它们作为治疗代谢疾病的新型疗法的巨大潜力。
产乳酸菌
产乳酸菌是一类耐酸的革兰氏阳性菌,通常不具运动性,主要通过发酵碳水化合物产生乳酸作为主要代谢产物。乳酸是厌氧呼吸中的重要代谢物,既是宿主能量代谢中关键的中间产物,也可作为底物被其他肠道菌群利用以产短链脂肪酸。
明星成员: 其中最著名、研究最广泛、应用最普遍的就是乳杆菌属和双歧杆菌属的成员。
动物研究,效果显著
在啮齿类动物模型中,补充多种乳酸生成菌可显著带来以下代谢益处:
在多项研究中,使用以下菌株治疗,显著改善小鼠的血糖控制:
乳杆菌属
双歧杆菌属
核心作用机制:巧妙抑制FXR信号,促进GLP-1分泌
产乳酸菌改善血糖的机制相当精妙,其中一个核心通路与胆汁酸受体FXR有关:
1
分泌“胆盐水解酶” (BSH)
许多乳杆菌能产生一种叫做“胆盐水解酶”的工具。
2
分解胆汁酸
胆盐水解酶这个工具可以将“结合型胆汁酸”分解为“游离型胆汁酸”。
3
抑制肠道FXR活性
“游离型胆汁酸”激活肠道FXR受体的能力较弱,因此,这一过程的最终结果是降低了肠道FXR信号的整体活性。
4
解放GLP-1
关键点来了,肠道中的FXR受体被激活时,会抑制GLP-1(一种重要的降糖激素)的分泌。因此,当产乳酸菌抑制了FXR后,就相当于解除了对GLP-1的束缚,从而促进了GLP-1的释放,改善了血糖控制。
双重协同作用:抑制FXR还能增强短链脂肪酸诱导GLP-1分泌的效果。同时,某些产乳酸菌自身也能促进丁酸等短链脂肪酸的产生。这种 抑制FXR + 增加短链脂肪酸的协同作用,可能共同放大了GLP-1的分泌。
🧍♀️ 人体临床研究,好坏参半
与动物实验的普遍成功形成鲜明对比,产乳酸菌在人体临床试验中的表现,结果好坏参半:
☺一项研究显示,包含多种产乳酸菌的复合益生菌产品,相比安慰剂,能够降低2型糖尿病患者的糖化血红蛋白(HbA1c)和空腹血糖。
☺另一项研究发现,单独使用植物乳杆菌也能降低餐后血糖和HbA1c。
☹ 然而,与安慰剂对照组相比,补充罗伊氏乳杆菌、嗜酸乳杆菌或乳双歧杆菌并没有显著改善健康或糖尿病患者的血糖控制或胰岛素敏感性。
☺一个值得注意的细节是,在一项研究中,乳双歧杆菌(B. lactis)虽然没有改善代谢综合征患者的指标,但成功维持了他们的胰岛素敏感性,阻止了其进一步恶化。
鉴于在糖尿病患者体内,许多产乳酸菌(尤其是双歧杆菌)的数量有所减少,那么通过“缺啥补啥”的思路来恢复它们的水平,理论上应是一种有前景的治疗方法。
然而,现有的人体临床证据有限,乳酸菌对改善代谢性疾病的作用不足,因为每个人的饮食、基线肠道菌群和疾病表现都千差万别(即高度异质性),想用标准化的益生菌对所有人都产生效果,是不容易的。因此,益生元等可以增加整体微生物群的多样性和丰富性,而不是单一细菌,这可能会为更广泛的人群提供更有效的治疗选择。
2型糖尿病的治疗策略
doi.org/10.1146/annurev-physiol-051524-094728
益生元被定义为:“能够被选择性发酵,并导致胃肠道微生物群组成和/或活性产生特定变化,从而对宿主健康带来益处的成分。”
简单来说,一种物质要被称为“益生元”,必须满足苛刻的条件:
基于这些标准,许多食物或成分都可以被归入益生元的范畴。在众多候选物质中,当前研究最为集中、并在糖尿病治疗中表现出潜在疗效的包括几类新型功能性益生元。
菊粉型果聚糖(ITFs)
菊粉型果聚糖(ITFs)——主要包括菊粉(inulin)、低聚果糖(OFS)和果寡糖(FOS),它们本质上是一类由果糖分子链组成的不可消化性碳水化合物。能够被肠道细菌发酵利用,从而促进宿主健康。
它们如何发挥作用?—— 多途径、多靶点的系统工程
核心作用:精准“施肥”,优化菌群
机制一:放大GLP-1信号,控制血糖
这是菊粉型果聚糖改善血糖的核心途径。
证据: 益生菌(特别是双歧杆菌)利用菊粉型果聚糖作为底物,发酵产生短链脂肪酸,如乙酸和丁酸。而短链脂肪酸是已知的肠道L细胞分泌GLP-1的强效刺激剂。
铁证: 在GLP-1受体被基因敲除的小鼠中,或者在使用了GLP-1受体拮抗剂的小鼠中,菊粉型果聚糖带来的所有降糖益处都完全消失了。这证明了GLP-1通路在其中的决定性作用。
菊粉型果聚糖也能显著提高人和动物的餐后GLP-1水平。
机制二:激活GLP-2信号,修复肠道屏障
GLP-2可以看作是GLP-1的兄弟,它主要负责维持和修复肠道屏障的完整性。
研究发现,补充菊粉型果聚糖能够增加内源性GLP-2的分泌。如果在小鼠中阻断GLP-2受体,那么菊粉型果聚糖带来的修复肠道屏障、抗炎等益处也大部分会消失。
机制三:调节内源性大麻素系统
这是一个更深层的机制。菊粉型果聚糖诱导的菌群变化(或AKK菌的增加)能够调节肠道的内源性大麻素信号系统(endocannabinoid),增加2-棕榈酰甘油(2-palmitoylglycerol)、2-油酰甘油(2-oleoylglycerol)和2-花生四烯酰甘油(2-arachidonoylglycerol);降低花生酰胺(anandamide)水平;进而增强肠道屏障功能,减少LPS泄漏。
🧍♀️ 人体临床证据
虽然不是所有研究都报告了积极结果,但大量的临床试验已经证实了菊粉型果聚糖在人体中的益处:
►▷
菊粉类果聚糖代表了一种非常有前景的、非侵入性的2型糖尿病治疗方案。它不像直接补充益生菌那样面临能否存活和定植的问题,而是通过为体内已有的有益菌(如Akk菌和双歧杆菌)提供精准的养料,激发一连串有益的生理反应——核心是驱动GLP-1和GLP-2的分泌,最终达到控制血糖和修复肠道屏障的双重目的。
其他膳食纤维
首先,一个基本共识是:增加膳食纤维的摄入量,能显著降低患上肥胖和2型糖尿病的风险。
膳食纤维主要分为两大类:
🧬 植物来源的主要可溶性纤维包括:
然而,研究发现,不同可溶性纤维的效果差异很大,这取决于纤维的用量、食物来源、补充方式(是直接吃食物还是吃提纯的纤维补充剂)等因素。
几种可溶性纤维的表现:
🧪 β-葡聚糖—— 全能选手
来源: 主要存在于燕麦和大麦中。
一项对比研究发现,在高脂饮食中添加富含β-葡聚糖的大麦粉,能增加肠道丁酸、改善血糖。但如果直接添加提纯的β-葡聚糖纤维,同样能改善代谢。这表明β-葡聚糖本身就是强效的功能成分。
⁎ 作用机制
无论是动物还是人体研究,都强有力地支持β-葡聚糖作为一种益生元,在改善血糖和治疗代谢疾病方面具有巨大潜力。
🌽 抗性淀粉—— 瞒过小肠的特工
抗性淀粉它本质上是淀粉,但由于其特殊的结构,能抵抗小肠的消化,完整地到达结肠,成为微生物的食物。
来源:冷却的米饭、土豆、未完全成熟的香蕉等。
⁎ 作用机制(与β-葡聚糖类似):
🧍♀️ 人体证据
在患有代谢综合征和2型糖尿病的人群中,补充抗性淀粉(特别是2型抗性淀粉,如高直链玉米淀粉)能够改善胰岛素敏感性并降低空腹血糖,同时也能观察到短链脂肪酸产量的增加。
一个有趣的发现:补充高直链玉米淀粉会特异性地增加双歧杆菌的丰度,而双歧杆菌正是一种擅长发酵抗性淀粉的细菌。
🍎 果胶 —— 机制独特
来源: 广泛存在于水果中,如苹果、柑橘等。
⁎ 作用机制(与其他不同):
►▷
简而言之,膳食纤维是“好菌的食物,也是代谢的调节器”:当你吃更多含纤维的天然食物(燕麦、豆类、全谷、蔬果),肠道菌群就会发酵产出丁酸等代谢产物,能修复肠道、提升GLP-1分泌、降低炎症、帮助降糖。β-葡聚糖与抗性淀粉尤其被视为下一代代谢健康促进纤维,未来可能成为糖尿病膳食疗法的核心成分。
合生元是一种同时包含益生菌和益生元的产品。
这个设计的初衷是,通过提供益生菌最喜欢吃的益生元,来帮助它在复杂的肠道环境中更好地存活、定植并发挥作用。
鉴于益生菌能产生短链脂肪酸,而益生元是产生短链脂肪酸的代谢前体物质(原料),那么将两者结合,应能够协同增加短链脂肪酸的产生,从而对代谢健康产生比单独使用任何一种都更强大的益处。
🧬 合生元的常见组合
双歧杆菌/乳杆菌 + 低聚糖/膳食纤维
这种组合的设计理念是:由益生元提供底物,使益生菌能够在肠道定植并活跃代谢,从而增强肠道生态修复与宿主代谢调节效应。
并未实现“1+1 > 2”的突破
动物与人体研究均表明,补充益生元或益生菌本身即可带来代谢性益处,合生元干预能够改善肠道菌群生态与增加粪便SCFA含量。然而,在大多数研究中,联合应用(合生元)并未显示出明显优于单独使用益生元或益生菌的效果。
为什么这个看似完美的策略效果不理想?
研究人员认为是由于缺乏精准匹配,也就是说大多数研究在设计合生元产品时,只是想当然地将一种常见的益生菌和一种常见的益生元组合在一起,但未能首先验证,这个益生菌是否真的喜欢吃、并且能高效利用配给它的那个益生元。
这并不意味着合生元的理念是错误的,而是说明我们的执行方式需要更加科学和严谨。
改进:在进行昂贵且复杂的人体临床试验之前,必须增加一个关键的验证步骤:
►▷
合生元的概念本身极具潜力,但需确保益生菌和益生元是真正的天作之合,这种“1+1>2”的协同效应才会在临床上有更好的效果。这要求我们对菌株和底物的特性有更深入的了解和更严格的前期验证。
外源化合物(Xenobiotics)被定义为:“在机体内非天然存在的外来化学物质。”这个范畴非常广泛,从化妆品、药物到膳食补充剂中的成分都可能属于外源物。
前文已提到二甲双胍(metformin)与GLP-1受体激动剂(GLP-1RA)的降糖作用同样被认为与肠道微生物介导机制相关,而这些药物本质上也属于外源化合物的范畴。
虽然很多外源物对健康有害,但我们这里聚焦的是那些有益的外源物,重点分析两种备受关注的有益外源物:多酚和小檗碱。
多 酚 类 化 合 物 (Polyphenols)
多酚是一大类存在于植物中的化合物,如白藜芦醇、类黄酮等。
多酚类化合物是植物来源的次级代谢物,主要包括:
这些分子既能调节肠道微生物群结构,也能改善2型糖尿病的多种代谢指标。
💊白藜芦醇(Resveratrol)
白藜芦醇是多酚中研究最为深入的代表性化合物之一。
来源: 葡萄皮、红酒、花生等。
它可显著改善胰岛素敏感性、葡萄糖稳态、血脂水平、高血压等。但它的生物利用度很低,口服后能进入血液循环的量很少,而且大部分还和蛋白质绑定,无法发挥活性。
那它是如何起作用的?
答案指向了肠道。
口服有效。 多项研究发现,口服白藜芦醇可以改善小鼠的血糖,但腹腔注射(绕过了肠道)则无效。这有力地证明了它的作用点在肠道内。
口服补充剂也有益地改变了啮齿动物的肠道微生物组,降低了厚壁菌门/拟杆菌的比例,增加了Akk菌、双歧杆菌和乳杆菌的丰度,这与改善葡萄糖稳态和炎症标志物有关。
最终证据——粪菌移植: 将服用过白藜芦醇的小鼠的粪菌移植给普通高脂饮食的小鼠,后者也出现了血糖改善的效果。
🧍♀️ 人体临床研究
尽管研究尚少,但已有临床试验发现,补充白藜芦醇可以增加代谢综合征男性体内的AKK菌,并轻微改善血糖。
💊 黄酮类化合物(Flavonoids)
除白藜芦醇外,黄酮类化合物也能增加肠道有益菌数量,并改善葡萄糖耐受性、抑制炎症反应、增强肠屏障功能。
来源: 广泛存在于各种水果、蔬菜、茶中。
动物实验研究
在高脂饮食诱导的肥胖或糖尿病小鼠模型中:
蔓越莓提取物可提高胰岛素敏感性、降低HOMA-IR与循环内毒素(LPS)水平;同时伴随AKK菌丰度显著上升与肠屏障完整性增强。
蓝莓原花青素含有丰富的花青素与原花青素,同样可改善葡萄糖耐受;增加AKK菌含量;并增厚胃肠道黏液层。
苹果原花青素处理高脂饮食小鼠时,也观察到一致的结果:肠道屏障功能及AKK菌丰度同步提升。
这些研究揭示不同植物来源的黄酮类多酚均通过促进有益菌的富集和黏液层重塑,实现改善肠屏障与系统代谢功能的作用。
🧍♀️ 人体及体外研究证据
尽管人群中关于单独考察黄酮类化合物作用的临床研究仍然有限,但已有体外模拟与部分干预研究提供了支持性证据:
红酒葡萄提取物或红茶多酚在人体肠道模拟模型中均能增加AKK菌的丰度。
可可黄烷醇则在健康人群中可显著增加双歧杆菌和乳杆菌的数量,表明其对肠道菌群结构也具有积极调节作用。
综上,黄酮类化合物以其独特的双重功能而受到关注:
这些作用共同促进了葡萄糖代谢与胰岛素敏感性的改善,为其作为代谢性疾病营养干预的潜在候选物提供了有力依据。
小 檗 碱
来源: 黄连、黄柏等中草药的主要活性成分。
小檗碱可以直接作用于肝细胞,激活AMPK(一个关键的能量代谢开关),从而改善血糖(增强胰岛素敏感性与葡萄糖稳态控制)。但它的口服生物利用度同样很低。
小檗碱是否进入循环系统,依赖肠道菌群
小檗碱只有在被肠道菌群代谢为更易吸收的衍生物后,其药效才能被充分发挥。
——肠道菌群:加工
肠道菌群能将小檗碱转化为更容易被人体吸收的形式,帮助它进入血液循环。
例如,某些肠道细菌可将小檗碱还原为二氢小檗碱,这种形式在肠上皮中的吸收效率更高,随后可重新氧化为小檗碱并在全身循环中发挥作用。
——肠道菌群:效应放大器
动物实验表明,口服(而非注射)小檗碱能增加肠道产丁酸菌的数量和丁酸产量,并改善空腹血糖。这说明小檗碱的另一部分功效是通过调节菌群-丁酸实现的。
临床研究与争议
动物研究:在动物模型中,小檗碱改善血糖的机制似乎与增加GLP-1/GLP-2、增加次级胆汁酸(DCA)从而激活TGR5受体、增加SCFA产量等有关。这是一个非常清晰、正面的通路。
人体研究的反转:迄今为止唯一一项相关的糖尿病人体研究却得出了矛盾的结果:小檗碱使血液中次级胆汁酸和有益的产短链脂肪酸菌的显著下降了,但同时它确实又显著降低了患者的糖化血红蛋白。
这凸显了小檗碱作用机制的复杂性。小檗碱确实是一种有效的降糖物质,但它究竟是如何通过菌群在人体内发挥作用的,远比我们想象的要复杂,目前仍是一个充满争议和未解之谜,其肠道依赖机制亟需更多临床研究验证来阐明。
►▷
小檗碱就像一个“需要肠道助手的药”:它自己难以被吸收,但一旦被肠道菌群“加工”成可利用的形式,便能帮助调节血糖、减少炎症、修复肠屏障。不过,因为每个人肠道菌群不同,它在不同人身上可能表现出截然不同的效果。
尽管大量动物研究已明确证实,肠道菌群在血糖稳态调控中扮演着核心角色,但将这些发现直接转化为对人类有效的通用疗法却挑战重重。其根本原因在于人类肠道菌群的复杂性与高度个体化。
这种个体差异正是许多干预措施(如益生元或益生菌)效果因人而异的关键。
益生元:当人们吃下富含β-葡聚糖的特制大麦面包后,只有一部分人的代谢状况得到了改善。科学家检查后发现,这些“有效者”在干预开始时,体内就存在着“无效者”所缺乏的特定肠道细菌。是这些细菌帮助他们更好地利用了膳食纤维。
益生菌:吃下益生菌,不代表它们就能在你的肠道里安家落户,一项研究发现,11种常见益生菌能否成功在肠道定植,取决于每个人已有的菌群构成。
既然每个人都是不同的,那么治疗方案也必须因人而异,兼顾菌群个体差异与动态变化。这个“个性化”会是什么样子呢?
比如,个性化饮食算法,这个算法不仅分析一个人吃了什么,更整合了这个人肠道菌群数据、血液指标等多种参数。这样不仅可以预测这个人吃下特定食物后的血糖反应,更能反过来为他量身定制一套可以最大程度平稳餐后血糖的个性化饮食方案。
在糖尿病前期人群中,通过整合基线菌群特征,机器学习模型,也能预测哪些患者能通过什么样的运动有效改善血糖,而哪些患者则收效甚微。
简而言之,要让基于微生物群的疗法真正在人体中奏效,我们需要摆脱“一刀切”的思路,而是把每个人的肠道菌群当作独特的生态系统。未来的糖尿病干预,可能需要“定制化的微生物处方”:先读取你的菌群模式,再精准投喂适合的菌与食物,让微生物群自己帮你稳糖、抗炎、调代谢。
深入理解并善用
每个人的独有菌群信息
将是我们开启
代谢疾病精准治疗
新时代大门的钥匙
注:本账号内容仅作交流参考,不作为诊断及医疗依据。
主要参考文献
Weninger, Savanna N., Andrew Manley, and Frank A. Duca. “Managing Glucose Homeostasis Through the Gut Microbiome.” Annual Review of Physiology 88 (2025).
Howard, Elizabeth J., Tony KT Lam, and Frank A. Duca. “The gut microbiome: connecting diet, glucose homeostasis, and disease.” Annual review of medicine 73 (2022): 469-481.
Cho, Hyoung-Soo, et al. “Structure of gut microbial glycolipid modulates host inflammatory response.” Cell 188.19 (2025): 5295-5312.
Sun, Hanxiao, et al. “GLP‐1 receptor agonists alleviate colonic inflammation by modulating intestinal microbiota and the function of group 3 innate lymphoid cells.” Immunology 172.3 (2024): 451-468.
Su, Lili, et al. “Health improvements of type 2 diabetic patients through diet and diet plus fecal microbiota transplantation.” Scientific reports 12.1 (2022): 1152.
Anhê, Fernando F., et al. “Metabolic endotoxemia is dictated by the type of lipopolysaccharide.” Cell reports 36.11 (2021).
Baroni, Irene, et al. “Probiotics and synbiotics for glycemic control in diabetes: A systematic review and meta-analysis of randomized controlled trials.” Clinical Nutrition 43.4 (2024): 1041-1061.

谷禾健康
近来,Bilophila wadsworthia在谷禾肠道菌群检测实践以及多项肠道研究中检出率及其相对丰度持续升高,我们不禁思考,这是否与人群中一些相同的生活习惯有关,并且是否可能带来一些不良的健康影响呢?
沃氏嗜胆菌(Bilophila wadsworthia)是一种革兰氏阴性、专性厌氧的耐胆汁杆菌。它存在于人类胃肠道中,其重要特征是产硫化氢(H₂S):过量H₂S可干扰上皮线粒体代谢、破坏紧密连接和黏液层稳态,诱发或加重炎症,并引发腹胀、腹痛与排便模式改变。这一过程可能与代谢异常和肠黏膜炎症相互促进,与肠道炎症、炎症性肠病及肠易激综合征等相关。
从定植与扩增的诱因来看,饮食与宿主环境是关键驱动:西方饮食尤其是高饱和脂肪/乳脂饮食会提升牛磺酸结合胆汁酸(如 TCA)的比例与可及性,为B.wadsworthia提供充足“燃料”;动物性饮食占比高、纤维摄入不足则削弱产丁酸菌与丁酸水平,降低对B.wadsworthia的代谢性制衡;抗生素或质子泵抑制剂的使用、胆汁酸吸收与信号(FXR/TGR5)紊乱、肠腔更还原的环境以及黏膜屏障受损与轻度炎症,都会叠加提高其定植与增长的概率。
值得庆幸的是,针对B.wadsworthia过度增殖已有一些可操作的干预方向:
•调整饮食脂肪“质与量”,减少饱和脂肪/乳脂与牛磺酸摄入(例如海鲜尤其贝类,动物内脏等);
•增加可发酵膳食纤维(如菊粉、抗性淀粉)以提升丁酸生态、降低肠腔 pH 并重建竞争格局;
•审慎使用可能影响胆汁酸与菌群的药物;
•通过生活方式与微生态支持手段降低H2S负荷、改善屏障功能。
本文将从基础特征、致病机制到饮食与干预策略,系统解析Bilophila wadsworthia与人体健康的关联。
沃氏嗜胆菌(Bilophila wadsworthia)是一种革兰氏阴性、专性厌氧的耐胆汁杆菌,属于变形菌门->脱硫弧菌目->脱硫弧菌科->嗜胆菌属,于1988年从阑尾炎患者的腹膜液和组织标本中分离出来后首次被描述。
它存在于人类胃肠道中,被认为是共生肠道菌群的一部分,但越来越被认为是腹腔内、泌尿生殖系统和软组织感染中潜在的机会性病原体。并且其胆汁耐受性和将硫化合物进行还原,从而产生硫化氢(H₂S)的能力增强了其致病性,当其丰度过高时,可能与与炎症性肠病、肠易激综合征和结直肠癌等疾病有关。
1
基础信息
命名由来:Bilophila源自拉丁文 “bilis”(胆汁)和“philus”(喜爱),意为“喜胆汁的微生物”。wadsworthia是为了纪念美国Wadsworth厌氧菌实验室。
模式菌株:WAL 7959;其他菌株编号如 ATCC 49260、CCUG 32349、DSM 11045 (RZATAU)。
DNA G+C 含量:约 59.2 mol%。
形态:小到中等大小的杆状菌,通常为 0.7–1.1 μm × 1.0–2.0 μm。
染色特性:革兰氏阴性,但染色可能不典型。
编辑
Gan F,et al.BMC Infect Dis.2025
来自患者血培养的 Bilophila wadsworthia 革兰氏染色。细菌被染色为革兰氏阴性杆菌,如深色箭头所示。
运动性:非运动性
芽孢:不形成芽孢
细胞壁:典型的革兰氏阴性菌结构,含内毒素,但其活性低于大肠杆菌等常见致病革兰阴性菌。
超微结构:通过电镜可见典型的内膜和外膜结构,无鞭毛结构。
2
生长条件与代谢能力
氧气需求:严格厌氧
最适生长温度:35–37°C(人体体温范围)
菌落形态(在BBE琼脂上):初期为小、透明至半透明、中心黑色的菌落;培养 3 天后,可变为黑色、不透明、低凸或脐状,常伴硫化氢(H₂S)沉淀(黑色 FeS)。
呼吸类型:严格厌氧呼吸
主要代谢途径:能利用肽类作为碳源和能源,产生 乙酸为主要终产物,以及少量琥珀酸。
小鼠和人类实验表明以动物脂肪和乳源性饱和脂肪为基础的饮食可以增加Bilophila wadsworthia。
电子供体/受体:能以甲酸作为电子供体,进行硫还原反应,将含硫氨基酸或牛磺酸还原为硫化氢(H₂S)和乙酸;
不还原硫酸盐,但能还原亚硫酸盐、硫代硫酸盐,并产生H₂S。
人类肠道细菌B.wadsworthia的代谢
doi: 10.1073/pnas.1815661116.
★ 关键生化特征:
•异硫醚裂解酶:介导肠道中 H₂S 的生成,属于甘氨酰自由基酶家族;
•具有很强的过氧化氢酶活性:尤其对15%H₂O₂;
•约 75–90% 菌株产脲酶;
•不发酵糖;凝胶酶阴性、淀粉与七叶苷水解阴性、卵磷脂酶/脂肪酶阴性、吲哚阴性。
•对20%胆汁耐受并被刺激;对香豆素类耐受。
3
耐药性与敏感性
✔普遍敏感的抗生素:
甲硝唑:几乎所有菌株均敏感;
✔可能耐药的抗生素:
•克林霉素
•亚胺培南
•氨苄西林/舒巴坦
•头孢西丁(cefoxitin,32 μg/mL)
注:超过85%的菌株产生 β-内酰胺酶,导致对青霉素类和头孢菌素类天然抵抗。
4
人群中的存在情况
✔主要分离来源:
•人类及动物(如狗)的消化道(胃肠道)、泌尿生殖道和口腔(尤其是牙周袋);
•感染性病灶:如脓肿、化脓性感染;
✔在人体中的分布:
•一般在健康人群粪便中占比较低,但是如果一段时间高饱和脂肪/乳脂或大量牛磺酸摄入(例如大量海鲜尤其贝类,动物内脏等)其丰度会增加;
•但在某些病理状态下(特别是穿孔性或坏疽性阑尾炎)是第三常见的厌氧菌分离株;
•可从血液、脑脓肿、肝脓肿、肺脓肿、盆腔感染、口腔感染、皮肤软组织感染等多种临床标本中分离出,通常为混合感染的一部分。
✔与饮食的关系
•高动物性脂肪/蛋白饮食(富含饱和脂肪与胆汁酸)可显著促进肠道中 B.wadsworthia的增殖;
该菌被认为是 “西方饮食相关菌”,与炎症性肠病等现代慢性疾病发展存在潜在关联。
5
在健康与疾病中的作用
✔健康状态下的角色
•在健康人群中通常为非优势菌,数量比较低甚至检测不到;
•可能作为肠道正常厌氧菌群的一部分,参与含硫氨基酸代谢与胆汁酸相关底物的降解;
•如果丰度高,则产生的过量 H₂S(硫化氢)可能影响肠道上皮细胞功能与黏膜稳态。
✔在疾病中的潜在作用
(1)感染性疾病
•腹腔感染:阑尾炎(尤以坏疽/穿孔型)、腹膜炎、肝脓肿、脾脓肿;
•软组织与皮肤:Fournier 坏疽(坏死性筋膜炎)、伤口感染;
•口腔与头颈部:牙周感染、颌面部脓肿、中耳炎;
•妇科:盆腔炎、Bartholin 囊肿感染;
•血流感染:菌血症;
•骨与关节:骨髓炎;
•肺部:肺脓肿、脓胸。
(2)与炎症及免疫反应的关联
•产生大量 H₂S:低浓度为信号分子,高浓度具细胞毒性与促炎作用。
•可抑制线粒体功能、破坏 DNA、诱导氧化应激并损伤肠上皮屏障。
•可能参与炎症性肠病(IBD)、溃疡性结肠炎和克罗恩病的发病机制。
•内毒素(LPS)虽活性较弱,仍可激活宿主免疫并促进局部炎症。
•与肠道菌群失调密切相关,尤其在高脂高胆汁饮食、肥胖和代谢综合征背景下易增殖。
(3)与胆汁酸及饮食的交互作用
•该菌依赖胆汁环境生长,是典型的胆汁耐受与利用菌;
牛磺酸代谢是其重要特征,与胆盐循环和肠道硫代谢密切相关;
高动物脂肪摄入 → 刺激胆汁分泌 → 增加胆盐水解 → 提供牛磺酸等底物 → 促进Bilophila wadsworthia增殖;这种机制可能是现代饮食相关慢性炎症疾病的潜在“菌-食-炎”轴之一。
6
与人体及其他菌群的相互作用
✔与宿主互作:
•通过代谢胆汁酸相关物质(如牛磺酸)、产生 H₂S,影响肠道生理与免疫平衡;
•可能通过破坏肠道屏障,促进内毒素入血与系统性炎症;
✔与其他微生物互作:
•常与其他厌氧菌(如 Bacteroides, Clostridium, Fusobacterium)共生,形成复杂的感染微生物群落;
•在肠道中可能与益生菌(如产丁酸菌)竞争营养或生态位,加重菌群失调;
•与硫酸盐还原菌(如 Desulfovibrio)有代谢相似性,但不完全相同,可能在硫循环中占据不同生态位。
增强:
•Bacteroidales
•Bacteroides
•Odoribacter
•Peptococcaceae
抑制:
•Bifidobacterium
•Coriobacteriales
•Adlercreutzia
•Collinsella
•Porphyromonas
•Prevotella
•Clostridium
•Clostridiales incertae sedis
•Clostridiales Family XIII. Incertae Sedis
•Blautia
•Coprococcus
•Dorea
•Lachnospiraceae
•Ruminococcaceae
•Ruminococcus
•Dialister
•Campylobacteraceae
•Erysipelotrichaceae
沃氏嗜胆菌(Bilophila wadsworthia)属于正常肠道菌群的可检出成员;但在特定饮食/环境下可由“共栖”转为“条件致病菌”。包括以下几种情况:
①感染性疾病
Bilophila wadsworthia在腹腔感染中(如穿孔/坏疽性阑尾炎、腹腔脓肿与肝脓肿)被检出,通常与其他厌氧或兼性致病菌共同存在,呈现典型的混合感染特征;此外,虽不常见,但亦有零星菌血症病例被报道。
②促进炎症
研究从一名患者粪便中分离Bilophila wadsworthia, 并经连续7天口服灌胃于SPF小鼠,观察到显著的体重与多部位脂肪量下降、肝脾肿大,以及血清炎症标志物SAA与IL-6升高;且16S rRNA测序显示整体肠道微生物群α/β多样性与OTU组成未发生显著改变。
上述结果表明,在不显著扰动整体肠道微生态的情况下,高负荷Bilophila wadsworthia可诱发系统性低度炎症,具有潜在致病性,并可能参与肥胖、糖尿病等慢性炎症相关代谢疾病的发生与进展。
③增加代谢障碍风险
该研究揭示高脂饮食(HFD)与Bilophila wadsworthia协同,加剧宿主的代谢失衡:其通过提升肠黏膜与全身炎症、破坏肠屏障、扰乱胆汁酸与短链脂肪酸(特别是丁酸盐)代谢,最终导致更差的血糖稳态与肝脂肪变性;多组学(宿主转录组与微生物群转录组)分析指向脂多糖生物合成上调与丁酸代谢通路下调是关键机制。
B.wadsworthia与高脂饮食协同引发代谢障碍
doi: 10.1038/s41467-018-05249-7.
④还可能影响认知功能
还有动物研究发现,沃氏嗜胆菌(Bilophila wadsworthia)会损害海马体,导致认知能力下降。
▸ B.wadsworthia过高意味着什么?
那么,当Bilophila wadsworthia水平升高时可能意味着几件重要的事情,也可能指向一系列值得关注的变化或信号:
1.潜在的肠道菌群失调:高于正常水平的B.wadsworthia可能表明肠道微生物组失衡。
2.炎症风险增加:B.wadsworthia会产生硫化氢,过量会导致肠道炎症,并与炎症性肠病和肠易激综合征等疾病有关。
3.饮食不均衡:水平升高可能与饱和脂肪含量高的饮食和富含牛磺酸的食物(如肉类和奶制品)有关,因为这些会刺激B.wadsworthia的生长。
4.代谢问题:研究表明,较高水平的B.wadsworthia已被证明会加剧代谢功能障碍,特别是与高脂肪饮食相结合时。这可能导致炎症增加、肠道屏障功能障碍和血糖调节问题。
5.潜在的健康风险:虽然健康个体中存在B.wadsworthia,但过度生长与各种健康问题有关,包括与结直肠癌的潜在联系。
6.胆汁酸代谢:由于B.wadsworthia在富含胆汁的环境中茁壮成长,因此水平升高可能表明胆汁酸代谢或产生发生变化。
值得注意的是,虽然水平升高可能会引起关注,但B.wadsworthia本身的存在并不一定有害。它是许多人正常肠道菌群的一部分。关键是平衡——太多可能会导致问题。
▸ B.wadsworthia产生硫化氢的机制及影响
✔产生机制
人肠道中的Bilophila wadsworthia厌氧利用牛磺酸产生硫化氢(H2S)的完整脱磺代谢途径,并鉴定出关键的甘氨酰自由基酶“异乙酸磺酸亚硫酸裂解酶”(IslA):
该途径先由已知的牛磺酸:丙酮酸氨基转移酶(Tpa)将牛磺酸转为磺乙醛,再由新发现的 NADH 依赖性还原酶(SarD)还原为异乙酸磺酸(isethionate),随后 IslA 催化新型自由基介导的 C–S 键断裂,生成亚硫酸盐与乙醛;乙醛被 AdhE 氧化为乙酰辅酶 A,而亚硫酸盐经异化亚硫酸盐还原酶(Dsr)还原为 H2S。
✔对人体健康的潜在影响
H2S在生理低剂量具信号分子功能,但在局部高浓度时可抑制线粒体细胞色素氧化酶、损伤上皮细胞,导致:
•肠黏膜屏障受损,肠通透性上升(“漏肠”);
•黏膜免疫激活与促炎介质上调;
•系统性低度炎症风险增加。
并且在高脂饮食背景下,B.wadsworthia扩增与H2S负荷上升与代谢失衡相关,可能导致:
•空腹血糖上升/胰岛素抵抗;
•肝脂肪堆积与胆汁酸谱失衡;
•微生物短链脂肪酸(尤其丁酸)减少,进一步削弱屏障修复与免疫稳态。
▸ B.wadsworthia对炎症的影响
研究发现,B.wadsworthia丰度过高具有促炎倾向:与黏膜TH1型免疫应答、全身低度炎症和结肠炎风险上升有关,尤其在遗传易感或屏障受损宿主中更显著。具体机制如下:
✔系统性炎症
短期高负荷B.wadsworthia会导致:体重和脂肪量显著下降、肝脾肿大、血清SAA与IL‑6升高;但结肠形态与局部炎症基因(Il6、Tnfα、Tlr4)未见显著变化,提示以全身性低度炎症为主,而非急性局部结肠炎。
✔结肠炎与TH1免疫
在IL‑10−/−或DSS处理等易感条件下,富乳脂饮食(MF)特异性促发B.wadsworthia“爆发式”增殖,并诱导TH1偏向(IFNγ↑、IL‑12p40↑),显著提高结肠炎发生率与严重度。
机制关键在于MF促进肝胆汁酸牛磺酸结合,为B.wadsworthia提供含硫电子受体与优势生态位。
▸ B.wadsworthia与消化系统的关联
✔炎症性肠病与结肠炎
在屏障受损情况下,B.wadsworthia扩增与结肠炎显著相关;人群研究亦提示产硫菌与炎症性肠病联系增强。
✔腹胀与功能性症状
过量H2S会抑制肠上皮细胞的能量代谢并破坏黏膜完整性,继而使屏障功能下降、通透性升高,诱发与气体积聚导致的腹胀和炎症相关的不适感与敏感症状;在动物研究中,Bilophila wadsworthia的扩增与全身性低度炎症及消化功能紊乱相伴出现,提示其代谢负荷上升与宿主应答有关。临床观察亦显示,B.wadsworthia常在腹腔感染与阑尾炎标本中被检出,其数量增加时产生的H2S负担随之上升,进一步加剧局部刺激与屏障受损。
总体而言,当B.wadsworthia过度增殖时,可能通过H2S增加而诱发一系列胃肠症状,包括腹胀、腹痛以及排便习惯的异常,加重患者的消化不适与炎症相关表现。
✔结直肠癌风险信号
部分研究提示,结直肠癌患者的结肠菌群中B.wadsworthia的相对丰度约为健康对照的近两倍,这一差异在多项独立样本中均有报告,具有一定一致性与指向性;同时,H2S所表现出的遗传毒性与对上皮屏障的损伤特征,为建立从菌群变化到黏膜损害再到肿瘤风险上升的致病链条提供了合理假说依据,但当前证据仍以相关性为主,尚缺乏明确的因果性验证与机制层面的决定性证明。
✔代谢并发症“肠–肝–代谢轴”
在高脂饮食背景下,B.wadsworthia的扩增与多种代谢异常呈相关,包括空腹血糖升高、胰岛素抵抗的加重、肝脏脂肪变性形成、胆汁酸组成与比例的紊乱,以及短链脂肪酸尤其是丁酸水平的下降等;并且,即使在采取抑炎措施的条件下,仍可观察到部分不良代谢表型持续存在,这一现象提示除炎症通路之外还存在直接的代谢层面影响,可能独立驱动或维持这些代谢失衡的发生与发展。
那么究竟有哪些因素会导致导致Bilophila wadsworthia丰度过高呢?接下来我们将从饮食、微生态以及宿主相关多方面入手,系统梳理并逐一说明,一起来详细了解其中的关键影响因素。
1
饮食与营养相关因素
✔高脂/高饱和脂饮食(尤其海鲜贝类,乳脂,动物内脏)
高饱和脂肪促进肝肠轴中牛磺酸结合胆汁酸(如 TCA)增加,提供Bilophila wadsworthia所需的含硫电子受体与生态位优势。富乳脂饮食可引发B.wadsworthia“爆发式”扩增,并与黏膜 TH1 型应答、炎症表型与代谢异常相关。
✔动物性饮食与低纤维饮食
动物性膳食可在短期内提高胆汁酸排入与肠腔 pH、氧化还原条件的改变,从而利于耐胆汁、硫代代谢菌扩张。
低发酵性纤维摄入减少丁酸等短链脂肪酸(SCFAs)与抑菌代谢物,使B.wadsworthia生态位竞争压力下降。
✔牛磺酸相关底物增加
加工肉类、能量饮料及部分补剂中牛磺酸摄入升高,或间接增加牛磺酸可利用性。
胆汁酸的牛磺酸结合比例上升(受饮食与宿主代谢影响)直接增加B.wadsworthia可利用的硫源。
2
胆汁酸代谢与宿主生理
✔胆汁酸流量与结肠通达性增加
胆汁酸吸收障碍、肠道转运异常或小肠结肠反流样改变,增加结肠胆汁酸负荷,利于耐胆汁菌群(含B.wadsworthia)。
✔胆汁酸信号通路扰动(FXR/TGR5)
FXR 被抑或信号异常时,宿主对胆汁酸合成/回收的精细调控受损,可能提升肠腔可发酵硫源。
✔肝胆疾病或代谢综合征
相关病理状态常伴胆汁酸谱紊乱(结合/去结合比例、次级胆汁酸↑),为B.wadsworthia提供适宜生态位。
3
免疫状态不佳
✔黏膜屏障受损或免疫调节缺陷
如 IL‑10 信号不足、屏障破坏等条件下,B.wadsworthia更易扩增并触发炎症正反馈。
✔炎症微环境的双向作用
低度炎症可改变黏液层、胆汁酸转运与上皮代谢,反过来提高B.wadsworthia的定植与利用底物效率。
✔胃肠动力与分泌改变
蠕动减缓或分泌节律异常,延长底物滞留并改变胆汁酸在远端肠段的浓度与形态,有利于B.wadsworthia聚集。
4
药物与医疗相关因素
✔质子泵抑制剂(PPI)与抗生素暴露
质子泵抑制剂(PPI)可改变胃酸屏障与肠道菌群,增加胆汁酸通达与上游底物流向结肠的机会;广谱抗生素则削弱竞争菌群,为B.wadsworthia腾挪生态位。
✔胆汁酸代谢相关药物或补充剂
某些降脂药、胆汁酸结合树脂或促进胆汁分泌药物,可能通过改变胆汁酸谱与流量间接影响B.wadsworthia(取决于具体药物对结合比例与肠腔到达量的影响)。
✔营养补充剂中的牛磺酸摄入
高剂量牛磺酸补充,理论上可提高可利用硫源,尤其在高脂饮食并存时,叠加风险更大。
当Bilophila wadsworthia丰度过高时有哪些具体且可行的干预措施呢?
▸ 饮食结构干预:减少“供料”,恢复生态位竞争
✔偏向植物性、高纤维的膳食模式
目标:提升可发酵纤维与短链脂肪酸(特别是丁酸)生态,抑制Bilophila wadsworthia。
做法:每日纳入全谷物、豆类、根茎类与绿叶蔬菜;逐步增加,以避免胀气不适。
✔限制高饱和脂肪和动物肉类及富含牛磺酸饮食
依据:高脂饮食与过量乳脂可促胆汁分泌与牛磺酸结合胆汁酸上升,为B.wadsworthia提供底物。
做法:适度下调饱和脂来源(黄油、奶油、全脂乳),以橄榄油、坚果、亚麻籽,芝麻中的不饱和脂肪为主,控制总脂能比至中等水平。
✔避免不必要的牛磺酸补充
依据:B.wadsworthia可利用牛磺酸作为电子受体生成 H2S。
做法:避免能量饮料与高剂量牛磺酸补剂的额外输入。
▸ 益生元与益生菌:“以友抑敌”,重塑代谢
✔益生元(优先证据:菊粉/菊粉型果聚糖)
人体随机双盲交叉试验证据:每日约12g菊粉可显著提升Bifidobacterium、Anaerostipes(产丁酸属),并显著下降Bilophila。
使用建议:从低剂量起步(如3–5g/d),1–2 周递增至目标剂量,监测胀气耐受。
✔益生菌:抑制B.wadsworthia过度扩张
鼠李糖乳杆菌CNCM I-3690 (Lr) 的每日口服管饲导致粪便B.wadsworthia丰度显著降低。同样,鼠李糖乳杆菌CNCM I-3690 能够进一步减少盲肠和小肠中的B.wadsworthia扩张。除了通过阻止其在体内扩张来抑制与B.wadsworthia相关的代谢功能障碍外,它还通过其调节胰岛素水平的固有能力来改善代谢功能。
临床可及替代策略:选择有助于提升双歧或产丁酸生态的复合益生菌;关注个人耐受与症状反馈。
▸ 胆汁酸相关策略:减少远端结肠“胆汁酸泛滥”
饮食先行:优先通过“脂肪质量与剂量管理+高纤”降低胆汁酸通达与牛磺酸结合比例的上行驱动。
✔避免促胆汁酸通达远端结肠的行为与药理因素
例如不必要的长期高剂量脂肪冲击式饮食;与医师评估某些药物对胆汁酸谱与流量的影响。
注:个别药物(如胆汁酸结合树脂)对肠道胆汁酸生态影响复杂,应用需由医生根据适应症与并发症风险综合判断。
▸ 微生态与生活管理
✔提升产丁酸菌生态
路径:可发酵纤维(菊粉、抗性淀粉、部分半乳寡糖)+ 多酚类食物(莓果、绿茶、可可等)+ 充足睡眠与规律运动。
目标:通过丁酸盐以强化上皮代谢与屏障功能,降低B.wadsworthia优势。
✔减少含硫发酵压力与蛋白质过量腐败
在干预期控制过量红肉/加工肉类,避免过量富含含硫氨基酸的“单一高蛋白”模式与吃法。
✔缓解低度炎症与氧化应激
富含抗氧化的全食物饮食、压力管理、保证睡眠;必要时与医生讨论是否需要针对性抗炎策略(如有基础疾病)。
主要参考文献
Sayavedra L, Yasir M, Goldson A, Brion A, Le Gall G, Moreno-Gonzalez M, Altera A, Paxhia MD, Warren M, Savva GM, Turner AK, Beraza N, Narbad A. Bacterial microcompartments and energy metabolism drive gut colonization by Bilophila wadsworthia. Nat Commun. 2025 May 30;16(1):5049.
Natividad JM, Lamas B, Pham HP, Michel ML, Rainteau D, Bridonneau C, da Costa G, van Hylckama Vlieg J, Sovran B, Chamignon C, Planchais J, Richard ML, Langella P, Veiga P, Sokol H. Bilophila wadsworthia aggravates high fat diet induced metabolic dysfunctions in mice. Nat Commun. 2018 Jul 18;9(1):2802.
Peck SC, Denger K, Burrichter A, Irwin SM, Balskus EP, Schleheck D. A glycyl radical enzyme enables hydrogen sulfide production by the human intestinal bacterium Bilophila wadsworthia. Proc Natl Acad Sci U S A. 2019 Feb 19;116(8):3171-3176.
Han S, Krothapalli TR, Zafar SJ, Gautham S. A rare case of Bilophila wadsworthia bacteremia presenting as multiple hepatic abscesses: A case report and literature review. IDCases. 2025 Aug 11;41:e02342.
Feng Z, Long W, Hao B, Ding D, Ma X, Zhao L, Pang X. A human stool-derived Bilophila wadsworthia strain caused systemic inflammation in specific-pathogen-free mice. Gut Pathog. 2017 Oct 26;9:59.
Devkota S, Wang Y, Musch MW, Leone V, Fehlner-Peach H, Nadimpalli A, Antonopoulos DA, Jabri B, Chang EB. Dietary-fat-induced taurocholic acid promotes pathobiont expansion and colitis in Il10-/- mice. Nature. 2012 Jul 5;487(7405):104-8.
Baron EJ. Bilophila wadsworthia: a unique Gram-negative anaerobic rod. Anaerobe. 1997 Apr-Jun;3(2-3):83-6.
Schumacher UK, Eiring P, Häcker FM. Incidence of Bilophila wadsworthia in appendiceal, peritoneal and fecal samples from children. Clin Microbiol Infect. 1997 Feb;3(1):134-136.
Summanen P, Wexler HM, Finegold SM. Antimicrobial susceptibility testing of Bilophila wadsworthia by using triphenyltetrazolium chloride to facilitate endpoint determination. Antimicrob Agents Chemother. 1992 Aug;36(8):1658-64.

谷禾健康
凌晨两点外卖订单又刷新了记录
刚下单的芝士炸鸡、烤串、肥宅快乐水…
这些号称“当代青年续命神器”的食物
在不知不觉中消耗着我们的情绪健康
越来越多人有这样的感觉
“吃饱” ≠ “快乐”
超加工食品,就是那些经过复杂工业加工的食物,主要由食物和添加剂制成的配方,几乎不含完整的天然食物,比如方便面、薯片、汉堡、冷冻披萨、各种包装零食等,与较差的身心健康结果相关。
一份涵盖15,262人的国际ALIMENTAL研究刚报道了一篇文章,发现女性/年轻人食用超加工食品后抑郁风险更高。
本文我们为大家介绍一下这项涉及15,262名参与者的大规模国际ALIMENTAL研究的核心发现,系统阐述了不同饮食模式与重度抑郁症风险之间的量化关联,了解不同饮食习惯可能会如何影响他们的抑郁症风险。基于研究结果,本文还提供了具有循证医学依据的饮食调整策略,为通过营养干预预防和辅助治疗抑郁症提供了科学指导。
研究采用横断面设计,通过在线问卷收集数据,使用主成分分析识别饮食模式,并通过多变量分析评估其与抑郁症的关联。
ALIMENTAL研究是一项模断面在线国际调查,在2021年11月~2023年6月期间进行。
研究获得了法国、德国和加拿大伦理委员会的批准,通过社交媒体、心理健康协会和医疗机构招募参与者。
为了确保研究结果的可靠性,研究团队设置了严格的筛选标准,这样做的目的是避免这些因素对结果造成干扰,确保观察到的关联确实来自饮食本身。
采用 Benjamini-Hochberg 法校正多重检验,以优势比(OR)和 95% 置信区间(CI)评估膳食模式与抑郁的关联强度。
然后用统计学方法,比如运用主成分分析(PCA)提取 13 种膳食模式,把复杂的饮食数据简化成几种主流的饮食模式,再分析这些模式跟抑郁症的关系。
主成分分析简单说,就是把一大堆食物信息压缩成几个关键的饮食模式因子,他们最终识别出了13个因子。
其中最引人注目的两个是:
其他的因子还包括了:
每个因子代表一类具有相似营养特征或加工程度的食物组合。这些因子就像是给我们的饮食习惯贴标签,方便后续分析。
1. 超加工食品增加抑郁风险,性别差异显著
核心发现:女性和年轻人最脆弱。
换句话说就是:
这个发现并不孤立,实际上是证实了之前科学界在2021年和2022年,研究人员发表的两项荟萃分析:
说完坏消息,再来说说好消息。
2.健康饮食可降低抑郁风险(仅女性有效)
健康饮食包括水果、坚果(杏仁或榛子)、绿色蔬菜(如四季豆、西兰花、芦笋)、橄榄油、菜籽油或大豆油、绿叶沙拉或苦苣、茶饮、全麦面包等。
3. 其他重要发现
除了超加工饮食和健康饮食之外,其他的饮食也值得关注,比如吃罐头食品、喝含糖饮料,似乎和女性抑郁症风险增加有关。
关于膳食补充剂和女性抑郁风险增加有关,这可能是因为,吃这些补充剂的人本身就可能已经有抑郁倾向,或者存在其他健康问题,所以才去补充。
不能排除这些食物的摄入与其他食物的排除呈负相关,这也可能有助于解释观察到的关联。
吃高血糖指数食物、乳制品等,反而和抑郁风险降低有关,这可能是因为这些食物提供了一些必要的营养素,比如说在营养不良或能量不足群体中(如老年/慢性病患者),高GI食物提供快速能量,短期改善情绪低落。
也可能是因为存在人与人之间本身存在代谢差异,某些体质对糖代谢更适应,这要根据个人肠道菌群结构来看,肠道菌群检测报告中也有相关指标,可以看出个体对于碳水、糖类的代谢能力。
混杂因素影响
该研究还发现,某些混杂因素在某些群体中与抑郁症风险降低相关,如更高的成就、营养知识、有在家居住的伴侣、在家居住的儿童;
而另一些混杂因素则与抑郁症风险增加相关,如当前每日吸烟、肥胖、失业、肤色等。
科学家们提出了几种可能的解释:
◆ 女性的身体构造不同
女性和男性的激素水平、新陈代谢方式都不一样,女性的激素水平在月经周期、怀孕、更年期等不同生理阶段会发生显著变化。超加工食品通常高糖、高盐、高脂肪,可能干扰女性体内激素的正常平衡。
比如说,雌激素会放大乳化剂对肠道紧密连接蛋白ZO-1表达的抑制作用,增加肠道通透性,肠漏则进一步影响免疫系统功能,体内炎症因子水平上升更明显。
女性的身体脂肪分布与男性不同,通常更容易在腹部、臀部和大腿堆积脂肪。超加工食品的高热量和高脂肪含量,会加剧这种脂肪堆积,这可能与心血管疾病、糖尿病等慢性疾病相关。
◆ 男女吃的不一样
男性和女性可能偏爱不同类型的垃圾食品,吃的量也不同。比如女性可能更爱吃甜食和零食,男性可能更偏爱油炸或肉类食品。这些”口味偏好”的差异,可能导致对心理健康的影响也不同。
女性可能更容易受到情绪的影响,而出现情绪性进食行为。超加工食品往往具有浓郁的口感和香气,能够快速满足情绪上的需求,但长期来看,这种饮食习惯会导致营养不均衡和体重增加。
比如说,膳食乳化剂可能对肠-脑轴产生影响,并通过微生物群依赖机制诱导暴露者的心理/行为障碍。
乳化剂中羧甲基纤维素和聚山梨酯80过量食用会导致微生态失调,粘液降解细菌过度生长,以及IL-10或Toll样受体5进一步缺乏。
乳化剂可能还会增加肠上皮屏障中病原微生物的易位,引起肠道炎症。
乳化剂和相关微生物代谢对大脑的影响
Tan H,Nie S.FEMS Microbiol Rev.2021
比如说一些冰淇淋、奶昔、预包装蛋糕里面都含有乳化剂,而女生相对更爱吃这类超加工食品,因此可能带来更高的抑郁症风险。
可以详见谷禾之前写过的文章:
抑郁症与肠道微生物群有何关联
抑郁、焦虑、压力的肠道故事——精神健康的改善新途径
食品添加剂:健康还是危险?——从肠道微生物角度分析
◆ 对健康信息的处理方式不同
** 需要坦诚地说,这项研究的参与者中女性比男性多很多。这在抑郁症研究中很常见,可能是因为:女性本来就更关注健康话题,而且研究主要通过医疗机构和社交媒体传播,这些地方本身可能女性用户更多。不过研究者认为,这种”男女比例不均”不太可能影响他们观察到的性别差异。
◆ 各年龄段的吃法本来就不一样
想想看,爷爷奶奶那一代和现在的年轻人,饮食习惯都不一样。最近的科学调查发现了一个很有意思的现象:
越年轻、住在大城市、单身或离异的人,
越爱吃超加工食品。
这背后有很现实的原因:年轻人可能工作忙、不会或不愿意做饭,单身的人懒得准备精致丰盛的食物,大城市生活节奏快、外卖方便——这些都让方便面、冷冻食品、各种包装零食成了救命稻草。
◆ “从小就被喂坏了”
现在的年轻人可以说是垃圾食品的原住民——从幼儿园开始就接触各种包装饮料、膨化食品、快餐。这种从小培养的饮食习惯,可能让年轻男性比老年男性更容易受到超加工食品的情绪攻击。
就像抽烟一样,越早开始接触,成瘾性和伤害性往往越大。
这里有个更可怕的发现:超加工食品不只是让人心情不好,它还会引发一连串的健康问题——糖尿病、高血压、心脏病、肥胖等等。而这些慢性病本身就容易让人患抑郁症,形成一个”恶性循环“。
吃垃圾食品→身体发炎、代谢乱套→得慢病→心情更差→可能更依赖安慰性食物→恶性循环
具体来说:
◆ 影响菌群
高糖、高脂、防腐剂、缺乏纤维等超加工食品,不利于有益菌的生长,人工添加剂改变肠道环境的酸碱度,当坏细菌占上风时,它们会产生有毒物质(如脂多糖),破坏肠道屏障,让本来不该进入血液的东西跑进去,触发炎症反应。
抑郁症个体与健康对照组相比,微生物群变化如下:
Basiji K, et al., Metab Brain Dis. 2023
◆ 肠-脑轴
迷走神经直接连接肠道和大脑;肠道菌群能产生血清素、多巴胺等代谢产物(我们90%的血清素其实是在肠道产生的)。
血清素,参与调节情绪、食欲、睡眠和其他身体功能,比如说:
这些代谢产物通过血液循环或直接通过迷走神经传递到大脑,影响我们的情绪和行为。肠道炎症也会激活大脑中的炎症反应。
微生物群-肠-脑异常导致抑郁症
DOI: 10.1007/978-981-19-7376-5_10
◆ 其他微生物代谢产物
超加工食品通过双重途径加剧抑郁症风险:
◆ 炎症反应
超加工食品会让身体产生慢性炎症,当大脑接收到来自肠道的炎症信号时,负责情绪调节的区域(如海马体、杏仁核)开始罢工,压力激素皮质醇飙升,可能带来焦虑、抑郁、注意力不集中等情况。
抑郁症患者的炎症标志物包括:血清 IL-6、IL-1β、C反应蛋白升高。
◆ 代谢紊乱
超加工食品中的高糖、高脂肪成分会导致血糖快速上升后迅速下降,这种波动会引起情绪的起伏。长期食用会干扰胰岛素敏感性,导致能量代谢紊乱,使人容易感到疲劳、注意力不集中。
◆ 心血管负担
超加工食品中的反式脂肪酸和高钠含量会增加心血管疾病风险,血管健康受损时,大脑供血也会受到影响,可能导致认知功能下降。
◆ 恶性循环启动
心情不好的人往往会更渴望高糖、高脂的”安慰性食物”(这是大脑的本能反应),更没有动力去准备健康食物,从而选择一些方便快捷的垃圾食品。
这种本能的自我安慰机制却可能成为抑郁发展的催化剂——当不健康的饮食选择形成恶性循环时,科学干预的价值就凸显出来。
这正是研究食物与抑郁关系的关键意义:揭示这些现象背后的生理机制,才能为精准的健康干预指明方向。
健康的饮食习惯会帮助摄入许多营养成分,可以减轻炎症。其中,蓝莓,姜黄素等存在的植物化学物质(例如多酚)具有很强的抗炎特性,可能有助于治疗多种精神疾病。
益生菌,单独乳酸菌或与双歧杆菌联合使用——可能会改善抑郁和焦虑。
益生元,每天 5 克的低聚半乳糖和 1 克或以下的二十碳五烯酸可以有效缓解抑郁症状。
Omega-3脂肪酸、多不饱和脂肪酸在鲑鱼等海洋食品中含量很高,具有抗炎特性,可以改善并延缓细胞因子诱发的抑郁症的发作。
维生素,例如抗坏血酸(维生素C)和α-生育酚(维生素E)具有直接清除自由基的特性。
营养素(例如硒,锌和半胱氨酸)是抗氧化剂系统(例如谷胱甘肽过氧化物酶和超氧化物歧化酶)的辅助因子。初步证据表明,补充抗氧化剂如n-乙酰半胱氨酸可以改善抑郁症状。
当心理健康成为
全社会关注的焦点时
答案或许就藏在
我们每一餐的选择里
主要参考文献:
Achour, Y.; Lucas, G.; Iceta, S.; Boucekine, M.; Rahmati, M.; Berk, M.; Akbaraly, T.; Aouizerate, B.; Capuron, L.; Marx, W.; et al. Dietary Patterns and Major Depression: Results from 15,262 Participants (International ALIMENTAL Study). Nutrients 2025, 17, 1583.
谷禾健康
艰难梭菌是一种革兰氏阳性、形成孢子的厌氧芽孢杆菌,是艰难梭菌感染(CDI)的病原体。该菌于1935年首次分离得到,1977年报道了第一例确诊的CDI病例。从那时起,CDI的发病率逐年上升,艰难梭菌感染现在是全世界医院腹泻的最常见原因。
艰难梭菌在我国健康成年人结肠的定植率约为4%-7%,而腹泻患者的检出率高达15%-40%。但为什么一些人群肠道中存在艰难梭菌,却没有出现任何症状?而另一些则会出现腹泻、腹痛,甚至发展为假膜性结肠炎?
这是因为艰难梭菌可分为产毒型和非产毒型,通常只有产毒型会引发临床症状,其感染的表现主要受多种毒力因子影响,这些毒力因子可能比艰难梭菌的存在更为重要。并且健康的肠道微生物组对艰难梭菌感染具有保护作用。平衡的微生物和宿主因子可抑制艰难梭菌的发芽和生长,同时微生物群与宿主免疫系统的相互作用调节免疫反应,刺激抗菌肽和分泌型IgA的产生,维持菌群平衡,通过营养竞争、生态竞争和生态位排斥等机制抵抗艰难梭菌的定植和感染。
例如一些有益菌通过产生短链脂肪酸降低管腔pH值(不利于艰难梭菌),并刺激粘蛋白和抗菌肽的生成以增强防御屏障。丁酸盐还能稳定缺氧诱导因子-1(HIF-1)、增强紧密连接,保护肠道上皮免受艰难梭菌毒素损害。
艰难梭菌的孢子和生长依赖特定胆汁酸,肠道共生细菌通过调节胆汁酸代谢产物,抑制其萌发和定植。例如,Clostridium scindens可催化胆汁酸7α-脱羟基化,生成次级胆汁酸,从而增强对艰难梭菌感染的抵抗力。
当肠道微生物组的平衡状态受到干扰或破坏时,艰难梭菌感染(CDI)的易感性会显著增加。例如由于使用抗生素,年龄增长、其他胃肠道疾病,营养状态不佳、肥胖、癌症化疗这些因素都会增加艰难梭菌感染的风险。
由于艰难梭菌的危害由毒力因子决定,检测产毒菌株或基因显得尤为重要。目前,一些检测方法只能识别艰难梭菌菌株,无法区分是否为产毒菌株,可能导致误诊或过度治疗。为提高诊断准确性,近年来开发了多种技术,包括检测毒素基因的分子诊断技术和直接检测毒素蛋白的免疫学方法。16S测序仅能分辨到物种层面,宏基因组测序(包括一些靶向的测序)则可识别毒力基因。这些技术能够较快速、准确地识别产毒菌株,帮助临床医生制定更有效的治疗方案,减少不必要的抗生素使用及相关并发症。
艰难梭菌感染的治疗和预防也是人们所关心的,其治疗方法包括针对细菌(抗生素)、针对毒素(抗体、结合剂)以及微生物群(保护或恢复)的方法,在暴发性病例或非手术治疗失败时,还可选择结肠切除术或其他微创手术。通过疫苗和益生菌预防艰难梭菌感染的研究逐渐显示出一定的临床效果。
希望通过本文的内容,能够帮助人们更加全面和清晰地了解艰难梭菌的相关知识,同时提高对其危害的认识,从而采取更加科学和有针对性的措施来预防和应对艰难梭菌感染。
艰难梭菌是一种革兰氏阳性、形成孢子的厌氧芽孢杆菌,近年来,由于抗生素的滥用导致肠道菌群失调,艰难梭菌感染(CDI)的发病率在中国和全球范围内不断上升,显示出这一公共卫生问题的严重性。
2022年,中国艰难梭菌感染治疗市场规模达34.14亿元,全球艰难梭菌感染治疗市场规模达到78.74亿元,预计全球艰难梭菌感染治疗市场规模将在2028年达到147.95亿元。
艰难梭菌的感染率不断上升,很多人可能想知道自己体内是否存在这种细菌,以及是否艰难梭菌存在于人体就会致病及造成危害?随着谷禾的视角一起往下看。
1
毒力因子影响艰难梭菌的致病性
首先要强调的一点是,艰难梭菌感染的临床表现受到多种毒力因子的影响,这些毒力因子可能比艰难梭菌的存在更为重要。艰难梭菌分为产毒型和非产毒型,通常只有产毒型会引发临床症状。
产毒艰难梭菌主要产生毒素A(肠毒素)和毒素B(细胞毒素),少部分仅产生毒素B。高毒力菌株(如027型)除了产生这两种毒素外,还产生二元毒素。
据国外综合医院统计,A(+)B(+)占艰难梭菌的57%,A(-)B(+)占34%,A(-)B(-)占9%。毒素A阳性,毒素B阴性的菌株尚未被发现,毒素B可以单独导致艰难梭菌致病。
◮ 艰难梭菌的毒力因子
毒素A:主要作用于肠道,导致肠道上皮细胞的损伤和炎症反应。它通过结合肠道细胞表面的受体,诱导细胞内信号转导,导致细胞凋亡和肠道通透性增加,从而引发腹泻。
毒素B:具有更强的细胞毒性,能够直接破坏细胞骨架,导致细胞死亡,破坏紧密连接并丧失肠道屏障功能。它在致病过程中,尤其是在高毒力菌株中,起着关键作用。
二元毒素:一种ADP-核糖基转移酶,导致肌动蛋白细胞骨架解聚(导致屏障功能丧失和紧密连接破坏)和微管突起(导致艰难梭菌粘附增加)。
致病性基因和毒素作用方式
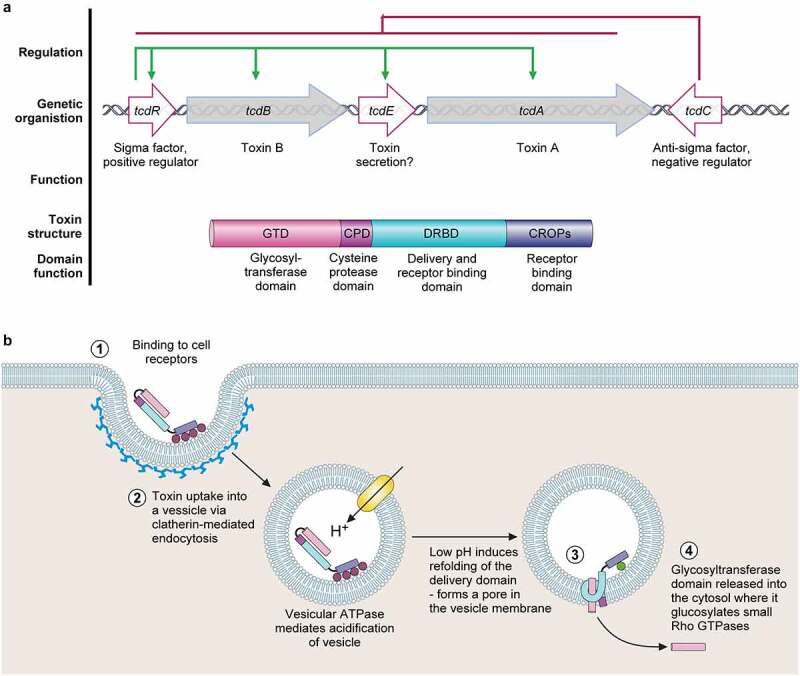
Buddle JE,et al.Virulence.2023
◮ 毒素诱导引发的免疫反应导致各种症状
这些毒素在致病性位点(PaLoc)内编码,能够与肠上皮细胞的受体结合并被内化。在细胞内,它们使小的Rho蛋白葡萄糖化,导致紧密连接破裂、上皮完整性降低,并增加细菌对宿主上皮的粘附。
毒素诱导的肠道屏障损伤会引发免疫反应,其特征是分泌促炎细胞因子和趋化因子,导致中性粒细胞、肥大细胞、单核细胞和先天性淋巴细胞的募集和激活;以及花生四烯酸代谢物的分泌、P物质和活性氧中间体的生产。这些细胞因子和免疫细胞的作用会引发艰难梭菌感染的临床症状。例如,肥大细胞脱颗粒刺激组胺释放,增加肠道屏障的通透性,导致大量液体流失到管腔中,从而引发严重的腹泻、痉挛、脱水和伪膜性肠炎等症状。
艰难梭菌的各种毒力因子

Buddle JE,et al.Virulence.2023
2
产毒艰难梭菌及我国的流行情况
目前已鉴定出几十种艰难梭菌菌株,其相对比例在过去几年中迅速变化,且毒力和感染能力可能存在差异。我们这里简单介绍几种高毒性艰难梭菌菌株以及我国的主要流行情况。
◮ 毒力较高的艰难梭菌
⑴027菌株
027菌株是近年来备受关注的高毒力菌株,部分027菌株在体外能够产生更多毒素,并且更容易与人类肠道上皮细胞结合,通常与严重腹泻和高死亡率相关。该菌株在北美和欧洲的医院中广泛传播,成为医院获得性腹泻的主要原因。
⑵017菌株
这种菌株在1990年代首次被识别,主要在亚洲地区流行。017菌株通常被认为是毒素A阴性、毒素B阳性的菌株。由于毒素A检测通常用于识别粪便样本中的艰难梭菌,因此可能会遗漏这种菌株。
⑶078菌株
078介导的艰难梭菌感染患者更常见于靠近农场的地区,078菌株是食用动物中最常见的类型,在牛和猪中都有发现,人可能通过食用动物导致感染。078菌株的毒力特征与027菌株相似,所有027和078菌株似乎都具有完整的肌动蛋白特异性ADP核糖基化毒素。
⑷其他菌株
除了027、017和078菌株,还有其他核糖型的艰难梭菌菌株,如001、106和053等。然而每种核糖型的相对比例在过去几年中迅速变化。核糖型001的比例从25.1%下降到7.8%,核糖型106的比例从26.2%下降到20.2%,且106几乎只在英国发现。
◮ 我国的艰难梭菌流行情况

一项荟萃分析统计了我国大陆部分省份的艰难梭菌感染发病率及主要流行和耐药的艰难梭菌。
艰难梭菌在健康成年人结肠的定植率约为4%-7%,而国内腹泻患者的检出率为15%-40%(共分析了15,313个样本)。在中国大陆,ST-37(017)和ST-3是最普遍的菌株;幸运的是,ST-1(027)和ST-11(078)等高毒力菌株迄今很少出现。
并且不同省份的阳性率存在差异显著:
湖北:23%
河北:19%
安徽:19%
四川:17%
宁夏:4%
河南:3%
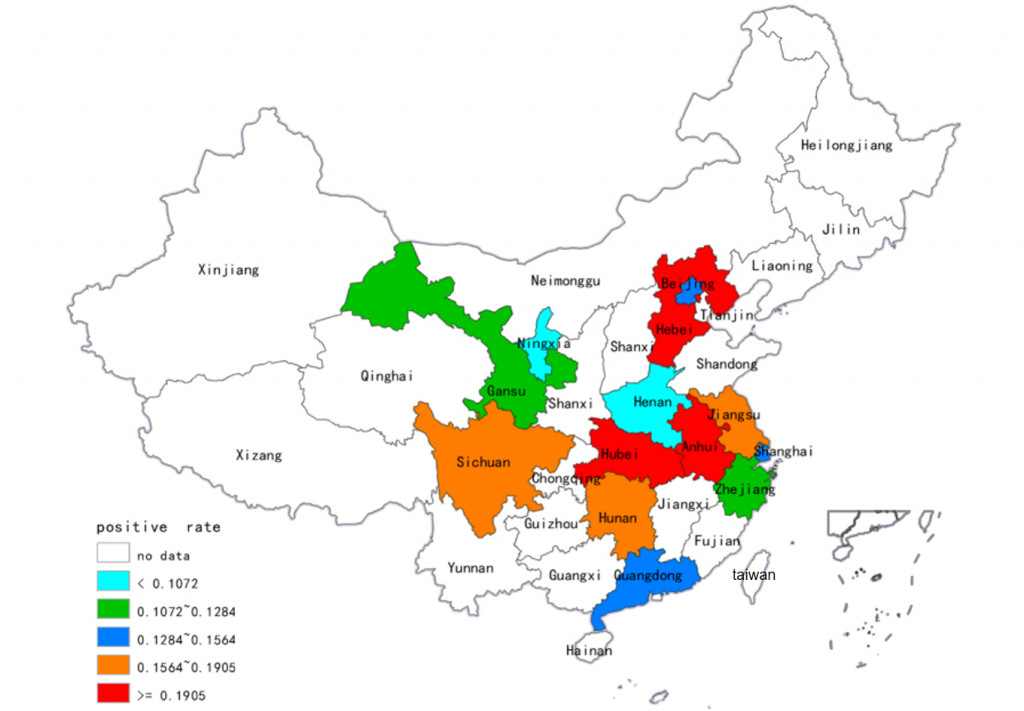
doi: 10.1038/srep37865.
中国临床艰难梭菌的分子特征
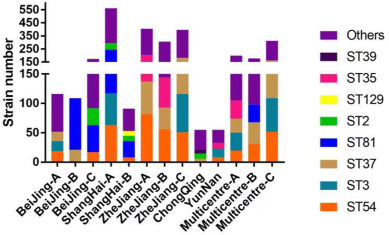
Wu Y,et al.Anaerobe.2022
中国大陆的流行艰难梭菌株并非高毒力类型,这可能是近年来没有艰难梭菌感染爆发的原因。此外,关于毒素A阴性和毒素B阳性菌株的报道逐渐增加,许多研究也发现了这一现象。在亚洲,毒素A阴性和毒素B阳性菌株的数量明显高于欧美国家。
◮ 我国的艰难梭菌耐药情况
我国的艰难梭菌对环丙沙星、克林霉素和红霉素的耐药率高于其他地区;然而,报道的艰难梭菌分离株均未对甲硝唑、万古霉素、替加环素或哌拉西林/他唑巴坦耐药。
3
非产毒艰难梭菌
◮ 菌株特性不同,不会致病
非产毒性艰难梭菌(NTCD)是指那些不产生致病毒素的艰难梭菌菌株。这些菌株能够在肠道中定殖,并且通常从无症状个体中分离出来。
非产毒性艰难梭菌菌株表现出与产毒性菌株不同的表型特征,如更高的甲硝唑耐药性和更高的孢子形成效率。
◮ 非产毒菌株定植可能具有保护作用
非产毒性艰难梭菌能够在肠道中定殖而不引起症状,并有研究发现其可能有助于降低由产毒性艰难梭菌引起的感染风险。研究表明,NTCD的定殖可以通过竞争性抑制机制,防止产毒性菌株的定殖和毒素产生。
临床应用与研究:在临床试验中,NTCD-M3等菌株已被用于预防艰难梭菌感染,通过诱导肠道和系统性免疫反应,从而减少产毒性艰难梭菌的附着和感染。
了解艰难梭菌感染的发病机制对于制定有效的疾病治疗和预防措施至关重要。让我们一起来看下人体是如何感染艰难梭菌以及感染后会出现的症状。
◮ 艰难梭菌主要通过孢子传播感染
艰难梭菌(C.difficile)作为一种专性厌氧菌,通常无法在大气中存活,那么它是如何传播到人体的呢?这是通过形成孢子来实现的,这些孢子即使在恶劣的环境条件下也能存活。除了提供对氧的抵抗力外,孢子还对紫外线、干燥、热、许多消毒剂和抗生素具有抵抗力。
注:艰难梭菌孢子已在各种环境来源中检测到,包括家畜、水源和土壤。
艰难梭菌感染的发病机制
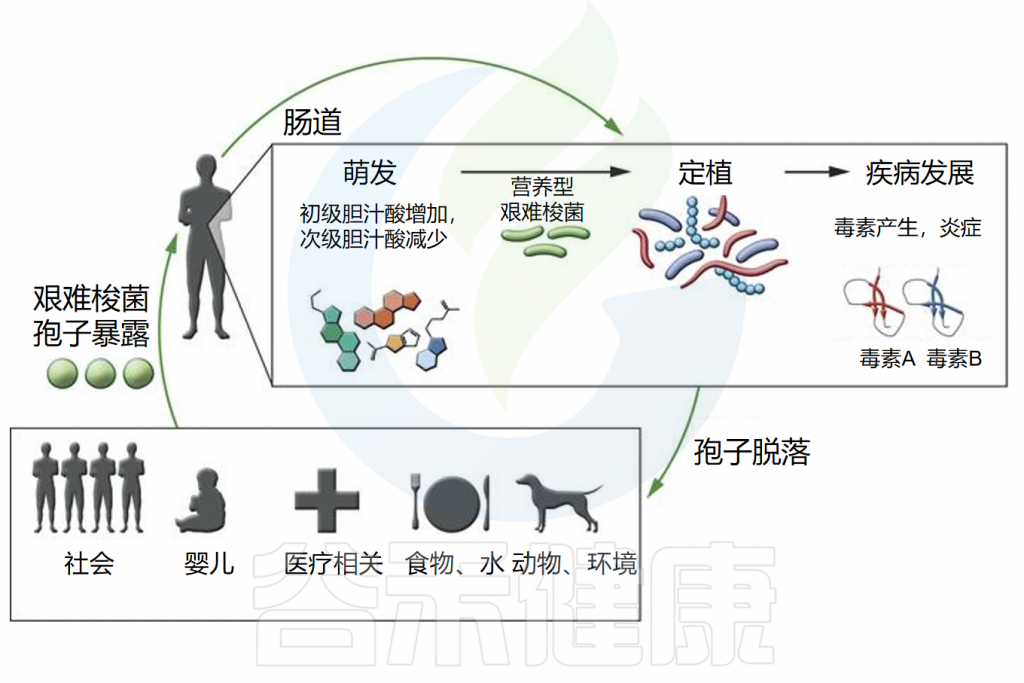
doi.org/10.1172/JCI72336.
1
感染过程
◮ 孢子生长必须依赖特定的胆汁酸
通过粪口途径摄入艰难梭菌孢子后,孢子需要发芽并生长为定植于胃肠道的营养细胞。然而,摄入孢子并不总是会导致定植,因为胃肠道环境必须适宜这一过程的发生。
体外研究表明,发芽和生长成营养形式取决于特定初级胆汁酸(如牛磺胆酸)的存在。相反,其他胆汁酸,如鹅去氧胆酸,可能会抑制艰难梭菌孢子的发芽。
胃肠道内的微生物在胆汁酸代谢中起关键作用,微生物群落的调节会影响代谢物的可用性。来自抗生素处理小鼠的盲肠提取物含有高水平的胆盐并促进孢子萌发,而来自未处理小鼠的盲肠提取物则没有。我们推测:抗生素的使用改变了肠道微生物群的代谢,导致胆汁酸种类更易促进艰难梭菌孢子的生长。
◮ 定植后毒素介导炎症和疾病
一旦定植,艰难梭菌会引发毒素介导的炎症和疾病。它产生两种主要毒素,即艰难梭菌毒素A和B(TcdA和TcdB),这些毒素在营养生长的静止期产生,主要导致粘膜上皮损伤和炎症反应。
另一种毒素,艰难梭菌二元毒素(CDT),会破坏肌动蛋白细胞骨架,研究表明其存在可能增加菌株的毒力。
由于孢子暴露和艰难梭菌定植不一定导致临床疾病,胃肠道微生物群和宿主在艰难梭菌的疾病发展中可能发挥重要作用。
2
艰难梭菌感染后的临床症状
产毒艰难梭菌菌株感染的临床表现通常从无症状携带到轻度或中度腹泻,或是暴发性,有时是致命的。症状在定植后不久开始,中位发病时间为2至3天。
◮ 常见的症状
腹泻:这是艰难梭菌感染最常见的症状,通常表现为水样腹泻,频率可达每天多次。腹泻可能伴有粘液或脓性分泌物。
腹痛和腹部不适:患者常感到腹部绞痛或不适,疼痛可能是间歇性的,且通常与腹泻发作相关。
发热:部分患者可能出现低热,体温通常在37.5°C至38.5°C之间。
恶心和食欲减退:患者可能会感到恶心,伴随食欲减退,进而导致体重下降。
脱水:由于频繁腹泻,患者可能出现脱水症状,如口干、尿量减少、皮肤弹性下降等。
腹胀:部分患者可能会感到腹部胀气或腹部膨胀。
◮ 严重并发症
在一些情况下,艰难梭菌感染可能导致更严重的并发症,包括:
伪膜性结肠炎:表现为严重的腹痛、腹泻和发热,肠道内形成伪膜。
肠穿孔:极少数情况下,感染可能导致肠道穿孔,表现为剧烈腹痛和急性腹膜炎。
中毒性巨结肠:具有全身中毒症状及全结肠或节段性结肠扩张的临床表现。是一种危及生命的并发症,表现为腹痛、腹胀、腹泻和全身症状加重,可能需要手术干预。
◮ 肠外表现
艰难梭菌感染不仅会导致肠道相关的症状,还可能引发一些肠道之外的表现,包括脱水、电解质紊乱、低白蛋白血症、低血压、肾功能衰竭、全身炎症反应综合征、关节炎、菌血症、败血症甚至死亡。
感染的核心是肠道菌群平衡被破坏
艰难梭菌感染发病机制的核心是微生物群的破坏。健康的肠道微生物群对于防止病原体定植(称为定植抗性)至关重要 。
未被破坏的微生物群能够抵抗病原体的定植,健康平衡的微生物和宿主因子均可抑制艰难梭菌的发芽和生长。同时微生物群和宿主免疫系统之间的串扰导致调节免疫反应。此外,微生物群可以刺激抗菌肽和分泌型IgA的产生,从而维持微生物群的组成。并且已经提出了多种机制来解释为什么微生物群被破坏会导致定植抗性丧失,包括营养竞争、生态竞争和生态位排斥。
而由于抗生素使用、药物、年龄变化、饮食或炎症等因素导致微生物群的破坏,可导致艰难梭菌感染的发展。由于结构或代谢环境的变化,菌群失调会导致定植抗性丧失。特定群落成员的损失可能会影响微生物和宿主产生的代谢物的水平,从而促进孢子萌发和艰难梭菌生长。菌群失调也可能通过免疫调节的丧失和促炎状态导致免疫反应失衡,这两者都会影响疾病的发展。营养型艰难梭菌产生的毒素可刺激炎性细胞因子、中性粒细胞和抗毒素抗体的生成。
微生物群对CDI期间病原体抗性和宿主的机制
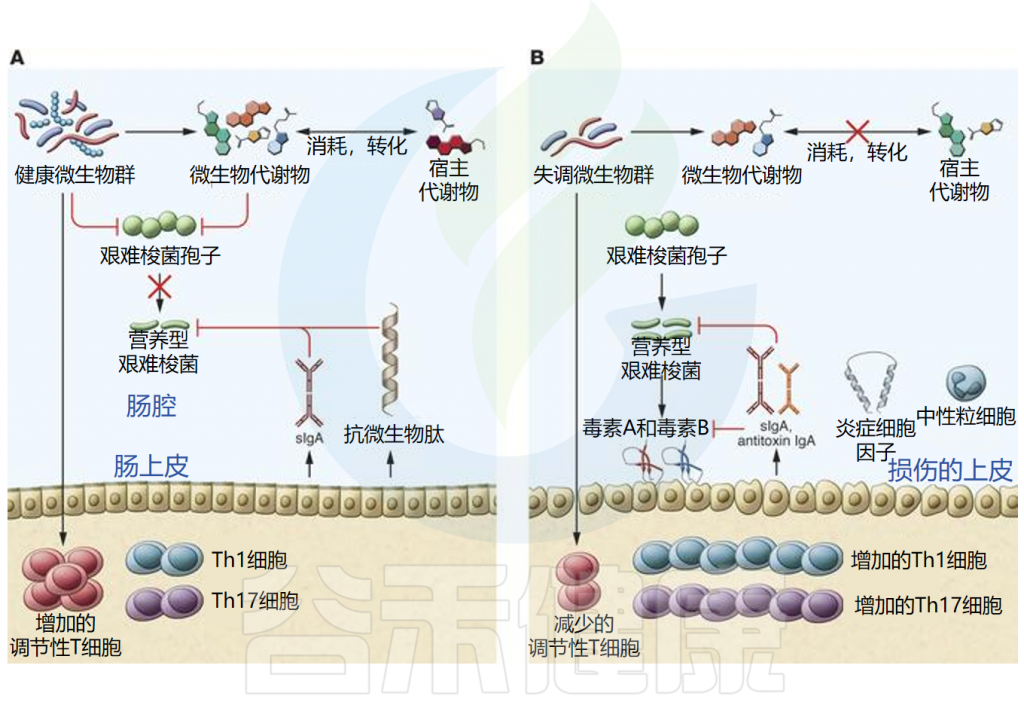
doi.org/10.1172/JCI72336.
据研究文献报道,以下这些因素会增加获得CDI的风险。
1
使用抗生素
◮ 使用过抗生素的人患病率更高
使用抗生素是艰难梭菌感染中最常见的诱发因素。一项大型回顾性研究分析了10154例艰难梭菌感染患者的数据,发现78%的患者在感染前3个月内使用过抗生素。
大多数抗生素都与艰难梭菌感染(CDI)发展相关,但最常见的药物包括青霉素、头孢菌素和氟喹诺酮类药物。在一项关于社区获得性CDI中抗生素使用情况的荟萃分析中,克林霉素发生社区获得性CDI的风险最高,然后依次是氟喹诺酮类药物、头孢菌素类、青霉素类、大环内酯类和磺胺类/甲氧苄啶类。
◮ 使用抗生素导致肠道微生物平衡被破坏增加艰难梭菌感染的风险
抗生素的使用,尤其是广谱抗生素,会显著改变肠道微生物群的组成和多样性,导致微生物群失调。这种失调主要表现为有益菌群(如双歧杆菌、乳酸菌等)数量减少,抑制艰难梭菌的生长和毒素产生的能力减弱,导致更易感染艰难梭菌。
艰难梭菌感染的发病机制
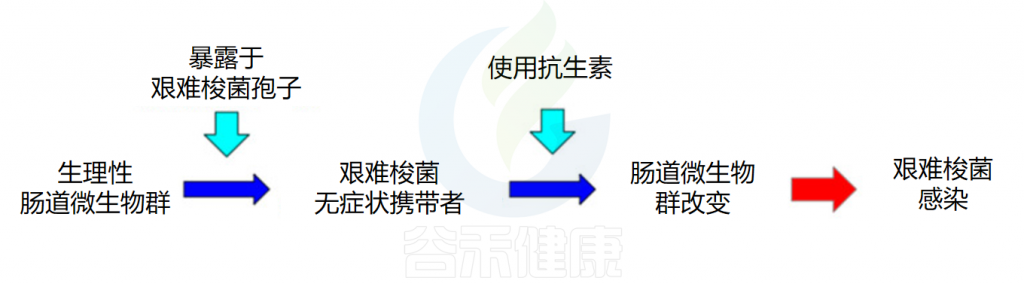
Piccioni A,et al.Int J Mol Sci.2022
2
高龄
◮ 高龄人群CDI的患病率和死亡率更高
正如多项研究所记录的那样,高龄是CDI的重要风险因素。65岁及以上的老人患病人数显著增加,人口发病率比其他年龄组高5倍以上。
并且还发现CDI的死亡率随着年龄的增长而显著升高。在2011年对美国CDI负担的最新研究中,发现65岁及以上的人大约占CDI病例总数的57%,但该年龄组的CDI死亡占CDI死亡总数的83%。
◮ 年龄增长免疫退化、微生物多样性下降
年龄增长会影响肠道微生物组结构。人类肠道微生物组在一生中经历显著变化,老年人群的微生物组多样性较低且不断变化。研究发现,老年人保护性物种(如双歧杆菌和部分厚壁菌门成员)减少,有害物种(如变形菌门)增加。这些变化与免疫系统退化(即免疫衰老)有关。
尽管年龄是CDI的独立危险因素,但其与抗生素使用增加、更频繁的医院就诊及疾病发展密切相关,这些因素共同提高了艰难梭菌的易感性。
新生儿与成人艰难梭菌感染的比较
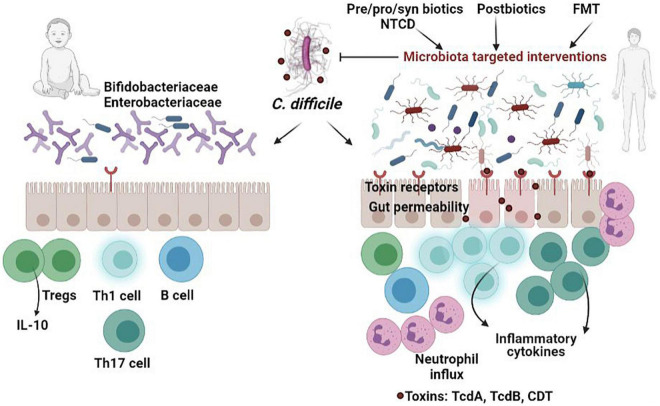
Vasilescu IM,et al.Front Microbiol.2022
3
其他胃肠道疾病
患有其他胃肠道疾病的患者也可能更容易感染艰难梭菌。炎症性肠病(IBD)已被证实是CDI的危险因素,并与更严重的疾病结果相关。IBD患者肠道菌群呈现多样性降低,同时存在以变形菌门为主的多种潜在致病菌。然而,这些微生物群落如何影响艰难梭菌易感性的具体机制较为复杂。
◮ 肠道炎症性疾病会促进艰难梭菌感染
宿主免疫反应能调节微生物群,而IBD加重CDI病情表明炎症可促进CDI发展。抗菌肽脂质运载蛋白-2和钙卫蛋白等炎症产物限制肠道环境中营养物质可用性,可能为艰难梭菌创造有利条件。肠道菌群类型影响粘膜IgA库,复发性CDI患者结肠活检中IgA产生细胞减少。
还观察到各种微生物会影响T细胞的亚群,例如梭菌属诱导Treg物种和分段丝状细菌诱导Th17细胞分化。这些微生物种群的调节,例如抗生素后,可能会影响艰难梭菌的定植。
4
其他风险因素
除此之外,还有一些因素也会增加艰难梭菌感染的风险。如:
医疗机构暴露:住院患者,特别是长期住院者,长期护理机构居住者容易艰难梭菌感染;
胃酸抑制剂使用:质子泵抑制剂(PPIs)和H2受体拮抗剂,降低胃酸可能导致艰难梭菌孢子存活率增加,长期使用与CDI风险增加相关。
手术和医疗操作:胃肠道手术、鼻胃管和胃肠营养管的使用、结肠镜检查会导致艰难梭菌感染风险升高;
营养状态不佳:低蛋白血症、营养不良的人群易感染艰难梭菌;
肥胖、癌症化疗也可能会增加艰难梭菌感染的风险。
肠道微生物群被破坏是艰难梭菌感染发病的关键机制。健康的肠道菌群对防止艰难梭菌定植和感染至关重要。那么,微生物群究竟如何在这一过程中发挥作用?那我们一起来看看。
艰难梭菌感染中的微生物群改变
正常的肠道菌群通过对艰难梭菌的定植抗性在预防 艰难梭菌感染中起着核心作用。这导致了一个问题,即是否存在一种微生物群紊乱模式,这种模式易导致艰难梭菌定植和感染。
◮ 菌群多样性降低,厚壁菌门增加
多项研究一致显示,与健康人群相比,艰难梭菌感染(CDI)患者的菌群复杂性和丰富度明显降低。这种多样性降低被认为是CDI发病和复发的关键因素。
厚壁菌门(Firmicutes)减少:CDI患者中厚壁菌门的丰度和多样性显著降低,尤其是瘤胃球菌科(Ruminococcaceae)和毛螺菌科(Lachnospiraceae)等保护性菌群。
拟杆菌门(Bacteroidetes)改变:CDI患者通常表现为拟杆菌门多样性降低,但有研究显示有症状患者中某些拟杆菌属(Bacteroides)可能增加。
变形菌门(Proteobacteria)增加:CDI患者体内变形菌门(特别是肠杆菌科)的比例明显增高。
◮ 产丁酸细菌减少,机会性病原体增加
接受多轮抗生素治疗的复发性CDI患者肠道微生物群组成遭受严重破坏。对比CDI患者、艰难梭菌阴性院内腹泻患者和健康对照受试者的远端肠道微生物群发现,艰难梭菌感染可能导致功能性菌群发生以下变化:
产丁酸盐细菌减少:包括罗氏菌属(Roseburia)、普拉梭菌(Faecalibacterium Prausnitzii)、假丁酸弧菌属等。
产乳酸细菌增加:特别是肠球菌属(Enterococcus)。
机会性病原体增加:研究发现,与健康者相比,白色念珠菌和光滑念珠菌在艰难梭菌阳性样本中更常见。
在艰难梭菌感染患者的肠道微生物群中,肠球菌、乳酸菌、大肠杆菌、肠杆菌、副拟杆菌、嗜粘蛋白阿克曼菌的相对丰度增加,以及粪杆菌、Roseburia、Blautia、Prevotella、链球菌的水平降低。
艰难梭菌感染相关的肠道微生物群失调

Vasilescu IM,et al.Front Microbiol.2022
生化和免疫紊乱影响感染
肠道菌群失调还引发多种生化和免疫紊乱:如短链脂肪酸(SCFA)水平降低、初级胆汁酸增多、碳水化合物可利用性提高、免疫功能受抑及竞争微生物缺乏。这些变化共同促进艰难梭菌的定植、孢子萌发和生长繁殖。
◮ 丁酸盐有助于减轻艰难梭菌毒素的损害
短链脂肪酸可以通过降低管腔pH值(对艰难梭菌不利)并通过产生粘蛋白和抗菌肽来刺激防御屏障。丁酸盐还可以通过稳定缺氧诱导因子-1(HIF-1)和增加紧密连接来保护肠道上皮免受艰难梭菌毒素的损害,抑制肠道炎症和细菌易位。
在小鼠的饮用水中添加丁酸盐,施用丁酸盐的前药、三丁酸甘油酯或富含菊粉的饮食(菊粉可以被肠道共生细菌发酵,产生短链脂肪酸,主要是乙酸盐、丙酸盐和丁酸盐)可使小鼠免受CDI的侵害。
◮ 胆汁酸会影响艰难梭菌的定植和生长
艰难梭菌孢子萌发由蛋白酶CspC和CspA感知胆汁盐和氨基酸复合物而调控。某些胆酸盐衍生物和甘氨酸可促进孢子萌发,而脱氧胆酸盐抑制艰难梭菌生长,鹅去氧胆酸盐则阻断牛磺胆酸盐介导的萌发过程。
共生肠道梭菌通过调节胆汁酸代谢产物,创造不利于艰难梭菌萌发和定植的环境。例如,Clostridium scindens能催化胆汁酸7α-脱羟基化,产生次级胆汁酸,增强对艰难梭菌感染的抵抗力。失去这类能将初级胆汁酸转化为具抗菌活性次级胆汁酸的微生物,将显著增加CDI风险。
◮ 艰难梭菌会刺激其他细菌产生吲哚造成不利肠道环境
最近的研究发现,CDI患者肠道腔中的吲哚水平增加(色氨酸代谢物参与微生物生长、毒力诱导、抗酸性、生物膜形成),艰难梭菌本身不能产生这种代谢物,但会刺激其他细菌产生吲哚,以阻止和抑制吲哚敏感菌株的生长和发展,包括保护性肠道微生物群代表, 从而确保有利于艰难梭菌生存的肠道环境。
微生物群介导艰难梭菌的定植和感染
一些人群中虽然有艰难梭菌定植,但并不会出现致病症状,这可能与肠道微生物群的保护作用相关。
◮ 婴儿艰难梭菌的定植率较高,但很少出现症状
由于婴儿肠道的不成熟和肠道微生物群的不稳定,其特别容易受到艰难梭菌定植的影响,但并不会出现症状和发展为疾病。
在<1个月大的婴儿中,艰难梭菌的平均定植率为 37%,范围在0到61%之间。在1到6个月大之间,定植率仍然很高,为30%,出生后第一年结束时下降到约10%。不同研究报告的12个月以下儿童的定植率从14%到71%不等,这个年龄组最常被艰难梭菌定植,并且他们没有症状。
无症状携带率在3岁左右下降至0-3%,接近成人水平。同时,出生至24个月间血清针对毒素A和B的IgG抗体浓度逐渐升高。3岁左右,儿童肠道微生物群趋于稳定并具备成人特征,这可能导致症状性CDI从该年龄开始增加。
注:新生儿微生物群以革兰氏阳性球菌、肠杆菌科或双歧杆菌科为主,逐渐过渡到以双歧杆菌科为主。双歧杆菌可通过上调肠道树突状细胞产生IL-10,解释了艰难梭菌定植婴儿无症状的原因。在剖宫产新生儿中,T细胞和CD4+辅助性T细胞水平降低,可能因未成熟的免疫系统无法激活炎症反应所致。
研究发现,配方奶喂养婴儿的艰难梭菌定植率高于母乳喂养婴儿,且母乳喂养婴儿的菌落计数明显更低,这可能与母乳中含有毒素A和B的抗体有关。
总之,新生儿艰难梭菌定植的高携带率可以用新生儿肠道的不成熟和肠道微生物群的存在来解释。然而,出生后的母乳喂养带有毒素抗体,加上艰难梭菌毒素受体的缺乏,可以帮助婴儿免受艰难梭菌毒素的有害影响。
◮ 肠道微生物多样性降低的人群和老年人更易受艰难梭菌影响
几项研究还比较了老年人群的肠道微生物样本,这些人群更容易受到艰难梭菌影响。
老年艰难梭菌感染患者的肠杆菌科、肠球菌属和乳酸杆菌的数量较高,而健康的老年人携带更多样化的拟杆菌属菌株。并且与任一老年人群相比,健康成年人也更有可能拥有更多的双歧杆菌和拟杆菌。最近使用16S rRNA 基因高通量测序的研究更深入地研究了艰难梭菌阳性人群的群落结构。观察到,与健康患者相比,活动性CDI患者的肠道微生物群多样性较低。
类似研究发现,与健康成人相比,CDI腹泻患者的肠道微生物群多样性显著降低,尤其是厚壁菌门的多样性较低。健康人群中以Lachnospiraceae、Ruminococcaceae和Bacteroidaceae为主导,而CDI和非CDI腹泻患者的微生物群落高度相似,表明腹泻或炎症可能与特定微生物群落相关。
在小鼠模型中进行了类似观察,与人类相似,抗生素降低了小鼠肠道微生物群多样性,使其更易患肠道疾病,包括CDI。研究发现,头孢哌酮、克林霉素或多种抗生素处理后,易感小鼠感染前以乳酸菌科和肠杆菌科为主,而对CDI具有保持抗性的动物以Lachnospiraceae为主。后续研究表明,被Lachnospiraceae定植的小鼠比被大肠杆菌定植的小鼠艰难梭菌定植减少且病情较轻。小鼠模型为识别CDI保护性成分提供了可测试的方法。
◮ 复发性CDI:微生物群恢复不完全
艰难梭菌感染(CDI)最常见的并发症是恢复不完全和反复感染。初次感染后复发率约为20-30%,3次感染后高达60%。研究发现,复发患者的微生物群多样性低于单次CDI患者,这表明可能可以根据感染期间存在的微生物群落预测复发。尽管一些研究在分析中包含了复发样本,但尚未确定复发性CDI患者特有的微生物特征。
另外有研究发现,复发性CDI患者体内初级胆汁酸浓度较高。粪菌移植后,次级胆汁酸浓度增加,接近健康供体水平,而这些酸在FMT前样本中未检测到。该结果与体外和小鼠研究一致,表明次级胆汁酸(如石胆酸和脱氧胆酸)可抑制艰难梭菌生长。尽管细菌群落决定代谢环境,但不同细菌群落可能通过相似功能实现相同代谢结果,仅靠群落结构可能不足以预测复发风险。
如何定义艰难梭菌感染病例?
只有产生毒素的产毒艰难梭菌菌株才具有致病性。根据欧洲临床微生物学和传染病学会(ESCMID)指南,CDI定义为:(i)符合CDI的临床表现,且粪便中检测到毒素A或毒素B的艰难梭菌,且无其他腹泻原因;或(ii)伪膜性结肠炎(PMC)患者。
美国医疗保健流行病学学会和美国传染病学会的定义类似:CDI病例需具备症状(通常为腹泻),且粪便检测产毒艰难梭菌或其毒素阳性,或结肠镜或组织病理学显示PMC。
那我们该如何检测艰难梭菌感染(CDI)?艰难梭菌感染检测通常包括以下方法:
1
临床评估
•症状:难梭菌感染病的主要症状包括腹泻(每天3次或以上稀便,持续2天以上)、腹痛、发热、恶心和脱水等。严重病例可能出现伪膜性结肠炎(PMC)、中毒性巨结肠或感染性休克。
•病史:重点关注患者的抗生素使用史(尤其是第三代头孢菌素、氟喹诺酮类等)、住院史、免疫抑制状态以及质子泵抑制剂(PPI)的使用。
2
实验室检测方法
◮ 细菌培养
用环丝氨酸头孢西丁果糖琼脂培养基(CCFA)等进行厌氧培养,需时72小时,灵敏度高且可获得菌株,但不能检测毒素不能区分非产毒株。
但分离菌株后,可以通过直接从菌落悬浮液或细菌生长的肉汤上清液中检测其体外毒素的产生来确定其致病潜力。
◮ 高通量测序
高通量测序可检测艰难梭菌菌株或毒力基因,16S测序仅能分辨到物种层面,可通过谷禾16S健康报告的解读,并结合自身有没有腹泻症状。然后进一步去判别是否存在产毒菌株。
与此同时,宏基因组测序(包括一些靶向的测序)则可识别毒力基因。
◮ 谷氨酸脱氢酶测定
谷氨酸脱氢酶(GDH)是所有艰难梭菌菌株表达的代谢酶,可通过ELISA或免疫层析法检测。阳性结果仅表明存在艰难梭菌,无法判断其是否产毒。由于其高阴性预测值(NPV,80.0%-100%),GDH阴性结果通常可排除感染,常用于初筛。
◮ 毒素检测
细胞毒性测定被认为是检测艰难梭菌的游离毒素(主要是毒素 B)的参考方法。
酶联免疫吸附试验(EIA):检测艰难梭菌毒素A或毒素B,快速但敏感性较低。
细胞毒素中和试验:检测毒素活性,敏感性和特异性较高,但耗时较长。
◮ 核酸扩增检测(NAATs)
实时PCR或环介导等温扩增法(LAMP) :检测艰难梭菌毒素基因,耗时短,敏感性高,但可能检测到无症状定植者,且成本高。
3
综合算法
根据欧洲临床微生物学和传染病学会(ESCMID)指南,推荐使用两步或三步算法:
初筛:谷氨酸脱氢酶(GDH)抗原检测或核酸扩增试验(NAAT)。
确认:毒素检测(EIA或细胞毒素试验)。
4
其他辅助检查
血常规:轻、中度感染者外周血白细胞可正常,严重感染者白细胞升高。
降钙素原(PCT):对诊断CDI意义不大,但PCT>0.2 ng/ml时,提示CDI有重症化趋势。
腹部CT:对重症CDI患者有辅助诊断意义,即结肠壁增厚、结节状结肠袋增厚、水肿厚度>4 cm,特别是炎症部位在升结肠。
内镜检查:内镜检查可作为辅助诊断,典型征象包括黏膜充血、水肿、糜烂、溃疡、直肠乙状结肠有多发性隆起的斑片或融合为大片的灰绿色、黄褐色伪膜覆盖黏膜表面。部分患者表现可不典型,尤其炎症性肠病合并艰难梭菌感染时多无特征性病变。伪膜性改变可能表明感染了产毒艰难梭菌。
艰难梭菌感染(CDI)的治疗包括针对细菌(抗生素)、针对毒素(抗体、结合剂)、宿主反应(调节炎症)或微生物群(保护或恢复)的方法,以及在暴发性病例或非手术方法失败的情况下,结肠切除术或其他侵入性较小的手术。选择取决于疾病严重程度、病史和宿主因素。
1
针对细菌——抗生素
停用有问题的抗生素以恢复正常肠道菌群是治疗CDI的理想方法。但在感染负担高或需持续抗生素治疗其他感染时,通常需要使用针对艰难梭菌的抗菌药物。
然而,几乎所有抗生素,包括针对艰难梭菌的药物,都可能进一步破坏肠道微生物群,延迟耐药性菌群的恢复,并增加再次感染的风险。目前用于治疗CDI的主要抗菌药物包括:
•万古霉素:万古霉素是美国食品药品监督管理局(FDA)批准的第一种CDI药物。最近的临床试验数据表明,万古霉素在治疗重症时优于甲硝唑。
•甲硝唑:与万古霉素的疗效相当,成本优势以及对万古霉素耐药肠球菌传播的担忧,甲硝唑成为CDI的推荐药物。但随着艰难梭菌流行菌株 BI/NAP1/027/III 的出现,甲硝唑治疗失败的报道越来越多。
•非达霉素:非达霉素也是获得FDA批准的其他治疗CDI药物。
•新型小分子抗菌剂:乳酸菌素3147是一种由乳酸乳球菌产生的双组分抗生素,它靶向细胞壁前体脂质II,抑制肽聚糖的生物合成,并在细胞膜上形成孔,实现细胞死亡。粪便发酵模型证明了乳酸素 3147 对一系列艰难梭菌分离株的强效细胞杀伤活性,在 30 分钟内完全消除艰难梭菌。
与传统药物相比,这种窄谱抗菌药物可能具有多种优势,包括减少对微生物组的影响、降低复发率、优于常规治疗以及改善药代动力学特征。然而,在保持非孢子形成厌氧菌和总革兰氏阴性厌氧菌完好无损的同时,这种抗菌剂对乳酸杆菌和双歧杆菌产生了负面影响。
2
针对毒素——阻断、中和毒素
CDI的发病机制以毒素介导为主,因此中和或阻断毒素是合理策略。但尽管抗毒素在动物模型中可改善疾病,但在人类中仅表现为减少复发性CDI。
•单克隆抗体:一项随机双盲安慰剂对照研究评估了针对艰难梭菌毒素A和B的两种中和单克隆抗体。在200名参与者中,治疗组的CDI复发率显著低于安慰剂组。然而,单克隆抗体未能缩短腹泻持续时间、降低严重程度或减少住院时间。住院、年龄较大、有严重潜在疾病或重症CDI的患者对治疗反应较差。
•Tolevamer:Tolevamer 是一种高分子量苯乙烯磺酸盐聚合物,可在体外中和艰难梭菌毒素。一项针对轻中度疾病的研究显示,6克剂量的Tolevamer与每日500毫克万古霉素疗效相当。
注:然而,Tolevamer的临床成功率低于甲硝唑和万古霉素。汇总分析显示,Tolevamer组的临床成功率为44.2%,显著低于甲硝唑组的72.7%和万古霉素组的81%。随着疾病严重程度增加,Tolevamer的疗效进一步下降。
•免疫球蛋白(IG):在人体研究中,针对毒素A和B的血清IgG抗体与保护相关,静脉注射IG治疗复发性或重症CDI的效果尚无系统研究支持,仅有少量病例报告和系列报道提供个案证据。剂量、给药次数和间隔存在较大差异。静脉注射IG对临床效果的差异可能与人群中抗毒素抗体水平的不可预测性有关。
3
微生物疗法
肠道微生物群的扰动是艰难梭菌感染(CDI)发生的关键因素。一些抗生素治疗无症状感染会导致艰难梭菌持续脱落和复发风险增加。通过特定微生物群恢复受损的肠道微生物群,已成为打破CDI-抗生素-CDI循环的策略。
• 粪菌移植的治疗效果优于仅用抗生素
粪菌移植(FMT)或微生物群替代疗法的原理是通过正常供体的粪便恢复CDI患者受损的肠道微生物群。系统评价显示,CDI患者接受FMT的腹泻消退率约为77%-90%。
一项随机对照试验比较了粪菌移植(FMT)与两种对照方案。FMT组在口服万古霉素(500mg,每天4次)4-5天后接受移植,对照组则接受14天相同剂量的万古霉素治疗。结果显示,FMT组3个月症状消退率为81%,显著高于万古霉素组(31%)和万古霉素加灌肠组(23%)。
尽管FMT已使用数十年,但其对严重复杂CDI的疗效、免疫功能低下患者的安全性及不明供体粪便长期安全性仍存疑。据报道,28.5%的患者出现FMT相关不良事件,最常见为腹部不适和排便异常,具体取决于给药途径。
• 口服微生物组疗法—SER-109
SER-109是一种由活性厚壁菌门细菌孢子组成的口服微生物组疗法,用于降低艰难梭菌感染复发风险。其机制可能通过与艰难梭菌竞争必需营养物质或调节胆汁酸谱来重建定植抵抗力,或两者兼具。
进行了一项3期、双盲、随机、安慰剂对照试验,其中艰难梭菌感染发作3次或以上(包括符合条件的急性发作)的患者在标准护理抗生素治疗后接受SER-109或安慰剂(每天4粒胶囊,持续3天)。
结果显示,在接受标准护理抗生素治疗后艰难梭菌感染症状消退的患者中,口服SER-109在降低复发感染风险方面优于安慰剂。
以微生物群为中心的治疗方法

Vasilescu IM,et al.Front Microbiol.2022
4
手术干预
艰难梭菌感染(CDI)的手术治疗通常用于严重或复杂病例,尤其是当药物治疗(如抗生素或粪便微生物群移植)无效,或患者出现危及生命的并发症时。以下是艰难梭菌感染的主要手术治疗方法:
• 全结肠切除术
适应症:严重的中毒性结肠炎、肠穿孔或肠坏死;严重的腹腔感染(腹膜炎),药物治疗无效且病情迅速恶化。
优点:快速去除感染源,降低死亡风险。
缺点:创伤较大,术后恢复时间长,可能影响生活质量。
• 分段结肠切除术
适应症:感染局限于结肠的某一部分。
优点:保留更多的肠道功能。
缺点:感染可能扩散,手术效果不如全结肠切除术稳定。
• 回肠造口术联合结肠灌洗
适应症:不适合全结肠切除的高危患者(如老年人或伴有多种合并症)。
优点:创伤较小,适合高危患者。
缺点:疗效可能不如全结肠切除术。
• 腹腔引流术
适应症:腹腔内脓肿或局部感染。
优点:辅助治疗,减轻感染负担。
缺点:仅适用于局部并发症,不能根治感染。
5
噬菌体疗法
噬菌体疗法利用天然噬菌体感染并裂解病原菌,是应对抗菌药物耐药性危机的潜在治疗方法。与抗生素不同,噬菌体具有进化能力,可持续克服细菌的抗性机制,从而避免疗法过时。
• 噬菌体可以降低艰难梭菌的生长和毒素水平
一些噬菌体在治疗艰难梭菌感染中表现出潜力。例如,ФCD27在CDI分批发酵模型中可显著降低艰难梭菌的生长和毒素水平。一种噬菌体组合已在体外完全裂解艰难梭菌,并在小鼠模型中减轻疾病症状和细菌定植。该组合进一步优化为4种噬菌体,成功在发酵容器中彻底根除艰难梭菌,显示出作为治疗选择的可行性。
总体而言,特异性以及对抗细菌耐药性的能力表明噬菌体治疗作为艰难梭菌治疗剂的巨大前景。
6
通过疫苗预防艰难梭菌感染
随着艰难梭菌感染(CDI)的发病率、死亡率和医疗成本不断上升,预防疾病的免疫接种成为理想选择。人类研究表明,对艰难梭菌毒素的强体液反应可减少复发和无症状定植。目前,多种候选疫苗正在开发中,包括基于类毒素、重组毒素肽、DNA和表面蛋白抗原的疫苗,但大多处于临床前阶段。
• 疫苗有助于减少复发和无症状定植
已发现部分纯化的类毒素A和B疫苗在30名健康成人中具有安全性和免疫原性,≥90%的受试者对两种毒素产生血清抗体反应。在一项试点研究中,3名多次复发CDI患者在第0、7、28和56天接受类毒素肌肉注射,其中2人对毒素A和B的IgG水平显著升高,且3人均在疫苗接种后停用万古霉素,随访6个月无复发。
两项2期试验已完成,测试疫苗在高危中老年人和首发CDI患者中的效果。一项3期试验正在17个国家中进行,计划评估疫苗在多达15,000名参与者中预防首发CDI的效果。其他候选疫苗包括基因和化学修饰的全长TcdA和B及重组融合蛋白IC84,其1期研究已完成,但结果尚未公布。
7
通过益生菌预防艰难梭菌感染
• 益生菌有助于预防艰难梭菌定植及相关腹泻
多项小型研究及荟萃分析表明,益生菌的使用可能与预防艰难梭菌相关腹泻有关。益生菌通常通过抑制艰难梭菌定植、调节肠道微生物群和胆汁酸代谢、破坏细胞壁和细胞膜、下调炎症反应、改善肠道屏障功能以及缓解病原性结肠炎来预防和治疗CDI。
最常研究的益生菌为嗜酸乳杆菌和双歧杆菌属。最近,一项多中心、随机、双盲、安慰剂对照研究测试了含嗜酸乳杆菌和双歧杆菌(双歧双歧杆菌和乳双歧杆菌)的高剂量益生菌制剂对≥65岁接受抗生素治疗患者的疗效。1,493名受试者接受益生菌,1,488名接受安慰剂。分析显示,益生菌组发生抗生素相关性腹泻和艰难梭菌感染的数量少于安慰剂组。
• 益生菌发挥抗菌活性抑制艰难梭菌定植
短双歧杆菌(YH68)通过抑制生长、孢子形成、毒力发生及毒力基因表达,展现出抗艰难梭菌活性,并增强抗艰难梭菌抗生素的体外效果或预防体内临床表现。
克劳氏芽孢杆菌和罗伊氏乳杆菌可分泌直接抑制艰难梭菌的可溶性化合物,而Clostridium scindens等产生次生胆汁酸的菌体可增强艰难梭菌的定植抗性。
此外,研究发现了一些可能有效的新型益生菌和制剂,如:
Bacteroides thetaiotaomicron,
E.thailandicus strain d5B,
B.amyloliquefaciens C-1,
B.longum JDM301,
Pediococcus pentosaceus LI05,
B.breve (YH68)
未来需要更大样本量的多中心双盲研究,以明确益生菌在CDI中的作用,同时考虑菌株和抗菌剂类型等因素。
艰难梭菌感染作为一种全球性公共卫生挑战,其发病率和医疗负担正不断攀升。通过本文的系统介绍,我们可以了解到,艰难梭菌感染的致病性主要取决于其产生的毒素,而非仅仅是菌株的存在。
健康的肠道微生物群在预防艰难梭菌感染中扮演着至关重要的角色,肠道微生物平衡的破坏是导致感染风险增加的关键因素。随着科学研究的深入,我们对艰难梭菌的检测、诊断、治疗和预防手段也在不断完善,从传统抗生素到粪菌移植、益生菌干预和疫苗开发等多元化策略均显示出积极成效。
了解艰难梭菌感染的本质和发病机制,对于临床医生制定合理治疗方案、减少不必要的抗生素使用以及患者接受适当预防措施至关重要。希望在未来研究的推动下,我们能够进一步降低艰难梭菌感染的发病率和复发率,减轻其对公共健康的威胁。
注:本账号内容仅供学习和交流,不构成任何形式的医疗建议。
主要参考文献
Buddle JE, Fagan RP. Pathogenicity and virulence of Clostridioides difficile. Virulence. 2023 Dec;14(1):2150452.
Piccioni A, Rosa F, Manca F, Pignataro G, Zanza C, Savioli G, Covino M, Ojetti V, Gasbarrini A, Franceschi F, Candelli M. Gut Microbiota and Clostridium difficile: What We Know and the New Frontiers. Int J Mol Sci. 2022 Nov 1;23(21):13323.
Wu Y, Wang YY, Bai LL, Zhang WZ, Li GW, Lu JX. A narrative review of Clostridioides difficile infection in China. Anaerobe. 2022 Apr;74:102540.
Arcay R, Barceló-Nicolau M, Suárez L, Martín L, Reigada R, Höring M, Liebisch G, Garrido C, Cabot G, Vílchez H, Cortés-Lara S, González de Herrero E, López-Causapé C, Oliver A, Barceló-Coblijn G, Mena A. Gut microbiome and plasma lipidome analysis reveals a specific impact of Clostridioides difficile infection on intestinal bacterial communities and sterol metabolism. mBio. 2024 Oct 16;15(10):e0134724.
Vasilescu IM, Chifiriuc MC, Pircalabioru GG, Filip R, Bolocan A, Lazăr V, Diţu LM, Bleotu C. Gut Dysbiosis and Clostridioides difficile Infection in Neonates and Adults. Front Microbiol. 2022 Jan 20;12:651081.
Maslanka JR, Gu CH, Zarin I, Denny JE, Broadaway S, Fett B, Mattei LM, Walk ST, Abt MC. Detection and elimination of a novel non-toxigenic Clostridioides difficile strain from the microbiota of a mouse colony. Gut Microbes. 2020 Nov 9;12(1):1-15.
Nibbering B, Gerding DN, Kuijper EJ, Zwittink RD, Smits WK. Host Immune Responses to Clostridioides difficile: Toxins and Beyond. Front Microbiol. 2021 Dec 21;12:804949.
Samarkos M, Mastrogianni E, Kampouropoulou O. The role of gut microbiota in Clostridium difficile infection. Eur J Intern Med. 2018 Apr;50:28-32.
Kelly CR, Fischer M, Allegretti JR, LaPlante K, Stewart DB, Limketkai BN, Stollman NH. ACG Clinical Guidelines: Prevention, Diagnosis, and Treatment of Clostridioides difficile Infections. Am J Gastroenterol. 2021 Jun 1;116(6):1124-1147.
Dawson LF, Valiente E, Wren BW. Clostridium difficile–a continually evolving and problematic pathogen. Infect Genet Evol. 2009 Dec;9(6):1410-7.

谷禾健康

副萨特氏菌属(Parasutterella)是一种革兰氏阴性,严格厌氧菌,在谷禾的人群肠道样本数据库中检出率为84.13%,说明这个菌在大部分人肠道存在,甚至长期定植共生。
Parasutterella属占据特定肠道生态位,影响宿主代谢:来自小鼠、大鼠和人的Parasutterella均不能降解糖,也无法还原硝酸盐或产生吲哚,但能合成琥珀酸盐,并且该菌可能参与人体胆汁酸稳态维持和胆固醇代谢。同时肠道内芳香族氨基酸、胆红素、嘌呤和胆汁酸衍生物等代谢物也受该菌的影响。
作为肠道共生菌成员之一,Parasutterella的相对丰度与不同的宿主健康结果有关,例如在肥胖、2型糖尿病、焦虑和抑郁、炎症性肠病患者中,Parasutterella的丰度增加;但是又有一些研究发现Parasutterella可以降低危重肺炎风险,并对肾上腺功能有一定的影响。副萨特氏菌属(Parasutterella)可能根据具体情况发挥二分作用。
在人体研究和动物试验中,发现Parasutterella对抗生素给药和其他饮食干预(如益生元和抗性淀粉补充剂)有反应。过量食用高脂、超加工食品,缺乏维生素A会导致Parasutterella丰度增加,而食用虫草素、小麦麸质、白藜芦醇、阿拉伯半乳聚糖、发酵豆乳等可以降低Parasutterella丰度。
副萨特氏菌属(Parasutterella)是β变形菌门下的一个属,与萨特氏菌属(Sutterella)相似但又有所不同。是一种革兰氏阴性,严格厌氧的球菌或球杆菌,不产生孢子,大小为0.5-0.8×1.0-1.5微米。
在37°C的GAM琼脂上培育72小时后,Parasutterella菌落呈完整、圆形、凸面、半透明,直径为0.5-0.7mm。
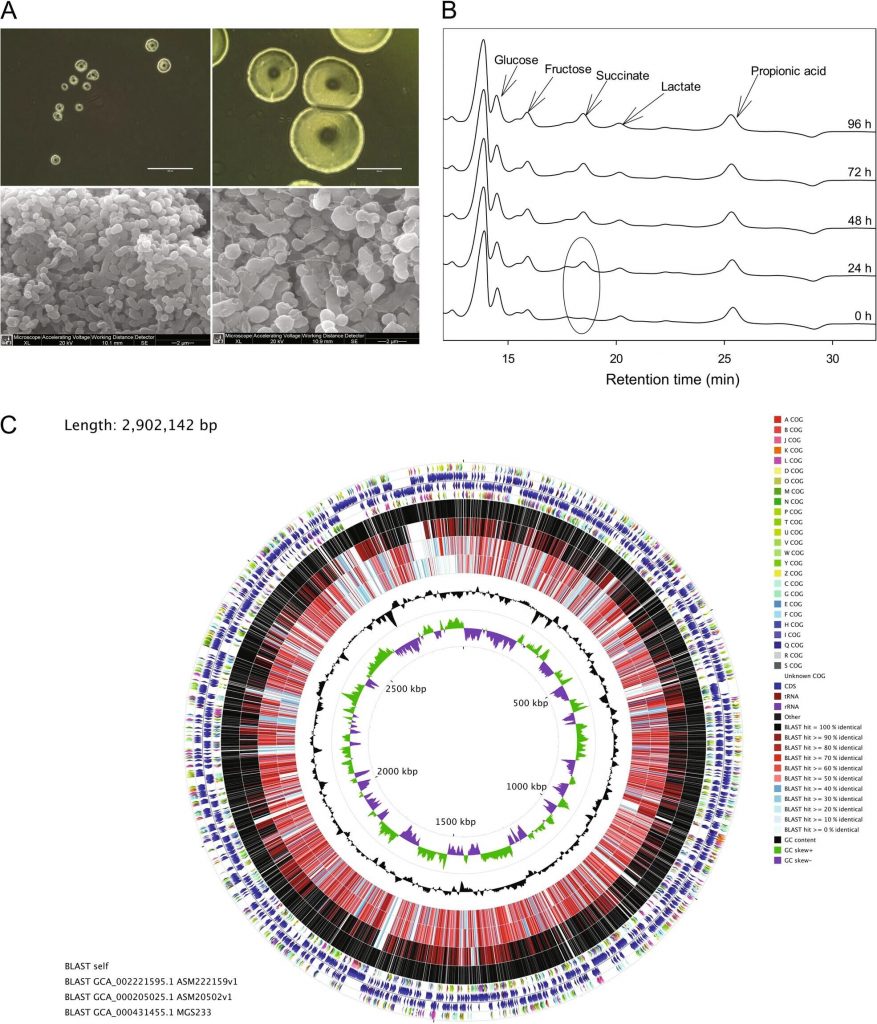
doi: 10.1038/s41396-019-0364-5.
物种与分布
Parasutterella属包含两种类型的菌株,Parasutterella excrementihominis YIT11859和Parasutterella secunda YIT12071,它们首先从人类粪便中分离出来。
Parasutterella excrementihominis是该菌属的模式物种。
Parasutterella属的成员也存在于其他物种中,包括小鼠、大鼠、狗、猪、鸡、火鸡和小牛。
生长与代谢
Parasutterella可在37°C厌氧环境下生长,这与人体肠道内的环境相似,并且在谷禾的检测报告中,Parasutterella有较高的检出率,说明Parasutterella是肠道菌群的共生成员。
来自小鼠、大鼠和人的Parasutterella均不能降解糖(肉汤培养物中未检测到葡萄糖、果糖或乳酸的变化),并且未检测到短链脂肪酸作为代谢的最终产物,此外对硝酸盐还原、吲哚生成、过氧化氢酶、脲酶和氧化酶活性以及七叶苷和明胶水解呈阴性。
但该菌能合成琥珀酸盐,其的定植还可引起小鼠肠道内芳香族氨基酸、胆红素、嘌呤和胆汁酸衍生物等菌群代谢物的改变。
胆汁酸的变化伴随着回肠胆汁酸转运基因、肝脏胆汁酸合成基因表达的改变,证明该细菌可能参与胆汁酸稳态维持和胆固醇代谢。
注:Parasutterella的丰度在发酵过程中降低,与氨的产生呈正相关。天冬酰胺是GAM肉汤中Parasutterella代谢最迅速和首选的氨基酸。
基因组信息
Parasutterella的完整基因组大小为2.8 Mb,G+C含量为44.1mol%。预测包含2648个独特基因,缺乏转运和代谢外源糖的基因。
具有编码L-天冬酰胺酶、天冬氨酸氨裂解酶和天冬氨酸脱氢酶的基因,表明天冬酰胺是其最快速和首选的氨基酸代谢物。
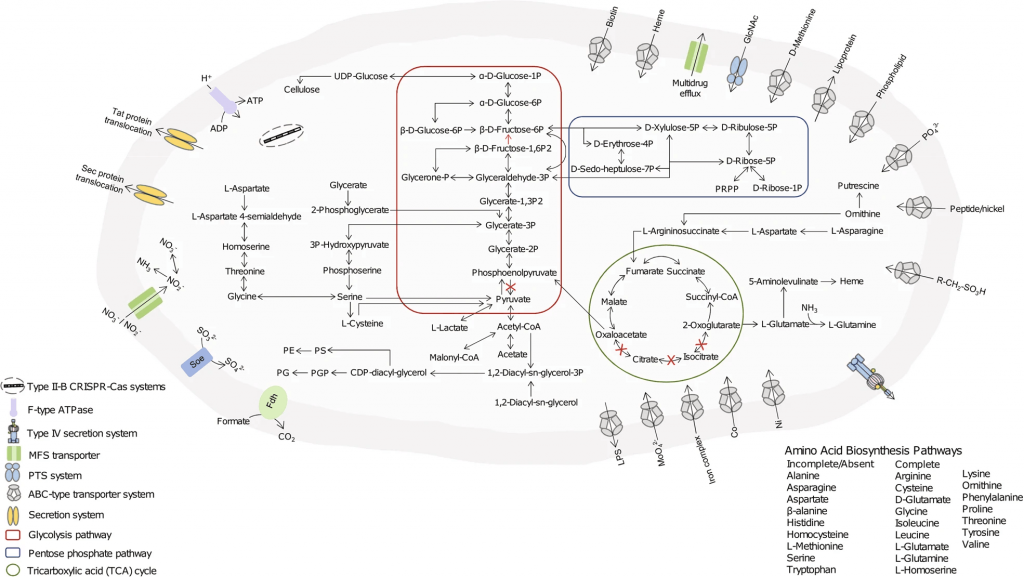
doi: 10.1038/s41396-019-0364-5.
此外,在Parasutterella mc1的基因组中没有鉴定出毒素毒力因子相关基因,这表明Parasutterella可能是肠道菌群的共生成员。但最近有许多研究和谷禾的检测报告中发现Parasutterella的丰度异常与一些疾病存在关联,让我们一起继续深入了解。
作为肠道微生物群中的一员,研究发现Parasutterella与炎症性肠病、肥胖、2型糖尿病、自闭症和肾结石等健康结果相关。
肥胖和2型糖尿病患者中增多 ↑↑
研究纳入了1544名受试者,分析肠道菌群组成,发现Parasutterella丰度与BMI以及2型糖尿病呈正相关,与膳食中碳水化合物摄入量呈正相关,但与肥胖中微生物组α/β多样性减少和低度炎症无关。
高丰度的Parasutterella与人体脂肪酸合成途径的激活有关,减肥干预试验中Parasutterella的丰度显著降低,Parasutterella增加或是影响体重增加的一个机制。
在代谢组学检测的126种血清代谢物中,L-半胱氨酸在Parasutterella丰度高的受试者中显著降低,因为Parasutterella是已知的高L-半胱氨酸消费者。
综上所述,Parasutterella在人类2型糖尿病和肥胖症中起一定作用,其中与L-半胱氨酸的联系可能与2型糖尿病的发展有关,并与肥胖症发展过程中富含碳水化合物的饮食导致体重增加的脂肪酸生物合成途径有关。
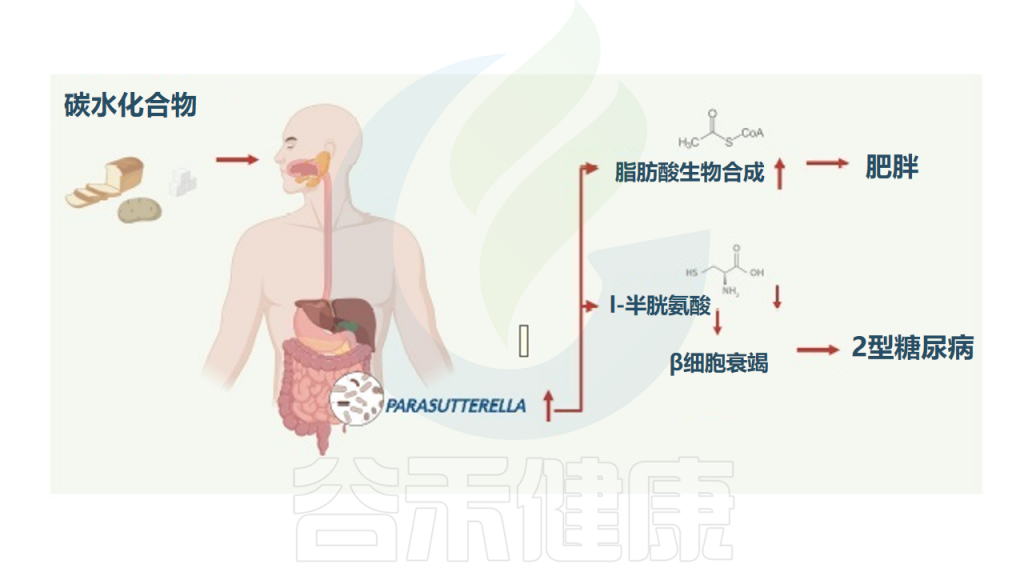
Henneke L,et al.Gut Microbes.2022
焦虑和抑郁人群中增加 ↑↑
与健康个体相比,社交焦虑症(SAD)患者体内的Parasutterella的丰度增加。

同时,16S rRNA分析发现,应激小鼠肠道中Bacteroides、Alistipes和Lactobacillus丰度降低,Parasutterella和Rikenellaceae_RC9_gut_group丰度升高。
KEGG通路分析表明,差异代谢物主要参与α-亚麻酸代谢、味觉传导、半乳糖代谢等下调通路。多种代谢物与Alistipes和Bacteroides呈正相关,而与Parasutterella呈负相关。
此外,Parasutterella的绝对丰度与身体不满意度呈正相关。
炎症性肠病患者中增加↑↑
在肠易激综合征(IBS)患者肠道菌群中,发现15个基因表达显著差异,Parasutterella的表达在筛选和验证实验中均显著不同,并与慢性肠道炎症相关,因此被认为与IBS的发生和发展有关。
Rnase4作为肠道抗菌蛋白在调节肠道微生物群和代谢物稳态中起关键作用,但在炎症性肠病(IBD)患者的肠道组织和粪便中观察到Rnase4水平降低,与Parasutterella的增加有关。
Parasutterella在小鼠体内定植虽然不会对整体微生物结构有明显影响,但会显著改变肠道代谢物,尤其是色氨酸代谢。
在肠上皮细胞和免疫细胞中表达的吲哚胺-2,3-双加氧酶1(IDO1)通过催化色氨酸转化为犬尿氨酸和其他下游代谢物,在肠道健康中发挥关键作用。这些代谢物具有免疫调节作用,并有助于维持肠道稳态,其产生失衡与IBD有关。
骨质疏松症患者中丰度改变
针对继发性骨质疏松症,研究发现酒精性骨质疏松大鼠厚壁菌门(Firmicutes)/拟杆菌门(Bacteroidetes)比例显著降低;高脂饮食诱导的骨质疏松小鼠肠道中双歧杆菌属(Bifidobacterium)、副萨特氏菌属(Parasutterella)和Odoribacter数量显著减少。
但最新的一项研究又发现了矛盾的结果,通过16S rDNA基因测序分析,发现骨质疏松症患者肠道微生物在属水平上的组成和结构明显不同。其中,uncultured_bacterium_f_Muribaculaceae,Allobaculum和Parasutterella丰度显著升高,Akkermansia显著降低,这可能对骨质疏松症(OP)的进展有显著影响。
其他疾病中的丰度变化
// 便秘患者中丰度增加
Parasutterella丰度与便秘大鼠中的炎症呈正相关。便秘是帕金森病患者常见的非运动症状,并在诊断为帕金森病的患者肠道内表现出升高的丰度,并与神经炎症和运动功能密切相关。
// 急性心肌缺血患者中丰度增加
与正常对照组相比,急性心肌缺血(AMI)患者中Parabacteroides、Butyricimonas、Odoribacter、Escherichia和Parasutterella的相对丰度显著增加。
// 酒精性肝病患者中丰度降低
研究也发现,酒精暴露导致小鼠肠道菌群结构显著改变,表现为Firmicutes丰度增加,Parasutterella丰度减少。这表明肠道菌群在酒精性肝病(ALD)的进程中起关键作用。
// 肾结石患者中丰度降低
肾结石患者中显著降低的菌群有:霍氏真杆菌、多尔氏菌属、啮齿杆菌、厌氧棒菌属、Ruminiclostridium_5、霍尔德曼氏菌属(Holdemania)、Fusicatenibacter、罕见小球菌属(Subdoligranulum)、戴阿利斯特菌属、Parasutterella、嗜胆菌属。
并且肾结石患者肠道中的Parasutterella菌属与血钠浓度呈负相关。
尽管Parasutterella丰度变化可能与某些疾病进展相关,但作为肠道共生菌,它也可能具有一些有益作用,如下所示。
可能降低危重肺炎风险 ↓↓

一项研究探讨了肠道菌群对危重肺炎的影响,分析了大规模肠道微生物群数据(n=18340)和危重肺炎基因组数据(病例n=2758和对照n=428607)。
结果显示,疣微菌科(Verrucomicrobiaceae)、嗜黏蛋白阿克曼菌属(Akkermansia)、Lachnospiraceae FCS020group、Parasutterella属、Prevotella7属和蓝细菌门与重症肺炎风险降低相关,而肠杆菌科、瘤胃球菌属UCG003和一些其他肠杆菌目则与风险增加相关。
影响肾上腺功能

研究表明Parasutterella与肾上腺球状带和束状带的功能之间存在因果关系,这会影响醛固酮和皮质醇水平。
Parasutterella生物学特性的研究发现,它显著调节胆汁酸和胆固醇。胆固醇是类固醇激素合成的主要底物,类固醇激素对肾上腺皮质激素的合成至关重要。胆汁酸还促进肠道对膳食胆固醇的吸收,肝脏中胆固醇的合成与胆汁酸的肠肝循环密切相关。
因此,Parasutterella对胆汁酸和胆固醇代谢的调节作用可能是影响肾上腺皮质激素(醛固酮和皮质醇)水平的重要途径。
对甲状腺疾病的保护作用
此外,还有研究发现Parasutterella对毒性单甲状腺结节(TSTN)的甲状腺毒症具有保护作用。
除了疾病外,其他生理状态或因素也会影响Parasutterella的丰度,我们在此列出了一些调节措施。
◮ 女婴中Parasutterella丰度更高
男婴肠道中的2种菌属——另枝菌属(Alistipes)和Anaeroglobus的平均相对丰度更高;而副萨特氏菌属(Parasutterella)、优杆菌属(Eubacterium)、Peptoniphilus和Anaerosporobacter在女婴肠道中的平均相对丰度更高。
◮ 孕妇肠道中Parasutterella增加
研究发现,在早孕期(孕10~15周),正常健康孕妇的肠道菌群拥有较高的α多样性,门水平主要由拟杆菌门、厚壁菌门和变形菌门组成,拟杆菌门为主要优势菌门;属水平上,主要由较多Parasutterella、Parabacteroides、Megasphaera、Dialister和Ruminococcaceae UCG 002/003/005组成。
◮ 缺乏维生素A会导致Parasutterela增加
维生素A缺乏使毛螺菌属_NK4A136组、颤杆菌的数量减少;然而,Parasutterela呈上升趋势。
◮ 高脂、超加工食品导致Parasutterella增加
与对照组相比,超加工食品组中Parasutterella的丰度更高,而Bacteroidetes和Rosebunia的丰度较低。
此外,与对照组相比,高脂高胆固醇饮食组小鼠Escherichia_shigella、Parasutterella和Allobaculum属相对丰度增加。这可能也是肥胖和2型糖尿病人群中Parasutterella较多的一个原因。
◮ 食用抗性马铃薯淀粉Parasutterella丰度增加

在食用抗性马铃薯淀粉(RPS) 的个体的肠道微生物组中,副萨特氏菌属(Parasutterella)的丰度趋于增加,并且副萨特氏菌的增加与服用RPS而不是安慰剂的参与者的低密度脂蛋白(LDL)水平降低相关。
将低密度脂蛋白(LDL)水平下降的RPS消费个体与没有降低的个体分开,发现低密度脂蛋白应答者在基线和服用RPS 12周后的Parashutterella水平明显较高。
▷ 黄莲解毒汤减少Parasutterella

传统中草药制剂黄莲解毒汤剂(HLJD)临床用于治疗腹泻和结肠炎。2和4g/kg剂量的HLJD通过抑制与集落刺激因子1受体(Csf1r)/Src通路相关的结肠组织中巨噬细胞活性受损来抑制炎症,从而缓解慢性结肠炎。
此外,黄莲解毒配方可以通过减少拟杆菌属、Odoribacter、Clostridium_sensu_stricto_1 和 Parasutterella 的丰度来改变肠道微生物群概况。
▷ 虫草素调节Parasutterella,改善肠道炎症

源自真菌的虫草素(CRD)具有抗炎和抗氧化特性,显示出对抗肥胖的潜力。CRD干预减轻了高脂饮食诱导的肠道炎症,改善了血糖水平,减少了脂肪堆积。
此外,冬虫夏草虫草素补充剂被证明能够通过调节关键代谢物的水平来调节内源性代谢紊乱,包括 DL-2-氨基辛酸、肌醇和6-脱氧法戈明。
虫草素影响了 Parasutterella、Alloprevotella、Prevotellaceae_NK3B31_group、Alistipes、unclassified_Clostridia_vadinBB60_group和 unclassified_Muribaculaceae等重要微生物群的丰度,最终导致内源性代谢的调节和肠道菌群紊乱的改善。
▷ 小麦麸油降低Parasutterella,改善脂肪堆积

麦麸是小麦的副产品,它含有膳食纤维、B族维生素、矿物质、酚类化合物和其他被认为对健康有益的植物化学物质。研究表明,麦麸对预防肥胖、心血管疾病、胃肠道疾病和一些癌症有积极作用
该研究发现小麦麸油(WBO)减少了体重增加、脂肪和脂质积累,并改善了肝脏脂肪变性和炎症。WBO处理增加了Romboutsia和 Allobaculum 的相对丰度,降低了Candidatus_Saccharimonas、Alloprevotella, Rikenellaceae_RC9_gut_group, Alistipes, Parabacteroides、Helicobacter、Colidextribacter 和 Parasutterella 的相对丰度。
▷ 世神丸调节肠道菌群,缓解肾阳虚腹泻
世神丸(SSP)是一种中药处方,通过调节肠道菌群、下调胆碱-三甲胺裂解酶(CutC)活性以及降低TMAO和炎症因子水平,显著缓解肾阳虚综合征腹泻症状。
相关性分析显示,CutC活性与粪杆菌属和Chryseobacterium呈正相关,与Prevotellaceae UCG-001、Rikenella、Acinetobacter、Parasutterella和Lacticaseibacillus呈显著负相关。
TNF-α 水平与Lacticaseibacillus、Prevotellaceae UCG-001、Parasutterella和Candidatus Saccharimonas呈显著负相关。
IL-6水平与Rikenella、Acinetobacter、Prevotellaceae UCG-001、Lacticaseibacillus和 Parasutterella呈显著负相关,并且与Faecalibaculum和Chryseobacterium呈显著正相关。
此外,还存在一些可以降低Parasutterella丰度的措施:
白藜芦醇
白藜芦醇(RSV)处理高脂饮食喂养的小鼠后,Parabacteroides 的丰度增加,而Parasutterella的丰度降低。
阿拉伯半乳聚糖
作为L-半胱氨酸的高消耗者,副萨特氏菌(Parasutterella)的定植可显著增加牛磺酸和N-乙酰蛋氨酸的水平。
而阿拉伯半乳聚糖(LBP-3)治疗显著降低了副萨特氏菌(Parasutterella)的相对丰度,从而降低了半胱氨酸、牛磺酸和炎性细胞因子(如TNF-α和IL-1β)的水平,从而有助于减轻溃疡性结肠炎(UC)的症状。
低FODMAP黑麦面包
一项随机临床试验比较低FODMAP黑麦面包与普通黑麦面包对肠易激综合征患者肠道菌群的影响,结果显示食用低FODMAP黑麦面包减少了拟杆菌、Flavonifractor、Holdemania、Parasutterella和克雷伯菌的丰度,并显示出双歧杆菌增加的趋势。
发酵豆乳
摄入发酵豆乳(FSM)可使Parasutterella、Turisibater和Bacteroide的相对丰度分别降低75%、62%和50%,而有益菌Akkermansiaceae、Lachnospiraceae、Alloprevotella和Dubosella的相对丰度分别增加28%、50%、80%和63%。
在动物实验中,经阿斯巴甜处理后,厚壁菌门和柔嫩梭菌属(Clostridiumleptum)的丰度较高,肠球菌和副萨特氏菌(Parasutterella)的丰度较低。
富含氢气的水(HRW)被发现减少了某些可能的致病性肠道微生物(Frisingicoccus和Parasutterella)。
主要参考文献
Ju T, Kong JY, Stothard P, Willing BP. Defining the role of Parasutterella, a previously uncharacterized member of the core gut microbiota. ISME J. 2019 Jun;13(6):1520-1534.
Henneke L, Schlicht K, Andreani NA, Hollstein T, Demetrowitsch T, Knappe C, Hartmann K, Jensen-Kroll J, Rohmann N, Pohlschneider D, Geisler C, Schulte DM, Settgast U, Türk K, Zimmermann J, Kaleta C, Baines JF, Shearer J, Shah S, Shen-Tu G, Schwarz K, Franke A, Schreiber S, Laudes M. A dietary carbohydrate – gut Parasutterella – human fatty acid biosynthesis metabolic axis in obesity and type 2 diabetes. Gut Microbes. 2022 Jan-Dec;14(1):2057778.
Yan H, Kuerbanjiang M, Muheyati D, Yang Z, Han J. Wheat bran oil ameliorates high-fat diet-induced obesity in rats with alterations in gut microbiota and liver metabolite profile. Nutr Metab (Lond). 2024 Oct 25;21(1):84.
Liu T, Ji H, Li Z, Luan Y, Zhu C, Li D, Gao Y, Yan Z. Gut microbiota causally impacts adrenal function: a two-sample mendelian randomization study. Sci Rep. 2024 Oct 7;14(1):23338.
Su S, Liu T, Zheng JY, Wu HC, Keng VW, Zhang SJ, Li XX. Huang Lian Jie Du decoction attenuated colitis via suppressing the macrophage Csf1r/Src pathway and modulating gut microbiota. Front Immunol. 2024 Sep 26;15:1375781.
Li Y, Fang M, Li D, Wu P, Wu X, Xu X, Ma H, Li Y, Zhang N. Association of gut microbiota with critical pneumonia: A two-sample Mendelian randomization study. Medicine (Baltimore). 2024 Oct 18;103(42):e39677.
Fu Y, Wang Q, Tang Z, Liu G, Guan G, Lyu J. Cordycepin Ameliorates High Fat Diet-Induced Obesity by Modulating Endogenous Metabolism and Gut Microbiota Dysbiosis. Nutrients. 2024 Aug 27;16(17):2859.
Xue S, Shi W, Shi T, Tuerxuntayi A, Abulaiti P, Liu Z, Remutula N, Nuermaimaiti K, Xing Y, Abdukelimu K, Liu W, Gao F. Resveratrol attenuates non-steroidal anti-inflammatory drug-induced intestinal injury in rats in a high-altitude hypoxic environment by modulating the TLR4/NFκB/IκB pathway and gut microbiota composition. PLoS One. 2024 Aug 12;19(8):e0305233.

谷禾健康

这篇文章总结了关于肠道微生物群(GM)在糖尿病中的作用的研究现状与结论,内容来自《Diabetes》、《Diabetes Care》和《Diabetologia》最近举办的一次国际专家论坛,该论坛在2023年的欧洲糖尿病研究协会年会上举行。论坛参与者包括在肠道微生物组和代谢领域的领军研究人员,其中既有临床医生,也有基础科学家。
讨论主要分为四个主题:流行病学、生理学和病理生理学、技术和方法以及临床应用。他们得出的结论如下:
肠道微生物群参与2型糖尿病的病理生理过程。微生物产生的代谢物与疾病有正面和负面的关联,而且最近通过人类的孟德尔随机化研究,发现了肠道微生物功能(如丁酸盐生产基因)与葡萄糖代谢之间的机制联系。
肠道微生物群的高度个体化特性是研究的一大障碍。需要大型队列和深度测序的方法来稳健地评估关联性和因果关系。
由于单次采样对于捕捉糖尿病个体内肠道微生物群的动态变化有些困难,建议未来需要要对个体多次重复测量的研究,就是要增加纵向队列的研究。
未来还需要大量研究来确定这些不断扩展的知识如何应用于糖尿病的诊断和治疗。新技术和改进的计算工具将对实现这一目标很重要。
研究小组承认,对肠道菌群在代谢疾病中的作用的理解存在许多差距,这并非糖尿病领域所独有,而是反映了更广泛的需求。开展更多控制良好的前瞻性和回顾性人体研究,并在机制上跟进模型系统研究,改进计算工具,将有利用将目前的微生物组数据应用于未来糖尿病的诊疗。
Perspectives
1)
肠道菌群与糖尿病之间的流行病学关联
肠道微生物群是人体最大且最复杂的微生物群落,它连接着我们的外部和内部环境。对肥胖症和心血管代谢疾病(包括2型糖尿病)中肠道微生物群进行流行病学研究的动机源于啮齿动物研究,这些研究证明了肠道微生物群、脂肪性和葡萄糖耐受性之间的联系。
在人类研究中,流行病学研究观察到肥胖症患者的微生物多样性降低,但通过对小型队列进行16S rRNA基因测序或全基因组宏基因组学分析的荟萃分析,并未发现普遍适用的与肥胖相关的肠道微生物特征(换句话说,微生物与疾病的研究需要大队列和大数据库)。
然而,一项对以色列和美国34057名个体进行深度测序全基因组宏基因组学的大规模肠道微生物研究显示,肠道微生物与表型之间存在一致的关联,并且基于微生物组数据训练的机器学习模型对体重指数(BMI)和糖化血红蛋白(HbA1c)的预测准确性可以在不同队列间复制。
通过对训练队列进行子采样,发现随着队列规模的增加,预测准确性也随之提高,约7500-10000个体的样本量可以获得可重复的结果(目前谷禾糖尿病模型使用了9989个样本队列)。这一发现强调了在人类肠道微生物横断面研究中使用大型队列(包含数百名个体)和深度测序组学的必要性,以充分代表人群中的个体异质性以及地区和人口统计学变异。
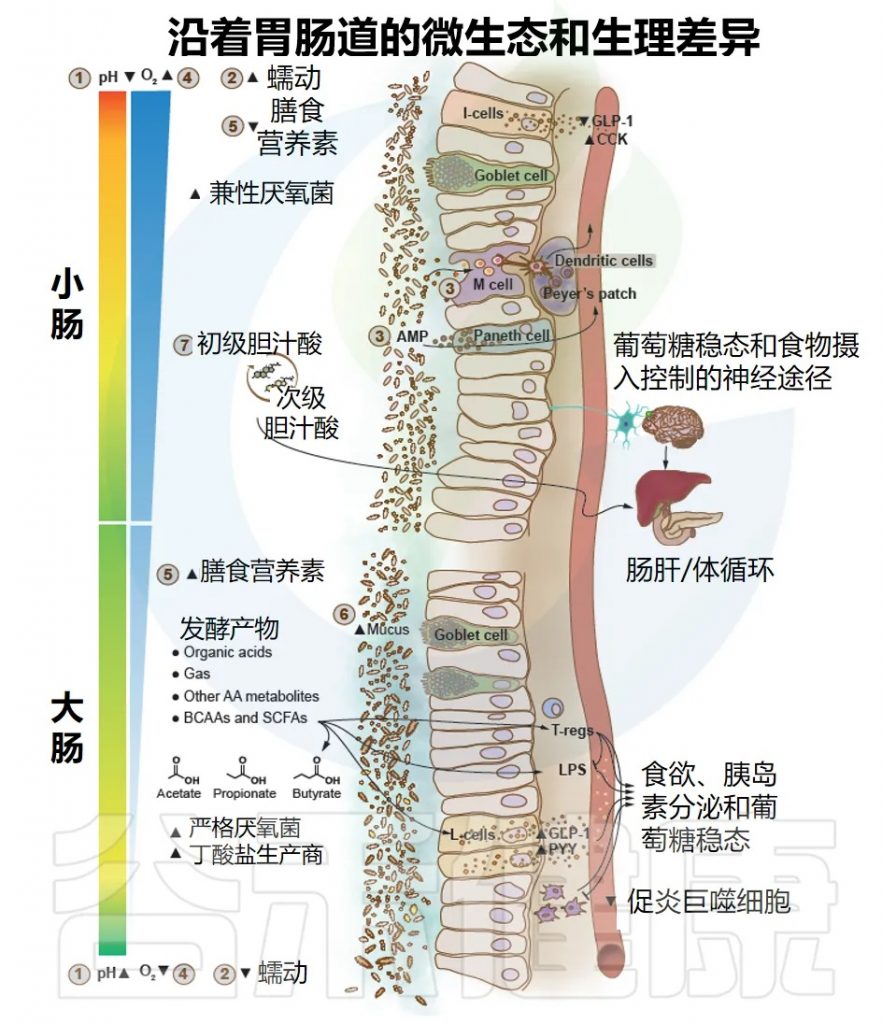
Byndloss M, et al.Diabetes Care.2024
胃肠道(GI)沿线的微生态和生理差异反映了各种环境因素的变化,这些变化依赖于物理、营养和生物学的宿主因素。这些因素导致肠道不同区域的细菌及其生理功能的适应和差异,通过可能影响葡萄糖代谢和糖尿病风险的多向交互产生效果。
以下是影响不同区域微生物数量和组成的主要因素:
pH值:从胃(pH1.0–4.4)到小肠(pH 5.5–7.0),然后更为渐进地到达结肠,在那里由于复杂碳水化合物(纤维)的微生物发酵,pH值可能再次下降(pH5.5)。在粪便中pH值再次升高(可达pH7.8)。
肠道蠕动:在小肠中,肠道通过时间较短,肠蠕动更为强烈,而在大肠中则不然。
肠道上皮细胞:小肠的泛素细胞分泌抗菌肽(AMPs),充当天生防御屏障以减少细菌定植;而M细胞从肠腔中捕获细菌。
氧气浓度:从小肠到大肠,氧气水平逐渐降低。
膳食营养:主要在小肠中由宿主酶消化和快速吸收蛋白质、脂肪和简单碳水化合物,因此限制了细菌对这些营养物质的获取;而部分未消化的膳食残留(例如复杂碳水化合物和部分水解的蛋白质/氨基酸)则积聚在大肠,为细菌提供营养。
宿主糖基:它是由杯状细胞产生的粘液层的一部分,在大肠中远比小肠厚,也是肠道细菌的营养来源,支持其生长。
胆汁酸:分泌至小肠,抑制和有利于某些参与其代谢和再循环的特定细菌的生长。
以上所有生物和非生物因素影响生态条件,使得细菌群体可以在向肠道最远端部分移动时更加密集(从十二指肠的每克102–104个细菌到回肠的107–109个,以及结肠的1011–1012个),并导致细菌组成的差异,其中兼性厌氧菌优先在小肠定殖,而严格厌氧菌在大肠内的微生物中占主导地位,包括丁酸盐生产者。
因此,为了在种族/民族、生活方式和其他人口特征差异之外识别疾病特异性的微生物特征,重要的是在大型人群中进行研究,并将来自不同研究的健康个体/对照参与者作为参考;这些方法已被证明可以提高疾病预测准确性。
2)
肠道微生物代谢与葡萄糖稳态的关联
多项观察性研究报告了肠道微生物群与2型糖尿病之间的关联。在全球流行病学研究中发现,2型糖尿病和糖耐量受损/空腹血糖异常患者的肠道微生物组成发生了一致的改变,这些改变在代谢综合征中也存在,主要特征是微生物多样性降低和产生短链脂肪酸(SCFA)丁酸盐的细菌丰度减少。一些研究还观察到机会性病原体的增加。
最近,粘液降解菌Ruminococcus gnavus被确定为代谢综合征多个特征的预测因子,包括低度炎症、腰围增大、血清甘油三酯升高、糖化血红蛋白升高和高密度脂蛋白胆固醇降低。然而,正如对不同疾病(包括胃肠道和代谢性疾病)肠道菌群改变的荟萃分析所指出的,这些特征中的几个并非疾病特异性,可能代表了一般的肠道菌群的失调。
与葡萄糖代谢和2型糖尿病相关的肠道微生物代谢物和信号分子,肠道微生物群的结构蛋白和分泌蛋白参与调节免疫反应和炎症,正如F. prausnitzii(普拉梭菌)分泌的蛋白质(微生物抗炎分子[MAM]),它能够抑制核因子-κB(NF-κB)通路。另一个例子是A. muciniphila(AKK菌)的外膜蛋白Amuc_1100,它能改善肠道屏障并降低炎症。
①短链脂肪酸
肠道菌群生成短链脂肪酸(SCFAs),SCFAs调节几个过程,包括肠道蠕动和pH值、肠道屏障免疫反应以及通过影响糖异生、胰岛素敏感性和胰岛素分泌的途径来调节系统代谢。
此外,SCFAs调节免疫细胞功能,增强肠道屏障,并刺激肠神经的信号传导。其中丁酸盐还为结肠细胞提供主要能量,并通过激活过氧化物酶体增殖物激活受体γ(PPARγ)增加结肠细胞的β-氧化(β-ox)。
然而,人类研究显示,2型糖尿病患者粪便或血液中不同SCFAs的水平存在广泛变异,这可能是由于方法学局限性造成的。支持SCFAs在调节葡萄糖代谢中作用的最强有力证据来自动物研究和最近一项使用孟德尔随机化统计方法的人类研究(参见下文)。
②胆汁酸
胆汁酸是两性分子,可介导膳食脂肪和脂溶性维生素的吸收。这些分子也被认为是调节脂质、葡萄糖和能量代谢的主要参与者。因此,在2型糖尿病和其他肥胖相关疾病中发现了胆汁酸池的改变,并被认为可能是2型糖尿病病理生理学的潜在贡献因素。
12α-羟基化胆汁酸水平的增加和6α-羟基化胆汁酸水平的降低与胰岛素抵抗有关,并在2型糖尿病患者中出现。胃旁路手术后观察到6α-羟基化胆汁酸水平增加,可预测2型糖尿病的缓解。
干预研究也调查了胆汁酸在人类代谢中的潜在重要性。在减肥手术后,系统性胆汁酸水平升高以及肠道信号激发GLP-1释放的现象得到了验证,尤其是餐后增加被认为特别重要。
然而,在一些进行过胆囊切除术的个体中发现胆汁酸反应过度,并与GLP-1和胰岛素反应的进一步增强相关联。在2型糖尿病患者中,已证明二甲双胍通过减少脆弱拟杆菌的丰度来改善葡萄糖代谢,这与肠道中甘牛胆酸水平的增加和法尼醇X受体(FXR)的抑制有关。
然而,对肠道微生物群与胆汁酸之间直接相互作用及其与2型糖尿病及相关疾病的发展和治疗的关联的理解仍然有限,还需要更多的人体研究来探索。
③色氨酸代谢物
肠道菌群色氨酸代谢物,如吲哚丙酸(IPA)和吲哚丙烯酸(IA),通过孕烷X受体(PXR)改善肠道屏障,并通过肠道免疫细胞上的芳香烃受体(AHR)进行信号传导,增加白介素-22(IL-22)的产生,从而调节免疫和代谢反应。
④其他代谢物
在血液中,IPA和IA还提供抗氧化和抗炎功能。研究还表明,3-吲哚丙酸(色氨酸的代谢产物)的循环水平升高与胰岛素分泌和敏感性改善以及2型糖尿病风险降低相关。
咪唑丙酸和支链氨基酸(BCAAs)通过激活雷帕霉素复合体1(mTORC1)的机制型靶标来损害胰岛素信号传导。
肠道菌群还产生乙醇,与脂肪肝病和胰岛素抵抗有关。
肠道微生物群产生的氨基酸代谢物也与2型糖尿病相关(前两个图)。研究表明,3-吲哚丙酸(色氨酸的代谢产物)的循环水平升高与胰岛素分泌和敏感性改善以及2型糖尿病风险降低相关。
此外,在存在胰岛素抵抗和2型糖尿病的个体中,血浆组氨酸代谢的细菌产物——咪唑丙酸水平增加。来自肠道菌群对芳香氨基酸代谢的这些代谢物和其他一些代谢物也与欧洲和美国独立队列中的心血管事件风险和死亡率有关。
肠道菌群还产生乙醇,与脂肪肝病和胰岛素抵抗有关。
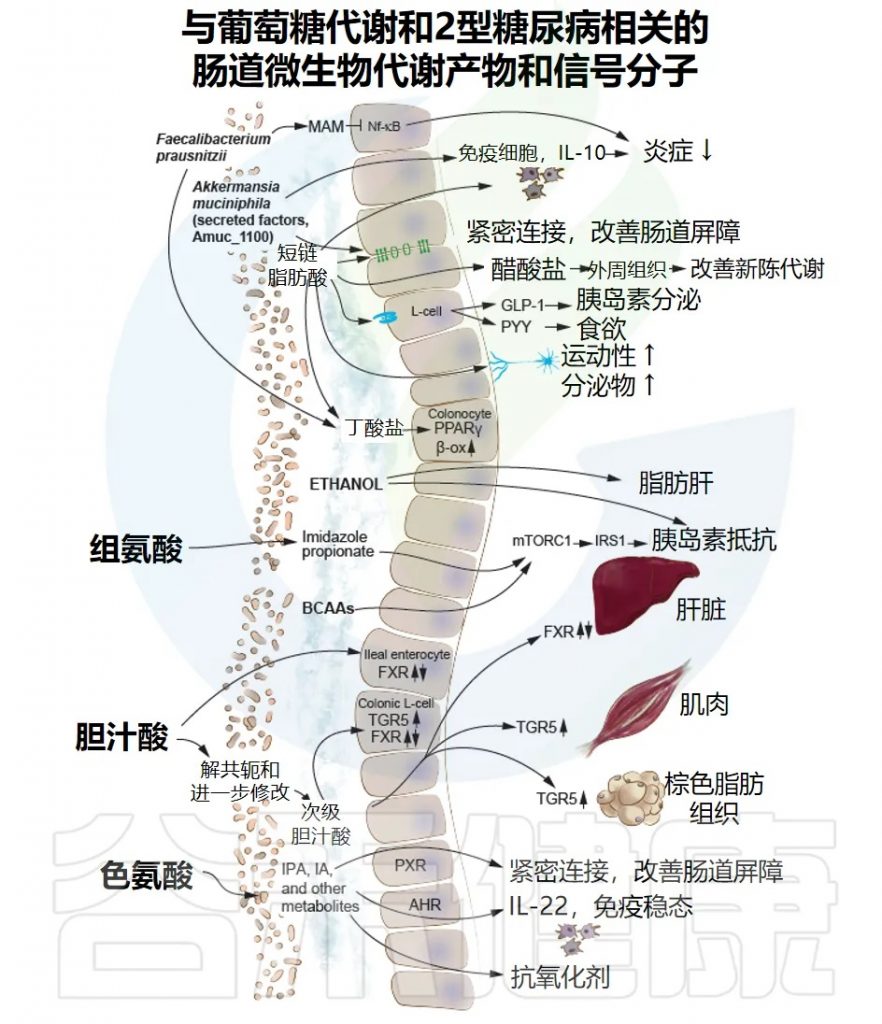
Byndloss M, et al.Diabetes Care.2024
3)
肠道菌群或其代谢产物和降糖药物治疗的关系
支持肠道微生物群在2型糖尿病中作用的证据已通过观察性和干预性研究得到加强。这些研究表明,二甲双胍使用者的肠道菌群中多种细菌物种的相对丰度发生了变化。
二甲双胍使用者肠道菌群发生显著变化
在多个涉及接受二甲双胍治疗个体的队列研究中,发现大肠杆菌(Escherichia coli)的相对丰度升高,而Intestinibacter bartlettii的丰度降低。
此外,最近一项大规模宏基因组研究发现,接受二甲双胍治疗的个体中Escherichia marmotae增加,而Romboutsia timonensis减少。
随机试验和对未使用药物的个体的研究为这些肠道菌群差异在2型糖尿病中的因果效应提供了支持。这些研究表明,肠道菌群组成的变化转化为丙酸盐和丁酸盐产生的增加以及胆汁酸池的调节,这可能介导了二甲双胍降血糖效应的一部分。
然而,肠道菌群也可能是约30%服用二甲双胍的个体经历短暂或持续肠道不适的原因(例如,通过一些大肠杆菌属种增加气体产生)。
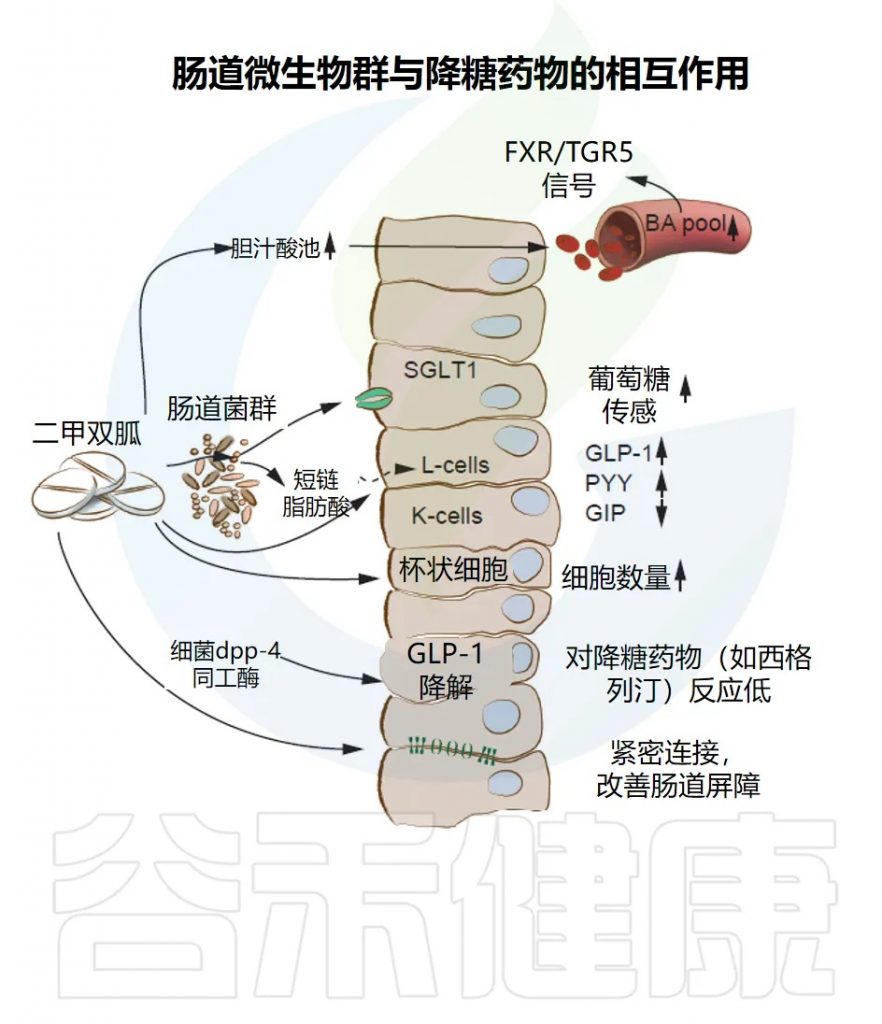
Byndloss M, et al.Diabetes Care.2024
肠道微生物代谢物参与二甲双胍的作用机制
肠道微生物代谢物参与二甲双胍的作用机制,包括通过胆汁酸受体FXR和TGR5进行胆汁酸信号传导,以及生产短链脂肪酸,这些都调节了内分泌细胞(K细胞和L细胞)中胰高血糖素样肽-1(GLP-1)、胃抑制多肽(GIP)和肽YY(PYY)等促胰岛素分泌激素的释放。
其他与二甲双胍作用相关的肠道菌群依赖机制包括通过钠-葡萄糖共转运蛋白1(SGLT1)改善葡萄糖感知和提高肠道屏障功能(例如,恢复紧密连接和增加产粘蛋白的杯状细胞)。
然而,肠道菌群通过表达二肽基肽酶-4(DPP-4)同工酶,可能降低GLP-1活性并影响降糖药物的疗效。
其他降糖药物与肠道微生物群的关联
关于其他口服降糖药物,研究表明二肽基肽酶4(DPP-4)抑制剂和α-葡萄糖苷酶抑制剂对肠道微生物群和微生物代谢物有影响,但钠-葡萄糖共转运蛋白2(SGLT2)抑制剂、噻唑烷二酮类和胰高血糖素样肽1(GLP-1)受体激动剂的影响较不明确。
迄今为止,大多数涉及SGLT2抑制剂的研究都是在小鼠模型中进行的,少数现有的人体研究结果存在矛盾,无法清楚地区分SGLT2抑制剂的效果与之前或同时使用二甲双胍治疗或同期生活方式改变的影响。
GLP-1受体激动剂可能通过激活上皮内淋巴细胞GLP-1受体产生抗炎作用,进而可能有助于调节肠道微生物群。尽管需要更多研究,但现有证据表明肠道菌群可能介导一些降糖治疗的益处,某些益生菌或益生元可能通过影响肠道微生物或其功能进一步改善这些药物的降糖效果。
需要进一步的干预和转化研究来确定药物诱导的肠道菌群变化是否在介导健康效应中起因果作用,并揭示潜在机制。
重要的是,肠道菌群还可能影响降糖药物的效果,例如通过表达人类DPP-4的同源物,这可能降低GLP-1的活性并影响葡萄糖代谢(下图)。由于细菌DPP-4同源物似乎对一些靶向人类DPP-4的药物具有耐药性,因此可能需要抑制细菌同工酶来改善当前药物的代谢反应。
4)
孟德尔随机化在阐明因果关系中的作用
肠道微生物群能够通过多种方式影响和与宿主健康互动,因果关系的方向通常是双向的甚至是多向的。肠道微生物群特征在不同层次(如群落、物种、途径、基因和代谢物)能影响宿主表型(例如改变肥胖的风险),同时,表型的发展(如肥胖)又可以反过来改变肠道微生物群。
孟德尔随机化(MR)是一种统计方法,利用与暴露相关的人类遗传变异体来区分疾病结果的因果效应、混杂、反向因果关系或其他因素导致的关联。为了应用MR研究肠道微生物与2型糖尿病的联系,所研究的肠道微生物特征需要受到一个或多个强烈的人类遗传变异体的影响,以便在工具变量分析中用作工具。
尽管已经有若干全基因组关联研究针对不同的肠道菌群特征(如肠道细菌分类群的相对丰度和人类粪便微生物代谢物)进行,但研究其在2型糖尿病中的因果作用的大型MR研究仍然有限,且尚未在重复研究中得到证实。
部分鉴定出与粪便短链脂肪酸(SCFA)水平相关的人类遗传变异体,并报告了肠道菌群丁酸盐生成潜力(即负责肠道丁酸盐生成的基因)与口服葡萄糖耐量测试中胰岛素反应改善之间的潜在因果联系。这些作者还发现异常的粪便丙酸水平与2型糖尿病风险增加之间存在因果关系。
另一项MR研究报告称,2型糖尿病和肾脏疾病提高了血浆中肠道菌群依赖的代谢物三甲胺氧化物(TMAO)的水平,并提出此前观察到的较高TMAO水平与心血管疾病风险升高的证据可能是由于混杂或反向因果关系,而非因果效应。
另一项近期研究则表明某些细菌属与2型糖尿病之间可能存在因果联系。考虑到MR(如多效性和与弱工具变量相关的问题)及肠道菌群研究(如方法学差异、个体间异质性和个体内可变性)的局限性,需要进行大型高质量研究,以评估使用MR的宿主遗传变异体模拟特定肠道菌群特征(无论是特定细菌物种、属还是代谢产物)的能力,以理解与2型糖尿病发病机制的因果关系。
Relationship
▸ 膳食纤维摄入量较少可能导致2型糖尿病
膳食纤维摄入量减少与2型糖尿病风险增加有关;因此,新的糖尿病管理饮食建议鼓励多食用加工程度低的植物性食物,如全谷物、蔬菜、全水果、豆类、坚果和种子。
饮食是肠道生态系统的驱动因素,微生物可及碳水化合物促进菌群多样性和短链脂肪酸生成,从而减少炎症并支持肠道屏障的维持。
就肠道菌群和葡萄糖代谢而言,增加纤维摄入量与不同菌种水平的增加有关,例如Prevotella copri(现已更名为Segatella copri)。研究还表明,纤维对 HbA 1c的有益作用可能是由特定的基线肠道菌群组成和纤维促进的短链脂肪酸产生菌的多样性介导的。
▸ 肠道微生物的特定成分会影响其宿主反应
然而,即使在控制良好的饮食干预中也会观察到不同的影响,而且鉴于肠道菌群的个体间差异很大,对肠道菌群的饮食反应是高度个性化的。
精准营养或“个性化”营养是一个不断发展的领域,它基于识别可用于设计饮食干预措施的个体特定反应预测特征。利用关于肠道菌群成分的个人数据以及血液生物标志物和饮食习惯等其他信息,机器学习方法已被用于预测标准化膳食后的血糖反应,其准确度高于其他预测方法。
这些研究表明,肠道微生物的特定成分会影响其宿主的特定反应(即在不同细菌存在的情况下,对饮食的反应不同)。因此,肠道菌群至少在一定程度上决定了人类代谢的异质性。肠道菌群可改变且代谢活性高,为更精确的生活方式干预和新疗法提供了可能性。
知识差距、挑战和机遇
目前已有数个大型的高质量参考基因组目录 ,它们为人类研究中肠道微生物的分类和功能表征提供了极大的便利。然而,这些数据库并非没有局限性。
对于流行病学分析而言,肠道菌群数据充满了挑战,包括个体间和个体内巨大的变异性、高维性(即观察到的肠道菌群特征的数量可能大于样本和受试者的数量)和稀疏性(即肠道菌群特征,如物种,仅在部分样本中检测到)。
在种群水平上,肠道菌群由数千个相互作用的物种组成,每个物种在不同宿主之间以及在同一宿主内随时间推移都具有遗传多样性;然而,常见的分析往往忽略了这种非独立性、微生物之间复杂的加性与相互作用效应,以及肠道菌群的可修改性和波动性。然而,最近的一些分析表明,不同细菌物种的个体内变异和对宿主生理的适应模式不同。
其他挑战与肠道微生物群可能影响和响应的大量表型和环境因素有关。大规模群体研究的重要性在人体遗传学中已被无可置疑地证明;大多数多基因性状已知受许多具有小效应的遗传变异影响,但这些变异可以汇总成具有临床重要性的强大多基因风险评分。
类似地,大规模宏基因组研究结果表明,单一的细菌物种可能与人类表型存在低效应大小的关联,或以低丰度存在。因此,需要大样本量以获得足够的统计能力和涵盖个体间变异性,以获得可复制的结果和高预测准确性。
为了更好地理解肠道菌群变异和动态对2型糖尿病的长期影响,前瞻性研究至关重要。在目前发表的少数前瞻性研究中,肠道菌群特征与中国地区多样人群中发生的2型糖尿病事件和西班牙一项临床试验的子集相关,这些研究均使用16S rRNA基因测序。
在一个拥有18年随访的大规模芬兰基于人群的队列研究中,肠道菌群特征也与2型糖尿病有关,使用的是浅层宏基因组测序。然而,在这些研究中,发生病例的数量有限,分析的分辨率也有限。
例如,Faecalibacterium prausnitzii是下一代益生菌最有希望的候选者之一,但也有其他有希望的候选者,如Akkermansia muciniphila和P. copri。关于F. prausnitzii,已在人体肠道中发现了几种潜在亚种,它们具有利用复杂多糖的不同功能潜力 。
与此观察一致,大型宏基因组学研究也发现了几种F. prausnitzii 亚种,但仅其中一部分亚种与 BMI 呈负相关。就P. copri 而言,已发现其与宿主代谢表型(如内脏脂肪和葡萄糖反应)呈正相关和负相关。
这些不一致的发现可以部分地用种内和种间多样性来解释。例如,这些差异可能将同一物种内的菌株定义为共生菌或致病菌,如脆弱拟杆菌和艰难梭菌的情况,这取决于该菌株是否编码毒力因子。
Perspectives
在进化过程中,哺乳动物必须适应充满微生物、病毒和真菌的世界。在无菌的宫内环境中,哺乳动物在出生期间和出生后立即暴露于潜在的有害微生物中。进化创造了实质性的屏障,包括胃肠道运输过程、免疫球蛋白A (IgA) 、粘液、上皮层、内皮屏障、淋巴结和肝脏,所有这些屏障阻止微生物易位进入体内,但为微生物生态系统创造了最佳储存库。上消化道中的微生物数量较少。同时,大肠内微生物密度和丰富度较高,从小肠到大肠,pH值和有氧/厌氧条件发生生理变化,大肠内为厌氧条件。
1)
微生物的基本功能
肠道微生物除了对哺乳动物造成潜在的有害威胁外,还为哺乳动物提供必需功能,包括训练免疫系统、保护其免受病原体的侵害(即抗定植)、代谢功能、营养物质供应(如维生素)、肠道蠕动和外来生物的解毒。
同时,微生物和宿主在小肠中竞争营养物质,微生物产生的常量营养素副产物被提供给宿主。
营养物质(即纤维)和哺乳动物代谢物(如葡萄糖醛酸苷、粘液多糖和胆汁酸)通过微生物代谢进行发酵或转化。微生物代谢以及微生物细胞的死亡和周转形成了外周血中微生物代谢物池,其中约30%的外周血代谢物与肠道菌群及其代谢物有关。
这些微生物代谢物被G蛋白偶联受体(GPCR) 或芳烃受体(AHR)等受体识别,或被哺乳动物酶(如 TMAO)进一步加工,通过表观遗传修饰调节哺乳动物基因表达,对代谢健康产生影响。
2)
不可消化纤维及其代谢物的作用
不可消化的碳水化合物是大肠中特定细菌的能量来源,这些细菌含有宿主所缺乏的酶,这些酶可以代谢这些纤维并促进SCFA的产生。大量研究表明,外源性短链脂肪酸(尤其是丙酸和丁酸)对糖尿病样表型的啮齿动物模型有益。然而,1型和2型糖尿病临床试验的证据尚不明确。
在结肠中,短链脂肪酸(SCFA)通过与GPCR和游离脂肪酸受体2和3结合激活肠内分泌细胞(EEC),诱导肠道肽(主要是GLP-1和肽YY)的释放。为了支持这一发现,啮齿动物和人类补充益生元可以改善葡萄糖耐量和胰岛素抵抗,并且与肠道肽水平升高有关 。
在一项研究中,高纤维饮食改善了2型糖尿病患者的葡萄糖耐量,这种效果与粪便丁酸水平和循环GLP-1水平升高有关。GLP-1通过增加胰岛素分泌、促进胰岛素敏感性和减少肝葡萄糖生成来调节葡萄糖稳态。
此外,短链脂肪酸(SCFA)对于维持整体肠道健康和肠道屏障至关重要,因为丁酸是结肠细胞的主要燃料来源。相反,丁酸减少会促使结肠细胞进行无氧糖酵解,从而增加上皮氧合,破坏结肠的厌氧环境。
3)
肠道菌群在肠道屏障功能中的作用
肠道微生物在肠道屏障功能中起着至关重要的作用。肠道屏障受损会导致肠漏,从而引发低度全身性炎症,这是肥胖和糖尿病的特征。尽管这些机制主要在实验模型中进行研究,但导致全身性炎症的一个潜在机制是来自革兰氏阴性细菌细胞包膜的脂多糖(LPS)内毒素增加,也称为代谢性内毒血症。
肠道菌群失调会导致促炎反应,影响葡萄糖稳态
脂多糖(LPS)可以作用于全身特定的病原体相关分子模式 (PAMP) — Toll 样受体 4 (TLR4) — 从而引发促炎免疫反应,从而对葡萄糖稳态产生负面影响。一系列研究表明A. muciniphila通过作用于 TLR4 和肠道屏障,在介导肠道微生物改变对全身炎症的一些影响方面发挥潜在作用;
然而,关于其在代谢疾病中介导葡萄糖代谢作用的证据较少 。然而,还需要更多的研究来确定TLR4以外的 PAMPs 对代谢物的感知是否与调节宿主-微生物串扰和人类肠道屏障完整性有关。
与此同时,在肥胖个体的肠道中观察到促炎性巨噬细胞的积聚、CD8αβ T 细胞浸润和 IgA+ 免疫细胞减少 ,导致胰岛素抵抗。肠道菌群调节策略可以减轻高热量饮食对肠道免疫的不利影响。例如,减少促炎性巨噬细胞的比例并增加 3 型先天淋巴细胞和调节性 T 细胞与改善葡萄糖代谢有关。
尽管如此,了解驱动肠道微生物与免疫相互作用的精确分子机制及其在人类中的应用也需要未来进行广泛的研究。
Progress
在微生物组领域,将现象学与实际生物学区分开来需要工具和方法来识别机制,以解析微生物组是否是代谢疾病的驱动因素或提供治疗机会。在这里,我们讨论了推动该领域发展的最有希望的技术发展。
模型系统
在比较研究肠道微生物与代谢疾病之间关系的模型系统时,必须同时考虑传统模型(例如无菌和无菌小鼠)和新兴技术(例如器官芯片和非鼠类GF模型,如斑马鱼和猪)。
无菌模型有利于研究肠道菌群与特定疾病的关联
无菌动物已被广泛用于研究人类肠道微生物在肥胖和糖尿病中的作用。这些动物出生时没有任何微生物群,可以在没有微生物组的情况下对干预措施进行研究。因此,我们可以深入了解微生物组是否对给定的生物过程必不可少。
通过将整个肠道菌群(通过供体粪便)或特定的分离菌株定植到无菌小鼠体内,建立无菌疾病模型。研究表明,将肥胖和2型糖尿病患者粪便中的微生物接种到无菌动物体内后,无菌动物成功复制了疾病表型,这为肠道菌群与代谢疾病的关联提供了证据。
此外,从患有病态肥胖和糖尿病的人的肠道中分离出一种过度生长的产生内毒素的细菌阴沟肠杆菌B29,它在无菌 C57BL/6J 小鼠中诱发了肥胖、脂肪肝和胰岛素抵抗,而这些小鼠对高脂饮食引起的代谢缺陷具有抵抗力。敲除B29菌株中产生内毒素的基因或C57BL /6J小鼠中的Tlr4基因可预防代谢缺陷,强调了特定肠道细菌和宿主反应在代谢疾病的发生和发展中的因果关系。
然而,某些关于肠道微生物小鼠的概念一直流传,而这些概念只是研究一种基因型的结果。例如,GF C57BL/6J 小鼠对饮食诱导的肥胖具有抗性,而 GF Swiss Webster 小鼠则不能;因此,由于大多数 GF 小鼠研究都使用 C57BL/6J 小鼠,因此 GF 小鼠通常必须比传统小鼠吃得更多才能维持体重,这已成为事实。这些模型对高脂饮食的不同反应凸显了遗传背景在研究结果中的重要性。
其他GF模型(如猪和斑马鱼)的存在补充了 GF 小鼠的使用。在开发与人类微生物群相关的无菌模型时,GF 猪和仔猪比小鼠能提供更多与人类相关的见解,尽管饲养它们所需的空间对于许多机构而言过于宽裕,或限制了研究只能使用少数动物。另一方面,无菌斑马鱼已被证明可用于研究肠道微生物和不同宿主细胞发育阶段 。
鱼体的透明度、在不同细菌存在下荧光标记和成像不同细胞类型的能力,以及饲养和繁殖斑马鱼的便利性,都有利于研究特定问题。这些模型不能完全复制人类生理学,但它们允许在严格控制的条件下进行纵向和侵入性采样,这在探究机制问题时非常重要。
器官芯片利于研究人体组织内的相互作用
器官芯片(如肠道芯片)提供了更多与人类相关的系统,因为它们可以直接从人体组织或血液来源的诱导性多能干细胞中获得,这些干细胞保留了宿主的遗传特征,因此,它们使我们可以在受控环境中研究复杂的人体组织和细胞相互作用。
最近的研究已经证明了在半厌氧环境中将微生物群接种到肠道芯片中的能力,目前许多研究小组正在测试在这些芯片上接种日益复杂的群落的效率。虽然肠道芯片模型缺少一些关键的细胞类型,如免疫细胞,但重大进展包括能够连接不同的器官芯片,如肠道芯片和神经元芯片,以模拟肠脑相互作用。利用器官芯片研究微生物组的创造性方法将继续涌现,并可能填补重要的空白,补充动物模型。
了解细菌基因和功能
对细菌全基因组进行测序和组装的能力是一种非常强大的方法,可用于识别菌株的谱系和相关性,以及识别可能与人类健康或疾病相关的特定细菌表型所涉及的假定途径。如果我们思考已从基因改造小鼠研究中阐明的人类疾病机制,就不难想象在细菌中进行同样研究可以获得的大量信息。敲除和操纵细菌基因的能力并不是什么新鲜事。
近80年的细菌遗传学研究已经阐明了病原体如何在肠道上皮中定植并分泌毒素从而导致霍乱等疾病,它们如何相互共享信息以适应不同的环境,以及营养选择如何驱动它们在宿主中的组成。大肠杆菌可以被认为是 C57BL/6 小鼠的细菌版本;其基因定义明确且易于改造,而且它已经成为在特定环境下测试改造效果的主力。然而,共生肠道细菌的多样性远不止大肠杆菌;因此,研究人员正在积极寻求对肠道j基因的更深入了解,例如使用拟杆菌和梭菌作为代表性生物 ,因为大量人类和小鼠研究已经证明了这些生物在健康和疾病中的重要作用。
人工智能等先进计算工具通过预测蛋白质的三维结构,为细菌基因组中未注释部分提供了新的见解,AlphaFold2 等技术极大地推进了这一任务。通过分析这些结构,研究人员可以根据它们的形状和结合位点推断出可能的功能。这些潜在作用可以通过生化和微生物学研究中的实验验证来证实。这些知识,特别是关于蛋白质如何影响代谢途径的知识,对于将微生物活动与糖尿病等健康状况联系起来至关重要,有助于深入了解疾病机制和潜在的治疗靶点。
无参考数据分析
目前,微生物组测序分析中依赖数据库的方法最关键的问题是它们在检测新型或研究不足的微生物方面存在局限性。当使用基于已充分表征的细菌的参考基因组的数据库分析微生物群落样本时,不匹配的序列会被忽略或错误分类。
这一过程导致对微生物生态系统的看法出现偏差,可能会遗漏在健康和疾病(包括糖尿病)中发挥重要作用的关键成分。因此,推进微生物组研究需要开发和使用能够发现和表征这些代表性不足的微生物实体的方法。
从宏基因组测序数据中从头组装基因组是微生物组研究中一种强大的方法,该方法涉及直接从测序读取构建基因组,而不依赖于参考数据库。
该方法使用先进的计算算法将样本中的 DNA 片段拼凑在一起,从而可以识别来自各种生物体的遗传物质,包括那些以前未测序或编目的生物体。通过组装这些基因组,研究人员可以发现新物种并揭示新的基因功能,从而大大扩展我们对微生物多样性及其在包括人体在内的各种环境中的潜在作用的理解。
对于16S测序来说,由于其经济和丰富的样本积累,对于构建疾病的大数据库来说存在很大的优势,虽然16S分辨率没有宏基因组高,但是通过方法和技术的弥补,可以大大提供16S的预测精准度。
例如谷禾健康结合宏基因组数据和已有的菌群构成数据,通过算法可以大大提高扩增子数据的物种分辨率。此外病毒、真菌、寄生虫和部分16S难区分的病原菌目前通过增加靶向引物进行tNGS的方式来实现,大大拓展了二代测序微生物多样性检测领域的涵盖范围。
这种方法在揭示微生物生命的全部范围方面特别有用,包括可能在健康和疾病中发挥关键作用的物种或基因。
了解小肠微生物群
小肠是营养吸收、肠肝循环和承受肠道激素刺激的主要部位;因此,深入了解人体这一部位的微生物功能至关重要。然而,我们对人类微生物组的大部分了解都基于粪便样本和结肠微生物群,因为即使使用现代内窥镜检查方法,获取小肠微生物群也很困难。
最近的进展使用了创新方法,例如可摄入的胶囊,它可以对整个胃肠道中的肠道物质进行取样。由于每个胶囊都由肠道中不同的 pH 值触发,因此这种方法可以提供肠道群落的微生物图谱。这些工具正在进一步完善和商业开发,以用于诊断和研究。但需要注意的是,样本采集到胶囊内后,微生物有可能继续生长,因此不能准确地代表原生微生物群落。
此外,这些胶囊和其他胶囊都是为空腹状态下的取样而开发的,因此对餐后反应的研究仍然有限,尽管这些反应对于全面了解微生物对葡萄糖代谢调节的贡献可能很重要。解决这些问题对于确保使用此类设备进行微生物组研究的可靠性和准确性至关重要。
同工酶和小分子筛选
微生物组研究中,同工酶和小分子筛选对于识别可以作为治疗目标的特定细菌产物至关重要。微生物同工酶是具有不同分子结构但催化与宿主酶相同反应的酶。筛选这些产物可以揭示微生物代谢的变化,这些变化可能会影响健康并可能干扰药物治疗,例如细菌 DPP-4 同工酶的情况。
小分子筛选专注于识别微生物产生的生物活性化合物 。这些化合物可对宿主的病理生理学产生显著影响。通过识别特定的同工酶和小分子,研究人员可以针对它们进行降解或增强,从而为糖尿病等疾病提供潜在的治疗策略。
Treatment
如上所述,目前尚未发现针对1型或2型糖尿病的诊断性和广义的粪便微生物群分类学特征。因此,未来的研究应转向在大规模前瞻性人群中进行菌种和菌株水平的研究,并在可能的情况下,重点研究胃肠道肠道微生物的功能分析,特别关注稳定同位素前体,以研究不同胃肠道区域重要微生物代谢物的生成和底物通量。
1
高纤维饮食和基于短链脂肪酸的治疗
关于基于肠道菌群的糖尿病疗法,高纤维饮食已被证明可有效控制1型和2型糖尿病患者的血糖水平并降低胰岛素抵抗。尽管膳食纤维通过肠道菌群直接起作用的方式仍有待证实,但这些试验强调了将肠道菌群调节策略纳入糖尿病干预试验的潜在重要性,特别是对于生产有益代谢物(如 SCFA)而言。
但是,如上所述,口服短链脂肪酸(丁酸盐)补充剂的干预试验并未显示在1型或2型糖尿病患者的血糖控制或其他糖尿病调节标志物上 ,可能是因为给药部位与内源性产生不同。对于其他短链脂肪酸,包括丙酸盐和乙酸盐,数据太少,无法得出关于对代谢调节的可能影响的任何结论。
2
传统益生菌和新一代益生菌
用于糖尿病的益生菌疗法可分为传统益生菌,特别是乳酸杆菌和双歧杆菌菌株,它们历来被用于发酵食品或补充剂中以促进健康,以及下一代益生菌,它们是最近被鉴定为人类肠道菌群成员的新菌种菌株。这些菌株与健康有关,但在疾病环境中存在会减少。
传统益生菌
关于传统益生菌,一项关于益生菌(双歧杆菌、乳酸杆菌和唾液链球菌菌株)的开放标签试验发现,益生菌对1型糖尿病患者的兄弟姐妹的1型糖尿病易感性和进展有益。
针对新发1型糖尿病的前瞻性随机对照试验 (RCT) 正在进行中(NCT03961854、NCT03961347、NCT04769037 和 NCT05767450),一项规模较小的试验显示,其对长期 1 型糖尿病仅有中等效果。
在2型糖尿病中,最近的一项荟萃分析描述了这些益生菌菌株在代谢控制和降低胰岛素抵抗方面具有一定功效。
新一代益生菌
关于下一代益生菌,在人体中产生的数据较少。例如,尽管特定菌株(例如Akkermansia)与健康的代谢表型相关,但使用A. muciniphila的 RCT 干预并未发现强烈的代谢影响。
这一发现可能是由于这些测试菌株与代谢综合征缺乏因果关系、通过胃后活力降低、剂量不足或引入人体肠道时缺乏定值。
由于小肠对1型和2型糖尿病的病理生理学都很重要,因此需要进一步分析1型和2型糖尿病患者的小肠微生物群,并研究确定的下一代益生菌菌株组合作为糖尿病的可能干预措施。然而,这种努力应该考虑细菌菌株的植入条件、对其他细菌成员的生态或功能依赖性、以及功能上的潜在冗余。
3
供体粪菌移植
在完成针对特定菌株组合的研究之前,供体粪菌移植(FMT)可能有助于了解调节肠道菌群的效果以及这种调节对糖尿病病理生理和潜在可逆性的影响。
最近发表了一项研究,探新鲜粪菌移植在维持残余β细胞功能和抑制新发1型糖尿病患者自身免疫方面的功效。其他针对 2 型糖尿病和胰岛素抵抗的研究显示,FMT 对胰岛素抵抗和非酒精性脂肪肝疾病有适度影响 ,而一项研究表明对这些参数没有影响。
此外,微囊供体 FMT 和纤维补充的联合干预显示出对葡萄糖代谢有益的影响,这表明干预设计不仅需要合成菌株联合体,还需要饮食支持(例如纤维来滋养菌株)。最后,评估生活方式干预后自体 FMT 是否有助于防止体重反弹的研究发现,饮食引起的低丰度细菌变化可能是维持减肥效果的原因,这可以指导更精准的干预措施,减少伦理负担,降低传播疾病的风险。
总体而言,与针对性菌株或代谢物的干预措施相比,供体 FMT 是一种更为分散的方法。此外,现有数据集中的粪便物质给药方式(胶囊与新鲜 FMT)、肠道 pH 值(例如由于抗酸药)和结肠转运时间存在差异,并且施用的粪便微生物群的数量似乎也会影响供体细菌菌株的植入。
关于糖尿病和基于肠道菌群的疗法的试验结果,使用随时间动态测量葡萄糖代谢(例如混合餐测试或连续血糖监测)可以更好地了解在 FMT 和施用确定的菌株组合期间肠道微生物、饮食和葡萄糖稳态之间的相互作用。
对小肠微生物组的研究仍不足,但对肠道微生物的新认识越来越多地将其与人类糖尿病联系起来。对人类 FMT 的干预研究已经能够从因果关系中分离出关联,并且确实显示出一些临床益处,虽然平均而言相对较小的治疗效果和伦理问题阻碍了这种治疗方法在糖尿病临床护理中的广泛实际应用。
因此,还需要在多民族队列中对肠道菌群和糖尿病之间的前瞻性关联进行更多研究。与此同时,还应探索合成的肠道菌群衍生的细菌菌株或群落和工程系统在糖尿病中靶向肠道输送已识别代谢物的治疗潜力。
Perspectives
在过去二十年中,肠道微生物的改变与糖尿病患者的异常葡萄糖代谢和脂肪变性有关。流行病学研究中的较大样本量现已开始显示肠道菌群与肥胖或2型糖尿病相关的人类代谢特征之间的相关性的大小和可能的一致性;然而,对于1型糖尿病,情况就不那么明朗了。
未来的研究应更严格地考虑糖尿病药物与种族和饮食摄入之间的相互作用。此外,近年来,人们对肠道菌群的功能有了更多的了解,而不仅仅是其成分,这些信息与之前关于特定代谢物(包括短链脂肪酸、支链氨基酸和胆汁酸)与肥胖和糖尿病之间联系的报告非常吻合。
关于肠道菌群成分,只有少数研究探讨了噬菌体和真菌的作用以及这些菌落与细菌菌株在糖尿病中的相互作用。显然,未来的研究还需要关注小肠微生物群的功能,以及开发足够的生物信息学流程和正确组装基因组。
我们还必须考虑到,迄今为止的大多数数据都是在小鼠研究中产生的,由于小鼠和人类在饮食、遗传和寿命方面存在巨大差异,其与人类糖尿病的相关性需要进一步证实。尽管如此,在人类糖尿病环境中对单一菌株和粪菌移植的人体干预研究表明,存在一系列临床代谢效应(与药物更一致的效果相比),但没有严重的副作用。
总之,经过近二十年的研究,我们仍然必须期待未来的努力,以阐明肠道微生物研究对人类糖尿病的临床诊断和治疗适用性。
主要参考文献
Caesar R. Pharmacologic and Nonpharmacologic Therapies for the Gut Microbiota in Type 2 Diabetes. Can J Diabetes. 2019 Apr;43(3):224-231.
Ridaura VK, Faith JJ, Rey FE et al (2013) Gut microbiota from twins discordant for obesity modulate metabolism in mice. Science 341:1241214.
Sze MA, Schloss PD (2016) Looking for a signal in the noise: revisiting obesity and the microbiome. mBio 7:e01018-16.
Duvallet C, Gibbons SM, Gurry T, Irizarry RA, Alm EJ (2017) Meta-analysis of gut microbiome studies identifies disease-specific and shared responses. Nat Commun 8:1784.
Pasolli E, Truong DT, Malik F, Waldron L, Segata N (2016) Machine learning meta-analysis of large metagenomic datasets: tools and biological insights. PLoS Comput Biol 12:e1004977.
Rothschild D, Leviatan S, Hanemann A, Cohen Y, Weissbrod O (2022) An atlas of robust microbiome associations with phenotypic traits based on large-scale cohorts from two continents. PLoS One 17:e0265756.
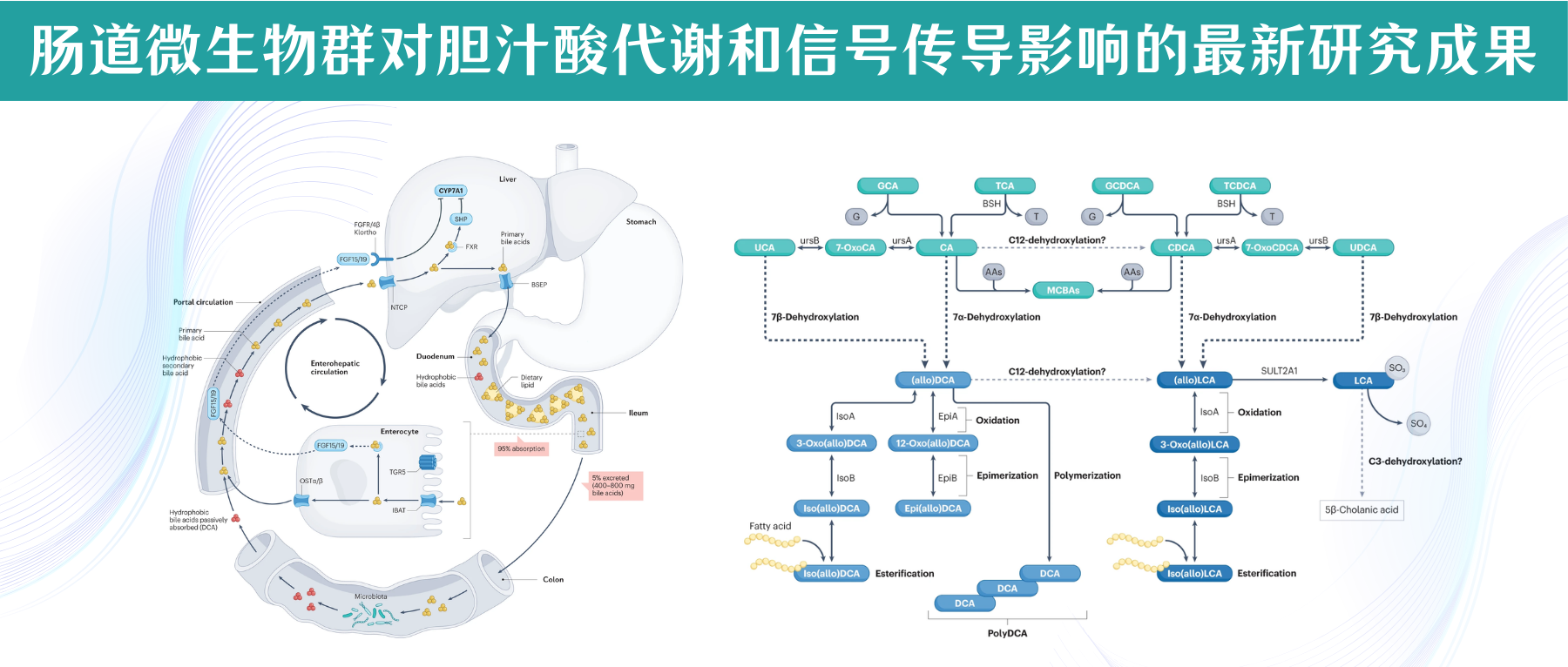
谷禾健康
消化是人体获取能量和营养的过程。膳食脂质因其在水中的不溶特性,从而导致其难以被小肠中的消化酶有效地识别和分解,而胆汁酸在脂质消化吸收中发挥关键作用,缺少胆汁酸会导致脂肪吸收不良和脂溶性维生素缺乏。
在过去,胆汁酸主要被认为是帮助消化和吸收脂肪及脂溶性维生素的消化剂。它们在消化过程中起到分解脂肪,使之能够在小肠中被水溶化和吸收的作用。
然而,随着科学研究的深入,人们对胆汁酸的理解发生了变化。胆汁酸被发现不仅仅是消化助手,它们还是强大的营养信号激素。胆汁酸通过真核生物、细菌和古细菌酶的作用进行结构调整,通过与特定的受体相互作用,如法尼醇X受体(FXR)和G蛋白偶联受体(TGR5),参与调节多种生理过程,包括脂质和葡萄糖代谢、能量平衡、炎症反应以及细胞增殖和死亡等。
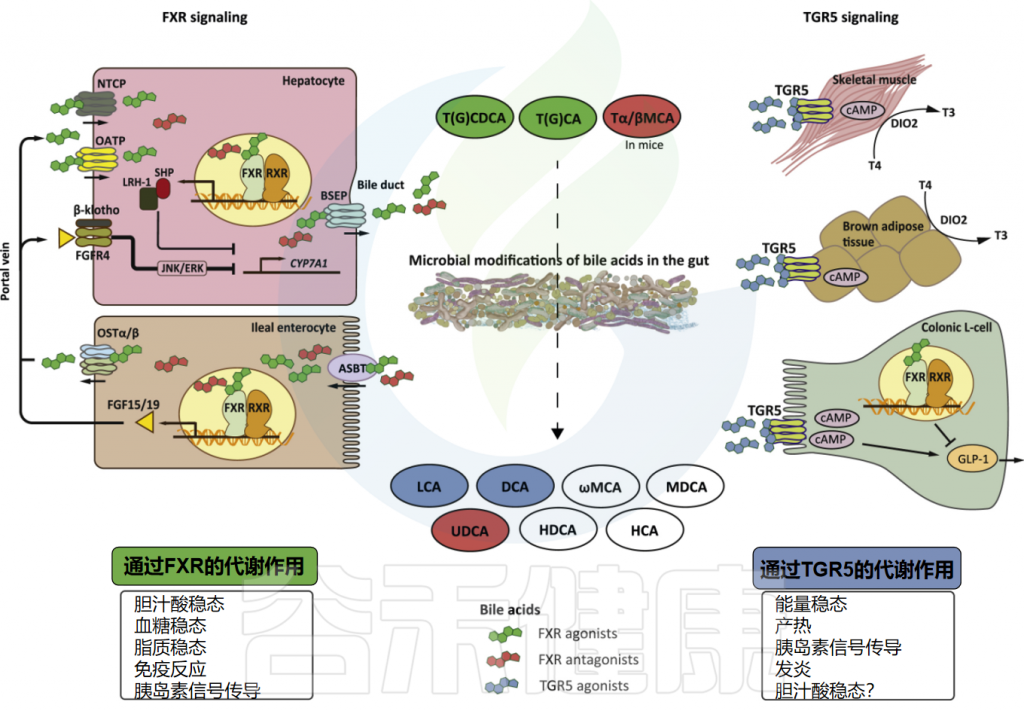
Wahlström A,et al.Cell Metab.2016
这些发现极大地扩展了我们对胆汁酸功能的认识,将其从单一的消化辅助因子转变为重要的内分泌调节因子,影响着包括胃肠道疾病和人体健康的多个方面。
在肠肝循环中,肠道微生物将来自宿主的初级胆汁酸转化为众多代谢物,即次级胆汁酸。胆汁酸的这种转化被认为是微生物与宿主之间交流的主要方式之一,同时也是宿主感知、反应并影响其共生微生物组成的关键双向互动模式。
值得注意的是,微生物代谢生成的疏水性次级胆汁酸,如脱氧胆酸(DCA)和石胆酸(LCA),成为众多宿主受体的首选配体,优于它们的原始初级胆汁酸。在过去几十年里,由于相对缺乏运动,以及偏好低纤维、高加工碳水化合物和饱和脂肪的饮食,导致胃肠道中胆汁量和胆汁酸库的疏水性增加,进而提高了人类患肝胆疾病和胃肠癌的风险。
微生物通过它们的代谢产物以独特的方式与我们沟通。在本文中,我们重点介绍了肠道微生物对一些次级胆汁酸的代谢影响。这些反应可能改变胆汁酸池以及它们的结构和功能,我们还总结了关于次级胆汁酸衍生物如何影响宿主免疫功能的最新发现。并希望通过采取相应的措施来调节受微生物代谢的胆汁酸所影响的多种人类疾病。
胆汁酸是生理清洁剂,可促进肠道吸收和运输脂质、维生素等营养物质。胆汁酸也是激活核受体和细胞通路的信号分子和炎症因子。
胆汁酸作为肝脏合成的一种重要物质,是人体胆汁的主要成分,具有多种重要作用,主要包括以下几点。
胆汁酸的结构与功能
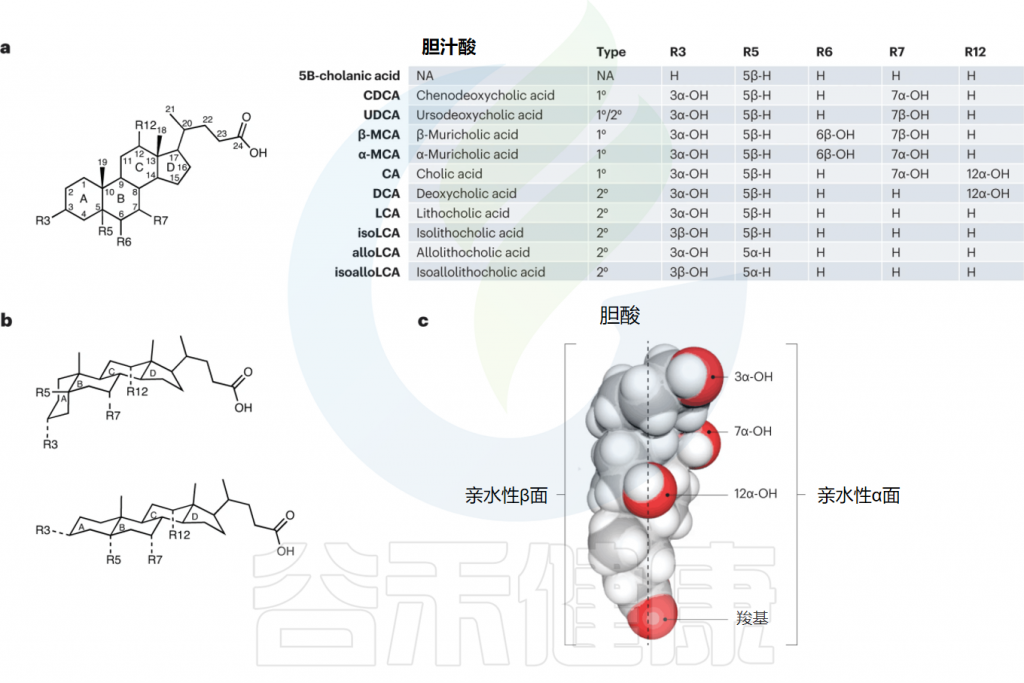
Ridlon JM,et al.Nat Rev Gastroenterol Hepatol.2024
1
促进脂质消化吸收、调节代谢
胆汁酸促进脂肪与脂溶性维生素(如维生素A、D、E、K)的消化吸收,通过乳化作用将大块脂肪球分解为细小颗粒,增加其与消化酶的接触面积,提升脂肪消化效率。
胆汁酸还激活多种核受体(例如FXR、TGR5),参与调控脂质和糖的代谢以及能量平衡,对保持代谢健康发挥着关键作用。
2
调节胆汁分泌、保护肝脏
胆汁酸参与调节胆囊的收缩,通过负反馈机制影响胆汁的储存和释放,维持体内胆汁酸水平平衡。当食物进入小肠时,胆汁酸的浓度变化会促使胆囊收缩,将胆汁排入小肠中,参与消化过程。
胆汁酸还能通过激活肝细胞核受体(FXR受体)促进肝细胞再生和修复,抑制多种促炎和促氧化应激的信号通路,减少肝脏中的炎症反应和氧化损伤,从而起到保护肝脏的作用。
3
排泄毒素、参与药物代谢
胆汁酸是肝脏排泄胆红素(血红蛋白代谢产物)和其他代谢废物的重要途径。通过与这些物质结合,胆汁酸有助于将它们从体内排出,维持体内环境的稳定。
胆汁酸还通过影响肝脏的药物代谢酶,参与药物的代谢过程,影响药物的清除速率和生物利用度。
4
调节胆固醇水平、预防胆结石
胆汁酸的合成是消耗胆固醇的主要途径之一。通过将胆固醇转化为胆汁酸,肝脏可以调节体内胆固醇的水平,有助于降低血清胆固醇,从而维持血脂平衡。
胆固醇结石形成的基础为胆固醇、胆汁酸以及卵磷脂等成分的比例失调,进而发生结晶、析出、结聚成石。而胆汁酸有助于减少胆固醇,进而预防胆固醇结石的形成。
5
免疫调节、抑制肠道中细菌的过度生长
胆汁酸通过影响肠道免疫系统,参与调节机体的免疫反应,有助于维持免疫系统的平衡。
胆汁酸具有一定的抗菌作用,能够抑制小肠中过度的细菌生长,保持肠道微生态的平衡。
胆汁酸在一些疾病中也发挥着重要作用,详细内容可见谷禾之前的文章。
胆汁酸在人体中的这些作用说明了它对于维持正常的生理功能和健康状态的重要性。然而,胆汁酸的异常代谢或积累也可能导致或加剧某些疾病,如胆石症、肝病和胆汁淤积性皮肤病等。
因此,维持胆汁酸的正常代谢与平衡对于健康极为重要。接下来,我们将重点介绍最新研究所总结的肠道微生物群对胆汁酸代谢影响的内容。
在人体复杂的生理系统中,肠道微生物群扮演着不可或缺的角色,尤其是在胆汁酸的代谢过程中。胆汁酸作为重要的消化液成分,不仅参与脂肪的消化和吸收,还与体内多种代谢途径紧密相关。
在这个过程中,肠道微生物群通过其多样化的酶系统,对胆汁酸进行一系列复杂的生物转化作用,影响着胆汁酸的结构和功能。
初级胆汁酸由胆固醇在肝细胞中合成,并通过转运蛋白BSEP分泌到胆汁中。吃饭时,胆囊会收缩,把胆汁释放至十二指肠,在那里与磷脂、脂肪酸、胆固醇及脂溶性维生素形成混合胶束,这些胶束由两亲性的共轭胆汁酸包裹。使其在通过肠细胞顶侧和底外侧的高亲和力转运蛋白通过门静脉循环转运回肝脏之前能够被吸收。
胆盐输出泵(BSEP)位于肝细胞胆小管面的细胞膜上,是胆汁酸外排最重要的转运蛋白,负责将胆盐从肝细胞输送到胆小管。
每天,数百毫克结合的胆汁酸脱离肠肝循环进入大肠,在大肠中被细菌胆盐水解酶(BSH)迅速解除结合,释放出牛磺酸或甘氨酸和游离胆汁酸。
注:胃肠道中存在几种利用牛磺酸的途径;然而,厌氧菌对牛磺酸的微生物呼吸导致硫化氢的形成,在人体研究和动物模型中硫化氢的过量形成与结直肠癌有关。
胆汁酸的反应与细菌胆盐水解酶相关
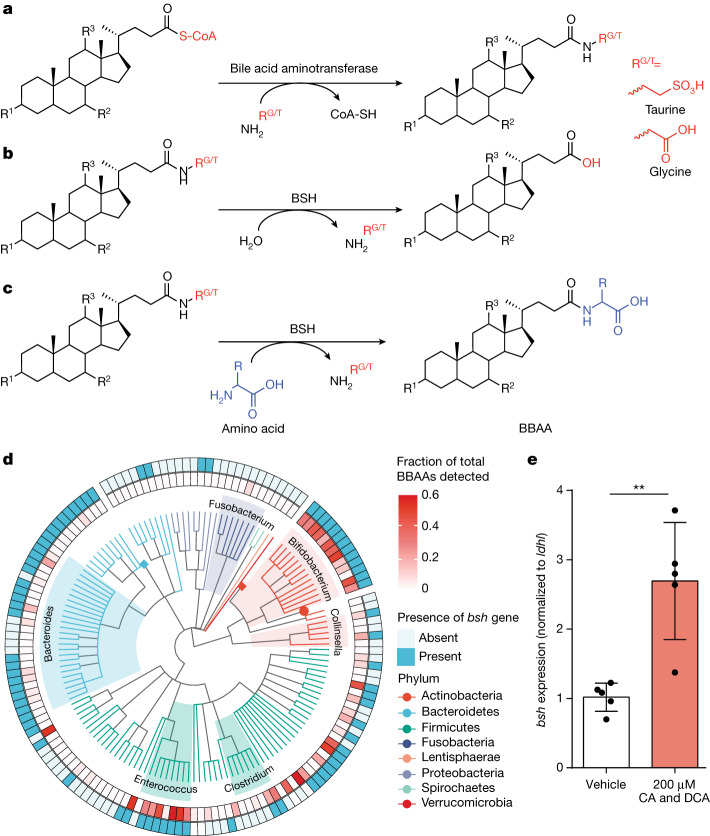
Rimal B,et al.Nature.2024
当结合胆汁酸到达回肠末端时,它们通过回肠钠-胆汁酸共转运蛋白(IBAT)转运到肠细胞中,与重组人脂肪酸结合蛋白6(FABP6)结合并通过肠细胞基底外侧表达的OSTα和OSTβ转运到门静脉循环中。
• 负反馈调节使胆汁酸水平保持稳定
作为胆汁酸合成负反馈功能的一部分,细胞内胆汁酸激活肠上皮细胞中的核法尼醇X受体(FXR),导致FGF15/19蛋白合成和分泌到门静脉循环中的上调。FGF15/19以依赖成纤维细胞生长因子受体FGFR4/β-Klortho受体的方式结合,导致肝脏胆汁酸生物合成的限速酶(CYP7A1)受到抑制。
返回肝脏的胆汁酸由牛磺胆酸共转运蛋白(NTCP)运输。肝细胞中FXR的激活抑制依赖于小异二聚体伴侣(SHP)和肝脏相关同源物1(lr h1)的CYP7A1表达。这个过程使胆汁酸水平保持在稳定状态。
• 肠道微生物改变胆汁酸的结构和功能
肠干细胞中TGR5的激活促进肠细胞的再生。大约5%的胆汁酸(每天400-800毫克)从回肠运输中逃逸并进入大肠,大肠是胆固醇排出体外的主要途径。在大肠中,胆汁酸的结构和功能因肠道微生物群而变化。这种多样化的一部分是增加大肠中胆汁酸的疏水性,允许结肠细胞被动吸收并进入门静脉循环,其中次级胆汁酸(主要是脱氧胆酸)积累到健康人体胆汁酸库的大约四分之一。
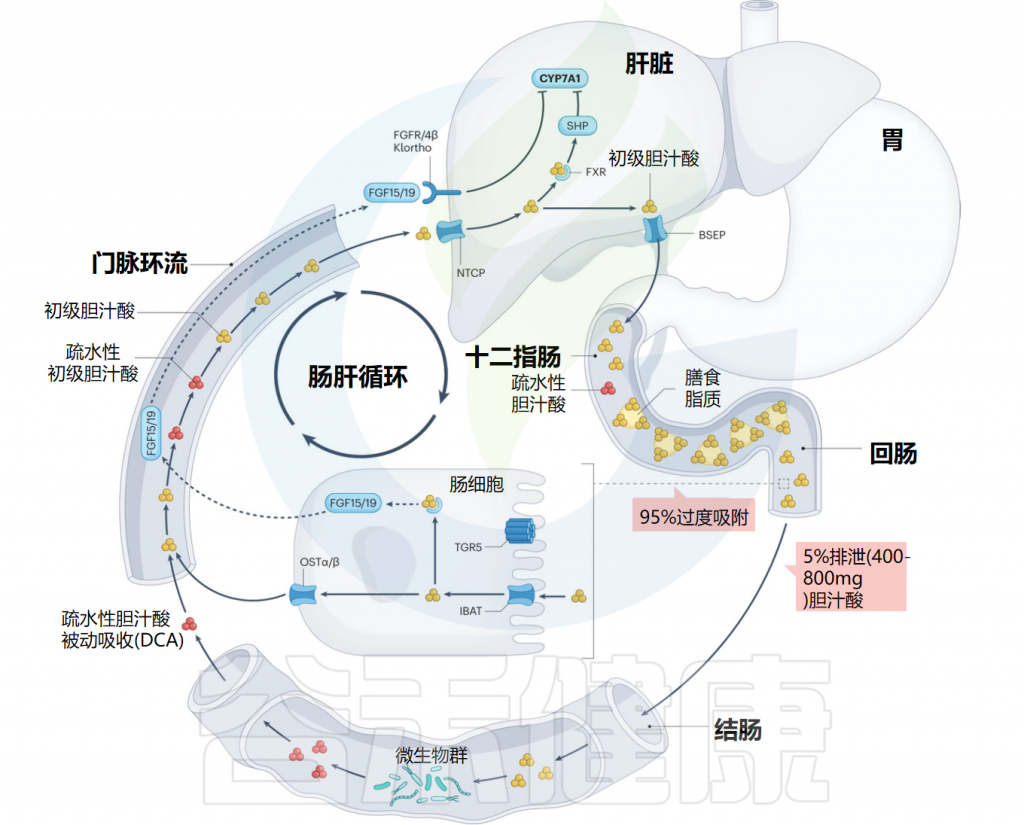
Ridlon JM,et al.Nat Rev Gastroenterol Hepatol.2024
宿主的初级胆汁酸通过肠道微生物代谢的首个证据是混合粪便细菌和微生物分离物对结合胆汁酸的解偶联。
• 众多肠道细菌中都存在胆汁酸代谢酶
胆盐水解酶(BSH)是研究最广泛的微生物胆汁酸代谢酶之一,在肠道微生物组内广泛存在,涵盖多个门类的各种物种。包括乳杆菌、双歧杆菌属和肠球菌在内的革兰氏阳性共生细菌,以及在拟杆菌属等革兰氏阴性菌,均表现出BSH活性。
哺乳动物胃肠道中常见的古细菌也表达BSH。系统发育分析表明BSH基因从芽孢杆菌(Bacillota)向肠道产甲烷菌的水平基因转移。BSH是病原体胃肠道定植所必需的,包括流产布鲁氏菌(Brucella abortis)和单核细胞增多性李斯特菌(Listeria monocytogenes)。
• 胆汁酸的检测可为胃肠道定植提供信号
结合胆汁酸的检测为胃肠道定植提供了重要的环境信号。BSH基因可能是一种定居因子,提供碳、氮、硫和能量来源的氨基酸组合;防止结合胆汁酸的去污剂特性,促进胃肠定植和持续存在;并增强细菌膜的抗张强度、流动性和电荷,保护细菌免受宿主免疫攻击。
应注意,BSH在不同分类群中发挥不同作用,且在可能的情况下,对BSH基因的同源性应通过产生突变体来确定其在细菌生理和宿主生理中的具体功能。
• BSH酶活性影响胆汁酸水平进而影响宿主代谢健康
相比之下,小肠中的BSH活性产生的非结合胆汁酸极性较低,并且通过回肠钠-胆汁酸共转运蛋白(SLC10A2)的转运效率较低,导致粪便中胆汁酸排泄增加。这种增加的胆汁酸排泄促使胆固醇更多地转化为胆汁酸或通过胆固醇反向转运回肝脏,从而降低血清胆固醇。BSH活性通过减少胶束脂质和胆固醇的重吸收以及增加粪便中胆汁酸的损失,并刺激胆固醇转化为胆汁酸,促使血清胆固醇降低。
一项针对2-7岁儿童的研究支持BSH与大环内酯类抗生素治疗引起的体重增加之间的负相关关系。最新的组学应用表明,BSH活性对宿主的生理影响可能主要通过肠道和肝脏中的细胞信号传导介导,而不仅仅是通过其洗涤剂作用和脂质吸收。
BSH活性影响宿主胃肠成熟并改变与昼夜节律、肝脏葡萄糖和脂质稳态以及免疫功能相关的肝脏和肠道基因表达。由于BSH酶在氨基酸缀合物(如甘氨酸和牛磺酸)和甾醇核底物特异性方面的差异,靶向BSH酶的子集可能是实现特定临床结果所需的。大规模宏基因组调查揭示了BSH基因与人类慢性病之间的联系,提示需要进一步的功能表征。
针对BSH酶的特异性抑制剂已被开发,对这些酶的不同亚群的药理学抑制的进一步改进可能对人类疾病和动物生产都有治疗作用。
肠道微生物产物能调节胆汁酸在肝脏的结合,展现出潜在的治疗优势。”三级胆汁酸”一词用以指代由二级胆汁酸在肝脏代谢后形成的特殊胆汁酸。
• 一些“三级胆汁酸”具有抗糖尿病效果
二级胆汁酸石胆酸(LCA)的II期代谢可产生三级胆汁酸3-磺基石胆酸。此外,石胆酸的微生物转化及其在回肠的吸收也促进了肝脏中其他胆汁酸的硫酸化。2021年的研究显示,接受部分袖状胃切除手术的人和小鼠粪便中,石胆酸诱导了7-硫酸胆酸的增加,这种胆酸是肠道特异性TGR5激活剂,能刺激胰高血糖素样肽1的释放,具有抗糖尿病的效果。
肠道微生物通过表达芳基硫酸酯酶,能从三级胆汁酸移除硫酸盐,这一过程与Peptococcus, Clostridium, Pseudomonas和Fusobacterium有关。但是,参与的微生物硫酸酯酶的具体身份还未确定。
肠道微生物群也可能在肠道内进行胆汁酸的硫酸化,这一机制过去被认为完全依赖宿主酶。如果这一假设得到验证,细菌对胆汁酸的硫酸化作用将淡化二级胆汁酸与三级胆汁酸之间的区别。
“异二级胆汁酸”(是一类特殊的胆汁酸,它们在化学结构上与常见的二级胆汁酸有所不同。在正常情况下,胆汁酸主要由肝脏合成,并以初级胆汁酸的形式分泌到小肠中。当初级胆汁酸进入肠道后,部分会被肠道微生物通过各种酶作用转化为二级胆汁酸。这一过程称为胆汁酸的微生物代谢。
“异二级胆汁酸”是在这一微生物代谢过程中,通过非典型或不常见的代谢途径生成的二级胆汁酸。这意味着它们的化学结构或代谢途径与通常所见的二级胆汁酸有所区别。
研究已经发现了生成异二级胆汁酸的两种途径。
• 直接途径通过酶催化转变
我们将第一种途径称为“直接途径”,其中初级胆汁酸通过hylemon–bjӧrkhem途径转化为alloDCA或alloLCA。
在限速的7α-脱水步骤(由BaiE催化)后,形成3-oxo-4-DCA或3-oxo-4-LCA中间体。在Hylemon–Björkhem途径中,3-氧代-4-DCA通过BaiCD(胆汁酸5β-还原酶)和BaiA(3α-羟基类固醇脱氢酶)的催化还原转化为脱氧胆酸。或者,3-氧代-4-DCA可经由BaiP或BaiJ(胆汁酸5α-还原酶)和BaiA的催化还原转化为alloDCA。
• 间接途径还需要细菌参与反应
第二种途径,我们称之为“间接途径”,首先依赖于能产生DCA或LCA的胆汁酸7-脱羟基细菌,如C.scindens。在此情境下,表达3α-HSDH、胆汁酸5β-还原酶和胆汁酸5α-还原酶的肠道微生物通过代谢调节DCA和alloDCA间的平衡,通过3-氧代-4-DCA中间体的环立体化学重置,产生异二级胆汁酸。
直接与间接途径对异二级胆汁酸形成的贡献程度目前尚不明确,这可能在不同个体之间存在差异。
石胆酸(LCA)是由鹅去氧胆酸(CDCA)和熊去氧胆酸(UDCA)经C7脱羟基反应后的微生物产物,属于单羟基化胆汁酸,是脊椎动物中最主要的胆汁酸之一。
• 石胆酸是一种潜在的致癌物
作为潜在的致癌物,石胆酸能产生活性氧和DNA加合物,通过抑制DNA修复酶,发挥肿瘤启动作用,促进体外抗凋亡细胞增殖。研究CDCA或UDCA治疗胆结石期间的人类石胆酸代谢揭示,LCA经过广泛硫酸化,形成3-磺基LCA(3-sulfoLCA)。
DNA加合物是DNA片段与致癌化学物质结合形成的复合物,在科学实验中通常作为暴露的生物标注物。
• 微生物代谢可产生不属于胆汁酸的新型物质
已知LCA是VDR的强配体,能诱导磺基转移酶SULT2A1表达。LCA的硫酸化在II期代谢中形成亲水性衍生物,促进其排泄,不易被肠道吸收。肠道细菌通过表达芳基硫酸酯酶,使3-磺基LCA解偶联,释放LCA,形成宿主II期代谢与微生物解偶联的“来回”过程。有证据显示,存在一种微生物代谢路径能跳出此循环,产生不再定义为胆汁酸的产物。
• C3脱羟基是胆汁酸代谢的一种重要方式
虽然胆汁酸脱羟基研究主要聚焦于Hylemon–Björkhem途径,但也报道了包括C3脱羟基在内的其他胆汁酸脱羟反应。C3脱羟基将胆汁酸转变为5β-胆烷酸衍生物,对胆汁酸代谢谱构成特殊挑战。
研究显示,人类粪便悬浮液能将3-磺基LCA转化为异LCA、Δ3-cholenic acid和5β-cholanic acid,肠道微生物在其中可能起到了重要作用。加入万古霉素抑制了3-sulfoLCA的代谢,而选择性培养3-sulfoLCA 代谢的革兰氏阳性孢子形成细菌(如经加热和酒精处理的粪便)则不受影响。梭菌纯培养物能从3-磺基LCA产生异LCA、Δ3-胆酸和5β-胆酸。
研究报告鹅去氧胆酸在人类粪便悬浮液中转化为7α-羟基-5β-胆甾烷-24酸,显示Hylemon–Björkhem途径产生LCA不需C3脱羟基先行。需要进一步研究以确定C3脱羟基及其机制,及其胆汁酸底物范围。
★ 胆汁酸C3脱羟基可能是预防胃肠道癌症的策略
5β-胆烷酸的生理影响尚不明确,但胆汁酸C3脱羟基可能是降低胃肠道胆汁酸浓度,预防胃肠道癌症的策略之一,类似于通过肠道细菌增强胆固醇转化为粪甾醇以降低血清胆固醇的方法。
一系列5β-胆烷酸衍生物被证明有效激活FXR,比羟基化胆汁酸更为有效。肝胃肠疾病背景下,肝细胞癌原位小鼠模型使用显示,FXR激动剂与TGR5拮抗剂结合使用,显著抑制肿瘤生长。因此,确认宿主或微生物衍生的5β-胆烷酸衍生物的生理相关性应非常重要。
拓展:胆汁酸7α-脱羟基的几个关键方面
在该领域的研究中,胆汁酸7α-脱羟基化的几个关键方面已经显现出来。首先,胆汁酸C24酰胺(结合胆汁酸)不是底物。因此,胆汁酸水解是胆汁酸7α-脱羟基的先决条件。值得注意的是,BSH抑制剂确实被观察到能使宿主富含初级胆汁酸。
第二,胆汁酸7α-脱羟基作用似乎只存在于相对较少的杆菌属物种中(Ruminococcaceae, Peptostreptococcaceae, Lachnospiraceae and Oscillospiraceae)。
第三,根据胆酸转化为脱氧胆酸的相对速率,将这些物种种群分为两组(低活性与高活性),其差异相差很大,约为100倍。
第四,尽管种群数量很小,但已确定的微生物群落的复杂性从少数到100个成员不等,这表明具有bai操纵子的生物体是脱氧胆酸和石胆酸形成所必需的。
第五,微生物中的bai途径酶已经演化出对其宿主产生的内源性胆汁酸的识别能力。因此,虽然肠道微生物可以将βMCA转化为脱氧胆酸,但在无菌小鼠中定植的人类肠道微生物群却无法将胆汁酸转化为脱氧胆酸或鹅去氧胆酸转化为石胆酸,熊去氧胆酸(UDCA)是个例外,它可以通过7β-脱羟基转化为石胆酸(LCA)。
最后,bai途径是一个涉及净双电子还原的氧化还原过程,即胆汁酸充当电子受体,这一点对其演化至关重要。在结肠这样一个高度还原、厌氧的环境中,微生物需要处理还原当量,而通过还原不饱和胆汁酸的脱羟基过程,微生物在一定程度上完成了这一任务。然而,还可能有同等或更重要的潜在动机,包括但不限于通过增加有毒胆汁酸的产生和增强与宿主之间的结构性信号交流来消除对关键营养素的微生物竞争,从而提高胆汁酸生产者在肠道环境中的适应性。
• 肠道菌群通过生物转化形成微生物结合胆汁酸
下一代测序技术的兴起和计算能力的增强共同推动了肠道微生物学的快速发展。非靶向代谢组学的显著进步为化学信息学家揭示新的微生物代谢产物铺平了道路。
这种化学信息学方法已成功鉴定了微生物结合胆汁酸(MCBA),微生物结合胆汁酸(MCBA)是一类由肠道微生物群通过生物转化作用产生的化合物。在这一过程中,肠道细菌(例如Enterocloster boltaea)通过特定的酶作用,将非传统的氨基酸或其他分子与胆汁酸发生结合(酰胺化反应),从而形成MCBA。
两项新研究表明,BSH酶能够产生具有特定氨基酸序列和结合特异性的MCBA。MCBA主要在小肠产生,且BSH酶活性最高。研究表明MCBA能够通过PXR和FXR发出信号,从而影响人体代谢。
• 肠道菌群通过短链脂肪酸等酯化胆汁酸可能降低毒性
胃肠道细菌能够通过醇类、短链脂肪酸和长链脂肪酸酯化胆汁酸。据报道,乳酸杆菌、真杆菌和拟杆菌相关的胆汁酸酯化过程依赖于乙醇的添加。细菌还能产生胆汁酸脂肪酸酯,其中长链脂肪酸(如C16和C18脂肪酸)以及短链脂肪酸(如乙酸盐)与异脱氧胆酸和异石胆酸的C3位点相连。
有研究描述了DCA(脱氧胆酸)分子的C24羧基与另一个DCA分子的3α-羟基通过低聚反应形成聚酯链。这些反应被认为是一种降低排泄物中疏水性次级胆汁酸以及有毒脂肪酸和醇浓度的解毒策略。
需要注意的是,粪便样本中的胆汁酸酯测量相对较少。健康人粪便样本的比较分析显示,总胆汁酸(主要是异DCA和异LCA)的10%至30%形成了酯化物。
因此,在设计粪便胆汁酸提取方案以解决特定临床和研究问题时,考虑细菌胆汁酸结合物的多样性和数量是至关重要的。目前,方法学的进步使得我们能够鉴定新的胆汁酸代谢产物,发现新的胆汁酸代谢酶,并通过靶向微生物菌株和生化途径来改变胆汁酸代谢。
历史上,初级胆汁酸被定义为含有7α-羟基的胆汁酸,而去除7α-羟基的过程产生的胆汁酸则被定义为次级胆汁酸。如今,次级胆汁酸被认为是宿主初级胆汁酸经过微生物反应产生的产物,这包括通过微生物氧化、差向异构化和脱羟基等过程的产物。胆汁酸结构的多样性反映了胃肠道中分布广泛的细菌和古菌门中存在多种酶途径。
• 过高疏水性次级胆汁酸与胃肠道癌症和结石相关
研究表明,过高的疏水性次级胆汁酸水平与胃肠道癌症和胆固醇结石的形成有关。因此,识别出负责产生脱氧胆酸和石胆酸的肠道细菌,了解这些转化过程中产生的胆汁酸中间体,以及鉴定催化这些生物转化的酶基因和每种反应的催化机制对于解释微生物组数据和设计预防或治疗疾病的胆汁酸代谢组干预措施至关重要。
据报道,bai操纵子在体内和体外都能催化胆酸转化为脱氧胆酸。人类粪便样本中bai基因的测量现在正成为炎症性肠病和抗生素治疗中胆汁酸失调或胃肠道癌症中胆汁酸过量的标记。
• 胆汁酸的水平可以反映出一些疾病
与胃肠道癌症密切相关的疏水性次级胆汁酸(如脱氧胆酸和石胆酸)在宿主免疫功能、血清素产生、细胞信号传递、预防艰难梭菌定植、营养吸收以及抵抗肠道病毒感染方面发挥着重要生理作用。
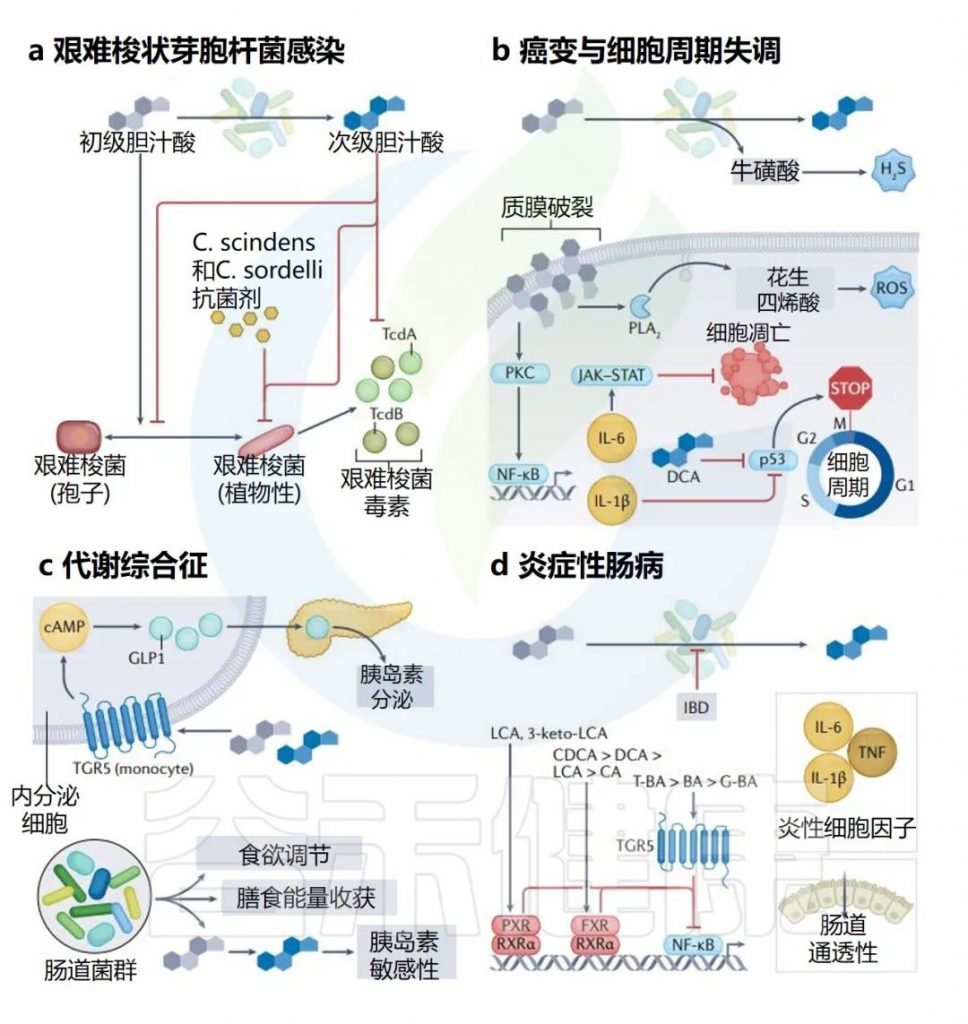
Collins SL,et al.Nat Rev Microbiol.2023
通过采用低动物蛋白和脂肪、高复合碳水化合物和纤维的饮食,可以降低肠道胆汁酸水平,保持疏水性胆汁酸的益处,同时减少因粪便中胆汁酸水平升高和脱氧胆酸富集而带来的风险。
与同龄健康人相比,肝硬化患者的胆汁酸库显著减少,7α-脱羟基胆汁酸生成细菌的丰度降低,粪便中脱氧胆酸和石胆酸含量减少,伴随有以毒性革兰氏阴性菌为特征的微生态失调。而肝硬化患者接受肝移植后,观察到胆汁酸分泌增加、粪便中次级胆汁酸含量上升、肠道微生物多样性提高和全身炎症减轻。
• 通过调节肠道菌群改善次级胆汁酸水平
粪便微生物群移植能恢复认知功能,改善炎症状况,与此同时,粪便中脱氧胆酸和石胆酸含量增加,伴随着与次级胆汁酸形成相关的革兰氏阳性菌数量增加。
此外观察到预后不佳的患者血清和粪便中次级胆汁酸水平显著降低,与次级胆汁酸生成相关的细菌基因数量减少,这些发现突显了维持疏水性次级胆汁酸和肝肠轴平衡的重要性。
人体肠道中胆汁酸的生物转化
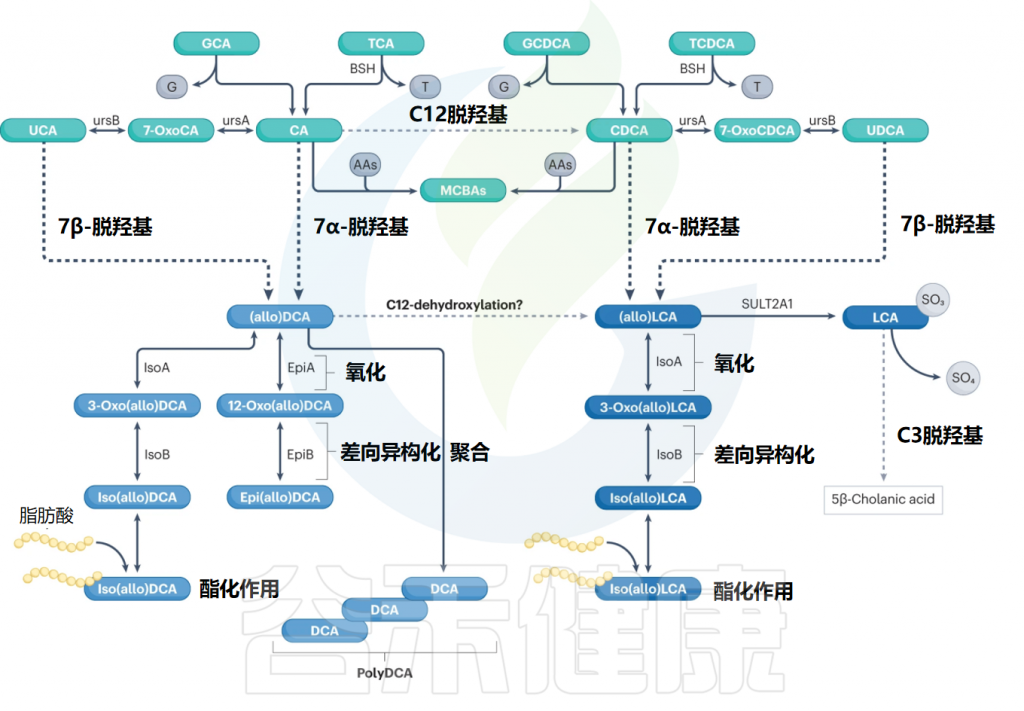
Ridlon JM,et al.Nat Rev Gastroenterol Hepatol.2024
人类结肠中参与胆汁酸代谢的细菌类群
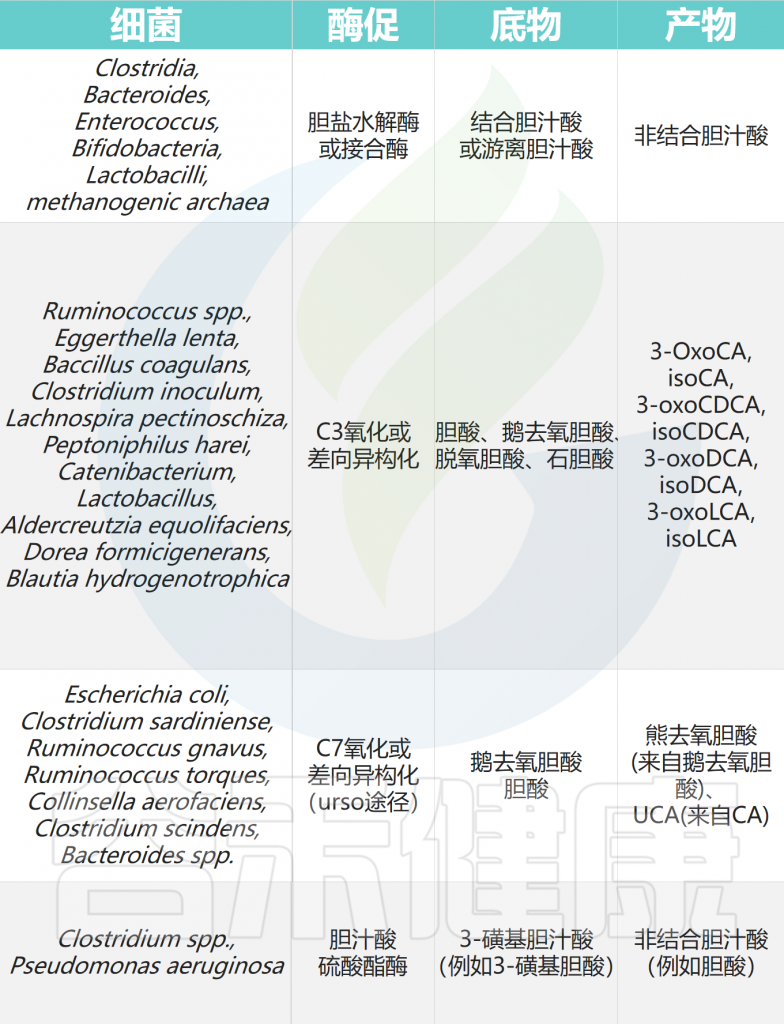
Ridlon JM,et al.Nat Rev Gastroenterol Hepatol.2024
重点:靶向微生物群-胆汁酸相互作用
作为胃肠和代谢疾病的潜在治疗方法
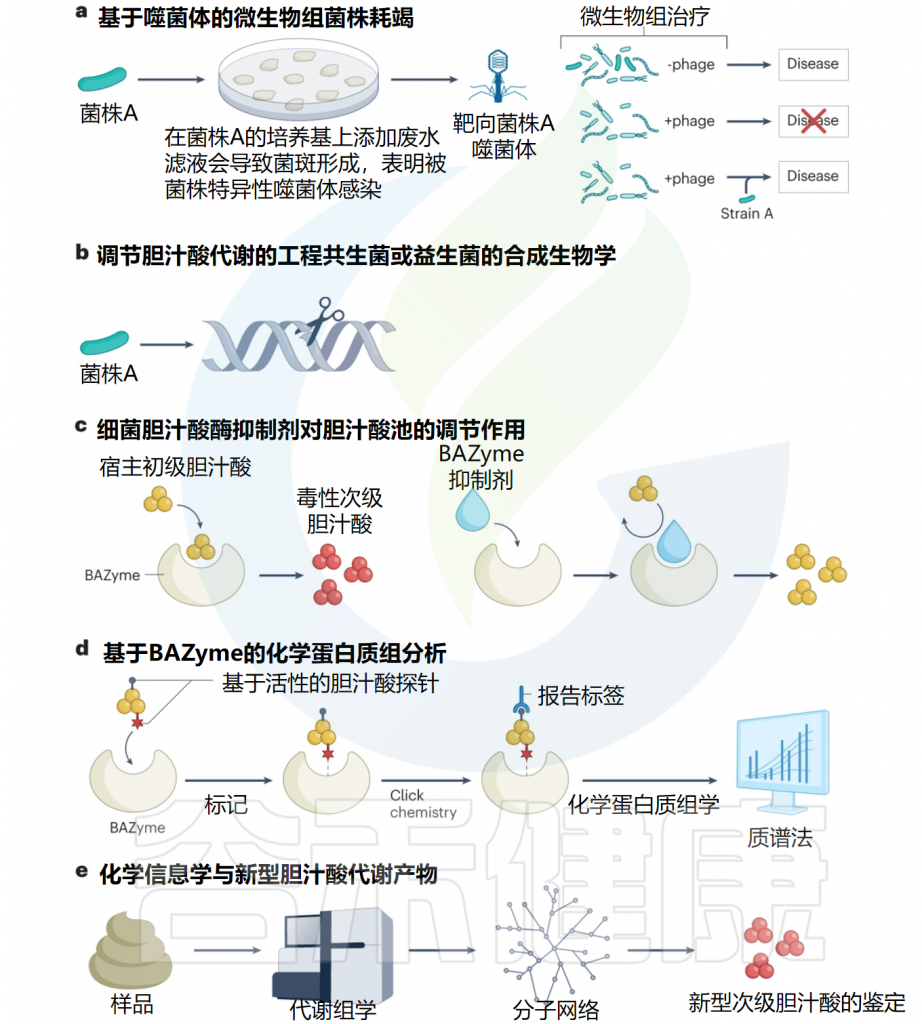
编辑
a.研究表明,选择细菌菌株依赖性噬菌体来去除在炎症性肠病等疾病中起因果作用的微生物菌株具有潜在的实用性。
b.合成生物学提供了合理设计共生菌或益生菌以调节活体胆汁酸代谢的潜力。
c.针对微生物组的特异性抑制剂的开发有望提供治疗潜力。胆汁盐水解酶(BSH)酶抑制剂的开发使人们能够探究改变胆汁酸代谢的影响。
d.使用化学胆汁酸探针的化学蛋白质组分析允许发现参与胆汁酸代谢的新型细菌酶。在胆汁酸探针与胆汁酸结合酶(BAZyme)共价结合后,蛋白质组学质谱法可以鉴定候选基因序列。
e.化学信息学将代谢组学与计算相结合,以获得代谢网络,其中一些节点代表揭示先前未知细菌代谢的新代谢产物。
胆汁酸羟基的氧化和差向异构化显著增加了胆汁酸代谢产物的多样性。早期研究发现,E.lenta、Blautia producta、Clostridium absonum、产气荚膜梭菌、副腐败梭菌、大肠杆菌、脆弱拟杆菌和瘤胃球菌等物种能够氧化和还原胆汁酸,这对于鉴定和表征编码这些酶的HSD基因至关重要。
这些过程涉及羟基在三个稳定位置(例如3α-OH、3-3-oxo氧代和3β-OH)之间的转换,由特异性和立体特异性的吡啶核苷酸依赖性HSDH酶催化。
•胆汁酸的异构化对代谢和免疫至关重要
含氧胆汁酸和胆汁酸差向异构体对生理具有重要影响。例如,7-OxoCDCA能够竞争性抑制肝脏11β-HSD2,影响糖皮质激素代谢。
研究还发现,破坏11β-羟基类固醇脱氢酶1(11β-HSD1)亚型的活性可增加饮食中普雷沃氏菌(Prevotellaceae)和西方饮食中拟杆菌(Bacteroidaceae)的相对丰度。
次级含氧胆汁酸如3-oxoLCA能够抑制胃肠道中辅助T细胞17的发育。胆汁酸和其衍生物的差向异构化,如鹅去氧胆酸和胆酸的可逆氧化及差向异构化,产生了熊去氧胆酸。熊去氧胆酸因其在治疗胆道和胃肠道疾病中的应用而具有悠久历史,是治疗原发性硬化胆管炎的一种疗法。
长期以来,次级胆汁酸与慢性炎症相关的胃肠疾病有关,包括炎症性肠病和结肠直肠癌,大量文献提供了与多种作用机制一致的数据,包括直接细胞毒性、直接DNA损伤、与NF-κB活化相关的炎症、活性氧诱导导致的细胞氧化还原平衡扰动以及通过激活各种细胞周期和炎症信号通路增强的细胞增殖。
一般认为,这些作用在不同程度上反映了次级胆汁酸的疏水性,导致宿主细胞的膜损伤,以及它们通过与细胞表面和核受体的相互作用激活许多细胞信号级联。还有大量报道称次级胆汁酸在离体和体外系统中发挥抗炎和免疫抑制反应。
“
通过微生物和宿主细胞控制次级胆汁酸的代谢可能是防止局部炎症的一种方式
如前所述,现在很清楚的是,通过多种酶促途径,肠道微生物群能够产生高度多样化的次级胆汁酸代谢组,由于分析技术不完善和缺乏次级胆汁酸含量较低的化学标准,很少对其衍生物进行测量。
正是这种多样的次级胆汁酸代谢组整体上可能有助于设定结肠中的炎症张力和肿瘤细胞生长的调节。需要更多的工作和新的组织和细胞工程方法来更完整和准确地了解次级胆汁酸代谢组如何促进局部炎症和生长控制。有了这些新知识,就有可能确定一系列无害的方法,通过微生物和宿主细胞来控制次级胆汁酸的共代谢,以防止局部炎症或恢复正常生长控制。
尽管如此,通过使用一种无菌小鼠,微生物工程和各种基于组学的方法,一些以前被忽视的胆汁酸衍生物的贡献正在出现新的见解,这些衍生物似乎可以调节致病性TH17炎症和具有抗炎特性的Treg细胞之间的平衡;简要总结如下。
“
石胆酸的衍生物对T细胞具有关键调节作用
研究通过在TH17细胞或Treg细胞分化条件下的体外试验中筛选30种初级和次级胆汁酸代谢产物的文库,发现了两种LCA衍生物——3-oxoLCA和isoalloLCA——对小鼠原始CD4+T细胞分化具有关键调节作用。
具体来说,3-oxoLCA能够抑制TH17细胞的分化,表现为IL-17a表达的减少,而异alloLCA则增强了Treg细胞的诱导,表现为FOXP3表达的增加。
FOXP3是一种调节性T细胞特异性转录因子,主要在调节性T细胞中表达,被认为是调节性T细胞的主要标志物之一。
进一步的研究表明,3-oxoLCA通过直接与关键转录因子视黄酸受体相关孤儿受体γt(RORγt)结合来抑制TH17细胞的分化,而异alloLCA则通过增强线粒体活性氧的产生来促进Treg细胞的分化,进而增加FOXP3的表达。
“
其他次级胆汁酸对TH17细胞和Treg细胞的调节作用
之前的研究已经表明,多种氧化甾醇能够与RORγt转录因子相互作用,这为3-oxoLCA通过直接与RORγt结合来抑制TH17细胞分化提供了先例。与此同时发布的其他研究进一步强调了次级胆汁酸在调节TH17细胞和Treg细胞分化中的重要作用。
研究发现石胆酸(LCA)和3-oxoLCA通过与核受体VDR相互作用调节表达RORγ+的FOXP3+Treg细胞的证据。通过筛选在小鼠和人类中发现的主要去偶联胆汁酸在体外提高Foxp3诱导能力的研究中,还发现异DCA(脱氧胆酸)通过降低树突状细胞的免疫刺激特性,从而增加Foxp3的诱导。
异DCA增强Treg细胞的生成依赖于树突状细胞中FXR的表达,这为异DCA与FXR在髓系细胞中相互作用的参与提供了证据,并可能有助于在小鼠肠道中诱导外周的Treg细胞。
次级胆汁酸异等位LCA通过与核激素受体NR4A1相互作用增强Treg细胞的分化,激活了Foxp3基因的转录,并在肠道拟杆菌门中鉴定了一个生物合成基因簇,该基因簇将3-oxoLCA转化为异等位。
通过分析HMP2 IBDMDB队列中132名参与者(包括克罗恩病、溃疡性结肠炎患者及对照组)的粪便样本的代谢组学和宏基因组图谱,发现炎症性肠病患者中异alloLCA及其生物合成基因显著减少。
值得注意的是,在HMP2队列的代谢组学数据中,与对照组相比,克罗恩病和溃疡性结肠炎患者中异alloLCA的倍数变化是所有已鉴定胆汁酸中最大的。
次级胆汁酸衍生物对炎症和免疫细胞分化及功能的调节
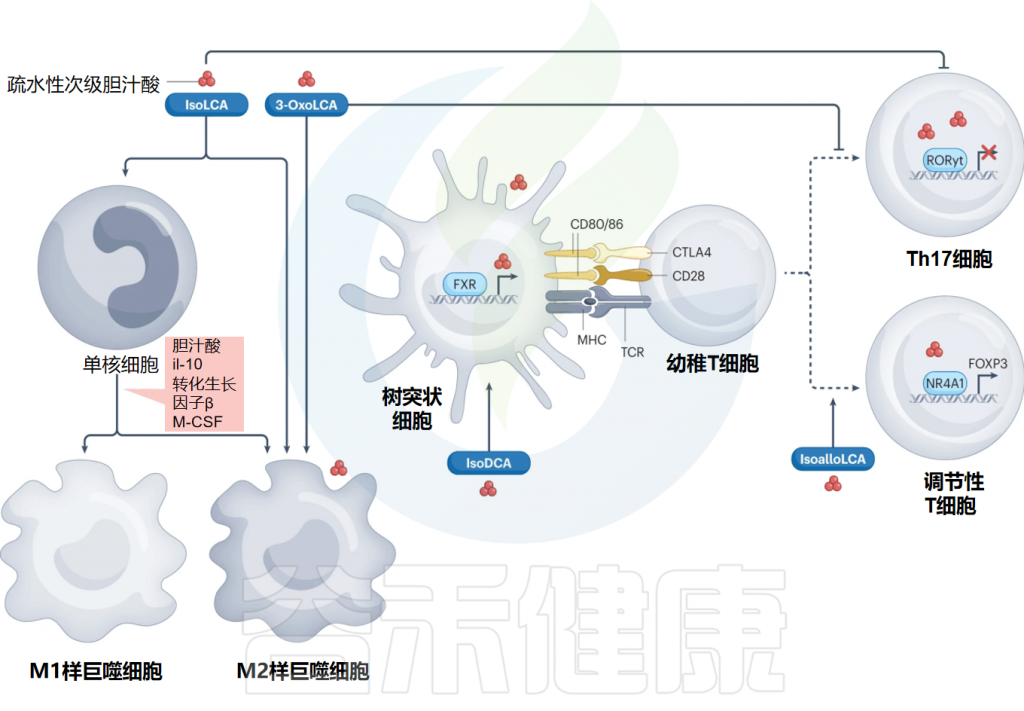
Ridlon JM,et al.Nat Rev Gastroenterol Hepatol.2024
小结
数据揭示了特定次级胆汁酸衍生物对巨噬细胞前体的分化、树突状细胞的抗原呈递能力以及CD4+T细胞早期分化过程有着不同的作用,这对胃肠道炎症的调节产生影响。
简而言之,异石胆酸(isoLCA)和3-oxoLCA影响巨噬细胞的极化状态,异脱氧胆酸(isoDCA)通过诱导树突细胞中FOXP3的表达来减弱其免疫激活特性,平面型异石胆酸通过与核激素受体NR4A1相互作用促进调节性T细胞(Treg)的分化,激活FOXP3基因的转录,而3-oxoLCA则抑制辅助性T细胞17的分化。
因此,多项研究证明了次级胆汁酸衍生物通过调节TH17细胞和Treg细胞之间的平衡,有效地影响肠道的炎症状态。
本文讲述了有关肠道微生物群对胆汁酸代谢和信号传导影响的最新研究进展,包括胆汁酸的水解、氧化、差向异构化以及C3脱羟基作用等。还介绍了异二级胆汁酸和三级胆汁酸等特殊胆汁酸的产生方式和作用。
特别强调了这些微生物修饰的胆汁素代谢产物与人类健康及疾病之间的联系,尤其是在免疫功能方面。考虑到胆汁酸在调节葡萄糖、脂质和能量代谢中的作用,它们可能成为肠道微生物群与代谢疾病之间联系的基础,包括肥胖、糖尿病和代谢功能障碍相关的脂肪性肝病。
了解肠道微生物对胆汁酸的多重作用,所获得的知识将推动基于微生物组的新干预措施的发展,通过调控胆汁酸库,以预防和治疗胃肠道疾病甚至是更多人类疾病。
主要参考文献
Ridlon JM, Gaskins HR. Another renaissance for bile acid gastrointestinal microbiology. Nat Rev Gastroenterol Hepatol. 2024 Feb 21.
Rimal B, Collins SL, Tanes CE, Rocha ER, Granda MA, Solanki S, Hoque NJ, Gentry EC, Koo I, Reilly ER, Hao F, Paudel D, Singh V, Yan T, Kim MS, Bittinger K, Zackular JP, Krausz KW, Desai D, Amin S, Coleman JP, Shah YM, Bisanz JE, Gonzalez FJ, Vanden Heuvel JP, Wu GD, Zemel BS, Dorrestein PC, Weinert EE, Patterson AD. Bile salt hydrolase catalyses formation of amine-conjugated bile acids. Nature. 2024 Feb;626(8000):859-863.
Mancin L, Wu GD, Paoli A. Gut microbiota-bile acid-skeletal muscle axis: (Trends in Microbiology, corrected proof). Trends Microbiol. 2023 Mar;31(3):322.
Garcia M, Thirouard L, Sedès L, Monrose M, Holota H, Caira F, Volle DH, Beaudoin C. Nuclear Receptor Metabolism of Bile Acids and Xenobiotics: A Coordinated Detoxification System with Impact on Health and Diseases. Int J Mol Sci. 2018 Nov 17;19(11):3630.
Pushpass RG, Alzoufairi S, Jackson KG, Lovegrove JA. Circulating bile acids as a link between the gut microbiota and cardiovascular health: impact of prebiotics, probiotics and polyphenol-rich foods. Nutr Res Rev. 2022 Dec;35(2):161-180.
Frisch K, Alstrup AKO. On the Evolution of Bile Salts and the Farnesoid X Receptor in Vertebrates. Physiol Biochem Zool. 2018 Mar/Apr;91(2):797-813.
Cai J, Sun L, Gonzalez FJ. Gut microbiota-derived bile acids in intestinal immunity, inflammation, and tumorigenesis. Cell Host Microbe. 2022 Mar 9;30(3):289-300.

谷禾健康

你是否有时会感到心悸、心慌、胸闷、气短、头晕、乏力?你是否有时感觉自己的心跳过快或过慢?
如果有上述情况,就要引起重视了,你可能存在心律失常。心律失常是最常见的心脏疾病之一,涉及到心脏的电活动节奏异常。根据发病机制和心电图特征被可以为不同类型,包括窦性心律失常、房性心律失常和室性心律失常。
长期熬夜,不健康的饮食,吸烟酗酒,压力大,过度劳累等各种因素都导致心律失常发病率越来越高和越来越年轻化。
与此同时,新冠肺炎的爆发也引起了人们对心律失常的关注。心律失常的治疗和预防,对于维持心脏健康和预防并发症的发生具有重要意义。
已有大量证据表明肠道微生物群及其代谢物对心血管健康具有重大影响,这为心律失常的治疗和预防带来了新的思路。

本文我们讨论了肠道微生物及其代谢物如何通过多种机制影响心律失常。目前公认的心律失常机制,包括结构重塑、电生理重塑、神经系统调节异常以及其他与心律失常相关的疾病。
最后介绍了与肠道微生物群相关的潜在的治疗策略,包括使用益生菌和益生元、粪便微生物移植和免疫调节剂等。
目录
1.了解心律失常
-心律失常的症状
-心律失常的分类
-发病率及高发人群
-心律失常的风险因素
2.心律失常患者的肠道微生物特征
-房性心律失常患者的肠道微生物
-室性心律失常患者的肠道微生物
-肠道菌群代谢物对心律不齐的影响
3.肠道微生物失调和心律失常的发生
-结构改造
-电生理重塑
-神经系统调节
4.其他疾病与心律失常的关系
-胃肠道疾病易诱发心律失常
-房颤患者易得胃肠道疾病
-与心律失常相关的其他疾病
5.心律失常的治疗
-饮食调整:多吃有益的脂质和膳食纤维
-补充益生菌、益生元
-药物与肠道微生物的相互作用
-粪菌移植
-免疫调节剂
-病因治疗和药物治疗
6.总结
以下是谷禾写过关于心血管疾病系列的文章,点击可查看:
-正文-
心律失常(cardiac arrhythmia)是指心脏电传导系统异常所引起的心跳不规则、过快或过慢等症状的总称。
正常心律起源于窦房结,频率60次~100次/分(成人),比较规律。窦房结冲动经正常房室传导系统顺序激动心房和心室,传导时间恒定(成人0.12~1.21秒)。
然而随着我国人口老龄化的进展和生活方式的改变,心律失常发病率快速上升,且呈年轻化和不断增长的趋势。
▼
心律失常的症状轻重不一,取决于发病的类型以及持续的时间,以及原发病的严重程度。
随着疾病的发生发展,患者发病早期可有心悸、出汗、乏力、透不过气等症状,此时,若心律恢复正常则无严重不适,若进一步发展可导致头晕、黑朦、晕厥,甚至猝死等。
▸ 心律失常可能伴随的症状
心律失常伴有明显的外周血流动力障碍时,还会出现相应器官受损的症状:
•脑:视力模糊、头晕、黑朦、晕厥等;
•胃肠道:腹胀、腹痛、腹泻等;
•肾:尿频、尿急、多尿等;
•肺:胸闷、气促、呼吸困难等。
▼
临床上根据心律失常的发生部位、机制及频率不同,可细分为许多种。
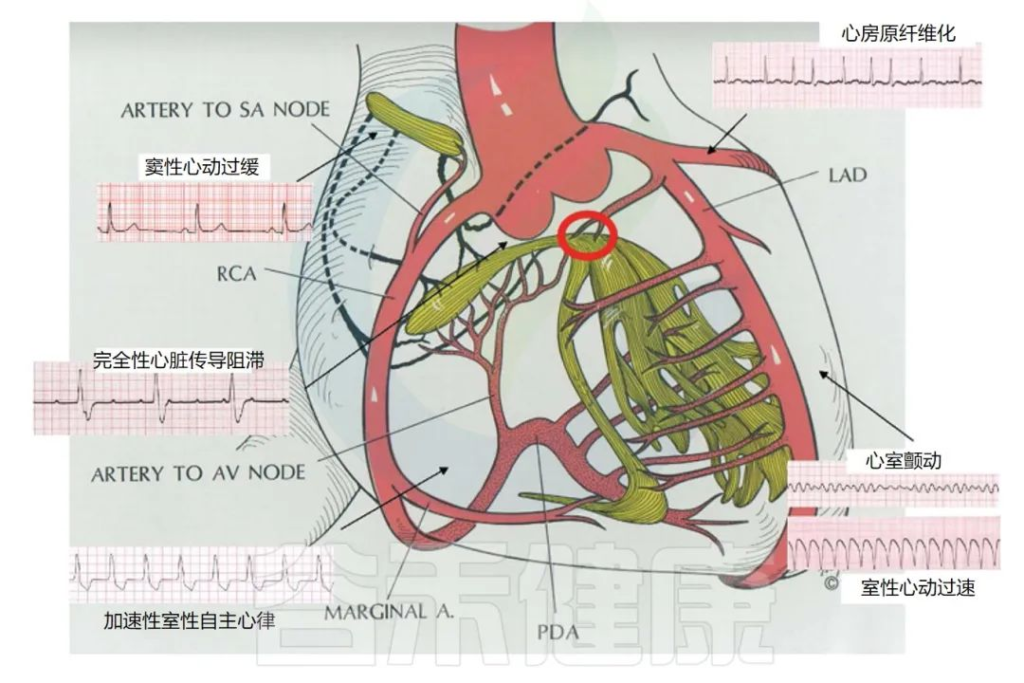
Frampton J,et al.Yale J Biol Med.2023
▸ 根据发病部位区分
按照心律失常发病部位可以分为窦性心律失常、房性心律失常、交界性心律失常、室性心律失常和束支心律失常。具体如下:
•窦性心律失常:包括窦性心动过速、窦性心动过缓、窦性停博、窦房传导阻滞、病态窦房结综合征;
•房性心律失常:包括房性早搏、房性心动过速、房室折返性心动过速、房室结折返性心动过速、房扑、房颤等;
•交界性心律失常:包括交界性早搏、交界性心动过速、房室传导阻滞等;
•室性心律失常:包括室性早搏、室性心动过速、室扑、室颤、室内传导阻滞等;
•束支心律失常:包括左束支传导阻滞、右束支传导阻滞、左前分支阻滞、左后分支阻滞等。
注:心房颤动(AF)是较为常见的心律失常。
▸ 根据发病机制区分
按发生机制可以分为冲动形成异常和冲动传导异常两大类:
•冲动形成异常:包括窦性心律失常,比如窦性心动过速、窦性心动过缓、窦性心律不齐、窦性停搏,还有异位心律失常,比如房性逸搏和逸搏心律,交界性逸搏和逸搏心律、室性逸搏和逸搏心律。
•冲动传导的异常:这种情况其实主要是包括传导阻滞,比如窦房传导阻滞、房室传导阻滞,另外还有完全性左束支传导阻滞、完全性右束支传导阻滞。
▸ 根据心律快慢区分
临床上常以心率快慢进行分类,分为快速型与缓慢型失常两大类。
•常见的缓慢型心律失常(心率<60次/分)包括:窦性心动过缓、窦性停搏、病态窭房结综合征、窦房传导阻滞。
•常见的快速型心律失常(心率>100次/分)包括:早搏、窦性心动过速、房性心动过速(心房扑动、心房颤动)、室上性心动过速、室性心动过速(心室扑动、心室颤动)等。▼
心律失常的确切发病率较难统计,根据研究数据显示,全球范围内心律失常的发病率大约在2%至4%之间,其中老年人中的患病率可能高达10%左右。
其中窦性心律不齐发病率最高,约占25%-27;窦性心动过速次之,约为20%-22%;窦性心动过缓,约13%-15%;室性早搏,约14%-16%;房颤,约11%-15%;房室传导阻滞,约5%-7%,其他各种心律失常约为5%-8%。
▸ 老年人和心血管疾病患者易发生心律失常
老年人和心血管疾病患者是心律失常的高发人群。
随着年龄的增长,心脏功能开始下降,心律失常的患病率也逐渐增加。
同时,存在高血压、冠心病、心力衰竭等心血管疾病的人群也更容易患上心律失常。
其他一些潜在因素,如家族史和遗传因素,也可能增加个体患上心律失常的风险。
▼
•年龄
随着年龄增长,心脏的功能会逐渐下降,从而增加心律不齐的风险。
•遗传
某些心律不齐类型可能与家族遗传有关,如果家族中有人患有心律不齐,那么你也可能面临较高的风险。
•心脏疾病
一些心脏疾病,如冠心病、心肌病、心脏瓣膜病等,可以增加心律不齐的风险。
•高血压
长期存在的高血压会对心脏造成损害,增加心律不齐的发生率。
•代谢紊乱
糖尿病、甲状腺功能异常等代谢紊乱疾病会对心脏功能产生影响,增加心律不齐的风险。
•药物滥用
某些药物(如某些心脏药物、精神类药物)滥用会干扰心脏的正常搏动。
•胸部手术
尤其是心脏手术、麻醉过程、心导管检查、各种心脏介入性治疗等可诱发心律失常。
此外,日常生活中也存在着很多诱发心律失常的因素,例如大量饮酒或咖啡、饮浓茶、情绪激动、剧烈运动等均可导致正常人发生快速性心律失常。
健康成年人体内存在数万亿微生物。值得注意的是,肠道微生物被称为与人类细胞基因组并列的“第二大基因组”。
几十年来,研究人员一直致力于探索心律失常的病因、机制和治疗方法。同时,不断更新的证据表明,肠道菌群不仅与人体健康和体内平衡维持密切相关,而且与包括心律失常在内的多种疾病的发生和发展密切相关。
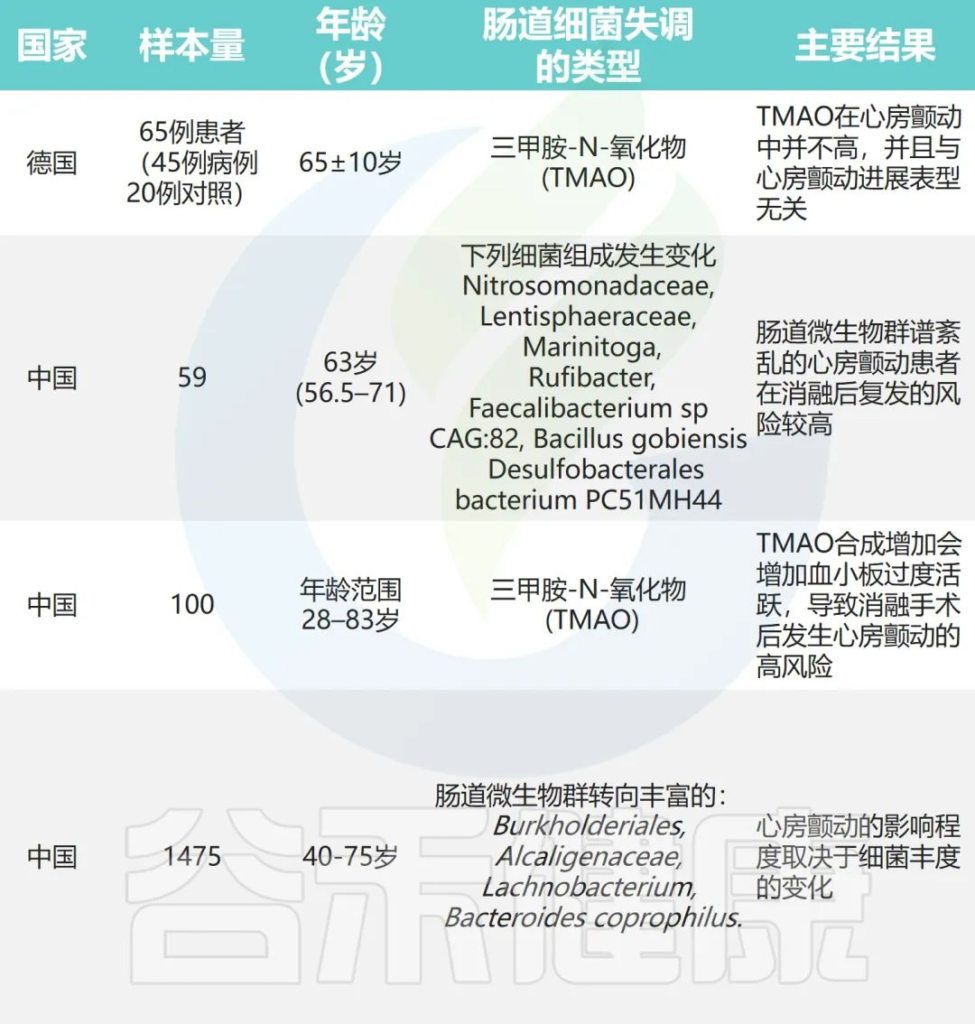


Rashid S,et al.Ann Noninvasive Electrocardiol.2023
▼
房颤,作为心律失常的一种重要类型。肠道微生物组与房颤的关系已得到初步认识,肠道微生物组及其代谢产物在心房结构重塑和电重塑方面与房颤的发生密切相关。
宏观基因组学和代谢组学分别作为研究肠道微生物组组成及其代谢物变化的重要研究工具,在探索肠道微生物组与心律失常的关系中发挥着重要作用。
最近,一些研究报告了与健康对照组相比,房颤患者中肠道微生物群变化的特征。
▷房颤患者体内有害细菌过度生长
使用宏观基因组学和代谢组学技术分析了50名健康对照者与50名房颤患者的肠道微生物群及其代谢物的组成。
研究发现,房颤患者的肠道微生物群中基因数量显著增加,样本内多样性(香农指数)也增加,这表明他们的肠道菌群具有更高的丰度和多样性。
较多的基因和属种表明房颤患者体内可能存在多种有害细菌过度生长。瘤胃球菌(Ruminococcus)、链球菌(Streptococcus)、韦荣氏球菌(Veillonella)和肠球菌(Enterococcus)等属在房颤患者中更为富集。
瘤胃球菌具有与炎症性肠病发展相关的促炎特性;链球菌在患有高血压、慢性心力衰竭和急性心血管事件的人群中也被证明是升高的。
来自日本的一项研究表明,与对照组相比,房颤患者的肠杆菌(Enterobacter)减少,而副拟杆菌(Parabacteroides)、Lachnoclostridium、链球菌(Streptococcus)和另枝菌属(Alistipes)增加。
▷胆汁酸、油酸含量显著下降
对健康受试者和房颤患者的粪便和血清样本进行代谢组学分析,其中胆汁酸、油酸、亚油酸和α-亚麻酸的含量显著降低。
研究表明,油酸、亚油酸和α-亚麻酸具有心脏保护作用,亚油酸和α-亚麻酸可以预防和终止由溶血磷脂酰胆碱或酰基肉碱引起的心律失常。
▷丁酸弧菌等有益菌的减少
心房颤动是一种进行性疾病。根据发作持续时间可分为阵发性房颤和持续性房颤。
采用宏基因组学和代谢组学相结合的分析方法来研究房颤持续时间与肠道微生物群之间的关系。
该研究包括20名健康个体、20名持续性房颤患者、12名房颤持续时间小于12个月和8名房颤持续时间大于12个月的患者。
与对照组相比,阵发性房颤组和持续性房颤组瘤胃球菌和链球菌等的丰度增加。丁酸弧菌属随病程呈下降趋势,丁酸弧菌属可产生短链脂肪酸并对宿主有有益作用。
粪弧菌属(Vibrio faecalis spp.)随时间呈上升趋势,粪弧菌可以极大地促进慢性精神分裂症患者发生冠心病。
心律失常组和对照组之间肠道微生物群的变化
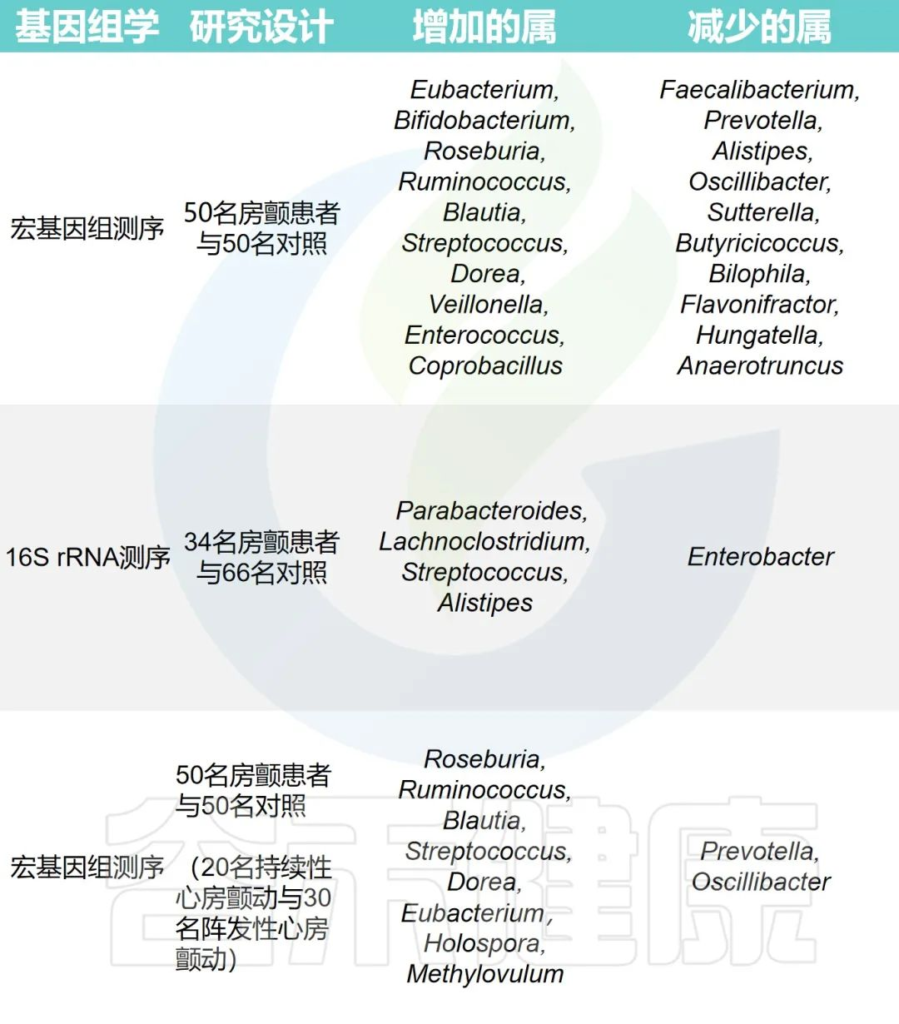

Fan H,et al.Front Cell Infect Microbiol.2023
这些证据表明,有益菌的减少或致病菌的增加以及代谢物的改变可能与心房颤动密切相关,甚至可能在心脏结构重塑中发挥关键作用。
▼
室性心律失常是临床最常见的心律失常之一。之前的一项研究发现左心室间隔或后壁厚度是室性心律失常发病率和复杂性增加的重要因素。而胎儿左心室生长可能是室性心律失常的原因之一。
▷新生儿肠道微生物多样性较低影响左心室后壁厚度
研究发现胎儿左心室生长与出生时肠道微生物群的组成有关,其中新生儿左心室后壁的厚度与肠道微生物群多样性较低有关,以及抗重塑作用相关的细菌(乳杆菌等)的耗竭和与炎症功能相关的细菌的富集(肠杆菌类等)。
肠道微生物群诱导的促炎特征在胎儿发育过程中促进心室生长,孕妇早期基于微生物群的调节可能会降低室性心律失常的发生率和不良结局。
肠道可以通过促进全身炎症和感染来影响危重患者。宿主防御机制在应激和粘膜缺氧的情况下分解,导致细菌和毒素的转移,从而通过内源性和外源性炎症反应引起心肌损伤。
▷婴儿早期室性心律失常与肠道微生物相关
根据研究,室性快速心律失常与50%至75%的心源性猝死直接相关。最近发现,与健康对照婴儿相比,在婴儿猝死综合症婴儿的肠道中发现了更高比例的艰难梭菌、Cl. innocuum和多形拟杆菌(B.thetaiotaomicron)。
多形拟杆菌(B.thetaiotaomicron)似乎介导粘膜-肠道屏障的形成,并通过其对物种特异性蛋白质抗生素表达的影响来帮助抵御病原体入侵。
致病性梭菌会破坏EC紧密连接或引发炎症反应,这两者都会损害肠壁的完整性。因此,婴儿早期室性心律失常可能与异常肠道微生物的建立有关。对于婴儿的健康和早期发育,创造健康的肠道微生物被认为是至关重要的。
▼
肠道微生物代谢就会产生生物活性代谢物,这些代谢物可以直接或间接影响宿主的生理过程。
肠道微生物群衍生的代谢物可以被宿主肠道吸收,影响肠道免疫细胞,并在宿主循环中检测到。它们充当信号分子影响重要的代谢途径。一些代谢物已被证明可以调节心律不齐的促进机制。
肠道微生物群衍生代谢物对心律失常的影响
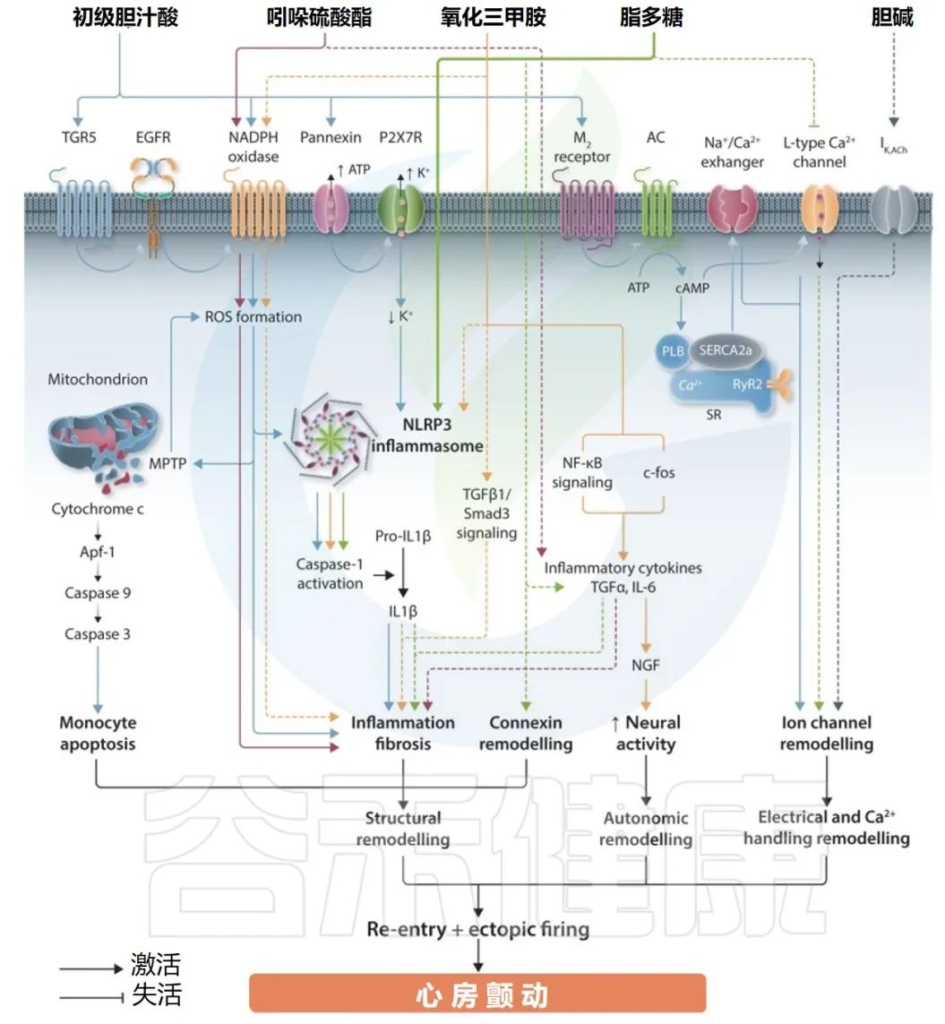
Gawałko M,et al.Cardiovasc Res.2022
1
氧化三甲胺
氧化三甲胺(TMAO)是含有肝黄素的单加氧酶氧化三甲胺的产物,也是参与房颤发病机制研究最广泛的微生物代谢产物。
氧化三甲胺过高影响房颤的发生
在犬模型中,局部注射氧化三甲胺激活心房自主神经节丛并促进心律失常,可能通过激活核因子-κB p65信号传导和增加炎症细胞因子的表达。
此外,在房颤患者的肠道中观察到三甲胺形成的微生物基因和三甲胺微生物生产者的显著增加。
尽管小型研究表明,血清氧化三甲胺水平升高可预测房颤患者的血栓栓塞事件,但这种关联的有效性和重要性需要在更多的房颤人群中进一步评估。
氧化三甲胺促进心律不齐的危险因素
此外,氧化三甲胺可能通过促进各种心律不齐危险因素(例如通过促动脉粥样硬化作用产生的代谢综合征和高血压、肾素-血管紧张素系统调节和主动脉硬化)来增强对房颤的易感性。
在蛋白质组学分析中,与非房颤受试者相比,房颤患者的心耳和血浆样本中的胆碱(TMAO前体)含量更高。
在对三个前瞻性队列进行的汇总分析中,血浆和膳食中胆碱的摄入量与后期房颤风险呈正相关。
2
硫酸吲哚酚
硫酸吲哚酚会引起氧化应激导致心律失常
在实验研究中,硫酸吲哚酚通过引起氧化应激和心肌细胞钙处理失调,增加肺静脉和左房心律失常的发生,并减少窦房结起搏器的活性。
在临床环境中,高浓度硫酸吲哚酚(≥0.65 μg/mL)可预测房颤复发风险3.7倍。相反,房颤的导管消融与硫酸吲哚酚血清浓度降低相关,这表明房颤本身可能会增加硫酸吲哚酚的产生。
在动物研究中,硫酸吲哚酚会增加促炎和促纤维化信号分子的表达,并引起氧化应激,从而可能导致房颤。
注:在这些实验研究中,所使用的硫酸吲哚酚浓度大大超出了其在血浆中的生理范围,使其在促进房颤中的潜在作用还不确定。
3
脂多糖
脂多糖是一种存在于革兰氏阴性菌(特别是埃希氏菌属)外层的内毒素。
脂多糖增加了心房促炎因子浓度
在犬模型中,给予脂多糖会增加心房促炎细胞因子的浓度,从而增加连接蛋白43的表达并导致连接蛋白偏侧化。
脂多糖会下调L型钙通道(α1C和β2亚基)的表达并缩短有效不应期。异常的钙处理和连接蛋白调节是诱导房颤的潜在机制。
L-型钙通道是一种电压依赖性钙通道。
脂多糖水平过高增加心血管疾病风险
尽管脂多糖对房颤发病机制的直接影响尚未研究,但脂多糖水平升高的房颤患者似乎有较高的不良心血管事件风险。
脂多糖可能通过加速动脉粥样硬化间接导致心律不齐,并可能诱发左心室功能障碍和心力衰竭,这两者都会增加心律不齐的风险。
4
胆汁酸
初级胆汁酸,例如鹅去氧胆酸,通过与氨基酸(牛磺酸或甘氨酸)结合形成胆汁盐,并进一步分泌到小肠中。
牛磺酸结合的胆汁酸可以通过心脏钠钙交换体刺激诱导膜电位变化并激活心肌细胞中毒蕈碱M2受体/乙酰胆碱调节的钾电流,这可能促进心房颤动。
鹅去氧胆酸等胆汁酸的水平影响心脏
鹅去氧胆酸已被证明可引起心房心肌细胞凋亡,这可能导致房颤的演变,促进结构重塑,通过法尼素X受体促进心脏损伤和纤维化,并通过NLRP3炎症小体激活加重炎症过程。
另一方面,熊去氧胆酸通过稳定细胞膜电位在预防心律失常中发挥作用。胆汁酸还可能通过参与葡萄糖和脂质代谢间接诱导房颤,并通过调节皮质醇和醛固酮水平的11β-羟基类固醇脱氢酶将血压维持在正常范围内。
5
短链脂肪酸
结肠微生物群发酵葡萄糖和膳食纤维会产生短链脂肪酸,主要是乙酸盐、丁酸盐和丙酸盐。
短链脂肪酸是房颤发病的潜在促成因素。短链脂肪酸负责促进粘液产生,从而改善肠道屏障功能,并且对于其中一些来说,还可以通过抑制组蛋白脱乙酰酶影响免疫调节。
短链脂肪酸水平过低会导致心律不齐风险升高
短链脂肪酸水平低会导致代谢物感应G蛋白偶联受体结合不良,从而损害肠道完整性并促进脂多糖等物质进入血液和组织。
丙酸盐刺激胰高血糖素样肽-1和肽YY的释放,降低肥胖风险并增加肾素释放,从而改变两个重要的心律不齐风险因素。
另外,乙酸盐会导致血脂异常,并通过大脑中副交感神经系统的激活增强胰岛素(由胰腺)和生长素释放肽(由胃粘膜)的分泌,从而促进肥胖。
心律不齐组和对照组之间的肠道微生物代谢
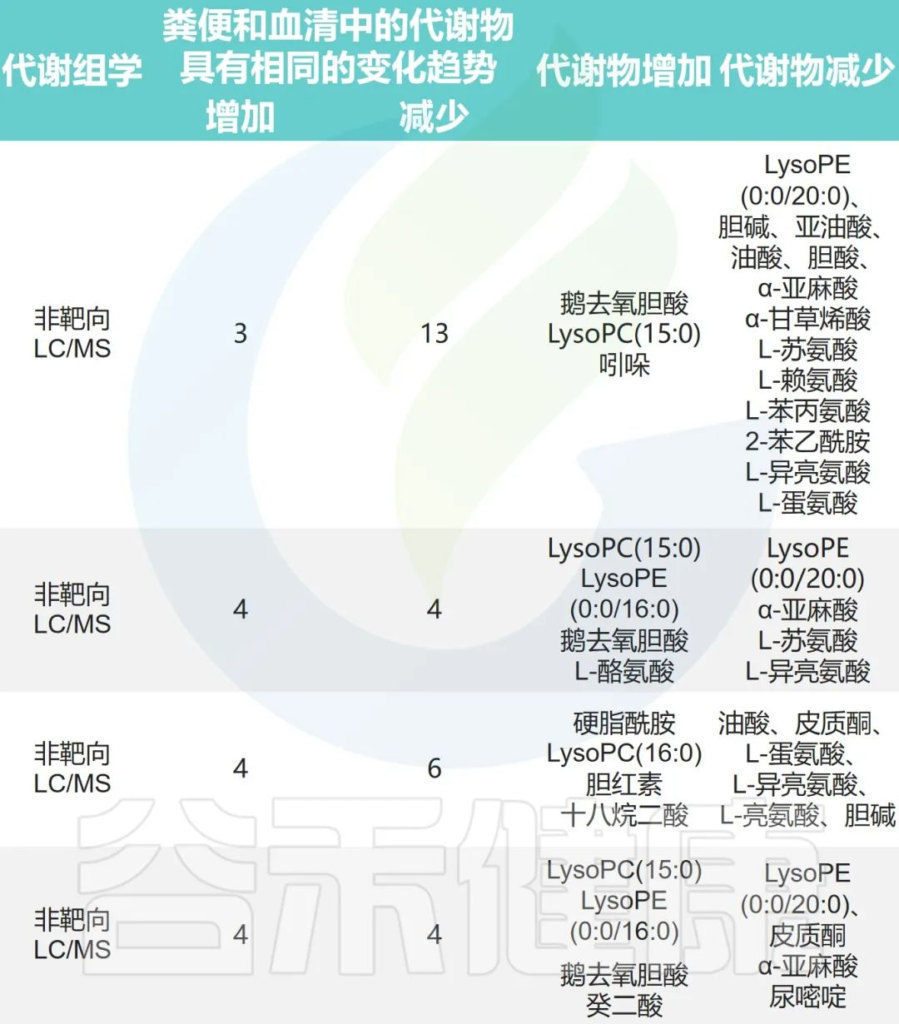
Fan H,et al.Front Cell Infect Microbiol.2023
小结
总之,这些研究表明:与健康人群相比,心律不齐人群经常伴随着肠道有益细菌的减少、心血管保护性代谢物的减少以及对健康有害的代谢物的增加。
近年来,越来越多的相关研究证明,肠道微生物紊乱与缺血性心肌病、心力衰竭、甚至心律失常有关。
下面将讲述肠道微生物如何利用代谢物、炎症因子、免疫细胞作为介质,通过神经、血液、直接作用于心肌组织,最终导致心律失常的发生。
肠道微生物群和代谢物引起心律失常的机制
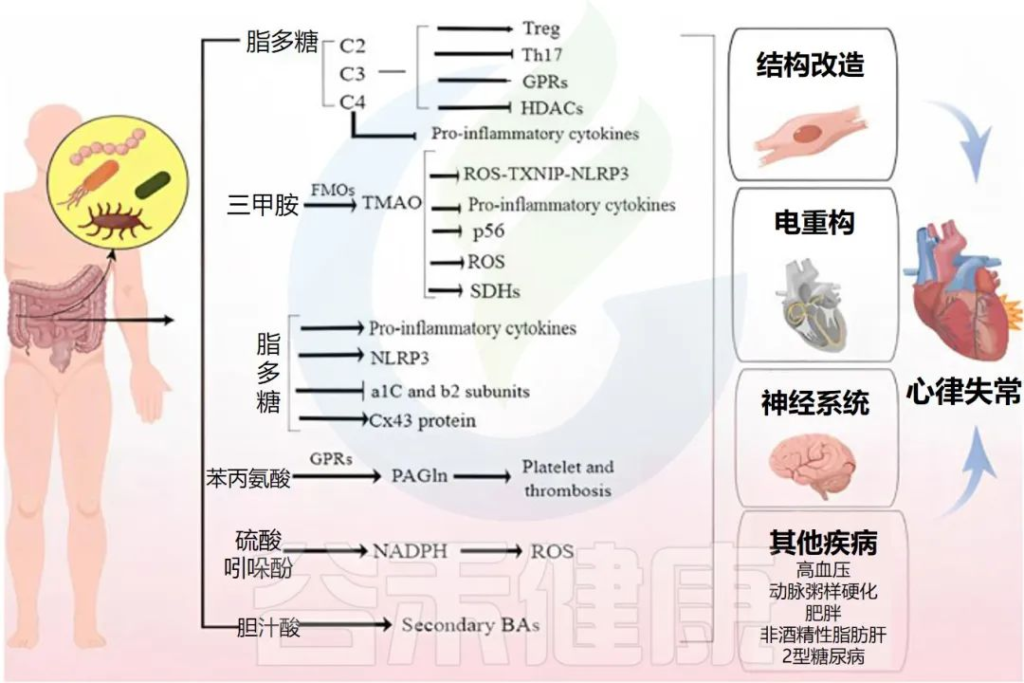
Fan H,et al.Front Cell Infect Microbiol.2023
▼
心肌重塑是指在快速心律失常的进展过程中,心肌原有的电生理和组织学特征发生了一定的变化。心肌重塑的主要表现之一是结构重塑,包括心肌细胞凋亡、心房基质纤维化等。
这主要是由于高血压、冠心病、糖尿病、肥胖等多种原因,导致心肌细胞内质网、线粒体等细胞器的结构、形态和数量发生变化,导致心肌细胞肥大、凋亡、坏死和心肌间质纤维化。
最后,肌壁不断增厚,心腔容积不断扩大,最终促进快速心律失常的发生。
短链脂肪酸通过减少炎症反应保护心血管
免疫炎症的减少可以通过肠道细菌产生的短链脂肪酸减轻心脏肥大、纤维化、血管功能障碍和高血压。
对免疫细胞的抗炎作用是通过短链脂肪酸实现的,例如丙酸可以诱导CD25+Foxp3+ Treg的分化和抑制功能。丙酸还通过抑制组蛋白脱乙酰酶或通过GPRs和嗅觉受体发挥心脏保护作用。
丙酸对心脏的保护主要取决于调节性T细胞的作用。
短链脂肪酸可以通过减少炎症反应对心血管的不利影响来预防或延缓心律失常的发生。
其他肠道代谢物通过炎症途径对心律失常的影响
肠道微生物产生的其他代谢物也可能通过炎症途径引起心律失常。
氧化三甲胺
氧化三甲胺激活NLRP3炎症小体导致人脐静脉炎症和内皮功能障碍。随着炎症标志物显著增加,活化的白细胞被招募来诱导血管炎症,这表明氧化三甲胺增强动脉粥样硬化和心血管风险的可能机制。
硫酸吲哚酚
硫酸吲哚酚可以通过氧化应激诱导肺静脉和房性心律失常。在窦性心律的患者中发现,射频电流导管消融后,患有高硫酸吲哚酚的房颤患者血清硫酸吲哚酚水平降低,这表明血清硫酸吲哚酚不仅可能诱发房颤,而且可能受到房颤的影响。
心肌肥厚和心肌纤维化影响心律失常
心肌肥厚和心肌纤维化是心律失常的重要原因。肠道微生物可以产生琥珀酸、乳酸、乙酰辅酶A,并进一步代谢成短链脂肪酸。其中一些与心肌肥大和心肌纤维化密切相关。
研究表明,丙酸可以在T细胞的帮助下减轻炎症反应,减轻小鼠心肌肥厚、纤维化、血管功能障碍和高血压。
亚油酸和α-亚麻酸抑制活性氧的产生并下调p38 MAPK途径β生长因子的激活和转化、发挥保护作用。它在心房纤维化中发挥调节作用,影响房颤的进展。
总之,有充分的证据表明,肠道微生物及其代谢物可以通过多种方式影响心肌肥大和纤维化,这很可能是心律失常发生的基础。
心肌细胞凋亡
鹅去氧胆酸已被证明可引起心房心肌细胞凋亡,这可能有助于结构重塑。鹅去氧胆酸与左心房低电压区呈正相关,可能促进心房肌细胞凋亡。
此外,丁酸通过抑制增殖和凋亡来促进血管平滑肌细胞的生长。氧化三甲胺通过琥珀酸脱氢酶复合物B亚基上调诱导活性氧促进血管内皮细胞凋亡,这可能有助于动脉粥样硬化病变的进展。
▼
心脏的功能就像机械泵一样,确保向全身和肺部持续供应血液。因此,人类心脏每天会进行100,000 次成功且协调的收缩。
由于心脏收缩受到严格的电调节,失衡会导致心律失常。这些收缩是由称为动作电位的电信号控制的。肠道微生物失衡引起的心肌重塑还反映在电生理重塑(心肌细胞膜表面离子通道的改变)。
通过钠离子通道影响心肌电活动
众所周知,钠通道是产生动作电位的关键通道,由此产生的细胞内和细胞外钠离子浓度的变化对心脏动作电位的产生很重要。
肠道微生物参与胆汁酸的代谢,胆汁酸诱导的心律失常发生的可能机制是与细胞膜和细胞膜离子通道或转运蛋白的相互作用。
研究发现牛磺胆酸通过刺激心肌中的钠钙交换诱导膜电位变化,导致内向电流密度增加和静息膜电位去极化,进而影响心肌电活动。
然而,也发现熊去氧胆酸在诱导心律失常方面无效,熊去氧胆酸偶联保护富含胆固醇的质膜免受疏水性胆汁酸的毒性作用,从而保护细胞免受心律失常的影响。
注:房颤患者的血清熊去氧胆酸偶联物水平明显较低,非熊去氧胆酸水平较高。
这表明,较高水平的毒性(致心律失常)和较低水平的保护性胆汁酸创造了一个心律失常阈值较低的环境,因此可能导致心律失常。
钾离子通道与持续性房颤相关
钾离子通道代表心脏中最多样化的离子通道,其中心脏乙酰胆碱激活的内向整流钾电流(IKACh)通道的激活是副交感神经系统对心脏功能的生理控制的重要组成部分。
目前,越来越多的研究证实,激活的内向整流钾电流被认为是持续性房颤中的背景内向整流器,因此有助于缩短动作电位持续时间并稳定高频电转子的形成,从而导致持续性房颤。
钙离子通过多种机制影响心律失常
Ca2+是一种普遍存在的第二信使,调节多种生物过程,包括激素产生、肌肉收缩、突触传递、增殖和死亡。越来越多的证据表明房颤和其他心脏疾病,与Ca2+相关。
因此,对心脏钙通道的任何影响都可能导致心律失常。在一项实验研究中,硫酸吲哚酚通过引起心肌细胞的氧化应激和钙处理失调,增加了肺静脉性心律失常和左心房心律失常的发生,并降低了窦房结起搏器的活性。
脂多糖还可以上调NLRP3系统,这除了引起结构重塑外,还可以导致心房动作电位的重新进入,促进收缩和舒张期间自发肌浆网Ca2+释放频率的增加,这可能导致去极化后延迟并触发异位活动,从而影响心肌电活动。
这些机制为钙调节促进心律失常提供了证据。
▼
人们对肠脑轴自下而上的信号传导知之甚少。然而,心脑轴的自上而下信号传导已被广泛研究。通过自主神经系统和迷走神经系统,神经系统可以控制心率。
心律失常可能是由于中枢神经系统限制副交感神经张力同时提高交感神经张力的能力而引起的。
注:神经系统调节心脏的机制非常复杂。植入的神经节丛中可能有数百到数千个自主神经元。
自主神经系统
心律失常的形成和维持在很大程度上取决于自主神经系统。
大脑和脊髓中的神经元以及连接心脏的神经组成了外源性心脏自主神经系统。在心脏本身以及沿着胸腔的大静脉中,自主神经元和神经构成了内在心脏自主神经系统的大部分。
•通过心脏自主神经系统调节房颤和室性心律失常
在犬模型中,局部注射氧化三甲胺可能通过激活 p65 核因子-κB 信号传导和增加炎症细胞因子的表达来激活心房自主神经丛并促进心律失常。
已经证明,房颤或室性心律失常的病理生理学是由心脏自主神经系统调节的。有证据表明,在发生室性心律失常之前,左心交感神经就已过度活跃,而左星状神经节的激活可大大增加室性心律失常发生的可能性。
研究结果表明,与对照组相比,静脉注射和局部氧化三甲胺治疗显著增强了左星状神经节功能和活性,从而提高了心脏交感神经张力,并恶化了缺血引起的室性心律失常。
同时,氧化三甲胺可显著促进促炎标志物的表达,如IL-1、IL-6、TNF-α,这可能进一步导致交感神经过度活跃并影响室性心律失常的发展。
迷走神经系统
调节心律受到迷走神经的负面影响。迷走神经放电增强钾通道电流,减少动作电位持续时间并稳定折叠转子。
•肠道微生物及其代谢物通过迷走神经影响心律
微生物群可以通过肠道内分泌细胞直接或间接触发迷走神经传入纤维。迷走神经传入纤维通过中枢自主神经网络刺激中枢神经系统。迷走神经传入纤维可以通过炎症反射触发传出纤维。
根据物质的不同,微生物群产生的不同代谢物可能以不同的方式激活迷走神经传入纤维。例如,油酸,一种长脂肪酸,通过胆囊收缩素介导的机制作用于迷走神经传入纤维;而丁酸,一种短脂肪酸,直接影响传入末梢。
Part 1
胃肠道疾病易诱发房颤
√较高的C反应蛋白增加心房颤动风险
炎症似乎在心律失常的发病机制中发挥着重要作用。C反应蛋白 (CRP) 升高与心房颤动相关,持续性心房颤动的平均C反应蛋白水平高于阵发性心房颤动中观察到的水平,表明炎症状态可能会促进心房颤动的持续存在。
C反应蛋白是一种非特异性炎性标志物,由肝脏合成的用于保护身体的急性时相反应蛋白。
在纵向研究中,较高的C反应蛋白会相应增加心房颤动风险。最后,在没有心血管合并症的情况下,严重败血症和急性全身炎症反应与新发心房颤动相关。
√炎症性肠病患者心房传导发生了改变
在一项研究中,观察到炎症性肠病患者的心房传导发生了改变,这是通过心电图上P波离散度的增加来衡量的。
在两项针对炎症性肠病患者的小型研究中,与参考对象相比,经胸超声心动图测量的心房机电传导时间延长。
丹麦的一项病例对照研究涉及24499例炎症性肠病病例和236275名年龄和性别匹配的对照,观察到在活动性炎症性肠病发作期间,房颤风险增加两倍,中风风险增加1.5倍。在炎症性肠病缓解期间,未观察到与房颤或中风的关联。
▼
在一些病例对照研究中,胃肠道恶性肿瘤,包括结直肠癌和食道癌,与房颤风险增加有关。
√结直肠癌患者发生房颤的风险更高
在一项研究中,与非癌症队列参与者相比,结直肠癌患者发生房颤的风险增加了一倍。
丹麦一项基于人群的病例对照研究观察到,结直肠癌患者的房颤患病率较高 [比值比为11.8],但患病率的增加仅限于癌症诊断后的前90天,这表明手术治疗癌症可能在很大程度上推动了这种关联。
√胃肠道手术后房颤风险增加
胃肠癌手术治疗后房颤的发生率很高,并且与手术结果不佳相关,包括肺部并发症、败血症、住院时间延长。
此外,在回顾性分析中,胃肠道癌症手术后发生房颤的患者在1年内发生心血管事件和60天内死亡的风险增加。
据报道,经胸食管切除术后房颤的发生率为10%至46% 。
Part 2
房颤患者易得胃肠道疾病
▼
在房颤患者中,缺血主要继发于心脏栓塞事件,而不是原位血栓栓塞。房颤患者心脏栓塞事件的主要风险因素包括既往卒中或短暂性脑缺血发作史,年龄大于75岁、高血压和结构性心脏病。
√房颤患者易发生肠系膜缺血
特别是,患有房颤的女性发生血栓栓塞的风险增加,包括肠系膜缺血。内脏-肠系膜血管系统栓塞是外周血栓栓塞疾病的第二常见部位,仅次于上肢和下肢的血管。
在一项基于房颤患者研究中,随着房颤评分的增加,发生肠系膜缺血的风险更高,评分为⩾2的患者与评分为0的患者相比,风险增加了三倍。
Part 3
与心律失常相关的其他疾病
▼
肠道微生物可以影响血压,而高血压患者通过多种作用方式参与心律失常。
√房颤、室性心律失常的发生率与高血压呈正相关
房颤、室性心律失常和猝死的发生率与以心脏重构为表现的高血压病程呈正相关。高血压患者心律失常发生的机制和表现通过心脏环境的宏观和微观变化影响心律失常的发展,导致电学和结构的改变。
高血压进一步促进左心室肥厚,这是心律失常的危险因素。长期升高的后负荷和心内压会导致心肌细胞肥大并激活心肌成纤维细胞。心肌细胞肥大和心肌成纤维细胞胶原沉积增加导致心肌质量增加,导致左心室肥厚。
已经确定,左心室肥厚可能通过诱发心肌缺血、心肌需氧量增加以及左心室舒张功能障碍而增加发生心律失常的风险。
肠道微生物群也会影响血压
据了解,缺乏肠道微生物的无菌小鼠的血压比传统小鼠的血压要低。与此同时,将人类高血压捐献者的粪便移植到无菌小鼠体内会导致这些小鼠血压升高。高血压中具有产生舒张代谢产物特性的细菌种类数量的减少也表明肠道微生物群会影响血压。
▼
动脉粥样硬化也是诱发心律失常的危险因素之一。当动脉粥样硬化影响传导系统,阻碍冲动传导时,就会引起各种心律失常。
√动脉粥样硬化会导致急性心肌梗塞与心律失常
急性心肌梗死是动脉粥样硬化的严重后果,经常与 心律失常一起发生,这会增加患者在医院接受治疗时突然死亡的风险和预后不良。
肠道微生物通过其代谢物参与动脉粥样硬化。具体而言,动脉粥样硬化患者的大肠杆菌(Escherichia coli)、克雷伯氏菌属(Klebsiella spp.)和产气肠杆菌(Enterobacter aerogenes)的丰度显著增加,而两种产生丁酸的细菌——Roseburia gutis和粪杆菌的丰度则下降。
肠道微生物的代谢产物可通过增加内皮活性氧的产生和损害内皮介导的血管舒张而参与动脉粥样硬化。
▼
肠道微生物研究表明,正常微生物群的失衡可能导致多种炎症性疾病,其中肥胖和胰岛素抵抗是肠道微生物失衡和能量失衡引起的主要疾病。
√糖耐量异常和肥胖是心律失常的重要原因
同时,糖耐量异常和肥胖也是心律失常的重要原因之一。糖尿病患者动脉粥样硬化和血栓形成的概率会增加,从而导致急性冠状动脉缺血性心脏病或心律失常。
细菌多样性的整体减少和细菌基因表达的改变被认为是影响代谢途径的主要原因,这可能与肥胖有关。
心律失常是一个缓慢发生且具有复杂机制的过程。从肠道菌群及其代谢物的角度出发,临床医生可以获得预防和治疗糖尿病/肥胖合并心律失常的新视角。尽管如此,还需要大量实验来证实。
▼
非酒精性脂肪性肝病是一种以肝脏细胞内脂肪过度沉积为主要特征的临床病理综合征,是最常见的肝脏疾病。
√非酒精性脂肪肝病提高了心律失常的易感性
非酒精性脂肪性肝病是一种多系统疾病,可能导致脂质和葡萄糖等代谢不良、炎症和氧化应激以及其他全身性有害后果。这些改变可能协同作用,增强心脏的结构、电和自主神经重塑,从而提高心律失常的易感性。
此外,心包脂肪体积或厚度与房颤的患病率和严重程度相关,大多数报告显示非酒精性脂肪肝病与心外膜脂肪体积或厚度呈正相关。
√肠道微生物通过肠-肝轴影响心律失常
肠-肝轴是肠道微生物群与肝脏之间的联系。肠道菌群功能障碍可能导致病原体相关分子模式的产生、粘膜屏障通透性增加导致肝脏炎症以及肝病的发生和进展,并且发现与健康人相比,肝病患者的微生物群多样性较低。
肠道及肝脏问题以多种方式显著影响心律失常。总之,非酒精性脂肪肝与心律失常密切相关,但现有证据并不完善,需要我们继续研究。
▼
阻塞性睡眠呼吸暂停综合征是一种在睡眠时导致呼吸暂停和通气不足的疾病,其特征是打鼾、睡眠模式紊乱、血氧饱和度频繁下降以及白天疲劳。
√睡眠呼吸暂停综合征通过多种途径诱发心律失常
阻塞性睡眠呼吸暂停综合征患者通过多种病理生理途径与心律失常的发生有关,包括呼吸暂停引起的缺氧、胸内压力变化、交感神经失衡、心房重塑、氧化应激、炎症和神经体液激活。
睡眠期间的缺氧会促进交感神经活动,这是诱发心房颤动的关键机制。因此,阻塞性睡眠呼吸暂停综合征本身可能促进心房颤动的发展。
现有的研究表明,患有心房颤动的人肠道中Ruminococcus gnavus为主的类型有所增加。因此,我们推测阻塞性睡眠呼吸暂停综合征和心房颤动病理生理过程的共同原因可能是由于肠道微生物群的改变,尤其是瘤胃球菌的增加。
▼
前不久的新冠肺炎对人类的影响是巨大的。SARS-CoV-2病毒主要影响上呼吸道,但也可能导致危及生命的肺部问题。在一些患有轻度至重度 COVID-19的人中,肠道微生物受到广泛干扰,这种干扰可能会持续长达一个月甚至更久。
√新冠肺炎是心律失常的危险因素
研究表明,新冠肺炎患者中存在心律失常的情况。这可能是由于病毒直接感染心肌细胞,或是由于免疫系统的异常反应所引起的。心律失常在新冠肺炎患者中可能表现为心率不齐、心动过速或心动过缓等症状,严重情况下甚至可能导致心脏骤停。
与其他呼吸道病毒感染一样,COVID-19可能与恶心、呕吐、腹痛和腹泻等胃肠道症状有关。由于影响肠道的途径是通过免疫和神经系统存在的,它们不仅对肠道微生物做出反应,而且还调节其组成。
循环淋巴细胞是两个器官之间的直接免疫接触,因为这些细胞不会停留在一个地方,它们在肠道和气道粘膜上巡逻。“肠肺轴”是这些器官“交流”的串扰。
综上所述,肠道微生物会通过各种分泌物引发心律失常,而SARS-CoV-2病毒由于“肠肺轴”的存在,可能是心律失常的危险因素。
心律失常作为一种心脏疾病,会给患者的健康和生活质量带来严重负面影响。因此,需要不断努力追求治疗心律失常的方法和策略。
在治疗心律失常方面,致力于整合多种治疗方法,包括药物治疗、手术治疗和其他创新疗法(例如肠道微生物干预)。需要根据患者的具体情况和心脏功能,制定最适合其需求的个性化治疗。
1
饮食调整: 多吃有益的脂质和膳食纤维
一些研究调查了不同食物成分和饮食模式对肠道菌群的影响,这可能是未来通过肠道微生物群治疗心律失常的重要目标。
•脂肪摄入过多会导致心律失常
最近的一项研究表明,房颤患者倾向于从动物脂肪中获取更多能量。至于肠道微生物群与脂肪摄入量之间的相关性,拟杆菌门与房颤患者的脂肪摄入量(特别是动物脂肪)呈弱负相关,而厚壁菌门则呈现相反的相关性。
•地中海饮食有助于降低心律不齐风险
代谢性内毒素血症和慢性炎症可能是脂肪摄入诱发房颤的机制。摄入油酸可以显著降低心血管疾病的风险,因为它可以抑制氧化应激,从而减轻心肌细胞损伤。
地中海饮食可以有益地影响肠道微生物群和相关代谢。以蔬菜为主的饮食人群具有更好的微生物代谢组。一项针对房颤患者的研究表明,地中海饮食可以降低氧化应激,从而降低房颤风险。
2
补充益生菌、益生元
研究表明,肠道微生物的失衡与心律失常的发生有关。肠道微生物在治疗心律失常方面具有潜力。因此,调整肠道微生物的组成可能成为未来心律失常治疗的一种新方法。
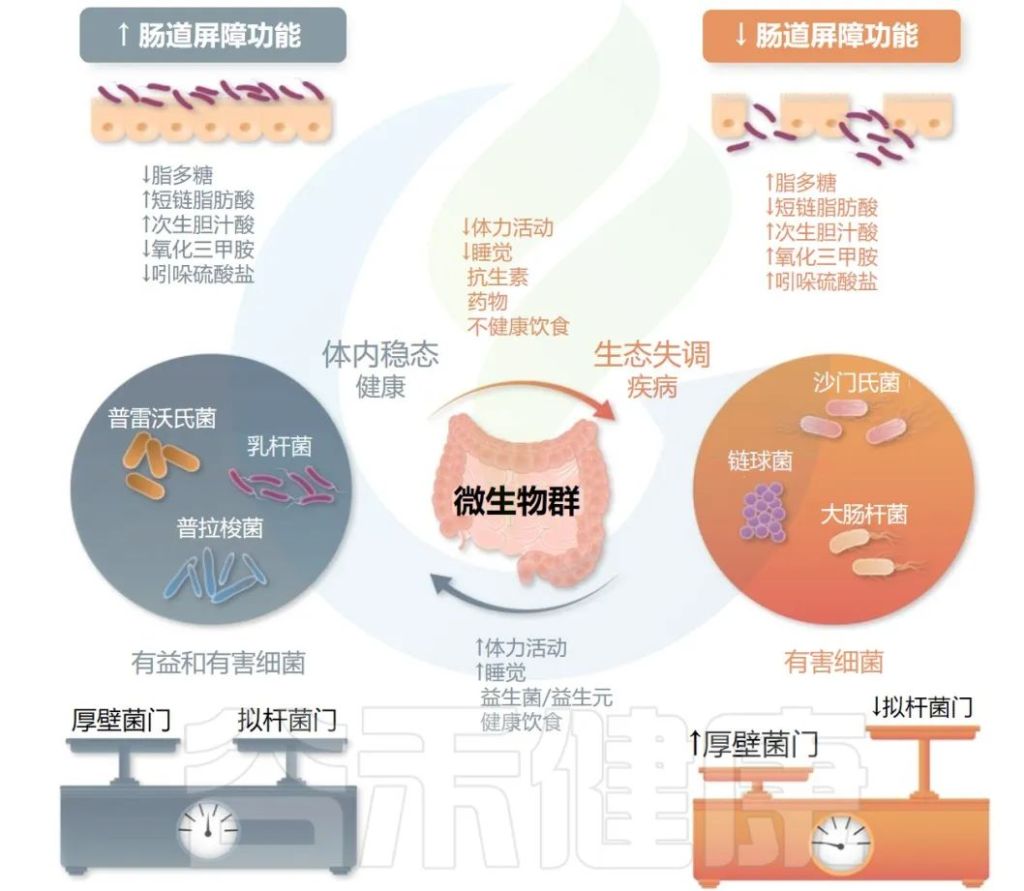
编辑
Gawałko M,et al.Cardiovasc Res.2022
•服用益生菌缓解了动脉粥样硬化
几项临床研究发现,口服嗜酸乳杆菌(L.acidophilus ATCC 4356)可以通过调节小鼠的氧化应激和炎症过程来缓解动脉粥样硬化的进展。
•益生菌促进了残留药物的降解
益生菌还可以影响药物的代谢。胺碘酮是市场上主要的抗心律失常药物,具有心外毒性,因此研究人员重点寻找改善体内残留胺碘酮代谢的方法。
研究发现酿酒酵母菌株OBS2是一种具有治疗潜力的益生菌,可以在体外和体内促进残留胺碘酮的降解。
•益生元可以减少心肌损伤
益生元是一类可促进肠道益生菌生长和活性的物质,其健康益处取决于微生物的新陈代谢。目前果聚糖(低聚果糖和菊粉)和半乳聚糖(低聚半乳糖)在益生元类别中的主导地位已被数十项研究证实。
一项在大鼠缺血再灌注模型中进行的研究得出结论,阿拉伯半乳聚糖可以抑制细胞凋亡,从而减少心肌损伤。
此外,源自红酒的多酚白藜芦醇通过抑制细胞内钙的释放而具有抗心律失常特性。在小鼠模型中,白藜芦醇通过肠道微生物群重塑降低氧化三甲胺水平并增加肝脏胆汁酸合成,从而减轻动脉粥样硬化。
3
药物与肠道微生物的相互作用
大量研究表明药物和肠道微生物群之间存在双向作用,这也可能调节药物代谢。例如,迟缓埃格特菌(Eggerthella lenta)通过还原内酯环产生无活性产物来灭活地高辛。
•肠道微生物增强了心血管药物的利用度
此外,肠道微生物酶活性参与了一些心血管药物的首次通过清除,包括钙通道阻滞剂和非甾体抗炎药,当患者接受抗生素预处理时,增加了这些药物的生物利用度。
•心血管药物对肠道微生物存在显著影响
同时,许多临床使用的药物可以增强或降低肠道微生物群或肠道微生物群衍生代谢物的生长速度。对荷兰一项队列研究的1135名参与者的粪便样本进行宏基因组测序显示,使用多种心血管药物,包括他汀类药物、抗血栓药物、 受体阻滞剂和血管紧张素转换酶抑制剂,对肠道微生物组有显著影响。
4
粪菌移植
粪便微生物移植作为一种安全的治疗方法被广泛应用于胃肠道疾病及胃肠外疾病的治疗。
•粪菌移植可以有效减轻甚至治愈疾病
从健康受试者到患有菌群失调相关疾病的受试者的菌群移植可以减轻甚至治愈这种疾病。在一项研究中,将血压正常大鼠的盲肠内容物移植到自发性高血压大鼠体内可降低血压,而对自发性高血压大鼠进行粪菌移植后,血压正常的大鼠会出现高血压。
最近,将来自高脂肪饮食喂养的小鼠的粪便微生物移植到正常饮食喂养的小鼠中,他们发现对房颤的易感性显著增加。
接受高脂饮食小鼠粪菌移植的小鼠遭受由脱硫弧菌(Desulfovibrionaceae)引起的代谢内毒素血症,该血症循环脂多糖升高,破坏肠道组织结构,并增加左心房促炎因子。
5
免疫调节剂
组蛋白脱乙酰酶在钙稳态、房颤发生和心力衰竭中起着至关重要的作用,因此组蛋白脱乙酰酶抑制剂可能是潜在的治疗方法。
•组蛋白去乙酰酶抑制剂降低了心律失常的发生
组蛋白去乙酰化酶抑制剂通过拯救线粒体生物能量学来治疗心脏功能障碍,即TNF-α诱导的线粒体功能障碍,降低能量利用率。
另一项在房颤兔身上进行的研究表明,组蛋白去乙酰化酶抑制剂可以降低钙稳态诱导的房颤和肺静脉心律失常的发生,房颤持续时间缩短。
注:MPT0E014处理的心肌细胞钙瞬态振幅、钠钙交换电流和ryanodine受体表达的降低可能是组蛋白去乙酰化酶抑制剂治疗心律不齐的潜在机制。
6
病因治疗和药物治疗
•病因治疗
病因治疗包括纠正心脏病理改变、调整异常病理生理功能(如冠脉动态狭窄、泵功能不全、自主神经张力改变等),以及去除导致心律失常发作的其它诱因(如电解质失调、药物不良副作用等)。
•药物治疗
药物治疗缓慢心律失常一般选用增强心肌自律性或加速传导的药物,如拟交感神经药(异丙肾上腺素等)、迷走神经抑制药物(阿托品)或碱化剂(克分子乳酸钠或碳酸氢钠)。
治疗快速心律失常则选用减慢传导和延长不应期的药物,如迷走神经兴奋剂(新斯的明、洋地黄制剂)、拟交感神经药间接兴奋迷走神经(甲氧明、苯福林)或抗心律失常药物。
多项证据表明肠道微生物群的变化可能是心律失常的重要诱发因素。肠道微生物可以通过短链脂肪酸、胆汁酸等代谢物,改变心肌细胞的电活动,从而调节心律。
其次,肠道微生物的失衡可能导致免疫系统的异常活化,诱发心律失常的发生。某些肠道菌群的代谢产物,如脂多糖、细菌毒素等,可能引发炎症反应,损伤心肌细胞,进而导致心律失常。
然而,肠道微生物与心律失常的具体关联和机制仍需进一步的研究和探索。目前,通过调整饮食结构、补充益生菌和使用粪菌移植等策略,可以尝试改善肠道微生物组成,从而对心律失常的治疗产生积极的影响。
但需要强调的是,个体差异和复杂性限制了一刀切的推广,治疗方案应当根据具体情况进行调整和制定。
主要参考文献
Fan H, Liu X, Ren Z, Fei X, Luo J, Yang X, Xue Y, Zhang F, Liang B. Gut microbiota and cardiac arrhythmia. Front Cell Infect Microbiol. 2023 Apr 25;13:1147687.
Gawałko M, Agbaedeng TA, Saljic A, Müller DN, Wilck N, Schnabel R, Penders J, Rienstra M, van Gelder I, Jespersen T, Schotten U, Crijns HJGM, Kalman JM, Sanders P, Nattel S, Dobrev D, Linz D. Gut microbiota, dysbiosis and atrial fibrillation. Arrhythmogenic mechanisms and potential clinical implications. Cardiovasc Res. 2022 Aug 24;118(11):2415-2427.
Frampton J, Ortengren AR, Zeitler EP. Arrhythmias After Acute Myocardial Infarction. Yale J Biol Med. 2023 Mar 31;96(1):83-94.
Li W, Li C, Ren C, Zhou S, Cheng H, Chen Y, Han X, Zhong Y, Zhou L, Xie D, Liu H, Xie J. Bidirectional effects of oral anticoagulants on gut microbiota in patients with atrial fibrillation. Front Cell Infect Microbiol. 2023 Mar 24;13:1038472.
Zuo K, Yin X, Li K, Zhang J, Wang P, Jiao J, Liu Z, Liu X, Liu J, Li J, Yang X. Different Types of Atrial Fibrillation Share Patterns of Gut Microbiota Dysbiosis. mSphere. 2020 Mar 18;5(2):e00071-20.
Li N, Durgan DJ, Wehrens XHT. Gut microbiota: a key regulator of ageing-associated atrial fibrillation? Cardiovasc Res. 2022 Feb 21;118(3):657-659.
Long MT, Ko D, Arnold LM, Trinquart L, Sherer JA, Keppel SS, Benjamin EJ, Helm RH. Gastrointestinal and liver diseases and atrial fibrillation: a review of the literature. Therap Adv Gastroenterol. 2019 Apr 2;12:1756284819832237.

谷禾健康
抑郁症·肠道菌群
当一个人面临抑郁症时,一切看似平常的事都会变得很有挑战性。上班、与朋友社交,甚至只是起床都感觉很困难。
抑郁症是如今已是世界上最普遍的精神障碍之一,一直是心理学和医学领域的研究热点。抑郁症是一种需要预防和治疗的疾病——它并不是软弱或失败的表现。
抑郁症影响着数百万计的人们,造成抑郁症的因素有很多,包括创伤、生活压力事件、遗传基因、环境因素、药物滥用和其他心理健康问题。
虽然我们目前仍然不完全了解导致抑郁症的原因,一个新的研究领域涉及微生物群-肠-脑轴,证明可以控制认知功能。微生物组通过内分泌、免疫和神经活性途径影响肠脑通讯。后者包括微生物源性神经递质(例如,γ-氨基丁酸、血清素)和代谢物(短链脂肪酸和胆汁酸),以及脑源性神经营养因子。

本文我们主要来了解一下关于抑郁症与肠道菌群之间的关系,它们之间的相互作用机制可能涉及肠脑轴、免疫调节、代谢途径、肠漏、神经炎症、HPA轴等多种途径,同时也列举了较多关于抑郁症的干预措施,希望为抑郁症的治疗和预防提供新的视角和方法。

-正文-
抑郁症是一种复杂的疾病,有许多影响因素,包括多种生活方式、饮食、遗传和环境因素。
据估计,全世界有超过3亿人至少经历过一次重度抑郁症。18-25 岁人群中重度抑郁发作的患病率最高。
一开始,抑郁发作的症状可能只是感觉忧郁、疲劳或“陷入困境”。因此,学习如何辨别平常的低落一天或只是感到忧郁和抑郁对于知道何时寻求帮助非常重要。
要符合抑郁发作的症状,个人必须在两周内几乎每天、全天经历抑郁情绪或兴趣丧失,以及同时经历其他四到五种症状。
▼
某些类型的抑郁症还可能出现以下症状:
▼
抑郁症的主要诊断标准包括:
然而,请注意,并非所有症状都必须出现才能被诊断为抑郁症:大多数患者仅具有完整“核心”症状的一部分。
▼
包括情绪低落或失去兴趣的症状,大多数情况持续至少两周,影响日常活动。
也称为心境恶劣或心境恶劣障碍,是指持续时间较长(通常至少 2 年)的不太严重的抑郁症状。
指怀孕期间或怀孕后发生的抑郁症。在怀孕期间开始的抑郁症是产前抑郁症,在婴儿出生后开始的抑郁症是产后抑郁症。
是一种随季节变化而出现和消失的抑郁症,症状通常在秋末冬初开始,在春季和夏季消失。
是抑郁症的一种严重形式,患者会出现精神病症状,例如妄想(令人不安的、错误的固定信念)或幻觉(听到或看到别人没有听到或看到的东西)。
其他还有:
以前称为躁狂抑郁症或躁狂抑郁症患者,也会经历抑郁发作,在此期间他们感到悲伤、冷漠或绝望,并且活动水平非常低。但双相情感障碍患者也会经历躁狂(或不太严重的轻躁狂)发作,或情绪异常升高,他们可能会感到非常高兴、烦躁或“兴奋”,活动水平显着增加。
▼
一些可能增加一个人患抑郁症风险的已知因素包括:
▼
神经递质是神经元用来将信号从一个细胞传递到另一个细胞的化学物质。神经递质有 100 多种不同类型,其中最著名的包括血清素、多巴胺和去甲肾上腺素等。
大多数最常见或广泛使用的抗抑郁药物(例如西酞普兰和许多其他药物)通常通过增加大脑中可用的神经递质血清素和去甲肾上腺素的量来发挥作用(即选择性血清素再摄取抑制剂或血清素-去甲肾上腺素再摄取抑制剂,或分别为“SSRI”和“SNRI”)。
注:西酞普兰是一种抗抑郁药,属于选择性血清素再摄取抑制剂(SSRI)类药物。是一种流行且用途广泛的处方药,用于治疗许多精神健康状况,包括抑郁、焦虑和创伤后应激障碍 (PTSD)。它于 2002 年获得 FDA 批准用于治疗抑郁症(成人和青少年)和广泛性焦虑症(成人)。
然而,其他一些抗抑郁药——例如安非他酮(Wellbutrin)——主要作用于多巴胺和去甲肾上腺素(即去甲肾上腺素-多巴胺再摄取抑制剂,或“NDRIs”)。
尽管如此,低水平的血清素或去甲肾上腺素是否直接导致抑郁症仍然是一个悬而未决的问题。许多科学尝试证实抑郁症患者实际上具有异常低水平的这些神经递质,但有时未能完全验证其中的联系。
我们理解的抑郁症的另一个主要方法学局限性是,尽管抗抑郁药已经建立了生化机制(例如抑制单胺氧化酶(MAO),或抑制特定神经递质的再摄取),但抑郁症的诊断和治疗很大程度上基于主观报告症状,而不是特定生化标志物或其他“客观”生物指标的任何离散测量。
换句话说,这并不是通过测量一个人这些化合物的水平,然后得出他们是否“患有”抑郁症那么简单。此外,虽然大多数 SSRI 会立即增加大脑中的血清素水平和活动,但许多患者在服用药物数周或数月后才报告情绪有显著改善。
诸如此类的发现表明血清素水平可能只是与抑郁症共同相关的更为复杂的机制和生物变化链中的一个部分。
虽然抑郁症的“血清素缺乏”假说仍然存在争议,并且并非 100% 被所有研究人员普遍接受,但目前根据迄今为止可获得的总体证据和数据,它通常被认为是最佳的工作假说。也就是说与调节情绪、思维和行为的大脑回路故障有关,大脑化学物质对于健康的神经细胞连接非常重要。
▼
正如识别抑郁症特定生化“标记”的尝试都失败了一样,许多识别导致抑郁症的特定基因或基因突变的尝试也只取得了有限的成功——可能是因为不同的抑郁症病例可能是由许多不同基因的突变以及独特的环境因素综合的。
几项综合研究(包括全基因组关联研究以及家族和双胞胎研究)报告的证据表明,对于某些情况或类型的抑郁症来说,大量个体基因之间的相互作用,以及这些基因与某些环境因素的复杂相互作用,可能只是部分原因。
例如,一项系统性全基因组关联研究(GWAS)报告称,许多与免疫系统功能和炎症相关的基因可能是影响一个人患抑郁症风险的可能遗传因素之一。
据报道,另一项全面的 GWAS 研究确定了许多与血清素功能、昼夜节律和其他神经递质相关的基因可能是抑郁症的遗传风险因素,如下表:
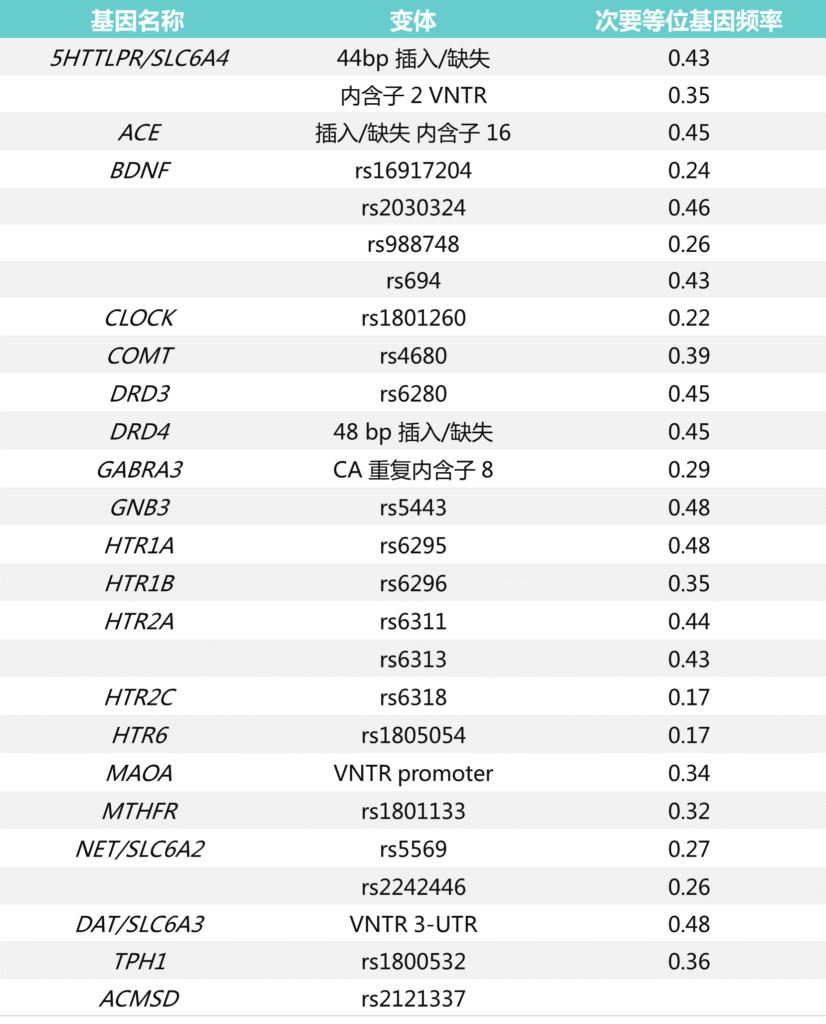
doi.org/10.1016/j.neuron.2014.01.027
对复发性/单相型重度抑郁症(“MDD-RU”)的家庭研究报告称,抑郁症诊断患者的一级亲属可能面临特别高的风险。
血清素转运蛋白基因( SLC6A4 ) 也与重度抑郁症相关。SLC6A4和其他参与大脑血清素能系统的基因现在被认为是抑郁症易感性的“候选基因”,这也符合许多最常见的抗抑郁药物被认为主要作用于该系统的事实。
其他五个与抑郁症风险相关的“候选基因”包括:
▼
肠道菌群与抑郁症之间存在一定的关联。肠道菌群是指人体消化道中的微生物群落,包括细菌、真菌、病毒等。它们与人体的健康和免疫系统密切相关。
微生物群-肠-脑轴
肠道和大脑之间存在着肠脑轴,通过神经、免疫和内分泌系统的相互作用进行沟通。肠道菌群可以通过产生代谢产物、神经递质和炎症因子等影响大脑功能和情绪调节。
炎症反应
肠道菌群失衡可能导致肠道黏膜的炎症反应,释放炎症因子进入血液循环,进而影响大脑功能。慢性炎症反应与抑郁症的发生和发展有关。
神经递质
肠道菌群可以影响神经递质的合成和代谢,如血清素、多巴胺和γ-氨基丁酸等,这些神经递质与情绪调节密切相关。
营养吸收
肠道菌群参与食物的消化和营养的吸收,它们可以合成维生素和其他有益物质,这些物质对大脑和情绪调节有影响。
而肠道菌群又受到多种因素的影响,比如:饮食、抗生素使用、生活方式、环境因素等。接下来章节,我们就肠道菌群与抑郁症展开了解它们之间密不可分的关联。
▼
一些研究发现,中度和重度抑郁症患者的肠道菌群特征是拟杆菌门富集,而重度患者中瘤胃球菌和真杆菌则减少。
抑郁症个体与健康对照组相比,微生物群变化的总结如下:
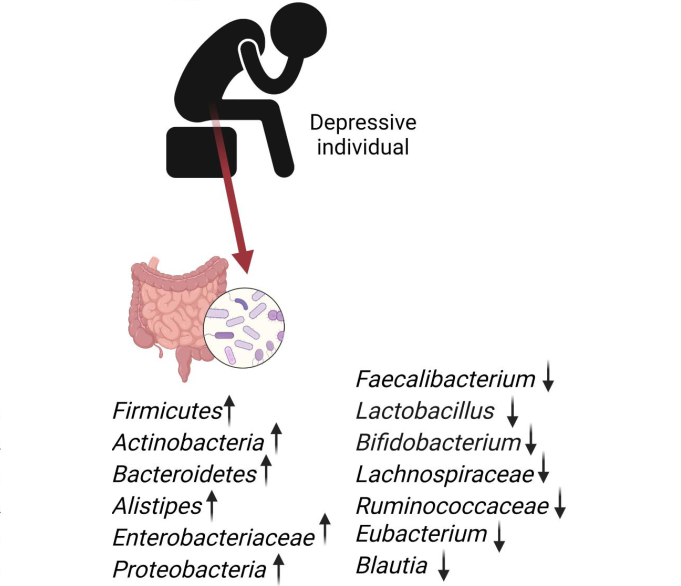
Basiji K, et al., Metab Brain Dis. 2023
▼
根据一项早期的动物研究,在没有肠道细菌的情况下生长的啮齿动物(无菌大鼠和小鼠)缺乏成熟的肠内分泌系统(胃肠道的激素产生系统)。
与具有更典型肠道细菌水平的对应物相比,它们的几种不同主要神经递质的水平和活性也有所不同。
一项初步的动物研究称,没有肠道细菌的小鼠可能会表现出自发运动的增加,该研究的作者将其解释为表明更加焦虑。他们进一步假设,这些行为差异可能是由于某些神经递质,包括血清素、多巴胺和去甲肾上腺素(去甲肾上腺素),在整个大脑中合成和代谢方式的差异造成的。
另一项研究着眼于肠道微生物与早期生活压力之间的潜在关系。在这项研究中,由于早年与母亲分离而经历压力和抑郁样症状的新生大鼠,当在其饮食中添加特定种类的细菌(双歧杆菌)时,其中一些症状会减轻。尽管抑郁相关行为的减少程度小于传统抗抑郁药物西酞普兰造成的减少,但这一初步发现仍然表明,理论上可以通过改变肠道微生物群的组成来“治疗”抑郁症。
其他一些来自动物研究的早期但有趣的证据表明,即使是复杂的行为也可以通过“粪菌移植”从一组小鼠“复制”到另一组小鼠。
一项动物研究报告称,抗生素(通过杀死肠道微生物组中的一些细菌种类来改变肠道微生物组)可能会影响小鼠表现出的“探索行为”的数量,甚至可能会改变大脑中某些重要化合物的水平,如脑源性神经营养因子(BDNF)。
▼
您以前可能听说过“益生菌”——这是指将特定菌株(菌种)引入胃肠道的食品或膳食补充剂。
一些初步证据表明,使用益生菌“修改”人类肠道微生物组可能会产生一些心理影响。例如,据报道,某些益生菌补充剂可以降低健康非老年个体以及诊断为重度抑郁症(MDD)的非老年患者的抑郁症状严重程度评分。
同样,另一项早期研究报告称,定期服用含有瑞士乳杆菌和长双歧杆菌菌株的益生菌可能有助于减少健康志愿者的抑郁症。
最后,另一项初步研究报告称,嗜酸乳杆菌、干酪乳杆菌和两歧双歧杆菌的组合可能有助于部分减轻抑郁症状。
虽然这些作用背后的潜在机制尚不清楚或不明白,但一些研究人员指出,这些“益生菌治疗”可能会导致胰岛素水平降低、胰岛素抵抗和 hs- CRP水平降低,以及谷胱甘肽(一种主要天然物质)水平升高。抗氧化化合物用于重度抑郁症患者。
总的来说,虽然这项早期研究充满希望且令人兴奋,但还需要更多的研究来充分证实这些效应,并找出哪些机制可能导致这些有趣的效应。
▼
“肠-脑轴”是指肠道微生物群与大脑之间假设的“双向”连接。
肠-脑轴可能包括许多不同的潜在机制,包括在许多不同的器官系统和所涉及的单个细菌物种之间产生的各种神经、化学、体液和免疫信号。
虽然许多不同的疾病和健康状况可能受到肠-脑轴的影响,但一些研究人员特别关注肠-脑相互作用在抑郁症发展中可能发挥的作用。
微生物群-肠-脑异常导致抑郁症
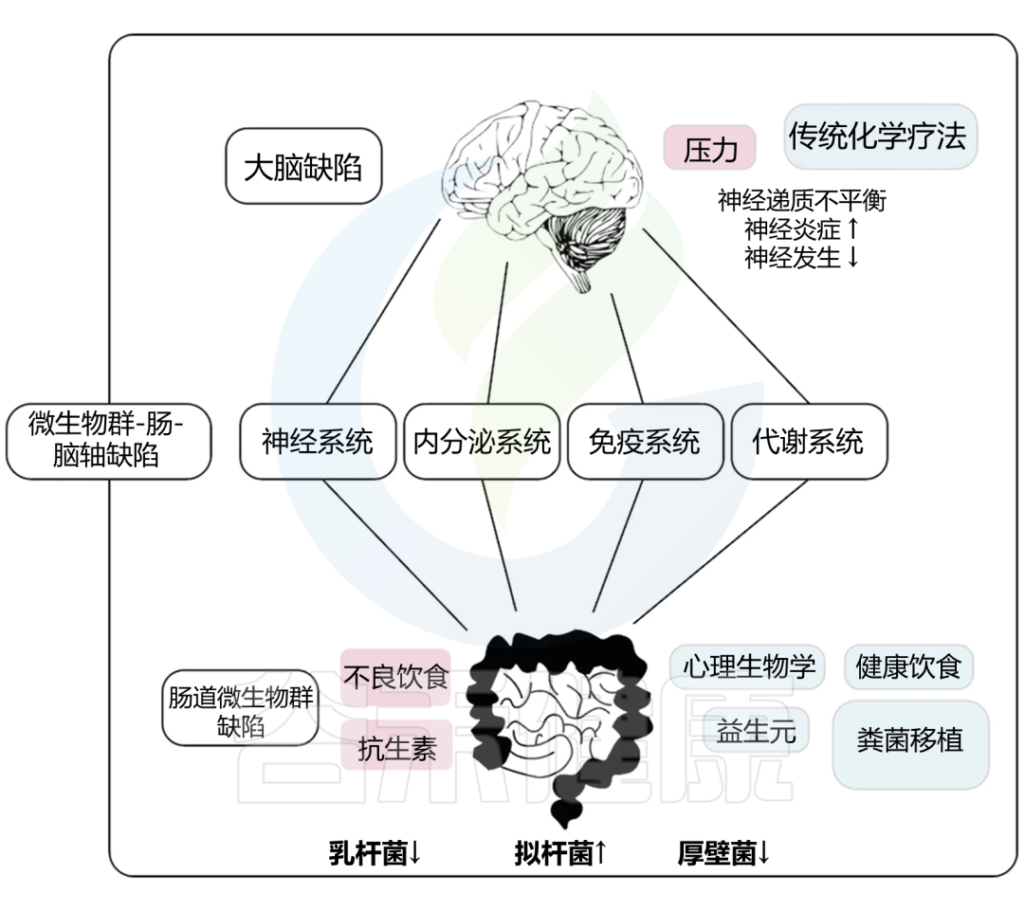
DOI: 10.1007/978-981-19-7376-5_10
▼
微生物群-肠道-免疫-神经胶质轴
微生物群对小胶质细胞稳态的重大贡献,无菌小鼠表现出小胶质细胞的整体缺陷,细胞比例改变和不成熟的表型,导致先天免疫特性受损。
值得注意的是,复杂微生物群的重新定殖,部分恢复了小胶质细胞的特征,而微生物群衍生的短链脂肪酸调节了小胶质细胞的稳态。
神经胶质细胞,包括小胶质细胞、星形胶质细胞、少突胶质细胞和室管膜细胞,与神经元相互作用,影响大脑健康和疾病(如抑郁症)。
神经胶质功能可能由肠道微生物群通过神经和化学信号途径驱动。肠道微生物群对小胶质细胞从促炎到抗炎的激活状态具有重要意义,小胶质细胞功能障碍可以触发抑郁症中神经炎症的信号级联反应。
脑功能、脑小胶质细胞(Iba1)和外周炎症细胞因子的改变(如TNF-α、IL− 1β 、IFN-γ,IL-12)。通过肠-脑轴调节小胶质细胞激活状态(M1、M2)可能是治疗抑郁症的一种有前途的治疗方法。
脑神经炎症中脑-肠-微生物轴(Th17/Treg)
许多临床前和临床研究表明,Th17 和 Treg 细胞对抑郁症有显著影响。
注:
TH17细胞是一种产生促炎细胞因子的T细胞亚群,TH17细胞的异常活化和功能异常与多种炎症性和自身免疫疾病的发生和发展有关,Treg细胞主要通过产生抑制性细胞因子和细胞接触来抑制免疫反应。
TH17细胞和Treg细胞之间的平衡是免疫系统正常功能的重要组成部分。当TH17细胞过度活化或Treg细胞功能受损时,可能导致免疫系统失衡,从而引发炎症性和自身免疫疾病。
肠道 Th17 和 Treg 细胞受到肠道微生物群的调节,而大脑相关的 Th17 和 Treg 细胞则维持免疫稳态,以控制怀孕期间的神经炎症、小胶质细胞激活、星形胶质细胞激活和大脑发育。
值得注意的是,Th17 和 Treg 细胞之间的不平衡,或 Th17/Treg 细胞的比例异常,在抑郁症中发挥着关键作用。
Th17/Treg 细胞是脑神经炎症中脑-肠-微生物轴调节所特别需要的。受肠道微生物群调节的 Th17 和 Treg 细胞之间的不平衡可能会赋予机体抵抗力和对压力的敏感性。
特定的肠道微生物群,如分节丝状菌、梭状芽胞杆菌、脆弱拟杆菌、罗伊氏乳杆菌和双歧杆菌,及其代谢产物如短链脂肪酸和ATP,也参与 Th17/Treg 活性,从而形成 Th17 和 Treg 细胞之间的不平衡。
除了脑神经炎症之外,炎症还可以发生在身体其他部位和系统,比如周围炎症,胃肠道炎症等。
▼
抑郁症和炎症的相互作用就像一个互相助长的恶性循环。炎症是抑郁症发展的主导力量之一。长期的神经炎症会影响大脑功能,这可能会决定个人的情绪和行为。
抑郁症的细胞因子假说来自于观察,即抑郁症的几种症状类似于“疾病行为”,例如嗜睡、发烧、食欲下降、对探索行为或性活动的兴趣下降等。
一些研究人员提出,从进化的角度来看,疾病行为可能是有意义的,因为其中许多行为可能有助于治愈或减少疾病的传播。例如,隔离病人可能会降低他们传播感染的几率。
抑郁症相关炎症因子变化
周围炎症与抑郁症密切相关。抑郁症患者的炎症标志物包括:
血清 IL-6、IL-1β、C反应蛋白升高。
肠道炎症性疾病患者抑郁行为的并发率很高
根据一些报告,患有胃肠道炎症等健康问题的人抑郁和焦虑症状的发生率在统计上有所增加。一些研究人员估计,高达 50-90% 的 IBS患者还同时患有某种精神疾病。
根据最近的《自然》杂志评论,尽管存在明显的异质性,但 IBD 抑郁症状(包括克罗恩病和溃疡性结肠炎)的总体患病率超过 20%。随着时间的推移,抑郁症状加剧与活动性IBD的几率增加有关。
前扣带皮层(ACC)可能是大脑中的一个交叉点,它会感知肠道炎症和不适当的反应,从而增加患抑郁症的风险。
用促炎细胞因子引发炎症的同时诱发抑郁
对人类或动物施用促炎细胞因子进行治疗会诱发抑郁症状。虽然 SSRIs(选择性血清素再摄取抑制剂)通常不会直接减轻“疾病行为”,但据报道,它们可以减少促炎细胞因子,并增加抗炎细胞因子,这一机制也与抑郁症的细胞因子假说一致。
给予脂多糖 LPS 会增加细胞因子的血浆浓度,同时诱发抑郁症状。
然而,抑郁症的正式诊断标准(由 DSM 定义)和“疾病行为”本身之间存在一些细微差别,并且关于炎症是否真的导致抑郁症的证据是相互矛盾的。
并非所有炎症患者都患有抑郁症,也并非所有抑郁症患者都具有高炎症标志物,炎症(可能与血清素缺乏相似)可能只是抑郁症的一个诱因,而不是唯一的直接原因。换句话说,炎症细胞因子的异常调节可能只是一个更加复杂的谜题的一部分,并且需要更多的研究来充分探索这些潜在联系所涉及的机制。
▼
肠粘膜屏障和粘膜免疫系统是帮助防止肠腔内的肠道微生物直接与肠道免疫系统相互作用的两个主要机制。如果这些屏障受到损害,细菌可能会易位,激活免疫系统,从而引发炎症。
注:这些屏障受到损害的情况有时非正式地被称为“肠漏”。
一项动物研究报告称,肠道屏障受损的小鼠表现出与焦虑相关的行为增加,并且一旦肠道屏障恢复或引入益生菌后,这些行为就会消退。
根据一项针对人类的初步研究的作者,IgA 和IgM等血清抗体通常会被激活以对抗有害的肠道细菌。因此,这些抗体的存在是肠道屏障受损的一种潜在生物指标,一项研究甚至报告称,这些抗体水平升高可用于识别抑郁症患者,准确率高达 90%。
尽管这种现象背后的机,但一些研究人员认为“坏”肠道细菌可能通过 TLR4 受体引发炎症。
诱发炎症
LPS 与 TLR4 结合激活免疫细胞,激活NF-κB(一种细胞内信号分子),进而促进促炎细胞因子的产生,包括 TNF-α 和 IL-1 以及环加氧酶-2。
加剧炎症
相同的过程还诱导氧化和亚硝化应激途径,通过进一步激活烟酰胺腺嘌呤二核苷酸磷酸氧化酶来增加诱导型一氧化氮的表达和活性氧 (ROS) 的产生。ROS 超载不仅会激活 NF-κB,还会导致 DNA 损伤和细胞死亡,这两个过程都会加剧炎症状态。
促炎循环——抑郁症
包括干扰素-α、IL-6、IL-1β 和 TNF-α 在内的细胞因子以及氧化和亚硝化应激途径可能会导致紧密连接屏障松动,从而在肠道通透性过高和宿主免疫反应之间形成促炎循环。
这个循环至少部分解释了抑郁症患者慢性低度但持续的炎症状态。
总的来说,这些机制及其影响复杂,值得更多的研究来验证这些初步发现。
▼
激素影响我们身体功能的许多方面,包括新陈代谢、生长、性健康和生殖系统功能。我们的心理健康受到激素的强烈影响,因为激素在情绪的调节中发挥着重要作用。这里我们来了解几种常见的和抑郁症相关的激素。
皮质醇
皮质醇是一种压力激素,由肾上腺分泌。这种激素负责通过选择使用哪种底物以及应消耗多少底物来调节能量。如果皮质醇水平过高或过低,可能会开始出现抑郁症。皮质醇水平低与过度疲劳、难以处理压力情况、不可预测和不稳定的情绪以及性欲下降有关。
雌激素
雌激素在大脑中扮演着重要的角色,它们参与调节神经递质的活动,如血清素、多巴胺和去甲肾上腺素等。这些神经递质与情绪调节密切相关,因此,雌激素的变化可能会对情绪产生影响。
女性患抑郁症的风险要高于男性,这与雌激素和孕激素变化有关。在月经周期、孕期和更年期等生理状态的激素波动可能影响情绪和抑郁症发病风险。
使用雌激素治疗抑郁症的疗效和安全性仍存在争议,因此,使用雌激素治疗抑郁症需要谨慎。
黄体酮
黄体酮有助于平衡体内雌激素水平。它还有助于改善睡眠模式,使人感到更平静。如果黄体酮水平不平衡,可能会变得烦躁或晚上无法入睡,这可能影响抑郁症。
▼
// 短 链 脂 肪 酸
短链脂肪酸在肠腔中具有多种功能,如氧化还原平衡、维持肠屏障完整性、肠道激素产生和表观遗传调节。然而研究表明,短链脂肪酸与抑郁症等精神疾病有关。
短链脂肪酸由肠道微生物群合成,主要由AKK菌、双歧杆菌、粪杆菌、毛螺菌科、乳酸杆菌和瘤胃球菌等物种合成。
短链脂肪酸与抑郁症的关联
已知短链脂肪酸调节神经反应的不同途径,如:
短链脂肪酸诱导肠道神经肽的释放,例如YY肽(YYP)和胰高血糖素样肽2(GLP-2)肽,以及参与维持肠道屏障、细胞代谢和饱腹感的激素。
戊酸与抑郁症有关,主要由Oscillibacter产生。缬草酸的结构与GABA,并可与其受体结合,这可能在严重抑郁障碍中发挥重要作用。
在抑郁症患者的粪便中发现了更高量的异戊酸,这表明微生物群和异戊酸与抑郁症有关。
在一项针对有抑郁症状患者的研究中,粪便中的乙酸盐水平与这些患者呈正相关,而丁酸盐和丙酸盐水平则呈负相关。
在一项针对患有抑郁症的波兰妇女的类似研究中,与非抑郁症患者相比,抑郁症患者粪便中的乙酸盐和丙酸盐水平降低,而异己酸含量增加。这些发现表明,为了保持心理健康,特定的短链脂肪酸水平和微生物群之间必须保持平衡。
// 胆 汁 酸
胆汁中的一种重要成分——胆汁酸,是由肝脏中的胆固醇产生的,它们与肠道菌群协同调节胆固醇代谢,帮助脂质消化和吸收。胆固醇通过肝细胞代谢为原代胆汁酸;之后被输送到胆囊,最终在十二指肠中被释放。到达肠道后,肠道细菌从初级胆汁酸中产生次级胆汁酸(脱氧胆酸和石胆酸)。只有一些细菌,主要是梭菌和真细菌,负责次级胆汁酸的合成。
胆汁酸改变了神经递质受体的功能,如M2和M3毒蕈碱乙酰胆碱、GABA和N-甲基-D-天冬氨酸(NMDA)受体。在对培养的下丘脑神经元的体外研究中,鹅去氧胆酸抑制GABA和NMDA受体。
胆汁酸与抑郁症的关联
中国的一项研究表明,与健康对照组相比,重度抑郁症患者的2,3-脱氧胆酸水平较高,而牛磺酸(TLCA)、甘胆酸(GLCA)和3-硫酸胆酸水平较低,这与汉密尔顿抑郁量表(HAM-D)评分呈负相关。
同样在这项研究中,这些菌Turicibacteraceae、Turicibacteriales和Turicibacter与TLCA和GLCA水平呈正相关。
在美国的另一项研究中,与不太严重的抑郁症患者相比,严重抑郁症患者的原发胆汁酸鹅去氧胆酸水平降低。因此,肠道菌群可以通过胆汁酸改变诱导中枢神经系统疾病,如重度抑郁症。
次级胆汁酸合成的减少会导致微生态失调,并改变肠道屏障的通透性,诱导促炎性基调,从而导致抑郁症的发病机制。
▼
肠道细菌是血液中化学物质(代谢物)的主要调节剂。其中一些是在大脑中制造神经递质的“成分”或“构件”(代谢前体)。
换句话说,这意味着肠道细菌可能能够对某些神经递质的水平和活动产生一些影响,这反过来又可能使它们能够影响大脑活动和行为(尽管是间接的)。
肠道细菌可以通过多种方式调节神经递质的产生
首先,肠道细菌可以合成和分解多种神经递质,如γ-氨基丁酸(GABA)、多巴胺、血清素等。这些神经递质可以通过门脉循环影响迷走神经的传入通路,它们在大脑中起到调节情绪、认知和行为的重要作用。
GABA是大脑中的主要抑制性神经递质。
谷氨酸是大脑中最丰富的兴奋性神经递质,负责在神经细胞之间发送信号,其在大脑中的合成取决于神经元和星形胶质细胞之间的合作,肠道中的肠内分泌细胞亚群能够合成谷氨酸,并利用它通过迷走神经将快速信号传输到大脑。关于谷氨酸详见我们之前的文章:
去甲肾上腺素在中枢神经系统内发挥作用,同时充当应激激素。它有助于“战斗或逃跑”反应,并与唤醒、注意力和聚焦机制相关。
多巴胺参与奖励处理和动机以及运动控制。
肠道微生物群对多巴胺代谢副产物的影响
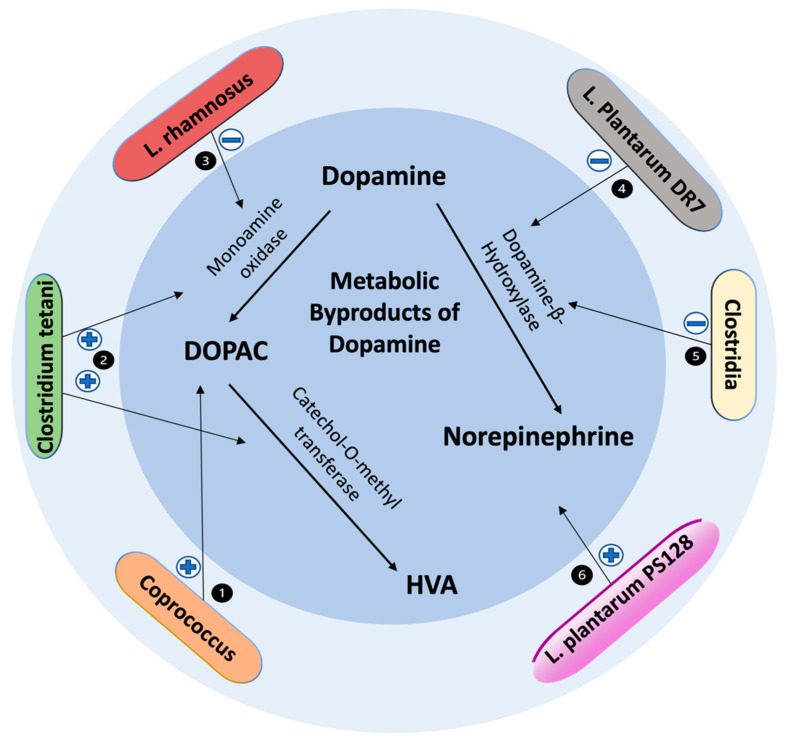
doi: 10.3390/biomedicines10020436
1) 粪球菌属Coprococcus comes和Coprococcus catus与多巴胺合成潜力密切相关
2) 破伤风梭菌对多巴胺具有降解作用,通过多巴胺中间体促进降解为高香草酸
3) 鼠李糖乳杆菌下调MAO
4) 植物乳杆菌DR7下调多巴胺β-羟化酶
5) 梭状芽孢杆菌显示下调多巴胺β-羟化酶
6) 植物乳杆菌PS128给药改善多巴胺代谢并增加去甲肾上腺素水平
血清素,也称为 5-羟色胺 (5-HT),参与调节情绪、食欲、睡眠和其他身体功能。
其次,肠道细菌可以影响神经递质的合成和代谢途径。例如,某些细菌可以产生短链脂肪酸,如丙酸、丁酸和乙酸,这些短链脂肪酸可以促进神经递质的合成和释放。
肠道细菌还可以通过与肠道上皮细胞和免疫系统的相互作用,间接影响神经递质的产生。肠道细菌可以调节免疫系统的活性,影响免疫细胞的分泌和反应,从而影响神经递质的合成和释放。
▼
氨基酸色氨酸是大脑用来产生神经递质血清素的主要“构件”(代谢前体)之一。虽然色氨酸消耗并不总是导致抑郁症,但一些研究人员认为,血清色氨酸偏低有时可能会导致易感人群抑郁症。根据前面,我们可以看出高血清脯氨酸和低血清色氨酸与抑郁症的发展有一定关系。
一些研究表明,某些促炎细胞因子(例如 IFN-α、IFN-γ和TNF-α)水平的增加可能会刺激吲哚胺-2,3-双加氧酶( IDO )的活性,从而在转刺激色氨酸转化为神经毒性化合物,包括犬尿氨酸和喹啉酸。
基于此,一些研究人员认为,可能是这些神经毒性物质,而不是色氨酸消耗本身,可能导致抑郁症的发生。
肠道细菌和炎症可能会影响血清素代谢:
色氨酸代谢途径的犬尿氨酸
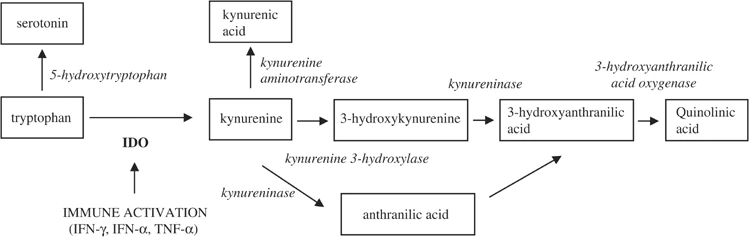
DOI: 10.1038/sj.mp.4001600
扩展阅读:
▼
重度抑郁症患者表现出应激反应系统(例如HPA 轴)过度活跃。它主要表现为腺体反应性增加、激素分泌破坏和负反馈失调。这些疾病可能进一步导致肠道炎症、神经元损伤和皮质醇过度产生,所有这些都与抑郁症相关。
此外,HPA 轴功能障碍的解决与抑郁症的缓解(“治愈”)密切相关,表明它们之间存在某种相互联系。
早期生活压力—肠道菌群—应激反应形成
一项针对大鼠的动物研究报告称,将新生儿从母亲身边带走所产生的压力(母亲分离压力)可能会导致后代肠道微生物组发生巨大的长期变化。母亲分离是早期生活压力的一种模式,它通过改变 HPA 轴、免疫系统和氨基酸代谢以及影响微生物群组成来诱发焦虑和抑郁。
早期生活压力可能使人以后对压力更加敏感。
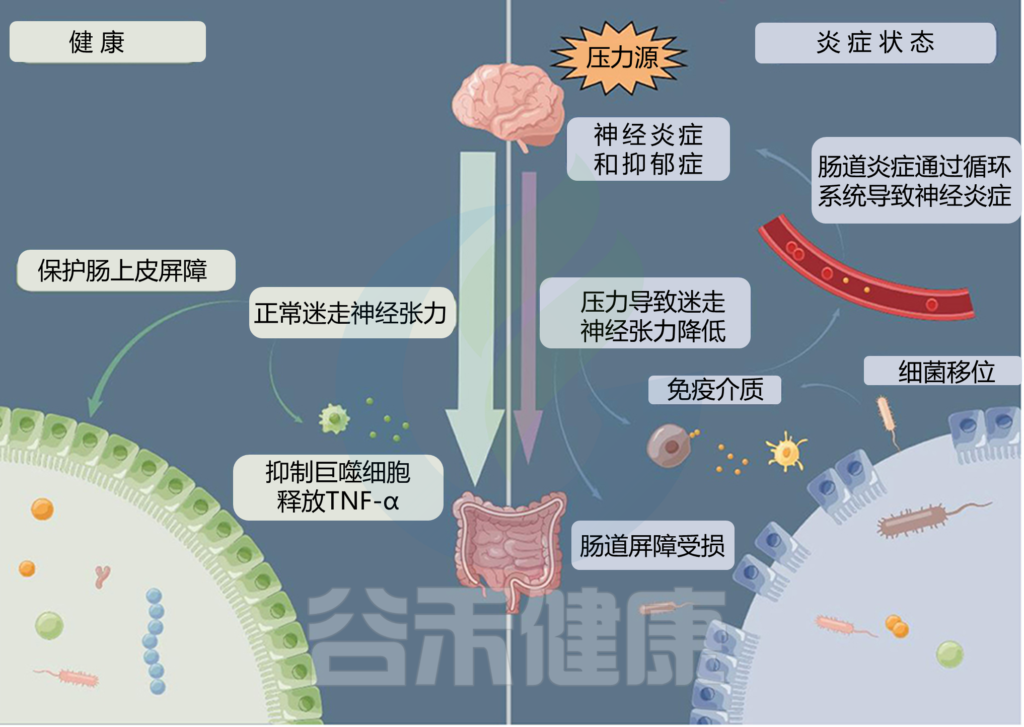
doi.org/10.3389/fneur.2022.1015175
▼
虽然迷走神经无法到达管腔内容物,但它可以通过与肠内分泌细胞的通信间接感知肠道信息。
迷走神经传入将信号从肠道菌群传递到中枢神经系统
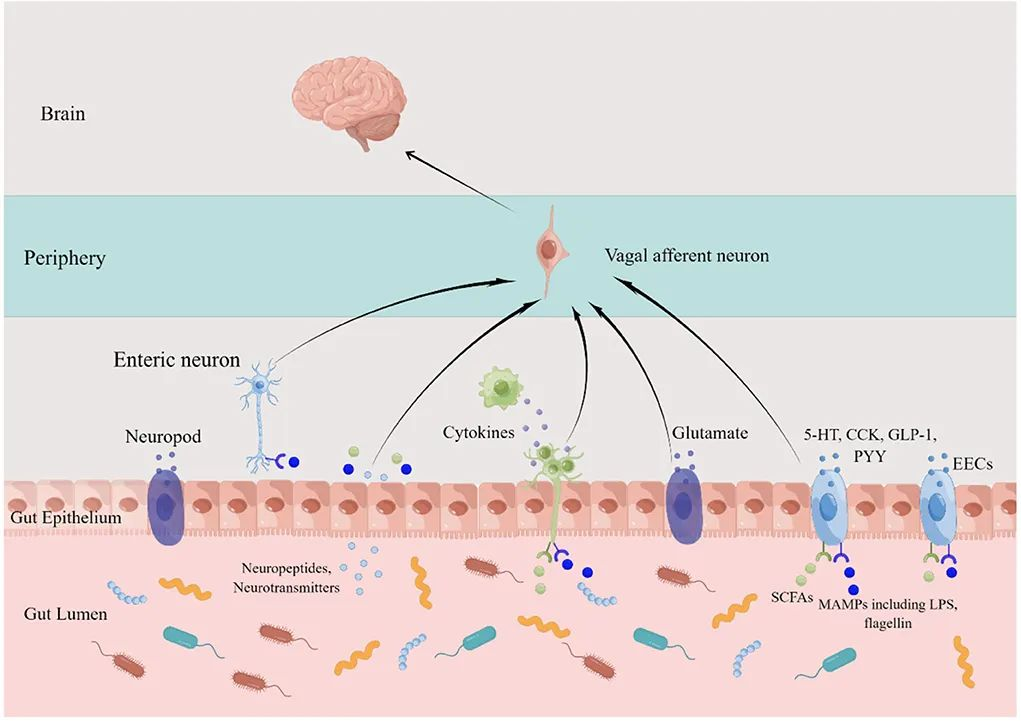
doi.org/10.3389/fneur.2022.1015175
▼
肠道微生物组可能用来与中枢神经系统沟通的其他机制之一是通过肠嗜铬细胞(ECC)和迷走神经。
例如,一些研究人员目前认为肠嗜铬细胞和迷走神经可能参与肠道细菌和大脑之间的通讯,尽管我们仍然不完全了解如何进行。
肠嗜铬细胞感知肠道细菌并分泌血清素
肠嗜铬细胞(ECC) 遍布整个消化道
▼
HPA轴是指下丘脑-垂体-肾上腺轴。HPA轴的功能紊乱可能导致患者出现情绪失调和应激反应的异常。
肠道菌群如何影响 HPA 轴?
肠道菌群失调与炎症之间存在密切关系。这些细胞因子也是 HPA 轴非常有效的激活剂。促炎细胞因子可以干扰皮质醇循环的负反馈,刺激HPA轴的活性。
肠道菌群还可以通过其他能够穿过血脑屏障的介质(例如微生物抗原和前列腺素)刺激 HPA 轴。
除了依赖这些介质之外,细菌还可以直接参与干预过程。例如,LPS和肽聚糖可以通过激活先天免疫系统来激活HPA轴,最终诱发抑郁症)。
还有证据表明,肠道菌群可以直接调节肠道和肾上腺中的类固醇生成,从而增强 HPA 轴反应。
肠道菌群衍生的代谢物也通过体液途径参与调节 HPA 轴。例如,慢性吲哚(拟杆菌属、乳杆菌属和梭菌属)可诱导肾上腺髓质 Pnmt 基因过度表达。它可以与去甲肾上腺素一起增加肾上腺素能系统中儿茶酚胺的生物合成途径。这样,吲哚可以增加小鼠在慢性轻度应激下的脆弱性,最终导致抑郁行为。
除此之外,肠道菌群还可以通过调节 HPA 轴在抑郁症中发挥积极作用。例如,其下游代谢物短链脂肪酸可以降低HPA轴中一些编码蛋白的基因表达,从而减弱HPA轴的应激反应。
最后,肠道菌群还可以影响膈下迷走神经的信号输入。孤束核通过去甲肾上腺素能神经元激活 HPA 轴。
据报道,单胺再摄取抑制剂(MAO-Is) 可以降低糖皮质激素受体抵抗,从而减少 HPA 轴功能障碍。这使得一些研究人员提出,针对大脑 HPA 轴的药物可能是治疗重度抑郁症的潜在有效方法。
▼
如果发现抑郁症的迹象,请及时进行身体检查,帮助确定症状是否可能与抑郁有关,并寻求专业医疗帮助进行抑郁症的诊断和治疗干预。
诊断抑郁症是一个多步骤的过程,通常当有人注意到自己感觉不太像自己时就开始了。在某些情况下,一个人的朋友和家人可能会首先注意到抑郁症的微妙迹象。相关判别方式有:
// 量表
医疗和心理健康专业人员使用既定的、研究支持的指南、筛查工具、检查表和其他标准来帮助他们诊断抑郁症。
DSM-5
心理健康专家可能使用美国精神病学协会出版的《精神障碍诊断与统计手册》(DSM-5) 中列出的抑郁症诊断标准。
注:《精神疾病诊断和统计手册》(DSM)是一本为诊断精神疾病的临床医生提供指南的手册。对每种情况进行分类,并给出一套明确的标准,必须满足这些标准才能做出诊断。
DSM-5 包含了评估自杀风险的新量表:一种针对成人,另一种针对青少年。
要诊断为重度抑郁症,一个人的症状必须符合 DSM-5 中概述的标准。悲伤、情绪低落和对日常活动失去兴趣的感觉必定标志着一个人以前的状态发生了变化,并且持续了至少两周。
这些感觉还必须伴有至少五种其他常见的抑郁症状,包括:
这些症状必定会导致个体出现临床上显著的痛苦或社交、职业或其他重要功能领域的损害。
这些症状不能归因于药物或物质滥用,也不能是由其他身体疾病引起的。
除了DSM-5,还有一些常用的抑郁症量表,用于评估抑郁症的严重程度和症状表现。常见的抑郁症量表包括:
用于评估抑郁症状的程度。
临床评估工具,用于评估抑郁症状的严重程度。
用于评估双相情感障碍,包括抑郁症和躁狂症。
这些量表可以帮助医生更全面地评估抑郁症的症状和严重程度,以指导治疗计划的制定。
抑郁症的诊断主要是基于临床评估和心理评估,其他也包括一些实验室测试来辅助判别。
// 实验室测试
用于识别生物标志物并应用于诊断重度抑郁症的基因组、蛋白质组和代谢分析仍处于起步阶段。
炎症标志物
严重抑郁症与细胞因子或其可溶性受体升高有关,包括:白细胞介素IL-2、可溶性 IL-2 受体 (sIL-2R)、IL-1b、IL-1 受体拮抗剂 (IL-1Ra)、IL -6、可溶性 IL-6 受体 (sIL-6R) 和 γ-干扰素。
一项病例对照研究发现,血清抵抗素(一种细胞因子和代谢标志物)水平与非典型抑郁症症状相关,抑郁症受试者的脂联素水平低于对照组。
BDNF(脑源性神经营养因子)
与对照组相比,抑郁症受试者的血清水平通常较低,并且血清BDNF水平在抗抑郁治疗后升高。血清BDNF可以作为区分单极性和双极性抑郁症的生物标志物。
皮质醇
HPA轴功能障碍已在抑郁症的病因中得到观察。抑郁症患者的高皮质醇血症表现为24小时平均血清皮质醇浓度升高和24小时尿液皮质醇排泄增加。
新型血液测试
一种新的血液测试被描述用于重度抑郁症的诊断。该测试由9种生物标志物组成,包括α-1抗胰蛋白酶、载脂蛋白CIII、BDNF、皮质醇、表皮生长因子、髓过氧化物酶、催乳素、抵抗素、可溶性肿瘤坏死因子αII型,均通过标准免疫测定进行测量。
促甲状腺激素
促甲状腺激素(TSH)被纳入并单独报道,用于评估抑郁症的总体评估中的甲状腺功能减退或甲状腺功能亢进。内源性抑郁症患者的基础血清TSH水平通常较低,从基线到峰值的TSH变化也较低。抑郁症可能与亚临床甲状腺功能减退或轻度甲状腺功能衰竭有关。
肠道菌群健康检测
某些菌群的异常与抑郁症之间可能存在相关性。肠道菌群检测可以在抑郁症的早期进行风险提示,当临床症状不明显或存在疑难病例时,结合肠道菌群检测结果,可以提供更加全面的信息,辅助医生进行准确的诊断。
▼
有时候,我们口头说的“抑郁症”很多情况是短暂的抑郁情绪,还不是重度抑郁症,可以趁抑郁症在早期阶段,通过改变生活方式对其进行干预和管理。
// 饮 食
饮食选择显著影响其他身体系统,例如内分泌、免疫和胃肠道系统。
避免不健康饮食
限制摄入食品添加剂、糖、饱和脂肪酸和精制碳水化合物等。
近年来,研究表明,西方饮食中富含加工或油炸食品、糖、精制谷物和酒精,与抑郁和焦虑症状呈正相关。2020 年的一项研究发现,食用加工食品会引发体内炎症,并对免疫系统产生连锁反应,可能会增加出现抑郁症状的风险。
富含脂肪的饮食可能促进焦虑和抑郁的发展或持续。高脂肪摄入不仅会导致肥胖,还会引起身体系统广泛的炎症。肠道微生物组可能会改变高脂肪饮食的有害影响,改善情绪和行为。
通过避免受污染的食物,改善饮食质量,增强身体的免疫力,并有助于抑郁症的治疗和康复。环境重金属污染的食物可能会含有铅、汞、镉等有害物质,海鲜也是需要格外关注的食物类型,因为海产品往往容易受到汞等重金属的污染。抑郁症患者需要特别留意,避免摄入这些污染物。
高脯氨酸食物与抑郁症相关
来自西班牙巴塞罗那赫罗纳生物医学研究所 (IDIBGI) 和庞培法布拉大学 (UPF) 的研究人员发现,较高的脯氨酸摄入量与抑郁症的发展有关。这项研究的结果发表在《细胞代谢》杂志上。
为了更多地了解饮食是否会导致抑郁症的发生,IDIBGI 研究人员将大约 100 名受试者分为三类:非抑郁症、轻度抑郁症和重度抑郁症。从那里,他们分析了抑郁症诊断与肠道微生物组组成之间是否存在关系。
通过对氨基酸的代谢物分析,研究人员能够将体内脯氨酸与抑郁症评分最紧密地联系起来。
为了了解这种脯氨酸从何而来,研究人员依靠包含参与者饮食信息的调查问卷。脯氨酸再次成为对抑郁症影响最大的饮食因素。
在健康的受试者中,脯氨酸的摄入量是与抑郁评分最相关的项目。在进一步确定小鼠体内脯氨酸/抑郁症的联系后,研究人员试图通过将人类受试者的肠道细菌移植到小鼠体内来证实他们的发现。接受脯氨酸含量最高的细菌的小鼠表现出更多的抑郁症状。
什么是脯氨酸?
我们体内的蛋白质由 20 种特定氨基酸的各种组合组成,其中 9 种被认为是“必需的”。身体无法自行制造这九种氨基酸,我们需要通过饮食摄入它们。
脯氨酸是一种非必需氨基酸,这意味着我们的身体在生命的大多数阶段都可以产生足够的量。然而,在压力、康复或成长时期,这种氨基酸变得至关重要,因为我们的需求量超过了我们身体的制造量。
富含脯氨酸的食物
脯氨酸主要存在于许多动物源食品中。“脯氨酸最重要的来源是明胶和动物皮,这些食物富含胶原蛋白,是这种氨基酸的天然来源。
事实上,脯氨酸约占胶原蛋白总氨基酸的 10%。因此,含有胶原蛋白的食物,如骨头汤、鸡翅(带皮)、猪皮和明胶,是这种氨基酸的丰富来源。
大多数肉类、鱼类和乳制品也含有脯氨酸。
需要避免脯氨酸来降低抑郁风险吗?
根据这些结果,看起来有必要从饮食中去除任何含有脯氨酸的食物,以降低患抑郁症的风险。
根据研究作者和我们经验还是不要那么绝对。毕竟许多富含脯氨酸的食物,包括肉类、鱼类和奶制品,都富含对正常生长、发育和免疫支持至关重要的营养素。
在建议减少饮食中这部分食物之前,我们认为需要进行更多的研究。
当然,关于抑郁症的饮食干预不只是避免某些食物的摄入,而是要建立一个全面健康的饮食习惯。
健康饮食
2019 年的一项研究发现,富含水果、蔬菜、鱼类和瘦肉的健康饮食有助于降低抑郁症的临床水平。
有研究发现西班牙护理学生坚持地中海饮食与心理健康问题之间存在很强的相关性。坚持地中海饮食的参与者比没有坚持的人的焦虑和抑郁分数要低得多。
地中海饮食(主要是纤维、鱼和全谷物),已被证明可以通过增加产短链脂肪酸菌丰度来调节肠道菌群组成,从而减少抑郁症的发作。
也有研究发现强有力的证据表明,适度限制热量的健康饮食有助于改善抑郁症状。
多酚还被证明可以通过抑制参与氧化应激和炎症的丝裂原激活蛋白激酶途径来改善抑郁症状。多酚还作为益生元为微生物提供营养,两者相辅相成。
一项干预性随机临床试验表明,富含类黄酮的橙汁可以通过增加BDNF和毛癣菌科Trichophyton来缓解抑郁症。
总的来说,富含 omega-3 多不饱和脂肪酸 (PUFA) 的食物,大量摄入蔬菜、水果、鱼、橄榄油、大豆、全谷物的健康饮食模式可能与降低抑郁风险相关。
相关阅读:
// 动起来
缺乏身体活动是抑郁和焦虑的常见危险因素。在治疗重度抑郁症方面有大量研究表明,体育锻炼已被证明有助于预防、缓解和治疗症状。
定期锻炼对身体有好处,有助于增强力量和健康,而且对大脑和神经系统也有帮助。在剧烈运动期间,身体会释放内啡肽和多巴胺等神经递质,这有助于增加愉悦感和幸福感。
// 注重睡眠质量
睡眠质量是幸福感的重要指标。80% 的抑郁症患者自我报告存在睡眠障碍。晚上适当的休息(不要太多或太少)是控制抑郁症和保持精力充沛的好方法。为了达到最佳健康状态,建议七到八小时。
除了适当的休息之外,充足的睡眠还有助于注意力、认知、记忆形成和情绪调节。
如果有睡眠问题,请持续保持良好的睡眠习惯。比如收起电子产品,睡前写日记,并制定一个轻松的睡前习惯来放松身心。
如果睡眠无法改善,请寻求医生的帮助。
// 冥想正念
当您处于抑郁状态时,很容易陷入消极的想法和情绪中。正念、冥想和呼吸练习可以成为抵御压力和焦虑、让你的大脑专注于当下的一种方法。还可以将正念应用于创造性追求,其中可能涉及日记、绘画、唱歌、玩耍、跳舞等活动。
从生物学角度来看,冥想对某些生理功能具有积极、显著的影响。练习冥想可以影响大脑结构、大脑网络,保持自主神经系统的稳态,甚至影响我们基因的运作方式。
练习正念也可以导致知觉转变。你的想法和情绪不再被视为压倒性的事件,而是一个有助于洞察和平静的时刻。
// 走出去,感受新鲜空气
抑郁症的症状之一是很难起床,完成基本任务可能需要付出巨大的努力。如果忽视户外活动而更多地待在室内,可能会扰乱睡眠和昼夜节律,并导致维生素D 不足。
维生素D 水平下降与抑郁症之间可能存在关联。尽管研究仍然很少,但越来越多的研究表明维生素D 可以在缓解抑郁症方面发挥治疗作用。然而,它在促进免疫功能健康、细胞生长和维持骨骼健康方面的益处是众所周知的。
为了摆脱抑郁症,充足的自然阳光照射有助于满足每日维生素D。拥抱自然疗法,感受皮肤上的阳光,并在街区周围散步以改变环境。
// 依靠爱的人
当你感到沮丧时,你很容易孤立并拒绝与人交往的尝试。或者你可能在人群中却仍然感到孤独。然而,人类天生就是社会性动物。如果你的社会支持质量下降,它可能会加剧抑郁症状,并产生更多的孤独、内疚、羞耻和疏远感。
建议适当社交,是提高自尊、适应力、爱的途径——所有这些都有助于产生积极的心理健康结果。数十年的研究证明,与社区的较高社会关系质量与降低压力水平和抑郁症状有关。
哈佛大学成人发展研究对幸福进行了一项长期研究,发现人际关系可以产生精神和情感刺激(情绪助推器),并有助于抵消孤立感。哈佛大学的研究人员指出,人际关系是幸福和生活满意度的有力预测因素。
// 尽可能寻找感激之情和欢笑
有可靠的科学证据表明,感恩可以改善认知和情感健康。研究的一项感恩干预措施是使用感恩情,在其中列出几周内每天让你感激的三到五件事。感恩练习有助于增加积极情绪、主观幸福感、生活满意度,并减少抑郁症状。
研究发现幽默可以成为对抗抑郁症状和焦虑的重要应对机制。当你沮丧时,很难从任何事情中找到乐趣。即便如此,寻找令人愉快的活动仍然是件好事,比如观看搞笑的单口喜剧、拥抱宠物、沉迷于一部让人感觉良好的电影、听音乐、犒赏自己一个热水澡,或者点你最喜欢的饭菜。做任何你喜欢做的事都可以带来快乐。
// 尝试摆脱情绪低落的小技巧
-简化生活,管理时间
列出日常任务清单,使用提醒便签,或者使用计划表有助于保持生活有条不紊。尽可能减少责任,为自己设定合理的目标。当感觉情绪低落时,允许自己少做一些事情。当感到沮丧时避免做出重大决定。
-写日记
作为治疗的一部分,可以通过表达痛苦、愤怒、恐惧或其他情绪来改善心情。
-阅读
阅读知名的自助书籍和网站。医生或治疗师会推荐书籍或网站以供阅读。
-战胜拖延
抑郁症的症状,例如疲劳和注意力不集中,很容易拖延。拖延事情会加剧抑郁。它会导致增加内疚、担忧和压力。制定短期目标并努力首先完成最重要的事情。成功完成的每一项任务都会帮你打破拖延的习惯。
-尝试社交或找到有用的团体
尝试参加社交活动,定期与家人或朋友聚会。许多组织支持联盟,提供教育、互助组、咨询和其他资源来帮助治疗抑郁症。参加各种心理小组也可以为心理健康问题提供帮助。抑郁症患者互助组可以与其他面临类似问题的患者建立联系并分享经验。
-避免酗酒
酒精似乎可以减轻抑郁症状,但从长远来看,它们通常会加重症状,使抑郁更难治疗。
▼
可以通过肠道菌群检测,了解整体菌群结构和异常指标,进行个性化干预。
如果发现核心菌属丰度低,有害菌丰度高,菌群结构紊乱,那么可以配合使用抗生素或益生元等抑制过多有害菌,加以改善。
或者通过粪菌移植的方式适当改变菌群结构,从而有效改善。
发现异常菌群,可以针对缺乏菌群,通过补充益生菌,功能性补充剂等方式加以改善。
// 益生菌 & 益生元
益生菌
最近的荟萃分析和系统综述证实了益生菌在临床研究中的抗抑郁功效。相关动物研究也表明,这种作用与肠道菌群结构的调节有关。
研究人员使用罗伊氏乳杆菌(Lactobacillus reuteri )干预CUMS小鼠,发现只有恢复乳杆菌水平才足以改善与应激相关的代谢变化和行为异常。
在另一项研究中,热灭菌的短双歧杆菌可以调节肠道菌群成分,从而预防慢性社交失败压力引起的抑郁症状。这种具有功能性食物成分的菌株可以用作新的疗法。


编辑
doi: 10.7759/cureus.40293
益生元
每天 5 克的低聚半乳糖和 1 克或以下的二十碳五烯酸可以有效缓解抑郁症状。虽然 EGCG 具有潜在的抗抑郁特性,但可能需要 3 克/天的较高剂量才能产生显着效果。
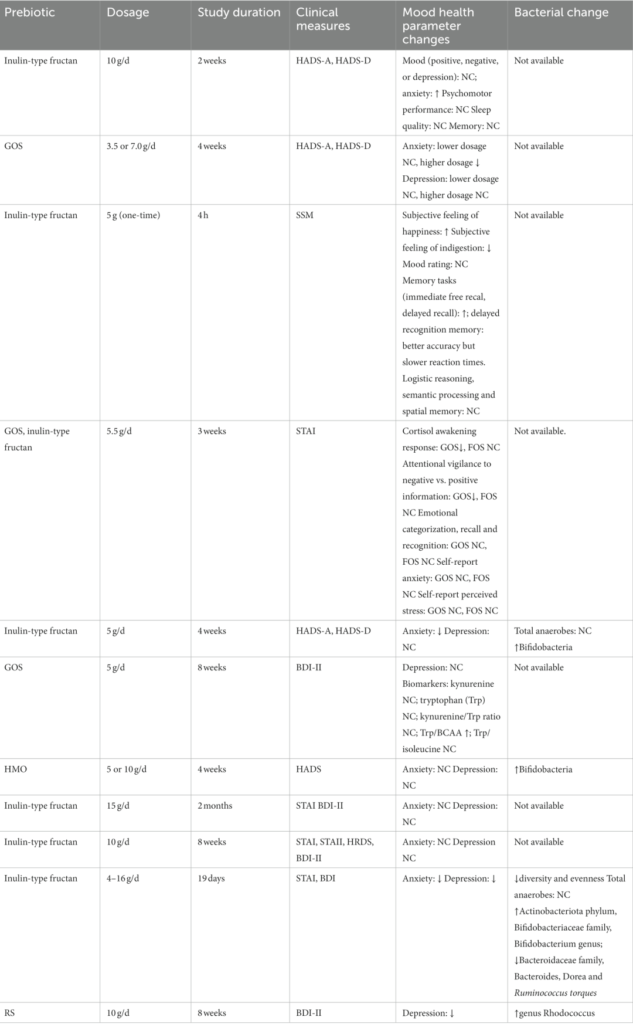
doi.org/10.3389/fnut.2023.1206468
益生菌和益生元联合给药
研究表明,益生菌和益生元的联合给药可以达到更大的抗抑郁效果。益生元的显著营养作用可能会提高益生菌的存活率,从而增强益生菌的抗抑郁能力。
没有相关研究报告益生菌引起的戒断反应和副作用等问题,这似乎是一种很有前途的抑郁症干预措施。益生菌菌株、剂量和方法的最佳组合尚不精确。为了解决这些问题,还需要更多的随机、双盲、安慰剂对照试验来解开这个谜题。
// 粪菌移植
一种直接干扰肠道菌群的方法是粪便微生物群移植(FMT)。它在抑郁症和微生物结构紊乱方面的优异表现使我们看到了新的治疗方向。
在一项动物研究中,NLRP3 KO菌群移植显著改善了受体小鼠的抑郁样行为。在他们的研究中,FMT机制主要依赖于抑制抑郁小鼠中circHIPK2的表达。
在人类受试者中,FMT也显示出类似的效果。在一份FMT作为抑郁症辅助治疗的病例报告中,入选的患者表现出抑郁症状的改善、肠道菌群多样性的增加以及胃肠道症状的缓解。
然而,这种影响并不持久,他们推测FMT的疗效与供体和受体的微生物相似性有关。FMT面临的主要挑战是提高成功率、最佳交付途径、捐赠者选择和其他需要探索的问题。
▼
// 药物
N-乙酰半胱氨酸(NAC)
NAC 通过其抗氧化、抗炎和谷氨酸调节活性,可能在多种精神疾病的治疗中发挥作用。
身体使用N-乙酰半胱氨酸(NAC)来制造自身的抗氧化剂。医学上,NAC用于治疗对乙酰氨基酚中毒;只要在服药过量后的前 8 小时内服用,几乎 100% 有效。
根据对多项单独研究数据(包括 574 名抑郁症患者和健康参与者的数据)的一项审查,据报道,NAC 在使用 3-6 个月内有可能改善抑郁症状和整体日常功能。此外,据报道,抑郁症患者的情绪在 3-4 个月后得到改善。
NAC 还可以通过减少大脑的氧化应激来平衡情绪。例如,一项针对 76 名抑郁症患者的研究报告称,服用 NAC 的患者大脑抗氧化水平较高。
以上益处仅得到有限的小规模临床研究的支持。在 NAC 推荐临床之前需要进行更长时间、更有力度的研究。
选择性血清素再摄取抑制剂(SSRI)
医生通常会先开一种 SSRI 药物。通常认为这些药物更安全,所产生的不适副作用一般少于其他类型的抗抑郁药。SSRI 药物包括西酞普兰(Celexa)、艾司西酞普兰(Lexapro)、氟西汀(Prozac)、帕罗西汀(Paxil、Pexeva)、舍曲林(Zoloft)、维拉佐酮(Viibryd)
血清素-去甲肾上腺素再摄取抑制剂(SNRI)
SNRI 药物包括度洛西汀(Cymbalta)、文拉法辛(Effexor XR)、地文拉法辛(Pristiq、Khedezla)和左米那普仑(Fetzima)
非典型抗抑郁药
这些药物不太适合归入其他任何抗抑郁药类别。这些药物包括安非他酮(Wellbutrin XL、Wellbutrin SR、Aplenzin、Forfivo XL)、米氮平(Remeron)、奈法唑酮、曲唑酮和伏硫西汀(Trintellix)。
三环类抗抑郁药
例如丙米嗪(Tofranil)、去甲替林(Pamelor)、阿米替林、多塞平、曲米帕明(Surmontil)、地昔帕明(Norpramin)和普罗替林(Vivactil)等这些药物可能都很有效,但是副作用往往比新型的抗抑郁药更严重。因此通常不会开三环类药物,除非您已经用过 SSRI,却没有起色。
单胺氧化酶抑制剂(MAOI)
反苯环丙胺(Parnate)、苯乙肼(Nardil)和异卡波肼(Marplan)等 MAOI 药物会产生严重的副作用,因此,一般在其他药物没有疗效的情况下才会开这些药物。使用 MAOI 时需要严格控制饮食,因为这类药物会和某些奶酪、泡菜、葡萄酒等食物以及某些药物和草本补充剂发生相互作用,危险甚至致命。司来吉兰(Emsam)是一种新型 MAOI,可以作为垫片贴在皮肤上,副作用少于其他 MAOI 药物。这类药物不能和 SSRI 药物联合使用。
鼻内艾氯胺酮
新药物,例如鼻内艾氯胺酮,可以快速发挥抗抑郁作用,特别是对于难治性抑郁症患者。以鼻喷雾剂的形式提供,通常在几个小时内迅速起效,缓解抑郁症状。使用艾氯胺酮的人通常会继续服用口服抗抑郁药以维持症状的改善。
多种药物
有时候可能需要尝试几种药物或联合用药,然后才能找到有效的药物。这需要耐心,因为对有些药物而言,完全起效及其副作用随着身体调整而缓解,需要数周或更长时间。
突然停药的风险
抗抑郁药需要一段时间(通常需要 4-8 周)才能发挥作用,睡眠、食欲和注意力问题通常会在情绪好转之前得到改善。
咨询医生前,请不要停止服用抗抑郁药。抗抑郁药一般不会上瘾,但有时会产生身体依赖性(这与上瘾不同)。突然停止治疗或多次漏服药物可能导致类似戒断的症状,突然放弃治疗可能导致抑郁症恶化。配合医生,逐渐安全减小剂量。
// 中药类
早在中国汉代,张仲景就记载了治疗抑郁症的经典方剂,但其具体药理机制尚不清楚。在最近的研究中,一些中药的抗抑郁作用已被证明与肠道菌群相关。
例如,舒肝颗粒可以显著改善慢性约束应激小鼠的异常行为和海马炎症。后续的机制研究表明,其给药丰富了小鼠肠道中的丁酸单胞菌和节疣念珠菌,降低了拟杆菌的丰度,并与PI3K/Akt/mTOR途径密切相关。
五味子可以通过抑制TLR4/NF-κB信号通路来减轻抑郁小鼠的肠道微生态失调。
除了调节炎症,中药还在调节神经递质水平方面发挥作用。
莲心碱治疗可以缩短抑郁小鼠的不动时间,增加海马中的DA、5-HT和NE等神经递质。同时,小鼠结肠中乳酸杆菌的相对丰度也有所增加。
在另一项研究中,特异性抗抑郁药中药的靶点可以集中在嘌呤代谢的调节上。与中药相关的动物研究,如肉苁蓉和藏红花酸,表明它们的抗抑郁作用与肠道菌群的调节密切相关。
除了动物研究,临床研究也提供了相应的证据。对患有抑郁症的癌症患者使用中药复方小柴胡汤进行干预。给药后,受试者的抑郁症状减轻,肠道微生态失调得到部分逆转(特别是减少了副拟杆菌、Blautia和瘤胃球菌科细菌的丰度)。有趣的是,这种抗抑郁的草药也表现出一些抗肿瘤作用,其潜在机制涉及TLR4/MyD88/NF-κB信号传导。
值得注意的是,这些途径在涉及微生物群的抑郁症发病机制中也发挥着重要作用。最近的系统综述和荟萃分析也表明,与抗抑郁药相比,中药可以减少不良事件。鉴于目前的研究数量有限,准确总结中药治疗抑郁症的益处和风险还为时过早。
// 专业治疗
一旦注意到抑郁症的迹象或症状,与心理健康专家交谈将是至关重要的一步。值得信赖的治疗师可以识别模式,帮助情绪调节。
心理治疗
几种类型的心理治疗(也称为谈话疗法或咨询),可以通过教抑郁症患者新的思维和行为方式以及如何改变导致抑郁的习惯来帮助他们。
治疗抑郁症的循证方法包括:
一种谈话疗法,旨在帮助改变任何可能导致或恶化抑郁症的消极思想或行为模式。这种疗法通常也是短期的,重点是解决当前的问题并学习新的应对技巧。
治疗师通过帮助个体识别和处理与人际关系有关的困难,以及改善与他人的交流方式,来促进情绪上的积极变化。 解决几个常见的人际问题,包括失去、冲突、角色变化和人际孤立感。个体可以增强情感的稳定性和归属感,提高应对人际问题的能力。
心理健康服务远程医疗的发展提供了面对面治疗的替代方案,在某些情况下使人们更容易、更方便地获得帮助。对于过去可能对寻求心理健康护理犹豫不决的人来说,远程心理健康服务可能是比传统心理健康服务更容易的第一步。
脑刺激疗法
如果药物或心理治疗不能减轻抑郁症状,脑刺激疗法可能是一种值得探索的选择。
拥有最多证据的脑刺激疗法包括:
ECT 和 rTMS 是使用最广泛的脑刺激疗法,其中 ECT 的使用历史最长。
替代疗法
每日晨光疗法是季节性情感障碍患者的常见治疗选择。光疗设备比普通室内照明明亮得多,被认为是安全的,但患有某些眼病或服用增加对阳光敏感性的药物的人不建议。
抑郁症不仅仅是一种精神疾病,还具有生理和解剖学改变,本文我们了解了抑郁症相关的基本知识,以及肠道菌群在抑郁症发展和症状表现中的重要性。深入了解抑郁症和肠道菌群之间的相互影响将有助于未来开发更有效的治疗策略,并提高患者的生活质量。
我们应该全面认识抑郁症,意识到其不仅仅是一种心理问题,而是一个涉及多个身体系统的综合性障碍。除了对心理状态的影响外,抑郁症还可以引起神经系统、免疫系统、心血管系统以及睡眠障碍等多方面的变化。
目前对于微生物组在口腔-肠道-脑轴中的作用已经有了一定的认识,这是一个重要的研究方向,从病理生理学到调节肠道微生物组对精神疾病产生影响。关于口腔微生物群与精神疾病的关联详见本次推文第二篇:
这些身体系统的紊乱可能进一步加剧抑郁症的症状,并对患者的整体健康状况产生负面影响。
在临床实践中,针对抑郁症的治疗需要不同科室的医生共同合作。未来更多需要整合心理治疗、药物治疗、营养治疗和包括菌群检测在内的综合性健康管理等多个领域的专业知识与技术,实施多学科联合治疗,为抑郁症的治疗提供全新的视角,并为未来研究和改进抑郁症治疗策略提供宝贵的经验。
吾日三省吾身:
每天给予自己足够的关怀和爱吗?
对自己的身心健康变化是否警觉并感兴趣?
是否意识到自己的情绪,并且能够充分处理和接纳它们?
…
希望大家都能健康快乐,远离抑郁。
注:本账号内容仅作交流参考,不作为诊断及医疗依据。
相关阅读:
环境污染物通过肠脑轴影响心理健康,精神益生菌或将发挥重要作用
主要参考文献:
Basiji K, Sendani AA, Ghavami SB, Farmani M, Kazemifard N, Sadeghi A, Lotfali E, Aghdaei HA. The critical role of gut-brain axis microbiome in mental disorders. Metab Brain Dis. 2023 Jul 12. doi: 10.1007/s11011-023-01248-w. Epub ahead of print. PMID: 37436588.
Chang L, Wei Y, Hashimoto K. Brain-gut-microbiota axis in depression: A historical overview and future directions. Brain Res Bull. 2022 May;182:44-56. doi: 10.1016/j.brainresbull.2022.02.004. Epub 2022 Feb 11. PMID: 35151796.
Bradlow RCJ, Berk M, Kalivas PW, Back SE, Kanaan RA. The Potential of N-Acetyl-L-Cysteine (NAC) in the Treatment of Psychiatric Disorders. CNS Drugs. 2022 May;36(5):451-482.
Chen Y, Xu J, Chen Y. Regulation of Neurotransmitters by the Gut Microbiota and Effects on Cognition in Neurological Disorders. Nutrients. 2021 Jun 19;13(6):2099. doi: 10.3390/nu13062099. PMID: 34205336; PMCID: PMC8234057.
Smith KM, Renshaw PF, Bilello J. The diagnosis of depression: current and emerging methods. Compr Psychiatry. 2013 Jan;54(1):1-6. doi: 10.1016/j.comppsych.2012.06.006. Epub 2012 Aug 15. PMID: 22901834; PMCID: PMC5502713.
Joe Cohen, BS. How Depression May Be Linked To Gut Microbes. 2022.12.selfhacked.
Major Depressive Disorder Working Group of the Psychiatric GWAS Consortium; Ripke S, Wray NR, Lewis CM, Hamilton SP, Weissman MM, et al., A mega-analysis of genome-wide association studies for major depressive disorder. Mol Psychiatry. 2013 Apr;18(4):497-511.
Zeng Y, Navarro P, Xia C, Amador C, Fernandez-Pujals AM, Thomson PA, Campbell A, Nagy R, Clarke TK, Hafferty JD, Smith BH, Hocking LJ, Padmanabhan S, Hayward C, MacIntyre DJ, Porteous DJ, Haley CS, McIntosh AM. Shared Genetics and Couple-Associated Environment Are Major Contributors to the Risk of Both Clinical and Self-Declared Depression. EBioMedicine. 2016 Dec;14:161-167.
Sharma A. Systems Genomics Support for Immune and Inflammation Hypothesis of Depression. Curr Neuropharmacol. 2016;14(7):749-58.
Flint J, Kendler KS. The genetics of major depression. Neuron. 2014 Feb 5;81(3):484-503. doi: 10.1016/j.neuron.2014.01.027. Erratum in: Neuron. 2014 Mar 5;81(5):1214.
Brundin L, Sellgren CM, Lim CK, Grit J, Pålsson E, Landén M, Samuelsson M, Lundgren K, Brundin P, Fuchs D, Postolache TT, Traskman-Bendz L, Guillemin GJ, Erhardt S. An enzyme in the kynurenine pathway that governs vulnerability to suicidal behavior by regulating excitotoxicity and neuroinflammation. Transl Psychiatry. 2016 Aug 2;6(8):e865.
Lohoff FW. Overview of the genetics of major depressive disorder. Curr Psychiatry Rep. 2010 Dec;12(6):539-46.
González-Arancibia C, Urrutia-Piñones J, Illanes-González J, Martinez-Pinto J, Sotomayor-Zárate R, Julio-Pieper M, Bravo JA. Do your gut microbes affect your brain dopamine? Psychopharmacology (Berl). 2019 May;236(5):1611-1622. doi: 10.1007/s00213-019-05265-5. Epub 2019 May 17. PMID: 31098656.
Qin J, Li R, Raes J, Arumugam M, Burgdorf KS, Manichanh C, Nielsen T, Pons N, Levenez F, Yamada T, Mende DR, Li J, Xu J, Li S, Li D, Cao J, Wang B, Liang H, Zheng H, Xie Y, Tap J, Lepage P, Bertalan M, Batto JM, Hansen T, Le Paslier D, Linneberg A, Nielsen HB, Pelletier E, Renault P, Sicheritz-Ponten T, Turner K, Zhu H, Yu C, Li S, Jian M, Zhou Y, Li Y, Zhang X, Li S, Qin N, Yang H, Wang J, Brunak S, Doré J, Guarner F, Kristiansen K, Pedersen O, Parkhill J, Weissenbach J; MetaHIT Consortium; Bork P, Ehrlich SD, Wang J. A human gut microbial gene catalogue established by metagenomic sequencing. Nature. 2010 Mar 4;464(7285):59-65.
Bercik P, Collins SM, Verdu EF. Microbes and the gut-brain axis. Neurogastroenterol Motil. 2012 May;24(5):405-13.
Mayneris-Perxachs J, Castells-Nobau A, Arnoriaga-Rodríguez M, Martin M, de la Vega-Correa L, Zapata C, Burokas A, Blasco G, Coll C, Escrichs A, Biarnés C, Moreno-Navarrete JM, Puig J, Garre-Olmo J, Ramos R, Pedraza S, Brugada R, Vilanova JC, Serena J, Gich J, Ramió-Torrentà L, Pérez-Brocal V, Moya A, Pamplona R, Sol J, Jové M, Ricart W, Portero-Otin M, Deco G, Maldonado R, Fernández-Real JM. Microbiota alterations in proline metabolism impact depression. Cell Metab. 2022 May 3;34(5):681-701.e10.
David LA, Maurice CF, Carmody RN, Gootenberg DB, Button JE, Wolfe BE, Ling AV, Devlin AS, Varma Y, Fischbach MA, Biddinger SB, Dutton RJ, Turnbaugh PJ. Diet rapidly and reproducibly alters the human gut microbiome. Nature. 2014 Jan 23;505(7484):559-63.
Bailey MT, Dowd SE, Galley JD, Hufnagle AR, Allen RG, Lyte M. Exposure to a social stressor alters the structure of the intestinal microbiota: implications for stressor-induced immunomodulation. Brain Behav Immun. 2011 Mar;25(3):397-407.
Diaz Heijtz R, Wang S, Anuar F, Qian Y, Björkholm B, Samuelsson A, Hibberd ML, Forssberg H, Pettersson S. Normal gut microbiota modulates brain development and behavior. Proc Natl Acad Sci U S A. 2011 Feb 15;108(7):3047-52.
Desbonnet L, Garrett L, Clarke G, Kiely B, Cryan JF, Dinan TG. Effects of the probiotic Bifidobacterium infantis in the maternal separation model of depression. Neuroscience 170: 1179-1188
Bercik P, Denou E, Collins J, Jackson W, Lu J, Jury J, Deng Y, Blennerhassett P, Macri J, McCoy KD, Verdu EF, Collins SM. The intestinal microbiota affect central levels of brain-derived neurotropic factor and behavior in mice. Gastroenterology. 2011 Aug;141(2):599-609, 609.e1-3.
Huang R, Wang K, Hu J. Effect of Probiotics on Depression: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. Nutrients. 2016 Aug 6;8(8):483.
Akkasheh G, Kashani-Poor Z, Tajabadi-Ebrahimi M, Jafari P, Akbari H, Taghizadeh M, Memarzadeh MR, Asemi Z, Esmaillzadeh A. Clinical and metabolic response to probiotic administration in patients with major depressive disorder: A randomized, double-blind, placebo-controlled trial. Nutrition. 2016 Mar;32(3):315-20.
Macpherson AJ, Harris NL.. Interactions between commensal intestinal bacteria and the immune system. Nat Rev Immunol 4: 478-485
Bailey MT. Influence of stressor-induced nervous system activation on the intestinal microbiota and the importance for immunomodulation. Adv Exp Med Biol. 2014;817:255-76.
García Bueno B, Caso JR, Madrigal JL, Leza JC. Innate immune receptor Toll-like receptor 4 signalling in neuropsychiatric diseases. Neurosci Biobehav Rev. 2016 May;64:134-47.
Nugent NR, Tyrka AR, Carpenter LL, Price LH. Gene-environment interactions: early life stress and risk for depressive and anxiety disorders. Psychopharmacology (Berl). 2011 Mar;214(1):175-96.
Ait-Belgnaoui A, Durand H, Cartier C, Chaumaz G, Eutamene H, Ferrier L, Houdeau E, Fioramonti J, Bueno L, Theodorou V. Prevention of gut leakiness by a probiotic treatment leads to attenuated HPA response to an acute psychological stress in rats. Psychoneuroendocrinology. 2012 Nov;37(11):1885-95.
Cryan JF, Dinan TG. Mind-altering microorganisms: the impact of the gut microbiota on brain and behaviour. Nat Rev Neurosci. 2012 Oct;13(10):701-12.
Bercik P, Verdu EF, Foster JA, Macri J, Potter M, Huang X, Malinowski P, Jackson W, Blennerhassett P, Neufeld KA, Lu J, Khan WI, Corthesy-Theulaz I, Cherbut C, Bergonzelli GE, Collins SM. Chronic gastrointestinal inflammation induces anxiety-like behavior and alters central nervous system biochemistry in mice. Gastroenterology. 2010 Dec;139(6):2102-2112.e1.
Bravo JA, Forsythe P, Chew MV, Escaravage E, Savignac HM, Dinan TG, Bienenstock J, Cryan JF. Ingestion of Lactobacillus strain regulates emotional behavior and central GABA receptor expression in a mouse via the vagus nerve. Proc Natl Acad Sci U S A. 2011 Sep 20;108(38):16050-5. doi: 10.1073/pnas.1102999108.
Bercik P, Denou E, Collins J, Jackson W, Lu J, Jury J, Deng Y, Blennerhassett P, Macri J, McCoy KD, Verdu EF, Collins SM. The intestinal microbiota affect central levels of brain-derived neurotropic factor and behavior in mice. Gastroenterology. 2011 Aug;141(2):599-609, 609.e1-3.
Mayneris-Perxachs J, Castells-Nobau A, Arnoriaga-Rodríguez M, Martin M, de la Vega-Correa L, Zapata C, Burokas A, Blasco G, Coll C, Escrichs A, Biarnés C, Moreno-Navarrete JM, Puig J, Garre-Olmo J, Ramos R, Pedraza S, Brugada R, Vilanova JC, Serena J, Gich J, Ramió-Torrentà L, Pérez-Brocal V, Moya A, Pamplona R, Sol J, Jové M, Ricart W, Portero-Otin M, Deco G, Maldonado R, Fernández-Real JM. Microbiota alterations in proline metabolism impact depression. Cell Metab. 2022 May 3;34(5):681-701.e10.
Lopez MJ, Mohiuddin SS. Biochemistry, Essential Amino Acids. 2023 Mar 13. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2023 Jan–.
Mokhtari V, Afsharian P, Shahhoseini M, Kalantar SM, Moini A. A Review on Various Uses of N-Acetyl Cysteine. Cell J. 2017 Apr-Jun;19(1):11-17.
Ershad M, Naji A, Vearrier D. N-Acetylcysteine. [Updated 2023 Feb 19]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2023 Jan-.
Fernandes BS, Dean OM, Dodd S, Malhi GS, Berk M. N-Acetylcysteine in depressive symptoms and functionality: a systematic review and meta-analysis. J Clin Psychiatry. 2016 Apr;77(4):e457-66.
Berk M, Dean OM, Cotton SM, Jeavons S, Tanious M, Kohlmann K, Hewitt K, Moss K, Allwang C, Schapkaitz I, Robbins J, Cobb H, Ng F, Dodd S, Bush AI, Malhi GS. The efficacy of adjunctive N-acetylcysteine in major depressive disorder: a double-blind, randomized, placebo-controlled trial. J Clin Psychiatry. 2014 Jun;75(6):628-36.
Fernandes BS, Dean OM, Dodd S, Malhi GS, Berk M. N-Acetylcysteine in depressive symptoms and functionality: a systematic review and meta-analysis. J Clin Psychiatry. 2016 Apr;77(4):e457-66.
Hasebe K, Gray L, Bortolasci C, Panizzutti B, Mohebbi M, Kidnapillai S, Spolding B, Walder K, Berk M, Malhi G, Dodd S, Dean OM. Adjunctive N-acetylcysteine in depression: exploration of interleukin-6, C-reactive protein and brain-derived neurotrophic factor. Acta Neuropsychiatr. 2017 Dec;29(6):337-346.
Das P, Tanious M, Fritz K, Dodd S, Dean OM, Berk M, Malhi GS. Metabolite profiles in the anterior cingulate cortex of depressed patients differentiate those taking N-acetyl-cysteine versus placebo. Aust N Z J Psychiatry. 2013 Apr;47(4):347-54.
Fekadu A, Demissie M, Birhane R, Medhin G, Bitew T, Hailemariam M, Minaye A, Habtamu K, Milkias B, Petersen I, Patel V, Cleare AJ, Mayston R, Thornicroft G, Alem A, Hanlon C, Prince M. Under detection of depression in primary care settings in low and middle-income countries: a systematic review and meta-analysis. Syst Rev. 2022 Feb 5;11(1):21.
Wickham SR, Amarasekara NA, Bartonicek A, Conner TS. The Big Three Health Behaviors and Mental Health and Well-Being Among Young Adults: A Cross-Sectional Investigation of Sleep, Exercise, and Diet. Front Psychol. 2020 Dec 10;11:579205.
Yates BE, DeLetter MC, Parrish EM. Prescribed exercise for the treatment of depression in a college population: An interprofessional approach. Perspect Psychiatr Care. 2020 Oct;56(4):894-899.
Belvederi Murri M, Ekkekakis P, Magagnoli M, Zampogna D, Cattedra S, Capobianco L, Serafini G, Calcagno P, Zanetidou S, Amore M. Physical Exercise in Major Depression: Reducing the Mortality Gap While Improving Clinical Outcomes. Front Psychiatry. 2019 Jan 10;9:762.
Peirce JM, Alviña K. The role of inflammation and the gut microbiome in depression and anxiety. J Neurosci Res. 2019 Oct;97(10):1223-1241. doi: 10.1002/jnr.24476. Epub 2019 May 29. PMID: 31144383.
Basso JC, Suzuki WA. The Effects of Acute Exercise on Mood, Cognition, Neurophysiology, and Neurochemical Pathways: A Review. Brain Plast. 2017 Mar 28;2(2):127-152.
Worley SL. The Extraordinary Importance of Sleep: The Detrimental Effects of Inadequate Sleep on Health and Public Safety Drive an Explosion of Sleep Research. P T. 2018 Dec;43(12):758-763.
Shen H, Chen M, Cui D. Biological mechanism study of meditation and its application in mental disorders. Gen Psychiatr. 2020 Jul 13;33(4):e100214.
Hölzel BK, Carmody J, Vangel M, Congleton C, Yerramsetti SM, Gard T, Lazar SW. Mindfulness practice leads to increases in regional brain gray matter density. Psychiatry Res. 2011 Jan 30;191(1):36-43.
Ljungberg T, Bondza E, Lethin C. Evidence of the Importance of Dietary Habits Regarding Depressive Symptoms and Depression. Int J Environ Res Public Health. 2020 Mar 2;17(5):1616.
Francis HM, Stevenson RJ, Chambers JR, Gupta D, Newey B, Lim CK. A brief diet intervention can reduce symptoms of depression in young adults – A randomised controlled trial. PLoS One. 2019 Oct 9;14(10):e0222768.
Wong SK, Chin KY, Ima-Nirwana S. Vitamin D and Depression: The Evidence from an Indirect Clue to Treatment Strategy. Curr Drug Targets. 2018;19(8):888-897.
Kaveladze B, Diamond Altman A, Niederhausen M, Loftis JM, Teo AR. Social relationship quality, depression and inflammation: A cross-cultural longitudinal study in the United States and Tokyo, Japan. Int J Soc Psychiatry. 2022 Mar;68(2):253-263.
Matthew Solan.The secret to happiness? Here’s some advice from the longest-running study on happiness.Harvard Health.
Cunha LF, Pellanda LC, Reppold CT. Positive Psychology and Gratitude Interventions: A Randomized Clinical Trial. Front Psychol. 2019 Mar 21;10:584.
Menéndez-Aller Á, Postigo Á, Montes-Álvarez P, González-Primo FJ, García-Cueto E. Humor as a protective factor against anxiety and depression. Int J Clin Health Psychol. 2020 Jan-Apr;20(1):38-45.
Reyes-Martínez S, Segura-Real L, Gómez-García AP, Tesoro-Cruz E, Constantino-Jonapa LA, Amedei A, Aguirre-García MM. Neuroinflammation, Microbiota-Gut-Brain Axis, and Depression: The Vicious Circle. J Integr Neurosci. 2023 May 8;22(3):65. doi: 10.31083/j.jin2203065. PMID: 37258450.