-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com




原创:谷禾健康
刚刚,来自爱尔兰 APC 微生物组研究所(APC Microbiome Ireland,简称APC)的APC John F Cryan,教授和 Timothy G Dinan教授在 Lancet Neurol《柳叶刀神经病学》上在线发表了综合评论文章:The gut microbiome in neurological disorders(肠道微生物群在神经系统疾病中的作用)。
小贴士:带你了解一下APC
APC (APC Microbiome Ireland) 微生物组研究所在肠道学术和产业方面都颇具国际影响力,集产学研一体,尤其是关于微生物组相关的生物医药和功能食品研发。其在微生物组研究和肠道相关疾病研究中可以排进全球前五,在益生菌研究和细菌素研究中名列第一。
APC 长期致力于微生物组的转化应用研究,在多个领域的产业化方面,包括食品、制药、婴儿营养、医疗食品、诊断、运动营养,以及动物健康等取得进展。
以下是文章内容。
在过去10年中,对肠道微生物群在调节大脑功能方面的作用的研究迅速增加,尽管主要是在动物模型中。
越来越多的临床和临床前证据表明,微生物群可能是神经系统疾病(包括阿尔茨海默病、自闭症谱系障碍、多发性硬化症、帕金森病和中风)的一个关键易感因素。横向临床研究正在支持改变微生物组成的概念,这有助于此类疾病的病理生理学。

然而,这一领域尚处于起步阶段,鉴于微生物组分受饮食和运动等多种因素的影响,对这些数据的解释往往很困难。需要对人体进行纵向研究和随机对照试验,以发现靶向微生物群是否能产生新的治疗策略。系统生物学方法在将此类数据与来自神经疾病临床队列的基因组和代谢组学数据集整合也很重要,可以帮助指导个体化治疗选择。
人们认为,当婴儿在分娩期间接触到母体微生物时,肠道的定植主要是在出生时开始的。早期生活中的各种因素可能影响这种定居,包括分娩方式、母乳喂养、早产、环境、宿主遗传学、抗生素暴露和母体感染、压力或肥胖。
在整个生活中,饮食可能对微生物群的组成产生最大的影响。
越来越多的研究调查了患有特定神经障碍个体与健康年龄匹配个体的微生物群组成。然而,这些研究仅仅提供了一个时间上的快照,纵向队列研究是有必要的。实验模型对于推动人类微生物群-肠-脑轴向前移动的研究是必不可少的。
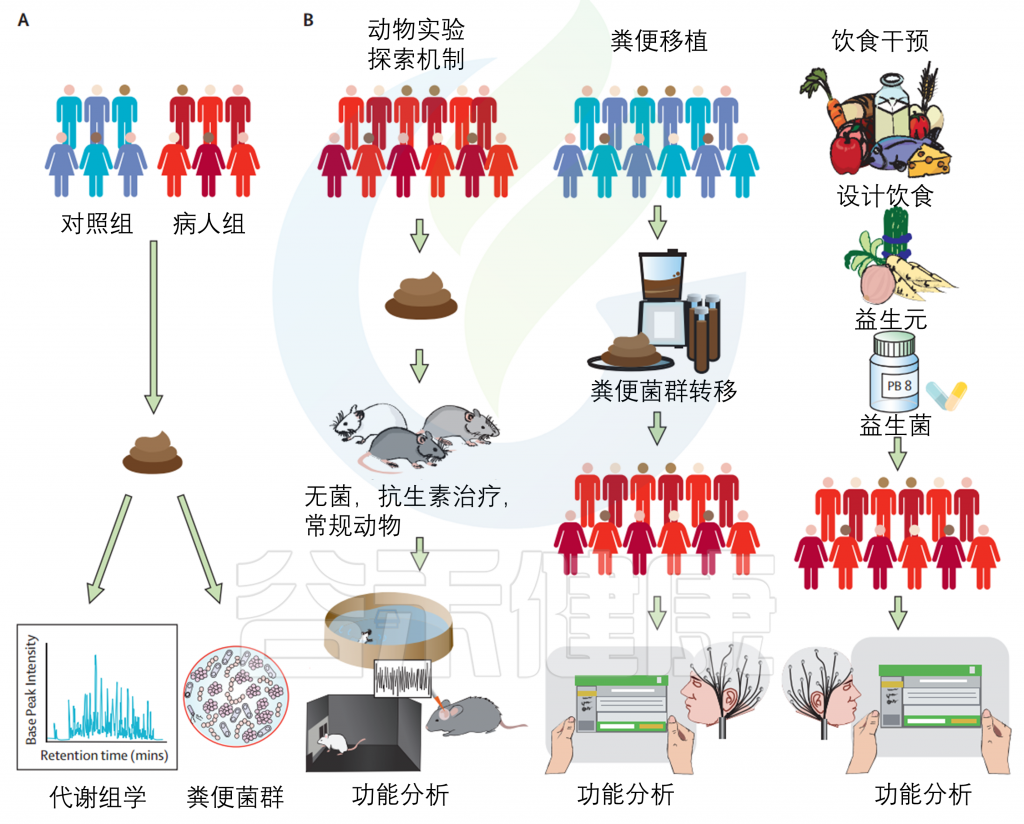

(A)对患者组和对照组的微生物群进行评估,并确定组成(有哪些细菌)和代谢组(他们正在做什么)的差异。注意,粪便样本通常用于微生物组分析,结肠细菌不是小肠微生物组的可靠替代物。
(B)在临床前和临床试验中使用人类微生物组的三种潜在方法,以研究疾病的机制和潜在治疗的效果。
动物实验探索机制:动物可以通过粪便微生物群移植来实现人性化,粪便物质取自人类,用于在啮齿类动物的肠道中重新填充与人类捐赠者相似的成分。这样可以在啮齿动物中重建与供应者人类相似的表型,为在人类中很难研究的机制提供了一种临床前的方法。功能分析可以通过一系列的动物行为测试,以及分子和成像技术进行的体外测试来完成。
粪便移植:如果存在微生物组分的差异,粪便微生物组移植可从对照个体或明确的细菌联合体进行。已报道了一些有前途的临床研究,包括自闭症谱系障碍患者的研究。
饮食干预:可实施选择性饮食、益生元或益生菌等。然而,这主要是在动物模型中进行的研究,现在有必要验证通过选择性饮食,益生元或益生菌对人体进行微生物组靶向的效果。
微生物群与神经发育
越来越多的关注是理解微生物-肠-脑轴在神经发育过程中的作用。
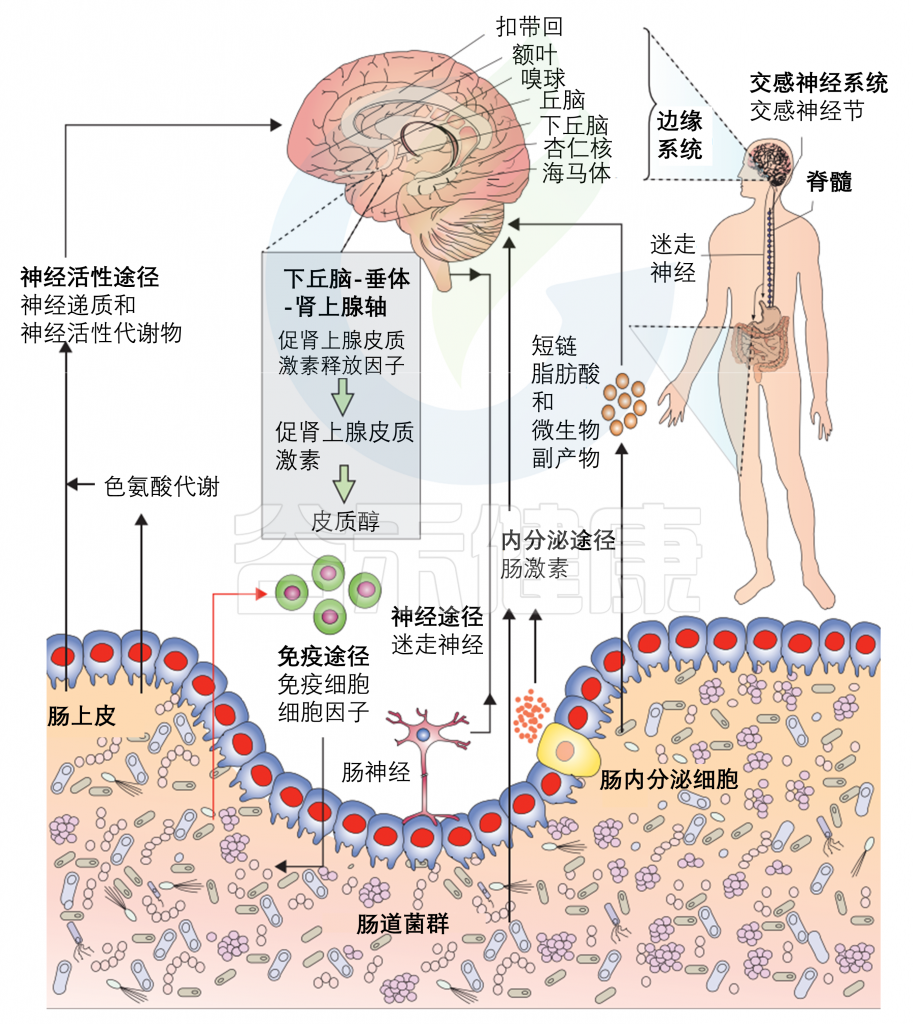

多种直接(如迷走神经)和间接(如短链脂肪酸、细胞因子和关键的膳食氨基酸,如色氨酸、酪氨酸和组氨酸)途径,通过肠道微生物群可以调节肠-脑轴。
它们包括神经活性途径,包括神经递质和神经活性代谢物;免疫途径(包括细胞因子);短链脂肪酸和微生物代谢物;神经途径(迷走神经、肠神经系统和脊神经);下丘脑-垂体-肾上腺轴;内分泌途径。
微生物群可以在动物和人的肠道局部合成神经递质(即GABA、去甲肾上腺素和多巴胺),这是重要的交流途径。神经活性细菌代谢物,以及来自饮食的代谢物,可以调节大脑和行为的方式仍在被阐明,包括影响上皮细胞改变肠屏障功能、肠内分泌细胞释放激素和树突状细胞调节免疫和小胶质功能,在衰老和神经系统疾病中起着重要作用。
然而,所涉及的确切的分子信号传导途径尚未明确。红色箭头表示免疫系统受到腔内容物的刺激,产生负面影响(宿主免疫激活)。
然而,对婴儿的研究很少,大部分是横向研究的。在一项对89名婴儿的研究中,2岁时的认知功能(用马伦早期学习量表评估)与1年前的微生物群组成显著相关。
在39名婴儿的队列中,微生物群α-多样性(一个描述样本内变异性的统计数据)也与支持运动区和下顶叶之间的功能连接有关。重要的是,这种功能联系也与2岁时的认知结果有关。
微生物群在神经发育中作用的最有力证据来自对无菌小鼠(即完全没有微生物群的小鼠)的研究。在这些模型中,基本的神经过程,如发育、髓鞘形成、神经发生和小胶质细胞的激活,已经被证明在很大程度上依赖于微生物群的组成。
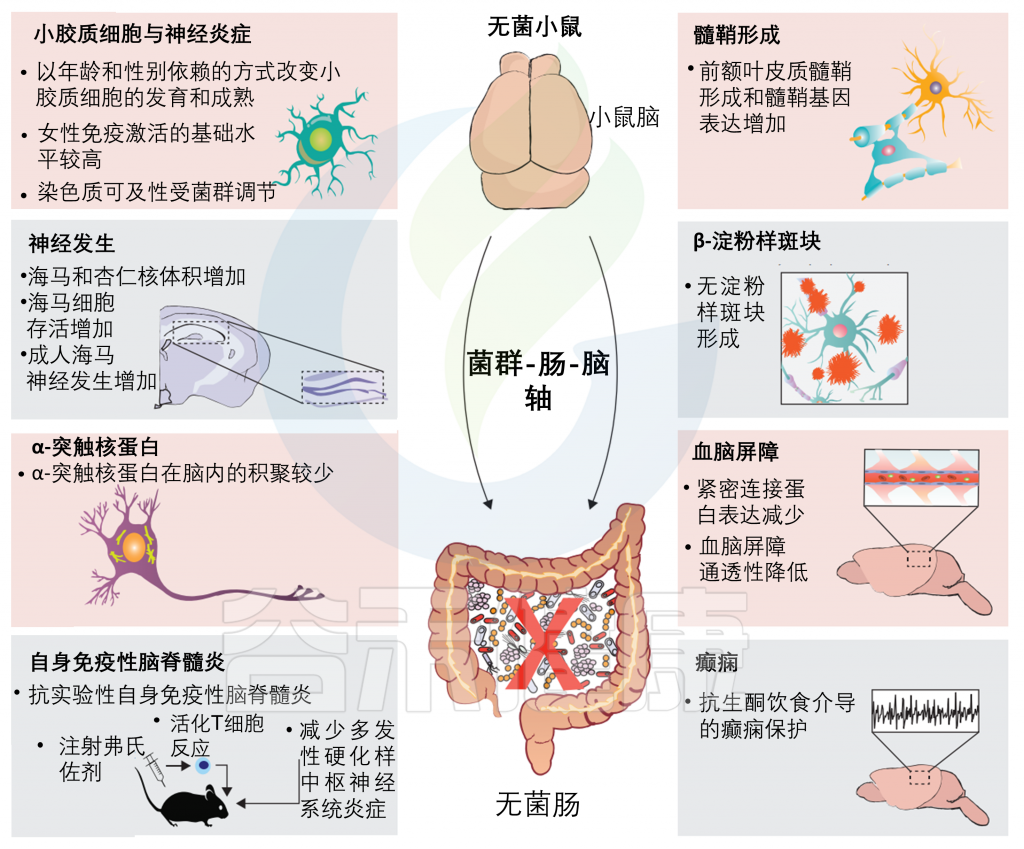

无菌小鼠的大脑无法正常发育;无菌小鼠缺乏微生物群会导致许多与各种神经系统疾病相关的神经生物学变化,包括应激依赖小鼠的行为依赖性改变、无菌小鼠海马体积减少和髓鞘形成减少。
研究报告显示前额叶皮质髓鞘形成增加,海马体神经发生增加,各种神经递质浓度改变,树突树状结构改变。
在功能上,无菌小鼠已经表现出微生物群与脑信号在社交能力、内脏疼痛、免疫功能、应激敏感性和恐惧和焦虑反应中的参与。
来自无菌小鼠的小胶质细胞是神经炎症的重要调节因子,表现出不成熟的表型,对细菌相关分子模式(如脂多糖)没有有效的反应。
无菌小鼠也显示血液-脑屏障的通透性增加。血脑屏障完整性的降低可能会使免疫细胞和细菌成分转移到大脑并影响神经炎症。
无菌小鼠对实验性自身免疫性脑脊髓炎、转基因介导的β-淀粉样斑块形成、α-突触核蛋白形成和生酮饮食诱导的癫痫保护作用也有抵抗力。
年轻大鼠(如产后4-13天)使用抗生素的研究也表明,微生物群在塑造与侵略性和内脏痛相关的神经发育轨迹方面也起着关键作用。。
肠道微生物群与大脑老化之间的关系也备受关注,因为许多神经系统疾病都发生在老年人身上。
年龄在65岁以上的178名爱尔兰Eldermet研究表明,肠道菌群的组成与总体的健康、虚弱和免疫功能指数相关。这项研究表明,微生物的多样性越大,健康结果越好。
值得注意的是,饮食的多样性与肠道微生物的多样性相关,人们吃加工食品,平淡的食物(通常是在养老院)减少了微生物的多样性,而饮食中富含水果和蔬菜的人肠道微生物群的多样性更多。因此,肠道微生物群的多样性是健康老龄化的潜在标志。


一项小型12周、双盲、随机化、安慰剂对照研究,没有随访,将36名健康的韩国人(20名男性和16名女性;60-75岁[SD4·14])分为益生菌饮食组(n=26)和安慰剂组(n=10)。这项小型研究表明,与服用安慰剂的个体相比,使用一种特定的细菌菌株(乳酸杆菌IDCC3801)使认知疲劳测试的每种形式都有所改善。
小鼠研究表明,与年龄相关的行为缺陷与微生物群的变化是同时发生的,并且可以通过针对微生物群的饮食干预(益生素菊粉)来改善与年龄相关的神经炎症。
此外,微生物群还被证明调节微胶质细胞的活动,其具有在衰老和神经变性中的关键作用。
看看微生物群在神经系统疾病中的作用的证据,其中在临床或动物研究中显示了肠道微生物群的作用是关键的。
下面的表格总结了人类对微生物群及其在神经系统疾病中的作用的研究,包括研究的固有局限性。根据微生物群如何影响参与健康神经发育和衰老的关键大脑过程,构建了微生物群与每种疾病之间的关系。从最有证据的疾病开始,以新生领域的描述结束。
鉴于肠道微生物对免疫系统的发育和成熟至关重要,那么要说这些微生物群与多发性硬化(一种免疫介导的神经系统疾病)的发病机制有关也并不奇怪。

横向研究主要显示,与无自身免疫疾病的健康儿童相比,在患有多发性硬化的儿童中,在2年内多发性硬化的儿童与年龄为18岁的健康儿童相比,在2年内多发性硬化的儿童中观察到细微的、离散的分类变化,而不是多尺度差异(描述不同样本之间的变异性的统计)。






两项研究将多发性硬化患者的微生物群移植到两种不同的实验性自体免疫性脑脊髓炎模型中,这是一种经过充分验证的多发性硬化症动物模型。这些研究强调了产生白细胞介素 IL10 的 CD4 T 细胞在肠道微生物群免疫调节作用中的重要性。
在无细菌的小鼠中的早期研究也表明,这些小鼠对发育实验性自身免疫性脑,特别是抵抗正常小鼠的粪便微生物群移植而逆转。此外,胃肠道中存在特异性的革兰氏阳性丝状菌,激活Th17细胞,显著影响实验性自身免疫性脑脊髓炎的严重程度。
多发性硬化症是一种脱髓鞘疾病,来自无菌小鼠和抗生素临床前研究的汇集数据表明,微生物群在调节小鼠前额叶皮质髓鞘生成中起作用。
血脑屏障完整性的丧失也是多发性硬化症的一个特征,而无菌小鼠的研究表明,微生物群在调节血脑屏障方面至关重要。
此外,短链脂肪酸或产生短链脂肪酸的菌群的饮食管理可以逆转血-脑屏障完整性的损失。饮食引起的微生物群组成的变化也被认为是实验性自身免疫性脑脊髓炎的表现。
越来越多的证据支持微生物群是神经炎症的关键调控者,然而,需要进一步的研究来了解这种关系如何有助于多发性硬化的病理生理学。
自闭症谱系障碍的一个重要且常被忽视的特征是与胃肠道症状有明显的共病性。
许多横向研究显示自闭症谱系障碍患者的微生物群组成发生了改变。然而,这些研究大多相对较小且不均匀,并不总是考虑饮食,也不能监测疾病进展的变化。动物研究有助于提供一个机械的理解微生物群如何可能在自闭症谱系障碍中发挥作用。




无菌小鼠在社会行为上有缺陷,重复行为增加表明,正常的社会发展需要适当的微生物组成。将来自自闭症谱系障碍捐赠者的肠道微生物群移植到无菌小鼠体内,发现患有自闭症谱系障碍患者的微生物群的定植足以诱导老鼠自闭症行为。
经流行病学证实的自闭症谱系障碍环境危险因素动物模型(包括母亲暴露于抗惊厥剂丙戊酸盐、孕妇暴露于孕期炎症和孕妇肥胖)报告了微生物群组成的改变。使用单一的细菌菌株,无论是脆弱的细菌或乳酸菌,可以逆转许多行为和胃肠道变化报告在人类研究和动物模型的自闭症谱系障碍。
此外,一些肠道微生物群落易受万古霉素的影响,而万古霉素能促进炎症状态,这与自闭症谱系障碍有关。


一项小型生物群转移治疗定义的微生物群的小规模试验研究表明,自闭症谱系障碍患者的治疗效果良好。
与治疗前相比,接受微生物转移治疗的自闭症谱系障碍儿童的腹痛、消化不良、腹泻和便秘明显减轻,与自闭症谱系障碍相关的行为显著改善,自微生物转移点起至少持续了两年。作者还指出,在治疗后,患者的细菌多样性显著降低,双歧杆菌、普雷沃氏菌和脱硫弧菌丰度显著增加。
α突触核蛋白,是大脑帕金森氏病病理学的标志性蛋白质聚集体,也已在帕金森综合症患者的粘膜和粘膜下神经纤维和神经节中被发现,一些临床前证据甚至表明α-突触核蛋白可以通过迷走神经将肠道中的蛋白转运到大脑。淀粉样蛋白可由菌群产生,并已被证明可增加老年大鼠的α-突触核蛋白病理学。


迷走神经特别适合作为从肠道到大脑的信号管道,可以通过小分子或大分子(如α-突触核蛋白的朊样移位)的运输,也可以通过电信号在神经元上传递。
越来越多的研究显示帕金森病患者的微生物群组成发生了变化。然而还需谨慎,因为这些数据主要来自于小群体,不能提供纵向视角。






当小鼠通过粪便微生物群移植与帕金森氏病患者的微生物群进行殖民时,它们会出现运动障碍和神经炎症,这是帕金森氏病的两个标志性症状。此外,当小鼠接受抗生素治疗时,其行为学症状改善。本研究提示短链脂肪酸是帕金森病动物模型神经炎症过程的驱动因素。
阿尔茨海默病
一些研究表明阿尔茨海默病可能是由微生物引起的。淀粉样蛋白可能在大脑中起抗菌肽的作用得到了精辟实验证据的支持。
然而,要证明阿尔茨海默病患者的神经炎症和神经变性有感染的原因,这在逻辑上和道德上都是很有挑战性的。


与帕金森病一样,肠蛋白与认知健康之间的关系得到了越来越多的关注,表明淀粉样蛋白样蛋白可由菌群产生,并增加迷走神经切断的老年大鼠的α-突触核蛋白的病理学。然而,在帕金森病患者中的确认是突出的。
横向研究表明,阿尔茨海默病患者粪便样本中与炎症介导有关的大肠杆菌和志贺氏菌类群与健康人相比有所增加。此外,阿尔茨海默病患者的微生物群变化与未刺激和未离心血液中的促炎细胞因子浓度有关。






促炎性大肠杆菌和志贺氏菌数量增加,抗炎性大肠杆菌数量减少可能与认知障碍和脑淀粉样变性患者的外周炎症状态有关,提示微生物群失调与全身炎症之间存在联系,后者可能引发或加剧阿尔茨海默病患者大脑中的神经变性。
需要注意的是,这些结果来自于小规模的研究,需要在更大的队列中进行纵向研究,以评估微生物群参与阿尔茨海默病的进展及其因果关系。
对无菌小鼠的精液研究表明,当微生物不存在时,淀粉样斑块的形成和神经炎症明显消失。同样,用抗生素混合物对转基因小鼠进行长期治疗可减少海马区淀粉样斑块周围的小胶质细胞和星形胶质细胞积聚,并减少不溶性淀粉样蛋白β斑块。
这些研究共同强调了微生物群在调节阿尔茨海默病的关键分子成分中的作用。
中风与脑损伤
横向研究报告了与健康、无症状对照个体相比,中风患者的微生物组成失调。肠道菌群代谢产物三甲胺N-氧化物与主要不良心血管事件、妊娠糖尿病、和阿尔茨海默病的风险增加相关,表明通过肠道微生物群的调节治疗疾病治疗的可能性。


在临床前模型中,脑缺血与改变的微生物群组成和胃肠动力和屏障通透性的功能性作用有关。
此外,将中风模型的粪便微生物菌群移植到无菌小鼠中,或将中风患者移植到经过抗生素处理的小鼠中,均加重了缺血性脑病引起的脑损伤体积和功能性缺损。


在缺血性损伤前使用广谱抗生素与小鼠预后明显恶化有关。抗生素诱导的微生物群失调还导致炎症性 IL-17 γδ T 细胞的转运减少和 IL-17 相关的趋化因子表达减少。因此,肠道微生物群似乎影响中风后神经炎症的程度,通过调节肠道T细胞向大脑的运输。
在脑缺血再灌注损伤的动物模型中,给药一种特殊的细菌——丁酸梭菌,具有神经保护作用。
外伤性脑损伤后微生物群组成发生了改变,丁酸梭状芽孢杆菌在这种损伤的小鼠模型中显示出神经保护作用。
已将重点放在开发富含益生元或益生菌的饮食中,以对抗与创伤性脑损伤相关的一些共病,但需要更多的临床试验来了解这种干预的治疗潜力。
癫痫、肌萎缩性侧索硬化和亨廷顿病
与其他疾病相比,与癫痫、肌萎缩性侧索硬化和亨廷顿病相关的微生物群证据要少得多。不过这些领域的研究人员和临床医生也开始关注微生物群在这些疾病中调节生理和行为的潜力。


癫痫:
无菌小鼠的研究表明,微生物群参与了癫痫发生的关键脑区的突触变化,生酮饮食被证明改变了患有癫痫的婴儿(表)和动物的微生物群。
同时也表明生酮饮食的有益作用取决于微生物群。随后的研究可能会更加强调微生物群作为癫痫介质的潜在作用。


肌萎缩侧索硬化:
肌萎缩侧索硬化小鼠模型提示肠道微生物群的改变与该病的发病有关。
例如,与健康小鼠相比,这些模型中产生丁酸的细菌的相对丰度较低,这与肠道通透性的改变有关。然而,人类的横向研究尚未发现微生物群与肌萎缩性侧索硬化疾病进展之间的任何关系。


亨廷顿病:
亨廷顿病患者体内微生物群变化的数据很少,可能是因为这种疾病主要被视为一种遗传性疾病。然而,内在因素(例如,蛋白质同质化的变化、线粒体功能紊乱和不受控制的皮质激素输入)和外在环境因素(例如,种族、地理区域、喝茶和烟酒)可以缓和亨廷顿病的进展。
一项代谢组学研究表明,与对照组相比,在一组患有先天性和早期亨廷顿氏病的患者血清中发现来自肠道微生物群的代谢物改变。
然而,有必要进行更多的研究,以充分了解肠道微生物群及其代谢物在发病、发病过程中的影响。
结论和未来
大量的基础研究表明,微生物群对大脑功能的正常发育和维持具有重要意义。从临床和动物研究中也积累了证据,表明微生物群在神经疾病中起作用。
支持微型生物群作用的最强证据是帕金森病、多发性硬化、和孤独症谱系障碍,在阿尔茨海默病和中风中的作用越来越高。
然而,这仍然是很早的事情,需要谨慎,避免过度解读这些数据。需要更好的控制和精心设计的研究。
为了从纯粹的相关观察研究,转向因果和功能性结果,需要更多地强调使用益生菌菌株、益生元和可能的粪便微生物移植疗法的介入方法。这些研究在设计上应该是纵向的,而不仅仅是横向的,以提供一个时间因素来确定微生物群是一种潜在的疾病生物标志物。
人脑成像和脑电图研究已经检查了微生物菌群变化对健康志愿者大脑功能的影响。这些研究使用有针对性的微生物群干预来支持良好的认知健康,以改善微生物-肠-脑轴的靶向,并为新疗法的发展铺平道路。
当然也需要进一步的研究来了解这些研究在多大程度上可以转化为神经系统的研究。
附 录
APC相当关注饮食-菌群-宿主之间的相互作用
以下是APC发表的部分文章:
【益生菌】一种特定的短双岐杆菌益生菌株可用于减少阿司匹林引起的小肠损伤
Mortensen B, Murphy C, O’Grady J, et al. Bifidobacterium breve Bif195 Protects Against Small-intestinal Damage Caused by Acetylsalicylic Acid in Healthy Volunteers[J]. Gastroenterology, 2019.
【老年】饮食和健康状况,影响老年人的肠道菌群
Claesson M J, Jeffery I B, Conde S, et al. Gut microbiota composition correlates with diet and health in the elderly[J]. Nature, 2012, 488(7410): 178.
【生物精神病学】FOS+GOS帮小鼠抗抑郁和焦虑
Burokas A, Arboleya S, Moloney R D, et al. Targeting the microbiota-gut-brain axis: prebiotics have anxiolytic and antidepressant-like effects and reverse the impact of chronic stress in mice[J]. Biological psychiatry, 2017, 82(7): 472-487.
谷禾健康 是谷禾面向健康领域的品牌,通过无创采集微量粪便样品,常温快递运输至谷禾检测中心,经全自动化样品处理和提取后大规模高通量测序获取菌群基因数据并进行分析解读,凭借全球领先的样本积累和业界独有的人工智能算法实现了基于肠道菌群的疾病预测和系统健康风险评估, 以及肠道菌群,病原物感染,重金属污染以及营养物质和激素代谢水平等在内的综合健康风险提示,并提供精准个性化的健康管理方案。公司成立于2012年,总部位于杭州,拥有优秀的研发团队和独立实验室,经过多年的积累,已完成近6万例临床肠道菌群样本检测,并构建了超过20万各类人群样本数据库。
谷禾健康的服务旨在通过持续不断的研发和改进,大量自动化提升效率,降低检测成本,为广大消费者提供更好更有价值的产品。
联系方式:400-161-1580
微信公众号:谷禾健康