-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康 原创

微生物群是免疫防御的原动力,但是防止感染的特定共生微生物的特性尚不清楚。相对的,病原体如何与其他微生物群落竞争以建立其宿主生态位也鲜为人知。
鉴定对病原体有保护作用的微生物群成员可以提供一种治疗对当前抗菌治疗有耐药性的感染的替代方法。
在这些抗药性微生物中,肠杆菌科是最大的临床问题。而肠杆菌科中的肺炎克雷伯菌对人类健康构成最紧迫的威胁,因为许多菌株对多种抗生素耐药,毒性很强,在成人和婴儿中都会引起疾病,并且很容易在宿主之间传播。
因此,预防肺炎克雷伯菌的定殖和传播显得至关重要。
近日, 国际顶级微生物学期刊《Nature microbiology》发表了由英国伦敦帝国理工学院传染病系分子细菌学与感染中心和外科与癌症系综合系统医学与消化疾病科合作研究最新成果:“Commensal Bacteroidetes protect against Klebsiella pneumoniae colonization and transmission through IL-36 signalling(共生拟杆菌通过IL-36信号预防肺炎克雷伯菌定植和传播)”。
该研究从机制上提供了一种视角,何时,何地,拟杆菌如何对抗肺炎克雷伯氏菌的定植和传染,深入了解如何利用这些保护性微生物来提供人群级别的预防肺炎克雷伯氏菌感染的保护。
肺炎克雷伯氏菌在人群宿主中有两个主要的定植渠道:上呼吸道和肠道。肺炎克雷伯菌建立定植必须与这两个位置的微生物群和免疫系统建立的防御系统抗衡。
该研究发现,成熟的微生物群推动了不同免疫防御程序的发展,从而在上呼吸道和肠道限制肺炎克雷伯氏菌在这些生态位内的定植。
肠道免疫保护取决于拟杆菌、白细胞介素IL-36信号和巨噬细胞的发育。拟杆菌的这种作用需要其保守的共生定植因子的多糖利用位点。相反,在上呼吸道,变形菌门通过IL-17A增强免疫力,但是肺炎克雷伯氏菌通过包囊IL-17A来克服这些防御进而有效定植。
最终发现肺炎克雷伯氏菌的宿主间传播主要发生在其肠道贮存器中,而产生共生定植因子的拟杆菌足以通过IL-36阻止宿主之间的传播。
首先我们先来看看,肺炎克雷伯菌这种菌在人群中的分布情况究竟是怎样的?
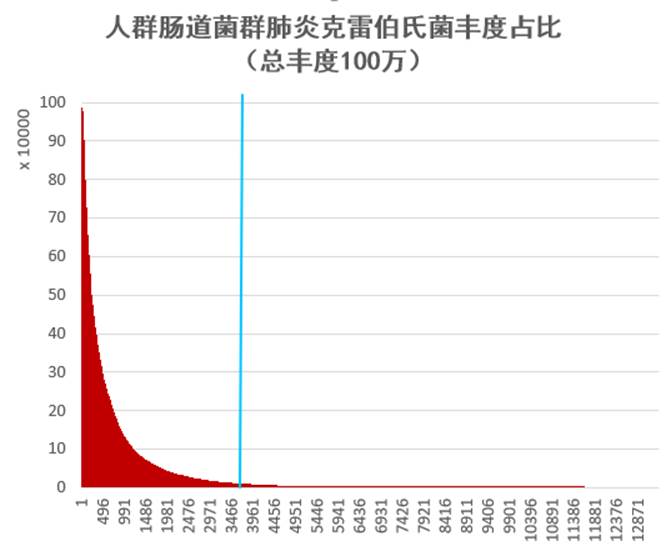
我们从谷禾健康2019年近期检测人群肠道菌群样本抽取1.3万例样本,人群共计13358人,涵盖0~103岁人群。
其中肺炎克雷伯氏菌丰度占比超过1%的人群有3765例,占比28.2%。
预 告
本文后面【交流探讨】章节会结合该论文的观点,对我们谷禾健康目前已测的人群数据进行整理分析。
由于肺炎克雷伯菌在婴儿和成人中引起疾病,研究人员希望研究在整个生命过程中微生物群介导的对肺炎克雷伯菌定植的防御能力的发展。为此,耗尽了新生和成年小鼠中的微生物群。
为了研究肺炎克雷伯菌在上呼吸道的定殖作用,研究人员使用了一个小的接种量,并且没有麻醉小鼠进行鼻内接种。这种方法意味着细菌保留在鼻腔和鼻咽,并不会到达肺。
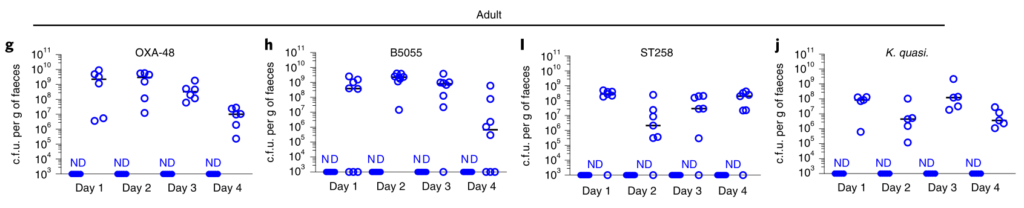
在新生小鼠中,肺炎克雷伯菌可能在上呼吸道和肠道都定居,这不受微生物群耗竭的影响(图1a–c)。同样,在成年上呼吸道中,对照动物和消耗微生物的动物中肺炎克雷伯菌的定殖水平相似(图1d–f)。相比之下,在成年肠道中,肺炎克雷伯菌只有在微生物群枯竭后才能建立可检测的定植(图1g–j)。
持续的广谱抗生素治疗(图1g-j)或临床上相关的短期抗生素治疗方案,消除了微生物群介导的防御。将成年菌群而非新生儿菌群转移至新生小鼠,以保护其免受肺炎克雷伯菌的肠道定殖(图1k–m)。
图1:成年微生物菌群可抵抗抗生素抗性肺炎克雷伯菌在肠中的定植,但不能防止上呼吸道定植。
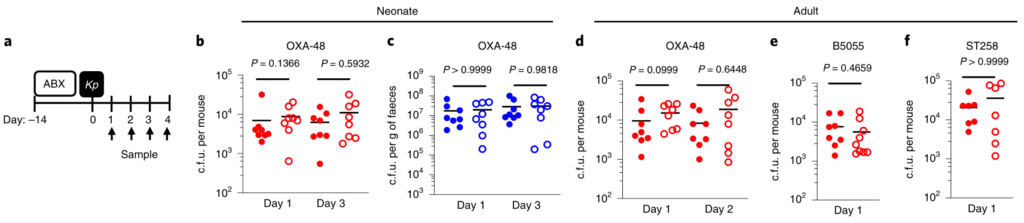
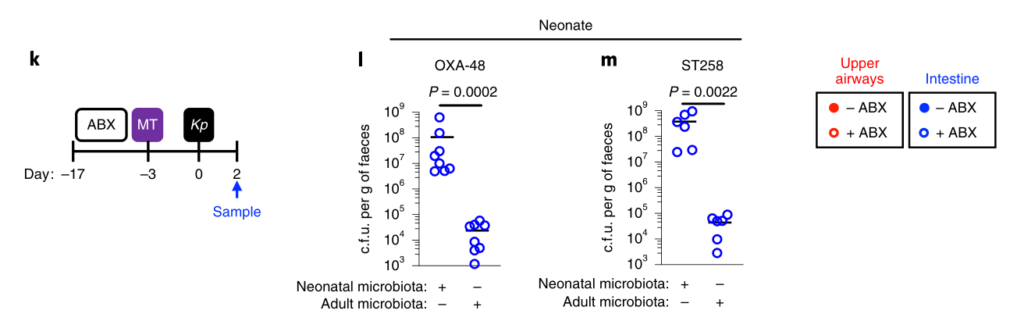
上呼吸道定植数据显示为红色,肠道定植数据显示为蓝色。所有统计比较均使用Mann-Whitney(双尾)进行;水平线表示中值;ND,未检出(肺炎克雷伯菌的检出限在粪便中= 10 3 cfu g -1)。
成人肠道菌群具有广泛的保护性,可通过临床分离株产生肺炎克雷伯菌,产生OXA-48碳青霉烯酶(图1g),流行性肺炎克雷伯菌 ST258(图1l)和近缘拟肺炎克雷伯菌亚种(图1j)。
在任一生态位定居期间均未观察到体重减轻,支持我们正在对无症状定殖进行建模的概念。这些数据表明,成年菌群的发育产生了足以阻断肺炎克雷伯菌在肠道内而不是上呼吸道定居的屏障。
这就提出了三个问题:
(1)成人肠道菌群中的哪些菌阻止肺炎克雷伯菌的定殖,其机制是什么?
(2)哪些因素可使肺炎克雷伯菌成功与上呼吸道菌群竞争,从而定居于这一生态位?
(3)在不同的粘膜贮库中,微生物群和肺炎克雷伯菌之间的竞争如何影响这种传染性病原体在宿主之间的传播?
下文将围绕这3个问题展开实验与探讨。
为了回答第一个问题,成人肠道菌群中的哪些菌阻止肺炎克雷伯菌的定殖,其机制是什么?
研究人员对新生小鼠和成年小鼠肠道菌群进行了测序,以确定这些允许和抑制微生物群落的各自组成。新生小鼠肠道菌群主要是来自厚壁菌门,尤其是乳杆菌科的成员(图2a,b)。相比之下,成年小鼠肠道菌群主要由拟杆菌门(拟杆菌门)和厚壁菌(梭状芽胞杆菌和乳杆菌)的共生菌组成,而放线菌门和变形菌门只占共生菌的一小部分(图2a,b)。
研究人员发现只有拟杆菌能促进肺炎克雷伯菌从肠道的清除,无论是在肺炎克雷伯菌定植之前还是之后(Fig. 2c–k)。拟杆菌在抗生素治疗(图2d-f,i,j)和无菌小鼠(图2g)中都具有保护作用,这与使用不同成分的共生体一致。
证实施用代表性的共生菌群的小鼠的肠道菌群由该菌群占主导地位,并且每个菌群的定植水平相似。
图 非抗生素处理、抗生素处理和共生联合体接种小鼠粪便中的细菌负荷和组成
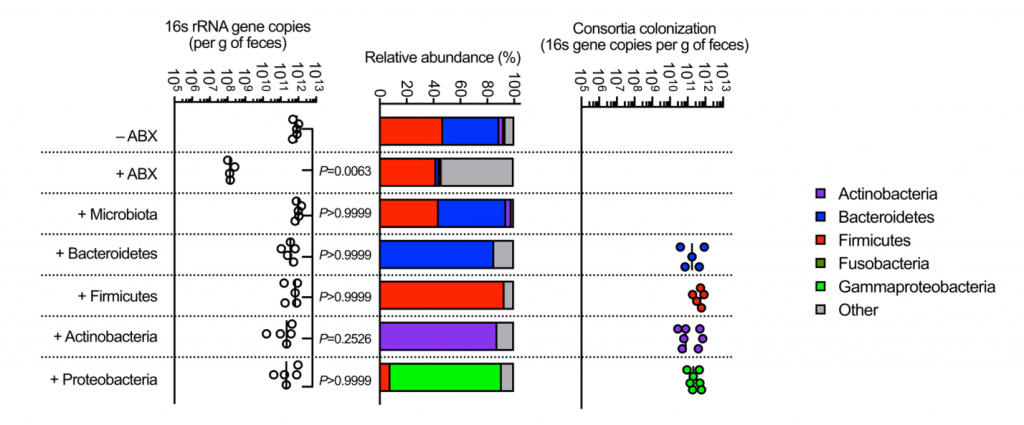

此外,还发现拟杆菌属特别保护新生小鼠免受肺炎克雷伯菌的肠道定植(图2k),这支持了这种共生体的发展可以保护成年小鼠免受肺炎克雷伯菌的侵害。
图2:肠内的拟杆菌属可以预防肺炎克雷伯菌的定殖。
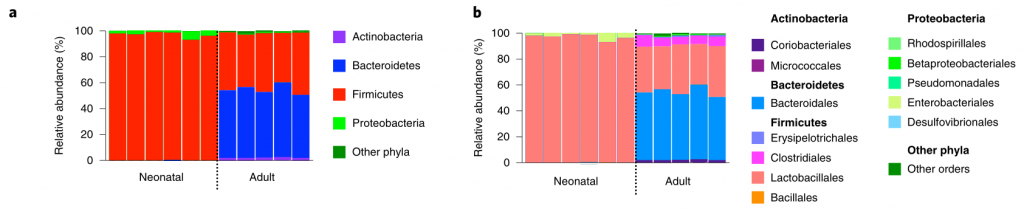

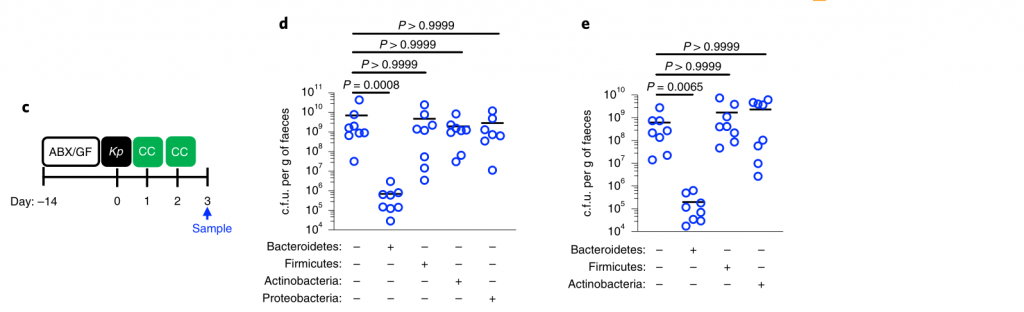

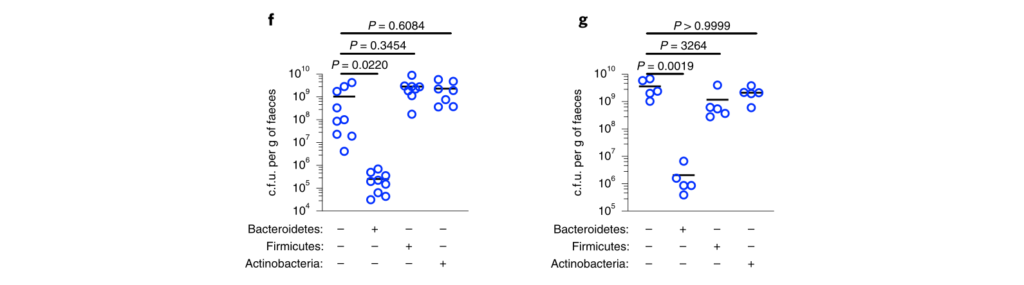
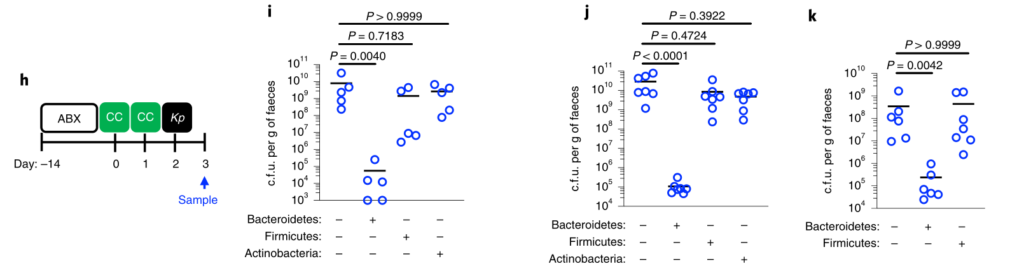
所有的统计比较都是用Kruskal-Wallis检验和Dunn对多重比较的修正进行的。水平线表示中值。
产生共生定殖因子(CCF)的拟杆菌属通过IL-36和巨噬细胞加强肠道免疫屏障,以防止肺炎克雷伯菌肠道定殖。
接下来,研究人员想确定拟杆菌的保护作用是否需要宿主免疫。因此,在肺炎克雷伯氏菌定植之前,将微生物群转移到施用了免疫抑制性地塞米松或媒介物对照的微生物群缺失小鼠中。地塞米松消除了微生物群对肺炎克雷伯菌定殖的抑制作用(参见图3a,b),表明该保护作用需要免疫信号。
此外,研究人员发现地塞米松对未经抗生素治疗的小鼠的治疗,使这些正常耐药的小鼠容易被肺炎克雷伯氏菌定殖。同样,拟杆菌属赋予的保护作用需要免疫信号传导。
为了确保地塞米松对免疫系统起作用而不是破坏微生物群,研究人员将微生物群从地塞米松或媒介物对照治疗的小鼠转移至微生物群枯竭的小鼠,然后研究了对肺炎克雷伯菌定植的抑制作用。这两个微生物群均提供了针对肺炎克雷伯菌定殖的同等保护作用。由此证明地塞米松不能消除微生物菌群的保护性优势,而是抑制微生物菌群对免疫系统的刺激作用。
然后,研究人员试图确定将拟杆菌属的作用转化为对肺炎克雷伯菌定植的抗性的免疫因子。在肠道中,从新生小鼠到成年的转变以许多细胞因子的稳态表达增加为标志,这些因子对维持宿主与微生物的动态平衡很重要。
为了确定拟杆菌的保护作用是否受这些细胞因子的驱动,他们取消了细胞因子的信号传导,该信号的稳定表达从新生小鼠到成年小鼠均以微生物群依赖性方式增加。
图3 拟杆菌通过IL-36信号和巨噬细胞保护肺炎克雷伯菌在肠道的定植。
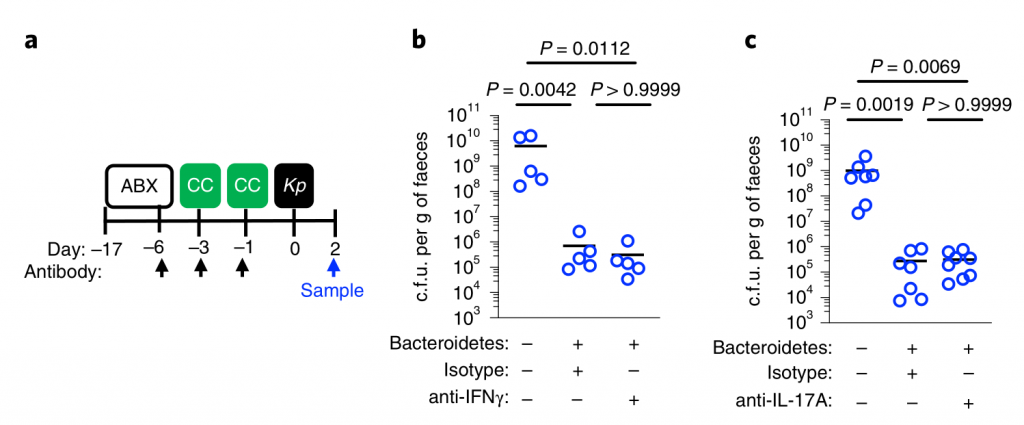
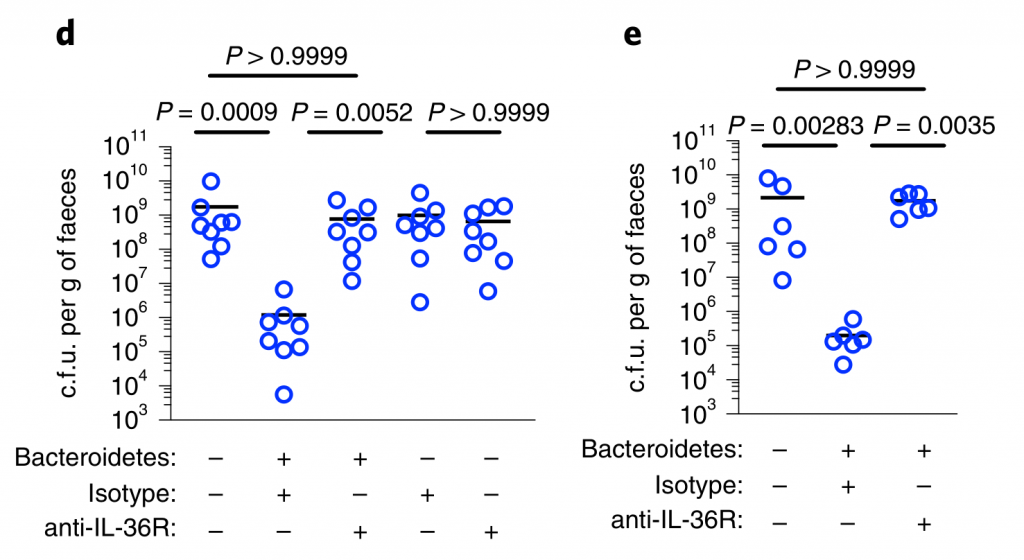
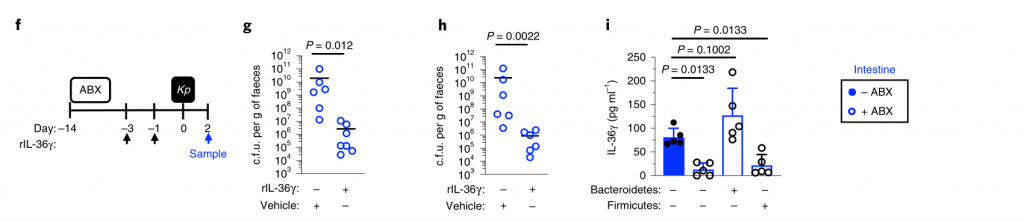



水平线表示中值,误差线为s.d.
用针对IL-36受体(IL-36R)信号的抗体治疗,但不针对IL-17A或干扰素(IFN)-γ的抗体治疗后,拟杆菌属对肺炎克雷伯菌的肠道菌落保护被取消(图3a-e)。支持IL-36的作用,重组IL-36γ处理可促进肠道肺炎克雷伯菌的清除(图3f–h),而微生物群落衰竭的动物中肠道IL-36γ的产生可通过拟杆菌特异恢复(图3i)
利用脂质体氯膦酸盐处理耗尽这些细胞来研究它们对肺炎克雷伯菌的保护作用。巨噬细胞耗竭后,拟杆菌不能预防肺炎克雷伯菌或调节IL-36γ(图3j–m)。相反,嗜中性粒细胞耗尽后,拟杆菌仍具有保护作用。
图 变形菌在定植过程中恢复了上气道的稳态IL-17A生成和肺炎克雷伯菌诱导的上气道TNF生成
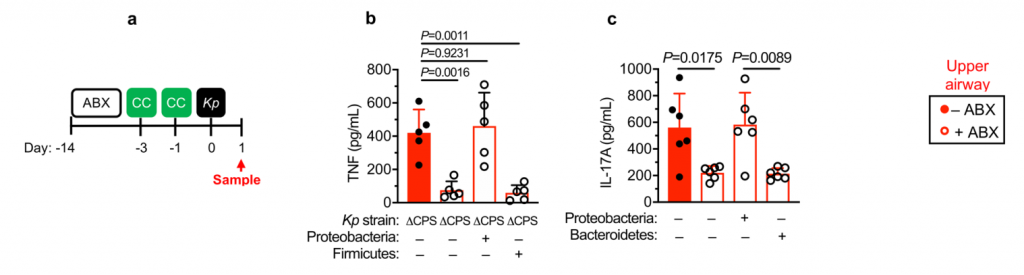

此外,在用氯膦酸盐处理的小鼠中,IL-36R信号的破坏不会增加肺炎克雷伯菌的定殖,这表明IL-36和巨噬细胞沿一条共同途径起作用(图3n)。
为了了解IL-36如何通过巨噬细胞控制肠道中的肺炎克雷伯菌水平,研究人员调查了IL-36是否促进了这些细胞的杀菌活性。然后发现IL-36γ刺激促进巨噬细胞杀死肺炎克雷伯菌的多种菌株。
接下来,研究人员想了解抗肺炎克雷伯菌定殖所需的拟杆菌属中的因素。调节肠道免疫力的常见方法是与宿主粘膜紧密接触以发挥其作用。拟杆菌内高度保守的是荚膜多糖产生位点CCFs,这促进了拟杆菌与肠黏膜的关联。
图4 拟杆菌需要它们的ccf来防止肺炎克雷伯菌在肠内的定植。
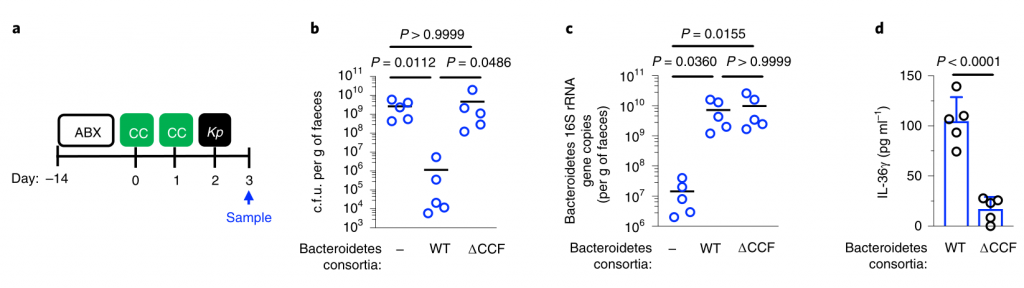
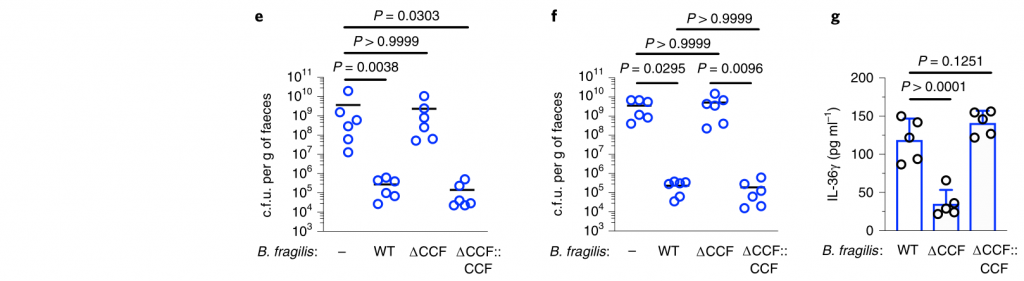



研究人员测试了假单胞菌抑制肺炎克雷伯菌定植所需的CCF的假设。与此一致,具有完整的CCF系统的拟杆菌属或单个拟杆菌属物种可以预防肺炎克雷伯菌的细菌定植和主要肠道IL-36γ的产生,但是在没有CCF的情况下会消失,并且可以通过CCF的互补来重新建立(图4a–g)。
与设想的在粘膜定植中的作用相一致,发现CCF促进了拟杆菌与粘膜的缔合(图4h),但是在存在或不存在CCF的情况下,粪便中的拟杆菌水平是相等的(图4i)。
以上,数据支持这样一个模型,其中产生细菌CCF的拟杆菌属成员与粘膜屏障结合,在肠内形成免疫屏障,从而防止肺炎克雷伯菌通过IL-36和巨噬细胞定居。
接着回答第二个问题:哪些因素可使肺炎克雷伯菌成功与上呼吸道菌群竞争,从而定居于这一生态位?
为此,研究人员检查了肺炎克雷伯菌包封的作用。传统上,包囊被视为一种毒性决定因素。然而,荚膜多糖的产生是常见的病原体和非病原体。特别是在上呼吸道中。
在具有微生物群的成年小鼠中,我们发现包封的肺炎克雷伯菌定植上呼吸道水平高于等基因的未包封的肺炎克雷伯氏菌突变体,并且,通过未封装的突变体的互补,恢复了抵抗微生物群介导的防御的能力(图5a,b)。
包囊化的这种优势在微生物群落缺乏的动物中消失了,在这些动物中,包囊化和未包囊化的肺炎克雷伯菌定殖到相似的水平(图5a,b)。
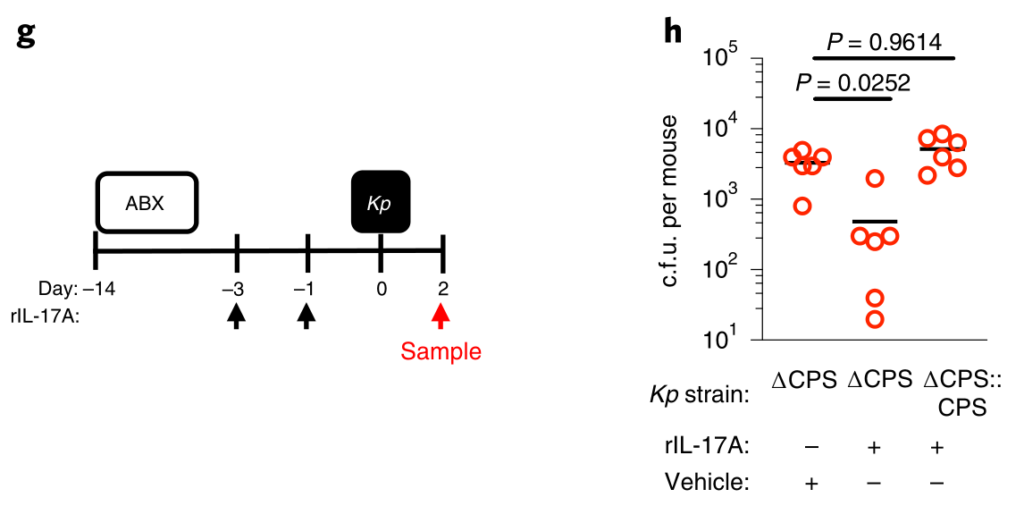
图5 变形菌通过IL-17A启动上呼吸道防御,但包封可以使肺炎克雷伯菌克服这些防御。
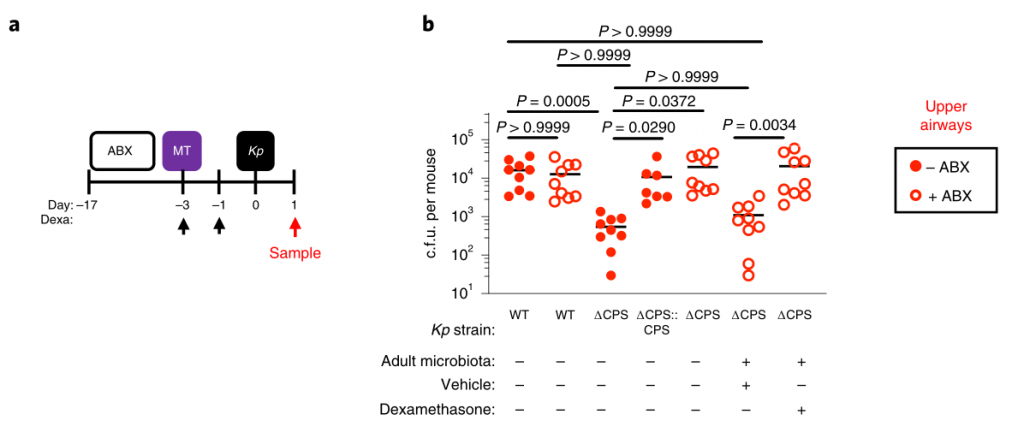

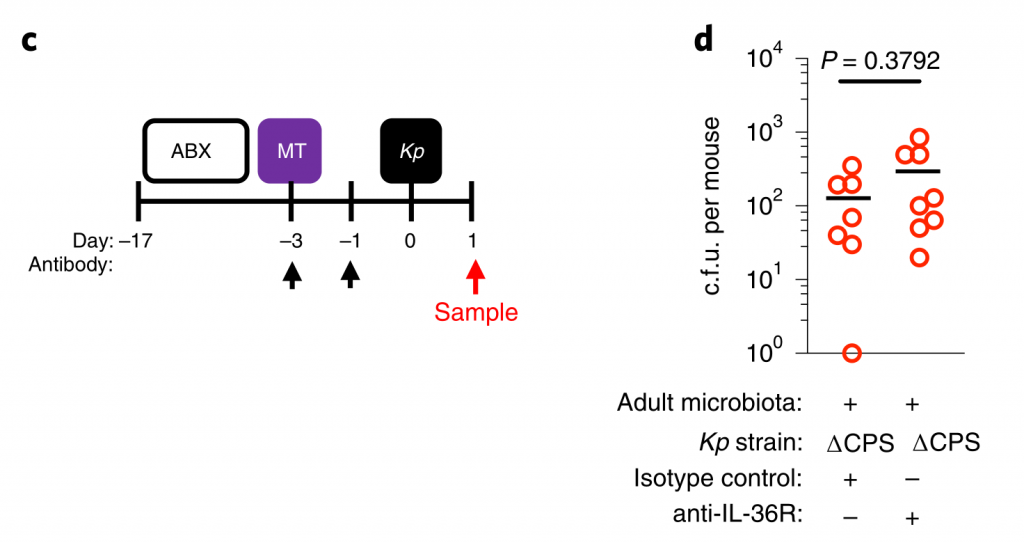

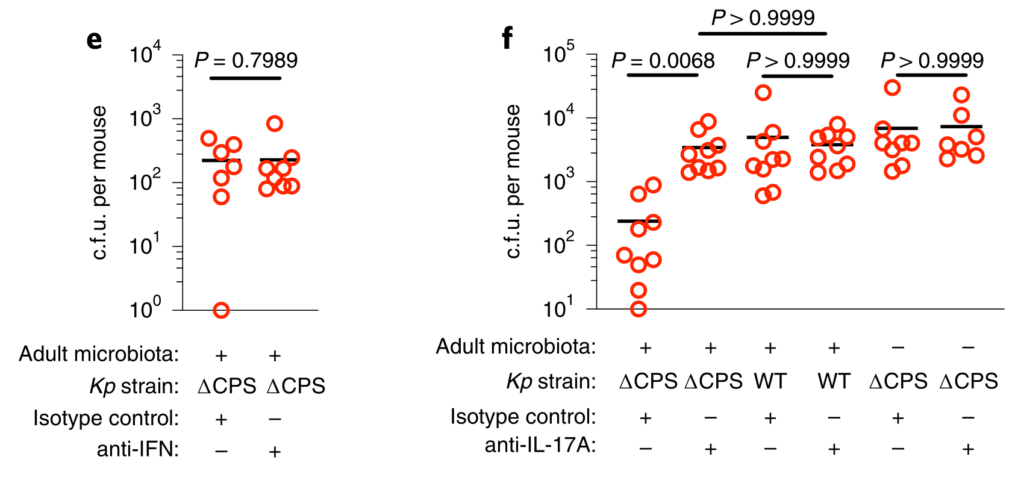
下一步,研究人员确定包封是否允许肺炎克雷伯菌抵抗上呼吸道内的直接微生物竞争,或通过免疫系统间接影响微生物群。为了解决这一问题,他们将微生物群转移回经地塞米松或载体控制治疗的微生物群衰竭的动物,然后再经鼻腔给药肺炎克雷伯菌。
微生物群转移减少未包封肺炎克雷伯菌在载体对照中的上呼吸道定植,但地塞米松治疗的动物却没有,这支持了微生物群通过免疫信号增强上呼吸道防御的观点。与此相符的是,在微生物群落衰竭的动物中,肺炎克雷伯氏菌在上呼吸道定植期间诱导的先天细胞因子产生(肿瘤坏死因子-α)减少,并通过免疫信号通过微生物群转移而恢复。
图 微生物群启动上呼吸道免疫,但封装使肺炎克雷伯菌克服这些防御
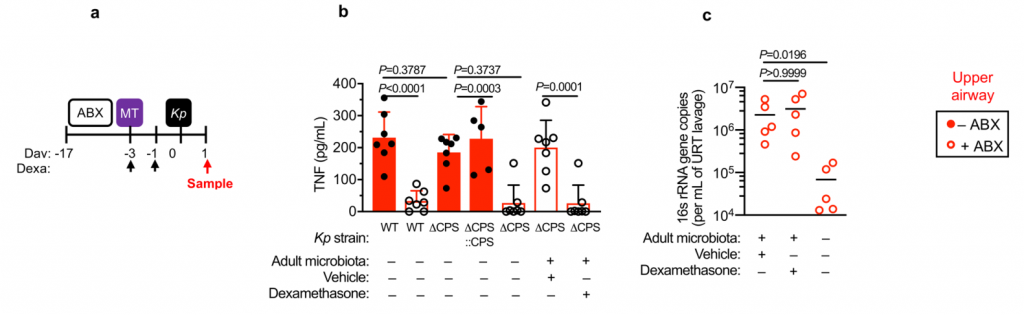

研究人员确认,微生物群转移后上呼吸道共生细菌的水平在媒介物和地塞米松治疗的小鼠之间是相同的,且微生物群的转移没有导致共生接种到肺中。
与肠道类似,上呼吸道的微生物防御启动是成年动物所特有的,因为封装和未封装的肺炎克雷伯菌都将新生的上呼吸道定居到相似的水平,并在缺乏微生物群和对照的动物中引起了同等的先天细胞因子反应。
从新生到成年的转变伴随着依赖于微生物群的上呼吸道多种细胞因子稳态表达的增加,因此,研究人员取消了这些细胞因子的信号传导,以了解成年微生物群是否需要它们才能在上呼吸道发挥其免疫调节作用。
IL-17A的破坏,而不是IFN-γ或IL-36R信号的破坏,抑制了微生物群介导的未包囊但未包囊的肺炎克雷伯菌从上呼吸道的清除(图5c–f)。
此外,用重组IL-17A处理足以促进未包封的肺炎克雷伯菌的清除(图5g,h)。小鼠上呼吸道菌群包括的菌来自放线菌门,拟杆菌,厚壁菌门和变形菌。
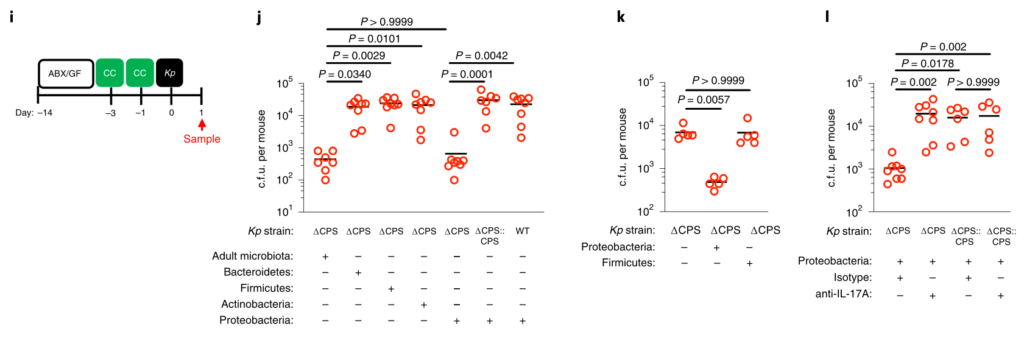
在这些共生体中,发现变形菌通过IL-17A信号(图5i-l)特异性地增强了抗生素治疗和无菌小鼠上呼吸道对未包被肺炎克雷伯菌的清除。变形菌还恢复了上呼吸道的稳态IL-17A生成和肺炎克雷伯菌定植诱导的细胞因子生成。
研究人员证实,给代表性共生体注射的小鼠上呼吸道微生物群主要由该共生体控制,并且每个共生体的定殖情况相似。
这些数据支持一种模型,通过该模型,变形菌可以在成年上呼吸道引发IL-17A依赖性免疫防御程序。但是,包囊可以使肺炎克雷伯菌经受住这些防御,从而成功地建立定植。
然后回答第三个问题:在不同的粘膜贮库中,微生物群和肺炎克雷伯菌之间的竞争如何影响这种传染性病原体在宿主之间的传播?
为了了解防止肺炎克雷伯菌在肠道定植的成人微生物群的发育如何影响传播,研究人员采取以下措施:
首先,将已建立肠道肺炎克雷伯菌定殖的成年小鼠与抗生素治疗或非抗生素治疗的小鼠接触,共同饲养。抗生素治疗的成年接触小鼠都获得了肺炎克雷伯菌,但对未经抗生素治疗的成年接触小鼠的传播有限。
研究人员再次确认从成年接触小鼠分离出的肺炎克雷伯菌的抗生素耐药谱与接种到索引小鼠中的肺炎克雷伯菌的抗生素耐药谱相匹配,确认从接触小鼠分离出的肺炎克雷伯菌来自索引动物。
图 接触小鼠肺炎克雷伯菌的耐药谱与对照小鼠肺炎克雷伯菌的耐药谱一致
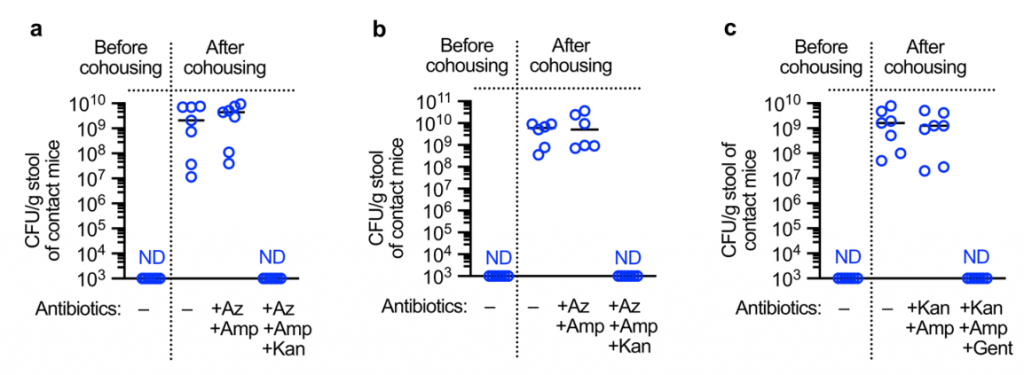


其次,在共寄居之前,将保护性拟杆菌属共接种到肺炎克雷伯菌定殖的新生指数小鼠和幼稚的新生接触小鼠中。这足以阻止宿主之间的肺炎克雷伯菌传播。为了检查传播是否需要与动物直接接触,将成年接触者关在先前装有肠道定殖的索引小鼠的笼子中。尽管在饲养前已从笼子中取出所有的索引小鼠和粪便材料,但所有接触的小鼠都被肺炎克雷伯菌定殖,这表明传播不需要动物之间或同食性的直接接触。
第三,在共寄居之前,将保护性的拟杆菌共生体口服到肺炎克雷伯菌定植的成年指数小鼠和未经抗生素处理的成年接触小鼠体内。发现拟杆菌特异性足以阻断肺炎克雷伯菌在宿主间的传播。在IL-36信号的破坏或没有CCF的情况下,拟杆菌的抑制作用丧失了。
综上所述,这些数据表明拟杆菌对肺炎克雷伯菌定植的保护作用限制了其在人群中的传播。研究人员质疑拟杆菌对肺炎克雷伯菌传播的抑制作用是否是由于拟杆菌减少了从指数动物身上脱落的肺炎克雷伯菌,或是在接触动物身上建立了针对肺炎克雷伯菌的保护屏障。
为了回答这个问题,拟杆菌只给肺炎克雷伯菌定植的索引小鼠或单纯接触者。发现,这两种方法都减少了肺炎克雷伯菌的传播,但将拟杆菌引入接触者比将拟杆菌引入索引小鼠的效果更为有效,证明拟杆菌控制传播的关键点是加强免疫屏障以防止肺炎克雷伯菌在新宿主中的建立。总之,数据显示,产生CCF的拟杆菌抑制了肺炎克雷伯菌在人群中的传播。
该文章最后提到,个体内的微生物群失调不仅会促进肺炎克雷伯菌在宿主体内的定植,而且会促进其向其他宿主的传播。因此,拟杆菌群可以通过防止肺炎克雷伯菌在宿主之间的传播提供人群级别的保护,这是控制传染病的最终手段。
在本文开头部分,我们已经看到从谷禾健康2019年样本中抽取样本的实际分布情况:
其中肺炎克雷伯氏菌丰度占比超过1%的人群有3765例,占比28.2%。
为了解感染携带肺炎克雷伯氏菌的人群和不携带人群的菌群构成,尤其是论文中拟杆菌对于肺炎克雷伯氏菌感染的防控作用在真实人类群体中的情况,我们将根据肺炎克雷伯氏菌的占比丰度分为两类人群。
其中肺炎克雷伯氏菌占比丰度5~50%的人群作为肠道感染携带者(1629例),占比<1%的人群(9593例)作为对照。
提取拟杆菌门和厚壁菌门的比例进行比较,结果如下:
肺炎克雷伯氏菌肠道感染人群菌群构成
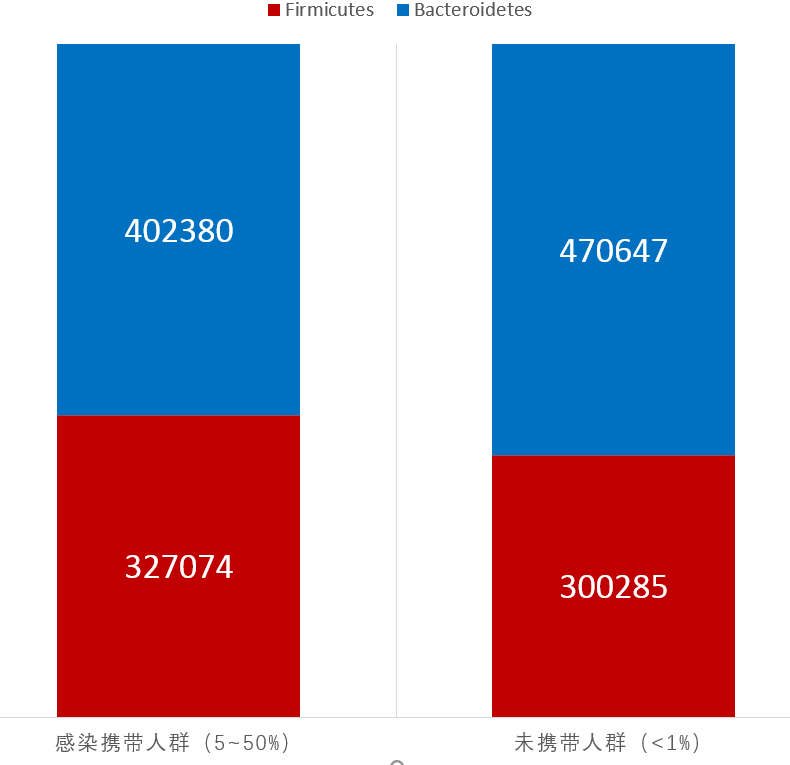

可以看到两组人群的拟杆菌门的丰度水平确实存在差异,未感染人群的拟杆菌门比例相对更高,统计检验是极显著。
论文的研究发现在人类群体中应该存在一定的作用,但是感染人群其拟杆菌并不是极低。
进一步使用MaAslin2进行检验肺炎克雷伯氏菌与其他菌属,结果如下:
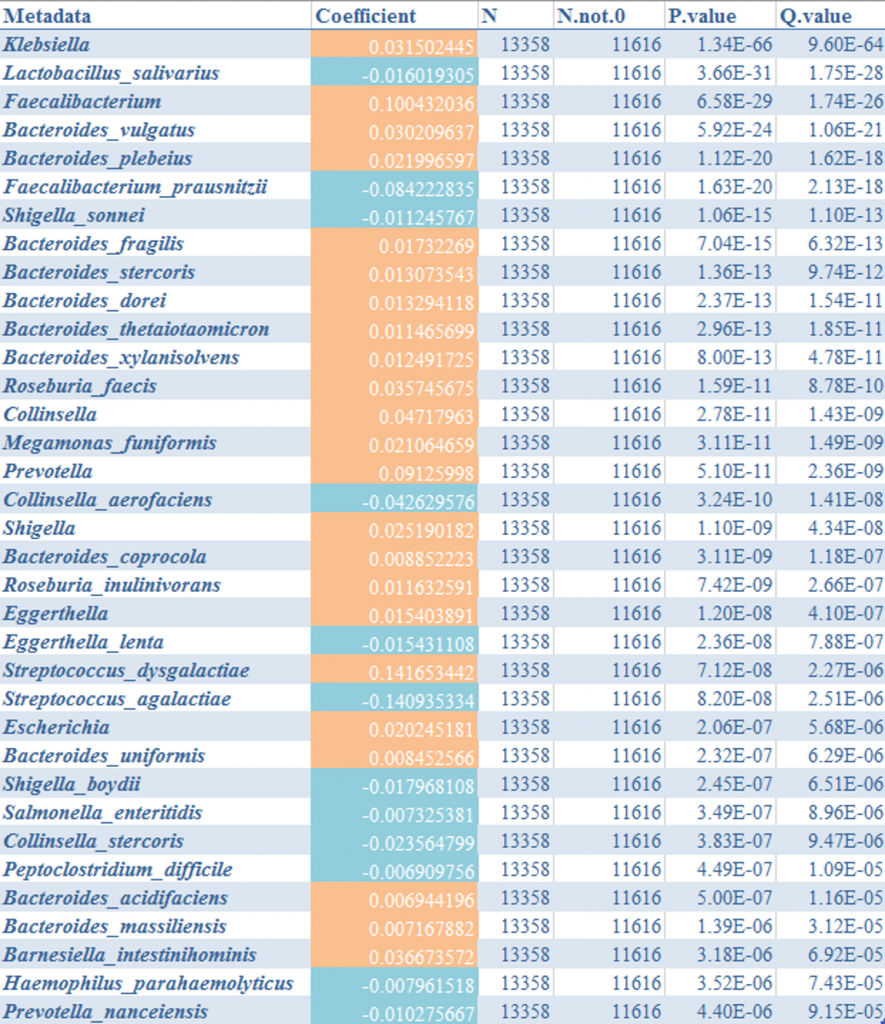

发现和预期的不太一样,拟杆菌与肺炎克雷伯菌的丰度水平之间显示是正相关,唾液乳杆菌和栖粪杆菌与其是显著负相关,另外其他病原菌与其负相关。
总之,论文的研究发现在人类群体中应该存在一定的作用,但是大样本人群肠道菌群检测结果分析表明单纯的拟杆菌存在并不能完全抵御肺炎克雷伯氏菌的定植和传播。
参 考 文 献
Sequeira, R.P., McDonald, J.A.K., Marchesi, J.R. et al. Commensal Bacteroidetes protect against Klebsiella pneumoniae colonization and transmission through IL-36 signalling. Nat Microbiol (2020)