-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康

俗话说:“病从口入”。饮食是决定个人健康状况的重要因素,饮食与疾病的发展有关,特别是胃肠道(GI)疾病。
与膳食相关的症状发生率很高,例如在吸收不良(如乳糖不耐症)情况下出现的腹痛和腹泻;乳糜泻、食物过敏人群在食用麸质类后出现的腹胀、腹痛、水肿;肠易激综合征患者在摄入一些刺激性食物后(酸、辣)的腹痛、排便异常等。饮食作为胃肠道症状的驱动因素已经逐渐被人们所认识。
然而对出现食物相关症状的机制仍不太清楚。随着对肠道微生物研究的深入,肠道微生物群也被认为是胃肠道疾病的重要影响因素,这促使人们研究微生物作为饮食和宿主生理之间的关键联系。
同样的饮食摄入效果会因人体的健康状况以及肠道个性化的微生物群落而产生的不同的效果。例如低聚果糖(FOS)会加重炎症性肠病(IBD)患者的炎症,但在健康个体中却具有抗炎作用。麸质、小麦、牛奶和大豆等物质直接注射到粘膜下层可以通过激活IBS患者的肥大细胞来引发免疫反应,但在健康受试者中则不然。还有纵向研究报告称,饮食蛋白质摄入量相似,但IBS-D患者的色氨酸和色胺水平(而非吲哚衍生物)高于健康人。另一方面,结肠内乙酸盐可增强对结肠直肠扩张的敏感性。具体影响可能取决于宿主健康和肠道中的整体代谢环境。
近年来,人们越来越认识到个性化的饮食干预在预防和治疗胃肠道疾病中的潜力。个性化饮食不仅考虑到个体的遗传背景、健康状况和生活习惯,还特别关注其独特的微生物群组成。通过分析和调整个体的饮食,可以优化肠道微生物群的平衡,增强其对疾病的抵抗能力。
在本文中,主要关注两种胃肠道疾病:肠易激综合征和炎症性肠病。宿主和肠道微生物群对膳食营养素的利用决定肠道中最终的生物活性代谢物特征以及这些代谢物对胃肠道生理学的生物效应。此外强调了单个代谢物的不同作用如何影响不同的胃肠道疾病,类似的饮食干预对多种疾病状态可能具有不同的影响。
食物在肠道内会被肠道菌群代谢、转化。食物成分本身的性质,加上肠道菌群作用后的代谢产物,共同决定了食物对人体健康的作用。因此,仅考虑食物成分是不够的,还要考虑个人肠道菌群状况,两者结合才能判断食物的健康效应。
例如,传统观点认为,大部分可消化的食物成分会通过小肠表面吸收。剩余的不可消化成分传递到远端,作为肠道微生物群的能量来源,产生如短链脂肪酸(SCFA)等发酵最终产物。
然而,这种观点简化了过程。肠道微生物群不仅依赖于难以消化的膳食成分,还可以从宿主上皮表面粘液层中的糖蛋白和多糖获取营养,尤其是在碳水化合物缺乏的情况下,如低纤维摄入时。
★ 不同的肠道微生物结构造就了独特的代谢
肠道微生物群与营养物质的利用:肠道微生物群如何利用营养物质取决于具体的营养成分和每种微生物的代谢能力。不同微生物有不同的代谢途径,使得营养利用变得复杂,而不是简单的化学计量问题。
微生物群落结构的影响:肠道中的微生物群落结构可以影响宿主和微生物之间的营养合作动态。比如,在体内平衡期间,宿主在小肠中有效吸收氨基酸,从而使得一些微生物无法获得这些氨基酸。
营养物质的竞争:某些细菌(如梭状芽孢杆菌)如果过度生长,就可能在一些情况下(如膳食蛋白质有限时)与宿主竞争氨基酸的吸收。
营养层次与利用率:更高级的营养物质(如单糖和双糖)的增加会降低某些细菌对氨基酸的利用率。这意味着营养物质的可用性对微生物代谢有影响。
调节信号的作用:肠道中的特定信号分子(如短链脂肪酸或肽YY)也能影响宿主对营养物质的利用方式。
在下面小节中,我们重点介绍两个例子(色氨酸和膳食纤维),以说明宿主和肠道微生物群在营养利用上的差异如何影响宿主的生理学。
色氨酸是一种必需氨基酸,是宿主神经递质血清素 (5-HT;胃肠道生理的重要调节剂) 的前体,也是微生物代谢物(如色胺和吲哚衍生物)的前体。色氨酸库很大程度上取决于饮食。
色氨酸被整合到蛋白质中并被宿主利用,通过不同的途径产生5-HT(1-2%)和犬尿氨酸(∼95%)。肠道微生物成员如Ruminococcus gnavus和Clostridium sporogenes含有色氨酸脱羧酶,可将色氨酸转化为色胺,而色胺则是血清素受体4(5-HT 4R)的激动剂。
同时,脆弱拟杆菌(Bacteroides fragilis)和大肠杆菌(Escherichia coli)等细菌含有色氨酸酶,这种酶有助于从色氨酸产生吲哚和吲哚衍生物。如吲哚乙酸和吲哚丙酸,可以通过激活芳烃受体(AHR)对宿主的免疫途径发挥生物学效应。
这些细菌产生的色氨酸衍生生物活性代谢物的水平取决于肠道菌群的组成、肠道细菌利用色氨酸的程度和位置,以及宿主色氨酸利用相关基因的活性。
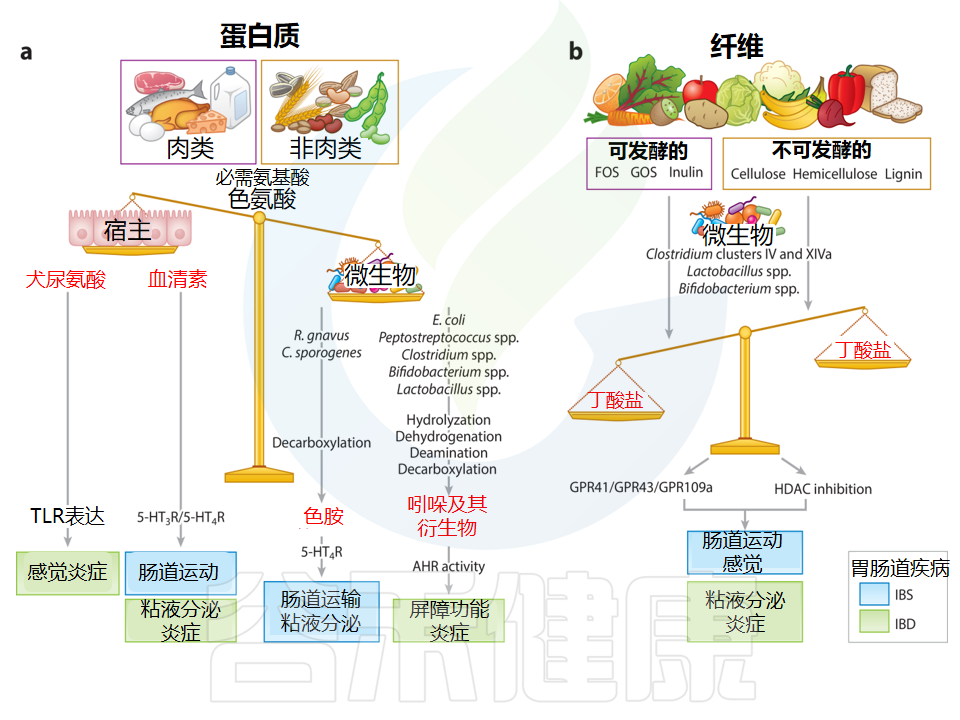
Jadhav A,et al.Annu Rev Nutr.2023
饮食衍生的代谢物可改变多种生物途径,而这些途径是多种胃肠道(GI)疾病的基础。
a)饮食蛋白质,包括肉类和非肉类(例如谷物、种子和坚果),都含有不同水平的氨基酸,例如色氨酸。可被宿主代谢产生犬尿氨酸和血清素(5-HT)。肠道微生物群还可以通过不同的代谢途径将色氨酸转化为色胺或吲哚和吲哚衍生物。色胺通过激活血清素受体4来增加肠道分泌和杯状细胞的粘液释放,而吲哚和吲哚衍生物是芳烃受体(AHR)的配体,在调节屏障功能和免疫反应中发挥重要作用。
b)膳食纤维包括可发酵[例如低聚果糖、低聚半乳糖和菊粉]和不可发酵(例如纤维素、半纤维素和木质素)纤维。根据肠道细菌的类型和纤维的类型,它们会发酵成不同的短链脂肪酸,例如丁酸盐和乙酸盐。丁酸盐可以增加血清素合成,增强结肠收缩力,缓解内脏过敏,增强屏障。
色氨酸衍生的生物活性代谢物取决于肠道菌群,那么纤维的发酵产物与微生物组成有关吗?
富含膳食纤维的饮食被认为是有益的,因为肠道微生物群会发酵纤维产生丁酸、乙酸和丙酸等短链脂肪酸,这些短链脂肪酸会影响宿主生理学的重要方面,包括代谢、细胞周转和免疫系统。
然而,人类研究表明,个体对纤维摄入量的反应存在显著差异,并且基于纤维类型的差异也很大。这并不奇怪,因为纤维是一个总称,包括具有不同连接和分子结构的不同碳水化合物群体。不同细菌携带的基因使它们能够利用具有特定连接和结构的碳水化合物。
膳食纤维的生物学效应取决于纤维的成分、个体肠道微生物群代谢特定纤维的潜力以及不同发酵最终产物的相对量。
▸ 低聚果糖在健康人体和炎症性肠病患者中作用大为不同
编辑
最近的一项研究发现,低聚果糖(FOS)会加重炎症性肠病(IBD)患者的炎症,而肠道细菌代谢它会减轻其在活动性炎症的IBD患者的炎症作用。
有趣的是,低聚果糖在健康个体中具有抗炎作用。因此,低聚果糖的炎症潜力取决于肠道微生物组成以及宿主疾病状态。
产生的短链脂肪酸的水平和类型可能因纤维组成和肠道微生物群而异。在饮食中添加菊粉会增加丁酸盐,但会降低乙酸盐的产生。相反,在消耗相同纤维量的患者亚组中,粪便丁酸水平较低,这归因于产生丁酸的细菌水平较低。这些结果有助于解释对纤维反应的个体间差异。
鉴于微生物代谢产物对宿主发挥多效性作用,因此,相同的代谢物可以影响多种宿主功能,每种功能都可能与不同的疾病状态相关。
色氨酸代谢物如色胺和5-HT会影响胃肠道转运,这与肠脑轴(DGBA)相关,而色胺和吲哚衍生物可以改变粘液和免疫反应,这对炎症性肠病具有影响。
同样,丁酸等发酵终产物会影响胃肠道运动以及上皮屏障功能,这分别与DGBA和IBD相关。
肠道微生物组的一个重要决定因素是饮食,它会对肠道微生物组产生长期和短期影响,它们会随着个体饮食的变化而变化。
与农业社会相比,工业化社会个体饮食的成分显著改变和肠道微生物多样性减少能证明习惯饮食的长期影响。
▸ 低纤维饮食会导致肠道微生物多样性逐渐减少
研究证明,低纤维饮食会导致人肠道微生物多样性逐渐丧失,这在早期阶段是可逆的,但可能会导致后代特定分类群的灭绝,而仅靠饮食干预是无法恢复的。
这一观察结果为西方人群中观察到的肠道微生物多样性较低提供了一种解释,并强调了微小的变化是如何在几代人的过程中积累起来的。因此,个体的微生物群落结构可能反映了人群的长期饮食模式。
▸ 短期饮食改变也会影响肠道微生物群,但可逆
短期的饮食改变也会改变肠道微生物组。虽然这些变化在不同程度上是可逆的,这取决于人体的基本恢复力和适应性,但短期变化可能在一定程度上解释慢性病患者症状的频率和严重程度不同。
这些短期影响也强调了微生物群导向的饮食干预作为治疗策略的潜力。
肠易激综合征(IBS)是一种常见的疾病,全球患病率约为11.2%。根据过去3个月内每周至少出现一次腹痛、伴有排便或大便频率或形式的变化并在过去6个月内出现症状进行诊断。
IBS一般可分为腹泻型(IBS-D)、便秘型(IBS-C)、混合型和未分类亚型。
胃肠道运输、分泌、感觉、免疫激活、肠道通透性和肠脑轴的改变等生理变化是IBS症状的基础。与IBS相关的危险因素包括宿主遗传、压力、抗生素使用和幼儿期经历,但饮食最常被认为是肠易激综合征的潜在罪魁祸首。基于人群的研究表明,近70%的IBS患者认为自己存在食物不耐受。
饮食引起症状的机制仍在研究中,但最近的研究已经开始阐明IBS中由饮食驱动的症状背后的微生物群独立机制和微生物群依赖机制。
研究发现将食物抗原(例如麸质、小麦、牛奶和大豆)直接注射到粘膜下层可以通过激活IBS患者的肥大细胞来引发免疫反应,但在健康受试者中则不然。
他们进一步表明,肥大细胞激活会引起内脏疼痛,并通过组胺刺激内脏神经元的敏化增加肠道通透性。虽然这项研究证明了一种独立于微生物群的机制,但其他研究发现,富含可发酵寡糖、二糖、单糖和多元醇(FODMAP)的饮食也可以通过Toll样受体4(TLR4)途径激活肥大细胞,这表明肠道微生物群的参与。
据报道,IBS-D患者中受饮食影响的微生物产物(如脂多糖和鞭毛蛋白)的血清水平显著升高。
脂多糖(LPS)是肠道细菌的一组异质细胞壁成分,充当TLR4的配体,在食用高脂肪饮食或高FODMAP饮食的个体中也会增加。除了在肥大细胞激活中的作用外,不同形式的LPS还能促进肠神经元的存活并增强平滑肌收缩力,这表明LPS浓度或结构的差异可能会驱动不同的宿主反应。
除微生物细胞壁成分外,宿主微生物代谢膳食成分产生的代谢终产物也可影响胃肠道生理,从而引发胃肠道症状。乙酸盐、丙酸盐和丁酸盐等短链脂肪酸由特定肠道微生物成员产生,其水平取决于微生物组成和膳食纤维摄入量。
丁酸盐是一种多效性代谢物,可通过G蛋白偶联受体(GPCR)直接发出信号,并通过表观遗传调控改变转录反应。丁酸盐可以浓度依赖性方式改变肠嗜铬细胞中的5-HT合成,通过直接影响肠道神经肌肉装置增加结肠收缩力,增强肠道上皮屏障,并通过与肠道神经胶质细胞相互作用调节内脏高敏感性。
另一方面,结肠内乙酸盐可增强对结肠直肠扩张的敏感性。具体影响可能取决于宿主健康和肠道中的整体代谢环境。
饮食、宿主粘液和微生物代谢都是肠道中氨基酸的主要来源。一项纵向研究报告称,尽管饮食蛋白质摄入量相似,但IBS-D患者的色氨酸和色胺水平(而非吲哚衍生物)高于健康人。
这种差异可能是由于肠道微生物群增加了色氨酸的产生和转化,或由于宿主对其利用率降低。胰蛋白酶激活肠细胞上的5-HT4R,进而增加肠液分泌。
另一项研究发现,IBS患者和健康受试者在结肠组织对色胺的5-HT4R表达或反应方面没有差异,这表明较高的色胺水平可能是腹泻的重要驱动因素。
在腹泻型(IBS-D)患者中,其他饮食和微生物驱动的途径也被描述了。无乳糜泻的IBS-D患者中经常报道麸质不耐症,这似乎部分依赖于宿主基因型和肠道微生物群组成。据报道,与阴性患者相比,HLA-DQ2/HLA-DQ8 阴性的IBS-D患者在无麸质饮食后腹胀显著减轻。
HLA-DQ2和HLA-DQ8基因是导致乳糜泻的主要基因。
其他研究表明,肠道微生物群可以对麸质的消化和免疫原性产生不同的影响。麸质对IBS-D影响的具体机制仍需进一步研究确定。
胆汁酸(BA)在肝脏中合成,储存在胆囊中,用于脂质乳化。膳食脂肪和姜黄是刺激初级胆汁酸释放到小肠中的重要因素。
近95%的初级胆汁酸在远端小肠中被重新吸收,剩余的初级胆汁酸在进入结肠后被肠道微生物去偶联、脱羟基和差向异构化为次级胆汁酸。
初级胆汁酸如鹅去氧胆酸通过氯化物通道增加结肠分泌,并降低健康个体的直肠感觉阈值。在啮齿类动物模型中,鹅去氧胆酸通过激活核受体法尼素X受体、释放神经生长因子和在背根神经节中下游表达瞬时受体电位香草素1(TRPV1),影响内脏敏感性。
▸ IBS-D患者的胆汁酸水平较高
IBS-D患者的粪便胆汁酸水平可能更高,这归因于胆汁酸吸收不良或肠道微生物群减少导致的继发性胆汁酸转化减少。因此,高脂肪饮食可以通过调节胆汁酸的释放,直接或通过胆汁酸的微生物代谢间接改变胃肠道生理学。
除此之外,最近的一项研究发现,感染后IBS-D患者的细菌编码的β-葡萄糖醛酸酶水平较低,这种酶可以解除胆红素的结合。
这些患者的结合胆红素水平较高,导致对宿主蛋白酶的抑制作用降低,肠道通透性增加,从而引发内脏超敏反应。
炎症性肠病(IBD)是一种特发性、慢性、使人衰弱的炎症性胃肠道疾病,包括两种疾病——克罗恩病(CD)和溃疡性结肠炎(UC)。克罗恩病表现为遍布整个胃肠道的斑片状透壁炎症,而溃疡性结肠炎则是结肠的持续性粘膜炎症。
这两种疾病都是由于环境、遗传和免疫因素共同作用下,对肠道微生物信号产生的不受控制的炎症反应引起的。从流行病学角度来看,IBD曾被认为是西方国家的疾病,欧洲和北美的发病率最高。但自20世纪90年代以来,IBD的高发区已大幅向东方扩展,在非洲、亚洲(如印度每10万人9.3例,中国每10万人3.3例)和南美洲的新兴工业化国家中,发病率迅速上升。
▸ 炎症性肠病的风险升高与饮食改变紧密相关
这些流行病的转变与全球饮食模式的转变相吻合,包括引入包装和加工食品;广泛接受和使用食品添加剂、防腐剂和抗生素;推广快餐连锁店,同时减少针对特定地区的当地饮食。
流行病学研究表明,饮食是形成炎症性肠病(IBD)的关键环境因素之一,从低发病地区迁移到高发病地区的人群中,IBD的患病率有所上升。此外,法国和西班牙的南北流行率差异也很微妙。在这些国家的北部地区观察到较高的IBD负荷,那里的个人食用更多的黄油、土豆、火腿、奶酪、香肠和啤酒,而南部地区的个人则遵循地中海饮食,主要由橄榄、新鲜水果和蔬菜、葡萄酒和海鲜组成。
饮食成分不仅可以直接影响炎症性肠病的病理生理学,而且还可以通过其在肠道微生物群中的转化间接影响疾病进程。让我们一起来了解下其中的具体机制。
饮食在炎症性肠病发病机制和预防中的作用
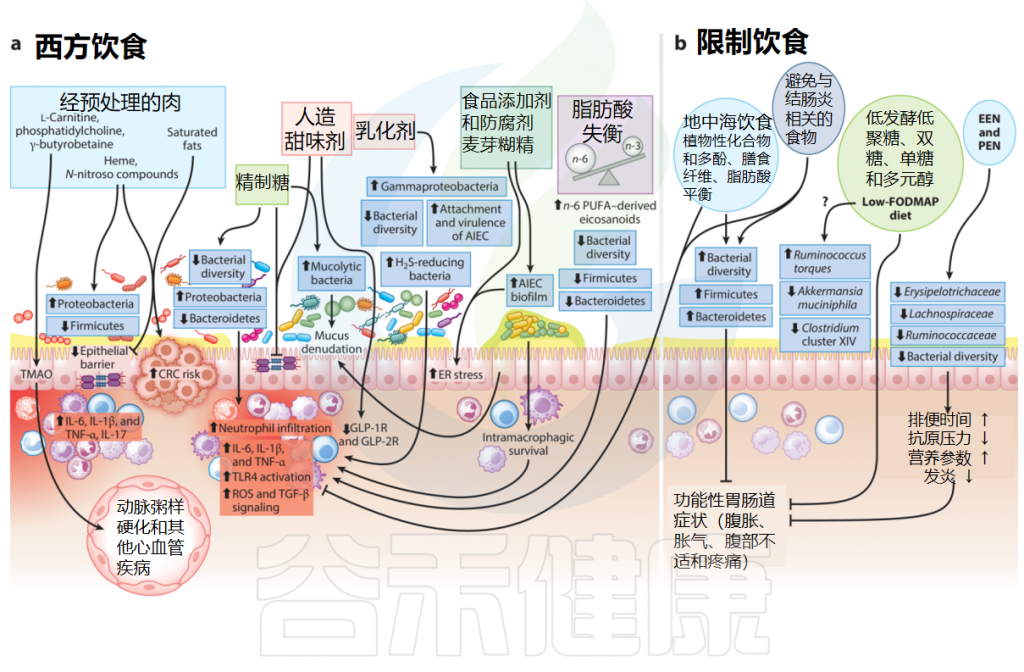
Jadhav A,et al.Annu Rev Nutr.2023
膳食中的大量营养素、微量营养素、添加剂和热量含量之间相互作用复杂;宿主免疫、遗传学和肠道微生物组可能是炎症性肠病(IBD)风险和临床病程的重要决定因素。
▸ 红肉饮食可能加剧炎症性肠病风险

最近一项由125445名参与者组成的大型前瞻性队列研究发现,西方饮食(包括红肉、家禽和加工肉类等动物蛋白)与溃疡性结肠炎发展可能性增加之间存在关联。
此外,红肉加剧炎症性肠病的影响在其他研究中也得到了证实。欧洲癌症和营养前瞻性调查队列表明,红肉摄入增加了亚油酸摄入量,从而使溃疡性结肠炎风险增加超过一倍。
同时,一项法国大型前瞻性问卷研究也支持这一观点。值得注意的是,加工红肉的摄入,与克罗恩病患者死亡率的显著增加有关。
▸ 红肉中的左旋肉碱等物质经微生物转化为氧化三甲胺与炎症呈正相关
红肉主要由蛋白质、脂肪和血红素组成,这些成分水平的增加会改变肠道微生物群的组成,进而对上皮细胞更新和肠道屏障完整性产生负面影响,并加剧肠道炎症。
值得注意的是,红肉中富含左旋肉碱、磷脂酰胆碱和γ-丁甜菜碱,这些物质通过肠道微生物代谢转化为三甲胺。三甲胺在宿主肝脏中通过含黄素单加氧酶形成氧化三甲胺(TMAO)。动物研究和人类流行病学研究表明,TMAO与炎症、心血管疾病、结直肠癌和死亡率之间有很强的正相关关系。
与传统的饮食习惯不同,西方饮食富含简单的精制碳水化合物、饱和脂肪以及超加工食品,而新鲜水果和蔬菜、豆类、全谷物和膳食纤维的含量较低。
超加工食品是在已经加工过的食品基础上再加工的食品,这类食品通常是高糖、高脂、高热量的食品。可涵盖多种食物,包括肉类、淀粉类零食、乳制品、豆类、水果和蔬菜。
研究报告了西方饮食对人类健康的不利影响,并将其与肥胖、糖尿病、炎症性肠病、慢性肾病和其他与生活方式相关的疾病联系起来。食品的(超)加工旨在提高其保质期、适口性以及储存和分销的便利性,其中涉及掺入许多非天然成分和添加剂,例如人造香料、稳定剂、防腐剂和乳化剂。
▸ 超加工食品的摄入量较高与炎症性肠病风险增加相关

最近一项针对来自7个地理区域 21个低收入、中等收入和高收入国家的大型前瞻性队列(116,087名成年人)的研究发现,超加工食品的摄入量较高与炎症性肠病风险呈正相关;然而,未加工的白肉、红肉、乳制品、淀粉、水果和蔬菜的摄入与炎症性肠病的发病率无关。
研究发现,炎症性肠病(IBD)风险与非酒精含糖饮料的消费存在正相关关系。
▸ 含糖饮料摄入过多增加炎症性肠病风险

最近的两项荟萃分析整合了关于饮料摄入量与IBD风险的观察性研究,表明高摄入量的含糖饮料与IBD风险增加相关。实验显示,高膳食糖摄入与炎症诱导和肠道微生态失调有关。一项基于问卷的研究比较了IBD患者与健康人群的饮食模式,发现IBD患者的含糖饮料消费量更高。
阿斯巴甜、糖精、安赛蜜和三氯蔗糖等人造甜味剂因其在不增加额外热量的情况下赋予食物甜味而广泛流行。然而,动物研究和健康人类试验报告称,这些非营养性甜味剂降低了肠道微生物多样性,使肠道炎症永久化,通过增加变形菌门(Proteobacteria)成员和减少有益微生物(如瘤胃菌科、毛螺菌科和梭状芽孢杆菌群XIVa)的比例来改变肠道微生物群,并损害肠道屏障的完整性。
▸ 麦芽糊精会加剧肠道炎症
麦芽糊精(E1400)是一种重要的食品添加剂,可用作加工食品的增稠剂,在小鼠结肠炎模型中,它通过诱导内质网应激和改变粘液层,以剂量依赖性方式加剧肠道炎症。小鼠模型中的报告还表明,麦芽糊精通过调节细菌基因表达,促进克罗恩病相关的粘附侵袭性大肠杆菌形成生物膜。
▸ 防腐剂会降低肠道微生物多样性
加工食品中的防腐剂会加剧有害影响。苯甲酸钠(E211)、亚硝酸钠(E250)和山梨酸钾(E202)这三种最常用的防腐剂会降低肠道微生物多样性,在人类肠道微生物群相关的小鼠模型中,变形菌门增加,梭状芽胞杆菌的减少。
注:尽管人类和动物研究已经提供了关于这些非营养性膳食添加剂对肠道菌群失调和肠道健康的负面影响的机制见解,但仍缺乏评估这些甜味剂对炎症性肠病人群影响的人体随机对照试验。
▸ 乳化剂过量食用会导致肠道微生物失调并促进慢性炎症
类似地,合成乳化剂,如聚山梨酯80和羧甲基纤维素,被用作增强质地和延长保质期的添加剂。在动物研究中,这些乳化剂被广泛认为会导致肠道微生态失调并促进慢性炎症。

▸ 摄入过多的脂肪增加炎症性肠病风险
进行的一项大型前瞻性流行病学研究,基于超过200,000名参与者的食物频率调查问卷,显示ω-6多不饱和脂肪酸的摄入量与溃疡性结肠炎(UC)风险增加之间存在显著关联。
高摄入总脂肪、ω-6多不饱和脂肪酸和肉类会增加患溃疡性结肠炎的风险;高摄入饱和脂肪、ω-6多不饱和脂肪酸和肉类也会增加患克罗恩病的风险。
▸ ω-6脂肪酸在炎症性肠病中具有促炎性
虽然主要的膳食ω-3不饱和脂肪酸,即二十碳五烯酸(EPA)和二十二碳六烯酸(DHA),及其下游类二十烷酸具有抗炎特性,但ω-6多不饱和脂肪酸,如花生四烯酸(AA)及白三烯、羟基二十碳四烯酸、脂氧素和环氧二十碳三烯酸等在炎症性肠病中表现出强烈的促炎活性。
这些介质增强中性粒细胞的趋化性;增强血管通透性;以及炎症细胞因子的产生,例如肿瘤坏死因子(TNF-α)、白细胞介素(IL)-1β、IL-6和IL-8。有趣的是,这些脂肪酸介质的代谢在炎症粘膜中发生了改变,ω-6 花生四烯酸水平较高,ω-3 EPA水平较低,这表明脂肪酸代谢与炎症性肠病之间存在关联。
▸ ω-6促进肠道炎症与肠道微生物失调相关
最近的动物研究和人体试验已经将饮食中的ω-6多不饱和脂肪酸与肠道微生物微生态失调联系起来。γ-亚麻酸水平越高,2型糖尿病的发病率越高;肠道微生物多样性降低;有益微生物如普雷沃菌属(Prevotella)、Odoribacter、粪杆菌属、Paraprevotella、经黏液真杆菌属(Blautia)和丁酸弧菌属,以及梭菌目、Rikenellaceae和Coriobacteriaceae的成员减少。
在断奶阶段补充ω-6高脂肪饮食的小鼠显示,成年期结肠炎症和增生性病变的数量增加,厚壁菌门、梭状芽孢杆菌和毛螺菌属成员显著减少。在衰老小鼠模型中,补充ω-6也有类似效果,高ω-6脂肪饮食减少了厚壁菌门和拟杆菌门的有益成员,并导致肠道炎症。而补充鱼油可以逆转观察到的肠道微生态失调。
饮食成分在肠易激综合征和炎症性肠病等胃肠道疾病的病理生理学中发挥作用,使得通过饮食调节成为一种无创、更日常便利的治疗方法。
然而,目前的饮食策略缺乏特异性,在具有不同病理生理学的胃肠道疾病(如肠易激综合征和炎症性肠病)中也采用类似的方法。最常见的策略是限制、改变或补充营养。
▸ 可发酵碳水化合物不利于肠易激综合征患者的健康
治疗肠易激综合征(IBS)最常见的饮食干预之一是减少FODMAP食物(通常是吸收不良的“可发酵”碳水化合物,包括果糖、乳糖、多元醇、果聚糖和低聚半乳糖)摄入12周,然后缓慢恢复上述食物组。
这类营养素被认为是疾病病理生理学的重要驱动因素。基于这样的观点:FODMAP会增加渗透负荷并产生更高水平的氢,从而导致管腔扩张。这些碳水化合物还会会被结肠中的细菌发酵,并引起肠易激综合征特有的腹胀、胀气和腹痛等症状。
▸ 低FODMAP饮食改善肠易激综合征患者症状

对澳大利亚肠易激综合征患者进行的一项关键研究显示,与西方饮食相比,低FODMAP饮食可显著改善症状。最近的一项荟萃分析纳入了397名患者的七项随机对照研究,结果显示,与对照干预相比,低FODMAP饮食可减轻整体症状。
然而,这项荟萃分析中的三项随机对照试验比较了低FODMAP饮食和严格的对照饮食,这些试验之间的异质性较小,且效应量有限。因此,虽然低FODMAP饮食能够使肠易激综合征患者受益,但数据的整体质量较低。
这一发现表明,几种不同的饮食干预措施都可以改善IBS症状,找到它们之间的共同点将会很有帮助。
▸ 低FODMAP饮食的效果会因肠道微生物组成不同而存在差异
有趣的是,一项针对健康受试者的研究发现,低FODMAP饮食并没有减少结肠体积,这表明症状改善背后可能存在其他机制。低FODMAP饮食的效应是与肠道菌群存在重要联系。
荟萃分析还发现无麸质饮食对肠易激综合征患者无显著益处。如上所述,这种影响可能取决于宿主基因型或其他宿主/环境因素。麸质主要存在于小麦、大麦和黑麦中,它们是高FODMAP饮食的一部分;因此,在部分患者中观察到的改善也可能是限制FODMAP的结果,而不仅仅是麸质的结果。
最近的一项综述显示,炎症性肠病患者中非腹腔麸质敏感性患病率很高;但几乎没有证据支持这些患者采用无麸质饮食。临床前研究发现无麸质饮食可以改善炎症和通透性,但缺乏针对人类受试者的高质量前瞻性研究。关于麸质微生物降解对炎症性肠病和乳糜泻都具有重要意义,是未来研究的重要领域。
地中海饮食(MD)富含水果、蔬菜、面包、谷物、豆类、坚果和初榨橄榄油,以及适量的乳制品、鱼和肉。地中海饮食被认为是一种平衡且健康的长期饮食选择。
地中海饮食和低FODMAP饮食的效果


Jadhav A,et al.Annu Rev Nutr.2023
▸ 地中海饮食的炎症性肠病患者症状减轻
最近的一项前瞻性、随机研究纳入了100名患有轻度至中度疾病的青少年炎症性肠病患者,比较了地中海饮食与常规饮食的疗效,结果显示,小儿克罗恩病活动指数和小儿溃疡性结肠炎活动指数的临床评分显著下降。以及较低水平的炎症标志物,例如血清C反应蛋白、钙卫蛋白、TNF-α、IL-17、IL-12和IL-13。
临床试验,也观察到地中海饮食对炎症性肠病的有益作用。这项研究涉及142名炎症性肠病患者(84名 溃疡性结肠炎和58名克罗恩病)。接受地中海饮食治疗6个月,显著改善了体重指数和腰围,并导致肝脏脂肪变性和营养不良相关参数显著减少。其中40%的轻度至中度克罗恩病患者在接受6-12周的地中海饮食治疗后病情得到缓解。
▸ 地中海饮食与健康有益的微生物特征相关
地中海饮食与有益的肠道微生物特征相关,特别是与膳食纤维代谢物的富集有关,例如普拉梭菌、解纤维素拟杆菌和普雷沃氏菌,以及参与植物多糖降解和短链脂肪酸和次级胆汁酸生产的其他微生物。
地中海饮食富含ω-3不饱和脂肪酸,使得ω-3和ω-6脂肪酸达到平衡。在前瞻性溃疡性结肠炎队列中证明了EPA和其他不饱和脂肪酸的积极作用,其中肠道炎症细胞因子水平与PUFA、EPA和二十二碳五烯酸呈负相关。
▸ ω-3 不饱和脂肪酸有助于对抗肠道相关炎症
涉及ω-3脂肪酸代谢的三个关键基因(CYP4F3、FADS1和FADS2)的单核苷酸多态性与克罗恩病风险增加相关,这显示了炎症性肠病饮食相关调节的额外遗传因素。
ω-3 不饱和脂肪酸可能通过下游脂质介质(例如消解素、保护素和噬消素(maresins))发挥抗炎作用,这些介质可以对抗IBD相关炎症。从机制上讲,ω-3 不饱和脂肪酸已被发现:
(a)降低中性粒细胞和单核细胞对各种化学引诱剂的趋化性;
(b)通过阻断丝裂原激活蛋白激酶释放核因子κB来抑制TLR4表达和NOD2信号传导;
(c)抑制NLRP3炎性体激活并随后阻碍促炎细胞因子的释放;
(d)增加产生丁酸盐的细菌属如双歧杆菌属、罗氏菌属和乳杆菌属以及毛螺菌科成员的丰度。
▸ 地中海饮食通过微生物产生的短链脂肪酸也有助于减轻肠道炎症
由于可发酵碳水化合物含量较高,地中海饮食可导致肠道微生物群产生更多的短链脂肪酸。此外还发现,地中海饮食可改善坚持饮食的肠易激综合征患者的腹胀和腹痛。
膳食纤维、益生元和合生元等营养物质具有促进细菌群落生长的作用,对健康有益,并被证明可以改善宿主肠道炎症。
益生元和合生元在IBS和IBD中的作用




Jadhav A,et al.Annu Rev Nutr.2023
▸ 可溶性膳食纤维有助于改善肠道炎症
对14项随机对照研究(包括906名肠易激综合征患者)进行的荟萃分析发现,可溶性膳食纤维可显著改善症状,但麸皮则不然。
注:但这些研究大多数都使用纤维补充剂;他们中很少有人改变饮食以增加纤维摄入量。尽管有几项研究调查了益生元和合生元,但没有足够的数据来提出建议。
炎症性肠病的临床前模型发现,高纤维(主要是车前草)、低蛋白饮食可增强肠道屏障功能并减少炎症。因此,可溶性纤维似乎对肠易激综合征患者和炎症性肠病患者都有益。
最近的一项荟萃分析还发现,膳食纤维摄入量与克罗恩病风险之间存在线性剂量依赖性关系,每天每增加10克纤维摄入量,克罗恩病风险就会降低 13%。
▸ 补充益生元可以降低疾病活动性
一项针对肠易激综合征患者的随机、平行、双盲研究比较了地中海饮食和益生元补充剂(β-低聚半乳糖)与低FODMAP饮食和安慰剂木糖补充剂的效果,发现肠易激综合征患者的症状有所改善,但补充益生元后肠道微生物群分布更有利。这一发现突显了饮食调整和补充作为胃肠道疾病管理中限制性饮食习惯的替代方案的潜力。
基于食物和补充剂的纤维和益生元干预研究报告指出,富含纤维的半素食、车前子种子、燕麦麸和发芽大麦食品在缓解和显著改善胃肠道症状(如腹痛和反流)方面取得了令人振奋的成果。
在接受低聚果糖(每天15克,持续3-4周)、富含低聚果糖的菊粉(每天两次,每次10克,持续4周)、全麦麸(每天0.5杯,持续4周)、菊粉型果聚糖(每天7.5克,持续9周)和发芽大麦食品补充的活动性疾病队列中也报告了类似的结果,特别是显著降低了疾病活性并提高了生活质量。
▸ 纤维和益生元的益处会因个体健康状况和肠道菌群组成而不同
一项评估纤维摄入量对肠道微生物组组成影响分析表明,与安慰剂/低纤维饮食相比,高膳食纤维摄入与双歧杆菌属和乳杆菌属的丰度显著增加以及粪便丁酸盐含量增加相关。
不过这些研究主要针对成年炎症性肠病患者进行,对儿童的益处尚不清楚。膳食纤维被广泛用于包括一系列复合碳水化合物(包括益生元)。但如上所述,膳食纤维的效果可能会因碳水化合物结构、健康状况和肠道微生物群组成而异。
一些研究表明合生元对成年溃疡性结肠炎患者有益。与安慰剂组相比,补充长双歧杆菌和富含低聚果糖的菊粉4周可改善症状,并降低炎性细胞因子(TNF-α和IL-1β)的表达。
在一项随机对照试验中报告了类似的结果,该试验涉及补充8周由屎肠球菌、植物乳杆菌、嗜酸乳杆菌、嗜热链球菌、乳双歧杆菌、长双歧杆菌和低聚果糖组成的合生元混合物。
纯肠内营养(EEN)已被接受为儿科克罗恩病患者的一线饮食干预措施。特指经消化道途径(包括口服和管饲)提供营养物质的一种营养支持治疗方式,包含所有必需的常量营养素和微量营养素。
▸ 纯肠内营养有助于减轻克罗恩病患者症状
许多研究表明,纯肠内营养(EEN)在诱导轻度至中度克罗恩病儿科患者缓解方面的效果与皮质类固醇相当。例如,在澳大利亚和西班牙的独立试验中,补充EEN8周分别使84%和80%的受试者达到临床缓解。
EEN对患有克罗恩病的围手术期成年患者也有效。两项前瞻性队列研究的荟萃分析显示,术前接受EEN的患者(22%)与未接受EEN的患者相比,术后并发症显著减少。尽管有限,但其他研究已经描述了EEN在治疗穿透性克罗恩病、狭窄性克罗恩病和肠外克罗恩病方面的益处。
▸ 纯肠内营养增强肠道微生物群的抗炎作用
从机制上讲,EEN可能通过改变肠道菌群的组成和功能发挥作用。尽管它反而降低了肠道微生物多样性和通常被认为有益的菌群的丰富度(粪杆菌属、瘤胃球菌属和双歧杆菌属以及丹毒丝科、毛螺菌科的其他成员),但它根据代谢物的变化增强了肠道菌群的功能。
由于EEN的组成简单,降低抗原压力和肠道休息也可能是其重要的作用机制。此外,EEN配方中的活性成分可以改善营养参数,并可能对肠上皮产生抗炎作用。
在成人中,EEN作为二线或三线治疗使用,而皮质类固醇则是主要的诱导治疗,因为这些药物比EEN更有效地诱导临床缓解。
▸ 排除饮食减少肠道微生物的有害变化有助于病情缓解
部分肠内营养(PEN),即补充患者一半的热量需求作为肠内营养和全食物饮食,有助于克罗恩病患者维持病情缓解。
一项儿科克罗恩病队列研究中,无限制的PEN与元素配方结合效果有限;因此,研究人员认为需要一种针对克罗恩病和溃疡性结肠炎的排除饮食,排除某些有害食物。
克罗恩病排除饮食(CDED)与PEN相结合,是一种全食物饮食制度,旨在减少与肠道微生物群有害变化(如变形杆菌的扩张)、屏障完整性受损和胃肠道炎症相关的饮食成分和食物的暴露。
CDED不包含加工食品,并含有有益的纤维,再加上液体配方奶粉,以满足患者的能量需求。一项前瞻性研究报告称,与EEN相比,CDED加PEN在CD队列中具有更好的耐受性和更有效的效果,并且75%的CDED加PEN患者获得了无类固醇的临床缓解。
饮食衍生的代谢物因宿主健康状况和肠道微生物群中不同代谢途径而异,这反过来影响了饮食的生物学效应。因此,同一种食物可能对不同人群的生理功能具有不同的作用,可以影响多种疾病的病理生理,这也解释了相同饮食干预对不同疾病有益。
我们仍处于研究饮食-宿主-肠道菌群相互作用产生的生物活性分子如何影响慢性胃肠道疾病的病理生理和治疗反应的早期阶段。一个重要的考虑因素是,在评估饮食干预的反应时观察到的显著个体间差异。这种差异可能源于饮食中生物可利用营养素的差异(由于成分和加工方式(如烹饪)的差异)、影响宿主代谢途径或免疫状态的基因多态性,以及肠道菌群代谢能力的差异。此外,其他环境和宿主因素也可能影响反应。我们需要考虑所有这些因素,以便能够为患者提供个性化的饮食建议。
编辑
Jadhav A,et al.Annu Rev Nutr.2023
总而言之,饮食与个性化微生物群在胃肠道疾病中的相互作用是一个复杂且充满潜力的研究领域。理解这种相互作用不仅有助于揭示疾病的发病机制,还为个性化医疗和精准营养提供了新的视角和方法。随着科学技术的不断进步,我们有理由相信,通过优化饮食和微生物群的相互作用,可以实现对胃肠道疾病更加有效的预防和治疗。
在应用方面,谷禾专注于高通量检测技术和人工智能的结合,通过精确、便捷、无创的检测方式,以肠道菌群为核心,结合蛋白质及代谢物检测的多组学检测,开发多模态表征和大模型框架。肠菌检测作为一种基于实证的工具,它不仅可以评估个人肠道菌群及营养状况,还可以从整个个性化营养生态的视角出发,多场景、全方位地为疾病预防和健康管理解决方案提供帮助。
注:本账号内容仅作交流参考,不作为诊断及医疗依据。
主要参考文献
Jadhav A, Bajaj A, Xiao Y, Markandey M, Ahuja V, Kashyap PC. Role of Diet-Microbiome Interaction in Gastrointestinal Disorders and Strategies to Modulate Them with Microbiome-Targeted Therapies. Annu Rev Nutr. 2023 Aug 21;43:355-383.
Armstrong HK, Bording-Jorgensen M, Santer DM, Zhang Z, Valcheva R, Rieger AM, Sung-Ho Kim J, Dijk SI, Mahmood R, Ogungbola O, Jovel J, Moreau F, Gorman H, Dickner R, Jerasi J, Mander IK, Lafleur D, Cheng C, Petrova A, Jeanson TL, Mason A, Sergi CM, Levine A, Chadee K, Armstrong D, Rauscher S, Bernstein CN, Carroll MW, Huynh HQ, Walter J, Madsen KL, Dieleman LA, Wine E. Unfermented β-fructan Fibers Fuel Inflammation in Select Inflammatory Bowel Disease Patients. Gastroenterology. 2023 Feb;164(2):228-240.
Dong C, Chan SSM, Jantchou P, Racine A, Oldenburg B, Weiderpass E, Heath AK, Tong TYN, Tjønneland A, Kyrø C, Bueno de Mesquita B, Kaaks R, Katzke VA, Bergman MM, Boeing H, Palli D, Masala G, Tumino R, Sacerdote C, Colorado-Yohar SM, Sánchez MJ, Grip O, Lindgren S, Luben R, Huybrechts I, Gunter MJ, Mahamat-Saleh Y, Boutron-Ruault MC, Carbonnel F. Meat Intake Is Associated with a Higher Risk of Ulcerative Colitis in a Large European Prospective Cohort Studyø. J Crohns Colitis. 2022 Aug 30;16(8):1187-1196.
Narula N, Wong ECL, Dehghan M, Mente A, Rangarajan S, Lanas F, Lopez-Jaramillo P, Rohatgi P, Lakshmi PVM, Varma RP, Orlandini A, Avezum A, Wielgosz A, Poirier P, Almadi MA, Altuntas Y, Ng KK, Chifamba J, Yeates K, Puoane T, Khatib R, Yusuf R, Boström KB, Zatonska K, Iqbal R, Weida L, Yibing Z, Sidong L, Dans A, Yusufali A, Mohammadifard N, Marshall JK, Moayyedi P, Reinisch W, Yusuf S. Association of ultra-processed food intake with risk of inflammatory bowel disease: prospective cohort study. BMJ. 2021 Jul 14;374:n1554.
Khademi Z, Milajerdi A, Larijani B, Esmaillzadeh A. Dietary Intake of Total Carbohydrates, Sugar and Sugar-Sweetened Beverages, and Risk of Inflammatory Bowel Disease: A Systematic Review and Meta-Analysis of Prospective Cohort Studies. Front Nutr. 2021 Oct 1;8:707795.
IBD in EPIC Study Investigators; Tjonneland A, Overvad K, Bergmann MM, Nagel G, Linseisen J, Hallmans G, Palmqvist R, Sjodin H, Hagglund G, Berglund G, Lindgren S, Grip O, Palli D, Day NE, Khaw KT, Bingham S, Riboli E, Kennedy H, Hart A. Linoleic acid, a dietary n-6 polyunsaturated fatty acid, and the aetiology of ulcerative colitis: a nested case-control study within a European prospective cohort study. Gut. 2009 Dec;58(12):1606-11.
Dionne J, Ford AC, Yuan Y, Chey WD, Lacy BE, Saito YA, Quigley EMM, Moayyedi P. A Systematic Review and Meta-Analysis Evaluating the Efficacy of a Gluten-Free Diet and a Low FODMAPs Diet in Treating Symptoms of Irritable Bowel Syndrome. Am J Gastroenterol. 2018 Sep;113(9):1290-1300.