-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com

冠状动脉疾病是世界范围内最常见的健康问题,也是导致发病率和死亡率的主要原因。肠道菌群在人类新陈代谢、免疫力等方面扮演重要角色,与冠状动脉疾病之间也存在相关性。
1、肠道微生物群与CAD发展之间的因果关系尚未得到证实。
2、必须通过微生物代谢产物和与免疫系统的相互作用,了解肠道微生物群与CAD发展之间潜在的直接和间接因果关系。
3、动态因素包括我们的饮食和人口因素,如年龄、性别和种族,也会影响我们的肠道微生物群和CAD的发展,并使这一问题复杂化。
4、需要跨学科的方法来揭示肠道微生物群的调节所涉及的因素及其与CAD发展的关系。
5、阐明系统层面的多方面因素参与微生物介导的机制和人类健康与疾病,可以进一步指导新的预防和治疗CAD的干预措施。
高血清胆固醇(高胆固醇血症)是最常见的心血管疾病(简称CVD,下同)的危险因素,称为冠状动脉疾病(简称CAD,下同)。
动脉壁内胆固醇沉积(斑块)的累积可导致动脉粥样硬化。

高胆固醇血症可能有遗传来源,并影响主要负责体内胆固醇稳态的身体功能,包括从头合成、肝脏分解代谢和胆汁分泌,以及肠道吸收。
胆固醇的来源
人体内的胆固醇来源于两种来源,在肝脏中从头合成,或通过饮食和富含胆固醇的食物进入人体。人体内大约四分之一的胆固醇来自膳食摄入(外源性),其余的是通过甲羟戊酸途径从头合成(内源性)。
冠状动脉疾病的形成
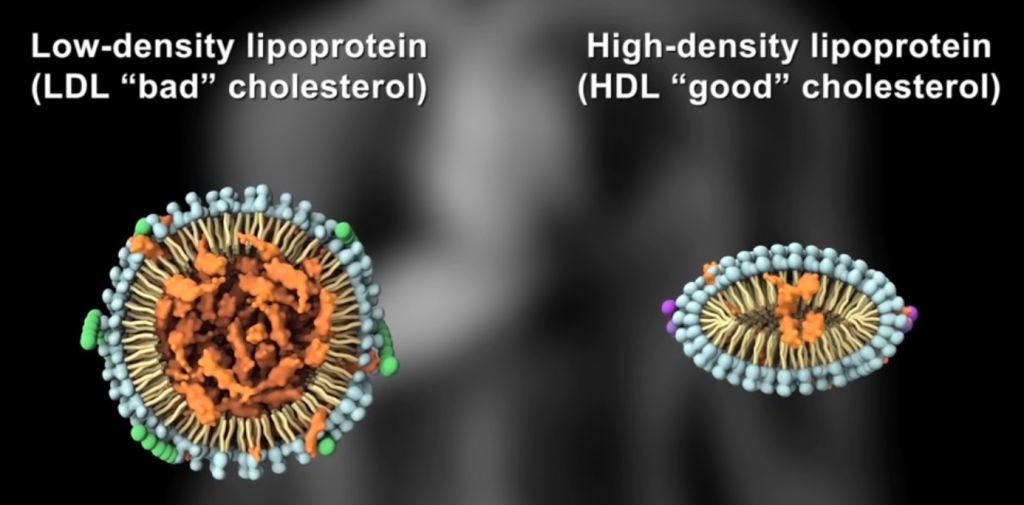

体内合成的胆固醇分为高密度脂蛋白胆固醇(简称HDL,下同)和低密度脂蛋白胆固醇(LDL),后者可进入循环系统,成为冠状动脉疾病的重要标志。
我们看看LDL如果多了会发生什么:
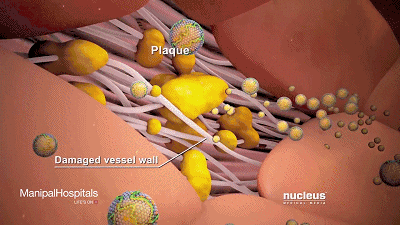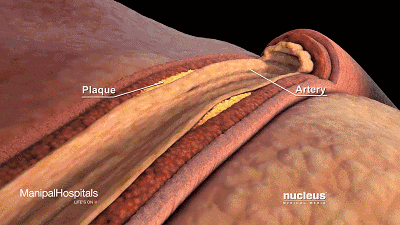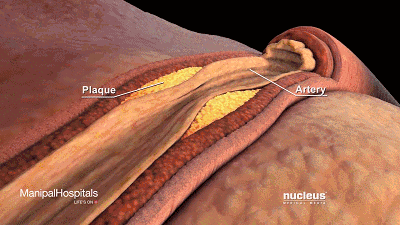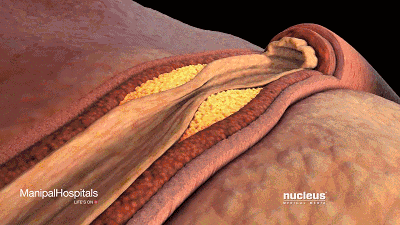

可以看到它聚积在动脉壁动脉,随着时间的推移脂肪沉积形成斑块,使动脉狭窄。
高密度脂蛋白胆固醇与CAD呈负相关,也就是说它在阻止CAD的形成。通过发挥抗炎和抗氧化作用以及促进反向胆固醇转运(RCT)而具有抗动脉粥样硬化的功能,RCT可以消除低密度脂蛋白胆固醇。
然而,在炎症、糖尿病和氧化应激等条件下,高密度脂蛋白可能会失去其抗动脉粥样硬化特性,并成为促动脉粥样硬化(功能失调)物质。此外,低密度脂蛋白胆固醇升高是冠状动脉疾病的危险因素,这可能是由于巨噬细胞摄取低密度脂蛋白胆固醇颗粒导致泡沫细胞和动脉粥样硬化。

肠腔在控制体内胆固醇平衡方面起着重要作用,并通过胆固醇吸收负责外源性摄入。管腔内胆固醇可以来自不同的来源,主要来源于(i)我们的饮食,(ii)通过肝胆途径的胆汁,(iii)通过经肠胆固醇流出途径的新胆固醇。
图1 腔内胆固醇的外源性和内源性来源
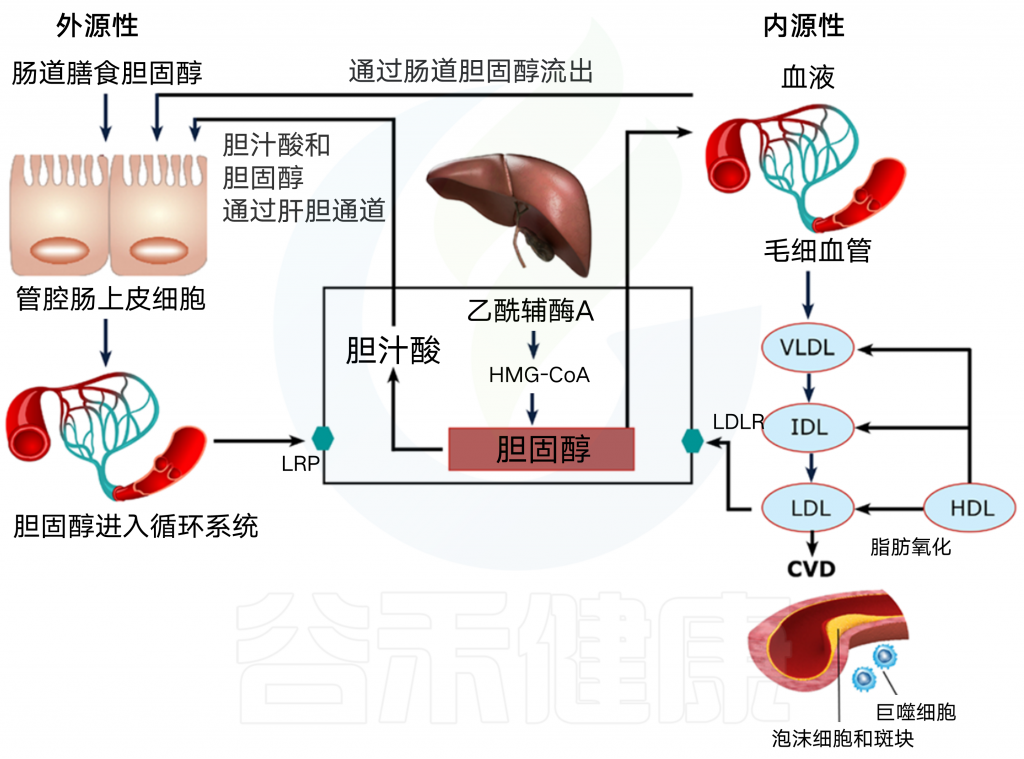

在肝脏中,胆固醇被代谢成胆汁酸,并通过肝胆途径分泌到胆汁中,其中ATP结合盒转运体G5/ATP结合盒转运体G8(ABCG5/G8)在胆固醇从肝细胞流出到胆汁中起关键作用。
TICE是肝胆通路的另一种途径,血液中的胆固醇可以通过低密度脂蛋白受体(LDL-R)直接进入肠细胞,并通过ABCG5/G8和ATP结合盒转运体B1(ABCB1a/b)进入肠腔。
然后,肠腔中的胆固醇通过Niemann-Pick C1-like 1(NPC1L1)被吸收到肠细胞中,并与乳糜微粒结合进入循环系统,或者被肠道微生物群还原为低吸收的粪烷醇(5B胆固醇-3B-ol),大部分排出体外。
其他因素影响胆固醇平衡和CAD发展
除了体内多种胆固醇来源的复杂相互作用外,还有许多其他因素可以影响胆固醇平衡和CAD的发展,包括肠道微生物群。
到目前为止,已经有人认为肠道微生物群的改变与代谢紊乱如肥胖、糖尿病和心血管疾病(与年龄、性别和宿主遗传学无关),包括动脉粥样硬化、血脂异常、高血压和心力衰竭之间的关系。
这种联系可以通过直接(通过代谢物)和间接途径(通过免疫系统)实现。
肠道微生物群在维持宿主健康方面发挥着多重关键作用,包括帮助宿主获得营养和能量、肠上皮内稳态、药物代谢和毒性、免疫系统反应以及抵御病原体。
微生物代谢产物影响
这些微生物还可以产生微生物产物,如尿毒症毒素、胆汁酸、氧化三甲胺(TMAO)、短链脂肪酸(SCFA)、脂多糖(LPS)、一氧化氮、维生素K、维生素B复合物、肠道激素和神经递质,它们可以改变宿主的新陈代谢和在健康和疾病状态下影响身体功能。例如,对动脉粥样硬化的易感性已经被证明可以通过小鼠模型中的微生物群移植进行转移。
迄今为止,许多传染源与动脉粥样硬化有关,包括幽门螺杆菌、巨细胞病毒、丙型肝炎病毒、肺炎衣原体和牙龈卟啉单胞菌。
Mitra等人的一项研究结果表明,在有症状和无症状的动脉粥样硬化斑块之间,微生物群表现出差异,无症状斑块有更多的宿主微生物群,包括卟啉单胞菌科、拟杆菌科、微球菌科和链球菌科。与此相反,有动脉粥样硬化斑块中含有越来越多的致病菌,包括螺旋杆菌科、奈瑟菌科和Thiotrichacaea.
此外,由于肠道微生物群整体状态的破坏而导致的肠道微生物群失调与炎症的增加有关,炎症与动脉粥样硬化的发展有关。
肠道菌群与高血压、心力衰竭、中风等有关
最近,肠道微生物群及其代谢产物的改变也与高血压和血管功能障碍有关。心力衰竭还与特定的肠道微生物种类有关,如增加的大肠杆菌、肺炎克雷伯菌、病毒性链球菌等。
一项研究表明,有症状的中风和短暂性脑缺血发作患者的肠道微生物群发生了改变,增加了机会致病菌,包括肠杆菌、巨球菌、Oscillibacter和脱硫弧菌。
此外,肠道微生物群有能力导致血脂成分的实质性变化,从而影响冠状动脉疾病的发展。例如,厚壁菌如罗伊氏乳杆菌与高密度脂蛋白相关,而Eggerthella属与低密度脂蛋白相关。
目前,肠道微生物群与CAD发展之间的因果关系尚不清楚,因为许多其他人口因素,如年龄、性别和种族,不仅会影响肠道微生物群和胆固醇水平,而且还会影响我们的饮食,这是影响肠道微生物群和全身胆固醇水平的另一个组成部分。因此,体内胆固醇的调节是一个复杂的机制,其中的各种因素在一个多方面的系统中交织在一起。
图2 CAD发展中涉及的多方面机制
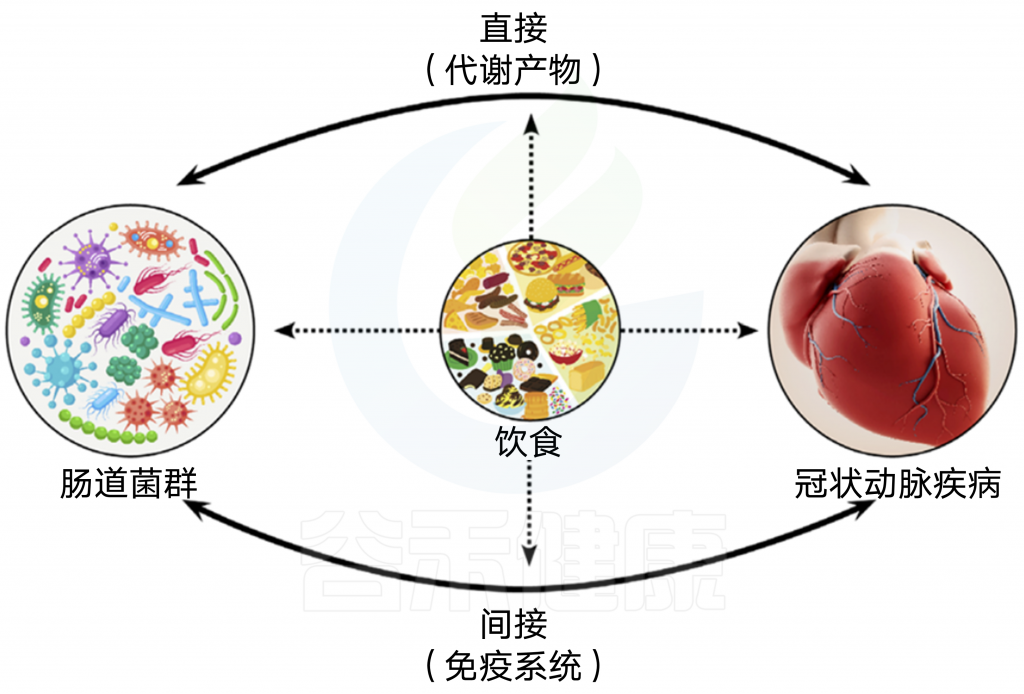

肠道微生物群可以直接(通过代谢物)和间接(通过免疫系统)导致CAD。
因此,需要进一步的研究,以了解潜在的机制,并确定哪些微生物菌株或其代谢物负责CAD的发展。
接着,将通过直接和间接途径探讨肠道微生物群的动态因素及其对高胆固醇血症和冠状动脉疾病发展的影响。
肠道微生物可以通过代谢产物如胆汁酸、粪甾醇、短链脂肪酸和三甲胺-N氧化物的产生直接影响高胆固醇血症和CAD的发育。
胆汁酸调节
肠道微生物可以影响肝脏胆固醇代谢的调节,并在改变胆汁酸中发挥作用,从而影响全身胆固醇水平(图3)。
图3 影响CAD的多方面机制
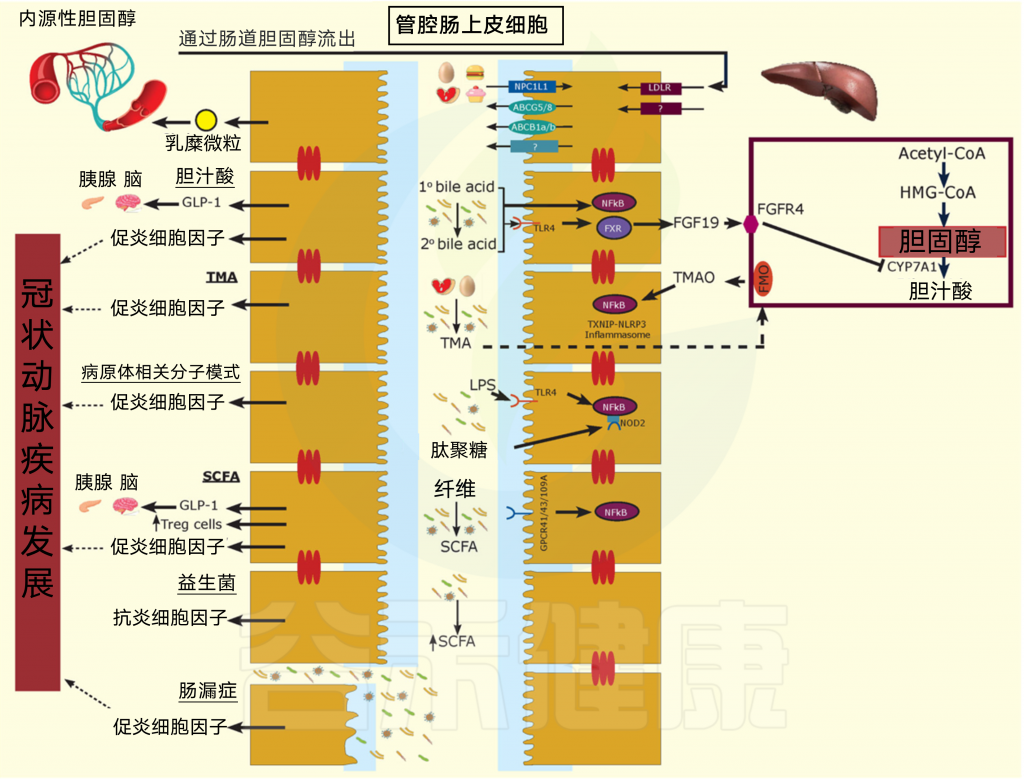

肠腔胆固醇和饮食的外源性和内源性来源,以及影响免疫系统和CAD发育的肠道微生物机制。
胆汁酸由限速酶胆固醇7-α-羟化酶(CYP7A1)形成,是肝脏中胆固醇的主要代谢产物,有助于脂肪、营养物质和亲脂维生素的吸收,也有助于调节脂质、葡萄糖和能量代谢。
初级胆汁酸
初级胆汁酸与氨基酸、牛磺酸或甘氨酸结合形成胆汁盐,分泌到胆汁中并储存在胆囊中,直到它们释放到小肠,在小肠中乳化脂肪并形成胶束,这些胶束被吸收到肠细胞中。
在肠道中,初级胆汁酸,如胆酸(Ca)和鹅去氧胆酸(CDCA)被肠道微生物和胆盐水解酶(BS H)去结合,形成次级胆汁酸,包括脱氧胆酸(DCA)、石胆酸(LCA)和熊去氧胆酸(UDCA)。
胆固醇水平如何升高
腔内所有共轭和未结合的胆汁酸可被重新吸收(95%)并转运回肝脏,但UDCA和LCA除外,它们大多在粪便中排出。肠道内胆汁酸等信号分子也能激活核受体法尼样X受体(FXR)和膜G蛋白偶联的胆汁酸受体Gpbar-1(aka TGR5)。通过这一机制,胆汁酸可以下调胆汁酸的合成,从而导致胆固醇水平升高。
胆汁酸激活FXR的顺序为CDCA>DCA>LCA>CA,FXR可诱导成纤维细胞生长因子19(FGF19)激活成纤维细胞生长因子受体4(FGFR4),抑制CYP7A1下调胆汁酸合成。
FXR还可以通过增加ATP结合盒B亚家族成员11(ABCB11)的表达,减少肝细胞对胆汁酸的摄取,增加胆汁酸的分泌。
原发性和继发性胆汁酸比值可能与高胆固醇血症和CAD的发生有关。例如,在Myerhofer等人的一项研究中,心力衰竭患者的血浆原发胆汁酸减少,继发胆汁酸与原发胆汁酸的比例更高,胆汁酸也可以通过以下途径在心血管功能中发挥作用。
肠道菌群调节胆汁酸比率
通过调节心房和心室心肌细胞的通道传导和钙动力学及调节血管张力来降低心率。此外,研究人员还提出,肠道微生物群调节胆汁酸比率,如果不平衡和处于不健康状态,可能导致继发胆汁酸减少,从而增加初级胆汁酸,如CDCA,激活FXR,降低胆汁酸生成,从而增加胆固醇和CAD的发展。因此,肠道微生物群及其相关的潜在机制需要进一步研究。
粪甾醇生产
某些肠道微生物群长期以来一直被认为具有将可吸收胆固醇转化为粪甾醇的能力,这是一种还原的不可吸收粪甾醇,可在粪便中排出。
人体内的粪甾醇的产生开始于生命第一年的后半段,并依赖于性别,年轻女性比年轻男性具有较高的转化能力。
此外,目前认为,人类群体中微生物胆固醇到粪甾醇的转化率是双峰的,高转化率显示几乎完全的胆固醇转化,而低转化率显示粪甾醇含量不到粪便中性固醇含量的三分之一。
迄今为止,分离出的降胆固醇菌株仅限于真杆菌属和拟杆菌属,但仍有许多有待发现。
使用动物模型,口服E. coprostanoligenes导致饮食诱导的高胆固醇血症兔的血浆胆固醇浓度显著降低,并在最后一次细菌喂养后持续至少34 天。
对于人体模型,已经有许多关于肠道胆固醇代谢的研究,并且已经提出了人类血清胆固醇与人类粪便中粪烷醇/胆固醇比率之与粪便中粪甾醇/胆固醇的比值呈反比。
然而,这些研究采用了非常小的样本量,样本群体的变化有限,缺乏不同的人口背景,包括未能成功地分离出导致粪甾醇/胆固醇转化的特定微生物菌株。此外,参与胆固醇在肠道内转化为粪甾醇的基因或酶仍然未知。
短链脂肪酸生产
SCFAs是一种微生物衍生的代谢物,由复杂的碳水化合物发酵形成,影响宿主的一系列过程,如宿主微生物信号、能量利用和结肠pH的控制,从而影响微生物群的组成和肠道运动。我们在前面的文章中也多次提到短链脂肪酸主要有乙酸、丙酸和丁酸。
拟杆菌门可以产生乙酸、丙酸,厚壁菌门可以产生丁酸。SCFAs与Alistipes putredinis、拟杆菌、罗斯氏菌(产丁酸盐的菌)、直肠真杆菌和普氏粪杆菌 呈正相关。
此外,它们通过调节紧密连接蛋白的表达,在维持肠屏障完整性方面起着不可分割的作用。
SCFAs还可以通过阻止胆固醇合成和/或将其转移到肝脏来降低血脂水平;因此,它们被认为是CAD发展中的一个保护因素。
在某些CAD患者和高血压患者的肠道失调中,通过激活G蛋白偶联受体41(GPR41),产生SCFA的细菌也减少了。因此,他们在体内的作用和目标需要进一步的研究。
三甲胺-N-氧化物(TMAO)生产
膳食胆碱、甜菜碱、磷脂酰胆碱、卵磷脂和左旋肉碱参与了TMAO的产生,TMAO是冠状动脉疾病发展的危险因素。
平时我们吃的包括红肉、鸡蛋、鱼、芸苔类蔬菜、花生和大豆等都有这种TMAO。


TMAO升高带来风险
具体来说,TMAO水平的升高与死亡和非致命性心肌梗死或中风的风险增加有关。肠道微生物通过(A)胆碱的产生和(B)中间分子三甲胺(TMA)的产生也在TMAO的产生中起作用。
最近才发现肠道微生物通过磷脂酶D(PLD)酶产生胆碱的能力。微生物介导的TMA分子可以进入宿主循环并进入肝细胞,在那里它被含黄素单加氧酶(FMO)代谢为TMAO,该酶由肝脏、肾脏和其他组织中的FMO基因编码。
高TMAO的产生会影响脂质,并导致43%的CAD风险,因为胆固醇转运的减少和胆汁酸运输、组成和细胞池大小的改变。TMAO还与C-反应蛋白(CRP)和内皮功能障碍有关,在肠道通透性增加的情况下,与LPS内毒素水平升高有关。此外,它还会导致钙的释放和血小板的高反应性,从而影响CAD。
与TMAO产生的有关菌群
肠道微生物群对TMAO的产生有重要影响。 健康人体内有大量产生TMAO的菌群,厚壁菌门与拟杆菌门的比例为2:1。在覆盖36个物种的102个基因组中发现了TMA的产生,TMA的产生者包括厚壁菌门,变形菌门,放线菌门,在拟杆菌门中不存在。


一项研究发现,来自于厚壁菌门和变形菌门的8种细菌,为生产TMA消耗了60%的胆碱,分别是:
产氢厌氧菌、天冬酰胺梭菌、C. hathawayi,
C. sporogenes, Escherichia fergusonii,
Proteus penneri, Providencia rettgeri, Edwardsiella tarda.
其他与高TMAO产生相关的肠道微生物包括:
阿克曼菌、孢子杆菌、普雷沃菌和瘤胃球菌,它们与动脉粥样硬化性冠心病相关。
因此,代谢物包括胆碱、TMA和甜菜碱可以帮助预测CAD的发展。 例如,益生菌或药理学干预可以用来抑制或阻断特定的微生物代谢途径,以减少产生TMAO的微生物。
肠道微生物也可以通过间接途径导致CAD的发展,如操纵我们的免疫系统。
动脉粥样硬化是由动脉粥样硬化血栓形成引起的一种慢性炎症性疾病,在这种疾病中:
(A)表面侵蚀可导致血栓形成
(B)细胞因子损伤的斑块破裂,从而导致暴露的凝血系统,导致血流抑制并诱导CAD。
因此,炎症引起的巨噬细胞和免疫系统与CAD有关。例如,最近高白细胞(WBC)计数被认为是CAD发展的危险因素。
此外,一项研究确定IL-22途径可作为代谢性疾病治疗干预的新靶点,因为IL-22能提高胰岛素敏感性,保护肠粘膜屏障和内分泌功能,减少内毒素血症和慢性炎症,调节肝脏和脂肪组织的脂质代谢。
在我们体内,氧化低密度脂蛋白(oxLDL)也可以通过激活内皮细胞、巨噬细胞和T细胞来发挥促动脉粥样硬化和促炎症作用。
巨噬细胞可吞噬oxLDL,导致炎性细胞因子如肿瘤坏死因子α(TNF-α)、白细胞介素1β(IL-1β)、IL-6、IL-18、IL-37和泡沫细胞,从而加重CAD。
TNF-α还通过激活蛋白激酶c(PKC)参与包括糖尿病在内的CAD危险因素,PKC增加胰岛素受体底物的磷酸化,导致其失活。
T细胞还可导致促炎细胞因子IL-2、IL-12和干扰素γ(I FN-γ),这与动脉僵硬有关。 泡沫细胞、T细胞和巨噬细胞一起会导致出现脂肪条纹,从而促进CAD的发展。
肠道菌群群落结构影响免疫系统
肠道微生物群的群落结构可以极大地影响我们的免疫系统。 例如,肠道微生物群的低基因计数(LGC)与高WBC计数有关,正如前面所说的,这是CAD的危险因素。 在我们的肠道微生物群中,Lactobacillus reuteri 的存在与高WBC计数有明确的联系。
低基因计数的个体患有代谢紊乱,导致脂蛋白异常和促炎状态,这可能导致CAD。 LGC也与高的CRP水平相关,而与高CRP水平相关的则是低Oscillibacter、粪便杆菌 和瘤胃球菌。
类似于TLRs的模式识别受体(PRRS)在肠道中的表达也受到肠道细菌的调节,这些细菌帮助宿主通过病原体相关的分子模式(PAMP)和共生细菌在病原体之间导航,以及激活免疫感觉细胞。
此外,我们的菌群会影响调节性T细胞(Treg),它们的减少会加剧感染结果,增加自身免疫性疾病、过敏和癌症的风险。例如,Prevotella可以通过Toll样受体2(TLR2)激活介导炎症反应,从而导致炎症和细胞17(Th17)免疫反应。
心肌炎
心肌炎(一种炎症性心脏病)进展为致死性心肌病,可能依赖于肌球蛋白特异性Th17细胞在肠道中由半乳糖苷酶模拟肽共同作用于多形拟杆菌和粪杆菌,可促进炎症性心肌病的发生。
梭菌簇IV增强Treg细胞丰度,并导致抗炎分子的产生。因此,TLR2与CAD发病机制有关。
NOD/CAD是另一类PRRS,通过激活炎症细胞因子和/或激活免疫系统转录因子NF-κb来识别应激反应并激活炎症半胱氨酸蛋白酶,从而产生炎症分子。
肠漏也会导致肠道微生物衍生成分如PAMP的易位,包括LPS,从而导致促炎细胞因子的产生。
SCFA既能抗炎也能导致炎症
肠道微生物代谢物,如SCFA,也可以影响免疫系统,通过激活G蛋白偶联受体41(GPR41)、GPR43和GPR109A,通过诱导由叉头盒P3(Foxp3)启动子控制的Treg细胞,发挥抗炎作用。
此外,它们还能产生抗炎的肠道激素,如胰高血糖素样肽1(GLP-1)。 虽然SCFAs有许多积极的作用,但它们的产生也可以通过激活Toll样受体4(TLR4)来改变细菌平衡并导致炎症。因此,它们在免疫系统中的作用有待进一步研究。
TMAO激活炎症小体影响免疫系统
肠道微生物衍生的TMAO也可以通过激活TXNIP-NLRP3炎症小体影响我们的免疫系统,导致炎症标记物如TNF-α、IL-6、IL-18和IL-1B的表达,这些炎症标记物可以通过产生胆固醇填充的泡沫巨噬细胞促进动脉斑块的形成,最终导致CAD。
TMAO还能促进PKC/NF-κb激活,促进血管细胞黏附分子1(VCAM-1)的表达和单核细胞的黏附。 除了影响高密度脂蛋白胆固醇和抗炎特性外,肠道微生物及其相关代谢物还可以通过非炎症诱导途径影响免疫系统。
胆汁酸抑制NF-κb转录
初级(肠道菌群解偶联)和次级胆汁酸,例如,可以通过FXR和TGR5受体抑制促炎细胞因子的NF-κb转录。激活TGR5也能保护LPS诱导的炎症和动脉粥样硬化。
细胞因子如IL-10的积极作用
此外,某些细胞因子,如IL-10,可以产生积极的作用,如通过诱导RCT增加动脉粥样硬化病变中乙酰化和oxLDL的摄取和流出,从而降低小鼠血清胆固醇和动脉粥样硬化斑块。
这种细胞因子还可以通过增强肝脏驻留的Kupffer细胞的吞噬作用来降低总胆固醇。 这些细胞代表体内80%-90%的巨噬细胞,可能是治疗的新靶点。
剖析免疫系统和代谢系统之间的复杂相互作用,将有助于深入了解CAD的生物学基础,以及当前和未来的治疗方法如何影响代谢。
饮食影响整个系统
如前所述,我们身体胆固醇的四分之一来自饮食摄入。 这导致了关于饮食胆固醇是否会影响CAD发展的越来越多的争论。
我们的饮食可以通过直接食用富含胆固醇的食物和间接地通过改变肠道微生物及其群落结构、胆汁酸的产生、粪甾醇的产生、SCFA的产生和TMAO的产生来影响胆固醇的调节和CAD的发展,从而使问题复杂化。例如,地中海饮食引起的肠道微生物群的有益修饰已被证明能改善肥胖、炎症、CAD和其他相关代谢改变。
图4 微生物群、饮食和CAD
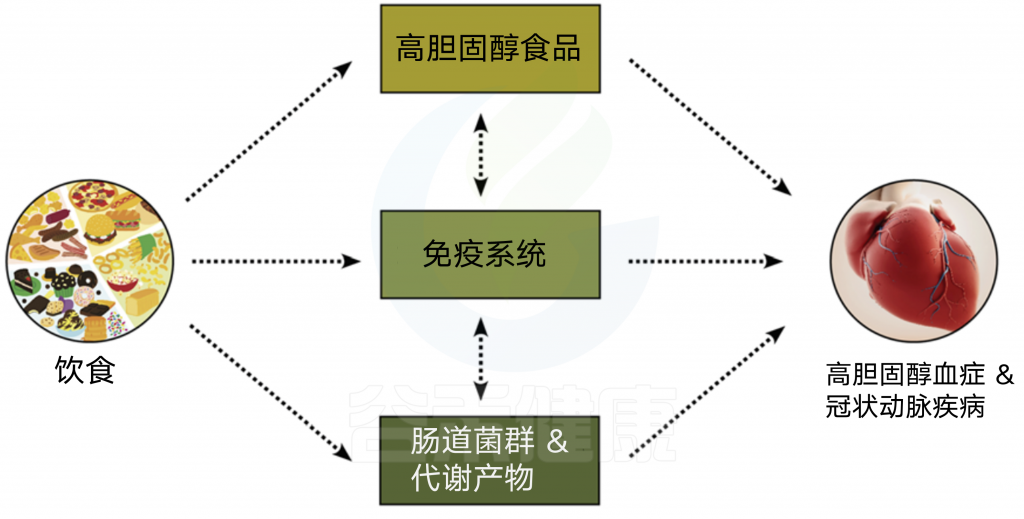

饮食通过食用富含胆固醇的食物直接或间接地影响胆固醇水平和CAD的发展,影响免疫系统,并导致肠道微生物群及其代谢产物如胆汁酸、黄连醇、短链脂肪酸和TMAO的调节。
这种饮食更加强调水果、蔬菜和豆类,并且与增加SCFA水平有关。此外,饮食可以通过改变与胆固醇有关的炎症反应来影响免疫系统调控和CAD发展。
一项结果表明,高盐摄入会影响肠道微生物群,特别是通过消耗鼠李糖乳酸菌和增加Th17细胞和高血压。补充L.Murinus 可以抑制Th17的激活,改善高血压。
此外,与高饱和脂肪组成的饮食相比,由高不饱和脂肪组成的西方饮食可导致拟杆菌增多、厚壁菌和Bilophila wadsworthia(亚硫酸盐还原微生物)减少,而由高饱和脂肪组成的饮食可导致LDL胆固醇和B.Wadsworthia菌增加,这种菌与血脂异常和炎症增加有关。
高蛋白和高脂肪饮食也与瘤胃球菌的增加和拟杆菌、梭状芽孢杆菌、双歧杆菌、直肠杆菌、赤霉菌的减少有关,并增加粪便中的胆汁酸浓度,包括DCA浓度的升高,这可能导致肝癌。
此外,这些饮食可以激活与炎症反应相关的TLR4,如促炎细胞因子、Th1、CD4和T细胞,从而导致Treg细胞的下调。在高脂饮食诱导的糖尿病中,来自肠道的细菌被转移到组织和血液中,这取决于CD14和NOD1。
通过益生菌逆转
然而,这种菌血症可以通过益生菌(双歧杆菌)逆转,这可以减少糖尿病期间细菌、脂肪组织和炎症的粘附和移位。
在另一项研究中,益生菌给药干酪乳杆菌可减少细菌易位,并通过增加Clostridium coccoides, C. leptum 和总乳酸杆菌来改变肠道微生物群。与纯素相比,杂食动物产生更多的TMAO,高纤维饮食导致更高的SCFA和增加肠道菌群多样性。
饮食影响人体胆固醇的概念是一个持续的争论,需要进一步研究。尽管许多研究表明高饮食胆固醇与CAD之间存在直接关系,但其他研究表明饮食中胆固醇的临床影响在疾病发展中可能很小或可忽略不计。
这场争论可能是由于对胆固醇水平管理中涉及的身体系统机制缺乏了解,以及由于人群和环境因素而异的正常肠道菌群所致。
饮食的抗炎作用
我们的饮食也可以通过与转录因子NF-κB和PPAR-Y相互作用的omega-2(n-3)多不饱和脂肪酸产生抗炎作用,下调促炎基因,抑制TLR4的激活,从而产生抗炎反应。例如,我们饮食中的花青素(如蓝莓)是一种抗氧化剂,可以通过增加其多样性影响肠道微生物群,从而减少炎症反应。
益生菌和益生元也被深入研究,并证明通过增强肠道屏障、调节免疫功能和预防致病性感染来改善肠道环境。它们与炎症减少和SCFA、拟杆菌、双歧杆菌和厚壁菌减少有关。口服益生菌甚至可以降低22-33%的胆固醇,这是由于BSH的活性。
例如,益生菌乳酸杆菌和双歧杆菌可以通过(a)增加胆固醇对从头合成胆汁酸的需求,或(b)降低胆固醇溶解度并减少其吸收,从而解除胆汁酸的结合并增加排泄。
尽管益生菌和益生元越来越受欢迎,但关于它们可能对健康和疾病产生的特定免疫和生理影响的问题仍然存在,因此需要进一步研究。
微生物群、人口因素和CAD
在精确医学时代,一个关键的挑战是弥合人口统计学因素、肠道微生物组成和心血管系统病理生理学之间相互作用的知识差距。
除了男性和女性之间的环境和社会差异(如职业危害、生活方式、社会压力和获得医疗保健)外,在疾病发展、性染色体和性激素方面的差异也会导致CAD患者的性别差异。更具体地说,最近已经显示了血脂和脂蛋白代谢的性别差异,以及针对血脂异常的性别特异性考虑因素。
尽管CAD被认为是一种“男性疾病”,但越来越多的证据也显示了CADs在女性中的重要性,并提高了在CADs的发生、诊断、治疗和预后方面性别相关差异的认识。
例如,女性在生命后期更容易患上这种疾病。 这可能是由于激素和更年期的变化,这可能会影响胆固醇的比率,随着雌激素的停止产生,脂蛋白向低密度脂蛋白转移,并远离高密度脂蛋白胆固醇的女性。
性别差异也与肠道微生物群的整体结构有关
正如前面所讨论的,这与CAD的发展有关。 例如,在一项研究中,分别在男性和女性中发现普氏菌属、巨单胞菌属、梭杆菌属、巨球型菌属、双歧杆菌属、瘤胃球菌属和阿克曼菌属的显著增加。
然而,男性和女性在微生物多样性方面没有显著差异。基于性别和性别相关的肠道微生物组成和CAD发展差异的研究仍然很少,需要在数量和深度上进行扩展。
种族差异影响高胆固醇血症和CAD发展
种族差异,虽然在研究中经常被忽视,但已知影响高胆固醇血症和CAD的发展。 种族差异可以捕捉来自社会、经济和文化差异、人类遗传变异、生物地理祖先差异以及生活方式和饮食差异的生物变异。
包括吸烟、血压、肥胖和胆固醇在内的CAD发展的危险因素也可能在不同的种族群体中有所不同,导致某些群体的CAD发病较早,预后较差。例如:
南亚人是一个高风险族裔群体,他们的体育活动率较低。
居住在美国的非裔美国人也有更高的CAD发展风险,这可能是由于生活方式、环境因素和社会经济因素。非裔美国人有相对较高的糖、较高的钠和较低的钾含量的饮食,这会导致更高的血压。
此外,种族和饮食差异与微生物组成和丰度的变化有关,甚至与肠道微生物群的变化相关性比遗传、年龄、性别和BMI等其他因素更强烈。例如,对健康个体中农村和城市地区微生物群的比较研究报告显示,与美国和欧洲的人口相比,居住在非西部和/或农村地区的人口具有更高的菌群多样性。
在Deschasaux等人的另一项研究中,在荷兰人口中观察到较高的肠道微生物群多样性,在南亚的肠道微生物多样性最小,加纳人、土耳其人和非洲人在中间。 在荷兰人群中也观察到了厚壁菌增多,拟杆菌减少。而在南亚人群中观察到了放线菌增多。
人口因素之间的相互作用,如性别、年龄和种族,以及它们与我们的饮食、肠道微生物组成和CAD发展的联系,说明了我们身体因素在健康和疾病状态中的复杂性。 因此,需要更多的研究努力来理解这些因素涉及肠道微生物群的变化和CAD的发展。
图5 微生物群、老化和CAD
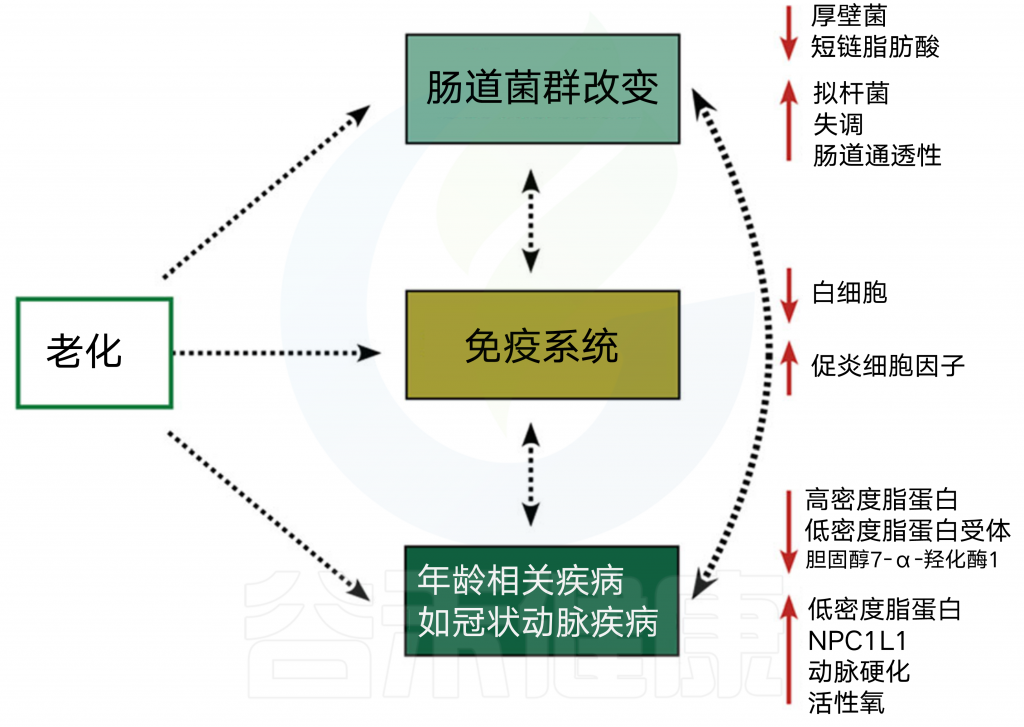

与全身炎症和不良健康结果相关的衰老机制。
身体中的胆固醇也会受到自然衰老过程的影响,这是一个无法控制的危险因素,会导致全身胆固醇代谢失调(图5)。到2030年,预计将有10亿人超过65岁。一般来说,衰老过程与心脏结构和功能的逐渐恶化有关,以及促进CAD发展。此外,通过衰老过程,LDL胆固醇水平可以增加,HDL胆固醇水平可以降低,这可能导致CAD的发展速度增加。
衰老过程引起的其他因素包括降低CYP7A1酶活性(减少胆汁酸合成的调节)、降低肝脏LDL胆固醇受体(降低LDL胆固醇清除率)和增加NPC1L1(胆固醇吸收介质)。衰老还影响肠道微生物群落,因为疾病的积累,饮食的变化,运动和行动能力的减少,以及某些药物的使用。然而,也有相反的发现表明不同年龄组参与者的肠道微生物结构没有显著差异。
总的来说,衰老与肠道失调增加有关,与肠道微生物多样性呈负相关。还有,参与SCFA生产的基因数量也随着年龄的增长而降低。 衰老影响免疫系统,全身炎症是衰老的标志之一,也是许多年龄相关疾病(包括CAD、糖尿病和癌症)风险增加的原因之一。
此外,衰老是由一个正反馈回路调节的,其中老年人的慢性全身炎症与发展和年龄相关的疾病有关,然后通过这些条件也导致炎症反应的增加。 由于这些原因,在精确的时代,包括年龄、性别和种族等人口因素的研究是有必要的。
精准医疗中的微生物群
目前,许多技术可以用来分析肠道微生物群与人类免疫学、神经学和内分泌学的关系。 由于这种关联及其在精确医学中的潜力,人类微生物群正在被广泛研究,作为粪便微生物移植、益生菌和益生菌的治疗靶点。.
尽管如此,对于大多数疾病,机械洞察力和翻译应用仍然很少。 人体微生物群在组成和空间上是动态变化的,微生物群个体内和个体间的变化可以通过药物的直接生物转化或微生物与宿主免疫系统的相互作用等间接机制影响药物的疗效和副作用分布。在此讨论了多种新出现的策略,以精确操作复杂的微生物群落,以改善心血管病的治疗结果。
预计在未来将朝着包含人类和微生物基因组以及它们的综合代谢活动的精确医学的包容性观点积极转变。
微生物群与药物治疗
目前治疗高胆固醇血症和CAD的方法包括能有效降低胆固醇水平的药物,并用于治疗高胆固醇血症和CAD预防。
他汀类药物可通过影响胆固醇合成中的限速酶达到疗效
羟甲基戊酰辅酶a(HMG-CoA)还原酶抑制剂,又称他汀类药物,可影响胆固醇合成中的限速酶,并已彻底改变了高胆固醇血症的治疗方法。在各种研究中,这类药物已被证明了显著降低总胆固醇、LDL胆固醇和甘油三酯的能力,并使HDL胆固醇增加18%、25%、11%和5%。
尽管他汀具有疗效,但它们对非LDL胆固醇的影响是有限的;因此,其他针对非LDL胆固醇的药物可能补充他汀类药物以降低心血管风险。例如,依泽替米贝是另一种降低LDL胆固醇的药物,它通过阻断NPC1L1来减少饮食和胆汁胆固醇的肠道吸收,从而降低LDL胆固醇。在一项随机对照的人类试验中,Ezetimibe(10毫克/天)与安慰剂相比,胆固醇吸收减少54%,总胆固醇和低密度脂蛋白胆固醇分别减少15%和20%。
药物副作用
虽然许多药物可以降低胆固醇,但它们往往是次优的,昂贵的,并带来许多不必要的副作用。例如,他汀类药物与骨骼肌、代谢和神经效应以及其他可能的副作用有关。他汀类药物治疗的停止也与心血管预后不良有关。此外,Ezetimibe还表现为肝脏内源性胆固醇合成的代偿性反馈上调,并可增加TICE,从而导致血清胆固醇升高。抑制肝NPC1L1还可提高胆汁中胆固醇饱和指数,并有可能导致胆结石。因此,虽然这些常规治疗提高了许多患者的生活质量和预后,但CAD和高胆固醇血症仍然是一种进行性疾病(注:进行性疾病是指症状不断加重、患者状况不断恶化的疾病。)。
另一个挑战是肠道微生物群可以通过干扰药物的药代动力学或药效学直接和间接地影响药物。例如,辛伐他汀、罗舒伐他汀和阿托伐他汀(3种常用的他汀类药物)显示了肠道微生物群调节的证据。 代谢物如胆汁酸,也可以影响药物的药代动力学,通过竞争药物运输机制跨越肠腔,或通过影响肝脏的摄取。 进一步研究肠道微生物群参与CVD和药物反应的分子机制将改善CVD患者的预后,并朝着微生物精确医学的方向发展。
接下来将提出纳米技术在揭示参与CAD开发的潜在机制以及针对微生物组的治疗工具方面的潜在作用。
基于微生物群和纳米医学的方法
纳米医学被美国国家卫生研究所(NIH)定义为纳米技术在控制生物系统、治疗、诊断和疾病监测方面的应用。这一新的医学分支是一个多学科的科学领域,其重点是开发至少在一个维度上位于0.1-100nm范围内的诊断和治疗纳米物体。
图6 纳米医学、微生物群和计算机辅助设计
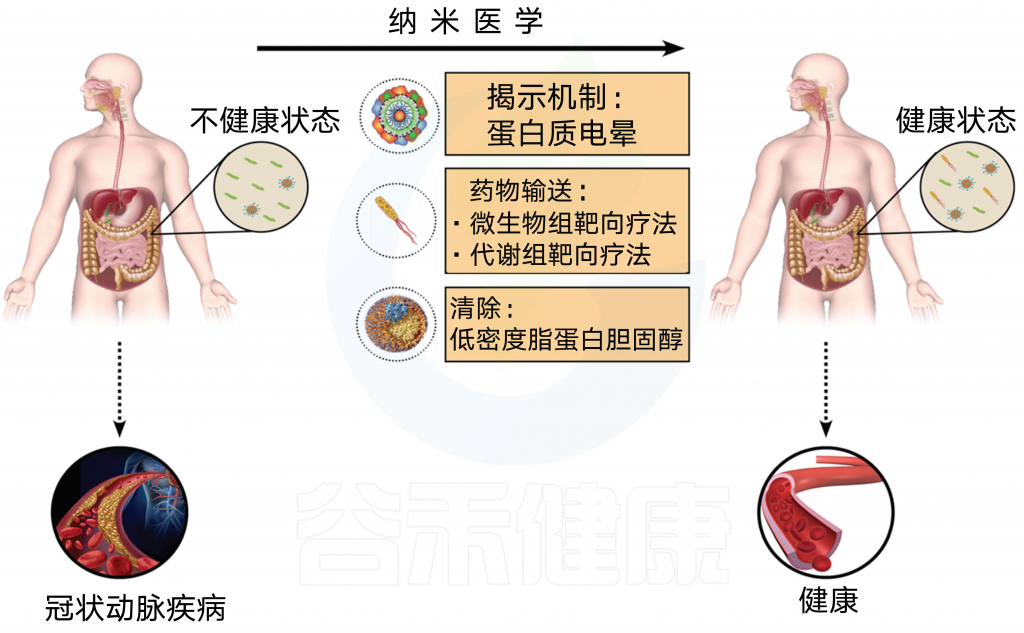

纳米粒子在纳米医学中有许多应用,可以帮助预防、诊断和治疗CAD。利用纳米颗粒了解潜在的身体机制(即蛋白质电晕分析)、药物传递(即微生物组和代谢组靶向治疗)和清除颗粒(即对于低密度脂蛋白胆固醇调节免疫系统)可以导致一个更健康的肠道微生物群和免疫系统,从而导致更好的整体健康状态,排除CAD的发展。
纳米医学的进一步发展也可能为现代医学中许多悬而未决的问题提供解决方案,包括高胆固醇血症和CAD(图 6)。 肠道微生物群与疾病发病机制之间关系的研究已被证明是一项困难的任务,特别是在找出原因方面。纳米医学中的纳米粒子可以帮助我们理解CAD发展的潜在机制。纳米粒子在体内应用的一个有用方面是生物分子/蛋白质电晕的形成(即一层生物分子,在纳米粒子与生物流体相互作用时覆盖其表面)。

在2014年,研究人员发现不同疾病患者的蛋白质电晕分布有很大的不同,尽管传统的血浆分析显示变化可以忽略不计。这种效应被称为“疾病特异性蛋白电晕”,已在其他地方复制,并用于早期发现疾病,包括神经退行性疾病。
最近发现,使用具有不同物理化学性质的纳米粒子(即称为蛋白质电晕传感器阵列技术)可以提高蛋白质电晕疾病检测的灵敏度、特异性和预测精度。
另一种更好地分析血浆蛋白并获得有关CAD发展的有用信息的潜在方法可能是磁悬浮。 研究人员最近使用超顺磁性氧化铁纳米粒子悬浮血浆蛋白,发现悬浮血浆蛋白产生椭球图案。
机器学习和液相色谱质谱法证明有用信息
利用机器学习和液相色谱质谱方法,研究人员证明悬浮血浆蛋白的模式包含了有关血浆供体健康光谱的有用信息。这一策略对于监测肠道微生物模式与CAD之间的相互作用是非常有帮助和可行的。
先进的数据分析技术提供机会
利用先进的数据分析,可以定义蛋白质/生物分子模式,与肠道微生物剖面的变化和CAD的发生和/或进展有很强的关联。关于重要生物分子变异的作用的知识可能提供一个宝贵的机会,不仅是根据特定的肠道微生物模式早期检测CAD(这反过来又会影响血浆生物分子的组成),但也用于开发新的治疗方法,基于肠道微生物的操作使用口腔纳米技术。
前瞻性诊断和治疗应用显示巨大潜力
目前的前瞻性诊断和治疗应用包括成像、组织工程、常规药物、蛋白质和遗传物质的传递以及清除低密度脂蛋白胆固醇。例如,肝素和壳聚糖共轭磁性纳米粒子在从血浆中去除LDL胆固醇方面显示出巨大的潜力。
纳米粒子还能调节免疫系统,并已被用于诱导抗炎作用。例如,广谱ROS清除纳米粒子已被用于小鼠研究,以有效地减少氧化应激和局部和全身炎症。
此外,壳聚糖纳米粒通过降低肠上皮单层的通透性和促炎细胞因子的分泌而诱导抗炎作用。而且,基于纳米粒子的TLR信号抑制剂已被用于减少炎症和治疗炎症性疾病。

纳米技术用于菌群调节来影响CAD发展
虽然纳米医学在CAD的诊断和治疗方面显示出相当大的和日益增长的能力,但其在调节肠道微生物群中的应用仍在研究中。 最近,研究人员提出了几种基于纳米技术的策略来控制肠道微生物的组成。通过调节肠道微生物有利于健康状态,可以直接(通过代谢物)和间接(通过免疫系统)以积极的方式影响CAD的发展。
为此,纳米粒子可用于传递与HDL增加、SCFA增加、LPs减少和促炎细胞因子减少有关的特定肠道微生物群。清除纳米粒子也可以优化(I)LDL胆固醇、(II)LPS、(III)促炎细胞因子和(IV)TMAO的摄取和去除。这些机制在预防、诊断和治疗CAD方面有很大的潜力,可用于替代目前具有各种负面副作用的药物。
然而,在设计安全有效的纳米粒子以预测和治疗CAD方面仍然存在挑战。此外,蛋白质电晕还会影响纳米载体的药物释放谱。因此,为了诊断和治疗CAD,需要进一步研究这些新的治疗平台的生物学特性。
临床微生物群研究的其他挑战
将人类肠道微生物群整合到临床设计和设置中并不是一项容易的任务,而且可能面临许多挑战。 通常,人类微生物群多年来保持稳定。尽管肠道环境中具有长期的稳定性和可塑性,但个体间变异和个体内变异是很重要的。
内部变异可能是由于婴儿过渡期(即出生胎龄、分娩类型和喂养方法)、年龄和抗生素使用等环境因素造成的。此外,肠道微生物群的变异可能是由于性别、肠型、体重指数(BMI)和生活方式、运动频率、种族、饮食和文化习惯等外部因素造成的。
这种个体间和个体内变异的研究可能会使旨在识别生物标志物和研究肠道微生物群组成和作为群体比较的功能的研究复杂化。因此,将微生物群科学纳入临床实践,可以通过考虑CVD患者的变异来确定生物标志物和治疗方法。
用于研究肠道微生物群的样本收集(即粪便样本)也会导致许多挑战,没有标准的协议和共识可用于质量保证和下游分析。例如,肠道微生物群在唾液、上消化道、下消化道和粪便样本中含有不同的微生物群落。上消化道显示孪生球菌、韦荣球菌属、奈瑟菌、梭菌、链球菌、普氏菌、假单胞菌和放线菌增加,而下消化道显示粪杆菌、瘤胃球菌和拟杆菌增加,这可能会产生方法上的挑战。
此外,粪便细菌群落的组成可能受到实验设计和收集、储存和DNA提取等程序等因素的影响。已经证明,粪便微生物群不是粘膜微生物群的代表,因此超越单一“以粪便为中心”的观点是至关重要的。 除了样本的类型外,纵向抽样可以增加对稳态的理解,但肯定会给病人带来负担。
测序技术和“组学”发展
最后,在过去的十年里,肠道微生物群研究的激增可归因于成本效益高的下一代测序(NGS)技术和人类基因组、代谢组学和蛋白质组学数据等“组学”数据的发展。NGS技术加上生物信息学的进步,彻底改变了微生物群的领域,取代了以培养为基础的方法,从而可以分析日益复杂的微生物群特征。
然而,局限性仍然存在。 例如,16SrRNA测序可以可以导致对细菌的观点是单一领域的,必须考虑生命的各个方面,包括真菌、原生动物和病毒。


宏基因组学研究可以将科学视角扩展到一个多领域的视角,但也存在局限性。 例如,由于参考数据库缺乏密切匹配,很大一部分数据无法分配功能特别是病毒数据。 因此,这些复杂的组学数据需要专门的统计模型来考虑成分、稀疏性、批效应、技术噪声、采样噪声和时空变化等因素。
解释“组学”数据也会产生挑战,因为特定肠道微生物丰度的变化可能不会被推断为对宿主有保护或有害的影响。例如,在Vandeputte等人的一项研究中,微生物的绝对数量(用定量微生物组谱测量)比经典的相对丰度谱更好,因为后者不能提供关于分类群丰度或代谢潜力变化的方向性程度的信息。
建立一个知识库,以巩固微生物群领域中不相连的知识片段,以及微生物组研究中的其他创新(包括自然语言处理,文本挖掘,分类学表示和全领域词汇标准化),可以加快理解并帮助推进因果关系。因此,为了建立肠道生态系统动力学的全球模型,需要在质量控制、方法学和使用流程方面进行进一步的研究和改进。
为了充分了解肠道微生物在人类健康中的作用,并指导高胆固醇血症和CAD发展的治疗干预措施,必须阐明相互关联的身体因素共同作用,影响肠道微生物群和疾病发展。
对这些复杂机制的进一步研究是阐明肠道菌群介导的机制的组成部分(例如,通过先进的纳米医学技术、数据科学以及种族和性别等因素),这反过来又可以导致更有效和高精度的基于微生物群的CAD预防和治疗方法,最终可以降低CAD的社会和经济成本。
相关阅读:
参考文献
Kazemian N, Mahmoudi M, Halperin F, et al. Gut microbiota and cardiovascular disease: opportunities and challenges[J]. Microbiome, 2020, 8(1): 1-17.