-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com

原创:谷禾健康
你可能听说过
肠道微生物群会影响大脑的生理和行为
但你是否清楚
肠道微生物群究竟是如何调节社会行为?
研究微生物群和社会行为之间的关系可以为我们带来什么?
近日发表在Science期刊上的一篇最新综述或许可以帮助你进一步了解微生物群和社会行为之间的关系。


肠道微生物群与中枢神经系统之间的双向通路,即微生物-肠-脑轴,影响动物王国中各种复杂的社会行为。一些动物已经进化出了它们自己与肠道微生物群的独特关系,这可能有助于它们与同种动物间的互动。肠道微生物群与社会行为之间的关系可能有助于解释在自闭症谱系障碍(ASDS)等情况下观察到的社会缺陷,并可能引领开发新的治疗方法。
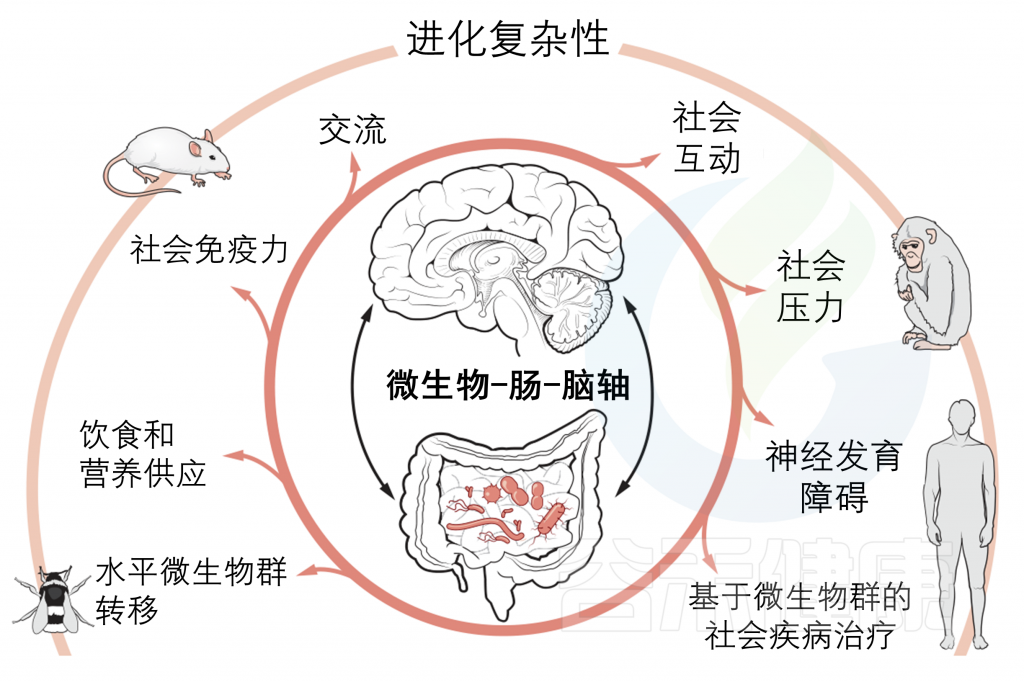
微生物-肠-脑轴与社会行为的关系

背景
微生物群-肠-脑轴
研究表明,胃肠道微生物可以通过多种途径向大脑发出信号,包括免疫激活、微生物代谢产物和肽的产生、迷走神经的激活以及肠道内各种神经递质和神经调节剂的产生。这种双向途径被称为微生物群-肠-脑轴。


虽然对肠道微生物在自然种群中的功能和生态影响的研究正在增加,但从进化的角度来看,目前尚不清楚微生物与社会大脑之间的关系是为什么和何时出现的。跨物种分析可以帮助我们理解人类的社交能力。
进展
社会行为
社会行为可以定义为只有当动物出现在一个群体中时才能观察到的行为。
社交性包括一系列复杂的互动行为,这些行为可以是合作的、中立的,也可以是敌对的。
社交能力可以促进互利的结果,如分工、合作照顾和增强免疫力,但社交能力也能促进消极结果,包括冲突、侵略和胁迫。
了解调节社会行为的内在和外在因素,对于揭示个体和种群如何繁衍生息,对于确定某些动物物种为什么进化成比其他物种更善于交际,对于阐明社会行为障碍的潜在病因,都是很重要的。
1973年,Konrad Lorenz等人在哺乳动物的遗传起源、发展和社会行为模式的启发方面的突破性研究获得了诺贝尔奖,为评估影响社会行为的各种内在因素和外在因素提供了基础。
从那时起,人们在理解行为方面取得了巨大的进步,尤其是社会行为,已经成为生物学研究中最有趣、最复杂的领域之一。
社会行为由多个相互连接的大脑边缘区域控制
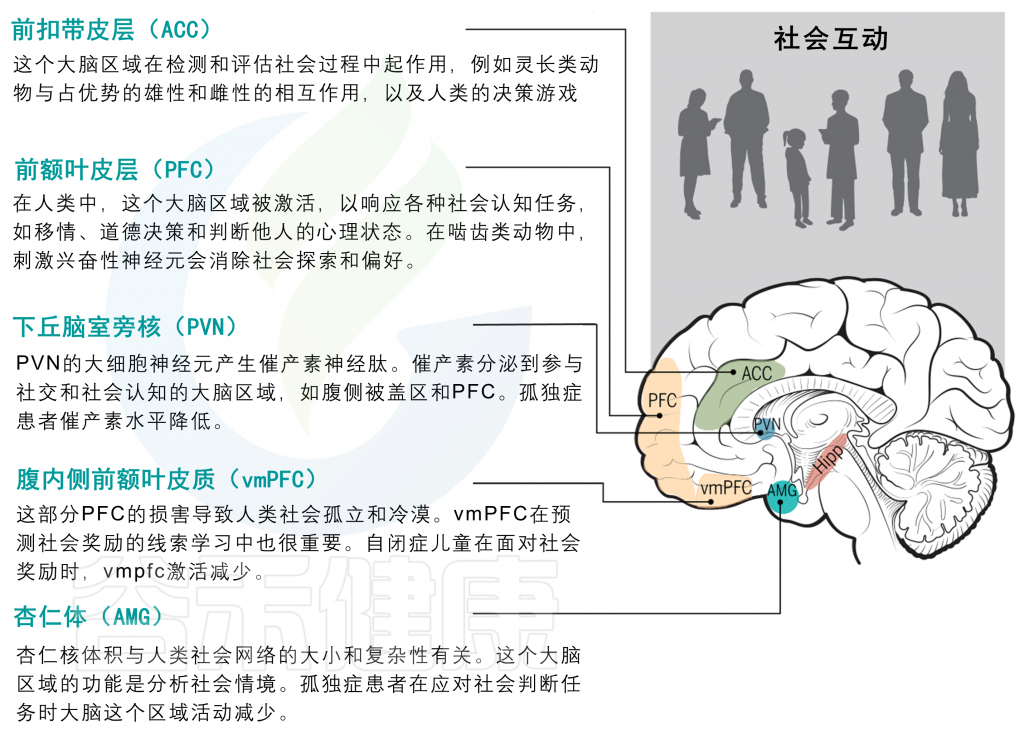

临床前和临床影像学研究有助于描绘人类和其他哺乳动物社会行为的神经回路。社会行为受几个皮质下前脑结构控制,如前额叶皮质(PFC)、前扣带皮质(ACC)、杏仁核(AMG)、海马体(HIPP)和下丘脑室旁核(PVN)构成一个完整网络的一部分,以促进这种复杂的行为。
对这些大脑区域中任何一个的损伤或功能障碍都会引起社会行为的不安。事实上,AMG和PFC等区域的神经生物学已经被证明在自闭症谱系障碍(ASDs)等社会大脑疾病中发生了改变。
动物界的研究
对宿主微生物相互作用的新认识导致人们前所未有地关注动物体内的微生物世界,包括无脊椎动物(如白蚁、蜜蜂、黄蜂)和脊椎动物(鸟类、鬣狗、人类)。
开创性的研究已经确定了胃肠道微生物群对健康的影响,微生物群在从早期到成年的神经发育过程中发挥作用,并影响神经传递、神经炎症和动物行为等神经过程。微生物产生的信号可能直接或间接地改变大脑功能,并且由于动物是在微生物世界中进化的,这些信号可能在整个进化过程中影响了动物的大脑。
动物界微生物群与社会行为的关系


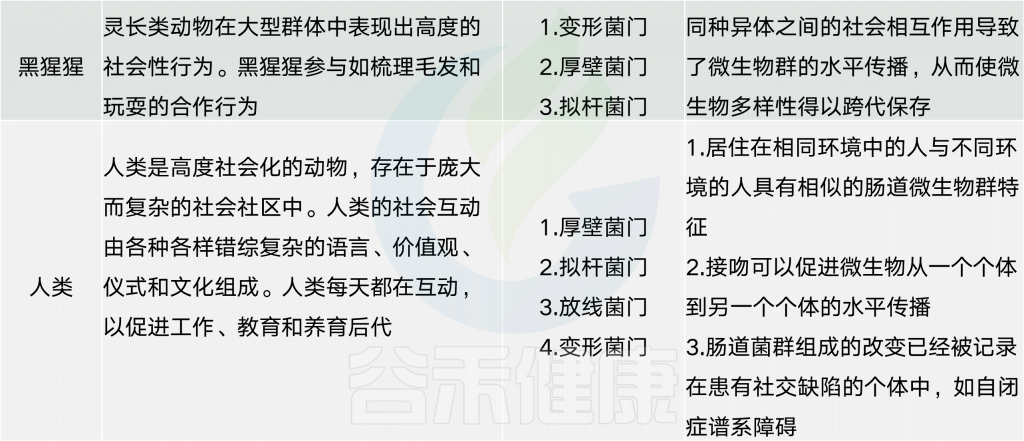



对社会物种和非社会物种的微生物群组成的研究表明,在许多动物物种中都存在相同的细菌门。然而,不同的物种以不同的方式利用它们的相关微生物群,以促进各种形式的社会互动。
对无脊椎动物和脊椎动物物种的观察表明,饮食和免疫等因素会产生选择压力,从而推动微生物群与社会行为之间的关系。
虽然微生物群可能通过调节肠脑轴而影响内源性行为,但一些动物物种可能已经进化成利用共生细菌来介导相同物种的成员之间的通信。例如,鬣狗从它们的气味腺体中产生一种有气味的糊状物,其中含有发酵细菌,这被认为是为了促进同种动物之间的社会凝聚力。动物和微生物群之间的这种复杂的关系提出了这样的假设:微生物可能影响着社会大脑和行为的进化,以此作为传播它们自己的遗传物质的手段。
肠道微生物群调控社会行为机制
越来越多的证据表明,在动物界观察到的许多行为反应可能在动物生命的不同阶段受到肠道微生物群的调节,在这个范式中,越来越强调阐明肠道微生物群与大脑交流的机制。
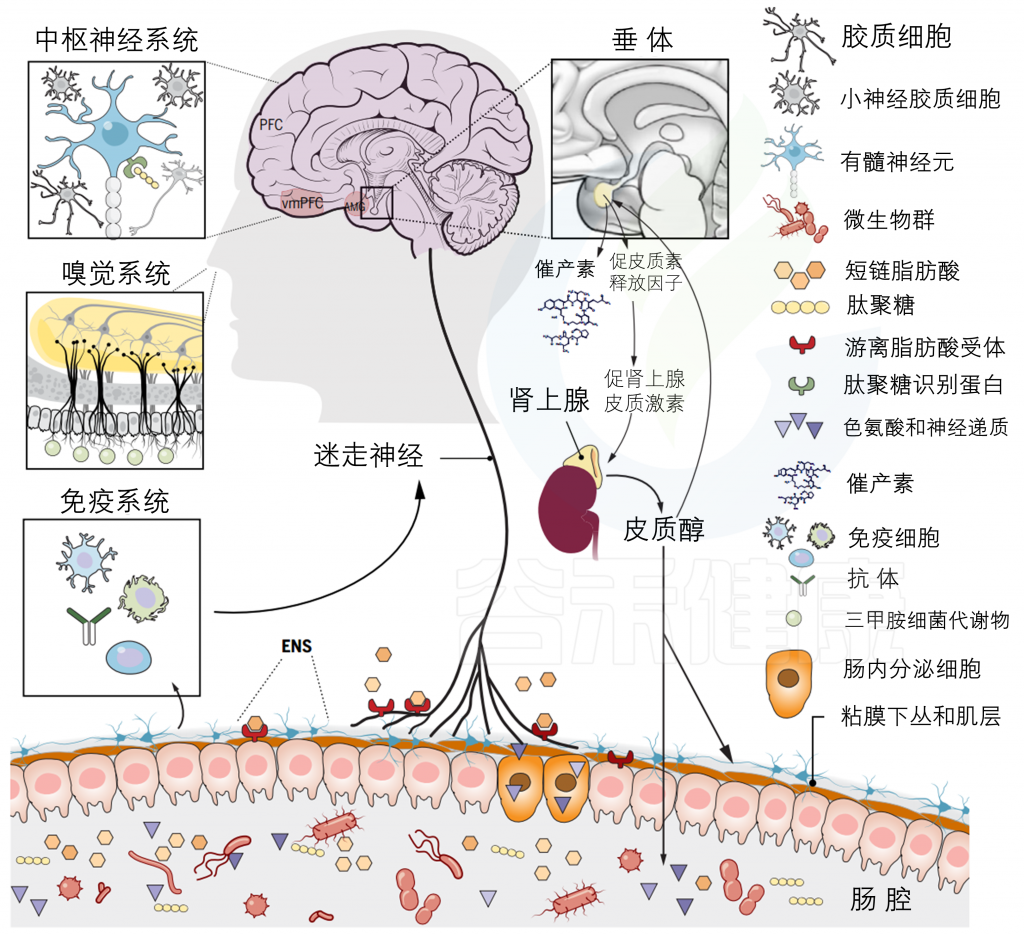

代谢产物
胃肠道中的细菌发酵和代谢导致神经递质和短链脂肪酸(SCFAs)等代谢产物的产生。SCFAs可能通过与迷走神经上表达的游离脂肪酸受体(FFAR)结合和激活,间接影响脑的生理和行为。
此外,它们在胃肠系统局部抑制组蛋白脱乙酰酶的能力可能间接影响各种介质对大脑的信号传导。
迷走神经
迷走神经最近被证明与肠内分泌细胞形成突触联系,这有助于通过谷氨酸能神经传递将营养信号传递给大脑。
迷走神经纤维富含5-HT3、Toll样受体4(TLR4)、游离脂肪酸受体(FFARs)和肠肽受体等受体;因此,它们是从肠腔向大脑传输信号的理想场所。
迷走神经切断术研究提供了经验证据,证明迷走神经是微生物群与大脑沟通的另一条途径。
免疫机制
肠道微生物群与免疫系统之间的联系是另一个被高度探索的途径,共生细菌可以通过这种联系对大脑生理和行为施加影响,在革兰氏阴性菌和革兰氏阳性菌细胞壁上表达的细菌肽聚糖能够通过激活在大脑(中枢神经系统插件)中表达的特定病原体识别受体,如PGLYRP2,影响社会行为的发展。
嗅觉机制
微生物群还可以通过排泄代谢物影响社会行为,代谢物充当嗅觉信息素。小鼠尿液中分泌的三甲胺可通过激活嗅觉受体(嗅觉系统插件)促进小鼠的社会凝聚力通过这些不同的途径,肠道微生物群已经被证明可以调节多种中枢生理过程,如神经炎症、5-羟色胺转换、髓鞘形成和亲社会激素催产素的分泌,从而提供了肠道菌群如何影响社会行为的机制性见解。
暴露于应激源后,促肾上腺皮质激素(ACTH)从垂体前叶(垂体内叶)释放,并刺激应激激素糖皮质激素的释放。
糖皮质激素影响新陈代谢和介导免疫激活等全系统效应。共生细菌暴露于糖皮质激素会降低它们的相对丰度。此外,在慢性应激条件下,糖皮质激素释放增加与肠道微生物多样性和丰富性降低有关。
社会大脑受到多种生物和环境因素的影响
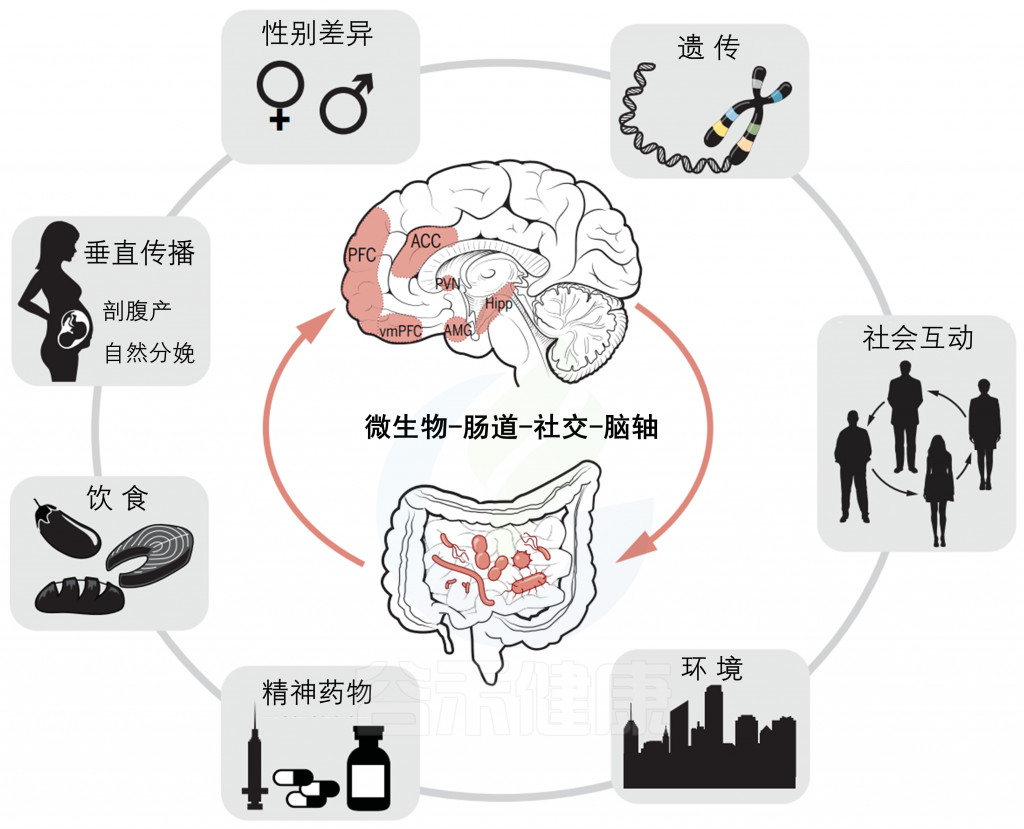

社会行为受多个相互关联的大脑区域(如下丘脑、杏仁核、前扣带皮质和前额叶皮质)支配,这些区域受多种外在和内在因素(如性别、遗传和表观遗传机制以及环境)的影响,这些因素都可能直接影响社会行为,也可以相互结合来塑造这种行为。例如,宿主遗传可以影响宿主胃肠道微生物群的组成,从而影响肠道菌群对社会行为的相对贡献。此外,饮食、精神药物和环境等外在因素也会影响微生物群的组成,从而间接地改变行为。
以微生物群为基础的干预治疗社会行为缺陷的临床和临床前研究自闭症谱系障碍
微生物群与社会失调之间的联系表明,瞄准微生物群可以改善社会行为缺陷。基于微生物群的策略已经证明了在各种临床前模型中改变社会行为的潜力,一些初步证据表明对人类的影响。






ASD,自闭症谱系障碍;ATEC,自闭症治疗评估清单;CFU,菌落形成单位;PBS,磷酸盐缓冲生理盐水;FOS,低聚果糖;GABA,g-氨基丁酸;GOS,低聚半乳糖;poly(I:C),聚肌苷:多胞苷酸;Shank3,SH3和多个ankyrin重复结构域3
展望
了解影响整个动物王国社会行为的发展和规划的因素不仅对重新思考大脑生理和行为的演变很重要,而且还有助于更深入地了解人类社会大脑的紊乱[包括自闭症谱系障碍(ASD)、社会恐惧症和精神分裂症]。
微生物群与这些疾病之间联系的证据正在增加,临床前和新出现的临床数据提出了这样的假设,即通过饮食或活的生物治疗干预以微生物为目标可以改善这类神经发育障碍的相关行为症状。需要进行更大规模的临床试验,以确认这种干预措施的有效性,然后才能被认为是神经发育障碍的一线治疗方法。
虽然目前肠道菌群和神经发育障碍之间的联系是一个有趣的研究领域,但微生物群在动物社会行为进化中的任何作用都不会取代其他因素。相反,它为这些复杂行为的产生增加了一个额外的视角。
参考文献
Sherwin E, Bordenstein S R, Quinn J L, et al. Microbiota and the social brain[J]. Science, 2019, 366(6465).