-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康
肠道微生物群通过代谢发酵膳食纤维等不被人体直接吸收的物质,产生了一类重要的代谢产物——短链脂肪酸。
短链脂肪酸主要包括乙酸盐、丙酸盐、丁酸盐,它们不仅仅是肠道上皮细胞的重要能量来源,更是联结肠道-免疫-代谢-大脑轴的信号分子。通过与特定受体(如GPR41/GPR43)结合,它们能调节肠道蠕动、维护肠屏障完整性、调节免疫反应、影响食欲和能量代谢,甚至可能影响神经系统功能。
随着微生物组研究的深入,我们逐渐认识到肠道微生物与人体健康之间存在着错综复杂的关系网络,而短链脂肪酸恰是这一网络中的核心。短链脂肪酸并非独立存在的简单分子,而是复杂生态系统平衡的产物和指标。它们反映了微生物群落的结构与功能,同时也塑造着宿主的生理状态。正是这种动态平衡的特性,使得短链脂肪酸在不同条件下表现出迥异的生物学效应。
因此,短链脂肪酸的健康效应高度依赖于机体状态、剂量水平以及具体应用场景,这远比简单的”好”与”坏”复杂得多。以丁酸盐为例,在健康状态下,它是肠道健康的守护者;但在肠道屏障受损或炎症状态下,同样的丁酸盐可能延迟伤口修复,甚至加重炎症反应。丙酸盐也展现类似特性:低浓度时可能有益肠道健康,但高浓度时可能产生毒性效应,甚至与自闭症等神经发育障碍存在争议性关联。
本文将全面梳理短链脂肪酸的生物学特性及健康影响,探讨短链脂肪酸异常的相关干预措施。更全面地理解短链脂肪酸,不仅有助于我们认识肠道微生物组与人体健康的深层联系,也为未来的个性化营养干预、精准医疗和健康管理提供了理论基础。
* 本研究参考并整合了微生物学领域知名专家Lucy博士和MacFabe博士的部分研究总结与学术观点。作为肠道微生物与人体健康研究方向的权威学者,他们长期致力于探索肠道菌群、营养代谢与疾病发生机制之间的科学关联。
短链脂肪酸是包含 6 个或更少碳分子的脂肪酸的一个子集。它们包括乙酸盐(C2)、丙酸盐 (C3)、丁酸盐(C4)、戊酸(C5)、己酸(C6)。最近的科学进展主要集中在乙酸盐、丙酸盐、丁酸盐上,因此这三个将是本系列文章的主要关注点。
可以在下面看到它们的化学结构:
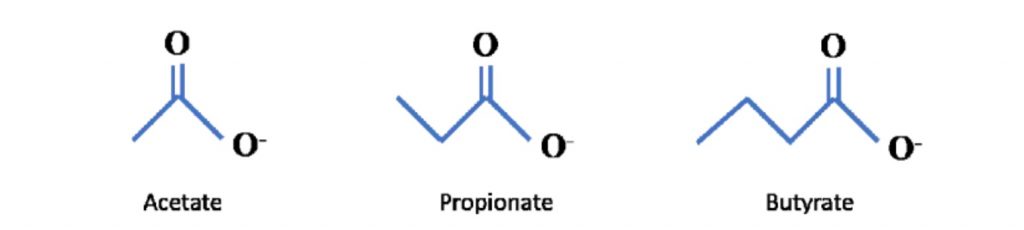
哺乳动物消化道不擅长代谢某些纤维。相反,菊粉、低聚果糖和抗性淀粉等膳食纤维很容易被肠道中的微生物发酵,短链脂肪酸是这种发酵的主要产物。
短链脂肪酸去哪里?
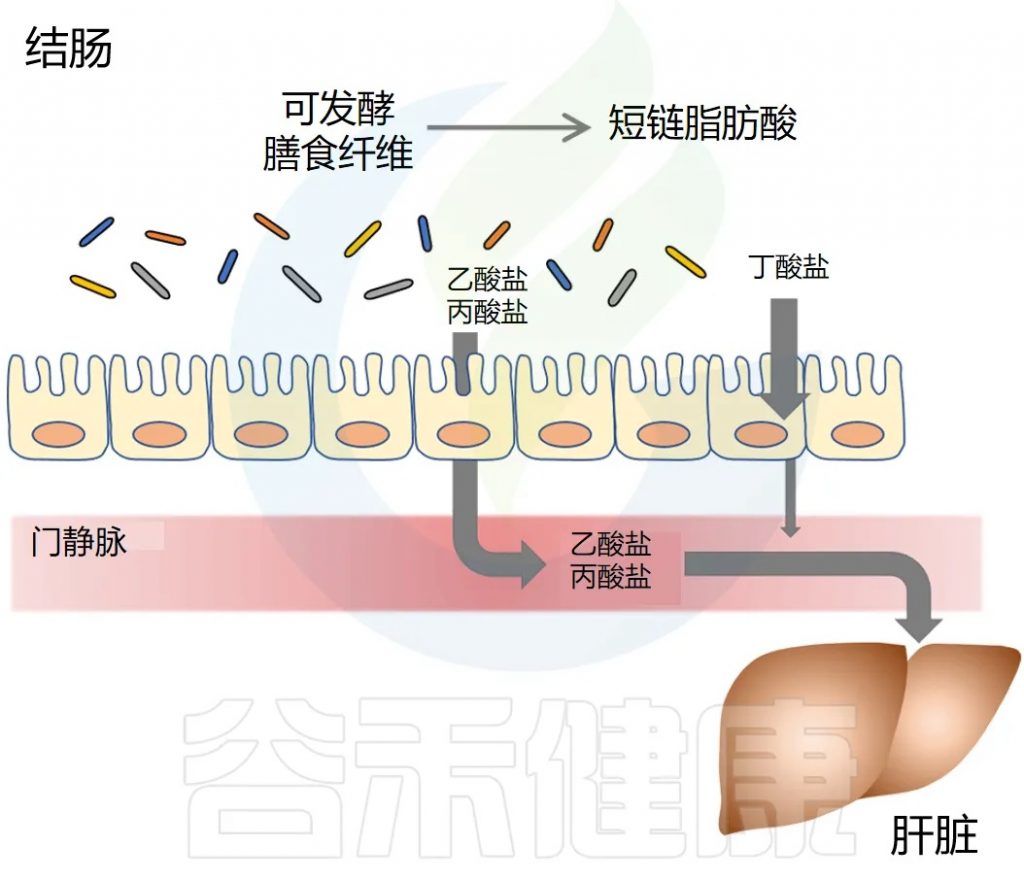
短链脂肪酸要么被肠道上皮细胞局部使用,要么通过肠道上皮运输到门静脉。
丁酸盐主要被结肠上皮细胞用作能量来源,而丙酸盐和乙酸盐主要通过门静脉运输到肝脏。
丙酸盐被肝细胞迅速代谢。乙酸盐可以留在肝脏中或释放到外周循环中。
信号分子和 HDAC 抑制剂
短链脂肪酸是有效的信号分子,与专门的 G 蛋白偶联受体(GPCR)结合,并最终改变细胞和组织的生物化学性质。这些受体可以在免疫细胞、神经细胞、甲状腺、肾脏、胰腺、脾脏、肝脏、其他组织上找到。
注:G蛋白偶联受体(G Protein-Coupled Receptors, GPCR)是一类重要的膜蛋白,在细胞信号转导中扮演关键角色。作为人体内最大的膜蛋白受体家族,GPCR参与调控众多生理过程。
它们也是基因表达的有效修饰因子,影响各种细胞类型的表观遗传学。特别是丁酸盐,它是组蛋白脱乙酰酶的有效抑制剂,组蛋白脱乙酰酶是负责确定 DNA 卷曲的紧密程度以及因此转录成 RNA 的程度的酶。
注:组蛋白脱乙酰是由组蛋白去乙酰化酶(HDACs)催化的过程,该过程通过调节染色质结构和基因表达参与几乎所有关键生物过程,包括基因表达,细胞分化,DNA修复和生长发育方面,是表观遗传调控的核心机制,也是重要的疾病治疗靶点。
SCFA 具有广泛的影响
通过这些机制,SCFA 能够对宿主生理产生广泛的影响。SCFA 决定结肠运动、血流和胃肠道 pH 值,这会极大地影响电解质和其他营养物质的摄取和吸收。它们也是结肠健康和肠道屏障完整性的重要促进剂,并在维持正常的肠道和免疫功能方面发挥着重要作用。
SCFA 也被证明会影响神经系统和大脑。丁酸盐已被证明可以调节小胶质细胞(大脑的免疫细胞) 的活性,而丙酸盐则被认为与自闭症谱系障碍的发展和进展有关,这个将在本系列的下面 部分中详细介绍这个主题。
SCFA 的产生也可能在塑造肠道微生物生态学中发挥重要作用。SCFA 在低浓度下表现出广谱抗菌活性。有趣的是,SCFA 对产生它们的细菌种类是相对惰性的抗菌剂,但对其他微生物具有相当强的抗菌活性。
注意,SCFA 总是好的吗?不一定。
SFCA 对宿主健康的总体影响存在广泛争议。例如,尽管刺激饱腹感信号,但 SCFA 也与增加从饮食中收集的能量有关。短链脂肪酸在高浓度或特定疾病条件下也可能具有毒性,将在下面详细讨论。
改变的SCFA水平会是疾病的原因吗?
SCFA 可能影响多种疾病的发病机制,包括过敏、哮喘、癌症、肥胖、代谢性疾病、自身免疫性疾病和神经系统疾病。但是请考虑以下事项:
一些研究仍在试图确定这些关联背后的机制。粪便 SCFA 测量有一些主要局限性,并且 SCFA 水平改变是这些疾病的原因还是结果仍然未知。更好地了解 SCFA 对于描述肠道和肠道微生物群在慢性疾病中的作用至关重要。
丁酸盐是肠道中产生的一种代谢物,对大脑、皮肤、免疫系统等都有好处,其分子结构如下:
编辑
丁酸盐保护肠道
丁酸盐是结肠细胞的首选底物,可提供结肠上皮细胞 60-70% 的能量需求。
丁酸盐抑制炎症、调节免疫、促进紧密连接蛋白组装,增强肠道屏障功能。
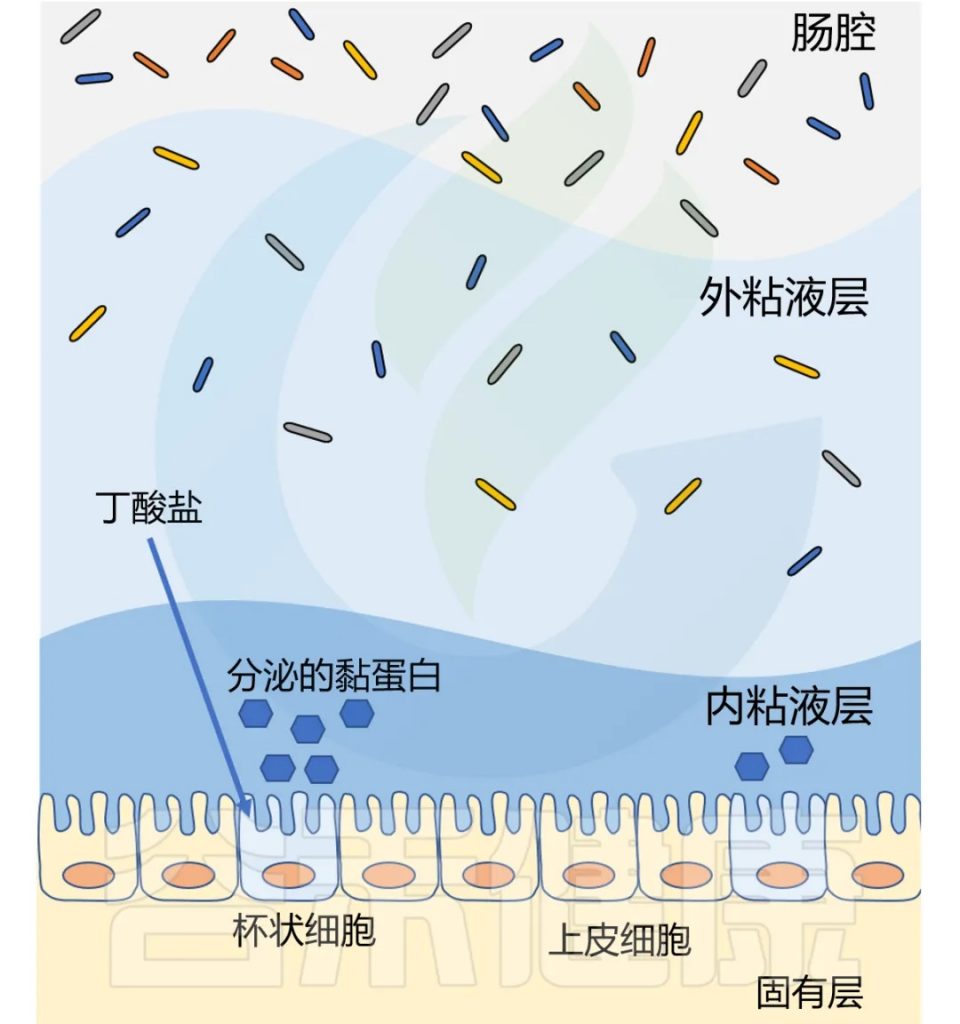
丁酸盐还影响粘液层,健康的结肠上皮覆盖着双层粘液。厚厚的内层致密无菌,保护上皮细胞免受微生物侵袭;外层松散,容纳以粘液层糖蛋白为食的细菌。
两个粘液层均由杯状细胞分泌的MUC2粘蛋白构成。研究表明,补充生理浓度的丁酸盐可增加人杯状细胞系中MUC2基因的表达和MUC2的分泌。
丁酸盐改善代谢功能
丁酸盐还影响新陈代谢。在肥胖小鼠模型中,补充丁酸盐被证明可以提高胰岛素敏感性、增加能量消耗和减少肥胖。它还增加了线粒体的数量及其在骨骼肌和棕色脂肪组织中的活性。一系列研究证实丁酸盐反应受体在脂肪组织中高度表达。
但是这种表达随着年龄的增长而下降,这可能解释了与年龄相关的胰岛素敏感性下降。丁酸盐还诱导饱腹感激素的产生,从而减少食物摄入量。
丁酸盐也可能对其他代谢疾病有益。研究表明,生命早期口服丁酸盐可延缓大鼠糖尿病的发展。丁酸盐补充剂还可以通过改善肠道屏障功能和纠正微生物失调来减轻饮食诱导的小鼠脂肪肝疾病。
丁酸盐改变基因表达
虽然我们的基因构成基本上是不可改变的,但基因的表达方式却具有高度可塑性。
在我们身体每个细胞的细胞核中,DNA 缠绕在组蛋白周围。
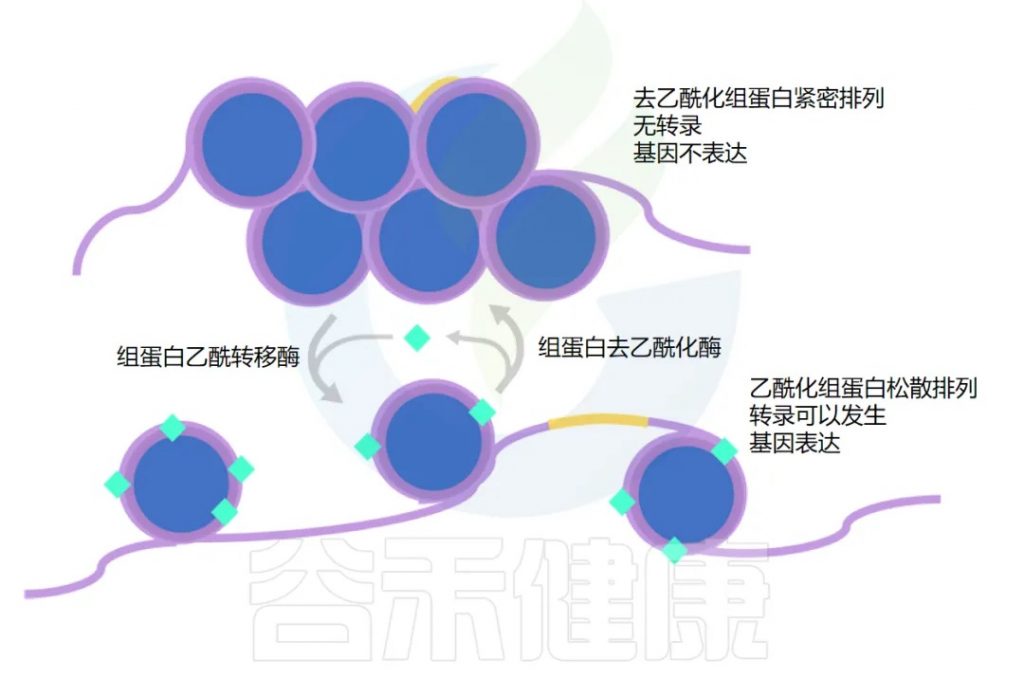
那么什么决定了基因是乙酰化还是去乙酰化呢?
组蛋白乙酰转移酶(HAT)负责添加乙酰基,而组蛋白去乙酰化酶(HDAC)负责去除。细胞内的许多信号分子可以影响这些酶的活性,丁酸盐就是其中之一。
丁酸盐通过两种不同的方式增加乙酰化,用于不同的基因集。
这两种机制都有助于增加乙酰化并保持基因“开启”。下一节将探讨其如何在癌细胞中发挥作用。
丁酸盐有抗癌作用
长期以来,人们一直知道丁酸盐可以刺激上皮细胞增殖,但同时对结肠癌具有保护作用。换句话说,丁酸盐可以在健康和癌变的结肠细胞中发挥不同的作用。
研究揭示了丁酸盐悖论背后的机制,实验表明 Warburg 效应是其解释的关键。Warburg效应描述了快速分裂的癌细胞的代谢特点。
注:Warburg效应是由德国生物化学家Otto Warburg于20世纪20年代发现的一种代谢现象,描述了肿瘤细胞的特殊能量代谢方式:即使在氧气充足的环境中,癌细胞也主要通过糖酵解而非有氧呼吸产生能量。
◆ 丁酸盐促进增殖
正常上皮细胞主要通过线粒体三羧酸循环(TCA循环)代谢丁酸盐等脂肪酸,产生能量。TCA循环通量增加,导致胞质溶胶中柠檬酸盐积累,柠檬酸盐可在细胞核中转化为乙酰辅酶A。该乙酰辅酶A为组蛋白乙酰转移酶(HAT)提供乙酰基,乙酰化调控上皮细胞增殖的基因。

◆ 丁酸盐的抑制作用
另一方面,癌细胞往往具有功能失调的线粒体,这意味着它们无法代谢脂肪酸(如丁酸盐)以获取能量。正因为如此,它们在很大程度上依靠葡萄糖代谢来产生能量,而丁酸盐等脂肪酸往往会在细胞中积累。这种细胞丁酸盐浓度的增加导致 HDAC 抑制增加,以及阻止癌细胞复制的基因表达。
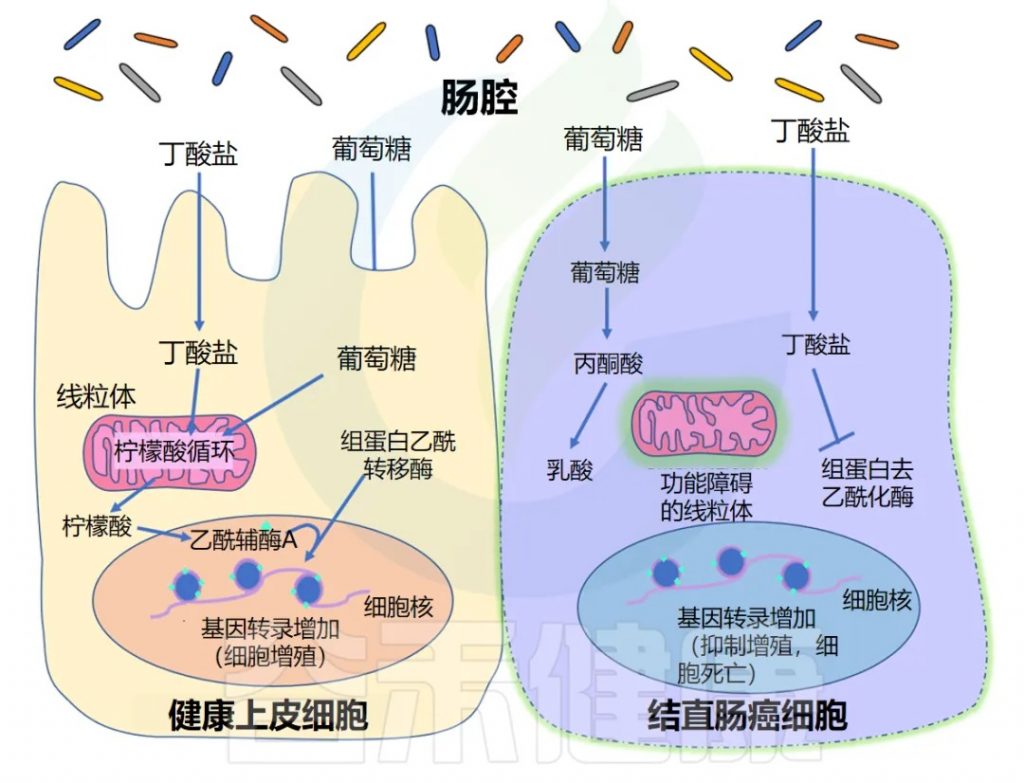
这种现象并非结肠癌所独有。丁酸盐已被确定在多种人类癌细胞系中具有抗癌活性,包括舌癌、前列腺癌、 肝癌、乳腺癌、肺癌、神经母细胞瘤等。
丁酸盐可能有益于大脑
丁酸盐对大脑健康的影响已在动物模型中得到广泛证实。
◆ 脑损伤保护
研究表明,给予丁酸钠或产丁酸梭菌的小鼠,在缺血性脑损伤后表现出神经发生增加、氧化应激减少和恢复改善。丁酸钠还能恢复血脑屏障的完整性,并减轻创伤性脑损伤后的神经功能缺损,同时可预防脊髓性肌萎缩症中的神经变性。
◆ 抗抑郁效应
在抗抑郁方面,丁酸盐可改变小鼠海马体和额叶皮层中脑源性神经营养因子(BDNF)等基因的表达,并增加血清素水平,同时减少药物诱导的双相情感障碍模型中的躁狂样行为,增加神经营养因子表达,并在慢性轻度应激和母体分离模型中减轻了认知障碍。
◆ 记忆增强作用
丁酸盐对记忆形成和保留也具有潜在作用。研究表明,丁酸盐通过抑制 HDAC 可以减轻海马胃泌素释放肽受体(GRPR)信号阻断导致的认知障碍,并使大脑处于“可塑性准备状态”,类似于运动的效果。
注:海马胃泌素释放肽受体 (GRPR) 的紊乱可能会抑制适当的记忆形成和消退,并导致与神经发育障碍相关的认知障碍。
最后,丁酸盐可能对自闭症谱系障碍有益,相关讨论将在SCFA不平衡和丙酸盐-自闭症连接部分展开。
丁酸盐调节免疫系统
丁酸盐在调节免疫系统方面也起着重要作用,几乎在所有类型的免疫细胞上都发现了丁酸盐反应受体。
丁酸盐信号传导产生抗炎效应,抑制促炎细胞因子的产生并上调抗炎细胞因子的产生,即使在脂多糖(LPS)等炎症刺激下也能发挥作用。这可能是通过 HDAC 抑制 NF-kB 通路来实现的,
注:NF-kB 通路是参与炎性细胞因子释放的主要通路。已在许多不同的免疫细胞类型中观察到丁酸盐介导的 HDAC 抑制。
丁酸盐还促进结肠和外周调节性T 细胞 (Treg) 的产生,这有助于抑制免疫反应,影响 Treg 和效应 T 细胞功能,并诱导抗菌肽素(Cathelicidin)的活性,从而增强对细菌感染的先天防御能力。
注:cathelicidin 是一种有效的抗菌剂,已知在结肠和肺上皮细胞中对细菌感染的先天防御中起重要作用。
丁酸盐和皮肤
由于很多朋友的小孩湿疹病史和对肠道皮肤轴的实验研究,小编感兴趣的是丁酸盐对皮肤健康的影响。
丁酸盐充当皮肤免疫系统的调节剂。皮下或局部应用丁酸盐被证明可以减少接触超敏反应,这可能是通过观察到调节性 T 细胞的增加和炎症效应 T 细胞的减少来解释的。丁酸盐还诱导胶原蛋白的合成,胶原蛋白是皮肤的重要结构成分。
丁酸盐改善骨骼健康
骨骼在成骨细胞(骨骼构建)细胞活性和破骨细胞(骨分解)细胞活性之间的微妙平衡中不断重塑。存在于骨髓中的间充质干细胞(MSC)可以分化成骨细胞(造骨细胞)或脂肪细胞(脂肪细胞)。
﹝仅供参考﹞
增加丁酸盐的方法
我们已经了解到丁酸盐是基因表达的有效修饰剂,对宿主健康有广泛的益处。想要增加丁酸盐,有几种方法可以做到这一点:
增加产生丁酸盐的细菌的丰度。具有特别高丁酸盐生产能力的细菌种类属于厚壁菌门和拟杆菌门,包括梭菌门、真杆菌属(Eubacterium)、罗氏菌属(Roseburia)、粪球菌属(Coprococcus)和普拉梭菌(Faecalibacterium prausnitzii)等。
双歧杆菌(Bifidobacteria)和乳酸杆菌(Lactobaccilus)等属也可能通过产生乙酸盐和乳酸盐来促进丁酸盐的产生,然后其他细菌可以将其转化为丁酸盐。
增加产生丁酸盐的细菌可用的底物。这意味着吃含有可发酵纤维的益生元食品,这些纤维会刺激丁酸盐的产生。一些最有效的产丁纤维包括抗性淀粉和低聚果糖。
补充剂。这应该非常谨慎,使用正确的补充剂形式。下面将对此进行说明。
过量的丁酸盐有毒吗?
目前各种形式的口服丁酸盐补充剂。但我们真的应该服用丁酸盐吗?丁酸盐过多是一件坏事吗?
查阅很多文献,发现一些研究表明,低浓度的丁酸盐是有益的,但高浓度可能是有害的,尤其是对于那些肠道受损的人。
在本文中,我们将分析几项阐明丁酸盐悖论的研究。首先,我们先来了解肠道解剖结构,这对于了解丁酸盐对肠道的影响至关重要。
肠道结构与丁酸盐的关联
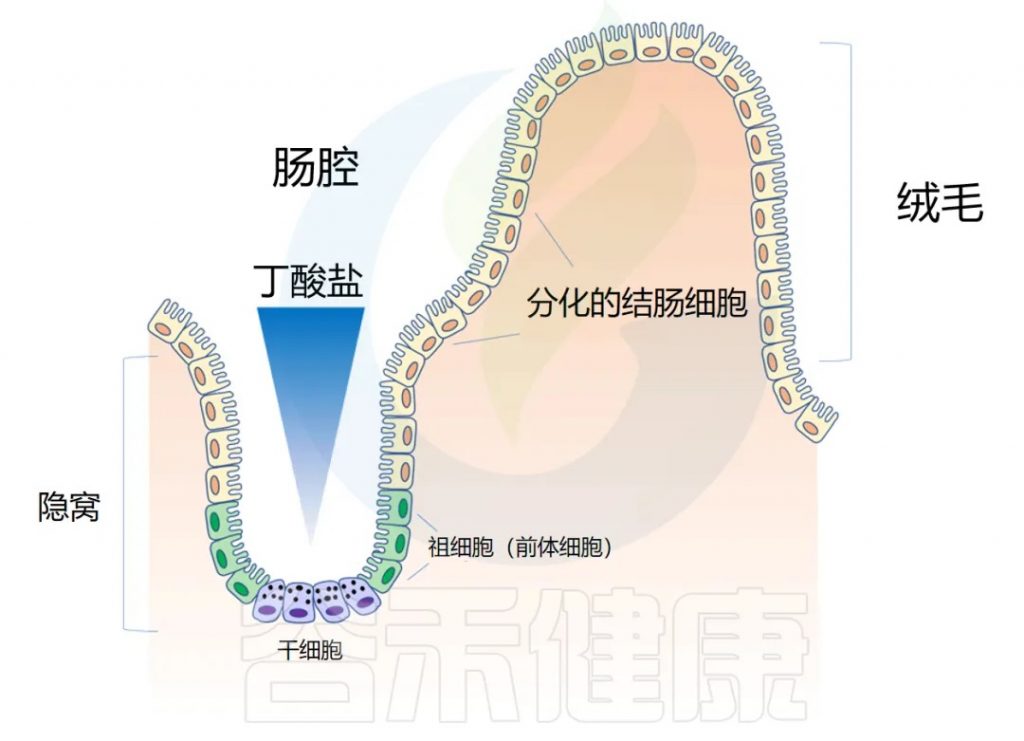
◆ 肠道解剖学:隐窝和绒毛
肠道上皮在人的一生中不断更新。肠壁内陷形成隐窝,而向外突出形成绒毛(villi)。隐窝有点像一个 “山谷”,把绒毛想象成 “山”。
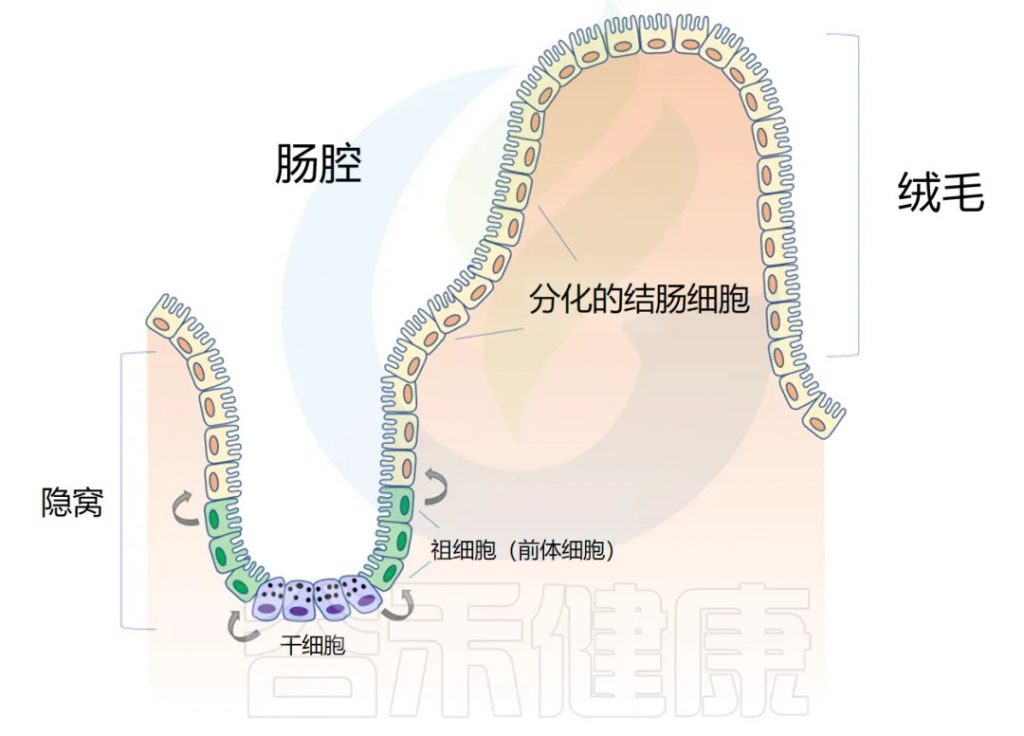
干细胞位于隐窝底部,周期性产生祖细胞,这些祖细胞在绒毛中向上移动时反过来分化为成熟的结肠细胞(colonocytes)。这补充了在顶部脱落的旧细胞。通过这个过程,整个肠道上皮大约每 4-5 天翻新一次。
注:肠道内壁覆盖着一层称为上皮的细胞组织,这些细胞负责吸收营养物质并形成保护屏障。这些上皮细胞不会长期存在,而是会定期死亡并被新细胞替代。这个更新过程非常快速 – 大约每4-5天,肠道内所有的上皮细胞都会被完全更换一遍。这种快速更新有几个重要作用:
这是人体中细胞更新最快的系统之一,反映了肠道作为消化和吸收器官以及防御屏障的重要性。
◆ 隐窝结构对干细胞的保护功能
人们已知隐窝已有数个世纪,但其结构功能直到近些年才被阐明。1974年,Cheng和Leblond提出隐窝可能保护快速分裂的干细胞和祖细胞,使其免受肠腔内的病原体和毒素侵害。

2016年,华盛顿大学的研究小组于《CELL》上发表的研究进一步佐证了该假设。他们利用高通量筛选方法研究微生物代谢物对干细胞增殖的抑制作用,结果他们发现在所有代谢物中,发现丁酸盐是抑制干细胞和祖细胞增殖最有效的抑制剂。
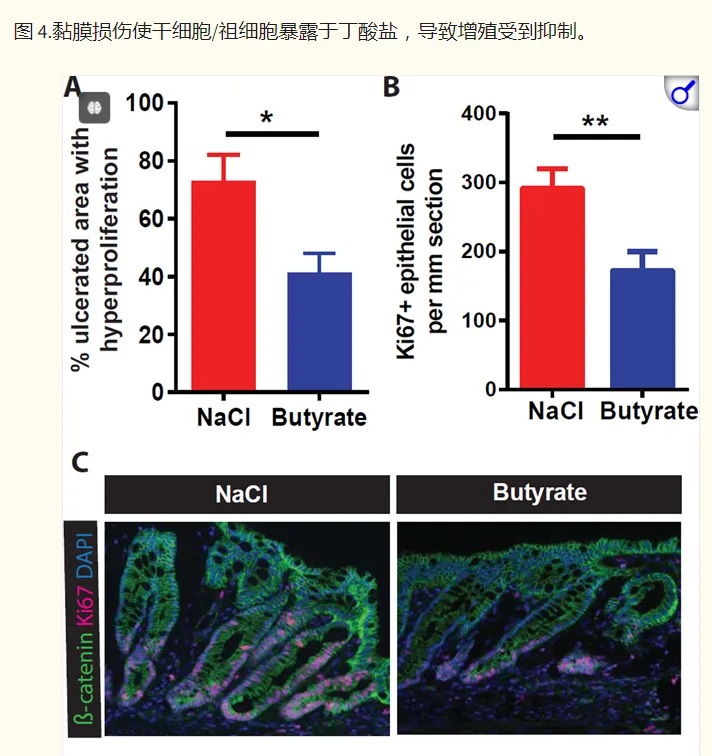
doi:10.1016/j.cell.2016.05.018
隐窝底部干细胞缺乏丁酸盐代谢酶 → 避免暴露于高浓度丁酸盐
然而,在活体生物中,丁酸盐并未导致这种抑制。他们想知道是否隐窝底部的干细胞没有代谢丁酸盐。为了找出答案,他们使用含有放射性标记13C的丁酸盐来评估不同位置丁酸盐代谢的速率。
他们发现,与隐窝底部的干细胞和祖细胞相比,隐窝顶部细胞中13C标记的乙酰辅酶A(丁酸盐氧化的最终产物)水平高出3倍。

作者总结了这些发现:
位于隐窝顶部的分化结肠细胞可以将丁酸盐作为能量来源代谢,从而可能防止干细胞生态位暴露于高水平的管腔丁酸盐。
炎症性肠病中的丁酸盐
◆ 丁酸盐延迟炎症模型中的伤口修复
然后,研究人员转向结肠炎的小鼠模型,以了解在丁酸盐存在下隐窝结构的破坏如何影响干细胞增殖。抑制干细胞增殖将阻止愈合粘膜损伤所需的上皮细胞更新。
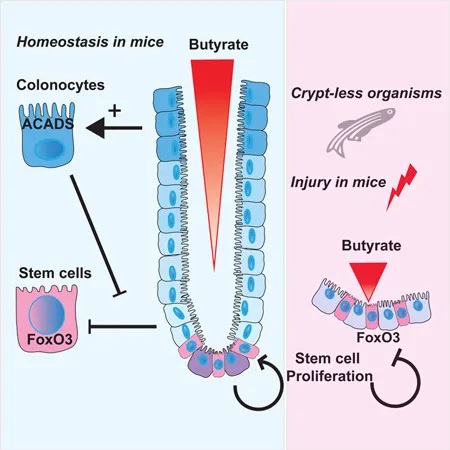
他们发现,给予丁酸盐可减少与结肠溃疡直接相邻的隐窝中的上皮增殖,并延迟伤口修复。
◆ 产丁酸菌与可发酵纤维在IBD中的双重效应
在另一项实验中,他们发现使用抗生素敲除产生丁酸盐的微生物可以减少结肠炎损伤后的溃疡大小。重新引入丁酸盐或产生丁酸盐的微生物导致大溃疡复发。
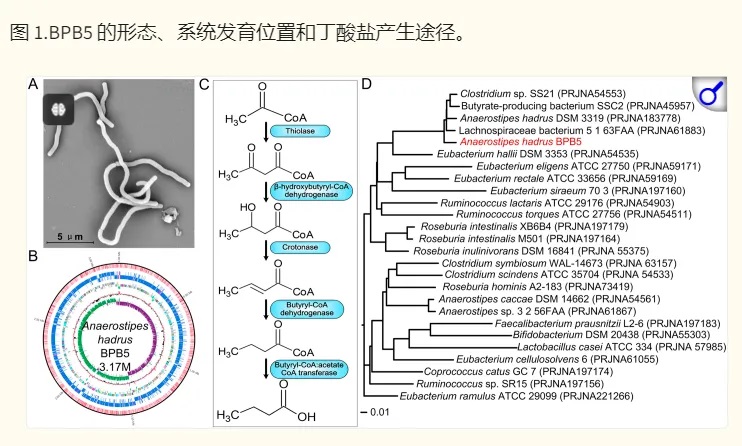
上海交大一项类似的研究(如下),将一种源自人类的产丁酸盐细菌株Anaerostipes hadrus BPB5 引入患有和不患有结肠炎的小鼠中。

另一项研究发现,补充已知可刺激丁酸盐产生的可溶性纤维菊粉导致 IBD 易感(IL-10 敲除)小鼠结肠中的促炎基因表达增加。这在对照野生型小鼠中没有发生。
总之,这些研究表明,丁酸盐、丁酸盐生产菌,甚至潜在的可发酵纤维的好处,都取决于肠道的状况。这些数据也可能部分解释为什么一些炎症性肠病患者在减少 FODMAP 摄入量后似乎有所改善。
同理,上海交大研究团队还指出:对健康个体可能有益的细菌也可能会成为入侵物种,从而对肠道微生物群被疾病破坏的宿主造成致命后果。这样的案例在免疫功能低下个体中引起感染甚至败血症、溃疡性结肠炎、短肠综合征、癌症等的报道均时有发生。
◆ IBD中,产丁酸菌丰度低:原因还是后果?
IBD 患者产丁酸菌水平降低,长期以来被认为是疾病的诱因。然而,一项研究引发了疑问:
缺乏丁酸盐生产者是否仅仅是疾病的结果?
炎症肠道有没有可能为了保护干细胞,抵抗丁酸盐生产菌,从而促进干细胞增殖和粘膜修复?
作者对自身研究的解读:
短期内,丁酸盐可能不利于伤口修复,但长期来看,它可能使宿主受益。通过抑制上皮损伤后干细胞的快速扩增,防止干细胞在接触遗传毒性管腔内容物时分裂。
尽管这个解释有其道理,但更严谨的科学需要不断验证。长期以来,丁酸盐都被认为是有益的,因此理解丁酸盐在肠道完整性受损时可能有害这一新范式颇具挑战。当然如果更多研究就更好了。
◆ 溃疡性结肠炎患者的丁酸盐氧化受损
体外和体内研究的证据表明,溃疡性结肠炎 (UC)患者丁酸盐的氧化受损。De Preter 等人发现,UC 活检中的平均丁酸盐氧化率降低到几乎是对照活检的一半。

根据疾病严重程度分层,非活动性和轻度疾病的丁酸盐氧化率与对照组无异,但中度和重度疾病的丁酸盐氧化率显著降低。值得注意的是,对照组之间的丁酸盐氧化也存在显著差异。
进一步研究丁酸盐动力学表明,丁酸盐浓度并非限制因素。对照组和UC活检的管腔丁酸盐浓度增加至1 mM以上并未提高丁酸盐氧化,表明超过1 mM的饱和点后,丁酸盐浓度不再是限制因素。
作者写道:
“…局部应用较高浓度的丁酸盐并不能克服UC中的粘膜能量不足,并且通过不可消化的碳水化合物或丁酸盐灌肠剂刺激丁酸盐的产生可能对治疗这种疾病无效。”
一项后续的研究表明,丁酸盐氧化减少是由于发炎粘膜对丁酸盐的吸收减少,这与促炎细胞因子下调 MCT1 的表达有关。MCT1 是一种转运蛋白,负责包括丁酸盐在内的多种分子的转运。此外,丁酸盐对 IBD 患者的抗炎作用也降低。
临床试验、动物研究和细胞培养实验显示结果喜忧参半
事实上,当在溃疡性结肠炎中测试丁酸盐灌肠剂或丁酸盐治疗时,动物研究和人体临床试验得出了相互矛盾的结果。
人类研究:丁酸盐灌肠剂研究的矛盾结果
在两项小型非安慰剂对照研究以及两项对照交叉研究中发现了丁酸盐灌肠剂的有益作用。
一项针对轻度至中度结肠炎患者的小型随机安慰剂对照研究发现,含有乙酸盐、丙酸盐和丁酸盐的 SCFA 灌肠剂具有有益作用

目前为止,大型的随机安慰剂对照试验(91名患者)表明,SCFA灌肠对结肠炎没有治疗价值,即使是病情较轻、发作短暂的患者也未能显著获益。
另一项大型随机安慰剂对照试验(38名患者)也未发现生理盐水安慰剂与丁酸盐灌肠之间存在显著差异,接受盐水灌肠的患者甚至比接受丁酸盐灌肠的患者临床改善比例更高(9/19 vs 7/19)。这些研究都没有显示丁酸盐的明确有害影响,但也没有评估其潜在粘膜毒性。

动物研究中的剂量依赖性效应
一项研究发现,口服丁酸钠可减轻小鼠的结肠炎。
但高浓度丁酸盐灌肠可诱导小鼠细胞凋亡和 UC 样病变。
在结直肠癌的小鼠模型中,菊粉和直肠内丁酸盐都已被证明可以改变结肠上皮并增加肿瘤的形成。
在小鼠中,慢性口服 SCFA 诱导 T 细胞介导的输尿管组织炎症,导致肾积水,即肾脏中的积液。
摘要如下:
“当 SCFA 以高于生理水平的水平全身给药时,会导致肾脏系统中的 T 细胞反应失调和组织炎症。”

细胞培养:浓度与环境决定效果
值得注意的是,现在有几项研究表明,SCFA 可以促进免疫调节或免疫激活,具体取决于炎症环境。换句话说,在正常状态下,SCFA 促进免疫调节;在炎症状态下,它们会促进免疫反应的放大。
此外,以低浓度(2mM)施用丁酸盐到上皮培养模型通过加速紧密连接蛋白的组装来改善肠道屏障完整性。然而,在高浓度(8mM)下,丁酸盐会增加屏障通透性。
丁酸盐还促进致病性大肠杆菌中毒力因子的表达。因此,这些大肠杆菌倾向于在丁酸盐水平最高的结肠中定植。
我们应该考虑补充丁酸盐吗?
有很多人发现了丁酸盐补充剂的好处,就如前面提到的。大部分试验中的一些患者确实看到了丁酸盐灌肠的临床改善,丁酸盐当然有很多好处。然而,目前还没有在人类中进行口服丁酸盐补充剂的双盲、安慰剂对照试验,所以需要谨慎的更细致入微的方法。
严重粘膜损伤时应避免直接补充
如果您有严重的粘膜损伤,例如高度活动性溃疡性结肠炎,倾向于建议不要使用丁酸盐灌肠剂或补充剂。
那些较轻的病例、缓解期或难治性结肠炎患者,或没有胃肠道疾病的人可以考虑丁酸盐。尽管如此,避免超生理水平还是很重要的。
直到最近,最广泛可用的丁酸盐形式是丁酸盐,例如丁酸钠或丁酸钙/镁。然而,丁酸盐可能会部分溶解在口中。高浓度口服丁酸盐与牙周炎有关,并可能抑制牙龈上皮细胞的增殖。
益生元:更自然的丁酸盐来源
由于肠道发酵的性质,益生元纤维也可能在结肠中提供更缓慢、更分散的丁酸盐释放。从肠道解剖结构和肠道生态学是在富含可发酵纤维的饮食中进化而来的,这是我们肠道最习惯的丁酸盐前体。
除了产生丁酸盐之外,益生元还有许多好处,包括对肠道上皮的抗炎作用和有益微生物的增殖。要注意的是,在严重的肠道炎症和粘膜损伤的情况下,即使是大量的益生元也可能不利于愈合。
健康状态下,丁酸盐通过多种机制促进肠道健康,包括增强肠屏障功能、促进黏蛋白MUC2的产生、调节免疫反应、抑制炎症,有抗癌潜力。它也是肠道上皮细胞提供主要能量来源。
然而,在肠道损伤或炎症状态下,丁酸盐的作用可能完全相反。研究表明,当肠隐窝结构受损,高浓度丁酸盐直接接触干细胞时,会抑制细胞增殖,延迟伤口修复。在炎症性肠病患者中,丁酸盐的代谢和转运机制受损,使得补充更多丁酸盐可能无法发挥预期效果,甚至可能加重病情。
这种复杂性表明,丁酸盐补充不应一刀切,而需根据个体健康状况、肠道完整性以及具体需求进行个性化评估和应用。肠道菌群检测成为个体化营养干预的重要工具。
对于产丁酸菌缺乏但肠道功能正常的个体,可适度补充丁酸盐;对于肠道屏障功能受损者,则应谨慎使用丁酸盐,可能需先修复屏障再考虑补充。
未来研究应关注丁酸盐作用的剂量-反应关系,明确不同肠道状态下的最佳干预策略,并将肠道菌群分析结果整合到个体化方案中,以实现丁酸盐益处的最大化和风险的最小化,从而更精准地应对不同人群的健康需求。
丙酸盐(Propionate)含有三个碳原子,羟基(-OH)位于第二个碳原子上。
而前面讲的丁酸盐(Butyrate)含有四个碳原子,羟基(-OH)位于第四个碳原子上。
丙酸盐通常由肠道细菌通过发酵L-鼠李糖、聚葡萄糖、阿拉伯木聚糖、D-塔格糖、甘露寡糖、昆布多糖等糖类物质产生。
丁酸盐可以通过肠道微生物群发酵富含抗性淀粉和果聚糖的食物来增加,如菊粉、马铃薯、洋葱等。
丙酸盐的生理作用
肠道健康与代谢调节
丙酸盐刺激肠道平滑肌收缩,增加黏液分泌,促进抗菌肽表达,扩张结肠动脉,并通过释放血清素调节肠道内分泌功能。它还能通过调节胆囊簇细胞促进胆汁释放,防御肠道细菌入侵。
糖代谢:丙酸盐是肝脏糖异生的主要能量来源,可激活三羧酸循环,影响下丘脑食欲调节神经肽,增加瘦素释放,抑制食欲。
脂代谢:抑制胆固醇合成,拮抗乙酸盐的促胆固醇作用,并降低脂肪细胞抵抗素表达,可能对肥胖有保护作用。但在某些研究中,丙酸盐可能通过升高胰高血糖素、去甲肾上腺素等激素增加糖尿病和肥胖风险,提示作用存在个体差异。
免疫调节与抗炎作用
丙酸盐通过激活GPR43/GPR41受体,促进调节性T细胞分化,抑制辅助T细胞活性,减少全身炎症反应。
心血管保护
丙酸盐减少促炎细胞因子(如TNF-α、IL-6),改善心脏纤维化和心功能。
血脑屏障保护
丙酸盐通过Nrf2信号通路减少氧化应激,增强紧密连接蛋白表达,保护血脑屏障完整性。
在前文中,我们看到了四碳丁酸盐,一种有效的抗炎和维持肠道屏障功能的关键分子,在高浓度下可能是有害的,特别是在粘膜炎症的情况下。有趣的是,类似的悖论可能适用于三碳丙酸盐,低浓度有益,但高浓度有毒。
生理双重性
在小鼠中,丙酸盐已被证明可以诱导肠道中产生饱腹感激素,以减少食物摄入并防止饮食诱导的肥胖。 最近的一项研究发现,短链脂肪酸丙酸的管理显著减弱脊柱关节炎。
然而,过量的丙酸盐可能是有问题的。在丙酸血症(代谢的遗传错误)中,丙酸盐的积累与酸中毒、发育迟缓、癫痫发作、氧化应激增加、线粒体功能障碍和胃肠道症状发作有关。肠易激综合征中也有过量丙酸的报道,当然还有自闭症。
丙酸盐与自闭症
近几十年来,自闭症和其他神经精神疾病的患病率急剧上升。环境因素肯定会发挥作用,包括肠道微生物群及其非常重要的代谢产物短链脂肪酸(SCFA)。
自闭症是一种复杂的神经生物学状况,影响多个身体系统,包括免疫和神经系统,表现为沟通和感官理解能力受损,通常在孩子很小的时候被诊断出来,且对男孩的影响更大。
近年来,自闭症的发病率呈上升趋势,在谷禾数据库,自闭症样本量也积累了超过5000例的样本。其特征包括社交和沟通障碍、感觉异常和重复行为等。越来越多的证据表明,自闭症不仅是一种大脑疾病,更是一种“全身”疾病,涉及代谢和免疫功能异常、胃肠道症状等。
多因素病因学挑战传统认知
遗传因素仅解释10%-20%病例,参与线粒体功能,免疫调节和神经回路形成的基因与自闭症有关。
环境因素在自闭症的发病中起着重要作用,肠道菌群失调、抗生素使用、饮食西化等环境因素显著增加ASD风险其中肠道微生物群及其代谢产物短链脂肪酸受到关注。
注:饮食西化这一点在从不发达国家向发达国家移徙的人口中尤其明显。每一个移民到西方国家的索马里人都注意到他们社区的ASD患病率增加。他们称之为“西方病”,因为他们在东非的家乡没有获得这种疾病。
关于自闭症我们以前的文章也有写过相关:
儿童神经发育异常的脑肠轴视角 – 自闭症早期风险判别和干预新路径

这意味着环境因素起着主要作用,自闭症是由基因与环境的复杂相互作用引起的。最近的证据表明,肠道微生物代谢物,特别是SCFA丙酸盐,可能发挥作用。
在动物模型中丙酸盐诱导自闭症样行为
在一项研究中,他们将丙酸盐直接注射到老鼠大脑的脑脊液中。与接受安慰剂输注的大鼠相比,在短短2-30分钟内,丙酸盐治疗的大鼠表现出重复行为,多动增加,社会行为受损和癫痫发作活动的证据。虽然丁酸盐和乙酸盐处理的大鼠确实显示出一些异常,但丙酸盐引起了最强烈的ASD样行为。

在另一项研究中,他们通过外周注射怀孕大鼠及其后代来观察系统性丙酸盐的影响。丙酸盐增加焦虑样行为和重复行为,特别是在出生前和出生后暴露的大鼠中。
丙酸盐与人类自闭症相关的证据
动物模型结果的外推需谨慎,需通过纵向人类研究逐步验证这些生物标志物与自闭症消退或临床改善的关联。
肠道微生物群改变是ASD相关症状的原因还是结果,尚不明确。
然而,普遍认为剖腹产、早期感染和抗生素暴露可能改变肠道微生物群,并增加ASD风险。
研究表明,ASD患儿粪便中丙酸盐水平升高,且ASD相关细菌包括多种丙酸盐产生菌,如梭菌、拟杆菌、脱硫弧菌等。
近期临床研究发现,ASD患者胃肠道活检中梭菌代谢物尿液标志物升高,碳水化合物代谢也发生改变。另有研究报告,使用抗生素治疗后暂时的行为改善,这些抗生素可降低产丙酸菌的水平。
机制:丙酸盐如何导致自闭症
✦【 间隙连接功能 】
MacFabe博士推测,丙酸盐的许多效应可能源于其关闭间隙连接的能力。间隙连接连接着相邻细胞的细胞质,允许小分子和离子在它们之间通过。这对于同步神经电活动至关重要,并在早期大脑发育中扮演着关键角色。间隙连接耦合的减少也可能抑制皮质修剪,这与 ASD 患者中发现的神经元密度增加的现象一致。
关于 Dr. MacFabe 与自闭症研究
Dr. MacFabe是Kilee Patchell-Evans自闭症研究小组的主任。他是温哥华不列颠哥伦比亚大学 iTARGET 自闭症倡议的核心成员。
该小组的核心重点是肠道微生物组的代谢产物如何控制自闭症患者的大脑功能和行为,以及相关的神经精神疾病,如强迫症、焦虑症、运动、饮食和学习障碍。尤其对肠道细菌短脂肪酸代谢物的作用及其在自闭症中的作用以及开发新的临床生物标志物和疗法以预防、识别、筛选和治疗该疾病特别感兴趣 。
此外,间隙连接“基因敲除”小鼠(即经过基因工程改造,不表达任何间隙连接蛋白的小鼠)表现出异常的大脑发育和行为、癫痫性疾病,以及对神经毒性损伤的过度反应。
✦【 线粒体功能障碍 】
ASD 通常伴有与线粒体功能障碍一致的遗传和生化变化。有证据表明,丙酸盐可能通过干扰线粒体 TCA 周期来引起这些变化。

线粒体三羧酸(TCA)循环是细胞能量产生的关键步骤。TCA循环的产物是 NADH 和 FADH2,它们将高能电子带到电子传递链(ETC),在那里它们的还原能力用于产生 ATP(细胞能量)。
从下图中可以看出,一轮TCA循环产生3个NADH分子和1个FADH2分子。丙酸盐通过转化为琥珀酰辅酶A进入TCA循环。少量有助于维持TCA循环中间体,并有利于细胞能量的产生。
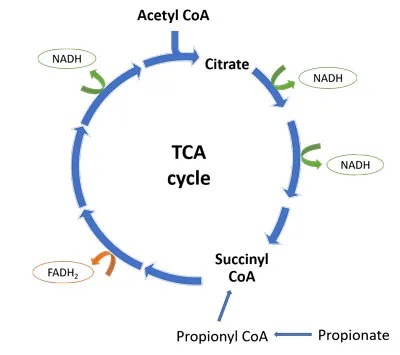
然而,进入TCA循环的大量丙酸绕过前四种TCA酶,并可能导致循环的转变。在循环的后半部分通量增加,产生柠檬酸盐积聚,而由于琥珀酰辅酶 A 的反馈抑制,前半部分则因“拥堵”而减缓。
这有几个后果:
首先,这改变了NADH : FADH2的比例,导致产量为1:1而不是3:1。当这些能量载体到达电子传递链时,NADH进入ETC复合物I,FADH2进入复合物II。
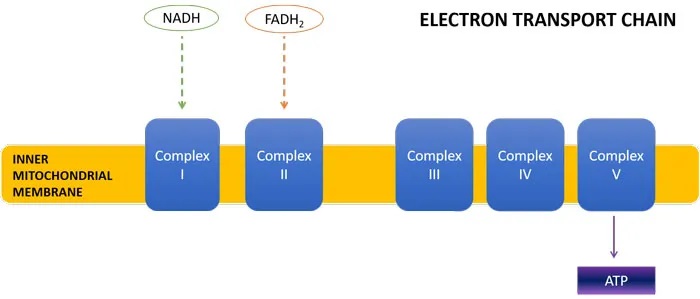
每个NADH分子导致产生3个ATP分子,而每个FADH2分子导致产生2个ATP分子。因此,丙酸盐诱导的TCA循环通量的转变将导致较少的NADH产生,以及复合物I处能量载体的缺乏,导致较少的总体ATP形成。事实上,ASD儿童已被证明缺乏ETC复合物。
其次,线粒体柠檬酸盐的积累将导致柠檬酸盐被转运到细胞胞质溶胶中。柠檬酸盐抑制磷酸果糖激酶,糖酵解的关键调节步骤。柠檬酸盐还增加了丙二酰辅酶A的形成,丙二酰辅酶A抑制CPT-1,CPT-1是将脂肪酸运送到线粒体中的转运蛋白。这有效地阻止脂肪酸氧化。
丙酸盐与线粒体功能:浓度与环境依赖性效应
为了更多地了解丙酸盐在线粒体功能障碍中的作用,McFabe博士实验室的学生培养了ASD和对照患者的免疫细胞,这些患者具有不同浓度的丙酸盐,有和没有活性氧(ROS)。
奇怪的是,他们发现如果ROS不存在,丙酸盐会改善线粒体功能;然而,在ROS存在的情况下,它会对线粒体功能产生负面影响。
换句话说:丙酸盐可以对线粒体功能产生有益和毒性作用,这取决于浓度,暴露时间和微环境。
作为一种弱酸,丙酸盐的摄取在细胞内酸化的条件下增加,并且可以在细胞内变得更加浓缩。像脱硫弧菌这样的菌群,它们产生丙酸和硫化氢。硫化氢的存在可能会增加丙酸盐损害线粒体功能的能力,可能是通过酸化细胞。
✦【 肉碱代谢障碍 】
肉碱代谢障碍也可能在神经发育障碍如ASD中发挥作用。肉碱是最有名的参与脂肪酸β-氧化。脂肪酸不能自由地穿过线粒体膜被代谢,而是必须与肉毒碱分子结合以穿过线粒体膜运输。
然而,肉碱也在脂质合成、胆碱能神经传递、膜稳定性和抗氧化活性中发挥作用。因此,肉碱对细胞能量,大脑发育和大脑功能很重要。

许多ASD患者有相对的肉碱缺乏症,这可能是由于遗传和后天因素。例如,已知某些抗生素可降低肉碱水平。口服肉碱及其衍生物乙酰-L-肉毒碱已被证明具有神经保护作用,并有望作为ASD和其他神经发育障碍的治疗剂。
如果肉碱缺乏,柠檬酸盐的积累阻止脂肪酸被运送到细胞中,不仅脑细胞会受到影响,肠道上皮细胞也会受到影响,后者依赖脂肪酸氧化(特别是丁酸代谢)来获得70%的能量,以维持肠道完整性。缺乏脂肪酸氧化会导致肠道通透性增加。研究表明,36%的ASD患者肠道通透性明显增加,近一半患者存在某种胃肠道症状。
进一步的研究可以探索肉碱补充在改善ASD患者的神经行为和胃肠道症状方面的具体益处,并确定最佳的剂量和给药方案。此外,还需要考虑个体化治疗方法。
关于丙酸盐调节的干预措施
有几种方法可以潜在地减少胃肠道丙酸盐的产生和丙酸盐的细胞水平。
抗生素
甲硝唑和万古霉素已用于ASD患者,取得了一定的成功。这些抗生素对革兰氏阳性菌具有广谱活性,包括产丙酸盐的梭菌属成员。在这两种药物中,万古霉素是更安全的,因为在正常情况下,口服万古霉素不会被显著吸收到循环中,而甲硝唑被全身吸收,可能具有不良的全身副作用。
然而,任何一种抗生素对丙酸盐产生的影响可能是短暂的。
一项为期8周的小型部分盲法临床试验发现,万古霉素对11名儿童中的8名ASD暂时有效,但这种益处并不持久。停止抗生素治疗后,梭菌很快又重新出现,可能是由于它们的孢子形成特性。因此,从长远来看,单独使用抗生素不足以降低丙酸盐的产量。
恢复胃肠道pH值和SCFA比值
改变肠道的pH值对肠道微生物群组成有重大影响。对人类粪便微生物群落的研究发现,在pH 5.5时,有益的丁酸盐产生菌占总菌群的20%。当pH值上升到6.5时,这些细菌几乎完全消失,产生乙酸盐和丙酸盐的细菌占主导地位。当然,恢复ASD患者的结肠pH值并非易事,目前也不是一种可行的治疗选择。

另一方面,丁酸盐已显示出治疗ASD和其他神经系统疾病的一些前景。当然,丁酸盐可以改善屏障功能,调节免疫系统,并可能有助于降低肠道的pH值,选择丙酸盐生产者。丁酸盐对转运蛋白的竞争也可能减少从肠道吸收到循环中的丙酸盐的量。需要更多的研究来确定SCFA比率如何影响ASD。
纠正营养缺乏症
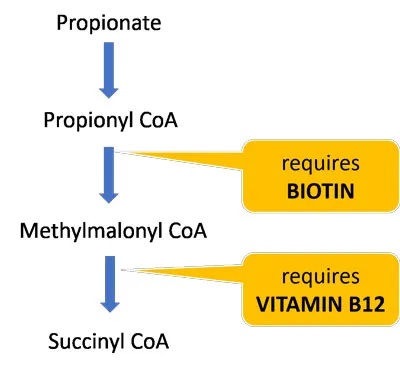
生物素和维生素B12是分解丙酸盐并使其进入TCA循环的酶的重要辅助因子。这些维生素的饮食缺乏可能进一步损害丙酸盐和肉毒碱代谢,并导致线粒体功能障碍(参考自lucy 博士博客内容)。
注:Dr lucy 以优异的成绩获得Kalamazoo College生物学学士学位和伊利诺伊大学厄巴纳-香槟分校营养科学博士学位,她花大量的时间研究饮食和运动对健康和疾病肠道微生物群的影响。
编辑
大约一半的生物素是由肠道微生物群产生的,因此那些肠道生态失调的人特别容易缺乏。
一项研究发现,与对照组相比,ASD儿童的生物素水平显着降低。一项后续研究发现,补充生物素水平与ASD症状改善高度相关,表明许多ASD患者可能受益于生物素补充剂。

无麸质、无酪蛋白饮食
在过去的十年中,无麸质,无酪蛋白(GFCF)饮食已成为ASD患者越来越受欢迎的治疗方法。虽然从饮食中去除这些免疫原性蛋白质可能具有独立的益处,但GFCF饮食也可能对丙酸盐产生影响。
值得注意的是,丙酸盐是小麦和乳制品中主要的动物青贮饲料和食品防腐剂,如丙酸钠或丙酸钙盐,并天然存在于一些乳制品中,如奶酪。

丙酸盐也由许多ASD相关细菌直接或间接产生,如梭菌属和脱硫弧菌属,来自精制糖和小麦糖的发酵。换句话说,当你喂这些细菌某些谷物和精制碳水化合物,他们开始制造更多的丙酸盐。
去除这些食物可能对丙酸代谢和肠道屏障功能有好处。上面提到的同一项研究发现,自闭症儿童的肠道通透性增加,发现那些GFCF饮食的肠道通透性评分低于对照组。
丙酸盐的其他饮食来源
除了小麦和乳制品,丙酸盐也被添加到许多精制食品中作为防腐剂。食品工业和农业越来越多地使用丙酸盐和相关的化学衍生物。硝基丙酸盐是许多植物和真菌产生的丙酸盐的衍生物。它是甘蔗、酱料和加工大米的潜在污染物,也是一种强效的线粒体和神经毒素。
其他食物刺激丙酸盐的产生。例如,人工甜味剂如糖精和糖精已被证明会显著增加啮齿动物肠道丙酸盐水平。
我们之前有写过关于食品添加剂相关的文章:
你的焦虑可能与食品添加剂有关,警惕食品添加剂引起的微生物群变化
2005年的一项研究发现,配方奶粉喂养的婴儿的丙酸盐水平比母乳喂养的婴儿高2.5倍。在配方中添加低聚糖仅部分改善了过量丙酸盐的产生。

GAPS饮食和碳水化合物
Natasha Campbell-McBride博士因其著作《肠道与心理综合征》而在自闭症社区中广为人知。麦克布赖德博士认为,包括自闭症在内的神经精神疾病是在肠道中产生的。她帮助许多儿童和成人扭转自闭症行为,并使用特定碳水化合物饮食(SCD)的修改版本(称为GAPS饮食)恢复正常的日常功能。
GAPS饮食在一段时间内从饮食中去除所有可发酵的碳水化合物,使炎症消退,肠道屏障愈合和密封。有趣的是,GAPS饮食排除了几乎所有的饮食丙酸盐来源和产丙酸菌的底物,这至少可以部分解释饮食对治疗神经系统疾病的成功。
在最初的消除阶段之后,重新引入富含菊粉的蔬菜,如西兰花和花椰菜,可能会优先喂养丁酸盐生产者。
GAPS饮食也是生酮的,特别是在早期阶段。生酮饮食对丙酸代谢的影响尚不清楚,尽管由于碳水化合物限制,丙酸产量可能要低得多。生酮饮食似乎还增加了整体NADH的产生和通过TCA循环右侧的通量,可能改善了由过量丙酸引起的左侧性。最后,酮与丙酸盐和其他SCFA使用相同的转运蛋白,因此可能通过竞争转运减少细胞中丙酸盐的积累。

回顾一下本章节主要的要点:
自闭症和其他神经系统疾病越来越普遍,这不能用遗传影响来解释。
丙酸盐在自闭症中的研究最多,但它也可能对其他神经系统和神经系统相关疾病有影响。即使是患有脑雾或疲劳的人也可能会有过量丙酸盐的影响。
丙酸盐在动物模型中可诱导ASD样行为。人类ASD患者的产丙酸盐菌丰度增加,粪便丙酸盐水平升高。
丙酸盐不是自闭症的唯一原因,但它可能在ASD患者的一个子集中起着重要作用。丙酸盐诱导间隙连接功能障碍、线粒体功能障碍、肉毒碱功能障碍,特别是在炎症和酸中毒的情况下。
抗生素可以暂时击倒丙酸盐生产者,但不是长期解决方案。
补充乙酰-L-肉毒碱、生物素、甲基维生素B12和/或丁酸盐可能有帮助。
丙酸盐在食品中的广泛使用需要注意。去除小麦、乳制品和其他丙酸盐的饮食来源可能会改善症状。
婴儿配方奶粉、精制碳水化合物和人造甜味剂会刺激产丙酸菌的生长。
GAPS饮食可以通过在一段时间内去除所有可发酵的碳水化合物来帮助调节丙酸盐的产生。之后,战略性地重新引入合适的纤维可能能够刺激有益的产丁酸菌的增长,并使丙酸盐生产者处于困境。
乙酸盐是含两个碳原子的短链脂肪酸,由肠道菌群发酵膳食纤维产生,也可通过外源性摄入。
乙酸盐的生理功能
能量代谢:作为细胞燃料参与三羧酸循环(TCA)。
抑制炎症反应:乙酸盐通过激活G蛋白偶联受体(GPR43),抑制促炎因子(如IL-6、TNF-α)表达。
调节肠道免疫:通过GPR43激活,促进肠黏膜屏障修复,减少细菌易位,并通过调节IgA与菌群结合维持肠道稳态。
神经调节:作为星形胶质细胞的主要能量源,参与神经递质合成(如GABA)。
维持肠道屏障:乙酸盐促进肠道上皮细胞增殖,改善血供,增强黏液分泌,保护黏膜完整性。
乙酸盐会让你发胖?
研究已经知道,微生物群的改变与代谢综合征和体重增加有关。
2006年,研究人员发现,遗传肥胖小鼠的微生物组具有更强的从饮食中收集能量的能力。此外,将肥胖小鼠的粪菌移植到无菌小鼠体内,会使无菌小鼠体重和脂肪增加。
在人类中,粪便乙酸盐水平升高与肥胖相关,但相关性不等于因果关系。
耶鲁大学研究人员开展了一项题为 “乙酸盐介导微生物组 – 脑 – β – 细胞轴以促进代谢综合征” 的研究,发表在《自然》杂志上,主要发现如下:
◆ 肥胖大鼠代谢更多乙酸盐,分泌更多胰岛素
在导致肥胖的饮食 3 天或 4 周后,大鼠的全身乙酸盐周转、血液乙酸盐和粪便乙酸盐浓度显著增加,肠道微生物群是乙酸盐升高的来源。喂食正常饮食并将乙酸盐输注到胃中的大鼠复制了肥胖大鼠中 GSIS 的增加。
◆ 乙酸盐激活迷走神经以驱动胰岛素分泌
作者接下来研究了乙酸盐是否可以通过直接影响 β 细胞(负责胰岛素分泌的胰腺细胞)来刺激 GSIS。他们发现乙酸盐不会刺激离体胰岛中的 GSIS,但通过影响副交感神经系统,特别是激活迷走神经,增加了 GSIS。
注:副交感神经系统调节β细胞胰岛素分泌。这通常被称为“休息和消化”神经系统,因为它会减慢心率并增加肠道活动。
研究人员发现,输注乙酸盐 60 分钟后,副交感神经活动增加了三倍。脑乙酸盐浓度也增加,证实了乙酸盐穿过血脑屏障的能力。
刺激迷走神经也被证明可以驱动胰岛素分泌。迷走神经从脑干开始,几乎支配每个腹部器官,包括肠道和胰腺。
乙酸盐是否激活了迷走神经?为了找出答案,他们比较了乙酸盐对迷走神经完整的大鼠和手术切除迷走神经的大鼠的影响。
研究发现,输注乙酸盐后,副交感神经活动和脑乙酸盐浓度增加,将乙酸盐直接输注到大脑也导致 GSIS 大幅增加。切断迷走神经的大鼠对乙酸盐的反应中血浆胰岛素浓度显著降低。
下图总结了他们的发现,显示了肠-脑-β细胞轴:
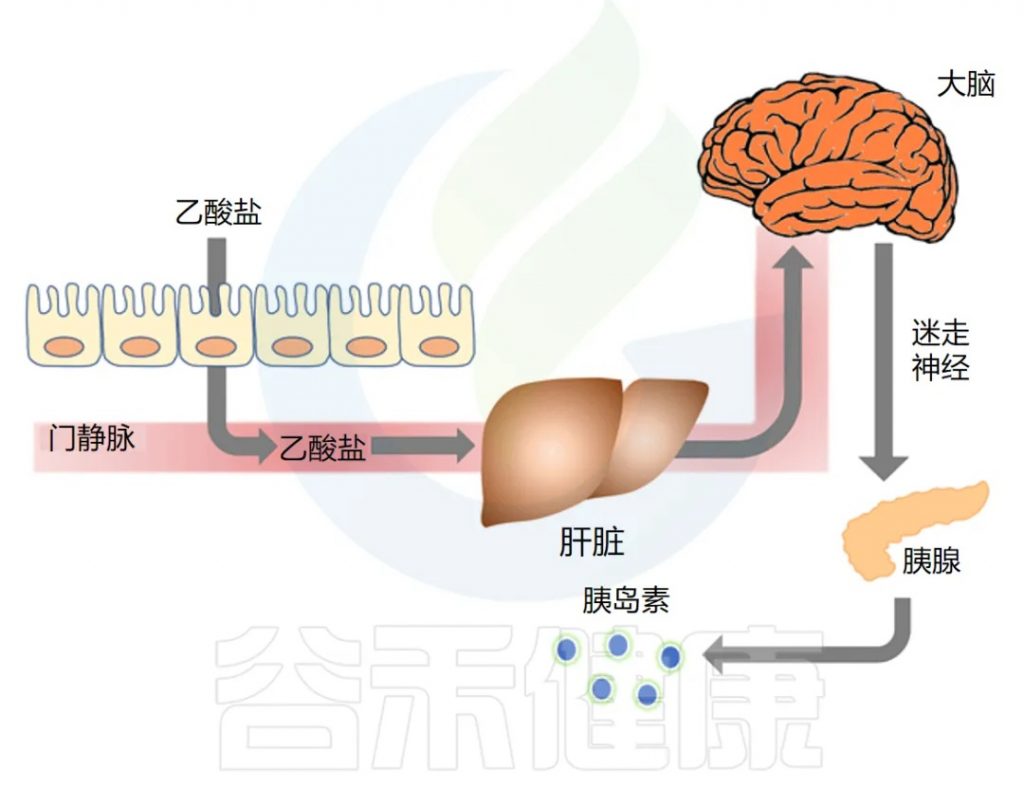
◆ 长期乙酸盐输注会导致肥胖和代谢综合征
最后,研究人员想确定乙酸盐本身会导致肥胖。他们给瘦大鼠连续输注乙酸盐到胃中10天,结果发现,接受乙酸盐输注的大鼠胰岛素分泌和胰岛素抵抗增加,副交感神经系统活动增加,血浆 grehlin (一种调节食物摄入的激素)激素增加了3倍,每日热量摄入量增加,体重显著增加,血浆、肝脏和骨骼肌甘油三酯含量增加。而迷走神经切断术的大鼠未出现这些作用。再次证明乙酸盐的作用是通过迷走神经介导的。
所以肠道来源的乙酸盐会导致肥胖,对吧?
还没那么快下定论。
这项研究的结果与体外研究和多项动物研究形成鲜明对比,那些研究认为乙酸盐对新陈代谢有益。
体外研究
乙酸盐与受体 GPR43 结合,在培养的肠道上皮细胞中,导致分泌一种调节能量代谢的肠道来源的激素;在脂肪组织中,激活 GPR43 抑制胰岛素信号传导并抑制脂肪堆积,从而提高胰岛素敏感性。
动物研究
缺乏乙酸受体 GPR43 的小鼠在喂食正常饮食时变得肥胖,而过表达 GPR43 的小鼠即使在喂食致肥胖饮食时也保持苗条。
给饮食诱导的肥胖小鼠纳米颗粒递送的乙酸盐。在肝脏中,乙酸盐减少了脂质积累,改善了肝功能,并提高了线粒体效率。在白色脂肪组织中,乙酸盐抑制脂肪分解,但会诱导“褐变”,增加代谢能力并导致体内脂肪减少。
菊粉、低聚果糖等益生元增加了乙酸盐的产生,并导致 Grehlin 的产生减少,从而导致食物摄入量、体重和脂肪量减少。
在饮食诱导的肥胖小鼠中,每隔一天禁食 (EODF)升高血清乙酸盐和乳酸水平,这与白色脂肪组织的褐变和代谢改善有关。
乙酸盐已被证明还有其他好处:
耶鲁大学的研究为理解乙酸盐在肥胖中的作用提供了一个新视角,但同时也引发了更多的疑问,为什么在不同研究条件下,乙酸盐对肥胖和代谢综合征的影响会出现如此大的差异呢?这促使我们进一步探讨可能影响乙酸盐作用的各种因素。
不同模型和条件下乙酸盐的差异
模型差异
Perry 等人使用大鼠进行研究,而其他关于乙酸盐和肥胖或代谢综合征的研究大多使用小鼠品系,不过大鼠和小鼠的生理机能相似,这一因素不太可能解释所有差异。
方式差异
胃内(进入胃)和口服或结肠乙酸盐之间可能存在差异。正如 Canfora 等人指出的那样,“连续胃内供应的乙酸盐可能会影响胃的 pH 值,从而可能影响胃排空和食物释放、消化和吸收以及激素调节。”
此外,乙酸盐受体的表达在整个胃肠道中并不均匀,不同位置的乙酸盐可能产生不同影响。稍后将讨论一些人体研究,这些研究发现根据乙酸盐的位置存在不同的影响。
剂量差异
正如我们在丁酸盐中看到的那样,SCFA 的剂量非常重要。Perry 等人使用的大剂量乙酸盐可能与肠道微生物群正常产生或在饮食中消耗的乙酸盐水平不符,剂量不同可能导致不同结果。
SCFA 比率差异
在大多数健康人中,SCFA 以 3:1:1 的比例存在,仅通过提供乙酸盐可能扭曲这个比率,导致不同的代谢效应。
那么,超生理剂量的胃内乙酸盐会引起代谢综合征吗?是的。Perry 等人证明了这一点。
但是肠道菌群产生的乙酸是否会导致代谢综合征?可能不是。
我们可以从 Perry 等人的研究中学到什么?
首先,乙酸盐周转受肠道影响,在肥胖时升高。其次,乙酸盐可能确实会激活迷走神经以引起胰岛素分泌,因为将乙酸盐注射到大脑中证实了胃内输注的结果。至少在动物中是这样的。
人类和动物受体对乙酸盐的反应不同?
无论如何,至少有三项研究表明,GPR43 是乙酸盐的主要受体,对小鼠和人类的刺激反应不同:
这只是动物模型无法准确模拟人类生理的常见案例之一,所幸已有相当数量的人体研究关注了乙酸盐。
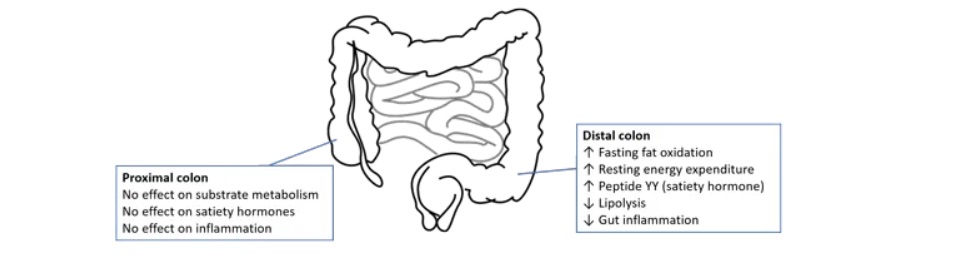
需要进一步的研究来明确阐明乙酸盐在人类中的作用。
关于乙酸盐和代谢综合征的动物研究结果喜忧参半,这可能是由于给药方式、剂量和 SCFA 比率的差异。
乙酸对大脑和免疫系统有益。
人类和动物对乙酸的响应不同 ,因此我们不能依赖动物研究来了解乙酸在人类中的作用。
有限的临床试验似乎表明乙酸对新陈代谢有有益作用。
乙酸盐的位置似乎很重要。在结肠更远端产生的乙酸盐似乎具有最有益的效果。
短链脂肪酸这些看似简单的分子,无疑是解读“微生物-宿主”对话的重要密码。短链脂肪酸研究引领我们重新思考健康的本质——健康并非某种单一指标的最优化,而是复杂生态系统的动态平衡。
正如肠道微生物群的多样性对健康至关重要,短链脂肪酸的种类、比例和浓度的平衡同样重要。未来的健康管理将从单一指标的”正常化”,转向生态系统的”平衡化“。
肠道菌群检测与短链脂肪酸代谢评估将成为个体健康”生态地图”的重要组成部分,谷禾肠道菌群检测报告中也有关于菌群代谢的短链脂肪酸相关指标。
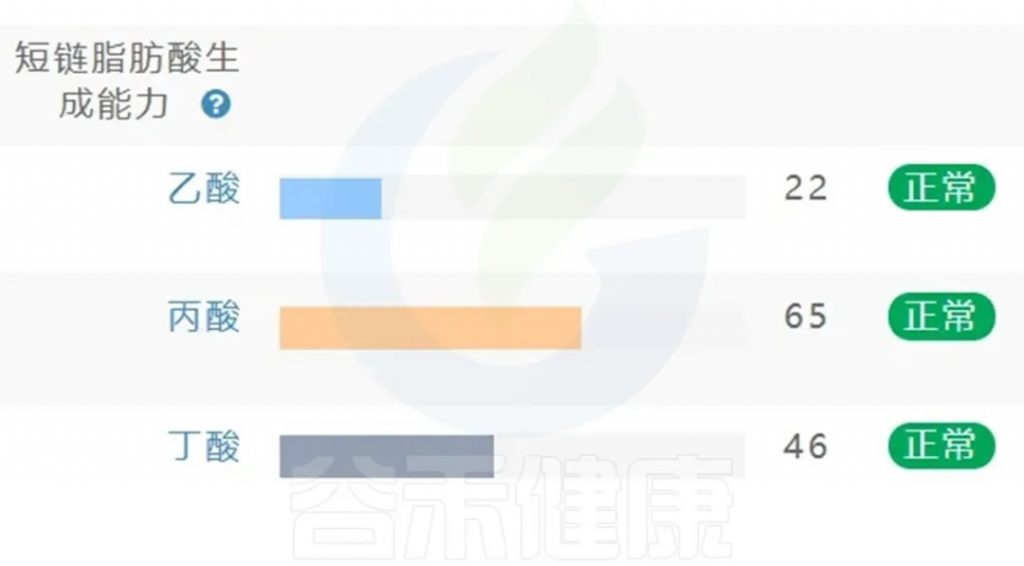
<来源:谷禾肠道菌群检测数据库>
随着对短链脂肪酸双面性理解的加深,未来的干预策略将更加精准和个性化。
针对短链脂肪酸不足的个体,可能会有靶向益生菌组合或特定结构的益生元配方,从小剂量开始逐步增加,避免肠道不适,有利短链脂肪酸的产生。但同时也需要结合其他指标,比如说肠道屏障功能是否正常,这在谷禾肠道菌群检测报告中也有相关指标。在肠道屏障薄弱的情况下,可以考虑优先修复肠道屏障,再补充短链脂肪酸。
而对于那些特定短链脂肪酸过高或对其敏感性增加的人群,可能需要定制化的饮食方案或特异性的益生菌干预,鉴别过度生长菌群比如说梭菌,可能需要优先考虑维持菌群平衡的相关干预策略,例如考虑低FODMAP饮食、减少添加剂摄入等方式,同时补充关键辅助因子如B族维生素、辅酶Q10等支持线粒体能量产生。
通过精准检测和个性化管理,我们可以逐步优化肠道微生态平衡,使短链脂肪酸保持在有利于健康的水平。
在药物开发方面,短链脂肪酸受体调节剂、缓释型短链脂肪酸制剂以及能够在特定肠道环境中释放活性成分的”智能”递送系统,都可能成为下一代肠道健康干预工具。
在日益关注肠道健康的今天,短链脂肪酸研究无疑将成为连接微生物学、营养学、临床医学的重要桥梁。
注:本账号内容仅供学习和交流,不构成任何形式的医疗建议。
主要参考文献
Singh, N. et al. Activation of Gpr109a, receptor for niacin and the commensal metabolite butyrate, suppresses colonic inflammation and carcinogenesis. Immunity 40, 128–139 (2014).
Chang, P. V., Hao, L., Offermanns, S. & Medzhitov, R. The microbial metabolite butyrate regulates intestinal macrophage function via histone deacetylase inhibition. Proc. Natl. Acad. Sci. U. S. A. 111, 2247–2252 (2014).
Zhou, D. et al. Sodium butyrate attenuates high-fat diet-induced steatohepatitis in mice by improving gut microbiota and gastrointestinal barrier. World J. Gastroenterol. 23, 60–75 (2017).
Donohoe, D. R. et al. The Warburg effect dictates the mechanism of butyrate-mediated histone acetylation and cell proliferation. Mol. Cell 48, 612–626 (2012).
Lucy Mailing, PhD., A brief introduction to short-chain fatty acids
Decrypting the butyrate paradox: can excess butyrate be toxic?
Does acetate make you fat? The skinny on acetate and metabolic syndrome
The propionate-autism connection
Sun, J. et al. Clostridium butyricum pretreatment attenuates cerebral ischemia/reperfusion injury in mice via anti-oxidation and anti-apoptosis. Neurosci. Lett. 613, 30–35 (2016).
Li, H. et al. Sodium butyrate exerts neuroprotective effects by restoring the blood-brain barrier in traumatic brain injury mice. Brain Res. 1642, 70–78 (2016).
Sun, J. et al. Antidepressant-like effects of sodium butyrate and its possible mechanisms of action in mice exposed to chronic unpredictable mild stress. Neurosci. Lett. 618, 159–166 (2016).
Kaiko, G. E. et al. The Colonic Crypt Protects Stem Cells from Microbiota-Derived Metabolites. Cell 165, 1708–1720 (2016).
Zhang, Q. et al. Accelerated dysbiosis of gut microbiota during aggravation of DSS-induced colitis by a butyrate-producing bacterium. Sci. Rep. 6, (2016).
Kuo, S.-M., Chan, W.-C. & Hu, Z. Wild-type and IL10-null mice have differential colonic epithelial gene expression responses to dietary supplementation with synbiotic Bifidobacterium animalis subspecies lactis and inulin. J. Nutr. 144, 245–251 (2014).
Machiels, K. et al. A decrease of the butyrate-producing species Roseburia hominis and Faecalibacterium prausnitzii defines dysbiosis in patients with ulcerative colitis. Gut 63, 1275–1283 (2014).
Belcheva, A. et al. Gut microbial metabolism drives transformation of MSH2-deficient colon epithelial cells. Cell 158, 288–299 (2014).
Park, J., Goergen, C. J., HogenEsch, H. & Kim, C. H. Chronically Elevated Levels of Short-Chain Fatty Acids Induce T Cell-Mediated Ureteritis and Hydronephrosis. J. Immunol. Baltim. Md 1950 196, 2388–2400 (2016).
Park, J. et al. Short-chain fatty acids induce both effector and regulatory T cells by suppression of histone deacetylases and regulation of the mTOR-S6K pathway. Mucosal Immunol. 8, 80–93 (2015).
Chambers, E. S. et al. Effects of targeted delivery of propionate to the human colon on appetite regulation, body weight maintenance and adiposity in overweight adults. Gut 64, 1744–1754 (2015).
Asquith, M. et al. Intestinal Metabolites Are Profoundly Altered in the Context of HLA-B27 Expression and Functionally Modulate Disease in a Rat Model of Spondyloarthritis. Arthritis Rheumatol. Hoboken NJ 69, 1984–1995 (2017).
MacFabe, D. F. Enteric short-chain fatty acids: microbial messengers of metabolism, mitochondria, and mind: implications in autism spectrum disorders. Microb. Ecol. Health Dis. 26, 28177 (2015).
Foley, K. A., Ossenkopp, K.-P., Kavaliers, M. & MacFabe, D. F. Pre- and Neonatal Exposure to Lipopolysaccharide or the Enteric Metabolite, Propionic Acid, Alters Development and Behavior in Adolescent Rats in a Sexually Dimorphic Manner. PLOS ONE 9, e87072 (2014).
Finegold, S. M. State of the art; microbiology in health and disease. Intestinal bacterial flora in autism. Anaerobe 17, 367–368 (2011).
Rossignol, D. A. & Frye, R. E. Mitochondrial dysfunction in autism spectrum disorders: a systematic review and meta-analysis. Mol. Psychiatry 17, 290–314 (2012).
Frye, R. E. et al. Modulation of mitochondrial function by the microbiome metabolite propionic acid in autism and control cell lines. Transl. Psychiatry 6, e927 (2016).
Reichardt, N. et al. Phylogenetic distribution of three pathways for propionate production within the human gut microbiota. ISME J. 8, ismej201414 (2014).
Suez, J. et al. Artificial sweeteners induce glucose intolerance by altering the gut microbiota. Nature 514, 181–186 (2014).
Napoli, E., Dueñas, N. & Giulivi, C. Potential Therapeutic Use of the Ketogenic Diet in Autism Spectrum Disorders. Front. Pediatr. 2, (2014).
Fernandes, J., Su, W., Rahat-Rozenbloom, S., Wolever, T. M. S. & Comelli, E. M. Adiposity, gut microbiota and faecal short chain fatty acids are linked in adult humans. Nutr. Diabetes 4, e121 (2014).
Kimura, I. et al. The gut microbiota suppresses insulin-mediated fat accumulation via the short-chain fatty acid receptor GPR43. Nat. Commun. 4, 1829 (2013).
Sahuri-Arisoylu, M. et al. Reprogramming of hepatic fat accumulation and ‘browning’ of adipose tissue by the short-chain fatty acid acetate. Int. J. Obes. 2005 40, 955–963 (2016).
Frost, G. et al. The short-chain fatty acid acetate reduces appetite via a central homeostatic mechanism. Nat. Commun. 5, (2014).
Everard, A. et al. Microbiome of prebiotic-treated mice reveals novel targets involved in host response during obesity. ISME J. 8, 2116–2130 (2014).
Li, G. et al. Intermittent Fasting Promotes White Adipose Browning and Decreases Obesity by Shaping the Gut Microbiota. Cell Metab. 26, 672–685.e4 (2017).
Wu, W. et al. Microbiota metabolite short chain fatty acid acetate promotes intestinal IgA response to microbiota which is mediated by GPR43. Mucosal Immunol. 10, 946–956 (2017).
Long, P. M. et al. Acetate supplementation as a means of inducing glioblastoma stem-like cell growth arrest. J. Cell. Physiol. 230, 1929–1943 (2015).
Trent, C. M. & Blaser, M. J. Microbially Produced Acetate: A ‘Missing Link’ in Understanding Obesity? Cell Metab. 24, 9–10 (2016).
Canfora, E. E. & Blaak, E. E. Acetate: a diet-derived key metabolite in energy metabolism: good or bad in context of obesity and glucose homeostasis? Curr. Opin. Clin. Nutr. Metab. Care 20, 477–483 (2017).
Ang, Z. et al. Human and mouse monocytes display distinct signalling and cytokine profiles upon stimulation with FFAR2/FFAR3 short-chain fatty acid receptor agonists. Sci. Rep. 6, srep34145 (2016).
Canfora, E. E. et al. Colonic infusions of short-chain fatty acid mixtures promote energy metabolism in overweight/obese men: a randomized crossover trial. Sci. Rep. 7, 2360 (2017).

谷禾健康

自闭症谱系障碍 (ASD) 是一种神经发育障碍,其特征是社交沟通和行为障碍,经常伴有兴趣或活动受限和重复的模式。遗传和环境都与自闭症有关。
近年来,多种类型的研究都将肠道菌群与自闭症的病因联系起来。前面我们的文章有提到,肠道微生物群影响宿主健康的许多方面,包括免疫系统控制、肠道激素调节和神经传递。它会改变摄入的药物及其代谢、毒素清除以及多种影响宿主的物质的产生。肠道菌群可以通过“肠-脑轴”的相互关系直接或间接地影响大脑。
近期研究表明,肠道微生物群可以通过中间细胞因子和代谢物诱发神经炎症。炎症偏差是肠道微生物群影响自闭症患者肠脑轴的潜在病因候选者。
神经炎症因素会导致肠道屏障完整性丧失、小胶质细胞激活和神经递质失调,从而导致自闭症。它强调了神经炎症中间体与自闭症患者肠道微生物群改变相关的潜在作用。具体而言,脑源性神经营养因子、钙卫蛋白、S100B、RANTES、嗜酸细胞趋化因子等细胞因子以及一些代谢物和微小RNA已被视为病因生物标志物。
了解肠道和大脑之间的相互作用,微生物群和神经炎症生物标志物的变化,是理解自闭症谱系障碍的病因、诊断、预后和治疗的基础背景。目前,自闭症谱系障碍的诊断是基于临床症状的,这可能会导致延误。基于与肠道微生物群相关的神经炎症过程的生物标志物可能是一种更客观精确可行的自闭症谱系障碍检测方法。
本文我们来详细了解一下神经炎症生物标志物在自闭症谱系障碍的发病机制和潜在诊断试验中的作用,还概述了益生菌及其他营养干预措施用作自闭症儿童的治疗策略及孕妇的饮食建议。
深入了解自闭症的复杂病理机制,结合生物标志物监测、肠道菌群管理和营养干预,或将为受影响的个体及其家庭提供更有针对性的支持和干预措施。
近 20 年前,有人提出了肠道菌群与自闭症之间的潜在关联。尽管自闭症的确切病因尚不完全清楚,但现有文献表明,自闭症患者存在肠道菌群失调和神经炎症。
自闭症的肠道菌群
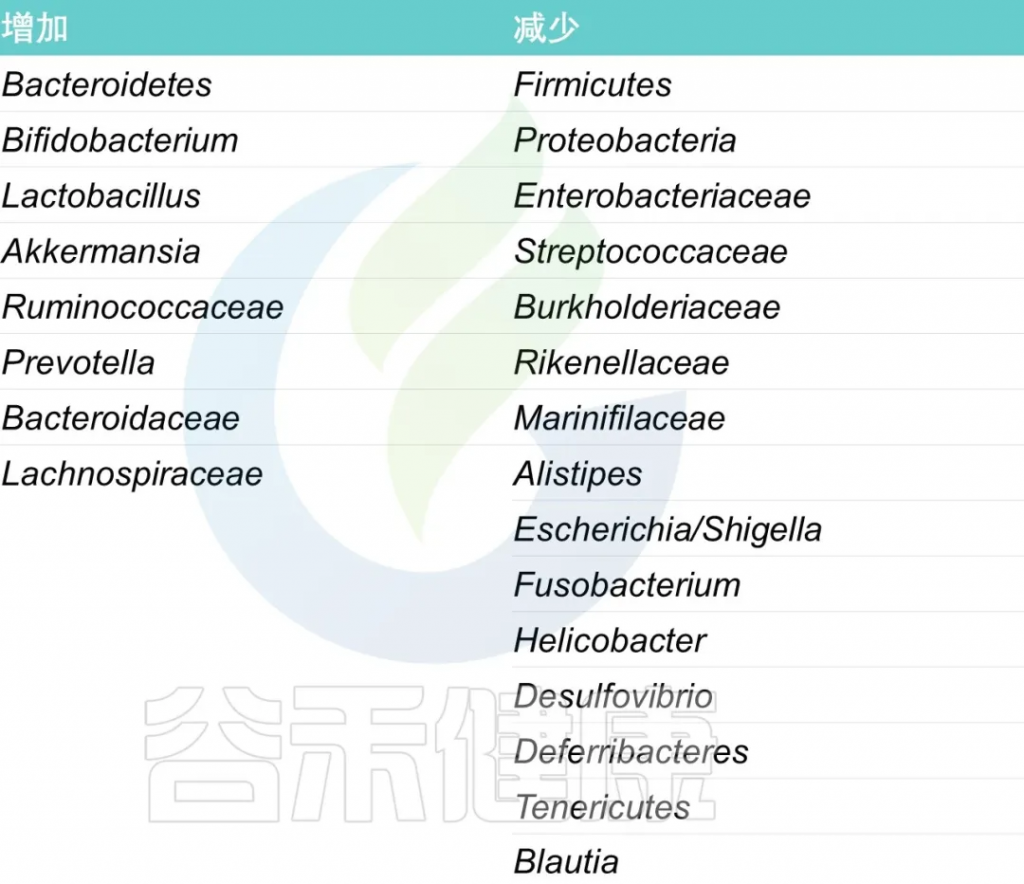
总体而言,自闭症人群表现出菌群失调的迹象,与健康对照组相比,下列菌群和许多其他微生物的丰度有所不同:
拟杆菌门 / 厚壁菌门
普雷沃氏菌
梭菌属
乳杆菌属
双歧杆菌属
粪杆菌属
链球菌属
肠杆菌科
疣微菌属
梭杆菌门
大肠杆菌
肠球菌属
阿克曼菌属
考拉杆菌属
肠道菌群失调的识别与炎症途径
最近也有研究指出,自闭症儿童的肠道菌群失调和炎症可通过宿主粪便 DNA 特异性甲基化来识别。患有菌群失调的自闭症患者的炎症和免疫途径显著丰富,包括IL-2、IL-6 和 IL-12 的产生以及 Toll 样受体 (TLR3) 信号通路的激活。
多项研究一致证实了早期的发现,即菌群失调在各种神经退行性和神经精神疾病中会引起神经炎症。
自闭症儿童微生物组改变的潜在影响

doi.org/10.1016/j.bbr.2024.115177
菌群失调:免疫信号通路中断与自闭症严重程度
NLRP3炎症小体、1型干扰素和NF-κB信号通路等免疫信号通路的中断是菌群失调可能导致的后果之一。Th17/Tregs比例发生改变,巨噬细胞极化、TNF-α、IL-1β、IL-18、IL-6 失衡也是可能的。
另一方面,炎症和免疫失调已被证明与自闭症的发展和/或严重程度有关。先前对自闭症病例的研究表明,TNF-α、干扰素-γ、IL-2、IL-4、IL-5、IL-6、IL-8、IL-17、IL-10 等炎症标志物的水平升高。
神经炎症生物标志物与微生物交替和自闭症行为的关联研究


doi.org/10.1007/s10753-024-02061-y
关于自闭症患者肠道微生物组成和代谢物与炎症,这三个因素之间的确切关系需要进一步研究。总体而言,肠道菌群似乎通过炎症在自闭症中发挥关键作用。
一些研究已将蛋白质和肽类生物标志物作为自闭症早期诊断的研究对象。S100 钙结合蛋白 β 亚基 (S100B) 在星形胶质细胞和其他神经外细胞(包括EGC)中表达。
注:EGC,enteric glial cells,肠神经胶质细胞,EGC是肠神经系统的重要组成部分。它调节肠道稳态、参与维持肠黏膜屏障功能,调控炎症反应,在消化及非消化系统疾病中发挥着重要作用。
S100B对神经元的影响取决于浓度
浓度在几纳摩尔剂量下可产生营养作用,在微摩尔水平下可产生毒性。
S100B 促进神经炎症
细胞外蛋白 S100B 与促炎细胞因子协同作用,在较高浓度下可作为细胞因子,从而显著促进神经炎症。
自闭症 S100B 显著升高
尽管存在争议,但多项研究发现与健康人相比,自闭症患者的 S100B 显著升高,支持该因素在 ASD 的病因和发展中可能发挥的作用。
外周 S100B 浓度升高的来源可能是受损的神经元或 EGC。
在最近的一项研究中,血浆 S100B 水平与粪便钙卫蛋白浓度(胃肠道炎症状态的客观标志物)之间的相关性表明,不仅脑星形胶质细胞,还有 EGC 也可能参与自闭症的病理生理学。
肠道微生物群与S100B的相互作用
有一种假说认为,自闭症患者肠道胶质细胞衍生的 S100B 表达的改变可能是由微生物群改变、肠道屏障破坏甚至致病菌引起的,这些因素共同诱发肠道炎症并将 EGC 转化为反应性 EGC。
另一项小鼠体内研究表明,肠道微生物群的多样性随着 S100B 水平或口服给药而增加。
厚壁菌门(包括乳杆菌)和拟杆菌门(包括Barnesiella和丁酸杆菌属)均受 S100B 水平的影响。然而,在一组自闭症儿童中观察到拟杆菌门水平较高,而厚壁菌门水平较低。可以考虑研究 S100B 作为自闭症诊断和治疗中的潜在生物标志物。
BDNF(脑源性神经营养因子) 是神经生长因子家族(神经营养因子)的蛋白质成员。BDNF 在突触前位点(调节神经递质释放)和突触后位点(增强离子通道功能)中都发挥着关键作用,因此它通常会影响神经可塑性,从而影响行为相关疾病。
BDNF与自闭症病理生理学的关联
多种神经系统疾病都存在 BDNF 水平异常,包括精神分裂症、抑郁症甚至自闭症。最近的研究显示,与对照组相比,自闭症患者的 BDNF 水平发生了改变,这表明 BDNF 可能在自闭症病理生理学中发挥作用。
与重度自闭症相比,轻度表型患者的 BDNF 水平相对较高,强调了该因子可能具有保护作用。自闭症患者脑内抗凋亡信号通路中 BDNF 的下调是自闭症病理生理的可能机制之一。
作为神经保护剂的 BDNF 表达减少可能是由炎症因子(包括 IL-1β 和 TNF)升高引起的;因此,它可能在神经炎症中起负调节作用。
肠道菌群与BDNF的相互影响
自闭症患者肠道菌群失调可能通过免疫失调和释放穿过血脑屏障的炎症因子(如 IL-1β)导致这种炎症状态。
还需要进一步研究了解自闭症患者肠道微生物改变的诱导和改变,是否可以通过 BDNF 水平进行监测和控制。
受激活、正常 T 细胞表达和分泌的调节,RANTES(CCL5)和嗜酸细胞趋化因子(CCL11)是由多种细胞释放的促炎趋化因子,包括血细胞、成纤维细胞、内皮细胞、上皮细胞、神经元和神经胶质细胞。
详情展开如下:
RANTES
RANTES是一种重要的趋化因子,属于CC亚家族的β趋化因子。它由多种细胞类型表达和分泌,包括T细胞、单核细胞、NK细胞、上皮细胞和血小板等。
RANTES的主要功能是通过与其特异性受体结合来诱导白细胞向炎症部位迁移,从而在炎症反应中起关键作用。
这些受体包括CCR1、CCR3、CCR4和CCR5。RANTES不仅能够促进T细胞的活化和增殖,还能调节Th1/Th2细胞效应平衡。
嗜酸细胞趋化因子
嗜酸细胞趋化因子是一类属于CC趋化因子家族的小细胞因子,主要作用是选择性地募集嗜酸性粒细胞。
这些因子在多种组织中表达,并通过与特定受体结合来诱导嗜酸性粒细胞向特定位置迁移。主要包括CCL11、CCL24和CCL26。
不仅在过敏性疾病如哮喘和过敏性鼻炎中发挥重要作用,还参与了其他炎症反应和肿瘤的发展。
RANTES和嗜酸细胞趋化因子在自闭症中的神经炎症作用
自闭症儿童的血浆中 RANTES和嗜酸细胞趋化因子水平明显较高。由于RANTES和嗜酸细胞趋化因子充当促炎介质,它们的升高意味着两者都在 自闭症中发挥神经炎症作用。
尽管Shen等人报告 RANTES 或嗜酸细胞趋化因子与自闭症的行为模式之间没有显著相关性,但Han 等人和 Hu 等人分别发现 RANTES 和嗜酸细胞活化趋化因子与自闭症相关。此外,其他研究表明这两个因素的增加都与自闭症相关。
肠道菌群诱导RANTES介导的炎症
早期研究发现,NOD 样受体家族含有吡啶结构域的 6-肠道菌群轴以及随后的 IL-6 和 TNF 释放是肠道菌群失调与 RANTES 介导的免疫失调之间的可能联系。
关于基因编码的表达,已发现肠道菌群可以操纵嗜酸细胞活化趋化因子的表达水平。在这方面,接受抗生素治疗的小鼠的微生物组发生了改变,嗜酸细胞活化趋化因子升高,小胶质细胞结构不同。
小胶质细胞是中枢神经系统中的常驻免疫细胞,是抵御病原体和损伤的第一道防线。它们不断探测大脑环境,寻找感染、损伤或疾病的迹象。小胶质细胞对全身炎症信号特别敏感。TNF-α和IL-6等促炎细胞因子水平升高可激活小胶质细胞,使其从静息状态转变为活化状态。
激活的小胶质细胞可以吞噬细胞碎片、死细胞和病原体,并释放细胞因子和趋化因子来协调免疫反应。它们在中枢神经系统中发挥双重作用:促进炎症以抵御威胁,并在威胁过去后促进组织修复和炎症消退。慢性小胶质细胞活化与神经炎症有关。
粪菌移植与行为改善
此外,研究发现,小鼠的嗜酸细胞活化趋化因子水平在粪菌移植后发生了变化。关于肠道微生物群与自闭症的关系,在自闭症小鼠中,通过肠道微生物群移植,研究人员观察到焦虑样行为和重复性行为得到改善,而 RANTES 和嗜酸细胞活化趋化因子的水平得到改善。
这些结果表明,RANTES 和嗜酸细胞活化趋化因子在中枢神经系统突触传递和发育中起着重要作用,它们的水平与小鼠的微生物群结构有关。
特定菌群与趋化因子水平呈负相关
研究发现,梭菌科、丹毒丝菌科、普氏菌科、CandidatusArthromitus、变形杆菌属与 RANTES 和嗜酸细胞活化趋化因子的水平呈负相关。
通过益生菌改善
体内外用和口服益生菌治疗已报告与RANTES有关的菌株,包括副干酪乳杆菌SGL04、植物乳杆菌SGL07、发酵乳杆菌SGL10、短乳杆菌 SGL12裂解物以及鼠李糖乳杆菌GG有关。
同样,含有嗜酸乳杆菌、鼠李糖乳杆菌 GG和双歧杆菌的益生菌也改变了动物体内嗜酸细胞活化趋化因子基因的表达。
总的来说,这些研究的重要发现表明肠道菌群通过 RANTES和嗜酸细胞活化趋化因子的炎症因子在自闭症发病机制和严重程度中的潜在机制。
细胞因子粒细胞-巨噬细胞集落刺激因子 (GM-CSF) 驱动髓系造血细胞生物学的许多方面,包括存活、增殖、分化和功能活动。它还通过树突状细胞和 T 细胞功能影响免疫系统。GM-CSF 可引发中枢神经系统慢性炎症,并作为神经元生长因子刺激神经元和神经胶质细胞分化。
GM-CSF在自闭症中的复杂作用
一些早期研究认为自闭症患者的 GM-CSF 水平较低,但随后的研究在自闭症患者大脑中发现 GM-CSF 水平较高。
研究发现,在同时出现胃肠道症状的自闭症儿童中,GM-CSF-IL-1α、TNF-α 和干扰素-α 的水平较高。自闭症中 GM-CSF 水平的变化可能表明炎症过程可能与发育和神经免疫障碍有关。
Takada 等人的共培养实验结果首次表明,GM-CSF 诱导的巨噬细胞可抑制自闭症个体神经元的树突状生长。这种现象是通过促炎细胞因子IL-1α和TNF-α的分泌介导的,并可能导致更严重的行为影响。
肠道菌群与GM-CSF的关联
有趣的是,GM-CSF 水平随着肠道菌群的变化而变化,且主要与 IL-17a有关,IL-17a 是一种与 自闭症患者行为症状严重程度相关的细胞因子。
不同种类的肠道细菌与 GM-CSF 有关,包括副拟杆菌、普氏菌、链球菌、梭菌、罗伊氏乳杆菌、卷曲乳杆菌、粪肠球菌、布劳特氏菌、丁酸单胞菌、罗斯氏菌、Anaerotruncus、Blautia。一项重要发现表明,肠道菌群代谢物(如短链脂肪酸)可能会改变 GM-CSF 水平。
一项研究表明,使用含有长双歧杆菌、保加利亚乳杆菌和嗜热链球菌的益生菌可增加神经免疫因子 GM-CSF。
总之,肠道菌群改变导致 GM-CSF 神经炎症因子的变化,为了解自闭症患者发病机制提供了思路。
高迁移率族蛋白 1 (HMGB-1) 是 HMGB 蛋白家族中最丰富的成员之一,具有许多潜在作用。作为核蛋白,它在DNA调控活动中起关键作用。作为一种细胞外因子,它在免疫细胞对炎症作出反应时主动释放,也会被坏死或受损细胞被动释放。
HMGB-1的多功能性和在炎症中的作用
HMGB1 具有多种膜受体,称为病原体识别受体,其中 TLR4、TLR9 和晚期糖基化终产物受体 (RAGE) 是主要受体。通过与这些受体的相互作用,HMGB1可促进细胞炎症。HMGB1 可以穿过血脑屏障,促进神经突生长和细胞迁移,或介导损伤后的神经炎症。
HMGB-1与自闭症严重程度的相关性
已知自闭症患者血浆中的HMGB-1水平会升高,并且与自闭症的严重程度呈正相关。
另一种有效的炎症分子——表皮生长因子受体与自闭症儿童的症状严重程度有关,而 HMGB1 水平与之相关。
肠道功能障碍与HMGB-1水平的联系
研究发现,自闭症患者的 HMGB1 水平较高与胃肠道功能障碍较高有关,这可能意味着肠道是发病机制的一部分。
类似的研究表明,粪便中的HMGB1水平与自闭症儿童的胃肠道体征严重程度相关,这与自闭症相关的菌群失调有关。伴有肠道炎症的微生物群失调可导致单核细胞的激活,上调 HMGB1 的排泄,从而形成促炎反馈回路。
扩展阅读:炎症回路和肠道微生物
HMGB-1与自闭症行为表现的关联
较高水平的 HMGB1 和 TLR4 也与小鼠的自闭症样行为有关,可能是通过激活 HMGB1/TLR4 信号级联实现的。
自闭症儿童血清中 TLR4 水平升高,并且与他们的多动评分呈正相关。这进一步强调了炎症因子在自闭症行为表现中的作用。
HMGB-1在神经炎症中的作用机制
HMGB1/RAGE/TLR4 轴的激活会导致白细胞浸润到神经细胞中,从而引起持续的中枢神经系统炎症。有研究表明,神经炎症与自闭症的发生密切相关,其机制是激活炎症小体系统。此外,HMGB1 可以与内源性分泌性 RAGE 结合,导致血浆 RAGE 水平下降。这可能通过干扰神经肽催产素从外周到大脑的运输,导致自闭症的病理生理。
益生菌和肠道菌群改变对自闭症患者 HMGB1 水平的影响可以强化这一想法,并可以进一步研究。HMGB1 可能通过神经炎症在自闭症发病机制中发挥关键作用,并可以指导治疗策略。然而,它是自闭症病理生理学中一个非常潜在的因素,尚未明确阐明,需要更多研究。
骨桥蛋白 (OPN) 是一种可溶性促炎细胞因子,在自身免疫性神经炎性疾病中发挥着明确的作用,同时也是控制骨组织生物矿化的非胶原骨基质的组成部分。
OPN的功能多样,根据其位置和环境,OPN 参与局部炎症、细胞粘附、免疫反应、趋化性和防止细胞凋亡。
OPN在免疫调节中的作用
Heilmann 等人认为 OPN 可以在急性炎症期间激活免疫系统、减少组织损伤并刺激粘膜修复,同时在慢性情况下促进 Th1 反应并增强炎症。
OPN与神经系统疾病的关系
OPN 与多发性硬化症和阿尔茨海默病等神经心理疾病的发病机制有关。CD11c + 细胞表达分泌性磷蛋白1 及其编码蛋白 OPN 与阿尔茨海默病的认知障碍和常见神经病变有关。
注:CD11c+ 是一种在多种免疫细胞上表达的分子,主要与树突状细胞(DCs)相关。CD11c+ 标记物在免疫系统中具有重要的生物学功能。例如,在炎症性关节炎模型中,CD11c+ 树突状细胞的存在与疾病的严重程度呈负相关。
OPN在自闭症研究中的发现
有研究发现血清中 OPN 水平升高与病情严重程度有关,表明 OPN 在神经炎症和大脑特异性自身抗体的产生中的作用。他们的发现可以支持 OPN 是自闭症机制中重要神经炎症因子的观点。
在代谢紊乱中,人们讨论了 OPN 与肠道微生物群之间可能存在的相互作用。然而,OPN 与肠道微生物群在神经系统疾病(尤其是自闭症患者)中的作用尚未得到研究,这可能是未来研究的一个潜在目标。
钙卫蛋白是一种与钙结合的蛋白质,主要存在于中性粒细胞中,中性粒细胞是一种白细胞,在炎症和细胞损伤时会增加。
粪便中的钙卫蛋白可以指示肠道炎症,并可作为生物标志物。
钙卫蛋白与自闭症
考虑到肠道炎症在自闭症发展中可能发挥的作用,许多研究已经研究了自闭症患者中钙卫蛋白水平的关联,但结果并不一致。
一些报告显示,自闭症患者及其亲属的钙卫蛋白水平可能高于对照组。
钙卫蛋白与炎症及自闭症的关联
钙卫蛋白水平也与巨噬细胞炎症蛋白 1β 的较高表达呈中等相关性,而巨噬细胞炎症蛋白 1β 与自闭症诊断观察计划的沟通分量表和总分相关,表明它可能在微生物-神经元串扰中发挥作用。不太可能的是,一些研究发现自闭症患者和对照组之间的钙卫蛋白水平没有统计学上显著差异,因此,有和没有胃肠道症状的自闭症患者的钙卫蛋白水平没有明显变化。
钙卫蛋白水平与肠道菌群的关系
Laghi 等人的研究表明,钙卫蛋白水平较高与肠道中普雷沃氏菌较多和阿克曼氏菌减少有关,表明这些细菌可能分别具有炎症或保护作用。
益生菌疗法对自闭症患者的影响
Santocchi 等人发现益生菌疗法(包括 多种链球菌、双歧杆菌、乳杆菌)对自闭症患者的适应功能有有利影响,但对有或无胃肠道症状的钙卫蛋白水平没有明显影响。这表明益生菌对自闭症患者的影响比减少肠道炎症更为复杂,钙卫蛋白作为可能的神经炎症介质的作用应得到进一步研究。
总体而言,钙卫蛋白研究的异质性可能是由于试验个体的多样性、所用方法的准确性以及对微生物群改变和钙卫蛋白的同时研究不足造成的。但我们仍然可理解宿主微生物群失调和炎症诱导的钙卫蛋白会触发导致自闭症方面的神经炎症机制。
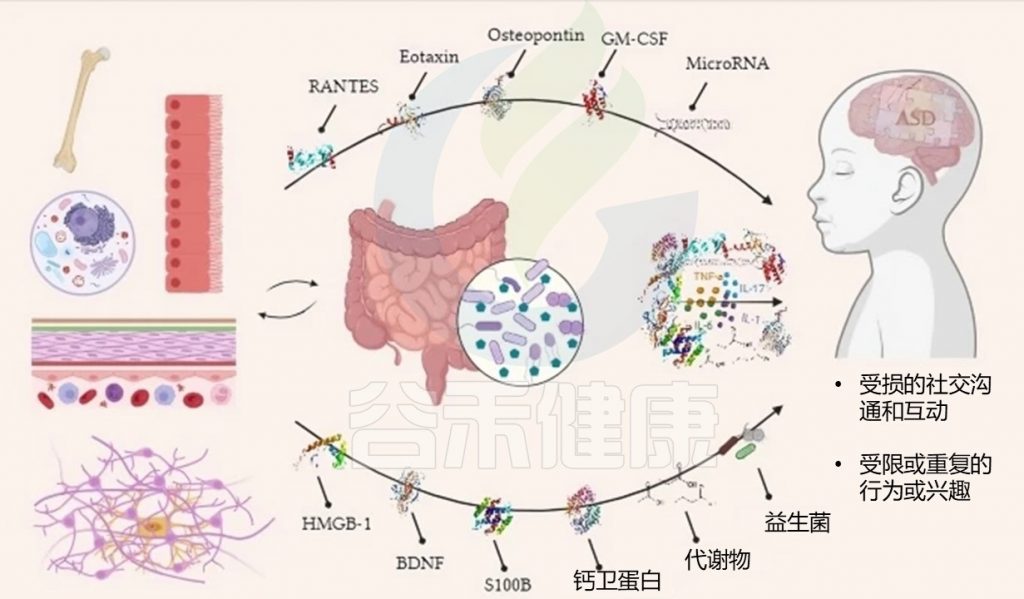
doi.org/10.1007/s10753-024-02061-y
在自闭症患者中,许多肠道微生物衍生的代谢物尤为突出,例如复合多糖或代谢氨基酸,它们可以作为神经递质。其中几种代谢物最近被讨论作为自闭症的早期诊断生物标志物。
特定菌群与短链脂肪酸的生产
肠道微生物通过一组重要的代谢物来调节宿主的生理机能,这些代谢物是短链脂肪酸,主要构成乙酸盐 (AA)、丁酸盐 (BTA) 、丙酸盐 (PPA)。
自闭症患者短链脂肪酸研究不一致
与某些研究不同,其他研究报告称自闭症患者的 乙酸盐、丙酸盐和丁酸盐水平高于对照组。这些肠道菌群相关的短链脂肪酸在宿主的炎症反应中表现出相互冲突的促炎和抗炎作用,可能是由于结合受体和局部浓度的差异。一些动物研究表明,补充微生物代谢物乙酸盐和丁酸盐可以逆转社会行为表型。
相反,在大鼠脑室内注射丙酸盐会诱发自闭症样症状,包括反应性神经胶质增生。丙酸盐可通过调节自闭症中的 PTEN/AKT 通路导致神经胶质增生、神经回路紊乱和神经炎症反应。
短链脂肪酸在自闭症和肠道微生物群中的意义

doi.org/10.1016/j.bbr.2024.115177
由于关于自闭症患者短链脂肪酸水平的发现数据不一致且尚待研究,因此需要进一步研究来验证短链脂肪酸在自闭症病理生理学中的潜在作用。它们可能被视为自闭症患者神经炎症生物标志物和肠道微生物群改变的指标。
COX1 和 COX2
脂质是大脑的主要成分,脂质代谢物是大脑发育和体内平衡的调节分子。作为脂质介质的主要脂质代谢物是前列腺素 (PG) 和白三烯 (LT),它们分别由花生四烯酸 (AA) 和其他不饱和脂肪酸在环氧合酶 (COX) 和脂氧合酶 (LOX) 的代谢下代谢。
已知 PGE2 信号在大脑形态形成中发挥作用,COX2/PEG2 信号受损与 MIA 模型中的自闭症发病机制有关。COX 通路涉及两种限速酶,COX-1 和 COX-2。
用于诱导 MIA 的内毒素和 MIA 模型中产生的炎症介质(IL-1β、IL-6、TNF-α、IFN、AA)均可诱导 COX-2。此外,有证据表明 COX-2 介导 N-甲基-D 天冬氨酸 (NMDA) 神经毒性。
COX2 和 自闭症
先前的研究使用自闭症患者的外周血单核细胞作为小胶质细胞的替代品,观察到在先天免疫刺激下上述细胞因子的产生增加。这种增加发生在有微生物感染后行为症状和认知功能波动史的自闭症患者中。有趣的是,自闭症患者血浆中的 COX-2 和 PGE2 升高,同时 α-突触核蛋白水平降低。因此,阻断 COX-2 可能有助于减轻自闭症患者的神经炎症和随后的神经元损伤。另一方面,脑中 COX-2 的上调可能具有神经保护作用,部分调节脑血流。
关于 COX-2 抑制剂在 ASD 患者中的临床试验数据很少。只有一项随机、双盲、安慰剂对照试验研究了 COX-2 抑制剂塞来昔布对 ASD 患者行为症状的疗效。
该试验将塞来昔布作为利培酮的辅助治疗,持续 10 周;使用异常行为检查表 (ABC) 评估行为症状。发现ABC分量表的易怒、嗜睡和刻板行为有显著改善。
当使用塞来昔布控制病毒性流感等综合征引起的 自闭症行为症状恶化时,也经常观察到 COX2 抑制剂塞来昔布减轻行为症状。吡格列酮具有多种抗炎作用,包括抑制小胶质细胞上 COX-2 的表达。吡格列酮对创伤性脑损伤有有益作用。
综上所述,COX-2抑制剂可能对有COX2激活迹象的自闭症患者有益,尤其是在急性和/或亚急性期。
自闭症患者中犬尿氨酸代谢产物的变化
例如,自闭症的患者尿液中神经毒性色氨酸代谢物的浓度增加。有报道称,自闭症患者中犬尿氨酸代谢物的靶分子 NMDAR 亚基的多态性 ,以及其他色氨酸代谢物的水平改变。
据报道,大约三分之一的自闭症患者具有高循环 5-HT 水平,这主要反映了肠道产生并储存在血小板中的 5-HT。5-HT 水平的变化可能与肠道 5-HT 代谢的变化和/或肝脏和肺部 5-HT 清除率的变化有关。然而,高血清素血症和特征性 ASD 行为症状之间的关联尚未得到一致证实。
同样,抑制 5-羟色胺再摄取转运蛋白 (SERT) 作用的选择性 5-羟色胺再摄取抑制剂 (SSRI) 对 自闭症患者并没有普遍有益的作用。这些发现表明,其中存在复杂的潜在机制。
有趣的是,对主要致病成分和生物内表型(包括血液中 5-羟色胺水平)的分析发现,与自闭症患者的免疫功能障碍有关。在同一研究人群中,免疫成分对表型变异的贡献最大;这些结果支持免疫激活对自闭症受试者血清素代谢的影响。
色氨酸影响大脑功能的 4 种不同途径
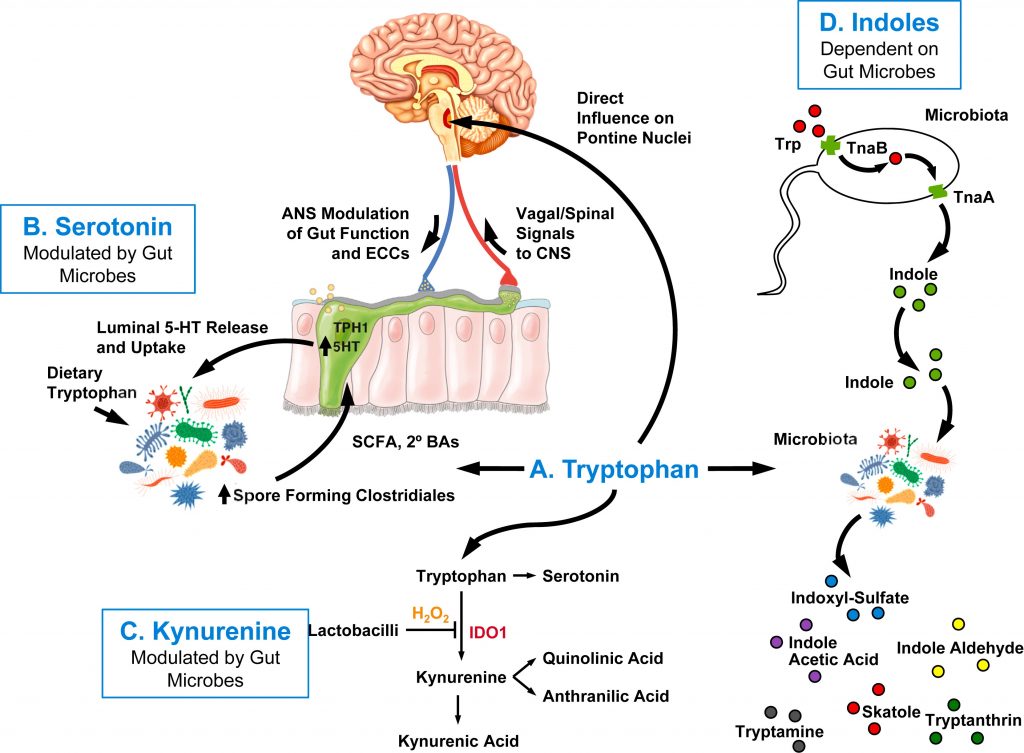
doi.org/10.1016/j.biopsych.2023.10.018
色氨酸[A]、血清素[B] 、犬尿氨酸[C]、吲哚[D]。其中三种途径依赖于肠道微生物代谢,而另一种途径中,色氨酸通过体循环到达缝核,无需微生物修饰。
自闭症与血清素代谢物研究的总结
SERT多态性与自闭症
米诺环素对色氨酸代谢的影响
当色氨酸代谢物的复杂稳态受损时,米诺环素可能对特定情况有效,从而导致犬尿氨酸代谢物的毒性作用恶化。将米诺环素用作自闭症患者的治疗选择需要谨慎选择自闭症患者。
miRNA 在神经系统中的作用
超过 60% 的人类基因受微小 RNA (miRNA) 控制,微小 RNA 是一种小型非编码 RNA,长度约为 18 到 24 个核苷酸,可作为表观遗传调控因子。miRNA 可改变大脑的可塑性和神经元的发育,其失调会导致多种神经系统疾病,包括自闭症。miRNA 已充分证实其可调控多种细胞和生理过程,包括造血、免疫反应、炎症。此外,miRNA 还受宿主-微生物群相互作用的影响,并在菌群失调和诱发炎症中发挥关键作用。
miR-146a 是自闭症中失调最严重的miRNA
一项深入研究发现,自闭症患者中存在过度表达的 miRNA,它们可能通过失调的炎症基因在神经发育受损中发挥作用。
此外,一些研究还发现,miRNA 通过与调节炎症小体表达的 3′-UTR 基因相互作用直接或间接激活炎症小体。具体而言,动物研究表明 miR-146a 的增加或减少可能是自闭症的潜在原因。
一项产后临床研究比较了自闭症和健康对照者的 miRNA,证实 miR-146a 是自闭症中失调最严重的 miRNA。
miR-146a 和 miR-155 在自闭症中的作用
另一项使用体外模型和死后人脑组织的研究也发现,早在儿童时期即可在自闭症患者脑中检测到 miR-146a 过表达。肠道菌群-宿主相互作用的变化可能诱导 miR-146a,从而促进神经炎症途径。值得注意的是,miR-146a 诱导的核因子 κB 增强了肠-脑轴的炎症信号通路。
研究表明,脆弱拟杆菌、鼠李糖乳杆菌 GG、嗜酸乳杆菌、保加利亚乳杆菌和大肠杆菌Nissle 1917与 miR-146a 表达相关。
另一项研究表明,miR-146a 对某些炎症细胞因子表达至关重要,其在大脑中的缺失会导致 miR-155整体补偿性上调。蛋白质羰基化增强和半胱氨酸硫醇水平降低是氧化应激介质激增导致神经炎症通量升高的额外指标。
miR-146a和miR-155如何与慢性炎症相关?
多项研究已将 miR-146a 和 miR-155 与慢性炎症所指的各种病理状况联系起来。一种可能的解释是,肠道毒素(如 LPS)能够穿过血脑屏障并进入体循环,可能激活 NF-kB-miRNA-146a-miRNA-155 信号通路。该通路会将来自微生物组的致病信号传递到大脑,这可能会扰乱先天免疫反应并导致神经炎症。
肠道菌群失调也可能改变 miR-155
一项研究增加了证据表明,自闭症儿童的杏仁核、额叶皮质和小脑中的 miR-155 表达增加。miRNA-155 参与细菌脂多糖对 TLR 的激活、肿瘤坏死因子-α 和 IL-6 的激活以及对树突状细胞上细胞因子信号传导抑制因子 1 的调节。这些活动,加上微生物群失调的变化,可以使 miRNA-155 成为肠脑轴和自闭症神经炎症机制中的候选角色。
早期研究发现,发酵乳杆菌、唾液乳杆菌、鼠李糖乳杆菌GG、嗜酸乳杆菌、德氏乳杆菌、双歧杆菌和大肠杆菌 Nissle 1917 等益生菌可以改变 miR-155的水平。
miR-181在自闭症中的潜在影响
研究发现自闭症患者的 miR-181 上调,预计会影响自闭症相关的神经连接蛋白 1基因。神经炎症和免疫失调是与 miR-181 家族相关的众多生理过程中的两种。
另一方面,一些研究表明肠道菌群可以调节小鼠的 miR-181。还有研究显示,鼠李糖乳杆菌和德氏乳杆菌益生菌会影响炎症疾病中 miR-181a 的表达。此外,来自肠道菌群的代谢物可能影响不同状态下的 miR-181表达。总之,这些证据强化了 miR 介导肠道微生物群可能通过自闭症中的神经炎症过程发挥作用的论点。
生酮饮食对miRNA及自闭症的影响
一项小型介入性随访研究,分析七名儿童包括在生酮饮食之前和生酮饮食 4 个月之后收集的血液和粪便样本。经过 4 个月的随访发现,生酮饮食 导致促炎细胞因子(IL-12p70 和 IL-1b)和脑源性神经营养因子 (BDNF) 的血浆水平下降。肠道微生物群的变化、肠道中丁酸激酶表达的增加以及血浆中 BDNF 相关 miRNA 水平的变化。这些队列研究结果表明,生酮饮食可能通过减少炎症、逆转肠道微生物群失调以及影响与大脑活动相关的 BDNF 通路对自闭症社交能力产生积极影响。
生酮饮食诱导的神经炎症变化的拟议间接途径
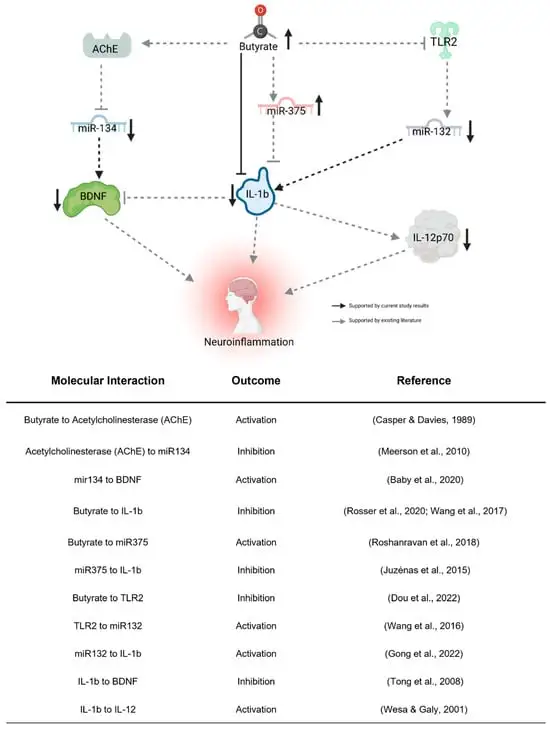
doi.org/10.3390/nu16101401
益生菌可以通过各种机制影响宿主的健康。据最近的研究,它们可以作为治疗工具,通过恢复肠道菌群的健康平衡、调节组织中的神经递质水平以及减少肠道炎症来治疗自闭症。
动物模型显示,益生菌显著改变了大鼠的社交和情感行为以及血液中 IL-6、IL-17a 和 IL-10 等细胞因子的水平。另一方面,只有少数试验从炎症调节和免疫系统调节方面评估了益生菌对自闭症的影响。
益生菌在炎症和自闭症管理中的作用试验

doi.org/10.1007/s10753-024-02061-y
有研究评估了婴儿双歧杆菌与牛初乳产品联合用于自闭症儿童的情况。一些患者出现胃肠道症状和异常行为的频率较低,可能是由于TNF-α和 IL-13 减少所致。
益生菌对自闭症儿童炎症标志物和症状的影响
有研究表明,粪便中TNF-α水平与自闭症严重程度之间存在很强的相关性,表明胃肠道炎症和通透性可能通过炎症途径参与自闭症。他们可以通过补充益生菌(包括乳酸杆菌、双歧杆菌和 链球菌)显著降低自闭症儿童粪便中的TNF-α水平。
在患有胃肠道问题的自闭症儿童亚组中,益生菌治疗组的一些胃肠道症状、适应性功能和感觉状况比安慰剂治疗组有较大改善。
益生菌混合物的应用
目前尚无针对自闭症核心缺陷的药物。因此,迫切需要为自闭症患者开发新的药理学方法。总体而言,这些发现表明益生菌可能是一种有前途的治疗方法,因为它们对自闭症症状有有益的影响。考虑到免疫系统功能障碍与行为异常之间存在关联,以及肠道微生物群可能通过炎症介质对 自闭症产生影响,建议在益生菌给药期间检查神经炎症变量,并确定改变这些变量的最有效配方。
无麸质和无酪蛋白饮食
研究发现,单纯的无麸质饮食对自闭症儿童的症状、行为或智力能力没有显著影响。
当无麸质饮食结合其他干预措施(如维生素、矿物质、必需脂肪酸、肉碱、硫酸镁浴、消化酶和无酪蛋白、无大豆饮食)时,观察到在非言语智力能力和自闭症症状方面有显著改善。
改良的生酮无麸质饮食
一项研究评估了补充MCT的改良生酮无麸质饮食对自闭症症状的影响,为期3个月的干预导致自闭症核心特征显著改善。
低FODMAP饮食
一项实施低FODMAP饮食的研究在自闭症儿童中未发现行为问题的显著差异。
适合自闭症谱系障碍儿童的饮食模式
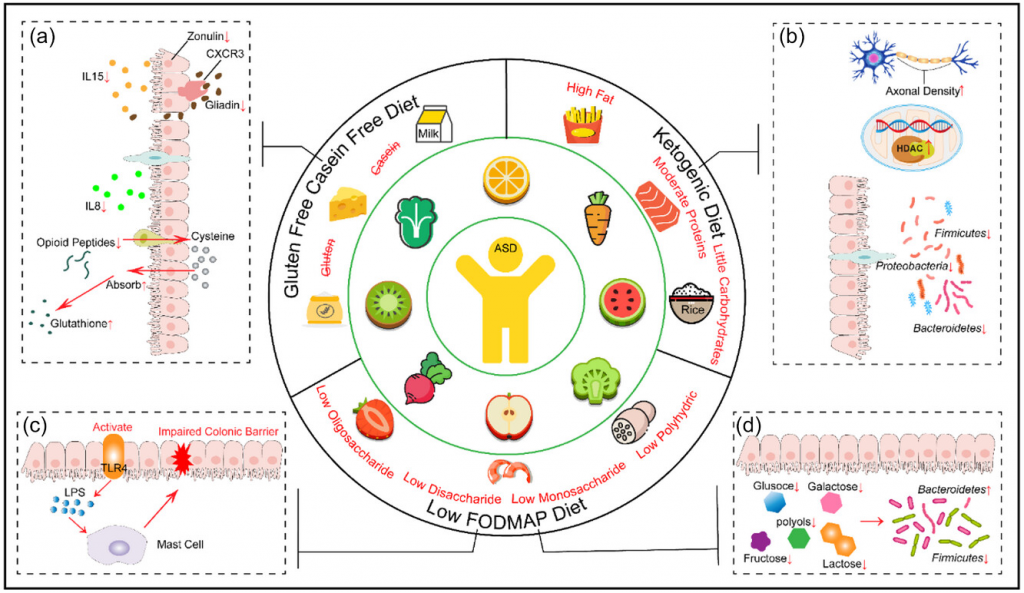
doi.org/10.1002/fft2.380
a)无麸质/无酪蛋白(GFCF)饮食可以使肠黏膜组织正常化,恢复肠上皮细胞对半胱氨酸的吸收,提高谷胱甘肽水平,增加甲基供体,防止甲基化抑制;
b)生酮饮食(KD)可以优化肠道菌群结构,降低厚壁菌门、拟杆菌门和变形菌的丰度,调节组蛋白去乙酰化酶活性,增加脑神经元轴突的密度;
c、d)低发酵寡糖-双糖-单糖-多元醇(FODMAP)饮食可以通过激活toll样受体修复受损的结肠屏障,同时调节肠道菌群以恢复肠道稳态。
必需脂肪酸补充
多项研究调查了ω-3脂肪酸补充对自闭症症状、发展年龄和营养状况的影响。综合分析显示,ω-3脂肪酸补充显著改善了干预组的刻板行为、多动、社交沟通、非言语智力能力、发展和营养状况。
肉碱
肉碱补充在自闭症患者的一年营养计划中显示出改善非言语智力能力和症状的效果。
萝卜硫素
萝卜硫素是一种存在于十字花科蔬菜中的膳食异硫氰酸酯,是一种营养保健食品。几项研究探索了萝卜硫素在自闭症治疗中的潜力,报告显示在行为和生化标志物方面有所改善。
多项研究调查了维生素补充对自闭症患者症状严重程度和生活质量的影响。
维生素A
维生素A补充对自闭症症状有显著缓解作用,特别是通过增加血清中的维生素A水平来改善社交响应性。
维生素D
维生素D补充在减少多动、减轻易怒方面有效,并可能与ω-3联合使用时进一步改善自闭症症状。
矿物质
锌的补充被认为可以增强自闭症患者的认知-运动功能。
肌肽
肌肽补充对自闭症儿童的睡眠障碍有积极作用,但对自闭症症状的严重程度影响不大。
益生元
一项针对 30 名自闭症儿童的为期 6 周的研究表明,益生元干预显著减轻了胃肠道不适并改善了排便,但对睡眠或胃肠道症状没有显著影响。研究发现,韦荣球菌科和双歧杆菌减少,拟杆菌属和普拉梭菌增加。
一项为期 12 周的小规模试点研究针对 8 名患有 自闭症和胃肠道合并症的儿童,发现益生元补充剂可显著减少异常行为(嗜睡、多动、刻板行为和易怒)并改善胃肠道症状,这可能是由于肿瘤坏死因子α 和IL-13 的产生减少所致。

doi.org/10.1016/j.rasd.2024.102352
近期研究表明,孕妇饮食中某些营养素含量高与患自闭症的风险增加有关。
在这些饮食因素中,孕妇饮食中水果和蔬菜上的农药残留可能是导致胎儿神经发育异常的重要暴露因素。
孕妇蛋白质营养不良和高咖啡因摄入量均与胎儿发育受限和后代患自闭症的风险增加有关。
每日盐的摄入量也可能是一个条件性危险因素。具体而言,盐摄入量增加对身体免疫系统和肠道微生物群有显著影响,导致肠道稳态失衡和炎症的发生,进一步通过菌-肠-脑轴导致神经发育异常。
母亲怀孕期间不良的饮食模式会增加后代患自闭症的风险。例如,高能量、高密度饮食和西式饮食均可导致自闭症发病率增加。
与这些不良饮食因素相反,怀孕期间摄入足够的维生素和 omega-3 多不饱和脂肪酸与后代自闭症发病率较低相关。
此外,增加孕妇膳食中的锌含量可以预防与自闭症相关的社交缺陷和焦虑症状。除了避免上述与孕期不良饮食有关的潜在风险因素外,患有糖尿病、肥胖或高血压等潜在风险的孕妇应特别注意每日膳食摄入量。
肥胖孕妇的饮食建议
基于人群的流行病学调查发现,母亲肥胖和怀孕期间体重大幅增加均与后代患自闭症的风险增加有关。
膳食纤维摄入不足会导致肠道中的短链脂肪酸水平异常。高膳食纤维干预和短链脂肪酸疗法可以缓解由此产生的后代的认知和社交功能障碍。高纤维饮食可能减少突触损伤和小胶质细胞缺陷,降低后代神经发育障碍风险。所有母亲无论胖瘦,都应在怀孕期间避免高脂肪饮食,以降低后代患精神疾病的风险。
动物研究表明,母鼠的高脂饮食选择性地促使雄性子代脑内免疫细胞过度消耗5-HT,从而导致神经系统异常。
孕期高脂、高糖饮食可能导致炎症介导的神经发育障碍,增加自闭症风险。肥胖女性在孕期应限制脂肪和糖摄入,增加膳食纤维摄入,以降低后代精神疾病风险。
糖尿病孕妇的饮食建议
众多研究发现母亲孕期患糖尿病与子代罹患自闭症风险增高显著相关。
短暂性高血糖可能引发持续性表观遗传改变和紧密连接蛋白表达抑制,伴随活性氧产生和超氧化物歧化酶(SOD)表达的抑制。动物研究显示,高血糖可诱导子代杏仁核中活性氧产生和SOD表达抑制,诱导自闭症样表型。
母亲糖尿病介导的氧化应激可能导致消化道功能障碍、肠道通透性增加、肠道微生物组成改变和神经元基因表达抑制,最终导致后代出现自闭症表型。母亲糖尿病可能抑制造血干细胞SOD表达、诱导炎性细胞因子,导致子代自闭症患者免疫功能紊乱。
妊娠期糖尿病女性应控制碳水化合物摄入,适量摄入具有抗糖尿病作用的食物,如洋葱和苦瓜。传统植物,如葱属、苦瓜属和荆芥属植物,含有抗糖尿病功效成分,可能有助于控制血糖。
维生素B6和维生素D的补充对降低后代罹患自闭症风险和改善糖尿病相关并发症有益。矿物质如锌和铬有助于保护糖尿病患者免于产生胰岛素抵抗。
妊娠高血压孕妇的饮食建议
妊娠期高血压与后代神经发育障碍和自闭症风险增加有关。
DASH饮食是一种有效的降低血压的饮食干预措施,通过增加粗粮、蔬菜、蛋白质、纤维素、钙和钾的摄入,并限制食盐摄入,可以显著降低血压。高质量的DASH饮食还与降低后代焦虑、行为缺陷和神经发育障碍的风险相关。
补钙和增加膳食钾的摄入也有助于预防妊娠高血压。此外,高血压的发病与肠道菌群有关,通过增加南美油藤的摄入量,可以缓解高血压。
类风湿性关节炎孕妇饮食建议
母亲类风湿性关节炎也与后代患自闭症的风险增加有关,可能通过炎症或免疫机制导致自闭症的发展。目前尚无特定的饮食模式来预防这种风险,但食用具有抗炎症或自身免疫反应的食物,如含有酚类和三萜类化合物的水果和蔬菜,可能是一种潜在的替代方案。
需要进一步研究来探索孕期饮食与菌群和炎症之间的联系,并开发有效的预防策略。
扩展阅读:深度解析 | 炎症,肠道菌群以及抗炎饮食
鉴于自闭症病理生理的复杂性和不明确性,近年来人们对炎症机制和免疫失调的作用进行了研究。自闭症中的失调途径在病因上也可以追溯到肠道微生物群失调。
这些变化可能通过释放的代谢物、BDNF的神经信号通路和神经炎症生物标志物(包括 S100B、HMGB-1、OPN、miRNA、RANTES、嗜酸细胞趋化因子和 GM-CSF)与自闭症症状和严重程度有关。
本文强调了介质作为触发机制和桥梁作用,一方面是肠道微生物群失调引起的炎症,另一方面是自闭症中枢神经系统神经炎症过程。益生菌作为恢复自闭症微生物群的适用治疗选择,表明肠道微生物群的相关性和潜在的有益影响。
然而,考虑到微生物群改变类型、神经炎症介质的巧合、干预时间长度以及自闭症年龄和症状等个体差异,评估个体肠道菌群状况以及不同益生菌及其他配方的功效对于自闭症的干预至关重要。
随着对微生物群与自闭症关系的深入理解,一个多维度的临床视角逐渐显现。我们可以通过分析微生物群的变化、相关的代谢产物、神经炎症介质以及它们与自闭症患者中枢神经系统的相互作用,在临床上描绘出自闭症的发展轨迹,这些研究的整合可能有助于我们构建一个综合的框架,用于自闭症的早期识别、干预和长期管理。
主要参考文献
Zarimeidani F, Rahmati R, Mostafavi M, Darvishi M, Khodadadi S, Mohammadi M, Shamlou F, Bakhtiyari S, Alipourfard I. Gut Microbiota and Autism Spectrum Disorder: A Neuroinflammatory Mediated Mechanism of Pathogenesis? Inflammation. 2024 Aug 2.
Yu R, Hafeez R, Ibrahim M, Alonazi WB, Li B. The complex interplay between autism spectrum disorder and gut microbiota in children: A comprehensive review. Behav Brain Res. 2024 Aug 2;473:115177.
Allan NP, Yamamoto BY, Kunihiro BP, Nunokawa CKL, Rubas NC, Wells RK, Umeda L, Phankitnirundorn K, Torres A, Peres R, Takahashi E, Maunakea AK. Ketogenic Diet Induced Shifts in the Gut Microbiome Associate with Changes to Inflammatory Cytokines and Brain-Related miRNAs in Children with Autism Spectrum Disorder. Nutrients. 2024 May 7;16(10):1401.
Li, Wentian, et al. “Dietary nutrients that potentially mitigate autism spectrum disorder and dietary recommendations for children and pregnant women.” Food Frontiers 5.3 (2024): 920-946.
Aldegheri, Luana, et al. “Impact of Human Milk Oligosaccharides and Probiotics on Gut Microbiome and Mood in Autism: A Case Report.” Microorganisms 12.8 (2024): 1625.
Ross FC, Mayer DE, Gupta A, Gill CIR, Del Rio D, Cryan JF, Lavelle A, Ross RP, Stanton C, Mayer EA. Existing and Future Strategies to Manipulate the Gut Microbiota With Diet as a Potential Adjuvant Treatment for Psychiatric Disorders. Biol Psychiatry. 2024 Feb 15;95(4):348-360.
Kim J. Autism Spectrum Disorder and Eating Problems: The Imbalance of Gut Microbiota and the Gut-Brain Axis Hypothesis. Soa Chongsonyon Chongsin Uihak. 2024 Jan 1;35(1):51-56.
Camberos-Barraza, J.; Guadrón-Llanos, A.M.; De la Herrán-Arita, A.K. The Gut Microbiome-Neuroglia Axis: Implications for Brain Health, Inflammation, and Disease. Neuroglia 2024, 5, 254-273.
Jyonouchi H. Autism spectrum disorder and a possible role of anti-inflammatory treatments: experience in the pediatric allergy/immunology clinic. Front Psychiatry. 2024 Jun 24;15:1333717.
谷禾健康
让食物成为你的药物,让药物成为你的食物
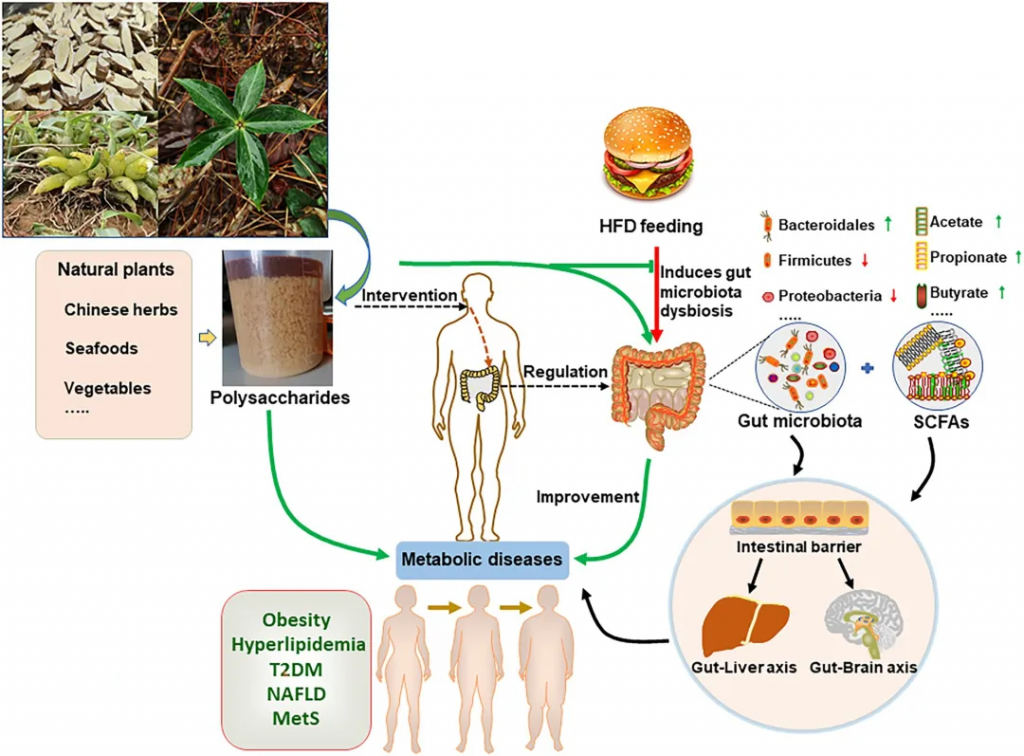
随着现代生活节奏的加快,疲劳、压力、不均衡的饮食,都在悄悄侵蚀着我们的健康。多糖,这些来自植物、真菌乃至海洋生物的天然赠礼,正以其独特的方式,为我们提供了一种全新的健康支持。
多糖由单糖通过糖苷键结合而成的高分子碳水化合物。研究表明,多糖具有多种生物活性,包括调节免疫功能、降低血脂和血糖、抗癌、抗病毒、抗肥胖、抗精神病、抗氧化、抗炎、抗凝血、止吐、抗辐射等作用。因此,多糖已成为最重要的天然成分之一,并引起了世界上越来越多研究者的关注。
虽然部分多糖如淀粉可以在人体胃和小肠中被消化吸收,但仍有许多特殊结构的多糖不能在这两个部位分解。对于那些不能被宿主消化的多糖,它们可以进入结肠,而结肠是大多数肠道菌群居住的地方。在结肠中,多糖可以与肠道菌群相互作用,从而发挥营养或药理作用。
多糖与肠道菌群之间相互作用可以影响健康,同时也通过肠道菌群的代谢作用,转化为有益的代谢产物,如短链脂肪酸,这些产物对维持肠道屏障的完整性、调节免疫反应发挥着至关重要的作用,甚至扩展到了全身的健康状况,可以影响我们的精力水平、情绪状态,对疾病的抵抗力等方方面面。
本文将深入探讨多糖,了解其在人体内的消化过程、与肠道菌群的相互作用,以及它们如何通过调节肠道菌群代谢物影响健康,如短链脂肪酸、三甲胺、色氨酸,还讨论了多糖在疾病预防和治疗中的应用,包括它们在改善代谢性疾病、炎症性肠病、缓解疲劳、改善肿瘤,神经系统疾病等方面的潜在效果。这为靶向肠道菌群开发新型的营养补充剂和药物提供了新的思路。

本文目录
01 多糖
02 多糖调节肠道菌群的组成
为什么多糖可以调节肠道菌群的组成?
多糖促进或抑制肠道微生物群
多糖分子量、糖苷键影响其细菌调节活性
03 肠道微生物将多糖代谢为短链脂肪酸
短链脂肪酸的生物学效应
人体内的多糖代谢
多糖补充与短链脂肪酸的生成
04 多糖调节其他肠道微菌群代谢物
三甲胺和氧化三甲胺(TMAO)
色氨酸及其代谢产物
胆汁酸、脂多糖、胃肠道气体
05 多糖调节肠道菌群修复肠道屏障
06 多糖通过肠道菌群改善疾病
2型糖尿病、非酒精性脂肪肝、肥胖、高血脂症
炎症性肠病、其他肠胃疾病、肿瘤
疲劳、神经系统疾病(认知障碍、抑郁等)
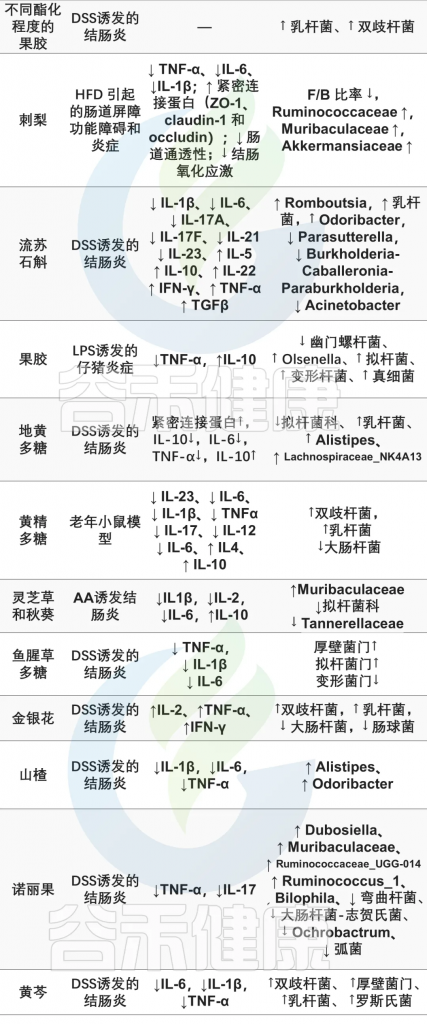
07 部分多糖营养与菌群调节
路易波士茶多糖、地黄多糖、五指毛桃根多糖
大蒜多糖、槐耳多糖、黄芩多糖、枸杞多糖
岩藻多糖、桑叶多糖、沙棘多糖、蘑菇多糖
08 结语
糖,这个小小的分子,是能量的源泉,是细胞的加油站。除了我们熟知的葡萄糖以外,还有一种叫做多糖,由许多糖分子手拉手组成,从植物的根茎到海洋生物的细胞壁,它们以复杂多样的形态存在。
根据糖单元的数量,碳水化合物可分为几类:
多糖是由多个单糖分子通过糖苷键连接而成的聚合物,属于高分子碳水化合物。它们广泛存在于自然界中,包括植物、真菌和海藻等生物体内。根据其来源和结构特性,多糖具有多种生物活性,如免疫调节、抗氧化、抗肿瘤等。
多糖是由10个以上相同或不同的单糖通过α或β糖苷键连接而成的大分子化合物,分子量从几万到数百万。
多糖的空间构象非常复杂,具有一级、二级、三级和四级结构。研究表明,多糖的活性与其结构密切相关。此外,通过分子修饰,如乙酰化、硫酸化、羧甲基化、硒化、磷酸化和磺化等可显著提高多糖的生物活性。
根据来源和结构的不同,多糖可以分为天然多糖和合成多糖,其中天然多糖又可根据其在自然界中的分布分为植物多糖、动物多糖、微生物多糖等。
例如,透明质酸和硫酸软骨素属于动物多糖,而纤维素、淀粉和糖原是常见的植物多糖。
淀粉
由大量葡萄糖分子通过α-1,4-糖苷键和α-1,6-糖苷键连接而成,形成直链淀粉和支链淀粉两种结构。广泛存在于谷物(如大米、小麦、玉米)、薯类(如土豆、红薯)等食物中。在人体消化过程中,被淀粉酶逐步分解为葡萄糖,为身体提供能量。
纤维素
由葡萄糖分子通过β-1,4-糖苷键连接而成,形成长而直的链状结构。是植物细胞壁的主要成分,在蔬菜(如芹菜、菠菜)、水果(如苹果)中含量丰富。由于人体缺乏分解β-1,4-糖苷键的酶,纤维素难以被人体消化吸收,但对促进肠道蠕动、预防便秘等具有重要作用。
果胶
是一种复杂的多糖,由半乳糖醛酸等组成。常见于水果(如柑橘、苹果)中。在食品工业中,常用于制作果酱、果冻等,增加其黏稠度和稳定性。
尽管功能性糖因其在健康和疾病预防中的潜在作用而受到越来越多的关注,但它们的天然可用性相对较小。这意味着,为了充分利用这些有益的分子,需要采用特定的提取方法来增加它们的可获得性,多糖提取常用的方法有热水提取、酸提取、碱提取和酶水解等。
近年来,一些新的方法,如超声波提取、微波提取、超滤、高压电场法、超临界流体萃取、亚临界水萃取等也用于多糖的提取。这些方法不仅能够提高多糖的提取率,还能够在一定程度上保护多糖的结构完整性,从而保留其生物活性。
通常,人体分泌的消化酶只能分解几种多糖,而纤维等许多多糖不能被吸收和直接使用。因此,多糖可以通过小肠进入结肠,这是大多数肠道细菌居住的地方,然后与肠道微生物群相互作用。
细菌在肠道中通过发酵降解多糖
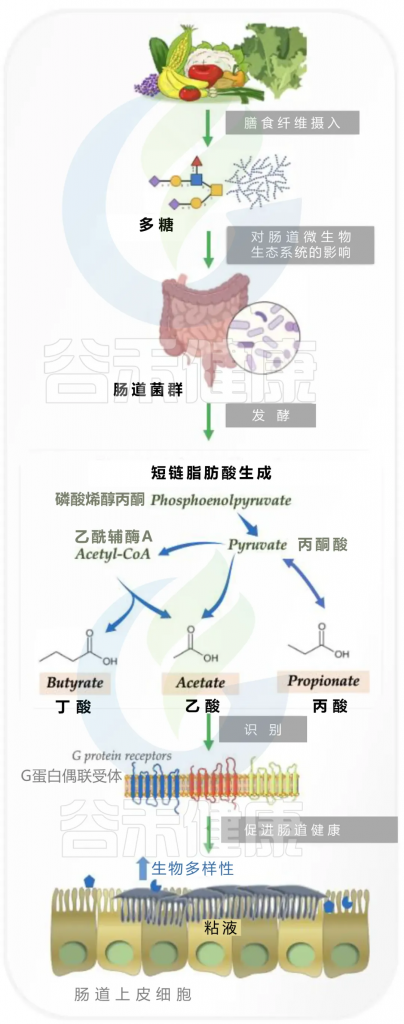
doi.org/10.3390/nu14194116
多糖转化为短链脂肪酸
首先与多糖能够发酵生成酸性的短链脂肪酸密切相关。未电离的短链脂肪酸能够穿过细菌细胞膜,对肠道细菌产生一系列影响,例如改变DNA合成和氨基酸摄取。
短链脂肪酸对肠道细菌的影响
例如,短链脂肪酸能够通过调节侵袭基因的表达,抑制沙门氏菌(一种常见的食源性病原体)的生长。因此,短链脂肪酸的增加可以改变肠道菌群的功能,进而影响其组成。
肠道pH值的变化
短链脂肪酸的增加还会导致肠道pH值下降,影响细菌的适应能力。每种细菌都有其适宜的pH范围,不同细菌在特定pH条件下的适应能力各异。
多糖的降解产物作为能量来源
多糖对肠道菌群组成的调节作用还与其降解产物有关。一些肠道细菌能够利用多糖的降解产物作为碳源和能量来源,而另一些细菌则不能。
综上所述,多糖通过影响肠道菌群的代谢功能,直接调节了肠道菌群的组成。这些发现为我们理解多糖如何通过肠道菌群影响宿主健康提供了新的视角。
多糖的益生元效应
具有选择性刺激有益微生物生长能力的多糖被称为益生元,例如果聚糖,它能丰富乳酸菌和/或双歧杆菌。这些有益细菌的减少与糖耐量受损密切相关。一些多糖能够丰富这些细菌,因此可以用来改善糖尿病表型。
多糖抑制病原菌
病原菌在胃肠道中的定植和增加会导致一系列疾病,而抑制它们可以控制疾病的严重程度。例如,致病性 Sutterella、Desulfovibrionaceae、Streptococcaceae 、Clostridium 的比例较高与肥胖发展呈正相关。
多糖的双向调节作用
疾病的发生是一个复杂的过程,涉及不同的微生物,包括有害细菌和有益细菌。例如:
多糖能够对肠道微生物发挥双向调节作用,即促进有益细菌的同时抑制有害细菌。
例如,口服灰树花多糖(GFHP)对非酒精性脂肪肝病的积极作用与调节肠道菌群有关。
在分子量方面,不同分子量的魔芋葡聚糖(KGM)对2型糖尿病(T2DM)大鼠的降血糖作用研究表明,中等分子量的KGM显著增加了Muribaculaceae,减少了Romboutsia和Klebsiella,但高分子量和低分子量的KGM对这些细菌的影响不显著。
灵芝的低分子量多糖(<10 kDa)具有更好的发酵和更高的产气能力,刺激肠道细菌快速生长。另一方面,高分子量多糖(>100 kDa)更难被肠道细菌发酵,并且在肠道中的停留时间更长,导致对肠道微生物群的影响更长。
高分子量的黄芪多糖具有一定的生物活性,但其相对分子量较大,溶解性差,生物利用度低,限制了其功效的发挥。低分子量的黄芪多糖具有较好的水溶性,能够在更大程度上刺激巨噬细胞摄取中性红、NK细胞增殖,发挥免疫活性。
多糖由各种通过糖苷键连接的单糖组成,糖苷键的类型和位置导致肠道微生物群的选择性发酵存在差异。
多糖的单糖组成越复杂,调节细菌的活性越强
一项关于龙眼多糖和燕麦多糖的研究表明,龙眼多糖能显著促进干酪乳杆菌、嗜酸乳杆菌、植物乳杆菌、粪肠球菌的增殖,但燕麦多糖的作用并不明显。原因是龙眼多糖由葡萄糖、甘露糖和阿拉伯糖组成,而燕麦多糖的单糖主要是葡萄糖。
短链脂肪酸(SCFA)是一组含有少于六个碳的脂肪酸,包括甲酸盐、乙酸盐、丙酸盐、丁酸盐、戊酸盐。
乙酸盐、丙酸盐和丁酸盐是肠道中的主要SCFA,约占所有SCFA的95%,三者的比例约为3:1:1。
作为肠道微生物群和宿主的重要能量来源,短链脂肪酸通过不同的作用模式在健康和疾病中发挥着重要作用。
作用机制
与GPRs的相互作用
抗炎作用
免疫调节
HDAC抑制作用
丁酸盐的作用
与疾病的关系
多糖对SCFA的调节及其对靶标的影响
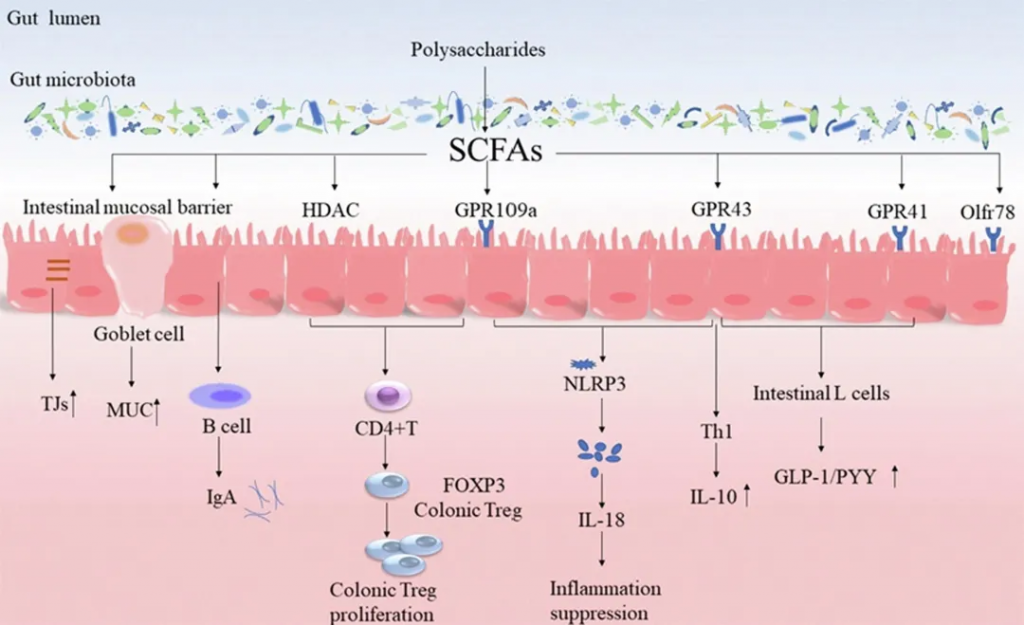
doi.org/10.1016/j.foodres.2022.111653
人体内消化酶的局限
在人体消化系统中,我们自身分泌的消化酶往往难以分解复杂的多糖。这些多糖分子,因其结构复杂,通常在我们体内无法被有效代谢。
肠道菌群的代谢作用
我们的肠道菌群拥有破解这些复杂多糖的秘密武器——一系列的酶,统称为碳水化合物酶(CAZymes)。这些酶能够分解多糖,将其转化为对人体健康有益的短链脂肪酸。
碳水化合物酶的种类
肠道菌群中的“专家”与“通才”
在肠道菌群中,拟杆菌门和厚壁菌门是编码CAZymes的两大主力。
多糖的初步降解
在属的水平上,多糖最初可以由某些微生物降解,例如双歧杆菌属、真杆菌属、梭菌属、罗氏菌属(Roseburia spp.)。
SCFAs的生成途径
尽管人体自身无法分解复杂的多糖,但我们的肠道菌群却具备了这一能力,它们通过一系列特殊的酶,将多糖转化为对人体健康有益的短链脂肪酸。
多糖对SCFAs生成的促进作用
饮食补充多糖可以为产生SCFAs的细菌提供有利的生长环境,从而促进SCFAs的生成。例如,沙棘多糖(CCPP)通过调节肠道菌群和SCFAs,能够缓解2型糖尿病。
沙棘多糖调节肠道菌群和SCFAs,缓解2型糖尿病
枸杞多糖调节肠道菌群,提高SCFAs
多糖结构对短链脂肪酸生成的影响
不同的多糖因其分子结构的不同,对SCFAs的调节作用也不尽相同。
多糖的疗效与SCFAs的非直接关联
尽管大多数多糖可以被代谢成SCFAs,但它们的疗效并不一定与SCFAs直接相关。
多糖通过调节肠道菌群和促进SCFAs的产生,对健康具有多方面的益处。然而,多糖的结构与它们对SCFAs生成的调节作用之间的关系仍需进一步研究。此外,多糖的疗效可能不仅限于SCFAs的产生,还可能涉及肠道菌群产生的其他分子。
在肠道微生物群的作用下,脂质和蛋白质等饮食成分可以代谢为一系列代谢产物,如三甲胺-N-氧化物(TMAO)、色氨酸、脂多糖(LPS)等。此外,肠道微生物群还可以与宿主合成和释放的化合物相互作用。例如,肠道微生物群可以将初级胆汁酸(BA)转化为次级胆汁酸。由于肠道微生物群的组成与肠道微生物群代谢物的产生直接相关,因此可以推断,除了SCFAs,多糖还可以调节其他肠道微生物群代谢产物,如BA。
三甲胺和TMAO的代谢过程
在肠道中,饮食中的四胺类物质如胆碱、L-肉碱和卵磷脂(来自红肉、鸡蛋、鱼、海鲜)首先被微生物胆碱三甲胺裂解酶分解成三甲胺(TMA)。随后,TMA被吸收进入门脉循环,并运输到肝脏,在黄素单加氧酶1和黄素单加氧酶3的作用下转化为三甲胺-N-氧化物(TMAO)。
TMAO的潜在危害
值得注意的是,TMAO是一种潜在的有害代谢产物。多项研究指出,TMAO水平的增加与多种疾病的发生和发展呈正相关。例如,TMAO可以直接增强血小板的反应性,促进血栓形成,并通过激活核因子κB(NF-κB)和NLRP3炎症体影响血管炎症。
多糖对TMA和TMAO代谢的影响
最近的研究表明,TMA和TMAO在理解多糖的作用机制中扮演重要角色。例如:
不同多糖对肠道菌群的调节作用
不同的多糖可以通过调节相同的肠道细菌来降低TMA和TMAO的代谢,例如变形菌门。研究表明,变形菌门负责TMA的转化,增加变形菌门可能导致TMA增加。然而,也有研究表明TMAO与变形菌门呈负相关,这表明多糖调节变形菌门与TMA产生的效应之间的关系需要进一步研究。
多糖通过调节肠道菌群,影响TMA和TMAO的代谢,从而可能对人体健康产生积极影响。然而,多糖与TMAO之间的关系复杂,需要更多的研究来阐明这些相互作用的确切机制。
色氨酸代谢的重要性
色氨酸(Trp)是人体必需的氨基酸。它的代谢可以分为内源性代谢和细菌性代谢。内源性代谢主要通过犬尿氨酸途径(KP)和5-羟色氨酸途径进行,前者产生犬尿氨酸(KYN)、犬尿酸(KA)、烟酸、黄嘌呤酸等,后者转化为5-羟色氨酸(5-HT)和褪黑素。
色氨酸代谢物的生理功能
增强免疫:色氨酸可加强免疫力,减少炎症。
神经保护:KA作为谷氨酸受体拮抗剂,具有神经保护和抗惊厥作用,还能调节能量代谢。
情绪调节:5-HT作为神经递质,可调节情绪、肠道通透性和肠道蠕动。
肠道菌群在色氨酸代谢中的作用
肠道细菌代谢色氨酸产生吲哚及其衍生物,如吲哚丙酸、吲哚乙酸等,这些物质可以缓解炎症,促进肠道上皮屏障功能。肠道菌群的色氨酸代谢异常与肠易激综合症、代谢综合症和结肠癌等疾病有关。例如,结肠癌患者常伴有色氨酸水平下降和KP代谢物水平升高。
多糖影响肠道微生物色氨酸代谢,从而改善疾病
吲哚是硫酸吲哚酚的前体,是一种蛋白结合尿毒症毒素,是心血管疾病的危险因素。对于患有终末期肾病心血管疾病的患者,吲哚水平升高,患者粪便中产吲哚细菌丰富。
总的来说,多糖可以通过调节肠道菌群来改变色氨酸代谢,最常见的是增加乳杆菌和阿克曼菌,从而缓解疾病。
胆汁酸的生物合成与功能
胆汁酸(BAs)是一类由肝脏产生的特殊类固醇分子,经过肠道菌群转化。肝脏中存在两种BA生物合成途径:
CA和CDCA是体内的主要胆汁酸。经过肠道菌群的改造,CA转化为脱氧胆酸(DCA),CDCA转化为鹅去氧胆酸(LCA)。
胆汁酸受体及其作用
胆汁酸受体包括细胞表面受体和细胞内受体。细胞表面受体包括TGR5,细胞内受体包括法尼酰X受体FXR、孕烷X受体、维生素D3受体(VDR)和组成型雄烷受体。胆汁酸通过激活相应的受体调节脂质、葡萄糖和能量代谢。例如,TGR5和VDR的激活导致GLP-1和FGF19分泌,GLP-1可以改善胰岛素敏感性,FGF19可以通过抑制脂肪生成减少肝脏脂肪变性。
多糖对胆汁酸代谢的调节作用
近年来的研究表明,多糖可以通过恢复胆汁酸的代谢来缓解疾病。
多糖对胆汁酸代谢影响的总结
多糖通过调节肠道菌群的组成,特别是Bacteroides、Lactobacillus、Clostridium、Ruminococcus、Bifidobacteria,影响胆汁酸的代谢。
某些多糖如岩藻聚糖和灰树花多糖减少了Clostridium的水平,这与文献报道的促进胆汁酸转化的作用似乎矛盾,需要进一步研究确认这些肠道细菌与多糖之间的关系。
脂多糖的危害
脂多糖(LPS)是由革兰氏阴性细菌(如大肠杆菌)产生的内毒素。持续暴露于LPS或LPS异常增加,可通过减少肠道上皮细胞活性、降低肠道细胞增殖、抑制肠道细胞迁移和诱导肠道细胞凋亡等方式,导致肠道损伤。
LPS的转移还能损伤肠道,并可能通过与多种受体的相互作用,如LPS结合蛋白、簇分化14、髓样分化2和Toll样受体4,引发糖尿病、非酒精性脂肪肝病、肥胖、动脉粥样硬化等一系列疾病。
多糖对LPS产生菌的抑制作用
许多多糖能够抑制产生LPS的细菌。例如,在链脲佐素(STZ)诱导的糖尿病肾病模型中:
多糖调节肠道菌群的矛盾效应
尽管多糖可以通过调节肠道细菌来抑制LPS,但对特定细菌的调节作用可能存在矛盾。例如,作为LPS产生菌的拟杆菌门,在多糖处理后的水平变化并不一致。有研究表明,黄精多糖和蝉花多糖增加了拟杆菌门的水平,而竹荪多糖却降低了它。这些研究表明,多糖对肠道菌群的调节效应有时可能相互矛盾,需要进一步研究以确认结果。
胃肠道气体的生成
胃肠道内通过细菌发酵食物,会产生一系列气体,包括氢气(H2)、甲烷(CH4)、二氧化碳(CO2)、硫化氢(H2S)和一氧化氮(NO)。这些气体在胃肠道中发挥着调节作用,例如影响结肠蠕动、神经通讯、血管功能和免疫反应等。
气体产生的部位和作用
CO2 主要在胃中产生,而其他气体如 H2、CH4、CO2 和 H2S 主要在小肠和结肠中产生。
这些气体对人体健康至关重要,它们可以调节肠道功能,影响营养物质的吸收和疾病的发生。
多糖对气体产生的调节
尽管多糖对 H2、CH4 和 CO2 的产生有明显影响,但关于多糖结构与气体产生之间具体关系的研究会相对较少。需要更多的研究来明确这些关系,以及多糖如何通过影响肠道菌群来调节气体的产生。
肠道菌群是一个复杂的微生物群落,具有显著的组成和功能多样性。不同的微生物可以介导相同或不同的代谢物的产生,相同的微生物也有助于不同代谢物的生产。
例如,持续的研究表明:
拟杆菌门(特别是Bacteroides thetaiotaomicron、Bacteroides fragilis)、厚壁菌门(如Clostridiaceae、Erysipelotrichia)、以及变形菌门可以促进TMA的产生。
放线菌门(如Bifidobacteria)、厚壁菌门(如Lactobacillus、Clostridium、Peptostreptococcus)、拟杆菌门(如Bacteroides)可以促进色氨酸(Trp)的转化。
双歧杆菌、乳酸菌、梭菌、Peptostreptococcus、拟杆菌也有助于次级胆汁酸(BAs)的产生。
因此,就像肠道菌群组成的调节一样,多糖对特定肠道菌群代谢物功能的调节作用不是孤立的。
肠道是我们抵御外界有害物质和病原体侵袭的第一道防线。它由多个层次的子屏障构成:
生物屏障:由肠道细菌和病毒组成;
化学屏障:包含免疫球蛋白A(IgA)、抗菌肽(AMPs)和粘液(MUC);
物理屏障:由肠道上皮细胞构成;
免疫屏障:含有T细胞、B细胞、巨噬细胞和树突细胞等免疫细胞。
这些子屏障协同工作,限制病原体与肠道的接触,维持肠道稳定。肠道屏障的损伤与多种疾病正相关,包括肠易激综合症(IBS)、代谢综合征、过敏、肝脏炎症等。
肠道菌群及其代谢物可以直接或间接影响肠道屏障:
越来越多的证据表明,多糖通过调节肠道菌群对肠道屏障有益。正常的肠道菌群组成可以通过竞争性排除,通过消耗营养源和占据附着位点,作为抵御外界病原体的屏障。
多糖→ 调节肠道菌群→ 修复肠道屏障
肠道菌群可以刺激宿主产生抗菌化合物,如IgA和AMPs,这些是化学屏障的关键组成部分。
例如,菊粉型果聚糖可以促进乳杆菌的丰度和IgA的分泌。在DSS诱导的溃疡性结肠炎小鼠模型中,金银花多糖通过增加双歧杆菌和乳杆菌,增加了分泌型IgA含量,从而调节肠道屏障。
在DSS诱导的结肠炎小鼠中,海蜇皮多糖增加Akkermansia,Akkermansia muciniphila作为粘液的降解者,可以增强肠道屏障的完整性,减少炎症。同时海蜇皮多糖增加结肠中TJs和MUC2的表达,保护了肠道屏障。
多糖→ 短链脂肪酸→ 修复肠道屏障
短链脂肪酸和胆汁酸等肠道菌群代谢物在调节肠道屏障功能中也扮演重要角色。
多糖→ 色氨酸和胆汁酸代谢→ 修复肠道屏障
这些研究表明,多糖可以通过调节肠道菌群及其代谢物,维护肠道屏障的完整性。
代谢性疾病包括一组因碳水化合物、脂质和蛋白质代谢错误而导致的疾病。2 型糖尿病 (T2DM)、非酒精性脂肪性肝病 (NAFLD) 和肥胖是常见的代谢性疾病。
生活方式干预、全身药物治疗和外科手术等多种方法被用于预防和治疗代谢性疾病。尽管代谢性疾病的药物治疗取得了最新进展,但潜在的不良反应仍然是关键挑战。
使用天然物质的药物治疗被认为是改善代谢疾病的一种有前途且可行的方法。
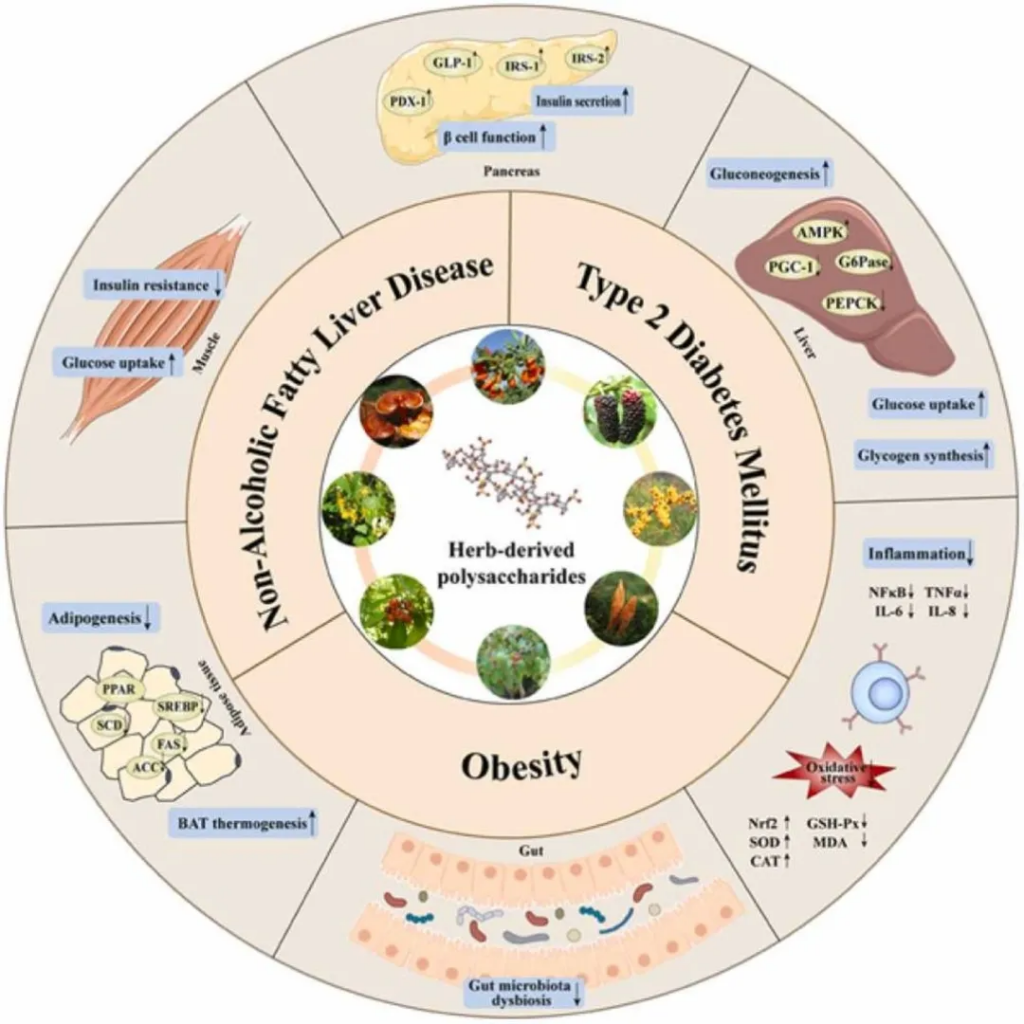
doi.org/10.1016/j.biopha.2023.114538
多糖通过多种机制在治疗2型糖尿病方面表现出良好的效果,比如:
肠道菌群在代谢紊乱,特别是 2 型糖尿病的发展中起着重要作用。
◤车前子多糖 对 STZ 诱导的 2 型糖尿病大鼠有抗糖尿病作用,这可能与其调节肠道菌群和增加短链脂肪酸水平有关。车前子多糖可显著增加糖尿病大鼠粪便中Bacteroides vulgatus、发酵乳杆菌、Prevotella loescheii、Bacteroides vulgates等结肠细菌的多样性和丰度,以及短链脂肪酸的浓度。
◤桑果多糖 可以丰富糖尿病小鼠的功能菌并调节微生物多样性。具体而言,该多糖显著富集了一些有益细菌(拟杆菌目、乳杆菌属、Allobaculum、拟杆菌属、阿克曼菌属),同时减少了一些致病菌(葡萄球菌、棒状杆菌属、Jeotgalicoccus、Aerococcus、Enterococcus、Facklamia)。
◤罗布麻叶的两种富含多糖的提取物改善了糖尿病小鼠的肠道微生物群失调,包括增加了Odoribacter、Anaeroplasma、Parasutterella、Muribaculum的丰度,并降低了肠球菌属、克雷伯菌属、Aerococcus的丰度。这可能有助于它们的抗糖尿病作用。
◤菊粉补充增加了双歧杆菌的丰度并增强了肠道屏障的完整性,这与2型糖尿病呈负相关。
◤青钱柳叶中分离的多糖通过增加 SCFAs 含量和有益的肠道细菌瘤胃球菌科来减轻 HFD/STZ 诱导的 2 型糖尿病大鼠的糖尿病症状。
◤苦瓜中的天然多糖通过增加 SCFAs 含量和Prevotella loescheii、Lactococcus laudensis 的丰度来改善 HFD/STZ 诱导的 2 型糖尿病大鼠的高血糖、高脂血症、高胰岛素血症。
◤天然南瓜多糖通过增加阿克曼氏菌和减少丹毒丝菌科(Erysipelotrichaceae)来显示出对 HFD/STZ 诱导的 2 型糖尿病的降血糖作用。此外,南瓜多糖还能增加 2 型糖尿病模型中肠道短链脂肪酸的产生。
◤灵芝多糖(GLP)通过恢复HFD/STZ诱导的肠道微生物群失调,特别是通过增加Blautia、拟杆菌、Dehalobacterium、Parabacteroides,以及减少有害的肠道细菌Aerococcus、Corynebacterium、Ruminococcus、Proteus,显示出抗糖尿病作用。
◤薏苡仁多糖通过降低厚壁菌门/拟杆菌门的比例和增加SCFAs的含量,在HFD/STZ诱导的T2DM小鼠模型中表现出降血糖活性。
◤葡甘聚糖作为铁皮石斛、芦荟和魔芋的天然多糖,通过增加厚壁菌门的丰度和减少拟杆菌门、变形杆菌的丰度,改善HFD/STZ喂养大鼠的T2DM代谢紊乱。
多糖对改善NAFLD具有有益作用,比如:
多糖可以改善肠道菌群失调并保护非酒精性脂肪性肝动物的肠道屏障完整性
◤枸杞多糖结合有氧运动通过改善肠道菌群失调改善 NAFLD,包括调节肠道菌群的丰度和多样性,增加微生物代谢产物 SCFA 的水平,减少变形菌和厚壁菌门/拟杆菌门的比例。厚壁菌门和拟杆菌门是参与宿主代谢和脂肪积累的关键细菌。
◤麦冬多糖可以通过调节肠-肝轴显著保护 NAFLD。具体来说,这种多糖显著降低了一些有害细菌的相对丰度,包括乳球菌、肠杆菌、Turicibacter、Clostridium- sensu-stricto -1、Tyzzerella、Oscillibacter,并增加一些有益菌的相对丰度,如Alistipes、Ruminiclostridium、Rikenella。这种多糖还显著增加了两种产SCFAs菌( Butyricimonas、Roseburia )的丰度以及乙酸和戊酸的水平,从而改善了炎症反应和肝脏脂质代谢。
◤灰树花杂多糖可通过调节肠道菌群来改善高脂饮食诱导的NAFLD,包括显著增加Allobaculum、拟杆菌属和双歧杆菌属丰度,减少Acetatifactor、Alistipes、Flavonifractor、Paraprevotella、Oscillibacter的丰度。
◤黄芪多糖可减轻HFD喂养小鼠的NAFLD,丰富了脱硫弧菌属,尤其是作为SCFAs、乙酸的产生者的Desulfovibrio vulgaris,减轻肝脂肪变性。
◤诺尼果多糖来源于辣木,通过促进短链脂肪酸的产生缓解HFD喂养小鼠的NAFLD,并通过改善肠道微生物群的多样性和组成逆转HFD诱导的肠道微生态失调。
◤核桃青皮多糖通过提高肠微生物群(包括普氏菌科、Allobaculum)的SCFAs含量和丰度,预防HFD喂养大鼠的肥胖和NAFLD。
◤从贻贝中提取的贻贝多糖,α-D-葡聚糖(MPA)可保护HFD喂养的大鼠的NAFLD,补充MPA可逆转HFD抑制的微生物微生态失调和SCFAs。
◤海带可溶性多糖通过降低厚壁菌门/拟杆菌门的比例,促进Verrucomirobia和丙酸盐产生菌拟杆菌和阿克曼菌,减轻高脂饮食喂养小鼠的NAFLD。
多糖通过多种机制表现出良好的抗肥胖作用,作用机制如:
◤枸杞多糖补充剂可降低厚壁菌门与拟杆菌门的比例,增加产短链脂肪酸菌,如Lacticigenium、Butyricicoccus、Lachnospiraceae_NK4A136_group数量,从而改善肥胖小鼠的肠道菌群失调。
◤桑叶多糖治疗可调节肥胖小鼠肠道菌群的组成和功能,这与增加Allobaculum、Parabacteroides、Porphyromonadaceae、Butyricimonas、Ruminococcus 的水平有关。
◤黄精多糖调节HFD喂养的肥胖大鼠的肠道微生物群结构,包括降低梭菌、肠球菌、Coprobacillus、乳球菌、Sutterella的相对丰度。
◤沙蒿多糖给药8周显著上调了屏障完整性的结肠基因,并通过增加有益细菌(双歧杆菌和Olsenella)和抑制有害细菌(Mucispirillum和幽门螺杆菌)改善了肥胖小鼠的肠道微生物微生态失调。同时,它显著富集了与促进SCFAs产生相关的碳水化合物代谢,同时显著抑制了与肥胖和肠道微生态失调相关的氨基酸代谢。
◤从海带中提取的天然多糖可通过使肠道菌群正常化来缓解小鼠HFD引起的肥胖,特别是通过增加拟杆菌目和Rikenellaceae的丰度。
◤从杏鲍菇中分离出的蘑菇多糖通过增加产生 SCFA 的肠道细菌Anaerostipes和Clostridium 的数量,在高脂饮食喂养的小鼠中表现出抗肥胖作用。
◤茶树菇多糖对HFD诱导的小鼠脂肪堆积和减肥的影响,发现脱硫弧菌减少,副拟杆菌增加,从而显著降低肥胖相关的TNF-α 和 IL-6 的水平。
◤从苦瓜中获得的多糖通过增加有益细菌(如放线菌、Coprococcus、乳酸杆菌)和减少有害细菌(变形菌和幽门螺杆菌)来改善HFD诱导的小鼠肥胖。
◤日本刺参的硫酸多糖通过富集益生菌Akkermansia、减少携带内毒素的变形杆菌和提高SCFAs含量来预防HFD诱导的小鼠肥胖。
◤ 破壁灵芝孢子多糖能逆转 HFD 喂养小鼠中许多细菌的相对丰度,特别是一些潜在的益生菌,包括Allobaculum、双歧杆菌,这与抗肥胖呈正相关。双歧杆菌、乳杆菌和阿克曼菌可促进SCFAs的产生,并抑制梭菌科、脱硫弧菌和肠球菌的丰度,这将有助于减少体重和脂质积累。
总的来说,多糖可通过作用于多个环节、调控多个疾病相关靶点来改善这三种代谢性疾病。
doi.org/10.3389/fmicb.2022.859206
高脂血症是指脂质代谢紊乱,其特征是甘油三酯 (TG)、总胆固醇 (TC) 和低密度脂蛋白浓度升高,同时高密度脂蛋白水平降低。
◤果胶多糖(高支链 RG-I,531.5 kDa)显著改善了 HFD 引起的脂质代谢异常,TG、TC、LDL-C 和游离脂肪酸水平降低。它还通过增加Roseburia、Clostridium等产生 SCFA 的细菌的数量来恢复肠道菌群失衡。
◤裙带菜多糖 ( Undaria pinnatifida )修复了高脂饮食引起的肠道微生物群改变,特别是Prevotellaceae_UCG-001,发现这与脂质代谢紊乱有关。
◤鲍鱼性腺多糖显著增加了丁酸水平,丁酸是一种重要的短链脂肪酸,它通过GPR依赖性途径抑制脂质相关基因的表达。
◤龙须菜多糖调节拟杆菌、瘤胃球菌_1和乳酸杆菌的相对丰度来增强胆固醇向BAs的转化。在遗传水平上,有人认为BA代谢的调节主要涉及CYP39A1和CYP7B1。
炎症性肠病 (IBD) 包括溃疡性结肠炎 (UC) 和克罗恩病 (CD),其特点是胃肠道持续炎症。IBD 的症状包括腹泻、腹胀、腹痛、便血、体重减轻和不适。
◤银耳多糖(TPs)通过多途径调节肠道菌群及其代谢物,改善了DSS诱导的溃疡性结肠炎。TPs可以增加Lactobacillus的丰度,从而改善色氨酸的分解代谢。这导致黄嘌呤酸、KA和吲哚衍生物(如5-羟吲哚、5-羟吲哚-3-乙酸、5-羟吲哚乙酰酸)的增加。
TPs还可以增加Romboutsia的水平,促进DCA的产生。因此,TPs可以通过影响色氨酸代谢和胆汁酸代谢来保护小鼠免受结肠炎的侵害。
◤金针菇多糖已被证明可以通过控制结肠微生物失调、增加短链脂肪酸和抑制 TLR4-NF-κB 信号通路来缓解结肠炎。能促进益生菌的生长,抑制致病菌的生长,恢复肠道稳态,缓解IBD症状。
◤竹荪多糖由59.84%的葡萄糖、23.55%的甘露糖和12.95%的半乳糖组成,已被证明可以通过增加粘蛋白和紧密连接蛋白的表达,抑制有害细菌(如γ-变形菌、变形菌、拟杆菌科、拟杆菌科和肠杆菌科)并增强有益细菌(如嗜酸乳杆菌)来改善肠道菌群组成和肠道屏障功能。
◤坛紫菜多糖通过上调紧密连接蛋白,增加粘液层及其分泌,调节肠道微生物群落,富集有益细菌,如拟杆菌、Muribaculum和乳酸杆菌,从而减轻DSS诱导的结肠损伤,从而改善结肠粘膜屏障的完整性。
◤白术多糖可以缓解在DSS诱导的溃疡性结肠炎小鼠模型炎症。白术多糖可以增加Butybacterium、Lactobacillus,同时减少Actinomyces、Akkermansia、Faecalibaculum、Verrucomicrobia、Bifidobacterium等。
肠道菌群的变化逆转了DSS引起的短链脂肪酸的减少以及色氨酸和色氨酸相关代谢物5-羟基-N-甲酰基犬尿氨酸和吲哚-3-乙酸的减少。白术多糖还剂量依赖性地逆转了LCA、DCA、缬氨酸、亮氨酸等的异常变化。
天然植物多糖治疗IBD的机制
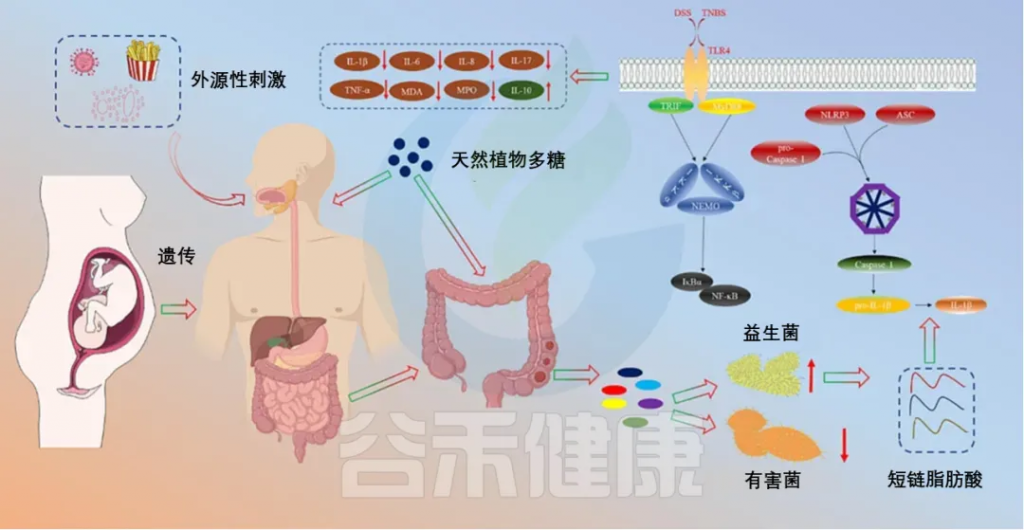
doi.org/10.1016/j.ijbiomac.2023.126799
◤甘草多糖GPS上调乳杆菌科、S24–7、Turicibacteraceae、Verrucomicrobiaceae和双歧杆菌科的丰度,下调脱硫弧菌科、瘤胃球菌科、毛螺菌科、肠杆菌科、丹毒丝菌科的丰度。GPS能促进乳杆菌、拟杆菌和产SCFAs菌的生长繁殖,起到减轻炎症、升高IL-10水平、抑制TLR4活化、降低血浆LPS水平的作用,从而保护肠道免受LPS诱导的炎症。
◤何首乌多糖(TSG)的给药显著增加了厚壁菌门和拟杆菌门的相对丰度,同时也降低了幽门螺杆菌和拟杆菌门的属水平,改善了肠道菌群,起到治疗IBD的作用。

doi.org/10.3390/nu15153321
◤乳果糖通过重塑肠道菌群组成和代谢物,改善了由洛哌丁胺引起的便秘小鼠模型中的肠道水和盐代谢。具体来说,乳果糖上调了Bacteroides的丰度,并显著降低了厚壁菌门和Verrucomicrobia的水平。
此外,乳果糖减少了胆汁酸(包括CA、DCA等)、粪便中高浓度的吲哚(高浓度吲哚对细胞有毒)并增加了丙酸。
◤西洋参多糖(WQP) 可增强大鼠肠道结构的恢复,降低炎性细胞因子水平,改善短链脂肪酸 (SCFA) 水平,促进肠道菌群和肠黏膜屏障的恢复,并减轻盐酸林可霉素引起的腹泻和菌群失调等抗生素相关副作用。
◤葛根多糖( PPL )可缓解抗生素相关性腹泻引起的结肠病理改变和肠道菌群失调。
◤紫菜中提取的多糖(Nemacystus decipiens)能显著缓解小鼠抗生素相关性腹泻(AAD)的症状,并且显著增加了 Muribaculum、Lactobacillus 和 Bifidobacterium 的丰度,降低Enterobacter 、Clostridioides 的丰度。
◤茯苓多糖(PCP)通过恢复7种肠道菌菌缓解了抗生素相关性腹泻小鼠的症状,包括:Parabacteroides distasonis、Akkermansia muciniphila、Clostridium saccharolyticum、Ruminococcus gnavus、Lactobacillus salivarius、Salmonella enterica、Mucispirillum schaedleri.
适当调节免疫反应可以降低炎症反应引起的病原体入侵的风险。
结直肠癌
◤灵芝多糖在缓解结直肠癌症状方面比瓜尔胶更有效,因为它们能增加Akkermansia、结肠长度,并下调直肠癌相关基因。灵芝多糖通过动态调节肠道菌群和宿主免疫反应,已证明具有预防和治疗癌症的功能。
灵芝多糖通过调节乳酸杆菌、双歧杆菌等有益菌的相对丰度,诱导SCFAs的产生,改善肠道屏障损伤,抑制TLR4/MyD88/NF-κB信号通路,从而降低结肠炎和致癌风险。
◤绞股蓝与灵芝多糖联合使用显著提高了SCFAs产生菌的丰度,提高了丁酸和异丁酸水平,抑制了硫酸盐还原菌的丰度。
乳腺癌
◤来自灵芝破壁孢子(分子量为 3659 Da)的多糖可作为乳腺癌治疗的天然佐剂,增加细胞毒性 T 细胞和辅助性 T 细胞的数量。
灵芝孢子提取物(ESG)重塑了4T1荷瘤小鼠的肠道菌群:厚壁菌门和变形菌门的相对丰度增加,放线菌、拟杆菌门和蓝藻的相对丰度降低。
◤灵芝多糖联合紫杉醇对4T1乳腺荷瘤小鼠有抗肿瘤作用。联合治疗能显著富集拟杆菌、瘤胃球菌等5个菌属,降低脱硫弧菌和Odoribacter的丰度,平衡肠道菌群,抑制肿瘤代谢。
疲劳是一种普遍的不适感,表现为极度疲倦和力竭,通常在生理、病理或心理失衡时出现。体力劳动、心理压力、高原缺氧和长期疾病都可能引发疲劳。疲劳不仅影响日常生活,还可能导致内分泌、免疫、代谢等系统功能受损,甚至与癌症、糖尿病等严重疾病相关。此外,疲劳还与焦虑、抑郁和神经系统疾病有关。
近年来,天然多糖因其在缓解运动性疲劳中的潜在效果和较少的副作用而受到关注。研究表明,肌肉功能与肠道菌群的多样性和组成密切相关,而天然多糖如决明子、灵芝、枸杞和冬虫夏草等可通过不同机制发挥抗疲劳作用。
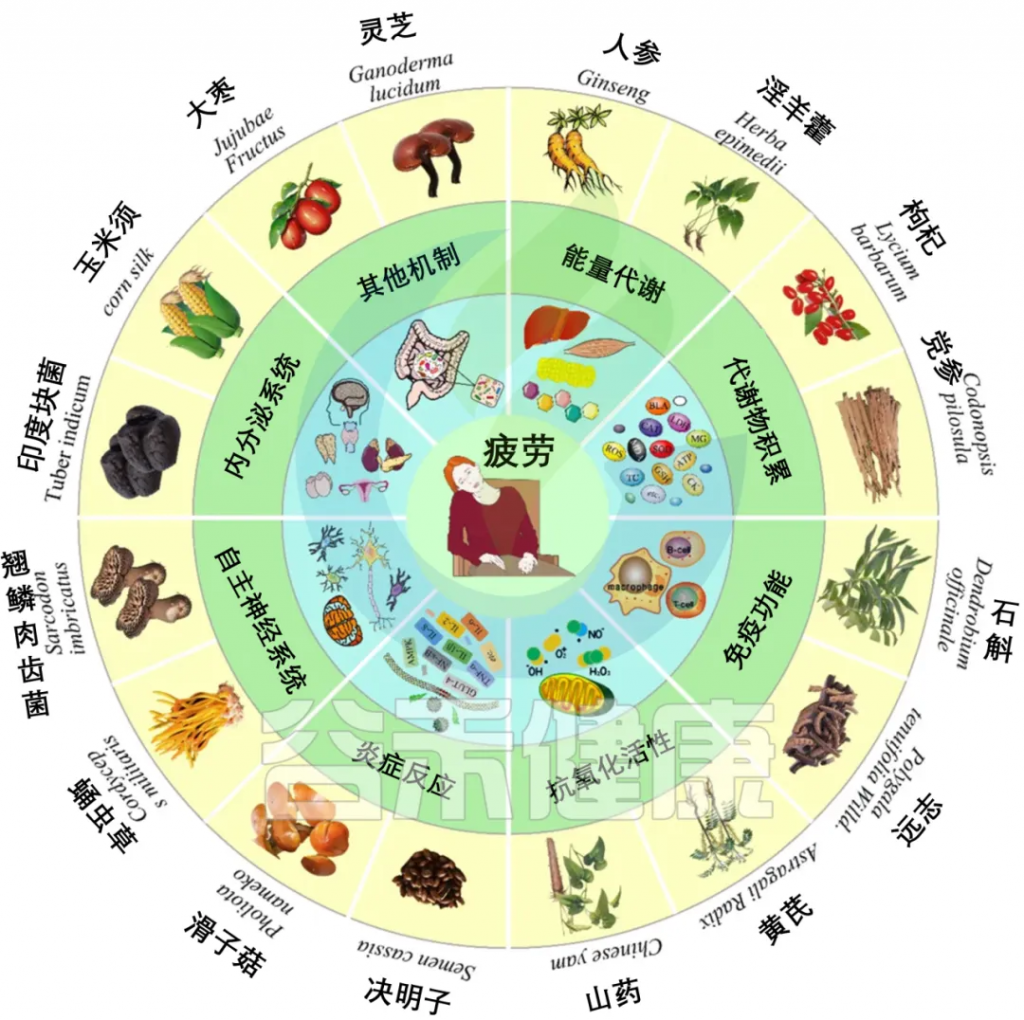
doi.org/10.3390/foods12163083
多糖抗疲劳机制如下:
抗疲劳多糖干预后肠道菌群的变化
doi.org/10.3390/foods12163083
肠道-肌肉轴是肌肉与消化道之间的双向沟通,微生物可以通过微生物-肠道-肌肉轴作用于全身的肌肉。肠道微生物在膳食多糖的作用下,产生一些代谢产物(短链脂肪酸等),有些代谢产物会直接穿过肠道上皮细胞,通过血液循环直接或间接作用于肌肉组织和细胞,引起细胞发生生理生化反应,对疲劳产生一定的影响。
补充膳食多糖通过作用于肠道菌群及其代谢产物,间接激活AMPK/PGC-1α、PI3K/AKT、NF-κB、Nrf2/Keap1信号通路,调节能量代谢,降低炎症水平,增强线粒体功能和抗氧化能力,进一步维持肌肉质量和功能,从而缓解疲劳。
扩展阅读:
◤银杏叶中的一种水溶性多糖(GPS)可减轻压力引起的抑郁症并逆转肠道菌群失调。GPS 治疗可以缓解压力引起的血清素阳性和多巴胺阳性细胞密度降低。GPS 逆转了与抑郁相关的肠道菌群失调,并增加了乳杆菌的丰度,而乳杆菌已被证明是缓解抑郁的途径。
◤从秋葵中提取的多糖,发现它对抑郁小鼠的肠道菌群有明显的恢复作用,表现为厚壁菌门比例上调,拟杆菌门和放线菌门相对比例下调。这种调节有助于强化肠黏膜屏障,维持肠道免疫系统正常功能,减少肠道炎症反应,对抗抑郁有效,抑郁症小鼠的抑郁症状有所改善。用秋葵多糖治疗的小鼠体内的SCFAs显著增加,而SCFAs作为重要的通讯介质,对抗抑郁障碍有积极的影响。
◤接受金针菇多糖 (FVP)治疗的小鼠的肠道微生物组成发生显著改变,放线菌、丹毒菌和拟杆菌的丰度增加,梭菌的丰度降低,并且接受FVP治疗的小鼠的学习和记忆能力得到改善。
◤肉苁蓉多糖可以通过恢复小鼠模型中D-半乳糖诱导的衰老引起的肠道菌群稳态来抑制氧化应激和外周炎症,从而改善小鼠的认知功能。
◤从黄芪中提取的一种多糖已被证明可以通过改变糖尿病小鼠的肠道菌群来改善认知障碍。
扩展阅读:
以下是关于一些多糖的详细介绍,包括其功效,与肠道菌群的关联等,更深入地了解多糖在人体中的重要作用。
路易波士茶是什么?
路易波士茶(Rooibos)又名Aspalathus linearis,中文也有译作“路易博士茶”,取自原产于南非的一种豆科植物的茎叶。虽然带有一个茶字,但路易波士茶并不是传统意义上的茶叶。
路易波士茶因不含咖啡因、单宁含量低而受到南非人的喜爱,并在全球范围内进行商业化种植和销售。2014年,中国卫生和计划生育委员会批准路易波士茶作为新的食品原料,丰富了中国的食品和药物资源。
路易波士茶具有良好的抗氧化、抗过敏、解痉和降血糖作用。也可以预防心血管疾病、神经退行性疾病、各种癌症、骨质疏松症等。
路易波士茶多糖
一项研究从路易波士茶中分离得到均一酸性多糖(ALPs) ,水溶性多糖ALP由β-糖苷键连接,含有吡喃糖环,主要由岩藻糖、鼠李糖、阿拉伯糖和半乳糖组成。
结合RT-PCR结果推测,ALP可能通过降低Cyp2e1和Keap1的mRNA表达,增加Nrf2和HO-1的mRNA表达,激活Cyp2e1/Keap1-Nrf2-HO-1信号通路,调控下游抗氧化酶活性和炎症因子表达,减轻氧化应激损伤和炎症反应造成的损伤,从而改善急性酒精性肝损伤。
路易波士茶多糖对肠道菌群的影响
多样性
急性酒精性肝病模型对照组(MC)的物种多样性和丰富度显著降低(p≤0.05)。高剂量和低剂量ALP处理组的物种多样性和丰富度有所增加,其中高剂量组的增加更为显著。
干预后改善的菌群
ALP 干预后疣微菌丰度显著升高(p≤0.01),而脱硫杆菌丰度及F / B值均降低,但差异不显著。
肠道菌群中乳酸杆菌科的丰度与肝脏 AST 和 ALT 水平呈负相关。小鼠ALP干预后,乳酸杆菌科的丰度显著增加(p ≤ 0.05),而Rikenellaceae的丰度显著降低(p ≤ 0.05)。
ALP 显著改善了小鼠急性酒精性肝损伤中Alloprevotella和Alistipes丰度显著降低的情况( p ≤ 0.05)。
“肠-肝轴”途径
对属级别排名前20位的菌种进行了 Spearman 相关性分析。
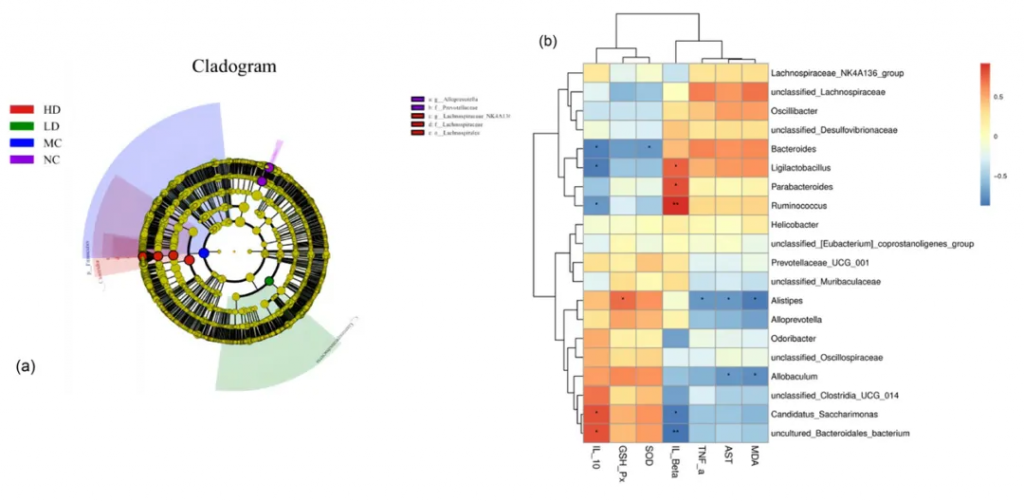
推测ALP可能通过“肠-肝轴”通路促进肠道菌群与抗氧化酶及炎症因子相互作用,从而减轻酒精性肝损伤,而上述菌群与酒精损伤标志物、抗氧化酶及炎症因子的表达均密切相关。
酒精及其代谢产物会影响肠道菌群的平衡和组成,导致肠道功能受损。这反过来又会影响肝脏健康,而肝脏健康与肠道菌群稳态密切相关。肠道和肝脏之间的相互作用被称为“肠-肝轴”通路。
地黄是玄参科地黄属植物,在我国拥有久远的药用历史,作为滋阴补肾的传统中药,也被《神农本草经》列为上品。
多糖是地黄中的主要活性成分之一。地黄多糖具有免疫调节、抗肿瘤、抗氧化、抗衰老等多种生物活性。
迄今为止,从地黄中分离纯化了20多种多糖,主要由阿拉伯糖、鼠李糖、半乳糖、葡萄糖、甘露糖、木糖、岩藻糖和半乳糖酸组成。
地黄多糖能增加DSS诱发小鼠的体质量指数和结肠长度、降低DAI评分,改善组织病理学损伤。同时,地黄多糖能阻断NF-κB信号通路,降低细胞内促炎因子表达,减轻炎症,增加紧密连接蛋白表达,维持肠道上皮屏障。
地黄多糖可能在肠道微生物作用下发酵转化为SCFAs,增加肠道中乙酸、丙酸和丁酸的含量,起到缓解IBD的作用。
拟杆菌属、乳酸杆菌属、Alistipes是导致DSS结肠炎组肠道微生物组失衡的关键细菌类型,而补充地黄多糖可以逆转这种有害变化。
五指毛桃,又叫粗叶榕(Ficus hirta Vahl),常被用作滋补品的草药成分,以其丰富的多糖含量和生物活性而闻名。
一项研究发现,FHVP-3 对肠道微生物群产生影响:
下列菌群富集:
FHVP-3 抑制了下列机会性致病菌属的丰度:
作为可发酵底物,FHVP-3 还增加了短链脂肪酸的浓度,包括乙酸盐、丙酸盐和丁酸盐。FHVP-3 对脂多糖 (LPS) 诱导的 RAW 264.7 巨噬细胞表现出显着的抗氧化活性和显着的抗炎作用。
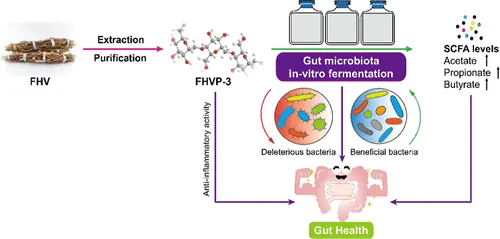
doi.org/10.1021/acsfoodscitech.3c00626
大蒜多糖 (GP) 占大蒜干重的 75% 以上。它们的特征是具有 2,1- β – d -Fruf 主链和 2,6- β – d -Fruf 分支的果聚糖。
研究表明,大蒜多糖在调节肠道微生物群方面发挥着作用,但它们是否具有维持肠道健康的全面功能并可作为有效的益生元仍不清楚。
为了探索这一点,通过管饲法给昆明小鼠施用不同剂量的大蒜多糖(1.25-5.0g/kg 体重)和菊粉(作为阳性对照),并评估它们对肠道上皮、化学和生物屏障的影响。还使用洛哌丁胺建立了便秘模型,以研究大蒜多糖对缓解便秘的潜在影响。
施用大蒜多糖显著上调昆明小鼠小肠组织中紧密连接蛋白和粘蛋白的表达。大蒜多糖提高了盲肠丁酸含量,降低了脱硫杆菌的丰度,并降低了厚壁菌门与拟杆菌门的比例(F/B)。大蒜多糖还促进了 Bacteroides acidifaciens、Clostridium saccharogumia的生长。
Tax4Fun 功能预测表明,大蒜多糖具有预防人类疾病的潜力,可降低胰岛素抵抗、传染病和耐药性的风险。
大蒜多糖还通过增强小肠转运、软化粪便稠度、加速排便和促进兴奋性神经递质的释放,在缓解洛哌丁胺引起的便秘症状方面表现出有益作用。
多年来,槐耳 (Trametes robiniophila Murr) 一直被用于药物治疗。槐耳含有多种成分,包括多糖、蛋白质、酮和生物碱,其中蛋白聚糖和多糖是主要的生物活性成分。
槐耳提取物具有免疫调节活性,并可通过激活自噬、抑制铁死亡、抑制内质网应激等过程对细胞发挥保护作用。研究表明,槐耳水提取物可通过抑制NLRP3炎症囊泡活化,减轻肠道屏障损伤和炎症反应,并抑制DSS和氧化偶氮甲烷 (AOM) 联合诱导的结肠肿瘤形成。
可缓解 DSS 引起的肠道菌群紊乱
一项小鼠研究显示,槐耳多糖干预显著逆转了 DSS 引起的Muribaculaceae_unclassified、Anaerotruncus、Ruminococcaceae_unclassified丰度的下降以及Escherichia-Shigella丰度的增加( p < 0.05)。
其中,Muribaculaceae_unclassified是健康人中发现的肠道微生物,参与丁酸代谢和色氨酸代谢,可产生对人体有益的短链脂肪酸。
相关性分析,Muribaculaceae_unclassified与结肠长度、SOD 和 T-AOC 呈正相关,而与 DAI 评分以及炎症和氧化指标呈负相关。
Anaerotruncus与结肠长度、SOD 和 T-AOC 呈正相关,但与炎症标志物 LPS、MDA 和 MPO 呈负相关。
黄芩的根通常用作药物,用于清热利湿、泻火解毒。多糖是黄芩的最重要成分之一。
一种来自黄芩的多糖通过抑制 NF-κB 信号传导和NLRP3 炎症小体活化来改善溃疡性结肠炎。在多糖的分离和纯化过程中,研究人员还获得了另一种名为 SP2-1 的均质多糖。SP2-1由甘露糖、核糖、鼠李糖、葡萄糖醛酸、葡萄糖、木糖、阿拉伯糖和岩藻糖组成。
研究人员发现其对肠道菌群紊乱、肠道屏障改善以及短链脂肪酸产生影响。
在UC患者中,SP2-1显著抑制了促炎性细胞因子IL-6,IL-1β和TNF-α。
溃疡性结肠炎患者的屏障完整性被破坏,TJ 蛋白的表达发生改变,SP2-1增加小鼠TJ蛋白的表达,修复肠道屏障。
SP2-1对肠道菌群的影响
SP2-1组的粪便微生物群多样性明显高于DSS组。
临床上,溃疡性结肠炎患者的双歧杆菌和乳酸杆菌的丰度降低。与模型组相比,SP2-1 组的双歧杆菌、乳酸杆菌和Roseburia的水平提高。
而拟杆菌和葡萄球菌的种群受到抑制。肠道菌群中存在过量的拟杆菌和葡萄球菌对肠道免疫系统有害。
Roseburia 通过调节调节性 T 细胞的发育和分化、增加抗炎细胞因子的分泌和抑制促炎细胞因子的产生来缓解UC。
枸杞多糖(简称LBPs)是从枸杞中提取的一类多糖物质。枸杞是一种多年生灌木,属于茄科,枸杞多糖因其多样的药理活性和生理功能而受到越来越多的关注。
枸杞多糖 (LBPs)作为最重要的生物活性分子,可通过肠道微生物参与有益作用,包括调节代谢、降血糖、神经保护、抗衰老、保护各种器官免受氧化应激相关疾病的侵害。
枸杞多糖对肠道菌群的影响
癌症
一般来说,抗癌化疗药物除了会诱导癌细胞凋亡外,还会对肠道菌群产生不利影响,主要表现在肠绒毛缩短,乳酸杆菌和肠球菌丰度下降,节段丝状菌丰度增加。而枸杞多糖治疗可通过增加有益菌相对丰度来改善肠道环境和免疫功能,逆转环磷酰胺引起的有害菌(瘤胃拟杆菌科、Longibraceae、脱硫弧菌和厌氧拟杆菌科)相对丰度的增加。
还发现毛螺菌科、瘤胃菌科、脱铁菌科、脱硫弧菌科、Aneoplasmataceae与细胞因子IL-2、IL-6、IL-1β、TNF-α、IFN呈负相关。因此,主要肠道菌群的相对丰度可能与免疫调节有关。
厚壁菌门与拟杆菌门(F/B)比例的变化与许多疾病状态有关,它被视为菌群失调的重要指标,有助于了解肝脏和代谢疾病的发展。枸杞多糖可降低高脂饮食大鼠的 F/B 比,表明补充枸杞多糖有助于调节肠道菌群失调。
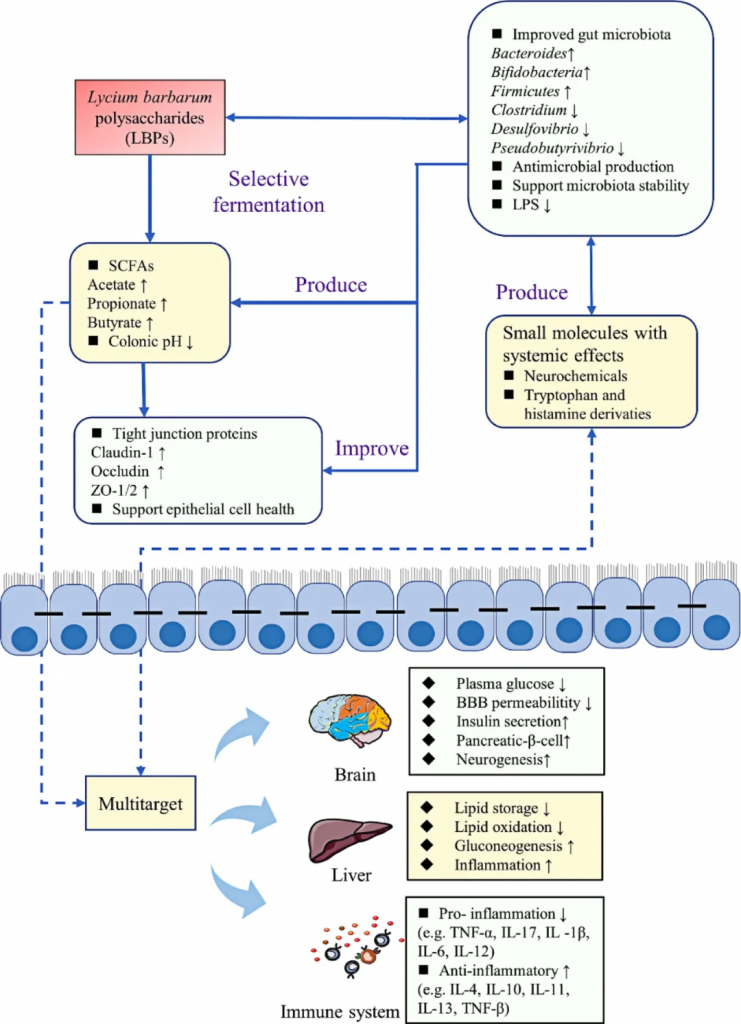
doi.org/10.1080/10408398.2022.2128037
神经系统
枸杞多糖可通过调节肠道菌群-肠-脑轴的神经免疫通路,对中枢神经系统产生多方面的保护作用。枸杞多糖可改善菌群失调、肠道屏障受损等问题,并通过抑制细胞凋亡、促进自噬等机制发挥神经保护效应。
肝脏
枸杞多糖能够影响NAFLD患者的肠道菌群组成、肠道屏障及肝脏炎症。
代谢(肥胖、糖尿病)
肥胖个体的研究中,肠道内F/B比例较高,因此推测肠道内F/B比例与肥胖呈显著正相关。
后续研究发现,LBPs可通过调节肠道菌群组成和短链脂肪酸生成来改善肥胖。
枸杞多糖可作为2型糖尿病的潜在辅助药物。
LBPs能调节肠道菌群,激活大鼠肠黏膜TLR2+上皮细胞γδT细胞,增强肠道屏障功能,改善糖尿病。此外,LBPs能明显降低血浆中促炎性细胞因子IL-1β、IL-6、IL-17A和TNF-α,而抗炎性细胞因子IL-10水平在糖尿病大鼠中有所升高。
哮喘
枸杞多糖还可以通过直接或间接地改变肠道菌群,参与炎症介质的调控,从而改善肺功能和过敏性哮喘症状。
肠道菌群测序分析显示,LBPs能够促进哮喘小鼠肠道中乳酸杆菌和双歧杆菌增加,并降低厚壁菌门和放线菌水平,通过肠道介导缓解哮喘。
岩藻糖(Fucose),参与构成肠上皮细胞(IEC)顶端表达的聚糖,并介导肠道中的许多生物过程,尤其是宿主-微生物相互作用。
释放的岩藻糖可被微生物用作膳食聚糖、能量来源或合成结构蛋白。肠道中岩藻糖的变化影响微生物群的定植。
岩藻多糖
岩藻多糖是一种含有岩藻糖和硫酸基团的多糖,可改善糖尿病肾病。
一项小鼠研究发现,岩藻多糖可显著改善肾小球滤过率高滤过和肾纤维化,其机制与短链脂肪酸产生菌富集、增加盲肠内乙酸浓度、提高肾脏ATP水平以及改善线粒体功能障碍有关。此外,岩藻多糖还可通过抑制MAPKs通路来改善肾脏炎症和纤维化。总之,岩藻多糖可通过改善线粒体氧化应激和抑制MAPKs通路,靶向肠道菌群-线粒体轴,改善早期糖尿病肾病。
桑叶的药用功能最早在2000多年前的汉代被发现,并记载于《神农本草经》。明代李时珍在《本草纲目》中对桑叶的药用功效有更详细的描述,包括活血化瘀、祛风、清热解毒等功能。桑叶已被列入国家卫生健康委员会公布的食药同源资源名单。
桑叶多糖(Mulberry Leaves Polysaccharides,MLPs)是从桑树(Morus alba L.)叶片中提取的一种植物多糖。它们是桑叶中主要的活性成分之一,由多种单糖组成,主要包括木糖、阿拉伯糖、果糖、半乳糖、葡萄糖、甘露糖等。
桑叶多糖对人体的影响
桑叶多糖具有多种生物学活性,包括降低血糖、抗氧化、免疫调节、抗肿瘤、抗菌、抗凝和调节肠道菌群等。这些活性使得MLPs在医药和食品领域具有广泛的应用前景。并且安全、有效、低毒、副作用小。
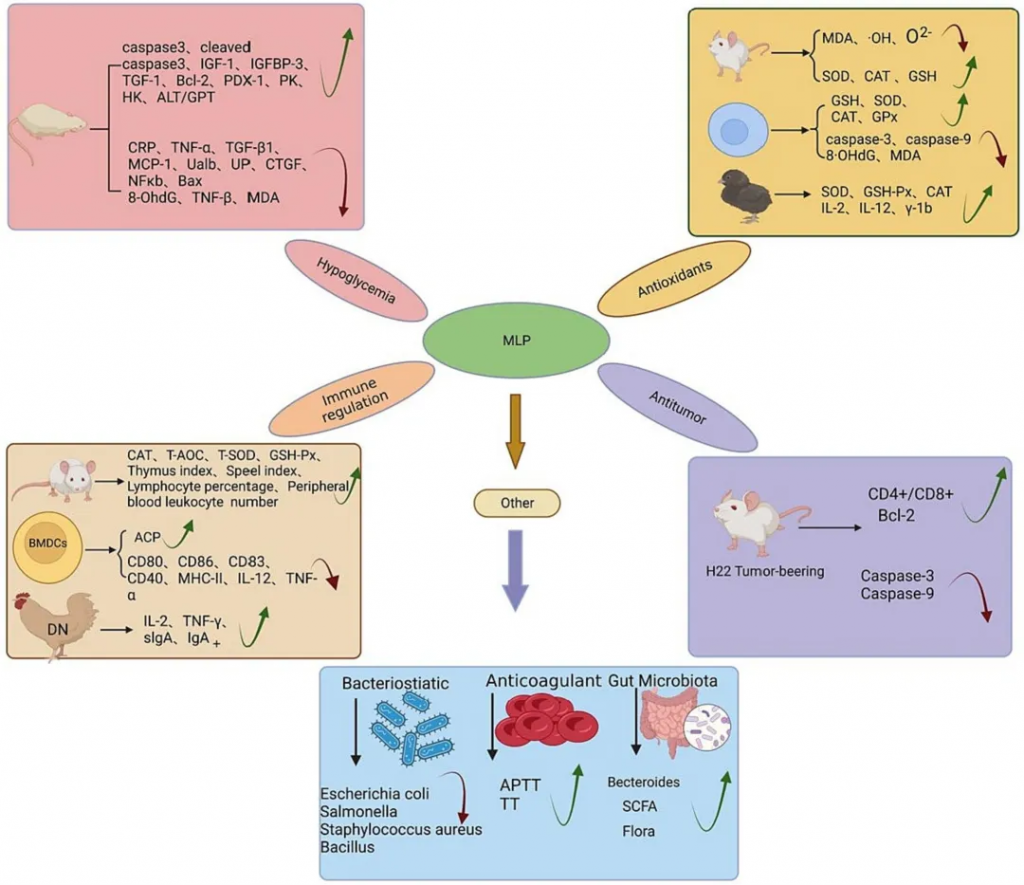
doi.org/10.1016/j.ijbiomac.2023.128669
桑叶多糖对肠道菌群的影响
桑叶多糖通过调节肠道菌群的平衡,进而对人体的健康产生积极的影响。以下是桑叶多糖影响的肠道菌群及其变化情况:

桑叶多糖能够调节短链脂肪酸和肠道菌群的相对丰度,降低真细菌与过敏性细菌的比例,从而改善肠道屏障功能。
沙棘果实在藏族食品和药物中已有数千年的传统。沙棘多糖 (SP) 是沙棘果实中的主要功能成分之一。
对高脂饮食诱导的肥胖小鼠:沙棘多糖治疗提高了 p-AMPKα 和 PPARα 蛋白的表达,刺激了小鼠肝脏中 ACC1 的磷酸化,并抑制了 FAS、PPARγ 和 CD36 的蛋白表达。
沙棘多糖上调Muribaculaceae_unclassified、双歧杆菌、Rikenellaceae_RC9_gut_group、Alistipes、Bacteroides的比例,并下调Lactobacillus、 Firmicutes_unclassified 、Dubosiella Bilophila、 Streptococcus 的比例,重组了HFD诱导的肥胖小鼠的肠道微生物群。
此外,粪便中的微生物代谢物短链脂肪酸 (SCFAs) 的产生也有所增加。此外,相关性分析结果表明沙棘多糖的肥胖改善作用与粪便中的SCFAs水平高度相关。因此,沙棘多糖对肝脏脂质代谢的调节可能是由于肠道微生物群的变化和SCFAs产生量的增加。这些结果表明,沙棘多糖可以通过调节肠-肝轴发挥改善肥胖的潜在营养保健作用。
蘑菇多糖是一类存在于蘑菇中的生物活性多糖,它们包括但不限于几丁质、甘露聚糖、半乳糖聚糖、木聚糖、葡聚糖、云芝多糖、灵芝多糖、半纤维素。这些多糖在蘑菇细胞壁中含量丰富,赋予蘑菇独特的结构和生物活性。
蘑菇多糖的功效
蘑菇多糖对人体具有多种潜在的健康益处。它们可以增强免疫系统、具有抗肿瘤活性、调节肠道菌群、抗氧化、抗糖尿病、抗衰老作用。
蘑菇多糖对肠道菌群的影响
促进益生菌生长
蘑菇多糖通过选择性地促进益生菌的生长,增强肠道健康。例如,灵芝和茯苓中的多糖被发现可以增加有益细菌的数量,这些细菌可以对抗肥胖、产生短链脂肪酸和乳酸。香菇中的多糖也显示出对嗜酸乳杆菌(Lactobacillus acidophilus)有促进作用。
抑制病原菌
蘑菇多糖能够通过增强肠道屏障功能和促进益生菌的生长来间接抑制病原菌。双孢蘑菇中的多糖已被证明可以限制大肠杆菌的生长。
增强肠道屏障功能
蘑菇多糖通过增强肠道上皮细胞的功能,提高肠道屏障的完整性,减少有害物质的渗透。云芝(Trametes versicolor)中的多糖肽PSK和PSP能够调节肠道菌群,增加有益菌双歧杆菌和乳杆菌的数量,同时减少有害菌如梭状芽孢杆菌和金黄色葡萄球菌。在降低腹泻、艰难梭菌感染、炎症性肠病等方面发挥作用。
调节免疫反应
蘑菇多糖通过激活肠道相关淋巴组织,增强机体的免疫反应。灵芝多糖能刺激和增加免疫细胞如自然杀伤细胞、T淋巴细胞和巨噬细胞的数量。
产生短链脂肪酸
蘑菇多糖在肠道发酵过程中产生短链脂肪酸,这些物质对维持肠道健康和调节宿主代谢具有重要作用。蚝菇(Pleurotus ostreatus)中的β-葡聚糖衍生物能够诱导前列腺癌细胞的凋亡,并且显示出免疫调节、巨噬细胞激活、抗肿瘤和免疫刺激活性。

多糖的多样性和复杂性使其在人体内的作用千变万化,它们能够通过与肠道菌群的互动,从调节免疫功能到改善代谢性疾病等。
然而,利用天然多糖通过肠道菌群治疗疾病仍存在一些限制和挑战。对肠道菌群和多糖之间相互作用的全面了解需要进一步研究,由于大多数研究都是在动物身上进行的,因此开展研究多糖-微生物组-疾病相互作用的临床试验并实现临床转化至关重要。
幸运的是,随着生命科学领域新兴技术的发展,我们有了更多的工具来揭示这些复杂问题。高通量测序技术、多组学技术、人工智能和大数据分析的交叉融合,为研究多糖和肠道菌群的相互作用提供了强大的技术支持,推动了这一领域的快速发展。
此外,多糖与肠道菌群之间的相互作用不仅揭示了多糖的生物活性,也突显了肠道菌群对健康的重要贡献。多糖与肠道菌群的相互作用为我们提供了一个全新的视角,了解个体的肠道菌群组成,不仅有助于我们理解自身的健康状况,更为个性化的营养和健康管理提供了科学依据。肠道菌群检测可以揭示个体对多糖等营养成分的响应差异,从而为制定个性化的饮食和治疗计划提供指导。
注:本账号内容仅作交流参考,不作为诊断及医疗依据。
主要参考文献
Xue H, Mei CF, Wang FY, Tang XD. Relationship among Chinese herb polysaccharide (CHP), gut microbiota, and chronic diarrhea and impact of CHP on chronic diarrhea. Food Sci Nutr. 2023 Aug 6;11(10):5837-5855.
Xu X, Wang L, Zhang K, Zhang Y, Fan G. Managing metabolic diseases: The roles and therapeutic prospects of herb-derived polysaccharides. Biomed Pharmacother. 2023 May;161:114538
Zhang D, Liu J, Cheng H, Wang H, Tan Y, Feng W, Peng C. Interactions between polysaccharides and gut microbiota: A metabolomic and microbial review. Food Res Int. 2022 Oct;160:111653.
Chen R, Zhou X, Deng Q, Yang M, Li S, Zhang Q, Sun Y, Chen H. Extraction, structural characterization and biological activities of polysaccharides from mulberry leaves: A review. Int J Biol Macromol. 2024 Feb;257(Pt 2):128669.
Lan Y, Sun Q, Ma Z, Peng J, Zhang M, Wang C, Zhang X, Yan X, Chang L, Hou X, Qiao R, Mulati A, Zhou Y, Zhang Q, Liu Z, Liu X. Seabuckthorn polysaccharide ameliorates high-fat diet-induced obesity by gut microbiota-SCFAs-liver axis. Food Funct. 2022 Mar 7;13(5):2925-2937.
Feng Y, Song Y, Zhou J, Duan Y, Kong T, Ma H, Zhang H. Recent progress of Lycium barbarum polysaccharides on intestinal microbiota, microbial metabolites and health: a review. Crit Rev Food Sci Nutr. 2024;64(10):2917-2940.
Cui L, Guan X, Ding W, Luo Y, Wang W, Bu W, Song J, Tan X, Sun E, Ning Q, Liu G, Jia X, Feng L. Scutellaria baicalensis Georgi polysaccharide ameliorates DSS-induced ulcerative colitis by improving intestinal barrier function and modulating gut microbiota. Int J Biol Macromol. 2021 Jan 1;166:1035-1045.
Tang YF, Xie WY, Wu HY, Guo HX, Wei FH, Ren WZ, Gao W, Yuan B. Huaier Polysaccharide Alleviates Dextran Sulphate Sodium Salt-Induced Colitis by Inhibiting Inflammation and Oxidative Stress, Maintaining the Intestinal Barrier, and Modulating Gut Microbiota. Nutrients. 2024 Apr 30;16(9):1368.
Zhao Q, Jiang Y, Zhao Q, Patrick Manzi H, Su L, Liu D, Huang X, Long D, Tang Z, Zhang Y. The benefits of edible mushroom polysaccharides for health and their influence on gut microbiota: a review. Front Nutr. 2023 Jul 6;10:1213010.
Álvarez-Mercado AI, Plaza-Diaz J. Dietary Polysaccharides as Modulators of the Gut Microbiota Ecosystem: An Update on Their Impact on Health. Nutrients. 2022 Oct 3;14(19):4116.
Tang M, Cheng L, Liu Y, Wu Z, Zhang X, Luo S. Plant Polysaccharides Modulate Immune Function via the Gut Microbiome and May Have Potential in COVID-19 Therapy. Molecules. 2022 Apr 26;27(9):2773.
Sun CY, Zheng ZL, Chen CW, Lu BW, Liu D. Targeting Gut Microbiota With Natural Polysaccharides: Effective Interventions Against High-Fat Diet-Induced Metabolic Diseases. Front Microbiol. 2022 Mar 15;13:859206.
Gan L, Wang J, Guo Y. Polysaccharides influence human health via microbiota-dependent and -independent pathways. Front Nutr. 2022 Nov 9;9:1030063.
Chen J, Gao Y, Zhang Y, Wang M. Research progress in the treatment of inflammatory bowel disease with natural polysaccharides and related structure-activity relationships. Food Funct. 2024 Jun 4;15(11):5680-5702.
Chen P , Hei M , Kong L , Liu Y , Yang Y , Mu H , Zhang X , Zhao S , Duan J . One water-soluble polysaccharide from Ginkgo biloba leaves with antidepressant activities via modulation of the gut microbiome. Food Funct. 2019 Dec 11;10(12):8161-8171.
Wang, A.; Liu, Y.; Zeng, S.; Liu, Y.; Li, W.; Wu, D.; Wu, X.; Zou, L.; Chen, H. Dietary Plant Polysaccharides for Cancer Prevention: Role of Immune Cells and Gut Microbiota, Challenges and Perspectives. Nutrients 2023, 15, 3019.
Zhou, Y.; Chu, Z.; Luo, Y.; Yang, F.; Cao, F.; Luo, F.; Lin, Q. Dietary Polysaccharides Exert Anti-Fatigue Functions via the Gut-Muscle Axis: Advances and Prospectives. Foods 2023, 12, 3083
Shen, Y.; Song, M.; Wu, S.; Zhao, H.; Zhang, Y. Plant-Based Dietary Fibers and Polysaccharides as Modulators of Gut Microbiota in Intestinal and Lung Inflammation: Current State and Challenges. Nutrients 2023, 15, 3321
Lv H, Jia H, Cai W, Cao R, Xue C, Dong N. Rehmannia glutinosa polysaccharides attenuates colitis via reshaping gut microbiota and short-chain fatty acid production. J Sci Food Agric. 2023 Jun;103(8):3926-3938.


短链脂肪酸这一词经常出现在谷禾的文章和报告中,那你真的了解短链脂肪酸吗?短链脂肪酸(SCFA)主要是肠道微生物群在结肠内通过发酵碳水化合物(包括膳食和内源性碳水化合物,主要是抗性淀粉和膳食纤维)和一些微生物可利用的蛋白质而产生的。
短链脂肪酸主要是乙酸、丙酸和丁酸,在结肠中的浓度比大致为60-70%:20-30%:10-20%。这些代谢产物能够被宿主利用,尤其是丙酸和丁酸,它们发挥一系列促进健康的功能。它们能被肠粘膜有效吸收,作为能量来源,还能作为基因表达调节剂以及特定受体识别的信号分子,对宿主生理产生重要影响。近几年的研究还发现其能够调节免疫细胞发育并抑制炎症。
然而,三种主要短链脂肪酸——乙酸盐、丙酸盐和丁酸盐——它们在体内的功能和组织分布不同,对宿主生理的影响存在显著差异。丁酸盐优先被肠粘膜用作能量来源,还具有抗炎特性,可增强肠道屏障功能和粘膜免疫。丙酸盐有助于抵抗肝脏中的脂肪形成、降低胆固醇、也有一定的抗炎和抗致癌作用。而乙酸在血液中浓度最高,可用作肝脏胆固醇和脂肪酸合成的底物,增加结肠血流量和氧气吸收,并通过影响回肠收缩来增强回肠运动。
其次,它们与宿主蛋白(如丁酸和丙酸抑制组蛋白去乙酰化酶)和受体的相互作用也不同。因此,特别需要考虑这些短链脂肪酸的微生物来源。与此同时,饮食结构和肠道生理变化如何影响这些脂肪酸的相对产量和在结肠中的浓度也是至关重要的。
本文将重点介绍丙酸盐和丁酸盐,因为这两种短链脂肪酸被认为对健康有重要影响,包括丁酸预防结直肠癌,丙酸促进饱腹感并降低胆固醇。而乙酸是大多数肠道厌氧菌的主要发酵产物,也可由还原性乙酸生成,而丙酸和丁酸则由不同的肠道细菌群产生。
我们将探讨在人类结肠微生物群中已知的形成这两种短链脂肪酸的途径,以及各种饮食和环境因素对其产生的调节可能性。详细了解肠道微生物群的短链脂肪酸代谢及其生理功能对于制定个性化的健康营养方案是必不可少的。
丙酸盐和丁酸盐在结构、来源、生理功能以及对健康的影响方面存在一些差异。
▸ 结构上的差异:
丙酸盐(Propionate)含有三个碳原子,羟基(-OH)位于第二个碳原子上。
丁酸盐(Butyrate)含有四个碳原子,羟基(-OH)位于第四个碳原子上。
▸ 来源上的差异:
丙酸盐通常由肠道细菌通过发酵L-鼠李糖、聚葡萄糖、阿拉伯木聚糖、D-塔格糖、甘露寡糖、昆布多糖等糖类物质产生。
丁酸盐可以通过肠道微生物群发酵富含抗性淀粉和果聚糖的食物来增加,如菊粉、马铃薯、洋葱等。
▸ 功能上的差异:
丙酸盐在体内的主要功能是作为肝脏中糖原合成的前体物质,有助于调节血糖水平,影响食欲。
丁酸盐是结肠上皮细胞的首选能源,有助于维持肠道屏障,发挥免疫调节和抗炎作用。丁酸盐还可以通过减少NF-kB信号传导和诱导凋亡来促进神经保护。
▸ 对健康的影响:
丙酸盐的健康益处主要是调节能量代谢和改善代谢综合征,可能对调节肠道菌群平衡也有积极作用,但其具体影响取决于个体的肠道菌群组成。
丁酸盐对健康的影响更为广泛,包括维持肠道稳态、促进肠道屏障的完整性、刺激绒毛的生长、促进粘蛋白的产生。以及改善认知功能、促进睡眠、调节社交行为和在糖尿病中的潜在益处。
丙酸盐是许多生物(从细菌到人类)的代谢副产物,产生丙酸的代谢途径可分为三类。主要发酵途径将不同的碳源分解代谢为丙酸盐(图A);分解代谢途径则能将多种氨基酸降解为丙酸盐(图B);此外,通过与从丙酮酸或二氧化碳生成生物质前体相关的合成代谢途径也可以生产丙酸盐(图C)。
产生丙酸盐的代谢途径
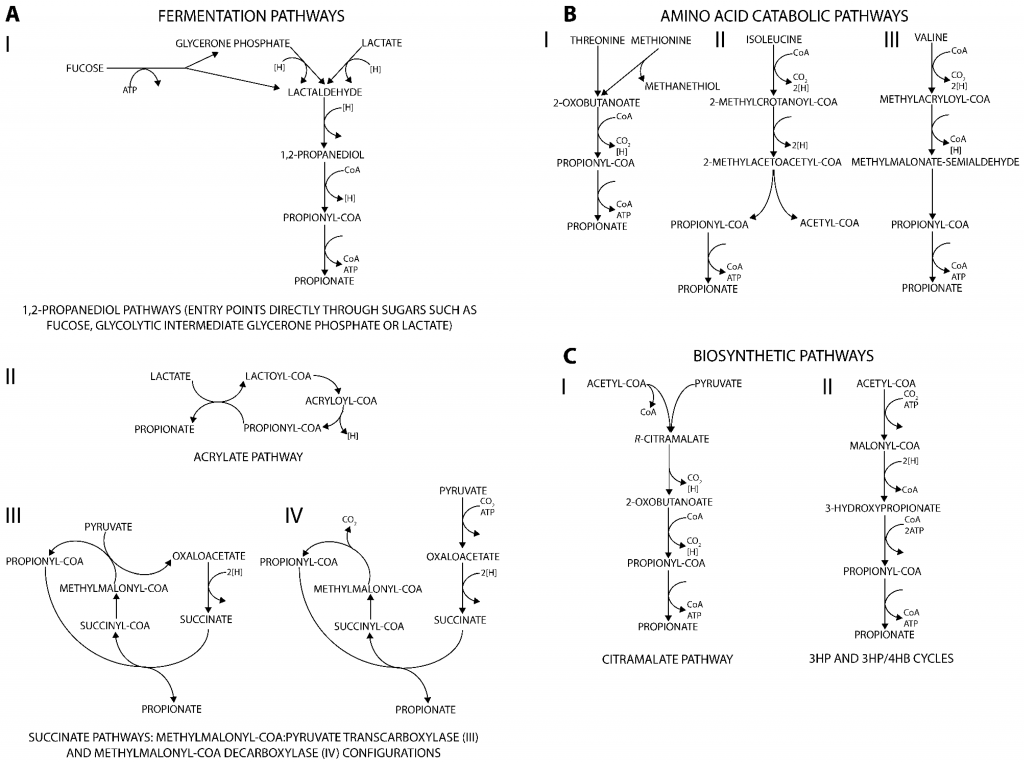
doi.org/10.3390/fermentation3020021
肠道微生物通过发酵不可消化的碳水化合物产生的丙酸盐是体内丙酸盐的主要来源。下面将讲述肠道中丙酸盐通过发酵碳水化合物的三种主要产生途径以及参与这些途径的微生物。
与氨基酸降解和生物合成途径相比,发酵途径不仅提供能量,还帮助消耗由糖分解代谢产生的还原辅因子。它们在能量产生和维持氧化还原平衡中的作用,使这些途径能够与细胞生长相耦合。
能够产生丙酸盐的微生物种类

doi.org/10.3390/fermentation3020021
▸
丙二醇相关途径
• 鼠伤寒沙门氏菌和Roseburia inulinivorans在这一过程可以产生丙酸
丙酸盐在肠胃中的生成是由1,2-丙二醇(PDO)发酵菌和PDO消耗菌组成的微生物联合作用的结果。已知一些生物体(如鼠伤寒沙门氏菌和Roseburia inulinivorans)能同时进行这两种过程。
在二醇脱水酶和两种常与乙酸代谢相关的混杂酶(辅酶A依赖性醛脱氢酶磷酸转酰基酶和乙酸激酶)的共同作用下,PDO分解代谢为丙酸,同时生成一个ATP和一个还原辅因子。
然而,通过该途径产生丙酸取决于可用于其他细菌生长的碳水化合物,据报道岩藻糖和鼠李糖是丙酸的前体。
通过1,2-丙二醇形成丙酸的微生物途径
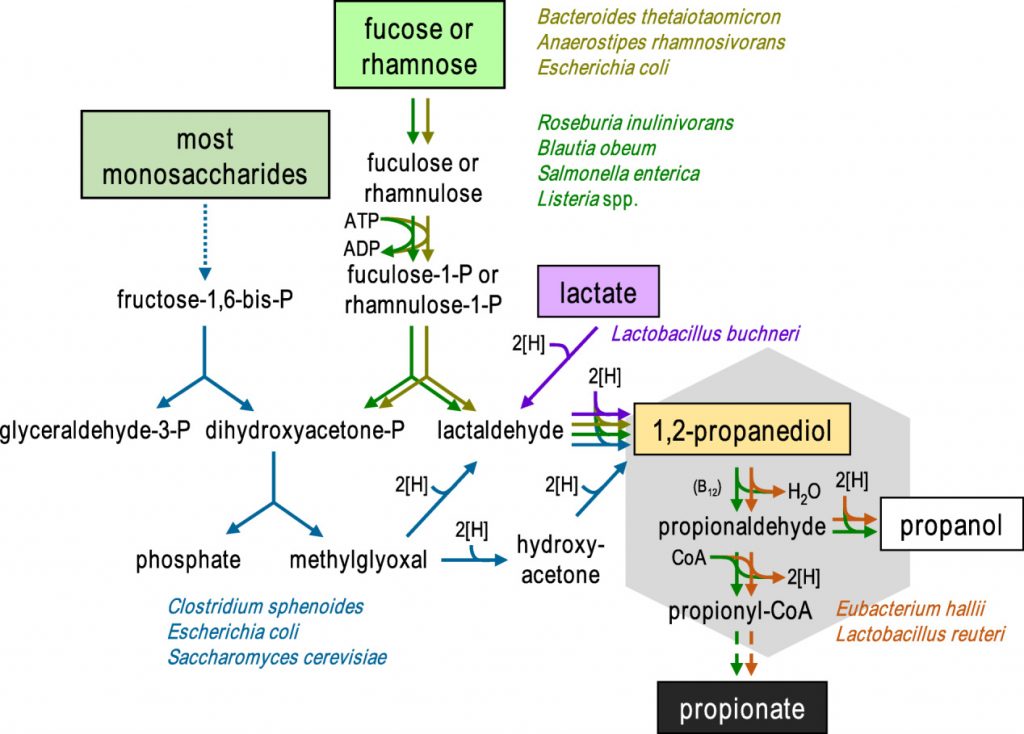
doi: 10.1111/1462-2920.13589.
霍氏大肠杆菌(E.hallii)和罗伊氏乳杆菌(Lactobacillus reuteri)虽然无法在岩藻糖或鼠李糖上生长,但仍然能够利用1,2-丙二醇产生丙酸和丙醇。此外,宏基因组研究表明,其他肠道厌氧菌,包括Flavonifractor plautii、Intestinimonas butyriproducens和Veillonella spp. 也可能能够从这种底物中产生丙酸。因此,不同细菌之间中间体 1,2-丙二醇可能在脱氧糖生产丙酸中发挥重要作用。
▸ 丙烯酸酯途径
丙烯酸酯途径在消耗NADH的情况下,使乳酸在ATP中性条件下转化为丙酸。该途径存在于几种细菌中,包括丙酸梭菌(Clostridium propionicum)、埃氏巨球菌(Megasphaera elsdenii)和瘤胃普氏菌(Prevotella ruminicola)。
虽然多种底物可以分解为丙酸和乙酸,包括乳酸、丝氨酸、丙氨酸和乙醇,但葡萄糖发酵在这过程中似乎不会导致任何天然生产者产生丙酸,这可能是因为葡萄糖发酵不会触发启动循环所需的乳酸消旋酶的表达。
▸ 琥珀酸途径
琥珀酸途径主要存在于拟杆菌门和厚壁菌门中,拟杆菌门的一些细菌从膳食碳水化合物生成丙酸,并且拟杆菌门的相对丰度与人类粪便中丙酸盐的相对水平相关。
• 琥珀酸转化为丙酸盐还需要维生素B12
琥珀酸是丙酸的前体,但在高pCO2(二氧化碳分压)和高稀释率等条件下,它可在磷酸烯醇式丙酮酸羧激酶受到抑制的拟杆菌属培养物中积累。琥珀酸转化为丙酸还需要维生素B12,如果缺乏B12,琥珀酸可能无法转化成丙酸盐。
人类结肠中的一些厚壁菌门细菌(例如Phascolarctobacterium succinatutens)能将琥珀酸转化为丙酸;其他革兰氏阴性菌通过琥珀酸途径(如韦荣氏球菌属)或丙烯酸酯途径(Megasphaera elsdenii)将乳酸转化为丙酸盐。
▸ 氨基酸降解产生丙酸
缬氨酸、苏氨酸、异亮氨酸和蛋氨酸的降解可导致通过丙酰辅酶A产生丙酸和ATP。
由于氨基酸的合成和随后的分解代谢途径存在于多种微生物中,因此可以使用氨基酸合成代谢和分解代谢途径的组合从葡萄糖生产丙酸。
几种拟杆菌在蛋白水解和肽形成丙酸方面发挥重要作用。
苏氨酸的产生和分解代谢已在大肠杆菌中得到广泛研究,作为丙酰辅酶A的可能来源,可用于生产各种化学物质,包括丙醇、红霉素和3-羟基戊酸。此外,考虑到氧化还原和能量平衡,缬氨酸/异亮氨酸和苏氨酸途径的组合具有协同作用,可以略微提高丙酸产量。
除此之外,可以利用丙酮酸经过柠檬酸途径产生丙酸,由于和菌群关联较小,在这就不展开描述了。
▸ 增加丙酸盐生成的底物
一些益生元等化合物可以影响丙酸盐的生产,不过由于浓度以及肠道微生物群落构成的不同,这些化合物的调节丙酸盐产生时具有一定差异。
• L-鼠李糖能够明显增加丙酸盐产量
L-鼠李糖或6-脱氧-L-甘露糖是一种天然脱氧糖。它存在于多种动物、植物和细菌多糖中。在短期体外实验中,L-鼠李糖已被证明能使丙酸产量增加四倍于乳果糖。
在一项人体体内研究中也获得了类似的结果,其中受试者在三个不同的时间被给予25克L-鼠李糖、乳果糖或D-葡萄糖。摄入后24小时测量血清丙酸,L-鼠李糖的血清丙酸明显高于乳果糖或D-葡萄糖的血清丙酸。
一项长期研究也证实了L-鼠李糖诱导丙酸的作用,该研究结果表明,与摄入D-葡萄糖作为对照相比,摄入25克L-鼠李糖可显著提高人体28天内的血清丙酸水平。
• 抗性淀粉有助于增加丙酸
抗性淀粉对淀粉酶降解具有抗性,但它会发酵成丁酸或丙酸。特别是,来自大米的抗性淀粉与丙酸产量增加有关。
研究了抗性淀粉在大鼠体内的发酵情况,饲喂抗性淀粉(630g/kg饲料)的大鼠的肝脏甘油三酯和总胆固醇浓度显著低于对照组。与此同时,血清丙酸浓度也显著增加。
• 菊粉对于增加丙酸和丁酸非常有效
菊粉属于果聚糖家族,主要由β-(2,1)连接的果糖基组成。它天然存在于菊苣和菊芋等开花植物中。作为益生元,菊粉已被证明对增加丁酸和丙酸的产量非常有效。使用人体肠道微生物体外模拟研究了菊粉增加丙酸的效果。
补充菊粉1周(5g/d)后观察到短链脂肪酸产生的代谢变化。较高浓度的短链脂肪酸源于丙酸和丁酸产量的增加。
此外一项针对喂食菊粉(10%)的大鼠的体内研究也导致丙酸产量大幅增加,高达 58.4mmol/。
• 聚葡萄糖
聚葡萄糖是一种支链、随机聚合的多糖,主要由葡萄糖合成,在胃肠道上部不会被消化。使用结肠模拟器研究了这种底物对结肠微生物组成和代谢活性的调节作用。与对照糖木糖醇(8.3mmol/L)相比,短链脂肪酸产量显著增加,尤其是丙酸盐(22.9mmol/L)。
• 阿拉伯木聚糖
阿拉伯木聚糖是许多谷物中发现的主要非淀粉多糖,是膳食纤维的一部分。
在体内研究中,比较了54只大鼠,这些大鼠分别喂食对照饮食(含710g/kg小麦)、阿拉伯木聚糖补充饮食(610g/kg小麦淀粉加100g/kg玉米阿拉伯木聚糖)和胆固醇补充饮食(不含或含2g/kg 胆固醇)。由于短链脂肪酸的积累,尤其是丙酸(摩尔百分比>45%),盲肠pH值从7降至6。然而,丁酸的产生不受影响。
车前草是一种可溶性纤维来源,可提供与麦麸阿拉伯木聚糖相当的多糖。在一项大鼠体内研究中,比较了车前草(5%)对盲肠和结肠发酵的影响与麦麸 (10%) 的影响。研究发现,车前草发酵可产生更高的短链脂肪酸,尤其是盲肠和所有结肠中的丙酸更多。
除此之外,D-塔格糖、甘露寡糖、昆布多糖等物质也可以增加人体丙酸盐的产生。
丙酸盐已被证明具有抗脂肪形成和降低胆固醇的作用。它还对体重控制和进食行为有很强的影响。此外,有研究表明,丙酸和丁酸一样,对结肠癌细胞具有抗增殖作用。
丙酸盐对健康的影响
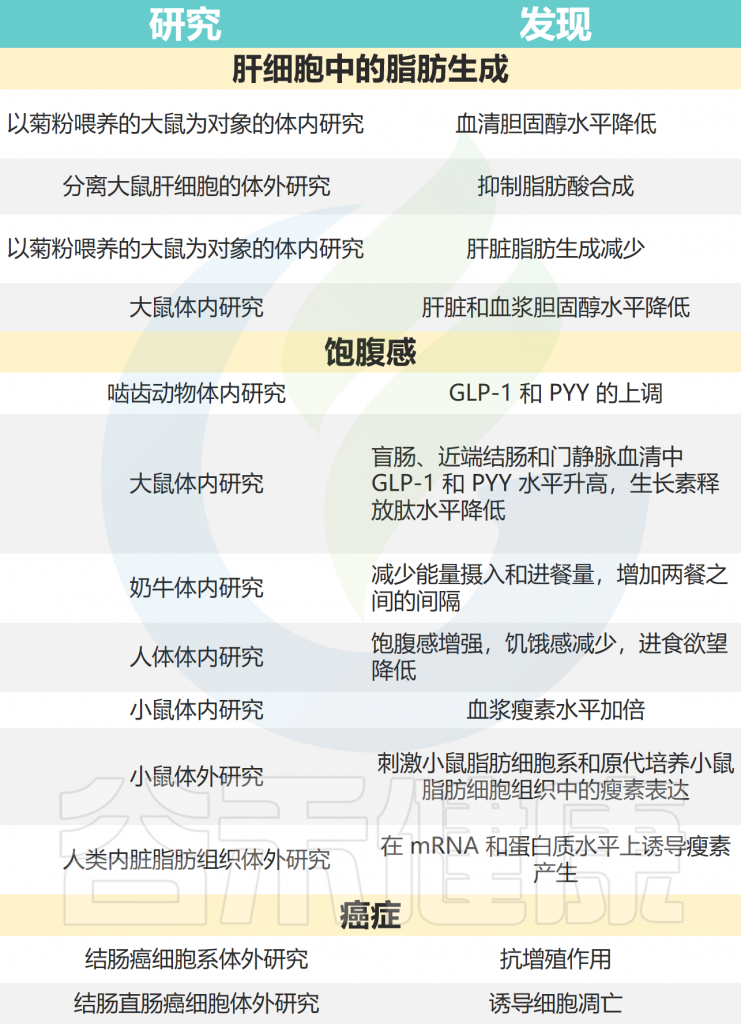
doi: 10.1111/j.1753-4887.
然而,与结肠细胞用作能量来源的丁酸不同,丙酸在血液循环中的浓度较高。因此,丙酸的生物活性可能不仅限于结肠本身,还扩展到人体的其他部位。需要强调的是,了解体内结肠丙酸浓度或短链脂肪酸浓度不足以推断健康状况。
▸ 影响肝细胞的脂质合成
肝脏的脂质合成包括将饮食来源的脂肪酸和甘油转化为具有不同脂肪酸组成的胆固醇和甘油三酯。然后,这些肝脏脂质分子被结合到脂蛋白中,从而通过循环分布到各种组织中。
• 脂质合成受到短链脂肪酸的强烈影响
有趣的是,肝细胞中的脂质合成受到肠道纤维发酵产生的短链脂肪酸的数量和类型的强烈影响。丙酸盐已被确定在其中一些过程中发挥重要作用。
对肝脏脂质合成的饮食调节早期观察显示,膳食纤维摄入与肝脏脂质合成密切相关。这种影响的部分原因如下:1)粪便中胆固醇和胆汁酸从肠道排出的增加;2)胆固醇向胆汁酸的肝脏转化率较高;3)通过减少乳糜微粒的大小和降低胆固醇在乳糜微粒中的掺入来优化脂蛋白的外周代谢。
• 降低血清胆固醇水平、抑制脂肪酸合成
短链脂肪酸作为微生物碳水化合物发酵的产物,在肝脏脂质合成中发挥着特定作用,已被证明在喂食大鼠时可降低血清胆固醇水平。对分离的大鼠肝细胞的体外研究表明,丙酸对脂肪酸合成有抑制作用,但对胆固醇合成没有抑制作用。
其他大鼠实验表明,加入纤维的饮食可降低肝和血浆胆固醇水平及血浆甘油三酯中的胆固醇,而肝甘油三酯没有受到影响。
尽管这些研究的结果令人信服,但其他研究并不总是能够证实丙酸盐对脂质代谢的抑制作用。例如,每天在面包中补充9.9克丙酸盐不会改变6名健康志愿者的脂质代谢,甚至会导致5名受试者的甘油三酯浓度升高。
在另一项研究中,比较了丙酸盐对人和大鼠肝细胞脂质代谢的影响。发现浓度为0.1mmol/L的丙酸盐对大鼠乙酸盐合成脂质有抑制作用。然而,在人类肝细胞中,需要更高浓度的丙酸盐(约10-20 mmol/L)才能获得同样的抑制作用。该值比门静脉血中丙酸盐的浓度高100-200倍,表明大鼠模型不能完全外推到人类的情况。
▸ 作为影响饱腹感的分子
丙酸盐不仅具有降低胆固醇和抗脂肪生成的作用,还可能通过刺激饱腹感来控制体重。已有研究表明,短链脂肪酸(如乙酸、丙酸、丁酸)具有诱发饱腹感的作用。
• 丙酸盐影响肠道激素的形成进而影响饱腹感
现有证据表明,细菌调节肠道激素(如胰高血糖素样肽1(GLP-1)和肽YY(PYY))的形成,是通过短链脂肪酸介导的。乙酸、丙酸和丁酸的生理浓度,以及pH值从7.5降至6.0,会显著增加肠内分泌结肠细胞系STC-1中的胰高血糖素原和PYY。
GLP-1和PYY是刺激饱腹感的激素,由L细胞(主要位于回肠和结肠)响应营养摄入而释放。GLP-1促进胰岛素分泌和胰腺β细胞增殖,同时控制肌肉细胞中的糖原合成;而PYY则减缓胃排空。相反,生长素释放肽刺激食欲,主要由胃中的P/D1细胞产生。
不易消化的碳水化合物,如低聚果糖、乳糖醇和抗性淀粉,通过调节肠道肽GLP-1、PYY和生长素释放肽的产生,有效地诱导饱腹感,这一机制还涉及肠道微生物群落。
• 丙酸盐对摄食行为有显著影响,诱导瘦素产生
在短链脂肪酸中,丙酸盐被重点研究作为一种饱腹感诱导剂,对能量摄入和摄食行为有显著影响。人体和动物试验表明,丙酸盐给药(体内范围为130-930mmol/L,体外范围为0.01-10mmol/L)显著增强饱腹感并降低进食欲望。
丙酸盐触发的饱腹感信号之一是瘦素,这是一种强效的厌食激素,通过中枢神经系统中表达的受体抑制食物摄入。研究显示,每天服用500µmol的丙酸盐几乎使小鼠血浆中的瘦素浓度翻了一倍。
在另一项研究中,浓度为3mmol/L的丙酸在mRNA和蛋白质水平上诱导了人内脏脂肪组织中瘦素的产生。这些数据表明,肠道微生物群对肥胖的调节作用可能部分由短链脂肪酸(特别是来自微生物碳水化合物发酵的丙酸)介导。
▸ 影响心脑血管健康
丙酸盐通过与肠道受体GPR 41和GPR 43(也称为脂肪酸受体FFAR2和FFAR3)相互作用,对心脑血管健康具有一些潜在的影响。
• 脑血管患者体内的丙酸盐含量较低
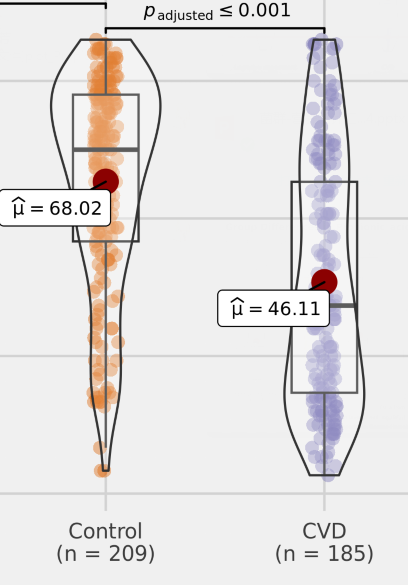
编辑
谷禾的数据中发现,与健康对照相比,脑血管疾病患者中的丙酸盐含量较低,并且具有明显的统计学差异。因此丙酸盐的含量可能是影响心脑血管健康的一个重要指标。
• 较高的丙酸盐浓度患冠状动脉硬化风险较低
最近一项大型横断面研究表明血浆丙酸浓度与冠状动脉疾病存在关联,较高浓度的丙酸盐与较低的冠状动脉粥样硬(CAD)风险相关,且与已知的心血管风险因素无关。
如上所述,越来越多的实验数据表明,丙酸盐可能对高血压、内皮功能障碍和高胆固醇血症等心血管风险因素产生有益影响。
▸ 丙酸盐在癌症中的潜在作用
短链脂肪酸对癌症(尤其是结肠癌)的影响已被广泛研究。丁酸能够调节基因表达,并对细胞凋亡和细胞周期的关键调节因子产生影响。
几种机制促成了丁酸对基因表达的调节作用。这些机制包括组蛋白和非组蛋白的过度乙酰化以及DNA甲基化的改变,从而增强了转录因子对核小体DNA的可及性。
• 丙酸盐诱导结直肠癌细胞凋亡
在一项研究中,丙酸盐和乙酸盐(浓度分别为26-40和9-16mmol/L)在人类结直肠癌细胞系中诱导了典型的细胞凋亡迹象。这些迹象包括线粒体跨膜电位的丧失、活性氧的产生、胱天蛋白酶3加工和核染色质凝聚。
• 抑制结肠癌细胞系的生长
短链脂肪酸对结肠上皮细胞增殖具有矛盾作用。虽然这些阴离子刺激正常隐窝细胞,但它们抑制结肠癌细胞系的生长。
丁酸盐和丙酸盐也是诱导分化和细胞凋亡的最有效脂肪酸。因此,它们通常可以预防癌症的发展,尤其是预防结直肠癌。虽然丁酸比丙酸更有效,但它主要被结肠细胞吸收作为能量来源。相比之下,丙酸和乙酸盐进入血液循环的浓度比丁酸高得多,并且它们被肝脏大量吸收(约60%)。由于这些阴离子在肝脏中的浓度很高,它们很可能会影响肝癌细胞以及已知会导致肝脏转移的其他典型癌细胞,例如乳腺癌和结肠癌。
一项针对猝死患者的研究表明,外周血中的短链脂肪酸数量可以量化。因此,这种循环中的丙酸盐、乙酸盐和丁酸盐的抗癌作用非常值得研究;例如,这种影响会在多大程度上延伸到小肠、大肠和肝脏之外,从而影响不同的组织?
!
• 丙酸盐过量可能与阿尔茨海默病相关
最近的几项研究提供了丙酸盐与阿尔茨海默病(AD)之间联系的证据。例如,分析了阿尔茨海默病患者和健康对照者的唾液样本,发现阿尔茨海默病患者的丙酸水平比健康对照者高出1.35倍。分析了轻度认知障碍者、阿尔茨海默病患者和健康对照者的唾液样本,也发现AD患者的丙酸水平显著升高。
几项啮齿动物研究也将粪便和循环中丙酸盐水平与阿尔茨海默病联系起来。接受AD患者粪便微生物群移植的小鼠丙酸水平高于对照组。
此外,发现阿尔茨海默病小鼠海马体中的丙酸增加了1.23倍。也发现阿尔茨海默病小鼠前额叶皮层中的丙酸浓度显著高于野生型小鼠,6个月大的阿尔茨海默病小鼠粪便中的丙酸浓度也显著更高。
• 丙酸血症的丙酸盐代谢异常
丙酸血症是人类最常见的有机酸代谢紊乱,是一种由丙酰辅酶A羧化酶基因缺陷引起的先天性代谢错误,丙酸过量且无法通过丙酰辅酶A转化。
丙酸血症患者的体内丙酸及其代谢物水平显著升高,会引起代谢性酸中毒、血氨升高,可能还会诱导一些严重的并发症如脑损伤、心肌病发生。
•有研究认为过多的丙酸盐可能导致肥胖和糖尿病
2019年哈佛大学公共卫生学院发表的一篇文献称:小鼠长期接触丙酸将导致肝细胞产生更多葡萄糖,形成高血糖症,这是糖尿病的一个典型特征。此外,研究人员还发现,长期服用丙酸盐剂量的小鼠,其体重会显著增加,胰岛素抗性也会增大。
还对14名健康人开展对照试验,受试者被随机分为两组,其中一组的餐食中添加1克丙酸盐,另一组添加安慰剂。结果显示,进餐后不久,丙酸盐组受试者血液中的去甲肾上腺素水平显著升高,胰高血糖素等激素水平也有所增长。这表明丙酸盐可能会作为“代谢破坏者”,增加人类患糖尿病和肥胖症的风险。
而这与前文丙酸盐会影响脂质合成与摄食行为相矛盾,因此,丙酸盐对人体的影响可能取决于其含量以及人体独特的肠道菌群结构与代谢能力。
内源性丙酸盐与外源性丙酸盐存在区别
内源性丙酸:指的是人体内部产生的丙酸,通常情况下,人体中的微生物能够在结肠中通过发酵未完全消化的碳水化合物来产生丙酸,这些丙酸对人体是有益的。
外源性丙酸:指的是从外部来源摄入的丙酸,比如通过食物摄入或作为补充剂。以及在一些药物中也可能含有丙酸盐。
★ 外源性丙酸盐摄入过多对代谢健康有害
但已经有各种研究表明,外源性地摄入和自体产生的丙酸作用并不一样,外来的丙酸对个体的许多代谢过程有不利影响。
哈佛大学公共卫生学院的研究人员完成了一项实验,发现从食品中摄入的丙酸在短期内会导致高血糖、胰岛素偏高,而且长期摄入将会造成肥胖和胰岛素抵抗等更严重的症状。
我们通过口腔摄入含丙酸添加剂的食物后,会激活我们的交感神经系统,并促使体内胰高血糖素和脂肪酸结合蛋白4等激素的升高。受到激素影响,肝糖原持续分解,血糖升高。身体开始分泌更多胰岛素进行代偿降低血糖浓度,最终导致胰岛素抵抗和肥胖产生。
这项研究表明,自身产生的丙酸和外界摄入的丙酸具有不同的功能,我们推测,这是因为从食物中摄入会极大地增加细胞和丙酸的接触,而细菌产生的仅仅只会局限在结肠部分。
在人体肠道中,丁酸由膳食纤维经细菌发酵产生,通过两种代谢途径。在第一条途径中,丁酰辅酶A被磷酸化形成丁酰磷酸,并通过丁酸激酶转化为丁酸。在第二条途径中,丁酰辅酶A的辅酶A部分通过丁酰辅酶A:乙酸辅酶A转移酶转移到乙酸盐,从而形成丁酸和乙酰辅酶A。其中丁酰辅酶A:乙酸辅酶A转移酶途径占主导地位。
对人类粪便微生物群的放射性同位素分析也表明,肠道中的大多数丁酸盐是由碳水化合物通过Embden-Meyerhof-Parnas(糖酵解途径)由乙酰辅酶A产生的。
• 少量的丁酸盐也可由蛋白质合成
除了碳水化合物,少量的丁酸也可以通过谷氨酸、赖氨酸、戊二酸和γ-氨基丁酸途径由蛋白质合成。厚壁菌种也对氨基酸表现出高活性,特别是肠单胞菌(Intestinimonas AF211),它通过不同的途径将葡萄糖和赖氨酸发酵成丁酸。
形成丁酸盐的微生物途径
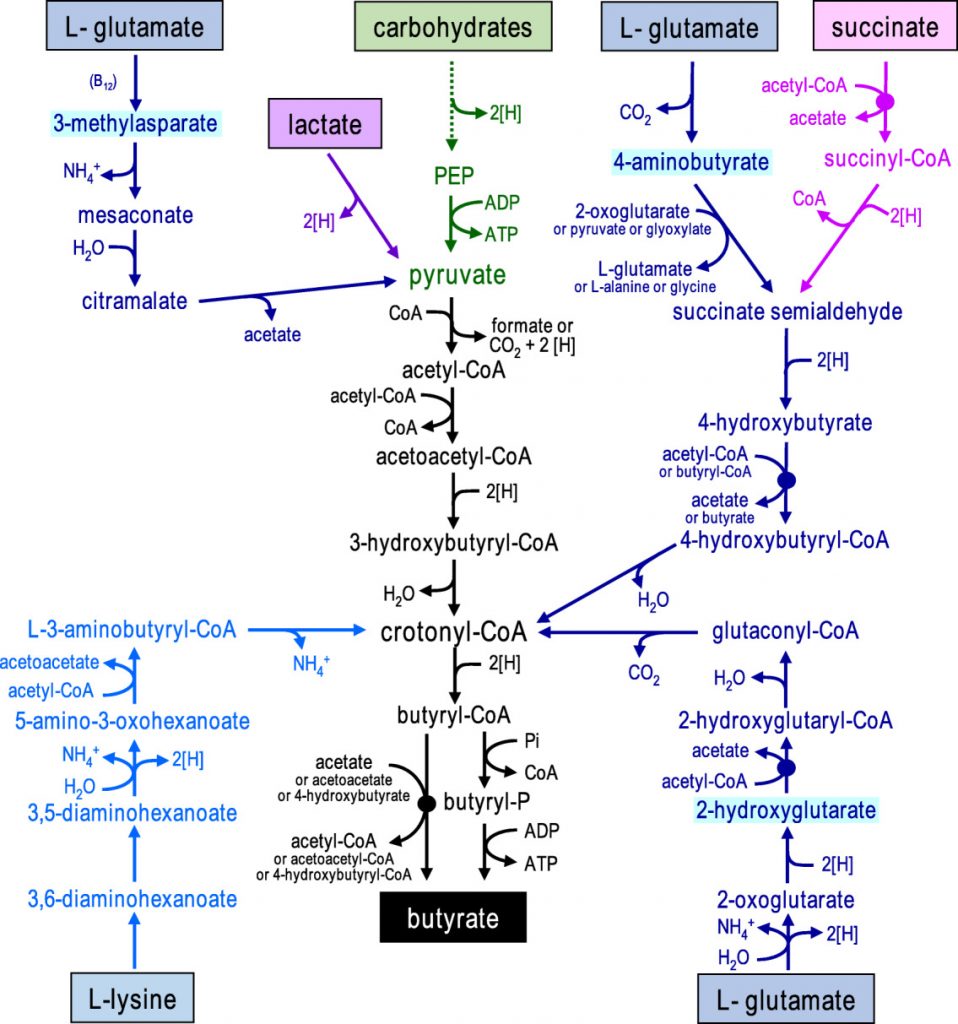
doi: 10.1111/1462-2920.13589.
碳水化合物通过糖酵解发酵为丙酮酸显示为绿色,从乙酰辅酶A形成丁酸盐显示为黑色,氨基酸发酵途径显示为蓝色(以中间体命名不同的谷氨酸途径),乳酸和琥珀酸发酵分别显示为紫色和粉色。
• 人结肠中的瘤胃球菌和毛螺菌是产丁酸的主力
除食源性丁酸,人体内丁酸主要是由盲肠和结肠的厌氧型细菌发酵产生,而由胃和小肠产生的丁酸含量极低。大肠产丁酸的菌种主要是梭菌属XIVa和IV族,以及真杆菌属和梭杆菌属
盲肠和结肠中丁酸的产生速度和数量主要取决于肠道微生物组成、日常膳食中可利用发酵成分组成等。在人的结肠中,厚壁菌门中的瘤胃球菌科(Ruminococcaceae)和毛螺菌科(Lachnospiraceae)这两个主要科,以及包括丹毒丝菌科(Erysipelotrichaceae)和梭菌科(Clostridiaceae)在内的其他厚壁菌门物种,都发现了丁酸生产菌种与非生产菌种的交替存在。
但应注意,许多人类结肠的主要厚壁菌门(例如Blautia spp.、Eubacterium eligens、Ruminococcus spp.)缺乏从碳水化合物中生成丁酸的能力。
产生丁酸盐的细菌被认为在生命的第一年内定植于宿主,并且在成年时占总细菌群落的20%以上。在消化道中发现的已知丁酸盐生产者中,大多数似乎属于毛螺菌科和瘤胃球菌科。我们将简要介绍两个丁酸生产菌。
▸ 普拉梭菌
普拉梭菌(Faecalibacterium prausnitzii)是健康人类微生物群中最丰富的菌种之一,也是主要的丁酸盐生产者之一。它通过丁酰辅酶A:乙酸辅酶A转移酶产生丁酸,并消耗乙酸。
虽然F.prausnitzii菌株是专性厌氧菌,但在核黄素(维生素B2)和还原性化合物(如半胱氨酸或谷胱甘肽)存在的情况下,低浓度氧气也能促进其生长。
氧气消耗会伴随丁酸形成的减少。F. prausnitzii分离株在利用食物多糖(如淀粉和半纤维素)生长方面能力有限,但一些菌株可以利用菊粉和果胶衍生物,并且普遍利用糖醛酸。
• 肠道炎症患者产生丁酸会减少
F. prausnitzii在炎症性肠病患者中很少见,尤其是克罗恩病,有证据表明它具有抗炎作用,因此引起了人们对其作为潜在治疗药物的兴趣。同样,据报道,Butyricicoccus pullicaecorum在炎症性肠病患者中较少见,并且也可能具有治疗潜力。
注:其他瘤胃球菌科细菌也能产生丁酸,但人们对大多数此类生物知之甚少。关于Faecalibacterium prausnitzii,详见:肠道核心菌属——普拉梭菌(F. Prausnitzii),预防炎症的下一代益生菌
▸ 毛螺菌科
直肠真杆菌(Eubacterium rectale)和密切相关的罗氏菌属(Roseburia)构成了产丁酸毛螺菌科的主要群体,它们具有相同的丁酰辅酶 A:乙酸辅酶 A 转移酶途径来生产丁酸,并且其丁酸合成基因的基因组组织也相同,从乙酰辅酶A到丁酰辅酶A。
• 罗氏菌属通过代谢饮食多糖产生丁酸
在某些Roseburia菌株中,特别是在弱酸性pH值下,丁酸几乎是唯一产生的发酵酸,乙酸的净消耗通常伴随着丁酸的形成。一些其他菌株和物种除了产生丁酸外,还产生甲酸和乳酸。基因组分析表明,该群体具有相当大的利用饮食来源的多糖的能力,包括淀粉、阿拉伯木聚糖和菊粉,不同菌株和物种之间的差异很大。
其他拥有丁酰辅酶A:乙酸辅酶A转移酶基因的毛螺菌科包括Eubacterium hallii、Anaerostipes hadrus、Coprococcus catus、与分离株SS3/4和M62/1有关的未鉴定物种。
• 一些毛螺菌科细菌利用乳酸和乙酸来产生丁酸
某些毛螺菌科能够在乳酸和乙酸盐存在下生长并产生丁酸,其总净化学计量为4mol乳酸和2mol乙酸盐产生3mol丁酸 。
这包括仅使用D-乳酸的物种Anaerostipes hadrus和能够利用两种乳酸异构体的E. hallii。
此外,双歧杆菌等常见益生菌配方中的微生物与丁酸盐生产者之间的交叉喂养相互作用已被证明是可以产丁酸盐的。
人体肠道中的主要丁酸生产者
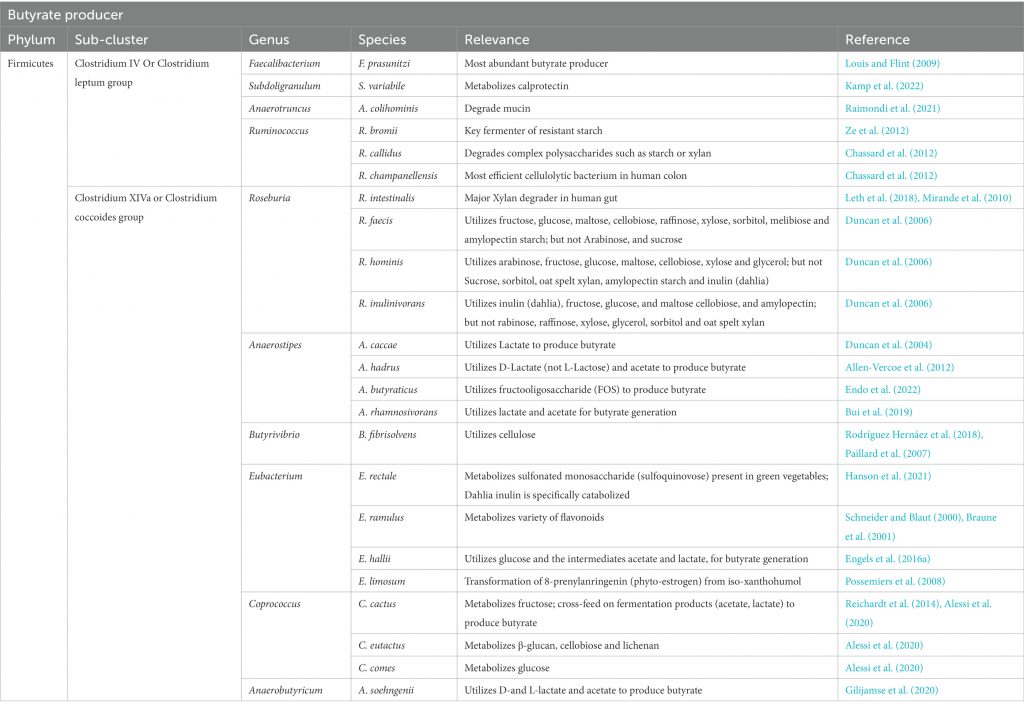
doi: 10.3389/fmicb.2022.1103836.
▸ 增加丁酸盐生成的食物
饮食对人体微生物群有显著影响,通过饮食干预可显著改变细菌数量并增加微生物多样性。富含纤维的饮食对丁酸盐的产生特别有益,因为它可以滋养产生丁酸盐的细菌。
• 高纤维饮食能够有效增加丁酸盐的生成
蔬菜、水果、豆类和全谷物,它们含有膳食纤维,可被肠道细菌发酵成丁酸盐等有机化合物。通过食物增强微生物群是促进消化系统健康和丁酸盐生成的有效且安全的方法。因此,增加丁酸盐产量的最佳方法是通过高纤维饮食。
• 高脂、低纤维饮食不利于丁酸盐的生成
高蛋白、高脂肪、低碳水化合物的饮食已被证明会破坏微生物组中丁酸盐的产生。在一项研究中,研究人员分析了短期饮食限制碳水化合物摄入量的肥胖参与者的微生物组,从而限制了他们对植物性膳食纤维的消耗。
在低碳水化合物饮食(每天24克)和中等碳水化合物饮食(每天164克)4 周后,短链脂肪酸的浓度低于高碳水化合物饮食(每天399克)。具体来说,当碳水化合物摄入量减少时,丁酸盐浓度会降低。
同时还发现,厚壁菌门细菌Roseburia和E.Rectale的密度与丁酸盐浓度之间存在联系,两者都随着碳水化合物摄入量的减少而降低。
一些食源性物质产生短链脂肪酸的量
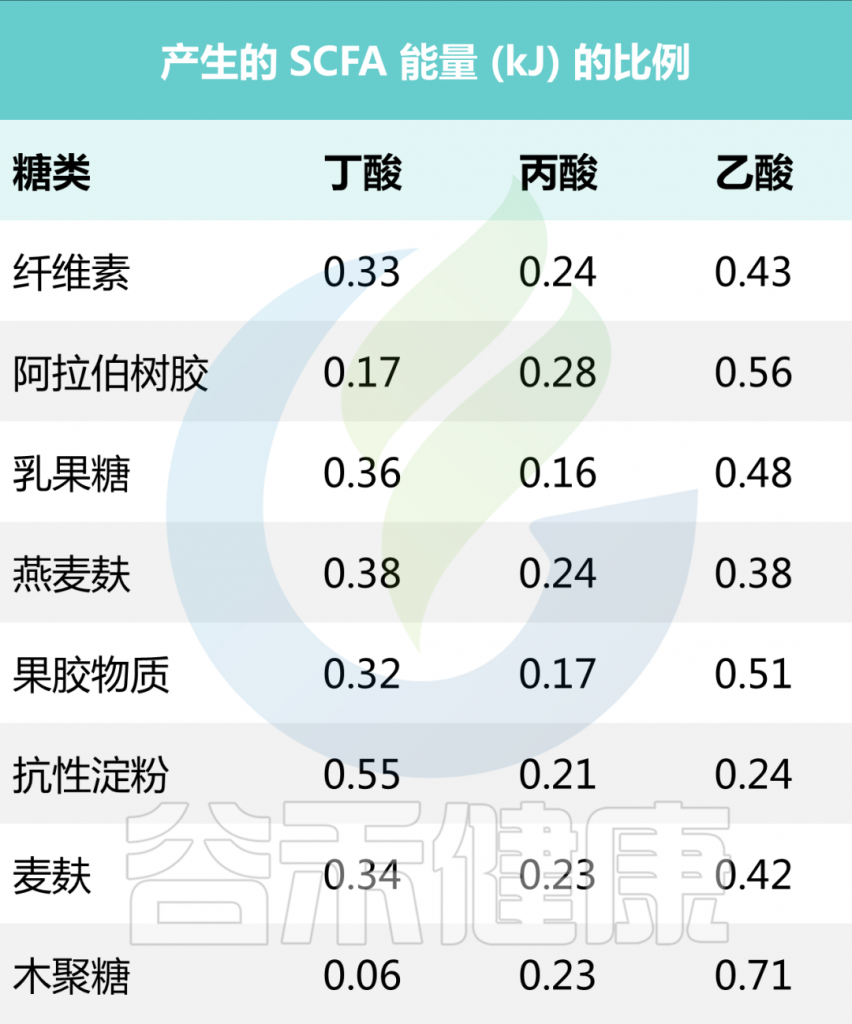
• 抗性淀粉
研究表明,从生马铃薯、高直链淀粉玉米和全谷物中提取的阿拉伯木聚糖中,含有高含量2型抗性淀粉的食物显著增加了丁酸盐的产量。
在174名健康年轻人的饮食中添加马铃薯抗性淀粉后,丁酸盐产量增加。玉米、菊苣和玉米中的抗性淀粉也进行了测试,但只有当食用土豆中的抗性淀粉时,粪便中的丁酸总量才会显著增加。
• 果聚糖(菊粉)
许多研究表明,菊粉可以增加短链脂肪酸的产量,包括丁酸盐。这可能解释了香蕉在溃疡性结肠炎和克罗恩病患者的饮食中如此有效的原因之一。然而,链长较短的果聚糖通常比链长的果聚糖(如菊粉)更容易喂养产丁酸菌。
也就说,抗性淀粉和果聚糖(短链低聚果糖和长链菊粉)在肠道中发酵时会产生丁酸盐。
富含抗性淀粉的食物:全麦面包、燕麦、大麦和糙米等全谷物;黑豆、红豆、绿豆等豆类;马铃薯、玉米、菊苣根、牛蒡根、魔芋根、亚麻籽。
富含果聚糖的食物:洋葱、菊苣、香蕉、朝鲜蓟、芦笋、大蒜、韭菜、西兰花、开心果。
需要注意的
由于人与人之间的常驻微生物存在显著差异,并且它们消化某些底物的能力不同,因此比较明智的选择是食用包含多种抗性淀粉和果聚糖的饮食。例如以马铃薯抗性淀粉、燕麦麸皮纤维或车前草种子或短链低聚半乳糖、长链低聚果糖和谷氨酰胺的混合物的形式短期补充,增加丁酸盐水平。
丁酸盐作为一种重要的的调节因子,是宿主-微生物串扰的关键介体。丁酸盐在体内可以通过脂肪酸氧化为机体供应能量,是肠道上皮细胞的主要供能物质。
丁酸盐还与机体健康密切相关,对调节肠道健康、修复肠道屏障、抑制炎症及癌症等病症意义重大。在养殖业中常添加丁酸盐保护动物健康生长,如预防断奶仔猪腹泻、调节鸡肠道菌群并增强其免疫力等。
▸ 为肠道细胞提供能量
丁酸盐是结肠细胞的主要能量来源,结肠细胞是构成肠道内壁的细胞。
与身体中使用糖(葡萄糖)作为主要能量来源的大多数其他细胞不同,肠道内壁细胞(结肠细胞)主要使用丁酸盐。如果没有丁酸盐,这些细胞就无法正确执行其功能。
• 丁酸盐为结肠细胞提供能量,细胞利于产丁酸盐细菌的生长
厚壁菌属的成员以产生丁酸盐而闻名,像Roseburia,Faecalibacterium prausnitzii,直肠真杆菌(E.rectale)等。
这种关系是相互的。丁酸盐为结肠细胞提供燃料,作为回报,这些细胞有助于提供一个无氧环境,有益的肠道微生物在其中茁壮成长。这可以控制炎症,保持肠道细胞健康,并使肠道细菌保持健康。
▸ 促进肠道运动
实验研究表明,丁酸盐通过作为短链脂肪酸受体的配体和激活剂,诱导肠道激素肽YY或介导肠嗜铬细胞释放5-羟色胺来促进肠道运动。
丁酸盐还可以通过上调Na+—H+交换器和诱导ATPase离子交换器基因来增强水和电解质的吸收。并且可能有益于预防某些类型的腹泻。
▸ 抗炎、抗癌特性
丁酸盐对肠道具有抗炎和抗癌功能。
肠道内壁会保持低水平的炎症,以防与微生物群接触的粘膜表面发生任何变化。低水平的炎症受到严格控制,但如果它被破坏,会导致氧化损伤,并可能在很长一段时间内导致癌症。
• 丁酸盐减少促炎细胞因子的产生
丁酸盐会阻止体内的一些促炎物质发挥作用。丁酸盐的抗炎作用可减少氧化应激并控制自由基造成的损害。
丁酸盐的抗炎特性,部分原因是其抑制核转录因子(NF-κB)的激活,通过下调NF-κB信号通路,丁酸盐可以调节促炎细胞因子的产生。
• 丁酸盐阻止结肠癌细胞的生长
丁酸盐也是一种组蛋白脱乙酰酶(HDAC)抑制剂。组蛋白脱乙酰酶是大多数癌症中产生的酶。因为丁酸盐是一种抑制剂,它实际上会改变基因表达,抑制细胞增殖,诱导细胞分化或凋亡。因此,它可以阻止癌细胞的发展。
有证据表明,结直肠癌(CRC)患者的微生物组图显示主要产丁酸菌属减少,包括罗氏菌属(Roseburia)、Clostridiales、Faecalibacterium和Lachnospiraceae科成员,而使用产丁酸的丁酸梭菌可有效减少癌细胞增殖并增强癌细胞凋亡。
▸ 修复肠道屏障,防止肠漏
肠上皮细胞的屏障功能是重要的第一道防线,确保上皮层具有适当的通透性。研究发现丁酸盐能够修复和增强肠上皮细胞的屏障功能。
• 丁酸盐上调粘蛋白的表达,增强粘液屏障
最新研究表明,丁酸对肠屏障功能具有保护作用。例如,丁酸能够上调粘蛋白2(MUC2)的表达。粘蛋白2是肠粘膜表面主要的粘蛋白,可增强粘膜层,从而限制有害物质通过肠道。
• 丁酸盐对肠道屏障的影响可能具有浓度依赖性
此外,丁酸还能增加三叶因子(TFF)的表达,这是一种粘蛋白相关肽,有助于维持和修复肠粘膜。丁酸还调节紧密连接蛋白的表达,以降低细胞旁通透性。其中一种机制是通过激活单分子层中的AMP活化蛋白激酶。
体外模型研究表明,丁酸对肠道屏障功能的影响可能具有浓度依赖性。丁酸在低浓度(≤2 mM)时可促进肠道屏障功能,但在高浓度(5或8 mM)时可能通过诱导细胞凋亡来破坏肠道屏障功能。
根据哺乳动物胃肠道中的生理浓度,目前体外模型中推荐使用的丁酸浓度为0-8mM。然而,考虑到大多数丁酸在结肠上皮中被代谢为能量底物,体内和体外模型中治疗剂量可能存在差异。
▸ 抗氧化能力
说起抗氧化,我们先了解一下自由基。它基本上是体内化学反应产生的废物。另一方面,抗氧化剂是身体抵御它们的防御措施。大量自由基会造成损害并压倒身体的修复系统。我们称之为氧化应激。氧化应激被认为是导致衰老和疾病的一个重要因素。
• 丁酸盐增加谷胱甘肽,可以中和自由基
结肠或大肠是身体产生的废物的储存容器。较高的丁酸盐水平已被证明会增加谷胱甘肽的水平,谷胱甘肽是一种在人体细胞中产生的抗氧化剂,可以中和肠道中的自由基(自由基与炎症和许多疾病有关),从而起到抗氧化作用。
▸ 调节肠道免疫
• 维持厌氧环境,阻止有害菌生长
丁酸通过增强结肠细胞的氧消耗和稳定缺氧诱导因子(HIF)来维持结肠内的厌氧环境,而丁酸的缺失则会促进潜在有害细菌和分子的积聚,例如沙门氏菌、大肠杆菌和一氧化氮(NO)。
肠道中丁酸水平降低,这促进了肠道上皮氧合和鼠伤寒沙门氏菌(S.Typhimurium)的生长,鼠伤寒沙门氏菌是食源性肠道炎症和腹泻的已知病因。
• 影响免疫细胞迁移、粘附
除了营造无氧环境外,短链脂肪酸,尤其是丁酸盐,还可以作为免疫细胞趋化和粘附的调节剂。丁酸可以调节肠上皮细胞介导的中性粒细胞向炎症部位的迁移,并且这种作用是浓度依赖性的。
此外,丁酸在细胞增殖和凋亡中发挥作用。丁酸刺激细胞生长和DNA合成,并诱导细胞周期G1期的生长停滞。虽然低浓度的丁酸会增强细胞增殖,但高浓度的丁酸会诱导细胞凋亡。
丁酸盐等短链脂肪酸可以在先天反应过程中通过影响巨噬细胞和粒细胞以及树突状细胞的抗原呈递发生,也可能在适应性免疫反应过程中通过影响T细胞和B细胞功能发生。
短链脂肪酸的免疫调节作用
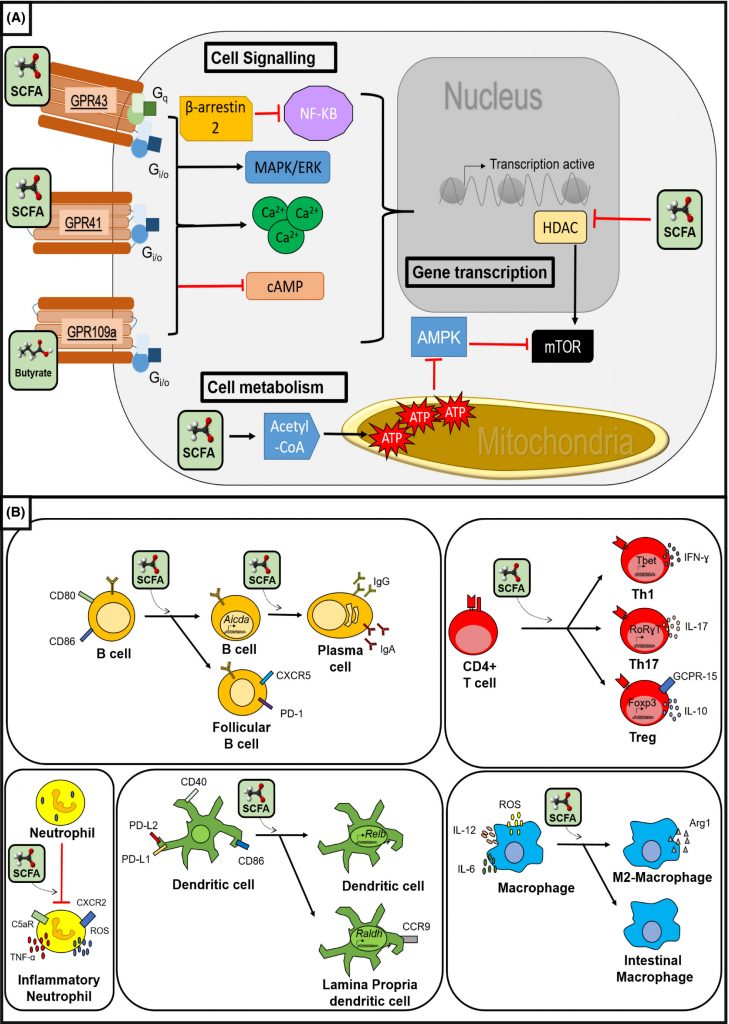
doi: 10.1111/apt.14689.
▸ 影响代谢健康
• 对肥胖存在一定影响,但还不能完全确定
包括丁酸盐在内的短链脂肪酸可通过激活肠细胞内的FFAR来降低食欲和体重。这促进胰高血糖素样肽1(GLP-1)和肽YY的释放,前者促进胰岛素分泌并抑制胰高血糖素分泌,后者降低食欲并减缓胃排空。
短链脂肪酸还能减少所谓的“饥饿激素”——胃促生长素(ghrelin)的分泌;FFAR2存在于ghrelin分泌细胞上,包括丁酸盐和丙酸盐在内的FFAR2激动剂可减少ghrelin分泌。
丁酸盐影响脂质代谢的机制
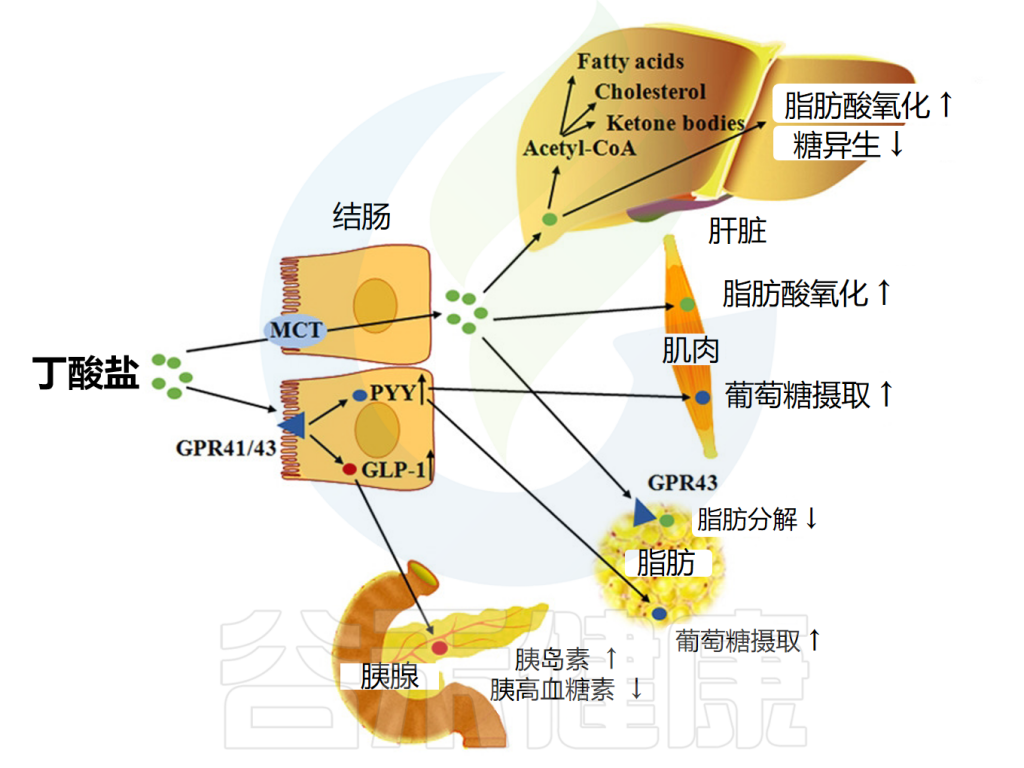
doi: 10.1093/advances/nmx009.
也有证据表明短链脂肪酸作用于交感神经系统,交感神经节中FFAR3的激活导致能量消耗增加。
然而,与丙酸盐一样,关于丁酸盐对食物摄入的影响,有相互矛盾的结果报道。
• 丁酸盐对控制血糖水平可能有潜在好处
研究发现,糖尿病患者和糖尿病前期受试者中丁酸盐水平降低。
丁酸在肠内分泌细胞(EEC)中与游离脂肪酸受体(FFAR)FFAR2和FFAR3结合,调节肠道激素释放,如胰高血糖素样肽1(GLP-1)和肽YY(PYY)。
丁酸盐通过多种途径影响糖代谢的调节
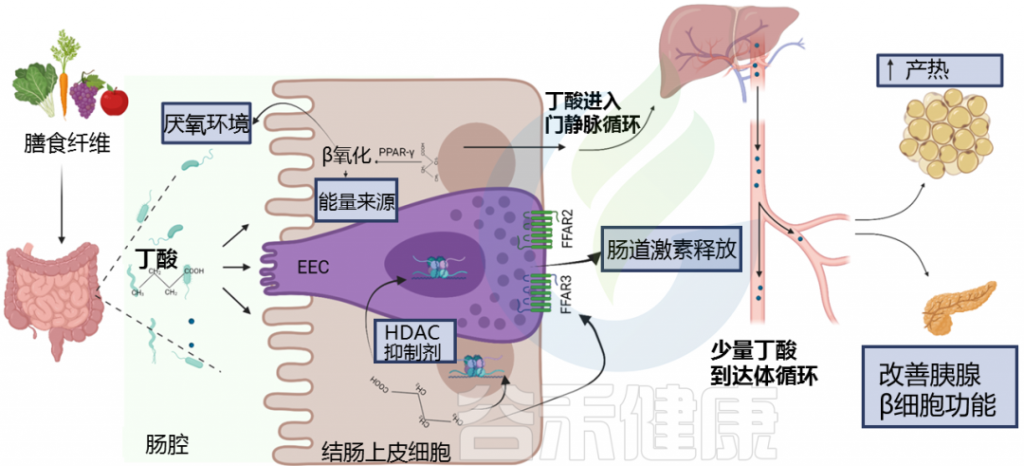
doi: 10.3389/fendo.2021.761834.
这些激素共同作用以保持血糖水平稳定。当血糖过高时,胰岛素会告诉身体的肌肉和脂肪细胞吸收多余的葡萄糖,所以说这些激素对肥胖和糖尿病很重要。丁酸盐增加这些肠道激素的释放,表明对控制血糖水平和防止体重增加有潜在的好处。
!
丁酸盐过低可能会导致以下危害:
•肠道屏障功能受损:丁酸盐有助于维持结肠的“生理性缺氧”,并提供能量给结肠细胞,有助于维持肠道稳态。丁酸盐的减少可能导致肠道屏障功能受损。
•增加慢性疾病风险:变形菌门的兼性厌氧细菌的扩张几乎总是伴随着产丁酸盐细菌丰度的减少,并与许多慢性疾病有关,包括炎症性肠病、肠易激综合症、结直肠癌、2型糖尿病、肥胖等。
•神经炎症:丁酸盐具有抗炎特性,对大脑健康具有重要意义。丁酸盐过低可能导致炎症增加,影响大脑健康。
•睡眠问题:丁酸盐可能作为细菌源性促睡眠信号,丁酸盐过低可能影响睡眠,导致睡眠问题。
•肠道菌群失衡:丁酸盐过低可能导致肠道菌群失衡,因为变形菌门的扩张伴随着产丁酸盐细菌的减少。
•不利于肠道损伤修复:在轻微炎症或轻度溃疡部位添加丁酸盐可以促进肠道损伤的修复,而丁酸盐过少可能不利于溃疡的恢复。
!
丁酸盐并不总是越多越好,低浓度丁酸促进细胞增殖和生长,高浓度丁酸反而抑制细胞增殖和生长,增加肠道的通透性。
• 不同部位对丁酸盐的耐受阈值存在差异
胃肠道不同部位对丁酸盐的耐受阈值也存在一定差异,胃和小肠对丁酸的耐受阈值低,结肠和盲肠耐受阈值高。
添加普通丁酸钠制剂(主要在肠道前端被吸收利用),反而造成肠道炎症、菌群失调。
• 肠道严重溃疡时丁酸盐可能加剧症状
更有意思的是,轻微炎症或者轻度溃疡部位添加丁酸盐可以促进肠道损伤的修复,在严重溃疡肠道部位添加,不利于溃疡的恢复,甚至加剧整个溃疡。
有学者发现溃疡部位的粘膜组织对丁酸的代谢降低,甚至只有正常粘膜组织的一半,主要是由于其转运载体和氧化相关的酶活降低。
主要参考文献
Louis P, Flint HJ. Formation of propionate and butyrate by the human colonic microbiota. Environ Microbiol. 2017 Jan;19(1):29-41.
Gill PA, van Zelm MC, Muir JG, Gibson PR. Review article: short chain fatty acids as potential therapeutic agents in human gastrointestinal and inflammatory disorders. Aliment Pharmacol Ther. 2018 Jul;48(1):15-34.
Hosseini E, Grootaert C, Verstraete W, Van de Wiele T. Propionate as a health-promoting microbial metabolite in the human gut. Nutr Rev. 2011 May;69(5):245-58.
Arora T, Tremaroli V. Therapeutic Potential of Butyrate for Treatment of Type 2 Diabetes. Front Endocrinol (Lausanne). 2021 Oct 19;12:761834.
Singh V, Lee G, Son H, Koh H, Kim ES, Unno T, Shin JH. Butyrate producers, “The Sentinel of Gut”: Their intestinal significance with and beyond butyrate, and prospective use as microbial therapeutics. Front Microbiol. 2023 Jan 12;13:1103836.
Gonzalez-Garcia, R.A.; McCubbin, T.; Navone, L.; Stowers, C.; Nielsen, L.K.; Marcellin, E. Microbial Propionic Acid Production. Fermentation 2017, 3, 21.
Reichardt N, Duncan SH, Young P, Belenguer A, McWilliam Leitch C, Scott KP, Flint HJ, Louis P. Phylogenetic distribution of three pathways for propionate production within the human gut microbiota. ISME J. 2014 Jun;8(6):1323-35.
Liu H, Wang J, He T, Becker S, Zhang G, Li D, Ma X. Butyrate: A Double-Edged Sword for Health? Adv Nutr. 2018 Jan 1;9(1):21-29.

谷禾健康

自闭症谱系障碍 (ASD) 是一组神经发育疾病,其特征是社交互动和沟通的质量障碍、兴趣受限以及重复和刻板行为。
环境因素在自闭症中发挥重要作用,多项研究以及谷禾队列研究文章表明肠道微生物对于自闭症的发生和发展以及存在明显的菌群和代谢物的生物标志物。
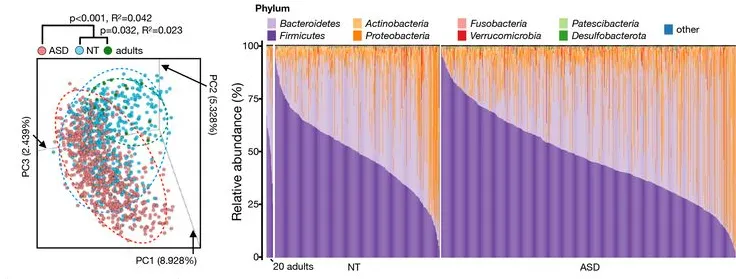
doi: 10.1136/gutjnl-2021-325115.
尽管环境因素在自闭症中发挥重要作用,但几乎没有确凿的证据将饮食与疾病的发生和进展联系起来。然而,最近关于饮食如何塑造肠道-大脑轴的研究可能会为环境对疾病机制的影响提供新的见解,并提出至少通过饮食改善某些自闭症谱系障碍症状的可能性。
此外,在谷禾检测实践过程中,也发现部分自闭症儿童的消化功能,以及饮食营养存在问题,主要集中表现为挑食,消化不良等。
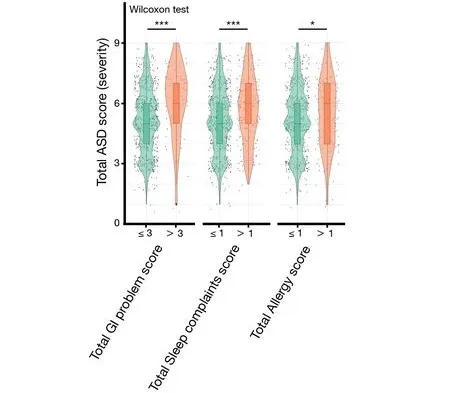
doi: 10.1136/gutjnl-2021-325115.
本文参考以往相关研究性文章,详细讨论饮食和肠道微生物群-肠-脑轴如何影响自闭症,主要概述肠道微生物群对分子代谢(各类氨基酸、γ-氨基丁酸、不饱和脂肪酸、短链脂肪酸、胆固醇、丁酸盐、乙酸盐、N-乙酰天冬氨酸、多酚等)和与自闭症发病和进展相关的酶(二糖酶、己糖转运蛋白和单羧酸转运蛋白等)。还回顾了饮食模式、益生菌和肠道微生物群在大脑发育中的作用及与自闭症的关联,这些都为自闭症的干预策略提供了重要的理论支持。
自闭症谱系障碍 (ASD) 是一组神经发育疾病,一般在 3 岁之前发病,其特征是社交互动和沟通的质量障碍、兴趣受限以及重复和刻板行为。
直到几十年前,自闭症谱系障碍还被认为相当罕见,但自 20 世纪 80 年代以来,全世界自闭症谱系障碍快速增加,这给自闭症谱系障碍患者的家庭和整个社会带来了重大的后果。
目前在临床上自闭症谱系障碍的诊断仍然是根据行为来定义的,通过详细的发展史、父母对孩子日常行为的描述以及对孩子的社交互动方式以及沟通和智力功能的直接评估。
一个重要问题让人对自闭症表型发病机制的理解变得更加复杂,简而言之,自闭症谱系障碍的发病和表现远非同质:
此外,除了核心症状之外,这些儿童通常还表现出一系列其他相关特征,例如:
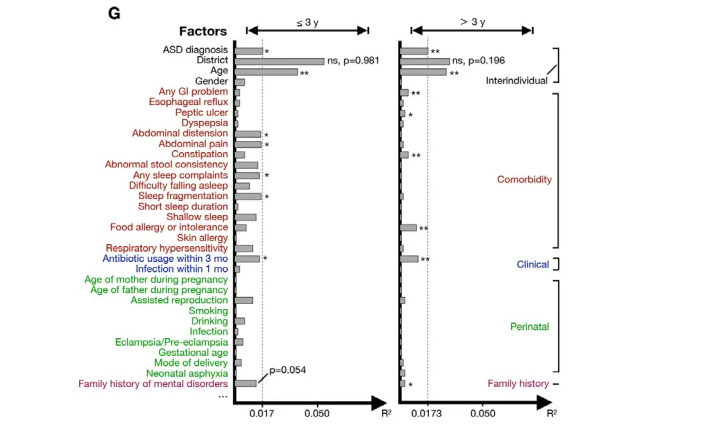
doi: 10.1136/gutjnl-2021-325115.
饮 食
人体必需氨基酸必须由食物供给,喂养可能代表环境因素和神经生物学因素之间的桥梁,因此可能在导致疾病表型的途径中发挥作用。从临床经验和文献中都知道,自闭症儿童往往与喂养和饮食态度有特殊的关系。
部分自闭症儿童可能有进食困难及胃肠道症状,对食物的味道和颜色非常挑剔。因此,自闭症儿童必需氨基酸 (赖氨酸、色氨酸、苯丙氨酸、组氨酸) 减少,可能部分是由于食物摄入不足或饮食习惯不良所致。
非常有限的饮食可能会使任何儿童面临营养缺乏和发育不良的风险,包括大脑发育。
遗 传
强有力的证据支持遗传因素对自闭症和相关疾病的疾病风险有影响。
然而,与自闭症风险有关的许多不同基因编码参与各种生理过程的各种不同蛋白质,包括大脑发育和功能、神经递质受体或转运蛋白、细胞粘附/屏障功能蛋白、免疫相关蛋白、参与胆固醇代谢或运输的蛋白质,以及影响线粒体功能的蛋白质。
近期,发表在《Cell》的一项研究对一个出生队列进行了 20多年的跟踪,详细的早期纵向问卷记录了感染和抗生素事件、压力、产前因素、家族史等饮食,在随访的 16,440 名瑞典儿童中,1,197 名患上神经发育障碍。下面一些有关自闭症风险的研究数据出自该文章:
家族病史
环 境
并非所有携带这些特定突变的个体都会患自闭症谱系障碍。最近的一项同卵双胞胎研究强调,环境因素可能解释了他们患自闭症谱系障碍相对风险的 55%,环境因素为自闭症谱系障碍型症状的出现提供了选择性压力,这些症状从各种不同的症状中出现。各种易诱发的遗传异常,结合起来会引起明显的疾病。
重大生活事件
化学物质暴露
早期感染和抗生素
儿童早期(出生至 5 岁)感染与自闭症风险增加显著相关,最显著的是第一年内中耳炎和反复湿疹。
微生物组
胃肠道症状长期以来表明,肠道和大脑之间存在着紧密联系,即”肠-脑轴”。
——胃肠道问题
在未来患有神经发育障碍的儿童中,早期胃肠道问题明显,情绪问题程度较轻。
——肠道菌群
肠道细菌可能在自闭症病理生理学中发挥一定作用。事实上,各种研究表明肠道微生物群在自闭症中发生了改变, 尽管文献中对于参与其中可能发挥作用的细菌几乎没有达成一致。
肠道细菌及其代谢产物不仅影响肠道功能和饱腹感,还可能与情绪、认知、行为、抑郁以及大脑发育等方面有关。
饮食在塑造哺乳动物代谢通量(包括神经化学物质的通量)以及塑造肠道微生物群及其活动方面具有重要作用。
例如,纤维和益生元尤其支持有益的糖分解肠道微生物群,其特征是双歧杆菌和乳酸菌的相对丰度增加以及短链脂肪酸 (SCFA) 的产生。来自水果、谷物和蔬菜等全植物食品的多酚也会影响肠道微生物群组成、免疫功能,充当抗氧化剂,防止大脑炎症并改善血脑屏障 (BBB) 功能。
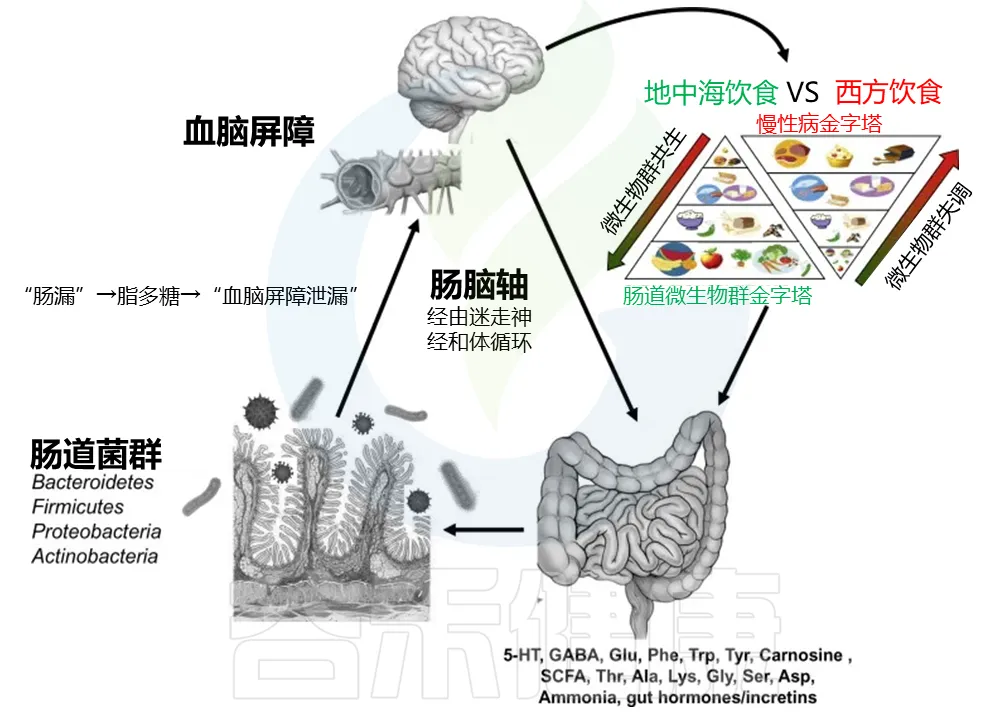
Kieran M. Tuohy, et al.,Diet and the Gut Microbiota,2015,225-245
接下来我们着重就微生物组这方面,详细探讨肠道微生物群如何在自闭症的发展中起作用,以及相关的最新研究进展。
肠-脑轴作为外部环境与人类大脑之间的沟通通路,在体内有重要的“内部”通道——人类肠道微生物群。许多营养物质和摄入的化学物质必须经过这些通道,转化为生物可利用和活跃的中间产物,然后通过肝门静脉被吸收并在全身分布。
许多对大脑重要的化学物质也由肠道微生物群在肠道中产生,包括色氨酸、多巴胺、血清素、GABA、β-羟基丁酸、胆碱、牛磺酸、乙酸盐、琥珀酸、乳酸、乙酰辅酶A、肌酐、甜菜碱、谷氨酸、谷氨酰胺、对甲酚、反式吲哚丙烯酸甘氨、脂肪酸和马尿酸。
一些其他化学物质可能由细菌(例如在消化和发酵过程中)调节,或者是细菌成分,如革兰氏阴性细菌细胞壁的组成部分脂多糖(LPS),它可剂量依赖性地减少人类肠道细胞对血清素的吸收,并在外周和大脑引发炎症,影响大脑功能。
神经递质:GABA、血清素
最近有研究表明,神经递质GABA在自闭症谱系障碍神经元发育中可能起作用,尤其是考虑到它在婴儿期从神经递质兴奋剂到抑制剂的转变。
另一种神经递质,血清素(5-羟色胺,5-HT),也被怀疑在自闭症中起作用。自闭症患者的血液中,血清素和 GABA 水平均发生了变化。有趣的是,这两种神经递质都是由氨基酸代谢产生的,分别是色氨酸和谷氨酸。
肠道代谢物是否直接影响大脑的神经发育?
取决于它们是否能够穿过血脑屏障(BBB)。
比如说,肠道细菌可以产生GABA,这个 GABA 可能会影响到肠道神经系统的工作,或者改变血液中 GABA 的含量。但是,在正常健康的情况下,肠道产生的 GABA 是不能直接穿过”血脑屏障”进入大脑的。
反之,乙酸盐作为肠道微生物群发酵碳水化合物的主要终产物和哺乳动物细胞胆固醇生物合成的底物,可以迅速通过血脑屏障。
然而,血脑屏障可能会因氧化或炎症压力等原因受到损伤,与胃肠道屏障类似出现“漏”,允许不需要的化学物质进入大脑。在自闭症患者中血脑屏障受到损伤。
为什么说肠道菌群可用于区分自闭症与非自闭症?
研究表明,肠道微生物群在影响自闭症谱系障碍(ASD)代谢产物谱和生理参数的过程中起着重要作用。
首先,自闭症患者的肠道微生物群与健康对照组或非自闭症的兄弟姐妹有显著差异,显示出异常的肠道微生物组成和活动是自闭症的一个特征。
研究报告显示,自闭症群体与非自闭症对照组之间在拟杆菌门、厚壁菌门、变形菌门和放线菌门的组成上存在差异。
前面提到的发表在《Cell》大队列的自闭症儿童研究,在 11.9 ± 2.9 个月时采集了 1,748 名婴儿的粪便样本,将所有可用的对照与未来的神经发育障碍进行比较,然后匹配风险因素和微生物组多样性混杂因素。
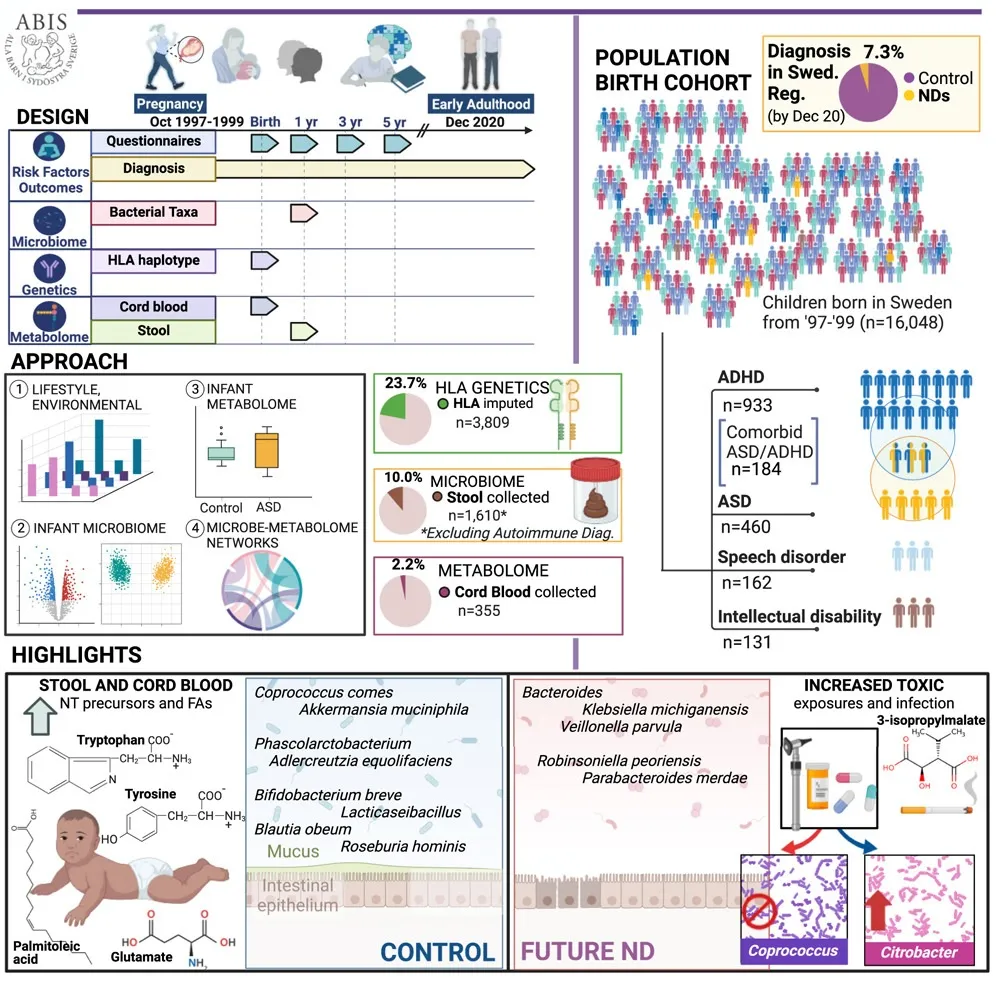
doi.org/10.1016/j.cell.2024.02.035
在未来的神经发育障碍中,下列菌群丰度较高:
在我们的GUT队列里,也发现自闭症儿童这个菌的Veillonella显著富集。
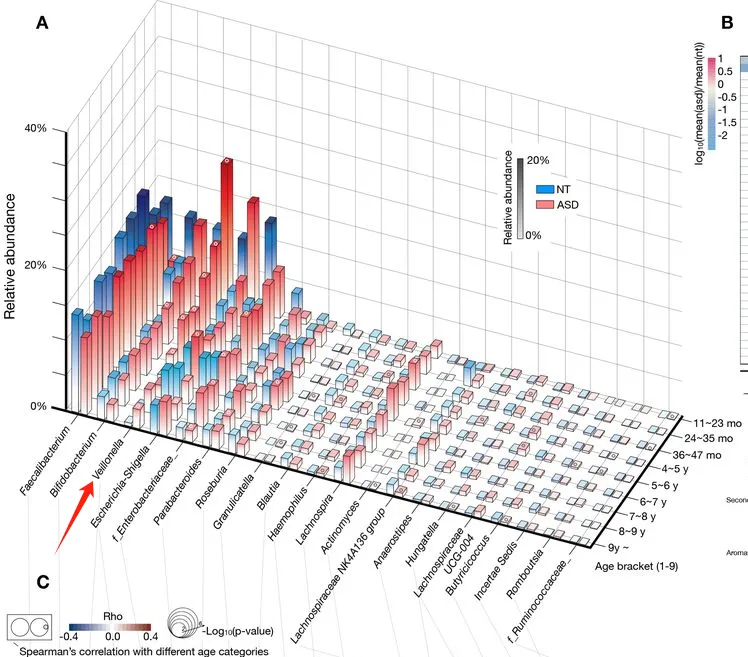
doi: 10.1136/gutjnl-2021-325115.
注:Veillonella是一种革兰氏阴性的厌氧球菌,正常情况下通常存在于人体口腔和胃肠道中。该菌以其乳酸发酵能力而闻名,能代谢乳酸产生丙酸、CO2和H2。
下列菌群始终较少富集:
这些菌属具有抗炎、维护肠道屏障、产生短链脂肪酸等有益作用,其减少可能导致肠道功能紊乱和免疫失调。
Akkermansia muciniphila在后来被诊断患有自闭症或自闭症-多动症合并的婴儿中不存在,并且与儿童早期的胃肠道和情绪症状呈负相关。
Akkermansia muciniphila促进粘蛋白并产生叶酸,丙酸和乙酸;以增强肠细胞单层完整性和强化受损的肠道屏障而闻名;并具有免疫调节特性。
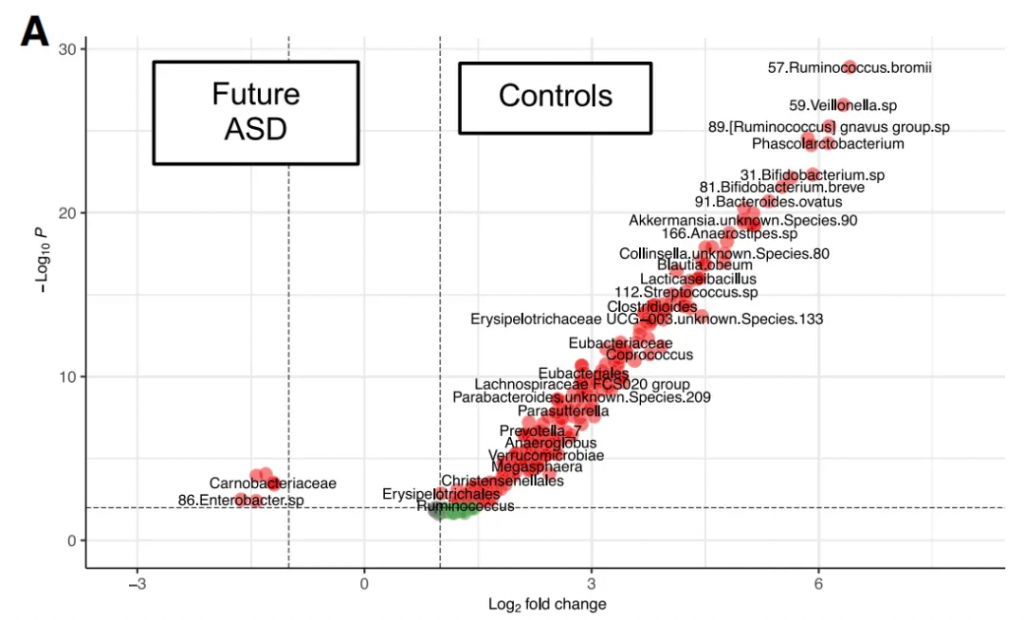
doi.org/10.1016/j.cell.2024.02.035
特定菌群:
与对照组(21.7%)相比,两种Klebsiella michiganensis菌株(HCXXMCOL0180 和 HCXXMCOL0513)在自闭症儿童中更普遍(43.6%),携带这两种菌株的婴儿日后患自闭症的风险更高。
携带这两种菌株的对照组婴儿抗生素使用频率更高(27.1%),提示抗生素暴露可能促进了这些菌株的定植。
性别和诊断年龄影响:
菌群自闭症男童的肠道菌群组成可能因诊断年龄不同而异,如晚期诊断与Akkermansia muciniphila丰度增加相关,而这种模式在女童中并不明显,女童中一些Bacteroides菌株丰度升高。
而早期诊断男童,Enterobacteriaceae科一些菌属如Enterobacter、 Klebsiella丰度升高。
这提示自闭症的肠道菌群变化可能具有性别特异性,且随年龄和病程进展而动态变化。
代谢物异常与菌群相关:
粪便代谢组学分析显示,自闭症儿童的某些代谢物如酪氨酸、色氨酸(儿茶酚胺、血清素前体)、精氨酸、赖氨酸等氨基酸,亚油酸等脂肪酸以及维生素B6等水平异常。
注:关于氨基酸,脂肪酸等详细介绍与自闭症的关联详见后面章节。
精氨酸水平与Roseburia、Coprococcus、Akkermansia丰度呈正相关,提示菌群失调可能影响宿主氨基酸代谢。
色氨酸代谢产物:吲哚-3-乙酸盐(AhR激动剂)在自闭症组中升高,且与Ruminococcaceae和Lachnospiraceae科菌属丰度正相关。
其他的一些与自闭症相关菌群的研究结果:
多样性降低
一些菌群减少,包括:
一些菌群增多,包括:
下列菌群可作为3-6岁有胃肠道症状儿童自闭症的可靠生物标志物:
菌群代谢产物LPS→慢性炎症→血脑屏障损伤
研究表明,细菌脂多糖(LPS)会引发慢性低度系统性炎症或“代谢性内毒素血症”,在动物模型中,这被证明会损害包括血脑屏障(BBB)在内的屏障功能。实际上,出生期暴露于LPS引发的系统性炎症的小鼠表现出永久性的血脑屏障损伤和渗透性增加,且在青少年和成年期表现出行为改变。对自闭症患者而言,血脑屏障功能的永久性损害将只会加剧肠道微生物及异常代谢产物输出所带来的病理后果。
母亲妊娠期:LPS诱导的系统性炎症如何影响孩子神经发育,增加自闭症风险?
妊娠期由LPS诱导的系统性炎症可以改变后代的神经发育和脑功能。自闭症中的这种先天性或细胞介导的炎症反应,可能会因获得性免疫系统中明显的自身免疫成分而加剧。由系统性炎症或母体自身免疫疾病触发的自身抗体在妊娠期间产生,现在被怀疑在胎儿异常神经发育和受损的血脑屏障发展中起作用,并影响婴儿期的大脑功能,包括增加自闭症的风险。
肠道菌群失调诱导产生自身抗体,影响神经系统发育
在自闭症患者中,对叶酸、血清素和GABA受体的自身抗体水平,以及一些重要的免疫相关酶如转谷氨酰胺酶2的抗体水平也有所升高。尽管自身抗体生成的分子触发机制尚不完全了解,但有一个可能性是,对关键代谢物如神经递质受体的自身抗体可能是在血液中异常代谢物浓度、早期生活中的不当免疫教育或由肠道细菌模拟引导下由免疫系统产生的。
这样的“代谢组-炎症组”调控网络也在其他自身免疫性疾病中出现,包括1型糖尿病和炎症性肠病(IBD),并且似乎与肠道微生物群密切相关。
氨基酸代谢在神经传递相关代谢物的生物合成中扮演着重要角色,长期以来被怀疑在自闭症谱系障碍中发挥作用。
血液分析氨基酸变化
Glu:Gln比率升高
有许多研究报告称,自闭症患者的血液中谷氨酸与谷氨酰胺(Glu:Gln)的比率升高。
将谷氨酸转化为谷氨酰胺是大脑中处理氨废物的主要方式,这对于避免氨中毒和在突触中谷氨酸的过度积累以减少兴奋性毒性非常关键。因此,血液中Glu:Gln比率的升高可能表明自闭症患者大脑中的氨解毒和谷氨酸循环发自闭症生了变化,这会影响行为。
注:低纤维高蛋白饮食可能会使这种氨中毒恶化,因为这样的饮食会导致肠道中的蛋白水解微生物群发酵氨基酸,从而增加系统性氨贡献。饮食中氨基酸的微生物分解会影响哺乳动物体内氨基酸的可用性和循环,也可能产生生物活性化合物,如短链脂肪酸、支链脂肪酸和生物胺。
蛋氨酸
一项包括87项研究的自闭症氧化应激生物标志物的汇总荟萃分析发现,参与甲基化循环和硫酸盐转移途径的几种代谢物异常。
蛋氨酸在硫酸盐转移途径中利用半胱氨酸合成,该途径连接蛋氨酸和谷胱甘肽的生物合成,蛋氨酸显著降低(p < 0.001),异常甲基化会增加自闭症谱系症状的风险 。
瓜氨酸
有研究发现,自闭症儿童的瓜氨酸水平与刻板行为(ADOS-2 上的 RRB 评分)之间存在正相关,且具有统计学意义。瓜氨酸和氨的累积暴露是经典瓜氨酸血症(精氨琥珀酸合成酶缺乏症)患者认知功能较差的最可靠标志。
尿液代谢物分析氨基酸变化
色氨酸
色氨酸因与自闭症症状相关而闻名,它是血清素 (5-HT) 的前体,血清素是一种抑制性单胺类神经递质,一些研究报告色氨酸水平升高,而另一些研究报告色氨酸水平降低 。
关于色氨酸,详见我们之前的文章:
苏氨酸
有研究发现,自闭症组男孩的苏氨酸含量明显高于对照组男孩。5 岁以下自闭症儿童的尿液苏氨酸含量高于 5 岁以上儿童。苏氨酸属于天冬氨酸家族,是一种蛋白质氨基酸,其分解产生乙酰胆碱酯酶 A 和甘氨酸,促进各种生理过程和整体身体稳态 ,它也可以通过影响色氨酸进入大脑,间接影响5-羟色胺的合成。
脯氨酸
有研究发现,5 岁以下自闭症儿童的脯氨酸含量明显低于 5 岁以上儿童。
与 22q11.2 染色体缺失的 CMPT158 基因型相关的脯氨酸水平异常升高,会影响自闭症谱系症状的严重程度,尤其是影响面部情绪识别、行为和认知。
β-丙氨酸
β-丙氨酸,在肉类中常见的氨基酸,会抑制肠道细胞(如Caco-2细胞)对GABA的吸收。β-丙氨酸也可以在肠道内由白色念珠菌产生的丙酸和氨反应形成,尽管这些化合物也由肠道内的许多其他微生物产生。
HPHPA
有研究报告了一种稀有代谢物3-(3-羟基苯基)-3-羟基丙酸(HPHPA)的出现。HPHPA是梭菌属细菌特有的代谢产物,会耗尽大脑中的儿茶酚胺,导致自闭症症状。
HPHPA在患有艰难梭菌感染的个体中也有发现,并且在急性精神病发作的精神分裂症患者中甚至达到非常高的水平。
以上这些研究是基于血浆、尿液氨基酸变化,血液和尿液中的氨基酸(AA)水平受许多因素影响,包括从食物中吸收的氨基酸、氨基酸和蛋白质的降解、宿主蛋白质的分泌和在粪便中的排泄。这些氨基酸相对比例的改变也可能对它们参与的代谢途径的产物产生连锁反应,包括不同神经递质的生产或相对比例。
肠道菌群代谢分析氨基酸变化
大多数氨基酸来自饮食或由体内合成,但肠道微生物群也会影响饮食氨基酸的回收以及氨基酸的生产或分解。
目前,我们对参与氨基酸生物利用度和肠道微生物群体生物转化的微生物种类或代谢过程知之甚少,对于其对神经功能的可能影响了解更少,也不清楚不同食物和食物成分如何相互作用以调节肠道微生物群对氨基酸的摄取或代谢。
有早期体外研究显示,人类肠道微生物群对氨基酸的发酵受到低pH值和可发酵纤维/碳水化合物(抗性淀粉)存在的抑制。然而,目前不知道这种过程在体内如何转化,或在自闭症等疾病状态或抗生素治疗下如何变化。
谷禾肠道菌群健康检测数据库中有这样的案例,一起来看一下:
一名5岁自闭症男孩,检测结果,自闭症为中等风险,符合实际情况。
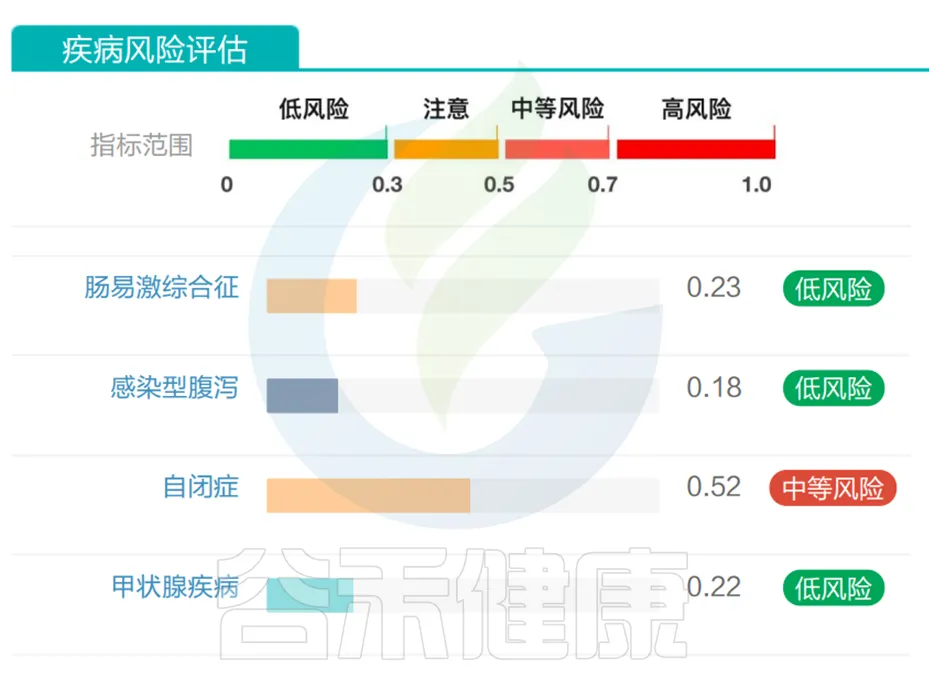
<来源:谷禾健康肠道菌群检测数据库>
这是谷禾利用几十万例的临床和人群样本数据(其中4895例自闭症患者),结合机器学习方法,使用肠道菌群数据进行疾病状态和风险的预测,并给出了的风险值。
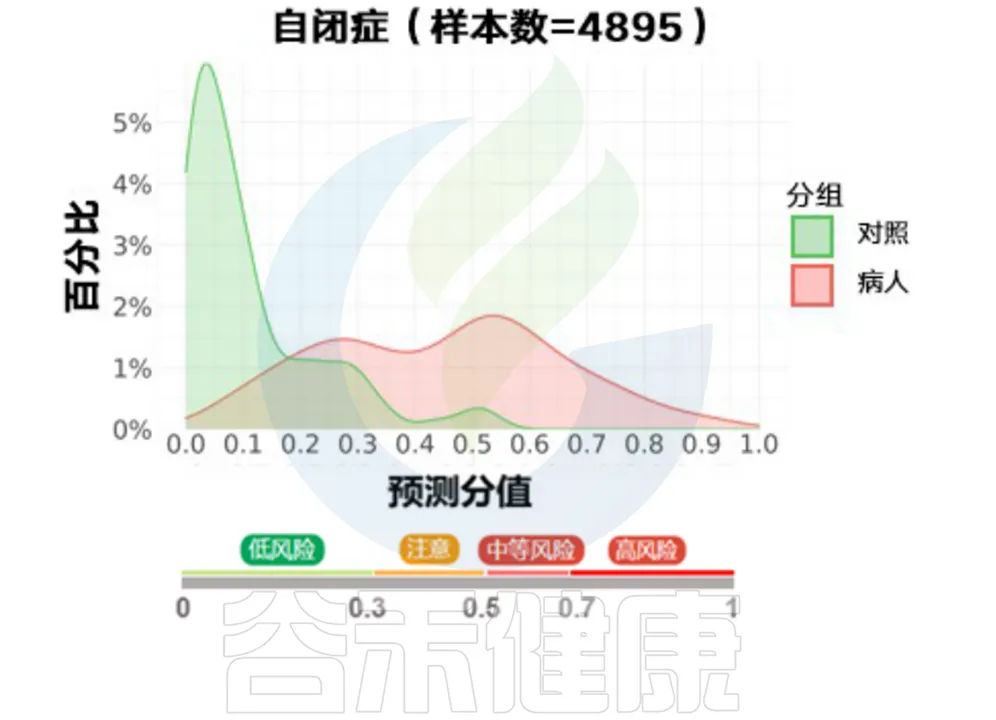
<来源:谷禾健康肠道菌群检测数据库>
从该患者肠道菌群检测报告可以看到,蛋白质,脂肪水平都相对偏低。
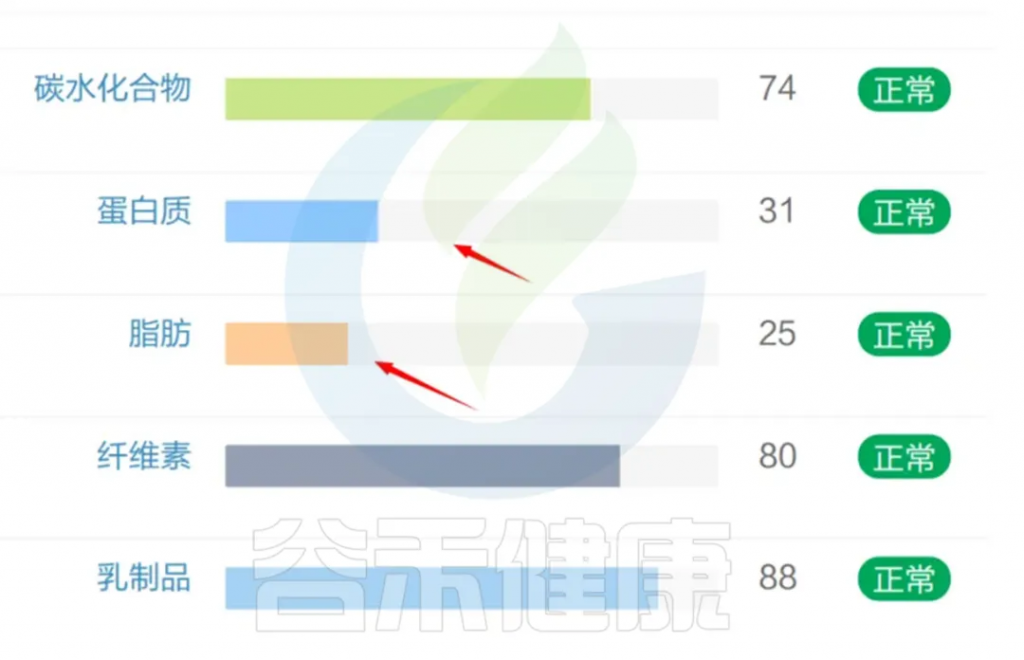
<来源:谷禾健康肠道菌群检测数据库>
我们再来看肠道菌群检测报告中的氨基酸水平,部分氨基酸严重缺乏,例如组氨酸;
其他氨基酸如酪氨酸、谷氨酸、甘氨酸、亮氨酸、赖氨酸、蛋氨酸也都相对偏低。
酪氨酸是一种与认知功能相关的儿茶酚胺前体。
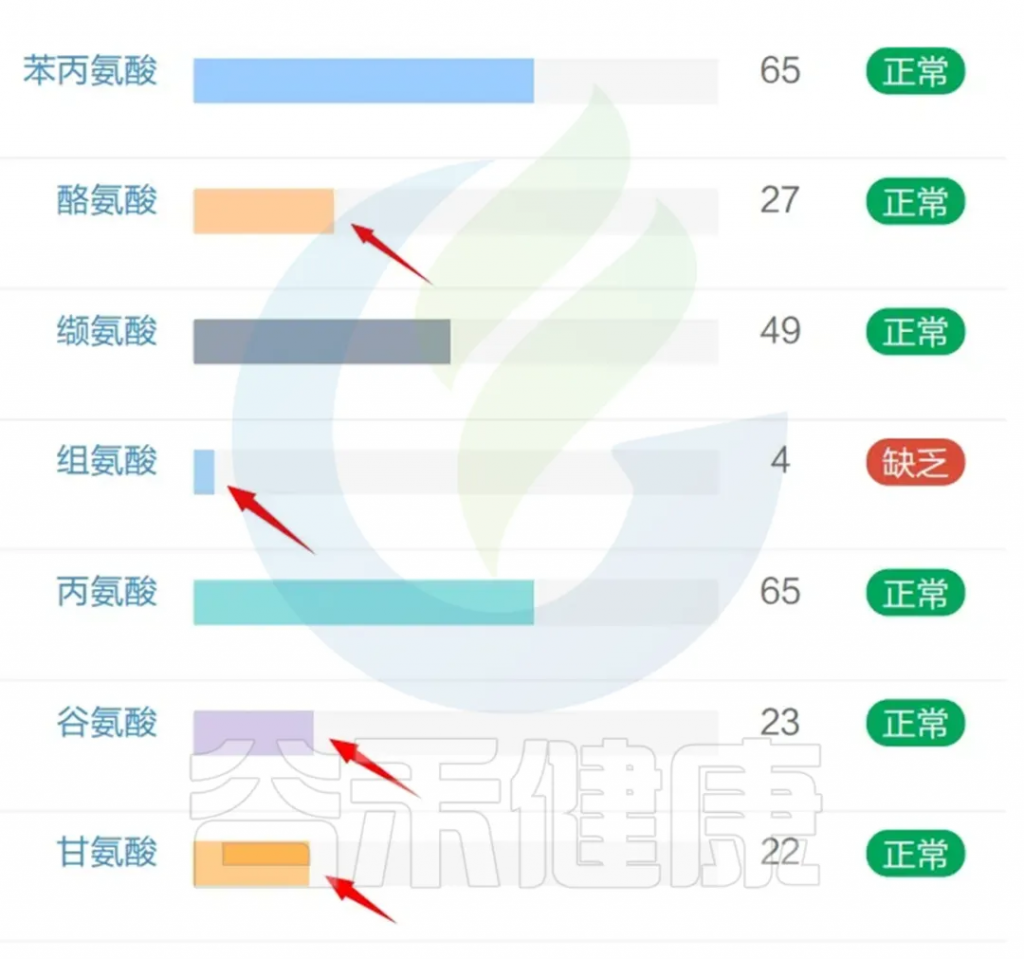
<来源:谷禾健康肠道菌群检测数据库>
组氨酸通过清除氧自由基发挥抗氧化作用,从而参与缓解氧化应激。组氨酸是肌肽的前体,肌肽是一种含有 β 丙氨酸和组氨酸的二肽,在人脑中起到缓冲剂和抗氧化剂的作用。肌肽可以调节与智力障碍相关的各种生物途径。
组氨酸是组胺的前体,而组胺是一种重要的神经递质和神经调节因子。关于组胺,详见之前的文章:
有小鼠研究显示,组氨酸缺乏的小鼠表现出一些类似自闭症的行为,如社交互动减少、刻板重复行为增多等。其他也有多项研究表明,组氨酸血症与自闭症和语言发育迟缓之间存在关联。
谷氨酸,可以调节记忆和学习等认知功能,而这些功能在自闭症患者中通常会受损,关于谷氨酸,详见谷禾之前的文章:
甘氨酸是一种具有抗炎、细胞保护和免疫调节特性的抑制性神经递质,甘氨酸以多种方式与线粒体代谢相关。
其他,赖氨酸,蛋氨酸,亮氨酸都属于人体必须氨基酸,是人体不能自行合成或以适合人体需要的速率合成的氨基酸,必须通过食物摄入来获取。
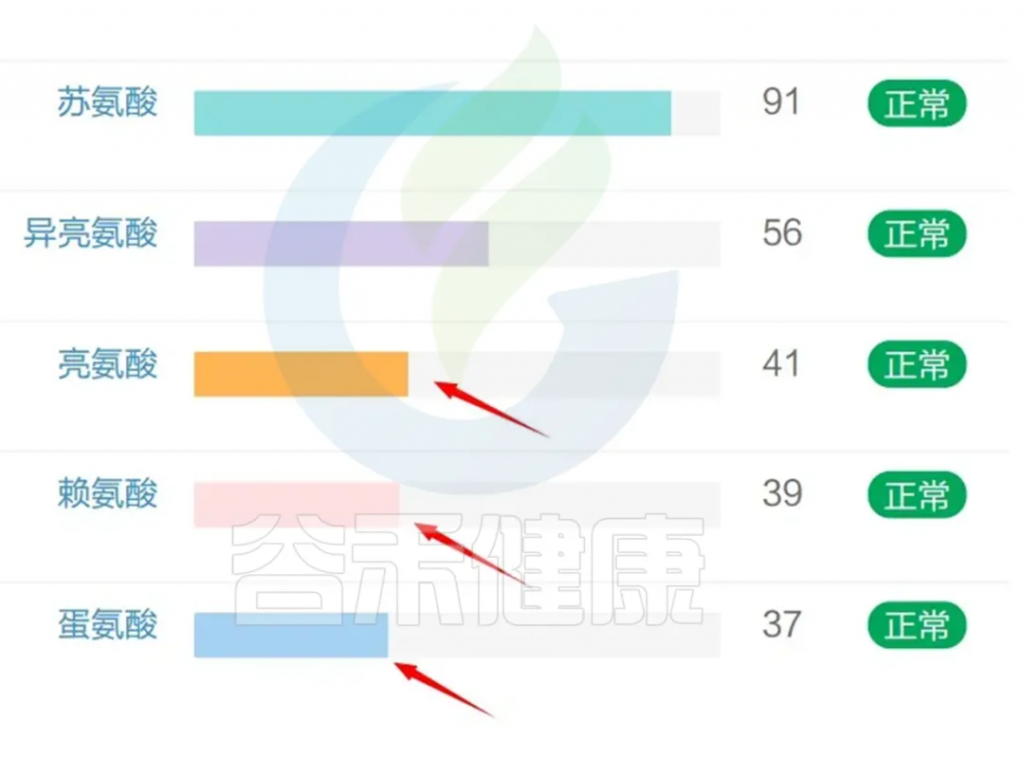
<来源:谷禾健康肠道菌群检测数据库>
亮氨酸,属于支链氨基酸,支链氨基酸生物合成与自闭症症状、甲基化潜力和细胞内 GSH 比率相关。支链氨基酸具有多种生理作用,包括调节葡萄糖和脂肪酸代谢以及调节重要的分子途径和促进蛋白质合成,它们通过琥珀酰辅酶 A 进入 CAC 与线粒体功能相连。大多数自闭症患者都会有线粒体功能障碍。
赖氨酸,是一种生酮氨基酸,通过合成谷氨酸作为其分解的副产物,参与肠道菌群-肠-脑轴。
经过几个月的干预,再次检测肠道菌群,该患者的自闭症风险有所下降,症状也有相应好转。

<来源:谷禾健康肠道菌群检测数据库>
未来患有自闭症的新生儿中关键脂质减少,如亚油酸、α-亚麻酸、胆汁酸、甘油三酯。
这些必需脂肪酸、它们的衍生物、相对比例和个体分子种类在许多哺乳动物的生理过程中起关键作用,包括磷脂生成、膜流动性和大脑发育。
亚油酸和α-亚麻酸
亚油酸和α-亚麻酸是哺乳动物不能自行合成的必需脂肪酸(EFA),必须通过饮食摄取。
注:亚油酸: LA,C18:2n-6,n-6脂肪酸的前体
α-亚麻酸: ALA,C18:3n-3,n-3脂肪酸的前体
它们对大脑具有抗炎作用,并调节自噬、神经传递和神经发生。它们通过抑制神经递质(例如GABA)的释放来调节内源性大麻素系统,从而影响突触功能和可塑性。
ARA、DHA、EPA
与其他身体组织相比,大脑中亚油酸和α-亚麻酸的浓度较低,而其衍生物,特别是ARA(花生四烯酸)和DHA(即二十二碳六烯酸)的浓度较高。
在妊娠晚期,胎儿大脑快速积累多不饱和脂肪酸,特别是DHA。
亚油酸和α-亚麻酸的衍生物可以进一步被宿主磷脂酶修饰,转化为主要来自ARA的二十碳烷类,如前列腺素、白三烯和血栓素。这些二十碳烷是促炎分子,作为局部激素来激活免疫细胞、启动血小板聚集和引发分娩。
相反,DHA和EPA可以进一步转化为抗炎的消退素(resolvins)和保护素(protectins)。
胆汁酸
关于胆汁酸,UDCA,熊去氧胆酸,一种天然存在的次级胆汁酸,在代谢性疾病、自身免疫性疾病、慢性炎症性疾病和神经病理学等疾病中显示出治疗前景。研究发现,UDCA在未来自闭症患者中较低。
ARA加DHA改善自闭症
一项双盲、安慰剂对照随机试验发现膳食补充ARA加DHA(ARA占优势)显著改善了自闭症患者(n=13)在异常行为检查表-社区量表测量的社交退缩和社交回应量表测量的沟通情况。虽然样本量较小,但这个研究证明了通过饮食调节大脑脂肪酸谱可能带来的好处,这种脂肪酸调节在动物研究中也可以通过益生菌达到。
n-3和n-6脂肪酸
一些小规模的n-3和n-6脂肪酸的膳食干预研究显示,自闭症患者的症状有所缓解,虽然并非所有研究都显示有改善。
自闭症患者可能与母乳喂养较少有关
自闭症和精神分裂症患者较少接受母乳喂养,而健康对照组则较多,这表明富含ARA、EPA和DHA的人类母乳对婴儿大脑发育的最佳饮食份额的重要性。相反,早期断奶与自闭症风险增加相关。这些观察结果不仅强调了早期产后饮食对大脑发育和自闭症风险的重要性,还暗示了肠脑轴和肠道微生物群在这一发育过程中的可能早期作用。
补充益生菌,改变脂肪酸
一些肠道微生物,最著名的是某些乳酸菌属和双歧杆菌属的菌种,具备进行脂肪酸生物氢化所需的酶,从而增加脂肪酸的不饱和度。
研究表明,饮食补充α-亚麻酸(ALA)会改变小鼠肝脏、脂肪组织和大脑中的脂肪酸谱,并且在联合补充α-亚麻酸与益生菌Bifidobacterium breve NCIMB 702258时,脂肪酸谱会进一步改变。
注:B. breve NCIMB 702258是高效生产共轭亚油酸(CLA)的菌。
相比于对照组喂养或单独补充α-亚麻酸的情况,食用n-3脂肪酸加益生菌的动物其大脑中的DHA水平升高,而ARA水平下降。
同一组作者随后表明,单独使用B. breve NCIMB 702258菌株,相比于另一种共轭亚油酸(CLA)产生的B. breve菌株和对照组,小鼠的大脑中DHA和ARA的水平也有所上升,证实了益生菌调节大脑脂肪酸谱的能力,并显示这种活动具有明显的菌株特异性。
LA和ALA不够,其他饱和脂肪酸来凑
尽管亚油酸(LA)和α-亚麻酸(ALA)是磷脂形成所必需的必需脂肪酸,但当饮食中这些脂肪酸含量偏低时,其他脂肪如饱和脂肪酸有时可作为替代品,从而对最终磷脂的结构和可能的功能产生影响。
磷脂代谢异常、脂肪酸缺乏或血脂异常已牵涉到多种神经和大脑发育或退行性疾病,包括精神分裂症、注意力缺陷多动障碍(ADHD)、抑郁症、广泛性发育障碍、发育性协调障碍、癫痫、双相情感障碍、阿尔茨海默病、帕金森病、尼曼-皮克病、亨廷顿舞蹈病、中风。
胆固醇代谢和磷脂代谢异常在自闭症中起作用
自闭症患者血液中磷脂酶A2水平较高,细胞膜中的ARA和DHA水平较低,并且可能具有更高的n-6脂肪酸与n-3脂肪酸的比例。
与健康对照组相比,自闭症儿童(n=16)的红细胞脂质谱被修改,表现为较低的胆固醇水平和细胞膜中单唾液四己糖神经节苷脂(GM1)的比例较高。研究人员认为这可能反映了更普遍的胆固醇合成缺陷,在大脑中,结合GM1表达的变化,可能会促成自闭症的病理生理机制。
BDNF对突触传递和神经元胆固醇合成的影响
自闭症与BDNF和益生菌的关联
然而,并非所有益生菌研究都显示BDNF与实验动物观察到的脑功能改善有关。
益生菌、益生元与改善脑功能
然而,需要在人类受试者和相关实验模型中进行基础研究,以验证这些假设的有效性并在机制上将肠道细菌与这些病情联系起来。
大脑占人体质量约2%,但却占胆固醇约20%。血脑屏障(BBB)对脂蛋白是不可通透的,这意味着大脑所需的胆固醇是内源性形成的。
其中星形胶质细胞和神经元分别是胆固醇的净生产者和使用者,体现了胆固醇生物合成机制的独特分区化。
神经元——胆固醇的使用者
神经元需要大量的胆固醇来维持其广泛的膜表面积并提供突触前囊泡的形成。它们还有稍微不同的酶途径,将鲨烯转化为胆固醇。出生后的胆固醇主要由星形胶质细胞提供,并优先来源于乙酸盐。
注:鲨烯(C30H50)是一种多不饱和烃类,也称为角鲨烯或三十碳六烯。 它是一种在人体胆固醇合成等代谢过程中产生的萜类化合物。鲨烯在自然界中广泛存在,尤其是在鲨鱼肝油中含量较高,同时也是橄榄油、米糠油等少数几种植物油中的成分。具有良好的生物活性,在食品、化妆品、保健品等领域广泛应用。
星形胶质细胞——胆固醇的净生产者
星形胶质细胞是包裹神经细胞的细胞,负责供应细胞外钾、谷氨酸、能量和抗氧化剂,并调节大脑中的活性依赖性血流,并可能影响突触活动。
星形胶质细胞在大脑胆固醇运输中的关键作用
ApoE缺乏的啮齿动物模型,表现出各种行为和神经系统症状,并在感觉系统中也有缺陷,这些缺陷与随年龄增长而丧失的突触和树突,突触膜胆固醇分布的改变有关。
CYP46,在维持大脑胆固醇稳态中的作用
短链脂肪酸——乙酸,对神经发育的作用
出生后乙酸在神经发育中重要,母乳喂养乙酸多
AceCS1的表达及其功能
乙酸是胆固醇的组成成分
乙酸的代谢去向
乙酸作为特殊代谢产物的重要性
NAA——乙酸的主要来源之一
N-乙酰天冬氨酸(NAA)在大脑中的作用
自闭症儿童大脑中NAA浓度降低
短链脂肪酸——丙酸,对大脑的负面影响
饮食如何影响大脑中短链脂肪酸的可用性?
自闭症中二糖酶和己糖转运蛋白减少
研究发现,在自闭症儿童中,二糖酶和己糖转运蛋白的表达显著减少,这些变化与肠道微生物群组成的变化相关。这些变化与厚壁菌门相对丰度较高,拟杆菌门较少,以及β-变形菌门升高有关。
注:至少是三种常见肠道二糖酶之一:蔗糖酶-异麦芽糖酶(SI)、麦芽糖酶-异麦芽糖酶(MGAM)、乳糖酶(LCT)
己糖转运蛋白:SGLT1、GLUT2
肠道二糖酶和糖转运蛋白的表达受到多种因素的调控,包括饮食、肠道微生物以及肠神经系统等。
丁酸:结肠健康的关键能量源与吸收机制
考虑到丁酸是结肠细胞的首选能量来源、黏膜更新和分化的介质,以及其生产率在早期肠道微生物群继发发育过程中发生变化,丁酸在肠黏膜成熟中的作用可能非常重要。
丁酸吸收机制:MCT1负责运输,GPR109A助攻
在了解了丁酸在肠黏膜中的重要性及其吸收机制之后,我们再探讨不同饮食和环境因素对MCT1表达的影响及其对丁酸和其他短链脂肪酸吸收的调节作用。
饮食影响短链脂肪酸(丁酸)吸收的机制
高纤维饮食和益生元→MCT1表达和短链脂肪酸吸收↑
高脂肪饮食→抑制短链脂肪酸在结肠中的吸收
肠道炎症和氧化应激→MCT1表达↓→丁酸吸收↓
以上我们知道,MCT1表达异常会影响丁酸吸收,不仅如此,MCT1表达异常还可能与肥胖相关的神经系统疾病有关。
在饮食诱导和遗传性肥胖动物中,MCT1-4 表达都增加,特别是在神经元和神经元胞体中,说明这种变化可能不全是饮食因素,也可能是由于肥胖引起的激素变化间接导致的。
前面我们知道,MCT与短链脂肪酸转运相关,那么MCT表达异常,短链脂肪酸也异常,可能会影响大脑的能量代谢,如果这些变化发生在生命早期,可能会影响神经系统的发育过程,并与个体成年后的肥胖易感性相关。
注:从母乳到固体食物的饮食结构转换可能会影响生理发育、代谢途径和营养转运蛋白(如MCT)的表达,从而对大脑功能产生重要影响。
谷禾发表在 GUT上的队列也表明,随着断奶或引入辅食,自闭症儿童的肠道菌群发育轨迹逐渐偏离健康儿童。如下:
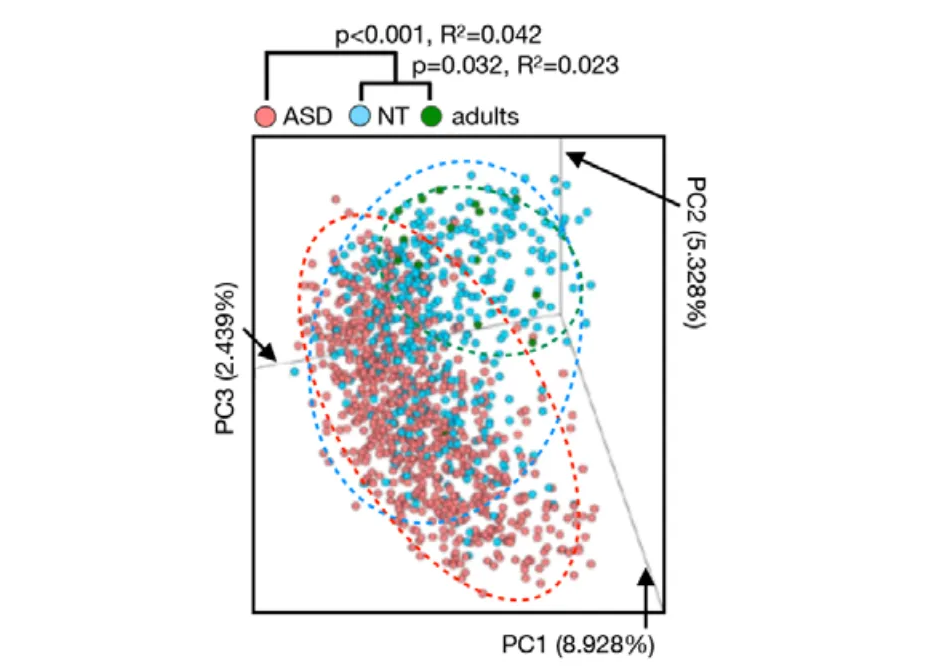
doi: 10.1136/gutjnl-2021-325115.
不良饮食,尤其是在断奶后采用现代西式饮食,实际上可能通过将营养素转运蛋白关闭,重定向营养流向,从而下调了必需营养素(如氨基酸、脂肪和SCFA)的肠道流动。
对比现代西式饮食和古老传统的饮食,有助于重新定义营养不良的范式。营养不良不再仅限于某些必需营养素的缺乏,还包括营养过剩和异常的营养素比例和结构。

在人类“超级有机体”中,这种改变的营养环境的代谢后果,最明显地体现在肠道微生物群与宿主能量代谢和大脑功能的相互作用中。
生命早期:母乳喂养
前面我们了解到,早期断奶与自闭症风险增加相关。很多自闭症患者较少接受母乳喂养,这表明母乳中含有ARA、EPA和DHA,是婴儿大脑发育的最佳饮食。
随着年龄增长:其他饮食
多酚及其代谢物
现有的研究确认了流行病学数据,表明多酚及其代谢物可能有助于促进大脑健康。提出的作用机制包括抗氧化活动、改善血管功能和脑部血流、直接增强神经元信号传递、缓冲钙离子、增强神经保护性应激蛋白和减少应激信号。
线粒体功能障碍在自闭症谱系障碍、神经退行性疾病和一般脑老化的发病机制中得到了关注。线粒体常被认为是氧化应激的启动者和目标,植物多酚代谢物可能具有保护作用。
体外研究在生理相关剂量下测试了选定多酚代谢物对高级糖化终产物形成的抑制能力以及对人类神经元细胞中轻度氧化应激的对抗能力。例如:
药用植物的多酚提取物
少数研究探讨了来自药用植物的多酚提取物对自闭症动物模型的影响,发现:
注:尚需确定这些高剂量植物提取物的抗氧化活性仅与减轻丙戊酸引起的氧化损伤相关,还是在氧化损伤可能只是一个影响因素的神经病理情况下更具广泛相关性。
——黄酮类化合物
肠道菌群对黄酮类化合物的吸收转化
估计有95%的膳食植物多酚在上肠道内无法消化和吸收,并最终到达结肠中的肠道微生物群。一些黄酮类糖苷进入结肠,被肠道菌群分解为更简单的代谢物,比如:
黄酮类化合物对肠道菌群的调节
膳食类黄酮调节肠道菌群改善自闭症
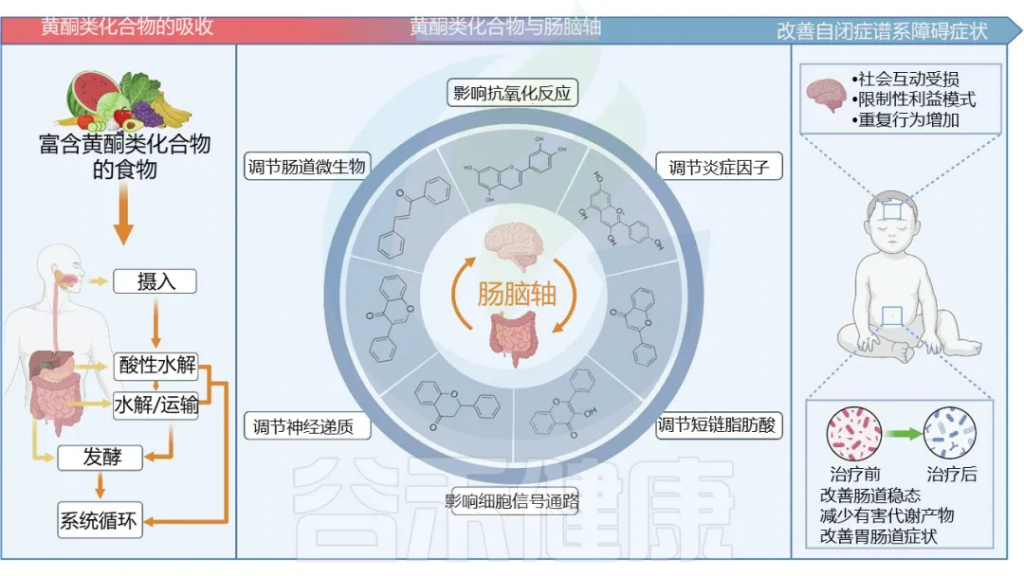
doi.org/10.1016/j.foodres.2024.114404
黄酮类化合物抗自闭症作用的实验研究


doi.org/10.1016/j.foodres.2024.114404
肥胖和不良饮食与抑郁症和自闭症谱系障碍发病率增加有关。同样,母亲的不良饮食(特别是高脂肪饮食),健康状况(特别是肥胖/代谢综合症),会影响胎儿和新生儿的大脑发育过程,从而增加焦虑、抑郁、注意力缺陷多动障碍(ADHD)和自闭症等神经系统疾病的风险。
神经内分泌系统,特别是下丘脑-垂体-肾上腺(HPA)轴,代表了肠道环境和中枢神经系统(CNS)之间的主要通信通道。
在动物模型中,使用各种益生菌微生物干预,既包括乳酸杆菌也包括双歧杆菌,已显示能够减轻标准动物应激挑战下的类似焦虑行为。
婴儿双歧杆菌
L. helveticus R0052 和 B. longum R0175
L. rhamnosus JB-1
脆弱拟杆菌NCTC 9343
注:脆弱拟杆菌是一个比较复杂的菌种,里面既有潜在的益生菌株,也有致病的病原菌株,具体可以查看我们以前文章:
益生元
最近的研究表明,饮食中补充益生元发酵纤维,可以选择性地刺激对人体有益的肠道细菌,如双歧杆菌,从而对大脑产生重要变化。
实验动物在摄入果寡糖(FOS)或半乳寡糖(GOS)后,海马中的BDNF和N-甲基-d-天冬氨酸受体(NMDARs)亚基NR1的表达增加,并且GOS似乎通过诱导肠道激素PYY来介导这一过程。FOS和GOS都能够上调肠道微生物群中短链脂肪酸的产生,特别是乙酸和丁酸,同时增加肠道双歧杆菌的相对丰度。
L-肌肽
胆固醇或DHA
从模拟人类婴儿营养的猪仔研究中,发现婴儿配方奶粉中的胆固醇补充会改变大脑中的氨基酸谱,降低谷氨酸、丝氨酸、谷氨酰胺、苏氨酸、β-丙氨酸、丙氨酸、蛋氨酸、异亮氨酸、亮氨酸和γ-氨基丁酸的浓度,同时增加甘氨酸和赖氨酸的浓度。
二十二碳六烯酸(DHA)也有类似的效果,但会降低牛磺酸水平,对异亮氨酸和赖氨酸没有影响。胆固醇或DHA膳食补充剂也会影响猪仔肝脏、肌肉和血浆中的氨基酸水平。DHA还会减少肌肉和大脑中的肌肽和氨的含量。
这些观察结果确实对食物选择或家庭饮食对营养可用性和代谢的影响有重要启示,进而影响早期儿童的大脑发育和功能,当然还需在人类队列中进一步研究其潜在机制。
药物
对自闭症儿童每周使用万古霉素治疗,可显著改善神经行为和胃肠道症状。
粪菌移植
一项开放标签研究对18名自闭症儿童进行了粪菌移植(每日口服8周),结果表明移植后其胃肠道症状和自闭症核心症状评分均有所改善。
移植后8周,受试者的肠道菌群多样性增加,厚壁菌门丰度下降,拟杆菌门和变形菌门丰度上升。
随访2年后,受试者的部分症状改善仍然维持。这提示通过重建肠道菌群可能成为干预自闭症的新策略。
关于粪菌移植,仍需更多深入研究。
自闭症谱系障碍 (ASD) 是一组神经发育疾病,一般在 3 岁之前发病,目前的发病率在全世界逐渐升高,与多种因素有关,其中饮食会影响和塑造肠道微生物群,孕期和幼儿期似乎是一个关键时期,尤其从哺乳/配方奶→断奶→成人“家庭”饮食的过渡过程中饮食和环境暴露影响较大。
人类微生物组对宿主代谢过程和膳食化合物加工的核心贡献,许多营养物质和摄入的化学物质必须经过肠道及肠道微生物,转化为生物可利用和活跃的中间产物,然后通过肝门静脉被吸收并在全身分布。
研究表明,大部分自闭症患者的肠道菌群异常,这可能与饮食习惯、抗生素使用等因素有关。同时,自闭症患者某些氨基酸水平也存在异常。
饮食作为塑造肠道微生物群的重要因素,可能在自闭症的发病中扮演重要角色。优化孕期和幼儿期的饮食结构,如母乳喂养、合理添加辅食、避免过多加工食品和添加剂等,有助于维持肠道菌群平衡,从而有助于大脑健康。
针对自闭症患者的饮食干预,如补充益生元、益生菌,调整膳食纤维和蛋白质比例等,可能对改善部分症状有一定帮助。但由于自闭症的高度异质性,饮食干预的效果可能因人而异,还需要更多的结合个体化健康信息及相应症状进行个性化指导和干预。
此外,幼儿早期尤其6-12个月能够更早判别出自闭症风险,对于神经发育的改善和行为的扭转非常重要,希望临床上与相关机构能够合作共同推进自闭症的研究和个性化干预。
注:本账号内容仅作交流参考,不作为诊断及医疗依据。
主要参考文献:
Lou M, Cao A, Jin C, Mi K, Xiong X, Zeng Z, Pan X, Qie J, Qiu S, Niu Y, Liang H, Liu Y, Chen L, Liu Z, Zhao Q, Qiu X, Jin Y, Sheng X, Hu Z, Jin G, Liu J, Liu X, Wang Y. Deviated and early unsustainable stunted development of gut microbiota in children with autism spectrum disorder. Gut. 2022 Aug;71(8):1588-1599.
Ahrens A P, Hyötyläinen T, Petrone J R, et al. Infant microbes and metabolites point to childhood neurodevelopmental disorders[J]. Cell, 2024, 187(8): 1853-1873. e15.
Chen, WX., Chen, YR., Peng, MZ. et al. Plasma Amino Acid Profile in Children with Autism Spectrum Disorder in Southern China: Analysis of 110 Cases. J Autism Dev Disord 54, 1567–1581 (2024).
Chang, X., Zhang, Y., Chen, X. et al. Gut microbiome and serum amino acid metabolome alterations in autism spectrum disorder. Sci Rep 14, 4037 (2024).
Kieran M. Tuohy, Paola Venuti, Simone Cuva, et al, Chapter 15 – Diet and the Gut Microbiota – How the Gut: Brain Axis Impacts on Autism, 2015, Pages 225-245, American Psychiatric Association. Diagnostic and Statistical Manual of Mental Disorders (4th ed.), American Psychiatric Association, Washington DC (1994)
Anastasescu, C.M.; Gheorman, V.; Popescu, F.; Stoicănescu, E.-C.; Gheorman, V.; Riza, A.-L.; Badea, O.; Streață, I.; Militaru, F.; Udriștoiu, I. Serum Amino Acid Profiling in Children with Autistic Spectrum Disorder: Insights from a Single-Center Study in Southern Romania. Healthcare 2023, 11, 2487
V. Hughes. Epidemiology: complex, disorder, Nature, 491 (2012), pp. S2-S3
S. Baron-Cohen, F.J. Scott, C. Allison, et al., Prevalence of autism-spectrum conditions: UK school-based population study. Br J Psychiatry, 194 (2009), pp. 500-509
T.S. Brugha, S. McManus, J. Bankart, et al., Epidemiology of autism spectrum disorders in adults in the community in England Arch Gen Psychiatry, 68 (2011), pp. 459-466
B.S. Abrahams, D.H. Geschwind., Advances in autism genetics: On the threshold of a new neurobiology, Nat Rev Genet, 9 (2008), pp. 341-355
Brister, D.; Rose, S.; Delhey, L.; Tippett, M.; **, Y.; Gu, H.; Frye, R.E. Metabolomic Signatures of Autism Spectrum Disorder. J. Pers. Med. 2022, 12, 1727.
S. Ozonoff, B.J. Williams, R. Landa, Parental report of the early development of children with regressive autism: The delays-plus-regression phenotype, Autism, 9 (2005), pp. 461-486
S. Ozonoff, G.S. Young, M.B. Steinfeld, et al., How early do parent concerns predict later autism diagnosis?
J Dev Behav Pediatr, 30 (2009), pp. 367-375
G. Esposito, P. Venuti, Symmetry in infancy: Analysis of motor development in autism spectrum., disorders, Symmetry, 1 (2009), pp. 215-225
Zhao Y, Wang Y, Meng F, Chen X, Chang T, Huang H, He F, Zheng Y. Altered Gut Microbiota as Potential Biomarkers for Autism Spectrum Disorder in Early Childhood. Neuroscience. 2023 Jul 15;523:118-131.
G. Esposito, P. Venuti, F. Apicella, F. Muratori, Analysis of unsupported gait in toddlers with autism, Brain and Development, 33 (2011), pp. 367-373
F. Happé, A. Ronald, R. Plomin, Time to give up on a single explanation for autism, Nat Neurosci, 9 (2006), pp. 1218-1220
T. Charman, C.R.G. Jones, A. Pickles, E. Simonoff, G. Baird, F. Happé, Defining the cognitive phenotype of autism, Brain Res, 1380 (2011), pp. 10-21
P. Krakowiak, C.K. Walker, A.A. Bremer, et al.,Maternal metabolic conditions and risk for autism and other neurodevelopmental disorders,Pediatrics, 129 (2012), pp. e1121-e1128
J.A. Hollway, M.G. Aman Pharmacological treatment of sleep disturbance in developmental disabilities: a review of the literature,Res Dev Disabil, 32 (2011), pp. 939-962
Shen L, Liu X, Zhang H, Lin J, Feng C, Iqbal J. Biomarkers in autism spectrum disorders: Current progress. Clin Chim Acta. 2020 Mar;502:41-54.
C.A. Molloy, P. Manning-Courtney,Prevalence of chronic gastrointestinal symptoms in children with autism and autistic spectrum disorders, Autism, 7 (2003), pp. 165-171
D.V. Keen , Childhood autism, feeding problems and failure to thrive in early infancy: Seven case studies, Eur Child Adolesc Psychiatr, 17 (2008), pp. 209-216
L.G. Bandini, S.E. Anderson, C. Curtin, et al., Food selectivity in children with autism spectrum disorders and typically developing children, J Pediatr, 157 (2010), pp. 259-264
S.A. Cermak, C. Curtin, L.G. Bandini, Food selectivity and sensory sensitivity in children with autism spectrum disorders, J Am Diet Assoc, 110 (2010), pp. 238-246
Y. Martins, R.L. Young, D.C. Robson, Feeding and eating behaviors in children with autism and typically developing children, J Autism Dev Disord, 38 (2008), pp. 1878-1887, View at publisher
E. Cornish, A balanced approach towards healthy eating in autism, J Hum Nutr Diet, 11 (1998), pp. 501-509
P. Whiteley, J. Rodgers, D. Savery, P. Shattock, A gluten-free diet as an intervention for autism and associated spectrum disorders: Preliminary findings, Autism, 3 (1999), pp. 45-65
K. Fitzgerald, M. Hyman, K. Swift, Autism spectrum disorders, Glob Adv Health Med, 1 (2012), pp. 62-74
E. Courchesne, K. Campbell, S. Solso, Brain growth across the life span in autism: age-specific changes in anatomical pathology, Brain Res, 1380 (2011), pp. 138-145
M. Rutter, Aetiology of autism: findings and questions, J Intell Disabil Res, 49 (2005), pp. 231-238, View at publisher
J.J. Michaelson, Y. Shi, M. Gujral, et al.
Whole-genome sequencing in autism identifies hot spots for de novo germline mutation, Cell, 151 (2012), pp. 1431-1442
B.N. Vardarajan, A. Eran, J.Y. Jung, L.M. Kunkel, D.P. Wall, Haplotype structure enables prioritization of common markers and candidate genes in autism spectrum disorder
Transl Psychiatry, 3 (2013), p. e262
Yu X, Qian-Qian L, Cong Y, Xiao-Bing Z, Hong-Zhu D. Reduction of essential amino acid levels and sex-specific alterations in serum amino acid concentration profiles in children with autism spectrum disorder. Psychiatry Res. 2021 Mar;297:113675.
J. Veenstra-Vanderweele, R.D. Blakely
Networking in autism: Leveraging genetic, biomarker and model system findings in the search for new treatments, Neuropsychopharmacol, 37 (2012), pp. 196-212
K.T.E. Kleijer, M.J. Schmeisser, D.D. Krueger, et al. Neurobiology of autism gene products: towards pathogenesis and drug targets, Psychopharmacology (Berl), 231 (6) (2014), pp. 1037-1062
Li H, Dang Y, Yan Y. Serum interleukin-17 A and homocysteine levels in children with autism. BMC Neurosci. 2024 Mar 12;25(1):17.

谷禾健康

肠道微生物群在食物消化、免疫激活和肠道内分泌信号通路的调节中扮演关键角色。同时,它们通过产生特定的代谢化合物与中枢神经系统(CNS)及身体其他部位进行密切交流。
这些代谢物包括次级胆汁酸、短链脂肪酸(SCFAs)、谷氨酸(Glu)、γ-氨基丁酸(GABA)、多巴胺(DA)、肾上腺素、吲哚、血清素(5-HT)和组胺等神经递质以及其他重要信号分子。
这些神经递质和主要菌群代谢物对肠道微生物及人体健康有着深远的影响。肠道细菌主要利用GABA、多巴胺、谷氨酸、血清素和组胺等神经递质,以及短链脂肪酸、色氨酸和次级胆汁酸等菌群代谢产物,与中枢神经系统进行双向通讯。这些信号分子通过传入迷走神经纤维传输到大脑,大脑则通过传出的迷走神经纤维将信号发送回肠壁中的肠神经细胞和粘膜免疫系统。下丘脑-垂体-肾上腺轴(HPA轴)也参与了这一复杂的信号调控网络。
这些神经递质和菌群代谢物的协调作用,对维持肠道生态平衡和免疫稳态至关重要。一旦出现失衡,就可能导致主要胃肠道疾病,甚至影响神经系统功能,引发神经退行性疾病。
相应的,通过对肠道菌群的分析和前期构建的研发数据队列,我们可以评估出血清中神经递质和菌群代谢产物的水平情况。因为肠道这些指标可以反映肠道微生物在神经递质代谢和信号传递中的作用,从而为评估个体的神经功能和代谢状态提供重要线索。
谷禾健康肠道菌群检测报告新增了这方面的相关指标,本文总结和解读这些神经递质及肠道菌群代谢物,并总结了含量过高和过低对人体健康的影响和一些饮食生活和药物干预措施。

编辑
细菌具有许多不同的代谢方式。一些细菌只需要二氧化碳作为它们的碳源,被称作自养生物。另外一些细菌依靠有机物形式的碳作为碳源,称为异养生物。而人体的肠道微生物群主要就是异养生物,他们通过消化膳食成分和其他人体内的物质来获取营养,从而维持它们的生存和繁殖。这些微生物对于人体健康至关重要。
肠道菌群是宿主消化的关键组成部分,分解复杂的碳水化合物,蛋白质,并且在较小程度上分解到达下胃肠道的脂肪。该过程产生大量微生物代谢物,其可以局部和全身起作用(在被吸收到血流中之后)。这些途径都可以产生潜在有益和潜在毒性的代谢物。
// 肠道菌群将膳食成分转化为各种代谢物
例如细菌可以将多糖、蛋白质、脂肪等大分子营养物质分解为单糖、小肽或氨基酸等,进而产生短链脂肪酸、次级胆汁酸、吲哚、苯酚、硫化氢、谷氨酸、组胺等物质。
细菌除了在分解和合成代谢中能产生多种代谢产物,还被证明可以产生或消耗多种神经递质,包括多巴胺、去甲肾上腺素、血清素或γ-氨基丁酸 (GABA)等。多项的研究证据表明,细菌对这些神经递质的操纵会对宿主的生理及健康产生影响。
注:初步的人体研究还表明,基于微生物群的干预也可以改变神经递质水平。
那么胃肠道与大脑、神经系统甚至全身其他器官是如何相互联系的呢?肠脑轴(Gut-Brain Axis)被称为肠-脑轴或肠道-大脑轴,指的是肠道和大脑之间存在着复杂的相互关系和通讯机制。
// 大部分信号通过双向迷走神经传递
大多数进出肠道的信号都通过双向迷走神经传输,该双向迷走神经在延髓处离开大脑,并在颈静脉孔处离开头骨。颈部迷走神经与控制吞咽和言语的咽喉肌肉通信,胸部迷走神经可降低心率。迷走神经通向胃肠道的分支放松和收缩平滑肌并控制腺体组织的分泌。迷走神经的的腹腔分支与十二指肠相连,其余部分与结肠的远端相连。
髓质迷走神经的节前神经元与固有层和外肌层的肌肉层和粘膜层通信。神经节中的感觉细胞向孤束核(NTS)发送信号,从孤束核向蓝斑(LC)、杏仁核、丘脑和延髓头端腹外侧发送信息。
胃肠道通过迷走神经与中枢神经系统连接
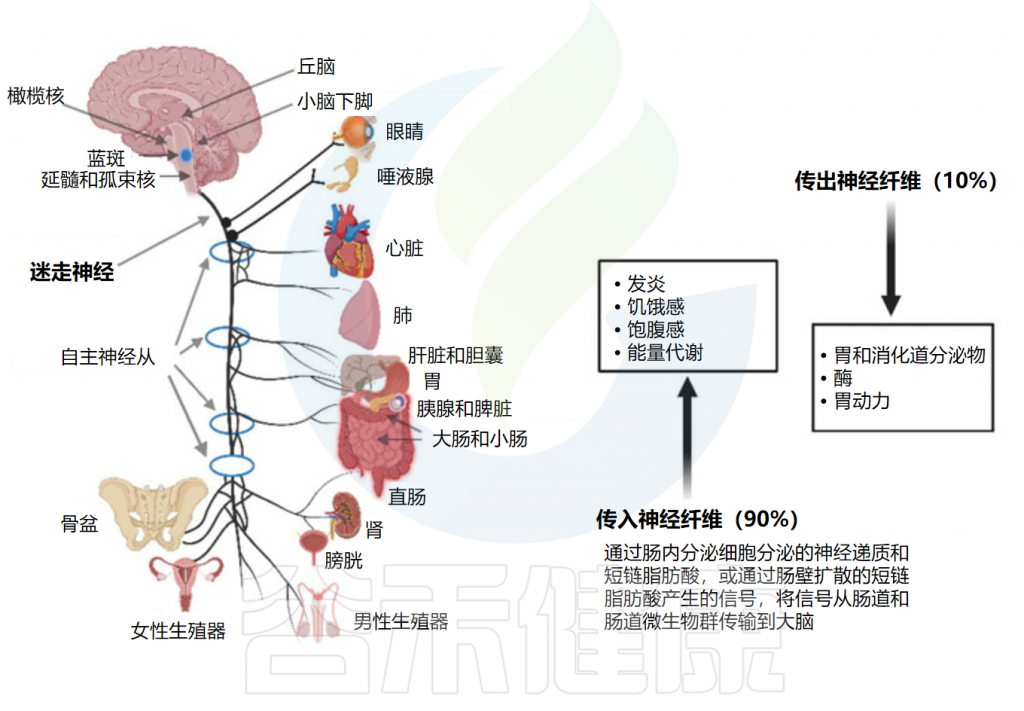
Dicks LMT.Microorganisms.2022
传入神经也与食道、肝脏和胰腺中的受体相连。尽管迷走神经与肠壁的所有层接触,但神经不穿过肠壁,因此不与肠道微生物群直接接触。信号一般通过肠壁粘膜下层和肌间神经丛的肠神经系统(ENS)中的1亿至5亿个神经元到达肠道微生物群。
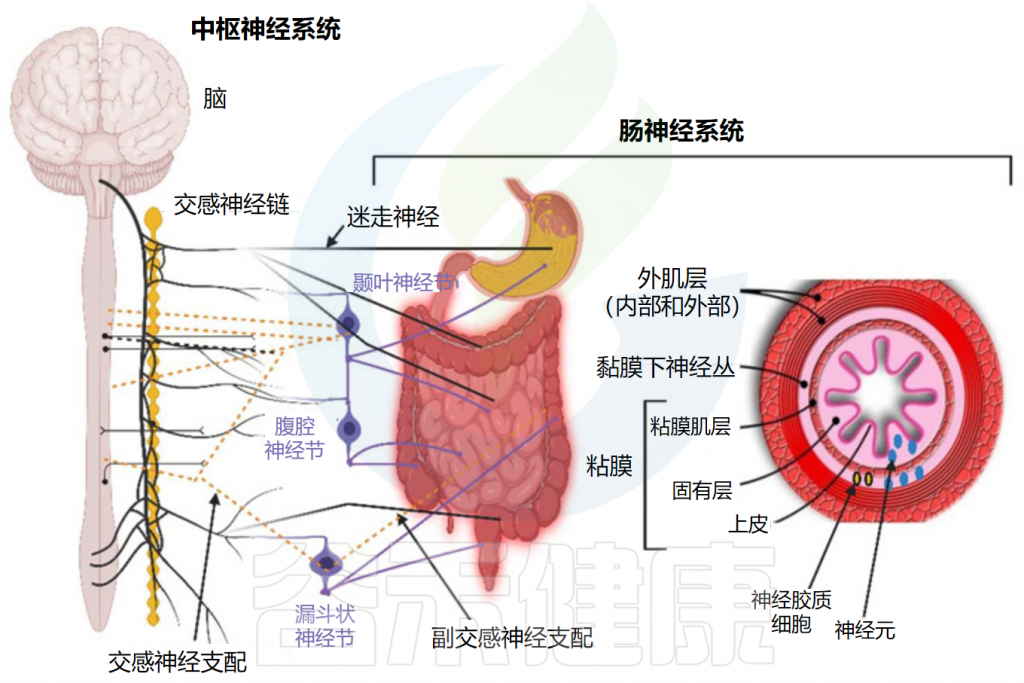
Dicks LMT.Microorganisms.2022
// 肠神经系统功能下降会导致便秘、排便障碍
尽管与迷走神经相关,但小肠和大肠中的部分功能独立于迷走神经。这可能是由于独立的感觉和运动神经元,能够调节肌肉活动、肠壁运动、液体分泌、粘膜层血流和粘膜屏障功能。
与肠神经系统相关的功能下降通常表现为便秘、失禁和排便障碍。这通常发生在老年人身上,被称为先天性巨结肠或肠假性梗阻。最近的研究表明,肠神经系统是动态的,并且不断变化,由细胞凋亡和神经发生过程维持。
与胃肠道相连的神经元有许多受体,它们与肠内分泌细胞(EECs)释放的激素或其他激素相互作用,在维持肠道稳态方面发挥着重要作用。
到目前为止,已经对十多种不同类型的EEC进行了表征。它们作为感觉细胞,协调血清素(5-HT)、神经肽Y(NPY)、血管活性肠肽(VIP)、胆囊收缩素(CCK)、γ-氨基丁酸(GABA)、生长抑素、胰高血糖素样肽(GLP)-1/2、胃饥饿素等的分泌变化。这些感觉细胞上的受体通常由肠道神经元表达,也由迷走传入神经、脑干和下丘脑表达。
// 胆囊收缩素、胰高糖素样肽-1等带来饱腹感
胆囊收缩素、胰高血糖素样肽-1(GLP-1)和肽YY(PYY)水平在餐后长达6小时内保持较高水平。富含蛋白质的饮食会刺激CCK的产生。CCK与胰腺中的特定受体(CCK-A受体)、大脑中的受体(CCK-B受体)以及中枢神经系统中的其他受体结合,这会带来饱腹感。
同时,胰腺释放脂肪分解酶、蛋白分解酶和碳代谢酶。当CCK与胰腺中的钙调神经磷酸酶相互作用时,转录因子NFAT 1-3被激活,刺激胰腺细胞肥大和增殖。
注:高CCK水平会增加焦虑,而生长抑素和胰腺肽可防止CCK的过度释放。
// 胃饥饿素、生长激素释放肽促进食欲
胃饥饿素(ghrelin)在禁食期间由胃释放,进入循环系统并穿过血脑屏障。胃饥饿素通过与位于迷走神经节上的Ghrelin受体(GHSR)的相互作用刺激食欲。
较高的ghrelin水平与升高的多巴胺(DA)水平相关,而多巴胺水平反过来又向中枢神经系统发送饱腹感信号。
一旦进入大脑,生长激素释放肽就会激活弓状核神经元上的受体,导致神经肽Y(NPY)和刺鼠关联蛋白(AgRP)的产生增加。
大脑和脊髓中高水平的NPY与其他神经递质(如GABA和谷氨酸)一起分泌。NPY刺激食欲,以脂肪的形式调节能量的储存,但也能减轻焦虑、压力和疼痛。NPY还调节睡眠模式并保持低血压。
富含低聚果糖和菊粉的饮食会抑制生长素释放肽的产生,并增加肠上皮内分泌L细胞GLP-1的产生。
// 胃饥饿素的产生受到一些肠道菌群的影响
一项研究总结了肠道微生物群对激素释放的影响。胃饥饿素的产生受到拟杆菌某些物种(Bacteroides)、Coriobacteriaceae、韦荣氏菌属(Veillonella)、普雷沃氏菌(Prevotella)、双歧杆菌某些种类(Bifidobacterium)、乳酸杆菌某些品种、粪球菌属(Coprococcus)和瘤胃球菌(Ruminococcus)的刺激,但受到双歧杆菌、链球菌、乳酸杆菌、粪杆菌、拟杆菌、埃希氏菌、志贺菌(Shigella)和链球菌(Streptococcus)的抑制。
这清楚地表明,激素水平的调节是物种特异性的,需要更多的研究来确定所涉及的特定因素。
// 拟杆菌等细菌还影响其他激素的作用
拟杆菌产生与胰岛素、神经肽Y和黑色细胞刺激素(α-MSH)同源的分子。这些分子诱导与循环系统中的免疫球蛋白发生交叉反应,直接对抗生长素释放肽、瘦素、胰岛素、肽YY和神经肽Y。
Rikenellaceae和梭菌科(Clostridiaceae)的一些菌株产生酪蛋白分解酶B(ClpB),可模拟α-MSH水平增加时产生的饱腹感。与ClpB相互作用产生的免疫球蛋白可对抗α-MSH并减少其厌食作用,导致饱腹感降低。
肠嗜铬细胞(EC)控制反射和胃酸分泌,但也产生血清素(5-HT)。D、G、I、K和L型细胞控制酶分泌,单核细胞启动肌电迁移,N细胞调节收缩,S细胞(位于小肠)调节酸度水平,A细胞分泌胃促生长素和内脂素-1,P细胞分泌瘦素。
胃肠道除了通过各种激素使大脑形成不同的感觉和反应外,神经递质也对胃肠道健康及其中的微生物群产生重要影响。谷禾最新的报告中已将神经递质作为健康的重要指标,让我们一起来了解一些重要神经递质对健康的影响。
神经递质一般可分为氨基酸(例如,谷氨酸、天冬氨酸、D-丝氨酸、GABA和甘氨酸)、单胺(多巴胺、去甲肾上腺素、肾上腺素、组胺和血清素)、微量胺(例如,苯乙胺、酪胺、章鱼胺、色胺)、肽(催产素、生长抑素、P物质、可卡因和阿片肽)、气体递质(一氧化氮、一氧化碳和硫化氢)、嘌呤(三磷酸腺苷和腺苷)等。
其中,血清素(5-HT)、γ-氨基丁酸(GABA)、谷氨酸、多巴胺、组胺和一氧化氮被认为是关键的神经递质,将进行更深入的讨论。

血清素又名5-羟色胺(5-HT),主要存在于中枢神经系统和肠道,是一种抑制性神经递质。在中枢神经系统中,血清素充当神经递质,参与调节情绪、睡眠和食欲。它有助于幸福感,有助于调节对压力和焦虑的反应。此外,血清素负责介导多种非神经元过程和功能,例如膀胱调节、止血、呼吸驱动、免疫反应、血管张力和肠道炎症。
血清素作为神经递质发挥着关键作用,但是大脑仅含有大约5%的血清素,而胃肠道系统中的肠嗜铬细胞(ECC)负责产生约90%的人体总血清素。血清素主要由色氨酸合成,而色氨酸则是一种必需氨基酸,必须通过饮食摄入。肠道血清素水平受色氨酸羟化酶TPH1和TPH2调节。
▸ 血清素的合成受到肠道微生物群的调节
肠道微生物群可以影响血清素的产生。研究表明,肠道菌群可以影响血清素的前体物质如色氨酸的代谢,促进血清素的产生。肠嗜铬细胞受到肠道微生物群(特别是短链脂肪酸)的刺激,产生血清素。短链脂肪酸会增加肠嗜铬细胞中的TPH1表达和血清素合成,从而导致循环血清素浓度升高。
一项研究表明乙酸钠(10-50 mM)显著增加人体中TPH1 mRNA 的表达。然而,较高水平的丁酸盐(8.0和16.0mM)分别抑制TPH1表达13.5和15.7倍。
另一项单独的研究表明,无菌小鼠的神经元功能障碍可以通过肠道微生物群的重新定植来逆转。多项研究证实了这一点,并提供了明确的证据表明5-HT的合成受到肠道微生物群的调节。
过高或过低的血清素含量都不利于人体健康
▸ 血清素含量过高的危害
血压异常、心血管问题:5-羟色胺是一种强血管收缩剂和平滑肌收缩刺激剂。高血清素水平可能导致血管过度收缩,增加血压和心血管疾病风险。
神经功能异常:5-羟色胺过高时,由于其抑制植物神经功能,使得交感神经过于兴奋,此时可导致植物神经功能发生紊乱。引起神经功能异常的表现,比如手抖、乏力、出汗、头晕、失眠、胸闷、心悸等。
与炎症性肠病有关:在对患有结肠炎的小鼠进行的研究中,观察到5-HT产量增加。随着5-HT水平的增加,固有层树突状细胞(DC)上7型血清素(5-HT7)受体的表达被激活,并触发促炎免疫反应。而抑制5-HT7受体可减轻肠道炎症。
注:5-HT4受体的激活在成人神经系统的成熟中起着重要作用,因为它调节神经元的形成并保护细胞。
▸ 血清素含量过低的危害
情绪低落、抑郁:5-羟色胺在大脑皮层及神经突触中的含量较高,是一种能产生愉悦情绪的信使。如果该物质的含量偏低,容易影响大脑活动,可能对患者的情绪造成影响,使患者处于较为低落的状态中,常伴有悲观、失落、忧愁等负面情绪。可能导致抑郁、焦虑和情绪波动等心理健康问题。
睡眠障碍:5-羟色胺是一种抑制性神经递质,如果其含量比较低,可能导致中枢神经系统持续处于较为兴奋的状态中,可能导致患者出现睡眠障碍的情况,常有入睡困难、早醒、多梦等表现。
记忆力衰退:在一定程度上,5-羟色胺通常能保护神经元,使其免受兴奋性神经毒素的影响。如果5-羟色胺的含量比较低,可能导致神经元受损,进而影响患者的记忆力。
消化问题:血清素在肠道中也扮演重要角色,过低的血清素含量可能导致消化问题,如胃肠道不适、食欲不振和胃肠道功能紊乱。
最近的一份报告表明一些神经递质可能作为肠道细菌的生长底物。高水平的血清素(5-HT)可能会降低肠壁通透性,而低水平的5-HT会降低人紧密连接蛋白(Occludin)的表达并削弱肠壁,导致通透性增加和肠漏的形成。
▸ 提高血清素水平的方法
一些精神疾病,例如抑郁症与大脑中异常的血清素水平有关。那么血清素过低时可以通过哪些方法来提高呢?
饮食调理:要想补充血清素,要多吃一些富含蛋白质的食物,如鸡蛋、坚果、瘦肉、鱼、虾等,其色氨酸含量较高,进入体内能够促进血清素的合成,升高血清素。
药物补充:血清素低一般可以在医生指导下通过口服药物辅助补充,如选择性血清素再摄取抑制剂(SSRI)、血清素-去甲肾上腺素再摄取抑制剂、三环类抗抑郁药等,可以抑制血清素再摄取,减缓血清素的分解,从而增加血清素的含量。
多晒太阳:阳光照射与血清素水平升高有关,色氨酸的光捕获对于血清素的合成有重要影响。吸收蓝光波会激发色氨酸的吲哚结构,使其失去吲哚环结构中的一个电子,从而被氧化。阳光对人类的血清素水平以及情绪、睡眠和自杀意念都有影响。
锻炼:锻炼对生理和心理健康有多种显著益处,包括提高血清素水平和对整体情绪产生积极影响。例如,一些人类研究报告称,从事有氧运动会导致大脑血清素水平增加,并且如果保持良好的运动习惯,这种增加可能会持久。
积极情绪诱导:正如低血清素水平可能会对我们的情绪产生负面影响一样,消极情绪也会导致血清素水平下降。一些证据表明,使用认知和行为策略积极诱导积极情绪可能有助于维持健康的血清素水平。血清素水平和情绪之间的这种“双向影响”可能会影响一系列身心健康问题。
使用补充剂:在体内,血清素是由5-HTP制成的,而5-HTP是由L-色氨酸制成的。因此,从理论上讲,增加这些“组成部分”(代谢前体)中的任何一个的水平都可以导致血清素总体水平的增加。
维生素D有助于身体(包括大脑)制造、释放和使用血清素。维生素D会激活一种酶,将色氨酸转化为血清素。如果维生素D水平较低,我们的大脑就会产生较少的血清素。因此,增加维生素D的摄入量可能会增加血清素水平,从而有可能支持心理健康。
▸ 血清素过高一般补充药物或补剂需注意
当人的系统中血清素过多时,就会出现血清素综合症。血清素综合征是由于药物、补充剂或草药的组合导致血清素升高至不安全水平而引起的。
最常与血清素综合征相关的抗抑郁药和抗焦虑药包括:
偏头痛药物(曲普坦类药物):曲坦类药物通常是医生为中度至重度偏头痛患者开出的第一种药物。曲普坦类药物还会激活大脑中的血清素受体,并存在发生血清素综合征的风险,特别是与阿片类药物或抗抑郁药联合使用时。
他们包括:
除此之外单胺氧化酶抑制剂、阿片类药物、丁螺环酮 (Buspar)、恶心药物、右美沙芬、迷幻剂,可卡因,以及一些草药和补品如圣约翰草、人参、姜黄、藏红花在使用时也需特别注意,可能会引起血清素综合症。
γ-氨基丁酸(GABA)是一种非蛋白氨基酸,于1950年首次在大脑中被发现,主要在中枢神经系统中发挥作用,是哺乳动物大脑中最主要的抑制性神经递质。GABA的作用是减缓神经系统的活动,帮助维持神经系统的平衡,防止过度兴奋导致的不良反应。
研究发现 , GABA具有激活脑内葡萄糖代谢、促进乙酰胆碱合成、降血氨、抗惊厥、降血压、改善脑机能、精神安定、促进生长激素分泌等多种生理功能。多项研究还证明GABA与一些神经系统疾病如
焦虑、抑郁、癫痫、自闭症谱系障碍(ASD)和注意力缺陷多动障碍存在关联。

▸ 人体肠道内的一些菌群也可以产生GABA
GABA可由多种生物体合成,包括人类、植物和细菌。在合成过程中,GABA由谷氨酸通过谷氨酸脱羧酶(GAD)产生。在人类微生物群中,几种胃肠道细菌含有编码GAD的基因,该基因负责GABA的产生。
双歧杆菌、乳酸杆菌和拟杆菌是最著名的GABA产生菌,尤其是脆弱拟杆菌(b.fragilis)。人们还描述了一种新的“吃GABA”物种,瘤胃球菌科中的Evtepia gabavorous。E.gabavorous对GABA的依赖性很明显,因为菌株只有在产生GABA的情况下才能生长。
▸ 一些微生物可以改变GABA受体的功能
已经描述了三类γ-氨基丁酸受体(GABAR),即GABAR A、GABAR B和GABAR C。GABAR B将从激素、神经递质和信息素接收到的信号转移到信号转移途径。
已知少数微生物可以改变GABAR的功能。鼠李糖乳杆菌JB-1改变大脑中GABAR的表达,从而减少焦虑和抑郁。因此,很可能某些乳酸杆菌在焦虑和抑郁的调节中起着关键作用。乳酸杆菌治疗可提高海马和前额叶皮层的GABA水平。结肠中微生物群产生的乙酸盐通过血脑屏障转移到下丘脑,并进入GABA神经胶质细胞循环途径。
▸ GABA含量过高的危害
神经系统抑制过度:GABA作为一种抑制性神经递质,过高的GABA水平可能导致神经系统抑制过度,影响神经传导和神经元活动,引发头晕、嗜睡和思维迟钝等症状。
肌无力、运动障碍:GABA可以影响肌肉的收缩和松弛,过高的GABA含量可能导致肌肉过度松弛,引起肌无力和运动障碍。
心律失常、血压下降:GABA的过高水平可能导致心血管系统的抑制,影响心脏的收缩力和心率,引起心律失常和血压下降。
情绪低落:神经系统受到GABA调节,过高的GABA含量可能导致情绪低落、注意力不集中和记忆力减退等情绪和认知问题。
呼吸困难:GABA过高可能影响呼吸中枢的功能,导致呼吸抑制,引起呼吸困难和缺氧症状。
▸GABA含量过低的危害
神经系统问题:GABA是一种重要的神经递质,含量过低可能导致神经传导异常,引发焦虑、抑郁和神经紊乱等问题。
睡眠障碍:GABA参与调节睡眠过程,GABA含量过低大脑容易兴奋,从而可能导致失眠、睡眠质量下降和睡眠障碍。
情绪不稳定:GABA也是一种帮助平静和放松的神经递质,是身体自产的一种有效的抗应激化学物质。GABA不足可能影响情绪调节功能,导致情绪波动大、易怒和情绪不稳定。
肌肉紧张:GABA参与肌肉松弛,含量过低可能导致肌肉紧张、痉挛和纤维肌痛。
▸ 调整GABA水平的方法
饮食:有些食物成分可以增加GABA水平,比如:燕麦、茶叶、核桃、香蕉、杏仁、菠菜和鱼类。还有矿物质镁,和维生素B6也可能增加GABA水平。
运动:瑜伽可以提高GABA水平,还有其他一些运动方式,也可以适当提高GABA水平。冥想的人会增加 GABA 水平,并降低皮质醇和去甲肾上腺素水平。
药物:调整体内GABA水平的药物和途径包括苯二氮䓬类药物(如苯巴比妥)和催眠药物(如扎来普隐)。此外,通过调整神经元GABA受体的活性和GABA转运体的功能也可以影响GABA水平。
草药类:
卡瓦对 GABA 的影响很复杂,因为该植物含有 6 种精神活性化合物。卡瓦主要的精神活性化合物之一是卡瓦因,在人类研究中,卡瓦改善了焦虑、失眠、抑郁、睡眠质量、认知、紧张和不安的症状
注:卡瓦与许多细胞色素酶有复杂的相互作用,这可能会影响肝脏。
厚朴在中药中被广泛应用,具有多种功效,可在动物和试管研究中,厚朴显示出抗氧化性能。还可保护大脑、心脏、肝脏,并具有抗癌和抗炎特性。
缬草中的活性成分主要存在于其根中,戊酸似乎是最有效的活性成分,戊酸通过多个 GABAA 受体亚基正向调节 GABA ,可以促进放松、减轻压力和改善睡眠。
黄芩,含有生物活性黄酮类化合物,可作为有效的抗氧化剂,不仅具有抗焦虑和抗惊厥作用,还可以改善认知、神经元再生。
柠檬香蜂草,具有复杂的药理学特征,含有许多精神活性有机化学物质,从多酚到萜烯。其中迷迭香酸是其最有效的精神活性化合物。迷迭香酸通过间接抑制将 GABA 转化为 L-谷氨酸的酶来增加 GABA 水平。
黑籽油,其提取物可改善炎症、血压和焦虑。
南非醉茄提取物与其他 GABA 正变构调节剂结合显示出协同效应,并且当 GABA 含量较低时似乎会增加 GABA 活性。
薰衣草,安全可靠地改善了焦虑和睡眠质量。
茶氨酸,可以减少心理和生理压力反应,同时改善情绪和放松,可以轻微增加大脑中的单胺水平,例如血清素、多巴胺、甘氨酸、GABA(增加约 20%)。
芹菜素,存在于许多传统使用的草药中,包括洋甘菊、小白菊、芹菜、金光菊、西番莲等。芹菜素通过其对苯二氮卓受体的活性增强 GABA 传输。它具有抗癌和抗氧化特性,甚至可以减少 tau 蛋白和β淀粉样蛋白的沉积和积累,这可能会降低患阿尔茨海默病和神经炎症的风险。它还会抑制谷氨酸家族的 NMDA 受体。
绿茶,EGCG(表没食子儿茶素没食子酸酯)是一种绿茶化合物,通过正向调节苯二氮卓受体来增加 GABA活性。
牛磺酸,一种与心脏和大脑健康有关的氨基酸,存在于许多饮食来源中,可以与 GABAA 和 GABAB 受体结合,每天摄入量少于 3 克其补充剂,不会产生副作用。
GABA 拮抗剂或“负调节剂”可阻断 GABA 的作用。
以下是可能阻断 GABA 的物质列表:
谷氨酸(Glu)是大脑中最丰富的游离氨基酸,也是大脑主要的兴奋性神经递质。在记忆存储中发挥着关键作用,它还可以帮助我们说话、处理信息、思考、运动、学习新事物和集中注意力学习等。
注:谷氨酸也是γ-氨基丁酸(GABA)的前体,这二者之间的平衡对于我们大脑健康非常重要。
谷氨酸被归类为非必需氨基酸,这意味着它可以在体内以足够的数量合成。对各种动物肠道进行仔细平衡研究的结果,结果表明膳食谷氨酸几乎在肠道内定量代谢,主要是通过肠细胞。
谷氨酸可以以两种不同的方式合成:首先,它可以通过谷氨酸脱氢酶或多种转氨酶从α-酮戊二酸合成。其次,谷氨酸可以由其他氨基酸合成;氨基酸的“谷氨酸家族”包括谷氨酰胺、精氨酸、脯氨酸和组氨酸。
▸ 谷氨酸的作用
化学信使:谷氨酸将信息从一个神经细胞传递到另一个神经细胞。作为主要的兴奋性神经递质,它向大脑和全身发送信号。它有助于认知功能、记忆、学习和其他大脑功能 。
脑细胞的能量来源:当细胞的主要能量来源葡萄糖储备低时,可以使用谷氨酸。
学习和记忆的调节:谷氨酸有助于随着时间的推移增强或减弱神经元之间的信号,以塑造学习和记忆。
疼痛传递器:较高水平的谷氨酸与增加的疼痛感有关。
影响免疫:谷氨酸受体存在于免疫细胞(T细胞、B细胞、巨噬细胞和树突状细胞)上,这表明谷氨酸在先天免疫系统和适应性免疫系统中均发挥作用。
保护肠道:谷氨酸是肠细胞的主要营养素之一。谷氨酸还可以通过帮助产生抗氧化剂谷胱甘肽来保护肠壁。一项动物研究发现,补充 L-谷氨酸有助于改善仔猪的肠道完整性,这有利于营养物质的消化和吸收。
注:谷氨酸还可以预防由于幽门螺杆菌和长期使用阿司匹林等非甾体抗炎药引起的胃肠道损伤。
睡眠和清醒的介质:大鼠模型研究表明,当我们清醒或快速眼动(REM)睡眠期间,谷氨酸水平最高。丘脑是个例外,在非快速眼动睡眠期间谷氨酸水平最高。
在过去的30年中,越来越多的研究进展还揭示了谷氨酸及其受体在神经退行性疾病疾病(阿尔茨海默氏症、肌萎缩侧索硬化症、多发性硬化症、癫痫、帕金森等)以及肠道疾病如克罗恩病和溃疡性结肠炎的病因中起核心作用。
▸ 谷氨酸含量过高的危害
谷氨酸是大脑中必不可少的(也是主要的兴奋性)神经递质。然而,谷氨酸在某些情况下会变得有害——这一过程称为谷氨酸兴奋性毒性 (GE)
由于谷氨酸是神经元的兴奋剂,过多会导致神经元过度激活并死亡,从而破坏神经元。
神经系统疾病:谷氨酸作为兴奋性毒素的作用,与多种神经退行性疾病有关,例如多发性硬化症、 阿尔茨海默病和肌萎缩性侧索硬化症。谷氨酸失调也被认为是纤维肌痛和慢性疲劳综合征的原因之一。
心理健康障碍:谷氨酸过多(或过少)也与抑郁症和精神分裂症等心理健康障碍有关。大量研究发现,在患有重度抑郁症的人中经常发现高水平的谷氨酸或过度活跃的谷氨酸受体。
偏头痛:高浓度的谷氨酸盐和偏头痛之间也有密切的联系。一项研究发现,偏头痛患者的血浆谷氨酸水平显著升高。另一项研究得出结论,GABA能药物(那些改变 GABA 作用的药物)可能有助于治疗偏头痛。
糖尿病:有一些证据表明,随着时间的推移,高水平的谷氨酸会导致1型和2型糖尿病的发生。一项研究发现,谷氨酸水平对两种类型的糖尿病中β细胞的损失都有直接和间接的影响。
▸ 谷氨酸含量过低的危害
注意力不集中:如果谷氨酸太少,我们无法对进入大脑的刺激做出快速反应,无法很好地记住事物,难以集中注意力,学习会更加困难。
情绪障碍:谷氨酸是大脑里需求量比较大的一种氨基酸,主要是参与脑内蛋白质或者是脂肪酸等的合成和代谢,过低可能影响人的精神状态,也可能诱发神经衰弱。研究人员发现,阻止大鼠吸收谷氨酸会导致类似抑郁的效果,这可能反映了快感缺失。
▸ 降低谷氨酸水平的方法
在饮食中降低:最好限制或避免使用富含谷氨酸的食物包括:酱油、硬奶酪、腌肉、谷物(尤其是含有麸质的)、骨汤,快餐、方便面、沙拉酱等。
PPAR -γ激活剂:PPAR -γ激活剂可能是对抗GE(谷氨酸兴奋性毒性)的最佳方法之一。许多食物和草药具有降低谷氨酸兴奋性毒性的能力。例如:黄芪、绿茶、紫锥菊、棕榈油、大豆、厚朴、奶蓟草、甘草、牛至、百里香油、高丽参、姜黄素、黑籽油、槲皮素 。
补充维生素:维生素B6有助于减少谷氨酸过量,因为参与将谷氨酸转化为GABA。维生素B6缺乏可能是谷氨酸过量积累并且不能正确转化为 GABA 的一个原因。辅酶Q10-也可以改善谷氨酸兴奋性毒性、线粒体功能和氧化应激 。
▸ 提高谷氨酸水平的方法
运动:锻炼的参与者的谷氨酸或GABA水平增加。即使在停止运动后效果仍然存在,这表明谷氨酸水平会随着运动而发生更持久的变化。
饮食:天然高谷氨酸食物包括:发酵、陈化、腌制、压力烹制的食品。其中包括:陈年奶酪、慢煮肉类和家禽、蛋、酱油、大豆蛋白、鱼露,某些蔬菜,如蘑菇、成熟的西红柿、西兰花和豌豆、核桃、大麦麦芽。
补充剂:身体将谷氨酰胺转化为谷氨酸。谷氨酰胺可以作为补充剂使用,也可以在肉类、鱼类、鸡蛋、奶制品、小麦和一些蔬菜中找到。
扩展阅读:
作为耳熟能详的一种神经递质,你真的了解多巴胺的全部作用以及利与弊吗?下面由谷禾带你一起了解下。
多巴胺(DA)主要在黑质、腹侧被盖区和下丘脑中产生,并释放到大脑的伏隔核和前额皮质中。它通常被称为奖励神经递质,在认知、奖励、饱腹感、运动、愉悦和动机等重要功能中发挥着重要的外周和中枢作用,影响睡眠、情绪、注意力、工作记忆和学习等。
▸ 肠道微生物群能够影响多巴胺的代谢
肠道微生物群是肠道和中枢神经系统中多巴胺生物利用度的主要贡献者。一些肠道微生物已被证明对多巴胺能神经元发挥神经保护作用,以减少多巴胺损失。另一方面,其他微生物可以通过内毒素刺激炎症反应,进一步降低多巴胺浓度,从而产生负面影响。
帕金森病肠道中的有益微生物群往往会减少,而诱发病理过程的微生物水平则会升高。
左旋多巴是多巴胺的天然前体,外周给药时可穿过血脑屏障,增加大脑中多巴胺的水平。然而,肠道微生物代谢的左旋多巴会降低其利用率,而外周产生的多巴胺会导致不良副作用。
将来,肠道微生物群的筛查或肠道微生物群的绘图可能对于选择用于精神治疗的药物变得重要。随着测序、克隆、基因操作、病毒(包括噬菌体)靶向、成像技术的最新进展,这将成为可能。
▸ 多巴胺的作用
调节情绪、影响认知:多巴胺参与调节情绪和情感反应,特别是与愉悦和奖赏感有关。多巴胺水平的变化可以影响人的情绪状态,使人感到快乐、满足或兴奋。
多巴胺还可以影响认知功能,包括记忆、学习、决策和注意力等。它促进神经元之间的连接和信息传递,有助于提高认知能力。
影响躯体运动:多巴胺是锥体系统中的重要递质,与躯体运动功能有密切关系。多巴胺在大脑基底神经元中起着关键作用,参与调节运动控制和协调。多巴胺的不足会导致运动障碍,如帕金森病。
调节体内激素水平:多巴胺也参与调节内分泌系统的功能,影响激素的分泌和调节身体的代谢。它与垂体前叶的调节密切相关,影响生长激素、泌乳素等激素的分泌。多巴胺还通过负反馈机制调节腺垂体激素的合成和释放,维持体内激素水平的稳定。
调节心血管活动:多巴胺的作用可以导致心率的增加,这是由于多巴胺通过激活β1-肾上腺素能受体增加心脏的兴奋性和传导速度,从而加快心率。然而,在高剂量下,多巴胺也可以通过抑制交感神经系统来降低心率。
多巴胺还通过激活β2-肾上腺素能受体来引起血管舒张,特别是在冠状动脉和周围血管中。这种血管扩张的作用有助于降低外周阻力,减少心脏的负担。
影响胃肠道功能:多巴胺在胃肠道系统中也扮演着重要的角色,调节胃酸、胃蛋白酶、胰腺碱性物和酶的分泌,影响十二指肠溃疡的病理演变。当中枢多巴胺功能缺损时易出现溃疡症,如帕金森病患者常患有溃疡症。而多巴胺功能亢进的精神分裂症患者很少有溃疡症。
多巴胺还可以影响胃肠道的消化和吸收功能。它可以调节肠道的血流和肠道蠕动,促进营养物质的吸收和利用。
与成瘾性相关:多巴胺与大脑中的奖赏系统密切相关。当个体接触到有奖赏性的刺激时,多巴胺会被释放,产生愉悦感和满足感。这种奖赏性体验会强化行为,促使个体不断追求这种奖赏。脑内奖赏效应可能是产生精神依赖性和强迫性觅药行为的主要原因。
▸ 多巴胺含量过高的危害
多巴胺过高可能会导致一系列健康问题和危害,包括但不限于:
情绪不稳定:多巴胺有兴奋的作用,含量过高会使得患者脾气暴躁,情绪波动过大,容易生气,对外界也过于敏感。可能导致焦虑、紧张和不安情绪,影响个体的心理健康。
血压、心律失常:多巴胺过多使得神经过度兴奋,出现血压增高,同时伴有头晕、头痛、阵发性颜面潮红以及恶心、呕吐等高血压的表现。还引起患者心率增快,心率增快可引起窦性心动过速,甚至引起心律失常的情况发生。
睡眠问题:多巴胺过高可能干扰睡眠,导致失眠或睡眠质量下降。使睡眠不深、易醒、睡眠中断等现象更为频繁,以及睡眠中的惊醒、噩梦等情况。
可能引起一些精神疾病:多巴胺过高与精神疾病之间存在密切的关系,特别是在以下几种精神疾病中:精神分裂症、躁郁症、药物成瘾、帕金森病。总的来说,多巴胺过高与多种精神疾病之间存在复杂的相互作用关系,多巴胺系统的异常可能是某些精神疾病发病机制的重要因素之一。
▸ 多巴胺含量过低的危害
抑郁和情绪低落:多巴胺是调节情绪的神经递质之一,多巴胺不足会影响大脑中与情绪调节相关的区域,导致情绪不稳定、抑郁和情绪低落等问题。
帕金森病:缺乏多巴胺会导致帕金森病,患者可出现静止性震颤、肌肉强直、运动迟缓,以及尿频、便秘、体位性低血压、不安腿综合征等症状,多巴胺严重缺乏时患者可出现全身肌肉僵硬、生活不能自理等。
精神疾病风险增加:多巴胺与精神疾病如精神分裂症等有关,多巴胺含量过低可能增加患上精神疾病的风险。
▸ 提高多巴胺水平的方法
饮食:在饮食方面有一些食物可以促进多巴胺的分泌,应该多吃富含酪氨酸的食物来促进多巴胺的分泌,建议患者多吃香蕉、橘子,以及巧克力等等这样的食物来促进多巴胺分泌。
体育锻炼:想要促进多巴胺的分泌,也可以通过参加体育锻炼来达到这样的目的。因为人在体育锻炼的时候血压升高、心率增快,这种情况会促进多巴胺分泌。
保持心情愉悦:观看有趣的事物、听音乐会提高身体的快感和愉悦感,可以刺激多巴胺的释放。
增加多巴胺的药物:增加多巴胺的药主要左旋多巴、普拉克索,另外还要配合抗胆碱药物金刚烷胺等药治疗。
多晒太阳:当皮肤暴露于阳光下时,身体会产生维生素D,同时也会促进多巴胺的释放。
▸ 降低多巴胺水平的方法
服用药物:多巴胺是一种神经递质,当多巴胺分泌过多时,会导致精神兴奋。患者可以在医生的指导下服用抗精神病药物进行治疗,如利培酮片、奥氮平片等,可以有效改善症状。
调整饮食结构:食用含色氨酸的食物可增加多巴胺分泌,减少摄入可降低多巴胺分泌。
心理调整:如果精神过于紧张或兴奋,多巴胺分泌会增多,建议及时调整心态,通过心理治疗、暗示治疗等方式来缓解情绪,从而能使多巴胺迅速下降。
组胺是人体内的一种生物胺,最为熟知的作用是作为过敏反应的介质,但也是神经系统、肠道、皮肤和免疫系统中重要的信号分子。
组胺还是肠道稳态的重要调节剂。通过增强分泌和蠕动,组胺促进潜在有毒物质的快速清除。这种生物胺对于肠道细菌的生存也至关重要。与健康个体相比,组胺不耐受患者的肠道菌群失衡或失调。
组胺主要由肥大细胞和嗜碱性粒细胞等免疫细胞产生和释放。一些细胞如树突状细胞或T细胞可以表达组氨酸脱羧酶,这是一种在刺激后合成组胺的酶。
尽管如此,一些食物中的微生物群和部分人体肠道微生物群也可以分泌组胺。
产生组胺的细菌包括乳杆菌属、乳酸乳球菌(Lactococcus lactis)、酒类酒球菌(Oenococcus oeni)、小片球菌、嗜热链球菌、摩根氏菌、肺炎克雷伯菌、肠杆菌属、弗氏柠檬酸杆菌和哈夫尼菌属(Hafnia alvei)。
▸ 组胺的作用
信号传导:在中枢神经系统中,组胺作为一种神经递质,参与睡眠调节和体温调节等生理过程。组胺对感觉神经末梢有强烈的刺激作用,尤其对调节痛和痒的神经,该效应由H1受体所调节。
除此之外,有研究发现组胺还会影响伤口愈合、食欲和情绪等方面。
介导过敏反应:当免疫系统对过敏原产生过度反应时,免疫细胞(如肥大细胞和嗜酸性粒细胞)会释放存储在细胞内的组胺。释放的组胺会结合到特定的受体上,引发一系列生理反应,例如瘙痒、肿胀、打喷嚏等。
扩张血管,影响血压:组胺对人心血管系统最突出的作用是扩张小血管。血管扩张使外周阻力降低,血压下降,并伴有潮红、头痛等症状。
组胺还增加毛细血管的通透性,使渗出增加,引起水肿,严重时甚至导致循环血量减少,可能引起休克。组胺对心脏的直接作用包括增强心肌收缩力、加快心率和减慢房室传导。
刺激胃酸分泌:首先,组胺可以刺激胃黏膜细胞中的H2受体,当组胺与H2受体结合时,会激活细胞内的信号转导通路,导致胃壁上的壁细胞释放胃酸。
其次,组胺还可以通过刺激嗜酸性细胞(胃窦细胞)来促进胃酸的分泌。嗜酸性细胞是胃黏膜中的一种细胞类型,它们包含大量的组胺。当胃黏膜受到刺激时,嗜酸性细胞会释放存储的组胺。释放的组胺通过与H2受体结合,刺激壁细胞分泌胃酸。
影响排便:一项研究中,发现细菌产生的组胺与小鼠结肠运动和粪便排出量增加有关,并且组胺受体拮抗剂治疗在很大程度上阻断了细菌组胺对结肠运动的影响。
收缩平滑肌:此外,组胺会诱导平滑肌细胞(包括支气管和肠道)收缩,哮喘患者对组胺比正常人敏感100~1000倍,组胺可引起支气管痉挛导致呼吸困难。组胺收缩胃肠平滑肌和子宫平滑肌还会引起痉挛性腹痛。
▸ 组胺含量过高的危害
组胺中毒:在健康人体内,会因摄入组胺含量高的食物(例如鲭鱼)导致血液中组胺浓度升高而出现严重症状——组胺中毒。
组胺中毒症状多种多样,可能包括口腔麻木、头痛、头晕、心悸、低血压、吞咽困难、脉搏微弱、荨麻疹、面部肿胀、潮红、呕吐、恶心和腹泻等。
组胺中毒的症状可能持续数小时或一天,但在极少数情况下,症状可能会持续数天。
过敏反应:组胺是一种重要的组织胺,过高的组胺浓度可能引发过敏反应,包括皮肤瘙痒、荨麻疹、呼吸困难等症状。
胃肠道反应:组胺过高可能引起胃肠道症状,如胃灼热、胃痛、腹泻和恶心和消化不良等问题。
肠道肥大细胞过度增生和过度活跃,使组胺浓度较高,还会导致粘膜炎症性疾病,产生腹泻和腹痛。
皮肤和呼吸道症状:组胺过高可能导致皮肤血管扩张和炎症反应,引发红肿、瘙痒和刺痛等皮肤问题。
除此之外,还会引起呼吸道症状,如喉咙发痒、喉咙肿胀、咳嗽和哮喘等呼吸系统问题。
▸ 降低谷氨酸水平的方法
低组胺饮食:组胺过高的基础是基于低组胺含量食物的消除饮食。一般来说,公认的饮食指南尚未制定;但是,建议避免食用富含组胺的食物如奶酪、油性鱼类和贝类,以及生发酵肉制品、腌菜、发酵豆制品、葡萄酒和啤酒、鸡蛋、巧克力和蘑菇。
此外,应避免食用会刺激内源性组胺释放的蔬菜和水果(如菠菜、西红柿、柑橘类水果、草莓、茄子、鳄梨、木瓜、香蕉、猕猴桃、菠萝和李子)。
施用抗组胺药物:纠正组胺不耐受的药物方案基于使用组胺受体阻滞剂、肥大细胞膜稳定剂和其他具有抗组胺活性的药物。在这方面,H1R拮抗剂是最有效的,特别是依巴斯汀。每天服用20毫克该药物,持续12周,46%的患者出现临床缓解。
补充生物活性物质:维生素C被用作纠正组胺不耐受的佐剂。每日剂量300-500毫克可增强组胺降解并抑制肥大细胞脱颗粒。
天然类黄酮(非瑟酮、山奈酚、槲皮素、芦丁和木犀草素)和活性生物碱小檗碱在体外抑制肥大细胞脱颗粒。这些都有助于减轻组胺不耐受。
▸ 组胺含量过低的危害
虽然组胺含量过低的情况相对较少见,但也可能会对身体产生一些影响,包括:
伤口愈合缓慢:组胺在人体中起着重要的调节作用,其能够帮助调节纤维细胞生长因子的生成,该成分可以加速局部肉芽的生长,帮助促进伤口的愈合。因此组胺含量较低时,伤口愈合能力也会减弱,速度会随之减慢。
消化不良:组胺可以通过刺激胃部,进而起到促进胃酸分泌的效果。若身体中没有组胺,则会导致胃酸减少,无法有效消化分解食物,进而引起消化不良的问题。
情绪问题:组胺还可以作为神经递质帮助调节中枢神经系统,而一旦没有组胺或缺少组胺,则会影响中枢神经系统稳定性,引起睡眠异常、激素水平紊乱等情况,进而导致情绪不良、抑郁和焦虑等心理问题。
血管扩张问题:组胺在血管平滑肌收缩和扩张中起到调节作用。组胺含量过低可能导致血管扩张不足,影响血液循环和血压调节。
免疫力下降:组胺对免疫细胞,如吞噬细胞、T细胞、B细胞等,起到增强活性的功效,因此组胺还具有增强免疫功能的作用。若人体缺少该物质,则人体免疫力会下降,无法有效抵抗细菌、真菌等有害物质的侵入。
扩展阅读:

一氧化氮(NO)是一种无色气体,是一种半衰期很短(平均5s后即失活)的神经递质。在人体内扮演着重要的生物学角色,一氧化氮具有以下作用:
▸ 一氧化氮的作用
神经信号传递:一氧化氮与传统的神经递质不同,它不是在突触前膜释放后通过突触间隙传递信号,而是可以直接穿透细胞膜,影响邻近的细胞。这种特性使得NO可以快速地在神经元之间传递信号,参与短期和长期的神经调节过程。
记忆和学习:一氧化氮在大脑的学习和记忆形成过程中发挥关键作用。研究表明,NO参与调节长时程增强(LTP)的过程,这是一种与学习和记忆形成密切相关的神经突触强化机制。
血管扩张:虽然这不是直接作为神经递质的功能,但一氧化氮在调节血管舒张中的作用也影响到大脑的功能。NO可以促进血管扩张,从而增加血流量,改善大脑的血液供应。这对于维持大脑健康和功能至关重要。
神经保护作用:一氧化氮在一定条件下可以发挥神经保护作用,帮助减轻神经损伤和促进神经修复。然而,NO的过量产生也可能导致神经毒性,因此其在神经保护中的作用是把双刃剑。
疼痛调节:一氧化氮在调节疼痛感知中也起着作用。它参与了疼痛信号的传递过程,可能通过调节疼痛相关神经递质的释放来影响疼痛感知。
提高运动表现:一氧化氮通过增强流向肌肉的血液、增加氧气和营养物质的输送以及减少运动过程中代谢废物的积累来提高运动表现。这可以提高耐力、力量和恢复时间。
▸ 一氧化氮含量过高的危害
一氧化氮(NO)作为一种神经递质,在适量情况下对人体具有重要的调节作用。然而,一氧化氮含量过高可能会对人体产生一些不良影响。
神经毒性:过高的一氧化氮含量可能对神经系统产生毒性作用,损害神经元的结构和功能,导致神经元凋亡和神经退行性疾病的发生。
过高的一氧化氮含量还可能干扰神经元之间的正常传导,影响神经信号的传递和神经网络的功能,导致神经系统失调和功能障碍。
氧化应激:过高的一氧化氮含量可能导致氧化应激反应的增加,引发细胞损伤和炎症反应,加速细胞老化和疾病的发展。
血管扩张过度:一氧化氮是一种强效的血管舒张因子,过高的一氧化氮含量可能导致血管扩张过度,造成血压下降和循环血容量不足,甚至引发休克。
免疫抑制:过高的一氧化氮含量可能抑制免疫系统的正常功能,降低机体对抗病原体的能力,增加感染和疾病的风险。
▸ 降低一氧化氮水平的方法
一氧化氮测定值过高,需要根据引起的原因进行处理,多考虑是慢性支气管炎引起的,但也不排除是支气管哮喘、阻塞性睡眠呼吸暂停低通气综合征等疾病导致的。
慢性支气管炎:多考虑是细菌感染引起的,但也不排除是长期吸烟或吸入有害的物质导致的,进而会导致气管、支气管黏膜等组织出现慢性非特异性炎症的情况,在临床通常会出现气促等症状。建议患者在医生的指导下服用盐酸溴己新片、硫酸沙丁胺醇片等药物治疗。
支气管哮喘:多考虑是遗传因素引起的,但也不排除是环境因素导致的,进而会出现气道慢性炎症的情况,在临床通常会出现呼吸急促等症状。建议患者在医生的指导下使用硫酸特布他林气雾剂、布地奈德气雾剂等药物治疗,必要时通过支气管热成形手术等方式缓解。
改善生活方式:降低体内一氧化氮水平的措施和药物包括改变饮食习惯、减少摄入高脂肪食物、增加运动量、避免暴饮暴食等。药物方面可以使用一氧化氮合成酶抑制剂或其他降低一氧化氮水平的药物。
▸ 一氧化氮含量过低的危害
神经传导障碍:一氧化氮作为神经递质在神经元之间传递信号,调节神经传导。一氧化氮含量过低可能导致神经传导障碍,影响神经网络的功能和神经元的正常活动。
情绪和认知问题:一氧化氮参与调节情绪和认知功能,影响大脑的神经传导。一氧化氮含量过低可能导致情绪波动、注意力不集中和认知功能下降。
勃起功能障碍: 有研究表明,NO是阴茎神经元(自主神经支配海绵体并穿透腺海绵体组织)和阴茎血管外膜层神经网络中勃起功能的生理促进剂。而一氧化氮含量过低可能会引起男性性功能障碍,使阴茎无法勃起。
炎症反应增加:一氧化氮在炎症过程中发挥重要作用,可以调节炎症反应和免疫反应。一氧化氮含量过低可能导致炎症反应增加,影响炎症的调节和细胞修复过程。
▸ 提高一氧化氮水平的方法
补充L-精氨酸或者L-胍氨酸:补充NO的途径第一种办法,最直接的方法是增加NO合酶原料L-精氨酸或者L-胍氨酸。大部分蛋白质都含有这两种氨基酸,比如,鱼类、瘦肉、牛羊肉、鸡鸭、蛋类、鱼虾、豆制品、坚果类、巧克力、芝麻、核桃、乳制品等。

适当运动:运动可以调节机体血管内一氧化氮合成酶,使其合成酶含量增加,可以较多地产生一氧化氮,并且运动时由于血液循环加速,也可使其辅助产生一氧化氮,达到较好的补充作用。
补充硝酸盐和亚硝酸盐:亚硝酸盐还原酶在生理条件下发挥功能,催化硝酸盐和亚硝酸盐生成NO增加。补充硝酸盐和亚硝酸盐最容易的是食用水果和蔬菜,其中含有大量硝酸盐和亚硝酸盐,在体内就可以转化为NO。而且我们平常吃的新鲜蔬菜和水果都含有大量天然抗氧化剂,可以防止补充硝酸盐和亚硝酸盐产生亚硝胺。例如茶叶和巧克力中的多酚类,葡萄里的白藜芦醇和原花青素,胡萝卜里的胡萝卜素,番茄里的番茄红素,核桃油和胡麻油中Ω3等。
除了神经递质,肠道菌群代谢物在人体健康中也扮演着重要角色。肠道菌群代谢物是由肠道微生物产生的化合物,可以影响人体的免疫系统、新陈代谢和神经系统等。

研究表明,肠道菌群代谢物与多种疾病的发展密切相关,包括肥胖、糖尿病和炎症性肠病。因此,了解和维护良好的肠道菌群代谢物平衡对于维持人体健康至关重要。
短链脂肪酸(SCFAs)是一类由1~6个碳原子组成的有机脂肪酸,主要包括乙酸、丙酸和丁酸,结肠是其主要产生部位,多由未消化吸收的碳水化合物经结肠内厌氧菌酵解产生。
在结肠中存在的总短链脂肪酸中,健康人体内的90%-95%是乙酸盐、丙酸盐和丁酸盐。
短链脂肪酸主要由双歧杆菌(Bifidobacterium)、乳杆菌(Lactobacillus)、毛螺菌科(Lachnospiraceae)、经黏液真杆菌属(Blautia)、粪球菌属(Coprococcus)、罗氏菌属(Roseburia)和粪杆菌属(Faecalibacterium)在结肠中产生,并为结肠上皮细胞提供能量。
这些短链脂肪酸粘附于游离脂肪酸受体(FFAR),例如位于肠上皮细胞表面的GPR43(FFAR2)和GPR41(FFAR3)。
• 降低肠道pH,减少有害菌生长
短链脂肪酸的存在会使回肠(小肠末端)到盲肠(大肠起点)的肠道pH值降低,从而防止有害细菌(如肠杆菌科和梭状芽胞杆菌)过度生长。
• 防止肠漏,保护肠道健康
短链脂肪酸有助于修复“肠漏”,通过增加粘蛋白2(MUC-2)的分泌来加强肠壁,丁酸盐通过上调紧密连接蛋白claudin-1来保护肠道屏障功能从而防止脂多糖穿过屏障。
患有炎症性肠病的个体粪便短链脂肪酸水平较低,伴随着厚壁菌门和拟杆菌门的减少。
• 为结肠细胞提供能量
丁酸盐是结肠细胞的主要能量来源,结肠细胞是构成肠道内壁的细胞。与身体中使用糖(葡萄糖)作为主要能量来源的大多数其他细胞不同,肠道内壁细胞(结肠细胞)主要使用丁酸盐。如果没有丁酸盐,这些细胞就无法正确执行其功能。
• 抗炎、抗癌特性
丁酸盐也是一种组蛋白脱乙酰酶抑制剂(HDAC抑制剂),通过诱导细胞凋亡(细胞自然死亡)来帮助预防结肠癌及癌症并发症,并在上皮细胞的氧消耗中发挥重要作用,氧气的平衡状态可以防止生态失调。
丁酸盐的抗炎特性,部分原因是其抑制核转录因子(NF-κB)的激活,通过下调NF-κB信号通路,丁酸盐可以调节促炎细胞因子的产生。
• 影响宿主食欲,调节体重
乙酸盐通过刺激生长素释放肽的分泌来降低食欲。与此相一致的是,丙酸盐喂养会诱导脑干、下丘脑和脊髓的背侧迷走神经复合体中FOS(fos原癌基因,AP-1 转录因子亚基)的表达,这引发了一个问题,即短链脂肪酸诱导的外周感觉神经元活动的刺激是否可以介导对宿主饮食行为的影响。
• 短链脂肪酸的其他生理功能
短链脂肪酸调节体内的其他几种生理功能,例如中枢神经系统中小胶质细胞的成熟和功能,血清素、GABA和多巴胺产生的信号向神经元的传输,以及结肠中阴离子的分泌。后者是由于刺激结肠中的烟碱类Ach受体,导致Ach产生增加,并刺激杯状细胞分泌更多粘液。
在免疫细胞中,短链脂肪酸调节T细胞的分化。在肠内分泌细胞中,短链脂肪酸刺激肠道激素的释放。胆汁盐与短链脂肪酸结合,在肠肝循环中发挥着不可或缺的作用,在神经元通路和中枢神经系统信号传导的调节中同样重要。
肠道微生物群产生的短链脂肪酸通过血管转运至大脑,调节神经元、小胶质细胞和星形胶质细胞的功能,并影响血脑屏障。
微生物产生的短链脂肪酸在微生物群-肠-脑轴通讯、保护肠道屏障和炎症反应中发挥着关键作用。特别需要注意的是,过量的短链脂肪酸和缺乏短链脂肪酸对人体健康都是不利的。例如丁酸并不总是越多越好,低浓度丁酸促进细胞增殖和生长,高浓度丁酸反而抑制细胞增殖和生长,增加肠道的通透性。

▸ 调整短链脂肪酸水平的方法
补充直接含有短链脂肪酸的食物:主要来源是乳制品,黄油等,其中含有丁酸盐。例如,黄油大约含有3%至4%的丁酸。这听起来可能不多,但它比大多数其他食物都多。
通过菌群调节增加短链脂肪酸的食物:吃大量富含纤维和抗性淀粉类的食物,例如水果、蔬菜和豆类,与短链脂肪酸的增加有关。
以下类型的食物最适合在结肠中产生短链脂肪酸:菊粉、低聚果糖、抗性淀粉、果胶、阿拉伯木聚糖、阿拉伯半乳聚糖。
扩展阅读:
脂多糖是革兰氏阴性细菌细胞壁外壁的组成成分,是由脂质和多糖构成的物质(糖脂质)。
脂多糖是一种内毒素(Endotoxin),当其作用于人类或动物等其他生物细胞时,就会表现出多种的生物活性。脂多糖的生理作用主要是通过存在于宿主细胞的细胞膜表面的Toll样受体(TLR4)而体现的。
▸ 脂多糖含量过高的危害
然而,高浓度的脂多糖在人体内可能会引发一系列潜在危害和不良影响。
引发炎症:在血液中,脂多糖与单核细胞、树突细胞、巨噬细胞和B细胞(这些都是白细胞)结合,并引导它们产生转录因子NF-κB和AP-1。然后,这些转录因子,刺激炎症细胞因子TNF-a、IL-1b、IL-6的产生。
脂多糖还可以增加一氧化氮,超氧化物(一种自由基)和类二十烷酸(增加炎症的脂肪分解产物,如PGE2)的产生。
内毒素作用:脂多糖中的脂蛋白部分即内毒素,具有毒性作用,如果血液中的脂多糖水平过高,还会引发脓毒血症,这是一种致命的毒素反应,可造成发热、组织功能损伤、器官衰竭甚至死亡。
因此,要注意控制脂多糖含量,避免过高的脂多糖摄入,保持身体的免疫平衡和健康状态,有助于预防上述危害的发生。及时监测和调节脂多糖水平,是维护身体健康的重要措施。
▸ 降低脂多糖水平的方法
首先,低密度脂蛋白胆固醇LDL可以和他结合,通过新的表位来降低脂多糖。
其次,研究显示,在小鼠中,益生菌双歧杆菌,可以通过改善肠道屏障功能,来降低LPS水平。即补充益生元和益生菌,有助于矫正肠道菌群失衡。最常用的益生菌,乳酸杆菌属和双歧杆菌属,是革兰氏阳性菌,因此不含LPS。
最后,许多植物营养素,如槲皮素和小檗碱,都通过作用于肠壁的紧密连接,来抑制肠道对内毒素的吸收。乙酰胆碱刺激迷走神经,可降低巨噬细胞中炎症细胞因子(TNF-a、IL-6等)的释放。
除此之外,Omega-3脂肪酸和乳铁蛋白,也有助于降低LPS的产生,适当的运动也是有益的。
在肠道中,结合的初级胆汁酸受微生物群作用并转化为次级胆汁酸,从而进一步增加胆汁酸库的多样性和整体疏水性。
主要通过胆汁酸水解酶进行的微生物去结合是肠道环境中微生物进一步修饰胆汁酸的关键一步。
胆汁酸水解酶编码基因已在各种肠道微生物中检测到并表征,包括双歧杆菌(Bifidobacterium)、乳杆菌(Lactobacillus)、肠球菌(Enterococcus)、梭菌(Clostridium)、拟杆菌(Bacteroides)等。
▸ 次级胆汁酸的作用
影响脂肪、胆固醇的消化吸收:次级胆汁酸在肠道中有助于脂肪的消化和吸收。它们可以促进脂肪乳化和吸收,帮助机体获取必要的营养。
次级胆汁酸还在胆固醇代谢中起着重要作用。它们参与胆固醇的代谢和排泄,有助于维持胆固醇的平衡。
影响肠道菌群的结构、多样性:胆汁酸是微生物群丰度、多样性和代谢活性的重要决定因素。在人体中,牛磺-β-鼠胆酸和牛磺酸胆酸对多种微生物的发展至关重要。
研究发现小鼠肠道微生物群落过度增殖和细菌易位,通过使用口服胆汁酸,以诱导法尼醇X受体激活,从而抑制细菌过度生长。
肠道微生物群和胆汁酸之间存在双向相互作用。肠道微生物群可以调节胆汁酸的合成和代谢,相反,胆汁酸可以改变肠道菌群的组成。
调节肝胆功能:次级胆汁酸可以影响胆囊的收缩和胆汁的排放,调节胆囊功能,维持胆汁的正常分泌和排泄。
次级胆汁酸还有助于肝脏代谢废物及药物,还可以刺激肝细胞的再生,有利于肝脏功能的恢复。
影响肠道屏障功能、调节免疫:微生物群和胆汁酸之间的相互作用会影响肠道屏障功能的维持,调节先天免疫和适应性免疫,并调节定植抵抗力。
胆汁酸也限制炎症小体的激活。FXR和SHP通过与NLRP3炎症小体和胱天蛋白酶-1的物理相互作用来抑制炎症小体的组装,而TGR5环磷酸腺苷(cAMP)途径的激活通过诱导其泛素化来阻断NLRP3炎性小体的激活,这最终限制了白细胞介素-1β和白细胞介素-18的产生。
▸ 次级胆汁酸含量过高的危害
胆汁反流:次级胆汁酸过高可能导致胆汁反流,即胆汁逆流到胃或食管中,引起胃灼热、食管炎等消化道问题。
胆囊结石、肝脏损伤:过高的次级胆汁酸水平可能导致胆囊内胆固醇结晶形成,增加胆囊结石的风险,引起胆囊疾病和疼痛。
过量的次级胆汁酸可能对肝脏产生负担,导致肝脏功能异常,容易形成肝硬化,还可能会导致肝炎的出现。
消化问题:高水平的次级胆汁酸可能干扰消化系统的正常功能,导致消化不良、腹泻等问题。
免疫系统异常:异常的次级胆汁酸水平可能影响免疫系统的平衡,导致免疫功能异常,增加感染和疾病的风险。
▸ 降低次级胆汁酸水平的方法
饮食调整:胆汁酸高的患者在饮食上应注意清淡,减少摄入高胆固醇、高脂肪食物和辛辣的食物,以减少胆汁酸的产生。增加膳食纤维摄入,有助于降低次级胆汁酸的含量。
药物治疗:医生可能会考虑使用胆汁酸螯合剂来帮助降低体内次级胆汁酸的含量。这些药物可以帮助排出多余的胆汁酸,从而减少其在体内的积累。
控制体重:肥胖会增加肝脏负担,导致脂肪肝等肝病,进而影响胆汁酸的代谢。通过合理饮食和适度运动,保持健康的体重,一定程度上可以达到降低总胆汁酸的效果。
治疗原发病:某些肝脏疾病,如肝炎、肝硬化等,可能会导致总胆汁酸升高。建议在医生指导下积极治疗原发病,如服用复方甘草酸苷片、消炎利胆片等药物,可以降低总胆汁酸。
▸ 次级胆汁酸含量过低的危害
消化问题、营养不良:次级胆汁酸的不足可能导致脂肪的消化和吸收受阻,影响脂肪和脂溶性维生素的吸收,可能导致营养不良。
增加脂肪肝风险:次级胆汁酸不足可能影响胆固醇的代谢和排泄,导致胆固醇积聚在体内,增加动脉粥样硬化等心血管疾病的风险。
次级胆汁酸不足还会增加脂肪肝的风险,影响肝脏功能和健康。
胆汁淤积:次级胆汁酸含量过少时,可能影响胆汁的流动性和排泄功能,导致胆汁在胆道中积聚和凝结,从而增加胆汁淤积的风险。
此外,次级胆汁酸的不足也可能影响胆汁的化学成分和性质,使其更容易形成胆固醇结晶或胆结石,进一步加剧胆汁淤积的情况。
▸ 提高次级胆汁酸水平的方法
饮食调整:增加摄入富含胆汁酸的食物,如动物肝脏、蛋黄、牛奶和奶制品等。此外,适量摄入脂肪和胆固醇也有助于促进胆汁酸的合成。
药物治疗:医生可能会考虑使用胆汁酸补充剂来增加体内次级胆汁酸的含量。包括亮菌甲素(胆汁分泌促进剂)、去氢胆酸、抑氨酚、利胆醇(苯丙醇)、鹅去氧胆酸、胆宁等等。这些补充剂可以帮助增加胆汁酸的合成和释放,从而提高其含量。
营养补充:一些营养素如维生素B12和叶酸被认为对胆汁酸的合成有益,可以通过补充来帮助提高次级胆汁酸的含量。
适当运动:适量的体育锻炼有助于促进胆汁分泌。有氧运动,如快走、跑步、跳舞,能够提高胆囊收缩力和肠蠕动,促进胆汁分泌与排泄。
扩展阅读:
对甲酚(p-Cresol)是人体肠道菌群的代谢产物之一,可由肠道中的一些厌氧菌代谢食物中的特定化合物如酪氨酸产生。因分子量极小极易通过肠道屏障和血脑屏障。
目前人类肠道菌群中至少有55种细菌可以产生“对甲酚”,包括双歧杆菌科、肠杆菌科、Coriobacteriae、拟杆菌科、梭杆菌科、乳杆菌科和梭状芽孢杆菌科等。
▸ 对甲酚含量过高的危害
虽然对甲酚是人体肠道菌群的代谢产物,但过多的对甲酚在肠道内积聚可能对人体健康产生不利影响。
可能导致孤独症:目前已在孤独症患者的血、尿、粪便样本中发现对甲酚和对乙酚水平明显异常升高,并发现孤独症患者的重复刻板行为、交流与认知障碍症状的加重与尿液中对甲酚升高密切相关。
器官损伤:对甲酚在一定浓度下可能对肠道黏膜有刺激作用,影响肠道的正常功能。此外,高浓度的对甲酚也可能对肾脏和其他器官产生毒性影响。
神经损伤:对甲酚极易穿过血脑屏障,过量的对甲酚可能对中枢神经系统产生影响,引起头晕、头痛、恶心、呕吐等神经系统症状。长期暴露还可能导致神经系统损伤和功能障碍。
其他问题:过量的甲酚还会导致便秘,以及可能对呼吸系统、循环系统、免疫系统等产生影响,引起呼吸困难、心血管问题、免疫功能异常等。
一些研究表明,高浓度的甲酚还可能对人体具有致癌作用,增加患结直肠癌的风险。
▸ 降低对甲酚水平的方法
增加膳食纤维摄入有助于促进肠道蠕动,减少有害代谢产物的积累,摄入益生菌和益生元可以减少有害菌的生长,降低对甲酚的产生。适量摄入蛋白质,避免过度摄入。此外过度加热食物可能会破坏其中营养成分增加有害代谢物产生。
内源性吲哚及其衍生物是来源于肠道菌群的色氨酸代谢物,具有一系列生物活性。
吲哚衍生物可以影响胃肠道的蠕动,会影响便秘或腹泻等状况;吲哚及其衍生物已被证明可以加强肠道屏障功能,有助于防止病原体和有害物质进入血液。
最近的研究表明,吲哚主要通过激活AhR和PXR受体来发挥抗炎活性,从而影响免疫系统的功能,显著改善肠道健康(炎症性肠病、出血性结肠炎、癌症结直肠癌),并进一步促进人类健康(糖尿病、中枢系统炎症和血管调节)。
吲哚在人体内可以作为一种信号分子,参与调节细胞生长、分化和凋亡等生物学过程。吲哚还可能对神经系统产生影响,包括调节神经传导、神经元活性和神经递质释放等。吲哚在神经系统中的作用与情绪调节、认知功能等有关。
吲哚还具有一定的抗氧化性质,可以帮助清除自由基和减轻氧化应激对细胞的损伤。吲哚可能在一定程度上保护细胞免受氧化损伤的影响。
▸ 吲哚含量过高的危害
尽管吲哚对于改善肠道甚至全身疾病至关重要,但过高的吲哚含量可能对健康造成一些危害,包括但不限于以下几个方面:
影响情绪:越来越多的证据表明吲哚和吲哚化合物对大脑代谢、生理和宿主行为有影响。在拥有产生吲哚的大肠杆菌的大鼠中,吲哚的慢性过量产生已被证明会增强焦虑样行为和抑郁。
导致肠道损伤:硫酸吲哚酚(IS)是吲哚的衍生物之一,而过量的硫酸吲哚酚会诱导肠上皮细胞(IEC)损伤。在IEC-6细胞中,硫酸吲哚酚处理可显著增加TNF-α的释放、环氧合酶-2和诱导型一氧化氮合酶的产生以及硝基酪氨酸的合成,表明肠上皮细胞是硫酸吲哚酚诱导的肠道炎症的靶点。
与硫酸吲哚酚一起培养的结肠显示出收缩性降低,这表明该毒素可能对结肠平滑肌细胞产生有害影响并导致肠道蠕动受损。
影响神经系统:其次,硫酸吲哚酚可损伤神经元和神经干细胞,损害神经营养因子和神经递质,诱发氧化应激和神经炎症。例如,通过作用于中枢神经系统胶质细胞,硫酸吲哚酚促进神经炎症并表现出促炎作用。
与肾病相关:并且强有力的证据表明,硫酸吲哚酚在肾功能不全的情况下积累时是有害的。硫酸吲哚酚会损害近端肾小管细胞并诱导炎症和纤维化发展。肾脏通过肾小管分泌实现硫酸吲哚酚的高清除率,而硫酸吲哚酚与血浆蛋白结合超过90%,受到蛋白结合的限制,并且血液透析患者的血浆水平相对较高,这也表明与肾脏疾病密切相关。
免疫抑制:吲哚含量可能影响免疫细胞的活性和功能。高浓度的吲哚可能抑制免疫细胞的功能,如抑制T细胞的活性、影响免疫细胞的增殖和分化等,从而降低机体对病原体的抵抗能力。
▸ 降低吲哚水平的方法
放松身心:高度紧张和某些精神疾病会导致体内吲哚水平过高,多洗热水澡,调节好神经和心理,改善睡眠有助于降低吲哚水平。
食用发酵食品:通过对14名健康男性进行随机交叉研究设计,探讨了发酵乳制品对人类血清代谢组的影响。与牛奶组相比,酸奶摄入组餐后血中吲哚-3-丙酸和吲哚乙酸浓度较低。
同样,C反应蛋白水平轻度升高的健康超重男性在接受抗炎膳食混合物后,饮用500mL餐后奶昔(由300mL蛋奶冻、150mL奶油干酪和50mL鲜奶油组成)。受试者在后期表现出吲哚-3-丙酸血浆浓度降低。
使用药物:一些药物可能影响吲哚类物质的生成。例如,一些抗生素和非甾体抗炎药物被发现可以改变肠道微生物群的组成和功能,从而影响吲哚类物质的生成。
此外,一些药物可能直接干扰色氨酸代谢途径,从而影响吲哚类物质的生成。
减少高蛋白饮食:吲哚是蛋白质的代谢产物,减少高蛋白饮食,尤其是富含色氨酸的食物,有助于降低体内的吲哚含量。
▸ 吲哚含量过低的危害
免疫失调:吲哚在一定浓度下可以调节免疫系统的功能,过低的吲哚含量可能导致免疫系统功能下降,增加感染、致病菌定植、炎症的风险。
神经系统问题:吲哚在神经系统中具有调节作用,过低的吲哚含量可能影响神经传导、神经递质释放等,导致神经系统功能异常,如情绪不稳定、认知功能下降等问题。
代谢紊乱、抗氧化能力下降:吲哚在人体内参与多种代谢过程,过低的吲哚含量可能导致代谢紊乱,影响体内物质的合成和代谢平衡。
吲哚具有一定的抗氧化性质,过低的吲哚含量可能导致机体抗氧化能力下降,增加氧化应激对细胞的损伤风险。
▸提高吲哚水平的方法
补充益生菌、益生元:临床试验表明,益生菌可以抵消肠道微生物失衡造成的负面影响,并可导致吲哚产生属及其衍生物的富集,如乳杆菌(Lactobacillus)。
益生元(包括菊粉和低聚半乳糖)已被证明可以显著提高产生吲哚的益生菌(例如双歧杆菌和乳酸杆菌)的丰度。在对肠道微生物失衡进行一定纠正后,吲哚作为具有调节作用的配体,对炎症反应具有抑制作用。
调节饮食:肠道微生物通过色氨酸调节吲哚水平。色氨酸是人体必需氨基酸之一,需要完全依赖饮食摄入。
以下是一些富含色氨酸的常见食物:肉类(牛肉、猪肉、鸡肉、火鸡)、鱼类(鳕鱼、鲑鱼、金枪鱼)、贝类(蛤蜊、扇贝)、蛋(鸡蛋、鸭蛋)、豆类(大豆、黑豆、红豆)、奶制品(牛奶、乳制品)。菠菜、花椰菜、蘑菇、芝麻、松子、香蕉、菠萝、樱桃、草莓、蓝莓。燕麦、大麦、小麦、黑米、糙米。核桃、杏仁、腰果、葵花子、南瓜子、亚麻籽。
粪菌移植:通过粪菌移植(FMT)将产生吲哚的益生菌(乳酸杆菌、双歧杆菌等)移植到患者的肠道中,可以改善肠道微生物群。据观察,肠道中产生吲哚的微生物群的丰度增加,吲哚及其衍生物的水平受到间接影响。
扩展阅读:
苯酚(Phenol)是一种常见的有机化合物,也是人体肠道微生物的代谢产物之一。在人体的肠道中,肠道微生物通过代谢食物中的复杂碳水化合物和蛋白质等产生苯酚。苯酚的生成通常是通过肠道微生物对酪氨酸(一种氨基酸)的代谢产生的。
苯酚在人体内具有一定的生理作用,苯酚在肠道内可以被吸收到血液循环中,进而影响全身的代谢和生理功能。
抗氧化作用:苯酚具有一定的抗氧化性质,可以帮助清除体内的自由基,减少氧化应激对细胞的损伤,有助于维护细胞健康。
免疫调节:苯酚可能对免疫系统产生一定调节作用,有助于平衡免疫反应,调节免疫细胞的活性,提高机体的抵抗力。
维护肠道健康:适量的苯酚可以促进肠道微生物的平衡,维持肠道健康,有利于消化吸收和排泄功能的正常进行。
▸ 苯酚含量过高的危害
但过高的苯酚含量可能对健康产生不利影响。过高的苯酚含量可能导致肠道菌群失衡、肠道炎症、毒素积累等问题,从而影响整体健康。
肠道健康问题:过高的苯酚含量可能导致肠道微生物失衡,影响肠道菌群的稳定性,进而引发肠道炎症、肠道细菌感染等肠道健康问题。
毒性作用:苯酚具有一定的毒性,过高的苯酚含量可能对肠道黏膜和组织造成损害,导致肠道溃疡、出血等严重问题。
神经系统问题:苯酚可能穿过血脑屏障影响神经系统功能,过高的苯酚含量可能导致神经系统问题,如头晕、头痛、神经炎症等。
代谢紊乱、肝脏负担增加:过高的苯酚含量会影响人体的代谢平衡,导致代谢紊乱,影响体内物质的合成和代谢过程。
苯酚在体内主要通过肝脏代谢,过高的苯酚含量会增加肝脏的负担,可能导致肝脏损伤和功能异常。
免疫系统问题:过高的苯酚含量可能影响免疫系统的功能,导致免疫调节失衡,增加感染和炎症的风险。
▸ 降低苯酚水平的方法
增加膳食纤维摄入,促进肠道健康减少苯酚产生。多摄入新鲜水果和蔬菜等富含维生素和矿物质,适量控制蛋白质摄入,避免添加剂和防腐剂的加工食品。增加饮食多样化。
肠道微生物可从鸟氨酸、精氨酸、赖氨酸、酪氨酸和组氨酸等氨基酸前体产生腐胺、胍胺、尸胺、酪胺和组胺等多胺。
腐胺具有一定的生理作用,如调节肠道运动,但是高浓度的腐胺可能与肠炎、癌症和神经退行性疾病的发展有关。
▸ 腐胺含量过高的危害
臭味问题:腐胺是一种具有刺鼻臭味的化合物,其在胃肠道中含量过高可能导致口臭等问题,影响个人的生活质量。
导致胃肠道疾病:高浓度的腐胺会对人体产生毒性作用,影响肠道黏膜的健康,导致肠道炎症,肠道通透性增加。从而易患结肠炎、炎症性肠病、结直肠癌。
致癌风险:一些研究表明,腐胺被认为是潜在的致癌物质,过高的腐胺含量可能通过诱发DNA损伤、促进细胞增殖、影响基因表达等途径参与致癌过程。
影响认知功能:过高的含量可能导致神经系统问题,如情绪不稳定、认知功能下降等。
▸ 调整腐胺水平的方法
腐胺主要来自于肠道菌群代谢转化,发酵食品,如豆腐、豆酱、酸奶奶酪,以及高蛋白特别是动物蛋白,加工肉类以及硝酸盐含量高的食物会促进腐胺转化。
想要降低体内腐胺水平,需要减少高蛋白摄入,适量控制动物蛋白摄入量,减少发酵食品以及高硝酸盐食物如加工肉类、腌制食品等,增加膳食纤维摄入,新鲜水果和蔬菜富维生素和矿物质有助于维持肠道菌群平衡减少腐胺转化。
硫化氢(H2S)是蛋氨酸、半胱氨酸等含硫氨基酸通过一些肠道微生物(如沙门氏菌、埃希氏菌、梭杆菌等)发酵产生的一种微生物代谢物。H2S也来源于无机硫酸盐和亚硫酸盐添加剂的还原,以及肠道磺胺类物质的分解代谢。
越来越多的研究发现它在哺乳动物体内广泛存在,微生物产生的H2S可能反过来塑造肠道微生物群落本身的组成。这对宿主的健康有很多影响,包括帮助训练和调节免疫系统,而且具有重要的细胞保护作用。它已经称为继一氧化氮和一氧化碳之后,被发现的第3种气体信号分子,具有舒张血管、调节血压等多种生理功能。其代谢异常与心脏病和高血压等多种心血管疾病有关。
▸ 硫化氢浓度过高的危害
虽然硫化氢在一定程度上也具有抗菌作用,但过量的硫化氢对人体健康可能造成负面影响。
中枢神经系统损害:硫化氢在高浓度下可能对神经元产生毒性作用,导致神经元损伤和神经元死亡,还会影响血脑屏障的功能,使得有害物质更容易进入大脑,从而引发神经系统疾病(如帕金森病、阿尔茨海默病)。
胃肠道疾病:高浓度的硫化氢会引发肠道阻塞、炎症反应,以及可以使覆盖在肠道上的保护性黏液层变性,出现黏膜损伤等问题。此外,一些研究还发现高水平的肠道内硫化氢与某些疾病如慢性炎症性肠病、结直肠癌等相关联。
胃胀气:硫化氢作为一种气体,如果在肠道中积累过多,可能会引起胃肠道胀气。
影响消化功能:硫化氢可抑制胃酸分泌,影响消化酶活性,导致消化不良、腹胀和腹泻。硫化氢还可能影响肝脏功能,导致转氨酶升高、出现黄疽等症状。
▸ 降低硫化氢水平的方法
减少高硫蛋白食物的摄入,比如蛋类、肉类、鱼类以及大豆制品等。多摄入富含维生素B6的食物,如香蕉等,此外高纤维食物也可减少硫化氢的转化产生。
扩展阅读:
谷禾肠道菌群检测基于大规模匹配血清代谢组和肠道菌群检测,构建了基于肠道菌群的神经递质和菌群代谢物评估。通过上文对各项指标的解读,我们可以了解其具体意义,以及对健康的影响机制。借助肠道菌群这一重要工具,让我们可以探知自身的情绪、神经系统以及免疫和重要代谢毒素的变化与异常。
此外通过调整肠道微生物群落的结构,可以影响神经递质的水平,调节免疫系统的功能,改善肠道黏膜屏障的完整性,从而减少炎症反应,改善疾病症状。因此,我们可以借此进行更加个性化和有效的干预。
主要参考文献
Dicks LMT. Gut Bacteria and Neurotransmitters. Microorganisms. 2022 Sep 14;10(9):1838.
Braga JD, Thongngam M, Kumrungsee T. Gamma-aminobutyric acid as a potential postbiotic mediator in the gut-brain axis. NPJ Sci Food. 2024 Apr 2;8(1):16.
Guzel T, Mirowska-Guzel D. The Role of Serotonin Neurotransmission in Gastrointestinal Tract and Pharmacotherapy. Molecules. 2022 Mar 3;27(5):1680.
Dicks L.M.T., Hurn D., Hermanus D. Gut Bacteria and Neuropsychiatric Disorders. Microorganisms. 2021;9:2583.
Yang X., Lou J., Shan W., Ding J., Jin Z., Hu Y., Du Q., Liao Q., Xie R., Xu J. Pathophysiologic Role of Neurotransmitters in Digestive Diseases. Front. Physiol. 2021;12:567650.
Strandwitz P. Neurotransmitter modulation by the gut microbiota. Brain Res. 2018;1693:128–133.
Van De Wouw M., Boehme M., Lyte J.M., Wiley N., Strain C., O’Sullivan O., Clarke G., Stanton C., Dinan T.G., Cryan J.F. Short-chain fatty acids: Microbial metabolites that alleviate stress-induced brain-gut axis alterations. J. Physiol. 2018;596:4923–4944

谷禾健康

目前越来越多营养概念诸如”低碳水化合物饮食”正在流行,然而,所有的碳水化合物都是不好的吗? 其实并非如此。
其中,抗性淀粉就是一种特殊的碳水化合物,它与我们通常所熟知的淀粉有区别。抗性淀粉之所以得名,是因为它能够抵抗人体消化酶的作用,逃离被吸收的命运,直接进入肠道。这种特性使得抗性淀粉拥有许多健康功效,它不仅能调节血糖,还能促进有益菌的生长,改善肠道功能,甚至还能增强饱腹感,帮助控制体重。
抗性淀粉天然存在于豆类(如扁豆、鹰嘴豆)、某些谷物(如大麦、燕麦)、块茎(如土豆、山药)等食物中。此外,各种食品加工和烹饪方法可以提高食品中的抗性淀粉含量,进一步使这种淀粉的潜在膳食来源多样化。
作为一种膳食纤维,抗性淀粉可以作为微生物发酵的底物,例如拟杆菌属,瘤胃球菌,双歧杆菌等可以发酵抗性淀粉。
一些肠道细菌促进抗性淀粉发酵产生短链脂肪酸。短链脂肪酸的主要功能是改善肠上皮屏障的完整性,缓解局部和全身炎症,产生全身效应,影响代谢健康、免疫功能,甚至可能影响大脑健康。
目前代谢性疾病负担正在增加,一些膳食可以通过调节肠道菌群干预疾病,其中抗性淀粉也很重要,它结合了传统和科学,促使研究人员和消费者重新审视传统饮食习惯并认识到其潜在的健康影响。
本文探讨了抗性淀粉和肠道微生物组之间复杂的相互作用,包括抗性淀粉影响微生物群落的机制、这些相互作用对健康的影响。此外,还讨论了富含抗性淀粉的饮食对肠道健康的影响。随着对肠道菌群在健康和疾病中的作用了解越来越多,强调从天然来源获取抗性淀粉的饮食将会不断增长,为营养干预提供新途径。
▼
什么是抗性淀粉?
抗性淀粉(RS)是一种不被人体消化酶分解的淀粉,被认为是膳食纤维。
淀粉作为葡萄糖的储存形式天然存在于植物中。食品中的淀粉可分为慢消化淀粉(SDS)、快速消化淀粉(RDS)或抗性淀粉(RS)。
一般淀粉在小肠中迅速分解并转化为葡萄糖,并迅速吸收到血液中,而抗性淀粉则抵抗正常消化,因此得名。它不会分解成葡萄糖,而是不受干扰地通过消化道,直到到达结肠。
首先,淀粉的基本结构基于两种不同的葡萄糖聚合物——直链淀粉和支链淀粉。
直链淀粉主要是由α-1,4-葡萄糖单元组成的线性分子,与支链淀粉的分支结构形成对比,支链淀粉还包含α-1,6键连接。
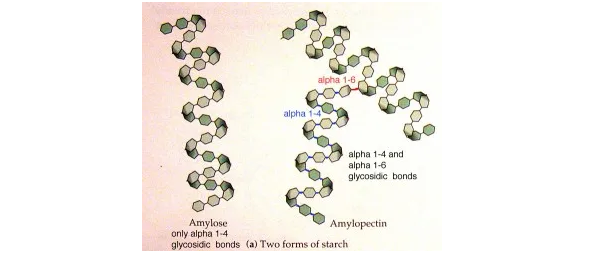
这两种组分的比例及它们在淀粉颗粒内的排列方式显著影响淀粉的可消化性。这些分子越密集、排列越紧密,消化酶就越难接近它们。
抗性淀粉(RS)是一种独特的膳食纤维,不是在小肠中消化,而是在大肠中发酵。不同食物类别(包括谷物、豆类、块茎和某些加工食品)中抗性淀粉的含量差异很大。
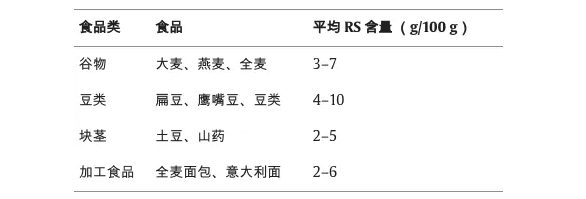
doi.org/10.1016/j.fochx.2024.101118
谷物,特别是大麦、燕麦和全麦等全谷类食物,是抗性淀粉的重要来源,尤其是在它们经过最低限度加工的情况下。比如,煮熟并冷却大米会增加其抗性淀粉含量,这是由于直链淀粉的逆淀粉化作用。
扁豆、鹰嘴豆等豆类也富含抗性淀粉。它们的抗性淀粉含量归因于它们的高直链淀粉和支链淀粉比率,这有助于它们缓慢的消化率。烹饪和冷却过程进一步增加了其抗性淀粉含量。
块茎,包括马铃薯和山药,含有抗性淀粉,尤其是在煮熟和冷却时,这是一个诱导淀粉回生的过程。这使得冷土豆沙拉等菜肴成为良好的抗性淀粉来源。
某些加工食品,特别是那些由全谷物制成或含有 抗性淀粉作为成分的食品,可能是重要的抗性淀粉来源。经过挤压烹饪等过程的全麦面包和意大利面保留了大量的抗性淀粉。
了解这些来源及其抗性淀粉含量对于饮食计划和营养优化至关重要。
在此基础上,抗性淀粉可以根据其起源和特性大致分为四种主要类型:
RS1型(RS1):由于食物基质和蛋白质外壳形成的保护屏障,这种形式的 RS 在物理上无法被酶接近。常见的来源包括全谷物和种子。
RS2型(RS2):RS2 的特点是其天然颗粒形式,主要存在于某些生食中。例子包括生土豆、青香蕉、高直链淀粉玉米。这些来源的高直链淀粉含量导致紧密堆积的颗粒结构,限制了酶的获取。
RS3型(RS3):也称为逆行淀粉,当某些食物煮熟然后冷却时会形成 RS3。这种冷却过程导致淀粉分子的重新排列和重结晶,进一步使它们对酶分解具有抵抗力。煮熟和冷却的土豆、意大利面和米饭等食物是 RS3 的主要来源。
RS4型(RS4):这种类型包括食品中天然不存在的化学改性淀粉,例如一些商业生产的面包和糕点。各种工业过程在淀粉分子中引入交联或取代,以增强其对消化的抵抗力。
部分分类有:
RS5型(RS5): 这是一个较新的类别。它需要通过加热和冷却含有特定脂质(例如脂肪或蜡)的淀粉类食品的过程产生的抗性淀粉。例如含有脂肪成分的面包或含有人工制造的淀粉-脂质复合物的食物。

虽然这些类别有助于讨论和研究,但许多现实世界的食物都含有抗性淀粉类型的混合物。此外,食品加工方法,储存条件和其他食品成分的存在等因素可以显着调节这些食品中的抗性淀粉含量。
抗性淀粉的潜在健康益处和生理影响主要来自其在大肠中的发酵。然而,这些益处的程度和特异性可能因抗性淀粉类型而异。例如,不同的抗性淀粉类型可能优先促进特定微生物物种的生长或导致挥发性脂肪酸的产生速率不同。
总之,抗性淀粉的生化结构和分类对于确定其与肠道微生物组的相互作用以及随后的健康结果至关重要。全面了解这些基础方面对于旨在利用抗性淀粉潜在益处的饮食干预的研究和应用至关重要。
保持血糖稳定
由于抗性淀粉消化缓慢,因此可以保持血糖水平稳定。这可以帮助减少餐后血糖峰值,这对糖尿病患者特别有益。
抗性淀粉具有第二餐的效果:根据一项小型研究的结果,早餐吃抗性淀粉可以降低午餐时的血糖。
2022年1月发表在《Frontiers in Nutrition》 的一篇评论指出,在饮食中添加抗性淀粉是一种简单的生活方式调整,可以帮助糖尿病管理。
促进心脏健康
2018年6月《Nutrition Research》发表的荟萃分析结果,抗性淀粉可以通过降低胆固醇水平有益于心脏健康。它还可以改善血糖控制,正如2017年《Nutrition Journal》上发表的一项针对超重成年人的小型研究所证明的那样,它通过促进肠道中健康细菌的生长来实现这一点,这些细菌产生具有有益作用的短链脂肪酸。
根据2022年3月发表在《国际分子科学杂志》上的一篇评论,短链脂肪酸有助于调节交感神经系统。抗性淀粉可能有助于治疗因神经系统过度活跃而加剧的心脏病,例如慢性心力衰竭、高血压和冠状动脉疾病。
减肥效果
抗性淀粉非常有饱腹感,可能会降低食欲。与其他碳水化合物相比,它的热量也较低,通过这些方式,抗性淀粉可能有助于减肥。
虽然早期研究表明抗性淀粉可能在减肥中发挥作用,但还需要进一步的研究来证实任何此类益处。2017 年《营养杂志》上发表的研究表明,每天吃 30 克抗性淀粉,持续六周,18 名超重成年人减少饥饿激素和无意识地吃零食,但不会改变身体成分。
支持肠道健康
抗性淀粉的作用类似于纤维,而纤维会被肠道中的健康细菌发酵。“这些有益的肠道细菌可以产生短链脂肪酸,这对肠道健康有帮助。
例如,短链脂肪酸可以帮助保持肠道内壁坚固,并有助于粘液产生和炎症,还可能有助于降低结直肠癌的风险。这在后面章节我们会详细阐述。
成人每天应摄入约15克抗性淀粉。然而,据估计大多数人每天的摄入可能不到这个量。
抗性淀粉食品含量表
(每100克食品的平均含量)
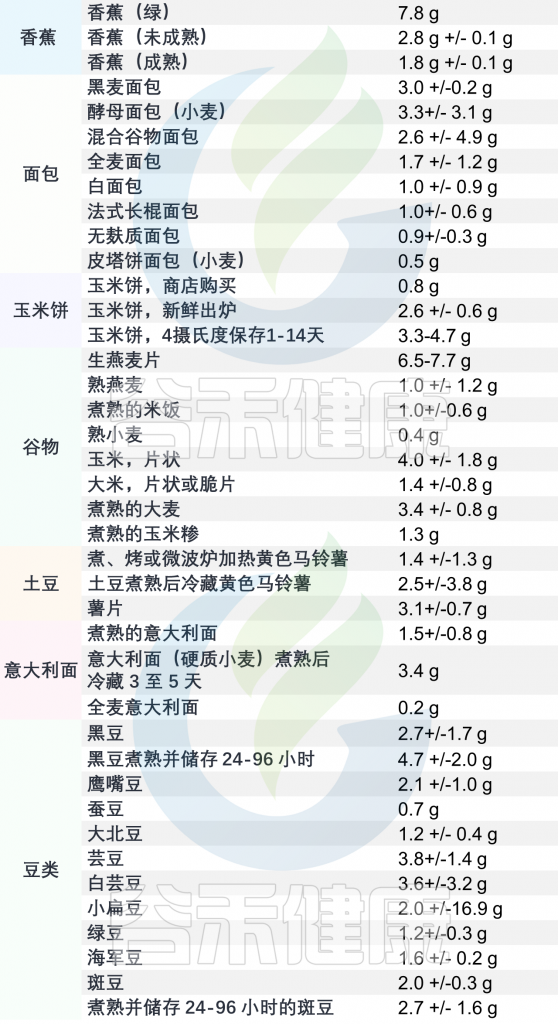
注:如果要增加摄入量时,请逐步增加,一下子吃太多可能会腹胀和胀气。
挤压烹饪,广泛用于生产即食谷类食品和零食,可以增加最终产品的抗性淀粉含量,取决于应用的条件,诸如含水量、螺杆速度和温度等参数可以进行调整以优化抗性淀粉的形成。
退火过程涉及水化淀粉颗粒而不使其明胶化,已发现这一过程可以增加一些谷物中的抗性淀粉含量。
发酵,是各种文化中历史悠久的烹饪和保鲜方法,具有提高抗性淀粉水平的固有能力。这一过程通常涉及有益细菌或酵母分解和发酵糖类,可以改变淀粉结构,使更多的淀粉对消化具有抗性。例如,将谷物发酵制成酸面包或某些传统非洲菜肴不仅赋予了独特的风味,还增加了它们的抗性淀粉含量。
虽然探索和应用这些方法可以显著增加抗性淀粉含量,但必须考虑更广泛的营养后果。并非所有增加抗性淀粉的方法都是普遍有益的。有些加工方法可能会剥夺食物的重要营养素,或引入不良化合物。
在增强抗性淀粉获得肠道健康益处,和确保食物整体营养价值保持完整之间取得平衡至关重要。
抗性淀粉(RS)与肠道微生物组之间错综复杂的相互作用主要发生在结肠,结肠是大多数未消化碳水化合物达到代谢目的的地方。
肠道微生物群发酵抗性淀粉
人类结肠内有着丰富多样、复杂的微生物群,对发酵未消化膳食成分,尤其是抗性淀粉,起着至关重要的作用。
抵达结肠后,抗性淀粉将被居住在肠道的微生物群体进行厌氧发酵。这一发酵过程导致了短链脂肪酸的产生,主要是乙酸、丙酸和丁酸,以及氢气、甲烷和二氧化碳等气体。
在短链脂肪酸中,丁酸在结肠健康中发挥着关键作用。作为结肠细胞的主要能源来源,丁酸还具有抗炎性能,加强结肠防御屏障,并潜在降低结肠癌的风险。此外,短链脂肪酸通过调节肠道pH值,有利于有益菌的生长,同时抑制致病菌株的增殖。
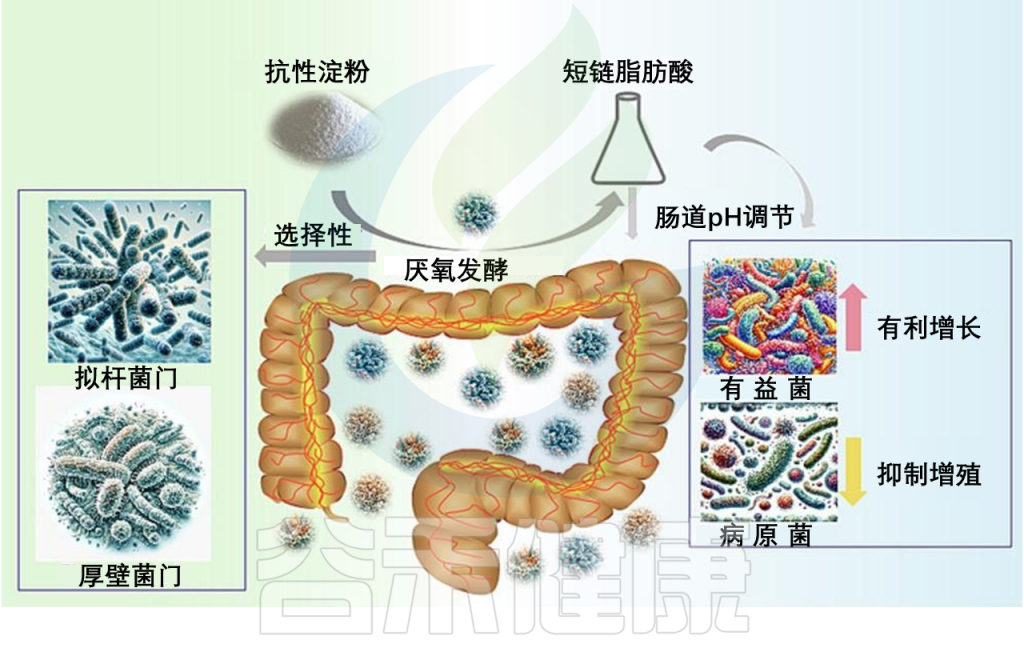
doi.org/10.1016/j.fochx.2024.101118
选择性发酵:抗性淀粉增多→有益菌随之增加
抗性淀粉发酵的另一个有趣的方面是其选择性。并非所有肠道微生物都能够有效发酵抗性淀粉;特定菌群,特别是来自拟杆菌门和厚壁菌门的细菌群,是主要的抗性淀粉发酵者。
这种选择性发酵会导致肠道微生物组成的变化。持续的抗性淀粉摄入可以促进这些抗性淀粉发酵细菌的增殖,使肠道富含有益微生物,进一步提高发酵效率和短链脂肪酸的产生。因此,抗性淀粉和肠道微生物群之间的动态相互作用有望进行有针对性的干预,有可能通过饮食策略调节肠道微生物组成和活性。
抗性淀粉为微生物发酵提供了底物,作为回报,肠道微生物会产生有益于宿主健康的代谢物。
前面我们了解了结肠中抗性淀粉发酵的机制,这里了解这一过程中的关键微生物参与者也很重要。
拟杆菌门
积极参与抗性淀粉发酵的主要群体属于拟杆菌门,尤其是拟杆菌属,拟杆菌的代谢能力使它们能够在各种复杂的碳水化合物中茁壮成长,包括抗性淀粉。它们的酶库有助于将抗性淀粉分解成更简单的单元,然后发酵以产生短链脂肪酸。
厚壁菌门
抗性淀粉发酵的另一个重要贡献者是厚壁菌门,尤其是瘤胃球菌属,瘤胃球菌是这一领域的关键物种,因其在启动抗性淀粉降解方面的无与伦比的效率。瘤胃球菌(R. bromii)进行的初步降解使抗性淀粉更易于其他微生物群进一步发酵。考虑到在摄入富含抗性淀粉饮食的个体中的统治地位,其重要性变得明显。此外,瘤胃球菌的丰度较高与改善的肠道健康状况相关,表明其潜在的保护作用。
放线菌门
虽然拟杆菌门和厚壁菌门脱颖而出,但另一个门放线菌门通过双歧杆菌属促进抗性淀粉发酵。双歧杆菌是备受推崇的益生菌,已知具有无数的健康益处。在抗性淀粉的背景下,双歧杆菌发酵它以产生短链脂肪酸,从而降低肠道 pH 值,从而创造不利于病原菌的环境。此外,抗性淀粉的双歧杆菌效应,即补充抗性淀粉导致双歧杆菌增加,已在各种研究中得到充分证明。
产甲烷古细菌
古菌,特别是产甲烷的Methanobrevibacter smithii,在抗性淀粉发酵领域也发挥作用。
M. smithii消耗其他微生物在抗性淀粉发酵过程中产生的氢气,将其转化为甲烷。这种氢气的去除至关重要,因为它防止了结肠中氢气的积累,否则可能会阻碍发酵过程。因此,M. smithii通过维持其他发酵者的适宜环境,间接支持抗性淀粉发酵过。
总而言之,结肠中的抗性淀粉发酵并不是归因于单个微生物分类群的孤立过程。这是一项涉及多个微生物群体的协同合作,每个微生物群体都为该过程及其健康益处做出了独特的贡献。
只有少数菌群如瘤胃球菌和青春双歧杆菌能够利用淀粉,这些细菌本身并不直接产生丁酸盐,而是依靠与其他肠道细菌的交叉喂养相互作用来产生丁酸盐。
他们的集体行动强调了肠道是一个代谢“器官”的概念,其中饮食成分,主要是抗性淀粉,以协调的方式代谢。
丁酸梭菌(Clostridium butyricum)是一种降解抗性淀粉的菌,能够在多种类型和来源的抗性淀粉上生长,在这个过程中产生大量的丁酸盐。它通过使用一种酶系统来实现这一点,该酶系统虽然是迄今为止在能够降解抗性淀粉的细菌中发现的最简单的酶系统,但在抗性淀粉的消化过程中表现出高度的协同作用和功能多样性。在一个生物体中,消化抗性淀粉和丁酸生产的结合有可能绕过交叉喂养网络的复杂性,而交叉喂养网络通常是抗性淀粉消耗过程中生产丁酸所必需的。
这种独特的性状组合表明,它可能作为一种与抗性淀粉协同使用的菌株,促进更广泛的丁酸反应,从而为更多人群解锁这种益生元的健康益处。
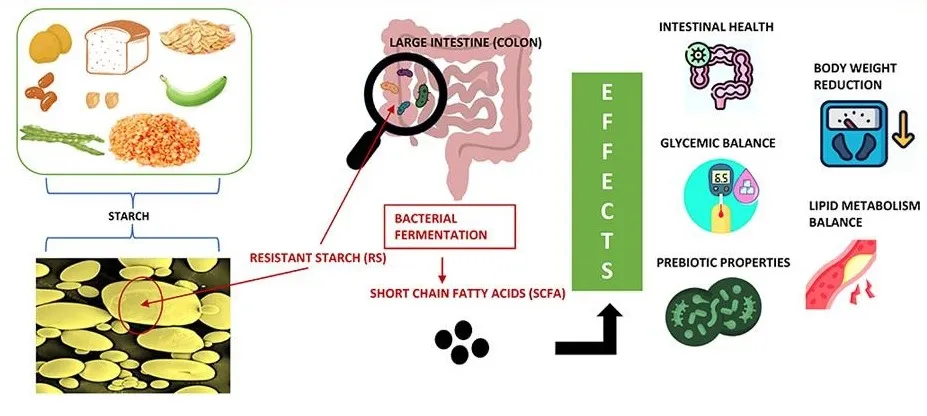
doi.org/10.1016/j.jff.2022.105094
我们了解到肠道微生物群领域及其与抗性淀粉的错综复杂互动是广阔而多层次的。抗性淀粉可以影响肠道微生物群的组成和功能,但同样明显的是,这些影响的程度和性质受到各种因素的调节。揭示这些因素可以增进我们对肠道健康复杂性的理解,并帮助更有效地定制膳食和治疗干预措施。
个体肠道微生物群的基线组成
一个主要决定因素是个体肠道微生物群的基线组成。每个人的肠道微生物群具有独特的特征,受到遗传、早期生活暴露、抗生素和饮食模式等因素的影响。引入膳食时,抗性淀粉可能会因个体肠道微生物的起始点而在个体之间产生不同效应。例如,基线拟杆菌水平较低的个体,在摄入抗性淀粉后,可能会比那些已经拥有更高丰度的个体出现这些细菌增加更显著。
不同类型的抗性淀粉会被特定菌群优先代谢
消费的抗性淀粉类型是另一个重要因素。根据其物理化学性质和来源,抗性淀粉有多种类型:RS1、RS2、RS3、RS4。每种类型可能会被特定微生物类群优先代谢。例如,瘤胃球菌对高直链淀粉玉米中的RS2表现出明显的偏好,而某些拟杆菌物种可能更青睐来自逆行淀粉的RS3。因此,膳食中包含的抗性淀粉类型可以引导微生物群变化的轨迹。
其他营养素的影响
抗性淀粉消费的膳食背景也不容忽视。其他膳食纤维、蛋白质、脂肪和微量营养素的存在可以影响抗性淀粉的可获得性和发酵性。例如,富含可溶性纤维的饮食可能通过促进有益菌(如乳杆菌)的生长来放大抗性淀粉的益生效应。相反,富含蛋白质的饮食可能会使一些结肠细菌转向蛋白质发酵,产生像氨之类的潜在有害化合物。
抗性淀粉摄入的持续时间
抗性淀粉摄入的持续时间也起着关键作用。初始引入抗性淀粉可能会导致微生物群组成的快速变化。然而,随着摄入时间的延长,微生物群可能会稳定下来,表明适应性。长期摄入抗性淀粉可以导致更具弹性和多样化的微生物群,这些微生物群更能抵抗干扰和潜在的菌群失调。
其他宿主相关因素
最后,宿主相关因素,如年龄、健康状况和遗传,调节着抗性淀粉与微生物群的相互作用。与微生物群的年龄相关变化、肠道传输时间的差异和酶活性可能会影响抗性淀粉在肠道中的发酵。同样,患有肠道紊乱症状如肠易激综合征(IBS)或炎症性肠病(IBD)的个体可能对抗性淀粉有不同反应,鉴于这些情况下肠道环境和微生物群的组成发生了改变。
总之,抗性淀粉与肠道微生物群之间的互动是一个受多种因素影响的动态过程。认识和理解这些因素对于个性化营养策略旨在利用抗性淀粉的肠道健康益处是至关重要的。这些见解呼唤着在营养和肠道健康领域采取更个性化的方法,更胜于一刀切的建议。
抗性淀粉已成为膳食的关键成分,其影响远远超出了其营养价值。抗性淀粉最重要的作用之一在于它能够维持肠道的屏障功能。这种错综复杂的粘膜细胞和细胞间连接是我们全身健康的关键,可防止病原体入侵并维持代谢平衡。鉴于肠道相关疾病的负担不断加重,了解抗性淀粉如何影响这一屏障可以为疾病预防和治疗干预提供关键的见解。
肠道屏障是一个动态和反应灵敏的系统,而不是一个静态的实体。在其核心,上皮细胞形成前线,作为对管腔环境的主要防御。
抗性淀粉促进粘蛋白分泌
抗性淀粉通过支持细胞更新和促进粘蛋白的分泌来增强上皮屏障,粘蛋白是一种糖蛋白,可润滑和保护上皮表面免受潜在病原体和研磨性食物颗粒的侵害。粘蛋白层不仅形成保护毯,还为共生细菌提供栖息地,有助于宿主和微生物群之间的双向关系。
抗性淀粉正向调节紧密连接蛋白
紧密连接蛋白,结合上皮细胞的微观结构,对于维持屏障完整性至关重要。这些蛋白质决定了屏障的渗透性,决定了哪些物质被允许通过,哪些物质仍然被排除在外。在“肠漏”的情况下,这些蛋白质会受到损害,导致肠道通透性增加。这种情况会允许不需要的物质(包括病原体和毒素)进入血液,引发全身炎症。研究表明,抗性淀粉正向调节这些蛋白质。抗性淀粉发酵产生短链脂肪酸,特别是丁酸盐,在上调紧密连接蛋白的表达、强化肠道屏障方面发挥作用。
抗性淀粉间接影响局部免疫反应
驻留在肠道粘膜内的免疫细胞为屏障的防御机制增加了另一层。在这里,抗性淀粉展示了其免疫调节能力。通过改变肠道微生物群组成,抗性淀粉间接影响局部免疫反应。它促进有益细菌的生长,进而与免疫细胞相互作用,指导它们的功能。这种串扰确保了潜在病原体的迅速消除,同时保持了对膳食抗原和共生微生物的耐受性。
抗性淀粉通过神经,免疫,血管等相互作用,间接提供保护
除了这些直接影响外,抗性淀粉诱导的肠道微生物群变化也会影响肠脑轴。肠道和中枢神经系统之间的这种双向沟通渠道对整体健康至关重要。肠道屏障功能的破坏与神经系统疾病有关,强调了抗性淀粉等膳食成分在神经保护中的重要性。
此外,肠道内的血管结构,包括血液和淋巴管,在屏障功能中发挥作用。它们确保营养吸收和免疫细胞运输。抗性淀粉通过其代谢物调节血管内皮屏障,优化营养吸收并确保有效的免疫监测。
总之,抗性淀粉与肠道屏障的细胞、免疫和血管成分错综复杂的相互作用,为应对环境挑战提供了强大的防御能力。拥抱抗性淀粉的治疗潜力可以重新定义面向胃肠道健康及其他方面的策略。
炎症是免疫系统对病原体、伤害或有害刺激发起的保护性反应,当放松管制时,可能会成为一把双刃剑。特别是在肠道内,持续的炎症会加剧从炎症性肠病发展到结直肠癌等多种疾病。人们的注意力已经转向可以调节炎症的饮食成分,其中抗性淀粉已成为一个至关重要的参与者。
抗性淀粉促进抗炎短链脂肪酸 (丁酸盐) 产生
与其他淀粉不同,抗性淀粉在小肠中抵抗消化,基本完好无损地到达结肠。一旦进入结肠,抗性淀粉就会充当某些有益肠道细菌的底物,导致短链脂肪酸的产生,主要是乙酸盐、丙酸盐和丁酸盐。值得注意的是,丁酸盐因其显着的抗炎作用而得到认可。丁酸盐通过抑制促炎细胞因子的产生来发挥作用,例如TNF-α和IL-6,它们在炎症传播中起着核心作用。
抗性淀粉影响免疫细胞分化
抗性淀粉发酵和随后的短链脂肪酸产生已被证明会影响免疫细胞分化,尤其是调节性 T 细胞(Tregs)。这些细胞在维持肠道免疫稳态方面起着不可或缺的作用。Tregs数量的增加与炎症减少有关,这证明了它们抑制异常免疫反应的能力。短链脂肪酸,特别是丙酸盐,影响幼稚T细胞分化为Tregs,确保肠道内平衡的免疫反应。
抗性淀粉影响肠道神经系统
肠道神经系统功能微妙,确保肠道蠕动和分泌,同时与免疫系统密切相互作用。肠道神经系统的破坏会导致肠道运动障碍,从而为细菌过度生长和炎症创造有利的环境。抗性淀粉通过其代谢物,尤其是丁酸盐,影响肠道神经系统功能。它有助于维持肠道神经元的健康和功能,随后促进肠道的定期肌肉收缩,最大限度地减少细菌停滞和炎症的机会。
抗性淀粉维持平衡的肠道pH值
此外,抗性淀粉可以通过调节肠道的 pH 值来影响肠道炎症。抗性淀粉发酵产生的短链脂肪酸导致结肠中的微酸性环境。这种酸度阻止了病原菌的生长,同时促进了有益共生细菌的增殖。这两个细菌群之间的平衡对于维持肠道健康至关重要,任何向致病性优势的转变,称为生态失调,都可能引发炎症。通过维持酸性 pH 值,抗性淀粉间接阻止炎症的发生和发展。
总之,抗性淀粉在调节肠道炎症中的复杂作用揭示了其潜在的治疗应用。它能够改变微生物组成,促进抗炎短链脂肪酸的产生,影响免疫细胞分化,并维持平衡的肠道pH值,这表明其在确保肠道稳态方面的多方面方法。随着肠道相关炎症的患病率不断上升,利用抗性淀粉的益处可以为提供预防和治疗潜力的新型饮食干预铺平道路。
肠道和免疫系统之间的界面是人体内最具活力的相互作用之一。我们整个免疫系统的近70%都存在于肠道内,随时准备对来自食物和病原体的各种抗原做出反应。正是在这种背景下,抗性淀粉等膳食成分占据了中心位置。抗性淀粉不仅仅是消化过程中的旁观者,它还以多种方式塑造和影响肠道的免疫反应。
抗性淀粉发酵产物,减少促炎细胞因子
抗性淀粉天然抵抗上消化道的消化,到达结肠基本保持不变。在结肠中,抗性淀粉由特定菌群发酵,导致短链脂肪酸的产生增加,主要是乙酸盐、丙酸盐和丁酸盐。除了作为结肠细胞的能量底物外,这些短链脂肪酸还调节各种免疫细胞功能。例如,短链脂肪酸可以降低炎性细胞因子的表达并增加抗炎介质,从而有效地抑制过度的免疫反应。特别是丁酸盐对中性粒细胞功能具有深远的影响,并减少炎症介质如TNF-α和IL-6的产生。
肠道相关淋巴组织 (GALT) 是免疫系统不可或缺的一部分,在维持肠道稳态方面起着至关重要的作用。在 GALT 内,树突状细胞不断对肠道的管腔内容物进行采样。这些细胞在遇到细菌代谢物(如抗性淀粉发酵产生的短链脂肪酸)时,其活性受到调节,导致调节性T细胞的产生增加,这些T细胞在控制炎症和自身免疫方面起着关键作用。此外,已经注意到短链脂肪酸对巨噬细胞的直接影响,观察到抗炎细胞因子产生增加和促炎细胞因子产生减少。
抗性淀粉增强屏障功能,减少LPS易位
抗性淀粉发酵产物会影响肠道屏障的完整性。维持肠上皮层连续性的紧密连接蛋白被短链脂肪酸上调,从而增强屏障功能,并减少细菌内毒素如脂多糖(LPS)进入体循环的易位。LPS易位减少导致内毒素血症相关免疫激活减少,有益于整体健康。
抗性淀粉促进有益菌生长,IgA升高
抗性淀粉作为一种益生元,选择性地滋养有益菌,进而积极调节免疫反应。例如,双歧杆菌和乳酸杆菌等有益细菌的富集通常与抗性淀粉消耗有关,与免疫球蛋白 A(IgA)的产生增强有关,IgA是粘膜防御中的一抗。升高的IgA水平在中和病原体和维持粘膜稳态方面起着关键作用。
从本质上讲,抗性淀粉与免疫系统之间的相互作用强调了饮食、微生物群和免疫力之间复杂的相互作用。通过其发酵产物和肠道微生物群的调节,抗性淀粉有可能成为调节免疫反应和维持肠道健康的重要膳食成分。它带来了全身益处,并为免疫调节的饮食策略开辟了途径。
抗性淀粉越来越被认为是一种重要的膳食成分,不仅因为它对肠道健康的直接影响,还因为它更广泛的代谢影响,特别是与代谢综合征有关。代谢综合征是一组疾病,包括血压升高、高血糖、腰部脂肪过多以及胆固醇或甘油三酯水平异常,会增加患心脏病、中风和糖尿病的风险。抗性淀粉减轻代谢综合征方面的潜力主要归因于其肠道微生物群发酵产物,如乙酸盐、丙酸盐和丁酸盐。
尤其是丁酸盐,在维持肠道屏障完整性方面发挥着重要作用,并具有抗炎特性,这对于对抗与代谢综合征相关的炎症过程至关重要。丁酸盐还通过增强结肠中的能量消耗和脂肪氧化,与改善胰岛素敏感性有关,胰岛素敏感性是代谢综合征的关键因素。此外,丙酸盐具有糖异生作用,有可能调节血糖水平,这对患有或有2型糖尿病风险的人至关重要。
此外,抗性淀粉在食欲调节中的作用也值得一提。随着短链脂肪酸的产生,它们会刺激厌食激素的释放,如肽YY(PYY)和胰高血糖素样肽-1(GLP-1),从而增加饱腹感并减少卡路里摄入量。这种食欲调节作用,加上对血脂和血压的潜在益处,使抗性淀粉消费成为预防或管理代谢综合征的有前途的策略。
体重管理和肥胖的全球挑战与饮食成分及其代谢结果有着内在的联系。肥胖的增加伴随着 2 型糖尿病、心血管疾病和几种癌症风险的增加,使其成为最重要的健康问题。从这个角度来看,抗性淀粉不仅作为一种膳食纤维脱颖而出,而且作为对抗肥胖症的潜在变革性膳食成分脱颖而出。
一些研究表明,抗性淀粉可能对体重管理有直接影响。一个主要机制是食物的热效应,这是消化和加工食物时消耗的能量的量度。抗性淀粉对立即消化具有抵抗力,往往会增加这种热效应,导致在大肠发酵过程中消耗更高的能量。这不仅有助于负能量平衡,还会影响脂肪储存并增强脂肪氧化,这对体重管理至关重要。此外,如前几节所述,抗性淀粉发酵导致短链脂肪酸的产生,短链脂肪酸通过释放 PYY 和 GLP-1 等激素在控制食欲方面发挥积极作用。调节食欲等同于减少热量摄入,这是体重管理的一个重要方面。
此外,抗性淀粉与改善肠道健康有关,这对肥胖有间接影响。健康的肠道生物群与更瘦的表型有关。当肠道微生物群发酵抗性淀粉时,它会导致微生物组成的变化,有利于与肥胖呈负相关的有益菌。
近日,一项针对 37 名超重或肥胖参与者的随机安慰剂对照交叉设计试验(ChiCTR-TTRCC-13003333) 中,研究人员测试了抗性淀粉作为膳食补充剂是否会影响肥胖相关的结果。
研究表明补充抗性淀粉 8 周有助于实现体重减轻(平均 -2.8 公斤)并改善体重超重个体的胰岛素抵抗。
补充青春双歧杆菌(一种与减轻研究参与者肥胖显著相关的物种)可以保护雄性小鼠免受饮食引起的肥胖。从机制上讲,抗性淀粉诱导的肠道微生物群变化会改变胆汁酸分布,通过恢复肠道屏障来减少炎症,并通过调节ANGPTL4抑制脂质吸收,提高脂肪组织对FGF21的敏感性。
次级胆汁酸,例如甘氨脱氧胆酸、脱氧胆酸、甘氨胆酸和牛磺脱氧胆酸,对于提高胰岛素敏感性和改善肝脂肪变性具有重要作用。胆盐水解酶负责次级胆汁酸的去偶联。补充抗性淀粉降低了胆盐水解酶的产生,增加了次级胆汁酸的水平。
抗性淀粉至少可以部分通过青春双歧杆菌促进体重减轻,并且肠道微生物群对于抗性淀粉的作用至关重要。
因此,持续食用富含抗性淀粉的食物可能会导致肠道环境不太容易使体重增加和肥胖。
糖尿病是一种以慢性高血糖为特征的代谢紊乱,是一个不断升级的全球健康问题,具有从个人健康恶化到国家经济负担的多方面影响。鉴于发病率不断上升,迫切需要饮食干预来缓解或可能逆转这种疾病的进展。抗性淀粉是一种引人注目的膳食成分,其多种代谢影响与糖尿病管理和血糖控制有关。
糖尿病管理的核心是调节餐后血糖和胰岛素反应。摄入抗性淀粉似乎有利地调节这些反应。与快速消化的淀粉不同,抗性淀粉不会直接导致餐后血糖峰值,因为它绕过了小肠的消化,它在大肠中的发酵会产生短链脂肪酸。特别是,丙酸盐可促进肝脏葡萄糖产生调节,降低餐后葡萄糖偏移的风险。此外,丁酸盐在促进胰高血糖素样肽-1(GLP-1)分泌中的作用。
注:GLP-1是一种增强胰岛素分泌和减少胰高血糖素释放的激素,协调血糖水平。
此外,长期服用抗性淀粉与提高胰岛素敏感性有关,这是 2 型糖尿病发病机制的关键因素。研究表明,食用富含抗性淀粉的饮食的胰岛素抵抗个体表现出胰岛素敏感性的显著改善。这种改善被认为与短链脂肪酸的抗炎特性有关,尤其是丁酸盐,以及它在减少氧化应激中的作用,氧化应激有助于胰岛素抵抗。此外,抗性淀粉培养有益肠道微生物群组成的能力对代谢健康有间接影响,进一步强调了其在糖尿病管理中的潜在作用。
莲子抗性淀粉抑制高脂血症大鼠中下列菌群的生长:
莲子抗性淀粉促进初级胆汁酸(CA、CDCA 、β-MCA)和次级胆汁酸(LCA、UDCA)的产生,降低高脂血症中TCA、DeHydro-LCA、isoLCA、LCA-3-S、THDCA的含量。
Blautia、norank_f__Muribaculaceae、norank_f__Eubacteria_coprostanoligenes_group与 DeHydro-LCA、isoLCA、TCA、LCA-3-S、 TCHO、TG和 LDL-C呈正相关。
莲子抗性淀粉通过调节肠道菌群并加速肝脏中胆固醇分解为胆汁酸来改善血脂水平。
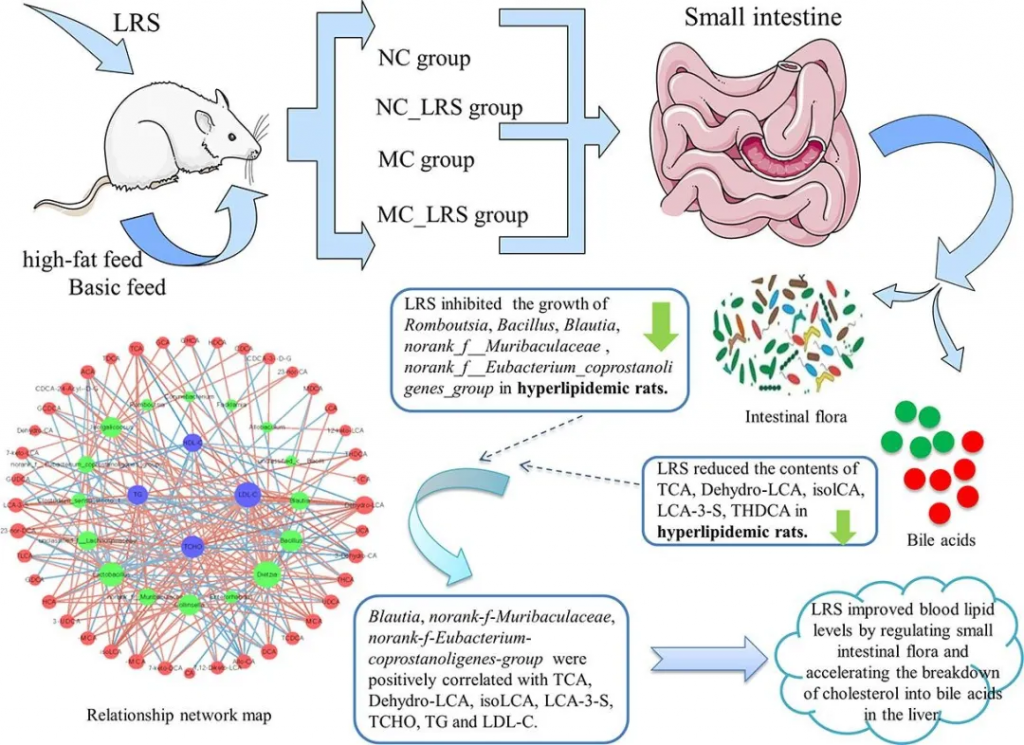
doi.org/10.1016/j.foodchem.2022.134599
认知能力下降是衰老的常见后果。缺乏纤维和高饱和脂肪的饮食模式会引发促炎症途径和代谢功能障碍,从而加剧认知障碍。新的证据强调了富含纤维的饮食对神经认知的益处以及肠道-微生物-大脑信号传导的关键作用。
经过为期20周的饮食方案,包括含有5%重量比来自芸豆(PTB)、黑眼豆(BEP)、扁豆(LEN)、鹰嘴豆(CKP)或菊糖纤维(INU)的抗性淀粉的西式饮食(实验组),与不含抗性淀粉的西式饮食(对照组),发现抗性淀粉特别是来自扁豆的抗性淀粉,可以改善西式饮食引起的认知障碍。
从机理上看,抗性淀粉通过改善肠道菌群-代谢组,包括增加短链脂肪酸和降低支链氨基酸水平,从而改善神经认知功能评估。这种肠道菌群-代谢物-大脑信号级联抑制了神经炎症、细胞衰老和血清瘦素/胰岛素水平,同时通过改善肝功能增强脂质代谢。总的来说,数据证明了抗性淀粉的益生菌效应可通过调节肠-脑轴改善神经认知功能。
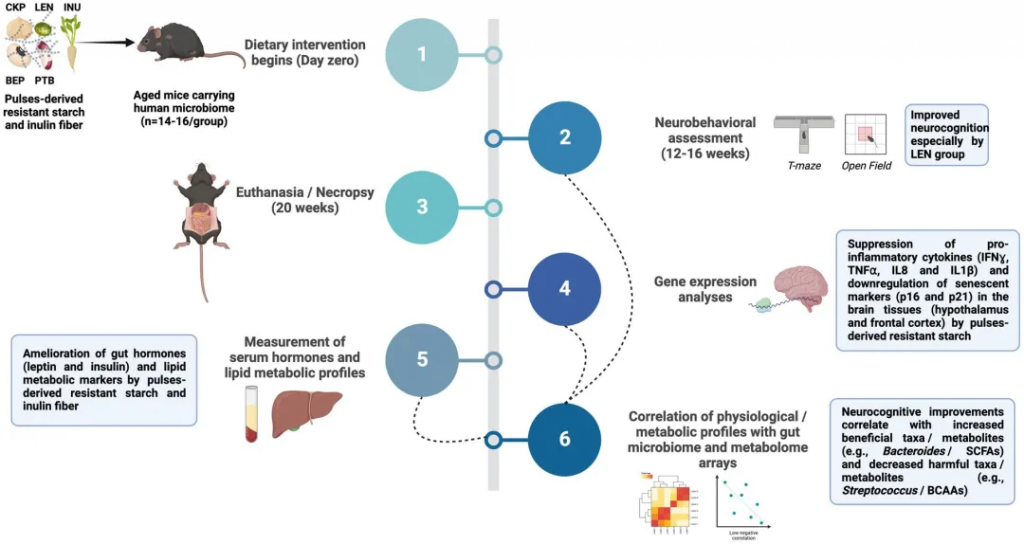
doi.org/10.3389/fnut.2024.1322201
溃疡性结肠炎是一种复杂的炎症性疾病,发病率不断上升。一项研究通过酶法分离方法从紫甘薯中获得抗性淀粉(PSPRS)。然后,研究了PSPRS的结构特性及其对葡聚糖硫酸钠诱导的结肠炎的保护功能。
结构表征结果表明,PSPRS的结晶度从CA型转变为A型,并且在酶水解过程中层状结构被完全破坏。与结肠炎小鼠相比,PSPRS给药以剂量依赖性方式显著改善病理表型和结肠炎症。
ELISA 结果表明,给予PSPRS的结肠炎小鼠表现出较高的 IL-10 和 IgA 水平,但较低的 TNF-α、IL-1β 和 IL-6 水平。同时,高剂量(300 mg/kg)的PSPRS显著增加了乙酸盐、丙酸盐和丁酸盐的产生。
16S rDNA高通量测序结果显示,PSPRS治疗组中厚壁菌门与拟杆菌门的比例以及潜在益生菌水平显著增加,如乳杆菌、Alloprevotella, 毛螺菌科_NK4A136_组、双歧杆菌。同时,高剂量 PSPRS 显著抑制了拟杆菌属、葡萄球菌属和阿克曼氏菌等有害细菌 (p < 0.05)。因此,PSPRS有潜力成为促进肠道健康、缓解溃疡性结肠炎的功能食品。
慢性肾病是与心血管疾病、发病率和死亡率风险增加相关的主要健康问题。最近的研究表明,慢性肾病的进展可能与肠道菌群的变化有关。抗性淀粉是一种膳食纤维,可以作为微生物发酵的底物。一些研究发现补充抗性淀粉可以改善慢性肾病患者的肠道菌群紊乱。
在 2022 年随机对照试验的荟萃分析中,发现补充抗性淀粉可以降低患有透析患者血液中硫酸吲哚酚、磷、IL-6和尿酸的水平。
抗性淀粉还对肠道环境产生有益影响,包括增加Ruminococcus bromide。
Ruminococcus brucei是厚壁菌门的主要成员之一,是一种主要的抗性淀粉发酵菌株。通过其针对抗性淀粉的特殊活性,Ruminococcus brucei从淀粉中释放能量以逃避宿主酶的消化。此外,摄入富含抗性淀粉的食物可以增加肠道短链脂肪酸水平,调节微生物代谢物,并改善葡萄糖稳态和胰岛素敏感性。
通过摄入抗性淀粉,胆固醇和甘油三酯降低,胰岛素敏感性提高,可以大大降低代谢综合征的发生率。慢性肾病患者也可能受益于更好的葡萄糖代谢、血脂水平和更好的体重管理。
近年来,富含抗性淀粉(RS)的食物因其多方面的健康益处而受到越来越多的关注,从肠道健康到调节全身新陈代谢。
益处
作为一种必需的膳食成分,抗性淀粉与典型的淀粉不同,主要是由于其对小肠消化的抵抗力,它基本上完好无损地到达大肠,在那里它作为微生物发酵的底物,产生有益的代谢物,如短链脂肪酸。
抗性淀粉中天然丰富的食物包括青香蕉、豆类、全谷物和某些类型的煮熟然后冷却的食物,如土豆和米饭。食用此类食物的好处之一是它们有可能增强血糖控制。富含抗性淀粉的食物具有较低的升糖指数,转化为较慢的餐后血糖升高。这一特性对患有糖尿病等代谢紊乱的人特别有益。此外,抗性淀粉发酵产生的短链脂肪酸,特别是丁酸盐,丁酸盐是结肠细胞的主要能量来源,并具有抗炎特性,使其对结肠健康不可或缺。
注意事项
抗性淀粉摄入量的快速和大量增加会导致胃肠道不适,包括腹胀、胀气和排便习惯改变。通常建议逐渐将富含抗性淀粉的食物引入饮食中,以使肠道微生物群有时间适应。此外,患有某些健康状况的人,例如患有肠易激综合征(IBS)或特定碳水化合物不耐受的人,应谨慎对待富含抗性淀粉的食物,并在专业指导下。抗性淀粉的发酵有时会加剧这些人的症状。
总之,虽然富含抗性淀粉的食物具有许多健康益处,尤其是在肠道健康和代谢调节方面,但个人应注意摄入饮食中的抗性淀粉的来源和数量。
最好取得平衡:优化健康益处,同时最大限度地减少潜在的不利影响。
抗性淀粉的作用超越了其个人益处,使其成为各种饮食模式和制度的关键成分。
地中海饮食
例如,当考虑因其保护心脏的益处而广受赞誉的地中海饮食时,我们发现豆类,抗性淀粉的天然来源,是其成分的基石。经常食用豆类,其丰富的抗性淀粉含量不仅有助于增强肠道健康,还有助于与这种饮食模式相关的心脏保护作用,因为抗性淀粉具有调节餐后血糖反应的潜力。
旧石器饮食
旧石器时代的饮食,俗称旧石器饮食,是另一个有趣的领域,其中抗性淀粉找到了相关性。对旧石器饮食的当代解释集中在块茎和某些根的消费上,当通过特定方法制备时,例如烹饪后冷却,这些根会富含抗性淀粉。这证实了我们的祖先可能已经消耗了大量的抗性淀粉,为他们的肠道微生物群提供了可发酵的底物。从理论上讲,肠道微生物与其宿主之间的共生关系已经共同进化了数千年,而抗性淀粉可能是推动这一进化过程的关键饮食元素。
低碳和生酮饮食
低碳水化合物和生酮饮食,在减肥和代谢健康方面很受欢迎,通常会限制淀粉的摄入。然而,将抗性淀粉整合到这些饮食中可以提供明显的优势。由于抗性淀粉不表现出与普通淀粉相同的消化率,因此它的加入不会显著提高血糖水平。这意味着这种饮食的人可以获得抗性淀粉的好处,例如增强肠道健康和饱腹感,而不会影响酮症或低碳水化合物方案的状态。从根本上说,抗性淀粉允许当代饮食方法之间的共生关系,重点是减肥或代谢益处,以及滋养肠道微生物群的古老进化重要性。
将抗性淀粉纳入饮食中不仅要承认其生理益处,还要了解其最佳摄入量并融入各种饮食中,以最大限度地发挥其潜力。随着越来越多的证据描绘抗性淀粉的多方面优势,从调节肠道微生物群到调节血糖水平,向更广泛的公众提供可操作的指南变得至关重要。
循序渐进
首先,身体可能需要一些时间来适应饮食中添加抗性淀粉。因此,需要循序渐进逐步添加。
添加少量抗性淀粉。例如,早餐中加入一根绿色香蕉,午餐中加入四分之一杯扁豆。
食物中获取
最好从食物中获取抗性淀粉,常见的食物补充包括:青香蕉、豆类(豌豆、扁豆)、全谷物(燕麦和大麦)、煮熟并冷却的米饭。
注:增加纤维摄入量时,要慢慢喝大量的水,以减少胃肠道副作用。

补充剂
补充性抗性淀粉通常以粉末形式服用,可混合到食品或饮料。如绿色香蕉粉、木薯粉等。
烹饪,可进一步提高抗性淀粉的含量
必须认识到并非所有抗性淀粉来源都是一样的。虽然豆类、全谷物和某些块茎天然富含抗性淀粉,但烹饪方法可以进一步调节其抗性淀粉含量。例如,烹饪然后冷却土豆或米饭等淀粉类食物可以增加其抗性淀粉含量,提供了一种直接的策略来提高饮食中的抗性淀粉水平,而无需任何剧烈变化。
抗性淀粉的推荐每日摄入量通常在 15-30 克之间。这可以通过多样化的饮食来实现,包括冷意大利面沙拉、隔夜燕麦或豆类菜肴等食物。
考虑个人的消化耐受性的重要性
抗性淀粉摄入量的突然激增会导致一些人的胃肠道不适。因此,谨慎的做法是在几周内逐渐增加抗性淀粉的摄入量,让肠道进行调整。此外,将富含抗性淀粉的食物与益生菌食物(如酸奶或开菲尔)相结合,可以产生协同效应,为有益的肠道细菌茁壮成长营造一个好的环境。与任何饮食改变一样,应根据个人口味、健康状况和饮食习惯定制抗性淀粉,确保方法既平衡又可持续。
抗性淀粉作为益生元可以调节肠道微生物群,对于肠道菌群失调相关的许多疾病包括炎症性肠病、肠易激综合征、结直肠癌等具有重要意义,为这些疾病辅助治疗的潜在用途奠定了基础。
抗性淀粉的另一个治疗意义在于其抗炎特性。慢性炎症在心血管疾病、2型糖尿病和某些癌症等多种疾病的发病和进展中发挥着关键作用。肠道微生物群发酵抗性淀粉会产生短链脂肪酸,尤其是具有抗炎作用的丁酸,可以抑制促炎细胞因子,使抗性淀粉成为减轻炎症引起的疾病的潜在候选者。
抗性淀粉也有望成为对抗肥胖和相关并发症的饮食策略。鉴于其调节饱腹感、提高胰岛素敏感性和调节脂质代谢的能力,抗性淀粉可以作为代谢综合征和相关病症的辅助或预防措施。例如,将抗性淀粉纳入饮食中可以改善糖耐量受损个体的餐后葡萄糖反应,强调其潜在的治疗相关性。
抗性淀粉在个性化营养方面的潜力也不容忽视,但仍需谨慎对待。剂量、持续时间和个体差异在决定抗性淀粉在任何治疗应用中的功效方面发挥着关键作用。
个体对抗性淀粉的反应可能存在很大差异。年龄、遗传、肠道微生物群组成和整体健康状况等因素会影响人们处理抗性淀粉摄入及益处。例如,摄入相同量抗性淀粉的两个人可能会表现出不同的餐后葡萄糖反应或结肠中不同的短链脂肪酸产生情况。此外,肠道微生物群将抗性淀粉发酵成有益代谢物的能力在个体之间可能有所不同,特别是在微生物群多样性高的人和微生物群较少的人之间差异较大。
这种个体差异突出了个性化营养方法的必要性。与其采取一刀切的抗性淀粉摄入建议,不如根据个人独特的代谢和菌群特征来定制饮食建议。随着深入探索个性化医疗时代,整合肠道菌群数据或许能为优化个人抗性淀粉摄入、获得健康效益提供更精准的建议。
主要参考文献:
Chen Z, Liang N, Zhang H, Li H, Guo J, Zhang Y, Chen Y, Wang Y, Shi N. Resistant starch and the gut microbiome: Exploring beneficial interactions and dietary impacts. Food Chem X. 2024 Jan 3;21:101118.
Li H, Zhang L, Li J, et al., Resistant starch intake facilitates weight loss in humans by reshaping the gut microbiota. Nat Metab. 2024 Mar;6(3):578-597.
Junejo SA, Flanagan BM, Zhang B, Dhital S. Starch structure and nutritional functionality – Past revelations and future prospects. Carbohydr Polym. 2022 Feb 1;277:118837.
Arp CG, Correa MJ, Ferrero C. Modified celluloses improve the proofing performance and quality of bread made with a high content of resistant starch. J Sci Food Agric. 2023 Apr;103(6):3041-3049.
Du X, Wu J, Gao C, Tan Q, Xu Y. Effects of Resistant Starch on Patients with Chronic Kidney Disease: A Systematic Review and Meta-Analysis. J Diabetes Res. 2022 Jul 18;2022:1861009.
Tekin T, Dincer E. Effect of resistant starch types as a prebiotic. Appl Microbiol Biotechnol. 2023 Feb;107(2-3):491-515.
Wang, Z.; Gao, M.; Kan, J.; Cheng, Q.; Chen, X.; Tang, C.; Chen, D.; Zong, S.; Jin, C. Resistant Starch from Purple Sweet Potatoes Alleviates Dextran Sulfate Sodium-Induced Colitis through Modulating the Homeostasis of the Gut Microbiota. Foods 2024, 13, 1028
Chen R, Zhang C, Xu F, Yu L, Tian F, Chen W, Zhai Q. Meta-analysis reveals gut microbiome and functional pathway alterations in response to resistant starch. Food Funct. 2023 Jun 6;14(11):5251-5263.
Kadyan S, Park G, Hochuli N, Miller K, Wang B, Nagpal R. Resistant starches from dietary pulses improve neurocognitive health via gut-microbiome-brain axis in aged mice. Front Nutr. 2024 Jan 24;11:1322201.
Pickens TL, Cockburn DW. Clostridium butyricum Prazmowski can degrade and utilize resistant starch via a set of synergistically acting enzymes. mSphere. 2024 Jan 30;9(1):e0056623.

谷禾健康
肥胖和代谢综合征在全球范围内日益流行,是21世纪人类健康面临的重大威胁之一。据世界卫生组织(WHO)全球数据估计,目前全球约13%(即近65亿)成年人口受肥胖症影响。

肥胖和代谢综合征对健康的危害包括增加患心血管疾病、糖尿病和高血压的风险,影响身体的免疫系统和内分泌系统,还可能导致肝脏疾病等。
更令人担忧的是,模型预测到2030年,约五分之一的成年人将患有肥胖症,这些数字突显了寻求新疗法的迫切需要,这些新疗法将独特地利用肥胖和代谢综合征背后的复杂途径来促进体重减轻以及代谢和免疫系统的调节。
“肥胖”是指身体过度脂肪堆积,超过正常范围的体重。通常是由于摄入热量过多,消耗热量不足导致的。同时肥胖患者还伴有慢性低度炎症,以及肠内分泌和神经激素的失调。
体重通过激素、神经和代谢途径之间复杂的相互作用进行调节,并受到许多环境因素的影响。能量摄入和支出之间的不平衡可能是由于多种因素造成的,包括饮食行为的改变、异常的饱腹感或饥饿感以及低能量支出。
目前主要有两种新兴的治疗方式:通过肠道微生物群和膳食纤维。肠道微生物群通过涉及粘膜和全身免疫、激素和神经系统的多种机制,深刻影响能量稳态的各个方面。
膳食纤维对新陈代谢和肥胖的益处也已通过机制研究和临床试验得到证明,在本文,我们讨论了不同纤维的理化特性、纤维和肠道微生物群如何相互作用以调节体重稳态的最新发现,以及与使用膳食纤维作为补充策略。
了解膳食纤维沿胃肠道的生理效应,包括肠道微生物群的作用,将支持开发利用微生物群和临床特征来预测个体对纤维补充反应的精准医学方法,用于调节免疫、代谢和体重稳态。随着临床前和临床研究继续探索膳食纤维能够促进哪些与健康相关的微生物群和代谢物,对这种纤维-微生物群的相互作用将为开发基于纤维的精准营养提供框架,以实现更优化、个性化的肥胖和代谢综合征相关治疗。
为了更好地预防和改善肥胖,我们需要先了解关于肥胖的一些知识。
✦ 肥胖患者肠内分泌和神经激素会失调
肥胖不仅仅是体重过高,其实是一种复杂的慢性进行性疾病,其特征是体内脂肪堆积过多以及肠内分泌和神经激素信号通路失调,从而增加食欲和能量储存。
✦ 肥胖还伴有慢性低度炎症
肥胖也被描述为一种慢性低度全身炎症,循环促炎细胞因子水平升高,对中枢神经系统(CNS)以及参与能量和代谢稳态的所有器官产生负面影响。
肥胖个体下丘脑尺寸的增加被认为是由于下丘脑炎症所致,这将加剧能量稳态失调。内脏脂肪组织和胃肠道失调似乎是全身炎症的主要原因。来自肥胖动物模型的大量证据支持肠道微生物群衍生的脂多糖数量增加通过增强细胞旁运动或通过乳糜微粒运输的跨细胞途径进入体循环的作用,从而启动许多炎症途径,进一步导致体重增加。
尽管来自人类研究的证据不如来自动物模型的结果清楚地表明肠道来源的脂多糖与肥胖之间的关联,但人体中的一些研究结果已将全身性脂多糖增加与肥胖联系起来,特别是与肥胖相关的代谢疾病风险。
此外,一些人类研究的结果表明,高水平的餐后内毒素血症先于2型糖尿病的发生,这表明存在潜在的致病作用。
在正常生理条件下,能量稳态通过调节饮食行为和能量储存的肠内分泌和神经激素信号通路受到严格控制。除了胰腺产生胰岛素和胰高血糖素之外,胃肠道和脂肪组织也会产生主要整合在下丘脑内的信号,以调节食物摄入和能量消耗。
✦ 肠内分泌激素有促食欲和抑制食欲两种作用
肠内分泌激素,由整个胃肠道中专门的肠内分泌细胞(EEC)响应营养和其他信号而释放。这些激素在胃肠道和远处器官中发挥局部作用,协调能量稳态的维持,包括饥饿、饱腹感、肠道屏障完整性、肠道转运、血糖控制和整体能量平衡。
肠内分泌激素的功能可根据其促食欲(刺激食欲)和厌食(抑制食欲)特性大致分类。胆囊收缩素(CCK)、肽 YY(PYY)、胰高血糖素样肽1(GLP1)、葡萄糖依赖性促胰岛素多肽(GIP)和胃泌酸调节素是主要由小肠EEC产生并在餐后释放以诱导饱腹感和减少食物的摄入。
从胃中释放的生长激素释放肽和从结肠中的EEC释放的胰岛素样因子5(INSL5)充当促食欲信号。瘦素和脂联素从脂肪组织中释放,也有助于调节饮食行为和能量稳态。
主要肠道激素及其对能量稳态的影响


Deehan EC,et al.Nat Rev Gastroenterol Hepatol.2024
✦ 进食速度和食物适口性也会影响能量摄入
然而,肠道源性食欲激素的水平并不一定与能量摄入相关;此外,一些研究表明,人类对急性饮食的激素反应并未表现出对常量营养素摄入量长期差异的实质性适应。这些发现表明,其他因素,例如食物能量密度和食物摄入速度以及食物的适口性,可能会增加人类的能量摄入。
✦ 中枢神经系统调节饥饿、饱腹感和能量储存
中枢神经系统是多种肠道源性激素的重要作用部位,也是通过整合涉及自主下丘脑回路、皮质执行回路和皮质边缘奖励通路的大脑网络来调节饥饿、饱腹感和能量储存的中枢调节器。
下丘脑的弓状核内有两个独立且相对的神经元群:促食欲NPY-AgRP神经元和促厌食POMC-CART神经元。
NPY-AgRP神经元被能量不足和信号(如生长激素释放肽)激活,以刺激食物摄入,并被胃肠道中营养物质的存在和饱足信号(如CCK和PYY)抑制。相比之下,瘦素等信号激活POMC-CART神经元会抑制进食,并由于释放与大脑黑皮质素受体结合的α-黑素细胞刺激激素而改变葡萄糖代谢。
✦ 肥胖患者的能量信号受损导致易暴饮暴食
有证据表明,肥胖成人中营养信号的受损会导致暴饮暴食和肥胖。在一项针对健康体重个体和肥胖个体的单盲、随机、对照交叉研究中,结果显示,肥胖个体在大脑对摄入营养素的反应中表现出整体和营养特异性受损。因此肠道和脂肪源性激素以及中枢神经系统共同是能量稳态治疗操纵的基本目标。
过去二十年的研究表明,肥胖代谢特征的特征是人类血清胆囊收缩素、胰岛淀粉样多肽、胃饥饿素、INSL5和胰岛素水平升高,同时瘦素、GLP1和PYY水平降低。
重要的是,这些血浆激素水平被发现随着减肥手术后肥胖的解决而恢复正常,从而强调了它们作为关键治疗靶点的作用。
✦ 激素药物的疗法会受到胃肠道耐受性的影响
针对肥胖的内源性神经分泌机制的药物是治疗肥胖和代谢综合征最有效的长期药物疗法。GLP1激动剂(索马鲁肽、利拉鲁肽和西他列汀)已被证明对持续减肥和改善心脏代谢功能具有良好功效。
使用作用于GIP、GLP1或胰高血糖素受体的双重和三重激素受体激动剂的临床试验已显示出在减肥和改善代谢参数方面的卓越功效。
然而,这些基于肠降血糖素的疗法的使用目前受到高成本、有限的医疗保健覆盖范围和胃肠道耐受性问题的限制。此外,人们还担心这些药物对肠道功能的长期影响。
✦ 基于饮食的疗法将是未来的趋势
由于这些限制,人们越来越有兴趣开发替代性肠促胰岛素靶向疗法,特别是基于饮食的方法,通过使肠促胰岛素激素(如GLP1和GIP)水平正常化来治疗肥胖并预防肥胖相关代谢功能障碍的发生。
在动物模型和人类中进行的大量研究表明膳食纤维摄入对宿主代谢和减肥有好处,因此增加膳食纤维摄入量作为一种基于饮食的肥胖疗法已引起广泛关注。
膳食纤维是碳水化合物的一种聚合物,主要存在于植物食物中,可抵抗哺乳动物基因组中编码的酶的消化;它们到达近端结肠,在其中经历肠道微生物群不同速率和程度的糖分解发酵。
✦ 目前大部分人群膳食纤维摄入不足
膳食纤维的生理益处多种多样,取决于其理化特性和摄入量,膳食纤维的推荐膳食摄入量为每1000kcal 14克(成年女性每天25克,成年男性每天38克)。然而,目前大部分人群通常每天摄入的纤维少于15克,即推荐量的一半左右。
✦ 肠道微生物在纤维代谢促进健康中起重要作用
几项大型前瞻性研究已经证明了纤维消耗与代谢健康之间的关联,目前的工作强调了肠道微生物群在将膳食纤维摄入与有益效果联系起来。
越来越多的证据表明,肠道微生物群通过涉及免疫、激素和神经系统影响的多种机制,深刻影响能量稳态的各个方面,并且肠道菌群失调或肠道微生物类群的异常组成可能会导致能量代谢紊乱并对脂肪组织、肌肉和肝脏造成影响。
肠道微生物群发酵纤维会释放出多种代谢物,包括短链脂肪酸、酚类和吲哚化合物、支链脂肪酸、乳酸、琥珀酸和各种气体(氢气、二氧化碳、甲烷、一氧化氮和含硫化合物)。
肠道微生物产生代谢物的途径和前体对饮食摄入具有高度适应性;因此,通过特定的饮食干预措施(例如膳食纤维)来针对微生物代谢是改善代谢功能障碍和肥胖的关键因素。
短链脂肪酸是通过微生物可接触的膳食纤维发酵产生的主要代谢物,人体肠腔中主要短链脂肪酸的相对比约为乙酸盐(60):丙酸盐(20):丁酸盐(20)。
短链脂肪酸可以通过与G蛋白偶联受体相互作用并抑制组蛋白脱乙酰化来介导多种局部和外周效应,从而导致基因表达的表观遗传调节变化。
丁酸盐在结肠中被结肠细胞用作能量来源,而丙酸盐和乙酸盐通过门静脉吸收到肝脏,其中丙酸盐主要用作糖异生和脂肪生成的底物;相反,乙酸盐以更高的量进入体循环。
✦ 短链脂肪酸影响激素分泌从而改善葡萄糖代谢
除了纤维对胃排空和抑制消化的影响已得到充分证明外,增加饮食中的纤维含量可能会通过产生短链脂肪酸来帮助减肥和葡萄糖代谢。
大量体外和小鼠研究表明,短链脂肪酸通过G蛋白偶联受体GPR41和GPR43(也称为FFAR3和FFAR2)直接刺激肠道肠内分泌细胞分泌胰高血糖素样肽-1(GLP-1)和肽YY(PYY)。
体内研究表明,急性直肠输注醋酸盐或短链脂肪酸混合物会增加PYY和GLP1的全身水平。此外,一项人体研究表明,与单独使用菊粉相比,在20名健康成年人中,急性口服菊粉丙酸盐会增加全身PYY和GLP1的水平,并减少食物摄入量,这表明丙酸盐水平增加在调节血糖新陈代谢方面发挥着作用。
✦ 短链脂肪酸影响神经系统抑制食欲和能量摄入
短链脂肪酸还可以直接与肠神经系统相互作用,从而允许肠道来源的短链脂肪酸向大脑直接发出信号。小鼠研究表明,短链脂肪酸给药可通过中枢神经系统相关机制抑制食欲和能量摄入。
此外,体外和小鼠研究表明,短链脂肪酸可以通过多种机制增强血脑屏障,包括减少氧化和促炎途径以及增加紧密连接蛋白。
在小鼠研究中,乙酸盐和丁酸盐已被证明可以穿过血脑屏障并刺激迷走神经和下丘脑,从而调节食物摄入量和饱腹感。使用功能性磁共振成像的人体研究表明,结肠丙酸盐输送减少了与食物渴望相关的大脑区域的活动,并减少了食物摄入量。
需要注意的是,尽管在人脑和脑脊液中发现了可测量浓度的短链脂肪酸,但人脑对循环短链脂肪酸的摄取似乎有限,这表明一些记录在案的循环短链脂肪酸对大脑活动的影响可能是这是由于短链脂肪酸诱导的与免疫和内分泌系统的相互作用,而不是大脑内的直接相互作用。
短链脂肪酸对能量稳态的作用机制
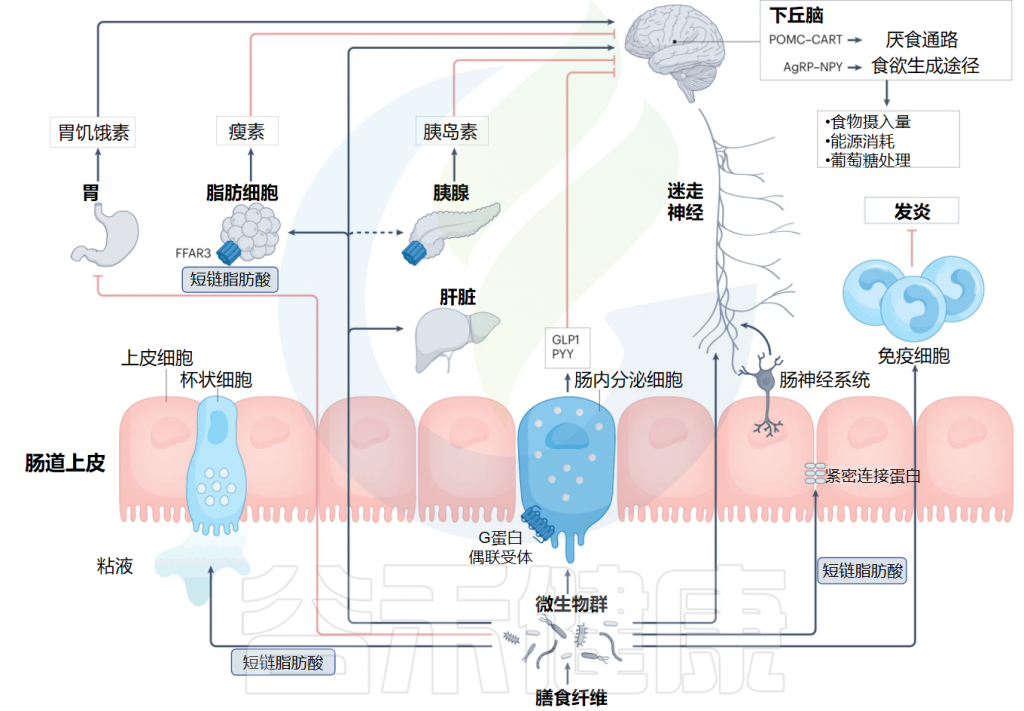
Deehan EC,et al.Nat Rev Gastroenterol Hepatol.2024
✦ 短链脂肪酸影响脂肪的分解和积累
在培养的小鼠和人类脂肪细胞中,乙酸盐和丙酸盐已被证明能够以G蛋白偶联受体依赖性方式促进脂肪分解并抑制脂肪生成,从而可能减少非脂肪组织和脂肪组织中的全身脂质循环和脂肪积累,同时还提高胰岛素敏感性。
在人类研究中,短链脂肪酸的直肠给药已证明可以促进全身脂肪分解,并且在体外培养的人类脂肪细胞中,短链脂肪酸也已被证明可以刺激瘦素分泌。短链脂肪酸还可以减少人类外植体脂肪组织的促炎细胞因子分泌,因此可能有助于减少与肥胖相关的全身低度炎症。
注意:仍然存在一些不确定性
然而,尽管大量工作支持短链脂肪酸在调节体重增加和宿主代谢方面具有潜在的有益作用,但该领域关于短链脂肪酸在肥胖中的作用仍然存在很大的不确定性,因为许多影响主要体现在小鼠模型无法在人类研究中复制。
事实上,据报道短链脂肪酸水平升高和降低都与肥胖有关。然而,大多数人类研究测量粪便样本中的 短链脂肪酸,这反映了生产、吸收和利用的净结果,并不一定反映可能更相关的全身水平。
为了支持这一观点,对160名BMI在19.2 kg/m2至41kg/m2且葡萄糖代谢正常或受损的参与者进行的横断面研究中证明,全身短链脂肪酸水平与空腹甘油呈负相关。三酰甘油和游离脂肪酸,与空腹GLP1呈正相关,而粪便水平与这些参数均无关联。此外还发现循环醋酸盐与胰岛素敏感性之间呈负相关,而丙酸盐与胰岛素敏感性呈正相关。
总体而言,研究短链脂肪酸对宿主代谢的生理影响的可用人体体内数据仍然有限。由于纤维、肠道微生物群和人体新陈代谢之间相互作用的复杂性,目前尚不清楚增加纤维摄入量的有益影响是由于微生物代谢和某些代谢物(例如短链脂肪酸)的产生或其他有据可查的影响而产生的纤维的变化,包括运输时间、营养吸收或粪便膨胀和结合的改变。
除了短链脂肪酸之外,肠道微生物群还在膳食纤维发酵过程中产生乳酸和琥珀酸,然而,这些代谢物通常被认为是微生物生产短链脂肪酸的中间体。
✦ 肥胖和代谢综合征患者乳酸和琥珀酸含量增加
乳酸和琥珀酸以低浓度存在于血液和组织中,与没有肥胖的人相比,在肥胖和代谢综合征患者中检测到的水平有所增加。乳酸是宿主衍生的葡萄糖代谢产物,当糖酵解通量超过线粒体氧化时,血液中的乳酸会增加。
✦ 乳酸可能作为活性信号分子减少促炎反应
因此,乳酸可以被认为是葡萄糖代谢受损的生物标志物。此外,体外和小鼠研究表明,乳酸可以作为活性信号分子,调节脂肪细胞功能和代谢,并通过GPR81依赖性和非GPR81依赖性来减少脂肪组织和免疫细胞功能中的促炎症反应。
由于这些有益的发现,有人建议通过增加纤维摄入量和由此产生的乳酸产量来靶向GPR81可能代表肥胖和代谢紊乱的新治疗靶点。
✦ 琥珀酸作为代谢稳态的一种信号分子
尽管琥珀酸传统上被认为是三羧酸循环的代谢物,但目前的研究已证明琥珀酸可作为参与应激和组织损伤的代谢信号。
肠腔中琥珀酸含量较低,但对小鼠的研究发现,细胞外琥珀酸的浓度随着纤维摄入量的增加而增加。琥珀酸可以通过与几种不同细胞类型(包括脂肪细胞和免疫细胞)上的琥珀酸受体1(SUCNR1;也称为GPR91)结合而充当信号分子。
在人类中,横断面研究报告称,血浆琥珀酸水平、肥胖和葡萄糖代谢损伤之间存在负相关。据报道,琥珀酸还可以充当生热激活剂和褐变剂,并且对脂肪分解具有影响。
一项使用脂肪细胞特异性Sucnr1敲除小鼠和从肥胖人群中分离出的人类脂肪细胞的研究发现,通过与SUCNR1相互作用调节脂肪细胞中的生物钟和瘦素表达,琥珀酸诱导的代谢效应具有新功能。
✦ 琥珀酸可能有助于解释代谢与炎症之间的联系
还有强有力的证据表明琥珀酸-SUCNR1信号传导可以充当代谢应激和炎症之间的联系。
利用人类原代巨噬细胞证明,细胞外琥珀酸可以诱导巨噬细胞产生抗炎作用。有趣的是,肥胖与全身琥珀酸水平高有关,但脂肪组织驻留巨噬细胞中琥珀酸受体的表达减少,这可能有助于解释为什么肥胖患者往往无法控制炎症。
在小鼠模型中,研究表明,肠道微生物群响应补充低聚果糖 的饮食而产生的琥珀酸增加,通过充当肠道糖异生的底物并随后减少肝脏葡萄糖的产生来改善血糖控制和能量代谢。
随着越来越多的研究检查琥珀酸诱导的生理效应,它可能有助于阐明细胞外琥珀酸的作用及其在调节宿主代谢中的局部和全身作用模式以及如何最好地针对这些途径。
✦ 微生物发酵膳食纤维产生的气体会导致一些胃肠道症状
膳食纤维经微生物发酵还会进一步产生H2、CO2和CH4等气体。然而,纤维发酵过程中气体产量的增加可能会引起不良症状,并且是个体不耐受高水平纤维的主要原因之一。
因此,还需要进行更多研究来增加肠道气体对宿主生理和代谢影响的了解,使用纤维和大量营养素的饮食控制来减轻患有与产气相关的胃肠道疾病的患者症状。
了解膳食纤维在胃肠道中的生理效应机制,包括其与肠道微生物群的作用,将有助于开发基于膳食纤维的补充策略,以调节免疫、代谢和体重稳态。
所有膳食纤维的共同特征是它们的低聚或多聚碳水化合物结构可抵抗小肠的消化,并且如果分离和合成,则对人类健康显示出生理益处。然而,纤维之间的化学和物理结构以及理化特性存在巨大的异质性。
常见分离和合成的商业膳食纤维
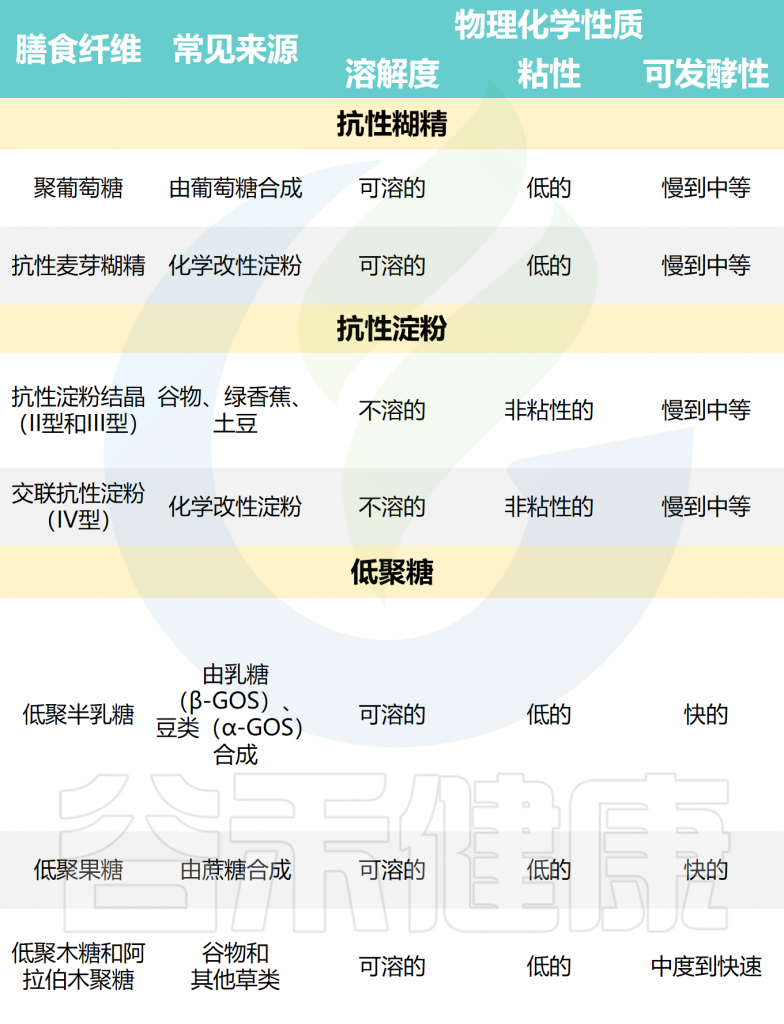

Deehan EC,et al.Nat Rev Gastroenterol Hepatol.2024
✦ 膳食纤维的差异会影响其对人体的作用
具有较长、无支链的线性碳水化合物结构(如纤维素)通常不溶于水性溶剂,阻碍了人类肠道微生物群对其进行发酵,使较少的微生物能够接触到这种结构。
相比之下,具有混合连接或支链的低聚合物和聚合物通常可溶于水,更容易被肠道微生物接近。因此,随着聚合度的增加,可溶性纤维倾向于将水和其他化合物截留在聚合物内和聚合物之间,从而以浓度依赖性方式增加粘度。分子量也会影响微生物的发酵和短链脂肪酸生产速率;然而,分子量与发酵之间的关系取决于纤维结构,且不一定是线性的。
尽管纤维通常根据物理化学性质(例如溶解度、粘度、结合能力或发酵性)进行分类,但这种分类并不能反映离散纤维结构所表现出的全部性质。
例如,来自高粱或稻米等草类的阿拉伯木聚糖低聚物或简单结构的聚合物很容易发酵,而复杂结构的阿拉伯木聚糖要么在整个结肠中缓慢发酵,要么很难被人类肠道微生物群作用。
因此,了解纤维的结构和理化特性,尤其是分离或合成后的纤维,对于更精确地应用纤维来治疗肥胖至关重要。
膳食纤维的理化特性影响它们在胃肠道中的作用,从而决定它们对炎症、代谢和能量稳态的影响。
✦ 粘性纤维和较大纤维会增加饱腹感并减少摄入
从口腔开始,粘性纤维和大纤维颗粒(如谷类麸皮)可以通过获得更坚硬和耐嚼的食物基质来延长咀嚼和口腔感官暴露,从而改变内分泌相对饱腹感的反应并减少能量摄入。
当食品应用中热量密集的糖和脂肪减少时,菊粉、低聚果糖和微纤丝纤维等纤维也可以保持感官特性(如甜味和口感)。天然食品中的纤维基质进一步充当唾液淀粉酶等消化酶的屏障。咀嚼过程中这些三维植物细胞壁结构的维持影响细胞内成分(如淀粉)沿胃肠道的生物利用度。
增加食糜粘度的纤维,例如较高分子量的混合连接或支化聚合物和微纤丝纤维,可促进胃扩张并延迟胃排空。小肠腔内增加的食糜粘度通过限制营养物质向粘膜扩散和内源性消化酶的活性进一步延迟营养物质吸收,这通过触发回肠破裂进一步减慢近端胃肠传输。
✦ 纤维结构影响脂质的吸收和利用率
除了粘度之外,某些纤维结构还可以结合或捕获化合物,例如常量营养素和微量营养素、酚类和胆汁酸,从而延迟或阻止小肠吸收。胆汁酸与膳食纤维的结合会干扰胆汁酸的肠肝循环并阻碍胶束形成,从而减少脂质的吸收和利用率。
此外,增加纤维结合胆汁酸向大肠的输送可能会导致微生物胆汁盐水解酶和 7α-脱羟酶将初级胆汁酸转化为次级胆汁酸。对人类和小鼠的研究以及使用分离的人类胰岛和哺乳动物培养细胞的体外实验表明,这些次级胆汁酸通过多种膜和核受体(包括G蛋白偶联胆汁酸受体(TGR5)和法尼醇X受体,导致饱腹感增加、肝糖原合成、肝脏、棕色脂肪和肌肉组织中的胰岛素分泌和能量消耗。
一项针对肥胖和2型糖尿病患者(n=23)的研究证明,将结合胆汁酸输送到回结肠区域可降低餐后血糖和空腹胰岛素水平,并增加GLP1分泌,这支持了胆汁酸在葡萄糖代谢中的作用。
✦ 膳食纤维会影响小肠对营养的反应
尽管了解甚少,但膳食纤维可能会进一步改变驻留的小肠微生物群,在大鼠模型中显示这种相互作用会影响小肠营养感应,特别是低聚果糖诱导的脂质感应,从而促进肠内分泌细胞(EEC)释放GLP1以增加饱腹感。
在培养细胞、动物模型和人类中进行的大量工作也表明微生物代谢物与胃肠道味觉受体表达和活性的改变有关,从而导致味觉偏好和食物摄入的改变。
最后,所有膳食纤维,无论是天然存在的、分离的还是合成的,都可以通过简单地用不可消化的碳水化合物代替一部分可消化的化合物来减少能量摄入,这与能够在不改变感官特性的情况下在食物中实现更高水平的较低粘性纤维相关。
总体而言,小肠的营养吸收率受到结构依赖性的影响,增加了纤维消耗的阻碍。这有助于促进饱腹感,减弱餐后血糖、血脂和炎症反应,而这些反应通常在肥胖症中失调。
纤维摄入量的增加相当于未吸收的营养物质增加,这些营养物质到达近端结肠并可供人体肠道微生物群利用。
膳食纤维对胃肠道的生理影响
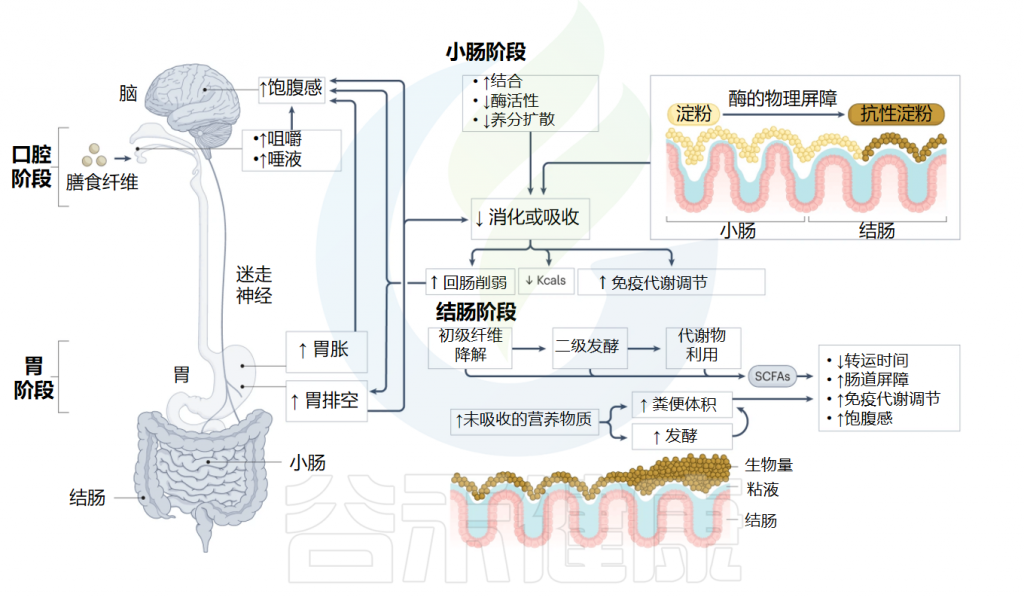
Deehan EC,et al.Nat Rev Gastroenterol Hepatol.2024
✦ 微生物对膳食纤维作用改善排便和减轻炎症
与小肠中的化合物结合的纤维进一步在结肠中被作用,使底物和其他生长因子接近利用它们的特定微生物。肠道微生物群对发酵缓慢或发酵不良的化学和物理结构,如大纤维颗粒、纤维素或车前草,通过刺激蠕动、粘膜分泌和抑制水的重吸收来提供其他胃肠道益处,这已被证明可以增加体积和软化人类粪便。
这些纤维通过抑制微生物发酵可能减少结肠转运时间,促进结合化合物的排泄并减轻全身炎症。尽管可发酵纤维还可以通过增加微生物生物量以及产生短链脂肪酸和气体来影响结肠转运时间,但纤维发酵的主要生理效应归因于假定有益微生物的结构特异性扩张以及随后结肠内短链脂肪酸和其他代谢物的产生。
✦ 富含膳食纤维的饮食使肠道微生物群更丰富
纤维到达结肠时会引发微生物群落内复杂的交互作用,这些群落共同获取、降解和利用代谢产物,最终丰富了成员多样性。
初级降解和次级发酵释放短链脂肪酸、气体和其他代谢产物,被代谢物利用者进一步转化,影响与结肠细胞的相互作用。
消耗可发酵纤维支持多种微生物群成员,解释了纤维结构多样的饮食与多样化微生物群的关联,这是健康肠道微生物组的特征。
结肠中成员的富集和代谢产物的促进取决于纤维结构、个体群落和生态因素,如结肠微环境。研究表明,特定饮食可增加能量利用,降低脂肪含量,并提高胰高血糖素样肽-1(GLP-1),而食物摄入量无显著变化。
✦ 复杂结构的膳食纤维增加结肠远端的短链脂肪酸产量对代谢有利
尽管纤维发酵过程中微生物群落产生的副产物主要发生在结肠近端,但通过消耗具有结晶或复杂结构的纤维可以减慢发酵速率,从而减轻肠道气体的产生并将短链脂肪酸输出转移到远端。
研究表明,增加短链脂肪酸远端产量可通过上调PYY和GLP1等肠内分泌激素,对人类的饱腹感、血糖和能量代谢产生有利影响。
事实上,在肥胖男性中,远端结肠中施用的醋酸盐增加了脂肪氧化和循环PYY;然而,当在近端结肠中施用醋酸盐时,没有看到效果。尽管向增加脂肪氧化和PYY产生的转变意味着有利的能量代谢,但仍需要进一步研究来确定是否可以通过增加远端结肠中纤维发酵和短链脂肪酸的产生来减少体重和肥胖。
✦ 远端结肠可能是未来治疗肥胖的靶点
糖分解发酵向远端结肠的扩展和延伸进一步减少了膳食和粘膜蛋白质的发酵。蛋白水解发酵的抑制部分是由于肠道微生物对碳水化合物而非氨基酸的普遍偏好,以及乳酸和纤维发酵过程中结肠pH值降低抑制蛋白水解酶。
人类蛋白水解发酵的减少可能会随后降低被认为有害和促炎的病原体(例如脱硫弧菌)和代谢物(例如氨或对甲酚)的水平。纤维和蛋白质发酵之间的平衡已在人类身上得到证实,因为增加抗性淀粉的剂量以及将饮食模式从高蛋白、低碳水化合物转变为体重维持饮食已被证明可以增加粪便中的短链脂肪酸并减少支链脂肪酸,支链氨基酸发酵产生的代谢物。
促进结肠中短链脂肪酸的产生可能会通过刺激粘液分泌、上调紧密连接蛋白、增加抗菌肽浓度和调节结肠上皮增殖来增强胃肠道屏障完整性,共同减轻细菌脂多糖的易位和随之而来的代谢性内毒素血症。总之,这些结果支持将远端结肠作为控制肥胖的治疗靶点。
除了膳食纤维结构之外,还有一些生态因素会影响纤维发酵过程中促进健康相关的微生物和代谢物的产生。
✦ 结肠转运时间影响微生物群和宿主代谢
结肠转运时间被认为是影响肠道微生物群和宿主代谢的关键因素,转运时间较慢与纤维发酵速率降低和短链脂肪酸减少、远端结肠pH值和蛋白水解发酵增加以及肠道对粪便能量的回收减少。
体外实验进一步表明,结肠pH值的降低可通过选择对酸敏感的微生物(如拟杆菌)来塑造参与纤维结构发酵的独特微生物群落。由于参与结肠纤维发酵的大多数共生微生物是专性厌氧菌,因此如在炎症中观察到的那样,结肠微环境中氧浓度的增加,也通过支持耐氧微生物(例如大肠杆菌)的大量繁殖来形成特殊菌群成员。
✦ 不同人群对补充膳食纤维会产生个性化反应
由于生态因素影响微生物对膳食纤维的个体化反应,因此在实施基于可发酵纤维的治疗策略来预防和治疗肥胖和代谢综合征时,需要从个人生态角度出发。
据报道,纤维引起的肠道微生物群变化仅限于少数主要反应类群,而其余成员和代谢副产物则发生更多个性化变化。
例如,数十年的人类研究证实,低聚果糖和低聚半乳糖等益生元寡糖可通过选择性促进经常用作益生菌的乳酸菌和双歧杆菌来增加乳酸和乙酸,从而为人类带来健康益处。
丁酸盐生产菌
体外研究还表明,厌氧丁酸菌、真杆菌、粪杆菌等丁酸盐生产菌可以通过乳酸和乙酸的交叉喂养或通过利用抗结晶淀粉、木聚糖和菊粉等底物来富集。
丙酸盐生产菌
另外,丙酸盐生产者,如拟杆菌属、副拟杆菌属、葡萄杆菌属和韦荣球菌属,可以通过交叉饲喂乳酸和琥珀酸盐或通过降解底物(如酯化抗性淀粉、果胶和木聚糖)来富集。
下一代益生菌
下一代益生菌有望改善患有肥胖和代谢综合征的成年人的代谢,其中包括Akkermansia muciniphila或Anaerobutyricum soehngenii ,这两种细菌已被证明可以通过补充纤维来丰富。
小结
因此,可发酵膳食纤维可用于选择性地扩大肠道微生物群内与健康相关的类群。然而,仍需要进行更多研究来阐明与肥胖和代谢功能障碍有因果关系的其他共生微生物和代谢物,并可通过选择膳食纤维来靶向。
肠脑轴连接肠道和中枢神经系统,促进双向通讯。这一过程牵涉到肠神经系统、迷走神经、内源性大麻素系统以及神经免疫和神经内分泌通路。
肠道代谢产物可直接调节神经系统活动,通过作用于肠神经元、迷走神经和交感神经末梢,或者经体循环传输至大脑。
★ 肠道微生物产生的多种神经递质会影响食欲
此外,肠道微生物还产生多种神经递质,如血清素、多巴胺、乙酰胆碱和GABA(γ-氨基丁酸),这些物质通过迷走神经在肠神经系统或中枢神经系统内发挥作用。一项小鼠研究指出,细菌肽聚糖片段与大脑下丘脑神经元上的NOD2相互作用,调节食物消耗和体温,进而影响食欲。
研究者还发现,从肥胖小鼠体内提取的微生物移植到瘦小鼠体内,可影响大脑奖励系统,与微生物代谢产物3-3′-羟苯基丙酸存在因果关系,影响多巴胺能和阿片类标记物,进而调节食欲行为和动机。进一步分析显示,嗜黏蛋白阿克曼菌(Akkermansia)、Muribaculum、普雷沃氏菌(Prevotellaceae)和副拟杆菌(Parabacteroides)的水平与3-3′-羟苯基丙酸血浆水平相关。
肥胖症中微生物群与肠道之间的相互作用
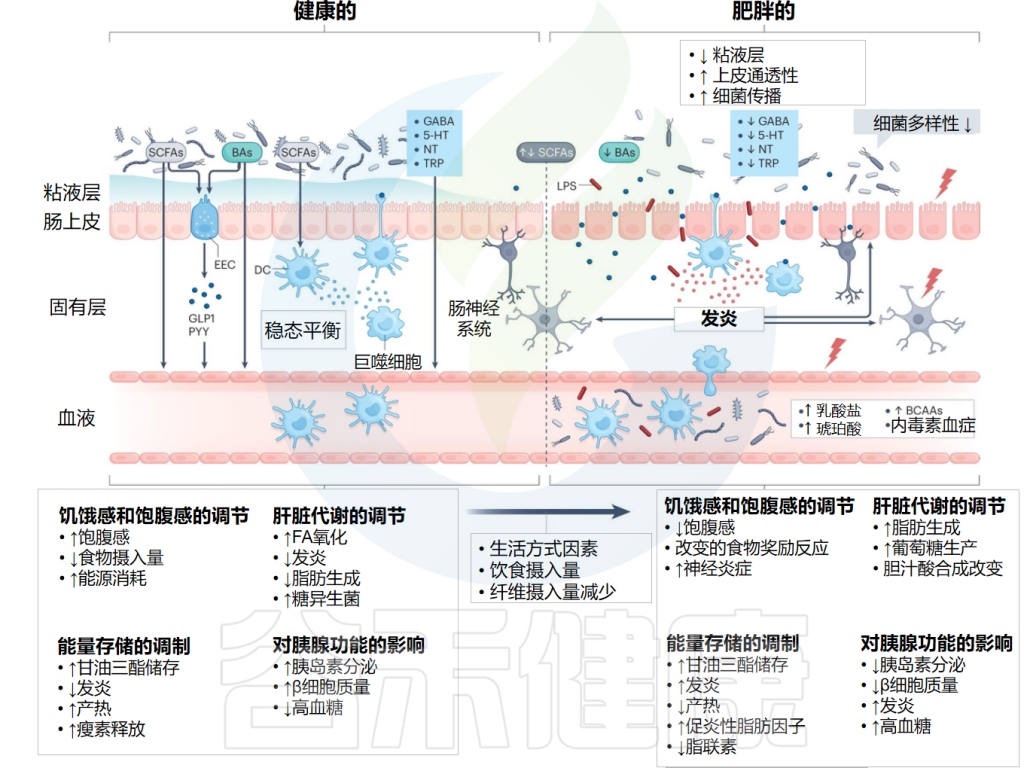
Deehan EC,et al.Nat Rev Gastroenterol Hepatol.2024
这些研究共同表明,肠道微生物群与宿主相互作用,通过不同的自主神经和体细胞神经内分泌途径改变新陈代谢,并且肥胖患者的这些相互作用发生了实质性改变。实际上,每个途径都代表了可以通过饮食干预(例如增加纤维摄入量)进行调节的潜在途径。
扩展阅读:
治疗肥胖症的精准医学方法是通过个性化的诊断和治疗方案来帮助患者减肥和改善健康状况。这种方法结合了先进的科学技术和专业知识,以确保每位患者都能得到最有效的治疗。
通过精准医学方法,医生可以根据患者的基因、生活方式、肠道微生物群和其他因素制定个性化的治疗计划,从而更好地管理和治疗肥胖。
对于减肥饮食干预的反应存在着高度的个体差异,这种差异可以归因于多种因素,包括遗传背景、微生物群组成以及生活方式因素(如进餐时间、睡眠、锻炼和昼夜节律)。为了实现减肥效果,需要确定影响个体对饮食干预反应的关键因素,并制定个性化的营养策略。
✦ 肠道微生物群是预测减肥效果的良好指标
研究表明,基线微生物宏基因组谱,尤其是与纤维降解相关的几个基因的存在,与随后的体重减轻密切相关。在一项为期6个月的减重研究中,研究人员发现,个体的肠道微生物群是预测体重减轻效果的一项重要指标。
特定的肠道细菌,如布劳特氏菌(Blautia wexlerae)和多氏拟杆菌(Bacteroides dorei),在含量丰富的个体往往能更好地预测体重减轻效果。
此外,体重减轻与活泼瘤胃球菌(Ruminococcus gnavus)、马赛拟杆菌(Bacteroides Massiliensis)和芬氏拟杆菌(Bacteroides Finegoldii)相关。
✦ 具有高发酵肠道微生物水平时增加纤维摄入有利于减肥
这些微生物群,如阿克曼氏菌和普雷沃氏菌,由于其处理植物来源复杂纤维的能力,与富含纤维的饮食密切相关。相比之下,食用低纤维饮食的个体通常具有更高水平的拟杆菌;而食用高纤维饮食的人群普雷沃氏菌更丰富。在人类减肥试验中,与普雷沃氏菌水平较高的个体相比,以拟杆菌为主的个体在摄入富含纤维的饮食时通常不太可能减肥或维持体重减轻效果。
这些发现表明,高水平发酵代谢的肠道微生物群(如普雷沃氏菌)可能更有利于减肥,尤其是在增加纤维摄入量时。
最后,试验(n=1002)的数据显示,肠道微生物群组成是餐后脂质和血糖反应,以及空腹心血管代谢标志物的良好预测因子。然而,必须指出的是,肠道微生物群组成仅解释了餐后甘油三酯、葡萄糖和C肽升高的5-7%变化,其他因素也在其中起作用。
将基于精准医学的方法应用于肥胖和代谢紊乱的另一种方法是根据个体的潜在病理生理学和行为特征使用针对表型的干预措施。
肥胖表型通常可分为四类:异常饱腹感、异常餐后饱腹感、情绪性进食和异常静息能量消耗。针对每种表型进行了可行性试验,比如通过使高纤维饱腹感异常的个体饮食,可以关闭大脑饥饿中枢并实现最大的胃扩张。支持这一概念的是,与接受标准治疗的参与者相比,接受表型定制生活方式干预的参与者减重更多,代谢和临床参数改善更显著。
✦ 根据不同表型采取饮食会有更好的效果
在一项为期12周的饮食干预试验中,患有肌肉胰岛素抵抗或肝脏胰岛素抵抗的人被随机分配到高单不饱和脂肪酸饮食或低脂肪、高蛋白和高纤维饮食。具有肌肉胰岛素抵抗的个体(n =149)在食用低脂肪、高蛋白和高纤维饮食时代谢参数有更多改善,而具有肝脏胰岛素抵抗的个体食用高单不饱和饮食时,肝脏胰岛素抵抗(n=93)有更大的改善。
需要注意的是,另一种基于代谢表型的方法根据CORDIOPREV-DIAB试验显示出相互矛盾的结果。可能是由于研究人群的差异或饮食干预措施的组成差异造成的,说明了基于某些表型设计精准饮食干预措施的还存在一些挑战。
通过营养干预进行个性化葡萄糖优化研究旨在测试这种通过根据组织特异性胰岛素抵抗表型调节膳食营养素含量来改善葡萄糖稳态参数和心脏代谢健康的方法。
尽管开发个性化营养干预措施存在相关的挑战,但这些原理验证研究总体上支持使用基于生物和表型因素开发个性化饮食干预措施的基本概念。
此外,了解肠道微生物及其基因途径如何与饮食成分相互作用可能有助于设计更有效的个性化疗法,并有可能提高饮食干预减肥的成功率。
膳食纤维的结构和理化多样性为开发基于纤维的策略提供了潜力,还能从一定程度上改善肥胖和代谢综合征药物和手术疗法。
富含纤维的天然食品,如全谷物、蔬菜、水果、豆类、坚果和种子,为以肥胖为中心的医学营养疗法提供了非淀粉多糖和抗性淀粉的混合来源,分离和合成的浓缩和均匀特征纤维为针对代谢综合征病理生理学的营养保健品开发提供了途径。
✦ 膳食纤维对于控制肥胖有重要作用
几种纯化的食品级膳食纤维已经作为食品成分或补充剂在市场上销售,其中许多可以被选定的微生物群落获取、降解和利用。
一项包含22项随机对照试验、总共1428名参与者的系统回顾和荟萃分析表明,使用分离的可溶性膳食纤维补充剂(菊粉、低聚果糖、抗性玉米糊精、瓜尔豆胶、亚麻籽粘液、海藻酸盐粉、葡甘露聚糖和黄原胶)的个体至少12周后, 与对照干预措施相比 ,体重减轻和代谢功能改善显著更高(可消化的碳水化合物),支持补充分离纤维在控制肥胖中的作用。
然而,体重的减少相对适度(平均差-1.25公斤),表明单独分离的可溶性纤维可能无法实现实质性的体重减轻。
!
补充膳食纤维需要和个体特征相匹配
使用基于膳食纤维的策略相关挑战在于需要什么剂量才能产生有益效果以及个人对这些剂量的反应如何?
通常,小鼠和大鼠模型中使用的剂量转化为人类每日摄入量>100 g ,这可能会导致严重的副作用。事实上,一项对18名参与者进行的纵向、随机交叉研究表明,补充30克菊粉会增加促炎细胞因子(如IL-6和TGFβ)以及肝酶的水平。
另一项结合使用人体组织样本、人体结肠活检离体培养和细胞培养模型的研究表明,饮食中的β-果聚糖可引发人体巨噬细胞和患有活动性肠道炎症的炎症性肠病患者的活检样本中的促炎症反应。研究人员推测,在缺乏发酵纤维(如β-果聚糖)所需的特定微生物类群(如罗氏菌属和普氏粪杆菌)的个体中,这些未发酵的纤维可能会在胃肠道中诱发炎症反应。
这些研究强调了基于将特定纤维混合物与宿主现有微生物功能特征相匹配的个性化饮食疗法的必要性。
了解膳食纤维如何沿着胃肠道表现并与人体肠道微生物群相互作用后,可以根据纤维独特的理化特性、对肠道微生物群的影响以及对饱腹感、血糖、血脂或炎症反应的影响来合理选择纤维。
✦ 根据对肠道微生物群的影响等选择合适的纤维
一个商业化的例子是PolyGlycopleX,它是海藻酸钠、魔芋胶和黄原胶的混合物,协同相互作用形成高粘性和凝胶形成的多糖复合物,先前已证明可以促进饱腹感并降低总胆固醇水平。
注:人们可以推测,将PolyGlycopleX与有利于丙酸产生的可发酵纤维混合物配对可能会增强临床反应,因为人类补充丙酸已被证明对饱腹感和胆固醇代谢有良好的影响。
39名患有高心脏代谢疾病风险的成年人服用含有七种可发酵纤维的专有混合物,可以改善葡萄糖和胆固醇代谢的替代标志物,并显著调节肠道微生物群的组成和功能特征。
快速(菊粉)和缓慢(抗性淀粉)发酵纤维的混合物,旨在将乙酸盐的产生扩展到远端结肠,也被证明可以在健康个体的餐后促进能量消耗并减弱血糖反应,但有趣的是,它并没有患有糖尿病前期的个体。
这些结果强调了微生物发酵能力的改变以及正常体重个体和肥胖或代谢功能障碍个体之间短链脂肪酸代谢的差异会影响对纤维补充剂的反应。
✦ 纤维引起的微生物变化会影响代谢、信号传导
虽然纤维混合物是一种新兴方法,可以部分克服对纤维补充的个性化反应,但仍需要精心设计的临床前和临床研究来开发和确定此类纤维混合物单独以及与治疗肥胖症和代谢综合征的护理标准相结合的功效。
对14名成年人进行的受控饮食研究中使用特定的纤维组合,证明不同的纤维组合在微生物功能基因表达和生长中引发了共同的和纤维特异性的反应。
例如,豌豆纤维和菊粉或豌豆纤维、菊粉、橙纤维和大麦麸的组合都促进了多种拟杆菌的生长,并增加了阿拉伯低聚糖和低聚木糖利用的途径。
此外,纤维诱导的特定微生物基因的变化可能与宿主葡萄糖代谢、钙调神经磷酸酶和AKT信号传导、细胞凋亡、激肽释放酶-激肽蛋白酶和免疫过程的变化相关。
尽管体外研究进一步证明了离散纤维结构能够操纵肠道微生物组的潜力,但仍需要在人体中进行额外的随机对照试验来确认纤维补充剂的生理效应。
膳食纤维和健康相关细菌基因组之间的联系表明,活体微生物的施用,无论是益生菌、活体生物治疗药物还是粪菌移植,都可能与选择性发酵的膳食纤维相互作用。
与将益生菌和益生元结合在一起的互补合生元不同,这种精确配对是协同合生元开发的基础,其中精确开发底物以供共同施用的活微生物选择性利用,从而为宿主带来健康益处。
✦ 膳食纤维协同合生元改善代谢和肥胖
一些早期的临床前和临床研究结果表明,协同合生元可能并不总是可预测地相互作用以促进健康。例如,根据三氯蔗糖与乳果糖的比率估计,在94名肥胖个体中补充益生元低聚半乳糖、益生菌青春双歧杆菌或协同合生元已被证明可以类似地增强肠道屏障完整性。
然而,根据系统评价和荟萃分析的报告,合生元补充剂,或益生元(或多种益生元)和益生菌(或多种益生菌)的一般配对,已显示出减轻体重和纠正肥胖代谢失调的希望。
一个例子是Pendulum Glucose Control,它是菊粉、低聚果糖、嗜黏蛋白阿克曼菌(Akkermansia muciniphila)、拜氏梭菌、丁酸梭菌和婴儿双歧杆菌专有混合物,已被证明可以改善2型糖尿病患者的葡萄糖代谢,这些患者单独通过饮食和运动治疗。
✦ 膳食纤维的摄入与粪菌移植的效果会相互影响
整个粪便微生物群落的管理可能会进一步受益于精确膳食纤维的共同管理,这些纤维支持群落内与健康相关的成员或调节防止微生物植入的环境限制。
在一项研究中,粪菌移植与不可获取的微晶纤维素 (n=17) 配对,但不是可发酵纤维混合物(n=17)(抗性麦芽糖糊精、IV型抗性淀粉和阿拉伯胶),改善了接受者中肥胖和代谢综合征患者的胰岛素敏感性。
微晶纤维素是一种食品添加剂,也常用作药物包衣材料。它是一种水溶性纤维素衍生物,具有优异的增稠、乳化、稳定等功能。在食品工业中,微晶纤维素常用于调制冰淇淋、奶油、果冻等产品;在药物制剂中,微晶纤维素常用作控释药物的包衣剂。
补充微晶纤维素有助于增加群落丰富度以及几种与健康相关的类群的植入或富集,例如Akkermansia、Christensenellaceae和Phascolarctobacter,这可能是通过将结肠环境转向更有利的条件,例如减少肠道炎症。
捐赠者在获得粪便之前的饮食会进一步影响粪菌移植的功效。例如,与遵循地中海减肥(n=16)或健康饮食指南(n=19)饮食后接受自体粪菌移植胶囊的个体相比,含有绿茶和较高膳食纤维的地中海饮食在粪菌移植后8个月可减弱体重增加。
总体而言,将益生菌、活生物治疗和粪菌移植疗法与具有离散结构的新型纯化的膳食纤维相结合,将有助于开发创新的营养保健品和药物疗法,通过平衡失调的肠道微生物群来针对代谢综合征的病理生理学。
主要参考文献
Deehan EC, Mocanu V, Madsen KL. Effects of dietary fibre on metabolic health and obesity. Nat Rev Gastroenterol Hepatol. 2024 Feb 7.
Lin D, Peters BA, Friedlander C, Freiman HJ, Goedert JJ, Sinha R, Miller G, Bernstein MA, Hayes RB, Ahn J. Association of dietary fibre intake and gut microbiota in adults. Br J Nutr. 2018 Nov;120(9):1014-1022.
Ricardo-Silgado ML, McRae A, Acosta A. Role of Enteroendocrine Hormones in Appetite and Glycemia. Obes Med. 2021 May;23:100332.
Crooks B, Stamataki NS, McLaughlin JT. Appetite, the enteroendocrine system, gastrointestinal disease and obesity. Proc Nutr Soc. 2021 Feb;80(1):50-58.
Brown SSG, Westwater ML, Seidlitz J, Ziauddeen H, Fletcher PC. Hypothalamic volume is associated with body mass index. Neuroimage Clin. 2023;39:103478.
She Y, Mangat R, Tsai S, Proctor SD, Richard C. Corrigendum: The interplay of obesity, dyslipidemia and immune dysfunction: a brief overview on pathophysiology, animal models, and nutritional modulation. Front Nutr. 2023 Oct 11;10:1304102.
Gill SK, Rossi M, Bajka B, Whelan K. Dietary fibre in gastrointestinal health and disease. Nat Rev Gastroenterol Hepatol. 2021 Feb;18(2):101-116.
Mah E, Liska DJ, Goltz S, Chu Y. The effect of extracted and isolated fibers on appetite and energy intake: A comprehensive review of human intervention studies. Appetite. 2023 Jan 1;180:106340.

谷禾健康

癌症是重要的死亡原因之一,影响着全球至少数百万人。据世界卫生组织统计,发现全球范围内癌症负担正在迅速增加。
癌症的发展不仅仅是癌细胞的生长和增殖,其肿瘤微环境(TME)也与之共同进化,主要参与肿瘤的发生、发展、转移和治疗反应。
肿瘤微环境包含肿瘤细胞、肿瘤浸润免疫细胞、肿瘤相关其他细胞、细胞外基质、非细胞成分和非癌性宿主细胞,微生物群也是肿瘤微环境中的细胞成分之一,发挥着重要且不可替代的作用,因为微生物群落可以调节各种生物过程,包括细胞代谢、生理学和免疫反应等。
谷禾以前的文章曾多次讲述,肠道菌群与肿瘤尤其是胃肠道肿瘤的发生、发展密切相关。肠道微生物群可以通过调节细菌的特定生物活性代谢物来影响肠道微环境。例如短链脂肪酸(SCFA)作为肠道细菌发酵产生的典型代谢物,在肠道稳态和人体健康中发挥着关键作用。
短链脂肪酸可以调节能量代谢、增强肠道屏障并发挥抗炎作用。短链脂肪酸作为免疫功能的关键调节剂,可以调节T细胞、B细胞、巨噬细胞和其他免疫细胞。短链脂肪酸由于与G蛋白偶联受体(GPCRs)的结合或对组蛋白脱乙酰酶(HDACs)的抑制,可以影响免疫反应的信号转导途径,调节免疫相关炎症介质的释放,从而调节肿瘤免疫微环境。
近年来,短链脂肪酸对肿瘤微环境的影响被广泛研究。在结直肠癌和胰腺癌实验模型中,已证明丁酸盐可以增强CD8+ T细胞的抗肿瘤作用。此外,独特组成的微生物群可能还有助于诊断和定位恶性肿瘤,全面了解肠道微生物群及其代谢物与肿瘤微环境之间的相互作用有望成为诊断、治疗和预防肿瘤的新方法。
在本文中,我们(1)讲述了微生物群及其代谢物短链脂肪酸对肿瘤微环境和宿主免疫的影响;(2)短链脂肪酸在癌症发生、发展和治疗方面的相互作用;(3)介绍基于微生物群的癌症诊断和预后;(4)讨论了靶向微生物-短链脂肪酸轴调整肿瘤微环境以最大限度地提高癌症治疗效果的各种方法,包括粪便微生物移植、饮食调整和施用益生菌。这将为未来基于肠道菌群和肿瘤微环境的癌症靶向治疗奠定基础。
什么是肿瘤微环境?
肿瘤微环境(TME)是指肿瘤细胞及其周围的局部环境,包括周围的血管、免疫细胞、细胞外基质、细胞间信号分子等。
肿瘤细胞和肿瘤微环境之间永久的相互关系不仅为肿瘤细胞提供了生长和扩散所需的物质和信息,还显著影响肿瘤的发生、进展、转移和治疗反应。
肿瘤微环境的组成部分
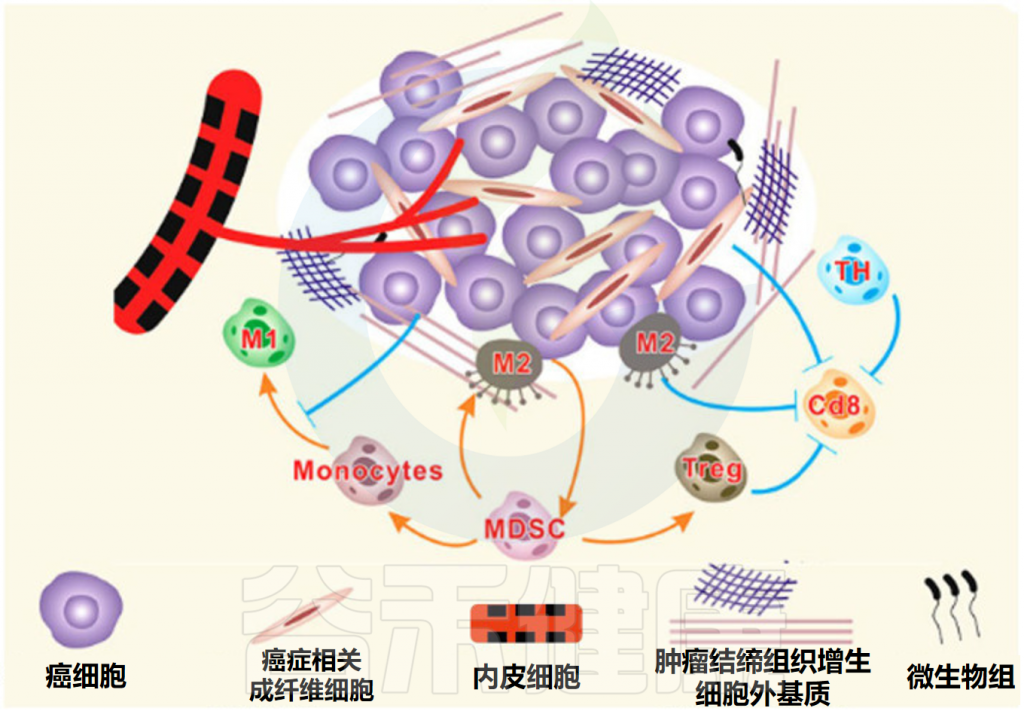
Feng P,et al.Front Microbiol.2024
▸ 前沿资料
最近,具有抗肿瘤能力的常规药物包括阿司匹林、塞来昔布、β-肾上腺素能拮抗剂、二甲双胍和他汀类药物,通过靶向肿瘤微环境成分显示出在联合治疗中的潜在用途。
★ 微生物群是肿瘤微环境的一个组成部分
肿瘤微环境是一个复杂的环境,其中微生物群被认为是一种新颖但必不可少的元素。微生物群在功能上减少肿瘤细胞代谢,例如炎症、基因毒素的产生以及具有各种特征的细菌代谢物的产生。
越来越多的证据表明,肿瘤微环境中微生物群及其代谢物之间的相互作用可以影响宿主免疫和肠上皮,最终驱动或抑制肿瘤生长。
研究报告称,肠道细菌可以调节人体免疫细胞的激活,使其迁移到肿瘤微环境来消除肿瘤细胞。此外,肠道微生物群和肿瘤微环境之间复杂的相互作用可能会使肿瘤细胞逃避免疫系统并增殖。了解这个系统将为癌症的预防、诊断和治疗带来希望。
肿瘤微环境在癌症免疫治疗中的作用
肿瘤微环境(TME)中肿瘤相关巨噬细胞(TAM)和其他免疫抑制细胞的大量积累对癌症的进展和治疗效果有重要影响。
★ 肿瘤微环境的免疫细胞影响癌症进展和治疗效果
CD163是一种标志物,主要表达在巨噬细胞表面,尤其是在肿瘤相关巨噬细胞(TAM)上。CD163阳性的TAM在肿瘤微环境中的高表达与免疫抑制环境的形成有关,这种环境可以促进肿瘤的生长和扩散,并且与病人的不良临床结果相关。
当CD163+ TAM的消耗导致免疫抑制减少,意味着通过减少这些免疫抑制性的巨噬细胞,可以增强细胞毒性T细胞(CTLs)的浸润和活性,从而有助于控制肿瘤的发展。这是当前癌症免疫治疗研究的一个重要方向,即通过调节肿瘤微环境中的免疫细胞组成来增强机体对肿瘤的免疫反应。
简而言之,CD163阳性的表达通常与肿瘤微环境中的免疫抑制状态相关,通过靶向这些细胞,可以改善免疫系统对肿瘤的攻击能力,为癌症治疗提供新的策略。
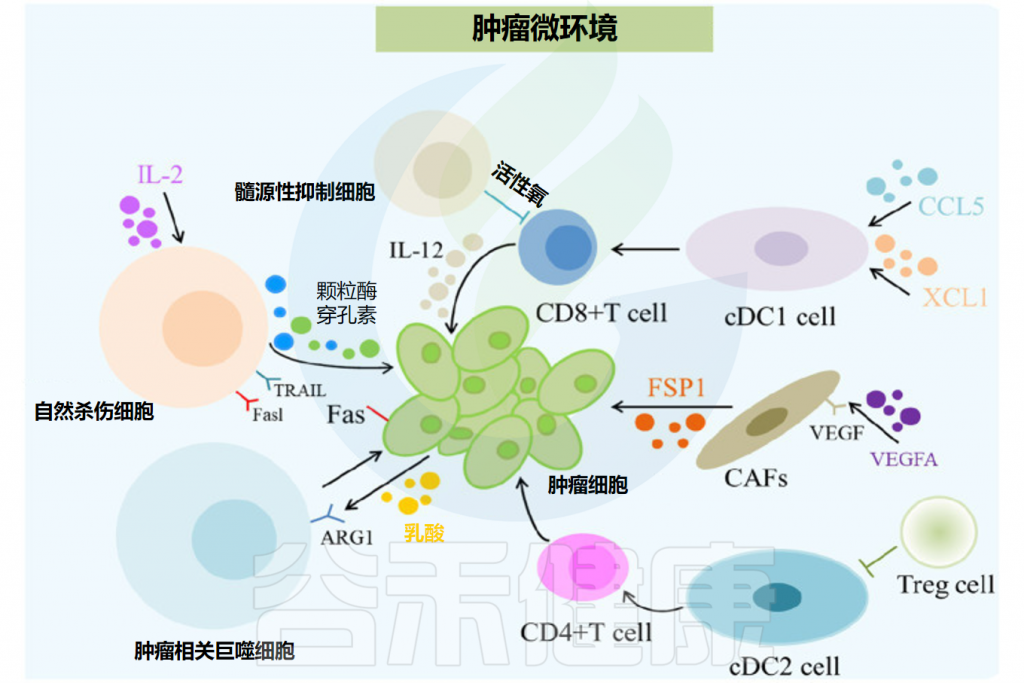
Feng P,et al.Front Microbiol.2024
★ 非细胞成分也调节癌细胞的增殖和治疗效果
肿瘤微环境的非细胞成分对于癌症进展、侵袭性和化疗耐药性也至关重要。细胞外基质的硬度促进肿瘤细胞存活和增殖,同时上调整合素信号传导。
透明质酸是一种CD44受体,在各种癌症的肿瘤微环境中含量丰富。它们的相互作用激活促癌信号通路并诱导非编码RNA种类的上调,例如miR-10b/miR-302/miR-21和lncRNA。在胰腺癌中,间质与不同的透明质酸高度反应,导致间质液压力升高,从而导致血管塌陷和化疗效果不佳。
注:使用重组透明质酸酶靶向胰腺肿瘤中的酶已被证明可以降解透明质酸并通过减少转移和提高生存率来增强治疗效果。
此外,肠道菌群的分泌成分也与肿瘤微环境有关。例如,外膜囊泡(OMV)可以将肿瘤微环境重新编程为pro-TH1模式,而代谢物(如丁酸盐和烟酸)可以介导结肠上皮中IL-18的Gpr109a依赖性诱导,抑制结肠炎和结肠癌症。
肠道微生物群对肿瘤微环境的影响
肠道微生物群对于宿主免疫系统的发育、维持和生长至关重要。肠道生态系统可以通过影响骨髓的流入、免疫环境、淋巴细胞以及炎症和代谢模式来影响局部和远处的肿瘤。
肠道微生物群参与多种细胞内信号通路的调节
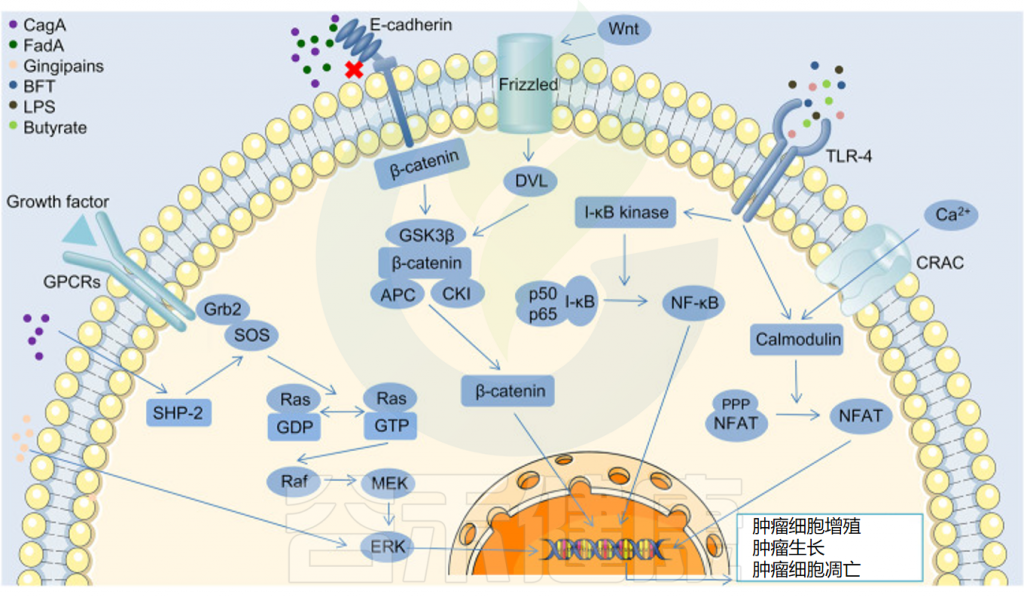
Sun J,et al.ISME J.2023
★ 肠道微生物群是肿瘤微环境的重要调节剂
肠道微生物群正在成为结直肠癌、胃癌和肝癌等各种癌症中肿瘤微环境的关键调节剂。例如,之前的一项研究报告称,具核梭杆菌(Fusobacterium nucleatum)等细菌可以通过抑制人类免疫反应来增强肿瘤生长。
此外,乳腺癌和卵巢癌与微生物群中的特定生物特征有关,例如卷曲乳杆菌(Lactobacillus crispatus)的丰度,它与癌症的发生呈负相关。
★ 肠道微生物群的代谢物影响肿瘤治疗
先前的研究发现,肠道微生物群代谢活动的产物显著影响与肥胖、血脂和能量稳态相关的宿主代谢途径。因此,揭示肠道微生物群的代谢物和亚代谢物如何影响免疫细胞并重塑肿瘤微环境可以极大地促进肿瘤治疗的发展。
肠道微生物群的代谢物进入宿主细胞并与人体免疫反应相互作用,促进各种肿瘤抑制和免疫调节分子的产生。它们还通过维持上皮屏障和肠道的完整性来抑制炎症。
肠道微生物代谢物,如短链脂肪酸和肌苷,直接或间接与肿瘤微环境相互作用,重塑它,从而影响癌症过程。短链脂肪酸有助于维持肠道稳态和调节肠道屏障功能。
肠道微生物代谢物影响抗癌免疫
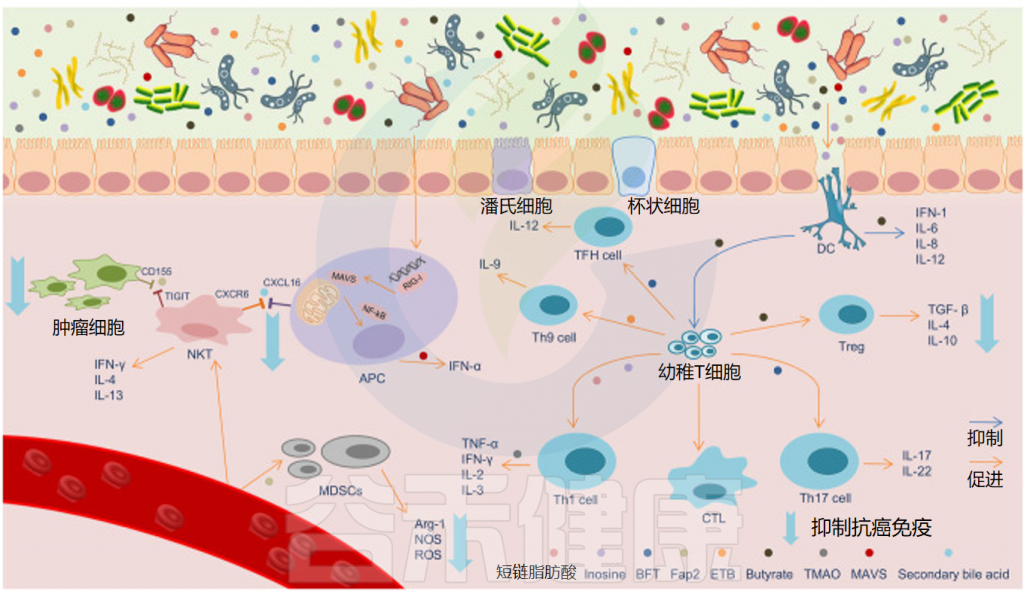
Sun J,et al.ISME J.2023
此外,一些脂肪酸和胆酸与炎症有关。丁酸盐等短链脂肪酸可由普拉梭菌(Faecalibacterium prausnitzii)产生,控制血管生成并减少促血管生成因子的表达。因此,增加丁酸盐浓度被认为可以减缓并阻止癌症的生长。
相反,脱氧胆酸和石胆酸可通过增加活性氧的产生而导致DNA损伤。最近的研究表明,肠道细菌假长双歧杆菌(B.pseudolongum)可以产生肌苷,在外源IFN-g存在的情况下驱动Th1细胞分化。
★ 影响免疫治疗的效果
此外,假长双歧杆菌(B.pseudolongum)通过与T细胞上的腺苷A2A受体相互作用,与免疫检查点治疗(例如抗CTLA-4和抗PD-L1)的反应相关。
CTLA-4和PD-L1是免疫检查点疗法的主要靶点,该疗法涉及膜结合分子,这些分子在初始刺激后会阻碍不受限制的T细胞反应。因此,癌细胞可以通过利用这种机制来逃避免疫监视。
然而,在重新激活低效T细胞的同时,免疫检查点抑制剂(ICIs)可以恢复对肿瘤抗原的反应。临床研究和临床前试验表明,肠道微生物群影响免疫检查点抑制剂的疗效,从而解释了患者对ICI反应的显著差异。因此,深入了解肠道微生物群、其代谢物和宿主免疫系统如何相互作用以重塑和调节肿瘤微环境,有望推动癌症免疫治疗的发展。
总体而言,肠道微生物群对肿瘤微环境的影响很复杂,目前尚未完全了解。然而研究表明,在控制肠道微生物以影响癌症治疗的有效性和改善患者预后方面具有潜在的应用前景。
近年来,微生物和微生物的代谢产物对宿主的影响越来越受到人们的关注。
短链脂肪酸由少于6个碳原子组成,是共生细菌通过膳食纤维在胃肠道中发酵产生的典型代谢产物,已被广泛研究。短链脂肪酸的产生是一个复杂的过程,由多种细菌在结肠中进行。在所有短链脂肪酸中,乙酸盐、丙酸盐和丁酸盐最具代表性。
短链脂肪酸对人体的基本作用
• 提供能量
当短链脂肪酸产生时,第一个功能是作为底物提供能量。大多数短链脂肪酸通过两种转运蛋白被结肠细胞吸收:单羧酸转运蛋白1(MCT-1)和钠偶联单羧酸转运蛋白1(SMCT-1)。
短链脂肪酸通过MCT-1以H+依赖性电中性方式转移,而短链脂肪酸阴离子通过SMCT-1运输。
• 调节生理反应
除了为结肠细胞提供能量外,短链脂肪酸还通过血液运输到全身的各个组织和器官,然后通过两种主要机制调节生物反应。
一方面,短链脂肪酸会降低组蛋白去乙酰化酶(HDAC)的活性或表达,从而导致组蛋白乙酰化增加。据报道,HDACs的异常激活存在于多种类型的癌症中。
另一方面,短链脂肪酸与G蛋白偶联受体(GPCR)结合,主要针对GPR41(更名为游离脂肪酸受体(FFAR)3)、GPR43(更名为FFAR2)和GPR109A,发挥相应的信号级联效应。一些研究表明GPCRs的异常表达或活性参与多种肿瘤进展。
短链脂肪酸调节炎症反应的机制
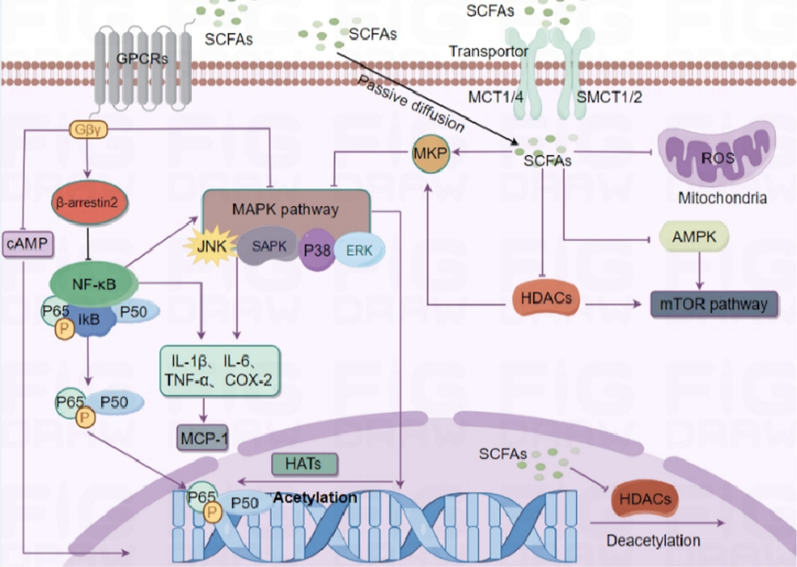
He M,et al.J Transl Med.2024
• 其他作用
既往研究总结了短链脂肪酸在调节能量代谢、保护肠道完整性、改善炎症反应等方面的作用,但短链脂肪酸对免疫系统的影响尚未引起足够的重视。一些作用罗列在下表中:


Dong Y,et al.Front Immunol.2023
短链脂肪酸对代谢稳态的影响
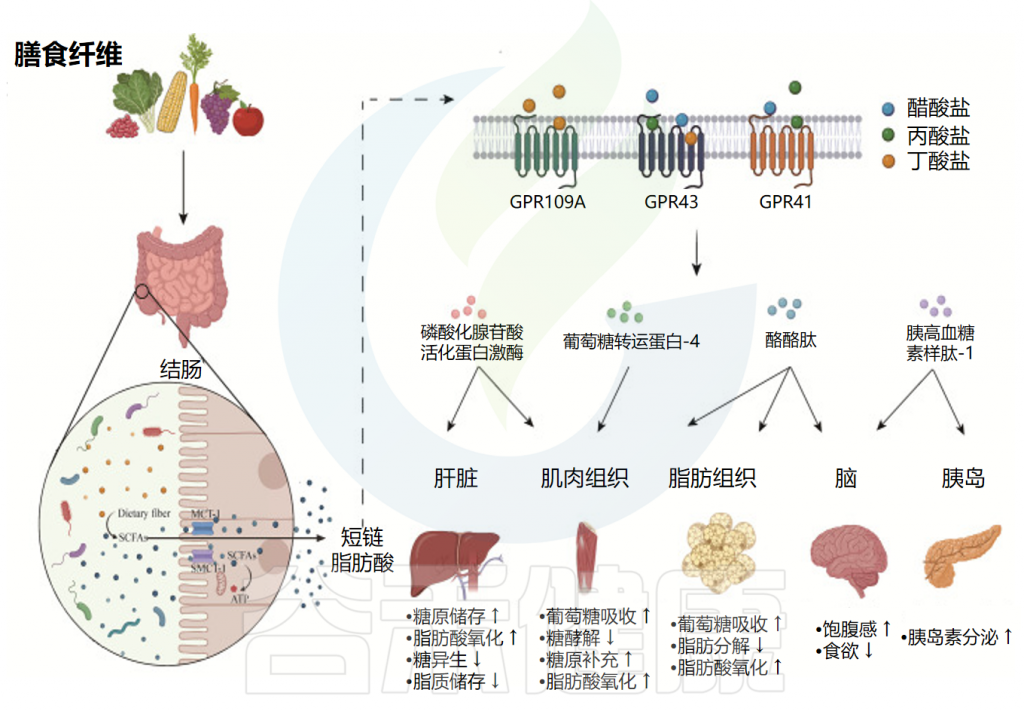
Dong Y,et al.Front Immunol.2023
在肿瘤免疫微环境中起重要作用
• 影响T细胞的分化
T细胞是肿瘤免疫微环境中的重要细胞,T细胞浸润减少或功能障碍会导致许多癌症治疗临床效果不佳。
由于幼稚T细胞在功能水平上表达时没有GPR41和GPR43,因此短链脂肪酸可以直接影响依赖于HDAC抑制剂活性的幼稚T细胞的分化。
通过这种方式,短链脂肪酸促进未成熟的CD4+ T细胞分化为不同的调节性T细胞和效应T细胞,这取决于不同的极化条件,比如细胞因子表型和免疫环境。
短链脂肪酸诱导mTOR-S6K和STAT3的激活,参与T细胞分化所需细胞因子的产生。无论极化条件如何,短链脂肪酸都会促进白细胞介素(IL)-10的表达,但只能在特定环境下促进IL-17或干扰素-γ (IFN-γ)的产生。
• 影响白细胞介素等细胞因子的含量
有趣的是,分化T细胞(例如辅助性T(Th)1细胞)中 IL-10的分泌取决于与GPR43的相互作用。此外,短链脂肪酸上调Blimp-1的表达,这与Th1细胞中IL-10的产生和T细胞功能的维持有关。
在高脂肪饮食治疗的小鼠中,IL-17和IFN-γ的水平升高,而转化生长因子-β(TGF-β)和IL-10的水平降低。这意味着T细胞向Th17和Th1细胞的分化程度较高,而向调节性T(Treg)细胞的分化程度较低,特别需要注意的是:短链脂肪酸可以扭转这种情况。
CD4+ T细胞和先天淋巴细胞中IL-22被发现可以通过短链脂肪酸进行调节。丁酸盐通过与GPR41结合增加转录因子HIF-1α和AhR的表达,同时伴随着STAT3和mTOR的激活。
同时,丁酸盐促进的HIF-1α与IL-22启动子的HRE结合涉及组蛋白乙酰化。CD4+ T细胞分化过程也受到表观遗传调控。不同的CD4+ T细胞亚群具有特定的转录因子,例如Th1细胞的T-bet、Th17细胞的RORγT和Treg细胞的FOXP3。丁酸盐通过乙酰化 H4K16增加分化的Th17细胞中RORγT的表达,但在Th17极化条件下对初始CD4+ T 细胞没有反应。
• 短链脂肪酸在抗肿瘤免疫中的其他作用
丁酸盐
低丁酸盐浓度以TGF-β1依赖性方式促进CD4+ T细胞向Foxp3+ Treg细胞分化,而高丁酸盐浓度无论在什么条件和亚群中都会诱导T-bet表达和IFN-γ释放。这似乎打破了我们对短链脂肪酸对粘膜免疫影响的传统认识。更重要的是,暴露于高浓度的短链脂肪酸,尤其是丁酸盐,可以抑制肠粘膜中CD4+ T细胞和其他CD4+ T细胞亚群的增殖和活化。这与组蛋白乙酰化和GPR43激活密切相关。
丁酸盐通过促进CD8+ T细胞作用参与抗肿瘤免疫。丁酸盐处理的细胞毒性T淋巴细胞(CTL)介导的抗肿瘤反应的促进作用依赖于一种称为ID2的转录调节因子,其水平在肿瘤微环境中的CD8+ T细胞中要高得多。丁酸通过抑制组蛋白脱乙酰酶(HDACs)的活性,诱导ID2表达并启动ID2-IL-12信号通路,从而提高奥沙利铂的化疗效果。
戊酸盐
戊酸通过抑制HDAC活性来增强CTL中IL-2、肿瘤坏死因子-α(TNF-α)、IFN-γ和其他效应分子的表达。
PVR/CD155 调节剂在恶性肿瘤中过度表达,并与具有Ig和ITIM结构域的T细胞免疫受体结合,介导免疫逃逸。
乙酸盐、丙酸盐
醋酸盐通过抑制PI3K/AKT通路抑制PVR/CD155水平,增强CD8+ T细胞的抗肿瘤能力。活化的γδ T细胞是IL-17的主要内源性来源。丙酸盐还通过抑制HDAC来抑制人γδ T细胞中IL-17、IL-22和其他细胞因子的分泌,从而防止癌症进展。
短链脂肪酸对肿瘤免疫微环境的影响
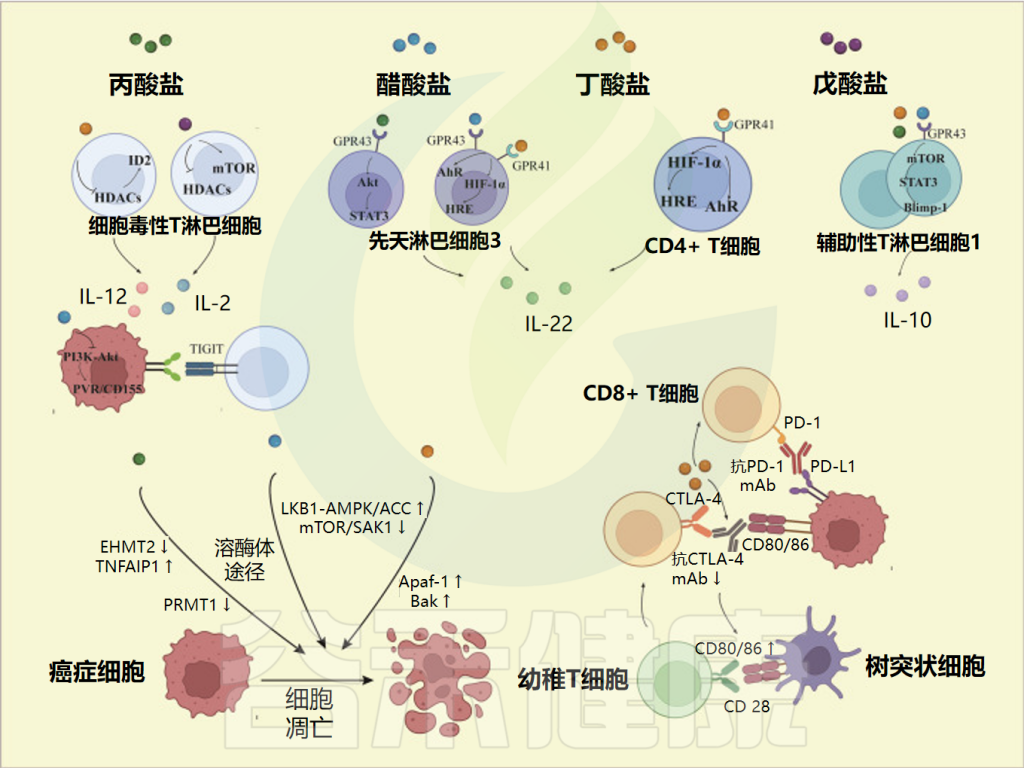
Dong Y,et al.Front Immunol.2023
密切相关的证据
实验研究和谷禾检测数据发现胃肠道肿瘤患者中短链脂肪酸和产生短链脂肪酸的细菌丰度明显较低,本节主要讲述短链脂肪酸可以通过多种机制影响胃肠道肿瘤的发展。而这也有助于未来将调节体内短链脂肪酸和肠道菌群的水平用作一种预防癌症或辅助治疗手段。
胃癌
• 短链脂肪酸可能用来评估胃癌的进展
在胃肠道化生或胃癌患者的血浆中检测到较低浓度的丙酸盐和丁酸盐。短链脂肪酸似乎可以用来评估胃癌的进展。
胃肠化生是指胃黏膜上皮转变为含有杯状细胞的肠黏膜上皮组织。肠上皮化生常见于慢性萎缩性胃炎,胃黏膜肠上皮化生属于胃的癌前病变。
此外,丁酸盐以剂量依赖性方式抑制KATO III细胞的增殖和迁移,这与其调节miRNA调控网络的作用有关。
• 影响胃癌治疗的效果
胃切除术后服用丁酸梭菌(C.butyricum)可以增加短链脂肪酸浓度,增强免疫力,减轻炎症,预防术后并发症。
体内实验证明,醋酸盐诱导胃癌细胞凋亡,随后体外实验证明氧化应激发挥了重要作用。大量摄入醋酸盐会增加胃癌细胞中活性氧的产生和MCT1的表达。
活性氧的过度表达上调了HCP1,两者均导致胃癌细胞对卟啉的摄入量增加。作为光动力疗法的光敏剂,卟啉的过度吸收增强了疗效。而作为HDAC抑制剂,丁酸盐修饰肿瘤抑制基因Per1和Per2并诱导它们在KATO III和NCI-N87中的表达。
与短链脂肪酸联合使用的传统疗法似乎具有更好的效果和更低的毒性。在裸鼠异种移植肿瘤模型中,丁酸盐-顺铂治疗抑制胃癌细胞的生长、迁移和侵袭,并依靠线粒体凋亡途径加速细胞凋亡。
此外,单独丁酸可以通过线粒体途径诱导胃癌细胞凋亡,这已在人细胞系BGC-823和SGC-7901中得到证实。
结直肠癌
先前的研究表明,结直肠癌高危人群中乙酸盐、丙酸盐和丁酸盐的浓度显著降低,并且短链脂肪酸水平较低的个体结直肠癌的发病率高于健康个体。各种短链脂肪酸均表现出抗癌行为。
注:与单独治疗相比,这些化合物具有叠加效应。
1
乙酸盐
•常规浓度下乙酸会增强癌细胞的凋亡并减少增殖
乙酸可以增强癌细胞的凋亡并减少增殖,已在不同的结直肠癌细胞系中得到证实,因此它已成为结直肠癌治疗的关键因素。
在结直肠癌患者中,短链脂肪酸减少,乙酸盐代谢转化为乙酰辅酶A。过去的研究表明,乙酸盐介导的细胞凋亡依赖于部分溶酶体膜透化触发的溶酶体途径。然而,溶酶体依赖性选择性死亡途径中随后释放的组织蛋白酶D降低了乙酸盐的敏感性。因此,组织蛋白酶D抑制剂与乙酸盐联合可能比单独使用乙酸盐效果更佳。
•注意:在缺乏氧气和葡萄糖的情况下乙酸盐可能导致癌细胞增加
然而,在没有氧气的情况下,乙酸盐会增加癌细胞的增殖,这依赖于ACSS2的上调和HIF-2的激活。
同时,在葡萄糖缺乏的情况下,乙酸盐通过激活 ACSS2/HIF-2 信号通路促进HCT-116(结肠癌细胞)和HT-29(结肠癌细胞)衍生肿瘤的生长。
因此,乙酸盐的抗癌作用可以根据环境和浓度的变化而改变。
此外,乙酸盐作为PI3K/AKT信号驱动的免疫检查点配体PVR/CD155的调节剂,可以增强肿瘤微环境中CD8+ T细胞的功能反应,促进IFN-γ的产生,有望成为促进肿瘤免疫的相关药物。基于上述讨论,免疫检查点抑制剂(ICIs)的功效可能受益于乙酸盐。
2
丙酸盐
研究发现结直肠癌组织中丙酸盐含量降低,并且向SW480细胞(人结肠腺癌细胞)中添加丙酸盐显著抑制癌细胞生长。
•丙酸盐调节免疫刺激来消灭癌细胞
短链脂肪酸调节免疫刺激和抑制配体,并参与免疫细胞介导的杀伤。丙酸盐诱导的NKG2D配体MICA/B的上调既不依赖于HDACs的抑制,也不依赖于GPR41/GPR43受体的组合,而是依赖于线粒体活性,而丁酸盐则取决于其HDACs抑制剂活性。丙酸盐的这种作用与介导肿瘤抑制蛋白p21表达的PEPCK-M酶和mTORC2/PDK1/AKT通路密切相关。
•丙酸盐通过调节表观遗传导致癌细胞凋亡
除了免疫调节之外,表观遗传调节也是短链脂肪酸发挥抗癌作用的一个有前景的靶点。丙酸盐通过阻止p70 S6激酶磷酸化导致PRMT1表达下调,从而导致结直肠癌细胞选择性死亡。
此外,丙酸盐诱导HECTD2上调,导致EHMT2降解,从而促进下游TNFAIP1的表达并最终促进癌细胞凋亡。
在丙酸盐介导的抗癌治疗中,表观遗传修饰是不可忽视的。然而,最新的孟德尔随机化分析发现,没有强有力的证据证明粪便中丙酸盐浓度与结直肠癌风险之间的相关性。可能有必要全面检测短链脂肪酸及其产生细菌。
3
丁酸盐
研究发现,丁酸盐抑制结直肠癌细胞的增殖,但滋养正常结肠细胞的生长。
•丁酸盐相比其他短链脂肪酸对癌细胞具有更强的抑制作用
与其他短链脂肪酸相比,丁酸盐对结直肠癌细胞系具有更强的抑制作用。
一方面,丁酸可以抑制促炎介质TNF-α、IL-1β、IL-6、IL-8,上调抗炎因子IL-10;另一方面,丁酸可以通过促进CD8+ T细胞发挥作用来促进抗肿瘤免疫。
此外,丁酸盐通过促进上皮细胞增殖、增加粘液层和改善紧密连接来维持肠道屏障的完整性。
在HCT 116细胞(人结肠癌细胞)中,丁酸介导的细胞凋亡与p300-Wnt信号传导密不可分。其中,致癌Wnt信号基因表达模式下的结肠癌细胞比受体介导的Wnt信号基因表达模式下对丁酸盐更敏感。
•丁酸盐影响结直肠癌细胞周期从而促进凋亡
结直肠癌中肠道微生物群的结构和稳定性发生显著改变,并与其进展密切相关。丁酸盐的施用改善了微生态紊乱,反映在病原体减少、厚壁菌门与拟杆菌门的比例减少以及益生菌丰度增加。
与乙酸盐和丙酸盐相比,丁酸盐对结直肠癌细胞周期至关重要的调节网络具有更强的影响。丁酸调节癌症相关miRNA的表达,其中miR-139和miR-542是众所周知的代表。具体来说,它们作为丁酸盐的协作对象来调节细胞周期中的EIF4G2和BIRC5基因。
丁酸盐调节c-Myc/p21通路,诱导细胞周期停滞在G2期,其中包含27个凋亡相关基因。此外,丁酸盐在G1期触发细胞周期阻滞,需要复杂的lncRNA-miRNA-mRNA调控网络。
补充丁酸盐可逆转CSE1L的过度表达,并似乎与p53表现出协同作用,最终将癌细胞抑制在G1和G2/M期。
同时,丁酸诱导的p21和γ-H2AX增加以及细胞周期蛋白B1减少导致细胞周期停滞在 G2/M 期。
•丁酸盐抑制癌细胞的迁移
不仅如此,丁酸盐还通过上调miR-200c并抑制其直接靶点BMI-1对癌细胞迁移产生抑制作用。
BMI-1是诱导依赖于AKT/GSK-3β/snail通路的上皮间质转化(EMT)驱动癌症转移的重要调节因子,丁酸盐阻止了BMI-1的作用。
丁酸盐处理还降低了结直肠癌细胞而非正常结肠细胞中Trx-1的表达。研究证明,Trx-1与S100P的相互作用通过AKT介导的S100A4上调促进EMT。通过施用丁酸盐,类器官证明细胞外基质-整合素/PI3K-Akt 轴参与结直肠癌细胞形态变化和细胞凋亡。
丁酸盐阻止结直肠癌细胞的迁移和侵袭,本质上是由于组蛋白脱乙酰酶(HDAC3)的抑制,从而阻断了AKT1和ERK1/2的激活。
•丁酸盐还改变表观遗传和代谢发挥抗癌特性
与其他短链脂肪酸不同,丁酸盐逆转前列腺素EP4受体的过度表达和环氧合酶2的产生,以减少从正常细胞到癌症的表型改变。
此外,丁酸盐通过激活LKB1-AMPK/ACC信号通路和降解β-catenin诱导结直肠癌细胞自噬。
丁酸盐致力于改变结直肠癌细胞的表观遗传学和代谢谱,发挥其抗癌特性。通过调节KEAP1的DNA甲基化,丁酸阻断NRF2-ARE信号传导,从而增强其抗癌潜力。
线粒体代谢和相关代谢物的变化参与了丁酸盐对表观遗传学的调节。丁酸激活三羧酸循环相关酶IDH1和PDH,从而下游产物α-KG水平升高。
作为一种信号分子,α-KG影响与细胞凋亡相关的MSH2和MLH1去甲基化。同时,α-KG减弱DNA和组蛋白H3K4me3的甲基化,导致结直肠癌中Wnt信号通路受到抑制。
丁酸盐通过促进PKM2的四聚化和去磷酸化来诱导有氧糖酵解的抑制,从而逆转癌细胞中的代谢优势。对于结直肠癌细胞,丁酸盐引起的代谢变化反映在促进氧化代谢而不是糖酵解。
此外,铁死亡是铁依赖性细胞程序性死亡的方式,丁酸盐通过CD44/SLC7A11信号通路诱导结直肠癌细胞中的铁死亡。
肝细胞癌
肝细胞癌是一种发生于肝脏的恶性肿瘤,它是全球范围内最常见的癌症类型之一。作为一个重要的危险因素,乙型肝炎病毒(HBV)会促进肝细胞癌(HCC)的进展。
• 丁酸盐促进肝癌细胞的凋亡和自噬
丁酸盐通过抑制SIRT-1从而促进p53乙酰化,显著抑制人肝癌细胞(Hep G2.2.15)的增殖和驻留乙型肝炎病毒的复制。
HBx是乙型肝炎病毒(HBV)编码的致癌蛋白,可能通过多种方式导致肝细胞癌的加速发生和发展。随着HBx相关途径的下调,短链脂肪酸导致肿瘤抑制因子DAB2的表达增加,从而延缓肝细胞癌的进展。
先前的研究表明,丁酸盐通过增加活性氧的产生来抑制AKT/mTOR通路,从而促进人肝癌细胞的凋亡和自噬。
• 短链脂肪酸延缓了肝癌进展
通过粪便罗伊氏乳杆菌(Lactobacillus reuteri)移植进行干预的肝细胞癌小鼠似乎也可以延缓癌症进展。相关机制是罗伊氏乳杆菌代谢产生的乙酸盐通过抑制HDAC和诱导Sox乙酰化,抑制先天淋巴细胞的效应分子IL-17A的产生。
另外,PD-1抑制剂与短链脂肪酸联合使用,在肝癌小鼠中显示出增强的抗肿瘤作用。Lachnospiracea具有减少肝纤维化的作用,部分原因是短链脂肪酸介导的。
已证明口服短链脂肪酸可以抑制万古霉素治疗的小鼠纤维化。
• 增强常规化疗药物的效果
此外,丙酸盐可以增强常规化疗药物在肝细胞癌中的化疗效果。研究表明,丙酸盐通过激活GPR41诱导TNF-α表达,并增加顺铂诱导的caspase-3激活,从而介导肝癌细胞凋亡。
肝细胞癌患者体内丁酸产生菌16s RNA表达降低,补充丁酸可促进肝癌细胞凋亡并抑制增殖。更重要的是,丁酸盐可以增强索拉非尼的治疗潜力,通过减少HK2对c-myc信号传导的依赖,丁酸盐可以抵抗糖酵解,从而增强索拉非尼的功效。
对于接受仑伐替尼治疗的肝细胞癌患者,无腹泻等不良反应的患者丁酸代谢相对丰富且活跃。最新研究表明,补充乙酸盐可以诱导人肝癌细胞中NAT2的水平,类似于葡萄糖和胰岛素,从而导致代谢相关基因的变化。
不仅如此,丁酸盐在胆管癌细胞中也表现出同样的抗癌作用。丁酸盐和HDAC6抑制剂在防止增殖、迁移和上皮间质转化方面具有协同作用。
• 短链脂肪酸改善一些癌前病变症状
酒精性脂肪肝病(AFLD)和非酒精性脂肪肝病(NAFLD)可进展为肝硬化,最终可能发展为肝癌。丁酸盐抑制gasdermin D 介导的细胞焦亡,改善肠道屏障破坏和内毒素血症,从而减轻AFLD中的肝脏脂肪变性和炎症。
此外,丁酸盐通过LKB1-AMPK-Insig信号通路的调节诱导肝脂质谱的改变并减轻肝脂肪变性来治疗 NAFLD 。
总而言之,短链脂肪酸限制了肝细胞癌前阶段的进展。
胰腺癌
研究发现,与对照组相比,胰腺癌患者的丙酸盐和丁酸盐水平降低,粪便微生物群的组成发生改变。
• 短链脂肪酸增强了对肿瘤细胞的杀伤能力
短链脂肪酸以肿瘤特异性免疫细胞为目标,无论单独使用还是与其他肿瘤疗法联合使用,都显示出强大的抗癌作用。
研究表明,与组蛋白脱乙酰酶(HDACs)抑制相关,丁酸和戊酸上调IL-2、CD25和mTOR的产生,这些物质参与T细胞激活的调节。通过触发增强的效应分子,丁酸盐和戊酸盐还增加了细胞毒性T淋巴细胞的肿瘤杀伤能力。
短链脂肪酸在过继性免疫治疗方面也显示出良好的前景。用丁酸盐或戊酸盐预处理的细胞在胰腺癌小鼠模型中显示出更好的治疗效果。
• 短链脂肪酸干扰胰腺癌的进展并减轻相关损伤
另一项研究表明,丁酸盐通过逆转胰腺腺癌患者的CD11b细胞的免疫抑制功能并增强CD8+ T细胞的免疫功能来延缓癌症的发展。
短链脂肪酸的影响不仅限于肿瘤微环境,还延伸至肿瘤相关基因。丁酸盐处理后,在AsPC-1细胞(人转移胰腺腺癌细胞)中可以观察到通过抑制组蛋白脱乙酰酶(HDACs)活性介导的p16INK4a、p14ARF和p15INK4b的上调。
在BxPC-3(人原位胰腺癌细胞)和PANC-1(胰腺癌细胞)细胞系中,丁酸盐单独或与吉西他滨联合使用可抑制增殖并诱导细胞凋亡。特别是联合用药减轻了吉西他滨引起的胃肠粘膜、肝、肾损伤。由于HDAC的抑制作用,丁酸盐还调节肿瘤微环境相关成分。
拓展:基于微生物群的癌症诊断和预后
癌症通常是在通过触诊或成像技术识别肿块后进行诊断,然后进行活检以确认细胞恶性肿瘤。断层扫描检测技术,包括PET-CT、MRI和CT,可以有效地识别体内的宏观病变。
基于微生物的癌症诊断
此外,研究已经证实,肠道微生物群动态可能有助于诊断和定位恶性肿瘤,例如根据胃肠道来源的解没食子链球菌菌血症。大多数基于微生物的癌症诊断侧重于对呼吸消化道内的肿瘤进行测序,包括结直肠癌、胰腺癌和肺癌。
有人提出,不同的癌症类型可能在呼吸消化道外具有独特组成的微生物群。一项研究了30多种癌症的瘤内微生物群,应用基于血液的诊断,并提供七种不同癌症中微生物瘤内空间分布和细胞内定位的视觉证据。
2017年的一项研究提出了结直肠癌粪便微生物组的宏基因组分析,以识别和验证不同种族群体中的细菌生物标志物。这项研究纳入了来自中国、丹麦、法国和奥地利的结直肠癌患者和对照样本,并强调了粪便宏基因组生物标志物在早期结直肠癌诊断中的潜力。
此后,更多的研究发现,粪便微生物DNA标记可以单独或与粪便免疫化学测试结合使用,作为新的测试来筛查无症状受试者的结直肠肿瘤。
此外,收集了41名肺癌患者和40名健康志愿者的粪便样本,并使用16S rRNA基因测序分析了肠道微生物群。他们发现, 肺癌患者中的放线菌属(Actinomyces)、韦荣球菌属(Veillonella)、巨球菌属(Megasphaera)、肠球菌属(Enterococcus)和梭菌属(Clostridioides)比健康个体更丰富。他们进一步证明肠道微生物及其相关代谢物是肺癌的潜在生物标志物和治疗靶点。
检查肠道微生物群的变化及其作为胰腺癌患者生物标志物的潜力。他们比较了患有癌前病变的胰腺癌患者、非酒精性脂肪肝患者和健康对照者的微生物群,发现了与胰腺癌相关的独特肠道微生物群特征。
主要特征是梭菌科、毛螺菌科的存在,瘤胃球菌科的缺乏,以及韦荣球菌科、阿克曼氏菌和Odoribacter的过度增加。
目前,已经开发了几种基于细菌的肿瘤检测策略,包括使用将肿瘤靶向细菌的特异性与生物标志物检测的敏感性相结合的工程细菌。使用远程诱导基因开关对减毒细菌进行工程改造,释放外源报告蛋白 ZsGreen。
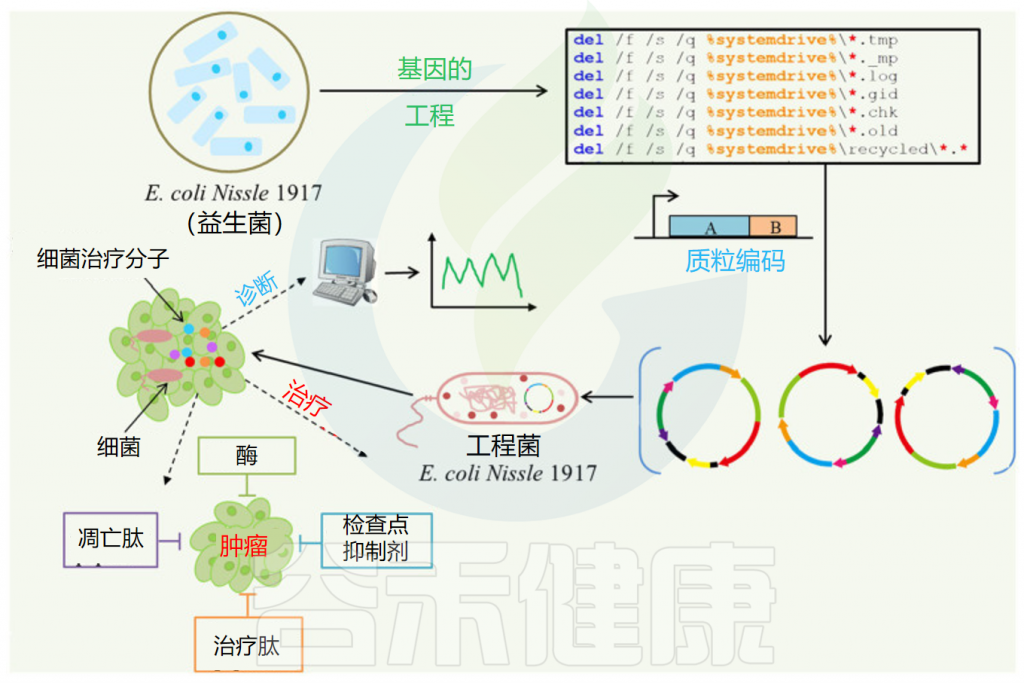
Feng P,et al.Front Microbiol.2024
体内和体外实验均表明,这些细菌可以通过对释放的ZsGreen的系统测量来识别肿瘤。尽管基于细菌的癌症诊断是一种有前景的策略,但它面临着一些挑战,例如相对于宿主的生物量较低以及试剂或环境污染物的干扰。因此,将基于肠道微生物群的方法与传统诊断技术(包括基因组测序、qPCR、免疫组织化学和电子显微镜)相结合,可以提供更准确、更有效的癌症诊断。
基于微生物的癌症诊断已成为一个新领域,专注于根据各种癌症或不同肿瘤阶段肠道微生物群的特定生物特征来设计或开发新策略。此外,深度学习和机器学习算法能够识别表明癌症的微生物特征,这是精准医学的基础。基于微生物的癌症诊断还具有改善癌症筛查和早期检测工作的潜力,有望为各种癌症开发更准确、更有效的诊断工具,并最终改善患者的治疗结果。
肠道微生物群作为潜在预后标志物
在预后方面,许多研究表明肠道微生物群可以作为癌症的潜在预后标志物。在一项结直肠癌患者预后模型的研究中,风险模型与结直肠癌患者的免疫状态和肠道微生物群相关,并且微生物组分析显示,高风险患者中拟杆菌(Bacteroidetes)和放线菌(Actinobacteria)的相对丰度低于低风险患者。
具核梭杆菌作为结直肠癌患者的预后标志物
研究发现肠道中高水平的具核梭杆菌(Fusobacterium nucleatum)和脆弱拟杆菌(Bacteroides fragilis)与结直肠癌患者术后预后不良相关。具核梭杆菌作为结直肠癌患者预后标志物的作用已被多次证明。
例如,收集了100个结直肠癌组织和72个正常粘膜组织,并确定具核梭杆菌水平有助于预测结直肠癌患者的临床结果,发现IV期结直肠癌患者具有较高水平的具核梭杆菌。
此外,研究证明特定的肠道微生物群与接受nabuliumab治疗的肝细胞癌患者的预后相关。具体而言,普雷沃氏菌/拟杆菌比率可用作纳武单抗治疗肝细胞癌的预后预测因子;该比率越高,疗效越好。
纳武单抗(nabuliumab)是一种人类免疫球蛋白G4单克隆抗体。纳武利尤单抗主要治疗三种疾病,包括非小细胞肺癌、头颈部鳞状细胞癌、胃或胃食管连接部腺癌。
治疗胃肠道肿瘤
微生物与抗癌疗法的结合早在19世纪就开始了,当时首次尝试将灭活的链球菌注射到人体肿瘤组织中来治愈癌症。此前的研究表明,微生物制剂直接注射到肿瘤组织或口服给药,可以对肿瘤细胞产生直接的细胞毒性作用或刺激机体局部抗肿瘤免疫反应。
最近的研究发现,传统的放疗、化疗和免疫疗法可以改变患者的肠道微生物群,而菌群的组成可以深刻影响这些治疗的疗效和副作用,包括癌症复发、耐药性和对肠道菌群的附带损害。
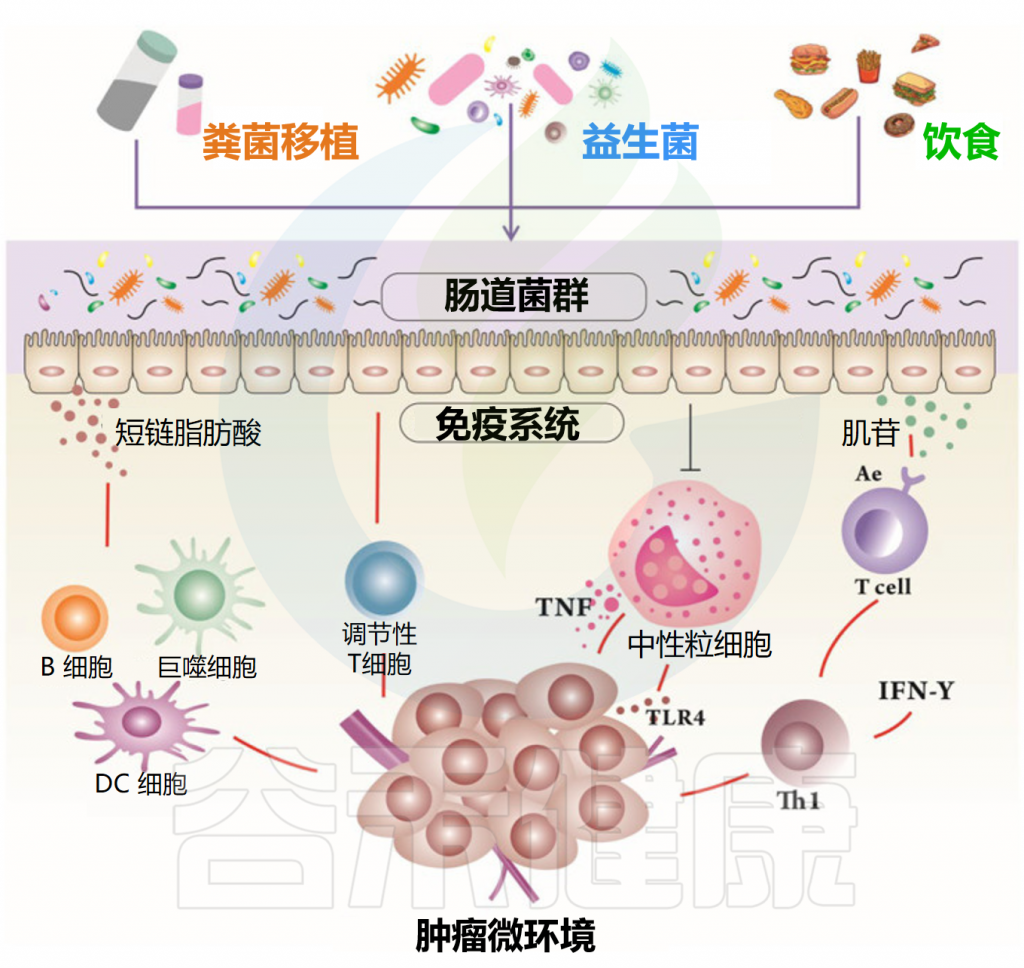
Feng P, et al.Front Microbiol.2024
施用益生菌
益生菌是一类存在于宿主体内并对宿主有益的细菌,给癌症患者服用益生菌的目的是重新激活患者受损的肠道微生物群,从而重建失败的共生微生物组的水平和功能。
益生菌在癌症辅助治疗中的作用


Sun J,et al.ISME J.2023
• 改善受损的肠道微生物群
益生菌还可以通过增加肠道微生物群的丰度、调节一些有助于产生致癌化合物的酶的活性以及改善肠道屏障来对抗胃肠道肿瘤。
23项随机对照试验表明,补充多种益生菌可改善结直肠癌患者的症状并提高生活质量,并减少传统治疗的不良反应。
• 增加短链脂肪酸的含量
增加短链脂肪酸的产量是一个关键途径。从人初乳中筛选出潜在益生菌唾液链球菌(Streptococcus salivarius),可抑制结直肠癌细胞增殖55%以上。唾液链球菌直接粘附并诱导癌细胞凋亡,促进短链脂肪酸的产生,并调节活化的B和T淋巴细胞。
丁酸梭菌(C.butyricum)依赖丁酸盐抑制胃肠道肿瘤的进展。C. butyricum调节Wnt/β-catenin的信号传导,减少高脂饮食诱导的结直肠癌,通过抑制NF-κB通路抑制结肠炎相关结肠癌,并增强免疫检查点抑制剂(ICIs)对肺癌的疗效。
一些产生短链脂肪酸的细菌有助于抗癌的例子
费氏丙酸杆菌(Propionibacterium freudenreichii)
通过产生作用于线粒体的丙酸和乙酸来诱导结直肠癌细胞的内在凋亡。
乳酸片球菌(Pediococcus acidilactici UAMS)是一种高产丁酸细菌,它能抑制人结肠癌细胞(HT29)和
SW480细胞(人结肠腺癌细胞)的增殖。
肠道Roseburia intestinalis、普拉梭菌(Faecalibacterium prausnitzii)、植物乳杆菌(Lactiplantibacillus plantarum)和Eubacterium callanderi也已被证明可增强结直肠癌中的抗癌免疫反应,同时产生丁酸盐。
用VSL#3益生菌治疗增加了丙酸盐和丁酸盐的水平,导致通过CCL20/CCR6轴募集Th17细胞,以减轻黑色素瘤的肺转移。鼠李糖乳杆菌GG ATCC 53103、罗伊氏乳杆菌DSM 17938、约氏乳杆菌LC1和其他益生菌不仅抑制结直肠癌细胞增殖,而且改善了化疗反应。
因此,补充益生菌可以在一定程度上增加短链脂肪酸,进而在癌症预防和治疗中发挥重要作用。
通过饮食成分改善
对于微生物群的组成和代谢功能,饮食可能是一种强大的调节剂。
• 摄入更多的膳食纤维可以降低结直肠癌等疾病的风险
膳食纤维作为短链脂肪酸的前体。研究证实,摄入更多膳食纤维可以降低患包括结直肠癌在内的多种疾病的风险。膳食纤维摄入量与患结直肠腺瘤和结直肠癌的几率之间存在统计学上显著且强烈的相关性。
作为代表性的膳食纤维,果胶显著增加了肠道微生物群的多样性,特别是产生丁酸的细菌,并促进肿瘤免疫微环境中的T细胞浸润,从而增强抗程序性死亡-1(抗PD-1)单克隆抗体(mAb)效果。
肥胖女性在一段时间内摄入富含菊粉和低聚果糖的混合物后,体内产生丁酸盐的细菌增多,还降低了餐后血糖水平。
• Omega-3等不饱和脂肪酸改善癌症治疗
Omega-3多不饱和脂肪酸(PUFA)人体不能合成,必须从食物中摄取,已被证明可以改善高脂血症、冠心病和动脉粥样硬化。每天服用更多的多不饱和脂肪酸时,可以观察到产生丁酸的细菌丰度增加。
与此同时,乳杆菌等益生菌增加,具核梭杆菌减少。研究表明,一些多不饱和脂肪酸可以辅助化疗药物5-氟尿嘧啶(5-FU)和奥沙利铂治疗结直肠癌并减少副作用。
• 益生元的摄入与结直肠癌呈负相关
益生元是不被宿主消化吸收、能选择性促进肠道内益生菌代谢和增殖的食物成分。常见的益生元包括菊粉、低聚果糖、半乳糖和一些藻类。益生元在癌症的发展中也发挥着重要作用。
最近进行的一项病例对照研究,包括1953名经组织学证实的结直肠癌患者和4154名对照者,发现结直肠癌风险与饮食中半乳糖摄入量呈负相关。
粪菌移植
除了补充益生菌、益生元外,粪菌移植也可能是增加短链脂肪酸、抵抗胃肠道肿瘤的一种选择。
• 粪菌移植有助于抗癌治疗的效果
在致癌物质诱导的常规小鼠或无菌小鼠中,来自结直肠癌患者的粪菌移植降低了肠道微生物群的丰富度并促进了胃肠道肿瘤的形成。
右旋糖酐硫酸钠或氧化偶氮甲烷的治疗可以在实验室小鼠中诱导结直肠癌,而从野生小鼠到实验小鼠的粪菌移植可以改善这一过程。
尽管没有临床证据表明粪菌移植可以直接治疗结直肠癌,但一项研究表明粪菌移植可以帮助提高化疗的疗效。将健康供体小鼠的粪便移植到FOLFOX治疗的小鼠体内,可以恢复FOLFOX治疗后破坏的肠道微生物群的组成,并减轻腹泻和肠粘膜炎症的严重程度。此外,粪菌移植通过增加微生物群多样性和调节免疫功能来增强抗PD-1治疗效果。
粪菌移植是塑造微生物组最直接的方式,通过粪菌移植直接增加产生短链脂肪酸的细菌,为胃肠道癌症的治疗提供了广阔的前景。
!
短链脂肪酸调节对化疗和免疫疗法的反应
短链脂肪酸还可以调节肿瘤对放化疗和免疫疗法的反应。临床研究发现,术前新辅助放化疗后,有反应的结直肠癌患者粪便中产生丁酸的细菌和短链脂肪酸水平比未接受治疗的患者更丰富。
• 丁酸盐协同增强抗癌作用
丁酸盐可作为奥沙利铂的增效剂,协同增强抗癌作用。丁酸盐通过调节CD8+ T细胞直接促进奥沙利铂的化疗疗效。
此外,与结直肠癌中无反应患者相比,有反应患者血清中的丁酸盐水平较高。与单独放疗相比,放疗-丁酸盐组合显著增强了抗癌效果。丁酸盐可以通过促进FOXO3A介导的转录来诱导细胞周期停滞,同时保护正常细胞免受辐射损伤。由于HDACs抑制剂已被证明可以增强放疗的敏感性,因此推测丁酸盐可能是因为抑制HDACs而增强了放疗的疗效。
丁酸盐还可以通过GPR109a-AKT信号通路增强5-氟尿嘧啶(5-FU)的功效。同时,短链脂肪酸降低了5-FU的促炎作用,并增加了粘膜中紧密连接蛋白的表达。
然而,产丁酸细菌的异常活性和患者体内过量的丁酸会导致对化疗药物的耐药性。结果表明,对丁酸盐具有抗性的结直肠癌细胞系表现出明显的化学抗性。
通过调节自身免疫细胞和免疫分子来靶向杀伤肿瘤细胞,同时减少对正常组织的损伤,已成为肿瘤免疫治疗的代表。
人类肠道微生物群在肿瘤生长、发展和治疗中发挥着关键作用。肠道菌群、宿主免疫系统和肿瘤之间的相互作用可以为调整肠道菌群以优化肿瘤微环境和增强癌症免疫治疗提供有价值的见解。
短链脂肪酸是肠道微生物群的重要产物,已被证明可以改变免疫细胞的分化和功能以及细胞因子的产生和释放,通过多种信号通路控制肿瘤的生长和转移并诱导细胞凋亡。此外,短链脂肪酸还有助于提高放疗和化疗的治疗效果,减少不良反应。
未来,个性化医疗可能会结合基于微生物组的诊断和治疗策略。以肿瘤免疫为目标,补充微生物源性 短链脂肪酸已成为诊断、治疗和预防肿瘤的新方法。可重点关注益生菌和粪便微生物移植以及合理的饮食,提高短链脂肪酸水平,调节胃肠道微生态,激活有效的抗癌作用。
主要参考文献
Feng P, Xue X, Bukhari I, Qiu C, Li Y, Zheng P, Mi Y. Gut microbiota and its therapeutic implications in tumor microenvironment interactions. Front Microbiol. 2024 Jan 23;15:1287077.
Dong Y, Zhang K, Wei J, Ding Y, Wang X, Hou H, Wu J, Liu T, Wang B, Cao H. Gut microbiota-derived short-chain fatty acids regulate gastrointestinal tumor immunity: a novel therapeutic strategy? Front Immunol. 2023 Apr 14;14:1158200.
Sun J, Chen F, Wu G. Potential effects of gut microbiota on host cancers: focus on immunity, DNA damage, cellular pathways, and anticancer therapy. ISME J. 2023 Oct;17(10):1535-1551.
He M, Wei W, Zhang Y, Xiang Z, Peng D, Kasimumali A, Rong S. Gut microbial metabolites SCFAs and chronic kidney disease. J Transl Med. 2024 Feb 18;22(1):172.
Hanus M, Parada-Venegas D, Landskron G, Wielandt AM, Hurtado C, Alvarez K, et al.. Immune system, microbiota, and microbial metabolites: The unresolved triad in colorectal cancer microenvironment. Front Immunol (2021) 12:612826.
Pansy K, Uhl B, Krstic J, Szmyra M, Fechter K, Santiso A, et al.. Immune regulatory processes of the tumor microenvironment under malignant conditions. Int J Mol Sci (2021) 22(24):13311.
Luu M, Riester Z, Baldrich A, Reichardt N, Yuille S, Busetti A, et al.. Microbial short-chain fatty acids modulate CD8(+) T cell responses and improve adoptive immunotherapy for cancer. Nat Commun (2021) 12(1):4077.
Kurokawa H, Ito H, Matano D, Terasaki M, Matsui H. Acetic acid enhances the effect of photodynamic therapy in gastric cancer cells via the production of reactive oxygen species. J Clin Biochem Nutr (2022) 71(3):206–11.
Marques C, Oliveira CS, Alves S, Chaves SR, Coutinho OP, Corte-Real M, et al.. Acetate-induced apoptosis in colorectal carcinoma cells involves lysosomal membrane permeabilization and cathepsin d release. Cell Death Dis (2013) 4:e507.

谷禾健康

在研究肠道菌群或复杂微生物样本构成时,“门”(Phylum)是细菌分类的高级分类单位之一。
细菌分类依次为门纲目科属种亚种,最大的分类层面是门,以前写过人群肠道菌群构成主要是以拟杆菌门和厚壁菌门为主,大部分人群占比超90%(个别的变形菌门或放线菌门占比也很高),作为两大“细菌王国”,这两大王国有着不同的生态和代谢属性,又有着相似的营养和生存需求,它们如同天平的两端的砝码,不同的人有着不同倾斜,即使同一个人不同时期不同身体状态下天平的倾斜都不一样。
拟杆菌门被比喻为肠道微生物群落的“多面手”,有超过7000种不同的革兰氏阴性菌组成,主要来自拟杆菌属、副拟杆菌属、普氏菌属和卟啉单胞菌属。它们的脂多糖和鞭毛蛋白与细胞受体相互作用,并通过细胞因子合成增强免疫反应。
拟杆菌门作为多糖降解联盟的成员,尤其是拟杆菌属和普雷沃氏菌属,具有多种可以利用多糖的聚糖和糖苷酶。它们有助于分解膳食纤维和淀粉释放能量,并且它们可能是丙酸盐的主要来源。
拟杆菌门一些细菌的功能还包括胆汁酸的解离。肠道微生物群,特别是肠道拟杆菌,一定程度上也具有使初级胆汁酸解离和脱水并将其转化为人结肠中次级胆汁酸的能力。它们也参与蛋白质分解过程中有毒产物的释放。比如氨,组胺,硫化氢等,这些高浓度的产物会对肠黏膜产生毒性。
该群体的成员具有一些可能有助于抑制炎症的活动,但它们也有可能促进炎症,其中一些已知是机会病原体。
厚壁菌门细菌大多为革兰氏阳性菌,通过短链脂肪酸合成在宿主的营养和代谢中发挥关键作用。
通过其代谢产物,厚壁菌门细菌与其他组织和器官间接连接并调节饥饿和饱腹感。厚壁菌门由大量功能更加多样化的核心细菌组成。从代谢的角度来看,共生梭菌簇 XIVa 和 IV 通过产生短链脂肪酸在宿主和肠道稳态中发挥着重要作用,使肠道通透性正常化,参与脑肠轴调节。许多厚壁菌门的能力与宿主的体重有关。
F/B比率升高或降低被视为生态失调,前者通常与肥胖,代谢障碍相关,这可能与从食物中提取热量增加、脂肪沉积和脂肪生成、胰岛素敏感性受损有关;而后者则与炎症性肠病,抑郁,阿尔茨海默病等相关,这可能与短链脂肪酸尤其丁酸的生成减少,蛋白代谢物组胺,脂多糖累积等相关诱导的免疫炎症反应相关。
目前许多研究工作都集中在识别特定的微生物特征,特别是与肥胖、2型糖尿病和炎症相关的微生物特征。
我们从谷禾肠道菌群检测数据库中随机抽取5万例样本,统计的人群厚壁菌门/拟杆菌门(F/B)比率如下:
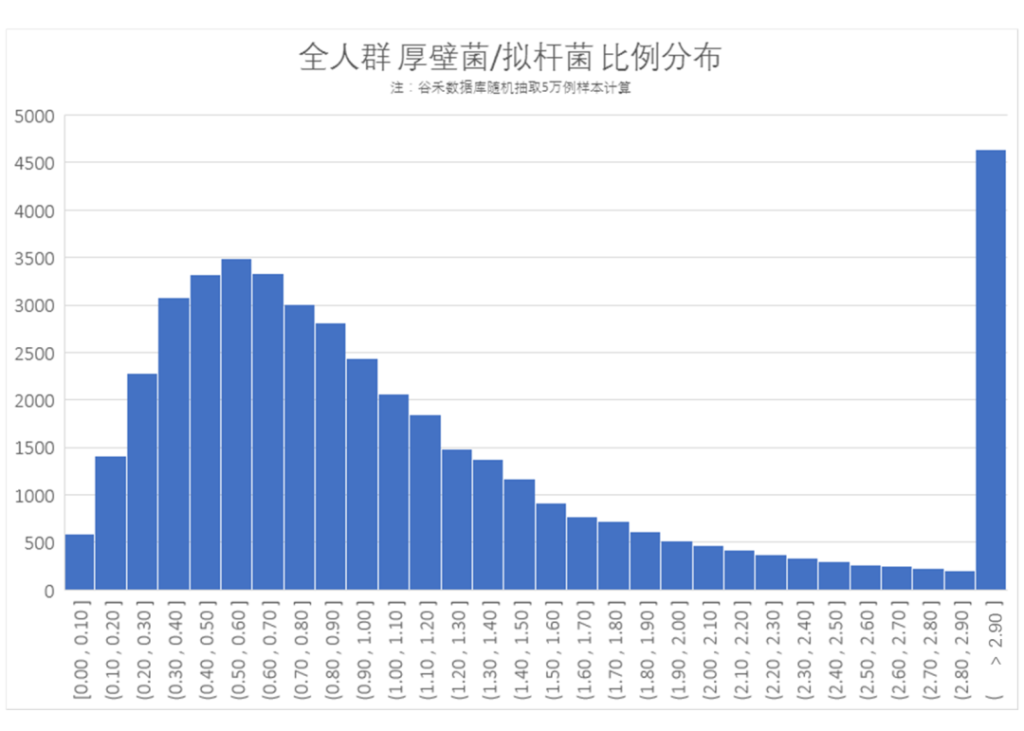
可以看出大部分人群的厚壁菌/拟杆菌比率在0.30-1.0之间(谷禾健康数据库随机抽样5万例样本),表明国人大部分人群肠道菌群的构成中拟杆菌占比多一点;同时抽样人群中1/10人厚壁菌/拟杆菌比率大于2.9,表明也有相当一部分人群厚壁菌门占比较高。
一般而言,从出生到成年,厚壁菌门/拟杆菌门的比例不断增加,并随着年龄的增长而进一步改变。该比率在婴儿、成人和老年人之间存在差异。它可能与生命不同阶段细菌谱的整体变化有关。
厚壁菌门/拟杆菌门比率是一个考虑高水平分类等级(即门)的指数,同一群体的受试者之间厚壁菌门和拟杆菌门的相对丰度差异很大。这可能是由于许多与生活方式相关的因素造成的,包括饮食、疾病状态、食品添加剂和污染物、抗生素消耗、体力活动等影响胃肠道微生物群组成的因素。
由于菌群是一个复杂的生态体系,门层面的简单划分只能提供一个最简单的线索,想要了解肠道菌群需要从最主要的核心菌属,常见的有害菌属以及大量功能菌属的构成来更加准确的分析,此外菌群的代谢通路也提供了不同角度的信息。
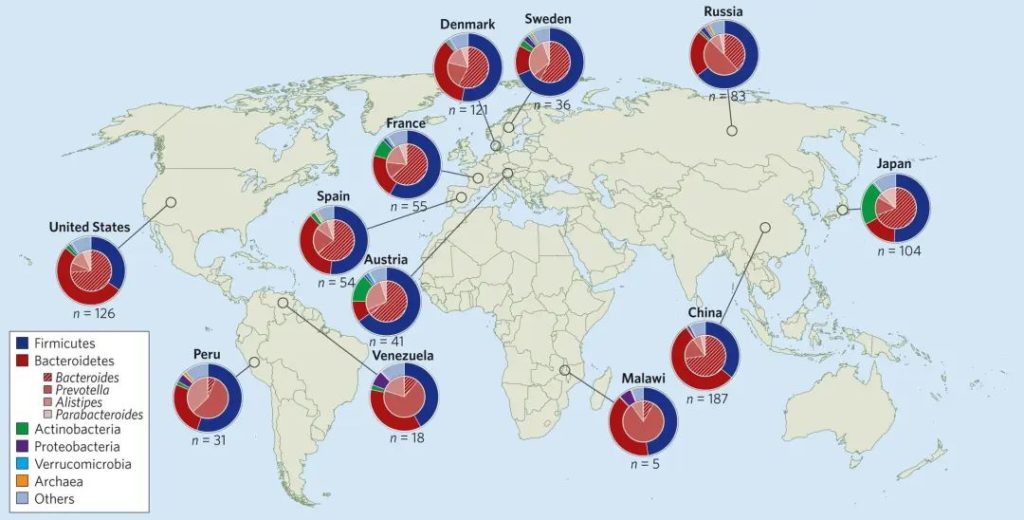
Wexler AG,et al.Nat Microbiol.2017
大多数健康成人微生物群仅由两个细菌门控制——革兰氏阳性厚壁菌门(许多属)和革兰氏阴性拟杆菌门(主要是拟杆菌属、另枝菌属、副拟杆菌属和普氏菌属)——它们共同构成了微生物中的大多数细菌分类群。
此外还有其他分类群包括变形菌门、放线菌门、梭杆菌门、疣微菌门、产甲烷古菌、真核生物(原生生物和真菌)和其他更短暂的定植者。
健康个体中发现的类群在家庭成员(例如父母及其子女)之间往往最相似,而在不同文化和地理空间(例如西方社会与非西方社会)之间则最不相似。
厚壁菌门(Phylum Firmicutes)是细菌的一个门,大多数具有革兰氏阳性细胞壁结构。然而,一些细菌,如巨球菌属、梳状菌属、月单胞菌属和嗜发酵菌属,具有多孔的假外膜,导致它们被染成革兰氏阴性。
科学家们曾经将厚壁菌门分类为包括所有革兰氏阳性细菌,但最近将它们定义为相关形式的核心组,称为低 G+C 组。与放线菌相反。它们有圆形细胞,称为球菌(单球菌),或杆状细胞(芽孢杆菌)。厚壁菌门缺乏脂多糖,而是向宿主呈现厚厚的肽聚糖层;研究人员已经发现了200多种不同类型的属于厚壁菌门的细菌。
★ 厚壁菌门中有许多有益的菌
厚壁菌门的成员包括许多有益的菌。比如乳酸菌是一种常见于酸奶和其他发酵乳制品中的益生菌,属于该门。这些微生物会产生醋酸盐(另一种促进健康的短链脂肪酸)以及乳酸和抗菌物质,以防止病原体定植。
又比如普氏栖粪杆菌(Faecalibacterium prausnitzii),又名:普拉梭菌,是人类肠道菌群中最重要的细菌之一,占健康人粪便样本中检测到的细菌总数的5-15%,是丁酸的重要生产者之一,具有抗炎作用,维持细菌酶的活性,保护消化系统免受肠道病原体的侵害。
★ 厚壁菌门中也存在一些致病菌
但是一些致病菌也属于该门。例如,产气荚膜梭菌是一种引起胃肠道感染的细菌。还有金黄色葡萄球菌,它是一些严重感染的常见原因。
丁酸盐是研究最深入的短链脂肪酸之一,是肠道上皮细胞营养的主要来源。丁酸盐的消耗与肠道屏障完整性受损有关。
注:研究支持,长寿、健康的老年人肠道内的丁酸细菌含量明显较高。
人类肠道包含一个非常密集的代谢活跃微生物群落。然而,只有有限数量的肠道细菌为丁酸生产者。人类肠道中大多数丁酸合成细菌分布于厚壁菌门。在厚壁菌门中,毛螺菌科、瘤胃球菌科、真杆菌科和梭状芽孢杆菌科是四个重要的丁酸合成科。
梭菌目的簇 IV、XIVa、XVI 和 I 包含大多数丁酸盐生产菌种。其中两个重要的物种,直肠真杆菌和普拉梭菌分别属于梭菌簇 XIVa 和梭菌簇 IV,占健康成人粪便样本中肠道菌群总数的12-14% 。此外,还有罗氏菌属,粪球菌属,瘤胃球菌属, Anaerostipes ,丁酸弧菌属和梭菌属。
分布在XIVa 簇中的Butyricicoccus pullicaecorum、Subdolicapsulu variabile、Anaaerotruncus colihominis和分布在 IV 簇中的Papillibacter cinnamivorans是其他产丁酸菌种。
据报道,属于韦荣氏球菌科、热厌氧杆菌科 III 的Megasphaera elsdenii和Caldocellum saccharolyticum也能合成丁酸盐。
最近,对人类样本的高通量宏基因组测序表明,Rawsonibactera saccharolyticus是瘤胃球菌科中的一个新物种,并且肠单胞菌AF211编码丁酰辅酶A:用于合成丁酸的乙酰辅酶A转移酶。
许多厚壁菌门细菌可以产生内生孢子,其耐干燥并且可以在极端条件下生存。孢子在细菌生长中起着重要的作用。细菌的孢子是一种休眠状态,可以在不利环境下存活,并在适宜条件下重新发芽成为活跃的细菌。这种休眠状态使得细菌能够在恶劣条件下存活并传播。
★ 内生孢子可以帮助细菌在恶劣条件下存活
内生孢子由细菌的DNA和部分细胞质组成,周围有一层非常坚韧的外层。它们可以在没有营养的情况下生存,并且能够抵抗紫外线、干燥、高温、极端冷冻和化学消毒剂。
厚壁菌门的代谢偏好
科学家发现,人类肠道微生物群虽然独特,但都可以按照几个分类划分下,称为肠型。第三种肠道型,被称为“谷物爱好者” ,通常以瘤胃球菌(厚壁菌门的成员)为主。
肠型往往可以追溯到长期的饮食习惯。顾名思义,具有“谷物爱好者”微生物组类型的人倾向于消耗更多全谷物中的抗性淀粉和膳食纤维。
✦ 高纤维饮食的人体内厚壁菌更丰富
高纤维饮食可以增加厚壁菌门的丰度并减少拟杆菌的丰度 ,从而增加肠道内短链脂肪酸的浓度。
而葡萄籽原花青素显著降低了肥胖大鼠肠道菌群中厚壁菌门的含量,提高了拟杆菌门的含量,显著降低了厚壁菌门与拟杆菌门比值。
✦厚壁菌偏向从膳食蛋白和循环尿素中获取氮
在厚壁菌门成员中,偏好尿素氮的属往往是菊粉的疯狂使用者,即使用菊粉和尿素合成自己的氨基酸。这包括一些脲酶阴性菌属,它们可能通过交叉喂养获得尿素氮。
此外,在厚壁菌中也看到了一些属更喜欢从膳食蛋白质中获得氮,而其他菌属更喜欢循环尿素。
静脉注射尿素以提高循环尿素浓度后,偏好尿素的厚壁菌以及阿克曼菌的丰度大幅增加。
膳食蛋白质和循环尿素是厚壁菌的主要氮原料,而分泌的宿主蛋白质为拟杆菌提供氮。
!
如果厚壁菌门过高意味着什么?
可能的原因:
– 不良的饮食习惯
– 生态失调
– 消化不良
– 胃酸过少
– 代谢疾病
可能的治疗方法和注意事项:
– 平衡共生细菌
– 当厚壁菌门含量较高时,考虑主要使用双歧杆菌益生菌和布拉氏酵母菌
– 乳杆菌属和芽孢杆菌属(益生菌中发现)可以提高厚壁菌门的数量
– 优化饮食结构:低脂肪饮食可能有助于厚壁菌门水平正常化
滋养肠道内厚壁菌门的食物
纤维和淀粉,是这些细菌的能量来源。富含水果、蔬菜、豆类和全谷物的饮食也是理想的。
研究表明,地中海饮食与更丰富的厚壁菌门有关,包括普拉梭菌。另一方面,富含动物蛋白、脂肪和糖的西方饮食会对有益的这些细菌产生负面影响。
如果想增加肠道中厚壁菌门的丰度,那么应该多吃高纤维食物。以下是一些可以添加到饮食中的食物,以支持您的肠道微生物组并促进厚壁菌门和丁酸盐的产生:
-苹果
-蒜
-大麦
-菊苣根
-燕麦
-亚麻籽
-洋葱
拟杆菌是肠道生态系统中非常成功的竞争者,表现出相当大的营养灵活性以及对宿主和肠道环境施加的压力做出反应的能力。很难权衡肠道拟杆菌对宿主是否产生负面或正面影响。
拟杆菌是复杂碳水化合物的主要降解者,迄今为止调查的所有生态系统中都普遍发现该属,在土壤以及人类和动物肠道中尤其占主导地位。大多数已测序的拟杆菌基因组编码大量多糖降解酶(CAZymes),表明代谢重点是聚糖降解。
CAZymes 在碳水化合物活性酶数据库中分为类别和家族,其中降解酶存在于糖苷水解酶(GH)、多糖裂解酶(PL)、碳水化合物酯酶(CE)和辅助活性酶 (AA) 类别中。
拟杆菌还通过与免疫系统的相互作用,在激活T细胞介导的反应中发挥作用,从而有助于宿主的整体健康。
✦ 防止特定炎症反应
基于多项研究,发现脆弱拟杆菌通过产生称为两性离子多糖的多糖来激活CD4+ T细胞。CD4+ T细胞的产生会刺激白细胞介素10的释放,从而防止特定的炎症反应和脓肿形成。
肠道免疫保护取决于拟杆菌、白细胞介素36信号和巨噬细胞的发育。拟杆菌的这种作用需要其保守的共生定植因子的多糖利用位点。
✦ 抑制胃肠道中的病原体
与胃肠道中发现的其他一些细菌相比,研究表明拟杆菌门的一些成员对各种抗生素和胆汁等物质具有耐药性,这给了他们竞争优势。
除了这种竞争优势之外,这些细菌还被证明在调节胃肠道中其他正常菌群和病原体的数量方面发挥着重要作用。
拟杆菌可以积极改善肠道环境,使其更适合自身和其他微生物。
✦降低肠道内氧水平从而促进厌氧菌生长
例如,许多编码细胞色素bd氧化酶,据推测该酶可以降低细胞内氧水平,进而降低肠道氧水平,从而允许严格厌氧菌生长,否则这些厌氧菌会被氧气的存在杀死。
这种耐受和降低氧气水平的能力可能有助于拟杆菌传播到新宿主,这可能是它们在哺乳动物中如此广泛传播的主要原因。
✦改变肠道的营养状况
它们还可以通过促进宿主的生理变化来诱导某些食物来源(例如岩藻糖基化糖蛋白)的产生,或通过从糖蛋白中释放岩藻糖和唾液酸残基来改变肠道的营养状况,这些残基可以被其他微生物消耗,包括病原体。
通过比较缺乏自身微生物的无菌动物和与单个拟杆菌属菌株和突变体单相关的无菌动物(出生时无菌但后来被微生物定殖),已经鉴定了许多这些拟杆菌属依赖性的肠道环境变化。
✦拟杆菌拥有多糖利用位点有助于代谢
尽管人们可能会想象肠道中的生命充满了微生物的过多食物选择,但在结肠(细菌密度最高的地方),简单、容易获得的糖大部分已经被消耗或吸收。其中的残留物是复杂的长链多糖,它们不能自由吸收,也不能被人类酶促消化。对于许多细菌来说,这些复杂的多糖同样难以处理,并且无法跨膜运输。
然而,早期研究证实拟杆菌是熟练的聚糖降解剂,具有识别和代谢十多种植物和宿主来源的多糖的不同寻常的能力。拟杆菌属物种通过基因簇来实现这一点,这似乎是拟杆菌特有的,称为多糖利用位点(PUL)。
多糖利用位点可以确定拟杆菌可以占据哪些代谢生态位,甚至可以确定它们在肠道内的生物地理位置。多糖利用位点被如此分类是因为它们的susC和susD的同系物,以及其他成分(糖苷水解酶、多糖裂解酶、糖基转移酶、碳水化合物酯酶),它们对于分解多种植物或宿主来源的聚糖很重要。
肠道细菌的其他谱系,包括革兰氏阳性放线菌,降解和输入膳食多糖的途径远不那么复杂,这在很大程度上是由于缺乏外膜屏障。例如,短双歧杆菌使用多结构域、细胞表面锚定酶(而不是一系列单独的酶),可以结合并降解聚合物,例如淀粉、支链淀粉和糖原。
拓展
比较基因组分析已在每个拟杆菌属中鉴定出数十种不同的多糖利用位点。例如,Bacteroides thetaiotaomicron是第一个对其基因组进行测序的拟杆菌属成员,将其 6.26 Mbp 基因组的近五分之一专用于88个不同的多糖利用位点。
拟杆菌不是同时表达所有多糖利用位点以捕获周围环境中可能存在的任何多糖,而是通过大量SusR样调节因子、混合双组分系统和涉及胞质外 σ/抗的跨包膜信号通路来严格调节其表达。
也许是由于在跨外膜运输之前需要部分降解长多糖链,B. thetaiotaomicron和其他肠道拟杆菌已经成功地将适当的多糖利用位点转录与其相应多糖分解中间体的丰度(而不是丰度)耦合起来。
这使得肠道细菌能够快速适应营养可用性的变化。糖分解物质形成甲酸盐、乙酸盐、乳酸盐、丙酸盐和琥珀酸盐作为主要发酵产物。拟杆菌可能是结肠中丙酸盐形成的主要贡献者。
由于多糖利用位点激活是肠道环境的产物,富含植物源性多糖和糖蛋白的饮食将导致多糖利用位点暂时上调,从而降解这些膳食营养素。然而,当这些底物稀缺时,例如在禁食期间或某些低纤维饮食期间(如高糖、高脂肪的西方饮食),亲糖拟杆菌会改变其转录谱以消耗宿主衍生的聚糖,这些暂时的转换可能是导致某些细菌在婴儿期最初在肠道定殖并在我们一生中持续存在的主要因素。
根据最近使用动物模型的研究,拟杆菌属可以在相对较短的宿主婴儿期主要依靠宿主聚糖生存,但当在多个宿主世代的时间内被迫以低纤维饮食为生时,它们最终可能会灭绝。
有的菌会通过破坏中性粒细胞趋化性等机制帮助逃避免疫系统(例如,伤寒沙门氏菌)和逃避宿主补体系统(例如肺炎克雷伯菌)。
相比之下,拟杆菌使用一种称为相变的过程,以开/关方式控制其荚膜多糖生物合成位点的表达。例如,脆弱拟杆菌从八个生物合成位点产生不同的荚膜多糖,其表达受到可逆启动子区域和反式位点抑制剂的严格调控,限制多个位点的同时表达,从而使脆弱拟杆菌的同基因群体共同表现出广泛的多样性。当脆弱拟杆菌漏入通常无菌的腹膜腔时,可能会发生腹膜炎。
注:绝大多数人类腹膜炎病例都是由脆弱拟杆菌引起的。
目前,拟杆菌门中研究的最充分的,包括拟杆菌属和普氏菌属以及卟啉单胞菌属。
✦ 卟啉单胞菌属可导致急性坏死溃疡性牙龈炎
卟啉单胞菌属的成员作为共生体或机会性病原体生活在人类口腔中。牙龈卟啉单胞菌引起临床上侵袭性牙龈炎,可导致急性坏死溃疡性牙龈炎或扩展到口腔和面部组织,这种情况称为坏疽性口炎或口腔癌。
✦ 普雷沃氏菌也是一种条件性致病菌
普氏菌属是一个大属,包括50多个不同的物种。大多数可以从口腔和肠道中分离出来。普雷沃氏菌属存在于人类中,帮助分解蛋白质和碳水化合物食物。也可作为条件致病菌,引起牙周和牙齿、肠道炎症、类风湿性关节炎、细菌性阴道炎等问题。
大型基因组计划,包括美国国立卫生研究院(NIH)资助的人类微生物组项目(http://nihroadmap.nih.gov/hmp/)和欧盟资助的 MetaHIT 项目 (http://www.metahit.eu)对50多种人类来源的拟杆菌门的拟杆菌和普氏菌分离株进行了测序。
基因组草图可从 Genbank 公开获得,并揭示这些物种拥有多种糖苷酶,这些糖苷酶具有预测的对抗植物和宿主来源的多糖的活性,以及维生素和辅因子合成的许多途径。
拟杆菌门的基因组大小相对较大,例如B.thetaiotaomicron 为 6.26 Mb。迄今为止在拟杆菌属中发现的16S rRNA基因的最高拷贝数为7个(在普通拟杆菌中)。
✦ 拟杆菌的组成和代谢受到饮食调节
在全基因组水平上,拟杆菌属与副拟杆菌属共享超过1000个蛋白质家族的核心,但与卟啉单胞菌属和普雷沃菌属共享较少数量的核心家族蛋白质家族。它们的组成和代谢活动在很大程度上受饮食调节。
拟杆菌与高脂肪和蛋白质的摄入量有关,而普雷沃氏菌与富含植物的饮食(高水平的复合碳水化合物和水果和蔬菜的摄入量)有关。因此,拟杆菌属和普雷沃氏菌属物种在人体内具有其特定的栖息地,因为它们大多数是拮抗的。
厚壁菌门与拟杆菌门之间的比率(F/B)与维持体内平衡有关,该比率的变化可能导致各种病理。
例如,特定厚壁菌门或拟杆菌门物种丰度的增加分别导致肥胖和肠道炎症。尽管人们非常关注 F/B 比率,但应该记住,这一比率可能会受到其他门的增加的影响,但是其他门的菌群失调增加或减少并不一定会改变 F/B 比率。
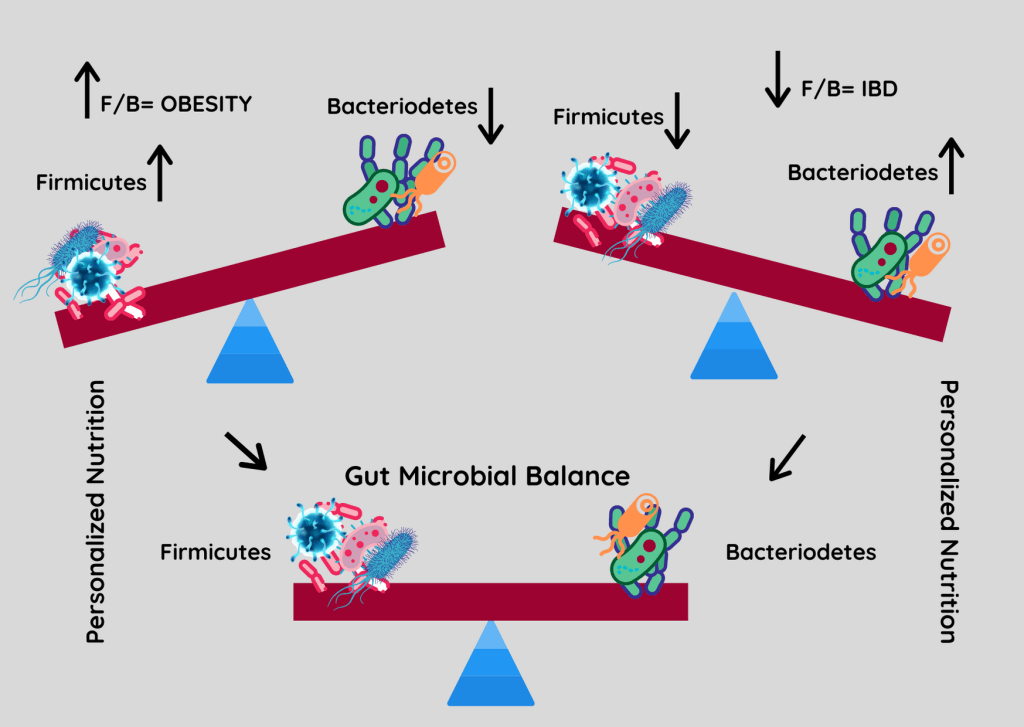
Stojanov S,et al.Microorganisms.2020
肥胖是一种复杂的、多因素的疾病,其原因包括宿主遗传背景、体力活动减少和食物摄入过多等多种因素。在过去的几十年里,肠道微生物群被认为是有利于脂肪储存、体重增加和胰岛素抵抗的额外因素。
世界范围内的研究正在不断寻找其致病因素。厚壁菌门和拟杆菌门的改变首先在肥胖动物和受试者中被描述,这些动物和受试者表现出厚壁菌门丰度增加,而拟杆菌门却减少了。
✦ F/B 比率较高时相同食物会吸收更多能量
当F与B的比例较高或体重增加和肥胖状态时,这两个细菌门影响我们体重的原因是它们调节我们吸收的脂肪量。想象一下两个人都消耗2000卡路里,但F与B的比例不同。F/B 比率较高的一种会吸收更多的卡路里,因此会比另一种增加更多的体重。因此,重点应该是平衡F与B的比例,一方面防止肥胖,另一方面预防炎症性肠病的发生。
当受试者接受热量限制饮食一年后,他们的拟杆菌门丰度增加,厚壁菌门/拟杆菌门比例正常化,同时体重减轻。这些研究得到了对喂食高脂肪或高纤维饮食的动物的研究的支持,这些研究显示厚壁菌门和拟杆菌门的丰度分别较高。
基于这些结果以及从肥胖动物和人类身上获得的其他结果,有人提出厚壁菌门比拟杆菌更能有效地从食物中提取能量,从而促进有效吸收热量和随后的体重增加。
肥胖双胞胎的微生物组富含编码营养转运蛋白的基因,而瘦双胞胎的微生物组富含编码与碳水化合物代谢相关的酶的基因。
最近发表的一项系统综述显示,大多数研究都支持 F/B 比率增加与肥胖之间的关系。
对肥胖和非肥胖日本受试者的粪便样本进行的一项研究显示,他们的 F/B 比率存在显著差异。厚壁菌门的百分比为 37.0 ± 9.1%(非肥胖者)和 40.8 ± 15.0%(肥胖者),而拟杆菌门的百分比为 44.0 ± 9.8%(非肥胖者)和 37.0 ± 14.0%(肥胖者)。
在61名乌克兰成年人中也报告了类似的结果,其中 F/B 比率与体重指数(BMI)显著相关。F/B 比率≥ 1 的个体超重的可能性比F/B 比率<1 的个体高出23%。
同样,卡塔尔受试者(37名肥胖者和36名瘦者)表现出肠道微生物群的改变;肥胖和瘦受试者的 F/B 比率分别为 2.25 ± 1.83 和 1.76 ± 0.58。在哈萨克族和比利时学童中,肥胖组的F/B比值显著高于对照组。
✦ 肥胖人群与正常人群拟杆菌存在差异
然而,两个拟杆菌属的存在差异:与肥胖组相比,正常组中拟杆菌属的高出20%,而肥胖组中普雷沃氏菌属比正常组高出19%。拟杆菌属和普雷沃氏菌属都属于拟杆菌门。
同一群体的受试者之间厚壁菌门和拟杆菌门的相对丰度差异很大。这可能是由于许多与生活方式相关的因素造成的,包括饮食、体力活动、食品添加剂和污染物、抗生素消耗等影响胃肠道微生物群组成的因素。
这种高度变异性可能解释了在比较正常体重和肥胖受试者之间的微生物群时观察到的矛盾结果,使得很难将厚壁菌门/拟杆菌门比率与确定健康状况联系起来。
重要的是要观察肠道微生物种群结构的整体组成,将其作为肥胖和肥胖相关病理(例如GSD)的指标,而不仅仅是厚壁菌门/拟杆菌门的比率。然而,在我们看来,可以修改这个比率,例如引入表征拟杆菌门底下的拟杆菌属或普氏菌属与梭状芽胞杆菌 XIVa 簇菌的比例。
!
F/B 比改变导致肥胖的争议
然而,与这些结果相反,许多研究没有观察到该参数的任何改变,甚至报告肥胖动物和人类中厚壁菌门/拟杆菌门的比例降低。
事实上,在大多数研究中,肥胖患者比瘦受试者表现出更少的细菌多样性,这表明在科、属或种水平上存在其他组成变化,这可能比厚壁菌门/拟杆菌门比率更相关。
✦肥胖增加可能与长期暴露脂多糖有关
关于这一点,代谢性内毒素血症的假说提出,肥胖增加和全身炎症的发展可能是由于长期暴露于脂多糖所致,脂多糖是一种源自革兰氏阴性细菌的促炎分子,它会通过肠腔进入血液。
这一假设与肥胖症中所报道的拟杆菌门丰度下降的情况并不相符,因为该门是肠道微生物群中革兰氏阴性菌的主要群体。
这种差异可以通过这样的事实来解释:来自拟杆菌门细菌的脂多糖的内毒素活性被认为低于来自其他革兰氏阴性细菌(例如属于变形菌门的细菌)的内毒素活性。有趣的是,在肥胖受试者或动物中也观察到变形菌门的增加,并且在无菌小鼠中施用变形菌门成员肠杆菌会导致这些动物出现肥胖和胰岛素抵抗。
✦ F/B比率增加与短链脂肪酸产生无关
另一方面,厚壁菌门/拟杆菌门比例的增加与肥胖个体中观察到的短链脂肪酸产生无关。事实上,据报道,拟杆菌门主要产生乙酸和丙酸,而厚壁菌门则产生更多的丁酸。丁酸盐被认为是一种促进健康的分子,因为它具有增加胰岛素敏感性、发挥抗炎活性、调节能量代谢和增加瘦素基因表达的能力。
结肠中的丙酸盐刺激L-肠内分泌细胞释放GLP-1和 PYY,从而抑制食欲。它还可能到达门静脉循环,主要被肝脏捕获,参与肝糖异生并减少参与脂肪酸和胆固醇从头合成的酶的表达。
乙酸也被吸收并到达全身循环和周围器官,包括脂肪组织、肌肉和大脑。在肝脏中,与丙酸盐相反,它刺激肝脏合成脂质,导致血脂异常。在大脑中,它激活副交感神经系统,分别促进胰腺和胃粘膜分泌胰岛素和生长素释放肽。
这些事件会导致脂肪储存和食欲增加,从而导致肥胖。根据这些结果,醋酸盐通常被认为更容易导致肥胖。肥胖个体中厚壁菌门/拟杆菌门比例的增加意味着这些受试者中丁酸盐的产量较高,丙酸盐和乙酸盐的产量较低,这一发现与这些短链脂肪酸各自的抗肥胖和致肥胖作用部分矛盾。一种解释是,肥胖个体中产生丁酸的细菌减少,并逐渐被属于同一门的其他细菌取代,导致结肠腔中丁酸的产生量降低。例如,葡萄球菌属和罗伊氏乳杆菌的丰度增加(均来自厚壁菌门)
肥胖状态还与A. muciniphila (疣微菌门)丰度较低有关,这是一种粘蛋白降解细菌,有助于稳定肠道屏障功能、分泌抗菌肽和控制炎症。
✦生理及病理状况都会影响肠道微生物群
另一方面,性别、年龄、宿主遗传学的差异。男性和女性的肠道微生物群存在差异,例如男性中拟杆菌-普雷沃氏菌群的水平较高,而女性中厚壁菌门的比例较高。然而,个别研究也发现女性中拟杆菌门的丰度最高。
此外,存在病理状况(糖尿病、心血管疾病、炎症性肠病等)。例如,Oddi括约肌松弛与胆管结石有关,可能是由于肠内容物回流增强改变了微环境所致。
治疗(抗生素、二甲双胍等)通过富集Akkermansia muciniphila以及几种产生短链脂肪酸的微生物群(丁酸弧菌、两歧双歧杆菌等)来改变肠道微生物群组成。
总之,这些导致厚壁菌门/拟杆菌门比率并不是与肥胖相关的微生物群失调的有力标志。
我们建议与肥胖相关的肠道微生物组研究不应该研究肥胖本身的分类标志物,而应侧重于确定用于将患者分层为亚组的分类标志物。引入微生物组患者分层将通过直接操纵患者微生物组来制定个性化治疗决策,从而改善肥胖的管理。
炎症性肠病代表小肠和大肠炎症反应引起的肠道疾病,由两种疾病组成:克罗恩病(CD)和溃疡性结肠炎(UC)。
溃疡性结肠炎是由结肠和直肠(从大肠末端开始到肛门结束的腔室)的长期炎症引起的,而克罗恩病是由结肠或回肠(小肠的最后部分)或两者的长期炎症引起的。
✦ 炎症性肠病患者厚壁菌门丰度下降
肠道微生物群会导致这些疾病。具体来说,当厚壁菌门减少或拟杆菌门相对于厚壁菌门增加时(两种情况下肠道菌群失调),就会导致慢性炎症和消化系统疾病,如克罗恩病和溃疡性结肠炎。
一项研究检查了克罗恩病和溃疡性结肠炎患者以及健康对照活检组织中的微生物多样性。观察到厚壁菌门丰度下降;更准确地说,克罗恩病患者中梭状芽胞杆菌类细菌减少,但溃疡性结肠炎患者或健康个体中则没有减少。
相反,与溃疡性结肠炎患者和健康个体相比,克罗恩病患者的拟杆菌丰度显著增加(分别为74.97%、64.31%和67.41%)。
✦肠道微生物变化与炎症性肠病严重程度相关
肠道微生物群的变化也与克罗恩病和溃疡性结肠炎的疾病活动度和严重程度相关。例如,与患有非活动性疾病的患者相比,患有活动性疾病的溃疡性结肠炎患者中厚壁菌门的含量较低。同样,与患有非侵袭性疾病的克罗恩病患者相比,患有侵袭性疾病的克罗恩病患者的厚壁菌门丰度显著降低。
具有抗炎作用的普氏粪杆菌减少
普氏粪杆菌(F. prausnitzii)是一种厚壁菌门物种,在炎症性肠病患者中减少,其减少与克罗恩病术后六个月复发相关。
普氏粪杆菌在体内和体外均表现出抗炎作用。在患有诱导性结肠炎的小鼠中,活普氏粪杆菌(或其上清液)降低了结肠炎的严重程度并纠正了生态失调。此外,普氏粪杆菌对血液单核细胞的体外刺激导致IL-10分泌增加以及IL-12和干扰素-γ(IFN-γ)分泌减少。
拟杆菌在炎症性肠病中增加
相比之下,拟杆菌在炎症性肠病中通常会增加,并与其进展和发展相关。对炎症性肠病患者和健康个体肠道炎症和非炎症区域的粘膜活检显示,炎症性肠病样本中厚壁菌门减少,拟杆菌门丰度增加,而肠杆菌科仅在克罗恩病患者中增加。活检还显示,与非发炎区域相比,发炎区域的细菌失调程度更高。
另一项对克罗恩病和溃疡性结肠炎患者进行粘膜活检和粪便菌群构成的研究证明了肠道微生物群和 F/B 比率的改变。克罗恩病和溃疡性结肠炎患者的F/B比值均较对照组显著降低。
此外,种、属和科的组成也发生了变化。与克罗恩病患者和对照组相比,溃疡性结肠炎患者中拟杆菌和乳酸菌的丰度较高;与对照组相比,溃疡性结肠炎患者中大肠杆菌的丰度也有所增加。相反,克罗恩病患者中球状梭菌减少。
✦ 不同拟杆菌种类与不同炎症性肠病程度相关
不同的拟杆菌与不同程度的炎症性肠病相关。在经过抗生素预处理且存在转化生长因子(TGF)βRII和IL-10R2信号传导缺陷的小鼠系中,在用普通拟杆菌和多形拟杆菌灌胃后观察到严重的溃疡性疾病。
与显示 F/B 比率对肥胖影响不大的研究类似,并不是在所有炎症性肠病病例中都观察到 F/B 比率降低。炎症性肠病患者粪便微生物分析显示,拟杆菌门、厚壁菌门和疣微菌门的丰度下降,而变形菌门、放线菌门和梭杆菌门的丰度增加。在48名克罗恩病患者中,粪便样本中的拟杆菌细菌丰度不到健康个体的10%,梭菌亚群 XIVab(厚壁菌门)也显著降低。
然而,大多数研究表明,拟杆菌因内毒素而表现出促炎特性,并影响细胞因子的产生,从而导致炎症性肠病。此外,厚壁菌门细菌具有抗炎作用,可以缓解炎症性肠病的进展。
2型糖尿病(T2DM)是一种代谢性疾病,其主要原因是与肥胖相关的胰岛素抵抗。然而,其他一些因素,如精神压力、感染和遗传倾向也可能导致糖尿病。
肥胖和糖尿病的特征都是慢性低度炎症状态,并伴有多种炎症介质(例如肿瘤坏死因子和白细胞介素)的异常表达和产生。
最近的研究基于大规模16S rRNA 基因测序、定量实时PCR (qPCR) 和荧光原位杂交 (FISH),显示了肠道微生物群组成与糖尿病等代谢疾病之间的关系。
有人提出,肠道微生物群引导增加肠道对单糖的摄取,并指示宿主增加肝脏产生与胰岛素抵抗相关的甘油三酯。
✦ 2型糖尿病患者中产丁酸厚壁菌门丰度降低
权威研究显示主要的丁酸盐合成菌厚壁菌门在2型糖尿病患者中显著减少。多项人体研究支持这样一个事实:与健康受试者相比,2型糖尿病受试者中合成丁酸的厚壁菌门丰度显著降低。
对这些患者的粪便微生物群分析显示,与正常耐糖受试者相比,新诊断或长期患有糖尿病的受试者中瘤胃球菌科和毛螺菌科等科的丰度有所下降。
还报告了罗氏菌属(Roseburia)和普拉梭菌(Faecalibacter prausnitzii)的丰度在健康对照中比2型或1型糖尿病患者更高。
对粪便样本进行深入的宏基因组学和宏蛋白质组学分析证实,在患有糖尿病前期 (Pre-DM) 或初治2型糖尿病 (TN-T2D) 的个体中,产生丁酸盐的菌含量显著降低。与正常耐糖个体相比, 患有糖尿病前期个体中的普拉梭菌的水平低于正常耐糖个体和初治2型糖尿病个体。
肠道微生物组可以反映整个身体的健康状况。厚壁菌门和拟杆菌门是结肠的主要门,可以影响与肥胖相关的疾病,这些疾病也是乳腺癌的危险因素。
✦ 乳腺癌患者F/B比值比健康人群低很多
因此,研究对乳腺癌患者和健康对照者的血清中提取细菌细胞外囊泡,使用微生物组测序分析厚壁菌门和拟杆菌门。分析乳腺癌的预后因素和血清学检测结果与 F/B 比值的相关性。发现乳腺癌患者的 F/B 比值比健康对照者低三倍。
此外,乳腺癌的危险因素,如空腹血糖,被发现与F/B比值有关。F/B比值可以作为乳腺癌的危险因素,并可能作为解释影响乳腺癌发生的潜在机制的线索之一。
健康对照者和乳腺癌患者中 F/B 的比率
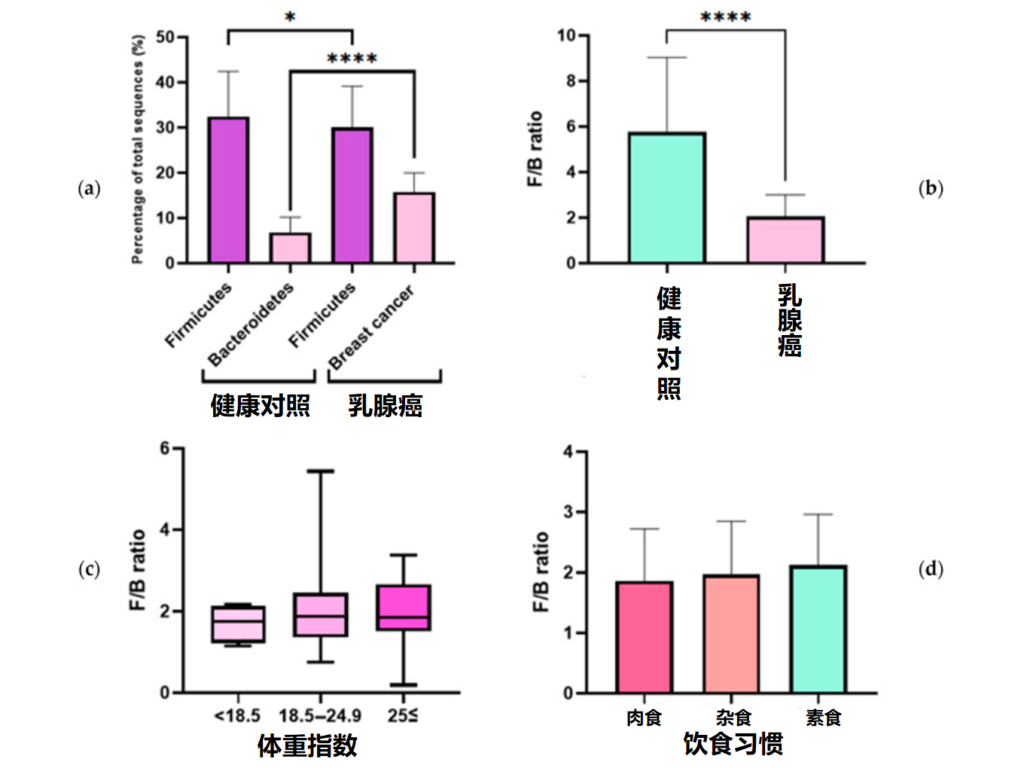
An J,et al.J Clin Med.2023
(a)健康对照组和乳腺癌患者中厚壁菌门和拟杆菌门占总微生物群的比例;(b)健康对照者和乳腺癌患者的F/B比率;(c)F/B比与体重指数之间的关系;(d)F/B比与饮食习惯的关系(*p≤0.05,**** p≤0.0001)。
调查研究发现中国饮食中的动物脂肪和蛋白质含量高于印度饮食中的全谷物和植物性素食。而印度参与者微生物组中拟杆菌的比例几乎是中国参与者的四倍,分别为16.39%和4.27%(p=0.001)。
✦ 动物产品食用较少与拟杆菌数量较多有关
据推测,印度人体内拟杆菌门的丰度较高是由于他们对动物产品的消耗较少;表明饮食中动物产品含量较低与拟杆菌数量较多有关。
对欧洲儿童和布基纳法索儿童的微生物群的比较也显示了由于饮食习惯不同而导致的微生物群组成的差异,欧洲儿童的饮食富含动物蛋白、糖、淀粉和脂肪,纤维含量低。以素食为主的饮食主要由碳水化合物、纤维和非动物蛋白组成。欧洲儿童微生物组富含厚壁菌门和变形菌门,而放线菌门和拟杆菌门在非洲儿童中较多。
✦ 营养不良儿童的肠道微生物多样性较低
研究发现,与同一地区中高收入家庭的健康儿童相比,孟加拉国贫困社会经济地位家庭的营养不良儿童的肠道微生物群多样性较低,其特点是拟杆菌门的相对丰度较低,变形菌门占主导地位。
注:拟杆菌门的存在率较低众所周知,它们可以消化复杂的膳食材料,从而提高从各种食物中提取能量,而潜在致病性变形菌的较高含量可能有助于解释营养不良儿童的健康状况不佳。
✦ 增加纤维摄入量可以增加厚壁菌门的数量
一项研究将西方饮食的美国儿童与食用大米、面包和扁豆等植物性饮食的孟加拉国儿童进行了比较。在食用西方饮食的美国儿童中,厚壁菌门/拟杆菌门的比例减少了三倍。
另一项研究要求参与者增加纤维摄入量并避免西方减肥食品。研究表明厚壁菌门:拟杆菌门比率增加了。
通过分析三名健康受试者6-12个月的肠道宏蛋白质组,进一步证实了这些结果。在这项研究中,参与碳水化合物运输和代谢的蛋白质占检测到的蛋白质的10%以上,构成了所有测试对象中发现的核心宏蛋白质组的一部分。
糖酵解途径尤其引人注目,并鉴定出几种相关酶。在为每个门的每个COG功能类别分配光谱命中后,很明显,厚壁菌门和放线菌门负责活跃的碳水化合物代谢,而拟杆菌门则显示出更多的混合功能。
这些例子反映了将某些门与特定饮食广泛联系起来主要挑战是需要考虑涵盖整个微生物组的微生物的状态和相互作用动态。
✦ 当F/B比率增加时
即更多厚壁菌门,拟杆菌较少。或两者兼而有之,厚壁菌门增长更快。可能导致以下疾病:
-肥胖(BMI较高)
-高血压中的肠道菌群失调
-自闭症谱系障碍
-慢性疲劳综合症
-肠易激综合症
-干燥综合症
-类风湿性关节炎
✦当F/B比率下降时
即厚壁菌门较少,更多拟杆菌。或两者兼而有之,厚壁菌门减少得更快。可能导致以下疾病:
-系统性红斑狼疮
-乳糜泻
-克罗恩病
-老龄化
我们审查评估了饮食干预如何影响微生物组成的相关文章。总体而言得出以下建议供参考:
✦ 增加植物蛋白摄入,避免摄入过量动物蛋白
总体而言,蛋白质摄入量,尤其植物蛋白的摄入与肠道拟杆菌门,细菌多样性呈正相关。乳清和豌豆蛋白可以增加双歧杆菌和乳酸菌的数量,而乳清还可以减少脆弱拟杆菌和产气荚膜梭菌的数量,这两种细菌都是致病性的。
此外,豌豆蛋白被发现可以增加短链脂肪酸水平,短链脂肪酸被认为具有抗炎作用,并在粘膜完整性中发挥作用。然而,一项研究发现,高动物蛋白/低碳水化合物饮食会导致罗氏菌属和直肠真杆菌(这两种有益细菌)减少。动物蛋白可能含有大量脂肪,而脂肪也会影响肠道微生物群。
✦ 尽量摄入不饱和脂肪
当研究人员观察脂肪时,发现并不是所有的脂肪都是平等产生的。在一项研究中,小鼠被喂食猪油或鱼的脂肪。喂猪油的小鼠中拟杆菌属和嗜胆菌属(Bilophila)增加,而双歧杆菌和Adlercreutzia、乳酸菌(乳杆菌和链球菌)和疣微菌属(Akkermansia muciniphila)在鱼油喂养的小鼠中增加。
猪油喂养的小鼠还出现白色脂肪组织炎症和胰岛素敏感性受损。喂食鱼油的小鼠总体表现更好,研究人员得出结论,肠道微生物群促进了高饱和脂肪饮食的整体炎症反应。
✦ 高纤维的饮食可以减少炎症
碳水化合物,包括可消化的(淀粉和糖)和不可消化的(纤维),可能是研究最多的常量营养素,因为它们具有改变肠道微生物组的能力。
人类喂食大量葡萄糖、果糖和蔗糖,双歧杆菌水平增加,拟杆菌减少。相反,当喂食糖精(一种人工甜味剂)时,拟杆菌丰度增加,罗伊氏乳杆菌减少,微生物发生与天然糖完全相反的变化。
纤维被认为是一种不易消化的膳食成分,有时被称为益生元,因为它通过刺激有益肠道细菌的生长而对宿主有益。
来源包括大豆、菊粉、未精制的小麦和大麦、生燕麦和不可消化的低聚糖,例如果聚糖、聚葡萄糖、低聚果糖 (FOS)、低聚半乳糖 (GOS)、低聚木糖 (XOS) 和阿拉伯低聚糖 (AOS)。
低纤维饮食与较低的细菌丰度有关,而富含这些不易消化的碳水化合物的饮食会增加双歧杆菌和乳酸杆菌。较高的纤维摄入量导致促炎细胞因子IL-6和胰岛素抵抗减少。
✦ 发酵食品可以增加双歧杆菌和乳杆菌水平
除了常量营养素和纤维对肠道细菌的影响外,含有乳酸菌的发酵食品(例如发酵乳制品)也被发现可以增加双歧杆菌和乳酸杆菌的水平。
✦ 多酚具有抗氧化活性能够减少一些致病菌
最后但并非最不重要的是多酚,包括儿茶素、黄酮醇、黄酮、花青素、原花青素和酚酸(存在于水果、种子、蔬菜、茶、可可制品和葡萄酒等食品中),被发现可以增加拟杆菌,减少金黄色葡萄球菌、鼠伤寒沙门氏菌和梭菌等致病菌。
拟杆菌门的成员被假设可以降低细胞内的氧水平,从而有利于厌氧菌的生长,从而促进肠道平衡的维持,并且它们被认为是关键的聚糖降解细菌比厚壁菌门等其他类群更能代谢多酚。
多酚可以改变肠道环境,它们可以被肠道细菌分解代谢,将它们转化为多种化合物比原始化合物具有更强的抗氧化活性。
厚壁菌门/拟杆菌门(F/B比率)作为一个指标在很多关于肠道菌群的研究中被提及和表征,从疾病发生进展,到药物饮食干预,涉及肠道菌群的研究,首先会描述细菌门水平的变化,而人类或动物肠道细菌约90%都属于厚壁菌门与拟杆菌门,而它们的比率也被认为是肠道菌群动态平衡的标志。
拟杆菌门主要为革兰氏阴性菌,能激活T细胞介导的免疫反应,降解多糖保护肠道和其他病原菌,厚壁菌门主要为革兰氏阳性菌,尤其产丁酸的菌,但是更容易吸收能量。
但是肠道菌群受到抗生素,药物,年龄以及分析注释数据库等的影响,此外随着肠道菌群研究队列的扩大,以及对菌群构成与不同疾病状态和药物饮食等因素的相关性研究的深入,F/B比率作为一个相对粗放的指标已经无法准确反映复杂的肠道菌群状况。我们需要更加深入和全面的通过菌属甚至菌种的构成变化来解释和分析肠道菌群特征,并进而更准确的解释肠道菌群和健康及生活方式的关联。
主要参考文献
Stojanov S, Berlec A, Štrukelj B. The Influence of Probiotics on the Firmicutes/Bacteroidetes Ratio in the Treatment of Obesity and Inflammatory Bowel disease. Microorganisms. 2020 Nov 1;8(11):1715.
Mariat D, Firmesse O, Levenez F, Guimarăes V, Sokol H, Doré J, Corthier G, Furet JP. The Firmicutes/Bacteroidetes ratio of the human microbiota changes with age. BMC Microbiol. 2009 Jun 9;9:123.
Gui X, Yang Z, Li MD. Effect of Cigarette Smoke on Gut Microbiota: State of Knowledge. Front Physiol. 2021 Jun 17;12:673341.
Grigor’eva IN. Gallstone Disease, Obesity and the Firmicutes/Bacteroidetes Ratio as a Possible Biomarker of Gut Dysbiosis. J Pers Med. 2020 Dec 25;11(1):13.
Vaiserman A, Romanenko M, Piven L, Moseiko V, Lushchak O, Kryzhanovska N, Guryanov V, Koliada A. Differences in the gut Firmicutes to Bacteroidetes ratio across age groups in healthy Ukrainian population. BMC Microbiol. 2020 Jul 22;20(1):221.
Indiani CMDSP, Rizzardi KF, Castelo PM, Ferraz LFC, Darrieux M, Parisotto TM. Childhood Obesity and Firmicutes/Bacteroidetes Ratio in the Gut Microbiota: A Systematic Review. Child Obes. 2018 Nov/Dec;14(8):501-509.
Hidalgo-Cantabrana C, Delgado S, Ruiz L, Ruas-Madiedo P, Sánchez B, Margolles A. Bifidobacteria and Their Health-Promoting Effects. Microbiol Spectr. 2017 Jun;5(3).
An J, Kwon H, Kim YJ. The Firmicutes/Bacteroidetes Ratio as a Risk Factor of Breast Cancer. J Clin Med. 2023 Mar 13;12(6):2216.