-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com

谷禾健康
铁是地球上几乎所有生命形式包括人体与微生物不可或缺的微量元素。它不仅支撑着人类的呼吸、免疫和能量代谢,更是肠道微生物争夺的“战略资源”。铁稳态的破坏与肠道菌群失调和多种疾病的发展密切相关。
然而科学家发现,铁在人体与微生物之间也是一把双刃剑:它既能维持生命,也可能通过氧化应激引发DNA损伤和疾病。过量的铁主要通过芬顿反应产生有害的氧化应激,导致DNA、蛋白质和脂质等大分子损伤。因此,人体细胞和微生物系统的铁水平受到复杂机制的严格管控,以维持体内平衡。铁失调可以作为多种人类疾病的原因和结果。更微妙的是,人体与肠道微生物之间围绕铁的“争夺战”,直接决定了我们的健康与疾病状态。
肠道菌群是铁稳态和宿主健康的关键参与者,肠道中未吸收的膳食铁会影响肠道微生物群的组成。铁稳态的破坏可以引发肠道微生态的失调,从而影响宿主的的生理和免疫系统。
近年来,《自然·微生物学》等顶级期刊的研究揭示,铁的动态平衡不仅影响贫血或感染,还与炎症性肠病、癌症等慢性病密切相关。肠道微生物群的组成和功能,甚至药物疗效,都可能被铁的波动彻底改变。本文将从铁的核心作用出发,解析宿主、微生物与铁之间的复杂博弈,并探讨如何通过精准调控铁代谢实现个性化健康管理。
1. 铁的生理功能
铁是血红蛋白和肌红蛋白的核心成分,负责氧气的运输与储存;它也是细胞色素和铁硫簇蛋白的辅因子,参与能量代谢(ATP生成)和DNA合成。人体每天需要约20-25毫克铁,但仅1-2毫克通过肠道吸收,其余来自红细胞回收。
膳食铁分为两类:血红素铁和非血红素铁。
一般来说,血红素铁的生物利用度高于非血红素铁。这是因为,非血红素铁与各种饮食成分复合摄入,抑制其在十二指肠的吸收。虽然铁的还原亚铁形式(Fe2+)是可溶性的能被人类吸收和利用,但亚铁在生理pH值和有氧条件下被氧化为不溶性的三价铁形式(Fe3+)。因此,最常见改善机制是降低环境pH值为酸性条件或通过微生物代谢产物,来改善非血红素铁的溶解度和生物利用率。
2. 铁的毒性风险
游离铁通过芬顿反应(Fenton Reaction)产生活性氧(ROS),攻击脂质、蛋白质和DNA。有研究表明,活性氧水平升高可导致衰老加速,呼吸道和心血管疾病、IBD和癌症的风险增加。总之,这一临床证据突出了维持铁稳态对整体健康的关键作用。
注:芬顿反应是一种基于亚铁离子(Fe²⁺)催化过氧化氢(H₂O₂)产生羟基自由基(•OH)的高级氧化过程,具有极强的氧化能力,广泛应用于环境治理、有机污染物降解等领域。
3. 铁的调控系统
为了维持铁稳态,人体进化出严密的铁调控系统:
图1人类的铁调节
doi.org/10.1038/s41564-025-02001-y
1.宿主的防御策略:营养免疫(Nutritional Immunity)
在急性感染期间,病原体急需铁在宿主内增殖。因此,严格的监管机制,以限制铁的可用性有助于防止感染性疾病的发展。这种宿主防御策略通过调节铁转运蛋白和铁螯合蛋白来执行,被称为“营养免疫”。
案例:
脂质运载蛋白-2能捕获大肠杆菌的肠菌素(Enterobactin),但沙门氏菌通过分泌“隐形铁载体”沙门菌素(Salmochelin)逃逸这一机制,凸显了攻防的进化博弈。
2. 微生物的反击策略
为了克服宿主组织内严重的铁缺乏,病原体已经演化出了各种铁获取机制。最突出的策略就是分泌小的铁螯合分子(铁载体):
图2 细菌在肠道中获取铁的策略
doi.org/10.1038/s41564-025-02001-y
1. 微生物代谢物如何影响铁吸收
肠道微生物通过分泌一系列酶和代谢副产物,这些酶和代谢副产物可以提高或限制膳食铁的利用率,从而影响铁的吸收。
临床意义:高纤维饮食通过增加SCFA改善缺铁性贫血,而长期使用质子泵抑制剂(PPI)因抑制胃酸,可能加剧铁缺乏和肠道菌群失调。
图3 微生物衍生代谢物调节宿主铁吸收
doi.org/10.1038/s41564-025-02001-y
2. 微生物群落结构的铁依赖性
虽然缺铁和铁过量都有风险的记录,但重度缺铁会不可逆地降低微生物的多样性和丰富度,削减宿主健康所需的代谢物(如短链脂肪酸SCFA)。
典型表现为:产SCFA菌(厚壁菌门、罗氏菌属/直肠真杆菌)比例下降;SCFA合成相关基因表达受抑,由于SCFA具备抗炎特性,菌群代谢衰减可能放大缺铁引发的炎症。
图4 铁失调和微生物群失调相关的人类疾病
doi.org/10.1038/s41564-025-02001-y
最新的研究表明,膳食铁是微生物群构成的关键变量,铁-宿主-微生物群的交互作用可显著影响炎症性肠病(IBD)及癌症的病程发展。
1. 炎症性肠病(IBD)
铁代谢失调与感染IBD之间复杂的关联性:
2. 癌症
研究表明,过量摄入红肉中的血红素铁,会损害肠道黏液保护屏障。更关键的是,它会促进一种能分解肠道黏液的细菌——艾克曼菌(Akkermansia) 的生长,从而刺激肠道上皮细胞过度增殖,为癌变埋下隐患。
除了感染和免疫,失衡的铁代谢(尤其是红肉中过量的血红素铁)也是结直肠癌的重要推手。它破坏肠道屏障、喂养有害菌、并直接“喂养”癌细胞。癌细胞还会“劫持”铁调节系统囤积铁,而限制铁供应或调控铁代谢,可能成为抗癌新思路。
长期食用红肉和高脂肪饮食,还与两种有害细菌的滋生密切相关:产肠毒素脆弱拟杆菌(Bacteroides fragilis)和具有基因毒性的特定大肠杆菌(E. coli)。这两种细菌分别产生脆弱拟杆菌毒素(BFT)和大肠杆菌素(colibactin),这些毒素已被证实与结肠癌的发生有直接关联。
不过,有趣的是,高浓度的铁环境本身又会抑制大肠杆菌素(colibactin)的产生。这提示我们,饮食中的铁、肠道致病菌(pathobionts)与结直肠癌发病率之间的具体联系非常复杂,仍需更多研究来阐明。
癌细胞是“铁瘾患者”与铁调控的“劫持者”
癌细胞疯狂生长,对铁元素的需求量巨大。与正常的结肠上皮细胞相比,结直肠癌细胞装备了高效的“铁输入系统”:它们会过量表达铁输入蛋白DMT1(二价金属离子转运蛋白1),导致肿瘤内部铁大量积聚,加速肿瘤生长。
同时,癌细胞还非常“狡猾”。它们会在局部分泌一种名为铁调素(hepcidin)的激素。铁调素的作用是抑制铁输出蛋白膜铁转运蛋白(Ferroportin, Fpn)的功能。这样一来,癌细胞就能成功地将铁囤积在自己内部,进一步促进其生长。实验证据支持这一点:缺乏铁调素能降低肿瘤负担,因为肿瘤细胞内的铁水平下降,进而抑制了其赖以生存的线粒体呼吸作用和合成DNA所需的核苷酸生物合成。
肿瘤微环境中的铁:巨噬细胞角色与治疗潜力
除了癌细胞自身,肿瘤微环境中的其他细胞,特别是肿瘤相关巨噬细胞(TAMs),在调控铁分布和影响癌症进程中可能扮演关键角色。例如,一项转录组研究发现,膜铁转运蛋白(Fpn)的表达水平不仅是肝癌中特定巨噬细胞亚群的标志,还是一个不良预后的指标。
更令人鼓舞的是,另一项研究发现,共生益生菌
植物乳植杆菌(Lactiplantibacillus plantarum)能够促进肿瘤内巨噬细胞表达铁螯合蛋白脂质运载蛋白-2(lipocalin-2),从而增强抗肿瘤免疫力。
这些发现都指向一个极具前景的研究方向:限制肿瘤对铁的获取,或调控铁在肿瘤微环境中的分布,可能具有显著的抗癌治疗潜力。当然,这需要未来更多的研究来深入探索和验证。
3. 感染性疾病
宿主、肠道微生物与铁元素之间复杂的相互作用,给制定人群层面的膳食铁摄入标准和口服铁剂补充方案带来了巨大挑战。早期研究曾指出补铁可能导致菌群失调并增加疾病风险,但后续针对不同地区人群的试验却发现:肠道微生物的初始构成决定了补铁是否引发菌群失调。
饮食结构和微生物组的个体差异,是当前微生物疗法效果不稳定的关键原因。这种差异性要求我们采取个性化医疗策略——根据患者具体情况搭配营养干预和微生物疗法。
过去30年,癌症治疗已实现从“无差别放化疗”到“靶向基因突变”的精准医疗跨越。同样,如果我们能锁定调控铁代谢的核心通路、以及影响铁稳态的特定微生物(如导致感染、炎症性肠病和癌症的菌株),便有望开发出新一代精准疗法。
1. 个性化补铁策略
2. 饮食与药物的协同管理
3. 未来方向:微生物组精准编辑
通过基因工程改造益生菌,使其分泌铁载体拮抗剂或免疫调节分子,或开发“铁载体-药物偶联物”,靶向递送抗生素至病原体。若鉴定出有益菌(如罗伊氏乳杆菌),可开发对应益生菌疗法;对有害菌则可用噬菌体或抑制剂精准清除。
微生物的“双面剑”特性
尽管传统研究聚焦病原体,但共生微生物的作用也同样引发关注。多形拟杆菌、阿克曼菌等“益生菌”在特定环境下可能会助推感染和癌症风险。关键在于解析环境因素(如铁浓度、菌群互作)如何影响微生物行为。
未来研究需突破两大方向:
① 揭示健康/疾病状态下,共生菌、条件致病菌与病原体的互动机制;
② 追踪铁元素如何通过改变微生物代谢通路影响宿主健康。
铁的平衡艺术——迈向精准健康时代
铁不仅是生命的基石,更是宿主与微生物、健康与疾病的交汇点。
微生物组在补铁过程中的“保护 vs 致病”双重角色,解释了为何相同的疗法对不同患者效果迥异。
随着微生物组学、代谢组学和基因编辑技术的进步,我们有望像定制癌症治疗方案一样,为每个人设计铁代谢的个性化蓝图。从饮食调整到微生物干预,科学的铁管理将成为预防和治疗慢性病的核心策略之一。
主要参考文献:
Choi, G., Bessman, N.J. Iron at the crossroads of host–microbiome interactions in health and disease. Nat Microbiol 10, 1282–1293 (2025).

谷禾健康
失眠是一种常见的睡眠障碍,近 40%的成年人表现出失眠症状,10.8%的成年人患有慢性失眠症。
失眠主要表现为睡眠质量差、入睡困难、睡眠时间不足等,并与认知能力下降、焦虑、慢性疲劳、注意力不集中和记忆力减退等身心后果相关。睡眠不足也会增加慢病风险(如心血管疾病、糖尿病和肥胖),形成恶性循环,进一步威胁患者的整体健康状况。
目前的失眠疗法主要包括药物治疗和心理治疗。然而,像苯二氮䓬类药物有不良影响,如过度的神经毒性、成瘾性和耐受性。心理疗法,如认知行为疗法,已显示出长期的有效性。然而,由于缺乏训练有素的理疗师和高昂的成本,其可用性有限。
近年来,随着微生物群-肠-脑轴理论的深入发展,研究人员发现了肠道微生物不仅参与消化代谢过程,还能通过多种途径影响脑功能和行为,为失眠的发病机制研究提供了全新的视角。
在这一背景下,中草药及其活性成分作为独特的益生元,展现出巨大的治疗潜力。它们不仅为肠道菌群的活动提供能量,还通过调节肠道菌群改善肠道微环境,从而影响身体的多种生理功能,特别是睡眠调节功能。例如:
本文阐述了肠道菌群如何通过肠道-脑轴的复杂通信网络调节睡眠质量,也介绍了利用中药及其活性成分调节肠道微生物群来改善睡眠质量的潜力,同时探讨了基于肠道菌群的其他针对失眠的干预措施,为失眠治疗开辟了一条融合传统智慧与现代科学的创新路径。
失眠意味着晚上难以入睡、难以保持睡眠,或两者都有,它是最常见的睡眠障碍之一。
仅数天的失眠发作称为短期(急性)失眠。当持续存在睡眠问题时,通常会被诊断为长期(慢性)失眠。
注:慢性失眠有许多不同的定义。一个普遍接受的定义是:每周超过3晚,持续至少3个月,或持续一个月或更长时间的失眠。
急性和慢性失眠都非常普遍。大约每3个成年人中有1个有可能出现失眠症状。
症 状
失眠症状可能包括:
哪些人群更容易失眠?
几乎每个人偶尔都会有失眠的夜晚。但下列人群更可能出现失眠的情况:
月经周期和更年期期间激素变化可能起作用。更年期时,夜间盗汗和潮热常常会扰乱睡眠。失眠在怀孕期间也很常见。
由于睡眠模式和健康状况的变化,随着年龄的增长,更有可能患有失眠。
可能是什么原因?
慢性失眠通常是由压力、生活事件或破坏睡眠的习惯引起的。慢性失眠的常见原因包括:
对工作、学校、健康、金钱或家庭的担忧会使思绪在夜间保持活跃,难以入睡。压力性生活事件,如亲人的去世或疾病、离婚或失业或搬家,也可能导致失眠。
身体的“内部时钟”,即昼夜节律,指导着诸如睡眠-觉醒周期、新陈代谢和体温等。破坏这些节律可能导致失眠。比如跨越多个时区的旅行导致的时差反应、上晚班或早班、频繁轮班或三班倒等都可能引发失眠。
包括每天上床睡觉和起床的时间不同、午睡、睡前过于活跃以及睡眠区域不舒服。
其他不良的睡眠习惯包括在床上工作、吃饭或看电视。在睡前使用电脑或智能手机、玩电子游戏或看电视可能会破坏睡眠周期。
睡前吃点清淡的小零食是可以的。但如果吃太多,可能会在躺下时感到不舒服。很多人还会出现胃灼热的情况。这是指胃酸反流到从口腔到胃的食物管道中。胃灼热可能会让人无法入睡。
焦虑症,如创伤后应激障碍,可能会扰乱你的睡眠。过早醒来可能是抑郁的迹象。失眠常常与其他心理健康问题同时发生。
许多处方药会影响睡眠,例如某些抗抑郁药和用于治疗哮喘或高血压的药物。许多非处方药,如一些止痛药、过敏和感冒药以及减肥产品,含有咖啡因和其他兴奋剂,这些物质会干扰睡眠。
与失眠相关的状况包括慢性疼痛、癌症、糖尿病、心脏病、哮喘、胃食管反流病(GERD)、甲状腺功能亢进、帕金森病和阿尔茨海默病。
睡眠呼吸暂停症会导致在夜间有时停止呼吸,从而扰乱睡眠。不安腿综合征会在你试图入睡时引起强烈的、不适的移动双腿的欲望,这可能无法入睡难以再次入睡。
咖啡、茶、可乐和其他含有咖啡因的饮料让人兴奋。在下午或晚上饮用会难以入睡。烟草产品中的尼古丁是另一种会破坏睡眠的兴奋剂。酒精可能会让你入睡,但它会阻止更深睡眠阶段,在半夜醒来。
肠道菌群可以通过肠-脑轴直接或间接地参与调节大脑的睡眠功能。肠道菌群的失调,通过减少肠道屏障完整性和短链脂肪酸含量以及增加触发炎症反应的炎症介质等机制,影响宿主的睡眠行为。详见下一章节。
失眠会影响肠道菌群的丰富度和多样性
与正常组相比,睡眠缺乏小鼠的Akkermansia muciniphila、拟杆菌和粪杆菌(Faecalibacterium)丰度显著降低,气单胞菌(Aeromonas)丰度显著增加。
临床研究中的失眠或其他睡眠障碍菌群特征
与对照组相比,失眠患者的Collinsella、Adlercreutzia、Clostridiales、Pediococcus、Erysipeltrichaceae、拟杆菌属、葡萄球菌属、Carnobacterium、Odoribacter、假单胞菌属、长双歧杆菌属、Phascolarctobacterium的丰度存在显著差异。
同样,阻塞性睡眠呼吸暂停患者在下列菌群丰度存在显著差异:乳杆菌属、瘤胃球菌科、 变形杆菌科、梭菌科(Clostridiaceae)、 颤螺菌科(Oscillospiraceae)、 克雷伯氏菌(Klebsiella)、脱硫弧菌科(Desulfovibrionaceae)、脆弱拟杆菌(Bacteroides fragilis)、普拉梭菌(Faecalibacterium prausnitzii)。
无论是与炎症相关的菌株的改变,如变形杆菌科、梭菌科、Oscillospiraceae、克雷伯氏菌,还是与肠道屏障完整性相关的菌株,如脱硫弧菌科、脆弱拟杆菌、F. prausnitzii,这些变化都与睡眠质量相关的参数显著相关。
失眠不仅会降低肠道的抗氧化能力、抗炎细胞因子水平、粘蛋白2(MUC2)和紧密连接蛋白表达,还会增加促炎细胞因子的水平,导致肠道黏膜损伤和屏障通透性增加。
实验证据:睡眠剥夺通过肠道菌群影响大脑功能
当睡眠剥夺动物的肠道微生物群移植到正常小鼠体内时,供体动物的肠道菌群发生了变化,导致脂多糖(LPS)和气单胞菌水平升高,丁酸盐和Lachnospiraceae_NK4A136水平降低,海马小胶质细胞活化和神经元死亡增加。
然而,用植物乳杆菌124或A.muciniphila预处理可以恢复被破坏的肠道微生物群,减少肠道中的氧化应激、炎症和屏障损伤,增加乙酸和丁酸水平,并防止LPS刺激的小胶质细胞-神经元共培养中的突触损失。
因此,肠道微生物群的破坏通过降低肠道屏障完整性和短链脂肪酸含量,增加引发炎症反应的炎症介质等机制,影响宿主的睡眠行为。
下面章节我们就来详细看一下肠道菌群参与失眠症调节的相关机制。
下丘脑-垂体-肾上腺轴
失眠激活并导致HPA轴功能障碍。微生物可能通过神经信号传导、短链脂肪酸、表观遗传学、肠道屏障完整性或血脑屏障(BBB)通透性影响HPA轴活性。因此,失眠引起的肠道微生物群失调可能与HPA轴的激活有关。
HPA轴的破坏与致病菌(包括肠杆菌科、链球菌科、韦荣球菌科)的增加和有益细菌(包括双歧杆菌和毛螺菌科)的减少有关。
某些特定的肠道微生物群可以抑制HPA轴的激活,并介导相关的脑功能。大肠杆菌(Escherichia coli)和粪肠球菌(Enterococcus faecalis)可以降低小鼠血清中的皮质醇水平,从而缓解压力和抑郁焦虑行为。
分析表明,粪便中的羟甲睾酮(Oxymesterone)可以介导皮质醇对副拟杆菌属(Parabacteroides)的负面影响,而3-(2,4-环戊二烯-1-基)-5α-雄甾烷-17β-醇可以介导皮质类固醇对气球菌(Aerococcus)的负面影响;洛伐他汀酸(Mevinolinic acid)还可以介导气球菌对皮质醇的负面影响。这表明肠道微生物群和HPA轴之间的信号传导是双向的。
doi: 10.3389/fphar.2025.1572007
微生物内分泌产物和代谢物
★ 褪 黑 素
什么是褪黑素?
褪黑素(Melatonin,MT)又称为”暗激素”,因为它主要在黑暗环境中分泌,是我们身体内重要的睡眠调节激素。夜幕降临,褪黑素水平开始上升,告诉我们的身体该睡觉了;当太阳升起时,它的分泌减少,帮助我们保持清醒。可以说,褪黑素就像是身体内部的生物钟管家,维持着我们正常的睡眠-觉醒周期。
色氨酸的”三岔路口”
要理解肠道微生物与褪黑素的关系,我们首先需要了解一个关键的氨基酸——色氨酸(Trp)。色氨酸是合成褪黑素的重要原料,但在正常情况下,人体内仅有不到5%的色氨酸用于合成血清素(5-HT)和褪黑素,而高达95%都通过肝脏中的犬尿氨酸(Kyn)途径进行代谢。
这就像是一个”三岔路口”:
压力→肠道菌群失调→褪黑素下降
长期压力会破坏肠道菌群平衡,导致失调,失调的微生物刺激犬尿氨酸通路过度活跃,本应用于合成褪黑素的色氨酸被大量转移到犬尿氨酸途径,最终导致循环中的褪黑素水平下降,影响睡眠质量。
有益菌的助眠作用
令人惊喜的是,肠道中的某些微生物也能够主动促进其合成。研究发现,罗伊氏乳杆菌和大肠杆菌这两种微生物激活TLR2/4/MyD88/NF-κB信号通路,促进关键酶AANAT(芳烷基胺N-乙酰基转移酶)的表达,推动褪黑素的合成。
微生物代谢产物的协同效应
除了直接合成,肠道微生物的代谢产物——短链脂肪酸(SCFA)也发挥着重要作用:
外源性褪黑素补充
不仅能直接改善睡眠,还能帮助生物钟恢复正常运转,改善肠道菌群的组成和功能,增加短链脂肪酸水平,改善肠脑交流,优化肠道与大脑之间的信息传递。
研究表明,褪黑素补充能够通过多个途径改善睡眠剥夺引起的认知障碍:
最后,这些在肠道中产生的褪黑素分子会通过血液循环系统到大脑,与大脑中的MT1或MT2受体结合,最终调节我们的睡眠行为。这就形成了一个完整的”肠道-血液-大脑“调节环路。
★ γ- 氨 基 丁 酸
什么是GABA?为什么它能帮助睡眠?
γ-氨基丁酸(GABA)是一种众所周知的促进睡眠的氨基酸,是一种天然的抑制性神经递质。当我们感到焦虑、紧张或难以入睡时,GABA帮助我们的神经系统冷静下来,促进放松和睡眠。
简单来说,GABA的作用就像给过度活跃的神经系统踩了一脚”刹车“,让我们从兴奋状态转向平静状态,为优质睡眠创造条件。
肠道:GABA的”第二生产基地”
许多人以为GABA只能在大脑中产生,但实际上,我们的肠道也是一个重要的GABA生产基地。在肠黏膜中,存在着一系列特殊的细胞——肠神经内分泌细胞(如STC-1和STC-2),它们就像是内置的”GABA工厂“,它们可以表达GABAA受体及其受体亚型(α1、α3、α5、β1、β3、δ)的mRNA。
除了胃肠神经内分泌细胞合成、储存和分泌GABA的能力外,肠道微生物群的某些成员也可以产生GABA。
乳酸菌和双歧杆菌是GABA产生的关键成员
– Limosilactobacillus fermentum L18:
高效分泌GABA的专业户,通过增加连接蛋白的浓度和有益肠道细菌的丰度来增强肠道屏障
– 鼠李糖乳杆菌GG:
除了保护肠道屏障外,还可以通过调节肠脑轴来提高海马和杏仁核中的脑源性神经营养因子(BDNF)和GABA受体水平。
– 短乳杆菌:
通过发酵产生高剂量GABA,可以提高肠道中有益细菌的相对丰度和SCFA的水平,进而可以上调GABA能和5-羟色胺能神经递质的mRNA和蛋白质表达水平。这将导致θ和δ波以及非快速眼动(NREM)睡眠的显著增加。
GABA如何在肠道中发挥多重功效?
– 维护肠道屏障:构建健康防线
刺激Ca²⁺信号传导;增加MUC2释放,强化肠道黏膜屏障;促进肠道干细胞增殖,维持肠道健康。
– 调节肠脑轴:远程遥控大脑
增加海马和杏仁核中的BDNF水平,促进神经元健康;上调大脑中GABA受体水平,增强镇静效果;拟杆菌丰度与GABA受体蛋白表达呈正相关。
GABA很难穿过血脑屏障直接作用于中枢神经系统,那么肠道产生的GABA是如何影响大脑和睡眠的呢?
肠神经系统:另辟蹊径的”高速公路”
有研究人员认为,肠道内分泌细胞中存在大量GABA受体,通过肠神经系统这个”第二大脑”发挥作用,不需要直接穿过血脑屏障,而是通过肠-脑轴的复杂网络影响大脑功能。
★ 血 清 素
什么是血清素?
血清素(5-羟色胺,5-HT),有时候被称为”快乐激素”,因为它不仅能让我们感到愉悦和放松,还是调节睡眠-觉醒周期的重要神经递质。当血清素水平充足时,我们更容易感到心情平静、思维清晰,也更容易获得优质的睡眠。
作为肠脑轴中的关键神经递质,血清素(5-HT,血清素)是肠道微生物群和大脑之间进行交流的重要介质,将肠道的信息准确传递给大脑,告诉大脑什么时候工作,什么时候该休息了。
肠道:血清素的主要生产基地
体内约95%的血清素来源于肠道,而大脑反而只是小作坊。
一般生产路径:
非经典调控途径:
肠道菌群如何助力血清素的生产?
肠道菌群代谢产生短链脂肪酸,短链脂肪酸通过调节血清素转运体(SERT);调节5-HT受体的敏感性;抑制色氨酸转化为犬尿氨酸,确保更多原料用于血清素合成来促进合成。
肠道菌群多样性影响血清素
肠道微生物群的多样性会影响5-HT水平,进而影响人体的睡眠模式。补充色氨酸和血清素已被证明可以改善肠道微生物群的多样性,增加肠道中短链脂肪酸的量,提高血清素的血液水平,所有这些都可以改善老年人和新生儿的睡眠质量。
血清素代谢失衡与睡眠障碍的病理关联
在用抗生素耗尽微生物群后,5-HT的表达水平降低,导致REM睡眠的发作频率增加,NREM和REM睡眠之间的频繁转换,最终对睡眠产生负面影响。
如何通过调节血清素改善睡眠?
例如,灵芝可以调节肠道微生物群和5-羟色胺相关途径,增加5-羟色胺和GABA的血清水平,同时降低HPA轴激素水平,有效缓解焦虑小鼠的失眠行为。显然,微生物群可以通过影响肠道中5-羟色胺的合成和释放来调节大脑中的睡眠行为。
影响睡眠的微生物群-肠道-大脑轴交流模式
Sen P, et al.,Trends Mol Med. 2021
★ 短 链 脂 肪 酸
短链脂肪酸(SCFA)是肠道细菌通过发酵我们吃下去的膳食纤维产生的主要代谢产物,被认为是神经调节物质,对肠道微生物群控制睡眠至关重要。通过免疫、神经、内分泌途径,微生物群与大脑睡眠过程形成密切联系;“肠-脑轴”是两者之间的纽带,SCFA起着信使的作用。
失眠会减少产短链脂肪酸的菌的数量
产短链脂肪的菌如粪杆菌(Faecalibacterium)、Roseburia、Ruminococacaceae,这反过来又降低了肠道中SCFA的数量,而SCFA的缺乏又会进一步影响睡眠质量,形成一个难以打破的恶性循环。
肠道短链脂肪酸水平升高可提高睡眠质量
相关研究表明,短链脂肪酸水平的升高可以通过穿越血脑屏障和调节大脑中血清素和多巴胺(DA)的产生来影响大脑发育。
短链脂肪酸不仅能直达大脑,在肠道局部也发挥着重要的睡眠调节作用。
增强睡眠相关物质:
调节压力系统:
调节免疫功能
SCFA调节HPA轴:缓解压力促进睡眠
通过显著增加SCFA含量,可以带来一系列积极变化:
短双歧杆菌207-1可以通过显著增加SCFA和GABA水平,整体抑制HPA轴相关激素来改善睡眠质量。
不同SCFA的作用
乙酸盐、丁酸盐、戊酸盐与HPA轴相关激素水平呈负相关;丙酸盐显示出相反的模式。
因此,微生物群产生的SCFA可以通过改善肠道屏障和肠道免疫环境来影响神经系统。它们通过增加肠道中SCFA的多样性和水平、刺激睡眠相关细胞因子的分泌和抑制炎症反应等机制,改善失眠。
★ 多 巴 胺
多巴胺(DA)被称为大脑中的”奖励分子”和”动力激素”,但在睡眠调节中,它是”人间清醒”。作为一种促进警觉性的强效神经递质,多巴胺对于控制我们的睡眠-觉醒周期至关重要。
当多巴胺水平充足时,我们会感到精神饱满、注意力集中、反应敏捷;而当多巴胺不足时,我们可能会感到昏昏欲睡、缺乏动力、思维迟钝。
多巴胺:肠道保护功能
多巴胺在肠道中并不仅仅是一个”过客”,它还承担着重要的肠道保护功能:
通过D5受体的作用:
通过D2受体的作用:
肠道菌群失调:多巴胺代谢的破坏者
肠道菌群可以影响多巴胺的水平,相关研究表明,肠道菌群失调导致多巴胺代谢紊乱(以高香草酸减少为特征),从而影响大脑的清醒和认知功能。
注:高香草酸是多巴胺代谢的重要产物,它的减少就像是”多巴胺工厂”生产效率下降的信号。
补充益生菌可以有效逆转这些紊乱
补充益生菌已被证明可以恢复Blautia、Dialister、F.prausnitzii、Ruminococcus、拟杆菌属,这些菌群与高香草酸水平呈显著正相关。这意味着它们能够有效修复多巴胺代谢通路,恢复正常的觉醒调节功能。
两种特别的”多巴胺生产专家”
粪肠球菌(Enterococcus faecalis)和屎肠球菌(Enterococcus faecium) 具有酪氨酸羟化酶和多巴脱羧酶活性,使其能够将酪氨酸转化为L-dopa(多巴胺的前体)。进一步的研究表明,粪肠球菌和屎肠球菌的移植增加了PGF小鼠肠道内多巴/多巴胺的合成,促进了多巴/多巴胺从肠道进入血液,从而提高了大脑中的多巴胺水平。
这表明,调节肠道微生物群中苯丙氨酸酪氨酸多巴多巴胺的生物合成途径可能会改善脑功能。
短链脂肪酸的协同作用
研究表明,肠道微生物群代谢产生的短链脂肪酸可以直接穿透血脑屏障,控制5-羟色胺和多巴胺的合成,进而影响大脑发育。因此,肠道细菌可以通过多种途径调节大脑的多巴胺能系统,从而影响大脑的唤醒能力和功能。
微生物群-迷走神经通路
迷走神经就像是连接肠道和大脑之间的一条专线电话,肠壁中富含迷走神经纤维,这些神经纤维就像是密布在肠道中的信号接收器,能够从肠道接收各种信号并将其精确地传递到大脑。可以说,迷走神经是肠道微生物群影响大脑功能、调节睡眠的重要通路之一。
肠道微生物如何启动迷走神经?
通过这条”迷走神经专线”,肠道细菌能够:
粪菌移植和罗伊氏乳杆菌
粪菌移植可以触发肠道的迷走神经系统,从而导致脑干和海马体的5-HT和DA神经传递途径的长期改变。
通过迷走神经依赖机制,罗伊氏乳杆菌还可以改变催产素和多巴胺能信号在腹侧被盖区(VTA)的传递方式。值得注意的是,海马体和VTA中的多巴胺能回路在维持睡眠-觉醒相关行为方面都起着至关重要的作用。
证据:迷走神经切断实验
为了证实迷走神经参与肠道和大脑之间的信息传递,研究人员进行了一个实验:膈下迷走神经切断术。就像是切断电话线,看看肠道和大脑之间的通讯是否会中断。
治疗效果消失:
注:选择性5-HT再摄取抑制剂是一类通过抑制突触前膜5-HT再摄取、增强突触间隙5-HT浓度的抗抑郁药物。
信号传递的机制
当肠道内的5-HT与迷走神经纤维上密集分布的5-HT受体结合时,迷走神经被激活。然后,神经元通过特定的投射对5-HT信号做出反应并进行分类,然后将其传递到大脑。
迷走神经刺激:治疗睡眠障碍的新策略
研究表明,迷走神经刺激可通过降低外周血和海马中IL-1β和IL-6的水平,以及防止星形胶质细胞和小胶质细胞激活,从而改善由睡眠剥夺引起的抑郁样行为。
微生物-免疫炎症通路
免疫炎症通路就像是身体内部的警报系统,当有危险信号出现时,它会迅速启动防御机制。在肠道微生物调节睡眠的过程中,它也扮演着至关重要的角色。这套系统运行正常时,我们能享受优质睡眠;而当系统失调时,就可能出现失眠、睡眠质量下降等问题。
微生物通过免疫炎症途径与大脑的睡眠调节功能建立复杂的相互作用。简单来说,肠道微生物可以通过调节免疫系统的炎症反应,间接影响大脑的睡眠中枢,就像是通过免疫语言与大脑进行对话。
睡眠剥夺:引发免疫炎症风暴的导火索
睡眠剥夺破坏肠道屏障和血脑屏障通透性,增加NLRP3水平,并激活肠道中的TLR4/NF-κB信号通路,导致炎症信号传递到大脑,从而加剧大脑中的神经炎症和小胶质细胞激活。
恢复被破坏的肠道微生物群可以缓解肠道氧化应激、炎症反应和屏障损伤,从而改善睡眠质量。
肠道微生物代谢物:TMAO的双面性
某些肠道微生物可以通过其代谢产物介导宿主的炎症反应来调节大脑的睡眠功能。例如,三甲胺N-氧化物(TMAO)是肠道微生物群的代谢产物,可以通过调节膜联蛋白A1信号传导来增强血脑屏障的完整性,保护大脑免受炎症损伤,还可以通过NF-κB信号通路促进NLRP3激活来影响睡眠。
特定菌群与炎症因子
睡眠剥夺会引发肠道微生物群失调,导致炎症因子如IL-1β、IL-6、TNF-α的表达失衡。
相关分析表明,IL-1β和TNF-α与肠道中的Ruminococcus_1和Ruminococcoccus e_UCG-005呈正相关。
– NLRP3炎症体:睡眠调节的关键开关
NLRP3是参与IL-1β调控睡眠的关键介质之一。NLRP3的组装可以激活caspase-1,激活的caspase-1随后将pro-IL-1β切割成成熟的IL-1β,然后调节中枢神经系统对生理睡眠的控制。
TNF-α和IL-1β受体通过配体激活介导NF-κB转录,触发参与睡眠调节和影响睡眠的炎症相关分子的转录。
这个指挥系统一旦启动,就会产生级联放大效应,小小的炎症信号最终可能对睡眠产生显著影响。
尽管睡眠剥夺对血脑屏障的影响在某种程度上是可逆的,但修复过程并不简单,即使在恢复正常睡眠模式后,恢复正常的血脑屏障功能仍然是一个漫长的过程。
这些发现为失眠的免疫治疗提供了新的思路,通过调节肠道微生物群来优化免疫炎症反应,进而改善睡眠质量。
源自中草药的药用食品及其生物活性化合物是独特的“益生元”,具有以下优点:副作用小、安全性高、提高患者依从性、适合长期食用。这些特性突显了这些草药在营养和治疗应用中的双重价值。此外,它们具有调节肠道微生物群稳定性的潜力,为通过调节肠道微生物组预防和治疗失眠提供了新的视角。
酸 枣 仁
酸枣仁(Ziziphi spinosae semen,SZR)是指鼠李科植物枣属种类中,中国枣(Ziziphus jujuba Mill. var. spinosa (Bunge) Hu ex H. F. Chou)的干燥成熟种子。
酸枣仁以其酸甜口味和中性特性为特征,靶向肝、胆囊、心经。它以“滋阴养心、补血养肝、安神安神”的功效而闻名,对治疗虚证和慢性失眠特别有效。正是因为其卓越的安神助眠功效,酸枣仁被誉为”东方睡眠果实“,在临床上广泛用于治疗失眠。
注:从历史角度看,酸枣仁在中医中一直受到高度重视,无论是作为单一草药还是复方制剂,都展现出了令人瞩目的疗效。
酸枣仁的”睡眠密码”:三大活性成分
皂苷、黄酮、生物碱是酸枣仁镇静和催眠作用的主要活性成分。先前的研究表明,酸枣仁可以调节氨基酸代谢、神经递质释放、炎症因子平衡和HPA轴稳态等生理过程,从而调节神经活动,实现神经系统的平衡,改善睡眠。
最近的研究表明,酸枣仁可以恢复失眠引起的肠道菌群失衡,增加大鼠体内有益菌的相对丰度,如乳杆菌、双歧杆菌、乳球菌、真杆菌,同时减少普雷沃氏菌的相对丰度。
菌群代谢产物——短链脂肪酸(SCFA)
梭菌和乳杆菌丰度的增加导致其代谢产物丁酸盐含量的增加,这进一步影响了体内的氨基酸代谢途径,从而显著恢复了患有睡眠-觉醒节律紊乱的小鼠的睡眠-觉醒节奏。
SCFA可以间接调节肠道和大脑中的5-HT水平。
研究表明,通过酸枣仁的微生物代谢增加的SCFA,可以调节结肠中TLR4/NF-κB/NLRP3相关信号通路中代表性因子的表达,从而调节微生物群-肠-脑轴,改善小鼠的失眠和抑郁行为。
注: TLR4:控制肠道免疫系统的”警报器”;NF-κB:调节炎症反应的”总开关”;NLRP3:影响炎症体的活化程度。
酸枣仁调节肠道菌群,而不是直接作用于大脑
显然,酸枣仁可以通过微生物群神经通路和微生物群免疫通路调节微生物群肠脑轴,从而实现对生物体睡眠行为的控制。这可能解释了酸枣仁的活性成分不能穿过血脑屏障,但仍然能改善睡眠质量。
卷 丹 百 合
在中医传统中,百合类植物一直被认为具有”润肺止咳、清心安神“的功效,而现代科学研究正在揭示其改善睡眠的深层机制。
卷丹百合(LB)可以通过降低血清中HPA轴激素的水平、增加5-HT和MT的水平、降低下丘脑中去甲肾上腺素(NE)的水平以及上调GABAA受体和5-HT1A受体的表达,来改善大鼠的下丘脑病理并缓解失眠行为。
肠道菌群调节:失眠改善的核心机制
卷丹百合调节肠道菌群的方式可能直接关系到它缓解失眠的效果。除了逆转失眠对肠道微生物群的多样性、丰度和粪便代谢表型的不利影响外,卷丹百合还控制花生四烯酸和色氨酸的代谢,从而降低与心理健康问题相关的化学物质犬尿氨酸的表达水平。
卷丹百合显著调节肠道内乳杆菌、埃希氏菌、Porphyromonadaceae的相对丰度,并积极调节下丘脑中的5-羟基-L-色氨酸,后者参与5-HT的代谢。通过卷丹百合干预,最重要和最基本的途径被认为是5-羟色胺能系统和花生四烯酸代谢途径。
复方协同:卷丹百合与地黄汤的联合
卷丹百合和地黄汤(LBRD)可以通过纠正肠道微生物群失调和避免肠道屏障受损或血脑屏障泄漏引起的炎症,来减轻与抑郁行为相关的神经元损伤。根据粪便微生物群移植和肠道微生物群组成研究,通过肠道-脑轴,乳杆菌、双歧杆菌、乳球菌(Lactococcus)被证明是地黄汤抗抑郁作用的重要因素。
灵 芝
灵芝的镇静作用与肠道菌群密切相关
当灵芝与罗伊氏乳杆菌发酵时,它可以增加血清中5-HT和GABA的水平,降低HPA轴激素的水平,有效缓解焦虑小鼠的失眠症状。
灵芝的乙醇提取物也对微生物组的结构产生了显著影响。
下丘脑的5-HT浓度与双歧杆菌和动物双歧杆菌呈正相关,这不仅提高了那里的5-HT水平,还增加了包括Tph2、Iptr3、Gng13在内的重要转录因子的产生。在用抗生素耗尽肠道微生物群后,灵芝乙醇提取物的促进睡眠作用以及与睡眠行为相关的粪便代谢物的变化完全消失。这表明肠道微生物群在灵芝的促睡眠作用中起着不可或缺的作用。
多糖成分的免疫调节与神经保护作用
来自灵芝的多糖已被证明可以提高小鼠大脑中的GABA和5-HT水平,并通过延长NREMS期间的δ波来提高其睡眠质量。
此外,灵芝多糖及其水解产物,即灵芝肽,通过各种途径表现出免疫调节活性。具体而言,灵芝多糖不仅降低了肠道中的F/B比值,而且显著上调了回肠中NF-κBp65、IL-2、IL-4的表达水平;它们还显著增强BDNF的表达,抑制促炎细胞因子的表达,并抑制小胶质细胞和星形胶质细胞的激活,从而发挥抗抑郁作用。
灵芝肽参与关键途径,如叶酸循环、脂肪酸的生物合成和代谢以及cAMP代谢。灵芝多糖在调节肠道微生物群稳态和提供神经保护方面具有巨大潜力。
茯 苓
茯苓(P.cocos)自古以来就被誉为”四时神药”,茯苓性平味甘,具有健脾利湿、宁心安神的功效,是古代人治疗失眠的首选核心药物之一,
传统核心药物的现代机制:多糖和三萜
茯苓含有多糖和三萜类化合物,是其镇静和诱导宁静的主要活性成分。研究表明,茯苓中的酸性多糖可以通过干预肠道微生物群和调节相关途径发挥镇静作用。
这些多糖不仅增加了肠道微生物群的丰度,如厚壁菌门、杆菌门、乳杆菌门、Fusicatenibacter、Prevotellaceae_UCG-001;它们还上调下丘脑中关键神经递质5-HT、DA、NE、GABA的水平,增加神经元细胞的数量,同时降低炎症因子的表达水平。
此外,来自茯苓的水提取物和水溶性多糖可以通过改善肠道微生物群失衡、缓解代谢紊乱、调节肠道神经肽和神经递质水平以及抑制TNF-α/NF-κB信号通路来有效预防焦虑的发作。
增加短链脂肪酸、促进色氨酸代谢
茯苓多糖可以通过增加肠道中的短链脂肪酸水平和促进色氨酸代谢来增强肠道屏障。它们不仅通过增加吲哚乳酸盐和吲哚-3-醛的水平来促进色氨酸代谢;还通过增加肠道中短链脂肪酸的水平、调节IL-2、IL-4、IL-6、IL-10、TGF-β、IFN-γ等关键免疫因子的表达,激活Wnt/β-Catenin信号通路来维持肠道屏障的完整性和功能。
色氨酸和短链脂肪酸的水平以及肠道屏障的健康稳态与肠道微生物群密切相关,对改善睡眠质量有重大影响。
人 参
人参被誉为”百草之王”,是中药中最珍贵的滋补品之一。作为五加科植物,人参含有丰富的活性成分,具有补元气、复脉固脱、补脾益肺、生津养血、安神益智等功效。现代研究发现,人参不仅能直接作用于大脑,还能通过调节肠道微生物群来改善睡眠质量。
多重活性成分的协同作用:跨越血脑屏障
人参中发现的肽、多糖、皂苷具有穿过血脑屏障并调节神经内分泌平衡和大脑代谢环境的能力。人参多糖通过增强肠道吸收和影响肠道微生物代谢来增强人参皂苷Rb1和微生物代谢产物的暴露。Rb1通过调节瑞士乳杆菌丰度和GABAA受体表达发挥神经保护作用。
人参皂苷Rg1(Rg1)对神经系统具有潜在的健康促进作用。Rg1可以改善吗啡诱导的肠道微生物群失调(特别是拟杆菌),抑制肠道微生物群衍生的色氨酸代谢,调节异常升高的血清素、5-羟色胺受体1B和5-羟色胺受体2A水平,使其回归正常范围。
人参皂苷的多途径神经保护机制
人参皂苷Rg可能影响肠道微生物群,并通过多种不同途径提供神经保护。
Rg1可以通过调节5-HT神经递质系统、阻止肠道微生物群产生的色氨酸代谢和改善肠道微生物群失调(特别是拟杆菌)来防止小鼠产生吗啡依赖。
Rg5不仅可以纠正不平衡的肠道微生物群,恢复肠道屏障的功能,还可以通过控制脂肪和葡萄糖的代谢,提高GABA/Glu比值,上调GABAA、GABAB和5-HT受体1A的表达,改变时钟相关蛋白质的节律特征,改善睡眠质量,进而影响GABA和5-HT神经递质系统。
复方协同与代谢循环优化
人参和酸枣仁的联合使用,可以改善肠道微生物群的结构,促进Glu/GBA-Gln代谢循环的正常运作,增加海马中GABA的合成和释放,从而显著改善失眠大鼠的睡眠状态。这表明人参可以通过多种途径干预肠道微生物群并调节大脑睡眠功能。
doi: 10.3389/fphar.2025.1572007
天 麻
天麻(G.Blume)是兰科植物天麻的干燥块茎,素有”定风草”之称,是著名的息风止痉、平抑肝阳的中药材。
天麻素的多重神经保护机制:从炎症调控到信号通路调节
从天麻中提取和分离天麻素(GAS)已被证明对中枢神经系统疾病有显著影响,包括但不限于失眠、焦虑、抑郁、认知障碍、缺血性中风。
天麻素通过控制IL-6、IL-1β等炎性因子的表达、B细胞淋巴瘤-2(Bcl-2)蛋白的活性以及p-ERK与ERK的比值,不仅改善了失眠小鼠的睡眠质量,而且通过调节TLR4/NF-κB和Wnt/β-catenin信号通路,改善了快速眼动睡眠剥夺引起的睡眠障碍。因此,天麻素在提高睡眠质量方面具有很大的潜力。
肠道微生物群调节
已经进行的研究表明,天麻素可以通过调节微生物群-肠-脑轴来抑制神经元凋亡,从而改善阿尔茨海默病小鼠的认知障碍和神经变性。
在抑郁的小鼠中,天麻的水提取物可以通过促进潜在有益菌(Alloprevotella、双歧杆菌、Defluviitaleaceae UCG-011、Akkermansia、Parabifidobacter)和粪便SCFA水平的增加和平衡,使结肠中5-羟吲哚乙酸与5-HT的比例正常化,并降低犬尿氨酸与色氨酸的比例来重塑肠道微生物组结构。抗生素混合物的给药部分消除了天麻素对阿尔茨海默小鼠的神经保护作用。
天麻及其活性成分对大脑功能的影响是显而易见的,因为它们部分针对微生物群-肠道-大脑轴。然而,支持天麻素可以通过这种微生物群-肠-脑轴调节大脑睡眠功能这一观点的确凿实验证据仍有待观察。需进一步研究来确定天麻素通过改变肠道微生物群来改善睡眠质量的确切过程,以便更谨慎地开发和使用天麻。
蒙 古 黄 芪
蒙古黄芪是豆科植物蒙古黄芪的干燥根,被誉为”补气圣药”,在中医药学中具有重要地位。黄芪性温味甘,具有补气固表、托毒排脓、利水消肿的功效,是临床上最常用的补气药之一。
现代研究发现,蒙古黄芪富含黄酮类化合物、多糖、皂苷,通过控制肠道微生物群的组成、代谢和活性,有助于保持肠道微环境的稳定。
黄芪多糖的免疫调节机制:特异性菌群调控的双向作用
研究发现,不同浓度的黄芪多糖(APS)对睡眠剥夺小鼠的脾脏和身体损伤具有缓解和保护作用。
进一步的研究表明,黄芪多糖可以通过调节与炎症和免疫反应、短链脂肪酸合成和TLR4/NF-κB通路有关的某些微生物来改善免疫功能障碍。
例如,黄芪多糖可以改善免疫功能低下的小鼠和大鼠的免疫功能,这是由于减少了Pseudoflavonifractor、Oscillibacter、Tyzzerealla、Paraprevotella、Lachnoclostridium的丰度,并增加了乳杆菌、双歧杆菌、Roseburia、脱硫原体、Paracoccus、副拟杆菌、Clostridium XIVb、Butyricicoccus的丰度。
然而,在肠道微生物群减少的免疫功能低下小鼠中,黄芪多糖并没有改善免疫功能。
肠脑轴的积极调控:从代谢产物到神经递质的全面优化
为了积极控制肠-脑轴,黄芪多糖不仅增加了肠道中乳杆菌和芽孢杆菌的相对丰度,还增加了粪便中短链脂肪酸和GABA的含量,提高了虾的免疫力。
此外,黄芪多糖可以显著减轻与年龄相关的肠道屏障破坏、胃肠酸碱平衡丧失、肠道长度缩短、肠道干细胞过度增殖以及衰老后的睡眠障碍。
因此,肠道微生物群不仅积极帮助身体吸收黄芪多糖,而且通过提高肠道SCFA水平来改善免疫功能障碍,并通过促进神经递质的释放来积极调节肠道脑轴。
龙 眼
龙眼肉,又称桂圆肉,自古以来就被誉为”智慧果”。在中医理论中,龙眼肉性温味甘,具有补益心脾、养血安神的功效,《神农本草经》将其列为上品药材。龙眼肉是中国传统医学中常用的治疗失眠的草药之一,但关于其改善睡眠质量的潜力的药理活性研究很少。
龙眼含有GABA,可以用作天然膳食补充剂。龙眼中富含多种氨基酸,如GABA和Glu,并且随着果实年龄的增长,其浓度也会增加。成熟后在冷藏温度下储存可以增加水果中的GABA含量。
此外,通过增加胃中Lactobacilli、Pediococci、 Bifidobacteria的数量,肠道微生物群对龙眼多糖的代谢可以提高琥珀酸和SCFA(乙酸、丙酸和丁酸)的水平,增强肠道免疫力。
无论是作为富含GABA的膳食补充剂还是通过调节肠道内的微生物代谢产物,龙眼肉都有可能通过影响肠道中GABA、MT、5-HT等睡眠相关神经递质的合成和释放来调节肠道微生物群-肠脑轴。这可以直接或间接地调节身体的睡眠-觉醒周期,从而发挥强大的睡眠促进作用。
其他中草药及其成分
中医药宝库中蕴藏着众多具有安神功效的珍贵药材,这些草药在千百年的临床实践中积累了丰富的应用经验。
除了前述的经典药材外,栀子、三七、莲子等传统药材同样具有改善睡眠的潜力,但它们通过肠道微生物群调节睡眠机制的研究相对较少。这里讨论了其他一些草药及其活性成分如何影响肠道菌群,从而提高睡眠质量的能力。
栀子、三七
研究表明,栀子可以通过调节肠道微生物群和降低TNF-α和IL-7β水平来改善睡眠质量和缓解焦虑症状。
由肠道微生物群代谢的三七总皂苷转化为人参皂苷Rg,其保护海马神经元并调节大脑中的神经递质水平,从而改善失眠、抑郁和认知障碍。
莲子、荷叶
莲子和荷叶都可以通过调节肠道微生物群的丰度和结构来调节GABA能系统,从而促进睡眠。然而,它们调节肠道微生物群的方式存在显著差异。具体而言:
枣、谷芽
枣具有改善睡眠质量和通过调节GABA能系统提供神经保护的潜力。具体而言,它可以上调Lachnoclosdium、Marvinbryantia的丰度,同时下调Alistipes、Akkermansia的丰度。
谷芽[Setaria italica(L.)Beauv]可能会增加肠道中普雷沃氏菌、乳酸菌、Ruminococcus的丰度,从而通过调节神经递质和炎症因子水平来提高SCFA水平并改善睡眠质量。
山茶、枸杞
山茶[(L.)Kuntze]可能通过改善肠道微生物群来影响神经内分泌途径和免疫系统,从而调节睡眠-觉醒周期。
枸杞可能通过改善肠道屏障和抑制TLR4信号通路来保护神经系统。
交泰丸
由黄连根茎和肉桂皮组成的交泰丸可以改善睡眠,并减轻慢性睡眠剥夺引起的炎症和胰岛素抵抗。组学结果表明,交泰丸治疗显著增加了小鼠中毛螺菌科、拟杆菌属、AKK菌属的相对丰度。
黄连温胆汤对失眠的机制可能与它抑制 5-羟色胺含量的降低和γ-氨基丁酸水平的升高有关。同样,研究发现甘麦大枣汤可以增加 NE 和 5-羟色胺的含量,改善睡眠,在一定程度上缓解抑郁,柴胡加龙骨牡蛎汤主要通过调节下丘脑-垂体-肾上腺轴(ACTH、CORT等)和脑单胺神经递质(NE、DA、5-羟色胺等)的水平来治疗失眠。
草药及其活性成分在改变肠道微生物群和提高睡眠质量方面的巨大潜力已经得到证实,尽管这一研究领域仍处于早期阶段。更多的研究不仅可以为治疗失眠提供坚实的支持,还可以通过阐明这些草药与微生物群-肠道-大脑轴相互作用的机制来调节与睡眠相关的大脑功能,从而帮助我们更明智地开发和使用这些草药。
针 灸
针灸治疗注重根据辨证选择穴位,基于辨证的针灸疗法可以取得良好效果并改善胃肠功能,针灸结合腹部环形按摩可以改善下丘脑和海马旁回的功能,从而达到改善失眠症状的效果。
此外,研究发现针灸可以抑制 HPA 轴的活性,从而改善失眠症状。
有研究在微生物-肠-脑轴理论指导下总结了针灸的原则:
可以直观地发现,这些针灸穴位与微生物-肠-脑轴的解剖部位有许多重叠。从健脾和胃治疗失眠的角度来看,主要穴位有中脘、关元、天枢、气海等。
这些针灸疗法可以通过调节神经递质和某些激素的分泌,以及下调 HPA 轴来抑制交感神经并改善内分泌,从而改善失眠症状,这些症状是微生物-肠-脑轴相同调节机制的一部分。
doi: 10.12998/wjcc.v12.i18.3314
饮 食 调 整
不良饮食模式的负面影响
长期高糖摄入会刺激免疫系统,诱发过度炎症反应,导致睡眠片段化。
肥胖人群中Faecalibacterium丰度显著下降,这在慢性失眠患者中同样存在。
健康饮食模式的积极作用
富含植物性食物、抗氧化剂和不饱和脂肪酸;促进产丁酸菌丰度增加,显著改变肠道微生物代谢活性,与更好的睡眠质量和更长的睡眠时间相关。
适用人群:肥胖青少年、结合增加体力活动
增加肠道中乳杆菌的丰度,乳杆菌以其促进睡眠的有益作用而闻名。
其他,如习惯性饮茶,可能通过肠道菌群-胆汁酸轴减轻慢性失眠引起的肠道菌群失衡和胆汁酸代谢紊乱。
益 生 菌
接受发酵益生菌 Lactobacillus brevis DL1-11 牛奶的小鼠表现出更短的睡眠潜伏期和更长的睡眠时间。因为 DL1-11 可以产生大量的 GABA,GABA 可以促进放松并增强睡眠。
Lactobacillus fermentum PS150TM通过增加下丘脑腺苷 A1 受体的表达,有效地促进了正常小鼠的睡眠,并缓解了咖啡因诱导失眠小鼠的失眠症状。PS150TM 能够恢复因首夜效应导致睡眠障碍的小鼠的非快速眼动睡眠,这可能是由于其重塑肠道菌群组成的能力,改变血清素能通路,减少慢性轻度压力大鼠的抑郁和焦虑。
Bifidobacterium breve CCFM1025 通过抑制 HPA 轴活性,改善了睡眠并缓解了压力水平。
Bifidobacterium adolescentis SBT2786 可以通过增加快速眼动睡眠时间来延长总睡眠时间,白天疲劳减少。
Lactobacillus plantarum PS128 显著增强了深度睡眠,并减少了疲劳和抑郁症状。
Lactobacillus gasseri CP2305 也已可以改善肠道微生物群组成,并降低唾液皮质醇浓度,从而减轻压力并增强睡眠 。
Lactobacillus casei Shirota 牛奶通过延长睡眠时间和减少觉醒时的嗜睡感,帮助面临考试压力的个体 。
Lactococcus lactis subsp. cremoris YRC3780 也显示出改善睡眠和缓解压力的潜力,这一点由日本进行的一项双盲、安慰剂对照的临床试验所证实,接受 YRC3780 干预的参与者主观睡眠质量和心理健康均有显著改善。
doi: 10.3390/ijms252313208
益 生 元
益生元饮食(由半乳寡糖、聚葡萄糖、乳铁蛋白和乳清蛋白浓缩牛奶脂肪球膜蛋白-10 组成)通过在正常情况下增强非快速眼动睡眠,并在压力情况下延长快速眼动睡眠,对小鼠的睡眠模式产生了积极影响。
接受益生元饮食(由半乳寡糖和聚葡萄糖组成)的大鼠在睡眠紊乱情况下表现出更长的非快速眼动睡眠和快速眼动睡眠。菌群分析发现,在益生组中,Parabacteroides distasonis 的相对丰度增加,这与促进睡眠和恢复昼夜节律有关。
在一项人体研究中,45 名参与者被随机分为三组,分别接受低聚果糖(FOS)、低聚半乳糖(GOS)或安慰剂。结果表明,低聚半乳糖组的参与者睡眠质量得到改善,唾液皮质醇觉醒反应显著降低。这种皮质醇的减少与肠道菌群中 Bifidobacteria 的相对丰度增加有关,这些菌具有代谢低聚半乳糖的能力,并对心理健康有积极作用。
抗性淀粉是另一种已被证明能通过减少炎症和 HPA 轴活性来改善 2 型糖尿病患者睡眠质量的益生元。
一项随机、双盲、安慰剂对照的研究也报道了益生元酵母甘露聚糖的改善睡眠效果。酵母甘露聚糖组的非快速眼动睡眠第 3 阶段睡眠时间和总睡眠时间均显著长于安慰剂组。
粪菌移植 (FMT)
目前,越来越多的研究将粪菌移植作为精神健康疾病的一种潜在治疗方法,因为肠道微生物群可以通过微生物群-大脑轴影响中枢神经系统。
临床研究表明,洗涤微生物群移植增加了有益细菌(如 Bifidobacterium、Ruminococcus gnavus 、Prevotella 7、Faecalibacterium)的相对丰度,并减少了有害细菌(如 Escherichia-Shigella 、 Streptococcus)的相对丰度,显著改善了患有各种潜在疾病的患者睡眠障碍。睡眠质量得到改善的患者在抑郁程度和 IBS 症状严重程度上也表现出更大的减少。
另一项开放标签的观察性研究发现,在患有胃肠道疾病且出现睡眠障碍的患者中,结果相似,作者认为整体改善归因于FMT治疗后菌群多样性的增加。
一项真实世界研究发现,粪菌移植显著改善了失眠患者的睡眠质量,缩短了睡眠潜伏期,并提高了睡眠效率。通过比较肠道菌群组成,研究人员发现,粪菌移植显著增加了产短链脂肪酸菌的相对丰度,包括 Lactobacillus、Bifidobacterium 、 Turicibacter。
注:所有这些研究都将失眠视为与其他疾病相关的共病,这表明睡眠的改善也可能归因于疾病症状的缓解,粪菌移植对睡眠障碍的有效性需要进一步研究。
随着现代医学对肠-脑轴研究的深入,传统中医药”治未病“的理念与现代微生态学理论完美融合,为失眠治疗开辟了全新视角。
未来研究应重点关注个体化精准治疗策略的制定。肠道菌群检测技术的应用将为临床实践提供重要指导,通过分析患者特异性的菌群结构,识别关键的失调菌群如拟杆菌、双歧杆菌、乳杆菌等,可为选择最适宜的中药配方提供科学依据。
同时,肠道菌群代谢产物如短链脂肪酸、GABA、血清素等关键代谢产物水平,这些在谷禾肠道菌群检测报告中也都有相应指标,结合肠道菌群检测报告有助于辅助评估治疗效果并优化用药方案。
<来源:谷禾肠道菌群检测数据库>
在中医药现代化进程中,应深入挖掘经典方剂如甘麦大枣汤、安神定志丸等复方的菌群调节机制,探索经典方剂与菌群协同效应的内在规律。同时,结合中医体质辨识与肠道菌群分型,建立”体质-菌群-证候“三位一体的诊疗模式。
通过构建中药-菌群相互作用数据库,为临床医师提供相对精准的用药指导,最终实现传统中医智慧与现代精准医学的深度融合,为失眠患者带来更加安全、有效的个性化治疗方案。
注:本账号内容仅供学习和交流,不构成任何形式的医疗建议。
主要参考文献
Wu C, Dou J, Song X, Yang F, Liu X, Song W, Zhang X. Gut microbiota: a new target for the prevention and treatment of insomnia using Chinese herbal medicines and their active components. Front Pharmacol. 2025 May 6;16:1572007.
Li C, Chen S, Wang Y, Su Q. Microbiome-Based Therapeutics for Insomnia. Int J Mol Sci. 2024 Dec 9;25(23):13208.
Ito H, Tomura Y, Kitagawa Y, Nakashima T, Kobanawa S, Uki K, Oshida J, Kodama T, Fukui S, Kobayashi D. Effects of probiotics on sleep parameters: A systematic review and meta-analysis. Clin Nutr ESPEN. 2024 Oct;63:623-630.
Patterson E, Tan HTT, Groeger D, Andrews M, Buckley M, Murphy EF, Groeger JA. Bifidobacterium longum 1714 improves sleep quality and aspects of well-being in healthy adults: a randomized, double-blind, placebo-controlled clinical trial. Sci Rep. 2024 Feb 14;14(1):3725.
Liwinski T, Lang UE, Brühl AB, Schneider E. Exploring the Therapeutic Potential of Gamma-Aminobutyric Acid in Stress and Depressive Disorders through the Gut-Brain Axis. Biomedicines. 2023 Nov 24;11(12):3128.
Li L, Wu L, Jiang T, Liang T, Yang L, Li Y, Gao H, Zhang J, Xie X, Wu Q. Lactiplantibacillus plantarum 124 Modulates Sleep Deprivation-Associated Markers of Intestinal Barrier Dysfunction in Mice in Conjunction with the Regulation of Gut Microbiota. Nutrients. 2023 Sep 15;15(18):4002.
Pan LM, Hong ZB, Guan RQ. Research progress on insomnia treated by traditional Chinese medicine and acupuncture based on microbial-gut-brain axis theory. World J Clin Cases. 2024 Jun 26;12(18):3314-3320.

谷禾健康

当前微生物组研究面临的主要挑战包括数据的成分特性、高维度、分类单元间的系统发育关系以及潜在的多种效应模式——即少数几个具有中等强度效应的微生物和大量具有微弱累积效应的微生物可能共同影响宿主健康。
为了应对这些挑战,近日,来自美国大通福克斯肿瘤中心和肯尼索州立大学等研究人员提出了一个新型模型——贝叶斯成分广义线性混合模型(Bayesian Compositional Generalized Linear Mixed Model, BCGLMM),其研究结果发表在《BMC Bioinformatics》上。
BCGLMM旨在提高利用微生物组数据进行疾病预测的准确性和解释性,它采用对数转换和对回归系数施加软性零和约束来处理成分数据;利用结合系统发育信息的结构化正则马蹄形先验来识别具有中等效应的关键分类单元;并通过引入基于样本间微生物组相似性的随机效应项来捕捉众多微小分类单元的累积影响。
模型在模拟数据和真实数据(炎症性肠病)的测试结果表明,BCGLMM在预测性能和识别相关微生物特征方面均优于现有的一些方法,证明了其在微生物组相关疾病预测领域的有效性和潜力。
BCGLMM模型构建在广义线性混合模型(GLMM)的框架之上,专门针对微生物组数据的特性进行了调整。
数据预处理
1. 对OTU计数使用中心对数比(CLR)变换,回归系数施加软性零和约束。
2. 通过16S rRNA基因序列构建系统发育树,计算Bray-Curtis距离矩阵。
BCGLMM模型结构
BCGLMM模型主要由三个关键部分组成:
将线性预测器的输出通过sigmoid函数转为概率pi,然后根据预设的阈值转为二分类输出(如患病/健康)。
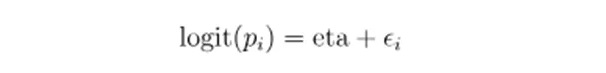
线性预测器(eta):
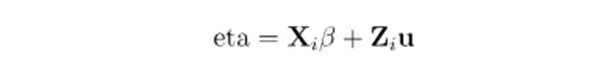
编辑
固定效应部分
随机效应部分
固定效应(如显著分类群)可能无法完全解释疾病风险,而大量微弱效应的分类群可能通过生态网络的整体扰动共同影响结果。随机效应用于建模这些样本层面的变异。两者结合后,模型既能抓住主要驱动因素,又能解释微生物生态系统的整体影响(如原文中IBD预测性能提升)。
后验分布输出
使用 R 包 brms(后端调用 rstan),通过 Hamiltonian Monte Carlo(HMC) 及其自适应变体 No-U-Turn Sampler (NUTS) 实现后验分布采样。
1
模拟数据测试模型
固定样本数量为400,分类单元数目分别选择100、300、500。
组合不同样本数量、中等效应数量和小效应数量,分别生成连续和二元数据,共得到了27种场景,每个场景下,测试三种模型,分别为:
下表是研究人员提供的当中等效应数量为6时,每个模型在不同数据集和小效应比例下的性能评估结果:
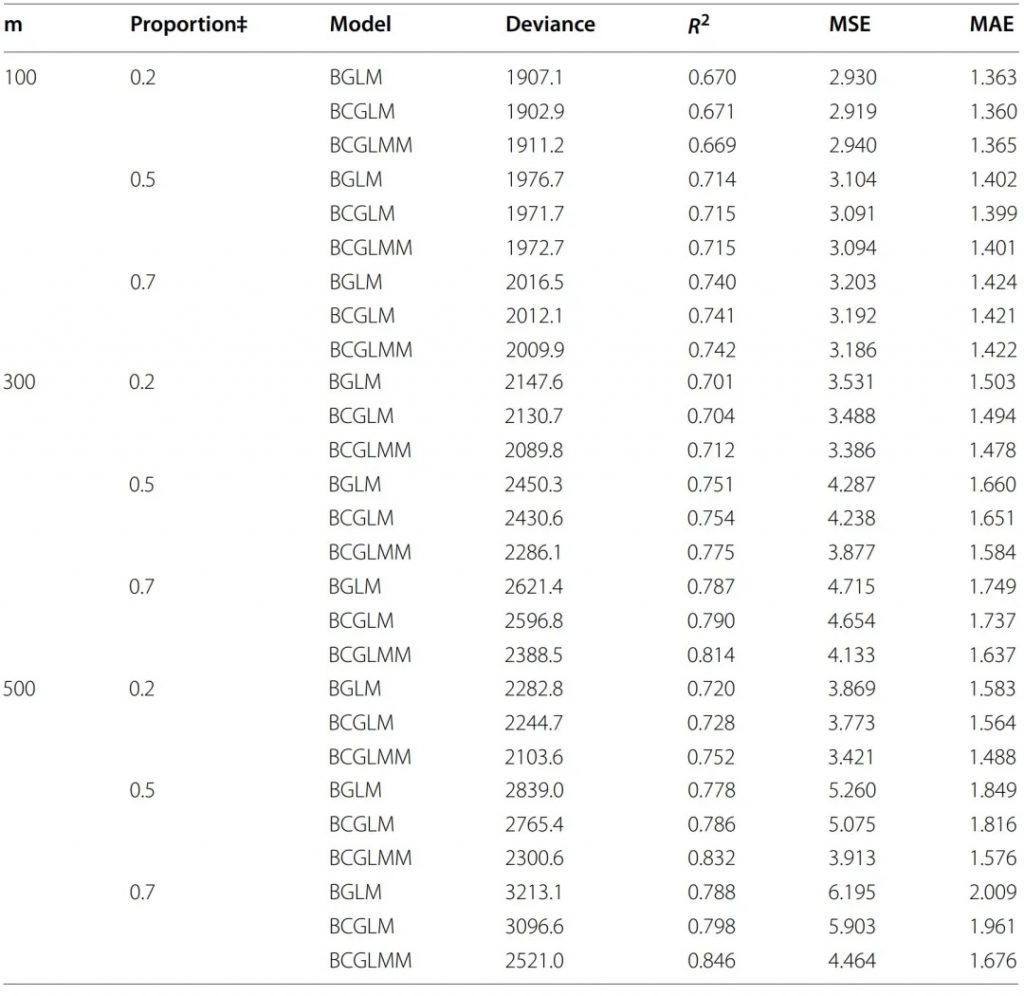
表1
结果显示,大部分场景下,模型性能从优到劣排序为:BCGLMM > BCGLM > BGLM
BCGLMM显示为R2最高、MSE和MAE最低。
这些都说明BCGLMM中的随机效应能够捕获所有标记的综合小效应。
另外,研究人员给出的相同场景下的二分类结果,显示BCGLMM准确性更好(更高的AUC值),如下表:
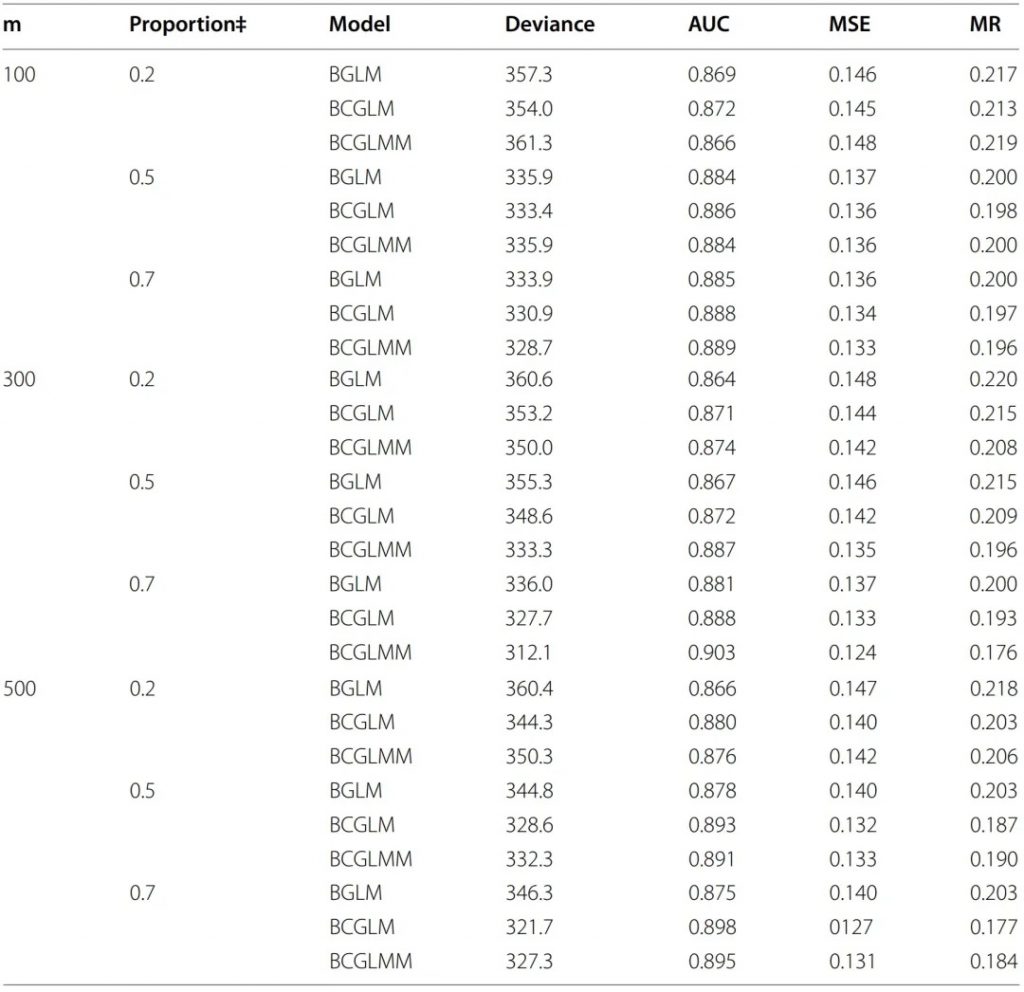
表2
对于其它中等效应数量的组合场景,结果如下图:
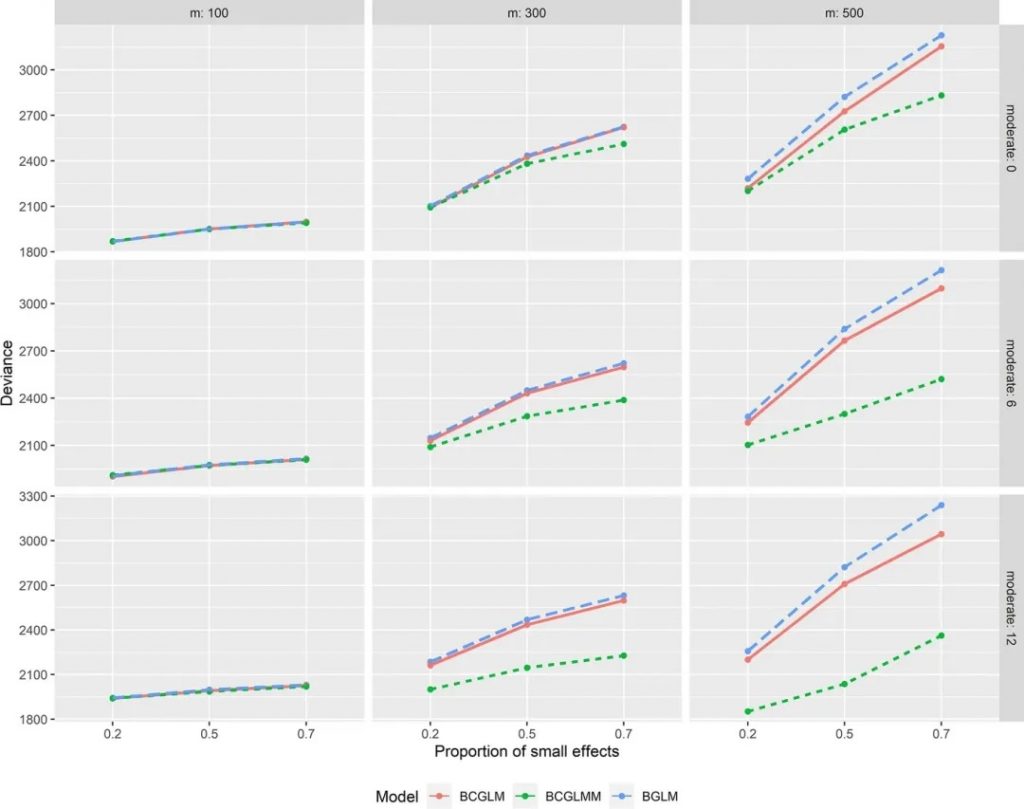
图1
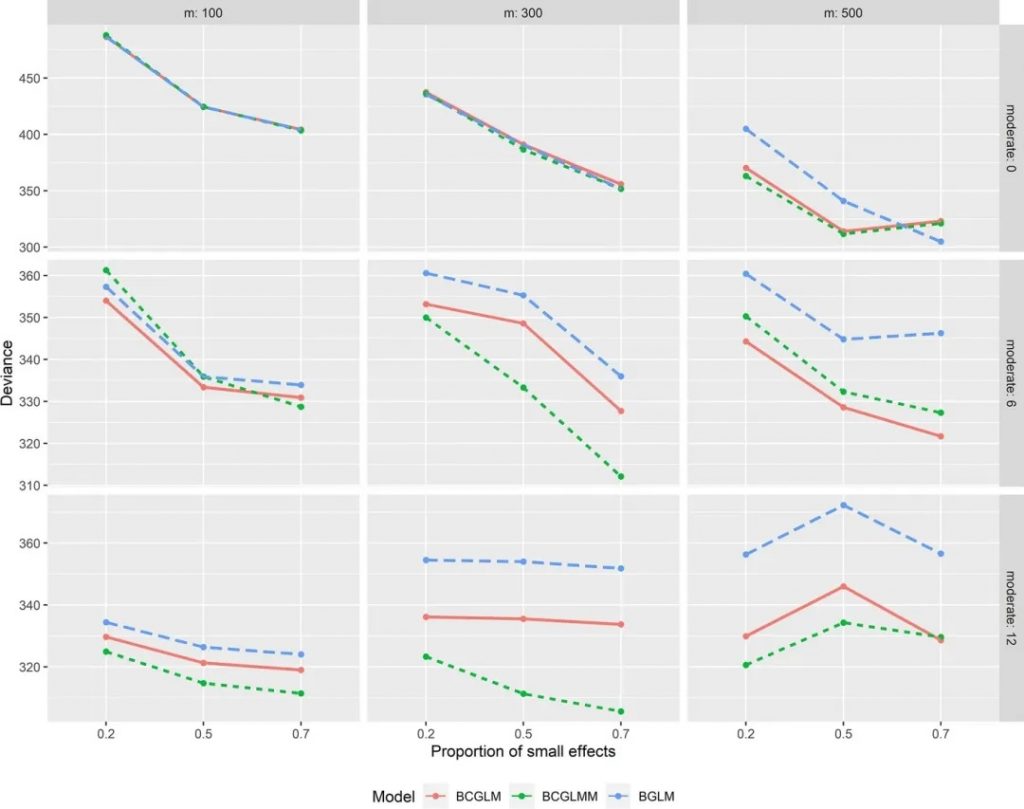
图2
图一对应表一(基于连续性结果的模型性能评估)
图二对应表二(基于二元结果的模型性能评估)
结果显示,在m介于300~500时,对比中等效应数量6,中等效应数量12场景下的BCGLMM模型性能更优。
2
真实数据测试模型
数据来自美国肠道项目(American Gut Project,AGP)的公开数据,旨在区分IBD患者和健康对照。含4684 个粪便样本和 1002 个物种数据。
基于“方法”对数据进行预处理后,分别应用BCGLMM(考虑了样本相关的随机效应和预测变量相关性)、BCGLM(仅关注预测变量相关性)、BGLM(不考虑随机效应和预测变量相关性)模型,比较三种模型的准确性。
根据AUC值判断,BCGLMM 、 BCGLM 和 BGLM 的交叉验证 AUC 值分别为 0.702 、 0.687 和 0.672,可以认为BCGLMM在真实数据集上的表现最优(AUC=0.702)。
基于模拟数据和真实数据的测试结果,可以得出结论,同时考虑样本相关的随机效应和预测变量相关性的BCGLMM模型能够识别出与疾病相关的潜在微生物特征,二分类任务下,提升疾病预测的准确性。
BCGLMM模型的局限性在于计算成本较高,在大规模研究中可能面临内存和CPU时间挑战。综合看,推荐使用场景为:高维微生物组数据(特征数≥300),预期存在大量小效应的疾病预测任务,需要考虑系统发育关系的研究,对预测精度要求较高且能承受计算成本的项目。
该研究中的BCGLMM模型,突破传统稀疏模型的限制,首次系统性地解决了微生物组数据分析中的核心挑战,通过混合模型框架,能够识别中等效应并累积大量小效应,显著提升了疾病预测的准确性。
BCGLMM模型具有很大的转化潜力。
总体而言,BCGLMM为微生物组驱动的精准医学提供了方法论基础,其兼顾统计学严谨性与生物学机制的框架有望成为探索微生物生态与疾病关联的核心技术之一。
主要参考文献
Zhang, L., Zhang, X., Leach, J.M. et al. Bayesian compositional generalized linear mixed models for disease prediction using microbiome data. BMC Bioinformatics 26, 98 (2025).

谷禾健康

在自然界中,一些引人注目的共生现象出现在能够改变宿主行为的微生物与其宿主之间。
这些病原体的“精神控制”能力激发了许多末日小说作品,如HBO剧集《最后生还者》中令人毛骨悚然的真菌感染场景。
延展小知识
关于细菌沃尔巴克氏体、狂犬病毒、偏侧蛇虫草菌
Wolbachia pipientis 操控昆虫生殖及神经
Wolbachia pipientis 被喻为生物基因“木马”,可以操控昆虫生殖。常见于节肢动物门和部分线虫体内,影响所寄生动物的生殖和发育。除了影响生殖外,当它们转移到一个新的物种时,会使新寄主产生各种严重的神经系统并发症。2009年开始,科学家发现Wolbachia pipientis阻止登革热病毒在蚊子体内复制增殖,从而阻隔登革热的传播。
2019年,中山大学的研究人员利用利用Wolbachia pipientis感染的雄蚊使得雌蚊无法繁殖下一代几乎消灭了世界上最具侵入性的蚊子种类 – 亚洲虎蚊(白纹伊蚊,本地俗称花脚蚊)。
狂犬病病毒 (Rabies virus)
狂犬病病毒(Rabies virus,RABV) 感染宿主中枢神经系统的重要人兽共患病,一旦发病死亡率接近100%,每年造成全球几万人死亡。
Ophiocordyceps unilateralis,僵尸蚂蚁
Ophiocordyceps unilateralis ,也被称为偏侧蛇虫草菌,是一种拟寄真菌,偏侧蛇虫草菌在感染蚂蚁后,能够通过释放化学物质改变和控制蚂蚁的行为,让变成蚂蚁自己的傀儡,直到最终死亡。HBO新剧《最后生还者》(The Last of Us)第一季让大家领教了真菌的厉害。剧中的这种致命真菌就是偏侧蛇虫草(Ophiocordyceps unilateralis),它能够入侵昆虫的大脑,使其成为僵尸。
然而,改变行为的微生物并不仅限于这些极端的寄生生物。在自然界中,已有关于共栖和互利微生物驱动宿主行为操控的描述。这个观点在发现胃肠道内的细菌可以调节宿主中枢神经系统后,得到了广泛关注和逐步证实。
肠道微生物群——这一动态且多样化的微生物群落,被认为是肠-脑相互作用的关键调节器。与自然界中那些极端的”精神控制”案例不同,人体肠道微生物群以更加微妙和复杂的方式影响着我们的情绪、认知和行为。
各种证据表明,肠道细菌发出的信号可以循环到大脑,或影响肠-脑轴免疫和内分泌细胞的功能。一个庞大的神经网络——外周神经系统,不断且迅速地在肠道和大脑这两个远距离器官之间传递信息,使大脑能够协调胃肠功能,而肠道也能够影响情绪、认知和行为。
临床意义:当微生物失衡遇上疾病
肠道微生物结构的改变与这些生物系统的变化相关,并对人类代谢、神经精神和肠道健康产生重要影响。焦虑、抑郁、自闭症谱系障碍(ASD)和帕金森病等多种神经疾病都具有明确的胃肠疾病合并症。诸如肠易激综合征(IBS)和炎症性肠病等胃肠疾病常常表现为心理症状。关键是,这些临床相关性与失衡的微生物群和紊乱的肠—脑信号密切相关。
四条通路:微生物与大脑的对话方式
目前已经比较清晰的知道,连接肠道微生物群和大脑的四种主要通信方式。
肠道微生物群-脑轴
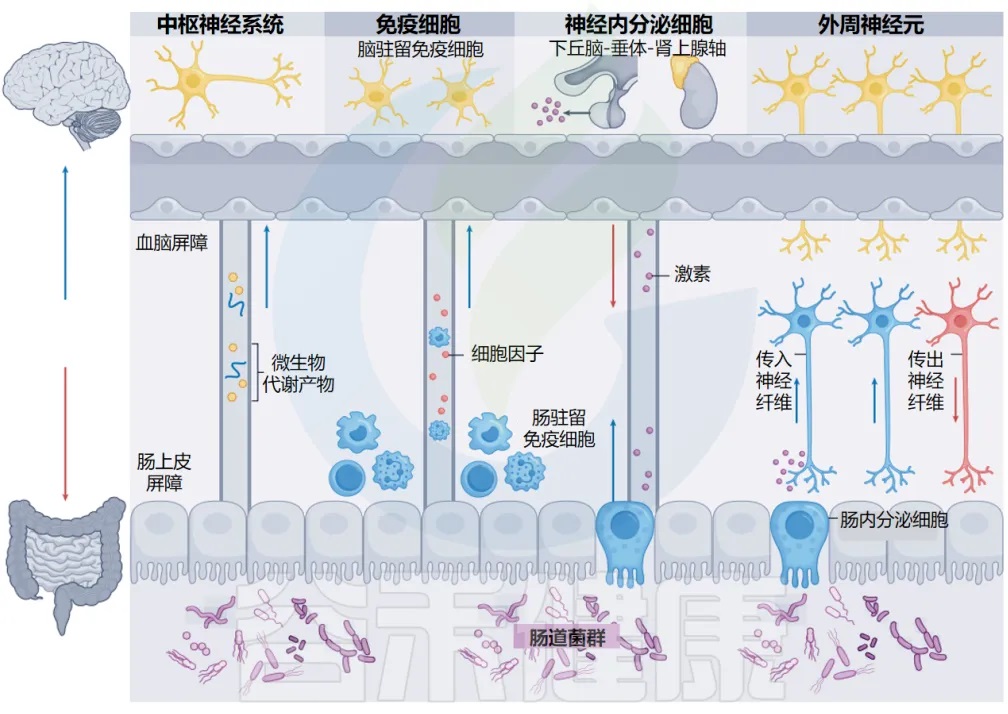
doi.org/10.1038/s41579-024-01136-9
聚焦核心:肠道神经上皮回路的精密机制
这些途径以多种方式相互交叉和影响。免疫细胞和周围神经元之间(神经-免疫轴)、神经内分泌细胞和免疫细胞之间(神经内分泌-免疫轴)、以及肠上皮细胞和周围神经元之间的双向串扰(肠神经上皮轴),为肠道和大脑之间的通信增加了额外的复杂性。
其中,肠上皮的化学感应细胞与支配肠道并延伸到中枢神经系统的周围神经元之间的关系尤为关键。这些肠道神经上皮回路代表了微生物-宿主相互作用的最前沿和最精密的机制。
本文我们将深入了解这些肠道神经上皮回路的分子机制、细胞间相互作用,以及它们如何导致疾病状态,揭示肠道微生物群如何通过这一精密的神经网络实现对宿主行为的影响。理解这些途径有助于促进基于微生物组的胃肠道和神经系统疾病新疗法的开发。
胃肠道免疫系统和神经系统
在哺乳动物中,胃肠道包含最大的免疫系统、微生物群生态系统和内源性神经系统,它们之间复杂的相互作用有助于维持正常的胃肠道生理功能。
特别是胃肠道的固有神经系统,即肠神经系统,调节着重要的胃肠道功能。肠神经系统回路的破坏会导致全身性的胃肠道症状,如腹泻、便秘、内脏疼痛等,这些症状影响着世界上高达40%的人口。
注:肠神经系统,enteric nervous system,简称 ENS,被誉为”第二大脑”。
神经免疫微环境的动态感知机制
胃肠道免疫系统和神经系统都进化出了感知和快速响应动态肠道环境的机制,能够实时监测并快速响应肠腔内的营养、微生物及病理性刺激信号。
许多神经将胃肠道粘膜中的局部免疫细胞连接起来,形成神经元免疫细胞单位,这些细胞单位可以通过肠道管腔营养来源和微生物来源的线索重塑。这些单元不仅能够独立启动局部免疫应答,还通过细胞间通讯网络进行信息整合,最终形成由肠道微生物群精密调控的”肠道神经-免疫轴”。这些协调一致的信号轴调节胃肠道屏障功能、免疫力和宿主保护。
病原感染中的神经免疫协同防御
肠道神经和免疫相互作用在感染期间尤为重要。感染应激可激活特定的胃肠道功能,可以通过腹泻反应快速清除病原体,腹泻反应可以通过增加局部水分泌到管腔中并促进推进性收缩模式来清除病原体,这两种反应都需要肠神经系统(ENS)的输入。
此外,感染或炎症引起的肠神经系统结构和/或活动紊乱可以促进或减少炎症,产生胃肠道症状,并限制组织病理学。
肠神经系统也可以再生,从而在损伤后恢复胃肠道功能。然而,在许多情况下,完全恢复往往受到限制,并且肠神经系统的损害可能产生长期后果,例如感染后胃肠道疾病。
肠道神经和免疫的相互作用的证据
尽管免疫系统与神经系统过去被分开单独研究,但现在越来越清楚,这两个复杂系统在功能上密切相关。这两个系统相互交流并不是一个新概念。两千年前,罗马医生Aulus Cornelius Celsus将炎症的四个主要症状归纳为:
疼痛、发红、肿胀、发热
其中疼痛由感觉神经系统引起,后三者则与血管和免疫功能相关。
神经对于宿主抵御病原体的调控也是进化上保守的特性,这一点从简单的多细胞动物(如线虫)到脊椎动物(如鱼和哺乳动物)的研究中都有明确证据。
过去几十年,科学家们发现神经—免疫交流在生理、抗感染、防御、修复和疾病中的多种作用。
肠道神经解剖——层层保护系统
肠道的神经解剖结构由居于器官内外的感觉神经元和自主神经元共同组成(感觉神经元负责感知信息,自主神经元负责自动控制),胃肠道在解剖学上由肠系膜、浆膜、肌肉、粘膜下层、固有层和上皮组成,由多个周围神经元群支配,这些神经元群与局部免疫细胞配合和协调反应。
肠系膜:是连接肠道与腹壁的重要结构,其主要功能是支撑、固定和保护肠道,同时为肠道提供血液供应和淋巴引流。
浆膜:保护器官,减少摩擦,参与免疫反应、维持器官位置。
肌肉:负责肠道蠕动的动力系统,推动食物通过消化道、进行机械性消化以及促进营养物质的吸收。
粘膜下层:提供营养和支持,还通过其神经和血管网络调节消化和分泌活动。
固有层:为上皮细胞提供结构支持,是免疫细胞聚集的防御前线,参与免疫防御、营养吸收和消化过程。
上皮:保护、分泌、吸收、免疫防御。
肠道支配神经元的命名法基于细胞体是位于胃肠道外部还是内部。肠道相关神经元通常归类为属于内源性肠道神经系统(ENS)。
相比之下,肠道外源性神经元包括体感神经元和自主神经神经元,其细胞体位于外周感觉或自主神经节、脊髓或脑干中。
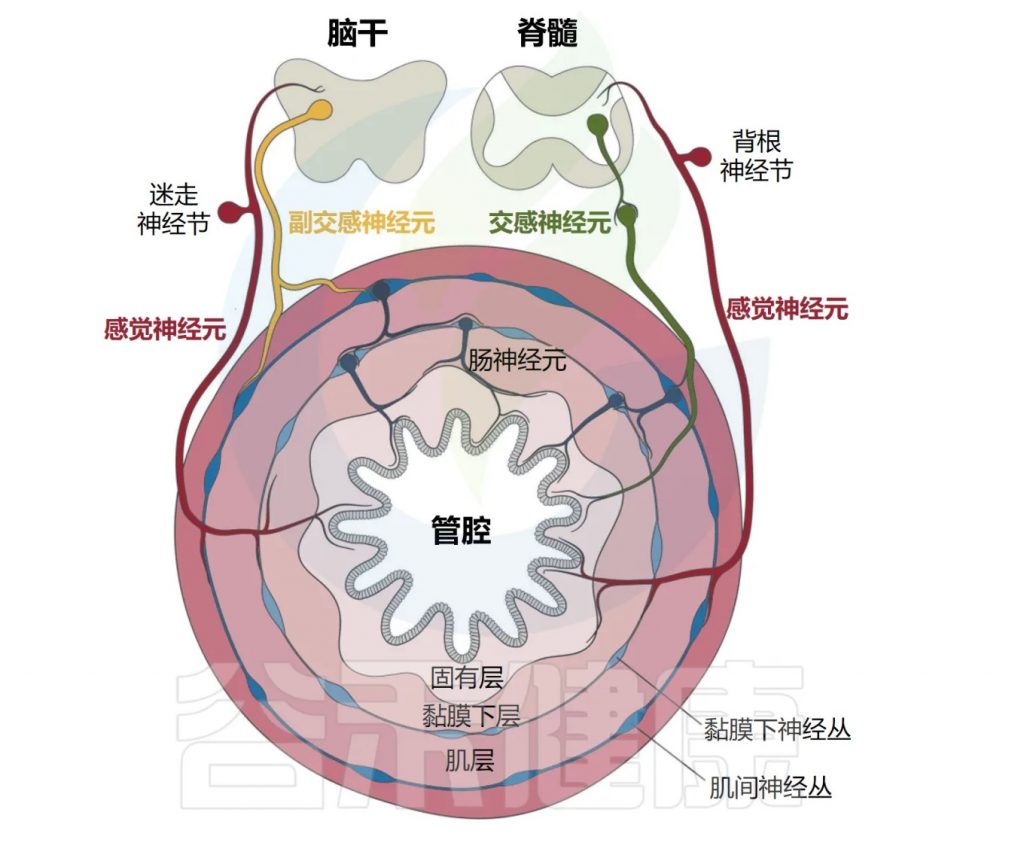
Yang et al. Cell Mol Immunol, 2023.
肠道外源性感觉神经元位于结节/颈静脉迷走神经节(VG)和背根神经节(DRG)中,分别将信号从肠道传递到脑干和脊髓。
自主神经神经元也支配肠道,包括迷走神经传出副交感神经运动神经元和位于自主神经节中的交感神经元。
肠道还拥有自己的内在和自主神经系统,由肠道神经元组成,它们的细胞体位于肌间神经丛和粘膜下神经丛中(如下图)。
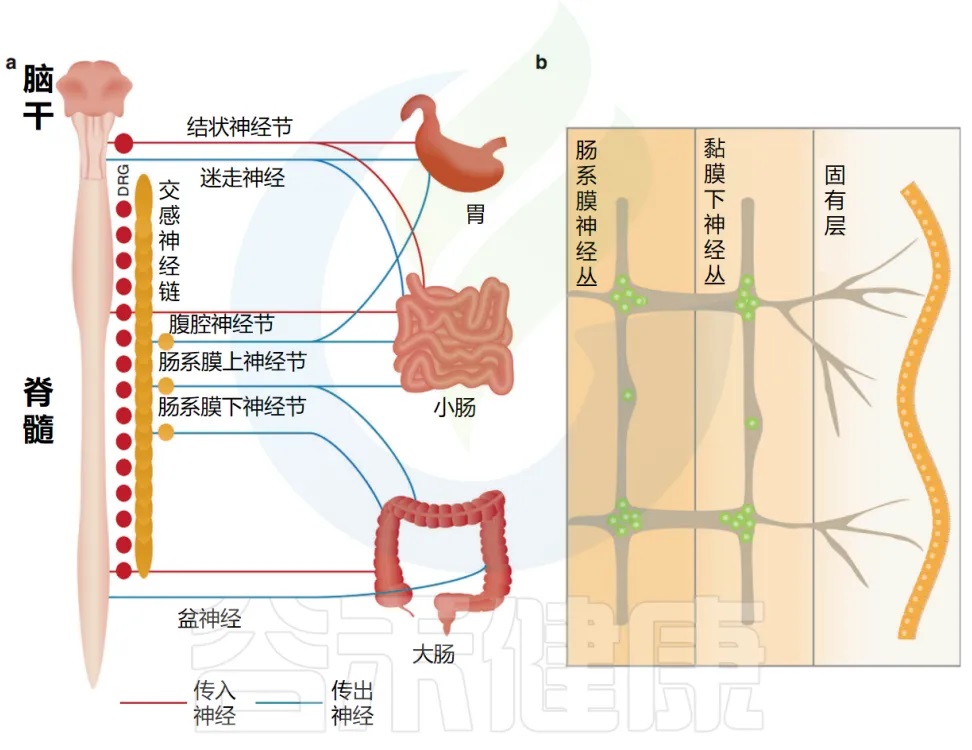
doi.org/10.1038/s41385-020-00368-1
交感神经 vs 副交感神经:肠道的刹车和油门
交感神经元和副交感自主神经神经元分别起源于脊髓和脑干,并介导从大脑到肠道的信号转导。
神经支配的地理分布
迷走神经副交感神经元沿前尾方向支配胃肠道,胃的神经支配密度最高,小肠和结肠的神经支配密度降低。
这种分布差异与不同肠段的消化功能需求相关:胃的高密度神经支配支持其机械研磨与酸性环境调控,而结肠的低密度则反映其以水分吸收和粪便塑形为主的生理特性。
交感神经元和副交感神经元都与肌间神经丛中的 ENS 形成连接,形成错综复杂的局部神经回路。
神经元——两根触手
它们能感知什么?
这些感觉神经元群检测营养物质、机械拉伸、管腔威胁和免疫刺激,包括细胞因子。
除了感知,还会“说话”
这些神经元还通过从周围神经末梢释放神经肽在肠道内发出信号(神经肽就像”化学信号”,用来和周围的细胞交流。)。迷走神经节神经元主要支配近端小肠,而 DRG 神经元支配整个胃肠道。
肠道神经网络的双层架构
肠道神经元完全驻留在胃肠道内,并组织成环绕肠管的神经节网络,并在空间上分为两层:肌间神经丛,位于圆形和纵向肌肉层之间,以及粘膜下层的粘膜下神经丛。
这两个神经丛通过中间神经元、运动神经元和肠神经胶质细胞紧密相连。它们一起形成介导蠕动和分泌功能的反射回路。
此外,它们还整合来自外源性感觉、副交感神经和交感神经神经元的信号,以介导肠道生理学。
肠道神经和免疫的共同语言
神经系统和免疫系统已经进化出一种共同的语言,在它们对环境损伤的每一步反应中进行交流,从起始到解决。
神经系统和免疫系统:互相听懂语言
微生物:神经-免疫对话的调节员
神经系统与免疫系统之间的交流机制从进化角度来看是有道理的,因为这种机制减少了应对某些损伤的代价,并使两个系统能够协调复杂的宿主反应。微生物组在调节神经元激活和免疫发育中也起着关键作用。
鉴于免疫细胞和神经元都可以直接或间接感知微生物,微生物组的组成在神经元分化或成熟中起着关键作用,以调节内脏疼痛、肠道蠕动和肠道生理的其他方面。
中枢神经系统的调节
短链脂肪酸它如何发挥作用?
尽管生物屏障严重限制微生物进入 CNS,但是某些肠道微生物代谢物,如短链脂肪酸(SCFA),可以穿过血脑屏障并起神经调节剂的作用。例如,乙酸盐优先被下丘脑吸收,下丘脑是参与食欲控制的大脑中枢,直接抑制摄食行为 。
尽管 SCFA 受体在大脑中通常以低水平表达,但这些纤维发酵产物可以通过抑制组蛋白脱乙酰酶来调节神经元基因表达。
4-乙基苯基硫酸盐,参与情绪处理的大脑区域
除了 SCFAs,最近有报道称微生物代谢物 4-乙基苯基硫酸盐可以改变参与情绪处理的大脑区域,例如海马体和杏仁核,并诱导小鼠的焦虑样行为。由于无菌动物在基线时表现出异常的大脑化学和结构,这些改变发生的时间已成为一个关键的研究重点。目前越来越多的工作揭示了母婴肠道微生物组对早期神经发育结果的影响。
免疫细胞的调节
在皮肤、肺和肠道等屏障组织中,免疫细胞和神经纤维紧密相邻,它们经常互相聊天,交换神经免疫调节分子来保护身体健康。
为什么要这样合作?
这种神经免疫轴在面对感染、过敏原或毒素时尤为重要,因为这些情况需要快速的组织保护反应,然后进行行为适应以避免未来再次遭遇。
具体怎么合作?
– 食物过敏的例子:
通过食物过敏的动物模型,两项最近的研究发现,肠道里的肥大细胞发现过敏原,它们向大脑发送特定信息,大脑记住这种食物,下次就会产生回避行为。
– 皮肤过敏的例子:
皮肤中的γδ T细胞受到微生物调节,它们能调节感觉神经元的活动,控制过敏反应的强度。肠道黏膜γδ T细胞是否参与神经元信号传递仍有待确定。
免疫细胞的远程通讯:如何向大脑发送消息?
免疫细胞不只是在局部工作。它们还有两种方式向大脑汇报:
方式一:血液快递
免疫细胞把细胞因子释放到血液中,就像发快递一样,把信息送到大脑。
方式二:亲自出差
肠道中某些免疫细胞,例如IgA+浆细胞(专门产生抗体)和自然杀伤细胞(专门杀死异常细胞),也能搬家到大脑或脑膜,从而在中枢神经系统中发挥作用。
肠道细菌的重要作用
这些细胞的功能成熟很大程度上依赖于来自肠道的微生物信号。
– 实验证据:
无菌动物(没有肠道菌群的动物)大脑中的IgA+浆细胞和“激活”的自然杀伤细胞数量会减少。
大脑常驻免疫细胞也会受到肠道细菌的影响
例如小胶质细胞和T细胞,也会受到来自肠道菌群的信号影响。 在这方面,细胞因子IL-17,特别是来自脑膜γδ T细胞的IL-17,作为肠道菌群和行为之间潜在的联系受到了广泛关注。
神经内分泌细胞的调节
下丘脑:身体的应激总指挥
下丘脑也是通过下丘脑-垂体-肾上腺(HPA)轴调节身体应激反应的关键指挥者。这个主要的神经内分泌系统包含几个严格调控的激素级联反应(就像接力赛一样,一个传一个),促进器官间的稳态。
肠道细菌影响压力反应
无菌动物具有夸大的HPA反应,并伴有应激诱导的糖皮质激素水平升高。
早期接触共生微生物对HPA轴的正常调节非常重要。简单说,婴儿期的肠道细菌会影响我们一生应对压力的能力。
肠内分泌细胞:肠道里的激素工厂
肠道也包含其自身的神经内分泌细胞群,称为肠内分泌细胞 (EECs):
这些激素调节消化、葡萄糖稳态、食欲。虽然主要在营养感知的背景下进行研究,但 EECs 越来越被认为是肠道菌群的关键传感器和肠-脑信号传导的介质。
肠道激素:连接肠道与大脑的信使
肠道菌群会影响多种循环激素的分泌:
这些激素作用范围很广
这些激素中的大多数在胃肠道神经纤维、下丘脑和其他大脑区域都有靶点。
由于这些激素及其前体也由身体的各种神经元和非神经元细胞产生,因此了解 EEC 来源的信号对动物行为的具体贡献一直是一个重大挑战,近年来随着基因工具的进步,解决这一问题成为可能。
外周神经元的调节
第四条高速路:外周神经系统的闪电传输
肠道微生物与大脑之间的第四个联系是外周神经系统 (PNS),特别是自主神经系统 (ANS),它具有副交感神经和交感神经两个分支。
神经传输有什么特点?
与前面提到的激素传输或细胞迁移不同,神经系统传输信息超级快:
肠道的双重神经网络:外在 vs 内在
– 外在
作为一种内脏器官,胃肠道由“外在”传入和传出神经纤维支配,其细胞体位于大脑或脊髓区域,分别介导肠道到大脑和大脑到肠道的信号传递 。
– 内在
“内在”肠神经系统 (ENS) 的神经纤维也分布在胃肠道中,其细胞体位于肠壁外层。它们在很大程度上自主地执行基本的肠道功能,并接收来自微生物组和中枢神经系统的输入。
迷走神经:肠脑对话的专线电话
迷走神经作为副交感神经系统的主要分支,尤其与肠-脑通讯密切相关,具有传入和传出神经纤维。它在维持肠道稳态以及调节情绪、食欲和能量平衡方面发挥重要作用。
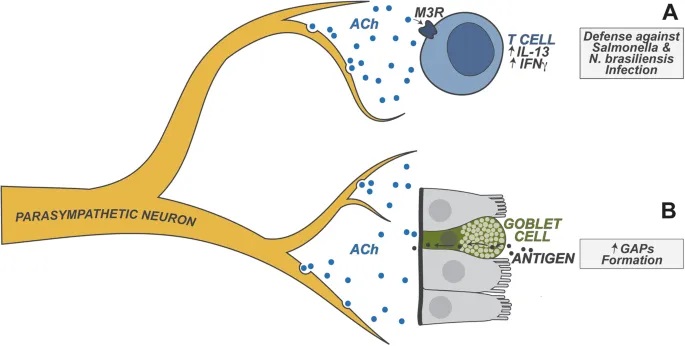
doi.org/10.1038/s41423-023-01054-5
实验证据
在迷走神经切断动物(即接受了迷走神经切断术的动物)中,肠道菌群的许多效应都会消失。然而,微生物信号是否能直接调节体内迷走神经的活动,目前证据仍然有限。
脊髓传入神经:疼痛信号的传递者
脊髓传入神经通过脊髓将感觉信息从肠道分别传递到大脑。我们对微生物组通过脊髓神经发出信号的许多了解都与内脏疼痛有关,因为许多这些纤维都是疼痛感应的。无菌动物表现出对结直肠扩张的超敏反应,而益生菌治疗可以缓解这种反应。共生微生物是否通过脊髓通路影响大脑生理或行为,目前仍不清楚。
交感神经系统:应激反应的调节者
交感神经系统调节多种胃肠道功能,尤其是在应对急性应激时。无菌小鼠的交感神经活动长期升高,这与这些动物体内HPA轴反应的增强相呼应。有趣的是,微生物群对交感神经活动的调节依赖于迷走神经传入纤维的信号,突显了周围神经系统相互关联的性质。
肠道神经元:免疫系统的调度员
肠道神经元是异质性的,能释放两大类物质来调节免疫功能:
– 细胞因子:
IL-18:调节抗菌肽的杯状细胞表达,抗菌肽介导宿主对肠道鼠伤寒沙门氏菌感染的保护
IL-6:抑制结肠中 RORγ+ 调节性T细胞的分化
– 神经肽:
NMU(神经调节素U)
CGRP(降钙素基因相关肽)
VIP(血管活性肠肽)
神经元与先天淋巴细胞的密切合作
肠道神经元还协调肠道先天淋巴细胞 (ILC) 的功能方面也起着重要作用。ILC 是协调下游适应性免疫的早期反应先天淋巴细胞。
– 空间优势
肠道神经元靠近 ILC,为这些神经元调节 ILC 功能奠定了细胞基础。
– ILC2的调节:过敏反应控制
ILC2 高度表达 NMUR1,NMUR1 是神经肽神经中介U(NMU)的受体。肠道感觉神经元的一个亚群表达 NMU,NMU 在过敏情况下释放。
– ILC3的调节:昼夜节律与宿主防御
肠道神经元在调节肠固有层 3 型 ILC (ILC3) 的功能中也起着关键作用。ILC3 表达高水平的 VIPR2,VIPR2 是神经肽 VIP 的受体。
肠道神经元的一个子集(以及迷走神经感觉神经元)表达高水平的 VIP,并且已发现它们在稳态和宿主防御期间调节 ILC3 功能。
– 具体调节过程
进食触发:食物消耗以昼夜节律方式触发VIP的神经元产生;
抑制作用:VIP抑制ILC3介导的IL-22产生,消除抗菌肽的肠道表达;
实验验证:VIP+神经元的化学激活导致IL-22+ ILC3比例降低,使宿主易受口腔啮齿柠檬酸杆菌感染。
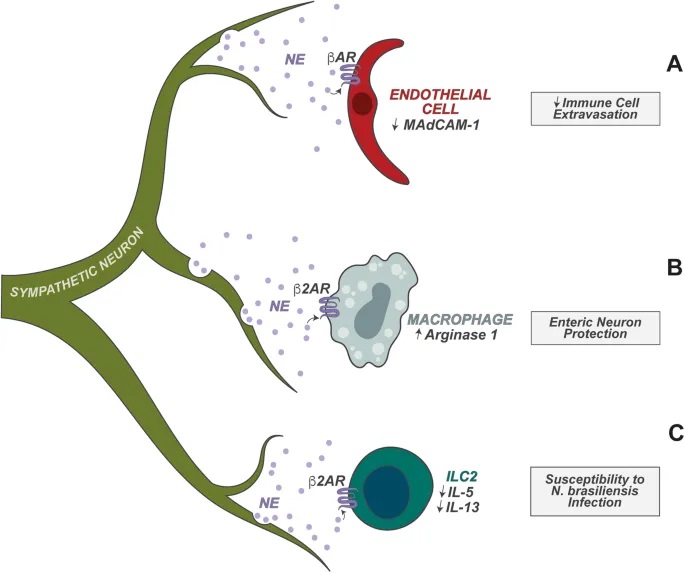
doi.org/10.1038/s41423-023-01054-5
肠道上皮每天都要面对来自食物和肠道菌群的各种化学物质。有时,有害刺激物和病原体会进入胃肠道,需要迅速采取损害控制措施。
为了理解管腔环境并区分“好”和“坏”,EEC(肠内分泌细胞) 和周围神经共同形成了一个广泛的肠道感觉网络。
信息处理:局部处理 vs 上报大脑
这些感觉信息有两种处理方式:
同时,大脑也会向肠道发送指令,引起特定的器官间反馈反应。
肠道神经上皮界面的肠道微生物群到大脑通路
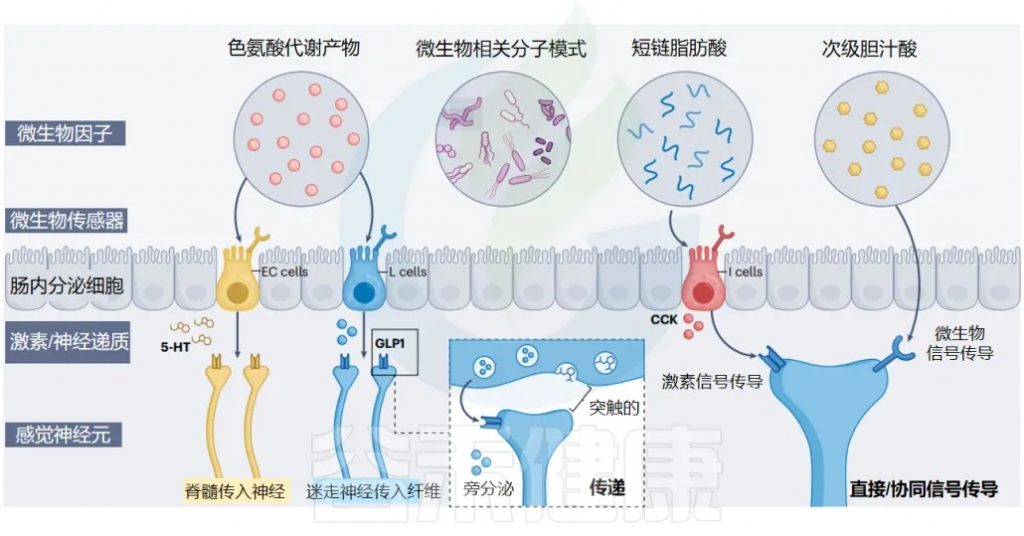
Ohara et al. 2025. Nat Rev Microbiol
肠内分泌细胞:肠道的化学传感器
肠内分泌细胞 (EECs) 是肠道的主要化学感应上皮细胞,通常根据其主要激素产物进行分类。产生 CCK、GLP1/PYY 和 5-HT 的 EEC 分别称为 I 细胞、L 细胞、肠嗜铬细胞(EC)。
在 EEC 家族中,这三个亚群最密切地参与肠-脑通讯:
EECs的灵活性
一些 EEC 在其生命周期中分泌多种不同的激素或经历激素转换,这表明 EEC 亚型并非完全固定。
重要的是,微生物组感应受体在远端肠道的 L 细胞和 EC 细胞中富集,这个区域正好是细菌载量最高的地方,并且主要被认为发生微生物-EEC 信号传导。
简单说,细菌最多的地方,正好是感应细菌信号的传感器最多的地方。
微生物相关分子模式 (MAMP)
MAMP
微生物相关分子模式(MAMP)就想是细菌身上的身份标识牌,是微生物上进化上保守的结构,就像每个细菌都带着固定的身份证。宿主细胞可以通过模式识别受体来读取这些身份信息,特别是先天免疫细胞,它们是识别细菌身份的专家。
Toll样受体
在模式识别受体中,Toll 样受体(TLR)在维持肠上皮细胞稳态中起着至关重要的作用。
肠内分泌细胞表达不同的TLR
体外和体内研究表明,肠内分泌细胞 (EECs) 表达几种不同的功能性 TLR,包括:
TLR信号如何影响激素分泌?
肠道中的 TLR 信号传导与 CCK(胆囊收缩素)、GLP1(胰高血糖素样肽1) 、5-HT(血清素)分泌的调节有关,但这仍有待进一步验证。
TLR4 也在感觉传入神经元中表达,但其与微生物组感应的相关性尚不清楚。
短链脂肪酸(SCFA)
短链脂肪酸(SCFA)是膳食纤维发酵的最终产物,由厌氧菌在结肠中大量产生。
特定的支链短链脂肪酸,如异戊酸盐和异丁酸盐,由肠道细菌通过支链氨基酸发酵制成。特征最明显的 SCFA 受体是游离脂肪酸受体2 (FFAR2)和 FFAR3,它们都在多个 EEC 亚群中表达,说明很多肠内分泌细胞都能听到SCFA的信号。
FFAR受体:如何传递SCFA信号?
FFAR 是一种 G 蛋白偶联受体,当被激活时,它与几个下游信号级联反应相连,就像按下按钮后,触发一连串的反应。
– 对L细胞的影响
SCFA 与 L 细胞上的 FFAR2 和 FFAR3 结合会触发细胞内钙动员(也就是钙离子在细胞内快速移动)以及 GLP1 和 PYY 的释放。
EC细胞:用嗅觉受体来感应SCFA
在结肠中,EC 细胞也通过 FFAR 以及嗅觉 G 蛋白偶联受体 OLFR78 和 OLFR558(refs)受到 SCFA 的调节。
不同种类的SCFA有不同的分工
尽管FFAR3在 I 细胞中广泛表达,但尚不清楚 SCFA 是否调节CCK的产生。FFAR2 和 FFAR3 在肠道支配感觉神经元中也有功能表达,表明传入神经纤维可能直接对SCFA做出反应。
次级胆汁酸
次级胆汁酸是肠道微生物群产生并被宿主识别的另一类重要代谢物。最初是肝脏产生的初级胆汁酸,这些初级胆汁酸到达远端肠道后,被肠道细菌进行”二次加工“,变成了次级胆汁酸。
简单说,这是肝脏和肠道细菌合作的产物。
主要的次级胆汁酸:两大明星分子
脱氧胆酸(DCA)和石胆酸是两种含量最丰富的次级胆汁酸,能够通过多种宿主受体发出信号,特别是 TGR5(也称为 G 蛋白偶联胆汁酸受体 1)和法尼醇 X 受体。两种受体都在 L 细胞中表达,并参与 GLP1 和 PYY 释放的调节,这就解释了为什么肠道细菌的变化会影响我们的血糖控制和食欲调节。
对EC细胞的影响:调节血清素产生
次级胆汁酸还向 EC 细胞发出信号,通过 TGR5 和可能通过 Tph1 的下游转录指导 5-HT 的产生,Tph1 编码 5-HT 生物合成的限速酶。
目前尚不清楚次级胆汁酸是否作用于 I 细胞,但这些胆汁酸的一部分可以通过肠肝循环到达近端肠道,并且表达 CCK A 型受体的迷走神经传入神经亚群以 TGR5 依赖性方式对 DCA 有反应。
色氨酸和吲哚衍生物
色氨酸是一种从膳食蛋白质中获得的必需氨基酸,人体无法自己制造,其分解产物代表了另一类有助于宿主健康的微生物代谢物。
吲哚途径:细菌的化学加工厂
在色氨酸降解的三个主要途径中,吲哚途径由肠道中的许多细菌物种进行,将色氨酸转化为吲哚及其衍生物,如吲哚-3-乙酸(IAA)和吲哚-3-醛。
吲哚类物质如何影响EECs?
吲哚是 L 细胞中 GLP1 分泌的已知诱导剂。也就是说,吲哚能够刺激L细胞释放GLP1。
在斑马鱼中,吲哚和吲哚-3-醛强烈激活 EEC 并通过瞬时受体电位锚蛋白 1 通道触发 5-HT 释放。
瞬时受体电位锚蛋白1:多功能的感应通道
瞬时受体电位锚蛋白 1 不仅能感应吲哚类物质,还有其他身份,它也是环境刺激物的传感器,比如能感应芥末油(这就解释了为什么吃芥末会有刺激感)。
瞬时受体电位锚蛋白 1 在哺乳动物EC细胞和感觉神经元中高度表达,可能是促进胃肠道蠕动和清除摄入毒素的机制。
在检测到微生物群衍生因子后,肠道感觉网络将此信息传递给CNS。这种传输究竟是如何发生的,特别是在脑-身体通信的背景下,是目前积极研究的一个领域。
新兴的经典肠道神经上皮通路涉及:
肠道感觉网络
肠内分泌细胞(EEC)和肠道支配感觉神经元在肠粘膜屏障处共同形成一个复杂的感觉网络,能够感知和响应各种微生物结构和代谢物。这些包括色氨酸代谢物、微生物相关分子模式、短链脂肪酸和次级胆汁酸。
结肠中的两大主力
在结肠中,有两类重要的EEC:
这两类细胞都表达这些微生物信号的受体,能够直接听到细菌的声音。
I细胞主要位于小肠中,生产胆囊收缩素(CCK),同样表达微生物传感器。
信号传递的两种方式
当EEC被激活时,它们会通过两种方式释放信号分子:
EEC会释放:
传递给:
不仅影响EEC,还直接影响神经
微生物输入还可以直接调节感觉神经纤维的敏感性,从而增强 EEC-神经荷尔蒙信号传导。
不同信号走不同高速路
根据所涉及的微生物传感器、EEC 亚群、神经肽和感觉神经元类型,不同的微生物线索可以通过不同的肠道神经上皮途径输送,最终对大脑功能和行为产生不同的影响。
感觉细胞多样性
肠道里的神经元是怎么工作的?
肠道中有两大类感觉传入神经负责不同的监测任务:
最近对迷走神经和脊髓神经元的分析发现了多种感觉神经元细胞类型,甚至在化学感受器和机械感受器中也是如此。
为什么需要这么多不同类型的神经元?
结合遗传的研究方法,得出一个研究的共识,即单个感觉神经元之间存在很大的分工。每种神经元都有自己的专业领域,就像专科医生一样。
这些神经元到底分工有多细?
一些具体的例子:
复杂分工的深层原因:系统的精密设计
这种刺激特异性神经元反应可能反映了肠道神经上皮水平信息感知和传递方式的复杂性,部分原因是 EEC 和感觉神经元群的异质性。这种精密的设计确保了肠道能够准确识别和传递各种不同的信号。
未来:寻找微生物组专属神经元
这些观察结果提出了一个有趣的问题,即是否有专门的“微生物组响应”感觉神经元来支配肠道,以及是否存在基于微生物刺激的亚型。
当然,GPR65 + 迷走神经神经元是不错的候选者,因为它们是在整个胃肠道中具有致密粘膜神经末梢的化学感受器。
然而,随着迷走神经支配沿结肠长度向远端减少,脊神经可能同样有助于将微生物线索传递给 CNS。
旁分泌传递与突触传递
传统方式:EEC的广播信号传递
当EEC受到刺激后,它们会采用最常见的信号传递方式:
这通常被认为以旁分泌方式发生——即最接近 EEC 范围,只要表达相关受体的纤维,就能接收信号并传播给大脑,也就是“近水楼台先得月”。
新发现:EEC的专线连接方式
科学家们发现了一种更直接的连接方式!研究发现了一种独特的 I 细胞和 L 细胞亚群,被称为”神经足”细胞。
– 什么是”神经足”细胞?
更多证据:EC细胞也有类似的专线
对于 EC 细胞和脊髓传入纤维提出了类似类型的连接。支持这种突触连接的证据:
然而,最近的高分辨率成像研究尚未发现令人信服的证据证明 EEC 和传入神经之间存在突触接触,这表明神经足细胞要么非常罕见,要么仅存在于某些 EEC 亚型中。另一种解释是,考虑到大多数 EEC 的寿命较短,EEC-神经突触是高度动态的。
了解 EEC 的特定子集是否可以直接进入大脑很有价值,因为它们将是影响与肠道微生物群相关的情绪和行为变化的候选者。
协作微生物-宿主信号传导
到目前为止,我们已经将肠道神经上皮回路描述为一条线性通路,信号在到达 CNS 之前从肠道微生物群传递到 EEC,再传递到内脏传入神经。
微生物群 → EEC → 内脏传入神经 → 中枢神经系统
新发现:微生物的捷径通道
一些微生物因子,包括 SCFA、次级胆汁酸、蛋白酶,可以绕过上皮层,并直接作用于感觉传入神经。
协同作用:1+1>2的效果
感觉神经纤维如何整合微生物和宿主来源线索的细节开始浮出水面。
– 例子1:DCA + CCK的强强联合
注:它是一种次级胆汁酸,由肠道菌群代谢初级胆汁酸而产生。
– 例子2:丙酸盐增强CCK效果
这些发现表明,微生物代谢物可以与肠道激素合作以影响感觉神经放电。
复杂的生物网络系统
鉴于最近对免疫细胞在协调脑-身体回路和肠胶质细胞在塑造肠道神经活动中的作用的见解,微生物群-神经上皮相互作用可能涉及多个细胞输入的影响,这个系统作为更大的互连生物系统网络的一部分,远比简单的线性通路复杂。
简单说,肠脑通讯不是一条高速公路,而是一个复杂的交通网络,有多条道路、多个路口,各种车辆(不同的信号分子和细胞)在其中协调运行。
肠道感觉网络收集的有关微生物组的信息,在组织本身、脑干和脊髓以及高级大脑区域内进行整合和处理。
大脑处理完信息后会做什么?
中枢神经系统的效应肢体会积极响应,主要包括:
它们的任务是对动态变化的肠道环境做出反应,调节胃肠道生理学的各个方面。
近年来,宿主通过局部和远程信号传导机制对肠道微生物群的定向作用受到了相当大的关注。
肠神经上皮界面的脑到肠道微生物群通路
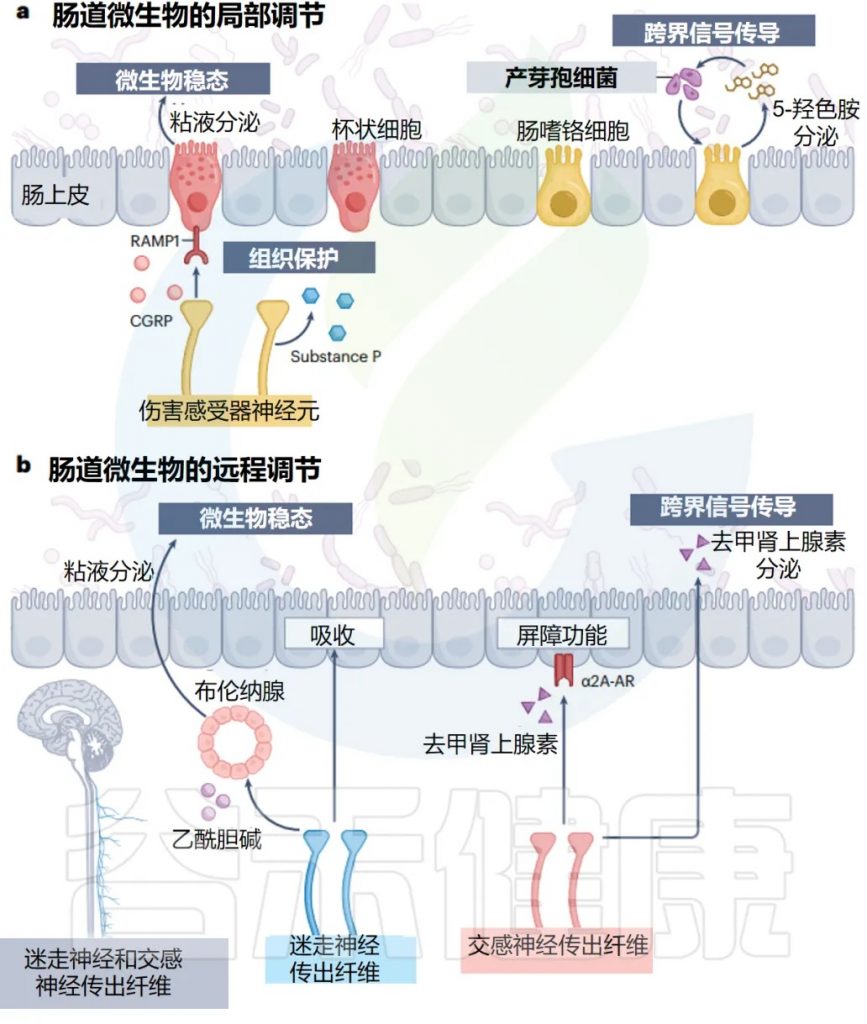
doi.org/10.1038/s41579-024-01136-9
局 部 调 控
传统认知:感觉神经只负责”上报”信息
传统上,感觉神经是将信息传递到 CNS 的传入纤维,就像信息传递员一样,只负责把肠道的情况报告给大脑。
新发现:感觉神经还有”管理”功能
现在人们普遍认识到,感觉神经元还通过在屏障组织局部释放各种神经肽和神经递质来执行传出功能。
– 管理方式:
通过作用于附近的免疫和非免疫细胞,感觉传入神经是维持组织健康不可或缺的一部分。
肠道中的疼痛神经:伤害感受器
在肠道中,许多具有局部效应功能的感觉神经元是伤害感受器,它们通常在皮肤中介导疼痛感。
– 伤害感受器:微生物管家
尽管它们的确切特征和功能正在阐明,但最近的两项互补研究发现,伤害感受器在调节肠道微生物稳态方面具有新作用。
– 实验证据:
在没有功能性伤害感受器的情况下,小鼠以微生物组依赖性方式更容易患结肠炎。
伤害感受器的保护机制:释放保护性分子
伤害感受器通过释放 P 物质和降钙素基因相关肽来促进组织保护,这些肽向邻近的肠道杯状细胞发出信号以驱动粘液分泌。
有趣的是,伤害感受器释放的 P 物质和降钙素基因相关肽受共生信号调节。因此,感觉神经元同时监测和调整肠道菌群的组成以支持肠道稳态。
EC细胞与5-HT的调节系统
一个显著的例子是 EC 细胞,它在压力、机械压力和迷走神经刺激下将 5-HT 释放到肠腔中。
– 微生物的影响:
微生物的策略:操控宿主为自己服务
因此,孢子形成细菌识别肠腔中的 5-HT,并通过结肠中的 EC 细胞进一步诱导宿主 5-HT 的产生,来促进自身在微生物组中的成员身份。
这种微生物群-EEC 串扰是孢子形成者独有的,还是其他细菌物种参与界间信号传导仍有待确定。
远 端 调 节
宿主调节微生物的双重策略:局部 vs 远程
宿主有两套不同的调节策略:
策略1:局部信号调节——就地解决问题
策略2:远程肠脑回路调节——统筹全局管理
ANS 的两个主要分支——迷走神经和交感神经,通过它们在胃肠道中的不同功能输出,来协调这种反馈反应。
迷走神经:身体休息和消化时的管家
虽然大多数迷走神经纤维将感觉信息传递到大脑,但有些也向肠道提供副交感神经流出,主要支配 ENS 并促进肠道蠕动和上皮分泌物,作为身体“休息和消化”反应的一部分。
最近的证据表明,迷走神经传出纤维在通过近端小肠 Brunner 腺调节肠道微生物群方面,具有惊人的作用。
– 对特定微生物的影响:
乳酸菌属对这种神经腺回路的扰动特别敏感,在迷走神经刺激时扩大,并在参与压力信号时丰度降低。
迷走神经传出神经元的活动,也极大地影响了肠上皮的吸收能力,可能会改变饮食-微生物群动力学和微生物代谢物对宿主的获取。
交感神经:压力状态下的应急管理员
– 交感神经的基本功能
交感神经为肠道提供肾上腺素能神经纤维,在那里它们支配 ENS 和肠粘膜,并释放去甲肾上腺素,尤其是在应对压力时。
– 对微生物群的具体影响
交感神经激活导致粘蛋白降解剂(如Akkermansia)增多,Turicibacter spp137 减少。
这些微生物组的变化伴随着粘液产生、抗菌基因表达和上皮周转率的变化,揭示了交感神经、上皮细胞和肠道细菌之间的密切关系。
交感神经的化学武器:去甲肾上腺素的直接作用
– 直接的化学信号传递
交感传出神经元影响微生物组的另一种机制是,通过将去甲肾上腺素释放到肠腔中。
– 跨界信号传导的例子
QseC 组氨酸激酶对宿主来源的儿茶酚胺(如肾上腺素和去甲肾上腺素)的细菌感应,是王国间信号传导的另一个例子。
– 对病原菌的影响
在某些大肠杆菌菌株中,儿茶酚胺可以改变毒力基因表达和致病性。有趣的是,肠腔中游离儿茶酚胺的水平部分受肠道微生物群的调节。
这可能具有临床意义,因为 GLP1 受体激动剂利拉鲁肽是一种常见的抗糖尿病药物,被发现可以激活交感神经传出纤维,触发去甲肾上腺素释放到肠腔中,并诱导大肠杆菌的扩增 。
总的来说,这些研究表明,交感神经可以直接影响肠道细菌定植。
神经免疫学是一个快速发展的领域。最近在不同的神经元亚群如何调节肠道免疫反应方面的突破,加深了我们对生理和病理条件下肠道免疫的理解。
除了被动接受和应对有害的威胁外,免疫系统还向神经系统发出信号以启动防御性反应。同时,神经系统在对潜在威胁的预期和感知下,积极调节肠道中的免疫反应。神经系统和免疫系统之间的协调使宿主能够正确处理复杂的刺激和不断变化的环境。
肠道微生物群也是调节肠脑轴中神经元和免疫激活的关键臂。结合微生物组、转录组、蛋白质组的多组学研究,配合光遗传学和化学遗传学等新兴技术,将深化我们对神经元如何塑造肠道生态系统的理解。
肠道菌群检测技术的应用将成为连接基础研究与临床实践的重要桥梁。基于微生物组构成和神经反应模式的个体化治疗将成为现实,通过功能性微生物组分析,结合肠道菌群检测报告中的神经递质等相关指标,实现疾病风险预测和治疗效果的个性化评估。自迷走神经电刺激在减轻炎症方面的发现以来,生物电子医学在临床应用中展现出广阔前景,无创迷走神经刺激已在克罗恩病临床试验中显示疗效。
神经递质和神经肽受体信号传导的治疗靶向为药物创新提供了新思路。β-肾上腺素能受体拮抗剂和CGRP受体拮抗剂等现有药物,凭借其调节肠道免疫的能力,可重新用于胃肠道功能障碍治疗,同时基于微生物代谢物的新药开发和靶向EEC的小分子化合物研究正在兴起。
这些突破将更大地改变焦虑、抑郁、自闭症、帕金森病等神经疾病以及肠易激综合征、炎症性肠病等消化系统疾病的治疗策略。通过微生物疗法、肠道靶向神经调节和神经-免疫平衡调节的联合治疗,未来,临床医生可能会根据患者的肠道菌群特征、免疫状态和神经系统表型制定个性化治疗方案。
医学正从标准化治疗转向个体化精准医疗,肠道-菌群-免疫-神经将成为未来疾病治疗的重要方向。短链脂肪酸、色氨酸代谢物以及其他菌群代谢产物正被开发为新型神经调节剂,它们能通过血脑屏障或迷走神经途径影响中枢神经系统功能。
早期干预肠道菌群失调可能成为预防神经精神疾病的关键途径,特别是对具有遗传风险的人群。肠道健康将成为整体健康管理的重要组成部分。
主要参考文献
Jacobson, A., Yang, D., Vella, M. et al. The intestinal neuro-immune axis: crosstalk between neurons, immune cells, and microbes. Mucosal Immunol 14, 555–565 (2021).
Ohara, T.E., Hsiao, E.Y. Microbiota–neuroepithelial signalling across the gut–brain axis. Nat Rev Microbiol 23, 371–384 (2025).
Yang, D., Almanzar, N. & Chiu, I.M. The role of cellular and molecular neuroimmune crosstalk in gut immunity. Cell Mol Immunol 20, 1259–1269 (2023).