-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康
肥胖与许多疾病的风险增加有关,包括糖尿病、心血管疾病和癌症。越来越多的证据也表明肠道菌群失衡与疾病有关。通过调节肠道菌群或许能逆转或干预这些现象。
本期介绍两篇,分别以饮食控制和维生素给予为变量,同时都研究了基线时和干预后肠道菌群的变化。又是新的思路,新的挑战。
第一篇文章研究了基线肠道菌群在饮食控制的前提下是否能预测减肥轨迹?
答案是可以的,研究结论表示作为节食前个人体重减轻轨迹的预测指标,基线肠道微生物的作用超过了其他因素。
研究中对83名受试者(男47人,女36人,年龄20~45岁)进行了为期6个月的在营养师指导下的饮食干预计划。受试人群以以下标准排除:
(1)重大疾病;
(2)怀孕或哺乳;
(3)高血糖或低血糖;
(4)胃肠疾病;
(5)自身免疫性疾病;
(6)甲状腺疾病;
(7)在纳入前1个月内使用抗生素或激素;
(8)预计在研究过程中经常旅行。这也排除了服用上述条件下处方药物(如二甲双胍)的受试者。
按照中国人民解放军总医院营养科的医生设计的膳食计划,即碳水化合物含量为60%-65%,蛋白质含量为24%-26%,脂肪含量为12%-14%(能量百分比)。也包括400-500克蔬菜和100-200克低血糖指数水果,严格遵循饮食建议,卡路里控制在男性1200-1680千卡/天,女性1050-1470千卡/天。
如图,结合电子秤与智能手机应用程序,纵向收集饮食、体力活动、体重和粪便微生物组数据以及SNP基因型,然后整合成高维数据用于后续分析。对采集的粪便样本进行宏基因组鸟枪法测序,得到的序列数据进行物种注释及KEGG功能注释。
1. 饮食因素与体重变化之间的联系因个体不同而不同。
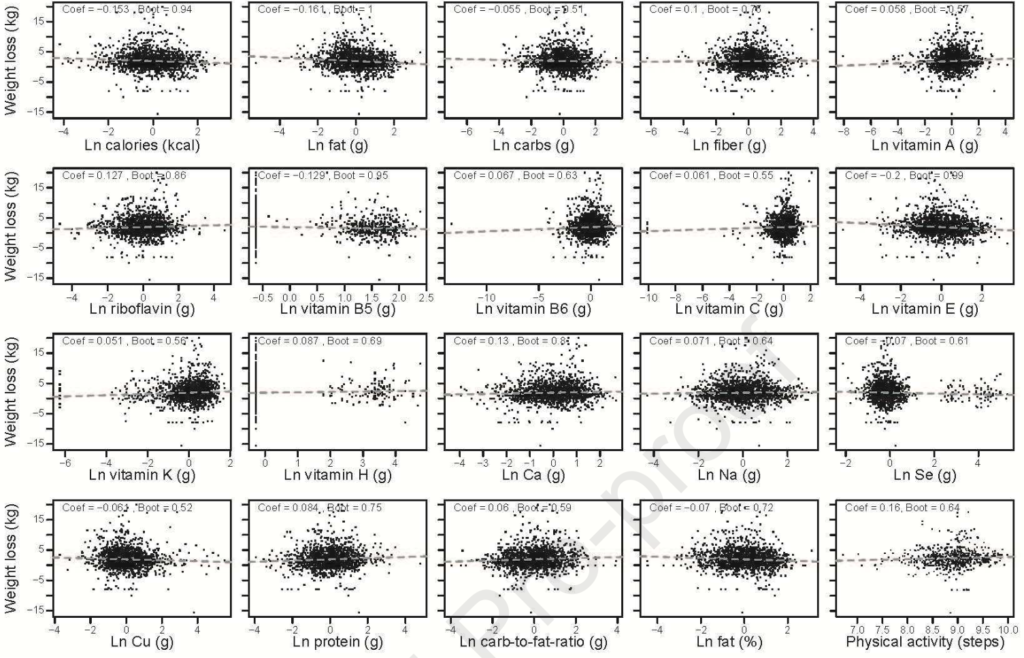
首先确定有哪些饮食因素与所有个体的体重下降有关。使用GLMMLASSO模型,结果如图,当coef为非零时被认为是显著的。发现,在所有受试者中,体重下降与卡路里摄入量(系数=-0.153)、膳食中大量营养素组成(脂肪,系数=-0.161;碳水化合物,系数=-0.055;蛋白质,系数=0.084;纤维,系数=0.1)、膳食微量营养素含量和体力活动之间的具有弱相关。
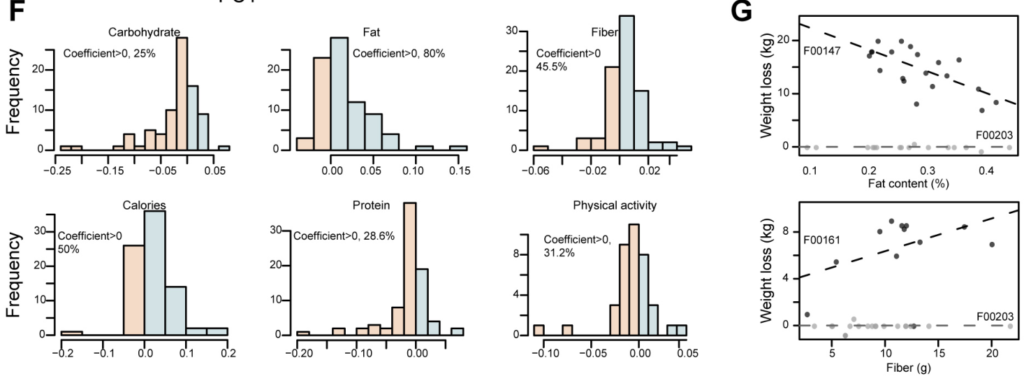
但是在个体间有很大差异。例如在受试者F00161中,纤维摄入量的增加与减肥之间存在正相关关系,而在F00147中,受试者的脂肪摄入量增加与体重减轻之间存在负相关关系。相反,尽管纤维或脂肪摄入量发生变化,F00203人仍然对体重变化不敏感(图G)。所以,即使是相似的膳食大量营养素,体重反应也是高度个性化的。蓝色,coef> 0;红色,coef< 0
2. 作为节食前减肥轨迹的预测指标,基线肠道菌群表现更好。
为了从饮食控制前的基线数据中建立预测体重下降的模型,开发了基于梯度增强回归的机器学习算法,并保留一个受试者进行交叉验证。为了识别除了饮食数据之外最相关的变量,这些模型分别在五组输入上进行了训练:
(1)膳食数据(包括卡路里摄入量、大量营养素组成、食物种类和饮食排序的前三个特征向量);
(2)膳食数据和肥胖相关SNPs;
(3)膳食数据和个人特征(年龄、性别和基线体重指数);
(4)膳食数据和基线肠道微生物群(包括细菌种类丰度和功能模块);
(5)膳食数据、个人特征、SNPs和基线肠道微生物群。

与不包含基线微生物群数据的模型相比,包含基线微生物群数据的模型的预测精度大大提高,而包括个人特征或肥胖相关的宿主基因组SNP对预测精度的贡献很小[(1)r=0.137;(2)r=0.073;(3)r=0.159;(4)r=0.523;(5)r=0.509]。因此,基线肠道菌群数据在预测6个月饮食控制计划期间体重变化方面优于其他因素(P <1e-14)。
之后,研究人员进行了更细致的模型训练,发现了对体重下降模型影响最大的几个物种:

在功能分析中,发现涉及赖氨酸生物合成(M00030)和多糖运输系统(M00216)的模块对预测模型的影响最大

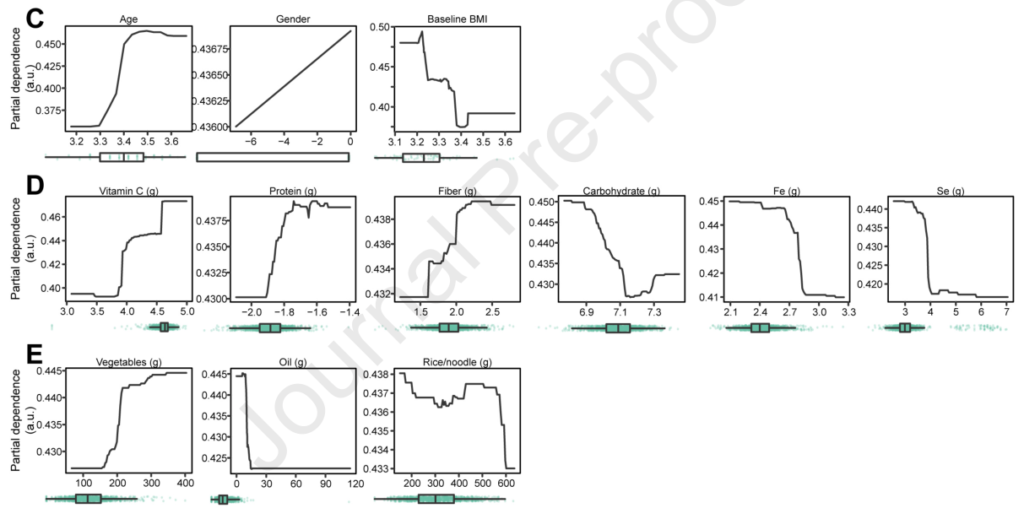
以及其他影响不那么显著的变量:年龄增加对模型产生积极影响,而基线BMI则相反;增加维生素C、蛋白质和纤维的摄入量对模型产生积极影响,而增加碳水化合物、铁和硒的摄入量则相反;剩下的几种维生素和矿物质、蔬菜、油、米和面条的摄入量以及与肥胖相关的6个SNP的基因型也对该模型产生了微弱的影响。以上这些变量都是重要的因素,可能有助于或阻止普通人群在长期节食期间的减肥轨迹。
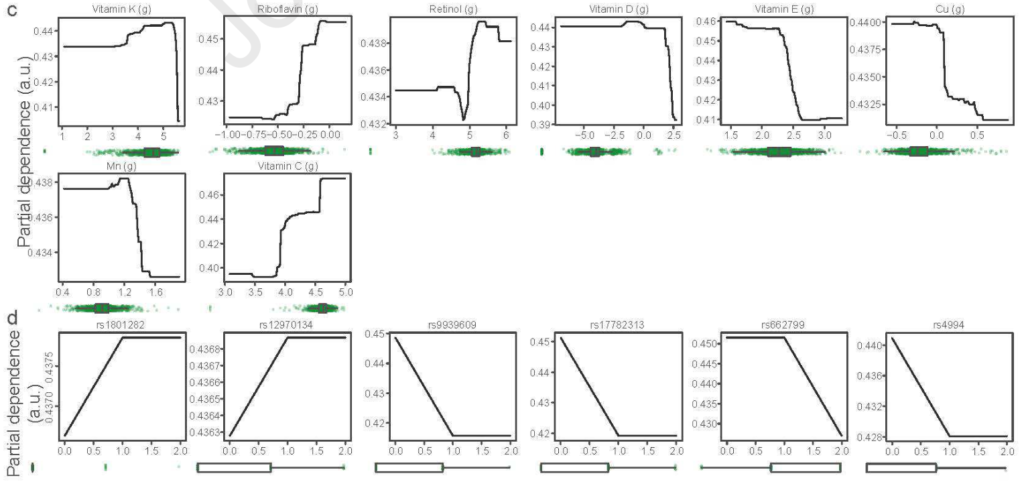
3. 饮食控制期间肠道菌群的组成变化是否会影响减肥轨迹。
研究发现许多参与者的肠道菌群组成发生了实质性的变化,0-3个月的微生物群的变化幅度与体重下降的程度呈正相关,有15个个体肠型被改变了,体重变化范围从20公斤到+7公斤。这两个时间段都是一致的。这一发现表明,在饮食控制计划中,饮食和肠道菌群之间存在着持续的相互作用。如图:
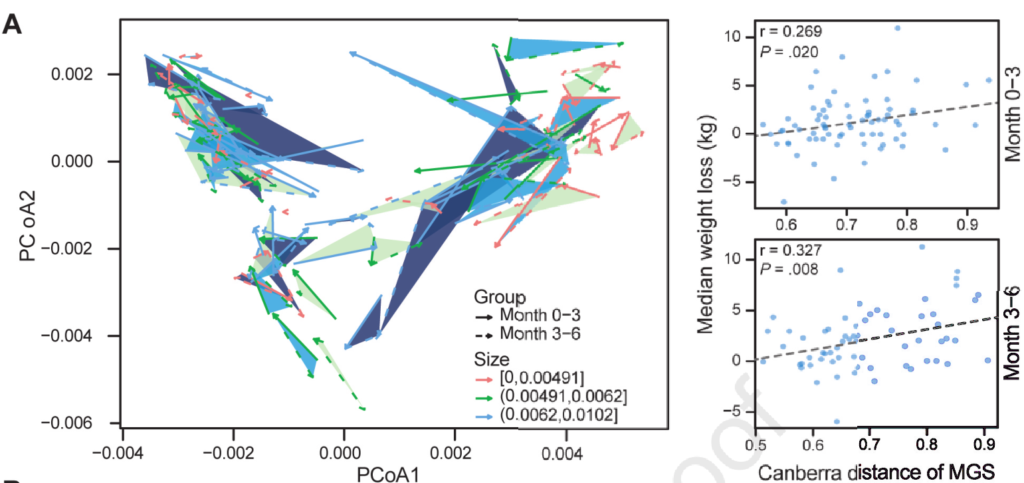
同时使用随机森林算法,基于相对于基线的种水平物种变化来预测体重下降,预测精度R=0.271,发现R. gnavus (MGS0160), Bacteroides massiliensis (MGS1424)和Bacteroides finegoldii (MGS0729)这三个物种在模型中贡献度最大。

继续统计了一些在肥胖个体中丰富或减少的物种和功能以及那些与体重变化共同变化的细菌种类。其中,粪球菌属Coprococcus sp. (MGS0232)、Holdemanellabiformis (MGS1464)、Solobacterium moorei (MGS0945)、活泼瘤胃球菌R. gnavus (MGS0160)和Clostridium (MGS0558) 在肥胖个体中显著富集,且它们的减少与体重下降显著相关;Coprobacter (MGS1138)、Bacteroides intestinalis (MGS0117和MGS1302)、阿克曼菌Akkermansia muciniphila (MGS0120)、Alistipes obesi (MGS0342)和坦纳菌属Tannerella sp. (MGS0276)在瘦人个体中显著富集,且其在饮食控制过程中的增加与体重下降显著相关;在瘦人个体中,编码脂肪酸生物合成(M00085)的基因在基线时显著富集,且其增加与体重减轻相关。如下图:
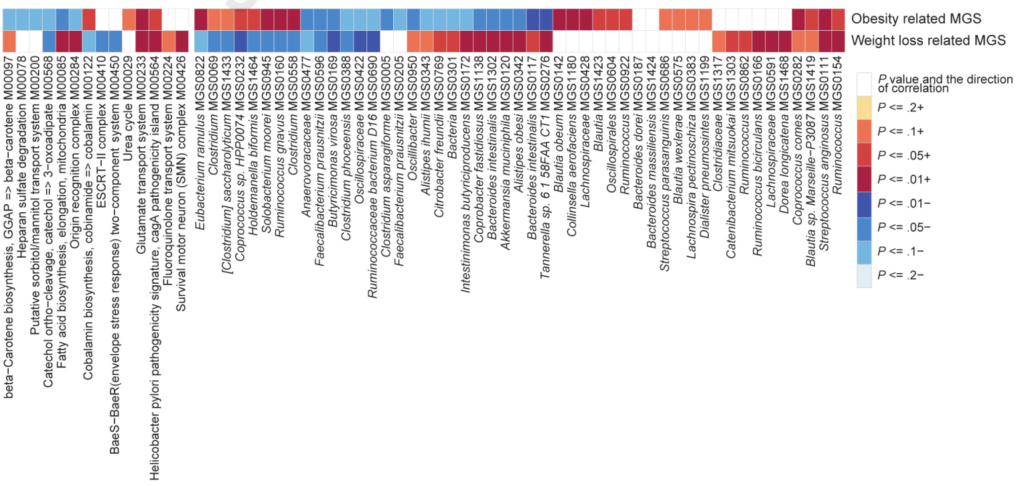
这些结果表明可以基于基线肠道菌群组成和饮食数据建立个性化的体重预测模型。我们可以利用肠道菌群的分布做个性化的饮食推荐,以此调节体重,进而促进宿主健康。文章中发现的R. gnavus (MGS0160)、B. massiliensis(MGS1424)和B. finegoldii (MGS0729)这三种物种与体重下降显著相关,它们的减少有利于体重下降。这可以记一下,要是有机会做肠道菌群检测,可以参考参考。
第二篇文章,主要研究对结肠靶向给维生素对人体肠道菌群的组成和代谢活性的影响。通过人类临床研究和体外的批量发酵实验,结合评估屏障和免疫功能的细胞模型,研究了结肠输送的维生素A、B2、C、D和E对肠道菌群的影响。大家都比较熟知益生元或一些益生元成分如低聚果糖(FOS)、低聚半乳糖(GOS)和菊粉对肠道的影响。
最近一篇使用高剂量维生素或结肠靶向配方的干预研究表示,维生素会影响肠道菌群。补充100 mg核黄素14d可以增加健康受试者每克粪便中丁酸产生菌(Faecalibacterium prausnitzii和Roseburia)的数量,并减少炎症性肠病(IBD)患者的肠杆菌科细菌数量。
一共96名健康志愿者参与了这项研究,其中12人分成6组不同的维生素组(维生素A、维生素B2、维生素C、维生素B2+C、维生素D3和维生素E),安慰剂组有24人参与。
排除标准如下:严重急性或慢性疾病;吸烟;怀孕;在过去3个月内使用抗生素;药物和/或酒精滥用史(每天2份以上);过去3个月的主要饮食变化;饮食障碍;素食或纯素食;灌肠;膳食补充剂,包括基线访问前4周内和干预期间的益生元、益生菌或富含纤维的补充剂;高纤维饮食(即>30克);治疗活动性胃肠道疾病的慢性药物(除非该产品在筛查前服用至少2个月,并在整个研究期间保持相同的剂量);最近排便习惯的改变(<3个月);以及腹痛。
所有受试者在为期4周的时间里每天服用维生素补充剂或安慰剂,一共三次数据采集:筛查,基线(筛查后1周),基线后4周。每次都采集空腹静脉血样本,填写问卷,并在基线时和干预4周后,从每个受试者身上收集两份粪便样本。用于获知粪便微生物组成、粪便短链脂肪酸水平、粪便氨含量、血浆和粪便维生素B2浓度、粪便氧化还原和pH值、生活质量和胃肠道症状问卷等信息。
对肠道菌群组成分析,比较了结肠注射维生素干预前后的多样性指数。
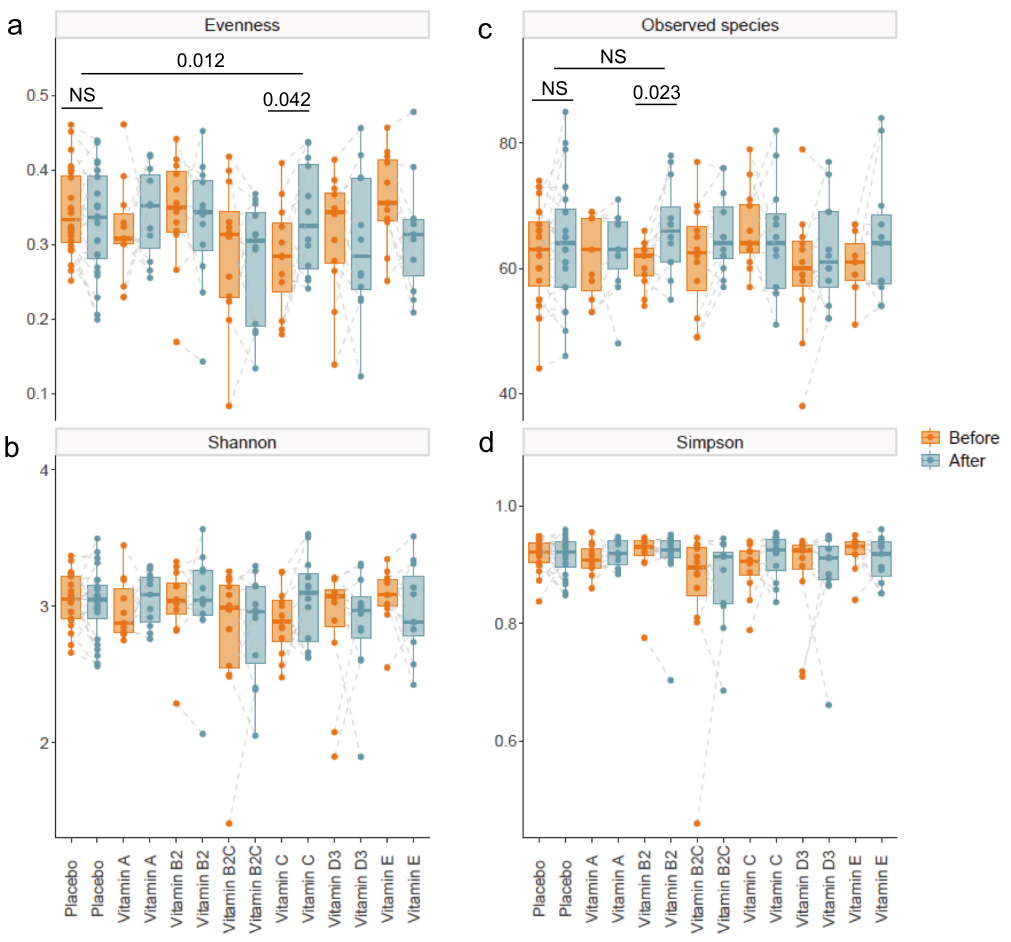
结果表明,与基线组(p=0.042)和安慰剂组(p=0.012)相比,维生素C在第四周显著提高了肠道微生物群落的均匀性。此外,与基线相比,维生素B2显著增加了观察到的物种数量(p=0.023)。
Bray-Curtis距离的置换多变量方差分析(PERMANOVA)表明,肠道微生物beta多样性的总体变化在组间或组内与基线相比没有显著差异。
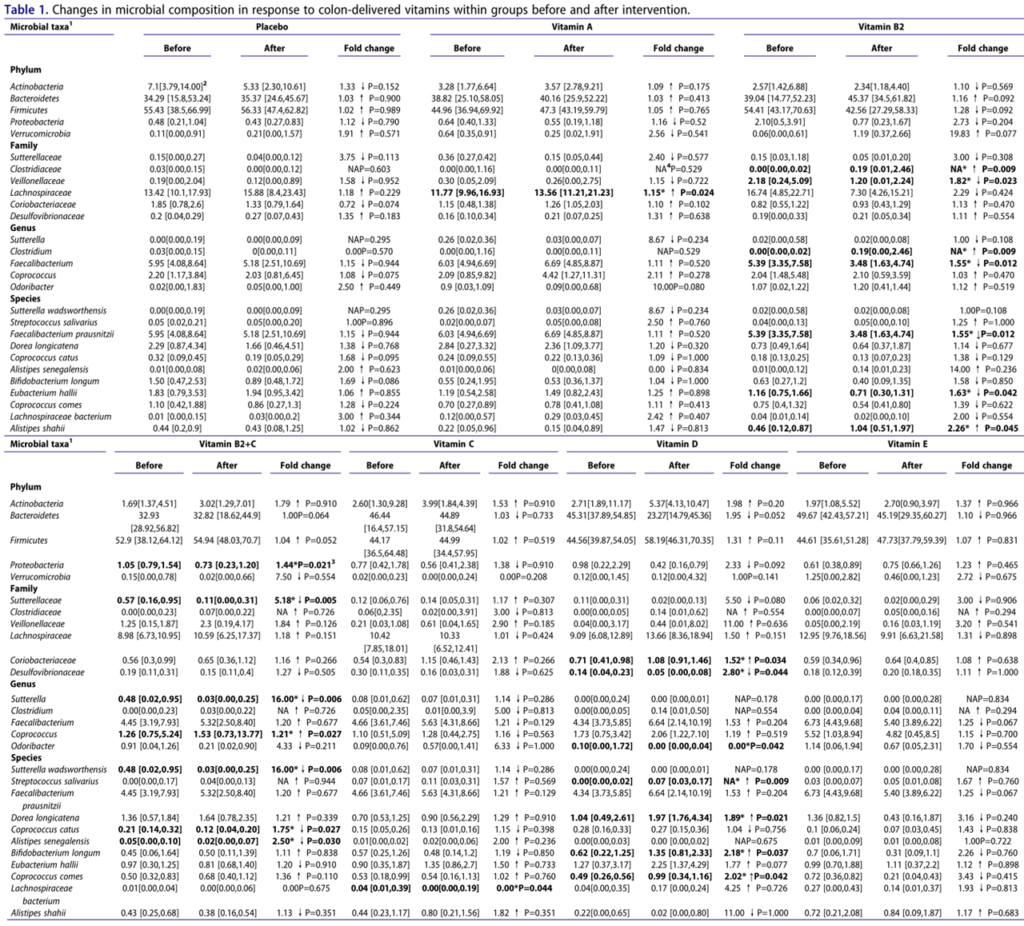
不同的维生素引起组内以及治疗组和安慰剂组在门、科、属和种水平上肠道微生物组成的变化。

门水平:维生素B2+C导致变形杆菌显著减少(p=.021),与基线相比菌落数量增加和拟杆菌数量减少。此外,服用维生素D后,与基线相比,拟杆菌有减少的趋势(p=.052),与安慰剂相比有显著差异(p=.038)。最后,与安慰剂相比,维生素D和维生素A显著增加了放线杆菌的数量(p=.033和p=.041)。
通过测量粪便中的SCFA浓度来评估肠道微生物群的代谢活性(下图)。
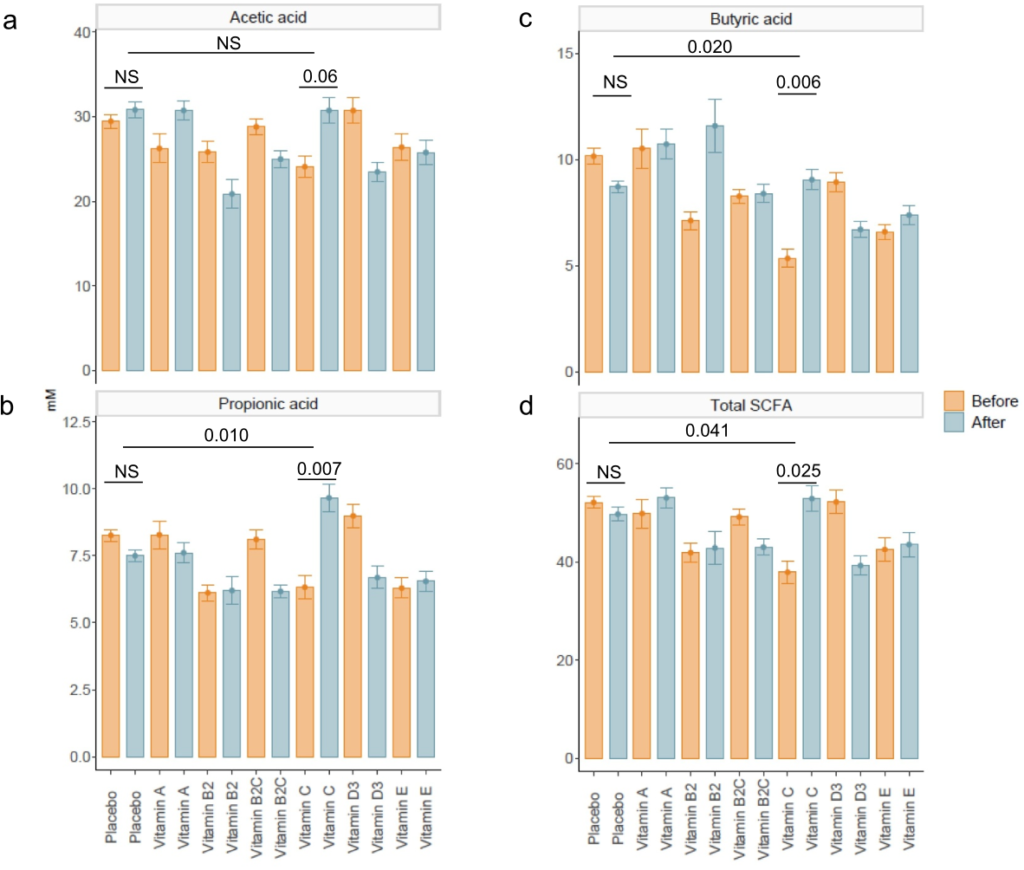
我们发现,与基线相比,维生素C显著增加了总SCFA(p=.025)、丙酸(p=.007)和丁酸(p=.006)浓度。与安慰剂相比,这些效果也很明显(分别为p=.041,p=.010和p=.020)。与安慰剂相比,服用维生素C对粪便pH值的降低更明显,但是,两组之间没有显著差异。
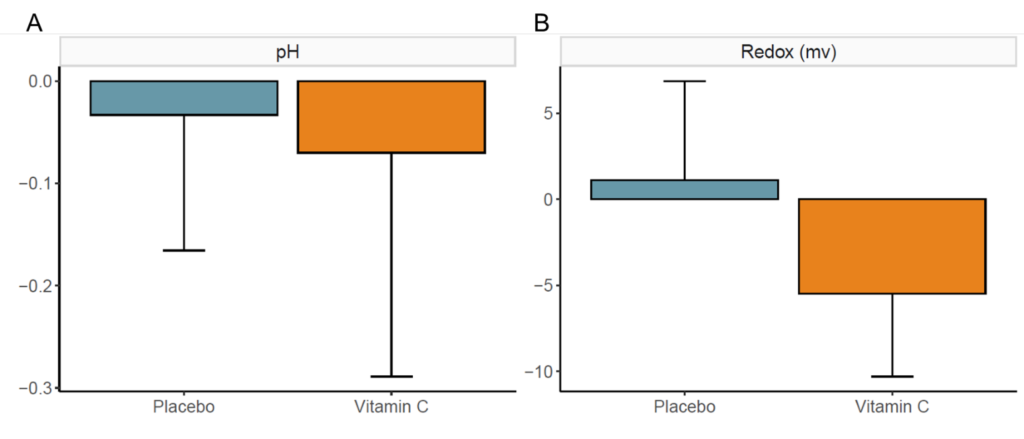
在服用维生素C后,粪便氧化还原电位降低,而服用安慰剂后,粪便氧化还原电位升高;然而,两组间也没有显著差异。最后为了确认维生素是否被输送到结肠,测量了干预前后粪便和血浆中维生素B2的浓度,并与安慰剂进行了比较。与基线(p=0.06)和安慰剂(p=0.05)相比,粪便中的维生素B2增加了。但是,这对血浆维生素B2浓度没有显著影响。
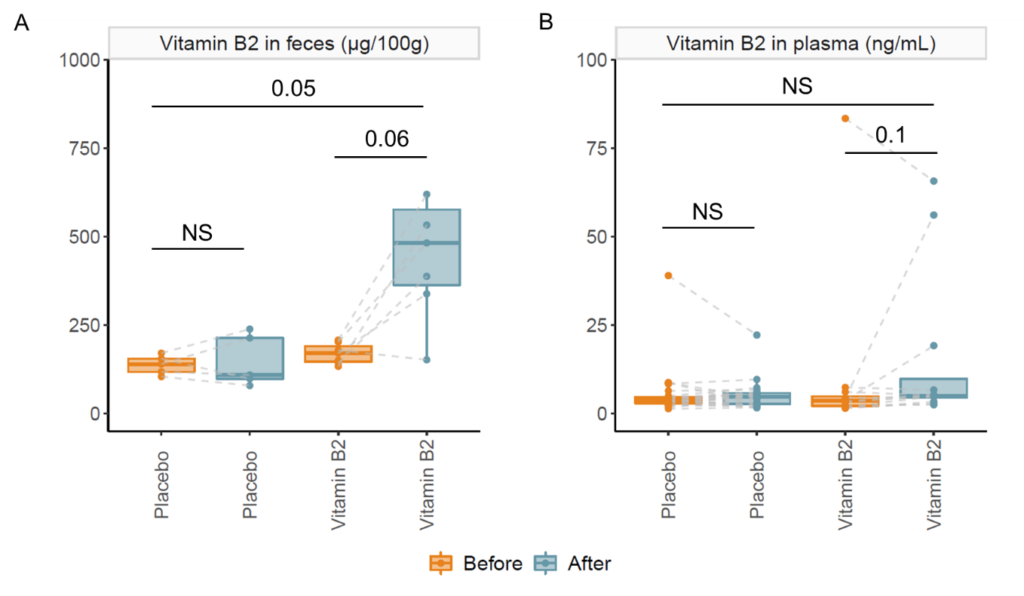
体外研究:
对3名粪便样本供体(男性,26岁;女性,35岁;女性,29岁)进行了短期结肠发酵实验,选出一名SCFA产量平衡的供体进入最终发酵实验。在发酵前(0h)和发酵后(48h)分别从每个发酵瓶采集出水样品,用0.22µm滤器过滤灭菌。样品用来分析粪便微生物组成、微生物体外代谢活性、Caco-2和HT29-MTX-E12细胞培养及屏障功能、HT29细胞培养和免疫功能。
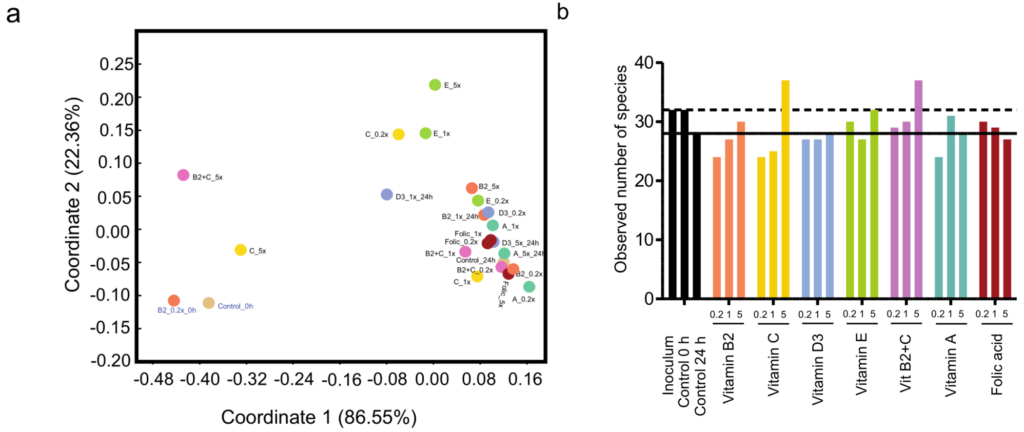
加权UniFrac距离的主坐标分析(PCoA)显示发酵前(0h)和发酵后(24h)样品之间的分离,表明发酵随时间的影响(图a)。大多数维生素处理24 h的微生物群与24 h对照样品聚集在一起,表明维生素和对照样品之间的beta多样性没有变化。
然而,经维生素E(1x和5x)、维生素C(0.2x和5x)、维生素D(1x)和维生素B2+C(5x)处理24h的样品与对照样品明显分离,表明维生素处理对发酵过程中微生物群落的组成有一定的影响。此外,添加不同浓度的维生素C、E、B2+C、B2、A和叶酸,与24小时的对照相比,观察到的物种数量增加,表明对α多样性有影响。
同时,经维生素处理后,所有分类水平都有了些许变化,在门水平上变化最明显的是放线菌门(Actinobacteria)、厚壁菌门(Firmicutes)和Verrucomicrobia的增加以及拟杆菌门(Bacteroidetes)的减少,特别是维生素E、B2、B2 + C和C的添加。
在属水平上,除维生素B2以外,所有维生素都使Roseburia增加,而维生素C、B2、B2 + C、D和E增加了Akkermansia、Bifidobacterium和Faecalibacterium的相对丰度。
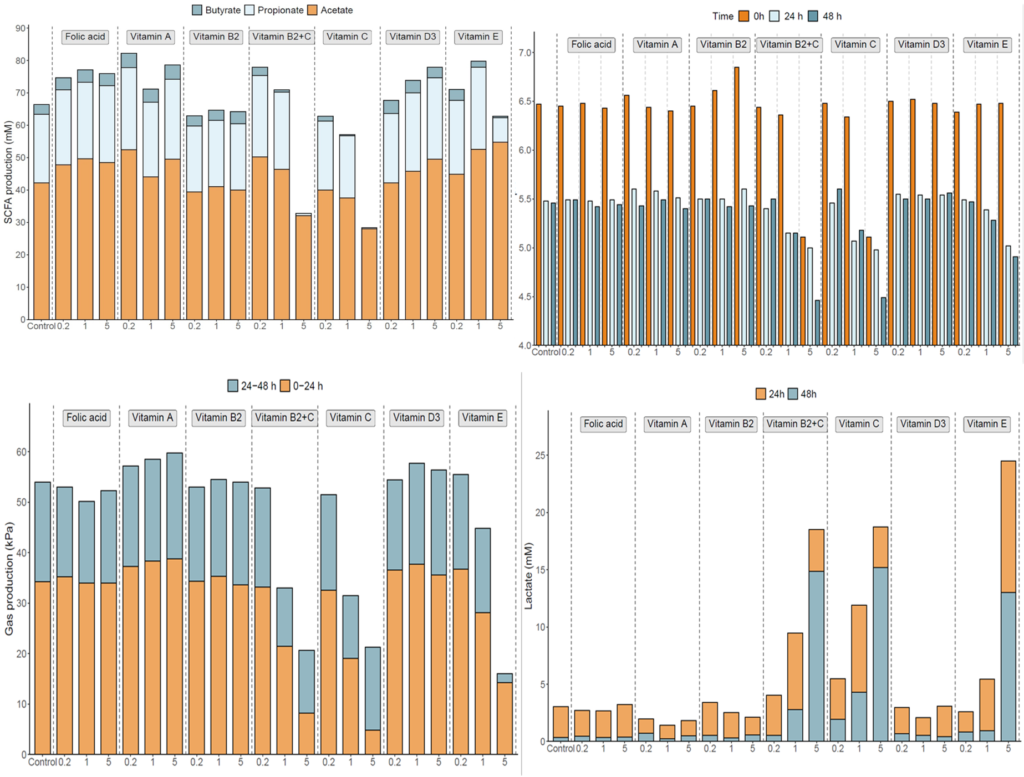
与对照相比,大多数维生素对SCFA的产生有明显的影响。维生素A处理的总SCFA浓度最高(0.2倍),而所有浓度的叶酸都持续增加总SCFA浓度。乳酸浓度、产气量和pH值为体外发酵系统的代谢活性提供了额外的衡量标准。在添加维生素C(1x和5x)和维生素E(5x)后,pH、产气量和乳酸积累量显著降低。
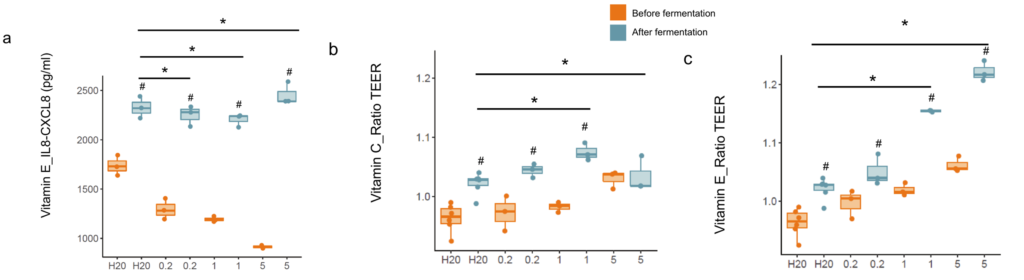
当HT29细胞与经维生素处理的微生物群的发酵样品孵育时,观察到IL8-CXCL8的分泌发生了变化。在所有浓度的维生素E中,IL8-CXCL8(956.67 pg/mL、1010.00 pg/mL、1544.00 pg/mL)与对照组(590.00 pg/mL)相比有轻微但一致的上调(p<0.05)。使用细胞肠道模型研究维生素C和维生素E对肠道屏障完整性的影响,发现在发酵之前,大多数维生素以剂量依赖的方式增加TEER。
此外,在发酵后用对照(水)上清液处理的细胞中,TEER显著增加,这一效果在所有实验中都是一致的(文章中只显示维生素C和E;其他维生素未显示)。橙色,发酵前;蓝色,发酵后。
这只是一项初步研究,文章中的研究人员也提到了有些许不足需要进一步验证的地方。但是这些图表数据也实打实的给出了一些结果。
经结肠传递的维生素对人体肠道菌群和相关代谢活动起了调节作用,根据在人体和体外观察到的效果,维生素C、B2和D似乎是被测试的维生素中影响最显著的。
在人类中,维生素C的效果最为明显,与安慰剂相比,维生素C显著增加了微生物α多样性和粪便SCFA。
在肠道菌群领域研究的科研人员从未停止脚步,如果肠道菌群是通往健康的其中一把钥匙,那么在大家的打磨之下,终将可以打开更加精准的个体化医疗技术大门。
参考文献:
Jie Zhuye,Yu Xinlei,Liu Yinghua et al.The Baseline Gut Microbiota Directs Dieting-Induced Weight LossTrajectories.[J] .Gastroenterology, 2021.
Pham Van T,Fehlbaum Sophie,SeifertNicole et al. Effects of colon-targeted vitamins on the composition and metabolicactivity of the human gut microbiome- a pilot study.[J] .Gut Microbes, 2021,13: 1-20.
相关阅读:

谷禾健康

感到疲惫?乏力?食欲不振?容易流血?皮肤发痒?腿肿?体重减轻?…这些有可能是慢性肝病的信号,慢性肝病是一个主要的健康问题,它可以发展为肝硬化和肝癌。
肝病按照病因划分,常见的有如下几大类:
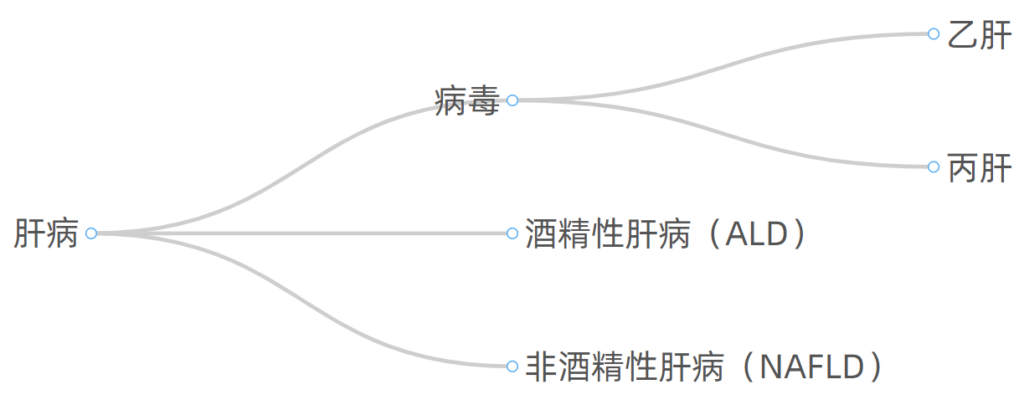
无论病因如何,肝病如果没有得到有效管理控制,进展的常见终末阶段是肝硬化。
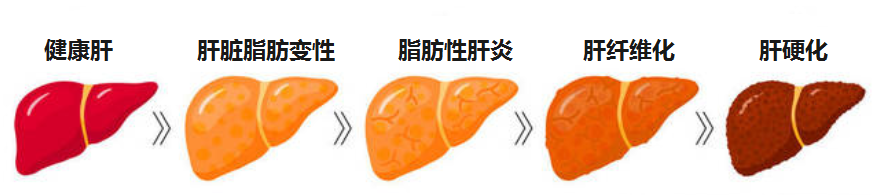

肝硬化可导致失代偿和肝细胞癌的发展。
发病率
目前由于疫苗接种计划和有效抗病毒治疗不断发展,乙肝和丙肝肝硬化的发病率正在下降,但由于以下两个原因导致另两种肝病发病率不断上升:
1、肥胖,导致非酒精性脂肪肝的发病率增加
2、饮酒,导致酒精性肝病的发病率增加。
本文带你详细了解肝病与肠道菌群:


肝脏也是胆汁产生的场所,在肠肝循环中具有重要作用。
肝脏,作为第一个接触微生物产物进入门静脉循环的器官,可能受到肠道微生物群及其变化的多种影响。肠道微生物群的成分或代谢物通过各种机制与肝脏相互作用。
肝脏中产生的胆汁酸(如胆酸和鹅去氧胆酸)与葡萄糖醛酸酶结合。一旦分泌到十二指肠肠腔,肠道菌群代谢和解共轭,产生尿胆原(排泄)和初级胆汁酸被吸收和循环。胆汁酸还通过内在的微生物调节活动来控制和影响菌群。
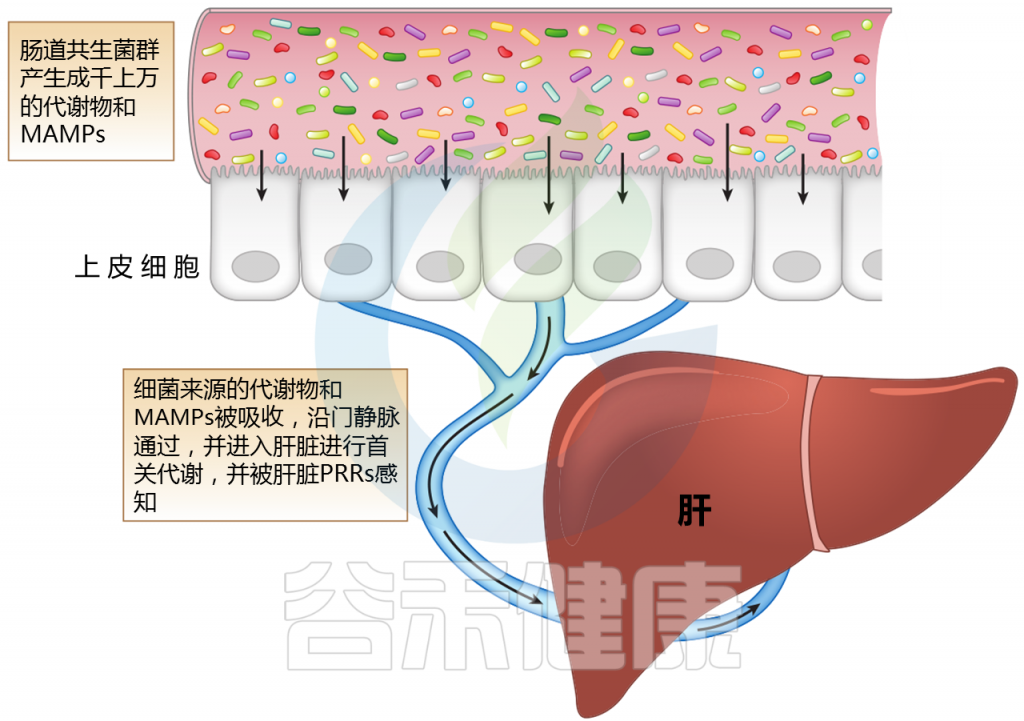

Jones R M,et al.,Annual Review,2020
注:MAMPs——微生物相关分子模式;PRR——模式识别受体
肝脏位于体循环和来自肠道吸收活动的大量外源性分子和微生物相关分子模式(MAMPs)之间的界面。
微生物产生的代谢物会随着微生物群的组成而变化;它们沿着门静脉分流并引发多种信号通路的激活。MAMP暴露过多会导致炎症。
肝硬化前期肠道菌群总体变化:
整体多样性减少,厚壁菌门减少,拟杆菌门和变形菌门增加。
在三种类型的肝炎中,肝硬化前期微生物参与非酒精性脂肪肝病和酒精相关性肝病的证据相对更为有力。
—— 非酒精性脂肪肝病
非酒精性脂肪性肝病(NAFLD)和非酒精性脂肪性肝炎(NASH)是一种以肝细胞内脂质(主要是甘油三酯)的微泡或大泡状积聚为特征的肝病,并伴有不同程度的炎症浸润。
在非酒精性脂肪性肝病中,研究人员发现粪便、血液和肝活检中的致病菌(如肠杆菌科和大肠杆菌)的相对丰度增加。随着病原菌数量的增加和厚壁菌门数量的减少,菌群失调。
—— 酒精性肝病
长期摄入酒精可导致人类和动物模型中菌群结构的变化,肠道通透性增加,随着持续的酒精滥用,致病菌的多样性进一步减少,相对丰度增加,如肠杆菌科和肠球菌科。
在小鼠中,乙醇可以降低肠道屏障功能,并允许增加局部炎症。从机理上讲,乙醇也能抑制抗微生物凝集素的表达,在慢性乙醇消耗模型中,无Reg3β和Reg3γ的小鼠表现出增加的细菌移位和NASH的发生。这些发现表明乙醇可能介导了肝脏潜在的促炎性刺激,有多个长期后遗症。
尽管肝硬化的病因可能有所不同,但在肝病的末期,微生物群与肝脏的相互作用在很大程度上与病因无关。也就是说无论哪种都可能发展为肝硬化。
前面我们知道,肝炎如果不能得到有效控制,久而久之会对肝造成永久性损伤,也就是肝硬化。肝硬化又分为两种,一种是代偿性肝硬化,一种是失代偿肝硬化。
代偿性肝硬化虽然肝功能减退,但机体仍能正常运行。
失代偿性肝硬化指肝硬化发展到一定程度,出现肝功能衰竭,可能出现严重并发症,如肾功能衰竭、静脉曲张出血和肝性脑病等。
肝硬化患者最初没有症状,等到了肝硬化失代偿(定义为腹水、肝性脑病、黄疸和/或胃肠道出血),就是肝硬化过程中的转折点。
——肝硬化失代偿期会发生什么?
代偿性肝硬化患者可能会保持多年稳定,死亡率非常低,每年< 1%。然而,在第一次住院治疗后,35%的患者将在28天内出现后续的失代偿,需要频繁入院。肝硬化急性失代偿可导致慢加急性肝衰竭(ACLF)。
注:慢加急性肝衰竭是一种综合征,以一个或多个主要器官或系统(肝、肾、脑、凝血、循环或呼吸)衰竭为特征。
慢加急性肝衰竭是失代偿性肝硬化的主要死亡原因。他们的慢加急性肝衰竭(ACLF)的中位时间为2-3年,死亡率每年约为10%。


Trebicka Jonelet al, Nat Rev Gastroenterol Hepatol,2020
每次失代偿后,慢加急性肝衰竭在28天内的发展约为30%,在此阶段死亡率在28天内攀升至40%。这些器官衰竭患者通常在重症监护室接受治疗,肝移植是唯一的治疗方法。
肠道菌群如何影响肝硬化失代偿?
肝硬化中微生物群-肠道-肝脏相互作用
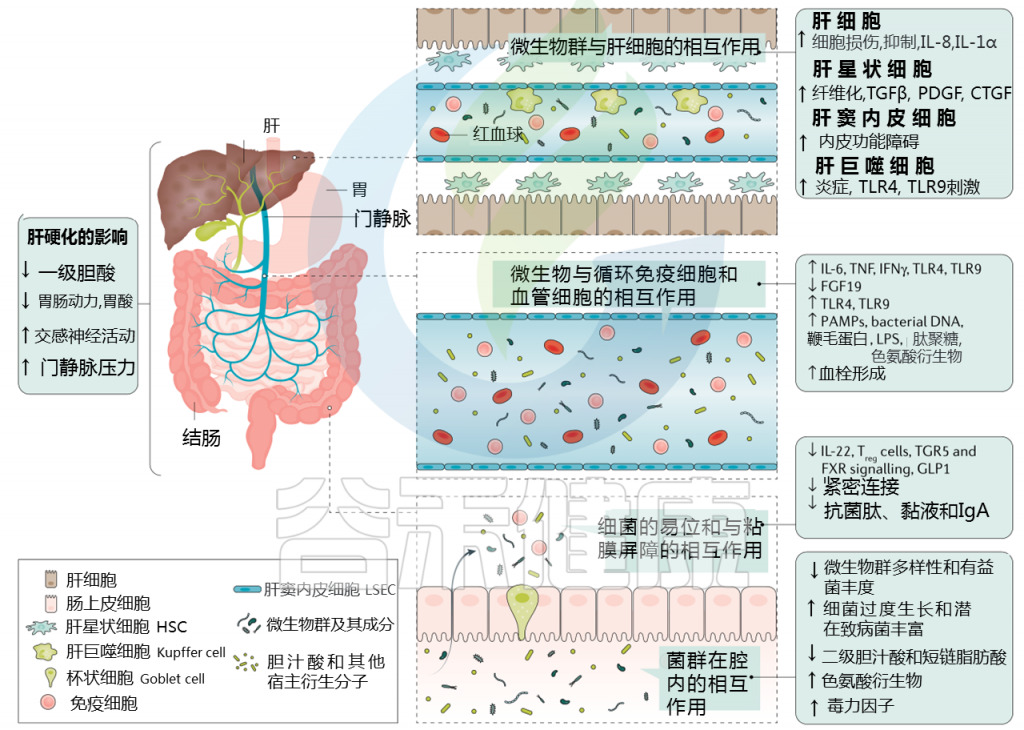

Trebicka Jonelet al, Nat Rev Gastroenterol Hepatol,2020
肝硬化发展过程中肠道微生物群的变化在很大程度上归因于肠道微生物群组成及其产物,产物可能具有致病作用。短链脂肪酸(SCFAs)、次级胆汁酸和色氨酸衍生物增加,而粘液蛋白的变化、功能失调的紧密连接和抗菌肽的减少促进了微生物组成分和/或其代谢物(病原体相关分子模式(PAMPs))跨肠屏障的移位。
接下来,就肠道菌群与肠道屏障,病变肝脏的相互作用,菌群代谢产物与转运,门静脉高压和酒精的作用这4个方面展开讨论。
1. 与肠道屏障相互作用
肠漏:
一个不正常的微生物群可以影响肠道上皮屏障,并导致内容物从肠道到肝脏和其他地方难以控制的转移。这种肠上皮屏障的损伤被称为漏肠。
在肝脏疾病期间,由于肝肠循环、肠道炎症和门脉高压的改变,宿主生理和肠道完整性发生重大变化。与此同时,肠道微生物组和肝脏之间的串扰也发生了重大变化:
肠道中的宿主粘膜蛋白和通路(例如FXR信号)被肠道微生物群代谢物(例如短链脂肪酸)改变,并可能导致肝脏损伤;
肝脏疾病进展引起的肠道内化变化可能会影响肠道屏障,促进肠道炎症,降低抑菌肽;
而肠道相关淋巴组织可能通过驱动肠道炎症,从而增加肠屏障的通透性参与肠屏障的功能障碍
由于穿过肠道上皮屏障的细菌成分会引发免疫反应,因此肠道渗漏被认为会增加慢性全身炎症。例如,在肝病患者,尤其是肝硬化患者中,细菌细胞壁脂多糖(LPS)水平升高,也被称为内毒素血症。
2018年的一项研究表明,从失代偿期肝硬化患者的循环血和其他“无菌”隔室中分离出的细菌是可行的,这表明即使是活的细菌也可以在失代偿期肝硬化期间通过肠屏障转位。
2. 与病变肝脏的相互作用
从失代偿到慢加急性肝衰竭的进展与全身炎症的广泛激活有关,影响许多细胞因子和炎症系统。
释放危险相关的分子模式来促进失代偿和炎症
慢加急性肝衰竭的发展,不同衰竭器官的死亡细胞和细胞外基质的重塑,特别是在肝脏,都通过释放危险相关的分子模式来促进失代偿和炎症,最终可能是慢加急性肝衰竭发展的先决条件。
这种联系在乙肝病毒引起的肝硬化和/或慢加急性肝衰竭患者中尤其常见。慢性乙肝病毒的再激活可能导致肝损伤,从而释放危险相关的分子模式,进而导致器官衰竭和慢加急性肝衰竭。
在慢性肝病和肝硬化患者中,甲肝病毒和戊肝病毒重叠感染也可能诱发慢加急性肝衰竭。
对病原体相关分子模式的免疫反应导致器官功能障碍
另一方面,这种炎症的爆发是由微生物或其成分的转移引起的,也称为病原体相关分子模式。对病原体相关分子模式的免疫反应可能在免疫病理学过程中导致器官功能障碍,在这种过程中,免疫反应会导致感染造成损害。
炎症标志物水平升高
血浆中全身性炎症标志物(如IL-8或IL-6)水平升高,无论是否有明显的细菌感染,都与肝硬化和慢加急性肝衰竭的急性失代偿有关。新的数据强化了改变后的肠道微生物群和慢加急性肝衰竭之间的联系。
血浆代谢物特征
除了肠道菌群衍生代谢物与慢加急性肝衰竭发展之间的关联之外,血浆代谢物特征(可能也来自肠道菌群)也与全身炎症和慢加急性肝衰竭密切相关。
这些发现可能解释了为什么肠道微生物群的改变和细菌易位的增加可能为不同器官的免疫病理发展为器官衰竭,加重全身炎症和诱导ACLF的环境。
酒精性肝病
2019年研究表明,乙肝病毒相关ACLF患者的循环细菌DNA显著增加,并与炎症标记物(如CXCL10,一种已知的趋化因子)相关,在非乙肝病毒病因中也与ACLF相关,尤其是酒精性肝硬化。
另外,在急性酒精性肝炎(ACLF的一个亚型)中,研究表明,与没有这种特殊菌株的患者相比,具有一种产生细胞溶血素的肠球菌菌株的患者具有极高的死亡率(180天内的死亡率分别为89%和3.8%)。
我们知道,急性酒精性肝炎与微生物变化密切相关,这可能决定患者的临床特征及其结果。在几乎一半的急性酒精性肝炎患者中,失代偿和慢加急性肝衰竭都会发生,但没有任何可识别的促发事件,这表明这与内源性机制有关(例如,门静脉高压症或细菌易位)。
3. 门静脉高压症和酒精的作用
即使肝硬化的门静脉高压症得到有效治疗,例如通过放置经颈静脉肝内门体分流术(TIPS)支架,许多患者仍出现进一步失代偿和ACLF(2年内约47%),尤其是由于全身炎症和随后的器官衰竭。
此外,与肝静脉、右心房和外周静脉血相比,腹水的存在决定了门静脉循环微生物群的组成(腹水:一种失代偿的指标),以及与炎症标记物和ACLF的发生相关的特定循环微生物群。
然而,应该指出的是,TIPS支架本身可能会加重高动力循环,从而导致内毒素水平的增加。从长远来看,TIPS支架降低了失代偿率,可能主要是由于这些肝硬化患者腹水的发生率降低。
失代偿性肝硬化和ACLF先于酒精性肝硬化发生。这一发现可能很重要,不仅因为酒精是失代偿期肝硬化最常见的病因,而且可能是由于酒精本身对肠道微生物群和肠屏障功能的直接影响。
在健康个体和动物模型中,已经证明急性酗酒会增加循环中的内毒素和细菌DNA水平。
酒精显著改变肠道微生物群的组成,降低拟杆菌的相对丰度,增加变形菌。
它的代谢物,特别是乙醛,可以破坏肠道上皮细胞的紧密连接,导致肠道渗漏,促进细菌和真菌的易位,这两者都可能与肝硬化的进展有关。
在不同病因的肝硬化(例如,非酒精性脂肪性肝炎或乙型肝炎引起的肝硬化)中也观察到微生物群组成的改变以及肠道的渗漏。
4. 微生物代谢产物和转运
肝硬化发展过程中肠道微生物群的变化在很大程度上不仅归因于肠道微生物群的组成,还归因于其产物,这些产物可能具有致病作用。
一项研究表明,在肝硬化向失代偿和ACLF发展的过程中,血液代谢物特征明显改变。
针对903人的大规模研究为某些强预测代谢物模式的微生物起源带来了重要的见解,但很难对这些发现作出有力的陈述。
另一项对602名患者进行的研究表明,微生物群衍生代谢物与ACLF的存在有关。其他微生物成分,如次级胆汁酸、短链脂肪酸和色氨酸代谢物也在肝硬化中发生较大变化,与疾病的进展有关。尤其是,胆汁酸通过下调FXR受体来改变肠道屏障功能,这为临床FXR激动剂已经可用提供了新的治疗机会。
间接证据表明肠道微生物群可能会影响肝硬化的预后。
首先,研究表明,使用非选择性β受体阻滞剂(一种预防肝硬化失代偿的常用方法)治疗可改善肠道屏障,减少肠道转运时间,从而降低肝硬化患者细菌转移的可能性。
第二,在静脉曲张破裂出血期间或作为失代偿期肝硬化的长期预防措施,抗生素治疗是一种推荐的治疗方法,因为它可以改善结果,其机制可能与减少细菌移位有关。
尽管这一观点尚未得到确凿的证实,但我们知道,一种特定的微生物组表型(所谓的肠型)会导致肝功能的病理改变,并且考虑到微生物群中存在着广泛的成员,如真菌或病毒,微生物组标志物可能是非常有用的临床工具,以确定有失代偿和ACLF风险的患者。
肠道微生物群可以作为疾病进展、严重程度和治疗反应的生物标志物。
不同肝病的菌群特征
肝硬化:
瘤胃菌科、毛螺菌科与其他菌(包括肠杆菌科和拟杆菌科)进行比较,菌群比率失调。随着ACLF的发展,肝硬化菌群失调比率恶化。
该研究表明,肝硬化患者的菌群比率失调
对129名患者的研究显示,毛螺菌科减少,巴斯德氏菌科(Pasteurellaceae)的丰度可以预测死亡率。
其他研究也提供了证据,表明特定的微生物组群特征可以区分肝硬化和健康对照组,并且微生物组的变化可能能够监测病情的严重程度和进展情况。
一组45例肝移植受者中,肝移植改变了肠道菌群,使微生物多样性增加,原生细菌增加(如毛螺菌科),潜在致病菌减少(如肠杆菌科)。
该研究强调了患病的肝脏会影响肠道菌群。
肝硬化和慢加急性肝衰竭:
慢加急性肝衰竭和肝硬化的肠道微生物群特征


Trebicka Jonelet al, Nat Rev Gastroenterol Hepatol,2020
中国肝硬化患者宏基因组全关联研究(MWAS)显示,与健康个体相比,肝硬化肠道菌群组成有大于34个显著差异的菌群。肝硬化患者中韦荣球菌属和链球菌增多,而产丁酸共生菌包括Faecalibacterium prausnitzii 和Coprococcus comes减少。(下表)
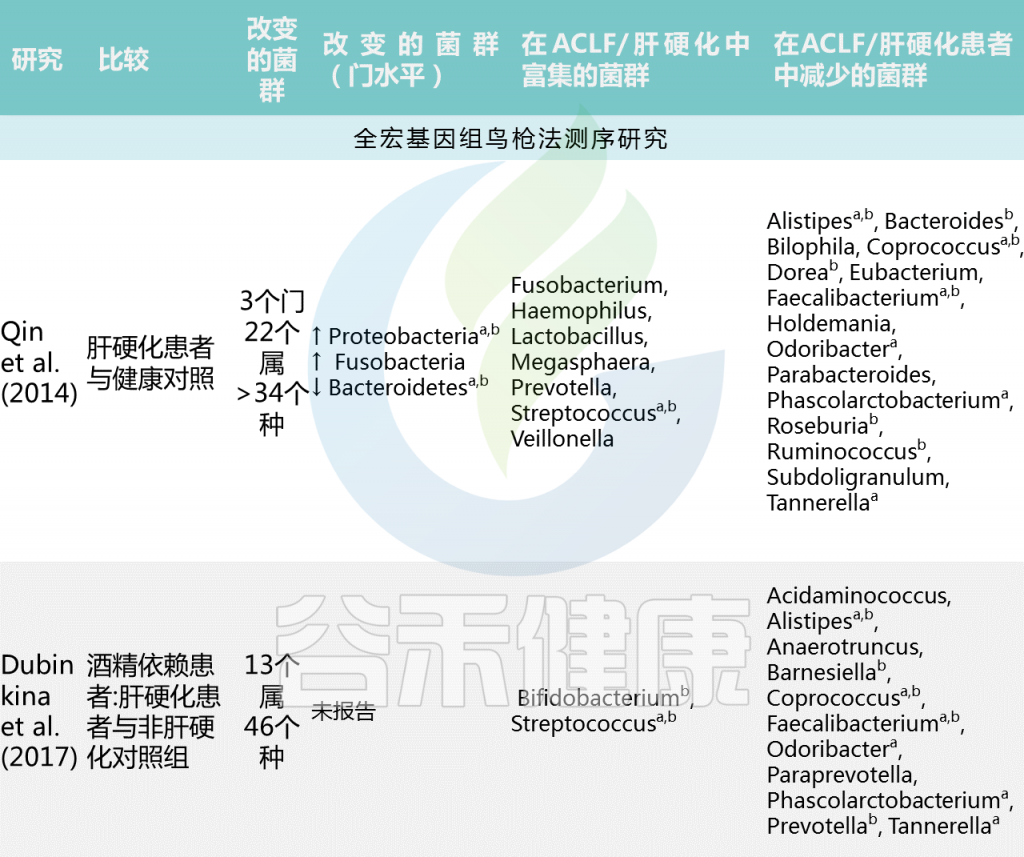

Trebicka Jonelet al, Nat Rev Gastroenterol Hepatol,2020
肝细胞癌(HCC)
持续的肝损伤和再生促进了肝细胞癌的发生,它是全球癌症死亡的第三大原因。
肝细胞癌HCC与肠道大肠杆菌过度生长有关,患者微生物群多样性增加,与产丁酸菌属(如Alistipes)减少有关,而致病性产脂多糖菌(如克雷伯氏菌)增加。
在与非酒精性脂肪性肝病相关的HCC,一项来自意大利的研究注意到拟杆菌和瘤胃球菌科增加,双歧杆菌减少。
不同部位菌群功能
肠道菌群:
从门诊病人的角度来看,肠道菌群可以证明是预测入院,MHE和晚期纤维化患者的有用工具。
一项针对NAFLD肝硬化的研究发现,粪便微生物分析中的27种细菌特征以及年龄,性别和体重指数(BMI)可预测NAFLD肝硬化。
晚期纤维化是NAFLD死亡率的重要预测指标,可以从粪便菌群中推断出纤维化,以帮助识别高危人群。
鉴于失代偿性肝硬化中存在预测的失调模式,因此将CDR(肝硬化失调率-毛螺菌科+瘤胃菌科+韦荣氏菌科/肠杆菌科+拟杆菌科)视为预测失代偿风险的工具(适用于所有常见的CLD病因)较低的分数预示结果较差,并且具有较强的预测价值。
粪便菌群也可以用来预测谁会在90天内再次入院和急性肝性脑病复发,因为急性肝性脑病和其他失代偿的粪便菌群有所不同。
唾液菌群:
唾液菌群失调比率是一种简单实用的临床工具(Lachnospiraceae + Ruminococcaceae + Veillonellaceae/ Streptococcaceae),可以预测有和无肝性脑病的失代谢性肝硬化患者90天的入院情况。
其他部位菌群:
一些研究表明,粪便微生物群和结肠黏膜相关微生物群是不同的。事实上,回肠、空肠和十二指肠粘膜样本或抽吸物的微生物群是不同的,它们可能对肝硬化具有重要的预后能力,主要表现为肝性脑病。然而,这些样本并不容易获得,而且很难将其作为生物标志物进行常规的护理点采集。
微生物工具的潜力
需要进一步的研究才能使人信服结论:患者在不同的条件和疾病下,它们的肠道微生物群既表现出疾病特异性的变化,也表现出非特异性的共同反应。因此,在其作为生物标志物的潜力得以实现之前,确定强有力的疾病特异性肠道菌群特征至关重要。
生物标志物和基于微生物的工具的潜力

Trebicka Jonelet al, Nat Rev Gastroenterol Hepatol,2020
要更准确地估计疾病对肠道微生物群的影响程度,就需要从世界各地获得强有力的大规模纵向数据,同时考虑各种混杂因素。理解和解释其他相关的混杂因素将使我们更接近以微生物组为基础的肝硬化生物标志物。
微生物组的整体观点,包括微生物基因表达和微生物衍生的代谢物或蛋白质,可能导致更准确和全面的生物标志物,类似于整合宿主遗传学与基因表达和表观遗传学时的强大疾病关联。这种包含宿主-微生物全生物的整体观点也可能支持诊断、分层和治疗的个体化,并可能开创全生物群关联研究的新时代,扩大宏基因组全关联研究领域。
我们知道,即使在没有肝病的情况下,微生物组也在调节情绪和潜在的认知中发挥作用。慢性肝病患者的脑功能改变是肠-肝-脑轴的结果,甚至在肝硬化之前就可以影响病程。
酒精使用障碍(AUD)
一项关于酒精使用障碍(AUD)患者肠-肝-脑轴的重要研究发现,抑郁、焦虑和酒精渴求与肠通透性增加相关,即使在戒酒后,肠通透性高的患者仍然存在抑郁、焦虑和酗酒。
最近发表的一篇关于AUD中这一轴的操纵的文章显示,对于AUD患者,在粪菌移植后,这些渴望、消费和长期的与AUD相关的住院治疗可能会降低。
肝性脑病
肝硬化中普遍存在的认知功能障碍是一种记忆障碍型,称为轻度或隐性肝性脑病。这可以发展为明显的肝性脑病,表现为嗜睡,迷失方向,晕眩和昏迷。
肝性脑病是肠肝轴中与微生物组相关的经典并发症,是全身性内毒素血症和炎症的结果,最终加重了神经炎症,而神经炎症是支撑肝性脑病发病机理的重要因素。
多年来,氨被认为是肝性脑病发病的关键,但后来发现全身炎症对于氨发挥其神经毒性作用是必不可少的。越来越多地描述了特定微生物群在肝性脑病和全身性炎症(包括性别影响)进程中的作用。在小鼠中,发现肠道微生物组是肝性脑病所特有的全身性炎症和神经炎症所必需的。
轻度肝性脑病和PTSD
在临床上,轻度肝性脑病需要专门的认知测试,例如心理计量学肝性脑病评分(PHES),抑制性对照测试,脑卒中诊断等。但这些测试最好在专门的环境中进行,并且需要专业知识。
轻度肝性脑病(MHE)和创伤后应激障碍(PTSD)肠道菌群之间也存在协同作用,与其他人相比,PTSD患者的菌群失调更为严重。PTSD,酒精滥用和肝硬化常常并存。微生物变化可能有助于将MHE与PTSD区别开来,并且可以帮助我们定义较新的疗法。
老年肠道-肝-脑轴改变
利用肠脑轴的主要挑战是老年人群(慢性肝病患者)。老年人患者的致病菌往往更具致病性,随着合并症,住院和抗生素暴露于更大的革兰氏阴性病原体中,病情恶化。
与类似的老年非肝硬化对照组相比,年龄较大(> 65岁)的肝硬化患者往往会改变肠道-肝-脑轴,从而增加炎症并损害记忆的认知能力。在相关网络分析的研究中,更重要的是,在老年肝硬化和非肝硬化组中也发现了类似的模式,这表明老年患者已经具有潜在的肠脑轴改变。
这对肝移植具有重要意义,因为尽管进行了肝移植,但与年龄相关的肠脑轴变化仍可能持续。人口老龄化往往会导致多种其他合并症和精神疾病,需要额外的照顾以确保最佳的移植后效果。
针对肝硬化肠道微生物群的策略
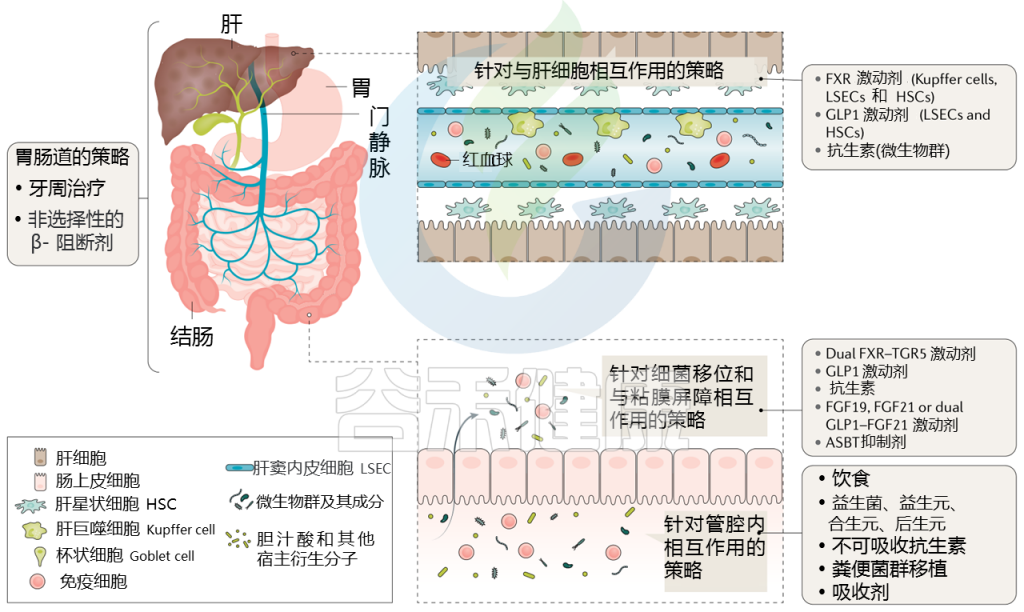

Trebicka Jonelet al, Nat Rev Gastroenterol Hepatol,2020
通过治疗(部分成立和部分试验)调节肠道微生物群可能改善肝硬化患者的预后,而微生物组生物标志物可能反映对这些治疗的反应。下表显示了不同的策略。
针对肠道微生物群的肝硬化干预措施

Trebicka Jonelet al, Nat Rev Gastroenterol Hepatol,2020
接下来主要介绍一些具体疗法:饮食、益生菌、抗生素、白蛋白、牙周、粪菌移植等,有些目前正在临床试验中。
饮 食
除其他因素外,饮食对肠道微生物群有重要影响,这一点已在各种疾病和条件下得到研究。一项针对国际肝硬化人群的研究报告称,咖啡、茶、蔬菜和酸奶的摄入都与微生物群落多样性的增加和住院率的降低有关,这为调节肠道微生物群落以促进肝脏健康提供了前景广阔的途径。(具体的饮食方面建议见文末附录部分)
益 生 菌
益生菌已经成为肝硬化临床研究的主题,特别是它们对脑功能的影响和肝性脑病的风险。
益生菌在肝硬化前可以改善NAFLD的组织学,在肝硬化中可以减少失调,对逆转OHE的二级预防有效,减少失代偿事件的住院率,但可能或不能改善认知能力(MHE)。
大多数制剂都含有乳酸菌,可产生短链脂肪酸,有利于结肠健康。一项短期(5天)口服两歧双歧杆菌和植物乳杆菌8PA3的小型试点研究表明,与单独标准治疗相比,口服两歧双歧杆菌和植物乳杆菌8PA3能恢复肠道菌群,并能更好地改善酒精性肝损伤。
以上是关于益生菌的前沿研究,如果想要尝试的话,最好是经过肠道菌群检测或者在医生的指导下服用更可靠。
抗 生 素
抗生素,也被用作失代偿期肝硬化的预防性治疗。
腹水患者发生自发性细菌性腹膜炎(SBP)的风险增加,接受抗生素预防来预防自发性细菌性腹膜炎的发展。这种SBP的一级预防已经被证明可以提高某些患者的生存率。
在一项多中心、随机对照试验中,对严重肝硬化患者使用抗生素,总体生存率没有任何益处,但是,同样,腹水中白蛋白浓度低的患者在接受抗生素治疗时,生存率得到了提高。
预防性抗生素治疗也同样有效建议用于其他临床情况,如静脉曲张破裂出血、既往SBP和复发性显性肝性脑病。然而,尽管对最脆弱的患者的短期效果可能是有益的,但在其他许多患者中,这些治疗不能阻止进一步的失代偿和ACLF。也许这种情况的部分原因是抗生素引起的微生物群落多样性减少。
因此,需要开发一种更具针对性的肠道微生物群来改善肝脏健康。
牙周卫生
也许你不知道,牙周卫生也会与肝硬化有关。已发表的人类MWAS表明,在肝硬化期间,肠道微生物组向口腔微生物组转变。
减少胃部充当天然屏障的酸性环境可能促成口腔微生物群转移到肠道,在肠道上皮屏障适应不同的微生物组分。如前所述,这些变化可能促进肠道微生物群通过肠道屏障的转移,进而导致并发症。因此,防止口腔微生物不必要的转移到肠道,可以成为未来肝硬化治疗的基础。
一项研究表明,与20名非肝硬化对照组相比,30名肝硬化患者的牙周卫生干预措施改变了肠道微生物群,改善了肝性脑病。
白蛋白作为潜在疗法
当肠道屏障被削弱时,它会双向泄漏,这也会导致重要的宿主分子从血液室泄漏到肠腔。例如,在酒精性肝病动物模型中,肠道通透性增加导致粪便白蛋白浓度升高。
随着肝硬化的进展,肝脏中的白蛋白合成受到损害:一方面,肝损伤导致肝细胞功能质量的丧失;
另一方面,肝脏僵硬程度的增加,白蛋白合成减少。不仅白蛋白减少,而且它能结合毒素和其他有害物质。这些观察结果将白蛋白水平定位为肝病严重程度的关键参数。
白蛋白还可通过前列腺素E2改善免疫B细胞功能,减少肝硬化患者的免疫反应,从而阻止与ACLF和死亡密切相关的全身炎症爆发。
长期白蛋白治疗肝损害和非自发性细菌性腹膜炎感染患者分别通过提高生存率和解决ACLF改善了临床结果。因此,白蛋白泄漏到肠腔可能会影响肠道微生物群并被其代谢,从而可能改变微生物组分,间接改变宿主。
粪菌移植(FMT)
失代偿期肝硬化中菌群移植的初步研究正在出现,其安全性也很高,为更大规模的研究铺平了道路。
菌群移植后变形菌减少,放线杆菌增多,肝脏疾病严重程度改善,严重酒精性肝炎患者3个月时的死亡率降低,1年生存率提高。
慢性乙型肝炎FMT组出现微生物改变,HBeAg降低。FMT减少了短期酒精渴求和消费,以及AUD相关的住院治疗。
一项包括20名复发性肝性脑病患者在内的开放性随机试验观察到,使用FMT灌肠剂减少了住院人数,改善了认知和菌群失调。
另一项研究也证明了这一点。使用口服胶囊制剂的FMT的新应用也显示出类似的安全性和对肝硬化和肝性脑病的治疗效果。然而,由于报告了一些由耐yao菌转移导致的FMT相关死亡病例,包括一些肝硬化患者,因此需要谨慎。因此,更好地理解和全面描述这些研究可能带来明确的微生物调节干预治疗失代偿期肝硬化。
加深菌群影响机制的理解
未来的研究应该探索和加深对肠道微生物组变化影响肝硬化进展和失代偿发展的动力学和机制的理解。
诊断、治疗
由于肝硬化表现为肠道微生物群与宿主的大量重要相互作用,微生物组诊断和治疗几乎是治疗疾病进展和失代偿发展的必经之路。需要进一步倡导基于微生物组检测和靶向疗法。
改善预后
针对不同水平微生物群与宿主相互作用的策略改善患者的预后。
产学研合作
使之更容易获得和更具成本效益,微生物检测需要更广泛地适应,因为它相对容易收集且信息量较大。可以帮助诊断,预测和潜在地个性化治疗。
多学科综合
多学科例如微生物学,宿主遗传学,基因组学,表观遗传学,代谢组学,营养学等相结合,更好地利用微生物帮助我们有效的进行慢病管理,预防为主,将指导落实到饮食、生活方式等具体应用上,用全新的视角帮助我们认识健康,保持健康。
饮 食 方 式
尽可能选择对肝脏友好的食物,帮你保护肝脏。以下是一些饮食技巧:
选择全麦谷物,面包和谷物。
多吃各种颜色的水果和蔬菜。
选择低脂乳制品。
选择瘦肉蛋白质。
选择植物油,例如橄榄油,而不是黄油。
零食坚果和种子食物。
减少钠摄入量。
每天喝8-10杯水。
避免含有反式脂肪的加工食品。
避免添加糖。
选择可以长期生活并遵循的饮食计划。
吃八分饱腹感
少吃多餐,每三到四个小时吃一顿小餐或吃零食,以补充精力。
限 制 饮 酒 量
肝脏是负责代谢营养物质和其他摄入物质的主要器官。如果体内酒精过多,肝酶可能没有足够的能力对其进行处理。过量的酒精会在身体的其余部分循环,产生负面影响。
定期减少饮酒量很重要。医生甚至可能建议你完全戒酒。
增 加 运 动 量
运动的好处不仅限于减肥和控制体重,还可以帮助减少肝脏周围的脂肪。定期运动也可以改善你的情绪,助你维持在最佳的健康状态。
开始时要循序渐进,比如可以每周进行150分钟运动开始,尽量选择你喜欢的运动,例如,跑步和步行的组合,多人参与的活动增加趣味性(如各种球类运动),健身房的器械训练等。
睡 觉
充足的睡眠对于保持健康状态非常重要(包括慢性肝病治疗期间睡眠很重要)。如果你觉得入睡困难,开始慢慢尝试练习良好的睡眠习惯,例如:
每天都在同一时间上床睡觉和起床,作息规律。
避免咖啡因,烟草和其他刺激物。
尽量保持卧室环境清爽舒适。
运动尽量安排在清晨或午后,不要在睡前剧烈运动。
相关阅读:
膳食胆固醇通过调节肠道微生物群和代谢产物驱动脂肪肝相关的肝癌
参考文献:
Grat M, Wronka KM, Krasnodebski M, et al. Profile of Gut Microbiota Associated With the Presence of Hepatocellular Cancer in Patients With Liver Cirrhosis. Transplant Proc 2016;48:1687-91.
Jones R M, Neish A S. Gut Microbiota in Intestinal and Liver Disease[J]. Annual Review of Pathology:Mechanisms of Disease, 2020, 16.
Acharya Chathur,Bajaj Jasmohan S,Chronic Liver Diseases and the Microbiome: Translating Our Knowledge of Gut Microbiota to Management of Chronic Liver Disease.[J] .Gastroenterology, 2020
Bajaj JS, Sharma A, Dudeja PK. Targeting Gut Microbiome Interactions in Service-related Gastrointestinal and Liver Diseases of Veterans: Meeting Summary.Gastroenterology 2019.
Liu R, Kang JD, Sartor RB, et al. Neuroinflammation in Murine Cirrhosis Is Dependent on the Gut Microbiome and Is Attenuated by Fecal Transplant. Hepatology 2020;71:611-626
Ren Z, Li A, Jiang J, et al. Gut microbiome analysis as a tool towards targeted non-invasive biomarkers for early hepatocellular carcinoma. Gut 2019;68:1014-1023.
Trebicka Jonel,Bork Peer,Krag Aleksander et al. Utilizing the gut microbiome in decompensated cirrhosis and acute-on-chronic liver failure.[J] .Nat Rev Gastroenterol Hepatol, 2020
Lang S, Fairfied B, Gao B, et al. Changes in the fecal bacterial microbiota associated with disease severity in alcoholic hepatitis patients. Gut Microbes 2020;12:1785251.
Ponziani FR, Bhoori S, Castelli C, et al. Hepatocellular Carcinoma Is Associated With Gut Microbiota Profile and Inflammation in Nonalcoholic Fatty Liver Disease. Hepatology 2019;69:107-120.
Gao B, Duan Y, Lang S, et al. Functional Microbiomics Reveals Alterations of the Gut Microbiome and Host Co-Metabolism in Patients With Alcoholic Hepatitis. Hepatol Commun 2020;4:1168-1182.
Duan, Y . et al. Bacteriophage targeting of gut bacterium attenuates alcoholic liver disease. Nature 575, 505–51 1 (2019)

谷禾健康
电离辐射可以引起造血系统,肠道系统以及心脑血管神经系统的多器官损伤。
放射治疗在临床上被广泛用于治疗多种肿瘤。但是由于放射射线不仅可以杀死癌细胞,还会对周围的正常细胞和组织造成损伤,因此放疗经常会引起各种副作用,比如疲劳,恶心,呕吐和腹泻等等。
肠道是辐射的主要目标,也是肠道菌群的最大生态位。虽然有小部分描述性研究表明,肠道微生物群与辐射损伤之间存在潜在的相关性,但这种关系的具体基础仍然不清楚。
近日,来自美国北卡罗拉纳大学教堂山分校的 Jenny P.Y. Ting 团队在 Science在线发表研究论文,题为“Multi-omics analyses of radiation survivors identify radioprotective microbes and metabolites”。

发现在致死剂量的全身性辐射模型中,肠道微生物群,特别是Lachnospiraceae和Enterococcaceae可以保护小鼠抵抗辐射引起的造血系统和肠道系统的损伤,从而在致死剂量的辐射后存活下来。并且这些有益的微生物在放疗副作用轻微的白血病病人的粪便中含量显著提高。
通过靶向性以及非靶向性代谢组学研究,该研究发现SCFAs和色氨酸代谢物能降低肿瘤坏死因子-α、白细胞介素-6、干扰素-γ等促炎细胞因子的生成,这些细胞因子都是辐射损伤的重要介质。
这些发现提出了肠道微生物群和代谢产物在辐射激发后疾病易感性调节中起关键作用的可能性。
研究人员发现,一小部分小鼠可以在高剂量的辐射下存活并正常生活。这些“精英幸存者”拥有一个独特的肠道微生物组,该微生物组是在辐射后形成的。
然后将这部分小鼠称为“精英存活小鼠”,并且收集了他们的粪便进行16srRNA的测序。与同年龄的对照小鼠相比,“精英存活小鼠”的肠道菌群有很明显的不同。
随后,研究人员通过多种不同的菌群干扰实验来直接验证肠道菌群是否可以影响机体对于辐射的反应。在“dirty cage sharing”(脏笼)实验中,作者将“精英存活小鼠”和同年龄常规饲养的的对照小鼠使用过的脏笼子收集起来,用来饲养SPF小鼠和接受者小鼠。
每一周他们都会将接受者小鼠转移到相对应的新鲜脏笼中。经过8周的 “dirty cage” 实验,对接受者小鼠进行致死剂量的辐射。
接受了 “精英存活小鼠” 脏笼子饲养后的接受者小鼠对致死剂量辐射具有了明显的抵抗效果,30天内生存率达到了70%。相反,接收对照组脏笼子饲养的接受者小鼠,30天存活率仅为20%左右。
另外,作者分别利用SPF小鼠和无菌小鼠进行了粪菌移植实验。
接下来他们直接收集了“精英存活小鼠”和对照小鼠的粪便,并将粪便处理物通过灌胃的方法转移到受体小鼠中。接收“精英存活小鼠”粪便移植的SPF小鼠和GF小鼠都表现出明显的抗辐射效果。
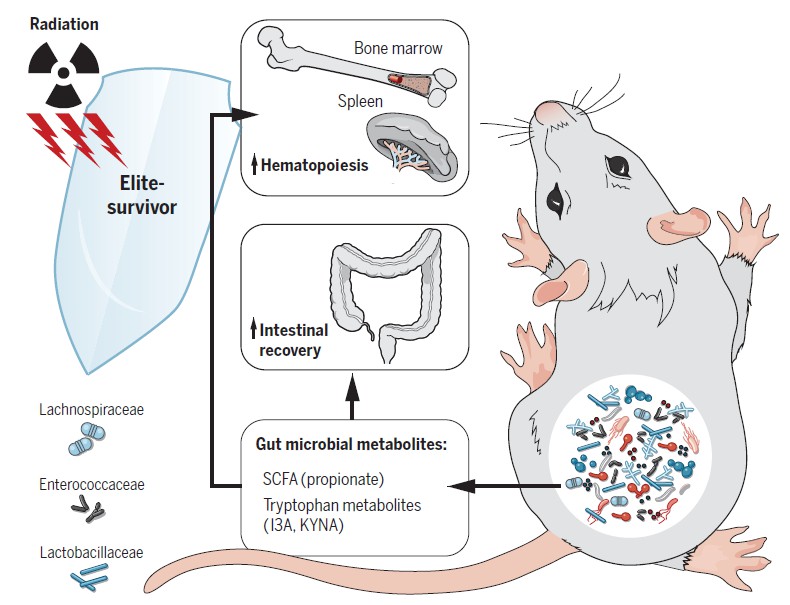
利用这一发现,结合粪便植入和‘dirty cage sharing’实验,证明来自精英幸存者的微生物群在无菌的和常规饲养的接受者中均提供了重要的放射防护,其特点是提高了存活率并改善了临床评分。
他们找出了8种在“精英存活小鼠”受体组显著升高的细菌以及5种显著下降的细菌。那么作者推测,这些在“精英存活小鼠”受体组显著升高的细菌就可能是使机体对辐射有抵抗效果的“有益菌”,相反在“精英存活小鼠”受体组显著下降的细菌则可能是“有害菌”。
那么,这些肠道菌群对辐射的影响在人体内是否也成立呢?
作者联合杜克大学以及纪念斯隆-凯特琳癌症中心的实验室,一起进行了一个小型临床研究。
他们收集了一些白血病病人的粪便并进行了16srRNA测序。由于腹泻是放疗之后常见的副作用,他们根据病人腹泻的持续时间,将病人样本分为轻度腹泻和重度腹泻两组。
肠道菌群分析
通过肠道菌群的分析发现,在轻度腹泻病人中,Lachnospiraceae,Enterococcaceae以及Lactobacillaceae这三种在小鼠中可能的“有益菌”数量明显高于重度腹泻的病人。Lachnospiraceae的数量与病人腹泻时间存在显著地负相关性。因此,作者推断在人体中,这些可能的“有益菌”也可以帮助病人降低放疗引起的副作用。
随后,作者挑选了三种可能的“有益菌”,三种可能的“有害菌”以及一种最著名的益生菌 Lactobacillus rhamnosus, 进行了单一菌株的体内实验。
组织学分析
作者发现,Lachnospiraceae对小鼠的保护作用极明显。并且,通过组织学分析,Lachnospiraceae极大地降低了辐射对于造血系统和肠道系统造成的损伤。骨髓和脾脏的组织结构和细胞死亡得到了极大地保护。大肠和小肠的损伤以及肠道渗透性也明显降低。
短链脂肪酸分析
由于Jenny Ting课题组和其他课题组已经报道过,Lachnospiraceae可以产生大量的短链脂肪酸,并且短链脂肪酸是调节机体免疫反应和炎症反应的重要物质,因此,作者检测了三种短链脂肪酸对辐射的影响。
他们发现,在接受了propionate丙酸处理后,小鼠可以有效地抵抗致死剂量辐射带来的造血系统和肠道系统的损伤,生存率也得到了极大的提高。
细胞分析
作者同时检测了骨髓中造血干细胞和祖细胞的比例,发现propionate处理小鼠要远高于对照小鼠。另外,辐射所导致的DNA损伤与活性氧的释放,在propionate处理后也明显降低。
非靶向性代谢组学分析
最后,作者通过非靶向性代谢组学研究发现了一系列的代谢产物在“精英存活小鼠”的粪便中含量显著提高。其中,升高最为明显的是色氨酸代谢通路的成员。作者选取了indole-3-carboxaldehyde (I3A)和kynurenic acid(KYNA)进行了体内验证。两个色氨酸途径代谢产物1H-吲哚-3-甲醛(I3A)和强尿酸(KYNA)在体内提供了长期放射防护。
该研究的发现强调肠道菌群作为宿主抵抗辐射的主要调节剂的关键作用,能够保护造血和胃肠系统。
“精英存活小鼠” 的肠道菌群组成和普通小鼠不同,他们的肠道中含有大量的Lachnospiraceae等“有益菌”。这些“有益菌”通过产生大量的短链脂肪酸和色氨酸代谢通路的代谢产物来促进造血发生以及肠道损伤修复,从而帮组机体抵抗辐射引起的损伤和死亡。
毛螺菌科和肠球菌科,以及以丙酸和色氨酸途径菌群为代表的下游代谢产物,对辐射防护起着重要作用。
这项研究揭示了微生物代谢物轴在产生广泛的抗辐射保护中所起的关键作用,并为治疗辐射暴露的不良副作用提供了有希望的治疗靶标。
Tips
该文做了很多生理,化学,生物代谢和病理等大小20多项实验,包括小鼠实验,辐射处理实验,“dirty-cage sharing”实验,FMT实验,细菌菌种管理实验,SCFA和色氨酸代谢处理实验,病理组织学,肿瘤接种和放射治疗实验,免疫染色和免疫印迹解折,肠通透性检测,骨髓干细胞,肠上皮细胞和肠上皮内淋巴细胞分离,ROS检测,流式细胞仪分析,粪便16S rRNA基因测序分析,气相色谱-质谱检测,非靶向代谢组实验。一篇高水平论文的研究思路和严谨的实验论证过程,值得我们借鉴和学习。
参考文献:
Guo Hao,Chou Wei-Chun,Lai Yunjia et al. Multi-omics analyses of radiation survivors identify radioprotective microbes and metabolites.[J] .Science, 2020, 370

谷禾健康
痘痘,粉刺,酒渣鼻等皮肤问题,困扰着一些爱美的朋友。这关乎到个人形象,甚至有些朋友还会因为这个感到焦虑,社交尴尬,严重影响自信。
为了祛痘,盲目往脸上涂抹太多祛痘护肤产品,正所谓“过犹不及”,涂抹太多,过量,不断刺激皮肤,雪上加霜。


改善皮肤和整体健康的关键,从你的肠道开始。
我们常常说,一个人由内而外散发着美。其实是有科学依据的。
你的肠道和皮肤有很多共同点:
· 都在保护你,不受外界影响。
· 各自都有微生物群,彼此直接交流。
· 都富含肥大细胞,是免疫系统抗病第一线。
· 它们在早期发育过程中来自同一类细胞。
为什么吃的东西会影响你的皮肤?
皮肤与周围的世界相互作用,而胃肠道则处理你吃的、呼吸的和吞咽的一切。你吃的食物经过新陈代谢,食物分解后的副产物会直接进入到你的皮肤。
把皮肤看成是肠道健康的窗口
以下是11种皮肤状况,实际上是从肠道开始的:


看过我们文章的小伙伴都知道,人体肠道中有大量的微生物群。那肠道微生物群是怎么和皮肤进行交流的呢?
这就涉及一个:肠道-皮肤轴。
肠道-皮肤轴是连接肠道及其微生物与皮肤的信号分子网络,跟脑-肠轴类似。
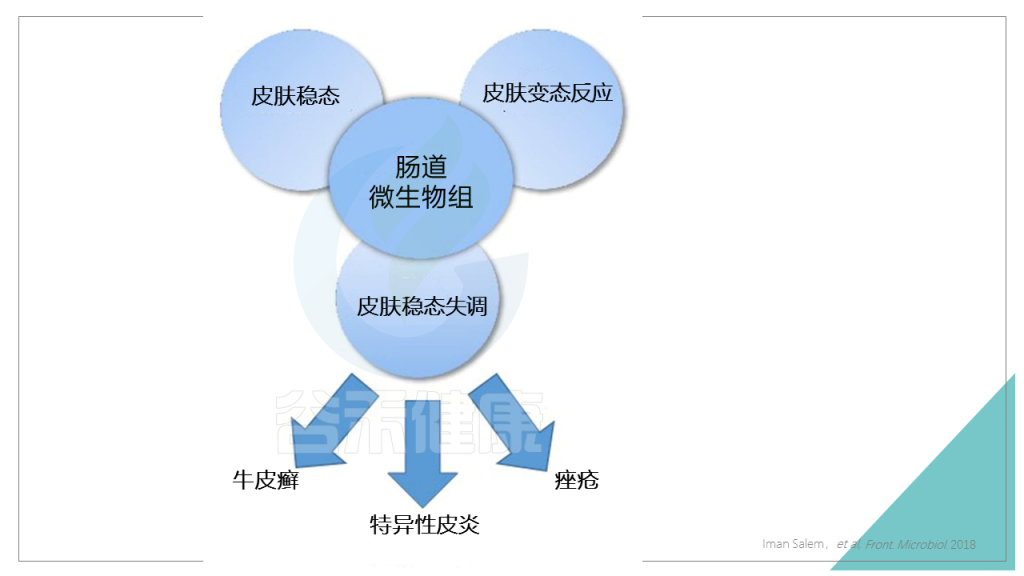

免疫系统、皮肤和大脑之间的沟通是通过微生物来调节的。
炎症—— 大多数疾病的根本原因。
氧化应激—— 炎症的主要原因。
组织脂质水平—— 健康新陈代谢的重要因素。
血糖—— 控制平衡血糖的能力。
神经肽水平—— 一个与你的情绪、疼痛耐受力和身体内环境平衡有关的因素。
致病菌—— 使你生病或引起疾病的坏细菌。
神经递质—— 调节情绪,例如,大约90%的血清素(你的快乐神经递质)是由肠道微生物群产生的。
肠道微生物组与以上协调皮肤稳态的各个途径都有关联,最终影响皮肤健康。
研究发现,痤疮与其说是皮肤的问题,不如说是肠道的问题。
脂多糖(LPS)内毒素是有害的革兰氏阴性菌的组成成分,已被证明对肠道和皮肤造成严重破坏。研究发现,当体内有高水平的脂多糖内毒素时,它们会干扰伤口愈合,使疤痕更严重。
LPS还与寻常痤疮(也就是粉刺)有关,使你更可能对大肠杆菌脂多糖内毒素(E.coli LPS)产生强烈反应。对E.coli LPS有很强的反应性意味着你更可能有纤维蛋白微凝块,这会导致小而疼痛的组织疤痕。
更可怕的是,高水平的脂多糖和大肠杆菌脂多糖会导致肠漏,使细菌进入血液,身体就会出现炎症,表现在皮肤上就是痤疮、粉刺等问题。它还会使你更容易患上肠易激综合征和焦虑症、抑郁症等。
另外,肠道菌群失衡,有害菌大量繁殖,促进炎性物质释放,从而也会引起痤疮等皮肤问题。
特应性皮炎是最常见的慢性瘙痒性炎症性皮肤病。
西方饮食的低纤维和高脂肪含量特征从根本上改变了肠道菌群,导致免疫调节代谢产物特别是短链脂肪酸的产生不足。短链脂肪酸对上皮屏障完整性起重要作用。
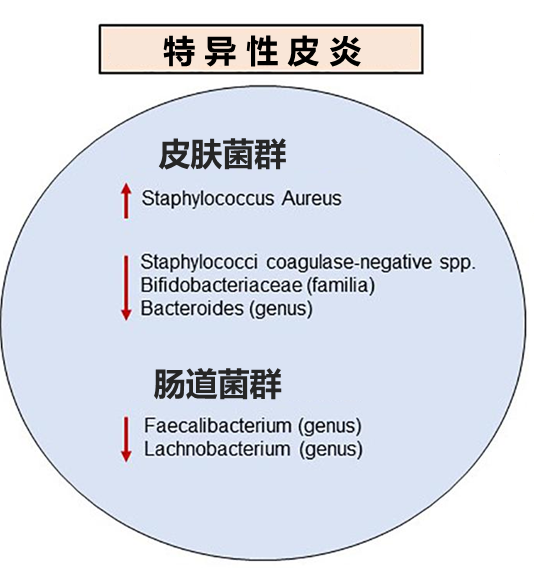
在两项韩国研究中,对特异性皮炎患者粪便样本的宏基因组分析显示,与对照组相比,普氏栖粪杆菌Faecalibacterium prausnitzii显著减少。
关于普氏栖粪杆菌的失调与上皮屏障破坏之间可能存在正反馈回路。肠屏障的破坏,允许消化不良的食物、微生物和毒素进入循环,到达目标组织包括皮肤,触发Th2免疫反应,导致进一步的组织损伤,从而促进该反馈回路。
关于特异性皮炎,更多详见:微生物群对三大过敏性疾病发展的影响
银屑病(俗称牛皮癣),是一种由免疫介导的慢性炎症性皮肤病,病程较长且易复发。
牛皮癣与胃肠道炎症的相关性特别强,7 – 11%的炎症性肠病(IBD)患者被诊断为牛皮癣。
某些共同的遗传和环境因素以及免疫途径在这两种疾病的发病机制中都有牵连。例如,Th17细胞及其细胞因子,已知在牛皮癣的发展中起主要作用,在IBD的病理生理学中也有牵连。
牛皮癣患者肠道菌群特征与IBD患者类似。与健康对照组相比,牛皮癣患者体内普氏栖粪杆菌Faecalibacterium prausnitzii的数量显著减少。
湿疹始于肠道。
当医生和皮肤科医生在寻找皮肤表面的解决方案时,他们忽略了湿疹是由免疫系统过度活跃引起的事实。这种过度活跃的免疫系统通常是肠道微生物群失调的结果。事实上,微生物多样性的下降会导致湿疹发作。
为了缓解湿疹症状,采取措施减少炎症和通过饮食增加微生物多样性是至关重要的。对抗湿疹的饮食需要针对你的微生物群和身体。
乳糜泻乳糜泻是一种常见的慢性疾病。它和皮肤状况密切相关。
患有乳糜泻的人更有可能有:
疱疹样皮炎、脱发、湿疹、
荨麻疹、白癜风、口腔黏膜病变
因为当患有乳糜泻的时候,免疫系统会释放出具有防御性质的抗体,也就是免疫球蛋白,它会在皮肤下面血管集中,导致皮疹的出现。
患有乳糜泻的人往往需要解决肠道的问题。他们有一个优势,就是他们会被引导去寻找与肠道有关的解决方案。
这就意味着,当他们进行无麸质或其他措施来减少乳糜泻的影响时,顺便在不经意间解决了皮肤状况。
至于其他的皮肤问题,往往需要比乳糜泻花更多的时间,才意识到原来肠道是问题的根源。
医生正在发现小肠细菌过度生长(SIBO)患者与酒渣鼻之间有着密切的联系。一些医生甚至报告说,当他们为患者治疗SIBO时,他们多年来的酒渣鼻会突然消失。
这对酒渣鼻患者来说绝对是个好消息。
SIBO是在2004年才被发现,许多人患有酒渣鼻,却不知道问题的根源可能是他们的肠道。现在可能许多人还不知道这一重要的联系。
每个人的肠道微生物组对他们来说都是独一无二的,因此每个人都有不同的适合自己的方法。
这里有些比较普适的建议。
减轻生活压力

持续的压力会对肠道菌群产生负面影响。减少压力时,进行规律饮食,保证良好睡眠,可以适当进行冥想、瑜伽、听音乐等方式,当然改善肠道健康也同样重要。
少吃糖

各种甜食虽然诱人,但还是尽量不要吃太多。糖分会刺激皮脂腺分泌,吃过多会导致皮肤爱出油、出油多自然容易长痘痘、粉刺等。另外,糖可以喂食许多有害菌,当你少吃糖时,提供给有害菌的能量少了,有害菌就会被饿死。
详见:深度解析 | 炎症,肠道菌群以及抗炎饮食 文中除了详细介绍机制外,还有相关的抗炎和促炎食物介绍。
均衡饮食
健康的饮食,最好由多种不同类型的食物组成,包含水果、蔬菜、谷物、肉类等。丰富的食物有利于肠道内不同类型细菌的生长,从而帮助肠道菌群多样性的增加。菌群多样性可能对恢复力起到积极作用,更能抵抗外界刺激引起的微生物群的扰动。
适量锻炼

适量锻炼,但不要太过 。锻炼对肠道微生物组有益,但如果锻炼过多,则无济于事。过度劳累又相当于形成了一种压力,并可能导致微生物失衡。
肠道菌群检测
每个人的肠道菌群都需要独特的饮食。对别人健康的食物可能对你来说并不理想。肠道菌群检测可以是一种工具,来帮你找到最适合你自己的健康食物。
其他方式,详见:
结 语
我们都知道分析问题要有整体观。面对疾病也一样,表面看是皮肤问题,实际可能是肠道的问题。
调理肠道健康,从根本上入手,一些皮肤问题也就迎刃而解了,而皮肤的改善提升颜值,带来的心情愉悦也可以进一步促进健康。
相关阅读:
参考文献:
Guo, Shuhong et al. “Lipopolysaccharide causes an increase in intestinal tight junction permeability in vitro and in vivo by inducing enterocyte membrane expression and localization of TLR-4 and CD14.” The American journal of pathology vol. 182,2 (2013): 375-87. doi:10.1016/j.ajpath.2012.10.014
O’Neill CA, Monteleone G, McLaughlin JT, Paus R. The gut-skin axis in health and disease: A paradigm with therapeutic implications. Bioessays. 2016 Nov;38(11):1167-1176.
Huang R, Wang K, Hu J. Effect of Probiotics on Depression: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. Nutrients. 2016;8(8):483. Published 2016 Aug 6. doi:10.3390/nu8080483
Bowe WP, Logan AC. Acne vulgaris, probiotics and the gut-brain-skin axis – back to the future? Gut Pathog. 2011 Jan 31;3(1):1. doi: 10.1186/1757-4749-3-1. PMID: 21281494; PMCID: PMC3038963.
Caproni M, Bonciolini V, D’Errico A, Antiga E, Fabbri P. Celiac disease and dermatologic manifestations: many skin clue to unfold gluten-sensitive enteropathy. Gastroenterol Res Pract. 2012:952-753.
Parodi A, Paolino S, Greco A, Drago F, Mansi C, Rebora A, Parodi A, Savarino V. Small intestinal bacterial overgrowth in rosacea: clinical effectiveness of its eradication. Clin Gastroenterol Hepatol. 2008 Jul;6(7):759-64.
Wollina U. Microbiome in atopic dermatitis. Clin Cosmet Investig Dermatol. 2017;10:51-56.
Juhlin L, Michaëlsson G. Fibrin microclot formation in patients with acne. Acta Derm Venereol. 1983;63(6):538-40. PMID: 6198846
Yang H, Hu C, Li F, Liang L, Liu L. Effect of lipopolysaccharide on the biological characteristics of human skin fibroblasts and hypertrophic scar tissue formation. IUBMB Life. 2013 Jun;65(6):526-32. doi: 10.1002/iub.1159. Epub 2013 May 7. PMID: 23653386

谷禾健康
焦虑,抑郁,双相情感障碍,这类词越来越多出现在我们的生活。
你也许不知道,饮食可以通过多种途径影响心理健康
即便知道了饮食干预可以改善抑郁,那么如何进行饮食干预呢?
饮食干预措施有好几大类,包括:营养干预措施(例如锌,omega-3脂肪酸);食品干预措施(例如绿茶,橄榄油);全饮食干预措施(例如地中海饮食)
什么样的饮食干预措施有效?
对哪些人有效?
在什么情况下有效?
……
要探索这些问题的答案
就需要了解支持这种关系的关键生物学机制。
将饮食与健康结果相关联的作用机制是复杂的,多方面的,相互作用的,并不局限于任何一种生物途径。
饮食可能影响心理和脑部健康的基本作用机制
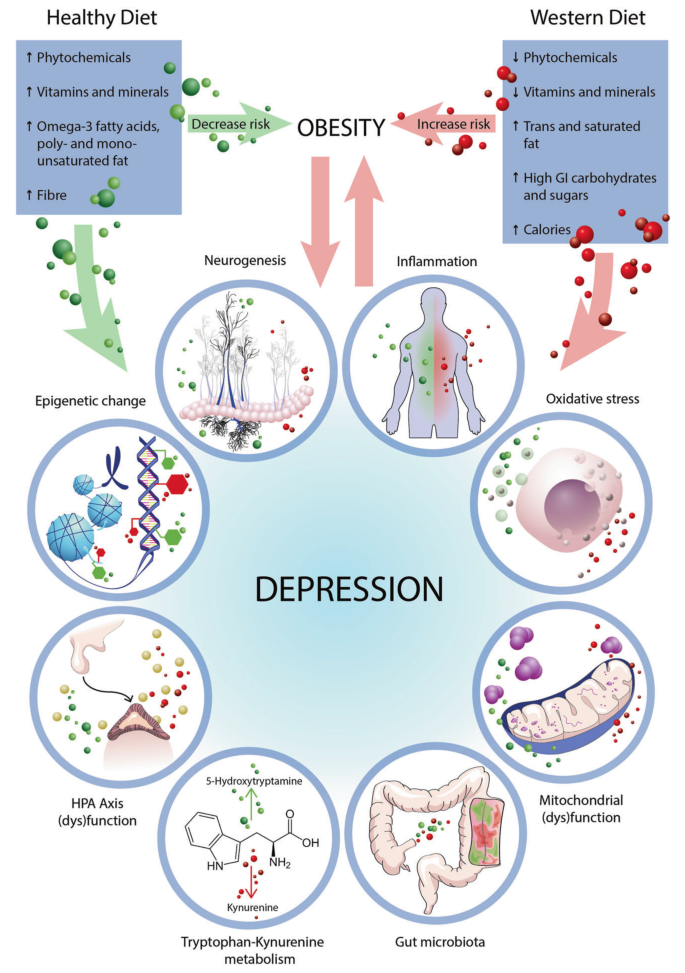
Wolfgang Marx,et al, Mol Psychiatry, 2020
有人说,抑郁和发炎有什么关系?
——大约25%的精神疾病患者(包括情绪障碍和精神分裂症)表现出较高的炎症水平。
炎症反应如何引起的?
免疫系统的这种过度激活是由多种因素引起的。生活中的困境,来自社会的压力,不良生活习惯(吸烟,缺少锻炼)等,都会引起炎症反应增加,从而促进抑郁症状。
典型的炎症反应包括三个主要成分:
炎症诱导剂(例如病原体或与受损相关的分子模式);
检测诱导物的传感器(例如免疫细胞表达的受体);
传感器诱导的炎症介质,包括细胞因子,趋化因子和前列腺素。
一旦被激活,这些炎症分子就可以影响与情绪障碍相关的生理领域,包括神经递质代谢,神经内分泌功能和大脑活动功能等。
抗炎剂可能辅助治疗抑郁症
用于医疗目的的细胞因子给药(如干扰素α注射)可引起情绪和行为的改变,例如情绪低落,疲劳,焦虑,睡眠障碍,快感缺乏和认知功能障碍,所有这些都与抑郁症的症状非常相似。Meta分析得出结论:抗炎剂,如细胞因子抑制剂、非甾体抗炎药和抗生素,包括米诺环素,可能是抑郁症的有效辅助治疗法。
健康饮食的抗炎特性
健康的饮食习惯(和单独的饮食成分)已显示出可能与精神疾病有关的抗炎特性。在慢性代谢疾病人群中进行的纵向观察研究和临床试验均表明,采用健康的饮食方式(例如地中海饮食)可以减少全身性炎症。
最近的研究还证实,患有严重精神疾病的个体比一般人群具有高得多的“饮食炎症”,即,促炎食物(如精制碳水化合物和反式脂肪)的摄入量较高,而抗炎食物的摄入量(主要来源于天然食品和植物)较低。
对纵向研究的Meta分析表明,具有炎性饮食模式的个体随着时间的推移发展为抑郁症的风险更大。
因此,促炎饮食改变为地中海或其他抗炎饮食模式,可能提供一种对抗与精神障碍的发作和严重程度相关的炎症状态的新策略。


抗炎食物
健康的饮食习惯会帮助摄入许多营养成分,可以减轻炎症。其中,蓝莓,可可和姜黄素等存在的植物化学物质(例如多酚)具有很强的抗炎特性,可能有助于治疗多种精神疾病。
Omega-3脂肪酸二十碳五烯酸和二十二碳六烯酸,多不饱和脂肪酸在鲑鱼等海洋食品中含量很高,具有抗炎特性,可以改善并延缓细胞因子诱发的抑郁症的发作。
氧化应激(氧化和抗氧化过程的不平衡)可能导致细胞对脂质,蛋白质和DNA的损伤。
持续的氧化应激是抑郁症和其他精神疾病的一种潜在的作用机制。
抑郁症氧化应激指标升高
对115项研究的Meta分析报告显示,与健康对照组相比,抑郁症患者的氧化应激指标(如丙二醛和8-F2-异前列腺素)升高,而抗氧化剂指标(如总抗氧化剂含量)较低。
此外,据报道抗抑郁药治疗后氧化应激标志物降低,证实了因果关系。一项验尸研究也显示,与健康对照相比,抑郁症、躁郁症和精神分裂症患者大脑中的氧化应激标志物升高。
除了氧化应激对细胞损伤的直接影响外,活性氧和氮的增加会导致线粒体功能障碍、炎症和色氨酸代谢改变,这些都与精神健康障碍有关。
西式饮食增加氧化应激的标志
饮食可以通过剥夺或增加具有抗氧化特性的饮食化合物的供应来加剧和改善氧化应激。动物研究表明,高脂肪西式饮食可以增加氧化应激的标志,如大脑和外周的蛋白质氧化和脂质过氧化反应。
提高膳食质量是可行的干预措施
营养丰富的饮食富含一系列具有直接和间接抗氧化特性的化合物,与氧化应激标志物(如f2 -异前列腺素和血浆氧化低密度脂蛋白)的降低有关。
维生素,例如抗坏血酸(维生素C)和α-生育酚(维生素E)具有直接清除自由基的特性。
营养素(例如硒,锌和半胱氨酸)是抗氧化剂系统(例如谷胱甘肽过氧化物酶和超氧化物歧化酶)的辅助因子。初步证据表明,补充抗氧化剂如n-乙酰半胱氨酸可以改善抑郁症状。
临床前研究表明,多酚还可以通过上调抗氧化防御系统来降低氧化应激,包括诱导核因子红细胞相关因子(Nrf)-2和调节炎症途径核因子κB(NFkB)和有丝分裂激活蛋白激酶(MAPK)。
肠道微生物群是饮食和大脑健康之间潜在的关键中介途径。
大量研究表明,肠道微生物群通过微生物群-肠-脑轴来调节生理过程,包括认知功能,神经精神疾病和行为。动物模型表明饮食、微生物群和与抑郁症相关的机制之间存在直接联系。
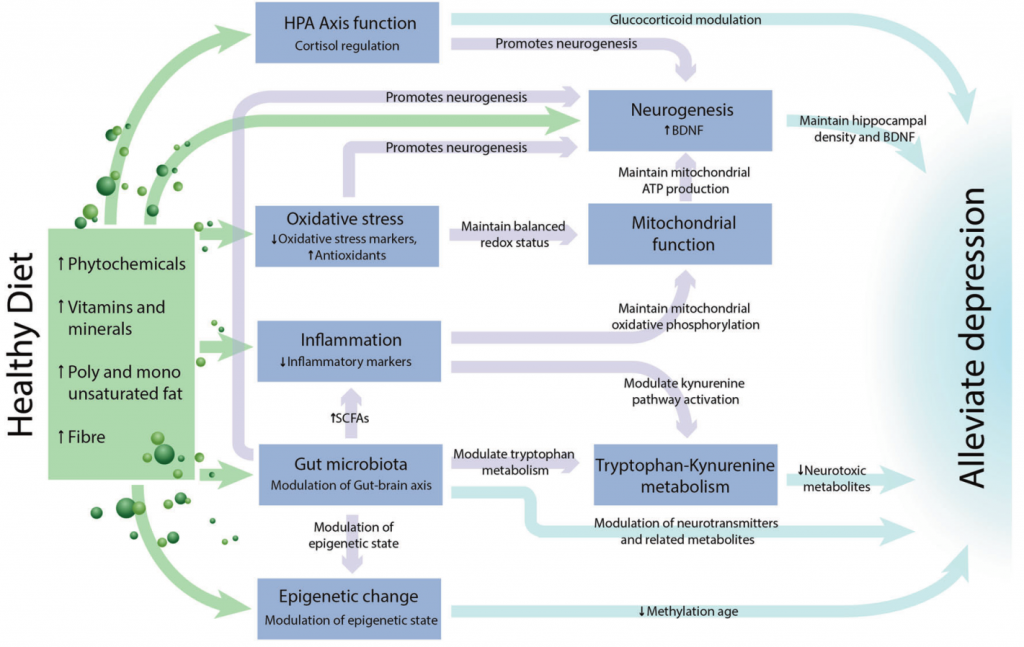

Wolfgang Marx,et al, Mol Psychiatry, 2020
高脂饮食导致焦虑样行为增加,记忆力下降
饮食引起的肠道微生物群的改变会导致行为改变,焦虑和抑郁。例如,在啮齿动物模型中,高脂肪西式饮食导致厚壁菌门/拟杆菌门比例增加,探索行为减少,焦虑样行为增加,记忆力下降。
其他临床前研究表明,高热量饮食会增加梭状芽孢杆菌 Clostridiales,疣微菌科 Ruminococcaceae 和拟杆菌目 Bacteroidales 的丰度,并导致认知灵活性较差,社会和物体识别能力受损。
益生元逆转慢性应激引起的肠道菌群变化
益生元补充剂(低聚果糖和低聚半乳糖)通过防止有益微生物(如双歧杆菌或乳杆菌)的减少,抑制正常的慢性应激诱导的促炎性细胞因子和小鼠的抑郁样行为的出现。
已经提出:肠道微生物群的多种直接和间接途径可以调节大脑功能和行为,包括微生物代谢产物(例如纤维细菌发酵产生的短链脂肪酸),神经元途径(例如迷走神经),神经活性途径(如5-羟色胺等神经递质和神经活性代谢物),下丘脑-垂体-肾上腺(HPA)轴,免疫和内分泌途径以及微生物群的直接神经活性代谢潜能。
饮食模式影响肠道菌群,影响情绪改变行为
短期营养摄入和长期饮食模式都是影响肠道菌群多样性,组成和代谢功能的因素。
迄今为止,只有一项不受控制的饮食干预研究的人类数据表明,富含菊粉的蔬菜饮食增加了双歧杆菌,导致饱腹感和个人能力水平的改善(但在情绪或感知压力方面没有差异)。

类似地,最近的一项研究表明,在老年参与者中,通过1年的地中海饮食干预,菌群变化与认知功能的改善和炎症标志物C反应蛋白和白细胞介素-17的减少有关。
营养素通过直接影响菌群调节大脑健康
例如,由肠道微生物群发酵膳食纤维产生的短链脂肪酸具有重要的免疫调节功能。这种关系也可能是双向的,肠道微生物群参与了这些化合物的生物利用度。
由此,我们可以想到,通过膳食补充剂(益生菌和益生元)和食物(例如发酵食品:泡菜,酸奶和酸菜等)来调节肠道菌群,以此作为调节菌群-肠-脑轴的一种手段。
益生菌和益生元
益生菌和益生元对精神健康影响的证据有限且变化很大。
研究表明,单独乳酸菌或与双歧杆菌联合使用——可能会改善抑郁和焦虑。
但也有Meta分析表明,与对照组相比,补充益生元后的抑郁或焦虑症状没有显著差异。然而,这是在大部分非临床参与者的有限样本(n = 4-5个)中进行的,一般来说,生物干预可能在临床参与者中显示疗效,而不是在非临床参与者中。
发酵食品是另一种具有操纵肠-脑交流的食品
研究表明,食用发酵食品后,有望改善情绪。由于益生菌的生存能力和可变定居能力,这可能解释了物种/菌株及其组合之间的效力不一致;包括各种植物食物来源的饮食模式,可能更有利于促进各种益生元底物和益生菌菌株消耗。

菌群通过食物过敏来介导饮食与大脑健康的联系
自我报告食物过敏在抑郁症患者中更为常见:
抑郁症vs.健康对照(13% vs. 9%)
真正的食物过敏,则饮食中的过敏原会触发胃肠道粘膜中肥大细胞的IgE致敏,导致一系列炎症介质,从而削弱肠道通透性。肠道通透性的提高与革兰氏阴性肠杆菌的易位性增强和免疫激活有关,可能导致全身性炎症,包括神经炎症,这是抑郁症的特征。
需要进一步对真正的食物过敏者进行大规模研究,以阐明其促进抑郁症的发展。对非IgE介导的食物超敏感(即食物不耐受)的研究(如麸质和酪蛋白),也可能揭示饮食诱导的肠道微环境变化如何影响情绪。
HPA轴由大脑(下丘脑),垂体和肾上腺组成,调节糖皮质激素的产生,并与精神疾病的病理生理有关。
超过60%的抑郁症患者表现出过多的皮质醇产生或对HPA系统产生其他干扰,例如对地塞米松抑制试验的反应改变和促肾上腺皮质激素水平降低。在临床恢复后,观察到HPA轴活性改变的一些指标的正常化,表明其在疾病病理生理学中发挥作用。
此外,儿童早期创伤可能会导致HPA轴永久失调,从而导致整个生命周期内出现精神疾病的风险增加。例如,与母亲分离的动物改变了HPA轴,从而表现出对成年期压力和记忆力障碍的反应。
营养素(例如维生素C)的临床干预试验报告显示,皮质醇对急性反应性降低健康成年人的生理压力。
Omega-3脂肪酸干预研究还表明,健康成年人和抑郁症患者的皮质醇水平都有改善。
同样,使用富含多酚的食物(如石榴汁和黑巧克力)进行的干预研究也报告了健康个体皮质醇水平的降低。


这种影响可能是通过心理应激后对下丘脑激活的促炎反应的调节而介导的。由于肠脑轴在心理健康中的新角色,益生菌也已被研究为针对HPA轴的潜在干预措施。
在健康成年人中进行的初步临床干预研究证实了这些结果。例如,在一项双盲,随机,对照试验中,与安慰剂相比,在健康个体中,多菌株益生菌干预24小时无尿皮质醇和自我报告的应激改善的结果。但在一项针对60名抑郁症患者的类似益生菌临床试验中,两组之间的血液皮质醇水平无显著差异。
成年海马体的神经发生水平与认知和情绪直接相关。
抑郁症患者的血清BDNF水平降低。
海马体是边缘系统的关键组成部分,在学习,记忆形成和情绪中起着核心作用。
啮齿类动物功能研究表明,成年海马体的神经发生水平与认知和情绪直接相关。例如,在小鼠中,海马神经发生水平增加与学习和记忆能力的改善有关,而海马神经元的减少通常与抑郁症某些方面行为有关。
BDNF(脑源性神经营养因子)是一种神经营养蛋白,在海马体中高度表达,并参与关键的细胞功能
确实,BDNF是典型的分子,可以解释饮食,运动和抗抑郁疗法对抑郁症和焦虑症行为的作用。重型抑郁症患者的血清BDNF水平降低,而BDNF对抑郁症发病机制的保护作用已获得了一些实验性支持。
证据表明,可以通过饮食调节BDNF和成人海马神经发生的调控。动物模型表明,高脂肪和高糖的西式饮食会损害神经发生并降低海马体内的BDNF水平,并对认知能力产生不利影响。
在动物模型中的大量研究表明,饮食成分(例如omega-3脂肪酸,益生菌和维生素)的有益作用。在精神病理,衰老和疾病的情况下,诸如白藜芦醇,蓝莓,绿茶,姜黄素和可可等多种多酚化合物,也已被证明可以逆转不良变化并保持成年海马神经发生的完整性。

此外,动物模型表明,其他饮食指标(包括卡路里摄入,进餐频率和进餐质地)可能会调节海马神经发生水平。
观察性研究提供了进一步的证据,表明健康的饮食习惯与较大的海马体积之间存在直接的联系,而不受多种解释因素(例如年龄,性别,教育程度)的影响。其他饮食范例,例如通过持续减少每日总食物摄入量或间歇性禁食(例如,每隔一天进食)来限制热量,也可能影响BDNF的表达。
最近的人类干预研究表明,西式饮食会损害海马依赖性学习和记忆能力。
当然,也可以通过本文中提到的其他途径,例如通过肠道菌群和炎症途径来调节神经发生。
色氨酸的主要生理途径是沿着犬尿氨酸途径,它会产生神经毒性的喹诺林酸和神经保护性的神经氨酸。
色氨酸是饮食中必须提供的一种必需氨基酸,是许多关键神经活性分子的重要组成部分。
在精神病学中,对色氨酸的可用性和代谢的关注主要集中在其转化为血清素,血清素是绝大多数抗抑郁药和一线抗焦虑药的治疗目标。
然而,色氨酸的主要生理途径是犬尿氨酸途径,它会产生神经毒性的喹诺林酸和神经保护性的神经氨酸。人们越来越多认识到导致犬尿氨酸产生增加的外周机制的重要性,并且认识到沿该途径产生的代谢物是一系列神经和精神疾病的重要神经生物学介质,包括但不限于抑郁症和精神分裂症。
此外,这种代谢级联反应的启动可能是由于压力或免疫系统和炎症途径的激活。这使得色氨酸在这一途径上的代谢可用性成为心理健康管理中的一个重要考虑因素。
我们日常生活中很多食物都含有色氨酸,包括鸡肉,金枪鱼,燕麦,花生,香蕉,牛奶,奶酪和巧克力。


尽管大部分来自摄入蛋白质的色氨酸都在小肠中吸收,但也还有大量可能到达结肠,肠道菌群在其命运和活动中起着关键作用。
在使用饮食干预措施进行心理健康预防和治疗的背景下,了解色氨酸的可用性和新陈代谢可能很重要。例如,增加的蛋白质摄入量可导致色氨酸的利用率增加,碳水化合物摄入量的变化会影响游离色氨酸的水平,非酯化脂肪酸可从生理上置换白蛋白中的色氨酸。
与色氨酸竞争通过血脑屏障运输的其他氨基酸的可用性波动也会影响中枢神经系统的代谢库。已经尝试了直接补充色氨酸作为抑郁症患者的一种干预措施,以改善血清素能信号传导。
还有一个研究调查了饮食干预通过其他方式调节尿氨酸代谢的作用,包括调节吲哚胺2,3双加氧酶(IDO)活性。体外和动物模型已经报道了个别的饮食成分,如姜黄素和绿茶,以及饮食方案,包括生酮饮食和禁食来调节尿氨酸途径的活性。
初步干预研究还表明,饮食方案,如热量限制和个人饮食成分,包括益生菌干预、白藜芦醇和红茶可能会调节尿氨酸代谢。例如,在最近一项针对60名抑郁症患者的试验中,与安慰剂相比,益生菌干预显著降低了尿氨酸水平,增加了3-羟基尿氨酸水平。
抑郁症的许多核心症状,如疲劳和认知障碍,都与中枢和外周线粒体功能障碍和生物发生减少相一致。
抑郁症和其他原发性精神疾病,包括双相情感障碍和精神分裂症一样,与线粒体功能障碍有关。
氧化磷酸化的破坏和线粒体ATP生成的受损可能导致神经可塑性失调和神经发生的减少,这两者都是抑郁症神经生物学的核心要素。
最近的一项研究显示,小鼠的线粒体移植恢复了海马体的ATP生成,逆转了脂多糖诱导的抑郁症模型,这一新证据支持了抑郁症的病理生理学因素。
大量临床前证据表明,不良饮食可能导致线粒体功能障碍。高脂饮食与线粒体生物发生异常有关,也与自由基生成增加、炎症和胰岛素抵抗有关。
高热量高碳水化合物饮食和高盐饮食有相似的作用,这些都是劣质西式饮食的核心成分。也有可能是由不良饮食引起的线粒体功能障碍的跨代遗传。在人类中,关于热量限制对线粒体功能的潜在有益影响,有不同的数据。
一些人类研究表明,限制热量的线粒体生物发生的标记物增加。
另一项研究显示,柠檬酸合成酶(一种线粒体含量的标志物)水平的提高和其他动物研究表明线粒体解偶联蛋白活性增强。到目前为止,还没有关于抑郁症患者热量限制的研究来测量线粒体功能障碍。


生酮饮食
有人提出了一种饮食模式来逆转线粒体功能障碍,特别是抑郁症患者从有氧到糖酵解能量的转变,就是生酮饮食。尽管在人类身上评估这一假设的临床试验仍在等待。生酮饮食增加线粒体解偶联蛋白的活性和水平。
注:生酮饮食(ketogenic-diet,简称KD)是一个超低碳,高脂肪饮食法。主要原理是用脂肪来替换碳水化合物,身体消耗完葡萄糖后,慢慢开始燃烧脂肪,给自己身体供能,身体慢慢进入生酮状态,最终,让身体进入一个高速燃脂的状态。
线粒体生物发生的改变在多大程度上介导了健康地中海饮食对抑郁症的有益影响尚不清楚。一些食物衍生物也有增加线粒体生物发生的假定作用,槲皮素,n -乙酰半胱氨酸和白藜芦醇都有一些支持的证据。
表观遗传过程可以影响DNA甲基化年龄,这与成年人的抑郁症有关以及许多其他神经发育结局和合并症,包括认知功能,酒精依赖,躁郁症和减少的海马体积,但不减少精神分裂症。
表观遗传学描述了在不改变基础DNA序列的情况下控制基因活性并使发育发生的分子机制。
极少有研究评估营养干预对甲基化年龄的影响,但已有研究发现其降低的证据。表观遗传状态受遗传序列,内部和外部环境以及发育过程中发生的随机过程的影响。产前发育,配子形成和青春期敏感时期的环境影响与患有与抑郁症有共同途径的慢性疾病风险有关,包括心脏代谢和神经发育障碍。这种现象被称为“健康与疾病的发展起源”(DOHaD)。
在DOHaD环境中,营养是对表观遗传学研究最多的环境影响因素。检验荷兰饥荒影响的研究表明,由于早期发育期间的营养不良,表观遗传失调与成人疾病风险有关。
很少有观察性的人类研究评估过表观遗传变化在介导早期营养对神经发育结局的影响中的作用,并且大多数是横断面的。最近的一项综述得出的结论是,有证据表明,某些早期营养摄入(例如母乳喂养和母亲肥胖)会影响表观遗传状态,进而可能介导儿童和青少年的心理病理学,例如内在化和外在化行为。
另外一项研究发现由于蛋白质和能量不足而在婴儿期住院的成年人在神经精神病风险基因中表现出DNA甲基化变化。体外细胞培养实验和啮齿动物研究表明,大量营养素的限制或过量存在对许多不同基因的多种表观遗传机制具有可再现的作用,包括与代谢和行为有关的基因。代谢扰动已成为基因组和表观基因组改变的驱动力,通过饮食,饮食中的影响得以保存在基因中。


营养丰富的饮食成分,包括叶酸,生物素,B6和B12等维生素;多酚,如姜黄素,白藜芦醇和染料木黄酮;脂肪酸和ω-3脂肪酸已通过多种机制影响表观遗传状态。此外,丁酸通常被认为是膳食纤维发酵过程中产生的有益微生物代谢产物,也可以影响宿主细胞的表观遗传状态。
饮食、情绪障碍和肥胖之间的多因素关系是双向和复杂的。Meta分析数据显示,肥胖症的男性和女性患抑郁症的风险增加55%,而抑郁症的个体患肥胖症的风险增加58%。
最近的一篇综述报道了饮食,情绪障碍和肥胖之间关系的几种相互关联的途径。途径包括HPA轴,其异常调节,过度活化以及糖皮质激素的过度合成和分泌与情绪障碍和肥胖症有关。
此外,研究表明接触高脂饮食(包括5-羟色胺和多巴胺)后,参与调节神经系统奖励回路,情绪和饮食摄入的各种神经递质水平降低。
为了减轻与压力有关的焦虑(由于被称为情感饮食和舒适食物的现象),长期压力和HPA轴过度活化可能导致过多食用西式食物和随后的肥胖。
在情绪障碍和肥胖症中都显示较高水平的炎症和相关细胞因子,提示其潜在病因之间存在另一个共同的联系。
在一项横断面研究中,肥胖在抑郁症与炎症标志物(即白介素6和C反应蛋白)之间的介导作用中,推测关系的因果关系是由抑郁症导致肥胖,炎症标志物升高。肥胖的这种发炎作用反过来推动体重增加和高复发率之间的关系。
不过这也说明了,限制热量和减肥饮食可能是减轻炎症状态和抑郁症状的可靠方法。同时,SMILES临床试验的结果表明,为期12周的地中海饮食干预对在没有体重变化的情况下降低临床抑郁症的症状。同样,前瞻性观察性研究反复报道了饮食质量与常见精神障碍之间的关联性证据,这些关联性与体重的测量无关。
性别差异也不能忽视
最近的一项Meta分析表明,饮食干预可能男性比女性受益。进一步的Meta分析显示,肥胖降低了男性患抑郁症的风险,而女性则增加了风险。可能有许多生物行为机制负责这种潜在的性别特异性效应,需要进一步研究。
首先,女性可能具有更大的改变脂肪或葡萄糖代谢的能力,以应对饮食干预。
其次, 男性在食物选择上更加以快乐为导向(这可能是由于多巴胺受体的差异所致),使得坚持健康饮食变得更加困难。
第三,男人更倾向于与男性气质相关的食物(例如红肉),而不是被认为更“女性化”的水果和蔬菜。
越来越多的证据支持饮食干预作为精神障碍的辅助治疗方法的潜在用途。本文主要讨论了饮食,肥胖和抑郁之间的相互作用(9种途径),当然饮食也可能通过其他慢性疾病影响抑郁,这些疾病通常与抑郁并存,包括糖尿病,代谢综合征和心血管疾病。
营养精神病学领域还处于萌芽状态。现有文献主要是临床前动物研究。还需要进一步的研究来确定可能影响饮食干预措施和饮食习惯的个体因素(例如年龄,BMI,共病),行为(例如改变的动机)和生物学(例如氧化应激,炎症)因素,可能影响治疗反应的因素等。
营养精神病学研究领域的扩展,使人们了解在什么情况下,哪类干预,适合什么人,为精神疾病患者制定新的针对性策略和临床指南,更加个性化地解决每个人的需求。
如果你深陷抑郁,请寻求专业治疗;
如果你朋友抑郁,那么请记得尊重。
相关阅读:
最新研究速递 | 柳叶刀:肠道微生物群在神经系统疾病中的作用
参考文献:
Lassale C, Batty GD, Baghdadli A, Jacka F, Sanchez-Villegas A,Kivimaki M, et al. Healthy dietary indices and risk of depressiveoutcomes: a systematic review and meta-analysis of observational studies. Mol Psychiatry. 2019;24:965–86.
Khalid S, Williams CM, Reynolds SA. Is there an associationbetween diet and depression in children and adolescents? Asystematic review. Br J Nutr. 2016;116:2097–108.
Borge TC, Aase H, Brantsæter AL, Biele G. The importance ofmaternal diet quality during pregnancy on cognitive and behavioural outcomes in children: a systematic review and metaanalysis. BMJ Open. 2017;7:e016777.
Hepgul N, Pariante CM, Baraldi S, Borsini A, Bufalino C,Russell A, et al. Depression and anxiety in patients receivinginterferon-alpha: the role of illness perceptions. J Health Psychol.2018;23:1405–14.
Köhler‐Forsberg O, Lydholm CN, Hjorthøj C, Nordentoft M,Mors O, Benros ME. Efficacy of anti‐inflammatory treatment onmajor depressive disorder or depressive symptoms: meta‐analysis of clinical trials. Acta Psychiatr Scand. 2019;139:404–19.
Rapaport MH, Nierenberg AA, Schettler PJ, Kinkead B, CardoosA, Walker R, et al. Inflammation as a predictive biomarker forresponse to omega-3 fatty acids in major depressive disorder: aproof of concept study. Mol Psychiatry. 2016;21:71–9.
Borsini A, Alboni S, Horowitz MA, Tojo LM, Cannazza G, SuKP, et al. Rescue of IL-1beta-induced reduction of human neurogenesis by omega-3 fatty acids and antidepressants. BrainBehav Immun. 2017;65:230–8.
Reichelt AC, Loughman A, Bernard A, Raipuria M, Abbott KN,Dachtler J, Van TT, Moore RJ. An intermittent hypercaloricdiet alters gut microbiota, prefrontal cortical gene expression andsocial behaviours in rats. Nutritional neuroscience.2020;23:613–27.
Long-Smith C, O’Riordan KJ, Clarke G, Stanton C, Dinan TG,Cryan JF. Microbiota-gut-brain axis: new therapeutic opportunities. Annual review of pharmacology and toxicology. 2020;60(Jan):477–502.
Marx Wolfgang,Lane Melissa,Hockey Meghan et al. Diet and depression: exploring the biological mechanisms of action.[J] .Mol Psychiatry, 2020
Liu RT, Walsh RF, Sheehan AE. Prebiotics and probiotics fordepression and anxiety: a systematic review and meta-analysis ofcontrolled clinical trials. Neuroscience & BiobehavioralReviews. 2019;102(Jul):13–23.71. Aslam H, Green J, Jacka FN, Collier F, Berk M, Pasco J,Dawson SL. Fermented foods, the gut and mental health: amechanistic overview with implications for depression andanxiety. Nutritional neuroscience. 2020;23(Sep):659–71.
Lerner BA, Green PH, Lebwohl B. Going against the grains:gluten-free diets in patients without celiac disease—worthwhileor not? Dig Dis Sci. 2019;64:1740–7.

谷禾健康
冠心病患者的肠道微生物群存在差异,这已成为共识。 研究表明,肠道微生物群与肥胖、糖尿病、血脂异常和高血压有关,这些都是冠心病的危险因素。肠道微生物群通过其代谢产物参与介导胆固醇代谢、尿酸代谢、氧化应激和炎症反应等基本代谢过程,可诱导动脉粥样硬化和冠心病的发生。 干扰肠道微生物群的组成,补充益生菌和粪便捐赠是潜在预防和治疗冠心病的热门研究领域。
研究表明,肠道菌群与肥胖,糖尿病,血脂异常和高血压有关,它们是冠心病的危险因素。
肠道菌群与肥胖
2004年,Bäckhed等人首先报道了肠道微生物群与肥胖有关,因为他们发现肠道微生物群可以调节实验小鼠的脂肪储存。在人和小鼠中都发现了与肥胖相关的相似的肠道菌群。在肥胖的小鼠和肥胖的人类肠道微生物群中,厚壁菌/拟杆菌比例更高。 他们的结果表明,肥胖患者的微生物组从饮食中获取能量的能力更强。 这一发现进一步证实了肠道菌群与肥胖之间的关系。
目前的研究表明,肠道菌群可能导致肥胖(图1)。 肠道微生物群会发酵宿主无法消化的物质,将其转化为小分子,例如短链脂肪酸(SCFA),并为宿主提供能量。 肠道菌群抑制禁食诱导的脂肪细胞因子(FIAF)的表达,增加脂蛋白脂肪酶的表达,并促进脂肪细胞中甘油三酸酯的储存(乙酰辅酶A羧化酶[ACC]和脂肪酸合成酶[FAS]是关键的调节剂),因此诱发肥胖。肠道菌群还调节内源性大麻素(CB)系统。
CB调节肠的通透性以及肠粘膜中紧密连接蛋白的定植和分布,从而导致肠通透性增强,脂多糖和炎症反应增加,从而导致肥胖。
图1 肠道微生物群对肥胖的影响

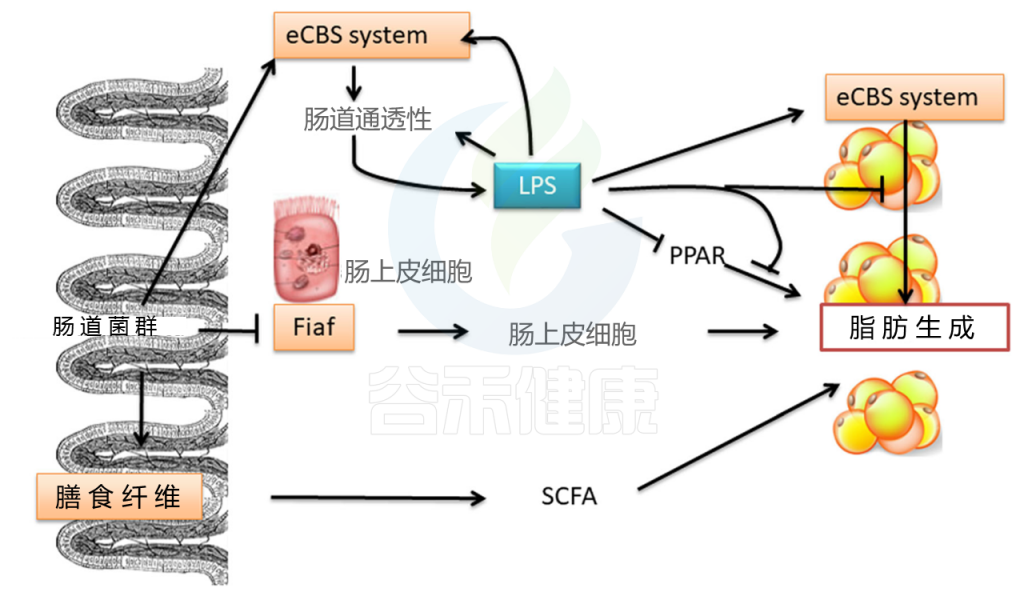
肠道菌群和糖尿病
糖尿病是冠心病的主要危险因素。糖尿病患者的冠心病发病率为55%,是非糖尿病患者的几倍。糖尿病的发病机制与环境因素和宿主遗传有关。 作为重要的环境因素,肠道菌群与糖尿病密切相关。 在人类粪便微生物群的研究中,这些有益细菌与改善胰岛素敏感性和改善糖尿病有关。增加糖尿病风险的细菌是有害的。
对我国345例糖尿病患者肠道微生物DNA的基因组学分析显示,中度菌群失调是2型糖尿病患者正常菌群平衡受到干扰的状态。 为了对2型糖尿病患者的肠道微生物含量进行分析,开展了一个全基因组关联研究(MGWAS),并根据shotgun法对来自345位中国人的肠道微生物DNA进行了两阶段的MGWAS分析。 此外,共生丁酸产生菌数量减少,而条件致病菌的数量增加。
对145名欧洲糖尿病女性的肠道菌群进行的研究也得出了相似的结果:产生丁酸的梭状芽孢杆菌数量减少,而乳酸杆菌属和链球菌属增加。
普氏菌(Prevotella copri)和普通拟杆菌(Bacteroides vulgatus)是支链氨基酸合成与胰岛素抵抗之间联系的驱动因素。 胰岛素抵抗者的血清代谢组的特征是支链氨基酸(BCAAs)含量升高,已证明Prevotella copri可以诱导胰岛素抵抗,加重葡萄糖耐量和增加小鼠BCAA的循环水平。普通拟杆菌可以引起胰岛素抵抗并增加循环支链氨基酸水平,从而介导糖尿病。 许多研究表明,肠道菌群通过影响胰岛素抵抗和胰岛素分泌失调来促进糖尿病(图2)。
图2 肠道微生物群对糖尿病的影响
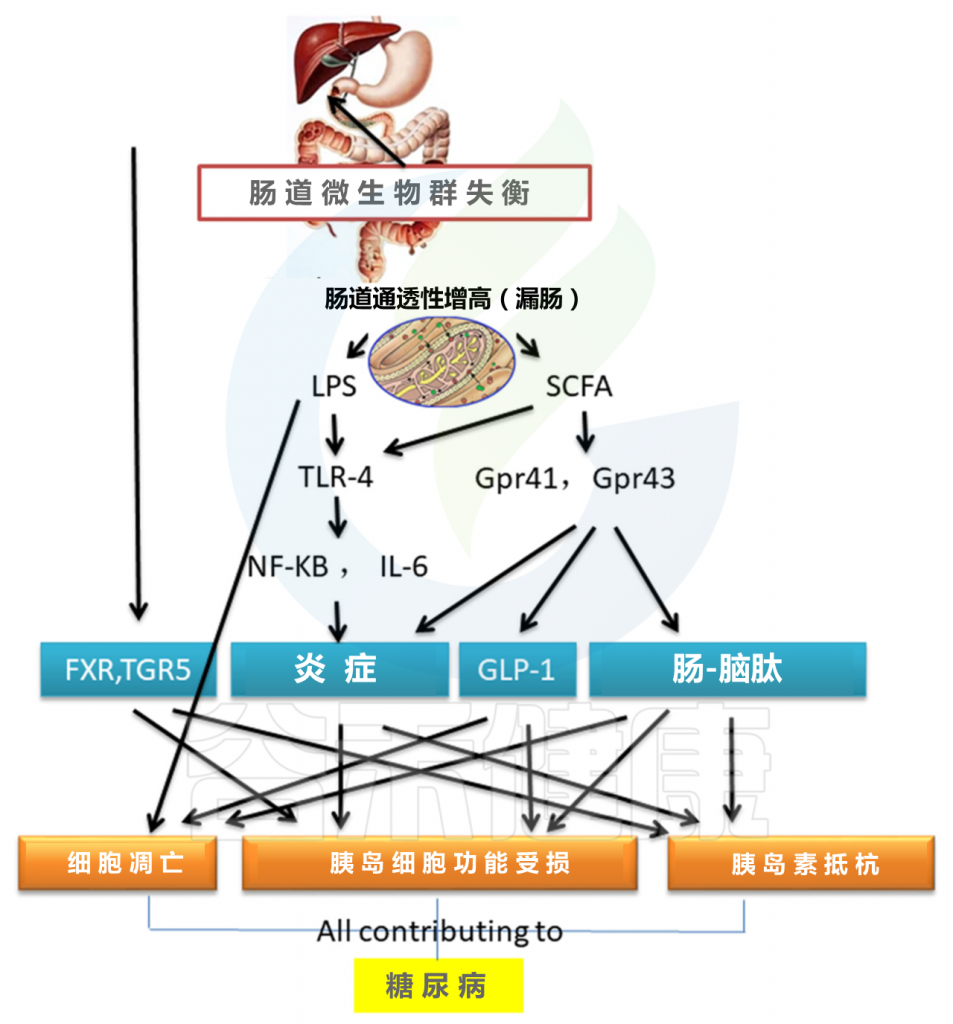

肠道菌群与2型糖尿病之间的重要联系是Toll样受体(TLR)。 肠道菌群的变化通过调节TLR4参与胰岛素抵抗诱导的肥胖。 来自肠道菌群的脂多糖(LPS)通过肠道吸收进入血液循环,这一过程称为代谢性内毒素血症。TLR4缺失对胰岛素抵抗的保护作用与其对代谢性内毒素血症信号转导的抑制有关 。LPS可以促进胰岛B细胞的凋亡并减少胰岛素分泌。
肠道菌群失衡会导致短链脂肪酸(SCFA)失调,这在调节肠道菌群,维持体液平衡,为肠上皮提供能量,抑制炎症因子形成以及促进肠黏膜修复方面起着重要的作用。增加的SCFA可以诱导TLR4信使RNA表达显着增加,并增强NF-κB与白介素(IL)-6结合。
SCFA与G蛋白偶联受体41/43结合也可影响抗炎和脑肠肽激素分泌功能,导致胰岛素抵抗和胰岛细胞功能障碍,并导致胰岛素样生长因子-1(GLP-1)分泌障碍(例如GLP-1可降低血糖和胰岛细胞凋亡)。
此外,肠道菌群的结构和体内稳态的变化会改变胆汁酸的转化,从而导致异常的TGR5和法尼醇X受体(FXR)信号通路。 这种变化会导致代谢紊乱,最终导致糖尿病。
肠道菌群和血脂异常
血脂异常与冠心病密切相关。饮食,肥胖,激素,基因和其他因素会导致血脂异常。
肠道菌群的生理和代谢活动对于调节和维持人类平衡的脂质代谢至关重要。厚壁菌和拟杆菌属是影响血脂改变的主要细菌菌群。 肠道菌群的脂质代谢产物(例如胆碱,三甲胺氧化物[TMAO]和甜菜碱)会促进动脉粥样硬化并增加患心血管疾病的风险。肠道菌群会影响血清甘油三酯和高密度脂蛋白胆固醇的转化。
三种机制很可能导致血脂异常。
首先,肠道菌群产生胆汁盐羟化酶,将结合的胆汁酸转化为二级游离胆汁酸。二级游离胆汁酸可通过G蛋白偶联受体调节肝脏和脂质的代谢,肠道菌群紊乱可导致胆汁酸分泌异常,从而引起血脂异常。
其次,肠道菌群将胆碱和肉碱从宿主转化为三甲胺(TMA),而TMA在肝脏中转化为TMAO。 TMAO可通过影响胆固醇的运输和代谢以及胆汁酸水平而引起血脂异常和动脉粥样硬化斑块。
第三,SCFAs可以抑制肝脏脂肪合成酶的活性,调节血液和肝脏中胆固醇的分布,从而在降低血清3-酰基甘油和胆固醇水平方面发挥作用。
细菌异常会导致SCFA分泌不足和血脂异常。 益生菌可以降低血清胆固醇并增加高密度脂蛋白含量,这表明正常的肠道菌群间接地参与了血脂水平的降低。
肠道菌群与高血压的关系
高血压是导致心血管疾病的关键因素。 本研究表明,除了公认的高血压病因(例如交感神经系统过度活跃,肾素-血管紧张素-醛固酮系统活化以及水和钠潴留),肠道菌群也与高血压密切相关(图3)。
图3 肠道微生物群对高血压的影响
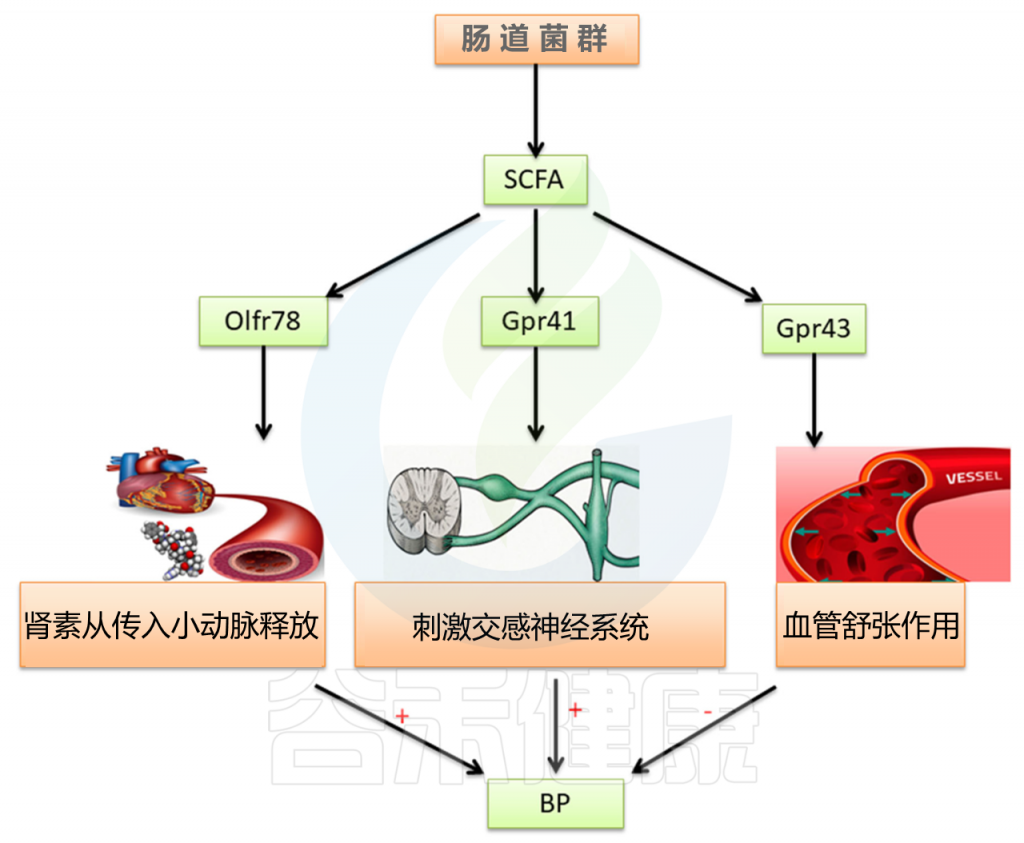

对原发性高血压大鼠粪便细菌的分析表明,细菌数量和多样性明显降低。厚壁菌和拟杆菌的比例增加,SCFA产量降低。
SCFA可通过与嗅觉受体78(OLFR78),G蛋白偶联受体41(GPR41)和G蛋白偶联受体43(GPR43)结合来调节血压。
SCFA在维持肠上皮屏障功能中发挥作用。它们可以减少炎症反应,直接影响免疫细胞,减少交感神经活动,从而改善高血压。 此外,一项研究还报道了肠道菌群可以影响血管活性激素(如5-羟色胺,多巴胺和去甲肾上腺素)的形成,从而在调节血压中发挥作用。
最近的一项临床研究对高血压患者的粪便菌群进行了分析,并发现了类似的结果。普雷沃氏菌和克雷伯氏菌的比例显著增加。将健康对照组和高血压组的肠道菌群移植到GF小鼠体内。用高血压患者粪便细菌移植治疗的小鼠血压显著升高。这表明肠道微生物群与宿主的血压有关,并进一步证实不平衡的肠道微生物群是高血压的重要致病因素。
肠道微生物群参与调节基本代谢过程,如胆固醇代谢、尿酸代谢、氧化应激和炎症反应,通过其代谢物,可导致动脉粥样硬化和冠心病的发展。
冠心病患者肠道菌群的变化
在2012年,Karlssion等人使用全基因组测序来确定肠道菌群变化与动脉粥样硬化性心脏病之间的可能联系。与健康人群相比,Collinsella菌的数量增加,而 Rothia 和 Eubacterium 菌数量减少。 使用宏基因组技术进行的进一步功能分析表明,冠心病患者肠道菌群中编码肽聚糖合成的基因增加,而编码八氢番茄红素去饱和酶的基因(与血清中β-胡萝卜素减少相关)减少。
2016年,Emoto等人使用末端限制性片段长度多态性(T-RFLP)和16S rRNA来研究冠心病患者和健康志愿者之间肠道菌群的差异。结果表明,在冠心病患者中,成熟的乳杆菌数量显着增加,而拟杆菌(双歧杆菌和普氏杆菌)显着下降。此外,厚壁菌/拟杆菌的比例明显增加。 该研究还发现,不使用抗生素的冠心病患者肠道菌群中乳酸菌的比例显着增加,而拟杆菌的比例显着下降。
2017年,这些作者在两项临床试验中再次验证了这些结果。首次将肠道菌群结构的变化直接鉴定为冠心病的诊断标记。
TMAO在冠心病中的作用
肠道菌群产生的代谢性TMAO是心血管疾病的关键机制(图4)。 食物中的胆碱(例如,磷脂酰胆碱,胆碱,L-肉碱和其他三甲胺[TMA])通过肠道微生物酶复合物来产生TMA。 然后TMA进入门静脉循环,并被宿主的肝酶进一步代谢,从而产生TMAO。
图4 TMAO对冠心病的影响
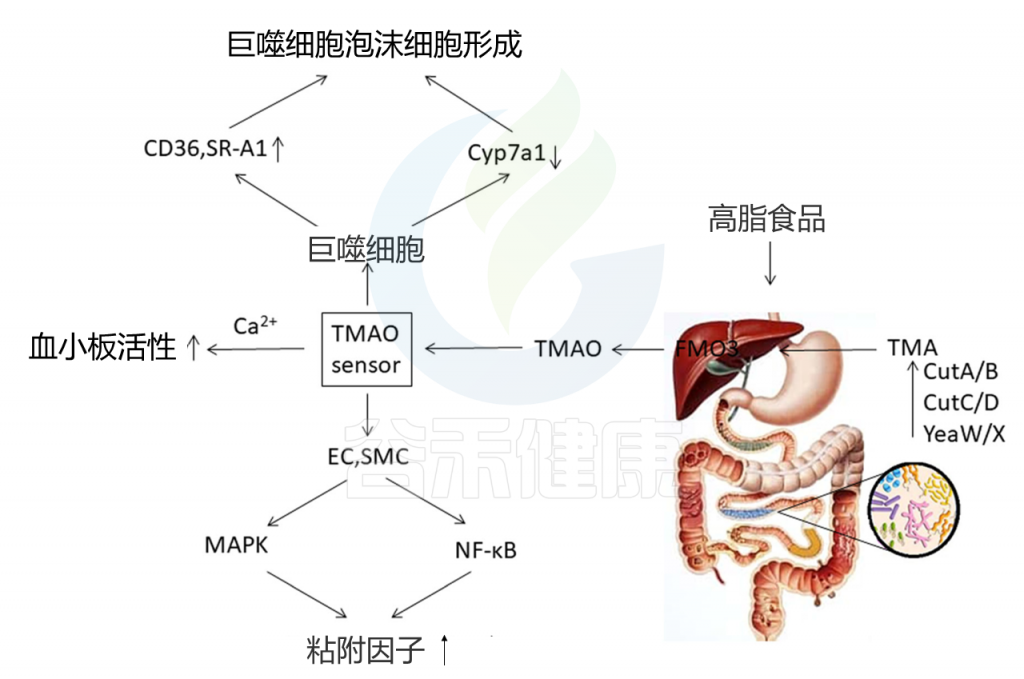

当前的研究表明,血浆TMAO水平与冠心病风险高度相关。临床研究还表明,TMAO增加了患心血管疾病的风险,并增加了急性心肌梗塞,心源性休克和死亡的发生率。
一项为期3年的研究(涉及4007名参与者)进行了选择性冠状动脉造影术。 结果表明,空腹血浆TMAO水平在独立于传统心血管危险因素的心脏事件预测中发挥作用。 这项研究表明,最高四分位数患者中,TMAO水平较高的患者恶性心脏事件的发生率比最低四分位数患者高2.5倍。 而且,TMAO的风险比显着高于低密度脂蛋白的风险比。校正传统的危险因素和肾功能后,TMAO水平仍是恶性心血管事件的独立预测因子。
Cyp7al是胆汁酸合成中的主要酶。Cyp7al的表达上调可以帮助扩大胆汁酸库,增加胆固醇的运输,并最终减少动脉粥样斑块的形成。TMAO可以降低Cyp7al的表达,抑制胆固醇的运输,引起胆固醇在细胞中的积累,并导致形成泡沫细胞。
TMAO还可以诱导血小板反应过度,因此成为动脉粥样硬化的危险因素。 TMAO与血小板之间的相互作用可能通过改变血小板依赖性钙信号传导而促进血小板高反应性并增强体内血栓形成。据报道血小板高反应性是心血管事件的危险因素。
最近的证据表明,TMAO可以在数分钟内迅速向细胞发送信号。 在内皮或平滑肌细胞中,TMAO可以迅速诱导丝裂原活化的蛋白激酶和NF-κB活化,并引起下游粘附分子的上调。 TMAO水平升高还与SMAD 3 蛋白的磷酸化增加有关。 SMAD 3是转化生长因子β(TGF-beta)途径中的关键信号。 在动物模型中,TMAO促进血管炎症并诱导主动脉内皮细胞活化和粘附蛋白上调。这些作用都是急性冠状动脉综合征的关键机制。
肠道菌群通过尿酸对冠心病的作用
血清尿酸水平可能是冠心病的独立危险因素。 尿酸在体内具有氧化特性。 血尿酸水平升高会导致血尿酸增加氧自由基,氧化应激,血管内皮功能障碍,炎症反应以及动脉粥样硬化的发展。
肠道菌群通过调节尿酸代谢来影响氧化应激过程。 大肠杆菌含量越高,尿酸分解越多。 冠心病患者血清尿酸水平升高与肠道菌群功能障碍有关。高尿酸血症也是动脉粥样硬化的危险因素。血清尿酸水平升高会增加氧自由基的产生,引起氧化应激,并引起内皮功能障碍。UA水平与循环类胡萝卜素成负相关。
与年龄,性别,总能量,蛋白质和维生素摄入量无关,循环尿酸水平与总类胡萝卜素(尤其是α-胡萝卜素,番茄红素,叶黄素,玉米黄质和硒)呈负相关。 类胡萝卜素作为抗氧化剂,具有抗心绞痛的作用。一项研究分析了动脉粥样硬化患者和正常对照组的肠道菌群结构,发现动脉粥样硬化患者的肠道菌群富含编码肽聚糖生物合成的基因,而正常对照组的肠道菌群富含类胡萝卜素编码基因。肠道微生物疾病会导致含有合成类胡萝卜素基因的细菌减少,从而降低血液中的类胡萝卜素水平并削弱抗氧化作用,从而促进动脉粥样硬化的发展。
肠道菌群失衡与冠心病的发病机制有关。 这是一种有效的靶向疗法,但缺乏与冠心病和心肌梗塞患者干预相关的数据。 Lam等人使用抗生素抑制肠道菌群,并观察这些变化对急性心肌梗死(AMI)小鼠预后的影响。 研究结果表明肠道菌群变化与心肌梗死之间存在联系,并证明益生菌补充剂可以减少心肌梗死率。 Gan等研究了给予益生菌以减轻心肌梗塞后心肌肥大的小鼠。作者确定,干扰肠道菌群结构并改善急性心肌梗死的预后可能成为AMI的新疗法。
在当前的临床实践中,益生元和益生菌是调节肠道菌群失衡的主要治疗工具。 为了确定益生菌是否可以改变心肌梗塞后患者的预后,研究人员建立了大鼠心肌梗死模型,并在大鼠饮用水中随机给予GR-1或安慰剂和益生菌。 16S rRNA用于对大鼠盲肠微生物组成进行测序,两组之间无明显差异。 但是,心钠素的基因表达有所不同。接受GR-1的动物的左心室肥厚较轻,血液动力学参数更好。 停止使用益生菌后的四个星期,两组仍然存在差异,这表明在治疗结束后GR-1的作用仍然存在。
益生菌可以用作预防冠心病和改善心肌梗死患者预后的潜在疗法。 益生元作为发酵底物,可以增强有益肠道菌群的活性,并有效改善血糖控制和血浆脂质分布。此外,益生元还可以改善肠道通透性,减少代谢性内毒素血症,减轻炎症,缓解糖尿病患者对葡萄糖不耐的症状。
研究人员认为,粪便捐赠是一种治疗由于微生物引起的肠外疾病的新疗法。研究表明,健康人向代谢综合征男性患者捐赠粪便样本后,在6周后就会增加胰岛素敏感性和丁酸水平。 但是,该研究并未证实改善肠道菌群结构是否可以预防冠状动脉粥样硬化或降低AMI发生率。 需要大样本的前瞻性队列研究来进一步探讨肠道菌群与冠心病之间是否存在因果关系。
最近,研究人员发现DMB可以抑制TMA的产生。 抑制TMA的产生可降低小鼠的TMAO水平和动脉粥样硬化斑块形成,且无不良反应。 此外,在一些天然安全食品中也富含DMB,例如醋,红酒,初榨橄榄油和葡萄籽。因此,可以通过食用DMB胆碱来调节潜在的动脉粥样硬化来防止TMA产生。
本文介绍了肠道菌群与冠心病之间的关系,以及目前对这种关系的研究。 已经达成共识,冠心病患者的肠道菌群存在差异。 无菌小鼠模型和菌群基因组学技术的出现可以帮助确定肠道菌群与冠心病之间的关系,并将肠道菌群研究的准确性提高到菌株水平。
展望未来,早期发现和抑制冠心病发展,并进行干预调节是预防冠心病发展的关键目标。
【参考文献】
Liu Huagang,Zhuang Junli,Tang Peng et al. The Role of the Gut Microbiota in Coronary Heart Disease.[J] .Curr Atheroscler Rep, 2020, 22: 77.
Belkaid Y, Hand TW. Role of the microbiota in immunity and inflammation. Cell. 2014;157(1):121-41.
CM O, K R. Heartbeat: the gut microbiota and heart failure. Heart. 2016;102(11):811 TMAO increases the risk of cardiovascular disease
Richards EM, et al. The gut, its microbiome, and hypertension. Curr Hypertens Rep. 2017;19(4):36
Pedersen HK, Gudmundsdottir V, Nielsen HB, Hyotylainen T, Nielsen T, Jensen BAH, et al. Human gut microbes impact host serum metabolome and insulin sensitivity. Nature. 2016;535(7612):376–81

谷禾健康
辅助化疗可导致约三分之一的女性体重增加,葡萄糖耐量下降和高血压。这些事件的潜在机制尚未定义。这项研究评估了乳腺癌和妇科癌症辅助化疗患者的微生物组与体重增加之间的关联。近日发表在《BMC Medicine》上题为“The intestinal microbiome, weight, and metabolic changes in women treated by adjuvant chemotherapy for breast and gynecological malignancies”的一项小样本研究评估了乳腺癌和妇科癌症辅助化疗患者的微生物组与体重增加之间的关联。
方法:在开始辅助治疗之前招募患者。前瞻性收集有关肿瘤治疗,更年期状态和抗生素使用的数据。如果在研究期间接受抗生素治疗,则将患者排除在外。在治疗前和治疗结束后4-6周测量体重和身高。体重增加定义为体重增加3%或更多。治疗前收集粪便样本。并进行16S rRNA基因可变V4区扩增测序。数据使用QIIME 2进行处理和分析,并使用DADA2通过q2-dada2对读取进行了去噪和聚类。每个样品的读数均> 9300。使用Swiss Webster无菌小鼠进行了患者的粪便移植实验。
结果:招募了33名患者;其中9人增加了基线体重的3.5–10.6%。在治疗后体重增加的妇女的治疗前微生物组的多样性和分类学与对照妇女明显不同。与使用对照妇女的粪便样本进行移植的小鼠相比,从体重增加的患者的样本中进行粪便微生物菌群的移植诱导了无菌小鼠的代谢变化。
结论:肠道化学组的组成及其多样性与乳腺癌和妇科恶性肿瘤辅助化疗后体重增加有关。小鼠FMT实验表明,微生物组介导了化学疗法的不良代谢作用。值得进一步研究微生物组的预测价值,以及其对化疗后体重和代谢变化的作用机理。

图一:化疗后体重增重的妇女的肠道微生物组与对照组妇女的肠道微生物组成不同

图二:对GF小鼠使用化疗后体重会增加的妇女的预处理样本进行FMT,与不会增加体重的妇女的FMT相比,FMT会引起显著体重等指标的变化。

图三 对GF小鼠使用化疗后体重会增加的女性预处理样本的FMT,与不会增加体重的女性(对照)相比,会引起显著的微生物变化。
参考文献:Uzan-Yulzari, A., Morr, M., Tareef-Nabwani, H. et al. The intestinal microbiome, weight, and metabolic changes in women treated by adjuvant chemotherapy for breast and gynecological malignancies. BMC Med 18, 281 (2020). https://doi.org/10.1186/s12916-020-01751-2
谷禾健康
越来越多的证据表明,肠道微生物组会影响大脑的发育和功能。肠脑连接可能是由胃肠道中产生的各种微生物分子介导的,这些微生物分子随后会渗透到许多器官,包括大脑。
动物模型研究确定了从肠道细菌传播到大脑的分子线索,这些线索可能影响神经功能和/或神经发育和神经退行性疾病。
本文描述了已知或疑似神经调节活性的细菌代谢产物,定义了从肠道菌群到大脑的信号传导机制,并讨论了肠道细菌分子可能对特定脑细胞发挥的直接作用。 许多发现是最近才发现的,本“观点”中描述的发现在很大程度上是新颖的,尚待广泛验证。
肠道微生物群(肠道菌群)包含细菌或其他微生物,包括病毒,真菌,原生生物和古细菌,它们永久或短暂地栖息在下胃肠道,特别是小肠和结肠。尤其是结肠,数量最多并且拥有高度动态的代谢活动,微生物与宿主之间的分子不断双向流动,其范围从肠道延伸到整个体内。
这好比一个化学“工厂”,它会影响孕产妇的环境,并在产前使胎儿受到微生物信号的影响。
出生后,肠道菌群迅速建立并在在生命的头两年趋于稳定,从而使宿主与共生微生物之间形成终生且非常密切的关系。个体之间的多样性水平和微生物群的特定成员之间可能存在很大差异,并且可以根据年龄,遗传,健康状况,饮食和生活方式在个体内发生变化。
胃肠道包含许多不同类型的细胞紧密相邻,并且在管腔侧暴露于包含饮食成分和肠道微生物群的外部环境中。肠道组织内含有约70%的人体免疫细胞,不断地采集微生物成分保持体内平衡。
此外还有完全位于肠道组织内的丰富的神经元(108个内在神经元)以及连接肠道与脊髓和大脑的神经元沿着肠道进行密集的神经支配。
迷走神经是肠道与大脑之间的主要神经元连接,包括一束神经元,它们直接在肠道组织(和其他器官)与脑干之间发送和接收信号。这些信息进一步传递到整个大脑。
通过研究比较了传统定植小鼠(也称为特定的无病原体小鼠)与完全没有微生物接触(无菌小鼠)的小鼠,肠道微生物群影响大脑发育和功能的证据开始出现。
未经抗生素治疗的动物表现出神经营养因子水平的改变,例如脑源性神经营养因子(BDNF)以及异常的神经肽和神经递质水平,所有这些反过来可以影响关键的神经发育过程,如神经发生,突触发生,突触成熟和修剪,以及神经活动。
在特定的无病原体和无菌小鼠之间,大脑的总体形态和体积也有所不同,尤其是在杏仁核,海马和丘脑区域,在各种细胞类型的细胞水平上都观察到了形态变化,包括神经元,少突胶质细胞和在无菌和抗生素条件下的小胶质细胞。
微生物暴露还会改变宿主的神经系统状况,并导致信号传导途径发生变化。例如,在无菌和经抗生素处理的小鼠中,下丘脑-垂体-肾上腺轴失调,这会导致糖皮质激素反应过度。
这些下丘脑-垂体-肾上腺轴的变化与一些测试模式中的行为模式有关,这些测试模式对社交活动,焦虑,认知功能和抑郁行为进行了建模。具有某些健康问题和健康对照的个体之间的肠道微生物群不同。肠道微生物群落的失衡与各种神经系统疾病和心理疾病有关,尽管还需要确定其中哪些因果关系是相关的。
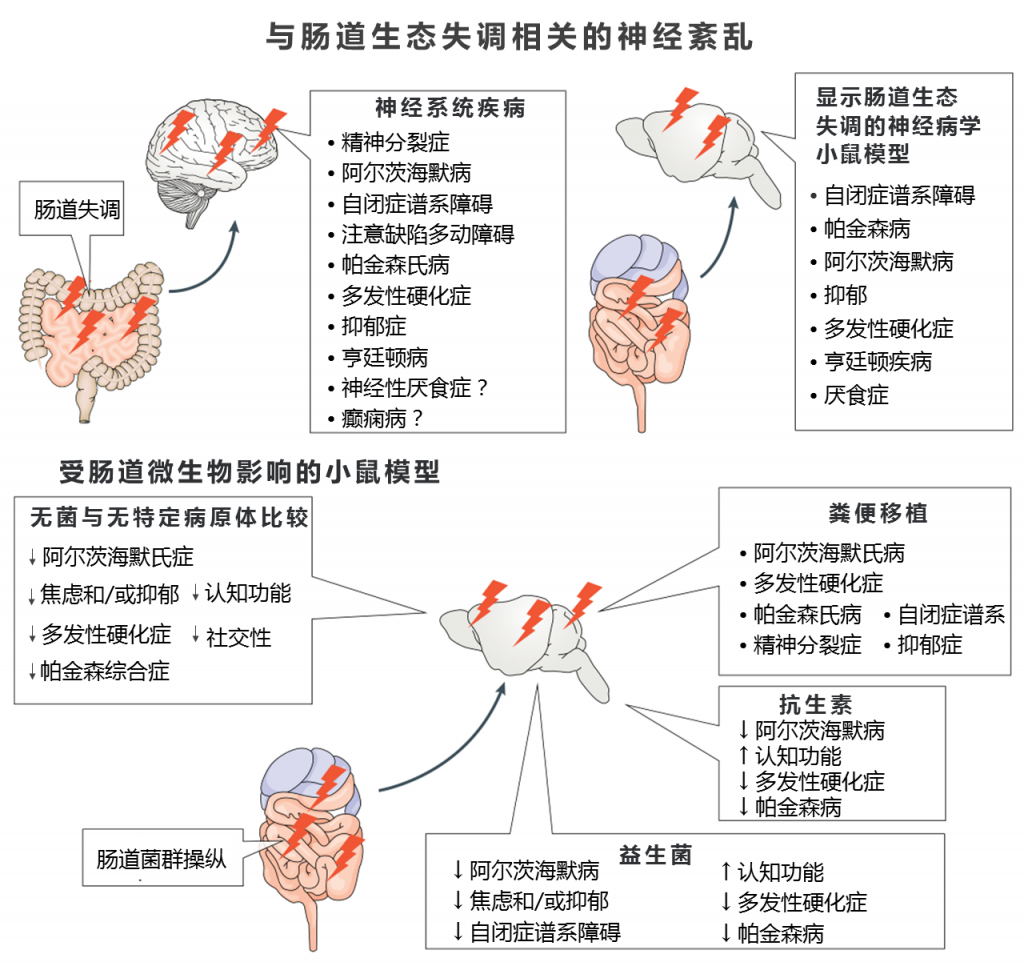

在自闭症,多发性硬化症,焦虑和抑郁症,认知缺陷的小鼠模型中,更成熟的细菌操作(例如用特定细菌治疗或用抗生素消灭细菌)已显示出改善疾病症状的作用。 同样,在帕金森病,自闭症,多发性硬化,焦虑和抑郁的人类模型中,细菌治疗对人脑活动的某些影响已可以通过在功能磁共振成像中观察到变化。 因此,越来越多的证据表明神经系统状态可能会受到肠道微生物及其副产物的影响。
已经描述了改变的微生物组谱与大脑疾病之间的各种关联,并且微生物群或特定细菌物种对行为,认知和神经变性的贡献不断建立。
此外,肠道微生物组具有惊人的遗传多样性,从人类肠道微生物种群中测序出超过2200万个基因,并且拥有庞大的独特酶库,能够产生和修饰多种化学结构基团。 我们基于这些基础发现来描述和概念化化学信息的解码,这些化学信息如何介导肠道-脑轴的观察效应,从而为理解和治疗多种神经系统疾病提供希望。
以下各节将按肠道细菌和微生物代谢产生的生物活性分子(下图)转化的前体来源(从新细菌,宿主或饮食中获取的来源)来描述类别。 还提供了对特定分子作用的简要描述。
肠道菌群代谢物
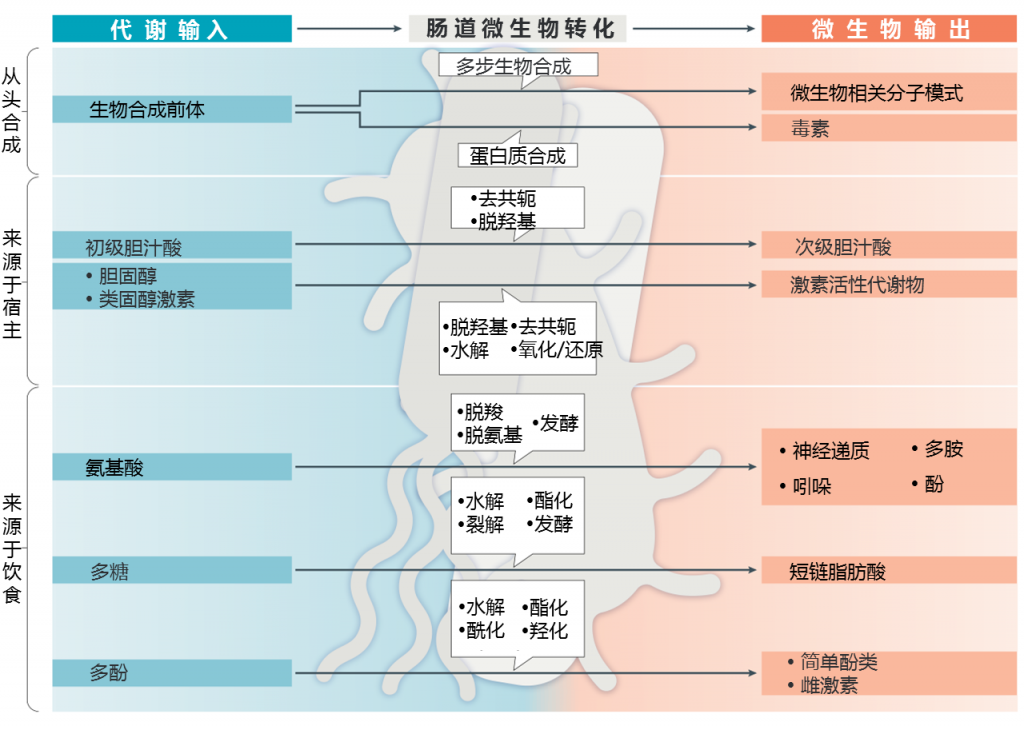

微生物会产生许多蛋白质,维生素和结构成分,这些物质或有益于宿主或对宿主产生负面影响。其中许多是通过多步生物合成途径产生的,而哺乳动物则没有这种途径。这些分子维持细菌功能,例如信号传导,结构成分和能源,尽管有些分子,如蛋白质毒素,主要以其影响宿主系统的作用而为人所知。
微生物相关分子模式(MAMP)
微生物相关的分子模式(MAMP)是微生物细胞保存完好的成分,它们在整个身体中会被宿主(包括脑部)敏锐地发现。MAMPs对所有种类的微生物的结构完整性和基本功能都起着至关重要的作用,是由核苷酸、脂类、碳水化合物和肽等不同化学基团组成的复杂分子。
无菌小鼠中缺乏MAMPs会导致免疫和神经发育不完全,但是如果宿主对MAMPs的反应仍然升高或不受控制,它们的存在会诱发与各种神经系统疾病有关的急性或慢性炎症。
两个主要的细胞表面成分MAMP似乎足以改变大脑发育和功能的是肽聚糖和脂多糖(LPS)。
肽聚糖是几乎所有细菌细胞壁的结构成分,最近被证明可转移到发育中的大脑中,影响基因表达和社会行为。
LPS是革兰氏阴性细菌的另一种普遍存在的表面分子,已在大鼠大脑中与其受体共定位。LPS注射会诱发小鼠疾病行为,认知障碍和急性抑郁样行为,并影响胎儿大脑发育。
此外,在自闭症,抑郁症,帕金森氏病和突触核病模型中,慢性或急性暴露于MAMPs可促进疾病相关症状的发生。
这些保守的微生物分子可能通过免疫介导的途径来调节哺乳动物的行为,它们通过大脑中表达的受体直接感知,或者激活全身炎症和细胞因子的产生,从而导致神经功能的改变、神经元应激或细胞死亡。
MAMPs的存在,结构和免疫调节活性随细菌种类的不同而变化,因此肠道菌群的变化可能会影响宿主对特定MAMPs的暴露水平和反应水平,进而影响后续的健康状况和行为。
毒 素
一些细菌产生的蛋白质毒素会对宿主神经系统产生负面影响。这些毒素在一般结构上通常是相似的,有多个亚基可以激活细胞表面或细胞内受体,并且可以由条件致病菌产生,它们可能在共生菌群中存在很长一段时间而不会在肠道或大脑中引起明显的疾病。
已知几种梭状芽胞杆菌会产生多种毒素,例如致命毒素,毒素B,ε毒素和肠毒素,它们可以通过全身循环到达大脑,破坏并穿过血脑屏障(BBB),抑制神经递质的释放和 /或降低从肠道到海马的目标神经元活力。
Staphylococcus spp.和 Bacillus spp.产生毒素,葡萄球菌肠毒素和蜡样芽孢杆菌毒素Cereulide,刺激迷走神经,向大脑发送信号并诱发呕吐和疾病行为。
其他种类,如沙门氏菌和大肠杆菌产生一类称为淀粉样蛋白的蛋白质,这些蛋白质在肠内聚集,并可能以朊病毒样疾病模式扩散到大脑,并可能导致神经退行性变,例如帕金森氏病和阿尔茨海默氏病。
随着营养物质的吸收和废物的分泌,持续的代谢流量通过肠上皮屏障得以维持。微生物群暴露于许多宿主分子并与其发生化学相互作用。肠道-大脑相互作用证据最多的两类宿主衍生代谢物是胆汁酸和类固醇激素。
胆汁酸
初级胆汁酸是宿主胆固醇代谢的产物,在脂肪代谢和能量代谢中(甚至在大脑中)也起着主要作用。
循环中的胆汁酸可以穿过血脑屏障,并可能直接作用于大脑中的受体,或者通过激活肠受体而具有更间接的作用,导致成纤维细胞生长因子和胰高血糖素样肽1等信号的释放,从而影响多个脑区或迷走神经的神经元活性。
许多肠道细菌物种通过脱水酶的脱羟基作用、氨基酸基团与胆盐水解酶的解偶联作用以及其他酶机制的进一步降解作用,将初级胆汁酸修饰成次级胆汁酸,从而帮助维持胆固醇稳态。
细菌修饰改变了胆汁酸在膜和核受体上的信号传导,并改变了它们的溶解度和循环。
胆汁酸的存在和清除的调节与大脑的正常功能有关,因为这些途径中的缺陷会导致小鼠和人类出现许多神经表型,例如脱髓鞘,运动功能障碍,神经炎症,癫痫发作和学习障碍。
细菌对胆汁酸结合和水平的影响可能正在影响这些脑表型。 例如,在帕金森病,阿尔茨海默病,多发性硬化症,酒精依赖和自闭症的人和小鼠模型研究中已观察到细菌相关胆汁酸水平的改变,已知胆汁酸会影响下丘脑—垂体—肾上腺轴。
实际上,在阿尔茨海默氏病患者的大脑中检测到了细菌产生的所有次级胆汁酸,并且次级胆汁酸比例的增加与它们的认知障碍和大脑影像学改变有关。
一些胆汁酸甚至被用作神经系统疾病的潜在药物,如肌萎缩性侧索硬化症和中风。肠道中细菌的存在会改变整个宿主的胆汁酸水平,肠道菌群中的群落变化会影响胆汁酸的水平和性质。这些变化可能是有利的,也可能是有害的。
胆汁酸的微生物代谢与潜在神经功能之间已知的最机械的联系可能是微生物群直接增加的脱氧胆酸水平足以诱导肠道肠嗜铬细胞中主要神经递质血清素的产生。
肠道5-羟色胺水平可能以未知的方式影响大脑功能,因为海马体中5-羟色胺的水平受小鼠微生物群的影响,但尚不清楚肠道与大脑5-羟色胺水平之间的任何进一步联系。 生物对胆汁酸的操作与脑功能之间的因果关系仍有待明确定义。
类固醇激素
类固醇激素信号对于正确的大脑结构发育,认知,记忆,决策和性行为至关重要,并且在防止社交孤立和抑郁样表型中起着重要作用。 每天产生的这些激素中,有多达15%在肠道中可以检测到,因为它们在体内循环,使它们与微生物群接触。
肠道菌群可以通过不同的降解和活化途径改变活性和非活性类固醇水平的比例来影响某些激素的水平。 两个研究最好的类别是雄激素和雌激素。
在许多情况下,可以结合激素排泄,细菌可以通过水解酶(例如β-葡萄糖醛酸糖苷酶(GUSs)和β-葡萄糖苷酶)去除结合基团,水解酶可重新激活该分子,从而持续循环并具有活性。
微生物群还可以将胆固醇转化为雄激素,激活前雄激素,并将睾丸激素代谢为其他有效的雄激素。人体粪便样品中的雌激素在氧化和还原反应中被分解。
实际上,“雌激素组”一词的产生是为了描述能够代谢雌激素的大量肠细菌基因。绝经后妇女肠道微生物群和类固醇激素水平的变化相互关联,但是,尽管宿主激素的微生物代谢潜力很大,但对脑功能的直接影响仍未经测试。
如果受微生物影响的雌激素确实具有直接的神经学作用,则它们可能具有神经保护作用,因为雌激素对小胶质细胞具有抗炎作用,并且由于微生物群落改变而引起的雌激素水平降低似乎会增加认知障碍和慢性炎症。
微生物可能足以满足这些表型的需要,因为某些类固醇激素水平可以通过微生物粪便移植在小鼠之间转移,但是需要进一步的工作将肠道微生物群产生的激素代谢物直接与神经系统疾病联系起来。
肠道菌群的组成在很大程度上取决于寄主的饮食投入。进餐的频率和食物的类型会影响被细菌代谢的底物的数量,这些细菌会大量吸收和减少,最终影响所产生的下游细菌代谢物的类型和数量。
此外,大量证据表明氨基酸,复杂植物多糖和多酚等微生物代谢产物对大脑产生影响。
氨基酸
微生物编码遗传机制以产生许多氨基酸,其中一些可以促进循环宿主水平。 但是,很可能微生物通过氨基酸水平对中枢神经系统的任何影响都是通过脱氨和脱羧途径对膳食氨基酸的修饰而发生的。
细菌氨基酸代谢的副产物包括氨,短链脂肪酸(SCFA),单酚,吲哚衍生物,神经递质,有机酸,气态化合物和胺。 那些最有可能影响脑功能的物质如下所述。
肠道细菌编码多种基因途径,这些途径将芳香族氨基酸酪氨酸,苯丙氨酸和色氨酸代谢成一大串下游产物,其中许多是神经递质。 酪氨酸代谢为酪胺,然后代谢为两种儿茶酚胺,多巴胺和去甲肾上腺素。 无菌小鼠肠中的酪胺也诱导5-羟色胺的产生。 去甲肾上腺素是由肠道细菌产生的,但人们对此尚不清楚。
然而,已显示多种细菌在体外合成去甲肾上腺素至毫摩尔范围。 由微生物群产生的儿茶酚胺可能足以改变行为,因为用抗生素治疗的小鼠对可卡因的多巴胺信号传导和行为影响更为敏感。 这些神经活性分子是否影响局部肠道神经系统,甚至间接影响大脑,是研究的一个活跃领域。
色氨酸被微生物群分解为吲哚衍生物以及色胺和犬尿氨酸代谢产物,所有这些都具有神经活性属性。 其中一些似乎仅是由微生物群产生的,因为直到细菌定殖之前在无菌小鼠中都无法检测到它们。其中许多可穿过血脑屏障,因此源自肠道的循环色氨酸代谢产物可有助于大脑中的水平。
吲哚衍生物(如吲哚丙酸)具有抗氧化性能,使其成为阿尔茨海默氏病的诱人靶标,而其他衍生物(如吲哚酚硫酸盐)在慢性肾脏疾病模型中诱发神经炎症。
Kynurenine代谢物作用于神经元谷氨酸受体,并影响记忆,焦虑样和压力样行为。实际上,在饮食色氨酸(以及所有色氨酸微生物代谢物)耗尽后,用于模拟抑郁样表型的行为测试中,无细菌小鼠与无特定病原体小鼠的反应不同。
除神经递质外,酪氨酸还可以被微生物群代谢为其他简单的酚类,例如4-乙基苯酚或对甲酚。 这些代谢物被宿主迅速硫酸化为4-乙基苯基硫酸盐(4EPS)或对甲酚基硫酸盐。
在患有自闭症和精神分裂症的小鼠模型以及患有自闭症的儿童样本中,4EPS升高,且注射入野生型小鼠中引起焦虑样表型。 对-甲酚硫酸盐已被确定为自闭症幼儿的潜在尿液生物标志物,并且与社交和抑郁样行为小鼠模型中的少突胶质细胞标志物相关,尽管这些发现目前仍具有相关性。
受肠道微生物影响的另一种氨基酸是主要的兴奋性神经递质谷氨酸,它被细菌的谷氨酸脱羧酶系统代谢,成为主要的抑制性神经递质GABA。
GABA可以被细菌进一步代谢,通过GABA氨基转移酶和琥珀酸半醛脱氢酶进行琥珀酸化。此外,还已经确定了影响宿主GABA系统的微生物群产生或受其影响的代谢产物,例如γ-谷氨酰胺基氨基酸,其降低的水平是饮食诱发的癫痫发作模型改善的介质。
已证明,产生GABA的细菌可减轻小鼠模型中的抑郁样和焦虑样行为,工程产生GABA的菌株足以降低对大鼠内脏痛的敏感性。产生GABA的微生物群与患者的抑郁呈负相关,并且据推测大脑中谷氨酸/ GABA回路的异常是焦虑症,重度抑郁症,双相情感障碍,精神分裂症和自闭症的关键。
精氨酸可被微生物群代谢为四种多胺,它们存在于所有哺乳动物细胞中,并在细胞生长和分化的许多一般过程中发挥作用,并通过谷氨酸受体调节突触可塑性和记忆形成。 这些多胺从精氨酸到胍丁胺依次产生,然后是腐胺,然后是亚精胺,然后是精胺。胍丁胺是大脑中α2-肾上腺素能和咪唑啉受体的配体。
多胺系统的失调与情绪障碍,抑郁症和阿尔茨海默氏病有关,并且多胺已被研究作为抑郁症和焦虑症行为,认知能力下降和药物依赖性的临床前治疗药物。 由于大多数哺乳动物神经递质是从氨基酸前体衍生的,因此我们推测,细菌将氨基酸转化为影响行为的分子可能代表了神经科学中新的微生物内分泌学重点,值得进一步研究。
复杂的植物多糖
由复杂碳水化合物多糖制成的膳食纤维不会被宿主消化并到达结肠,在结肠中,肠微生物会通过肠道微生物将其与各种糖苷水解酶和多糖裂解酶一起发酵,形成毫摩尔水平的SCFAs。
SCFA主要是丁酸,丙酸和乙酸,是结肠上皮细胞的丰富能量来源,剩余的钙进入体循环,可能随后影响神经系统的功能和发育,视情况而定会变好或变坏。
例如,SCFA足以加重无菌帕金森病小鼠模型中的运动症状,但它们改善了实验性中风小鼠模型的恢复能力。 醋酸盐已被证明可穿越小鼠的血脑屏障,并减少进食行为。
由复杂碳水化合物多糖制成的膳食纤维不会被宿主消化并到达结肠,在结肠中,肠微生物会通过肠道微生物将其与各种糖苷水解酶和多糖裂解酶一起发酵,形成毫摩尔水平的SCFAs。SCFA主要是丁酸,丙酸和乙酸盐,是结肠上皮细胞的丰富能量来源,剩余的钙进入体循环,可能随后影响神经系统的功能和发育,视情况而定会变好或变坏。
例如,SCFA足以加重无菌帕金森病小鼠模型中的运动症状,但它们改善了实验性中风小鼠模型的恢复能力。 醋酸盐已被证明可穿越小鼠的血脑屏障,并减少进食行为。
多 酚
多酚包含数千种至少包含一个酚基团的植物衍生分子,目前正在广泛研究作为神经疾病的治疗剂。
大多数多酚通常很难被吸收,直到被肠道菌群转化为可利用的生物活性代谢产物。 细菌水解,酰化和/或酯化后,在这些代谢物重新进入胃肠道或到达其他周围组织之前,通过甲基化,硫酸化,羟基化或葡糖醛酸化来修饰宿主。
口服母体多酚后,大脑中酚类代谢物的水平会发生变化。在大脑中检测到的口服多酚治疗的特定细菌代谢物,例如3-羟基苯甲酸和3-(3′-羟基苯基)丙酸,能够抑制标志性淀粉样蛋白聚集并减缓阿尔茨海默氏病的病理生理学进展。
多酚还通过减少炎症并通过代谢产物(例如槲皮素-3-O-葡萄糖醛酸和麦维京-3-O-葡萄糖苷)调节突触可塑性,来预防应激诱导的抑郁样行为。
带有阿魏酸酯酶基因的肠道微生物将一种多酚阿魏酸释放到循环中。 阿魏酸的施用刺激了皮质酮治疗的抑郁症小鼠模型的神经发生,并且在阿尔茨海默氏病和脑缺血的小鼠模型中具有保护作用。
葡萄籽提取物和白藜芦醇等治疗中的多酚显示出有望治疗阿尔茨海默病,帕金森病和tauophathies小鼠模型的神经病理学和认知缺陷,但还需要进一步用纯多酚进行测试。
最近,在帕金森病模型中,表明植物来源的表没食子儿茶素没食子酸酯可以预防由特定肠道细菌引起的运动症状。 一些多酚是植物雌激素,被肠道细菌代谢成雌马酚和肠内酯衍生物。植物雌激素代谢物可以是雌激素受体的激动剂或拮抗物,并且可能对经典雌激素受体配体激活的神经保护途径有影响,尽管该结构类别很大且是异质的,对大脑的直接影响仍有待确定。
其他代谢物
肠道中的微生物GUS酶可去除标记代谢物以被宿主排泄的葡糖醛酸基团。结果,微生物群恢复了原始分子并促进了该分子重新摄取回到血液。已证明该过程直接调节本文所述的许多外源和内源化合物的水平。
肠道菌群还产生维生素B和K,以及独特的脂质代谢物,例如共轭亚油酸,羟基脂肪酸和鞘脂,其中一些在宿主健康和疾病中显示出生物学活性,并且已知由 特定细菌。 由于大脑发育过程中需要维生素B和K,大脑中的高脂质含量以及脂质在信号传导途径中的重要性,未来的工作可能会阐明微生物脂质和维生素代谢产物与脑功能的联系。
对细菌代谢产物的产生和功能的研究已经确定,从肠道到大脑都会发生活跃的化学信息传递。 其他细菌分子可能具有尚未定义的神经活性特性,包括来自肠道微生物群的数千种最近鉴定(但仍未表征)的短肽中的任何一种。 鉴于鉴定和表征微生物群产生的小分子和肽谱是一项相对较新的尝试,可能会继续发现更多的神经活性微生物代谢产物。确定作用机制可能导致各种健康应用。
肠道菌群与大脑之间的通讯管道包括迷走神经的激活,内分泌细胞(包括肠嗜铬细胞)的刺激,免疫介导的信号传导以及肠道衍生代谢产物从循环系统向大脑的运输。 认为所有由肠-脑轴组成的路径都被微生物群所影响,以影响大脑的活动和行为,并且通过它们中的任何一条发出的信号都可能与其他路径交织在一起。
迷走神经激活
迷走神经直接沿着胃肠道将肌肉和粘膜层连接到脑干,并且是建立良好的信号通路,影响进食,焦虑样,抑郁样和社交行为。
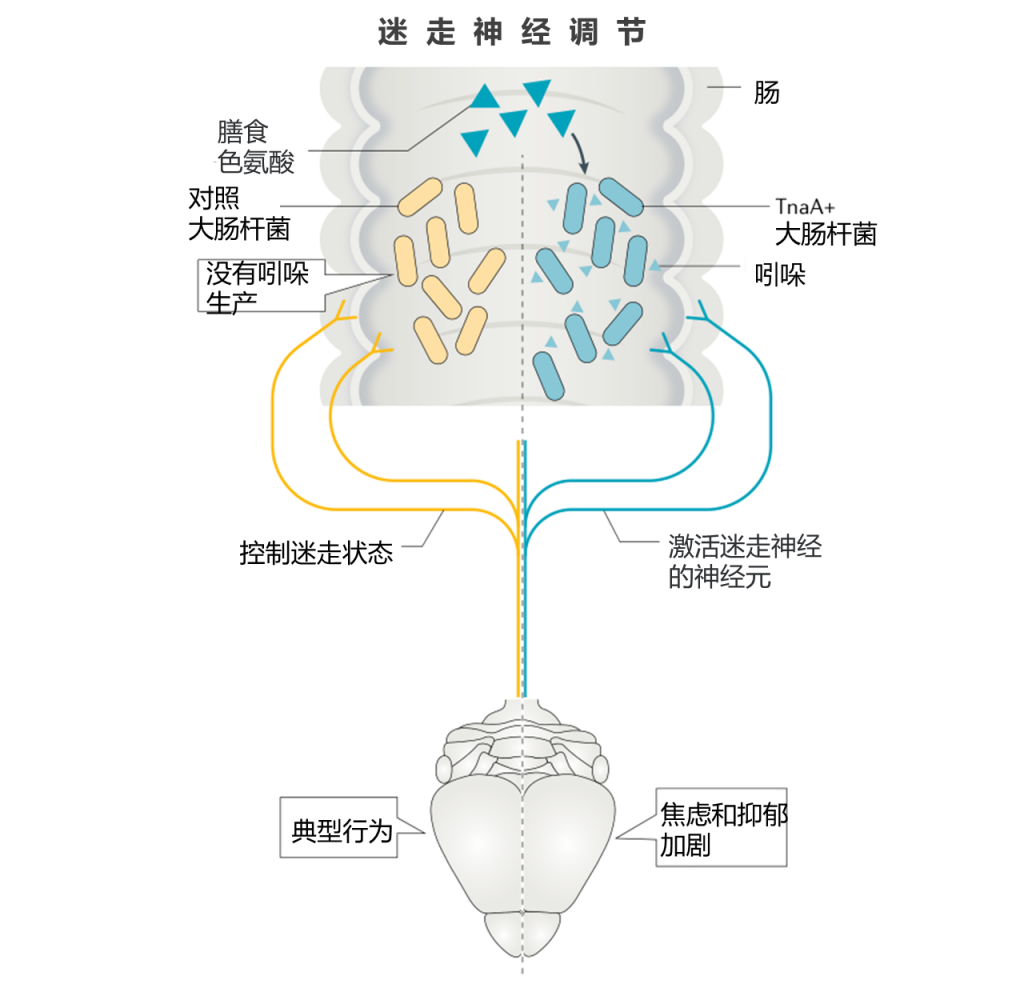

肠道病原体和益生菌通过迷走神经元的激活影响这些行为,然后改变下游的神经活动,包括脑中BDNF,GABA和催产素信号的改变。 这些反应在迷走神经切断迷走神经后被消融,但是介导这些作用的特定细菌代谢物仍不清楚。
最近的一项研究确实通过迷走神经信号传导来测量特定代谢物的作用,尽管也可能涉及其他信号传导途径。在这项工作中,将大鼠转化为能转化的大肠埃希氏菌菌株饮食中将色氨酸与TnaA色氨酸酶或吲哚生产缺陷的突变大肠杆菌转化为吲哚。 暴露于肠道吲哚的大鼠表现出增加的焦虑样和抑郁样行为并激活迷走神经元。
肠嗜铬细胞刺激
肠嗜铬细胞是肠壁中的内分泌细胞,可响应持续的肠道信号而产生并分泌人体90%的血清素。血清色素的肠嗜铬细胞产生会影响其循环水平,并具有直接或间接影响大脑活动的潜力。
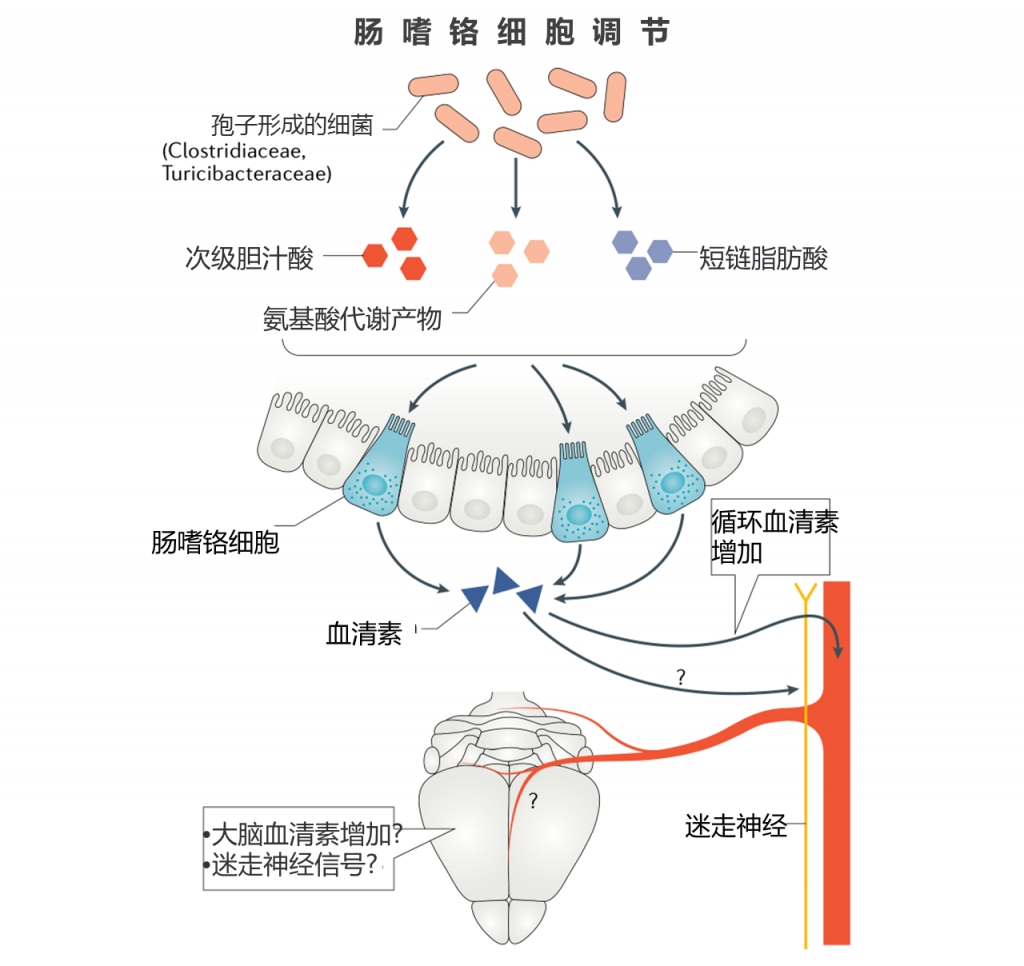

通过双歧杆菌属菌的益生菌治疗,已显示出在抑郁症小鼠模型中性能的提高。在一项研究中,该研究同时观察到大脑中5-羟色胺水平的增加以及体外肠嗜铬细胞中5-羟色胺前体的分泌增加。 然而,细菌处理,潜在的5-羟色胺调节与抑郁样表型之间没有机械联系。结肠肠嗜铬细胞确实表达各种微生物代谢物的受体并对其作出反应,包括MAMP,SCFA,芳香族氨基酸代谢物和次级胆汁酸。
最近鉴定出的一种细菌亚群可以极大地促进肠嗜铬细胞合成5-羟色胺生物合成的细菌,是孢子形成细菌,如梭状芽胞杆菌。
已证明这些细菌在体内产生的代谢产物足以在体外产生5-羟色胺诱导活性,包括α-生育酚,丁酸酯,胆酸盐,脱氧胆酸盐,对氨基苯甲酸酯,丙酸酯和酪胺。 还通过暂时的肠内给药单独测试了一个子集,并且脱氧胆酸盐,α-生育酚,对氨基苯甲酸酯和酪胺都足以诱导肠嗜铬细胞分泌5-羟色胺。
有趣的是,最近的研究表明,口服选择性5-羟色胺再摄取抑制剂可提高肠道5-羟色胺的生物利用度并用于治疗抑郁症,可能依赖迷走神经的激活来改善小鼠的抑郁样行为。 这支持了5-羟色胺的肠嗜铬细胞产生的潜力,可能通过在发育和急性环境中与其他已知的肠脑信号传导途径相交,将信号传递到肠外并到达大脑。
免疫介导的信号传导
肠道菌群为神经免疫系统的成熟提供了线索,而在发育过程中这些线索的丢失导致该系统终身功能失调。但是,由于肠道菌群变化和肠道通透性增加而导致的慢性暴露于炎症也可能会导致各种神经系统疾病。
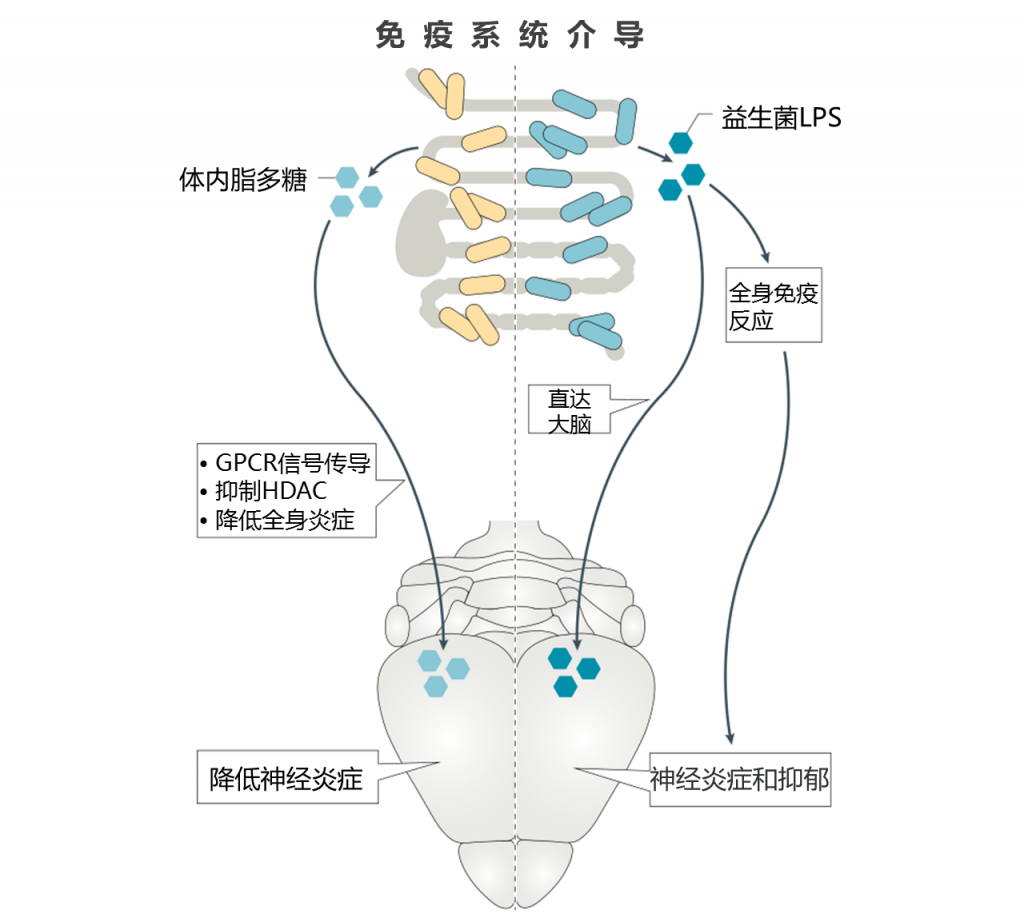

用作MAMP的细菌代谢物(例如LPS)已被用于在ASD和精神分裂症模型中激活免疫系统,并在小鼠中诱发抑郁样症状。
其他肠道代谢物可能会减轻慢性炎症。 例如,SCFA通过激活GPCR和抑制HDAC活性而与免疫系统密切相互作用。 高纤维饮食会导致较高水平的SCFA,从而导致较低水平的循环促炎细胞因子。
SCFA激活GPCR(FFA2和GPR109a)可以抑制炎症信号通路,SCFA(尤其是丁酸盐)对HDAC的抑制作用可以降低体内炎症。
这些例子可能代表了微生物分子对神经免疫信号的潜在影响的初步发现。
代谢物直接转移到大脑
肠道中产生的许多微生物代谢产物可以不同水平和速率进入全身循环。 一个例子是多酚代谢物组,最近的研究表明,在血液或尿液中几乎检测不到母体多酚,但由多酚前体产生的细菌代谢物进入循环的水平足以发挥生物学作用。
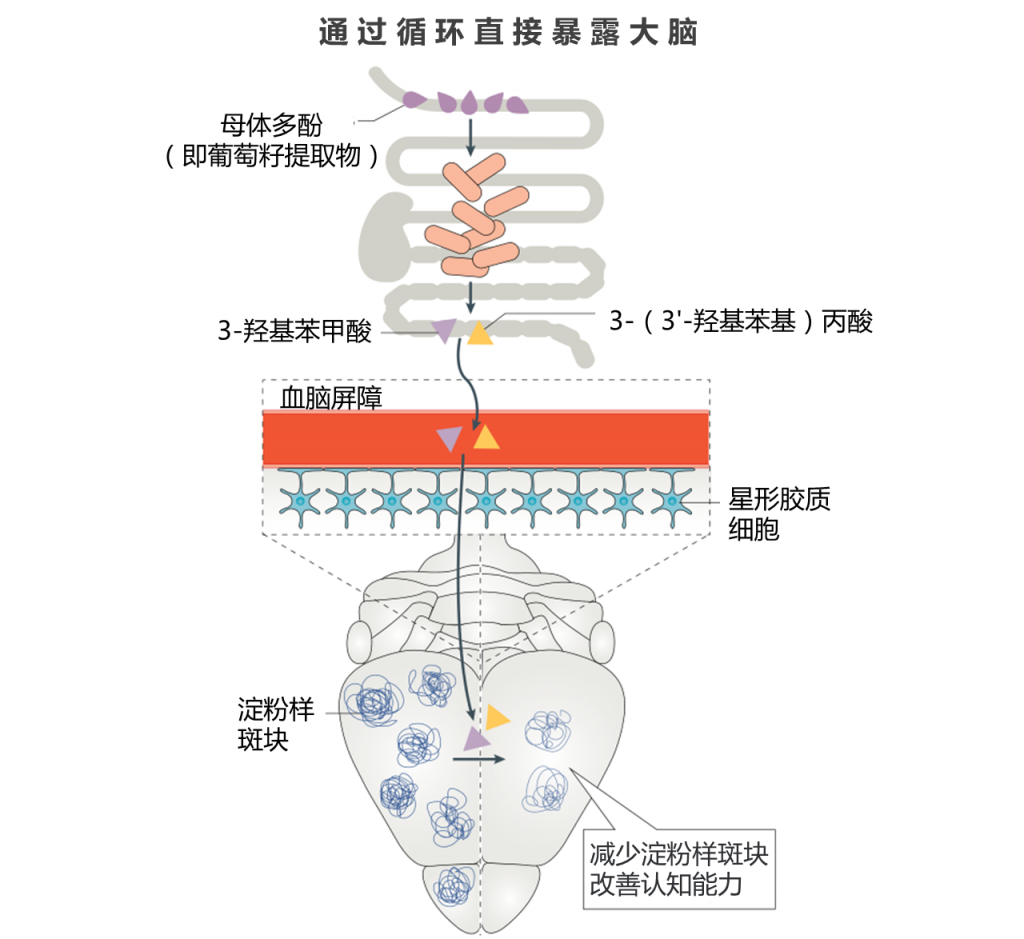
实际上,大脑似乎是某些多酚类微生物代谢产物的主要目标。尽管仍然缺乏体内证据,但体外培养物显示多酚代谢物能够穿越BBB模型系统并对神经元培养物发挥保护作用,主要是通过减少炎症反应。
此外,在大鼠的血液和脑中测定了口服多酚治疗的衍生物,发现它们可减少神经毒性聚集物的聚集并促进神经可塑性。
尽管建立了良好的肠道与大脑的联系,但通过每个导管工作的细菌分子的清晰机械细节仍然有限。 了解从肠道到大脑的微生物组信号的方式可能会提供对针对胃肠道靶标的合理药物发现平台的见解,这可能会克服当前将药物输送到大脑靶标的挑战。
研究继续建立在对肠脑轴的基础上,以探索大脑中哪些细胞受到特定细菌代谢产物的直接或间接影响。 需要大量工作来系统地证明源自肠道细菌的这些化学信使会影响特定脑细胞的发育或功能。 在这里,我们总结了肠道微生物代谢产物可能影响大脑细胞的现有证据。
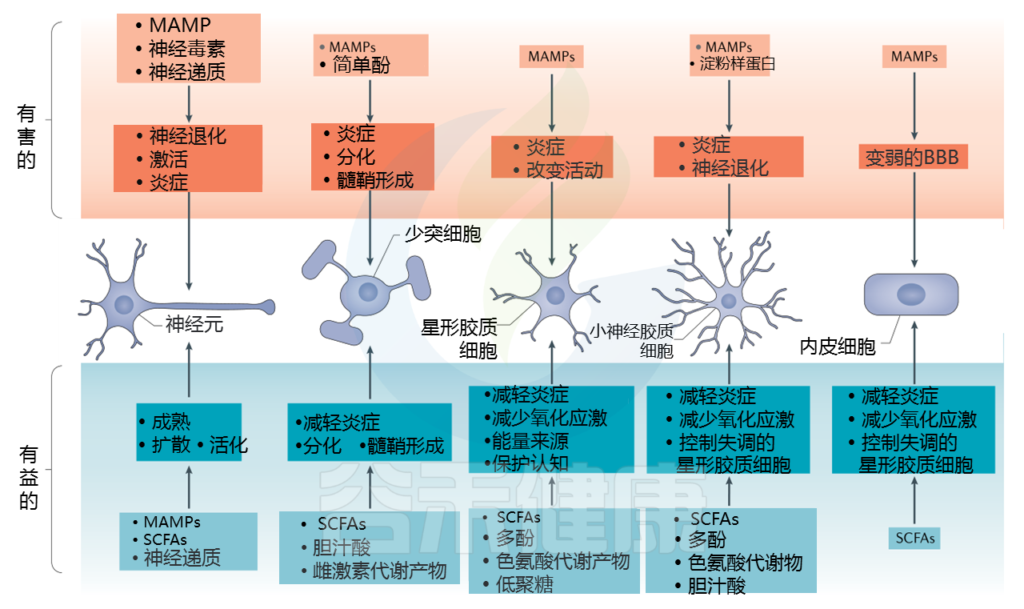
神经元
作为大脑控制行为的主要信号传导细胞,神经元从本质上讲可能是受此观点中描述的每种代谢物影响的最终靶标。 发挥影响迷走神经的细菌群落作用的所有未知代谢物都可能激活神经元。
更具体地说,神经毒素是细菌分子影响神经元的一个明显例子。 一些神经毒素由微生物群落的共生成员产生,并发挥局部或中枢神经系统的作用,从而使神经元失调或杀死神经元。
微生物群还产生或诱导神经递质及其前体的产生,包括5-羟色胺,肾上腺素,GABA,组胺,乙酰胆碱,谷氨酸和多巴胺,它们可显着影响肠,迷走神经,周围神经和中枢神经元中兴奋性和抑制性神经传递的平衡。
神经元还表达模式识别受体,并且这些受体的激活已显示出可以调节神经元分化,增殖和轴突生成以及神经炎症。 其中一些可能是由于宿主配体引起的,但是在大脑中也检测到MAMPs,例如肽聚糖,并且可能是激活受体,例如TLR2,PGLYRP2或NOD1,它们通过类似的机制在神经元中表达。
神经元也受SCFA的影响,因为乙酸进入大脑并激活下丘脑中的神经元。 最后,体外筛选鉴定了肠道微生物产生的神经活性分子,例如群体感应分子,这些分子会影响神经元的活力,形态,分化和炎症反应。
尽管后者需要在体内验证,它们说明了神经元与微生物代谢产物之间存在大量界面的可能性。
星形胶质细胞
星形胶质细胞为其他细胞提供支持并修复大脑中的损伤。 代谢物,包括特定的寡糖和多酚,SCFA和色氨酸代谢物,可能会影响星形胶质细胞的功能。
色氨酸代谢物调节星形胶质细胞中的芳烃受体,并通过降低其炎症状态和改变它们与小胶质细胞的相互作用来影响其活性。
多酚代谢产物和纯短链脂肪酸(例如丁酸)对星形胶质细胞具有体外影响,并已显示出可减少神经炎症和氧化作用。
大脑中的这些细胞将SCFA乙酸盐用作能源。 寡糖和多酚(例如来自植物巴戟天的多酚和多酚)已被细菌代谢成SCFA和其他脂质衍生物,已显示通过星形胶质细胞功能对阿尔茨海默氏病具有保护作用。星形胶质细胞还表达G蛋白偶联的胆汁酸受体1(TGR5),其可以被胆汁酸激活,从而导致神经炎症的减少,并且可能与肝性脑病有关。
少突细胞
少突胶质细胞产生隔离神经元轴突的髓鞘,,即使在整个成年期,两种细胞类型之间也会发生动态串扰。
代谢产物对少突胶质细胞增殖,分化和功能的影响可能对神经系统健康产生广泛影响。 在脱髓鞘疾病多发性硬化症的小鼠模型中,治疗性肠道菌群的操作已经成功,并伴随着与减轻的疾病症状相关的代谢组学谱的改变。
有一些证据表明,这种改善可能是由于炎症性LPS水平降低,SCFA升高以及胆汁酸改变所致,尽管尚不清楚是否存在对少突胶质细胞的直接活性或它们是否间接受益于炎症减轻。在体外,细菌性酚类代谢物对甲酚可能直接损害少突胶质细胞的成熟和髓磷脂的产生。
已知影响少突胶质细胞分化和髓鞘形成的另一类分子是雌激素分子。 微生物确实修饰了许多雌激素代谢物,但尚未证明这些代谢物的体内微生物产生与少突胶质细胞之间的结论性联系。
内皮细胞
血管内衬有内皮细胞,内皮细胞是负责维持血脑屏障BBB的主要细胞类型,BBB在很大程度上决定了分子进入大脑的速度。 微生物代谢产物对血脑屏障通透性的调节可极大地改变药物,宿主分子和其他肠道代谢产物的吸收,但是这种机制的具体例子仍然难以捉摸。
例如,细菌代谢物(例如来自某些细菌物种的LPS)以剂量依赖性和细菌应变依赖性的方式增加体内渗透性,并且无菌小鼠的BBB似乎比常规小鼠泄漏。 LPS刺激内皮细胞也会导致脑海绵状畸形,进而导致癫痫发作和中风。 已经显示SCFA通过激活内皮细胞中表达的SCFA受体来降低BBB的通透性,并同时增加紧密连接蛋白的表达,紧密连接蛋白将这些细胞密封成成功的屏障。
小胶质细胞
大脑中的主要免疫细胞称为小胶质细胞,因此,它是许多与神经炎症相关的损伤的罪魁祸首,如帕金森病,阿尔茨海默病。
因此,来自MAMP的促炎信号会诱导成熟并产生细胞因子的小胶质细胞,而通常来自多酚,SCFA和胆汁酸代谢产物的抗炎信号会通过小胶质细胞来降低大脑的氧化应激。 但是,这些信号中的某些信号对小胶质细胞的影响是复杂的,因为SCFA和其他微生物信号可能会加剧帕金森氏病无菌小鼠模型中的症状。
另一项最新研究发现,微生物色氨酸代谢物(如硫酸吲哚-3-)可控制小胶质细胞的活化,进而改变星形胶质细胞的行为。
尽管迄今为止,微生物组对细胞的特定作用的例子都很少,而且还进行了表面描述,但这些基础研究仍是揭示肠道微生物组-脑轴的潜在神经元回路,大脑区域和系统级连接的关键步骤。
对肠道微生物群研究的日益重视可能会导致生物医学的变革性进步。 识别和表征特定微生物和微生物群落的原因或贡献,应该是肠道微生物组-脑研究的主要重点。直接和间接化学信号传递的各种途径并不互相排斥,某些代谢物可能会对通向大脑的多个导管产生影响。随着微生物分子信息及其肠脑信号传导途径的特殊作用不断被发现,开发新的治疗原理和方法的潜力不断增加。
随着神经疾病中肠—脑连接的机制研究深入,微生物组和神经科学研究的合并为理解肠脑轴的基本“线路”和功能的提供了可能,并且还为人类健康可采取的行动提供了潜在的机会。
参考文献:
Needham Brittany D,Kaddurah-Daouk Rima,Mazmanian Sarkis K,Gut microbial molecules in behavioural and neurodegenerative conditions.[J] .Nat Rev Neurosci, 2020, undefined: undefined.
相关阅读: