-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康
炎症性肠病(Inflammatory Bowel Disease, IBD)是一种复杂的、多因素驱动的慢性胃肠道炎症性疾病,研究显示其发病率在全球范围内持续上升。
研究表明,IBD的病因涉及遗传易感性、环境因素、肠道微生物动态变化以及宿主免疫调控的复杂相互作用。近年来,随着多组学技术和临床研究的深入,科学界对IBD在临床前阶段有了更深刻的认知框架。
前瞻性队列研究证实,基于高风险人群的纵向队列数据揭示,在临床确诊前5-10年,个体已呈现特征性的亚临床病理改变:肠道屏障功能渐进性损伤、微生物生态结构失衡、抗微生物抗体谱系异常,糖基化修饰的系统性改变等。比如,粪便钙卫蛋白等生物标志物的动态变化模式,为追踪疾病自然史提供了可量化的监测指标。
当这些亚临床病理改变突破代偿阈值,便表现为典型的IBD临床症状。
本文依据现有研究资料,系统性地阐述了IBD的定义、分类、流行病学特征、多重危险因素,重点剖析了临床前IBD的启动与发展阶段,涵盖肠道屏障功能、微生物生态、宿主免疫应答、蛋白质组学及糖基化修饰等多个层面的动态变化;在此基础上,我们还将探讨当前靶向菌群的干预策略与未来预防医学新范式,为IBD的早期识别与精准管理提供理论依据。
目 录
1. 炎症性肠病(IBD)概述
2. IBD的危险因素与决定因素
3. 临床前IBD:从启动到扩展
4. IBD综合发展模型方向
5. 治疗措施与预防机会
6. 结论与展望
IBD的定义与主要形式
炎症性肠病(IBD)是一组以胃肠道慢性、复发性炎症为特征的免疫介导的疾病。
其主要包括两种类型:
病变部位和病理特征
克罗恩病的炎症可累及从口腔到肛门的整个消化道,呈节段性、非对称性分布,炎症可穿透肠壁全层,导致狭窄、穿透(瘘管)等并发症。
溃疡性结肠炎的炎症通常局限于结肠黏膜和黏膜下层,自直肠开始呈连续性、弥漫性向近端蔓延。
尽管两者在病变部位和病理特征上有所区别,但它们共同的病理生理基础是宿主对肠道微生物群产生异常且持续的免疫反应,最终导致组织损伤。
肠道免疫系统在稳态和炎症状态下显著差异
在健康状态下(稳态),肠道上皮细胞形成完整的物理屏障,潘氏细胞(Paneth cell)分泌抗菌肽,杯状细胞(Goblet cell)分泌黏液,共同抵御微生物入侵。固有层中的免疫细胞,如调节性T细胞(Treg)和分泌IgA的浆细胞,共同维持对共生菌的免疫耐受(如下图 左边)。
编辑
doi.org/10.1038/s41590-025-02197-5
在IBD炎症状态下,这种平衡被打破。肠道屏障受损,潘氏细胞和杯状细胞功能下降,导致抗菌物质和黏液减少。
病原菌如克雷伯菌属(Klebsiella)增殖,共生有益菌菌(如普拉梭菌 F. prausnitzii)减少。大量炎症细胞(如TH1/TH2/TH17细胞、炎症性巨噬细胞)浸润肠道组织,分泌促炎细胞因子,并产生IgG抗体,导致慢性炎症和组织破坏(如上图右边)。
流行病学趋势
历史上,IBD主要被认为是西方工业化国家的疾病。然而,进入21世纪,IBD的全球发病率和患病率呈现出显著的上升趋势,尤其是在亚洲、南美和东欧等新兴工业化国家和地区,IBD已成为一个全球性的健康挑战。这种流行病学转变清晰地表明,除了遗传背景外,与工业化和城市化相关的生活方式、饮食结构和环境暴露等因素在IBD的发病中扮演着至关重要的角色。
针对不同种族和移民群体的研究也发现,IBD的临床表现、遗传易感性和治疗反应存在差异,这进一步凸显了基因-环境相互作用在IBD发病中的复杂性。
IBD的病因是多因素的,涉及遗传、环境、免疫和微生物等多个层面。这些因素相互交织,共同决定了个体患病的风险和疾病的表型。
遗 传 易 感 性
IBD具有明显的家族聚集性,遗传因素在其发病中起着基础性作用。单卵双生子研究显示,克罗恩病的一致性高达50%。通过全基因组关联研究(GWAS),目前已发现超过300个与IBD相关的易感基因位点。这些基因大多与免疫功能相关,特别是那些调节宿主与微生物相互作用的通路。例如:
值得注意的是,大多数遗传位点仅赋予个体一定概率的疾病风险,这也表明IBD是一种多基因疾病,其发病需要遗传与环境因素的共同作用。此外,不同种族人群的遗传背景差异也导致了IBD易感基因频率和效应的不同。
环 境 因 素
环境因素被认为是近年来IBD发病率快速上升的主要驱动力。这些因素在生命早期和成年期均可发挥作用,深刻影响肠道微生态和免疫系统的发育与功能。
✦ 饮食
西式饮食,即高脂肪、高糖、高加工食品和低纤维的饮食模式,被认为是IBD的重要风险因素。食品乳化剂(如羧甲基纤维素)会破坏肠道黏液屏障,改变微生物群组成,促进炎症。相反,富含纤维的饮食则有助于产生具有抗炎作用的短链脂肪酸(SCFAs)。
✦ 抗生素使用
尤其是在生命早期,抗生素的广泛使用会严重扰乱肠道微生物群的正常定植和发育,降低菌群多样性,增加IBD的长期风险。
✦ 感染
特定的肠道感染,如沙门氏菌、弯曲杆菌、诺如病毒,被发现与IBD的发病风险增加有关。这些感染可能作为“触发事件”,在遗传易感个体中打破免疫耐受。
✦ 吸烟
吸烟是影响IBD的明确环境因素之一。有趣的是,吸烟会增加克罗恩病的风险并加重其病情,但对溃疡性结肠炎却显示出一定的保护作用,其机制尚不完全清楚。
✦ 卫生假说
生命早期过度清洁的环境可能导致免疫系统未能充分接触微生物,从而发育不全,更易在日后对无害抗原产生过度反应。
✦ 其他因素
还包括空气污染、非甾体抗炎药(NSAIDs)的使用、社会经济地位以及心理压力等。
IBD的遗传和环境决定因素
编辑
doi.org/10.1038/s41590-025-02197-5
人群的免疫反应强度呈钟形分布。IBD可发生于免疫反应过弱(如NOD2缺陷导致对微生物抵抗力差)或过强(如IL-10调节缺陷导致对微生物耐受性差)的两个极端。
左下角的曼哈顿图代表遗传易感性,右下角的图标代表饮食、吸烟和微生物等环境因素。这些因素的相互作用决定了个体是否会滑向疾病的两端。
炎症反应的遗传与环境决定因素
个体的免疫反应强度存在连续的变异谱,从免疫缺陷到免疫超敏。IBD可以在这个谱系的两个极端发生。
编辑
◄ 免疫缺陷
一方面,某些遗传缺陷(如NOD2、ATG16L1功能丧失)会导致肠道先天免疫和屏障功能减弱,使宿主对微生物的抵抗力下降,易受机会性病原菌感染而引发炎症。
► 免疫超敏
另一方面,另一些遗传背景(如IL-10、IL-10R功能缺陷)则导致免疫调节功能受损,对正常的肠道共生菌产生过度的免疫反应,即免疫耐受丧失,从而引发炎症。
▲ 健康平衡
健康个体则处于两者之间的平衡状态,既能有效清除病原体,又能耐受共生菌。个体的遗传组成决定了其对特定环境暴露(如饮食、感染)的反应阈值和反应模式。
因此,IBD的发生是独特的遗传背景与特定环境因素相互作用(G×E)的结果,这也解释了为何暴露于相似环境中的人群只有少数遗传易感者会发病。
大量证据表明,IBD的临床诊断之前存在一个漫长的临床前阶段,在此期间,一系列病理生理变化已悄然发生。理解这一阶段是实现IBD早期预测和预防的关键。这一阶段可进一步细分为风险期、启动期和扩展期。
临床前IBD的分期模型
一个被广泛接受的模型将IBD的发展过程分为几个连续的阶段:
风险期
个体携带遗传易感基因,并可能在围产期、婴幼儿期及童年期暴露于某些环境风险因素(如抗生素、感染、母亲吸烟等)。这些因素共同启动了免疫系统的易感状态,但个体并无任何症状或病理改变。
临床前启动期
在某个未知的“触发事件”(如特定感染或饮食改变)后,疾病开始启动。这一阶段可持续多年(甚至在诊断前10年),其特征是出现亚临床的病理变化,如肠道通透性增加、微生物失调、以及针对微生物或自身抗原的低水平抗体应答。这些变化通常是无症状的。
临床前扩展期
在临床诊断前约2年,疾病进入扩展期。此时,病理变化加剧,全身性和肠道局部的炎症标志物(如CRP、粪便钙卫蛋白)显著升高,患者可能开始出现非特异性症状并开始出现要就诊的症状。这一阶段代表了从亚临床状态向临床显性疾病的过渡。
临床诊断期
当炎症累积到一定程度,导致明显的组织损伤和持续的临床症状(如腹痛、腹泻、便血)时,患者最终被诊断为IBD。
IBD临床前阶段的演变模型
编辑
doi:10.1038/s41575-023-00854-4.
IBD风险因素、发病途径和累积风险的时间演变
编辑
doi:10.1038/s41575-023-00854-4.
该图谱从生命阶段(怀孕至成年)的角度,展示了遗传风险和环境风险如何随时间累积。
在临床前阶段,微生物组扰动、屏障功能丧失、免疫功能障碍、代谢变化和糖基化改变等途径相互作用,共同推动IBD累积风险的增加,直至最终诊断。这也提示了不同生命阶段的预防干预窗口。
肠道屏障功能障碍与通透性改变
肠道屏障是维持肠道内环境稳态的第一道防线,其完整性在IBD发病中至关重要。
在临床前阶段,肠道屏障功能就已出现障碍。肠道屏障由物理屏障、化学屏障、生物屏障、免疫屏障构成。
☾ 物理屏障
由单层肠上皮细胞(IECs)及其间的紧密连接蛋白(如Claudin, Occludin)构成。
编辑
研究发现,在克罗恩病高风险亲属中,即使没有症状,其肠道通透性(以乳果糖/甘露醇比值LMR衡量)也显著增加,并且这种高通透性是未来发病的独立危险因素。
肌球蛋白轻链激酶(MLCK)的异常激活被认为是导致紧密连接开放、通透性增加的关键机制之一。
☾ 化学屏障
主要指覆盖在上皮表面的黏液层和由潘氏细胞分泌的抗菌肽(AMPs)。
编辑
黏液层由杯状细胞分泌的黏蛋白(主要是MUC2)构成,能有效隔离细菌与上皮细胞的直接接触。
在IBD中,黏液层变薄、不连续,其糖基化修饰也发生改变。同时,潘氏细胞功能受损,导致α-防御素等AMPs分泌减少,削弱了对微生物的控制能力。
☾ 生物屏障
编辑
肠道菌群中有益菌通过竞争营养、产生抑菌物质等方式抑制致病菌生长。另外通过产生短链脂肪酸,维持肠道酸性环境等。
☾ 免疫屏障
编辑
包括分泌型IgA(sIgA)和上皮内淋巴细胞(IELs)等。sIgA能中和并清除入侵的微生物,而在IBD中,针对特定病原菌的IgA反应可能不足或异常。
屏障功能的早期损害,使得肠腔内的微生物及其产物(如LPS)更容易易位至固有层,从而持续激活下方的免疫系统,启动炎症级联反应。
编辑
doi.org/10.1038/s41575-022-00604-y
肠道微生物群失调
肠道微生物失调是IBD的核心特征,既是疾病的结果,也可能是其驱动因素。在临床前阶段,微生物群的改变就已经出现。
✎ 菌群结构改变
IBD患者的肠道微生物多样性显著降低。
产短链脂肪酸菌,如普拉梭菌(Faecalibacterium prausnitzii)、罗氏菌属(Roseburia)等厚壁菌门细菌丰度减少。
而一些具有潜在致病性的需氧或兼性厌氧菌,如大肠杆菌(特别是黏附侵袭性大肠杆菌AIEC)、克雷伯菌属等变形杆菌门细菌,具核梭杆菌(Fusobacterium nucleatum)等则异常增殖。
✎ 真菌与病毒的改变
除了细菌,肠道真菌和病毒的失调也参与IBD。例如,白色念珠菌(Candida albicans)、马拉色菌(Malassezia)等真菌在IBD患者肠道中增多,某些高毒力菌株可通过分泌念珠菌溶血素(Candidalysin)等毒素加剧炎症。同时,噬菌体和某些肠道病毒的组成和丰度也发生改变。
编辑
doi.org/10.1038/s41579-025-01163-0
✎ 功能与代谢改变
微生物失调导致其功能和代谢产物的改变。丁酸等短链脂肪酸的产生减少,削弱了其对肠上皮细胞的营养支持和对免疫细胞的抗炎调节作用。相反,一些有害代谢物,如硫化氢、或诱导DNA损伤的吲哚胺类物质可能增多。胆汁酸的代谢也发生紊乱,影响了FXR、TGR5等核受体的信号,进而影响免疫调节。
这种失调的微生物群落,一方面无法提供维持肠道稳态所需的有益信号,另一方面其本身或其产物又成为持续刺激免疫系统的炎症来源。
编辑
doi.org/10.1038/s41579-025-01163-0
基因-微生物相互作用
特定的遗传背景与特定的微生物失调相结合,是驱动IBD发病的核心机制。研究表明,IBD相关的易感基因突变,往往导致宿主对特定微生物的反应异常。
NOD2与微生物
携带NOD2功能缺陷变异的个体,其肠道中脆弱拟杆菌(Bacteroides fragilis)等特定共生菌的调节能力下降,无法有效诱导Treg细胞,导致免疫耐受受损。
近期研究进一步揭示,粪肠球菌(Enterococcus faecium)分泌的DL-内肽酶SagA能够产生激活NOD2的信号分子MDP。在健康个体中,这一通路通过髓系细胞的NOD2激活,诱导IL-1β分泌,进而促进ILC3和CD4+ T细胞产生保护性的IL-22,促进组织修复。
然而,在IBD患者中,由于炎症环境中REG3等抗菌蛋白的过度产生,导致对REG3敏感的Efm被清除,从而使这一保护性通路中断。更重要的是,携带常见NOD2风险变异(如R702W)的个体,即使存在Efm,也无法有效启动这一保护性信号,导致炎症持续。这一发现为理解基因(NOD2变异)与微生物(Efm缺失或功能障碍)之间可能存在的相互作用机制提供了重要线索,提示它们在疾病发生与发展过程中潜在协同机制。
✨粪肠球菌
粪肠球菌在健康与IBD中的双重作用机制
编辑
doi.org/10.1016/j.chom.2023.08.002
健康状态下,粪肠球菌(E. faecium)通过其分泌的SagA激活髓系细胞的NOD2通路,最终诱导IL-22产生,促进组织再生和抑制炎症。
而在IBD中,一方面炎症环境产生的REG3蛋白会清除E. faecium;另一方面,NOD2的遗传变异会使该保护通路失效,导致炎症循环加剧。
ATG16L1与病毒
携带ATG16L1 T300A风险变异的小鼠,在感染鼠诺如病毒(MNV)后,其潘氏细胞会发生严重的细胞死亡和功能障碍,而野生型小鼠则不受影响。
这表明遗传易感性(ATG16L1变异)与环境触发(病毒感染)的结合,是导致特定细胞表型和病理变化的关键。
自身免疫与抗微生物体液应答
在IBD临床前阶段,体液免疫系统已经出现异常活化,表现为多种抗体水平的升高。这些抗体既可以靶向肠道微生物,也可以靶向宿主自身成分。
抗微生物抗体
在IBD诊断前数年,即可在患者血清中检测到针对肠道微生物成分的抗体。例如,抗酿酒酵母抗体(ASCA)是克罗恩病的经典标志物,其在诊断前5年甚至更早就已升高。
其他抗体还包括抗大肠杆菌外膜孔蛋白C(OmpC)抗体、抗鞭毛蛋白(CBir1, FlaX)抗体等。这些抗体的出现,反映了肠道屏障受损后,免疫系统与肠道微生物发生了异常的相互作用和免疫识别。
编辑
自身抗体
除了抗微生物抗体,一些自身抗体也在临床前阶段出现。例如,抗粒细胞-巨噬细胞集落刺激因子(GM-CSF)自身抗体在克罗恩病诊断前6年即可检出,并与更复杂的疾病表型相关。
部分研究提示,抗整合素αvβ6自身抗体在溃疡性结肠炎诊断前长达10年就已升高,并具有很高的预测价值。这些自身抗体的出现,标志着免疫系统打破了对自身组织的耐受,是疾病向自身免疫方向发展的重要证据。
蛋白质标志物的变化
利用高通量蛋白质组学技术,研究人员在IBD临床前患者的血清中鉴定出了一系列变化的蛋白质标志物。这些标志物反映了疾病早期潜在的病理过程。
◑ 炎症相关蛋白
在诊断前数年,全身性炎症标志物如C反应蛋白(CRP)和白细胞介素-6(IL-6)水平已轻度升高,提示存在潜在的炎症反应。
其他与炎症、免疫应答相关的蛋白,如肿瘤坏死因子受体(TNFR)、补体成分、脂多糖结合蛋白(LBP)等也发生改变。
◑ 趋化因子和细胞因子
趋化因子如CXCL9、CXCL11、CCL11在临床前阶段升高,这些分子与免疫细胞的招募和迁移有关,提示在临床症状出现前,免疫细胞的动态平衡可能已被打破。
◑ 组织重塑相关蛋白
基质金属蛋白酶(MMPs)如MMP10、MMP12等的水平变化,可能反映了疾病早期微小的组织损伤与修复过程。
这些蛋白质标志物的组合,有望构建预测模型,用于识别高风险人群,其预测准确性随着接近诊断时间点而提高。
糖基化修饰的改变
糖基化是蛋白质和脂质最常见和最复杂的翻译后修饰之一,形成的聚糖(Glycans)在细胞识别、信号转导、免疫调节中发挥关键作用。
在炎症性肠病(IBD)的发生和发展过程中,糖基化模式发生了显著变化。
N-聚糖和O-聚糖
聚糖主要分为N-连接聚糖(N-glycan)和O-连接聚糖(O-glycan)。
肠道不同部位的上皮细胞表达不同的O-聚糖核心结构,如结肠主要表达Core 3和Core 4。
常见的N-聚糖和O-聚糖结构
编辑
doi.org/10.1038/s41385-021-00466-8
该图展示了N-聚糖的核心与扩展形式(高甘露糖型、复杂型、混合型),以及O-聚糖的四种核心结构(Core 1-4)及其扩展形式。这些复杂的糖链结构是细胞功能的重要调节者。
炎症诱导的糖基化改变
在IBD的炎症黏膜中,一个普遍特征是出现不成熟或截短的聚糖结构。
例如,肿瘤相关的Thomsen-Friedenreich(TF)抗原(Galβ1-3GalNAc,即Core 1结构)在正常结肠中被掩盖,但在UC患者的炎症上皮中异常暴露。这种改变不仅影响细胞粘附,还可能通过与外源性凝集素(如花生凝集素PNA)结合,促进上皮细胞过度增殖,增加癌变风险。
编辑
关于凝集素可以详见我们之前的文章:
黏蛋白(Mucin)糖基化
MUC2是构成肠道黏液层的主要黏蛋白,其重度O-糖基化是维持黏液屏障功能的关键。
然而,在IBD中,MUC2的糖链变短,硫酸化水平降低,岩藻糖基化和唾液酸化模式也发生改变。这些改变削弱了黏液的保护功能,使其更容易被细菌降解,进而影响肠道的健康。
编辑
免疫细胞糖基化
免疫细胞的糖基化状态也影响其功能。例如,血清IgG的糖基化模式在IBD中发生改变,如半乳糖基化水平下降(agalactosylated IgG),这会改变其与Fc受体的亲和力,从而影响其促炎或抗炎功能。T细胞表面的聚糖分支(如β1-6分支)减少,会降低其激活阈值,使其更易被激活。
编辑
这些糖基化的改变,构成了IBD病理生理学中一个复杂但重要的层面,它们既是炎症的结果,也反过来驱动和维持炎症。
肠道稳态与炎症状态下的黏膜糖基化变化
编辑
doi.org/10.1038/s41385-021-00466-8
左图为稳态,具有完整的黏液层、正常的微生物群和成熟的细胞表面聚糖。
右图为炎症状态,黏液层降解,微生物失调,上皮细胞、免疫细胞和黏蛋白(Muc-2)的糖基化模式均发生显著改变,出现不成熟或异常的聚糖结构。
亚临床炎症
在IBD的临床前扩展期,一个关键特征是亚临床肠道炎症的出现。这可以通过非侵入性生物标志物——粪便钙卫蛋白(fecal calprotectin)的升高来检测。
钙卫蛋白是中性粒细胞释放的一种蛋白,其在粪便中的水平与肠道炎症程度密切相关。在克罗恩病高风险亲属中,基线粪便钙卫蛋白水平升高是未来发病的重要预测指标。
在这方面,谷禾肠道菌群检测报告(临床版)中基于肠道菌群特征预测了粪便钙卫蛋白这指标,若菌群检测提示有害菌过度增殖(如变形菌门)、有益菌减少(如双歧杆菌),且预测钙卫蛋白显著升高,常提示肠道可能存在活动性炎症(如 IBD、感染性肠炎)。
编辑
此外,一些高风险个体在接受胶囊内镜检查时,即使无任何症状,也可能发现小肠黏膜存在炎症性病变。这些亚临床炎症的存在,表明免疫系统的失调已经从分子和细胞水平进展到了组织层面,是疾病即将进入临床期的警报。
综合上述证据,可以构建一个多重组合的IBD发病模型。该模型强调,IBD并非由单一因素引起,而是遗传易感性与一系列环境“刺激”协同作用、累积效应的结果。
第一次刺激(遗传与早期环境)
个体出生时携带IBD易感基因(如NOD2、ATG16L1变异),这构成了发病的遗传基础。在生命早期,暴露于抗生素、不良饮食或特定感染等环境因素,导致肠道微生物群的早期定植异常和免疫系统的“错误编程”,使个体处于高风险状态。
第二次刺激(触发事件)
在随后的生命历程中,一次或多次环境经历,如特定的肠道感染(如诺如病毒)、饮食改变、药物使用或严重的心理压力,成为点燃炎症的“导火索”。这个触发事件在遗传易感个体中打破了原有的免疫稳态。
炎症的启动与自我维持
触发事件导致肠道屏障受损,微生物及其产物易位,激活了固有层的免疫细胞。在具有遗传缺陷的背景下(如NOD2信号通路受损),免疫系统无法进行有效的耐受或清除,而是产生持续的、过度的炎症反应。
例如,促炎细胞因子(TNF, IL-23)大量产生,而抗炎信号(IL-10, SCFAs)减弱。这种炎症环境本身又会进一步加剧微生物失调(如耗氧菌增殖)和屏障破坏(如上皮细胞死亡),形成一个“炎症-失调-屏障破坏”的恶性循环。
疾病的扩展与慢性化
随着时间的推移,这种自我维持的炎症循环导致免疫记忆的形成(如产生针对共生菌的致病性T细胞和IgG抗体)、组织重塑(如成纤维细胞活化导致纤维化)和淋巴结构破坏。当累积的损伤超过机体的代偿能力时,临床症状出现,疾病进入慢性、复发-缓解的病程。
在这个模型中,不同的基因-环境组合可能导致不同的疾病表型。例如,NOD2突变与特定细菌的相互作用可能主要导致小肠炎症,而ATG16L1突变与病毒感染的组合可能以潘氏细胞功能障碍为突出表现。这种异质性也解释了IBD患者在临床过程和治疗反应上的巨大差异(如下图)。
IBD的多重刺激疾病模型
编辑
doi.org/10.1038/s41590-025-02197-5
该图展示了从无疾病到临床前阶段再到晚期IBD的演变过程。遗传变异(如NOD2, ATG16L1)和环境因素(如感染、饮食)共同作用,在临床前阶段引发了微生物失调、免疫细胞活化(如IL-23/TNF产生)和早期上皮损伤。随着疾病进展,炎症加剧,大量免疫细胞浸润,肠道结构遭到严重破坏,形成晚期IBD。图中还标示了潜在的治疗干预靶点。
基于对IBD发病机制,特别是临床前阶段的深入理解,为开发新的治疗和预防策略可能提供了前所未有的机会。
当前治疗策略的挑战
目前的IBD治疗主要依赖于免疫抑制剂,包括糖皮质激素、免疫调节剂(如硫唑嘌呤)和生物制剂(如抗TNF、抗整合素、抗IL-12/23抗体)以及小分子药物(如JAK抑制剂)。这些药物通过抑制炎症反应来控制症状和促进黏膜愈合。但是这些治疗方法目前存在诸多局限:
–非特异性免疫抑制
大多数药物会全面抑制免疫系统,可能增加机会性感染和肿瘤的风险。
–原发性或继发性无应答
有相当一部分患者对初始治疗的疗效欠佳,或在治疗过程中疗效逐渐下降。
–症状缓解而非病因治疗
这些疗法主要通过控制炎症来改善临床症状,但对屏障功能缺陷、肠道菌群失调等根本病因的直接干预相对不足,停药后疾病容易复发。
–不良反应
长期用药可能引发多种药物相关的不良反应,需在临床实践中加强监测。
因此,开发更安全、更具针对性、能够实现无免疫抑制下长期缓解的疗法,是IBD领域的核心目标。
靶向肠道微生物的干预
鉴于微生物失调在IBD中的核心作用,靶向微生物的疗法成为研究热点。这些策略旨在恢复健康的肠道微生态,减少炎症刺激源。
靶向微生物组的干预策略
编辑
doi.org/10.1038/s41579-025-01163-0
微生物组分析可用于IBD的诊断前风险评估、诊断和预后预测。基于此,多种靶向微生物的干预措施正在被探索,包括饮食干预、益生菌、粪菌移植、限定细菌联盟、噬菌体疗法、真菌群调节以及更前沿的工程菌和酵母等。
🌈 饮食干预
特定饮食模式,如全肠内营养(Exclusive Enteral Nutrition, EEN),在儿童克罗恩病中显示出与激素相当的诱导缓解率,其机制可能与改变微生物组成和代谢、减轻肠道抗原负荷有关。
注:EEN 是一种液体单食谱疗法,要求患者在疗程期间完全排除所有固体食物和普通饮料,仅摄入特殊配方奶粉(或者说液体营养补充剂)作为唯一的营养来源。注意,它的蛋白质、脂肪、碳水化合物、维生素和矿物质均已科学配比,能够满足人体全部营养需求。切勿将其误解为普通的“清肠”或“断食”饮食。
—全肠内营养(研究最多的饮食干预措施之一)
全肠内营养(EEN),即在约8周内仅摄入营养完整的液体。EEN在儿童克罗恩病(CD)患者中显示出疗效,约80%的患者在这种饮食后进入缓解期。
目前尚不清楚EEN如何改善IBD症状,但有证据表明它会引起微生物组的变化,多项研究显示EEN饮食下微生物组的多样性降低。尽管微生物组多样性的减少通常与炎症状态相关,但在接受EEN的患者中,这种多样性的减少通常归因于EEN饮食成分的有限性。
对接受EEN饮食的儿童CD患者的粪便微生物组和代谢组分析发现,响应治疗的患者的两者均发生了变化:观察到与IBD发病机制相关的代谢物(包括微生物代谢物尸胺和三甲胺)减少,以及先前升高的氨基酸(丝氨酸、甘氨酸、丙氨酸)水平降低。
降低动物蛋白与动物脂肪摄入:研究表明,动物蛋白会促进肠道致病菌的生长,加重结肠炎。
个体化饮食:由于肠道菌群高度个体化,可通过肠道菌群检测制定更适合精准的饮食方案。
注意:虽然饮食干预是安全的辅助治疗手段,但对于活动期严重的 IBD 患者,饮食调整不建议替代药物治疗。应在专业医生或营养师的指导下进行,并定期监测体重、肠道菌群和营养状态。
编辑
注:现行美国胃肠病学会(AGA)指南指出,除非存在禁忌情况,否则所有IBD患者都可能从地中海饮食中受益。
—关注高发酵食品
一项临床试验比较了高纤维植物性饮食与高发酵食品饮食在健康成年人中的效果:吃发酵食品的个体具有更高的微生物多样性,同时伴随几种炎症标志物(包括IL-6、IL-10和IL-12b)的减少;而高纤维饮食组的微生物多样性保持稳定,微生物组编码的糖苷酶活性酶增加,特定短链脂肪酸亚群减少。
这些发现表明,特定的饮食干预(特别是增加发酵食品的摄入)可以改变微生物组的组成并减少肠道炎症。
这些例子强调了前临床模型在研究膳食添加剂的效果时的重要性,特别是在不同情况下的影响,以及在进行人体干预时考虑特定疾病状态的必要性。因此,这些方法应该被纳入临床研究中。
结合IBD的疼痛机制的营养饮食计划
为炎症性肠病患者制定饮食计划需要综合考虑疼痛机制、营养需求和个体差异。
-核心饮食模式
地中海饮食作为基础,采用高纤维、低饱和脂肪的饮食结构,富含坚果、油性鱼、水果、蔬菜和全谷物。
减少含添加剂、高盐、高糖和高饱和脂肪的食品,研究显示西方饮食模式通过增加氧化应激和免疫激活,加剧疼痛感知。
-个体化饮食调整(根据疼痛类型调整)
伤害性疼痛:活动期避免高纤维食物、坚果、种子和豆类;采用软食或流质饮食减少肠道机械刺激。
神经病理性疼痛:重点补充维生素B12、铜、锌等微量营养素,特别是术后患者。
中枢敏化性疼痛:增加富含抗氧化剂的食物,减少促炎食物,考虑肠-脑轴调节。
-关键营养干预
——维生素B12管理
高风险人群,比如回肠切除患者即使血清水平正常也应考虑补充。
缺乏者每周1000μg注射4周后每月维持,或口服1000-2000μg/天,改善神经性疼痛、疲劳,预防多维生素缺乏。
——维生素D
常规筛查和补充,改善骨健康和免疫调节。
——锌和铜
短肠综合征或长期腹泻患者特别需要关注
锌:慢性腹泻患者每日25-50mg,长期补充需同时补铜1-2mg
铜:减肥手术或短肠患者每日2-4mg,监测神经功能
——肉碱与能量支持
适用:慢性疲劳、神经性疼痛患者。
L-肉碱500-1000mg每日2-3次,可与辅酶Q10(100-200mg/天)联用。
食物质地优化
蒸煮、切碎、浸泡软化高纤维食物。
狭窄风险者控制食物颗粒<5mm,术后早期采用泥状食物
软化而非完全排除纤维,保留营养价值。
实施要点
基线全面评估→风险分层→个体化处方→多学科协作→4-8周随访调整(菌群动态监测)。
通过菌群数据指导精准营养干预,使其成为IBD综合治疗的核心组成部分。
🌈 益生菌
在炎症性肠病(IBD)中,益生菌的临床试验结果不一,这部分可能是由于现有益生菌在改变微生物组的组成和功能方面效果有限。
一种包含多种菌株的混合益生菌(如Lactobacillus spp.、Bifidobacterium spp.、Streptococcus spp.,即VSL#3),在诱导轻度至中度溃疡性结肠炎的缓解方面比安慰剂更有效,并且在预防复发性袋状结肠炎方面也显示出疗效。
E. coli Nissle 1917在溃疡性结肠炎患者中也表现出临床疗效,但相关研究较为有限。
新型益生菌菌株
近期研究发现,源自人乳的新型益生菌菌株短双歧杆菌SHMB 8001在DSS诱导的小鼠结肠炎模型中展现出显著治疗潜力。
该菌株通过多重机制发挥保护作用:增强肠道屏障功能(上调MUC2、occludin和claudin-1蛋白表达)、调节免疫炎症反应(上调IL-10并抑制IL-1β、IL-6和TNF-α)、提高粪便短链脂肪酸水平和结肠GPR43受体表达,以及重塑肠道微生物群(富集产短链脂肪酸菌属如双歧杆菌、乳酸杆菌)。
编辑
🌈 益生元
在炎症性肠病中研究最多的益生元包括低聚果糖和菊粉,其益处不一致。新研究有望通过引入合理设计的菌株群落,使其能够以条件依赖的方式定植或递送益生元,需要更多研究。
编辑
🌈 合生元
合生元通过益生菌与益生元的协同作用,在IBD治疗中展现出独特优势。临床前研究证实,多种合生元组合能有效减轻肠道炎症、调节免疫反应、增强屏障功能并改善菌群平衡。
编辑
未来需要更多研究来阐明作用机制、确定最佳组合方案,并探索其与常规疗法的协同效应。
🌈 后生元
后生元是指灭活微生物及其组分或代谢产物,能为宿主带来健康益处。这些成分通过调节免疫反应、抑制NF-κB通路、激活自噬等机制发挥抗炎作用,同时能重塑肠道菌群平衡。
编辑
相比活菌制剂,后生元具有稳定性高、安全性好、易于制剂开发等优势,为IBD治疗提供了新的微生物组靶向策略,但其临床应用仍需更多研究验证。
🌈 粪菌移植(FMT)
将健康捐赠者的粪便微生物群移植给患者,旨在重建健康的肠道生态。FMT在治疗复发性艰难梭菌感染中取得了巨大成功,但在IBD中的疗效尚不稳定,尤其是在克罗恩病中。其成功率受供体选择、移植方式以及受体宿主环境(如免疫状态)等多种因素影响。
在五项FMT的随机对照试验中,由于供体、给药方式和持续时间的不同,四项显示出统计学上的显著益处,缓解率在24%~53%之间。在FOCUS试验的长期随访中,35名在8周内通过每周FMT达到缓解的患者中,有34%在1年后仍保持缓解,这部分得益于自我启动的FMT(3名患者)或饮食改变(9名患者)。
间歇性低频FMT
在一项研究中,87%的患者能够通过每8周进行一次FMT维持临床缓解,持续达48周,尽管不到一半的患者实现了内镜缓解。
供体和受体特定因素
在一项针对UC的随机对照试验中,使用两个不同供体的反应率分别为10%和39%,这表明疗效存在差异。Roseburia inulinivorans和Eubacterium halli的富集,以及粪便短链脂肪酸的增加与缓解相关,而Escherichia spp.、Fusobacterium spp.和Candida spp.的增加则与缺乏反应相关。
FMT前Candida spp.丰度的增加与临床反应相关,而FMT后Candida spp.丰度的降低则表明疾病严重程度减轻。
在UC患者中,FMT前高丰度的白色念珠菌与FMT后细菌多样性增加和治疗成功率提高相关,表明真菌生态可能在细菌定植中发挥作用。
肠道菌群检测结合粪菌移植(FMT)可提高治疗炎症性肠病的疗效。通过持续干预和菌株动态管理,有助于用有益菌株替代疾病相关菌株,确保长期稳定性和定植。
🌈 限定细菌联盟与工程菌
基于对有益菌功能的理解,开发由特定功能的、明确的细菌菌株组成的活体生物药是更精准的策略。例如,包含产丁酸菌的菌群联盟或下一代益生菌。
关于下一代益生菌,详见谷禾文章:
更进一步,可以利用合成生物学技术,设计能够感知肠道炎症信号并原位分泌抗炎分子(如IL-10)或降解有害代谢物的“智能”工程菌。
🌈 噬菌体疗法
噬菌体(phages)是一种自我复制的病毒,能够感染细菌并利用其细胞机制进行复制。噬菌体针对多重耐药细菌的能力使其在炎症性肠病中的应用成为可能。
一种针对克雷伯氏肺炎菌的五种噬菌体组合在人体肠道IBD模型中有效抑制了肠道炎症,且健康志愿者食用后显示出良好的安全性和在下肠道的积累。
VE202是一种活性生物治疗产品,含有有益的梭状芽孢杆菌菌株,已在健康成年人中显示出安全性,为溃疡性结肠炎患者的潜在治疗试验铺平了道路(NCT05370885)。
一种包含10个菌株的18种厚壁菌门菌群(SER-301)在轻度至中度UC患者中测试,初步结果良好,但在2期试验中未能诱导临床缓解。
另一项涉及六种菌株的组合(MH002)的2a期随机对照试验显示,轻度至中度UC患者在使用该组合后,内镜Mayo评分改善了17%,并且粪便钙卫蛋白显著减少。
利用对细菌具有高度特异性的噬菌体,可以精准清除肠道中的特定病原菌(如AIEC、肺炎克雷伯菌),而不影响有益菌群,是一种极具潜力的微生物手术刀。
编辑
doi.org/10.1016/j.bpg.2025.102060
促进黏膜愈合的非免疫抑制疗法
与抑制炎症不同,直接促进肠道上皮修复和再生是另一条有吸引力的治疗路径,有望在不依赖免疫抑制的情况下实现黏膜愈合。
增强屏障功能
开发靶向紧密连接的药物,如MLCK抑制剂(如Divertin),可以直接增强上皮屏障的完整性,减少微生物易位。
靶向干细胞微环境
肠道干细胞(ISCs)是上皮再生的源泉。利用促进ISC增殖和分化的生长因子,如IL-22、GLP-2类似物(如替度格鲁肽),或通过移植间充质干细胞(MSCs)来改善干细胞微环境,是促进组织修复的潜在策略。
2024年2月23日,武田中国宣布,GLP-2(胰高血糖素样肽-2)类似物替度格鲁肽,正式获得NMPA批准,适用于治疗短肠综合征(SBS)成人和1岁及以上儿童患者。由此,替度格鲁肽由此成为中国首个治疗短肠综合征的GLP-2类似物。GLP-2的核心作用,则是调节胃肠道细胞的生长、增殖。
GLP-2当前唯一明确的适应症,是用于治疗短肠综合症,帮助患者吸收营养物质。短肠综合症主要病因是大规模小肠切除手术导致的肠道面积减少,从而引发营养吸收不良,造成其他综合症状。
目前,已有的治疗方式是通过肠外营养技术,为患者直接提高营养物质;或通过肠道修复增加对营养物质的吸收。
GLP-2药物恰好能够达成这一目标,其能够增加肠道上皮细胞,扩大接触面积,同时抑制肠胃蠕动,延长胃排空时间,从而增加肠道吸收。从临床数据来看,替度格鲁肽也的确给患者带来了新希望。
类器官移植
利用患者自身的干细胞在体外培养出“迷你肠道”(肠道类器官),再将其移植回受损的肠道黏膜,有望实现自体组织的再生和修复。这一技术虽然仍处于实验阶段,但展现了巨大的应用前景。
然而,促进再生也需警惕潜在风险,如过度增殖可能增加肿瘤形成的风险,以及再生与纤维化通路之间的重叠。因此,需要精准调控这些再生通路。
促进黏膜愈合的潜在治疗靶点
编辑
doi.org/10.1038/s41575-022-00604-y
黏膜愈合涉及多个层面,包括微生物群、饮食、肠道屏障、免疫细胞和干细胞微环境。图中展示了针对这些不同层面的潜在疗法,如通过饮食干预调节微生物,通过MLCK抑制剂增强屏障,通过IL-22或干细胞移植促进干细胞微环境的再生。
临床前干预与预防的展望
IBD漫长的临床前阶段为疾病预防提供了宝贵的时间窗口。未来的策略将聚焦于在高风险人群中进行早期筛查和干预。
风险分层
通过整合遗传风险评分、家族史、环境暴露史以及临床前生物标志物(如血清抗体、粪便钙卫蛋白、微生物组特征),可以识别出IBD的高风险个体。
早期干预
对于高风险人群,可以在临床前阶段采取干预措施。
例如,对于低风险个体,可以推荐改善饮食和生活方式;对于中高风险个体,可以考虑使用益生菌、益生元或靶向微生物的疗法。
对于即将进入临床期的极高风险个体,甚至可以考虑使用低剂量的免疫调节剂或靶向药物进行“截断治疗”,以阻止疾病的最终发生,类似于在1型糖尿病和类风湿关节炎领域已取得成功的预防性治疗。
实现这一目标需要更精准的生物标志物来动态监测疾病进程,以及更安全有效的早期干预手段。同时,必须关注并解决不同人群在疾病风险和医疗可及性上的差异。
炎症性肠病是一种由遗传与环境因素复杂相互作用驱动的慢性免疫介导疾病。其发病并非一蹴而就,而是经历了一个漫长的、多阶段的临床前演变过程。在这一过程中,肠道屏障功能的逐步丧失、微生物生态的持续失调、以及宿主免疫应答的异常活化和耐受丧失,共同构成了驱动疾病发展的核心病理生理学基础。基因-微生物相互作用,如NOD2通路的功能障碍,以及糖基化等翻译后修饰的改变,在这一过程中扮演了关键的调控角色。
未来的研究应致力于开发更灵敏、更特异的生物标志物组合,以实现对高风险人群的精准识别和疾病进程的动态监测。其中,肠道菌群检测作为评估微生物生态状态的重要手段,结合宿主免疫标志物和遗传风险评分,有望为临床前IBD的早期识别提供多维度的评估依据。如文中所述,特定菌群特征的变化可能先于临床症状出现,这为疾病风险分层和早期干预提供了潜在的时间窗口。
治疗上,应从单一的免疫抑制转向更加多元化和个体化的策略,包括靶向微生物组的生态疗法、直接促进黏膜修复的再生医学方法,以及在疾病极早期进行干预的截断治疗。科学界越来越关注在疾病自然史的早期阶段实施精准干预的可能性,通过整合多组学数据和动态生物标志物监测,有望在正确的时间对合适的个体实施优化的干预策略,从而改变IBD的疾病轨迹,推动临床实践从疾病治疗向风险预防的范式转变。
注:本账号内容仅供学习和交流,不构成任何形式的医疗建议。
主要参考文献:
Cadwell K, Loke P. Gene-environment interactions shape the host-microbial interface in inflammatory bowel disease. Nat Immunol. 2025 Jul;26(7):1023-1035.
Iliev ID, Ananthakrishnan AN, Guo CJ. Microbiota in inflammatory bowel disease: mechanisms of disease and therapeutic opportunities. Nat Rev Microbiol. 2025 Aug;23(8):509-524.
Deleu S, Sabino J. Cutting edge developments and novel targets in IBD: Microbiome in IBD. Best Pract Res Clin Gastroenterol. 2025 Sep;78:102060.
Vaghela, P., Dave, B., Dabhade, A. et al. Redrawing the gut map: evolving probiotic approaches to microbiota modulation in inflammatory bowel disease. Antonie van Leeuwenhoek 119, 51 (2026).
Villablanca EJ, Selin K, Hedin CRH. Mechanisms of mucosal healing: treating inflammatory bowel disease without immunosuppression? Nat Rev Gastroenterol Hepatol. 2022 Aug;19(8):493-507.
Brazil JC, Parkos CA. Finding the sweet spot: glycosylation mediated regulation of intestinal inflammation. Mucosal Immunol. 2022 Feb;15(2):211-222.
Rudbaek JJ, Agrawal M, Torres J, Mehandru S, Colombel JF, Jess T. Deciphering the different phases of preclinical inflammatory bowel disease. Nat Rev Gastroenterol Hepatol. 2024 Feb;21(2):86-100.
Jang KK, Heaney T, London M, Ding Y, Putzel G, Yeung F, Ercelen D, Chen YH, Axelrad J, Gurunathan S, Zhou C, Podkowik M, Arguelles N, Srivastava A, Shopsin B, Torres VJ, Keestra-Gounder AM, Pironti A, Griffin ME, Hang HC, Cadwell K. Antimicrobial overproduction sustains intestinal inflammation by inhibiting Enterococcus colonization. Cell Host Microbe. 2023 Sep 13;31(9):1450-1468.e8.
Liu G, Wang X, Hao Y, Tu L, Mei Y, Zhang T, Wang Y. Bifidobacterium Breve SHMB 8001 Alleviates DSS-Induced Colitis in Mice Via Modulating the Intestinal Barrier and Gut Microbiota. J Food Sci. 2026 Feb;91(2):e70903.

谷禾健康
明明滴酒未沾,却突然出现醉酒症状:说话含糊、步态不稳、意识模糊,严重者甚至被交警查出酒驾。
这听起来像天方夜谭,但在医学上,这是一种真实存在的罕见疾病——自酿综合征(Auto-Brewery Syndrome, ABS),也称为肠道发酵综合征。
其核心特征是:在未摄入外源性酒精的情况下,肠道微生物异常发酵碳水化合物,产生并吸收过量乙醇,使血液/呼气酒精水平可达到甚至超过法定阈值,从而出现类似醉酒的一系列神经与胃肠道症状。由于临床表现与饮酒高度相似,自酿综合征在现实中常被误解为酒精依赖、精神问题或刻意隐瞒饮酒史,患者往往经历漫长的误诊与社会压力,甚至常面临法律纠纷。
研究显示,70%的自酿综合征患者报告曾被朋友或家人怀疑撒谎,40%因此失去工作。提高公众和医疗界对ABS的认知,是改善患者生活质量的关键。
近期发表在《Nature Microbiology》的一项研究,通过对22名ABS患者和21名健康家庭成员的系统分析,首次揭示了这种罕见病的微生物学机制,为我们打开了一扇理解肠道菌群与人体健康关系的新窗口。
编辑
本文从自酿综合征的临床表现切入,结合最新《Nature Microbiology》上发表的研究队列从“菌群组成—功能通路—代谢物—体外发酵验证”四个层面系统呈现 ABS 的微生物学机制:发作期以变形菌门(肠杆菌科)异常富集为特征,血液酒精浓度与其相对丰度正相关;宏基因组功能注释显示混合酸发酵、异型乳酸发酵及乙醇胺利用等产醇相关通路显著增强,代谢组学提示乙酸显著升高并与醉酒程度关联。
在此基础上,本文进一步梳理易感人群与诱因、诊断思路与鉴别要点,并结合宏基因组与代谢证据说明产乙醇菌群的形成与维持机制;鉴于常规干预在部分患者中疗效有限且复发风险较高,本文还引入 FMT 个案,作为微生态“重置”策略的临床补充证据,为理解菌群干预与症状逆转之间的关联提供线索。
编辑
从未喝酒,为何会醉酒?
自酿综合征(简称ABS)是一种由于肠道微生物异常发酵碳水化合物,产生过量乙醇(也就是酒精)而导致的罕见代谢紊乱疾病。
患者在没有摄入任何酒精的情况下,血液酒精浓度可达到甚至超过法定酒驾标准(80 mg/dL),出现典型的醉酒症状。这种疾病最早于1948年由Ladkin和Davies首次报道,当时一名5岁非洲男孩因肠道异常发酵导致严重腹胀和穿孔死亡。
在日本,这种疾病被称为”meitei-sho”(肠内酒精发酵综合征),并在20世纪70年代有过系列报道。而在现代医学中,自酿综合征仍然常常被误诊为酒精依赖或精神疾病,许多患者在确诊前往往经历数年的误诊和社会误解。
患者的真实困境:从酒鬼到患者
Malik等人在2019年报道了一个典型案例:一名46岁男性在接受头孢类抗生素治疗拇指外伤后,出现性格改变、抑郁和脑雾症状。一次清晨,他因疑似酒驾被捕,血液酒精浓度高达200 mg/dL,但他坚称未饮酒。经过多次辗转,最终通过粪便检测发现大量酿酒酵母(Saccharomyces cerevisiae),确诊为自酿综合征(ABS)。
“最令人心碎的是,连医生和警察都不相信我没有喝酒。我被贴上了酒鬼的标签,失去了工作和朋友的信任。直到确诊ABS,我才终于洗清了冤屈。”
—— ABS患者自述
这种疾病不仅带来身体上的痛苦,更带来严重的社会和法律问题。据统计,已有多起ABS患者因酒驾被起诉后,通过医学证据最终被判无罪的案例。
如果说自酿综合征(ABS)是一个没喝酒也会醉的怪病,那么它的本质,其实就是肠道微生态,被重塑成了一座高效的小型酿酒厂。这一章节,我们就沿着最新《Nature Microbiology》队列研究的证据,看看这座酿酒厂是如何一步步搭建起来的。
自酿综合征:从正常发酵到病理酿酒
正常情况下,肠道菌群处于动态平衡状态,少量乙醇的产生会被肝脏迅速代谢。但在ABS患者中,这种平衡被打破,特定微生物过度生长,将摄入的碳水化合物大量转化为乙醇。
而在 ABS 患者身上,发生了三件关键的事:
1
菌群结构改变
原本占主导的共生菌减少,某些能高效产乙醇的细菌占位。
2
代谢通路重编程
多条能把糖和乙醇胺酿成酒的通路被全面激活。
3
代谢产物堆积,并进入血液
乙醇与相关代谢物(尤其是乙酸)在肠道内大量生成、被吸收,超出肝脏清除能力,如果超过一定量,甚至会诱发系统性中毒。
下面我们分步骤拆解这三层变化。
菌群失衡:谁在主导酿酒?
变形菌门(Proteobacteria)显著富集
在这项纳入 22 名经严格口服葡萄糖激发试验证实的 ABS 患者、21 名家庭伴侣和一组健康对照的研究中,宏基因组测序有一个醒目的共同点:
编辑
编辑
⭐️ 三个关键的酿酒菌(产乙醇)
多变量分析(校正家庭环境影响)指出了三种重要的菌群:
大肠杆菌(Escherichia coli)
肺炎克雷伯菌(Klebsiella pneumoniae)
Ruminococcus gnavus
⭐️ 有益菌下降
编辑
总的来说,ABS患者整个微生态从多样而稳定,滑向“低多样性 + 病理性富集”的状态。
产乙醇代谢通路拉满
如果说上述菌群失衡回答了谁在干,那代谢通路分析则是回答了他们在干什么。
研究利用宏基因组功能注释,对代谢通路进行比对,发现:
其中,与乙醇生产直接相关、在发作期明显富集的关键通路包括:
编辑
⭐️ 混合酸发酵通路(Mixed‑acid fermentation)
编辑
⭐️ 异型乳酸发酵通路(Heterolactic fermentation)
⭐️ 乙醇胺利用通路(Ethanolamine utilization)
乙醇胺来自于肠道上皮细胞膜磷脂的分解,是一种内源性氮源和碳源。一些细菌可以通过专门的乙醇胺利用操纵子,把乙醇胺转化为乙醛、乙酰‑CoA,最终还原为乙醇。
在 ABS 发作期:
编辑
⭐️ 基因水平与血液酒精浓度高度相关
研究者发现,所有与酒精脱氢酶活性相关基因总丰度,与患者的血液酒精浓度高度相关(Spearman R = 0.72,P=2.7×10⁻⁶)。
编辑
这就把微生物基因层面与临床醉酒程度直接关联起来,不是只有菌在那儿摆着,而是在真正参与乙醇的大量生产。
体外实验证实:这些菌真的在酿酒
为了避免一切只是推测,研究团队还做了一个非常关键的实验——体外粪便厌氧培养测乙醇。
取 100 mg 粪便,在含葡萄糖的厌氧培养基中培养 24 小时,并在 0、6、24 小时测定培养液中的乙醇浓度(HPLC/酶法)。结果显示:
ABS 发作期样本:中位乙醇浓度约 14.47 mg/dL;
同一患者缓解期样本:约 8.76 mg/dL;
家庭伴侣样本:约 5.00 mg/dL。
ABS 发作期(flare)样本的体外产乙醇能力更强,并且与采样时的血液酒精浓度相关。
关键菌群:细菌而不是真菌
自 ABS 被提出以来,很多早期病例把矛头指向肠道酵母过度生长,临床上因此常常首选抗真菌药物治疗。但这项队列研究给出了更细致的答案。
在体外培养体系中加入不同药物:
广谱抗生素——氯霉素
广谱抗真菌药——两性霉素B
代谢产物:乙酸是ABS的生物标志物
除乙醇外,ABS患者的粪便代谢组学分析显示,ABS 发作期患者的粪便乙酸水平显著高于家庭伴侣(P=1.2×10⁻⁵),且与血液酒精浓度呈正相关(R=0.6, P=0.00018)。
乙酸是乙醇代谢的中间产物,同时也可作为底物被某些细菌用于乙醇合成,形成乙醇-乙酸循环,这可能是ABS患者乙醇持续产生的另一重要原因。
编辑
在菌群–代谢物相关性分析中:
乙酸水平与 Escherichia、Blautia 等菌属呈正相关;与 Akkermansia 等典型有益菌负相关。
也就是说,比起频繁做口服葡萄糖激发试验,监测粪便乙酸或许在随访中更具可行性。
抗生素
多项研究表明,抗生素使用是ABS常见的诱因。抗生素会破坏肠道正常菌群平衡,导致产乙醇菌过度生长。
在Malik报道的案例中,患者在使用头孢氨苄(cephalexin)3周后出现ABS症状。
另一项研究发现,长期使用阿莫西林-克拉维酸、甲硝唑等广谱抗生素的患者,肠道变形菌门比例显著增加,ABS风险提。
基础疾病:肠道动力障碍与吸收不良
ABS常与以下基础疾病相关:
短肠综合征
肠道切除后,食物通过加快,碳水化合物未充分吸收即进入结肠,成为产乙醇菌的底物。
克罗恩病
肠道炎症和狭窄导致食物滞留,促进细菌过度生长。
糖尿病
高血糖环境促进酵母和某些细菌生长,研究显示糖尿病患者内源性乙醇水平显著高于健康人。
胃轻瘫
胃排空延迟导致食物在胃肠道停留时间延长,增加发酵机会。
饮食因素:吃太多碳水化合物
饮食中的碳水化合物是肠道菌群产乙醇的原料。研究发现,ABS患者在摄入高碳水化合物食物(如面包、 pasta、含糖饮料)后,症状明显加重,血液酒精浓度可在2-8小时内达到峰值。
一项病例报告显示,一名ABS患者在食用披萨和苏打水后,血液酒精浓度迅速升至400 mg/dL,出现严重醉酒症状。
遗传因素:酒精代谢酶的个体差异
酒精脱氢酶(ADH)和乙醛脱氢酶(ALDH)的基因多态性可能影响ABS的临床表现。
亚洲人群中常见的ALDH2*2突变(导致乙醛脱氢酶活性降低),可能使ABS患者更容易出现乙醛蓄积,加重醉酒症状。
警惕这些不寻常的醉酒症状
ABS的临床表现与普通醉酒相似,但具有以下特点:
关键诊断试验:碳水化合物激发试验
碳水化合物激发试验具体步骤如下:
1. 患者需禁酒48小时,空腹8小时
2. 基线血液酒精浓度和尿酒精代谢物(乙基葡萄糖醛酸苷、乙基硫酸酯)检测
3. 口服100-200克葡萄糖(或标准化碳水化合物餐)
4. 在0.5、1、2、4、8、12、24小时监测血液酒精浓度。
5. 若任何时间点血液酒精浓度≥0.01 g/dL(10 mg/dL),且排除外源性酒精摄入,则可诊断ABS。
注意:该试验需在严格医疗监督下进行,因为部分患者可能出现严重醉酒,甚至酒精中毒。
微生物检测
通过肠道菌群检测,可以从产乙醇相关菌群(如大肠杆菌、肺炎克雷伯菌)是否超标,以及相关代谢通路是否异常,来辅助判别是否存在自酿综合征的可能。
排除其他疾病
ABS需与以下疾病鉴别:
-酒精依赖
患者通常隐瞒饮酒史,尿酒精代谢物检测阳性
-肝性脑病
肝功能异常,血氨升高,无肠道产乙醇证据
-糖尿病酮症酸中毒
血糖显著升高,尿酮体阳性
-药物中毒
如苯二氮䓬类、阿片类药物过量
-罕见神经系统疾病
如发作性共济失调、卟啉病
饮食干预:减少酿酒原料
低碳水化合物饮食是ABS的基础治疗。具体建议包括:
一项病例系列研究显示,80%的ABS患者在严格低碳水饮食(每日碳水化合物<50克)6周后,症状显著改善,血液酒精浓度恢复正常。
抗生素治疗
根据微生物检测结果选择针对性药物,例如利福昔明、甲硝唑等。需注意,抗生素可能进一步破坏肠道菌群平衡,因此通常仅在严重病例中短期使用,可以考虑同时联合益生菌治疗。
益生菌调节
益生菌可通过竞争营养和黏附位点,抑制产乙醇菌生长。研究显示,Lactobacillus acidophilus、Bifidobacterium infantis等菌株可降低ABS患者肠道pH值,减少乙醇产生。
一项病例报告显示,一名ABS患者在使用多菌株益生菌(含12种细菌)1.5年后,症状缓解,可正常饮食。
长期管理:预防复发的关键
ABS治疗后复发率较高,长期管理需注意:
虽然前述多种常规治疗手段(包括抗生素、限制碳水、益生菌等)能在部分病例短期内缓解 ABS 症状,但对病情较重或反复发作的病例而言,疗效往往不够理想,难以在短时间内达到预期的控制目标。
对于难治性ABS,粪菌移植(FMT)可能是一种值得考虑的选择。该研究报道了一例ABS患者接受多轮FMT并长期随访的案例。这不仅丰富了我们对ABS发生机制的认识,也为探索菌群干预在临床治疗中的应用潜力提供了重要参考。
因此,我们将在下一章对 FMT 的这个案例进行专门介绍。
这个FMT案例是围绕单个患者的多轮 FMT、长期随访与宏基因组分型,系统性地提供了微生态干预下 ABS 逆转的因果证据。
粪菌移植干预过程和结果
患者背景
第一次 FMT:暂时好转
在 FDA 单例扩展使用批准下,接受:
结果:
第二次FMT
在首次FMT后9个月接受了第二次FMT。
采样时间线
编辑
这次口服万古霉素、甲硝唑和复方新诺明预处理3天,随后进行肠道准备。
注:
文中对该方案的解释:第一次用利福昔明与新霉素主要为肠腔内抗生素,全身吸收很少;
而第二次加入的甲硝唑与复方新诺明为可全身吸收抗生素,旨在不仅作用于肠腔内微生物,也可覆盖肠腔外/黏膜相关部位,包括绒毛刷状缘与肠隐窝等微生物,可能以生物膜或低代谢状态持续存在的部位。
给药与维持:预处理后先给 3 次、每次 15 粒胶囊;随后在不再预处理的情况下,用同一供者来源胶囊进行每月维持 15 粒,持续 6 个月。
辅助措施(促进定植):
同时嘱咐每日服用一大汤匙马铃薯淀粉,约 60% 抗性淀粉,溶于水;
复合益生菌每日 1 粒,含 Bifidobacterium infantis、Clostridium butyricum、Clostridium beijerinckii、Anaerobutyricum hallii、Akkermansia muciniphila,以促进移植菌群的持续存在/定植。
结果:
肠道菌群变化与临床关联
粪菌移植后菌群结构变化
第一次 FMT 后的缓解期样本,在主成分图上与供体的菌群组成聚在一起;
症状复发时,样本又跑回类似初始发作期的菌群结构。
第二次 FMT 后,菌群持续稳定且不同于术前/家庭成员菌群。
编辑
主成分贡献最大的菌
编辑
发作期 E. coli 丰度高;K. pneumoniae、R. gnavus 未显著增加。
编辑
FMT后大肠杆菌丰度、血液酒精浓度和发酵通路基因显著降低。
代谢和临床指标相关性
菌群应答、血乙醇浓度、AST/ALT、产醇相关通路丰度紧密相关。
编辑
同一时间轴上同时给出 BAC(血/呼气酒精)、AST/ALT、以及 fermentation pathway enrichment(混合酸发酵/异乳酸发酵/乙醇胺利用等的富集指标),并与菌群变化/发作缓解标注对应。
症状与供者菌株植入率正相关;与术前菌株保留(post-FMT 与 pre-FMT 共享比例)负相关。
编辑
总的来说,对这位患者而言,ABS 的发生与一个特定高产乙醇耐乙醇的大肠杆菌菌株群落密切相关;通过 FMT + 系统性抗生素预处理,成功完成菌群置换,症状得以长期缓解。
自酿综合征(ABS)表面上是一种罕见而离奇的疾病,却在机制、诊断与干预的层层展开中,清晰指向同一个核心事实:肠道菌群具备强大的代谢能力,其结构与功能的失衡,足以在人体内酿出可被检测、可致症状的乙醇水平。
面向未来,ABS 的意义并不止于罕见病本身。研究提示,即便在非 ABS 人群中也可能存在低水平内源性乙醇产生,这一现象或与非酒精性脂肪肝、肥胖等代谢异常相关;例如,肺炎克雷伯菌产生的乙醇可诱导动物出现肝脏脂肪变性。由此,ABS 也可能成为理解“菌群—代谢疾病”连接机制的窗口,并为常见代谢病提供新的干预靶点。
治疗层面,ABS 有望走向更具针对性的精准医疗路径:
与此同时,提高诊断率同样关键——ABS 的真实患病率可能被低估(有研究估计每 10 万人中或有 1–2 例),推动临床认知、完善流程并探索更便捷的检测手段(如肠道菌群检测),将有助于患者更早被识别、更少陷入误解与法律困境。
当肠道菌群喝醉,我们需要做的不仅是控制血液酒精和缓解症状,更是把 ABS 放回宿主—微生物共生系统的框架中重新理解:这并非人体的例外,而是微生物代谢能力在特定条件下的极端呈现。
通过提高认知、规范诊断与发展靶向菌群治疗,我们或许不仅能更好地帮助 ABS 患者,也能借此进一步理解菌群在代谢健康中的位置与边界。
在这个由 100 万亿微生物组成的“超级器官”面前,我们对生命的理解或许才刚刚开始。
主要参考文献
Hsu CL, Shukla S, Freund L, Chou AC, Yang Y, Bruellman R, Raya Tonetti F, Cabré N, Mayo S, Lim HG, Magallan V, Cordell BJ, Lang S, Demir M, Stärkel P, Llorente C, Palsson BO, Mandyam C, Boland BS, Hohmann E, Schnabl B. Gut microbial ethanol metabolism contributes to auto-brewery syndrome in an observational cohort. Nat Microbiol. 2026 Jan 8.
Dinis-Oliveira RJ. The Auto-Brewery Syndrome: A Perfect Metabolic “Storm” with Clinical and Forensic Implications. J Clin Med. 2021 Oct 10;10(20):4637.
Malik F, Wickremesinghe P, Saverimuttu J. Case report and literature review of auto-brewery syndrome: probably an underdiagnosed medical condition. BMJ Open Gastroenterol. 2019 Aug 5;6(1):e000325.
Xue G, Feng J, Zhang R, Du B, Sun Y, Liu S, Yan C, Liu X, Du S, Feng Y, Cui J, Gan L, Zhao H, Fan Z, Cui X, Xu Z, Fu T, Li C, Huang L, Zhang T, Wang J, Yang R, Yuan J. Three Klebsiella species as potential pathobionts generating endogenous ethanol in a clinical cohort of patients with auto-brewery syndrome: a case control study. EBioMedicine. 2023 May;91:104560.
Tameez Ud Din A, Alam F, Tameez-Ud-Din A, Chaudhary FMD. Auto-Brewery Syndrome: A Clinical Dilemma. Cureus. 2020 Oct 16;12(10):e10983.

谷禾健康
精神分裂症(SCZ)是一种严重的持续性精神障碍,表现为阳性症状(如妄想和幻觉)、负性症状(如动力丧失和社交退缩)以及认知症状(包括工作记忆和认知灵活性缺失)。此外,大多数精神分裂症患者伴有显著的睡眠障碍(SD),常出现入睡困难、睡眠维持问题、睡眠结构紊乱和昼夜节律失调。
睡眠障碍这种共病会加重精神症状,导致更频繁的偏执意念、幻觉和思维紊乱,以及更高程度的抑郁和焦虑。还显著影响治疗依从性和长期预后。
精神分裂症的发病机制涉及遗传、环境、免疫和神经发育等多种因素的相互作用。与此同时,现有研究表明,肠道微生物群通过微生物群-肠道-大脑轴调节大脑功能,影响神经递质的代谢和免疫炎症反应,因此可能在精神分裂症和睡眠障碍的发生和发展中发挥重要作用。
精神分裂症患者常表现出产丁酸细菌减少、产乳酸菌增加,以及与谷氨酸和γ-氨基丁酸(GABA)代谢相关的细菌增加。特别是,在精神分裂症患者中,这种肠道微生物群破坏可能通过影响神经递质平衡、促进神经炎症和干扰昼夜节律等机制,促成精神症状和睡眠问题的发展。
本文整合了现有研究,首先介绍了精神分裂症(SCZ)和睡眠障碍(SD)患者的肠道微生物群特征。探讨了SCZ和SD中关键微生物群及其代谢物的共同影响,以及肠道微生物群通过神经免疫、内分泌和神经递质通路的作用机制。最后,提出了针对肠道微生物群的干预策略在改善精神分裂症伴随SD中的潜在应用。
精神分裂症(SCZ)是一种严重的精神障碍,表现为阳性症状(超出正常范围的行为和思维)如妄想和幻觉;负性症状(缺乏正常的情感和行为)如动力丧失和社交退缩;以及认知症状,包括工作记忆和认知灵活性的缺失。
★ 许多精神分裂症患者伴有睡眠障碍
除了典型的精神症状外,睡眠障碍(SD)是精神分裂症最常见的共病之一,表现为失眠、睡眠片段化、慢波睡眠减少和昼夜节律紊乱。
研究显示,约80%的精神病患者至少患有一种类型的SD。睡眠质量的恶化会加重精神症状,导致更频繁的偏执意念、幻觉和思维紊乱,以及更高程度的抑郁和焦虑。研究发现,睡眠质量受损和昼夜节律紊乱的精神分裂症(SCZ)患者在负性症状评估上得分更高,认知功能障碍更为明显。
此外,SD不仅加重精神分裂症的精神病症状,精神分裂症的核心症状也会破坏睡眠生理。多导睡眠图研究表明,更严重的阳性症状与短的快速眼动(REM)潜伏期、长的入睡潜伏期和低睡眠效率相关,而明显的负性症状与非快速眼动(NREM)睡眠中的慢波振幅降低和REM起始潜伏期缩短有关。
这些发现表明精神分裂症与睡眠障碍之间存在双向病理循环,睡眠障碍不仅是精神分裂症的常见共病,也是影响其症状表达和疾病进展的关键因素。
1
流行病学特征
研究表明,精神分裂症(SCZ)患者的睡眠障碍(SD)患病率显著高于普通人群,影响其生活质量和疾病预后。
精神分裂症患者快速眼动睡眠时间缩短
通过睡眠脑电图(EEG)观察精神分裂症患者与健康对照组的睡眠结构差异发现,精神分裂症患者的快速眼动(REM)潜伏期缩短,REM密度增加,并且REM睡眠比例与症状严重程度密切相关。在非快速眼动(NREM)睡眠期间,精神分裂症患者呈现慢波睡眠减少、纺锤体波密度和振幅下降,以及持续时间缩短。
不同精神分裂症患者睡眠障碍也表现出差异
同时,不同精神分裂症患者组间的睡眠障碍表现也存在显著差异,例如,住院患者在睡眠时间、活动水平和生物钟稳定性方面较门诊患者表现更加严重。这表明精神分裂症临床症状的严重程度不仅取决于病理机制,还受到患者生活环境和治疗状态等多种因素的影响。
2
睡眠障碍对精神分裂症的影响
夜间睡眠不足会进一步导致白天功能障碍和生活质量下降。大量临床研究证实,睡眠障碍与精神分裂症患者核心症状组之间存在显著且特异的关联模式。
睡眠障碍会加重精神分裂症症状并影响治疗效果
睡眠障碍不仅加重精神分裂症的阳性症状(如幻觉和妄想),还会加重负性症状(如情感冷漠和社交退缩),进而影响患者的认知功能。此外,患有睡眠障碍的精神分裂症患者表现出治疗依从性差、静坐不能和攻击性言语。
睡眠障碍的精神分裂症患者自杀行为风险增加
在一项为期八年的纵向研究中,结合Kaplan–Meier生存分析和对数秩检验,发现患有精神分裂症谱系障碍且频繁失眠的患者,其累计自杀行为风险显著增加,证实睡眠障碍会增加这些患者的自杀风险。这些结果显示睡眠问题对精神分裂症患者产生负面影响,强调了加强临床关注精神分裂症患者睡眠的必要性。
3
现有治疗的局限性
目前,治疗合并睡眠障碍(SD)的精神分裂症(SCZ)患者主要依赖传统抗精神病药物,特别是非典型抗精神病药物如氯氮平、奥氮平、喹硫平、利培酮、齐拉西酮和帕利立酮。
这些药物有助于提高精神分裂症患者的总睡眠时间和睡眠效率。然而,它们在改善SD方面的疗效有限,并伴有如体重增加和代谢综合征等副作用,部分患者在接受治疗后仍出现睡眠质量差和睡眠结构障碍。
药物疗法存在副作用,生物行为疗法逐渐兴起
尽管药物治疗是主要干预手段,但患者对药物依赖和副作用的担忧使得部分人不愿长期使用。此外,认知行为疗法(CBT)在改善持续妄想或幻觉患者的睡眠上已显示一定效果,但其临床应用仍需更多研究支持。这表明当前治疗精神分裂症合并睡眠障碍的方法面临显著局限,需探索新的治疗靶点和方法。
近年来,褪黑素的研究显示其在调节睡眠-觉醒节律、改善睡眠质量和缓解精神分裂症症状方面有效。同时,生物反馈疗法及其他非药物干预(如光疗和睡眠卫生教育)也被认为是有效的辅助治疗方式,可以改善患者睡眠质量。
总体而言,现有精神分裂症与睡眠障碍的联合治疗方法在疗效和耐受性上存在明显局限,迫切需要通过进一步研究和临床试验来探索新的治疗方案,以为患者提供更有效和安全的治疗选择。
近年来,研究发现肠道微生物群在调节精神健康和睡眠质量方面扮演着重要角色。数据显示,精神分裂症患者的肠道微生物群与健康个体存在显著差异,表现为多样性降低和特定微生物群落的失衡。与此同时,睡眠障碍的发生也与肠道微生物群的组成变化密切相关,这种相互作用可能通过微生物群-肠道-大脑轴影响患者的情绪、认知功能和睡眠模式。
1
精神分裂症患者的肠道菌群失调
多项研究发现,肠道微生物群与精神分裂症(SCZ)的病理机制、症状和认知功能密切相关。
关于精神分裂症患者肠道微生物群变化的研究
编辑
编辑
变形菌增加,拟杆菌减少,这会影响代谢健康
高通量测序结果表明,与健康对照组相比,精神分裂症患者的肠道微生物群丰富度指数(Chao)和多样性指数(Shannon)均较低,且特定微生物群的组成和丰度存在显著差异。曼-惠特尼U检验显示,精神分裂症患者的拟杆菌门(Bacteroidetes)显著减少,而变形菌显著增加。
Faecalibacterium等产生丁酸盐的抗炎菌减少
在属层面,与抗炎和神经保护作用相关的丁酸产生菌Faecalibacterium、Coprococcus和Bacteroides的丰度下降,而Prevotella和Collinsella丰度增加。短链脂肪酸(SCFAs)产生菌减少和促炎细菌增加可能与精神分裂症(SCZ)患者的病情严重程度有关。
微生物群的差异可能有助于判断疾病不同阶段
在不同疾病阶段的研究中,急性精神分裂症患者的嗜血杆菌属(Haemophilus)和Faecalibacterium数量减少,而缓解期患者则表现出巨单胞菌属(Megamonas)和Megasphaera的增加。
注:在这里小编推测嗜血杆菌属(Haemophilus)在肠道里变少可能更像“口源菌/黏膜相关菌”的信号,急性期患者的黏膜生态位与免疫/炎症微环境发生了系统性改变,而不是单纯少了一种好菌或坏菌,也可能是研究存在饮食,治疗等的混杂因素。
此外,口腔常驻细菌如Veillonella atypica、唾液链球菌(Streptococcus salivarius)和Bifidobacterium dentium在精神分裂症患者肠道微生物群中显著富集,这种病理状态可能削弱肠道屏障和免疫功能,为口腔细菌的肠道定殖提供有利条件。
一项涵盖细菌、真菌、古菌和病毒的综合多界微生物组分析发现,精神分裂症患者肠道中链球菌、脱硫弧菌(利用氨基酸或脂肪酸作为碳源)和Methanobrevibacter smithii等微生物数量增加,而丁酸盐产生菌的数量减少。
精神分裂症人群中吸烟率、牙周状况差异常见;如果口腔来源菌输入或口腔生态改变,使得口腔菌更容易通过吞咽等进入肠道并在那里存活、甚至黏附定殖肠道菌群组成更像“口腔来源的组合”,常见于炎症、屏障受损或环境改变的肠道。可以推测病源菌增加 + 产丁酸菌(如 Faecalibacterium)下降+ 屏障/炎症指标异常(如 LPS/DAO/zonulin、粪便钙卫蛋白、炎症因子),可能是未来辅助判别急性精神分裂症的重要标志组合。
2
与睡眠障碍相关的微生物群变化
在具有睡眠障碍(SD)的人类和动物模型中也观察到了微生物群变化。
关于睡眠障碍患者肠道微生物群变化的研究
编辑
微生物群的多样性与睡眠效率和睡眠时间正相关
对健康成年人睡眠的研究发现,微生物群的多样性与睡眠效率和总睡眠时间呈正相关,而与睡眠碎片化呈负相关。简而言之,肠道微生物群的多样性促进了更健康的睡眠。
此外,针对学龄前儿童的研究表明,夜间睡眠时间较长的孩子肠道微生物群结构与睡眠时间较短的孩子不同,且微生物群中的双歧杆菌和拟杆菌与睡眠时间延长、睡眠效率提高和夜间清醒时间缩短相关。
睡眠紊乱导致肠道菌群失调,普雷沃氏菌等增加
研究还表明,睡眠和昼夜节律紊乱会导致人类和动物模型中的肠道微生物群失调,表现为致病菌增加和有益菌减少。在人类中,睡眠不足和质量差常与普雷沃氏菌科(Prevotellaceae)和丹毒丝菌科(Erysipelotrichaceae)的增加及瘤胃球菌属(Ruminococcus)的减少有关。
在动物模型中,睡眠剥夺和破碎会导致毛螺菌科(Lachnospiraceae)和丹毒丝菌科(Erysipelotrichaceae)增加,而乳杆菌科(Lactobacillaceae)和双歧杆菌科(Bifidobacteriaceae)减少。
人类和小鼠的平行实验显示,不同物种的肠道微生物群存在昼夜节律振荡。此外,将人类在经历时差反应前后的肠道微生物群移植到无菌小鼠中,会导致微生物群结构改变,并出现代谢异常,如体重增加、血糖升高和体脂肪堆积。
不同类型的睡眠障碍患者显示出微生物群的特征差异
不同类型的睡眠障碍(SD)患者似乎表现出不同的肠道微生物群特征。慢性失眠患者主要表现为放线菌门数量增加,抗炎菌属Faecalibacterium含量减少,这一变化可能与长期低度炎症状态相关。
相比之下,急性失眠患者的肠道微生物群中,厚壁菌门增加而拟杆菌门减少,这一模式与急性24小时睡眠剥夺实验的发现高度相似,表明这种短期微生物失衡可能是对睡眠模式突然变化的压力反应。
此外,厚壁菌门数量增加,而拟杆菌门减少,导致(F/B)比例升高。关于急性睡眠时间表延迟的研究进一步证实,睡眠与觉醒周期的改变会增加F/B比。研究还报告指出,急性昼夜节律紊乱促进疾病相关的嘌呤代谢和丁酸生成乙酰辅酶A发酵途径,这些通路与宿主能量代谢和炎症反应相关。
注:这些代谢变化在恢复期内往往会逆转。
3
精神分裂症与睡眠障碍的微生物共性
基于研究发现,精神分裂症(SCZ)患者和睡眠障碍(SD)患者的肠道微生物多样性均降低,且特定微生物群组成发生类似变化。这种多样性的缺乏可能削弱肠道微生态系统的稳定性,增加疾病风险。
能代谢膳食纤维的菌种减少,而促炎菌增加
在微生物群组成方面,抗炎菌减少、促炎菌增加,这与疾病易感性密切相关。此外,结肠中的微生物如拟核菌、双歧杆菌和Faecalibacterium能发酵不易消化的碳水化合物和寡糖,从而合成短链脂肪酸(SCFAs)。这些属的减少显著影响丁酸盐、丙酸酯和乙酸盐的生产。
微生物群通过肠脑轴影响精神分裂症和睡眠障碍
与睡眠密切相关的特定微生物群在精神分裂症患者中数量减少。例如,双歧杆菌的减少与睡眠效率降低和睡眠碎片化有关,而Prevotella的增加可能干扰睡眠结构。
在关于睡眠与肠道微生物组组成的研究中,曼-惠特尼U测试显示,Ellagibacter isourolithinifaciens和Senegalimassilia faecalis在睡眠质量良好的患者中显著富集。在属层面,Senegalimassilia与患者的较好睡眠质量呈正相关。
这些微生物改变的特征表明,精神分裂症和睡眠障碍通过微生物群-肠道-大脑轴(MGBA)相互作用。这一过程涉及短链脂肪酸生成减少、全身炎症加剧和昼夜节律紊乱等机制,这些因素共同促进并加重两种疾病的共存和进展。
在肠道微生物群影响精神疾病的复杂病理网络中,宿主的遗传背景和环境因素共同构成了疾病易感性的基础。全基因组多效性分析揭示了胃肠疾病与精神疾病之间的广泛遗传相关性、共同的致病基因和通路,以及它们与肠道微生物群的遗传关联,证实了微生物群-肠道-大脑轴(MGBA)在这两类疾病的共同遗传基础中的关键作用。
多种环境因素,如地理位置、饮食和生活方式,动态调节肠道微生物群的丰富性和多样性,同时影响MGBA的功能稳态。MGBA作为宿主与微生物相互作用的调控枢纽,通过神经、内分泌和免疫系统之间的多层次双向通信网络,整合肠道微生态系统与中枢神经系统的功能耦合。
具体而言,肠道微生物群通过迷走神经直接调节中枢神经系统的活动,影响血脑屏障的通透性、神经炎症及通过细胞因子介导的免疫调节通路促进神经递质的合成和代谢。MGBA功能障碍可能导致病理变化,如下丘脑-垂体-肾上腺(HPA)轴异常激活及小胶质细胞持续激活,这些与精神疾病如精神分裂症(SCZ)和睡眠障碍(SD)的共病机制密切相关。
肠道微生物群及其代谢物通过肠-脑轴相互作用
编辑
1
神经递质调控
肠道菌群通过神经递质影响精神状态和睡眠
在精神分裂症(SCZ)和睡眠障碍(SD)研究中,神经递质的异常代谢被认为是影响症状的重要因素,而肠道微生物群及其代谢物在神经递质的产生和功能调控中发挥关键作用。如血清素(5-HT)、GABA和多巴胺(DA)的代谢异常可能妨碍SCZ的神经传导及SD的睡眠调节。
研究显示,肠道微生物群通过调控色氨酸代谢直接影响5-HT的生物合成。在松果体中,5-HT经历一系列酶转换,通过N-乙酰化转化为N-乙酰丝氨酸,并进一步O-甲基化合成褪黑素。该生物合成途径的完整性直接影响内源性褪黑素的生成,进而影响睡眠的开始和维持。
因此,肠道微生物群可以通过影响色氨酸的可用性来调控该代谢途径,从而通过特定微生物群增加色氨酸转化为5-HT而非犬尿氨酸途径,从而提高5-HT和褪黑素的水平。
乳杆菌和双歧杆菌通过GABA影响精神分裂症
研究表明,特定微生物群如乳杆菌和双歧杆菌不仅能促进色氨酸转化为血清素(5-HT),还可以直接合成GABA。作为中枢神经系统的主要抑制性神经递质,GABA与精神分裂症(SCZ)患者的焦虑和抑郁症状密切相关,其代谢异常对症状产生影响。通过与GABA受体结合,它有效降低神经兴奋性,延长慢波睡眠时间。
总之,神经递质的代谢在精神分裂症和睡眠障碍的病理机制中扮演重要角色。肠道微生物群通过影响神经递质的水平,不仅影响精神症状,还通过改变睡眠加重病情。因此,针对神经递质代谢的干预措施为治疗SCZ合并SD患者提供了新的思路与策略。
2
免疫炎症通路
肠道微生物群组成的变化会促进神经炎症,而这种炎症被认为是多种精神疾病(包括精神分裂症(SCZ)和睡眠障碍(SD))的重要病理机制。
IL-6和TNF-α等促炎细胞因子增加易导致精神分裂症恶化
肠道微生物群及其代谢物是调控小胶质细胞的成熟、形态和功能的关键分子。微生物群的变化可激活胶质细胞,促使IL-6和TNF-α等促炎细胞因子的释放,这影响神经元的存活与功能,破坏血-脑屏障的完整性,使外周炎症细胞因子和神经活性代谢物渗透中枢神经系统,最终诱发神经炎症反应。
针对SCZ患者的纵向研究显示,IL-6和TNF-α水平较高与脑源性神经营养因子(BDNF)水平下降及认知障碍相关。这些炎症标志物水平较高的SCZ患者更可能出现症状恶化。免疫系统在特定症状中也发挥作用,炎症刺激能改变健康个体腹侧纹状体区域的神经活动,导致动机减弱和奖赏处理缺陷,表明炎症与负性和认知症状之间的病理生理关系。
急性炎症升高也影响睡眠时间和深度
此外,睡眠障碍(SD)与炎症标志物如C反应蛋白(CRP)和IL-6的增加有关,急性炎症升高可改变睡眠的时间和深度。使用曼-惠特尼大学测试的统计分析发现,与对照组相比,接受72小时快速眼动(REM)睡眠剥夺的小鼠血浆内脂多糖浓度升高和TNF-α显著上调。
限制大鼠睡眠后,血-脑屏障的选择性过滤功能减弱,降低了阻断有害物质的能力,增加了神经炎症的风险。
通过调节肠道菌群的抗炎治疗有助于改善精神分裂症合并睡眠障碍
在临床干预中指出,使用认知行为疗法(CBT)治疗慢性和原发性失眠的老年患者后,炎症风险标志物减少,显示免疫炎症通路与睡眠障碍存在显著关联。
抗炎治疗可能是改善SCZ合并SD患者的重要策略。通过降低炎症通路则可减少小胶质细胞的激活和促炎细胞因子的产生,从而改善患者的整体症状和生活质量。
未来的研究应集中于探索特定的抗炎干预方法(如细胞因子拮抗剂或微生物组调控)对精神分裂症(SCZ)合并睡眠障碍(SD)患者的治疗效果及潜在神经保护机制。
3
神经内分泌调节
下丘脑-垂体-肾上腺轴(HPA)是神经内分泌系统的核心部分,在调节应激反应中发挥关键作用,其功能障碍已成为肠道微生物群介导睡眠障碍(SD)的重要机制之一。
压力下的高糖皮质激素导致认知障碍和焦虑增加
在压力条件下,下丘脑分泌的促肾上腺皮质激素释放因子(CRF)激活垂体前叶,释放促肾上腺皮质激素(ACTH),随后刺激肾上腺皮层合成糖皮质激素,如皮质醇。
长期过度暴露于糖皮质激素会影响大脑不同区域的神经元可塑性。这些结构重塑与认知功能障碍和动物实验中焦虑类行为增加密切相关,表明糖皮质激素介导的异常神经回路可能是慢性压力和精神障碍中认知缺陷和情感症状的重要病理基础。大量临床证据表明,HPA轴功能障碍在精神分裂症中普遍存在。
具体而言,精神分裂症患者的皮质醇觉醒反应(CAR)呈现明显异常模式,包括过度多动或钝化。这些患者的晨间基础皮质醇水平显著高于健康人群,而这种HPA轴功能障碍的模式具有疾病特异性,在高风险精神病人群中未观察到类似变化。
精神分裂症患者松果体受损影响褪黑素合成分泌
神经影像学研究显示精神分裂症(SCZ)患者的松果体体积减少、钙化加重,导致褪黑素合成和分泌功能受损。这种多层次内分泌障碍与SCZ临床症状的严重程度相关,并扰乱睡眠与觉醒周期,增加睡眠起始潜伏期和睡眠连续性受损情况。
可见,神经内分泌异常与睡眠障碍(SD)在SCZ中形成复杂的双向调控网络。睡眠不足激活下丘脑CRF神经元,导致HPA轴过度激活和皮质醇增加,而高皮质醇水平则抑制褪黑素合成,干扰睡眠调节,进一步加重SD。这一过程形成“内分泌障碍-睡眠问题-疾病恶化”的病理闭环,促进SCZ的进展和症状维持。
4
代谢物介导的调控
肠道微生物群生成的代谢物,如短链脂肪酸(SCFA)、色氨酸衍生物和胆汁酸,直接或间接参与中枢神经系统的调控,影响神经递质的平衡、维持免疫稳态,并调节昼夜节律。
丁酸盐有助于改善精神分裂症状和睡眠质量
菌群失调可破坏肠道屏障的完整性,增加肠道通透性,损害血-脑屏障的功能。这些双重屏障的破坏使得细菌代谢产物和促炎细胞因子等有害物质更易进入中枢神经系统,引发神经炎症反应。
丁酸盐作为关键代谢物,不仅对维持肠道黏膜的完整性至关重要,还能穿越血-脑屏障,通过激活迷走神经调节睡眠和清醒周期。动物研究发现,静脉注射丁酸盐显著延长了大鼠的非快速眼动睡眠(NREMS)时间。
此外,血清丁酸盐水平的升高与精神分裂症(SCZ)患者阳性和阴性综合征量表(PANSS)的阳性症状分数下降相关,暗示其潜在的神经保护作用。
血清素和胆汁酸水平下降可能是影响精神分裂症和睡眠障碍的重要机制
精神分裂症(SCZ)患者还表现出显著的色氨酸代谢障碍,研究发现其血浆色氨酸水平通常较低,这可能由于色氨酸向犬尿氨酸的转化增强和5-羟色胺(5-HT)合成途径的减少。这种转变导致神经递质5-HT和褪黑素的合成减少,由于这些物质在睡眠调节中起关键作用,其缺乏会加重精神分裂症患者的睡眠障碍(SD)。
代谢物分析显示,精神分裂症患者胆酸通路中的代谢物如糖果酸、牛磺酸脱氧胆酸和牛磺鹅脱氧胆酸的浓度显著降低,胆汁酸水平的下降通过影响抗炎信号通路,促进慢性低度炎症微环境的形成,从而增加神经退行性疾病和精神障碍的风险。研究还发现慢性失眠与特定胆酸结构和组成之间存在关联。
因此,代谢轴的异常不仅是精神分裂症的典型生物标志物,也是精神分裂症中睡眠障碍发病的关键机制之一。针对肠道微生物群及其代谢物的干预措施可为改善精神分裂症合并睡眠障碍患者提供新的治疗靶点。
5
昼夜节律紊乱
肠道微生物群与昼夜节律密切相关,其组成会随宿主生物钟的变化而波动,反之肠道微生物群的紊乱也会影响生物钟、肠道免疫功能和营养代谢。
肠道微生物群影响人体生物钟在精神疾病中发挥重要作用
肠道微生物群的组成和代谢物对宿主时钟基因(如CLOCK和Bmal1)的表达具有独特的调控作用。研究发现,微生物代谢物可以调节中枢神经系统和肝脏的生物节律,比如,短链脂肪酸(SCFAs)直接调控肝细胞中的时钟基因表达,影响宿主生物节律的稳定性。
肠道微生物群失衡在精神分裂症(SCZ)患者中较常见,这种失衡可能通过肠道-大脑轴影响宿主时钟基因的表达。分析首次发作SCZ患者的单核血细胞发现,与健康对照相比,患者的CLOCK、PER2和CRY1基因表达显著降低。而在慢性SCZ患者的成纤维细胞中,时钟基因CRY1和PER2的节律表达丧失。这些研究揭示了肠道微生物群通过代谢物与时钟基因的相互作用,对SCZ患者昼夜节律的稳定性至关重要。
时钟基因表达的变化不仅影响肠道微生物群的结构,还进一步影响核心昼夜节律输出通路的效率。研究表明,昼夜节律紊乱与肠道-大脑轴(MGBA)之间存在显著相互作用,MGBA在精神疾病的整个过程中持续影响患者的健康状况和临床症状。
昼夜节律调节神经内分泌活动影响精神分裂患者临床症状
结合本文前面的内容,昼夜节律通过调节神经内分泌活动和自主神经系统活动,调节睡眠、新陈代谢和免疫等生理过程。该输出通路的失效可能导致睡眠结构紊乱、压力激素节律失调,以及代谢和免疫反应的周期性紊乱,这些共同构成了精神分裂症患者常见的临床症状基础。与此同时,时钟基因表达的变化反过来会影响肠道微生物群的组成,显示出丰富度和多样性的减少,形成复杂的相互作用网络。
例如,研究显示宿主昼夜节律的核心激活基因(Bmal1)和抑制基因(Per1, Per2)共同调节肠道微生物群组成的昼夜振荡。这些时钟成分的基因敲除消除了这些节律波动,改变了小鼠的微生物群落结构。
深入研究肠道微生物群与其代谢物及时钟基因之间的关系,不仅有助于理解精神分裂症的发病机制,还将为基于肠道微生物群干预的未来治疗策略提供新思路。例如,通过调整饮食或补充益生菌以改善肠道微生物群的组成,调控时钟基因的表达以优化昼夜节律信号的传递效率,改善精神分裂症患者的临床症状。
小编总结
这组证据总体在说明:睡眠/昼夜节律紊乱本身就是一个能“驱动”肠道微生态改变的上游因素,而这种改变不仅是“相关”,还可能通过菌群把代谢风险传递出去。菌群不是静态的,它会随进食时间、胆汁酸分泌、肠蠕动、激素(如皮质醇/褪黑素)等出现日内波动,群落结构不稳定和功能(例如短链脂肪酸、胆汁酸转化、内毒素负荷)也会随之波动。
如果精神分裂症患者同时存在常见的睡眠/昼夜节律紊乱,那么观察到的某些肠道菌群特征(如特定门、科/属的增减,口源菌富集,以及产丁酸菌减少等)可能并非完全由疾病本身导致,而是共同受到多条路径的影响,包括:疾病相关应激、药物与生活方式,以及睡眠—生物钟失调这一通路。
与此同时,膳食纤维代谢菌减少提示菌群功能发生改变:尤其是短链脂肪酸(SCFAs)生成能力下降,可能削弱其对肠道屏障维护与免疫调节的作用;而促炎菌增加、抗炎菌减少则意味着机体更偏向促炎状态与肠道高通透,进而可能通过“肠—免疫—脑”轴影响中枢免疫激活与神经炎症。
在监测精神分裂症菌群时,睡眠状态可能是重要的混杂因素,也可能是可干预的上游靶点(改善睡眠可能间接改善菌群与代谢/炎症表型)。
尽管睡眠障碍与多种精神疾病的发生和发展密切相关,但针对精神分裂症(SCZ)合并发病的干预研究仍然不足。目前大多数治疗策略集中于症状控制,如通过抗精神病药物改善核心精神症状,而较少关注肠道微生物群失调机制。
因此,以下讨论提出针对肠道微生物生态的新治疗策略,包括特定益生菌、益生元、饮食干预、粪便微生物移植(FMT)和靶向代谢物治疗,旨在调节肠道-脑轴功能,以改善精神分裂症患者的睡眠问题及相关精神症状。
针对精神分裂症患者的微生物群干预方法
编辑
1
个性化补充益生菌
个体间肠道微生物群的差异会影响药物的疗效和毒性,因此个性化的肠道微生物群调控有助于改善药物反应。
通过检测精神分裂症(SCZ)患者的肠道微生物群,可以制定个性化益生菌方案,有效调节肠道微生物组成,从而改善症状。
长双歧杆菌等益生菌能改善精神状态
益生菌的疗效因菌株而异,不同菌株在调节炎症和压力方面表现出不同作用机制。例如,婴儿双歧杆菌(Bifidobacterium infantis 35624)已被证明能逆转HPA轴功能障碍,并与抗炎和促炎细胞因子比例的正常化相关,具有临床意义。
鼠李糖乳杆菌(Lactobacillus rhamnosus,JB-1)能降低压力诱发的皮质酮水平,缓解焦虑和抑郁行为。长双歧杆菌(Bifidobacterium longum NCC3001)通过MGBA内的迷走神经通路传递信号,使低度肠道炎症小鼠的焦虑行为和海马BDNF水平恢复正常。该菌株在人类试验中也显示抗抑郁效果,与多个情绪处理脑区活动变化相关。
益生菌有助于改善炎症相关、情绪状态及睡眠
在一项针对失眠患者的双盲研究中,参与者接受了植物乳杆菌(Lactobacillus plantarum PS128)或安慰剂。结果显示,PS128组在疲劳水平、脑电波活动和深度睡眠期间醒来次数方面有所改善,同时也缓解了焦虑和抑郁症状。这表明特定益生菌菌株可能通过微生物群-肠道-脑轴的机制(如GABA能系统调控)影响睡眠结构和情绪状态。
一项针对双相情感障碍和精神分裂症谱系障碍患者的双盲随机安慰剂对照试验表明,补充多株益生菌配方能改善与肠道通透性和炎症相关的生物标志物,并对认知功能产生积极影响。
这些研究结果揭示了益生菌补充剂在调节神经功能方面的潜在治疗价值,为进一步探索益生菌的干预机制提供了重要理论基础。
2
膳食益生元补充
益生元是一类能够抵抗宿主消化酶的功能性膳食成分,能选择性促进有益肠道微生物群的代谢活动,从而发挥生理调节功能。
菊粉等益生元改善精神分裂症的精神和行为症状
多项研究发现,半乳糖、菊糖型果聚糖及其合成制剂能够降低促炎因子(如高敏感性CRP、IL-6和TNF-α)的水平,表明特定的益生元干预可以调控炎症相关生物标志物的表达。菊粉作为可溶性膳食纤维,已被证实改善精神分裂症(SCZ)模型小鼠的精神和行为症状,同时增加有益菌数量并改善肠道通透性。
服用低聚果糖和低聚半乳糖的复合制剂也改善了SCZ模型小鼠的肠道功能。这些变化可能通过重塑肠道微生物群、降低促炎细胞因子水平以及增强肠道通透性,从而减少病原体与肠道黏液层的接触,为改善多种精神疾病的核心症状提供重要的病理生理基础。
益生元调节神经递质平衡改善精神状态及睡眠
另一项研究表明,短链半乳糖与长链果糖的联合干预显著促进了短链脂肪酸中乙酸和丁酸的生成。这些益生元成分还有效调控下丘脑和海马体中核心时钟基因BMAL1和CLOCK的表达。
这表明益生元通过多重靶点的协同效应发挥神经调节功能。特别是,益生元对时钟基因的调节可能通过恢复昼夜节律改善睡眠问题,并通过调节神经递质平衡潜在改善精神分裂症核心症状。
为促进益生元疗法在精神疾病临床实践中的应用,后续研究应明确不同益生元的应用价值、个体化剂量策略以及治疗的安全性和有效性评估。
3
饮食调整干预
特定饮食成分通过与肠道菌群互作影响睡眠质量
饮食调整是个性化治疗的重要部分,已有大量科学证据证明饮食与睡眠之间存在关系。健康饮食有助于改善睡眠质量,而加工食品和高糖食物则与睡眠质量较差相关。
特定饮食成分(如脂肪和蛋白质)及习惯(如牛肉、咖啡和干果摄入)通过与肠道微生物群相互作用影响睡眠。
生酮和高纤维饮食有助于改善睡眠质量和免疫
近年来,生酮饮食受到广泛关注,已被证明是改善伴有代谢异常的精神疾病患者心理和代谢健康的一种可行辅助治疗方法。根据匹兹堡睡眠质量指数(PSQI)评估,接受生酮饮食干预后,双相情感障碍和精神分裂症(SCZ)患者的主观睡眠质量有所改善。这表明,生酮饮食可以纳入精神疾病患者的综合治疗策略,有望在控制精神症状、调节代谢和改善睡眠方面带来多重益处。
此外,从高纤维饮食的角度来看,短链脂肪酸(SCFAs)是通过肠道共生细菌发酵膳食纤维产生的。当膳食纤维摄入不足时,SCFAs的生成水平会降低,这将对宿主的各种生理功能产生不利影响。增加膳食纤维摄入以促进SCFA的产生,不仅能增强血液和脑屏障的保护功能,维持肠道黏膜的完整,还能调节肠道微生物群的组成,从而协同促进免疫稳态的建立。
基于这一机制,这种饮食干预策略为改善精神障碍患者的睡眠提供了新思路。通过缓解肠道炎症状态并调节神经递质水平,它可以改善患者的精神症状和睡眠质量。
4
粪菌移植
粪菌移植(FMT)是一种以重建微生物群落为核心的生物治疗策略,通过将健康供体的粪便移植到患者的胃肠道,直接重组受体的肠道微生物群,促进微生物生态系统的平衡,从而实现临床治疗目标。
粪菌移植有助于调节情绪、行为和睡眠质量
作为一种突破性干预方法,粪菌移植(FMT)在动物模型和初步临床研究中展现出独特优势。研究发现,通过移植精神分裂症(SCZ)患者的肠道微生物群,被移植小鼠出现了类似SCZ的行为,包括多动、焦虑增加、社交互动受损和记忆缺陷。
注:这些小鼠还显示出周围和中枢神经系统中色氨酸代谢犬尿氨酸-犬尿酸通路的显著激活,前额叶皮层基底细胞的多巴胺能神经递质释放增强,以及海马体5-HT水平升高,同时谷氨酸能神经递质浓度下降,谷氨酰胺和GABA水平上调。
FMT在人体临床研究中展现出重要价值。比较接受健康供体FMT前后的粪便样本显示,α多样性显著增加,柯林斯氏菌属(Collinsella)和双歧杆菌的丰度也有所上升。FMT治疗还显著降低了患者的血液皮质醇水平,同时改善了睡眠和情绪相关评估指标。
作为潜在治疗干预,FMT通过调节肠道微生物群的组成和功能,促进神经递质及其前体物质的合成,从而发挥治疗作用。这些研究表明,FMT能够有效调节情绪和行为,促进多种精神疾病患者的症状缓解。
!
注意事项
尽管粪菌移植(FMT)展现了广泛的治疗前景,但其临床应用面临标准化不足、疗效不一及长期安全性验证的挑战。高通量测序技术可帮助识别健康稳定的供体。口服FMT胶囊相比传统灌肠方法更方便,患者依从性更高。多样化的给药途径,如结肠镜输注、鼻肠管插管或口服胶囊,有助于平衡疗效与患者依从性。建立安全监测系统可预防和控制感染风险,加强安全监管。
此外,在进行FMT治疗时,必须密切关注精神障碍患者的知情同意能力,确保他们能够在充分了解潜在风险和益处的基础上做出自主决策,并通过伦理审查委员会的批准进行标准化申请。尽管仍需更多研究验证FMT在精神分裂症(SCZ)和睡眠障碍(SD)治疗中的长期效果,但作为个性化治疗的一部分,FMT显示出广泛的应用前景。
5
靶向代谢物药物治疗
在精准医疗领域,靶向代谢物药物治疗正成为新研究方向。尽管传统微生物群移植在临床应用中取得了一定成效,但个体肠道微生物群的差异严重限制了其治疗效果的稳定性和重复性。因此,直接补充微生物代谢物或前体物质为解决这一问题提供了新思路。
靶向代谢物能够避免个体菌群差异,更精准治疗
这种策略能够绕过微生物群移植中的个体差异,直接作用于人体代谢网络,实现更精确的调控。短链脂肪酸(SCFAs)和色氨酸代谢在生理和病理过程中起着关键作用。
以吲哚胺2,3-二氧加氧酶(IDO)抑制剂为例,IDO是色氨酸代谢中的限速酶,其过度活化可导致色氨酸耗竭和一系列神经毒性代谢物的产生,进而引发异常免疫反应和神经功能障碍。IDO抑制剂通过抑制其活性,可以有效调节免疫反应,减少神经毒性代谢物的产生,展现出治疗多种疾病的潜力。
SCFAs和色氨酸代谢物与精神分裂症(SCZ)发病机制及睡眠调节密切相关。未来研究应进一步探讨代谢物的具体作用机制,推动其临床应用的发展,为合并睡眠障碍的SCZ患者提供更安全、更有效的治疗选择。
治疗策略总结
并非所有精神分裂症(SCZ)患者都适合微生物组靶向干预。潜在候选者的识别应基于具体特征,例如明显的胃肠道症状、抗精神病药物反应不良或显著副作用、异常睡眠结构与疾病活动的强相关性,以及肠道微生物组分析结果显示与健康对照有显著偏差。
根据临床表型和微生物特征进行对应治疗选择
目标群体应根据临床表型和微生物特征的组合进行选择。在推进微生态干预时,应明确不同策略的优先级,优先考虑低风险、非侵入性的方法。例如,补充特定益生菌和益生元可作为基础干预,而饮食模式调整可作为长期管理策略。
相比之下,高风险且难以预测的治疗如粪便微生物移植(FMT)应仅考虑用于难治症状、对传统疗法反应不足及严重肠道菌群失调的患者,并在充分知情同意和严格伦理监督下使用。
此外,实施时需认真考虑个体差异和潜在风险。益生菌和益生元干预应考虑菌株特异性效应和个体耐受性,饮食干预需关注患者的依从性和营养平衡。对于FMT,严格的供体筛查至关重要,并需密切监测感染、免疫和代谢不良反应,以及长期精神病学结局,同时建立动态的疗效-安全性评估体系。
本文分析了精神分裂症(SCZ)及其相关睡眠障碍患者的典型肠道微生物群特征。研究发现,这两种状况均表现出肠道微生物群α多样性下降、短链脂肪酸产生细菌减少以及促炎微生物群比例增加。由此可以推测,SCZ患者的肠道菌群失调可能是导致睡眠质量下降的重要因素,而睡眠质量恶化又通过反馈机制加重精神症状,形成恶性循环。
肠道菌群失调、中枢神经系统功能障碍和睡眠稳态紊乱在宿主体内形成自我延续的动态循环,导致精神病理表现和生理节律紊乱的周期性恶化。这些发现为理解精神分裂症患者共病睡眠障碍的机制提供了重要的理论框架。针对肠道微生物群以打破这一恶性循环,为这类患者提供了有前景的新颖治疗视角。
现有研究表明,治疗应采取综合策略。虽然非典型抗精神病药物能改善精神病症状,但对睡眠结构的复杂影响仍需深入评估。认知行为疗法同样对失眠有效,但需根据精神病症状进行调整。因此,针对肠道微生物群的干预策略正在向多层次和精准化方向发展,具体包括补充特定益生菌和益生元,结合饮食调整,通过多途径共同改善精神症状和睡眠质量。尽管粪便微生物移植(FMT)作为高级干预措施展现出潜力,但其效果仍需通过标准化研究来验证。实施时应重点关注胃肠道症状、药物反应不足、精神症状严重程度与睡眠节律紊乱以及肠道微生物群特征显著偏离健康标准的患者。整合临床表型与微生物特征的模型将为精准应用干预策略提供基础,最终推动微生物群靶向治疗的系统化及个性化发展。
我们每个人都在不断追求身心健康的道路上前行,理解肠道微生物群在我们的心理与生理健康中所扮演的角色,不仅能增进我们对自身健康的认识,更能激励我们在日常生活中关注饮食、生活方式等易被忽视的细节。希望未来的研究能够持续启发我们,推动科学领域的进步,为那些受到精神障碍困扰的人们带来新的希望和解决方案。通过这样的努力,我们将共同迈向一个更加健康和明亮的未来。
注:本账号发表的内容仅是用于信息的分享,在采取任何预防、治疗措施之前,请先咨询临床医生。
主要参考文献:
Huang, Z., Huang, Z., Du, Z., Gao, X., Jiang, Y., Zhou, Z., & Zhu, H. (2026). Role and mechanism of gut microbiota and metabolites in schizophrenia complicated with sleep disorder. Gut Microbes, 18(1). https://doi.org/10.1080/19490976.2025.2607817.
McCutcheon RA, Reis Marques T, Howes OD. Schizophrenia-An Overview. JAMA Psychiatry. 2020 Feb 1;77(2):201-210.
Meyer N, Faulkner SM, McCutcheon RA, Pillinger T, Dijk DJ, MacCabe JH. Sleep and Circadian Rhythm Disturbance in Remitted Schizophrenia and Bipolar Disorder: A Systematic Review and Meta-analysis. Schizophr Bull. 2020 Sep 21;46(5):1126-1143.
Reeve S, Sheaves B, Freeman D. Sleep Disorders in Early Psychosis: Incidence, Severity, and Association With Clinical Symptoms. Schizophr Bull. 2019 Mar 7;45(2):287-295.
McGuinness AJ, Davis JA, Dawson SL, Loughman A, Collier F, O’Hely M, Simpson CA, Green J, Marx W, Hair C, Guest G, Mohebbi M, Berk M, Stupart D, Watters D, Jacka FN. A systematic review of gut microbiota composition in observational studies of major depressive disorder, bipolar disorder and schizophrenia. Mol Psychiatry. 2022 Apr;27(4):1920-1935.
Mayeli A, LaGoy AD, Smagula SF, Wilson JD, Zarbo C, Rocchetti M, Starace F, Zamparini M, Casiraghi L, Calza S, Rota M, D’Agostino A, de Girolamo G; DiAPAson Consortium; Ferrarelli F. Shared and distinct abnormalities in sleep-wake patterns and their relationship with the negative symptoms of Schizophrenia Spectrum Disorder patients. Mol Psychiatry. 2023 May;28(5):2049-2057.
Penninx BWJH, Lange SMM. Metabolic syndrome in psychiatric patients: overview, mechanisms, and implications. Dialogues Clin Neurosci. 2018 Mar;20(1):63-73.
Zhu C, Zheng M, Ali U, Xia Q, Wang Z, Chenlong, Yao L, Chen Y, Yan J, Wang K, Chen J, Zhang X. Association Between Abundance of Haemophilus in the Gut Microbiota and Negative Symptoms of Schizophrenia. Front Psychiatry. 2021 Jul 30;12:685910

谷禾健康
氨基酸(AA)稳态对人体健康至关重要,其紊乱与多种疾病的发生和进展密切相关,如2型糖尿病和炎症性肠病(IBD),并且常常是治疗结果的决定性因素。
肠道微生物群可能通过多种机制调节宿主氨基酸的可用性,例如影响消化酶(如胰蛋白酶)的活性。肠道微生物群定殖还可能改变肠道通透性,从而影响胃肠道中游离氨基酸的运输和吸收。此外,肠道微生物可能直接利用或代谢肠道中的氨基酸,或合成并向宿主提供氨基酸。以往研究表明,肠道微生物组的变化(或其存在)可能影响肠道氨基酸谱。然而,参与调控宿氨基酸稳态的关键菌株及代谢基因仍未完全明确。
今天分享的这一篇发表在《Cell Host & Microbe》期刊上的研究论文”Microbiota metabolism of intestinal amino acids impacts host nutrient homeostasis and physiology”,通过比较Met无菌(GF)小鼠与无特异病原体(SPF)小鼠的分解物谱已证明,肠道细菌定殖会影响胃肠道(GI)中游离氨基酸谱,还通过高效代谢肠道氨基酸来重塑宿主氨基酸的格局。为确定责任微生物/基因,该研究开发了基于代谢组学的检测法,筛查了104个共生菌,并识别出能高效利用氨基酸的候选基因,并发现这些基因调控了肠道和循环氨基酸的可用性。
结果显示,不同氨基酸具有特定的细菌消费者,消耗效率差异明显。例如,天冬酰胺和谷氨酸被拟杆菌和部分梭菌高效利用,而芳香族氨基酸(色氨酸、酪氨酸)及支链氨基酸(BCAAs)仅为部分厚壁菌门成员所代谢,效率较低。值得注意的是,支链氨基酸与色氨酸代谢相关的微生物基因还能通过调节外周血清素间接影响宿主葡萄糖平衡。
总体而言,该研究首次系统揭示了肠道微生物群编码的氨基酸代谢活动对宿主营养稳态的深远影响,为理解微生物介导的氨基酸利用及其对宿主代谢调控机制提供了关键分子依据。
氨基酸稳态对人类健康至关重要,其紊乱与2型糖尿病和炎症性肠病(IBD)等多种疾病的进展密切相关。虽然传统上认为肠道和肝脏是调控营养代谢的主要器官,但最新研究发现,肠道微生物群通过代谢氨基酸能够深刻重塑宿主的氨基酸谱。
★该研究的核心意义在于:
•揭示了肠道微生物群通过代谢肠道氨基酸影响宿主氨基酸稳态的分子机制;
•鉴定了高效消耗氨基酸的特定肠道微生物及其代谢基因;
•阐明了微生物群氨基酸代谢基因如何通过外周血清素调节宿主葡萄糖稳态;
•为通过调节肠道微生物群代谢活性改善人类健康提供了新的靶点和策略。
▸ 肠道微生物群对宿主氨基酸水平的影响
研究首先通过比较无菌(GF)小鼠、无特定病原体(SPF)小鼠以及接受SPF微生物群移植(FMT)的GF小鼠,证实了肠道微生物群定植显著降低了肠道和循环氨基酸水平。
靶向代谢组学分析显示,SPF小鼠或接受SPF微生物群的GF小鼠肠道和循环氨基酸浓度普遍降低,这与之前的研究结果一致,表明微生物对肠道氨基酸的利用可能是影响宿主氨基酸稳态的主要途径之一。
▸ 高效代谢氨基酸的肠道微生物筛选
为识别高效代谢肠道氨基酸的微生物,研究者建立了一种基于活细胞的高通量代谢组学筛选方法,对104种肠道共生菌进行了系统分析。该方法综合考虑多个因素:
•生长阶段差异:绘制各菌株生长曲线并进行参数拟合,确保在可比生长阶段进行筛选;
•时间动态分析:分别在15、30和60分钟测定氨基酸消耗量,以精确评估不同菌株对特定氨基酸的利用速率;
•营养条件优化:在测定缓冲液中除氨基酸外,补充无机氮源、微量矿物质、维生素及额外碳源(如葡萄糖),以避免因营养限制导致的氨基酸非特异性快速消耗。
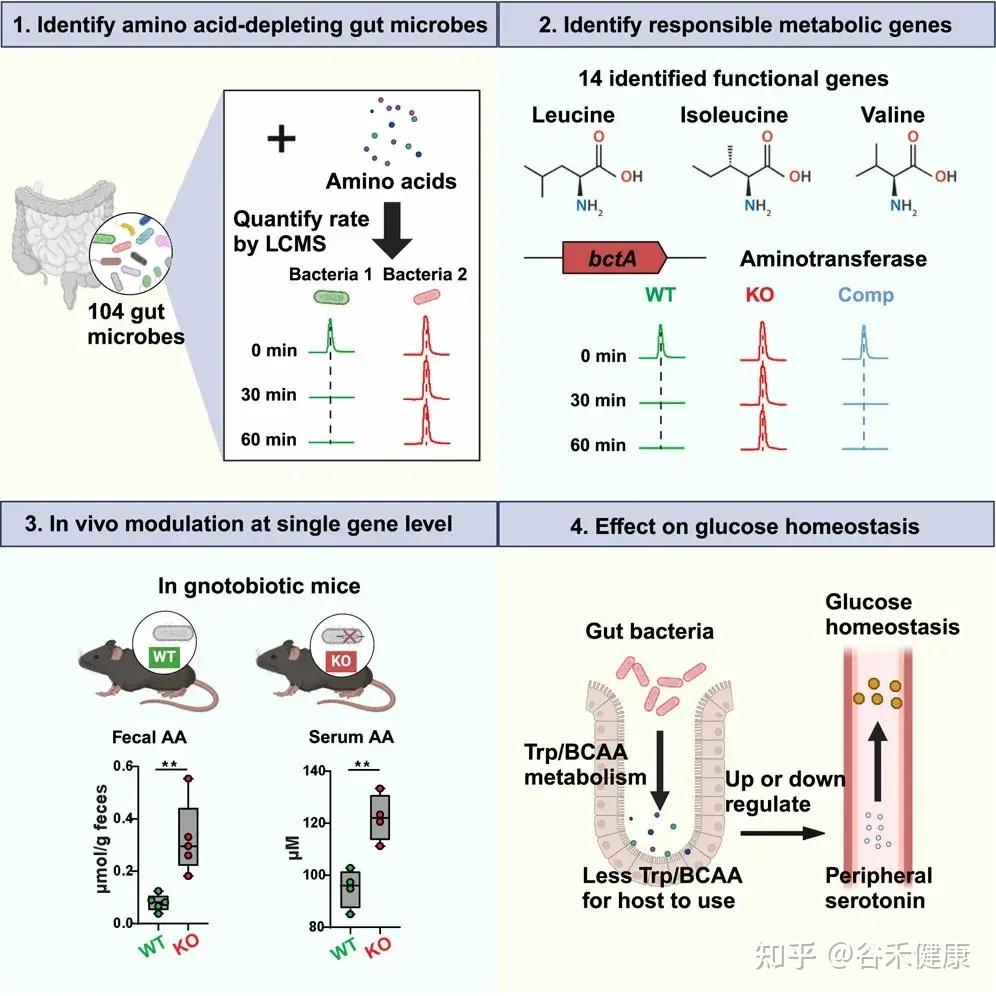
研究流程图展示了从识别消耗氨基酸的肠道微生物、鉴定负责的代谢基因、单基因水平的体内调节到对葡萄糖稳态影响的完整研究路径。
▸ 微生物代谢基因的鉴定与功能验证
研究利用CRISPR-Cas9和ClosTron等基因编辑技术,在系统发育多样的肠道微生物中开展大规模基因缺失分析,以鉴定氨基酸代谢的关键基因。筛选标准包括:
1.代谢基因编码的酶以氨基酸为直接底物;
2.这些基因存在于高效代谢氨基酸的肠道菌株中;
3.携带相关基因的菌株能稳定定植于无菌(GF)小鼠肠道,并降低宿主体内相应氨基酸水平。
通过构建基因敲除和互补菌株并结合代谢组学分析,研究识别出多种氨基酸代谢相关基因,并在单菌定植的GF小鼠模型中验证了其对肠道及血清氨基酸水平的调控作用。
▸ 高效代谢氨基酸的肠道微生物鉴定
通过大规模筛选,研究发现不同肠道微生物对氨基酸的代谢效率和偏好存在显著差异:
鉴定高效利用氨基酸的肠道微生物候选者
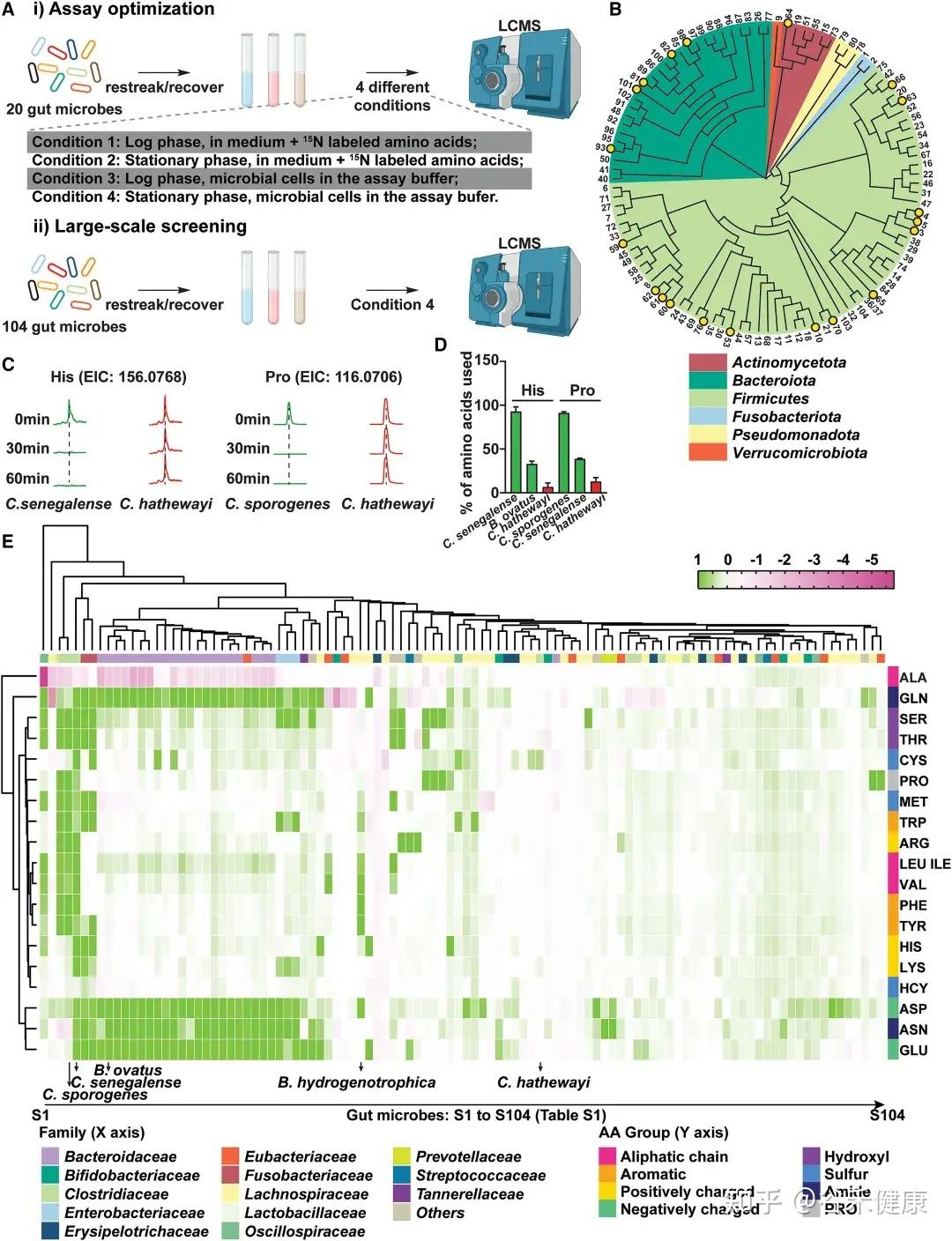
热图展示了104种肠道微生物对不同氨基酸的代谢情况,揭示了微生物系统发育与氨基酸代谢效率之间的复杂关系。
★ 关键发现包括:
•梭菌属微生物:如Clostridium sporogenes ATCC15579和Clostridium senegalense DSM25507,可高效代谢多种氨基酸,包括精氨酸、芳香族氨基酸、支链氨基酸、组氨酸、赖氨酸和脯氨酸等。
•拟杆菌属共生菌:作为肠道多糖的主要利用者,也能有效代谢天冬酰胺(Asn)、天冬氨酸(Asp)和谷氨酰胺(Gln)等氨基酸。
•氨基酸特异性代谢:不同氨基酸具有特定的细菌“消费者”,消耗效率差异明显。天冬酰胺和谷氨酸通常被拟杆菌和部分梭菌快速利用,而芳香族氨基酸(色氨酸、酪氨酸)及BCAA仅被部分厚壁菌门或梭菌较低效地代谢。
▸ 氨基酸代谢相关微生物基因的鉴定
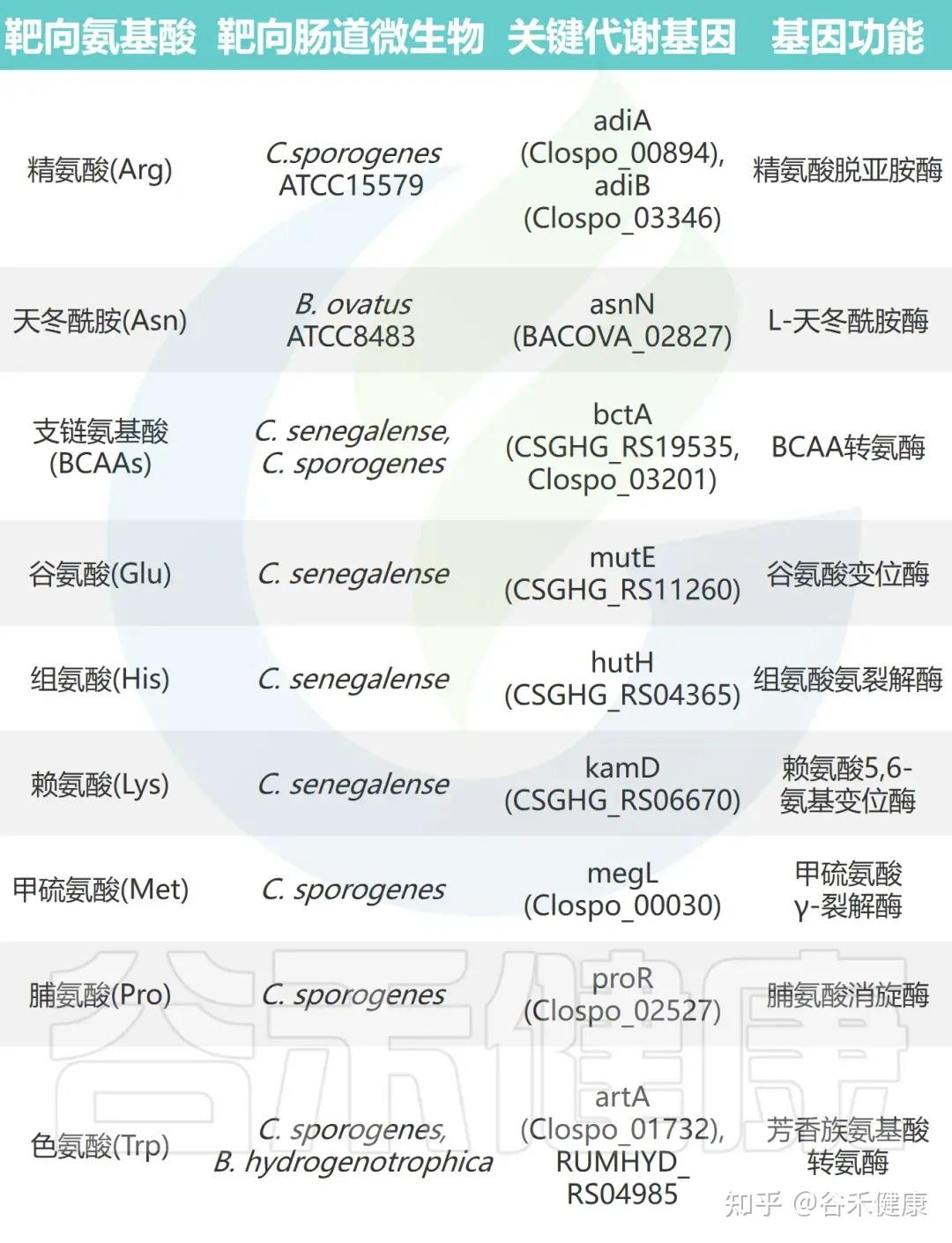
通过对高效代谢氨基酸的肠道微生物进行大规模基因缺失分析,研究鉴定出多种关键氨基酸代谢基因。这些基因编码的酶包括转氨酶、脱羧酶、消旋酶和氨裂解酶等,具有以下特征:
•功能冗余性:单株细菌常含多个具有相似功能的基因。例如,C. sporogenes 携带两种精氨酸脱亚胺酶基因(adiA 和 adiB),单基因敲除影响较小,而双敲除可完全消除其精氨酸代谢能力。
•底物特异性:代谢酶展现高度底物选择性。例如,C. sporogenes 的转氨酶 ArtA 特异作用于色氨酸和酪氨酸,但对苯丙氨酸代谢影响极小。
•催化多样性:不同类型的酶参与多条代谢途径。支链氨基酸和色氨酸经转氨途径代谢,脯氨酸通过还原反应被 C. sporogenes 利用,而谷氨酸、甲硫氨酸、丝氨酸和苏氨酸则由氨裂解酶快速分解。
•功能可转移性:这些酶的催化功能具有可转移性,在其他肠道共生菌中表达其编码基因可赋予相应氨基酸的消耗能力。
▸ 微生物代谢基因调控宿主氨基酸稳态
通过将野生型菌株及其代谢基因缺失突变体分别单菌定植于GF小鼠,研究发现这些基因显著影响宿主肠道及循环系统中的氨基酸水平:
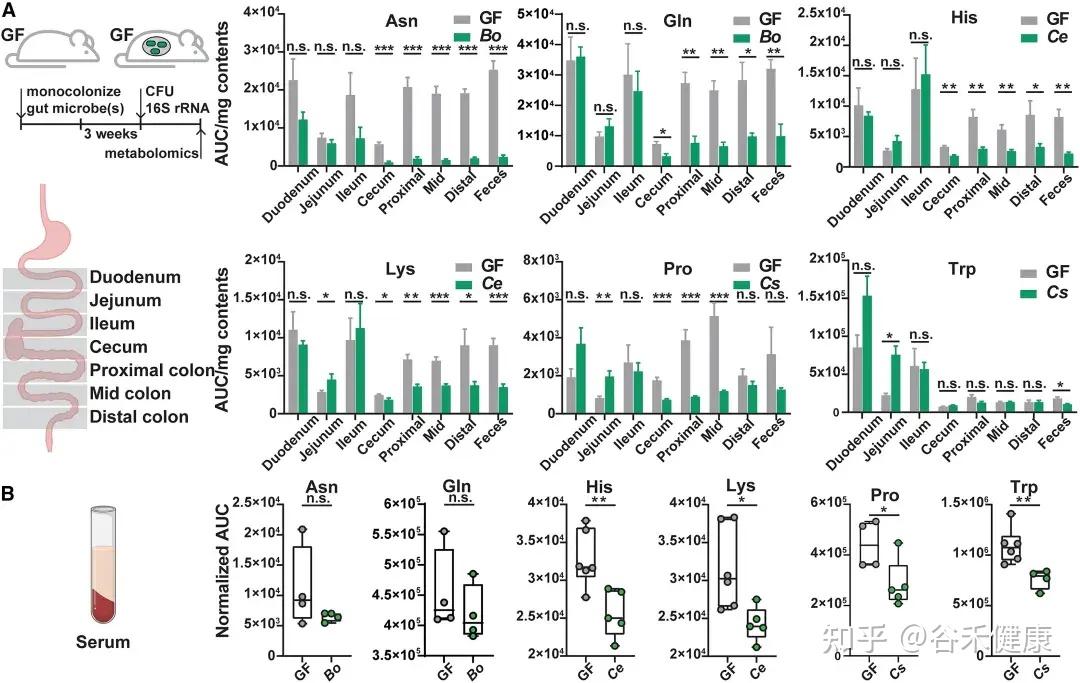
无菌小鼠单一定植B. ovatus、C. senegalense和C.sporogenes野生型菌株后,肠道和血清中特定氨基酸浓度显著降低。
★ 主要发现包括:
•肠道氨基酸稳态调控:多数鉴定出的微生物代谢基因或酶影响肠道氨基酸平衡。由于突变体的相应代谢途径被阻断,肠道内容物和粪便中相关氨基酸显著积累。
•循环氨基酸谱变化:部分代谢基因还影响宿主血清氨基酸水平。定植 Asn、Leu/Ile、Pro 和 His 利用缺陷突变体的无菌小鼠,其血清中对应氨基酸明显升高。
•系统性调节的复杂性:循环氨基酸水平的变化并不总与微生物在肠道中的代谢能力一致。例如,定植 C. sporogenes 精氨酸利用缺陷突变体可显著提高肠道精氨酸水平,但对循环精氨酸影响有限,提示肠上皮或肝脏代谢等额外机制亦参与精氨酸的全身稳态调控。
单基因水平的微生物群氨基酸代谢调控
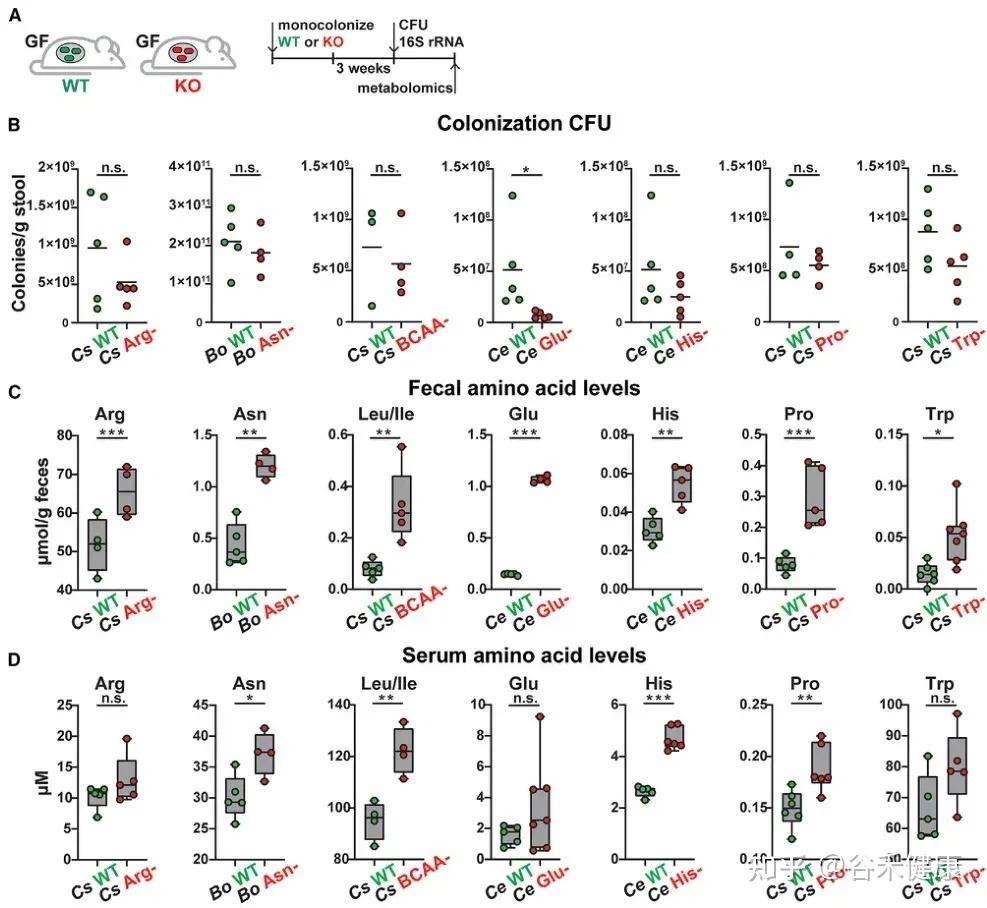
单基因水平的体内调节实验显示,氨基酸代谢基因缺陷突变体定植的无菌小鼠粪便和血清中相应氨基酸水平显著升高。
▸ 微生物氨基酸代谢通过外周血清素调控宿主葡萄糖稳态
研究发现,微生物中支链氨基酸(BCAAs)和色氨酸代谢相关基因可通过外周血清素间接调节宿主葡萄糖稳态。将 C. sporogenes 野生型、BCAA 缺陷型及色氨酸缺陷型突变体分别单菌定植于 GF 小鼠,并进行口服葡萄糖耐量试验(OGTT),结果显示以下关键发现:
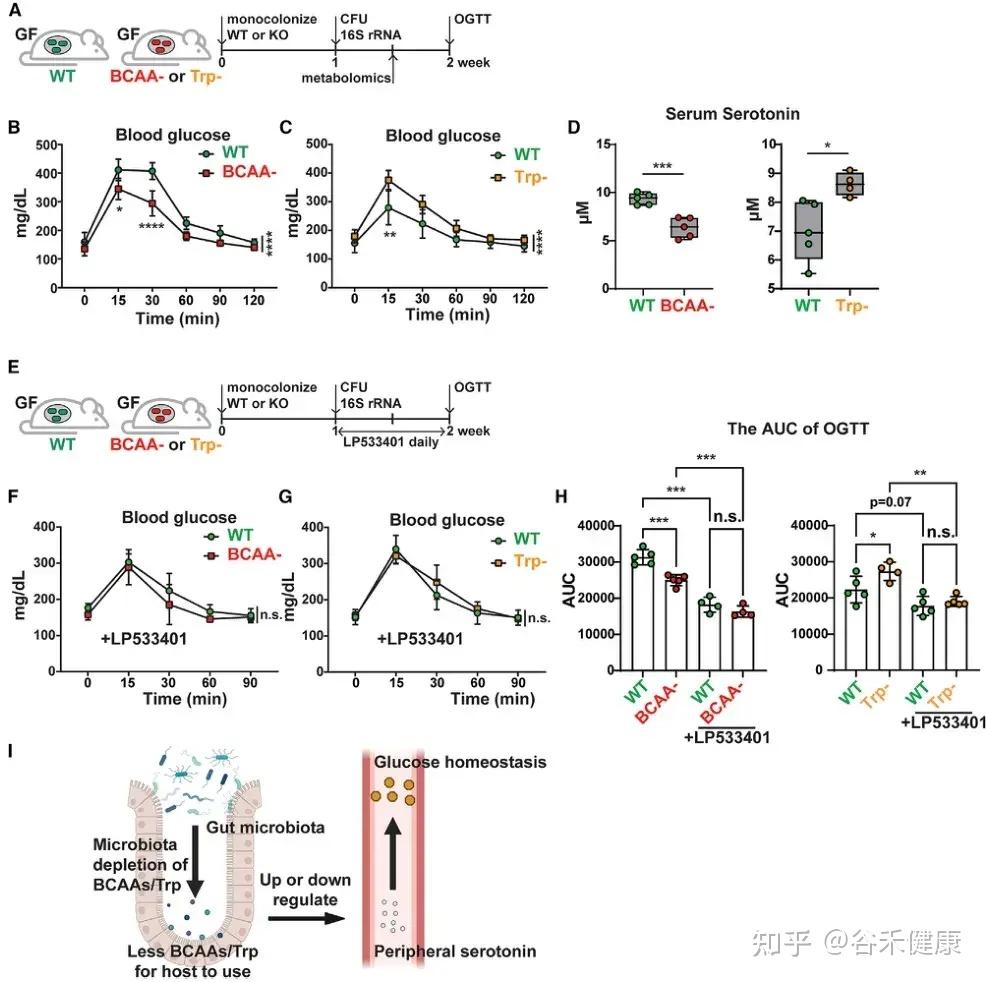
微生物支链氨基酸和色氨酸代谢通过调节外周血清素水平影响宿主葡萄糖稳态的机制示意图及实验验证。
•BCAA代谢与葡萄糖耐受性:定植 BCAA 缺陷突变体的小鼠葡萄糖耐受性显著增强,伴随血清素水平下降。
•色氨酸代谢与葡萄糖耐受性:定植色氨酸代谢缺陷突变体的小鼠表现相反,葡萄糖耐受性下降,血清素水平升高。
•血清素介导机制:应用 Tph1 抑制剂 LP533401 阻断外周血清素合成后,野生型与突变体定植小鼠间的葡萄糖处理差异显著减小,证实微生物氨基酸代谢通过调控外周血清素影响宿主葡萄糖稳态。
这一发现揭示了肠道微生物群、氨基酸代谢、外周血清素及葡萄糖稳态间的复杂关联,为理解代谢性疾病的机制提供了新思路。
!
研究局限性
尽管该研究取得了重要发现,但仍存在一些局限性:
1.微生物氨基酸代谢的多样性:研究主要关注肠道微生物对氨基酸的消耗,而其合成、转运等途径也可能影响宿主氨基酸稳态。体外测定仅反映特定条件下的代谢效率,难以全面代表其在宿主体内的作用。
2.模型简化的局限性:研究采用单菌定植的 GF 小鼠模型,未来应在更接近生理状态的模型(如定植简化微生物群的 GF 小鼠)中验证这些机制。
3.复杂微生物群中基因操作的挑战:虽然本研究成功在宿主定植背景下操纵单一氨基酸代谢途径,但在复杂微生物群中实现精确基因操作仍需进一步技术突破。
4.宿主响应机制研究不足:研究揭示了野生型与突变体共生菌定植小鼠间的生理差异,但尚需深入解析相关宿主细胞类型及信号通路的具体调控机制。
未来的研究在单基因分辨率下揭示了肠道微生物群如何通过代谢肠道氨基酸影响宿主氨基酸稳态。研究鉴定出多种积极代谢肠道氨基酸的细菌,并通过大规模基因缺失分析确定了其关键代谢基因。功能实验显示,这些代谢途径通过直接调控宿主肠道和循环氨基酸的生物利用度,或间接影响外周血清素合成,从而调节宿主的葡萄糖代谢和整体营养稳态。
研究表明,定植微生物群可能以“竞争”模式与宿主共同调控营养平衡,为理解其分子层面的调节机制提供了新视角。更值得关注的是它揭示了一个新的通路:微生物氨基酸利用 → 改变宿主血中氨基酸/代谢产物 → 改变激素/神经递质(如外周 5‑HT)→ 改变葡萄糖代谢等生理功能,所以这些菌在肠道里的存在,更可能是:微调宿主营养和代谢状态,而不是简单的“好/坏”。
参考文献:
Li TT, Chen X, Huo D, Arifuzzaman M, Qiao S, Jin WB, Shi H, Li XV; JRI Live Cell Bank Consortium; Iliev ID, Artis D, Guo CJ. Microbiota metabolism of intestinal amino acids impacts host nutrient homeostasis and physiology. Cell Host Microbe. 2024 May 8;32(5):661-675.e10.

谷禾健康
麦角硫因 (EGT) 是一种含硫的抗氧化剂,由某些微生物合成,大量存在于蘑菇、发酵食品和其他膳食产品中。人体无法自主合成,需要通过饮食摄取和积累。
麦角硫因(EGT)由哺乳动物细胞输入,可以在哺乳动物组织中积累到低毫摩尔浓度,在那里它与保护健康作用有关。 同样,许多宿主相关微生物输入EGT,EGT通过其抗氧化特性增强细胞内氧化还原稳态。某些细菌物种也编码降解 EGT 的酶。事实上,最近的研究发现 EGT 可以被人类粪便细菌的复杂群落代谢。 粪便群落的 EGT 代谢因人而异,表明微生物组组成的个体间差异可能影响 EGT 代谢。
许多与宿主相关的微生物都会吸收EGT,通过其抗氧化特性增强细胞内氧化还原稳态。某些细菌物种也编码降解 EGT 的酶。因此研究人员提出假设并进行验证:EGT是否会先被部分菌种代谢生成某种可用物质,再由后续菌种接力还原,从而获能(促进ATP合成与生长)?
为此,研究人员结合群落模型、分离菌株和共培养实验、代谢物时间序列实验、多队列宏基因组数据再分析等技术进行了研究和验证。完整重现了Clostridium symbiosum和Bacteroides xylanisolvens这两种细菌在厌氧环境下”EGT→TUA(thiourocanic acid)→还原产物(3-(2‑thione‑imidazol‑4‑yl)‑propionic acid)”的代谢接力过程。在对24份健康人粪便群落进行48小时培养的功能表型测试中,有18/24样本显示EGT代谢活性并产生TMA,且其中11/18检测到还原TUA产物;相应的宏基因组分析显示,具EGT代谢活性的样本中ergothionase基因显著富集。在四个独立结直肠癌队列的粪便宏基因组数据分析中,发现ergothionase基因在其中两队列中显著富集,在另外两队列中呈增加趋势。
这些发现揭示了饮食抗氧化分子在肠道微生物能量代谢与潜在疾病风险差异中的功能纽带,为未来通过调控微生物EGT代谢改善肠道健康提供了方向。
1
确定麦角硫因代谢菌和酶
已知麦角硫因酶(EGT trimethylammonia lyase)可将EGT裂解为TMA与TUA。Treponema denticola SP33 ergothionase (TdETL) 是已被表征的“参照”,用其氨基酸序列做同源搜索,在人肠道可培养菌株库里寻找麦角硫因(ergothionase)同源物,从而锁定了C. symbiosum CLOSYM_01531和C. symbiosum CLOSYM_03165。
通过LC-MS/LC-MS-MS对C. symbiosum+EGT-d9的培养上清与细胞组分进行非靶与靶向代谢组学分析,验证其将EGT裂解为TMA与TUA,并显示TUA主要分泌到胞外。异源表达验证实验(将CLOSYM_01531这个基因装进E. coli里表达),观察到EGT-d9在约6小时内被完全转化为TMA-d9与TUA。
2
小鼠粪便菌群
来自不同来源的雌性6周龄的C57BL/6小鼠(JAX、TAC、CR)做粪便群落48小时厌氧培养+EGT-d9,比较EGT代谢能力差异。对CR群落做非靶代谢组学,鉴定得到新的代谢物(m/z 173.0379),经标准品比对,确认为还原的TUA产物3-(2‑thione‑imidazol‑4‑yl)‑propionic acid
3
细菌共培养
通过对CR 和 TAC 粪便微生物组的16S rRNA 测序分析,发现CR群落中Bacteroides acidifaciens富集。研究人员选取与 B. acidifaciens 亲缘关系较近、且在人肠道常见并已知具备多糖与宿主营养代谢能力的代表物种 B. ovatus 与 B. xylanisolvens 作为候选,检验其是否具有将 TUA 还原为 3-(2thioneimidazol4yl)propionic acid 的活性。并测试还原过程对能量代谢与生长的影响。
单培养与共培养添加EGT-d9的C.symbiosum和B.xylanisolvens时,进行长时间跟踪。同时用表达CLOSYM_01531的工程E.coli替代C.symbiosum重复共培养过程。进一步证明接力关键在于EGT产生的胞外TUA与下游还原步骤的耦合。
4
健康人队列粪便菌群
对24份健康粪便样本做48小时厌氧培养+EGT-d9,查看EGT代谢能力和产物,发现有18/24个样本把EGTd9代谢掉了。在这18个样本中,对其中3个TUA还原能力强的样本做了时间跟踪,还原代谢轨迹。同时将其中23份宏基因组数据分为两组(有代谢活性 vs 无代谢活性),做配对分析,查看ergothionase基因富集情况。
5
结直肠癌队列宏基因组功能分析
基于EGT稳态与结直肠癌(CRC)的文献线索,汇总四个已发表CRC粪便宏基因组数据集,采用统一流程定量ergothionase基因丰度,然后进行组间差异分析。
▸ C.symbiosum可将EGT代谢为TMA与TUA,且TUA主要分泌到胞外
如上图所示,经EGT-d9处理的培养物的细胞沉淀物(C. symbiosum ATCC 14940)中检测到EGT-d9和TMA-d9,表明C. symbiosum ATCC 14940导入并代谢EGT。
在C. symbiosum ATCC 14940培养上清液中检测到一种单一的代谢物(m/z 171.0223,图C),对比未经EGT-d9处理的样品,m/z 171.0223显著上调(Log2(fold change) ≥ 2, p ≤ 0.05) ,经标准品对比(图D、E),确认为TUA。用或不用EGT-d9处理C. symbiosum培养物48小时后的EGT-d9、TMA-d9和TUA含靶向定量结果显示(图F),EGT‑d9下降与TMA‑d9、TUA上升在计量上匹配,符合EGT代谢为“两段”——TMA与TUA的表现。
将CLOSYM_01531异源表达于E. coli(图C),发现其可在约6小时内将EGT‑d9完全转为TMA‑d9与TUA(图D),空载对照(Ec_EV)无此活性(图G)。此外,C. symbiosum中还鉴定到第二个同源物CLOSYM_03165,异源表达同样具活性。
▸ 小鼠粪便菌群的代谢组学分析鉴定出“还原产物”
不同来源小鼠展现出群落差异,如图A,发现CR群落48小时内可将EGT‑d9完全代谢为TMA‑d9,TAC群落仅中等程度代谢并积累TUA,JAX群落则基本无代谢。
编辑
但在CR培养物上清液中并未检测到TUA,而是发现了一个新的代谢物(m/z 173.0379),且呈显著上调(log2(fold change) ≥ 3, p ≤ 0.05),经标准品比对,确认是3‑(2‑thione‑imidazol‑4‑yl)‑propionic acid,由TUA进行2e−/2H+加氢还原所得(图E)。CR群落可将外源TUA完全转为该还原产物,而JAX、TAC不能(图G)。
▸ TUA还原增强了B.xylanisolvens在厌氧条件下的ATP合成和生长
16S rRNA 分析CR和TAC样本的菌群,发现它们具有相似的菌群多样性(图A、B),且Bacteroides acidifaciens在CR群落中显著富集(图C)。研究人员又提出假设, B. ovatus和B. xylanisolvens或许可以将TUA还原为3‑(2‑thione‑imidazol‑4‑yl)‑propionic acid。
事实也的确如此,在添加了TUA的培养基中于厌氧条件下培养这两种菌48h,定量结果显示两种菌株都消耗了培养基中的TUA,并产生了等量的3‑(2‑thione‑imidazol‑4‑yl)‑propionic acid(下图A)。B. xylanisolvens约6小时内可将TUA完全转化,且产物主要在胞外(上图E、F)。在缓冲体系中,B. xylanisolvens因TUA或TUA+甲酸钠而ATP合成约提升4倍(下图B),并伴随还原产物累积(下图C);在厌氧环境中且缺乏其它电子受体(也就是能增强ATP合成的化合物)的最小培养基中,发现TUA显著提升其生长(下图D)。
▸ C.symbiosum和B.xylanisolvens互相利用EGT的代谢产物
鉴于C. symbiosum和B. xylanisolvens可以分别代谢EGT和TUA,研究人员先假设这两个菌种可以共同将EGT转化为3‑(2‑thione‑imidazol‑4‑yl)‑propionic acid,然后通过共培养实验进行验证。验证结果显示,C.symbiosum在单独培养时会将EGT‑d9转为TMA‑d9和TUA,不产生3‑(2‑thione‑imidazol‑4‑yl)‑propionic acid,这表明C. symbiosum不能还原TUA。B.xylanisolvens则对EGT‑d9无作为。两者共培养时,EGT‑d9消耗程度与C.symbiosum单独培养时相当,但TUA几乎不积累,反而是还原产物显著积累。(图E培养4天、图F培养7天)
代谢组火山图显示细胞沉淀和培养上清液中分别仅富集TMA‑d9与还原产物,符合跨物种接力还原产物的代谢模式“EGT→TUA→3‑(2‑thione‑imidazol‑4‑yl)‑propionic acid”(图I、L)。
用表达CLOSYM_01531的E.coli与B.xylanisolvens共培养,也再现了“EGT→TUA→3‑(2‑thione‑imidazol‑4‑yl)‑propionic acid”反应(图G)。
▸ 人群普遍性和个体差异
研究人员筛选了24名健康成人,获得其粪便样本。在添加EGT-d9培养基中共同培养48小时,观察EGT代谢活性差异。发现24个样本中,有18个样本在48小时内显著代谢EGT‑d9,且均产生TMA‑d9(图A-D),这表明麦角硫因介导的EGT代谢的一个特征是消除TMA。虽然在24个样本中都没有检测到TUA,但能够代谢EGT‑d9的18个样本里,有11个样本积累了还原产物(图D)。
对3个TUA还原能力强的样本做时间序列分析,发现6–12小时内TUA短暂出现并随EGT‑d9下降而上升,随后被转化为还原产物,这直接展示了跨物种接力还原产物的代谢模式。
▸ 肠道EGT稳态的改变可能与结直肠癌有关
编辑
研究人员量化了来自四个独立结直肠癌队列和健康对照队列的粪便宏基因组数据集中ergothionase基因的相对丰度,发现有两个CRC组存在ergothionase基因显著富集的现象,另两队列呈上升趋势,这提示EGT代谢能力可能是癌症相关肠道菌群的功能特征之一。
过去更多讲的是“单个细菌把EGT彻底分解”,现在发现EGT还能被“分工协作”重塑成能增强ATP合成的化合物。这项“分工协作“的主角分别是C. symbiosum和B. xylanisolvens,重点工作内容是,C.symbiosum将EGT代谢为TUA和TMA-d9,B.xylanisolvens将TUA还原为3-(2-thione-imidazol-4-yl)-propionic acid,同时提高了自己的ATP产量,促进了自己的生长。B. xylanisolvens作为一种益生菌,目前被认为与宿主健康密切相关。根据现有发现,通过添加TUA或在有“产TUA菌”背景下添加EGT,理论上有助于B. xylanisolvens的定植。
研究中虽然提示EGT→TUA轴与疾病生态有关,但当前缺乏动物与人体定植/功能结果的直接验证。
总而言之,如果在合适的群落背景下提升B.xylanisolvens的定植或TUA还原能力,理论上可以带来:更稳的肠道生态位占据、更高效的厌氧能量代谢、潜在更好的底物利用与有益代谢物输出,并可能通过改变供给-利用格局而影响与疾病相关的微生态失衡。
主要参考文献
Zhou Z, Jiang A, Jiang X, Hatzios SK. Metabolic cross-feeding of a dietary antioxidant enhances anaerobic energy metabolism by human gut bacteria. Cell Host Microbe. 2025 Aug 13;33(8):1321-1332.e9.

谷禾健康

人体复杂的内部环境中栖息着种类繁多、功能各异的微生物群,这些微生物群落对人类的基本生理功能和各种疾病状态都产生着深刻而持续的影响。
人类胃肠道系统代表着宿主机体与宿主相关微生物群落之间最为重要和最大规模的生物接触界面。长期定植于这一特殊环境中的常驻细菌群体,经过漫长的进化历程,已经发展出高度专门化和精细调节的生物学机制,以实现对现有营养物质的最优化获取和高效利用,这些独特的适应性机制使得它们能够在激烈的生存竞争中胜过其他微生物,并在整个肠道的不同区域中成功建立起稳定而特定的微生物群落结构。
宿主与微生物群之间的众多复杂相互作用主要基于各种代谢物的交换和信号传递,因此无论是在生理稳态条件还是在各种疾病状态下,这些相互作用都会受到微生物代谢活动和环境中营养物质可用性的显著而持续的影响。
举例来说,结肠组织在正常生理稳态条件下维持着严格的厌氧环境特征,这种特殊的环境条件特别有利于那些主要通过底物水平磷酸化过程获取生存必需能量的专性厌氧微生物的成功定植和繁殖。
然而,当机体处于各种疾病条件下时,无论这些病理状态是由外来病原体感染引起,还是由非感染性自身免疫疾病如溃疡性结肠炎和克罗恩病等慢性炎症性疾病所导致,肠道上皮细胞的代谢模式都会发生显著变化,这些变化最终导致原本稀缺的氧气分子流入肠腔空间,从而为那些能够有效利用氧气进行有氧呼吸的兼性厌氧菌创造了有利的生长环境,促进了这类微生物的快速扩增和繁殖。
微生物对碳源和能量的高效获取能力始终是决定群落组成结构和功能表现的最主要驱动力量。肠道微生物群和各种肠道病原体经过长期的适应性进化,已经成功发展出多种多样的生物学机制来获得膳食来源的碳水化合物如糖醇类化合物和Amadori产物,以及来源于宿主机体的各种内源性代谢物如与粘蛋白分子密切相关的代谢产物。
注:Amadori产物是糖类与氨基酸或蛋白质发生非酶糖化反应(Maillard反应)的重要中间产物。
除此之外,微生物对各种关键微量营养素的成功获得,包括多种维生素化合物和重要的金属元素如铁、锰、铜、锌、钼、镍等,也在很大程度上控制和调节着微生物群落的整体结构组织。
本文将全面而深入地介绍肠道共生细菌和病原菌如何采用各种不同的生物学策略来获取和代谢肠道环境中丰富的宏量营养素,以实现高效的能量产生并促进其在宿主肠道中的成功定植和长期生存。
★ 不同细菌的能量代谢来源各异
环境细菌和人体相关细菌表现出惊人的代谢多样性。微生物生理学的一个关键决定因素是能量代谢,微生物根据其首选的碳源(有机物与CO2)、能源来源(阳光与化学反应)和氢供体来源(有机与H2O)可大致分类。
任何生物体要想存活,必须通过化学反应产生足够的吉布斯自由能来合成ATP并建立离子梯度。
注:吉布斯自由能可以简单理解为反应的”净可用能量”。
例如,硫杆菌属(Thiobacillus spp)等硫氧化细菌使用元素硫、硫化氢(H2S)或硫代硫酸盐作为电子供体,以氧为电子受体生成硫酸盐和其他氧化硫化合物;并通过电子传递链建立质子动力。
而大多数肠道共生菌降解有机化合物,从膳食和宿主来源(化学有机异养生物)中获得能量和代谢中间体。虽然肠道微生物营养策略多样,但人体结构严格限制了不同肠段栖息的细菌类型及其代谢模式。
▸ 肠道不同部位微生物群结构和代谢不同
人体已经进化出专门的机制,使特定微生物在肠道不同部位选择性定植,从而塑造微生物群落结构和代谢模式。
饮食和宿主因素决定了肠道微生物群的代谢

Muramatsu MK,et al.Cell Host Microbe.2024
★ 小肠以需氧和兼性厌氧菌为主,密度较低
小肠pH值从胃部酸性逐渐升至回肠末端的微酸性或中性,影响微生物群落多样性。十二指肠和空肠主要栖息耐酸需氧菌和兼性厌氧菌,如乳酸杆菌属(Lactobacillus)和链球菌属(Streptococcus)以及变形菌门(假单胞菌属)。
此外,肝胆系统释放的初级胆汁酸(BA)和牛磺酸或甘氨酸偶联的胆汁酸(CBA)以及潘氏细胞释放的抗菌肽抑制了小肠中许多细菌的生长。因此,小肠微生物密度远低于大肠,从近端至远端小肠的每克约103-7个细菌增加到结肠中的每克1011-12个细菌。
★ 大肠环境有利于专性厌氧菌定植
大肠塑造了与小肠截然不同的微生物群落结构和代谢模式。结肠的主要过滤器是缺氧环境,有利于专性厌氧菌定植。
结肠细胞大量消耗氧气进行β氧化,维持上皮缺氧状态,限制氧气从血管向肠腔扩散,促进厌氧厚壁菌门和拟杆菌门等专性厌氧菌定植。微生物产生的丁酸盐促进结肠细胞β氧化,形成宿主-微生物代谢反馈回路。由于氧气稀缺,兼性厌氧菌仅占次要地位。
大部分胆盐在回肠被吸收,剩余的初级胆盐由大肠微生物代谢。饮食营养在胃中分解后,单糖和氨基酸在小肠被吸收,而不可消化的碳水化合物(膳食纤维)和多元醇进入结肠,成为细菌的主要碳源和能源。
肠道微生物群的代谢构成了人体内最为活跃和复杂的生化反应工厂,这一庞大的微观生态系统依靠多元化的能量来源维持着自身的生存繁殖和功能发挥。肠道微生物主要是将宿主无法消化的复杂碳水化合物、膳食纤维、抗性淀粉以及内源性黏蛋白转化为可被利用的能量物质。
▸ 降解复杂多糖
由于大多数简单的营养物质在小肠中被吸收,因此大肠微生物群的许多成员主要碳和能量来源是膳食复杂多糖(纤维)。这类分子包括植物来源的聚糖,如纤维素、半纤维素、β-葡聚糖、菊粉和果胶,以及动物来源的糖原。
★ 拟杆菌等菌属具有强大的复合多糖降解能力
复杂多糖含有多样化的糖苷键,需要特异性糖苷水解酶降解。拟杆菌属等革兰氏阴性专性厌氧菌,如 Bacteroides spp. 和 Prevotella spp.,在复杂多糖的降解方面表现极强的能力。这些细菌拥有大量的碳水化合物活性酶(CAZymes),例如由不同多糖利用位点编码的碳水化合物结合蛋白、糖苷水解酶和多糖裂解酶。
拟杆菌淀粉利用系统(SUS)是多糖利用位点的经典例子:淀粉结合蛋白(SusD、SusE、SusF)识别并固定细菌表面的淀粉分子,糖苷水解酶(SusG)将其降解为寡糖,寡糖通过外膜蛋白SusC转运至周质,再被糖苷水解酶(SusA、SusB)进一步降解为单糖,最终转运至细胞质并发酵产生乙酸、琥珀酸和丙酸。拟杆菌编码众多SUS样系统和CAZymes,与膳食聚糖的多样性相匹配。
B.thetaiotaomicron中的淀粉利用系统(SUS)

Muramatsu MK,et al.Cell Host Microbe.2024
★ 毛螺菌和瘤胃球菌也能降解复杂多糖并产生短链脂肪酸
毛螺菌科(Lachnospiraceae)和瘤胃球菌科(Ruminococcaceae)等革兰氏阳性梭菌同样降解复合多糖并产生短链脂肪酸。
革兰氏阳性菌的降解机制涉及细胞外CAZymes和高亲和力转运蛋白(如ATP结合盒转运蛋白、主要促进子超家族转运蛋白和磷酸转移酶系统),底物特异性酶活性通常以基因簇形式编码。
注:虽然纤维素体降解植物细胞壁的能力在瘤胃微生物中常见,但在大多数人类肠道微生物中缺失,仅在农村和狩猎采集人群的微生物组中观察到此类活性。
▸ 代谢膳食糖醇和多元醇
多元醇是由糖类通过醛或酮基还原形成醇基而天然合成生成的糖醇。自然界中发现的主要多元醇包括赤藓糖醇、山梨糖醇、木糖醇、甘露醇和麦芽糖醇等天然形式,以及乳糖醇、异麦芽酮糖醇和氢化淀粉水解物等合成形式。
由于在胃肠道中吸收不完全,多元醇常用作低卡路里人造甜味剂。高脂肪饮食联合抗菌治疗会消耗氧敏感的多元醇降解梭菌,导致山梨糖醇不耐受。
★ 大肠杆菌能够利用甘露醇
甘露醇代谢在多种细菌中被广泛研究。在大肠杆菌中,甘露醇通过特异性磷酸烯醇式丙酮酸磷酸转移酶系统被吸收并磷酸化为甘露醇-1-磷酸,随后被甘露醇-1-磷酸脱氢酶转化为果糖-6-磷酸进入糖酵解途径。
另一途径是甘露醇以半乳糖基-甘露醇偶联物形式进入细胞,被β-半乳糖苷酶水解后,甘露醇通过甘露醇-2-脱氢酶转化为果糖,再被己糖激酶磷酸化。
★ 双歧杆菌代谢异麦芽酮糖醇并产生丁酸盐
除了甘露醇外,其他多元醇同样可被肠道微生物代谢。中等剂量的异麦芽酮糖醇和乳糖醇摄入后,肠道微生物群组成偏向双歧杆菌,为某些共生菌提供生长优势。体外实验显示双歧杆菌可代谢异麦芽酮糖醇,增加丁酸盐产生,这对维持结肠上皮细胞厌氧环境至关重要。
★ 沙门氏菌会与共生大肠杆菌竞争半乳糖醇
半乳糖醇天然存在于某些植物中,酵母也可产生。沙门氏菌通过gat操纵子利用半乳糖醇,包含磷酸转移酶系统gatABC将其转运并磷酸化,最终转化为磷酸二羟基丙酮和3-磷酸甘油醛。半乳糖醇是定植抗性的关键代谢物,沙门氏菌与共生大肠杆菌竞争这一有限资源。
▸ 粘蛋白:微生物的”应急储备”
肠道微生物群落还可分为管腔、黏液相关和上皮/隐窝相关群体。黏蛋白形成重要屏障,保护肠道上皮免受微生物侵害,其中MUC2是主要类型。小肠黏液层呈多孔状,含抗菌肽(如肠道α防御素)和凝集素(如RegIIIγ),限制微生物与上皮相互作用的同时允许营养吸收。
★ 食物缺乏时,某些细菌会消化黏蛋白
结肠黏液则形成细菌无法穿透的致密内层和松散外层,而嗜黏蛋白阿克曼菌(Akkermansia muciniphila)等可利用外层获取营养。在没有膳食纤维的情况下,肠道微生物开始消化粘蛋白,增加了患结肠炎的风险。
黏蛋白是富含脯氨酸、苏氨酸和丝氨酸的大糖蛋白家族。丝氨酸和苏氨酸残基作为N-乙酰半乳糖胺(GalNAc)的O-连接糖基化附着点,可被半乳糖和N-乙酰葡糖胺等单糖进一步修饰,形成长支链聚糖并用唾液酸、岩藻糖和硫酸盐残基末端修饰。
十二指肠、空肠和回肠的黏蛋白高度唾液酸化和硫酸化,结肠黏蛋白则含唾液酸化、硫酸化和岩藻糖化聚糖。近端结肠唾液酸化程度较高,远端结肠硫酸化程度较高。
类似膳食聚糖降解,黏蛋白的微生物消化需要多种降解菌(如嗜黏蛋白阿克曼菌及拟杆菌门、厚壁菌门成员)协同形成营养网络。降解过程由岩藻糖苷酶和唾液酸酶水解末端糖结构,硫酸酯酶去除硫酸盐基团引发。
★ 降解过程中可为其他细菌提供营养
去除这些末端结构可能会成为粘蛋白降解的潜在瓶颈,因为这些末端结构可以保护底层聚糖链免受糖基水解酶的降解,并且需要特定的酶。肠道微生物群的不同成员编码的酶可以去除这些结构并使其成为其他细菌的营养来源。
例如,扭链瘤胃球菌(Ruminococcus torques)很容易使用细胞外CAZymes消化肠粘蛋白上的聚糖。Bacteroides thetaiotaomicron通常更喜欢膳食聚糖而不是粘蛋白,并且在体外使用粘蛋白生长不佳。但R.torques产生的低聚糖的交叉喂养促进了B.thetaiotaomicron在粘蛋白上的生长。
同样,卵形拟杆菌(Bacteroides ovatus)和Roseburia intestinalis降解半纤维素成分β-甘露聚糖。而普拉梭菌(Faecalibacterium Prausnitzii)无法自行有效降解 β-甘露聚糖,但可以获得卵形拟杆菌和R.intestinalis释放的甘露寡糖。
这些例子强调了肠道营养网络的重要性以及定植于肠道的一些细菌之间的互惠关系。
唾液酸和岩藻糖降解—糖利用的例子
唾液酸和岩藻糖是复合多糖降解的常见中间体,为肠道微生物糖利用提供典型例子。
唾液酸的代谢
唾液酸(N-乙酰神经氨酸,Neu5Ac)是一种9碳单糖,通过α2-3/6键与半乳糖和GalNAc残基结合,覆盖胃肠道黏蛋白聚糖链末端。人乙状结肠MUC2分析显示,结肠中最常见表位是与α2-6 N-乙酰半乳糖胺醇结合的Neu5Ac,而小鼠中与GlcNAc结合的Neu5Ac更常见。
两物种的微生物群均编码特异性唾液酸酶,可识别特定糖苷键并去除末端Neu5Ac残基,启动糖苷水解酶的分解代谢。
部分细菌(如脆弱拟杆菌)可直接裂解和代谢唾液酸,而其他细菌仅能清除游离唾液酸分子。唾液酸转运(NanT)后,醛缩酶(NanA)将Neu5Ac代谢为丙酮酸和N-乙酰甘露糖胺(ManNAc)。ManNAc经ManNAc激酶(NanK)磷酸化,再由差向异构酶(NanE)转化为磷酸化N-乙酰葡糖胺(GlcNAc-6-P),最终代谢为果糖-6-磷酸进入糖酵解途径。
扭链瘤胃球菌(Ruminococcus torques)采用独特的唾液酸代谢策略获得竞争优势。其编码的分子内反式唾液酸酶在糖蛋白裂解时产生2,7-脱水-N-乙酰神经氨酸(2,7-anhydro-Neu5Ac)而非唾液酸,阻止其他利用唾液酸的细菌使用该底物。进入细菌细胞后,新型氧化还原酶(NanOx)将2,7-脱水-Neu5Ac转化为唾液酸。
肺炎链球菌和沙门氏菌等病原体中也检测到NanOx直系同源物和推定的2,7-脱水-Neu5Ac转运蛋白,表明该化合物可能是病原体体内定植的重要代谢物。
岩藻糖的代谢
L-岩藻糖是一种6碳脱氧糖,广泛存在于生命各分支。人和小鼠中,岩藻糖基转移酶Fut2负责胃肠道大部分岩藻糖基化,将岩藻糖附着在聚糖的基端α(1,6)和末端α(1,2)、(1,3)或(1,4)位。胃肠道中,岩藻糖通过肠道微生物分泌的α-L-岩藻糖苷酶从膳食或宿主黏蛋白聚糖中释放,随后被部分肠道微生物吸收代谢。
大肠杆菌的岩藻糖利用已被广泛研究,其编码岩藻糖利用操纵子(fucOAPIKR)。岩藻糖通过专用通透酶(FucP)导入细胞,经异构酶FucI转化为L-岩藻酮糖,再被激酶FucK磷酸化。岩藻酮糖1-磷酸被醛缩酶(FucA)裂解为乳醛和DHAP。
厌氧条件下,乳醛被氧化还原酶(FucO)还原为1,2-丙二醇;有氧条件下(如肠道炎症期间),乳醛转化为乳酸并氧化为丙酮酸进一步代谢。缺乏fucK和fucAO的大肠杆菌突变体虽能在小鼠肠道初步定植,但无法长期稳定定植,表明岩藻糖获取和利用能力是维持哺乳动物肠道环境的关键。多形拟杆菌和脆弱拟杆菌也利用岩藻糖在小肠中保持竞争优势。
有趣的是,共生肠道细菌可诱导小鼠肠道宿主Fut2表达,形成富含岩藻糖的生态位,既保护宿主聚糖又允许岩藻营养细菌扩增。无菌小鼠经常规小鼠粪便浆液处理可诱导小肠岩藻糖基化。广谱抗生素处理的常规小鼠杯状和柱状上皮细胞岩藻糖基化严重减少,表明共生菌在宿主Fut2表达和肠聚糖岩藻糖基化中发挥作用。
一些细菌的存在,如丝状细菌、多形拟杆菌和沙门氏菌等细菌可在无菌小鼠回肠诱导宿主岩藻糖基化。虽然肠道共生体诱导Fut2介导岩藻糖基化的信号分子仍不明确,但葡聚糖硫酸钠和霍乱毒素等促炎环境压力源可诱导岩藻糖基化。
除饮食偏好(高脂肪西餐vs富含纤维饮食)、食物类别(蔬菜vs肉类)和食品添加剂外,食物制备方法也影响微生物代谢。
▸ 食物制备方法会影响微生物代谢
法国科学家Maillard最早描述了一种导致烹饪中观察到的褐变效应的反应,称为美拉德反应。当单糖羰基与氨基酸氨基反应时产生Amadori产物,其聚合形成更复杂的类黑精。常见食品加工方法(加热、干燥)产生多种Amadori化合物,如果糖-谷氨酰胺(F-Gln)、果糖-苯丙氨酸(F-Phe)和果糖-天冬酰胺(F-Asn)。
注:美拉德反应(Maillard reaction)是食品工业中广泛存在的一种非酶褐变现象,由还原糖与氨基化合物(如氨基酸、蛋白质)在常温或加热条件下发生复杂反应,生成类黑精等棕色物质,并产生大量风味物质。类黑精是指含有半缩醛羟基的化合物(醛、还原糖)与含有氨基的化合物等经缩合、聚合反应生成的高分子量聚合物。
★ 肠道共生菌和病原菌均可利用美拉德反应产物
人肠道分离株肠单胞菌AF211(毛螺菌科成员)可代谢果糖赖氨酸(F-Lys)并产生丁酸盐、乳酸盐和氨。F-Lys通过ABC转运蛋白输入,被YhfQ磷酸化形成6-磷酸果糖-赖氨酸,再被6-磷酸果糖-赖氨酸脱糖酶(Yhfn)转化为6-磷酸葡萄糖(G6P)和赖氨酸。
肠道病原体沙门氏菌通过fra操纵子(fraRBDAE)利用F-Asn作为碳氮源。F-Asn首先被果葡天冬酰胺酶FraE转化为果糖-天冬氨酸(F-Asp),再由F-Asp转运蛋白FraA导入。随后F-Asp被FraD磷酸化形成F-Asp-6-磷酸,再被脱糖酶FraB代谢为G6P和天冬氨酸。
▸ 发酵是能源生产的主要模式
发酵作为厌氧环境中的关键生化过程,构成了肠道微生物能源生产的主要模式,这一代谢途径在维持微生物群落的生存和功能发挥方面起着至关重要的作用。
肠道微生物会使用大量的分子,特别是通过复合多糖降解释放的单糖以及氨基酸(Stickland 反应),进行发酵。
注:Stickland反应为专性厌氧细菌的梭菌属中常见的一种反应。
★ 发酵产生乳酸、短链脂肪酸等产物
发酵过程中需在细菌细胞内平衡氧化还原反应,避免还原当量(如NADH)积累。维持适当的NAD+/NADH比率对氧化还原稳态和NAD+依赖性酶功能至关重要。
最简单的发酵中,葡萄糖在Embden-Meyerhof-Parnas途径中转化为两个丙酮酸分子,净产生两个ATP和四个还原当量。丙酮酸代谢物用于恢复NAD+/NADH平衡,如将丙酮酸还原为乳酸(乳酸发酵)或将乙醛还原为乙醇(乙醇发酵)。肠道发酵的常见终产物包括乳酸、甲酸、琥珀酸及短链脂肪酸(乙酸、丙酸、丁酸)。
一些发酵途径广泛存在,如从丙酮酸产生乙酸的Pta-AckA途径。铁氧还蛋白氧化还原酶、丙酮酸甲酸裂解酶或丙酮酸脱氢酶将丙酮酸转化为乙酰辅酶A,再经磷酸乙酰转移酶转化为乙酰磷酸。乙酸激酶活性从乙酰磷酸和ADP生成ATP,同时产生乙酸。
发酵是肠道共生细菌产生细胞能量的主要方式
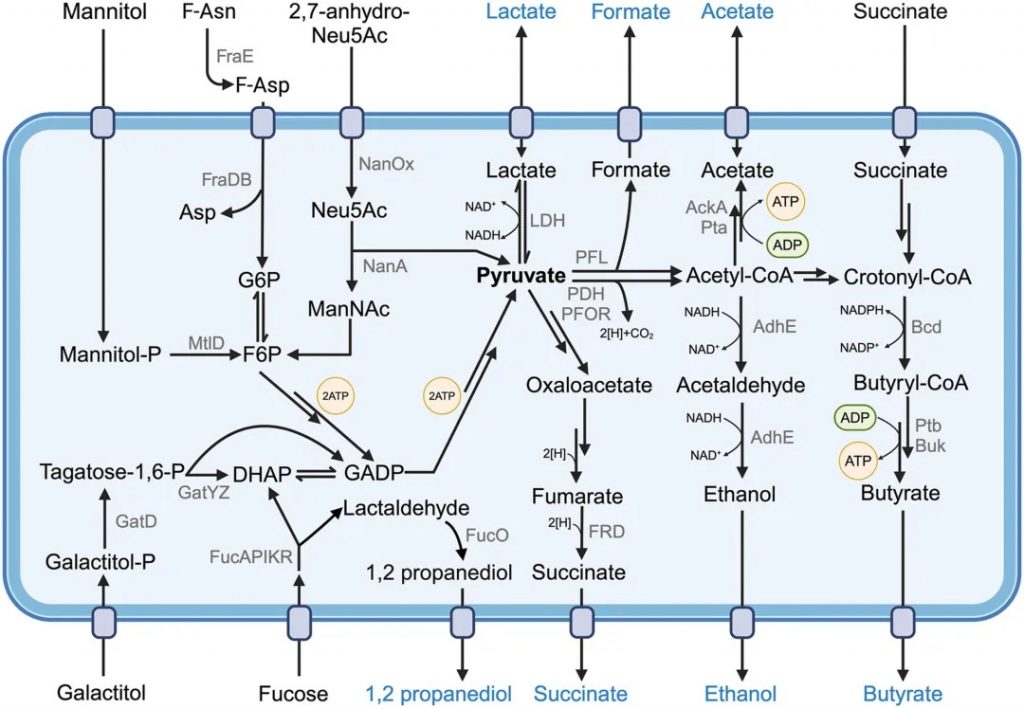
Muramatsu MK,et al.Cell Host Microbe.2024
★ 短链脂肪酸变化可反映肠道健康状态改变
丁酸主要由毛螺菌科和瘤胃球菌科成员通过聚糖直接降解或交叉发酵乳酸、乙酸、琥珀酸产生。两个乙酰辅酶A分子融合形成乙酰乙酰辅酶A,经数步转化为巴豆酰辅酶A和丁酰辅酶A,平衡NAD+/NADH池。类似Pta-AckA途径,丁酰辅酶A产生ATP并形成丁酸。另外,琥珀酸可在多步过程中还原为4-羟基丁酰辅酶A,再转化为巴豆酰辅酶A和丁酰辅酶A。戊二酸和赖氨酸也可转化为巴豆酰辅酶A。
短链脂肪酸的产生是关键代谢输出,指导结肠上皮进行β氧化,维持肠腔厌氧环境。该过程在肠道病原体感染、口服抗菌剂或高脂饮食时被破坏,导致肠道微生物群显著改变、丁酸产生减少和兼性厌氧菌扩增。
★ Stickland反应是肠道代谢物的重要来源
Stickland反应是某些肠道细菌产生能量的特殊发酵过程。在此反应中,成对氨基酸同时脱氨,一个被氧化,另一个被还原,产生ATP和NAD+。该反应主要见于梭菌属,已鉴定出特定的供体氨基酸(丙氨酸、缬氨酸、丝氨酸)和受体氨基酸(甘氨酸、脯氨酸、天冬氨酸)组合。氧化反应中供电子氨基酸转化为羧酸并产生ATP;还原反应中受电子氨基酸将NADH氧化为NAD+,产生乙酸、5-氨基戊酸、异己酸等代谢物。
编码甘氨酸还原酶途径基因的生物体可通过甘氨酸还原产生ATP、氨和乙酸。氨基酸氧化或还原可补充其他能量产生形式。丙氨酸和丝氨酸氧化脱氨产生的丙酮酸可用于TCA循环。氨基酸还原发酵通过再生NAD+等高能电子载体辅助糖酵解。编码和使用红杆菌氮酶(RNF)样复合物的生物体可将氨基酸代谢与质子驱动力产生结合以提高ATP产量。在厌氧菌具核梭杆菌(Fusobacterium nucleatum)中,RNF复合物的破坏导致ATP生成减少、氨基酸代谢减少和毒力受损。
肠道细菌中的Stickland发酵和硫代谢

Muramatsu MK,et al.Cell Host Microbe.2024
Stickland反应产生大量在小鼠肠道和人血中发现的代谢物。人肠道共生梭状芽孢杆菌(C.sporogenes)通过丝氨酸脱水酶氧化发酵丝氨酸和还原精氨酸产生ATP。由脯氨酸和芳香族氨基酸Stickland反应形成的还原代谢物(5-氨基戊酸、苯丙酸、3-(4-羟基苯基)丙酸、吲哚丙酸)也存在于人血中,表明还原Stickland反应衍生代谢物可离开肠道进入循环系统。这表明Stickland反应是哺乳动物肠道和远端部位代谢物的重要但被低估的来源。
★ 艰难梭菌的胶原蛋白降解与脯氨酸利用策略
许多依赖Stickland反应的细菌具有蛋白水解作用,可通过细胞外蛋白酶快速降解蛋白质。肠道病原体艰难梭菌导致宿主释放胶原蛋白应对毒素介导的炎症。胶原纤维主要由脯氨酸、甘氨酸和羟脯氨酸组成。艰难梭菌降解这些纤维,将反式-4-羟基-L-脯氨酸转化为L-脯氨酸,通过prd操纵子进行还原发酵产能。缺乏4-羟脯氨酸脱水酶HypD的突变菌株致病力受损。其他梭状芽胞杆菌如Paeniclostridium spp.在体外与艰难梭菌竞争脯氨酸,影响其发酵能力。
综上所述,这表明反式-4-羟基-L-脯氨酸的利用是艰难梭菌用于在体内获得脯氨酸的一种策略,并且脯氨酸发酵在艰难梭菌的体内存活中发挥作用。
呼吸作用过程中,电子通过电子传递链转移至外源电子受体,通过酶复合物质子泵活动或标量化学形成质子动力。
厌氧呼吸,特别是富马酸还原,在肠道细菌中常见。伯克氏菌科(Burkholderiaceae)、爱格氏菌属(Eggerthella)和丹毒丝菌科(Erysipelotrichaceae) 成员对膳食电子受体表现出种属特异性利用。
▸ 胆汁酸的利用
胆汁酸(BA)是消化系统重要组成部分。肝脏产生的主要胆汁酸包括胆酸(CA)和鹅去氧胆酸(CDCA),分泌前与牛磺酸或甘氨酸结合。人体内牛磺酸与甘氨酸结合胆汁酸的比例取决于饮食,牛磺酸主要来源于肉类、鱼类和贝类。
★ 胆汁酸有助于发酵过程中的能量转化
胆汁酸(BA)经细菌活动进一步修饰,包括转化和解偶联。在胆酸(CA)向脱氧胆酸和CDCA/熊去氧胆酸向石胆酸的多步转化中,7-羟基被去除,使梭菌科和爱格氏菌属(Eggerthella)能够将NADH转化为NADPH,有助于发酵过程中维持理想的NAD+/NADH比率。共生微生物从BA中解离牛磺酸,导致肠道游离牛磺酸浓度升高。胆盐水解酶通过催化类固醇部分C-24位置与BA氨基酸侧链间的酰胺键水解促进解偶联。
★ 肠道存在多种胆盐代谢细菌,包括致病菌
肠道微生物群含有许多编码不同底物特异性胆盐水解酶的细菌。厚壁菌门和放线菌门成员可降解大多数结合胆汁酸,而拟杆菌门菌株偏爱牛磺酸结合胆汁酸,双歧杆菌属和约氏乳杆菌(Lactobacillus johnsonii)乳杆菌等富含胆盐水解酶。结合胆汁酸的解离高度依赖于产胆盐水解酶微生物的位置:小鼠近端小肠中的乳酸杆菌开始解离,而人类中解离直到末端回肠和结肠才发生。
释放的牛磺酸可被不同肠道微生物利用。沃氏嗜胆菌(Bilophila wadsworthia)是肠道微生物群的亚硫酸盐还原致病菌,虽仅占正常肠道微生物群的0.01%,但与多种临床疾病相关。当IL-10缺陷小鼠饲喂低脂饮食并补充牛磺酸结合胆汁酸时,会导致肠道B.wadsworthia种群激增。B.wadsworthia利用异化亚硫酸盐还原酶复合物(Dsr)从有机磺酸盐释放的亚硫酸盐产生H2S。
牛磺酸转运入细胞后,B.wadsworthia利用两个基因簇(ald-tpa-sarD和adhE-islA-islB)代谢牛磺酸。牛磺酸首先被Tpa和Ald转化为磺基乙醛,再被SarD转化为乙硫磺酸盐。异羟乙基磺酸进入细菌微区室后,IslAB形成甘油自由基酶,促进C-S键裂解,将其转化为乙醛和亚硫酸盐。乙醛被AdhE代谢成乙酰辅酶A,再通过Pta-AckA途径转化为乙酸,而亚硫酸盐被Dsr系统用作亚硫酸盐呼吸中的电子受体。
▸ 硫酸酯酶和硫酸盐的利用
多糖常被硫酸盐修饰,需释放硫酸盐基团才能接触糖基团。GlcNAc和半乳糖的硫酸化发生在不同羟基位置,特别是GlcNAc的6-羟基(6S-GlcNAc)和半乳糖的3-、4-或6-位置。利用O-糖核心结构中这些硫酸盐基团需要能识别并裂解特定糖苷键的碳水化合物硫酸酯酶。
★ 硫酸酯酶表达菌释放硫酸盐供硫酸盐还原菌利用
表达硫酸酯酶的细菌释放的硫酸盐通过交叉喂养被硫酸盐还原细菌(SRB)利用。SRB存在于约50%的人群中,进行异化硫酸盐还原,将硫酸盐还原为腺苷-5′-磷酸硫酸盐、亚硫酸盐,并进一步还原为H2S。与缺乏成熟硫酸酯酶的B.thetaiotaomicron 菌株相比,当与从肠道粘蛋白中释放硫酸盐的B.thetaiotaomicron菌株共定植时,其在体内的相对丰度增强。H2S具有剧毒,宿主将其解毒为硫代硫酸盐,后者可用作Desulfovibrio spp.的电子受体。
▸ 外部电子转移
寻找合适的电子供体和受体对是细菌产能的关键。部分细菌已开发利用外源性电子受体的策略。外部电子转移(EET)连接细胞质氧化还原反应,将电子转移至与细菌直接接触或远端的外部电子受体。该过程已在环境细菌中广泛描述,近期在哺乳动物微生物群和肠道病原体中也有报道。
★ 细菌具有直接电子转移和介导电子转移两类
革兰氏阴性菌的胞质膜、肽聚糖层和外膜对EET构成物理屏障。为克服这些障碍,电活性细菌进化出两类方法:直接电子转移和介导电子转移(MET)。直接电子转移主要见于环境生物体如Shewanella oneidensis,电子直接传输至与外膜接触的外部电子受体。
MET则需要电子穿梭介导电子从细菌转移至外部电子受体。铜绿假单胞菌释放苯嗪(含氮杂环化合物)将电子转移至分子氧,植物乳杆菌利用醌1,4-二羟基-2-萘甲酸还原铁。P.prausnitzii与上皮细胞相关,该专性厌氧菌可能使用黄素和硫醇作为细胞外电子穿梭来减少宿主组织释放的氧气。
★ 细菌获取外部电子的方式影响其环境适应性
在革兰氏阳性肠道病原体单核细胞增生李斯特菌中,基于黄素的EET(FLEET)途径将NADH脱氢酶(Ndh2)产生的电子穿梭至质膜中脂溶性去甲基甲萘醌衍生物,再转移至膜结合脂蛋白(PplA)上的黄素或黄素单核苷酸基团,最终传递给末端电子受体。
研究表明,单核细胞增生李斯特菌厌氧条件下代谢糖醇需要FLEET通路,ndh2突变体在小鼠肠道定植能力受损。FLEET通路基因的直系同源物在数百种厚壁菌门和人类病原体中均有发现。这些研究突出了电子受体的重要性,表明细菌已进化出复杂机制获取外部电子受体池,以增强其在特定环境中的生长能力。
▸ 肠道炎症时的能量代谢
肠道炎症会导致微生物群水平变化,变形菌门(尤其是兼性厌氧肠杆菌科)丰度增加。呼吸电子受体的释放是这些群落变化的关键驱动因素,重塑了肠道细菌的能量代谢。
★ 电子受体的释放影响肠道菌群的能量代谢
例如,沙门氏菌(Salmonella)诱导胃肠炎时,活性氧(ROS)将宿主产生的硫代硫酸盐氧化为连四硫酸盐。沙门氏菌编码连四硫酸盐利用基因簇(ttrRSBCA),实现厌氧连四硫酸盐呼吸。炎性ROS和活性氮(RNS)分解产生硝酸盐,为沙门氏菌提供高能电子受体。
肠道炎症改变了末端电子受体的可用性

Muramatsu MK,et al.Cell Host Microbe.2024
★ 炎症导致氧气泄漏促进需氧病原体增殖
此外,炎症相关的结肠细胞代谢变化使氧气泄漏至肠腔,支持肠道病原体生长。电子受体的可用性不仅实现高效的电子传输产能,还可利用发酵终产物(如琥珀酸、乳酸和1,2-丙二醇),将其完全氧化为二氧化碳。
类似的机制正在驱动非感染性结肠炎期间肠道微生物群的水平变化。硝酸盐和氧气呼吸有助于共生肠杆菌科细菌的繁殖,例如非感染性结肠炎小鼠模型中的大肠杆菌、肠杆菌属和克雷伯氏菌属。上皮细胞释放的活性氧被过氧化氢酶解毒,过氧化氢酶是一种产生分子氧的反应,支持大肠杆菌的呼吸。
此外,口服抗菌治疗期间产生丁酸盐的梭状芽胞杆菌的耗竭会改变结肠细胞代谢;氧气的流入导致肠杆菌科种群的扩大。
呼吸电子受体可用性增加引起微生物群水平变化表明,碳和氮并非细菌生长的限制因素,而能量代谢和从有限底物库产能的能力才是肠道微生物群组成和功能的关键决定因素。
本文介绍了共生菌和病原菌在肠道中获取营养素和产生能量的机制。细菌可氧化有机和无机化合物产生生长必需的能量。在不同微环境中的产能能力是群落结构的关键决定因素。
人体肠道包含多个动态生态位,肠道微生物群在受宿主营养摄入、栖息地过滤器和疾病炎症影响的环境中调节能量产生。
人类微生物组研究传统上侧重于识别与健康和疾病相关的关键细菌种类(如炎症性肠病、艰难梭菌感染、抗生素相关菌群失调等)。但宿主-微生物和微生物间相互作用及其代谢机制同样重要。研究显示,细菌有效利用特定营养物质的能力(无论独立利用还是通过细菌营养网络)是微生物群组成和功能的关键驱动因素。
对宿主健康而言,微生物执行的代谢功能非常重要。这在致病性菌群相关的生态失调中显而易见,共生微生物因面临新代谢环境和成员间相互作用挑战而异常增殖并致病。
发现疾病相关代谢途径对个性化医疗具有重要意义。未来,随着对肠道微生物代谢功能理解的不断深入,我们有望开发出更加精准的个性化医疗策略,包括恢复特定代谢缺陷的微生物疗法,以及深入理解宿主-微生物代谢相互作用的分子机制。通过调节肠道微环境、优化营养网络以及恢复关键代谢途径,我们将能够更有效地治疗与微生物群失调相关的疾病,为人类健康开辟新的治疗途径。
主要参考文献
Muramatsu MK, Winter SE. Nutrient acquisition strategies by gut microbes. Cell Host Microbe. 2024 Jun 12;32(6):863-874.
Yersin S, Vonaesch P. Small intestinal microbiota: from taxonomic composition to metabolism. Trends Microbiol. 2024 Oct;32(10):970-983.
Murdoch CC, Skaar EP. Nutritional immunity: the battle for nutrient metals at the host-pathogen interface. Nat Rev Microbiol. 2022 Nov;20(11):657-670.
Miller BM, Bäumler AJ. The Habitat Filters of Microbiota-Nourishing Immunity. Annu Rev Immunol. 2021 Apr 26;39:1-18.
Salzman NH, Hung K, Haribhai D, Chu H, Karlsson-Sjöberg J, Amir E, Teggatz P, Barman M, Hayward M, Eastwood D, Stoel M, Zhou Y, Sodergren E, Weinstock GM, Bevins CL, Williams CB, Bos NA. Enteric defensins are essential regulators of intestinal microbial ecology. Nat Immunol. 2010 Jan;11(1):76-83.
La Rosa SL, Ostrowski MP, Vera-Ponce de León A, McKee LS, Larsbrink J, Eijsink VG, Lowe EC, Martens EC, Pope PB. Glycan processing in gut microbiomes. Curr Opin Microbiol. 2022 Jun;67:102143.
Eberl C, Weiss AS, Jochum LM, Durai Raj AC, Ring D, Hussain S, Herp S, Meng C, Kleigrewe K, Gigl M, Basic M, Stecher B. E. coli enhance colonization resistance against Salmonella Typhimurium by competing for galactitol, a context-dependent limiting carbon source. Cell Host Microbe. 2021 Nov 10;29(11):1680-1692.e7.
Schaus SR, Vasconcelos Periera G, Luis AS, Madlambayan E, Terrapon N, Ostrowski MP, Jin C, Hansson GC, Martens EC. Ruminococcus torques is a keystone degrader of intestinal mucin glycoprotein, releasing oligosaccharides used by Bacteroides thetaiotaomicron. bioRxiv [Preprint]. 2024 Jan 16:2024.01.15.575725.

谷禾健康

人体肠道微生物组对消化、免疫调节、代谢平衡、抵抗病原体及整体健康至关重要。在儿童发育中,生命最初两到三年的肠道微生物组发展是影响终生健康的关键期。
出生时几乎无菌的婴儿肠道迅速发展为复杂的微生物生态系统,经历连续的群落更替和成熟。这一过程不仅是对环境的被动适应,更是与宿主生理发育协同的积极进程,对免疫系统和代谢功能的正常发展具有决定性作用。
近年来,随着高通量测序技术的进步,我们对婴儿肠道微生物组的理解已经从描述性分析转向更深入的功能和临床相关性研究。然而,目前关于婴儿微生物组发育轨迹的大规模纵向研究依然有限,尤其缺乏将微生物群落动态变化与远期健康结果相关联的研究。
婴儿微生物组发展能否预测未来健康状况?是否存在”健康”或”最优”的微生物组发展模式?哪些环境因素和早期暴露会影响微生物组的发展方向?

近期发表的一项大规模纵向队列研究或许能解答此问题。研究人员对芬兰赫尔辛基地区967名3周至24月龄婴儿进行肠道微生物组纵向跟踪(谷禾肠道菌群数据库也纳入了该队列数据),旨在揭示其婴幼儿生长发育的规律,并通过建立和评估微生物组健康指数(MWI)探明与其远期健康的关联性。
研究发现肠道微生物组的发展遵循可预测的轨迹,这些轨迹受到出生方式、喂养类型和早期抗生素暴露等因素的调节,并与儿童期的健康状况具有重要关联。通过这项研究,我们期望为理解肠道微生物组在早期生命中的作用提供关键见解,并为指导干预措施优化婴儿肠道微生物组提供科学依据。
★ 研究意义
1.证明肠道微生物群的重要性
2.对早期生活的影响
3.健康预测
★ 研究特点
1.大规模队列:研究使用了一个包含近1000名婴儿的大型纵向队列,监测了从出生到5岁的健康数据。
2.多时间点采样:收集了婴儿前两年内的6203份粪便样本,进行肠道微生物群的分析。
3.微生物群发展轨迹:通过聚类和轨迹建模,识别出五种不同的肠道微生物群发展轨迹。
4.健康指数:创建了一个基于健康发展轨迹的肠道微生物群健康指数,用于评估婴儿的整体健康状况。
5.关键微生物:研究发现双歧杆菌和拟杆菌是早期的关键微生物,指导微生物群的发展,并持续预测积极的健康结果。
6.影响因素:研究分析了多种因素(如分娩方式、饮食、抗生素使用)对肠道微生物群发展的影响。
★ 研究目标
1.描述婴儿前两年内肠道微生物群的发展模式。
2.识别与健康相关的微生物群发展轨迹。
3.创造一个肠道微生物群健康指数,用于预测婴儿的健康风险。
本研究旨在提供对婴儿肠道微生物群发展的深入理解,说明肠道微生物群在预测健康方面起着重要的作用,并为改善婴儿健康提供新的工具和方法。
研究使用了来自芬兰赫尔辛基的一个纵向出生队列,共收集了984名婴儿的粪便样本和健康数据。样本在婴儿3周、6周、3个月、9个月、12个月和24个月时采集。
儿童健康、发育和健康相关数据是从父母填写的问卷中收集的,由两种类型的变量组成:
(a)2岁时医生诊断的过敏性疾病,或5岁时确诊的特应性皮炎、过敏性鼻炎或哮喘;表型过敏,即基于ISAAC问卷的上述疾病在2或5岁时的症状;2或5岁时按世卫组织标准的异常身高或体重(>2或<-2SD);下呼吸道和上呼吸道感染、胃肠感染、耳部感染、痘病毒感染或发热的发生率。罕见感染(N<5)被排除。
(b)正常变异和主观评估:2或5岁时轻度异常身高或体重(>1或<-1SD);父母用VAS量表(0-100mm)对儿童健康状况较低评分;2岁前胃肠功能(排便、胃痛、胀气)表现;3个月龄时基于哭闹时间的婴儿分类。
•纵向出生队列
-采用纵向队列研究设计,跟踪婴儿从出生到2岁,甚至到4-5岁,以观察肠道微生物群随时间的变化。
•样本收集
在婴儿的3周、6周以及3、9、12、18和24个月时收集粪便样本。
•微生物组测序
对粪便样本进行16S rRNA基因测序,以分析肠道微生物群的组成。
•数据分析
-使用统计软件(如R语言)进行数据分析。
-应用线性混合模型(LMM)来分析微生物群随时间的变化。
-使用机器学习算法(如随机森林)来识别与过敏性疾病相关的微生物特征。
•问卷调查
通过在线问卷收集关于母亲和婴儿的信息,包括生活方式、环境暴露、儿童饮食、健康等。问卷在多个时间点进行,以跟踪变化。
•过敏性疾病诊断
根据国际疾病分类(ICD-10)代码或医生诊断记录来确定过敏性疾病的发生。包括食物过敏、哮喘、湿疹和过敏性鼻炎。
•统计分析
-使用多变量回归分析来评估肠道微生物群与过敏性疾病之间的关系。
-考虑潜在的混杂因素,如母亲的过敏史、抗生素使用、分娩方式等。
通过这些综合方法,能够全面评估婴儿肠道微生物群的发展轨迹,并探索其与过敏性疾病风险及健康结果之间的关联。
1
影响婴儿肠道微生物组的因素
在肠道微生物群组成中观察到一个明显的年龄梯度,婴儿肠道微生物群在生命的前两年逐渐接近,但没有达到成人样组成。
在最初的6个月(26周),婴儿肠道微生物群的组成在个体之间差异很大,但此后趋于一致。
984名婴儿的肠道微生物群
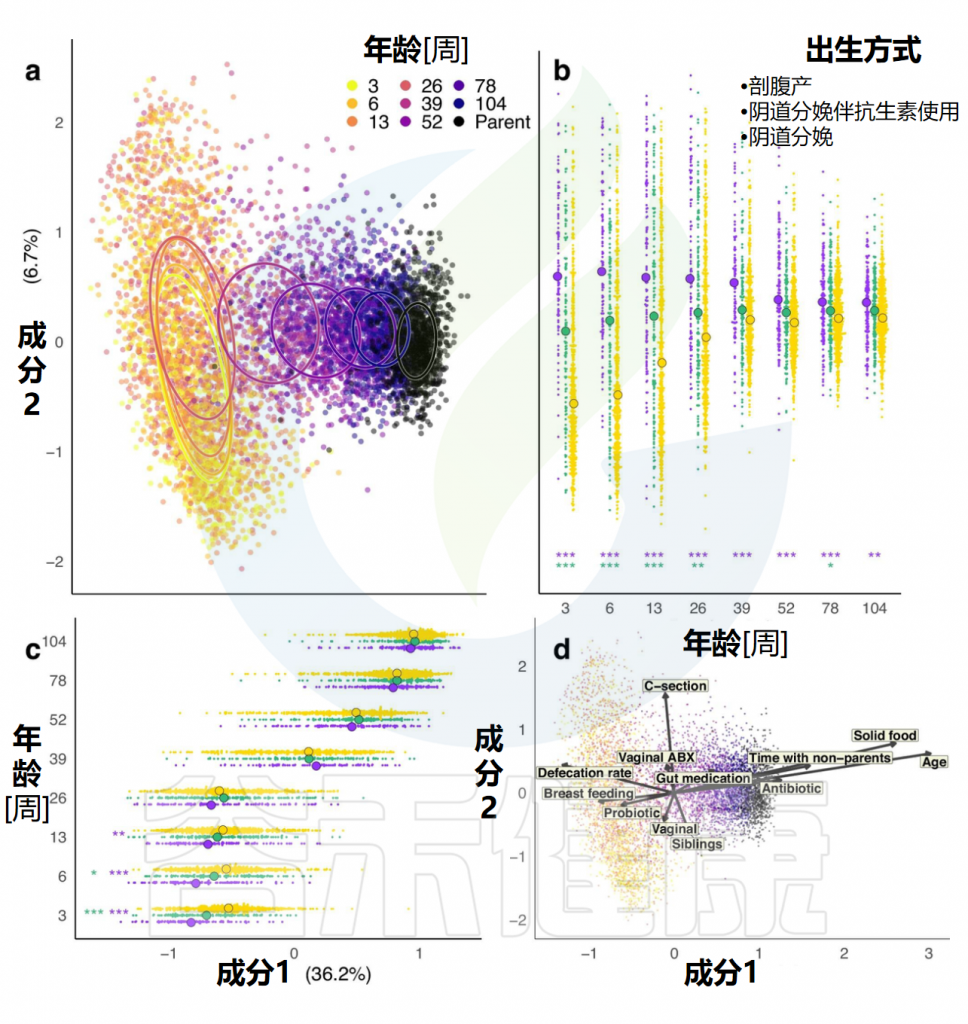
doi: 10.1038/s41467-024-52561-6.
注:主坐标分析展示了对数转换微生物属相对丰度的Pearson相关距离。图中不同颜色代表3至104周的婴儿年龄,父母微生物群以黑色表示。图b和图c分别显示PC组件2和PC组件1与年龄和分娩方式的关系,组中值用大圆圈标识。
肠道菌群组成的最重要决定因素是前26周的出生方式、抗生素暴露、第一年的排便率以及1至2岁(52-104周)的饮食和家庭组成。母亲特征在所有时间点都有适度且一致的影响,并且母亲微生物群组成在26周时变得有影响力,随着时间的推移而增加。
婴儿肠道微生物组的影响因素
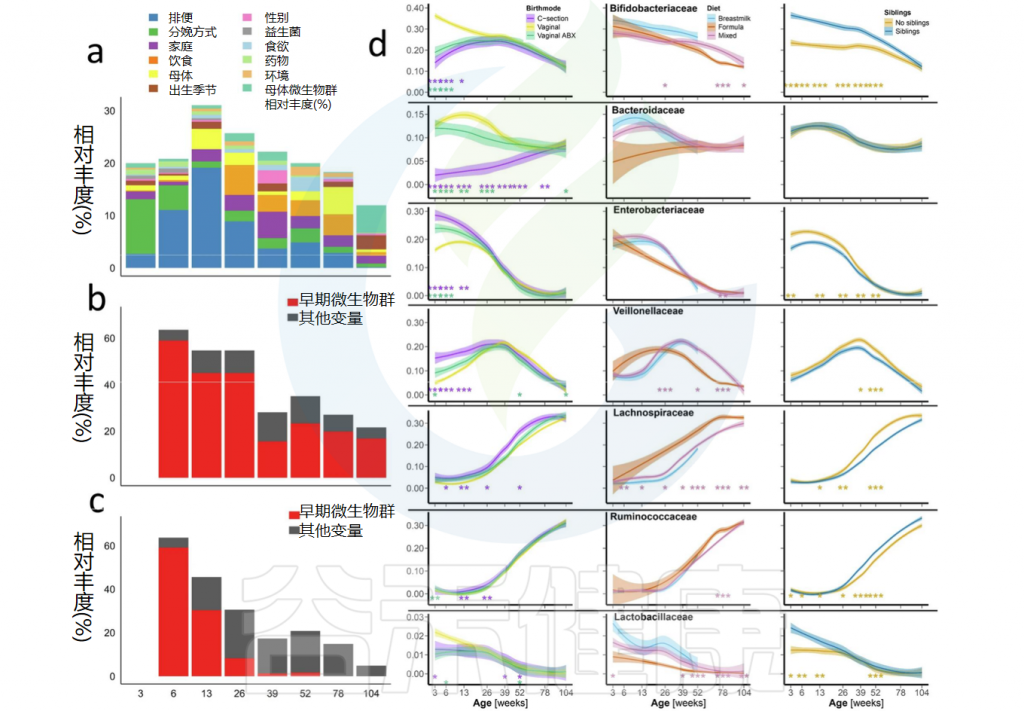
doi: 10.1038/s41467-024-52561-6.
2
婴儿微生物群落类型
研究者使用K-means聚类和log-pearson距离方法,在属水平上对婴儿样本进行分析,确定了四种主要的微生物群落类型(C1-C4),这些类型随着婴儿年龄发展而呈现规律性变化。
•C1型(绿色)
主导菌群:双歧杆菌属(39.2%)和拟杆菌属(12.8%);
特点:放线菌门和拟杆菌属成员覆盖超过50%的相对丰度;
时间分布:主要在婴儿生命的前26周出现;
常见于:未接触抗生素的阴道分娩婴儿;
粪便特征:多为黄色粪便。
•C2型(蓝色)
主导菌群:几乎没有双歧杆菌(4.8%),梭菌科(13.4%)和肠杆菌科(25.7%)相对丰度高;
特点:微生物丰富度最低,潜在致病菌相对丰度最高;
时间分布:主要在婴儿生命的前26周出现;
常见于:剖腹产婴儿和接触抗生素的阴道分娩婴儿;
粪便特征:相比C1更容易出现绿色粪便。
•C3型(橙色)
主导菌群:双歧杆菌科(27.3%)、乳杆菌科(18.5%)和韦荣球菌科(20.1%);
时间分布:39-52周(9-12个月)时常见;
常见于:大多数婴儿在9个月左右;
粪便特征:棕色。
•C4型(红色)
主导菌群:毛螺菌科(30.0%)和瘤胃球菌科(30.0%)为主;
特点:微生物丰富度最高;
时间分布:52周(12个月)后常见;
粪便特征:多为棕色粪便,反映固体食物增加。
微生物群落类型
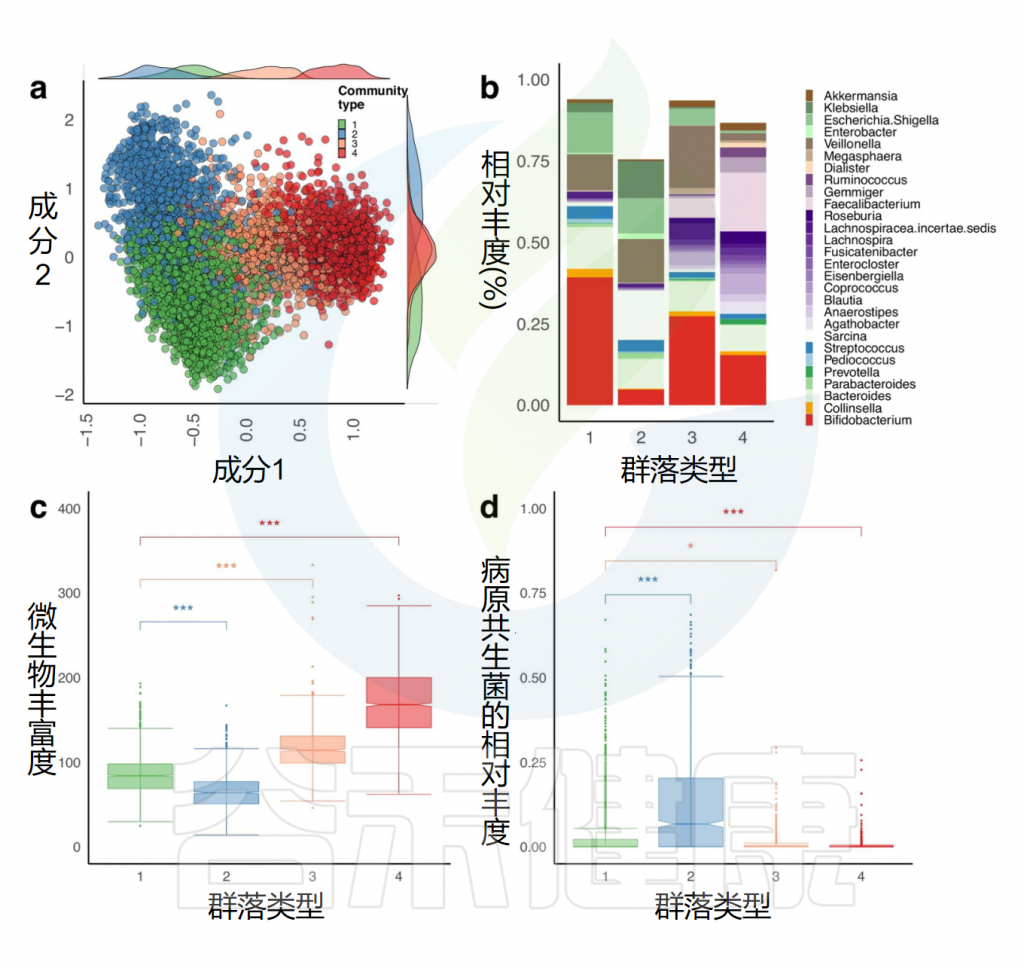
doi: 10.1038/s41467-024-52561-6.
微生物丰富度存在差异
微生物丰富度在群落类型之间差异很大,C4最高,C2最低,并且通常显示与婴儿年龄的相关性越来越大。潜在致病菌的相对丰度在C2中最丰富。
群落决定因素和健康关联
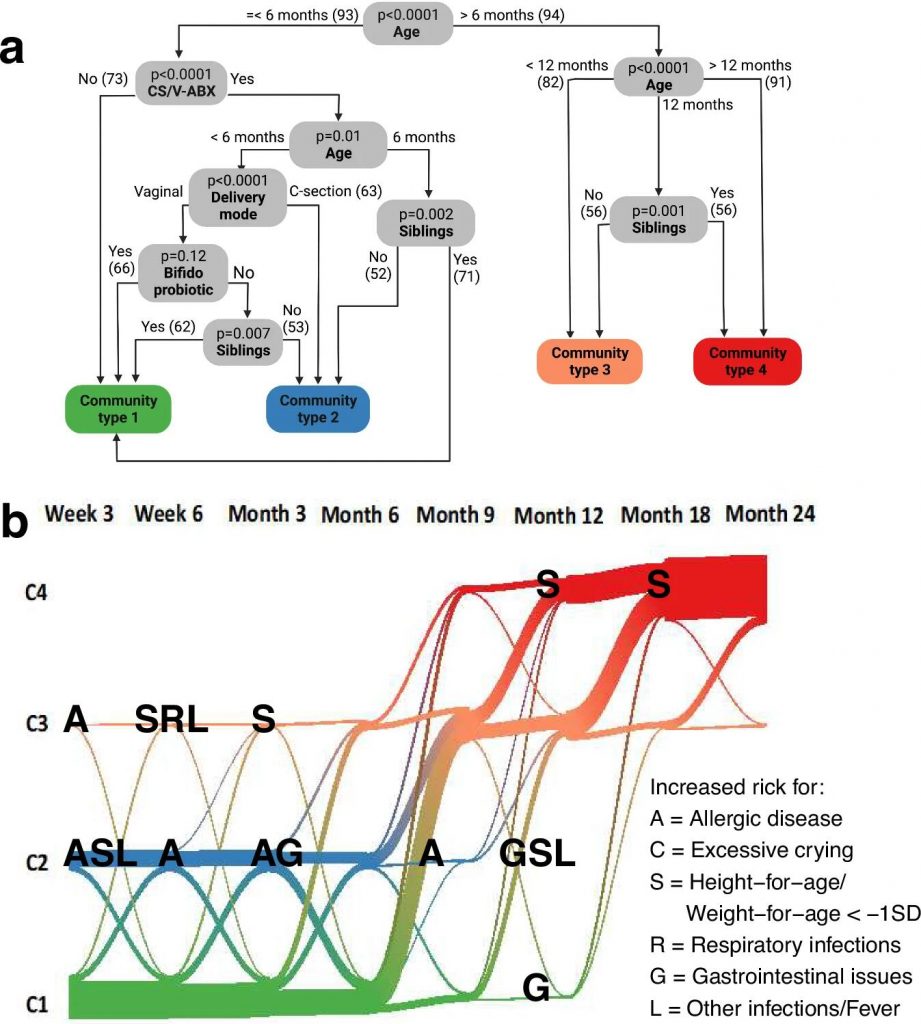
doi: 10.1038/s41467-024-52561-6.
(a)微生物群落类型决定因素的分区树;
(b)使用负广义线性模型分析了不同年龄段微生物群落类型之间的时间演变及其与5岁时健康结果的关联。
不同微生物类型与健康结果相关
分析各时间点微生物群落类型与2岁和5岁健康结果的关联发现,C2型与不良健康结果尤其是过敏性疾病风险增加相关。
6个月前属于C3型的儿童过敏性疾病风险增加,5岁时身高Z评分低于-1标准差。12个月前过渡到C4型与2岁时身高Z评分低于-1标准差相关,但C4型与2岁时哮喘诊断呈负相关。12个月时,C1型与胃肠道感染有关。
3
微生物组发展轨迹
婴儿肠道微生物组发展高度可预测,遵循五种轨迹之一。
T1轨迹(最常见,47%)
特征:前6个月C1成员稳定,9个月过渡到C3,12-18个月过渡到C4;
菌群:这些婴儿的双歧杆菌的初始相对丰度很高,其相对丰度逐渐下降,最初被韦荣氏球菌属取代,然后被粪杆菌和毛螺菌科的成员所取代;
相关因素:未接触抗生素的阴道分娩、母乳喂养、有兄弟姐妹;
健康关联:与较好的健康结果相关;
微生物稳定性:最稳定的微生物群组成。
T2轨迹(11%)
特征:最初位于C1,但在转移到C3之前转移到C2;
菌群:双歧杆菌迅速减少,梭菌和克雷伯菌短暂增加;
微生物稳定性:9个月大时表现出最大的波动性
T3轨迹(9%)
特征:开始于C1,但在前6个月在C1和C2之间反复振荡;
微生物稳定性:3-12周时表现出最高的波动性
T4轨迹(18%)
特征:T3的反向模式,从C2开始的婴儿在前6个月在C1和C2之间波动,在6-9个月时双歧杆菌达到峰值。
T5轨迹(14%)
特征:前6个月持续处于C2状态;
菌群:梭菌和克雷伯氏菌相对丰度较高。
微生物群发展轨迹、决定因素和与健康结果的关联
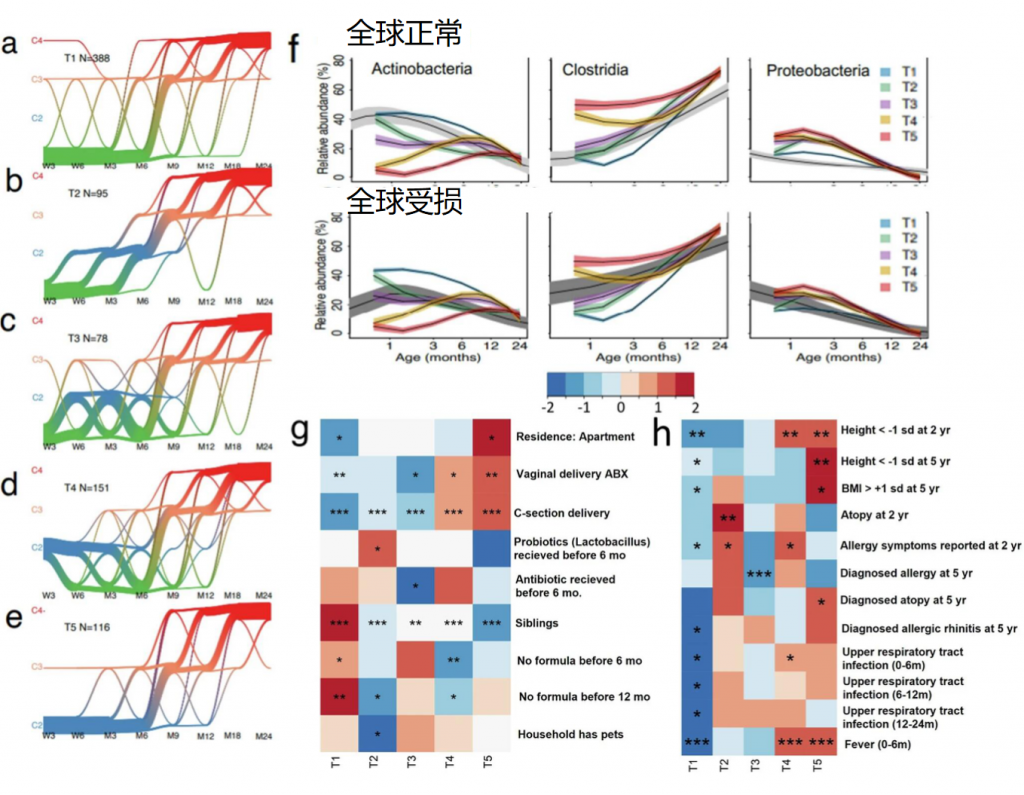
doi: 10.1038/s41467-024-52561-6.
影响微生物发展轨迹的因素:
轨迹T1-T3与阴道分娩相关,T4和T5则与剖腹产及阴道分娩预防性抗生素使用相关。T1独特地与有兄弟姐妹、住单户住宅和前12个月纯母乳喂养相关。
T2婴儿向C2型过渡可能由配方奶喂养或无兄弟姐妹促成,这些婴儿更常接受益生菌。T3中C1和C2间波动主要与缺乏兄弟姐妹及较低社会经济地位相关。T4的微生物群自发校正可能由母乳喂养或其他高社会经济地位相关因素驱动。
不同微生物轨迹的健康结果:
T1与多项健康指标呈负相关:前2年过敏症状和上呼吸道感染风险降低,0-6个月发烧报告减少,5岁时过敏性鼻炎诊断减少,5岁时ISO-BMI Z评分不超过1标准差,2岁和5岁时身高Z评分不低于-1标准差。
T2与2岁时特应性风险和前2年父母报告的过敏症状增加相关。
T3与2岁时父母报告的过敏症状减少有关。
T4和T5均与2岁时身高Z评分低于-1标准差,以及0-6个月间上呼吸道感染和发热相关。由于T4的微生物群校正,这些婴儿5岁时未表现出T5所见的生长改变或过敏性鼻炎风险增加。T5还与5岁时特应性风险增加相关。
总体而言,微生物组轨迹与健康结果的相关性强于单个时间点的微生物组类型,表明纵向发育分析提供更多信息。
与年龄相关的细菌属:
数据分析中,我们识别出一组随年龄变化的细菌属。这些分类群在各发育轨迹中展现相似模式,主要分为早期(放线菌门、拟杆菌属、肠杆菌门、Negativicutes、Bacilli)和晚期(主要是梭状芽胞杆菌)两组。
然而,某些关键类群,如双歧杆菌属和拟杆菌属,在不同的轨迹中表现出不同的时间模式。
4
微生物组健康指数
微生物组健康指数(MWI)是研究者基于大型婴儿队列(近1000名婴儿)的健康发展轨迹开发的一种评估指标,用于预测婴儿整体健康状况。该指数代表了基于微生物群落组成估计婴儿属于健康参考组的概率。
★ 关键有益指示菌:
最强的总体积极关联见于双歧杆菌(Bifidobacterium)和拟杆菌(Bacteroides),这两类菌群一致地指示健康参考微生物组。
随年龄增加积极关联增强的菌群:Eisenbergiella, Oscillibacter, Parabacteroides, Anaerostipes, Streptococcus。
★ 负面指示菌:
随年龄增加负面关联增强的菌群:Lachnospira, Faecalicatena, Lacrimispora, Klebsiella, Sutterella。
★ 年龄依赖性:
大多数指示菌显示年龄依赖性关联;
某些菌群展示暂时性负面关联(Roseburia, Faecalibacterium);
某些菌群展示暂时性正面关联(Citrobacter, Blautia, Gemmiger, Hungatella)。
微生物群健康指数
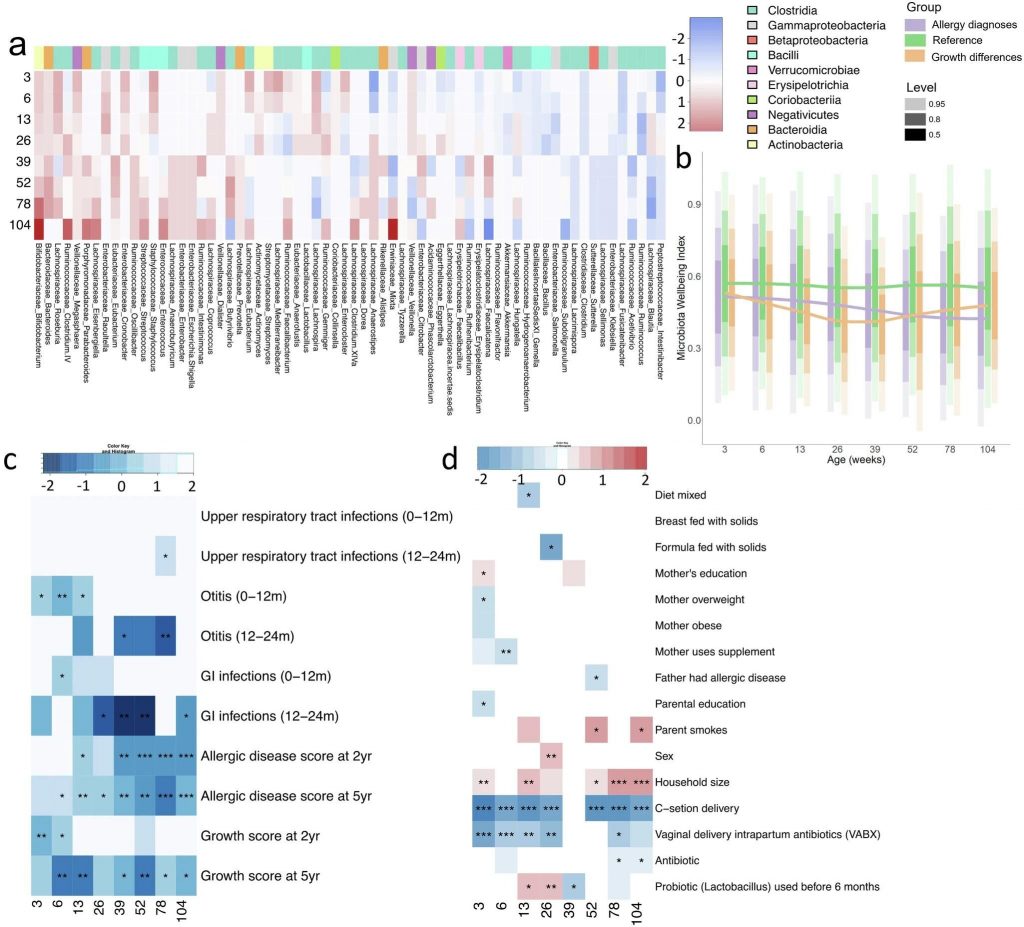
doi: 10.1038/s41467-024-52561-6.
★ 健康预测能力:
MWI在患有过敏性疾病或生长差异的婴儿中显著降低;
在详细分析中,MWI与多种健康结果相关,包括从过敏性疾病到2岁和5岁时的生长指标;
可预测感染发生率。
★ MWI的优势:
整体评估:超越单个菌群评估,考虑整个微生物群落结构对宿主健康的影响;
发展视角:将肠道菌群演替视为婴儿生理发育的一部分,与免疫系统成熟有关;
预测能力:可预测前5年的总体健康状况,有助于早期识别健康风险;
实用性:相比成熟度指数,能更好地区分不同的发育轨迹和捕捉各种健康关联。
通过对近1000名婴儿的前瞻性纵向队列研究,首次系统阐明了人类婴儿肠道微生物组发展的规律性和可预测性。确定了四种主要的微生物群落类型(C1-C4),这些类型随着婴儿年龄发展而呈现规律性变化。并且不同微生物类型与健康结果相关。
婴儿肠道微生物组发展遵循五种主要轨迹的预设路径,非随机发生,并受出生方式、喂养类型及抗生素使用等因素显著影响。研究确立了双歧杆菌和拟杆菌作为关键早期定植微生物,它们在引导整个微生物组健康发展中起着决定性作用。
基于这些发现,建立的微生物组健康指数(MWI)不仅能够评估婴儿当前肠道微生物组的健康状态,还能预测未来5年的整体健康结果,包括过敏性疾病风险、生长发育状况和感染易感性。这一指数的建立将微生物组分析从描述性研究提升至具有临床预测价值的工具,为精准医疗提供了新的维度。
需要注意的是,该研究仅使用了来自芬兰地区的婴幼儿样本,其开发的微生物健康指数(MWI)目前仅适用于北欧地区的婴幼儿样本,更大范围的应用还需要纳入更多地区和年龄的样本。
主要参考文献:
Hickman B, Salonen A, Ponsero AJ, Jokela R, Kolho KL, de Vos WM, Korpela K. Gut microbiota wellbeing index predicts overall health in a cohort of 1000 infants. Nat Commun. 2024 Sep 27;15(1):8323.
谷禾健康
今年,国产AI大模型DeepSeek,凭借其强大的技术实力、低成本和开源策略,长居热搜榜,很想知道这位顶流AI对于肠道菌群行业的了解程度,于是就和它聊了聊。

编辑
当我问deepseek…
AI时代,肠道微生物行业相关应用与发展将会如何?
AI技术的快速发展为肠道菌群行业带来多维度革新,从药物研发到健康管理均产生显著利好,肠道微生物行业将迎来技术革新与产业升级的黄金期,其核心应用与发展趋势如下:
微生物组大数据挖掘
AI通过分析海量肠道微生物组数据(宏基因组、代谢组等),快速筛选潜在药物靶点。肠道微生物群落种类繁多、结构复杂,其产生海量数据。AI强大的数据处理能力可挖掘微生物间的相互关系,为新药研发指明方向,为攻克诸多疾病带来希望。
缩短研发周期
传统药物研发需10年以上,AI可将候选菌株筛选时间缩短70%。通过“IT(数据分析)+BT(实验验证)”模式,推进多款微生态药物进入临床,覆盖神经系统、肿瘤和免疫三大领域。
例如,在传统的筛选方法中,可能需要逐一测试大量的菌株,而AI可以通过算法和模型,快速排除那些不具备潜力的菌株,直接聚焦于最有希望的候选菌株,从而节省了大量的时间和精力。这不仅加速了药物研发的进程,还有望降低研发成本,为患者带来更多的治疗选择。
创新药物形态
包括粪菌移植(FMT)、配方菌(如复合益生菌)、代谢产物(如抗癌肽)、基因工程菌等。
FMT:分析不同供体和患者的肠道微生物组成差异,预测FMT的效果和可能出现的不良反应,为个性化治疗方案的制定提供依据,提高治疗的成功率和安全性。
配方菌:例如复合益生菌,是经过精心挑选和组合的多种有益菌群。深入了解不同菌种之间的相互作用和协同效应。通过分析大量的微生物组数据,确定最佳的菌种组合和配比,使其在调节肠道菌群、增强免疫力、改善肠道功能等方面发挥更显著的作用。还能根据不同人群的肠道特点和健康需求,定制个性化的复合益生菌配方。
代谢产物(如抗癌肽):挖掘出肠道菌群中具有抗癌活性的短肽分子,为肿瘤治疗提供新方向。
基因工程菌:通过分析微生物的基因组数据和代谢网络,确定合适的基因编辑靶点和调控策略,使基因工程菌更高效地生产目标产物,或者具备更强的环境适应性和生存能力。
工程化菌群靶向递送抗癌药物至肠道特定区域。还可以为工程化菌群赋予智能反馈机制,使其能够实时感知肠道微环境的变化,并根据需要调节药物的释放量。
菌群分型与疾病预测
AI模型通过关联肠道菌群特征与疾病标志物(如SCFAs、TMAO),可预测心血管疾病、肠癌等风险。
AI模型在疾病预测中准确性的提高是一个多维度且持续探索的重要课题,涉及到数据、算法、模型优化等多个关键方面。
首先,数据质量和数量是基础。高质量的数据是确保AI模型准确性的基石。
一方面,要注重数据的收集过程,确保数据的完整性、一致性和准确性。在收集与疾病相关的肠道菌群数据以及疾病标志物数据时,需要严格遵循标准化的采集、处理和存储流程,避免数据偏差和误差。
同时要尽可能收集大规模的样本,因为丰富的数据可以让AI模型学习到更多的模式和规律。通过整合多个来源的数据,如不同地区、不同年龄段、不同疾病状态人群的数据,可以增加数据多样性,提高模型的泛化能力。

其次,算法的选择和优化至关重要。对于疾病预测,需要选择合适的机器学习和深度学习算法,并根据具体情况进行调整和优化。
例如,深度学习中的卷积神经网络(CNN)在处理图像数据方面具有优势,而循环神经网络(RNN)及其变体(如长短期记忆网络LSTM)则更适合处理序列数据。
再者,特征工程也是提高AI模型准确性的关键环节。在疾病预测中,需要对肠道菌群数据和疾病标志物数据进行深入分析,挖掘出与疾病相关的关键特征。
特征工程是指从原始数据中提取、选择和转换有意义的特征,以提高模型的性能。例如,通过统计分析、相关性分析等方法筛选出与疾病发生发展密切相关的菌群特征和代谢产物指标。还可以采用特征降维技术,如主成分分析(PCA)、线性判别分析(LDA)等,将高维数据转化为低维数据,减少数据复杂性,提高模型的训练效率和准确性。
此外,模型的融合和集成也是一种有效的提高准确性的方法。不同的AI模型在不同的数据集和任务上可能具有各自的优势和局限性。通过将多个不同的模型进行融合和集成,可以综合各个模型的优点,提高整体的预测性能。

动态干预方案
基于AI的宏基因组分析,可为患者提供定制化膳食、益生菌及粪菌移植方案。AI技术则如同一个智能的“导航员”,能够从这些复杂的数据中挖掘出有价值的信息,为患者量身定制个性化的干预方案。
比方说,以高血压患者为例,高血压作为一种常见的慢性疾病,其发病机制复杂,涉及遗传、环境、生活方式等多种因素。针对高血压患者,AI可识别普雷沃菌属丰度异常并推荐靶向菌株。这些靶向菌株可以通过益生菌的形式补充到患者体内,调节肠道菌群的平衡,进而影响血压水平。
除了益生菌方案,定制化膳食也是动态干预方案的重要组成部分。AI可以根据患者的肠道菌群特征和疾病状态,为患者设计个性化的膳食方案。
动态干预方案的实施并非一蹴而就,而是一个持续监测和调整的过程。在治疗过程中,需要定期对患者的肠道菌群健康检测,以评估干预效果,并根据分析结果及时调整干预方案。
合成生物学应用
AI辅助设计基因工程菌(如产丁酸菌株),直接调控宿主代谢功能。
传统的基因工程菌设计主要依赖于科研人员的经验和试错,过程繁琐且效率较低。而AI拥有强大的数据分析和模式识别能力,能够处理海量的生物学数据,包括基因序列、蛋白质结构、代谢通路等信息。通过对这些数据的深入学习,AI可以预测基因的功能、设计优化的基因表达系统,并为基因工程菌的设计提供精准的指导。
产丁酸菌株可调控宿主代谢功能,丁酸作为信号分子能调节宿主代谢,菌株间相互作用也间接影响宿主代谢。AI通过构建模型设计最优菌株和策略,还能优化生产工艺。不过,其面临生物学复杂、数据质量等挑战,但前景广阔。
上游检测技术升级
检测手段日益多样化,16S rRNA测序能快速评估菌群组成多样性,宏基因组测序可揭示更全面信息。技术上不断优化,如多重PCR扩增提高检测覆盖率和分辨率,AI辅助数据分析提升结果准确性。
肠道菌群检测结果将更多地被纳入临床诊断体系。AI可以分析大量的临床病例和肠道菌群数据,找出肠道菌群变化与疾病之间的关联模式,为医生提供诊断参考。
例如,在一些疑难病症(如自闭症、帕金森病等)的早期诊断中,肠道菌群的异常特征可能成为重要的辅助诊断指标。
结直肠癌(CRC):识别肠道菌群中具核梭杆菌(Fusobacterium nucleatum)等促癌菌的异常增殖,结合粪便隐血检测,提升早期筛查灵敏度。
肠道细菌在结直肠癌发生和进展中的影响
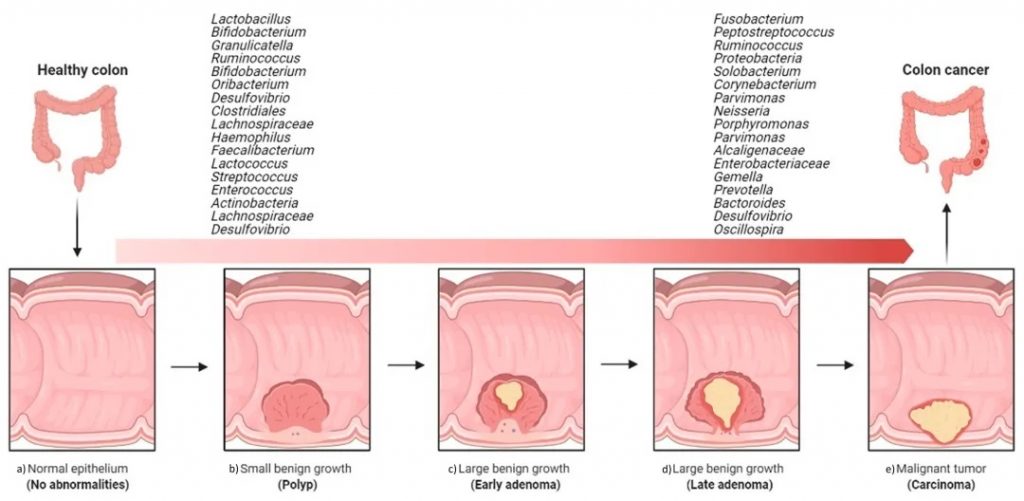
Torres-Maravilla, E. et al.,Microorganisms 2021
炎症性肠病(IBD):
促炎菌增殖:肠杆菌科(Enterobacteriaceae)丰度显著升高,其代谢产物(如脂多糖)可激活TLR4通路,加剧肠道炎症反应;
抗炎菌缺失:具有抗炎功能的共生菌——普氏菌(Faecalibacterium prausnitzii)和产丁酸盐的罗斯氏菌(Roseburia)丰度普遍降低或缺失,导致短链脂肪酸合成不足,肠道屏障修复能力下降。
早期筛查:在血清标志物(如CRP)升高但未出现典型症状的人群中,检测到上述菌群失衡模式可提示早期IBD风险,推动结肠镜进一步确诊;
疗效监测:治疗过程中动态监测罗斯氏菌的恢复水平,可评估免疫抑制剂(如抗TNF-α药物)对黏膜修复的促进作用。
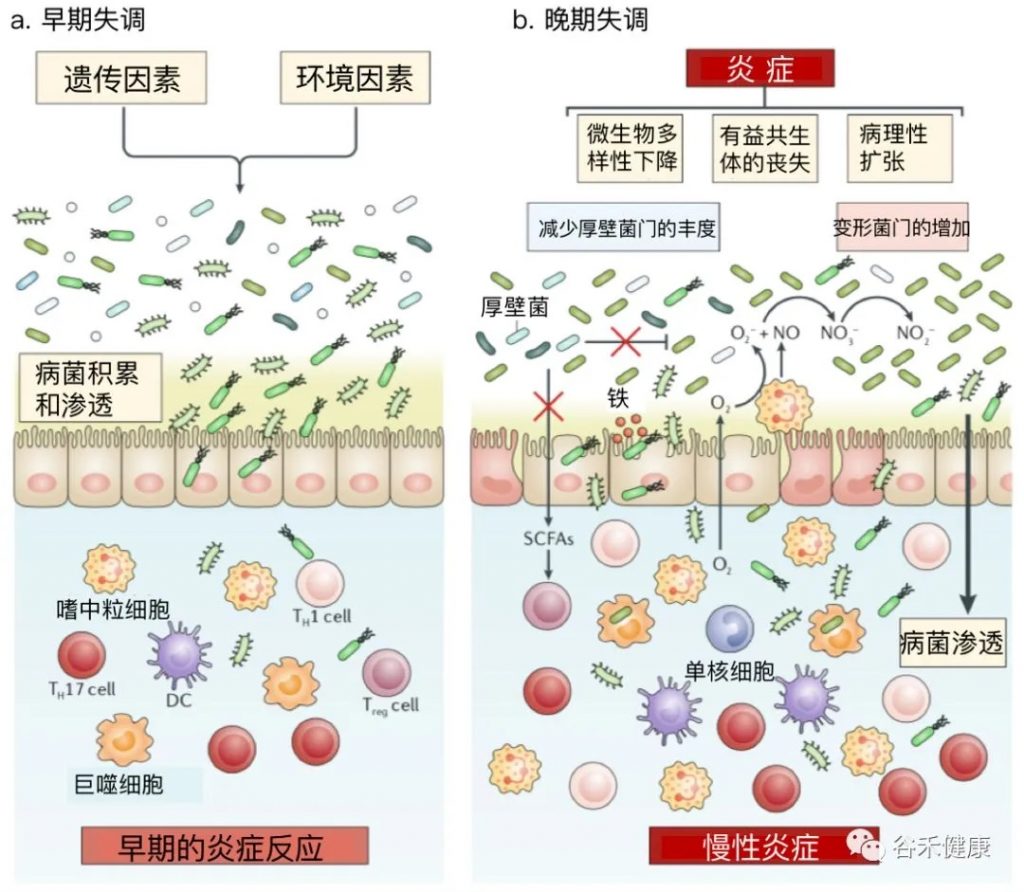
糖尿病:结合肠道菌群中产丁酸盐菌的减少与宿主血糖代谢数据,预测胰岛素抵抗风险。
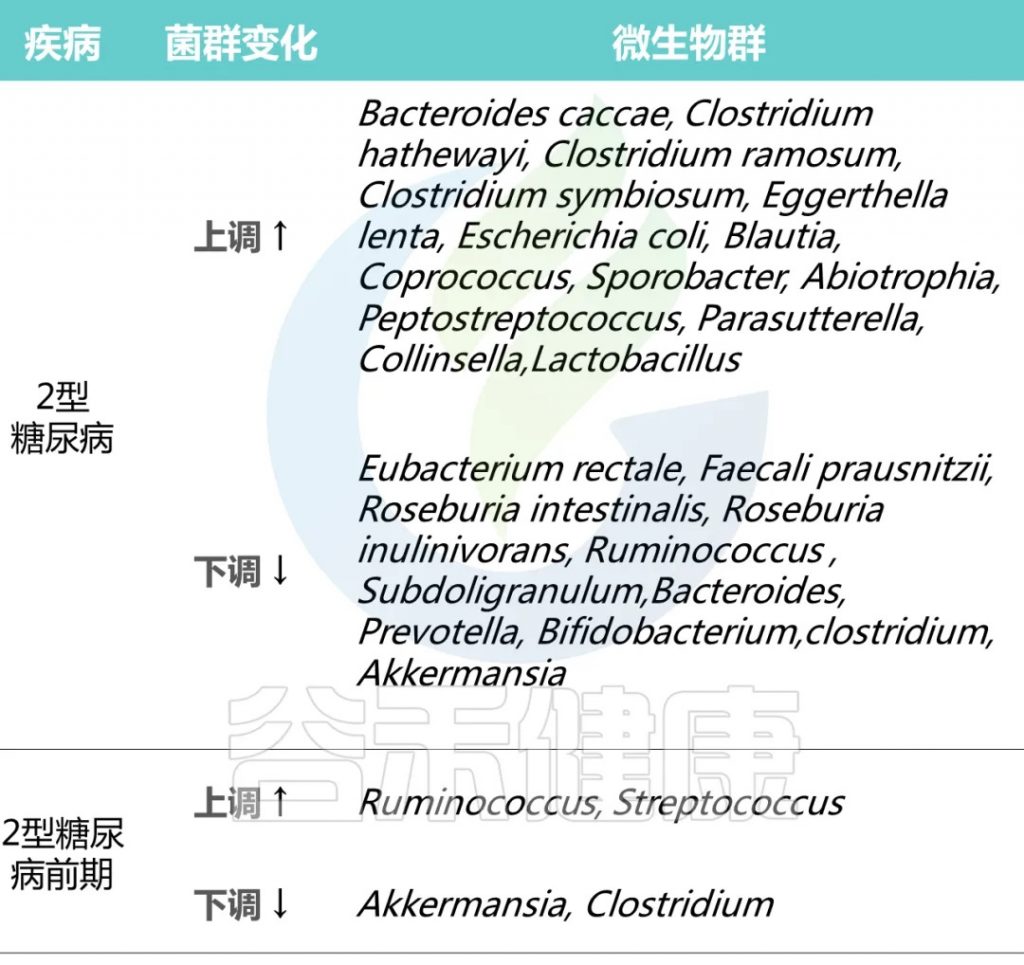
Cunningham A L et al., Gut Pathog, 2021
菌群分型指导治疗:通过16s测序、宏基因组测序和代谢组分析,建立患者肠道菌群特征图谱。例如,补充AKK菌(Akkermansia muciniphila)仅在基线菌群低丰度人群中有效,需结合个体差异制定阈值。
通过连续监测肠道菌群变化(如抗生素使用后菌群恢复情况),辅助医生评估治疗效果。
例如:癌症化疗患者的化疗药物可能破坏肠道菌群平衡,导致免疫力下降。AI实时分析菌群数据,预警感染风险并推荐相关干预方案。
中游标准化建设
AI整合全球微生物组数据,推动菌株库建设、临床试验设计标准化。
硬件上,便携设备基于微流控技术实现高效处理,新型传感器提高敏感度。
软件上,智能数据分析系统实时处理数据并提供个性化建议,机器学习模型助力精准识别。
参与标准制定,获取ISO等认证,确保产品质量和安全。
下游健康管理服务
建立完善的用户教育体系,通过在线课程、健康顾问平台等帮助消费者理解检测结果。通过健康管理服务,将检测结果转化为具体的健康建议, 有利于公众对肠道菌群产品的应用。
肠道菌群健康管理将与营养学、微生物学、医学、心理学等多学科融合。AI作为协调者,根据肠道菌群检测结果,组织多学科专家团队为用户提供综合的健康管理服务。
例如,对于因肠道菌群失调导致情绪问题的患者,营养师调整饮食,心理医生进行心理疏导,微生物学家给出改善肠道菌群的具体措施。
针对高风险人群定制膳食或益生菌组合。
如蒙牛开发的青钱柳提取物组合通过抑制菌源DPP4,在动物实验中显著降低血糖 ,未来或成为糖尿病预防新手段。
结合实时监测技术(如便携式纳米孔测序),AI动态优化益生菌、膳食纤维摄入量或粪菌移植方案。
精准肠道菌群移植门诊通过线上线下结合模式服务患者。
跨界融合
肠道菌群通过代谢物(如5-羟色胺、GABA)影响大脑功能,可开发针对抑郁症、焦虑症的菌群干预产品。
益生菌菌株(如长双歧杆菌NCC3001)在临床试验中显示缓解焦虑效果。未来可能推出“精神健康益生菌+认知行为疗法”联合方案。
潜力:肠道菌群失衡与痤疮、湿疹等皮肤病相关,可探索口服益生菌或局部菌群移植(如皮肤微生物组喷雾)改善皮肤状态。
技术结合:AI分析肠道与皮肤菌群关联,定制内外协同治疗方案。
市场空白:针对宠物(如猫狗)的肠道菌群检测及定制化食品/补充剂,解决腹泻、肥胖等问题。
延伸场景:动物园或濒危动物保护中的菌群干预,提升圈养动物生存率。

特定人群管理
➦ 母婴菌群管理
剖宫产婴儿的母体菌群移植(阴道菌群纱布擦拭),降低过敏和免疫疾病风险。
孕期肠道菌群监测,预防早产或妊娠糖尿病。
产品形态:母婴菌包、菌群健康评估套餐。
智能监测手环:实时监测婴儿肠道气体(如氢气),反馈菌群定植效果。
➦ 肥胖人群管理
菌群特征:厚壁菌门/拟杆菌门比值(F/B比)升高,阿克曼菌(Akkermansia)丰度降低。
干预手段:
补充阿克曼菌改善肠道屏障功能,减少脂质吸收。菌群导向饮食(Microbiome-Directed Foods)抑制促肥胖菌(如阴沟肠杆菌)。
案例:比利时鲁汶大学开发的阿克曼菌口服制剂,可使肥胖者体重平均下降2.3kg(12周试验)。
产品形态设想:
控血糖菌群面包:添加抗性淀粉(促进罗斯氏菌增殖)+ 基因工程酵母菌(分泌GLP-1类似物)。
菌群血糖联动仪:连续血糖仪数据同步至菌群检测APP,动态调整。
肥胖菌群管理手环:根据肠道菌群数据(如厚壁菌/拟杆菌比)释放电信号,刺激迷走神经产生饱腹感。
菌群溶脂贴片:透皮递送Akkermansia muciniphila冻干粉,激活棕色脂肪产热。
➦ 老年人群管理
衰老相关菌群特征:多样性降低,促炎菌(如变形菌门)增加。
干预手段:
地中海饮食+益生元(菊粉)促进良性菌群定植。
个性化益生菌(如长双歧杆菌BB536)改善肌肉流失和认知衰退。
养老院菌群健康管理系统:
群体化菌群管理,降低集体感染风险。
中央监测平台:批量分析老人菌群数据,预警群体性致病菌传播(如艰难梭菌)。
自动配餐机器人:根据每位老人菌群报告,调配个性化餐食(如低FODMAP饮食+益生元添加)。
老年群体的肠道菌群产品需兼顾 “功能刚性”(如疾病预防)与 “体验友好”(如无创检测、语音交互)。通过菌群干预推迟慢性病发生,延长寿命,提高生活质量。
未来趋势可能是 “菌群-衰老-疾病”三联检测体系 与 “居家-社区-机构”三级服务网络的深度融合。
技术创新方向
➦ 菌群冷冻保存与“菌群银行”
概念:年轻时储存健康肠道菌群,年老或疾病时进行自体移植(类似脐带血储存)。
挑战:菌群复苏后的活性维持技术,需低温生物学突破。
➦ 其他形式检测
通过呼吸或血液标志物间接反映肠道菌群状态(如挥发性有机化合物VOCs分析)。
➦ 地域特异性菌群数据库
针对不同地区饮食和文化(如亚洲高纤维饮食 vs. 西方高脂饮食),建立菌群-健康关联模型,开发本地化产品。
比如,日本基于本土菌株开发的“FK-23益生菌”免疫调节产品。通过调节肠道微生态,改善消化健康,增强机体的免疫功能。
➦ 菌群农业与可持续食品
通过调控农作物或牲畜肠道菌群,减少抗生素使用,提升产量(如益生菌饲料添加剂)。
开发菌群发酵技术,生产高蛋白昆虫食品(如蟋蟀蛋白粉),减少碳排放。
数据壁垒
—挑战
个体菌群差异大,菌群构成受饮食、生活方式、年龄、地理位置、基因、种族、性别、药物等多元因素影响,单一数据库难以覆盖人群多样性,解读准确性受限。样本量碎片化,难以挖掘深层规律。
—破局关键:需建立更大规模数据库★
建立大规模数据库不仅是肠道菌群行业的“基础设施”,更是检测解读从“经验驱动”迈向“科学驱动”的核心引擎。其价值可归结为:
◑ 更准:通过人群细分与机制解析,降低个体差异导致的误判。
例如,高纤维饮食者与高脂饮食者的“健康菌群基线”截然不同,若缺乏细分人群数据,可能误判干预方向;东亚人群因乳糖酶基因缺失比例较高,其乳糖代谢相关菌的丰度与功能特征与欧洲人群不同,若仅依赖通用参考标准,可能误判菌群状态。
◑ 更深:揭示菌群与疾病的因果链,推动干预策略从“对症”转向“对因”;海量数据能增强统计效力,挖掘低频但强关联的菌群-疾病机制,推动科研向临床转化。
例如,在药物研发过程中,药物的疗效和安全性可能受到个体微生物群落的影响,某些药物的代谢可能依赖于肠道菌群中的特定酶。了解特定人群的正常微生物参考,可以帮助研发人员预测药物在不同人群中的代谢情况和疗效差异,从而优化药物设计和开发更具针对性的药物。
◑ 更活:动态模型随数据增长持续进化,使解读建议与时俱进。长期追踪数据可构建“菌群变化预测模型”,预警糖尿病、结直肠癌等慢性病风险,真正释放微生物数据在疾病防控、健康管理和药物研发中的潜力。
因果关系的模糊性
—挑战
菌群变化是疾病的“因”还是“果”难以确定(例如,抑郁症患者菌群失调是诱因还是结果?)。
—应对方案
纵向队列研究:开展长期追踪(如10年以上的肠道菌群动态监测),结合干预实验验证因果关系。
动物模型验证:利用无菌小鼠移植特定菌群,观察其对宿主生理的影响(如肥胖、免疫反应)。
数据解读的局限性
—挑战
用户对肠道菌群专业检测报告的理解有进步空间(如菌群丰度、α多样性指数)。
部分消费者可能对肠道菌群检测的认知停留在“保健品”层面,对科学价值的信任度不足。
—应对方案
开发可视化工具(如菌群“健康评分”仪表盘),提供通俗化建议。
通过科普内容(短视频、互动问答)提升公众对菌群健康的认知。
通过学术会议、继续教育课程让更多临床医生了解菌群检测的临床价值。
临床验证不足
—挑战
检测产品缺乏大规模临床验证,医学界对菌群诊断的接受仍然有限。
—应对方案
与医疗机构合作:推动菌群检测纳入临床试验(如辅助癌症免疫治疗疗效预测)。
商业模式单一
—挑战
盈利模式缺乏可持续性。
—应对方案
检测+干预产品(如个性化益生菌定制)。
订阅制服务:如每月菌群监测+营养师咨询;
或者比如每季度检测肠道菌群,生成动态健康报告,推荐阶段性干预措施(如季节性饮食调整预防过敏等)。结合可穿戴设备数据(运动、睡眠)提供综合建议。
与保险机构合作,将菌群健康管理纳入健康险增值服务。
伦理争议
—挑战
菌群移植(FMT)可能引发未知风险(如病原体传播、长期生态影响)。
—应对方案
严格供体筛查:建立菌群库的标准化筛选流程(如供体健康史、病原体检测等)。
知情同意强化:向用户明确告知菌群干预的潜在风险和不确定性。
未来趋势(2025-2030年)
多组学融合:AI整合代谢组、免疫组数据,解析菌群-宿主互作机制 。
例如,卷积神经网络(CNN)将菌群数据转化为图像,精准预测2型糖尿病患者的丁酸弧菌干预靶点。
全球市场扩张:中国微生态药物市场规模预计2030年达500亿元,年复合增长率超30%。
政策支持:国家“精准医学”专项将肠道微生物组列为重点,推动产学研合作。
AI与肠道微生物组的深度融合将重塑医疗健康产业,从药物研发、疾病防治到健康管理均迎来革命性突破。未来十年,具备“AI+”能力的企业将引领行业变革,推动个性化医疗的发展,而构建数据库、临床验证等将是行业持续增长的关键支撑。
总的来说,人们将逐渐理解“人类是超级生物体”(宿主+微生物)的概念,改变“杀菌至上”的传统健康观念。
精准菌群干预将推动医疗模式向预防化、个性化、数字化转型:
疾病管理:从“发病后治疗”转向“风险预测-早期干预”;
临床落地:推动菌群检测进入诊疗指南(如IBD、IBS的辅助诊断)。
治疗方案:从“通用型”升级为“动态定制型”,医疗资源从“中心化”向“分布式+远程化”重构;
最终,肠道菌群行业的目标是构建一个全面的“人体生态系统管理”体系,这一理念超越了单纯的疾病治疗,而是着眼于维护整个生态系统的平衡。未来十年,随着技术成熟和政策完善,肠道微生物组有望成为继基因组之后,精准医疗的第二大核心支柱。
在AI技术与肠道微生物研究的深度融合下,精准健康管理已从概念走向现实。通过此前的分析可以看到,肠道菌群检测正逐步渗透至疾病预防、临床诊断、母婴健康、老年抗衰等多元场景,而数据驱动的个性化干预将成为行业核心。
为赋能临床医疗、健康管理机构、检测机构等合作伙伴,谷禾推出 AI肠道菌群报告解读与咨询助手,就是下面这个小海豚:

AI报告解读助手将有助于合作方和客户更好的理解报告和应用肠道菌群检测。合作方可提升解读效率降低成本,定制精准营销策略,快速扩展菌群管理服务生态,构建差异化竞争力,实现用户健康改善与商业增长的双重目标。

饮用水(DW)中含有多种微生物物种和化学特性。水构成了我们日常饮食的最大部分,既可单独饮用,也用于食物制备。
饮用水是我们主要的液体来源,对维持体内平衡至关重要,还可以提供必需矿物质。
有限的证据表明,饮用水在塑造肠道微生物群方面发挥作用,这意味着它可能影响人类健康。尽管饮用水对饮食有重要贡献,但在研究饮食对肠道微生物群的影响时,饮用水常被忽视。
本文探讨饮用水与肠道微生物群之间联系的理解——这是人类微生物组科学中研究不足的领域。
对饮用水与肠道微生物群关系的深入理解将有助于理解肠道微生物群结构及其与人类健康的关系。这可能导致针对失调状态的具体建议,优化饮用水处理过程,并为研究人员制定具有定制益生菌或化学特征的饮用水铺平道路。
干预措施可能包含或排除特定化学物质甚至益生菌,到优化例如氯离子含量,调节pH值,来促进健康的肠道微生物群。
人们普遍认为人类肠道微生物群对人类健康具有重要影响。饮食因素在决定肠道微生物组成中的作用已明确,各个因素都会影响原核生物的相对丰度和绝对丰度,以及它们的生长动态。
在对肠道微生物群的影响方面,一个被人们忽视的关键饮食因素是饮用水 (DW)。饮用水主要来自地下水和地表水,每种水源都有不同的物理和化学属性及相关微生物群。根据水质,源水通常会经过各种处理和消毒过程,以去除有害化学物质和微生物,生产出可饮用水。许多源水中的微生物能够耐受处理过程,处理后的饮用水中存在多样化的微生物群,细菌浓度约为106–108个细胞/升。
不同源水的化学和微生物学特性因源环境的生物地球化学而显著不同,这些因素与所应用的处理过程相结合,影响了最终的饮用水微生物群。
饮用水是我们饮食的核心组成部分。鉴于饮食模式和因素在塑造肠道微生物群结构中起关键作用。饮用水可以通过直接(即通过驻留的饮用水微生物群)或间接(即由于其化学成分)方式与肠道微生物群相互作用。然而,在研究饮食因素对肠道微生物群影响的队列研究中,饮用水很少被考虑。在少数考虑的几项研究中,发现其具有显著影响。
研究发现,饮用水的化学、物理和生物特性在塑造肠道微生物群结构和功能中起着关键作用,并对人类健康产生连锁效应。
在此,我们总结了从各个领域和不同设计的研究中获得的关于饮用水对肠道微生物群直接和间接影响的有限知识。
个体之间以及饮用水之间的高度变异性将使未来的研究工作复杂化,但这些挑战已经在肠道微生物群研究领域得到解决。
肠道对水的吸收发生在小肠和大肠中。渗透梯度驱动水的吸收,这通常与离子和营养物质的运输有关。在小肠中,葡萄糖和半乳糖转运蛋白 SGLT1 以及 Na+/H +反向转运蛋白负责从肠腔中运输大部分水。
水分吸收和体内平衡是大肠的主要功能之一,而大肠也是肠道微生物的主要聚集地。水分与离子(主要是钠)一起穿过肠上皮,钠离子的运输产生渗透梯度,推动水分吸收。
早在1998年,有一项研究就证实大肠中存在的水量通过改变肠道中的 pH 值和运输时间来影响肠道微生物组的组成。
饮用水中其他成分的吸收通过多种机制并在肠道的特定位置发生。复杂的有机化学物质可能被肠道微生物群发酵并转化为脂肪酸,或者在没有吸收或转化的情况下被排除。肠道中微生物细胞的最高丰度是在大肠中,近端大肠被认为是最高微生物增殖的地方,因为发酵底物的可用性很高。
我们预计饮用水中的化学物质和生物与肠道的相互作用方式与其他摄入的化学物质和生物类似。由于益生元和益生菌在这方面的研究相对较多,我们使用来自该领域的数据来描述潜在的相互作用。
然而值得注意的是,饮用水中的化学物质和生物可能并非都具有有益影响,区分对宿主产生有益和有害影响的相互作用是制定优化饮用水成分以支持公共健康的策略的关键。
A) 饮用水微生物群和肠道微生物群之间的潜在相互作用
B) 识别饮用水和肠道微生物群之间联系的建议方法
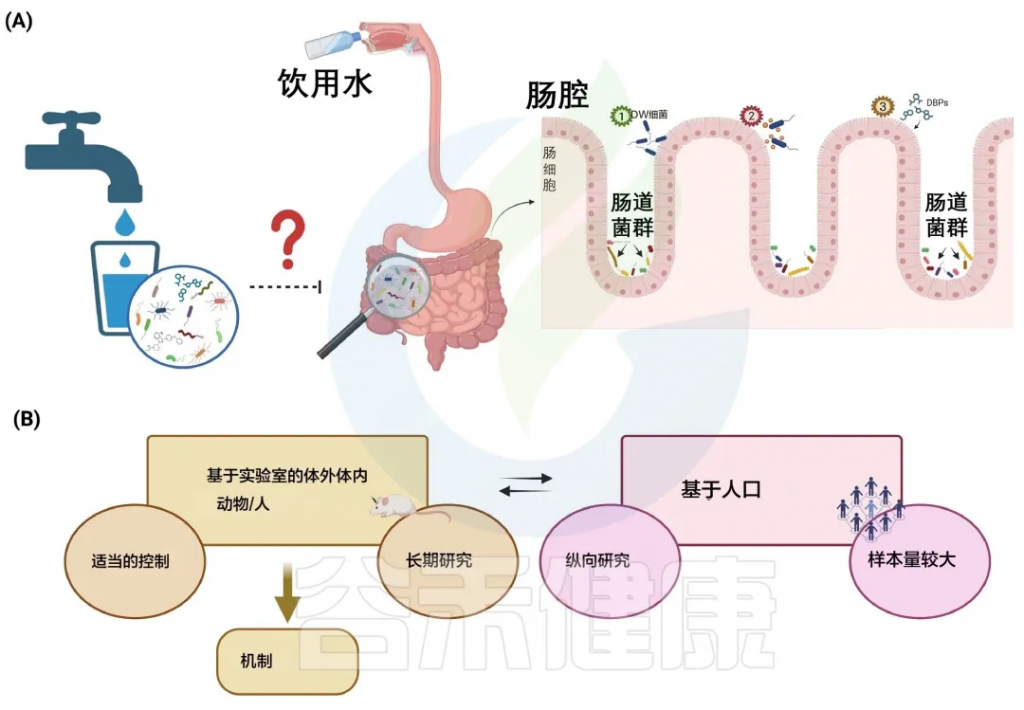
Moghaddam HS et al., Water Res. 2024
饮用水对肠道微生物群的影响途径:
饮食是塑造肠道微生物群落的主要驱动因素之一。成人每日建议饮水量约为2.0-3.7升。
两项研究使用不同的方法检查了肠道微生物群和饮用水微生物群之间的重叠。使用 16S rRNA 基因扩增子数据鉴定出 35 个属,它们属于 5 个门(假单胞菌门、放线菌门、芽孢杆菌门、拟杆菌门和蓝藻门),存在于经过处理的饮用水和肠道微生物群中。
来自 131 个饮用水样本宏基因组的组装重叠群,并将它们与来自同一国家的 196 个粪便样本的宏基因组进行了比较。通过关注饮用水中大量存在的属,他们确定了与肠道微生物群共享的 6 个关键属:
肠道菌群和肠道菌群重叠程度最大的是假单胞菌门(Pseudomonadota),两项研究都在肠道和饮用水群落中发现了鞘氨醇单胞菌属(Sphingomonas)、假单胞菌属(Pseudomonas)和伯克霍尔德菌属(Burkholderia)。
然而,当应用类似的宏基因组学方法来评估一个人的粪便菌群和饮用水菌群之间的直接联系时,他们只发现了一种常见的生物,即Curvibacter(弯钩菌),这表明,如果饮用水微生物能够在人体肠道中定植,那么存在一些重要的决定因素,这些因素是生物体固有的,也是肠道中生物和非生物条件的共同决定因素。
显然,饮用水和肠道之间存在共同的属并不意味着饮用水是这些微生物的来源。假单胞菌属、鞘氨醇单胞菌属等属广泛存在于各种自由生活和宿主相关环境中。
饮用水质量与肠道微生物群的长期影响
在考虑饮用水对肠道微生物群的长期影响时,也值得考虑劣质饮用水的影响,因为全球超过27%的人口无法获得安全管理的水源。

为了研究水资源不安全和肠道病原体暴露如何影响肠道微生物群的发展,Piperata等人2020年的研究分析了尼加拉瓜儿童的家庭饮用水和粪便样本。在水和粪便样本中观察到了高浓度的沙门氏菌(Salmonella)、弯曲杆菌属(Campylobacter)和大肠菌群(coliforms)。
沙门氏菌(Salmonella)是世界范围内肠道感染(食物中毒)的最常见原因之一。尤其在卫生条件差的地方。沙门氏菌是能动的生物,它们利用鞭毛将自身导向肠细胞,有时候也依赖入侵基因来穿透宿主肠细胞。入侵基因在宿主细胞中介导广泛的动作重排,导致细胞膜变形并使生物体能够入侵。
研究根据饮用水中的大肠菌群含量将家庭分为高含量和低含量两类(高含量为每毫升≥29个菌落形成单位)。虽然这项研究没有直接比较饮用水和粪便样本的微生物组成,但他们发现,饮用高大肠菌群饮用水家庭的儿童,其肠道微生物群的多样性低于饮用低大肠菌群家庭的儿童。
简单来说,肠道微生物群的多样性可能与抵抗肠道病原体的能力有关。也就是说,肠道内的微生物种类越丰富,可能越能抵抗有害细菌的侵袭。不过,某些特定微生物的存在似乎比整体的多样性更为重要。
这强调了确保全球安全和良好管理的饮用水供应的重要性。
除了建立饮用水和肠道微生物群之间的机制联系的重要性之外,抗菌素耐药性基因 (ARG) 从饮用水到肠道的传播也同样重要。饮用水中存在各种携带 ARG 的微生物和可能含有 ARG 的 eDNA。
Tips:这里的eDNA也可能是提取了环境中的微生物内的DNA,很难直接判断:即使没有活的微生物,ARG也可能通过环境DNA的形式存在于水中。
各种水处理工艺都可用于改变耐药基因的丰度。耐药基因从饮用水传播到肠道微生物群的速度尚未得到很好的研究。

2020的如上项目研究了上海和北京饮用水中耐药基因 blaNDM and mcr-1的丰度。他们随后证实,免疫缺陷 (BALB/c) 小鼠能够从饮用水中分离出的微生物中获得这些耐药基因,而这些微生物的浓度与饮用水中相当。这就引发了一个问题:免疫功能低下和/或健康的人是否也可能从饮用水中获得抗菌素耐药性微生物或基因。
饮水来源与肠道微生物群多样性
虽然饮用水和肠道中同一属的成员之间的重叠并不意味着存在直接联系,但两项人群水平的研究已将饮用水来源确定为解释肠道微生物组多样性变化的最重要因素之一。这两项研究都调查了分布在全球不同地区的多个人群,并使用了粪便微生物的16S rRNA基因测序数据。

2022年,Vanhaecke 等人调查了来自美国和英国 3413 个体肠道菌群组成的主要影响因素。微生物群、生活方式和饮食数据来自美国肠道微生物组计划。使用线性和逻辑模型分析了肠道菌群与不同饮用水来源 (瓶装、过滤、自来水和井水) 之间的关联。
饮用水来源是肠道菌群 α 和 β 多样性的关键因素,其效应大小与酒精摄入量和饮食类型相似。
参与者的地理位置多样,这可能导致饮用水的物理化学和生物参数存在较大差异。然而,研究发现市政自来水饮用者与其他类型饮用者之间,以及私人井水饮用者与瓶装水饮用者之间的肠道微生物群存在显著差异。
不同组之间观察到几种物种的丰度差异,包括瓶装水和市政自来水饮用者中链球菌属(Streptococcus)、拟杆菌、Odoribacter的丰度较高,而井水饮用者中Dorea属的丰度较高。
每日饮水量也影响了β多样性(组间差异性),每日饮水量少于1升的人群中弯曲杆菌属(Campylobacter)的丰度较高。
Dorea菌属于厚壁菌门毛螺菌科,广泛存在于人体肠道内,谷禾数据显示该菌在人群的检出率超89%。该菌最早也是从人体粪便中分离出来。
该菌是一类革兰氏阳性厌氧菌,主要存在于人类和动物的肠道中,可以利用多种底物进行发酵代谢,包括葡萄糖、果糖、乳糖和芳香族化合物等。它可能通过诱导Treg并抑制Th17细胞的分化和功能,从而调节肠道免疫反应,维持肠道黏膜屏障的完整性和稳定性。
在多发性硬化症、炎症性肠病患者,甚至结直肠癌、自闭症谱系障碍以及肥胖人群中的Dorea菌高丰度富集,被认为具有促炎作用。多数研究证实Dorea与体重指数 (BMI)、腰围和舒张压呈正相关。基线肠道内富含高丰度的Dorea菌的人群,在减重方面更困难。
然而Dorea菌在抑郁患者和患有食物过敏人群中减少,研究还表明Dorea菌可以预防或治疗过敏性鼻炎。

美国加利福尼亚州斯坦福市斯坦福大学人类微生物组研究中心团队2018年通过研究喜马拉雅山脉 4 个具有不同觅食程度和采用农耕方式时间的人群,研究了区分农耕和觅食生活方式的肠道微生物群的因素。这些人群分为觅食者、过渡到自给性农业的觅食社区和过去两个世纪完全过渡到农耕的人群。
从 56 个人采集了粪便样本。对应分析 (CA) 和微生物多样性分析表明,饮用水是与肠道微生物组成显着相关的两个因素之一。
各组之间没有观察到 α 多样性的显著差异,但几个β多样性指标表明与饮用水来源相关的组成变化。
在将这项研究扩展到坦桑尼亚的猎人采集者人群——哈扎人(Hadza)的季节性肠道微生物群数据时,研究发现饮用水对肠道微生物群组成也有类似的显著影响。这表明饮用水来源在不同生活方式的人群中对肠道微生物群有重要作用。

饮水中的化学成分与口腔及肠道微生物群
随后,英国研究团队于2020年开展的一项研究,他们调查了自来水中溶质浓度(钠、氯和硫酸盐)与肠道微生物群之间的关联。研究对象为英国的36对单卵双胞胎。结果表明,自来水中钠的日均摄入量(ADD)增加显著降低了肠道微生物群的丰富度,而微生物群的组成在硫酸盐和氯的日均摄入量的影响下有所不同。然而,这些关联较弱,并且研究中没有量化一些可能影响肠道微生物群的其他变量。
与饮用水和肠道微生物群之间的相互作用类似,关于饮用水对口腔微生物群影响的研究也很少。一项研究发现,在西班牙青少年的口腔微生物群中,自来水是所有调查因素中影响最大的。
饮用水的几个特征,包括碱度、硬度,以及氟化物和几种离子的存在,对特定菌属的丰度有显著影响。另一项研究也证实了饮用水中的氟化物对口腔微生物群的影响,该研究在小鼠中得出了类似的结果。除了饮用水对口腔微生物群的影响可能间接影响肠道微生物群外,饮水还可能将口腔中的微生物引入肠道。
总之,这些研究表明,饮用水属性对肠道菌群的组成有重要影响。有必要进一步研究这种关系是如何介导的,以及它如何影响人类健康。
关于饮用水(DW)与肠道微生物群关系的研究大多集中在饮用水的物理化学特性上,通常是在动物模型中进行,少数情况下涉及人类。需要注意的是,饮用水的物理化学性质,包括化学成分和处理过程,直接影响其微生物群,这反过来可能直接或间接影响肠道微生物群。一项荟萃分析表明,饮用水的化学性质在动物模型的微生物群研究中起到混杂作用,因此研究时需要注意。特别是,饮用水的 pH 值似乎会改变实验动物的肠道菌群。
■ 灭菌与否

2018年,一项实验动物研究了四种水源对小鼠肠道微生物群的影响:
他们观察到高压灭菌水和非高压灭菌水的肠道菌群存在差异,喂食高压灭菌水的小鼠中,属于芽孢杆菌属(Bacillota)和不动杆菌属(Acinetobacter)的操作分类单元 (OTU) 的丰度降低。
在喂食未高压灭菌水的小鼠中,没有观察到显着差异。这些差异的原因尚不清楚,并且该研究没有评估饮用水微生物群。
■ PH值
实验室研究中使用的动物通常被喂食酸化水,以防止动物护理设施中的微生物污染。酸化水导致 1 型糖尿病发病率增加,并导致小鼠肠道微生物群发生变化。
研究饮用水的pH值对健康成年男性血糖调节和肠道微生物群的影响,参与者在两个为期两周的周期内分别饮用中性(pH7)或碱性(pH9)水。研究未发现血糖调节或肠道微生物群的显著变化,尽管这种差异可能是由于所饮用水的pH值不同所致。
先前的人体研究表明,饮用酸性水与1型糖尿病之间存在关联,但尚未研究其对肠道微生物群的影响。
此外,已知肠道微生物群会影响葡萄糖稳态,而酸性pH值会不同程度地影响肠道常驻微生物的生长速率,这提示了可能的关联。从实际角度来看,市政供水中暴露于酸性饮用水是不常见的,因为饮用水通常以中性到微碱性的条件分配,以防止管道腐蚀。
■ 富含碳酸氢盐/硅酸盐
饮用富含碳酸氢盐的矿泉水或偏硅酸盐碱性矿泉水可能会通过改变肠道微生物群来影响宿主的生理机能(下表)。
饮用水微生物群和化学物质对肠道微生物群的影响

Moghaddam HS et al., Water Res. 2024

上面两篇研究分别在人类和猪仔和发现,饮用富含重碳酸盐的矿泉水或以偏硅酸为基础的碱性矿泉水可能通过改变肠道微生物群影响宿主生理。其中一些观察到的益处包括减少仔猪腹泻发生率,降低与胰岛素抵抗相关的某些标志物。
因此,值得进行样本量更大且具有适当对照组的综合研究将为矿泉水对肠道微生物群和宿主生理的影响提供更有力的证据。
■ 氯化物
自 20 世纪 50 年代以来,氟化物就被引入到饮用水和牙科用品中,如今大多数牙科产品和许多市政水源都已含氟。尽管氟化物使用范围很广,但很少有研究调查其对宿主相关微生物群落的影响。
最近一项关于水氟化对小鼠微生物组影响的研究表明,氟化水对口腔有选择性影响,但对肠道微生物组没有影响(上表)。
流行病学研究已将饮用水氯化和/或接触消毒副产物 与结直肠癌和膀胱癌联系起来。在小鼠结肠直肠癌模型中,高浓度的水氯化(10 mg/L)增加了肿瘤发生。
肠道微生物群中产气荚膜梭菌(C.perfringens)和肠杆菌科(Enterobacteriaceae)等专性厌氧菌同时减少。同样,由于未评估饮用水微生物群,因此无法建立饮用水与肠道微生物群之间的直接联系。
此外,这些发现与实际饮用水系统的相关性尚不清楚,因为这远远超过了正常的氯浓度。美国可接受的最大氯浓度为 4 mg/L。
根据世界卫生组织(WHO)的有关数据,人体对氯的耐受量为每天每公斤体重0.15毫克,假设这些氯全部来自于饮用水,得到自来水氯的允许含量为每升5毫克。根据我国的相关规定,出厂水的余氯含量最低不能低于0.05毫克/升,最高上限为4毫克/升。

在如上一项关于水氯化对 6-61 个月儿童肠道微生物群影响的研究中,未发现氯化对肠道菌群有显著的长期影响,但氯化处理组的腹泻发作和抗生素使用次数较少。氯化水处理组中某些微生物物种的丰度略有增加,抗生素耐药基因 (ARG) 的丰度也有所增加。
耐药基因丰度的增加归因于肠杆菌科细菌相对丰度的增加,这些细菌含有可移动的耐药基因,但被认为最终是有益的肠道居民。
由于本研究再次未测量水中的微生物群,因此这些耐药基因的来源尚不清楚。先前的研究表明,饮用水中存在的大多数耐药基因表现出垂直传播模式,而不是水平传播模式。这些耐药基因可能来自饮用水,或者可能有其他来源,但氯的存在会在肠道中创造一种环境,从而有利于这些肠杆菌科细菌的繁殖。
迄今为止,已有少数研究考察了水氯化对模型生物肠道菌群的影响。几种水氯化会导致肠道菌群发生变化,但这些变化仅在高于饮用水中通常测量的浓度时才会观察到。这些研究中的暴露时间通常也很短。对水中氯离子相关浓度的慢性暴露进行进一步研究将有助于得出与现实世界相关的结论。
众所周知,自来水会影响人体健康,但其影响机制尚不明确。
随着技术的发展,我们现在有很多工具可以帮助研究饮用水对人类肠道微生物群的影响。现代的DNA测序技术已经变得更加经济实惠,使我们能够分析饮用水中的微生物群落。这些技术的应用可以显著提升我们对这一领域的理解。
此外,各种可用的组学技术,包括代谢组学、蛋白质组学和转录组学,以及成像技术,提供了可用于动物模型和人类的工具,以研究饮用水微生物组与水特性和肠道微生物组之间的关系。
综合饮用水对肠道菌群及进一步身体健康的影响,还需要以下研究:
1) 长期研究
大多数现有研究侧重于持续 1 至 3 个月的短期治疗。纵向方法将考虑肠道微生物群和水质与微生物群的时间变化,并有助于了解微生物群和化学性质之间的长期关系。增强我们当前知识的一个简单方法是将饮用水属性(如水源、化学性质和消费模式)纳入肠道微生物群的纵向队列研究中。这还将改善样本量限制,因为许多队列包括数百名参与者。
2) 饮用水微生物群的影响
以前的研究主要集中在水的特性上,例如 pH 值、温度、消毒剂和溶质。然而,了解饮用水微生物群与肠道微生物群之间的直接关系对于理解其对人类健康的潜在影响至关重要。因此,未来的研究工作应该同时考虑饮用水微生物群及其化学属性。这项工作还应考虑耐药基因从饮用水到肠道微生物群的潜在传播。
3) 以人为本的研究
使用动物模型进行的研究有助于在严格控制的环境中检验假设和开发机械联系。需要进行更多研究来直接检查人类和类似人类的状况,因为这些状况可能与动物模型中的状况不同。
最近的创新如可复制的肠道微观生态系统,可能在可控环境中进行类似人类的研究。这些系统减少了对活体动物研究的需求,可用于调查多种因素、肠道发育的不同阶段及其他条件。
在体外系统中获得的重要发现可以通过人类试验并结合运用基因组学、转录组学/蛋白质组学和代谢组学来验证。这种以人为重点的研究将显著有助于理解饮用水微生物群与人类肠道微生物群之间的联系,以及在现实环境中如何体现,为公共卫生考量提供相关见解。
主要参考文献:
Moghaddam HS, Abkar L, Fowler SJ. Making waves: From tap to gut- exploring the impact of drinking water on gut microbiota. Water Res. 2024 Sep 21;267:122503.
Piperata BA, Lee S, Mayta Apaza AC, Cary A, Vilchez S, Oruganti P, Garabed R, Wilson W, Lee J. Characterization of the gut microbiota of Nicaraguan children in a water insecure context. Am J Hum Biol. 2020 Jan;32(1):e23371.
Vanhaecke T, Bretin O, Poirel M, Tap J. Drinking Water Source and Intake Are Associated with Distinct Gut Microbiota Signatures in US and UK Populations. J Nutr. 2022 Jan 11;152(1):171-182.
Khan H, Miao X, Liu M, Ahmad S, Bai X. Behavior of last resort antibiotic resistance genes (mcr-1 and blaNDM-1) in a drinking water supply system and their possible acquisition by the mouse gut flora. Environ Pollut. 2020 Apr;259:113818.
Jha AR, Davenport ER, Gautam Y, Bhandari D, Tandukar S, Ng KM, Fragiadakis GK, Holmes S, Gautam GP, Leach J, Sherchand JB, Bustamante CD, Sonnenburg JL. Gut microbiome transition across a lifestyle gradient in Himalaya. PLoS Biol. 2018 Nov 15;16(11):e2005396.
Bowyer RCE, Schillereff DN, Jackson MA, Le Roy C, Wells PM, Spector TD, Steves CJ. Associations between UK tap water and gut microbiota composition suggest the gut microbiome as a potential mediator of health differences linked to water quality. Sci Total Environ. 2020 Oct 15;739:139697.
Murakami S, Goto Y, Ito K, Hayasaka S, Kurihara S, Soga T, Tomita M, Fukuda S. The Consumption of Bicarbonate-Rich Mineral Water Improves Glycemic Control. Evid Based Complement Alternat Med. 2015;2015:824395.
Chen J, Xu XW, Kang JX, Zhao BC, Xu YR, Li JL. Metasilicate-based alkaline mineral water confers diarrhea resistance in maternally separated piglets via the microbiota-gut interaction. Pharmacol Res. 2023 Jan;187:106580.
Murakami S, Goto Y, Ito K, Hayasaka S, Kurihara S, Soga T, Tomita M, Fukuda S. The Consumption of Bicarbonate-Rich Mineral Water Improves Glycemic Control. Evid Based Complement Alternat Med. 2015;2015:824395.

谷禾健康

血清素,5-羟色氨(5-HT)不仅充当体内系统的神经递质和激素,而且还是胃肠系统中的旁分泌信使。
5-HT神经元系统起源于中脑中缝核,下面示意图强调了血清素(5-HT)神经元与释放不同神经递质的其他神经元以及神经胶质细胞之间的解剖相互作用。
中枢神经系统几乎所有区域的神经末梢都会释放5-HT。换句话说,可能很难找到不受5-HT调节的神经元/细胞通信的单一参与者。血清素是一种抑制性神经递质,会抑制其它神经递质的分泌,比如(多巴胺,肾上腺素等)。所以它有时也被人们称为:“幸福激素”或“幸福神经递质”。
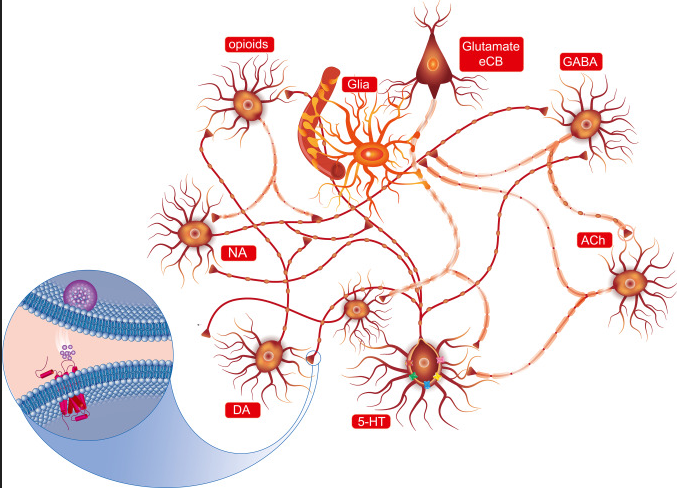
目前(血清素)5-HT系统是开发治疗中枢神经系统疾病药物的重要靶点。但是血清素仅有5%左右来自中枢神经产生,体内大约95%的血清素是由肠嗜铬(EC)细胞(胃肠道中最常见的神经内分泌细胞类型)通过感测来自肠腔和循环系统的信号合成和分泌的。肠道菌群及其代谢物、营养物质和激素是调节EC细胞分泌5-HT的主要因素。要注意,由于5-HT不能穿过血脑屏障,中枢和外周5-HT系统在解剖学和功能上是分开的。
循环血小板可以从胃肠道中隔离5-HT,并将其存储或需要时释放以促进止血并将其分布到身体各个部位。因此,肠道来源的5-HT调节多种功能,包括肠运动和分泌反射、血小板聚集、葡萄糖稳态、免疫反应和骨骼发育和心脏功能。
此外,血清素的生理作用受到多种蛋白质的调节,这些蛋白质调节其合成、储存、释放、再摄取和降解。血清素信号传导由至少14种不同的受体介导。
研究发现血清素传输的改变发生在许多中枢神经系统(CNS)疾病中,血清素过低或血清素使用障碍与精神分裂症、焦虑症、抑郁症、成瘾、癫痫、肥胖、强迫症、多发性硬化症、帕金森病和阿尔茨海默病的有关。因此,各种精神活性药物和药物的作用通常通过直接或间接机制涉及5-HT系统。
血清素产生和随后分解的速度之间的相对平衡是决定一个人拥有多少可用的“活性”血清素的主要因素之一。研究表明,一些补充剂能够增加血清素水平,如色氨酸,抗抑郁药物,维生素D、omega-3脂肪酸和某些益生菌,具有较强证据支持。此外,阳光照射,适当锻炼、积极思考、社交互动等也是增加血清素的重要手段。
与此同时,由于药物、补充剂或草药的组合导致也会血清素升高至不安全水平而引起血清素综合征。它可能导致意识混乱、发烧、呕心、不自主的肌肉痉挛、癫痫发作甚至死亡。任何食用改变血清素水平的产品的人都应该注意到这些症状。
然而,迄今为止,缺乏在体内相关探测这种难以捉摸的神经递质所需的有效工具。最近的技术进步,例如血清素 FSCV(”阶段性”测量)和 FSCAV(”环境”测量),刚刚开始揭示血清素活性对行为相关时间尺度的复杂性和影响。此外,血液高效液相色谱法也被用来测定血清素水平。
但是,血清素的变化受多方面因素的影响,其中大部分血清素是在肠道产生的。血清素与肠道菌群之间存在密切关系。因此利用肠道菌群的大数据库可以帮助我们从新的角度评估血清素,尤其是肠源性血清素的变化尺度和动态,可以反映个体整体的生理状态和代谢特点。
本文将探讨血清素的发现进化及其与光的作用,产生代谢,影响的生理功能和疾病,以及增加血清素水平的潜在自然方法。此外还有血清素综合征的定义,危害以及注意事项。希望本文的能够为5-HT在营养、临床医学和健康领域的应用提供一些见解。
血清素存在于身体的大部分器官中,例如皮肤、肠道、肺、肾、肝脏和睾丸中,以及地球上几乎所有生物体中,包括真菌、植物和动物中。血清素在系统发育上很古老,并且在植物和神经元出现之前就已进化。
根据文献,血清素的进化始于近三十亿年前单细胞生物中的前体色氨酸。色氨酸合成血清素需要氧气和光。保守的血清素生物合成途径始于蓝藻、绿藻和真菌的单细胞系统,并不断进化到目前在人脑中的位置。
▸ 阳光对血清素的合成以及水平有重要影响
血清素进化分析中出现的一个重要概念是它与光的关系。从色氨酸吲哚环的光吸收特性开始,随着系统发育的进一步发展,阳光对人类的血清素水平以及情绪、睡眠和自杀意念都有影响。与色氨酸结合并减轻与季节性情感障碍(SAD) 相关的抑郁症的最有效的光类型是蓝光。
色氨酸的光捕获特性归因于其吲哚结构。叶绿体中的色氨酸合成特别高,叶绿体吸收蓝光波会激发色氨酸的吲哚结构,使其失去吲哚环结构中的一个电子,从而被氧化。叶绿体细胞器含有色氨酸合成所需的基因和酶,类似于蓝细菌中的基因和酶。水果、蔬菜和坚果中的色氨酸含量要高得多。
拓展:除此之外,色氨酸产生烟酸及其所有前体。 NAD+和NADP+辅因子几乎参与细胞代谢的所有方面。从色氨酸从头合成NADH是这些辅酶比利用膳食烟酰胺或烟酸更重要的来源。在细胞核中,烟酸对于DNA修复很重要,并且色氨酸捕获光似乎是导致DNA光损伤的原因,该损伤与突变和缺乏修复的细胞死亡相关。
尽管光合作用具有营养价值,但对细胞来说却是一个主要风险。破坏光收集率和光利用率之间的平衡会扰乱光合作用,导致活性氧(ROS)的产生。如果不加以控制,活性氧会损害蛋白质功能和膜完整性,并对光合生物构成严重威胁。色氨酸产生荧光光产物,抑制培养的受精海胆卵和小鼠成纤维细胞的生长和分化。
因此,从细菌到哺乳动物的多种细胞都会受到光氧化色氨酸的损害。阳光对人体皮肤造成的损害很大程度上归因于色氨酸通过吡咯酶、犬尿氨酸和烟酸途径代谢的作用。
大约于1937年从纯化浓缩的牛血清中鉴定出一种具有吲哚核的血管收缩物质,并将其命名为“5-羟色胺”(5-HT)。5-HT后来被称为“血清素”,该术语源自其衍生物“血清”及其调节血管内张力的能力。
1960年,人们发现肠道是5-HT生物合成的主要枢纽;对大鼠进行全胃肠切除术导致尿液中5-HT和主要代谢物5-羟基吲哚乙酸(5-HIAA)大幅减少。这一发现以及大脑中完整的5-HT水平表明,神经元5-HT生物合成独立于其肠道来源。
▸ 血清素(5-HT)合成
人体也是从色氨酸生物合成血清素。色氨酸被色氨酸羟化酶(TPH)分解,产生前体5-羟基色氨酸(5-HTP),然后被氨基酸脱羧酶(AADC)转化为5-HT。
TPH是5-HT合成中的特异性限速酶,它包含两种亚型,即TPH1和TPH2。TPH1负责外周5-HT的合成,主要在肠道肠嗜铬(EC)细胞中表达。TPH2主要表达于中枢神经系统(脑干裂齿核)和肠神经系统 。
色氨酸羟化酶(TPH)需要分子氧(O2)和四氢生物蝶呤(tetrahydrobiopterin,简写为BH4)作为共底物。该酶对亚铁(Fe2+)有绝对需求。
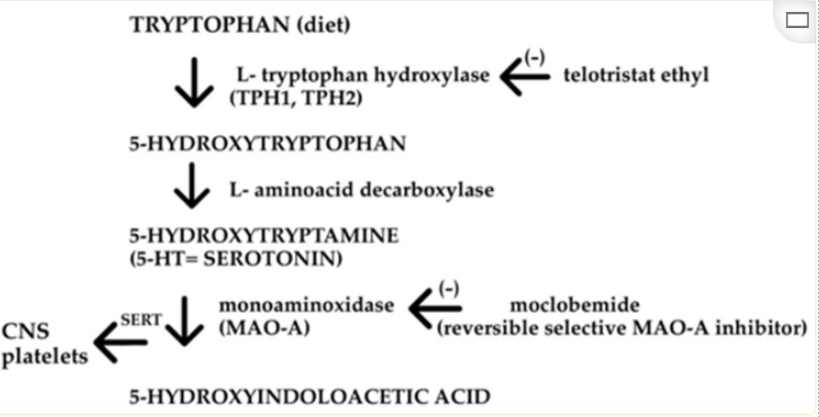
Guzel T and Mirowska-Guzel D.Molecules.2022
拓展:
四氢生物蝶呤(tetrahydrobiopterin)是一种天然存在的营养素,简写为BH4。是参与5-羟色胺、多巴胺、去甲肾上腺素、肾上腺素、褪黑素、一氧化氮生物合成的酶的重要辅助因子;
四氢生物蝶呤缺乏症是一种常染色体遗传性疾病,是迄今得以确认的5000~6000种人类的罕见病之一,四氢生物蝶呤缺乏症通过对新生儿进行疾病筛查,检出高苯丙氨酸血症(HPA)后可得到进一步确诊。BH4缺乏症主要会对人的神经系统造成损害,导致患儿出现智力低下、癫痫等症状。
♢色氨酸羟化酶活性影响血清素的水平
色氨酸羟化酶(TPH)是神经递质血清素 (5-HT) 生物合成中的限速酶。因此,TPH催化活性的增加或减少会导致神经元5-HT含量的相应变化。
TPH需要还原蝶啶辅助因子、分子氧和非血红素铁来羟基化其底物L-色氨酸。这四个因素中任何一个的组织含量的改变都可能改变TPH活性。TPH的翻译后修饰,包括磷酸化和半胱氨酸氧化,会导致其催化活性发生显著变化。
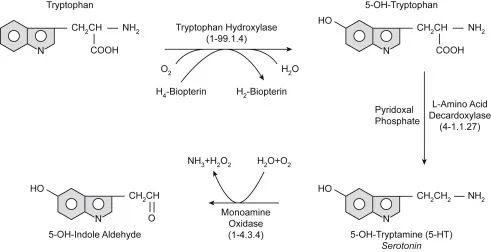
doi.org/10.1016/B978-0-444-64125-0.00001-3
上图显示了从色氨酸合成血清素的过程。色氨酸羟化酶和一般L-氨基酸脱羧酶的作用与必要的辅助因子一起显示。血清素代谢为5-OH-吲哚醛,与生长素(吲哚醛)类似,生成过氧化氢(H2O2 )。血清素也是脊椎动物合成褪黑激素的前体。
♢肠嗜铬细胞合成全身95%的血清素
除了在CNS(中枢神经系统)中合成外,胃肠粘膜内的肠嗜铬细胞(EC细胞)合成和分泌高达95%的全身血清素,也存在胰岛、乳腺和脂肪组织中。这些细胞对化学和机械刺激做出反应,但也收集来自肠道微生物群的信号以释放血清素。
肠嗜铬细胞(EC细胞)细胞激活将血清素释放到附近细胞的间隙中。 EC细胞感知胃肠道内的餐后变化,包括pH值、营养和毒素。
EC细胞产生高浓度的血清素,而调节系统从肠道间质空间去除高水平的血清素,该调节系统抑制血清素能传递并防止血清素中毒。血清素在肠细胞中循环或隔离以去除间质血清素。肠粘膜的肠细胞通过 SERT 吸收血清素,单胺氧化酶将其分解,然后粘膜下毛细血管将血清素转运到血液中。
▸ 血清素的吸收
我们现在知道,几乎血液中的所有5-HT都由血小板携带,血小板不会产生5-HT,而是在肠道循环时吸收它。因此,血清素在肠道中分泌并被血小板吸收后,就变成了“血清血清素”。
一旦5-HT被释放到固有层,它就会通过血清素再摄取转运蛋白(SERT)被上皮细胞吸收。接下来,5-HT 扩散到血流中,被血小板吸收并转运到外周靶组织。然而,血清素在体内可以通过多种方式被吸收和代谢,并且其吸收可以根据给药途径而变化。
一般来说,口服血清素不容易被吸收,因为它的活性形式很难穿过血脑屏障。中枢和外周血清素库在功能上彼此不同,因为它们分别控制大脑和外周区域的血清素依赖性行为。这就是为什么脑细胞必须从L-色氨酸或5-羟色氨酸(5-HTP)(L-色氨酸的副产品)产生自己的血清素。
注释:血清素再摄取过程,例如细胞X若是释放出了很多血清素,与其相靠近的细胞Y就会检测到周围血清素浓度的变化。信号发出后一段时间,细胞X会“回收”周围的血清素。这个过程叫神经递质的再摄取。再摄取不仅可以减少细胞X所需要生成的血清素,更能控制细胞之间信号的的传输。
▸ 血清素(5-HT)降解
过量的血清素以及大脑和肠道会通过几种不同的机制“失活”。例如,称为血清素转运蛋白的蛋白质可以有效地“清理”或“去除”(重新摄取)神经突触中的血清素,并将其带回神经元中以供重复使用,或者,释放到血液中的血清素要么被血小板吸收,要么在肝脏和肺部被单胺氧化酶(MAO-A)、乙醛和乙醇脱氢酶等酶分解(代谢)。
血清素主要被单胺氧化酶(MAO)分解代谢为5-羟基吲哚醛(5-HIA),然后被醛脱氢酶(ALDH)代谢为5-羟基吲哚乙酸(5-HIAA)。
单胺氧化酶有两种亚型:MAOA和MAOB。前者对5-HT的亲和力较高。5-HT也可以通过芳烷基胺N-乙酰基转移酶(AANAT)代谢为N-乙酰基血清素(NAS),随后通过羟基吲哚O-甲基转移酶(HIOMT)转化为褪黑激素。
此外,吲哚胺2,3-双加氧酶(IDO)对色氨酸、5-HTP、5-HT和褪黑激素等多种血清素通路成分的吲哚部分具有广泛的底物特异性。因此,5-HT也可以通过IDO进入犬尿氨酸途径。与抑郁症相关的血清素减少和犬尿氨酸增加与IDO活性有关。因此,除了Tph之外,犬尿氨酸途径对于调节血清素合成和可用性至关重要。
▸ 血清素周转和传递的复杂性
血清素(5-HT)在体内的周转速度非常快,尽管大脑中的5-HT含量只占体内总量的很小一部分(3%~5%),但在大脑中的循环速度却非常迅速。
♢血清素的周转速率非常快
研究表明,在健康的大鼠身上,5-HT的周转速率为15分钟到一个多小时。使用多室模型时,5-HT的合成、释放和降解可以被视为“后进先出”,这意味着这些过程发生得非常迅速,不到5分钟就会完成。
5-HTP是5-HT的前体,无需转运蛋白即可轻松穿过血脑屏障,并增加大脑5-HT水平,从而产生抗抑郁样作用。然而,5-HTP的快速药代动力学(在人体中的半衰期约为2小时)使其作为药物不切实际,神经药理学界将注意力转向更有效和安全的选择性血清再吸收抑制剂(SSRI)。
SSRIs可以通过阻断血清素转运蛋白(SERT)来提高大脑中细胞外5-HT水平,从而具有抗抑郁功能。根据临床反馈,目前SSRIs的药理潜力有限,只有三分之一的患者在治疗后情绪得到改善。因此,单独使用SSRIs抑制SERT活性可能不足以提高细胞外5-HT水平以引发大脑的抗抑郁反应,而用第二种协同药物治疗抑郁症则可以提高细胞外5-HT水平,从而超出其效果(这个不在本文讨论范围,下次有机会再讨论SSRIs与其他药物的协同互作)。
▸ 血清素(5-HT)受体
哺乳动物的受体存在巨大的多样性。有数百个血清素受体克隆,人脑至少有20个独立的5-HT受体神经元转录本。血清素与人脑中至少14种特定受体蛋白特异性结合,调节神经元中的离子通道、c-AMP 水平和激酶活性。
5-HT受体存在于身体的每个细胞中。为什么这么多,为什么分布这么大?可以推测,是由于动物体内制造和获取色氨酸的困难导致血清素利用率低。受体的功能是警告细胞环境中存在化学物质,而不去除或改变化学物质。
♢人体拥有众多的血清素受体
因此,如果化学物质供应短缺,受体分子的出现允许其作用传递到整个生物体。为了使其发挥最大效果,需要一种有效的血清素分配机制。动物的血液中含有特定的色氨酸和血清素结合蛋白,有助于将这些分子转运到特定的目标区域,例如大脑。
血脑屏障交界处的神经胶质细胞具有特殊的转运蛋白,用于浓缩色氨酸并将其递送至血清素神经元。血清素能神经元发育出长的无髓鞘轴突,可以吸收色氨酸并利用整个大脑和肠道合成血清素所需的酶。总之,色氨酸的丧失促进了高度分支、无髓鞘的神经网络和大量特定受体的形成,以最大限度地发挥血清素的作用。
迄今为止,已鉴定出14种血清素能受体,可以精确、快速地传递血清素的神经化学信息。此外,多种机制影响血清素再摄取,包括除SERT之外的其他单胺转运蛋白(例如多巴胺转运蛋白[DAT]、去甲肾上腺素转运蛋白[NET]和有机阳离子转运蛋白[OCT])对血清素的混杂再摄取。进一步强调该系统的复杂性,对血清素再摄取的显著控制是通过与SERT偶联的G蛋白的血清素自身受体实现的。
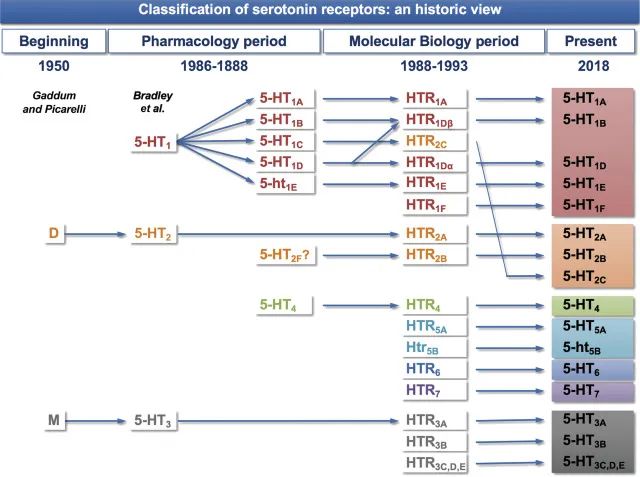
doi.org/10.1016/B978-0-444-64125-0.00005-0
过去了近10年。 5-HT受体的数量保持不变:14种受体亚型分为7个家族。
新发现与表达5-HT受体的细胞表型的鉴定及其与其他相关神经递质和神经递质受体的共定位有关,其中一些在神经元中,另一些在神经胶质细胞或星形胶质细胞中。免疫组织化学的应用增加了有关这种共定位的新信息。许多研究都集中在与偏头痛相关的大脑区域中5-HT受体的表达。
具有相似化学结构的血清素代谢物在细胞外的浓度可能比血清素本身高出近500倍,进一步阻碍测量,表明代谢过程很复杂。快速再摄取机制与快速代谢相结合,不仅减少了血清素可检测的时间,而且一些代谢物已被证明会显著降低微电极检测探针的完整性。总之,这些情况使体内血清素的测量和理解以及最终血清素活性与行为的对应关系变得复杂。
▸ 血清素(5-HT)反馈
血清素神经元在形态、连接性、电生理参数和基因表达方面表现出相当大的多样性。血清素神经元具有多种共递质,包括GABA或谷氨酸,以及许多不同的神经肽。
这些神经元能通过相同的神经递质语言进行交流,感知并相互调节血清素的释放,形成反馈回路。
反馈机制包括直接和间接的多突触途径,调节血清素系统的功能。不同区域的血清素神经元对反馈抑制的敏感性存在差异,与行为环境有关。
♢血清素的反馈机制可能影响人体系统功能
反馈机制可能不是维持血清素神经元稳态的主要作用,而是控制系统功能的重要机制。反馈的改变可能与多种与血清素相关的疾病有关,血清素选择性再摄取抑制剂可能通过重新平衡不同亚群间的相互作用发挥作用。
总而言之,血清素系统内的大量反馈机制在调节网络动态和塑造血清素神经传递的时间和空间方面发挥着关键作用。
▸ 肠道微生物与血清素合成,传递
肠道微生物群可以通过多种机制影响大脑中的血清素水平和神经传递,包括肠道中血清素的产生、SERT的调节、免疫系统相互作用、迷走神经通讯以及短链脂肪酸等代谢物的产生。
使用无菌小鼠或抗生素相关微生物群扰动进行的干预研究提供了令人信服的证据,研究使用无菌(GF)和抗生素治疗的小鼠,这些小鼠的外周5-HT水平显著降低,这种现象在正常肠道微生物定植后会逆转,表明5-HT和肠道微生物群之间的新型相互作用对于维持肠道稳态至关重要。
♢肠道微生物群对合成血清素有重要影响
越来越多的证据表明,外周5-HT是宿主与微生物群相互作用的关键介质,这对于维持肠道健康至关重要。膳食色氨酸(Trp)的很大一部分要么进入犬尿酸途径,要么被肠道微生物分解代谢为吲哚;只有一小部分用于外周5-HT合成。话虽如此,肠道微生物却是宿主5-HT合成的重要介质,这一过程主要由微生物代谢物驱动,向EC细胞发出信号并促使宿主机通过TPH1生成5-HT。
此外,宿主血清素能系统受到TLR2的严格调节。TLR2激活会降低5—羟色胺转运蛋白(SERT)表达和活性,而高水平的5-HT对TLR2表达产生负反馈效应。与此同时,TLR2 缺陷的小鼠表现出结肠5-HT水平和Tph1表达降低,非造血细胞(很可能是肠上皮细胞)中TLR2的激活负责肠道中5-HT的产生。这些发现与之前的观察结果一致,即Akkermansia muciniphila的外膜蛋白(Amuc 1100)通过TLR2信号传导促进5-HT生物合成。
此外,多形拟杆菌和齿双歧杆菌已被证明可以通过短链脂肪酸(例如乙酸盐和丙酸盐)的作用恢复EC细胞网络,从而促进5-HT合成,并增加肠道5-HT水平。
相反,胃内施用假长双歧杆菌可通过减少EC细胞数量来降低结肠5-HT水平,而鼠李糖乳杆菌GG上清液则上调结肠中的SERT表达。
此外,一些细菌菌株,如大肠杆菌、肺炎克雷伯菌和植物乳杆菌,可以直接转化色氨酸以从头合成5-HT ,而一些葡萄球菌则表达葡萄球菌AADC(sadA)基因负责转化5-HTP至5-HT。尽管已有证据,但这些细菌中5-HT的生理功能以及这种细菌来源的5-HT是否与宿主具有任何生物学相关性仍然难以捉摸。
虽然肠道产生的血清素不能穿过血脑屏障,它会影响血脑屏障的通透性,从而导致大脑炎症。此外,肠道微生物群对迷走神经的刺激可以改变动物和人类大脑中血清素、GABA 和谷氨酸的浓度,无菌雄性小鼠实验表现出类似焦虑的行为,并改变大脑中血清素的丰度。
♢使用精神药物产生的个体副作用差异可能与肠道菌群有关
其实抗抑郁和治疗精神障碍的药物包括SSRIs引起的副作用存在个体差异的事实可以用肠道微生物失调来解释。肠道血清素能神经元参与肠道蠕动的调节,这一事实可以很好解释恶心、便秘或腹泻等不良反应。
最近来自一项专门针对大鼠的氟西汀的小型临床前研究,其中体重增加伴随着某些细菌菌株(例如乳酸菌)的破坏,已知乳酸菌与体重调节有关。从临床试验和临床经验来看,一些患者似乎特别反应大,并且可能因使用SSRIs而体重显著增加 。这是否是由于个体的肠道微生物组成造成的,这也可能未来治疗领域需要关注的领域。
然而,在许多不同的精神疾病中也检测到其水平的改变。一些胃肠道功能障碍的症状可能是由于神经内分泌免疫刺激导致中枢神经系统活动失调、外周水平(肠)失调或两者(脑肠轴)的组合所致。此外,多项研究证明了5-HT在肝脏中的促纤维化作用,表明它与血小板衍生生长因子协同作用,刺激肝星状细胞增殖。
♢血清素是宿主与微生物群互作的关键介质
最近的一项研究指出大约50%的肠道来源5-HT受到肠道微生物群的调节,特别是以梭状芽孢杆菌科(Clostridiaceae)和苏黎世杆菌属(Turicibacteraceae)为主的孢子形成细菌,对宿主肠道蠕动、止血和骨化产生下游影响。
虽然大部分肠道5-HT由肠嗜铬细胞从基底外侧分泌到周围肠道组织中,但一些肠嗜铬细胞含有的5-HT则从顶部分泌到肠腔中,这表明肠道微生物暴露于宿主-衍生的5-HT。事实上,微生物对宿主肠嗜铬细胞的影响不仅调节肠道组织和血液中的5-HT水平,而且还调节肠腔和粪便中的5-HT水平。
一项新的研究表明,产孢肠道细菌(Turicibacter sanguinis)中的一种新型血清素传感器可能对宿主脂质和类固醇代谢很重要。这些发现支持了一个新兴概念,即双向信号通路可以影响细菌群落结构并对宿主生理产生影响。
为了解决粘膜血清素和肠道微生物组之间的串扰本质上是否是双向的,并可能导致细菌功能反应改变的问题,研究人员通过口服补充血清素或进行基因改造来限制血清素再摄取,他们发现粪便血清素水平的增加与肠道微生物群落结构的改变有关,特别是孢子形成细菌相对丰度的增加。生物信息学方法显示, Turicibacter属的孢子形成细菌表达蛋白质 CUW_0748,该蛋白质与哺乳动物血清素转运蛋白 (SERT) 具有序列和预测同源性,SERT 是一种膜转运蛋白,负责包括肠道在内的许多器官中血清素的再摄取和失活。
培养实验表明,细菌种Turicibacter sanguinis能够摄取血清素,而且这种作用可被选择性血清素再摄取抑制剂(SSRI) 氟西汀抑制。单独使用血清素或与氟西汀联合暴露时, T. sanguinis的转录组分析产生了基因表达的强烈变化,进一步支持了血清素介导的细菌反应作用。
总的来说,这些数据可能对抗抑郁药物的使用具有重要的临床意义。未来的研究将产生负责细菌对宿主血清素反应及其对宿主生理机能的后续影响的替代机制。
血清素有助于控制不同生物群体的新陈代谢。除了中枢神经系统和肠神经系统中发生的神经元交换之外,血清素还影响身体周围的组织。此外,血清素负责介导多种非神经元过程和功能,例如膀胱调节、止血、呼吸驱动、免疫反应、血管张力和肠道炎症。
血清素通过胃肠道中的5-HT受体在分泌、血管舒张、蠕动、疼痛感知和恶心中发挥关键作用。中枢血清素在调节情绪和行为以及通过降低食欲影响整体能量平衡方面发挥着至关重要的作用。
注:几种调节中枢血清素功能的药物(例如芬氟拉明、西布曲明和氯卡色林)最初被批准并用作抗肥胖治疗,但随后由于其不良心血管和致癌作用而被撤回。
在过去的十年中,人们利用特定血清素相关基因敲除的动物模型,对外周血清素在控制全身能量代谢中的作用进行了广泛的研究。以下是汇总的一些关键的相关的健康功能。
众所周知,脑干含有离散的含血清素(5-羟色胺,5-HT)神经元组,从尾髓质延伸到中脑头端。各种类型的血清素受体在整个大脑中分布不均匀,对目标部位的作用也不同。
血清素能神经元位于脑干中缝核,从那里它们投射到多个大脑区域并刺激多种血清素受体亚型。血清素能功能障碍与多种精神疾病有关,并且可能主要导致焦虑和抑郁等负面情绪。
血清素功能障碍会导致负面情绪和行为
突触内血清素的摄取受血清素转运蛋白(5-HTT)的功能和可用性的调节。血清素再摄取率的双重差异与5-HTT基因调节区域的功能多态性有关,并可能导致产生负面情绪状态的风险。
除了焦虑和抑郁等负面情绪状态外,血清素能功能障碍也可能有助于冲动行为、攻击性和过量饮酒的发病机制和维持。
脑干5-HTT可用性的增加与压力引起的血清素周转率下降相关。研究结果表明,产前和产后的压力暴露可以引起应激激素轴激活的长期改变,并可能影响血清素能神经传递。
血清素影响神经兴奋进而与一些精神疾病有关
5-HT在控制由神经网络振荡产生的节律性电活动方面至关重要,神经网络振荡是由反复兴奋和反馈以及前馈抑制的协调活动产生的兴奋和抑制平衡(E/I)之间的精确平衡决定的。血清素能功能的功能改变与多种疾病的缺陷有关,例如抑郁症、焦虑症、精神分裂症和明显的癫痫症。这些病理情况与5-HT的改变及其与不同神经递质系统的相互作用相关,例如GABA、多巴胺(DA)、大麻素(CB)等。导致E/I平衡改变并影响突触可塑性。
中枢神经系统中突触5-HT可用性的增加与情绪升高和焦虑减少相关,这构成了几类广泛使用的抗抑郁药的基础,这些抗抑郁药可通过以下方式防止5-HT从突触间隙中去除:阻断血清素转运蛋白(SERT)。
有一些证据表明血清素能系统在丛集性头痛(CH)病理生理学中的潜在作用。研究数据表明,丛集性头痛(CH)的特点是血浆血清素代谢升高,这表明中枢 5-羟色胺系统可能参与丛集性头痛的发生。
血清素的神经营养作用
在脊椎动物、线虫和果蝇等动物中,存在着一类称为星形胶质细胞的支持细胞,它们可能是最早出现的用于增强血清素营养作用的次级细胞。
1957年就有人提出血清素系统是一个”营养系统”。血清素可以通过受体介导的葡萄糖利用率和营养因子释放的变化。血清素纤维可以被认为是大脑的“滴灌系统”。只要轴突完好无损,血清素就能有效地释放到整个大脑中。而在老年和神经退行性疾病中,人脑中的血清素轴突会退化。
在哺乳动物中,血清素通过与神经胶质细胞的相互作用,形成了一种间接但重要的营养关系。高亲和力血清素受体已在星形胶质细胞、小胶质细胞、双极细胞和雪旺细胞等上发现。
血清素受体的激活可以促进神经胶质细胞的分化,诱导神经营养因子mRNA的表达,还可以刺激星形胶质细胞释放营养因子S100。
反过来,星形胶质细胞为血清素能神经元提供色氨酸,两者之间存在密切的营养相互作用,在海马体尤为明显。
季节性情感障碍和自杀
血清素的减少会对正常的大脑稳态(结构和功能)产生严重影响,并影响一个人继续生活的愿望。令人惊讶的是,阳光对人类大脑的血清素系统具有显著的作用。
几十年前就报道了情感障碍的季节性变化,并且从有记录的历史最早时期就已经注意到了。有些北半球文化制定了特殊的节日来纪念地球上的光的最低点,并举行庆祝活动来对抗冬季的阴暗(例如农神节和冬至)。
季节性情感障碍包括秋季/冬季复发性重度抑郁发作,春季/夏季缓解,可通过血清素药物和/或光疗法有效治疗。光疗法或抗抑郁药物治疗与心理社会功能和生活质量评估的显著改善相关。
光疗法对人体血清素参数有影响。研究表明,健康受试者和非季节性抑郁症患者在重复可见光照射后,血液血清素会增加。101 健康男性的颈静脉血样显示,冬季大脑中血清素的周转率最低,并且与明亮阳光的持续时间直接相关。
通过该程序测量的血清素的产生随着亮度的增加而迅速增加。无论一年中的什么时间,在明亮的日子里,血清素水平都较高,并且血清素的含量反映了特定一天暴露在阳光下的时间——前一天的条件没有影响。在一组有季节性情感障碍病史的患者中,测量到的血浆生物蝶呤和色氨酸水平显著降低,而光疗后则升高。
蓝光可有效增加叶绿体光合作用过程中色氨酸的吸收,并且这种光可有效治疗患有季节性情感障碍的患者。正如植物叶绿体系统所提到的,在人类研究中蓝光可能是最有效的。蓝光可以抑制褪黑激素水平并有助于昼夜节律相移。当使用窄带蓝光(468nm)时,光疗法可有效显著减少 HAMD21。
有人提议,应根据有关光的神经生物学效应的新知识重新评估家庭和工作场所的照明标准。这可能被认为是一个社会为实现有利于增强普通人群血清素功能的条件而采取的第一步,也是对血清素与阳光的特殊关系的承认,这种特殊关系在地球生命之初就开始出现。
外周血清素在调节肠道感觉、运动、肠腺分泌、维持肠道平衡等方面发挥着重要作用,健康状态下它不会穿过血脑屏障,影响中枢神经系统。
在人类肠道中,内皮细胞充当肠道内容物的传感器。在乙酰胆碱、腔内压力升高、低pH等一定刺激下, 肠嗜铬细胞(ECs)释放5-HT,激活肠壁内源性感觉神经元,引起肠内分泌反射和蠕动,而外源性神经元则也可被5-HT激活,引起疼痛、不适、恶心和呕吐。
血清素的分泌增加会导致肠道产生不适症状
当肠道受到刺激时,5-HT增加并与外源性初级传入神经末梢的5-HT 3受体结合,使肠神经系统(ENS)和内脏传入神经高度敏感,从而产生不适、腹痛、和腹泻。还有报道称,IBS-D 患者肠粘膜中的5-HT 和 5-HT 3受体显著高于健康对照者,表明 IBS 患者的 5-HT 系统受损。
在胃肠道中,血清素会引发恶心、肠道分泌和蠕动等反应,并且还与肠易激综合征等胃肠疾病有关。
例如,阿洛司琼(一种 5-HT 3拮抗剂)被证明可有效治疗伴有腹泻的IBS,而替加色罗(一种 5-HT 4激动剂)可有效治疗伴有便秘和慢性便秘的 IBS。5-HT 3拮抗剂阻断肠嗜铬细胞释放的 5-HT 对肌间神经丛固有初级传入神经元的影响,5-HT 4激动剂可引起蠕动反射。
这些作用机制可能涉及5-HT调节感觉神经传递和肠道反射运动。但这些药物的安全性存在问题,临床应用受限,需要进一步探索新的治疗靶标。此外,对肠嗜铬细胞5-HT作用的认识也需要重新审视。
5-羟色胺是一种肠神经系统生长因子
5-羟色胺(5-HT)不仅是肠神经系统(ENS)中的重要神经递质,也是ENS发育所需的关键生长因子。5-HT能够促进神经嵴源性前体细胞的分化和新神经元的生成,对ENS的出生后生长和维持至关重要。
缺乏神经元5-HT合成酶TPH2会导致ENS神经元数量显著降低,表明5-HT在ENS正常发育中的关键作用。此外,环境刺激可能通过改变5-HT能神经元的活动,从而对ENS的结构和功能产生持久影响,这为理解肠易激综合征等胃肠道功能障碍的发病机制提供了新线索。
血清素促进肠粘膜生长
肠神经元中的5-HT不仅影响肠粘膜的生长和维持,也影响ENS的生长和维持。缺乏5-HT再摄取转运蛋白SERT的小鼠,其肠粘膜生长和细胞增殖明显增强,因为SERT负责5-HT的失活。给予选择性5-HT再摄取抑制剂(SSRI)也会产生类似效果。这种作用主要是通过神经元5-HT而非肠嗜铬细胞5-HT介导的,因为删除TPH2(神经元5-HT合成酶)会减弱SERTKO小鼠的效果,而删除TPH1(肠嗜铬细胞5-HT合成酶)则不会。
5-HT 2A受体阻滞剂和乙酰胆碱拮抗剂都可以抑制SERTKO或SSRI增强肠粘膜生长的效果,表明这种作用是通过5-HT 2A受体介导的,而该受体主要表达在粘膜下胆碱能神经元上。这些神经元为上皮细胞提供神经支配,可能是促进粘膜干细胞/增殖细胞增殖的关键机制。
肠嗜铬细胞衍生的5-羟色胺与肠道炎症
缺失5-HT再摄取转运蛋白(SERT)会延长和增强粘膜中5-HT的作用,加重TNBS诱导的结肠炎和IL-10缺失相关的结肠炎。这是因为肠细胞通常表达SERT,缺失SERT会放大肠嗜铬细胞释放的5-HT的作用。
增强5-HT的作用会增强炎症,表明5-HT具有促炎作用。实验证实,这种促炎作用依赖于肠嗜铬细胞分泌的5-HT,因为缺失TPH1(肠嗜铬细胞5-HT合成酶)可以保护肠道免受炎症。
肠嗜铬细胞分泌的5-HT可以刺激树突状细胞上的5-HT 7受体,启动先天免疫反应,最终导致适应性免疫反应和肠道炎症。免疫系统的许多效应细胞也表达5-HT受体并对5-HT有反应。
相反,缺失TPH2(神经元5-HT合成酶)会增加炎症的严重程度,表明神经元5-HT具有抗炎作用,可能通过保护ENS免受炎症的神经毒性作用。
因此,5-HT在肠道中可以同时发挥”剑”(促炎)和”盾”(抗炎)的作用,其平衡对肠道健康非常关键。肠嗜铬细胞分泌的5-HT在肠道炎症发生和发展中起关键作用。
血清素受体及其在胃肠道中的功能
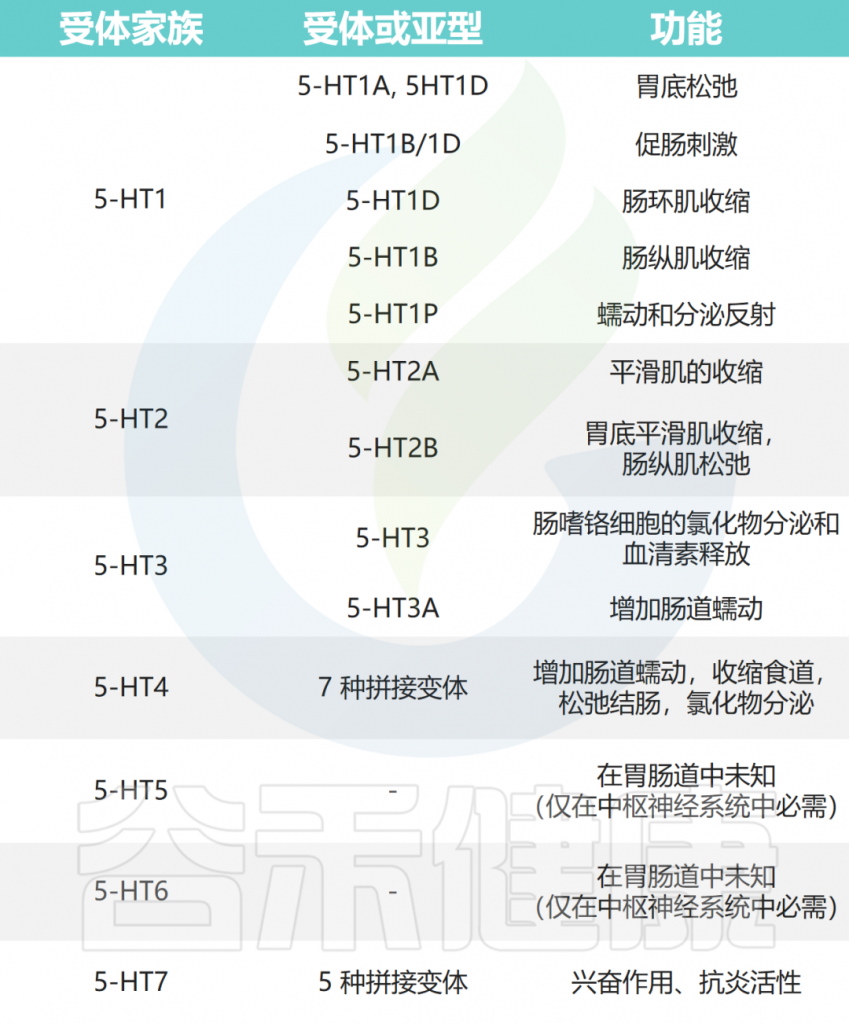
Guzel T and Mirowska-Guzel D.Molecules.2022
重点:血清素与肠脑轴
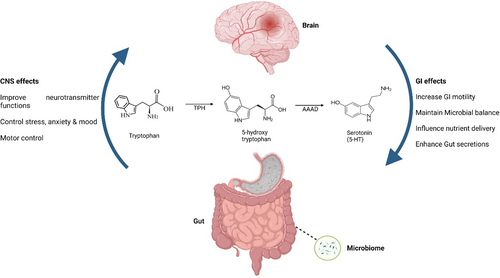
胃肠道和中枢神经系统通过称为脑肠轴的通讯途径连接。该路径允许信息双向流动。在这个网络的起点和终点,血清素作为神经递质发挥着关键作用
一项研究评估了Akkermansia muciniphila及其细胞外载体(EVs)对小鼠结肠和海马血清素能系统相关基因的影响,对Akkermansia muciniphila进行干预4周,观察结肠、海马和血清中的血清素水平通过ELISA测量小鼠以及人结肠癌细胞(Caco-2)的细胞活性。结果显示,通过肠-脑轴的血清素信号传导/代谢可能被考虑用于改善血清素相关疾病的新治疗策略。
在最近的一项研究中,衍生的齿双歧杆菌(B.dentium)已被用来调节哺乳动物的血清素能水平和肠脑轴,结果显示与齿状双歧杆菌相关的小鼠粪便中乙酸盐增加,研究结果表明齿状双歧杆菌和细菌代谢物乙酸盐是能够调节多个宿主组织中血清素能系统的关键组成部分,并与成人行为的功能变化相关。
下表显示了对益生菌补充剂通过肠-脑轴改善血清素信号传导的系统评价:

doi.org/10.1002/fsn3.3826
血清素被认为是一种重要的循环激素因子,它通过直接作用于心脏细胞或通过刺激心脏的化学敏感神经而与正常心血管功能有关。
类癌肿瘤患者血清素水平升高
类癌肿瘤(一种罕见的缓慢生长的癌症)患者心血管系统中的血清素活性水平升高,这与心律失常等某些症状有关,从而导致血流阻塞和瓣膜纤维增生。
类癌瘤又称类癌,是一组发生于胃肠道和其他器官嗜铬细胞的新生物,其临床、组织化学和生化特征可因其发生部位不同而异。此种肿瘤能分泌5-羟色胺(血清素)、激肽类、组织胺等生物学活性因子,引起血管运动障碍、胃肠症状、心脏和肺部病变等。
此外,据报道,暴露于显著升高的血清素水平(无论是由于高浓度的 5-HT 本身,还是用高水平的选择性血清素再摄取抑制剂 (SSRI) 处理)的小鼠胚胎在许多不同的部位都表现出异常生长。
血清素控制血管平滑肌的收缩
血清素被认为负责控制全身血管平滑肌细胞的收缩——这些肌肉细胞在整个循环系统中尤为突出,它们负责通过收缩或扩张血管来控制血流。据信,“S2”型血清素受体在这一功能中发挥着关键作用。
事实上,对血清素(5-HT)的一些最早的科学研究是由于它的血管收缩作用——通常直到后来它的其他生理和心理作用才变得明显。
例如,动物研究报告称,静脉注射血清素可以引起心血管系统的多种反应,导致血压升高或降低,具体取决于它在体内活跃的位置和时间。
血清素还可以通过其他“间接”机制来控制血压,例如通过放大其他血管活性物质(如NET、血管紧张素II和组胺)的反应。
血清素系统血清素(5-HT)是睡眠和清醒时大脑的关键调节剂/递质,中缝背侧(DR)和中缝(MR)是脑干的主要含5-HT核团,为前脑提供广泛的血清素能神经支配。这些中缝核涉及多种高阶功能,尤其是睡眠和意识。
血清素可用于调节睡眠和清醒
中缝背侧和中缝与脑干、下丘脑、视前区以及对清醒和睡眠至关重要的皮质结构具有相互联系。虽然血清素能DR/MR细胞的电生理学特性表明其在唤醒/觉醒中发挥作用,但血清素能传递的多样性(部分与5-HT受体的异质性相关)表明5-HT也可用于调节睡眠。
现在新出现的证据表明,5-HT DR 神经元是复杂神经回路的关键组成部分,其中(1)DR对前脑发挥兴奋作用,部分由来自外侧下丘脑的食欲素输入驱动;(2)DR在清醒时抑制腹外侧视前区(VLPO)的睡眠活跃神经元;(3)DR 与对睡眠压力做出反应的神经元相互作用,因此与腺苷一起,可以通过VLPO 神经元亚群的 5-HT 兴奋将生物体从清醒状态转变为NREM 状态;(4)DR/MR 在快速眼动(REM)睡眠中发挥着许可作用,因为它们在REM期间的虚拟沉默会抑制REM活跃神经元,从而触发REM睡眠状态。
血清素受体已在所有主要类型的骨细胞(成骨细胞、骨细胞和破骨细胞)中被发现。最近的数据表明,肠道来源的血清素可能介导低密度脂蛋白(LDL)受体相关蛋白的骨骼效应。
一些证据表明,使用SSRI(选择性血清素再摄取抑制剂)(可增加全身血清素水平)可能与骨量减少、骨质流失增加和骨折风险增加有关。
血清素过高会导致骨量减少、骨质流失增加
LRP5(LDL受体相关蛋白5)在成骨细胞和肠嗜铬细胞中表达,是Wnt信号的辅助受体。LRP5抑制肠嗜铬细胞中色氨酸羟化酶(TPH1)的表达,从而降低5-HT的分泌,导致血液和血小板中5-HT水平下降。
成骨细胞表达5-HT 1B受体,可直接响应循环中的5-HT,抑制成骨细胞增殖。因此,肠嗜铬细胞5-HT生物合成的降低,最终导致成骨细胞增殖增加,骨量增加。
而抑制肠道TPH1可增加骨量,说明使用不穿过血脑屏障的外周TPH抑制剂可能是一种治疗骨质疏松症的有效方法。
注:与外周5-HT的促骨作用不同,中枢5-HT通过抑制交感神经活动而抑制骨量增长。
总之,肠嗜铬细胞分泌的5-HT具有内分泌激素的作用,在调节骨代谢中发挥重要作用。这为开发新的治疗骨疾病的靶向药物提供了新思路。
除了对骨骼代谢的影响,肠嗜铬细胞分泌到血液中的5-HT还对肝脏再生产生作用。
在肝脏中,5-HT作为一种生长因子,可促进部分肝切除后的肝脏再生。肝脏再生的能力与血小板携带5-HT的数量直接相关。
血清素有助于推动肝脏再生
5-HT可激活肝细胞表面的5-HT2受体,从而促进肝细胞的增殖和DNA合成,推动肝脏再生。
缺乏色氨酸羟化酶1(TPH1)的小鼠,其肝脏再生能力受损,证实了肠嗜铬细胞来源的5-HT在这一过程中的关键作用。
总之,肠嗜铬细胞分泌的5-HT通过激活肝细胞上的受体,发挥了促进肝脏再生的内分泌功能。这为利用5-HT调节肝脏损伤后的再生提供了新的治疗思路。
禁食期间,内源性葡萄糖产生和脂肪分解增加,而葡萄糖摄取降低。这由激素(胰岛素、胰高血糖素等)和自主神经系统协调调节。
进食后,代谢转向合成代谢状态,胰岛素增加抑制内源性葡萄糖产生,促进肌肉和脂肪组织的葡萄糖摄取。
血清素可以提高胰岛素敏感性
下丘脑、脑干和皮质边缘区域参与葡萄糖感应,形成复杂的神经元网络,调节机体能量代谢。5-HT可通过中枢和外周机制影响葡萄糖代谢,包括调节胰岛素和胰高血糖素分泌。
5-HT1D和5-HT2A受体介导的作用可抑制胰高血糖素分泌,从而改善高血糖。5-HT可通过促进肌肉葡萄糖摄取和糖原合成来提高胰岛素敏感性。
此外,胰腺β细胞具有合成5-HT的机制,因为人类胰岛中存在编码关键酶色氨酸羟化酶(TPH)和芳香族氨基酸脱羧酶(AADC)的基因。
血清素会减少胰高血糖素分泌
5-HT1D和5-HT2A受体亚型也存在于胰腺α细胞中,表明5-HT在胰高血糖素分泌中发挥着额外作用。事实上,在人类胰岛中,研究表明5-HT会减少胰高血糖素分泌。
在体内,5-HT1D受体激动剂舒马普坦降低了人体胰高血糖素水平。从机制上讲,葡萄糖诱导邻近β细胞分泌5-HT,通过5-HT1F 受体降低α细胞中的环 AMP水平,并抑制胰高血糖素分泌。
与此一致,5-HT1F 受体的药理学激活减少了糖尿病小鼠的胰高血糖素分泌和血浆葡萄糖。据推测,α细胞的血清素控制受损可导致高胰高血糖素血症,从而导致高血糖。因此,5-HT1F 受体激动剂可能是治疗糖尿病等高血糖疾病的一种有前途的治疗方法。
5-羟色氨酸(5-HTP)被认为与主要饮食失调(例如厌食症)相关的许多心理和行为症状有关。由于这些原因,一些研究人员建议补充色氨酸可能有潜力治疗厌食症。
色氨酸是血清素的前体,也是一种只能在饮食中获得的必需氨基酸,因此,过度的饮食限制可能会导致大脑5-HT储存减少。血清素作用于多个大脑部位来调节进食行为,包括脑干中的多个核团、下丘脑亚区域(例如弓状核和室旁核)以及中皮质边缘多巴胺系统。
血清素调节饱腹感从而影响食欲
血清素和含下丘脑肽的细胞之间以及与缩胆囊素和其他肽之间存在重要的相互作用。血清素在行为水平上具有多种影响,其范围从调节短期饱腹感和饱足感以响应胃扩张和肠道营养素的存在,到调节奖赏和由条件线索引起的行为反应。
对血清素系统在控制食欲和摄食中的作用的大部分了解是从20世纪70年代到90年代初使用血清素释放剂和再摄取抑制剂芬氟拉明进行的研究中发展起来的,最初使用外消旋dl-芬氟拉明,后来使用更有效的异构体d-芬氟拉明。事实上,直到1997年,芬氟拉明因与瓣膜性心脏病相关而被撤回作为抗肥胖治疗药物,它一直是研究支持食物摄入和饱腹感的血清素机制的典型化合物。
d-芬氟拉明通过增加这些受体的5-HT可用性来间接减少食物消耗,而不是直接刺激突触后受体。然而,在大鼠中证明,d-芬氟拉明在服用一定剂量后仍然能够减少食物摄入量,并阻断 d-芬氟拉明增加下丘脑内侧区域 5-HT 传输的能力。这些发现清楚地表明d-芬氟拉明对5-HT受体有直接作用。
细胞外血清素水平升高通常会导致食物摄入量
减少,反之亦然
大脑中血清素能神经元的活动增强通常会导致食物摄入量减少和体重减轻,但也有其他研究报告了一些例外情况。据推测,大脑中5-HT容量传输通常会减少食物摄入量,因为一方面,5-HT水平升高会引起吞咽不足,另一方面,5-HT水平降低会导致食物摄入量增加,即食欲亢进。
事实上,通过脑血管内注射5,7-二羟色胺(血清素能神经元的神经毒素)或对氯苯丙氨酸(通过抑制5-羟色氨酸羟化酶减少5-HT合成)诱导的5-HT 水平降低,可诱导喂食大鼠的食欲亢进。
一些研究人员指出,某些神经元群释放到大脑中的血清素量似乎很大程度上取决于食物摄入量。这导致了这样的假设:血清素系统可能在食欲和饮食行为的调节中发挥着至关重要的作用——尽管这种潜在功能的确切性质尚不完全清楚。
在大脑中,自主神经和随意神经系统中的血清素能系统会导致饮食不足和过量。
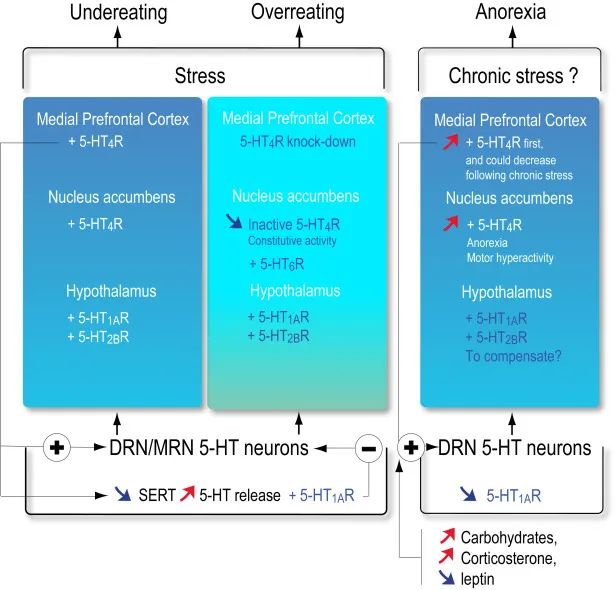
doi.org/10.1016/B978-0-444-64125-0.00028-1
药理学和遗传学之间的合作关系:特定血清素受体有助于减少和增加食物摄入量
大量药理学研究,无论是否结合使用 5-HTR KO 小鼠,收集的证据表明5-HT容量传输通常有助于减少食物摄入通过大脑特定区域的特定 5-HTR,破译了饮食行为的一些细胞内基础。
一些初步证据表明,碳水化合物的摄入尤其可能会影响血清素——可能是通过与胰岛素分泌相关的机制发挥作用。其他大量营养素,例如蛋白质,似乎没有这种作用,这表明这种作用可能特定于某些类型的营养素或食物。
血清素调节外周其他激素进而影响能量代谢
现在越来越多的证据表明外周血清素作为一种能够调节外周代谢的激素具有明显的作用。与经典的禁食激素胰高血糖素类似,由于肠道Tph1表达上调,循环 5-HT 因禁食而显著升高。禁食期间,5-HT 有效促进脂肪细胞的脂解作用,从而为肝糖异生提供底物,而5-HT也显著上调这一过程。
另一方面,肠道来源的5-HT还可以通过降低敏感性激素的激活,抑制白色脂肪组织的褐变和棕色脂肪组织的产热过程,从而有效地减少能量消耗。并减少负责产热的解偶联蛋白1的表达。因此,肠道来源的 5-HT 通过增加短期能量可用性和促进长期能量保存,在驱动对营养缺乏的多种生理适应方面发挥着关键作用。
矛盾的是,在肥胖条件下,循环5-HT水平也会升高。肥胖人类和啮齿动物高脂肪饮食后,循环和肠道来源的5-HT水平会升高。外周 5-HT 调节胰岛中葡萄糖刺激的胰岛素分泌,高脂饮食导致外周5-HT水平增加,通过肝脏中脂肪储存的增加导致肝脂肪变性。
肠道5-HT的药理学或遗传减少可预防饮食引起的肥胖、肝脂肪变性和葡萄糖不耐受,说明肠道来源的5-HT升高在驱动代谢功能障碍中的致病作用。在人类肥胖中,EC细胞的密度和TPH1的表达都会增加 ,但驱动这种变化的机制仍然未知。
先前的文献表明,5-HT及其受体升高可能作为一种有效的营养物质、促有丝分裂和抗凋亡因子,然而还可能促进致癌进展。文献进一步证明5-HT受体在许多癌症类型中表达,包括结直肠癌(CRC)、胰腺癌、肝细胞癌(HCC)、乳腺癌、肺癌和前列腺癌,它们促进肿瘤细胞的生长和存活。
多种肿瘤中血清素水平较高
较高的全身5-HT水平存在于多种肿瘤中,并且与肿瘤复发和不良生存密切相关 。肿瘤细胞和正常细胞对5-HT刺激有不同的反应。 5-HT促进CRC细胞增殖,但不增加正常结肠隐窝细胞的有丝分裂率。正常结肠隐窝的增殖受到自主神经和内分泌调节,而结肠癌细胞的分裂仅需要内分泌信号传导。
在人胆管癌组织中,TPH1表达增加和MAOA表达减少促进5-HT的分泌。通过抑制5-HT1A、2A、2B、4和6或TPH1可以特异性逆转分泌。
血清素水平会影响肿瘤血管生长
5-HT也是肿瘤血管生成中有效的血管生成因子。低浓度的5-HT在体外可诱导内皮细胞增殖、迁移和管形成,体内血管生成通过5-羟色胺受体依赖于TR3/Nur77,而与血管内皮生长因子A(VEGF-A)无关。人体内大部分5-HT储存在血小板中。在肿瘤微环境中,血小板聚集导致5-HT大量释放,促进肿瘤微血管的形成。
此外,5-HT阳性细胞的存在与较高的微血管密度和VEGF表达相关。在肿瘤发生过程中,肿瘤微环境中 VEGF(一种血管生成介质)的释放促进了血管生长的增加和异常血管重塑。
在TPH缺陷小鼠的结肠癌同种异体移植物中,与野生型小鼠相比,微血管密度降低。TPH 缺陷小鼠中 VEGF 和 VEGFR2 的表达相似,但基质金属蛋白酶12 (MMP-12) 和血管抑制素的表达较高。
MMP-12可以将纤溶酶原裂解成血管抑制素,血管抑制素是一种内源性血管生成抑制剂。小鼠的肺癌和黑色素瘤的同种异体移植物也比野生型小鼠小,这可能是由于eNOS浓度降低(导致血管舒张)以及肿瘤生长的血液补充不足所致。然而,有研究报道5-HT作为血管收缩剂,可以通过选择性地收缩肿瘤小动脉来抑制结肠癌的生长。
近年来,5-HT与肿瘤浸润免疫细胞之间的关系也被揭示。例如,5-HT通过激活5-HTR来抑制TNF-α和IL-1β的释放。在单核细胞/巨噬细胞中,5-HT调节细胞因子的分泌并介导中性粒细胞募集和T细胞激活。
与身体和大脑中的其他生物活性物质一样,血清素水平需要精心平衡,以维持整体健康的最佳状态。
但是人们常常错误地认为“更多”总是“更好”,而事实并非如此!举例来说,血清素水平升高可能导致血清素综合症,这是一种可能致命的严重疾病。
此外,血清素水平升高有时会使其他已有疾病(例如强迫症)的症状恶化。
血清素综合症是由于药物、补充剂或草药的组合导致血清素升高至不安全水平而引起的。它可能导致意识混乱、发烧、不自主的肌肉痉挛、癫痫发作甚至死亡。虽然有点罕见,但血清素综合症是一种严重的疾病,任何食用改变血清素水平的产品的人都应该意识到这一病症。
▸ 什么是血清素综合症?
当人的系统中血清素过多时,就会出现血清素综合症——无论是由于过量服用一种药物,还是由于组合使用多种药物来增加血清素水平。这可能非常危险,并会导致许多严重的并发症,从轻度(意识模糊、腹泻、颤抖)到严重(谵妄、癫痫发作、昏迷)。
尽管有些人可能更容易患血清素综合症,并且严重程度可能有所不同,但任何血清素水平升高的人都会出现症状。即使服用一剂改变血清素的药物也可能导致血清素综合征。
警告:血清素综合症是一种潜在的致命疾病,需要紧急治疗。如果您使用过精神活性药物/草药/补充剂并注意到下述任何症状,请尽快寻求医疗帮助。
▸ 症状
由于血清素会激活全身的许多受体,因此血液中过量的血清素会产生广泛的影响。这些症状从轻微到危及生命不等。
大脑中血清素过多会导致:
困惑
搅动
对刺激的敏感性增加(高度警惕)
焦躁不安
焦虑
发烧
对心脏和血管的影响包括:
心率过快
血压飙升
通过作用于肠道,过量的血清素会导致 :
腹泻
恶心
呕吐
它还可能导致:
出汗过多
肌肉痉挛或肌张力增加
瞳孔扩张
发抖
震颤(有节奏的颤抖)
危及生命的症状包括:
谵妄
代谢性酸中毒
横纹肌溶解症(肌肉组织分解,释放有毒蛋白质)
体温极高(超过41°C)
昏迷
血清素综合征最明显的症状可能是重复的、不自主的肌肉收缩。
♢症状会持续多久?
症状通常在服用改变体内血清素水平的药物后6至8小时出现,并且症状非常严重。如果治疗得当,轻微症状通常会在24-72小时内消失,但可持续长达3天。更严重的病例需要住院治疗,并且可能需要更长的时间才能康复。
♢长期影响
血清素综合征症状的持续时间完全取决于违规药物在您的系统中停留的时间。一旦治疗得当,一般不会产生长期影响。然而,如果不及时治疗,严重的血清素综合征可能会导致死亡。康复后,重新评估所有当前药物以防止血清素综合征再次发生非常重要。
▸ 血清素综合症的原因
影响血清素水平的多种药物和补充剂之间的相互作用是导致血清素综合征的最常见原因。
♢非处方药和处方药
1) 抗抑郁药和抗焦虑药
选择性5-羟色胺再摄取抑制剂(SSRI)、5-羟色胺-去甲肾上腺素再摄取抑制剂(SNRI)和三环类抗抑郁药(TCA)是治疗抑郁和焦虑的常用药物。它们通过延长大脑中血清素的活性来发挥作用。
最常与血清素综合征相关的抗抑郁药和抗焦虑药包括:
西酞普兰(Celexa)
艾司西酞普兰(Lexapro)
氟西汀(百忧解)
帕罗西汀(Paxil、Pexeva)
舍曲林(左洛复)
维拉佐酮(Viibryd)
氟伏沙明(Luvox)
文拉法辛(Effexor)
氯米帕明(Anafranil)
丙咪嗪(托法尼)
沃替西汀(Trintellix,Brintellix)
2) 单胺氧化酶抑制剂
单胺氧化酶抑制剂(MAOIs)是用于帮助治疗各种情绪障碍和帕金森病的药物。它们通过阻断单胺氧化酶发挥作用,单胺氧化酶会分解大脑中发现的几种神经递质,包括血清素。这会产生更多的血清素来作用于大脑。
滥用 MAOIs 或与其他增加血清素的药物联合使用可能会导致血清素综合征。这些包括但不限于:
司来吉兰
联非美烷
吗氯贝胺
吡林多(吡拉齐多)
托洛沙酮(胡莫酰)
利奈唑胺(Zyvox)
3) 抗生素
利奈唑胺是一种抗生素,常用于治疗对其他抗生素(如链球菌、VRE 和 MRSA)耐药的细菌感染。利奈唑胺还可以稍微阻断血清素的分解(通过阻断 MAO)。
4) 偏头痛药物(曲普坦类药物)
曲坦类药物通常是医生为中度至重度偏头痛患者开出的第一种药物。曲普坦类药物还会激活大脑中的血清素受体,并存在发生血清素综合征的风险,特别是与阿片类药物或抗抑郁药联合使用时。
他们包括:
阿莫曲坦(Axert)
那拉曲坦(Amerge)
利扎曲普坦(Maxalt)
舒马曲坦(Imitrex)
佐米曲普坦(佐米格)
5)阿片类药物
目前用于缓解疼痛的阿片类药物处方和阿片类药物滥用呈上升趋势。一些阿片类药物可以延长血清素的作用(通过阻止再摄取),从而导致大脑中产生更多的血清素。阿片类药物可引起血清素综合征,尤其是与其他改变血清素的药物联合使用时。
阿片类药物包括但不限于:
曲马多
哌替啶
美沙酮
芬太尼
吗啡
他喷他多
6) 丁螺环酮 (Buspar)
丁螺环酮通常用于改善焦虑,并与其他抗抑郁药联合治疗情绪障碍。它激活血清素受体。过量单独使用或与其他抗抑郁药联合使用可能会导致血清素中毒。
7) 治恶心药物
甲氧氯普胺 (Reglan) 通常用于治疗胃部问题,如胃灼热、恶心、呕吐和消化不良。据报道,有两例患者因联合服用甲氧氯普胺和抗抑郁药而导致血清素综合征。
任何与血清素受体相互作用的恶心药物都会增加血清素综合征的风险。示例包括:
格拉司琼(Kytril,Sancuso)
昂丹司琼(Zofran)
8) 右美沙芬
右美沙芬是一种止咳药,存在于许多非处方药中,例如 Robitussin、Delsym、NyQuil 和 Dimetapp。右美沙芬可以延长大脑中血清素的作用(阻止再摄取)。
在一份病例报告中,一名 63 岁的抑郁女性在服用右美沙芬-异丙嗪止咳糖浆与抗抑郁药艾司西酞普兰 (Lexapro) 组合两周后出现了血清素综合征 。
9) 过敏药物
在一项案例研究中,一名患者服用曲马多治疗颈部疼痛并联合苯海拉明治疗季节性过敏后出现血清素综合征。
♢草药和补品
1) 圣约翰草
圣约翰草是一种草药,几个世纪以来一直被用来治疗抑郁症,其疗效已得到临床证明。然而,圣约翰草可以与许多药物(包括 SSRI)产生负面相互作用,这些组合可能会导致血清素综合征。
2) S-腺苷-L-蛋氨酸 (SAM-e)
在多项试验中, SAMe改善了抑郁症状,也改善了对传统SSRI药物无反应的患者的抑郁症状。SAM- e可以显著提高血清素的产生,因此理论上,如果大剂量服用或与其他药物联合使用,可能会带来患血清素综合征的风险。
3) 人参
临床试验表明,人参可以降低更年期女性的抑郁症。它会增加大脑中的血清素(尤其是海马体),但是当大量服用或与影响血清素水平的其他药物联合使用时,会带来患血清素综合征的风险。
4) L-色氨酸
L-色氨酸直接增加血清素的产生。如果服用剂量过高,或与另一种增加血清素水平的药物(例如单胺氧化酶抑制剂,MAOI)联合使用,则存在发生血清素综合征的潜在风险。
♢食品
由食物引起的血清素综合症的可能性极小,因为以标准量摄入时,这些食物中的活性化合物含量相对较低。然而,重要的是要了解哪些食物有可能增加血清素水平,尤其是与血清素药物结合使用。
1)姜黄(姜黄素)
姜黄含有高含量的姜黄素,在临床试验中已被用于改善人类患者的情绪。在小鼠中,姜黄素会增加血清素水平,在服用其他增加血清素的药物时应谨慎使用。
2) 藏红花
在多项临床试验中,与服用SSRIs类似,藏红花可以减轻患者的抑郁症。对大鼠的研究表明,藏红花与血清素系统相互作用,因此它可能会影响血清素综合症 。
3)富含色氨酸的食物
当有血清素综合症的风险时,应避免食用色氨酸含量高的食物,因为色氨酸会直接增加血清素的产生。这些包括火鸡、鸡肉、大豆、鸡蛋、南瓜子、花生和一些奶酪。
一些精神疾病——例如抑郁症,与大脑中异常的血清素活动有关。由于这些联系,研究人员非常关注研究针对血清素系统的不同方法(通常是为了提高血清素的水平或整体活性)。
最著名和最广泛使用的抑郁症治疗方法之一,选择性血清素再摄取抑制剂(SSRI)可显著增加整个大脑的血清素水平(具体来说,通过防止神经元突触“清除”血清素,从而使其对整体大脑活动产生更持久、更强的影响)。
然而,SSRIs仍然有几个相当大的缺点。其一,许多抑郁症患者对此没有成功的反应。其次,即使对这些药物治疗有反应的患者,SSRIs 也经常会引起许多明显的副作用,包括恶心、皮肤反应、体重增加、睡眠障碍和性功能障碍。此外,来自动物研究的一些初步证据表明,长期使用 SSRI 可能会加重潜在的血清素缺乏症。
由于这些原因,一些人不愿意依赖药物治疗,而更愿意尝试非化学治疗。
在下面的部分中,我们将讨论一些已提出的可能增加血清素水平或活动的各种生活方式、饮食和基于补充剂的方法。然而,请记住,这些背后的科学大多仍处于初步阶段,并且这些生活方式策略或补充剂均未获得正式批准用于治疗抑郁症或任何其他精神或医疗状况。
这些只是补充方法,这意味着虽然它们可能有助于支持和增强传统治疗的有效性,但仅靠它们可能还不够。与往常一样,在采取本文讨论的任何“补充”策略之前,请务必先与你的医生讨论任何重大的生活方式、饮食或其他变化!
▸ 生活方式和行为因素
已经确定了几种可能影响大脑中血清素系统的行为方法和其他生活方式因素。
1)锻炼
锻炼对生理和心理健康有多种显着益处,包括提高血清素水平和对整体情绪产生积极影响。
例如,一些人类研究报告称,从事有氧运动会导致大脑血清素水平增加,并且如果保持良好的运动习惯,这种增加可能会持久。
如果可能的话,户外锻炼可能会更有益。例如,阳光照射与血清素水平升高有关,这反过来又可能转化为整体情绪的改善。
2)积极情绪诱导
一些证据表明,像听积极的音乐这样简单的事情,或参与其他愉快的经历,如在大自然中散步,可能会对大脑的血清素水平产生影响。
一项针对20名健康受试者的研究报告称,听愉快的音乐可以短期提高他们的血清素水平,并改善他们的情绪。此外,参加自然散步、冥想和按摩等有趣的活动都可能对血清素水平和整体情绪产生潜在的有益影响。
然而,值得注意的是,这些“情绪诱导”效应也可能产生相反的效果:例如,据报道,听“消极”或“不愉快”的音乐和其他刺激会降低人的情绪。
3)社交互动
一些证据还表明,积极的社交互动也可能对血清素水平和情绪产生潜在的有益影响。
例如,据报道,一个人经历的积极的面对面社交互动的数量与血清素水平有很强的相关性。
4)健康的睡眠习惯
毫不奇怪,睡眠对于大脑和整体心理健康非常重要。据报道,拥有健康且均衡的睡眠时间表对于维持整个大脑的血清素平衡非常重要。据信,造成这种情况的至少部分原因是大脑在睡眠期间产生并释放大量的血清素。
相反,睡眠不足会使血清素受体“脱敏”。反过来,这可能会扰乱大脑血清素系统的整体活动——睡眠不足甚至与抑郁症可能性增加有关。
▸ 饮食因素和补充剂
除了上述一些与生活方式相关的和其他“基于行为”的技术之外,研究人员还确定了许多饮食因素和基于补充剂的方法,它们也可能对一个人的血清素总体水平产生影响。
然而,值得注意的是,这些补充剂的功效仍然“没有足够的证据”,并且需要在健康人群中进行更多的后续研究来证实它们的效果。与往常一样,请务必先与您的医生讨论任何饮食改变或新的补充剂,因为这是避免与其他生活方式或健康相关因素发生任何潜在负面相互作用的最佳方法。
考虑到所有这些要点,研究表明以下一些补充剂可能有助于增加血清素并支持情绪平衡。
1) L-色氨酸和5-HTP
在体内,血清素是由5-HTP制成的,而5-HTP是由L-色氨酸制成的。因此,从理论上讲,增加这些“组成部分”(代谢前体)中的任何一个的水平都可以导致血清素总体水平的增加。
有限的研究表明,服用 L-色氨酸可能会提高血浆血清素水平,并可能改善缺乏血清素的人的某些认知、运动或肠道问题。
2)益生菌
在消化道中,益生菌恢复肠道微生物组并影响肠脑轴。肠道细菌的重要性之一是因为它们产生大量的色氨酸,而色氨酸是用来制造血清素的。一些研究表明,帕金森病等神经系统疾病与肠道细菌多样性较低或较少有关。
根据一项研究,据报道,为期8周的益生菌疗法(2.0×10^9 CFU/g瑞士乳杆菌和2.0×10^9 CFU/g长双歧杆菌)可增加110名抑郁症患者的色氨酸水平。理论上,增加色氨酸可以增加血清素的产生。
同样,一项动物研究报告称,给予大鼠14天的益生菌(婴儿双歧杆菌)可提高血液色氨酸水平。
3)维生素D
维生素D有助于身体(包括大脑)制造、释放和使用血清素。然而,补充剂的益处尚不确定。
维生素D会激活一种酶,将色氨酸转化为血清素。因此,增加维生素D的摄入量可能会增加血清素水平,从而有可能支持心理健康。
4) Omega-3 脂肪酸
虽然维生素D有助于神经元产生血清素,但omega-3多不饱和脂肪酸 EPA(二十碳五烯酸)、DHA(二十二碳六烯酸)和ALA(α-亚麻酸)可能有助于神经元释放血清素,并提高其整体活性(例如例如通过增加血清素受体的敏感性)。
在一项针对大鼠的动物研究中,低水平的omega-3脂肪酸——特别是α-亚麻酸(ALA)——与较低的血清素活性有关。相关地,DHA缺乏与仔猪大脑血清素水平降低有关。
在另一项动物研究中,几组怀孕的老鼠被喂食缺乏或富含α-亚麻酸的饮食。研究发现,与富含ALA饮食的大鼠相比,缺乏ALA饮食的大鼠前额叶皮层中的血清素水平降低了 65%,这进一步表明 omega-3 脂肪酸与血清素水平及整体健康之间存在潜在联系。
5) B族维生素
身体需要维生素B6来从其前体(例如5-HTP)产生血清素(具体而言,维生素B充当酶辅因子)。此外,维生素B12和叶酸(维生素B9)都是叶酸循环所必需的,叶酸循环有助于将色氨酸转化为血清素。
几种不同的B族维生素(包括B6、B9和B12)被认为对于血清素的产生和释放至关重要。在一些初步研究中,维生素缺乏症与认知结果不佳有关,尽管补充这些维生素是否对健康人类使用者具有直接的心理健康益处尚未完全确定。
6) 锌
根据一些早期研究,一些科学家认为锌可能靶向并激活血清素受体。根据对17项观察性研究数据的一项荟萃分析,据报道,与非抑郁个体相比,抑郁个体的血锌水平较低,这可能暗示了血清素相关机制。
另一项针对37名重度抑郁症患者的研究显示,连续12周每天补充25毫克锌可减轻抑郁症状。除了直接补充外,膳食锌还可以通过红肉、牡蛎、螃蟹、全谷物等几种常见食物获得。
7) 镁
研究人员推测,镁补充剂可能会通过增加大脑中血清素的可用性(减少再摄取)来提高血清素水平。
例如,根据一项初步研究,60名被诊断为轻度至中度抑郁症的患者每天补充500毫克镁(氯化镁)8周,可显著改善抑郁症状。据报道,这种镁治疗对焦虑症状也有显著的效果。
8) 肌醇
来自细胞和动物研究的一些早期证据表明,“类维生素”化合物肌醇可能会增加血清素受体的敏感性 。
由于其与大脑血清素系统的相互作用,一些研究人员提出,肌醇的作用可能类似于常见的血清素靶向抗抑郁药物(例如选择性血清素再摄取抑制剂 SSRI)。
根据一项针对30名患有经前综合症相关情绪障碍症状的女性的研究,据报道,在六个月经周期(约6个月)内使用肌醇治疗可减轻情绪症状并改善整体情绪。
虽然其中一些早期发现很有希望,但仍需要更多的研究来证实这些对人类的影响。
中枢血清素功能障碍与多种临床疾病的焦虑感、威胁感和不安全感增加有关。患有重度抑郁症和酒精依赖的患者中,焦虑与血清素转运蛋白可用性降低直接相关。由于威胁感和不安全感与特定性别的行为模式和荷尔蒙调节相互作用,冲动攻击可能是血清素能功能障碍的次要相关因素。在强迫症中,血清素周转率的增加而不是减少可能会干扰丘脑“噪声过滤器”和逆转学习期间的眶额功能,从而导致额-纹状体-丘脑神经回路过度激活和行为不灵活。
血清素功能障碍可能是由发育早期的社会压力因素引起的,并且似乎可以调节青少年和成年人以及非人类灵长类动物对压力和镇静药物。第一项表观遗传学研究表明,DNA 甲基化的改变可能导致五羟色胺转运蛋白基因(5-HTT) mRNA 转录减少,从而减少中枢血清素转运蛋白的表达。血清素系统的药物遗传学还需要考虑各种基因,尤其是 5-HTT、色氨酸羟化酶 2(TPH2)和A 型单胺氧化酶(MAO-A) 的基因,所有这些基因证明了功能上重要的多态性,并且发现或可能影响血清素的突触活性。这些超出了本章的范围,尽管读者需要记住它们与此处描述的血清素受体药物遗传学相互作用的潜力。
注意,血清素只是神经递质“单胺”家族的一员,该家族还包括其他主要神经递质,如去甲肾上腺素和多巴胺。研究人员目前认为所有这些神经递质共同作用来影响和调节情绪和神经疾病。
身体的所有细胞和器官,尤其是大脑,都受到血清素系统的影响。阳光的作用可能是帮助维持身心平衡。这与血清素参与人类体内平衡的观点是一致的并有助于心智的出现。
通过总结发现5-HT和其他系统建立的串扰对于每个系统都是特定的。这意味着药物作用机制的精确确定是极其复杂的,但它也代表了一个令人难以置信的来源,可以从中汲取灵感,为中枢神经系统疾病开发新的治疗策略。
主要参考文献:
Müller, C. P., & Cunningham, K. A. (Eds.). (2020). Handbook of the Behavioral Neurobiology of Serotonin. Volume 31.
Liu N, Sun S, Wang P, Sun Y, Hu Q, Wang X. The Mechanism of Secretion and Metabolism of Gut-Derived 5-Hydroxytryptamine. Int J Mol Sci. 2021 Jul 25;22(15):7931.
Li H, Wang P, Zhou Y, Zhao F, Gao X, Wu C, Wu T, Jiang L, Zhang D. Correlation between intestinal microbiotal imbalance and 5-HT metabolism, immune inflammation in chronic unpredictable mild stress male rats. Genes Brain Behav. 2022 Jul;21(6):e12806.
Kwon YH, Wang H, Denou E, Ghia JE, Rossi L, Fontes ME, Bernier SP, Shajib MS, Banskota S, Collins SM, Surette MG, Khan WI. Modulation of Gut Microbiota Composition by Serotonin Signaling Influences Intestinal Immune Response and Susceptibility to Colitis. Cell Mol Gastroenterol Hepatol. 2019;7(4):709-728.
Yano JM, Yu K, Donaldson GP, Shastri GG, Ann P, Ma L, Nagler CR, Ismagilov RF, Mazmanian SK, Hsiao EY. Indigenous bacteria from the gut microbiota regulate host serotonin biosynthesis. Cell. 2015 Apr 9;161(2):264-76.
Wu L, Ran L, Wu Y, Liang M, Zeng J, Ke F, Wang F, Yang J, Lao X, Liu L, Wang Q, Gao X. Oral Administration of 5-Hydroxytryptophan Restores Gut Microbiota Dysbiosis in a Mouse Model of Depression. Front Microbiol. 2022 Apr 28;13:864571.
Haq S, Wang H, Grondin J, Banskota S, Marshall JK, Khan II, Chauhan U, Cote F, Kwon YH, Philpott D, Brumell JH, Surette M, Steinberg GR, Khan WI. Disruption of autophagy by increased 5-HT alters gut microbiota and enhances susceptibility to experimental colitis and Crohn’s disease. Sci Adv. 2021 Nov 5;7(45):eabi6442.
Akram N, Faisal Z, Irfan R, Shah YA, Batool SA, Zahid T, Zulfiqar A, Fatima A, Jahan Q, Tariq H, Saeed F, Ahmed A, Asghar A, Ateeq H, Afzaal M, Khan MR. Exploring the serotonin-probiotics-gut health axis: A review of current evidence and potential mechanisms. Food Sci Nutr. 2023 Dec 7;12(2):694-706.
Guzel T and Mirowska-Guzel D. The Role of Serotonin Neurotransmission in Gastrointestinal Tract and Pharmacotherapy. Molecules. 2022 Mar 3;27(5):1680.
Kwon YH, Khan WI. Peripheral serotonin: cultivating companionship with gut microbiota in intestinal homeostasis. Am J Physiol Cell Physiol. 2022 Aug 1;323(2):C550-C555.