-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康
发酵食品被定义为“通过受控微生物生长以及通过酶作用转化食品成分而生产的食品或饮料。许多食物历史上都经历过发酵,包括肉和鱼、乳制品、蔬菜、大豆、其他豆类、谷物和水果。

发酵过程中存在多种变量,包括微生物、营养成分和环境条件,从而产生了数千种不同的发酵食品。历史上,食品发酵被用作一种保存方法,因为抗菌代谢物(例如有机酸、乙醇和细菌素)的产生降低了病原微生物污染的风险。
发酵还用于增强感官特性(例如,味道和质地),一些食物,例如橄榄,如果不经过发酵去除苦味酚类化合物,就无法食用。
近年来,发酵食品越来越受欢迎,发酵食品在世界上几乎所有文化的美食中都占有一席之地。发酵食品越来越受欢迎,主要原因包括发酵食品对健康的益处以及人们对胃肠健康的兴趣高涨。发酵食品可以通过多种机制对健康和疾病发挥有益作用。
首先,在肠道中,发酵食品所含的共生微生物主要通过与病原菌竞争资源,以及产生具有调节免疫和神经功能的发酵副产物来发挥其生理作用。
其次,发酵产生的代谢物可能对健康有益。例如,乳酸菌(与乳制品和非乳制品发酵食品相关)产生生物活性肽和多胺,对心血管、免疫和代谢健康具有潜在影响。
第三,发酵可以将某些化合物转化为生物活性代谢物。例如,乳酸菌可以将酚类化合物(如类黄酮)转化为具有生物活性的代谢物。
第四,发酵食品中的食品成分,如益生元和维生素,也可能对健康产生益处。
最后,发酵可以减少毒素和抗营养物质,例如,大豆发酵可以降低植酸浓度,酸面团发酵可以减少可发酵碳水化合物(例如,可发酵低聚糖、二糖、单糖和多元醇、FODMAP)的含量,这可能会增加肠易激综合征等功能性肠道疾病患者对这些产品的耐受性。
本文带大家一起了解发酵食物/食品的来源,方法,种类,包括的微生物以及对人体健康的益处和作用机制。
虽然人们已经食用发酵食品有数千年,在公元前 7000 年的陶器中,发现了有意应用发酵的最早证据,这些陶器用于发酵大米、蜂蜜和水果。但最近在了解肠道微生物组(肠道中细菌、病毒和真菌的组成)方面取得的进展,重新燃起了人们对发酵食品消费的兴趣。传统上,食品被发酵作为一种保存手段,用来提高保质期、食品安全性和可及性。
发酵还用于改善食物的消化耐受性、味道和质地。发酵食品在文化饮食模式中的突出地位和悠久的使用历史,让消费者和研究人员想知道发酵食品如何适应当前的饮食建议、个人应该多久食用它们以及有什么好处。
为了更好地了解它们的健康益处,首先了解发酵食品的构成非常重要。国际益生菌和益生元科学协会(ISAPP)专家共识将发酵食品和饮料定义为“通过所需的微生物生长和食品成分的酶促转化而制成的食品”。
尽管微生物对于发酵过程至关重要,但由于加热和加工的原因,微生物在食用时可能存在也可能不存在(下表)。
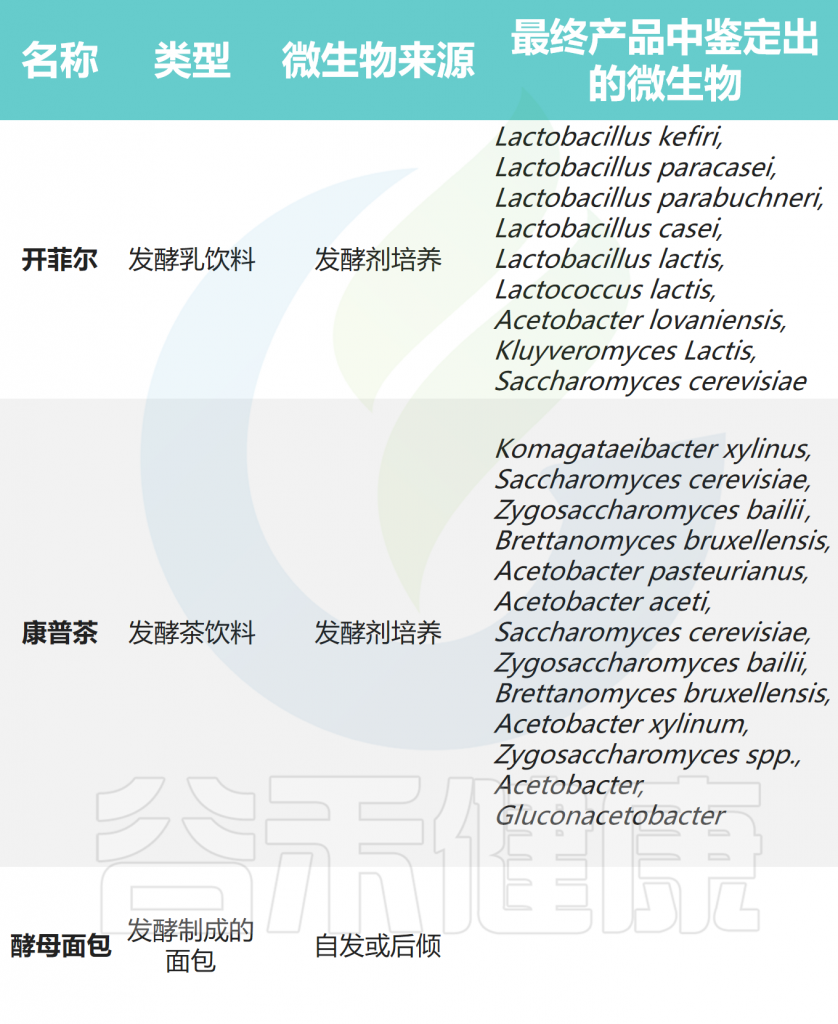


Dimidi E, et al., Nutrients. 2019
不是所有酸菜都是发酵食品
值得注意的是,一些食品需要发酵才能通过其通用名称来识别,例如酸奶;其他食品则可能不需要,例如,酸菜可以腌制或发酵,因此并非所有酸菜都是发酵食品。
注:腌制食品通常是通过浸泡制成的,不一定需要微生物或符合发酵食品的定义。
发酵食品和益生菌有什么区别?
发酵食品和饮料有时被定性或标记为“益生菌食品”或“含有益生菌”。然而:
由于以上这些原因,术语“发酵食品”和“益生菌”不能互换使用。
大多数发酵食品不符合益生菌的定义,因为它们的菌株尚未定义,并且不能保证在整个保质期内维持足够的菌落形成单位 (CFU)。
许多发酵食品含有具有益生菌潜力的细菌
这些细菌要么是在制造过程中添加的,要么是外来细菌,例如奶酪中发现的非发酵剂乳酸菌 (NSLAB),它们能够在发酵食品中生长和繁殖。
一般来说,大多数发酵产品含有足够多的微生物,其浓度根据产品的地区、年龄、消费时间等多个变量而变化。周围的食物基质似乎通过其针对肠道条件(例如低 pH 值、胆汁酸)的缓冲和保护作用,在益生菌菌株的存活中发挥着重要作用。
事实上,许多研究表明,发酵食品中的微生物可以到达胃肠道,这可能因产品而异。
发酵食品影响肠道微生物组的方式
食品发酵有两种主要方法
首先,食物可以自然发酵,通常被称为“野生发酵”或“自发发酵”,其中微生物天然存在于生食或加工环境中,例如酸菜、奶酪和某些发酵豆制品。
其次,食物可以通过添加发酵剂进行发酵,称为“依赖于培养物的发酵”,例如开菲尔、康普茶和纳豆。进行依赖于培养物的发酵的一种方法是“backslopping”,其中将少量先前发酵的批次添加到生食品中,例如酵母面包,用于启动发酵的发酵剂可以是天然的,也可以是精选的商业发酵剂,以标准化最终产品的感官特征。
注:backslopping是一种发酵过程中的一种方法,指的是将之前发酵批次中的一小部分加入到新的原始食物中,以启动新的发酵过程(有点类似于以前和面用的“醒子”)。
上面“野生发酵”或“自发发酵”利用空气中恰好存在的微生物或发酵原料上的微生物,而发酵剂则用于最初接种食物以启动发酵。在使用发酵剂时,微生物可能会经历产品标准化的选择过程。在研究发酵食品的健康益处时,由于生产方法而导致的食品成分和微生物的变化导致文献中存在显着的异质性。
发酵食品和饮料作为“功能性食品”的一部分,在传统和现代饮食中占有重要地位,对食物链价值有显著贡献,并具有额外的健康促进或疾病预防效果。
发酵过程及其与肠道健康的关联
发酵过程在无氧条件下将糖转化为有机酸、气体、醇和二氧化碳,带来多种益处,如新的口感和质地、营养增强、有毒或不良成分的去除、益生菌的传递以及食源性病原体的抑制。
发酵食品有助于提供益生菌,以维持健康的微生物群,对免疫系统和代谢功能影响显著。发酵食品的处理涉及人类、动物、环境、食品和微生物群之间的联系,这些联系影响食品的感官和理化特性以及人类健康。肠道控制并处理我们健康的各个方面,如消化方式、食物敏感性与情绪、行为、能量、体重、食欲、激素平衡和免疫力等均有关联。
营养与微生物群的协同效应
营养物质与微生物群的相互作用决定了整体健康。食用和饮用发酵食品和饮料,尤其是有机未削皮和未经巴氏消毒的水果和蔬菜,能提高食物生物活性成分的生物可及性和生物利用度,提供膳食纤维和必需的微量元素、植物化学物质以及酶、乳酸菌和有机酸,这些对健康至关重要。
发酵能增强各种食品的好处
包括乳制品、草药和饮料,影响它们次生代谢产物和化学元素的吸收和活性。尽管难以区分微生物内容和食物基质的潜在贡献,但消费者对发酵食品和饮料的健康益处有着明显的认知,这不仅仅是因为它们对胃肠功能障碍的影响,而且还与肠道微生物群、人类健康以及多种传染性、炎症性和肿瘤性疾病进程以及大脑功能有关。
发酵食品在精神健康和慢性疾病中扮演重要角色
尤其是与糖尿病和心血管疾病相关的肠道微生物组的变化。发酵和食物消化过程中产生的生理活性肽具有多种功能,能够作为促进健康的营养素配方。
尽管对于精神障碍的病因、分类和医疗护理存在分歧,但当前关于发酵食品、微生物组及其对人类健康影响的研究,特别是全球精神健康流行病,描述了与现代生活方式和高糖高饱和脂肪的西方饮食有关的问题。肠道黏膜的退化削弱了对有害物质入侵的紧密屏障,以及对无处不在的无害化合物的反应保护,是多种疾病的主要原因。
摄入活性益生菌,尤其是在发酵食品中,对平衡肠道通透性和屏障功能有显著积极改善,对代谢综合征、动脉粥样硬化、炎症性肠病和结肠癌有直接影响,并对抑郁、愤怒、焦虑和压力激素水平有间接影响。
酸奶与降低慢性疾病风险相关
酸奶是倍受认可的发酵食品之一。在流行病学研究中,饮用酸奶与降低 II 型糖尿病、心脏病和癌症的风险有关。此外,它还与改善骨骼健康和体重管理有关。
酸奶可提高乳糖不耐受者的乳糖消化率
牛奶发酵通过降低生产中的乳糖含量,以及通过活微生物表达 B-半乳糖苷酶的消化过程中的乳糖含量来提高乳糖的消化率。
虽然一些研究表明,饮用酸奶有助于减少抗生素相关性腹泻,但结果并不一致。虽然所有酸奶都是发酵的,但只有部分酸奶同时符合发酵食品和益生菌食品的标准,这意味着它们的菌株具有足够的特异性,具有治疗剂量,并且已针对特定的健康益处进行了研究。

酸奶可能含有特定的益生菌菌株,对身体有益处
这可以支持特定的治疗效果,包括改善便秘、减轻肠易激综合征 (IBS) 的症状,降低艰难梭菌 (C. difficile) 和抗生素相关性腹泻的发病率。值得注意的是,这些发现不能推广到酸奶本身,而是涉及到存在的益生菌菌株。除了乳糖消化不良和添加益生菌的酸奶具有特定菌株的治疗作用之外,支持饮用酸奶改善特定消化系统疾病的研究尚未阐明。
食用发酵牛奶、奶酪后对肠道菌群的影响
有八项研究分析了在食用发酵乳制品后的肠道菌群,包括发酵牛奶、酸奶和奶酪。发酵乳制品通常由乳酸菌(LAB)发酵,特别是嗜热链球菌(Streptococcus thermophilus)和乳杆菌属,此外还有双歧杆菌属。卡蒙贝尔奶酪还会使用明串珠菌属(Leuconostoc spp.)、Hafnia alvei、Geotrichum fungi 进行发酵。这些额外的奶酪发酵剂可能是导致其对肠道菌群影响多样化的原因。
食用酸奶对肠道菌群影响的研究
一项研究中,6名健康参与者连续6周食用酸奶,未发现与肠道细菌丰度存在任何统计学上显著的变化。
相反,也有报告显示,含有益生菌的酸奶进行4周干预,与对照组相比,能降低感染幽门螺杆菌儿童肠道大肠杆菌与双歧杆菌的比例(研究开始前1个月内使用抗生素为排除标准)。这种干预还降低了感染儿童体内的幽门螺杆菌,提高了血清IgA浓度,这为用酸奶治疗该感染提供了一条途径。
►
虽然测试的发酵乳和酸奶是用相似的细菌发酵的,但每种产品中特定的乳酸菌和乳酸菌的含量并不相同。这些差异可能是发酵奶和酸奶干预研究结果差异的原因。
为了进一步阐明食用酸奶产品的潜在益处,有必要开展更大样本量的研究,可能还需要开展干预时间更长的研究,来测试酸奶对肠道菌群的影响。
传统的开菲尔起源于高加索山脉,是一种具有奶油般质地、酸味和微妙气泡感的发酵乳饮料。通过向牛奶中添加一种名为“开菲尔粒”的发酵剂来生产开菲尔。
开菲尔粒由共生的乳糖发酵酵母(如Kluyveromyces marxianus)和非乳糖发酵酵母(如Saccharomyces cerevisiae、Saccharomyces unisporus),以及产乳酸和乙酸的细菌组成,它们位于称为开菲尔兰的多糖和蛋白质基质中。乳酸、风味生成成分(如乙醛)、乙醇和二氧化碳都是发酵的副产品,它们共同决定了开菲尔的感官特性。
在开菲尔粒中已经鉴定出多种微生物物种
常见的包括乳杆菌属:
链球菌属:
醋杆菌属:
酵母菌属:
假丝酵母菌属:
克鲁维酵母属:
乳杆菌科:
注: 如Leuconostoc mesenteroides 常见于蔬菜、乳制品和其他发酵食品中。它们在食品工业中扮演重要的角色,尤其是在发酵过程中,例如在制作泡菜、某些奶酪和腌制蔬菜等食品的过程中。这种细菌可以发酵糖类产生乳酸,有助于食品的保存和发酵过程中特定风味的形成。
它也能产生多种有益的代谢产物,如二乙酰(diacetyl),这是一种具有奶油味的化合物,常用于增强奶制品的风味。此外,这种细菌还能产生一种被称为白藜芦醇的多糖,这种物质具有良好的稳定剂和增稠剂特性,可以用于食品工业。
发酵过程中开菲尔的微生物组成可能会变化
例如,虽然在开菲尔粒的初级培养中L. kefiri并不是最主要的乳杆菌种类,但在最终发酵饮料中L. kefiri可以占所有乳杆菌种类的80%。
联合国粮食及农业组织(FAO)和世界卫生组织(WHO)建议开菲尔粒中至少应含有107个形成菌落单位(CFU)/克的微生物,最终产品中至少应含有10^4 CFU/克的酵母。
还有一种不含乳制品的开菲尔版本,称为水开菲尔,它是由水、糖和水开菲尔粒发酵而成的饮料,含有细菌和酵母,与传统开菲尔的发酵剂不同。

开菲尔抵抗病原菌,有益健康
多项体外研究已探究开菲尔的抗菌活性,这种活性归因于与病原体竞争可用营养物质,以及产生有机酸、细菌素、二氧化碳、过氧化氢、乙醇和乙酰乳酸等物质。
体外研究显示c对多种微生物如白色念珠菌、伤寒沙门氏菌、肠炎沙门氏菌、志贺氏菌、大肠杆菌、枯草杆菌、粪肠球菌和金黄色葡萄球菌表现出抗菌活性。
发酵衍生的生物活性肽已在动物模型中显示出刺激免疫系统的能力,而开菲兰则减少了小鼠哮喘模型中由卵清蛋白诱导的细胞因子产生。体外和动物研究还表明开菲尔可能具有抗氧化、降血压、抗癌以及降低胆固醇和血糖的潜在效果。
开菲尔有潜力在人类肠道中定植
多项体外、动物及人体研究已探讨开菲尔及其组成微生物对肠道菌群的影响。虽然尚未在体内得到证实,但从开菲尔中分离出的几种菌株已显示能够粘附于类人肠上皮Caco-2细胞,表明其有潜力在人类肠道中定植。
开菲尔或其组成菌株对肠道菌群有相当大影响
大量动物研究表明,它会增加乳杆菌、乳球菌和双歧杆菌的浓度,并降低变形菌和肠杆菌的浓度。此外,一项研究发现,与对照组相比,给予开菲尔乳杆菌(开菲尔乳杆菌本身不是开菲尔本身)(开菲尔谷物中常见的菌株)的小鼠体内,厚壁菌门、拟杆菌门和普雷沃氏菌浓度更高,粪便重量和粪便水分也更高。
食用开菲尔后,胃肠道中真菌丰度也会变化
一项针对高脂肪饮食诱导的肥胖小鼠模型的研究表明,与对照小鼠相比,摄入 0.2 mL 开菲尔的小鼠粪便总酵母菌和念珠菌随菲尔数量显着增加。
开菲尔在炎症性肠病中的应用
在人类中,一项针对 45 名炎症性肠病患者的研究表明,在每天摄入 800 毫升开菲尔的 4 周后,大多数参与者的粪便中都发现了一种开菲尔特有的菌株,即开菲尔乳杆菌,并且粪便中总乳酸杆菌丰度显着增加。与对照(无开菲尔)相比,克罗恩病患者发现了这一结果。
乳酸杆菌是一类益生菌,它们对维持肠道微生物平衡和促进肠道健康具有重要作用。这些菌株可以帮助改善肠道屏障功能,减少炎症,以及可能对免疫系统产生有益的调节效应。
在这项研究中,与未摄入开菲尔的对照组相比,克罗恩病患者在摄入开菲尔后的这些变化,可能表明开菲尔对改善他们的肠道微生物群和肠道健康有积极作用。这可能是由于开菲尔中的益生菌和发酵产物对肠道环境产生了积极影响。
开菲尔改善乳糖吸收不良
开菲尔对乳糖吸收不良的人具有良好的耐受性,因为它含有表达β-半乳糖苷酶的细菌(例如Kluyveromyces marxianus),可以水解乳糖,从而降低饮料中的乳糖浓度。
注:酵母全身是“宝”,无论酵母形式是农场生产的酵母醪糟,啤酒或白酒企业生产的酵母副产物,或专门生产用于饲喂动物的酵母产品。其中马克斯克鲁维酵母(Kluyveromyces marxianus)。这种酵母又叫“乳清酵母”,可以利用牛奶糖或乳糖作为底物,通过代谢过程将其分解,从而生长和繁殖。
这个特性使得Kluyveromyces marxianus特别适合用于乳制品工业的副产品,例如乳清。乳清含有乳糖和其他营养素,而乳清酵母可以将这些乳糖转化为酒精和二氧化碳(在发酵过程中),同时还能产生一些有益的副产品,如维生素和酶。
开菲尔含有比原味酸奶多 60% 的 β-半乳糖苷酶,而与未发酵奶相比,开菲尔的乳糖含量降低了 30% 。与牛奶相比,开菲尔还导致肠胃胀气严重程度显着降低,但肠胃气胀频率、腹痛和腹泻没有差异。总体而言,这项研究表明,对于乳糖吸收不良的人来说,食用开菲尔的胀气严重程度比牛奶低,并且与酸奶一样具有良好的耐受性。
开菲尔有助于根除幽门螺杆菌
另一项双盲随机对照试验研究了每天500毫升开菲尔与每天250毫升牛奶相比,在消化不良且幽门螺杆菌感染的患者中,对于配合2周三联抗生素疗法的幽门螺杆菌根除率的影响。研究发现:
这表明在治疗幽门螺杆菌感染期间,开菲尔可能是有益的辅助疗法。
然而,开菲尔研究的一个重要限制是每批可能包含不同的微生物。这可以解释一些异质性。需要进一步的高质量随机对照试验来确定开菲尔对肠道微生物群的影响及其对便秘等其他胃肠道疾病的影响。
开菲尔有助于改善便秘
几项非随机研究也探讨了开菲尔对便秘的影响。


doi: 10.3390/nu11081806
一项针对42名住院患者(这些患者有便秘问题以及精神和身体障碍)的非随机交叉研究显示,与对照组的粉状牛奶相比,6克冻干开菲尔对使用泻药的频率、大便的一致性和体积没有影响,然而在开菲尔干预12周后,不需要任何泻药的患者数量比基线时更高。
另一项小型非随机、无对照试验包括了20名功能性便秘患者,研究显示连续4周每天摄入500毫升开菲尔显著增加了大便频率,改善了肠道满意度评分,并且与基线相比,缩短了肠道传输时间。
考虑到样本小和研究设计的局限性(开菲尔的形式不同,没有随机化,无对照,验证程序的使用有限),需要进一步的高质量试验来确定开菲尔对便秘的影响。
康普茶(Kombucha) 是一种古老的发酵茶,康普茶距今已经有上千年的历史,起源于中国,后随丝绸之路引入亚洲和欧洲各国。
康普茶的发酵
传统的康普茶是通过细菌和酵母的组合对红茶(也可能使用绿茶)和白糖进行有氧发酵而生产的,称为细菌和酵母的共生培养物(SCOBY)。
酵母将蔗糖转化为乙醇(除了有机酸和二氧化碳),乙酸细菌将蔗糖转化为乙醛和乙酸。康普茶的微生物和代谢物组成根据 SCOBY 的具体组成、茶和糖的类型和浓度、氧气浓度、发酵时间、温度和储存时间而变化。

红茶菌的低pH值,主要是由于高浓度乙酸的产生,能够阻止幽门螺杆菌、大肠杆菌、鼠伤寒沙门氏菌和空肠弯曲菌等致病菌的生长。即使在中性pH值和经过热变性处理后,红茶菌在体外也能抑制病原体的生长,这表明除了乙酸以外的其他化合物也具有抗菌效果。
SCOBY是用于制作康普茶的一种共生菌群
它主要由乙酸细菌(例如乙酸杆菌属和葡萄糖酸杆菌属)、乳酸细菌(例如乳杆菌属和乳球菌属)以及酵母(例如酿酒酵母属Saccharomyces,和接合酵母属Zygosaccharomyces)组成。
高通量测序分析的研究表明,在康普茶发酵过程之后,假丝酵母属(Candida)和接合酵母属(Zygosaccharomyces)的酵母变得占主导地位,而在细菌中,则是酿酒酵母属(Komagataeibacter)、鱼腥藻属(Lyngbya)、葡萄糖酸杆菌属(Gluconobacter)、乳杆菌属和双歧杆菌属的数量最多。
在动物研究中:
康普茶对血糖水平、氧化应激、糖尿病引起的体重减轻、化学物质引发的肾脏毒性、高胆固醇血症、胃溃疡有影响。
研究假设在这些有益效果中起作用的化合物包括D-葡萄糖酸-1,4-内酯(DSL),这是在发酵过程中由葡萄糖酸杆菌产生的,在大鼠中它能够抑制氧化应激和糖尿病引起的肾损伤以及对乙酰氨基酚引起的肝损伤。尽管如此,目前还没有人类数据来证实这一作用机制。
茶中的多酚和黄酮类物质的含量会随着发酵的进行而增加。此外,康普茶发酵过程中,体外超氧阴离子清除能力、还原能力和总酚类化合物浓度也会增加。
虽然说康普茶是乙酸、乳酸菌和酵母的丰富来源,但目前还没有公开发表的研究探讨食用康普茶对动物或人类肠道微生物群落组成或功能的影响。有趣的是,康普茶在体外已显示出抗菌效果。
酸菜起源于中国,最早可以追溯到东汉,西周时期。酸菜是一种利用蔬菜经过发酵而制成的食品,可以延长保存时间并增加风味。酸菜在中国各地都有不同的制作方法和口味,是中国传统的发酵食品之一。
发酵酸菜的方法
古籍中记载的酸菜关于“酸菜”的形成历史。“请君伐菹薪,煮沸水为盐”;而《释名》中对“菹”的解释更为透彻,“菹,阻也。生酿之,遂使阻于寒温之闲,不得烂也”,这其实也写出了发酵酸菜的具体方法。

酸菜是最常见的腌制卷心菜形式之一,由切碎的卷心菜和2.3%至3.0%的盐混合制成的,然后让其自然发酵,通常涉及的菌种包括:
最终产品的低pH值使得卷心菜得以保存。
酸菜中的菌群
目前,通过培养依赖的技术,研究表明自制和商店购买的酸菜中含有多种细菌,一般包括:
当添加一种鼠李糖乳杆菌11MZ-5-1的启动培养物时,所制作的酸菜主要包含乳杆菌属和乳酸链球菌属(Lactococcus),这与自然发酵的酸菜相比,除了含有乳酸链球菌和乳杆菌外,自然发酵酸菜还含有显著数量的肠杆菌(Enterobacter)和假单胞菌(Pseudomonas),并且在微生物组成上更为多变。酸菜主要含有明串珠菌属和乳杆菌属。
从酸菜中分离出的某些乳杆菌种显示出益生菌潜力,它们能够耐受低pH环境,在Caco-2细胞上附着,并且在体外可以对抗病原体。常见于酸菜中的副干酪乳杆菌HD1.7(Lactobacillus paracasei HD1.7),能够产生一种广谱细菌素,这可能在酸菜的保存过程中发挥作用。
酸菜的健康益处,抗氧化,解毒,抗病原菌
在Wistar大鼠中口服酸菜汁导致谷胱甘肽S-转移酶(GST)、NAD(P)H:醌氧化还原酶1(NQO1)活性增加,这两种酶是肝脏和肾脏解毒过程中的关键酶。酸菜中含有的某些乳酸菌能够产生共轭亚油酸,关于共轭亚油酸,在动物实验中有证据表明它具有抗癌和抗动脉粥样硬化的活性。
从酸菜中分离出的植物乳杆菌P2(Lactobacillus plantarum P2)显著诱导TNF-α和IL-12的表达,并防止沙门氏菌肠炎亚种(Salmonella enteritidis)附着和侵入Caco-2细胞。
酸菜含有硫代葡萄糖苷分解产物,包括山奈酚(一种黄酮类化合物)、异硫氰酸酯、吲哚-3-甲醇、硫代甘蓝素、烯丙基腈和腈类化合物。尽管这些植物化学物质对人类健康的具体影响尚不明确,但山奈酚具有清除自由基的活性,能够保护机体免受氧化损伤,并在体外减轻细胞因子诱导的活性氧物种。
异硫氰酸酯已被证明具有抗菌特性,可以防止包括大肠杆菌、艰难梭菌、空肠弯曲菌(C. jejuni)和产气荚膜梭菌(C. perfringens)在内的多种物种的生长。
酸菜改善了肠易激综合征
酸菜是为数不多的几种发酵食品之一,其在功能性肠道疾病方面进行了临床试验。
一项随机双盲试验,比较了含有活性乳酸菌(LAB)的酸菜,对58名符合罗马III标准诊断的任何亚型肠易激综合症(IBS)患者的胃肠症状和微生物群的影响。
患者被随机分配每天食用75克的巴氏杀菌(对照)或未经巴氏杀菌(干预)含有LAB的酸菜,持续6周。在两个研究组中,从试验开始到结束,肠易激综合症严重性评分系统(IBS-SSS)得分都显著降低,但是饮食组之间的症状没有差异;
16S rRNA测序显示两个研究组之间或者在任一组的开始和结束时的微生物群组成没有差异。这可能表明,人们感知到的酸菜的健康益处与活微生物无关。这项研究的一个局限性是按方案分析,即只有完成研究的患者(n=34)被纳入主要结果的分析。此外,因为没有生卷心菜对照组,所以无法确定胃肠症状的改善是与发酵产物还是卷心菜本身有关。
酸菜可能与胃肠道癌症关联
在中国参与者中进行的另一项研究表明,大量食用酸菜实际上可能与胃肠癌症的不良健康结果有关。具体来说,这项病例对照研究显示,酸菜摄入量最高的人群与喉癌的风险增加有显著关联,比值比高达7.27。虽然这可能与酸菜中的高盐分有关,但在我国进行的另一项关于喉癌风险因素的研究并未发现与腌制蔬菜的摄入有关联。此外,酸菜中的高钾含量可能有助于抵消盐分可能引起的高血压效应。
尽管存在这些潜在的风险,一项试验发现,无论是经过巴氏杀菌处理的还是未经处理的酸菜,都能降低肠易激综合症(IBS)的严重程度,但这种效果似乎并非由改变胃肠道微生物群引起的。这意味着酸菜可能通过其他未知机制影响胃肠道症状。然而,目前关于酸菜对其他健康状况影响的证据还很有限。
最早已知的发酵大豆制品起源于中国和日本,包括发酵黑豆和腐乳。亚洲不同地区有许多发酵大豆制品,包括豆饼,豆豉(tempeh)、日本纳豆(natto)、日本味噌(miso)、中国腐乳(sufu)、豆腐乳(douche)、酱油以及韩国的豆瓣酱(doenjang)等。
豆 豉
豆豉是中国传统特色发酵豆制品调味料。豆豉(Glycine max)以黑豆或黄豆为主要原料,利用毛霉、曲霉或者细菌蛋白酶的作用,分解大豆蛋白质,达到一定程度时,用加盐、加酒、干燥等方法,抑制酶的活力,延缓发酵过程而制成。

在豆豉的制作过程中,主要的微生物包括:
豆豉霉(Aspergillus oryzae)或豆豉曲霉(Aspergillus sojae):这些霉菌负责初期的发酵过程,它们会分解大豆中的蛋白质和淀粉,产生一系列风味物质。
酵母:在发酵过程中,酵母也会参与作用,它们可以产生酒精和其他香气化合物。
乳酸菌:在某些豆豉的发酵过程中,乳酸菌可能会参与,有助于发酵过程的进行,并增加产品的酸味。
不同地区和不同生产商的豆豉可能会有所差异,微生物的种类和比例也可能会有所不同,这也是导致各种豆豉风味差异的原因之一。
豆 饼
豆饼是一种传统的印尼食品,通过在室温下用根霉Rhizopus oligoporus菌种发酵煮熟并去壳的大豆35-37小时来生产。这样可以制作出质地柔软、口感有嚼劲且带有类似蘑菇风味的白色豆饼。豆饼的微生物组成因生产工艺的不同而有所变化。
豆饼中含有乳酸菌、粪肠球菌,以及根霉属的丝状真菌(Rhizopus filamentous fungi)。研究表明,大豆的发酵能够降低蛋白酶抑制剂、植酸和酚类这些在生大豆中含量较高的抗营养因子,这可能与豆饼中根霉属表达的植酸酶有关。

在Sprague-Dawley大鼠中,与食用未发酵大豆的大鼠相比,补充豆饼后大鼠粪便中的拟杆菌门、厚壁菌门、艰难梭菌和脆弱拟杆菌的丰度增加。
在体外肠道模拟器模型中,应用大豆和豆饼对人类微生物群,可以增加双歧杆菌、乳酸杆菌、大肠杆菌和肠球菌的丰度。在一项对10名健康志愿者进行的开放标签非对照研究中,食用豆饼导致粪便中AKK菌的丰度和免疫球蛋白A浓度增加,这表明豆饼可能会影响人类的肠道微生物群。
在体外实验中,豆饼比未发酵的大豆显示出更强的自由基和超氧化物清除能,这可能与发酵后大豆中多酚含量和可消化性的变化有关。
但是迄今为止,关于豆饼消费对人类影响的随机对照试验(RCTs)还不存在。对人体的健康效果需要在人类试验中进行研究。
纳豆(Natto)
纳豆是一种传统的日本发酵大豆食品。纳豆是通过用枯草芽孢杆菌(一种益生菌)发酵煮熟的黄大豆制成的。这样制作出来的食品粘稠,有独特的风味和强烈的气味。
纳豆的特性根据大豆的蒸煮时间、相对湿度、发酵时间和温度而有所不同。纳豆发酵产生许多生物活性因子,包括纳豆激酶、杆菌肽酶F、维生素K2和吡啶二羧酸。
纳豆含槲皮素,对代谢、炎症、癌症预防有益
与未发酵的豆制品相比,纳豆中异黄酮槲皮素的含量更高,这些与代谢和炎症性疾病以及致癌预防有关。一种对肺炎链球菌和枯草芽孢杆菌具有抗菌活性的肽已从纳豆中分离出来,尽管尚未在人体中进行研究,但它在治疗肺炎链球菌感染方面具有潜在的临床重要性。
注:异黄酮类化合物是一类存在于豆类食物中的天然植物化学物质,具有类似于雌激素的生物活性,因此也被称为植物雌激素。
槲皮素(Genistein)是一种特定的异黄酮化合物,主要存在于大豆及其制品中。槲皮素因其多种生物学功能而受到关注,包括其抗氧化、抗炎、抗肿瘤的潜在效果,以及对骨密度和心血管健康的积极影响。

纳豆激酶由枯草芽孢杆菌变种产生。纳豆激酶除了增加组织纤溶酶原激活剂和减少血小板聚集外,还具有直接的体外和体内纤溶活性。纳豆激酶的抗血栓和抗高血压活性已在人体小型随机对照试验中得到证实。
食用含纳豆味噌汤:芽孢杆菌和双歧杆菌增加
关于纳豆对人类胃肠道微生物群影响的证据有限。关于纳豆对人类肠道微生物的影响,证据有限。有研究显示,8名健康志愿者连续两周食用含纳豆的味噌汤后,其粪便中的芽孢杆菌和双歧杆菌增加,而梭菌和肠杆菌科细菌减少。此外,粪便中的短链脂肪酸增加,氨和硫化物下降。然而,无法区分味噌汤(也是一种发酵大豆产品)的效应和纳豆的可能效应。
在每周排便3-5次的个体中,连续两周每天食用含有枯草芽孢杆菌K-2的50克纳豆,与每天食用50克煮豆相比,可以增加粪便频率和粪便中双歧杆菌的比例,尽管没有提供样本量。
味噌(Miso)
味噌是一种传统的日本发酵大豆酱,用于制作味噌汤。制作味噌的过程中,会用到一种名为“麴”的发酵剂,它是由霉菌Aspergillus oryzae(即麴菌)产生的,尽管有时也会使用酿酒酵母(Saccharomyces cerevisiae)和乳酸菌。与其他发酵大豆食品一样,味噌的生产在原料、温度和发酵时间、盐浓度以及使用的A. oryzae菌株方面都有很大差异。
味噌的微生物分析
对不同时间点的味噌进行微生物分析,发现在发酵过程中存在:
但在最终产品中只剩下枯草芽孢杆菌的细菌,关于枯草芽孢杆菌,详见:
此外,一系列味噌样本还含有乳球菌属的GM005菌株,它能产生一种具有强大抗菌活性的细菌素,能够抑制包括枯草芽孢杆菌、乳酸乳球菌(Pediococcus acidilactici)和植物乳杆菌在内的多种细菌的生长。
中国和日本的高大豆摄入量历史上一直被假设为相对较低的结肠癌和前列腺癌发病率的原因。支持这一假设的一个可能机制是在大豆中发现的异黄酮类化合物和大豆苷元的高浓度。异黄酮类在结构上与雌激素相似,可能通过与雌激素受体结合影响乳腺癌风险,这在体外实验中已得到证明。
进一步的体外研究表明,槲皮素可能通过促进细胞周期停滞、诱导凋亡和减少癌细胞迁移对癌症风险产生影响。如前面讨论过的,与未发酵的大豆制品如豆浆和豆腐相比,发酵大豆制品如味噌和纳豆中的槲皮素和大豆苷元含量可能更高。
味噌与癌症之间的关联,研究不一致
许多日本队列研究已经调查了味噌摄入量与癌症风险之间的关联。这些研究在饮食摄入评估(食物频率问卷,通常反应有限的摄入量)和可能存在的大量混杂因素方面是有限的。考虑到这些方法学局限性,队列研究观察到日本男性频繁摄入味噌汤与胃癌风险呈反向关联。相反,队列和病例对照研究显示频繁摄入味噌汤与日本成年人的单发和多发胃癌之间呈正相关。此外,一些队列研究显示味噌汤的摄入量与各种类型癌症的风险之间没有关联。
味噌对胃肠道疾病和肠道菌群的影响
目前还没有随机对照试验(RCTs)研究味噌对功能性肠道疾病的影响。因此,关于味噌对胃肠疾病和肠道菌群影响的证据是有限的。有几项观察性研究显示味噌的摄入与胃癌风险之间存在关联,然而这些关联的强度和方向仍然不明确。
酸菜、豆制品和泡菜对胃肠道健康和疾病影响的干预研究

doi: 10.3390/nu11081806
泡菜是一组腌制和发酵蔬菜的术语。它主要由大白菜或萝卜组成,并加入各种调味料(例如,辣椒、胡椒、大蒜、洋葱、生姜)、调味品(例如,盐、酱油、芝麻)以及其他辅助食材(例如,胡萝卜、苹果、梨、虾)。
泡菜的制作发酵
制作泡菜的过程中,首先将大白菜腌制并排水,然后添加剩余的调味品、香料和食品,与大白菜混合,最后进行发酵。发酵是由大白菜和混合物中食物自然存在的微生物发生的,尽管发酵剂培养物可用于泡菜的商业生产,但大白菜菜和混合物中天然存在的微生物会自发地进行发酵。
发酵前后的菌群变化
在发酵前,泡菜混合物中包含了来自明串珠菌属(Leuconostoc)、乳酸杆菌属(Lactobacillus)、假单胞菌属(Pseudomonas)、泛菌属(Pantoea)和魏斯氏菌属(Weissella)等多个不同细菌属的各种细菌物种。
然而,一旦开始发酵,细菌多样性就会下降,并在发酵后仅3天内迅速被明串珠菌属(Leuconostoc)主导。在这个属中,柠檬明串珠菌(Leuconostoc citreum)是发酵前最丰富的物种,但在发酵3天后其比例就很低,此时伴气明串珠菌(Leuconostoc gasicomitatum)和冷明串珠菌(Leuconostoc gelidum)变得占主导地位。
泡菜与其他食物的联合效应
由于泡菜可以包含各种各样的食材,其微生物组成会根据所含食物的类型和数量而有所不同。例如,当泡菜中含更多大蒜时,发现乳酸杆菌的浓度更高; 而添加红辣椒粉会导致魏斯氏菌(Weissella)比例增高,明串珠菌属和乳酸杆菌属比例降低。
一项动物研究显示,含有肠膜明串珠菌(Leuconostoc mesenteroides) DRC 0211的泡菜摄入可通过降低小鼠肝脏脂肪生成相关基因的mRNA表达和降低附睾脂肪组织中与炎症相关的单核细胞趋化蛋白-1和IL-6,展现出潜在的体重控制作用。
在大鼠身上,摄入由泡菜乳酸菌(Leuconostoc kimchi) GJ2发酵的泡菜后,血清总胆固醇、三酰甘油、低密度脂蛋白胆固醇水平以及动脉粥样硬化指数也显示出降低。
一项人体研究表明,摄入发酵8周的泡菜可导致与代谢途径和免疫相关的基因表达发生变化。在一种小鼠结肠炎模型中,从泡菜中分离出的嗜酸乳杆菌(Lactobacillus paracasei) LS2菌株可减少细胞因子产生、髓过氧化物酶活性以及固有层淋巴细胞中的巨噬细胞和中性粒细胞数量,提示其具有潜在的抗炎作用。

泡菜具有抗癌特性
一项体外研究显示泡菜可抑制胃癌细胞生长。值得注意的是,由于泡菜包含多种成分,其对肠道菌群和健康的影响被认为是其所含微生物以及食物制备过程中使用的食材营养成分(如植物化学物、纤维、维生素)的协同效应结果。例如,泡菜中的食物成分如红辣椒籽和大蒜也被认为具有抗菌和抗氧化效果。
小鼠实验:泡菜增加Adlercreutzia的比例
一项针对饮食诱导的肥胖小鼠模型的研究显示,从泡菜中分离出的植物乳杆菌(Lactobacillus plantarum) HAC01可以增加Adlercreutzia的比例,并降低拟杆菌属、Mucispirillum和瘤胃菌属(Ruminococcus)的比例,与对照组小鼠相比。
人体实验:泡菜增加乳杆菌,普雷沃氏菌属,明串珠菌,降低经黏液真杆菌属
在人体研究中,一项非随机对照研究纳入了6名韩国参与者,结果显示每天摄入300克泡菜4周,与每天摄入60克泡菜相比,可以增加粪便中的乳杆菌和明串珠菌的浓度,并降低粪便pH值。
其他几项非随机对照的人体研究也发现了类似的结果。在一项随机对照试验中,比较了24名肥胖女性摄入发酵泡菜和新鲜(未发酵)泡菜的影响,随机分配每天摄入180克发酵泡菜8周的女性显示,与基线相比,肠道核心菌属——经黏液真杆菌属(Blautia)的丰度降低,而普雷沃氏菌属(Prevotella)和拟杆菌属的丰度增加,但两组(发酵和未发酵泡菜)变形菌门和放线菌门的丰度都有所增加。
扩展阅读:
肠道核心菌属——经黏液真杆菌属(Blautia),炎症肥胖相关的潜力菌
不同成分的泡菜都增加产短链脂肪酸菌
另一项随机对照试验则比较了两种不同成分和数量制作的泡菜:
泡菜I 包含了白菜、萝卜、辣椒粉、大葱、大蒜、生姜、鳀鱼汁和糖;
而泡菜II 包含有机白菜、萝卜等多种成分,以及每克106个菌落形成单位的植物乳杆菌。
两组泡菜的摄入都导致产生短链脂肪酸的细菌,如粪肠球菌属(Faecalibacterium)、罗氏菌属(Roseburia)和考拉杆菌属(Phascolactobacterium)的丰度增加,同时降低了梭状芽孢杆菌属(Clostridium)和大肠杆菌(Escherichia coli)的丰度。
扩展阅读:
尽管没有直接比较两组泡菜的效果,但泡菜I被显示出与基线相比,放线菌门(Actinobacteria)的相对丰度增加,而变形菌门(Proteobacteria)的相对丰度减少。相比之下,泡菜II则产生了相反的效果,这表明泡菜中不同类型和数量的成分可能会以不同的方式影响肠道菌群。
酸面包发酵种是通过面粉中的乳酸菌和酵母发酵产生的,这些乳酸菌和酵母来源于面粉本身以及周围环境。
酸面包发酵
制作酸面包发酵种平均需要7天,过程中需要每天用新鲜面粉和水重新喂养微生物。一旦发酵种准备好,会取出一小部分加入酸面包的基本配料中,以启动酸面包的发酵过程——这种方法通常被称为“回种法”。与仅通过快速酵母发酵生产的标准面包不同,酸面包的共生发酵同时包含细菌和酵母,这被认为可以改善面包质量,包括质地、风味、营养含量和保质期,并且替代添加剂。
在发酵过程中,会发生微生物和酶引导的谷物碳水化合物、蛋白质、脂肪和酚类化合物的转化。微生物和酶的活性是相互关联的,例如,乳酸菌会导致pH值降低,调节谷物酶的活性和底物的溶解性(如麸质),反过来酶可以提供底物支持微生物的生长。

酵母发酵剂的微生物含量取决于所使用的传统做法,因此,最终产品的味道和质地以及营养成分都可能有很大差异。
酸面团发酵剂的微生物:乳杆菌常见
一般来说,酸面团发酵剂中已鉴定出乳杆菌属、明串珠菌属、魏斯氏菌属、片球菌属(Pediococcus)和链球菌属的几种菌种。
乳杆菌属是最常见的,而Lactobacillus sanfransiscensis是从大多数发酵剂中分离出来的关键细菌。酿酒酵母 (Saccharomyces cerevisiae)是最丰富的酵母菌种,其次是Candida milleri、 Candida humilis、小酒酵母 ( Saccharomyces exigious )和东方伊萨酵母 (Issatchenkia orientalis )。
酸面包带来健康益处,主要是通过其制作过程对面包营养成分的影响
例如,酸面团工艺可以降低面包中不可消化的低聚糖果聚糖和棉子糖(FODMAP 的类型)的含量,从而使 IBS 患者对面包的耐受性更好 。这种变化是由于酵母微生物,特别是如酿酒酵母和克鲁维酵母对寡糖的降解而发生的。
酸面团及其组成微生物也具有抗菌、抗高血压和降低胆固醇的特性,但这些都是基于体外研究,检查酸面团提取的细菌的影响,而不是烘烤的酸面团面包的影响。
酵母面包对肠道微生物群的影响:变形菌减少
与未发酵的面包相比,添加发酵 8 小时的酸面包后,健康对照样品中的双歧杆菌显着增加。与基线(接种前)相比,IBS 患者和健康捐赠者接种酵母面包发酵 8 小时后,δ-变形菌和 Gemmatimonadetes 显着减少。
此外,与未发酵面包和用酵母发酵16小时的面包相比,发酵8小时的酸面包在IBS样品接种15小时后产生的气体显着降低。作者认为这可能表明肠道微生物群发酵这种酵母面包的速度更慢。
然而,在体内,一项在20名健康成人中进行的随机交叉研究显示,每天摄入145克全麦酸面包1周,与每天摄入110克白小麦面包相比,在粪便微生物群组成上没有显著差异,整个两种面包干预期间,微生物群保持稳定。
酵母牛角面包:腹部不适、腹胀和恶心明显减轻
在一项双盲、交叉随机对照试验中,17 名健康成年人被随机分配吃一顿 2 个酵母牛角面包或 2 个啤酒酵母牛角面包,然后对胃排空进行磁共振成像分析。与啤酒酵母牛角面包相比,食用酵母牛角面包后胃总体积显着减少 11%,氢气产量显着减少 30%。腹部不适、腹胀和恶心明显减轻,表明酵母牛角面包比啤酒酵母牛角面包的耐受性更好。
此外,一项非常小的随机交叉试验包括7名报告轻微胃肠症状的参与者,结果显示食用酸面包黑麦面包后呼出的挥发性有机化合物(VOC)剖面与富含生物处理黑麦麸的小麦面包相比有显著不同,然而并未测量对胃肠症状的影响。这表明酸面包黑麦面包的潜在健康效果可能确实是通过肠道微生物群介导的。

编辑

doi: 10.3390/nu11081806
奶酪
奶酪的制作过程涉及到牛奶中的乳糖被乳酸菌等微生物发酵转化为乳酸的步骤。这个过程不仅使得奶酪产生独特的酸味,还有助于凝固奶蛋白,形成奶酪的固体结构。
在不同类型的奶酪生产中,可能会使用不同种类的发酵微生物,包括乳酸菌(如嗜热链球菌、乳酸乳球菌等)、霉菌(如青霉菌、白霉菌等)和其他发酵剂。
发酵橄榄
橄榄本身含有苦味物质,通常不能直接食用,需要通过发酵或其他处理方法来去除苦味并增加风味。
发酵橄榄的过程通常涉及将橄榄浸泡在盐水溶液中,有时还会添加其他调味料,如香料、柠檬酸、醋等。在这个环境中,有益的乳酸菌会繁殖并开始发酵过程,这些微生物会消耗橄榄中的糖分,产生乳酸,从而降低溶液的pH值。这个酸性环境有助于防止有害微生物的生长,并且随着发酵的进行,橄榄的苦味会逐渐减少,风味也会得到改善。

发酵橄榄的过程可能需要几周到几个月的时间,取决于所使用的具体方法和所需达到的风味强度。这个过程不仅增加了橄榄的可食性和风味,还提高了其保质期。发酵完成后的橄榄可以作为小吃、沙拉配料、披萨配料或其他菜肴的一部分来食用。
发酵辣酱
发酵辣酱是一种发酵食品。发酵辣酱的制作过程通常涉及将辣椒与盐混合,有时还会加入其他成分,如蒜、姜、蔬菜等。这些原料混合后会放置在适当的条件下进行自然发酵或控制发酵。这些是益生菌的良好来源。
在发酵过程中,盐水溶液(盐溶于辣椒释放的水分中)为乳酸菌等有益微生物提供了生长环境。这些微生物会消耗混合物中的糖分,产生乳酸,从而降低辣酱的pH值,形成酸性环境。这个环境有助于抑制有害微生物的生长,并且使辣酱具有独特的酸味和复杂的风味。
鱼露
鱼露是东亚和东南亚美食中的主食,是一种由发酵小鱼(通常是凤尾鱼)和盐制成的调味液,所得酱汁是咸鱼的液体副产品。在发酵过程中,鱼类和盐的混合物会自然分解,其中的蛋白质被酶和微生物分解成氨基酸,产生独特的强烈风味和鲜味。这个过程中产生的液体就是鱼露,它通常具有咸味和鱼的鲜味,是许多东南亚菜肴不可或缺的风味增强剂。鱼可以发酵几个月或长达几年,发酵过程中会出现活细菌,除非鱼露经过巴氏灭菌。
醋
醋是一种通过发酵过程制成的食品。醋的生产通常涉及两个基本的发酵步骤:

不同类型的醋使用不同的原料和发酵方法。例如,白醋通常由谷物酒精发酵而成,苹果醋来自苹果或苹果汁,而葡萄酒醋则是由葡萄酒发酵制成。每种醋都有独特的风味特点,这些特点取决于原料、发酵过程、成熟时间以及是否有其他调味成分的添加。
生姜啤酒
传统酿造生姜或根汁啤酒的制备方法与康普茶类似;酵母和乳酸菌的共生菌落有助于将生姜、糖和水发酵成美味的碳酸饮料。
生姜作为缓解消化不良的天然家庭疗法已经被世世代代使用,并且由于现代科学研究,我们现在知道生姜具有多种治疗作用。生姜含有抗氧化、抗炎和免疫支持化合物。
发酵啤酒的制作过程涉及到使用特定的微生物——酵母,来将麦芽中的糖分转化为酒精和二氧化碳。酵母是一种单细胞真菌,能够进行有氧或厌氧代谢。在啤酒的发酵过程中,酵母主要进行的是厌氧代谢,即酒精发酵。
因此,这种富含益生菌的饮料可能是比其他替代甜碳酸饮料更好的选择。话虽如此,需要知道即使是姜汁啤酒也可能含有多余的糖分。
客观的说,发酵食品的健康益处目前还是常常被夸大了。虽然发酵食品确实与健康益处有关,但是其他像治疗“渗漏性肠炎”或替代抗生素疗法的声明却缺乏足够的证据。
发酵食品确定的健康益处
包括:食品保存、提高营养的生物利用度、改善消化耐受性。利用发酵作为食品保存的手段可以提高食品安全性、可获得性,并保留营养成分。
通过发酵过程,食物成分的转化还可以通过降低抗营养因子(如植酸和单宁)的含量来提高营养的生物利用度。通过降低这些抗营养因子的含量,钙、铁和镁等微量元素的生物利用度就会提高。
发酵食品微生物的短暂性
当前的研究表明,来自发酵食品的微生物是短暂存在的。个体的微生物组已经建立并且对于定植有抵抗力;没有可以定植的生态位,因此它们的益处是可能短暂的。由于这些微生物的短暂性,我们可以推断,发酵食品的益处也可能只在个体食用的期间存在。
通常食用发酵食品的影响是短暂的,但某些影响,例如微生物群组成变化,可能会持续存在
活菌的摄入与肠道菌群和免疫系统积极互动,抑制病原菌,降低疾病风险
许多流行病学研究表明,随着发酵食品摄入量的增加,慢性疾病(如糖尿病和心血管疾病)的患病风险往往会降低。目前的理论是活菌的摄入会与我们自身的肠道微生物和先天免疫系统产生积极互动,有助于抑制病原菌的生长,并提供发酵代谢产物,从而对我们的健康有益。虽然一些益处已经被广泛研究,但其他一些益处更多是理论假设,还需要进一步的研究证实。
发酵食品摄入量逐步增加:炎症细胞因子下降,菌群多样性提高
一个最近的研究探讨了总体发酵食品摄入量对人体免疫系统的调节作用。该随机前瞻性研究纳入36名患者,要么接受高纤维饮食,要么增加发酵食品的摄入。研究监测了患者干预前3周的状况,然后进行为期4周的“逐步增加”阶段,参与者逐步增加高纤维或高发酵食品的饮食,维持6周饮食,以及4周的“自选饮食”,参与者在这期间根据自己的意愿维持饮食。
研究人员发现,在发酵食品组中,每天摄入约6份发酵食品的人(基线时每天仅摄入0.4份发酵食品)的炎症性细胞因子有所下降。
此外,随着发酵食品摄入量的增加,微生物多样性也有所提高。这是首个评估总体发酵食品摄入量及其对免疫功能影响的研究。虽然还需要进一步研究,但它开始探索膳食建议如何转变为包含总体发酵食品目标,以积极影响人类健康。
在世界各地,每种文化都有其独特的食品文化和传统,其中包括发酵食品。在发展中国家,生活在贫困中的人们的主要优先事项并非食品卫生、安全和营养因素,他们消费的食物中可能含有化学、微生物、人畜共患病以及其他危害,可能对健康构成风险。
非洲:大量食用乳酸发酵产品的地方,精神障碍和抑郁症的率比较低
非洲的传统发酵食品和饮料自古以来就被使用,整个大陆上有多种多样的发酵食品和饮料,主要是酸性粥和饮料。
在发展环境中,乳酸发酵和酒精发酵是最受欢迎的发酵类型,约80%的人口仍然寻求传统医治者的帮助,他们会开具本土产品。
在非洲,大量食用乳酸发酵产品的地方,精神障碍和抑郁症的率比较低,但疾病的发生率并不低于发达社会,除了饮食以外还有其他可能加剧疾病的因素,如社会经济变化、城市化、饮食习惯的改变,以及最近青年中的久坐行为。
撒哈拉以南非洲的人民常常遭受内战、干旱、洪水、饥荒和疾病的困扰,但拥有巨大的植物和草药生物多样性,他们倾向于依赖传统医治者,后者通常将精神疾病解释为附身或诅咒,并通过仪式以及推荐传统植物、草药、发酵食品和饮料来处理精神健康问题。
非洲的许多农村社区完全依赖传统发酵食品作为营养的主要来源
同时也用于文化传统实践。在莫桑比克和津巴布韦,传统发酵食品用于四个月大的婴儿断奶。最常见的发酵食品是mahewu,这是一种传统的、发酵的、麦芽的、酸的、非酒精性的玉米或木薯稀粥,酸奶和酸粥。
坦桑尼亚的发酵糊状食品togwa,可以在卫生条件较差的地区防止食源性疾病。但每个人在需求和营养上都是独一无二的。我们大多数人在想到过敏时只会想到组胺,但实际上作为潜在益生菌来源的本土发酵食品和饮料对一些人可能有治疗作用,而其他人可能对组胺不耐受,因为没有无组胺饮食,而这种胺在身体中有许多功能,自然发生,是中枢神经系统中的一种神经递质。
在非洲,水果和蔬菜由于其高水活性和营养价值而容易腐烂。这一现象在热带和亚热带国家更为严重,这些国家的气候有利于腐败微生物的生长。在非洲、亚洲和拉丁美洲的发展环境中,可能对益生菌和发酵食品的需求最大,因此许多发酵果蔬食品被开发出来。
食品发酵的主要目的是增加食品或饮料的保质期,并因此提高其安全性以供消费。发酵通过多种方式达到这个目的,包括通过产生有机酸来降低水分活性和pH值。
用于发酵的微生物是非致病性的,被认为是安全的。尽管对大多数人来说是安全的,但应该注意,发酵的一些副产品可能对健康产生负面影响,最值得注意的是酒精和生物胺。例如组胺和酪胺等生物胺的产生,可能对被诊断有肥大细胞疾病的患者或正在使用单胺氧化酶抑制剂(MAOIs)的患者产生负面影响。
通过发酵,氨基酸被脱羧释放出生物胺,这些生物胺在发酵的肉类和鱼类产品、奶酪、葡萄酒和啤酒中含量较高。对于那些服用单胺氧化酶抑制剂的人来说,限制生物胺和发酵食品的摄入可能是明智的,对于那些有组胺不耐症或肥大细胞激活症的人来说,这样做可能也有帮助。
发酵是一种古老的实践,用于保存食物和饮料,以提供更好的口味,改善营养和食品安全,有机保存食品,并促进健康属性。
食物和饮料的发酵可以改善产品的储存时间、安全性、功能性、感官品质和营养品质。发酵不仅有助于延长货架寿命,还可以安全有效地增强营养属性。
多种食物包括乳制品、蔬菜、豆类、谷物、淀粉根类和水果以及肉类和鱼类,都可以发酵。
在某些人群中,发酵食品和饮料可能占人类饮食的5-40%。
肠道微生物群可能会接触到多种逃避肠道消化的饮食成分,并可能受到植物化学物的影响。植物化学物质是存在于水果、蔬菜、全谷物、豆类、豆科植物、草药、香料、坚果和种子中的非营养性天然化学物,负责产生生理属性,并保护植物作物免受各种环境压力的侵害。
关于发酵食品和饮料与益生菌概念之间存在相当的混淆,重要的是要澄清发酵食品并不等同于益生菌的常见误解。尽管发酵食品可能包含益生菌,但它们的活性微生物含量是未定义的。
益生菌能够通过有益微生物更新、修复和生长消化道内衬组织,中和有害微生物。有用的活性微生物能够正确发酵我们的食物,从而改善我们的健康。尽管发酵食品和饮料对胃肠健康和疾病有影响,但它们的健康益处或推荐消费量尚未广泛纳入全球食品指南。
当发酵食品和饮料补充了益生菌细菌时,它们提供了许多额外的营养和健康特性。发酵食品和饮料比以往任何时候都更受欢迎,而对其健康益处的研究相对较新。并非所有发酵食品都含有活性微生物;例如,啤酒和葡萄酒在生产过程中经历了去除微生物的步骤,其他如面包的发酵食品则经过热处理,微生物被灭活。

目前消费者越来越频繁问到 “我应该食用发酵食品吗,或食用哪些发酵食物比较好?”或者遇到试图利用发酵食品来治疗他们消化症状的患者。
发酵食品通常被认为对健康有益,特别是对肠道健康。但是正如前面上面提到的,目前关于发酵食品对胃肠道健康有效性的科学证据仍然有限,且研究质量参差不齐。因此,当推荐消费者食用发酵食品时,应该提供以下建议:
逐量添加:如果消费者不习惯食用发酵食品,建议他们逐渐添加到饮食中。这样可以帮助肠道微生物群逐步适应,并减少可能出现的消化不适,如胀气或腹泻。
个体化选择:由于每个人的身体和健康状况不同,建议消费者选择适合自己的发酵食品。例如,乳糖不耐受的人可能需要避免含乳糖的发酵乳制品,转而选择非乳制的发酵食品,如泡菜或豆豉。
了解发酵食品:不同的发酵食品具有不同的营养和健康益处。例如,酸奶和开菲尔富含益生菌,有助于维持肠道微生物平衡;泡菜和酸菜含有丰富的维生素C和纤维,可以促进消化;而味噌和天然酿造的酱油则提供了丰富的氨基酸。
注意食品来源:推荐消费者选择自然发酵且未经高度加工的食品,这些食品更有可能含有活性的益生菌。选择未经过度加工和含有活性微生物的发酵食品。市场上的一些产品可能经过巴氏杀菌处理,这会杀死有益的微生物。因此,查看标签并选择含有“活性微生物”或“活性益生菌”的产品。
监测身体反应:建议消费者在尝试新的发酵食品时,留意身体的反应。如果发现消化不适或其他不良反应,应该减少摄入量或停止食用,并咨询医生。
谨慎治疗性使用:如果消费者试图通过食用发酵食品来治疗消化症状,应该提醒这种做法的证据基础不足。鼓励寻求专业医疗建议,并将发酵食品作为整体治疗计划的一部分,而不是唯一的治疗手段。
整体饮食模式:发酵食品应该作为均衡饮食的一部分。确保饮食中还包含了丰富的蔬菜、水果、全谷物、蛋白质和健康脂肪,以支持整体健康。
通过这些建议,可以更好地将发酵食品融入你的饮食中,同时确保这些食品对自己的健康带来积极的影响。
主要参考文献
Dimidi E, Cox SR, Rossi M, Whelan K. Fermented Foods: Definitions and Characteristics, Impact on the Gut Microbiota and Effects on Gastrointestinal Health and Disease. Nutrients. 2019 Aug 5;11(8):1806.
Leeuwendaal NK, Stanton C, O’Toole PW, Beresford TP. Fermented Foods, Health and the Gut Microbiome. Nutrients. 2022 Apr 6;14(7):1527.
Marco ML, Sanders ME, Gänzle M, et al. The International Scientific Association for Probiotics and Prebiotics (ISAPP) consensus statement on fermented foods. Nature Reviews Gastroenterology & Hepatology. 2021;18(3):196-208.
Dimidi E, Cox SR, Rossi M, Whelan K. Fermented foods: definitions and characteristics, impact on the gut microbiota and effects on gastrointestinal health and disease. Nutrients. 2019;11(8):1806.
Rul F, Béra-Maillet C, Champomier-Vergès M, et al. Underlying evidence for the health benefits of fermented foods in humans. Food & Function. 2022;13(9):4804-4824.
Wastyk HC, Fragiadakis GK, Perelman D, et al. Gutmicrobiota-targeted diets modulate human immune status. Cell. 2021;184(16):4137-4153.
Gardini F, Özogul Y, Suzzi G, Tabanelli G, Özogul F. Technological factors affecting biogenic amine content in foods: A review. Frontiers in microbiology. 2016;7:1218.
Maintz L, Novak N. Histamine and histamine intolerance. The American journal of clinical nutrition. 2007;85(5):11851196.
Weinstock LB, Pace LA, Rezaie A, Afrin LB, Molderings GJ. Mast cell activation syndrome: a primer for the gastroenterologist. Digestive Diseases and Sciences. 2021;66(4):965982.
Savaiano DA, Hutkins RW. Yogurt, cultured fermented milk, and health: A systematic review. Nutrition reviews. 2021;79(5):599-614.
Patro-Golab B, Shamir R, Szajewska H. Yogurt for treating antibiotic-associated diarrhea: systematic review and metaanalysis. Nutrition. 2015;31(6):796-800.
Skokovic-Sunjic D. Clinical Guide to Probiotic Products Available in Canada. probioticchart.ca. Accessed September 14, 2022.
Turan İ, Dedeli O, Bor S, İlter T. Effects of a kefir supplement on symptoms, colonic transit, and bowel satisfaction score in patients with chronic constipation: a pilot study. Turk J Gastroenterol. 2014;25(6):650-656.
Bekar O, Yilmaz Y, Gulten M. Kefir improves the efficacy and tolerability of triple therapy in eradicating Helicobacter pylori. Journal of medicinal food. 2011;14(4):344-347.
Nielsen ES, Garnås E, Jensen KJ, et al. Lacto-fermented sauerkraut improves symptoms in IBS patients independent of product pasteurisation–a pilot study. Food & function. 2018;9(10):5323-5335.
Fujisawa T, Shinohara K, Kishimoto Y, Terada A. Effect of miso soup containing Natto on the composition and metabolic activity of the human faecal flora. Microbial ecology in health and disease. 2006;18(2):79-84.
Altobelli E, Del Negro V, Angeletti PM, Latella G. LowFODMAP diet improves irritable bowel syndrome symptoms: a meta-analysis. Nutrients. 2017;9(9):940.
Loponen J, Gänzle MG. Use of sourdough in low FODMAP baking. Foods. 2018;7(7):96.

谷禾健康

俗话说病从口入,饮食对人体具有重要的影响,蔬菜和水果作为每日饮食中必不可少的成分,为人类提供了重要的营养物质,包括各种必需的维生素和矿物质。
此外,蔬菜和水果上栖息着数量惊人的微生物,高度多样化的微生物组是机会性病原体和益生菌的重要储存库。新鲜蔬菜和水果可能成为一些食源性病原微生物的重要来源。
许多研究还发现,食用新鲜蔬菜和水果会影响肠道微生物的组成,同时对人体健康和相关代谢也存在一些有益的影响,例如可以增加碳水化合物活性酶的丰度,影响短链脂肪酸和维生素的生成。
除了新鲜的蔬菜和水果外,牛奶也是人们生活中重要的饮食,牛奶富含蛋白质、维生素、矿物质、必需氨基酸等多种营养,但同时非常容易滋养微生物。不当的保存方法会促进微生物的生长和繁殖,从而对食品质量和食品安全产生负面影响。
本文从食品中的微生物角度,主要阐述了蔬果中存在的一些微生物群对肠道微生物群结构和人类健康的影响。此外还介绍了一些影响食物中微生物生长的因素,以及导致牛奶及奶制品腐败的微生物。
人们对动物体内的微生物研究较多,有时可能忽略了植物中的微生物,你可能想象不到,一个普通的苹果就含有约1亿个细菌。
★ 蔬果中的微生物会影响人体健康
蔬果中高度多样化的微生物群是机会性病原体和益生菌的储存库。其中很少细菌是致病的,大多数是无害的,有些甚至是有益的。
随着饮食的摄入,定植于植物组织内部和外部的微生物可以在人类营养和健康中发挥作用,例如十字花科蔬菜的微生物群,研究表明它们为人类宿主提供了抵御真菌病原体和针对抗癌分子的保护。
此外,一些植物微生物与植物激素协同作用产生的代谢物,也可能与人类肠道微生物甚至整体健康相关。
研究发现蔬菜含有以放线菌门、拟杆菌门、厚壁菌门和变形菌门为主的多种细菌群落,但每种蔬菜物种的组成显著不同。
★ 肠杆菌是蔬菜微生物中的重要组成部分
这些差异通常可归因于肠杆菌科(Enterobacteriaceae)相对丰度的差异。这个革兰氏阴性菌大家族除了许多无害的共生体之外,还包括许多熟悉的机会性病原体,例如大肠杆菌(Escherichia coli)、沙门氏菌(Salmonella)、克雷伯菌(Klebsiella)。然而,肠杆菌科是蔬菜微生物组的重要组成部分。
★ 发酵的蔬菜中含有大量的乳酸菌
除了新鲜蔬菜外,发酵的蔬菜也是全世界饮食的重要组成部分,并且不同地区存在特定的传统产品,例如韩国的“泡菜”或中国的“酸菜”。
通过使用本土细菌或发酵剂进行乳酸发酵会引起细菌群落的转变。它们携带内源性乳酸菌群落,这些群落在发酵过程中变得丰富。例如,腌制橄榄含有大量乳杆菌(Lactobacillus),可能具有益生菌作用。
另一类发酵食品以奶酪和其他乳制品为代表,将在本文后面的章节讲述。
★ 不同蔬果中的微生物组成存在差异
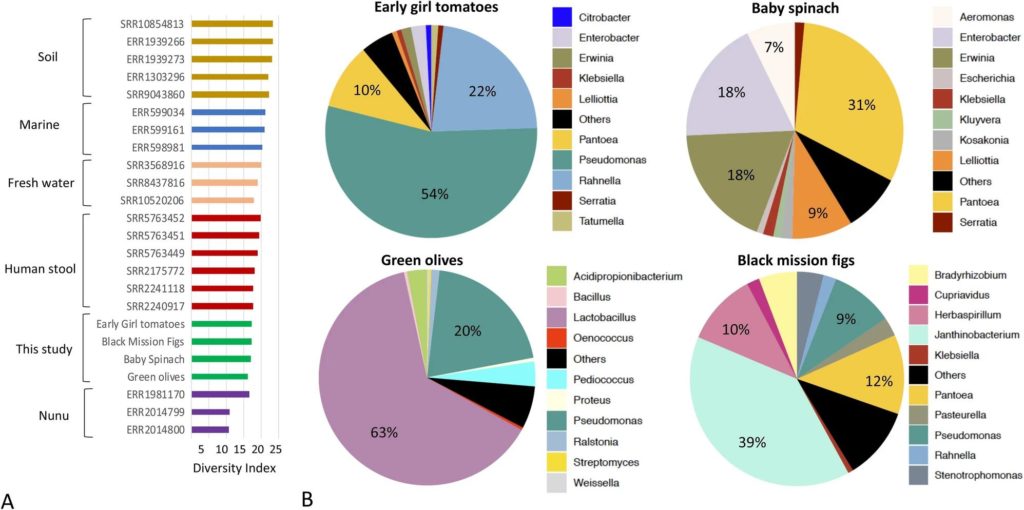
基于宏基因组读数的分类注释表明,大部分样品中的微生物群落均以变形菌门为主,但绿橄榄除外,其中最丰富的门是厚壁菌门(占总数的69.7%)。
与其他样品相比,绿橄榄中的放线菌含量也高出10 倍(平均为4.2%对0.4%)。在属水平上,蔬菜和水果中含有不同的微生物成员(上图B所示)。
番茄中假单胞菌非常丰富
例如,假单胞菌属(Pseudomonas)是番茄中最丰富的分类群(54%),其次是拉恩氏菌属(rahnella)(22%)和泛菌属(Pantoea)(9%)。
小菠菜以泛菌属(Pantoea)(30%)为主,其次是欧文氏菌属(Erwinia)(20%)和肠杆菌属(19%)。
绿橄榄以乳杆菌(62%)为主,其次是假单胞菌(21%)、丙酸杆菌(3%)和片球菌(3%)。
黑无花果中有较高丰度的真菌
黑无花果中的细菌以紫色杆菌属(Janthinobacterium)(38%)为主,其次是泛菌属(12%)和草螺菌属(12%)。
基于从宏基因组中恢复的 16S 和 18S rRNA 基因序列的分类学图谱表明,黑无花果拥有属于真菌的最高比例的测序读数,主要分为曲霉属(30%)、未分类的散囊菌目(Eurotiales)(29%)和未分类的Trichocomaceae属(26%) 属。
注:在任何宏基因组中均未检测到古菌序列。
小结
蔬菜微生物组高度多样化,不同品种蔬菜的物种组成各不相同,并受到地理方面以及农业和食品加工的强烈影响,肠杆菌科是关键物种。
★ 蔬菜中具有潜在有益细菌和病原体
生菜在蔬菜中有着特殊的地位。它是最受欢迎的生吃蔬菜之一,并为特定微生物提供了栖息地。
研究发现,在田间种植的长叶生菜的叶际中,存在高丰度10^5–10^6菌落形成单位(cfu)g和肠杆菌科细菌比例较高的多样性。肠杆菌科分类群不仅包含潜在的有益细菌,而且还存在潜在的病原体。
在德国病原体监测系统中,在所调查的生菜样本中,1.3%发现了产维罗细胞毒素的大肠杆菌,3.8%发现了大肠杆菌。
植物,特别是其内层和根茎,是新出现机会性病原体的重要储存库。
★ 多种病原体能够在蔬菜中定值
近年来,记录在案与食用生蔬菜有关的人类感染的数量有所增加。多种人类病原体能够在蔬菜中定殖,包括大肠杆菌等致病菌。
下图显示了细菌处理后大肠杆菌通过气孔侵入生菜叶片。
大肠杆菌在生菜叶片上的定值
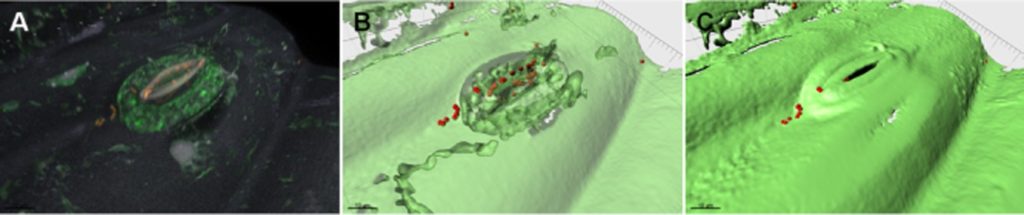
Berg G,et al.Microb Biotechnol.2014
A.共聚焦Z堆栈体积的渲染。
B和C.显示造口内细菌的A的等表面模型。
★ 植物中的一些菌属和人体存在相互作用
有许多与植物相关的菌属,包括伯克霍尔德菌属(Burkholderia)、肠杆菌属、假单胞菌属、罗尔斯通氏菌属(Ralstonia)、沙雷氏菌属、葡萄球菌属和寡养单胞菌属(Stenotrophomonas),它们与植物和人类之间相互作用。
这些属的一些成员表现出促进植物生长以及对抗植物病原体的优异拮抗特性;然而,许多菌株也会定植于人体器官和组织,从而引起疾病。一个原因是相似或通常相同的因素允许识别、粘附和入侵植物和人类宿主。
机会致病菌在芝麻菜叶层中的分类结构
Berg G,et al.Microb Biotechnol.2014
这一群体中研究得很好的例子是革兰氏阴性,通常具有多重耐药性的铜绿假单胞菌和嗜麦芽窄食单胞菌。两者都是植物微生物群中丰富的成员,属于这些物种的菌株在基因型和表型水平上具有高度的多样性。
铜绿假单胞菌分布较广,会引起人体感染
令人惊讶的是,铜绿假单胞菌的泛基因组比人类基因组具有更大的遗传库,这解释了铜绿假单胞菌广泛的代谢能力及其在栖息地中的普遍分布。
此外,流行的植物模型拟南芥已被用于成功鉴定与毒力相关的新铜绿假单胞菌基因。
铜绿假单胞菌感染人体后,可引起病人的血液感染、肺炎、心内膜炎、尿路感染等;对植物亦是机会性感染的,感染后会流出绿色的脓汁和渗出液。
当人体自身微生物群减少时,可能被嗜麦芽窄食单胞菌感染
嗜麦芽窄食单胞菌菌株表现出相似程度的多样性。临床和环境嗜麦芽窄食单胞菌种群的多态性突变频率解释了对新生态位的适应,与植物相关的种群具有更广泛的多样性,只有突变频率高的种群(超突变者)才能适应临床环境和人类宿主。
尽管嗜麦芽窄食单胞菌菌株引起大量感染,但仅鉴定出非特异性毒力因子,例如蛋白酶和铁载体。属于该物种的菌株持续存在并表现出多重抗性;只有本土微生物群减少,病原体才有机会感染人类。
在自然栖息地中,嗜麦芽窄食单胞菌菌株定植于双子叶植物中,这些植物能够产生多种次生抗菌代谢物。
为了在这样的植物中生存,需要使用外排泵,这也是它们对临床使用的抗生素具有多重耐药性的原因。然而,研究表明,菌株水平上的基因组和表观基因组具有高度可塑性和特异性,这可能有助于强毒菌株的发展。
农业技术和加工对植物相关微生物群落的组成有重要影响。在过去的二十年里,更大规模的生产和更有效的新鲜蔬菜分配导致了疾病爆发数量的增加。
有机农业实践可能与传统农业实践不同,包括使用的肥料和农药的类型,这些差异有可能影响与蔬菜相关的微生物群落结构;它们通常具有较高的微生物多样性的特点。
★ 抗生素和农药的使用增加了相关耐药基因
在过去的几十年中,抗生素在畜牧业中的使用极大地促进了农场环境中抗生素耐药性的发展和丰富。特别是,粪便是耐药细菌和抗生素化合物的储存库,其应用于农业土壤被认为会显著增加抗生素耐药基因和土壤中耐药细菌种群的选择。
这些种群可以从根际侵入植物的内部,并进入人类的食物链。新鲜产品的病原体污染可能起源于收获之前或之后,一旦被污染,产品就很难消毒。
★ 动物粪便中携带的病原体可能增加了蔬菜中的病原体
食品加工也会对蔬菜微生物组的结构和食品安全产生重要影响。例如,中等干扰(例如轻微的生物或非生物影响)可以增加肠杆菌科细菌的相对丰度。
与志贺氏菌(一种以人类为主要宿主的有机体)收获前污染相关的爆发相对较少,而与沙门氏菌或产生志贺毒素的大肠杆菌相关的爆发相对较高,以动物为主要宿主的生物体,强调了家养动物和野生动物作为沙拉等蔬菜收获前污染的主要来源的作用。
既然植物中存在如此丰富的微生物组,那么其在植物生长的时候是否存在一定的作用,当人类将其作为食物摄入时又是否会对人体健康产生影响?在这一章节谷禾将具体讲述植物中微生物的相关作用。
植物微生物组对植物生长和健康起着重要作用,取决于植物种类、栽培品种和土壤类型等因素。
▷ 植物中的微生物会促进营养吸收
植物中的一些微生物可以支持营养吸收并产生多种植物激素。
例如根瘤菌和固氮菌,能够与植物共生,将大气中的氮转化为植物可利用的氮化合物。这种共生关系使植物能够吸收到更多的氮,从而促进其生长。
溶磷细菌和真菌,能够分解土壤中的有机磷化合物,将其转化为可溶性的无机磷,为植物提供营养。
一些微生物能够产生植物生长激素,如生长素和激动素,这些激素可以促进植物的生长和发育。微生物通过与植物根系接触,释放这些激素,从而影响植物根系的吸收能力。
注:激动素是一种内源的细胞分裂素,除具有促进细胞分裂的作用外,还具有延缓离体叶片和切花衰老,诱导芽分化和发育及增加气孔开度的作用。
▷ 一些植物中的病原菌会影响产量
许多病原体会对植物产生负面影响,特别是真菌、卵菌和线虫;据估计,全球三分之一以上的产量损失是由它们造成的。
病原菌会直接侵害植物的组织,破坏植物的生长和发育过程。例如,霉菌和真菌可以感染植物的叶片、茎和根部,这会削弱植物的光合作用和养分吸收能力。
此外,病原菌还可以分泌毒素,对植物产生毒害作用。这些毒素会破坏植物的细胞结构和功能,干扰植物的正常代谢过程,使植物受到氧化应激和细胞死亡的影响。
最终导致叶片枯萎、果实腐烂、凋萎和死亡等症状,从而降低产量。
植物微生物可能还通过刺激人体的免疫系统和增强肠道微生物组的多样性对人类健康发挥积极作用。
最近,通过与肠杆菌科细菌的显著相互作用证明了细菌多样性与特应性之间的相关性。研究发现健康人外周血单核细胞中不动杆菌(Acinetobacter)的丰度与白细胞介素10的表达呈正相关。
白细胞介素10是一种抗炎细胞因子,在维持对无害物质的免疫耐受性方面发挥着核心作用。
▷ 植物相关微生物可能成为“天然疫苗”
已知源自革兰氏阴性菌(例如肠杆菌科)的内毒素具有过敏保护和免疫调节潜力。如果植物是肠杆菌科细菌的天然储存库,那么这些细菌一定长期以来一直是我们饮食的“天然”组成部分。
考虑到全世界人们食用的蔬菜和水果量,植物相关微生物组可能可以作为免疫刺激剂或“天然疫苗”。
▷ 植物相关细菌影响肠道微生物的多样性
在人体肠道中可检测到水果和蔬菜相关细菌
有趣的是,植物和人类肠道微生物组在物种组成和功能方面存在重叠。最近的研究表明,胃并不像以前认为的那样对微生物通道构成严格的屏障。它栖息着许多物种。
最近还提供了食源性微生物(包括动物性和植物性饮食)在通过消化系统后仍能存活的证据,并且食源性菌株可能在肠道中具有代谢活性。
植物和人类相关细菌的分类及其在人类肠道中的丰度
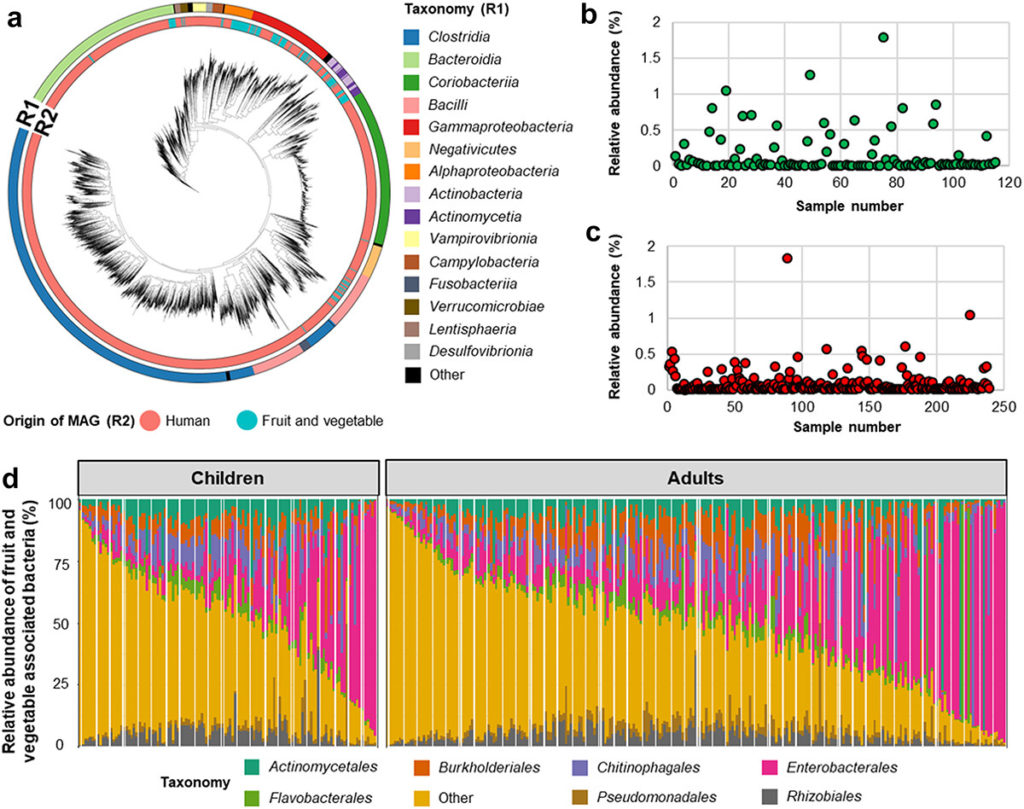
Wicaksono WA,et al.Gut Microbes.2023
(a)R1中的不同颜色表示细菌分类,R2表示MAG(宏基因组组装基因组)的起源。
水果和蔬菜相关细菌的相对丰度及其在儿童(b)和成人(c)中的丰度。条形图显示了人类肠道中与水果和蔬菜相关的细菌组成在目水平上的相对丰度。
(d)水果和蔬菜相关细菌的相对丰度是通过使用包含仅映射到水果和蔬菜相关细菌基因组读数的数据集获得的。不同的颜色代表不同的级别分类,不太丰富的细菌目包括在“其他”中。
通过基于每月粪便样本鸟枪宏基因组测序(对儿童肠道微生物组进行纵向研究,进一步尝试确定水果和蔬菜相关细菌对人类肠道整体微生物多样性的贡献。
婴儿时期喂养蔬果有助于肠道微生物的发育
有趣的是,水果和蔬菜相关细菌的多样性从1个月大到12个月大的受试者有所增加,但从此时开始下降,在24个月以上的受试者中达到最低水平。
除了母乳喂养之外,引入固体食物(即水果和蔬菜)是生命早期的事件,有助于肠道微生物组的变化和发育。
在队列中,一些儿童在前4个月内已经接触了根类蔬菜(n=269中的71名)、水果(n=269中的81名)和蔬菜。此外,制备自制婴儿食品的常见烹饪方法可能无法完全消除植物微生物群。
由于食源性微生物可以在消化道中生存,我们推测,儿童肠道宏基因组中检测到的植物相关细菌数量的增加是由于断奶早期食用的自制或生水果或蔬菜中的植物微生物群的转移和定植所致。
水果和蔬菜相关细菌平均占2.2%(最小值:0.8%,最大值:13.6%)
▷ 植物微生物随着时间的推移在体内持续存在
人类肠道中与水果和蔬菜相关的细菌群落随着宿主年龄的变化而变化,根据图中的年龄梯度,可以看到清晰的聚类。评估表明,宿主年龄影响水果和蔬菜相关的细菌群落结构(P=0.001),但只能解释5.3%的细菌变异。
有趣的是,婴儿的国籍也对水果和蔬菜相关的细菌群落结构产生了较小程度的影响(P=0.001,R2=2.2%)。这一结果可能是由于不同国家的婴儿之间的辅食喂养模式不同所致。
沿梯度富集的细菌类群主要是革兰氏阳性菌,尤其是布氏乳杆菌、乳杆菌属和乳球菌属,它们取代了早期占主导地位的泛菌属、欧文菌属和不动杆菌属。
注:与临床菌株相比,源自植物的聚集泛菌菌株同样能够定植于人类宿主。
肠道微生物的变化可能由于氧气浓度和食物种类
我们假设,由于新生儿肠道中存在氧气,来源于水果和蔬菜的兼性厌氧γ-变形菌,即泛球菌、欧文氏菌和不动杆菌,可以在断奶早期的婴儿肠道中定植。然后,由于氧气浓度降低,厌氧细菌,即布氏乳杆菌和乳杆菌属,在第8-12个月出现。
在婴儿期,肠道微生物群的生态演替是一个动态过程,然后在儿童期达到稳定阶段。随着宿主年龄的增加,人类肠道中与水果和蔬菜相关的细菌组成变得更加异质(即相对于中位数分布的差异更大)。这可能是由于通常随着婴儿年龄的增加而提供的食物种类更加多样化,也可能因个体而异,导致观察到与宿主年龄相关的异质性。
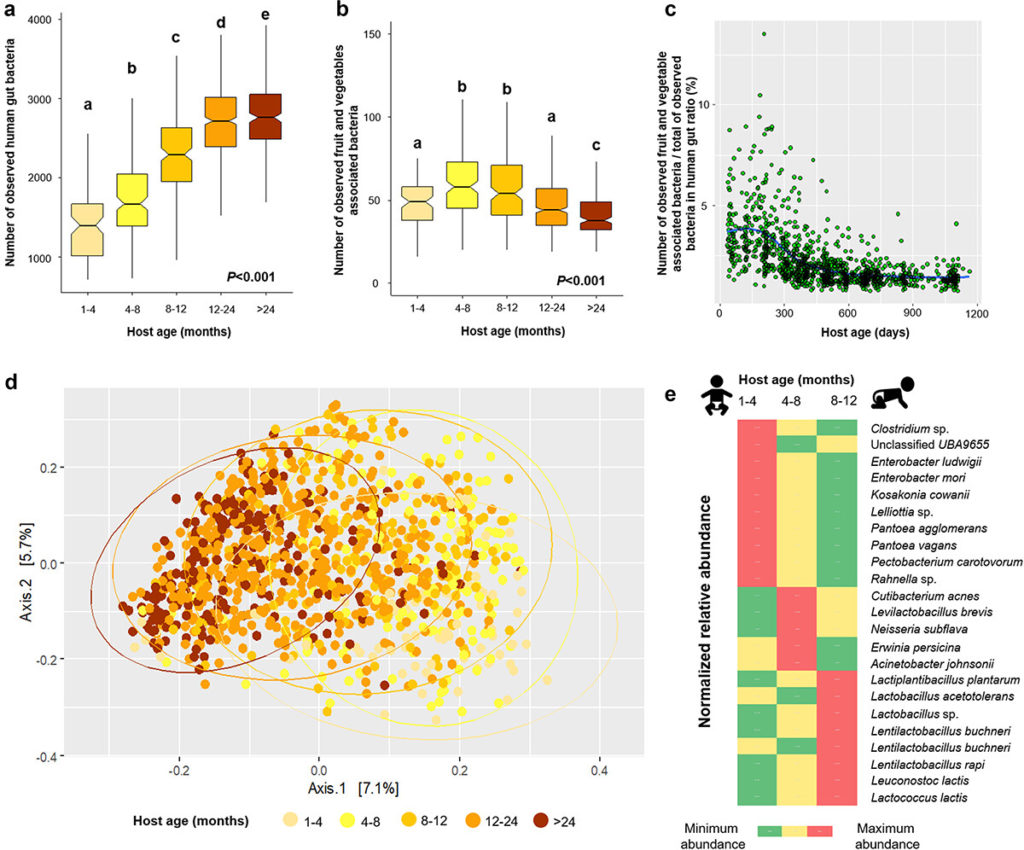
Wicaksono WA,et al.Gut Microbes.2023
箱线图包括基于观察到的肠道宏基因组观察到的人类肠道相关细菌(a)和水果和蔬菜相关细菌(b)。
箱形图上方的不同字母表示不同宿主年龄内的Kruskal-Wallis检验,然后进行成对比较(P<0.05)。散点图显示了观察到的水果和蔬菜相关以及人类肠道相关细菌宏基因组组装基因组沿年龄梯度的比率(c)。使用二维PCoA图并基于 Bray-Curtis 相异矩阵(d)显示了人类肠道中水果和蔬菜相关细菌的群落聚类。
LEfSe分析表明,水果和蔬菜相关的细菌宏基因组组装基因组在不同年龄组中富集(e)。
▷ 蔬果消费频率和多样性会影响人类肠道中与水果和蔬菜相关的细菌丰富度
食用水果和蔬菜的频率和多样性可能会影响人类肠道中与水果和蔬菜相关的细菌丰富度。
为了检验这一假设,研究人员使用了美国肠道项目的数据集,这是一项大型公民科学开放平台研究,收集了自我报告的饮食数据和粪便样本。
使用Kraken2,总共746个样本的读数超过500000个,这些读数被指定为细菌。保留这些样本进行进一步分析,以检查肠道微生物多样性与植物消费频率和多样性之间的关联。
分析表明,人类肠道中水果和蔬菜相关细菌的丰富度与受试者食用蔬菜的频率和多样性有关。
食用蔬菜更丰富的人群肠道微生物多样性更高
对于α多样性分析,将数据集二次采样至500000个读数后,计算了人类肠道中检测到的水果和蔬菜相关宏基因组组装基因组(MAG)的数量。
与其他组相比,经常食用蔬菜和每周食用超过10种植物的受试者中检测到的与水果和蔬菜相关的宏基因组组装基因组数量更高。然而,水果消费频率对检测到的相关宏基因组组装基因组的数量没有显著影响。
蔬菜消费频率的增加和所消费植物的多样性也增加了人类肠道中水果和蔬菜相关细菌的相对丰度。
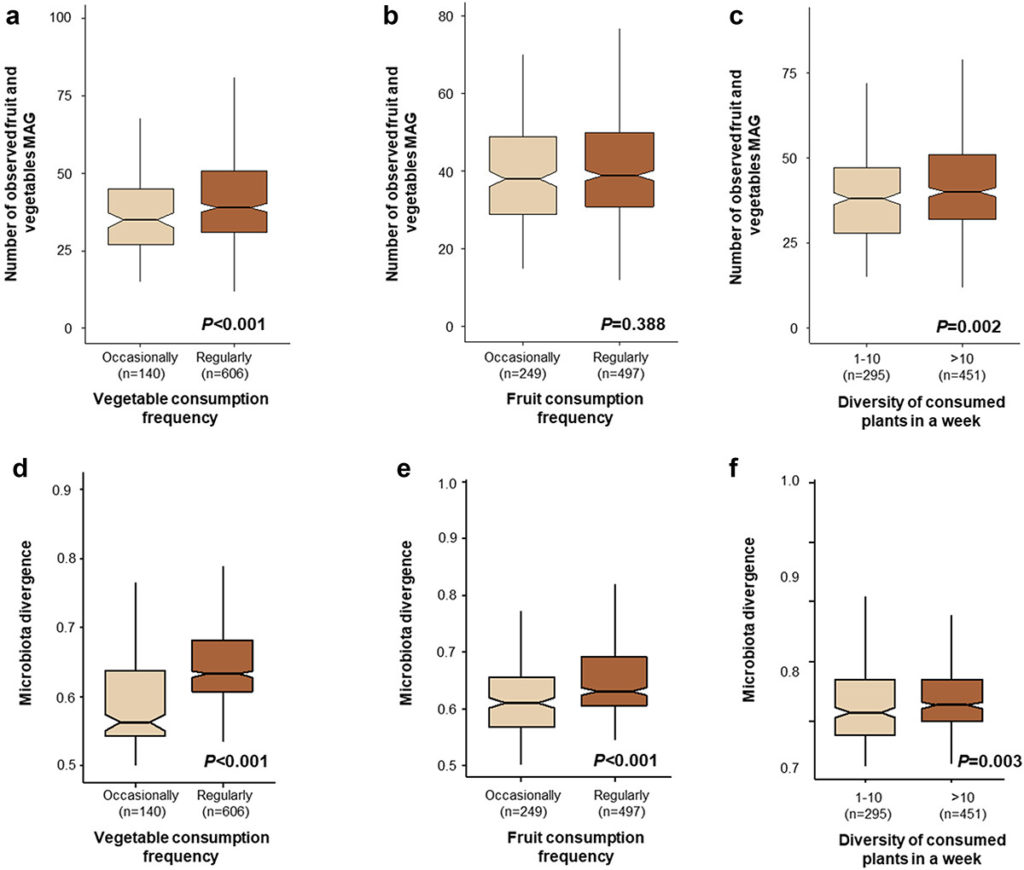
Wicaksono WA,et al.Gut Microbes.2023
一周内蔬菜消费频率、水果消费频率和消费植物多样性对观察到的水果和蔬菜相关细菌数量以及水果和蔬菜细菌群落组成总体异质性的影响。
箱线图显示了肠道(ac)中观察到的与水果和蔬菜相关的宏基因组组装基因组。其他图显示了肠道中水果和蔬菜相关宏基因组组装基因组组成的总体异质性(df)。
与研究结果一致,经常食用蔬菜、水果和自制发酵乳制品的农村贝都因人的细菌多样性明显高于城市沙特人,城市沙特人每周只吃1-2次蔬菜和水果。
另一组研究人员也提出了类似的观点,患者因每天食用帕尔马干酪而在人类肠道中发现了与奶牛相关的细菌定植。
基因本体论(GO)生物学过程的预测表明,宏基因组读数的很大一部分与代谢功能有关,如核酸代谢、蛋白质代谢和碳水化合物代谢。
★ 植物中不同的微生物组成导致代谢存在差异
对四个样本中注释基因的比较表明,并非所有生物代谢过程都是均匀分布的。在新鲜菠菜中,与其他样品相比,我们发现分配给果胶分解代谢、甘油醚代谢、海藻糖生物合成、L-苏氨酸分解代谢为甘氨酸和L-丝氨酸生物合成过程等过程的高频读取。
在无花果中,我们发现木葡聚糖代谢和聚羟基丁酸酯生物合成更加频繁。与其他样品相比,番茄中的乙醛酸分解代谢更为频繁。
此外还确定了与人类肠道微生物组稳态相关的代谢途径的存在,包括谷氨酸、萜类化合物、核黄素(VB2)、硫胺素(VB1)、叶酸、谷氨酰胺和生物素的生物合成。
除绿橄榄外,所有样品中都存在类胡萝卜素生物合成过程,而对氧化还原状态、乳糖代谢过程以及脂磷壁酸、磷壁酸和异戊烯基二磷酸生物合成过程的响应仅在绿橄榄中被发现。
总体而言,这些数据揭示了食用植物微生物组具有多样化的基因组库,且不同样本之间存在差异。
▷增加碳水化合物活性酶的丰度
为了进一步了解这些植物微生物组的功能,我们研究了碳水化合物活性酶 (CAZymes) 的丰度,这是一组参与植物细胞壁分解的酶,有可能进一步转化为人体肠道中的有益代谢物。
碳水化合物活性酶根据蛋白质序列和结构相似性进行分类,包括糖基转移酶(GTs)、糖苷水解酶(GHs)、碳水化合物酯酶(CE)、多糖裂解酶(PL)、辅助活性酶(AA)和碳水化合物结合模块(CBM)。
本研究中所表征的植物相关微生物群中的假定碳水化合物活性酶是使用来自宏基因组和碳水化合物活性酶数据库的预测开放阅读框进行鉴定的。
糖基转移酶和糖苷水解酶是宏基因组中预测最丰富的碳水化合物活性酶(约占总数的30%至57%)。样品中鉴定出较少百分比的辅助活性酶(约1-6%)、碳水化合物结合模块(2-5%)、碳水化合物酯酶(3-9%)和多糖裂解酶(1-4%)。
具体而言,碳水化合物活性酶数据库中的133个糖苷水解酶家族中有79个在样本中被检测到,其中 GH13、GH23和GH1是最常见的家族。GH13是人类肠道微生物组中最常见的家族之一,其特点是分解淀粉。
部分糖苷水解酶与人类肠道的有益作用相关
研究还观察到糖苷水解酶明显分布在特定样本中,并且与人类肠道的有益作用相关。
例如,番茄酶与木聚糖酶一起是GH10的成员。番茄红素酶促进抗真菌番茄红素降解为非致癌底物。
黑无花果中真菌的存在可能与GH10酶的存在有关,GH10酶使真菌毒素呈惰性。
GH1包含参与纤维素降解的β-葡萄糖苷酶,纤维素是叶类蔬菜中最丰富的纤维之一。肠道微生物利用GH1酶将聚糖水解成葡萄糖和糖酵解前体葡萄糖-6-磷酸。
含有海藻糖磷酸化酶的GH65在绿橄榄样品中含量最高。海藻糖是一种二糖,可以防止植物干燥,存在于橄榄叶中。海藻糖酶也存在于脊椎动物的小肠中,肠球菌等细菌已被证明可以代谢海藻糖。
GH28家族含有与果胶降解相关的酶。果胶被认为是一种益生元,番茄中存在的欧文氏菌属(Erwinia)和假单胞菌属(Pseudomonas)是常见的果胶分解酶生产者。
总之,这些数据进一步支持了这样一种观点,即植物中存在的微生物在作为饮食的一部分食用时可以为人类提供代谢益处,因为它们含有大量碳水化合物活性酶,对人类健康和植物细胞壁中存在的底物起着至关重要的作用。
▷ 影响短链脂肪酸产生的代谢途径
与人类健康相关之一的微生物代谢物是短链脂肪酸。短链脂肪酸源自复杂碳水化合物的微生物发酵,既可作为重要的调节信号分子,又可作为宿主的额外燃料来源。
所分析的四个样品中最普遍的短链脂肪酸途径是乳酸氧化和L-赖氨酸分解代谢过程为乙酸。在新鲜菠菜和绿橄榄的宏基因组中也发现了乳酸代谢过程。最不常见的途径是丁酸代谢过程,因为宏基因组包含的丁酸激酶读数最少。
蔬果中的微生物组有助于产生乙酸和丙酸
有趣的是,研究中具有最广泛短链脂肪酸代谢潜力的样品是腌制的绿橄榄,这表明腌制过程可能会选择具有广泛短链脂肪酸生产能力的微生物。样品中最具代表性的酶是与乙酸(乙酸激酶)和乳酸(D-乳酸脱氢酶)生产相关的酶。
这些数据表明,水果和蔬菜的微生物组含有产生乙酸和丙酸(与人类健康相关的微生物代谢物家族)所需的基因和途径,但缺少丁酸生物合成,因为它主要与样品中未见的严格厌氧菌有关。
▷ 与维生素合成相关
众所周知,微生物可以合成维生素,这对于各自宿主的多种代谢反应至关重要。
本研究的宏基因组中参与维生素生物合成和摄取转运蛋白酶的鉴定是基于先前在人类粪便宏基因组和益生菌菌株克劳氏芽孢杆菌(Bacillus clausii)中鉴定的KEGG同源物(KOs)注释基因。
植物微生物中存在编码维生素合成的基因
研究结果表明,植物相关宏基因组中存在编码酶的基因,这些酶是钴胺素(维生素B12)、生物素(维生素H)和泛酸(维生素B5)生物合成途径的一部分,叶酸(维生素B9)、甲基萘醌(维生素K2)和烟酸(维生素B3)生物合成的基因簇较少。
此外,在宏基因组中检测到了很高比例的与钴胺素代谢相关的基因,并且在早期番茄和绿橄榄中发现了略高丰度的钴胺素代谢基因。
钴胺素(维生素B12)是人类必需的辅助因子,由一些细菌和古细菌合成,参与介导微生物-微生物相互作用和宿主-微生物作用。钴胺素缺乏会导致贫血、神经系统疾病等。
植物和动物来源的食物都在微生物生长中发挥着重要作用。微生物在食品中生长或繁殖的能力取决于食品环境。
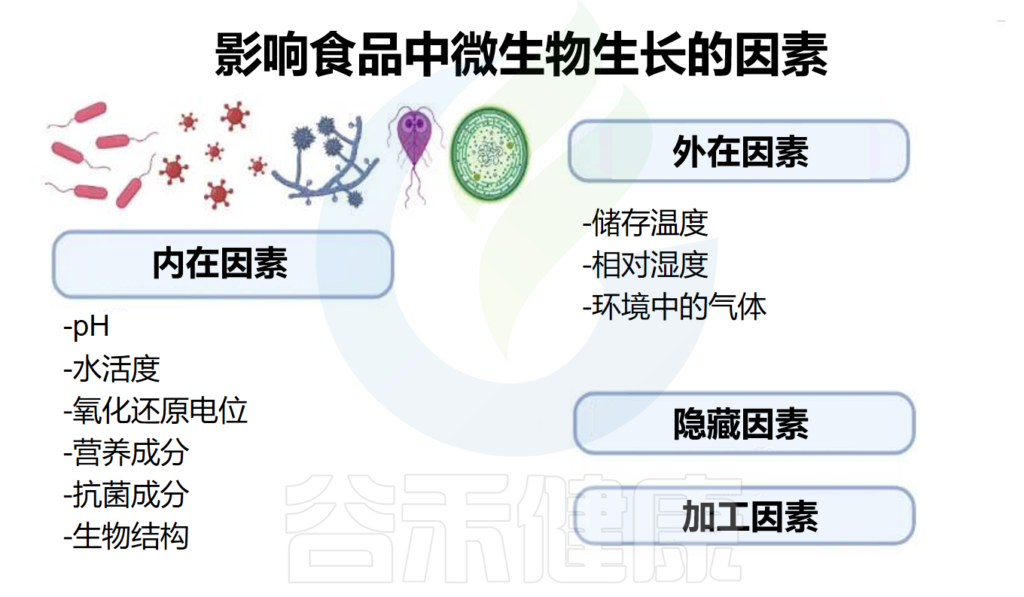
食品的内在因素、外在因素、隐性因素包括各种食品加工方法分别对微生物的生长产生作用。这些因素决定了食物中微生物的生长以及它们用来产生能量和代谢产物的特定途径。
Part 01
内在因素
1
酸碱度
一般来说,与细菌相比,霉菌和酵母菌可以在较低的pH值下生长,并且革兰氏阴性菌比革兰氏阳性菌对低pH值更敏感。
霉菌生长的pH范围为1.5至9.0;对于酵母生长的pH范围为2.0至8.5;革兰氏阳性菌生长的pH范围为4.0至8.5;革兰氏阴性菌生长的pH范围为4.5至9.0。
根据 pH 范围,微生物可分为:
中性菌在pH值5至8范围内生长最佳;
嗜酸菌在pH值低于5.5时生长最佳;
嗜碱菌在pH值高于8.5时生长最佳。
以下是一些常见微生物生长所需的pH值:
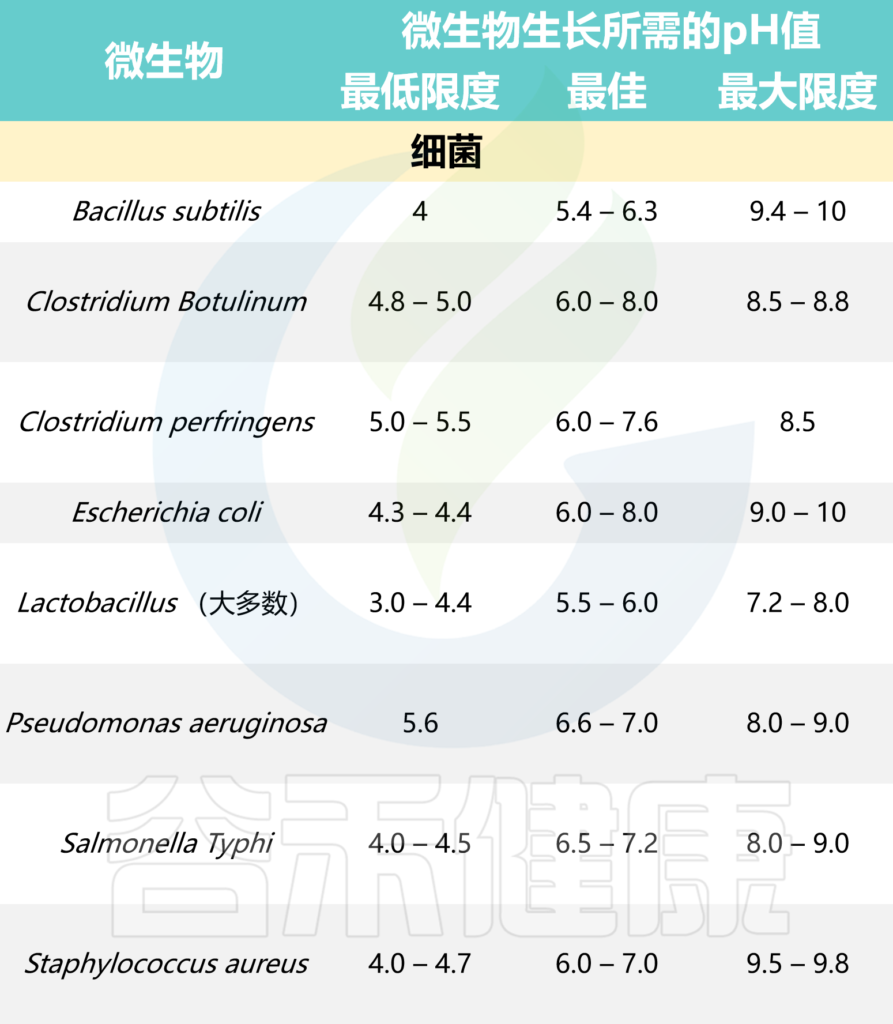
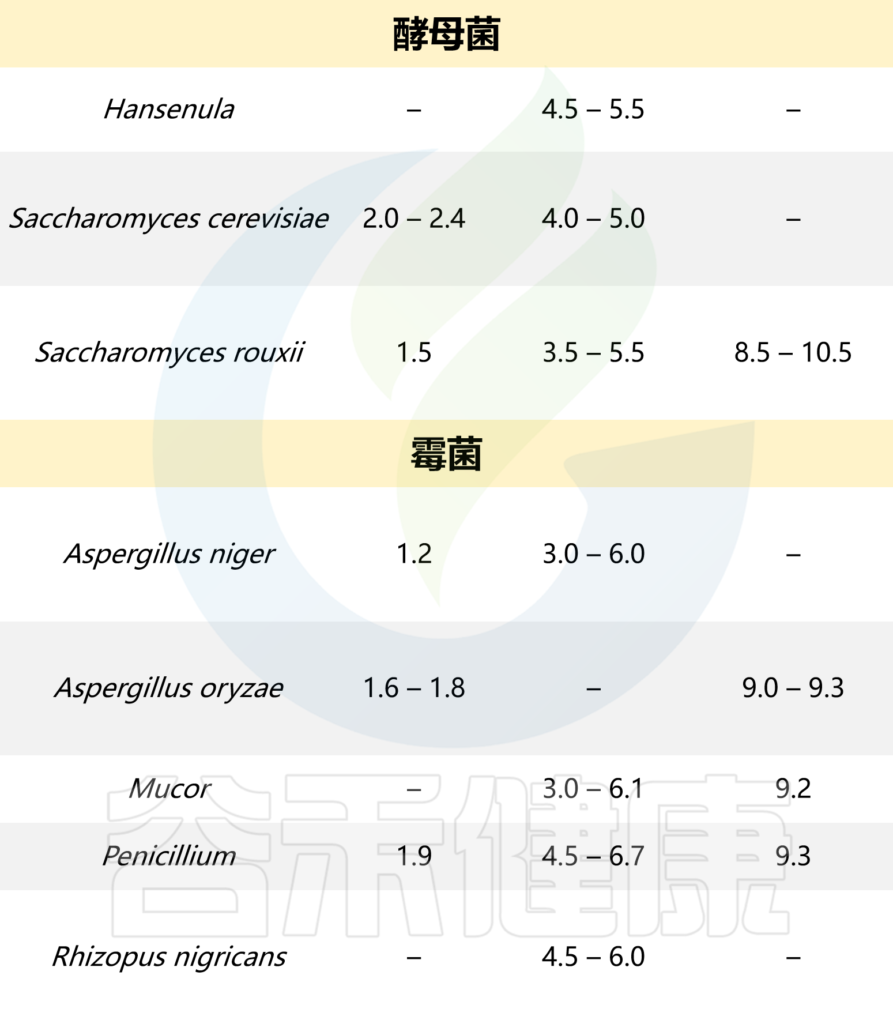
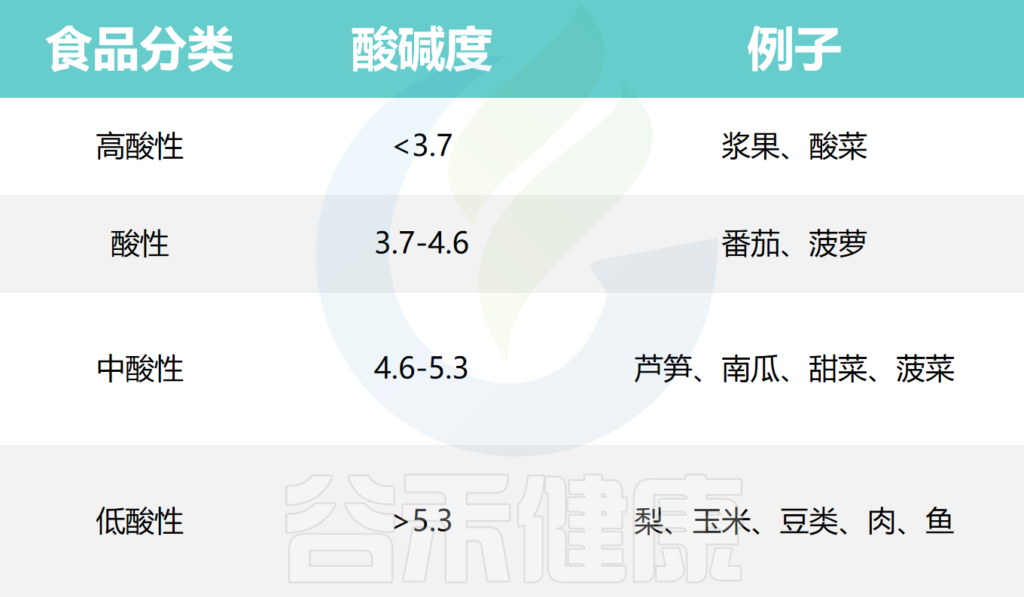
根据pH值,食物一般可分为以下几类:
2
水分活度
水分活度(aw)是可用于生物功能的水量,可因渗透效应而减少。微生物需要可用形式的水才能在食物中生长。
食物的水分活度可以用相同温度下食物的水蒸汽压与纯水的水蒸汽压力的比值来表示,0<它的范围是<1。
与真菌相比,细菌的生长需要更高的水分活度。细菌不会在低于0.91的水平生长,霉菌可以在低至0.80的水平生长。革兰氏阴性菌比革兰氏阳性菌对低水分活度更敏感。
3
氧化还原电位
物质的氧化还原或氧化还原电位被定义为原子或分子之间电子转移的测量值。氧化还原电位通常写为Eh,并以毫伏(mV)为单位进行测量。
不同类群微生物生长所需的Eh范围如下:
需氧菌在+500至+300mV下生长最佳,如霉菌、酵母、芽孢杆菌、假单胞菌、卡他莫拉菌和微球菌;
兼性厌氧菌在+300至+100mV下生长最佳,例如乳酸菌和肠杆菌科细菌;
厌氧菌在+100至–250mV或更低的电压下生长最佳,例如梭菌属。
4
营养成分
微生物的生长和代谢功能需要蛋白质、碳水化合物、维生素、脂质、水、以及硫、磷、氮等矿物质。
人们的食物是微生物生长的最佳营养来源,但食品中常见的微生物对营养的需求差异很大,能够大量利用现有营养的微生物通常在食品中占主导地位。
首先利用简单的碳水化合物和氨基酸,然后是这些营养素的更复杂形式。革兰氏阳性菌的营养需求高于酵母菌,其次是革兰氏阴性菌,霉菌的营养需求最低。
因此许多食物中都会出现霉菌
5
抗菌成分
部分食品具有天然的抗菌成分,这些成分可以抑制微生物的生长和繁殖。因此其中一些可以用作天然的保存剂。
下面罗列了一些常见食物中的抗菌成分:


6
生物结构
有些食物具有防止微生物进入的生物结构,天然覆盖物可防止损坏并减少微生物腐败的机会。
例如水果的外壳、坚果壳、蛋壳、肉类具有筋膜和皮肤等结构,可以防止食源性病原体和腐败微生物的进入。
Part 02
外部因素
受外部条件控制的因素称为外在因素,这些因素包括温度,相对湿度等。
1
储存温度
酶促反应和微生物生长受到环境温度的影响。例如酵母菌和霉菌的生长温度范围很广,为10–35°C。
根据温度,细菌通常可分为以下几类:
–嗜冷菌可以在0-20°C的温度范围内生长,例如假单胞菌属(Pseudomonas)和肠球菌属(Enterococcus)。
–嗜温菌是可以在25°C-40°C之间生长的微生物,最适生长温度接近37°C。 这些包括沙门氏菌、葡萄球菌、梭菌、志贺氏菌。
–嗜热菌是在45°C以上高温下生长的微生物,最适生长温度在50°C-70°C之间。其中包括芽孢杆菌属、梭菌属和地热芽孢杆菌(Geobacillus)。
注:病原菌一般均为嗜温菌,最适温度为人体的体温,即37℃,故实验室一般采用37℃培养细菌。
2
相对湿度
相对湿度是大气或食品环境中的水分含量。相对湿度会影响食品的水分活度水平,从而影响微生物的生长。
低湿环境(相对湿度低于30%):低湿环境会导致细菌细胞失水,从而抑制其生长和繁殖。细菌在干燥环境中往往处于休眠状态,无法进行正常的代谢活动。因此,低湿环境对于细菌的生长是不利的。
中等湿度(相对湿度在30%至70%之间):中等湿度是细菌生长的最适宜条件之一。在适度湿润的环境中,细菌可以获得足够的水分来维持其细胞活动,并且可以更好地利用营养物质进行生长和繁殖。因此,中等湿度下的细菌生长速度较快。
储存在较高湿度环境中的干燥谷物会吸收水分并发生霉变。
3
气体浓度
气体浓度可以对微生物的生长产生影响。不同的微生物对气体浓度有不同的适应能力和偏好,因此气体浓度的变化可能会对微生物的生长速率和代谢活性产生影响。
以下是一些常见气体对微生物生长的影响:
-氧气:氧气是许多微生物生长所必需的,被称为好氧微生物。它们需要氧气进行呼吸作用,以产生能量和完成生物化学反应。然而,有些微生物是厌氧微生物,它们在缺氧或无氧条件下生长。氧气浓度过高会抑制厌氧菌的生长甚至导致其死亡。
-氮气:氮气在大气中的浓度很高,但大多数微生物无法直接利用氮气。一些微生物具有固氮能力,能够将氮气转化为可利用的氨或亚硝酸盐,从而为其他微生物提供可用的氮源。
-甲烷:甲烷是一种重要的温室气体,也是一些微生物的产物。产甲烷菌(Methanogenus)是一类厌氧微生物,它们能够利用无机或有机化合物产生甲烷。这类微生物对甲烷浓度的变化非常敏感。
Part 03
隐性因素
第三个因素被称为隐性因素。该因素包含了生物体本身的特性以及一些食品加工手段对微生物生长的影响。
•一种微生物对其他微生物可能存在抑制作用
微生物可以抑制或刺激另一种微生物的生长。一些微生物可能会产生对其他生物体具有抑制性或致命性的物质,例如抗生素、细菌素、过氧化氢和有机酸。
•食品加工
在食品加工过程中,微生物会受到各种物理或化学压力。这些加工因素包括加热、冷冻、干燥、减少气压、辐射和各种化学物质:
加热通过破坏细胞质膜、改变代谢和酶活性来帮助降低食物中的微生物水平。
冷冻通过降低pH值和增加水分活度的抑制作用来减少微生物的生长。
干燥会减少微生物的生长,因为它会导致代谢损伤,从而损害细胞的增殖。
牛奶被称为均衡食品和高营养食品,富含蛋白质、脂肪、碳水化合物、维生素、矿物质、必需氨基酸等。是许多人日常生活中常摄入的食品之一。
但牛奶的高水分活度、适中的pH值(6.4–6.6)和高营养含量,也成为许多微生物(即细菌、病毒、真菌和原生动物)的极佳生长培养基。
★ 牛奶及奶制品非常容易受微生物的影响
牛奶及其制品,如酸奶、黄油、奶油和奶酪都很容易受到微生物的影响而腐败。
生奶和巴氏奶中都含有多种微生物,它们都是冷藏保存的,但保质期有限。
在巴氏灭菌前的冷藏(奶牛场和加工厂)期间,只有耐冷菌可以在冷藏奶中生长,例如假单胞菌(Pseudomonas)、黄杆菌(Flavobacterium)、产碱杆菌属(Alcaligenes)、单核细胞增生李斯特氏菌、小肠结肠炎耶尔森氏菌、某些大肠菌群和芽孢杆菌。
其中一部分是致病菌,会引起食物中毒,使人出现呕吐、腹泻、头晕等症状,严重时甚至可导致死亡,建议大家避免直接食用生奶。
在巴氏灭菌中存活下来的是一些耐热微生物,如微球菌、一些肠球菌、链球菌、一些乳杆菌以及梭状芽胞杆菌。霉菌和酵母菌通常在巴氏灭菌过程中被消除。
在较小程度上,原生动物病原体如隐孢子虫和贾第鞭毛虫也已被发现污染牛奶。
★ 微生物引起的牛奶变化
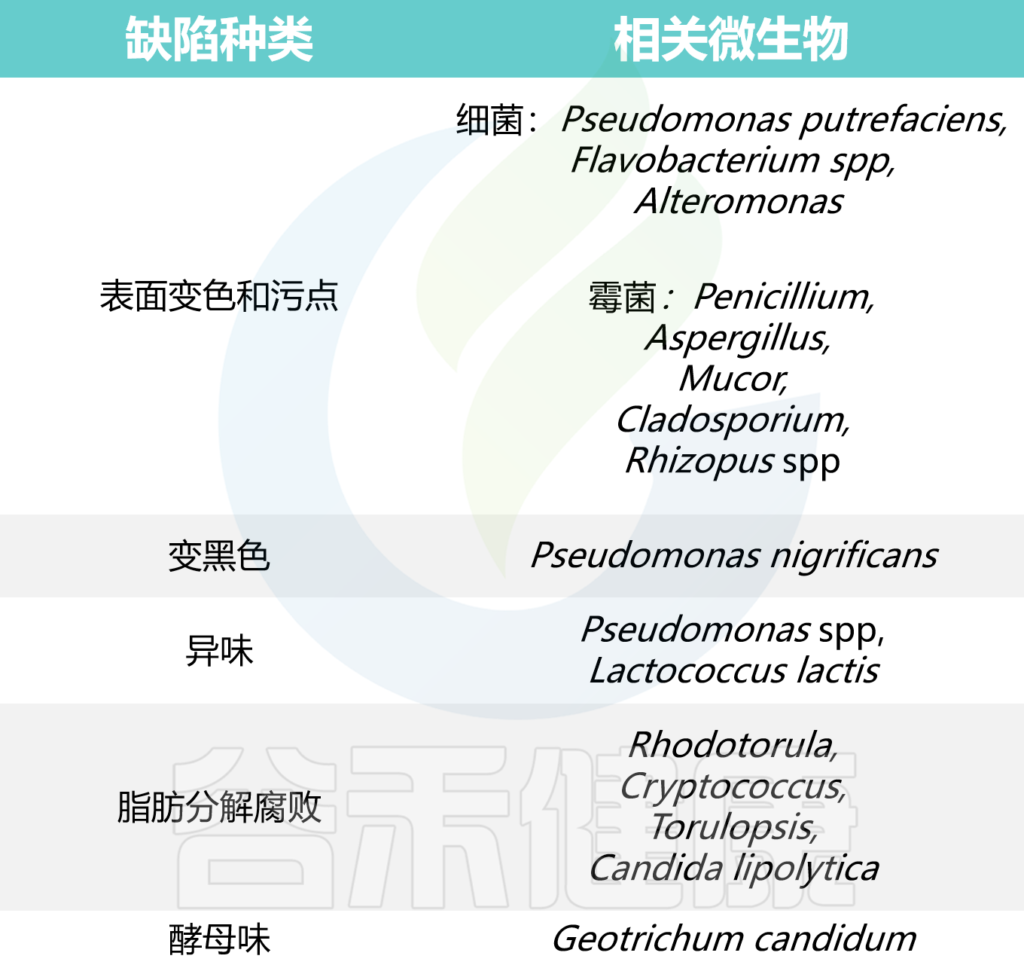
一些微生物可能引起牛奶出现以下变化:
-出现异味
-变色
-产生气体
-脂肪分解并发生酸败
-蛋白水解
-在低酸度下凝结
谷禾在下表列出了一些微生物对应的牛奶变化:

人们可能觉得乳制品经过加工后,不太容易变质,但事实上,在常温下许多乳制品还是会被相关微生物污染并引起腐败。
乳制品的微生物量主要取决于:
•使用的奶和奶制品的类型(生奶、炼乳、奶粉、奶油、黄油等);
•用于增强其功效的产品,如明胶、水果、糖、巧克力、着色剂等;
•各类设备的卫生水平、巴氏灭菌的效率、生产和包装过程中的卫生水平。
接下来为大家简单介绍一下引起乳制品变质的相关微生物。
•奶油变质
奶油是由均匀化前沉积在牛奶顶部的乳脂层制成的。
冷却牛奶用于生产奶油,因此嗜冷菌是腐败的主要原因,包括假单胞菌属、产碱杆菌属、不动杆菌属、气单胞菌属和无色杆菌属。
在室温下,引起奶油腐败的微生物是棒状杆菌(Corynebacterium)、芽孢杆菌(Bacillus)、微球菌(Micrococcus)、乳杆菌(Lactobacillus)和葡萄球菌(Staphylococcus)。
奶油对大肠杆菌、鼠伤寒沙门氏菌和单核细胞增生李斯特氏菌等病原微生物高度敏感。

•黄油变质
黄油是通过牛奶分离和随后的奶油搅拌制成的奶制品。奶油是黄油的原材料,因此黄油中发现的微生物主要来源是奶油。
引起黄油腐败的主要微生物是霉菌,例如Thamnidium、Cladosporium和Aspergillus。
此外,引起黄油变质的病原微生物有李斯特菌、布鲁氏菌、分枝杆菌、弯曲杆菌、小肠结肠炎耶尔森氏菌、鼠伤寒沙门氏菌等。
•奶酪变质
奶酪是一种发酵乳制品,是通过使用凝乳酶凝固牛奶中的酪蛋白而制成的。奶酪的成熟是各种微生物的蛋白水解和脂肪分解活性而实现的。
新鲜的软奶酪由于pH值较高、水分含量较高且盐度较低,因此很容易变质;硬质和半硬质成熟奶酪的水分含量较低,与细菌相比,更容易受到真菌的侵害。
细菌引起的奶酪变质
细菌性奶酪变质是由梭菌属(尤其是C.pasteurianum,C.butyricum,C.sporogenes和C.tyrobutyricum)、多粘芽孢杆菌(Bacillus polymyxa)、黄杆菌、假单胞菌、产碱杆菌和无色杆菌引起的。
真菌引起的奶酪变质
酵母菌也是引起奶酪腐败微生物之一,例如念珠菌属、汉斯德巴氏酵母菌、白地霉和毕赤酵母。由霉菌引起的腐败主要是青霉菌和枝孢菌。
奶酪中发现的主要致病菌是李斯特菌、沙门氏菌和大肠杆菌。

•酸奶变质
酸奶是牛奶经过巴氏杀菌后再添加有益菌(主要是嗜热链球菌和保加利亚乳杆菌)发酵后制成的。
霉菌和酵母菌是酸奶中的主要污染物
导致酸奶腐败的常见霉菌是曲霉属、青霉属、根霉属、镰刀菌属和木霉属。
导致酸奶腐败的常见酵母菌是念珠菌属、汉斯德巴氏酵母菌、克鲁维酵母菌、球拟酵母属。
霉菌和酵母使酸度下降,导致细菌蛋白水解和腐败,产生气体、异味和变色等。
据报道,酸奶中常见的食源性病原体有大肠杆菌、金黄色葡萄球菌、李斯特菌和小肠结肠炎耶尔森菌。
食物中的微生物对于食品的口感、可消化性和安全性都起着重要作用,伴随饮食摄入的微生物可以调节肠道微生物结构甚至影响人体健康。
例如新鲜水果和蔬菜中的微生物具有大量的分类学和功能多样性,可以增加人体肠道微生物的多样性,调节碳水化合物、短链脂肪酸及维生素的相关代谢。
与此同时,蔬果微生物组是机会性病原体的储存库。在免疫功能低下的个体中,机会性病原体可引起严重感染。这些感染包括肺炎、血液感染、尿路感染、手术部位感染和腹泻等。
在免疫能力强的宿主中,植物相关微生物可能成为“天然疫苗”,刺激免疫系统并增强微生物多样性以维持我们的健康。
生活中对于食品的保存也至关重要,不当的保存方法会导致有害微生物大量繁殖,影响食物的风味及安全,进而影响人体健康。
了解食品微生物的组成和功能及其相互作用对于人体微生物多样性和系统健康非常重要。微生物检测、多组学整合可以提供技术解决方案,而益生菌、益生元和合生元可以提供改善方案。
主要参考文献
Wicaksono WA, Cernava T, Wassermann B, Abdelfattah A, Soto-Giron MJ, Toledo GV, Virtanen SM, Knip M, Hyöty H, Berg G. The edible plant microbiome: evidence for the occurrence of fruit and vegetable bacteria in the human gut. Gut Microbes. 2023 Dec;15(2):2258565.
Soto-Giron MJ, Kim JN, Schott E, Tahmin C, Ishoey T, Mincer TJ, DeWalt J, Toledo G. The Edible Plant Microbiome represents a diverse genetic reservoir with functional potential in the human host. Sci Rep. 2021 Dec 15;11(1):24017.
Berg G, Erlacher A, Smalla K, Krause R. Vegetable microbiomes: is there a connection among opportunistic infections, human health and our ‘gut feeling’? Microb Biotechnol. 2014 Nov;7(6):487-95.
Abdelfattah A, Tack AJM, Lobato C, Wassermann B, Berg G. From seed to seed: the role of microbial inheritance in the assembly of the plant microbiome. Trends Microbiol. 2023 Apr;31(4):346-355.
Abdelfattah A, Freilich S, Bartuv R, Zhimo VY, Kumar A, Biasi A, Salim S, Feygenberg O, Burchard E, Dardick C, Liu J, Khan A, Ellouze W, Ali S, Spadaro D, Torres R, Teixido N, Ozkaya O, Buehlmann A, Vero S, Mondino P, Berg G, Wisniewski M, Droby S. Global analysis of the apple fruit microbiome: are all apples the same? Environ Microbiol. 2021 Oct;23(10):6038-6055.
Mendes R, Garbeva P, Raaijmakers JM. The rhizosphere microbiome: significance of plant beneficial, plant pathogenic, and human pathogenic microorganisms. FEMS Microbiol Rev. 2013 Sep;37(5):634-63.
Li J, Wang Z, Karim MR, Zhang L. Detection of human intestinal protozoan parasites in vegetables and fruits: a review. Parasit Vectors. 2020 Jul 29;13(1):380.

谷禾健康
乳杆菌属(Lactobacillus)是厚壁菌门乳杆菌科下的一类革兰氏阳性菌,最早于19世纪在酸奶中发现。
乳杆菌在自然界中分布很广,在植物体表、乳制品、肉制品、葡萄酒、发酵面团、污水以及人畜粪便中,均可分离到。在人类中,乳杆菌属成员定植于胃肠道、口腔和女性泌尿生殖道。
★ 乳杆菌的特性
• 消化和代谢蛋白质和碳水化合物
• 合成B族维生素和维生素K
• 分解代谢胆汁盐
• 增强先天性和获得性免疫力
• 抑制促炎介质
• 对一系列病原体具有抗菌活性
✦乳杆菌的应用
乳杆菌被广泛应用于各种领域中:
•食品工业
乳杆菌被广泛应用于食品工业中,如酸奶、奶酪的制作中。乳杆菌能够发酵乳糖产生乳酸,使得食品呈现出酸味和口感。
•医药领域
乳杆菌被用于制作口服制剂、肠内营养制剂、抗生素辅助治疗等药物。能够调节肠道微生物群落的平衡,促进食物消化和营养吸收,缓解肠道炎症和感染。
•保健品领域
乳杆菌被应用于保健品领域,如乳酸菌饮料、乳酸菌片等。乳杆菌能够改善肠道菌群平衡,增强免疫力,促进身体健康。
•环境领域
乳杆菌被应用于环境领域,如土壤修复、废水处理等。乳杆菌能够分解有机物质,促进土壤肥力和水质净化。
★ 乳杆菌对人体健康非常重要
随着对微生物群落的研究逐渐深入,乳杆菌的作用也逐渐被人们所认识。
乳杆菌对人体有着重要的作用,在肠道健康及女性阴道健康中扮演不可或缺的角色。具有多种生理功能,能够维护菌群平衡、改善消化功能、提高免疫力,除此之外还会影响一些疾病的进展。
本文主要讨论和介绍乳杆菌的菌属特性,生态代谢特征,对人体肠道健康、阴道健康以及一些疾病的影响,在最后还介绍了一些补充乳杆菌的方法。
目录/contents
Part1:认识乳杆菌
Part2:乳杆菌与肠道健康
Part3:乳杆菌与阴道健康
Part4:乳杆菌与其他疾病
Part5:如何补充乳杆菌
Part6:结语
▸ 乳杆菌、乳酸杆菌和乳酸菌
乳杆菌属(Lactobacillus),有时也会翻译成乳酸杆菌,是革兰氏阳性兼性厌氧或微需氧的棒状细菌,通常是乳酸菌的一种。
乳杆菌属包括多种菌种,如乳酸杆菌、嗜酸乳杆菌、肠道乳杆菌等。它们通常是革兰氏阳性、非芽孢杆菌,能够在无氧或微氧条件下进行发酵,产生乳酸等有益物质。
乳酸菌包括多种菌属,如乳杆菌属、双歧杆菌属、嗜酸乳球菌属等。它们能够在无氧或微氧条件下进行发酵,产生乳酸等有益物质。乳酸菌在人体内具有多种功能,如维护肠道菌群平衡、增强免疫力、促进营养物质吸收等。
因此,乳杆菌属(乳酸杆菌)是乳酸菌的一种,而乳酸菌则是一个更广泛的概念,包括多种菌属。
▸ 形态特征
乳杆菌属于革兰氏阳性菌,呈细长的杆状,但无分枝,无芽孢,一般大小约为0.5-1.5μm×2-10μm(某些大杆菌如保加利亚乳杆菌可能更大)。菌落呈圆形、白色(有时黄色)、半透明。
细胞壁:乳杆菌的细胞壁主要由肽聚糖和多糖组成,具有较强的抗菌作用。
运动性:乳杆菌通常是非运动性的,即不具有鞭毛或纤毛。菌毛首先在鼠李糖乳杆菌(Lactobacillus rhamnosus GG)中观察到,它从细菌细胞中突出,在粘附到上皮细胞中起主要作用。
乳杆菌菌落


Talib N,et al.Molecules.2019
注:a是在MRS培养基上从开菲尔样品中分离的乳酸杆菌菌落; b是在MRS培养基上从开菲尔样品中单筛选分离的乳酸杆菌
▸ 分类及主要种群
乳杆菌属是乳杆菌科中最大的一个属。该属的成员已经有超过200种。具体见附录一。
主要有德氏乳杆菌保加利亚亚种(保加利亚乳杆菌)、嗜酸乳杆菌、干酪乳杆菌、罗伊氏乳杆菌、惰性乳杆菌等。
此外卫生部公布可用于生产普通食品的乳杆菌还有卷曲乳杆菌、德氏乳杆菌乳亚种、发酵乳杆菌、格氏乳杆菌、瑞士乳杆菌、约氏乳杆菌、副干酪乳杆菌、植物乳杆菌、唾液乳杆菌等。
乳杆菌属中最具代表性的物种以其在食品发酵中的应用而闻名,并且特定菌株已被认为具有益生菌特性。乳酸杆菌的健康方面促使许多研究人员积极筛选这些细菌的许多潜在来源。因此,在过去 15 年中观察到新物种的爆炸式增长。
尽管许多早期描述的物种被转移到新创建的属(Atopobium、Carnobacterium、Eggerthia、 Weissella 、Fructobacillus等)该属在系统发育和表型标记方面仍然存在异质性。Pediococcus属、Paralactobacillus 属与Lactobacillus 混合在一起,表明对该属进行进一步的分类学细分很可能甚至是必要的。
▸ 生长环境和条件
乳杆菌广泛存在于自然界中,包括土壤、水体、植物、动物等环境中。乳杆菌作为一种常见的益生菌,也存在于人体的口腔、肠道、阴道等部位。
乳杆菌的生长环境主要包括以下几个方面:
pH值:乳杆菌适宜生长的pH范围一般在4.5-6.5之间(某些耐酸种群可能在3.8仍能生长),其中以5.5-6.0最为适宜。
温度:乳杆菌的生长温度一般在20-45℃之间,其中以30-40℃最为适宜。
氧气需求:乳杆菌是一种厌氧菌,不需要氧气就能生长。
营养物质:乳杆菌需要一定的营养物质才能生长,主要包括碳源、氮源、矿物质、维生素等。
注:不同种类的乳杆菌对营养物质的需求可能会有所不同
▸ 乳杆菌的代谢
乳杆菌是过氧化氢酶阴性革兰氏阳性微生物,主要产生乳酸作为碳水化合物发酵的主要代谢终产物。
参与的KEGG途径具体见附录二。
▸ 乳杆菌的作用
乳杆菌是一种益生菌,对人体健康有着重要的作用。以下是乳杆菌的主要作用:
维护肠道菌群平衡:乳杆菌能够抑制有害菌的生长,维护肠道菌群平衡,防止肠道感染和炎症。
改善消化功能:乳杆菌能够分解食物中的纤维素和其他难以消化的物质,促进食物消化和营养吸收。
提高免疫力:乳杆菌能够增强肠道黏膜屏障的功能,防止有害物质进入血液循环,提高免疫力。
缓解过敏反应:乳杆菌能够调节免疫系统的反应,减轻过敏反应的症状。
降低胆固醇:乳杆菌能够降低血液中的胆固醇水平,预防心血管疾病。
改善口腔健康:乳杆菌能够抑制口腔中有害菌的生长,预防龋齿和口臭。
总之,乳杆菌对人体健康有着多方面的益处,是一种非常重要的益生菌。
• 乳杆菌也有可能是机会性病原体
乳杆菌中主要的病原菌或致病菌包括:
它们也有可能是机会性病原体,可引起脓肿、菌血症、心内膜炎、肺部感染和新生儿脑膜炎等多种感染。
注:大多数由乳酸杆菌引起的疾病都发生在免疫功能低下的人或那些有糖尿病等易感病症的人身上。
乳杆菌在人体的位置及与人体的关系
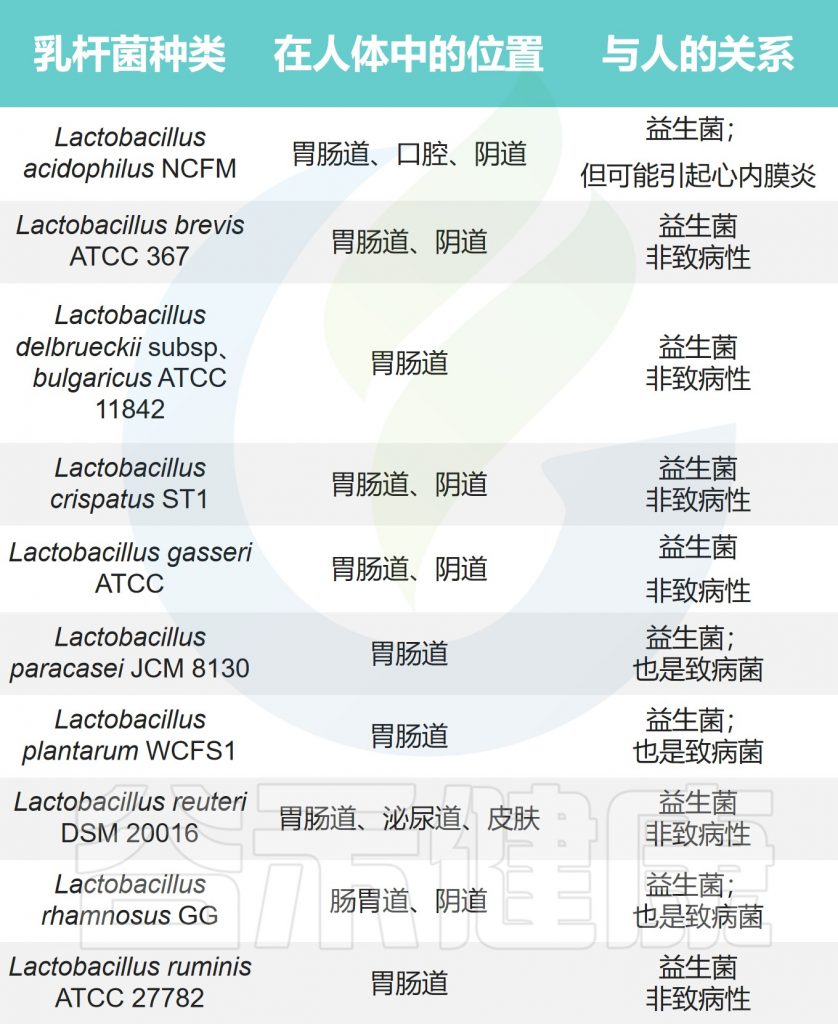

Zafar H,et al.Genes (Basel).2020
▸ 乳杆菌的表面活性分子
乳杆菌的益生菌特性被认为是由乳杆菌表面活性分子 (SAM) 贡献的。据报道,支持益生菌作用的表面活性分子包括肽聚糖、细菌多糖和磷壁酸等。
乳杆菌细胞表面结构
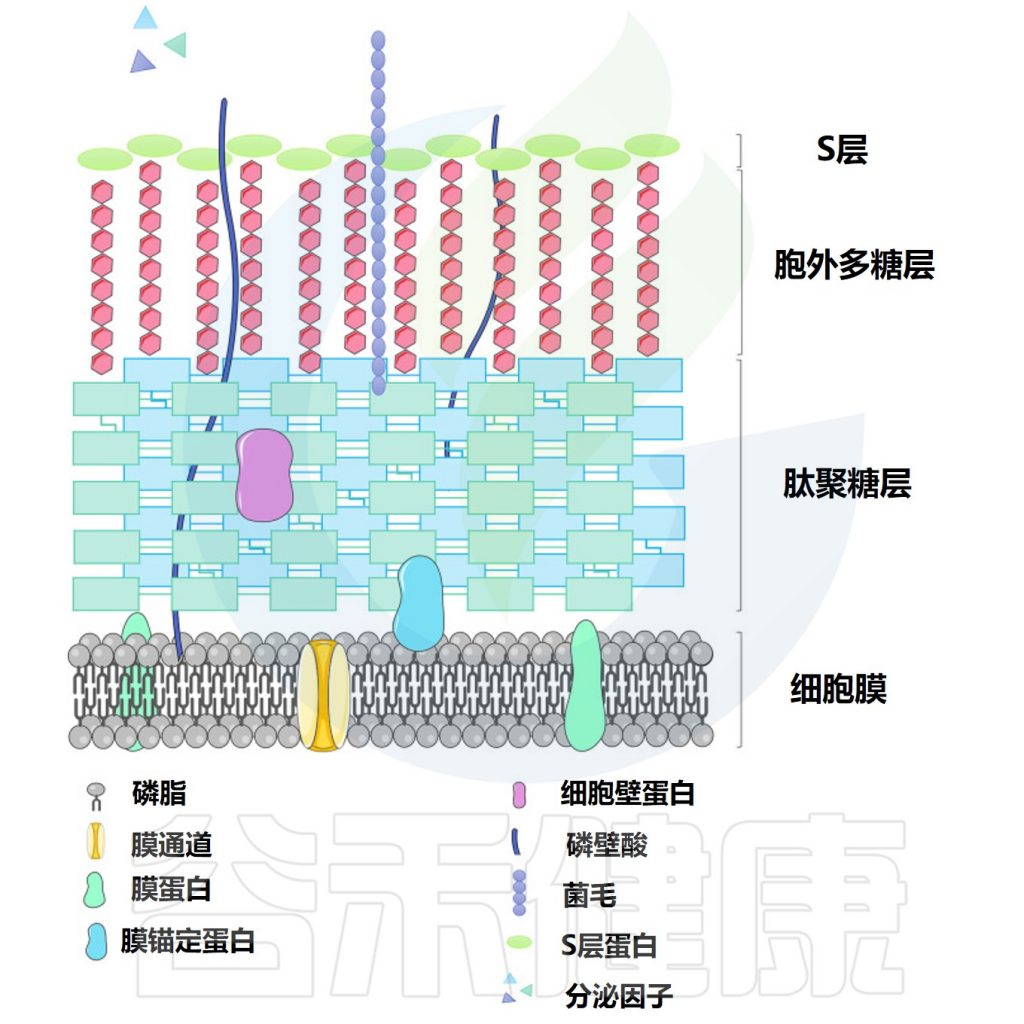

Dempsey E,et al.Front Immunol.2022
通常,乳杆菌的细胞质膜被肽聚糖和其他生物聚合物包围,即磷壁酸、S层蛋白和多糖。
• 肽聚糖
肽聚糖(PG)是一种生物聚合物,包含由N-乙酰氨基葡萄糖(GlcNAc)和N-乙酰胞壁酸(MurNAc)侧链连接的聚糖链,形成革兰氏阳性菌(如乳杆菌和双歧杆菌)的细胞表面。
改善宿主先天免疫
乳杆菌肽聚糖在改善宿主先天免疫反应方面表现出出色的免疫调节活性。例如,干酪乳杆菌(L.casei)肽聚糖能够通过toll样受体2和核苷酸结合寡聚化结构域2(NOD2)诱导小鼠腹腔巨噬细胞产生白细胞介素12。
此外,植物乳杆菌(L. plantarum CAU1055)肽聚糖通过抑制一氧化氮合酶、环氧合酶-2(COX-2)和细胞因子(TNF-α和白细胞介素-6),显示出改善小鼠巨噬细胞中一氧化氮诱导的炎症的能力。
• 脂磷壁酸
乳杆菌肽聚糖通常用磷壁酸或脂磷壁酸修饰。脂磷壁酸由磷酸甘油的聚合产生,并与细胞质膜结合。
调节宿主的信号通路
脂磷壁酸与其他表面活性分子一起调节宿主模式识别受体和宿主的几种信号通路,这些信号通路是乳杆菌的益生菌和抗病原体作用的原因。
植物乳杆菌脂磷壁酸显著抑制粪便大肠杆菌生物膜的形成,并在人类牙本质切片上形成生物膜,这表明脂磷壁酸可以作为粪便大肠杆菌感染的预防和治疗措施。
• 细菌多糖
细菌在细胞表面形成紧密连接的聚合物,并将其作为胞外多糖(EPS)(松散未附着的黏液)释放到环境中。
细菌分泌的胞外多糖对于宿主-微生物相互作用过程中的粘附和细胞识别至关重要。乳杆菌的胞外多糖还能抑制蜡样芽孢杆菌(Bacillus cereus)产生的细菌毒素。
▸ 影响乳杆菌的因素
乳杆菌对人体健康有着重要的作用。然而乳杆菌的数量和种类受到多种因素的影响,包括以下几方面:
饮食因素:饮食中富含益生元的食物,如蔬菜、水果、全麦面包等,可以促进乳杆菌的生长。相反,高脂肪、高糖、高盐等不健康的饮食习惯会抑制乳杆菌的生长。
药物因素:长期使用抗生素、非甾体抗炎药等药物会破坏肠道菌群平衡,抑制乳杆菌的生长。
生活方式因素:缺乏运动、长期处于压力状态等生活方式因素也会影响肠道菌群的平衡,抑制乳杆菌的生长。
年龄因素:婴幼儿期肠道菌群构成不稳定,乳杆菌数量较少,随着年龄的增长,乳杆菌数量逐渐增加。
综上所述,保持健康的饮食习惯、合理使用药物、积极的生活方式等都有助于促进乳杆菌的生长。
乳杆菌已被证明对改善胃肠道健康具有重要作用,本章节将具体展开讲述。
胃肠道粘膜是机体最大也是最关键的屏障部位之一,外来抗原、微生物和潜在病原体都在这里与宿主的免疫系统密切接触。
它是一种半透性屏障,允许吸收营养和免疫感应,同时限制潜在有害抗原或微生物的流入。
胃肠道屏障由四个主要元素组成:共生微生物群、粘液层——含有分泌型免疫球蛋白A(sIgA)和抗微生物肽、肠上皮细胞单层和肠道相关淋巴组织(GALT)构成胃肠道隔室中的各种免疫细胞群。
肠道屏障破坏与多种疾病相关
肠道屏障功能的丧失被认为是各种胃肠道疾病发病机制的早期事件,例如乳糜泻和炎症性肠病,以及包括I型糖尿病、肥胖症和多发性硬化症在内的全身性疾病。所以肠道屏障的完整性对于健康至关重要。
★ 乳杆菌可以增强肠道屏障
肠道屏障功能可以通过摄入非致病微生物来增强,这些微生物可以增强粘液层的物理屏障,增强对病原体的先天防御并降低肠上皮细胞的细胞旁通透性。
作为益生菌食用的乳杆菌被认为可以通过多种作用机制调节天然肠道微生物群并改善健康。如图所,益生菌通过增加粘液的产生、刺激抗微生物肽的释放和分泌性免疫球蛋白A的产生来增强肠道屏障功能,增加肠上皮细胞的紧密连接完整性并提供对病原体的抵抗力。
乳杆菌增强肠道屏障的机制
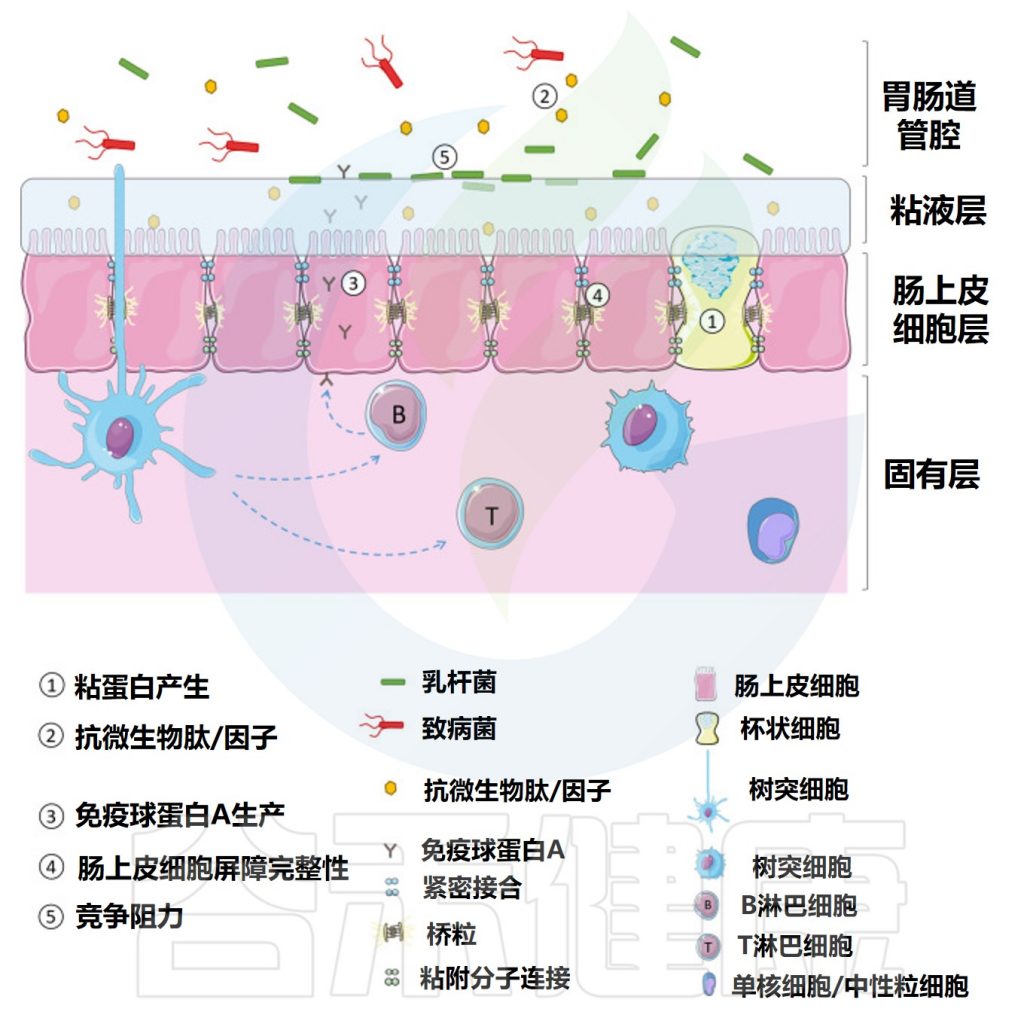

Dempsey E,et al.Front Immunol.2022
1 粘液分泌
胃肠道的杯状细胞表达杆状粘蛋白,这些粘蛋白要么粘附在上皮细胞上,要么释放到胃肠道腔中。这些粘蛋白高度糖基化并通过二硫键连接在一起形成糖蛋白基质,保护肠上皮免受肠腔内容物(含有消化酶)的影响,防止致病抗原/细菌与上皮单层之间的相互作用,并有助于胃肠道运动。
粘液层的厚度通常在50-800µm之间,在健康个体中,最靠近上皮表面的前30µm应该没有微生物。
乳杆菌通过促进粘液分泌增强胃肠道屏障
乳酸菌种被认为通过促进粘液分泌来增强肠道屏障防御。体外研究表明,来自干酪乳杆菌(L.casei T21)的条件培养基可以上调受到艰难梭菌攻击的结肠上皮细胞中的粘膜保护性基因。
在体内研究方面, L. rhamnosus CNCM I-3690 最近被证明可以保护或恢复杯状细胞种群并保护小鼠在低度结肠炎症后的粘液层厚度。
类似地,施用两种罗伊氏乳杆菌(L. reuteri R2LC 或4659)菌株之一并暴露于结肠炎的小鼠表现出降低的结肠炎严重程度,归因于给予益生菌的小鼠粘液厚度增加。
2 抗菌肽、抗菌因子
宿主产生的胃肠道抗菌肽通常分为导管素和防御素。抗菌肽可以被丁酸盐激活。
丁酸盐由肠道微生物群产生,但很少有研究检查益生菌对导管素表达的影响。
防御素进一步分为β-防御素,由整个肠道的上皮细胞产生,以及α-防御素,在小肠中表达。防御素在胃肠道中组成型表达,对许多细菌、真菌和一些病毒显示出抗微生物活性。
乳杆菌诱导抗菌肽表达
嗜酸乳杆菌(L. acidophilus PZ1138)和发酵乳杆菌(L. fermentum PZ1162)显示可通过促炎机制在细胞中诱导人β-防御素-2基因的表达。除了上调促炎介质外,给肉鸡施用罗伊氏乳杆菌(L.reuteri)还与盲肠和回肠中的抗菌肽调节相关。
除了宿主衍生的抗菌肽刺激外,共生细菌还产生抗菌因子以帮助宿主屏障防御。这些因素包括短链脂肪酸、过氧化氢和细菌素。
短链脂肪酸刺激紧密连接的形成
乳杆菌产生包括乙酸盐、丙酸盐和丁酸盐在内的短链脂肪酸,这些短链脂肪酸已被证明在体外通过抑制NLRP3炎症小体和自噬来增加跨上皮电阻并刺激肠上皮细胞中紧密连接的形成。
细菌素抑制或杀死其他细菌
细菌素是由多种细菌产生的核糖体合成的热稳定肽,其功能是抑制或杀死其他细菌的生长。
革兰氏阳性菌产生的细菌素通常通过破坏膜功能发挥其抗生素作用,通常针对其他革兰氏阳性菌,但一些革兰氏阴性菌也可能易感。
植物乳杆菌产生多种细菌素,这些细菌素对食源性病原体(如李斯特菌)和食品腐败菌具有抗微生物活性,可用于食品生产以减少化学防腐剂的使用。
3 免疫球蛋白A
免疫球蛋白A的产生是胃肠道在非炎症模式下产生免疫保护的重要方式。IgA二聚体(由位于淋巴结或固有层的肠道B细胞分泌)与上皮细胞基底外侧表面的受体相互作用,转移到上皮细胞表面并作为分泌型免疫球蛋白A(sIgA)释放。
分泌型免疫球蛋白A(sIgA)是一种非常重要的抗体分子,在人体抵抗疾病的第一道防线起决定性作用。
sIgA主要通过结合饮食抗原和粘液中的潜在病原体并下调共生细菌上促炎细菌表位的表达来促进肠道中合适的共生细菌群落的维持。
此外,sIgA通过阻断参与上皮粘附的微生物成分增强肠道屏障,促进上皮内防御病原体和微生物产物。
乳杆菌可以增加小肠中slgA水平
已知包括副干酪乳杆菌(L.paracasei MCC1849)、加氏乳杆菌(L.gasseri SBT2055)和植物乳杆菌在内的各种乳杆菌菌株可增加小肠中的sIgA水平。
在一项针对12至24个月大儿童的临床试验中,补充植物乳杆菌增加了sIgA粪便滴度,并且观察到这与TGF-β1/TNF-α比率之间存在显著正相关。
4 上皮细胞屏障
如前所述,肠上皮细胞形成单层细胞,充当肠腔外部环境和宿主免疫系统之间的物理屏障。该屏障的完整性由紧密连接确保,紧密连接是将细胞紧密结合在一起的多蛋白复合物以及粘附连接、间隙连接和桥粒。
紧密连接位于上皮细胞的顶端侧。它们由跨膜蛋白组成,这些蛋白在细胞外与邻近细胞中紧密连接的类似蛋白质相互作用,在细胞内通过封闭小带蛋白和丝状肌动蛋白与细胞自身的细胞骨架相互作用。
病原菌感染会破坏紧密紧密连接蛋白
在慢性炎症性疾病中观察到紧密连接完整性的丧失,在肠道病原体如艰难梭菌、大肠杆菌、鼠伤寒沙门氏菌、霍乱弧菌等的感染中观察到破坏紧密连接蛋白以突破胃肠道屏障的机制。
乳杆菌增强紧密连接蛋白和闭合蛋白表达
已证明鼠李糖乳杆菌上调Caco-2细胞中的紧密连接蛋白1(ZO-1)的表达。这种益生菌菌株可提高ZO-1的表达水平并增强闭合蛋白(claudin-1)的分布,作为对抗肠出血性大肠杆菌感染的保护机制。
使用各种植物乳杆菌菌株(L. plantarum WCSF1、L. plantarum CGMCC 1258和L. plantarum MB 452)也观察到紧密连接蛋白和闭合蛋白的表达增加。
乳杆菌增强肠上皮屏障保护作用
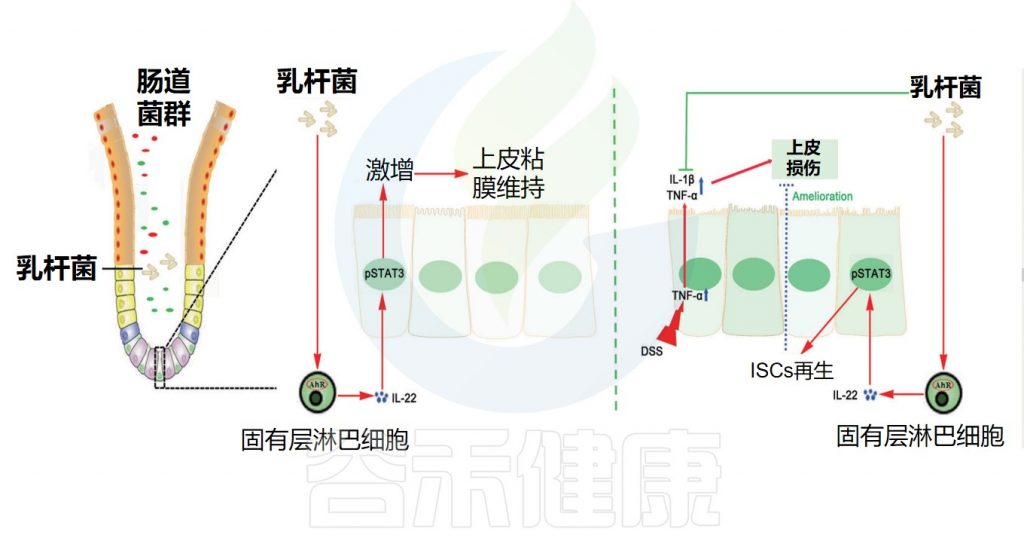

Hou Q,et al.Cell Death Differ.2018
增加E-钙粘蛋白表达,稳定粘附连接
乳杆菌还可以通过增加E-钙粘蛋白的表达,以及通过增强β-连环蛋白的磷酸化来加强E-钙粘蛋白/β-连环蛋白复合物(将粘附连接到细胞骨架)来稳定粘附连接。
钙黏蛋白E——又名上皮细胞钙粘素和CD324,是一种钙依赖性的细胞粘附分子。
在小肠屏障功能的临床研究中,活检样本表明植物乳杆菌(L. plantarum strain TIFN101)和较小程度上L. plantarum WCFS1和CIP104448调节紧密连接和粘附连接蛋白基因表达的增加。
5 竞争结合位点抵抗病原体
乳杆菌还通过竞争肠上皮细胞、粘液层中的糖蛋白或细胞外基质的纤溶酶原上的结合位点来帮助肠道屏障抵抗入侵病原体。
为了促进与宿主细胞的相互作用,乳杆菌属物种在其外表面展示各种不同的成分。这些可能包括细胞壁蛋白、S层蛋白、菌毛蛋白和月光蛋白。
这些表面蛋白促进乳杆菌与宿主的粘附,例如在几种乳杆菌菌株中发现的LPXTG蛋白是与肽聚糖层共价结合的细胞表面蛋白,可以结合粘液和上皮细胞。
通过阻断病原体与位点结合显示抗病毒活性
嗜酸乳杆菌(L. acidophilus ATCC)的S层蛋白通过阻断病原体与C型凝集素受体(DC-SIGN)的粘附而显示出抗病毒活性
C型凝集素受体(DC-SIGN)是一种强烈促进病毒感染的附着因子
如前文所述,乳杆菌通过促进粘液产生和屏障相关蛋白,分泌抗微生物物质(如短链脂肪酸、细菌素)抑制病原体的生长或杀死病原体,来保护肠道屏障免受感染,并通过调节宿主对病原体的免疫反应,防止病原体粘附和竞争结合位点。
★ 乳杆菌可以抑制病原菌感染
因此,乳杆菌能够预防某些细菌感染引起的肠道损伤。乳杆菌已被证明可以抑制病原菌感染的发展,例如艰难梭菌和产气荚膜梭菌、空肠弯曲杆菌、肠炎沙门氏菌、大肠杆菌、金黄色葡萄球菌和耶尔森氏菌等。
由感染引起的两种主要胃肠道疾病,幽门螺杆菌感染和抗生素相关性腹泻,已被证明可以极大地受益于乳杆菌,概述如下。
幽门螺杆菌感染与乳杆菌
幽门螺杆菌感染是世界上最常见的细菌感染之一,全球一半以上的人口受到感染。幽门螺杆菌感染胃的上皮细胞内壁,导致消化性溃疡病、慢性胃炎和胃癌等疾病。
许多感染者没有症状,20%的感染患者会出现胃炎症状、胃或十二指肠溃疡或非霍奇金胃淋巴瘤。
目前推荐的幽门螺杆菌感染治疗方法包括多种抗生素药物和质子泵抑制剂,但随着幽门螺杆菌抗生素耐药性的上升,这种治疗的有效性正在下降。
在各种随机对照试验中,添加乳杆菌(分别为干酪乳杆菌DN-114 001和干酪乳杆菌Shirota)和嗜酸乳杆菌后生元已被证明可以提高该疗法的疗效。
√使幽门螺杆菌活力丧失
来源于干酪乳杆菌(Lactobacillus caseistrain Shirota)的无细胞废培养上清液在体外表现出对幽门螺杆菌的杀菌活性。约氏乳杆菌(L. johnsonii NCC533)和嗜酸乳杆菌均导致幽门螺杆菌活力丧失。
此外,来自这三种乳杆菌菌株的培养物上清液导致幽门螺杆菌的形态改变为U形或球形体,这是细菌的休眠形式,而球形体定植和诱导炎症的能力较低。
已知约氏乳杆菌NCC 533和干酪乳杆菌Shirota也能产生对幽门螺杆菌有活性的细菌素。
√影响幽门螺杆菌运动
幽门螺杆菌是一种螺旋形细菌,具有多个鞭毛,使其能够在胃粘液层中游动并与上皮细胞相互作用,这是在胃中定植所需的能力。
干酪乳杆菌已被证明会导致幽门螺杆菌失去鞭毛运动,这是由于其转化为没有鞭毛的休眠形式,以及通过分泌抑制游泳能力的小型抗微生物化合物。
类似地,约氏乳杆菌(L. johnsonii NCC533)也分泌抑制幽门螺杆菌游泳能力的化合物。
√阻止幽门螺杆菌粘附
为了在胃的低pH中生存,幽门螺杆菌将脲酶表达为一种表面蛋白,以中和周围的酸性环境。嗜酸乳杆菌和约氏乳杆菌的培养物上清液已被证明可降低幽门螺杆菌的脲酶活性。
就粘附性而言,嗜酸乳杆菌阻止了幽门螺杆菌粘附到人HT-29细胞上,导致粘附细胞死亡,并降低了导致其裂解的剩余粘附细胞的脲酶活性。
HT-29细胞——人结直肠腺癌细胞
抗生素相关性腹泻与乳杆菌
抗生素相关性腹泻 (AAD) 是由抗生素破坏肠道正常微生物群引起的,其症状从轻度腹泻到更严重的疾病,如伪膜性结肠炎 (PMC) 。
抗生素相关性腹泻发生在5-30%接受抗生素治疗的患者中,无论是在抗生素治疗期间还是在治疗停止后长达2个月内。
与抗生素相关性腹泻相关的主要病原体之一是艰难梭菌,它导致10-30%的轻症病例和90-100%的重症病例。
注:尽管产气荚膜梭菌、金黄色葡萄球菌和催产克雷伯氏菌等其他微生物与这种疾病有关,但它们并不常见。
√乳杆菌治疗是预防抗生素相关性腹泻的有效措施
虽然在这种情况下益生菌的作用机制尚不清楚,但它们的功效似乎是维持肠道菌群、战胜病原菌、保护肠道屏障功能和潜在的免疫调节。用包括鼠李糖乳杆菌和格氏乳杆菌(L. gasseri)在内的几种乳杆菌菌株治疗已被证明是治疗抗生素相关性腹泻的有效预防措施。
一项分析总结了51项随机对照试验,发现鼠李糖乳杆菌比其他益生菌更有效,但干酪乳杆菌对艰难梭菌感染最有效。另一项研究显示了类似的结果,得出结论认为安全地给予鼠李糖乳杆菌以预防抗生素相关性腹泻并另外控制急性胃肠炎的症状。
前文中有提到乳杆菌在宿主的胃肠道中发挥免疫作用,可增强肠道屏障并保护免受潜在病原体的侵害。
✦乳杆菌的免疫调节作用
乳杆菌的免疫调节作用是通过释放细胞因子实现的,包括白介素、肿瘤坏死因子、干扰素、转化生长因子和来自免疫细胞的趋化因子。
炎症过程取决于促炎细胞因子与抗炎细胞因子,益生菌可以通过这种方式以免疫调节或免疫刺激的方式发挥作用。
降低炎症反应
免疫调节益生菌可降低炎症反应,保护宿主免受自身免疫性疾病、炎症性肠病和过敏的侵害,其特点是产生白细胞介素-10和调节性T细胞。
白细胞介素-10是由单核细胞、T细胞、B细胞、巨噬细胞、NK细胞产生的抗炎细胞因子,可抑制促炎细胞因子、趋化因子和趋化因子受体,从而防止肠道炎症。
免疫刺激性益生菌通过产生白细胞介素-12来激活NK细胞和发育Th1细胞,保护宿主免受感染和癌症发展,并通过平衡Th1和Th2的产生来保护宿主免受过敏。
越来越多的证据表明,乳杆菌有可能预防或治疗某些炎症性疾病:
下调白细胞介素12的产生
L.casei Shirota、L.johnsonii JCM 2012 和L.plantarum ATCC 14917的肽聚糖已被证明可通过Toll样受体2下调白细胞介素-12的产生。
增强了免疫反应
来自鼠李糖乳杆菌(L.rhamnosus CRL1505)的肽聚糖在小鼠鼻腔给药时表现出先天性和适应性免疫反应的增强,改善了Th2型免疫反应。
引发抗炎反应
植物乳杆菌的脂磷壁酸已被显示通过抑制 白细胞介素-8在人和猪肠上皮细胞中引发抗炎反应。
鼠李糖乳杆菌的菌毛的敲除突变体表明,这些菌毛不仅对粘附至关重要,而且具有免疫调节作用。
在小鼠中,源自德氏乳杆菌保加利亚亚种发酵酸奶的胞外多糖具有免疫刺激作用,激活自然杀伤细胞并诱导脾脏产生γ干扰素。
✦乳杆菌代谢物的免疫调剂作用
短链脂肪酸的抗炎作用
一些免疫调节作用是由乳杆菌的代谢物介导的,例如短链脂肪酸,特别是丙酸盐、乙酸盐和丁酸盐。这些后生元与肠上皮细胞上的特定受体结合,以抑制嗜中性粒细胞和巨噬细胞的促炎活性和Treg抑制作用。
丁酸盐灌肠剂已被证明有效并成为转移性结肠炎的公认治疗方法,尽管这被认为是由于对平滑肌的松弛作用。
减少氧化应激作用
乳酸杆菌还能够产生抗氧化剂,如谷胱甘肽 (GSH),并能减少氧化应激。在结肠炎大鼠模型中,保加利亚乳杆菌的两个菌株已被证明可以减少脂质过氧化,增加抗氧化酶的测量值,并减少氧化应激。
在胃损伤小鼠模型中,发酵乳杆菌(L.fermentum Suo)显著降低了丙二醛(一种氧化损伤的量度)浓度和IL-6、IL-12、TNF-α 和IFN-γ的血清浓度。
在健康的人类受试者中,干酪乳杆菌与益生元菊粉一起服用,显著降低了丙二醛和谷胱甘肽二硫化物(另一种氧化测量)的浓度,并增加了抗氧化指标的浓度。
✦分泌蛋白化合物调节免疫
乳杆菌还可以通过分泌蛋白质化合物来调节免疫系统。从鼠李糖乳杆菌(L. rhamnosus GG ATCC 53103)释放的蛋白质p40和p75都激活了Akt信号通路,抑制了肿瘤坏死因子诱导的人和小鼠结肠上皮细胞和小鼠结肠外植体细胞凋亡。
减少炎症损伤
在诱导小鼠结肠炎之前用鼠李糖乳杆菌进行预处理可显著减少结肠炎症和损伤,抑制细胞因子诱导的细胞凋亡并减少过氧化氢诱导的紧密连接破坏。
在鼠李糖乳中发现的两种可溶性蛋白质p40和p75的消耗消除了这些抗炎作用。鼠李糖乳杆菌通过分泌可溶性肽增加小鼠结肠细胞中热休克蛋白HSP25和 HSP72 的产生,这些肽通过激活MAPK信号转导途径发挥作用。
乳杆菌属不仅在人体肠道健康中起着重要作用,在女性阴道健康与相关疾病中的作用也不容忽视。
阴道微生物组在人类阴道健康方面起着重要作用。使用高通量宏基因组和16S rRNA测序,已在人类阴道中鉴定出超过250种细菌。
其中,乳杆菌是健康阴道中最常检测到的微生物,包括卷曲乳杆菌、惰性乳杆菌、詹氏乳杆菌和格氏乳杆菌。
几十年来,乳杆菌通过产生有机酸、细菌素和其他抗菌化合物来防止病原体入侵,被认为对阴道生态有益。
健康阴道中主要乳杆菌的相对丰度决定了细菌群落群的类型,称为群落状态类型(CST)。群落状态类型分为CST I、II、III、IV、V五种。
每个群落均由卷曲乳杆菌(L. crispatus)、加氏乳杆菌(L. gasseri)、惰性乳杆菌(L. iners)、包括乳杆菌和细菌性阴道病相关细菌(BVAB)在内的多种微生物群落占主导地位。
✦阴道微生物群会随时间和外因变化
人类阴道微生物群组成在不同的生命阶段会发生变化,包括婴儿、青春期、怀孕和更年期。
荷尔蒙的变化、抗生素的不受控制的使用、月经和阴道冲洗是导致人类阴道微生物群暂时变化的常见因素。
阴道生态系统破坏的特征是乳杆菌种类的枯竭和非乳杆菌微生物的过度生长。通常,厌氧菌的过度生长会导致异常情况,例如细菌性阴道病以及妊娠相关并发症。
与肠道菌群相比,健康个体阴道微生物环境的一个典型特征是较低的细菌多样性。阴道生态失调的定义是细菌多样性高和厌氧菌混合,通常与多种妇科疾病有关。
惰性乳杆菌(L. iners)存在于健康女性的阴道中,或者存在于阴道生态失调的女性中,例如细菌性阴道病,甚至在接受抗菌治疗的女性中。
▷乳杆菌的丰度与阴道健康有关
许多研究报告说,卷曲乳杆菌(L. crispatus)在阴道中的存在与身体健康有关,而以惰性乳杆菌(L. iners)为主的群落无法提供足够的保护以防止阴道生态失调。
惰性乳杆菌与炎症反应有关
惰性乳杆菌的存在与较高水平的促炎因子有关,例如白细胞介素-1α、白细胞介素-18、巨噬细胞迁移抑制因子和肿瘤坏死因子,它们负责激活阴道中的炎症反应。
惰性乳杆菌甚至被认为在阴道生态失调中起作用,尽管惰性乳杆菌的确切作用仍有争议。然而,惰性乳杆菌的丰度似乎保持相对恒定,惰性乳杆菌不易被病原体或感染条件取代。
惰性乳杆菌在各种条件下的卓越生存能力表明该物种可能是宿主防御的重要成员,并且可能是一种持久的共生乳杆菌可以维持和恢复阴道微生物组的物种。
细菌性阴道病是育龄妇女最常见的阴道炎类型。它的特点是乳杆菌种类显著减少或消失,伴随着以厌氧和兼性厌氧细菌为主的更多样化的微生物群的出现,例如加德纳菌属、普雷沃氏菌属和阴道曲霉。
注:惰性乳杆菌通常是唯一可以在细菌性阴道病期间检测到的与细菌性阴道病相关细菌共存的阴道乳杆菌。由于其能够响应和调节其基因组功能,它可以在细菌性阴道病急剧变化的阴道环境下持续存在。
▷惰性乳杆菌作为微生物指标
由于惰性乳杆菌在细菌性阴道病中共存,惰性乳杆菌的流行可以作为预测细菌性阴道病发病或中期状态的微生物指标。
此外,惰性乳杆菌对甲硝唑具有抗性,即使在用甲硝唑处理后也是阴道中主要的乳杆菌属物种。惰性乳杆菌显示出更强的竞争优势并共存于被破坏的微生物组中。
因此,惰性乳杆菌的持久性可能会导致长期的阴道生态失调,尤其是在重复治疗周期后。需要进一步的研究来阐明该物种是否只是阴道微生物群转变的生物标志物或细菌性阴道病的促成因素。
尽管如此,最近的一项研究发现了一种名为副格氏乳杆菌(Lactobacillus paragasseri)的人类肠道菌株产生的三种细菌素活性肽。
这些细菌素对惰性乳杆菌具有很强的选择性抑制活性,而卷曲乳杆菌(L. crispatus)、加氏乳杆菌(L. gasseri)和詹氏乳杆菌(L. jensenii)仅受到轻微抑制,表明这些乳杆菌衍生的惰性乳杆菌有效抑制剂可以与甲硝唑联合使用,以改善目前的治疗
▷抗生素和乳杆菌组合可显著降低复发率
传统的治疗方法是使用甲硝唑等抗生素。事实上,口服甲硝唑治疗后的复发率非常高,全身使用抗生素有很大的副作用。在这种情况下,急需新的治疗策略。
益生菌的使用可以改善阴道菌群,增加有益菌,减少有害菌的数量,进一步维持阴道菌群环境的稳定。如今,越来越多的证据表明益生菌可有效治疗 细菌性阴道病。
在对30项研究的荟萃分析中,发现益生菌干预降低了复发率,提高了治愈率。
在另一项荟萃分析中,发现与单独使用抗生素相比,抗生素和益生菌的组合使用可显著降低细菌性阴道病的复发率。
乳杆菌在治疗细菌性阴道病的临床研究


Mei Z,et al.Front Cell Infect Microbiol.2022
生物膜是紧密附着在细菌表面的结构,已知它们比一般细胞对宿主免疫反应和抗生素治疗更具抵抗力。
▷生物膜与阴道感染相关
已经表明,阴道上皮细胞上的生物膜形成与阴道感染密切相关。有足够的证据表明细菌性阴道病与多种微生物生物膜的存在有关。
据推测,加德纳菌属(Gardnerella spp.)启动了生物膜的形成,这支持其他细菌性阴道病相关细菌(BVAB)附着在阴道上皮上,进一步增强了生物膜厚度。
此外,加德纳菌生物膜是抗生素的屏障,通过阻止抗生素的渗透来保护其他其他细菌性阴道病相关细菌。人们普遍认为,细菌性阴道病的高复发率是由于生物膜的形成,生物膜可以保护细菌免受抗生素治疗。
▷乳杆菌可以在一定程度上清除生物膜
先前的研究使用了乳杆菌,试图清除多微生物生物膜,并抑制人类阴道中的感染。
据报道,植物乳杆菌可显著降低HT-29细胞系中大肠杆菌、鼠伤寒沙门氏菌、金黄色葡萄球菌和铜绿假单胞菌的粘附,这使其成为治疗细菌性阴道病的潜在抗生物膜剂。
卷曲乳杆菌(L.crispatus)大大降低了来自健康女性和患有细菌性阴道病女性的阴道加特纳菌(G.vaginalis)对宫颈上皮细胞的粘附。
需要注意的是,惰性乳酸杆菌(L. iners)显著降低了健康女性阴道加特纳菌的粘附力,但增强了致病性阴道加特纳菌的粘附。表明惰性乳酸杆菌可以与细菌性阴道病相关的加特纳菌共存,并可能有助于阴道加特纳菌主导的生物膜形成。
进一步了解阴道共生乳杆菌与生物膜的结构和功能之间的相互作用,对于确定生物膜相关感染的新治疗方法至关重要。
宫颈癌是女性生殖道的恶性肿瘤,每年约有30万人死于宫颈癌。
▷感染人乳头瘤病毒后破坏阴道微生态
感染人乳头瘤病毒(HPV)后,可破坏阴道微生态平衡,使乳杆菌数量减少,增加异常菌群的粘附定植。这进一步导致人乳头瘤病毒蛋白表达上调,促进宫颈上皮内瘤变(CIN)的发展,甚至导致宫颈癌的发生。
研究发现HPV阳性女性的阴道细菌多样性更为复杂,阴道微生物群的组成也不同。持续的高危型HPV感染和宫颈微环境的改变加快了宫颈癌前病变的发生发展。
▷乳杆菌对抵抗宫颈癌具有抵抗作用
一项研究首次证明口服卷曲乳杆菌(Lactobacillus curlicus)可以改变阴道群落状态类型并增加HPV清除率。
乳杆菌作为一种阴道益生菌,不仅可以酸化阴道环境,稳定阴道菌群,增强阴道上皮细胞功能,还可以杀灭宫颈癌细胞。增加益生菌摄入量与减缓癌症进展之间存在重要联系。
乳酸菌激活免疫系统,通过分泌多种抗肿瘤代谢物,包括磷酸化多糖和细胞外多糖,抑制恶性肿瘤的增殖。
抑制癌细胞增殖
乳杆菌吸附并占据阴道上皮,防止引起恶性肿瘤的侵袭性病原菌的粘附。乳酸菌可以通过分泌肽聚糖和胞外多糖来抑制癌细胞增殖。
促进细胞因子产生
乳杆菌主要是增强机体的免疫过程,促进细胞因子的产生,抑制单核细胞的增殖。最近的研究表明,乳杆菌如干酪乳杆菌和鼠李糖乳杆菌通过激活自然杀伤细胞和树突状细胞的成熟发挥抗癌作用。
影响体液免疫和细胞免疫
乳杆菌还能影响细胞免疫和体液免疫,促进胸腺源性细胞的增殖和分化,进一步促进骨髓源性细胞的免疫识别和增殖。
对宫颈癌细胞具有细胞毒性
此外,乳杆菌代谢物对宫颈癌细胞也有细胞毒作用。乳酸杆菌的增加属与高危亚型HPV感染、宫颈上皮内瘤变和癌检出率下降有关。
微生物群在癌症的治疗中发挥着越来越重要的作用。乳酸菌作为一种很有前途的非化疗替代疗法,在恢复和维持正常阴道菌群和治疗宫颈癌方面引起了广泛关注。下面总结了一些乳杆菌对宫颈癌细胞的作用:
乳杆菌在宫颈癌中的作用研究


编辑
Mei Z,et al.Front Cell Infect Microbiol.2022
月经周期是扰乱阴道微生物组多样性的最重要因素之一。卷曲乳杆菌(L.crispatus)通常在育龄妇女的阴道中占据主导地位,而惰性乳杆菌(L.iners)在月经周期期间过度生长并取代卷曲乳杆菌。
▷月经期间阴道微生物变化显著
最近的一项研究报告说,惰性乳杆菌(L.iners)是卵泡期最常见的微生物;惰性乳杆菌和CST IV类型(微生物多样性)在排卵期占主导地位;在黄体期,最常见的类型也是CST IV。
事实上,惰性乳杆菌的丰度在月经期间显著增加,通常与阴道加特纳菌或阴道阿托波氏菌(Atopobium vaginae)的增加有关;然而,在没有干预的情况下,它们随后会在月经后减少。
▷感染人乳头瘤病毒后破坏阴道微生态
由于阴道微生物的动态变化,在同一个体月经周期的不同时间具有不同特征,因此月经周期的采样时刻对于阴道群落分析非常重要。
在怀孕期间保持阴道微生物群中乳杆菌的自然和健康平衡尤为重要。早期的研究证实,怀孕期间阴道中的高雌二醇水平和随之而来的高糖原水平会导致阴道酸化更强,从而随着妊娠的进展促进乳杆菌属的流行。
▷怀孕期间阴道微生物可能存在失调
许多研究表明,以惰性乳杆菌(L.iners)为主的阴道微生物组在怀孕期间更有可能转向生态失调。研究发现,在健康孕妇的孕中期和孕晚期,惰性乳杆菌的丰度显著下降,而卷曲乳杆菌(L.crispatus)的丰度在孕中期与孕早期相比有所增加。
▷乳杆菌丰度与早产直接存在关联
越来越多的证据表明细菌性阴道病是导致不良妊娠结局的主要原因之一,尤其是早产。惰性乳杆菌占主导地位的阴道微生物组,被推测是早产的危险因素。
怀孕早期健康女性的阴道涂片中检测到的惰性乳杆菌可能与早产有关。一项研究报告称,在妊娠16周时,由惰性乳杆菌主导的阴道微生物组是短宫颈和早产(<34周)的一个风险因素。
在更具种族多样性的队列中,卷曲乳杆菌的主导地位对早产具有保护作用。来自不同国家的最新研究也表明,乳杆菌与早产发病率增加之间存在显著关联。


先前的研究报告称,在体外受精辅助生殖失败的患者中,高达40%的患者有异常的生殖道微生物组。
阴道生态失调,包括pH值升高、菌群多样性增加、细菌性阴道病、外阴阴道念珠菌病和滴虫性阴道炎,被认为是不孕的危险因素。
▷惰性乳杆菌丰度与不孕相关
一项研究报告称,惰性乳杆菌的丰度与不孕率的增加有关。最近还报道了以惰性乳杆菌为主的阴道微生物组与输卵管性不孕症和沙眼衣原体感染有关。人们认为,以惰性乳杆菌(L. iners)为主的阴道微生物组是怀孕的不利因素。
乳杆菌属作为人体数量最多的细菌之一,不仅仅只是影响了肠道和阴道健康,在全身其他疾病中也有一定作用。
特应性皮炎(AD)是一种慢性炎症性皮肤病,患者经常会因并发过敏性疾病而出现并发症。
尽管特应性皮炎的发病机制尚不清楚,但数十年的研究表明,特应性皮炎的发病机制可能与遗传因素、环境暴露、皮肤屏障受损、免疫功能异常和微生物失衡有关。
•乳杆菌在预防和治疗特应性皮炎中发挥作用
肠道在免疫反应中起着重要作用。乳杆菌是应用最广泛的益生菌。已经研究了几种乳杆菌用特应性皮炎预防和治疗。
乳杆菌通过对致病菌的竞争性排斥和抗菌活性,刺激先天免疫,促进微生物群落平衡。
据报道,这些乳杆菌可以产生多种物质,如有机酸、过氧化氢、低分子量抗菌剂、细菌素和粘附抑制剂。
乳杆菌的给药降低了免疫球蛋白E(IgE)的血清水平,并实现了Th1/Th2的平衡。乳杆菌加速免疫系统的成熟,维持肠道稳态,改善肠道微生物群,最终改善特应性皮炎症状。
用于治疗和预防特应性皮炎的乳杆菌


Xie A,et al.Front Cell Infect Microbiol.2023
肠道屏障、免疫功能和皮肤屏障在给予乳杆菌后得到了改善。下面列出了一些乳杆菌的作用机制。乳杆菌对患有特应性皮炎的动物和人类都显示出一定的作用。
乳杆菌治疗特应性皮炎的作用


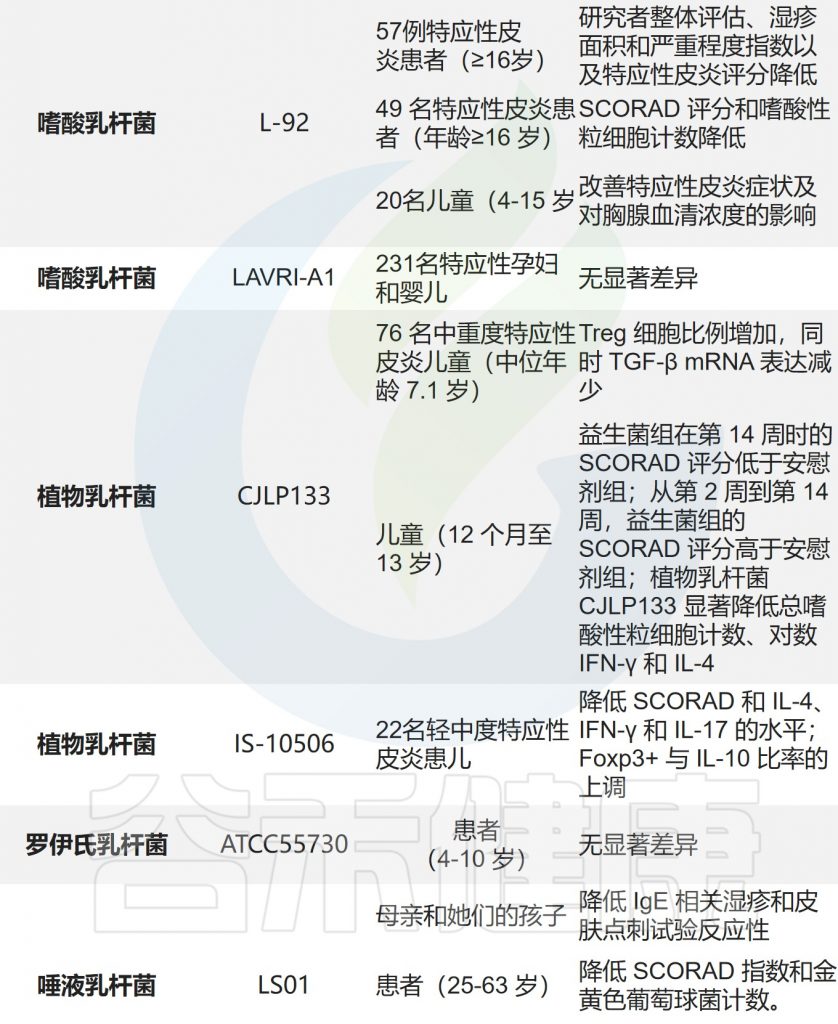



编辑
Xie A,et al.Front Cell Infect Microbiol.2023
肠道微生物群在调节影响全身健康的宿主代谢中起着关键作用。迄今为止,多项研究证实了微生物群与宿主相互作用、调节免疫、控制稳态环境和维持全身状况。
据报道,植物乳杆菌(L. plantarum)具有将亚油酸转化为共轭亚油酸的潜力。根据分子和化学结构,乳杆菌通过多不饱和脂肪酸过程产生的代谢物为10-羟基-顺式-12-十八烯酸(HYA)、10-羟基-十八烯酸(HYB)、10-羟基-反式-11-十八烯酸 (HYC)、10-氧代-顺式-12-十八碳烯酸(KetoA)、10-氧代-十八烷酸(KetoB)和10-氧代-反式 -11-十八碳烯酸 KetoC )。
•乳杆菌代谢物有益于牙周稳态
乳杆菌衍生的生物活性代谢物能带来牙周稳态。HYA和KetoC具有抗氧化、抗炎、抗菌和上皮屏障连接改善剂的作用。
乳杆菌的生物活性代谢物有助于牙周稳态
Sulijaya B,et al.Molecules.2020
• 乳杆菌也可能引起龋齿
虽然链球菌家族细菌(例如变形链球菌)是蛀牙的最常见原因,其他种类的微生物也会引起龋齿。例如,一些乳杆菌属物种与龋齿病例有关。乳酸具有腐蚀牙齿的能力,唾液中的乳杆菌数多年来一直被用作“龋齿测试”。
这是支持在牙膏中使用氟化物的论据之一。乳杆菌的特征是导致现有的龋齿病变进展,尤其是那些在冠状龋齿中的病变。
然而,这个问题很复杂,因为最近的研究表明益生菌可以让有益的乳酸杆菌在牙齿上生长,防止链球菌病原体占据并导致蛀牙。
乳酸菌与口腔健康相关的科学研究是一个新领域,目前发表的研究和结果还很少,需要更多研究。
呼吸道感染是世界上发病率和死亡率最高的疾病之一。尽管许多呼吸道感染具有轻微和自限性,但它们每年在全世界造成400万人死亡。
最近几年严重急性呼吸系统综合症冠状病毒2(也称新型冠状病毒) 在全球肆虐。许多呼吸道病原体没有有效的疫苗,耐药微生物的增加使得呼吸道感染的有效治疗极具挑战性。因此,找到一种安全有效的方法来降低呼吸道感染的风险是很重要的。
•乳杆菌通过肠肺轴影响呼吸系统健康
近年来,许多研究报道肠和肺之间存在串扰,这种被描述为肠-肺轴的联系似乎是双向的 。口服一些益生菌,尤其是乳杆菌,可以通过肠肺轴促进呼吸系统健康。
乳酸杆菌通过肠肺轴调节呼吸免疫的潜在机制
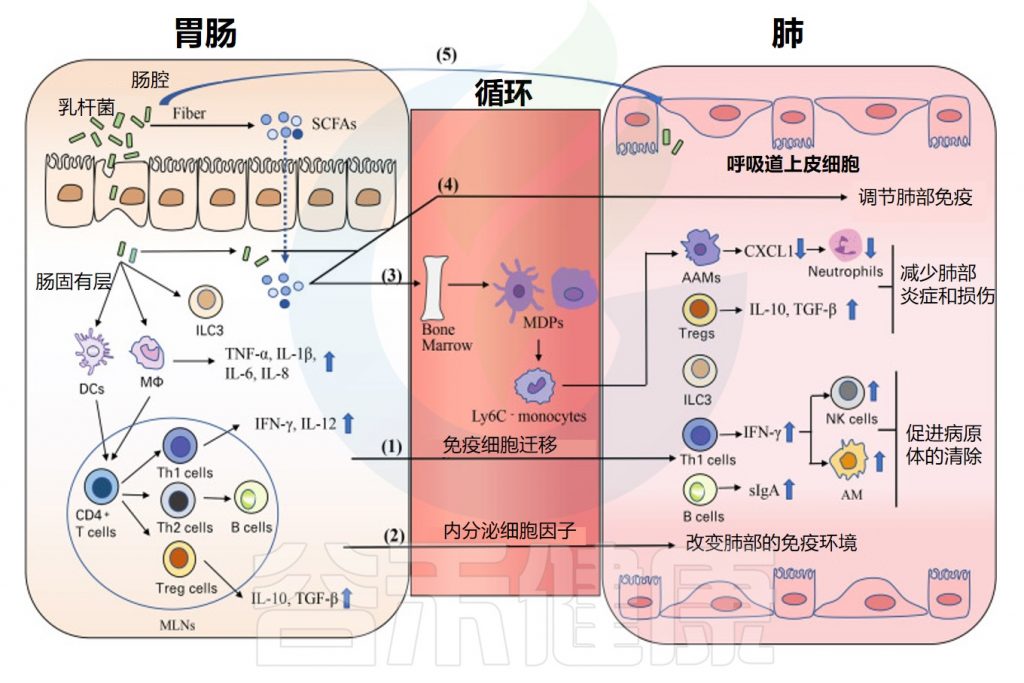

Du T,et al.Front Immunol.2022
最近,乳杆菌已被用于对抗各种呼吸道感染,包括病毒和细菌感染。许多乳杆菌显示可以预防流感病毒感染,包括以下菌株:
L. rhamnosus GG、
L.casei Shirota、
L. plantarum DK119、
L. paracasei MCC1849、
L. gasseri SBT2055、
L. fermentum CJl-112、
L. kunkeei YB38。
此外,乳酸菌由于其安全性和生物技术优势,作为疫苗或佐剂在预防流感病毒感染方面也具有出色的作用。
值得注意的是,补充相同乳杆菌菌株(如鼠李糖乳杆菌CRL1505)的活菌和灭活菌通常具有相似的效果, 表明活力对于乳酸菌达到保护性免疫调节作用不是必需的。
下面是一些通过施用乳杆菌来预防细菌或病毒性呼吸道感染的研究:
乳杆菌预防细菌和病毒性呼吸道感染的研究






Du T,et al.Front Immunol.2022
系统性红斑狼疮是一种慢性自身免疫性疾病,影响大约一半患者的肾脏。狼疮性肾炎(LN)是系统性红斑狼疮发病和死亡的重要危险因素。
狼疮性肾炎与肠壁充血、代谢性酸中毒、频繁使用抗生素有关,所有这些都会对肠道紧密连接产生影响,并导致穿过肠道屏障的细菌代谢产物增加。此外,胃肠道尿素输出增加导致肠道微生物失调。
•乳杆菌混合物有助于恢复黏膜屏障减少肾脏病变
研究发现,5种乳杆菌的混合物(Lactobacillus oris、Lactobacillus rhamnosus、Lactobacillus reuteri、Lactobacillus johnsonii和Lactobacillus gasseri) 通过增加调节性T细胞和抑制致病性Th17细胞来恢复粘膜屏障功能并减少肾脏病变。
表明乳杆菌和乳杆菌衍生的生物活性代谢物在治疗系统性红斑狼疮中具有潜在有益功能。
乳杆菌及其代谢物在系统性红斑狼疮中的有益作用


Wang W,et al.Front Immunol.2022
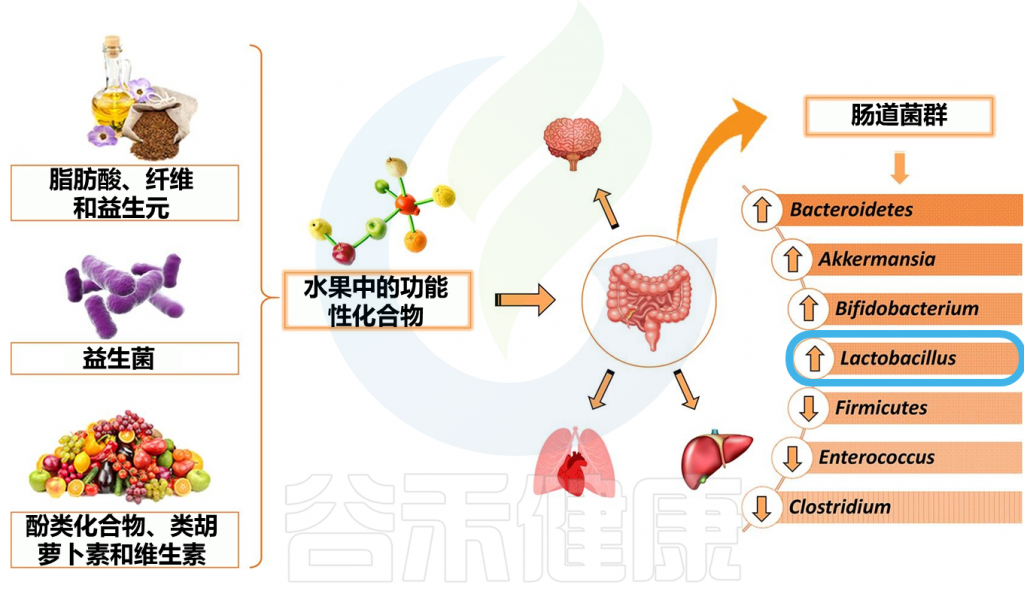

doi.org/10.1016/j.foodres.2022.111809
乳杆菌在人体健康以及一些疾病中起着重要的作用,作为人体不可缺少的一种细菌,我们应该如何补充呢?以下是一些补充乳杆菌的方法:
常见水果
水果中的生物活性物质,包括如胡萝卜素、多酚化合物、维生素和纤维素等,富含这些生物活性物质的水果如香蕉、木莓(树莓)、苹果、芒果、柠檬、石榴、木瓜、猕猴桃等,可以促进乳杆菌属的生长。


食用发酵食品
酸奶、奶酪、酸菜、泡菜、开菲尔、味噌、豆豉等发酵食品中含有丰富的乳杆菌,可以通过食用这些食品来补充乳杆菌。
益生菌
市面上有很多乳杆菌制剂,如乳杆菌素、乳酸菌片等,可以通过口服来补充乳杆菌。
由于补充剂含有不同数量的细菌,因此请阅读包装上的说明。根据补充剂中微生物的数量适量补充。
如果正在服用抗生素,请在抗生素服用2小时之前或者2小时之后服用乳杆菌制剂。
益生元
益生元是一种可以促进肠道内有益菌生长的物质,可以通过食用含有益生元的食品来促进乳杆菌的生长。例如低聚半乳糖(GOS)、低聚果糖(FOS)和母乳低聚糖(HMO)等。
从牛蒡中提取的菊粉促进了有益细菌的生长。菊粉显着增加了小鼠中的乳酸杆菌和双歧杆菌。
将龙舌兰中菊粉等果聚糖添加到正常小鼠饮食中,发现小鼠体内乳酸菌、双歧杆菌数量增加。
全麦谷物可以增加双歧杆菌和乳酸杆菌的相对数量。
一项临床试验(NCT02227602),10名参与者连续8周每天服用200-400克芒果果肉,显著增加乳杆菌、植物乳杆菌、罗伊氏乳杆菌和乳酸乳杆菌的丰度。
还包括其他一些常见食物,例如大蒜、洋葱、韭菜、芦笋、全谷物等,都有助于促进肠道中乳杆菌的生长。


合生元
一项临床试验(NCT 编号:03123510),20 名受试者在接受合生元3个月后,乳杆菌和双歧杆菌显著增加。
注:该研究中的合生元:益生菌成分含有嗜酸乳杆菌DDS-1、乳酸双歧杆菌UABla-12、长双歧杆菌UABl-14和两歧双歧杆菌UABb-10的专利菌株的混合物,益生元成分是一种反式低聚半乳糖混合物。
其他补充剂
乳清和豌豆蛋白的摄入可以增加双歧杆菌和乳酸杆菌的丰度。
灵芝孢子油具有很强的免疫增强活性,有助于肠乳杆菌丰度升高。
绿茶与异麦芽低聚糖联合使用,通过预防小鼠肠道生态失调来对抗高脂肪饮食诱导的代谢改变,双歧杆菌、乳杆菌、罗氏菌属丰度升高。
补充维生素A、维生素C都可以使乳酸杆菌增加。
姜黄素、白藜芦醇、杏仁/杏仁皮可以增加乳酸杆菌。
膳食褐藻糖胶可以增加乳酸杆菌和瘤胃球菌科的丰度。
补充2周葡萄多酚显著提高了断奶后小鼠的乳酸杆菌和Akkermansia的丰度。


中医
对溃疡性结肠炎的患者应用益阳愈溃汤结合针刺治疗,对照组仅给予益阳愈溃汤,治疗后实验组双歧杆菌、乳酸杆菌等均高于对照组。
在连续给药3周后,黄芩促进大鼠结肠的乳酸菌的生长。栀子对乳酸菌双向调节。
黄柏对大鼠肠道乳酸菌的影响:整体表现为促进。
黄连提取物显著促进乳酸菌、双歧杆菌的生长。
吴茱萸碱(EVO)是从吴茱萸中分离出的喹诺酮类生物碱,通过增加嗜酸乳杆菌水平和乙酸盐产生对溃疡性结肠炎具有治疗效果。
山药多糖灌胃健康小鼠一段时间后,发现小鼠盲结肠内的双歧杆菌、乳酸菌均增殖。
马齿苋多糖可使衰老小鼠肠道双歧杆菌及乳酸杆菌数量增加。
蒲公英多糖、黄芪多糖能改善小鼠菌群失调,显著增加双歧杆菌和乳酸杆菌数量。
麦冬多糖 MDG-1 对膳食诱导型肥胖小鼠肠道益生菌群有增殖作用,尤其是一些鼠乳杆菌和台湾乳杆菌。
魔芋低聚糖对三硝基苯磺酸 (TNBS) 诱导溃疡性结肠炎大鼠有保护机制,结肠内乳酸杆菌和双歧杆菌数量增多。
泰山蛹虫草多糖对环磷酰胺 (CY) 免疫抑制小鼠的作用,发现多糖组双歧杆菌、乳酸菌数量均较 CY 模型组增加。
七味白术散能促进小鼠肠道乳酸菌和双歧杆菌的增殖(P<0.05),恢复肠道菌群平衡。
肺癌患者放射治疗后服用养阴清肺汤,治疗12周后,乳酸菌和双歧杆菌含量较对照组均上升(P<0.05)。


辣椒素可降低2型糖尿病小鼠体内乳酸杆菌的丰度。
高盐饮食会使乳酸杆菌的丰度降低。
一些疾病的存在可能与乳杆菌降低相关:
包括阿尔茨海默症、自闭症、炎症性肠病、慢性肝病、过敏疾病、肿瘤、肥胖、牙周病、免疫缺陷病、干燥综合征、系统性红斑狼疮、类风湿关节炎、肾脏疾病等。
注意
虽然乳杆菌在大部分情况下对人体都是有益的,但是过量补充也是不可取的。那么我们如何知道自己体内的乳杆菌含量以及补充是否足够呢?
✔肠道菌群检测可以直观地反映体内乳杆菌丰度
肠道菌群检测是目前较为直观地反映补充剂和食物对肠道乳杆菌影响的方法,通过使用高通量测序技术评估肠道中乳杆菌的菌群丰度。
如果通过检测发现乳杆菌处于正常水平,则不需要额外补充,过高的乳杆菌水平并不一定代表更健康;如果发现乳杆菌缺乏,那么可以通过前文所讲的方法进行补充,有助于营造更健康的身体。
补充乳杆菌并不是一劳永逸的事情,需要长期坚持。同时,对于某些人群,如免疫力低下、肠道疾病患者等,应在医生的指导下进行补充。
总之,乳杆菌是一类非常重要的益生菌,它们能够帮助我们维护肠道和阴道的健康、提高免疫力、改善消化功能,并且可有效治疗各种疾病,包括细菌性阴道病、特应性皮炎和呼吸道感染,对人体健康有着重要的作用。
我们可以通过食用富含乳杆菌的食物或者补充乳杆菌制剂来增加体内乳杆菌的数量,从而更好地保护我们的健康。
此外,乳杆菌对于食品、化工业、保健品和医药行业也都具有重要价值。有必要进一步研究乳杆菌,在未来发掘它更深层的价值。
附录一:乳杆菌种类
· Lactobacillus acetotolerans
· Lactobacillus acidifarinae
· Lactobacillus acidipiscis
· Lactobacillus acidophilus
· Lactobacillus agilis
· Lactobacillus algidus
· Lactobacillus alimentarius
· Lactobacillus alvei
· Lactobacillus alvi
· Lactobacillus amylolyticus
· Lactobacillus amylophilus
· Lactobacillus amylotrophicus
· Lactobacillus amylovorus
· Lactobacillus animalis
· Lactobacillus animata
· Lactobacillus antri
· Lactobacillus apinorum
· Lactobacillus apis
· Lactobacillus apodemi
· Lactobacillus aquaticus
· Lactobacillus aviarius
· Lactobacillus backii
· Lactobacillus bifermentans
· Lactobacillus bombi
· Lactobacillus bombicola
· Lactobacillus brantae
· Lactobacillus brevis
· Lactobacillus brevisimilis
· Lactobacillus buchneri
· Lactobacillus cacaonum
· Lactobacillus camelliae
· Lactobacillus capillatus
· Lactobacillus casei group
· Lactobacillus catenefornis
· Lactobacillus ceti
· Lactobacillus coleohominis
· Lactobacillus collinoides
· Lactobacillus composti
· Lactobacillus concavus
· Lactobacillus coryniformis
· Lactobacillus crispatus
· Lactobacillus crustorum
· Lactobacillus curieae
· Lactobacillus curvatus
· Lactobacillus delbrueckii
· Lactobacillus dextrinicus
· Lactobacillus diolivorans
· Lactobacillus equi
· Lactobacillus equicursoris
· Lactobacillus equigenerosi
· Lactobacillus fabifermentans
· Lactobacillus faecis
· Lactobacillus faeni
· Lactobacillus farciminis
· Lactobacillus farraginis
· Lactobacillus fermentum
· Lactobacillus floricola
· Lactobacillus florum
· Lactobacillus formosensis
· Lactobacillus fornicalis
· Lactobacillus fructivorans
· Lactobacillus frumenti
· Lactobacillus fuchuensis
· Lactobacillus furfuricola
· Lactobacillus futsaii
· Lactobacillus gallinarum
· Lactobacillus gasseri
· Lactobacillus gastricus
· Lactobacillus ghanensis
· Lactobacillus gigeriorum
· Lactobacillus ginsenosidimutans
· Lactobacillus gorillae
· Lactobacillus graminis
· Lactobacillus guizhouensis
· Lactobacillus halophilus
· Lactobacillus hammesii
· Lactobacillus hamsteri
· Lactobacillus harbinensis
· Lactobacillus hayakitensis
· Lactobacillus heilongjiangensis
· Lactobacillus helsingborgensis
· Lactobacillus helveticus
· Lactobacillus herbarum
· Lactobacillus heterohiochii
· Lactobacillus hilgardii
· Lactobacillus hokkaidonensis
· Lactobacillus hominis
· Lactobacillus homohiochii
· Lactobacillus hordei
· Lactobacillus iatae
· Lactobacillus iners
· Lactobacillus ingluviei
· Lactobacillus insectis
· Lactobacillus insicii
· Lactobacillus intermedius
· Lactobacillus intestinalis
· Lactobacillus iwatensis
· Lactobacillus japonicus
· Lactobacillus jensenii
· Lactobacillus johnsonii
· Lactobacillus kalixensis
· Lactobacillus kefiranofaciens
· Lactobacillus kefiri
· Lactobacillus kimbladii
· Lactobacillus kimchicus
· Lactobacillus kimchiensis
· Lactobacillus kisonensis
· Lactobacillus kitasatonis
· Lactobacillus koreensis
· Lactobacillus kullabergensis
· Lactobacillus kunkeei
· Lactobacillus larvae
· Lactobacillus leichmannii
· Lactobacillus letivazi
· Lactobacillus lindneri
· Lactobacillus malefermentans
· Lactobacillus mali
· Lactobacillus manihotivorans
· Lactobacillus mellifer
· Lactobacillus mellis
· Lactobacillus melliventris
· Lactobacillus mindensis
· Lactobacillus mixtipabuli
· Lactobacillus mobilis
· Lactobacillus mucosae
· Lactobacillus mudanjiangensis
· Lactobacillus murinus
· Lactobacillus nagelii
· Lactobacillus namurensis
· Lactobacillus nantensis
· Lactobacillus nasuensis
· Lactobacillus nenjiangensis
· Lactobacillus nodensis
· Lactobacillus odoratitofui
· Lactobacillus oeni
· Lactobacillus oligofermentans
· Lactobacillus oris
· Lactobacillus oryzae
· Lactobacillus otakiensis
· Lactobacillus ozensis
· Lactobacillus panis
· Lactobacillus pantheris
· Lactobacillus parabrevis
· Lactobacillus parabuchneri
· Lactobacillus paracasei
· Lactobacillus paracollinoides
· Lactobacillus parafarraginis
· Lactobacillus parakefiri
· Lactobacillus paralimentarius
· Lactobacillus paraplantarum
· Lactobacillus pasteurii
· Lactobacillus paucivorans
· Lactobacillus pentosus
· Lactobacillus perolens
· Lactobacillus plantarum
· Lactobacillus pobuzihii
· Lactobacillus pontis
· Lactobacillus porcinae
· Lactobacillus psittaci
· Lactobacillus rapi
· Lactobacillus rennanquilfy
· Lactobacillus rennini
· Lactobacillus reuteri
· Lactobacillus reuterii
· Lactobacillus rhamnosus
· Lactobacillus rodentium
· Lactobacillus rogosae
· Lactobacillus rossiae
· Lactobacillus ruminis
· Lactobacillus saerimneri
· Lactobacillus sakei
· Lactobacillus salivarius
· Lactobacillus sanfranciscensis
· Lactobacillus saniviri
· Lactobacillus satsumensis
· Lactobacillus secaliphilus
· Lactobacillus selangorensis
· Lactobacillus senioris
· Lactobacillus senmaizukei
· Lactobacillus sharpeae
· Lactobacillus shenzhenensis
· Lactobacillus sicerae
· Lactobacillus silagei
· Lactobacillus siliginis
· Lactobacillus similis
· Lactobacillus songhuajiangensis
· Lactobacillus sp.
· Lactobacillus sp. 66c
· Lactobacillus sp. 7_1_47FAA
· Lactobacillus sp. Akhmro1
· Lactobacillus sp. BL302
· Lactobacillus sp. C30An8
· Lactobacillus sp. C4I18
· Lactobacillus sp. C4I5
· Lactobacillus sp. CR-609S
· Lactobacillus sp. NRCT-KU 1
· Lactobacillus sp. S16
· Lactobacillus sp. TAB-22
· Lactobacillus sp. TAB-26
· Lactobacillus sp. TAB-30
· Lactobacillus sp. Thmro2
· Lactobacillus sp. oral taxon 052
· Lactobacillus sp. oral taxon 461
· Lactobacillus sp.A A18
· Lactobacillus sp.A A21
· Lactobacillus sp.A A25
· Lactobacillus sp.A A29
· Lactobacillus sp.A A35
· Lactobacillus sp.A A44
· Lactobacillus sp.A A45
· Lactobacillus sp.A A48
· Lactobacillus sp.A A49
· Lactobacillus sp.A A85
· Lactobacillus sp.A A96
· Lactobacillus sp.B A100
· Lactobacillus sp.B A101
· Lactobacillus sp.B A102
· Lactobacillus sp.B A103
· Lactobacillus sp.B A12
· Lactobacillus sp.B A13
· Lactobacillus sp.B A14
· Lactobacillus sp.B A16
· Lactobacillus sp.B A19
· Lactobacillus sp.B A20
· Lactobacillus sp.B A23
· Lactobacillus sp.B A31
· Lactobacillus sp.B A33
· Lactobacillus sp.B A34
· Lactobacillus sp.B A36
· Lactobacillus sp.B A37
· Lactobacillus sp.B A41
· Lactobacillus sp.B A42
· Lactobacillus sp.B A52
· Lactobacillus sp.B A53
· Lactobacillus sp.B A64
· Lactobacillus sp.B A65
· Lactobacillus sp.B A76
· Lactobacillus sp.B A78
· Lactobacillus sp.B A81
· Lactobacillus sp.B A86
· Lactobacillus sp.B A87
· Lactobacillus sp.B A89
· Lactobacillus sp.B A90
· Lactobacillus sp.B A91
· Lactobacillus sp.B A95
· Lactobacillus sp.B A97
· Lactobacillus sp.B A98
· Lactobacillus sp.B AB1
· Lactobacillus sp.B CG1
· Lactobacillus sp.B CG3
· Lactobacillus sp.B CG53
· Lactobacillus sp.B CG63
· Lactobacillus sp.B CG71
· Lactobacillus sp.B CG76
· Lactobacillus spicheri
· Lactobacillus sucicola
· Lactobacillus suebicus
· Lactobacillus sunkii
· Lactobacillus taiwanensis
· Lactobacillus thailandensis
· Lactobacillus tucceti
· Lactobacillus ultunensis
· Lactobacillus uvarum
· Lactobacillus vaccinostercus
· Lactobacillus vaginalis
· Lactobacillus vermiforme
· Lactobacillus versmoldensis
· Lactobacillus vini
· Lactobacillus wasatchensis
· Lactobacillus xiangfangensis
· Lactobacillus yonginensis
· Lactobacillus zymae
附录二:参与的KEGG途径
主要参考文献
Chee WJY, Chew SY, Than LTL. Vaginal microbiota and the potential of Lactobacillus derivatives in maintaining vaginal health. Microb Cell Fact. 2020 Nov 7;19(1):203. doi: 10.1186/s12934-020-01464-4. PMID: 33160356; PMCID: PMC7648308.
Zheng N, Guo R, Wang J, Zhou W, Ling Z. Contribution of Lactobacillus iners to Vaginal Health and Diseases: A Systematic Review. Front Cell Infect Microbiol. 2021 Nov 22;11:792787. doi: 10.3389/fcimb.2021.792787. PMID: 34881196; PMCID: PMC8645935.
Dempsey E, Corr SC. Lactobacillus spp. for Gastrointestinal Health: Current and Future Perspectives. Front Immunol. 2022 Apr 6;13:840245. doi: 10.3389/fimmu.2022.840245. PMID: 35464397; PMCID: PMC9019120.
Mei Z, Li D. The role of probiotics in vaginal health. Front Cell Infect Microbiol. 2022 Jul 28;12:963868. doi: 10.3389/fcimb.2022.963868. PMID: 35967876; PMCID: PMC9366906.
Chen CM, Wu CC, Huang CL, Chang MY, Cheng SH, Lin CT, Tsai YC. Lactobacillus plantarum PS128 Promotes Intestinal Motility, Mucin Production, and Serotonin Signaling in Mice. Probiotics Antimicrob Proteins. 2022 Jun;14(3):535-545. doi: 10.1007/s12602-021-09814-3. Epub 2021 Jul 29. PMID: 34327633; PMCID: PMC9076750.
Sulijaya B, Takahashi N, Yamazaki K. Lactobacillus-Derived Bioactive Metabolites for the Regulation of Periodontal Health: Evidences to Clinical Setting. Molecules. 2020 Apr 29;25(9):2088. doi: 10.3390/molecules25092088. PMID: 32365716; PMCID: PMC7248875.
Xie A, Chen A, Chen Y, Luo Z, Jiang S, Chen D, Yu R. Lactobacillus for the treatment and prevention of atopic dermatitis: Clinical and experimental evidence. Front Cell Infect Microbiol. 2023 Feb 16;13:1137275. doi: 10.3389/fcimb.2023.1137275. PMID: 36875529; PMCID: PMC9978199.
Wang W, Fan Y, Wang X. Lactobacillus: Friend or Foe for Systemic Lupus Erythematosus? Front Immunol. 2022 May 23;13:883747. doi: 10.3389/fimmu.2022.883747. PMID: 35677055; PMCID: PMC9168270.
Du T, Lei A, Zhang N, Zhu C. The Beneficial Role of Probiotic Lactobacillus in Respiratory Diseases. Front Immunol. 2022 May 31;13:908010. doi: 10.3389/fimmu.2022.908010. PMID: 35711436; PMCID: PMC9194447.
Sergeev IN, Aljutaily T, Walton G, Huarte E. Effects of Synbiotic Supplement on Human Gut Microbiota, Body Composition and Weight Loss in Obesity. Nutrients. 2020 Jan 15;12(1):222. doi: 10.3390/nu12010222. PMID: 31952249; PMCID: PMC7019807.
Kim H, Venancio VP, Fang C, Dupont AW, Talcott ST, Mertens-Talcott SU. Mango (Mangifera indica L.) polyphenols reduce IL-8, GRO, and GM-SCF plasma levels and increase Lactobacillus species in a pilot study in patients with inflammatory bowel disease. Nutr Res. 2020 Mar;75:85-94. doi: 10.1016/j.nutres.2020.01.002. Epub 2020 Jan 10. PMID: 32109839.
Wang MX, Lin L, Chen YD, Zhong YP, Lin YX, Li P, Tian X, Han B, Xie ZY, Liao QF. Evodiamine has therapeutic efficacy in ulcerative colitis by increasing Lactobacillus acidophilus levels and acetate production. Pharmacol Res. 2020 Sep;159:104978. doi: 10.1016/j.phrs.2020.104978. Epub 2020 May 30. PMID: 32485282.
Lu F, Li Y, Wang X, Hu X, Liao X, Zhang Y. Early-life polyphenol intake promotes Akkermansia growth and increase of host goblet cells in association with the potential synergistic effect of Lactobacillus. Food Res Int. 2021 Nov;149:110648. doi: 10.1016/j.foodres.2021.110648. Epub 2021 Aug 20. PMID: 34600650.
Borgonovi TF, Virgolin LB, Janzantti NS, Casarotti SN, Penna ALB. Fruit bioactive compounds: Effect on lactic acid bacteria and on intestinal microbiota. Food Res Int. 2022 Nov;161:111809. doi: 10.1016/j.foodres.2022.111809. Epub 2022 Aug 27. PMID: 36192952.
朱晨,段学清,段智璇,谢鑫,张其,田维毅.清热解毒中药黄芩和栀子对大鼠不同肠段菌群的影响[J].中华中医药学刊,2023,42(03):52-57.DOI:10.13193/j.issn.1673-7717.2023.03.012.
朱晨,陈瑞,谢鑫,张其,瞿慧琴,段学清,田维毅.黄柏对大鼠不同肠段主要菌群的影响[J].时珍国医国药,2021,32(12):2851-2855.
崔祥,陶金华,江曙,魏晓燕,徐君,钱大玮,段金廒.黄连提取物与肠道菌群的相互作用研究[J].中草药,2018,49(09):2103-2107.
周欣,付志飞,谢燕,王晓明,李楠,张鹏.中药多糖对肠道菌群作用的研究进展[J].中成药,2019,41(03):623-627.
谭周进,吴海,刘富林,蔡莹,蔡光先,张华玲,曾奥.超微七味白术散对肠道微生物及酶活性的影响[J].生态学报,2012,32(21):6856-6863.
潘婷婷,张爱琴.养阴清肺汤对肺癌患者放疗后皮肤损伤和肠道菌群的影响[J].辽宁中医杂志,2023,50(01):97-100.DOI:10.13192/j.issn.1000-1719.2023.01.028.

谷禾健康
在谷禾肠道菌群健康检测中,我们会看到结果报告中关于维生素的评估如下:

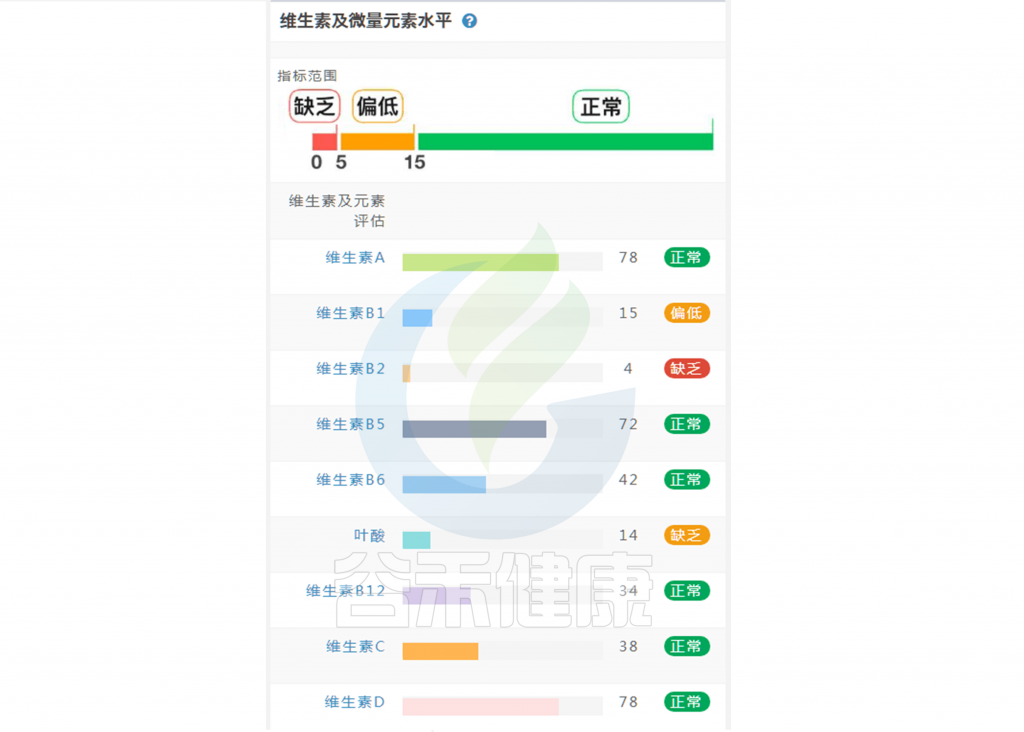
摄入水平建议保持在70-80分之间最佳,如果单项指标低于5表明摄入比例在人群中属于最低的5%,评估为缺乏,如上图中维生素B2;低于15评估为偏低,如上图中叶酸;达到或超过95则表明该项指标可能摄入比例偏高,可适当减少摄入;其余则为正常范围。
上图可以看到,像维生素C这项指标分值在38,虽然正常但相对于最佳来说是偏低的。
一些小伙伴可能会存在这样的疑惑:
为什么肠道菌群检测可以评估维生素?
这些维生素指标的分值代表着什么含义?
肠道菌群和维生素之间有什么样的关联?
它们如何影响人体健康/疾病?
如何判断维生素是否缺乏?
该如何补充?
…
本文就以上问题进行详细解答,同时也包括维生素-微生物群之间的相互作用,维生素维持肠道菌群稳态和减少肠道炎症以预防癌症的机制,产生维生素的益生菌,补充调节维生素的方式包括饮食、益生菌等。
在阅读本文之前,可以先了解一下各类常见的维生素功能,缺乏导致的症状。


每个维生素的详细介绍可以点开以下查看(请在谷禾健康微信公众号找到这篇文章查看)。
维生素B1(硫胺素)
维生素B2(核黄素)
维生素B3(烟酸)
维生素B5(泛酸)
维生素B6(吡哆醇)
维生素B7(生物素)
维生素B9(叶酸)
维生素B12(钴胺素)
以上每个都有关于该维生素的详细介绍,包括:
—正文—
维生素是一种微量营养素,在人体的生长、新陈代谢和发育中起着至关重要的作用。
在谷禾肠道菌群健康检测报告中,维生素分值即代表该维生素的膳食摄入水平和菌群代谢能力(报告中显示的分值是经过一系列计算得到的一个相对值)。
其中B族维生素很多需要通过肠道菌群对初始原料进行代谢之后才会产生,因此肠道菌群相应的基因和代谢途径的丰度水平也会直接反映这些维生素的摄入水平。
我们知道维生素的缺乏可能引起一些不良后果,导致维生素缺乏的原因有很多,摄入不足,吸收不良等都会导致维生素缺乏。
我们日常主要从饮食中获取维生素,肠道是主要吸收部位。例如,维生素 A 主要在近端空肠吸收,维生素 D 在远端空肠吸收最佳,维生素 E 和 K 主要在回肠吸收。因此,肠道功能受损可能会影响维生素的吸收。当然,影响维生素吸收的其他原因还包括年龄,某些疾病,药物等因素。
那么肠道菌群和维生素之间有什么关联?
肠道菌群是人体生理和健康的重要决定因素。肠道菌群帮助吸收营养,并参与维生素代谢。
肠道有益菌:乳酸菌和双歧杆菌,可以重新合成B族和K族维生素,为宿主提供约30%的每日摄入量。与从食物中获得的维生素不同,微生物产生的维生素主要在结肠中吸收。接下来了解一下具体哪些菌群,如何产生维生素。
前一章节我们知道,除了通过饮食提供维生素外,人体肠道中的细菌也可以产生一些维生素,如果吸收得当,可以部分满足人体的需要。
可以把这些细菌微生物想象成小小的维生素工厂。细菌确保为自己和与他们共生的微生物朋友提供维生素,同时也会为人体提供维生素。
合成的B族维生素的菌群较多
研究人员估计了人体肠道细菌可以提供维生素每日参考摄入量的百分比,得出的结论是可以提供:
40-65% 的人体肠道菌群具有合成 B 族维生素的能力。两种最常见的合成维生素是维生素B2和B3,预测分别有 166 和 162 个生产者。
可以合成 B 族维生素的细菌以及B 族维生素缺乏对肠道健康的影响
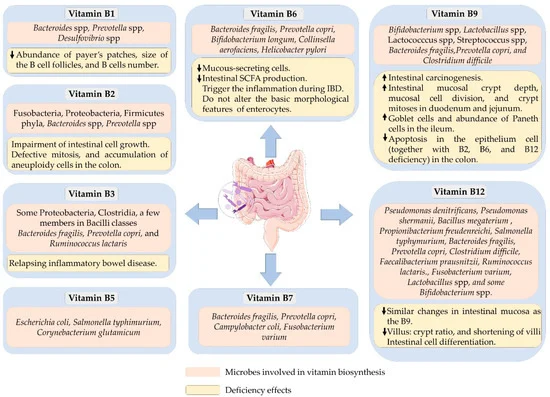
doi.org/10.3390/microorganisms10061168
大部分肠道菌群都参与维生素的合成
随着基因组注释方法的不断完善,研究人员可以预测维生素代谢途径并评估维生素生物合成潜力。通过检索 UniProt 数据库,研究人员发现:
厚壁菌门是维生素的主要代谢相关菌,其次是变形菌门,再然后是拟杆菌和放线菌。这四种菌群是人体肠道菌群的主要组成部分,占总菌群的60%-90%.
下表列出了参与合成B族维生素的肠道菌群,以及相应的代谢机制。


以上是肠道菌群对维生素产生的影响,而维生素和肠道菌群之间的作用是双向的,维生素也会影响肠道菌群,下一章节我们详细了解维生素对肠道菌群的影响。
维生素通过调节免疫力、细菌生长和新陈代谢来改变肠道微生物群的组成。
例如,膳食补充剂中的维生素 B、C、D 和 E 通过有利于双歧杆菌、乳酸杆菌和罗斯氏菌等有益菌属的肠道黏膜扩张和定植,在很大程度上有助于微生物组的组成。
肠道微生物组和宿主之间的微量营养素交换
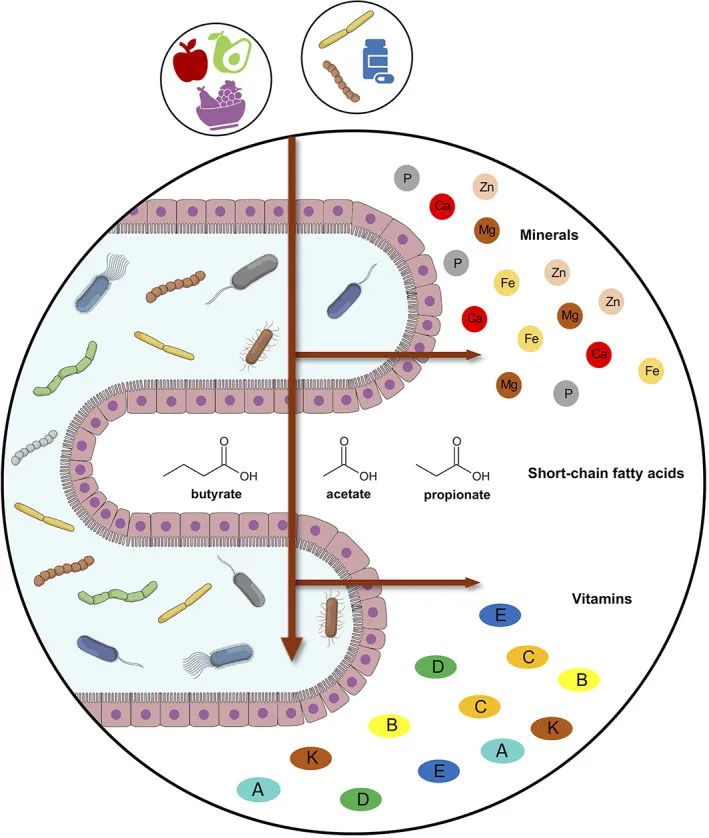
doi: 10.1002/biof.1835
一项研究调查了 96 名健康志愿者,结果表明:
补充维生素 B2 后肠道微生物的种类数量显着增加;联合补充维生素 B2 和 C 导致Sutterella显着减少,但Coprococcus数量增加;
维生素C显着提高肠道微生物的α多样性;
服用维生素D后,促进放线菌的生长和抑制拟杆菌的生长。
补充维生素对人体肠道菌群的影响

doi.org/10.3390/nu14163383
/ 维生素A /
维生素 A 的充足状态可能与微生物多样性增加有关。在小鼠实验中,普通拟杆菌(Bacteroides vulgatus )在维生素 A 缺乏期显着增加。维生素 A 缺乏导致的粘膜反应受损,粘蛋白和防御素 6 表达减少,可能使病原菌更容易穿透肠道屏障。
维生素A缺乏使厚壁菌门中毛螺菌_NK4A136_群、厌氧菌、颤杆菌的数量减少,毛螺菌的含量也降低;然而,Parasutterella呈上升趋势。TLR4 可能参与了维生素 A 调节微生物群的过程。
/ B族维生素 /
研究人员在一个小的成年志愿者群体中进行了一项试点研究,该群体补充了过量核黄素(100mg),持续14天。他们发现,在补充期间,每克粪便中的Faecalibacterium prausnitzii数量增加。作者还注意到厌氧菌Roseburia 增加,大肠杆菌减少。
其他关于B族维生素对肠道菌群的影响详见:
/ 维生素C /
补充维生素 C 可减少肠杆菌科细菌的数量,增加乳酸杆菌的丰度,抑制有害菌的生长,促进有益菌的增加。
也有研究表明,维生素 C 服用4周导致 α 多样性增加,短链脂肪酸浓度增加。

/ 维生素D /
维生素 D 和肠道微生物群的相互作用对免疫稳态至关重要。补充高水平的维生素 D 增加了普氏菌,减少了韦荣氏菌和嗜血杆菌。
婴儿饮食中补充维生素 D 对早期微生物组成的变化有重要影响,而儿童缺乏维生素 D 会导致细菌多样性降低。
最近的一项研究表明,维生素D的活性代谢物1,25-二羟基胆钙化醇,维生素D受体的配体(VDR),影响美国不同地区老年人肠道菌群的α -和β -多样性。
研究人员报告了通过食物频率问卷评估的微量营养素摄入量与孕妇微生物群组成之间的相关性。他们观察到,高脂溶性维生素,特别是维生素D的膳食摄入量与微生物α多样性降低有关(P值<0.001),维生素D和视黄醇与变形菌相对增加有关,变形菌门是一个已知包含多种病原体并具有促炎特性的门。
/ 维生素E /
维生素E对变形菌有抑制作用,而维生素E(和纤维)的摄入量较低与Sutterella水平较高相关,据报道,自闭症和某些胃肠道疾病婴儿的Sutterella水平大量增加。
体外维生素E 可以防止几种人类病原体的生物膜形成,特别是金黄色葡萄球菌和表皮葡萄球菌。
/ 维生素K /
一项动物实验表明,缺乏维生素 K 的小鼠的肠道中,瘤胃球菌、毛螺菌科、Muribaculaceae的含量较多。
关于维生素对人体肠道微生物组直接影响的研究
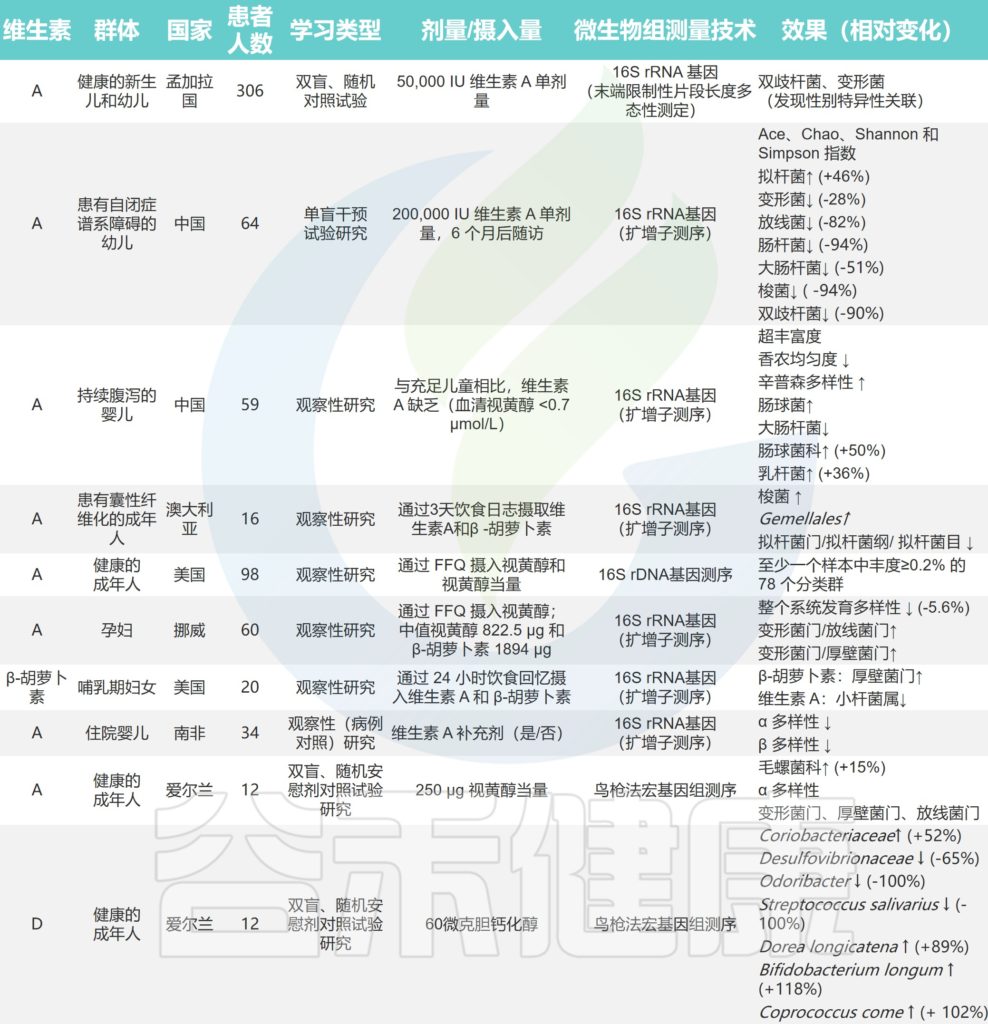
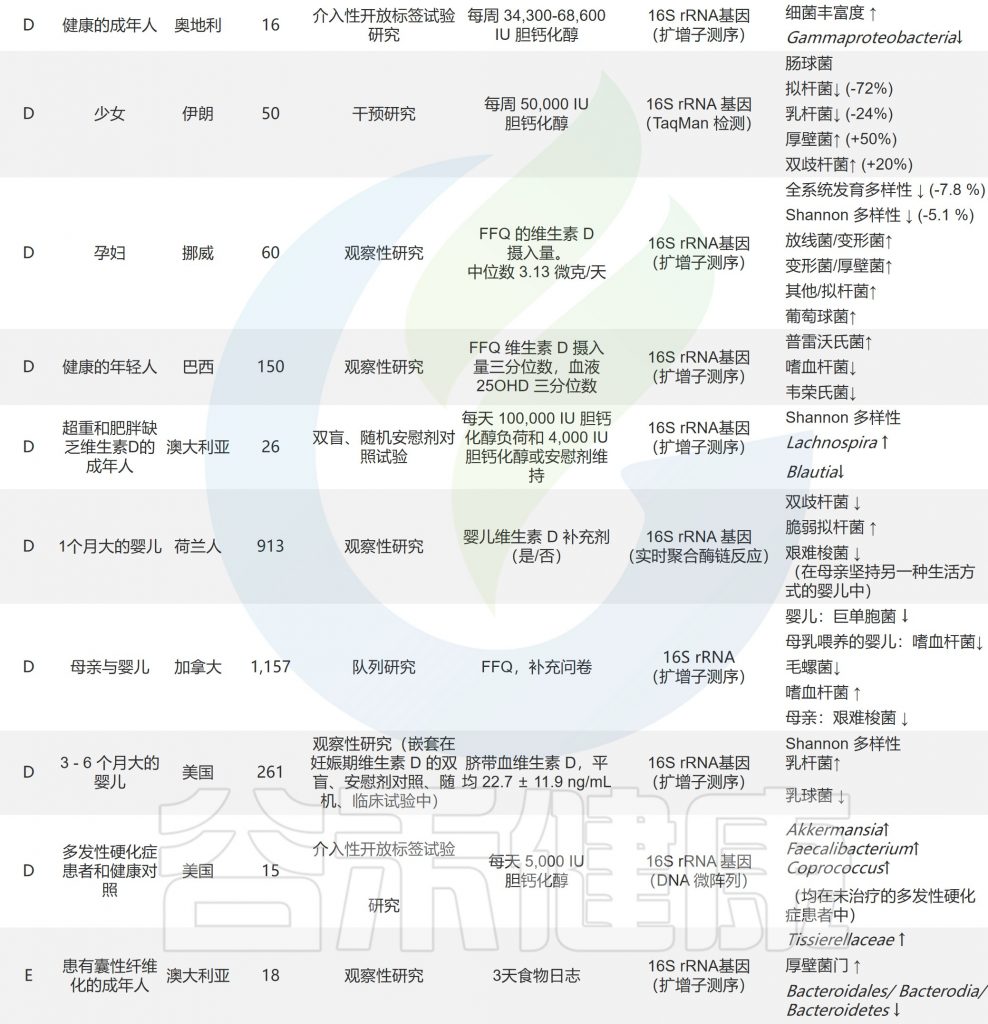
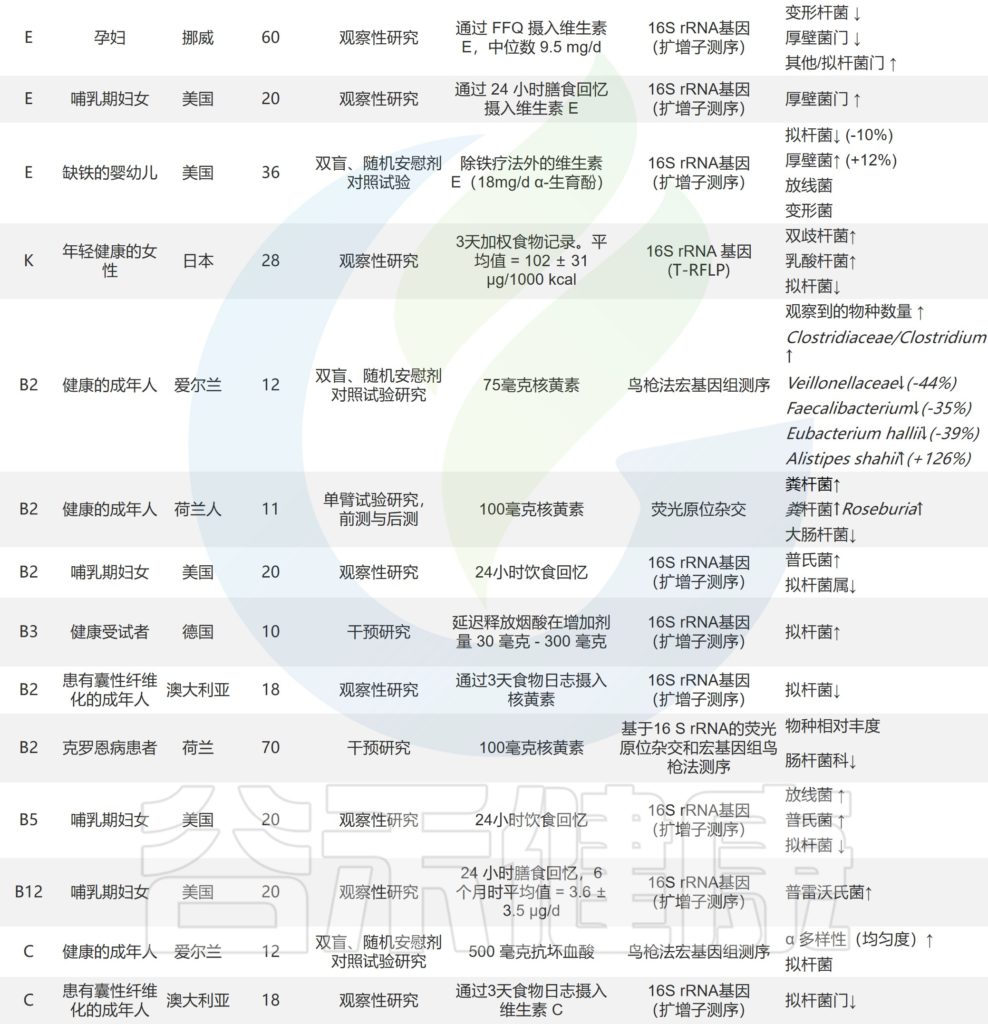
doi.org/10.1016/j.nutres.2021.09.001
饮食是维生素的主要来源,通过饮食补充维生素也会影响菌群。
注:由于测试饮食干预效果所需的随机试验的样本量和持续时间,相关发病率的研究具有挑战性。此外,由于特定的营养素不是孤立地消耗的,而是作为饮食模式的一部分,并且饮食成分之间相互作用,因此饮食带来的实际影响可能只有作为一个整体考虑时才会变得明显。
因此这里我们主要考虑饮食模式,例如地中海饮食等饮食方式。
地中海饮食是营养均衡饮食的典型代表,其特点是大量且频繁地摄入重要的纤维来源(谷物、蔬菜、豆类、水果和坚果)和具有抗氧化特性的化学成分(维生素、类黄酮、植物甾醇、矿物质、萜烯和酚类)。

同时地中海饮食还富含复杂和不溶性纤维含量。我们知道,大量摄入膳食纤维可促进肠道中有益菌群的生长,例如增加拟杆菌、普雷沃氏菌属、罗斯氏菌属、瘤胃球菌属、普拉梭菌等菌属的丰度,从而在肠道中产生高水平的短链脂肪酸,包括丁酸盐。
响应地中海饮食而增殖的细菌可以充当“基石”物种,也就是说它们对于稳定的“肠道生态系统”至关重要。这些变化主要是由于膳食纤维和相关维生素和矿物质的增加,特别是维生素C、B6、B9、铜、钾、铁、锰和镁。
总之,维生素似乎是微生物-宿主间代谢相互作用的重要媒介。
越来越多证据表明,维生素缺乏会导致肠道菌群紊乱,进而引发肠道疾病,甚至促进炎症和肿瘤的发展。下一章节详细讨论,维生素-微生物群相互作用对健康/疾病的影响。
最近的几项观察表明,微生物群失调和维生素缺乏是相互关联的。
维生素对宿主健康的影响

doi.org/10.1016/j.nutres.2021.09.001
这种关系可能直接影响宿主健康:例如,克罗恩病恶化与参与抗炎介质核黄素、硫胺和叶酸生物合成的微生物基因减少有关。
此外,2型糖尿病受试者在与微生物介导的维生素代谢相关的基因丰度谱中显示出显著变化。
营养不良儿童的微生物群显示,参与B族维生素代谢的多种途径(包括烟酸/NADP生物合成)显著减少。
在经历饮食振荡以诱导急性短期维生素A缺乏的灵长类小鼠模型中,Hibberd等人观察到细菌群落结构和宏转录组的调节,其中Bacteroides vulgatus是显著的应答者,在缺乏维生素A的情况下其丰度增加。有趣的是,B.vulgatus是在人类肠道微生物群的灵长类小鼠模型中鉴定的一种生长差异物种。
所有这些观察结果表明,维生素缺乏可能会改变肠道微生物群,从而影响人体健康。
下面我们以肠道疾病和精神类疾病两大类疾病为例,来具体了解维生素-微生物相互作用及其在疾病中的影响。
维生素 A 和 D 分别在近端和远端空肠吸收。维生素E和K主要在回肠吸收;微生物产生的维生素主要在结肠中吸收。维生素缺乏会加重肠道炎症,甚至通过多种机制促进癌症。
肠道菌群->维生素->肠道疾病中的作用
慢性 IBD 发生和发病机制中的关键作用是微生物(尤其是共生菌群)对宿主黏膜免疫功能的影响。同时,肠道微生物群和慢性炎症已被证明与肿瘤发生密切相关。
维生素具有调节肠道菌群和保护肠道的功能。因此,维生素和微生物群的相互作用可能在 IBD 和结直肠癌的治疗中具有巨大的潜力。
维生素A通过促进黏膜愈合、促进产生ASCFA的相关菌增加、降低UC相关菌的水平来达到治疗UC的效果。
费氏丙酸杆菌ET-3 产生维生素 K2 的前体,即 1,4-二羟基-2-萘甲酸 (DHNA),可激活芳烃受体 (AhR) 以改善结肠炎并调节肠道微生物群。
维生素 D 的缺乏会增加拟杆菌门、变形杆菌门和螺杆菌科的丰度,降低厚壁菌门和去铁细菌的丰度门,并且还影响 E-钙粘蛋白表达并减少耐受树突状细胞的数量。
然而,在治疗 IBD 时,维生素 D 与利福昔明的共同给药会影响肠道菌群和利福昔明的疗效。维生素 D 促进A. muciniphila的生长以保护肠粘膜屏障,这些作用对于对抗结直肠癌的发展尤为重要。
研究表明,维生素 E 及其代谢物在调节肠道菌群、减少炎症和抑制癌变方面具有巨大潜力。此外,维生素 Eδ-生育三烯酚 (δTE) 及其代谢物δTE-13′-羧基色原酚 (δTE-13′) 增加了肠道中的乳球菌和拟杆菌,并抑制炎症因子的产生。
维生素->肠道菌群->肠道疾病中的作用
▸维生素在IBD和结直肠癌中的作用不容忽视
大量临床研究表明,缺乏维生素 B 和维生素 D 的人群中结直肠癌的患病率较高。同时,IBD 的长期不愈合使患者面临更高的结直肠癌风险。维生素 D 水平低的 IBD 患者疾病严重程度和预后较差。
▸为什么肠道炎症容易导致癌症高风险?
在炎症背景下,敲除 IKKbetaβ(炎症与癌症之间的联系)可减少由于上皮细胞凋亡增加而导致的癌症发生。在一项关于结肠炎相关癌前癌 (CApC) 的研究中,IL-6 反式信号转导的存在增加了炎症性致癌的风险。如果不及时治疗,由肠道菌群紊乱和维生素缺乏引起的肠道炎症最终可能发展为癌症。
维生素 A 在肠道炎症和癌症中的作用
维生素 A 及其活性代谢物视黄酸 (RA) 在人体免疫系统中发挥着关键作用,并可能对辅助 T 细胞的分化产生影响。
炎症下:视黄酸从保护转变为破坏作用
在非炎症条件下,视黄酸能够抑制 IL-6 受体的表达和 Th1/Th17 的产生。
在炎症条件下,视黄酸从对粘膜的保护作用转变为破坏作用;这反映在活动期 IBD 患者黏膜中视黄酸水平显着升高,伴随着 CD4 和 CD8 分泌的 IL-17 和 IFN-γ 的上调。
维生素A及其代谢物:发挥抗炎作用
维生素 A 及其代谢物通过阻断 Th1 和 Th17 的激活,抑制 IL-17、INF-γ 和 TNF-α 的产生而显示出抗炎作用。同时,它们可以通过与TGF-β协同作用,提高Foxp3的水平,发挥免疫功能,从而促进抗炎因子的发挥。
一项数据显示,低水平的维生素 A 会激活核 NF-kB 并促进胶原蛋白的形成,从而加剧结肠炎的炎症。补充维生素后,肠道炎症明显缓解。
全反式维甲酸 (AtRA) 可降低 UC 和结直肠癌患者结肠黏膜分泌的 TNF-α 和一氧化氮合酶 2 (NOS2) 蛋白的表达。

维生素A保护肠黏膜屏障,其潜在机制是拮抗LPS的肠道破坏作用
在一项关于维生素 A 缺乏对结肠炎和结直肠癌发展的影响的检查中,研究人员使用葡聚糖硫酸钠 (DSS) 诱导小鼠结肠炎;此外,偶氮甲烷 (AOM) 预注射和 DSS 结肠炎的组合诱导了结直肠癌。缺乏维生素的小鼠肠道炎症水平较高,黏膜愈合较慢,免疫反应增强,更容易发生结直肠癌。
AtRA具有抗癌作用,结直肠癌中AtRA 水平降低
在结直肠癌小鼠模型中,肠道细菌引起的炎症影响 AtRA 代谢;这导致其水平下降。在 UC 及其相关结直肠癌的临床样本中发现 AtRA 代谢酶活性降低和 AtRA 水平降低。同时,AtRA通过激活CD8 + T细胞发挥抗癌作用;这为 CAC 的治疗提供了新的见解。
视黄醇和视黄醇结合蛋白(RBP)的结合激活致癌基因STRA6,促进结直肠癌的发生;Holo-RBP/STRA6 通路可通过促进成纤维细胞的致癌作用进一步发挥致癌作用。
在一项关于维生素 A 缺乏对结肠炎和结直肠癌发展影响的动物实验中,当维生素 A 处于低水平时,小鼠体内的维生素 A 脂滴会被降解,免疫反应会增强,结肠炎症会加重,癌变进程将加快。
维生素 B12 和叶酸在肠道炎症和癌症中的作用
IBD 患者缺乏维生素 B12 和叶酸的原因有很多,包括回肠和空肠微生物过度生长、维生素 B12 摄入不足或身体需求增加、维生素肠道破坏增加或吸收能力降低、某些药物(如甲氨蝶呤或柳氮磺胺吡啶)的不良反应、一些病理原因例如蛋白丢失性肠病、肝功能异常、回肠相关病变或手术切除、肠瘘等。
维生素 B12 缺乏不会影响健康的肠道微生物群组成;然而,它会导致实验性结肠炎中肠道菌群失调,并促进条件致病菌的生长。出乎意料的是,维生素 B12 缺乏减少了结肠组织的损伤;这可能与抗炎细胞因子 IL-10 的增加有关。

对甲基缺乏饮食 (MDD) 的潜在作用进行了一项研究,该饮食可降低维生素 B12 和叶酸的血浆浓度,并提高同型半胱氨酸水平,对 DSS 诱导的小鼠结肠炎的影响。喂食 MDD 的 DSS 治疗小鼠比其他治疗组患有更严重的结肠炎。
尽管超氧化物歧化酶和谷胱甘肽过氧化物酶活性保持稳定,但 caspase-3 和 Bax 的水平受到影响。除Bcl-2表达增加外,炎症相关标志物如胞质磷脂酶A2和环氧合酶2的表达也有明显增加趋势;这伴随着金属蛋白酶组织抑制剂(TIMP)3蛋白的表达降低。因此,维生素 B12 缺乏可能会加重实验性 IBD 的炎症程度。
高维生素 B12 水平可通过减少 DNA 甲基化来降低结直肠癌的风险
在结直肠癌患者中,与低血清维生素 B12 组相比,高维生素 B12 组的肿瘤区域和外周血单个核细胞 (PBMC) 中长散布的核元素 1 (LINE1) 甲基化被证明是降低的;肿瘤区域的LINE1甲基化水平也低于周围的非肿瘤区域。
氧化应激是结直肠癌发病机制之一;此外,叶酸和维生素 B12 的水平与体内抗氧化剂谷胱甘肽的水平呈正相关。提高 AOM 诱导的结直肠癌中的叶酸和维生素 B12 水平显示出显着的抗凋亡、抗氧化应激和抗 AOM 细胞毒性。
在对 4517 名 IBD 患者的系统评价和荟萃分析中,补充叶酸被证明可以降低 IBD 患者的结直肠癌风险并防止结直肠癌发展。
有趣的是,有证据表明缺乏甲基供体营养素叶酸、胆碱、蛋氨酸和维生素 B12 会抑制 Apc 突变小鼠的肿瘤发展。总而言之,维生素B12和叶酸在肠道疾病中的作用需要更深入的研究。
维生素 D 在肠道炎症和癌症中的作用
流行病学和动物实验表明,维生素 D 缺乏是 IBD 和 结直肠癌的高危因素。维生素 D 补充剂有助于降低疾病严重程度,可能通过多种机制,包括调节免疫细胞运输和分化,以及抗菌肽合成。
维生素D可以维持肠黏膜屏障的正常功能,提高机体的先天性和适应性免疫
1α,25-二羟基维生素 D3(骨化三醇)是维生素 D 的活性形式,可与 TGF-β 结合,提高 IL-2 水平,调节 T 细胞抑制炎性细胞因子的产生,增强 Foxp3 + Treg 细胞的存活和功能。

维生素D受体(VDR)是维生素D调节免疫和发挥抗炎作用的重要途径
相关资料显示,VDR对肠道有保护作用;它可以通过调节 JAK/STAT 通路来维持肠道稳态并预防癌症。
在 IBD 患者 中,结肠上皮中VDR的含量明显低于正常人。在实验性结肠炎模型中,与缺乏 VDR 的小鼠相比,表达 hVDR 的转基因小鼠的结肠炎症较少。用 hVDR 转基因恢复上皮 VDR 表达可减轻严重结肠炎并降低死亡率。内在机制是 VDR 通过抑制 NF-κB 活化发挥抗凋亡作用,以保护肠道屏障缓解结肠炎。
肠道菌群通过犬尿氨酸通路(合成维生素),在精神健康方面发挥作用
关于肠道细菌在心理健康方面的作用的关键方面,是它们通过犬尿氨酸通路参与调节色氨酸代谢。微生物群能够合成犬尿氨酸途径 (KP) 的酶促辅助因子,如维生素 B2 和 B6。

犬尿氨酸是主要的色氨酸代谢途径,其中 95% 的这种氨基酸被代谢为各种免疫和神经调节犬尿氨酸/色氨酸分解代谢物 (TRYCAT),在大脑中,犬尿氨酸途径主要在神经胶质细胞中分隔。
犬尿氨酸通路在精神、神经退行性和神经系统疾病中的作用是至关重要的,包括重度抑郁症,双相情感障碍,精神分裂症,阿尔茨海默病,亨廷顿病和帕金森病,与 HIV 感染相关的痴呆,手术后认知能力下降,肌萎缩侧索硬化(ALS) 等。
精神病理学和炎症中维生素缺乏与高同型半胱氨酸血症有关
精神病理学和炎症中维生素缺乏的另一个关键机制与高同型半胱氨酸血症(hHcy)有关,这可能是由叶酸、维生素 B6 和 B12 缺乏引起的。
高同型半胱氨酸血症和维生素 B 缺乏在重度抑郁症、精神分裂症、双相情感障碍、自闭症、焦虑症和痴呆症(包括阿尔茨海默病和帕金森病)中起关键作用。
同型半胱氨酸(Hcy)是在蛋白质消化过程中获得的另一种氨基酸蛋氨酸代谢过程中形成的氨基酸和中间体。该反应需要维生素 B12 作为酶促辅因子和叶酸衍生物(5-甲基四氢叶酸)作为甲基供体。
注:Hcy-同型半胱氨酸,是人体内含硫氨基酸的一个重要的代谢中间产物,可能是动脉粥样硬化等心血管疾病发病的一个独立危险因子。
此外,Hcy 可以在需要维生素 B6 作为酶辅因子参与的途径中转化为半胱氨酸。
因此,Hcy 被认为是叶酸和维生素 B12 缺乏的敏感标志物。
高同型半胱氨酸血症导致神经和精神病理学的机制包括:
促进免疫炎症反应、增加肠道和血脑屏障通透性、NMDA受体激动和神经毒性、诱导神经元凋亡、氧化应激、线粒体功能障碍和由于甲基化受损导致的单胺能神经递质合成失调。
目前对体内维生素水平的检测例如:
抽取血液检测其中维生素的含量水平,可以判断是否存在维生素的缺乏情况。
其他,例如通过肠道菌群健康检测,也可以查看近期体内维生素状况。
与通过血液进行维生素检测不同,肠道菌群的评估更加反映一段时间 ( 一般2周左右 ) 的长期状态,如部分B族维生素无法在体内留存,需要每日补充,血液检测波动较大。
注:菌群会受检测前一天饮食的影响,造成15~30%的菌群改变,同样也会反映在营养状况的评估上,因此建议检测前一天尽量保持近期正常饮食 ,这样能更好的反映真实的营养饮食状态。
在了解补充维生素的干预措施之前,我们先从肠道菌群的角度,来了解一下影响维生素合成吸收的因素。
人类基因的变异与肠道结构和微生物组组成有关。人类肠道微生物群中存在不同的维生素 B 生物合成途径支持人类遗传变异影响维生素 B 合成的观点。
维生素的合成吸收不仅需要靠饮食补充,还与吸收相关。而维生素的吸收涉及到相关基因,例如:
MTHFR 基因的突变会影响我们产生加工维生素 B9的酶——亚甲基四氢叶酸还原酶。
亚甲基四氢叶酸还原酶是叶酸代谢通路中的一种重要的辅酶,亚甲基四氢叶酸还原酶基因缺陷,容易造成叶酸在体内的代谢障碍,MTHFR基因最主要的两种突变为C677T、A1298C基因多态性。该两种位点同时突变可显著降低MTHFR活性进而降低叶酸水平。
VDR基因(维生素 D 受体):维生素 D(来自阳光、食物或补充剂)经过转化步骤后,活性形式骨化三醇 (1,25(OH)2D3 ) 可以通过VDR在细胞内发挥作用,是打开或关闭基因的转录因子。该基因突变可能导致维生素D缺乏引起的佝偻病。
维生素缺乏是一个严重的问题,尤其是在老年人中。随着年龄的增长,营养需求会随之变化。
由于食物中的维生素B12 需要胃酸及胃蛋白酶的作用才能释放出来被吸收,而老年人胃酸及胃蛋白酶分泌减少,就会影响维生素B12 的吸收。
患有维生素B12缺乏症的老年人可能出现神经精神或代谢缺陷。
一些药物会改变营养物质的吸收或代谢方式。例如,抗惊厥药也会减少叶酸的吸收。
肠道菌群通过各种代谢途径影响维生素的合成,例如拟杆菌属、肠球菌属和双歧杆菌属等人类肠道共生菌可以从头合成维生素 K 和大多数水溶性 B 族维生素,这在前面第二章节的表已经详细阐述。
在 B 族维生素合成中暴露于抗生素的反应因使用的抗生素类型而异。例如,在饮食中添加青霉素和金霉素会增加雄性大鼠的肝脏维生素 B2 浓度,以及 B2 和 B3 在尿液中的排泄。然而,链霉素和放线菌酮的施用降低了肝脏中维生素 B9 和 B12 的浓度。维生素合成对抗生素暴露的混合反应尚不清楚,但它们可能是由肠道微生物群的选择性改变引起的。
自由基是含有不成对电子的化学物质,可以诱导氧化应激。一个这样的例子是一氧化氮,它与金属离子形成复合物,包括钴,维生素 B12 的一种结构成分,因此使其无法用于细菌维生素 B12 的生物合成。此外,维生素生产者(如脆弱拟杆菌)暴露于过氧化氢等自由基会抑制其生长 ,从而降低维生素的生物合成能力。
维生素主要在小肠中吸收,其生物利用度取决于食物成分,相关相互作用等。
饮食和膳食的组成会通过影响肠道转运时间和/或混合胶束的肠道形成来影响某些维生素的吸收。
饮食中足量的水和膳食脂肪对于分别吸收水溶性和脂溶性维生素至关重要。
*水溶性维生素包括:B族维生素,维生素C;
脂溶性维生素包括:维生素 A、D、E 、K.
doi: 10.7717/peerj.11940
由于脂溶性维生素可以溶解在脂肪中,因此与膳食脂肪一起食用时最容易被吸收。例如,一种富含维生素 A 的小胡萝卜,如果单独食用,将在食物中获取维生素 A,但如果它是在含有一些膳食脂肪的食物成分中(比如说,橄榄油),将增加体内维生素 A 的吸收。
食物的性质(物理状态)也会影响维生素的吸收效率。例如,存在于可消化性较差的纤维植物材料中的类胡萝卜素已被证明相对于维生素A表现出较低的生物利用度。
当我们看到维生素缺乏的时候,可能希望通过饮食来补充相应缺乏的维生素,下表列出了常见的维生素的食物来源,可供参考。
此外,宿主饮食作为肠道中细菌的底物,其对肠道微生物分布的影响已被广泛研究。含有益生元和其他膳食营养素(如微量营养素和多酚)的饮食可以显着影响有益细菌的生长,包括维生素生产菌。
一些维生素,如核黄素,可作为氧化还原介质并刺激营养缺陷菌(如Faecaibacterium prauznitsii)的生长。
在即将形成共生关系的环境中,限制这些基质会增加微生物和微生物与宿主之间的竞争。
除了通过饮食直接补充之外,我们还可以通过补充益生菌来调节维生素水平,从而改善疾病。
双歧杆菌
在健康成人中补充益生菌菌株青春双歧杆菌DSM 18350、青春双歧杆菌DSM 18352 和假链双歧杆菌DSM 18353,导致粪便中叶酸浓度显着增加。
乳酸菌
乳酸菌通过不同的机制抑制炎症过程,包括调节IBD患者肠道菌群紊乱、保护肠道屏障和黏膜的正常功能、调节人体免疫反应等。乳酸菌通过产生核黄素(维生素 B2)和叶酸发挥抗炎和抗氧化作用。
产维生素的乳酸菌不仅对急性肠炎有抗炎作用,还能有效缓解复发性结肠炎。此外,在与美沙拉秦合用过程中,可有效降低不良反应,提高疗效。
研究人员发现注射产生叶酸的乳酸菌会缓解 5-FU 引起的肠炎小鼠的腹泻,改善结肠组织的结构和功能。这一发现降低了癌症化疗期间发生的肠黏膜炎症的严重程度,并提高了药物有效性;因此,这提高了患者的生活质量。
此外,乳酸菌 和 5-FU 的联合使用可减少 5-FU 引起的血细胞计数减少,并使患者获得完整的治疗周期。
产维生素的益生菌在肠道疾病中的作用

doi.org/10.3390/nu14163383
研究人员从 150 个收集的人类粪便样本中分离出三种产生核黄素和叶酸的益生菌;他们用它们来治疗乙酸引起的大鼠结肠炎。他们发现这些益生菌可以保护结肠黏膜,促进溃疡性病变的愈合;此外,它们具有抗炎和抗氧化应激作用。
一种新分离的具有产生叶酸能力的细菌——清酒乳杆菌LZ217,具有促进丁酸产生和改善肠道菌群组成的作用。
Akkermansia muciniphila 是肠道中的一种常见细菌,可调节 CLT 以保护肠道免受炎症和肿瘤侵袭;它还产生维生素 B12 以缓解 IBD 患者的维生素缺乏症。
研究发现,丙酸杆菌菌株 P. UF1 合成维生素 B12;这对肠道免疫和肠道健康有积极的调节作用。
大肠杆菌通过产生维生素来缓解 IBD. 使用大肠杆菌生产两种产生β-胡萝卜素的菌株来治疗维生素A缺乏症。这些结果显示出巨大的临床潜力。
维生素 A 及其代谢物与短乳杆菌KB290 的组合提高了 CD11c + MP/CD103-DC 比率;因此,这在结肠炎的治疗中起着积极的作用。
此外,肠道中的分段丝状细菌 (SFB) 可以产生 AtRA,以抵消感染对肠道的损害。
益生菌对维生素D及其受体活性有积极作用,如鼠李糖乳杆菌GG(LGG)和植物乳杆菌(LP);同样在沙门氏菌结肠炎模型中,使用 VDR (-/-) 小鼠验证 LGG 对 IBD 的缓解作用是通过 VDR 信号通路。
此外,胆汁盐水解酶 (BSH)活性罗伊氏乳杆菌NCIMB 30,242 可调节血浆中的活性维生素 D 水平。磷虾油 (KO)、益生菌罗伊氏乳杆菌和维生素 D 的混合物显着降低病理评分和炎症因子的释放,促进黏膜愈合并减少机会性感染的发生。
经益生菌 VSL#3 预处理后,VDR 水平显着提高,共同保护肠黏膜,防止损伤;这对预防CRC的发展起到一定的作用。
用从韩国泡菜中分离的乳酸菌条件培养基处理 HCT116 细胞或肠类器官后,其分泌的蛋白质 P40 和 P75 与 VDR 的表达增加有关;它们还增强自噬反应,共同具有抗炎作用。肠道微生物合成的石胆酸 (LCA) 充当连接 VDR 与微生物的桥梁,从而提高维生素 D 水平。
益生菌配方有助于抑郁症患者维生素水平的增加
一项随机对照试验中,重度抑郁症患者接受了多种益生菌配方,其中含有双歧杆菌W23、乳双歧杆菌W51、乳双歧杆菌W52、嗜酸乳杆菌W22、干酪乳杆菌W56、副干酪乳杆菌W20、植物乳杆菌W62、唾液乳杆菌W24、乳酸乳杆菌W19。
此外,益生菌组和安慰剂组的患者接受了相同剂量的维生素 B7。在两组中,抑郁症的临床参数都有所改善,然而,益生菌干预组与安慰剂组相比,仅在微生物 β 多样性方面存在差异,临床结果指标没有差异。有趣的是,尽管两组都接受了相同剂量的生物素,但接受益生菌的那组维生素 B6 和 B7 的合成上调。
多种益生菌相结合通过增加叶酸和维生素 B12血浆水平,改善精神疾病
八周的个性化饮食与含有多种益生菌的菌株相结合:婴儿双歧杆菌DSM 24737、长双歧杆菌DSM 24736、短双歧杆菌DSM 24732、嗜酸乳杆菌DSM 24735 、德氏乳杆菌、保加利亚乳杆菌DSM 24734、副干酪乳杆菌DSM 24733、植物乳杆菌DSM 24730 、嗜热链球菌DSM 24731 (VSL#3),在健康老年人中增加了叶酸和维生素 B12 血浆水平并降低了 Hcy 血浆水平。
此外,益生菌的添加导致粪便双歧杆菌浓度增加,这种变化与叶酸和维生素 B12 水平呈正相关。
在精神病患者中引入高同型半胱氨酸的评估和治疗可能非常有价值,益生菌可能成为治疗工具之一。
维生素是相互关联的、具有协同作用的微量营养素,当它们处于适当的平衡状态时,它们的全部潜力就会得到充分发挥。
因此,在食用益生菌和发酵食品时,应考虑维生素生产者与代谢者之间复杂的相互作用。
除了以上方式干预菌群之外,也可以通过良好的生活方式调理菌群,从而使维生素达到一个相对健康稳定的水平,减少各类疾病风险。
▸在服用维生素的同时可以服用益生菌吗?
可以。在大多数情况下,服用益生菌不会影响其他补充剂的效果。
一项 2021 年对临床试验的系统评价发现,益生菌可以改善健康人群的微量营养素水平,特别是维生素 B12、叶酸(维生素 B9)、钙、铁和锌。
2017 年的一项非随机临床试验发现,服用益生菌和铁补充剂的参与者比不服用益生菌的铁吸收明显更多。
有研究表明,维生素 D 和益生菌之间存在协同关系。
随机对照试验发现,维生素 D 补充剂与益生菌一起可以改善多囊卵巢综合征患者和同时患有冠心病的糖尿病患者的各种心理健康参数、一般健康状况、代谢和炎症标志物。
2019 年对随机对照试验的系统评价和荟萃分析发现,维生素 D 强化酸奶(富含益生菌嗜酸乳杆菌)有助于改善维生素 D 和胆固醇水平、代谢功能和身体测量值。
然而以上研究都没有单独研究维生素 D 和益生菌的作用,因此尚不清楚结果是否与两者的综合影响有关。
研究人员认为,无论有没有维生素,服用益生菌的时间很重要。作为一般规则,服用益生菌的最佳时间是空腹,大约在进食前 30 分钟。
研究人员担心胃酸的存在会影响益生菌的生存能力。在餐前或餐后几个小时服用时,当胃酸自然降低时,益生菌可以进入肠道,从而提高其生存几率。
何时服用维生素取决于维生素的种类。复合维生素通常最好在早上第一时间服用,非常适合搭配早餐前的益生菌。脂溶性维生素,如 A、D、E 和 K 以及一些矿物质,包括铁和镁,最好与食物一起服用。否则可能会导致胃部不适。
▸应该从食物中补充维生素还是通过维生素补充剂?
2020 年的一篇文献综述发现,与浓缩补充剂相比,许多微量营养素在其全食物形式中的生物利用度更高。因此提倡补充方式以食物为先。
一般认为,对于健康人来说,营养均衡的饮食可以提供身体需要的维生素,不需要额外补充,但对于可能存在免疫功能、肠道健康、吸收不良等问题的人群,可以考虑维生素补充剂进行补充,具体补充剂量请遵医嘱。
下表是维生素易缺乏的高风险人群:

▸可以长期服用维生素补充剂吗?补充过量会带来副作用吗?
一般健康人不需要长期服用维生素补充剂。
对于服用复合维生素片,多余的维生素会被排出体外,因此不用过于担心会带来危害。但是如果长期十倍以上的用量,对身体是有危害的。

doi: 10.7717/peerj.11940
在发现维生素缺乏的症状的时候,我们可能希望通过补充相应的维生素补充剂来改善健康。然而服用任何补充剂之前,我们应该寻找其根本原因而不是直接根据症状盲目补充。
通过肠道菌群健康检测可以了解维生素缺乏状况,且可以根据各类菌群丰度来推断维生素的菌群代谢状况。如果是由于菌群的代谢异常,可能直接补充并没有太大效果,这时候优先调节菌群或许是更好的选择。
如果维生素指标都显示正常没有缺乏(如下图),保持常规饮食不需要刻意补充。还想要更健康,指标更接近70的话,可以在数值略小的指标上,针对性地通过饮食进行补充调理。
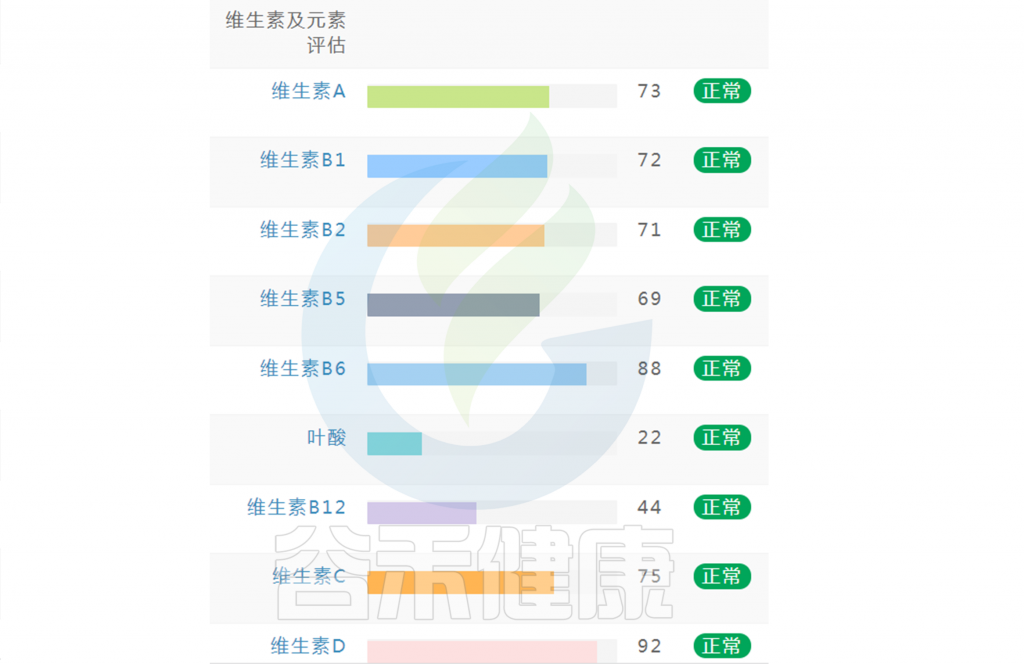

如果维生素指标中出现个别指标缺乏或偏低(如下图),可以通过饮食针对性地进行改善调整,如果已经出现对应症状,例如缺乏维生素A,同时出现干眼症或者夜盲症等相应的症状,可以使用相应的维生素补充剂进行干预,或者根据菌群代谢通路判别,通过菌群调理进行相应干预。
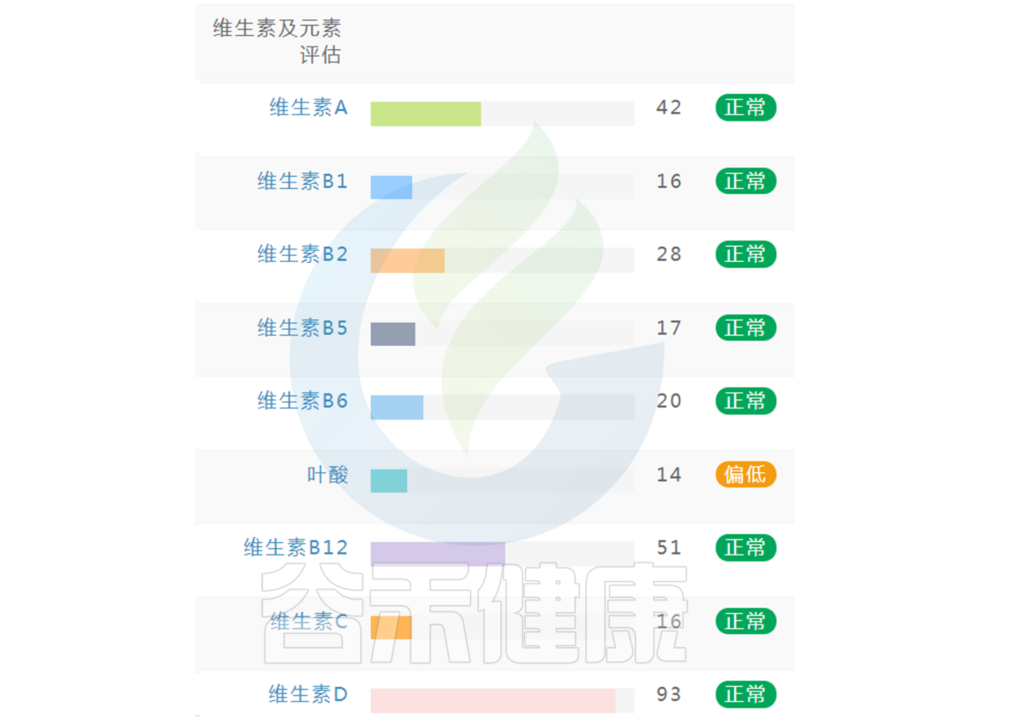
如果维生素指标中出现缺乏或偏低的指标较多,则需要选用复合维生素,各类维生素之间可能存在协作关系,同时配合饮食、菌群进行干预。
选择补充剂,应优先考虑生产规范良好的产品,比如说可以查看是否有“OTC”标志。
注:本账号内容仅作交流参考,不作为诊断及医疗依据。
主要参考文献:
Zhai Z, Dong W, Sun Y, Gu Y, Ma J, Wang B, Cao H. Vitamin-Microbiota Crosstalk in Intestinal Inflammation and Carcinogenesis. Nutrients. 2022 Aug 17;14(16):3383. doi: 10.3390/nu14163383. PMID: 36014889; PMCID: PMC9414212.Zhai Z, Dong W, Sun Y, Gu Y, Ma J, Wang B, Cao H. Vitamin-Microbiota Crosstalk in Intestinal Inflammation and Carcinogenesis. Nutrients. 2022 Aug 17;14(16):3383. doi: 10.3390/nu14163383. PMID: 36014889; PMCID: PMC9414212.
Bellerba F, Muzio V, Gnagnarella P, Facciotti F, Chiocca S, Bossi P, Cortinovis D, Chiaradonna F, Serrano D, Raimondi S, Zerbato B, Palorini R, Canova S, Gaeta A, Gandini S. The Association between Vitamin D and Gut Microbiota: A Systematic Review of Human Studies. Nutrients. 2021 Sep 26;13(10):3378. doi: 10.3390/nu13103378. PMID: 34684379; PMCID: PMC8540279.
Ofoedu CE, Iwouno JO, Ofoedu EO, Ogueke CC, Igwe VS, Agunwah IM, Ofoedum AF, Chacha JS, Muobike OP, Agunbiade AO, Njoku NE, Nwakaudu AA, Odimegwu NE, Ndukauba OE, Ogbonna CU, Naibaho J, Korus M, Okpala COR. Revisiting food-sourced vitamins for consumer diet and health needs: a perspective review, from vitamin classification, metabolic functions, absorption, utilization, to balancing nutritional requirements. PeerJ. 2021 Sep 1;9:e11940. doi: 10.7717/peerj.11940. PMID: 34557342; PMCID: PMC8418216.
Steinert RE, Lee YK, Sybesma W. Vitamins for the Gut Microbiome. Trends Mol Med. 2020 Feb;26(2):137-140. doi: 10.1016/j.molmed.2019.11.005. Epub 2019 Dec 17. PMID: 31862244.
Pham VT, Dold S, Rehman A, Bird JK, Steinert RE. Vitamins, the gut microbiome and gastrointestinal health in humans. Nutr Res. 2021 Nov;95:35-53. doi: 10.1016/j.nutres.2021.09.001. Epub 2021 Oct 21. PMID: 34798467.
Hossain KS, Amarasena S, Mayengbam S. B Vitamins and Their Roles in Gut Health. Microorganisms. 2022 Jun 7;10(6):1168. doi: 10.3390/microorganisms10061168. PMID: 35744686; PMCID: PMC9227236.
Rudzki L, Stone TW, Maes M, Misiak B, Samochowiec J, Szulc A. Gut microbiota-derived vitamins – underrated powers of a multipotent ally in psychiatric health and disease. Prog Neuropsychopharmacol Biol Psychiatry. 2021 Apr 20;107:110240. doi: 10.1016/j.pnpbp.2020.110240. Epub 2021 Jan 9. PMID: 33428888.
Barone M, D’Amico F, Brigidi P, Turroni S. Gut microbiome-micronutrient interaction: The key to controlling the bioavailability of minerals and vitamins? Biofactors. 2022 Mar;48(2):307-314. doi: 10.1002/biof.1835. Epub 2022 Mar 16. PMID: 35294077; PMCID: PMC9311823.

谷禾健康
人类肠道菌群复杂多样,在与人类长期的共同进化过程中,具备了调节人体免疫应答、影响疾病发展等作用。这种作用与肠道菌群本身的多样性和关键核心菌种的是否存在等具有紧密联系。
在前面的文章我们已经了解到,肠道菌群失调与很多疾病相关,详见:
肠道菌群失衡的症状、原因和自然改善
造成菌群失调的原因有很多,比如抗生素的使用,膳食营养不均衡,感染,重金属污染,疾病发生以及过渡清洁肠道等。
一般肠道菌群失衡可以通过一些明显的迹象表明肠道菌群失衡,如腹胀气、腹泻、便秘、间歇性或慢性腹泻、肠易激综合征、溃疡性结肠炎和克罗恩病,频繁呼吸道感染、过敏、神经问题、免疫低下或代谢异常等来判别。
说到对改善修复肠道菌群,一般是针对菌群存在异常或者偏离健康状态的特定情况才进行针对性调节,这些调节思路主要包括 “清除”,“补充”,“置换”,“塑造”。常用的手段或措施如,使用抗生素或抗菌剂,益生菌,益生元,膳食纤维,粪菌移植,饮食或天然补充物等。
以上改善措施单一或者组合对改善和调节宿主微生态平衡发挥重要作用。不过个体的菌群构成和状态差异很大,由此带来的干预对不同个体和状态的干预效果同样有很大差异,这也反映在很多菌群干预临床研究上。
所以盲目的补充益生菌,益生元等单纯的从菌量或功效来评价益生菌产品的好坏,都可能不利于有效的改善健康状况和调整微生态平衡。除了对比如益生菌菌株,益生元结构区分等进行更加精细化的功能分析外,还需要结合肠道菌群检测,基于不同肠道菌群特点进行精准化的匹配干预和临床研究。
今天我们主要简单讲下不同的一些益生菌、益生元、天然调节剂等对肠道菌群的调节以及对宿主健康的影响及其差异化。
益生菌的现代定义为“活的微生物,当给予足够的剂量时,会赋予宿主健康”。益生菌主要存在于人体肠道内,通过维持肠道微生物平衡,在宿主体内发挥有益作用。在日常生活中,常见的益生菌,如乳酸杆菌或双歧杆菌,通常作为活性菌制剂食用。
近年来,益生菌的研究取得了重大进展。例如,益生菌益生菌可以改善肠道菌群的组成缓解便秘,IBS,IBD,改善腹泻,修复多种与肠道相关的损伤等,此外,益生菌可以在慢性炎症性疾病的治疗中发挥作用,具有抗癌、抗肥胖和抗糖尿病等作用。
本章节我们列举一些常见的益生菌及其功效。
双歧杆菌
人体内双歧杆菌的数量实际上随着年龄的增长而下降。双歧杆菌在提高整体免疫力、减少和治疗胃肠道感染以及改善腹泻、便秘和湿疹等方面发挥作用。
双歧杆菌中常见的种类有:双歧双歧杆菌、长双歧杆菌、婴儿双歧杆菌、乳酸双歧杆菌、短双歧杆菌等。
双歧双歧杆菌B.bifidum是一种通常用于改善消化问题的益生菌。B.bifidum与健康饮食相结合还可以改善血糖控制、减轻压力并帮助对抗感染,有助于增强免疫系统并减少过敏。
双歧双歧杆菌是在母乳喂养婴儿中发现的第二大菌种。在成年期,双歧杆菌的水平显著下降,但保持相对稳定 (2-14%),在老年时再次开始下降。
对其他肠道菌群的影响
在一项针对 27 名健康志愿者的临床试验中,双歧杆菌的摄入量减少了普氏菌科和普氏菌属,并增加了瘤胃球菌科和Rikenellaceae。
在一项针对 53 名慢性肝病患者的临床试验中,双歧双歧杆菌是成功防止小肠细菌过度生长的益生菌之一。同样,在一项针对 66 名酒精性肝损伤患者的试验中,它与植物乳杆菌(后面会讲到)的组合恢复了肠道菌群。
在对 30 人进行的另一项试验中,双歧双歧杆菌与嗜酸乳杆菌(后面会讲到)结合也在抗生素治疗后恢复了肠道菌群。
健康益处


双歧杆菌除在以上列举的疾病发挥作用之外,还在压力、过敏等方面发挥作用(小规模研究或临床试验单一)。
安全性
B. bifidum一般都是安全的,但应避免在免疫功能低下的个体、器官衰竭和“肠漏”的人群中使用。在这些情况下,益生菌可能会导致感染。在具有自身免疫性甲状腺疾病遗传易感性的人群中,双歧杆菌可能导致其发展和恶化。
短双歧杆菌是一种有益细菌,可以在人类母乳以及婴儿和成人的胃肠道中找到。随着个体年龄的增长,其肠道内的短双歧杆菌减少。
对肠道菌群的影响
在一项对 30 名没有其他畸形、染色体异常或宫内感染的低出生体重婴儿的研究中,早期给予短双歧杆菌促进了双歧杆菌的定植和正常肠道菌群的形成。
B. breve还显著减少了 10 名极低出生体重婴儿的吸入空气量并改善了体重增加。
健康益处


短双歧杆菌除在以上列举的疾病发挥作用之外,还在肥胖、坏死性小肠结肠炎、乳糜泻、感染等疾病中发挥作用(小规模研究或临床试验单一)。
目前已有文献中,部分关于短双歧杆菌菌株的研究:
短双歧杆菌M -16V (B. breveM-16V) 显着抑制 Th2 和 Th17 淋巴细胞亚群。
同时,B. breve M-16V 可能激活 MyD88 表达并促进 Th1 相关细胞因子 IL-12 的产生。此外,B. breve M-16V 可能部分恢复肠道菌群失调。
B. breve CCFM1025 是一种很有前途的候选精神生物菌株,可减轻抑郁症和相关的胃肠道疾病。
B. breve FHNFQ23M3可以缓解腹泻症状。
母乳分离的益生菌菌株B. breve CECT7263 是一种安全有效的婴儿绞痛治疗方法。
B. breve UCC2003 在生命早期驱动肠上皮稳态发育中发挥着核心作用。
安全性
B. breve被证明是适合早产儿常规使用的益生菌。
与使用短双歧杆菌相关的不良事件发生率极低,且严重程度较轻。
长双歧杆菌是一种革兰氏阳性、杆状细菌,天然存在于人体胃肠道中。它可以改善人体免疫反应并帮助预防肠道疾病。早期证据表明,它还可以抑制过敏、降低胆固醇和改善皮肤健康。
我们之前这篇文章有详细介绍,详见:双歧杆菌:长双歧杆菌
乳酸杆菌
鼠李糖乳杆菌是一种革兰氏阳性乳酸菌,是人类正常肠道菌群的一部分。通常都是安全的,并已广泛用于食品和保健品中。
健康益处


鼠李糖乳杆菌除在以上列举的疾病发挥作用之外,还在体重管理、肝功能、牙齿健康、免疫、怀孕与分娩等方面发挥作用(小规模研究或临床试验单一,证据还不够充分)。
注意事项
鼠李糖乳杆菌在健康成人中是安全的并且耐受性良好,并且似乎不会对年轻或老年受试者造成不良影响。
但是,免疫功能低下的人不应服用它,因为它可能导致菌血症。在器官衰竭、免疫功能低下状态和肠道屏障功能失调的患者中使用益生菌可能导致感染。
短乳杆菌L. brevis是一种植物来源的乳酸菌,L. brevis可以在酸菜和泡菜等发酵食品中找到。它也是人体肠道微生物群的正常组成部分。
健康益处


短乳杆菌除在以上列举的疾病发挥作用之外,还在睡眠、口腔黏膜炎等方面发挥作用(小规模研究或临床试验单一,证据还不够充分)。
注意事项
L. brevis被认为对人类食用是安全的。
L. brevis可以产生生物胺,如酪胺和腐胺。
对于器官衰竭、免疫功能低下和肠道屏障机制功能障碍的患者,应避免使用益生菌,因为可能会导致感染。为避免任何不利影响或意外相互作用,请在服用短乳杆菌之前咨询医生。
干酪乳杆菌是一种革兰氏阳性、非致病性乳酸菌。它存在于发酵乳制品(例如奶酪)、植物材料(例如葡萄酒、泡菜)以及人类和动物的生殖和胃肠道中。
作为一种营养补充剂,干酪乳杆菌已被证明可以改善肠道微生物平衡、关节炎、2 型糖尿病,并具有潜在的抗癌特性。
干酪乳杆菌在动物消化道中的运输过程中增强了免疫系统,可以刺激一氧化氮、细胞因子和前列腺素的产生。
干酪乳杆菌通过激活自然杀伤 (NK) 细胞、细胞毒性 T 细胞和巨噬细胞来促进小鼠化疗药物引起的免疫抑制的恢复。这些都是识别和消除肿瘤细胞和感染细胞的白细胞。
对其他肠道菌群的影响
干酪乳杆菌与普氏菌属、乳酸杆菌属、粪杆菌属、丙酸杆菌属、双歧杆菌属和一些拟杆菌科和毛螺菌属呈正相关,与梭菌属、芽孢杆菌属、沙雷氏菌属、肠球菌属、志贺氏菌属和希瓦氏菌属的存在呈负相关。
在志愿者实验中,L. casei 抑制了潜在有害的假单胞菌和不动杆菌。
含有干酪乳杆菌的发酵乳保留了肠道微生物群多样性,缓解了腹部功能障碍,在学业压力的健康医学生中,它并防止了皮质醇水平升高。
健康益处


干酪乳杆菌除在以上列举的方面发挥作用之外,还在压力、免疫力、呼吸道和胃肠道感染、病毒感染、炎症、关节炎、过敏、牙齿健康、心血管疾病、糖尿病、吸烟的并发症等方面发挥作用(小规模研究或临床试验单一,证据还不够充分)。
注意事项
干酪乳杆菌通常具有良好的耐受性。应避免在器官衰竭、免疫功能低下和肠道屏障功能障碍的患者中使用益生菌。为避免不良反应,请在开始任何新的益生菌补充剂之前咨询医生。
格氏乳杆菌是一种乳酸菌,具有抗菌活性、产生细菌素以及调节先天和适应性免疫系统。
健康益处


格氏乳杆菌除在以上列举的疾病发挥作用之外,还在胆固醇、免疫力、肠道健康(腹泻、溃疡、幽门螺杆菌)、过敏、疲劳、子宫内膜异位症等方面发挥作用(小规模研究或临床试验单一,证据还不够充分)。
注意事项
一般认为是安全的。然而,应避免在器官衰竭、免疫功能低下状态和肠道屏障功能障碍的患者中使用益生菌。为防止不良副作用,请在开始服用新的益生菌补充剂之前咨询医生。
嗜酸乳杆菌是一种革兰氏阳性乳酸菌,传统上广泛用于乳制品行业,最近还用作益生菌。
嗜酸乳杆菌因其风味和益生菌作用而被添加到商业酸奶和乳制品配方中,并且是最常选择的用于饮食的乳酸菌之一。
对其他肠道菌群的影响
接受嗜酸乳杆菌和纤维二糖的健康志愿者表现出乳酸杆菌、双歧杆菌、柯林氏菌和真杆菌的水平升高,而Dialister降低了。
酸奶中的嗜酸乳杆菌可正向改变肥胖小鼠的肠道微生物群并增加肠道双歧杆菌。
嗜酸乳杆菌增加了大鼠中乳酸杆菌和双歧杆菌的数量,增加了乙酸、丁酸和丙酸的水平,并降低了人体微生物群模拟器中的铵盐。


嗜酸乳杆菌除在以上列举的疾病发挥作用之外,还在改善儿童叶酸和 B12 状态、糖尿病、轻微肝性脑病、老化、疲劳等方面发挥作用(小规模研究或临床试验单一,证据还不够充分)。
注意事项
嗜酸乳杆菌通常耐受性良好。然而,应避免在器官衰竭、免疫功能低下状态和肠道屏障功能障碍的患者中使用益生菌,因为它可能导致感染。
肠道微生物植物乳杆菌是一种很有前途的,用于治疗腹泻、高胆固醇和特应性皮炎的益生菌。植物乳杆菌是一种广泛分布的乳酸菌。它常见于许多发酵的植物产品中,例如酸菜、泡菜、卤橄榄和韩国泡菜。
植物乳杆菌是一种具有抗癌、抗炎、抗肥胖和抗糖尿病特性的抗氧化剂。植物乳杆菌可以减少促炎细胞因子(IL-6、IL-8和MCP-1)的产生,增加抗炎细胞因子 ( IL-10 ) 的产生,降低 ALT 和 AST,减少NF-κB.
营养益处
从生牛奶中分离出的植物乳杆菌能够产生 B 族维生素核黄素(B2) 和叶酸(B9)。
植物乳杆菌可使健康女性从果汁饮料中吸收的铁增加约 50%。
植物乳杆菌可以将女性从燕麦基质中的铁吸收提高 100% 以上。
含有植物乳杆菌的发酵乳表现出更高的钙保留摄取。


植物乳杆菌除在以上列举的疾病发挥作用之外,还在改善肥胖、血糖、伤口愈合、牙齿健康、免疫、过敏、念珠菌病等方面发挥作用(小规模研究或临床试验单一,证据还不够充分)。
注意事项
在大鼠中未观察到任何类型的不良反应,即使在大量食用后也是如此。然而,与其他益生菌一样,用于器官衰竭、免疫功能低下状态和功能失调的肠道屏障机制的患者可能会导致感染。为了避免不良事件,请在使用益生菌之前咨询医生。
菊粉(不要与胰岛素混淆,胰岛素是一种控制血糖水平的激素)是一种存在于多种植物中的可溶性纤维。纤维是不被人体肠道消化或吸收的化合物。可溶性纤维吸水并在消化过程中变成凝胶。
来源及用处
菊粉存在于 36,000 种植物中,包括我们日常饮食中食用的植物,如小麦、洋葱、香蕉、大蒜和芦笋。它们也存在于不太常见的食物中,例如菊芋,尤其是菊苣,菊粉是商业提取菊粉的主要来源。
菊粉的其他天然来源有:菊苣根、龙舌兰、雪莲果根、新鲜香草等。不太常见的菊粉来源是蒲公英根、松果菊、牛蒡根等。
含有菊粉的植物用它来储存能量和抵御低温。当暴露于低温时,菊粉起到防冻剂的作用。
菊粉的溶解度使其能够吸收大量水分。当它膨胀时,它会形成一种凝胶,沿途聚集脂肪颗粒并将它们排出体外。
此外,它通过充当有益菌的食物,来增加肠道中有益细菌的数量。
对其他肠道菌群的影响
前面我们知道,双歧杆菌是肠道中的有益菌。菊粉基本上是双歧杆菌的食物并刺激它们的生长和活动。
多项研究表明,菊粉可刺激双歧杆菌的生长。例如:
8 名健康受试者被给予低聚果糖 15 天,并监测他们的粪便。虽然粪便中的细菌总数没有变化,但双歧杆菌成为主要类型。
在另一项研究中,10 名便秘的老年患者服用菊粉 19 天,并监测他们的大便情况。这些患者还表现出双歧杆菌数量增加,同时有害细菌减少。
此外,其他菌群似乎也受到菊粉的影响。
在一项针对 165 人的临床试验中,这种纤维还增加了厌氧菌的丰度(可以通过产生丁酸改善消化,甚至预防结肠癌),并减少嗜胆菌(与大便和便秘有关)。
不一样的研究结果
对实验室培养的细菌进行的一些研究表明,菊粉还会增加沙门氏菌等有害细菌,以及那些不会在正常人中引起疾病但可能导致免疫系统较弱的人感染的细菌,例如克雷伯氏菌和大肠杆菌。然而,其他实验室研究表明,菊粉通过增加双歧杆菌的生长来抑制艰难梭菌等有害细菌的生长。


菊粉除在以上列举的疾病发挥作用之外,还在增加钙和镁的摄取、骨骼健康、炎症性肠病、预防结肠癌的发展等方面发挥作用(小规模研究或临床试验单一,证据还不够充分)。
注意事项
菊粉可能对敏感个体产生某些副作用,或者如果使用的剂量太大产生不良反应。这些包括:
肠道不适,包括胀气、腹胀、胃部噪音、嗳气和痉挛、结肠肿胀、腹泻等。
此外可能会发生严重的过敏反应,但很罕见。在一些孤立的案例中,它会导致过敏反应,可能与食物过敏反应有关。
此外,对于在怀孕和哺乳期间补充菊粉的效果知之甚少。因此,孕妇应避免服用菊粉补充剂。
对于肠易激综合征 (IBS) 患者,低剂量可能会调节肠道细菌并减轻症状,但大剂量可能会产生中性甚至负面影响。
果胶是一种复杂的碳水化合物(多糖),存在于植物细胞壁中,有助于维持其结构。它是一种粘性可溶性纤维,具有形成凝胶的能力。果胶由主要在大肠(结肠)中的有益菌群发酵,产生短链脂肪酸。
由于其凝胶状稠度,果胶是一种流行的食品添加剂,作为增稠剂和纤维的重要来源,具有许多潜在的健康益处。研究表明,它可能有助于治疗高胆固醇、反酸、减肥和糖尿病。
果胶含量高的水果和食物
果胶存在于水果、蔬菜、豆类和坚果中。柑橘皮中的果胶含量最高,如橙皮、柠檬皮和葡萄柚皮(30% 至 35%)和苹果果肉(15% 至 20%)。其他主要来源包括木瓜、李子、醋栗、樱桃、杏子、胡萝卜等 。


在食品工业中用作胶凝剂(用于果酱和果冻)或用作稳定剂(用于糖果、果汁和奶饮料)的果胶主要从苹果果肉或柑橘类水果的果皮中提取。


果胶除在以上列举的疾病发挥作用之外,还在改善糖尿病、减肥、辐射损伤、便秘、呕吐、降血压、溃疡性结肠炎、铅毒性等方面发挥作用(小规模研究或临床试验单一,证据还不够充分)。
对肠道菌群的影响
果胶在结肠中由不同的细菌属发酵,如双歧杆菌、乳酸杆菌、肠球菌、直肠真杆菌、普氏粪杆菌、梭菌、厌氧菌、Roseburia属,以促进其生长。
果胶的降解由不同的细菌衍生酶(如果胶酶、甲基酯酶、乙酰酯酶和裂解酶)促进,产生不同的POS,其取决于微生物群组成和果胶结构。
体外发酵系统报告的果胶效应


Blanco-Pérez F, et al., Curr Allergy Asthma Rep. 2021
果胶通过增加拟杆菌的丰度来改变肠道菌群的组成,并改善酒精诱导的肝损伤(在非酒精性脂肪肝中,拟杆菌的丰度降低)。
膳食纤维果胶可以改变肠道和肺微生物群中厚壁菌门与拟杆菌门的比例,增加粪便和血清中短链脂肪酸的浓度。
通过果胶产生的短链脂肪酸进行免疫调节
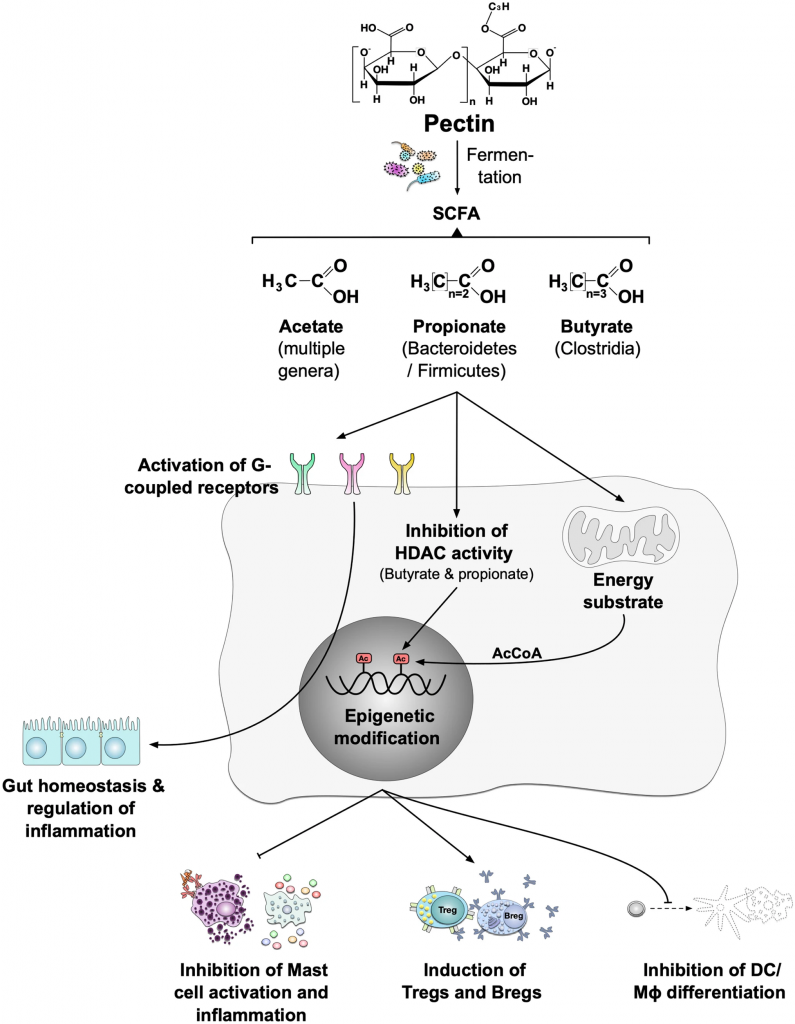

Blanco-Pérez F, et al., Curr Allergy Asthma Rep. 2021
果胶经肠道菌群发酵可产生短链脂肪酸。不同的属可以产生不同的短链脂肪酸。例如,乙酸盐可以由许多不同的属生产;丙酸主要由拟杆菌门和厚壁菌门产生,丁酸主要由梭状芽胞杆菌产生。短链脂肪酸结合“代谢感知”G蛋白偶联受体,如GPR41、GPR43、GPR109A和嗅觉受体(Olfr)-78。这些受体促进肠道内稳态和炎症反应的调节。GPRs及其代谢产物影响Treg活化、上皮完整性、肠道稳态、DC生物学和IgA抗体反应。通过抑制HDAC的表达或功能,短链脂肪酸还影响许多细胞和组织中的基因转录。
过敏:果胶在过敏反应中的作用存在争议
一些临床报告表明,食用果胶后出现过敏反应,这可能归因于果胶和过敏原之间的交叉反应。此外,果胶还被描述为防止胃中过敏原的消化,促进完整的过敏原分子到达肠道并诱发过敏反应。
然而,其他人则认为果胶有直接和间接免疫调节作用。已经提供了一系列广泛的证据,描述了应用果胶诱导有益微生物群的转变和SCFA水平的增加,这两者都与减少体内外的炎症和过敏反应有关。由于不同的果胶增加或减少了与人类健康相关的细菌数量,因此,施用果胶可能会对肠道中的菌群进行特异性调节。
果胶能够通过与TLR2的静电相互作用直接与免疫细胞(如DC和巨噬细胞)相互作用,从而抑制促炎症TLR2-TLR1途径,同时不影响TLR2-TLR6耐受途径。
此外,它能够结合LPS,影响其与TLR4的结合。其他类型的细胞,如T细胞、B细胞和NK细胞也被果胶激活,而腹腔巨噬细胞中的iNOS和COX-2表达则被IKK活性、MAPK磷酸化和NF-κB激活抑制,表明其具有抗炎特性。
炎症性肠病:果胶调节IBD相关菌群
在短链脂肪酸中,丁酸能滋养结肠细胞并抑制结肠肿瘤,因此在大肠中表现出促进局部健康的特性。
产丁酸菌(主要属于厚壁菌门)的流失被认为是IBD期间微生物失调的一个特征。果胶可以促进厚壁菌门中许多丁酸生产者的生长。
果胶物质在调节 IBD 相关肠道微生物群中的综合概况
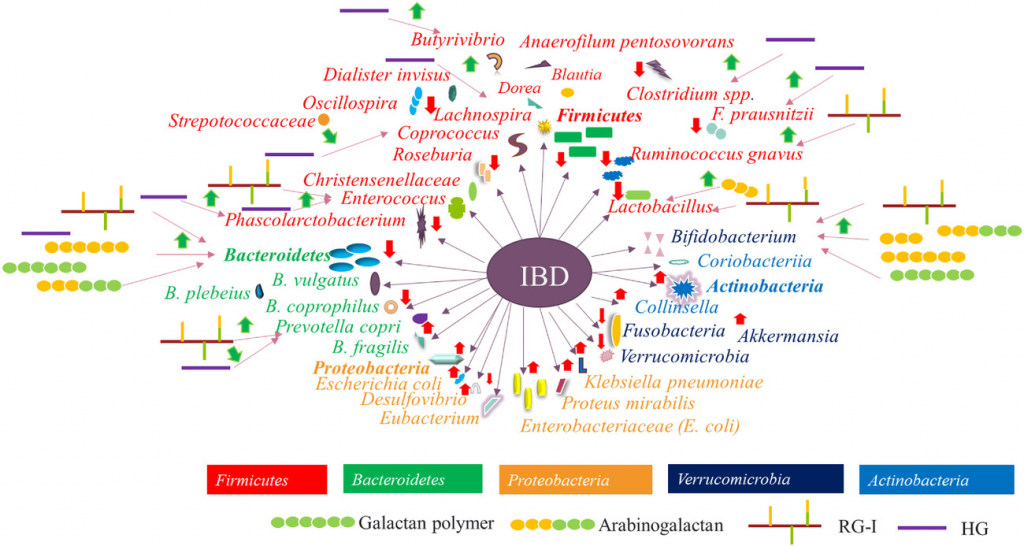

Wu D, et al., Compr Rev Food Sci Food Saf. 2021
注:不同颜色表示不同的细菌门。绿色箭头表示果胶物质对细菌的调节作用,红色箭头表示 IBD 与特定微生物群之间的正相关或负相关。
注意事项
果胶通常对人类食用是安全的。然而,在临床试验中,纤维与果胶的混合物(每天 20 克,持续 15 周)会引起一些与肠道相关的副作用,例如腹泻、肠胃胀气和稀便。
与药物相互作用:
在 3 名高胆固醇患者中,每天服用 15 克果胶和 80 毫克降胆固醇药物(洛伐他汀)会增加 LDL 水平。
建议把果胶和地高辛分开至少 2 小时。
在一项对 7 名健康受试者进行的研究中,他们服用 12 克柑橘果胶和 25 毫克 β-胡萝卜素,果胶将 β-胡萝卜素(维生素 A的前体)血液水平降低了 50% 以上。
姜黄是一种来自植物的香料,通常用于调味或着色咖喱粉、芥末和其他食物。姜黄根也用于制造替代药物。
姜黄已被用于替代医学中,作为降低血液胆固醇、减轻骨关节炎疼痛或缓解慢性肾病引起的瘙痒的一种可能有效的帮助。
姜黄含有几种被称为类姜黄素的主要成分,姜黄素是姜黄中最活跃的植物化学物质。它占类姜黄素的 77%.
姜黄素的健康益处
姜黄素和整个姜黄根茎在治疗慢性疾病如胃肠道、心血管和神经系统疾病、糖尿病和几种癌症方面具有一些有益作用。


姜黄素除在以上列举的疾病发挥作用之外,还在关节痛和关节炎、克罗恩病(肠蠕动、腹泻和胃痛)、狼疮、糖尿病、经前综合症等方面发挥作用(小规模研究或临床试验单一,证据还不够充分)。

姜黄素目前已被认为可以治疗许多疾病,肠道微生物群在姜黄素生物活性机制中可能产生的作用,是一个有趣且有吸引力的研究领域。下面我们来看它们之间有怎样的互作关系。
姜黄素与肠道菌群的相互作用
★ 姜黄素直接调节肠道菌群
食用姜黄素与梭状芽孢杆菌、拟杆菌属物种的增加以及Blautia、Ruminococcus的减少有关。
研究证实,口服姜黄素能够显著改变肠道微生物群落中有益细菌和有害细菌的比例,有利于有益细菌菌株的生长,如双歧杆菌、乳酸杆菌和产丁酸菌,并减少致病菌的丰度,如普雷沃氏菌科、Coriobacteries、肠杆菌、Rikenellaceae.
姜黄素治疗会物种的微生物丰度,例如发现结直肠癌患者粪便中的普雷沃氏菌多。患有结肠癌的小鼠被喂食不同的颗粒饲料,姜黄素的计算人体等效剂量为8/mg/kg/天-162 mg/kg/天。最高剂量的姜黄素给药可减少或消除结肠肿瘤负担,增加乳酸杆菌,减少Coriobacteries。
还清楚地证明,姜黄素治疗可减少几种瘤胃球菌;这是一个有趣的发现,因为瘤胃球菌种类的增加与大肠癌的发生有关。此外,在使用致突变化合物治疗的小鼠中,膳食姜黄素能够将乳酸杆菌的数量恢复到控制水平,这已被证明具有抗肿瘤功能。
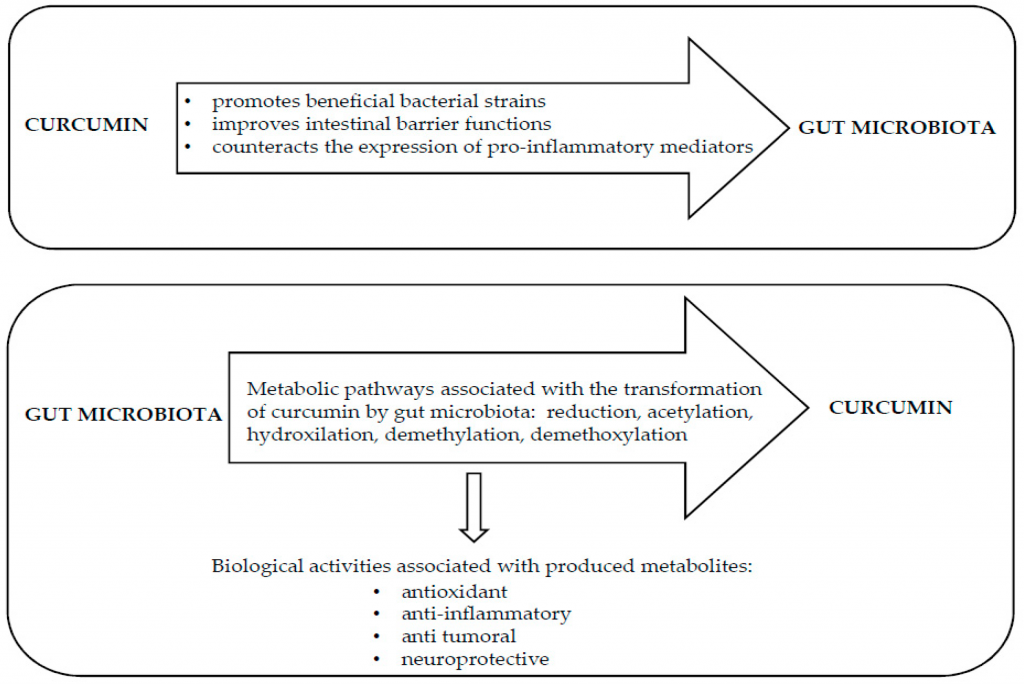

Scazzocchio B, et al., Nutrients. 2020
★ 肠道菌群对姜黄素进行生物转化,产生活性代谢物
姜黄素的代谢转化不仅发生在肠细胞和肝细胞中,还通过肠道微生物群产生的酶进行,这些酶产生许多活性代谢物。姜黄素代谢产物的生物活性可能不同于天然姜黄素,姜黄素的特定生物学特性实际上取决于肠道微生物群消化产生的生物活性代谢产物。
已经鉴定出几种能够修饰姜黄素的肠道细菌:对从人类粪便中分离的微生物的分析表明,大肠杆菌代表了姜黄素代谢活性最高的细菌,通过NADPH依赖的姜黄素/二氢姜黄素还原酶。这种酶能够将姜黄素转化为二氢姜黄素,然后转化为四氢姜黄素。
其他菌群,如长双歧杆菌、假链状双歧杆菌、粪肠球菌、嗜酸乳杆菌和干酪乳杆菌,代表了能够代谢姜黄素的相关菌株,母体化合物的还原率高于50%.
姜黄素代谢物具有与姜黄素相似的特性和效力:四氢姜黄素表现出与母体化合物相同的生理和药理特性,可能是通过β-二酮部分以及酚羟基。此外,四氢姜黄素能够预防氧化应激和神经炎症,还表现出抗癌作用,这可能是由于抑制了显着的细胞因子释放,例如 IL-6 和 TNFα。因此,在对姜黄素的进一步研究中应考虑细菌分解产物,因为它们可能具有有益作用。
对肠道屏障的影响
体外研究表明,姜黄素是一种潜在的化合物,可以恢复被破坏的肠道通透性。在 CaCo2 细胞中,姜黄素能够减轻肠上皮屏障功能的破坏,抵消 LPS 诱导的 IL-1β 分泌并防止紧密连接蛋白破坏。此外,姜黄素还能够减少由 IL-1β 诱导的 p38 MAPK 活化,以及随后紧密连接蛋白磷酸化的升高。
对肠道炎症的影响
代谢组学分析显示姜黄素对氧化应激和炎症的生物标志物具有有益作用,作者认为,姜黄素治疗抵消了非酒精性脂肪肝进展过程中一些细菌菌株的增加。
一项活体动物研究报告,新开发的纳米姜黄素通过抑制促炎介质的表达和诱导Treg扩张(同时伴随粪便丁酸水平的增加)积极改善DSS-结肠炎小鼠的炎症。将姜黄素与正常啮齿类动物饮食的粉末形式(含有0.2%(w/w)纳米姜黄素)混合:该化合物能够抑制NF-κB的激活和治疗小鼠结肠上皮细胞中促炎症介质的表达。
或者,姜黄素可以通过抑制TLR4/MyD88/NF-κB信号通路的激活来减轻LPS诱导的炎症。此外,姜黄素能抑制NF-κB核转位,并减轻其他在癌症中过度激活的促炎症基因的表达。
在喂食添加姜黄素(300 mg/kg姜黄素,与正常饲料混合)28天的断奶仔猪中,Gan等人证明,这种多酚能够通过抑制大肠杆菌增殖来减轻炎症,下调TLR4的表达。
虽然姜黄素迄今为止在体内研究中描述了所有有益的作用,但这些结果必须通过更大的人体临床试验得到一致的支持。
潜在风险和副作用
姜黄素通常耐受性良好。
常见的副作用包括便秘、消化不良(消化不良)、腹泻、腹胀、胃食管反流(胃酸反流)、恶心、呕吐和其他肠道问题。
极少的情况下,姜黄素会引起瘙痒或凹陷性水肿。
姜黄涂在皮肤上可能会引起过敏性接触性皮炎。
在高剂量体外模型中,姜黄素可引起细胞毒性和 DNA 损伤。
协同效应
添加胡椒碱(来自黑胡椒)可能会增加姜黄素在血液中的吸收。研究人员估计它可能会将姜黄素的生物利用度提高多达 2000%.
白藜芦醇是一种多酚,主要存在于葡萄皮和红酒中。
白藜芦醇是一种小多酚,在 1990 年代引起了科学界的关注。这种化合物被戏称为“瓶中的法国悖论”,因为在红酒中发现了白藜芦醇,法国人喜欢在高饱和脂肪饮食的同时食用不太适量的白藜芦醇。然而,法国人的心脏病发病率非常低。
虽然红酒中的白藜芦醇不太可能完全解释这一悖论,但一些科学家表示它可能是一个促成因素。
葡萄皮中的白藜芦醇含量很高,因为葡萄会产生白藜芦醇来防御毒素和寄生虫。它也存在于各种浆果、花生、大豆中。
有限的研究探索了它的抗氧化、抗炎、抗衰老和植物雌激素活性。白藜芦醇确实具有改善慢性疾病的一些潜力。
白藜芦醇有一个主要缺陷:生物利用度差。
白藜芦醇比其他多酚(如槲皮素)更容易从肠道吸收到血液中。但它会很快分解,在血液中留下很少的游离白藜芦醇。
与肠道菌群之间的关系
白藜芦醇和肠道菌群之间的双向相互作用:肠道菌群进行白藜芦醇生物转化,白藜芦醇对肠道菌群进行相互靶向,从而维持肠道稳态。
白藜芦醇的长期摄入改变了DSS诱导小鼠的肠道菌群,厚壁菌门/拟杆菌门的比例显著提高,这反过来又改变了白藜芦醇的代谢。
白藜芦醇补充对肠道生态系统的作用
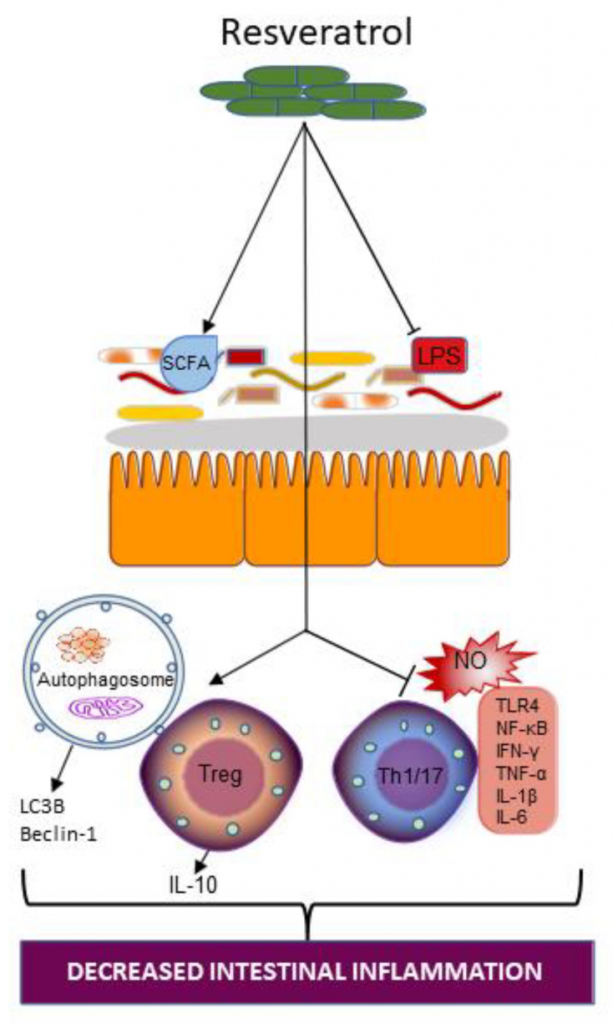

Wellington VNA, et al., Int J Mol Sci. 2021
白藜芦醇添加增加了产短链脂肪酸菌,同时减少了产生LPS的肠道细菌。
补充白藜芦醇也可以通过增加自噬小体的数量和诱导微管相关蛋白1A/1B-light chain 3和Beclin-1的表达来恢复自噬,这两种蛋白在自噬中都是重要的蛋白。白藜芦醇补充也可能会中断Th1/17和细胞因子依赖的促炎通路,一氧化氮依赖的促氧化通路,并干扰toll样受体(TLR) 4信号转导。
白藜芦醇能减轻LPS对小鼠肠道和肝脏的炎症损伤。白藜芦醇减少了拟杆菌和Alistipes的相对丰度,增加了乳酸杆菌的相对丰度。白藜芦醇治疗降低了肝脏中TNF-α、IL-6、IFN-γ、髓过氧化物酶和丙氨酸转氨酶的水平。
此外,益生菌Ligilactobacillus salivarious Li01促进白藜芦醇大量代谢为二氢藜芦醇、硫酸白藜芦醇和白藜芦醇葡萄糖苷酸。在代谢产物中,二氢藜芦醇水平升高最为显著。
肠道菌群的存在促进了二氢藜芦醇的产生,同时促进了硫酸白藜芦醇和白藜芦醇葡萄糖苷酸的消除。

补充剂量
大多数补充剂含有 50 – 500 毫克白藜芦醇。有些含有更高的剂量,高达 1,200 毫克。
临床数据仍然有限。可用的临床研究使用典型的白藜芦醇剂量:
口服纯白藜芦醇的剂量在 150 – 500 毫克/天之间变化。每天喝 1 – 2 杯葡萄酒(100 – 300 毫升)可降低患心脏病的风险并改善血管健康。不含酒精的葡萄酒可能更有益,尤其是对于已经有患心脏病风险的人。
注意:对于有自身免疫和组胺问题的人来说,葡萄酒可能不合适。某些慢病患者如果不确定每天喝一杯葡萄酒是不是安全,请咨询医生。
在接受高剂量(每天 2.5 克或 5 克)白藜芦醇 29 天的人中观察到频繁的胃肠道不适/腹泻。根据 NOAEL 研究,使用 10 倍的安全系数,对于体重 60 公斤的个体,每日 450 毫克白藜芦醇的剂量被认为是安全的。
补充形式
白藜芦醇有多种形式作为口服补充剂:
大多数研究得出结论,反式白藜芦醇是更活跃的白藜芦醇形式。
增加生物利用度的方法
一些可能增加白藜芦醇生物利用度的方法包括:
协同效应
在研究中探索了以下白藜芦醇协同作用:


与药物相互作用
白藜芦醇可能与肠道或肝脏中的药物相互作用,尤其是那些被相同肝酶 (CYP450) 分解的药物。
白藜芦醇还可以减少血液凝固,增强抗凝血药物(抗凝血剂或抗血小板药物,如阿司匹林、氯吡格雷、达肝素、肝素和华法林)的活性。
一起来看下白藜芦醇可能与之相互作用的药物:
“
他汀类药物(Mevacor)
降低高血压的药物(如硝苯地平)
用于减少心律失常的药物(胺碘酮)
抗真菌剂(Sporanox)
抗组胺药(Allegra)
镇静剂/抗焦虑药(安定等苯二氮卓类药物)
抗抑郁药(Halcion)
抗病毒药物和 HIV 药物(蛋白酶抑制剂)
降低免疫反应的药物(免疫抑制剂)
勃起功能障碍(ED)药物
抗凝血药物
NSAID 止痛药/抗炎药,如双氯芬酸 (Voltaren)、布洛芬 (Advil, Motrin)、萘普生 (Anaprox)
……
来源
你知道葡萄酒中含有多少白藜芦醇吗?
通常,白藜芦醇的总浓度为:
红葡萄酒中 0.2 – 5.8 mg/L(平均约为 2 mg/L)
白葡萄酒中仅约 0.68 mg/L
红葡萄酒的反式白藜芦醇含量是白葡萄酒的六倍;白葡萄酒含有高水平的顺式白藜芦醇。红葡萄酒是在不去除葡萄皮的情况下提取的。
白藜芦醇的其他食物来源包括:
黑巧克力、各种浆果、大豆和生或煮花生。
1 杯煮花生含有 1.28 毫克白藜芦醇,大多数食物中的白藜芦醇含量可能太低,无法指望太多特定的健康益处。
副作用
在对健康人进行的临床研究中,每天服用 500 毫克的白藜芦醇具有良好的耐受性。
给予癌症患者高剂量的高生物利用度白藜芦醇(每天 5 克)不会引起任何严重的副作用,但一些患者会出现恶心和胃部不适。
由于缺乏适当的安全数据,儿童应避免使用白藜芦醇。
有人提出,补充白藜芦醇在怀孕期间有益于平衡新陈代谢和产前健康。不过,没有充分的临床研究调查孕妇中的白藜芦醇。
注意事项
白藜芦醇可减少铁吸收和/或血液水平,这可能会恶化贫血。
白藜芦醇转向代表涉及铁代谢(肝素)的重要蛋白质的基因,这可能降低铁吸收。另一方面,白藜芦醇对铁代谢的影响可能是有益的铁过载。
“
肠道菌群的维护和有益菌等的获得以及核心菌群的定植等,与每个人自身的饮食,遗传,生活环境等息息相关,尽量保持饮食多样化,每天食物应该包括蛋白,肉,全谷物,蔬菜,水果,坚果,鱼油/亚麻籽,发酵和多酚食物,食材选择新鲜,无过渡添加/烹饪同时清洁干净的食物,此外,不滥用抗生素或过渡清洁肠道,合理睡眠,适量运动,保持乐观,将有利于肠道和菌群健康。
主要参考文献:
Kato-Kataoka A, Nishida K, Takada M, et al., Fermented Milk Containing Lactobacillus casei Strain Shirota Preserves the Diversity of the Gut Microbiota and Relieves Abdominal Dysfunction in Healthy Medical Students Exposed to Academic Stress. Appl Environ Microbiol. 2016 May 31;82(12):3649-58. doi: 10.1128/AEM.04134-15. PMID: 27208120; PMCID: PMC4959178.
Segers ME, Lebeer S. Towards a better understanding of Lactobacillus rhamnosus GG–host interactions. Microb Cell Fact. 2014;13 Suppl 1(Suppl 1):S7. doi:10.1186/1475-2859-13-S1-S7
Ren JJ, Yu Z, Yang FL, et al. Effects of Bifidobacterium Breve Feeding Strategy and Delivery Modes on Experimental Allergic Rhinitis Mice. PLoS One. 2015;10(10):e0140018. Published 2015 Oct 7. doi:10.1371/journal.pone.0140018
Diaz Ferrer J, Parra V, Bendaño T, Montes P, Solorzano P. Utilidad del suplemento de probioticos (Lactobacillus acidophilus y bulgaricus) en el tratamiento del sindrome de intestino irritable [Probiotic supplement (Lactobacillus acidophilus and bulgaricus) utility in the treatment of irritable bowel syndrome]. Rev Gastroenterol Peru. 2012 Oct-Dec;32(4):387-93. Spanish. PMID: 23307089.
Jeun J, Kim S, Cho SY, Jun HJ, Park HJ, Seo JG, Chung MJ, Lee SJ. Hypocholesterolemic effects of Lactobacillus plantarum KCTC3928 by increased bile acid excretion in C57BL/6 mice. Nutrition. 2010 Mar;26(3):321-30. doi: 10.1016/j.nut.2009.04.011. Epub 2009 Aug 19. PMID: 19695834.
Yoo JY, Kim SS. Probiotics and Prebiotics: Present Status and Future Perspectives on Metabolic Disorders. Nutrients. 2016;8(3):173. Published 2016 Mar 18. doi:10.3390/nu8030173
Tursi A, Brandimarte G, Giorgetti GM, Forti G, Modeo ME, Gigliobianco A. Low-dose balsalazide plus a high-potency probiotic preparation is more effective than balsalazide alone or mesalazine in the treatment of acute mild-to-moderate ulcerative colitis. Med Sci Monit. 2004 Nov;10(11):PI126-31. Epub 2004 Oct 26. PMID: 15507864.
van Zanten GC, Krych L, Röytiö H, Forssten S, Lahtinen SJ, Abu Al-Soud W, Sørensen S, Svensson B, Jespersen L, Jakobsen M. Synbiotic Lactobacillus acidophilus NCFM and cellobiose does not affect human gut bacterial diversity but increases abundance of lactobacilli, bifidobacteria and branched-chain fatty acids: a randomized, double-blinded cross-over trial. FEMS Microbiol Ecol. 2014 Oct;90(1):225-36. doi: 10.1111/1574-6941.12397. Epub 2014 Sep 5. PMID: 25098489.
Kadooka Y, Sato M, Ogawa A, Miyoshi M, Uenishi H, Ogawa H, Ikuyama K, Kagoshima M, Tsuchida T. Effect of Lactobacillus gasseri SBT2055 in fermented milk on abdominal adiposity in adults in a randomised controlled trial. Br J Nutr. 2013 Nov 14;110(9):1696-703. doi: 10.1017/S0007114513001037. Epub 2013 Apr 25. PMID: 23614897.
Fujii T, Ohtsuka Y, Lee T, Kudo T, Shoji H, Sato H, Nagata S, Shimizu T, Yamashiro Y. Bifidobacterium breve enhances transforming growth factor beta1 signaling by regulating Smad7 expression in preterm infants. J Pediatr Gastroenterol Nutr. 2006 Jul;43(1):83-8. doi: 10.1097/01.mpg.0000228100.04702.f8. PMID: 16819382.
Kanjan P, Hongpattarakere T. Prebiotic efficacy and mechanism of inulin combined with inulin-degrading Lactobacillus paracasei I321 in competition with Salmonella. Carbohydr Polym. 2017 Aug 1;169:236-244. doi: 10.1016/j.carbpol.2017.03.072. Epub 2017 Apr 1. PMID: 28504142.
Micka A, Siepelmeyer A, Holz A, Theis S, Schön C. Effect of consumption of chicory inulin on bowel function in healthy subjects with constipation: a randomized, double-blind, placebo-controlled trial. Int J Food Sci Nutr. 2017 Feb;68(1):82-89. doi: 10.1080/09637486.2016.1212819. Epub 2016 Aug 5. PMID: 27492975.
Blanco-Pérez F, Steigerwald H, Schülke S, Vieths S, Toda M, Scheurer S. The Dietary Fiber Pectin: Health Benefits and Potential for the Treatment of Allergies by Modulation of Gut Microbiota. Curr Allergy Asthma Rep. 2021 Sep 10;21(10):43. doi: 10.1007/s11882-021-01020-z. PMID: 34505973; PMCID: PMC8433104.
Wu D, Ye X, Linhardt RJ, Liu X, Zhu K, Yu C, Ding T, Liu D, He Q, Chen S. Dietary pectic substances enhance gut health by its polycomponent: A review. Compr Rev Food Sci Food Saf. 2021 Mar;20(2):2015-2039. doi: 10.1111/1541-4337.12723. Epub 2021 Feb 16. PMID: 33594822.
Scazzocchio B, Minghetti L, D’Archivio M. Interaction between Gut Microbiota and Curcumin: A New Key of Understanding for the Health Effects of Curcumin. Nutrients. 2020;12(9):2499. Published 2020 Aug 19. doi:10.3390/nu12092499
Ding S, Jiang H, Fang J, Liu G. Regulatory Effect of Resveratrol on Inflammation Induced by Lipopolysaccharides via Reprograming Intestinal Microbes and Ameliorating Serum Metabolism Profiles. Front Immunol. 2021 Nov 15;12:777159. doi: 10.3389/fimmu.2021.777159. PMID: 34868045; PMCID: PMC8634337.
Wellington VNA, Sundaram VL, Singh S, Sundaram U. Dietary Supplementation with Vitamin D, Fish Oil or Resveratrol Modulates the Gut Microbiome in Inflammatory Bowel Disease. Int J Mol Sci. 2021;23(1):206. Published 2021 Dec 24. doi:10.3390/ijms23010206
Yao M, Fei Y, Zhang S, et al. Gut Microbiota Composition in Relation to the Metabolism of Oral Administrated Resveratrol. Nutrients. 2022;14(5):1013. Published 2022 Feb 28. doi:10.3390/nu14051013
Del Follo-Martinez A, Banerjee N, Li X, Safe S, Mertens-Talcott S. Resveratrol and quercetin in combination have anticancer activity in colon cancer cells and repress oncogenic microRNA-27a. Nutr Cancer. 2013;65(3):494-504. doi: 10.1080/01635581.2012.725194. PMID: 23530649.
Malhotra A, Nair P, Dhawan DK. Curcumin and resveratrol synergistically stimulate p21 and regulate cox-2 by maintaining adequate zinc levels during lung carcinogenesis. Eur J Cancer Prev. 2011 Sep;20(5):411-6. doi: 10.1097/CEJ.0b013e3283481d71. PMID: 21633290.

谷禾健康
乳酸菌属益生菌是使用最广泛的益生菌之一。罗伊氏乳杆菌( L. reuteri ) 是一种经过充分研究的益生菌,可以在大量哺乳动物中定殖。
罗伊氏乳杆菌是一种革兰氏阳性杆状细菌,已在各种食物中发现,尤其是肉类和奶制品。在人类中,罗伊氏乳杆菌存在于不同的身体部位,包括胃肠道、泌尿道、皮肤和母乳。罗伊氏乳杆菌的丰度因个体而异。
可能的优势
● 可能促进皮肤光泽和头发浓密
● 可能有助于对抗感染
● 可能减少炎症并加强免疫
● 可能会改善肠道健康(减少 IBS 和 IBD 症状)
● 可能降低胆固醇
可能的副作用
● 可能对组胺不耐受的人不利
● 可能导致某些人体重增加
● 缺乏大规模临床研究
● 长期补充的安全性未知
罗伊氏乳杆菌(Lactobacillus reuteri)名字来自德国微生物学家 Gerhard Reuter,他在1960 年代在人类肠道和粪便样本中发现了它。1960 年代被发现时,罗伊氏乳杆菌自然存在于 30-40% 的人体内,现在大约降至10-20%。科学研究者将这种下降与生活方式的改变联系起来。我们不像以前那样吃发酵食品,如酸菜,而是使用防腐剂,这会杀死食物和体内的细菌。
罗伊氏乳杆菌在发酵过程中能够产生葡聚糖和果聚糖。其中一种葡聚糖,α-1,4/1,6 葡聚糖,分子量为 40 MDa,支化度约为 16%,似乎是一种饱腹感诱导剂,对胰岛素和血糖水平有良好的影响在人类。葡聚糖不会在胃和空肠中降解,而是在结肠中完全降解。由于其慢淀粉特性,这种葡聚糖可能是烘焙应用中一种促进健康的成分。
不同菌株的Lactobacillus reuteri已被证明具有不同的生理作用。例如,Lactobacillus reuteri DSMZ 17648用于治疗幽门螺杆菌(H. pylori),而Lactobacillus reuteriNCIMB 30242 用于治疗高胆固醇。
但是,罗伊氏乳杆菌补充剂尚未获得批准用于医疗用途,而且有的益处和副作用缺乏可靠的临床研究。法规制定了补充剂的制造标准,但不保证它们是安全或有效的。
大多数关于Lactobacillus reuteri的研究是在动物或细胞中进行的。临床研究很少,而且大多数是低质量的、小规模的或可能存在偏见的。此外,使用的确切菌株因不同研究而异。
尽管罗伊氏乳杆菌在人类中是正常的,但并不是每个人的胃肠道中都有它。口服补充剂可以增加和补充胃肠道罗伊氏乳杆菌,然而它不一定会长期留在那里。
同样,罗伊氏乳杆菌的良好来源是乳制品和肉类,素食者和大多数素食者都避免食用这些食品,因此补充剂很重要。在母乳喂养时服用罗伊氏乳杆菌补充剂的女性更有可能将这些有益细菌转移给婴儿。
为消化和吸收而建,胃肠系统的某些部位已发展为对微生物定植不利。这方面的例子可以在由小肠上部胃酸和胆汁盐引起的低 pH 条件下看到。因此,在胃肠道定植的第一步就是在这样的环境中生存。幸运的是,罗伊氏乳杆菌对低 pH 值和胆汁盐具有抵抗力。这种抗性被认为至少部分取决于其形成生物膜的能力。