-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康
当我们刷牙、吃饭、吞咽时,可能很少意识到:口腔其实是全身健康尤其胃肠道健康的第一道防线。
随着研究不断深入,牙周炎——这类发生在牙齿周围、因免疫失衡而持续炎症的常见疾病——正从一个“口腔小问题”跃升为影响胃肠功能障碍甚至全身的重要信号来源。越来越多证据显示,牙周炎不仅关乎牙龈是否出血、牙齿是否松动,更可能通过微生物及其产物远距离“跨界”,扰乱肠道菌群,牵动代谢、免疫与多器官功能,进而影响肠道健康。
牙周炎的发生,源于牙齿表面微生物生物膜与宿主免疫的长期博弈。诸如牙龈卟啉单胞菌(Porphyromonas gingivalis)、幽门螺杆菌(Helicobacter. Pylori)、链球菌(Streptococcus)、 韦荣球菌(Veillonella)、微小单胞菌(Parvimonas micra)、具核梭杆菌(Fusobacterium nucleatum)、消化链球菌(Peptostreptococcus)等“问题角色”,在局部引燃炎症反应,促使牙龈与牙周组织释放促炎因子、活性氧与急性期蛋白,逐步破坏软组织与牙槽骨。同时,这一炎症火种并不止步于口腔:研究已将牙周炎与糖尿病、心血管疾病、类风湿关节炎乃至多种癌症联系起来。
其中,“口腔—肠道轴”是关键通道。部分牙周病原体及其分子产物会随唾液被持续吞咽,抵达肠道后成功生存与定植,进一步打破原有微生态平衡。以 P. gingivalis 和 F. nucleatum 为代表的口腔致病菌,凭借脂多糖、挥发性硫化物等毒力因子,削弱肠上皮紧密连接,提升肠黏膜通透性,形成所谓的“肠漏”。这不仅放大先天与适应性免疫反应,扰动 Treg/Th17 等免疫平衡,上调 IL-1β、IL-6、TNF-α 等促炎因子级联,还通过代谢与表观遗传层面的重编程,改写上皮与免疫细胞功能,推动全身性炎症与氧化应激的恶性循环。最终,一个由“菌群失调—屏障受损—免疫失衡”相互放大的炎症正反馈环路就此形成。
近年来,口腔细菌与炎症性肠病、脂肪肝与肝纤维化、肝细胞癌以及胰腺癌等多种胃肠道疾病的联系日益清晰。尽管牙周炎与这些疾病的相关性已被证实,但口腔菌群如何精确地改写肠道微生态与免疫网络,其复杂的分子机制仍有待全面阐明。
本文将以最新研究为证据,系统梳理牙周病原体如何通过“口腔—肠道轴”引发肠道菌群失调与功能障碍:从毒力因子破坏屏障、免疫失衡级联放大,到代谢与表观遗传层面的细胞重编程。通过这条贯穿口腔与肠道的隐秘通道,我们将看到:口腔健康不仅影响容貌与社交,更可能作为维系机体稳态的前线屏障,关系到全身系统的平衡稳态。
近年来,随着宏基因组测序与培养技术的进步,研究者在肠道生态系统中频繁检测到源自口腔的细菌群落。
★ 肠道中可检出多种常见的口腔相关菌
肠道微生物群以厌氧菌为主,主要隶属于:拟杆菌门、厚壁菌门、放线菌门、变形菌门和疣微菌门,其中不少为典型口腔常驻菌。
肠道中常见的口腔相关类群包括:小单胞菌(Parvimonas)、卟啉单胞菌(Porphyromonas)、消化链球菌(Klebsiella Peptostreptococcus)、克雷伯菌、链球菌、嗜血杆菌、梭杆菌及部分变形菌门成员。
检出的代表性口腔物种有:幽门螺杆菌、微小微单胞菌(Parvimonas micra)、P.gingivalis、T.forsythia、T.denticola、P.intermedia、具核梭杆菌、流感嗜血杆菌,以及大肠杆菌、克雷伯氏菌属、Filifactor alocis、弯曲杆菌和粪链球菌等。
★ 许多口腔细菌定植于患病个体肠道
多种口腔细菌被检测到定植于患病个体的肠道与相关组织,其中以幽门螺杆菌最为常见,常出现于慢性胃炎、消化性溃疡、炎症性肠病和胃癌患者。肝硬化、非酒精性脂肪性肝病、肝细胞癌、溃疡性结肠炎(UC)与克罗恩病(CD)患者的粪便中亦可检出牙周病原体。
幽门螺杆菌、具核梭杆菌与粪链球菌在胰腺癌、结肠癌、肝病及IBD患者的胰腺组织与导管、肝脏、肠道及结肠中均有发现。与单纯肝细胞癌相比,合并肝硬化的患者体内大肠杆菌和梭杆菌水平更高。
作为牙周关键病原体的牙龈卟啉单胞菌(porphyromonas gingivalis),还被证实与胰腺导管腺癌(PDAC)的发病风险和死亡率升高呈正相关。
具核梭杆菌(F.nucleatum)被认为是慢性肝病、肝硬化、IBD、胰腺癌、肝细胞癌和结直肠癌(CRC)的潜在标志物。在 CRC 来源的生物膜中其丰度升高,而健康结肠组织通常检测不到。所有分离的生物膜均为多菌种组成,且肿瘤与配对的健康组织的生物膜样本均含侵袭性细菌。由此可见,CRC 相关生物膜在结构和致病性上与口腔疾病相似,可能参与 CRC 的肿瘤发生。
★ 致病性牙周菌在肠道可能推动疾病发生
其他研究还表明,肠道生物膜除了含有致病性牙周细菌(如F.nucleatum、P.gingivalis)外,还含有口腔共生菌(Parvimonas、Peptostreptococcus、Prevotella),这可能导致结直肠癌的发展。
研究显示,健康与 CRC 组织中可共同检出口腔厌氧菌,如具核梭杆菌、弯曲杆菌和纤毛菌属;在肿瘤组织内,它们与牙龈卟啉单胞菌等共同构建协作性多菌群网络。弯曲杆菌还能与具核梭杆菌共聚集,后者作为桥接微生物,吸引其他相容口腔菌定植于肠黏膜。
肝硬化患者的口源性菌在粪便中亦明显增多。多项研究报道,牙周病患者的肠道菌群呈厚壁菌门/拟杆菌门比值上升,并富集 Euryarchaeota、Verrucomicrobia 和变形菌门。IBD 患者肠黏膜中嗜血杆菌与韦荣球菌属显著升高;类似地,结直肠肿瘤也促进口腔菌在肠道的定植。
口腔细菌可以通过多种机制诱导肠道变化。口腔细菌诱发肠道功能障碍的一些潜在致病机制如下:
• Toll样受体的激活和促炎细胞因子的释放
• 补体系统的调制
• 氧化应激的改变和活性氧的释放
• 炎症小体的激活
• 激活急性期反应和释放急性期蛋白
• microRNA的激活
• 挥发性硫化合物的释放
• 宿主细胞的坏死毒性
牙周病、口腔细菌和胃肠道功能障碍之间联系
Mukherjee S,et al.Crit Rev Microbiol.2025
牙周炎症(牙龈炎和牙周炎)的发作以促炎介质(如IL1、IL8、IL17 和 TNF)的大量释放为标志,以及各种信号通路和宿主受体的激活,如Toll样受体 (TLR)、补体系统、核因子κ-β (NF-Kb)。这些促炎介质通过血管或唾液进入体循环,并到达肝脏,在那里它们触发急性期反应和急性期蛋白(如 C 反应蛋白 (CRP) 的释放。这会增加全身炎症负担和氧化应激。炎症负荷的增加反过来又会影响肠道的各个部位并导致胃肠道功能障碍。
▸ 激活Toll 样受体
口腔细菌进入肠道后可附着并激活分布于肠上皮、固有层及免疫细胞(巨噬细胞、中性粒细胞、Kupffer 细胞)上的多种Toll样受体(TLRs)(如 TLR2/3/4/5)。
其中 TLR2/4 是牙周病中最常被激活的受体,并与胃肠功能障碍相关。TLR 作为“肠道传感器”,在维持稳态、调控免疫与塑造微生物群方面至关重要;其遗传变异与菌群结构改变相关。
TLR 功能异常及多态性/突变与肠道免疫反应、微生物特征和炎症直接相关。促炎介质外流与 TLR 过度激活会重塑微生物特征,驱动多种肠道与相关疾病,包括胃炎、非酒精性脂肪性肝病、炎症性肠病(CD、UC)、消化性溃疡、肝纤维化及多种肿瘤(肝癌、CRC、胰腺癌)。
✔ 口腔细菌与TLR相互作用激活炎症通路
口腔细菌与Toll样受体(TLRs)相互作用后,可激活肠道多条炎症通路(NF‑κB、JNK、PI3K、MAPK、AP‑1、p38),诱导促炎因子(TNF‑α、IL‑1β、IL‑6、IL‑12、IL‑18)与抗炎因子(IL‑10)释放。
其中 NF‑κB‑MyD88 是肠道炎症与肿瘤发生的核心通路,其激活依赖细菌黏附与脂多糖通过 TLR‑MyD88 传导。口腔菌源脂多糖结合 MD2/TLR4 复合体,触发先天免疫;脂多糖结合蛋白(LPS‑BP,60 kDa 血清糖蛋白)存在于肠道、肝脏和胃肠上皮中,并在口腔细菌入侵时被激活。
与牙周病原体和胃肠道功能障碍相关的研究
Mukherjee S,et al.Crit Rev Microbiol.2025
▸ 触发炎症通路、增加炎症
✔ 慢性炎症信号可推动肠道炎症及结直肠癌等疾病的发生发展
慢性 NF‑κB 信号是炎症性肠病(UC、CD)、肠道炎症及胰腺癌、结肠癌、胃癌发生的关键驱动。MAPK 通路在牙龈卟啉单胞菌入肠后显著上调;牙周炎期释放的 TNF 亦可激活 MAPK,增加 CD、UC 风险。
TNF 还能改变胰腺 TLR4 表达,诱发胰腺炎;TLR4 促使胰腺组织大量释放弹性蛋白酶与硫酸乙酰肝素,破坏实质并加剧炎症。研究还发现,牙龈卟啉单胞菌的含脂多糖微囊泡可如“微子弹”般穿透肠黏膜,放大肠道炎症。
牙龈卟啉单胞菌可与补体受体(C5aR)与 TLR2 串扰,上调 IL‑1、IL‑6、IL‑17 和 TNF 的分泌;并可激活补体受体(CR)与 NOD 受体,进一步提高肠道细胞因子水平。由 NF‑κB 与 TLR 诱导的细胞因子(如 IL‑1β、IL‑6、IL‑17)还能通过激活 STAT3 通路促使 CD4(+)T 细胞增殖,并增强癌细胞的增殖、易位与转移。STAT3 激活与胰腺癌、胃癌和结直肠癌相关。
✔ 口腔细菌进入肠道会影响通透性和炎症
口腔细菌还激活 TLR4,导致肠上皮中的 Cox-2 受体激活。这导致受伤肠道增殖,并在肠道中释放促炎介质,这些促炎细胞因子与微生物一起影响肠道中的紧密连接蛋白“zonula occludens-1”和“occludin”,并导致导致肠道炎症和通透性增加。
肠上皮通透性升高促进细菌穿透并周期性加剧炎症。P. gingivalis 诱导的炎症与菌群失衡还会改变肠道代谢物谱,增加钙化风险。口源性脂多糖与 CpG DNA 作用于 TLR4/TLR9,可能联结原发性胆汁性肝硬化与原发性硬化性胆管炎的硬化进程。
口腔细菌及其副产物如何损伤胃肠道功能
Mukherjee S,et al.Crit Rev Microbiol.2025
口腔细菌与肠道中的 Toll 样受体 (TLR) 相互作用并导致促炎细胞因子(白细胞介素 (IL1、IL8)、前列腺素 (PGE2)、肿瘤坏死因子 (TNF)。一些口腔细菌还会释放挥发性硫,如硫化氢、二甲硫、二甲基二硫化物和甲硫醇,导致上皮通透性可逆增加和屏障功能丧失。
硫化氢还被证明可以通过诱导肠粘膜中的 DNA 低甲基化来增加隐窝形成和溃疡。这些炎症介质还会影响细胞粘附分子,如小带闭塞和闭塞蛋白,并增加通透性。这有助于细菌轻松进一步侵入肠道组织,增加肠道和肠道炎症中微生物菌群失调的风险。
✔ 具核梭杆菌能与P. gingivalis一起增加肠道炎症负担
具核梭杆菌(F.nucleatum) 是另一种潜在的口腔细菌,可以损害肠道上皮完整性、激活 TLR 并增加肠道通透性。研究还指出,具核梭杆菌诱导的 TLR4 激活可导致肝窦内皮细胞通过 NF-κB 激活产生更多的 TNF-α 和活性氧 (ROS),从而导致肝功能障碍和肝细胞增殖。
当具核梭杆菌激活TLR4信号传导时,Nf-kB和miRNA21表达也会升高。一项研究发现,结直肠癌患者组织中的 miRNA21 和具核梭杆菌DNA 水平较高。这些标志物表明 CRC 患者的风险更大且预后不良。具核梭杆菌还可以与牙龈假单胞菌等口腔病原体共同聚集和感染,并增加肠道组织中的炎症负荷。
!
总结与要点:
1) 关键信号轴线与级联
NF-κB 为核心炎症驱动:慢性激活贯穿 IBD、黏膜炎症到消化道肿瘤发生。
MAPK 通路被放大:受P.gingivalis入侵与 TNF 上调共同促推,连接牙周炎与肠道炎症风险。
TLR4–胰腺炎通路:TNF 改变胰腺 TLR4 表达;TLR4 触发弹性蛋白酶与肝素硫酸盐释放,破坏实质组织,形成炎-损伤正反馈。
2) 口腔致病菌的多受体串扰
含脂多糖微囊泡穿透黏膜,提升局部脂多糖负荷与免疫识别。与C5aR–TLR2串扰,上调 IL-1/6/17 与 TNF。
激活补体受体与 NOD 样受体,进一步扩增炎症网络。
这说明口源菌不仅通过 TLR4–LPS,还通过补体与胞内模式识别受体共同塑造高炎症微环境。
3) 炎症—肿瘤耦合的信号枢纽:STAT3
NF-κB/TLR 诱导因子 → STAT3 激活:IL-6、IL-1β、IL-17 驱动 STAT3,促进 CD4(+) T 细胞增殖与肿瘤相关表型(增殖、侵袭、迁移)。
疾病谱系关联:STAT3 的持续活化与胰腺癌、胃癌、CRC 的进展密切相关。
▸ 激活补体系统与胃肠道功能障碍
补体系统是由30余种可溶性蛋白和膜结合蛋白组成的精密免疫反应系统,存在于血清和组织液中,通过经典、旁路和凝集素三条途径激活,具有清除病原体、调节免疫和介导炎症等功能。
✔ 牙周细菌诱导的炎症介质可激活补体受体
牙周细菌及牙周炎产生的炎症介质可激活补体受体(CR)。牙周菌黏附于受体后大量释放 C3a、C5a(强效趋化因子),招募肠道中性粒细胞、淋巴细胞与巨噬细胞,触发吞噬并启动免疫反应。C3a/C5a 与其受体 C3aR/C5aR 结合,进一步激活先天与适应性免疫通路。
正常情况下,C5aR 在肝脏 Kupffer 细胞和星状细胞中构成性表达,其水平可随 IL‑1、IL‑6、TNF 等炎症因子上调。补体系统还可调控肠道微生物,从而影响胃肠功能与肠道稳态。
✔ 补体系统的失衡与胃肠道疾病相关
补体系统的失衡与多种胃肠道疾病相关,包括结直肠癌、溃疡性结肠炎、克罗恩病、肝纤维化、病毒性肝炎、酒精性肝病及肝缺血/再灌注损伤。
多项研究在患者肠道组织中检测到补体成分:如 UC 患者固有层与上皮基底外侧膜的 C3、IgG 强阳性;腺癌与 CD 患者小肠隐窝及绒毛‑隐窝区可见 C3、C4 沉积。还发现黏膜 C3 mRNA 升高并与 IBD 患者的 IL‑17 水平相关;IL‑17(牙周炎中升高)与上皮下肌成纤维细胞产生 C3 呈正相关。
总体上,C3、C4 水平升高与溃疡性结肠炎、克罗恩病病情严重度相关。
✔ 口腔病原体可加剧肠道炎症与失衡
基于现有证据,补体经典通路在溃疡性结肠炎(UC)患者的上皮细胞中更为活跃,而替代通路在克罗恩病(CD)患者中更显著。CD 患者组织中可检测到 C4 mRNA;IBD 患者结肠黏膜 C3 mRNA 的升高与 IL‑17 mRNA 呈正相关。免疫组化显示,暴发性与急性肝炎患者坏死区周围存在 MAC 沉积,提示补体参与肝损伤发病机制。
牙周炎诱导的 IgG 可在 UC 上皮细胞触发经典通路,致 C3b 与 MAC 沉积。口腔病原体(如 P. gingivalis)可下调 CR3a/CR5a 以逃逸免疫,进而加剧肠道炎症与失衡;其还可通过赋予 C5 转化酶样活性并促凝血酶原激活,裂解 C5 生成 C5a。
通过 C5a 介导的途径,牙龈蛋白酶诱导 M1 巨噬细胞极化,促进P.gingivalis感染扩散。P.gingivalis 介导的 C5a‑C5aR 激活增强肠道 Gi 依赖的细胞内 Ca2+ 信号,协同放大其微弱的 cAMP 反应,提升 TLR2 激活与促炎因子产生;持续高 cAMP 还削弱 NO 杀菌效应,并激活 PKA 使 GSK‑3 失活。C5aR‑TLR2 串扰除抑制 TLR2 诱导的 IL‑12p70 外,还上调 IL‑1、IL‑6、IL‑17、TNF,推动胃肠黏膜炎症。
类似地,Interpain A(InpA)可激活血清 C1 复合物,使 C1q 沉积于菌体表面;中间普雷沃氏菌的半胱氨酸蛋白酶 Interpain A(InpA)可裂解 C3,释放过敏毒素 C3a,提升局部与全身炎症负荷。
牙周病原体,尤其是牙龈卟啉单胞菌(P.gingivalis),可上调共刺激分子 CD80/CD86,激活多种T细胞亚群。牙周炎触发的补体激活同时诱导Th1与Th2反应:前者促释 IL‑12、IL‑1、IFN、TNF、IL‑18,后者促释 IL‑4、IL‑5、IL‑13。
这些细胞因子激活多类免疫细胞,包括Th细胞、T 抑制细胞、Treg 及抗原呈递细胞(巨噬细胞、树突状细胞)。Th 细胞促进浆细胞分化,产生IgG、IgA、IgM;Th1 为 IFN‑γ 等介质的主要来源,有助于清除肠道内的细胞内病原体。Th 细胞还支持生发中心 B 细胞分化与高亲和力抗体(含肠道 IgA)生成。肠黏膜富含非常规 T 细胞(γδ T、NKT、MAIT),共同维持屏障功能与免疫稳态。
▸ Th17轴:连接牙周炎与肠黏膜炎症的关键
✔ 发炎的牙周组织会产生大量Th17影响炎症性肠病风险
Th17 细胞被视为肠道功能障碍的关键介质。发炎的牙周组织大量产生 Th17,提升其体循环水平。P.gingivalis 可经 TLR2/4 与 RORγt 促进 IL‑17、IL‑1β、IL‑6、IL‑23 分泌,增强 Th17 分化;Th17 通路激活进一步提升肠黏膜中IL‑1β、IL‑6、IL‑17、IL‑22、IL‑23,增加活动性UC与CD风险。
IL‑17 升高及 RORC2 mRNA 上调还促进血栓素样蛋白 TSP‑1 释放,关联 IBD/UC/CD 风险上升。P.gingivalis‑LPS 通过增强单核细胞 δ‑样配体 4 表达放大 Th17 反应,促炎并促肿瘤发生;其牙龈蛋白酶可直接诱导 T 细胞 CD69/CD25 表达并驱动 IL‑17 产生,还可通过激活缓激肽 B2 受体或蛋白酶激活受体 2 引发 IL‑17 反应。
相反,P.gingivalis 亦可经 TLR4 下调 Treg 转录因子(Foxp3、TGF‑β、IL‑10)。UC 与 CD 患者的炎症黏膜中 IL‑17 mRNA 明显升高。P. gingivalis 蛋白酶还能降解驱动 Th1/Th17 的细胞因子,以获取营养并助长其他肠道微生物。除P.gingivalis 外,肠杆菌与克雷伯菌等口腔菌在肠道异位定植同样与 Th17/Th1 积累相关;研究发现,肺炎克雷伯菌可通过口腔‑肠道迁移显著增强Th1反应。
▸ 口腔炎症跨黏膜迁移驱动肠道炎症
T细胞介导的细胞因子可加重黏膜炎症与胃肠通透性,改变胃动力、延迟胃排空,并在IBD、CD、UC 中引发结肠症状;同时提升胃癌与肝细胞癌(HCC)风险。免疫组化研究显示,IBD/UC/CD 患者的炎症黏膜中 CD68 阳性细胞、Th17 与 IL‑17 表达升高;IBD 患者黏膜中由Th17共产生的IFN‑γ约为健康者的5.5倍。
✔ 口腔炎症会通过T细胞影响肠道菌群及炎症
口腔病原体可激活Th17,局部产生的Th17经口腔引流淋巴结迁移至肠道;T细胞在肠系膜淋巴结(MLN)获得肠道归巢“印记”,依赖 MAdCAM‑1 与 CCL25 通过血循环进入肠道。由此,口腔炎症可产生口源性致病反应性 T 细胞,这些细胞迁移至肠道后激活肠道菌群并诱发炎症。
口腔致病菌通常不定植于健康个体胃肠道;其异位定植需要破坏常驻微生物群的定植抵抗。肠道炎症削弱这种抵抗力,使口腔菌有机会取代本地菌群;肠杆菌与克雷伯菌的定植与 Th17/Th1 积累增加相关。小鼠实验亦证实,口腔炎症期诱导的 Th17 细胞可迁移至肠道并触发肠炎。
▸ 口腔致病菌进入肠道激活肠道炎症
连接牙周病原体与肠道疾病的另一机制,是口腔致病菌迁移入肠并被激活,从而推动口腔 Th17 TEM 向产生 IFN‑γ 的 Th17/Th1(致病性 Th17)转化,进而放大肠道炎症并激活肠道内已定植的口源微生物群,加剧结肠炎与其他胃肠病。证据显示,牙周炎期间出现的口源致病性T细胞具致结肠性,可能是多种胃肠道疾病的诱因。
Mukherjee S,et al.Crit Rev Microbiol.2025
✔ SFB与牙周菌对肠道 Th17/Treg 轴的影响
发炎牙周组织促进口源致病性Th17的迁移,这些细胞在牙周炎过程中获得肠道归巢受体(如 α4β7 整合素、CCR9),易位至肠黏膜后被口源菌群再激活,恶化结肠炎等胃肠道疾病。口腔致病菌的异位定植既为这些口源T细胞在肠内扩增提供抗原刺激,也可能通过诱导 IL‑1β 促进其激活与扩张。口腔细菌还能激活炎症小体并诱导 IL‑1β,在结肠炎的发生中起核心作用。
近期发现,肠道共生的分节丝状细菌(SFB)是强效的 Th17 细胞刺激物。少数研究提示,肠道内 Th17 可发生致病性转化,形成产生 IFN‑γ 的 Th1 样 CD4 T 细胞;SFB 诱导的 ex‑Th17 同样具有致病性并引发重度肠炎。
牙周病原体如何激活各种免疫细胞并增加肠道炎症
Mukherjee S,et al.Crit Rev Microbiol.2025
牙周细菌还可通过激活TLR,促进 CD4⁺ LAP⁺ 细胞释放,增强肠道 T 细胞免疫。CD4⁺ LAP⁺ 细胞为新型 Treg 亚群,表达潜伏相关肽(LAP),在潜伏 TGF‑β 复合物中起作用,阻断 TGF‑β 与受体结合,从而维持稳态并抵御肠道细菌入侵。
Th17与Treg是肠黏膜最丰富的 CD4 T 细胞群之一。Th17 在 TGF‑β 与 IL‑6 共同作用下经 RORγt 诱导,关键在于防御肠道真菌与细菌,并通过分泌 IL‑17/IL‑22 维持稳态;其异常活化与多种肠道自身免疫病相关。CD25⁺Foxp3⁺ Treg 则依赖 IL‑10 与 TGF‑β 发挥不可替代的稳态维持作用。
牙周炎产生的促炎细胞因子(IL‑1、IL‑6、IL‑8、TNF)进入肝脏,诱导多种急性期蛋白(APP)生成与释放,包括C-反应蛋白(CRP)、纤维蛋白原、五联蛋白、α‑1 酸性糖蛋白、α‑1 蛋白酶抑制剂、α‑1 抗胰凝乳蛋白酶和结合珠蛋白。
▸ 急性期蛋白与炎症
APP入血与促炎细胞因子协同,增强全身氧化应激与炎症。牙周炎被视为 APP 升高的风险因素:与无牙周炎者相比,严重牙周炎或牙列缺失者CRP升高约三分之一;牙周炎患者 CRP为健康者约两倍。
✔ 克罗恩病、炎症性肠病患者中急性期蛋白升高
克罗恩病、炎症性肠病、胃炎及胰腺癌患者亦常见 CRP 升高;在克罗恩病中,重度病例的血清 CRP 高于轻中度,提示牙周炎相关 CRP 增加或提高 CD、UC 风险。CRP可结合白细胞Fcγ受体(FcγR)激活免疫细胞并促进 IgG 产生,连接先天与适应性免疫;在钙存在下与细菌多糖结合后可激活补体并促进吞噬。
升高的 APP,尤其C-反应蛋白,还可刺激肠上皮与实质组织中的中性粒细胞、淋巴细胞和巨噬细胞。在 C3a、C5a 参与下,CRP 与细菌多糖结合,增加中性粒细胞浸润并放大全噬作用,提升肠道损伤与炎症风险。CRP 还能识别某些革兰阳性口腔菌的病原相关组分与受损细胞壁,进一步加剧炎症与氧化应激。
除 CRP 外,纤维蛋白原亦在牙周炎时沉积于肠道;牙周炎上调肠组织促炎介质,促进富含纤维蛋白的微血栓形成。APP 与促炎介质还可促使肝细胞增殖并诱发纤维化进程。
▸ 牙周炎影响炎症介质的产生
✔ 牙周病原体增加促炎介质导致肠道炎症
研究发现,牙周病原体可增加促炎介质(如IL-1、IL-6、TNF-α)的释放,从而激活肝细胞释放 CRP 和纤维蛋白原。此外,还观察到“455G/A 基因多态性”与β-纤维蛋白原基因启动子中纤维蛋白原水平增加之间的关联。
纤维蛋白原作为多种细胞(如白细胞、内皮细胞、血小板、成纤维细胞和平滑肌细胞)表面受体(VE-钙粘蛋白、ICAM-1、αIIbβ3、α5β1、αVβ3、αMβ2 和 αXβ2)的配体,其激活促进了肠道局部炎症与组织损伤。
牙周炎诱导的细胞因子和内毒素(如 LPS 和外膜蛋白)共同激活重要的急性期蛋白Pentraxins的释放。Pentraxins 可通过多种细胞因子激活巨噬细胞、内皮细胞、髓系细胞和树突状细胞。PTX3 是一种 TNF 刺激基因,能够诱导细胞增殖、胃炎症和细胞损伤,并与树突状细胞和巨噬细胞上的补体 C1q 相互作用,激活补体系统经典途径。
PTX3 水平的增加与溃疡性结肠炎(UC)和克罗恩病(CD)的风险上升相关。活动性UC患者的 PTX3 水平高于健康个体和非活动性UC患者,表明 PTX3 存在于肠道隐窝脓肿中的中性粒细胞中。PTX3 的表达主要在 UC 患者的结肠黏膜中,伴随中性粒细胞招募。炎症反应高组织学分级中,表达 PTX3 的细胞及炎症中性粒细胞数量增加,表明 PTX3 的表达与结肠组织对炎症的反应相关。研究发现,PTX3 蛋白可能促进 UC 患者发炎结肠组织中的细胞介导的免疫反应,尤其在隐窝脓肿病变中。
✔ 牙周炎诱导炎性小体激活
炎症小体是先天免疫系统中的多聚体蛋白结构,能够调节细胞死亡并诱导炎症,以应对源自宿主蛋白的感染性微生物和分子。
注:炎症小体的传感器分子涵盖多个模式识别受体(PRR)家族,包括核苷酸结合结构域和富含亮氨酸的重复蛋白(NLR, 即 NOD 样受体)。多种炎症小体以其激活的传感器命名,包括 NLRP1、NLRP3、NLRP4、NLRP6、NLRP12、NLRC4、AIM2 和 RIG-I 样受体。这些炎症小体与多种肠道炎症性疾病相关。
炎症小体可由多种因素激发,如慢性感染(如牙周炎)、组织损伤或代谢失衡。牙周细菌(如牙龈卟啉单胞菌、A.actinomycetemcomitans和F.nucleatum)被认为是炎症小体的有效激活剂,这些细菌通过与宿主上皮细胞上的 PRR 相互作用,激活 NLRP 信号通路,从而导致炎症小体形成。其中 NLRP3 是肠道稳态的重要调节因子。
NLRP3 的激活促使半胱天冬酶1活化,从而引发白细胞介素1β(IL-1β)和 IL-18 的分泌。这两种细胞因子的升高与炎症性肠病和肠道肿瘤的风险增加相关,炎症小体介导的 IL-1β 分泌在共生致病性 IBD 的发病机制中具有核心作用。众多研究已确认 NLRP3 炎性小体与牙周炎的强相关性,进一步证明了牙周炎与胃肠道疾病之间的联系。
中枢神经系统(CNS)通过下丘脑-垂体轴(HPA)连接肠道。多种神经肽,如P物质、血管活性肠肽(VIP)、神经激肽A(NKA)、激肽原和速激肽,形成肠神经系统(ENS)、中枢神经系统和肠道之间的主要联系。
这些神经肽不仅作为细胞内信号分子,直接影响肠道中免疫球蛋白(IgA、IgG 和 IgM)的产生,还与其相应的受体(如 G 蛋白偶联受体、神经激肽(NK 1、2 和 3)受体)结合,增加细胞因子(如 IL-1β、IL-6、IL-8 和 TNF-α)的产生。与炎症介质共同激活后,神经肽可增强淋巴细胞的有丝分裂、趋化性、吞噬作用、中性粒细胞溶酶体释放、迁移及肠道免疫效应细胞的归巢模式。
牙周组织与中枢神经系统和肠道相连
Mukherjee S,et al.Crit Rev Microbiol.2025
中枢神经系统(CNS)通过下丘脑-垂体轴(HPA)与肠道相连。各种神经肽,如P物质、血管活性肠肽 (VIP)、降钙素基因相关肽、神经激肽 A (NKA)、激肽原和速激肽,是肠神经系统 (ENS)、中枢神经系统和肠道之间的主要纽带。
牙周细菌还会增加激肽原和P物质的释放。这些神经肽影响肠神经系统(迷走神经和肠系膜神经),并影响肠道活动度、胃酸分泌和炎症介质的释放。这些神经肽充当细胞内信号分子,直接影响免疫球蛋白的产生、淋巴细胞有丝分裂发生、趋化性、吞噬作用、中性粒细胞溶酶体释放和迁移以及肠道中免疫效应细胞的归巢模式。
▸ 肠道神经肽与微生物的相互作用
当神经肽在肠道神经末梢释放时,它们会扩散到周围的肌肉、上皮、内皮和免疫细胞,导致肠/结肠粘膜的炎症。研究发现,在肠道炎症和炎症性肠病患者中,结肠神经损伤以及粘膜神经支配和神经肽表达的变化显著。
UC 和 CD 患者的结肠组织和神经纤维中都观察到 P 物质的表达增加。IBD 还会影响肠道的运动,P 物质及神经激肽 1 受体(NK1)在这一过程中发挥作用。多项证据表明,P 物质、NKA、降钙素基因相关肽和 VIP 与肠道运动变化、肠道过敏反应、感染、创伤和压力相关。
✔ 肠道微生物群可以合成多巴胺、血清素等神经肽
此外,肠道中的一些微生物如肠球菌、念珠菌、大肠杆菌和链球菌能够合成神经肽,例如 5-羟色胺;酵母菌属、芽孢杆菌属和大肠杆菌属可产生多巴胺或去甲肾上腺素;乳酸杆菌属则合成乙酰胆碱,以及 γ-氨基丁酸(GABA),由乳酸杆菌属和双歧杆菌属产生。
微生物衍生的多巴胺会进入肠腔,影响结肠的吸收能力。此外,肠道中的乳酸杆菌、拟杆菌、幽门螺杆菌、大肠杆菌和念珠菌也分泌与食欲调节相关的蛋白质。同时,针对 NPY、瘦素、α-黑色素刺激激素、生长素释放肽、刺豚鼠相关蛋白(AgRP)及其他神经肽/肽的 IgG 和 IgA 自身抗体也参与了食欲控制。
✔ 牙周病原体会增加神经肽分泌导致肠道炎症
牙周病原体进入肠道也会增加各种神经肽的分泌,特别是 P 物质、激肽和 VIP。发炎的牙周组织是激肽(激肽原)的增加来源。牙周炎症期间释放的激肽原被降解形成缓激肽,从而加剧了局部和全身炎症过程。
缓激肽的释放导致血管舒张,进而导致血浆外渗和肠道中其他介质的释放,特别是 P 物质和降钙素基因相关肽。牙周炎期间释放的 P 物质进入系统循环,这可以上调缺氧诱导因子1α(HIF-1α)。HIF-1α调节细胞对低氧水平的适应,创造缺氧微环境,并改变肠道屏障的功能。
注:在慢性缺氧中,HIF-1α 及其一些靶基因产物(如 iNOS、COX-2、IL-6 和 IL-8)被激活,导致肠道炎症增加、免疫改变和细胞凋亡。
研究还发现,牙周炎患者中其他神经肽的水平升高,例如降钙素基因相关肽、VIP、神经激肽A、激肽原和速激肽。速激肽具有促炎细胞因子样特性,速激肽分泌增加与微血管通透性增加、GIT 中血浆蛋白外渗、水肿形成、运动功能改变和肠道收缩刺激有关。 香草素受体-1 是另一种神经肽受体,在牙周期间上调,可能是牙周炎和炎症性肠病之间的关键联系。
▸ 牙周炎诱导miRNA影响胃肠道功能障碍
牙周炎会改变全身 miRNA 水平,从而影响多种肠道功能。miRNA 是一类小的非编码 RNA,负向调节蛋白质表达,并与肠道的多种生理和病理机制有关。牙周炎被认为是促使这些 miRNA 增加及诱导肠道功能障碍的潜在因素。
✔ 一些肠道疾病患者中miRNA增加
在牙周炎发作期间,由多形核细胞和单核细胞中的 TLR4 激活的核因子 kappa B(NF-κB)诱导的 miRNA-9 会增加肠粘膜通透性,进而导致水肿形成。
研究发现,一些 miRNA 在肠道疾病患者中存在差异。例如,miRNA-155 在牙周病和肝病患者中均有增加,参与了巨噬细胞中的抗原呈递和TNF通路的激活。
✔ miRNA 的异常表达会导致多种疾病
miRNA 的异常表达会导致先天和适应性免疫反应中多个细胞过程的失调。这些 miRNA 不仅在合成它们的细胞中发挥作用,还可以在细胞外与脂质和蛋白质结合。它们能够在全身循环中传递信号,改变受体细胞的基因表达。发炎的牙周组织中产生的 miRNA 可以进入血液循环,导致多种全身性疾病。
注:与牙周炎相关的常见miRNA包括miRNA-9、miRNA-155、miRNA-203a、miRNA-147、miRNA-182、miRNA-183、miRNA-664a、miRNA-501和miRNA-21。
这些 miRNA 在与炎症性肠病、慢性肝炎、非酒精性脂肪肝以及肠道炎症和癌症的病理生理过程中都发挥着重要作用。miRNAs 是免疫反应的关键调节因子,能够干扰肠道中特定靶基因的转录后表达。肠道 miRNA 的失调会损害组织完整性,改变屏障功能,并增加肠道炎症。
✔ 肠道炎症、癌症患者中的miRNA与健康个体存在显著差异
多项研究发现炎症性肠病患者与健康个体之间在数百种 miRNA 的谱上存在显著差异,包括儿童和成人患者、发炎和非发炎粘膜,以及疾病活动度相关的 miRNA。
IBD 中研究最多的 miRNA 之一是 miR-21,该 miRNA 在血浆中全身过度表达,并在结肠组织中局部过度表达。与健康对照相比,IBD 患者的固有层、巨噬细胞和 T 细胞亚群中 miR-21 的水平也显著增加。miR-21 与溃疡性结肠炎(UC)相关,但与克罗恩病(CD)无关,并且与疾病活动和严重程度有联系。
注:与小儿UC患者相比,成人肠道病变中 miR-21 水平显著升高。因此,miR-21 被强烈推荐作为健康与 IBD、UC 和 CD、活动期与缓解期的生物标志物。
与对照组相比,IBD 患者及结肠炎小鼠发炎粘膜中的 miR-31 水平也升高。研究表明,miR-31 直接靶向 IL-25 的表达,IL-25 是 Th1/Th17 炎症反应中的关键反调节细胞因子。研究还显示,克罗恩病患者及小鼠模型中 IL-25 与 miR-31 之间存在负相关关系。
此外,miRNA 还在多种恶性肿瘤中显示出差异表达,包括结肠癌。宿主细胞与肠道微生物群之间通过 miRNA 实现双向相互作用,miRNA 在肠上皮细胞分泌后参与塑造肠道微生物群,并在粪便中累积。反过来,宿主的 miRNA 表达也可能受到微生物衍生代谢物的影响,这些代谢物可能影响宿主的生理功能。最近的研究表明,miRNA 功能的失调与炎症性肠病的发病机制有关。
最近观察到某些细菌物种诱导其他微生物和宿主细胞死亡以获取营养,这一过程被称为“坏死毒力”或“细菌坏死性”。被杀死的细菌释放的营养物质为幸存的细菌提供了生存所需的资源,尤其在营养匮乏时。
▸ 口腔细菌影响肠道内的毒力基因
死亡细菌的增多为口腔生态系统中存活的细菌提供了丰富的营养来源(如C、N、P和Fe),并促进了生物膜的形成。死细菌的存在刺激其他口腔病原体的生长,并诱导新表型,进而上调细菌的毒力基因,造成对宿主组织的细胞毒性。
研究发现,口腔中含有大量死细菌,这些细菌为活微生物提供了营养。日常使用的漱口水和抗菌牙膏等产品导致了口腔微生物的大规模死亡,幸存细菌附近则聚集了大量的死细菌,使得病原菌能够利用这些微生物残体作为生长营养。
✔ 牙龈卟啉单胞菌的毒力基因在死细菌的存在下显著增加
在不同种类的死口腔细菌存在下,牙周病原体展现出坏死性生长。死细菌的存在促进了多物种生物膜中一些牙周病原体的生长,特别是“P.intermedia”和“牙龈卟啉单胞菌”的毒力基因在死细菌存在的情况下显著增加。
口腔中的死细菌还通过吞咽唾液进入肠道,刺激肠道内的各种病原体,导致新表型和细菌毒力的上调。
✔ 毒力基因上调可能导致肠道生态失调
研究指出,当可用于一个活细胞的死细菌数量达到至少10个时,P.gingivalis和P.intermedia显示出显著的生长增加。同时,研究还发现,在死亡的P.intermedia存在的情况下,牙龈卟啉单胞菌的牙龈蛋白酶基因 rgpA、rgpB 和 kgp 被上调,其表达增加可能促进了肠道细菌的进入、存活,导致严重的炎症和生态失调。
▸ 硫化物的释放与胃肠道功能障碍
食物颗粒的微生物降解会产生挥发性硫化合物(VSC),其中与口臭最相关的包括甲硫醇(CH3SH)、硫化氢(H2S)、二甲基硫化物((CH3)2S)、吲哚、粪臭素以及多胺(如腐胺)。这些 VSC 能进入体循环,影响多种器官系统,从而引发微生物生态失调、组织和器官的代谢活动及全身性疾病。它们作为致癌物,在肿瘤发生和细胞功能中起着关键作用。
✔ 硫化氢会增加肠道通透性和炎症
硫化氢是一种遗传毒性和促炎物质,能够增加肠道上皮的通透性并导致屏障功能丧失。研究表明,硫化氢可通过诱导肠粘膜中的 DNA 低甲基化来促进隐窝形成。过量的硫化氢会导致其在肠道内清除减少,从而促成溶酶体定植,成为溃疡性结肠炎(UC)的病因。硫化氢破坏了肠上皮细胞的凋亡、增殖和分化之间的微妙平衡。
硫化氢的增加还会影响结肠中罗丹酶(RHOD)和硫醇甲基转移酶(TMT)的功能,这些酶在去除硫化氢中发挥重要作用,并与溃疡性结肠炎的发病密切相关。
此外,硫化氢刺激 IL-10 的产生,同时抑制促炎细胞因子(如 IL-1β、IL-6、IL-8、IL-18、TNF-α 和 IFN-γ)。多项研究表明,IL-10 与炎症性肠病(IBD)之间存在关系,且 IL-10 分泌不足会加重 IBD 的炎症。硫化氢通过血管舒张增加血流量,以保护肠道粘膜,减少因胆汁、酸和消化酶等刺激物引起的损伤,并促进损伤后的组织修复。
牙周炎绝非局限于口腔的“局部炎症”。通过口腔—肠道轴,它能够持续重塑微生态、扰动免疫网络,并深刻牵动全身稳态,尤其与多种胃肠道功能障碍密切相关。
实践上,建议形成“口腔端—肠道端”的协同策略:
口腔端:规范的牙周治疗与维护、个体化生物膜管理、温和而精准的抗菌与抗炎方案,以降低系统性炎症负荷。
肠道端:基于微生态的综合干预(定向益生元/益生菌/合生元、黏膜营养支持如丁酸盐、个体化低硫或低FODMAP饮食),促进屏障修复与免疫重建,减少复发与并发症。
警示:避免非选择性、强力抗菌导致的“生态反噬”,坚持精准与生态友好的干预原则。
当我们以微生态与免疫稳态为框架重塑诊疗范式时,牙周炎将不再只是口腔科的“老问题”,而有望成为预防与干预消化系统疾病以及多种慢性全身性疾病的关键突破口。
主要参考文献
Mukherjee S, Chopra A, Karmakar S, Bhat SG. Periodontitis increases the risk of gastrointestinal dysfunction: an update on the plausible pathogenic molecular mechanisms. Crit Rev Microbiol. 2025 Feb;51(1):187-217.
Alarcón P, González M, Castro É. Rol de la microbiota gastrointestinal en la regulación de la respuesta inmune [The role of gut microbiota in the regulation of the immune response]. Rev Med Chil. 2016 Jul;144(7):910-6. Spanish.
Albuquerque-Souza E, Sahingur SE. Periodontitis, chronic liver diseases, and the emerging oral-gut-liver axis. Periodontol 2000. 2022 Jun;89(1):125-141.
Altaf-Ul-Amin M, Karim MB, Hu P, Ono N, Kanaya S. Discovery of inflammatory bowel disease-associated miRNAs using a novel bipartite clustering approach. BMC Med Genomics. 2020 Feb 24;13(Suppl 3):10.
Ansari SA, Iqbal MUN, Khan TA, Kazmi SU. Association of oral Helicobacter pylori with gastric complications. Life Sci. 2018 Jul 15;205:125-130.
Atarashi K, Suda W, Luo C, Kawaguchi T, Motoo I, Narushima S, Kiguchi Y, Yasuma K, Watanabe E, Tanoue T, Thaiss CA, Sato M, Toyooka K, Said HS, Yamagami H, Rice SA, Gevers D, Johnson RC, Segre JA, Chen K, Kolls JK, Elinav E, Morita H, Xavier RJ, Hattori M, Honda K. Ectopic colonization of oral bacteria in the intestine drives TH1 cell induction and inflammation. Science. 2017 Oct 20;358(6361):359-365.
Berkovich L, Gerber M, Katzav A, Kidron D, Avital S. NF-kappa B expression in resected specimen of colonic cancer is higher compared to its expression in inflammatory bowel diseases and polyps. Sci Rep. 2022 Oct 5;12(1):16645.
Bunte K, Beikler T. Th17 Cells and the IL-23/IL-17 Axis in the Pathogenesis of Periodontitis and Immune-Mediated Inflammatory Diseases. Int J Mol Sci. 2019 Jul 10;20(14):3394.

谷禾健康
梭杆菌属(Fusobacterium),是梭菌门最主要的菌属,厌氧革兰氏阴性细菌,与拟杆菌属、普氏菌属、卟啉单胞菌属一样都是医学上重要的厌氧革兰氏阴性杆菌。
梭杆菌属是人类和动物的身体共生菌之一,主要定植在人类和动物的粘膜中,两个最主要的聚集地是口腔和结肠,某些类型物种属于机会性病原体,会引起菌血症和各种快速进展的感染。这些微生物比大多数正常的厌氧菌群更具毒性,产生重要的 脂多糖(LPS),内毒素和溶血素等,这可能是毒力的原因。
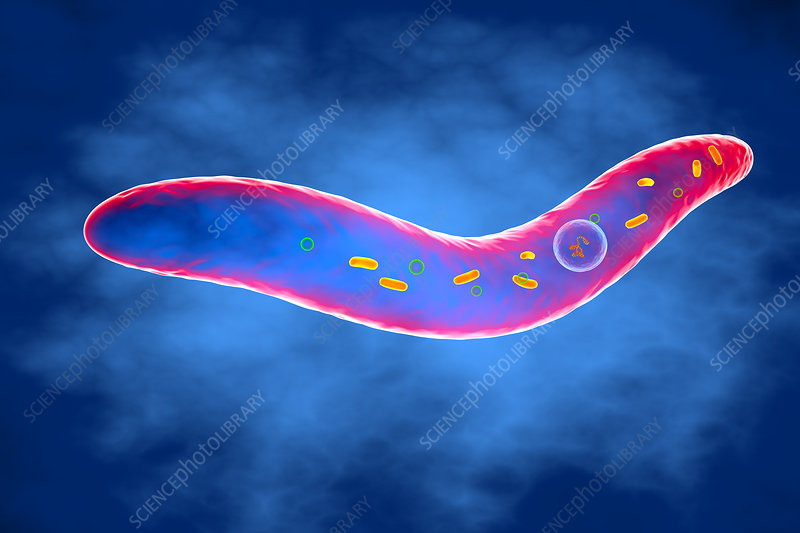
其中具核梭杆菌(Fusobacterium nucleatum, 简F. nucleatum)和坏死梭杆菌(Fusobacterium necrophorum,简F. necrophorum) 是可怕的厌氧病原体之一,最常存在于口腔、牙菌斑中,与牙周病、急性坏死性牙龈炎、口腔癌、溃疡性结肠炎、克罗恩病和结直肠癌有关。
此外,梭杆菌与大约一半的头颈部厌氧菌感染有关,包括牙龈和牙齿感染、慢性扁桃体炎、慢性鼻窦炎、中耳炎、咽旁感染以及口腔感染。它们不仅在这些组织中繁盛,而且很容易扩散,有时会引起肿瘤、息肉、囊肿和其他无害组织块的破坏。即使是局部炎症环境的变化也可能导致无功能组织过度生长,因此也称为“癌杆菌”。
梭杆菌属对粘菌素和卡那霉素敏感,这将它们与拟杆菌属和卟啉单胞菌区分开来。一些菌株产生β-内酰胺酶并对青霉素耐药。
梭杆菌
梭杆菌是一种独特的细菌门,是以前研究不足的分类群中的一个主要例子。该门下研究广泛的主要是梭杆菌属。
梭杆菌属细菌是革兰氏阴性、不形成孢子的厌氧菌,球状、多形性小球(坏死梭杆菌)到杆状的一系列细胞形态。当杆状时,梭杆菌细胞具有平行的壁,具有圆形或锥形末端,可分为运动和不运动。
梭杆菌属DNA(G + C)含量约为26~34mol%,正常存在于人或动物的口腔、消化道和土壤中,已知对人和动物致病的有十几种以上,其中主要代表为具核梭杆菌(F. nucleatum)和坏死梭杆菌(F. necrophorum).
在健康人的粪便中,发现以下数量的梭杆菌:
幼儿: 108-109 CFU/g
成人: 107-1010 CFU/g
老年人:108-109 CFU/g
通常,在成人的口腔中,含有 102 -104 CFU/g 的梭杆菌。
在血琼脂上,梭杆菌会形成圆形或不规则的针状菌落,一些物种,如具核梭杆菌,在孵化 3 至 5 天后会形成伞形“煎蛋”菌落。根据菌株的不同,它们可以是溶血的,并且一些菌株具有血凝作用。
临床感染中最常见的梭杆菌属有:
具核梭杆菌、坏死梭杆菌。
它们几乎存在于儿童的所有类型的感染中,包括菌血症,与耳科疾病相关的脑膜炎 ,内脏破裂后的腹膜炎,以及口腔或肛门口附近的皮下脓肿等。
致病梭杆菌在生物膜(特别是软组织)中粘附革兰氏阴性和革兰氏阳性菌斑微生物的卓越能力使其成为一种高度侵入性的病原体。
最常存在于口腔、牙菌斑中,与牙周病、急性坏死性牙龈炎、溃疡性结肠炎和克罗恩病有关。在免疫缺陷中,可引起继发性坏疽和化脓性坏疽过程。对于扁桃体炎,疱疹性口炎,儿童营养不良,免疫缺陷病,可能会发生梭菌病,扁桃体,口腔粘膜的坏死性炎症过程。
梭杆菌具有独特的代谢能力, 梭杆菌细胞通过发酵碳水化合物和蛋白获得能量。这种发酵产生丁酸盐,在某些情况下产生乙酸作为主要的代谢副产物。这是梭杆菌属物种与其他革兰氏阴性、非孢子杆状细菌的区别。
致病性
在革兰氏阴性厌氧菌中,梭杆菌作为主要病原体侵入人类宿主的能力很强。已经描述了许多毒力决定因素,包括白细胞毒素、蛋白水解酶、脂多糖(LPS)和血凝素的表达。
虽然是人体组织正常菌群的一部分,但梭杆菌可以在手术或意外创伤、水肿、缺氧和/或组织破坏后侵入组织。
★ 坏死梭杆菌 (F. necrophorum)
坏死梭杆菌在其细胞壁中含有特别强大的内毒素脂多糖,并产生一种促进凝块形成的凝固酶。此外,它还产生多种外毒素,包括杀白细胞素、溶血素、脂肪酶和细胞质毒素,所有这些都可能导致其致病。
坏死梭杆菌的粘附素和菌毛在宿主细胞附着中起关键作用。
白细胞毒素是已知的坏死梭菌的毒力因子,可能促进脓肿形成。内毒素和溶血素似乎也是脓肿形成和局部感染组织坏死增加的重要毒力因子。血凝素和尚未确定的导致血小板聚集的因素与Lemierre 综合征中发现的血栓形成后果相关性很大。
★ 具核梭杆菌 (F. nucleatum)
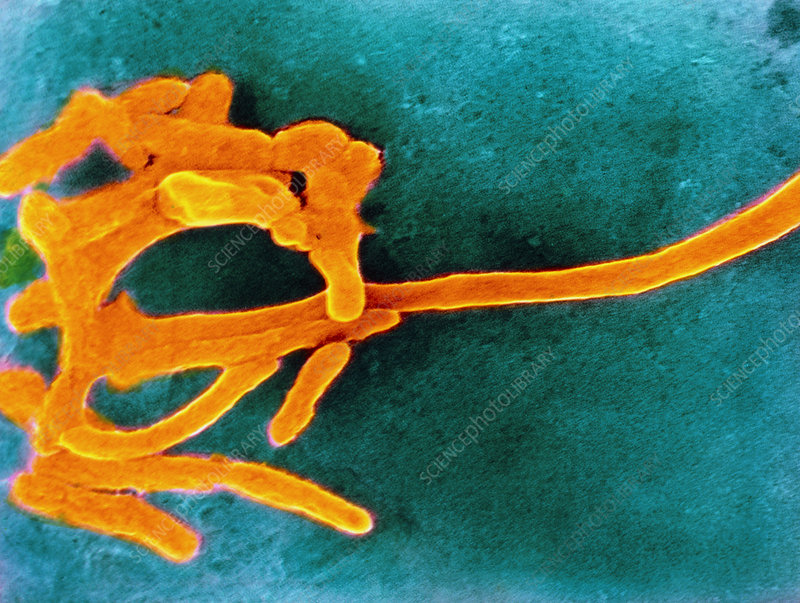
具核梭杆菌是少数利用氨基酸分解代谢来提供能量的非产孢厌氧物种之一,能使用谷氨酸、组氨酸和天冬氨酸。梭杆菌代谢通过消耗氨基酸和释放氨自然增加其局部环境的 pH 值,从而使酸敏感细菌(如牙龈卟啉单胞菌)生长。
但是,具核梭杆菌不使用葡萄糖作为其主要能源。现有数据表明,葡萄糖用于细胞内分子的生物合成,而不是能量代谢。具核梭杆菌也可以在低至 5 的 pH 值下存活。
——粘附各种细菌和细胞
具核梭杆菌是革兰氏阳性和革兰氏阴性物种之间物理相互作用的中心物种,可能对生物膜的形成很重要。
F. nucleatum具有外膜,于其细胞外表面上有大量蛋白质,可以发现细菌与宿主细胞表面上的各种互补结构具有特定的相互作用。这种粘附是由粘附素介导的。这种依从性对于易感宿主中感染的定植和建立非常重要。
它是附着在牙齿和上皮表面的共生体与真正的病原体。F. nucleatum有两种物质:菌毛和非菌毛粘附素,用于附着在其他细菌和细胞上。这些物质有助于定植以及细菌发病机制和感染。
——梭杆菌粘附 A (FadA)
梭杆菌粘附A (FadA) 是一种菌毛粘附蛋白,最近被证明是细菌附着和侵入牙龈上皮和内皮细胞所必需的。它在栖息于口腔黏膜的梭杆菌属中是保守的,并且对细胞结合很重要。
FadA 是一种含有 129 个氨基酸的蛋白质,具有 18 个氨基酸的信号肽。它具有一种分泌形式,可导致 β-连环蛋白途径和 Wnt 基因表达上调,这两种重要的发育途径在失调时都是致癌的主要原因。
FadA 的晶体结构揭示了一种独特的“亮氨酸链”结构,该结构在发生突变时会破坏宿主细胞的结合。尽管他们没有确定 FadA 的受体结合位点,但他们认为 FadA 作为细丝发挥作用,该区域的治疗靶点可能适用于未来的临床治疗。
梭杆菌多样性和生态位
从 1880 年代和 1890 年代开始,科学家们在各种人畜共患病和人类样本中发现了梭形杆状物,包括健康和患病的口腔。
以前梭杆菌属区分开来的特征主要是代谢与发酵和分泌的有机酸谱、吲哚和硫化氢的产生以及胆汁敏感性有关。尽管这些指标在区分梭杆菌中无法真正有效,从基因组上层面区分和鉴定梭杆菌属是在测序时代,而且还提高了对梭杆菌内部差异的理解。
目前梭杆菌属鉴定的有30 多个物种,包括:
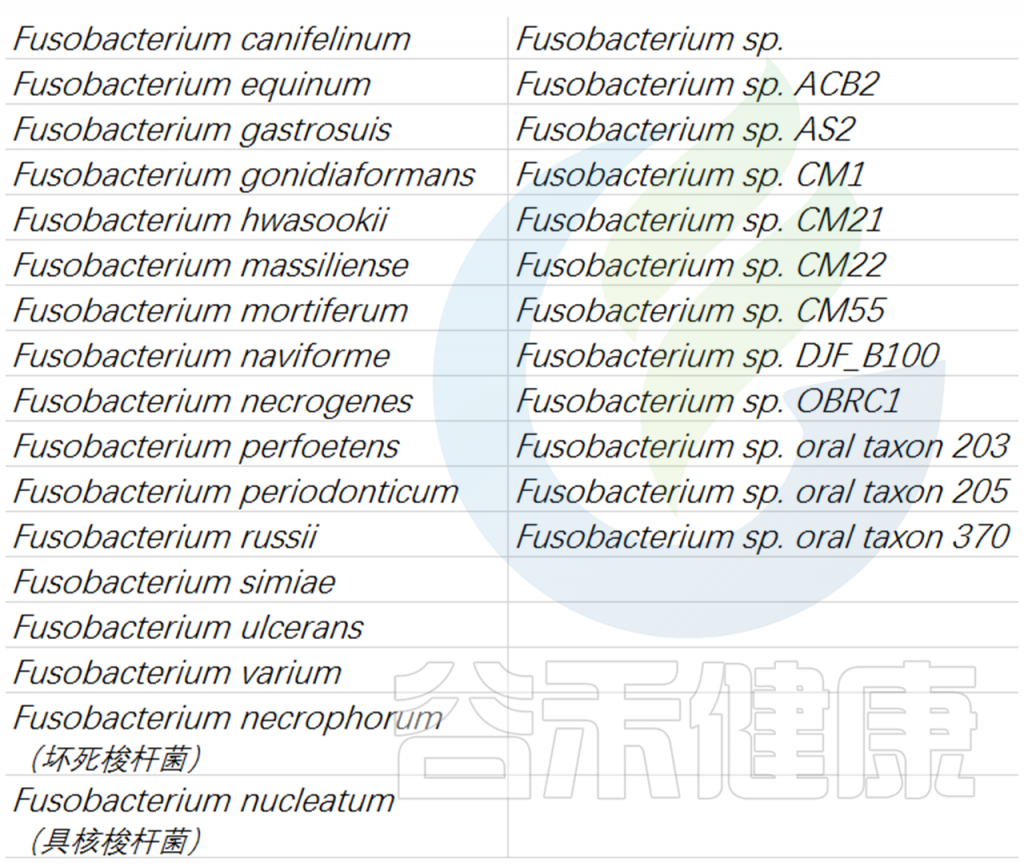
通过对 16s rRNA 序列的系统发育分组分析,发现F. nucleatum与拟杆菌属和黄杆菌属密切相关。
比较基因组学研究表明,梭杆菌物种之间主要可以分为三个谱系。在这个模型中,F. nucleatum 进化为与牙周梭杆菌的谱系,这些物种不仅共享一个生态位,而且还具有与宿主细胞入侵相关的相似功能。
F. nucleatum本身可进一步划分为四个亚种:nucleatum、animalis、vincentii、polymorphum
虽然有人认为这些亚种在 DNA 水平上有足够的差异,可以被认为是独立的物种。
梭杆菌栖息在人类和动物的粘膜中,是两者的病原体。由于其致病性和寄生性,梭杆菌不会直接影响环境,但它可能会通过对受感染宿主动物菌群的影响来改变生态系统。
常见感染
一些梭杆菌菌株会导致多种人类疾病,包括牙周病、Lemierre 综合征和局部感染或溃疡。
较早的研究表明梭杆菌在人类口咽部很常见,但目前的共识是梭杆菌应始终被视为病原体。与拟杆菌属相比,梭杆菌属具有强效的脂多糖。
在与牙周病统计学相关的所有牙周菌群中,具核梭杆菌是在其他身体部位发现的临床感染中最常见的。
“具核梭杆菌心包炎”——一名疑似感染分枝杆菌的 49 岁男子胸部发现具核梭杆菌心包炎。被认为分枝杆菌是原因,因此对他使用了抗结核药物。然而,这是F. nucleatum导致的。这一发现使人们认识到,具核梭杆菌通过口咽入口进入是导致此类疾病的原因。这是较早的发现之一,即具核梭杆菌也可能影响除口腔以外的其他体腔。
一些身体感染包括:皮肤溃疡、扁桃体周围脓肿、脓肌炎和化脓性关节炎、菌血症、肝脓肿、宫内感染、细菌性阴道病、尿路感染、心包炎和心内膜炎、肺和胸膜肺感染。巧合的是,它更常见于儿童体内。
F. necrophorum 在某些类型的感染中可能具有很强的毒性。在心绞痛后脓毒症(Lemierre 综合征)中,感染始于膜感染,如扁桃体炎,然后发展为伴有转移性感染的败血症,包括肺脓肿、脓胸、肝脓肿、骨髓炎和化脓性关节炎。
梭杆菌属以多种方式与其他细菌相互作用。相对于人类口腔和胃肠道中同时存在的微生物,梭杆菌属可以是互惠者、促进者、拮抗者和/或协同者。
梭杆菌代谢的副产物可以促进其他细菌种类的生长。上面提到的梭杆菌粘附素库就允许与许多不同的菌属共聚集,甚至可以促进其他非侵入性细菌物种的入侵。
担当调解者——连接主要定植菌和厌氧菌——有益牙周健康
F. nucleatum在有助于牙周健康和疾病的生物膜中发挥不可或缺的有益作用。在牙菌斑生物膜中,具核梭菌作为桥梁生物在结构上起到支持作用,将主要定植菌(如链球菌属)与主要厌氧的次级定植菌(牙龈卟啉单胞菌和Aggregatibacter actinomycetemcomitans )连接起来。
许多口腔微生物,包括梭杆菌属是专性厌氧的,并且作为生物膜的一部分存在于口腔的富氧环境中。然而,溶解在唾液中的氧气可能会通过牙龈下生物膜中的通道深入渗透到牙龈下生物膜中。尽管在单一培养中,对氧气极为敏感的口腔菌斑衍生微生物(如牙龈卟啉单胞菌)无法在这种微通气条件下存活,但与更耐氧的具核梭菌共培养可以促进专性厌氧菌的生长,这可能是由于梭杆菌对局部还原条件的贡献。
能在酸性条件存活,增加pH值,促进其他菌生长
除了在低氧水平下生长的能力,F. nucleatum也可以在低至 5 的 pH 值下存活。梭杆菌代谢通过消耗氨基酸和释放氨自然增加其局部环境的 pH 值,从而使酸敏感细菌(如牙龈卟啉单胞菌)生长。除了促进其他细菌的生长,梭杆菌细胞可以将它们的 “同居者” 固定在适当的位置。
梭杆菌属,特别是具核梭杆菌,已显示与所有测试的口腔细菌属可以发生共聚集。然而,这种聚合并不是无差别的。在每个属中,梭杆菌分离物优先与特定的某些菌株而非其他菌株共聚集。由于这种相互作用,具核梭菌是口腔生物膜发育的重要贡献者,是早期和晚期定植者之间的桥梁。
接下来,我们了解一下,F. nucleatum可能与之共聚的细菌。
与肠源性细菌共聚集——协同作用
梭杆菌细菌素可以通过去除特定的口腔和/或肠道微生物来促进其他微生物的生长,从而促进互惠相互作用的选择性。
通过与具核梭菌的侵入性菌株共聚集,一种具有粘附和侵入哺乳动物细胞能力的梭杆菌分离物——非侵入性细菌“乘客”可以穿梭到哺乳动物细胞中。
例如,具核梭菌的侵入性菌株,促进一些源自口腔的非侵入性细菌能够侵入人类口腔细胞。有趣的是,尽管F. nucleatum原产于人类口腔已证明菌株但是能够与人类胃肠道结直肠区域的原生细菌共聚集。
细菌共聚集可能对人类健康产生的影响
这种共聚集能力可能通过协同相互作用在结直肠癌(CRC)的病因中发挥作用。
尽管大量研究调查了结肠微生物群与结直肠癌进展之间的联系,结直肠癌病例相关的细菌包括F. nucleatum、产肠毒素脆弱拟杆菌(ETBF)、致肠致病大肠杆菌(EPEC)、侵入性大肠杆菌(AIEC)、粪肠球菌、弯曲杆菌属和Leptotrichia spp 等。
已发现具核梭杆菌和以上菌可能协同加速结直肠癌进展和/或转移。
早在 1936 年,科学家就将梭杆菌感染与颈静脉血栓性静脉炎联系起来。
最近,梭杆菌感染的发病率有所增加。虽然这种增加的原因尚不清楚,但抗生素使用减少和检测技术改进有关的理论可能解释了这种变化。
临床医生能够发现梭杆菌属感染的早期迹象至关重要,这种感染会迅速出现一系列并发症,如 Lemierre 综合征(心绞痛后脓毒症)、菌血症、骨髓炎和感染性休克。
儿童发病 ↓↓↓
儿科人群中的梭杆菌感染主要影响头部和颈部区域,因为细菌主要存在于口腔内。急性中耳炎是最常见的感染部位,尤其是在 2 岁及以下的儿童中。
一项研究了 27 名中位年龄为 3.5 岁的儿童的梭杆菌感染的神经系统表现,发现其中 5 人出现意识水平下降,7 人在开始治疗前癫痫发作。
厌氧菌引起的中耳感染不到 1%;但是,如果不及时治疗,可能会出现严重的并发症,例如骨膜下和硬膜外脓肿。
菌血症是一种严重的并发症,常见于高达 77% 的儿童梭杆菌病例,可能是由于颅内窦靠近乳突骨所致。在 40% 的患者中也观察到骨髓炎,并且通常是多灶性的,需要长期静脉内抗生素治疗。
成年发病
在免疫功能正常的患者中,男性和女性的发病率相等。最初的症状包括发烧(38°C ~ 39°C)并伴有急性中耳炎,通常进展为乳突炎。实验室评估显示炎症标志物升高:C 反应蛋白水平、白细胞计数和中性粒细胞绝对计数。
梭杆菌引起的脑膜炎罕见且被描述少于 20 次;然而,人们经常注意到它会导致严重的发病率和死亡率。
Lemierre 综合征
有人提出,Lemierre 或 Lemierre 样综合征的发展通常发生在梭杆菌感染中耳之后。这是由于中耳感染延伸到静脉窦血栓形成。
Lemierre 综合征是梭杆菌感染的严重并发症。
在一项对 12 名感染患者的研究中,58% 的患者发展为 Lemierre 或 Lemierre 样综合征。该综合征以颈内静脉脓毒性血栓性静脉炎或血栓形成为特征,可在肺部或其他无菌部位引起脓毒性栓塞性病变。
坏死梭杆菌(F. necrophorum)是导致 Lemierre 综合征的梭杆菌属物种,是造成 10% 的急性咽喉痛和 21% 的复发性咽喉痛的原因,其余由引起由A 组链球菌或病毒引起。
F. necrophorum的其他并发症包括脑膜炎,并发脑静脉血栓形成, 以及泌尿生殖道和胃肠道感染。
菌血症
具核梭杆菌引起的菌血症不常见,但死亡率高
一些危险因素包括恶性肿瘤、年龄较大、酗酒、免疫抑制和透析;通常是通过医院感染。然而,F. nucleatum菌血症的死亡率可达 10%,并且与基础疾病的严重程度相关。
有一项研究调查了有梭杆菌属感染事件病例。研究期间的菌血症(每年 0.55 例/100,000 人),具核梭杆菌是最常见的物种(61%),其次是坏死梭杆菌(25%)。
许多具核梭杆菌菌血症发生在不同的疾病患者(糖尿病、肠道、肺部、肝脏或妇科疾病),其中口咽部、胃肠道、泌尿生殖道和呼吸道,通常是F. nucleatum定植,可能成为感染源。
在强化化疗后患有恶性肿瘤(白血病和淋巴瘤)的血液病患者中,发生了具核梭杆菌菌血症。在大多数情况下,发生在口腔粘膜炎患者中。值得注意的是,F. nucleatum菌血症的病程似乎比由F. necrophorum等梭杆菌属引起的其他菌血症更有利,后者通常会导致 Lemierre 综合征。
F. nucleatum 感染与新冠感染有关
比利时研究团队报告了2020 年 3 月和 2020 年 4 月,比利时布鲁塞尔的 2 家主要医院观察到 4例 具核梭菌感染病例,均与冠状病毒病(COVID-19)患者的严重急性呼吸综合征冠状病毒 2(SARS-CoV-2)感染有关。
在口腔中,细菌、真菌、病毒和古细菌在不同的栖息地自然定殖,包括牙齿、牙龈沟、舌头、脸颊、软硬腭和扁桃体。口腔微生物群是指这些生物的高度多样化和复杂的生态系统。超过 700 种细菌是口腔特有的,而本土口腔菌群则可以防止外来细菌的定居。
口腔菌群的两面性
口腔中的一些细菌是有害的,会导致严重的疾病,而同时也有许多口腔细菌上对预防疾病是有益的。
现在已经确定,许多慢性炎症状况是由宿主-微生物群相互作用之间的不平衡引起的。口腔共生菌在口腔疾病的发展中起着至关重要的作用,包括牙周病和牙齿脱落,以及维持正常的口腔生理环境。此外,已知口腔共生菌参与了肺炎、心血管疾病、糖尿病、痴呆等系统性疾病的发病和发展。
梭杆菌在口腔疾病中的作用
梭杆菌是口腔中常见的专性厌氧革兰氏阴性菌,可充当牙菌斑中早期和晚期定植细菌之间的桥梁,并在口腔和口腔外感染中发挥作用。
具核梭杆菌是一种常见于人类牙菌斑中的细菌。这种细菌已被证明在牙菌斑形成和牙龈炎等其他疾病中起着核心作用。
这是因为它能够粘附广泛的革兰氏阳性和革兰氏阴性菌斑微生物,例如牙龈卟啉单胞菌。与牙周炎以及头部和颈部、胸部、肺部、肝脏和腹部的侵入性人类感染密切相关。由于其粘附能力,它可以与病毒相关联,病毒粘附在宿主组织细胞上作为入侵并调节宿主的免疫反应。
口腔鳞状细胞癌中的梭杆菌
最近已经表明,在口腔鳞状细胞癌(OSCC)组织中检测到梭杆菌一种口腔共生细菌。OSCC 组织表面生物膜内需氧菌和厌氧菌的比例约为 1:2,而健康对照组为 2:1,表明 OSCC 表面为厌氧菌提供了重要的储存库。梭杆菌在 OSCC 组织中的分布可能与健康口腔粘膜组织中的分布不同。
具核梭杆菌侵入上皮细胞
与P. gingivalis相比,F. nucleatum 显着粘附并侵入人牙龈上皮细胞 (HGEC) 。具核梭菌的自发突变体无法侵入HGEC ,这表明它们的侵入需要细菌成分。
此外,葡萄糖抑制试验表明,凝集素样相互作用参与了具核梭菌与 OSCC 细胞的附着。
具核梭杆菌在上皮细胞促进细胞迁移
具核梭杆菌的感染在人类上皮细胞中促进细胞迁移,可能通过刺激 Etk/BMX、S6 激酶 p70 和 RhoA 激酶,并通过激活丝裂原活化蛋白激酶 p38 增加 MMP-13(胶原酶 3)的产生 。
然而,梭杆菌在 OSCC 细胞中的粘附以及具核梭杆菌介导的OSCC细胞侵袭的详细机制仍不清楚。但是,普遍共识认为在OSCC 患者的口腔中富含具核梭杆菌这一事实似乎在口腔癌的肿瘤发生和/或进展中很重要。
具核梭杆菌通过产生有毒代谢物成为牙周病原体
这些有毒成分具有杀死或阻止附近牙周正常细胞(成纤维细胞)增殖的能力。
F. nucleatum形成的硫化物可能为细菌提供了一种避开宿主免疫系统的方法。丁酸(以组织刺激性丁酸的形式)、丙酸和铵离子,由具核梭菌产生,抑制人牙龈成纤维细胞的增殖。
具核梭杆菌有穿透牙龈上皮的能力
且在与牙周炎相关的斑块中,以高水平存在。
因此,它们可能对产生牙龈炎等口腔疾病具有非常重要的作用。
毒素的作用对细胞来说不是致命的,但成纤维细胞增殖的抑制很严重,因为伤口快速愈合的潜力受到了损害。
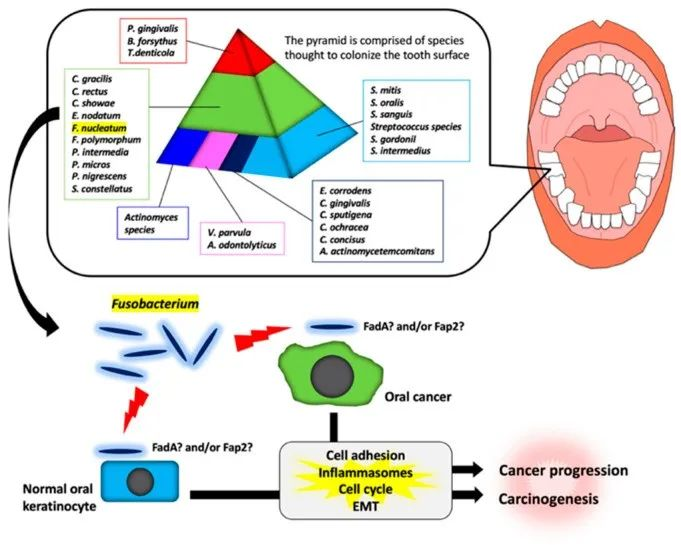
通过对龈下菌斑样本进行聚类分析,发现牙菌斑中的细菌之间存在特定关联。如下图,如金字塔所示,存在各种细菌。具核梭杆菌在金字塔的中间。
梭杆菌属参与口腔癌发生和癌症进展的示意图
编辑
Fujiwara, Natsumi et al, INT J MOL SCI, 2020
在金字塔中部的物种中,具核梭菌在牙菌斑形成后期的牙齿生物膜中占优势。
如上所述,梭杆菌感染通过各种反应影响 OSCC 的肿瘤发生和发展。然而,梭杆菌的靶分子仍然未知。需要进一步的研究来阐明梭杆菌参与 OSCC 肿瘤发生和发展的证据。
梭杆菌属物种可能与炎症性肠病 (IBD) 有关,包括溃疡性结肠炎和克罗恩病。IBD 是一个已知的危险因素,它是结直肠癌的三个最高风险因素之一。
已报道了几种梭杆菌菌株与 IBD 相关。然而,大多数 (69%) 与F. nucleatum相关。
F. nucleatum和其他梭杆菌属物种可以引发宿主促炎反应,并具有促进它们与宿主上皮细胞粘附的毒力特征以及它们侵入上皮细胞的能力细胞。
因此,与正常邻近组织和健康对照中的水平相比,结直肠癌中的具核梭杆菌富集,这些微生物可能导致肿瘤发生的可能性,可能在有限的患者亚群中,最可能是通过炎症介导的机制。
具核梭杆菌在结直肠癌患者中丰度及作用
最近的一项荟萃分析表明,与邻近的健康组织和对照组的健康组织相比,结直肠肿瘤组织中检测到具核梭杆菌DNA 的几率更高。与对照组的健康组织相比,结直肠息肉组织中的具核梭杆菌DNA 也较高。
结直肠癌患者粪便样本中,具核梭杆菌高
研究表明,结直肠癌患者的粪便样本中F. nucleatum 含量丰富。Meta 分析发现,与健康对照组相比,结直肠癌患者粪便样本中具核梭菌阳性的综合几率更高;与结直肠息肉患者相比,结直肠癌患者更高;但与健康对照相比,结肠直肠息肉患者的情况并非如此。
F. nucleatum已从消化道其他部位的癌症中分离出来,即胰腺 、食道和胃。
肿瘤内具核梭杆菌可能起源于口腔
有趣的是,已经表明结直肠癌中的具核梭杆菌菌株与从口腔中分离的该物种的菌株相同,这表明肿瘤内具核梭杆菌可能起源于口腔。如果来自口腔的具核梭菌在口腔外部位的癌症发展中起作用,那么假设这种细菌可能导致口腔本身的致癌作用是合理的。
具核梭菌感染诱导特定的肿瘤分子事件
F. nucleatum曾经被认为是胃肠道中的被动细菌。然而,现在人们认识到,具核梭菌感染可以在结直肠癌中诱导一系列特定的肿瘤分子事件,包括 CpG 岛甲基化表型、微卫星不稳定性以及BRAF和TP53的基因突变。
肿瘤内有具核梭杆菌的存在,与较差生存率相关
此外,许多这些研究已经确定,肿瘤内有具核梭杆菌的存在与较差的生存率有关 。还观察到,具核梭杆菌感染与更差的临床病理学特征相关,例如更大的肿瘤、更差的分化、淋巴结和远处转移、晚期肿瘤分期和更深的肿瘤侵袭。
总之,结直肠癌微生物组的基因组分析揭示了这些癌症中梭杆菌属的显着富集,尤其是与具核梭杆菌、死亡梭菌和坏死梭杆菌具有最大相似性的种系型。这种富集通过肿瘤组织的组织学分析以及结肠肿瘤转移中梭杆菌DNA 的鉴定得到证实。
梭杆菌介导结直肠癌发生,随着肿瘤转移进肝脏
2017年发表在《Science》肠道细菌Fusobacterium介导结肠癌的发生及伴随肿瘤的转移。作者进行以下操作:
结果发现,10个患者里面,只有2个患者的原位病灶和肝转移病灶中Fusobacterium含量不一样,其他8个病人是高度吻合的(Fuso-qPCR)。
由以上结果我们可以得知:Fusobacterium阳性的患者中,原发灶和肝转移灶中的细菌谱是高度相似的。Fusobacterium很有可能能够随着结肠癌一起进入肝脏。
接下来,作者从病人体内分离出Fusobacterium,通过给小鼠口服Fusobacterium,发现可以诱导结肠癌的产生。同时再次分离小鼠结肠癌中的细菌,通过测序发现,小鼠结肠癌中的细菌谱跟之前病人结肠癌中的细菌谱也是高度一致的。
是否可通过抗生素消灭具核梭杆菌及其他细菌,能否抑制结肠癌的生长?
作者先使用了没有Fusobacterium的细胞系HT-29,通过皮下成瘤,发现甲硝唑并不能够抑制肿瘤的生长。然后使用了从结肠癌患者的肿瘤组织中分离出Fusobacterium,诱导产生结肠癌。发现甲硝唑能够显著抑制肿瘤的生长。
具核梭杆菌高与复发相关
此外,上海交通大学仁济医院房静远教授团队在《Cell》上发表了相关论文,发现在肿瘤复发患者中肠菌具核梭杆菌含量明显升高,并明确了该菌诱导癌细胞自噬而导致化疗耐药与肿瘤的术后复发机制,从而引起大肠癌患者五年生存率降低。
另外,2017年发表在《Gastroenterology》上复旦大学肿瘤研究所领衔完成和《Oncotarget》(由西南医科大学领衔完成)杂志上的两篇也从另外的角度阐述了具核梭杆菌促进肿瘤发生发展的分子机制。
总结一下梭杆菌与结肠癌的进展:
1)研究发现Fusobacterium在结肠癌组织中大量富集;
2)研究发现Fusobacterium能够抑制免疫,减少T细胞的在肿瘤组织中的浸润;
3)研究发现Fusobacterium能够促进结肠癌的发生和发展,通过给小鼠口服Fusobacterium可以诱导结肠癌的产生;
4)研究发现Fusobacterium在结肠癌原位和肝转移灶都能检测到,意味着Fusobacterium可能能够跟随肿瘤细胞一起转移到肝;
5)研究发现使用抗生素消灭Fusobacterium后可以抑制结肠癌细胞的生长(这里使用甲硝唑做实验并不代表今后治疗中可以直接使用,毕竟这是个广谱抗生素)。
那这些研究对我们临床有什么启示呢?
近些年来的很多研究都表明,Fusobacterium与结直肠癌的发生有很大的关联性。我们知道肿瘤防治重点在于防而不在于治。关于肿瘤跟细菌的相关研究,大家最熟悉的是幽门螺杆菌和胃癌的研究。
2017年8月《Nature》首度报道了幽门螺杆菌导致胃癌发生的机制。通过对幽门杆菌的清除可以将胃癌的患病风险降低65%,那么通过以后监测Fusobacterium以及清除Fusobacterium可能为以后结肠癌的预后提供新的思路。同时,为什么Fusobacterium能够介导结肠癌的发生也同样值得研究。
越来越多的证据表明,微生物会影响癌症治疗的效果。具核梭杆菌在具有不同微卫星不稳定性 (MSI) 状态的结直肠癌中,诱导不同的免疫反应。
增强PD-L1阻断剂疗效
高F. nucleatum水平与结直肠癌患者对 PD-1 阻断的治疗反应改善相关。此外,F. nucleatum增强了 PD-L1 阻断剂对小鼠结直肠癌的抗肿瘤作用并延长了生存期。结合F. nucleatum补充免疫疗法,挽救了 PD-L1 阻断的治疗效果。
激活信号,诱导 PD-L1 表达
此外,具核梭杆菌通过激活 STING 信号传导诱导 PD-L1 表达,并在 PD-L1 阻断治疗期间增加干扰素-γ (IFN-γ) + CD8 +肿瘤浸润淋巴细胞 (TIL) 的积累,从而增强肿瘤对PD-L1 阻断。
最后,源自患者的类器官模型表明,增加的具核梭菌水平与改善对 PD-L1 阻断的治疗反应相关。这些发现表明,F. nucleatum可能会调节结直肠癌的免疫检查点治疗。
1
与其他微生物共聚集
F. nucleatum是早期和晚期定植者之间的关键“桥梁”生物,其外膜粘附素 Fap2 部分负责促进多物种生物膜的形成 。当口腔生物膜中报告牙龈卟啉单胞菌(P. gingivalis)时,始终存在F. nucleatum,这表明它先于该物种,并且是其殖民化所必需的。
P. gingivalis是一种酸敏感细菌,但F. nucleatum可以通过发酵谷氨酸和天冬氨酸产生氨,从而为P. gingivalis定殖提供更中性的环境。
F. nucleatum和P. gingivalis可能协同工作,通过引发慢性炎症来促进肿瘤变化,刺激了人 OSCC 细胞的体外增殖 。
白色念珠菌是一种机会性致病酵母,常见于胃肠道和口腔。最近的真菌生物组研究表明,OSCC 中包括白色念珠菌在内的几种真菌种类的丰度增加 。众所周知,口腔中的念珠菌属具有乙醇脱氢酶,负责催化酒精产生乙醛,乙醛是一种有效的致癌物质 。已经表明,具核梭菌与念珠菌共聚集,这可以促进定殖。念珠菌口腔白斑的定植与F. nucleatum水平升高有关。F. nucleatum可能通过增加口腔黏膜与念珠菌产生的乙醛的接触而间接增加口腔癌的风险。
2
激活细胞增殖
最简单的癌症是不受控制的细胞生长,而有核梭菌已被证明通过与内皮钙粘蛋白(E-钙粘蛋白)相互作用来影响癌细胞的增殖。梭杆菌 FadA 与在宿主细胞膜表面表达的 E-钙粘蛋白结合。E-cadherin 是一种通过 β-catenin 发挥作用的肿瘤抑制因子。梭杆菌 FadA 与 E-cadherin 的相互作用激活 WNT/β-catenin 信号传导,导致细胞增殖并增加致癌和炎症基因的表达。
类似地,已显示F. nucleatum通过激活 Toll 样受体 4 (TLR4) 向 MYD88 发出信号来增加小鼠异种移植物中的 CRC 增殖,从而导致核因子 NFκB 的激活和 miR21 的表达增加;这种 miRNA 降低了负责控制细胞增殖和分化的 RAS GTPase RASA1 的水平 。
由细胞周期蛋白激活的细胞周期蛋白依赖性激酶促进细胞周期进程。F. nucleatum感染与细胞周期蛋白 D1 的激活有关,这促进了肠道肿瘤的发生 。在 OSCC 中,F. nucleatum和P. gingivalis均被证明能够通过上调 cyclin D1 和 c-Myc显着刺激 OSCC 细胞增殖。
TLR4 的细菌激活导致白细胞介素 6 (IL-6) 的表达增加,白细胞介素 6 (IL-6) 反过来又激活了 STAT3,这是一种负责调节细胞周期蛋白 D1 和 c-Myc 的关键信号分子 。而且,F. nucleatum通过降低 p27(一种细胞周期蛋白依赖性激酶抑制剂)的表达和加速细胞周期来引起 DNA 损伤并促进口腔癌细胞的细胞增殖 。此外,具核梭菌下调 DNA 修复蛋白 Ku70 和 p53,从而削弱细胞修复能力。
最近的一项研究发现,HNSCC 中具核梭菌的富集与宿主基因启动子甲基化有关,包括肿瘤抑制基因LXN和SMARCA2的高甲基化。SMARCA2是一种参与与 DNA 修复和复制相关的 ATP 依赖性染色质重塑的基因。这表明F. nucleatum感染可能通过表观遗传沉默导致细胞增殖。
3
炎症的诱导
F. nucleatum的促炎潜力已得到充分证明,因为它可以促进活性氧 (ROS) 的产生和细胞因子的产生 。慢性炎症在致癌过程中起着关键作用,并且可以解释牙周炎与 OSCC 高风险之间的密切关联。已发现具核梭菌与 CRC 和 OSCC 中的高细胞因子水平相关,从而产生支持肿瘤进展的炎症微环境 。LPS,存在于细胞外膜中F. nucleatum激活 TLR4 介导的 NF-κB 信号通路以产生促炎细胞因子,如 IL-6、IL-8 和肿瘤坏死因子 α 。
4
抗肿瘤免疫反应
F. nucleatum在 ApcMin/+ 小鼠模型中已显示将骨髓来源的抑制细胞募集到肿瘤微环境中。髓源性抑制细胞可抑制 T 细胞增殖并诱导 T 细胞凋亡 。
这与最近发现的F. nucleatum的数量与结肠直肠癌和乳腺癌组织中 CD3 和 CD4 T 细胞的密度之间的负相关的发现一致。
还观察到 OSCC 中具核梭菌负荷与 B 淋巴细胞、CD4 T 辅助淋巴细胞、M2 巨噬细胞和成纤维细胞的标志物之间存在显着负相关。
F. nucleatum抑制蛋白还可以通过将细胞阻滞在细胞周期的 G1 期来抑制人类 T 细胞活化 。梭杆菌 Fap2 粘附素结合并激活具有 Ig 和 ITIM 结构域 (TIGIT) 的 T 细胞免疫受体,TIGIT 是 T 细胞和自然杀伤 (NK) 细胞中的一种免疫调节信号受体。这种 Fap2-TIGIT 相互作用可保护具核梭菌和附近的肿瘤细胞免于被免疫细胞杀死。局部免疫抑制也可能发生,因为有核梭菌的Fap2和 RadD 外膜蛋白会诱导淋巴细胞中的细胞死亡。
F. nucleatum还通过促进有核梭菌相关 CRC中巨噬细胞的 M2 极化发挥免疫抑制作用,可能通过 TLR4/IL-6/p-STAT3/c-MYC 信号通路。
5
细胞迁移和侵袭
基质金属蛋白酶 (MMP) 是一个锌依赖性内肽酶家族,它们共同能够降解细胞外基质 (ECM) 的所有成分。MMP 在 ECM 过度降解的病理状况中发挥作用,包括肿瘤侵袭和转移。P. gingivalis和F. nucleatum都可以通过不同的机制产生 MMP,从而促进癌细胞的侵袭和转移。
在 OSCC 中,已观察到暴露于牙龈卟啉单胞菌和具核梭菌导致 MMP-1 和 MMP-9 的诱导。同样,与F. nucleatum一起孵育的 AT3 小鼠乳腺癌细胞也表现出 MMP-9 的过表达。
上皮-间质转化 (EMT) 定义为上皮细胞采用间充质表型的过程,是在癌症发展和进展中观察到的现象。
一般来说,进入 EMT 的细胞表现出上皮标志物(如 E-钙粘蛋白)的下调和间充质标志物的上调,包括神经钙粘蛋白(N-钙粘蛋白)和波形蛋白 。这种细胞分化行为的转变是由一组转录因子控制的,包括锌指 E-box 结合同源框 1 和 2 蛋白 (ZEB1/2)、SNAIL 和 TWIST。
CRC 中高水平的具核梭杆菌与 E-cadherin 表达呈负相关,但与 N-cadherin 表达呈正相关。同样,OSCC 细胞系暴露于F. nucleatum与 E-cadherin 转录的显着降低以及 N-cadherin、vimentin 和 Snail 的上调有关。
F. nucleatum可以上调ZEB1 在口腔癌细胞中诱导这种间充质状态,一种先前已在H. pylori感染的胃上皮细胞中发现的机制。
痛风
痛风患者中普氏杆菌(Prevotella)、梭杆菌(Fusobacterium)和拟杆菌(Bacteroides)的相对丰度增加,而肠杆菌科(Enterobacteriaceae)和产丁酸盐菌的相对丰度减少。
胃肠道肿瘤
梭杆菌属(Fusobacterium)在胃肠道肿瘤的发生和发展中起重要作用。与正常组织样本,尤其是正常血源性样本相比,原发肿瘤中梭杆菌较多。泛癌分析还显示,在原发肿瘤组织和邻近正常组织样本中,将所有胃肠道癌(n = 8)与非胃肠道癌(n = 24)进行比较时,梭杆菌丰富度都是较高的。
胰腺导管腺癌
与其他肿瘤相比,胰腺导管腺癌中的肿瘤相关细菌 Gammaproteobacteria较多,尤其是肠杆菌Enterobacterales,与胃癌和结肠癌不同的是,它们的梭杆菌fusobacteria 较少。
口腔和唾液微生物群组成的改变与PDAC(胰腺癌主要是指胰腺导管腺癌,简称PDAC)的风险相关。最近的研究表明,口腔中参与PDAC肿瘤发生的主要致病菌有:
在健康对照组和胰头癌患者中分别观察到嗜血杆菌、卟啉单胞菌、纤毛杆菌、梭杆菌的丰度有显著差异。
PDAC肿瘤内梭杆菌的定殖与PDAC患者的预后更差相关。这项研究的结果表明,梭杆菌属可以作为PDAC的预后生物标志物。
梭杆菌的严重程度和传播范围,决定了所需治疗程度
一般所有梭杆菌感染都必须用抗生素治疗,并且通常对 β-内酰胺类药物敏感,例如青霉素或头孢菌素或其衍生物。
一些梭杆菌菌株被发现含有 β-内酰胺酶,因此建议使用特定的厌氧抗生素,例如甲硝唑或克林霉素。
适当的抗生素治疗与手术清创相结合可预防并发症
抗生素治疗通常通过肠胃外给药 1 至 2 周,然后进行大约 10 天的口服治疗。有些孩子需要切除坏死组织或手术引流。
在一项对 7 名小于 2.2 岁的梭杆菌感染患者的监测研究中,除了乳突切除术外,所有患者都需要一根通气管。
在以色列对 22 名感染梭杆菌的儿童进行的一项为期 14 年的研究中,5 名出现 Lemierre 综合征的患者中有 3 名接受了低分子量肝素治疗以缓解脑窦静脉血栓形成的症状,但是该治疗仍存在争议。
一项 40 年文献回顾确定了, 12 例 2 岁以下儿童的梭杆菌感染病例;所有儿童都出现了乳突炎,并接受了乳突切除术和抗生素治疗,无论严重程度如何,都取得了成功。
早期发现和适当治疗,可以有效阻止和逆转感染的进展
梭杆菌感染在 2 岁及以下的儿童中,临床表现为急性中耳炎,但如果不及时治疗,则会发展为乳突炎和更严重的菌血症、骨髓炎症状,并可能出现 Lemierre 综合征和感染性休克。
使用适当的抗菌检测技术以及适当的成像程序应允许及时使用抗生素和手术参与,以防止感染的进一步传播。
虽然对梭杆菌感染的研究和分析有限,但对感染症状和严重程度的重要认识可以帮助临床医生发现感染的早期发作并将患者引导至适当的专科医生处。
口腔牙周病感染中,高达 90% 的菌群由专性厌氧菌组成,钙化合物已被证明是牙科中有价值的材料。钙与酯的配方在牙齿结构的愈合过程中表现出显着的特性。根据国外“Calcium Therapy Institute”研究所的介绍,他们长达16 年的时间里,发现使用钙化合物来开发治疗牙髓和牙周(牙龈和骨)感染的牙周治疗钙法 (CMPT)具有重要意义。
口腔厌氧菌分散的一个原因是梭杆菌在上颌骨中获得了稳定的立足点,以增殖并将其大量的毒素释放到多孔的上颌骨、上颚和下牙列中。这个过程与人体正常的进食、呼吸、说话和吸吮机制相联系,是梭杆菌对人体细胞异常失衡的完美寄生关系。
北美该研究人员最近报告了的一项突破,发现厌氧细菌被局部刺激或炎症所吸引,会开启“饥饿触发”信号,向侵袭性细菌发出信号,释放一种酶以减少抗生素的影响。
这种自我饥饿细菌的“饥饿信号”会产生一种冬眠状态,或者说是防御状态,直到不再使用抗菌药物。他们进入休眠状态,只是为了在更有利的条件下重新发动进攻。
该研究所实验人员发现舌下颌下腺唾液肽的生物学特性,以及用于根管和牙周治疗的钙材料有助于深入了解答案。
它们是具有解热、抗炎、定时释放特性的非类固醇。几项临床研究表明,长期摄入唾液腺分泌物和对组织有益的钙材料具有积极的全身作用。
——降低有害菌的复制率
在 1980 年代中期,一些的血清研究表明,某些钙质材料不会杀死细菌,而是“降低”它们的复制率,而流行的抗菌剂在几毫秒内杀死一切,包括健康的细胞和细菌。在那项研究中,根据对口腔组织钙治疗的多年临床观察,消除细菌需要十个小时。关键因素是时间。
鉴于饥饿细菌的发现,钙材料会发出警报,但不会造成伤害。
——饿死那些“自我饥饿的细菌”
几十年来,钙疗法已被证明对口腔或皮肤的任何正常健康细胞无害,同时它们还能维持环境“围攻”。不是直接杀死它们,而是逐渐将饥饿细菌饿死。
然后,由于几乎没有复制能力,它们开始消亡,而健康细胞迅速蓬勃发展并主导该领域,尤其是在定时释放钙离子的情况下。
如果厌氧梭杆菌最常存在于口腔、牙菌斑中,并且与牙周病和炎症性牙龈炎有关,那么梭杆菌的下一个最有利的栖息地是结肠,可以刺激溃疡性结肠炎、癌症和克罗恩病。
口腔和结肠这两个区域很容易受到异常水平的梭杆菌的影响,这会长时间造成炎症环境并增强细胞的扩散或分布,甚至会扩散到以厌氧微生物而臭名昭著的身体远处器官。众所周知,生物膜菌落容易引起囊性和脓肿感染。
梭杆菌的管理,中和它们的毒素仍然在控制厌氧微生物环境的范围内。同样,健康的一个主要考虑因素是限制侵入性病原体的局部和全身传播。
从用钙材料管理口腔环境可以明显看出,下颌前切牙上的斑块沉积快速愈合和减少。对口腔黏膜和牙周组织进行长期钙治疗的患者会显著减少牙菌斑和牙石。
考虑到梭杆菌的两个最主要的聚集地,口腔和结肠,那么未来继续研究钙材料应该是价值的。这种病原体比预期的更容易控制,至少在口腔和下消化道的炎症和感染的早期阶段是如此。
声明:关于药物、诊断和治疗方法的部分中提供的信息仅供医疗专业人员交流使用,并非使用说明。
主要参考文献:
Brennan CA, Garrett WS. Fusobacterium nucleatum – symbiont, opportunist and oncobacterium. Nat Rev Microbiol. 2019 Mar;17(3):156-166. doi: 10.1038/s41579-018-0129-6. PMID: 30546113; PMCID: PMC6589823.
Susan Bullman et al. Analysis ofFusobacteriumpersistence and antibiotic response in colorectal cancer, Science (2017). DOI: 10.1126/science.aal5240
Castellarin M, Warren RL, Freeman JD, Dreolini L, Krzywinski M, Strauss J, Barnes R, Watson P, Allen-Vercoe E, Moore RA, Holt RA. Fusobacterium nucleatum infection is prevalent in human colorectal carcinoma. Genome Res. 2012 Feb;22(2):299-306. doi: 10.1101/gr.126516.111. Epub 2011 Oct 18. PMID: 22009989; PMCID: PMC3266037.
Kostic AD, Gevers D, Pedamallu CS, Michaud M, Duke F, Earl AM, Ojesina AI, Jung J, Bass AJ, Tabernero J, Baselga J, Liu C, Shivdasani RA, Ogino S, Birren BW, Huttenhower C, Garrett WS, Meyerson M. Genomic analysis identifies association of Fusobacterium with colorectal carcinoma. Genome Res. 2012 Feb;22(2):292-8. doi: 10.1101/gr.126573.111. Epub 2011 Oct 18. PMID: 22009990; PMCID: PMC3266036.
Vidaurrazaga MM, McKinley GF, Camins BC. Postpartum Fusobacterium gonidiaformans bacteremia. Anaerobe. 2020 Apr;62:102168. doi: 10.1016/j.anaerobe.2020.102168. Epub 2020 Jan 28. PMID: 32045837.
Centor RM, Huddle TS. Should the risk of Fusobacterium necrophorum pharyngotonsillitis influence prescribing empiric antibiotics for sore throats in adolescents and young adults? Anaerobe. 2021 Oct;71:102388. doi: 10.1016/j.anaerobe.2021.102388. Epub 2021 Jun 2. PMID: 34089856.
Duncan SH, Hold GL, Harmsen HJM, Stewart CS, Flint HJ. Growth requirements and fermentation products of Fusobacterium prausnitzii, and a proposal to reclassify it as Faecalibacterium prausnitzii gen. nov., comb. nov. Int J Syst Evol Microbiol. 2002 Nov;52(Pt 6):2141-2146. doi: 10.1099/00207713-52-6-2141. PMID: 12508881.
Arane K, Goldman RD. Fusobacterium infections in children. Can Fam Physician. 2016 Oct;62(10):813-814. PMID: 27737977; PMCID: PMC5063768.
Peluso EA, Scheible M, Ton-That H, Wu C. Genetic Manipulation and Virulence Assessment of Fusobacterium nucleatum. Curr Protoc Microbiol. 2020 Jun;57(1):e104. doi: 10.1002/cpmc.104. PMID: 32539234; PMCID: PMC7398570.
Broadley M, Schweon SJ. Get the facts about Fusobacterium. Nursing. 2017 May;47(5):64-65. doi: 10.1097/01.NURSE.0000515524.23032.d5. PMID: 28445341.
Tadepalli S, Narayanan SK, Stewart GC, Chengappa MM, Nagaraja TG. Fusobacterium necrophorum: a ruminal bacterium that invades liver to cause abscesses in cattle. Anaerobe. 2009 Feb-Apr;15(1-2):36-43. doi: 10.1016/j.anaerobe.2008.05.005. Epub 2008 May 24. PMID: 18595747.
Mark J. Manhart DDS, Thomas B. Steg DDS,2011, Calcium Method of Fusobacteria Management. Alciumtherapy.com