-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康

“民以食为天”,人的一生都离不开“吃”,并且“病从口入”,饮食直接或间接影响着我们的健康。不健康的饮食不仅导致多种疾病发生,甚至还可能减少寿命!
2019年,著名医学期刊《柳叶刀》发表了一篇大规模研究,分析了195个国家和地区饮食结构造成的死亡率和疾病负担。研究发现不良饮食造成的死亡人数超过吸烟等任何其他风险,改善饮食习惯可以预防全球五分之一的死亡。

并且可能颠覆以往认知的是,我国因为饮食结构而导致的高死亡率和疾病发生率,最大“杀手”可能不是糖和脂肪,而是钠摄入量高,全谷物摄入量低,水果摄入量低。换句话可以理解为:我们吃的食物偏咸、全谷物类食物摄入不足、蔬菜水果摄入太少,甚至疾病风险比高糖高油饮食的欧美国家还要高出了许多。
终止高血压饮食(DASH饮食) 和地中海饮食等健康饮食模式已被验证有益心血管健康,但考虑到西方饮食模式不易被中国人广泛接受,以及中国膳食文化、习惯的复杂性,今年,由北京大学临床研究所,复旦大学附属华东医院临床营养科、广东省食品营养与健康重点实验室、四川大学公共卫生学院营养系牵头共同发表在《美国临床营养杂志》,研究指出,中国心脏健康(CHH)饮食有效降低了血清总胆固醇(TC)和10年心血管疾病风险,并降低轻度高血压中国成年人的血糖水平。DASH饮食可将10年心血管疾病(CVD)风险降低10.3%。该研究中采用CHH饮食的影响更显著(降低27%)。

该研究的CHH饮食在开发阶段借鉴了健康膳食的主要食物特点,如低盐、富含蔬菜水果、增加全谷物和豆类等,以及主要营养素含量,包括脂肪、蛋白质、碳水化合物的比例、膳食纤维、钾、钙,并降低钠的摄入等。
CHH膳食方案经过严格的多中心随机对照试验证明了,只要食物搭配合理,符合中国人口味的健康中餐也能有效降低血压水平。
与此,同时《美国新闻与世界报道》今年发布了2024年度最佳饮食榜单。在这份最佳饮食排行榜中,“地中海饮食”仍牢牢稳居榜首,这也是该饮食模式7年蝉联榜首。“地中海饮食”确实在减重、减少“三高”、降低心血管疾病风险、防癌等方面有突出优势。
这些权威饮食研究表明只要将不健康的膳食转变为健康的膳食,就能够大幅度降低血压,并改善血脂和血糖,炎症且有望显著减少疾病事件。这一研究结果促使人们认识到通过健康膳食能够预防疾病、促进健康的巨大作用。
比起DASH饮食能够将10年内心血管疾病风险降低10.3%,中国心脏健康(CHH)饮食的效果更为显著,能降低27%,造成这一差异的可能原因是什么?
“一方水土养育一方菌”。
众多研究证明,饮食是塑造肠道微生物群的主要和关键因素。例如:
◆ 精制谷物、乳制品和茶或咖啡的摄入与颤螺菌目 (Oscillospirales)相对丰度增加有关;
◆ 甜饮料和甜点、动物脂肪和土豆与未分类的普雷沃氏菌种的相对丰度增加有关;
◆ 蔬菜和全谷物的摄入量与 Subdoligranulum丰度相关。
因此,肠道微生物组的独特性可能是CHH饮食显著降低心血管风险的重要原因。
一个人在日常生活中选择的食物的种类、数量、进食频率和时间安排等方面构成了他的饮食模式。不同的饮食模式具有不同的特点和健康益处或疾病风险。
不同人群可能需要符合自身需求的饮食模式。以下总结了一些主流饮食模式,帮助您了解其特点、益处和潜在不足,以便选择更适合自己的健康饮食。

首先要介绍一种典型的不健康饮食模式,也是现在很多年轻人都喜爱的西方饮食模式。
西方饮食是一种现代饮食模式,在西方社会中普遍存在。近年来,随着生活节奏加快,这种饮食在我国也越来越受欢迎。
“
西方饮食有什么特点?
•高糖和高碳水化合物: 西式饮食中的高糖和高碳水化合物主要来自于精制食品,如白面包、糕点、甜点和含糖饮料。
•高饱和脂肪酸: 这类饮食含有大量的饱和脂肪酸,主要来源于红肉、全脂奶制品和某些植物油(如棕榈油和椰子油)。
•高动物蛋白: 西式饮食中动物蛋白的摄入量较高,主要来自于牛肉、猪肉、鸡肉和奶制品。
•低膳食纤维: 膳食纤维摄入量低,因为这类饮食中新鲜水果和蔬菜的比例较低。
“
为什么这么多人选择西方饮食?
•口感和风味诱人:西式饮食的多样化和丰富的口味可以给人们带来饮食上的享受。
•方便快捷:许多西式食品,如快餐和即食食品,准备起来非常方便和快速,适合忙碌的现代生活节奏。
“
西方饮食对健康有哪些危害?
西方饮食在带来味觉上享受的同时,也伴随着许多健康隐患。
•易导致炎症:西方饮食与全身性慢性炎症和脂多糖易位有关,高脂饮食的摄入增加了促炎细胞因子的产生,导致全身性慢性炎症和脂多糖易位。这可能增加患心血管疾病、糖尿病和其他炎症性疾病的风险。
•增加慢性病风险: 长期摄入西方饮食与多种慢性疾病的风险增加有关,包括心血管疾病、某些类型的癌症、代谢综合征和认知能力下降。
•影响免疫系统: 西方饮食可能会影响免疫系统的功能,增加自身免疫性疾病和感染性疾病的风险。
“
对肠道微生物群有什么影响?
西方饮食中易于消化的非细胞营养素增加,可能会改变肠道pH值、微生物群组成和新陈代谢,影响肠道微生物群稳态的调节和维持。
与其他饮食相比,西方饮食与肠道微生物组多样性的显著降低有关,其肠道特征转向以拟杆菌属为主的肠道特征。其他丰富的物种属于Ruminococcus、Faecalibacterium、双歧杆菌属、Alistipes、Blautia、Bilophila。
并且由于纤维摄入较少和不同的微生物组成,相关的微生物群产生的短链脂肪酸也较少。
小结
综上所述,西方饮食虽然在某些方面为人们提供了便利,但其对健康的负面影响不容忽视。
为了改善健康状况,建议采取更加均衡和多样化的饮食模式,如地中海饮食,同时限制加工食品和高糖食品的摄入。

地中海饮食已经七年位于饮食榜单总体排名第一。
“
什么是地中海饮食?
地中海饮食是一种以蔬菜水果、鱼类、五谷杂粮、豆类和橄榄油为主的饮食风格,源自希腊、西班牙、法国和意大利南部等地中海沿岸的南欧国家。
这种饮食风格强调食物的天然、简单和清淡,富含营养,有助于减少患心脏病的风险,保护大脑免受血管损伤,降低中风和记忆力减退的风险。
“
地中海饮食有什么特点?
•植物性食物的丰富性:地中海饮食模式强调大量摄入水果、蔬菜、豆类、全谷物、坚果和种子。
•健康的脂肪来源:以橄榄油为主的不饱和脂肪,特别是单不饱和脂肪酸,作为主要的脂肪来源。
•适量的动物蛋白:适量摄入鱼类、海鲜、鸡蛋、家禽和低脂或脱脂乳制品。
•限制红肉和加工肉类:减少红肉和加工肉类的摄入,这些食品通常含有较多的饱和脂肪。
•适度饮酒:适量饮用红酒,尤其是晚餐时。
•香料的使用:使用香料和草药代替盐来增加食物的风味。
•高膳食纤维:通过食用全谷物、豆类和蔬菜来增加膳食纤维的摄入。
地中海饮食推荐的食物
特级初榨橄榄油;
新鲜水果,如蓝莓、草莓、无花果、桃子、芒果、梨和苹果;
新鲜蔬菜,如菠菜、羽衣甘蓝、芝麻菜、洋蓟、茄子、西葫芦、红薯、球芽甘蓝、芹菜、洋葱和胡萝卜;
藜麦、燕麦、鹰嘴豆、扁豆、杏仁、核桃、亚麻籽、奇亚籽;
植物奶,如杏仁奶或燕麦奶、希腊酸奶;
肉类如鸡胸肉、火鸡肉末、三文鱼、金枪鱼;
鸡蛋;
香草(新鲜或干燥)和香料,包括罗勒、牛至、迷迭香、百里香和大蒜
“
地中海饮食应该避免吃哪些食物?
地中海饮食的优点之一是限制性不强。这种饮食方法不禁止食用任何食物或食物种类,但会鼓励您限制食用某些食物的量。
•红肉:可以将红肉作为配菜。
•甜食:将甜食视为偶尔的庆祝食物,而不是日常的放纵。
•酒精:虽然适量饮用红酒是可以的,但过量饮酒可能会损害健康。不建议目前不喝酒的人饮酒。
•黄油:用更健康的替代品来代替黄油,比如橄榄油。
•全脂乳制品:减少食用冰淇淋和其他全脂乳制品。
•含糖饮料:不建议饮用含糖饮料,包括果汁。
“
地中海饮食的健康益处有哪些?
大量研究发现,地中海饮食存在以下的健康益处:
•降低患心脏病和中风的风险;
•预防认知能力下降和痴呆症;
•可能预防2型糖尿病;
•可能减轻炎症和自身免疫性疾病(如类风湿性关节炎)的症状和进展;
•可能有助于缓解抑郁症
改善心血管健康
地中海饮食已得到广泛研究,并一直被证明对心脏健康有益。
在希腊、意大利和日本等七个国家的一项大规模研究调查了13000名男性的饮食与心脏病之间的关系。研究表明,摄入的膳食脂肪类型(特别是不饱和脂肪)比脂肪总量更有益于心脏健康。
此后,包括2019年的PREDIMED研究和2022年的随机临床试验在内的众多研究发现,坚持地中海饮食与降低血压、胆固醇和体重有关,从而降低心血管疾病、死亡率、冠心病和中风的发病率。
降低癌症死亡率及糖尿病风险
一项对美国25,315名女性的前瞻性研究显示,那些坚持地中海饮食模式的人在25年的随访期间全因死亡率降低了23%。
这项研究还显示,较高的地中海饮食摄入量与20年随访期间未来2型糖尿病风险降低30%相关。地中海饮食模式可能还对癌症有保护作用。实际上,高度遵守这种饮食与普通人群中的癌症死亡率降低、癌症幸存者的全因死亡率降低,以及降低发展结直肠癌、头颈癌、呼吸、胃、肝和膀胱癌风险有关。
改善大脑健康
地中海饮食以海鲜、坚果、种子、特级初榨橄榄油、豆类、绿叶蔬菜和全谷物为主,对大脑健康有诸多益处。
多项研究表明,地中海饮食可以减缓人们大脑的衰老迹象。此外,越来越多的研究表明,这种均衡的饮食可以降低患痴呆症和阿尔茨海默病的风险。
事实上,一项2023年的研究和2018 年的研究表明,坚持地中海饮食的人患痴呆症的风险降低了 23%,并且对阿尔茨海默病进展的保护期为1.5至 3.5 年。地中海饮食不仅可以改善认知功能和预防神经退行性疾病,还可以改善心理健康。
一项2019年的研究显示,补充了鱼油的地中海式饮食改善了抑郁症患者的心理健康。多吃蔬菜、水果、全谷物、坚果和豆类,同时限制不健康食品,可以显著改善包括抑郁症在内的心理健康状况。
“
地中海饮食可以帮助减肥吗?
地中海饮食有助于减肥,特别是如果你从高糖、高钠和高饱和脂肪的饮食转变过来,但如果你想快速减肥,地中海饮食可能不适合你。
虽然地中海饮食不是为减肥而设计的,但这种饮食强调高纤维食物,如水果、蔬菜和全谷物,可以帮助你更长时间保持饱腹感。此外,用不饱和脂肪代替不健康的饱和脂肪已被证明可以改善代谢健康并有助于减肥。
地中海饮食已被证明可以促进长期减肥
多项研究表明,地中海饮食以植物为主的全食健康饮食方式对想要减肥的人有益。例如,2015 年的一项研究发现,与低脂饮食的人相比,遵循地中海饮食一年多的人减掉的体重更多。
利于体重维持和管理
2018年的一项大型纵向研究对32000多名参与者进行了评估,结果发现,对于基线体重正常的参与者而言,遵循地中海饮食可降低6至20年后体重增加和肥胖的风险,并降低腹部脂肪的风险。
“
对肠道微生物群有什么影响?
这些因饮食而导致的微生物组变化与短链脂肪酸产量的增加和代谢副产物(如乙醇、对甲酚和二氧化碳)产量的减少有关。
地中海饮食中富含的膳食纤维能够促进有益细菌的生长,如双歧杆菌、粪杆菌、Tenericutes、Dorea等。
膳食纤维还能增加产丁酸菌的丰度,如Roseburia hominis、Agathobaculum butyriciproducens、Faecalibacterium prausnitzii和厌氧菌Anaerostipes hadrus,这些细菌能够产生短链脂肪酸,对维持肠道屏障功能和抗炎作用至关重要。
两项干预研究将地中海饮食与特定分类特征联系起来,增加Faecalibacterium prausnitzii、Roseburia丰度,减少Ruminococcus gnavus、Collinsella aerofaciens、Ruminococcus torques丰度。
此外,地中海饮食中的植物化学物质,包括多酚、硫代葡萄糖苷、萜类等,也是肠道微生物群的重要底物,可以促进有益菌的生长,并通过微生物群依赖的生理效应,如短链脂肪酸介导的胰岛素抵抗衰减,对宿主健康产生积极影响。
并且地中海饮食中推荐的鱼类和海鲜是长链ω-3脂肪酸EPA和DHA的主要来源,这些脂肪酸对心脏健康有益,并且可能通过调节肠道微生物群的组成和功能来发挥作用。
这些因饮食而导致的微生物组变化与短链脂肪酸产量的增加和代谢副产物(如乙醇、对甲酚和二氧化碳)产量的减少有关。
“
地中海饮食是否存在不足?
•文化和可获得性:地中海饮食可能不适合所有人或每种文化,且某些地区可能难以获得地中海饮食中推荐的食物。
•成本:一些地中海饮食推荐的食物,如特级初榨橄榄油、新鲜海鲜和坚果,可能成本较高。
•个体差异:每个人的营养需求和健康状况都不同,地中海饮食可能需要根据个人情况进行调整。
•饮酒问题:虽然适量饮酒是地中海饮食的一部分,但并不适合所有人,特别是那些有酒精依赖或其他健康问题的人。
“
哪些人不适合地中海饮食?
地中海饮食通常对所有人都是安全的,包括老年人、儿童和孕妇。
小结
地中海饮食因其丰富的蔬菜、水果、全谷物和健康脂肪来源,被视为一种健康的饮食模式,有助于降低多种慢性疾病的风险并改善肠道健康。
但也存在一些局限性和不足,在采纳这种饮食模式时,应考虑个人的健康状况、文化背景和经济能力。

被评为最佳快速减肥饮食第一名的是生酮饮食。
“
什么是生酮饮食?
生酮饮食(keto)是一种高脂肪、低碳水化合物的饮食,旨在让你的身体进入酮症状态,燃烧脂肪以帮助人们减肥。这种饮食的目的是快速减肥,而不会感到饥饿或渴望。
“
生酮饮食为什么有助于快速减肥?
碳水化合物是人体首选的能量来源。当碳水化合物被摄入时,肝脏会将其转化为葡萄糖来为身体提供能量。然而,在生酮饮食中,你摄入的碳水化合物会比你平时少得多。
当你剥夺身体的碳水化合物,就会欺骗它,让它相信自己正在挨饿,迫使它几乎完全依赖脂肪,你的身体就会开始分解储存的脂肪来获取能量,这会导致你减肥。
研究表明,生酮饮食在短期内可以有效减肥,但从长远来看,它可能并不一定比摄入更多碳水化合物的低脂饮食更好。
“
生酮饮食有什么特点?
•高脂肪:生酮饮食中,脂肪通常占总热量摄入的70%至80%,这包括了饱和脂肪、单不饱和脂肪和多不饱和脂肪。
•适量蛋白质:蛋白质的摄入量需要控制,以避免身体将过多的蛋白质转化为葡萄糖,从而影响生酮状态。
•极低碳水化合物:碳水化合物的摄入量通常限制在每天20至50克,远低于一般饮食的摄入量。
•生酮比例:生酮饮食的生酮能力定义为脂肪克数与碳水化合物和蛋白质克数之和的比值,常见的生酮比为4:1或3:1。
•包括特定食物:饮食中鼓励摄入的食物包括肉类、鱼类、蛋类、健康脂肪(如橄榄油、椰子油)、非淀粉性蔬菜等。
“
生酮饮食有哪些健康益处?
生酮饮食对一些人的健康有益,包括:
•短期内减轻体重:生酮饮食通过限制碳水化合物的摄入,迫使身体燃烧脂肪来获取能量,有助于体重减轻。
•减少糖尿病患者对胰岛素的需求:生酮饮食有助于降低血糖水平,对糖尿病患者可能有积极影响。
•改善认知功能:一些研究表明,生酮饮食可能有助于提高认知功能和记忆力。
•减少炎症:生酮饮食中富含的抗炎食物,如浆果等,有助于减少身体的炎症反应。
•可能的神经保护作用:生酮饮食可能有助于改善线粒体功能,对某些神经退行性疾病有潜在的保护作用,并被发现可以减少癫痫患者的发作。
•癌症治疗的潜在辅助:一些研究表明,生酮饮食可能有助于减少某些癌症治疗的副作用,并可能对癌细胞的生长有一定的抑制作用。
生酮饮食已被证明可以帮助糖尿病患者降低糖化血红蛋白水平并减少胰岛素剂量。在一项临床试验中,采用极低碳水化合物生酮饮食的参与者将胰岛素剂量减少了一半,并在24周内达到正常血糖水平,比采用低热量饮食的另一组更快。
研究表明,生酮饮食可能对患有某些神经系统疾病的成年人有治疗作用,包括癫痫、阿尔茨海默病、偏头痛和神经胶质瘤,这些疾病是由人体代谢营养物质的方式发生紊乱引起的。
“
生酮饮食可能存在的健康风险?
虽然生酮饮食可以在短期内快速减轻体重,但同时也存在一些健康风险。包括以下几点:
•生酮饮食可能增加心血管疾病风险,如增加低密度脂蛋白(“坏”胆固醇)水平较高。
•水果和蔬菜摄入量减少可能导致营养缺乏,如维生素和矿物质摄入不足。
•可能影响肌肉消耗和运动表现。
•高蛋白质摄入可能增加代谢疾病的风险。
•肉类和乳制品的增加可能促进某些有害肠道细菌代谢产物产生,如氧化三甲胺和硫化氢。
•此外生酮饮食还可能导致肾结石和其他肾脏问题,脂肪肝和其他肝脏问题或是心脏病。
“
对肠道微生物群有什么影响?
临床前研究也表明,肠道微生物组的组成在响应生酮饮食时发生了显著变化,最明显的是:
•Akkermansia,乳杆菌属、Roseburia、副拟杆菌属(Parabacteroides)增加
•Turicibacter、Desulfovibrio、大肠杆菌和志贺菌属物种大幅减少。
——超重成年人
在涉及17名超重成年人的研究中,为期4周的生酮饮食显示在人肠道中放线菌门(Actinobacteria)和厚壁菌门的大量减少。具体来说,有益的双歧杆菌的19种物种减少了,而拟杆菌门丰度增加。这些变化部分是通过宿主产生酮体诱导的。
——癫痫儿童
在涉及12名严重癫痫儿童的为期3个月的研究中,遵循生酮饮食的儿童显示健康促进和消耗纤维的双歧杆菌属、直肠真杆菌(E.rectale)和Dialister属的丰度大幅减少。相反,儿童显示拟杆菌属和大肠杆菌属的丰度增加,后者部分归因于大肠杆菌(Escherichia coli)的增加。
“
哪些人不适合遵循生酮饮食?
不建议以下人群食用生酮饮食:
•患有胰腺疾病的人;
•患有肝脏疾病的人;
•甲状腺有问题;
•脂肪代谢紊乱;
•饮食失调或有饮食失调史;
•胆囊疾病或已切除胆囊的人
此外,孕妇、未接受过减肥医学建议的儿童、患有某些类型癌症的人、患有心脏病的人和高水平运动员都不应尝试这种饮食。
这种饮食还会对胰岛素和生殖激素产生巨大影响。糖尿病患者采用生酮饮食是有争议的,尤其是接受胰岛素治疗的人,至少需要仔细的医疗监测。
小结
总的来说,生酮饮食是一种特殊的饮食模式,它最大的优势在于能够快速减肥,并可能具有一定的神经保护作用,减轻炎症、改善认知功能,但同时也存在潜在的风险和挑战。
在开始生酮饮食之前,建议咨询医生或营养专家,以确保这种饮食模式适合个人的健康状况和生活方式。并且由于生酮饮食具有严格的限制性,不建议长期使用。

DASH饮食是一种预防及控制高血压的饮食模式,也是除地中海饮食外,最利于心脏健康的饮食模式。
“
什么是DASH饮食?
DASH饮食是推荐给想要预防或控制高血压的人的饮食计划。它通过增加纤维、水果、低脂(或脱脂)奶,和有益心脏健康的矿物质(包括钙、钾和镁)的摄入量,同时减少钠和不健康脂肪的摄入量来实现这一目标。
特点
•多不饱和脂肪:DASH饮食强调摄入多不饱和脂肪,如橄榄油、亚麻籽油、山茶油等,这些脂肪有助于改善心血管健康。
•全谷物:饮食中包括丰富的全谷物,如糙米、全麦面包和全麦意大利面,它们提供膳食纤维和必要的维生素和矿物质。
•蔬菜和水果:鼓励大量摄入各种蔬菜和水果,以提供抗氧化剂、维生素和矿物质。
•低脂乳制品:推荐食用低脂或无脂牛奶、酸奶和奶酪,这些乳制品是钙和维生素D的良好来源。
•限制饱和脂肪和胆固醇:减少黄油、起酥油、人造黄油、奶酪和熏肉等饱和脂肪和胆固醇含量高的食物的摄入。
•减少钠的摄入:DASH饮食建议减少钠的摄入,将钠的每日摄入量限制在2300毫克,以帮助降低血压。
“
如何开始DASH饮食?
您无需对饮食做出重大改变,只需从饮食习惯的小变化开始 DASH 饮食即可。
例如:
•每餐添加一份蔬菜或水果;
•每周吃两顿或两顿以上的无肉餐;
•使用香草和香料可以使食物更美味,而无需加盐;
•吃杏仁、山核桃或其他坚果代替薯片;
•尽可能将白面粉换成全麦面粉;
•午餐或晚餐后(或两者皆有)散步15分钟;
“
DASH饮食有哪些健康益处?
•降低血压:DASH饮食能够有效降低高血压,减少心血管疾病的风险。
•改善心脏健康:通过减少饱和脂肪和胆固醇的摄入,以及增加多不饱和脂肪和膳食纤维的摄入,有助于改善心脏健康。
•促进消化系统健康:富含膳食纤维的食物有助于维持肠道健康,预防便秘。
•控制体重:DASH饮食由于其高纤维和低脂肪的特点,有助于控制体重。
•预防糖尿病:研究表明,DASH饮食有助于预防2型糖尿病。
•抗炎作用:由于富含抗氧化剂和抗炎成分,DASH饮食可能有助于减少慢性炎症。
“
对肠道微生物群有什么影响?
DASH饮食与地中海饮食有许多相似之处,包括对全谷物、蔬菜、水果和低脂乳制品的摄入。因此,我们可以合理推测,DASH饮食也可能对肠道微生群产生积极影响,包括:
•增加有益菌群:DASH饮食中丰富的纤维和植物性食物可能促进有益菌群的增长,如双歧杆菌和乳酸杆菌、部分产短链脂肪酸菌,这些菌群与健康状态相关。
•改善肠道环境:DASH饮食可能通过增加肠道中的短链脂肪酸(SCFA)产生,改善肠道环境。SCFA有助于维持肠道屏障的完整性,调节免疫反应,并提供能量。
•减少炎症:DASH饮食中较低的饱和脂肪和反式脂肪含量可能有助于减少肠道炎症,改善肠道健康。
•促进肠道蠕动:DASH饮食中丰富的纤维摄入有助于促进肠道蠕动,预防便秘,并为肠道微生物提供营养。
“
可以通过DASH饮食减肥吗?
可以通过DASH饮食安全且可持续地减肥。但是,诀窍是留意份量并考虑您选择食物的卡路里含量。
通常,当人们从正常的饮食模式过渡到DASH饮食方式时,他们可能会自动减少卡路里,因为他们在饮食中添加了更多的蔬菜和均衡的膳食。
短期减肥
虽然DASH饮食并不是专门为减肥而设计的,但它可以帮助人们减肥。临床试验的荟萃分析表明,与采用对照饮食方案的患者相比,DASH 饮食方案的患者在8至24周内额外减轻了3.1磅体重,在24周内腰围减少了1.05厘米。
在另一项随机临床试验中,与对照饮食相比,DASH 饮食八周后体重和BMI显著下降。
长期减肥
如果您像 DASH 饮食一样从饮食中去除加工、含糖、含盐和高脂肪的食物,并定期锻炼,您很可能会继续减肥。
体重维持和管理
一旦达到目标体重,就应该能够通过DASH饮食来维持体重。纤维和蛋白质会让人有饱腹感,而卡路里含量足以让人精力充沛。
“
DASH饮食有什么优缺点?
优点
✔营养丰富;
✔不用计算碳水化合物或卡路里;
✔能够带来饱腹感——富含高纤维食物;
✔一份包含食谱的明确计划;
✔多样的食物和口味;
✔具有已证实的健康益处。
缺点
•成本:DASH饮食中推荐的食物,如新鲜水果、蔬菜和全谷物,可能比加工食品和快餐更昂贵;
•口味适应:一些人可能需要时间适应DASH饮食中推荐的健康食物,特别是如果他们习惯于高盐、高脂肪的食物;
•便利性:在外就餐时,遵循DASH饮食可能较为困难,因为餐馆的食物往往含有较多的钠和不健康脂肪。
•食物选择限制:需要避免或减少某些食物的摄入,如高饱和脂肪和高胆固醇的食物,这可能限制了食物的选择。
“
哪些人不适合尝试DASH饮食?
DASH饮食对大多数成年人来说都是健康的选择,除非医生建议限制某种营养素。例如,患有肾病的人可能需要低钾饮食。
小结
总的来说,DASH饮食是一种对大多数人来说健康且有益的饮食模式,特别是对于那些需要控制血压的人。
然而,DASH饮食可能不适合所有人。例如,严格素食者可能会发现在不摄入动物产品的情况下很难遵循DASH饮食的建议,因为它包括了低脂奶制品。
此外,对某些食物成分有过敏或不耐受的人,如乳糖不耐受者,可能需要调整DASH饮食以适应他们的特定需求。肾脏疾病患者也可能需要在遵循DASH饮食时调整蛋白质的摄入量。

亚洲饮食,通常指的是东亚、东南亚和南亚等地区的食物习惯,如中餐、日本料理和韩国料理,具有其独特的特点和对肠道微生物群及整体健康的影响。
亚洲饮食强调整体健康和平衡,注重天然食材的使用,富含蔬菜、水果、全谷物、豆类、鱼类和适量的肉类。以下是亚洲饮食的主要特点以及它们对肠道微生物群和健康的潜在影响。
“
亚洲饮食的特点
•蔬菜和水果的高摄入量:亚洲饮食通常包含大量的新鲜蔬菜和水果,它们是膳食纤维和各种植物化学物质的重要来源。
•全谷物:亚洲饮食中的主食经常是全谷物,如糙米、燕麦和小米,富含B族维生素和矿物质。
•豆类和豆制品:豆类,包括大豆、绿豆和红豆,以及豆制品如豆腐和味噌,是亚洲饮食中蛋白质的主要来源。
•鱼类和海鲜:亚洲饮食中常见的鱼类和海鲜,如三文鱼、金枪鱼和鳕鱼,是优质蛋白质和omega-3脂肪酸的丰富来源。
•适量的肉类:与西方饮食相比,亚洲饮食中的肉类摄入量通常较少,更倾向于使用瘦猪肉、鸡肉和偶尔的红肉。
•传统发酵食品:亚洲饮食中常见的发酵食品,如泡菜、味噌、纳豆和酸奶,含有益生菌,有助于肠道健康。
“
亚洲饮食对健康有什么影响?
•降低慢性疾病风险:亚洲饮食通常包含大量的蔬菜、水果和全谷物,这些食物富含纤维、维生素和矿物质,有助于维持消化系统的健康,预防慢性疾病,与较低的心血管疾病、2型糖尿病和某些癌症风险相关。
•改善消化健康:亚洲饮食中的高纤维和发酵食品有助于改善消化健康,减少便秘和肠易激综合征的症状。
•抗炎抗氧化:亚洲饮食中的茶、香料和某些蔬菜(如姜、大蒜)富含多酚和抗氧化剂,这些成分具有抗炎和抗氧化作用,能够减少氧化应激和炎症反应。
•促进体重管理:亚洲饮食中的食物通常热量较低,有助于控制体重和减少肥胖的风险。
•增强免疫力:亚洲饮食中的抗氧化剂和免疫调节成分有助于增强免疫力,减少感染的风险。
•改善认知功能:一些研究表明,亚洲饮食中的成分,如omega-3脂肪酸和多酚,可能有助于改善认知功能和预防神经退行性疾病。
“
亚洲饮食存在哪些不足?
•营养不均衡:在某些亚洲饮食中,可能缺乏足够的蛋白质和某些维生素(如维生素D和B12),特别是在素食主义者中。
•高盐摄入:一些亚洲饮食,特别是中国和韩国的饮食,可能含有较高的盐分,这与高血压和心血管疾病的风险增加有关。
•饮酒文化:在某些亚洲文化中,饮酒被视为社交活动的一部分,过量饮酒可能导致肝脏疾病和其他健康问题。
•加工食品的增加:随着全球化的影响,亚洲饮食中加工食品和快餐的摄入量有所增加,这可能导致不健康脂肪和糖分的摄入增加。
•传统烹饪方法:某些传统的烹饪方法,如油炸和烧烤,可能增加不健康脂肪的摄入。
•食物过敏和不耐受风险:亚洲饮食中可能含有一些常见的过敏原,如花生、海鲜等,可能会引起一些人的食物过敏或不耐受,影响其健康。
小结
亚洲饮食的健康益处主要体现在其丰富的植物性食物、低饱和脂肪和高纤维摄入。然而,高盐、高糖和加工食品的摄入也是亚洲饮食中需要注意的潜在健康隐患。
为了最大化亚洲饮食的健康益处并减少潜在风险,建议采取均衡的饮食方式,减少加工食品和高盐、高糖食品的摄入,同时增加蔬菜、全谷物和健康蛋白质的摄入。

素食饮食包括纯素饮食(Vegan Diet)和现在新出现的一种弹性素食。
纯素饮食是指一种不包含任何动物产品的饮食方式,包括肉类、鱼类、奶制品、鸡蛋、蜂蜜等。纯素饮食者通常会食用植物性食品,如蔬菜、水果、全谷物、豆类、坚果和种子等。
而弹性素食饮食又称为半素食饮食,不像传统素食饮食那样严格,而是多吃植物性食物少吃肉。不用完全遵循无肉生活方式又可获得素食主义带来的健康益处。可以大多数时候选择无肉餐,但在特殊场合仍可享用汉堡或牛排等肉类。
“
素食饮食的特点
•植物性食品的高摄入量:纯素饮食强调食用大量的植物性食品,包括全谷物、豆类、坚果、种子和蔬菜。
•更高的纤维摄入:由于植物性食品通常富含纤维,纯素饮食者可能会摄入更多的纤维。
•低饱和脂肪:由于不食用动物产品,纯素饮食通常含有较低的饱和脂肪。
•可能的高抗氧化剂和植物化学物质摄入:植物性食品富含抗氧化剂和植物化学物质,这些对健康有多种益处。
“
素食饮食对健康有什么影响?
•降低心脏病风险:由于纯素饮食中饱和脂肪和胆固醇的含量较低,可以降低心脏病的风险。
•改善血糖控制:纯素饮食有助于改善血糖控制,对于预防和控制2型糖尿病有益。
•促进健康的体重:由于富含纤维和低热量密度,纯素饮食有助于维持健康的体重。
•可能降低某些癌症的风险:一些研究表明,植物性食品中的抗氧化剂和其他植物化学物质可能有助于降低某些类型癌症的风险。
•改善肠道健康:高纤维饮食有助于维持肠道健康,促进良好的肠道菌群平衡。
“
对肠道微生物群有什么影响?
首先,素食饮食通常富含碳水化合物和纤维,增加了肠道微生物的多样性和丰富性。这种饮食模式特征是拟杆菌门、普雷沃氏菌属的数量增加,而厚壁菌门与拟杆菌门的比例降低。
此外,纯素饮食中的纤维成分,是结肠微生物的主要营养来源。膳食纤维在结肠中经细菌酵解可以形成短链脂肪酸,这对维持结肠细胞的营养和功能完整是必需的。短链脂肪酸如丁酸和丙酸对维持肠道屏障功能、调节免疫反应和降低炎症具有重要作用。因此,纯素饮食通过提供丰富的膳食纤维,有助于促进短链脂肪酸的生产,进而有益于肠道健康。
另一方面,纯素饮食中也包含多种植物化学物质,如多酚、类胡萝卜素、植物甾醇、木脂素和生物碱,这些物质已被证明对肠道微生物群具有调节作用。例如类胡萝卜素,有助于维持肠道免疫稳态,可能通过诱导IgA产生来提高抗肿瘤效率。
同时,纯素饮食中可能包含的益生元,如低聚半乳糖,对肠道微生物群也有积极影响。纯素饮食中的益生元成分可能有助于改善肠道微生物群的组成,促进有益菌的生长。
“
素食饮食存在哪些潜在不足?
•营养缺乏的风险:纯素饮食者可能面临某些营养素缺乏的风险,特别是维生素B12、铁、钙、锌和ω-3脂肪酸。
•蛋白质摄入可能不足:虽然植物性食品也含有蛋白质,但纯素饮食者需要更加注意蛋白质的来源和质量,以确保足够的必需氨基酸摄入。
•社会和文化挑战:在某些文化和社会环境中,纯素饮食可能会遇到社会接受度和可获得性方面的挑战。
•需要更多的计划和教育:为了确保营养均衡,纯素饮食者需要更多的计划和教育,以确保他们能够从植物性食品中获得所有必需的营养素。
小结
纯素饮食可以是一种健康的饮食方式,特别是当它被精心规划以确保足够的营养摄入时。然而,它也需要对食物选择和营养需求有更深入的了解,以避免潜在的营养不足。
对于那些选择纯素饮食的人,定期咨询营养专家或评估营养状况并提供个性化建议是非常重要的。

过去50年中,一种受到极大关注的饮食疗法是日常热量限制(CR),它被定义为在保持充足营养的同时,将饮食摄入量减少至低于维持体重所需的能量水平。观察性、临床前和临床试验的发现表明,CR可能将寿命延长1-5年,同时改善生活质量。
“
热量限制饮食的健康益处
最严格的CR随机试验来自国家老龄化研究所资助的CALERIE(减少能量摄入长期效应综合评估)联盟。CALERIE研究的发现显示,短期和长期CR都可以减少体重、皮下脂肪、内脏脂肪和肝内脂肪含量。
•这些改善与多种代谢益处相关,包括增加胰岛素敏感性、增强胰岛β细胞功能和降低空腹胰岛素。
•改善了代谢灵活性,降低了血压、低密度脂蛋白胆固醇和甘油三酯水平,并提高了高密度脂蛋白胆固醇水平。
•心血管疾病的10年风险降低了29%,这归因于氧化应激和炎症的减少,以及CR过程中维持的内皮一氧化氮功能的保护。
热量限制饮食减少了微生物表达的酶
这些酶能够使脂多糖A生物合成,从而限制了脂多糖(LPS)的产生,并以药理学上已知能刺激脂肪细胞褐化和减少内脏脂肪的方式抑制了LPS-TLR4途径。
“
热量限制饮食可能存在的不足?
•营养不足:如果热量限制不当,可能会导致某些营养素的摄入不足,影响身体健康。
•难以持续:长期的热量限制可能会导致饥饿感和食欲增加,使得饮食计划难以持续。
•可能的肌肉损失:如果热量限制过于严格,可能会导致肌肉质量的损失,影响身体的代谢率和整体健康。
•社会和心理压力:严格的饮食限制可能会影响社交活动和心理健康,造成压力和焦虑。
小结
综上所述,热量限制饮食在实施时需要综合考虑个人的营养需求、生活方式和健康状况,以确保既能达到减肥目标,又能维持健康。
思考
传统饮食与新兴饮食个性化饮食的兴起

地中海饮食长期以来一直被广泛认为是一种有效且均衡的减肥方法,可改善肥胖、2 型糖尿病和非酒精性脂肪肝等代谢疾病患者的代谢状况。
个性化饮食结合各种因素和不同人群,提高预测准确性
最近的研究表明,地中海饮食在人际间存在差异,即使个体食用同质饮食,依赖微生物组的代谢物的变异系数也不会显著下降。因此,营养学领域——与医学的许多其他领域一样——正朝着采用“个性化方法”的方向发展,以满足不同患者群体的特殊需求。因此,在 100 名糖尿病前期患者中,将地中海饮食的有效性与机器学习系统开发的个性化餐后目标饮食 (PPT) 进行了比较。
PPT 饮食基于一种人工智能算法,该算法整合了临床和微生物组特征来预测个人餐后血糖反应。
PPT 饮食的饮食建议以菜单的形式提供,餐点从研究生成的餐食库中选择。菜单设计有各种食物和餐食选项,以实现多样性,确保均衡饮食,并满足参与者的个人口味和喜好。
PPT 饮食平均总能量摄入量为 1881.0 kcal/天,碳水化合物、蛋白质和脂肪平均摄入量分别为 182.7、85.9 和 84.9 克/天。
结果表明,经过 6 个月的营养干预后,与地中海饮食相比,PPT 饮食导致 alpha 多样性显著增加,肠道微生物组成的变化更为显著。关于心脏代谢结果,作者发现坚持 PPT 饮食与 HbA1c、HDL 胆固醇和甘油三酯值的改善相关,并且通过因果中介分析,他们表明这种关联部分由属于拟杆菌目、毛螺菌科、颤螺菌目的三种细菌介导。
这些研究结果表明,虽然像地中海饮食这样的传统饮食评分依赖于将微量营养素、食物和慢性病风险联系起来的研究,在预测一般人群的结果方面相当有效。但较新的评分系统正在出现,它们考虑到各种因素和不同人群的独特特征,从而提高预测准确性。
其他的例子如:
黑色素瘤患者研究
对115名接受免疫检查点抑制剂治疗的黑色素瘤患者进行的分析表明,肠道微生物特征与治疗效果和免疫相关不良事件相关。
以瘤胃球菌科为主的微生物群患者相比拟杆菌科为主的患者反应更佳。纤维和omega-3脂肪酸减少摄入可能导致免疫疗法反应不佳。
溃疡性结肠炎管理
一项研究将标准治疗与从多名农村捐赠者获得的新鲜粪便微生物群移植(FMT)以及抗炎饮食相结合,发现这种组合能显著提高轻度至中度溃疡性结肠炎患者的临床反应和缓解率。
这些发现强调了个性化方法在增强肠道微生物的多样性和变化组成方面的潜在益处,这反过来可以在影响心血管健康标志物、癌症治疗反应和炎症性肠病缓解方面发挥关键作用。

个性化饮食离不开好的营养筛查工具
20多年来,营养风险筛查一直被认为是营养护理过程中的关键步骤。在临床营养领域,营养风险筛查被定义为“一种快速识别营养风险个体并分类进行营养干预的过程”。
在过去的几十年里,全球范围内为将营养风险筛查纳入议程付出了巨大的努力。这些努力取得了显著成效,最终促使许多国家的医院将营养风险筛查作为常规实践。然而,国际指南对于如何选择筛查工具缺乏明确规定。目前,不同人群和医疗保健环境中使用了多种筛查工具。
人工智能与机器学习在临床营养决策中的应用前景
近年来,医学领域见证了人工智能和机器学习的兴起。机器学习是人工智能的一个分支,涉及计算机(“机器”)从数据中学习的方式。这些技术不依赖于预先编程的规则,而是通过接触实例进行学习和改进,旨在帮助临床决策并提高护理质量和效率。随着患者病情和医疗技术的日益复杂,机器学习在医学中的重要性日益凸显。
机器学习可以通过广泛筛查、促进诊断、个性化治疗、预测临床结果、提供早期预警和评估患者对治疗的反应性等多种方式改善临床决策。
谷禾健康多年来一直在积累和构建不同人群样本数据库,利用机器学习技术,结合大量的肠道菌群数据和粪便代谢组学数据,以及人体测量、生化和临床数据和饮食习惯,获得了数十万独特的数据特征。这些数据被用来创建机器学习模型,实现预测不同的营养需求。根据肠道菌群和代谢数据,使用机器学习算法可以给出个性化的饮食建议,干预后的临床结果表现出了显著的改善。
通过对训练队列进行子采样,发现随着队列规模的增加,预测准确性也随之提高。模型方法旨在对出现特定可诊断症状之前检测出整体健康的潜在不利变化。这种检测可以指导饮食或生活方式的改变,以防止轻微问题升级为严重的健康问题,或促使进一步的诊断测试。
与现有的疾病特定指数不同,我们的指数涵盖多种疾病和多种营养,强调了泛疾病(或者说,一般健康)肠道微生物组特征。这种广泛的适用性在临床场景中可能特别有用,例如在选择粪菌移植(FMT)捐赠者时,肠道健康可以作为整体健康状况的反映。
主要参考文献
Best Diabetes Diets 2024,U.S.NEWs World Report
GBD 2017 Diet Collaborators. Health effects of dietary risks in 195 countries, 1990-2017: a systematic analysis for the Global Burden of Disease Study 2017. Lancet. 2019 May 11;393(10184):1958-1972.
Willett WC, Stampfer MJ. Current evidence on healthy eating. Annu Rev Public Health. 2013;34:77–95.
World Cancer Research Fund/American Institute for Cancer Research Diet, nutrition, physical activity and cancer: a global perspective. Continuous Update Project Expert Report. 2018.
Lloyd-Jones DM, Hong Y, Labarthe D. Defining and setting national goals for cardiovascular health promotion and disease reduction: the American Heart Association’s strategic Impact Goal through 2020 and beyond. Circulation. 2010;121:586–613.
GBD 2015 Risk Factors Collaborators Global, regional, and national comparative risk assessment of 79 behavioural, environmental and occupational, and metabolic risks or clusters of risks, 1990–2015: a systematic analysis for the Global Burden of Disease Study 2015. Lancet. 2016;388:1659–1724

谷禾健康

饮食在塑造肠道微生物群的组成、功能和多样性方面起着关键作用,各种饮食对肠道内微生物群落的稳定性、功能性和多样性有着深远的影响。了解不同饮食对微生物群的深远影响至关重要,改善代谢和肠道健康,预防和减缓由饮食不当引起的特定饮食相关疾病的发生。
在生命早期,分娩方式、喂养、饮食和环境等因素会塑造肠道微生物群。在成年期,虽然微生物群趋于相对稳定,但外界因素,尤其是饮食,会大大影响其组成和功能。营养素、微生物群和免疫系统之间的这种复杂相互作用是维持体内平衡和防御外部病原体的重要调节机制。
精准营养承认每个人对饮食的代谢反应会有所不同,因此针对人群健康的广泛饮食指南在个人层面上并不理想。一些大规模研究已开始将微生物组概念纳入精准营养,发现纳入肠道微生物组组成的预测模型远远优于仅基于宿主、饮食和身体活动因素的预测模型。
比如从控制体重来说,我们常常关注卡路里的摄入与消耗,却可能忽略了肠道菌群层面的理解。不同人群可以选择不同的方式,高纤维饮食可以促进产生短链脂肪酸的肠道细菌的生长,这些短链脂肪酸不仅有助于维持肠道健康,还可能通过调节食欲和能量代谢等方式来帮助控制体重。
鉴于测序和机器学习等方面技术的最新进展,极大地提高了人们对饮食及其对微生物群影响的理解。在此基础上,本文讨论了常见整个饮食方式(如地中海饮食、高纤维饮食、植物性饮食、高蛋白饮食、生酮饮食、西方饮食、间歇性禁食、热量限制饮食等)影响肠道微生物群的机制,还包括生命早期和成年期肠道微生物群相关的饮食相关慢性疾病,临床实践中用于缓解或预防疾病进展的特定饮食等。
微生物组研究成果的迅速扩展使多种长期营养原则变得复杂,同时也为干预提供了新的机会。更深入地了解饮食、宿主和微生物之间的因果关系,可以为开发精准营养和基于微生物组的疗法提供新的视角。
饮食对肠道微生物群的组成和功能有相当大的有益或负面影响。
下图是常见饮食方式对肠道菌群的影响,这在后面我们会详细展开阐述。
全膳食的常量营养素组成及其对肠道菌群的影响

doi.org/10.1038/s41579-024-01068-4
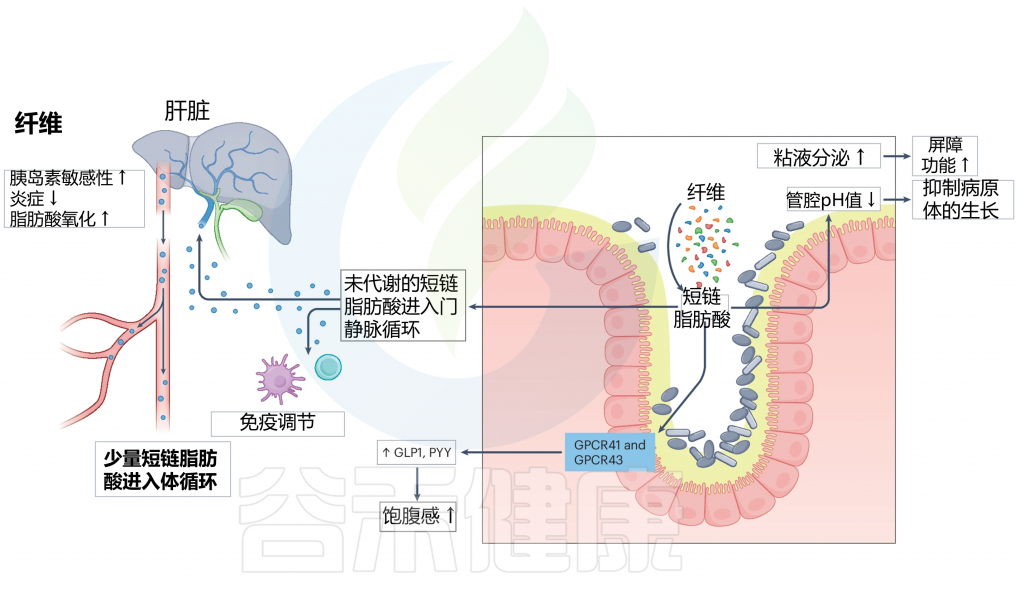
当膳食纤维到达肠道时,会经过肠道微生物群的发酵,产生如乙酸盐、丙酸盐和丁酸盐等短链脂肪酸(SCFA)。这些短链脂肪酸随后进入门脉循环,对宿主健康产生一系列积极影响。
激活GPCRs
短链脂肪酸激活G蛋白偶联受体GPCRs 41和43,这是它们发挥作用的初步机制。
触发肠道激素分泌
激活的受体进一步触发胰高血糖素样肽(GLP)和肽YY(PYY)等肠道激素的分泌。
注:GLP1和PYY在调节食欲、减缓胃排空和促进饱腹感方面起着关键作用。
增强肠道屏障功能
SCFAs通过增加粘液分泌和降低肠腔pH值来增强肠道屏障功能,保护肠道内壁,防止有害病原体进入血液。
抗炎与免疫调节作用
SCFAs具有抗炎和免疫调节作用,有助于维持整体肠道健康,并降低胃肠道疾病的风险。
肠道微生物群对纤维的分解及其对屏障功能和免疫力的影响
doi.org/10.1038/s41579-024-01068-4
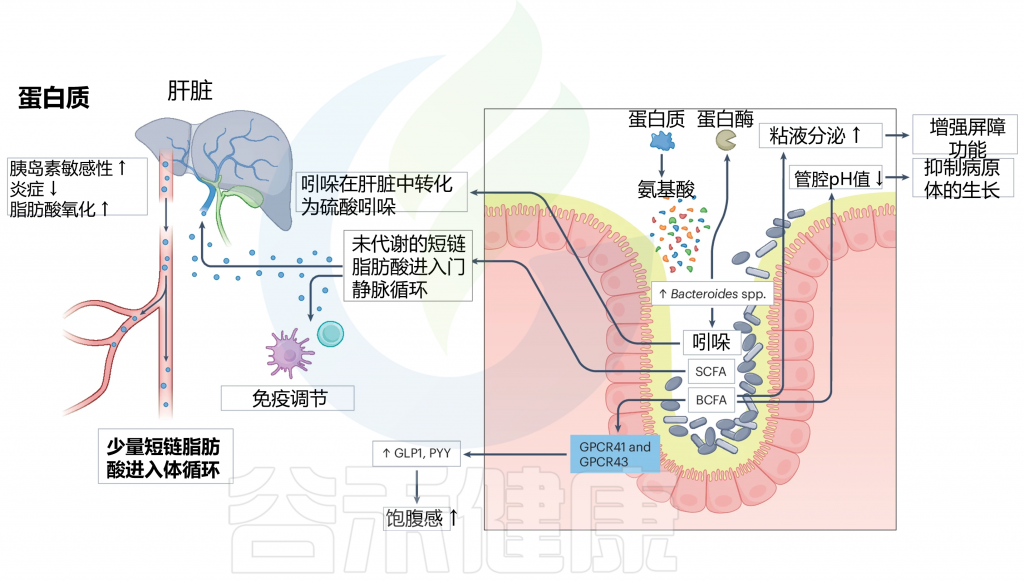
在肠道中,膳食蛋白质经过肠道微生物群的代谢,这与拟杆菌属的增加有关。这导致产生各种代谢产物,包括短链脂肪酸、支链脂肪酸(BCFAs)和吲哚。
支链脂肪酸可以激活 GPCR41 和 GPCR43,从而触发 GLP1 和 PYY 等肠道激素的分泌。此外,BCFAs 可以增加粘液分泌并降低腔内 pH 值,从而增强肠道屏障功能并保护肠道内壁。
肠道微生物群对蛋白质的代谢以及SCFA和吲哚对人类健康的后续影响
doi.org/10.1038/s41579-024-01068-4
SCFAs、BCFAs、GLP1 和 PYY 等肠道激素、粘液分泌和腔内 pH 对人体健康的影响,包括改善胃肠功能、调节食欲、减少炎症、改善胰岛素敏感性和脂肪酸氧化,从而促进整体肠道健康。
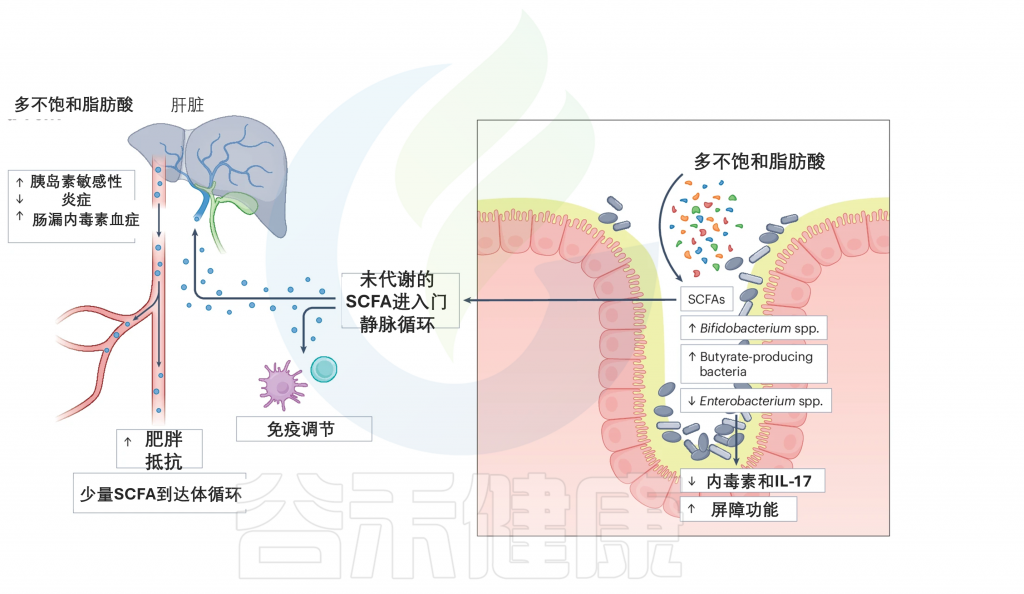
当膳食PUFAs到达肠道时,它们会被肠道微生物群代谢。这一过程增加了特定细菌的丰度,如双歧杆菌属和产丁酸菌。因此,产生了各种代谢产物,如短链脂肪酸,例如丁酸盐。
PUFAs可以减少促炎的肠杆菌属(Enterobacterium)的丰度,从而减少炎症并改善肠道屏障功能。这可能导致内毒素和IL-17的产生减少,进而减少炎症并改善对人类健康的影响。由PUFA代谢产生的未代谢SCFAs进入系统循环,在其中发挥免疫调节作用。它们可以通过改善胰岛素敏感性、减少炎症和改善肠道渗漏症内毒素血症来增强抵抗肥胖的能力。
doi.org/10.1038/s41579-024-01068-4
多酚类物质被肠道细菌代谢,因此被分解成生物活性微生物代谢产物。多酚已被证明可以增加肠道腔中有益细菌的丰度,如双歧杆菌、Akkermansia、乳酸杆菌属。这些细菌在维持肠道屏障功能、调节免疫系统、促进肠道稳态和抑制病原菌生长方面起着至关重要的作用。
此外,多酚在肠道内表现出显著的抗炎和抗氧化作用。多酚代谢的副产物,缺乏酚类的代谢产物,在系统循环中被吸收,在那里它们发挥显著的免疫调节作用。例如,这些代谢产物已被证明可以通过减少炎症和氧化应激,以及改善内皮功能,从而改善肺部、大脑和心脏功能,增加周围血流。
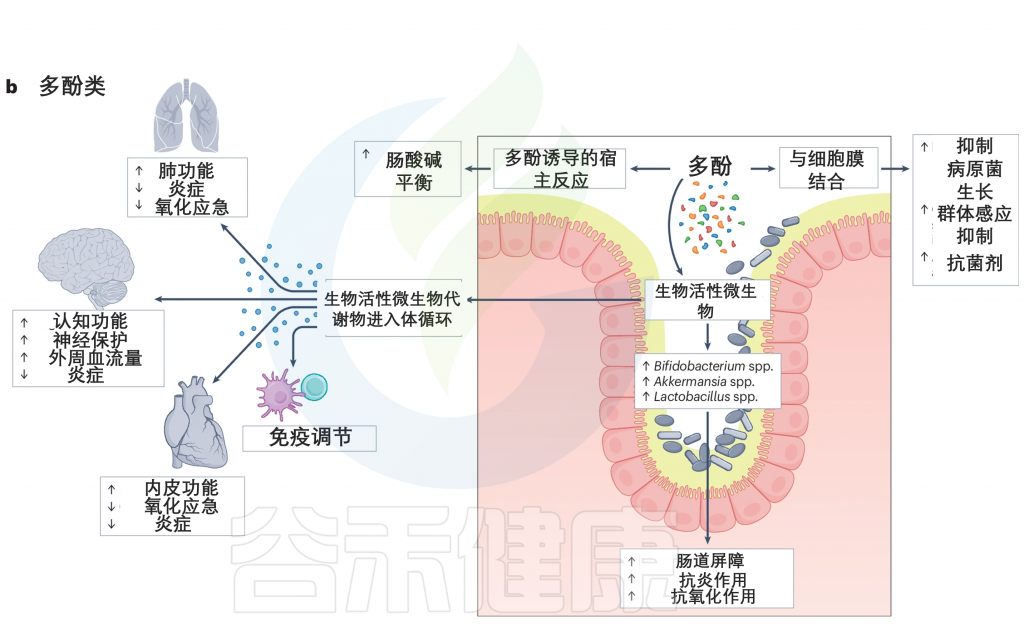
doi.org/10.1038/s41579-024-01068-4
肠道微生物组的差异性影响
不同肠道微生物群对宿主能量状态的贡献存在差异,与肥胖相关的肠道微生物组特征可能会加剧宿主的表型。
遗传性肥胖小鼠及其瘦弱的同窝小鼠在肠道微生物组成上存在差异,从ob/ob供体获得的肠道微生物群受体增加的体脂,比从遗传性瘦弱供体获得的微生物群受体多。
将适应高脂高糖(HFHS)饮食的小鼠肠道微生物群与适应低脂高植物多糖饮食的小鼠肠道微生物群进行移植,一致地增强了接受控制饲料的无菌受体小鼠的脂肪积累。
这些研究表明,无论是由遗传还是饮食驱动的肥胖表型,都可以通过肠道微生物群传播。
肠道微生物组与营养不良
患有夸希奥科病(kwashiorkor)的儿童的肠道微生物群表现出发育不良的特征,并通过在无菌小鼠中定植后与健康对照相比,损害了营养吸收,从而在因果上对营养不良有所贡献。
肠道微生物群的变化也已被证明有助于极低热量饮食(VLCDs)和Roux-en-Y胃旁路手术后的快速减重。
例如,对超重或肥胖的绝经后妇女进行每天800千卡的极低热量饮食,导致肠道微生物群的变化和改善的代谢表型,如体重减轻和减少的脂肪量,这些变化可以在接受了节食前后肠道微生物群的无菌小鼠受体中重现。
肠道微生物组的能量缓冲作用
与低消化性饮食相关的更高营养流入结肠可以以一种增强其对宿主能量状态贡献的方式改变肠道微生物群,表现为接受低消化性饮食条件的微生物群的无菌小鼠受体体重增加和脂肪量更多。
在这个宿主-微生物组生态共生的例子中,宿主的营养吸收较低被肠道微生物群衍生的代谢产物及其下游效应所部分缓冲,例如增加宿主的能量摄入。这样的能量缓冲在能量受限条件下可能有助于宿主的代谢健康,但在能量过剩条件下也可能妨碍体重管理。
肠道微生物组的环境和饮食依赖性
肠道微生物群对宿主能量平衡的贡献可能依赖于环境和饮食背景,即使不通过饮食操纵宿主能量平衡也是如此。
来自肥胖不一致的人类双胞胎的无菌小鼠受体通常模仿了它们供体的代谢表型,但是当差异性定植的受体动物共同饲养时,来自瘦弱供体的微生物群侵入了来自肥胖供体的微生物群,结果是两者都保持了瘦弱。
当共同饲养的受体动物被喂食高脂肪和低水果蔬菜的饮食时,与瘦弱相关的微生物群的传播性被破坏了。
这些复杂的相互作用强调了饮食对宿主-微生物组代谢相互作用的影响有时可能难以追踪。
肠道微生物通过其代谢产物影响健康
短链脂肪酸可以被各种宿主组织转化为ATP,其中:
SCFAs具有多样的信号功能,影响能量平衡。
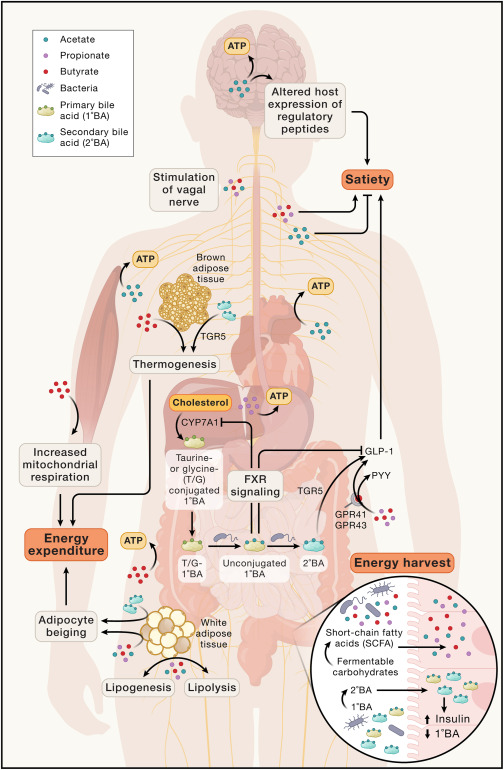
doi.org/10.1038/s41579-024-01068-4
SCFA通过各种方法影响能量摄入,包括乙酸盐穿过血脑屏障,介导调节性神经肽的表达,丙酸盐和丁酸盐结合肠内分泌L细胞中的GPR41和GPR43受体,刺激GLP-1和PYY的释放,以及通过迷走神经的肠脑信号传导,乙酸盐与SCFA混合物可能不同地介导这些信号传导。
SCFA通过促进棕色脂肪组织的产热、白色脂肪组织的米色和骨骼肌的线粒体呼吸来影响能量消耗。SCFA还可以影响脂肪生成和脂肪分解的动力学,据报道,丁酸盐促进脂肪分解,而乙酸盐和丙酸盐促进脂肪生成。
此外,肠道微生物组可以使宿主肝脏分泌的牛磺酸或甘氨酸结合的初级胆汁酸(T/G-1°BA)脱偶联和脱羟基,产生调节宿主能量代谢各个方面的非偶联初级胆汁酸和次级胆汁酸。未结合的初级胆汁酸通过法尼醇X受体(FXR)发出信号,抑制CYP7A1,CYP7A1是初级胆汁酸合成的限速步骤,对饮食脂肪吸收具有潜在的下游影响。次级胆汁酸激活TGR5,促进棕色脂肪组织的产热、白色脂肪组织的米色和胰腺β细胞的胰岛素产生。
肠道微生物胆汁酸代谢也可能通过对厌食素GLP-1的对比作用来影响能量摄入,2°BA激活的TGR5信号促进L细胞分泌GLP-1,1°BA活化的FXR信号在小鼠中显示出抑制GLP-1活性。这些多效性效应强调了对SCFA和胆汁酸的看法正在发生变化,从能量收获的载体转变为能够对宿主能量状态产生净积极和净消极影响的代谢调节因子.
地中海饮食(MD)强调摄入大量未加工的全植物性食品、橄榄油、乳制品、适量家禽和鱼类,以及少量红肉。
降低癌症死亡率及糖尿病风险
一项对美国25,315名女性的前瞻性研究显示,那些坚持地中海饮食模式的人在25年的随访期间全因死亡率降低了23%。这项研究还显示,较高的地中海饮食摄入量与20年随访期间未来2型糖尿病风险降低30%相关。地中海饮食模式可能还对癌症有保护作用。实际上,高度遵守这种饮食与普通人群中的癌症死亡率降低、癌症幸存者的全因死亡率降低,以及降低发展结直肠癌、头颈癌、呼吸、胃、肝和膀胱癌风险有关。
增加产丁酸菌
两项干预研究将地中海饮食与特定分类特征联系起来,增加Faecalibacterium prausnitzii、Roseburia丰度,减少Ruminococcus gnavus、Collinsella aerofaciens、Ruminococcus torques丰度。这些因饮食而导致的微生物组变化与短链脂肪酸产量的增加和代谢副产物(如乙醇、对甲酚和二氧化碳)产量的减少有关。
地中海饮食与特定功能途径有关
之前研究用宏基因组测序分析了307名男性长期饮食信息的微生物组数据。结果显示,地中海饮食与36条功能途径有关,这些途径大多类似于植物性饮食,具有丰富的微生物功能,用于SCFA发酵和膳食纤维降解。对地中海饮食的坚持显示出与特定功能途径的正相关,如用于果胶分解的d-果糖醛酸降解途径和用于半纤维素分解的甘露聚糖降解途径。地中海饮食的坚持和降低心血管疾病风险在P. copri水平较低的个体中更为明显。
地中海饮食plus版——更积极的变化相关
最近,DIRECT-PLUS研究包括294名肥胖或血脂异常的参与者,发现与地中海饮食相比,绿色地中海饮食与更显著的组成变化相关。绿色地中海饮食是地中海饮食的增强版,它增加了植物性食品的摄入量,减少了红肉的摄入,并且每天还摄入富含多酚的绿茶和Mankai水生植物。
这种饮食在微生物组成和多样性上产生了更大的变化,包括增加普雷沃特氏菌的丰度和支链氨基酸降解酶(异亮氨酸降解),减少双歧杆菌和支链氨基酸生物合成酶(缬氨酸和异亮氨酸生物合成)。这些变化与体重和心代谢指标的积极变化相关联。
膳食纤维对人类健康至关重要,它有助于降低长期体重增加,低纤维摄入量会增加患2型糖尿病和结肠癌的风险。
高纤维饮食会改变肠道微生物的组成,包括显著增加乳酸杆菌属和双歧杆菌属的丰度。
断奶后饮食变化,引起代谢复杂多糖的菌增加
不同的膳食纤维组分对肠道微生物的影响各不相同。例如,母乳喂养的婴儿表现出更高丰度的适应于利用人乳寡糖(HMOs——母乳中大量存在的不可消化的益生元糖类)的双歧杆菌。断奶后,肠道微生物组成会发生明显变化,这主要归因于饮食组成的改变。这导致能代谢更复杂多糖的拟杆菌门和厚壁菌门的扩张。
超重个体:改善菌群预防代谢疾病
在超重的个体中,阿拉伯木聚糖低聚糖的干预增加了普雷沃氏菌和直肠真杆菌(Eubacterium rectale)的丰度,伴随着代谢组学特征的有利变化,可能有助于预防代谢性疾病。
全谷物和小麦麸皮:双歧杆菌、乳杆菌↑↑
在31名志愿者中补充全谷物和小麦麸皮,导致双歧杆菌属和乳酸杆菌属的水平增加。全谷物消费者中的增加更为明显;两组都经历了总胆固醇的降低。
燕麦:厚壁菌门↑ 拟杆菌门↓ 心血管疾病风险↓
来自燕麦的高分子量β-葡聚糖减少了厚壁菌门,增加了拟杆菌门,并伴随着心血管疾病风险标志物的减少。
抗性淀粉:影响短链脂肪酸产生
以IV型抗性淀粉形式的膳食纤维对肠道微生物群的组成和功能以及丁酸盐或丙酸盐的产生了不同的影响。
简单碳水化合物在小肠中吸收,而复杂碳水化合物如膳食纤维则经历结肠微生物发酵,从而产生短链脂肪酸。人类只产生非常有限的用于碳水化合物降解的碳水化合物活性酶(CAZymes),因此依赖于肠道微生物群间接代谢几种膳食纤维。低纤维的饮食与肠道微生物群中减少的CAZyme储备相关。
短链脂肪酸的健康益处
包括前面文中提到过的,通过GPCRs传递信号,以及刺激肠道内分泌细胞分泌饱腹感激素(GLP-1和肽YY)。这影响了食欲调节,并调节了调节性T细胞的功能,以及脂质和葡萄糖代谢,在调节宿主能量代谢和结肠稳态中发挥关键作用。
丁酸盐作为结肠细胞的能量来源,通过肠细胞(巨噬细胞和树突状细胞)介导抗炎特性,并增强粘液产生,这突出了其在优化肠道吸收和肠道屏障功能中的作用。
短链脂肪酸与GPCRs及其他细胞的作用和互动不仅限于肠道,还扩展到外周组织、器官和免疫细胞。在小鼠模型中的报告表明,SCFAs和高纤维饮食可能在降低1型糖尿病、2型糖尿病、哮喘和压力的风险,减少脂肪酸合成和脂肪分解方面发挥作用,从而减轻体重并增强神经认知发展。SCFA的吸收导致肠腔pH值降低,这抑制了对pH敏感的病原体如梭菌纲和肠杆菌科的生长,并增加了营养素吸收。
全谷物中的不可溶纤维影响肠道传输速率和细菌发酵
两项随机对照交叉试验涉及50名超重或有代谢综合征风险的个体,表明全谷物饮食增加了粪便中的丁酸盐和己酸盐,改善了血脂水平,减少了炎症标志物,并与精制谷物饮食相比改善了体重减轻。产短链脂肪酸的菌与结肠传输时间显示出负相关关系。这进一步有助于调节肠道微生物组成和多样性,从而缓解各种肠道疾病,如肠易激综合症、炎症性肠病、结直肠癌和胃癌以及便秘。
微生物群与人类健康之间的相互作用强调了采取整体方法和更大规模的人类研究的必要性,以便深入认识饮食碳水化合物、肠道微生物群组成和疾病易感性之间复杂的关系。
植物性饮食富含多酚类、宿主可消化和不可消化的碳水化合物,并发挥益生元和后生元的双重效应。素食饮食导致形成独特的细菌环境,这一点从细菌功能能力的转变中得到证实。
素食者:拟杆菌↑ 普雷沃氏菌属↑
例如,素食者表现出低肉碱降解但增加氮同化。与杂食者饮食相比,这些饮食促进了拟杆菌门和普雷沃氏菌属的丰度,尽管由于微生物个体差异和研究方法的不一致性,研究结果有时会出现矛盾。
某些属或种的对比水平可以归因于饮食快速与逐渐转变对微生物造成的压力、健康与不健康饮食成分的存在,以及各种生物活性化合物的来源。例如:
植物性饮食的这些特性使其在预防和管理慢性疾病,如心血管疾病、2型糖尿病和某些癌症方面显示出潜力。然而,需要更多的研究来充分理解植物性饮食对肠道微生物组的具体影响,以及这些变化如何影响宿主的健康和疾病风险。
多酚类物质的吸收:少量在小肠,大量在结肠
多酚类物质,分为类黄酮和非类黄酮,是植物的次级代谢产物,存在于水果、蔬菜、谷物、葡萄酒、茶、咖啡等食物中。
少量的多酚类物质(5%~10%)在小肠中被吸收,主要是那些具有单体和二体结构的多酚。吸收后,苷元在肠细胞内经历生物转化,然后在肝细胞内继续转化。这些代谢产物通过循环系统运输到肾脏和肝脏等器官,并最终随尿液排出。
大部分多酚类物质(90%-95%)在回肠和结肠中与肠道微生物发生作用,它们促进双歧杆菌、Akkermansia、乳杆菌等物种的丰度,从而提供显著的抗炎和抗病原体特性,以及心血管保护作用。
最近一项涉及超过2万名成年人的随机对照试验表明,食用富含多酚的可可提取物减少了心血管疾病导致的死亡。然而,心血管疾病的发生并没有减少。
多酚类物质的抗菌和抗病原体特性
多酚类物质可以通过几种机制抑制细菌生长,包括结合并改变细胞膜的功能特性。它们还展现出对食源性病原体的抗菌活性,并以剂量依赖性方式作为群体感应抑制剂和抗菌剂。
肠道微生物群代谢多酚
肠道微生物群双向调节并代谢多酚类物质,将它们转化为更具生物活性的微生物代谢产物,并提高其相对于原始化合物的吸收。
代谢产物的健康益处
研究表明,食用生物活性微生物代谢产物对人类健康有益处。例如:
多酚类物质对肠道微生物群的调节
多酚类物质可以通过改变肠道微生物群的组成和影响各种微生物酶的功能,调节肠道微生物代谢产物,包括短链脂肪酸、TMAO、多巴胺、脂多糖、胆汁酸。
这最终可以通过多种方式引起多酚类物质诱导的宿主反应,例如,作为调节肠道酸碱平衡的调节器。多酚类物质对肠道微生物群的调节已被证明支持肺功能、中枢神经系统功能和肠道屏障完整性的稳态。
植物和动物源食物类型不同,对菌群影响有差异
植物和动物源性食物中蛋白质和脂肪类型的不同导致了肠道微生物组成和代谢组的差异。例如,基于动物的饮食导致耐胆汁细菌种类的丰度增加,如Alistipes、Bilophila,同时减少了厚壁菌门的丰度,降低了支链氨基酸(BCAAs)的水平,并增加了SCFAs和二甲基硫化物。
其他植物化合物,如纤维、萜类和类胡萝卜素,也已显示出健康益处。个体在从饮食多酚中产生酚类衍生代谢产物的量上的差异归因于每个人肠道微生物组的独特组成。
因此,分析多酚代谢产物可以作为一种有价值的方法,以更深入了解生物活性化合物效应,并为理解个体间的显著多样性提供全面的认识。
每日蛋白质摄入量超过1.5克/千克体重的饮食通常被认为是高蛋白饮食。这种饮食通常用于运动员或为超重人群减肥时所推荐。
蛋白质的消化和吸收
饮食中的蛋白质主要由宿主的蛋白酶分解,但每天有12-18克的蛋白质可到达大肠并被微生物群代谢。
不同类型的复杂蛋白质具有不同程度的可消化性,以及不同的氨基酸组成。
参与蛋白质分解的菌群
一些细菌物种参与蛋白质分解,并在高蛋白饮食者的肠道微生物群中富集,主要是拟杆菌属、芽孢杆菌属(Bacillus)、梭菌属(Clostridium)、Phocaeicola、丙酸杆菌属(Propionibacterium)、梭杆菌属(Fusobacterium)、乳杆菌属、链球菌属。
其他细菌可以直接利用氨基酸,并从蛋白质分解中受益,形成交叉喂养的相互作用。
蛋白质分解细菌使用多种酶
蛋白质分解细菌使用多种外肽酶、蛋白酶(包括金属、丝氨酸、半胱氨酸、天冬氨酸、苏氨酸、谷氨酸和天冬酰胺蛋白酶)和内肽酶来释放短肽和游离氨基酸。
氨基酸代谢产生短链脂肪酸
大多数氨基酸被发酵成短链脂肪酸:
部分发酵产物可能带来的健康危害
其他发酵产物包括可能的炎症化合物,如来自芳香族氨基酸(例如色氨酸)的吲哚和酚类化合物,以及氨、胺、有机酸和气体(即由含硫氨基酸半胱氨酸和甲硫氨酸产生的硫化氢,以及二氧化碳)。
值得注意的是,这些最终产物中的一些可能与疾病有关。吲哚和吲哚相关化合物可以到达肝脏并转化为硫酸吲哚酚,这是一种对肾脏有害的有毒代谢产物,并参与内皮功能障碍。此外,硫化氢可能具有致突变性,并可能在炎症中发挥作用,增加结肠癌的风险。
生酮饮食是一种极低碳水化合物、适量蛋白质和高脂肪的饮食模式,模拟了禁食期间的代谢反应,这种状态下循环酮体水平升高。
注:酮体是脂肪酸衍生的分子,当葡萄糖可用性受限时作为替代能量来源。这些酮体(KBs)包括β-羟基丁酸(βHB)、乙酰乙酸和丙酮,主要在肝脏中产生。
生酮饮食长期以来一直作为治疗癫痫的饮食疗法,并且越来越多的研究表明这种饮食在治疗阿尔茨海默症、肥胖症、癌症等各种疾病方面的益处。
注:传统的长链甘油三酯生酮饮食遵循脂肪(克)与蛋白质和碳水化合物总和的4:1比例。变体包括中链甘油三酯生酮饮食、改良阿特金斯饮食和低血糖指数治疗,每种方法都有稍微不同的宏观营养素比例。
在人类中,诱导生酮状态需要严格限制碳水化合物摄入(5%–10%千卡/天),适量蛋白质摄入(30%–35%),和高脂肪摄入(55%–60%)。
生酮饮食的潜在风险和副作用
生酮饮食(利于拟杆菌门) ≠ 高脂饮食(利于厚壁菌门)
典型的高脂饮食通常会增加厚壁菌门的丰度并减少拟杆菌门;然而,生酮饮食的效果不同。
——超重成年人
在涉及17名超重成年人的研究中,为期4周的生酮饮食显示在人肠道中放线菌门(Actinobacteria)和厚壁菌门的大量减少。具体来说,有益的双歧杆菌的19种物种减少了,而拟杆菌门丰度增加。这些变化部分是通过宿主产生酮体诱导的。
——癫痫儿童
在涉及12名严重癫痫儿童的为期3个月的研究中,遵循生酮饮食的儿童显示健康促进和消耗纤维的双歧杆菌属、直肠真杆菌(E. rectale)和Dialister属的丰度大幅减少。相反,儿童显示拟杆菌属和大肠杆菌属的丰度增加,后者部分归因于大肠杆菌(Escherichia coli)的增加。
生酮饮食对肠道微生物组的影响
临床前研究也表明,肠道微生物组的组成在响应生酮饮食时发生了显著变化,最明显的是:
酮体βHB↑ 双歧杆菌↓
一项分析生酮饮食对肠道微生物组组成的变化的潜在机制的研究报告了在人类和鼠类受试者中,双歧杆菌属和酮体β-羟基丁酸(βHB)之间的显著负相关,也就是说,随着βHB水平的增加,双歧杆菌属的水平会降低。
来自人类、啮齿动物和细胞培养的数据支持β-羟基丁酸抑制NLRP3炎症体的能力。高水平的酮体可以降低血压并增加血管功能。循环酮体水平的增加还可以减少心脏炎症和心力衰竭的可能性。酮体也可能通过刺激胰岛素受体,通过诱导AMP激活蛋白激酶(AMPK)和下调mTOR来改善胰岛素敏感性。高水平的酮体可能减少食欲,从而使体重减轻。
生酮饮食→双歧杆菌↓→减少诱导Th17→促炎降低
将生酮饮食者的粪便微生物群移植到无菌小鼠中,研究揭示了肠道TH17细胞的变化。
注:Th17细胞是一种辅助性T细胞亚群,其主要特征是能够产生多种促炎细胞因子,如IL-17、IL-21和IL-22等。
双歧杆菌属对肠道TH17细胞的有强烈诱导作用,而生酮饮食改变肠道菌群(双歧杆菌降低)也减少了诱导Th17的能力,可能导致这些细胞的促炎性降低,从而影响肠道和脂肪组织的炎症状态,
然而,由于有益的肠道微生物群的减少和促炎性及病原性肠道细菌的促进,需要进一步的研究来了解生酮饮食对宿主健康的长期影响。
西方饮食的特点是高热量含量,富含动物蛋白、饱和脂肪、简单糖和超加工食品,同时纤维、水果和蔬菜的摄入量不足。
西方饮食:多样性下降,拟杆菌为主
与其他饮食相比,西方饮食与肠道微生物组多样性的显著降低有关,其肠道特征转向以拟杆菌属为主的肠道特征。其他丰富的物种属于Ruminococcus、Faecalibacterium、双歧杆菌属、Alistipes、Blautia、Bilophila。
由于纤维摄入较少和不同的微生物组成,相关的微生物群产生的短链脂肪酸较少。
红肉中胆碱→TMAO→多种慢病相关
红肉中的特定化合物,如胆碱和肉碱,也可以被肠道微生物群转化为三甲胺,然后在肝脏中转化为与慢性疾病相关的三甲胺-N-氧化物(TMAO)。
加工食品和添加剂的影响
加工食品包含各种添加剂、防腐剂和乳化剂,能够直接或间接与肠道微生物群相互作用。
非营养性人造甜味剂,如低热量或饮食食品和饮料中的糖精、三氯蔗糖和阿斯巴甜,对微生物组多样性和组成的潜在长期影响尚不清楚。
其他添加剂,如卡拉胶(一种从红海藻中提取的增稠剂或凝胶剂,存在于许多加工食品中,如乳制品),已知会促进肠道炎症和破坏粘液层,导致肠道微生物组的变化。
人工食品色素,如糖果和烘焙产品中的Allura Red AC,赋予颜色并通过与肠道细菌的相互作用改变硫的稳态。
一些防腐剂,如加工肉类中的硝酸钠,也可以调节肠道微生物组的组成,而乳化剂,如羧甲基纤维素(一种存在于酱汁中的增稠剂)和聚山梨醇酯-80(一种存在于酱汁和烘焙食品中的乳化剂和稳定剂),直接冲击肠道微生物组的组成和功能。
详见我们之前的文章:
你的焦虑可能与食品添加剂有关,警惕食品添加剂引起的微生物群变化
糖,功能糖,代糖,如何从健康角度看这些肠道菌群的“甜蜜伙伴”
总体而言,西方饮食与慢性炎症的激增有关,导致与饮食相关的疾病,包括肥胖和其他非传染性疾病。
过去50年中,一种受到极大关注的饮食疗法是日常热量限制(CR),它被定义为在保持充足营养的同时,将饮食摄入量减少至低于维持体重所需的能量水平。观察性、临床前和临床试验的发现表明,CR可能将寿命延长1-5年,同时改善生活质量。
最严格的CR随机试验来自国家老龄化研究所资助的CALERIE(减少能量摄入长期效应综合评估)联盟。CALERIE研究包括CALERIE第一阶段(三项为期6至12个月的CR小规模试点研究)和CALERIE第二阶段(一项大型、多中心、为期2年的CR随机试验)。
注:这些研究招募了体重正常且健康状况良好的成年人。每项试验中实施的CR程度不同,但通常涉及日常能量摄入量减少10%至30%,同时确保其他关键营养素的充足摄入。
CR的健康益处
CALERIE研究的发现显示,短期和长期CR都可以减少体重、皮下脂肪、内脏脂肪和肝内脂肪含量。
CR减少了微生物表达的酶
这些酶能够使脂多糖A生物合成,从而限制了脂多糖(LPS)的产生,并以药理学上已知能刺激脂肪细胞褐化和减少内脏脂肪的方式抑制了LPS-TLR4途径。
将经过CR调节的与对照肠道微生物群移植到未经处理的无菌小鼠中,导致体重和体脂肪的增加减少,胰岛素敏感性提高,UCP1+(即褐/产热)脂肪细胞增加,这表明CR诱导的肠道微生物组变化在这些效应中起到了因果作用。
Dorea弱预测了CR诱导的体重减轻
人类的CR研究报道了肠道微生物组组成和功能的多种变化,但据所知,还没有研究表明这些变化是代谢益处的基础。
最近一项随机对照试验比较了147名超重或肥胖成年人中12周间歇性与持续性CR的效果,发现体重减轻与细菌相对丰度、群落α多样性或循环微生物代谢产物(例如短链脂肪酸)的变化之间没有关联。尽管如此,基线微生物组组成——特别是Dorea的相对丰度——弱预测了CR诱导的体重减轻。
超重人群日常热量限制后相关菌群变化
同样,一项涉及80名超重或肥胖成年人进行14周CR的前瞻性研究发现,体重减轻5%或以上与Collinsella和Christensenellaceae的丰度正相关,与大肠杆菌/志贺菌属、克雷伯菌属、巨球形菌属(Megasphaera)、Sellimonas、乳杆菌属的丰度负相关。
微生物组特征与特定代谢健康标志物之间的关联
如Akkermansia和Christensenellaceae与基于HOMA-IR的胰岛素敏感性之间的关系。需要额外的功能研究来测试这些微生物组特征与代谢反应之间的联系是因果关系还是其他生理状态的共线性结果。
解决开始和维持饮食模式重大转变挑战的一个潜在解决方案来自于一组数据,即间歇性禁食可以导致显著的体重减轻。
最常见的间歇性禁食形式是时间限制性进食(TRE),它涉及将进食窗口限制在4-10小时内,并在一天剩余的14-20小时内禁食。
TRE的做法
在进食窗口期间,个人不需要计算卡路里或以任何方式监测食物摄入,这种简单性可能解释了近期TRE受欢迎度的上升。在禁食窗口期间,个人被鼓励大量饮水,也可以消费无能量饮料,如不加添加剂的茶和咖啡。当肥胖成年人将进食窗口限制在每天4-10小时时,他们通常会将能量摄入减少200-550千卡/天,这种能量限制程度与日常CR(热量限制)相当。
TRE的减重效果
随机对照试验显示,TRE在降低体重和改善一些心血管健康标志物方面是有效的。体重通常在2-12个月的TRE后减少3%-5%,减少主要来自脂肪质量和内脏脂肪质量的减少,而不是瘦体重。
然而,并非所有关于人类TRE的研究都报告了体重减轻。有研究表明,3个月的8小时TRE(下午12点至晚上8点的进食窗口)对肥胖成年人的体重与无干预对照组相比没有影响。
注:然而,这项研究是在自由生活的参与者中进行的,他们在试验期间与研究团队的接触很少。
当进食窗口较早时,降血压效果才较为明显
即使实现了减重,也不是所有受试者都表现出代谢改善。血压通常在2-12个月的TRE后降低5-10毫米汞柱,但这些效果通常只有在进食窗口设在一天中较早的时候(即下午2点前)才会被注意到。早期进食窗口可能通过促进钠尿(通过肾脏在尿液中排泄钠)来降低血压,因为当盐分摄入转移到一天中较早的时候,由昼夜节律系统调节的钠排泄会增加。TRE似乎并不影响低密度脂蛋白胆固醇、高密度脂蛋白胆固醇或甘油三酯水平。循环炎症标志物,如C反应蛋白(CRP)、白细胞介素-6(IL-6)和肿瘤坏死因子-α(TNF-α),也不受TRE影响,尽管数据有限。
TRE改善血糖效果明显(早点吃,进食时间短)
临床试验发现,TRE在改善前驱糖尿病和肥胖个体的空腹胰岛素和胰岛素敏感性方面表现出相当一致的效果。TRE还改善了葡萄糖耐受性并减少了血清葡萄糖波动。这些改善更常见于早期进食窗口(即在下午3点前吃完所有食物)和较短的进食窗口(4-6小时)。
在2型糖尿病成人中,TRE改善了糖化血红蛋白水平,与每日CR相当,并且没有增加低血糖的风险。
TRE如何改善糖调节?
来自人类试验的数据显示,身体在TRE期间经历了代谢转换。
肠道微生物群发挥作用
在小鼠中,时间限制性喂养(TRF)通过恢复肠道细菌相对丰度的昼夜变化,减轻高脂高糖(HFHS)饮食的影响。
这些变化在远端小肠(回肠)最为明显,并与促胰高血糖素基因Gcg的表达增加和GLP-1的血浆水平升高相对应。
经抗生素处理和无菌小鼠的研究支持肠道微生物群在昼夜GLP-1释放中发挥因果作用,但具体的微生物效应因子仍不清楚。
一个概念验证来自于肠道共生菌Akkermansia muciniphila的研究,它分泌一种84kDa的蛋白质(P9),足以通过与细胞间粘附分子2(ICAM-2)相互作用诱导GLP-1的分泌。
需要更多的工作来理解参与TRE的糖调节和其他有益效应的微生物群的全范围,以及它们的临床相关性。
TREplus版:肠道菌群变化更显著
值得注意的是,最近的一项临床研究比较了CR与能量匹配的TRE加蛋白质plus(定义为每天四次均匀间隔的餐食;TRE-P)方案在超重或肥胖成年人中的效果,发现TRE-P与肠道微生物组组成的更显著变化相关,包括之前与减重和蛋白质消费有关的类群的丰富,如Christensenellaceae。此外,在TRE-P干预期间,体重减轻高与低的参与者之间观察到肠道微生物组组成和功能能力的差异,但这些微生物组变化是否对TRE-P诱导的代谢改善有因果贡献仍不清楚。
母乳是大量生物活性化合物的来源,包括人乳寡糖(HMOs)、免疫球蛋白G(IgGs)、免疫细胞和微小RNA(miRNA),其中一些可以影响婴儿的肠道微生物群。与配方奶相比,母乳喂养会导致粪便钙保护素和β-防御素2等炎症标志物水平更高,这反映了随着促炎血清细胞因子减少,免疫成熟的过程。
双歧杆菌和拟杆菌利用HMOs,因此占主导地位
HMOs被双歧杆菌属(包括Bifidobacterium breve、Bifidobacterium bifidum、B. longum、B. infantis、Bifidobacterium pseudocatenulatum)以及拟杆菌属物种利用,导致这些物种在母乳喂养的婴儿肠道中占主导地位。
这可能会改变宿主中微生物与代谢产物之间的关系,如降低的肌苷水平与长双歧杆菌丰度增加之间的相关性所证明的,这表明其可能在婴儿的免疫和神经发育中发挥作用。
HMOs作为益生元发挥作用
乳铁蛋白和溶菌酶具有抗菌特性,能够调节对感染的保护。
肠道中由HMO利用形成的SCFAs被宿主用作能量来源。
非母乳喂养的肠道菌群
非纯母乳喂养的配方奶喂养婴儿拥有更高丰度的链球菌属、肠球菌属、韦荣球菌、梭菌属,并表现出在更多碳水化合物代谢途径上的功能能力差异,这证明了饮食对肠道微生物组的重要性。
较短的母乳喂养时间,菌群多样化
较短的母乳喂养持续时间与早期生活中高度多样化且类似成人的微生物组成相关联。
母乳中的HMOs调节婴儿肠道微生物群,并提供若干健康益处,如长期保护免受过敏、特应性皮炎和肥胖的影响,以及增强肠道屏障功能。同样,引入辅食会导致肠道微生物群的变化,这些变化促进了碳水化合物的利用、维生素的合成和外源性物质的降解,结果是厚壁菌门和拟杆菌门中的微生物水平增加。
最近的研究报道,涉及脂肪和糖摄入的孕妇饮食干预改变了婴儿肠道微生物组的功能,而另一项研究则报告没有关联。
小鼠实验:母亲孕期低纤维饮食,幼鼠呼吸感染的严重程度增强
最近的研究显示,在怀孕期间接受低纤维饮食的小鼠在后代中经历了延迟的浆细胞样树突状细胞和调节性T细胞扩增的扰动,导致呼吸感染的严重程度增强。同样,在无纤维饮食的小鼠中,幼崽中的比例较低的Akkermansia muciniphila、固有淋巴细胞和TH17细胞,而缺乏AKK菌属且被喂食纤维的小鼠显示出减少的固有和适应性RORγt‐阳性免疫细胞亚群。
小鼠实验:富含发酵食品,减少新生儿结肠炎症
另一项在母猪和小鼠上进行的研究表明,富含发酵食品的母亲饮食影响了新生儿肠道微生物群的发展,并通过p38丝裂原激活蛋白激酶和c-Jun氨基末端激酶激活的caspase 3的磷酸化减少了结肠炎症。母亲饮食对婴儿长期健康影响的程度需要进一步研究。
肠道微生物群在调节宿主代谢方面发挥着关键作用,微生物组成的某些变化和多样性的减少与多种代谢性疾病发病率的上升有关。
肥胖与肠道菌群有关
利用无菌啮齿动物模型,研究人员已经建立了肠道微生物群与肥胖之间的联系。将肥胖小鼠的肠道微生物群定植到无菌小鼠体内,导致体重和胰岛素抵抗显著增加,而当无菌小鼠被喂食西式饮食时,肥胖的发展则不存在,这突显了肠道微生物群在肥胖中的作用。然而,其他几项同意微生物群在能量稳态中的作用的研究未能显示其在肥胖发展中的决定性作用,并指出需要更多的研究来探索这种复杂的关系。
2型糖尿病和肥胖的个体的肠道菌群特征
患有2型糖尿病和肥胖的个体通常表现出产丁酸菌减少,乙酸盐及促炎物种增加,这些与胰岛素抵抗性升高有关。在肥胖小鼠上进行的研究支持肠道微生物群在2型糖尿病中的作用。双歧杆菌属、拟杆菌属、Faecalibacterium、Akkermansia与2型糖尿病负相关,其中双歧杆菌增加了胰高血糖素样肽-2(GLP-2)的水平,从而改善肠道通透性并减少代谢性内毒素血症。
注:二甲双胍,一种常见的2型糖尿病药物,与肠道微生物群相互作用,可能通过调节葡萄糖稳态和短链脂肪酸的产生来介导其抗糖尿病效应。
饮食、肠道微生物组、代谢性疾病
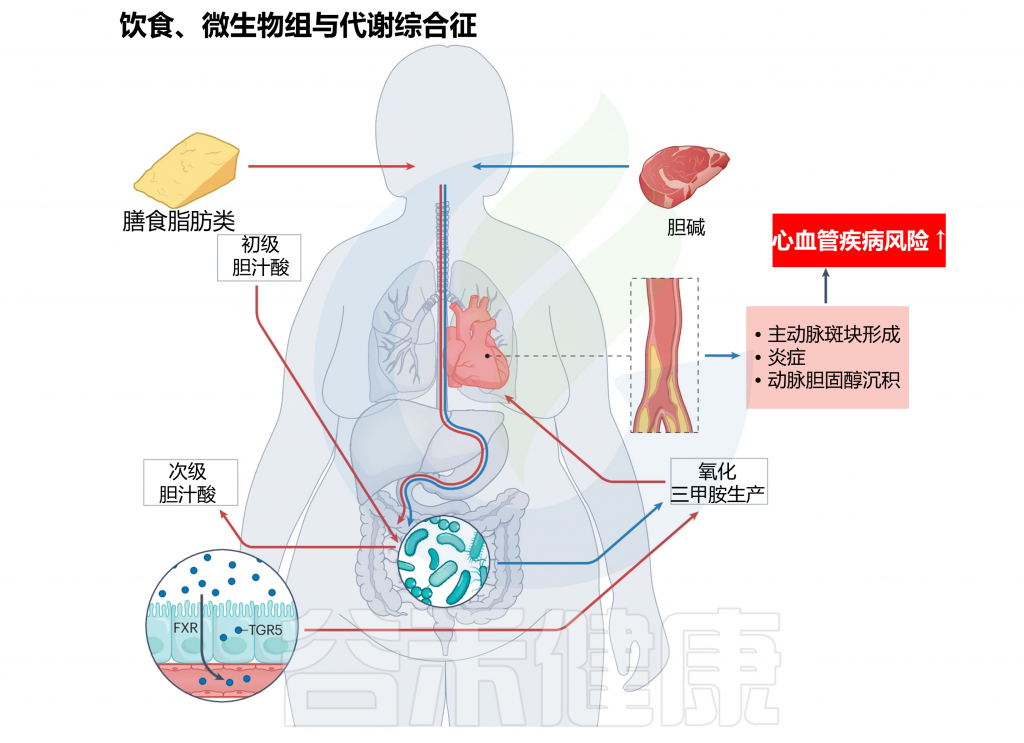
doi.org/10.1038/s41579-024-01068-4
注:红色箭头表示饮食脂肪可以通过何种作用机制对宿主健康产生下游影响,最终导致CVD风险。此外,蓝色箭头显示了主要存在于动物产品中的胆碱如何引起CVD风险。
心血管代谢疾病的个体的肠道菌群变化
特征是增加的肠杆菌科(Enterobacteriaceae)物种和减少的拟杆菌属以及抗炎的F. prausnitzii。肠道微生物群的这些变化与更具炎症性和较少发酵性的肠道环境有关。
TMAO
三甲胺-N-氧化物(TMAO),一种由肠道细菌从饮食化合物产生的代谢产物,与动脉硬化、血小板聚集和血栓形成有关。
在小鼠和人类的研究表明,饮食因素影响TMAO水平,某些情况下抗生素降低了TMAO,而杂食饮食增加了它。TMAO水平升高与心力衰竭患者的高死亡率相关。然而,结果并不一致,一些研究表明某些饮食成分如左旋肉碱和富含TMAO的食物可能有助于预防动脉粥样硬化,这引发了关于饮食、微生物组和宿主遗传学在动脉粥样硬化发展中复杂相互作用的问题。
增加的饮食脂肪可以影响FXR和TGR5等胆汁酸受体的激活,它们在脂质和葡萄糖代谢中发挥重要作用。这些途径的调节失常可能导致心血管疾病的发展。
由于微生物组改变导致的能量稳态的微小变化可能具有长期效应,在代谢性疾病中发挥作用,既是因果因素也是促成因素。此外,它们可以作为使用微生物组靶向治疗改善这些状况的目标。
饮食在肠道疾病的病理生理学中起着关键作用,特别是炎症性肠病、肠易激综合症和结肠癌。
肠易激综合征
过敏、食物不耐受、微生物群组成的转变、轻度粘膜炎症和肠道通透性的增加可能促成了肠易激综合症的表现。
研究发现,类似于病原性肠易激综合症的人类微生物组表现出拟杆菌门的丰度减少,以及厚壁菌门和与氨基酸及碳水化合物代谢相关的基因丰度增加。
饮食成分与炎症性肠病风险
饮食也可以改变炎症性肠病(包括克罗恩病和溃疡性结肠炎)的肠道微生物群落组成,影响短链脂肪酸和纤维等物质的代谢,这反过来又可能促成疾病的发生。
动物蛋白、乳制品、碳水化合物和多不饱和脂肪酸等食物成分与发生炎症性肠病的风险有关。
动物蛋白与炎症性肠病的机制
一个将炎症性肠病与动物蛋白联系起来的机制涉及小肠中的氨基酸和血红素吸收不良,导致产生酚类和氢气等有害副产物。这通过抑制丁酸盐的产生和减少肠道屏障中的二硫键,促成了炎症性肠病的发病机制。
高脂肪饮食也与炎症性肠病强烈相关
在实验模型中,高脂肪饮食可以破坏肠细胞间的结合蛋白功能,从而改变粘液层的组成和肠道微生物群。
持续且控制不当的炎症性肠病,以及由于不良饮食模式(如西方饮食)导致的慢性胃肠道炎症,是影响结肠炎相关结直肠癌风险的主要外部因素。这些因素影响免疫反应、肠道组织平衡和肠道微生物组。
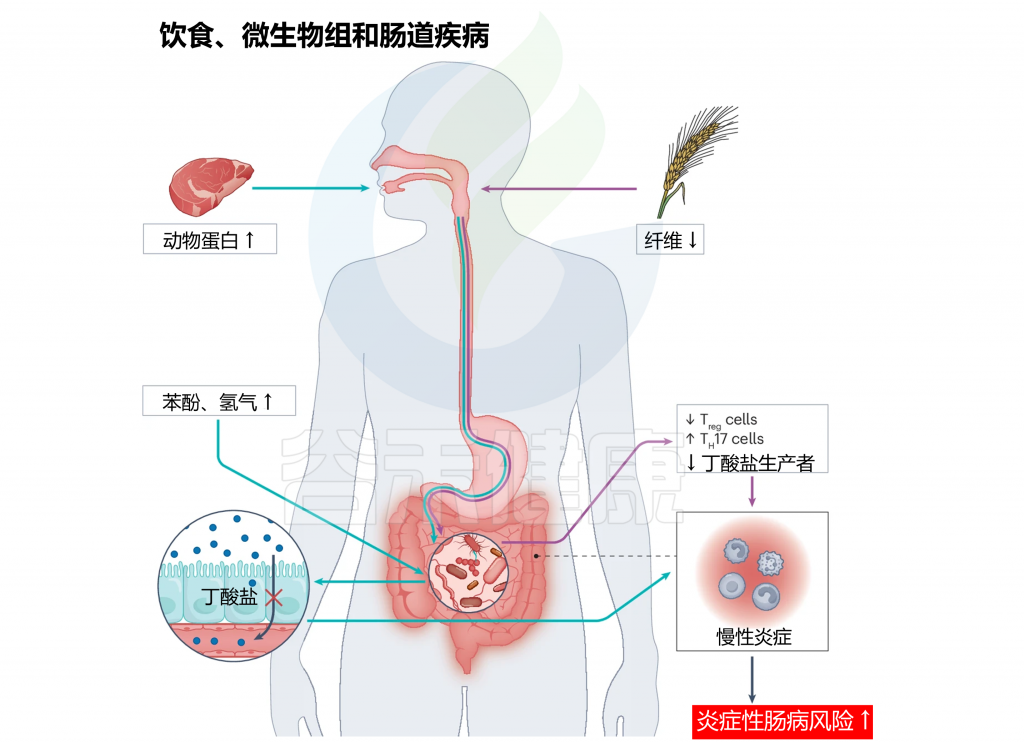
doi.org/10.1038/s41579-024-01068-4
注:增加的动物蛋白(绿色箭头)和低纤维(紫色箭头)饮食可能对生理功能和宿主健康产生下游影响。
增加红肉消费可导致胆碱水平升高,由于血红素吸收不良,在小肠中产生更多的氢气和苯酚。这反过来可以减少胃肠道中的丁酸盐生产,导致炎症增加。同样,饮食中纤维摄入减少可能通过增加TH17的产生,同时减少Treg和短链脂肪酸产生,对肠道健康产生负面影响。这种不平衡最终导致胃肠道内慢性炎症加剧。肠道内长期的慢性炎症可能大幅增加发展成炎症性肠病的风险。
饮食在散发性结直肠癌中的作用
研究发现,低纤维、高脂肪饮食与Fusobacterium nucleatum有关。拟杆菌属通过激活E-钙粘蛋白-β-链球蛋白信号、表观遗传变化和改变肿瘤微环境等机制与结直肠癌有关,从而促进恶性转变。同样,诸如产毒脆弱拟杆菌(Bacteroides fragilis)等致癌细菌被假设通过直接与结肠上皮细胞相互作用和改变局部微生物群组成来触发结直肠癌的发病。
人类肠道是真菌和病毒群的栖息地,分别称为肠道真菌组和病毒组。尽管这些群落只占肠道中总微生物的0.1%-1%,但它们都受到饮食的影响。
婴儿肠道真菌组中,酿酒酵母(Saccharomyces cerevisiae)是优势物种,断奶后被其他酵母属(丝孢酵母属Cystofilobasidium、曲霉属Ascomycota、单孢子酵母属Monographella)取代。
城市居民的肠道真菌组成包括酿酒酵母和较少的产短链脂肪酸菌,农村居民则有更多样化的真菌物种。
念珠菌属(Candida species)与富含碳水化合物的饮食相关,与富含蛋白质的饮食负相关。
母乳喂养和配方奶喂养婴儿的肠道病毒组组成差异由肠道微生物群变化和母乳垂直传递病毒引起。
高脂饮食与Siphoviridae病毒丰度减少和Microviridae噬菌体丰度增加有关。
无麸质饮食则与相反的变化有关,Siphoviridae在Microviridae之上,占主导地位。
肥胖和1型及2型糖尿病患者的病毒组成也发生变化,高脂饮食喂养小鼠的粪便病毒移植降低肥胖风险。
肠道耐药组,赋予微生物抗微生物药物耐药性的所有基因或遗传物质的集合,随着细菌微生物组和病毒组的变化而变化。
一些研究报告γ-变形菌纲(Gammaproteobacteria)属拥有丰富的抗生素抗性基因(ARG)储备。
配方奶喂养的婴儿ARG负荷更高,与细菌组成有关。
纯素和鱼素食饮食个体肠道中的微生物组成不同,但他们的耐药组档案并没有显著差异,表明耐药组主要由抗微生物药物暴露而非饮食塑造,可能的例外是含有特定防腐剂的食物。
需要进行详细的饮食干预研究,以了解饮食是否可以减少ARG的负担。
地中海饮食在缓解和管理多种疾病方面已被证明是有效的,包括心血管疾病、2型糖尿病、炎症性肠病、肠易激综合症、认知能力下降和抑郁症。此外,对这种饮食的调整,如MIND饮食,已成功降低阿尔茨海默病的风险并减缓认知能力下降。同样,DASH(阻止高血压的饮食方法)饮食已证明在治疗高血压方面有效。
特定的碳水化合物饮食在临床实践中用于治疗炎症性肠病的症状。特定的碳水化合物饮食在儿童和成人队列中已证明其有效性,并已与改善的临床参数和炎症标志物相关联。然而,使用这种饮食时必须保持营养控制,以避免营养不足和体重下降。
对于肠易激综合症的治疗,通常使用低发酵性低聚糖、二糖、单糖和多元醇(低FODMAP)饮食,有50%~80%的患者有积极的临床反应。
在41名患者中进行的为期四周的低FODMAP饮食研究显示,从类似病原性肠易激综合症的肠道微生物组向健康相关的肠道微生物组发生了组成和功能上的转变。
同样,研究表明,坚持低FODMAP饮食,双歧杆菌(Bifidobacterium adolescentis)方面表现出显著降低,这种细菌会破坏肠道屏障功能并改变紧密连接的完整性,从而支持低FODMAP饮食的积极效应是通过肠道微生物群介导的假设。
无麸质饮食目前是治疗乳糜泻的方法,研究已证实这种饮食在缓解胃肠道症状方面的有效性。采用这种饮食方案与肠道微生物组成和肠道微生物途径的改变有关。
最近一项研究分析了乳糜泻患者的小RNA和宏基因组测序数据,研究结果显示,采用无麸质饮食改变了miRNA和微生物群落的轮廓。该研究还揭示了乳糜泻患者中的miRNA-细菌关系和特定的分子模式,表明可能存在用于监测无麸质饮食依从性和评估肠道炎症状态的生物标志物。
对于慢性肾病的管理,推荐采用低蛋白饮食,目的是减缓进入终末期肾病的进展,并推迟对肾脏替代治疗的需求。
综述表明,极低蛋白饮食可能有效减少4期或5期肾病的发生。然而,仅采用低蛋白饮食并未影响终末期肾病的发展。
此外,五篇文章的系统综述和元分析发现,低蛋白饮食增加了拟杆菌科、乳酸菌科、咽峡链球菌Streptococcus anginosus的丰度,同时减少了Roseburia faecis和Bacteroides eggerthii的丰度。但是,在没有微生物多样性和丰富度的整体构成变化的情况下,这些主要在物种和科水平上的变化似乎不足以影响代谢或临床结果。
用于管理2型糖尿病的血糖指数饮食,因其对肠道微生物群的影响及其在影响疾病发展和严重程度方面的潜在作用而受到关注。
这种饮食包括消耗低血糖指数的碳水化合物(例如,豆类、燕麦和小麦),促进血糖水平逐渐且持续上升。尽管关于这种饮食对肠道微生物群影响的研究有限,但小鼠研究表明,它与因摄入大麦而增加的乳酸杆菌属、普雷沃特氏菌属和纤维降解S24-7细菌的丰度有关,或因摄入全谷物燕麦而增加的双歧杆菌属和乳酸杆菌-肠球菌属(Lactobacillus-Enterococcus)有关。
肠道微生物组在人体生理学中的中心作用彻底改变了我们对健康的看法,并日益渗透到营养研究和建议中。
目前,全球饮食指南普遍达成共识,但不幸的是,这种均质性也延伸到了微生物组,只有少数几个国家(例如美国和南非)明确考虑了饮食-微生物组相互作用。
很多文章已经讨论了肠道微生物组知识如何与当前的营养指南相结合,为包含微生物组的精准营养提供了机会,并广泛考虑了将微生物组科学纳入研究、教育、政策和公共卫生沟通的更广泛问题。
几乎所有方面的人类营养最终都需要根据饮食-微生物组相互作用对人类健康的直接和间接后果重新评估。
这里强调微生物组知识挑战营养科学的三个原则:
宿主卡路里≠宿主-微生物组卡路里
由美国化学家威尔伯·奥林·阿特沃特(Wilbur Olin Atwater)在19世纪末提出的阿特沃特系统,用于估算食物中各种营养成分的热量值,反映了食物中的平均化学能量减去粪便、尿液、分泌物和气体中排泄的平均分数。
阿特沃特系统估算热量含量的方法存在三个关键疏漏:
1、食物基质效应
没有捕捉到更广泛食物基质的效果,如植物性宏观营养素在细胞壁或亚细胞结构中的封装。
2、饮食诱导的热生成
没有捕捉到消化的代谢成本,这基于宏观营养素含量、餐食的可口性和食物加工而变化。
3、宿主与微生物组的卡路里区分
只在很小程度上区分了对人类可利用的卡路里和对肠道微生物组可利用的卡路里。
营养学领域长期以来一直合理地关注那些被吸收进入人体组织的饮食成分,因为这些成分有潜力直接影响健康。然而,大量证据表明肠道微生物组对饮食消化性很敏感,并且饮食引起的肠道微生物组的变化可以在不同情况下因果地塑造宿主的健康和疾病,这日益凸显了未吸收营养素的重要性。
未吸收营养素的重要性
与被吸收的营养素不同,未吸收的营养素可靠地到达结肠中最密集的微生物群落。此外,随着消化液在胃肠道内向下推进,未吸收的营养素会因为被吸收的营养素和水分的消失而浓缩。因此,可以预期,未吸收的营养素在塑造肠道微生物组及其对健康和疾病的下游影响方面,可能比被吸收的营养素具有更大的影响力。
饮食与肠道微生物组的相互作用
目前研究主要关注食物入口时的状态,而未充分考虑小肠末端的消化残余物。
虽然历史上对回肠消化性的描述依赖于体外模型或复杂的体内模型,例如插管动物、回肠造口术后的人类患者、健康人体中的侵入性鼻-回肠或结肠插管,以及在血浆中检测同位素标记的营养素,但受微生物组启发的新方法可能证明是有希望的。
深入理解饮食-微生物组相互作用的新视角
例如,基于DNA的饮食底物表征——一种称为DNA metabarcoding的技术,可能与基于DNA的微生物组分析相结合,研究特定排泄样本中直接的饮食-微生物组相互作用。可以在动物模型中或使用新的可吞咽装置在人体中执行对饮食和微生物组信号的双重表征,这些装置能够在由pH变化确定的胃肠道间隔处采样消化液。
许多食品物质已根据美国食品药品监督管理局(FDA)基于动物毒理学试验和/或过去在人类中广泛使用且未产生已知有害影响的基础上,被授予“通常认为安全”(GRAS)的认定。
潜在健康影响
然而,GRAS评估通常并未考虑这些物质对肠道微生物组的影响,或者通过微生物组介导的间接健康效应的潜力。
专注于宿主组织的危险通过发现乳化剂如卵磷脂和人造甜味剂如糖精等GRAS物质在饮食相关水平下可能通过影响肠道微生物组诱导肥胖和胰岛素抵抗的情况得到了说明。
牛磺胆酸可能通过菌群与肠道病理的关联
GRAS化合物牛磺胆酸及其化学成分,GRAS化合物牛磺酸和胆酸,可能与肠道微生物组相互作用,促进肠道病理。具体来说,由Bilophila wadsworthia细菌在牛磺胆酸的脱结合过程中释放的牛磺酸产生遗传毒性的硫化氢,同时释放的胆酸作为微生物产生促炎的次级胆汁酸脱氧胆酸的基质。因此,补充牛磺胆酸的饮食导致了B. wadsworthia的增长和易感基因型(IL-10−/−)小鼠中结肠炎的发展。
肠道微生物组可能转化为更有害的形式:杂环胺的肠肝循环
此外,肠道微生物组可能使用其广泛的酶库将饮食化合物或宿主代谢产物转化为更具有害的形式。例如,细菌β-葡萄糖醛酸酶有助于致癌的杂环胺(如IQ,2-氨基-3-甲基咪唑[4,5-F]喹啉)的肠肝循环,这些物质通过肝脏的葡萄糖醛酸化被解毒。
在暴露于IQ时,常规小鼠比无菌小鼠显示出更多的DNA加合物和DNA损伤。单核子大肠杆菌携带功能性与非功能性uidA基因(编码β-葡萄糖醛酸酶)的大鼠表现出增加的结肠遗传毒性,与这种化合物排泄的多个峰值相结合,这与肠肝循环一致。
三聚氰胺污染+肠道微生物组→肾脏病理
肠道微生物组还与由饮食污染物三聚氰胺引起的肾脏病理有关,三聚氰胺是一种用于许多食品制备工具的塑料添加剂。体外和体内实验表明,存在于一些婴儿肠道中的克雷伯菌可以将三聚氰胺转化为三聚氰酸,三聚氰酸现在已知与三聚氰胺形成不溶性的肾脏聚集体。
有益效应
另一方面,肠道微生物组对未吸收的饮食化合物的生物转化可能有助于有益效应,这些效应如果只关注饮食对宿主的直接影响则可能被忽视。
对抗乳腺癌的保护作用
例如,植物衍生的饮食木脂素(如全谷物、种子、豆类和坚果中发现的)的肠道微生物生物转化被认为是它们对抗乳腺癌的保护作用的基础。一组肠道细菌类群(例如,Eggerthella lenta、Blautia producta、Gordonibacter pamelaeae和Lactonifactor longoviformis)将饮食木脂素松香转化为具有抗癌作用的雌激素模拟物enterodiol和enterolactone。
因此,与无菌动物相比,在化学诱导乳腺癌时,能够从饮食木脂素前体产生enterodiol和enterolactone的细菌群落定植的无菌大鼠显示出较少的肿瘤数量和较小的肿瘤大小。
扩展阅读:
肠道菌群有助于饮食解毒改变疾病风险
例如,肠道细菌Oxalobacter formigenes参与草酸盐的分解,草酸盐是一种螯合饮食毒素,通过结合游离金属阳离子,有助于肾结石和肾衰竭。缺乏O. formigenes与高草酸尿症的风险增加有关,其在大鼠中的施用以剂量依赖性的方式减少了饮食诱导的高草酸尿症。
在探索肠道微生物群与饮食之间错综复杂的关系后,我们不难发现,这个微小的生态系统对我们的健康有着深远的影响。从调节能量平衡到影响免疫功能,从塑造情绪到预防疾病,肠道微生物群的作用远远超出了我们的想象。
当然,饮食也只是众多生活方式因素之一,例如身体活动、环境暴露和睡眠,这些因素都会影响宿主的能量平衡和肠道微生物群。此外,药物的广泛使用已经显著改变了饮食干预的背景。例如,GLP-1 激动剂延迟胃排空,这对消化有着深远的影响,包括肠道微生物代谢可用底物的变化。
即使仅考虑饮食,现在也非常清楚,肠道微生物影响宿主代谢的多种途径,加上关键的饮食和微生物组相关代谢物(如短链脂肪酸、次级胆汁酸等)的多效性作用,使预测特定饮食或微生物组特征的代谢影响变得复杂。
实现基于微生物组的精准营养方法需要对人类进行实验研究,以测量整个生物体水平的综合影响,涵盖地理、性别、种族和年龄等各种因素,以及更大规模的横断面研究,针对饮食成分、肠道微生物组结构和功能以及宿主健康之间的特定联系。
这些数据将受益于机器学习的快速发展并将人工智能与实施精准医疗方面的结合起来。随着技术的进步和数据的积累,肠道菌群检测有望成为精准营养和个性化医疗的重要组成部分,帮助我们更好地管理健康,预防疾病,并提升生活质量。
主要参考文献
Carmody RN, Varady K, Turnbaugh PJ. Digesting the complex metabolic effects of diet on the host and microbiome. Cell. 2024 Jul 25;187(15):3857-3876.
Ross FC, Patangia D, Grimaud G, Lavelle A, Dempsey EM, Ross RP, Stanton C. The interplay between diet and the gut microbiome: implications for health and disease. Nat Rev Microbiol. 2024 Jul 15.
Ahmad S, Moorthy MV, Lee IM, Ridker PM, Manson JE, Buring JE, Demler OV, Mora S. Mediterranean Diet Adherence and Risk of All-Cause Mortality in Women. JAMA Netw Open. 2024 May 1;7(5):e2414322.
McEvoy CT, Jennings A, Steves CJ, Macgregor A, Spector T, Cassidy A. Diet patterns and cognitive performance in a UK Female Twin Registry (TwinsUK). Alzheimers Res Ther. 2024 Jan 23;16(1):17.
Link VM, Subramanian P, Cheung F, Han KL, Stacy A, Chi L, Sellers BA, Koroleva G, Courville AB, Mistry S, Burns A, Apps R, Hall KD, Belkaid Y. Differential peripheral immune signatures elicited by vegan versus ketogenic diets in humans. Nat Med. 2024 Feb;30(2):560-572.
Staudacher HM, Mahoney S, Canale K, Opie RS, Loughman A, So D, Beswick L, Hair C, Jacka FN. Clinical trial: A Mediterranean diet is feasible and improves gastrointestinal and psychological symptoms in irritable bowel syndrome. Aliment Pharmacol Ther. 2024 Feb;59(4):492-503.
谷禾健康

肠道微生物群之间编织了一个复杂的相互作用网络,影响人体的营养吸收和代谢,免疫功能等,对我们的健康状态有很大的影响。
我们知道,肠道微生物群具有多样性,平衡性,稳定性等特征,但同时也具有异质性,也就是说不同个体之间存在差异。不同人群对食物,膳食补充剂的健康需求不同。
特定的营养素、食物、整体饮食结构等诸多因素都会影响特定的肠道菌群,从而影响整体健康。
随着当前研究技术的不断进步,我们对肠道菌群和健康之间的关系认知不再停留在初级关联阶段,而是逐步走向精细化调节层面。
怎样通过这些看起来日常的饮食,益生菌补充剂等方式,去操纵肠道菌群以达到获得健康的目的,是一个值得深入探讨的话题。
本文,我们从肠道菌群的角度来了解一下,饮食模式、发酵食品、益生菌、益生元和其他相关化合物对我们健康的影响。
本文主要从五个方面讲述
●发酵食品对肠道菌群和健康的影响
●不同饮食模式与菌群及健康
●益生菌调节肠道微生物群和人体健康
●益生元化合物对肠道菌群的影响
●后生元和精神生物制剂与健康
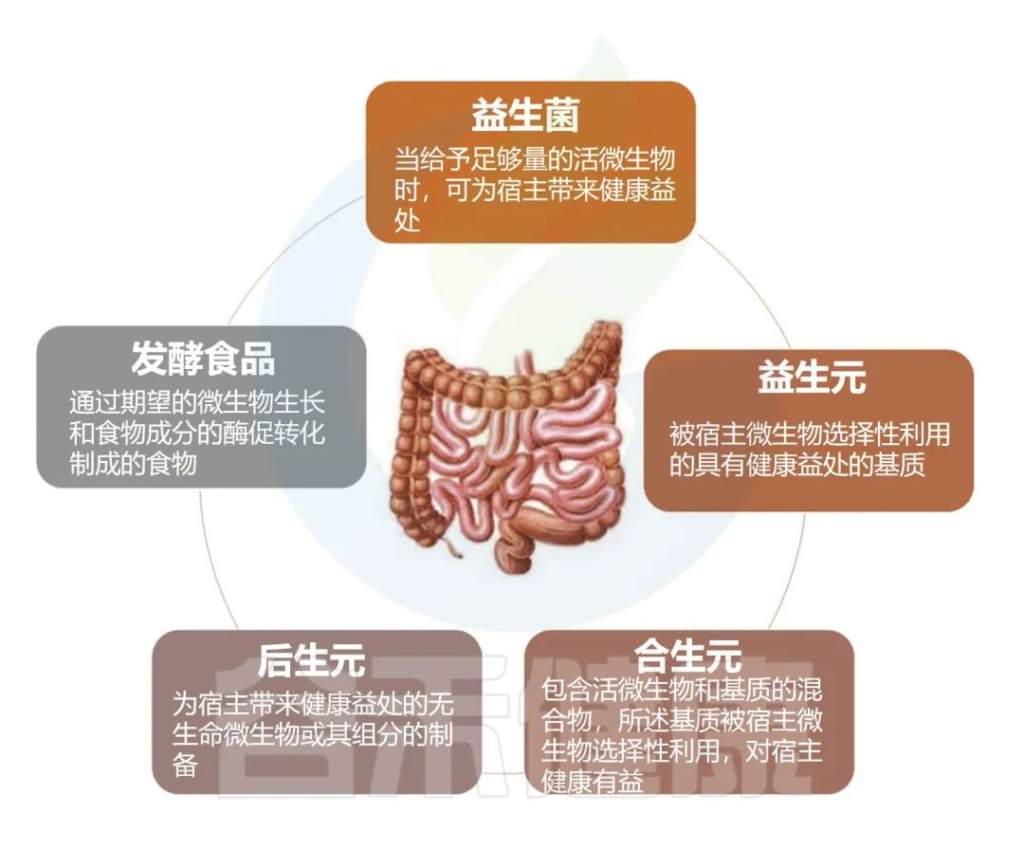
Nma B,et al.Elsevier Inc.2022
发酵食品被定义为“通过理想的微生物生长和食物成分的酶促转化制成的食品”。
许多发酵食品已被证明通过不同的方式对人体具有促进健康的作用,包括生物活性分子的合成、肠道微生物群的调节以及与免疫系统的相互作用。
✦发酵食品产生多种代谢物,促进有益作用
在食品发酵过程中,微生物进行酶促转化,提供多种具有不同生理活性的代谢产物(多肽、低聚糖、游离氨基酸、改性多酚、有机酸等)。
这些转化发生在食物摄入之前,发酵食品也是微生物进入我们肠道的绝佳载体,与我们的微生物群的其他成员一起,可以转化和代谢我们肠道中的食物成分,产生具有不同功能的微生物代谢物(短链脂肪酸、维生素、细菌素等)。
据报道,某些发酵食品或其成分能够以某种方式促进有益的效果,而这些效果有时与我们微生物群的变化有关。在本节中,我们将讨论发酵食品对微生物群的影响及其可能的有益作用。
发酵乳制品对健康的影响已经被深入研究了一个多世纪,但直到最近,随着新的组学技术和大规模测序方法的使用,我们才能够详细了解食用发酵乳制品对微生物群的影响。
1 酸奶

•酸奶有助于改善乳糖消化不良
酸奶是研究最多的发酵乳制品之一。它是通过两种乳酸菌(德氏乳杆菌保加利亚亚种和嗜热链球菌)在牛奶中的联合活性获得的。欧洲食品安全局已经认识到酸奶发酵剂的有益作用,认为活酸奶培养物可以改善乳糖消化不良患者的乳糖消化。
•饮用酸奶增加了嗜热链球菌,减少了拟杆菌丰度
一些动物模型的临床前研究表明,长期摄入酸奶改变了小鼠菌群中拟杆菌门(Bacteroidetes)和厚壁菌门(Firmicutes)之间的比例,并增加了链球菌科(Streptococcaceae)成员的数量,这可能是由于摄入了酸奶中存在的嗜热链球菌(S. thermophilus)。
此外,一些在人体中进行的干预试验表明,饮用酸奶会增加人体微生物群中的一些细菌数量:其中,乳酸菌的丰度较高,而拟杆菌(Bacteroides)的种类则相应减少。
2 奶酪

奶酪,也是一种发酵的牛奶制品,其性质与酸奶有相似之处,都是通过发酵过程来制作的,也都含有可以保健的乳酸菌,但是奶酪的浓度比酸奶更高,近似固体食物,营养价值也因此更加丰富。
•食用奶酪可以增加产丁酸盐细菌丰度,可能缓解特应性皮炎
研究了奶酪和乳制品引发肠道微生物群变化并促进相关健康影响的能力。最近进行了一项健康食品选择与肠道微生物群组成之间的广泛关联研究,表明α多样性与低脂奶酪之间存在强烈的正关联。
临床前研究报告称,给小鼠服用奶油奶酪后,产生丁酸盐的细菌水平增加,T细胞(Treg)介导的免疫反应和IgE水平降低,表明对缓解特应性皮炎有潜在的有益作用。
•奶酪中的发酵菌可以存在人体一段时间
在人类中,两项干预试验评估了食用卡门贝尔奶酪对不同肠道菌群成员的影响,结果表明,食用奶酪后粪肠球菌(Enterococcus faecalis)的丰度显著增加,并且卡门贝尔奶酪中存在的微生物,如乳酸乳球菌(Lactococcus lactis)、肠膜明串珠菌(Leuconostoc mesenteroides)和白地土菌(Geotricum candidum),在食用奶酪期间出现在个体的粪便中。在停止干预15天后,粪便样本中存在肠膜明串珠菌。
3 开菲尔
开菲尔是一种由微生物混合物发酵的产品,通常包括几种乳酸菌和酵母,其发酵和生产过程根据其生产的地理区域和传统的细化过程而显著变化。
因此,很难对开菲尔的效果得出一般性的结论,更谨慎的做法是根据所研究的开菲尔的类型来具体说明这些效果。
•改善机体代谢,抗肥胖
有证据表明,食用开菲尔可能有有益的代谢作用。开非尔能够调节啮齿动物体内的微生物群组成。向肥胖的人类微生物群相关大鼠喂食西藏开菲尔牛奶表明,微生物群变化与胆汁酸和氨基酸代谢有关。
此外,连续四周每天给小鼠服用克非尔显示了对厚壁菌门/拟杆菌门比率的影响,以及对性能和身体疲劳的改善。
另一项研究通过建立社区特征和几种生物标志物之间的相关性,证明了开菲尔在小鼠体内的抗肥胖作用,这表明食用开菲尔诱导的微生物群和真菌群调节可能与预防肥胖和脂肪酸代谢有关。
•改善炎症性肠病、代谢综合征
一项针对炎症性肠病患者的随机对照试验表明,定期食用开非尔可以改善生活质量,减少腹胀。
此外,一项平行组随机对照干预试验显示,代谢综合征患者接受开菲尔12周后,在开菲尔组中放线菌的相对丰度增加,对代谢综合征标志物有一些有利的影响。
•还可能影响宿主行为和免疫状态
对小鼠施用开非尔还被证明可以增加短乳杆菌(Lactobacillus brevis)的流行率和微生物群产生γ-氨基丁酸的能力,影响宿主行为和免疫状态。
这些临床前证据表明,开非尔对宿主的微生物群和代谢有影响,包括肥胖、糖尿病、肝脏和心血管疾病、免疫和神经系统变化。
除了发酵乳制品外,关于其他动物性发酵食品调节微生物群的信息较少。然而,有证据表明植物发酵食品对肠道微生物群的影响,以及其与健康影响的潜在关系。
在这方面,酸菜、泡菜、红茶菌和其他发酵的植物性食物已经被研究过,并显示出对肠道微生物群的不同影响,尽管需要更多的证据来建立它们对人类健康的明确联系。
1 酸面包
•低蛋白饮食相关细菌减少、影响升糖反应
酸面包是一种发酵食品,也显示出了显著的效果。采用元蛋白质基因组学方法分析了酸面包对大鼠微生物组的影响,结果显示低蛋白质饮食相关的细菌类群减少。
在另一项研究中,食用手工酸面包引起的升糖反应与食用工业白面包不同。这些反应是个体特异性的和微生物相关的。
每个人的血糖反应可以根据干预研究前确定的微生物组谱进行预测。
2 发酵豆制品
•促进脂肪酸分解代谢
关于发酵豆制品,一些临床研究显示了微生物群调节活性和各种生理效应。在啮齿动物中研究了大豆发酵产品对代谢过程的影响,表明发酵大豆能够促进小鼠脂肪酸分解代谢和主要细菌门的变化。
•影响其他代谢物水平
鼠李糖乳杆菌发酵的豆浆通过增加一些细菌类群,如拟杆菌(Bacteroides),对小鼠微生物群有影响,这是一种通过尿液排泄的异黄酮代谢物的来源。
此外,用解淀粉芽孢杆菌(Bacillus amyloliquefaciens)发酵的大豆降低了2型糖尿病大鼠模型中的高血糖,引起疣微菌(Verrucomicrobiales)种群的增加和肠杆菌(Enterobacteriales)的减少,以及其他微生物群的变化。
•改善认知功能
值得注意的是,在小鼠中摄入植物乳杆菌发酵的大豆后,观察到对认知功能的积极影响,以及乳酸菌和双歧杆菌种群的增加。
含有植物乳杆菌(L.plantarum C29)的发酵产品在一组轻度认知障碍患者中进行的为期12周的人类临床试验中显示出认知能力的改善。
•可能改善皮肤状况
最后,摄入含有干酪乳酸菌代田株(Lactobacillus casei Shirota)的发酵豆乳对健康绝经前日本女性的皮肤状况有显著影响,乳酸菌和双歧杆菌的数量有增加的趋势,而肠杆菌科和紫单胞菌科(Porphyromonadaceae) 的数量则有下降的趋势。
由于各种食物已经证明了调节特定细菌和肠道微生物群整体结构的能力,因此短期和长期的饮食模式可以影响肠道微生物组的构成和良好功能。
★ 饮食对肠道菌群的多样性至关重要
我们肠道菌群的多样性可能反映了我们饮食的多样性,因此,饮食可能是我们控制和平衡肠道菌群组成和代谢的最强大的武器。
以下部分旨在概述过去几年来产生的关于不同饮食和饮食习惯对调节肠道菌群的潜力的一些现有知识。
西式饮食、地中海饮食和素食这几种可能是世界上最常见的人类饮食模式,每一种都与一些特定的健康/疾病状况有关。
✦不同饮食模式的差异主要是碳水化合物和纤维的含量
宏量和微量营养素方面的显著差异决定了这些饮食模式,其中复合碳水化合物和纤维的含量可能是最显著的之一。
事实上,复杂的碳水化合物和纤维可能是产生最确凿证据的食物成分,它们是肠道菌群的有益调节器,在碳水化合物消耗仅24小时后就会发生快速转变。
西式饮食,是一种以高含量精加工糖和碳水化合物、高含量饱和脂肪酸、高含量动物蛋白以及低含量膳食纤维为特征的一种现代饮食方式,不能否认的是这种饮食好吃还容易上瘾。
✦西式饮食导致易患许多代谢疾病
这种饮食模式在人类历史上是最近才出现的,通常与城市生活方式有关,通常与炎症和代谢疾病有关,包括2型糖尿病和肥胖等。
✦西式饮食下的肠道微生物显著改变
此外,在将祖先生活方式和农业人口的饮食与西方化生活方式的饮食进行比较时,观察到肠道微生物群的组成发生了显著变化,总体特征是纤维降解细菌的减少和蛋白质代谢细菌的增加。
变形菌、拟杆菌等蛋白质代谢菌较丰富
最近的研究已经指出,与这些生活方式相关的一些疾病生物标志物可能是通过西方饮食对肠道微生物群的干扰作用介导的,其特点是多样性低。
蛋白质和胆汁代谢细菌占主导地位,包括产生三甲胺n-氧化物(TMAO)的物种,变形菌和拟杆菌通常更为丰富。
事实上,在动物模型中,西方化饮食的引入会迅速转化为微生物群的变化,并增加感染和代谢疾病的风险,在向新动物移植不良微生物群后,这些表型可以重现。
这表明,饮食模式影响人类健康的一些机制是通过调节肠道微生物群来实现的,并表明通过饮食调节肠道微生物群可能会降低一些疾病风险。
地中海饮食的特点是大量摄入新鲜水果、蔬菜、豆类和全谷物,同时摄入少量动物蛋白、加工食品和饱和脂肪。
✦地中海饮食改善代谢、降低慢性病患病率
长期以来,这种饮食习惯与改善代谢和心血管健康、健康老龄化、降低死亡率和慢性疾病患病率有关。
纤维降解细菌丰度增加、短链脂肪酸增加
其中一些影响与肠道菌群特征及其相关代谢组和免疫调节的特定变化有关。就地中海饮食对肠道菌群的具体影响而言,它通常与纤维降解物种的高度多样性和代表性有关,如普雷沃氏菌(Prevotella)和毛螺菌属(Lachnospira)。
其代谢导致短链脂肪酸的产生;以及一些瘤胃球菌的减少。事实上,严格坚持地中海饮食的人的短链脂肪酸水平似乎更高。
值得注意的是,与地中海饮食相关的有益肠道菌群调节并不完全与其长期食用有关,因为饮食习惯向这种模式转变,即使是相对较短的时间,通常也会改善微生物和健康生物标志物,这在各种炎症、代谢和认知障碍的动物模型以及人类临床试验中都得到了证明。
例如,对一组超重和肥胖的参与者进行了8周的地中海饮食干预,即使在保持能量摄入的情况下,也导致微生物群多样性显著增加,纤维降解细菌的表现包括普拉梭菌、一些拟杆菌属和一些罗氏菌属、颤螺菌属和毛螺菌,这些细菌负责短链脂肪酸的产生,包括丁酸盐生产者。其中一些还被认为具有抗炎特性。
✦有效改善炎症
此外,在饮食干预后,潜在的促炎细菌(如Ruminococcus gnavus)减少,胆固醇水平、炎症标志物和胰岛素抵抗全面改善。
地中海饮食对肠道菌群结构的好处也在其他健康受试者的队列中被揭示出来。在欧洲各国的老年人群中进行了一项大型饮食干预试验,表明在12个月的时间内坚持地中海饮食模式有利于调节微生物群中的关键物种,导致与较低虚弱和改善认知功能标志正相关的类群的丰富,并与炎症负相关,包括以下几种菌属:
普拉梭菌(Faecalibacterium);
罗氏菌属(Roseburia);
优杆菌属(Eubacterium);
多型拟杆菌(Bacteroides thetaiotaomicron);
普雷沃氏菌(Prevotella)。
素食
素食是一种不食肉等动物产品的饮食方式,有时也戒食奶制品和蜂蜜。在另一个极端,许多研究评估了长期素食和杂食饮食对微生物群、代谢组和疾病风险的影响。
✦素食对健康促进的具体作用暂不明确
长期以来,素食饮食一直被认为具有促进健康的作用,但与杂食性饮食相比,素食饮食也可以培养不同的肠道微生物群结构,总体上增加了多样性和丰富性;拟杆菌(Bacteroidetes)经常以较高的相对频率出现。
然而,报告了一些相互矛盾的结果,一些控制良好的喂养研究发现,生活在同一地理区域的杂食性和素食者之间的肠道微生物群只有适度的差异。不过两组在代谢组中都表现出很大的差异,这可能部分归因于微生物群产生的代谢物。
低FODMAP饮食
还有一种与潜在微生物群调节能力相关的饮食模式是低FODMAP饮食。
什么是FODMAP?
FODMAP是一组人体吸收较差的短链碳水化合物,包括果糖、果聚糖、乳糖、多元醇及半乳糖寡糖等。
其特点是可发酵低聚糖、双糖、单糖和多元醇的含量降低,虽然其中一些成分可能作为益生元对健康受试者的肠道菌群进行有益的调节,但它们也可能引发肠易激综合征(IBS)和其他肠道疾病患者的不良反应。
✦缓解肠易激综合征
低FODMAP饮食长期以来可以证明缓解了肠易激综合征患者的症状,但其有益效果似乎强烈依赖于患者的基础微生物群特征。
✦影响健康促进有关细菌的丰度
在微生物区系水平上,FODMAP消耗的减少通常会导致一些与健康促进有关细菌的肠道减少,如:
普拉梭菌(Faecalibacterium Prausnitzii)↓↓↓
双歧杆菌(Bifidobacterium)↓↓↓
嗜黏蛋白阿克曼菌(Akkermansia)↓↓↓
巨球型菌属(Megasphaera)↓↓↓
片球菌属(Pediococcus)↓↓↓
放线菌(Actinobacteria)↓↓↓
以及产生丁酸盐的细菌减少
同时伴随着其他气体消耗细菌的增加,如雌马酚产生者Adlercreutzia,甚至是Ruminococcus torques。细菌通常在肠易激综合征患者中检测到高丰度。
因此,低FODMAP饮食可以导致症状的改善,尽管所涉及的机制尚不清楚,但是同时,也可以诱导更明显的肠道菌群失调。
有趣的是,低FODMAP饲粮降低了结肠pH值和细菌总数,而短链脂肪酸浓度不受影响,这进一步支持了低FODMAP饮食下肠道菌群代谢中存在重要的重组。
注意
虽然人们普遍认为地中海和素食饮食可以改善肠道微生物群的多样性和纤维降解细菌的表现,但在不同的研究中,一些具体的类群有所不同,这阻碍了在饮食模式、微生物群变化和健康反映之间建立具体的因果关系。
这可以归因于不同食物组合的可变影响,以及对饮食干预的反应可能高度依赖于基础肠道微生物群组成,以及其他个体遗传和环境特征、宿主遗传、季节、地理和文化差异。
在考虑将饮食干预作为精确调节肠道微生物群的手段时,另一个需要考虑的关键方面不仅是宏观和微量营养素的具体组成,还包括摄入次数、饮食行为和饮食干预的持续时间。
一般来说,虽然相对短期的饮食干预足以对肠道菌群产生可测量的影响,但在恢复习惯性饮食后,这些变化会迅速恢复,甚至,根据基础菌群配置,可能需要更大的干预才能产生明显的效果;建议永久性的饮食适应,以确保提供持续的基质来源,为有益的肠道种群提供燃料及其相关的长期益处。
因此,虽然在该领域已经取得了重大进展,但为了建立旨在通过调节肠道微生物群来改善人类健康的个性化饮食策略,有必要进行进一步的研究。
益生菌被定义为“当施用足量时,对宿主的健康有益的活微生物”。
益生菌已被认为在不同水平上发挥其有益功能,包括:
•营养物质的代谢,以促进消化,产生维生素或具有全身作用的分子;
•神经系统信号的改变;
•免疫调节的诱导;
•对生理应激的保护;
•直接和间接的病原体拮抗;
•改善肠道上皮的屏障功能;
•调节微生物
益生菌可以在不同程度上对宿主产生有益作用
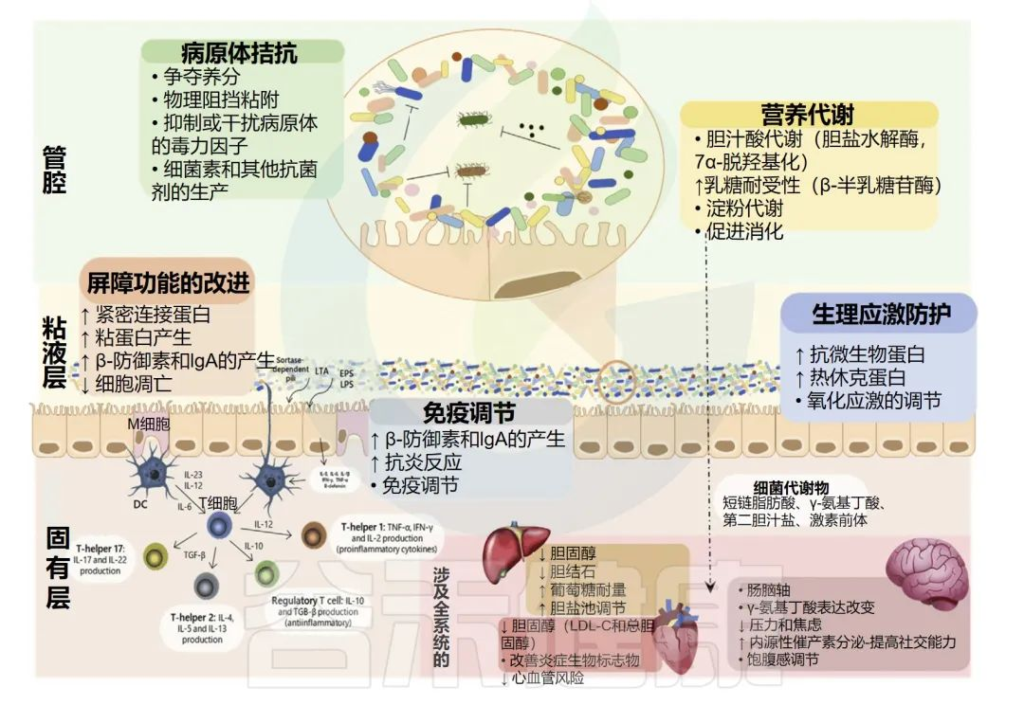
Nma B,et al.Elsevier Inc.2022
这些功能可以是接触依赖的或由表面分子介导的,如脂磷酸和梭酸依赖菌毛,或由分泌分子介导的,如短链脂肪酸和细菌素。
总的来说,突出了免疫调节和病原体拮抗活性,它们对于维持肠道微生物组中细菌群落与宿主之间的平衡至关重要。
一些研究,不仅在体外和动物模型中,而且在人类志愿者中,分析了益生菌对与人类疾病相关的特定细菌病原体或群体的抑制作用,如产气荚膜梭菌 (Clostridium perfringens)、肠炎沙门氏菌(Salmonella enteritidis)和大肠杆菌(Escherichia coli);以及其对生理或炎症标志物和免疫特征的影响。
益生菌也被认为能够调节整体肠道微生物群。事实上,有人提出所需的益生菌效果与肠道中的微生态变化有关。
✦益生菌治疗改变了肠道微生物组成
对动物模型的不同研究表明,用不同菌株的乳酸菌和双歧杆菌以及其他微生物(如布拉氏酵母菌)进行治疗,明显影响小鼠肠道的微生物群组成,促进微生物群落的结构和功能的变化。
注:这些研究大多使用细菌计数或qPCR分析来研究肠道微生物群分布的变化,只获得了生态系统的一小部分图像。在这方面,随着下一代测序技术和生物信息学工具的发展,我们可以对肠道微生物组进行更深入的研究,不仅可以从结构和组成层面,还可以从功能层面深入研究益生菌对微生物群落的影响。
缓解肥胖相关的肠道微生物失调
在动物模型上报道了鼠李糖乳杆菌、嗜酸乳杆菌、植物乳杆菌、两歧双歧杆菌、长双歧杆菌和粪肠球菌对饮食诱导的肥胖小鼠肠道微生物群的调节作用,缓解了饮食诱导的肥胖和相关的肠道微生物群失调。
此外一些益生菌,如茯砖茶中的冠突散囊菌(Eurotium cristatum),也显示出调节肠道真菌和细菌群落的能力,表现出与健康动物中观察到的情况更接近的特征,并减轻饮食引起的肥胖症状。
下面是益生菌调节肠道菌群的一些证据:
调节抑郁症的肠道生态失调
肠道生态失调
在抑郁症小鼠模型中,使用含有L.plantarum LP3、L.rhamnosus LR5、Bifidobacterium lactis BL3、Bifidobacterium breve BR3和Pediococcus pentosaceus PP1的益生菌配方进行干预,可对微生物组产生调节作用,使其与健康动物中观察到的情况相似,从而减少与疾病相关的肠道生态失调。
结肠炎生态失调得到改善
同样,在诱导结肠炎小鼠模型中,摄入布拉迪酵母菌(Saccharomyces boulardii)或两株发酵乳杆菌(Lactobacillus fermentum )已显示出能够调节肠道微生物组,增加生物多样性,并显著改善结肠炎动物的肠道生态失调特征。
结直肠癌的致病菌得到抑制,有益细菌增加
另外,在结直肠癌小鼠模型中,丁酸梭菌(Clostridium butyricum)的干预减弱了致病菌的增加,促进了有益菌的生长,并改变了次生胆盐和短链脂肪酸等微生物源性代谢产物。
在小鼠哮喘模型、抗生素诱导的生态失调小鼠和健康动物中也报道了这些调节作用,显示生物多样性和有益细菌丰度的增加。
益生菌对微生物群的调节在人类中并不明显,因为有的研究显示了相互矛盾的结果。可能还需一系列深入研究来了解益生菌对人体肠道微生物群的具体影响。
下面是存在争议的一些数据:
在最近的一项工作中,研究表明,以嗜酸乳杆菌(L. acidophilus)、乳酸乳杆菌(B. lactis)、长双歧杆菌(B. longum)、双歧双歧杆菌(B. bifidum)、和半乳糖低聚糖混合物组成的共生生物作为益生元进行干预,显示出在一组肥胖患者中调节肠道微生物群落的能力,观察到不同健康相关菌群(如双歧杆菌、毛螺菌和乳杆菌)的比例有所增加;以及与肥胖正相关的慢性炎症相关群体的减少,如瘤胃球菌科(Ruminococcaceae),普雷沃氏菌(Prevotella)和巨球型菌属(Megasphaera) 。
然而,先前对肥胖患者的研究显示了相互矛盾的结果,因此其中一些研究报告称,在益生菌干预后,肠道微生物群落没有变化,质疑这种对肠道微生物组的调节作用的存在。
与此同时,对影响全球数百万人的炎症性肠病患者的研究也显示出有争议的结果。尽管在动物模型中已经报道了对肠道微生物群落的调节作用,但在一组溃疡性结肠炎患者中,用含有短双歧杆菌(B. breve)的某品牌益生菌治疗,在研究过程中,两个治疗组之间没有显著差异。
另一方面,摄入含有L.acidophilus La-5和B. animalis亚种的益生菌酸奶。促进了一组炎症性肠病患者中乳酸菌、双歧杆菌和拟杆菌水平的增加,尽管这项工作没有从宏基因组的角度分析微生物组。
✦特定菌属水平增加,整体菌群组成变化不大
一些研究报道,益生菌不影响整体菌群组成,但可以改变特定属的比例。
例如,在高危特应性疾病婴儿中,在产前最后阶段和出生后第一年摄入益生菌混合物促进了双歧杆菌和乳酸杆菌水平的增加,但在肠道微生物组中没有检测到显著变化。
同样,在一组有功能性便秘症状的个体中,混合使用益生菌的干预促进了瘤胃球菌(Ruminococcus)水平的增加和丹毒丝菌科(Erysipelotrichaceae) 成员的减少,但α多样性指数和整体微生物组组成显示出与安慰剂组检测到的水平相似。
在一组HIV感染个体中,在使用鼠李糖酵母菌GG干预8周后,也描述了相同的趋势。
✦增加与健康相关共生细菌,减少病原体相关细菌
其他研究表明,益生菌可以引起肠道微生物种群的变化,增加与健康相关的共生细菌的水平,减少与病原体相关的群体,甚至恢复被改变的微生物群落的平衡。
在这方面,干酪乳杆菌(Lactobacillus casei Lcr35)在一组患有急性腹泻的儿童中,促进了拟杆菌、粪杆菌和瘤胃球菌属的增加,并降低了大肠杆菌和梭状芽孢杆菌的水平。
在一项针对乳糖不耐受患者的研究中,使用B.longum BB536和L.rhamnosus HN001进行30天的干预也导致肠道微生物组成发生积极变化。
在感染幽门螺旋杆菌的患者中也观察到了这种趋势。他们报告了多重耐抗生素的屎肠球菌LAB制剂与抗生素联合使用时,在正常肠道微生物群方面的有效效果,防止α多样性值的下降,并恢复受抗生素治疗影响的微生物群的水平。
同样,在一组患有早期败血症的成年人中,益生菌的干预导致α多样性的增加以及益生菌的增加,如不同种类的乳酸菌(Lactobacillus)和屎肠杆菌(E.faecium)。
此外,一些研究表明,益生菌不仅可以引起特定细菌种群的变化,还可以引起相关微生物群代谢物的变化。
✦肝硬化患者肠道失调得到改善
在肝硬化患者中,摄入8周鼠李糖乳杆菌GG不仅能调节肠道微生物组,降低肠杆菌科(Enterobacteriaceae)和紫单胞菌科(Porphyromonadaceae)的相对丰度,增加共生菌毛螺菌科(Lachnospiraceae)和瘤胃球菌科(Ruminococcaceae)的丰度,还能调节代谢物的分布,从而改善肠道生态失调和微生物-代谢组的联系。
在摄入增强结肠短链脂肪酸生成的发酵牛奶后,也有类似的趋势被报道;在乙型肝炎诱导的肝硬化患者中摄入含有丁酸梭菌(C.butyricum)和婴儿双歧杆菌(Bifidobacterium infantis)的益生菌混合物3个月后,促进了不同肠粘膜屏障完整性生物标志物的改善。
考虑到来自动物模型和人体试验的这一证据,最近有人提出将益生菌作为预防和治疗结直肠癌的新策略。
注:迄今为止,缺乏针对人类患者的研究,专注于分析益生菌对与CRC相关的肠道菌群紊乱的可能调节作用。
✦健康人群病原相关菌丰度下降
就健康人群而言,只有少数干预研究分析了益生菌摄入量对肠道微生物群的影响,而肠道微生物群可以根据参与者的年龄进行分类。
在一项对3至12个月大的婴儿的研究中,使用三种益生菌菌株进行干预(B.longum subsp. infantis R0033, Lactobacillus helveticus R0052和B. bifidum R0071)。8周后,一些病原相关类群如柯林斯菌属(Collinsella),肠球菌(Enterococcus)和克雷伯氏菌(Klebsiella),粪杆菌(Faecalibacterium)和瘤胃球菌(Ruminococcus)水平下降。
此外,在干预期间,一些细菌群保持稳定,而在安慰剂组中,它们增加了,如大肠杆菌志贺氏菌(Escherichia-shigella)和韦荣氏球菌属(Veillonella)的情况下
增加有益细菌,减少病原体相关菌的一些证据:
在另一项对健康婴儿的研究中,在生命的第一年摄入补充了4种双歧杆菌菌株的配方,促进了脆弱拟杆菌(Bacteroides fragilis)和经黏液真杆菌属(Blautia)水平的下降,以及代谢物谱的差异,尽管没有检测到整体微生物组的变化。
在成人人群中,有研究表明,益生菌摄入量对肠道微生物群落的影响与肠道菌群的基础组成密切相关。每天食用干酪乳杆菌(L.casei)14天,增加了某些有益细菌的相对丰度,如乳酸杆菌(Lactobacillus)、罗氏菌属(Roseburia)、粪球菌属(Coprococcus),而一些有害细菌的水平则降低了。
在用Lactobacillus kefiri LKF01治疗后,以及B.longum BB536和L.rhamnosus HN001进行干预后,也报告了类似的结果,显示出强大的调节肠道微生物群组成的能力,导致有益细菌的增加,并显著减少直接参与促炎反应和胃肠道疾病发作的潜在有害菌群。
✦产丁酸盐细菌增加
此外,每天食用两歧歧杆菌(B.bifidum strain Bb)4周会影响粪便微生物群中优势类群的相对丰度,并调节粪便丁酸盐水平,因此作者观察到普雷沃氏菌(Prevotellaceae)的数量减少,而瘤胃球菌(Ruminococcaceae)和Rikenellaceae的比例更高。
这些研究支持了之前的研究,即益生菌对肠道菌群的调节作用。有趣的是,最近有人提出了益生菌“ salami”的潜力,尽管微生物组的整体结构没有发现显著变化,但摄入益生菌萨拉米会促进产生丁酸盐的细菌的增加。
在益生菌摄入过程中检测到粘附相关基因的差异表达和大量参与细菌运动性的基因,提示益生菌干预可以通过调节其表达模式来调节肠道微生物组。
小结
总之,在过去的几十年里,大量的科学报告已经证实了益生菌对宿主健康的积极作用。然而,尽管存在不同的动物模型和人体研究,显示益生菌可能对肠道微生物群落及其功能具有调节作用,但在人体试验中报道的还存在一定的争议。
现有的研究使用了不同的益生菌菌株、广泛的年龄范围、疾病和疾病状态,以及摄入不同饮食和营养素的志愿者;因此,研究组表现出较高的个体内部和个体间的变异性,使得阅读结果变得困难。
另一方面,正如前面提到的,我们必须考虑到益生菌的作用不仅取决于菌株,还取决于基础微生物群,而最常用的益生菌(主要属于乳酸杆菌和双歧杆菌)不一定在肠道定植,并且可以在益生菌干预后释放,从而使确定益生菌调节宿主肠道微生物群的具体机制变得更加复杂。
为了阐明益生菌对肠道环境和微生物群影响的分子机制,我们应该进一步研究更大、更均匀的群体,也许还应该研究从人类肠道环境中分离出来的下一代益生菌,它们能够在肠道粘膜上定植,产生长期效应。
益生元概念首次定义为“不易消化的食物成分,通过选择性地刺激一种或少数已经存在于结肠中的细菌的生长或活性而有益地影响宿主”。
然而,这一概念多年来一直在发展。当前的国际益生菌和益生元协会共识小组提出了以下益生元的定义:“一种被宿主微生物选择性利用的对健康有益的底物”。
各种益生元
应该指出的是,目前确立的益生元是基于碳水化合物的,尽管其他物质如酚类化合物和多不饱和脂肪酸转化为各自的共轭脂肪酸可能符合这一定义。
几十年来,只有少数几类碳水化合物被认为是益生元,包括人乳寡糖(HMOs)、菊粉和低聚果糖(FOS)、低聚半乳糖(GOS)和乳果糖。
一些益生元及相关研究
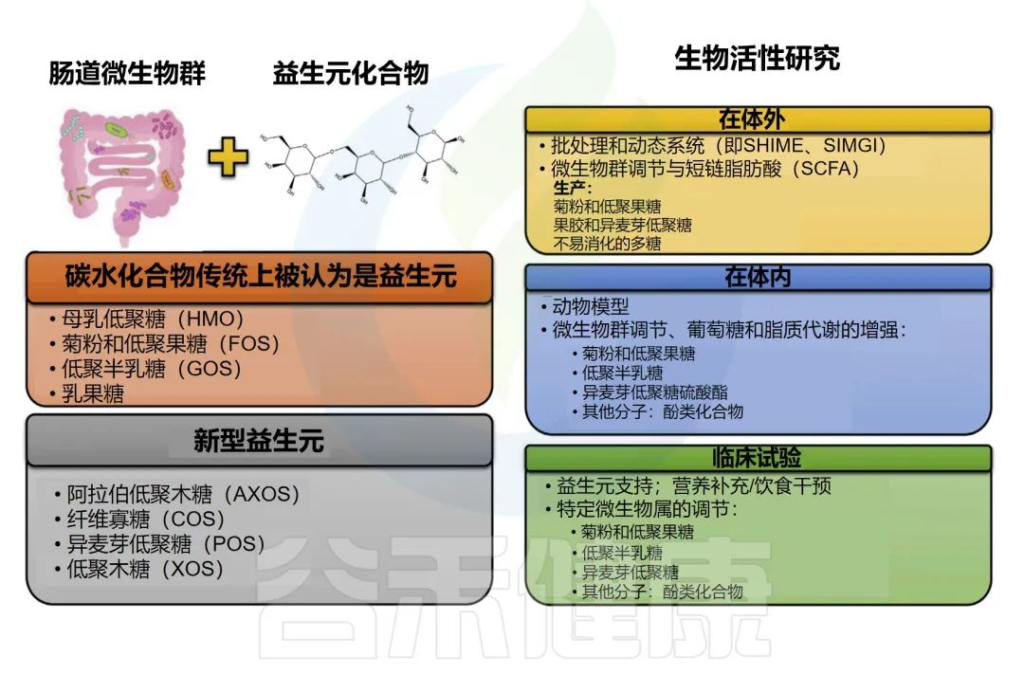
Nma B,et al.Elsevier Inc.2022
•人乳寡糖
人乳寡糖包括由5个单体(葡萄糖、半乳糖、n-乙酰葡萄糖胺、焦糖和唾液酸)通过多达12个不同的a-和b-糖苷键结合形成的广泛的低聚糖结构。
人乳寡糖对新生儿肠道菌群发育有很大影响,促进双歧杆菌(Bifidobacteriaceae)和拟杆菌(Bacteroidaceae)生长。
•低聚果糖
另一方面,低聚果糖是通过蔗糖的果糖转基化或菊粉的部分水解获得的,是唯一主要由果糖单位组成的碳水化合物。
•低聚半乳糖
相比之下,低聚半乳糖包括含有b键的b-GOS和来自乳糖延伸的b-GOS,以及存在于各种蔬菜来源中的a-GOS,如棉子糖和水苏糖。
•其他益生元
其他潜在的益生元低聚糖包括异麦芽糖-低聚糖(IMOS),由糖化植物淀粉中获得的由a键连接的葡萄糖单位形成的分支结构;
低聚木糖(XOS)和阿拉伯低聚糖(AXOS),由木聚糖和阿拉伯低聚木聚糖水解产生的含有阿拉伯糖酰和葡萄糖醛基分支的低聚木糖物组成;
纤维寡糖(COS),由木质纤维素生物质酶解获得,由b键连接的葡萄糖单位形成;
果胶寡糖(POS),由果胶部分水解产生,由半乳糖醛酸线性链形成,可能显示含有鼠李糖、阿拉伯糖、木糖和半乳糖等中性糖的分支结构域。
许多研究通过动物模型来评估体内益生元化合物的潜在生物活性。
✦增强代谢和生物利用度
通过16S rRNA基因测序和鸟枪法测序,大鼠给予低聚果糖和低聚半乳糖可导致普雷沃氏菌(Prevotella)水平升高,并由于普雷沃氏菌的代谢功能而增强了人参总苷的生物转化和生物利用度。
深度宏基因组测序实验已经报道了低聚果糖在高脂饮食喂养小鼠中促进了以下菌群的生长:
Allobaculum ↑↑↑
Oribacterium ↑↑↑
普雷沃氏菌(Prevotella) ↑↑↑
并降低了以下菌群:
嗜胆菌属(Bilophila) ↓↓↓
Butyrivibrio LE30 ↓↓↓
鸟枪测序分析还显示,菊粉处理的高脂饲料饲养的小鼠后代的葡萄糖和脂质代谢途径增强。
以下菌群水平增加:
B. breve ↑↑↑
B. acidifaciens ↑↑↑
Clostridium sp. CAG 343 ↑↑↑
Eubacterium sp. CAG 786 ↑↑↑
下列菌群水平下降:
B. massiliensis ↓↓↓
Oscillibacter sp. 1-3 ↓↓↓
Ruminococcus gnavus CAG 126 ↓↓↓
✦降低致病菌丰度
在肉鸡等其他动物模型中测试了低聚果糖补充剂作为抗生素的替代品,导致致病性脱硫弧菌属(Desulfovibrio)和幽门螺杆菌(Helicobacter)的丰度降低。
研究集中在其他寡糖家族,如异麦芽低聚糖,揭示了绿茶与异麦芽低聚糖联合使用,通过预防小鼠肠道生态失调来对抗高脂肪饮食诱导的代谢改变,显示了有益细菌(如Akkermansia muciniphilia,双歧杆菌,乳酸菌和罗氏菌属)丰度的增加。
✦非碳水化合物类益生元可以改善肥胖和肠道炎症
非碳水化合物的调节作用也在体内进行了研究,并通过元分类学评估了微生物种群的变化。已有研究证明,富含多酚的蔓越莓提取物可预防饮食诱导的肥胖、胰岛素抵抗和肠道炎症,并增加小鼠肠道微生物群中嗜黏蛋白阿克曼菌(Akkermansia muciniphila)丰度。
同样,槲皮素对高脂饮食诱导的非酒精性脂肪肝疾病的保护作用,以及类黄酮通过调节厚壁菌门/拟杆菌门比率来改善肥胖诱导的小鼠肠道生态失调的潜力已被描述。
临床试验
已经进行了几项临床试验,以测试不同益生元化合物的潜在作用。
✦增加新生儿双歧杆菌丰度
经荧光原位杂交测定,含有低聚半乳糖和低聚果糖混合物(比例为9:1)的配方可促进婴儿体内双歧杆菌的生长,而补充相同比例的短链低聚半乳糖和长链低聚果糖可导致丙型肝炎病毒感染母亲的新生儿粪便双歧杆菌和乳酸菌数量增加。
此外,肠内补充80%短链低聚半乳糖和长链低聚果糖(比例9:1)和20%酸性果胶寡糖的益生元混合物可导致早产儿双歧杆菌和出生后肠道定植增加。
✦抑制了艾滋病患者中一些有害菌的生长
在人类免疫缺陷病毒1型(HIV-1)感染的成人中,类似的益生元混合物促进了双歧杆菌的生长,并抑制了以下细菌的生长:
Clostridium coccoides ↓↓↓
直肠真杆菌(Eubacterium rectale) ↓↓↓
Clostridium lituseburense ↓↓↓
Clostridium histolyticum ↓↓↓
✦改善肥胖人群肠道菌群构成
同样,服用低聚半乳糖导致50岁以上男性和女性双歧杆菌丰度增加,并增加双歧杆菌数量,减少超重成人粪便样本中拟杆菌和Clostridium histolyticum的数量。
临床试验还报告了低聚果糖和果聚糖的益生元效应,结果表明菊粉型果聚糖导致双歧杆菌和普拉梭菌(F. prausnitzii)的增加;根据16S rRNA基因测序数据,这两种细菌都与血清脂多糖水平呈负相关,并且还降低了肥胖女性的肠道拟杆菌、Bacteroides vulgatus和丙酸杆菌(Propionibacterium)。
✦增加健康成年人体内双歧杆菌含量
此外,根据对健康成年人粪便微生物群的分析,菊粉给药增加了铁含量低的女性的粪便双歧杆菌,大豆寡糖、棉子糖和水苏糖可以被双歧杆菌选择性代谢。
✦其他益生元的作用
研究还评估其他益生元化合物的潜在效应。
食用聚葡萄糖可增加健康男性体内戴阿利斯特杆菌属 (Dialister)、普拉梭菌(Faecalibacterium)和考拉杆菌属(Phascolarctobacterium)的丰度。
这几类细菌的作用在谷禾之前的文章中有具体讲述
根据两项研究中获得的16S rRNA基因测序数据,B. animalis subsp. lactis 420促进了阿克曼菌、Christensenellaceae和Methanobrevibacter的生长,并降低了健康超重或肥胖个体中Paraprevotella的生长。
在健康个体中,部分水解瓜尔胶的饮食干预促进了拟杆菌、普拉梭菌、Fusicatenibacter和瘤胃球菌的生长,并减少了经黏液真杆菌属、毛螺菌科和罗氏菌属的生长。
值得注意的是,这些影响在男性参与者中更为明显。
同样,根据16S rRNA基因测序数据,女性不孕症患者口服部分水解瓜尔胶可导致双歧杆菌丰度增加,拟杆菌丰度降低,改善肠道生态失调和妊娠成功。
每日饮用红酒多酚可增加健康男性中的菌群数量,包括以下菌属:
拟杆菌属(Bacteroides) ↑↑↑
双歧杆菌属(Bifidobacterium) ↑↑↑
肠球菌属(Enterococcus) ↑↑↑
普雷沃氏菌属(Prevotella) ↑↑↑
Blautia coccoides ↑↑↑
Eggerthella lenta ↑↑↑
直肠真杆菌(E.rectale) ↑↑↑
益生菌定义中的关键词是“活的”,这意味着微生物必须是活的(在施用时)才能发挥有益的作用。
但是,在过去的几年里,越来越多的证据表明,不可活的细菌,它们的成分或它们分泌的代谢物,也可能在对健康的积极影响中发挥关键作用。
“后生元”一词于2011年首次提出,指的是摄入后对健康有益的灭活、不可存活的微生物细胞。
这一概念是基于观察到非活细菌或其提取物(破碎的细菌)具有调节宿主免疫反应的能力。
✦后生元相较益生菌的优势
将后生元与益生菌进行比较发现,后生元生产的复杂性较低,具有更好的长期稳定性。
对于某些高炎症状态的患者,使用后生元可能是更安全的替代方案,避免了使用活微生物时反应加剧。
在对术语进行分类的尝试中,提出了“true probiotics”(活的和活跃的细胞)、“pseudo-probiotic”(活的和不活跃的细胞,无论是营养细胞还是孢子细胞)和“ghost probiotics”(非活的或死亡的细胞,完整的或破裂的。
此外,活微生物对食物基质成分的活性也可能释放对健康有积极影响的副产物。例如,牛奶蛋白中加密的生物活性肽。
✦后生元的组成
后生元的组成可以是可变的。除了灭活的(无生命的)微生物生物量,细胞壁的成分(肽聚糖、蛋白质、糖蛋白、磷壁酸)、细胞质膜(磷脂、蛋白质)或细胞外成分,如胞外聚合物(EPS)。此外,分泌到培养基上清液或特定发酵食品的代谢物也可能存在。
后生元的成分示例及显微镜下图像
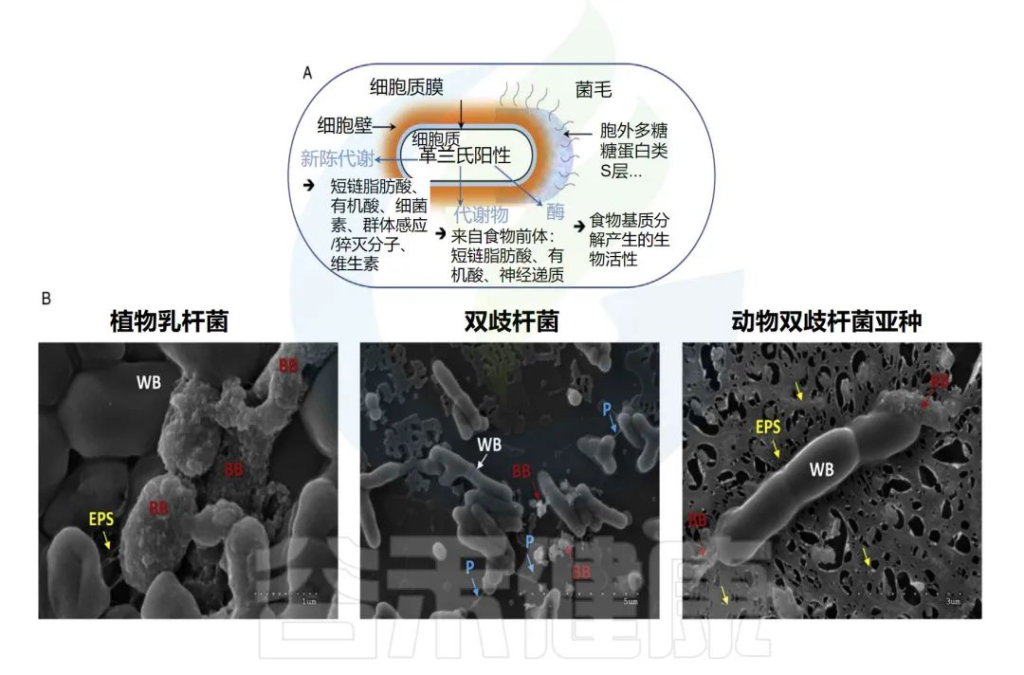
Nma B,et al.Elsevier Inc.2022
✦后生元的作用
后生元作用机制与益生菌的类似,即调节有益菌群的能力、对病原体的拮抗作用、增强肠上皮屏障功能的能力以及调节免疫反应或宿主的其他生理功能。
•刺激免疫反应
双歧杆菌产生的EPS,作为报道的对产生细菌有益作用的关键成分之一。无论是被聚合物包围的紫外线灭活双歧杆菌还是纯化的EPS本身,都能够以不同的方式刺激免疫反应,这取决于聚合物的物理化学特性。这些细菌EPS能够与肠上皮细胞的TLR4相互作用。
•促进脂质代谢和葡萄糖稳定
此外,双歧杆菌EPS是能够积极调节菌群组成的碳水化合物,因为它们被用作肠道某些细菌的选择性发酵底物。特异性EPS还促进饮食诱导的肥胖小鼠模型的脂质代谢和葡萄糖稳态的变化。
含有能够释放抗菌化合物的活益生菌,也可以被视为后生物制剂,可能有助于提高发酵产品的安全性。
将后生元应用于食品,虽然是改善我们健康的一种新方法,但仍然具有挑战性。
精神生物制剂
关于肠道菌群在维持我们生理系统(被称为微生物-肠道轴)方面的知识越来越多,这促使了与调节这种双向对话的饮食策略相关的新概念的发展。这些轴之一是研究的热点,即微生物-肠道-大脑轴。
这是基于对肠道微生物群活动可能参与神经疾病和随着年龄增长而维持认知功能。
▸ 精神生物制剂
针对这目标,提出了与益生菌相关的新定义:精神生物制剂是一种“活的有机体,当摄入足量时,会对患有精神疾病的患者产生健康益处”。
最近,这一定义扩大到包括能够调节肠-脑轴影响肠道微生物群的底物;因此,精神生物制剂是“有益的细菌(益生菌)或对影响细菌-大脑关系的细菌(益生元)的支持”。
研究强调,某些微生物代谢物可以作为某些代谢紊乱的调节因子。同样,在肠道-大脑相互作用的机制中,微生物代谢物也是关键角色。
✦改变行为
已经证明一些微生物来源的精神生物制剂能够有效地改变行为。在一种优雅的实验中,产生酪胺的Providencia能够以一种对共生和宿主都有益的方式操纵秀丽隐杆线虫(Caenorhabditis elegans)的“感官”决定;在食物选择测定中,被Providencia定植的线虫选择了含有这种细菌的食物。
然而,肠道微生物群代谢组的操纵非常复杂,因为肠道微生物的大量多样性之间存在着一种微生物代谢物生产者和消费者之间持续反馈的串扰。
例如,γ-氨基丁酸GABA——(中枢神经系统的主要抑制递质)可以由肠道微生物从饮食前体(如谷氨酸)合成,但它被用作支持该生态位中其他生物生长的营养素。
✦减轻疼痛
神经调节的精神生物学已经被提出,通过体外实验和在大鼠模型上的进一步验证,表明嗜酸乳杆菌菌株(Lactobacillusacidophilus NCFM)能够在肠道水平诱导鸦片样物质和大麻素受体的合成,从而作为一种镇痛药减轻疼痛。
✦调节焦虑
对无菌小鼠口服乳酸菌(Lactiplantibacillus plantarum PS128) 可增加小鼠大脑特定区域的多巴胺和血清素水平,并调节动物的焦虑样行为。
关于能够产生γ-氨基丁酸(中枢神经系统的主要抑制递质)的益生菌,已经在一些乳酸菌和双歧杆菌中描述了不同的代谢途径,其中Levilactobacillus是迄今为止量化产量最高的物种。
不同的策略,如优化培养基组成,可用于提高其他物种的γ-氨基丁酸产量。此外,其中一些乳酸菌也被用于发酵乳制品,以改善这种神经递质在食物中的合成。
//建议
通过γ-氨基丁酸前体的生物转化将食物与γ-氨基丁酸进行天然生物强化,以及使用食物或补充剂作为在肠道中输送能够合成γ-氨基丁酸的益生菌的载体,可能是调节大脑活动的一种策略。
上述的一些证据已经证明,发酵食品、健康的饮食模式、益生菌、益生元以及后生元等都是促进肠道健康的重要因素。通过食用这些食物和补充这些营养素,可以增加肠道内有益菌的数量和种类,并在一定程度上抑制病原相关菌群的丰度,维持肠道菌群的平衡,从而促进肠道健康。
饮食在塑造肠道微生物群的组成和活性方面起着重要作用,对营养饮食与健康肠道微生物组之间相互作用的深刻理解,将为我们理解其在疾病预防和治疗中的作用奠定基础。
任何饮食的好处都将在很大程度上取决于此人的微生物组,每个人根据自己独特的肠道微生物群摄入不同的饮食的方式,将会使我们迎来新时代的饮食模式。
除了肠道健康之外,针对多个健康维度例如提升免疫力,改善情绪,体重管理,皮肤管理等领域产品和食品的需求都在日益提升,这些与肠道微生物组之间又都存在密不可分的关联。因此基于肠道微生物组重要性的开创性研究,可能会从根本上改变消费者偏好及健康食品行业的走向。
主要参考文献
Nma B , Csa C , Ica C , et al. Mechanisms of Gut Microbiota Modulation by Food, Probiotics, Prebiotics and More – ScienceDirect.
Agus, A., Clément, K., Sokol, H., 2021. Gut microbiota-derived metabolites as central regulators in metabolic disorders.
Ali, A., Kamal, M., Rahman, H., Siddiqui, N., Haque, A., Saha, K.K., Rahman, A., 2021. Functional dairy products as a source of bioactive peptides and probiotics: current trends and future prospectives. J. Food Sci. Technol.
Barros, C.P., et al., 2020. Paraprobiotics and postbiotics: concepts and potential applications in dairy products. Curr. Opin. Food Sci. 32, 1–8.
Bellini, M., Tonarelli, S., Nagy, A.G., Pancetti, A., Costa, F., Ricchiuti, A., de Bortoli, N., Mosca, M., Marchi, S., Rossi, A., 2020. Low FODMAP diet: evidence, doubts, and hopes.Nutrients 12 (1), 148.
Cunningham, M., Acarate-Peril, M.A., Barnard, A., et al., 2021. Shaping the future of probiotics and prebiotics. Trends Microbiol.
Fiore, W., Arioli, S., Guglielmetti, S., 2020. The neglected microbial components of commercial probiotic formulations. Microorganisms 8, 1177.