-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康

分娩标志着孩子和母亲的一个相当大的变化,对于母亲来说,分娩是一个转折点,过去我们常常将关注点集中在宝宝的成长发育上,却往往忽视了产后妈妈的身体恢复,如激素急剧变化、在营养补充和维持身材之间难以取舍、代谢异常、睡眠减少等困扰。
更隐秘的危机在精神领域悄然蔓延。世卫组织2023年的报告显示,全球每5位产妇就有1位陷入产后抑郁的泥沼,这些被激素风暴与育儿压力双重撕扯的母亲,往往在”为母则刚”的社会期待中被迫沉默。当一位母亲在产后面临身体不适时,对孩子的照料、家庭的和睦乃至整个社会都带来深远影响。
分娩后,女性体内发生着一系列显著的激素变化:雌激素和孕激素的急剧下降,催产素的波动,皮质醇等应激激素的起伏。激素变化会直接影响肠道菌群的组成和功能,而这些变化又与产后女性的代谢状态、食欲调节和营养吸收密切相关。
一方面,产妇需要充足的营养支持身体恢复和维持母乳喂养;另一方面,也希望逐渐恢复孕前体重。在这种情况下,找到产后营养补充与健康体重管理之间的平衡点变得尤为重要。理解肠道菌群与营养的双向互动关系,可以制定更有效的产后恢复策略,这一点在产后体重管理中尤为重要。
而当产后激素波动导致肠道菌群失衡时,不仅会影响营养物质的吸收和能量代谢,还可能通过炎症因子和神经递质的变化影响情绪,与产后抑郁等心理问题密切相关。
针对产后抑郁倾向的女性,菌群检测可与传统量表评估相结合,构建多模态评估体系,推动产后心理健康管理从单纯症状评估向生物标志物预警转变,提供更精准的个性化干预方案,有效支持产后女性的全面康复过程。
本文将重点探讨肠道菌群在产后女性健康中的关键作用,以及如何通过调节肠道菌群,为这群被忽视的重要人群提供更全面的关怀与支持。
疼痛修复期的身心挑战
产后女性经历着人类生物学中剧烈的生理重构,其变化涵盖内分泌、代谢、免疫等多个系统,并与肠道菌群形成复杂的双向调控网络。
生理层面——连锁效应
“肚子阵阵拧着疼”
很多女性在产后2-3天,下腹持续出现类似痛经的阵发性绞痛,哺乳时疼痛加剧,甚至需要咬牙忍耐。
子宫通过强烈收缩恢复孕前大小,宫底每日下降1-2厘米,约6周完成复旧。肌纤维缩短压迫血管止血。伴随这一过程,子宫内膜脱落形成恶露,初期为血性(持续3-4天),逐渐转为浆液性(持续约10天),最后为白色恶露(持续3周),全程4-6周。
哺乳时婴儿吸吮刺激催产素分泌,进一步强化宫缩。这种疼痛虽难熬,却是子宫复旧的积极信号。
“打个喷嚏就漏尿”
咳嗽、大笑时突然漏尿,尴尬又无奈。孕期增大的子宫压迫盆底肌长达数月,分娩时肌肉和神经被过度拉伸甚至断裂。松弛的盆底肌无法有效支撑尿道,导致腹压增加时尿液失控。
本文后面章节有介绍盆底肌修复的相关干预措施。
心理层面——从甜蜜到崩溃
“前一秒笑着哄娃,下一秒突然崩溃大哭”
分娩后24小时内,雌激素水平暴跌至孕前1/10,直接影响大脑5-羟色胺分泌,导致情绪调节功能紊乱。同时,睡眠剥夺(平均每天仅4小时碎片化睡眠)加剧前额叶皮层代谢异常。
“镜子里的我像个陌生人”——身材焦虑爆发
妊娠纹、松垮的肚皮、下垂的乳房引发强烈外貌焦虑。产后体内脂联素水平持续偏低,导致脂肪代谢减缓,而镜像神经元对体像改变的过度关注会激活杏仁核恐惧回路。
以上是产后康复涉及身体的方方面面,产后生理层面的变化是产后康复研究与实践的核心关注点。这些变化涉及多个系统,包括泌尿系统、体重管理、疼痛感知以及心理健康等方面,需要综合考虑各系统的代谢机制。
产后康复对于保障母婴健康、提升产妇生活质量具有关键意义。接下来们将聚焦于产后营养与体重管理这一关键领域,探讨如何通过科学的饮食策略来支持身体恢复并维持健康体重。
产后女性面临着双重挑战:一方面需要充足的营养来恢复体力、促进伤口愈合并支持母乳喂养;另一方面又期望逐渐恢复孕前体态。
产后超重一方面源于孕前超重或孕期增重过多,另一方面与产后体重滞留有关。
什么是产后体重滞留?
产后体重滞留(Postpartum Weight Retention, PPWR)是女性产后普遍面临的代谢失衡问题,定义为产后一年内体重较孕前增加≥5kg的状态。
主要以产后42天(产后6~8周)、产后6个月和产后12个月作为产后体重监测时点。
能量代谢重构与激素波动
脂肪储备与能量失衡
孕期母体脂肪储备量增加约3-4 kg,主要分布于腹部和臀部,用于支持胎儿发育及哺乳。
产后能量消耗模式改变:哺乳期基础代谢率较孕前提高15%-20%,但若能量摄入(尤其是高脂高糖饮食)超过哺乳消耗(约650 kcal/天),脂肪持续堆积。
激素与代谢调节紊乱
雌激素骤降:产后雌激素水平下降50%-70%,导致脂蛋白酶活性降低,脂肪分解受阻。
胰岛素抵抗:妊娠期胎盘分泌的激素(如胎盘催乳素)诱导胰岛素抵抗,产后恢复期若糖代谢未正常化,易引发脂肪合成亢进。
初始体重减轻幅度
分娩后,产妇体重平均减少约5-10斤(胎儿、胎盘、羊水等重量),但仍有60%-80%的增重需通过后续干预消除。
2013年中国不同产后时间和地区的乳母体重滞留量比较
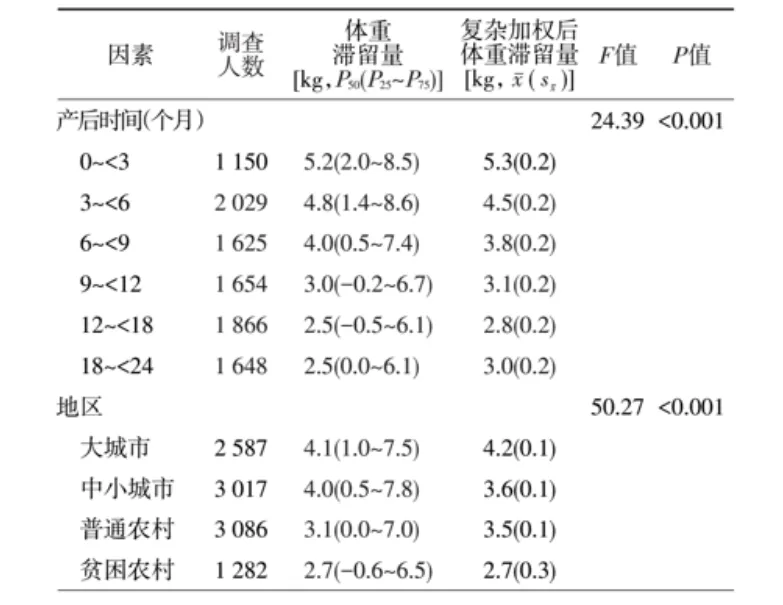
产后女性的肠道菌群变化
门水平
厚壁菌门(Firmicutes)是产后早期(<6周)和晚期(6周至1年)的优势菌门,部分研究还发现放线菌门(Actinobacteria)在产后期间的比例显著增加。
属水平
拟杆菌属在产后早期具有主导地位,也有研究发现Clostridiales在分娩后和产后4-6周内占优势。研究中常见的丰富菌属还包括:
为什么产后有些人很容易瘦,有些不容易?
产后肠道菌群组成的变化不仅仅是微生物学现象,更是体重调节与代谢健康的关键因素。肠道微生物组直接参与能量提取、内分泌代谢与脂肪分解过程,充当产后女性代谢调节网络中的核心枢纽。
当然,体重也会涉及其他方面因素,这里我们从肠道菌群的角度来分析:
★ 基线菌群组成不同
每个产妇初始肠道菌群组成存在个体差异;不同菌群组成可影响从相同食物中提取的能量总量,具有特定微生物组特征的人在相同热量摄入条件下,体重变化轨迹可能完全不同。
那些具有”瘦菌群”特征的产妇(如双歧杆菌、阿克曼氏菌丰度高,F/B比值低)更容易恢复体重;菌群多样性高的产后女性通常代谢恢复更为理想。
妊娠期遗留的菌群变化
妊娠期激素水平和代谢变化会改变肠道菌群,这些变化可能在产后持续存在,影响能量提取效率和代谢调节;菌群变化的恢复速度存在个体差异,检测肠道菌群的变化可以了解其恢复程度。
菌群对能量平衡、激素的调节
基于菌群特征,有些产妇从相同食物中获取更多能量,肠道菌群影响短链脂肪酸产生,进而影响脂肪燃烧和储存。
短链脂肪酸通过多种机制影响脂肪组织代谢:
特定菌群可促进脂肪组织褐变,增加能量消耗。
某些肠道菌如Dysosmobacter welbionis产生的12,13-diHOME能促进脂肪酸转运至棕色脂肪组织,增加能量消耗。
阿克曼氏菌被证明能增加褐变、脂肪酸氧化和棕色脂肪组织(BAT)活性,这一转化对能量消耗和代谢健康至关重要。
肠道菌群还通过影响胆汁酸代谢,间接影响激素水平,菌群可能影响产后激素敏感性,进而影响脂肪分解和糖代谢。
肠道屏障与炎症
肠道屏障功能受损时,细菌内毒素LPS可进入循环系统,激活炎症途径;LPS暴露改变脂肪因子分泌,与脂肪组织中巨噬细胞积累和促炎状态相关。
总之,产后体重恢复的个体差异在很大程度上取决于肠道菌群的组成与代谢功能,这些因素通过影响能量提取、脂肪储存、激素调节和炎症状态等多种机制,共同决定了产后女性体重恢复的难易程度和速度。了解和调节个人肠道菌群可能是未来产后体重管理的关键策略。
基于这一认识,产后营养补充不再是简单的能量与宏量营养素摄入,而应转向”营养-微生物-代谢”的整体观念。
产后营养
合理的产后营养不仅关乎体重管理,更是整体康复过程的基石。适当的营养摄入能够提升免疫功能,加速产后恢复,调节激素平衡,甚至对缓解产后抑郁情绪也有积极作用。
产后体重管理的重要时间窗口
产后1年内是体重恢复的关键时期,产后6个月左右恢复到孕前体重的女性,其后续10年超重的风险会较低。
因此,理解产后身体的特殊需求,并据此制定个性化的饮食策略,是帮助产后妈妈顺利度过产后恢复期的重要支持手段。
首先,产后的营养需求有什么特点?
产后女性对食物的吸收利用率往往有所变化,激素波动会影响消化系统功能,影响营养素吸收。
◆ 能量需求增加哺乳期每天额外需要约500卡路里能量以支持乳汁分泌。
《美国膳食指南(2020-2025)》建议,与哺乳期的孕前需求相比,哺乳期妇女在产后前6个月额外摄入330卡路里,6-12个月额外摄入400卡路里。
我国传统月子餐文化源远流长,”坐月子”被视为产后恢复的关键。传统观念认为产后女性处于特殊”虚弱”状态,需通过特定食物”补”回元气。传统月子餐通常以高能量、高蛋白、温热食物为主,如猪蹄、鸡汤、鲫鱼汤等。这些食物含有丰富蛋白质和胶原蛋白,有助于伤口愈合和组织修复。
然而,传统月子餐也存在局限性:过度强调高油高糖食物,食用红糖、米酒等”温补”食物可能导致血糖波动;单一食谱导致营养素摄入不均衡等。
◆ 蛋白质需求提高 乳汁分泌和身体组织修复都需要优质蛋白质支持。膳食蛋白质不仅是宿主营养的来源,也是肠道微生物的关键营养底物。
肠道菌群在蛋白质代谢中发挥着重要作用,特定菌群如拟杆菌属、梭状芽胞杆菌属和乳酸杆菌属能有效分解未消化的蛋白质,生成短链脂肪酸和多种氨基酸。产后如果肠道菌群紊乱,可能导致菌群分解能力下降,从而引起蛋白质消化不良,影响营养吸收效率。
适量优质蛋白摄入可促进双歧杆菌和乳杆菌等有益菌生长,形成良性循环,而过高或过低的蛋白质摄入都可能导致菌群失衡,影响产后恢复。此外,一些肠道菌群还能从头合成赖氨酸等必需氨基酸,并将其整合到宿主蛋白质中,为产后女性提供额外的营养支持。
◆ 微量营养素需求钙、铁、锌等微量元素与多种维生素的需求量也显著增加,比如铁、钙流失和骨质疏松风险上升,微量营养素缺乏对产后女性健康恢复造成显著影响。单纯补充有时并不有效,甚至可能产生不良副作用(如补铁引起的消化问题)。
肠道菌群在微量营养素代谢中扮演着关键角色,它们能够合成、转化和影响多种微量营养素的吸收与利用。
例如,特定的乳杆菌如Latilactobacillus sakei能产生叶酸(维生素B9),帮助改善宿主叶酸状态,同时增加短链脂肪酸产生;研究发现,维生素A的摄入与肠道微生物多样性呈正相关,特别是在孕期和产后,类胡萝卜素摄入充足的女性肠道微生物α多样性更高。
铁是许多细菌生长必需的营养素,但铁补充不当可能导致条件致病菌增殖,产生肠道不适。同时,某些菌群可提高微量营养素的生物利用度,如乳酸乳球菌N8和布拉酵母菌可将发酵食品中的核黄素和叶酸浓度提高40%-90%。
在这其中,肠道菌群与微量营养素之间存在重要的双向相互作用,在营养补充策略中需要加以考虑。
母乳喂养
美国儿科学会 (American Academy of Pediatrics) 推荐前 6 个月进行纯母乳喂养,然后继续母乳喂养并辅食至少 2 年。哺乳是一种能量密集型状态,理论上可以引起净负平衡,从而使产后体重减轻。
《美国膳食指南(2020-2025)》建议,与哺乳期的孕前需求相比,哺乳期妇女在产后前6个月额外摄入330卡路里,6-12个月额外摄入400卡路里。有稳定乳汁且想减重的女性可每天减少500卡路里摄入(相当于哺乳消耗的能量),但每天至少保持1800卡路里。这样可以每周减重1磅,4个月后可恢复孕前体重而不影响婴儿生长。
在哺乳期,坚持均衡的饮食,包括所有类别的常量营养素,对于维持母乳的成分和产量至关重要。一些流行的几种时尚饮食(例如,极低碳水化合物、旧石器时代、极低脂肪)可能会导致哺乳期妇女营养缺乏,应该避免。
膳食计划应强调营养丰富的全食物,如水果、蔬菜、豆类、全谷物和健康脂肪。选择纯素饮食的患者应评估并补充叶酸、维生素B12、铁、锌、胆碱、碘和EPA/DHA。
运动干预
剖宫产后,建议早期下床活动作为促进剖宫产后恢复(ERAC)方案的一部分。早期行走可缩短肠功能恢复时间、血栓形成风险和产后住院时间。
NICE指南:建议所有产后女性在6-8周后进行体重管理。

分期渐进:产后0-6周以低强度恢复性训练为主(如凯格尔运动、腹式呼吸),6周后逐步增加有氧与抗阻训练强度。
产后2天起:产褥期保健操(每1-2天增加1节,每节8-16次)。
产后6周后:逐步引入有氧运动(如散步、瑜伽),每周≥150分钟中等强度运动,分4-5次完成。
力量训练:针对核心肌群,改善基础代谢率。
为了安全起见,避免过早负重或高强度运动,运动强度以心率<140次/分钟为宜。
个体化:剖宫产者需延迟腹部加压训练至伤口愈合(通常8-12周),重点关注多裂肌与膈肌协同。
有效运动模式:
高强度间歇训练(HIIT)
RCT显示,每周3次、每次20分钟的HIIT(如自行车+深蹲组合)在12周内显著降低体脂率(-3.2% vs对照组-1.1%),且不影响母乳产量。
抗阻-有氧联合训练
对比静态核心训练与瑞士球训练,发现两者均能改善腰围(平均减少4.3cm)和内脏脂肪面积,但需结合饮食控制才能实现体重下降。
注:以上需结合自身状况,避免盲目锻炼。
中药调理
中药调理通过使用具有健脾祛湿功效的中药材,改善体内湿气过重。产后体虚、气血不足时,可在医生指导下服用补血益气类中药。
产后体重管理与全面康复是产后女性身体健康的一个方面,心理健康同样不容忽视,而肠道菌群失衡不仅影响代谢和体重,也直接参与情绪调节。产后激素波动引起的菌群变化,可能形成生理-心理-微生物的复杂互动网络。
当产后女性面临身体恢复压力的同时,还可能经历产后抑郁的困扰。这种情绪障碍影响产后妈妈健康的同时,也有可能传递给婴儿,影响下一代发育。因此,我们需要将产后照护视角从单纯的体重恢复拓展至情绪健康领域,探索肠道菌群在产后抑郁中的关键作用。
神经系统
产后抑郁症(PPD)是女性分娩后的常见疾病,症状包括情绪低落、易怒、睡眠障碍,严重时还会出现自杀或自杀意念。与产后抑郁相关的自杀是产后妇女死亡的主要原因,仅次于其他原因。
产后抑郁的发生率因地理位置而异,在经济发达国家为6.9%~12.9%,在经济欠发达或发展中国家超过20%。
近年来,社会和生活压力的增加与产后抑郁发病率的上升有关,这对患者的生活质量和身心健康产生了负面影响。病理机制很复杂,目前还不完全清楚。大多数学者认为,产后抑郁的发展可能是多因素的,受遗传、生理、心理、社会和家庭因素的影响。

一项荟萃分析显示,以下危险因素与产后抑郁相关:
• 妊娠糖尿病(OR = 2.71, 95%CI 1.78-4.14, I2 = 0.0%)
• 妊娠期抑郁(OR = 2.40, 95%CI 1.96-2.93, I2 = 96.7%)
• 孕妇生男孩 (OR = 1.62;95% CI 1.28-2.05;I2 = 0.0%)
• 妊娠期抑郁病史 (OR = 4.82,95%CI 1.32-17.54,I2 = 74.9%)
• 抑郁病史 (OR = 3.09,95%CI 1.62-5.93,I2 = 86.5%)
• 分娩时硬膜外麻醉 (OR = .81,95%CI .13-4.87,I2 = 90.1%)
产后抑郁症不仅影响母亲的身心健康和家庭关系,还通过多种途径传递给宝宝,影响宝宝的大脑发育。
抑郁状态下的妈妈往往缺乏与宝宝的积极互动,减少了皮肤接触和情感交流,这也会影响婴儿的神经系统发育。
可能通过喂养习惯的改变和照料质量下降影响宝宝,也可能通过母乳微生物群影响宝宝的肠道菌群定植,进而影响宝宝的认知发展和情绪调节能力。
产后一个月的这段时期对婴儿肠道菌群建立至关重要,而这正是大多数婴儿完全依赖母乳的阶段。一项研究发现,产后母亲压力与母乳微生物组成之间存在关联,研究发现,高压力组母亲的乳汁中链球菌、Gemella、Veillonella含量显著降低,而葡萄球菌、棒状菌和不动杆菌的含量升高,这些部分是条件致病菌。母亲的压力状态会影响乳汁的微生物组成,这可能会进一步影响婴儿肠道菌群的定植和后续的健康发展。
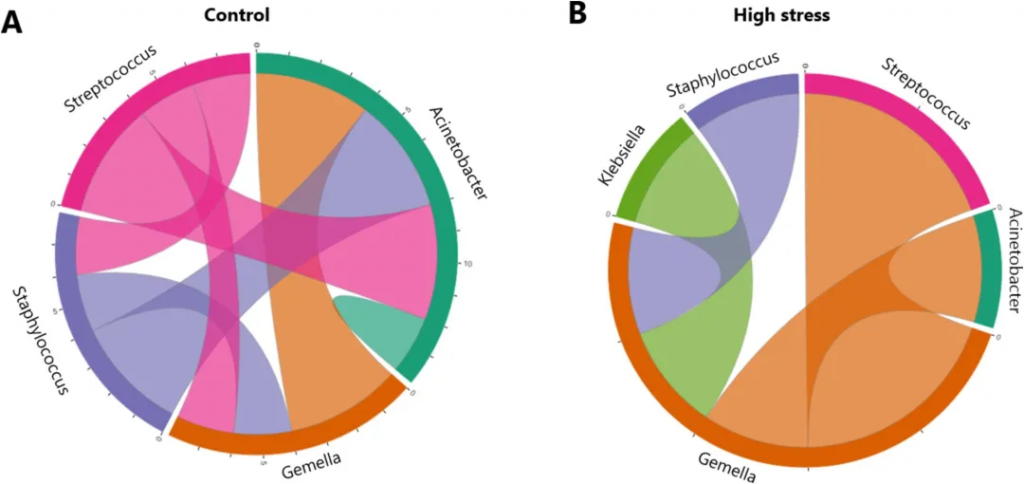
doi.org/10.1016/j.bbi.2024.11.020
链球菌和Veillonella的减少可能通过影响短链脂肪酸(SCFAs)的产生影响大脑发育,短链脂肪酸可穿过血脑屏障,对神经发育至关重要。
这种情况如果得不到及时干预,宝宝发育问题可能让产后妈妈的情绪雪上加霜,陷入恶性循环,导致抑郁症状加重,而对宝宝的影响也将长时间持续。
这种早期的微生物群失衡可能对宝宝的神经发育产生长期影响。研究发现,早期肠道菌群不健康与儿童期注意力缺陷、认知障碍、情绪调节问题甚至自闭症谱系障碍风险增加相关。由于大脑发育的关键期正是生命最初几年,这种影响可能会一直持续到青少年甚至成年期,形成跨代际的健康问题传递。
因此,针对产后抑郁的早期识别和干预至关重要。
产后抑郁治疗的困境
目前产后抑郁的治疗通常包括抗抑郁药、心理干预和激素补充。然而,这些方法经常出现副作用,表现出不一致的长期有效性,并可能在母乳中积聚,可能影响婴儿,从而限制其临床效用。
***
科学界开始逐渐认识到产后期女性不仅经历着激素的剧烈波动,也同时面临着肠道微生物生态的显著变化。这种变化并非独立存在,而是通过”肠-脑轴“与产后情绪密切相关。研究表明,肠道微生物通过产生多种神经递质和生物活性物质,如血清素(5-HT)、γ-氨基丁酸(GABA)、多巴胺等,直接影响中枢神经系统功能。
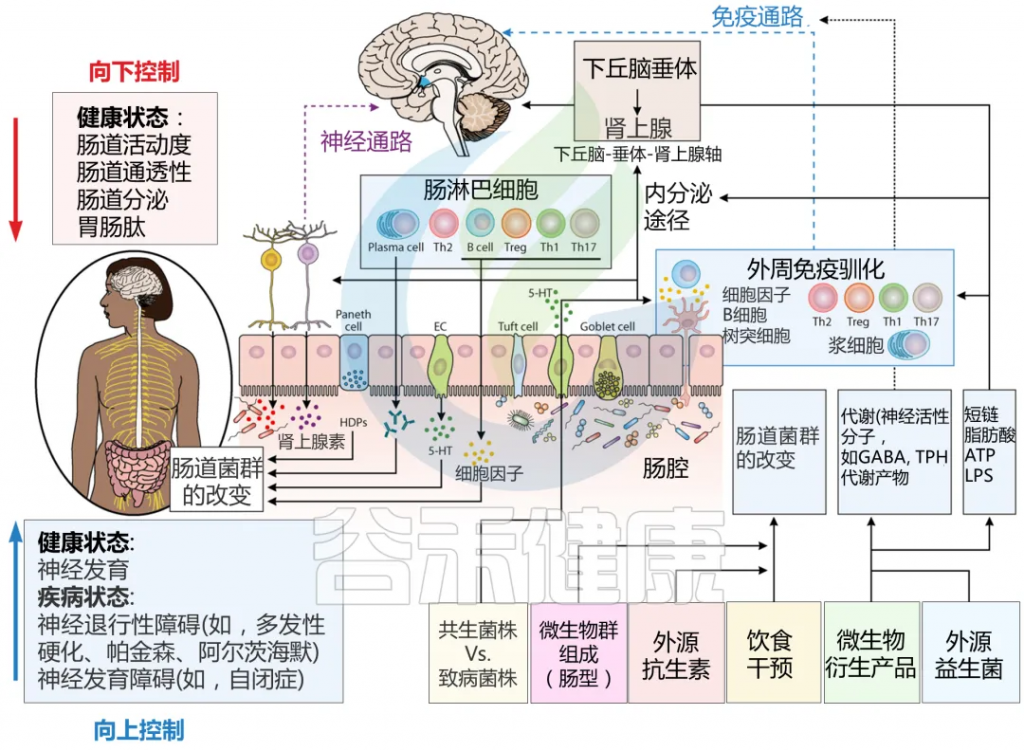
Sorboni SG, et al.,Clin Microbiol Rev. 2022
关于肠-脑轴详见我们之前的文章:
特别值得注意的是,血清素的合成受到肠道微生物群的显著调节,而血清素水平的异常与抑郁症状密切相关。肠道微生物还通过产生短链脂肪酸等代谢物,调节免疫系统功能,改善肠道屏障完整性,减少炎症反应。
这些发现为我们打开了理解产后抑郁的新视角——肠道微生物群的失衡可能是连接激素波动、免疫功能改变和情绪障碍的关键环节。
一项孟德尔随机化分析研究表明,产后抑郁患者的厚壁菌门与拟杆菌门之比(F/B)显著增加,这种菌群失衡与促炎状态相关。
α-变形杆菌属(属于变形杆菌门)、Clostridialesvadin BB60(属于拟杆菌属)和韦荣球菌科(属于厚壁菌门)与抑郁症风险的发展有关。
菌群“守护者”与“破坏者”的博弈
韦荣菌科(Veillonellaceae)通过代谢短链脂肪酸和脂多糖,增强肠道通透性,并激活Toll样受体通路,促进炎症因子释放,进而影响神经可塑性,这可能解释其在抑郁风险中的双重作用。
Clostridiales vadin BB60的保护作用可能通过调节F/B比值实现,与5-HT水平呈正相关,可能通过维持色氨酸代谢稳态发挥保护效应,但其具体机制需结合其对色氨酸代谢的影响进一步阐明。
RuminococcaceaeUCG011(保护性菌群)丰度下降会直接削弱其对5-HT的正向调节作用,5-羟色胺是一种与积极情绪相关的神经递质。
在产后抑郁大鼠模型中,该菌属的减少导致5-羟色胺合成酶(TPH)表达降低,从而引起5-羟色胺水平下降,可能导致情绪和行为调节障碍。
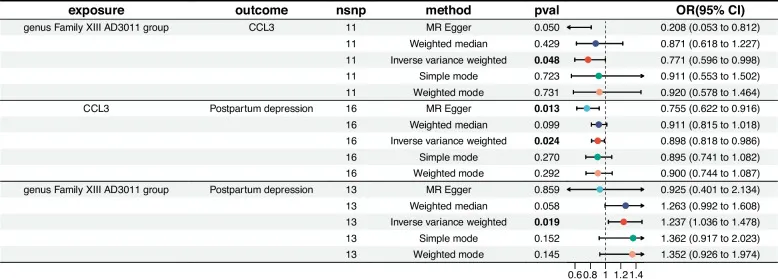
doi: 10.1186/s12884-025-07304-w
炎症——连接肠道菌群与产后抑郁的另一关键
血清趋化因子CCL5(OR=0.878)和CCL3(OR=0.898)水平升高与产后抑郁风险降低显著相关,但其作用机制独立于Family XIII AD3011属的致病效应。
动物实验证实,LPS诱导的神经炎症可导致海马神经元损伤和下丘脑-垂体-肾上腺(HPA)轴过度激活,最终引发皮质醇水平持续升高及突触可塑性受损。
通过对炎症介质的调节,可能能够降低产后抑郁的风险。这一理论为寻找新的干预手段提供了可能的方向。例如,益生菌或其他饮食干预策略被认为能够改善肠道菌群组成,并且有潜力减轻与产后相关的情绪障碍。
目前临床主要通过量表筛查进行初步判断,例如爱丁堡产后抑郁量表(EPDS),然而,量表评估依赖主观感受,可能存在漏诊或延迟干预的风险。近年来科研领域开始关注肠道菌群等相对客观生物标志物与产后抑郁的关联。
纵向研究表明,不同抑郁症状强度的孕产妇肠道菌群存在差异。
产后早期:在产后住院期间(产后1-3天)
中重度抑郁症中Enterobacteriaceae高
中重度抑郁症状组(MG组) Enterobacteriaceae细菌相对丰度显著高于轻度/无抑郁症状组(4.9%vs1.0%,p<0.05)。
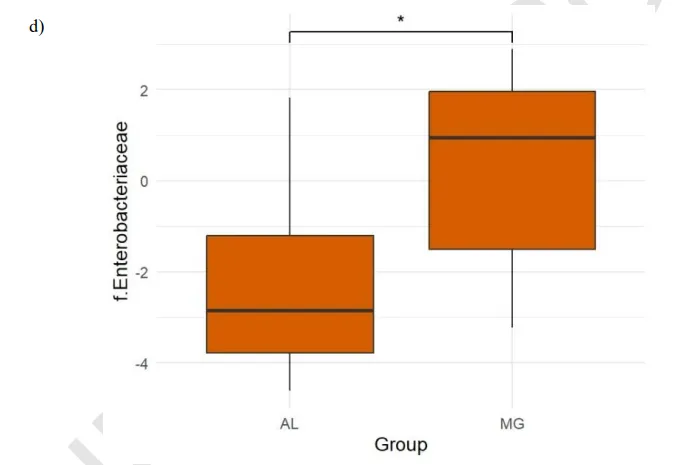
doi.org/10.47626/1516-4446-2024-3721
肠杆菌科细菌由革兰氏阴性菌组成,这些细菌可以转移到循环和淋巴系统,促进免疫反应的增加和炎性细胞因子的释放,如IL-1、IL-6等,这些细胞因子可以穿过血脑屏障并导致神经炎症,这是抑郁症女性的常见情况。
双歧杆菌属增加与抑郁症状评分(EPDS)降低存在相关趋势(p=0.2, cor= -0.19);Enterobacteriaceae与双歧杆菌属之间存在负相关趋势(cor:-0.14, p=0.2)。在接受精神治疗的中重度抑郁组中,双歧杆菌属的丰度随着时间的推移而增加。轻度/无症状组产后Faecalibacterium属丰度较高。
这项研究突显了将肠杆菌科(Enterobacteriaceae)视为妊娠晚期和产后恢复期间母体抑郁症状发作的合理生物标志物或促成因素的重要性。
识别出具有潜在预防或治疗意义的生物标志物,将有助于早期干预和个体化的治疗方案制定,最终减轻产后抑郁对母婴健康的影响。
临床应用思路
像上述研究证据,可以构建多模态评估体系:
通用益生菌、益生元等干预方式
编辑
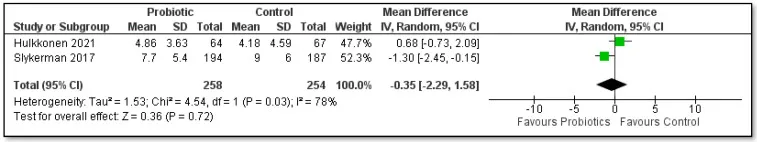
——直接干预:产后母亲补充益生菌
鼠李糖乳杆菌HN001
针对438名孕妇的双盲试验显示,补充HN001组产后6个月抑郁评分(EPDS)降低(Slykerman et al., 2017)。结果显示,焦虑评分(STAI-6)降低34%,抑郁风险减少50%(p=0.037)。
复合菌株干预
超重孕妇补充鼠李糖乳杆菌HN001+动物双歧杆菌420,产后12个月抑郁症状减轻(Hulkkonen et al., 2021)。
局限性:需联合鱼油使用,单独益生菌效果未达统计学显著。
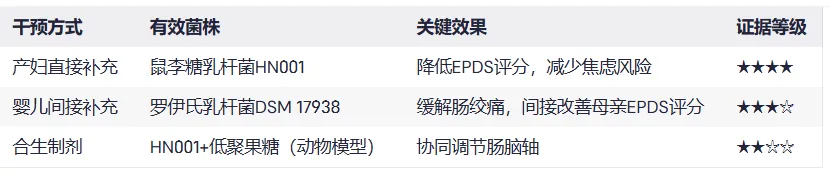
doi: 10.3390/healthcare10060970
——间接干预:婴儿补充益生菌
罗伊氏乳杆菌DSM 17938
42名肠绞痛婴儿补充该菌株28天,母亲EPDS评分较安慰剂组降低2.3分(p<0.01)(Mi et al., 2015)。减少婴儿哭闹时长,缓解母亲育儿压力。
doi: 10.3390/healthcare10060970
个性化干预
基于上述纵向研究,如果产后女性情绪波动较大,量表评分趋于临界值,肠道菌群检测报告中有上述特征,肠杆菌较高,双歧杆菌较低,则可以针对性补充双歧杆菌来平衡肠道微生态,或者补充相关益生元为肠道有益菌提供养分,或者针对肠杆菌较高的情况进行饮食干预,吃西兰花、菠菜、胡萝卜等,具体情况因人而异。
有时候并不是简单地通过一个菌的高低来判别,而是要看个人肠道生态平衡状态,谷禾肠道菌群检测报告提供了更为精准的个体化干预方案。报告通常包含肠道菌群多样性评估、关键菌种分析以及代谢功能预测,尤其可以关注与情绪调节相关的微生物组成变化,如果偏高或者偏低,则有相关饮食、生活方式等干预措施,为产后女性提供个性化的调整建议。
产后女性可以在传统治疗方法之外,获得一种安全有效的补充干预途径,帮助她们更好地度过产后适应期,降低产后抑郁的风险。
维生素D
维生素D通过调节下丘脑-垂体-肾上腺轴(HPA轴)和促进神经递质合成发挥抗抑郁作用。
伊朗一项病例对照研究发现,维生素 D 水平低的妇女在分娩后 6-8 周患抑郁症的风险更大。
一项荟萃分析研究表明,低水平的维生素 D(低于 50 nmol/l)与产后抑郁的风险增加 3.67 倍相关。
从肠道菌群的角度,补充维生素D增加肠道菌群多样性,普氏菌属丰度增加,而嗜血杆菌和韦荣氏球菌丰度降低;促进双歧杆菌等益生菌生长,这些菌群参与血清素合成。维持肠道屏障完整性,减少促炎因子释放,调节免疫系统,改善Th17/Treg平衡。
一项研究发现,在怀孕的最后 2 周和分娩后的前 8 周每天服用 2,000 单位维生素 D 可以降低患产后抑郁的风险。
一项临床研究还发现,服用 2000 IU/d 的维生素 D 可以减轻抑郁症状。
B族维生素
维生素 B1 (硫胺素)
硫胺素是一种水溶性维生素,不会储存在体内,必须每天从牛肉、鸡肉、谷物、坚果和豆类等来源摄入。孕妇和哺乳期妇女每日需求量为 1.4 毫克。它对神经递质合成和能量产生至关重要,其缺乏会导致脑干变化和抑郁症状。补充硫胺素可以改善这些症状。
维生素 B2 (核黄素)
核黄素常见于乳制品、瘦肉、肝脏、绿叶蔬菜和酵母中,一项队列研究表明,适量摄入维生素 B2 有助于降低患产后抑郁的风险。
维生素 B6 (吡哆醇)
维生素 B6 或吡哆醇可以来自肉类、家禽、鱼、蛋、白土豆和淀粉类蔬菜。这种维生素对于血清素和多巴胺等必需神经递质的生物合成至关重要,这些神经递质可以改善情绪和认知功能。
抑郁症患者的同型半胱氨酸水平通常较高,而叶酸和维生素 B6 水平较低。同型半胱氨酸是一种非必需的硫氨基酸,对血管有毒并导致氧化应激和细胞死亡。 一项研究表明,服用维生素 B6 可以独立降低产后抑郁的发病率。
维生素 B12
血液中维生素B 的正常水平在147.6~664.2 pmol/L 之间。VB12 缺乏导致同型半胱氨酸水平增加以及叶酸和 VB12 效率降低,因为它被困在 5-甲基四氢叶酸循环中,而不是四氢叶酸的活性形式。
叶酸和VB12 在中枢神经系统的几种代谢途径中起着至关重要的作用。血清同型半胱氨酸水平升高表明VB12 和叶酸缺乏,见于抑郁症患者。
也有一项系统评价发现血清VB12、叶酸、铁蛋白水平与产后抑郁风险之间没有关联。
补充VB12 和叶酸可能在一定程度上提供保护作用,降低这些疾病的发病风险。
关于B族维生素和肠道菌群的关联,在我们之前的文章中有详细阐述:
铁
红肉、肝脏、种子、豆类和牡蛎等食物是铁的丰富来源。各种研究表明,与其他母亲相比,患有贫血的女性往往会经历更严重的产后抑郁。妊娠期贫血的诊断和治疗有助于降低患产后抑郁的风险。此外产后低铁蛋白水平也会导致产后抑郁。
中国一项涉及 1,592 名女性的队列研究表明,从怀孕期间开始摄入铁超过 6 个月有助于降低分娩后 6 个月和 12 个月患抑郁症的风险。
然而,另一项研究发现母体血清铁与产后抑郁症状之间没有关联。
一项对 649121 样本进行的 10 年高质量队列研究表明,在分娩后第一年,贫血和抑郁症之间存在显著关联。
维生素 C
维生素 C 在防止氧化应激方面起着至关重要的作用。它还充当一组酶的辅助因子,这些酶负责调节和合成整个身体的重要功能。
一项研究表明,高剂量的维生素 C(每天 3 克)可以降低 PPD 的严重程度。然而,另一项研究发现,压缩的橙皮滴剂对 PPD 或焦虑没有任何影响。
锌
锌是一种稀有金属离子,是人体中仅次于钙的第二大元素。它在免疫和内分泌系统中都起着至关重要的作用。锌负责刺激和抑制中枢神经系统中的化学介质。
根据一项全面的荟萃分析,抑郁症女性的血锌水平(1.85 μmoll/L)低于非抑郁症女性。
此外,一项系统评价发现,低锌水平与产后抑郁风险较高有关。然而,几项研究表明血清锌水平与产后忧郁综合征之间没有相关性。
此外,一项临床试验发现,锌对减轻产后焦虑和抑郁症状没有显着影响。
必需脂肪酸
必需不饱和脂肪酸,也称为多不饱和脂肪酸 (PUFA),分为两大类:n-6 和 n-3。
Omega-3 是一种亚麻酸,来自三个脂肪组,即 α-亚麻酸(ALA)、二十碳五烯酸(EPA)、二十二碳六烯酸(DHA)。n-3 多不饱和脂肪酸摄入量与产后抑郁之间的显著正相关。
研究表明,低水平的 omega-3 脂肪酸与产后抑郁高风险之间存在联系。其中,DHA 的作用更为明显。怀孕和哺乳自然会降低 DHA 水平。
然而,DHA 和产后抑郁之间的联系并不一致。在一项干预研究中,即使血清水平较低的女性每天摄入 200 毫克 DHA,产后前 4 个月内产后抑郁的患病率也没有变化。
一些研究发现鱼类摄入量或 omega-3 补充剂与产后抑郁之间没有相关性。一般来说,系统评价无法在omega-3脂肪酸和产后抑郁之间建立有效的关系。然而,素食中产后抑郁的患病率高于杂食性饮食。
碳水化合物
碳水化合物在能量产生中起着至关重要的作用,会影响情绪。研究表明,怀孕会导致胰岛素抵抗,这会使女性更容易患抑郁症和葡萄糖耐量受损。
一项队列研究发现,患有妊娠糖尿病的女性在怀孕和产后患抑郁的风险明显更高。此外,据推测,分娩后胰岛素水平降低,会降低血清素水平并导致抑郁症。血糖水平的波动也会导致炎症和脂肪因子标志物的分泌,例如白细胞介素IL-6,这些标志物与产后抑郁有关。
一项队列研究发现血糖指数与产后抑郁之间没有关联。
最后,低碳水化合物饮食往往会增加患抑郁症的风险,因为它们会减少大脑中血清素的产生。然而,富含碳水化合物的食物通过触发色氨酸的产生来促进幸福感。
临床实践中,产后女性补充维生素可以结合肠道菌群检测报告,针对个体差异制定个性化补充方案,以达到改善肠道菌群结构、提升情绪状态的最佳效果。
整合检测与干预
基线评估:产后进行首次肠道菌群检测与心理健康评估,建立个体基准数据。
分层干预:
动态监测:3个月左右复查肠道菌群和情绪状态,及时调整干预方案。
通过”检测-干预-评估-调整”的模式,产后女性可以获得高度个性化的维生素补充方案,靶向调节肠道菌群生态,有效支持情绪调节系统,实现身心健康的协同优化。
产后便秘、高血糖
产后便秘在新妈妈中较为常见,据相关研究显示,产后便秘的发生率在不同地区和人群中有所差异,但总体上可达到 20% – 40%。顺产和剖宫产的产妇均可能出现便秘问题,但剖宫产产妇由于手术和卧床休息等因素,便秘的发生率相对更高。长期便秘还可能增加患肠道疾病的风险。
分娩过程中抗生素使用、应激反应以及生理变化都会扰乱原有的肠道菌群平衡。特别是剖宫产女性,抗生素使用可能导致肠道菌群短期内显著改变,抗生素引起的生态失调会导致胆碱能神经元和整体肌间神经元减少,影响肠道蠕动。
产后盆底肌肉松弱或损伤会影响排便功能,而肠道运动减慢进一步导致粪便在肠道停留时间延长。关于盆底肌康复在下一章节介绍。
产后女性饮食习惯改变(如纤维摄入不足)、活动减少、水分摄入不足等因素,直接影响肠道菌群组成。
干预措施
饮食
增加膳食纤维的摄入是缓解产后便秘的重要方法。产妇应多吃蔬菜、水果、全麦面包等富含膳食纤维的食物,以增加粪便体积,促进肠道蠕动。同时,保持充足的水分摄入也很重要,每天至少饮用1500-2000毫升水,有助于软化粪便,使其更容易排出。
生活方式
适当运动可以促进肠道蠕动,缓解便秘症状。产后身体条件允许的情况下,新妈妈可以进行一些简单的运动,如散步、产后瑜伽等。
每天坚持 30 分钟左右的运动,有助于增强腹肌力量,促进排便。
定时排便训练
晨起或餐后2小时内尝试排便,利用生理性肠蠕动高峰(胃结肠反射)建立规律。
药物辅助
在医生指导下使用开塞露等药物,但不宜长期使用,以免形成依赖。乳果糖口服溶液也可在医生指导下使用,增加大便体积,缓解便秘。
中药如黄连上清丸、枳实导滞丸等,具有健脾消食、通腑泻下的作用,适用于产后气血虚弱所致的便秘。
腹部按摩
顺时针方向轻柔地按压下腹部,每次持续5-10分钟,有助于促进肠胃蠕动,缓解便秘症状。
以上是普适性的干预方式,我们也了解到,产后便秘的发生与肠道菌群失调密切相关,每个人肠道菌群不一样,便秘的原因也可能不一样。通过专业的肠道菌群检测,可以了解产后女性肠道微生物组成的具体情况,比如产丁酸菌的丰度、双歧杆菌和乳杆菌等有益菌的数量,以及潜在致病菌如艰难梭菌的水平。
如果是菌群紊乱的原因,那么结合菌群检测结果进行精准干预效果会更为显著。例如,对双歧杆菌缺乏的产妇可重点补充特定双歧杆菌株;对产丁酸菌不足者,可增加膳食纤维和低聚果糖等益生元摄入。
谷禾肠道菌群检测报告有便秘相关菌群过多或过少的提示,根据个人菌群报告可以有针对性地干预。
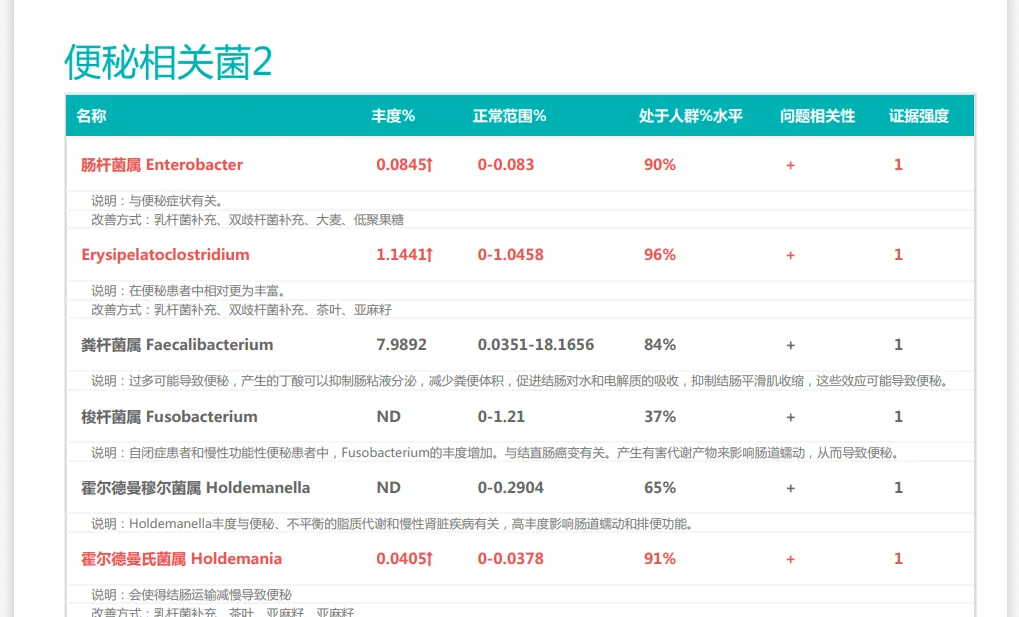
<来源:谷禾健康肠道菌群检测数据库>
这种个性化的微生物干预策略,不仅能更有效缓解便秘症状,还能从根本上改善肠道微生态环境,促进产后整体健康恢复。
一小部分女性产后出现血糖调节能力异常的状况,更有甚者这些女性可能会在产后5-10年内发展为2型糖尿病。
产后高血糖的常见表现
餐后异常疲劳感、口渴增加、排尿频繁、视力模糊、伤口愈合缓慢,以及无法解释的体重变化。
为什么产后会出现血糖波动?
分娩后胎盘激素急剧下降,理论上有利于胰岛素敏感性恢复,但实际情况更为复杂。
产后激素变化剧烈,催乳素和皮质醇水平波动可直接影响血糖;激素变化也会改变肠道菌群组成。
研究表明妊娠期糖尿病患者的肠道菌群失调在产后8个月仍然存在,拟杆菌减少,厚壁菌增加,这种菌群失衡直接影响肠道产生的短链脂肪酸水平,进一步影响胰岛素敏感性。
睡眠不足和作息紊乱会增加应激激素分泌,干扰胰岛素功能;这些因素也会改变肠道微生态环境,导致肠道通透性增加,使细菌代谢产物和内毒素进入血液循环,引发低度炎症反应。
产后恢复期能量消耗模式变化,哺乳消耗增加而活动量可能减少;
产后子宫收缩、伤口愈合和组织修复过程会导致代谢状态波动。同时,身体组成变化如脂肪分布调整也会影响葡萄糖代谢。这些生理变化通过改变肠道微环境pH值、氧气含量和营养物质分布,进一步影响肠道微生物组成。
这些因素共同作用,使产后血糖波动大且不可预测,特别是在产后头三个月。
产后阶段是女性身体快速恢复和调整的关键期,尤其对于妊娠期糖尿病的新妈妈,这一时期的营养管理更为重要,直接关系到恢复质量和未来健康风险。
肠道菌群检测帮助早期风险预警,辅助干预
相比传统血糖检测,菌群变化可能是代谢异常的更早期信号,为高风险人群提供预防性干预的时间窗口。
通过肠道菌群检测识别个体特异性的菌群失衡模式,结合临床指标(如炎症因子IL-6、皮质醇水平)建立个人”菌群-代谢”关联模型。
跟踪干预措施对肠道菌群的调节效果,为调整干预方案提供客观依据。
相关产后康复中心或临床营养或健康管理机构,可以根据菌群结构设计低血糖指数的膳食模式,针对特定菌群不足,选择相应的益生元食物。基于个体菌群特性,调整蛋白质、脂肪和碳水化合物的比例。
这种微生态层面的干预不仅能帮助产妇更有效地管理血糖,还能从根本上改善代谢健康,降低未来发展为2型糖尿病的风险。
盆底肌损伤
产后盆底肌损伤是许多产妇面临的常见问题。盆底肌损伤会引发尿失禁、漏尿、性生活质量下降、盆腔器官脱垂、衰老等问题。研究表明,产后妇女盆底功能异常发生率为50-64%。
什么是盆底肌?
盆底肌是指位于骨盆底部的一组肌肉和筋膜组织,像一张“吊网”一样支撑着盆腔内的器官,包括膀胱、子宫、阴道和直肠等。盆底肌在维持盆腔器官正常位置、控制排尿和排便、支持性功能以及保持盆腔稳定等方面发挥着重要作用。
编辑
盆底肌损伤的原因
分娩压力:分娩过程中,胎儿通过产道时会对盆底肌肉施加巨大压力,导致肌肉损伤或拉伸,同时阴部神经牵拉导致神经传导功能下降,引发肌肉失用性萎缩。
激素变化:妊娠期孕激素和松弛素水平升高,抑制胶原蛋白合成,降低盆底肌的承托能力;产后雌激素骤降则延缓肌肉修复进程。
体重增加:怀孕期间体重的增加也会对盆底肌肉造成额外负担。
产后盆底肌修复
盆底肌训练(PFMT)
盆底肌训练是预防和治疗产后尿失禁的有效方法。训练通常包括收缩和放松盆底肌肉的动作,如凯格尔运动(Kegel exercises),并建议在专业理疗师或护理护士的指导下进行。
具体做法是找到盆底肌肉,在排尿时尝试中断尿流,然后收紧并上提盆底肌,保持5秒钟,然后放松10秒钟,每天进行3次,每次10-15分钟。
注:美国妇产科医生 Dr. Arnold Kegel 于 1948 年创建了盆底肌锻炼法,简称 Kegel 法,即指导患者做提肛运动。通过自主的、反复的盆底肌肉群的收缩和舒张,增强支持尿道、膀胱、子宫和直肠等脏器的盆底肌张力,恢复盆底肌功能。
生物反馈疗法
生物反馈疗法通过监测盆底肌肉的活动,让产妇直观了解自身肌肉收缩情况,帮助患者正确执行训练动作,提高康复效果。
电刺激疗法
电刺激疗法则通过特定频率和强度的电流刺激盆底肌肉或腹部肌肉,促进肌肉收缩,增强肌力。
一般来说,一周 3-5 次治疗,一疗程 10 次,每次 20-30 分钟,2-3 疗程。
但电刺激治疗需要专业设备和技术支持,且治疗过程可能会给产妇带来不适感。
中医调理
补肾固涩类方剂:如四神丸、金匮肾气丸等,用于调节内分泌系统,缓解压力性尿失禁。
健脾利水类中药:适用于气血虚弱导致的尿失禁及漏尿。
针灸疗法:通过在特定穴位如百会穴、关元穴等进行针刺,促进血液循环,帮助盆底肌修复。
手术治疗
对于严重的盆底肌损伤,如盆腔器官脱垂,严重尿失禁,影响日常生活,可能需要手术治疗。
尿道中段悬吊术(TVT/TOT):治愈率达85%-90%,但5年内复发率约10%-15%,且可能引发膀胱穿孔。
其他
使用盆底康复仪进行训练,可以帮助患者更有效地进行盆底肌锻炼。
针对性训练如腹式呼吸、脚趾叩击等也有助于增强盆底肌肉的力量。
多模式康复方法
多模式康复方法通过综合多种手段,以达到最佳康复效果。
Wang 等人的研究中,48 名产后腰骶骨盆疼痛女性参与随机对照试验,干预组接受为期 12 周的盆底肌训练结合腰背部肌肉神经肌肉电刺激,对照组仅接受神经肌肉电刺激。结果显示,干预组在 6 周和 12 周时疼痛、功能障碍和生活质量的身体领域均有显著改善。
进一步的研究由 Bhat 等人完成,比较了结合性唤起的凯格尔训练与单独凯格尔训练对产后盆底肌力和性功能的提升效果,涉及性活跃的初产阴道分娩女性。结果显示,结合性唤起的组别在每月评估中盆底肌力和性功能均有显著提升。这进一步证实了多模式康复方法的有效性,为产后康复提供了更多选择和可能性。
总的来说,骨盆底训练成为最常见的方法,躯干稳定练习和电刺激也强调恢复骨盆和核心力量。此外,创新技术,如脊椎按摩疗法,针灸等也是不断发展的产后护理方式。
这些产后康复方法不仅关乎生理恢复,更与产妇心理健康密切相关。研究表明,身体不适与心理健康之间存在双向互动关系。当产后女性遭受尿失禁、便秘或持续疼痛等困扰时,往往伴随着自尊心降低和社交回避倾向。
随着症状改善,产后女性对身体恢复的信心增强,减轻对永久性损伤的焦虑;其次,运动本身促进内啡肽分泌,天然调节情绪;运动通过影响肠道菌群组成间接改善了与情绪调节相关的神经递质平衡。
每一位母亲的产后康复都应被视为身心一体的整体康复过程。专业机构在设计产后康复方案时,如果超越传统的身体功能修复视角,整合肠道菌群调节的微生态方法,则能建立更全面、更有效的产后健康支持体系,帮助每位妈妈在迎接新生命的同时,也能守护自己的身心健康。
产后女性经历剧烈的生理重构,从激素波动到代谢变化,这些变化直接影响肠道微生态,而肠道菌群失衡又反过来影响产后恢复质量,形成复杂的双向调控网络。正是这种复杂的生理重构过程,使得产后康复面临独特挑战。
肠道菌群作为人体最大的微生态系统,不仅参与营养物质代谢和免疫调节,还通过肠-脑轴直接影响情绪和认知功能,是连接产后各种健康问题的核心纽带。通过解析产后女性独特的菌群变化特征,可以更精准地把握康复关键,从根本上促进身体各系统协调恢复。
目前,在临床应用中,肠道菌群检测不仅可辅助诊断产后抑郁、便秘和血糖异常等问题,更能通过”菌群-疾病”关联模型指导个性化治疗方案设计,减少药物依赖,缩短治疗周期。
月子中心可基于菌群检测结果定制营养餐,调节双歧杆菌、产丁酸菌等关键菌群,同时通过环境菌群优化降低感染风险,为母婴健康奠定微生态基础。
对健身机构而言,菌群检测结合训练能显著提升燃脂效率,使腰围减少更显著。健康管理机构通过菌群监测预警代谢风险,实施早期干预,避免产后5-10年内发展为2型糖尿病的风险。
未来,肠道菌群检测将与数字技术深度融合,推动产后康复服务从”经验型”向”精准型”转变。菌群检测+AI分析将实现健康异常早期预警;功能性菌株筛选与应用将催生新一代产后康复产品;母婴菌群联动管理将形成全新的家庭健康解决方案。
临床-科研-产业-政策四维联动机制,可以共同构建如”产后菌群健康分级评估指南”,制定产后菌群健康指导标准,推动产后菌群药物和营养品开发,为产后康复提供科学指导。
注:本账号内容仅供学习和交流,不构成任何形式的医疗建议。
主要参考文献
Mota AS, Sparvoli LG, Vanzele PAR, Naspolini NF, Tobaruela EC, Yoshizaki CT, Francisco RPV, Oliveira AMSS, Galletta MAK, Tess VLC, Taddei CR. Longitudinal Gut Microbiota Composition During Perinatal period in Women with Different Intensities of Depressive Symptoms. Braz J Psychiatry. 2024 Sep 21.
Wallace CJ, Audet MC. Diet and the gut microbiota-immune axis in the context of perinatal mental health: Protocol for a prospective cohort study. Womens Health (Lond). 2024 Jan-Dec;20:17455057241277072.
Wallace CJ, Audet MC. Diet and the gut microbiota-immune axis in the context of perinatal mental health: Protocol for a prospective cohort study. Womens Health (Lond). 2024 Jan-Dec;20:17455057241277072.
Macphail MG, Juul S, Wollny K, Negre JY, Metcalfe A, Chaput KH, Butalia S, Nerenberg KA. Nutrition Interventions for Lowering Cardiovascular Risk After Hypertensive Disorders of Pregnancy: A Systematic Review. CJC Open. 2023 Nov 4;6(2Part B):195-204.
Trifkovič KČ, Mičetić-Turk D, Kmetec S, Strauss M, Dahlen HG, Foster JP, Fijan S. Efficacy of Direct or Indirect Use of Probiotics for the Improvement of Maternal Depression during Pregnancy and in the Postnatal Period: A Systematic Review and Meta-Analysis. Healthcare (Basel). 2022 May 24;10(6):970.
Strobel KM, Juul SE, Hendrixson DT. Maternal Nutritional Status and the Microbiome across the Pregnancy and the Post-Partum Period. Microorganisms. 2023 Jun 13;11(6):1569.
Weerasuriya W, Saunders JE, Markel L, Ho TTB, Xu K, Lemas DJ, Groer MW, Louis-Jacques AF. Maternal gut microbiota in the postpartum Period: A Systematic review. Eur J Obstet Gynecol Reprod Biol. 2023 Jun;285:130-147.
Ghaedrahmati M, Alipour Z. The Association between Post-Partum Depression and Nutrition and Dietary Patterns: Systematic Review. Iran J Nurs Midwifery Res. 2024 Jul 2;29(3):280-289.
Neumann CJ, Pausan M-R, Haid V, Weiss E-C, Kolovetsiou-Kreiner V, Amtmann B, Winkler P, Mahnert A, Jantscher-Krenn E, Moissl-Eichinger C. The dynamics of the female microbiome: unveiling abrupt changes of microbial domains across body sites from prepartum to postpartum phases. Microbiol Spectr. 2024 Jun 25;12(8):e0014724.
Dellapiana, G., Nguyen, Q.T. & Naqvi, M. Navigating Postpartum Weight Loss: Evidence and Interventions. Curr Obstet Gynecol Rep 13, 207–212 (2024).
Ionescu RF, Enache RM, Cretoiu SM, Gaspar BS. Gut Microbiome Changes in Gestational Diabetes. Int J Mol Sci. 2022 Oct 25;23(21):12839.
Hasain Z, Mokhtar NM, Kamaruddin NA, Mohamed Ismail NA, Razalli NH, Gnanou JV, Raja Ali RA. Gut Microbiota and Gestational Diabetes Mellitus: A Review of Host-Gut Microbiota Interactions and Their Therapeutic Potential. Front Cell Infect Microbiol. 2020 May 15;10:188.
Hasain Z, Mokhtar NM, Kamaruddin NA, Mohamed Ismail NA, Razalli NH, Gnanou JV, Raja Ali RA. Gut Microbiota and Gestational Diabetes Mellitus: A Review of Host-Gut Microbiota Interactions and Their Therapeutic Potential. Front Cell Infect Microbiol. 2020 May 15;10:188.
Ohene-Agyei P, Iqbal A, Harding JE, Crowther CA, Lin L. Postnatal care after gestational diabetes – a systematic review of clinical practice guidelines. BMC Pregnancy Childbirth. 2024 Nov 4;24(1):720.
Xu H, Liu R. Comprehensive management of gestational diabetes mellitus: practical efficacy of exercise therapy and sustained intervention strategies. Front Endocrinol (Lausanne). 2024 Oct 3;15:1347754.
Gunabalasingam S, Kyrka A, Hopkins L, Lebrett R, Dyer E, Forde R, Heslehurst N, Meek CL, Schoenaker DAJM, Flynn AC, White SL. Interventions in women with type 2 diabetes mellitus in the pre-pregnancy, pregnancy and postpartum periods to optimise care and health outcomes: A systematic review. Diabet Med. 2025 Jan;42(1):e15474.
Juncker HG, Jakobsen RR, Naninck EFG, Davids M, Herrema H, van Goudoever JB, de Rooij SR, Korosi A. Maternal stress in the early postpartum period is associated with alterations in human milk microbiome composition. Brain Behav Immun. 2025 Feb;124:74-84.

谷禾健康

Bacteroides stercoris(粪便拟杆菌)是一种革兰氏阴性厌氧菌,是人类肠道微生物组的常见居民,人群检出率超过97%,也被鉴定为阴道微生物群的组成部分。
编辑
它被归类为拟杆菌属,以降解碳水化合物和产生短链脂肪酸(SCFA)的能力而闻名。和拟杆菌属的大多数物种一样,B.stercoris呈杆状、无鞭毛、不运动、不形成孢子、过氧化氢酶阴性。B.stercoris上还存在岩藻糖基化糖蛋白,生长的最佳温度为37°C。
B.stercoris可以参与葡萄糖、甘露糖、木糖的代谢,并产生琥珀酸盐和短链脂肪酸(如丙酸、乙酸和少量异丁酸盐及异戊酸盐)。吲哚试验呈阳性(能够分解色氨酸生成吲哚)。还能够水解七叶苷,但不能发酵纤维二糖。Bacteroides stercoris HJ-15 还可降解多种糖胺聚糖(GAG),并具有肝素裂解酶活性,能够降解肝素、硫酸乙酰肝素、硫酸阿托品和硫酸软骨素。
Bacteroides stercoris对青霉素有抗性,但对甲硝唑、碳青霉烯类和β-内酰胺/β-内酰胺酶抑制剂组合敏感。
典型菌株:ATCC 43183(VPI B5-21)
DNA的G+C含量:46 mol%。
此外还有B.stercoris CCUG 38733;
B.stercoris NCTC 13053;
B.stercoris ATCC 43183;
B.stercoris DSM 19555;
B.stercoris CIP 104203;
B.stercoris JCM 9496;
B.stercoris KGMB 02265等菌株。
虽然Bacteroides stercoris(粪便拟杆菌)广泛存在于人体肠道中,但其丰度在一些疾病中会发生显著变化,包括非酒精性脂肪肝、肝细胞癌、糖尿病肾病、克罗恩病、自闭症谱系障碍、胃食管反流病、结肠炎和一些出血性疾病等。这些变化可能与疾病存在因果关系,有望作为生物标志物用于早期诊断和预防。并且粪便拟杆菌(B.stercoris)中的特定菌株可能对人体具有一定的有益作用。
多项科学研究和微生物组分析发现,粪便拟杆菌(Bacteroides stercoris)在某些病理状态和疾病条件下的相对含量和绝对数量均呈现明显上升趋势。
1
粪便拟杆菌(B.stercoris)丰度较高反映非酒精性脂肪肝
▸ 证据强度:高
上海六院内分泌代谢科、上海市糖尿病重点实验室的贾伟平教授和李华婷教授等人的团队在Cell Metabolism期刊发表了相关研究论文。

研究团队在非酒精性脂肪性肝病(NAFLD)患者中开展了一项为期4个月的随机、双盲、平行对照临床试验(n=200),通过精准的临床指标评估抗性淀粉干预对NAFLD的治疗作用,同时进行多组学研究全面分析肠道微生物和代谢物的改变,探索抗性淀粉改善NAFLD的潜在机制,并进一步对其中发挥作用的关键菌种和代谢物进行因果验证。
研究发现,非酒精性脂肪性肝病(NAFLD)患者Bacteroides stercoris丰度更高。并且与对照组相比,接受Bacteroides stercoris干预的小鼠NAFLD组织学表现、肝酶水平、肝内甘油三脂含量及血清脂多糖水平均显著升高,肝脏炎症及纤维化相关基因表达显著增加,提示了Bacteroides stercoris可以促进NAFLD的进展。另外,接受Bacteroides stercoris灌胃小鼠的粪便支链氨基酸水平显著更高,尤以缬氨酸最明显。
使用抗性淀粉减少了粪便拟杆菌,改善疾病
宏基因组学分析显示,抗性淀粉(RS)干预后菌群多样性显著变化,其中粪便拟杆菌(Bacteroides stercoris)丰度较对照组显著下降。其与肝内甘油三酯、谷丙转氨酶(ALT)、谷草转氨酶(AST)呈显著正相关,并与代谢物缬氨酸显著正相关。在欧洲(肝活检)和中国的其他队列中也发现,NAFLD患者的Bacteroides stercoris丰度显著高于健康对照组。
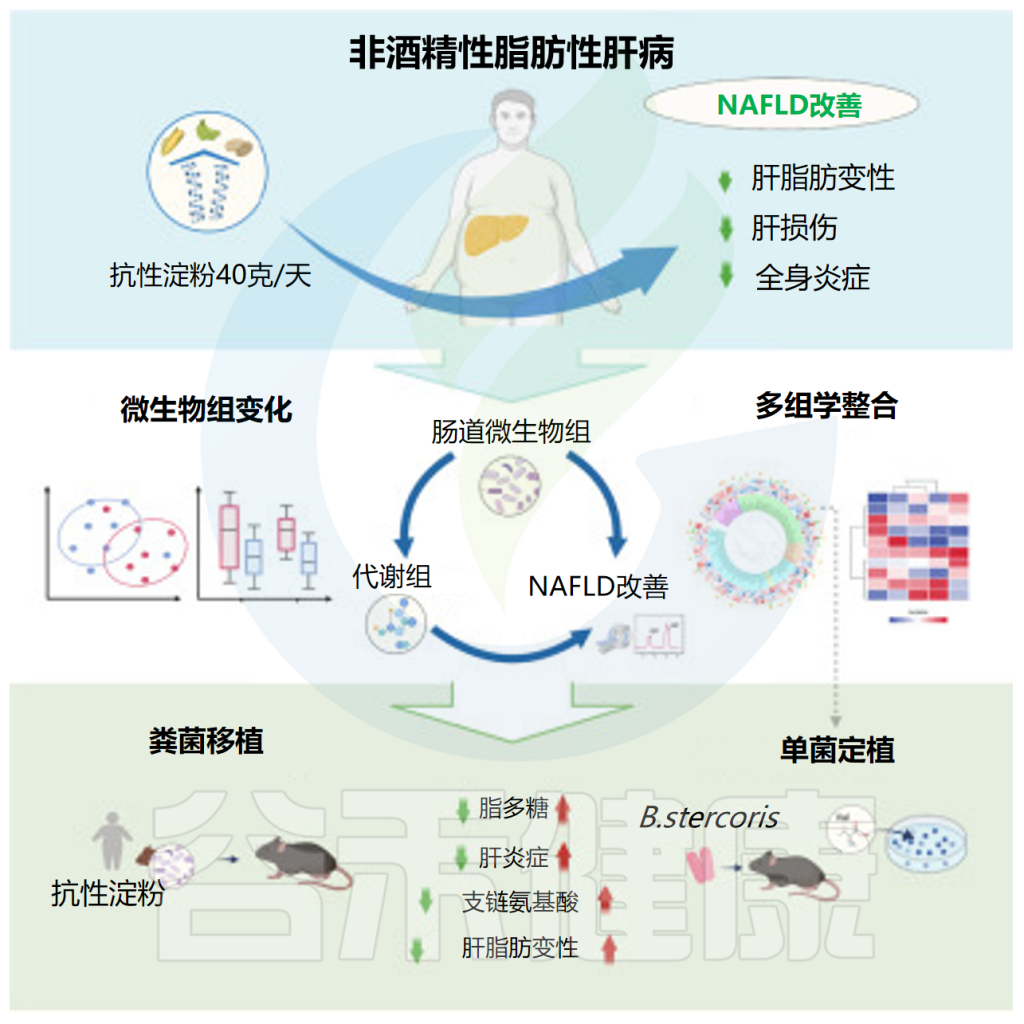
doi: 10.1016/j.cmet.2023.08.002.
抗性淀粉干预后丙氨酸转氨酶(ALT) 、天冬氨酸转氨酶(AST)和γ-谷氨酰转肽酶(GGT)显著降低,这表明肝损伤的改善。RS干预也缓解了血脂异常,表现为总胆固醇(TC)、甘油三酯(TG)、低密度脂蛋白胆固醇(LDL-C)和高密度脂蛋白胆固醇(HDL-C)的改善。
编者小结
根据这项大型研究,我们推测粪便拟杆菌(B.stercoris)丰度升高可能可以作为非酒精性脂肪性肝病(NAFLD)的一个生物标志物,并且通过施用抗性淀粉降低了粪便拟杆菌丰度,并改善了肝损伤。该菌的丰度变化也有助于用于评估NAFLD的治疗效果。
2
粪便拟杆菌(B.stercoris)丰度变化可能反映肝细胞癌进展
▸ 证据强度:一般
法国前瞻性队列研究了51名肝细胞癌(HCC)患者的肠道微生物群,以阐明肠道微生物群如何随着HCC进展而变化。
研究发现,B.stercoris在肝细胞癌(HCC)早期患者的肠道微生物组中占较高比例,平均占其肠道微生物组的0.7%(图 C)。但在晚期肝细胞癌患者的粪便样本中非常低,只在一名患者中检测到,并且相对丰度低于0.01%(图D)。
肝细胞癌患者肠道微生物组分析
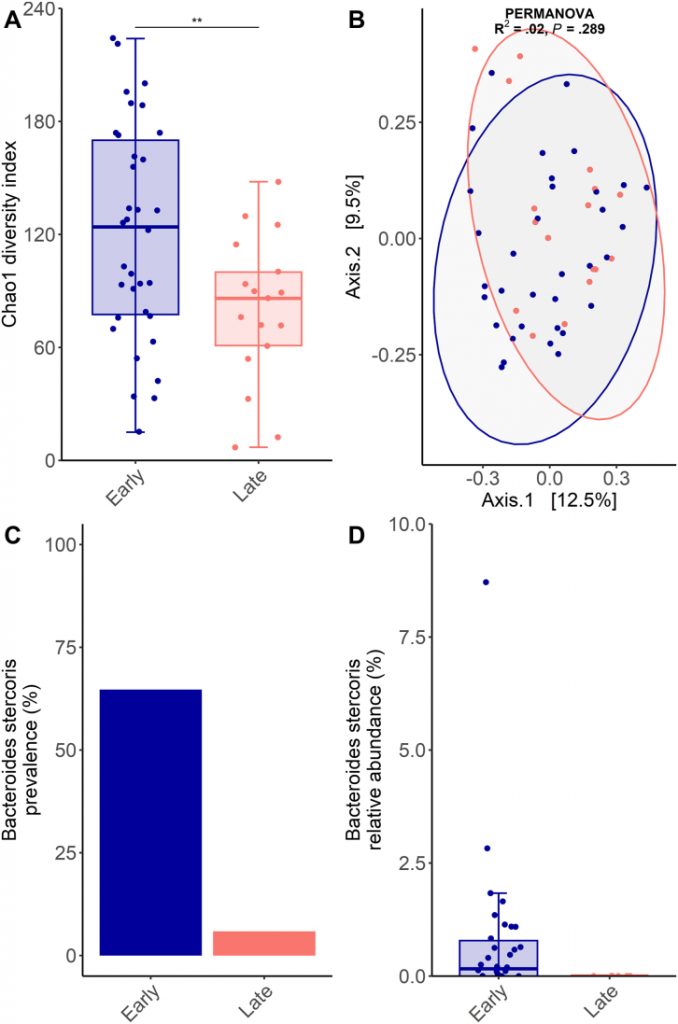
doi: 10.1016/j.gastha.2024.07.020.
Bacteroides stercoris在早期肝细胞癌(HCC)患者的粪便样本中显著富集,在晚期HCC中显著降低。
通过这些结果,研究人员认为B.stercoris可用作一种新的无创粪便生物标志物来评估肝细胞癌(HCC)进展。
3
粪便拟杆菌(B.stercoris)在糖尿病肾病患者显著富集
▸ 证据强度:低
糖尿病肾病(DN)是终末期肾病的主要原因,越来越多的研究表明,肠道微生物群在糖尿病(DM)和糖尿病肾病中起着关键作用。使用来自健康对照和2型糖尿病(T2DM)患者的粪便样本进行宏基因组学测序,并分析肠道微生物群。
发现糖尿病肾病患者的粪便样本中肠道微生物群失衡,2型糖尿病和糖尿病肾病患者产生丁酸盐的细菌(Clostridium、Eubacterium、Roseburia intestinalis) 和潜在益生菌(Lachnospira和Intestinibacter)的相对丰度显著降低。而Bacteroides stercoris在糖尿病肾病患者的粪便样本中显著富集。
4
克罗恩病患者中粪便拟杆菌(B.stercoris)增加
▸ 证据强度:低
有研究报道克罗恩病(CD)患者粪便中粪便拟杆菌(Bacteroides stercoris)丰度增加。血清对B.stercoris和B.vulgatus的IgG结合谱显示个体间差异,并强调克罗恩病血清对这些拟杆菌的强反应性。
克罗恩病患者对拟杆菌属的IgG反应性显著增加,B.stercoris上存在岩藻糖基化糖蛋白,表明对岩藻糖化寡糖的增强反应可能由携带岩藻糖的肠道细菌诱导。增强的抗体对岩藻糖基化表位的反应可能通过改变循环抗体与内源性糖蛋白的结合产生全身效应。
5
胃食管反流病中粪便拟杆菌(B.stercoris)占比较高
▸ 证据强度:低
对24例胃食管反流病(GERD)患者的粪便微生物群进行16S rRNA测序显示,小肠细菌过度生长(SIBO)的GERD患者中单形拟杆菌(bacteroides uniformis)和粪便拟杆菌(bacteroides stercoris)为优势菌群。
注:GERD和SIBO患者的代谢物存在差异,主要与ATP结合盒转运蛋白(ABC转运蛋白)相关。
研究确定了几个关键微生物类群是GERD伴SIBO患者的独特粪便微生物群,包括Bacteroides uniformis、Bacteroides stercoris、Anaerostipes、Clostridium XVIII、Anaerotruncus和Alistipes indistinctus。这些微生物可能在小肠细菌过度生长合并胃食管反流病患者的肠道微生物群失调中发挥重要作用。
6
出血性疾病—与粪便拟杆菌(B.stercoris)正相关
▸ 证据强度:低

有研究认为微生物组特征可以作为凝血缺陷、紫癜和其他出血性疾病(CPH)早期识别和监测的生物标志物。例如,粪便拟杆菌(Bacteroides stercoris)、肠杆菌和粪球菌属 ART55/1 的异常水平可能有助于预测CPH的发生,从而允许及时干预。
他们认为粪便拟杆菌(Bacteroides stercoris)丰度与凝血缺陷、紫癜等出血性疾病的风险呈正相关。
一些研究还表明,粪便拟杆菌(B.stercoris)的丰度在某些疾病状态下呈现明显降低的趋势。
1
自闭症—B.stercoris相对丰度减少
▸ 证据强度:一般
研究表明,自闭症谱系障碍(ASD)儿童的肠道微生物组组成显著异于健康儿童。
利用宏基因组学技术对30名健康儿童和30名自闭症儿童(C-ASD)进行队列分析。结果显示,两组基因数目存在差异,C-ASD组的物种丰富度估计量指数和香农指数显著降低,表明其α多样性下降,且群落结构存在显著差异。
检验结果表明自闭症儿童(C-ASD)组的Bacteroides stercoris、Bacteroides plebeius和Bacteroides plebeius的相对丰度显著低于对照组。
2
显微镜下结肠炎—B.stercoris耗尽
▸ 证据强度:一般
一项研究纳入了683名参与者,其中131名患有活动性显微镜下结肠炎(MC),159名患有慢性腹泻,以及393名年龄和性别匹配的对照,没有腹泻。
注:显微镜下结肠炎是一种以慢性水样腹泻、结肠镜下结肠黏膜正常而病理学检查在显微镜下可见特异性改变的一组临床病理综合征。
与对照组和MC的缓解期相比,活动性MC中粪便微生物组的特征是较低的α多样性。如Blautia glucerasea和Bacteroides stercoris,在MC中耗尽。
前面已经详细讨论了粪便拟杆菌(Bacteroides stercoris)在多种疾病中的丰度变化情况,那么作为一种在人类肠道中常见的共生菌,它是否也具有一些潜在的有益作用呢?答案是有的,我们在一些研究中发现了其特定菌株的有益作用。
1
B.Stercoris KGMB02265—利于减重
▸ 证据强度:高
近期的一项研究发现粪便拟杆菌的一个特定菌株Bacteroides stercoris KGMB02265具有抗肥胖作用。

编辑
抑制高脂饮食诱导的的体重增加
为了在验证Bacteroides stercoris KGMB02265的减肥特性,使用高脂肪饮食(HFD)诱导的肥胖模型进行小鼠实验。HFD喂养9周后,与低脂饮食(LFD)喂养组相比,HFD喂养的小鼠体重增加了29.53%。然而,施用Bacteroides stercoris KGMB02265组的体重与LFD喂养的组相比仅增加了13.46%。
此外,用Bacteroides stercoris KGMB02265无细胞上清液(BsCFS)处理后,脂肪细胞脂质含量降低。还测量了附睾白色脂肪组织的重量,结果显示,施用KGMB02265的组附睾脂肪重量显著低于HFD组。由此可见,口服KGMB02265减少了HFD喂养小鼠的脂肪沉积,导致体重下降。
恢复葡萄糖耐量,降低瘦素和甘油三酯水平
肥胖不仅表现为体重增加,还伴随多种血清参数的变化。由于胰岛素敏感性下降,肥胖患者难以维持葡萄糖稳态。通过口服葡萄糖耐量试验(OGTT)评估胰岛素敏感性,结果显示Bacteroides stercoris KGMB02265改善了葡萄糖耐量并降低了OGTT期间的最大峰值。
此外,瘦素作为调节食欲的脂肪因子,在肥胖个体中因脂肪比例较高而水平升高。HFD喂养的小鼠血清瘦素水平显著升高,而施用KGMB02265后显著降低。
血清甘油三酯水平与肥胖密切相关,HFD喂养组甘油三酯水平升高,但KGMB02265表现出明显的抑制作用。
编者小结
综上所述,Bacteroides stercoris KGMB02265通过改善高脂饮食下的葡萄糖耐量、瘦素和甘油三酯水平,显示出明显的抗肥胖效果,未来有望应用于减重领域。
2
可能降低SARS-CoV-2感染风险
▸ 证据强度:低
研究发现,高SARS-CoV-2(2019新型冠状病毒)传染性人群的粪便样本中,Collinsella aerofaciens、Collinsella tanakaei、Streptococcus infantis和 Morganella morganii丰度较高,这些菌群都具有一定的促炎作用,同时核苷酸从头合成、氨基酸合成及糖酵解功能增强。
而低或无SARS-CoV-2传染性人群粪便样本中,短链脂肪酸产生菌如Parabacteroides merdae、粪便拟杆菌(Bacteroides stercoris)、Alistipes onderdonkii 和Lachnospiraceae bacterium 1_1_57FAA丰度较高。
B.stercoris可能的保护机制如下:
产生短链脂肪酸:作为Bacteroides属成员,B.stercoris是已知的短链脂肪酸产生菌,短链脂肪酸在增强宿主免疫力方面起着关键作用。
调节ACE2受体:动物研究表明,B.stercoris与抑制结肠ACE2表达相关,ACE2是SARS-CoV-2的主要细胞入口点,抑制ACE2可能减少病毒进入肠道上皮细胞的机会。
粪便拟杆菌是人类肠道微生物组的常见成员,是典型的人体共生菌。
该菌与多种疾病有关联:在非酒精性脂肪肝患者中丰度显著升高,与肝内甘油三酯、肝酶水平呈正相关,且通过动物实验证实其可促进非酒精性脂肪性肝病进展;此外,其丰度变化还见于糖尿病肾病、早期肝细胞癌、克罗恩病及胃食管反流病患者。
同时,初步研究显示其特定菌株(B.Stercoris KGMB02265)具有减重潜力,能减少高脂饮食小鼠的脂肪沉积,改善葡萄糖耐量和血脂指标。该菌在低SARS-CoV-2传染性人群中丰度较高,可能通过产生短链脂肪酸增强免疫力。
作为肠道微生物组中的重要成员,粪便拟杆菌展示了成为疾病生物标志物和潜在益生菌的双重价值,值得继续关注和深入研究。针对特定菌株的研究是未来发展的重要方向,通过临床试验验证其在不同健康指标和疾病防治中的实际效果,可能是实现微生物干预的重要一步。
主要参考文献
Ni Y, Qian L, Siliceo SL, Long X, Nychas E, Liu Y, Ismaiah MJ, Leung H, Zhang L, Gao Q, Wu Q, Zhang Y, Jia X, Liu S, Yuan R, Zhou L, Wang X, Li Q, Zhao Y, El-Nezami H, Xu A, Xu G, Li H, Panagiotou G, Jia W. Resistant starch decreases intrahepatic triglycerides in patients with NAFLD via gut microbiome alterations. Cell Metab. 2023 Sep 5;35(9):1530-1547.e8.
Esparteiro D, Fouquet G, Courtois A, Naassila M, Nguyen-Khac E, Marcq I. Shotgun Metagenomics Reveals Bacteroides stercoris as a Fecal Biomarker Depleted in Late-Stage Hepatocellular Carcinoma. Gastro Hep Adv. 2024 Aug 30;4(1):100539.
West KA, Yin X, Rutherford EM, Wee B, Choi J, Chrisman BS, Dunlap KL, Hannibal RL, Hartono W, Lin M, Raack E, Sabino K, Wu Y, Wall DP, David MM, Dabbagh K, DeSantis TZ, Iwai S. Multi-angle meta-analysis of the gut microbiome in Autism Spectrum Disorder: a step toward understanding patient subgroups. Sci Rep. 2022 Oct 11;12(1):17034.
Zuo T, Liu Q, Zhang F, Lui GC, Tso EY, Yeoh YK, Chen Z, Boon SS, Chan FK, Chan PK, Ng SC. Depicting SARS-CoV-2 faecal viral activity in association with gut microbiota composition in patients with COVID-19. Gut. 2021 Feb;70(2):276-284.
Ryu SW, Moon JC, Oh BS, Yu SY, Bak JE, Heo ES, Jeong JH, Lee JH. Anti-obesity activity of human gut microbiota Bacteroides stercoris KGMB02265. Arch Microbiol. 2023 Dec 12;206(1):19.
Wang ZT, Tan WT, Huang JL, Zhang PF, Li Q, Wang MM, Meng MM, Su H, Guo CM, Liu H. Correlation Between Gastroesophageal Reflux Disease and Small Intestinal Bacterial Overgrowth: Analysis of Intestinal Microbiome and Metabolic Characteristics. J Inflamm Res. 2025 Jan 4;18:33-51.
Ren R, Huang X, Wei D, Guo Q, Wang C, Li M, Yang L, Lang H, Chen S. Microbe-immune interactions: new perspectives on coagulation deficiencies, purpura, and other hemorrhagic conditions under the regulation of the gut microbiota. Front Immunol. 2024 Oct 8;15:1461221.
Zhang L, Wang Z, Zhang X, Zhao L, Chu J, Li H, Sun W, Yang C, Wang H, Dai W, Yan S, Chen X, Xu D. Alterations of the Gut Microbiota in Patients with Diabetic Nephropathy. Microbiol Spectr. 2022 Aug 31;10(4):e0032422.

谷禾健康

近年来,随着微生物组学研究的深入,科学家们发现肠道菌群与人体年龄之间存在着远比想象更密切的关联。一系列突破性研究表明,肠道菌群不仅能够反映个体的实际年龄,更可能是调控生物学年龄的关键因素之一。这一发现正在改变我们对发育、衰老和健康的传统认知。
最新研究揭示,肠道菌群的组成和功能会随年龄发生系统性变化。这种变化表现在多个层面:从婴幼儿期菌群的快速建立与稳定,到成年后菌群多样性的动态平衡,再到老年期特征性菌群的衰退。基于这些规律,研究人员开发出了一系列基于肠道菌群的年龄预测模型,其准确度已经达到前所未有的水平。
更引人注目的是,肠道菌群年龄与多种疾病的发生、发展密切相关。研究发现,肠道菌群年龄的加速老化往往预示着代谢紊乱、免疫功能下降,甚至认知能力衰退。相反,保持年轻和健康的肠道菌群,可能是延缓衰老、预防疾病的重要途径。
本文将重点探讨三个核心问题:
通过梳理最新研究进展,我们将看到肠道菌群不仅是年龄的被动标记物,更可能是一个可调控的”生物时钟”。这一认识正在开启精准医疗和个性化健康管理的新篇章。
doi: 10.14218/ERHM.2024.00008
随着研究的深入和技术的进步,基于肠道菌群的年龄干预策略很可能成为未来医学实践的重要组成部分。
从无菌到共生——婴幼儿肠道菌群的“黄金塑造期”
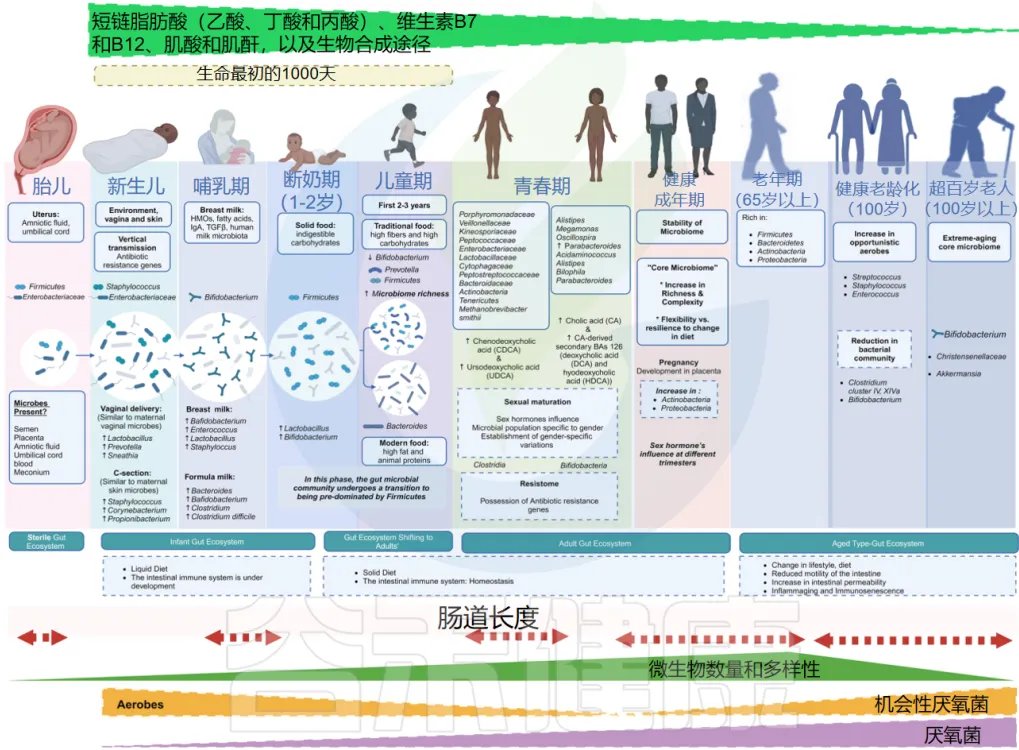
近年来研究表明,肠道微生物群在婴幼儿早期发育阶段的变化与其发育年龄密切相关。婴幼儿的肠道微生物群呈现出明显的年龄相关性变化特征:在早期阶段主要表现为不稳定的群落结构和较低的微生物成熟度,随着年龄增长,菌群组成从以Firmicutes和Bifidobacterium为主,逐渐过渡到以Bacteroides和Prevotella为主导。这种转变具有确定性和可预测性,为年龄预测模型的建立提供了基础。
肠道微生物群的发育受多种因素影响,包括喂养方式、出生方式、地理位置和环境暴露等。研究发现,母乳喂养与Bifidobacterium的高水平密切相关,而停止母乳喂养则会加速肠道微生物群的成熟。此外,出生方式也显著影响微生物群的发育,如阴道分娩的婴儿肠道中Bacteroides的水平较高。尽管存在这些普遍性特征,但个体间的肠道微生物群发育轨迹仍存在差异,这与特定的生活方式和环境因素密切相关。
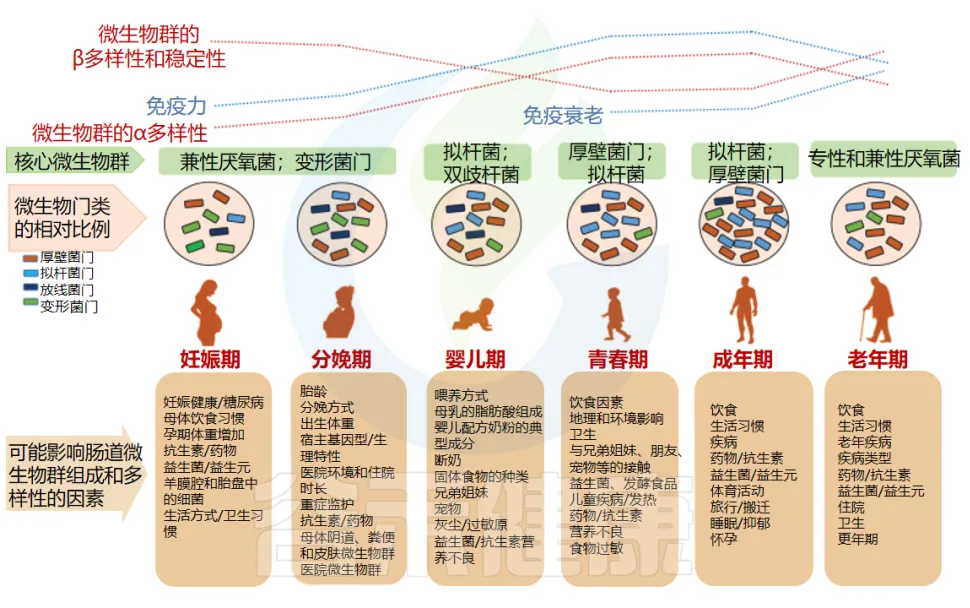
doi: 10.3233/NHA-170030
在预测模型研究方面,近年来取得了显著进展。2025年发表在《Nature Communications》上的研究开发出了一个高精度的预测模型,该研究分析了来自12个国家的1,827名婴幼儿的3,154个样本,使用随机森林模型进行预测,预测误差仅为2.56个月。
研究还识别出了关键的分类学预测指标,包括双歧杆菌的减少和粪杆菌的增加。另一项2024年的研究则开发出了“肠道微生物群健康指数”,该指数不仅能够预测婴幼儿在前5年的整体健康状况,还提供了一个可靠的微生物群年龄评估基准。
最新研究进一步证实,婴幼儿肠道微生物组的发育成熟度与年龄高度相关,仅通过肠道微生物群组成就能准确预测婴儿的年龄。研究人员建立了”微生物组年龄”的评估标准,这不仅可以用于年龄预测,还可以作为评估早期肠道发育的重要指标。这些研究成果不仅证实了基于肠道菌群预测婴幼儿年龄的可行性,还为评估婴幼儿的发育状况和健康水平提供了新的工具和方法。
肠道菌群发育滞后会对婴幼儿的多个系统产生深远影响。
在神经系统方面,可能导致认知发育迟缓、语言发育延迟、注意力不集中,甚至增加自闭症谱系障碍(ASD)的风险;
在免疫系统方面,常见表现包括反复呼吸道感染、特应性皮炎、食物过敏,以及哮喘等过敏性疾病的发生率升高;
在代谢系统方面,可能引起生长发育迟缓、体重增长异常、微量元素吸收不良等问题;在消化系统方面,则可能出现腹泻、便秘、肠痉挛等功能性胃肠道疾病。
特别是在出生后最初1000天这个关键期内,肠道菌群的发育状况对婴幼儿的长期健康具有决定性影响。
在这种情况下,规范的肠道菌群检测在婴幼儿发育评估中具有重要意义。检测内容应包括微生物多样性指数、关键菌群(如双歧杆菌、乳酸菌、粪杆菌等)的丰度,以及潜在致病菌的监测。
建议在以下关键时间点进行检测:出生后1-2个月、辅食添加期(4-6个月)、断奶期(12个月左右)以及2岁左右。对于高危人群,如早产儿、剖宫产婴儿、有过敏家族史或自身免疫性疾病家族史的婴幼儿,需要更频繁的监测。
研究显示,及早发现和干预菌群异常可以显著改善预后。具体干预措施包括:调整饮食结构(如添加低聚糖、膳食纤维等益生元),补充特定益生菌(如婴儿双歧杆菌、鼠李糖乳杆菌等),改善生活习惯(如规律作息、适度运动),以及环境因素的调整(如避免不必要的抗生素使用、增加户外活动时间)。对于特定问题,如食物过敏,可以通过补充特定菌株(如常见的LP299V益生菌)来改善症状;对于免疫功能低下,则可以考虑添加具有免疫调节作用的益生菌。
因此,建议在婴幼儿发育的关键时期进行系统的肠道菌群检测和跟踪监测。这种检测不仅能够及早发现发育风险(如自闭症倾向、过敏风险、免疫功能异常等),还能为个性化干预方案的制定提供科学依据。特别是对于已经出现发育迟缓、免疫功能低下、消化吸收障碍等问题的婴幼儿,定期的肠道菌群检测对评估干预效果和及时调整治疗方案具有重要的临床指导意义。
通过肠道菌群的视角:解密衰老时钟背后的微生物密码
➤ 老年肠道菌群的三大特征:
多样性下降、促炎菌增加、代谢功能衰退
随着年龄增长,我们的肠道菌群会发生显著变化。研究发现,老年人的肠道菌群具有三个显著特征,这些变化与多种衰老相关的健康问题密切相关。
◆ 首先是菌群多样性的显著下降
与年轻人相比,老年人的肠道菌群种类明显减少,特别是厚壁菌门数量减少,而拟杆菌门的比例相对升高。同时,一些对健康有益的细菌,如双歧杆菌和瘤胃球菌等数量也显著减少。这种多样性的降低会影响肠道微生态的稳定性。
◆ 第二个特征是促炎菌群的增加
老年人肠道中肠杆菌科(Enterobacteriaceae)和肠球菌属(Enterococcus)等促炎菌群数量明显增多,而具有抗炎作用的普拉梭菌(Faecalibacterium prausnitzii)等益生菌则显著减少。这种失衡会导致肠道处于慢性低度炎症状态,不仅影响局部肠道健康,还可能加速整体衰老进程。
◆ 第三个特征是代谢功能的衰退
老年人肠道中产丁酸菌如真杆菌(Eubacterium)、瘤胃球菌等数量减少,这些菌群对维持肠道健康至关重要。它们的减少会影响营养物质的吸收和能量代谢,同时也会降低肠道屏障功能,增加肠道通透性。这种变化可能导致营养吸收不良,并增加有害物质进入血液的风险。
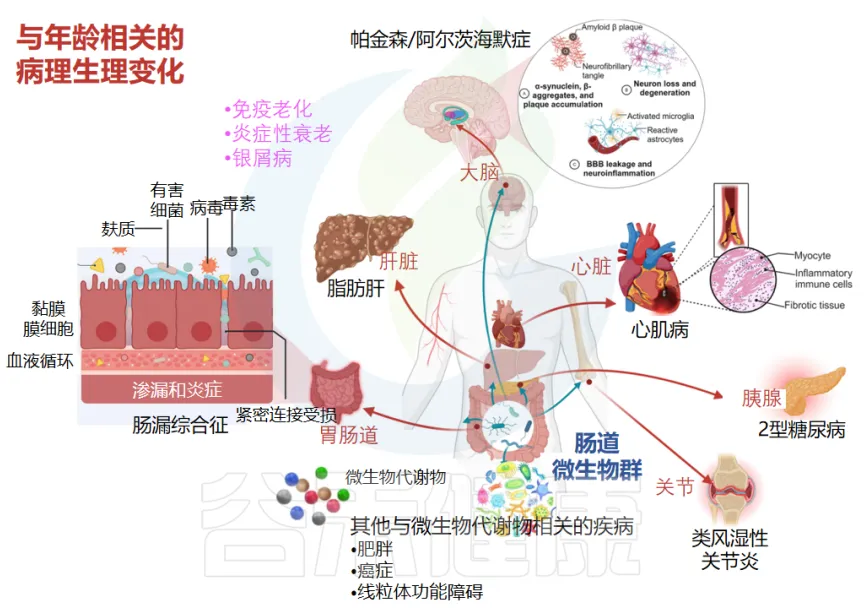
这三个特征之间相互关联,共同构成了一个复杂的失衡网络。例如,菌群多样性的下降会影响代谢功能,促炎菌群的增加又会进一步降低有益菌群的数量。这种恶性循环可能是老年人更容易出现各种健康问题的重要原因之一。了解这些特征对于开发针对性的干预策略,改善老年人健康状况具有重要意义。
➤ 虚弱的菌群特征
虚弱是老年人一种特殊的临床状态,表现为机体对内外压力源的脆弱性增加,往往伴随着食欲下降、肌肉减少、认知功能下降、活动能力减弱以及独立生活能力的丧失。近年来的研究发现,肠道菌群的改变与虚弱程度之间存在着密切的关联,这种关联并不完全依赖于年龄因素。
研究显示,虚弱老年人的肠道菌群具有独特的“虚弱特征”。首先是普氏菌(Prevotella)和普拉梭菌(F. prausnitzii) 的显著减少,这些菌群对维持肠道健康和免疫功能具有重要作用。其次是产丁酸菌,如Eubacterium halii和Eubacterium rectalis的含量降低,这与肌肉蛋白合成的减少密切相关。
研究人员还观察到,在虚弱评分较高的老年人中,乳酸菌(Lactobacilli)、拟杆菌/普氏菌(Bacteroides/Prevotella)等有益菌群显著减少,而瘤胃球菌属(Ruminococcus)、Atopobium和肠杆菌科(Enterobacteriaceae)等菌群则明显增加。
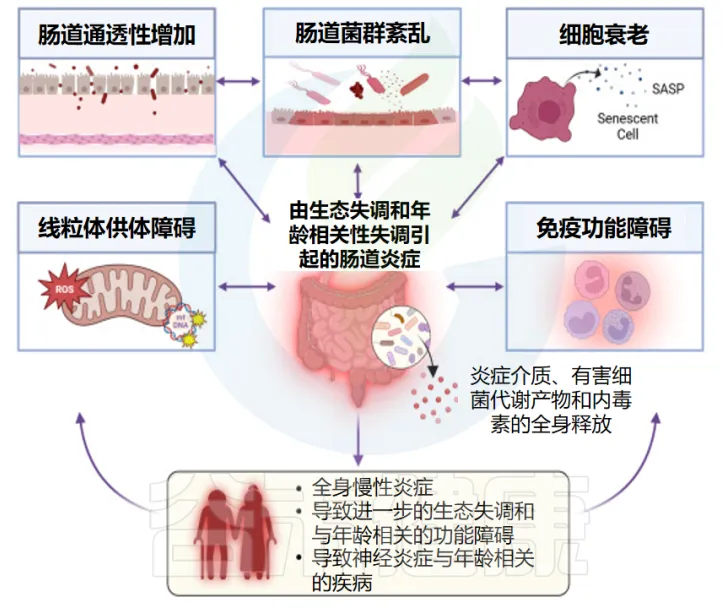
doi: 10.1016/j.advnut.2025.100376
这些菌群变化的意义重大。产丁酸菌的减少会影响能量代谢和肌肉功能,而有益菌的减少则可能导致免疫功能下降和炎症水平升高。相反,在功能状态良好的老年人中,往往可以观察到较高水平的产丁酸菌,特别是普拉梭菌(Faecalibacterium prausnitzii)的含量,这进一步证实了菌群组成对机体功能的重要影响。
这些发现为我们理解和干预老年虚弱提供了新的视角。通过调节肠道菌群,特别是补充特定的益生菌和益生元,可能有助于改善老年人的虚弱状态。这也提示我们,在老年医学实践中,应当将肠道菌群作为评估和干预虚弱的重要靶点之一。
➤ 百岁老人长寿菌群的特殊组成
研究发现,百岁老人的肠道菌群具有独特的“长寿特征”,这种特征不仅区别于普通老年人,更展现出与健康长寿密切相关的微生物组成模式。这一发现为我们理解人类长寿的生物学机制提供了新的视角。
在菌群组成上,百岁老人的肠道中普遍存在较高水平的拟杆菌和罗氏菌属(Roseburia)。这两类菌群在维持肠道健康和免疫平衡方面发挥着重要作用。作为重要的丁酸盐产生菌,能够通过产生短链脂肪酸来调节肠道微环境,增强肠道屏障功能。
更引人注目的是,百岁老人的肠道中还富含Christensenella、双歧杆菌和阿克曼氏菌(Akkermansia)。这些菌群被认为是“长寿菌群”的代表。其中,长寿菌群与人类的遗传因素高度相关,被认为是最具遗传性的菌群之一;双歧杆菌能够维持肠道健康,增强免疫功能;而阿克曼氏菌则在调节代谢、维持肠道屏障完整性方面发挥关键作用。
研究还发现了一些在百岁老人肠道中特有的菌种,如腐生链菌(Alistipes putredinis)和气味杆菌(Odoribacter splanchnicus)。这些特殊菌群的存在可能与长寿个体特有的代谢特征和免疫调节功能有关,为我们理解长寿的微生物学机制提供了重要线索。
这些发现不仅帮助我们理解了百岁老人独特的肠道菌群特征,更为延缓衰老、促进健康长寿提供了新的思路。通过深入研究这些”长寿菌群”的功能和调节机制,有望开发出基于微生物组的健康干预策略,为实现健康老龄化提供新的方案。
值得注意的是,这些长寿相关的菌群特征并非简单的个体差异,而是反映了人体在长期健康状态下的微生态平衡。这种平衡可能是遗传因素、生活方式和环境因素长期共同作用的结果,对于我们理解和促进健康长寿具有重要的指导意义。
➤ 菌群-肠-脑轴在认知衰退中的作用路径
肠道菌群与大脑的关系远比我们想象的要复杂。研究表明,肠道菌群通过复杂的菌群-肠-脑轴与认知功能密切相关。这条轴线不仅包括神经元的直接连接,还涉及神经递质、激素和免疫介质等多重信号分子,构成了一个精密的双向调控网络。
◆ 第一个关键通路是神经递质调节
肠道菌群可以直接产生或调节多种神经递质的合成。研究发现,乳酸菌和双歧杆菌能够将肠道中的谷氨酸转化为GABA(γ-氨基丁酸),这是大脑中主要的抑制性神经递质,对情绪调节和认知功能具有重要作用。
此外,肠道菌群还参与乙酰胆碱和多巴胺等神经递质的产生。动物实验证实,补充Lactobacillus helveticus NS8可以通过降低血浆中皮质醇和促肾上腺皮质激素的水平来改善应激反应,同时提高血清素和去甲肾上腺素的水平。
◆ 第二个重要机制是免疫-炎症通路
随着年龄增长,肠道菌群失调会导致肠道通透性增加,使脂多糖(LPS)、脂蛋白和细菌RNA等细菌代谢产物进入血液循环。这些物质可以激活免疫系统,导致TNF-α、IL-1β、IL-6等促炎因子的释放,引发系统性炎症反应。
这些炎症因子可以穿过血脑屏障,在大脑中引起神经炎症,加速认知功能的衰退。值得注意的是,小胶质细胞(占中枢神经系统固有免疫细胞的约10%)在这个过程中发挥着重要作用,它们能够快速识别和响应环境变化,参与维持神经系统的稳态。
◆ 第三个关键环节是神经营养因子的调节
肠道菌群对脑源性神经营养因子(BDNF)和神经生长因子(NGF)的表达具有重要影响。这些神经营养因子对神经元的存活、突触可塑性和神经回路的重塑起着关键作用。研究发现,某些益生菌的补充可以提高BDNF的水平,改善认知功能。例如,在小鼠实验中,补充长双岐杆菌(Bifidobacterium Longum)能够显著改善动物的推理能力。
此外,肠道菌群还通过产生短链脂肪酸等代谢产物发挥作用。这些代谢产物可以调节血脑屏障的完整性,影响神经元功能和神经胶质细胞的活化状态。研究还发现,某些菌群数量变化与认知功能直接相关,如Alcaliganeceae和Porphyromonadaceae的数量增加与推理能力下降呈正相关。
在治疗干预方面,益生菌的应用显示出了积极的效果。例如,Lactobacillus、Bifidobacterium、S. thermophilus、Enterococcus、Bacillus等益生菌可以通过增加色氨酸衍生的神经营养因子水平来促进神经递质的释放。
然而,益生菌补充的效果会受到多种因素的影响,如剂量、菌株、补充时间以及患者的年龄、疾病状态、药物使用(尤其是抗生素)、饮食和生活方式等。
需要指出的是,尽管菌群-肠-脑轴的研究取得了显著进展,但仍有许多问题需要进一步探索。目前的研究主要基于动物模型和临床观察,还需要更多的多学科、多系统的研究来阐明相关机制和干预机会。这些研究将有助于开发以肠道菌群为靶点的早期干预策略,为预防和治疗神经退行性疾病提供新的思路。
用AI构建年龄的生物标记——肠道菌群的年龄预测模型
近年来,随着测序技术的进步和机器学习方法的发展,基于肠道菌群的年龄预测模型取得了显著进展。2020年,研究人员通过深度学习方法分析了4000多份来自18-90岁人群的宏基因组数据,构建出预测误差为10.6年的模型。同年,另一项基于随机森林算法的研究分析了4434份样本的16S rRNA测序数据,将预测误差控制在11.5岁。这些早期研究证实了利用肠道菌群特征预测年龄的可行性。
2022年的突破性研究展示了多维度数据整合的优势。通过分析4478份成年人粪便样本,研究发现单独使用分类特征或代谢途径特征的预测模型误差分别为9.5年和10.2年,但将两类特征结合并考虑宿主因素后,预测误差可降至8.3年。这一发现为后续模型开发指明了方向。
2024年一项新研究开发出了基于肠道微生物组多维数据的生物学年龄预测模型(gAge)。该研究通过创新的机器学习方法,成功整合了微生物组的分类学和功能学特征,显著提高了年龄预测的准确性。研究团队识别出164个标志物物种和35个关键代谢通路与宿主年龄变化密切相关,并根据其对衰老的影响将其分类为促进和抑制两类。
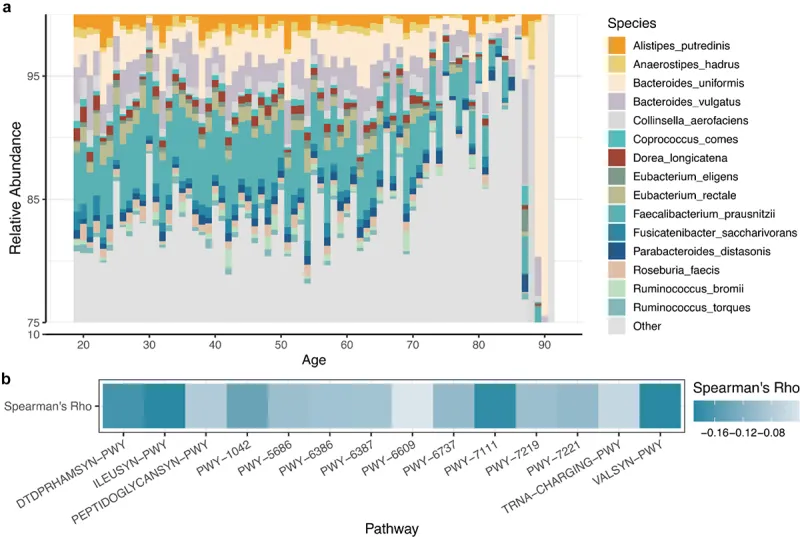
doi: 10.1080/19490976.2023.2297852
研究验证显示,gAge模型及其预测残差与个体健康状况和虚弱程度高度相关。特别是在老年群体中,模型识别的年龄相关标志物与多种疾病和虚弱特征显著重合,为评估和预测衰老风险提供了新的工具。
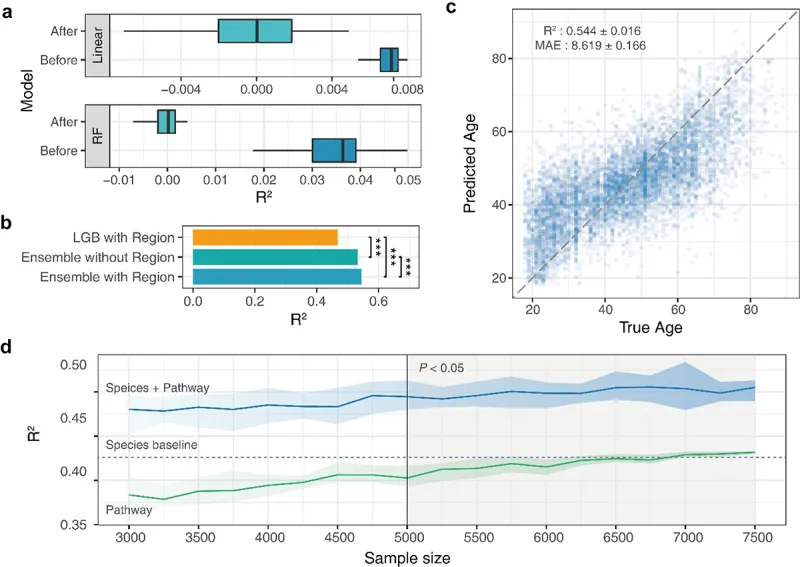
doi: 10.1080/19490976.2023.2297852
在这些研究基础上,谷禾开发的GUHEAge模型实现了更大的突破。该模型基于60万例不同年龄人群的6万个菌群特征,首次完整分析了从0-120岁的肠道菌群演变过程。通过深度神经网络,我们识别出381个标记物种和1574个标记基因,并根据其对衰老的影响将其分为促进和抑制两类。
在这些标记物中,产短链脂肪酸的有益菌(如双歧杆菌属、嗜粘蛋白阿克曼氏菌和拟杆菌属)表现出抑制衰老的作用。这些菌群可增强肠道屏障功能,调节机体代谢、炎症和免疫反应。相反,某些致病菌(如大肠杆菌和空肠弯曲杆菌)则显示出促进衰老的特征。
更重要的是,GUHEAge模型不仅能准确预测年龄,其预测结果还与个体健康状况和虚弱程度高度相关。验证集表明,模型识别的年龄相关标志物与多种疾病和虚弱特征显著重合,这为精准医疗和个性化健康管理提供了新的思路。
这些进展表明,基于肠道菌群的年龄预测模型已经发展成为一个可靠的生物年龄评估工具。通过整合多维度数据和先进的机器学习方法,为干预衰老提供新的靶点。
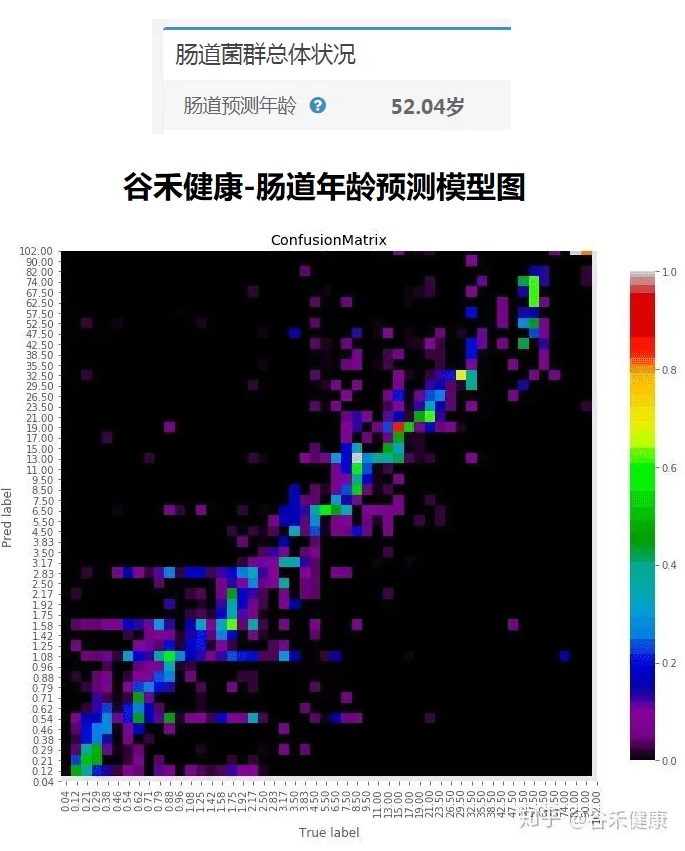
<来源:谷禾健康肠道菌群数据库>
可以看到,肠道年龄和实际年龄基本是符合的。健康人的肠道菌群年龄恰恰是最符合真实年龄的,与真实年龄差异大意味着肠道菌群出现偏离。
健康的人存在更多样化且平衡的肠道菌群。微生物群中与年龄相关的变化归因于生理,生活方式和健康状况。这些因素中的每一个都与某些菌群的相对丰度变化有关。
例如,饮食、卫生、兄弟姐妹、宠物、过敏、儿童疾病和抗生素是影响儿童微生物组的一些突出因素。到了成年期微生物群相对稳定,而到了老年期,一些有益菌开始逐渐下降,菌群又向另一个阶段过渡。
理解肠道年龄超越数字的生物学意义
➤ 发育迟缓儿童的菌群年龄滞后现象
发育迟缓儿童的肠道菌群呈现出明显的“年龄滞后”特征,这种现象反映在菌群的多样性、组成结构和功能等多个方面。研究表明,这些儿童的肠道菌群发育水平往往落后于其实际年龄,这种滞后可能是导致发育迟缓的重要因素之一。
我们之前发表在《Gut》上的针对自闭症儿童菌群发育的研究显示,自闭症儿童的菌群发育要滞后于健康儿童。
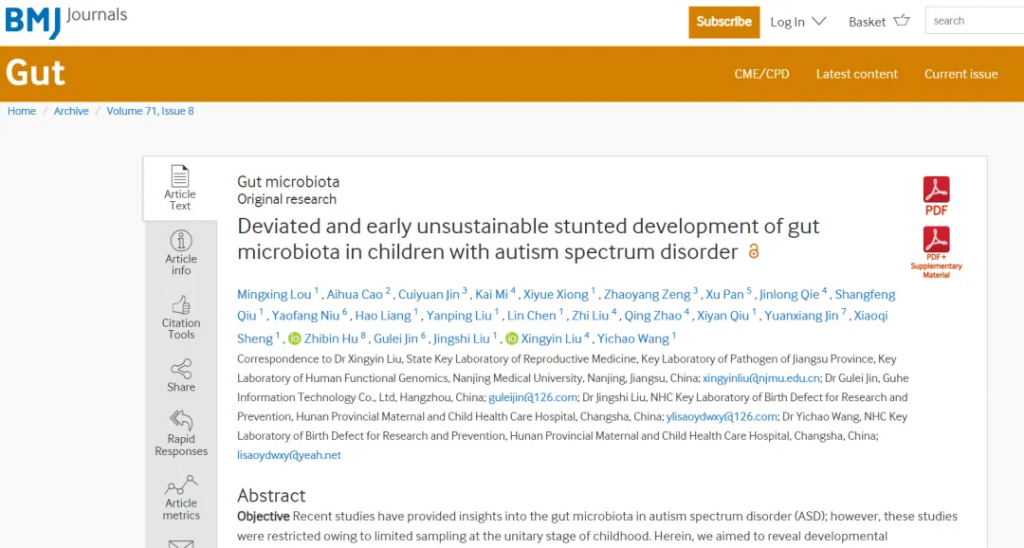
在菌群组成方面,发育迟缓儿童表现出显著的特征性改变。首先是有益菌群的明显减少,特别是双歧杆菌和乳杆菌的含量显著低于同龄健康儿童。这些菌群对维持肠道健康、促进营养物质吸收和调节免疫功能具有重要作用。同时,研究还发现这些儿童的肠道中普氏菌(Prevotella)和粪杆菌(F. prausnitzii)等核心菌菌含量也明显降低。
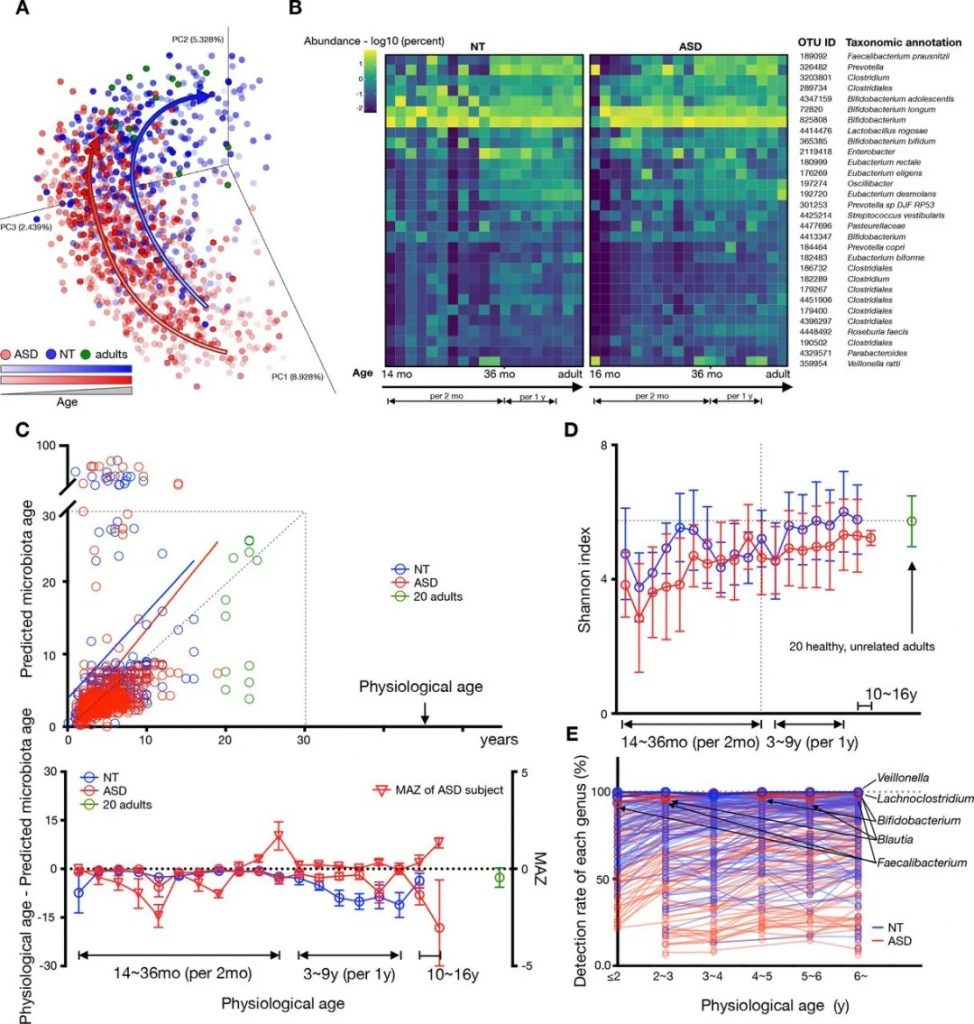
doi.org/10.1136/gutjnl-2021-325115
这种菌群滞后现象可能通过多个机制影响儿童发育:
免疫调节机制:菌群失调导致肠道免疫功能发育不良,增加炎症风险,影响生长发育。研究发现,这些儿童体内往往存在低度慢性炎症状态。
营养代谢影响:关键有益菌群的减少影响营养物质的吸收和利用效率。特别是产丁酸菌的减少,会影响能量代谢和营养物质的吸收。
神经-内分泌调节:菌群失调可能通过菌群-肠-脑轴影响生长激素和其他内分泌激素的分泌,进而影响生长发育。
针对这一问题,目前研究提出了几种潜在干预策略,包括结合营养补充、运动干预和益生菌治疗或全面的菌群置换可以有效改善儿童的生长发育状况。
通过调节肠道菌群,有望开发出更有效的干预策略,帮助发育迟缓儿童实现健康生长。同时,这也提示我们在儿童保健实践中,应当将肠道菌群作为评估和干预的重要指标之一。
➤ 早衰综合征患者的菌群年龄加速特征
早衰综合征患者的肠道菌群呈现出显著的“年龄加速”特征,其菌群组成和功能状态明显超前于实际年龄水平。研究发现,这种菌群年龄加速现象与多种生理功能的提前衰退密切相关。
doi: 10.2147/CIA.S414714
在菌群组成方面,早衰患者表现出显著的特征性改变。有益菌群如粪杆菌(Faecalibacterium prausnitzii)、直肠真杆菌(Eubacterium rectale)和扭链瘤胃球菌(Ruminococcus torques)的含量明显降低。同时,代谢通路也发生了重要变化,包括支链氨基酸代谢通路(如L-缬氨酸和L-异亮氨酸合成)的显著下降,丙酮酸发酵(PWY-7111)能力减弱,以及NAD合成相关代谢通路的异常。
这些改变通过多个机制影响机体功能。首先是炎症反应的加速,表现为促炎因子(TNF-α、IL-6和IL-1)水平升高,导致慢性低度炎症状态持续存在。其次是代谢功能的紊乱,包括氨基酸代谢异常、能量代谢效率下降和营养物质吸收受损。此外,肠道屏障功能受损也是重要特征,导致肠道通透性增加,细菌代谢产物进入血液循环,进一步加重系统性炎症反应。
针对这些问题,研究提出了几种潜在的干预策略:
精准菌群干预:通过补充特定益生菌,如双歧杆菌和乳酸菌,同时添加益生元促进有益菌群生长。研究表明,这种干预方式可以改善肠道菌群组成,延缓衰老进程。
代谢通路调节:包括补充NAD前体物质、调节氨基酸代谢和改善能量代谢。特别是NAD水平的提升,已被证实可以预防衰老和相关疾病。
生活方式干预:优化饮食结构,增加膳食纤维摄入;保持适度运动,提高体能状态;改善睡眠质量,维持昼夜节律。
综合干预方案:结合营养补充、心理支持、运动康复和定期监测菌群状态,全面改善患者状况。
通过对肠道菌群的精准干预,有望延缓早衰进程,改善患者生活质量。
➤ 糖尿病/心血管疾病的菌群老化预警
在代谢性疾病领域,肠道菌群年龄作为一个新兴的生物标志物展现出重要的预警价值。研究发现,糖尿病和心血管疾病患者的肠道菌群往往表现出提前衰老的特征,这种菌群老化现象通常早于临床症状的出现,为疾病的早期预警提供了新的时间窗口。
在菌群组成方面,研究显示代谢性疾病患者的肠道菌群存在显著变化。这些变化与血清生化指标密切相关,特别是与碱性磷酸酶和胰岛素水平显著相关。研究还发现,某些代谢通路的改变,如支链氨基酸代谢通路(BCAA)、NAD合成相关代谢通路的异常,可能是疾病发展的早期信号。
通过肠道年龄预测模型的应用,研究人员发现菌群年龄与多种疾病风险指标具有显著相关性。在一项针对老年人群的研究中,gAge预测残差与个体健康状况和虚弱程度呈现高度相关。特别是在2型糖尿病(T2D)患者中,尽管疾病本身可能不会显著影响预测年龄,但菌群组成的特定改变可以作为疾病进展的预警指标。
在心血管疾病方面,研究发现血清碱性磷酸酶水平与心脑血管疾病风险显著相关,而这一指标与肠道菌群年龄存在明显关联。通过分析不同gAge残差人群的菌群特征,研究者识别出了一系列可能与心血管健康相关的关键菌种和代谢通路,为疾病预防提供了新的干预靶点。
这些发现为代谢性疾病的早期筛查和预防提供了新的思路。通过监测肠道菌群年龄的变化,结合传统的临床指标,可以更早地识别疾病风险,实现更精准的健康管理。随着检测技术的进步和预测模型的完善,基于肠道菌群的疾病预警系统有望成为临床实践中的重要工具。
实现从被动治疗到主动预防的转变
随着人口老龄化加剧,深入理解和干预衰老过程变得愈发重要。近年来,肠道微生物组研究为我们提供了全新的视角,从发育到衰老的全程监测和干预成为可能。
肠道年龄概念的提出,标志着生物学年龄评估领域的一次重要范式转变。这一转变不仅打破了传统chronological age的局限,更是将微生物组这一动态指标引入健康评估体系,为个体化健康管理提供了新的思维框架。
在发育领域,研究发现肠道菌群年龄可以有效反映儿童发育状况。发育迟缓儿童往往表现出明显的”菌群年龄滞后”现象,这为早期干预提供了新的靶点。同时,在早衰综合征患者中观察到的菌群加速衰老特征,以及在糖尿病、心血管疾病患者中发现的菌群老化预警信号,都展示了微生物组在疾病预防和健康管理中的重要价值。
谷禾团队通过分析60万例不同年龄人群的6万个菌群特征,这种基于海量数据的个体化健康监测方法,为微生物组研究开辟了新的范式。通过持续监测个体肠道菌群的动态变化,有助于更早地发现健康隐患,实现疾病的早期预警和干预。
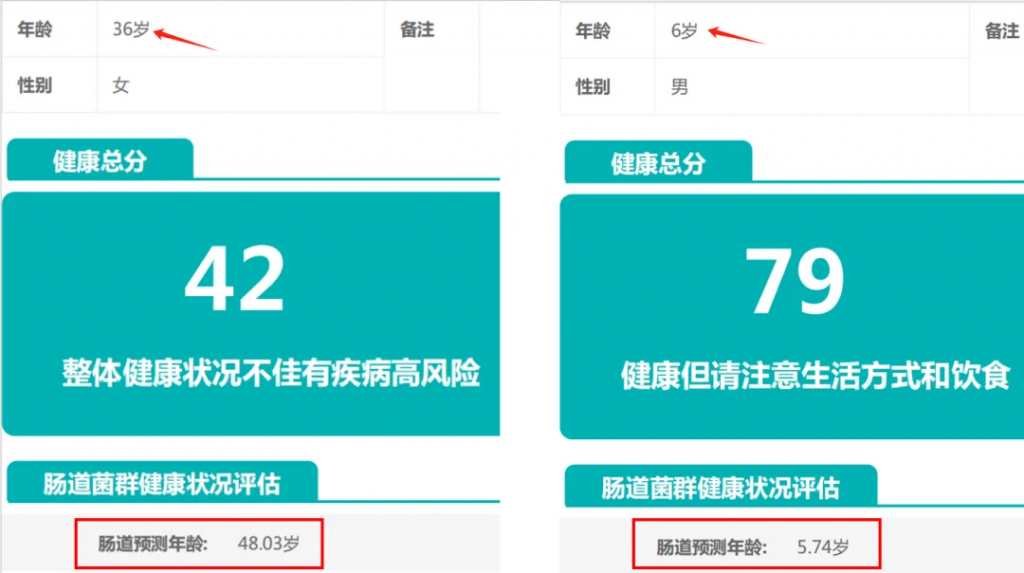
<来源:谷禾健康肠道菌群检测数据库>
从精准医学的角度来看,肠道年龄的概念为个体化健康管理提供了新的工具。通过整合微生物组数据与传统临床指标,我们可以构建更全面的健康评估体系。这种多维度的评估方法不仅能够反映个体当前的健康状态,还能预测未来的健康轨迹,为精准医疗干预提供决策依据。
尽管目前研究已取得显著进展,但仍面临诸多挑战:微生物组与衰老的因果关系有待厘清,个体差异和环境因素的影响需要进一步研究,预测模型在特定人群中的适用性也需要验证。此外,如何将研究成果有效转化为临床应用,实现精准干预,也是未来需要重点解决的问题。
展望未来,随着高通量测序技术的进步和人工智能算法的优化,结合多组学数据的整合分析将帮助我们更全面地理解肠道微生物组在人体发育和衰老过程中的作用。精准医学的未来将更加依赖于这种整合的、动态的健康评估体系,结合人工智能分析,可以更好为每个个体制定个性化的健康管理方案,实现从被动治疗到主动预防的转变。
主要参考文献:
Min M, Egli C, Sivamani RK. The Gut and Skin Microbiome and Its Association with Aging Clocks. Int J Mol Sci. 2024 Jul 8;25(13):7471.
Hohman LS, Osborne LC. A gut-centric view of aging: Do intestinal epithelial cells contribute to age-associated microbiota changes, inflammaging, and immunosenescence? Aging Cell. 2022 Sep;21(9):e13700.
Tao X, Zhu Z, Wang L, Li C, Sun L, Wang W, Gong W. Biomarkers of Aging and Relevant Evaluation Techniques: A Comprehensive Review. Aging Dis. 2024 May 7;15(3):977-1005.
Wang H, Chen Y, Feng L, Lu S, Zhu J, Zhao J, Zhang H, Chen W, Lu W. A gut aging clock using microbiome multi-view profiles is associated with health and frail risk. Gut Microbes. 2024 Jan-Dec;16(1):2297852.

谷禾健康

通过膳食来改善健康的观点已逐渐深入人心,目前越来越多的食品,尤其功能性食品,特膳甚至药膳等成分表中常出现低聚果糖(果寡糖)、低聚半乳糖等成分。
低聚糖又名寡糖,通常被视为介于单糖(如葡萄糖、果糖)和多糖(如淀粉、纤维素)之间的物质。简单来说,单糖是最基本的糖单位,就像盖房子的小砖块,而低聚糖就是由几个这样的小砖块连接起来的 “小建筑”,但又没有淀粉、纤维素这种“高楼大厦”那么大。
低聚糖是一种新型功能性糖源,集营养、保健、食疗于一体,甜度和热量都低于传统糖类。
除了具备“糖”的作用外,低聚糖最大的特点是其益生元功能。低聚糖可以作为肠道有益菌的“食物”,促进双歧杆菌等有益菌的生长,调节肠道菌群平衡,改善肠道功能。并且不同低聚糖可特异性促进某些有益菌增殖,你可以理解为不同的益生菌擅于利用不同的低聚糖。
低聚糖除了作为益生元促进肠道有益菌增殖外,对人体还有多种益处。一些低聚糖具有直接的抗菌作用,部分低聚糖可以与免疫细胞相互作用,调节免疫功能。母乳喂养的婴儿具有较强的免疫力,这其中“母乳低聚糖”发挥了不可或缺的作用。
低聚糖还可以通过靶向肠道微生物群和微生物代谢物来增强肠道屏障,改善肠道功能;调节血糖水平,影响胰岛素敏感性;调节脂肪代谢,降低血脂;影响神经递质的产生;调节炎症反应等。这些能力在改善便秘、治疗或减轻肥胖、糖尿病、炎症性肠病、抑郁症等疾病中发挥了重要作用。还有研究发现,低聚糖对于减轻COVID-19(新型冠状病毒)的长期后遗症具有一定效果。
尽管目前的证据大多表明低聚糖对肠道菌群和人体健康有益,但是不同人群的菌群构成不同,身体健康状况存在差异,如何更好的选择合适的,单独的低聚糖产品或与低聚糖组合的产品需要更多的数据和了解。
本文今天将详解介绍什么是低聚糖,常见的低聚糖种类,来源和差异,在此基础上我们通过检索的研究资料总结汇总不同低聚糖对肠道菌群以及人体健康的影响差异,阐述它们如何通过调节肠道微生物和相关代谢物影响宿主的免疫系统、炎症水平和能量代谢,从而影响糖尿病、肥胖、抑郁、炎症性肠病及便秘等慢性疾病的发生发展。这可能是通过饮食干预促进人类健康和对抗慢病的新策略。
什么是低聚糖?
在谷禾营养素那篇文章(什么是营养,什么是营养素,什么是宏量和微量营养素?)简单地提到过低聚糖,低聚糖是一类由2到10个单糖分子通过糖苷键连接而成的碳水化合物。
自然界中典型低聚糖的结构
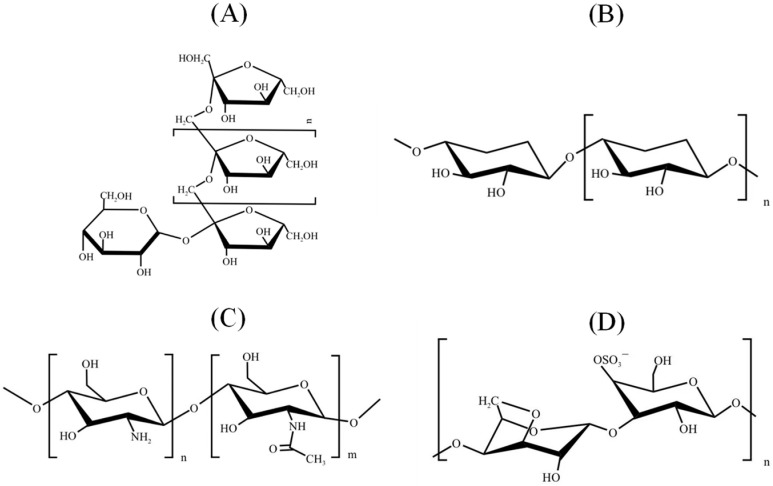
Cheong KL,et al.Pharmaceuticals (Basel).2023
(A):典型的低聚糖结构,多个单糖单位通过糖苷键连接在一起,如麦芽低聚糖或纤维低聚糖。
(B):线性低聚糖结构,单糖单位通过1,4-糖苷键连接,是纤维素或类似的低聚糖。
(C):含有氨基修饰的低聚糖,可能是壳寡糖或类似的氨基低聚糖。
(D):这是一个含有硫酸基团(-OSO₃⁻)的低聚糖,是硫酸化低聚糖(如硫酸软骨素或硫酸化海藻糖)。
低聚糖广泛存在于自然界,尤其是在植物中,如洋葱、大蒜、香蕉、燕麦和大豆等食物中,具有多种生物学功能和健康益处。
低聚糖(寡糖)主要根据单糖组成和结构进行分类,常见种类:
低聚果糖(FOS),组成:果糖+葡萄糖,主要来源有菊苣、洋葱、香蕉,可以促进双歧杆菌增殖。
低聚半乳糖(GOS),组成:半乳糖+葡萄糖,主要来源母乳、乳制品等,被报道可以增强钙吸收。
低聚异麦芽糖(IMO),组成:葡萄糖(α-1,6糖苷键),主要来源发酵食品、麦麸、蜂蜜,常用于烘焙。
低聚木糖(XOS),组成:木糖,来源有玉米芯、甘蔗渣等。
除此之外,还有其他一些分类方式
•按单糖组成分类
同质低聚糖:由相同的单糖分子聚合而成。比如麦芽低聚糖,它是由多个葡萄糖分子以α-1,4糖苷键连接而成。
异质低聚糖:由不同种类的单糖分子聚合而成。例如低聚乳糖,由半乳糖和葡萄糖以β-1,4糖苷键连接而成。
•按来源分类
天然低聚糖:天然存在于各种动植物中的低聚糖。
人工合成低聚糖:通过化学合成或生物技术手段制备得到的低聚糖。
目前市场上的低聚糖主要是提取来自食物或药材,主流原料来源:
•豆科植物:大豆低聚糖占全球产量35%;
•菊科植物:菊苣根提取低聚果糖(FOS);
•乳制品:乳清加工获取低聚半乳糖(GOS);
•中药材:黄芪、党参等含黄芪低聚糖。
提取技术对低聚糖的纯度影响比较大,水提醇沉法到固定化酶解再到色谱分离,已经可以达到食品级纯度了。
此外,低聚糖也可以通过生物合成路径合成,主要是三大生产路线:
1.酶法合成(主流工艺)
果糖基转移酶生产FOS,转化率达75%
β-半乳糖苷酶制备GOS
2.微生物发酵
芽孢杆菌发酵玉米淀粉产低聚异麦芽糖(IMO)
酵母工程菌产低聚木糖(XOS)
3.化学合成
酸水解法制备低聚壳聚糖(COS)
★ 不同低聚糖与益生菌和食药组合的健康改善效果不同
不同常见低聚糖的主要靶向菌群和产物
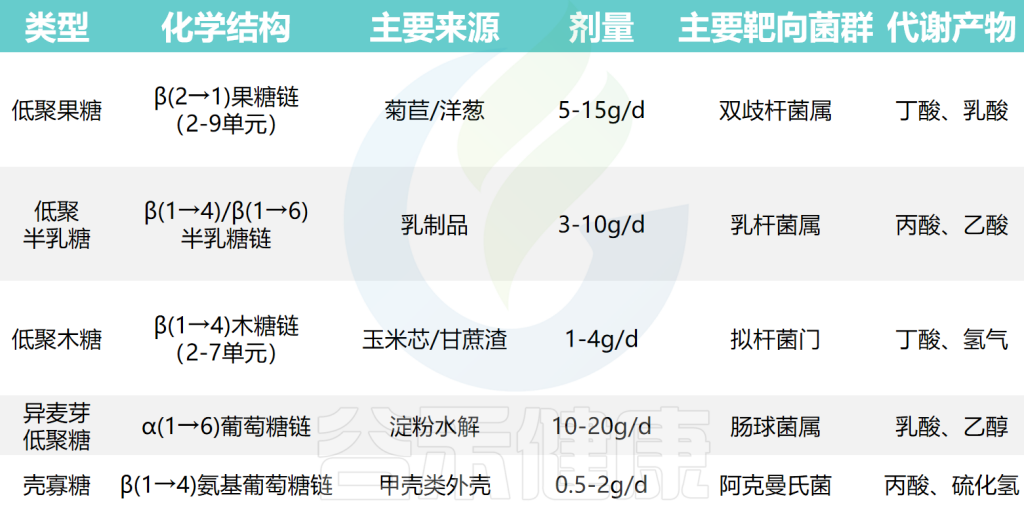
低聚糖与药食成分组合的效果

不同低聚糖与菌群互作的功效
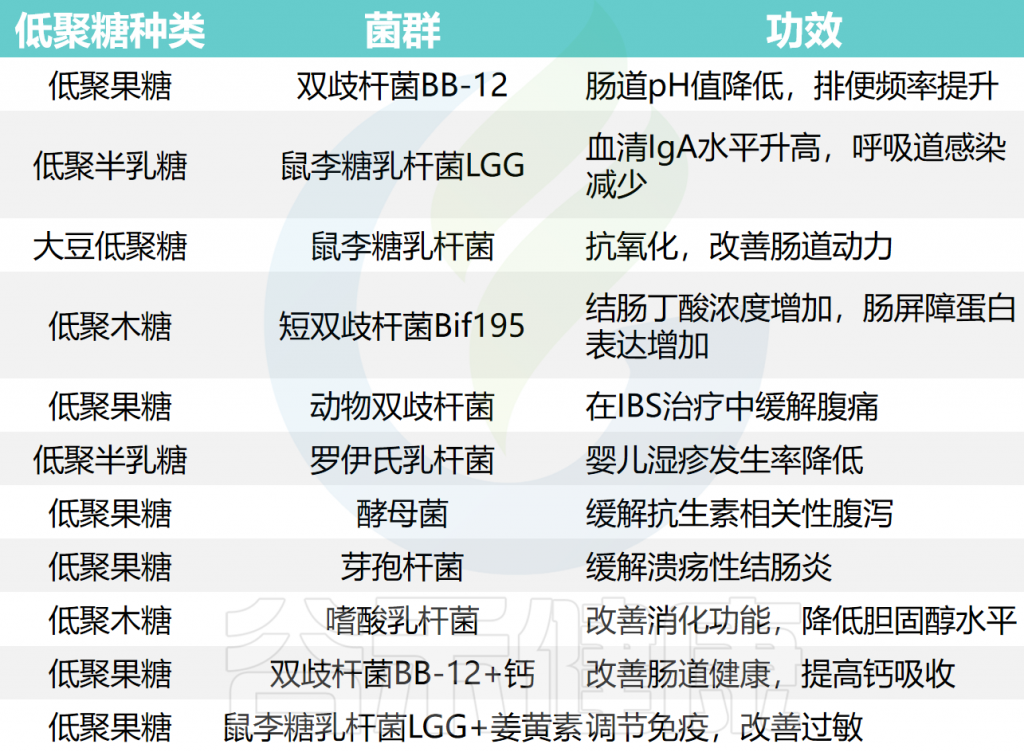
注意:以上部分支持性证据不是很足,尤其有些未完成人类的临床试验,若使用需根据自身情况咨询医疗建议后选择。
① 促进有益菌生长
低聚糖是肠道中特定有益细菌(如双歧杆菌和乳酸杆菌)的 “食物”,可被其选择性利用发酵。这些细菌通过糖苷酶分解和发酵低聚糖,使其茁壮成长并主导肠道微生物群落,在肠道内形成优势菌群,有助于抑制有害菌的生长,改善肠道微生态环境。
② 增强肠道屏障,改善肠道功能
肠道有益菌的增加能够促进肠道蠕动,帮助消化和吸收食物中的营养成分。同时,低聚糖在肠道内发酵产生短链脂肪酸,如丁酸、丙酸等,这些短链脂肪酸可以为肠道细胞提供能量,促进肠道细胞的生长和修复。
通过与G蛋白偶联受体(GPCR)结合,增强肠道屏障功能,有助于维持正常生理功能,预防便秘和腹泻等肠道问题。
③ 具有抗菌、抗病毒活性
低聚糖中的一些种类,如母乳低聚糖(HMO)可抑制病原体生长。研究发现,多种HMO显著抑制B组链球菌(GBS)三种菌株的生长,表明其具有抗菌活性。这一结论通过比较有无HMO条件下的细菌生物量得出,并在不同生长条件下显示出显著抑制作用。
HMO还能通过显著降低多种抗生素(如庆大霉素、红霉素等)对GBS的最低抑菌浓度,增强抗生素对耐药菌的有效性。此外,HMO可提高甲氧苄啶的效力,使其对GBS的MIC显著降低。
在病毒感染方面,体外研究表明HMO(如2’FL、LNnT等)具有预防流感和呼吸道合胞病毒(RSV)感染的能力。6′SL和LNnT预处理24小时可减少呼吸道上皮细胞中的流感复制,而2′FL预处理在两种细胞系中均显示出对RSV的保护作用,3′SL仅在一种细胞系中有效。
④ 调节血糖水平,影响胰岛素敏感性
低聚糖的化学结构和物理性质使其在胃肠道内不易被消化酶完全水解,吸收速度较慢。摄入含低聚糖的食物后,碳水化合物的消化吸收过程被延缓,避免血糖短时间内急剧升高,使血糖上升曲线更平缓。这对糖尿病患者控制血糖水平至关重要,有助于稳定血糖,减少波动带来的并发症风险。
一些研究表明,低聚糖的摄入可能通过调节肠道菌群等机制,改善机体的胰岛素敏感性。胰岛素敏感性的提高意味着身体细胞能够更有效地利用胰岛素,将血液中的葡萄糖转运到细胞内进行代谢,从而降低血糖水平,减轻胰岛素抵抗,对预防和管理糖尿病具有积极作用。
⑤ 与免疫细胞相互作用,调节免疫功能
低聚糖被认为在调节免疫反应中发挥作用,已知与低聚糖相互作用的免疫细胞包括源自先天和适应性免疫系统的巨噬细胞、树突状细胞、B细胞、T细胞和自然杀伤细胞等。
低聚糖增强巨噬细胞的吞噬活性,提高其吞噬和消除病原体的能力;影响树突状细胞(DC)的成熟状态;还可以影响NK细胞的活化状态和表型;并影响B细胞产生抗体。
母乳低聚糖与肠道免疫轴相互作用
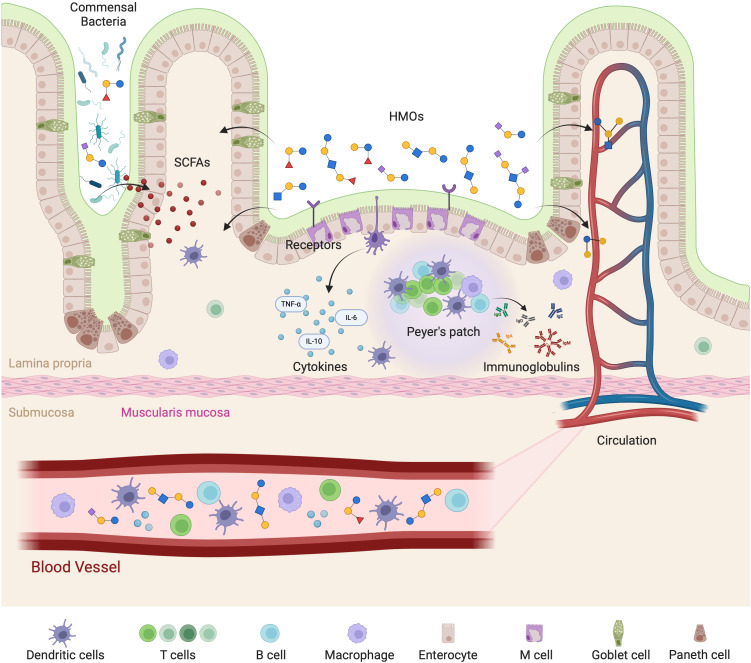
Slater AS,et al.Front Immunol.2025
⑥ 影响炎症反应,可能有助于治疗IBD
低聚糖具有调节免疫系统和减少炎症的能力,可能通过平衡Th1和Th2反应来实现。HMO增加了CD25+/CD4+T细胞的数量,这是T细胞的调节亚群,表明HMO有助于建立Th1/Th2平衡。
低聚糖还可以调节T细胞产生细胞因子,从而影响促炎和抗炎免疫反应之间的平衡。研究表明,某些低聚糖能够增强IL-10等抗炎细胞因子的产生,同时减少T细胞产生IFN-γ和IL-17等促炎细胞因子。
低聚糖被视为炎症性肠病(IBD)的潜在治疗剂。临床前研究表明,唾液酸化HMO(如3′-SL和6′-SL)具有抗炎特性,有助于维持肠道屏障完整性。
正在进行的临床试验评估HMO补充剂在缓解IBD症状和减少炎症方面的疗效,部分已显示症状改善。动物模型中,HMO在减轻炎症和改善肠道屏障功能方面表现出潜力,但仍需临床试验进一步验证其在人类IBD治疗中的效果。
⑦ 调节脂肪代谢,降低血脂
低聚糖在肠道内可与胆汁酸结合,阻止其重吸收,促使肝脏利用血液中的胆固醇合成新的胆汁酸,从而降低血液中的胆固醇含量。同时,低聚糖还调节肠道菌群,影响胆固醇的代谢,减少胆固醇吸收,有助于降低血脂水平,特别是降低低密度脂蛋白胆固醇(LDL-C,即“坏胆固醇”),从而降低心血管疾病的风险。
低聚糖通过调节肠道菌群及其代谢产物,可能影响脂肪代谢相关基因的表达和信号通路,减少脂肪合成,促进脂肪分解和代谢,有助于控制体重,预防肥胖及其相关的心血管疾病和代谢紊乱。
⑧ 预防龋齿
低聚糖在口腔环境中不易被细菌利用产酸。与传统糖类不同,低聚糖不会为致龋菌(如变形链球菌)提供能量,从而减少了口腔细菌产生酸性物质对牙齿的腐蚀。这有助于维持口腔微生物群落的平衡,降低龋齿发生风险,保护牙齿健康。
⑨ 可能具有抗肿瘤活性

还有研究分析了低聚糖的抗肿瘤活性。低聚糖通过重塑肠道菌群、促进短链脂肪酸生成、激活免疫应答及直接调控肿瘤细胞代谢,形成多层次抗肿瘤网络。
例如短链脂肪酸通过AMPK/mTOR通路调控能量代谢,抑制肿瘤细胞增殖。丁酸通过组蛋白修饰抑制癌基因(如c-Myc)表达,同时激活抑癌基因(如p21、p53)。
•化学结构与聚合度:传统糖类中的单糖,如葡萄糖和果糖,是最简单的糖结构,无法进一步水解为更小的糖单位。双糖如蔗糖由一分子葡萄糖和一分子果糖组成,麦芽糖则由两分子葡萄糖构成。低聚糖由2到10个单糖聚合而成,聚合度高于单糖和双糖,但低于多糖(多糖由超过10个单糖聚合而成,如淀粉和纤维素)。
•甜度:一般来说,传统糖类甜度较高,例如蔗糖甜度较高,是常见的甜味剂。而低聚糖的甜度普遍低于传统糖类,有的低聚糖甜度仅为蔗糖的30%-60%左右。
•消化吸收特点:单糖可以直接被人体吸收,为身体提供能量。双糖在消化酶的作用下水解为单糖后被吸收。低聚糖在胃肠道内部分可被消化吸收,但速度较慢;另一部分则无法被消化酶完全水解,进入大肠供肠道有益菌利用。
•血糖反应:传统糖类摄入后迅速被吸收,导致血糖快速上升并产生较大波动。相比之下,低聚糖的消化吸收较慢,对血糖的影响更为平缓,不会引起急剧升高,更适合需要控制血糖的人群。
•生理功能:传统糖类主要为人体提供能量。低聚糖除了提供一定能量外,还具有特殊的生理功能,如作为肠道有益菌的“食物”,促进双歧杆菌等有益菌的生长,调节肠道菌群平衡,改善肠道功能,并具有调节血脂和增强免疫力等潜在健康益处。
•化学成分与来源:代糖是一类甜味剂,包括天然代糖(如甜菊糖苷、罗汉果甜苷等,提取自植物)和人工合成代糖(如阿斯巴甜、糖精钠等,通过化学合成制备)。低聚糖是天然存在的碳水化合物,来源于多种动植物,但含量较低,当然也可以由人工合成。
•甜度:代糖的甜度差异较大,部分人工合成代糖如阿斯巴甜的甜度是蔗糖的180-220倍,远高于低聚糖和传统糖类。天然代糖的甜度则各异,有些与蔗糖相近或略低。
•热量:代糖的热量通常极低或几乎没有,因此被广泛用于替代传统糖类,以满足人们对甜味的需求并减少热量摄入。虽然低聚糖的热量相对传统糖类较低,但每克仍能提供约2-4千卡的能量。
•安全性与健康影响:一般来说,在规定使用范围内,代糖被认为是安全的,但一些人工合成代糖的长期大量摄入潜在健康影响仍存在争议。低聚糖是天然碳水化合物,适量摄入对大多数人安全,并具有调节肠道菌群和改善代谢等健康益处。然而,肠道敏感人群大量摄入低聚糖可能会引起胃肠道不适。
拓展:不适合摄入低聚糖的人群
通常情况下,大多数人都能适量摄入低聚糖并从中受益,但以下几类人群可能不太适合或需要谨慎摄入:
肠道敏感人群:部分肠道极为敏感的人群,如患有肠易激综合征(IBS)且症状较为严重的患者,在摄入低聚糖后,肠道可能无法适应。低聚糖虽然一般可促进有益菌生长,但对于这类肠道极度敏感的人,可能会迅速改变肠道内的微生物环境和渗透压,引发肠道不耐受反应,如腹胀、腹痛、腹泻等症状加重。他们的肠道本身就处于高敏状态,对这类物质的耐受性较差。
对低聚糖过敏人群:极少数过敏体质者可能对低聚糖产生过敏反应,免疫系统将其视为有害物质并引发免疫反应,导致皮疹、瘙痒、呼吸急促、口腔肿胀等症状。这类人群应严格避免摄入可能致敏的低聚糖。
正在使用特定抗生素或药物的人群:某些抗生素在杀灭有害菌的同时也会影响有益菌。使用此类抗生素期间,若大量摄入低聚糖,由于有益菌数量减少,低聚糖可能在肠道内过度发酵,导致胃肠不适。
特殊阶段的糖尿病患者:低聚糖对血糖的影响虽小于传统糖类,但糖尿病患者在血糖控制不稳定或急性并发症(如酮症酸中毒、高渗高血糖综合征)发作期,应严格控制碳水化合物摄入,即使是低聚糖也可能引起血糖波动,需在医生指导下谨慎食用。此外,某些因基因突变导致糖代谢异常敏感的特殊糖尿病患者,也应谨慎摄入低聚糖,以避免血糖失控。
此外,正在服用可能影响肠道菌群或糖代谢的药物(如某些免疫抑制剂、化疗药物等)的患者,在摄入低聚糖前应咨询医生,因为药物与低聚糖之间可能存在相互作用,影响药效或对身体产生不良影响。
糖苷键以多种方式连接,不同的排列组合形成了多种低聚糖,赋予它们各自不同的特性和功能。
这些低聚糖的功能和来源多样,使其在营养和健康方面的作用各不相同。常见的天然低聚糖包括母乳低聚糖(HMO)、低聚木糖(XOS)、阿拉伯木质低聚糖(AXOS)、异麦芽低聚糖(IMOS)、甲壳素低聚糖(NACOS)、甘露寡糖(MOS)、低聚半乳糖(GOS)和低聚果糖(FOS)。

1
母乳低聚糖
母乳在婴儿大脑和免疫系统的发育中至关重要,这很大程度上归功于母乳中的低聚糖。母乳低聚糖(HMO)是由乳腺中的乳糖生物合成的一组低聚糖,是母乳中仅次于乳糖和脂质的第三丰富固体成分。
母乳的组成成分
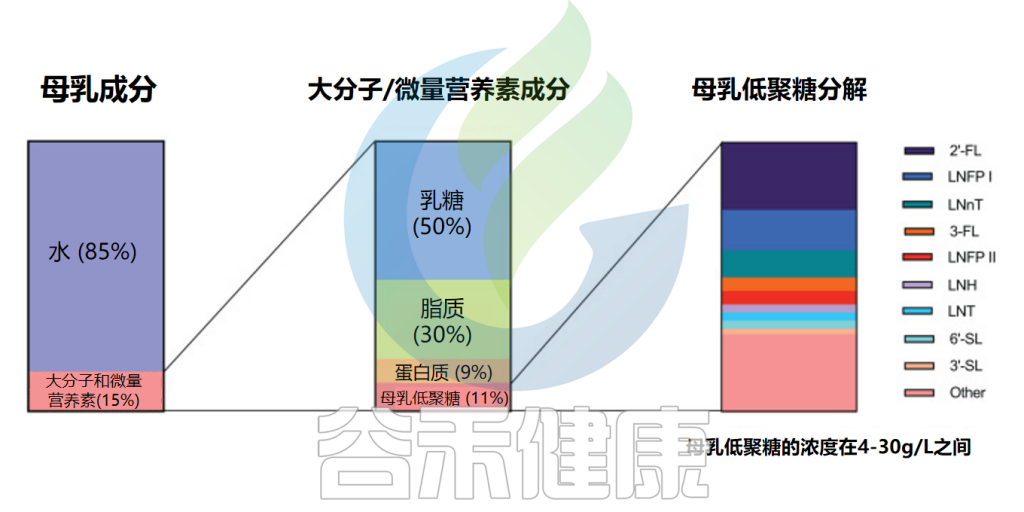
Slater AS,et al.Front Immunol.2025
• 母乳低聚糖对婴幼儿免疫系统的影响重大

最近发表的一项研究发现,母乳低聚糖对婴幼儿的免疫系统及肠道健康和功能具有重要影响:
(1)母乳低聚糖减少免疫系统中选择素介导的细胞间相互作用,降低白细胞在活化内皮细胞上的滚动,从而减少粘膜白细胞的浸润和活化,影响免疫细胞动力学。
(2)母乳低聚糖直接影响肠上皮细胞,调节参与各种细胞过程的基因表达,导致细胞表面聚糖和其他细胞反应发生变化,从而影响肠道健康和功能。
(3)母乳低聚糖能调节淋巴细胞产生细胞因子,促进平衡的Th1/Th2免疫反应。
母乳低聚糖对免疫反应的影响
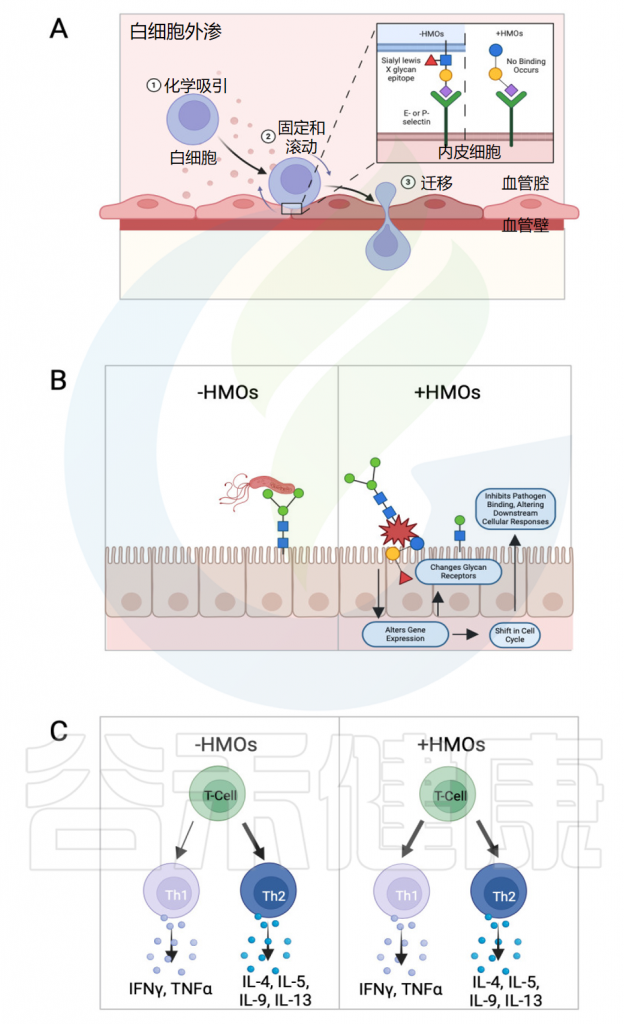
Slater AS,et al.Front Immunol.2025
• 促进有益细菌的生长,抑制宿主感染
作为一种益生元,母乳低聚糖选择性地促进共生肠道细菌的生长而不是病原体,以保护宿主。母乳低聚糖是婴儿肠道中特定有益细菌(如双歧杆菌和乳酸杆菌)的营养来源。
多样化的肠道微生物组与改善整体健康相关,包括更好的营养吸收、增强免疫功能和抵御病原体。母乳低聚糖通过促进粘蛋白产生维持肠道屏障完整性,防止有害细菌和毒素进入血液。
它还可以通过扮演诱饵受体的作用来抑制宿主感染,这些诱饵受体结合病原体以抑制细胞粘附。
2
低聚果糖
低聚果糖(FOS)是一种天然存在于多种植物中的短链碳水化合物,通常被视为益生元。它广泛存在于人们常食用的植物中,如香蕉、黑麦、大蒜、牛蒡、芦笋根、小麦、洋葱、马铃薯、雪莲果、菊芋和蜂蜜等。
• 促进消化吸收,增强肠粘膜
低聚果糖是一种天然活性成分,存在于水果、蔬菜和蜂蜜中,无法被胃肠道的消化酶分解,是优质的水溶性膳食纤维。此外,FOS可增强肠黏膜的保护功能,从而减少胃肠道疾病的发生。摄入低聚果糖可使粪便松软,并促进肠道功能。
• 促进有益菌生长,抑制病原体感染
研究表明,摄入低聚果糖后,肠道内双歧杆菌的数量可明显增加,有害菌如大肠杆菌、梭状芽孢杆菌等的数量则会相应减少。这有助于改善肠道功能,增强肠道屏障功能,预防便秘、腹泻等肠道疾病,还能降低肠道感染的风险。
低聚果糖通过与肠壁上的受体竞争来抑制病原体,从而降低感染风险,并有效竞争营养物质以预防感染。
• 促进矿物质吸收
低聚果糖有助于增加肠道对钙、镁等矿物质的吸收,对骨骼健康起到积极作用。
• 控制血糖和胆固醇
低聚果糖作为一种新型食疗剂,能有效降低血清胆固醇、甘油三酯和游离脂肪酸的含量,对因高血脂引起的高血压和动脉硬化等心血管疾病有良好改善作用。研究显示,在小鼠饲料中添加10%低聚果糖,饲养8周后,实验组小鼠的血浆总胆固醇水平显著低于对照组,表明低聚果糖可能有助于调节血脂代谢。
3
低聚木糖
低聚木糖(XOS)是木聚糖的水解产物,是一种新型的功能性低聚糖。天然低聚木糖,通常占少数,主要存在于一些植物中,例如橄榄、甘蔗、杨树。
一些食物中也含有低聚木糖,包括:燕麦、大麦、黑豆、红豆、竹笋、甜菜、胡萝卜、洋葱和香蕉。
• 促进双歧杆菌增殖的能力是其他低聚糖的数倍
与其他低聚糖(如低聚果糖和低聚异麦芽糖)相比,它对肠道双歧杆菌的增殖促进作用更强,其双歧因子功能是其他低聚糖的10-20倍。
注:双歧因子是促进双歧杆菌生长的营养物质。
• 在抗肿瘤活性中发挥作用
低聚木糖在抗肿瘤活性方面发挥两种作用。首先,其能高度选择性地促进肠道中双歧杆菌的增殖,双歧杆菌是重要的益生菌,能够抑制有害菌生长并减少内源性致瘤物质的产生,同时通过增加免疫细胞数量和活性发挥抗肿瘤作用。
其次,低聚木糖促进短链脂肪酸(SCFA)的产生,短链脂肪酸具有显著的抗肿瘤作用,能降低肠道pH值,从而抑制病原菌和有害菌的生长,降低肿瘤发生率。
此外,低聚木糖还在调节血糖、降低血脂和预防肠道疾病方面发挥重要作用。
4
阿拉伯木质低聚糖
阿拉伯木质低聚糖(AXOS)是阿拉伯木聚糖(AX)的一种酶解产物。在没有外源木聚糖降解酶的情况下,阿拉伯木聚糖可以通过木聚糖酶等降解酶转化为 AXOS,这些酶由肠道中的拟杆菌门等细菌分泌。AXOS通过特定的运输载体进入细菌,并被糖苷水解酶进一步降解为单糖,如木糖和阿拉伯糖。嗜酸乳杆菌、短乳杆菌和双歧杆菌等物种产生这些酶。
• 可产生短链脂肪酸
阿拉伯木质低聚糖可被肠道微生物群用于产生短链脂肪酸(SCFA),研究表明,分子量小于400Da的AXOS具有更好的活性。丁酸可作为结肠细胞的能量来源,刺激结肠上皮细胞的生长并抑制结肠肿瘤细胞的生长。发酵产生的乙酸和丙酸被吸收,并分别参与体内的脂质代谢和糖代谢。
5
低聚异麦芽糖
淀粉中发现的低聚异麦芽糖(IMO)通常以支链淀粉或多糖的成分形式存在,除了在淀粉、玉米、牛奶、麦麸、豆浆、酱油和蜂蜜中存在外,很少以游离状态天然存在。
• 改善肠道环境,维持菌群平衡
低聚异麦芽糖(平均分子量900Da)可被肠道微生物群降解,从而改善肠道环境,选择性地促进双歧杆菌的增殖,并维持肠道微生物群的平衡。
同时,IMO还可以通过产生短链脂肪酸(SCFA)和有机酸等发酵产物,预防手足口病(HFMD)引起的全身和组织炎症、葡萄糖耐量不良、全身性肥胖等症状。
6
低聚半乳糖
低聚半乳糖(GOS)是天然低聚糖,动物的乳汁中存在微量的低聚半乳糖,母乳中含量稍多。此外,某些豆类、魔芋和卡拉胶中也存在低聚半乳糖。
• 能够促进多种有益菌的增殖
低聚半乳糖(GOS)与低聚果糖(FOS)和低聚异麦芽糖(IMO)相比,是三种低聚糖中唯一能被人体肠道内八种有益菌利用的。它是双歧杆菌和嗜酸乳酸杆菌等有益菌的优质营养源和增殖因子,有助于改善肠道的消化吸收功能。
• 低聚半乳糖对婴儿消化和免疫很重要
新生儿的消化功能比较薄弱,母乳中含有的低聚半乳糖,它不但能改善婴儿的消化功能,还能促进钙的吸收,增强婴儿的免疫力。
不同的低聚糖在聚合程度、糖苷键和整体结构复杂性(如侧链)等方面存在差异。这些差异导致与低聚糖相互作用的多种微生物群,表现为有益细菌增殖程度、有害细菌受抑制程度以及酸和气体产生的差异。
以木聚糖为例,进入肠道后,被拟杆菌门分泌的糖苷水解酶降解为低聚木糖(XOS),并转运至细胞周质中。木聚糖及其代谢产物可通过转运蛋白进入双歧杆菌或其他细菌中,并被革兰氏阳性菌PUL编码的碳水化合物活性酶进一步降解。
• 低聚木糖可被降解为单糖用于产生短链脂肪酸
低聚木糖(XOS)可被肠道微生物分泌的d-木糖苷酶和阿拉伯糖苷酶水解为单糖,用于生产短链脂肪酸,如乙酸盐、丙酸盐、丁酸盐、乳酸和琥珀酸。研究表明,XOS可显著增加有机酸含量,摄入阿拉伯糖—低聚木糖后乙酸浓度也显著升高。
SCFA作为有机酸,可降低肠道pH值,促进胃肠蠕动,抑制硝酸盐还原菌的生长,从而预防肠道疾病。此外,SCFA通过调节表皮屏障、免疫介导炎症和抑制肠道病原体感染,影响宿主免疫功能,并通过抑制结直肠肿瘤细胞的生长、诱导分化和凋亡发挥抗肿瘤作用。
肠道中木聚糖和低聚木糖的代谢
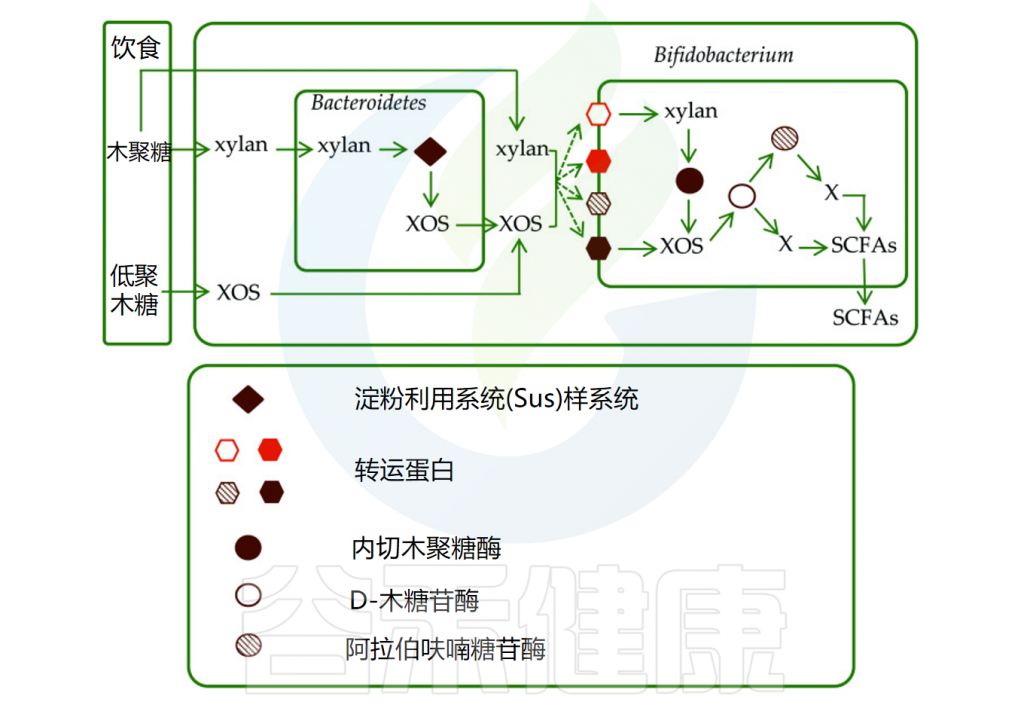
doi: 10.1039/d0ra00344a.
具有不同聚合度(DP)的低聚糖可以被不同的菌株利用。例如,DP3低聚果糖(FOS)在体外促进双歧杆菌生长,同时抑制梭菌增殖,显示出更优越的选择性刺激活性。
• 不同细菌喜好代谢不同的低聚糖
研究证明乳双歧杆菌(Bifidobacterium lactis DR10)消耗的低聚糖(低聚半乳糖)具有较高的聚合度,而鼠李糖乳杆菌(Lactobacillus rhamnosus DR20)更喜欢使用半乳糖。
评估了具有不同DP的竹笋壳低聚木糖(XOS)的益生元能力,结果显示高聚合度(>X5)的低聚木糖增加有益菌(如拟杆菌属)的丰度,而低聚合度(X2-X3)则促进其他有益菌(如Lachnochlostridium)的增殖。青春双歧杆菌(Bifidobacterium adolescentis)和嗜酸乳杆菌(Lactobacillus acidophilus)主要利用X2-X3组分。
• 低聚合度的聚糖更能支持肠道菌群增殖
微生物降解高聚合度的低聚糖通常需要更多能量,因为微生物优先将其降解为低聚合度的低聚糖,这限制了肠道微生物群的代谢能力。相反,低聚合度的低聚糖的分解较简单,所需能量较少,因此更能支持肠道微生物群的生长和增殖。
例如,关于低聚糖的研究表明,DP3-4(≥80%)的成分被所有益生菌菌株利用,DP5-6的部分被一些菌株利用,而DP≥7的部分仅被乳酸菌(LAB)和双歧杆菌利用。DP3-5中的异麦芽糖比DP2更易消化,尽管其到达结肠的几率更高,但对有益益生菌的发酵选择性较低。
• 不同聚合度的低聚糖经菌群产生的代谢物不同
不同聚合度的低聚糖对肠道菌群产生的主要代谢物影响不同。首先,具有不同聚合度的低聚糖导致肠道微生物群产生不同类型和比例的短链脂肪酸。高聚合度的低聚糖发酵较慢,逐渐释放更多丁酸盐,作为诱导产丁酸盐细菌增殖的潜在底物;而低聚合度聚糖快速发酵,产生更多乙酸盐和丙酸盐。
此外,具有不同聚合度的低聚糖在发酵过程中产生的气体(如氢气和二氧化碳)数量也不同。通常,高聚合度的低聚糖因发酵速度较慢,产气量较少,而低聚合度的低聚糖发酵速度较快,产气量较多。
低聚糖在肠道中的发酵过程涉及低聚糖的摄入,这些低聚糖首先被细菌膜上的模块化聚糖酶识别并水解为低聚合度的低聚糖。随后,低聚合度的低聚糖通过膜转运蛋白进入细胞,并被酶分解为二糖和单糖。
• 不同低聚糖经分解后的产物不同
例如,低聚半乳糖(GOS)被β-半乳糖苷酶水解为半乳糖和葡萄糖,随后进入Leloir途径和糖酵解。低聚果糖(FOS)首先通过ABC转运蛋白被嗜酸乳杆菌吸收,降解为β-葡萄糖苷,进一步被果糖苷酶和β-呋喃糖苷酶分解为果糖和葡萄糖。在婴儿双歧杆菌亚种中,母乳低聚糖(HMO)底物通过ABC转运蛋白完整运输,随后由多种细胞质糖苷酶水解,包括α-岩藻糖基化酶和2,3/6-α唾液酸酶。
• 益生菌的诱导生长能力与糖苷键相关
低聚糖的不同结构对肠道微生物组有不同影响,包括糖苷键类型和连接模式。例如,异麦芽低聚糖(IMO)中形成的α-(1→3)-和α-(1→2)-连接的葡萄糖寡糖(GlcOSs)促进了双歧杆菌属和乳酸杆菌属的生长,其发酵选择性高于仅含α-(1→6)-连接的IMOs。
研究了不同二糖键的低聚糖对乳酸菌的影响,发现大多数物种对α-(1→6)-IMOs的生长速率较低,而β-(1→4)-连接的纤维二糖和β-(1→6)-连接的龙胆二糖显著促进了短乳杆菌(L.brevis ATCC 8287)、鼠李糖乳杆菌(L.rhamnosus ATCC 53103)、植物乳杆菌(L.plantarum WCFS1)和加氏乳杆菌(L.gasseri ATCC 33323)的增殖。
同样,研究了二糖的益生元指数(PI),发现α-葡萄糖二糖的PI高于β型。比较了β-低聚糖、β-低聚半乳糖和α-低聚半乳糖对肠道菌群代谢的影响,结果显示含β-糖苷键的低聚果糖和低聚半乳糖是双歧杆菌的首选底物,对微生物组成影响显著。
此外,摄入含β-1,3、β-1,4和β-1,6糖苷键的低聚果糖在健康志愿者中显示出更好的益生元效应。双歧杆菌、乳酸杆菌和屎肠球菌对主要含有β-1,3和β-1,6糖苷键的低聚果糖的发酵活性优于含单个β-1,4糖苷键的低聚果糖。这与另一项研究的结论相似,后者发现双歧杆菌、乳酸杆菌和链球菌更偏好含β-1,6糖苷键的半乳糖,而非β-1,4糖苷键的半乳糖。
总之,益生菌的生长诱导能力与糖苷键的类型相关,因此了解低聚糖的结构-活性关系至关重要。
• 取代基的数量和类型影响微生物的组成和发酵速率
低聚糖中取代基的数量会影响微生物的发酵速率。低取代的低聚糖优先被发酵,导致高取代的低聚糖积累,表明取代基的存在可能延迟或完全阻碍发酵。
研究表明,木糖低聚糖(XOS)上的取代基会影响双歧杆菌的发酵,导致乳酸产量不同。未取代的XOS中乳酸含量高于取代的XOS,说明未取代的XOS更易被肠道微生物发酵。此外,已有研究描述了双歧杆菌在体外和体内对低取代XOS的偏好,表明微生物可能根据低聚糖的结构优先生长或被抑制,从而改变微生物群落的组成。
低聚糖中取代基的类型同样影响微生物的发酵速率和组成。在人类粪便体外发酵实验中,线性木糖低聚糖和阿拉伯糖取代的木糖低聚糖(AXOS)的发酵速度快于乙酰化木糖低聚糖,而含有4-O-甲基葡萄糖醛酸基团(GlcAmeXOS)的木糖低聚糖发酵速度最慢。与AXOS相比,使用XOS作为唯一碳源时,拟杆菌门表现出优异的生长性能,其降解XOS的过程包括细胞外降解和骨骼的分枝,随后是寡聚体的细胞内水解,最终产生乙酸盐、丙酸盐和丁酸盐作为主要代谢产物。
• 低聚糖的链长和形状特异性地影响菌群生长
此外,低聚糖的链长和形状也很重要。例如,长链低聚糖对上肠的水解和降解具有更强的抵抗力,能更有效地刺激双歧杆菌、普雷沃菌属和乳酸菌的生长。
双歧杆菌在利用不同链长的低聚果糖(FOS)时表现出选择性特异性,通常短链FOS优先被发酵,其次是长链FOS。环状异麦芽低聚糖(IMO)已被证明可以抑制链球菌,而具有更多分支的小麦阿拉伯木聚糖水解物则只能部分被双歧杆菌和拟杆菌发酵。
综上所述,聚合度、取代基和糖苷键类型显著影响益生菌的活性和增殖能力,因此针对不同的益生菌需要施用对应特点的低聚糖。
低聚糖作为一种重要的功能性食品成分,近年来在多种疾病的治疗中显示出显著的潜力。其通过调节肠道微生物群、改善代谢功能和增强免疫反应等机制,成为研究的热点。
接下来将探讨低聚糖在不同疾病人群中的治疗效果,特别是在肥胖、糖尿病、肠道疾病、抑郁症和便秘等方面的应用。甚至还有研究发现了低聚糖在新型冠状病毒(COVID-19)感染后的潜在调节作用。
肠道微生物失调是肥胖患者和动物模型的常见特征。研究表明,益生元低聚糖(如低聚果糖、低聚木糖和低聚半乳糖)通过调节肠道微生物群具有抗肥胖作用。
• 低聚糖通过调节肠道菌群发挥抗肥胖作用
一项针对肥胖小鼠模型的研究发现,低聚糖的给药增加了拟杆菌门的丰度,降低了厚壁菌门的丰度,并改变了100多个细菌类群。另一项研究发现低聚木糖饮食减少了小鼠的内脏脂肪,这与肠道微生物群的变化有关,具体表现为拟杆菌门增加和厚壁菌门减少。在科和属水平上,f_S24-7_Unclassified显著增加,而链球菌科、粪球菌属、瘤胃球菌属和乳球菌属显著减少。
此外,高脂饮食(HFD)导致血浆脂多糖(LPS)水平持续升高,进而引发全身炎症反应,促进肥胖患者的胰岛素抵抗。在一项针对肥胖女性的研究中,低聚果糖干预后双歧杆菌和普拉梭菌的丰度增加,肠道菌群的变化与脂肪量、血清脂多糖水平和代谢(如马尿酸、乳酸和血浆蛋白C)的变化相关。
同样,食用低聚木糖可降低肥胖小鼠的代谢内毒素血症。结果表明,低聚糖可以抑制促炎菌的生长,如瘤胃球菌、变形菌门和一些产生毒素的梭菌属,并促进有益细菌(如双歧杆菌、乳酸杆菌和普雷沃氏菌)的生长,从而有助于缓解肠道炎症并降低肥胖风险。
因此,通过低聚糖调节肠道微生物群的组成被认为是预防和治疗肥胖的有效方法。
• 通过代谢产生短链脂肪酸抑制脂肪合成
肥胖的直接原因是脂肪合成的速度超过脂肪消耗的速度。因此,阻断脂肪合成和增加能量消耗是对抗肥胖的最有效策略。低聚糖对减肥的影响主要归因于肠道微生物群产生短链脂肪酸,因为它们在调节食物摄入和能量代谢中起着重要作用。
乙酰辅酶A羧化酶(ACCase)是脂肪酸合成过程中的关键酶。通过抑制ACCase活性,可以减少脂肪酸的合成,这有助于预防肥胖。乙酸盐被催化成乙酰辅酶A,丁酸盐被转化为丁酰辅酶A,作为限速酶(ACCase)脂肪酸合成的抑制剂,以减轻肥胖。
丁酸盐通过摄入低聚糖而丰富,调节肠道微生物群中丁酸盐与乙酸盐的比例是治疗肥胖的潜在策略。研究表明,低聚半乳糖通过调节短链脂肪酸的合成改善小鼠的脂质代谢。膳食补充甘露寡糖可以通过重塑肠道微生物组成和增强短链脂肪酸的形成来减少肥胖。
• 通过影响胆汁酸的合成和释放调节能量代谢
低聚糖还可以通过影响与胆汁酸(BA)代谢相关的肠道微生物群来调节胆汁酸的合成和释放,例如梭菌、拟杆菌门、乳酸杆菌和双歧杆菌。
研究发现,几丁寡糖干预后,肠道菌群可以促进胆汁酸的释放,进而激活TGR5,增强棕色脂肪产热和TGR5主导的脂肪酸氧化信号通路,从而在减肥和降脂方面发挥作用。
其他研究表明,低聚半乳糖显著影响了小肠中胆汁酸的浓度,改善了葡萄糖代谢,并通过调节脂质消化影响脂质吸收。果胶低聚糖也被证明可以通过肠道微生物群及其代谢物介导胆固醇代谢。
// 编者小结
肠道微生物群能够利用低聚糖产生营养代谢物,这些代谢物充当细菌群落的“信使”,影响宿主能量稳态并调节宿主代谢,从而有助于对抗肥胖。
低聚糖对肥胖和2型糖尿病的影响
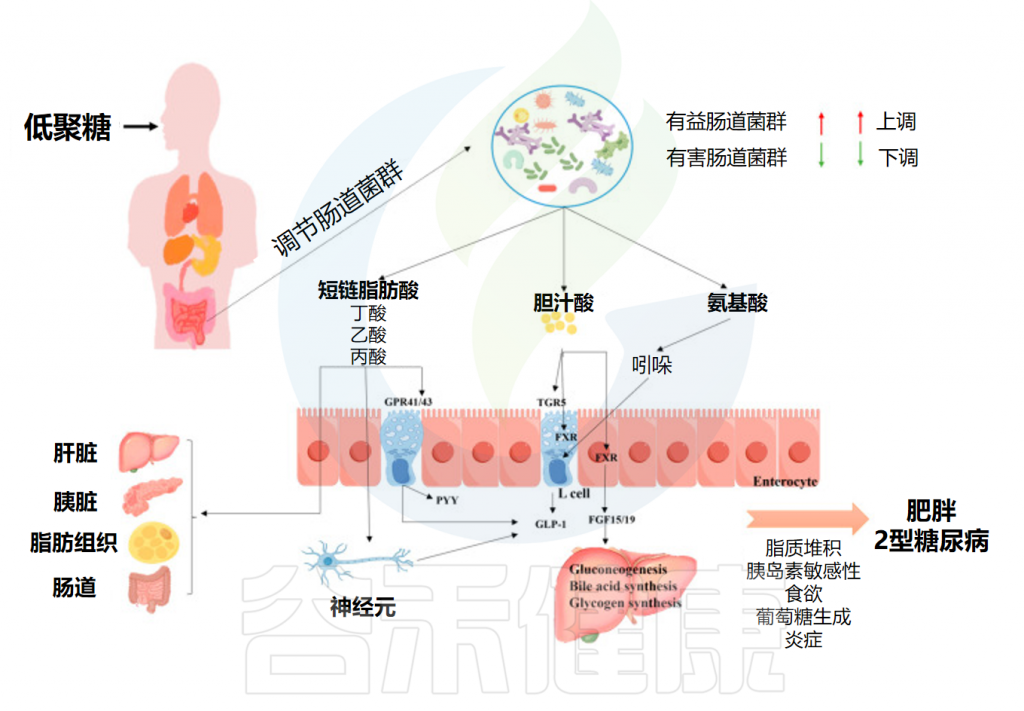
Yuan M,et al.Foods.2024
糖尿病是一种以高血糖为特征的慢性疾病,主要由胰岛素分泌绝对或相对不足和利用受损引起。目前,增加膳食纤维摄入量是2型糖尿病(T2DM)患者的推荐饮食疗法之一。
• 低聚糖通过增加双歧杆菌等特定有益菌,改善糖尿病
研究表明,低聚糖(NDO)能够通过调节肠道菌群,丰富或减少特定微生物,从而有效改善糖尿病。例如,在T2DM大鼠中,双歧杆菌属、罗氏菌属、粪杆菌属、拟杆菌属和阿克曼氏菌属这些有益菌的丰度下降,而脱硫杆菌属、颤杆菌克属、梭杆菌属、瘤胃球菌属和Blautia属的丰度增加。
经过16周的低聚果糖治疗,T2DM模型大鼠的物种α多样性降低,双歧杆菌的相对丰度增加,瘤胃球菌的相对丰度显著降低。后续对低聚果糖和低聚半乳糖的研究发现了Phascolarctobacterium、Coprococcus和Oscillospira的丰度也有所降低。
• 产生短链脂肪酸影响胰岛素敏感性
此外,低聚糖通过影响微生物产生的有益代谢物,如短链脂肪酸(SCFAs)、氨基酸代谢物和生物活性多肽,来调节胰岛素敏感性、血糖和脂质代谢,从而缓解糖尿病的发病和进展。
研究表明,SCFA调节胰腺的胰岛素分泌,防止胰岛素抵抗并增强胰岛素敏感性。丙酸盐通过多种机制增强葡萄糖刺激的胰岛素释放,并维持胰腺β细胞的功能和数量,包括抑制细胞凋亡、促进细胞增殖和减少α细胞向β细胞的反向分化。因此,丙酸盐有助于维持胰岛功能的完整性和稳定性。
此外,丁酸盐在小鼠模型和大型人群队列中被证明能提高胰岛素敏感性并防止胰岛素抵抗,其机制与促进能量消耗和刺激线粒体功能有关。
作为信号分子的SCFA通过激活G蛋白偶联受体GPR41和GPR43来调节胰岛素水平并抑制肝脏糖异生,从而维持宿主能量稳态。它们还促进胰高血糖素样肽-1(GLP-1)和肽YY的分泌,GLP-1通过降低血糖水平和改善胰岛素分泌与抵抗参与葡萄糖稳态。SCFA在T2DM的发展中起着关键作用,并可作为代谢紊乱或体内平衡的标志物。
• 摄入低聚糖形成的氨基酸代谢物影响血糖水平
摄入低聚糖可产生多种氨基酸代谢产物,影响血糖水平和胰岛素敏感性。一些氨基酸可被特定肠道微生物转化为生物活性代谢物,例如吲哚、丙酸咪唑和酪胺。
色氨酸(Trp)可被多种细菌代谢成吲哚,并调节GLP-1的分泌。Trp也可被某些肠道微生物转化为吲哚丙(IPA),如C.caloritolerans和C.paraputrificum,IPA可显著降低大鼠的空腹血糖和胰岛素水平,改善胰岛素抵抗。
此外,研究发现,低聚糖干预后T2DM模型大鼠中糖原氨基酸(如脯氨酸、丝氨酸和亮氨酸)的含量增加。丝氨酸和谷氨酰胺的增加可降低T2DM的风险。
总之,低聚糖通过调节肠道菌群和碳水化合物、脂质、蛋白质的代谢。同时,肠道微生物群产生的众多代谢物可反馈到大脑,影响许多胃肠道过程。
炎症性肠病(IBD)是一种常见的非特异性慢性胃肠道炎症性疾病,包括克罗恩病(CD)和溃疡性结肠炎(UC)。越来越多的证据表明,功能性低聚糖作为天然活性物质,可以有效改善IBD。
• 丰富肠道菌群的多样性
低聚糖可以通过调节肠道菌群来缓解肠道炎症。研究发现,IBD患者粪便中大肠埃希菌和粪肠球菌的水平显著高于正常人,而乳酸菌和双歧杆菌的丰度显著降低。肠道微生物失调导致肠粘膜生态失衡,促炎细胞因子的产生增加,抗炎细胞因子的产生减少。
低聚果糖通过促进乳酸菌的生长来缓解肠道炎症。增加的有益菌产生短链脂肪酸可被肠上皮细胞吸收并抑制促炎细胞因子IL-8和IL-6的产生,从而减轻结肠上皮细胞的炎症反应。
总之,低聚糖可以通过减少促炎菌的丰度、增加抗炎菌的丰度和促进短链脂肪酸的产生来缓解IBD的症状。
• 保护肠道屏障
在炎症性肠病中,紧密连接蛋白(如claudin1、occludin和ZO-1)和粘附连接蛋白(如E-钙粘蛋白和β-catenin)的改变通常伴随肠道通透性增加和肠道结构破坏。
低聚糖通过调节肠道微生物群的多样性来帮助恢复粘膜屏障的完整性。例如,母乳低聚糖恢复了结肠炎小鼠的紧密连接蛋白和MUC-2的表达,抑制了脂多糖和内毒素结合蛋白的产生,并恢复了肠道屏障的完整性。此外,魔芋低聚糖增加了小鼠结肠中短链脂肪酸的浓度,促进IL-18并修复IEC的完整性。
• 免疫稳态的调节
肠上皮细胞和免疫细胞中的Toll样受体(TLR)识别并响应不同的微生物结构。当病原体入侵时,巨噬细胞通过TLR识别病原体相关分子模式(PAMP)并分泌各种促炎细胞因子(如TNF-α、IL-1β、IL-6、IL-12等)。
IBD患者的调节性T(Treg)细胞数量减少。短链脂肪酸可以诱导T细胞分化为调节性T细胞细胞,促进抗炎细胞因子的合成以调节免疫反应,并恢复Th1/Th2和Th17/调节性T细胞的平衡。一项研究表明,低聚木糖被代谢成SCFAs,丙酸盐和丁酸盐可以促进CD4+ T细胞分化为调节性T细胞,从而减缓炎症性肠病。同样,阿魏酰化寡糖促进了调节性T细胞的百分比和相应特异性细胞因子的产生,从而调节炎症性肠病的Th17/调节性T细胞免疫稳态。
此外,肠道微生物群还可以刺激B细胞产生影响其他免疫细胞和免疫球蛋白(如sIgA)的抑制性细胞因子(如IL-10和TGF-β)。
低聚糖通过调节肠道微生物群来缓解炎症性肠病
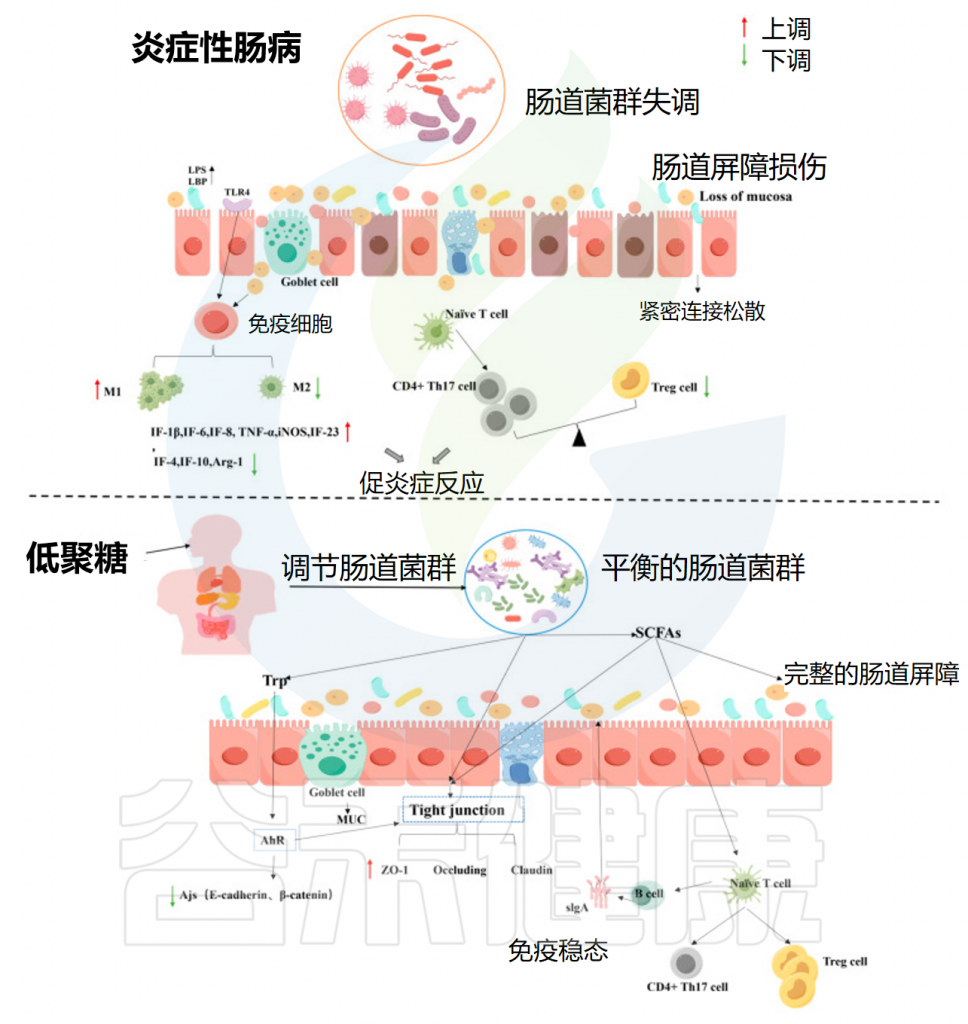
Yuan M,et al.Foods.2024
低聚糖可能通过调节肠道微生物群影响抑郁症的发展。例如,低聚果糖抑制抑郁相关细菌(如Lachnospiraceae incertae sedis、Oscillibacter、Proteobacteria和Streptococcus)。
• 使用低聚糖后减轻了抑郁症状
此外,低聚果糖(FOS)和低聚半乳糖(GOS)的组合已被证明可以减轻抑郁症状,具体来说,它们增加了海马脑源性神经营养因子(BDNF)和皮质血清素的水平,同时降低了升高的皮质酮水平和体温。三周的慢性社交压力显著减少了社交互动,而FOS+GOS给药可以防止这种影响。FOS和GOS的组合还降低了开放空间测试和迷宫测试中的焦虑水平。
在微生物水平上,有证据表明两者的结合可以防止放线菌和变形菌门比例的变化,这是重度抑郁症患者的典型特征。对低聚果糖和标准抗抑郁药氟西汀进行了比较分析,指出它们具有相似的效果,并且FOS和氟西汀都促进了Dialister属的生长。
注:最近的一项队列研究报道,在抑郁患者中未发现Dialister。换句话说,FOS和氟西汀可能通过调节Dialister的存在来改善抑郁症状。
• 低聚糖的菌群代谢物是保护神经系统的关键
肠道微生物可以通过神经、免疫和内分泌途径以及微生物代谢物影响大脑,甚至通过微生物产生的神经递质刺激肠道的迷走神经末梢。已知受肠道菌群影响的神经递质包括短链脂肪酸(SCFA)、γ-氨基丁酸(GABA)、色氨酸(Trp)和血清素(5-HT)。
例如,丁酸盐的增加可能直接影响中枢神经系统。发现口服丁酸盐会影响脑代谢和海马神经发生。因此,低聚糖补充剂可能通过增强SCFA的形成来抑制抑郁症的发展,包括改善认知功能和缓解焦虑行为。
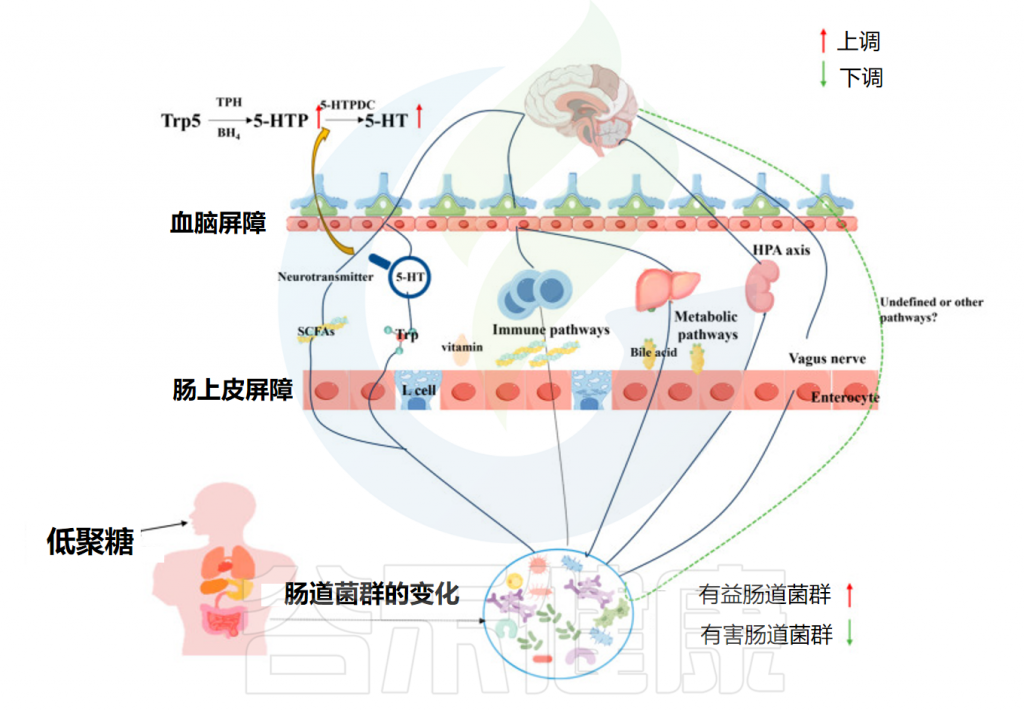
另一个重要途径是色氨酸→血清素(5-HT)。色氨酸是合成神经递质5-HT的唯一前体,影响抑郁症的发展。阿魏酰化寡糖(FOs)通过调节5-HTP(血清素前体)表现出抗抑郁和抗焦虑作用,表明肠道微生物群和微生物代谢是支持FOs保护神经系统的关键介质。
同样,另一项研究揭示了巴戟天寡糖(MOO)调节肠道菌群中的5-HT合成途径(Trp→5-HTP→5-HT),肠道菌群中升高的5-HTP被吸收到血液中,然后穿过血脑屏障,提高大脑中的5-HT水平。这些发现表明,肠道微生物群可以调节神经递质水平以影响抑郁症的发展。
肠道菌群与低聚糖互作改善抑郁症
Yuan M,et al.Foods.2024
肠道蠕动受肠道免疫系统、分泌物、微生物群及其发酵产物的相互作用调节,蠕动受损可导致便秘。益生菌(如双歧杆菌和Alistipes)丰度增加,以及与结肠运输相关的细菌丰度减少,有助于缓解便秘。
• 低聚糖促进肠道蠕动改善便秘
低聚糖,如低聚果糖、异麦芽低聚糖和低聚半乳糖,能显著提高排便频率并缩短结肠转运时间,且副作用小。除了低聚糖本身占据肠道体积以增加粪便量和促进蠕动外,研究还表明低聚糖在微生物群重塑方面对缓解便秘有显著益处。
具体而言,乳酸菌利用低聚果糖提高粪便稠度并减少排便时间。异麦芽低聚糖有效改善受试者的粪便稠度和排便频率,可能是由于结肠发酵后某些微生物丰度增加。莲子低聚糖通过刺激宿主肠道有益菌的生长促进蠕动和排便,从而缓解便秘。
• 通过代谢产生的短链脂肪酸来改善肠道蠕动
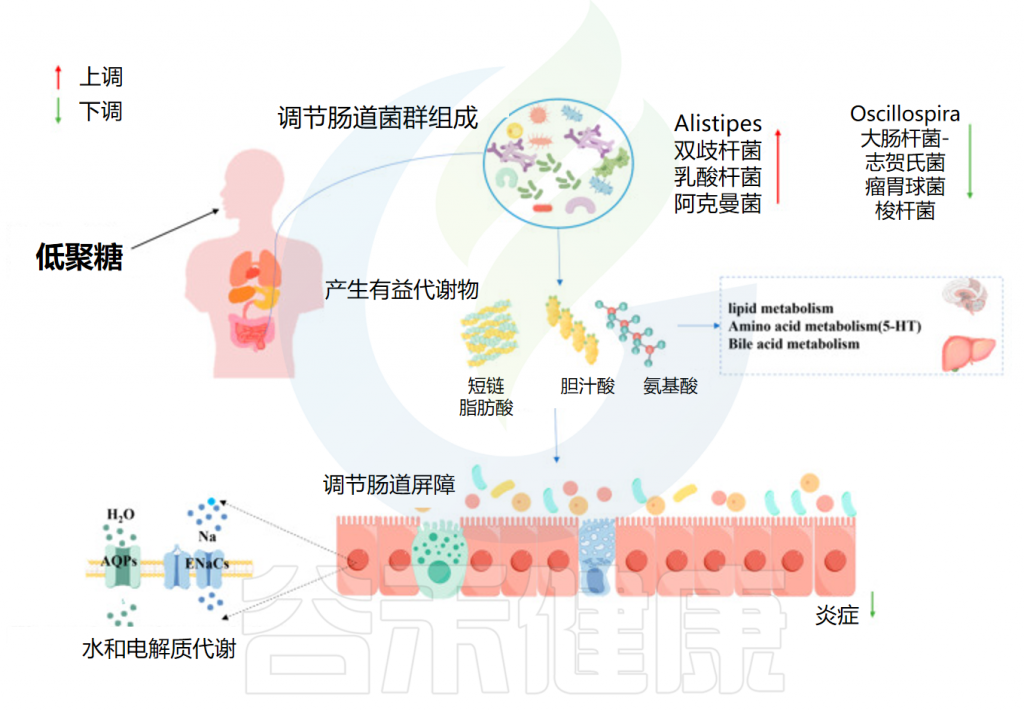
此外,研究证明低聚半乳糖可以通过调节肠道代谢物的产生改善便秘。低聚糖的摄入增加了益生菌发酵的底物量并促进了短链脂肪酸的产生。特别是丁酸盐、乙酸盐和丙酸盐,与刺激结肠上皮细胞的生长有关,从而恢复肠道形态并增加肠道蠕动以缓解便秘。
目前的研究表明,丁酸盐可以通过影响水和电解质代谢来改善肠道蠕动。同样,低聚半乳糖通过恢复恶化的水电解质代谢(包括AQP3/4和ENaC-β/γ)表达来缓解便秘。其中,AQP3/4将水从肠腔输送到结肠上皮,ENaC-β/γ介导Na+摄取到结肠上皮细胞中。
• 调节代谢途径,改善便秘
低聚糖改善便秘可能与调节代谢途径有关,包括脂质代谢、胆汁酸代谢和色氨酸代谢。代谢异常与肠道炎症反应相关,炎症会破坏肠上皮完整性,减少神经递质和激素分泌,影响胃肠蠕动并诱发便秘。
胃肠道激素在中枢和周围神经系统中作为神经递质和调节剂,促进肠道蠕动和内容物运输。内皮素、生长抑素和血管活性肠肽为抑制性神经递质,而褪黑激素和P物质为兴奋性神经递质。
此外,色氨酸代谢对胃肠蠕动有显著促进作用。L-色氨酸、5-HTP及其他中间代谢产物是神经递质和调节剂的底物,可增强内脏神经敏感性并刺激蠕动。研究表明,NDO 可通过激活5-HT信号通路缓解便秘。同时,胆汁酸通过肠道细菌的代谢调节便秘也发挥重要作用。
// 编者小结
低聚糖可以通过促进肠道蠕动、增强屏障功能和调节免疫反应,有效缓解便秘。这些发现表明低聚糖在治疗便秘方面的潜在价值,进一步支持了通过靶向肠道微生物群及其代谢功能来改善便秘的研究方向。
低聚糖缓解便秘的作用机制
Yuan M,et al.Foods.2024
COVID-19(新型冠状病毒)大流行对全球健康产生了深远影响,许多人面临长期后遗症,需制定有效的管理策略应对COVID-19后综合征,如腹泻、疲劳和慢性炎症。
食物中存在的低聚糖被证明具有益生元作用,且新证据表明其可能具备免疫调节和抗炎作用,这对缓解COVID-19的长期影响尤为重要。
• 低聚糖通过阻止病毒复制,减轻后遗症
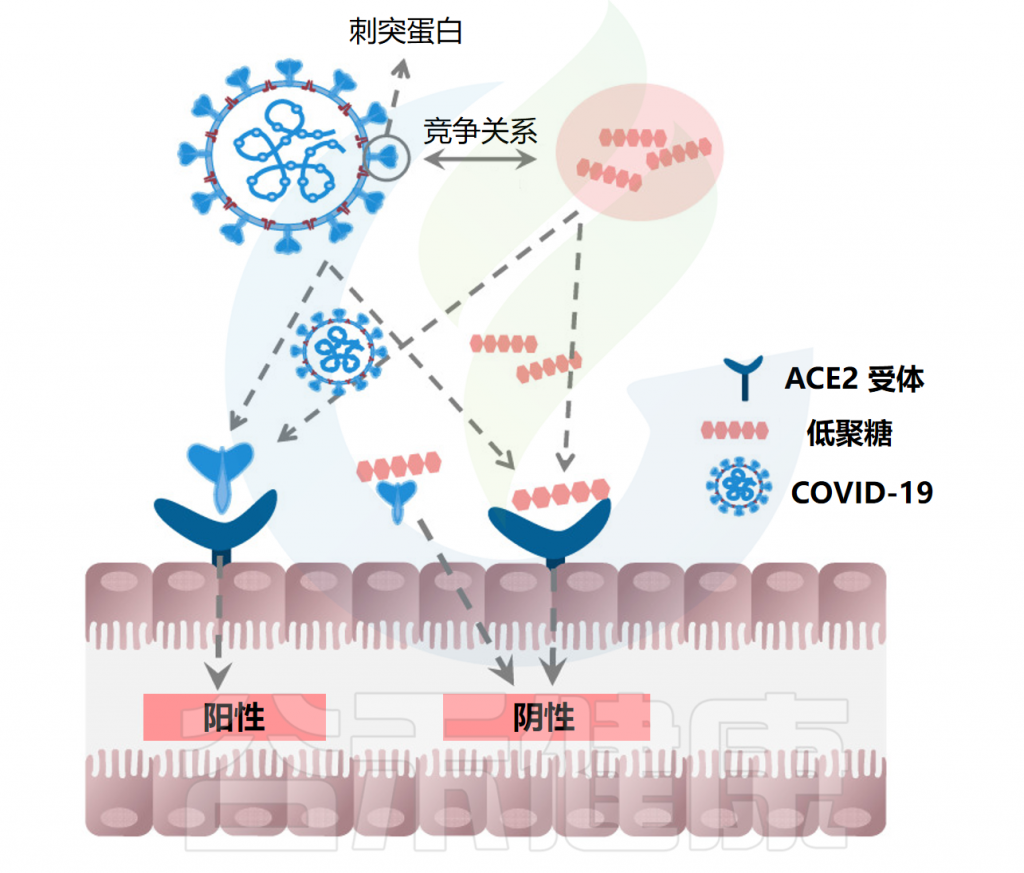
感染COVID-19后患者即使从急性期恢复,体内也可能携带少量病毒载量,这会激活肠道ACE2受体并引起腹泻等胃肠道症状。低聚糖具有生物活性特性,能够增强免疫系统,抑制病毒复制和传染性,并提供对病毒感染的保护。
注:ACE2存在于人体的各种细胞上,包括呼吸道和胃肠道的细胞,已被确定为新型冠状病毒的功能宿主受体。
低聚果糖、低聚木糖、低聚半乳糖等低聚糖可选择性促进双歧杆菌和乳酸杆菌等有益菌的生长。这些益生菌产生的脂肽分子(如解淀粉芽孢杆菌的枯草杆菌蛋白酶、卷曲乳杆菌的curvacin A、沙克乳酸杆菌的sakacin P和乳酸乳球菌的乳球菌素Gb)与人ACE2具有更高的结合亲和力,通过竞争性抑制阻止SARS-CoV-2与表达ACE2的宿主上皮细胞结合和繁殖。
低聚糖抑制COVID-19病毒复制
Cheong KL,et al.Pharmaceuticals (Basel).2023
• 增加肠道有益菌丰度及相关代谢物,调节炎症反应
临床研究表明,低聚果糖可通过肠-脑轴调节微生物群与大脑的交流,改善肠道多样性,减少高5-羟色胺状态和多巴胺代谢紊乱。粪便代谢物分析显示,COVID-19患者在疾病消退前后短链脂肪酸浓度显著降低。
有证据表明,低聚糖可以增加产生短链脂肪酸的细菌和短链脂肪酸的产生。例如,蔓越莓阿拉伯木聚糖和果胶低聚糖促进了嗜酸乳杆菌、植物乳杆菌和发酵乳杆菌等乳酸菌物种的生长,也增加了短链脂肪酸的产生,其中丁酸盐是最突出的SCFA。
此外,果胶低聚糖或菊粉可以通过特异性增加B.vulgatus的丰度来差异调节炎症反应。B.vulgatus具有强大的免疫调节作用,有助于预防结肠炎等炎症。
低聚糖在减少COVID-19后综合征方面的潜在影响

Cheong KL,et al.Pharmaceuticals (Basel).2023
低聚糖已广泛存在于我们的食品和生活中,作为一种重要的益生元,它通过调节肠道微生物群的组成和功能,促进有益代谢物的生成,从而对人体健康产生积极影响。在缓解各种人类慢性疾病(如糖尿病、抑郁症、便秘、结肠炎和肥胖)方面展现出巨大潜力。
但我们想要更好地利用低聚糖来开发新的膳食补充剂和功能性食品,为慢性疾病提供有效的预防和治疗策略。需要进一步研究低聚糖与肠道菌群之间的相互作用,进一步探索低聚糖在不同慢病中的具体机制,并比较不同低聚糖类型的作用。
这将有助于揭示低聚糖的功能差异,为开发针对特定疾病的个性化营养干预方案提供科学依据,并推动低聚糖在功能性食品和临床治疗中的应用。
注:本账号内容仅供学习和交流,不构成任何形式的医疗建议。
主要参考文献
Slater AS, Hickey RM, Davey GP. Interactions of human milk oligosaccharides with the immune system. Front Immunol. 2025 Jan 14;15:1523829.
Yuan M, Zhang Z, Liu T, Feng H, Liu Y, Chen K. The Role of Nondigestible Oligosaccharides in Alleviating Human Chronic Diseases by Regulating the Gut Microbiota: A Review. Foods. 2024 Jul 8;13(13):2157.
Wu Y, Chen Y, Lu Y, Hao H, Liu J, Huang R. Structural features, interaction with the gut microbiota and anti-tumor activity of oligosaccharides. RSC Adv. 2020 Apr 24;10(28):16339-16348.
Cheong KL, Chen S, Teng B, Veeraperumal S, Zhong S, Tan K. Oligosaccharides as Potential Regulators of Gut Microbiota and Intestinal Health in Post-COVID-19 Management. Pharmaceuticals (Basel). 2023 Jun 9;16(6):860.
Wu D.-T., Nie X.-R., Gan R.-Y., Guo H., Fu Y., Yuan Q., Zhang Q., Qin W. In Vitro Digestion and Fecal Fermentation Behaviors of a Pectic Polysaccharide from Okra (Abelmoschus esculentus) and Its Impacts on Human Gut Microbiota. Food Hydrocoll. 2021;114:106577.
Wang X., Yang Z., Xu X., Jiang H., Cai C., Yu G. Odd-Numbered Agaro-Oligosaccharides Alleviate Type 2 Diabetes Mellitus and Related Colonic Microbiota Dysbiosis in Mice. Carbohyd. Polym. 2020;240:116261.
Huang C., Yu Y., Li Z., Yan B., Pei W., Wu H. The Preparation Technology and Application of Xylo-Oligosaccharide as Prebiotics in Different Fields: A Review. Front. Nutr. 2022;9:996811.
Divyashri G., Karthik P., Murthy T.P.K., Priyadarshini D., Reddy K.R., Raghu A.V., Vaidyanathan V.K. Non-Digestible Oligosaccharides-Based Prebiotics to Ameliorate Obesity: Overview of Experimental Evidence and Future Perspectives. Food Sci. Biotechnol. 2023;32:1993–2011.
谷禾健康
今年,国产AI大模型DeepSeek,凭借其强大的技术实力、低成本和开源策略,长居热搜榜,很想知道这位顶流AI对于肠道菌群行业的了解程度,于是就和它聊了聊。

编辑
当我问deepseek…
AI时代,肠道微生物行业相关应用与发展将会如何?
AI技术的快速发展为肠道菌群行业带来多维度革新,从药物研发到健康管理均产生显著利好,肠道微生物行业将迎来技术革新与产业升级的黄金期,其核心应用与发展趋势如下:
微生物组大数据挖掘
AI通过分析海量肠道微生物组数据(宏基因组、代谢组等),快速筛选潜在药物靶点。肠道微生物群落种类繁多、结构复杂,其产生海量数据。AI强大的数据处理能力可挖掘微生物间的相互关系,为新药研发指明方向,为攻克诸多疾病带来希望。
缩短研发周期
传统药物研发需10年以上,AI可将候选菌株筛选时间缩短70%。通过“IT(数据分析)+BT(实验验证)”模式,推进多款微生态药物进入临床,覆盖神经系统、肿瘤和免疫三大领域。
例如,在传统的筛选方法中,可能需要逐一测试大量的菌株,而AI可以通过算法和模型,快速排除那些不具备潜力的菌株,直接聚焦于最有希望的候选菌株,从而节省了大量的时间和精力。这不仅加速了药物研发的进程,还有望降低研发成本,为患者带来更多的治疗选择。
创新药物形态
包括粪菌移植(FMT)、配方菌(如复合益生菌)、代谢产物(如抗癌肽)、基因工程菌等。
FMT:分析不同供体和患者的肠道微生物组成差异,预测FMT的效果和可能出现的不良反应,为个性化治疗方案的制定提供依据,提高治疗的成功率和安全性。
配方菌:例如复合益生菌,是经过精心挑选和组合的多种有益菌群。深入了解不同菌种之间的相互作用和协同效应。通过分析大量的微生物组数据,确定最佳的菌种组合和配比,使其在调节肠道菌群、增强免疫力、改善肠道功能等方面发挥更显著的作用。还能根据不同人群的肠道特点和健康需求,定制个性化的复合益生菌配方。
代谢产物(如抗癌肽):挖掘出肠道菌群中具有抗癌活性的短肽分子,为肿瘤治疗提供新方向。
基因工程菌:通过分析微生物的基因组数据和代谢网络,确定合适的基因编辑靶点和调控策略,使基因工程菌更高效地生产目标产物,或者具备更强的环境适应性和生存能力。
工程化菌群靶向递送抗癌药物至肠道特定区域。还可以为工程化菌群赋予智能反馈机制,使其能够实时感知肠道微环境的变化,并根据需要调节药物的释放量。
菌群分型与疾病预测
AI模型通过关联肠道菌群特征与疾病标志物(如SCFAs、TMAO),可预测心血管疾病、肠癌等风险。
AI模型在疾病预测中准确性的提高是一个多维度且持续探索的重要课题,涉及到数据、算法、模型优化等多个关键方面。
首先,数据质量和数量是基础。高质量的数据是确保AI模型准确性的基石。
一方面,要注重数据的收集过程,确保数据的完整性、一致性和准确性。在收集与疾病相关的肠道菌群数据以及疾病标志物数据时,需要严格遵循标准化的采集、处理和存储流程,避免数据偏差和误差。
同时要尽可能收集大规模的样本,因为丰富的数据可以让AI模型学习到更多的模式和规律。通过整合多个来源的数据,如不同地区、不同年龄段、不同疾病状态人群的数据,可以增加数据多样性,提高模型的泛化能力。

其次,算法的选择和优化至关重要。对于疾病预测,需要选择合适的机器学习和深度学习算法,并根据具体情况进行调整和优化。
例如,深度学习中的卷积神经网络(CNN)在处理图像数据方面具有优势,而循环神经网络(RNN)及其变体(如长短期记忆网络LSTM)则更适合处理序列数据。
再者,特征工程也是提高AI模型准确性的关键环节。在疾病预测中,需要对肠道菌群数据和疾病标志物数据进行深入分析,挖掘出与疾病相关的关键特征。
特征工程是指从原始数据中提取、选择和转换有意义的特征,以提高模型的性能。例如,通过统计分析、相关性分析等方法筛选出与疾病发生发展密切相关的菌群特征和代谢产物指标。还可以采用特征降维技术,如主成分分析(PCA)、线性判别分析(LDA)等,将高维数据转化为低维数据,减少数据复杂性,提高模型的训练效率和准确性。
此外,模型的融合和集成也是一种有效的提高准确性的方法。不同的AI模型在不同的数据集和任务上可能具有各自的优势和局限性。通过将多个不同的模型进行融合和集成,可以综合各个模型的优点,提高整体的预测性能。

动态干预方案
基于AI的宏基因组分析,可为患者提供定制化膳食、益生菌及粪菌移植方案。AI技术则如同一个智能的“导航员”,能够从这些复杂的数据中挖掘出有价值的信息,为患者量身定制个性化的干预方案。
比方说,以高血压患者为例,高血压作为一种常见的慢性疾病,其发病机制复杂,涉及遗传、环境、生活方式等多种因素。针对高血压患者,AI可识别普雷沃菌属丰度异常并推荐靶向菌株。这些靶向菌株可以通过益生菌的形式补充到患者体内,调节肠道菌群的平衡,进而影响血压水平。
除了益生菌方案,定制化膳食也是动态干预方案的重要组成部分。AI可以根据患者的肠道菌群特征和疾病状态,为患者设计个性化的膳食方案。
动态干预方案的实施并非一蹴而就,而是一个持续监测和调整的过程。在治疗过程中,需要定期对患者的肠道菌群健康检测,以评估干预效果,并根据分析结果及时调整干预方案。
合成生物学应用
AI辅助设计基因工程菌(如产丁酸菌株),直接调控宿主代谢功能。
传统的基因工程菌设计主要依赖于科研人员的经验和试错,过程繁琐且效率较低。而AI拥有强大的数据分析和模式识别能力,能够处理海量的生物学数据,包括基因序列、蛋白质结构、代谢通路等信息。通过对这些数据的深入学习,AI可以预测基因的功能、设计优化的基因表达系统,并为基因工程菌的设计提供精准的指导。
产丁酸菌株可调控宿主代谢功能,丁酸作为信号分子能调节宿主代谢,菌株间相互作用也间接影响宿主代谢。AI通过构建模型设计最优菌株和策略,还能优化生产工艺。不过,其面临生物学复杂、数据质量等挑战,但前景广阔。
上游检测技术升级
检测手段日益多样化,16S rRNA测序能快速评估菌群组成多样性,宏基因组测序可揭示更全面信息。技术上不断优化,如多重PCR扩增提高检测覆盖率和分辨率,AI辅助数据分析提升结果准确性。
肠道菌群检测结果将更多地被纳入临床诊断体系。AI可以分析大量的临床病例和肠道菌群数据,找出肠道菌群变化与疾病之间的关联模式,为医生提供诊断参考。
例如,在一些疑难病症(如自闭症、帕金森病等)的早期诊断中,肠道菌群的异常特征可能成为重要的辅助诊断指标。
结直肠癌(CRC):识别肠道菌群中具核梭杆菌(Fusobacterium nucleatum)等促癌菌的异常增殖,结合粪便隐血检测,提升早期筛查灵敏度。
肠道细菌在结直肠癌发生和进展中的影响
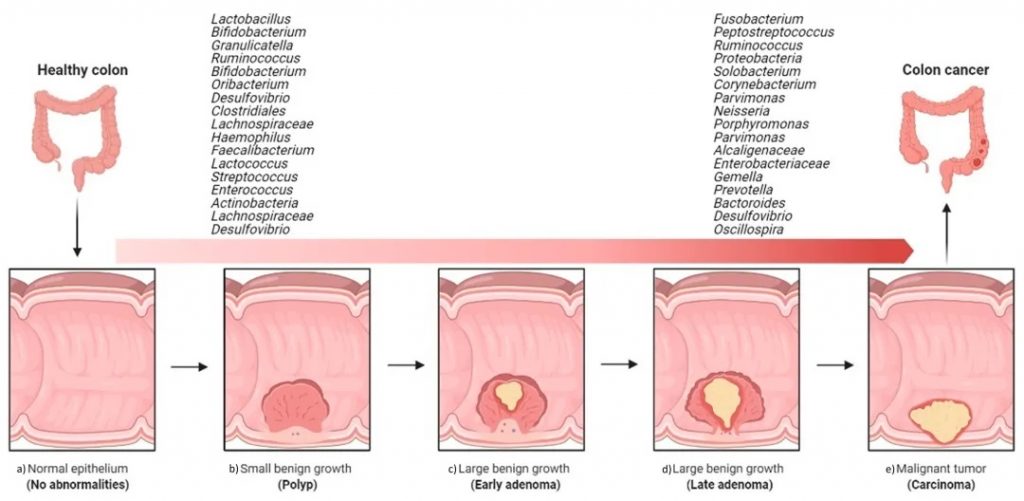
Torres-Maravilla, E. et al.,Microorganisms 2021
炎症性肠病(IBD):
促炎菌增殖:肠杆菌科(Enterobacteriaceae)丰度显著升高,其代谢产物(如脂多糖)可激活TLR4通路,加剧肠道炎症反应;
抗炎菌缺失:具有抗炎功能的共生菌——普氏菌(Faecalibacterium prausnitzii)和产丁酸盐的罗斯氏菌(Roseburia)丰度普遍降低或缺失,导致短链脂肪酸合成不足,肠道屏障修复能力下降。
早期筛查:在血清标志物(如CRP)升高但未出现典型症状的人群中,检测到上述菌群失衡模式可提示早期IBD风险,推动结肠镜进一步确诊;
疗效监测:治疗过程中动态监测罗斯氏菌的恢复水平,可评估免疫抑制剂(如抗TNF-α药物)对黏膜修复的促进作用。
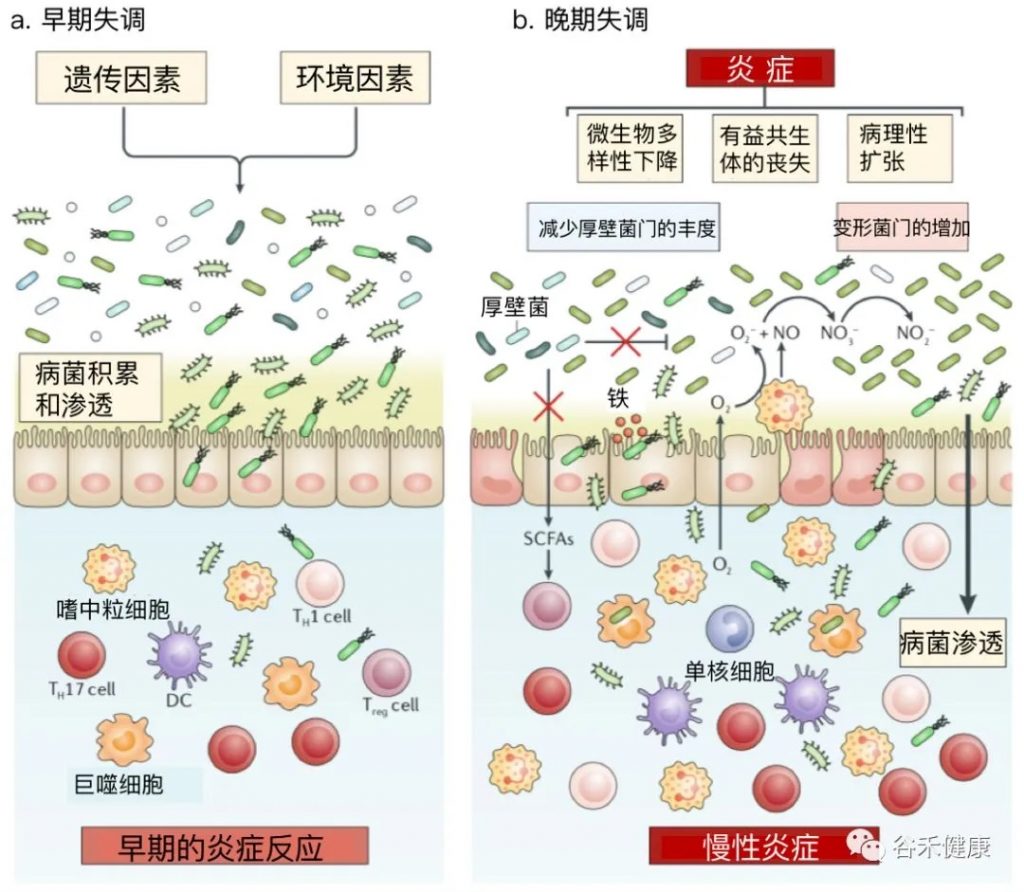
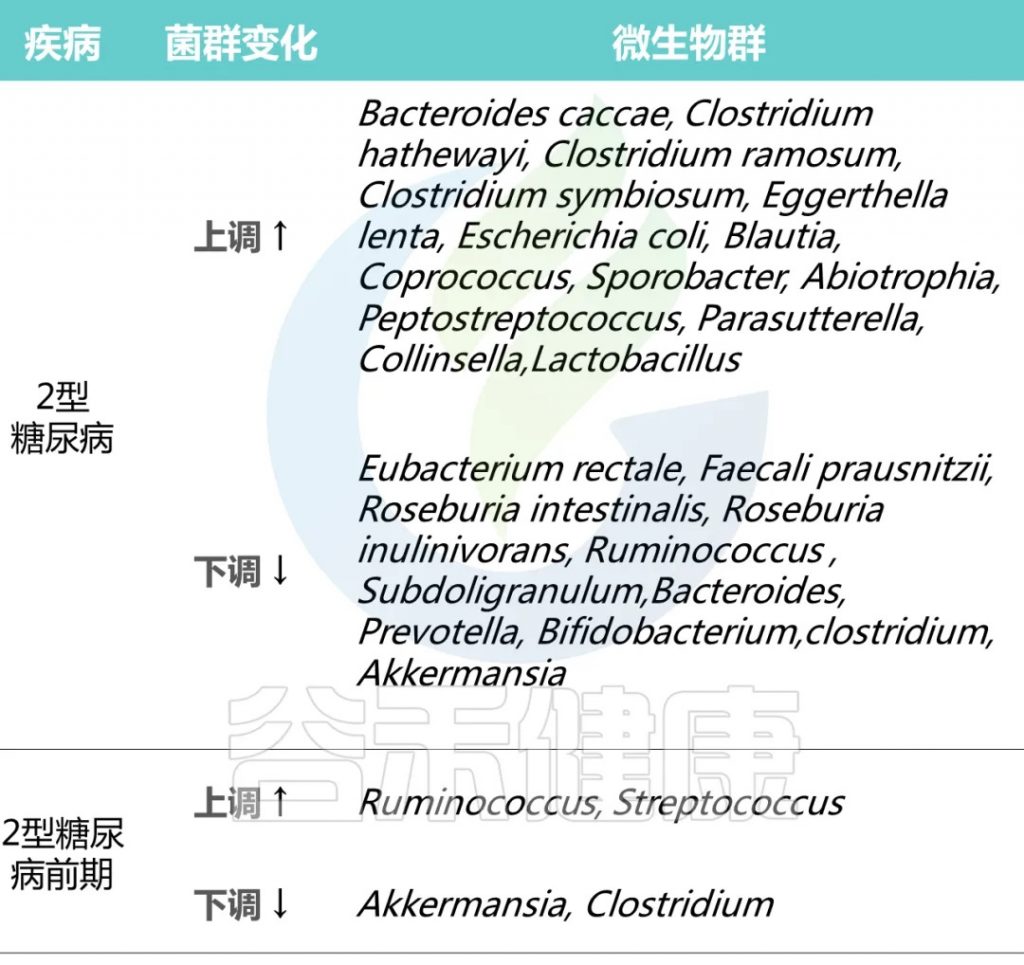
糖尿病:结合肠道菌群中产丁酸盐菌的减少与宿主血糖代谢数据,预测胰岛素抵抗风险。
Cunningham A L et al., Gut Pathog, 2021
菌群分型指导治疗:通过16s测序、宏基因组测序和代谢组分析,建立患者肠道菌群特征图谱。例如,补充AKK菌(Akkermansia muciniphila)仅在基线菌群低丰度人群中有效,需结合个体差异制定阈值。
通过连续监测肠道菌群变化(如抗生素使用后菌群恢复情况),辅助医生评估治疗效果。
例如:癌症化疗患者的化疗药物可能破坏肠道菌群平衡,导致免疫力下降。AI实时分析菌群数据,预警感染风险并推荐相关干预方案。
中游标准化建设
AI整合全球微生物组数据,推动菌株库建设、临床试验设计标准化。
硬件上,便携设备基于微流控技术实现高效处理,新型传感器提高敏感度。
软件上,智能数据分析系统实时处理数据并提供个性化建议,机器学习模型助力精准识别。
参与标准制定,获取ISO等认证,确保产品质量和安全。
下游健康管理服务
建立完善的用户教育体系,通过在线课程、健康顾问平台等帮助消费者理解检测结果。通过健康管理服务,将检测结果转化为具体的健康建议, 有利于公众对肠道菌群产品的应用。
肠道菌群健康管理将与营养学、微生物学、医学、心理学等多学科融合。AI作为协调者,根据肠道菌群检测结果,组织多学科专家团队为用户提供综合的健康管理服务。
例如,对于因肠道菌群失调导致情绪问题的患者,营养师调整饮食,心理医生进行心理疏导,微生物学家给出改善肠道菌群的具体措施。
针对高风险人群定制膳食或益生菌组合。
如蒙牛开发的青钱柳提取物组合通过抑制菌源DPP4,在动物实验中显著降低血糖 ,未来或成为糖尿病预防新手段。
结合实时监测技术(如便携式纳米孔测序),AI动态优化益生菌、膳食纤维摄入量或粪菌移植方案。
精准肠道菌群移植门诊通过线上线下结合模式服务患者。
跨界融合
肠道菌群通过代谢物(如5-羟色胺、GABA)影响大脑功能,可开发针对抑郁症、焦虑症的菌群干预产品。
益生菌菌株(如长双歧杆菌NCC3001)在临床试验中显示缓解焦虑效果。未来可能推出“精神健康益生菌+认知行为疗法”联合方案。
潜力:肠道菌群失衡与痤疮、湿疹等皮肤病相关,可探索口服益生菌或局部菌群移植(如皮肤微生物组喷雾)改善皮肤状态。
技术结合:AI分析肠道与皮肤菌群关联,定制内外协同治疗方案。
市场空白:针对宠物(如猫狗)的肠道菌群检测及定制化食品/补充剂,解决腹泻、肥胖等问题。
延伸场景:动物园或濒危动物保护中的菌群干预,提升圈养动物生存率。

特定人群管理
➦ 母婴菌群管理
剖宫产婴儿的母体菌群移植(阴道菌群纱布擦拭),降低过敏和免疫疾病风险。
孕期肠道菌群监测,预防早产或妊娠糖尿病。
产品形态:母婴菌包、菌群健康评估套餐。
智能监测手环:实时监测婴儿肠道气体(如氢气),反馈菌群定植效果。
➦ 肥胖人群管理
菌群特征:厚壁菌门/拟杆菌门比值(F/B比)升高,阿克曼菌(Akkermansia)丰度降低。
干预手段:
补充阿克曼菌改善肠道屏障功能,减少脂质吸收。菌群导向饮食(Microbiome-Directed Foods)抑制促肥胖菌(如阴沟肠杆菌)。
案例:比利时鲁汶大学开发的阿克曼菌口服制剂,可使肥胖者体重平均下降2.3kg(12周试验)。
产品形态设想:
控血糖菌群面包:添加抗性淀粉(促进罗斯氏菌增殖)+ 基因工程酵母菌(分泌GLP-1类似物)。
菌群血糖联动仪:连续血糖仪数据同步至菌群检测APP,动态调整。
肥胖菌群管理手环:根据肠道菌群数据(如厚壁菌/拟杆菌比)释放电信号,刺激迷走神经产生饱腹感。
菌群溶脂贴片:透皮递送Akkermansia muciniphila冻干粉,激活棕色脂肪产热。
➦ 老年人群管理
衰老相关菌群特征:多样性降低,促炎菌(如变形菌门)增加。
干预手段:
地中海饮食+益生元(菊粉)促进良性菌群定植。
个性化益生菌(如长双歧杆菌BB536)改善肌肉流失和认知衰退。
养老院菌群健康管理系统:
群体化菌群管理,降低集体感染风险。
中央监测平台:批量分析老人菌群数据,预警群体性致病菌传播(如艰难梭菌)。
自动配餐机器人:根据每位老人菌群报告,调配个性化餐食(如低FODMAP饮食+益生元添加)。
老年群体的肠道菌群产品需兼顾 “功能刚性”(如疾病预防)与 “体验友好”(如无创检测、语音交互)。通过菌群干预推迟慢性病发生,延长寿命,提高生活质量。
未来趋势可能是 “菌群-衰老-疾病”三联检测体系 与 “居家-社区-机构”三级服务网络的深度融合。
技术创新方向
➦ 菌群冷冻保存与“菌群银行”
概念:年轻时储存健康肠道菌群,年老或疾病时进行自体移植(类似脐带血储存)。
挑战:菌群复苏后的活性维持技术,需低温生物学突破。
➦ 其他形式检测
通过呼吸或血液标志物间接反映肠道菌群状态(如挥发性有机化合物VOCs分析)。
➦ 地域特异性菌群数据库
针对不同地区饮食和文化(如亚洲高纤维饮食 vs. 西方高脂饮食),建立菌群-健康关联模型,开发本地化产品。
比如,日本基于本土菌株开发的“FK-23益生菌”免疫调节产品。通过调节肠道微生态,改善消化健康,增强机体的免疫功能。
➦ 菌群农业与可持续食品
通过调控农作物或牲畜肠道菌群,减少抗生素使用,提升产量(如益生菌饲料添加剂)。
开发菌群发酵技术,生产高蛋白昆虫食品(如蟋蟀蛋白粉),减少碳排放。
数据壁垒
—挑战
个体菌群差异大,菌群构成受饮食、生活方式、年龄、地理位置、基因、种族、性别、药物等多元因素影响,单一数据库难以覆盖人群多样性,解读准确性受限。样本量碎片化,难以挖掘深层规律。
—破局关键:需建立更大规模数据库★
建立大规模数据库不仅是肠道菌群行业的“基础设施”,更是检测解读从“经验驱动”迈向“科学驱动”的核心引擎。其价值可归结为:
◑ 更准:通过人群细分与机制解析,降低个体差异导致的误判。
例如,高纤维饮食者与高脂饮食者的“健康菌群基线”截然不同,若缺乏细分人群数据,可能误判干预方向;东亚人群因乳糖酶基因缺失比例较高,其乳糖代谢相关菌的丰度与功能特征与欧洲人群不同,若仅依赖通用参考标准,可能误判菌群状态。
◑ 更深:揭示菌群与疾病的因果链,推动干预策略从“对症”转向“对因”;海量数据能增强统计效力,挖掘低频但强关联的菌群-疾病机制,推动科研向临床转化。
例如,在药物研发过程中,药物的疗效和安全性可能受到个体微生物群落的影响,某些药物的代谢可能依赖于肠道菌群中的特定酶。了解特定人群的正常微生物参考,可以帮助研发人员预测药物在不同人群中的代谢情况和疗效差异,从而优化药物设计和开发更具针对性的药物。
◑ 更活:动态模型随数据增长持续进化,使解读建议与时俱进。长期追踪数据可构建“菌群变化预测模型”,预警糖尿病、结直肠癌等慢性病风险,真正释放微生物数据在疾病防控、健康管理和药物研发中的潜力。
因果关系的模糊性
—挑战
菌群变化是疾病的“因”还是“果”难以确定(例如,抑郁症患者菌群失调是诱因还是结果?)。
—应对方案
纵向队列研究:开展长期追踪(如10年以上的肠道菌群动态监测),结合干预实验验证因果关系。
动物模型验证:利用无菌小鼠移植特定菌群,观察其对宿主生理的影响(如肥胖、免疫反应)。
数据解读的局限性
—挑战
用户对肠道菌群专业检测报告的理解有进步空间(如菌群丰度、α多样性指数)。
部分消费者可能对肠道菌群检测的认知停留在“保健品”层面,对科学价值的信任度不足。
—应对方案
开发可视化工具(如菌群“健康评分”仪表盘),提供通俗化建议。
通过科普内容(短视频、互动问答)提升公众对菌群健康的认知。
通过学术会议、继续教育课程让更多临床医生了解菌群检测的临床价值。
临床验证不足
—挑战
检测产品缺乏大规模临床验证,医学界对菌群诊断的接受仍然有限。
—应对方案
与医疗机构合作:推动菌群检测纳入临床试验(如辅助癌症免疫治疗疗效预测)。
商业模式单一
—挑战
盈利模式缺乏可持续性。
—应对方案
检测+干预产品(如个性化益生菌定制)。
订阅制服务:如每月菌群监测+营养师咨询;
或者比如每季度检测肠道菌群,生成动态健康报告,推荐阶段性干预措施(如季节性饮食调整预防过敏等)。结合可穿戴设备数据(运动、睡眠)提供综合建议。
与保险机构合作,将菌群健康管理纳入健康险增值服务。
伦理争议
—挑战
菌群移植(FMT)可能引发未知风险(如病原体传播、长期生态影响)。
—应对方案
严格供体筛查:建立菌群库的标准化筛选流程(如供体健康史、病原体检测等)。
知情同意强化:向用户明确告知菌群干预的潜在风险和不确定性。
未来趋势(2025-2030年)
多组学融合:AI整合代谢组、免疫组数据,解析菌群-宿主互作机制 。
例如,卷积神经网络(CNN)将菌群数据转化为图像,精准预测2型糖尿病患者的丁酸弧菌干预靶点。
全球市场扩张:中国微生态药物市场规模预计2030年达500亿元,年复合增长率超30%。
政策支持:国家“精准医学”专项将肠道微生物组列为重点,推动产学研合作。
AI与肠道微生物组的深度融合将重塑医疗健康产业,从药物研发、疾病防治到健康管理均迎来革命性突破。未来十年,具备“AI+”能力的企业将引领行业变革,推动个性化医疗的发展,而构建数据库、临床验证等将是行业持续增长的关键支撑。
总的来说,人们将逐渐理解“人类是超级生物体”(宿主+微生物)的概念,改变“杀菌至上”的传统健康观念。
精准菌群干预将推动医疗模式向预防化、个性化、数字化转型:
疾病管理:从“发病后治疗”转向“风险预测-早期干预”;
临床落地:推动菌群检测进入诊疗指南(如IBD、IBS的辅助诊断)。
治疗方案:从“通用型”升级为“动态定制型”,医疗资源从“中心化”向“分布式+远程化”重构;
最终,肠道菌群行业的目标是构建一个全面的“人体生态系统管理”体系,这一理念超越了单纯的疾病治疗,而是着眼于维护整个生态系统的平衡。未来十年,随着技术成熟和政策完善,肠道微生物组有望成为继基因组之后,精准医疗的第二大核心支柱。
在AI技术与肠道微生物研究的深度融合下,精准健康管理已从概念走向现实。通过此前的分析可以看到,肠道菌群检测正逐步渗透至疾病预防、临床诊断、母婴健康、老年抗衰等多元场景,而数据驱动的个性化干预将成为行业核心。
为赋能临床医疗、健康管理机构、检测机构等合作伙伴,谷禾推出 AI肠道菌群报告解读与咨询助手,就是下面这个小海豚:

AI报告解读助手将有助于合作方和客户更好的理解报告和应用肠道菌群检测。合作方可提升解读效率降低成本,定制精准营销策略,快速扩展菌群管理服务生态,构建差异化竞争力,实现用户健康改善与商业增长的双重目标。
谷禾健康
近年来,肠道微生物群作为人体健康的“隐形器官”备受关注,其在免疫调节、代谢平衡和疾病防御中的作用已被广泛认可。然而,当微生物群的平衡被打破时,可能会引发一系列健康问题,包括感染易感性增加。特别是在严重感染的背景下,肠道微生物群的失调可能不仅是疾病的结果,更可能是疾病发生的潜在驱动因素之一。
谷禾总结发现一些疾病或潜在健康风险人群肠道微生物群存在如下类型的几种失衡的潜在特征:
1
产丁酸菌减少,同时有害菌抬头
2
单一或几种菌属占比过高导致其他核心菌群丰度不足或偏低,尤其产生短链脂肪酸的菌
3
多样性单一或偏低,同时有害菌占比较高或几种机会病原菌超标
4
益生菌缺乏或不足,核心菌丰度占比较低同时构成比例不佳
5
变形菌门或梭杆菌门上升占比太高
以上情况可能单一或同时存在。如果同时存在,一般菌群和健康状况均不佳。
本文主要分享第一个菌群特征,产丁酸菌不足。
先说本文的结论:
肠道微生物群多样性和组成,特别是产丁酸菌丰度较高,与普通人群中因感染住院的风险降低有关。厌氧的产丁酸菌能够在一定程度上保护宿主免受全身性感染的侵害。
该结论的支持证据:
第一 荟萃研究分析和得出的假设验证,分析了10699名参与者的肠道微生物群【4248 (39.7%)来自推导队列,6451(60.3%)来自验证队列】。其中602例(5.6%)受试者【152例(3.6%)来自推导队列; 450例(7.0%)来自验证队列】在随访期间因感染住院或死亡。
这些参与者的肠道微生物群组成与未因感染住院的参与者不同。具体而言,产丁酸菌的相对丰度较高与感染住院风险降低相关(推导队列每增加10%产丁酸菌的原因特异性风险比为0.75 [95%CI 0.60 – 0.94],p= 0.013;验证队列每增加10%的原因特异性风险比为0.86 [0.77-0.96],p= 0.0077)。在调整人口统计学、生活方式、抗生素暴露和合并症后,这些相关性保持不变。
第二,谷禾的队列和2个独立的欧洲队列
【包括荷兰城市健康生活(HELIUS)研究(推导队列)和芬兰FINRISK 2002年人口调查(验证队列)】。
美国的Kullberg博士团队对在如上两个独立的观察队列中进行了这项研究验证:HELIUS是一项在荷兰阿姆斯特丹进行的多种族、基于人群的前瞻性队列研究。成年人(年龄18-70岁)从阿姆斯特丹市政登记处随机抽样,按种族分层,并邀请参加。HELIUS参与者与国家住院和死亡登记处相关联,涵盖2013年1月1日至2020年12月31日期间所有荷兰医院的入院和死亡情况。FINRISK 2002年队列是一项人口调查,包括来自芬兰六个地区的成年人(年龄25-74岁)的随机样本,按性别、地区和10岁年龄组分层。FINRISK参与者与芬兰医院出院和死亡原因登记册相关联。
在两个队列中,参与者完成问卷调查,接受体格检查,入选时提供粪便样本(HELIUS参与者为2013年1月3日至2015年11月27日,FINRISK参与者为2002年1月21日至4月19日)。在705名HELIUS参与者的子集中提供了饮食变量。为了纳入Kullberg博士团队研究,他们提供粪便样本并成功测序。在Illumina系统上用16S rRNA V4区测序。
目前全球约25%的死亡是由于感染。这一负担凸显了新的预防策略的必要性。因感染性疾病住院的患者经常表现出肠道紊乱,甚至是在抗生素治疗之前。
数据已经表明,这些患者的肠道厌氧菌丰度较低,潜在致病性肠道细菌数量增加。目前尚不清楚这些变化是否是疾病本身的结果(例如由全身性炎症或饮食变化引起),或者肠道微生物群的破坏从一开始就增加了对感染的易感性。
小鼠模型支持后一种假设,并表明肠道微生物群的扰动(通过使用驱虫处理或无菌小鼠)减弱了炎症反应,并增加了感染的易感性和严重性。微生物组的有益的全身效应通常归因于肠道厌氧菌产生的代谢物。
例如,临床前研究表明,微生物群代谢物丁酸盐增加单核细胞的抗微生物活性,并影响肺中的免疫环境。
检索了PubMed从数据库开始到2023年7月10日的数据,没有语言限制,在标题或摘要中使用检索词(“gut”或“intestinal”)AND(“microbiome”或“microbiota”)AND(“infection”或“infectious”)AND“risk”AND(“patients”或“participants”或“cohort”或“men”或“women”)。
本次检索识别出656篇文章。大多数人类研究描述了感染性疾病住院或重症监护病房住院期间的肠道微生物组破坏。
研究结果表明,基线肠道微生物群组成(感染发作前)与两个大型独立人群队列中因感染性疾病住院的风险有关,共有10699名参与者和602起事件(即因任何感染性疾病住院或死亡)。
在选定的极易感染的患者人群中(例如,在严重疾病期间或干细胞移植后),微生物多样性丧失、革兰氏阴性菌过度生长和产生短链脂肪酸丁酸的厌氧菌丰度低与(医院获得性)感染风险增加相关。
在这两个队列中,厌氧产丁酸菌的肠道定殖与预防感染性疾病住院有关。通过多变量比例风险模型和匹配病例(因感染住院的参与者)与对照(无感染相关住院的参与者),发现这种关系是稳健的,而且在调整年龄,性别,种族,生活方式,近期抗生素暴露和合并症后没有改变。
结合临床前研究,谷禾的检测实践和选定的严重感染高风险患者的发现,据我们所知,这是第一个提供证据证明厌氧肠道微生物群对人类一般人群感染易感性的影响。
这些主要结局是在研究入选时采集粪便样本后随访期间因任何感染性疾病而住院或死亡,以HELIUS(5-7年随访)或FINRISK(6年随访)。非传染性疾病导致的死亡被视为竞争风险。对于多次因感染入院的参与者,仅考虑第一次入院。
研究小组先前描述了在选定的高感染风险患者(例如,中风或异基因造血干细胞移植后)中,产生丁酸盐的厌氧肠道细菌的消耗与呼吸道感染风险增加之间的关联。厌氧的、产丁酸菌的有益影响可能超出这些高度易感的人群。
大型流行病学研究描述了与没有此类暴露的住院患者相比,在假定微生物群破坏(如艰难梭菌感染或广泛的抗生素治疗)的情况下,住院后因严重脓毒症再次入院的风险高出65-70%。
研究详细描述了统计分析方法,并在附录中提供了具体细节。研究主要评估了肠道微生物群的关键特征(包括群落组成、α多样性和产丁酸菌的相对丰度)与感染相关住院风险之间的关联。
产丁酸菌的丰度基于16种已知主要产丁酸菌的累积相对丰度计算,其预测粪便丁酸盐浓度的准确性已被独立验证。
敏感性分析包括:
1) 扩展研究范围至所有感染性疾病住院病例,而不仅限于以感染为主要诊断的住院病例;
2) 使用替代的产丁酸菌列表重新计算其丰度。
群落组成的差异通过基于Bray-Curtis距离的多变量方差分析(PERMANOVA)评估,驱动群落差异的细菌则通过DESeq2和ANCOM-BC方法识别。
基于HELIUS队列,研究构建了个体化的微生物群感染相关住院风险评分,并通过正则化Cox回归和10折交叉验证计算每种细菌的权重。随后,在FINRISK队列中验证了该风险评分。
竞争风险回归模型用于评估微生物群特征(多样性、产丁酸菌丰度和风险评分)与感染相关结局之间的关联,计算特定原因风险比(csHR)。
产丁酸菌作为连续变量时,csHR表示其相对丰度每增加10%时的风险变化。研究还进行了嵌套匹配病例对照分析,以比较HELIUS队列中感染相关住院病例与未住院对照的肠道微生物群差异。
多变量模型调整了基线年龄、性别、种族(仅限HELIUS队列)、吸烟、饮酒、身体活动、抗生素暴露(HELIUS为采样前3个月,FINRISK为4个月)以及合并症(如高血压、糖尿病、癌症、心血管疾病、肺部疾病和胃肠道疾病)。
缺失数据极少,并在多变量分析中作为分类变量处理。
对10699名参与者的肠道微生物群进行了表征,其中4248名(39.7%)来自HELIUS研究(推导队列,荷兰),6451名(60.3%)来自FINRISK(验证队列,芬兰),并用于本研究。
在两个队列中,肠道微生物群主要由厚壁菌门和拟杆菌门组成。
从样本采集到2020年12月31日,HELIUS研究的152名(3.6%)参与者因感染性疾病住院或死亡。在FINRISK研究中,450名(7.0%)参与者在6年随访期间因感染住院或死亡。
下呼吸道感染是两个队列中感染相关住院的最常见原因(表1)。
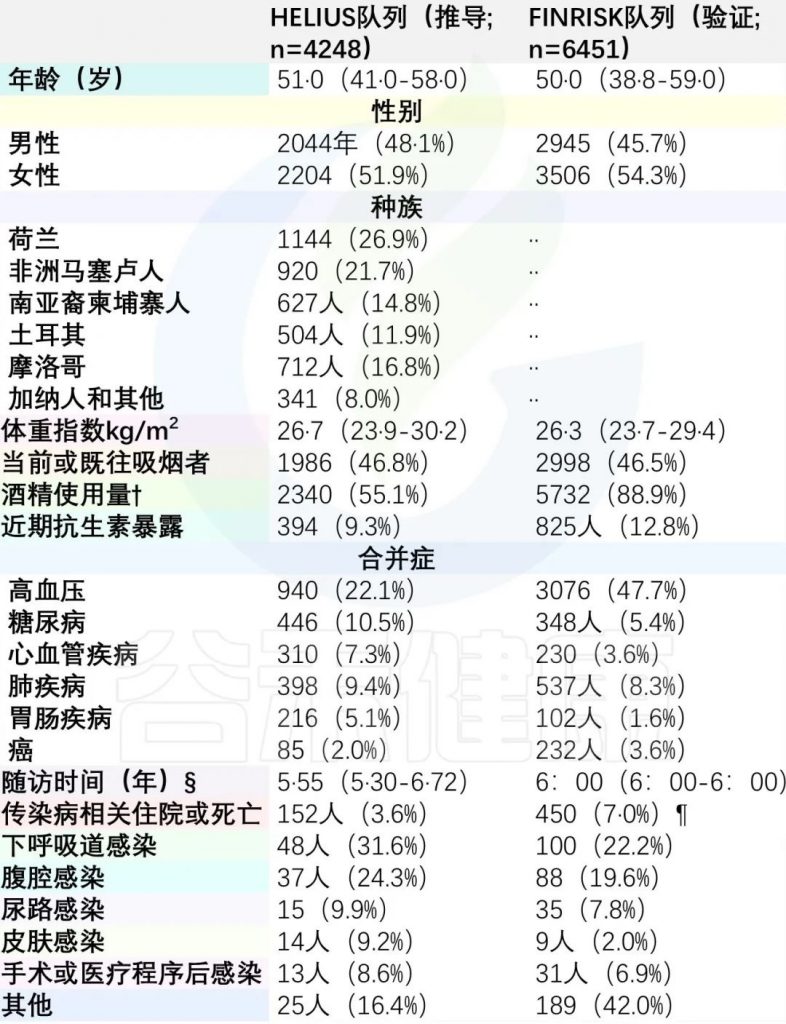
DOI: 10.1016/S2666-5247(24)00079-X
住院/死亡与非住院者肠道菌群是否有差异?
首先检查了因感染住院或死亡的HELIUS参与者与未因感染性疾病住院的参与者(包括死于非感染性原因的参与者)之间肠道微生物群组成是否存在差异。
这些结果组之间存在可检测的分离(图1A),这通过排列检验(R2=0·00035,p=0·041)在统计学上得到证实。
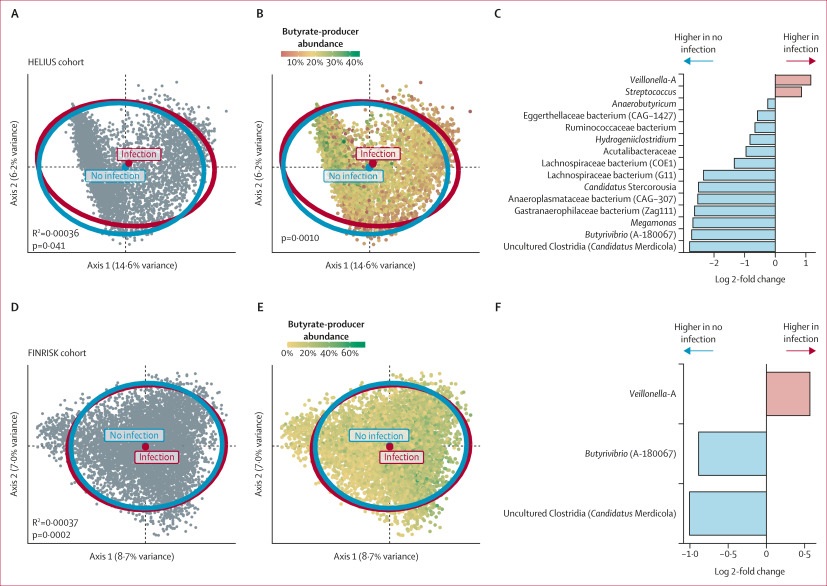
Kullberg RFJ et al., 2024. Lancet Microbe.
这种分离在更高的分类学水平(属水平p= 0.040;科水平p= 0.024)和遗传学感知距离(加权UniFrac p= 0.040)下是稳健的,尽管效应量很小-即使考虑到多个经典决定因素(人口统计学,饮食,合并症,药物,社会经济和技术因素)通常解释微生物群组成的差异很小(R2= 0.09 – 0.12)。
产丁酸菌的相对丰度与微生物群组成相关,如通过主坐标分析的颜色编码所显示的(p=0·0010;图1B)。
使用DESeq 2模型来识别导致结果组之间差异的特定细菌,发现:
当使用ANCOM-BC代替DESeq 2时,获得了相似的结果。在验证队列(FINRISK)中,还观察到因感染住院的参与者与未因感染住院的参与者之间的肠道微生物群差异(R2=0·00037,p=0·0002;图1D,E)。
与推导队列一致,来自验证队列的因感染住院的参与者具有较低的丁酸弧菌相对丰度和较高的韦荣氏球菌相对丰度(图1F)。
总之,这些数据表明,在两个独立的队列中,基线肠道微生物群组成在随访期间因感染而住院的参与者和没有感染相关住院的参与者之间存在差异,这同样是由韦荣氏球菌的增加和专性厌氧菌丁酸弧菌的减少所驱动的。
产丁酸菌丰度是否与严重感染风险相关?
在衍生队列的4248名参与者中,产丁酸菌相对丰度的增加与未来因感染性疾病住院的风险降低相关。换句话说,每增加10%产丁酸菌的相对丰度,感染相关住院的csHR为0.75。
当比较产丁酸菌的三分位数时,也观察到这种关联:最高三分位数的1416名参与者中有42例严重感染,而最低三分位数的1416名参与者中有69例严重感染。
在验证队列中,观察到产丁酸菌相对丰度较高与感染住院风险较低之间存在相同的相关性。在推导和验证队列中,多变量分析中潜在混杂因素(年龄、性别、种族、吸烟、饮酒、体力活动、抗生素暴露和合并症)的校正对效应估计值和显著性均无实质性影响。
鉴于肠道微生物群和肥胖之间的双向关系,BMI不被认为是真正的混杂因素。然而,当BMI额外纳入多变量模型时,相关性未改变。 使用中心对数比转换校正微生物组数据的组成性质也不会影响这些发现。因此得出结论,在推导和验证队列中,产丁酸菌的定植与严重感染风险降低相关。
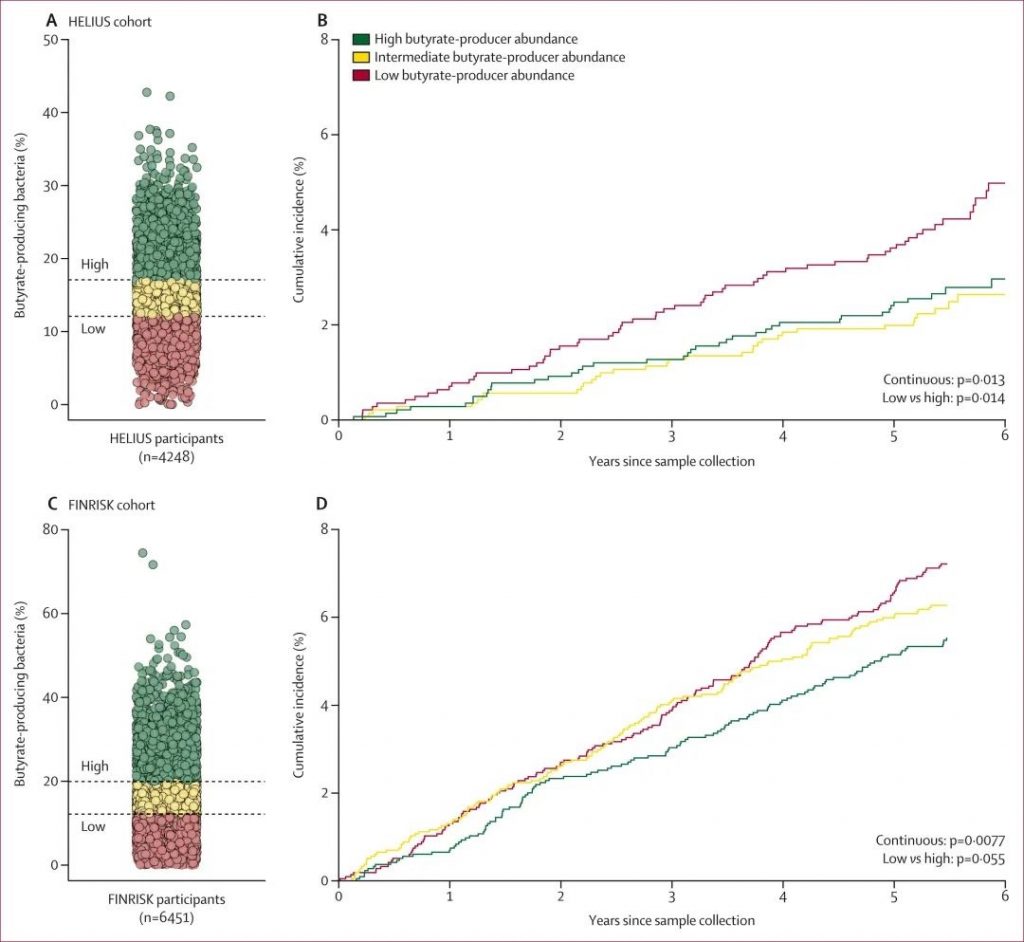
doi: 10.1016/S2666-5247(24)00079-X.
产丁酸菌相对丰度与感染疾病住院之间关联的多变量病因特异性竞争风险回归分析
在衍生队列的敏感性分析中,任何感染住院均被视为事件(而不是感染作为主要诊断)。观察到肠道微生物群与感染住院风险之间存在类似关联。此外,使用替代方法重新计算产丁酸菌的相对丰度也得到了与主要分析相似的结果,显示了微生物群-感染相关性的稳健性。
在衍生队列的嵌套、匹配、病例对照分析中,随访期间因感染住院的HELIUS参与者(病例)与未因感染性疾病住院的HELIUS参与者(对照)在年龄、性别、种族、抗生素暴露、糖尿病以及肺部和胃肠道合并症方面以1:1的比例匹配。病例和对照组的肠道微生物群多样性没有差异。
然而,与整个队列的数据一致,随访期间因感染性疾病住院的参与者与匹配的对照组相比,基线产丁酸菌相对丰度较低,总体肠道微生物群组成不同。
在进一步的探索性分析中,通过计算对比来检查人口统计学、生活方式因素、抗生素和合并症是否改变了产丁酸菌对感染风险的影响估计。
虽然有几个协变量(如性别,年龄,BMI和糖尿病)与产丁酸菌的相对丰度和因感染性疾病住院的风险相关,但产丁酸菌和因感染性疾病住院之间的关系并不受大多数协变量的影响。然而,在BMI为30或更高的参与者中,产丁酸菌与感染相关住院风险之间的关联似乎不存在。值得注意的是,未观察到微生物群-感染关联与种族之间的相互作用,饮食变量也与产丁菌密切相关。
在这些独立的大型观察性队列中,Kullberg博士团队发现肠道微生物群与一般人群中感染性疾病相关住院和死亡的风险相关。更高丰度的厌氧产丁酸菌与预防严重感染有关,即使在调整人口统计学,生活方式,抗生素暴露和合并症时也是如此。
不同地理位置的肠道微生物群与感染相关住院风险之间存在相似的关联。
这些研究结果表明,肠道微生物群可能是感染相关住院治疗的潜在可改变的风险因素,因此有必要进行干预性研究。
肠道微生物群经常在因严重感染住院的患者中被破坏,这与临床结果有关。然而,这些破坏可能是疾病的结果,或者在感染之前并影响易感性。
在感染发作前表征的肠道微生物群在随访期间因感染住院的参与者和那些没有因感染住院的参与者之间存在差异,表明肠道微生物群与严重感染的易感性相关。 在独立的队列中,结果组之间微生物群组成的这种差异同样是由Veillonella (韦荣氏球菌、一种包括与SARS-CoV-2感染期间出现严重症状的风险增加相关的机会性病原体并在COVID-19住院患者中富集的属)增加、Butyrivibrio(丁酸弧菌、一种产丁酸菌属)和严格厌氧未培养的菌Clostridia Candidatus减少引起的。
临床前研究表明,微生物代谢产物丁酸盐增强了对感染的保护,同时预防了免疫相关的病理学。丁酸盐诱导抗微生物肽的产生,增加定植抗性,并减少小鼠流感感染期间嗜中性粒细胞向气道的募集,从而限制组织损伤。
研究表明,减少产丁酸菌(仅为严格厌氧菌)会增加中风,肾移植和异基因造血干细胞移植后的感染风险。
此外,2023年发表的一项研究将3032名机械通气患者的观察数据与动物模型相结合,结果显示早期使用抗厌氧抗生素治疗会降低总体和无感染生存率。 在15908名急诊科患者中证实了抗厌氧菌抗生素的这些不良反应。有趣的是,通过这样的抗生素消耗厌氧微生物群导致肠杆菌科的扩增,并且先前确定了肠杆菌科相关微生物群特征与一般人群中的全因死亡率之间的关联。
本文的研究结论有荟萃和大型不同地理位置的独立队列支持。结论的可推广和参考性很强,这些发现表明厌氧、产丁酸盐的肠道微生物群在严重感染高危患者和普通人群中的重要性,并建议应重新考虑广泛使用抗厌氧抗生素。
但是基于这些在单个时间点表征微生物群,考虑肠道微生物群可能会随着时间的推移而变化,这可能会掩盖在遥远的时间点对结果的影响。然而,单个微生物群的组成非常稳定,许多细菌在几十年内都是居民。
此外,产丁酸菌的潜在有益作用可能超出丁酸盐,因为几种产丁酸菌能够生物合成次级胆汁酸和具有潜在免疫调节以及交叉喂养其他共生菌的作用。
本文分享有助于重新评估肠道微生物导向疗法(如靶向输送产丁酸细菌或限制肠道厌氧菌消耗)的干预性的潜在机会,有望降低对全身感染的易感性。

谷禾健康

在谷禾的检测实践中发现很多自闭症和情绪障碍人群的对甲酚含量很高,并且结合现有文献,有充分的证据认为对甲酚与自闭症存在相关性。

<来源:谷禾健康自闭症儿童检测示例>
什么是对甲酚?对甲酚是人体中特定细菌(例如艰难梭菌、部分梭杆菌、肠杆菌)降解蛋白质中的l-酪氨酸产生的一种酚类化合物。
目前在自闭症谱系障碍(ASD)患者的血液、尿液和粪便中均已发现对甲酚及其人体代谢物对甲酚硫酸盐的水平明显升高,并发现ASD患者的重复刻板行为、交流与认知障碍症状的加重与尿液中对甲酚和对甲酚硫酸盐水平升高密切相关。
分析还发现,尿液中的对甲酚和对甲酚硫酸盐水平能够很好地区分开ASD儿童与健康儿童,有望作为自闭症谱系障碍的生物标志物和客观定量指标。
作为经过肠道代谢和吸收的物质,过量的对甲酚对肠道健康也存在一定的危害。高浓度对甲酚对结肠细胞具有毒性,会抑制细胞的增殖并增加线粒体耗氧量;还与肠道菌群失衡相互促进,促使耐受和产生对甲酚的细菌进一步增长,并损害肠道上皮细胞,导致屏障功能受损。
除了在自闭症中展现出的相关性及对肠道的危害外,过量的对甲酚还可作为一种尿毒症毒素。在慢性肾脏疾病(CKD)中,血浆中对甲酚和对甲酚硫酸盐的显著升高被检测到,在肾小管细胞中,对甲酚和对甲酚硫酸盐增加氧化应激,影响线粒体功能,并导致细胞死亡,加重慢性肾脏疾病进展。并且对甲酚硫酸盐被发现与肾纤维化有关。
对甲酚和对甲酚硫酸盐也被怀疑在CKD相关的不良心血管事件中发挥作用,因为它们影响内皮细胞的增殖和迁移,降低内皮伤口修复的能力,增加内皮细胞的衰老,并与心肌细胞功能障碍相关。
在这种背景下,本文详细讲述了对甲酚及其代谢产物对自闭症、肠道细胞及菌群和外周组织细胞(即肾小管细胞和血管内皮细胞)的影响。此外,我们将回顾最近的证据,探讨肠道微生物群和对甲酚的产生与自闭症之间的关联,以及该化合物在自闭症中可能发挥的机制。
如何检测自身对甲酚水平,并通过饮食或药理手段降低对甲酚或对甲酚循环浓度也是人们所关心的。在本文的最后一个部分,我们列举了当前主要的一些降低体内对甲酚水平或减轻其危害的措施,包括使用克里美净等药物;多食用富含原花青素的水果,减少红肉的摄入;保持平衡的肠道菌群状态;以及一些合生元疗法。降低对甲酚水平还可能有助于改善自闭症、慢性肾脏疾病和相关的心血管障碍。
对甲酚过高的危害
我们发现,当人体中对甲酚浓度过高时,会存在以下的危害:
•可能是介导自闭症的关键因子
•导致肠道菌群失衡
•对结肠细胞具有毒性
•诱导肠道屏障功能的改变
•会加重肾脏疾病
•与心血管功能障碍相关
作为栖息在我们肠道中的微生物群落,其就像一个个小型的加工厂,可以产生许多代谢产物。
▸肠道菌群代谢酪氨酸产生对甲酚
人体内的对甲酚主要来源于肠道菌群的代谢。在微生物代谢可用的底物中,肠道微生物群降解未消化(或未完全消化的蛋白质)释放的芳香族氨基酸(苯丙氨酸、酪氨酸和色氨酸),产生酚类和吲哚类产物。在这些化合物中,酚类化合物对甲酚(4-甲基苯酚)由l-酪氨酸产生。
如下图所示,以梭菌属为代表的细菌可表达脱羧酶,该酶可将酪氨酸的中间代谢产物对羟基苯乙酸和对羟基苯丙酸脱去羧基形成对甲酚和对乙酚。
肠道细菌似乎使用几种酪氨酸衍生的代谢产物,如4-羟基苯丙酮酸、4-羟基苯乳酸、3-(对羟基苯基)丙酸和4-羟基苯乙酸作为对甲酚合成的中间体。
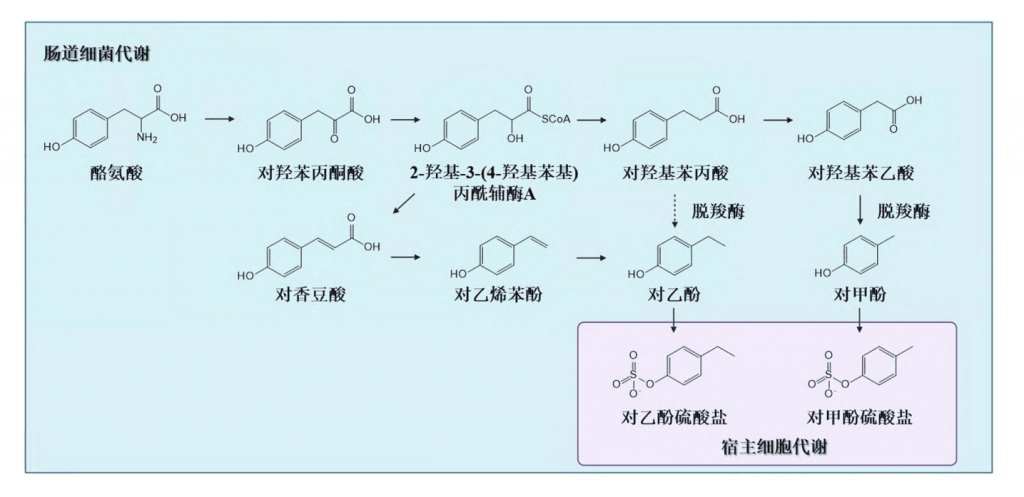
DOI︰10.20059/j.cnki.pps.2023.08.1011
▸艰难梭菌、乳杆菌科等可以产生对甲酚
分析表明,在人类肠道中存在的细菌中,特定的细菌家族,如梭杆菌科、肠杆菌科、梭菌科、拟杆菌科、乳杆菌科和红椿菌科(Coriobacteriaceae),是强对甲酚生产者,部分双歧杆菌科也可代谢产生对甲酚。
其中以艰难梭菌的对甲酚产量最高,可达其他细菌的10~1000倍。因此,感染艰难梭菌的患者体内可能会出现对甲酚含量升高的情况。

在另一项研究中,通过使用补充有酪氨酸及其代谢物的培养基鉴定产生对甲酚的肠道细菌。发现B.longumsubsp.infantis YIT 4018亚种、艰难梭菌 YIT 10084T、Cl. paraputrificum YIT 10074T和F.necrogenes YIT 10362T具有产生对甲酚的能力。
▸乳酸可以减少对甲酚的产生
艰难梭菌产生对甲酚的能力与其相对于其他肠道细菌的竞争优势有关,从艰难梭菌感染的小鼠模型中可以看出,过量生产对甲酚会影响肠道微生物群的生物多样性。
乳酸是另一种细菌代谢产物,已被证明可以在体外减少细菌对甲酚的产生。利用这一特点,我们推测提升产乳酸细菌的丰度有助于减少对甲酚的产生。
▸高蛋白摄入量会增加对甲酚浓度
在哺乳动物中,饮食中蛋白质摄入量的增加会提高粪便和尿液中的对甲酚浓度,这可能是由于来源于未消化蛋白质的底物l-酪氨酸在细菌代谢活动中的可用性增加。
相反,含有抗性淀粉和麦麸提取物的饮食会减少对甲酚的粪便含量。
人体细胞由于缺乏相关的酶,自身并不会产生对甲酚。
对甲酚除了可经肠道细菌代谢产生以外,石油、颜料、香水、化妆品等日用品中含有对甲酚,对甲酚也是部分食品用防腐剂的原料,因此人体内的对甲酚也可能来源于饮食直接摄入或气体挥发吸入。
对甲酚虽然不是宿主合成的,但在吸收过程中及吸收后可在宿主组织中被修饰。肠上皮细胞吸收对甲酚,产生几种共代谢产物,最终这些产物会在尿液中排出。
▸结肠黏膜结合生成对甲酚硫酸盐
结肠黏膜与硫酸盐和葡萄糖苷酸结合酚类物质的能力已得到证实,分别允许产生对甲酚硫酸盐(p-CS)和对甲酚葡糖苷酸(p-CG)。
在一项研究中,比较了有结肠和没有结肠的血液透析患者血浆中的p-CS水平,表明结肠在p-CS的产生中起着重要作用。从肠道门静脉释放的未代谢的对甲酚由肝脏代谢,主要产生对甲酚硫酸盐,在较小程度上产生对甲酚葡糖苷酸以及其他次要代谢物。
肠道菌群和宿主组织对甲酚代谢的示意图
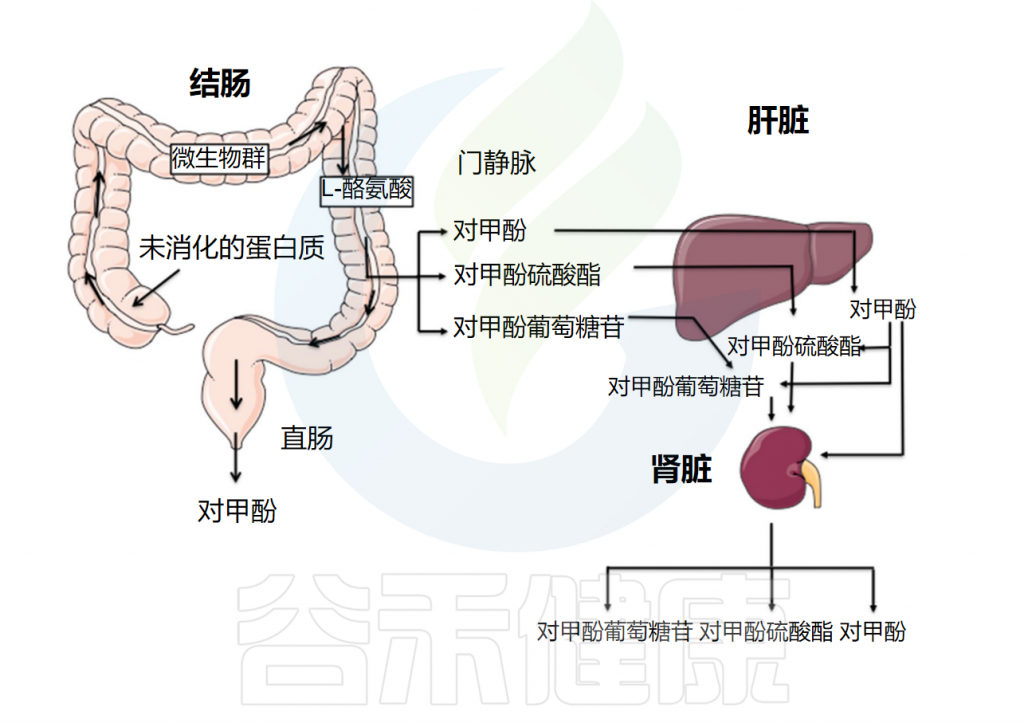
doi: 10.1007/s00726-021-03064-x.
▸与白蛋白结合保持血液中的含量平衡
对甲酚、p-CS和p-CG以可逆的方式与血浆白蛋白结合,导致血液中结合和游离部分之间的平衡。健康受试者血液中对甲酚的总浓度为9-13µM,而总p-CS的循环浓度为13-15µM。在血液中,游离形式的p-CS浓度平均仅为0.31µM,约占总量的2%。
最后,未与白蛋白结合的对甲酚、p-CS和p-CG会通过尿液排出。志愿者尿液中对甲酚的平均浓度为340µM,个体值之间存在显著差异。这些研究中未报告志愿者的饮食状况,加上个体肠道微生物群组成的差异,可能解释了这种差异。
▸素食者的对甲酚浓度会较低
值得注意的是,一项针对少数食用素食或无限制饮食的健康志愿者的研究表明,素食者的p-CS尿排泄量明显低于无限制饮食者,这可能是因为素食者的膳食纤维含量较高,蛋白质摄入量较低。
在一项针对志愿者的随机、平行、双盲试验中,研究表明,与等热量对照组(不补充蛋白质,摄入相似量的膳食纤维)观察到的微生物群组成相比,补充膳食蛋白质会导致细菌代谢向氨基酸降解转变。
与对照组相比,服用酪蛋白补充剂的组尿p-CS较高,而服用大豆蛋白补充剂的组则没有,这表明膳食蛋白质的来源可能对肠道微生物群对对甲酚的产生或宿主对这种细菌代谢物的代谢产生不同的影响。
▸对甲酚硫酸盐具有神经毒性,与自闭症相关
有临床研究表明对甲酚硫酸盐可能具有神经毒性,是部分神经系统疾病的潜在病因。
目前在自闭症谱系障碍(ASD)患者的血液、尿液和粪便中均已发现对甲酚和对甲酚硫酸盐的水平明显升高,并发现ASD患者的重复刻板行为、交流与认知障碍症状的加重与尿液中对甲酚和对甲酚硫酸盐水平升高密切相关。
我们将在后面的章节中详细讨论对甲酚在自闭症中的作用及其机制。
▸高浓度对甲酚对结肠细胞具有毒性
在体外实验中,浓度为1000µM及以上的对甲酚对人结肠细胞表现出剂量依赖性的遗传毒性。在不同底物的情况下,结合对人类结肠细胞发酵上清液的遗传毒性测试,发现对甲酚是这些上清液中对结肠细胞遗传毒性的最大预测因子。
▸过量的对甲酚减少增殖和线粒体耗氧量
浓度为800µM的对甲酚减缓了人结肠细胞HT-29 Glc−/+的增殖,伴随S期细胞的积聚和细胞分离的轻微增加。在这项研究中,800µM对甲酚的急性处理减少了集落细胞中的线粒体耗氧量。
此外,预处理细胞1天后,基础和最大耗氧量增加,可能抵消了对甲酚对细胞呼吸的不利影响。预处理的细胞中测量到阴离子超氧化物产量增加。在较高浓度(1600和3200µM)下,对甲酚预处理也显示出类似效果,但处理1天后,质子通过线粒体内膜的泄漏增加,降低了线粒体的生物能量代谢效率。
用浓度在800至3200µM之间的对甲酚预处理结肠细胞3天后,细胞内ATP浓度呈剂量依赖性降低。因此,在这个体外模型中,过量的对甲酚被确定为能量代谢的干扰物和对结肠细胞的遗传毒性物质。
对甲酚对结肠上皮的主要作用
doi: 10.1007/s00726-021-03064-x.
▸抑制革兰氏阴性细菌的生长繁殖,同时对对甲酚不敏感的菌群具有生存优势
进一步研究发现肠道中的对甲酚水平和肠道菌群失衡存在相互促进的关系。对甲酚可抑制脆弱拟杆菌等革兰氏阴性肠道细菌的生长繁殖,造成艰难梭菌等对对甲酚不敏感的革兰氏阳性肠道细菌具备生存优势,进而导致肠道菌群组成及多样性的改变;而艰难梭菌正是肠道中产生对甲酚最多的细菌,其相对丰度升高又会进一步造成肠道中对甲酚水平升高。
▸过量的对甲酚促使菌群失衡,失衡的菌群进一步升高对甲酚水平
即肠道中过量的对甲酚促使肠道菌群失衡,失衡的肠道菌群又可进一步升高肠道中的对甲酚水平并加剧菌群的失衡。
关于对甲酚及其代谢物对炎症性肠病病因的影响数据很少。一项研究发现,克罗恩病患者尿液中p-CS的含量低于健康对照组,这提出了炎症性肠病患者结肠细胞中对甲酚代谢/解毒可能受影响的假设。
▸损害肠道上皮细胞,屏障功能受损
研究发现,对甲酚可通过抑制结肠上皮细胞线粒体呼吸链造成ATP产量减少,并促使结肠上皮细胞产生超氧阴离子引发DNA损伤,导致结肠上皮细胞活性及增殖能力受损,造成结肠上皮细胞层完整性受损、细胞间透过性增加,说明对甲酚可通过损害肠道上皮细胞造成肠道屏障功能受损。
使用人Caco-2结肠细胞单层,1600-6000µM的对甲酚剂量依赖性地增加了细胞之间的旁运输,表明高浓度对甲酚可诱导肠屏障功能的改变。在后续研究中,水果提取物中的多酚混合物阻止了对甲酚诱导的旁运输变化,但植物提取物中化合物发挥作用的机制仍需进一步确定。
★ 对甲酚是肠道菌群参与自闭症发生的重要介质
过量的对甲酚被怀疑会对中枢神经系统产生有害影响,这种影响可能与自闭症谱系障碍(ASD)的病因有关。对甲酚、对甲酚硫酸盐在自闭症谱系障碍(ASD)患者体内水平升高且与异常行为的程度呈明显的正相关关联,说明对甲酚可能是肠道菌群参与ASD发生发展的重要中介物质。
有什么证据支持尿液和粪便中对甲酚含量升高可能作为ASD早期有价值的生物标志物,并可能在自闭症病因中发挥作用?接下来将介绍对甲酚在自闭症谱系障碍(ASD)中的潜在致病机制及其与ASD病因和生理变化的关系。
▸自闭症儿童粪便和尿液中对甲酚含量高于正常儿童
首先,与年龄和性别匹配的对照儿童相比,自闭症儿童晨尿中对甲酚浓度较高。这些浓度差异在7岁前都能明显检测到。在另一项研究中,8岁以下的自闭症幼儿尿中对甲酚及其共代谢物对甲酚硫酸盐(p-CS)和对甲酚葡糖苷酸(p-CG)含量高于同年龄、同性别的对照儿童,但在大一点的儿童中则没有。
尿中对甲酚和对甲酚硫酸盐的水平与刻板印象和强迫/重复行为有关。另外两项研究也对自闭症儿童和对照组儿童粪便中的对甲酚进行了测量,结果表明自闭症儿童粪便中对甲酚含量高于对照组儿童。
▸额外注射对甲酚会导致焦虑行为及大脑结构发生改变
在小鼠模型中,单次静脉注射1mg/kg的对甲酚可诱导焦虑和运动活动增加。在10mg/kg的较高剂量下,对甲酚加剧了小鼠自闭症的核心症状,并显著减少了小鼠之间的社会互动偏好。此外,研究中进行了脑区特异性神经化学分析,结果表明这些行为变化与大脑某些区域(如杏仁核、伏隔核和背尾状壳核)多巴胺周转量的剂量依赖性增加相关。
值得指出的是,自闭症不应该仅仅被视为一种“脑部疾病”,因为免疫系统和消化道的异常也存在于自闭症。
大鼠腹腔注射对甲酚(30mg/kg)可改变伏隔核和海马体中N-甲基-D-天冬氨酸谷氨酸受体(NMDARs)亚基的表达,表明对甲酚可能损害这些结构中NMDAR依赖的活性。NMDARs在学习、记忆和突触发育中发挥核心作用。
此外,对甲酚在体外抑制少突胶质细胞的分化,这些细胞是中枢神经系统的髓磷脂形成细胞,源自胶质祖细胞。
中脑边缘多巴胺奖赏环路的正常激活是形成社会动机和产生奖励行为的基础。奖赏环路的激活可产生愉悦感并促进相关奖赏行为的重复,同时促进社交意向等社会动机的形成;而其激活失常则可能导致重复刻板行为和社会交往障碍等ASD核心症状。
该环路由中脑腹侧被盖区(VTA)的多巴胺神经元通过释放多巴胺,向伏隔核、杏仁核和前额叶皮质等脑区的多巴胺敏感神经元发出投射,从而调节行为动机与奖赏反馈。
目前,临床神经影像学技术已观察到ASD患者中脑腹侧被盖区(VTA)与伏隔核之间的结构性和功能性损伤,并在多种ASD模型小鼠中检测到奖赏环路下游神经元兴奋性降低,提示多巴胺奖赏环路受损可能是ASD的重要潜在发病机制。
▸补充对甲酚后社交缺陷加重、多巴胺及其代谢产物水平升高
研究表明对甲酚可能是诱发自闭症谱系障碍(ASD)的重要机理。ASD模型小鼠在服用对甲酚后,其社交缺陷、刻板行为和焦虑样行为明显加重,且在伏隔核等脑区内多巴胺及多巴胺代谢终产物高香草酸的水平显著升高,提示对甲酚可提高多巴胺在奖赏环路中的蓄积与代谢水平;而健康小鼠在服用对甲酚后不仅既可呈现出社交缺陷和重复刻板行为等AS样表现,其VTA多巴胺神经元的兴奋性和兴奋传导能力也显著降低,表现为神经元动作电位的产生数量减少、自发性兴奋性突触后电流的频率和振幅降低,这一现象符合由血清皮质酮升高所引发的神经生理改变。
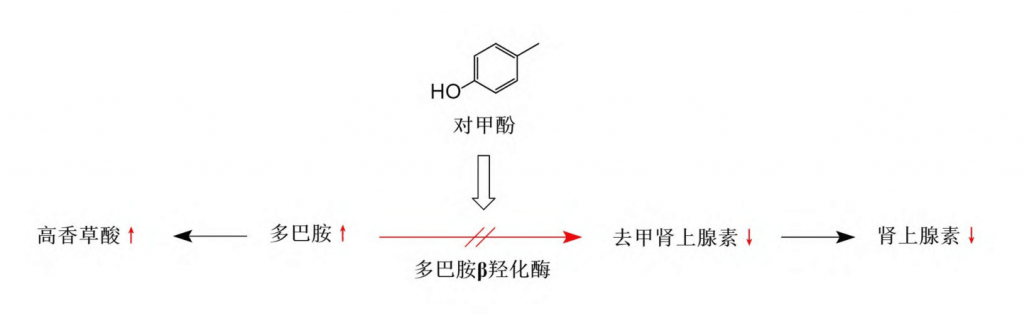
DOI︰10.20059/j.cnki.pps.2023.08.1011
▸奖赏环路功能受损、神经元兴奋性受抑制
此外,研究还发现升高血清对甲酚硫酸盐水平可显著提升小鼠的血清皮质酮水平,皮质酮是一种受下丘脑和垂体调控、由肾上腺皮质分泌的激素,通常在机体应激时分泌增加从而升高血糖并使精神紧张。提高血清皮质酮水平会提高应激反应,从而造成社交活动减少等ASD样症状。给予其口服式活性炭AST-120则可同时降低其血清对甲酚硫酸盐水平和血清皮质酮水平。
注释:AST-120是一种口服式活性炭,服用后可通过物理作用非特异性地吸附肠道中的酚类物质及其他芳香族化合物并随着肠道的蠕动排出体外,目前已在临床上应用于肾功能衰竭患者的治疗康复。
以上结果说明,对甲酚在体内被代谢为对甲酚硫酸盐后,可引发肾上腺糖皮质激素分泌增加,进而引发奖赏环路中多巴胺水平异常升高和多巴胺D2受体过度激活,造成奖赏环路功能受损、神经元兴奋性和兴奋传导受抑制,进而导致自闭症相关行为异常。
▸抑制多巴胺β羟化酶活性
此外,体外实验还发现对甲酚可使多巴胺β羟化酶不可逆地失去活性,而该酶是催化多巴胺向去甲肾上腺素转化的关键酶。
这一结果说明对甲酚除了可以通过升高血清肾上腺糖皮质激素提高VTA中的多巴胺水平以外,还可能通过抑制多巴胺向去甲肾上腺素的转化从而进一步导致神经系统及奖赏环路中多巴胺的蓄积以及多巴胺代谢水平升高,继而参与ASD的发病机制。
综上所述,对甲酚可能通过提高肾上腺糖皮质激素的分泌和抑制多巴胺β羟化酶的活性,导致多巴胺蓄积并引发中脑边缘多巴胺奖赏环路损伤,进而参与社交障碍等ASD症状的发生发展。
大脑前额叶皮质负责调控情绪、认知、决策等高级功能,参与威胁性刺激的解析评估、恐惧记忆的储存与消退并调节应激反应。临床研究显示ASD患者前额叶皮质的功能以及与其他脑区的连接性明显降低,小鼠实验表明社交障碍等ASD症状与前额叶皮质中多种神经元兴奋性异常有关,提示该脑区功能异常可能是诱发ASD的重要病因。
▸对甲酚硫酸盐诱发氧化应激和神经炎症
有研究发现对甲酚硫酸盐可在小鼠前额叶皮质中蓄积并诱发氧化应激与神经炎症,造成前额叶皮质神经元和神经干细胞受损凋亡。在服用AST-120后,该小鼠前额叶皮质中对甲酚硫酸盐的水平显著下降,同时前额叶皮质的氧化应激与神经炎症水平明显降低,神经元与神经干细胞的活性损伤得以修复,小鼠行为异常与ASD样症状随之得到改善,说明对甲酚硫酸盐可能通过影响前额叶皮质功能从而参与ASD的发病机制。
▸对甲酚硫酸盐可增加CD68的表达
研究还发现,对甲酚硫酸盐显著增加小鼠前额叶皮质中CD68分子的表达,而前额叶皮质中对甲酚硫酸盐水平的降低伴随CD68表达水平的下降。CD68可激活小胶质细胞,参与脑内免疫应答并介导炎症反应。
多项临床研究表明,ASD患者脑内小胶质细胞密度增加且过度激活,导致的神经系统炎症可能是引发ASD症状的重要因素。这提示对甲酚硫酸盐可能通过间接激活小胶质细胞,导致前额叶皮质的神经炎症与功能损伤,从而引发ASD症状。
▸自闭症患者存在线粒体功能障碍
线粒体是细胞中直接能源物质腺苷三磷酸(ATP)的产生场所,同时也参与细胞的应激反应与自噬凋亡。ASD患者常伴随线粒体功能障碍,临床上已借助脑磁共振波谱成像在ASD患者的多个脑区观察到线粒体功能障碍。
线粒体中的谷胱甘肽能起到解毒和抗氧化的作用,有助于维持线粒体内氧化还原反应平衡,保障线粒体产能功能的正常行使。肠道宏基因组测序显示,在ASD患者的肠道菌群中,谷胱甘肽合成酶及相关通路出现明显缺陷,说明肠道菌群的潜在线粒体保护功能受损;血液学检测显示ASD患者血浆中还原型谷胱甘肽与氧化型谷胱甘肽的比例明显降低,ASD患者有可能存在较为广泛的线粒体功能障碍。
▸耗竭细胞中的还原型谷胱甘肽
体外实验发现,对甲酚和对甲酚硫酸盐可耗竭细胞中的还原型谷胱甘肽,并显著提升胞内氧化型谷胱甘肽的水平。体内实验也发现对甲酚硫酸盐可显著降低小鼠前额叶皮质中的还原型谷胱甘肽水平,而通过服用AST-120降低小鼠体内的对甲酚硫酸盐能有效恢复前额叶皮质中的还原型谷胱甘肽水平。
谷胱甘肽的合成减少与解毒功能减弱是可能造成线粒体功能障碍并引发ASD症状的重要机制。
研究发现,对甲酚硫酸盐可增强细胞对葡萄糖和氧的摄取,提高线粒体的有氧呼吸,但显著降低ATP产量。这是因为对甲酚硫酸盐降低了与氮代谢和酸碱平衡相关的酶(如谷氨酰胺酶和谷氨酸脱氢酶)及抗氧化防御相关酶(如烟酰胺核苷酸转氢酶)的表达,同时激活NADPH氧化酶,导致线粒体能量消耗和氧化应激水平升高,从而引发线粒体ATP产量下降、分裂和凋亡。
上述证据反映了,对甲酚可能通过消耗细胞中的还原型谷胱甘肽、提高线粒体的氧化应激水平,造成线粒体功能障碍和能量代谢失衡,进而参与ASD的发病机制。
▸自闭症患者的肠道症状与菌群和行为异常有关
自闭症谱系障碍(ASD)患者常出现腹痛、胀气等肠道不适症状,严重者可长期伴随呕吐、便秘、腹泻等肠道功能紊乱表现,且患者的肠道症状与其行为异常之间存在程度上的显著关联。临床研究发现ASD患者肠道菌群组成失衡,提示肠道菌群失调可能是引发ASD相关行为异常的重要潜在诱因。
研究发现,将ASD患者的肠道菌群移植给无菌小鼠可导致小鼠脑中出现ASD相关基因的可变剪接,并表现出ASD样行为。特定的肠道细菌及其代谢产物能够调节小鼠行为并诱发ASD样表现,而移植健康人肠道菌群则不会引发这些变化。
▸过量的对甲酚导致肠道菌群紊乱及ASD症状
进一步研究发现,长期服用对甲酚的小鼠出现肠道菌群紊乱和社交障碍等ASD样症状。将这些小鼠的肠道菌群移植给健康小鼠后,后者也表现出ASD样症状和肠道中对甲酚水平上升。而将另一健康小鼠的肠道菌群移植给长期服用对甲酚的小鼠,则可降低其肠道中对甲酚水平,缓解VTA神经元兴奋性异常,并改善ASD样行为。
肠道中的对甲酚水平和肠道菌群失衡存在相互促进的关系。即肠道中过量的对甲酚促使肠道菌群失衡,失衡的肠道菌群又可进一步升高肠道中的对甲酚水平并加剧菌群的失衡,这可能是对甲酚参与 ASD发病机制的重要途径。
▸过量对甲酚损害肠道屏障功能
除了肠道菌群失调,肠道屏障功能受损也是ASD患者常见肠道症状的可能原因和潜在诱因。活检结果显示,75%的ASD患者小肠上皮细胞中维持肠道屏障完整性的紧密连接组分表达量减少,说明ASD患者普遍存在肠道通透性增加。这导致肠道中细菌、毒素及外源性蛋白质(包括细菌和食物来源)进入血液,成为引发ASD的潜在病因。
研究发现,对甲酚通过抑制结肠上皮细胞的线粒体呼吸链减少ATP产量,并促使细胞产生超氧阴离子引发DNA损伤,导致结肠上皮细胞活性和增殖能力受损,进而影响细胞层的完整性和增加细胞间透过性。这说明,对甲酚可能通过损害肠道上皮细胞来影响肠道屏障功能,这可能是其参与ASD发病的另一潜在机制。
编者小结
综上所述,对甲酚及其代谢产物对甲酚硫酸盐可能通过四种潜在途径参与ASD的发生发展:
①引发多巴胺蓄积和中脑边缘多巴胺奖赏环路受损;
②导致线粒体功能障碍;
③前额叶皮质神经炎症;
④以及肠道菌群失调和肠屏障功能受损。
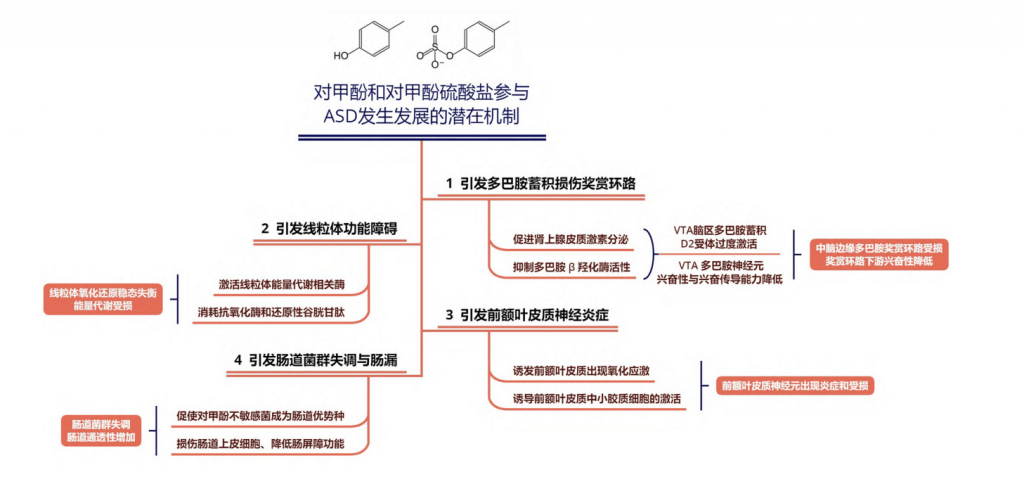
DOI︰10.20059/j.cnki.pps.2023.08.1011
在慢性肾病(CKD)患者中,肾功能障碍的进展与血浆中蛋白结合和水溶性尿毒症溶质的积累有关。在这些尿毒症溶质中,对甲酚及其代谢物对甲酚硫酸盐(p-CS)在很大程度上被怀疑会加重CKD。因为它们与血清蛋白结合的能力很强,容易在血液中积累。
相比之下,血清中另一种对甲酚共代谢物对甲酚葡糖苷酸(p-CG)的蛋白结合程度远低于p-CS。
▸慢性肾病和透析患者血液中对甲酚浓度更高
慢性肾病和血液透析患者血液中的对甲酚和p-CS浓度远高于健康人。在血液透析患者中,总对甲酚的5-7%以游离形式存在,其余为共轭形式。CKD患者的p-CS血药浓度为50-120µM,血液透析患者为110-220µM,其中约7%以游离形式存在。相比健康人,CKD/血液透析患者的对甲酚和p-CS浓度分别高出4-19倍和4-16倍。
并且血液透析患者肾小管分泌对甲酚硫酸盐的清除率显著低于健康人,表明CKD患者的p-CS分泌受损。
对甲酚和p-CS作为尿毒症毒素参与CKD进程。一项针对CKD患者的研究显示,p-CS基线水平可预测CKD进展,而血液透析患者血清中对甲酚的游离浓度与死亡率相关。
▸对甲酚硫酸盐与肾纤维化有关
体外研究和部分肾切除小鼠经对甲酚硫酸盐(p-CS)治疗4周的体内数据表明,p-CS可能与肾纤维化相关。由于肾小管分泌是肾处理p-CS的主要途径,p-CS可能通过诱导氧化应激导致肾小管细胞损伤。
在体外,p-CS浓度为5-26µM时,会以与炎症反应相关的方式改变近端肾小管细胞的基因表达;浓度为5-260µM时,会损害线粒体功能和生物发生。此外,对甲酚在12-52µM时对肾小管细胞具有凋亡作用,而在144-577µM时可诱导细胞自噬死亡。
有趣的是,在接受维持性血液透析的终末期肾病患者中,摄入含有抗性淀粉的饮食8周能够降低血清中对甲酚浓度。此外,在透析患者中,在饮食中补充不可消化的碳水化合物可降低血浆中p-CS的浓度,从而表明这种饮食干预在减少结肠源性对甲酚的产生方面是有效的。
▸不可消化的碳水化合物有助于减轻对甲酚过量引起的症状
未消化的碳水化合物可能通过减少对甲酚在结肠的吸收间接降低其循环浓度。在慢性肾病中,尿素流入结肠后被脲酶活性细菌转化为铵,过量的铵会损伤结肠黏膜,增加通透性,并引起结肠黏液层和吸收性结肠细胞的形态学改变,同时减少短链脂肪酸氧化。
下图总结了对甲酚及其代谢物在过量时对肾细胞的有害影响。低蛋白饮食(0.6-0.8g/kg/天)通常被推荐用于延缓CKD进展和推迟透析治疗,这与高蛋白饮食显著增加肠道微生物群合成对甲酚所需l-酪氨酸正好相反。
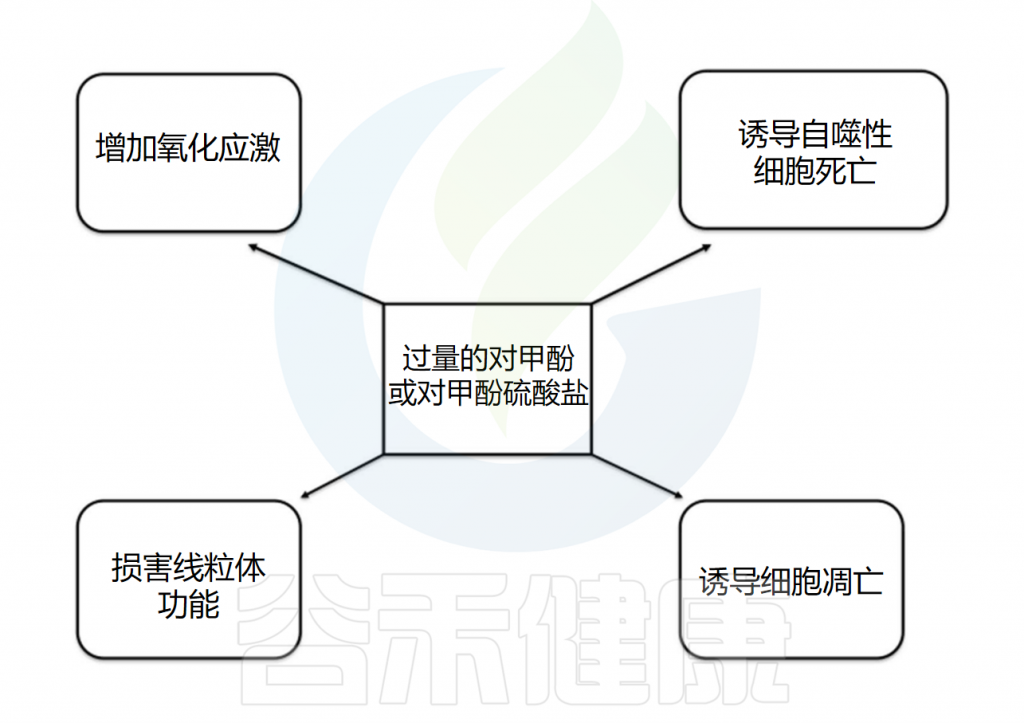
doi: 10.1007/s00726-021-03064-x.
对甲酚及其次生代谢物作为尿毒症毒素受到广泛关注,其对心血管系统的有害影响主要来自肾病患者的观察性研究和内皮细胞的体外实验。
▸对甲酚浓度与心血管疾病风险相关
观察研究发现,血清游离对甲酚浓度是慢性肾病(CKD)患者心血管疾病的风险预测因子,而在血液透析患者中,血清游离和总对甲酚浓度与心血管事件相关。
尿中对甲酚硫酸盐(p-CS)的高排泄与CKD患者的心血管事件直接相关。血清游离对甲酚浓度与首次心血管事件的发生和心血管疾病相关,并可能预测老年人心血管疾病的死亡率。
▸不同浓度对甲酚对内皮细胞的影响
内皮功能障碍在心血管疾病发展中起重要作用,几项实验研究测试了对甲酚对内皮细胞生理的影响。
在白蛋白存在下,对甲酚浓度为100-500µM时,剂量依赖性地抑制内皮细胞增殖和伤口修复。浓度为185-739µM时,抑制作用部分源于细胞周期G0/G1期细胞的积累,伴随细胞周期抑制剂p21/WAF1/Cip1表达增强和cyclin D1表达抑制。此外,对甲酚显著增加内皮通透性,并在90-3000µM范围内导致细胞周期G2/M期积累,损害内皮祖细胞增殖和迁移。浓度为92-740µM时,其对内皮祖细胞增殖的抑制与p38和Erk1/2磷酸化的激活有关。
370µM浓度的对甲酚(自由形式或与白蛋白结合)会增加内皮细胞释放内皮微泡。内皮微泡是从活化或凋亡的内皮细胞和血细胞中释放的膜泡,大小为0.1-1.0µm,反映内皮细胞损伤程度。这些由细胞质膜起泡脱落形成的微泡被认为是调节血管生理的活跃细胞信使。内皮微泡释放的增加会降低内皮细胞迁移能力,促进成熟内皮细胞衰老,从而影响内皮修复。
▸影响内皮细胞的生物学和修复
在血液透析患者中,游离血清对甲酚浓度与循环内皮微泡的数量相关。最近有研究表明,对甲酚在230µM浓度下时,可增强内皮细胞中微囊泡的释放;当在92-920µM范围内时,可以激活内皮细胞中的整合素连接激酶。该激酶是整合素信号复合体的关键组成部分,参与血管完整性和血管生成。在体外获得的大量实验证据清楚地表明,对甲酚可能影响内皮细胞的生物学和修复。
下图概述了对甲酚对内皮细胞的影响:
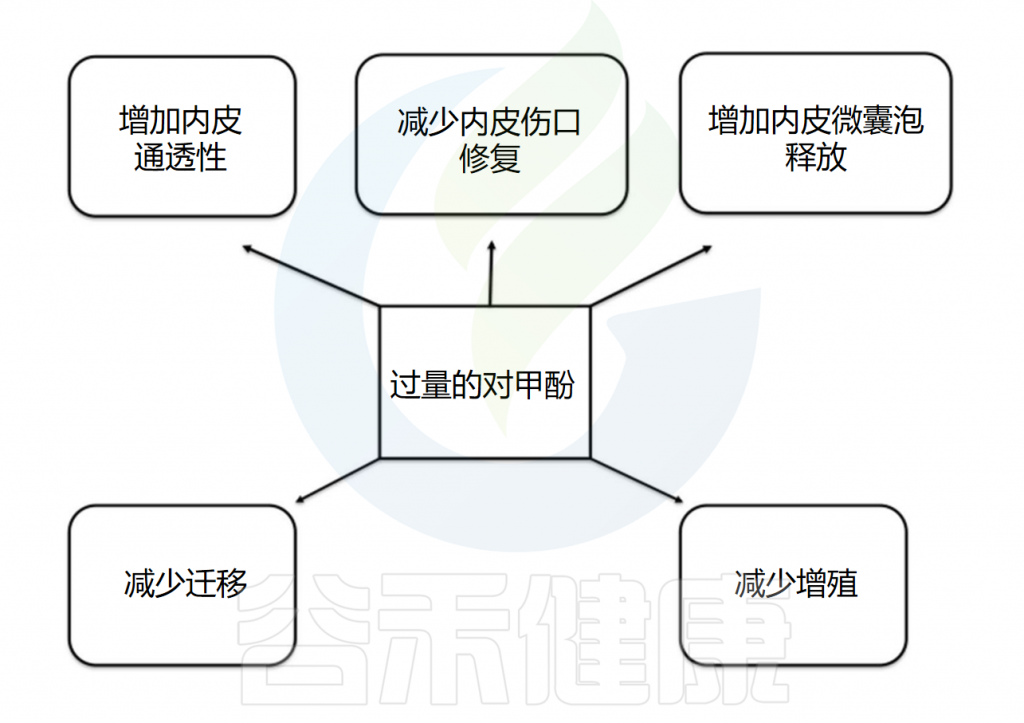
doi: 10.1007/s00726-021-03064-x.
▸对甲酚过量与心肌细胞功能障碍相关
对甲酚在心肌细胞中的作用研究表明,在230-920µM范围内,对甲酚可逆地降低新生儿心肌细胞的自发收缩率,并引发间隙连接分解,说明其过量与心肌功能障碍的关联。
间隙连接在心肌细胞间的电偶联和脉冲传播中起关键作用。此外,相同浓度下,对甲酚还会破坏心肌细胞的粘附连接,可能进一步影响心肌细胞功能。
1
克里美净等药物降低对甲酚水平
▸克里美净降低对甲酚水平并改善自闭症症状
临床研究表明,给12-17岁的自闭症谱系障碍(ASD)儿童服用克里美净(AST-120),可明显降低受试儿童尿液中对甲酚硫酸盐的水平,同时显著改善了受治儿童的重复刻板行为和社会动机异常等ASD症状,并且未发现明显的不良副作用。
对于具有严重情绪障碍的ASD儿 童 还 可 显 著 降 低 其 焦 虑 和 易 怒 程度。克里美净(又名AB-2004、AST-120)是一种可食用的活性碳颗粒,可非选择性地吸附肠道内的酚类物质及其他芳香族化合物。由于AST-120本 身 并 不 参 与 体 内 生 化 反应,仅起到物理吸附作用,不会被人体所吸收,因此具有良好的安全性。这也从侧面表明临床上降低肠道中对甲酚水平具有改善孤独症症状的能力。
▸阿卡波糖减少对甲酚的生成和浓度
其他研究还发现,小肠α-葡萄糖苷酶抑制剂,如阿卡波糖(Glucobay®)可增加到达结肠的未消化碳水化合物的数量,并可降低蛋白质结合的尿毒症溶质对甲酚的生成和血清浓度。
注:本文不作为医疗建议,药物需在医生建议下服用
2
高纤维,低蛋白饮食调整
▸富含原花青素和多酚提取物的果蔬可预防对甲酚的有害作用

一项研究在暴露于对甲酚的结肠上皮细胞中评估了来自苹果、牛油果、蔓越莓、葡萄或其他含有原花青素和多酚提取物水果的保护作用。
对甲酚会显著增加乳酸脱氢酶(LDH)渗漏并降低 ATP 含量,而在Caco-2细胞中,它显著降低跨上皮电阻并增加葡聚糖的细胞旁转运。蔓越莓和牛油果中提取的原花青素类物质阻止了对甲酚诱导的细胞的改变。
原花青素细菌代谢物减少了LDH泄漏,改善了细胞活力,但未改善细胞内ATP。所有多酚提取物和原花青素细菌代谢物都阻止了对甲酚诱导的屏障功能改变。这些结果表明,含原花青素的多酚提取物和原花青素代谢物可能有助于保护结肠粘膜免受对甲酚的有害影响。
▸增加膳食纤维和抗性淀粉摄入,降低对甲酚水平
已经研究了补充纤维在降低透析前慢性肾脏病 (CKD)患者对甲酚的影响。在血液透析(HD)患者中,纤维补充已被证明可显著降低血浆对甲酚浓度。提供豌豆壳纤维和菊粉可使血清对甲酚减少24%,与低聚果糖和菊粉在HD患者中的效果相似,表明补充纤维对疾病早期患者有潜在益处。
3期和4期CKD患者在补充益生菌和6.6克/天菊粉后,15天和30天内对甲酚减少40%,需要注意的是,益生菌可能也在降低对甲酚方面发挥作用。
该研究支持这样一个结论,即提供高度可发酵的纤维,如菊粉,可能通过抑制蛋白水解和增强糖发酵来减少对甲酚的产生。豌豆壳纤维也可能通过缩短肠道运输时间来帮助减少蛋白水解发酵从而减少对甲酚的产生。
还有研究比较了食用抗性淀粉或表没食子儿茶素没食子酸酯(EGCG)对体内对甲酚含量的影响。研究表明,抗性淀粉可以在大鼠模型中有效降低结肠和尿液中的对甲酚水平。
表没食子儿茶素没食子酸酯(EGCG):这种茶多酚中最有效的活性成分,通过调节肠道微生物群,减少对甲酚生成细菌的含量,从而降低其血浆和尿液浓度。
▸高蛋白和酪氨酸摄入会增加体内对甲酚水平
我们知道,蛋白质中的酪氨酸是对甲酚产生的原料,因此饮食中蛋白质摄入量的增加会提高粪便和尿液中的对甲酚浓度,这可能是由于蛋白质的底物l-酪氨酸在细菌代谢活动中的可用性增加。
3
通过调整肠道菌群,减少对甲酚的产生
▸减少艰难梭菌等产对甲酚的细菌
在人类肠道中存在的细菌中,梭杆菌科、肠杆菌科、梭菌科、拟杆菌科、乳杆菌科和红椿菌科,是对甲酚生产者,部分双歧杆菌科也可产生对甲酚。
其中艰难梭菌的对甲酚产量最高,可达其他细菌的10~1000倍。因此,感染艰难梭菌的患者体内可能会出现对甲酚含量升高的情况。
并且肠道中的对甲酚水平和肠道菌群失衡存在相互促进的关系。对甲酚会抑制一些革兰氏阴性肠道细菌的生长繁殖,并造成艰难梭菌等对对甲酚不敏感的革兰氏阳性肠道细菌具备生存优势,导致肠道菌群组成及多样性的改变;而艰难梭菌正是肠道中产生对甲酚最多的细菌,其相对丰度升高又会进一步造成肠道中对甲酚水平升高。
因此,减少艰难梭菌等产对甲酚的细菌,相当于对“生产机器”进行了阻断,减少了体内对甲酚的产生。
▸产乳酸细菌有助于抑制对甲酚
乳酸是另一种细菌代谢产物,已被证明可以在体外减少细菌对甲酚的产生。利用这一特点,我们推测提升产乳酸细菌的丰度有助于减少对甲酚的产生。
嗜酸乳杆菌(Lactobacillus acidophilus)、干酪乳杆菌(Lactobacillus casei)、长双歧杆菌(Bifidobacterium longum)、婴儿双歧杆菌(Bifidobacterium infantis)和乳链球菌(Streptococcus lactis)是常见的产乳酸细菌,一些发酵乳制品及益生菌产品中常有其存在,通过提高其肠道占比可能有助于减少对甲酚的产生。
▸一些粪肠球菌菌株有助于对甲酚的解毒

还有研究发现,粪肠球菌(Enterococcus faecalis)的三个菌株(UTD-1、UTD-2和UTD-3),能够以很高的速率降低细胞外对甲酚浓度(30μg/ml),说明肠道分离株粪肠球菌可能是减轻对甲酚危害的潜在候选方法。
▸粪菌移植使肠道菌群正常化也降低了自闭症患者的对甲酚水平
此外,临床研究发现粪菌移植治疗可持续降低自闭症儿童肠道中过高的对甲酚水平,并且可以改善患者的肠道不适以及情绪和行为异常。
同时也进一步提示,菌群失调造成菌群代谢物紊乱继而引发肠道功能失调和菌肠脑轴失衡可能是自闭症的重要潜在病因,对甲酚等菌群代谢物具有作为 自闭症诊断和治疗靶标的潜力。
4
短期合生元治疗有助于降低对甲酚水平

一项初步研究调查了Probinul-neutro®(一种使肠道菌群正常化的合生元)是否可以降低血浆对甲酚浓度并减轻未透析慢性肾脏病(CKD)患者的胃肠道症状。
每包含有冻干细菌(5×109植物乳杆菌、2×109干酪乳杆菌亚种和2×109加氏乳杆菌、1×109婴儿双歧杆菌和1×109长双歧杆菌、1×109嗜酸乳杆菌、1×109唾液乳杆菌和1×109产孢乳杆菌和5×109嗜热链球菌)、益生元菊粉(2.2克;VB Beneo Synergy 1) 和1.3克木薯淀粉。
在两组中观察到对甲酚的相反变化:在接受安慰剂治疗的患者中,观察到但不显著的增加趋势,而在合生元组中显著降低。治疗开始后15天,血浆总对甲酚浓度比基线低约40%,然后一直保持在该水平直到研究结束。
这种影响可能源于共生诱导下肠道中产生对甲酚的细菌减少。益生菌和益生元成分均可调节肠道微生物组,合生元干预可显著降低3-4期慢性肾脏病患者的血浆总对甲酚浓度。
自闭症谱系障碍(ASD)患者的肠道菌群及体内对甲酚水平与健康人群相比呈现出显著差异,菌群多样性较低,产对甲酚细菌显著增多,并且对甲酚水平明显偏高。
对甲酚过量可能通过:①引发多巴胺蓄积和中脑边缘多巴胺奖赏环路受损;②导致线粒体功能障碍;③前额叶皮质神经炎症;④以及肠道菌群失调和肠屏障功能受损这几个方式促进自闭症的发展。
对甲酚水平过高还会导致肠道菌群失调和肠道屏障功能受损,菌群失调造成菌群代谢物紊乱继而引发肠道功能失调和肠脑轴失衡及一些代谢物通过“肠漏”进入血液可能是自闭症的重要潜在病因,对甲酚、对甲酚硫酸盐等菌群代谢物具有作为自闭症诊断和治疗靶标的潜力。
此外,对甲酚作为一种“尿毒症毒素”对肾脏和心血管的危害也不容小觑,在肾小管细胞中,对甲酚和对甲酚硫酸盐增加氧化应激,影响线粒体功能,并导致细胞死亡,加重慢性肾脏疾病进展。它还影响内皮细胞的增殖和迁移,降低内皮伤口修复的能力,增加内皮细胞的衰老,并与心肌细胞功能障碍相关。
《黄帝内经》中曾提到,“上医医未病,中医医欲病,下医医已病”。自闭症和慢性肾病一旦确诊,想要完全治愈极为困难,及时并准确地获取体内对甲酚水平和肠道菌群组成,可能是提前预测并预防自闭症和慢性肾脏疾病的一个方法。
谷禾的肠道菌群检测,能够以较为快速且精准的方式,获取人体肠道菌群的组成情况、菌群的多样性和占比以及包括对甲酚、吲哚等重要的菌群代谢物等关键信息。根据这些检测结果和数据,可以更有针对性地制定个性化的治疗方案或预防措施,做到对症下药。这不仅大大提高了治疗的效果,还能减少不必要的治疗手段和药物使用,为人们的健康提供更精准、有效的保障。
注:本账号内容仅作交流参考,不作为诊断及医疗依据。
主要参考文献
Blachier F, Andriamihaja M. Effects of the L-tyrosine-derived bacterial metabolite p-cresol on colonic and peripheral cells. Amino Acids. 2022 Mar;54(3):325-338.
Toft PB, Vanslette AM, Trošt K, Moritz T, Gillum MP, Bäckhed F, Arora T. Microbial metabolite p-cresol inhibits gut hormone expression and regulates small intestinal transit in mice. Front Endocrinol (Lausanne). 2023 Jul 18;14:1200391.
Stewart Campbell A, Needham BD, Meyer CR, Tan J, Conrad M, Preston GM, Bolognani F, Rao SG, Heussler H, Griffith R, Guastella AJ, Janes AC, Frederick B, Donabedian DH, Mazmanian SK. Safety and target engagement of an oral small-molecule sequestrant in adolescents with autism spectrum disorder: an open-label phase 1b/2a trial. (2022) Nature Medicine, Advance online publication.
Chen B, Morioka S, Nakagawa T, Hayakawa T. Resistant starch reduces colonic and urinary p-cresol in rats fed a tyrosine-supplemented diet, whereas konjac mannan does not. Biosci Biotechnol Biochem. 2016 Oct;80(10):1995-2000.
Meijers BK, Claes K, Bammens B, de Loor H, Viaene L, Verbeke K, Kuypers D, Vanrenterghem Y, Evenepoel P. p-Cresol and cardiovascular risk in mild-to-moderate kidney disease. Clin J Am Soc Nephrol. 2010 Jul;5(7):1182-9.
Salmean YA, Segal MS, Palii SP, Dahl WJ. Fiber supplementation lowers plasma p-cresol in chronic kidney disease patients. J Ren Nutr. 2015 May;25(3):316-20.
Vijayasarathy M, Kiran GK, Balaji S, Jabastin J, Bruntha Devi P, Brindha Priyadarisini V. In Vitro Detoxification Studies of p-Cresol by Intestinal Bacteria Isolated from Human Feces. Curr Microbiol. 2020 Oct;77(10):3000-3012.
Chang MC, Chang HH, Chan CP, Yeung SY, Hsien HC, Lin BR, Yeh CY, Tseng WY, Tseng SK, Jeng JH. p-Cresol affects reactive oxygen species generation, cell cycle arrest, cytotoxicity and inflammation/atherosclerosis-related modulators production in endothelial cells and mononuclear cells. PLoS One. 2014 Dec 17;9(12):e114446.
Wong X, Carrasco-Pozo C, Escobar E, Navarrete P, Blachier F, Andriamihaja M, Lan A, Tomé D, Cires MJ, Pastene E, Gotteland M. Deleterious Effect of p-Cresol on Human Colonic Epithelial Cells Prevented by Proanthocyanidin-Containing Polyphenol Extracts from Fruits and Proanthocyanidin Bacterial Metabolites. J Agric Food Chem. 2016 May 11;64(18):3574-83.

谷禾健康

春节假期期间,亲朋好友欢聚一堂,美食佳肴各种狂炫,然而当传统节日遭遇现代饮食文化,频繁的高脂高蛋白摄入、不规律的进食节奏,正不断冲击着肠道屏障的免疫调控网络,部分人群可能正被食物过敏困扰。
食物过敏(FA)是一个当今面临公共卫生问题。一个人可以在任何时候对任何食物过敏,但有引起过敏反应最普遍的食物包括:牛奶、鸡蛋、花生、坚果、大豆、小麦、鱼类和贝类。这些过敏反应范围从肿胀和荨麻疹到危及生命的过敏性休克。
更不乐观的是,食物过敏在当今全球工业化社会中的流行率呈现显著代际增长(一代比一代增强)。与此同时食物过敏率的上升与很多疾病的增加相呼应,包括肥胖、糖尿病、哮喘、自闭症和炎症性肠病(以及其他疾病)。我们如何解释这种代际变化?
食物过敏是过敏性疾病的一部分,被称为I型超敏反应,是由食物蛋白(抗原)通过肥大细胞和/或嗜碱性细胞表面上的免疫球蛋白同种型E(IgE)交联引起的,这与由食物成分引起的食物敏感性不同(例如,乳糖不耐症)。
与此同时,我们的肠道相关淋巴组织(GALT)每天都面临着相当大的挑战。它遇到的抗原估计来自1014微生物和每年超过约30公斤的食物蛋白质。这要求它必须将这些无害的抗原与潜在的病原体区分开来,并能同时引起适当的宿主免疫应答。
目前越来越明确的是,与先天免疫细胞和常驻微生物群密切相互作用的功能性上皮屏障对于建立和食物过敏以及口服耐受性至关重要。而口服耐受性的形成取决于年龄、遗传学、粘膜屏障状态、抗原的物理性质、暴露剂量和频率以及肠道微生物群。
是什么驱动了对食物抗原的过敏反应,近年来有关微生物群在调节抗原摄取和抗原呈递中的作用开始被解开。在4至6个月大的婴儿中早期引入致敏性食物已被证明有希望降低部分但并非所有儿童的IgE-食物过敏(IgE-FA)发病率。
IgE-FA尚无明确的治愈方法,金标准治疗是在发生过敏反应时避免使用对症治疗。幸运的是,疾病修饰疗法,包括免疫疗法,生物制剂等有希望。
本文汇总和依托这些文献结果,讨论了IgE-食物过敏在其自然史的背景下,发展的风险因素,免疫生物学,诊断和治疗,包括新兴疗法。同时,我们也将探讨肠道微生物群在食物过敏中的作用,以及如何通过调节肠道微生物群来预防和管理食物过敏。
食物过敏是一种由免疫球蛋白E(简称IgE)引起的过敏反应。这种病近几十年来越来越常见,可能会威胁生命。特别是对于那些难以完全避开的食物(比如牛奶或鸡蛋)过敏的人来说,生活质量会受到很大影响。
对牛奶、鸡蛋、小麦和大豆的过敏,随着年龄增长可能会慢慢好转。
对花生、坚果和海鲜的过敏,通常会伴随终身。
食物过敏常常和其他过敏性疾病一起出现,比如:
虽然理论上任何食物蛋白质都可能引起过敏,但最常见的是:
小麦过敏和乳糜泻是两种不同的病:
小麦过敏是对小麦蛋白的过敏反应;
但在乳糜泻中,部分水解的麦醇溶蛋白被小肠粘膜中的组织转氨酶脱酰胺。这种特异性和有序的脱酰胺作用增强了小肠固有层中CD4+T细胞对麦胶蛋白的识别,导致免疫应答。细胞因子的后续释放导致肠粘膜的组织学变化。
◆ 过敏疾病是如何发展的?
医生们发现,很多孩子的过敏疾病会按照一定规律逐步发展,这个过程被称为“过敏进行曲”。大约有30-50%的过敏儿童会经历这个过程。不过每个孩子的发展过程可能不太一样。
◆ 过敏疾病通常会按这个顺序出现:
湿疹(特应性皮炎):通常在出生后6个月内最先出现
食物过敏:在1岁前就可能出现
过敏性鼻炎和哮喘:在有湿疹的孩子中,差不多三分之二会在3岁前出现这些症状。
特别提醒:如果湿疹控制得不好,更容易得其他过敏病。
◆ 为什么会得食物过敏?
食物过敏的形成和很多因素有关:
个人因素:
严重的早期湿疹
父母有过敏病史
环境因素:
接触过敏物的时间
肠道中的菌群平衡情况
环境因素如何影响过敏?
新出现的数据表明,在免疫系统发育过程中暴露于非微生物环境因素,包括空气过敏原、清洁剂、污染物和微塑料,可能会导致屏障功能障碍。霉菌、蟑螂和尘螨等空气过敏原含有促进上皮蛋白分解的蛋白酶,导致上皮渗透性增加,例如,清洁剂破坏角质层内的紧密连接和脂质依赖性相互作用,从而增加细胞旁渗透性。
◆ 食物过敏的风险因素:
对过敏原蛋白的反应会受到多种因素的影响,包括:
个人的敏感程度:有些人对过敏原特别敏感,而有些人反应较轻。
过敏原的特性:不同食物中的过敏原性质不同,反应也会有所差异。
食物加工方式:加工过程可能会改变过敏原的性质,比如加热可能降低或增强过敏性。
有的加工对某些过敏原有帮助,比如鸡蛋中的卵清蛋白和卵粘蛋白在加热后过敏原性下降。
但对某些过敏原(如花生蛋白)可能起反作用,加热会使其形成更稳定的抗性结构,增加过敏原性。
◆ 胃肠道屏障与过敏风险
婴幼儿风险更高: 由于他们的胃肠道屏障和免疫系统尚未成熟,食物过敏更容易发生。
胃酸不足: 服用抗酸剂可能降低胃酸浓度,使更多未被分解的蛋白质进入肠道,增加过敏风险。
肠道通透性增加: 肠道屏障功能受损可能导致更多过敏原进入免疫系统,增加致敏和过敏反应的可能性。
食物成分的相互作用:食物中的其他成分可能会影响过敏原的作用。
◆ 过敏反应的严重程度
敏感人群的过敏反应可能从轻微到严重不等,严重时甚至可能危及生命(如过敏性休克)。因此,避免接触过敏原是目前最有效的预防方法。
◆ 为什么食物过敏难以治疗?
目前还没有针对食物过敏的有效治疗方法,因为科学家对引发过敏的分子机制还没有完全弄清楚。因此,过敏患者最好的办法就是避免食用含有过敏原的食物。但问题是,只有在明确知道食物中含有过敏原时,才能做到有效避免。
◆ 食品标签的重要性
食品标签是帮助消费者了解食物中是否含有过敏原的重要手段。然而,确保全球食品标签的准确性并不容易,主要有以下几个挑战:
◆ 哪些食物最容易引发问题?
牛奶是最常见的未标注过敏原,其次是小麦和大豆。这些食物经常出现在食品召回事件中,很大程度因为它们被意外添加或未正确标注。
对于过敏患者来说,了解食品标签和避免过敏原是保护自己的关键。但由于标签错误、交叉污染等问题,完全避免过敏原仍然具有挑战性。
食物过敏原主要是一类特殊的蛋白质(糖蛋白),它们通常能溶于水,而且比较”顽固”-不容易被热、酸和消化酶破坏。
不过,不同的过敏原特性会有很大差异。有的需要糖分子的修饰才能发挥作用,有的则不需要。
过敏原的结构特点:
大小不一:从小分子到大分子都有。
结构多样:有的是单个分子,有的会几个分子组合在一起。
稳定性强:通常含有特殊的化学键(二硫键),使它们不容易被破坏。
结合能力:能与金属、脂肪等物质结合,这种结合会让过敏原更稳定。
不同食物的过敏原如果结构相似,可能会导致交叉过敏。
常见的交叉过敏组合:
过敏原的识别位点(表位):
直线型表位:像一串珠子一样排列的氨基酸片段
立体型表位:蛋白质折叠形成的特殊立体结构
一般认为直线型表位更重要,因为它们更稳定,不容易被破坏。
但在某些情况下,立体型表位也能在食物中保持稳定,发挥作用。
了解这些特性有助于预测哪些食物可能会引起交叉过敏;改进食物加工方法,降低过敏风险;开发更好的过敏预防和治疗方案。
致敏是指免疫系统首次接触到某种过敏原后,开始产生针对它的特异性抗体(IgE),但此时不会引发过敏症状。
致敏的主要途径:
小麦过敏是一种IgE介导的I型过敏反应,部分人群对小麦中的某些蛋白质成分较为敏感,即使在护肤品中接触也可能出现过敏症状。
如果你已知对小麦过敏,或者属于敏感肌肤,建议谨慎使用含有水解小麦蛋白的护肤品。
花生过敏者可能因皮肤接触花生而致敏,尤其是皮肤屏障受损的人。
胃肠道致敏(1类食物过敏): 最常见的方式,食物过敏原通过消化道进入身体,导致过敏反应,尤其常见于婴幼儿,因为他们的肠道屏障和免疫系统尚未完全发育。常见过敏原包括牛奶、鸡蛋和豆类。
吸入性致敏(2类食物过敏): 通过呼吸道接触到空气中的过敏原(如花粉、动物毛发等),随后对相关食物产生过敏。
皮肤接触致敏: 通过皮肤接触到过敏原而致敏。例如:
蜱叮咬致敏: 蜱叮咬可能导致对红肉的过敏反应,这是一种特殊的皮内致敏途径。
子宫内暴露: 胎儿可能通过胎盘接触到母体食物中的过敏原(如牛奶、鸡蛋和花生),但目前没有确凿证据表明母亲的饮食会直接影响婴儿的食物过敏风险。
B细胞的双重角色 | 引起过敏/预防过敏
什么是B细胞?
B细胞是我们身体里的一种免疫细胞,它最重要的工作就是产生抗体(免疫球蛋白)。在食物过敏中,B细胞主要产生一种叫IgE的抗体。
食物过敏发生的过程:
第一步: 识别“入侵者”
B细胞会产生IgE抗体,这些IgE能够识别食物中的特定蛋白质(过敏原)。
第二步: 设置“警报器”
IgE会附着在特殊的免疫细胞(肥大细胞和嗜碱性粒细胞)表面,这些细胞就像身体的“警报器”。
第三步: 过敏反应的触发
当吃到过敏食物时,IgE认出并抓住过敏原
“警报器”被触发,免疫细胞释放出化学物质,这些化学物质引起过敏症状(如皮疹、呼吸困难等)。
关于IgE的特点:
IgE在所有抗体中数量最少,但它在过敏反应中起着关键作用。
B细胞的变化过程:
B细胞可以通过特殊方式转变,开始产生IgE,这个转变需要其他免疫细胞(T细胞)的帮助,还需要特定的信号分子(IL-4和IL-13)的参与。
对花生过敏的研究发现,科学家从花生过敏患者的血液中找到了产生IgE的B细胞。这些B细胞寿命较短。
不同过敏患者的IgE抗体可能会以相似的方式识别花生中的过敏原,这些发现帮助我们更好地理解食物过敏的发生机制,为开发新的治疗方法提供线索,从而可能帮助预防或减轻过敏反应。
图 控制对过敏原反应的免疫过程
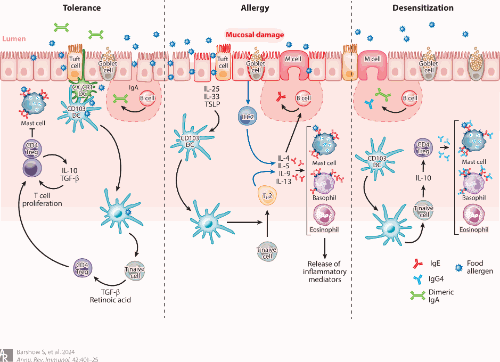
(左)耐受性:耐受性是一种主动免疫过程,在此过程中暴露于过敏原不会引发过敏性炎症。耐受性可涉及特异性抗原呈递细胞、TcB的诱导和活化以及B细胞同种型转换为伊加。
(中)过敏症:在过敏症中,上皮细胞功能障碍使抗原进入并触发alarmins IL-25、IL-33和TSLP的释放。幼稚T细胞分化成TH2细胞,其分泌促炎性TH2细胞因子IL-4、IL-5、IL-9和IL-13,其导致B细胞同种型类别转换为IgE。IgE通过高亲和力IgE受体(FcεR1)与肥大细胞和嗜碱性粒细胞结合,导致急性过敏性炎症。
(右)脱敏:过敏原免疫疗法的脱敏与IL-10的Treg产生相关。B细胞类别从IgE转变为IgG 4和伊加产生。IgG 4和伊加可通过分别与IgE竞争变应原结合位点和直接结合食物变应原而充当阻断抗体来抑制TH2适应性免疫应答。缩略语:DC,树突状细胞;TH2,2型辅助性T细胞; Treg,调节性T细胞; TSLP,胸腺基质淋巴细胞生成素。
不是所有抗体都会引起过敏;B细胞除了能产生引起过敏的IgE抗体,还能产生其他种类的保护性抗体,这些保护性抗体可以帮助预防食物过敏。
保护性抗体是如何工作的?
科学家通过小鼠实验发现粘膜中的IgA抗体能阻止过敏原被肠道吸收。
IgG抗体有两种保护作用:
直接捕获并中和过敏原;
通过FcγRIIb受体的作用抑制过敏反应。
此外,治疗食物过敏的新发现在口服免疫治疗(OIT)中观察到,保护性抗体IgG4会明显增加,IgG4与致敏抗体IgE的比值升高。这些变化与患者对食物的耐受性直接相关。
调节性B细胞的重要性
研究发现牛奶过敏患者与健康人对比,过敏患者的调节性B细胞明显减少,这些细胞产生的IL-10也较少。
IL-10的重要作用可以减少致敏抗体IgE的产生,促进保护性抗体IgG4的产生。
B细胞的信使功能:
B细胞也可通过IgE促进的抗原呈递作用作为T细胞的抗原呈递细胞(APC),其中IgE-过敏原复合物被低亲和力IgE受体CD 23(FcεRII)内化,后者在B细胞上表达。
值得注意的是,最近的一项研究表明,B细胞上CD 23的表面密度通过IgE促进的抗原呈递决定了过敏原特异性T细胞的活性,并与总血清IgE水平呈正相关。抗CD 23单克隆抗体鲁昔单抗通过靶向CD 23-IgE相互作用抑制IgE合成。
B细胞治疗方面潜力:
预防方面:
T细胞在食物过敏中的角色
1. TH2细胞:过敏反应的”指挥官”
研究发现,TH2细胞是引发食物过敏的核心细胞,它通过三种方式发挥作用:
2. 治疗的新发现
口服免疫治疗(OIT)的研究显示:能够抑制TH2细胞的活动,减少过敏相关物质的产生,帮助建立对食物的耐受性。
3. 新发现的重要T细胞类型
最新研究发现Tfh13细胞在食物过敏中的重要作用,动物实验证明,这种细胞对产生高效过敏抗体必不可少,能直接影响过敏反应的强度。
注:Tfh13(滤泡辅助性T细胞13)是一种特殊的免疫细胞亚型,属于CD4+ T细胞家族。它在免疫反应中起着重要作用,尤其是在过敏反应和IgE抗体的产生过程中。
此外,还有TH2A细胞,这是一种特殊的记忆性T细胞,该细胞只在过敏人群中发现,其表面有特定标记物(CD161、CRTH2、CD49d)。发现该细胞不仅与食物过敏有关,还与其他过敏病相关,例如,湿疹、过敏性鼻炎、哮喘和食管炎。
4. T细胞的共同识别标记
研究人员通过CD154标记发现:花生过敏患者的T细胞有特殊特征,17%的特定序列在不同花生过敏患者中相同。这说明花生过敏可能有共同的免疫机制。
5. 调节性T细胞(Treg):过敏的“刹车系统”
Treg细胞是免疫系统的调节者,有两种来源:
动物实验显示,牛奶过敏小鼠经过治疗后:Treg细胞数量增加,产生更多保护性物质(IL-10和TGF-β)。
人类研究发现,鸡蛋过敏儿童成功治疗后:特定类型Treg细胞增加。与此同时,花生过敏治疗后:Treg相关基因活性增加。
T细胞在诊断和治疗方面应用潜力:
肥大细胞:驻扎在“人体边防”的过敏触发器
主要在身体的”边界”位置:皮肤、呼吸道、消化道。
研究发现:对胃肠道过敏患儿的活检发现,他们的胃部和结肠中,肥大细胞数量比健康孩子多(通过CD117和类胰蛋白酶标记检测)。
临床观察:在食物过敏患者的肠道检查中发现,过敏相关物质明显增加:
特定条件下可能缓解过敏
小鼠实验发现,肥大细胞表面有个“刹车开关”(FcγRIIb),能接收IgG抗体的“停战指令”,抑制过敏反应,这可能是未来治疗的关键靶点。
嗜碱性粒细胞:血液中的哨兵
基本特征:在血液中数量很少(仅占白细胞的0.5-1%),但在过敏反应中作用重要。
临床应用:可以通过流式细胞术(BAT)检测,使用CD63和CD203c作为标记,帮助诊断食物过敏,监测治疗效果。
治疗相关发现:口服免疫治疗(OIT)研究显示,成功治疗后:
小鼠实验发现:在 IgE-FA 的小鼠模型中,嗜碱性粒细胞耗竭减轻了腹泻的发生率,临床过敏反应减弱。同一项研究表明,嗜碱性粒细胞来源的 IL-4 对于肥大细胞募集和/或增殖至关重要。
临床意义:可以通过检测这两种细胞,判断过敏严重程度,评估治疗效果。
治疗方向:可以破坏 IgE-FA 中肥大细胞和嗜碱性粒细胞反应性的新型干预措施,可能代表未来研究的有吸引力的治疗靶点。
抗原呈递细胞(APCs):免疫系统的“情报分析员”
主要包括三类细胞:
抗原呈递细胞是如何工作的?
➤ 发现并捕获食物过敏原 → 分解成小片段(肽段) → 用MHC II分子“举牌”展示
➤ 指挥CD4+ T细胞分化成不同细胞(TH1/TH2/Treg等)
不同派系的树突状细胞:过敏派 vs 和平派
◈ 过敏派(CD209+树突状细胞)
锁定目标:锁定致敏蛋白,如花生、坚果等。
煽风点火:释放信号诱导T细胞变身TH2(分泌IL-4/IL-5/IL-13)
研究证据:
◈ 和平派(CD103+树突状细胞)
维稳专家:在小鼠肠道训练T细胞成为Foxp3+ Treg(分泌IL-10),有助于预防过敏。
制衡机制:表达诱导性T细胞共刺激配体(ICOS-L),促进“调解员细胞”生成。
树突状细胞功能的其他重要考虑因素包括共刺激分子如 CD80 和 CD86 等表达,它们是 CD28 的天然配体;这些分子与 T 细胞表达的 CD28 的相互作用受损可能导致激活减少或缺失,并最终导致 T 细胞无反应。
花生口服免疫治疗降低了APC上CD86的表达,尽管这些变化可能是暂时的。
诊断方面:通过分析树突状细胞的亚型特征和活化状态,可评估个体过敏风险等级,并预测潜在的过敏反应发生概率。
治疗突破:为过敏治疗开辟了新路径。
1)精准调控不同功能亚型DC的比例平衡;
2)靶向干预DC表面关键分子(如共刺激分子)的表达;
3)特异性增强具有免疫调节功能的DC活性。
总之,免疫系统的多个部分协同作用。
正常耐受状态是B细胞生产保护性抗体(IgA),调节性T细胞(Treg)担任”指挥”角色,共同抑制过度反应,防止肥大细胞引发过敏症状。
过敏状态TH2细胞过度活跃,产生大量致敏物质,指导B细胞产生过敏抗体(IgE)。多种免疫细胞被激活,包括肥大细胞、嗜碱性粒细胞、嗜酸性粒细胞等。受损的肠道细胞会释放:IL-25、IL-33、TSLP,这些物质进一步加重过敏反应。
成功的脱敏治疗会带来以下变化:
T细胞方面,抑制致敏T细胞(TH2)、增加调节性T细胞;
B细胞方面,增加保护性抗体(IgA和IgG4)、减少致敏抗体(IgE)。
来自人类和动物研究的越来越多的证据支持肠道微生态失调在食物过敏发展中的关键作用。
基于16S rRNA测序的研究发现,与没有食物过敏的儿童相比,患有食物过敏的儿童具有独特的肠道微生物组结构。
表. 在有和没有FA的小儿患者之间主要的肠道微生物组差异(基于16S-rRNA测序的研究)
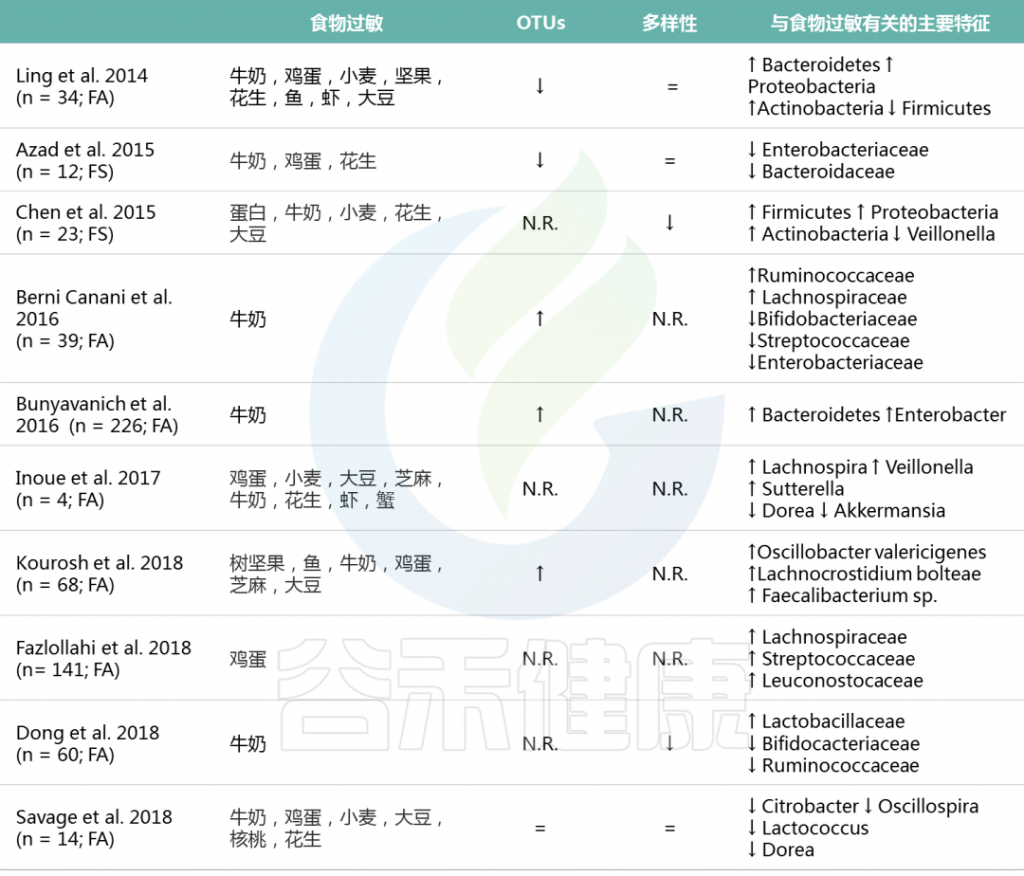
M.D.Costanzo et al, Int.J.Mol.Sci. 2020
FA:食物过敏; FS: 食物过敏; OTUs:操作分类单元; N.R.: 未报道过的; ↑ : 增加;↓: 减少; =: 不变.
表1中所有研究均调查了IgE介导的食物过敏。有趣的是,关于46例受非IgE介导的牛乳过敏(CMA)影响的患者的数据显示,与健康对照组相比,失调的菌群中拟杆菌Bacteroides (Bac 12) 和Alistipes丰富,IgE介导的CMA儿童的特征重叠,是从健康到IgE介导的CMA患者的拟杆菌逐渐增加。
在同一项研究中,患有非IgE介导的CMA的儿童的粪便中丁酸浓度明显低于健康人。
菌群失调先于食物过敏发作
来自人体研究的可用数据表明,菌群失调先于食物过敏发作。
Azad 等人研究发现,在婴儿早期肠道微生物组含量较低的情况下,肠杆菌科(Enterobacteriaceae) / 拟杆菌科(Bacteroidaceae)的比率增加和Ruminococcaceae的丰度较低与随后的食物敏感性相关,这表明早期肠道菌群失调对食物过敏的后续发展有促进作用。
此外,人类研究的可用数据表明,生命早期,尤其是生命的头6个月,微生物组构成与食物过敏的发展更为相关;
在出生后的前 6 个月内,在食物过敏儿童的肠道菌群中占比过高的菌如下:
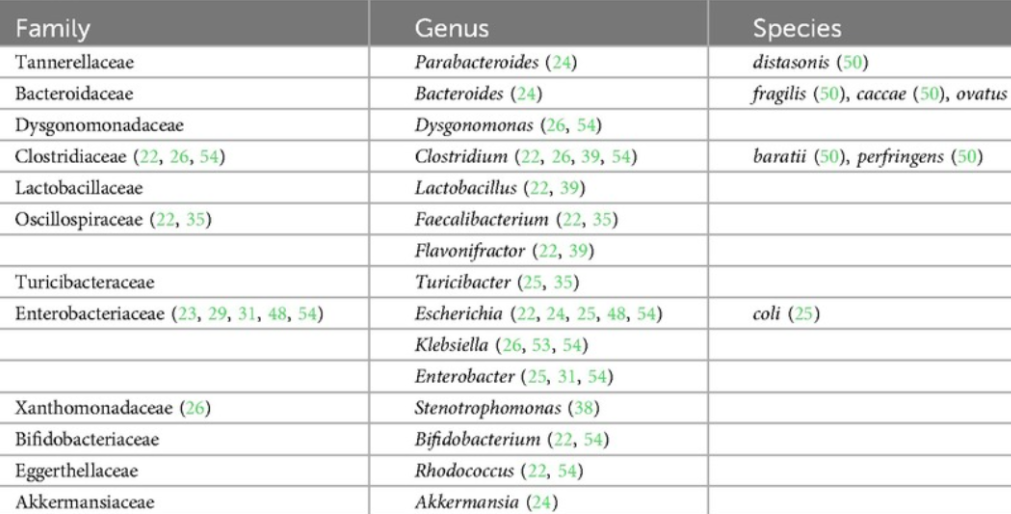
doi.org/10.3389/falgy.2024.1438252
在出生后的前 6 个月内,在食物过敏儿童的肠道菌群中缺乏的菌如下:
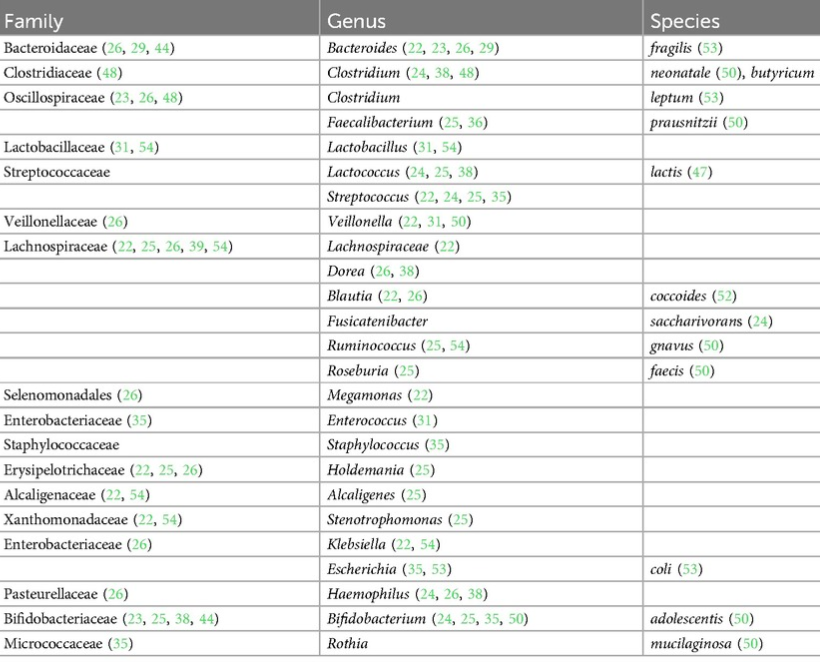
doi.org/10.3389/falgy.2024.1438252
▲ 有害菌增加:
肠杆菌等有害菌释放脂多糖(LPS)等毒素:
▼ 有益菌减少:
双歧杆菌、乳杆菌等能分解食物纤维,产生短链脂肪酸(如丁酸),这类物质:
调节免疫耐受
肠道菌群通过调节Tregs细胞的分化和功能,增强对食物抗原的耐受性。例如,梭菌和双歧杆菌能够通过其代谢产物(如SCFAs)和信号分子(如IL-10、TGF-β)促进Tregs的分化和增殖,从而抑制过敏反应。
肠道菌群还通过调节树突状细胞(DCs)的功能,影响免疫反应。例如,健康的肠道菌群能够使DCs产生TGF-β和视黄酸(RA),从而诱导Tregs的分化。
共生菌介导免疫耐受
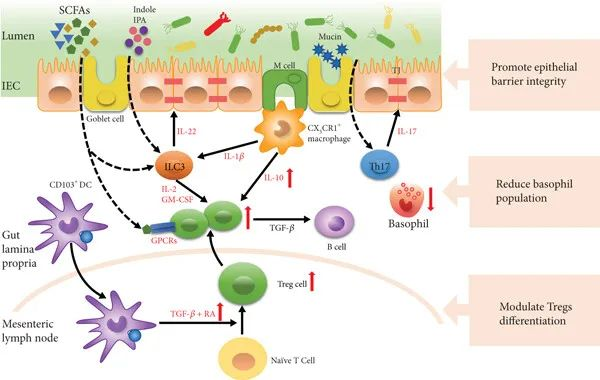
doi.org/10.1155/2023/9575410
增强肠道屏障功能
肠道菌群通过产生短链脂肪酸(如丁酸)和色氨酸代谢产物(如吲哚)来增强肠道上皮屏障的完整性。这些代谢产物能够促进黏液分泌和紧密连接蛋白的表达,从而防止食物抗原进入血液循环,减少过敏反应的发生。
例如,丁酸能够通过诱导IL-22的产生,增强肠道上皮细胞的屏障功能,减少过敏原的渗透。
调节过敏效应细胞
肠道菌群能够调节过敏效应细胞(如嗜碱性粒细胞)的数量和功能。例如,抗生素处理或无菌小鼠的嗜碱性粒细胞数量增加,而补充益生菌可以减少这些过敏效应细胞的数量,从而减轻过敏症状。
关于肠道菌群的干预措施,我们将在06章节详细阐述。
IgE-食物过敏的诊断依赖于临床病史和过敏试验的结合,如食物特异性IgE的存在。诊断指南和标准临床实践在国际上各不相同。这些差异主要是由于多种方法可用于评估IgE-FA;这些方法在灵敏度、特异性、成本、时间和可及性方面各不相同。准确的诊断对于防止不必要的食物避免和提供及时和适当的治疗建议至关重要。
金标准
双盲安慰剂对照食物激发试验(DBPCFC)是最可靠的确诊方法。由于12.9%的试验可能出现安慰剂反应,其准确性优于非盲法试验。
确定IgE对给定食物致敏的两种主要方法是:
体内皮肤点刺试验(SPT)
操作:将微量食物(新鲜的或更常见的作为提取物)刺入皮肤表层
判读标准:15-20分钟后,检查皮肤刺痛部位,若出现比阴性对照大3mm以上的红肿包块(因肥大细胞释放组胺所致)即为阳性。
编辑
血清特异性IgE(sIgE)
sIgE测定定量外周血中存在的过敏原特异性IgE的量。
传统标准:≥0.35 kU/L为阳性
新型检测:临界值可低至0.1 kU/L
注意:两项检测结果必须谨慎解释,均需结合症状分析,因可能出现”致敏但无过敏反应”的假阳性。
检测结果优化策略:
使用较大的SPT包块直径或较高的sIgE临界值可增加临床反应性的可能性,但这是以牺牲敏感性为代价的。
组合检测优势:
对1247例食物激发试验数据分析显示:
SPT+sIgE联合检测或sIgE/总IgE比值(sIgEr)
的阳性预测值显著优于单项检测。
应用价值:在临床试验等场景中可替代部分激发试验,但仍需更多验证。
现存挑战:许多具有临床相关IgE-FA的患者的SPT和/或sIgE值可能低于已发表的临界值,强调需要更稳健的诊断方法来取代口服食物激发试验。
食物过敏检测升级版:成分检测与表位检测有什么用?
除了常规的皮肤点刺、抽血验IgE,医生手里还有两把更精细的“放大镜”——成分检测和表位检测。它们能帮你区分“假警报”和“真危险”,甚至预测过敏反应有多严重。
成分检测:锁定过敏食物里的“关键蛋白质”
原理:
食物过敏其实是对其中某些蛋白质过敏。比如花生含有Ara h1、Ara h2等多种蛋白质,成分检测(CRD)可以单独测出你对哪一种蛋白质过敏。
实际用途:
区分“花粉过敏连带反应”和“真过敏”。
比如有人吃花生过敏,但检测发现只对Ara h8蛋白敏感,这通常是因为它和桦树花粉蛋白相似,属于“交叉反应”(可能症状轻微,比如口腔发痒)。
但如果对Ara h1/2/3敏感,则是真正的花生过敏,严重时可能引发全身反应。
预判过敏风险高低
研究证实:对花生中的Ara h2蛋白过敏的人,严重过敏风险更高;而另一种Ara h6蛋白(与Ara h2结构相似)阳性,也可能指向真实过敏。

表位检测: 看清IgE攻击的“精确靶点”
原理:如果把过敏蛋白比作一根长绳,表位就是绳子上被IgE抗体“咬住”的具体位置(分线性和构象两种结构)。表位检测能识别这些关键攻击点,帮助判断过敏是否会长期存在或容易引发严重反应。
在花生过敏的儿童和成人中,针对花生过敏的BBEA表位检测法(检测Ara h2蛋白的两个线性表位):灵敏度92%,特异性94%,准确度碾压常规检测:比皮肤点刺、普通IgE检测更准。
另一个相关的体液测试是 过敏原特异性IgG4
IgG4抗体通过充当阻断抗体而在IgE-FA中具有保护作用。一项研究发现,花生致敏但临床耐受或花生过敏并接受OIT治疗的儿童的血浆能够抑制花生诱导的肥大细胞活化。重要的是,当血浆中的IgG4耗尽时,肥大细胞的活化不能完全恢复。
但是目前需要进一步的研究来更全面地了解IgG4单独或与其他生物标志物结合在食物过敏诊断和/或预后中的作用。
编辑
诊断方法仍然主要限于研究环境,包括嗜碱性粒细胞活化试验(BAT)和肥大细胞活化试验(MAT)。
BAT与MAT的优劣对比:
BAT和MAT都是基于体外流式细胞术的实验室检测,用于测量过敏原刺激后活化标志物的表达。
BAT检测(嗜碱性粒细胞活化试验)
需要采集新鲜血液立即检测。
BAT在诊断IgE-食物过敏时的特异性高于SPT和sIgE水平,在花生过敏中的特异性为98%,灵敏度为75%。
但存在15%人群天生对检测无反应。
MAT检测(肥大细胞活化试验)
可用冷冻血清来激活培养的原代人血源性肥大细胞。
在花生过敏诊断中比BAT更准确。
重复检测结果高度一致(组内相关性:MAT 0.96 VS BAT0.43)。
新的诊断方法包括:
评估食物过敏原特异性B和T细胞
外周血中的过敏原特异性B和T细胞由于其稀缺性而历来难以分离。由于技术的进步,这些罕见的细胞现在可以通过几种方法来识别。
关于T细胞,这些方法包括:
a)用所选抗原或肽体外刺激PBMC,然后通过表达特异性活化标志物经由流式细胞术鉴定活化的T细胞;
b)用重组肽-MHC(pMHC)复合物离体染色T细胞。pMHC四聚体或多聚体技术也可用于鉴定变应原特异性B细胞。
多组学研究
包括基因组学、表观基因组学、转录组学、蛋白质组学、代谢组学、微生物组学和免疫组学在内的组学科学有望成为研究过敏性疾病(包括IgE-FA)的高通量方法。需要多组学方法来全面识别生物标志物,如基因,蛋白质和/或代谢产物,可以提高IgE-食物过敏诊断和预后的准确性。
此外,非常需要鉴定可预测IgE-食物过敏反应严重程度的生物标志物。特别令人感兴趣的是血小板活化因子乙酰水解酶(PAF-AH)。之前的研究已经证实,PAF-AH可以通过灭活PAF来预防过敏级联反应的进展。
肠道菌群检测
通过高通量测序技术获得菌群组成和功能数据,结合机器学习模型(如随机森林、神经网络)识别过敏相关特征。肠道菌群检测报告菌群失衡程度、关键菌群丰度及代谢物水平,提示过敏风险。
干预后复查菌群,观察过敏症状是否缓解,验证菌群与过敏的因果关系。
该方法是非侵入性的,且可以早期预警,因为很多时候菌群失衡可能早于过敏症状出现。通过个性化干预,指导益生菌、膳食调整等精准治疗。
肠道菌群检测可作为食物过敏的辅助诊断工具,为个性化治疗提供依据。可以结合临床传统方法(如食物激发试验)综合判断,通过连续检测评估过敏风险和干预效果,整合IgE检测、皮肤点刺试验和菌群数据,提高准确性。
1. 当前的食物过敏治疗方式
目前,食物过敏没有治愈方法,治疗的核心是避免接触过敏原。如果意外接触导致过敏反应,通常使用肾上腺素和抗组胺药进行处理。
由于食物过敏带来的严重健康和经济负担,科学界投入了大量资源研究新的治疗方法。
2. 预防的转变:从回避到早期接触
过去建议高过敏风险的婴儿(如父母有过敏史)避免接触过敏性食物,比如花生。
但后来研究发现,在婴儿早期引入过敏性食物(如花生)反而可以降低过敏风险。这项发现改变了过敏预防的建议,也激发了对免疫疗法的研究热情。
3. 免疫疗法的探索
免疫疗法的目标是通过逐步改变免疫系统的反应,让身体对过敏原“习惯”并耐受。方法包括:
其中,口服免疫疗法(OIT)效果最好,但也存在风险。比如,患者可能会出现轻微不适(如口痒、肚子痛),甚至更严重的过敏反应(如全身性过敏或嗜酸性食管炎)。
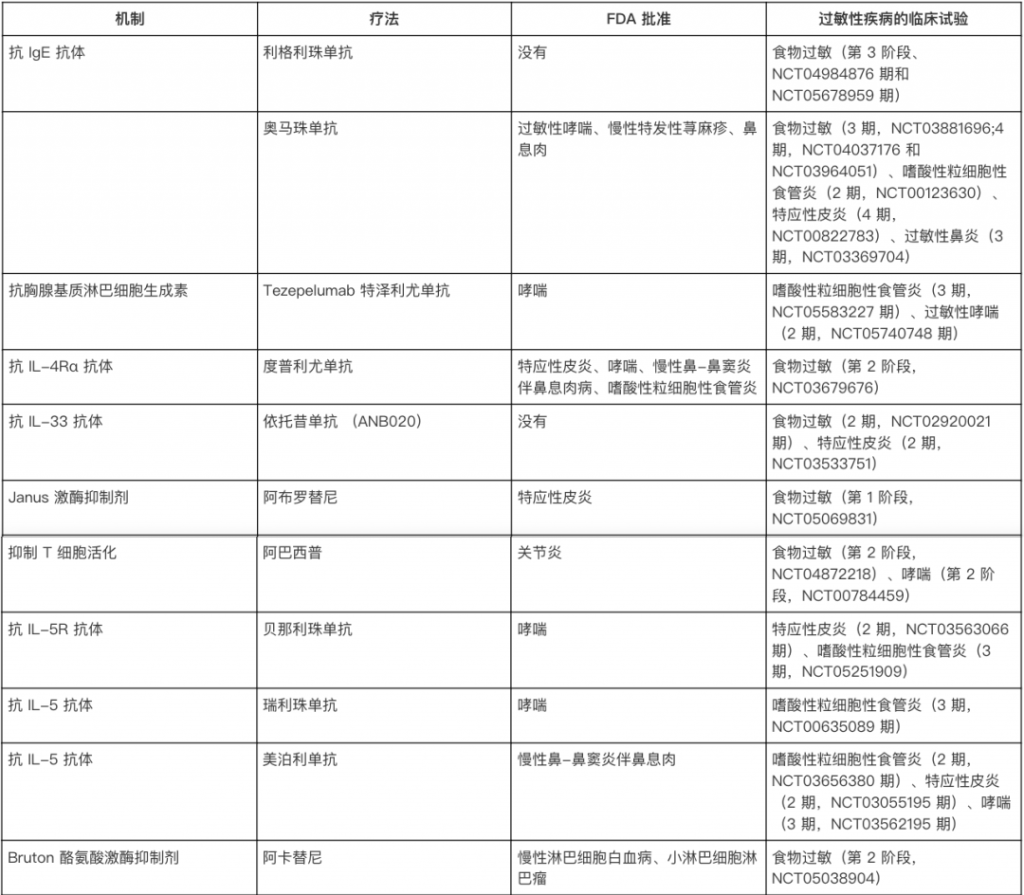
doi.org/10.1146/annurev-immunol-090122-043501
4. 辅助治疗:提高疗效,减少副作用
为了让免疫疗法更安全有效,科学家正在研究辅助治疗:
此外,新的治疗IgE-FA包括疫苗、纳米颗粒、Janus激酶(JAK)和布鲁顿的酪氨酸激酶抑制剂。
5. 基于微生物群的干预
研究发现,肠道中的某些细菌和它们的代谢产物(如丁酸盐)可以调节免疫系统,帮助身体更好地耐受过敏原。下列措施可以在调节肠道菌群的基础上干预食物过敏。
饮 食
增加膳食纤维
高纤维饮食(如全谷物、蔬菜、水果)可促进双歧杆菌、乳酸菌等有益菌增殖,增加短链脂肪酸的生成,抑制促过敏的Th2免疫反应。
举例:
菊粉(如洋葱、大蒜):增加双歧杆菌。
果胶(如苹果、柑橘):改变厚壁菌门与拟杆菌门的比例,增加血清和粪便中SCFA的含量,并通过损害树突状细胞功能来预防炎症的发展。
高纤维摄入通过重塑肠道微生物群和增加SCFA水平,特别是乙酸盐和丁酸盐水平,保护小鼠免受花生过敏。此外,这种保护作用取决于SCFA的受体GPR43和GRP109A,因为缺乏其中一种的小鼠表现出更严重的食物过敏。
减少高脂高蛋白饮食
过多动物蛋白和脂肪可能促进拟杆菌属等菌群占优,增加炎症风险,间接诱发过敏。建议适量摄入,平衡植物蛋白(如豆类)。
高脂饮食诱导的肠道菌群变化也被证实可以诱导食物过敏。
一项研究显示,高脂饮食通过增加Ruminococcaceae(梭菌目)、Desulfovibrionaceae(δ-变形菌纲)和Rikenellaceae(拟杆菌纲)的相对丰度,同时减少Muribaculaceae和Prevotellaceae的丰度来诱导食物过敏。
增加优质脂肪
ω-3脂肪酸,ω-3主要来自海洋来源(如鱼油、藻类)和某些植物(如亚麻籽):通过抑制树突状细胞(DCs)的激活、抑制CD4 T细胞的增殖和活化、减少促炎因子、降低IgE水平以及抑制肥大细胞脱颗粒,从而减轻食物过敏。
增加膳食多酚
多酚是次生植物代谢产物,富含水果、蔬菜、谷物、咖啡和茶。非结合多酚通过肠道菌群调节、紧密连接蛋白表达和 β-防御素分泌来缓解食物过敏。
可可多酚:
研究表明,富含可可多酚的饮食可以减少厚壁菌门和变形菌门,增加Tenericutes和蓝藻门(Cyanobacteria),从而抑制特定抗体和肠道IgA的合成,有助于减少过敏反应。
矢车菊素-3-O-葡萄糖苷(Cyanidin-3-O-glucoside):
通过增加有益菌(如乳酸杆菌和Odoribacter)和减少有害菌(如幽门螺杆菌和Turicibacter)来上调紧密连接蛋白的表达,促进分泌型IgA和β-防御素的分泌,并平衡Th1/Th2水平,有助于增强肠道屏障功能,减少过敏原的渗透,从而减轻食物过敏症状。
槲皮素(Quercetin):
槲皮素具有抗氧化、抗炎和抗癌活性。它可以通过与卵清蛋白(OVA)结合,减少OVA的致敏性,并降低特异性免疫球蛋白水平,从而减轻过敏反应。
咖啡酸和表儿茶素没食子酸酯(Epigallocatechin-3-gallate, EGCG):
与乳清蛋白结合后,可以减轻乳清蛋白引起的口服致敏反应,降低小鼠血清中特异性抗体和mMCP-1水平,并减少体外CD4 T细胞的增殖,有助于减少乳清蛋白引起的过敏反应。
益生菌
双歧杆菌(Bifidobacterium)
乳杆菌(Lactobacillus)
丁酸梭菌(Clostridium butyricum)
混合益生菌
注意:
益生元
通过特定益生元干预食物过敏的机制主要是调节肠道菌群,促进短链脂肪酸生成,抑制过敏相关炎症反应。以下为具体益生元及研究证据:
临床试验显示,补充该组合可显著降低高风险婴儿食物过敏发生率,可能与促进双歧杆菌生长有关。
2’-岩藻糖基乳糖(2’-FL)和乳糖-N-新四糖(LNnT):添加到配方奶粉中可缓解牛奶蛋白过敏(CMA),降低IgE水平和炎症因子(如IL-4、IL-6)。
乳-N-岩藻五糖III(LNFP III):摄入量高的婴儿CMA风险更低。
动物实验表明,母体补充可诱导免疫耐受,降低后代小麦过敏风险。
多不饱和脂肪酸(PUFA)等可能减少儿童食物致敏风险。
合生元
合生元是一种包含活菌(益生菌)和宿主微生物选择性利用的底物(益生元)的混合物,能够为宿主带来健康益处。
在一项多中心随机对照试验(RCT)中,研究了含有短双歧杆菌M-16V和低聚果糖(scGOS/lcFOS)的氨基酸配方(AAF-S)对IgE介导的牛奶过敏(CMA)婴儿的安全性。
结果显示,与普通氨基酸配方(AAF)相比,AAF-S在控制过敏症状和促进正常生长方面同样有效,但在减少感染、用药次数和住院率方面效果更好。具体数据如下:AAF-S组婴儿的感染发生率显著降低、使用的药物更少、住院率显著降低(8.8% vs. 20.2%,p = 0.036)。
粪便微生物组分析显示,AAF-S组婴儿的双歧杆菌丰度显著增加,而Eubacterium rectale和C. coccoides的丰度显著降低。
代谢产物变化:AAF-S组婴儿的粪便中乙酸和L-乳酸水平显著升高,粪便pH值显著降低。
粪菌移植
最近,一项小鼠模型研究表明,FMT抑制了特应性皮炎小鼠中OVA诱导的过敏反应。
除了恢复肠道微生物群外,FMT还降低了IgE水平;受监管的Tregs;肥大细胞、嗜酸性粒细胞和嗜碱性粒细胞减少;提高了SCFA的含量;恢复Th1/Th2平衡。
与其他方法相比,FMT是一种相对简单的治疗策略,可以改变人体肠道微生物群;然而,迄今为止,这项研究还不够充分,需要开展大量工作来提高我们对用FMT治疗食物过敏的理解。
中草药
中药因其低成本、高安全性以及高生物活性,近年来在食物过敏治疗中受到越来越多的关注。虽然传统中医中没有“食物过敏”的具体术语,但一些中药方剂在现代研究中显示出对食物过敏的潜在治疗效果。
食物过敏草药配方-2(FAHF-2):
来源:FAHF-2是从传统的“乌梅丸”(Wu Mei Wan)中开发而来的。
临床研究:在一项多中心、双盲、随机、二期临床试验中,68名12-45岁的食物过敏患者每天三次服用FAHF-2或安慰剂,持续六个月。结果显示,FAHF-2安全且耐受性良好。
免疫调节作用:FAHF-2能够显著抑制外周血单个核细胞(PBMCs)产生的IL-5,并增加IL-10和调节性T细胞(Tregs)的生成,显示出良好的免疫调节效果。
改进形式:由于FAHF-2的剂量较大,研究者开发了两种改进形式:丁醇纯化的FAHF-2(BF2)和乙酸乙酯及丁醇纯化的FAHF-2(EBF2)。在花生过敏的小鼠模型中,EBF2显示出很强的抑制IgE产生的能力,被认为是对花生过敏最有潜力的治疗药物。
尽管中药在治疗过敏性疾病中被广泛应用,但关于食物过敏的临床研究样本量小,且研究受限,需要进一步验证中药在食物过敏治疗中的效果。
从概念上讲,人类食物供应中的任何蛋白质都可能是潜在的过敏原,因此建立“无过敏原食品”体系不现实。由于不同个体的免疫系统对相同的过敏原可能会有不同的反应,因此很难对食物过敏做出普遍适用的定义。
现有诊断工具(如特异性IgE检测)可靠性有限,过敏原结构、加工方式及食物基质相互作用均影响致敏性。
引起个体过敏反应所需的最小量(阈值)也取决于个体的敏感性。大多数过敏性食物的阈值尚未确定,导致警示标签(如“可能含”)难以精准保护敏感人群。 需开发特异性强、灵敏度高的检测方法,并基于主要过敏食物(如牛奶)建立分级阈值标准——从鉴定关键过敏原及其表位入手,明确检测目标。
肠道菌群可能通过调节免疫耐受影响过敏风险。未来可探索菌群检测(如特定菌群丰度与过敏表型关联)作为辅助诊断工具,或通过益生菌等多种干预手段重塑菌群平衡,降低致敏性。
协同策略:
整合免疫学、微生物组学与食品加工技术,推动从“一刀切”警示转向动态风险评估,实现过敏防控的精准化与人性化。
注:本账号内容仅作交流参考,不作为诊断及医疗依据。
主要参考文献:
Iweala OI, Nagler CR. The Microbiome and Food Allergy. Annu Rev Immunol. 2019 Apr 26;37:377-403.
Januszkiewicz, Emilia, et al. “The importance of the gut microbiome in the development of allergic diseases.” Alergologia Polska-Polish Journal of Allergology 10.3 (2023): 202-209.
Venter, Carina. “Immunonutrition: Diet diversity, gut microbiome and prevention of allergic diseases.” Allergy, Asthma & Immunology Research 15.5 (2023): 545.
Jiachen Liang, Baodong Zheng, Yi Zhang, Hongliang Zeng, Food allergy and gut microbiota, Trends in Food Science & Technology, Volume 140, 2023, 104141, ISSN 0924-2244
Farnetano M, Carucci L, Coppola S, Oglio F, Masino A, Cozzolino M, Nocerino R, Berni Canani R. Gut microbiome features in pediatric food allergy: a scoping review. Front Allergy. 2024 Sep 25;5:1438252.

谷禾健康

微生物学作为一门研究微生物及其与环境、宿主和其他生物相互作用的科学,涵盖了广泛的学科领域和专业术语。然而,由于微生物学的快速发展和跨学科融合,许多术语的定义和使用在不同领域中可能存在差异甚至混淆。
随着新冠疫情的全球蔓延,越来越多的人开始关注微生物知识,但专业的微生物学术语往往让普通大众感到困惑和难以理解。因此一个通俗易懂的微生物学词汇表可以搭建一座连接专业知识与公众理解的桥梁。
本文借助前人的整理增编和归纳整理和科普微生物学术语与定义,合理解释微生物学词汇,帮助人们更好地理解与微生物相关的知识,让每个人都能够在这个充满微生物的世界中做出更明智的生活选择。
微生物既是我们的朋友也是敌人,需要我们正确认识和对待。
本文列举的术语总览如下:


肠道微生物领域词汇
1、肠道微生物群
(gut microbiota)
肠道微生物群是指生活在人体肠道内的庞大微生物群体,包括细菌、古菌、真菌、病毒等多种微生物。它们与宿主(人体)之间形成了一个复杂的共生生态系统。
2、肠道微生物组
(gut microbiome)
肠道微生物组是指生活在人体肠道内的微生物群体及其基因组的总称。这些微生物包括细菌、真菌、病毒等,它们的遗传物质和代谢产物共同构成了一个复杂的生态系统。
3、益生菌
(Probiotics)
活的微生物,当摄入足够量时,对宿主健康有益。
4、益生元
(Prebiotics)
一种不可消化的食物成分,能够选择性地刺激肠道有益菌的生长。
5、共生菌
(Symbiotic Bacteria)
与宿主互利共生的肠道微生物。它们为宿主提供营养物质或保护作用,同时从宿主获取生存所需物质,在维持生态平衡中发挥重要作用。
6、致病菌
(pathogenic bacteria)
致病菌是引起疾病的细菌,也称为病原菌。当它进入身体时,就会破坏细胞或干扰身体的正常活动,人可能会患上轻微疾病或致命疾病。
7、肠道屏障
(Intestinal Barrier)
肠道屏障是由肠道上皮细胞及其紧密连接、黏液层、免疫系统等组成的复合防御系统,具有选择性通透功能,可阻止有害物质进入机体,同时允许营养物质吸收,是维持肠道健康的重要屏障。
8、菌群失调
(dysbacteriosis)
菌群失调是指肠道微生物群落的平衡被打破,导致微生物群落组成、多样性和功能发生显著改变的状态。
9、肠道微生物代谢产物
(Microbial Metabolites)
肠道微生物代谢产物是肠道菌群在代谢过程中产生的活性物质,主要包括短链脂肪酸、次级胆汁酸、色氨酸代谢物等。这些物质参与宿主能量代谢、免疫调节和生理功能维持,是肠道菌群影响宿主健康的重要媒介。
10、短链脂肪酸 (SCFA)
(Short-Chain Fatty Acids)
肠道菌群发酵产生的重要代谢产物,包括乙酸盐、丙酸盐、丁酸盐,具有免疫调节功能。
11、紧密连接蛋白
(Tight Junction Protein)
紧密连接蛋白是上皮和内皮细胞之间形成紧密连接的关键蛋白质复合物,是细胞屏障功能的重要组成部分。
12、大肠杆菌
(Bacterium Coli (E. coli))
大肠杆菌是人和动物肠道中最常见的革兰氏阴性菌,多数株系与宿主和谐共生,参与维生素合成和免疫调节,但某些致病性菌株(如肠出血性大肠杆菌O157:H7)可引起严重疾病,包括腹泻等。它也是重要的模式生物,广泛应用于科学研究。
13、拟杆菌门
(Bacteroidetes)
一种常见于人类肠道细菌,革兰氏染色阴性、无芽孢、专性厌氧的小杆菌。具有强大的多糖降解能力,可分解复杂碳水化合物,参与宿主营养代谢和免疫系统调节,与多种疾病的发生发展相关。
14、厚壁菌门
(Firmicutes)
细菌界中一个重要的门类,其特征是细胞壁含有大量肽聚糖,形成厚实的细胞壁结构。部分是重要的益生菌,对宿主健康有益;也包含一些致病菌,如产气荚膜梭菌。
15、脆弱拟杆菌
(Bacteroides Fragilis)
一种常见于人类肠道的细菌,具有降解复杂多糖、维持免疫系统平衡的功能。它是人体肠道微生物组的优势菌种之一,但在特定条件下也可能致病,引起腹腔感染等疾病。
16、金黄色葡萄球菌
(Staphylococcus aureus)
指的是金黄色葡萄球菌,一种致病性细菌,以引起各种感染而闻名。包括皮肤感染、食物中毒、肺炎等,且易产生耐药性,是临床上重要的致病菌。
17、变形菌门
(Proteobacteria)
细菌界最大的细菌门类之一,主要为革兰氏阴性菌。包括大肠杆菌、沙门氏菌等重要菌属,在自然界分布广泛,在生态系统和人类健康中发挥重要作用。其成员在营养循环、共生关系和致病性方面具有重要意义。
18、炭疽杆菌
(Bacillus Anthracis)
引起炭疽的细菌。炭疽杆菌是革兰氏阳性、非运动、兼性厌氧、孢子形成和杆状细菌。是一种人畜共患病的病原体,是一种专性病原体,因为细菌的繁殖周期只发生在合适的宿主中。
19、鼠疫耶尔森菌
(Yersinia pestis)
鼠疫耶尔森菌是一种小型、非运动的革兰氏阴性细菌,属于肠杆菌科。鼠疫耶尔森氏菌是鼠疫的病原体,鼠疫是一种罕见但高度致命的人畜共患病。
20、芽孢杆菌
(Bacillus)
一类革兰氏阳性、能形成芽胞的细菌。包括枯草芽胞杆菌、蜡样芽胞杆菌等重要种类,广泛应用于工业发酵、生物制品生产和益生菌制备。多数种类对人体无害。
21、蜡样芽孢杆菌
(Bacillus Cereus)
一种可引起食物中毒并与胃肠道疾病有关的细菌。
22、枯草芽孢杆菌
(Bacillus Subtilis)
一种常见的土壤细菌,常用作实验室研究的模式生物。
23、多粘芽孢杆菌
(Bacillus Polymyxa)
一种以其在固氮和土壤健康中的作用而闻名的细菌。
24、嗜热脂肪芽孢杆菌
(Bacillus Stearothermophilus)
一种用作指示生物的嗜热细菌,用于测试灭菌过程的有效性。
25、类霉菌芽孢杆菌
(Bacillus Mycoides)
一种以其在土壤健康中的作用及其独特的菌落形态而闻名的细菌。
26、不动杆菌
(Acinetobacter)
一类革兰氏阴性菌,广泛分布于自然界,具有强大的环境适应能力。其中最著名的是鲍曼不动杆菌。
27、鲍曼不动杆菌
(Acinetobacter baumannii)
一种革兰氏阴性菌,以其在医院获得性感染和多重耐药性中的作用而闻名。
28、16S rRNA
16S rRNA 代表16S核糖体核糖核酸 (rRNA),其中S(Svedberg) 是测量单位(沉降率)。该rRNA是原核核糖体小亚基(SSU)以及线粒体和叶绿体的重要组成部分。
29、宏基因组
(Metagenome)
宏基因组是指特定环境中全部微生物基因组的总和,包括可培养和未可培养微生物的全部遗传信息。它是环境微生物群落的基因总库,反映了特定环境中微生物的整体遗传特征。
微生物领域基础名词
30、琼脂
(Agar)
从红藻类中提取的多糖类物质,具有独特的凝胶特性:在热水中溶解,冷却后形成凝胶。它是细菌培养的重要基质,在微生物学研究中不可或缺,其稳定性和不被多数微生物降解的特点使其成为理想的培养基材料。
31、琼脂糖
(Agarose)
从琼脂中提取的多糖,用于凝胶电泳分离核酸。
32、氨基酸
(Amino Acid)
氨基酸是含有氨基(-NH2)和羧基(-COOH)的有机化合物,是蛋白质的基本组成单位。根据人体是否能合成可分为必需和非必需氨基酸。它们不仅是构建蛋白质的基石,还参与多种生理过程,如神经递质合成、能量代谢等。
33、厌氧
(Anaerobic)
指在没有氧气存在的情况下发生的环境或过程。
34、厌氧菌
(Anaerobes)
在缺氧环境中生长的微生物。
35、抗生素
(Antibiotic)
一类能够抑制或杀死微生物的药物,包括天然和人工合成的化合物。它们通过多种机制发挥作用,如抑制细胞壁合成、干扰蛋白质合成等。在治疗细菌感染方面发挥重要作用,但滥用会导致细菌耐药性。
36、需氧
(Aerobic)
指需要氧气才能生存或生长的过程或生物体。
37、需氧菌
(Aerobes)
需要氧气才能生长的微生物。
38、耐酸
(Acid-Fast)
耐酸性是微生物在酸性环境中生存的能力,通过细胞膜适应、质子泵系统等机制维持细胞内pH平衡。这一特性在食品安全和发酵工业中具有重要意义,也是筛选胃肠道益生菌的关键指标。
39、嗜酸菌
(Acidophiles)
在酸性环境中生长的微生物。
40、抗菌剂
(Antiseptic)
抑制微生物在活组织上生长的物质。
41、无菌技术
(Aseptic Technique)
用于防止实验室工作中微生物污染的程序。
42、减毒
(Attenuation)
降低病原体毒力的过程,常用于疫苗开发。
43、高压灭菌器
(Autoclave)
一种使用高压蒸汽对设备和介质进行灭菌的装置。
44、琼脂平板
(Agar Plate)
装满琼脂培养基的培养皿,用于培养和分离微生物。
45、琼脂斜面
(Agar Slant)
一种琼脂培养基,以一定角度在试管中固化,用于培养细菌。
46、变形虫
(Amoeba)
一种形状灵活的原生动物,以其用于运动和进食的伪足而闻名。
47、无性生殖
(Asexual Reproduction)
没有配子融合的生殖,常见于细菌和某些真菌。
48、抗菌剂
(Antimicrobial)
杀死或抑制微生物生长的物质。
49、抗菌素耐药性
(Antimicrobial Resistance)
微生物抵抗药物作用的能力,一旦杀死或抑制它们。
50、α溶血
(Alpha Hemolysis)
是细菌在血琼脂平板上形成的部分溶血现象,表现为菌落周围出现绿色环。这是由于细菌将红细胞中的血红蛋白氧化成高铁血红蛋白所致。草绿色链球菌和肺炎链球菌是典型的α溶血菌,这一特征在细菌鉴定和临床诊断中具有重要意义。
51、粘附
(Adhesion)
微生物附着于宿主细胞或表面的能力。
52、非典型细菌
(Atypical Bacteria)
不符合标准分类系统的细菌,如支原体或衣原体。
53、乙酸杆菌属
(Acetobacter)
一个已知的将乙醇转化为乙酸(醋生产)的细菌属。
54、抗菌肽
(Antimicrobial Peptides)
由生物体产生的短蛋白质,可杀死或抑制微生物的生长。
55、阿米巴病
(Amebiasis)
一种由溶组织内阿米巴(一种原生寄生虫)引起的感染。
56、节肢动物媒介
(Arthropod Vector)
能够传播病原体的节肢动物,包括蚊虫、蜱类、跳蚤等。它们在多种传染病的传播中起关键作用,如蚊虫传播疟疾和登革热,蜱传播莱姆病。在公共卫生领域,对节肢动物媒介的监测和控制是预防相关传染病的重要手段。
57、藻类
(Algae)
水中的简单光合生物,其中一些可产生影响人类健康的毒素。
58、抗原转换
(Antigenic Shift)
一种剧烈的病毒抗原变异,主要发生在流感病毒中。它通过不同病毒亚型之间的基因重排,产生全新的抗原类型。这种变异可导致人群普遍缺乏免疫力,具有引发流感大流行的潜在风险。
59、抗原漂移
(Antigenic Drift)
病毒基因发生点突变导致的渐进性抗原变异,主要见于流感病毒。这种变异通过RNA复制过程中的错误逐步积累,造成病毒表面蛋白的微小改变。它是季节性流感发生的主要原因,也是每年需要更新流感疫苗的原因。与抗原转换相比,抗原漂移的变化较小但更为频繁。
60、琼脂糖凝胶电泳
(Agarose Gel Electrophoresis)
用于基于大小和电荷分离核酸的技术。
61、过敏原
(Allergen)
能引起机体产生过敏反应的物质,通常是蛋白质。主要包括食物过敏原(如花生、海鲜)、吸入性过敏原(如花粉、尘螨)和接触性过敏原(如某些金属)等。它们通过刺激机体产生IgE抗体,引发肥大细胞脱颗粒等一系列免疫反应。
62、脓肿
(Abscess)
一种局限性化脓性炎症,特征是组织液化坏死形成充满脓液的腔隙。主要由细菌感染引起,最常见的致病菌是金黄色葡萄球菌。临床表现为局部红肿热痛,可触及波动感,严重时可出现发热等全身症状。治疗原则是及时切开引流,配合适当的抗生素治疗和局部护理。
63、放线菌
(Actinomycetes)
一组革兰氏阳性的丝状细菌,在土壤生态学和抗生素生产中很重要。
64、抗微生物治疗
(Antimicrobial Therapy)
使用针对微生物的药物治疗感染。
65、营养菌
(Auxotroph)
需要其野生型对应物不需要的额外营养的微生物。
66、两性霉素B
(Amphotericin B)
一种用于治疗全身真菌感染的抗真菌药物。通过与真菌细胞膜中的甾醇结合,破坏膜的通透性来发挥杀菌作用。
67、曲霉菌属
(Aspergillus)
曲霉是一类常见的丝状真菌,广泛分布于自然环境中。某些种类可引起人体感染,造成曲霉病;另一些种类在食品发酵、酶制剂生产等工业领域具有重要应用价值,如黄曲霉、黑曲霉等。
68、无形体
(Anaplasma)
革兰氏阴性、专性细胞内细菌,主要通过蜱叮咬传播给人类,引起人粒细胞无形体病(HGA)。感染后常见症状包括发热、寒战、头痛、肌肉酸痛等。
69、杀螨剂
(Acaricide)
一种用来杀死螨和蜱的化学药剂。
70、防腐技术
(Antiseptic Technique)
用于防止无菌环境污染的方法。
71、气生菌丝
(Aerial Hyphae)
真菌的丝状结构,长出培养基表面。
72、乙酰化
(Acetylation)
蛋白质或核酸的化学修饰,可影响其功能和相互作用。
73、黄曲霉毒素
(Aflatoxin)
由某些真菌产生的一种真菌毒素,可污染食品和饲料。
74、变形虫运动
(Amoeboid Movement)
细胞通过伪足的伸展而运动。
75、虫媒病毒
(Arbovirus)
一种由节肢动物传播的病毒,如蚊子或蜱。
76、抗菌剂
(Antiseptic)
通过抑制活组织上微生物的生长来防止感染的物质。
77、抗菌谱
(Antimicrobial Spectrum)
受抗菌剂影响的微生物范围。
78、抗菌肽
(Antimicrobial Peptides)
通过破坏微生物膜在先天免疫中发挥作用的小蛋白质。
79、抗生素敏感性测试
(Antibiotic Susceptibility Testing)
用于确定抗生素对特定细菌的有效性的程序。
80、酸性染料
(Acidic Dye)
是一类带负电荷的染料,分子中含有酸性基团(如-SO3H, -COOH)。它们通过静电相互作用与组织中的碱性物质结合,主要用于染色碱性细胞结构。常见的酸性染料包括伊红、酸性品红等,在组织学和细胞学染色中广泛应用。
81、抗病毒药物
(Antiviral Drug)
通过抑制病毒复制来治疗病毒感染的药物。
82、阿米巴痢疾
(Amoebic Dysentery)
一种由溶组织内阿米巴引起的疾病,导致严重腹泻。
83、抗真菌药
(Antifungal)
用于治疗真菌感染的药物或物质。
84、抗病毒药
(Antiviral)
抑制病毒生长或复制的物质。
85、节肢动物
(Arthropod)
昆虫和蜘蛛等无脊椎动物,可作为疾病的传播媒介。
86、固氮菌
(Azotobacter)
革兰氏阴性、专性好氧的固氮细菌,能在无机氮源缺乏的条件下固定大气中的分子氮,同时产生植物生长激素、维生素和抗菌物质。
87、抗毒素
(Antitoxin)
能特异性结合和中和毒素的抗体或抗体制剂,主要来源于免疫动物血清,用于治疗细菌毒素、蛇毒等引起的中毒,具有快速中和毒素的作用。
88、吸收营养
(Absorptive Nutrition)
指机体通过消化道将营养物质从肠腔转运到血液或淋巴液的过程。主要发生在小肠,通过不同的转运机制(如主动运输、被动扩散、促进扩散等)吸收各类营养物质,包括糖类、氨基酸、脂肪酸、维生素和矿物质等。
89、琼脂扩散试验
(Agar Diffusion Test)
一种测定抗菌药物敏感性的经典方法,原理是利用抗菌药物在琼脂培养基中的扩散形成浓度梯度,通过测量抑菌圈大小来判定微生物对药物的敏感程度。
90、自养生物
(Autotroph)
能利用无机物(如CO2)作为碳源,通过光能(光合自养)或无机物氧化(化能自养)获取能量来合成有机物的生物。主要包括绿色植物、藻类、光合细菌(光合自养)和某些细菌如硫细菌、铁细菌(化能自养)等。
91、生长素
(Auxin)
Auxin(生长素)是一类重要的植物激素,以吲哚乙酸(IAA)为代表,具有促进细胞伸长、维管组织分化、顶端优势维持、向性反应调节等多种生理功能。
92、抗原呈递细胞(APC)
(Antigen-Presenting Cell)
处理抗原并将抗原呈递给T细胞以启动免疫应答的细胞。
93、自养细菌
(Autotrophic Bacteria)
能利用CO2作为唯一或主要碳源的原核生物,分为两大类:光合自养细菌(如紫色细菌、绿色细菌)利用光能合成有机物;化能自养细菌(如硫细菌、铁细菌、硝化细菌)通过氧化无机物获取能量。
94、非典型肺炎
(Atypical Pneumonia)
由不常见病原体引起的肺炎,如肺炎支原体或肺炎衣原体。
95、厌氧消化
(Anaerobic Digestion)
在无氧条件下,各类微生物协同作用将有机物降解转化为生物气(主要是甲烷和二氧化碳)的生物化学过程。该过程包括四个主要阶段:水解、酸化、产乙酸、产甲烷。广泛应用于有机废物处理、沼气生产、污水处理等领域。
96、节孢子
(Arthrospores)
一种无性繁殖孢子,由菌丝细胞分裂后断裂形成。它们通常呈圆柱形或矩形,具有厚壁结构,能够在不利环境下存活。
97、抗原决定簇
(Antigenic Determinant)
是抗原分子上能够被抗体或T细胞受体特异性识别的特定区域。可分为线性表位(由连续氨基酸序列构成)和构象表位(由空间折叠形成的非连续氨基酸序列)。它决定了抗原的特异性,是免疫系统识别外来物质的关键结构。在疫苗设计、免疫诊断、单克隆抗体制备等领域具有重要应用价值。
98、抗菌药物敏感性
(Antimicrobial Susceptibility)
微生物对抗菌药物的敏感性,通过测试指导治疗选择。
99、消毒冲洗液
(Antiseptic Rinse)
一类用于杀灭或抑制微生物生长的消毒液体,常见成分包括氯己定、碘伏、过氧化氢、季铵盐等。它们通过破坏微生物细胞壁、干扰代谢或抑制蛋白质合成等机制发挥杀菌作用。
100、阿米巴肝脓肿
(Amoebic Liver Abscess)
一种由溶组织内阿米巴感染引起的肝脓肿。
101、抗体滴度
(Antibody Titer)
是血清中特定抗体的浓度量度,通常表示为能够产生特定免疫反应的血清最大稀释倍数。它通过系列稀释和免疫测定方法(如ELISA、中和试验等)来确定。抗体滴度可用于评估疫苗接种效果、诊断感染性疾病、监测免疫应答状态,以及确定治疗方案。
102、琼脂糖电泳
(Agarose Electrophoresis)
一种使用琼脂糖凝胶根据大小分离核酸的技术。
103、抗菌剂
(Antimicrobial Agents)
杀死或抑制微生物生长的化学品。
104、营养性衰弱
(Abiotrophy)
指生物体或细胞、组织因退化或功能丧失而导致的活力下降或功能障碍,这种退化并非由明显的外伤或感染引起。
105、酸性环境
(Acidic Environment)
pH值较低的环境,会影响微生物的生长和存活。
106、无氧呼吸
(Anaerobic Respiration)
生物在无氧条件下,通过分解有机物产生能量的过程。与有氧呼吸相比,能量产生效率较低,最终产物可能是乳酸、乙醇等,是微生物和某些组织细胞重要的能量获取方式。
107、抗微生物化疗
(Antimicrobial Chemotherapy)
使用药物治疗由微生物引起的感染。
108、气生菌丝体
(Aerial Mycelium)
真菌从基质表面向空中生长的特化菌丝结构。它们主要用于形成和传播孢子,是真菌进行无性繁殖的重要结构,同时也是真菌分类鉴定的重要特征之一。
109、酰基载体蛋白(ACP)
(Acyl Carrier Protein)
一种小分子蛋白质,在脂肪酸合成过程中起关键作用。它含有硫泛醇基团,能够共价结合并转运酰基中间体,在脂肪酸合成酶复合体的各个催化位点之间传递底物。这种蛋白质结构高度保守,是细胞脂肪酸代谢和生长的必需因子。
110、两性霉素B耐药性
(Amphotericin B Resistance)
某些真菌抵抗抗真菌药物两性霉素B作用的能力。
111、曲霉菌病
(Aspergillosis)
由曲霉菌属引起的感染,通常影响肺部。
112、厌氧培养箱
(Anaerobic Chamber)
一种专门用于培养厌氧微生物和进行无氧实验的密闭设备。它具有良好的气密性,配备气体置换和净化系统,可维持稳定的无氧环境。广泛应用于微生物学、临床诊断和生物技术研究中。
113、根癌农杆菌
(Agrobacterium tumefaciens)
一种革兰氏阴性土壤细菌,携带Ti质粒,能够将T-DNA片段转移并整合到植物基因组中,导致植物产生冠瘿病,用于基因工程。
114、α-内酰胺酶
(Alpha-Lactamase)
细菌产生的一种酶,可分解β-内酰胺抗生素,导致耐药性。
115、青蒿素
(Artemisinin)
一种从植物青蒿中提取的抗疟疾化合物,用于治疗疟疾。
116、黄曲霉毒素中毒
(Aflatoxicosis)
一种由暴露于黄曲霉毒素引起的疾病,可导致肝损伤和癌症。
117、变形虫类原生动物
(Amoeboid Protozoa)
利用伪足移动和捕获食物的原生动物,如变形虫。
118、噬菌体
(Bacteriophage)
一种感染细菌并在细菌内复制的病毒,由蛋白质外壳和核酸组成,能特异性识别和裂解细菌。在分子生物学研究中发挥重要作用。
119、细菌培养
(Bacterial Culture)
细菌在受控环境中生长,通常在营养培养基中。
120、细菌内生孢子
(Bacterial Endospore)
由某些细菌产生的休眠、坚韧和非繁殖结构(例如,芽孢杆菌属和梭菌属)在恶劣条件下生存,高度抗逆休眠结构,具有耐高温、耐干燥、耐辐射、耐化学物质等特点。
121、菌血症
(Bacteremia)
指细菌从局部感染灶或侵入部位进入血液循环,是严重感染性疾病的重要表现之一。
122、细菌接合
(Bacterial Conjugation)
通过直接接触在细菌细胞之间转移遗传物质。这是细菌获得新基因的重要途径,对抗生素耐药性传播具有重要影响。
123、杀菌剂
(Bactericidal)
杀菌剂是一类能直接杀死微生物的化学制剂,其作用不可逆。通过破坏微生物细胞结构或代谢功能达到杀灭效果。
124、抑菌剂
(Bacteriostatic)
抑菌剂是一类能够抑制微生物生长繁殖但不直接杀死微生物的化学物质,其作用可逆。
125、生物膜
(Biofilm)
微生物粘附在表面的复杂聚集体,嵌入在自生的细胞外基质中。
126、细菌
(Bacterium)
细菌是一类原核单细胞微生物,具有细胞壁但无细胞核和细胞器,通过二分裂方式进行无性繁殖。它们广泛分布于自然界,可与人类形成共生或致病关系,在生态系统和人类健康中发挥重要作用。
127、β-内酰胺酶
(Beta-Lactamase)
一种由细菌产生的酶,可使β-内酰胺抗生素(如青霉素)失活。
128、细菌毒素
(Bacterial Toxin)
细菌产生的具有生物毒性的物质,主要分为内毒素和外毒素两大类。外毒素是细菌分泌的蛋白质毒素,具有高度特异性和强烈毒性,如破伤风毒素、白喉毒素等。内毒素是革兰氏阴性菌细胞壁脂多糖(LPS)成分,可引起发热、休克等症状。
129、细菌性阴道病
(Bacterial Vaginosis)
一种常见的阴道微生态失衡性疾病,特征是阴道内正常乳酸杆菌减少,厌氧菌过度生长。主要表现为阴道分泌物增多,呈灰白色,有特征性气味。
130、细菌质粒
(Bacterial Plasmid)
一种小的环状DNA分子,存在于细菌中,与染色体DNA分离,通常携带抗生素抗性基因。
131、β-溶血
(Beta-Hemolysis)
某些细菌在血液琼脂平板上生长时,通过分泌溶血素完全破坏红细胞而形成的透明溶血环。这种现象表现为菌落周围出现完全透明的溶血区,是细菌致病性的重要标志之一。
132、细菌鞭毛
(Bacterial Flagellum)
细菌重要的运动器官,由基体、钩子和丝体三个主要部分组成。基体含有复杂的蛋白质运动马达系统,能将质子动力转化为机械能,驱动鞭毛旋转。
133、细菌荚膜
(Bacterial Capsule)
某些细菌细胞壁外层的保护性结构,主要由多糖或多肽组成。荚膜具有多种重要功能:保护细菌免受不利环境影响、抵抗宿主免疫系统的吞噬作用、增强细菌的粘附能力。
134、生化试验
(Biochemical Test)
检测生物体代谢活动和化学特性的实验方法。在微生物学中,它是细菌鉴定的重要手段,包括IMViC试验(吲哚试验、甲基红试验、VP试验和枸橼酸盐试验)、糖发酵试验、氧化还原试验等。
135、细菌-宿主相互作用
(Bacteria-Host Interaction)
细菌细胞与其宿主生物体之间的复杂相互作用。
136、杀菌抗生素
(Bactericidal Antibiotic)
杀死细菌而不仅仅是抑制细菌生长的抗生素。
137、细菌病原体
(Bacterial Pathogen)
能够引起宿主疾病的致病细菌。这些病原体通过多种毒力因子(如内毒素、外毒素、侵袭酶等)损害宿主,可通过不同途径(如呼吸道、消化道、伤口等)感染宿主。
138、细菌培养基
(Bacteriological Media)
用于在实验室中培养细菌的营养丰富的物质。
139、苏云金芽孢杆菌
(Bacillus Thuringiensis)
一种产生杀虫毒素的细菌,用于害虫控制。
140、细菌学技术
(Bacteriological Techniques)
研究和操作细菌的一系列标准方法和程序。主要包括细菌培养(使用各种培养基和培养条件)、分离(获得纯培养物)、鉴定(形态学观察、生化试验、血清学试验等)和检测技术(显微镜检查、染色技术、分子生物学方法等)。
141、噬菌体疗法
(Bacteriophage Therapy)
使用噬菌体治疗细菌感染,特别是那些对抗生素有抗药性的细菌。
142、细菌基因组
(Bacterial Genome)
是细菌所有遗传信息的总和,主要由环状染色体DNA和质粒DNA组成。细菌基因组通常比较紧凑,大小一般在0.5-10Mb之间,具有高度的基因密度和少量非编码区。
143、细菌转化
(Bacterial Transformation)
细菌接收并整合外源DNA的过程,这是细菌获得新遗传特性的重要方式之一。转化可以自然发生,也可以通过人工方法(如化学法、电击法)诱导。
144、细菌性脑膜炎
(Bacterial Meningitis)
由细菌感染引起的脑膜炎症,主要病原体包括肺炎球菌、脑膜炎奈瑟菌和流感嗜血杆菌等。临床表现包括发热、剧烈头痛、颈项强直和意识改变等。
145、细菌菌毛
(Bacterial Pili)
细菌表面的毛状突起,由多个蛋白亚基组装而成。有助于粘附于表面和宿主组织;参与细菌间DNA转移(结合配偶过程);促进生物被膜形成。
146、生物反应器
(Bioreactor)
一种用于进行生物化学过程的装置,通过控制温度、pH值、溶氧、搅拌等参数,为微生物、细胞或酶的生长和代谢提供最适环境,主要类型包括搅拌式发酵罐、气升式反应器、固定床反应器和膜生物反应器等。用于工业或研究目的。
147、细菌性痢疾
(Bacillary Dysentery)
一种由细菌引起的肠道感染,以严重腹泻和腹痛为特征。
148、β-内酰胺抗生素
(Beta-Lactam Antibiotics)
一类抗生素,包括青霉素和头孢菌素,其特征在于它们的β-内酰胺环结构。
149、生物危害
(Biohazard)
对人类健康或环境构成威胁的生物物质。它包括病原微生物(如细菌、病毒)、生物毒素、感染性物质等。根据危害程度,生物危害通常分为四个安全等级(BSL-1到BSL-4)。
150、细菌内毒素
(Bacterial Endotoxin)
革兰氏阴性细菌细胞壁中脂多糖(LPS)的主要成分,由脂质A、核心多糖、O特异性多糖三部分构成,可引起全身炎症和发热。
151、细菌生长曲线
(Bacterial Growth Curve)
细菌种群随时间生长的图形表示,包括滞后期、对数期、稳定期和死亡期。
152、细菌内毒素血症
(Bacterial Endotoxemia)
血液中存在内毒素,可导致败血性休克。
153、生物信息学
(Bioinformatics)
生物信息学是结合生物学、计算机科学、数学和统计学的交叉学科,主要研究生物数据的收集、存储、分析和解释。其核心任务包括生物序列分析、蛋白质结构预测、基因组学数据处理、进化分析等。该学科运用各种计算工具和算法,构建生物数据库,开发分析软件,为现代生命科学研究提供重要支持。
154、细菌学研究
(Bacteriological Research)
科学研究的重点是细菌及其在健康,疾病和环境中的作用。
155、细菌质粒载体
(Bacterial Plasmid Vector)
用作将外源DNA引入细菌细胞的载体的质粒。
156、卡介苗(BCG)
(Bacillus Calmette-Guérin)
是由卡尔梅特和盖兰通过连续传代培养减毒牛型分枝杆菌制成的活疫苗。它是目前唯一在临床使用的预防结核病疫苗,主要通过诱导细胞免疫产生保护作用。
157、细菌致病性
(Bacterial Pathogenicity)
细菌引起疾病的能力,通常涉及毒素和粘附机制等因素。
158、细菌DNA重排
(Bacterial Recombination)
细菌DNA重排或交换的过程,导致遗传变异。
159、生物测定
(Bioassay)
抗生素浓度测定法通过测量一种物质(如抗生素)对活的有机体的影响来确定其浓度或效力的实验方法。
160、细菌DNA测序
(Bacterial DNA Sequencing)
通过现代分子生物学技术测定细菌基因组DNA序列的方法,用于物种鉴定、进化分析、致病机制研究和耐药性检测等,是细菌研究的重要手段。
161、杀菌浓度
(Bactericidal Concentration)
杀死细菌种群所需的抗菌剂的最低浓度。
162、细菌形态学
(Bacterial Morphology)
研究细菌的形状、大小和排列的学科。
163、细菌学分类
(Bacteriological Classification)
细菌分类法根据细菌的特征,如形态、生化特性和遗传成分,将细菌分类。
164、细菌内吞作用
(Bacterial Endocytosis)
细菌通过细胞膜内陷将外界物质转运入细胞内的过程,对细菌获取营养物质和应对环境变化具有重要作用,在细菌生长代谢中发挥关键作用。
165、细菌裂解
(Bacterial Lysis)
细菌细胞的分解或破坏,通常由抗菌剂或宿主免疫反应引起。
166、细菌学分析
(Bacteriological Analysis)
对样品中的细菌进行检查和研究,以确定其存在和特性。
167、生物控制
(Biological Control)
生物控制是一种利用自然天敌来减少或缓解害虫及其危害的环保且有效的方法。它广泛应用于农业、林业、水生生态系统、城市环境等领域,涉及病毒、微生物、线虫、昆虫、杂草和脊椎动物等害虫的管理
168、细菌二重感染
(Bacterial Superinfection)
在初次感染期间或之后发生的由不同菌株或细菌种类引起的继发感染。
169、细菌粘多糖
(Bacterial Mucopolysaccharides)
由细菌产生的复杂碳水化合物,常作为荚膜或生物被膜的重要组成部分,具有保护细菌、增强致病性和提高抗药性等作用。
170、细菌外毒素
(Bacterial Exotoxin)
细菌外毒素是细菌分泌到细胞外的蛋白质性毒素,具有高度特异性和强烈毒性,能够直接损伤宿主细胞或干扰细胞功能。
171、细菌学
(Bacteriology)
细菌学是研究细菌形态结构、生理生化特性、分类鉴定、致病机制及其与环境关系的微生物学分支学科,是微生物学的重要组成部分。
172、细菌分离株
(Bacterial Isolate)
细菌分离株是从自然界或临床样本中分离并经纯培养获得的单一菌株,具有独特的遗传特性和表型特征,是微生物研究、临床诊断和菌种保藏的基本单位。
173、生化需氧量(BOD)
(Biochemical Oxygen Demand)
指在特定条件下,微生物分解水中有机物过程中所消耗的溶解氧量,通常以mg/L表示,是反映水体有机污染程度的重要指标,广泛应用于环境监测和污水处理。
174、细菌突变
(Bacterial Mutagenesis)
细菌突变是指细菌基因组DNA序列发生改变的过程,包括自发突变和人工诱导突变两种方式,是研究基因功能、获得新菌株和进行分子进化研究的重要手段。
175、细菌趋化性
(Bacterial Chemotaxis)
细菌趋化性是细菌对环境中化学物质浓度梯度做出的定向运动反应,包括趋向有利物质(正趋化性)和远离有害物质(负趋化性),这种行为通过特定的信号转导系统调控,对细菌的生存和适应环境具有重要意义。
176、细菌转导
(Bacterial Transduction)
细菌转导是指通过噬菌体将供体细菌的遗传物质传递到受体细菌的过程。根据转导机制,分为普遍性转导和局限性转导。
177、细菌吞噬作用
(Bacterial Phagocytosis)
细菌吞噬作用是机体免疫细胞(如巨噬细胞、中性粒细胞)将细菌包围、吞入并在胞内消化降解的防御过程,是机体抵抗细菌感染的重要先天免疫机制。
178、细菌细胞壁
(Bacterial Cell Wall)
细菌细胞壁是细菌细胞最外层的刚性结构,主要由肽聚糖等物质组成,维持细胞形态、防止渗透压破裂、参与物质运输。
179、细菌内源性毒素
(Bacterial Endogenous Toxin)
是革兰氏阴性细菌细胞壁中脂多糖(LPS)的毒性成分,在细菌死亡或裂解时释放,可引起发热、休克等症状,是重要的致病因子。
180、细菌基因工程
(Bacterial Genetic Engineering)
利用分子生物学技术对细菌基因进行修饰、重组和表达的技术,包括基因克隆、DNA重组和基因表达等,在医药、农业和工业生产中具有广泛应用。
181、枯草芽孢杆菌孢子
(Bacillus Subtilis Spores)
该菌在不利环境条件下形成的休眠结构,具有耐热、耐干燥、耐化学药品等特点,能在恶劣环境中长期存活,在发酵工业、生物防治和益生菌制剂中有重要应用价值。
182、细菌毒力因子
(Bacterial Virulence Factor)
细菌致病的重要物质基础,包括内毒素、外毒素、侵袭酶等多种成分,通过不同机制损害宿主或帮助细菌定植、侵袭和逃避免疫。
183、蜡状芽孢杆菌毒素
(Bacillus Cereus Toxin)
由蜡状芽孢杆菌产生的一类致病性毒素,主要包括呕吐毒素(耐热性)和腹泻毒素(易热不稳定),可引起食物中毒,主要症状为恶心呕吐或腹泻。
184、细菌转座子
(Bacterial Transposon)
一种可在细菌基因组内移动的遗传元件,通常携带抗生素抗性基因。
185、细菌质粒复制
(Bacterial Plasmid Replication)
质粒在细菌细胞内复制的过程,是细菌遗传和基因工程的重要基础。
186、细菌抗原
(Bacterial Antigen)
被免疫系统识别为外来物的物质,引起免疫应答。
187、细菌细胞质膜
(Bacterial Cytoplasmic Membrane)
包围细菌细胞并调节物质进出运动的脂质双层。
188、细菌噬菌体展示
(Bacterial Phage Display)
一种通过在噬菌体表面展示肽或蛋白质来研究蛋白质相互作用的技术。
189、细菌孢子形成
(Bacterial Sporulation)
某些细菌(如芽孢杆菌)在不利环境条件下的一种分化过程,经过前孢子、原孢子、成熟孢子等阶段,形成具有多层保护结构的休眠体,具有耐热、耐干燥、耐化学药品等特性,能在恶劣环境中长期存活。
190、细菌基因表达
(Bacterial Gene Expression)
DNA信息转录成RNA并翻译成蛋白质的过程,具有原核生物特有的操纵子结构和调控机制,包括转录起始、延伸和终止,以及翻译的起始、延伸和终止,受到多层次调控,如启动子强度、阻遏物、激活物等。
191、炎症
(inflammation)
炎症是指具有血管系统的活体组织对各种损伤因子刺激所发生的一种以防御反应为主的基本病理过程。炎症的主要表现包括红、肿、热、痛和功能障碍,这些特征是由于局部血管扩张、血流加快、白细胞浸润以及炎症介质的作用。
192、抗原
(Antigen)
能够刺激机体免疫系统产生特异性免疫应答,并能与免疫应答产物抗体或致敏淋巴细胞结合的物质。抗原通常具有两个基本特性:一是免疫原性,即能诱导免疫应答;二是反应原性,即能与免疫应答产物发生特异性结合。抗原多为蛋白质、多糖等大分子物质,广泛应用于疫苗研发、疾病诊断和免疫治疗等领域。
193、抗体
(antibody,Ab)
抗体是一类能与抗原特异性结合的免疫球蛋白,是由B细胞在抗原刺激下增殖分化为浆细胞后产生的一类能与相应抗原特异性结合的糖蛋白。抗体的主要功能是介导体液免疫反应,帮助机体识别和清除病原体。
194、先天性免疫
(adaptive immunity)
机体与生俱来的非特异性防御系统,是抵抗病原体入侵的第一道防线。它包括以下几个层面的防御机制:
物理和化学屏障:皮肤、黏膜、酸性环境等;
细胞成分:巨噬细胞、中性粒细胞、NK细胞、树突状细胞等;
分子成分:补体系统、炎症因子、干扰素等。
195、适应性免疫
(adaptive immunity)
也可以称为获得性抗感染,是一种抗原特异性免疫类型,是宿主免疫系统识别和破坏特定微生物、其产物和其他侵入体内的异物的获得性能力。它是基于宿主先前暴露于特定病原微生物或抗原而引发的特定类型的免疫应答。
196、抗原变异
(Antigenic Variation)
抗原变异是病原体表面抗原结构发生改变的现象,包括点突变导致的抗原漂移和基因重排导致的抗原转换,使病原体能够逃避机体免疫识别。
197、自身免疫性疾病
(Autoimmune Disease)
免疫系统错误地攻击人体自身组织的一种疾病。可分为器官特异性(如I型糖尿病、重症肌无力)和系统性(如系统性红斑狼疮、类风湿关节炎)两大类。
198、细菌感染
(Bacterial Infection)
细菌感染是致病菌侵入并在机体内定植、繁殖,引起组织器官损伤和机体防御反应的病理过程,可引起发热、炎症等症状,是常见的感染性疾病类型。
199、急性感染
(Acute Infection)
指病原微生物侵入机体后快速发展的感染过程,特征是起病急骤、症状明显、病程较短(通常在2周以内)。主要表现包括发热、寒战、疲劳等全身症状,以及感染部位的特异性表现。
200、细菌耐药性
(Bacterial Resistance)
细菌对抗菌药物产生的抵抗能力。这种现象可通过多种机制实现,包括产生降解药物的酶、改变药物作用靶点、增强细菌外排系统、降低细胞膜通透性等。耐药性可分为自然耐药和获得性耐药。
微生物学作为一门深邃而广博的学科,在其不断发展演进的过程中,衍生出了丰富的专业术语体系。由于学科内容的庞大性和复杂性,本文难以对所有相关术语进行全面阐述。我们计划在后续内容中,特别针对肠道菌群领域的专业术语进行系统性的梳理和解读,为大家提供更加完整和参考知识。
主要参考文献:
World of Microbiology and Immunology K. Lee Lerner and Brenda Wilmoth Lerner, Editors. Volumes 1 and 2. 2003. The Gale Group, Inc. 27500 Drake Road Farmington Hills, MI, 48331-3535.
Prescott’s Microbiology, 12th Ed. 2019. Joanne Willey, Kathleen Sandman and Dorothy Wood. McGraw Hill Publication.
Textbook of Microbiology by Surinder Kumar. 2012. Jaypee Brothers Medical Publishers (P) Ltd. ISBN : 978-93-5025-510-0
Jawetz, Melnick and Adelberg’s Medical Microbiology. 25th Eds. International Edition. 2001. McGraw Hill Publication
Textbook of Microbiology and Immunology. 2nd Eds. By Subash Chandra Parija. Elsevier publication.
Essentials of Medical Microbiology. 4th Eds. By Rajesh Bhatia and Rattan Lal Ichhpujani. 2008. Jaypee Brothers Medical Publishers (P) Ltd
Leber, Amy L., editor in chief. (2016). Clinical microbiology procedures handbook (Fourth edition). Washington, DC : ASM Press 1752 N St., N.W., [2016]
Tille, P. M., & Forbes, B. A. (2014). Bailey & Scott’s diagnostic microbiology (Thirteenth edition.). St. Louis, Missouri: Elsevier.
Microbiology from A to Z explained– biologynotesonline

谷禾健康

人体肠道微生物群作为一个重要的“微生物器官”,在人类健康和疾病中发挥着至关重要的作用,影响着人体的代谢、免疫,甚至神经系统功能。随着测序技术和分析方法的进步,大规模人群队列研究已经成为理解肠道微生物群与宿主遗传、环境因素以及人类健康结局之间复杂相互作用的强有力工具。
这些人群队列研究,特别是那些样本量超过1,000名参与者的研究,为识别不同人群中一致的微生物组模式、建立与各种健康参数的关联,以及理解地理位置、饮食和文化因素对微生物群组成的影响提供了独特的机会。大样本量和使得研究能够进行稳健的统计分析,有助于控制混杂因素,并能够识别那些在小规模研究中可能被忽视的微弱但显著的关联。此外基于大规模人群队列的多组学数据也为我们了解肠道菌群与其他如代谢、蛋白、饮食和基因等关联提供了绝佳的材料。
与人类基因组相比,微生物组在治疗上更易于处理,它的可操控和可干预性显著支撑了微生物组的治疗进展和快速发展,因此具有良好的诊断和治疗前景。但实现这一愿景需要了解正常微生物组的构成。
建立正常微生物组参考一直是微生物组科学中的一大挑战。正常或健康微生物组的定义一直难以达成共识或一致。人类微生物组的惊人变化与地理位置,种族,生活方式,饮食,年龄,性别和药物等有关。并且由于迄今为止少数群体和全球主要地区在微生物组研究中的代表性不足。相比起来,我们国家人群的微生物研究数据是相对比较大的。
为什么需要特定人群的正常微生物参考?建立特定人群的正常微生物参考有助于精确诊断和个性化治疗;更好地评估健康状态和制定预防策略;深入了解人群差异并指导药物研发;辅助判断临床干预效果还能确定特定人群的疾病易感性。
在这篇文章中,我们主要关注肠道微生物组(最大和研究最广泛的微生物群落),从非患病人群中已知的微生物组开始,并简单分享不同人群中的正常肠道微生物组,分析与健康相关的微生物组特征变化的主要驱动因素,还概述了一些广泛研究的疾病微生物组相关治疗干预措施,同时探讨和关注这些偏差的来源以及与定义人群特异性微生物组参考基础相关的挑战。
1
利于精确诊断和治疗
每个人体内都有独特的微生物群落(微生物组),这些微生物组的构成受到个人年龄、性别、生理状态、生活方式及遗传背景等差异的影响,其正常的微生物群落组成存在特定特征。但同一个群体(如同一个家庭或地区)内的人们往往具有相似的微生物组构成。
同时,在健康人体内,微生物组会与人体形成一种平衡关系,这种平衡是适应了特定的宿主(人体)和环境条件的,这种状态被称为“稳态”,是维持健康的重要因素。
精确诊断:对于特定人群,有了正常微生物参考,可以更准确地判断其微生物群落是否偏离正常状态,从而为疾病的早期诊断提供依据。一些疾病如炎症性肠病与特定的促炎细菌(Fusobacterium nucleatum、Ruminococcus gnavus)异常增多或产短链脂肪酸细菌(Akkermansia Muciniphila、Lactobacillus)减少有关,通过与该人群的正常微生物参考对比,可以更敏锐地发现这些异常变化,提高诊断的准确性和及时性。
举个简单的例子:
如果一个人的多种菌都超过了正常范围,除了疾病和菌群紊乱,是不是还有一种可能,因为他的生活方式或地区不适用原有的菌群范围。比如纯素食者的菌群与肉食者的菌群无论在多样性和关键菌群特征上都有明显的不同,如果简单的将两类人群合并,按比例范围给出一个正常范围,结果就是两类人群差异的特征菌的范围异常宽泛,导致无法辨识是否存在异常。这就对于未来构建全面的肠道菌群数据库提出了要求和标准,也是谷禾致力于建立细分数据库的根据。
个性化治疗:在治疗疾病时,了解特定人群的正常微生物参考有助于制定个性化的治疗方案。由于微生物组具有群体特异性(不同群体有不同特点),在使用相同药物时可能会产生不同的反应。
例如在使用抗生素治疗感染性疾病时,不同人群的肠道菌群对不同抗生素的反应可能不同。如果知道特定人群的正常菌群组成,医生可以选择对其肠道菌群影响较小的抗生素,或者在治疗过程中同时采取措施保护肠道菌群,如补充益生菌等。
此外,对于一些与肠道菌群失调相关的疾病,如炎症性肠病、肠易激综合征等,通过恢复患者的肠道菌群至正常状态可以作为一种治疗策略。而特定人群的正常微生物参考可以为确定治疗目标和选择治疗方法提供重要参考。
2
健康管理和预防
评估健康状态:特定人群的正常微生物参考可以作为评估该人群健康状态的一个重要指标。通过检测个体的微生物群落组成,并与同人群的正常参考进行比较,可以了解个体的健康状况是否良好,是否存在潜在的健康风险。
例如,对于孕妇来说,孕期的肠道菌群变化可能与妊娠并发症的发生风险相关。如果能够监测孕妇的肠道菌群,并与正常孕妇的菌群参考进行对比,可以在早期发现潜在的风险因素。
制定预防策略:对于一些特定人群,如老年人、婴幼儿、患有慢性疾病的人群等,了解他们的正常微生物参考可以帮助制定针对性的健康管理和预防策略。
例如,对于老年人,可以通过调整饮食、补充益生菌等方式维持肠道菌群的平衡,预防肠道疾病和其他慢性疾病的发生。对于婴幼儿,建立健康的肠道菌群对于其免疫系统的发育和整体健康至关重要。
3
科学研究和药物研发
深入了解人群差异:特定人群的正常微生物参考为科学研究提供了重要的基础数据。通过比较不同人群的微生物群落组成,可以深入了解人群之间的差异及其背后的生物学机制。
例如,研究不同种族人群的肠道菌群差异,可能有助于揭示遗传和环境因素对肠道菌群的影响,以及这些差异与疾病易感性的关系。此外,特定人群的微生物参考还可以为研究微生物与宿主相互作用提供重要线索,推动微生物学、免疫学、营养学等多个领域的发展。
指导药物研发:在药物研发过程中,考虑特定人群的微生物特征非常重要。药物的疗效和安全性可能受到个体微生物群落的影响。某些药物的代谢可能依赖于肠道菌群中的特定酶。了解特定人群的正常微生物参考,可以帮助研发人员预测药物在不同人群中的代谢情况和疗效差异,从而优化药物设计和开发更具针对性的药物。
此外,针对特定人群的肠道菌群特点,还可以开发新型的益生菌、益生元或其他微生物相关的治疗方法,为疾病的治疗提供新途径。
4
判断临床干预效果
微生物组在人群之间存在差异,因此需要针对特定人群(如不同地区、文化或生活方式的人群)进行分析。通过这种人群特异性分析,可以识别出哪些微生物标志(特定的微生物或微生物群)与健康状态(非疾病状态)相关。这些标志可以用来定义健康人群中微生物的“正常范围”(即参考流行范围和丰度分布)。
如果对微生物组进行干预(比如通过饮食、益生菌、药物等),可以通过观察这些健康相关微生物标志在干预前后的变化来评估干预的效果。也就是说,干预是否有效,可以通过看这些标志是否恢复到健康人群的正常范围来判断。
目前已经有一些指数或统计方法被提出,用来衡量微生物组干预的效果。但这些方法大多是针对特定人群(比如某些研究中的特定群体)设计的,或者主要集中在少数地区的人群上。这意味着这些方法可能无法很好地适用于其他人群。
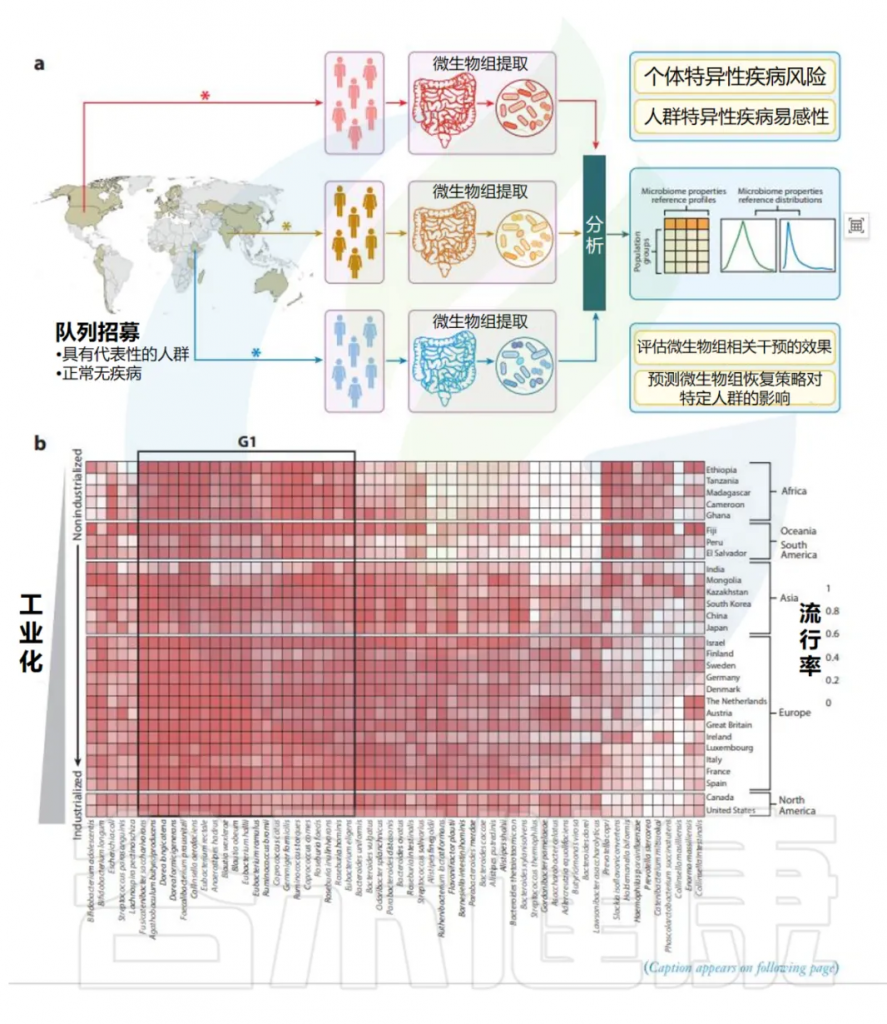
上图分析包括来自29个国家进行的65项研究的21117个明显健康个体的肠道微生物组(来自curatedMetagenomicData存储库)。这些优势物种是从至少两个民族的前30个流行分类群中选出的。除了捕获某些分类群的一些已知地理特异性流行模式(与工业化状况有关)外,该分析还揭示了存在一个共同的核心微生物组,由29个民族中流行的21个物种组成。
(a)该方法的模式和需要人群特异性正常微生物组参考的四个主要原因。
(b)热图显示了来自不同民族的肠道微生物组中优势微生物物种的流行率。
另外还需要通过以相同基准进行比较,比如同一个体的前后比较,并根据个体的人群特征分类对变化的菌的程度进行判定。
5
确定特定人群的疾病易感性
正常不等于健康。微生物组不仅可以反映当前的健康状况不佳,还可以反映疾病发展的风险。此外,虽然微生物组和疾病风险之间的一些联系在多项研究中得到了一致的再现,但有可能识别出那些处于特定风险中的人。例如,一项研究对坦桑尼亚城乡梯度人口的调查表明,城市化群体的微生物组结构在暴露于体外细菌刺激物时易患炎症状态。这也在实验小鼠中建模。
因此,在明显未患病的人群中存在特定微生物组“配置”的情况下,特定标志物的较高基线水平的组合可以预测某些疾病的易感性,并能够加强公共卫生监测的重点。
6
不同微生物组干预恢复策略对不同人群的有益和有害影响
研究表明,大多数微生物组干预策略是基于工业化或西方化人群的研究结果设计的,但对于农村人群或过着传统生活方式的人群,这些策略可能效果较差,甚至会带来负面影响(这也是谷禾一直花大力气构建本地区能覆盖全国的人群样本菌群数据库的主要原因)。
例如,在城市化、工业化人群中,嗜粘蛋白的阿克曼氏菌(AKK)被认为有多种益处,比如抗衰老和改善胰岛素抵抗。然而,由于它以粘蛋白为食,这种菌可能并非对所有人都有同样的好处。在一些粘蛋白层较薄、屏障完整性较差的人群中,它可能反而会带来有害影响。
同样,对于缺乏纤维降解细菌的人,如果直接补充β-果聚糖,可能会导致炎症增加。接下来,我们将总结不同人群中微生物组差异的相关研究。
多个大规模人群微生物组测序项目,包括LifeLinesDEEP、佛兰芒肠道微生物项目、荷兰微生物组项目、美国肠道、瑞典心脏病生物成像研究、芬兰慢性非传染性疾病风险因素人群调查(FINRISK)、广东项目、谷禾健康项目肠道微生物组和日本4D微生物组项目提供了不同人群中正常肠道微生物组的一些数据。
此外,小规模的研究已经描述了特定国籍,种族和偏远地理位置的焦点群体中具有不同生活方式或生活方式转变的非患病个体的微生物组,其他项目已经调查了患有各种疾病的匹配对照患者队列。
公开的微生物组数据存储库促进了对多个地理区域人群特异性正常微生物组特征的研究,并揭示了大致的模式。
首先肠道菌群与生长发育是相伴随的,婴幼儿和青少年以及老年人的菌群在不同阶段是跃迁式变化的,而且不同的年龄阶段,菌群的变化频率也不同。因此不能简单的将不同年龄阶段的人群合并给出菌群范围,需要针对不同年龄阶段计算相适应的年龄范围,这样才能准确的反映菌群的异常情况。
1
婴儿的微生物群落
婴儿的微生物群落已经被观察到,在不同的地理位置有相当大的相似性。它们以肠杆菌科(Enterobacteriaceae)、双歧杆菌科(Bifidobacteriaceae)、肠球菌科(Enterococcaceae)、韦荣氏球菌科(Veillonellaceae)和葡萄球菌科(Staphylococcaceae)的成员为主。
婴儿肠道微生物组似乎主要受饮食模式,城市化和环境暴露的影响(这反过来可能会推动间接的地理特异性关联)。
2
正常成人的肠道微生物组
肠道微生物组在成熟至成年后达到独特的组成。典型的正常成人肠道微生物组由拟杆菌门(例如普雷沃氏菌属(Prevotella)、拟杆菌属(Bacteroides)、Alistipes、Barnesiella、Odoribacter)和厚壁菌门(例如粪杆菌属、Roseburia、真杆菌属、粪球菌属、毛螺菌属),其次是变形菌门(埃希氏菌属)、线菌门(双歧杆菌属、Collinsella、Eggerthellaceae)和疣微菌门(Akkermansia),尽管这些成员在患病人群中存在相当大的差异。
一些研究强调了工业化对微生物组的独特影响,以及工业化和非工业化社会中城乡梯度的影响。 城市化与属于拟杆菌、Alistipes和Akkermansia等分支的微生物成员的增加有关,与属于Prevotella、Catenibacterium、Treponema和Succinatimonas分支的成员的减少有关,以及与瘤胃球菌科和真杆菌属分支的特定成员的减少有关。
为了进一步阐明不同国家正常微生物组中的这些差异,对从全球微生物组数据库curatedMetagenomicData获得的全球数据集(包括来自29个国家的65项研究的21117名正常,明显未患病受试者的肠道微生物组)进行了调查,结合谷禾的检测数据库,确定了正常成人肠道微生物组的共同核心菌属。(下图)
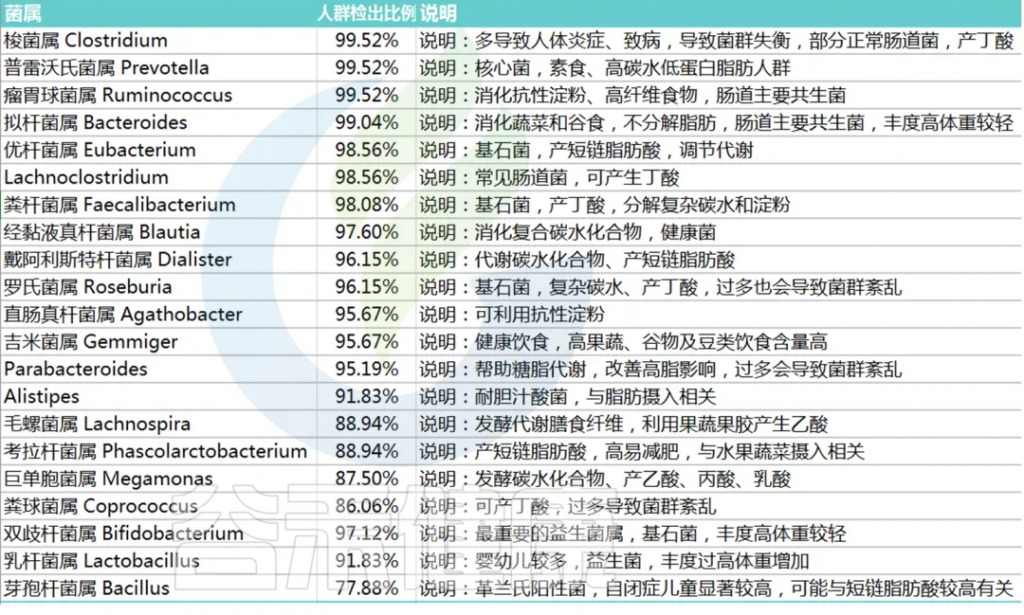
<来源:谷禾肠道菌群检测数据库>
♢除核心菌外的微生物与工业化程度及生活方式存在很大联系
其他微生物类群在不同程度上与国家的工业化程度相关。两种双歧杆菌(长双歧杆菌和青春双歧杆菌)在除非洲国家外的所有队列中普遍存在。与之前的观察相反,Prevotella copri——非工业化肠道微生物群的标志,在一些工业化国家仍然普遍存在,尽管出现了减少,以及其他与城市化负相关的成员,如Holdemanella biformis。
与工业化负相关程度最高的3个物种分别是Catenibacterium mitsuokai、
Phascolarctobacterium succinatutens、
Prevotella stercorea。
同样,虽然拟杆菌和另枝菌属(Alistipes)与工业化社会的肠道微生物群有关,但这些谱系的差异是明显的。虽然Bacteroides uniformis、B.vulgatus和Odoribacter在非工业化社会中也很普遍,但该分支的其他成员,如B.dorei、B.xylanisolvens、B.caccae、Barnesiella、Alistipes和Parabacteroides在欧洲、北美和亚洲国家普遍存在,但在其他国家却没有。
城市化生活方式的形成是多个因素的综合结果,包括卫生条件改善、药物摄入增加、久坐不动的生活方式、昼夜节律紊乱、饮食缺乏季节性变化、富含蛋白质或脂肪的饮食、家庭规模较小以及与宠物或其他动物接触较少。这些因素可能单独或共同影响肠道微生物组的组成变化。
♢特定的饮食习惯与肠道微生物也密切相关
某些肠道微生物通常与特定的饮食习惯有关。例如,耐胆汁的谱系如拟杆菌属和嗜胆汁菌属通常与肉类摄入有关,而产生丁酸盐的糖解谱系如罗氏菌属、瘤胃球菌属和粪杆菌属及普雷沃氏菌与富含植物和地中海饮食有关。
普雷沃氏菌属也与食用谷物(尤其是全谷物)有关。同样,虽然粪杆菌属和罗氏菌属与红酒摄入有关,但富含乳化剂的饮食(通常与加工食品有关)与有害的Ruminococcus gnavus增加有关。
详见: 活泼瘤胃球菌(Ruminococcus gnavus)——多种疾病风险的潜在标志物
♢衰老以特定的方式影响肠道微生物群
随着年龄的增长,与青年相关的、产生丁酸盐的微生物群减少,潜在有害分类群(致病菌)增加,以及替代核心成员(如阿克曼菌属、克里斯滕森菌属、颤杆菌属、丁酸弧菌属和丁酸单胞菌属)的比例增加。这些是肠道微生物组在未患病个体中适应与衰老相关的宿主生理变化的一部分种群。
奇怪的是,一些看似无关的因素与肠道微生物组组成也有着联系。例如,养宠物和更多的人际接触(如在大家庭中)与普雷沃氏菌属和脱硫弧菌属的增加以及有益的孢子形成、丁酸盐产生的厚壁菌门物种(如粪杆菌、真杆菌、罗氏菌属、粪球菌属)的增加有关,与富含谷物的植物性饮食相关的同一谱系的嗜酸乳杆菌和脆弱拟杆菌的减少有关。
同样,大多数通常与多药相关的微生物成员(如拟杆菌属、拟副杆菌属、爱格氏菌属、链球菌属)也与工业化人群有关。
3
真菌组成
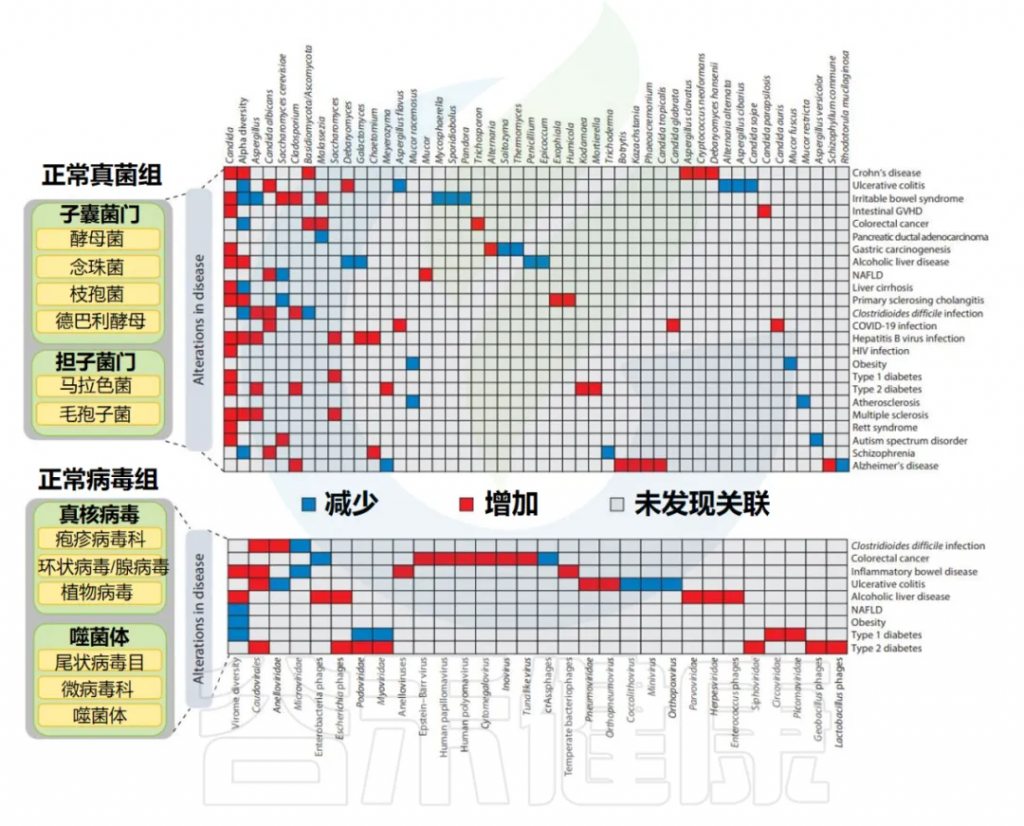
doi: 10.1146/annurev-med-051223-031809.
上图总结了目前对正常肠道真菌群落的了解以及多种疾病中一些变化。主要由子囊菌门和担子菌门两门组成。婴儿的肠道菌群主要包含子囊菌目(Ascomycota)和马拉色菌目(Malasseziales)(担子菌门)的成员。
与细菌组一样,真菌组也随着年龄的增长而变化。正常成人肠道真菌组由三个属占主导地位,即酵母菌属、假丝酵母菌属和枝孢属(均属于子囊菌门),其次是其他属,如德巴利酵母属和毕赤酵母属(均属于子囊菌门)以及马拉色菌属、汉纳酵母和隐球菌属(均属于担子菌门)。
♢不同人群真菌组成更加个性化
与细菌组/古菌组相比,真菌组在种或属水平上表现出较少的受试者内多样性和显著更高的受试者间变异性,表明真菌组更加个性化。尽管真菌生物群系受到城市化、饮食、出生模式、药物和种族等因素的影响,这些因素同样影响细菌组/古菌组,但与每个宿主相关因素的进化枝在队列中表现出一致性较小。与不同宿主生化标记相关的真菌分支也显示出高度个性化的群体特异性关联模式。
♢真菌生物群与宿主性状和疾病存在关联
真菌生物群与宿主性状和疾病之间存在一致的关联。例如,多项研究发现,曲霉菌和青霉菌在老年人中的流行率增加,除了念珠菌和酵母菌外。克罗恩病和溃疡性结肠炎中白色念珠菌和德巴利酵母菌增加;马拉色菌在肠易激综合征(IBS)、结直肠癌和胰腺癌中也有所增加;多种疾病中真菌生物群的α多样性显著提高。
过多的真菌谱系如念珠菌已被证明对细菌微生物组的多样性和组装产生负面影响,导致促炎微环境。
4
病毒组成
人体的病毒生物群也是个性化的,并受到地理,城市化和种族的影响。
尽管有这些影响,但多项研究就正常肠道病毒组的典型构成达成了共识。这包括真核病毒(感染人类宿主细胞以及膳食植物材料)和噬菌体(感染微生物组细菌/古菌成员的病毒)。
上图总结了目前关于正常肠道病毒组和某些疾病中的一致发现。主要的宿主感染真核病毒谱系,包括疱疹病毒、无核病毒和腺病毒,在正常个体中通常处于低丰度和休眠阶段,可能有助于启动免疫系统。
而人类肠道中的主要噬菌体谱系包括有尾噬菌体目、微小噬菌体科和交叉组装噬菌体(crAssphages)。crAssphage是一种粪便病毒谱系,是通过使用交叉组装方法对宏基因组数据集进行计算分析而发现的(因此得名)。
♢肠道病毒组以特定的变化影响着宿主健康
肠道微环境的变化,如炎症,pH值的变化,氧化应激或抗生素引起的变化,可能会触发噬菌体生命周期的变化。
噬菌体组还可以以不利的方式(即通过促进毒素产生、定殖/粘附、生物膜产生和抗生素抗性)或有益的方式(即通过使用免疫球蛋白样结构域粘附于宿主细胞并形成病原体防御层或调节宿主炎症状态)。
多项研究已确定肠道病毒组中特定的疾病相关变化,其中一些在临床前模型中得到了验证。常见模式包括肠道炎性疾病中病毒多样性的增加,以及多种疾病中微病毒科的减少和尾状病毒目的增加。然而,大多数关于宿主相关因素对正常肠道病毒组影响的研究仍局限于西方国家和东亚的特定亚群,缺乏来自全球其他地区的数据。
1
人群样本代表性可能不足
扩大我们对特定人群正常微生物组知识的主要障碍是缺乏来自非工业化发展中国家和低收入国家的微生物组数据。下图a突出了这一问题。我们将不同国家的全球人口份额与其在全球微生物组数据库中的代表性进行了关联,这些数据库包括MetagenomicData(v3)、Human Microbiome Compendium和GMrepo。与其全球人口代表性相比,肠道微生物组代表性显著较低的国家主要是最不发达和发展中国家。
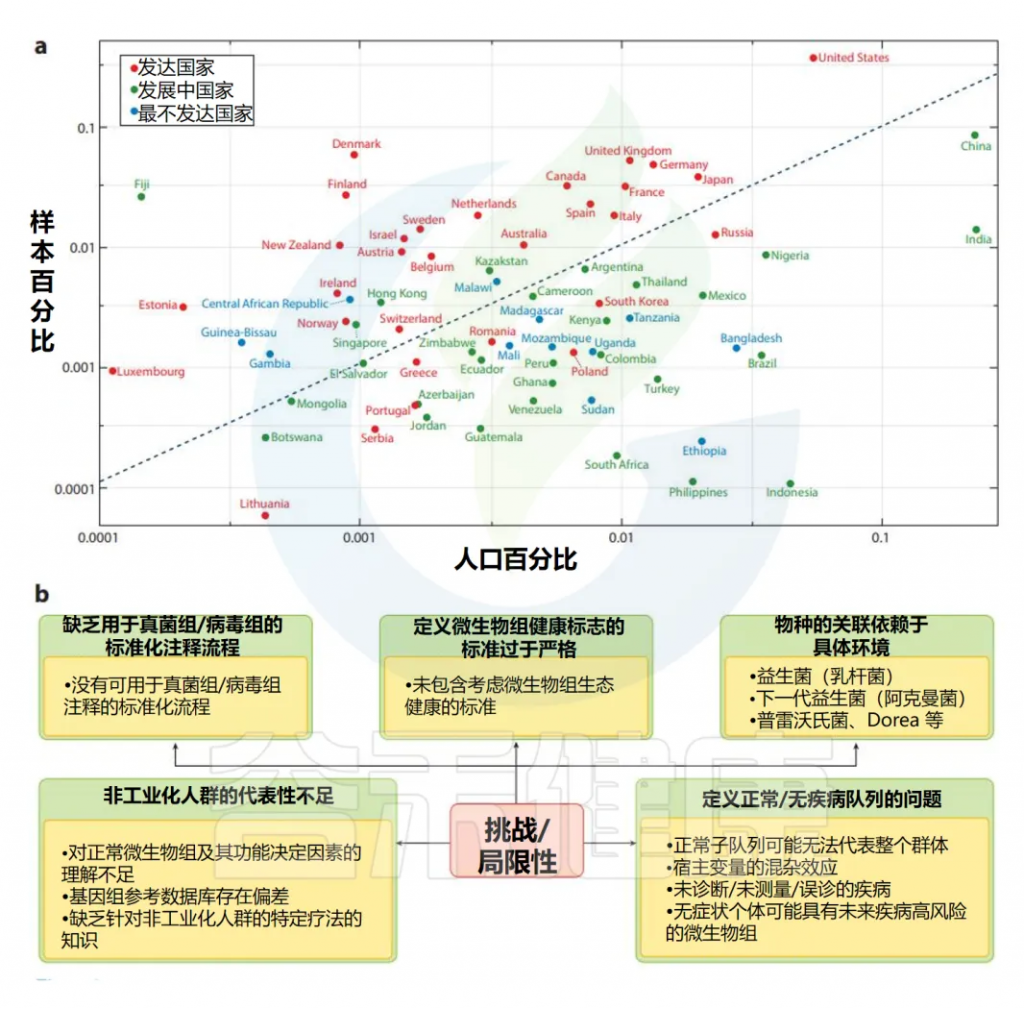
(a)在全球微生物组数据库中缺乏来自发展中国家/最不发达国家的肠道微生物组的代表性。散点图是通过结合来自三个主要微生物组数据库的肠道微生物组概况进行的全球数据分析的一部分,其中包括来自71个国家的221983个肠道微生物组。1y轴代表每个国家在微生物组计数方面的比例份额。x轴显示了全球人口在log 10尺度上的相同份额。
具体国家的人口来自联合国人口基金的世界人口仪表板(https://www. unfpa.org/data/world-population-dashboard)。根据经济状况(发达国家、发展中国家或最不发达国家)进行的国家分类取自联合国发布的《2023年最不发达国家报告》(https://unctad.org/publication/least-developed-countries-report-2023。
(b)界定特定人群正常人口范围的挑战和局限性的简要说明。
此外,相同国家也存在地域代表性差异,广东的研究队列显示即便是广东同省,不同地区的菌群特征也存在明显的差异。
♢代表性不足的后果
这种代表性不足有两个主要后果。首先,它限制了我们对大多数人口正常微生物组的理解。其次,它导致参考数据库的基因组表示主要偏向于工业化或西化城市人群的物种(或亚分支/菌株变体)。这不仅限制了来自非工业化发展中国家和最不发达国家的新数据集的分类和功能注释,还使得确定这些人群中与弹性和健康相关的微生物组功能决定因素变得困难。
事实上,这些传统种群中许多新的适应宿主的功能特征(包括识别随着城市化而丢失的新纤维素降解物种)已在少数高深度测序项目中出现,这些项目主要集中在尼泊尔部落、斐济人以及埃塞俄比亚、加纳和马达加斯加等的小型农村亚群。
我们之前已表明,健康和疾病相关的类群在工业化和非工业化人口中存在差异。因此,非工业化人口的健康功能决定因素可能与工业化人口不同,并可能适应相关的环境压力。这对基于工业化国家开发的微生物组治疗在非工业化和发展中国家的应用具有显著影响。此外,来自发展中国家的数据在真菌组和病毒组方面的代表性不足更为明显。
2
定义正常亚群的挑战
目前对正常微生物组的理解是基于人群水平的微生物组分析或比较患者和对照组的以疾病为重点的研究。有四个混杂因素需要考虑。
首先,在许多以疾病为中心的研究中,匹配的正常亚组由居住在同一地区的个体亚组组成。这大大限制了代表正常人群的数据。
其次,在许多以疾病为重点的研究中,正常对照组包括除试验组中感兴趣的疾病之外的一系列疾病的受试者。
第三,尽管人群水平的测序项目解决了以疾病为重点的报告的许多局限性,但它们经常包括自我宣称正常但患有未诊断或误报疾病的个体,这些疾病扭曲了正常微生物组特征的分析。
第四,最近的研究表明,微生物组的改变早在明显的疾病之前[例如,炎症性肠病(IBD)和阿尔茨海默氏症]是明显的。
3
基因型与表型的关系
肠道微生物与疾病之间的关系严重依赖于环境。在一个遭受饥荒的国家,微生物组可能适应于最大限度地提取卡路里和营养,而在肥胖环境中则可能产生负面影响。同样,单个微生物在健康和疾病中可能呈现相反的相关性。
♢大多数情况下有益的细菌可能在一些疾病中也丰度过高
例如,广泛用作益生菌的乳酸杆菌在炎症性肠病、2型糖尿病(T2D)和肝硬化等疾病中也显示出增加的丰度;目前用作下一代益生菌的嗜粘蛋白阿克曼氏菌也与帕金森病、阿尔茨海默病和多发性硬化等神经系统疾病有关;与改善宿主代谢和葡萄糖稳态正相关的Prevotella copri也在类风湿性关节炎和肝病等疾病中富集。
特定分类群的疾病相关性需要开发创新的评分指标,以选择用于治疗的分类群。
4
缺乏标准化的微生物组分析和注释
识别正常微生物组标志物的典型方法是探索在疾病中通常获得或失去的物种或分类群。然而,这种方法是有限的,无法解决微生物组的生态健康问题(即其随时间的稳定性和弹性)。事实上,一些广泛用于微生物组补充策略的分类群(如乳杆菌)已被证明缺乏这种特性。
正常微生物组参考应在不同人群中具可比性,这需要减少研究间的实验和测序变量,并标准化计算注释协议。然而,目前尚未建立标准化的注释,尤其是针对真菌组和病毒组。不同研究使用了多种非均质实验技术进行宏基因组DNA提取、测序文库制备和测序,导致生成的微生物组谱在不同研究中难以比较。
尽管识别正常(或未患病)肠道微生物组面临许多挑战(如在全球人群中定义正常微生物组的限制),微生物组相关的治疗干预在解决多种疾病方面取得了显著成功。然而,其成功程度依赖于疾病和干预的性质。为进一步阐明这些方面,我们将在下一节提供基于PubMed的文献调查总结,针对一些广泛研究的疾病的不同微生物组相关治疗干预措施。
与肠道微生物组相关的治疗干预措施可大致分为四类:
1.益生菌(具有推定治疗潜力的活微生物);
2.益生元(由宿主相关的、无害的有益肠道微生物选择性地利用以用于其生长的化合物,其可以赋予健康益处);
3.膳食干预(治疗性饮食方案或对个体常规饮食的改变,其可以直接或通过调节肠道微生物组赋予多种健康益处);
4.粪便微生物组移植(FMT;将粪便微生物从明显健康的供体转移到不健康的受体)。
此外,还有其他干预措施,如合生元(益生菌和益生元的组合)和后生元(postbiotics)(微生物细胞或热灭活微生物的成分,可以赋予健康益处)。
为了调查针对一些主要微生物组相关疾病的干预试验的情况,我们使用抽象检索字符串进行了PubMed文献检索,如下表所述。

下图a显示了410项针对一些广泛传播、广泛研究的疾病的微生物组相关干预措施人体试验的疾病病灶分布总结。
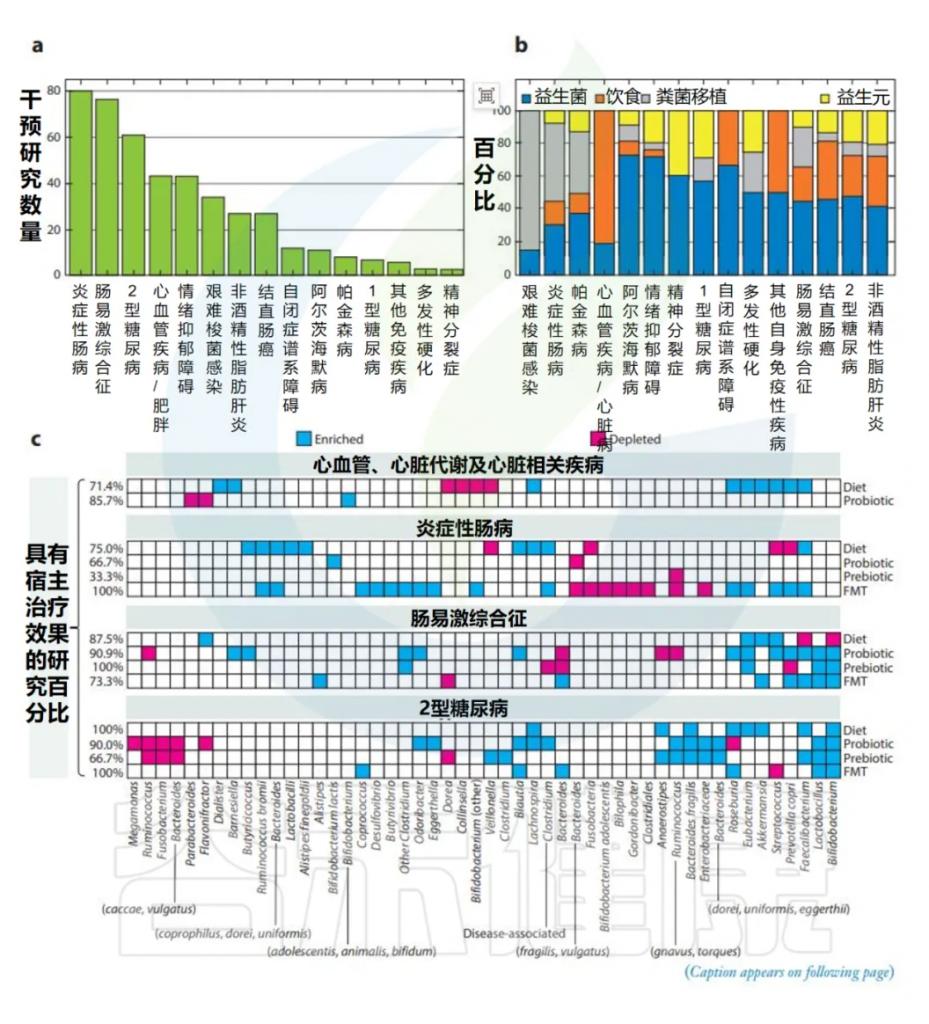
doi: 10.1146/annurev-med-051223-031809.
(a)使用条形图总结干预研究的疾病焦点。
(b)每种疾病的四种干预类型的相对代表性。根据干预措施的数量重点关注前四种疾病,仅选择随机安慰剂对照试验,并研究了宿主和微生物组的影响。还确定了一项显示至少一种宿主相关临床性状改善的研究。
(c)热图总结了针对前四种疾病的四种干预类型所观察到的微生物群相关影响。对于每种疾病干预组合,在至少两项研究中显示富集或耗尽的微生物谱系分别标记为富集或耗尽,并提到具有宿主相关有益作用的研究百分比。这些观察结果强调了启动大型基于微生物组的分析研究的必要性,以确定不同人群的正常微生物组参考,为人群定制的微生物治疗和诊断提供未来路线图。
肠道相关疾病如炎症性肠病(IBD)和肠易激综合征(IBS)占这些干预措施的最大比例(410例中的155例,或38%),其次是2型糖尿病和、心血管和心脏相关疾病(410例中的104例,或25.3%)。神经、心理和脑相关疾病,如抑郁症、自闭症谱系障碍、阿尔茨海默病、帕金森病和精神分裂症,共占19%(410人中的77人)。其他疾病包括艰难梭菌感染(CDI; 7.7%),结直肠癌(6%),肝脏相关疾病如非酒精性脂肪肝和非酒精性脂肪性肝炎(6%),以及其他自身免疫性疾病,包括1型糖尿病和多发性硬化症(累计占3.6%)。 因此,尽管优先关注某些疾病,但微生物相关干预的疾病焦点是多样化的。
1
不同疾病需要特定的干预措施更有效
干预措施的性质显示出疾病特有的趋势(图b)。针对CDI的干预主要是粪便微生物组移植(82.3%),FMT的第一个随机临床试验涉及复发性CDI患者,至今仍是最成功的干预措施,尤其在真正的生态失调环境中。
这与针对心血管、心脏代谢和心脏疾病的干预形成对比,这些干预主要是饮食(80.9%)。虽然肠道相关疾病(如IBS和IBD)主要使用粪菌移植和益生菌,但饮食干预和益生菌在2型糖尿病和非酒精性脂肪性肝病/非酒精性脂肪性肝炎的微生物组干预中占主导地位。
不同的神经、心理和大脑相关疾病也表现出不同的干预类型。阿尔茨海默病、抑郁症和精神分裂症主要针对益生菌干预,而帕金森病则有相当多的基于粪菌移植的干预试验。
对这些干预研究的深入调查(仅关注前四种主要疾病的安慰剂对照试验,即IBS,IBD,T2D以及心血管,心脏代谢和心脏疾病,这些疾病的干预研究数量最多)提供了对其影响的进一步见解(图c)。对于疾病干预型组合,至少三分之二的研究报告了宿主相关临床特征之一的显著改善。
许多与微生物组相关的影响也表现出合理的一致性。例如,除了益生菌如乳杆菌外,一些与消化道健康/正常肠道微生物组相关的谱系,如粪杆菌属、真杆菌属、阿克曼氏菌属、双歧杆菌属、紫单胞菌科和经黏液真杆菌属,显示出针对多种疾病的不同干预类型的富集。 这表明这些谱系可用作微生物组衍生的终点,以计算不同微生物组相关干预措施的有效性。
2
不同疾病和干预措施存在差异和冲突
不同疾病和不同干预措施的变化模式也存在差异和冲突。在特定情况下,这些变化可能与更广泛的干预类别的不同亚型有关。例如,粪杆菌属谱系在针对IBD、T2D和心血管、心脏代谢和心脏疾病的饮食干预后正富集,但在针对IBS的饮食干预后耗尽。
这可能是因为,虽然前三种疾病的大多数饮食干预是基于地中海/素食/素食主义者制度,但IBS的大多数饮食干预是基于低发酵寡糖,二糖,单糖和多元醇(FODMAP)饮食。
微生物组相关干预措施的反应在宿主或微生物组水平上与性别和年龄等人口统计学因素相关。先前研究发现,在缺乏特定应答分类群的情况下,微生物组干预可能对宿主产生有害影响。因此,对一个群体有效的干预措施可能对另一个群体有害。目前,我们尚不清楚这些针对特定人群的干预措施的效果,因为大多数研究是在工业化国家进行的,而在非工业化人口中的实施相对较少。
这些观察结果为启动大型基于微生物组的分析研究奠定了基础,以确定不同人群的正常微生物组参考。
提高对人群正常微生物组构成的理解需要在多个方面进行重点研究。
1
增强非工业化国家和不同地域的微生物组数据
这应包括整个非洲和特定的亚洲次区域的微生物组采样和测序。全世界范围来说,需要整个非洲和特定的亚洲次区域的微生物组采样和测序。国内的样本数据量,相对东部来说,西部地区人群的肠道样本量偏少,尤其青海,西藏或一些偏远的山区等。群体水平的微生物组测序项目应包括代表整个群体的不同个体亚群的数据。
2
促进前瞻性队列研究
微生物和疾病和其他相关健康指标的探索和确定需要更多的前瞻性队列研究。
前瞻性队列有两大优势。首先,确定了纵向微生物组稳定性和弹性的功能决定因素(换句话说,微生物组的生态健康)。其次,它们有助于识别疾病特异性风险相关的微生物组配置。
因此,纵向研究对于完善可能被认为是正常的微生物组至关重要。
3
整合宿主相关多组学、人口统计学和生活方式与微生物组的分析
将宿主相关的基本信息、健康数据(人口统计、饮食和药物使用)与微生物组分析相结合,确定相关的菌群特征分类群,将有助于研究宿主适应的机制基础,并进一步帮助识别与某些疾病未来发展相关的个体(和微生物组特征)。
4
改进鉴定微生物组和宿主健康功能决定因素的方法
将宿主相关的健康数据(人口统计、饮食和药物使用)与微生物组分析相结合,将有助于研究宿主适应的机制基础,并进一步帮助识别与某些疾病未来发展相关的个体(和微生物组特征)。
谷禾多年来一直从事微生物的研究和检测实践,我们收集和整理了世界范围内包含肠道微生物组数据的主要人群队列研究。我们特别关注了欧洲的大型研究计划(这些研究建立了广泛的生物样本库和详细的表型数据收集协议)、规模可观的中国人群研究(这些研究提供了亚洲人群肠道微生物群特征的见解),以及美国的目标性研究(这些研究结合了普通人群采样和特定疾病调查)。总结这些队列的关键特征,包括研究设计、人群统计学特征、数据收集方法和数据可及性,此外,每项队列还简要描述了每个队列的特点,突出了不同人群之间的共性和差异,为研究人员提供有价值的参考资源。理解这些现有资源可以促进未来的研究合作,实现跨队列的荟萃分析,并指导新的微生物组研究的设计。
谷禾长期专注于肠道菌群研究和临床转化,通过对全球肠道菌群队列数据以及谷禾数十万肠道菌群样本数据的整合,目前已清洗整理超200万例以肠道菌群数据为核心,涵盖临床病例、饮食调查、代谢指标以及蛋白和临床检测在内的超大规模样本队列数据。有效的整合和利用这些数据将能极大的推动肠道菌群在健康和医疗领域的落地和解析肠道菌群与全维度生物表征的内在关联。
例如,瑞典 SCAPIS 队列:
队列基本信息
来源和设计:
SCAPIS(The Swedish CArdioPulmonary BioImage Study)是一项前瞻性的人群基础观察研究,旨在改善心血管疾病、慢性阻塞性肺病和相关代谢紊乱的风险预测和理解。
研究在瑞典的六个市政区域进行,参与者为50至65岁的男性和女性。
人群数量:
总共招募了30,154名参与者。
本研究基于来自乌普萨拉和马尔默两个研究地点的11,287名参与者的子集。
数据收集:
参与者在家中收集粪便样本,并在研究中心进行血液样本采集。
粪便样本用于宏基因组分析,血浆样本用于代谢组学分析。
最终,8,583名参与者的数据被用于分析,这些参与者拥有高质量的宏基因组和代谢组学数据。
数据访问
数据存储和访问:
匿名化的宏基因组测序数据已存储在欧洲核苷酸档案中。
代谢组学分析由Metabolon公司在美国德克萨斯州进行,部分光谱数据存储在MetaboLights中。
由于数据包含敏感的个人信息,需通过瑞典伦理审查委员会和SCAPIS数据访问委员会的批准才能获取。
研究人员需获得伦理批准,并遵循SCAPIS数据访问委员会的申请程序和条件。
通过这些策略,可以帮忙我们更全面、更精准地理解人体微生物组与健康的复杂关系,为未来的精准医疗和个性化干预奠定坚实的数据库基础。

主要参考文献
Shete O, Ghosh TS. Normal Gut Microbiomes in Diverse Populations: Clinical Implications. Annu Rev Med. 2024 Nov 18.
Fan Y, Pedersen O. 2021. Gut microbiota in human metabolic health and disease. Nat. Rev. Microbiol.19:55–71
Mayer EA, Nance K, Chen S. 2022. The gut–brain axis. Annu. Rev. Med. 73:439–53
Ruff WE, Greiling TM, Kriegel MA. 2020. Host–microbiota interactions in immune-mediated diseases.Nat. Rev. Microbiol.18:521–38
Ghosh TS, Shanahan F, O’Toole PW. 2022. Toward an improved definition of a healthy microbiome for
healthy aging. Nat. Aging 2:1054–69
He Y, Wu W, Zheng HM, et al. 2018. Regional variation limits applications of healthy gut microbiome reference ranges and disease models. Nat. Med. 24:1532–35