-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


每个人都想长生不老,但没有人想变老。我们渴望长寿,但是对衰老又非常恐惧。研究发现长寿者和体弱者的微生物群之间存在着深刻的差异,与年龄相关的微生物失调会导致肠道通透性、全身炎症和过早死亡,但这些差异在多大程度上促进或阻止了晚年的健康尚不清楚。肠道微生物群随着年龄的增长而变化,但目前尚不清楚这些变化在多大程度上是由于生理变化、年龄相关性炎症或免疫衰老、饮食、药物或慢性健康状况引起的。
近日,加拿大麦克马斯特大学(McMaster University)的研究团队发表在《细胞》子刊《Cell Host & Microbe》究肠道微生物群与不健康衰老进行了回顾讨论分析。

与年龄相关的肠道生理变化可能会改变微生物群
生命早期微生物群的动态特性是众所周知的,但更多细微的多样性变化一直持续到中年(大约40岁),此时存在相对稳定期。这种稳定性丧失和年龄相关性失调开始的时间点可能因个体而异,如果部分是由衰老生理学变化引起的,则可能与生物年龄(即生理年龄)比时间年龄(即寿命数)的相关性更大。弄清年龄、药物、饮食和共病性对微生物失调的相对贡献是一项挑战性的工作(图1);然而,在像老鼠、鱼、线虫和果蝇这样的模型生物,表明至少某种程度的生物失调是衰老的一个特征。
同样,对老年人的饮食、生活方式和药物进行的大量仔细调查表明,某些微生物物种的增加和减少是随着年龄的增长而变化的。肠道生理学随着年龄的增长而变化,由于微生物群在很大程度上是由生理学形成的,这些变化可能有助于某些微生物的持续或生长。在模型生物体中,预防肠道生理学中的年龄相关变化可缓解微生物失调并延长寿命。例如,老鼠的粘液分泌随着年龄的增长而减少,形成一个更薄且不连续的粘液层。粘蛋白在胃肠道内提供一层保护膜,防止微生物直接与上皮细胞相互作用,当这一层丧失时,通常不会与上皮层相互作用的微生物会引起炎症反应。它也是梭状科、阿克曼菌科、双歧杆菌科和拟杆菌科中许多菌株的营养来源,所有这些菌株都显示出随着年龄的变化而变化。
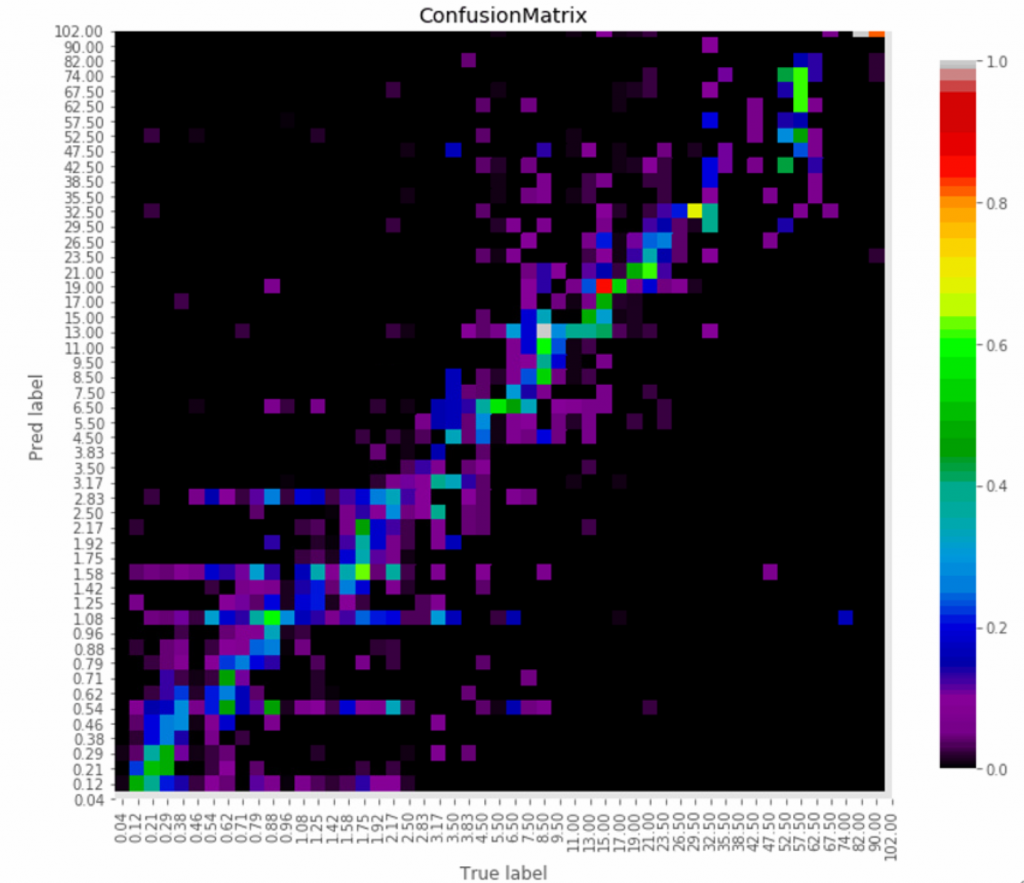

谷禾健康-肠道年龄预测模型图
从上图看出肠道年龄和生理年龄基本是符合的,说明人体真实年龄与肠道菌群的年龄特征是相符合的。
健康相关的行为也有助于健康的微生物群,如果微生物群随着年龄的增长而变化,不同老年人之间的肠道微生物差异比不同年轻人之间更大。
早期年龄段的菌群变化更加迅速,基本上出生第一年每个月都有其对应的年龄菌群特征,之后到菌群的年龄特征范围变宽,在30~50岁左右以5年为一个年龄段。50岁以后基本以10年为一个年龄段,而且肠道菌群由于疾病状态和菌群紊乱等情况导致的年龄偏差会变大。
与通常认为的越健康的人肠道菌群越年轻,或者越健康的宝宝肠道年龄更早熟的认知不同,健康人的肠道菌群年龄恰恰是最符合真实年龄的,与真实年龄差异越大,无论是年轻还是年老,都意味着肠道菌群出现问题。
粘液代谢微生物如Akkermansia muciniphila, Bacteriodes fragilis, Bacterioides vulgatus, Bifidobacterium和 Prevotella 等是否对粘液层的降解起作用尚不清楚,尤其是因为粘液代谢物种,如类杆菌属和嗜粘杆菌在百岁老人中增多,因此被认为是有益的。嗜粘液单胞菌代谢粘蛋白的能力与其刺激粘蛋白产生的能力相结合。因此,补充一些菌株已被证明可以改善年龄相关的粘蛋白损失,并具有积极的健康和免疫益处,包括延长类幼鼠的寿命。
肠功能是否存在老年性变化存在相当大的争议。然而,合理一致的报告支持细胞旁通透性增加和结肠运输减少。一般的共识是结肠运输减少可能是由于老化肠道的生理变化,而通透性增加是由于年龄或健康状况相关的炎症。局部炎症可以通过微生物群的变化直接或间接调节。
炎症是肠道通透性和微生物失调的驱动因素
衰老,以及伴随衰老而来的慢性健康和代谢状况,其特征是轻度慢性炎症的增加。炎症细胞因子水平高于年龄平均水平的个体,其中最常测量的是白细胞介素(IL)-6和肿瘤坏死因子(TNF),更容易发展成慢性健康状况或虚弱者,活动较少,面临过早死亡。“炎症老化”影响肠道完整性,并可能与微生物群的变化有因果关系(如下图)。
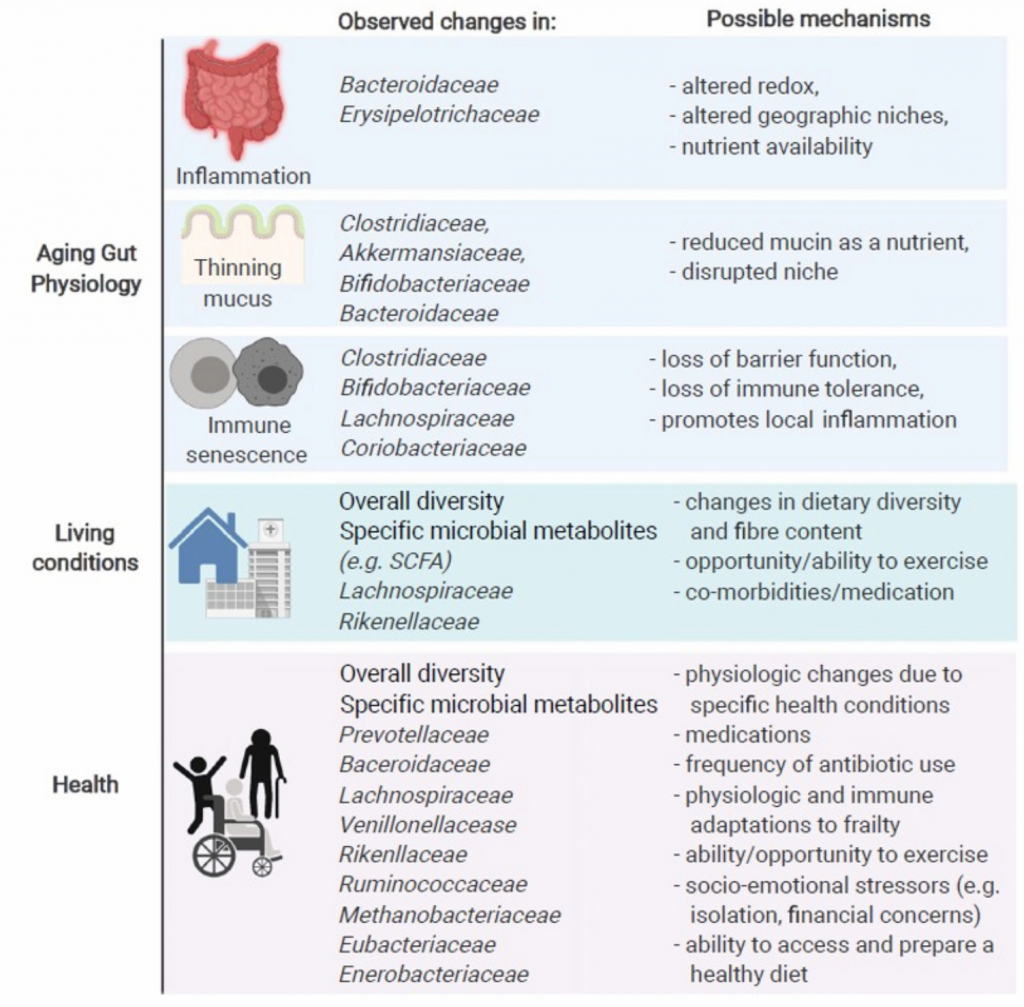

图1 老化微生物区系的变化
微生物群中与年龄相关的变化归因于生理,生活方式和健康状况。这些因素中的每一个都与微生物群某些成员的相对丰度变化有关。列出了一些可能解释观察到的增加或减少的行为,代谢和生理机制
老的TNF基因敲除小鼠(18个月以上)与野生型(WT)小鼠不同,老年小鼠(但不是年轻小鼠)的微生物群落在抗TNF治疗后发生变化。同样,在缺乏炎症信号负性调节因子NLRP12的小鼠中,保护的结肠炎Lachnospiraceae菌减少,而促进结肠炎的Erysipelotrichaceae以TNF-和IL-6-依赖的方式增加。这两项研究都发现这些物种相对丰度的变化依赖于肿瘤坏死因子,这表明这些物种的变化更可能依赖于炎症而不是年龄。这些微生物能够更好地适应当地氧化还原和营养环境的变化,这将使它们在发炎的肠道中获得竞争优势。这可以解释为什么几乎所有慢性炎症性疾病(如心血管疾病、痴呆症和炎症性疾病)都与微生物失调有关。一个补充的解释可能是在炎症反应过程中,特定的微生物生态位丢失或受到干扰。炎性细胞因子的表达增加会降低紧密连接蛋白(例如,zonulin和claudins)的表达,这会增加通透性,并可能导致炎症持续。
肠道驻留和招募的髓样细胞对于维持肠道完整性以应对微生物群的扰动至关重要。髓系对年龄相关性炎症的影响特别敏感。慢性炎症损害单核细胞和中性粒细胞的发育和组织巨噬细胞功能。这些细胞吞噬能力下降,调节失调或过度炎症反应导致病理学改变。髓系免疫衰老在多大程度上导致屏障功能受损或微生物组功能障碍尚未完全阐明,但减少慢性炎症可改善髓系功能障碍并减少失调。
虽然年龄相关的变化在肠道内的淋巴细胞中的作用尚未完全确定,但淋巴细胞群体中似乎存在微生物群依赖性和年龄依赖性变化。衰老肠道的变化与艾滋病毒携带者的变化有着强烈的相似性。在这两种情况下,驻留T细胞(尤其是CD4+T细胞)的数量或功能降低,这被认为是导致微生物失调、肠道通透性和全身炎症的原因。尽管淋巴组织年龄相关的变化与微生物失调之间的因果关系尚未被证实,但在猿猴免疫缺陷病毒(SIV)感染的灵长类动物中的研究表明,当CD4+数量因抗病毒治疗而增加时,微生物失调至少部分被逆转。有趣的是,在发炎的肠道中,无论是在衰老、艾滋病病毒或炎症性肠道疾病的情况下,微生物的分布都相当保守,这意味着这些微生物对炎症肠道的适应能力更强,与特定的健康状况无关。
长寿者与虚弱者的区别
对长寿老人(即百岁老人和超级百岁老人)的研究发现,他们的微生物群落往往更为多样,与健康状况较差的个体相比,微生物类群数量更多(图1)。事实上,α多样性似乎是长寿的合理预测因素,这意味着,但并非证明,维持或促进多样性的饮食和其他干预措施可能值得老年人采用。
即使在地理位置不同的百岁老人中(即中国人与意大利人),毛螺菌科、疣微菌科和艾克曼菌的成员也很丰富,这意味着这些可能是长寿和健康微生物群的普遍特征。这一发现尤其引人注目,因为特定微生物和疾病之间的许多联系因地理位置而异。对长寿者的微生物组进行的宏基因组分析发现,一些与获取营养有关的基因得到了丰富;然而,在所有与长寿和健康相关的生活方式因素中,饮食,特别是高纤维饮食是最常被采用的。微生物组组成的差异是造成这些个体异常年龄的原因,还是谨慎生活方式的结果,这将是一个挑战性的解剖。相比之下,动物模型的数据表明,老化相关的微生物失调会导致过早死亡。
当中年杀手鱼补充了年轻的微生物群时,它们的寿命延长了,而果蝇的老化微生物群促进了肠道通透性和过早死亡。
体弱者的研究说明了不健康衰老的极端情况。
体弱被定义为“由于多种生理系统的衰老相关的储备和功能下降,从而构成应对日常或急性应激源的能力,而导致衰老的临床可识别状态”。 体弱并非健康状况不佳的必然状态,健康状况相对较年轻的个人可能会体弱。 尽管我们经常在衰弱的个体中发现许多与衰老相关的疾病(例如,肌肉减少症,行动不便,慢性健康状况),但这些疾病中的任何一种的存在并不一定意味着一个人处于衰弱状态。 量化体弱性很复杂,但很关键,因为与年代年龄相比,体弱性可以更好地预测寿命和风险。 因此,体弱者的微生物组的组成与老化的微生物组不同,并且它们是不可互换的。 虚弱者的研究补充但不替代疾病相关的营养不良的研究。
体弱者的微生物群最一致的特征是多样性的丧失。 丧失多样性的原因很复杂,其范围包括饮食变化,运动能力或机会降低,长期护理设施中的居住,抗生素暴露量的增加以及药物的改变。 居住社区的老年人在服用抗生素时多样性急剧下降,但他们的微生物群最终会“反弹”,类似于他们的抗生素前微生物群。 虚弱者的老年人服用抗生素后多样性的丧失就不那么明显了,因为他们一开始就没有那么多的多样性。除了降低的α多样性外,虚弱者的微生物群中某些类群或种类也增加了,包括梭菌和肠杆菌科的成员。但是Lachnospiraceae, Ruminococcaceae,Erysipelotrichaceae,Prevotella却减少了,包括潜在的“益生菌”物种,如Faecalibacterium prausnitzii。 虚弱者的微生物群的组成与虚弱者程度,精神健康,肌肉减少症,全身性炎症和其他健康状况相关,但尚不清楚这些因素是因果还是相关的。
全身性衰老在衰弱方面有充分的文献记载,但没有数据表明虚弱者的肠道具有更高的渗透性或粘液消耗性,或者它是否具有与微生物营养不良有关的其他特征 老肠。 相比之下,饮食是导致虚弱者的微生物群特征的原因的证据令人信服。 饮食,特别是低纤维/蔬菜和高饱和脂肪/糖饮食会导致虚弱者的微生物组。 不幸的是,缺乏纤维的饮食似乎是导致长期居住在长期护理机构中的微生物群死亡的主要原因。
体弱者和长寿者的一个共同特征是与营养获取相关的特定微生物代谢产物的变化,炎症调节和肠道完整性。 一直有报道说短链脂肪酸(SCFA)的产生减少, 但是由于富含纤维的食物的减少似乎与虚弱者密切相关,因此很难确定原因和结果。 SCFA包括丁酸酯,丙酸酯,乙酸酯,乳酸和乙酸,其中丁酸酯是屏障功能的重要介体,因为它促进上皮细胞增殖并增加紧密连接蛋白的表达。 其他SCFA是肠道常驻微生物的能源,从而支持多样性。 观察到的与年龄和体弱相关的SCFA产生物种(如Lachnospiraceae和Ruminococcus)的下降。 是否直接导致屏障功能障碍或晚年健康尚待确定。 在一项衰老小鼠研究中,饮食不随年龄而变化,粪便丁酸增加,这表明观察到的人的SCFA与年龄和体弱相关的下降可能是由于饮食的改变而不是按年龄或健康状况。 有趣的是,来自老年小鼠的富含丁酸盐的微生物群对神经发生有有益作用,但并未改变肠的完整性,这表明丁酸盐的有益作用并不局限于其在肠道完整性中的作用。
微生物和肠道生理的性别差异
生命早期微生物群的动态特性众所周知,但多样性的细微变化一直持续到中年,此时存在一段相对稳定的时期。
这种稳定性丧失和与年龄相关的生物失调开始的时间点可能因人而异,并且如果部分是由于衰老生理学的改变引起的,则与生物学年龄(即生理年龄)的相关性要比按时间顺序(即 年)。 区分年龄,药物,饮食和合并症对微生物营养不良的相对贡献具有挑战性(图1); 但是,据报道,模型生物如小鼠,鱼类,线虫和果蝇与年龄有关的变化,提示至少某种程度的营养不良是细菌的特征。在C57BL/6小鼠中,雌性小鼠的乳杆菌科相对丰度更高,而雄性小鼠则有更多的瘤胃球菌科和Rikenellaceae菌科。
这些差异对易感性或对健康状况的保护作用的程度尚不清楚,但是当用雌性小鼠的菌群定植无病菌小鼠时,与雄性微生物菌落定殖的无病菌小鼠相比,细胞炎症减少了。 重要的是,这些变化与受体小鼠的性别无关。 在人类中,性别差异并未得到很好的研究,尽管年轻(<40岁)女性的α多样性更高,而且细菌和拟杆菌科的相对丰度因性别而异。 在小鼠中,由于雌激素介导的紧密连接蛋白增加,已证明与年龄相关的性激素变化会影响通透性。
性激素对人体肠道生理的影响以及最终对人体微生物失衡的贡献尚待确定。 在人类中,饮食,地理和健康状况对微生物群的影响可能大于生物学性别。
老龄化干预
由于肠道生理的改变而导致的老化微生物组的改变将不容易被修改。 然而,那些可归因于饮食或与年龄有关的炎症的疾病是干预的目标,饮食和运动可改善疾病本身。 尽管涉及饮食调整和/或益生菌使用的干预措施已在健康的年轻人中显示出适度和短暂的影响,但衰老微生物组多样性的降低可能使其更易于操作。 确实,在小鼠模型中,干预中年会改善某些晚年结局。
正如讨论的那样,肠道微生物组中许多与年龄和体弱相关的变化是不良饮食的特征。
与此相一致,已发现老年人采用富含纤维的“地中海”饮食的干预措施可改善健康状况,并将全因死亡率降低多达50%。 此外,这些饮食干预措施已显示可增加微生物多样性和SCFA,并减少全身性炎症。 尽管通过采用健康饮食也可以改善或预防与全身性炎症相关的晚年健康状况(例如心血管疾病,虚弱),但要确定人与人之间是否存在因果关系仍是一项挑战。 益生元和益生菌也已用于改善免疫功能,通过改善疫苗接种反应和减少感染,虚弱者和其他后期健康状况(例如,心血管疾病)。 当前的益生菌方法基于通常不是人类肠道固有的菌株,不会占据永久居所,并且可能通过非特异性机制(例如定植抗性)发挥其有益作用。鉴定具有促进健康作用且随年龄或年龄相关健康状况而降低的共生微生物可以在改善晚年健康状况方面更为成功,而在衰老过程中重新引入微生物代谢物ost可能与引入活菌一样有效和安全。
未来方向
模式生物已经并将继续领导对肠道通透性和早期死亡率的特定微生物-宿主相互作用的研究。最初的临床试验证明了使用人类共栖体的价值。随着我们发现更多与健康衰老相关的菌株和特定的微生物基因途径和代谢物,我们将能够针对特定的健康状况量身定制治疗方法,或对抗微生物群危害药物或条件的影响。在我们了解单个微生物或微生物基因改变衰老轨迹的机制之前,我们需要使用更广泛的干预措施。一些微生物类群随着年龄、慢性病和其他炎症条件的变化而不断变化,这意味着减少全身性和局部性炎症可能会带来立竿见影的健康益处。用饮食中的钨酸盐或铁来改变发炎肠道的氧化还原状态已被证明可以防止大肠杆菌科细菌的生长。同样,一些常见的廉价药物,如二甲双胍,除了具有预期的代谢作用外,还可以降低微生物失调的发生率。这些疗法可能是非特异性的,但它们也有便宜的优势,因此很容易融入健康的老龄化计划。
结论
高龄是一个独特的发展阶段,老年人不仅仅是慢性健康状况的总和。衰老的微生物群,就像衰老本身一样,似乎承受着韧性下降的痛苦。接触抗生素、饮食、药物和生活方式的改变对老年人肠道菌群的组成有很大的影响(如果不是灾难性的)。尽管缺乏弹性是个问题,但它也可能提供一个机会之窗。虽然饮食和益生菌干预措施对健康的年轻人的影响通常很小且持续时间很短,但在老年人和体弱的成年人中,它们似乎有更明显和更持久的影响。
采用“保护微生物”饮食的障碍与遵守任何饮食建议是一样的。流动性、独立性和经济自主性的老年人已经遵守公共卫生建议,以实现健康和均衡的饮食,而经济、行动能力和自主性受到限制的老年人愿意但无法遵守。具有讽刺意味的是,开发益生菌或益生元预防性“药物”来改善与年龄相关的健康状况,可能比饮食干预更容易纳入常规护理,因为获得药物的社会经济障碍在获得普遍医疗保健的老年人中不那么严重。
在人口水平上,老龄化是一个不平衡和不公平的过程,我们中的一些人衰老的速度比其他人要快;然而,虚弱或亚健康人群肠道微生物事最容易被控制的。这一事实,再加上公众对微生物组学知识的热情,可以为改善老年人的健康状况提供一个独特的干预点。
参考文献:
DeJongEN, Surette MG, Bowdish DME. The Gut Microbiota and Unhealthy Aging:Disentangling Cause from Consequence. Cell Host Microbe. 2020;28(2):180-189.doi:10.1016/j.chom.2020.07.013