-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com

谷禾健康
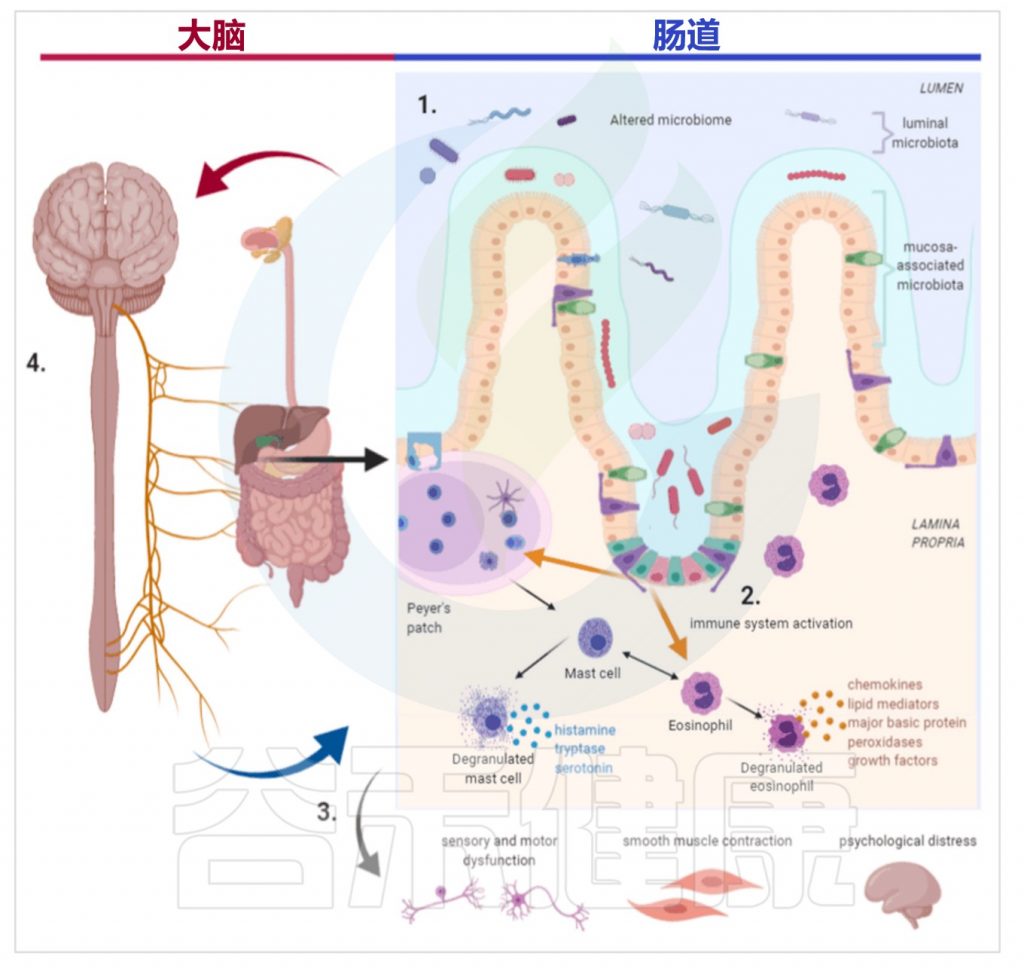
近年来,肠道屏障通透性异常增加(intestinal hyperpermeability)的临床诊断呈上升趋势,其病理生理机制涉及多个层面的复杂相互作用。
肠道屏障就像一堵城墙,一旦“城门大开”,各种“异类分子”如病原信号(PAMPs)、脂多糖(LPS)、未消化的蛋白碎片就会趁机溜进固有层和血液,掀起一场免疫风暴。
肠道固有层宛如“安检总站”,这里的树突状细胞和巨噬细胞负责利用“雷达”——比如Toll样受体——扫描入侵分子,然后拉响警报,释放大量炎症信号分子(TNF-α、IL-1β、IL-6)和趋化因子,引发局部炎症反应。
被激活的免疫细胞及其炎症介质通过门静脉循环和淋巴系统进入全身循环,触发远端器官的炎症反应,这种”肠-器官轴”的病理连接可能是类风湿关节炎、强直性脊柱炎、系统性红斑狼疮等自身免疫性疾病以及过敏性疾病、神经退行性疾病的潜在发病机制。
同时,肠道屏障功能受损导致肠道微环境稳态失调,有益共生菌群数量下降而潜在致病菌过度增殖,形成肠道菌群失调,进一步破坏肠道屏障功能并释放更多内毒素,加剧炎症反应,形成病理性正反馈循环。
造成肠道屏障告急的“罪魁祸首”很多:慢性压力、滥用抗生素、非甾体消炎药、高脂快餐、食品添加剂、各种感染和遗传易感性都可能“推波助澜”。理解这套复杂机制,有助于我们探索科学高效的“修复之路”。
本文介绍了目前肠道屏障受损的成因、健康影响和尝试干预改善过度渗透的肠屏障的一些方法。研究表明,预防肠道屏障受损以及在屏障受损时开发治疗方法至关重要。
肠上皮细胞是外界环境和体内环境之间最大的接触部位。胃肠道上皮屏障的功能是防止外来抗原和微生物进入,同时允许吸收必需的营养物质、水和电解质。
肠道屏障由物理屏障、生化屏障、免疫屏障和微生物屏障组成。
肠道屏障
Macura B,et al.Clin Exp Med.2024
▸ 物理屏障
物理(上皮)屏障是整个肠道屏障的重要组成部分。它由单层特化细胞组成:肠上皮细胞、杯状细胞(产生粘蛋白)、潘氏细胞(产生抗菌肽和蛋白质)、肠内分泌细胞、M细胞和肠干细胞。
这些细胞每3-5天更新一次。上皮细胞具有多种功能,并且紧密相连。
▸ 生化屏障
生化屏障由粘液构成,覆盖并保护上皮细胞免受病原体和有害物质侵害。
粘液是一种富含水分(90%–95%)、电解质、脂质(1%–2%)和蛋白质的稀薄分泌物,其中粘蛋白(1%–5%)为其主要结构和功能成分。
doi: 10.1007/164_2016_107.
上图展示了小肠和大肠粘液的生成与分布,包括内外粘液层的结构,并标示了杯状细胞从粘液产生到分泌和扩散的全过程(步骤1至7)。
粘液分泌是一个复杂的过程:杯状细胞在从隐窝底部迁移时用Muc2填充其分泌囊泡,并含有其他成分,例如IgG结合蛋白(FCGBP)的Fc片段、氯通道附件1(CLCA1)、酶原颗粒蛋白16(ZG16)和前梯度同源物2(AGR2)。这些囊泡与顶膜融合后,通过胞吐作用释放内容物,实现粘液分泌。
最后,粘蛋白可以分为两种不同的类型:跨膜粘蛋白和形成凝胶的粘蛋白。
▸ 免疫屏障
免疫屏障与肠道中淋巴组织的存在有关,称为肠道相关淋巴组织(GALT)。GALT系统分布于肠道粘膜及粘膜下层紧邻上皮细胞处,包括上皮内淋巴细胞、派伊尔集合淋巴结和淋巴细胞簇。
GALT系统含有抗原呈递细胞、T细胞、B细胞、浆细胞、巨噬细胞、肥大细胞和粒细胞,并且分泌型IgA(sIgA)主要在肠道中合成。
▸ 肠道屏障的功能-紧密连接调节通透性
大多数膳食蛋白质通过肠上皮细胞进行内吞作用。溶酶体降解导致蛋白质分解成更小的肽,从而避免激活免疫系统。液体和溶质在细胞之间运输。这种转运由紧密连接(TJ)调节。
紧密连接构建蛋白通过特殊的封闭小带蛋白(ZO)与肌动蛋白结合,肌动蛋白是细胞骨架的一部分。 这些蛋白质是调节紧密连接功能的分子的靶元件,因此负责调节肠屏障的通透性。
肠道屏障在外源性或内源性因素的作用下会受到损害,从而导致其正常功能被破坏。
▸ 饮食因素
不良饮食模式
高脂肪、高糖、高盐饮食
过度加工食品和快餐
缺乏膳食纤维的精制食品
过量饮酒
特定食物成分
人工添加剂、防腐剂
过量的乳化剂
某些人工甜味剂
过敏原食物(因人而异)
▸ 药物因素
抗生素:破坏肠道菌群平衡
非甾体抗炎药(NSAIDs):直接损伤肠粘膜
质子泵抑制剂:长期使用影响胃酸分泌
化疗药物:对肠道上皮细胞有毒性作用
▸ 生活方式因素
压力相关
慢性心理压力
睡眠不足或质量差
过度疲劳
运动相关
久坐不动的生活方式
过度剧烈运动(可能增加肠通透性)
▸ 环境因素
空气污染和化学毒素暴露
重金属污染
农药残留
吸烟
▸ 疾病和感染
肠道感染(细菌、病毒、寄生虫)
炎症性肠病
自身免疫疾病
糖尿病等代谢性疾病
▸ 年龄因素
衰老过程中肠道屏障功能自然下降
婴幼儿肠道屏障发育不完善
▸ 空气、水、食物污染等破坏了肠上皮屏障
近几十年来,城市化与全球化带来了巨大的环境变化,污染和气候变化,工业和家庭中常用的化学化合物,生态系统变化,不健康的饮食以及兴奋剂,主要是酒精,烟草和电子烟,可能会破坏皮肤和粘膜表面的上皮屏障。
空气、水、食物污染、微塑料、纳米颗粒、家用化学品和烟草烟雾是常见的上皮屏障破坏因素。这些因素复杂交互,但对生物体的影响取决于其组合及个体易感性。
▸ 微塑料和纳米颗粒会减少肠道粘液产生
近年来,食品和饮用水中的化学污染显著增加,即使是常用的食品添加剂、杀虫剂和饲料添加剂也在其中。最近,关于微塑料和纳米颗粒污染食品的报道越来越多。这些物质可以很容易地穿透组织并与细胞结构相互作用。
微塑料会改变蛋白质结构,与细胞膜脂质相互作用,诱导炎症基因转录,增加促炎细胞因子,导致内质网和线粒体功能障碍,甚至引发细胞因氧化应激而死亡。
纳米颗粒也能引起类似的蛋白结构变化和细胞膜相互作用。纳米塑料已被证明可以诱导炎症基因的转录,增加促炎细胞因子的水平,并改变某些蛋白质的表达。微塑料在胃肠道内吸收率高,可在体内外环境中积累。动物实验证实,聚苯乙烯微塑料会损伤肠道屏障并减少粘液分泌。
下表总结了被认为对肠道屏障状态具有有害影响的主要因素:微塑料,纳米颗粒,洗涤剂和乳化剂,肠道微生物群状态和饮食。
doi: 10.1007/s10238-024-01496-9
暴露于环境因素可以直接削弱肠道上皮屏障的完整性并改变微生物组结构。上皮屏障渗漏和肠道菌群失调常同时出现,促进炎症发生,部分原因是由于免疫细胞紧邻上皮层。
上皮屏障受损时,免疫系统被激活,引发局部炎症,炎症可通过免疫细胞及其分泌的细胞因子扩散至其他系统和器官。因此,多种疾病的发展与上皮屏障渗漏相关。肠上皮受损后,机会性病原体易定植,菌群多样性下降。微生物可移位至更深组织,导致微炎症。此外,化合物暴露还能诱导免疫系统表观遗传变化,促进某些疾病的发生。
▸ 生态失调→上皮损伤→慢性炎症
大量证据表明,微生物组对肠道上皮健康至关重要。正常微生物群调节紧密连接蛋白表达、血管生成、通透性和免疫功能。上皮屏障渗漏时,细菌和病原体穿透上皮,引发炎症并参与多种疾病。过敏性疾病的上升可能与菌群失调和多样性下降有关。
微生物群受到饮食、药物(特别是抗生素、精神药物、质子泵抑制剂)及遗传等影响。与人体共生的非致病性菌群有助于免疫调节,有利于预防慢性疾病并维持免疫平衡。
健康的微生物群通过调控屏障通透性、紧密连接和局部免疫,维持上皮屏障功能。缺乏免疫调节因子,如短链脂肪酸,可导致免疫系统过度激活、上皮炎症和疾病。这种反应主要由TH2细胞、ILC2和嗜酸性粒细胞介导,肥大细胞和巨噬细胞等也参与其中。而菌群失调、上皮损伤和慢性炎症会形成恶性循环,阻碍上皮再生。
同时损伤上皮中的炎症持续激活免疫细胞,可导致炎症扩散至其他器官。
微生物群变化、肠道屏障受损与疾病相互依存,但其因果关系仍有争议。尚不清楚是菌群失调导致屏障功能障碍和疾病,还是疾病先引发炎症和屏障损伤,进而加重细菌移位和器官损害。
因此,肠漏究竟是疾病的起因还是结果?此外,有研究表明,呼吸道或肠上皮屏障破坏以及其他屏障(如血脑屏障、血管内皮屏障)减弱,可能会促进代谢及自身免疫性疾病的发生。
▸ 胃食管反流病患者食管壁存在渗漏
胃食管反流病(GERD)最常见的症状是烧心和反酸,影响全球超过10%的成年人。胃镜检查显示,只有约30%的患者存在明显糜烂,其余70%(非糜烂性反流病,NERD)虽无可见损伤,但仍有症状。
GERD就像胃酸不断冲刷食管墙壁,表面虽完好但可能已“渗漏”,问题可能在于连接细胞的“水泥”。研究发现,GERD患者食管中即使无表面破损,其“水泥”成分也发生了变化:部分蛋白(如E-钙粘蛋白)减少,而其他蛋白(如CLDN-1和桥粒蛋白)则增加。
▸ 功能性消化不良存在十二指肠黏膜屏障渗漏
功能性消化不良(FD)是一种常见的胃肠道疾病,表现为早饱、腹胀、上腹痛或灼热,且常规检查无法发现明确病因。
最新研究发现,FD的核心问题在于十二指肠黏膜屏障渗漏,不仅离子,大分子也能穿透。该屏障损伤与肥大细胞和嗜酸性粒细胞增多,以及ZO-1和钙粘蛋白等紧密连接蛋白减少有关,说明低度炎症和屏障受损是FD的主要致病机制。
▸ 肠易激综合征与“肠漏”有关
肠易激综合征(IBS)是一种常见的功能性胃肠疾病,典型表现为反复腹痛和排便习惯改变(如腹泻、便秘或交替)。
尽管具体病因不明,但大量证据表明,其核心机制与“肠漏”有关。研究发现,几乎所有类型的IBS患者都存在肠道屏障通透性增加的问题。这具体表现为:肠道细胞间的“水泥”(即紧密连接蛋白ZO-1等)被破坏或减少,同时存在低度的黏膜炎症(如肥大细胞活化)。
这种屏障功能的损害,使得肠道内容物更容易“渗漏”过去,激活免疫系统,最终导致了IBS特有的腹痛和排便紊乱等一系列症状。
▸ 高血压患者肠道屏障功能障碍患病率较高
近年来,越来越多的研究关注肠道微生物群与高血压之间的关系。大量证据显示,肠道菌群的生态失调不仅可能促进高血压的发生和发展,还可能加重病情。
与此同时,高血压本身也会对肠道微生物群的组成产生影响,进一步加剧生态失调。研究表明,维持适当和健康的微生物群状态有助于血压的正常化,改善心血管系统的健康,而理想的血压水平同样有助于微生物群落的维持与恢复。
已有结果显示,高血压患者较非高血压患者更易出现肠屏障功能障碍,肠屏障的损伤被认为可能与高血压的发病机制密切相关。这一发现为进一步研究血压调控与肠道健康之间的复杂联系提供了新的思路,也提示改善肠道屏障功能或许有助于高血压的防治。
▸ 炎症性肠病患者即便无症状也会出现肠道通透性增加
炎症性肠病(IBD)患者的肠道微生物群特征主要表现为促炎细菌数量的明显增加,同时多种细胞因子的表达也发生了显著变化。这些变化会导致机体免疫反应失衡,加剧炎症进程。
值得注意的是,在患者尚未出现明显的临床症状之前,尽管处于无症状期,肠道的通透性实际上已经发生了异常改变。这表明肠道屏障功能的损伤可能早于症状表现,为疾病的早期诊断和干预提供了理论依据。
▸ 肠道屏障和菌群稳定影响肝脏健康
研究数据显示,肠上皮细胞和血管屏障的损伤在非酒精性脂肪肝的发展过程中起着关键和必要的作用。肠上皮屏障功能的破坏,使得肠道内容物更容易进入血液循环,进而促进肝脏炎症和脂肪堆积。
此外,肠道菌群的失调以及肠道菌群结构的破坏与这一过程密切相关。肠道菌群异常会导致有害菌数量增加,正常菌群比例下降,其产生的代谢产物也会对肠道细胞产生毒性作用,影响细胞功能和屏障完整性。
这些机制不仅涉及非酒精性脂肪肝的发生与发展,在酒精性肝病中同样存在。酒精摄入可加重肠上皮与血管屏障的损伤,进一步削弱肠道屏障功能,从而成为酒精性肝病患者肠上皮功能障碍的主要原因之一。由此可见,肠道屏障及菌群的稳定性对于肝脏健康至关重要。
▸ 免疫性疾病患者存在菌群失调和屏障渗漏
类风湿性关节炎患者表现为血清zonulin水平升高、肠道菌群失调和屏障渗漏,强直性脊柱炎患者可见亚临床肠道炎症。潘氏细胞对肠道菌群失调的激活可能是疾病早期症状的原因,并证实了脊椎-关节轴的存在。
▸ 帕金森、自闭症患者存在胃肠道症状
在帕金森病中,患者在诊断前数年就表现出胃肠道症状。α-突触核蛋白是帕金森病的典型蛋白质,在肠道中合成,然后通过迷走神经运送到中枢神经系统。相比之下,自闭症谱系障碍儿童会出现肠道症状,如便秘、腹痛和腹泻。对肠道微生物群的研究表明,微生物群多样性与神经系统疾病、拟杆菌减少以及肠粘膜中紧密连接蛋白表达减少之间存在负相关关系。
▸ 糖尿病患者的肠道通透性发生变化
研究显示,肠道通透性变化早于1型糖尿病的临床症状出现,并且与紧密连接蛋白和生态失调的改变,尤其是丁酸盐产生菌减少密切相关。2型糖尿病患者的肠道菌群失调加重了屏障损伤,并促进了炎症状态,导致胰岛素抵抗和β细胞功能障碍。
此外,2型糖尿病患者的高血糖有助于持续的促炎状态。肥胖则与慢性低度炎症密切相关,主要表现为脂肪组织中促炎巨噬细胞的活性增加。代谢紊乱在肥胖人群中也更为常见。
doi: 10.1007/s10238-024-01496-9
在间接或直接诊断试验中,可以评价肠屏障通透性水平。
▸ 口服物质测试
间接检测方法包括口服试剂后测定其在血液或尿液中的浓度,最常用的是糖。乳果糖/甘露醇(L/M)试验是评估小肠通透性的常用方法,通过测量尿中两者的排泄量进行判断。乳果糖为大分子,仅在细胞间连接受损时吸收,甘露醇为小分子能自由通过肠屏障。L/M试验非侵入性且灵敏度高,此外还可使用其他单一或多种糖类的检测方法。
▸ 测量内源物质水平
此外,还可以测量血液中内源性物质的水平。这样的生物标志物包括例如连蛋白、脂肪酸结合蛋白(FABP)、瓜氨酸、胰高血糖素样肽(GLP)-2、脂多糖、脂多糖结合蛋白(LBP)或粪便α1抗胰蛋白酶(AAT)。然而,这些测试不像糖测试那样敏感。
▸ 新型影像技术
新的成像技术,特别是共聚焦激光显微内镜,允许在体内评价静脉注射荧光素作为造影剂后肠屏障的完整性。共聚焦激光显微内镜目前用于诊断胃肠道癌症,以及肠易激综合征或乳糜泻。放大1000倍可以检测肠上皮内的病理变化。
▸ 肠道菌群检测
肠道菌群检测可以提供非常重要的间接线索和风险评估。肠道菌群与肠道屏障健康密切相关。菌群测序可以发现一些可能导致或指示肠道屏障通透性增加的风险因素,例如:嗜黏蛋白菌,AKK菌以及扭链瘤胃球菌等菌对的丰度,以及产丁酸菌减少,特定有害菌增多:某些细菌(如部分革兰氏阴性菌)会产生脂多糖(LPS),这是一种强烈的炎症触发物,会破坏肠道屏障。菌群多样性降低:通常一个多样性低、不稳定的菌群生态系统,其维护屏障功能的能力也会下降。
总之,肠道菌群检测可以揭示与肠道屏障功能受损相关的菌群失衡状态,提供有力的间接证据和风险预警。
功能性胃肠道疾病(FGID)在临床上发病率高、症状慢性且治疗效果有限,已成为重大公共卫生问题。多种病理机制被提出,其中屏障通透性受损是常见特征。局部免疫激活与屏障损伤的先后关系及其在症状发生中的作用仍需进一步研究。
目前的研究表明,治疗这些疾病的一个很有前景的策略,就是直接针对这道受损的屏障进行修复。
这主要包括两大类治疗方法:
一是直接使用药物来加固和修复肠道细胞间的连接,恢复屏障的完整性;
二是通过靶向调节局部的免疫反应,减轻炎症,从而间接保护和修复肠道屏障。
对屏障功能的直接影响
①谷氨酰胺可修复部分人群的肠道通透性
谷氨酰胺是一种非必需氨基酸,是肠细胞和结肠细胞的重要能量来源。谷氨酰胺在接受腔内禁食的Caco-2细胞中保持蛋白质合成和对离子和4 kDa葡聚糖分子的细胞旁渗透性。它还可降低大分子渗透性(40 kDa),其剥夺可促进TNF-α诱导的细菌易位,而不影响TEER。这些和其他体外研究表明,谷氨酰胺补充通过干扰泄漏途径恢复了对离子和小分子增加的细胞旁渗透性。
然而,在人身上的研究结果却不那么一致,有时甚至相互矛盾。这可能是因为补充谷氨酰胺的时机很关键——最好是在肠道屏障还没受损或者刚刚受损时就介入。
不过,最近一项针对腹泻型肠易激综合征(IBS-D)患者的研究带来了好消息:口服谷氨酰胺显著改善了患者的症状,并成功修复了他们受损的肠道通透性。这表明,对于特定人群,谷氨酰胺可能是一种修复“肠漏”的有效治疗选择。
②MLCK抑制剂有助于减轻肠漏
如前所述,通过肠上皮细胞的泄漏途径和细菌移位由肌球蛋白轻链激酶(MLCK)控制。因此,MLCK抑制剂可能是治疗或预防屏障功能改变的潜在药物。
MLCK的物质是控制肠道屏障“阀门”的关键开关。当它被激活时,肠道细胞间的连接就会松开,导致“肠漏”和细菌穿透。因此,开发能抑制MLCK的药物(即MLCK抑制剂)就成了一种非常有前景的治疗思路。
目前,这类药物在动物实验中已有效预防压力或毒素引起的肠道通透性增加及内脏高敏。如果能在人类中安全应用,MLCK抑制剂有望成为治疗“肠漏”相关胃肠疾病的新选择。
③Zonulin肽抑制剂可能修复通透性并预防肠炎
研究发现,Zonulin是一种调节肠道通透性的关键物质。当肠道受麸质或特定细菌等刺激时,Zonulin释放,可打开细胞间紧密连接,增加肠道通透性,导致“肠漏”。
基于此,科学家开发了Zonulin肽抑制剂(如醋酸拉唑肽),能有效阻断Zonulin作用,“锁上”肠道屏障。动物实验显示该药物可修复通透性并预防肠炎,但其在人类中的疗效尚需验证。
临床试验中,虽然乳糜泻患者用药后自觉症状改善,但肠道通透性并无明显下降。因此,Zonulin抑制剂是否能真正用于胃肠道疾病治疗,还需进一步研究确证。
对免疫激活的影响
研究发现,FGID中的炎症主要与肥大细胞、嗜酸性粒细胞和T细胞的轻度活化有关。因此,目前的治疗尝试大多集中在稳定“肥大细胞”上,因为它在肠易激综合征(IBS)等疾病中扮演了核心角色。
①药物治疗
一些药物已经显示出潜力:
-5-氨基水杨酸:可以减少炎症细胞的浸润。
-酮替芬和色甘酸二钠:作为肥大细胞稳定剂,它们在改善IBS和功能性消化不良(FD)的症状方面取得了良好效果,但其具体如何修复肠道屏障的机制还有待阐明。
此外,一些靶向神经调节和抑制肥大细胞的新型药物(如CRF拮抗剂、大麻素类物质)在动物实验中也表现不错,但它们在人体中的实际效果还需要进一步的临床研究来验证。
②缓解肠道炎症的药物
生物治疗主要包括促炎细胞因子抑制剂和整合素拮抗剂:抗TNF治疗、抗IL-12/23治疗、抗整合素治疗。生物疗法,尤其是抗TNF疗法是有效的治疗方法,但对TNF抑制剂的原发性无效或部分患者的继发性无效需要寻找新的治疗方案。
重要的是,炎症环境可能会对上皮干细胞的功能产生负面影响,因此可能会阻碍健康上皮的重建。 肠漏的治疗应该开始尝试确定肠屏障损伤的原因,然后消除这个因素。在肠道屏障恢复之前,使用缓解肠道炎症的药物似乎是合理的。
③恢复肠道微生物群
益生菌是活的微生物,对宿主的健康有有益的影响。益生菌管理减少肠渗漏,其中,影响肠道免疫调节和抗炎作用(例如,sIgA产生的增加)、抗炎作用、加强上皮屏障(例如,粘蛋白和短链脂肪酸(SCFA)的合成增加,以及限制病原微生物生长的细菌素(例如β防御素)的产生。
益生菌还可以增加构成紧密连接的蛋白质的合成。对肠道屏障状态具有保护作用的益生菌主要有鼠李糖乳杆菌GG、乳双歧杆菌BB-12、嗜酸乳杆菌、植物乳杆菌、双歧杆菌、大肠杆菌等。
恢复正常肠道微生物群的另一种方法是粪便微生物群移植(FMT)。该疗法涉及将从健康供体获得的胃肠道微生物群转移到受体的胃肠道。实施前需准确评估患者和供体的肠道及菌群状况,避免盲目移植导致免疫反应和屏障损伤。
④低FODMAP饮食并增加多酚摄入
FODMAP饮食以短链碳水化合物和多元醇为主,这些成分吸收不良且易发酵,因渗透性强会增加肠腔含水量。FODMAP对肠道微生物群和屏障功能有益,但IBS或IBD患者采用低FODMAP饮食更能减少气体和肠腔扩张,减轻症状。
研究显示,维生素A和D可多途径改善肠道屏障,充足摄入能提升微生物多样性、强化紧密连接、调节免疫反应。
膳食纤维通过发酵生成短链脂肪酸(如丁酸盐),有助于加强粘蛋白和紧密连接,调节免疫,防止屏障通透性增加。
多酚类物质有助于增强紧密连接和黏液分泌,提高抗氧化力,富含多酚的饮食有助于降低肠道屏障障碍风险。
部分草药如普洱茶、芙蓉、蒲公英、姜黄等具备调节微生物群、强化屏障和抗炎作用,但其机制和疗效尚不完全明确,需注意提取纯度。
蘑菇富含维生素D、多酚和多糖,是益生元来源,可通过调节儿茶酚胺及炎症反应影响肠道微生物群。
⑤适当体力活动可降低肠道屏障障碍风险
众所周知,体育活动或锻炼可以增加肠道微生物群的多样性,增强SCFA的产生并刺激抗炎机制,主要是有氧运动,如跑步,骑自行车,健身运动,可以降低肠道屏障功能障碍的风险。
研究结果表明,体力活动以依赖于运动强度的方式调节肠道屏障通透性水平。定期、中等强度的体育锻炼对肠道上皮状态和肠道屏障完整性有积极影响。运动增加了肠道微生物组的多样性,有助于维持肠道屏障的完整性,还显示出抗炎和抗氧化作用。适度的体力活动可能是治疗肠漏的一个有利因素。
但是,高强度的体力活动,典型的竞争性或极限运动,与胃肠道疾病和肠道通透性增加的症状的高发病率相关。这是身体的应激源,由于体内血液的重新分配,体温过高和脱水,导致肠细胞缺氧。
近几十年来,过敏性和自身免疫性疾病的发病率显著增加,例如哮喘、特应性皮炎、过敏性鼻炎、慢性鼻窦炎、食物过敏、乳糜泻和炎症性肠病。全身性和代谢性疾病,如糖尿病、肥胖症、多发性硬化症、类风湿性关节炎、红斑狼疮、强直性脊柱炎以及阿尔茨海默病、帕金森病、慢性抑郁症和自闭症谱系障碍也成为日益严重的健康问题。
现代生活中的食品添加剂、抗生素滥用、环境污染物、慢性压力和过度依赖加工食品等因素正是导致这一代人屏障功能普遍衰退的隐形杀手。面对这一挑战,当前的科学建议首先聚焦于预防屏障损伤,通过建立标准化检测体系、开发肠道友好型产品替代有害化学物质、推广个性化营养干预等手段来实现。
食品工业也将从”填饱肚子”向”滋养健康“转型、医疗健康从”治疗疾病”向”维护屏障”转变、营养保健从”营养补充”向”功能修复“升级等多个行业带来了前所未有的发展机遇。
通过将传统医疗手段与肠道屏障修复、微生物群调节相结合,不仅能显著提高疾病治疗效果,更重要的是实现从“治病”到”防病”的医疗模式转变。
主要参考文献:
Macura B, Kiecka A, Szczepanik M. Intestinal permeability disturbances: causes, diseases and therapy. Clin Exp Med. 2024 Sep 28;24(1):232.
Farré R, Vicario M. Abnormal Barrier Function in Gastrointestinal Disorders. Handb Exp Pharmacol. 2017;239:193-217.
Brandl C, Bucci L, Schett G, Zaiss MM. Crossing the barriers: Revisiting the gut feeling in rheumatoid arthritis. Eur J Immunol. 2021;51(4):798–810.
Ramakrishna BS. Role of the gut microbiota in human nutrition and metabolism. J Gastroenterol Hepatol. 2013;28(Suppl 4):9–17.
Bäumler AJ, Sperandio V. Interactions between the microbiota and pathogenic bacteria in the gut. Nature. 2016;535(7610):85–93.
Ostaff MJ, Stange EF, Wehkamp J. Antimicrobial peptides and gut microbiota in homeostasis and pathology. EMBO Mol Med. 2013;5(10):1465–83.
Hansson GC. Role of mucus layers in gut infection and inflammation. Curr Opin Microbiol. 2012;15(1):57–62.
Gerbe F, Legraverend C, Jay P. The intestinal epithelium tuft cells: specification and function. Cell Mol Life Sci. 2012;69(17):2907–17.
Anderson JM, Van Itallie CM. Physiology and function of the tight junction. Cold Spring Harb Perspect Biol. 2009;1(2):a002584.
Drąg J, Goździalska A, Knapik-Czajka M, Matuła A, Jaśkiewicz J. Nieszczelność jelit w chorobach autoimmunologicznych. Państwo i Społeczeństwo. 2017;17(4):133–46.
Camilleri M. Leaky gut: mechanisms, measurement and clinical implications in humans. Gut. 2019;68(8):1516–26.
Wood Heickman LK, DeBoer MD, Fasano A. Zonulin as a potential putative biomarker of risk for shared type 1 diabetes and celiac disease autoimmunity. Diabetes Metab Res Rev. 2020;36(5):e3309.
Chelakkot C, Ghim J, Ryu SH. Mechanisms regulating intestinal barrier integrity and its pathological implications. Exp Mol Med. 2018;50(8):1–9.
Wright SL, Kelly FJ. Plastic and human health: a micro issue? Environ Sci Technol. 2017;51(12):6634–47.
Yee M-L, Hii L-W, Looi CK, et al. Impact of microplastics and nanoplastics on human health. Nanomaterials.2021;11(2):496.
Holloczki O, Gehrke S. Can nanoplastics alter cell membranes? ChemPhysChem. 2020;21(1):9–12.
Holloczki O, Gehrke S. Nanoplastics can change the secondary structure of proteins. Sci Rep. 2019;9(1):16013.
Xu M, Halimu G, Zhang Q, Song Y, Fu X, Li Y, Li Y, Zhang H. Internalization and toxicity: a preliminary study of effects of nanoplastic particles on human lung epithelial cell. Sci Total Environ. 2019;694:133794.
Jin Y, Lu L, Tu W, Luo T, Fu Z. Impacts of polystyrene microplastic on the gut barrier, microbiota and metabolism of mice. Sci Total Environ. 2019;649:308–17.
谷禾健康

消化是人体生命活动的重要组成部分,分解食物提供能量、促进生长发育、参与免疫功能,然而越来越多的人出现了消化不良。
★ 消化不良在人群中很常见
消化不良在全球范围内都是一种常见的疾病,其发病率在不同地区和人群中有所不同。在中国,消化不良的发病率较高,尤其是城市人群中更为常见。据统计,中国城市居民中消化不良的发病率约为20%-30%。
消化不良主要分为器质性消化不良和功能性消化不良(本文主要讲述功能性消化不良)。功能性消化不良其广义上是一种胃肠道多种症状的综合征,主要包括上腹痛或灼热感,餐后饱胀感及早期饱腹感。
随着对功能性消化不良了解的深入,目前研究发现,消化不良病理生理与脑–肠–微生物群轴紊乱、内脏高敏感性、局部低度炎症、胃肠道感染等因素相关。
肠道菌群可以帮助人体消化吸收,同时还可以合成一些对人体有益的物质,在消化过程中扮演着重要角色。肠道菌群作为新的研究切入点,将有助于探索新的改善功能性消化不良的方法。
在了解消化不良前,我们先来看看人体消化的生理过程:
膳食摄入的消化反应

Livovsky DM,et al.Nutrients.2020
在禁食期间,胃肠道会进行周期性的运动,这种运动被称为迁移运动复合体(MMCs)。迁移运动复合体的功能是将残留物从小肠推进到结肠,以便在新的食物进入之前清空肠道。迁移运动复合体包括静止期和强烈的运动和分泌活动期之间的交替,这种刻板模式有助于保持肠道的健康和功能正常。
在进食开始之前,消化系统已经开始做准备工作,例如,预期即将进食的膳食会刺激唾液和胃液的分泌。当食物进入口腔并被吞咽后,消化系统会进入消化间期运动模式。
食物进入胃后,胃壁会收缩并几乎塌陷,这种主动放松被称为胃适应。固体颗粒通过蠕动活动激活胃窦,启动研磨过程,将食物转化为食糜。
餐后阶段胃会逐渐重新收缩,将食糜推入小肠。胃和小肠的活动会适应消化过程的要求,从口腔开始并延伸到末端回肠,食物被消化并随后被吸收。未被吸收的残留物最终到达结肠,成为肠道微生物群的底物,这些微生物会影响宿主的生理和消化功能。
因此,消化系统的正常活动对于人体的健康和营养摄入非常重要。如果消化系统不正常,可能会导致消化问题和其他健康问题。
消化不良是一种常见的临床症状,主要分为器质性消化不良和功能性消化不良。
器质性消化不良是指由某种器官疾病引起的消化不良。一般通过检查,可以明确诊断是由某个器官的病变引起的消化不良症状,例如肝病、胆道疾病、胰腺疾病、糖尿病等。
✦疾病影响消化
这些疾病会影响到消化道内部的消化酶分泌、肠道蠕动、食物吸收等消化过程,导致消化不良症状的出现,如腹胀、腹泻、便秘、恶心、呕吐、胃痛等。

功能性消化不良是最常见的消化系统疾病,大部分消化不良患者都是属于功能性消化不良。功能性消化不良没有明显的器质性病变,但出现了消化不良症状。
由于功能性消化不良患者病情的反复性与迁延不愈,其生活质量明显降低,同时,所带来的社会医疗成本的增加和生产力的下降也不容忽视。
▸ 发病率
在全球范围内,功能性消化不良女性发病率普遍高于男性。不同地区功能性消化不良的患病率也存在明显差异 :西方国家总体较高,约为10%~40%,亚洲国家较低约为5%~30%。
▸高发人群
•饮食不规律的人群:饮食不规律、暴饮暴食、偏食等不良饮食习惯容易导致消化不良。
•长期服用药物的人群:长期服用某些药物,如抗生素、非甾体抗炎药等,可能破坏肠道菌群平衡,导致消化不良。
•精神压力大的人群:精神压力大、情绪波动较大的人群容易出现消化不良症状。
•高龄人群:随着年龄的增长,人体消化功能逐渐下降,高龄人群容易出现消化不良症状。
•婴幼儿:婴幼儿是消化不良的高发人群之一。由于婴幼儿的消化系统尚未完全发育成熟,消化酶的分泌不足,肠道菌群的构成不稳定等因素,使得婴幼儿容易出现消化不良的症状。

▸ 诊断标准与症状
功能性消化不良的诊断标准:
•餐后饱胀感:即在正常量的膳食后感到不舒服;
•早饱:进食后不久即有饱感,以致摄入食物明显减少,无法完成正常量的膳食;
•上腹疼痛或灼痛:上腹胀多发生于餐后,或呈持续性进餐后加重。
注:满足以上一项或多项,并且没有可以解释这些症状的任何结构性疾病(包括上消化道内窥镜检查)的证据;则可以判断为功能性消化不良
根据主要临床症状可大致分为上腹痛综合征和餐后不适综合征两种亚型。
✦持续时间长,并伴有精神症状
在病程中症状也可发生变化,起病多缓慢,经年累月,持续性或反复发作,不少患者有饮食,精神等症状。
早饱和上腹胀常伴有嗳气。恶心、呕吐并不常见,往往发生在胃排空明显延迟的患者,呕吐多为当餐胃内容物。
不少患者同时伴有失眠、焦虑、抑郁、头痛、注意力不集中等精神症状。这些症状在部分患者中与“恐癌”心理有关。
▸ 功能性消化不良和其他胃肠道疾病的关系
伴有肠易激综合征
许多功能性消化不良患者报告伴有肠易激综合征症状,并且这两种症状经常一同出现在更严重的患者中。
注:虽然这两种情况或多或少都与特定的胃肠道症状有关,但没有结构或生化异常可以解释这些症状。
胰腺功能异常
少数但一定人群的功能性消化不良患者存在胰酶异常或胰腺外分泌功能障碍。胰酶异常和胰腺外分泌功能障碍是否直接影响功能性消化不良症状尚不清楚。
肝脏疾病与消化不良直接存在关联
肝脏疾病如肝硬化、肝炎等也可能导致功能性消化不良症状,如腹胀、食欲不振等。这些疾病可能会影响肠道菌群的平衡,导致消化不良。
功能性消化不良的发病机制尚未完全阐明,可能与胃肠运动异常、内脏超敏反应、肠道菌群紊乱、病原微生物感染、遗传因素、社会心理和神经因素、环境因素等多方面调控异常有关。
需要注意的是,肠道菌群数量和紊乱是功能性消化不良的重要病因之一,将在下文中重点讲述。
➤ 1
√功能性消化不良患者胃排空受损
功能性消化不良的发病机制涉及胃调节、胃排空和十二指肠运动的紊乱。
胃排空——食物由胃排入十二指肠的过程称为胃排空。
一项随机、双盲对照研究发现,功能性消化不良患者的症状与胃调节受损之间存在密切关系 。几份报告表明,一些功能性消化不良患者胃排空受损,一项荟萃分析表明,几乎35%的功能性消化不良患者胃排空明显延迟。
√内脏高敏感性影响功能性消化不良
内脏高敏感性是导致功能性消化不良发展的关键病理生理机制。内脏超敏反应可以通过对肠道机械化学刺激的感知增加,这通常表现为疼痛和灼痛感加重。
辣椒素受体(Trpv1)的激活由神经生长因子 (NGF)、热刺激、辣椒素、前列腺素、酸性pH值和炎症介质触发,进一步释放加剧内脏痛觉的神经肽。
那么一般哪些因素会引起或导致人体胃排空受损或内脏高敏感性,常见的原因如下:
1.神经调节失衡:人体内部的神经系统对内脏的感知和调节非常重要。如果神经系统出现失衡,会导致内脏高敏感性,从而引起胃排空受损以及消化不良等症状。
2.饮食不当:食物的种类、质量和摄入量都可能影响胃排空。比如,吃得太快、咀嚼不充分、进食过多或者过少都会导致胃排空受损。
饮食中过多的刺激性食物(如辛辣、油腻的食物)或者过多的咖啡因、酒精等刺激物质,都可能刺激内脏,导致内脏高敏感性。
3.精神压力:长期的精神紧张、焦虑、抑郁等情绪问题,也会影响人体内部神经系统的平衡,进而导致胃排空受损或内脏高敏感性。
4.慢性疾病:一些慢性疾病,如炎症性肠病、胃溃疡等,也会引起胃排空受损以及内脏高敏感性,从而导致消化不良等症状。
5.长期用药:某些药物,如非甾体类抗炎药、抗生素等,长期使用也可能导致内脏高敏感性。
➤ 2
社会心理因素会导致功能性消化不良症状。
√心理对功能性消化不良具有重要影响
一项针对瑞典人群的研究表明,在10年的随访后,焦虑会使患功能性消化不良的风险增加近8倍。在日本,儿童时期的被虐待与功能性消化不良和功能性消化不良症状的严重程度有关。
此外,病理生理学研究表明,社会心理因素和精神障碍可能通过调节大脑中的信号处理在功能性消化不良中发挥作用以及应激激素对痛觉的影响。
社会心理因素和应激激素也会影响胃肠道的其他方面,例如运动、免疫系统激活、渗透性和微生物群。
√功能性消化不良对精神疾病也有反作用
多项研究强调,与健康人相比,功能性消化不良患者的焦虑和抑郁患病率显著增加。这些观察结果表明,精神疾病在功能性消化不良的发病机制中起着重要作用。
另一方面,由于低度肠道炎症中的细胞因子反应,功能性消化不良症状被认为会诱发焦虑或抑郁,这在功能性消化不良患者心理困扰的发展中起着重要作用。
➤ 3
家族史和遗传多态性可能与功能性消化不良相关。许多研究报告了功能性消化不良风险与遗传多态性之间的关联。
遗传多态性是在同一群体中,某个基因座上存在两个或两个以上的等位基因,且等位基因的频率大于0.01的现象。
GNB3 825C>T、SCL6A4 5HTTLPR、CCK-1R 779T>C等基因多态性被认为与功能性消化不良相关。最近的一项荟萃分析发现,GNB3 825C>T中的次要等位基因 (T) 与上腹疼痛综合征亚型的易感性增加有关。
➤ 4
运动不足、睡眠障碍、高脂肪摄入和饮食不规律等生活方式因素与功能性消化不良的病理生理学有关。
√不健康生活方式导致功能性消化不良发病率高
研究发现,睡眠障碍和运动不足与功能性消化不良相关;脂肪摄入过多会加重功能性消化不良的临床症状,不规律的饮食模式也与功能性消化不良相关。
➤ 5
研究表明,沙门氏菌、幽门螺杆菌、空肠弯曲菌、蓝氏贾第鞭毛虫和诺如病毒等病原微生物导致的急性肠胃炎均与功能性消化不良症状有关。
其机制可能与导致胃肠道Cajal间质细胞(ICC)和肌间神经节受损有关,其发生率在功能性消化不良患者约为10%。
√病因微生物感染会加重消化不良症状
最近的一项荟萃分析证实,根除病原体后症状改善比未治疗的对照组效果更好。在持续时间超过4-12周且内镜检查已排除器质性原因的消化不良患者中,成功根除幽门螺杆菌可使症状缓解率提高10%至15%(或至少症状改善)。
➤ 6
来自动物和临床研究的证据表明,肠道菌群在功能性消化不良中起着重要的作用,影响许多致病机制,包括胃肠动力受损、内脏敏感性、免疫激活、粘膜通透性增加和肠脑轴功能改变等。
在人体中,微生物(包括细菌、古细菌、病毒和真菌)的数量远远超过宿主细胞的数量。
微生物组在调节生理功能(包括胃肠运动功能、上皮屏障保护以及肠道和中枢神经系统之间的相互作用)中发挥着重要作用。然而,微生物失调在功能性消化不良患者中非常常见。
•普雷沃氏菌丰度降低
一项研究将功能性消化不良患者的胃液成分与健康对照组进行了比较,报告称与对照组相比,功能性消化不良中普雷沃氏菌属(Prevotella)的频率显著降低。
这种生态失调的原因可能是胃排空延迟,这可能会改变胃的酸度、粘液稠度和部分氧合作用,从而改变胃的细菌定植。
扩展阅读:肠道重要基石菌属——普雷沃氏菌属 Prevotella
•拟杆菌与变形菌比例增加
功能性消化不良患者胃液的微生物群显示拟杆菌与变形菌的比例增加,而未检测到酸杆菌(Acidobacteria)。然而,健康人的胃液中含有酸杆菌,并且拟杆菌与变形菌的比例较低。
•细菌代谢物分泌出现异常
与对照组相比,功能性消化不良患者的胆汁酸阳性胃液样本比例增加更多。由于胆汁酸从十二指肠反流到胃中,生理上发生在胃运动期间,功能性消化不良患者可能会出现胃动力障碍。
物种丰富度的增加表明胃液微生物群的数量和多样性足以使细菌的代谢物和成分影响胃。因此,可能表明肠道的有毒细菌细胞成分,如脂多糖,刺激白细胞产生促炎细胞因子,引发胃部炎症,从而增加粘膜通透性,这可能导致胃肠神经系统功能障碍。
由于脂多糖和胆汁酸会增加粘膜的通透性,因此患者的炎症可能是由含有此类潜在毒性物质的液体回流引起的。
当比较功能性消化不良患者和健康对照组的上消化道微生物组时,功能性消化不良组口腔、食道、胃和十二指肠中的链球菌(Streptococcus)水平较高。
链球菌丰度与上消化道不适呈正相关,表明链球菌与功能性消化不良患者的胃肠道症状之间存在联系。此外,功能性消化不良组表现出更高水平的厚壁菌门。
• 厚壁菌、变形菌丰度增加
根据这些发现,在一项比较功能性消化不良患者和健康受试者十二指肠粘膜微生物群的不同研究中,十二指肠粘膜中最普遍菌属中也有链球菌。
此外,通过分析功能性消化不良和肝郁脾虚综合征大鼠的粪便样本的微生物组成,与对照组相比,该模型中厚壁菌门、变形菌门(Proteobacteria)和蓝藻门(Cyanobacteria)的水平升高,而拟杆菌门的丰度较低。
上述研究表明,功能性消化不良中的微生物改变并不局限于胃肠道中的一个部位,突出了稳态失衡在这些疾病的发病机制中的潜在重要性。
小肠细菌过度生长 (SIFO) 的定义是小肠中存在过量的细菌,并且与胃肠道症状有关。
最近的研究分析了功能性消化不良患者十二指肠的细菌属水平。
链球菌相对丰度增加
澳大利亚的一项研究报道,与对照组相比,功能性消化不良患者的链球菌(Streptococcus)相对丰度增加,尽管不显著(这可能是因为样本量小),并且链球菌的丰度与厌氧属普雷沃氏菌、韦荣球菌(Veillonella)和放线菌(Actinomyces)的丰度之间存在负相关,这些菌群功能性消化不良患者中显著减少。
β多样性发生显著变化
此外,报告的十二指肠的β多样性在患者和对照组之间存在显著差异,而α多样性保持不变,表明该疾病可能涉及更复杂的微生物群结构变化,而不是仅特定属的相对丰度变化。
奈瑟菌和卟啉单胞菌丰度降低
最近的一项研究表明,在使用质子泵抑制剂(PPI)治疗之前,功能性消化不良患者和对照组的十二指肠粘膜奈瑟菌(Neisseria)和卟啉单胞菌(Porphyromonas)丰度降低,但微生物负荷没有差异。
总体而言,研究证实功能性消化不良患者中确实发生了微生物数量和多样性方面的明显变化。
功能性消化不良患者的微生物变化




Brown G,et al.Neurogastroenterol Motil.2022
谷禾还检测了一些功能性消化不良人群的肠道菌群,虽然个体直接存在一定差异,但是共同之处是菌群紊乱,核心菌异常较多,多项病原菌超标。
案例一
基本信息和病症:
1岁3个月,食物过敏,厌食,功能性消化不良,生长发育不良
菌群构成:
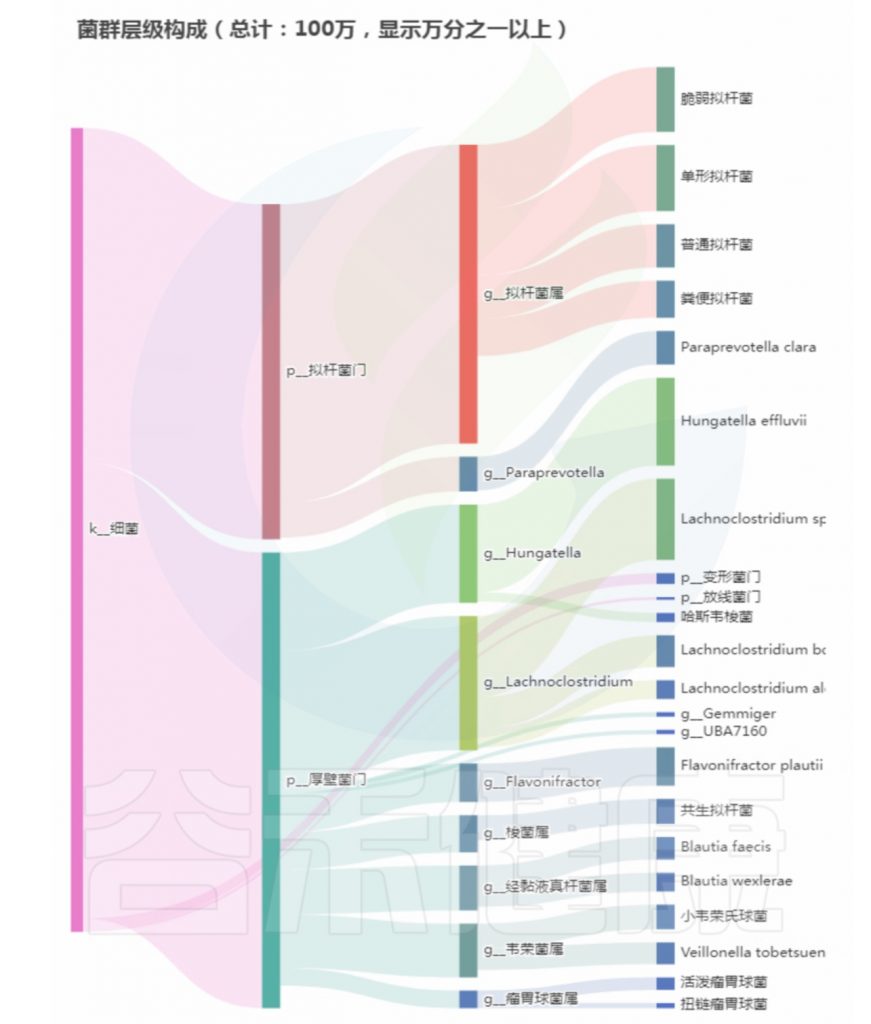

重要菌群情况:
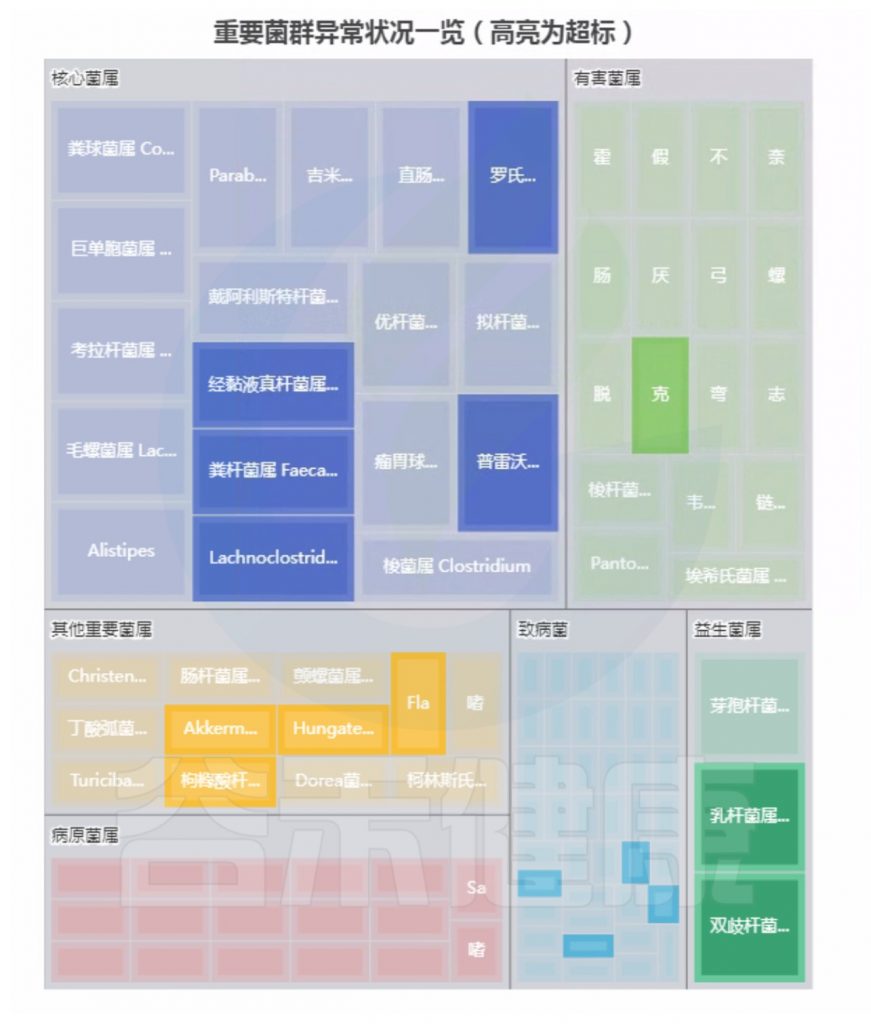



注:高亮部分是异常菌属。
总结:菌群失衡,核心菌属异常较多,普雷沃氏菌属(Prevotella)缺乏,多种致病菌超标。
案例二
基本信息和病症:
43岁,每天大便不成形;容易急性肠胃炎;消化不良
菌群构成:
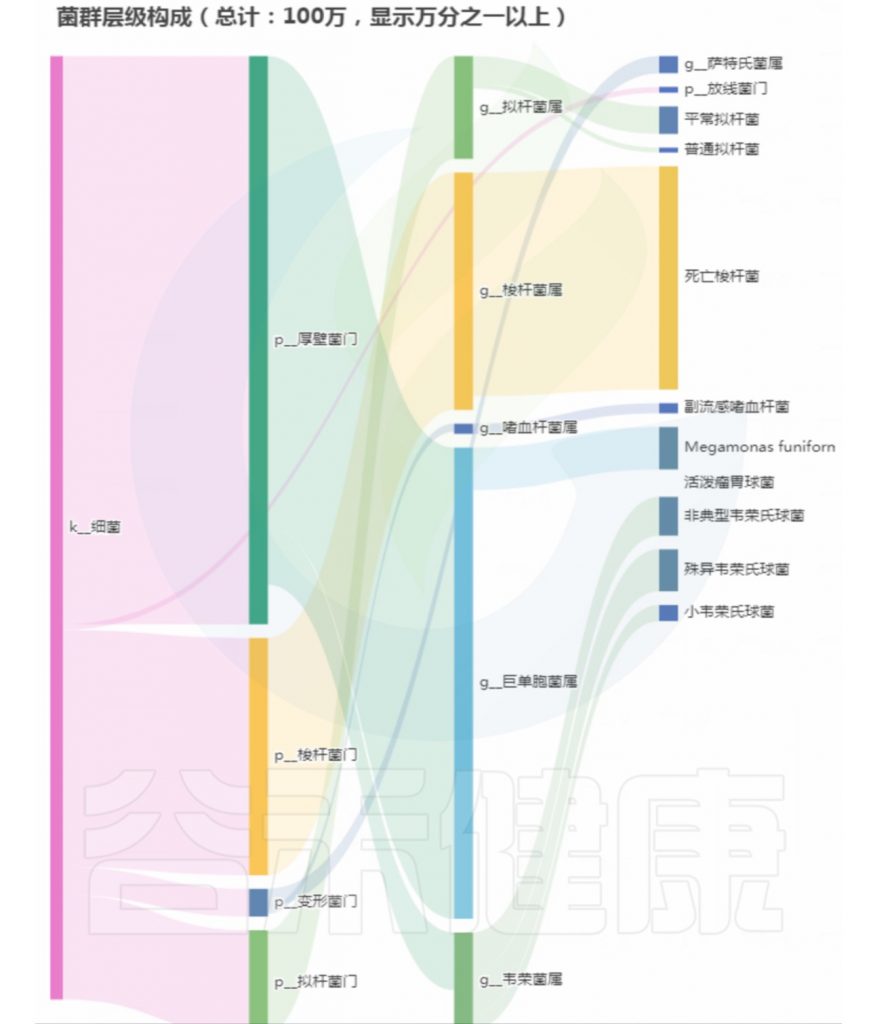

重要菌群情况:
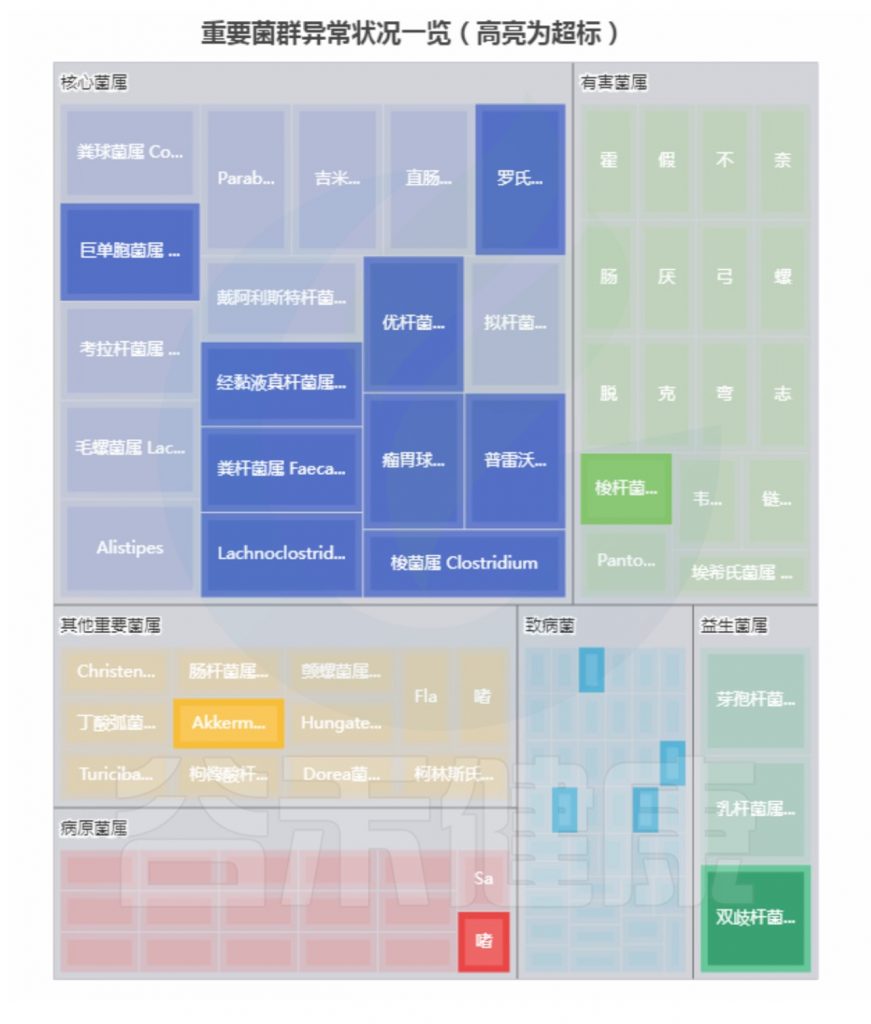



<来源:谷禾健康肠道菌群检测数据库>
总结:菌群失衡,菌群多样性低,核心菌属大量异常,致病菌和病原菌多项超标。
功能性消化不良是一种复杂的多因素导致的功能性胃肠疾病,目前其确切的发病机制尚不明确。
★ 肠道菌群在功能性消化不良中起重要作用
多个研究表明,肠道菌群紊乱在功能性消化不良的发生发展起着重要作用,是功能性消化不良的重要发病机制。影响包括胃肠动力受损、内脏高敏感性、免疫激活、粘膜通透性增加和中枢神经系统疾病。
肠道微生物群参与功能性消化不良发病机制
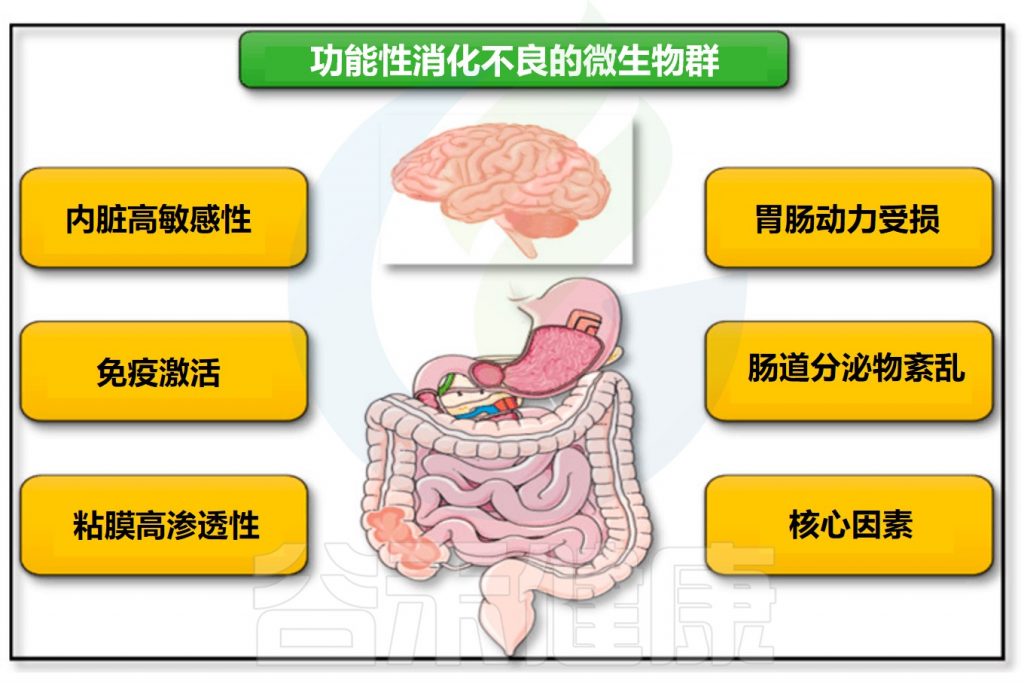

Tziatzios G,et al.Microorganisms.2020
胃肠运动异常是功能性消化不良的基本病理机制,包括胃排空延迟、胃容受性舒张受损及消化期间移行性复合运动(MMC)III期异常。
✦外来菌的增殖抑制胃肠道蠕动
消化期胃和小肠移行性复合运动可将胃肠内容物和致病菌机械性地迁移向远端肠道,而功能性消化不良患者经常出现非传播性和逆传性活动,这可能诱导或加重近端小肠细菌随反流十二指肠液迁移到胃。
而胃排空延迟又导致反流菌能较长时间保留在胃和十二指肠中,引起菌群分布失调的同时,外来菌的增殖可产生内毒素脂多糖刺激免疫应答,进而,抑制胃肠道蠕动,加重功能性消化不良症状。
✦细菌代谢物是胃肠动力的重要来源
短链脂肪酸是肠道共生菌发酵膳食纤维代谢物,除了作为胃肠动力的重要能量来源,也可直接激活肠神经系统以调控肠内分泌细胞合成和分泌某些胃肠激素,如肠激素肽、胆囊收缩素、胰高血糖素样肽等,进而调节胃肠道动力及胃排空。然而在代谢组学研究中发现功能性消化不良大鼠存在短链脂肪酸水平显著降低。
更准确地说,细菌产生的短链脂肪酸不仅调节功能性消化不良中十二指肠碳酸氢盐的分泌,同时它们在十二指肠的快速吸收也可能影响管腔细菌定植抑制。
5-羟色胺影响胃肠道动力
相关研究证实肠道微生物群在调节5-羟色胺(5-HT)合成中起着关键作用,而5-羟色胺水平是影响胃肠道动力的重要因素之一。
大肠杆菌产生的脂多糖延迟胃排空
此外,已发现大肠杆菌(Escherichia coli)产生的细菌脂多糖会导致胃排空显著延迟 ,而双歧杆菌当用作益生菌使用时时可显著增强小肠蠕动。
由上述研究可知,胃肠动力异常可能诱发菌群失调,而菌群失调可反过来进步一步影响胃肠动力,介导功能性消化不良发生发展,但菌群失调与功能性消化不良的因果关系仍需更深入的研究加以验证。
✦心理因素和肠道炎症相互影响
功能性消化不良患者处于十二指肠低度炎症状态。这种慢性低级别的炎症反应会引起疼痛和敏感性。
此外,焦虑或抑郁等心理学因素似乎与慢性炎症反应相互影响,心理压力和由此产生的皮质醇释放激素分泌也会增加十二指肠的局部炎症和全身炎症反应。
✦炎症状态下肠屏障功能发生改变
多项研究报道了功能性消化不良患者肠道中免疫细胞(如肥大细胞、巨噬细胞和嗜酸性粒细胞)数量的增加。
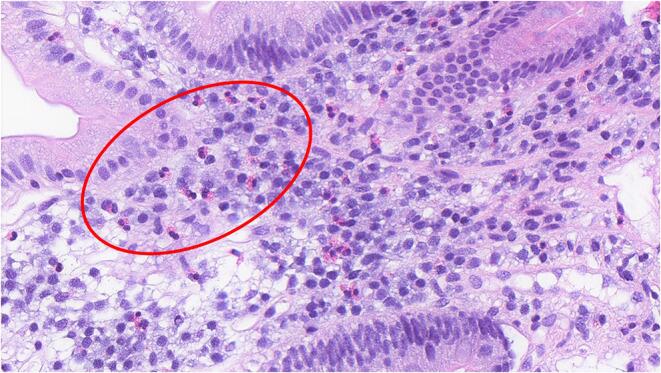
十二指肠活检切片中嗜酸性粒细胞增多

Hari S,et al.Front Allergy.2022
活化的肥大细胞释放细胞因子、组胺、前列腺素和类胰蛋白酶,它们与肠屏障功能障碍和伤害感受通路的改变有关。
嗜酸性粒细胞影响肠道通透性
在生理条件下,十二指肠屏障由粘液层、上皮和下面的固有层组成。在功能性消化不良中,屏障的功能障碍体现为粘膜完整性丧失和通透性增加。
此外,功能性消化不良中嗜酸性粒细胞的募集和激活也发生,这可能使组织损伤和屏障功能障碍持续存在。
正常与功能性消化不良的屏障功能对比
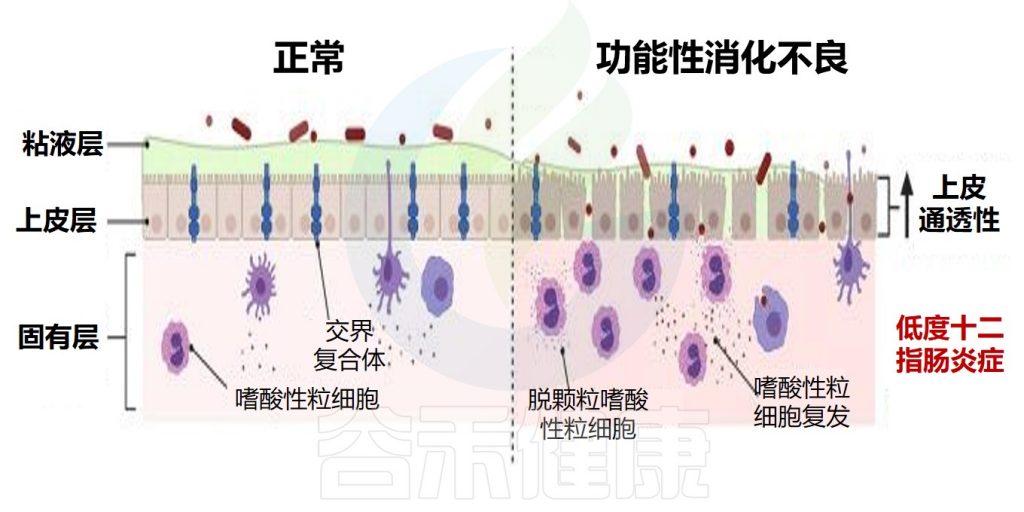

Hari S,et al.Front Allergy.2022
✦肠道菌群也会破坏肠道通透性
肠腔黏膜表面是毒性和免疫原性颗粒面对黏膜相关免疫系统的第一道屏障。肠道微生物菌群失调在功能性消化不良中非常常见。
有害菌破坏紧密连接增加肠道通透性
有研究表明,霍乱弧菌(V.cholera)、艰难梭菌(Clostridium difficile)和产毒素的大肠杆菌的各种菌株已显示可通过直接破坏紧密连接(TJ)、毒素或蛋白酶的产生以及炎症级联反应的活化来增强肠道通透性。
益生菌可以促进屏障完整性
相反,肠道益生菌可以通过增加闭合蛋白、紧密连接蛋白ZO-1和ZO-2的表达来促进屏障完整性。
另外,肠道菌群的某些代谢产物也能够破坏肠道通透性,例如,细菌细胞壁脂多糖易位可以诱导免疫反应和炎症反应,加剧肠道屏障损害并进一步增加肠道的通透性。
扩展阅读:什么是肠漏综合征,它如何影响健康?
除了影响黏膜屏障功能,微生物群也参与调节免疫系统的发育和功能,在先天免疫系统中起关键作用。
✦肠道菌群调节肠上皮免疫功能
研究发现,肠道微生物区系通过激活肠上皮细胞的模式识别受体和内质网应微信号促进免疫系统的发育,从而促进肠上皮细胞的增殖、抗菌肽和黏液的产生,调节与免疫功能相关细胞因子的分泌,如白细胞介素1β、白细胞介素18和白细胞介素25。
✦微生物代谢物也可促进免疫反应
肠道微生物群及其代谢物还通过Toll样受体(TLRs-TLR2、TLR4)干扰信号,并促进促炎细胞因子的产生和免疫反应。
此外,它们的代谢物也可能具有炎症特性或对T细胞分化产生直接影响。
小结
综上所述,肠道菌群失调在影响黏膜生物屏障的同时,可能也导致黏膜机械屏障、化学屏障及免疫屏障等多种屏障功能低下,并可能介导黏膜低度炎症和内脏高敏性的发生。
生物失调的影响
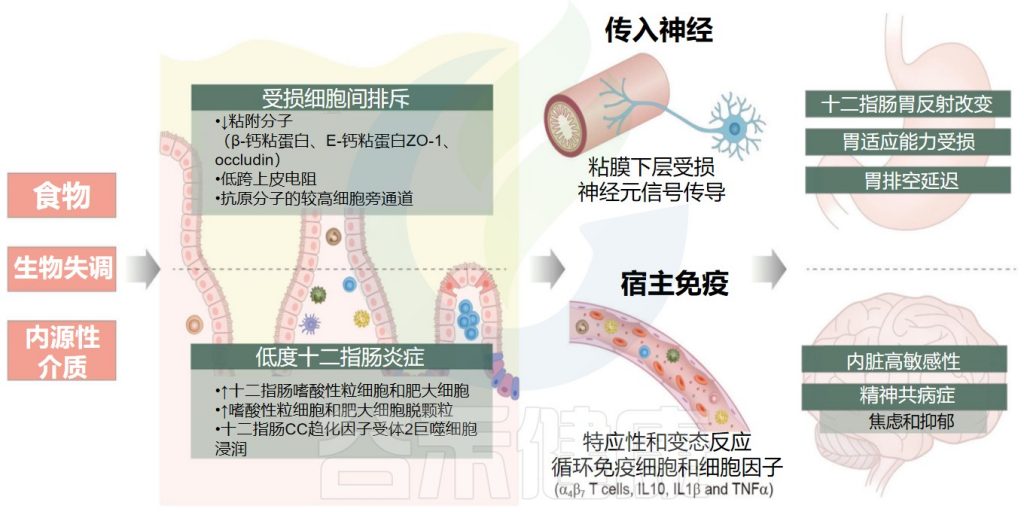

Kim SH.Korean J Gastroenterol.2022
脑-肠轴是连接胃肠道和中枢神经系统的传导通路,包括中枢神经系统、脑和脊髓、自主神经系统、肠神经系统和下丘脑垂体肾上腺轴。
肠道菌群与脑-肠轴存在双向交互作用:
肠道菌群通过神经、内分泌、免疫等至少三种途径与中枢神经系统相通;中枢神经系统调节肠道的运动、分泌及肠道黏膜通透性来影响肠道菌群,或通过肠腔分泌的激素直接调节菌群的基因表达而影响肠道菌群的组成和功能。

Brown G,et al.Neurogastroenterol Motil.2022
肠道菌群通过肠-脑轴影响5-羟色胺、脑源性神经营养生长因子(BNDF)等神经递质的合成、释放和下丘脑-垂体-肾上腺轴的发育,调节中枢神经系统的发育、功能和行为,影响焦虑、抑郁样情绪障碍和应激反应。
✦功能性消化不良患者伴有精神症状
功能性消化不良属于典型的身心疾病,常有焦虑、抑郁的表现。一项为期12年的前瞻性研究也说明功能性消化不良患者中有1/2~2/3先出现焦虑再有胃肠道症状,提示了功能性消化不良的中枢发病机制。
功能性消化不良患者的中枢神经系统改变
功能性神经影像学,如功能核磁共振,使我们能直接观察到中枢神经系统的改变,证明其与功能性消化不良症状的相关性。
结果显示功能性消化不良患者额叶皮层、感觉皮层、脑岛、前扣带皮层、丘脑、海马体和杏仁核的改变,与功能性消化不良内脏超敏反应、消化不良症状、生活质量及焦虑和抑郁有关。
精神心理应激影响内脏高敏感性
有研究认为功能性消化不良患者在精神心理应激的情况下可通过刺激中枢神经系统的情感活动系统参与患者内脏高敏感性的形成,从而对胃肠道产生影响。
因此,研究人员推测肠道菌群通过脑-肠轴对中枢神经系统的调节,导致消化不良伴焦虑抑郁的发生发展。
✦肠道菌群对肠脑轴具有重要作用
随着研究不断深入,越来越多证据证实肠道菌群与脑-肠-菌群轴功能密切相关。
菌群代谢物影响中枢神经系统信号
一方面,肠道微生物能通过合成和释放短链脂肪酸、次级胆汁酸和色氨酸等代谢物,与肠内分泌细胞,自下而上影响激活内源性中枢神经系统信号机制。
此外,肠道菌群失调会增加脂多糖的产生和分泌,而脂多糖不仅是影响中枢神经系统功能的一个强有力的因素,还会促进其他炎症因子的产生,如肿瘤坏死因子﹣α、白细胞介素﹣1β等,以上炎症因子可影响中枢神经系统的功能, 紊乱神经肽的合成和分泌。
激活肠神经系统信号
另一方面,肠道微生物也可独立完成或促进某些神经活性物质的合成和分泌,如5-羟色胺、γ-氨基丁酸、去甲肾上腺素、多巴胺等,这些小分子物质能通过与肠内分泌细胞相互作用,激活肠神经系统信号机制。
上述研究表明,肠道菌群失调可能诱导脑-肠-微生物群轴功能紊乱,其机制涉及神经、免疫和内分泌信号传导。
✦迷走神经的作用
在生态失调和胃肠道不适的精神状况的背景下,应该注意的一个重要方面是迷走神经的作用。
众所周知,压力会增加肠道通透性并通过各种神经调节剂改变胃肠道微生物组的组成,同时压力可以减少迷走神经活动,这可能会促进胃肠道炎症。
注:虽然目前还没有关于迷走神经刺激对胃肠道微生物组影响的数据,但可以推测迷走神经可能通过其对肠道通透性的影响对肠道微生物组产生影响。
迷走神经的传出可能在肠道中具有抗炎作用,同时降低肠道通透性——这两种作用都可能归因于通过迷走神经活动加强紧密连接。
心理治疗对功能性消化不良患者微生物群和胃肠道症状的影响,也可以用迷走神经的影响来解释。
心理疾病对功能性消化不良的表现有影响
现在人们可能想知道心理疾病的患病率是否在不同的功能性消化不良亚组中有所不同。
已经表明情绪和焦虑障碍在非疼痛主导型功能性消化不良患者中,比在疼痛主导型功能性消化不良患者中更常见。
另一项研究还表明上腹痛与神经质、虐待和躯体化之间存在相关性。
这些发现强调了未来重点关注功能性消化不良患者的心理合并症和特定症状之间的可能联系,研究心理治疗对功能性消化不良患者特别是微生物组的这些有趣影响。
未来随着研究深入,有望更好地理解脑-肠-微生物组轴,功能性消化不良的治疗方法也能更加个性化。
药物经口服途径进入人体,不可避免地与肠道菌群发生相互作用。
多项研究表明,肠道微生物能通过编码多种酶,影响口服药物在体内的吸收、代谢、转化等过程,进而影响药物活性成分的有效性和毒性。
改变微生物群的药物在治疗消化不良中得到了有效证实。
利福昔明是一种广谱抗生素,具有革兰氏阳性、革兰氏阴性、需氧和厌氧覆盖,在胃肠道腔内生物利用度高,全身不良反应极小。
•消化不良症状缓解
在一项随机试验中,利福昔明治疗优于安慰剂治疗,其中79%的患者在服用利福昔明后报告消化不良症状缓解,而安慰剂组在8周时这一比例为47%。
•利于有益细菌生长
在其他胃肠道疾病中,利福昔明治疗已被证明可以保护结肠菌群,增加乳酸杆菌和双歧杆菌(Bifidobacterium)的丰度,从而产生积极效应,利于有益细菌的生长,从而改变整体成分。
扩展阅读:肠道核心菌属——双歧杆菌,你最好拥有它
•益生菌治疗后餐后腹胀改善
益生菌可能在功能性消化不良中发挥治疗作用,三项研究表明,在幽门螺杆菌阳性和阴性消化不良患者中服用益生菌加氏乳杆菌(Lactobacillus gasseri OLL2716)12周后,餐后饱腹感和腹胀症状得到改善。
35.5%的幽门螺杆菌阴性功能性消化不良患者的症状得到了缓解,而安慰剂患者的症状缓解率为17%。
扩展阅读:如果你要补充益生菌 ——益生菌补充、个体化、定植指南
•恢复胃液微生物群
加氏乳杆菌还被证明可以“恢复”功能性消化不良患者异常的胃液微生物群。在服用益生菌12周之前,功能性消化不良患者的胃液显示拟杆菌比变形菌占优势,并且不存在酸杆菌(Acidobacteria),益生菌治疗后,这些比例发生了变化,以反映与健康志愿者相似的微生物群组成。
此外,虽然没有收集小肠细菌数据,但用凝结芽孢杆菌(Bacillus coagulans MY01)和枯草芽孢杆菌(Bacillus subtilis MY02)治疗8周后,功能性消化不良患者的有效率比安慰剂提高了28%。
这些发现提供了初步证据,表明患者症状与肠道微生物群中某些属的丰度有关,这些微生物群可以通过治疗性抗生素和益生菌制剂进行调节。
尽管有这些显著的具体变化,但仍需要对更多不同地理区域的患者群体进行进一步研究,以验证疾病中的微生物组变化。
15项观察性研究和一项随机对照试验的系统回顾发现,高脂肪、小麦、FODMAP(可发酵低聚糖、双糖、单糖和多元醇)和咖啡因等天然食品化学物质含量高的食物与功能性消化不良有关。
扩展阅读:肠道微生物群与健康:探究发酵食品、饮食方式、益生菌和后生元的影响
饮酒与功能性消化不良症状的关联尚不明确,可能取决于酒精的类型。
以下是一些饮食调理建议:
•少食多餐:每天分成5-6餐,每餐食量适中,避免暴饮暴食。
•避免过度饮酒和吸烟:酒精和烟草会刺激胃肠道,加重消化不良症状。
•避免食用刺激性食物:如辛辣、油腻、烧烤等食物,容易引起胃肠道不适。
•增加膳食纤维摄入量:膳食纤维可以促进肠道蠕动,缓解便秘症状。建议多食用蔬菜、水果、全谷类食品等富含膳食纤维的食物。
•注意饮食卫生:避免食用过期食品、生冷食物等容易引起胃肠道感染的食物。
•喝足够的水:保持足够的水分摄入可以促进肠道蠕动,缓解便秘症状。
•食用易消化的食物:如米粥、面条、煮熟的蔬菜等,可以减轻胃肠道负担,缓解消化不良症状。
注意:饮食调理虽然可以缓解功能性消化不良症状,但如果症状持续或加重,建议及时就医进行诊断和治疗。
扩展阅读:20种有效改善肠道健康的科学方法
胃酸抑制的主要药物包括两类药物:质子泵抑制剂(PPI)和组胺H2受体拮抗剂。
•上腹痛和反流症状缓解
一项荟萃分析发现,在两到八周内服用标准剂量的质子泵抑制剂,在减少功能性消化不良症状方面优于安慰剂。
注:治疗益处仅出现在有上腹灼痛和反流样疼痛的患者身上,而不出现在有运动障碍相关问题的患者身上。
•消化不良症状的风险降低
组胺H2受体拮抗剂也是功能性消化不良治疗的一种选择。十二项随机对照试验将H2拮抗剂与安慰剂进行了比较,显示消化不良症状的相对风险降低了23%。
对于以进餐相关症状为特征的功能性消化不良伴餐后窘迫综合征的患者,促胃肠动力药可以减轻症状。
对29项比较促动力药(主要是西沙必利)与安慰剂的试验的回顾发现,功能性消化不良的整体症状显著减少。
对功能性消化不良患者的12项随机对照试验的回顾发现,心理治疗(即认知行为治疗和其他形式的心理治疗)比对照组具有统计学上的显著益处。
认知行为疗法:是一种心理治疗方法,旨在通过调整患者的思维方式和行为习惯,来改善其身体和心理健康问题。在功能性消化不良患者治疗中,认知行为疗法可以帮助患者意识到自己不良的思维和行为习惯,如过度焦虑、负面情绪、饮食习惯不当等,从而通过改变这些不良习惯,减轻和预防消化不良症状的发生。
此外,认知行为疗法还可以帮助患者学会应对压力和情绪问题的技巧,提高其身心健康水平。
•症状严重程度、疼痛强度减弱
认知行为疗法 (CBT)导致症状严重程度、疼痛强度减弱,并进一步降低疾病对患者生活的影响。
•胃动力显著增加
此外,与对照组相比,干预组胃排空率显著增加,胃动力参数发生变化。基于这些结果,认知行为疗法可被视为功能性消化不良患者的有效治疗选择。
注:心理治疗不应作为功能性消化不良的一线治疗,因为数据质量低,缺乏盲法心理干预和主观症状评分导致偏倚风险高。如果药物治疗无效,可以考虑心理治疗。
中药具有多成分、多靶点和多途径的优势,目前中医对功能性消化不良肠道菌群的研究仍处于探索阶段。
中药在治疗功能性消化不良方面具有一定的疗效,可以缓解消化不良症状,改善消化功能,提高生活质量。研究证实,中药能逆转肠道菌群失调,维持肠道微生态平衡。
注:中药治疗功能性消化不良应根据患者的具体情况进行个体化治疗,避免不必要的药物过敏或不良反应。同时,中药治疗应在专业医生的指导下进行。
基于菌群干预后,原先消化不良患者的肠道菌群有了好转:
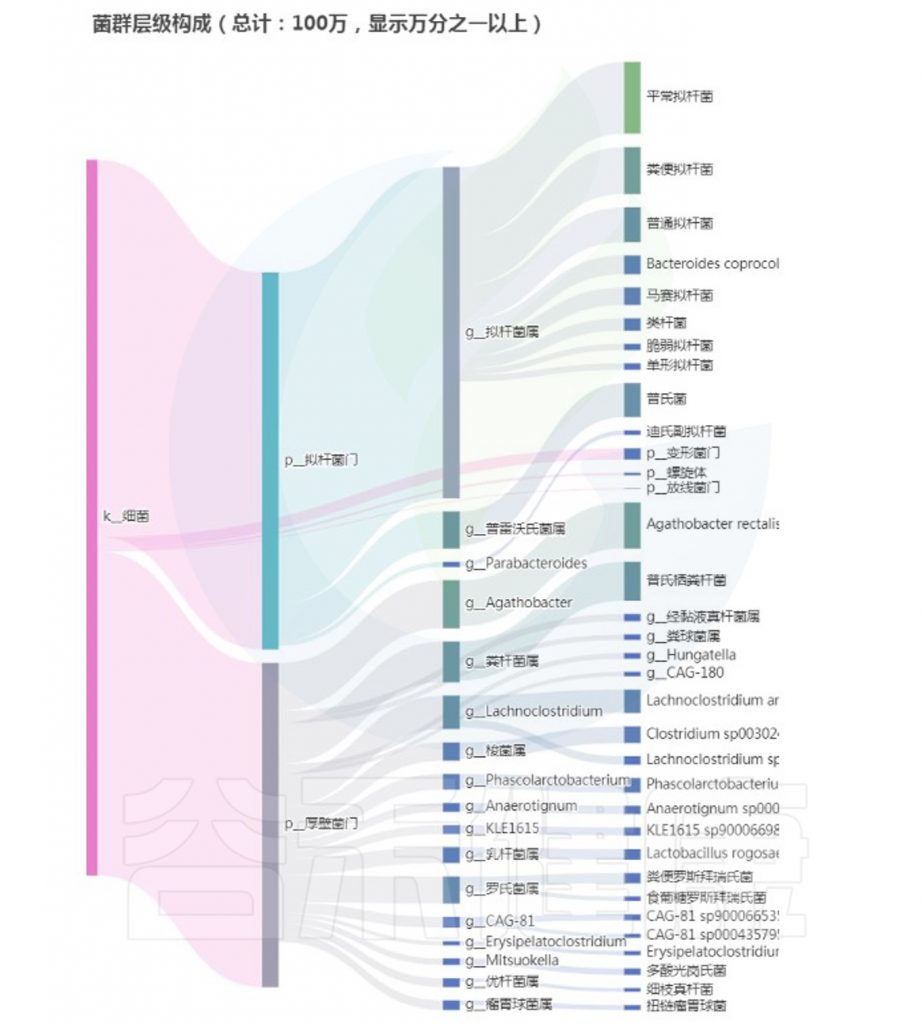

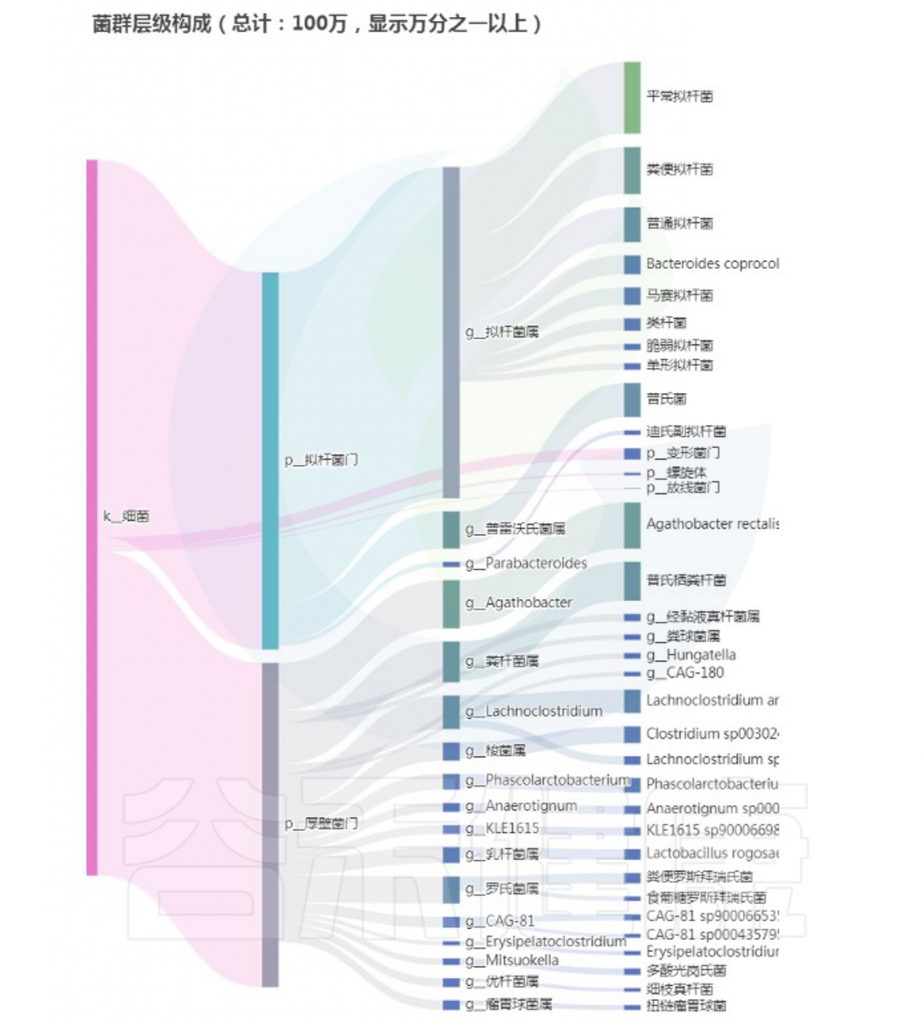






<来源:谷禾健康肠道菌群检测数据库>
从以上菌群评估报告显示,核心菌属和重要菌属没有异常,整体菌群平衡和多样性良好,健康评分显著提升,检测者反馈消化不良症状大幅减轻。
功能性消化不良是一种常见的消化系统疾病,其症状包括腹胀、腹泻、便秘等,给患者带来很大的困扰和痛苦。目前,传统的治疗方法主要是针对症状进行缓解,但效果并不理想。近年来的研究表明,肠道微生物与功能性消化不良密切相关,肠道菌群干预成为了治疗功能性消化不良的新途径。
谷禾的肠道菌群检测经验和研究表明肠道菌群的紊乱和异常特征可以对部分功能性消化不良患者症状背后的病理进行分类和解析,为针对性干预和改善提供了新的可能。对肠道微生物与功能性消化不良之间的关系的进一步深入研究和应用有望带来更有效的治疗方法。
主要参考文献
Singh R, Zogg H, Ghoshal UC, Ro S. Current Treatment Options and Therapeutic Insights for Gastrointestinal Dysmotility and Functional Gastrointestinal Disorders. Front Pharmacol. 2022 Jan 25;13:808195. doi: 10.3389/fphar.2022.808195. PMID: 35145413; PMCID: PMC8822166.
Martinez-Guryn K, Hubert N, Frazier K, Urlass S, Musch MW, Ojeda P, Pierre JF, Miyoshi J, Sontag TJ, Cham CM, Reardon CA, Leone V, Chang EB. Small Intestine Microbiota Regulate Host Digestive and Absorptive Adaptive Responses to Dietary Lipids. Cell Host Microbe. 2018 Apr 11;23(4):458-469.e5. doi: 10.1016/j.chom.2018.03.011. PMID: 29649441; PMCID: PMC5912695.
Shah A, Talley NJ, Holtmann G. Current and Future Approaches for Diagnosing Small Intestinal Dysbiosis in Patients With Symptoms of Functional Dyspepsia. Front Neurosci. 2022 May 6;16:830356. doi: 10.3389/fnins.2022.830356. PMID: 35600619; PMCID: PMC9121133.
Miwa H, Nagahara A, Asakawa A, Arai M, Oshima T, Kasugai K, Kamada K, Suzuki H, Tanaka F, Tominaga K, Futagami S, Hojo M, Mihara H, Higuchi K, Kusano M, Arisawa T, Kato M, Joh T, Mochida S, Enomoto N, Shimosegawa T, Koike K. Evidence-based clinical practice guidelines for functional dyspepsia 2021. J Gastroenterol. 2022 Feb;57(2):47-61. doi: 10.1007/s00535-021-01843-7. Epub 2022 Jan 21. PMID: 35061057; PMCID: PMC8831363.
Mounsey A, Barzin A, Rietz A. Functional Dyspepsia: Evaluation and Management. Am Fam Physician. 2020 Jan 15;101(2):84-88. PMID: 31939638.
Tziatzios G, Gkolfakis P, Papanikolaou IS, Mathur R, Pimentel M, Giamarellos-Bourboulis EJ, Triantafyllou K. Gut Microbiota Dysbiosis in Functional Dyspepsia. Microorganisms. 2020 May 8;8(5):691. doi: 10.3390/microorganisms8050691. PMID: 32397332; PMCID: PMC7285034.
Brown G, Hoedt EC, Keely S, Shah A, Walker MM, Holtmann G, Talley NJ. Role of the duodenal microbiota in functional dyspepsia. Neurogastroenterol Motil. 2022 Nov;34(11):e14372. doi: 10.1111/nmo.14372. Epub 2022 Apr 11. PMID: 35403776; PMCID: PMC9786680.
Hari S, Burns GL, Hoedt EC, Keely S, Talley NJ. Eosinophils, Hypoxia-Inducible Factors, and Barrier Dysfunction in Functional Dyspepsia. Front Allergy. 2022 May 31;3:851482. doi: 10.3389/falgy.2022.851482. PMID: 35769556; PMCID: PMC9234913.
Rupp SK, Stengel A. Bi-Directionality of the Microbiota-Gut-Brain Axis in Patients With Functional Dyspepsia: Relevance of Psychotherapy and Probiotics. Front Neurosci. 2022 Feb 28;16:844564. doi: 10.3389/fnins.2022.844564. PMID: 35295092; PMCID: PMC8919856.