-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康
随着中央国务院关于《健康中国2030指导意见》、《 “十四五”国民健康规划的通知》、《国民营养计划(2017—2030年)》等重要文件的发布,人们对日常膳食营养的关注度和认知也越来越高。自己吃的是否健康?怎么样吃的更健康?已经成为国民关注的重中之重。
在现代社会,随着物质生活的极大改善,传统意义上由饥饿导致的营养不良问题已大幅减少。然而,新的营养挑战正在浮现:即便在食物丰富的情况下,人们仍可能面临营养不良的风险。这种现象的根源在于人们往往忽视了营养均衡的重要性,特别是微量营养素的摄入。
近日,哈佛大学研究团队在世界著名期刊《柳叶刀·全球健康》上发表一项重磅研究成果。
该研究团队分析了185个国家超70亿人的15种微量营养素的摄入量。调查数据得出:
在同一国家和同一年龄人群组中不足量的有:
碘、维生素 B12、铁和硒:女性高于男性
镁、维生素B6、锌、维生素C、维生素A、维生素B1和维生素B3:男性高于女性。
因此,本文基于柳叶刀调查的结果,我们按照微量元素缺乏率由高代顺序,依次与大家介绍这些大人群容易缺乏的微量元素是什么?参与哪些生理生化活动?缺乏或过量对人体有哪些影响?风险因素是什么?有哪些检测方法?如果通过饮食改善或预防缺乏?
最重要的,我们需要清楚地了解自身是否缺乏这些微量营养素,以及缺乏了该如何补充改善,怎样才能更好地吸收利用?希望本文的内容对你们未来的合理膳食和健康有帮助。
碘是世界上最常见的营养素缺乏之一,超过50亿人存在碘缺乏。
碘是正常甲状腺功能的必要矿物质,是甲状腺素(T4)和三碘甲状腺原氨酸(T3)的重要组成部分。这两种激素对肝脏、肾脏、肌肉、大脑和中枢神经系统的功能至关重要。
碘对胎儿和儿童的神经发育、器官功能至关重要,并调节新陈代谢率,对心血管、免疫和生殖健康也有重要作用。
我国目前一般人群整体处于碘营养适宜的状态,但也存在碘缺乏和碘过量的问题。
特定人群如儿童、孕妇等可能存在碘营养缺乏的风险。
我国曾是世界上碘缺乏病流行严重的国家之一,自1995年实施普遍食盐加碘以来,碘缺乏病得到了有效控制,在2015年底实现了94.2%的县消除碘缺乏病的目标。
随着缺乏问题的缓解,碘过量的问题又凸显出来。
有研究指出,中国居民膳食碘摄入量较高的地区在内陆。
在水源性高碘地区,居民可能会受到高碘的危害,如甲状腺肿、亚临床甲状腺功能减退等。
根据《中国居民膳食营养素参考摄入量(2023版)》的建议:
0-0.5岁婴儿的适宜摄入量(AI)约为85微克/天。
0.5-1岁婴儿的AI约为115微克/天。
1-11岁儿童的推荐摄入量(RNI)为90微克/天。
12-14岁的RNI为110微克/天。
15岁(含)以上及成人的RNI为120微克/天。
孕妇的RNI为230微克/天。
乳母的RNI为240微克/天。
① 地理因素
某些地区的土壤和水中天然碘含量低,尤其是远离海洋的内陆地区和高山地区,这些地方的食物中碘含量普遍较低。
② 饮食因素
不食用或少食用富含碘的食物,如海产品(海鱼、海藻)和加碘盐。
素食者如果不注意摄入富含碘的植物性食物,可能会导致碘摄入不足。
③ 怀孕和哺乳期碘需求量增加
孕妇和哺乳期妇女对碘的需求增加,如果饮食中碘摄入不足,容易导致缺乏。
④ 环境污染
工业化进程中,大量的汞、氯和硫等元素的排放和使用,会干扰体内碘的吸收与代谢,使碘在体内的利用率降低。
⑤ 自身健康状况
某些健康状况或疾病(如甲状腺疾病)可能影响碘的吸收和代谢。
⑥ 药物因素
硫脲类抗甲状腺药物、四环素、磺胺类、咪唑类等药物会干扰碘的吸收和利用
碘缺乏症是最常见的营养素缺乏症之一,影响到世界上近三分之一的人口,而下列这些人群缺碘的风险更高。
高危人群:孕妇、胎儿、新生儿最容易出现碘缺乏症,因为碘在怀孕和生命早期的大脑发育和甲状腺功能中起着关键作用。
儿童也面临很高的风险,碘缺乏会损害生长、认知和运动功能。
生活在缺碘山区的人:一些内陆地区或高山地区的土壤和水中碘含量较低,导致当地居民容易缺碘。
素食者:如果饮食中缺乏富含碘的食物(如海产品),素食者可能面临缺碘的风险。
不使用碘盐的人群:如果饮食中不使用碘盐,可能会增加缺碘的风险。
有甲状腺疾病的人:某些甲状腺疾病可能影响碘的吸收和利用。
碘缺乏会出现下面的一些症状,快来自查一下你是否存在碘缺乏。
碘缺乏的最常见症状是甲状腺肿大,也称为甲状腺肿。它还可能导致心率加快、呼吸短促和体重增加。
生长和神经发育受损
严重的碘缺乏可能导致智力迟钝和发育异常。怀孕期间和婴儿期缺碘可能会损害生长和神经发育,导致儿童认知和运动功能障碍。
妊娠期间严重缺碘可导致呆小症,这是一种以严重智力和身体发育迟缓为特征的疾病。
甲状腺功能障碍
碘缺乏可导致甲状腺功能障碍,包括甲状腺肿大和甲状腺功能减退(甲状腺功能低下)。
慢性碘缺乏可导致毒性结节性甲状腺肿和甲状腺功能亢进,因为甲状腺受到长期刺激。
围产期和婴儿死亡率增加
怀孕期间碘缺乏可能导致流产、早产、死产和先天性畸形。并且可能生下甲状腺功能减退的新生儿,影响婴儿的生长和神经系统发育。
免疫功能下降
碘缺乏可能削弱免疫系统,使机体更易感染疾病。
心血管问题
长期碘缺乏可能影响心血管健康,导致心率减慢和血压异常。
◮ 大部分碘会进入甲状腺
膳食中的碘在小肠中被吸收,以碘化物(I−)的形式进入血液循环,然后通过Na+/I−同向转运体(NIS)清除,进入甲状腺,在甲状腺中,碘在滤泡细胞中浓缩为I2,用于甲状腺激素的生物合成。
它还被转运到乳腺等其他组织,为新生儿提供I−或由肾脏清除。在甲状腺功能正常的成年人中,甲状腺含有约70%–80%的身体I2 ,而I2的吸收量因营养状况的不同而有很大差异。
注:除了钠/碘同向转运体(NIS)之外,在肠道中,碘还可以通过钠多维生素转运体(SMVT)和囊性纤维化转运体(CFTR)吸收,不过,吸收程度很小。
◮ 垂体促甲状腺激素刺激碘代谢
垂体促甲状腺激素(促甲状腺激素(TSH))刺激甲状腺碘代谢的各个阶段,包括NIS介导的碘转运到甲状腺,以及甲状腺素(T4)和三碘甲状腺原氨酸(T3)的合成和分泌。大约90%的不必要的I−通过尿液排出,其余10%通过粪便和汗液排出。
◮ 影响碘吸收的因素
其他微量元素:日粮中的钙会妨碍碘的吸收,抑制甲状腺素的合成,加速碘的排出;磷与碘具有协同作用,但钙和镁会阻碍碘的吸收,当饮食中钙、氟、镁离子较多时,会妨碍碘的吸收。
硫氰酸盐:食物中的硫氰酸盐(如木薯、玉米等)在胃肠道逆转化为硫氰酸根,竞争性地抑制碘离子向甲状腺输送,使碘排出增多。
低蛋白、低能量:低蛋白、低能量可使血清中T3、T4、血浆蛋白结合碘(PBI)降低,血清促甲状腺素(TSH)升高,促使酷氨酸分泌减少,降低碘的有机化。
◮ 健康的肠道菌群支持正常的甲状腺功能
健康的肠道菌群可支持免疫系统并确保碘等必需微量营养素的供应,从而对甲状腺功能产生积极影响。
◮ 菌群失调会导致碘代谢异常
肠道菌群失调或不平衡常见于桥本甲状腺炎和格雷夫斯病等自身免疫性甲状腺疾病(AITD),并且可以通过改变营养吸收来影响碘代谢。
在炎症性肠病(IBD)中,已经观察到肠道菌群多样性降低,厚壁菌门和拟杆菌门丰度降低。碘吸收不良是IBD的常见后果,反之亦然,表明二者之间存在相互关系。
一篇论文展示了肠道菌群在调节大鼠碘吸收中的作用:与传统饲养的大鼠相比,用卡那霉素(一种可降低大鼠体内细菌总数的抗生素)治疗的动物在治疗3小时以及治疗42和72天后碘吸收量降低。
谷禾健康经过多年检测实践和与临床的合作,已经积累了超过2000例的甲状腺患者肠道菌群样本,从初步的研究结果看,甲状腺功能减退症和碘吸收异常患者有明显的肠道菌群特征。
碘缺乏症的全球性要求维持和加强碘营养监测计划。那么目前有哪些方法可以评估人体的碘含量呢?
① 测定尿液中的碘水平
世界卫生组织将碘缺乏症的指标从甲状腺肿患病率改为尿液中位碘排泄水平,即近期碘摄入量的主要指标,这一关键决定大大提高了患病率数据的准确性。然而,由于个人每天的碘摄入量都不同,对尿液碘值的解释需要谨慎。
② 尿碘/肌酐比
另一种方法是根据年龄和性别调整碘/肌酐比,这比基于每升浓度的随意报告更为准确,但可能导致在蛋白质摄入量低(尿肌酐低)的情况下估计过高,在肌酐排泄量高的情况下估计过低。
③ 血清TSH和血清甲状腺球蛋白
血清促甲状腺激素(TSH)和血清甲状腺球蛋白(Tg) 是碘状态的互补“功能性”生化指标,反映了对营养状态的中期反应。
然而,虽然TSH是新生儿碘状态的敏感指标,但它对年龄较大的儿童和成人相对不敏感,特别是在存在边缘碘缺乏的情况下。
•海产品,包括海带、海藻、深海鱼类(如三文鱼、金枪鱼、鳕鱼)、海虾、海蟹、蛤干、干贝、海参等,这些食物不仅含碘量高,而且易于吸收,是补充碘的良好选择。
•肉类:牛肉、猪肉、鸡肉等肉类食物,通常也含有一定的碘元素,适量食用可为身体补充一定的碘。
•乳制品和蛋类,牛奶、奶酪和酸奶等乳制品通常含有一定量的碘。鸡蛋,尤其是蛋黄,含有碘。
•碘盐,使用碘化食盐是许多国家预防碘缺乏的有效措施。
•水果和蔬菜,如柑橘类水果(橙子、柠檬)、葡萄、草莓、苹果、梨、香蕉以及菠菜、花椰菜、胡萝卜、芹菜、茄子、土豆、洋葱等,虽然碘含量相对较低,但适量食用仍能为身体补充一定的碘元素。
缺铁也是世界上常见的微量营养素缺乏症,超过40亿人的铁摄入不足,尤其是在婴儿、儿童、青少年和妇女中。
全球缺铁情况估计值
.png)
doi.org/10.1016/B978-0-12-802861-2.00002-X
(A)15-49岁孕妇;(B)6-59个月婴儿和儿童
铁是一种人体必需的矿物质。它是红细胞的一个重要组成部分,它与血红蛋白结合,将氧气输送到你的细胞。铁在新陈代谢和免疫防御中都起着重要作用。
缺铁会导致贫血、疲劳、免疫系统减弱和大脑功能受损、宿主发育迟缓等。
一般我们常见的缺铁,主要是以下几个原因:
① 铁摄入不足
这很好理解。我们的身体不能制造铁,需要从食物中获取。如果你每天摄入的铁量没有达到身体需要的量,就会出现缺铁。
② 铁需求增加
快速生长会增加铁需求,因此儿童、孕妇和哺乳期女性更可能缺铁。此外,进行耐力锻炼的人更容易患低铁症。
③ 铁流失过多
出血和失血会增加铁的流失,包括:月经出血、分娩、溃疡、痔疮、因受伤或手术而出血、献血等。长期使用消炎药(布洛芬、萘普生、双氯芬酸)会增加肠道出血的可能性。
需要注意的是,缺铁性贫血的一个常见且常被忽视的原因是月经过多。随着时间的推移,这种缓慢的血液流失通常会导致铁流失过多。
④ 铁隔离
在慢性炎症性疾病中也会出现缺铁,例如自身免疫性疾病、慢性感染、慢性肾病或癌症。因为铁对病原体和癌细胞的生长很重要,所以当发生感染或炎症时,身体会试图通过锁定铁来抑制病原体或恶性细胞的生长。
受感染或炎症影响的组织会释放降低铁血水平的细胞因子,从而导致贫血的发展。
⑤ 铁吸收不足
消化系统的疾病会降低铁的吸收,包括:乳糜泻、炎症性肠病、胃炎、幽门螺杆菌感染、小肠细菌生长过度等,此外,减肥手术也会减少营养吸收,包括铁。
铁吸收不足的其他原因包括大量摄入抑制铁吸收的食物或药物,包括:植酸盐(全谷物、豆类)、多酚(茶、咖啡、葡萄酒)、抗酸药、H2受体阻滞剂、四环素或消胆胺等药物等。
⑥ 肠道菌群紊乱,病原菌定植
还有一个很重要的我们可能会忽略的因素,就是菌群。大肠杆菌、铜绿假单胞菌、肺炎克雷伯菌、金黄色葡萄球菌和结核分枝杆菌。这些病原菌的定植会与宿主进行铁的竞争吸收,同时诱发肠道炎症,改变肠腔环境,影响菌群构成,进一步导致缺铁加剧。
学龄前儿童:这个数字在学龄前儿童中上升到47%。除非给他们提供富含铁或强化铁的食物,否则他们非常可能缺乏铁。
月经期妇女:大约30%的月经期妇女由于每月失血过多也可能缺乏,高达42%的年轻孕妇也可能缺乏。
素食主义者:此外,素食者铁缺乏的风险增加,因为他们只摄入非血红素铁,而非血红素铁的吸收率不高。
贫血是缺铁最常见的危害
缺铁最常见的后果是贫血,据估计,女性贫血平均有50%是由于缺铁引起的,孕妇这一比例上升至60%,儿童约为42%。
由于贫血氧气输送能力下降,会出现呼吸困难(气短)和静息时心输出量增加、心血管压力增大等症状。
疲劳和身体虚弱
缺铁通常与疲劳、身体耐力下降和嗜睡有关,即使没有贫血。
认知和心理影响
注意力、专注力和记忆力下降等认知障碍与缺铁有关。此外,情绪低落、焦虑和烦躁等症状也很普遍。
异食癖
缺铁会导致异食癖,尤其是食冰癖(渴望和咀嚼冰块或其他冰冻食物),这与铁含量低密切相关。
不安腿综合症(RLS)
研究发现缺铁与不安腿综合征之间存在密切联系,补铁可改善症状。
免疫功能和感染风险
缺铁会损害免疫功能,特别是T细胞免疫,使人更容易受到感染。
头发和指甲的变化
缺铁患者还报告了脱发和指甲纹理变化等身体症状。
◮ 血红素铁吸收率更高
•血红素铁:这种铁的吸收率非常高。它只存在于动物性食物中,在红肉中含量特别高。
•非血红素铁:这种类型的铁在动物和植物食物中都有,比较常见。它不像血红素铁那样容易被吸收。
血红素铁和非血红素铁通过两种不同的途径吸收,血红素铁被十二指肠刷膜边缘的血红素载体蛋白1(HCP1) 吸收。
非血红素铁通常呈三价铁形式,不具有生物利用度,必须通过十二指肠细胞色素b(DCYTB)将其还原为二价铁形式,然后再由二价金属转运蛋白(DMT1)转运到十二指肠刷膜上。
肠上皮细胞对非血红素铁的吸收
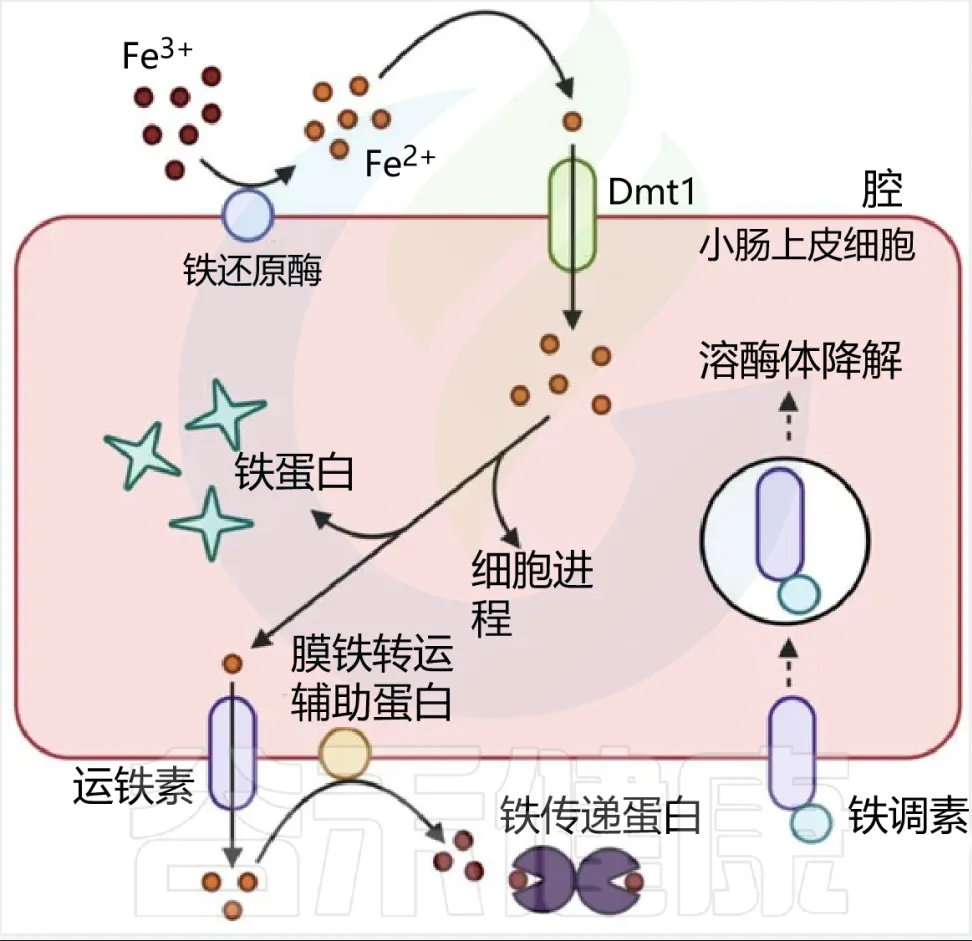
肠道内的微生物群可能与宿主竞争可用铁,也可能通过其他方式促进或抑制铁的吸收。
◮ 一些细菌可以直接利用铁
细菌可以通过分泌铁载体摄取Fe3+。铁载体是一种Fe3+特异性的螯合剂,对Fe3+具有超强的络合力。而大多数革兰氏阳性菌存在直接吸收血红素而获得铁元素的转运系统。
除此之外,细菌也可以产生分泌的或位于膜上的铁还原酶,将Fe3+还原成更容易溶解的Fe2+形式,并通过Feo、Yfe、Efe等转运系统来摄取Fe2+。
◮ 部分菌群调节肠道环境有助于更好地吸收铁
许多食物基质中的非血红素铁与抑制剂(例如多酚、纤维或植酸盐)相连,这些抑制剂可以被专用细菌酶降解,从而更好地吸收铁。
细菌还可以通过发酵饮食中的不可消化碳水化合物来产生短链脂肪酸,这会降低管腔pH值,从而将三价铁还原为二价铁,从而提高其被细菌和宿主的吸收。
其他一些有机酸(例如乳酸)是由许多细菌产生的,存在于整个消化道中。酸化的肠道环境还可以降解螯合微量营养素的复合物并促进铁的吸收。
特定的微生物代谢物,如羧酸,还可以通过防止肠道中的铁沉淀来增强铁的吸收。
◮ 一些肠道菌群代谢物会抑制铁的吸收

但是需要注意的是,还有研究发现肠道微生物群产生的代谢物会抑制缺氧诱导因子(HIF-2α)(肠道铁吸收的主要转录因子)并增加铁储存蛋白铁蛋白,从而导致宿主肠道铁吸收减少。
这可能是肠道微生物群通过抑制肠道HIF-2α活性和上调铁转运蛋白(FPN)表达来调节宿主全身铁稳态,有效防止全身铁过载。
评估缺铁的生化测试包括血清总铁、总铁结合能力(TIBC)、转铁蛋白、可溶性转铁蛋白受体(sTfR)、血清铁蛋白和红细胞锌原卟啉。
① 测定血红蛋白
血红蛋白是评估铁状态最常用的参数,因为它简单易用。然而,当单独使用时,它缺乏特异性,因为它受维生素B12和叶酸状态以及感染和血红蛋白病的影响。
② 测定血清铁蛋白
血清铁蛋白被认为是检测早期缺铁的较好生物标志物。然而,作为一种急性期反应物,其血清浓度受炎症状态影响,并可能因长期饮酒而升高,从而限制了其在缺铁性贫血(IDA)诊断中的实用性。
③ 测定血浆铁(PI)/总铁结合能力
血浆铁(PI)/总铁结合能力(TIBC)比值反映转铁蛋白饱和度,可通过在自动化平台上常规分光光度法分析的PI和TIBC轻松获得。
直接测量转铁蛋白已被提议作为一种更好的生物标志物,并且已经开发出自动化免疫化学方法,但在临床实验室中应用并不广泛。最近描述了一种使用合成转铁蛋白肽的LC-MS/MS方法用于测量血清转铁蛋白。它可以成为参考方法的基础,从而提高免疫学方法的准确性。
④ 测定可溶性转铁蛋白受体(sTfR)
可溶性转铁蛋白受体(sTfR)测量是最近描述的一种铁状态评估方法,通常可以区分缺铁性贫血(IDA)和慢性病性贫血(ACD) ,尤其适用于识别同时患有炎症性疾病(其中铁蛋白(一种急性期蛋白)增加)的患者的IDA。
⑤ 红细胞锌原卟啉
红细胞锌原卟啉是血红素合成异常的产物,在无并发症的铁缺乏症(缺铁性红细胞生成)的初步筛查中特别有价值,并且与sTfR一起用于在排除铅中毒(如今很少见)时监测补铁疗法。
低成本和能够用即时血荧光计直接测量一滴血中的红细胞锌原卟啉/血红素比率是该检测的主要优点。然而,自动化检测的困难限制了它在中心临床实验室中的使用。
⑥ 含铁血黄素
最后,可以检查骨髓以评估网状细胞中的含铁血黄素含量。然而,这种技术是侵入性的、半定量的、依赖观察者的,不能在临床病理实验室中常规使用。
考虑到缺铁对人体健康影响重大,因此实施适当的策略来解决这一问题至关重要。
最常见的策略是食物中的铁补充、益生菌、益生元、铁药物补充剂等方法。
◮ 富含铁的食物
前面我们知道,膳食铁有两种形式:血红素和非血红素。血红素铁具有较高的生物利用度,而非血红素铁的吸收要低得多。
血红素铁主要存在于以下食物中:
•红肉,尤其是牛肉,是血红素铁的重要来源,每 100克牛里脊肉含有约3毫克血红素铁;
•血液制品,例如猪血和鸭血,含有极其丰富的血红素铁,每100克含9.2至15.4毫克;
•内脏,尤其是肝脏,是血红素铁的极佳来源。例如,每100克猪肝含有约2.3毫克血红素铁;
•某些贝类,如青口贝、蛤蜊和牡蛎,也富含血红素铁,每100克含4.0至9.1毫克。
非血红素铁:
•豆类,如大豆、蚕豆。食用豆类是非血红素铁的重要来源;
•种子和坚果,芝麻和南瓜子是非血红素铁的良好来源;
•深色多叶蔬菜,西兰花、甘蓝和菠菜含有丰富的铁,此外韭菜、芹菜、黑木耳、豆芽等也含有一定的铁含量;
•全谷物,如燕麦、藜麦、糙米;
•鱼类,鳕鱼、鲤鱼、鲑鱼等鱼类中也有一定的非血红素铁。
◮ 维生素C:促进铁的吸收
特别注意的是,维生素C可以促进铁的吸收。与富含铁的食物一起吃富含维生素C的食物,像冬枣、柑橘、猕猴桃、草莓、西红柿等都含有丰富的维生素C,可以帮助你最大限度地吸收铁。
◮ 铁补充剂
不同形式的铁补充剂补充铁以亚铁和铁的形式存在。由于铁形态必须在体内转化为亚铁形态以供吸收,因此亚铁形态更具生物利用度。
常用的口服亚铁补充剂包括:
•柠檬酸亚铁
•硫酸亚铁
•葡萄糖酸亚铁
•铁琥珀酸亚铁
•氨基酸螯合物(如双甘氨酸铁、天冬氨酸铁)
•血红素铁
◮ 益生菌
一些益生菌可以产生乳酸,这可能会降低pH值,从而增加铁的溶解度,帮助其吸收。
例如,植物乳杆菌 299v 有助于预防缺铁性贫血。这种益生菌可以改善活跃的高加索欧洲人的膳食非血红素铁吸收。
发酵乳杆菌是人类微生物群中的一种主要益生菌,具有显著的铁还原活性。对羟基苯乳酸是该菌株产生的代谢物,通过DMT1转运体将Fe3+还原为Fe2+来增加肠细胞对铁的吸收。
◮ 益生元
益生元是功能性食品成分,可刺激肠道中有益细菌的生长和定植,最终改善身体健康。
几项研究将益生元或合生元的摄入与铁可用性的增加联系起来,主要是通过将Fe3+转化为Fe2+(由于它们的铁还原活性),并促进肠细胞对铁的吸收。
!
特别提醒
除非你真正需要,否则绝不应该补充铁,因为过多的铁可能非常有害。
钙对你身体的每个细胞都是必不可少的。它能使骨骼和牙齿矿化,特别是在快速生长的时期。除其结构功能外,钙还参与多种生命功能,包括受精、血液凝固、肌肉收缩、神经冲动传递、分泌活动、细胞死亡、免疫反应、细胞分化和酶活化。
获得和保持所需的钙量对于儿童骨骼的发育、强度和密度以及预防老年人的骨质流失和骨质疏松性骨折至关重要。充足的钙摄入量还有助于降低患高血压、高胆固醇血症、结肠癌、肾结石和腹部肥胖等各种慢性疾病的风险。
世界卫生组织(WHO)建议,年轻人的每日推荐钙摄入量(RDI)为1000毫克/天,65岁以上男性、绝经后女性和9至18岁的儿童的每日推荐钙摄入量为1300毫克/天。
然而之前的一项调查发现,只有不到15%的少女、不到10%的50岁以上的妇女、不到22%的少年和50岁以上的男子符合建议的钙摄入量。虽然目前这些数字略有增加,但大多数人仍然没有获得足够的钙。最新的研究表明,全球人口有超50亿存在钙不足(占66%)。
钙缺乏症是影响各类人群的全球健康问题,对骨骼健康和其他生理功能有重大影响。了解钙缺乏的原因对于制定有效的干预措施和政策以减轻其影响至关重要。
① 饮食摄入不足
世界上大约一半的人口无法获得足够的膳食钙,其中低收入和中等收入国家面临的风险最大,尽管高收入国家中的许多人也没有达到推荐摄入量。
对于儿童来说,钙摄入不足是缺钙的主要原因,而生长和骨骼发育对钙的需求较高,则加剧了缺钙现象。
② 生理和代谢因素
成人缺钙通常是由于钙通过肠道、肾脏和皮肤流失,而无法通过饮食摄入得到补偿。
在绝经后妇女中,尿钙流失增加和钙吸收不良导致钙缺乏和骨质疏松症。
③ 维生素D缺乏症
维生素D缺乏会导致钙吸收受损,从而导致钙缺乏症和佝偻病和骨软化症等相关疾病。
④ 荷尔蒙影响
激素变化,如绝经后女性的雌激素水平下降,会增加骨质吸收和钙质流失,加剧钙缺乏症。
此外,甲状旁腺激素(PTH)和骨化三醇水平因缺钙而升高,导致骨吸收以维持血钙水平。
⑤ 遗传和健康状况
影响矿物质代谢的遗传、先天或后天性疾病可能导致儿童继发性钙缺乏症。
⑥ 环境和生活方式因素
缺乏日光照射导致维生素D不足,以及含有钙结合剂(例如磷酸盐、草酸盐)的饮食习惯会损害钙的吸收。
老年人:老年人由于钙和维生素D摄入量低、日照时间短、肠道吸收能力下降、肾功能下降等因素,特别容易出现钙缺乏症。
绝经后的女性:由于雌激素水平下降,骨质流失加快,容易导致钙缺乏。
孕妇和哺乳期妇女:由于胎儿和婴儿对钙的需求增加,母体可能会出现钙不足。
素食者:如果饮食中缺乏富含钙的植物性食物,可能会导致钙摄入不足。
乳糖不耐受者:由于无法摄入乳制品,可能会导致钙摄入不足。
青春期青少年:由于快速生长发育,对钙的需求增加,如果饮食中钙摄入不足,容易缺钙。
长期服用某些药物的人:如长期服用类固醇药物,可能会影响钙的吸收和代谢。
患有某些疾病的人:如甲状旁腺功能亢进、肾病或胃肠道疾病,可能会影响钙的吸收和利用。
钙缺乏症的症状和健康危害主要包括以下几个方面:
骨折、骨质疏松症
当钙摄入量低或钙吸收不良时,就会发生骨吸收,骨骼中储存的钙用于维持正常的生物功能。长期钙缺乏会导致成年人骨质疏松,增加骨折的风险,尤其是绝经后女性和老年人。
佝偻病
更为严重的饮食性缺钙的症状包括儿童的软骨(佝偻病),钙缺乏会影响儿童骨骼生长和发育,表现为骨骼畸形、生长迟缓等。
某些疾病和特定饮食,如素食,可能会导致钙缺乏。炎症性肠病患者也需要补钙,尤其是使用皮质类固醇/糖皮质激素的患者。
妊娠期并发症
除了骨骼健康之外,孕妇钙缺乏可能增加患妊娠期高血压疾病、早产、低出生体重等妊娠并发症的风险。补钙最有据可查的好处之一是显著降低孕妇先兆子痫和产妇发病率以及早产的风险。
其他健康影响
钙缺乏还可能与其他健康问题有关,如牙齿问题、肌肉痉挛、心血管疾病、情绪不稳定等。
对于非妊娠成人,补钙可能对降低血压有轻微作用,尤其对于年轻人。补钙还与胆固醇代谢的有利变化有关,包括低密度脂蛋白的减少和高密度脂蛋白的增加。
钙以离子形式(即Ca2+)在胃肠道中吸收。肠道钙吸收是维持Ca2+稳态的重要过程,并通过两种不同的运输机制进行:跨细胞主动饱和转运和旁细胞被动不饱和转运。
◮ 钙的跨细胞主动转运
跨细胞运输发生在十二指肠和空肠上段,受维生素D刺激,包括三个基本步骤:
(1)钙进入细胞(通过正电化学梯度);
(2)扩散;
(3)从细胞中排泄。
一旦进入细胞,钙就会被转运到基底侧膜,与缓冲蛋白钙结合蛋白-D9K(CaBP-9K)结合,该蛋白对 Ca2+有很高的亲和力。另一种钙结合蛋白钙调蛋白可能有助于钙在细胞内的易位,但其作用程度不如钙结合蛋白-D9K。
钙通过位于基底侧膜的钙泵ATPase(PMCA1)和钠钙交换器(NCX1)的作用从上皮细胞挤出到间质空间。PMCA1对钙的吸收至关重要,在人体中,它存在于十二指肠、回肠和结肠中。PMCA1活性受钙调蛋白(CaM)、钙结合蛋白-D28K(CaBP-28K)和钙调节。
◮ 钙的旁细胞被动扩散
钙的旁细胞被动扩散主要发生在小肠中,该扩散不可饱和且不依赖于维生素D;随着钙摄入量的增加,通过旁细胞扩散的吸收增加,当钙摄入量高时,旁细胞吸收占主导地位。
旁细胞吸收通过整个小肠的紧密连接发生,紧密连接是存在于肠细胞顶端区域的细胞间结构,可调节离子和分子的旁细胞运输,而肠道微生物群对于紧密连接的构成至关重要。
◮ 当钙摄入不足时,骨骼会释放出钙进而引起骨质疏松
血液中的钙浓度受到严格的调节,任何多余的钙都会储存在骨骼中。如果你的摄入量不足,你的骨骼就会释放出钙。
这就是为什么缺钙最常见的症状是骨质疏松症,其特点是骨骼更软、更脆弱。
健康人的血钙维持在一个相对稳定的水平,主要依靠血液与细胞外液之间钙代谢的快速交换与平衡,而调控骨骼、肠道、肾脏等重要器官和核心环节的大型钙库则受钙调节因子的控制。例如经典的钙调节因子1,25-二羟基维生素D3。
维生素D3首先在肝脏中羟基化生成25-羟基维生素D3,然后在肾脏中经1α-羟化酶作用生成活性最强的1,25-二羟基维生素D3。活性维生素d3通过增加肠道钙吸收、减少肾脏钙排泄、调节骨代谢等作用而升高血钙。
◮ 肠道微生物可以影响钙调节因子水平
已有多项研究调查了不育小鼠血浆中25-羟基维生素d3和1,25-二羟基维生素d3水平非常低,而不育小鼠在植入肠道微生物群 2周后血清钙水平恢复至正常水平。

在一项临床试验中,参与者被给予NCIMB 30242罗伊氏乳杆菌胶囊后,服用益生菌胶囊的患者25-羟基维生素d3水平较服用安慰剂胶囊的对照组显著升高。
◮ 短链脂肪酸有助于增强钙的吸收
肠道微生物群还能产生短链脂肪酸(SCFAs)。实验证明,SCFAs的存在可以增加小鼠结肠腔内钙的转运,而单独用盐酸处理并不能增加钙的转运,SCFAs可能通过其他机制促进钙的吸收。
SCFAs是肠黏膜细胞的重要能量供应者,尤其是丁酸,是结肠和盲肠黏膜细胞所青睐的。所以SCFAs能促进肠道细胞生长,增加肠道吸收面积,从而增强钙的吸收。
此外,丁酸可以诱导骨调节T细胞的形成,进而达到甲状腺激素诱导的骨代谢,降低血钙的目的。
◮ 维生素D与肠道微生物群共同作用调节钙吸收
维生素D是人体唯一能合成的维生素,其来源主要是皮肤在太阳紫外线照射下合成的维生素D,其次是天然食物。维生素D与肠道微生物群相互作用,共同作用于机体对钙的吸收。
肠道菌群的组成可因维生素D状态或暴露而变化,维生素D摄入量与普氏菌的丰度相关,与拟杆菌呈正相关。另一方面,有数据支持菌群也影响维生素D代谢,一些细菌表达参与类固醇羟基化的酶,因此它们可以加工和激活维生素D。细菌CYP105a1(苍白链霉菌)可以通过两个独立的羟基化反应将维生素D3转化为1,25(OH) 2 D3,这表明细菌功能相当于维生素D代谢酶。
维生素D对机体钙平衡的调节作用是通过调节肠道、肾脏对钙的吸收,以及骨的成骨、破骨细胞生成过程来实现的,能促进小肠黏膜对钙的吸收。有研究表明,当维生素D由不足转为正常时,肠道对钙的主动吸收增加45~65%,而血清25-羟基维生素D低于30ng/ml时,肠道对钙的吸收明显降低。
① 饮食评估
膳食钙摄入量是广泛使用的钙状态测量指标,可用于得出人口状态指标(例如,摄入量充足或不足的个体比例;平均摄入量)。膳食评估方法可分为间接方法(如食物平衡表),利用二手数据估计国家和家庭层面可供消费的食物,以及直接方法(如24小时回忆),从个人收集原始膳食数据。
② 离子钙测量
直接测量离子钙(Ca2+)被认为是评估真实钙状态的黄金标准,因为它不受白蛋白等血清蛋白的影响。重症监护室通常使用血气分析仪进行离子钙测量,但其成本较高,且需要及时处理样品,因此受到限制。
③ 测量血清中的总钙
总钙通常用作一线检测,使用原子吸收光谱法的标准化参考方法可以准确测量血清中的总钙,但它们没有考虑离子钙。通常需要根据白蛋白或总蛋白进行调整才能估算离子钙。然而,这些调整通常与直接离子钙测量值不一致,可能无法准确反映真实的钙状态。
④ 骨量测量
虽然骨量测量结果与近期膳食钙摄入量没有很好的相关性,但它们反映了长期钙的充足性,并受整体钙状态的影响。
⑤ 空腹尿钙:肌酐比率
这种方法有望成为一种简单且廉价的指示近期钙状态的方法,尽管目前尚未广泛使用。
◮ 摄入高钙食物
摄入富含钙的食物是满足每日钙需求的最佳方式。
-高钙食物包括乳制品(牛奶、酸奶、奶酪);
-深海鱼类,深海鱼的含钙量比普通的鱼肉要高,虾皮含钙量高达991毫克/百克;
-蛋类,鸡蛋、鹌鹑蛋、甲鱼蛋等蛋类也含有丰富的钙元素;
-坚果,例如榛仁含钙达815毫克/百克;
-一些蔬菜,例如紫衣甘蓝、西兰花、香菇、木耳等食物也含有较多的钙。
◮ 使用钙补充剂
对于无法从饮食中摄取足够钙质的人,可能需要补充钙质。常见的钙质包括碳酸钙和柠檬酸钙,后者更容易被吸收。补充剂应根据个人需求量身定制,通常每天约500毫克,以补充饮食摄入量并达到推荐的每日摄入量。
钙与维生素D结合补充可增强钙的吸收,并具有其他健康益处,例如改善血脂状况并降低老年人的骨折风险。
注:建议每日摄入1000-1200毫克钙和800国际单位(IU)维生素D,尤其是对于老年人。
◮ 适当运动、晒晒太阳
运动不仅可以增强自身体质,还可以在户外增加晒太阳的时间,适当的阳光照射是皮肤合成维生素D的重要来源,对钙的吸收都有益处。
◮ 不吸烟、少喝酒
吸烟会增加肺癌的患病率,还有可能成为缺钙的重点人群。少喝酒,少摄入咖啡因。酒精和咖啡因会影响钙的吸收,也是造成骨质疏松的不可忽视的因素。
镁是人体内含量第四多的元素(Ca²+>K+>Na+>Mg²+),也是人体内细胞中含量第二多的阳离子,仅次于钾。
★ 镁在许多生理功能中发挥着重要作用
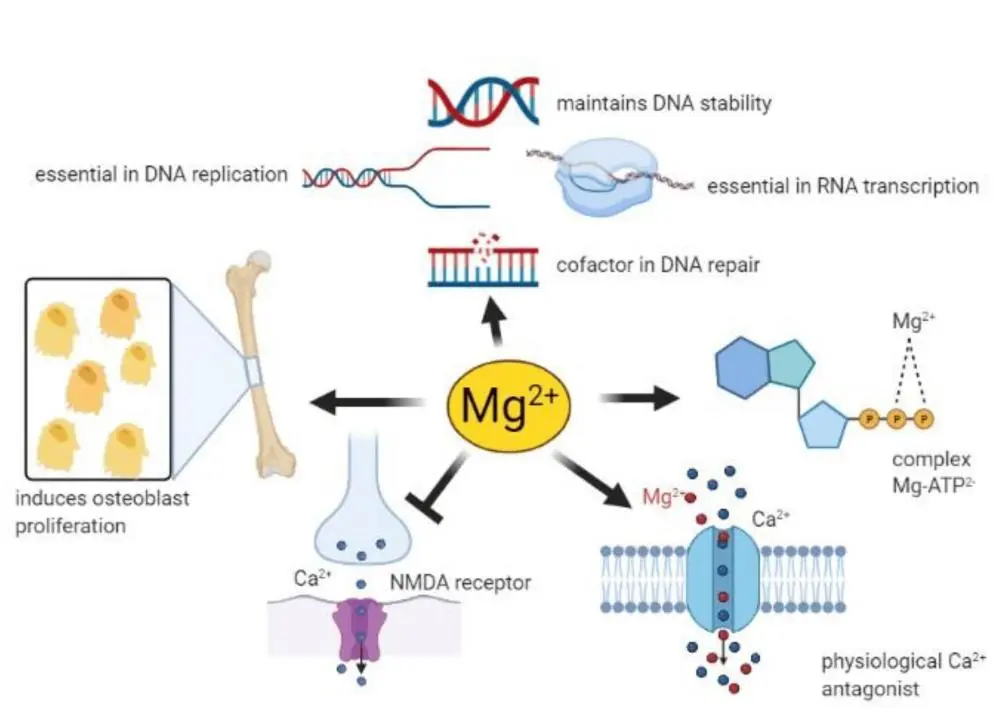
doi: 10.3390/nu13041136.
–MgATP复合物是许多酶活性所必需的。一般来说,Mg2+在所有涉及ATP利用和转移的反应中都起辅助因子的作用,包括细胞对生长因子的反应和细胞增殖,因此几乎参与了细胞中的每个过程。
–Mg2+是DNA和RNA聚合酶保持正确结构和活性所必需的,在DNA复制、RNA转录和蛋白质形成过程中必不可少,从而参与控制细胞增殖。此外,Mg2+对维持基因组和遗传稳定性至关重要,鉴于这些影响,Mg2+可用性低可能与癌症的发展有关。
-血清Mg2+浓度与骨代谢密切相关,骨表面Mg2+不断与血液中的Mg2+进行交换。此外,Mg2+会诱导成骨细胞增殖。
-Mg2+参与控制许多组织中某些离子通道的活性。这些能力与镁对心血管系统、肌肉和大脑的影响有关。
-神经元镁离子浓度会下调N-甲基-D-天冬氨酸(NMDA)受体的兴奋性,而这种受体对于学习和记忆中的兴奋性突触传递和神经元可塑性至关重要。出于这些原因,人们推测许多神经系统疾病都与Mg2+缺乏有关,例如偏头痛、癫痫、阿尔茨海默病、帕金森病和中风,以及焦虑和抑郁。
在普通人群中,镁缺乏症并不少见,并且男性的镁缺乏量要大于女性,因为雌激素会增强镁的利用率,有利于组织对镁的吸收。但由于不同原因和情况,习惯性摄入镁不足或过度流失会导致镁缺乏。
① 膳食摄入和不健康饮食
相当一部分人的镁摄入量未达到平均水平,这主要是由于现代西方饮食中镁含量低。此外,过去一个世纪里,蔬菜中的矿物质含量大幅下降,人们的蔬菜摄入量也减少,导致膳食中镁的摄入量降低。同时研究表明加工食品会阻碍镁的吸收。
② 胃肠道的pH值影响吸收
镁形式(无机盐、有机盐、螯合物等)的溶解度是一个重要因素,溶解度增加与吸收增加相关。胃肠道的pH值会影响镁形式的溶解度,pH值较低时镁的溶解度增加。而pH升高时,镁的吸收变得越来越困难。胃肠道中产生短链脂肪酸的细菌减少,可能会导致镁的吸收减少。
③ 药物的使用
某些药物,如利尿剂和质子泵抑制剂,可能导致镁缺乏。常用的质子泵抑制剂奥美拉唑影响体外被动运输。奥美拉唑通过使管腔酸度升高,抑制了镁的被动吸收。
④ 雌激素的水平
性别也会影响镁的状态,因为雌激素会增强镁的利用率,有利于软组织和硬组织对镁的吸收。年轻女性的镁保留能力比年轻男性更好,尤其是在排卵期或服用口服避孕药期间,此时雌激素水平最高。
⑤ 胃肠道和肾脏疾病
由于各种潜在的健康状况和治疗,住院患者,尤其是重症监护病房的患者,经常会缺乏镁。胃肠道和肾脏的流失是导致镁缺乏的重要因素。影响这些系统的疾病会导致镁排泄增加。
老年人:老年人从肠道吸收的镁较少,而由于肾脏排泄增加,镁流失较多,慢性镁缺乏症在老年人中确实很常见,通常是由于饮食摄入和肠道吸收减少所致,并且可能因雌激素缺乏而加剧,雌激素缺乏发生在老年女性和男性身上并导致高镁尿症。
患有胃肠道疾病的人:如克罗恩病、炎症性肠病和乳糜泻。特别是,除了乳糜泻导致的吸收效率低下之外,无麸质饮食还发现缺乏纤维和微量营养素,如镁。因此,患有乳糜泻的人是特别容易受到镁缺乏症的影响。
酗酒的人:酒精会影响肠道,并导致肠道吸收不良。乙醇还会导致近端肾小管功能障碍,增加尿镁流失。
使用一些药物的人:正在接受药物治疗(如利尿剂、质子泵抑制剂、他克莫司、免疫抑制剂、化疗药物和一些磷酸盐类药物)的人。
过去30年来,多项实验、临床和流行病学研究表明,慢性镁缺乏与多种疾病有关,或会加重这些疾病。
急性低镁血症
急性低镁血症具有明显的临床特征(严重痉挛、眼球震颤、心律失常等),并且易于检测。相反,亚临床或慢性镁缺乏症经常被低估,因为它反映的是细胞和骨骼内镁含量的降低,而不是细胞外镁含量的降低。
糖尿病
镁能诱导胰岛素受体的自身磷酸化,并调节这些受体上的酪氨酸激酶活性,从而起到胰岛素增敏剂的作用。多项研究报告称,细胞内镁水平降低会导致胰岛素抵抗增加。
骨质疏松症
镁缺乏可能是骨质疏松症的一个危险因素。研究发现,膳食镁、骨矿物质密度(BMD)和降低骨质疏松症风险之间存在正相关。

心血管疾病
越来越多的流行病学研究、随机对照试验和荟萃分析证据表明,镁摄入量与心血管疾病(CVD)呈反比关系。事实上,高镁摄入量与主要心血管风险因素(如高血压和糖尿病)、中风和总CVD的发生概率降低相关。此外,缺血性和冠心病风险降低与循环中镁含量较高有关。
癌症
多项流行病学研究表明,缺乏镁的饮食会增加患癌症的风险。镁是参与DNA修复机制的酶辅因子,在维持基因组稳定性和保真度、调节细胞周期进程、细胞增殖、分化和凋亡方面发挥着重要作用。镁缺乏会导致DNA突变,从而导致肿瘤发生以及癌症的风险和预后。此外,最近有报道称镁对化学致癌作用具有保护作用。
神经系统疾病
一篇文献非常详尽的总结了关于镁在预防和辅助治疗最常见的神经系统疾病方面所起的作用,镁缺乏可能导致偏头痛、中风、癫痫、阿尔茨海默病和帕金森病,以及常见的焦虑和抑郁并发疾病。
Mg2+主要通过小肠吸收,尽管有些也通过大肠吸收。Mg2+转运系统有两种,一种是被动的旁细胞机制,另一种是通过专门的Mg2+通道和转运蛋白进行的跨细胞转运。
Mg2+稳态由肠道、骨骼和肾脏在激素控制下维持。镁跨细胞膜的转运表现出组织差异,在人体组织中,心脏、肝脏、肾脏、骨骼肌、红细胞和脑的转运较高。
因此,镁的转运、镁稳态的生理学和细胞的代谢活动是紧密相关的。以下一些因素会影响膳食镁的吸收和利用:
◮ 饮食因素
膳食中钾含量过高会显著降低镁的吸收;钙和磷酸盐摄入量增加会损害镁的吸收。
某些膳食纤维(如半纤维素、纤维素、木质素)、植酸和草酸会抑制镁的吸收,而蛋白质和某些碳水化合物(如抗性淀粉、菊粉)则会促进镁的吸收。
◮ 维生素D
药理剂量的维生素D可增加镁的吸收,但相当一部分镁的吸收与维生素D无关。
◮ 激素水平
激素也会调节跨细胞Mg2+的吸收。最近的一项研究报告称,甲状旁腺激素(PTH)和成纤维细胞生长因子23(FGF-23)系统性地直接抑制十二指肠、空肠和回肠的跨细胞而非旁细胞Mg2+吸收。
◮ 肠道pH值
肠道内pH浓度会影响Mg2+溶解度和肠道Mg2+吸收,管腔pH升高导致可溶性Mg2+降低,从pH5.15时占管腔总Mg含量的79.61%下降到pH7.8时占管腔总Mg含量的8.71%。因此,腔内酸性可增强人体小肠和上皮样 Caco-2 单层细胞对Mg2+的吸收。
◮ 质子泵抑制剂的使用
自2006年以来,已有报道称质子泵抑制剂(PPI)诱发人类低镁血症(PPIH)和低镁尿。静脉补充Mg2+或停用PPI可使PPIH患者的血浆和尿液Mg2+水平迅速恢复正常,但口服补充Mg2+则不能。这些发现表明PPI可以抑制肠道Mg2+的吸收。
肠道菌群在结肠Mg2+吸收中可能发挥的作用已有人提出。
◮ 肠道菌群失调导致毒性物质产生增加
长期质子泵抑制剂(PPI)治疗可导致肠道菌群失调,例如负责维持粘膜屏障功能的放线菌和双歧杆菌属的减少。此外,长期使用PPIs治疗会导致小肠细菌过度生长,毒性物质的产生增加,如血清内毒素和刺激促炎细胞因子分泌的细菌化合物,这些有毒物质会干扰镁的吸收。
◮ 肠道微生物群会影响肠道吸收表面的变化
除了这些发现之外,我们之前的研究还显示低镁血症(PPIH)大鼠小肠存在潘氏细胞功能障碍和慢性炎症。肠道微生物代谢物的合成也可能导致肠道吸收表面的变化或刺激基因表达。
◮ 产短链脂肪酸的细菌有利于镁的吸收
在结肠中,双歧杆菌等细菌发酵会产生短链脂肪酸导致结肠酸化,有利于Mg2+的吸收。在人体小肠中,占主导地位的细菌门是链球菌属,它是一种厌氧菌,能够以较高的速率发酵相对简单的碳水化合物,而腔内酸性会显著诱导小肠对Mg2+的吸收。
自从认识到镁对人类健康的重要性以来,人们就提出了一个问题:如何才能清楚了解自身镁的状态?
① 原子吸收光谱法
原子吸收光谱法(AAS)可能是最古老、应用最广泛的评估生物样品中镁含量的技术。它的重要优点是可以应用于所有类型的生物样品,但其主要缺点是样品制备、仪器校准和分析耗时。
② 离子选择电极
Mg2+可用离子选择性电极进行电位测定,离子化的 Mg2+可以在全血、血清或血浆,或在红细胞等细胞中测量。该技术的主要缺点是电极缺乏特异性和反应时间较长。
③ 光学化学传感器
用于测定镁的光学化学传感器由于其良好的选择性、灵敏度和制备简单而成为重要且日益增长的应用领域。提出了几种荧光和比色测定方法,包括比色法和酶法测定和荧光化学传感器,前者的选择性和灵敏度更高。
④ 元素生物成像
化学成像是一个相当新的研究领域,它能够以高灵敏度和空间分辨率检测元素,另一个优势是它可以同时评估多种元素或分子。
镁是生物体必需的营养物质,因此必须定期从饮食中补充,以达到推荐摄入量,防止缺镁。当食物中的镁摄入不足时,可能就需要使用镁补充剂。
◮ 饮食补充
镁广泛分布于食物中,尽管食物中的镁含量受多种因素影响,包括灌溉的土壤和水、肥料、保护以及精炼、加工和烹饪方法。一般来说,种子、豆类、坚果(杏仁、腰果、巴西坚果和花生)、全麦面包和谷物(糙米、小米)、一些水果(杏和香蕉)和可可被认为是镁的良好来源。
◮ 镁补充剂
镁补充剂有多种配方,包括无机盐(例如氧化镁、氯化镁、硫酸镁)和有机化合物(例如柠檬酸盐、苹果酸盐、吡多酸盐、牛磺酸盐)。
不同种类补充剂对镁的吸收并不相同。此外,吸收取决于受试者的镁状态。Mg2+的吸收量取决于摄入剂量。例如,当膳食中Mg2+摄入量较低时,相对吸收率可达80%,而在Mg2+丰度状态下,相对吸收率降至20%。通常,Mg2+以离子形式被吸收。可溶性镁比溶解性较低形式的镁更容易被肠道吸收。
◮ 菊粉、寡糖、抗性淀粉等有助于增强镁吸收
含有膳食非发酵纤维的食物确实含有高含量的镁,但其生物利用度较低,与铁类似。相比之下,可发酵的碳水化合物(如菊粉、寡糖、抗性淀粉、甘露醇和乳果糖)可增强 Mg2+的吸收。
◮ 生活方式调整
减少摄入过多的酒精和咖啡因,因为它们可能影响镁的吸收。
通过适当的运动和减压活动来改善整体健康,从而促进镁的吸收和利用。
下图展示了镁的主要来源、镁补充剂以及增加或减少镁生物利用度的因素:
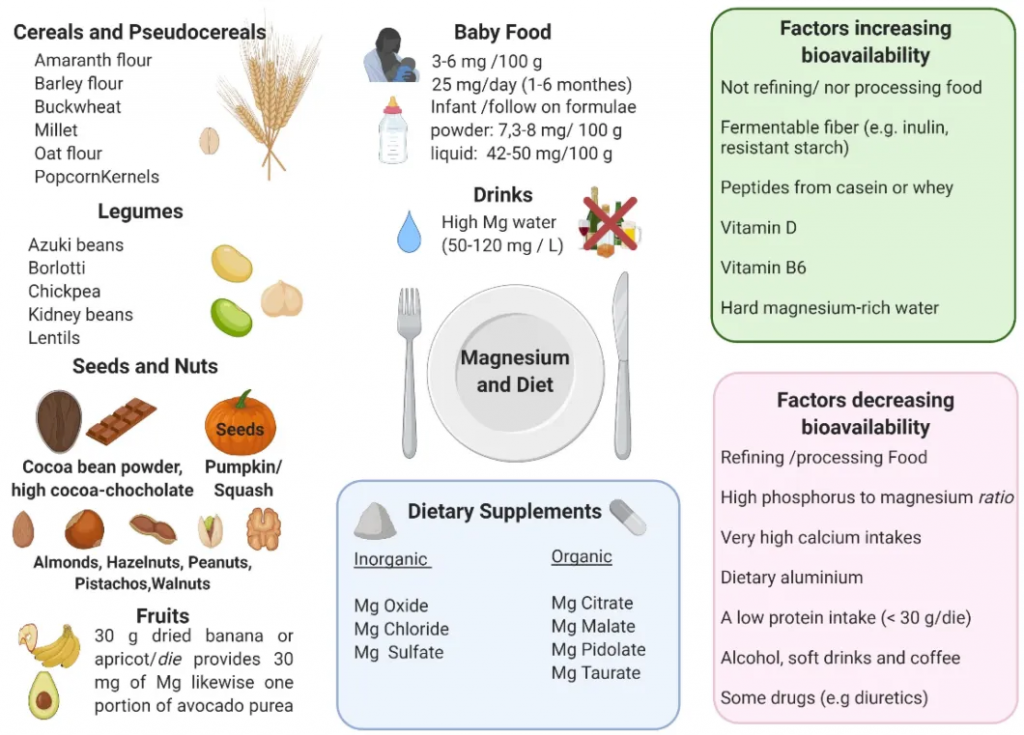
doi: 10.3390/nu13041136.
硒是一种重要的微量营养素,主要通过硒蛋白(可作为结构蛋白或酶)来支持多种生理功能。它在抗氧化防御、甲状腺激素代谢、免疫功能、生殖健康以及潜在的癌症预防和慢性疾病管理中发挥着重要作用。
硒缺乏在人体中也不罕见,并且女性中硒缺乏量高于男性。硒缺乏的原因可以归结为多种因素,以下是详细的说明:
① 生活在低硒地区、饮食中缺硒
某些地区的土壤中硒含量低,如中国的克山病和大骨节病的重病区,这些地方的植物和动物产品中硒含量较低。
海产品和动物内脏是硒的良好食物来源,如鱼子酱,海参,牡蛎蛤蜊和猪肾等。饮食中缺乏硒的来源,导致营养性缺硒。
② 农药、化工产品阻碍硒的吸收
环境污染,农药、化肥、化工原料的残留物可拮抗硒元素的吸收,造成农作物缺硒,进而导致人体缺硒。
③ 体质和疾病状况
进入中老年后,人体的消化、吸收能力也会逐渐降低,影响硒元素的吸收。
疾病加剧缺硒、缺硒加剧疾病,例如,肿瘤、心血管病、克罗恩病、溃疡性结肠炎、糖尿病、肝病患者体内往往处于缺硒状态。
④ 特殊人群的硒需求量增加
长期酗酒、吸烟、情绪紧张的人体内的硒流失量远高于健康人,此外,包括孕妇和哺乳期妇女、儿童和青少年、老年人、癌症患者、运动员和体力劳动者的硒需求量增加。
人体缺硒的表现主要为脱发、脱甲;部分患者会出现皮肤症状;少数患者可出现神经症状及牙齿损害等问题;严重缺硒可导致溶血性贫血、克山病和大骨节病。
硒缺乏还被认为是几种慢性疾病的风险因素,这些疾病涉及胃肠道、肌肉和神经系统的氧化应激和炎症有关。
克山病
克山病亦称地方性心肌病,这种病是由硒缺乏和柯萨奇病毒突变株的存在相互作用而引起的,患者主要表现为急性和慢性心功能不全,心脏扩大,心律失常以及脑、肺和肾等脏器的栓塞。
大骨节病
缺硒还与大骨节病(一种地方性骨软骨病)有关,大骨节病被认为是硒缺乏和谷物中霉菌毒素以及饮用水中腐殖酸含量高共同引起的。
◮ 硒主要在十二指肠、盲肠、结肠中被吸收
膳食中摄入的有机或无机硒均在胃肠道中吸收,研究表明,有机硒的吸收率高于无机硒。硒的主要吸收部位是十二指肠、盲肠和结肠。
硒氨基酸通过各种膜转运机制在十二指肠、盲肠和结肠中主动转运,而硒酸盐则通过 SLC26 基因家族的阴离子交换剂转运。
从十二指肠吸收的硒首先进入血液,与血浆中的红细胞、白蛋白或α球蛋白结合,也可结合β球蛋白、血浆高密度脂蛋白或低密度脂蛋白,随后转运至肝脏,在肝脏中代谢并用于生成硒蛋白,然后分布至身体的其他组织。
硒的主要排泄形式是通过尿液,然而,在过量摄入的情况下,可能会发生呼吸道排泄。在适量摄入硒的情况下,通过肾脏排出的主要单甲基化合物是硒糖,即1β-甲基硒N-乙酰-D-半乳糖胺。食物中未被吸收的硒被吸收到胆汁、胰腺和肠道分泌物中,并在粪便中排出。
硒的吸收、代谢和分布
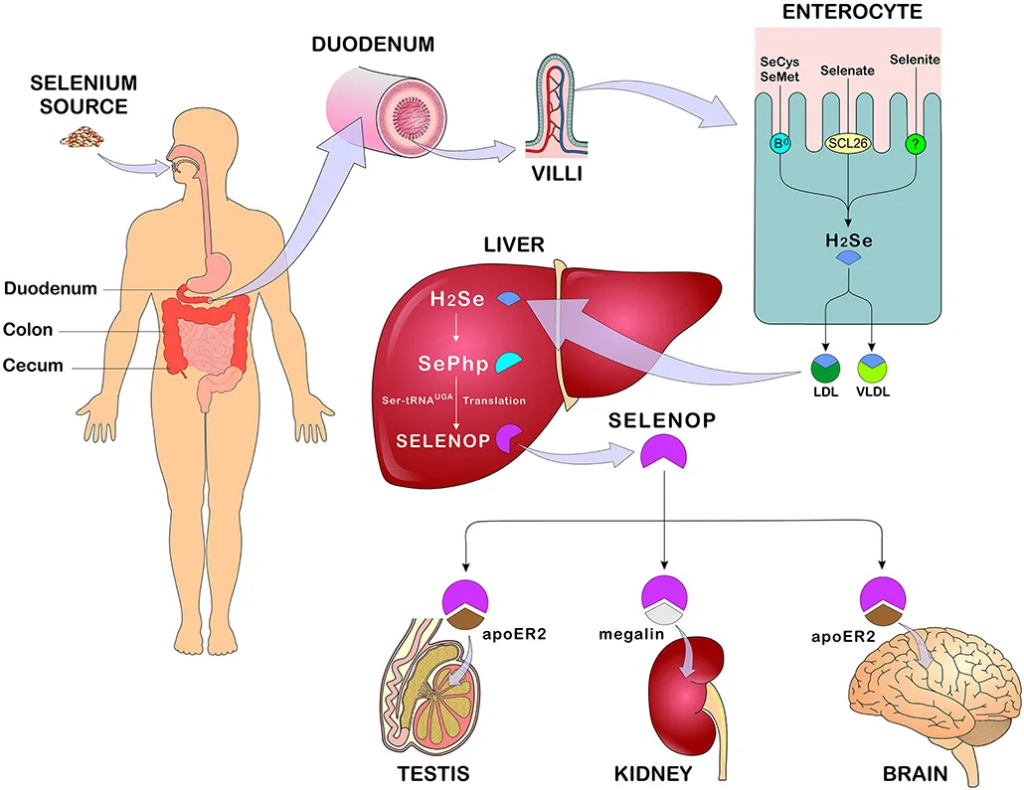
doi: 10.3389/fnut.2021.685317.
肠道微生物群的调节取决于硒的状态和硒衍生物的生物转化。
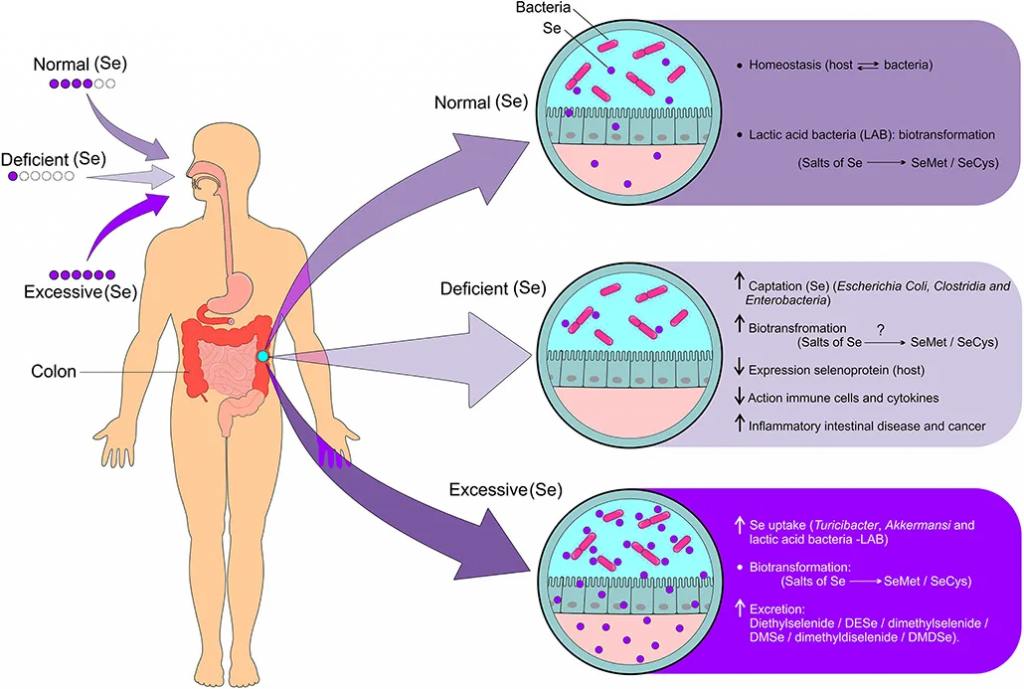
doi: 10.3389/fnut.2021.685317.
◮ 硒摄入充足时,肠道菌群有助于更好地转化和利用硒
如果硒摄入量充足,由于肠道和宿主细菌之间的有益关系,会导致硒化合物的生物转化(硒盐代谢为硒蛋氨酸和硒半胱氨酸),从而形成体内平衡。
一项研究表明,大鼠肠道菌群将几种无机和有机硒化合物代谢为硒蛋氨酸,并且硒蛋氨酸被整合到细菌蛋白质中。含有硒蛋氨酸的蛋白质可作为宿主动物的硒库,在肠道菌群中积累。尿液中的主要硒代谢物 SeSug1 被肠道菌群转化为营养上可利用的硒化合物。最后,在肠道菌群中观察到一些生物硒化合物(如SeCN、MeSeCys和SeSug1)对生物利用度有积极影响。
◮ 硒含量较低时,菌群会与宿主竞争导致更缺乏
尽管宿主和肠道菌群互利共生,但当微量营养素供应有限时,这两个环境就会变成竞争对手。肠道细菌对硒的吸收会对宿主体内硒蛋白的表达产生负面影响,导致硒蛋白在硒限制条件下的含量降低2到3倍。
硒缺乏会导致细菌(大肠杆菌、梭菌和肠杆菌)对硒的吸收增加,硒化合物的生物转化(硒盐代谢为硒蛋氨酸和硒半胱氨酸),宿主硒蛋白的表达减少,硒免疫细胞的活性降低,促炎细胞因子增加,炎症性肠病和癌症的风险增加。
◮ 一些菌群可以通过硒来增强毒力和致病性
一些细菌物种能够从硒中获益,从而触发致病机制。具有硒依赖性酶的细菌可以在哺乳动物肠道的厌氧条件下存活。因此,这些细菌通过使用硒来增加其毒力和致病性,从而对宿主产生一定危害。
硒状态可从三个层面进行评估,即摄入量、保留量/排泄量和组织浓度的生物标志物以及功能性生物标志物。
① 摄入量的评估
硒摄入量的评估可以使用评估食物消费的方法来执行,例如食物频率问卷。使用食物成分表可以估算食物中的硒含量。由于食物成分表中营养成分缺乏精确度,因此根据食物消费预测硒状态仍然是一个挑战,因为食物中硒浓度的变化与土壤中硒含量有关。
② 尿液硒浓度可以反应食物中的硒含量
测量尿液中的硒浓度被认为是硒状态的潜在可行生物标志物。此外,尿液中的硒浓度可用于识别硒状态的区域差异,并可能反映食物中硒含量随土壤类型的差异。
③ 指甲硒浓度可以反应硒的长期暴露情况
指甲中的硒浓度被认为是硒状态的优质生物标志物,因为它可以提供长期暴露(长达1年)的综合测量数据,而血液生物标志物则可指示短期暴露情况。注:脚趾甲被认为是非侵入性基质,并用于大型流行病学研究,因为它们生长缓慢、易于采集、受外部污染的影响较小。
④ 血浆硒浓度可以有效反应硒的摄入量情况
考虑到硒在血浆中的稳定性,血浆硒浓度是评估人体硒状态更有用的生物标志物。血浆中硒的测量已被证明可有效反映基线时硒浓度中等或较高的个体的摄入量 (补充) 变化。此外,强调了红细胞和全血中硒作为状态标志物的实用性,这两者都被报告为长期状态的标志物。
⑤ 硒功能的生物标志物
硒功能性的生物标志物包括SELENOP(占血浆硒的20-70%)、GPX3(占血浆硒的10-25%)和GPX1(可在红细胞、淋巴细胞、口腔细胞和组织活检标本中检测)。
血浆SELENOP被认为是硒摄入量相对较低的人群中硒状态的有用生物标志物,但不适用于硒摄入量高、在开始补充前硒水平就已经很高的人群。
GPX是细胞抗氧化防御系统的主要硒蛋白之一。由于硒蛋白的层次结构,推荐的硒摄入量是根据最佳血浆 GPX3 活性计算得出的。它还考虑了其他生物硒化合物正常浓度所需的硒量。
◮ 食物补充
巴西坚果、谷物、肉类、鱼类、海鲜、牛奶和坚果是硒的最佳来源。但鱼类和海鲜与汞相互作用会产生不溶性硒衍生物,从而降低硒的生物利用度。此外,饮食中的蛋白质、脂肪和重金属含量也会影响硒的生物利用度。
硒的生物利用度主要取决于其化学形态。一般而言,有机形态吸收更快。
◮ 药物补充
硒酵母胶囊:是一种常见的补硒药,主要成分为硒酵母,临床多用于治疗低硒的肿瘤、肝病、心脑血管疾病等。
亚硒酸钠片:属于一种常见的微量元素补充药,临床主要用于防治缺硒引起的疾病,如克山病、大骨节病等。
与矿物质相比,维生素在过去几年已经引起了广泛关注,市场上也涌现出众多维生素补充产品。因此,我们将维生素的讨论放在后面,但这并不意味着维生素的重要性被低估。顾名思义,维生素是“维持生命的重要元素”,它们在身体的正常运作、代谢过程以及免疫系统的健康中都扮演着不可或缺的角色。
维生素E又称生育酚,是一种脂溶性的维生素,是人体最主要的抗氧化剂之一。其对人体健康有多方面的作用,简单概况如下:
•抗氧化、抗自由基作用
•维持生育功能
•维持免疫功能
•减少细胞耗氧量
•改善脂质代谢
•抑制癌细胞分化
•促进红细胞膜稳定及红细胞的合成
•重要的血管扩张剂和抗凝血剂
•保护皮肤免受紫外线和污染的伤害
•对晶状体有一定保护作用
•促进蛋白质的更新合成
•治疗口腔溃疡
•治疗痔疮
最新的研究报告显示超过50亿人的维生素E摄入不足(占67%),这值得引起我们的重视。
根据最新的研究结果,探讨了维生素E缺乏的主要原因和促成因素。
① 营养缺乏
饮食中维生素E摄入不足,长期摄入低脂饮食或极低脂肪饮食可能导致维生素E摄入不足,因为维生素E是一种脂溶性维生素,主要存在于植物油、坚果和种子中。
缺乏富含维生素E的食物,如坚果、种子、植物油、绿叶蔬菜等。
② 吸收不良症
维生素E缺乏症通常是由脂肪吸收不良引起的,这种疾病会阻碍这种脂溶性维生素的正常吸收。脂蛋白代谢异常和α-生育酚转移蛋白缺陷等情况都可能导致维生素E缺乏。
③ 氧化应激和感染
发展中国家的人更容易出现维生素E缺乏症,因为他们更容易受到疟疾和艾滋病毒感染或其他氧化应激源的影响,而这些因素会增加人体对维生素E等抗氧化剂的需求。
④ 年龄和性别脆弱性
儿童和老年人更容易缺乏维生素E。此外,男性的风险可能高于女性,尽管这种性别差异的原因尚不完全清楚。
⑤ 减肥手术
接受减肥手术的患者,尤其是涉及吸收不良手术的患者,由于术后脂肪吸收受损,更容易出现维生素 E 缺乏症。
⑥ 遗传因素
家族性维生素E缺乏症是一种罕见的遗传综合症,会导致严重缺乏,并与氧化应激引起的多器官并发症有关。
⑦ 特殊人群需求量增加
饮用氯消毒自来水的人需要多摄入维生素E,心血管病患者、帕金森病患者、孕妇、中老年人和摄入酒精和激素的人维生素E的需求量也增大。
大多数人缺乏维生素E时,可能会导致贫血、免疫力下降、人体代谢紊乱、早衰、肌肉无力等症状。
•儿童
小儿缺乏维生素E时,可引发脊髓小脑病和轻度溶血性贫血。最为常见的是溶血性贫血,此外还可发生黄疸、全身性水肿、以及神经系统的症状,主要表现为小脑共济失调、色素性视网膜病、眼肌麻痹、眼球震颤和肌无力,反射减弱等。
•男性
男性严重缺乏维生素E会引起男性激素分泌不足、睾丸萎缩、精子生成障碍、精子减少或不成熟、精子活力不足等,甚至会导致不育。
•女性
女性缺乏维生素E容易导致黄体激素不足,易造成流产、不孕症、早产等,还容易造成皮肤干燥、易衰老。中年女性缺乏维生素E,很容易诱发更年期综合征、卵巢早衰。
•孕妇
孕妇若缺乏维生素E,所生婴儿会比较瘦小,发育较慢;孕妇严重缺乏维生素E会造成胚胎和胎盘萎缩,从而引起流产。
通过日常饮食调节维生素E是最便捷的方法,那么哪些食物中含有较高的维生素E呢?
种子植物的油,特别是小麦、黄豆、豌豆、棉籽和玉米胚芽油是含维生素E最丰富的来源(0.5-3mg/g)。
人造黄油也含有丰富的维生素E,而奶制品则含量较少,人和牛的初乳所含维生素E约比成熟乳含量高10倍。
其他植物如生菜,芹菜和甜薯也含有维生素E,但含量不高。蛋类、鸡(鸭)胗、绿叶蔬菜中也含有一定量的维生素E;肉,鱼类动物性食品,水果及其他蔬菜的维生素E含量较少。
维生素C,也称为抗坏血酸,是一种水溶性维生素,对人体健康非常重要。它在许多身体功能中起着关键作用,简单概况如下:
•抗氧化
•促进氨基酸中酪氨酸和色氨酸的代谢
•改善贫血
•增强免疫力
•促进胶原蛋白的形成
•防癌抗癌
•解毒排毒
•参与蛋白质合成
•改善脂肪和类脂特别是胆固醇的代谢
•提高钙的利用
① 饮食摄入不足
人体不能合成维生素C,必须从外界摄入。如果摄入不足,就有可能导致维生素C缺乏。
缺乏富含维生素C的食物:长期不摄入新鲜水果和蔬菜,如柑橘类水果、草莓、番茄、绿叶蔬菜等。
不均衡饮食:偏食或饮食单一,导致维生素C摄入不足。
② 吸收障碍
消化系统疾病:如克罗恩病、溃疡性结肠炎等,可能影响维生素C的吸收。
胃肠道手术:如胃切除术后,可能影响维生素C的吸收。
此外,维生素C遇热、碱或金属也极易被破坏,从而影响维生素C的利用。
③ 需求增加
生长发育期:儿童和青少年在快速生长阶段对维生素C的需求增加。
妊娠和哺乳期:孕妇和哺乳期妇女对维生素C的需求增加。
感染或疾病:在感染、手术或创伤后,身体对维生素C的需求可能增加。
④ 生活方式因素
吸烟:吸烟者体内维生素C的代谢加快,需求量增加。
酗酒:长期酗酒可能导致营养不良,包括维生素C缺乏。
维生素C缺乏症也称为坏血病,刚缺乏维生素C的时候症状不明显,大约一个月的时间才会出现症状。体内维生素C总含量低于300-400mg会出现明显症状。
•初期症状
缺乏维生素C初期常有一些非特异性表现,如易激、性情暴躁、倦怠、食欲减退、体重减轻和面色苍白等,也可出现易感染、伤口不易愈合或低热、呕吐、腹泻等消化功能紊乱症状。
•出血症状
随着病情的发展,可出现大小不等、程度不等的出血。常见长骨骨膜下出血;皮肤及黏膜出血多见于骨骼病变附近,膝部、踝部多见。
牙龈黏膜常肿胀、出血;也可出现鼻出血,眼结膜出血,眼眶骨膜下出血可引起眼球突出;偶见消化道出血、尿血甚至颅内出血。
•骨骼症状
维生素C缺乏症的较晚阶段患者下肢会由于骨膜下出血较多而肿胀、疼痛;部分患者肋骨与肋软骨的交接处会因骨干骺半脱位而隆起,形成坏血病串珠,内侧可扪及凹陷。
•长期症状
维生素C不足可影响铁的吸收和利用,加上长期出血会导致缺铁性贫血。当叶酸代谢障碍时,患者可能同时缺乏叶酸,从而出现巨幼红细胞贫血。
◮ 含维生素C的食物
维生素C广泛存在于新鲜蔬菜和水果中。番茄、花菜、柿子椒、深色叶菜、苦瓜、柑橘、柚子、苹果、葡萄、猕猴桃、冬枣中均富含维生素C。
一些维生素C含量较高的食物
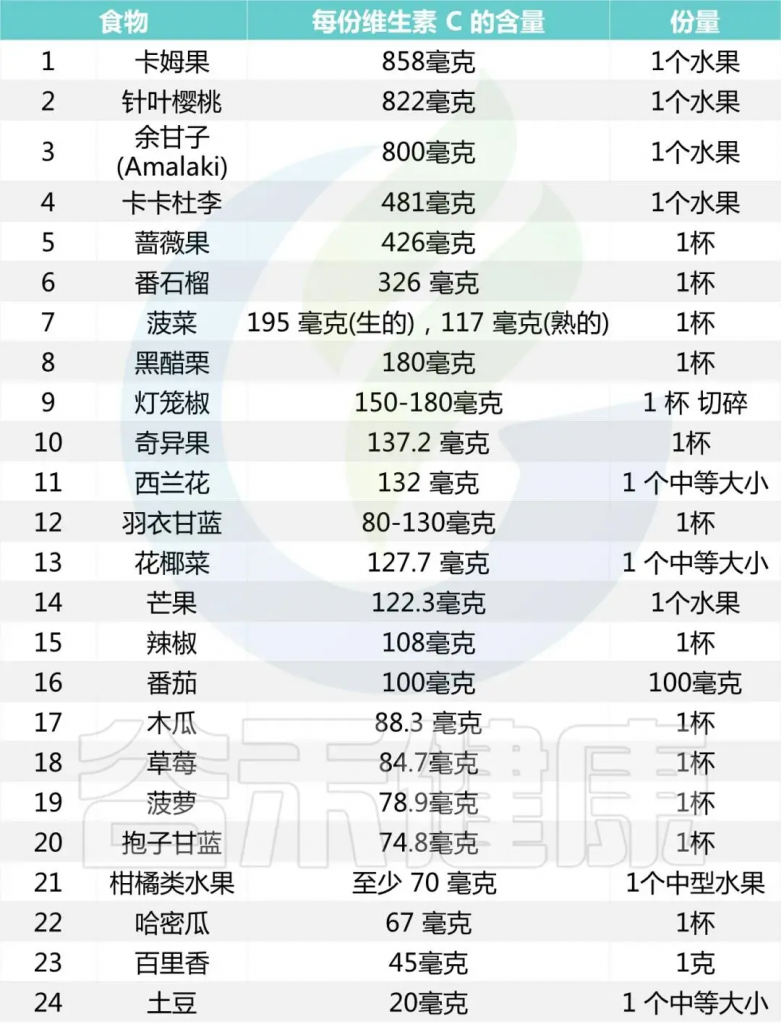
◮ 维生素C补充剂
可以补充维生素C的药品多种多样,包括:
(1)维生素C片;
(2)维生素C泡腾片;
(3)抗坏血酸钙;
维生素A是一种重要的脂溶性维生素,又称抗眼干燥症因子。需要注意的是,维生素A并不是单一的化合物,而是一系列包括视黄醇、视黄醛、视黄酸、视黄醇乙酸酯和视黄醇棕榈酸酯等的视黄醇衍生物。
维生素A是最受关注的营养素之一,它对于维持正常的视力、基因表达、生殖、胚胎发育、生长和免疫功能都是极为重要的。维生素A在人体具有广泛而重要的功能:
•参与暗光视觉的物质循环,使机体可适应暗光环境
•保持皮肤和黏膜的完整
•细胞核激素样作用
•维持和促进免疫功能
•促进生长发育和维持生殖功能
•对骨骼代谢有影响
•抗氧化、防癌
•促进血红蛋白生成
自然界的维生素A包括维生素A1、维生素A2两种。维生素A1即视黄醇,多存在于哺乳动物及咸水鱼的肝脏中;维生素A2即3-脱氢视黄醇,常存在于淡水鱼的肝脏中,其生理活性为维生素A1的40%。
75%以上吃西方饮食的人获得的维生素A是足够的,不需要担心缺乏的问题。然而,在许多发展中国家,维生素A的缺乏是非常普遍的。在某些地区,大约44-50%的学龄前儿童有维生素A缺乏症。并且柳叶刀最新研究公布的数据显示,男性摄入的维生素 A不足量估计高于女性。
维生素A缺乏症的公共卫生数据
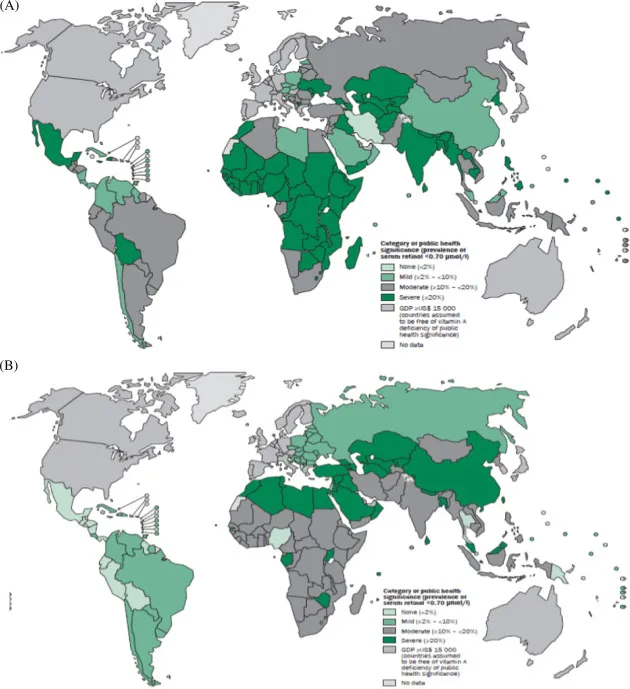
doi.org/10.1016/B978-0-12-802861-2.00002-X
上图反应了截止2018年的全球维生素A缺乏症情况:
(A)学龄前儿童;(B)孕妇
那么为什么一部分人会存在维生素A缺乏?主要是以下几点原因:
① 摄取不足
长期不摄入富含维生素A的食物,如动物肝脏、鱼肝油、乳制品、蛋黄,以及富含β-胡萝卜素的蔬菜和水果(如胡萝卜、甘薯、菠菜等)。
注:β-胡萝卜素,是一种原维生素A,你的身体能将其转化为维生素A。
② 排泄增加
肿瘤、泌尿系统疾病、急慢性感染性疾病等,可能会导致维生素A的消耗和流失增加,使得更易缺乏维生素A。
③ 吸收障碍
维生素A是脂溶性维生素,任何导致脂肪吸收不良的情况都会影响维生素A的吸收。这包括慢性胰腺炎、胆汁淤积、囊性纤维化等。
一些肠道疾病,如乳糜泻、克罗恩病等,这些疾病会影响肠道对维生素A的吸收。
④ 代谢异常
患有合成蛋白质和锌减少的疾病,如肝病、甲状腺功能低下、糖尿病等,导致胡萝卜素无法转变成维生素A。
维生素A的储存和代谢主要在肝脏进行,肝功能不全可能影响维生素A的代谢。
⑤ 需求增加
生长发育期:儿童和青少年在快速生长阶段对维生素A的需求增加。
妊娠和哺乳期:孕妇和哺乳期妇女对维生素A的需求增加。
无法通过正常饮食摄入足够的维生素A就可能导致这些人群缺乏。
•眼睛症状
维生素A的缺乏初期表现为眼睛干涩,随后可能出现夜盲;进一步发展会导致暂时和永久的眼睛损伤,甚至可能导致失明。这种缺乏是世界上主要的失明原因。
•皮肤症状
初期表现为皮肤干燥、脱屑;进一步发展可在大腿和手臂出现大量的丘疹,后期可蔓延至颈、腹、背等部位。
•生长发育障碍
长期缺乏维生素A,患儿可表现为骨骼粗短,牙齿发育不良、生长缓慢、智力轻度落后等。
•贫血
维生素A可以促进铁的吸收,当维生素A缺乏时,铁不能正常地被红细胞吸收,会造成贫血。
•免疫力下降
由于维生素A直接影响上皮细胞的体液免疫和细胞免疫,对机体的特异性免疫和非特异性免疫都具有一定作用,如果缺乏维生素A会导致机体的免疫力下降,容易继发感染性疾病。
•其他影响
缺乏维生素A还可能影响味觉、嗅觉的功能,导致食欲下降。
维生素A存在于动物体内,在鱼类特别是鱼肝油中含量很多。维生素A主要来源于各种动物肝脏和其他脏器类肉品,蛋黄、鱼油、奶油和奶制品。
植物中并不含有维生素A,但许多蔬菜和水果却含有维生素A原,维生素A原是指在人体内能转变为视黄醇,发挥维生素A生理功能的类胡萝卜素。富含维生素A原的食物包括各种红、黄、绿色蔬菜和水果,如胡萝卜、红心甜薯、菠菜、水芹、羽衣甘蓝、芥菜、南瓜、莴苣、西兰花等。
维生素B12,又称钴胺素,是一种水溶性维生素。维生素B12家族有四个成员,即氰钴胺、羟钴胺、腺苷钴胺和甲钴胺。
维生素B12对多种基本代谢功能至关重要,包括:
•促进红细胞发育
•促进人体神经细胞发育
•促进甲基转移
•提高叶酸利用率
•还参与脱氧核糖核酸(DNA)的合成,以及脂肪、糖类、蛋白质的代谢
•促进维生素A在肝脏的储存
维生素B12缺乏症非常常见,尤其是在素食者、孕妇和老年人中。同时数据表明女性摄入的维生素 B12不足量估计高于男性。
而导致维生素B12缺乏的原因可能是以下几种:
① 先天储备不足
孕妇多因长期素食、恶性贫血、胃肠道手术等引起体内维生素B12缺乏,从而导致新生儿维生素B12先天储备减少。
② 饮食结构不合理
长期素食或苯丙酮尿症患者长期拒绝动物蛋白摄入可引起体内维生素B12缺乏。
③ 吸收异常
包括以下几种情况:内因子的异常或缺失、维生素B12释放缓慢、回肠吸收面积减小、回肠维生素B12结合受体异常。
④ 先天性维生素B12代谢障碍
钴胺转运蛋白II是维生素B12的主要转运蛋白,先天性钴胺转运蛋白II缺乏可导致维生素B12转运障碍,从而出现维生素B12缺乏。
⑤ 其他因素
麻醉剂氧化亚氮可导致维生素B12失去生物活性,引起脊髓变性;大剂量维生素C可导致食物中维生素B12的利用率下降;不适当补给叶酸可诱导或加重维生素B12缺乏。
缺乏维生素B12导致的疾病有巨幼红细胞性贫血、神经系统损害、高同型半胱氨酸血症。
•血液系统
缺乏维生素B12可表现为贫血,乏力、肝脾大,重症患者可有皮肤瘀点、瘀斑等。严重者有发热,皮肤、巩膜轻度黄染。
•神经系统
症状出现较迟,有神经障碍、脊髓变性,脱髓鞘和严重的精神症状,患者有手指和脚对称性麻木及感觉异常、出汗障碍,指端和关节突处溃疡、行动困难、共济失调、健忘、易激、甚至痴呆。年幼患者有精神抑郁、智力减退,头、四肢和躯干震颤,亦可因昏迷而死亡。
•消化系统
消化道症状有呕吐,腹泻和舌炎,舌乳头萎缩,舌面有炎性小疱或浅溃疡,自觉疼痛。
•心脑血管
维生素B12缺乏会引起同型半胱氨酸过高,导致动脉粥样硬化、心脑血管疾病。
•小儿缺乏维生素B12
早期表现为精神情绪异常、表情呆滞。少哭少闹、反应迟钝、睡眠多等症状,最后可能出现贫血。
肠道菌群可以是维生素B12的消费者或生产者。
◮ 肠道细菌过度生长会导致维生素B12缺乏
胃肠道中大约80%的微生物群被认为是维生素B12的消费者。因此,细菌过度生长可能会与宿主竞争外源性维生素B12,从而降低生物利用度。在小肠细菌过度生长中,厌氧菌增加对维生素B12的消耗被认为是维生素B12缺乏症状的主要原因。
减少维生素B12消耗细菌的数量对维生素B12缺乏症有益。例如,每日使用益生菌治疗乳酸杆菌对细菌过度生长和维生素B12吸收均有益,这表明益生菌治疗可以改善维生素B12缺乏症。
◮ 一些肠道菌群可以产生维生素B12
据报道,有几种细菌是维生素B12的生产者,如罗伊氏乳杆菌和屎肠球菌。从发酵食品中分离出的植物乳杆菌和棒状乳杆菌产生维生素B12,而动物双歧杆菌在牛奶发酵过程中合成维生素B12。
此外,可能参与维生素B12合成和代谢的菌还有:
大约三分之一的嗜黏蛋白阿克曼菌(A.muciniphila)分离株能产生类似于A.glycaniphila的维生素B12。多种结肠微生物可以产生可供A.muciniphila利用的维生素B12。
据推测,补充产生维生素B12的细菌可以改善胃肠道对维生素B12的利用率。这种假设已在喂食缺乏维生素B12饮食的小鼠身上得到证实。补充产生维生素B12的菌株罗伊氏乳杆菌CRL1098可预防维生素B12缺乏的症状,表明肠道细菌对维生素B12缺乏症具有治疗作用。
◮ 肠道菌群改善了维生素B12的吸收利用
肠道菌群除了生产或消耗维生素B12外,还可能通过影响吸收相关的生理因素间接改变维生素B12的生物利用度。
与酸分泌或酶含量减少有关的胃肠道疾病可能会干扰食物中维生素B12的释放或维生素B12转化为内在因子。在以肠道通透性异常为特征的炎症性肠病中也观察到维生素B12吸收减少。
作为益生菌,Lacidofil治疗显著改善了H.pylori感染的胃酸分泌,从而有助于食物中维生素B12的释放。一些肠道细菌也表现出对炎症性肠病的缓解作用,这可能通过使肠道通透性正常化来改善维生素B12的吸收。
然而,肠道菌群与宿主之间的过度竞争可能会干扰维生素B12的生物利用度。例如,多形拟杆菌 (Bacteroides thetaiotaomicron)表达一种对维生素B12运输至关重要的表面暴露脂蛋白,名为BtuG。BtuG的结合亲和力较高,可能会将维生素B12从内在因子中移除,从而降低维生素B12的吸收。
饮食和微生物群的在维生素B吸收中的作用
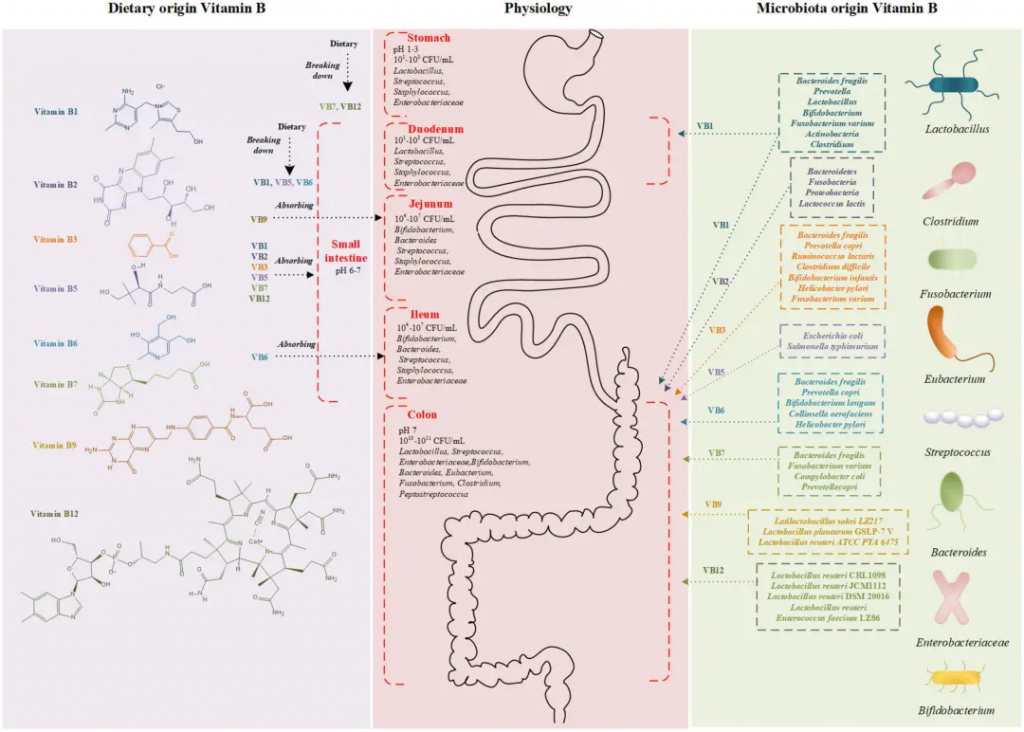
Wan Z,et al.Front Nutr.2022
维生素B12的膳食来源主要为动物性食品,含维生素B12较丰富的食物为动物内脏(肝、肾、心)、双壳贝(蛤、蚶和牡蛎)、脱脂奶粉、蟹、石鱼、鲑鱼、沙丁鱼和蛋黄,其他还有龙虾、鳕鱼、比目鱼、金枪鱼、发酵奶酪、鲜奶制品。
豆制品经发酵也会产生一部分维生素B12。
!
小贴士
有的人可能会担心维生素B12补充过量是否会存在一定风险,大量的维生素B12并不有害,因为它通常吸收不好,容易排出体外。
目前对体内维生素水平是否缺乏有以下几种方法:
1
临床症状观察
观察身体是否出现特定维生素缺乏的症状。例如,维生素C缺乏可能导致牙龈出血,维生素D缺乏可能导致骨骼疼痛或软化。
2
血液检测
血清维生素水平:通过血液检测直接测量特定维生素的浓度,如维生素D、B12、A等。
代谢产物检测:测量血液或尿液中某些代谢产物的水平,间接反映维生素状态。
3
饮食评估
饮食记录分析:记录几天的饮食,分析是否摄入足够的维生素。
食物频率问卷:通过问卷了解饮食习惯,评估维生素摄入情况。
4
肠道菌群健康检测
通过肠道菌群健康检测,也可以查看近期体内维生素状况。
与通过血液进行维生素检测不同,肠道菌群的评估更加反映一段时间(一般2周左右)的长期状态。
注意,菌群会受检测前一天饮食的影响,造成15~30%的菌群改变,同样也会反映在营养状况的评估上,因此建议检测前一天尽量保持近期正常饮食 ,这样能更好的反映真实的营养饮食状态。
5
功能性测试
红细胞溶血试验:用于评估维生素E的抗氧化能力。
骨密度测试:用于评估维生素D缺乏对骨骼的影响。
在了解维生素的重要性和缺乏带来的危害后,我们还需要了解一下影响维生素合成吸收的因素。
1
年龄变化
维生素缺乏是一个严重的问题,尤其是在老年人中。随着年龄的增长,营养需求会随之变化。
例如食物中的维生素B12需要胃酸及胃蛋白酶的作用才能释放出来被吸收,而老年人胃酸及胃蛋白酶分泌减少,就会影响维生素B12的吸收。
2
饮食摄入
不同的食物含有不同种类和数量的维生素。新鲜水果、蔬菜、全谷物、坚果、种子、肉类和乳制品是维生素的主要来源。饮食中缺乏这些食物会导致维生素摄入不足。
维生素主要在小肠中吸收,其生物利用度取决于食物成分,相关相互作用等。饮食和膳食的组成会通过影响肠道转运时间或混合胶束的肠道形成来影响某些维生素的吸收。
饮食中足量的水和膳食脂肪对于分别吸收水溶性和脂溶性维生素至关重要。
由于脂溶性维生素可以溶解在脂肪中,因此与膳食脂肪一起食用时最容易被吸收。例如,一种富含维生素A的小胡萝卜,如果单独食用,将在食物中获取维生素A,但如果它是在含有一些膳食脂肪的食物成分中(比如说,橄榄油),将增加体内维生素A的吸收。
doi: 10.7717/peerj.11940
食物的性质(物理状态)也会影响维生素的吸收效率。例如,存在于可消化性较差的纤维植物材料中的类胡萝卜素已被证明相对于维生素A表现出较低的生物利用度。
3
药物的使用
一些药物会改变营养物质的吸收或代谢方式。例如,抗惊厥药会减少叶酸的吸收。
抗生素的使用会影响众多维生素特别是B族维生素的吸收。例如,在饮食中添加青霉素和金霉素会增加雄性大鼠的肝脏维生素B2浓度,以及B2和B3在尿液中的排泄。然而,链霉素和放线菌酮的施用降低了肝脏中维生素B9和B12的浓度。
4
遗传因素
人类基因的变异与肠道结构和微生物组组成有关。人类肠道微生物群中存在不同的维生素B生物合成途径支持人类遗传变异影响维生素B合成的观点。
维生素的合成吸收不仅需要靠饮食补充,还与吸收相关。而维生素的吸收涉及到相关基因,例如:
MTHFR 基因的突变会影响我们产生加工维生素B9的酶——亚甲基四氢叶酸还原酶。
亚甲基四氢叶酸还原酶是叶酸代谢通路中的一种重要的辅酶,亚甲基四氢叶酸还原酶基因缺陷,容易造成叶酸在体内的代谢障碍,MTHFR基因最主要的两种突变为C677T、A1298C基因多态性。该两种位点同时突变可显著降低MTHFR活性进而降低叶酸水平。
VDR基因(维生素D受体):维生素D(来自阳光、食物或补充剂)经过转化步骤后,活性形式骨化三醇 (1,25(OH)2D3 ) 可以通过VDR在细胞内发挥作用,是打开或关闭基因的转录因子。该基因突变可能导致维生素D缺乏引起的佝偻病。
5
菌群影响维生素的合成吸收
肠道菌群通过各种代谢途径影响维生素的合成,例如拟杆菌属、肠球菌属和双歧杆菌属等人类肠道共生菌可以从头合成维生素K和大多数水溶性B族维生素。
6
暴露于自由基
自由基是含有不成对电子的化学物质,可以诱导氧化应激。一个这样的例子是一氧化氮,它与金属离子形成复合物,包括钴,维生素B12的一种结构成分,因此使其无法用于细菌维生素B12的生物合成。此外,维生素生产者(如脆弱拟杆菌)暴露于过氧化氢等自由基会抑制其生长 ,从而降低维生素的生物合成能力。
1
通过饮食直接补充
当我们知晓维生素缺乏的时候,可能希望通过饮食来补充相应缺乏的维生素,下表列出了常见的维生素的食物来源,可供参考。

此外,宿主饮食作为肠道中细菌的底物,含有益生元和其他膳食营养素(如微量营养素和多酚)的饮食可以显著影响有益细菌的生长,包括维生素生产菌,从而有利于产生更多的维生素。
一些维生素,如核黄素(维生素B2),可作为氧化还原介质并刺激营养缺陷菌(如Faecaibacterium prauznitsii)的生长。
2
通过产维生素的益生菌调节
除了通过饮食直接补充之外,我们还可以通过补充产维生素的益生菌来调节,从而改善疾病。
双歧杆菌—叶酸
在健康成人中补充益生菌菌株青春双歧杆菌DSM 18350、青春双歧杆菌DSM 18352和假链双歧杆菌DSM 18353,导致粪便中叶酸浓度显著增加。
乳酸菌—核黄素
乳酸菌通过产生核黄素(维生素B2)和叶酸发挥抗炎和抗氧化作用。乳酸菌通过不同的机制抑制炎症过程,包括调节炎症性肠病患者肠道菌群紊乱、保护肠道屏障和黏膜的正常功能、调节人体免疫反应等。
AKK菌—维生素B12
Akkermansia muciniphila是肠道中的一种常见细菌,可保护肠道免受炎症和肿瘤侵袭;它还产生维生素B12以缓解炎症性肠病患者的维生素缺乏症。
产维生素的益生菌及其作用

doi.org/10.3390/nu14163383
3
使用补充剂
在饮食无法满足需求时,可以考虑使用维生素补充剂,特别是对于特定人群(如孕妇、老年人、素食者等)。
个性化营养方案:在使用补充剂前,最好咨询医生或营养师,以制定个性化的饮食和补充方案,以满足特定的维生素需求。
4
调整生活方式
避免过度烹饪:过度烹饪会导致食物中的维生素流失,因此在烹饪食物时应尽量减少烹饪时间和温度。
避免吸烟和饮酒:吸烟和饮酒会影响身体对维生素的吸收和利用,因此应尽量避免吸烟和饮酒。
适量运动:适量运动有助于改善整体健康,促进营养吸收。
晒太阳:阳光中的紫外线可以促进合成维生素D,因此适当晒太阳可以帮助维持体内维生素D的水平。
5
定期健康检查
通过血液检测等方式监测维生素水平,及时发现缺乏或过量。在谷禾肠道菌群健康检测中,我们也能看到结果报告中关于维生素的评估。
治疗基础疾病,保持健康状态:某些疾病(如消化系统疾病)可能影响维生素的吸收,治疗这些疾病有助于改善维生素水平。
微量营养素(矿物质和维生素)缺乏是全球最常见的营养不良形式之一,尤其在中低收入国家的妇女、幼儿和青少年、老年人中更为严重。这种缺乏及其负面后果是许多地区的重要公共卫生问题,影响国民健康和经济。
世界卫生组织(WHO)和联合国粮食及农业组织(FAO)确定了改善微量营养素缺乏症的四大策略:营养教育,提高饮食多样性和质量;食品强化;补充;以及疾病控制措施。
当微量营养素缺乏较严重时,应采用补充剂。补充剂可以每日服用,也可以间歇性服用。补充剂作为一种策略,要求补充剂的提供切实可行,并有足够的计划来确保依从性。但补充剂并不能解决缺乏的根本原因,只是提供了一种相对经济有效的短期解决方案。人们越来越担心补充营养素可能表现出与食物中的营养素不同的生理反应和吸收:叶酸、锌和铁就是一个例子。
与补充剂相比,饮食改善是一种更长期的对抗微量营养素缺乏的策略。改善饮食与补充剂的不同之处在于,改善饮食意味着摄入丰富多样的食物,这些食物中含有多种微量营养素以及其他对健康有益的成分,同时食物中的微量营养素通常以天然的形式存在,与其他成分相互配合,使得它们更容易被人体吸收和利用。并且食物中的微量营养素其含量和比例相对较为安全,不至于补充过量。
一种新兴方法是生物方法,即可以通过改善肠道菌群来调节微量营养素水平,从而改善疾病。肠道菌群可以改善微量营养素的吸收利用,而肠道细菌过度生长会导致与宿主竞争,进而微量营养素缺乏。
注:本账号内容仅作交流参考,不作为诊断及医疗依据。
特别说明:本文中营养缺乏状况是基于柳叶刀-全球健康研究的185个国家的调查情况,中国居民的膳食营养缺乏可能与其存在一定差异,比如我国由于长期使用添加碘盐,碘缺乏的人群比例要远低于该研究。
主要参考文献
Singer P, Robinson E, Raphaeli O. The future of artificial intelligence in clinical nutrition. Curr Opin Clin Nutr Metab Care. 2024 Mar 1;27(2):200-206.
Barone M, D’Amico F, Brigidi P, Turroni S. Gut microbiome-micronutrient interaction: The key to controlling the bioavailability of minerals and vitamins? Biofactors. 2022 Mar;48(2):307-314.
Das NK, Schwartz AJ, Barthel G, Inohara N, Liu Q, Sankar A, Hill DR, Ma X, Lamberg O, Schnizlein MK, Arqués JL, Spence JR, Nunez G, Patterson AD, Sun D, Young VB, Shah YM. Microbial Metabolite Signaling Is Required for Systemic Iron Homeostasis. Cell Metab. 2020 Jan 7;31(1):115-130.e6.
Knezevic J, Starchl C, Tmava Berisha A, Amrein K. Thyroid-Gut-Axis: How Does the Microbiota Influence Thyroid Function? Nutrients. 2020 Jun 12;12(6):1769.
Wang J, Wu S, Zhang Y, Yang J, Hu Z. Gut microbiota and calcium balance. Front Microbiol. 2022 Dec 20;13:1033933.
Shkembi B, Huppertz T. Calcium Absorption from Food Products: Food Matrix Effects. Nutrients. 2021 Dec 30;14(1):180.
Shlisky J, Mandlik R, Askari S, Abrams S, Belizan JM, Bourassa MW, Cormick G, Driller-Colangelo A, Gomes F, Khadilkar A, Owino V, Pettifor JM, Rana ZH, Roth DE, Weaver C. Calcium deficiency worldwide: prevalence of inadequate intakes and associated health outcomes. Ann N Y Acad Sci. 2022 Jun;1512(1):10-28.
Fiorentini D, Cappadone C, Farruggia G, Prata C. Magnesium: Biochemistry, Nutrition, Detection, and Social Impact of Diseases Linked to Its Deficiency. Nutrients. 2021 Mar 30;13(4):1136.
Farsinejad-Marj M, Saneei P, Esmaillzadeh A. Dietary magnesium intake, bone mineral density and risk of fracture: a systematic review and meta-analysis. Osteoporos Int. 2016 Apr;27(4):1389-1399.
World J Gastroenterol. Jan 14, 2023; 29(2): 332-342Published online Jan 14, 2023.
Ferreira RLU, Sena-Evangelista KCM, de Azevedo EP, Pinheiro FI, Cobucci RN, Pedrosa LFC. Selenium in Human Health and Gut Microflora: Bioavailability of Selenocompounds and Relationship With Diseases. Front Nutr. 2021 Jun 4;8:685317.
Valdes AM, Louca P, Visconti A, Asnicar F, Bermingham K, Nogal A, Wong K, Michelotti GA, Wolf J, Segata N, Spector TD, Berry SE, Falchi M, Menni C. Vitamin A carotenoids, but not retinoids, mediate the impact of a healthy diet on gut microbial diversity. BMC Med. 2024 Aug 7;22(1):321.
Singer P, Robinson E, Raphaeli O. The future of artificial intelligence in clinical nutrition. Curr Opin Clin Nutr Metab Care. 2024 Mar 1;27(2):200-206.
Ian Darnton-Hill,Chapter 2 – Prevalence, Causes, and Consequences of Micronutrient Deficiencies. The Gap Between Need and Action,Editor(s): M.G. Venkatesh Mannar, Richard F. Hurrell,Food Fortification in a Globalized World,Academic Press,2018,Pages 13-28,
ISBN 9780128028612.
Wan Z, Zheng J, Zhu Z, Sang L, Zhu J, Luo S, Zhao Y, Wang R, Zhang Y, Hao K, Chen L, Du J, Kan J, He H. Intermediate role of gut microbiota in vitamin B nutrition and its influences on human health. Front Nutr. 2022 Dec 13;9:1031502.

谷禾健康

维生素C是一种广泛存在于自然界中的水溶性维生素。维生素C在人体新陈代谢中具有多种重要功能,包括抗氧化、参与胶原蛋白合成、增强铁的吸收等。由于其众多生理益处,维生素C被广泛地应用于修复伤口、治疗感冒、癌症等多种疾病。
人体无法自行合成维生素C,需要从膳食来源(如水果、蔬菜)中获取。维生素C的代谢过程涉及多个酶和转运蛋白。肠道微生物群可能通过影响这些酶和蛋白的活性或表达,来影响维生素C的代谢吸收过程。
维生素C也可以直接调节肠道微生物群,或通过修复肠道屏障、改变氧化还原电位等方式间接对肠道微生物群的平衡起到调节作用。
个体之间的差异、饮食习惯和生活方式等因素各不相同,这些都可能对维生素C与肠道菌群的相互作用产生影响。
本文将从维生素C的结构、功能、吸收和代谢、与肠道菌群的关联等多角度,全面探讨维生素C的作用及其对人体健康的影响,同时介绍了一些维生素C的食物来源、人体需要的剂量、如何补充、注意事项等。
▼
本文主要内容:

编辑
维生素C,也称为抗坏血酸,是一种水溶性维生素,对人体健康非常重要。它在许多身体功能中起着关键作用,包括增强免疫力、抗氧化、胶原蛋白的合成等。
▼
维生素C的化学名称是L-抗坏血酸,它是一种有机化合物。无臭,味酸,易溶于水,微溶于乙醇,不溶于乙醚。
维生素C结构简单,化学式为C6H8O6:
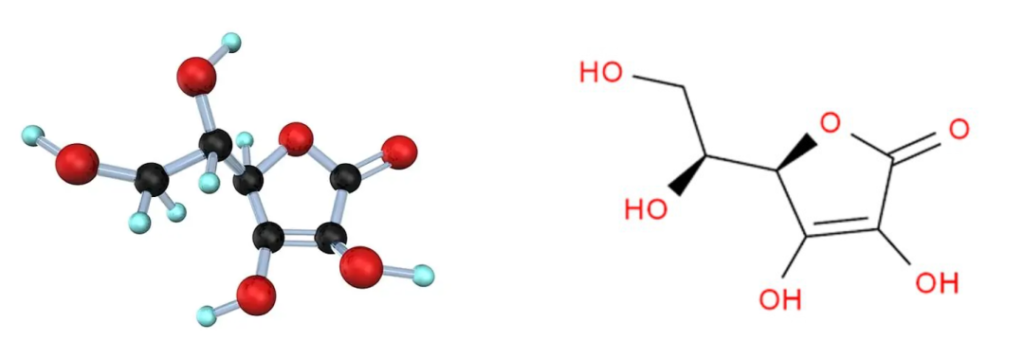
这种结构使维生素C具有抗氧化性质,能够捕捉自由基,并保护细胞免受氧化损伤。
注:体内的分子暴露于环境污染物、吸烟和慢性炎症等情况时,它们会变成自由基。自由基是不稳定的分子,会破坏细胞并导致疾病,维生素C可以通过中和自由基来减缓或预防某些健康问题。
由于其与葡萄糖的结构相似,维生素C可以在许多化学反应中取代葡萄糖,并且可以防止蛋白质的非酶糖基化。
▼
维生素C参与胶原蛋白、激素、肉碱的合成,促进铁离子的吸收,此外,它在免疫系统的功能和调节中发挥着重要作用,对维持内部环境的平衡和中枢神经系统的正常功能极为重要。
维生素C的大部分功能是由于其作为抗氧化剂和辅助因子的能力。由于人类缺乏L-gulono-1, 4-lactone氧化酶,无法自行合成维生素C,因此完全依赖于维生素C的饮食摄入。
▼
从食物中获取营养总是最好的。大约90%的日常需求来自蔬菜和水果,它们是这种维生素的极好来源,例如奇异果、橙子、芒果、草莓、红椒、青椒等。
一些维生素C含量较高的食物

注:单位“杯”是一个常见的非正式计量单位,美规和英规略有区别,大约是237毫升-250毫升左右,涉及到果蔬的份量时,一杯通常是指将果蔬切碎后填满一杯容器的量。
▼
维生素 C 对大脑健康非常重要。大脑在长期缺乏维生素 C 的情况下以牺牲其他组织为代价来保留维生素 C,并且可以维持比其他器官(例如肝脏和肾脏)高很多倍的浓度,如下图。
维生素C的分布在身体各器官之间差异很大
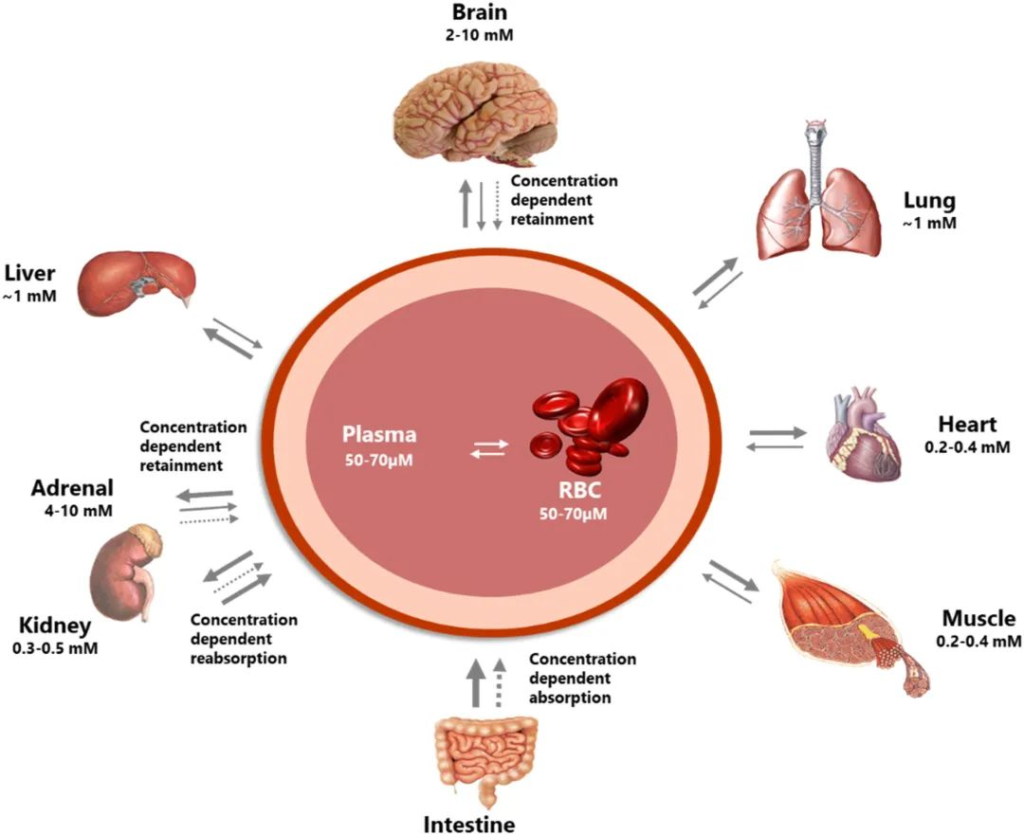
doi.org/10.1016/j.redox.2020.101532
维生素C供应不足时,首先保证大脑里的浓度,那么维生素C对于大脑而言有什么作用?
▼
维生素 C 对胶原蛋白的稳定作用对于形成整个身体的结缔组织框架至关重要;包括皮肤、骨骼、软骨、肌腱、韧带、血管等。
胶原蛋白生产的最后步骤取决于维生素 C,维生素 C 在前胶原脯氨酰和赖氨酰残基的羟基化中充当电子供体。
▼
维生素 C 可增强其他营养素的生物利用度,例如维生素 E 和非血红素铁,这可能会增强含维生素 C 的食物的健康效果。
维生素C经常添加到含铁的口服制剂中,以增加铁的吸收。
▼
维生素 C 是否可以预防或减轻包括普通感冒在内的感染的严重程度是一个有争议的话题。大多数证据都支持其好处。
▼
维生素C对正常骨骼发育至关重要。维生素C水平与骨骼健康之间存在正相关关系,如骨密度、骨折概率、骨转换标志物等。
▼
维生素 C 有助于维持健康的皮肤。
▼
肺部的维生素C水平是血液中的30倍。
维生素C在抵御氧化剂的同时也会被消耗,这表明即使是单剂量的维生素C,也能有效抵御肺部氧化应激的急性增加。
▼
根据现有证据,摄入足够的维生素 C 可能有助于保持健康的情绪。
焦虑
抑郁
▼
人类慢性低维生素 C 状态与神经退行性疾病有关。但是,尚未确定因果关系。
▼
维生素 C 可以通过抑制炎性细胞因子来减轻炎症。
▼
除上述主要的功能之外,在部分小型研究中提到的关于维生素C的功能如下:
助孕育:
助减肥:
降血压、防中风:
降血糖:
助排毒:
助抗癌:
牙周健康:
水溶性维生素在人体内储存较少,从肠道吸收后进入人体的多余的水溶性维生素大多从尿中排出。因此,摄入较多的水溶性维生素一般不会引起中毒现象,但是若摄入量过少,则会很快出现缺乏症状。
▼
刚缺乏的时候症状不明显,饮食中缺乏VC需要大约一个月的时间才会出现症状。
体内维生素C总含量低于300-400mg会出现明显症状。
维生素C的缺乏会出现什么症状?
由于维生素C功能的复杂性及其被不同还原剂的部分替代性,维生素C与坏血病症状的直接联系不容易确定。
如果发展为坏血病,典型症状是:
肌肉无力、牙龈肿胀和出血、牙齿脱落、瘀点出血、自发性瘀斑、贫血、愈合障碍、角化过度、虚弱、肌痛、关节痛和体重减轻(也可能因肿胀而出现矛盾的体重增加),而早期表现包括嗜睡、倦怠、易激惹,甚至呼吸困难等。
在生化上,维生素C血浆水平低于11μM被认为与坏血病的临床症状一致。
在专业医疗人员的指导下,补充维生素C可以轻松有效地逆转坏血病。许多症状可以在几周内轻松解决。富含维生素C的饮食将防止坏血病的发展。
什么人群更容易发生维生素C缺乏?
▼
NIH 认为,成人可耐受的上限是每天 2000 毫克,仅仅靠含有维生素 C 的食物几乎不可能达到这一上限,所以食物可以放心吃。服用补充剂则需注意剂量,可能存在过量的风险。
更高的剂量更有可能导致副作用。
维生素C过量可能会出现什么症状?
单次口服5-10克维生素C会产生短暂的渗透性腹泻和/或腹胀伴疼痛,不建议这样做。
随食物一起摄入可减少这些不良反应。
每天超过 2000 毫克的剂量可能会增加腹泻和肾结石的风险。如果有肾结石病史,每天摄入超过 1000 毫克可能会增加患结石的几率。
那么到底应该怎么补充?每日摄取多少维生素C 合适呢?
▼
科学界对维生素C的最佳剂量方案(摄入量和频率)最健康存在持续争论。
对于大多数健康人来说,通过食物可以获得足量的维生素 C。
维生素C摄入量标准在不同地区有所不同:
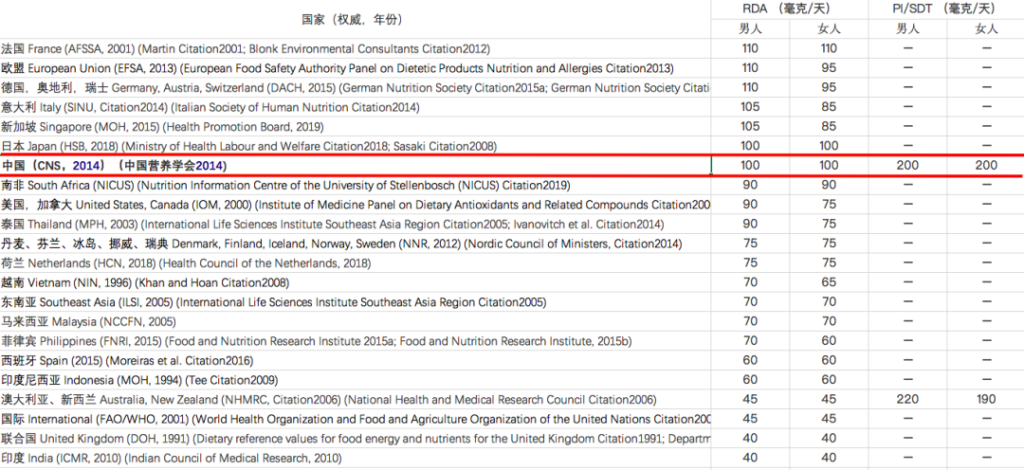
注:RDA – 推荐膳食摄入量,
PI – 建议摄入量,SDT – 建议膳食目标
在中国营养学会编著的《中国居民膳食指南》2022版中对维生素C的推荐摄入量:
中国居民膳食指南2022版
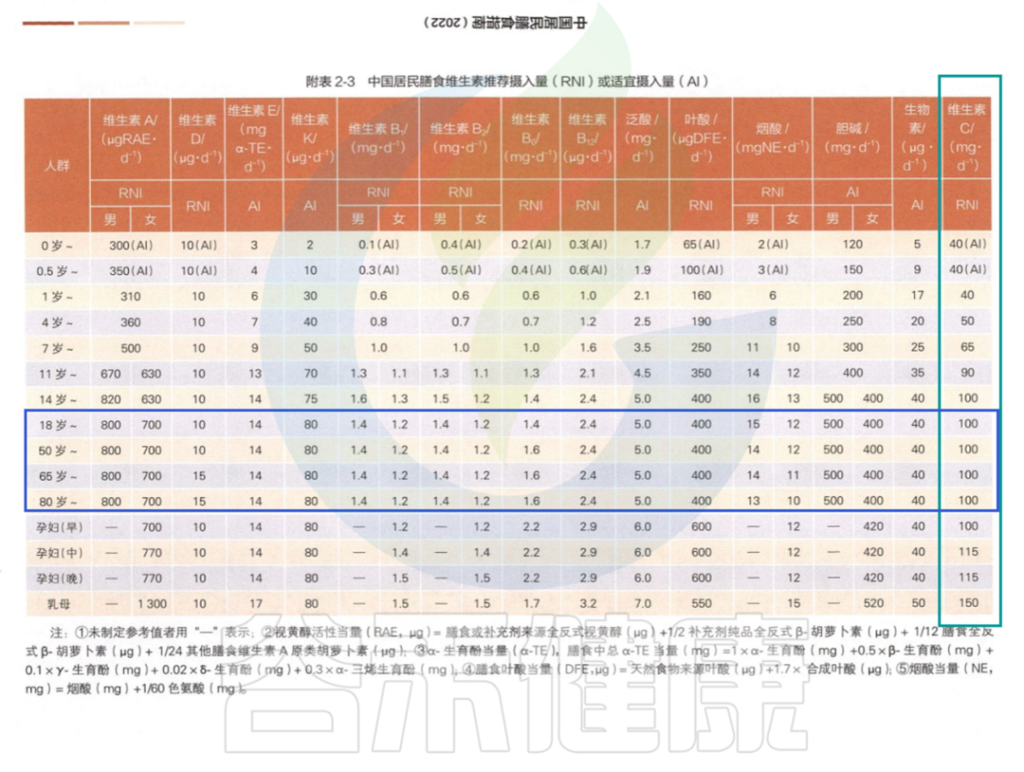
为什么不同地区的标准不一样呢?
这主要是由于RDA标准的基本前提从预防坏血病(~45 mg/d)至健康优化(~200 mg/d)。许多权威机构建议使用最低量的维生素C,但这可能无法满足不同亚群的健康需求。
例如,吸烟者和肥胖者比普通人群有更高的要求。一些国家的吸烟率继续上升,有证据表明,吸烟者每天至少摄入200 mg的维生素C。
随着全球肥胖率的增加,以及与肥胖相关的合并症,如代谢综合征、糖尿病和心血管疾病,需要更多地考虑适当的建议,以优化快速增加的亚健康人群中的维生素C状态。
以上是维生素C的摄入量标准,具体该如何补充,应该注意什么?详见下一章节。
▼
食物:如何才能最大程度地保留其维生素C?
——烹饪方式
长时间烹饪,特别是用大量水煮沸会导致维生素C浸出到水中,显著降低食物中的维生素C含量。
在少量水中蒸或煮,且持续时间较短,是保存维生素C的更温和的方法。
即使将所有外部因素消除到最低限度,也会发生损失,因为由于抗坏血酸氧化酶的存在,材料内部会发生氧化反应。因此,理想的加工方法是用最少量的水快速热灭活酶,然后快速冷却。
——长期保存条件
温度对储存稳定性也有很大影响。随着温度的升高,会出现更显著的损失。然而,在长期储存期间,即使维持短期储存期间仅发生少量损失的条件,维生素C的量也会显著减少。
损失主要是由于酶催化的氧化反应,其程度尤其取决于pH、材料完整性和温度。
总之,为了使水果和蔬菜的维生素C含量保持更长时间,最温和的方法是深度冷冻。
补充剂:一天中分几次服用
食物和许多补充剂中的维生素 C 是一种抗坏血酸的形式。
当肠道面临较低水平的抗坏血酸(即低于约 400 毫克)时,主动运输系统会吸收维生素 C(即,将营养物质通过肠道并进入血液,到身体需要的地方)。
一旦这些主动运输变得不堪重负,被动扩散就会接管吸收其余的维生素 C(这是一个相当低效的过程)。吸收并不像听起来那么容易,事实上抗坏血酸有吸收上限。
身体一次可以处理大约 300 – 400 毫克的纯抗坏血酸形式的维生素 C,更多量一下子难吸收。
所以如果能记得的话,一天中分几次服用比较合适。
▼
维生素C补充剂并非适合所有人。如果遇到以下任何情况,请首先与医生联系:
也不要认为维生素C服用越多越好,每天服用 1000 毫克或更多,实际上会使吸收率降低约 50%。
▼
维生素C可以增加某些药物的吸收,例如:
服用维生素C可以增加含铝药物(如磷酸盐粘合剂)对铝的吸收。这可能对有肾脏问题的人有害。抗酸剂中含铝:不要同时服用维生素C和抗酸剂。服用维生素C后至少等待两个小时,然后再服用抗酸剂。服用抗酸剂后等待四个小时服用维生素C。
维生素C可能会增加左旋甲状腺素的吸收。
补充维生素C会降低一些药物的疗效:
口服维生素C可能会降低这些抗病毒药物的作用。
当与维生素C一起服用时,烟酸和他汀类药物的影响可能会降低,这可能有益于高胆固醇的人。
高剂量的维生素C可能会降低人体对这种抗凝剂的反应。
其他还包括:
维生素C增加或减少药物副作用的风险
如果服用雌激素或基于雌激素的避孕药,维生素C可能会增加激素副作用的风险。这是因为维生素C可能会减缓雌激素离开身体的速度。
一些早期的研究认为, 维生素C可能有助于预防阿司匹林和非甾体抗炎药引起的胃部不适。
▼
维生素 C 和益生菌对肠道健康和免疫力有不同的好处,它们可以很好地互补,这意味着它们可以安全地一起服用。
一项针对学龄前儿童的双盲、随机、安慰剂对照初步研究中,发现益生菌与维生素 C 联合预防呼吸道感染的功效(URTI;33%,P =0.002)。
Lab4 益生菌和维生素 C 组合补充 6 个月的儿童显示,上呼吸道感染症状的发生率和持续时间有所减少,降低感染的严重程度。
注:Lab4 益生菌包含:嗜酸乳杆菌CUL21(NCIMB 30156)和CUL60(NCIMM 30157),双歧杆菌CUL20(NCIMB 30153)和动物双歧杆菌乳亚种CUL34(NCIMM 30172)。
注意:根据说明书剂量服用或遵医嘱。
以上并不是维生素C可能发生的相互作用的完整列表。在开始补充维生素C或调整摄入量之前,请与医生或药剂师沟通,让医生知道你正在服用的所有药物,包括处方药和非处方药、其他维生素或微量营养素、草药补充剂等。
▼
静脉注射和口服给药,这两者可能具有不同的药代动力学特征。
药理学模型显示,口服维生素C,即使是在非常大和频繁的剂量下,也只能适度地增加血浆浓度,从0.07 mM增加到最大0.22 mM。
而静脉注射剂量预计会导致血浆维生素C峰值水平比口服剂量高60倍以上,尿液浓度比口服剂量低140倍。
分子的实际生物利用度由许多因素控制,包括肠道和其他组织的吸收、肾脏的吸收和排泄以及其他患者特异性因素。
除了通过静脉给药和口服给药的浓度差异外,口服给药将维生素C直接输送到肠道微生物组,而不是通过血液;因此,它对肠道微生物的影响可能与动力学和浓度有关,这与影响血浆水平的动力学和浓度完全不同。
静脉注射维生素C常用于临床医疗环境中,用于治疗某些疾病或特殊情况下的高剂量补充,如感染、外伤、手术恢复等。专业医生会给予相应的建议。
口服给药适用于一般的日常维生素C补充,维持正常的维生素C水平。
有几种方法可以评估人体中的维生素C状态。这些包括测量血浆、尿液、组织、粪便中维生素 C 的浓度。
▼
检测血浆维生素C,血浆样品中维生素C的定量测定常见的有两种方法:酶法和色谱法。
酶促维生素C测定
有几种基于维生素C的酶促转化的商业试剂盒,产生可以用光光谱法检测的信号。通常,抗坏血酸氧化酶用于这种类型的测定。这些测定的常见方法是酶联免疫吸附测定(ELISA),它非常适合分批处理样品,但不太方便立即测定少数样品中的值。
根据欧洲外部质量评估计划(Instand EQAS)中报告的方法,基于酶的分析方法在医院中并不常规使用。如果临床对立即测定维生素C的需求增加,由于其直接的技术性质,这些基于酶的测定可用于护理点或集中平台。
色谱法测定维生素C
抗坏血酸和DHA的定量测量目前是通过高效液相色谱(HPLC)方法进行的。如果必须分析具有相似性质的多种化合物,或者如果存在许多可能干扰感兴趣化合物定量的物质,则HPLC方法是优越的。
将酸化样品注射到HPLC仪器中后,通过通过基于化合物的物理性质不同地保留化合物的柱来分离化合物。结果,在分离柱的末端,可以选择性地检测抗坏血酸和DHA,而不受其他化合物的干扰。
目前有两种方法可以检测分离后的抗坏血酸和DHA,一种是电化学检测,另一种是紫外线检测。这两种检测方法给出的结果相同,但由于相对技术简单,紫外线检测更广泛地用于日常检测。
其他检测技术,如荧光检测,需要在柱前对抗坏血酸和DHA进行化学改性,但使用较少。比色/荧光法可能会产生更高的DHA浓度,因为该方法缺乏特异性。
▼
可以查看近期体内维生素状况。
肠道菌群可以影响食物中的营养物质的吸收和利用。肠道菌群的失调可能会影响维生素C吸收,从而出现维生素C缺乏,引发一系列健康问题。因此,检测肠道菌群的状况,可以帮助我们更好地了解维生素C的吸收和利用情况。
与抽血检测不同,肠道菌群的评估更加反映一段时间 ( 一般2周左右 ) 的长期状态,如部分维生素无法在体内留存,需要每日补充,血液检测波动较大。
肠道菌群与维生素C的水平之间存在怎样的关联?
为什么肠道菌群检测报告可以了解维生素情况?
我们来看下一章节。
我们在日常生活会看到,同样吃食物,有些人的维生素吸收状况比较好,有些人就容易缺乏,这是为什么呢?
为什么大剂量补充对一些人的身体有益,而少数人因为过量出现了肾结石呢?
这其实都与肠道微生物群相关。
这里我们分为两个方面来讨论:
一个是肠道微生物群对维生素C的影响,
一个是维生素C的补充对肠道微生物群的影响。
维生素C在人体代谢过程中的吸收和利用,与肠道微生物群相关。了解肠道微生物群对维生素C的吸收和利用的影响,可以帮助我们更好地理解其与人体健康之间的关系。
▼
微量营养素使用各种特定的吸收途径和机制,既可以是被动的,也可以是主动的。
膳食维生素 C 很容易通过钠依赖性维生素 C 转运蛋白(SVCT1 和 SVCT2)在肠道中吸收,其他比如维生素A 、维生素D 的吸收通过小肠中的被动扩散发生。
肠道微生物群是人体肠道中的有效生物反应器,可将各种化合物转化为有益或有害的代谢物,因此对其生物利用度起着至关重要的作用。
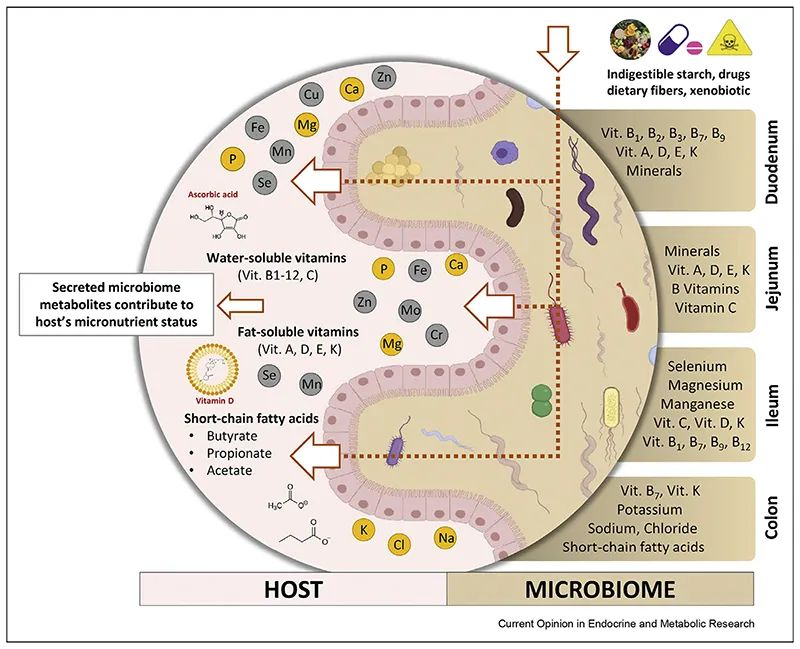
doi: 10.1016/j.coemr.2021.100285
胃肠道各部分理化特性的差异,以及位点特异性受体的存在,使得不同的维生素和矿物质能够沿胃肠道吸收。不同微生物在每个不同部分的定殖会影响当地环境,从而对微量营养素的生物利用度产生积极或消极的影响。
微生物可以干扰维生素C的吸收
微生物可以通过干预生物合成过程和调节吸收,来调节微量营养素的水平,包括维生素C。
来自革兰氏阴性菌的脂多糖降低SVCT-1的表达,进而降低SVCT-1-介导的维生素C的摄取。
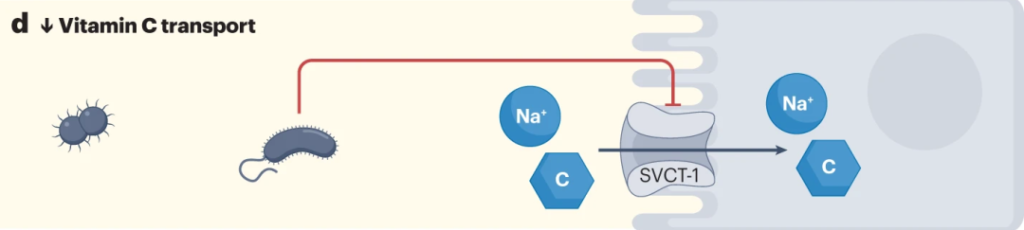
Chmiel JA, et al.,Nat Rev Urol. 2023
大肠杆菌可以通过释放脂多糖来减少宿主对抗坏血酸的摄取,从而增加NF-κB依赖性TNF的产生,其进而通过抑制SLC23A1和SLC23A2启动子(分别编码SVCT1和SVCT2),来降低钠依赖性维生素C转运蛋白SVCT1与SVCT2的表达。从而对维生素C的吸收率产生负面影响。
细菌可以与宿主竞争维生素C
大肠杆菌抗坏血酸转运蛋白对抗坏血酸的亲和力高于哺乳动物SVCT1,这表明细菌可以与宿主竞争维生素C。
因此,肠道菌群中大肠杆菌等革兰氏阴性菌占比较多的情况,可能不利于维生素C的吸收,这在谷禾肠道菌群检测报告中也是可以反映的。
▼
肠道细菌如大肠杆菌和乳酸杆菌代谢维生素C。
利用ula基因簇,大肠杆菌等细菌可以将抗坏血酸代谢为D-木酮糖,宿主细胞可以进一步加工木酮糖以产生草酸盐。
在肺炎链球菌、沙门氏菌、福氏志贺菌、粪肠球菌、肺炎克雷伯菌等病原菌中,也发现了相同的ula基因簇。
带ula的致病菌与草酸盐:携手制造结石
结石形成者(比如肾结石患者)微生物群更常见地富含携带ula基因簇的致病菌,并且这些患者在接受口服维生素C时,草酸盐增加的水平比非结石者增加得更多。高草酸盐水平增加了结石的风险。
因此,如果在肠道菌群检测报告中发现以上提到的致病菌占比较多,则有可能在代谢维生素C的时候产生的草酸盐过多,增加了结石的风险。
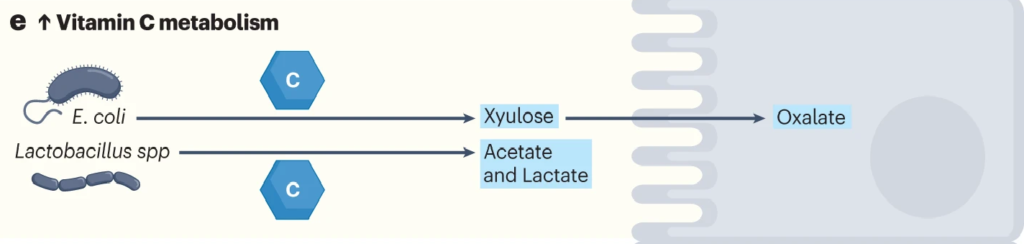
Chmiel JA, et al.,Nat Rev Urol. 2023
“
以上通过微生物群代谢维生素的机制,有助于我们更好地理解结石形成的机制。
既然有促进结石的细菌,自然也有降解的细菌:
一些乳酸杆菌可以将维生素C转化为乙酸盐和乳酸盐,这是一种无毒的代谢产物,通过生物能量途径增加微生物组的功能,并可能促进这些草酸降解细菌的定植。
Oxalobacter formigenes是一种革兰氏阴性厌氧细菌,可降解肠道草酸盐并促进原发性高草酸条件下肠道草酸盐的分泌。该菌在肠道定植可降低尿液或血浆中的草酸盐浓度。
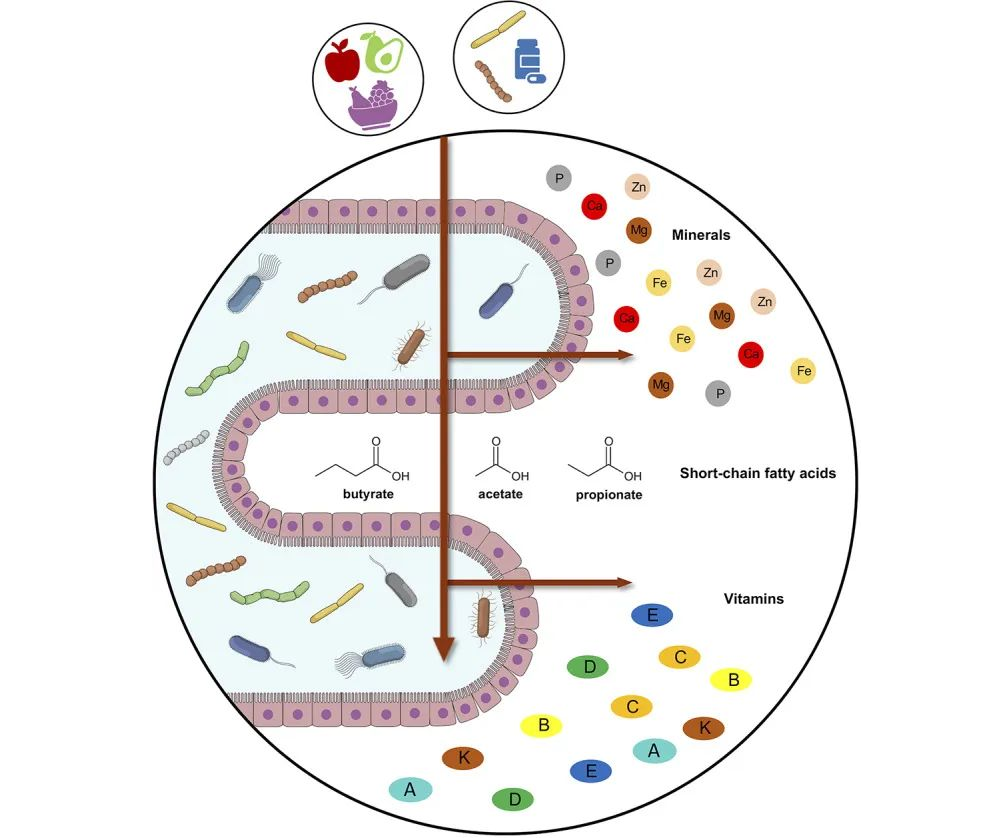
Barone M, et al., Biofactors. 2022
我们看到生活中有人认为不能吃生菠菜,会得肾结石,但有些人每天吃生菠菜也没事…其实可能是因为人家的肠道菌群中致病菌较少,而降解草酸的菌群又在拼命干活…
因此,健康的肠道菌群结构非常重要,菌群在该干活的时候各司其职,井井有条,那么你的身体抵抗疾病的能力也随之提升。
以上是肠道菌群对维生素代谢吸收的影响,反过来,维生素C的补充也可以影响肠道菌群的组成。
二、
补充维生素C可以直接调节肠道微生物群,也可以通过改变氧化还原电位、修复肠道屏障,改善肠道条件,支持部分有益菌生长,防止有害菌泄漏到身体其他部位。
▼
维生素C直接调节肠道菌群
与安慰剂组相比,补充维生素C已被证明可以显着增加微生物生态系统的多样性,以及Collinsella的相对丰度和粪便水平的短链脂肪酸,特别是丁酸盐和丙酸盐。
在健康受试者中,每日高剂量维生素C补充(1000 mg/天):
下列菌群的相对丰度升高
下列菌群的相对丰度下降
一项观察性研究探讨了微量营养素维生素C对肠道微生物组组成和多样性的影响。结果表明,维生素C增加了肠道中双歧杆菌属的丰度,在科水平上,毛螺菌科和双歧杆菌科显著增加。
双歧杆菌属的成员是有益菌,例如增加ATP生成、调节免疫系统、黏膜屏障完整性、短链脂肪酸的产生,对健康有益,维生素C通过增加肠道有益菌促进健康。
研究发现,囊性纤维化患者维生素C摄入量的增加与厚壁菌门的丰度呈正相关,与拟杆菌门的丰度呈负相关。
▼
改变氧化还原电位
调节微生物组的机制类似于维生素B2:通过改变氧化还原电位,改善消化道中的厌氧/耐氧平衡,从而选择性地支持微生物生长,改善肠道条件。
与安慰剂相比,维生素C组粪便样本中的粪便pH值和氧化还原平衡降低。
▼
修复肠道屏障
我们知道,肠道屏障受损,细菌和有害物质有可能会穿过屏障进入血液循环,对人体产生各种负面影响,导致诸如过敏、炎症、自身免疫疾病等多种反应。
关于肠漏可以详见我们之前的文章:
而维生素 C 具有维持肠粘膜屏障完整性和修复粘膜屏障的作用。
这里介绍两种修复肠屏障机制。
——通过激活Notch 信号
Notch 信号影响细胞正常形态发生的多个过程,与许多人类疾病有关,包括IBD,因此被认为是癌症治疗的潜在靶点。Notch 信号通路的激活会改变紧密连接蛋白的表达并影响其分布的连续性,从而降低细胞屏障通透性。
豚鼠结肠组织相关基因检测表明,低剂量的维生素C可强烈激活Notch/Hes-1信号通路,对DSS诱导的结肠炎豚鼠的肠粘膜具有一定的保护作用。肠上皮受损时,Notch-1表达增加可促进上皮细胞增殖,有利于损伤部位的修复和重建。
——通过增加肠道胶原蛋白合成
增加维生素 C 摄入量的另一个潜在好处是肠道胶原蛋白合成增加,从而改善屏障功能。这一提出的机制与抗坏血酸的辅酶功能一致,即羟基化脯氨酸和赖氨酸以交联胶原蛋白。
例如,对具有吲哚美辛诱导的屏障功能障碍的 T84 人隐窝样上皮细胞系的研究表明,细菌通过跨细胞途径穿过上皮细胞,维生素 C 治疗可消除该途径。因此,肠道中抗坏血酸状态不佳可能会加剧屏障功能障碍,从而增加 LPS 衍生的革兰氏阴性菌的易位,从而加剧炎症。
维生素C修复肠道屏障后,肠道屏障可以正常发挥吸收、分解和转换营养物质等功能,同时可以帮助促进健康微生物群栖息和生长,从而促进整体健康。
以上我们了解到,维生素C可以通过多种方式影响肠道菌群,从而促进整体健康。那么当我们看到肠道菌群报告中菌群多样性较低,部分菌群失调,尤其是上面提到的毛螺菌科、肠球菌属、Collinsella、Gemmiger formicilis等,可以考虑通过补充维生素C来调节。
我们首先可以考虑通过食物补充,如卡姆果、针叶樱桃等维生素C含量很高的食物,或者一些常见的蔬菜水果例如:猕猴桃、番石榴(芭乐)、青椒、羽衣甘蓝等。也可以考虑通过维生素C补充剂调节。
人体维生素研究面临着许多挑战,维生素通常是通过食物摄入的,而食物中同时存在多种营养素,这使得难以研究单一维生素的作用;某些高剂量维生素的使用可能存在潜在的风险,进行研究时涉及到人体试验和干预,需要遵循伦理准则,并确保研究的安全性;不同人对维生素的需求和代谢能力存在个体差异,基因、环境和生活方式等因素都可能影响维生素的吸收、利用和代谢。
肠道菌群研究可以揭示不同个体之间菌群组成的差异,这有助于理解个体差异对维生素代谢和利用的影响。可以通过检测肠道菌群的组成和丰度,了解维生素的代谢情况,从而辅助评估维生素水平。
综合运用多种研究方法和技术,结合肠道菌群检测,可以考虑多个因素对维生素代谢和利用的综合影响,进一步理解维生素的作用机制,对人体健康具有重要意义。
注:本账号内容仅作交流参考,不作为诊断及医疗依据。
主要参考文献
Barone M, D’Amico F, Brigidi P, Turroni S. Gut microbiome-micronutrient interaction: The key to controlling the bioavailability of minerals and vitamins? Biofactors. 2022 Mar;48(2):307-314.
Chmiel JA, Stuivenberg GA, Al KF, Akouris PP, Razvi H, Burton JP, Bjazevic J. Vitamins as regulators of calcium-containing kidney stones – new perspectives on the role of the gut microbiome. Nat Rev Urol. 2023 May 9:1–23.
Pham VT, Dold S, Rehman A, Bird JK, Steinert RE. Vitamins, the gut microbiome and gastrointestinal health in humans. Nutr Res. 2021 Nov;95:35-53.
Li XY, Meng L, Shen L, Ji HF. Regulation of gut microbiota by vitamin C, vitamin E and β-carotene. Food Res Int. 2023 Jul;169:112749.
Yang Q, Liang Q, Balakrishnan B, Belobrajdic DP, Feng QJ, Zhang W. Role of Dietary Nutrients in the Modulation of Gut Microbiota: A Narrative Review. Nutrients. 2020 Jan 31;12(2):381.
Steinert RE, Lee YK, Sybesma W. Vitamins for the Gut Microbiome. Trends Mol Med. 2020 Feb;26(2):137-140.
Gomes-Neto JC, Round JL. Gut microbiota: a new way to take your vitamins. Nat Rev Gastroenterol Hepatol. 2018 Sep;15(9):521-522.
Rowland I, Gibson G, Heinken A, Scott K, Swann J, Thiele I, Tuohy K. Gut microbiota functions: metabolism of nutrients and other food components. Eur J Nutr. 2018 Feb;57(1):1-24. doi: 10.1007/s00394-017-1445-8. Epub 2017 Apr 9. PMID: 28393285; PMCID: PMC5847071.
Traber MG, Buettner GR, Bruno RS. The relationship between vitamin C status, the gut-liver axis, and metabolic syndrome. Redox Biol. 2019 Feb;21:101091.
Rozemeijer S, Spoelstra-de Man AME, Coenen S, Smit B, Elbers PWG, de Grooth HJ, Girbes ARJ, Oudemans-van Straaten HM. Estimating Vitamin C Status in Critically Ill Patients with a Novel Point-of-Care Oxidation-Reduction Potential Measurement. Nutrients. 2019 May 8;11(5):1031.
Otten AT, Bourgonje AR, Peters V, Alizadeh BZ, Dijkstra G, Harmsen HJM. Vitamin C Supplementation in Healthy Individuals Leads to Shifts of Bacterial Populations in the Gut-A Pilot Study. Antioxidants (Basel). 2021 Aug 12;10(8):1278.

谷禾健康
在谷禾肠道菌群健康检测中,我们会看到结果报告中关于维生素的评估如下:

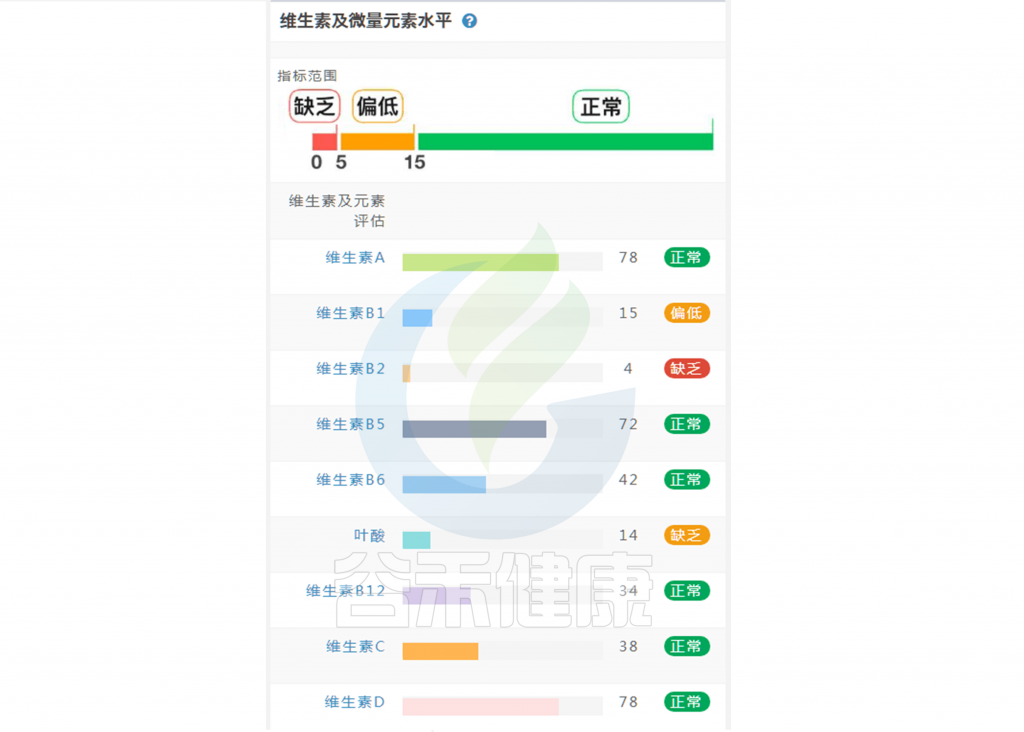
摄入水平建议保持在70-80分之间最佳,如果单项指标低于5表明摄入比例在人群中属于最低的5%,评估为缺乏,如上图中维生素B2;低于15评估为偏低,如上图中叶酸;达到或超过95则表明该项指标可能摄入比例偏高,可适当减少摄入;其余则为正常范围。
上图可以看到,像维生素C这项指标分值在38,虽然正常但相对于最佳来说是偏低的。
一些小伙伴可能会存在这样的疑惑:
为什么肠道菌群检测可以评估维生素?
这些维生素指标的分值代表着什么含义?
肠道菌群和维生素之间有什么样的关联?
它们如何影响人体健康/疾病?
如何判断维生素是否缺乏?
该如何补充?
…
本文就以上问题进行详细解答,同时也包括维生素-微生物群之间的相互作用,维生素维持肠道菌群稳态和减少肠道炎症以预防癌症的机制,产生维生素的益生菌,补充调节维生素的方式包括饮食、益生菌等。
在阅读本文之前,可以先了解一下各类常见的维生素功能,缺乏导致的症状。


每个维生素的详细介绍可以点开以下查看(请在谷禾健康微信公众号找到这篇文章查看)。
维生素B1(硫胺素)
维生素B2(核黄素)
维生素B3(烟酸)
维生素B5(泛酸)
维生素B6(吡哆醇)
维生素B7(生物素)
维生素B9(叶酸)
维生素B12(钴胺素)
以上每个都有关于该维生素的详细介绍,包括:
—正文—
维生素是一种微量营养素,在人体的生长、新陈代谢和发育中起着至关重要的作用。
在谷禾肠道菌群健康检测报告中,维生素分值即代表该维生素的膳食摄入水平和菌群代谢能力(报告中显示的分值是经过一系列计算得到的一个相对值)。
其中B族维生素很多需要通过肠道菌群对初始原料进行代谢之后才会产生,因此肠道菌群相应的基因和代谢途径的丰度水平也会直接反映这些维生素的摄入水平。
我们知道维生素的缺乏可能引起一些不良后果,导致维生素缺乏的原因有很多,摄入不足,吸收不良等都会导致维生素缺乏。
我们日常主要从饮食中获取维生素,肠道是主要吸收部位。例如,维生素 A 主要在近端空肠吸收,维生素 D 在远端空肠吸收最佳,维生素 E 和 K 主要在回肠吸收。因此,肠道功能受损可能会影响维生素的吸收。当然,影响维生素吸收的其他原因还包括年龄,某些疾病,药物等因素。
那么肠道菌群和维生素之间有什么关联?
肠道菌群是人体生理和健康的重要决定因素。肠道菌群帮助吸收营养,并参与维生素代谢。
肠道有益菌:乳酸菌和双歧杆菌,可以重新合成B族和K族维生素,为宿主提供约30%的每日摄入量。与从食物中获得的维生素不同,微生物产生的维生素主要在结肠中吸收。接下来了解一下具体哪些菌群,如何产生维生素。
前一章节我们知道,除了通过饮食提供维生素外,人体肠道中的细菌也可以产生一些维生素,如果吸收得当,可以部分满足人体的需要。
可以把这些细菌微生物想象成小小的维生素工厂。细菌确保为自己和与他们共生的微生物朋友提供维生素,同时也会为人体提供维生素。
合成的B族维生素的菌群较多
研究人员估计了人体肠道细菌可以提供维生素每日参考摄入量的百分比,得出的结论是可以提供:
40-65% 的人体肠道菌群具有合成 B 族维生素的能力。两种最常见的合成维生素是维生素B2和B3,预测分别有 166 和 162 个生产者。
可以合成 B 族维生素的细菌以及B 族维生素缺乏对肠道健康的影响
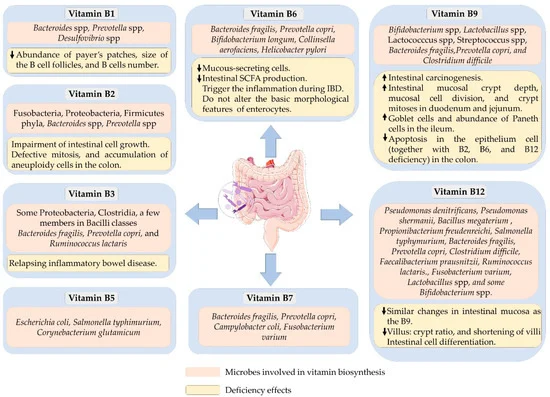
doi.org/10.3390/microorganisms10061168
大部分肠道菌群都参与维生素的合成
随着基因组注释方法的不断完善,研究人员可以预测维生素代谢途径并评估维生素生物合成潜力。通过检索 UniProt 数据库,研究人员发现:
厚壁菌门是维生素的主要代谢相关菌,其次是变形菌门,再然后是拟杆菌和放线菌。这四种菌群是人体肠道菌群的主要组成部分,占总菌群的60%-90%.
下表列出了参与合成B族维生素的肠道菌群,以及相应的代谢机制。


以上是肠道菌群对维生素产生的影响,而维生素和肠道菌群之间的作用是双向的,维生素也会影响肠道菌群,下一章节我们详细了解维生素对肠道菌群的影响。
维生素通过调节免疫力、细菌生长和新陈代谢来改变肠道微生物群的组成。
例如,膳食补充剂中的维生素 B、C、D 和 E 通过有利于双歧杆菌、乳酸杆菌和罗斯氏菌等有益菌属的肠道黏膜扩张和定植,在很大程度上有助于微生物组的组成。
肠道微生物组和宿主之间的微量营养素交换
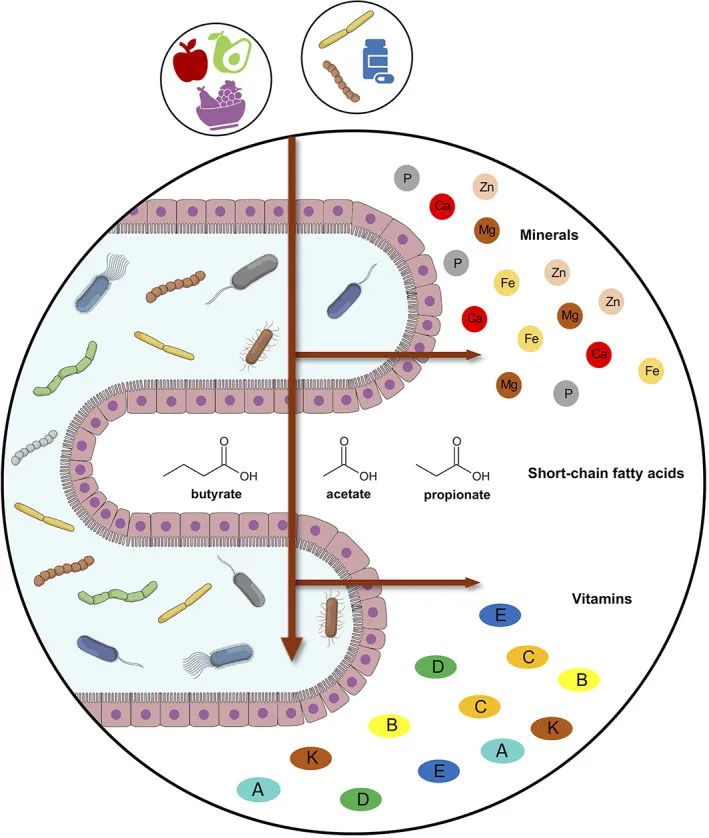
doi: 10.1002/biof.1835
一项研究调查了 96 名健康志愿者,结果表明:
补充维生素 B2 后肠道微生物的种类数量显着增加;联合补充维生素 B2 和 C 导致Sutterella显着减少,但Coprococcus数量增加;
维生素C显着提高肠道微生物的α多样性;
服用维生素D后,促进放线菌的生长和抑制拟杆菌的生长。
补充维生素对人体肠道菌群的影响

doi.org/10.3390/nu14163383
/ 维生素A /
维生素 A 的充足状态可能与微生物多样性增加有关。在小鼠实验中,普通拟杆菌(Bacteroides vulgatus )在维生素 A 缺乏期显着增加。维生素 A 缺乏导致的粘膜反应受损,粘蛋白和防御素 6 表达减少,可能使病原菌更容易穿透肠道屏障。
维生素A缺乏使厚壁菌门中毛螺菌_NK4A136_群、厌氧菌、颤杆菌的数量减少,毛螺菌的含量也降低;然而,Parasutterella呈上升趋势。TLR4 可能参与了维生素 A 调节微生物群的过程。
/ B族维生素 /
研究人员在一个小的成年志愿者群体中进行了一项试点研究,该群体补充了过量核黄素(100mg),持续14天。他们发现,在补充期间,每克粪便中的Faecalibacterium prausnitzii数量增加。作者还注意到厌氧菌Roseburia 增加,大肠杆菌减少。
其他关于B族维生素对肠道菌群的影响详见:
/ 维生素C /
补充维生素 C 可减少肠杆菌科细菌的数量,增加乳酸杆菌的丰度,抑制有害菌的生长,促进有益菌的增加。
也有研究表明,维生素 C 服用4周导致 α 多样性增加,短链脂肪酸浓度增加。

/ 维生素D /
维生素 D 和肠道微生物群的相互作用对免疫稳态至关重要。补充高水平的维生素 D 增加了普氏菌,减少了韦荣氏菌和嗜血杆菌。
婴儿饮食中补充维生素 D 对早期微生物组成的变化有重要影响,而儿童缺乏维生素 D 会导致细菌多样性降低。
最近的一项研究表明,维生素D的活性代谢物1,25-二羟基胆钙化醇,维生素D受体的配体(VDR),影响美国不同地区老年人肠道菌群的α -和β -多样性。
研究人员报告了通过食物频率问卷评估的微量营养素摄入量与孕妇微生物群组成之间的相关性。他们观察到,高脂溶性维生素,特别是维生素D的膳食摄入量与微生物α多样性降低有关(P值<0.001),维生素D和视黄醇与变形菌相对增加有关,变形菌门是一个已知包含多种病原体并具有促炎特性的门。
/ 维生素E /
维生素E对变形菌有抑制作用,而维生素E(和纤维)的摄入量较低与Sutterella水平较高相关,据报道,自闭症和某些胃肠道疾病婴儿的Sutterella水平大量增加。
体外维生素E 可以防止几种人类病原体的生物膜形成,特别是金黄色葡萄球菌和表皮葡萄球菌。
/ 维生素K /
一项动物实验表明,缺乏维生素 K 的小鼠的肠道中,瘤胃球菌、毛螺菌科、Muribaculaceae的含量较多。
关于维生素对人体肠道微生物组直接影响的研究
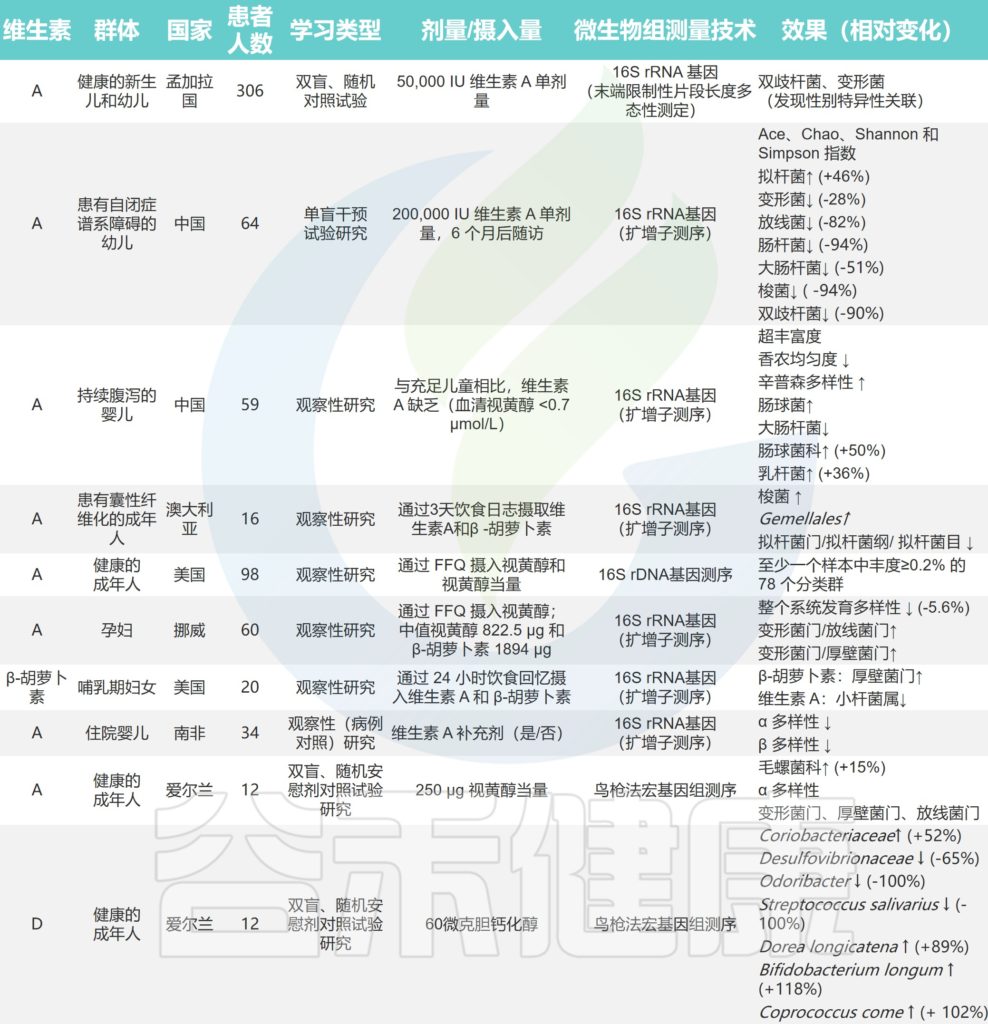
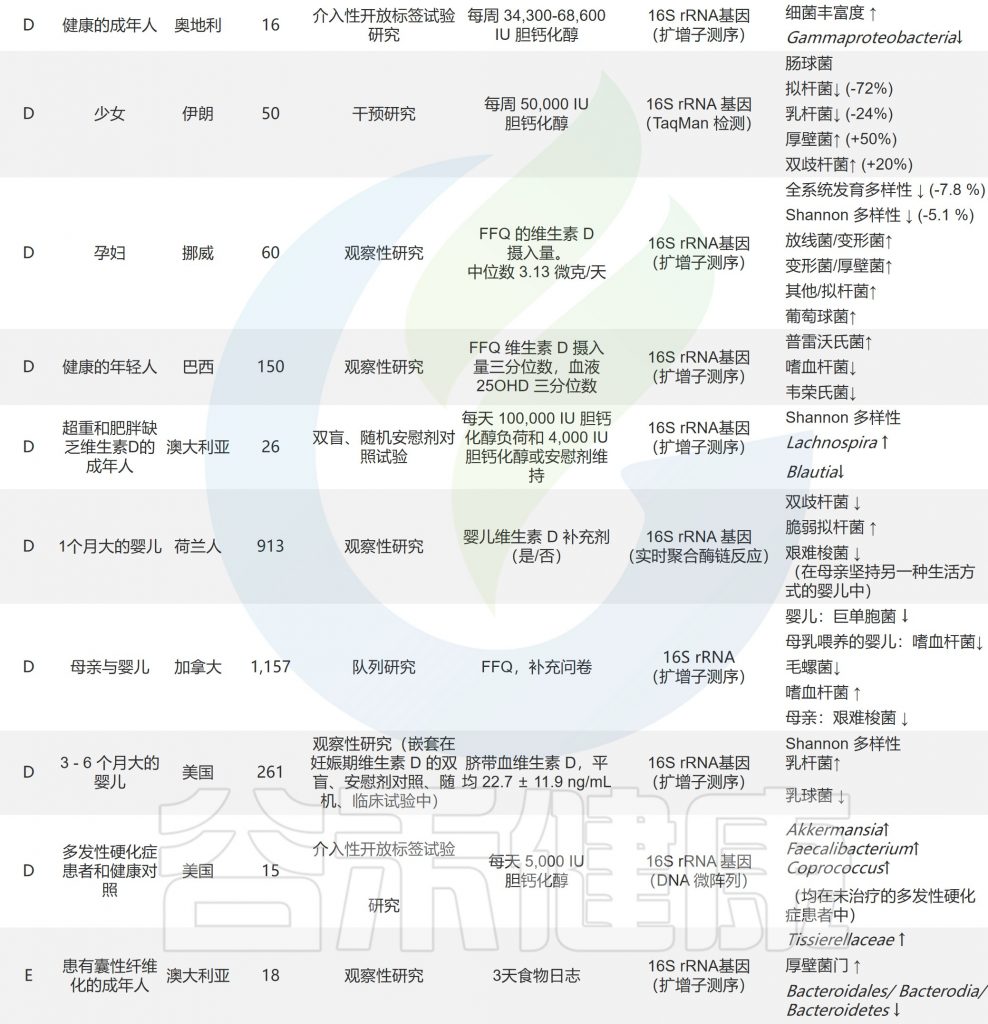
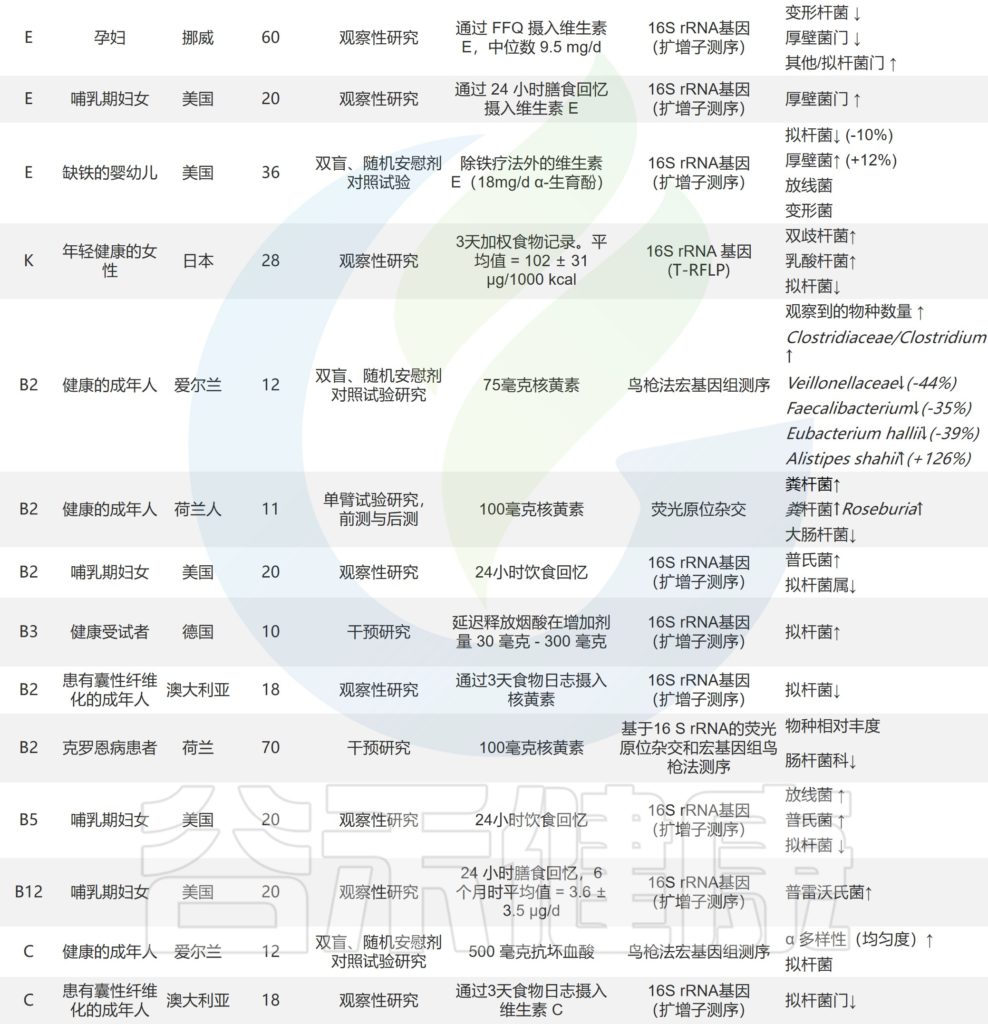
doi.org/10.1016/j.nutres.2021.09.001
饮食是维生素的主要来源,通过饮食补充维生素也会影响菌群。
注:由于测试饮食干预效果所需的随机试验的样本量和持续时间,相关发病率的研究具有挑战性。此外,由于特定的营养素不是孤立地消耗的,而是作为饮食模式的一部分,并且饮食成分之间相互作用,因此饮食带来的实际影响可能只有作为一个整体考虑时才会变得明显。
因此这里我们主要考虑饮食模式,例如地中海饮食等饮食方式。
地中海饮食是营养均衡饮食的典型代表,其特点是大量且频繁地摄入重要的纤维来源(谷物、蔬菜、豆类、水果和坚果)和具有抗氧化特性的化学成分(维生素、类黄酮、植物甾醇、矿物质、萜烯和酚类)。

同时地中海饮食还富含复杂和不溶性纤维含量。我们知道,大量摄入膳食纤维可促进肠道中有益菌群的生长,例如增加拟杆菌、普雷沃氏菌属、罗斯氏菌属、瘤胃球菌属、普拉梭菌等菌属的丰度,从而在肠道中产生高水平的短链脂肪酸,包括丁酸盐。
响应地中海饮食而增殖的细菌可以充当“基石”物种,也就是说它们对于稳定的“肠道生态系统”至关重要。这些变化主要是由于膳食纤维和相关维生素和矿物质的增加,特别是维生素C、B6、B9、铜、钾、铁、锰和镁。
总之,维生素似乎是微生物-宿主间代谢相互作用的重要媒介。
越来越多证据表明,维生素缺乏会导致肠道菌群紊乱,进而引发肠道疾病,甚至促进炎症和肿瘤的发展。下一章节详细讨论,维生素-微生物群相互作用对健康/疾病的影响。
最近的几项观察表明,微生物群失调和维生素缺乏是相互关联的。
维生素对宿主健康的影响

doi.org/10.1016/j.nutres.2021.09.001
这种关系可能直接影响宿主健康:例如,克罗恩病恶化与参与抗炎介质核黄素、硫胺和叶酸生物合成的微生物基因减少有关。
此外,2型糖尿病受试者在与微生物介导的维生素代谢相关的基因丰度谱中显示出显著变化。
营养不良儿童的微生物群显示,参与B族维生素代谢的多种途径(包括烟酸/NADP生物合成)显著减少。
在经历饮食振荡以诱导急性短期维生素A缺乏的灵长类小鼠模型中,Hibberd等人观察到细菌群落结构和宏转录组的调节,其中Bacteroides vulgatus是显著的应答者,在缺乏维生素A的情况下其丰度增加。有趣的是,B.vulgatus是在人类肠道微生物群的灵长类小鼠模型中鉴定的一种生长差异物种。
所有这些观察结果表明,维生素缺乏可能会改变肠道微生物群,从而影响人体健康。
下面我们以肠道疾病和精神类疾病两大类疾病为例,来具体了解维生素-微生物相互作用及其在疾病中的影响。
维生素 A 和 D 分别在近端和远端空肠吸收。维生素E和K主要在回肠吸收;微生物产生的维生素主要在结肠中吸收。维生素缺乏会加重肠道炎症,甚至通过多种机制促进癌症。
肠道菌群->维生素->肠道疾病中的作用
慢性 IBD 发生和发病机制中的关键作用是微生物(尤其是共生菌群)对宿主黏膜免疫功能的影响。同时,肠道微生物群和慢性炎症已被证明与肿瘤发生密切相关。
维生素具有调节肠道菌群和保护肠道的功能。因此,维生素和微生物群的相互作用可能在 IBD 和结直肠癌的治疗中具有巨大的潜力。
维生素A通过促进黏膜愈合、促进产生ASCFA的相关菌增加、降低UC相关菌的水平来达到治疗UC的效果。
费氏丙酸杆菌ET-3 产生维生素 K2 的前体,即 1,4-二羟基-2-萘甲酸 (DHNA),可激活芳烃受体 (AhR) 以改善结肠炎并调节肠道微生物群。
维生素 D 的缺乏会增加拟杆菌门、变形杆菌门和螺杆菌科的丰度,降低厚壁菌门和去铁细菌的丰度门,并且还影响 E-钙粘蛋白表达并减少耐受树突状细胞的数量。
然而,在治疗 IBD 时,维生素 D 与利福昔明的共同给药会影响肠道菌群和利福昔明的疗效。维生素 D 促进A. muciniphila的生长以保护肠粘膜屏障,这些作用对于对抗结直肠癌的发展尤为重要。
研究表明,维生素 E 及其代谢物在调节肠道菌群、减少炎症和抑制癌变方面具有巨大潜力。此外,维生素 Eδ-生育三烯酚 (δTE) 及其代谢物δTE-13′-羧基色原酚 (δTE-13′) 增加了肠道中的乳球菌和拟杆菌,并抑制炎症因子的产生。
维生素->肠道菌群->肠道疾病中的作用
▸维生素在IBD和结直肠癌中的作用不容忽视
大量临床研究表明,缺乏维生素 B 和维生素 D 的人群中结直肠癌的患病率较高。同时,IBD 的长期不愈合使患者面临更高的结直肠癌风险。维生素 D 水平低的 IBD 患者疾病严重程度和预后较差。
▸为什么肠道炎症容易导致癌症高风险?
在炎症背景下,敲除 IKKbetaβ(炎症与癌症之间的联系)可减少由于上皮细胞凋亡增加而导致的癌症发生。在一项关于结肠炎相关癌前癌 (CApC) 的研究中,IL-6 反式信号转导的存在增加了炎症性致癌的风险。如果不及时治疗,由肠道菌群紊乱和维生素缺乏引起的肠道炎症最终可能发展为癌症。
维生素 A 在肠道炎症和癌症中的作用
维生素 A 及其活性代谢物视黄酸 (RA) 在人体免疫系统中发挥着关键作用,并可能对辅助 T 细胞的分化产生影响。
炎症下:视黄酸从保护转变为破坏作用
在非炎症条件下,视黄酸能够抑制 IL-6 受体的表达和 Th1/Th17 的产生。
在炎症条件下,视黄酸从对粘膜的保护作用转变为破坏作用;这反映在活动期 IBD 患者黏膜中视黄酸水平显着升高,伴随着 CD4 和 CD8 分泌的 IL-17 和 IFN-γ 的上调。
维生素A及其代谢物:发挥抗炎作用
维生素 A 及其代谢物通过阻断 Th1 和 Th17 的激活,抑制 IL-17、INF-γ 和 TNF-α 的产生而显示出抗炎作用。同时,它们可以通过与TGF-β协同作用,提高Foxp3的水平,发挥免疫功能,从而促进抗炎因子的发挥。
一项数据显示,低水平的维生素 A 会激活核 NF-kB 并促进胶原蛋白的形成,从而加剧结肠炎的炎症。补充维生素后,肠道炎症明显缓解。
全反式维甲酸 (AtRA) 可降低 UC 和结直肠癌患者结肠黏膜分泌的 TNF-α 和一氧化氮合酶 2 (NOS2) 蛋白的表达。

维生素A保护肠黏膜屏障,其潜在机制是拮抗LPS的肠道破坏作用
在一项关于维生素 A 缺乏对结肠炎和结直肠癌发展的影响的检查中,研究人员使用葡聚糖硫酸钠 (DSS) 诱导小鼠结肠炎;此外,偶氮甲烷 (AOM) 预注射和 DSS 结肠炎的组合诱导了结直肠癌。缺乏维生素的小鼠肠道炎症水平较高,黏膜愈合较慢,免疫反应增强,更容易发生结直肠癌。
AtRA具有抗癌作用,结直肠癌中AtRA 水平降低
在结直肠癌小鼠模型中,肠道细菌引起的炎症影响 AtRA 代谢;这导致其水平下降。在 UC 及其相关结直肠癌的临床样本中发现 AtRA 代谢酶活性降低和 AtRA 水平降低。同时,AtRA通过激活CD8 + T细胞发挥抗癌作用;这为 CAC 的治疗提供了新的见解。
视黄醇和视黄醇结合蛋白(RBP)的结合激活致癌基因STRA6,促进结直肠癌的发生;Holo-RBP/STRA6 通路可通过促进成纤维细胞的致癌作用进一步发挥致癌作用。
在一项关于维生素 A 缺乏对结肠炎和结直肠癌发展影响的动物实验中,当维生素 A 处于低水平时,小鼠体内的维生素 A 脂滴会被降解,免疫反应会增强,结肠炎症会加重,癌变进程将加快。
维生素 B12 和叶酸在肠道炎症和癌症中的作用
IBD 患者缺乏维生素 B12 和叶酸的原因有很多,包括回肠和空肠微生物过度生长、维生素 B12 摄入不足或身体需求增加、维生素肠道破坏增加或吸收能力降低、某些药物(如甲氨蝶呤或柳氮磺胺吡啶)的不良反应、一些病理原因例如蛋白丢失性肠病、肝功能异常、回肠相关病变或手术切除、肠瘘等。
维生素 B12 缺乏不会影响健康的肠道微生物群组成;然而,它会导致实验性结肠炎中肠道菌群失调,并促进条件致病菌的生长。出乎意料的是,维生素 B12 缺乏减少了结肠组织的损伤;这可能与抗炎细胞因子 IL-10 的增加有关。

对甲基缺乏饮食 (MDD) 的潜在作用进行了一项研究,该饮食可降低维生素 B12 和叶酸的血浆浓度,并提高同型半胱氨酸水平,对 DSS 诱导的小鼠结肠炎的影响。喂食 MDD 的 DSS 治疗小鼠比其他治疗组患有更严重的结肠炎。
尽管超氧化物歧化酶和谷胱甘肽过氧化物酶活性保持稳定,但 caspase-3 和 Bax 的水平受到影响。除Bcl-2表达增加外,炎症相关标志物如胞质磷脂酶A2和环氧合酶2的表达也有明显增加趋势;这伴随着金属蛋白酶组织抑制剂(TIMP)3蛋白的表达降低。因此,维生素 B12 缺乏可能会加重实验性 IBD 的炎症程度。
高维生素 B12 水平可通过减少 DNA 甲基化来降低结直肠癌的风险
在结直肠癌患者中,与低血清维生素 B12 组相比,高维生素 B12 组的肿瘤区域和外周血单个核细胞 (PBMC) 中长散布的核元素 1 (LINE1) 甲基化被证明是降低的;肿瘤区域的LINE1甲基化水平也低于周围的非肿瘤区域。
氧化应激是结直肠癌发病机制之一;此外,叶酸和维生素 B12 的水平与体内抗氧化剂谷胱甘肽的水平呈正相关。提高 AOM 诱导的结直肠癌中的叶酸和维生素 B12 水平显示出显着的抗凋亡、抗氧化应激和抗 AOM 细胞毒性。
在对 4517 名 IBD 患者的系统评价和荟萃分析中,补充叶酸被证明可以降低 IBD 患者的结直肠癌风险并防止结直肠癌发展。
有趣的是,有证据表明缺乏甲基供体营养素叶酸、胆碱、蛋氨酸和维生素 B12 会抑制 Apc 突变小鼠的肿瘤发展。总而言之,维生素B12和叶酸在肠道疾病中的作用需要更深入的研究。
维生素 D 在肠道炎症和癌症中的作用
流行病学和动物实验表明,维生素 D 缺乏是 IBD 和 结直肠癌的高危因素。维生素 D 补充剂有助于降低疾病严重程度,可能通过多种机制,包括调节免疫细胞运输和分化,以及抗菌肽合成。
维生素D可以维持肠黏膜屏障的正常功能,提高机体的先天性和适应性免疫
1α,25-二羟基维生素 D3(骨化三醇)是维生素 D 的活性形式,可与 TGF-β 结合,提高 IL-2 水平,调节 T 细胞抑制炎性细胞因子的产生,增强 Foxp3 + Treg 细胞的存活和功能。

维生素D受体(VDR)是维生素D调节免疫和发挥抗炎作用的重要途径
相关资料显示,VDR对肠道有保护作用;它可以通过调节 JAK/STAT 通路来维持肠道稳态并预防癌症。
在 IBD 患者 中,结肠上皮中VDR的含量明显低于正常人。在实验性结肠炎模型中,与缺乏 VDR 的小鼠相比,表达 hVDR 的转基因小鼠的结肠炎症较少。用 hVDR 转基因恢复上皮 VDR 表达可减轻严重结肠炎并降低死亡率。内在机制是 VDR 通过抑制 NF-κB 活化发挥抗凋亡作用,以保护肠道屏障缓解结肠炎。
肠道菌群通过犬尿氨酸通路(合成维生素),在精神健康方面发挥作用
关于肠道细菌在心理健康方面的作用的关键方面,是它们通过犬尿氨酸通路参与调节色氨酸代谢。微生物群能够合成犬尿氨酸途径 (KP) 的酶促辅助因子,如维生素 B2 和 B6。

犬尿氨酸是主要的色氨酸代谢途径,其中 95% 的这种氨基酸被代谢为各种免疫和神经调节犬尿氨酸/色氨酸分解代谢物 (TRYCAT),在大脑中,犬尿氨酸途径主要在神经胶质细胞中分隔。
犬尿氨酸通路在精神、神经退行性和神经系统疾病中的作用是至关重要的,包括重度抑郁症,双相情感障碍,精神分裂症,阿尔茨海默病,亨廷顿病和帕金森病,与 HIV 感染相关的痴呆,手术后认知能力下降,肌萎缩侧索硬化(ALS) 等。
精神病理学和炎症中维生素缺乏与高同型半胱氨酸血症有关
精神病理学和炎症中维生素缺乏的另一个关键机制与高同型半胱氨酸血症(hHcy)有关,这可能是由叶酸、维生素 B6 和 B12 缺乏引起的。
高同型半胱氨酸血症和维生素 B 缺乏在重度抑郁症、精神分裂症、双相情感障碍、自闭症、焦虑症和痴呆症(包括阿尔茨海默病和帕金森病)中起关键作用。
同型半胱氨酸(Hcy)是在蛋白质消化过程中获得的另一种氨基酸蛋氨酸代谢过程中形成的氨基酸和中间体。该反应需要维生素 B12 作为酶促辅因子和叶酸衍生物(5-甲基四氢叶酸)作为甲基供体。
注:Hcy-同型半胱氨酸,是人体内含硫氨基酸的一个重要的代谢中间产物,可能是动脉粥样硬化等心血管疾病发病的一个独立危险因子。
此外,Hcy 可以在需要维生素 B6 作为酶辅因子参与的途径中转化为半胱氨酸。
因此,Hcy 被认为是叶酸和维生素 B12 缺乏的敏感标志物。
高同型半胱氨酸血症导致神经和精神病理学的机制包括:
促进免疫炎症反应、增加肠道和血脑屏障通透性、NMDA受体激动和神经毒性、诱导神经元凋亡、氧化应激、线粒体功能障碍和由于甲基化受损导致的单胺能神经递质合成失调。
目前对体内维生素水平的检测例如:
抽取血液检测其中维生素的含量水平,可以判断是否存在维生素的缺乏情况。
其他,例如通过肠道菌群健康检测,也可以查看近期体内维生素状况。
与通过血液进行维生素检测不同,肠道菌群的评估更加反映一段时间 ( 一般2周左右 ) 的长期状态,如部分B族维生素无法在体内留存,需要每日补充,血液检测波动较大。
注:菌群会受检测前一天饮食的影响,造成15~30%的菌群改变,同样也会反映在营养状况的评估上,因此建议检测前一天尽量保持近期正常饮食 ,这样能更好的反映真实的营养饮食状态。
在了解补充维生素的干预措施之前,我们先从肠道菌群的角度,来了解一下影响维生素合成吸收的因素。
人类基因的变异与肠道结构和微生物组组成有关。人类肠道微生物群中存在不同的维生素 B 生物合成途径支持人类遗传变异影响维生素 B 合成的观点。
维生素的合成吸收不仅需要靠饮食补充,还与吸收相关。而维生素的吸收涉及到相关基因,例如:
MTHFR 基因的突变会影响我们产生加工维生素 B9的酶——亚甲基四氢叶酸还原酶。
亚甲基四氢叶酸还原酶是叶酸代谢通路中的一种重要的辅酶,亚甲基四氢叶酸还原酶基因缺陷,容易造成叶酸在体内的代谢障碍,MTHFR基因最主要的两种突变为C677T、A1298C基因多态性。该两种位点同时突变可显著降低MTHFR活性进而降低叶酸水平。
VDR基因(维生素 D 受体):维生素 D(来自阳光、食物或补充剂)经过转化步骤后,活性形式骨化三醇 (1,25(OH)2D3 ) 可以通过VDR在细胞内发挥作用,是打开或关闭基因的转录因子。该基因突变可能导致维生素D缺乏引起的佝偻病。
维生素缺乏是一个严重的问题,尤其是在老年人中。随着年龄的增长,营养需求会随之变化。
由于食物中的维生素B12 需要胃酸及胃蛋白酶的作用才能释放出来被吸收,而老年人胃酸及胃蛋白酶分泌减少,就会影响维生素B12 的吸收。
患有维生素B12缺乏症的老年人可能出现神经精神或代谢缺陷。
一些药物会改变营养物质的吸收或代谢方式。例如,抗惊厥药也会减少叶酸的吸收。
肠道菌群通过各种代谢途径影响维生素的合成,例如拟杆菌属、肠球菌属和双歧杆菌属等人类肠道共生菌可以从头合成维生素 K 和大多数水溶性 B 族维生素,这在前面第二章节的表已经详细阐述。
在 B 族维生素合成中暴露于抗生素的反应因使用的抗生素类型而异。例如,在饮食中添加青霉素和金霉素会增加雄性大鼠的肝脏维生素 B2 浓度,以及 B2 和 B3 在尿液中的排泄。然而,链霉素和放线菌酮的施用降低了肝脏中维生素 B9 和 B12 的浓度。维生素合成对抗生素暴露的混合反应尚不清楚,但它们可能是由肠道微生物群的选择性改变引起的。
自由基是含有不成对电子的化学物质,可以诱导氧化应激。一个这样的例子是一氧化氮,它与金属离子形成复合物,包括钴,维生素 B12 的一种结构成分,因此使其无法用于细菌维生素 B12 的生物合成。此外,维生素生产者(如脆弱拟杆菌)暴露于过氧化氢等自由基会抑制其生长 ,从而降低维生素的生物合成能力。
维生素主要在小肠中吸收,其生物利用度取决于食物成分,相关相互作用等。
饮食和膳食的组成会通过影响肠道转运时间和/或混合胶束的肠道形成来影响某些维生素的吸收。
饮食中足量的水和膳食脂肪对于分别吸收水溶性和脂溶性维生素至关重要。
*水溶性维生素包括:B族维生素,维生素C;
脂溶性维生素包括:维生素 A、D、E 、K.
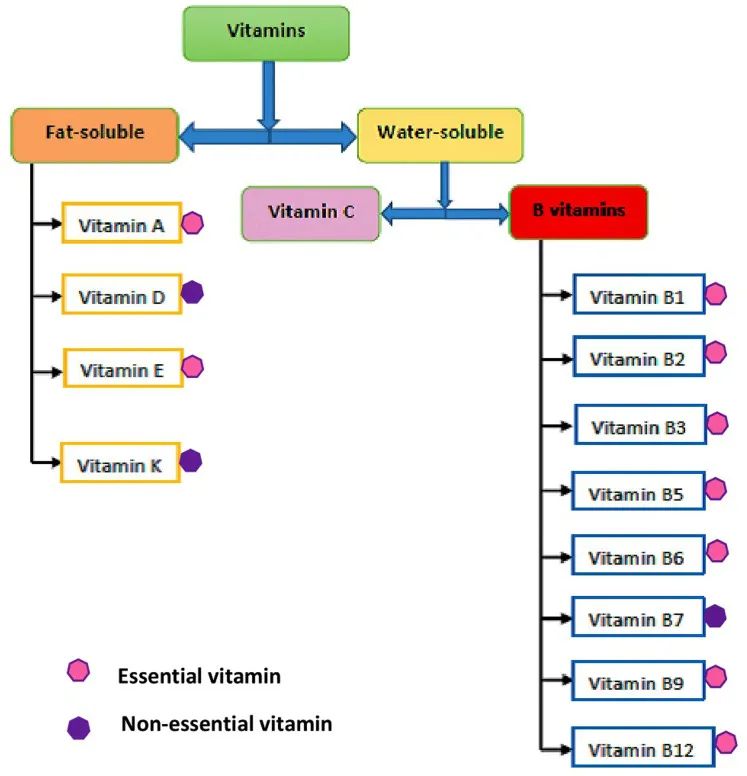
doi: 10.7717/peerj.11940
由于脂溶性维生素可以溶解在脂肪中,因此与膳食脂肪一起食用时最容易被吸收。例如,一种富含维生素 A 的小胡萝卜,如果单独食用,将在食物中获取维生素 A,但如果它是在含有一些膳食脂肪的食物成分中(比如说,橄榄油),将增加体内维生素 A 的吸收。
食物的性质(物理状态)也会影响维生素的吸收效率。例如,存在于可消化性较差的纤维植物材料中的类胡萝卜素已被证明相对于维生素A表现出较低的生物利用度。
当我们看到维生素缺乏的时候,可能希望通过饮食来补充相应缺乏的维生素,下表列出了常见的维生素的食物来源,可供参考。
此外,宿主饮食作为肠道中细菌的底物,其对肠道微生物分布的影响已被广泛研究。含有益生元和其他膳食营养素(如微量营养素和多酚)的饮食可以显着影响有益细菌的生长,包括维生素生产菌。
一些维生素,如核黄素,可作为氧化还原介质并刺激营养缺陷菌(如Faecaibacterium prauznitsii)的生长。
在即将形成共生关系的环境中,限制这些基质会增加微生物和微生物与宿主之间的竞争。
除了通过饮食直接补充之外,我们还可以通过补充益生菌来调节维生素水平,从而改善疾病。
双歧杆菌
在健康成人中补充益生菌菌株青春双歧杆菌DSM 18350、青春双歧杆菌DSM 18352 和假链双歧杆菌DSM 18353,导致粪便中叶酸浓度显着增加。
乳酸菌
乳酸菌通过不同的机制抑制炎症过程,包括调节IBD患者肠道菌群紊乱、保护肠道屏障和黏膜的正常功能、调节人体免疫反应等。乳酸菌通过产生核黄素(维生素 B2)和叶酸发挥抗炎和抗氧化作用。
产维生素的乳酸菌不仅对急性肠炎有抗炎作用,还能有效缓解复发性结肠炎。此外,在与美沙拉秦合用过程中,可有效降低不良反应,提高疗效。
研究人员发现注射产生叶酸的乳酸菌会缓解 5-FU 引起的肠炎小鼠的腹泻,改善结肠组织的结构和功能。这一发现降低了癌症化疗期间发生的肠黏膜炎症的严重程度,并提高了药物有效性;因此,这提高了患者的生活质量。
此外,乳酸菌 和 5-FU 的联合使用可减少 5-FU 引起的血细胞计数减少,并使患者获得完整的治疗周期。
产维生素的益生菌在肠道疾病中的作用

doi.org/10.3390/nu14163383
研究人员从 150 个收集的人类粪便样本中分离出三种产生核黄素和叶酸的益生菌;他们用它们来治疗乙酸引起的大鼠结肠炎。他们发现这些益生菌可以保护结肠黏膜,促进溃疡性病变的愈合;此外,它们具有抗炎和抗氧化应激作用。
一种新分离的具有产生叶酸能力的细菌——清酒乳杆菌LZ217,具有促进丁酸产生和改善肠道菌群组成的作用。
Akkermansia muciniphila 是肠道中的一种常见细菌,可调节 CLT 以保护肠道免受炎症和肿瘤侵袭;它还产生维生素 B12 以缓解 IBD 患者的维生素缺乏症。
研究发现,丙酸杆菌菌株 P. UF1 合成维生素 B12;这对肠道免疫和肠道健康有积极的调节作用。
大肠杆菌通过产生维生素来缓解 IBD. 使用大肠杆菌生产两种产生β-胡萝卜素的菌株来治疗维生素A缺乏症。这些结果显示出巨大的临床潜力。
维生素 A 及其代谢物与短乳杆菌KB290 的组合提高了 CD11c + MP/CD103-DC 比率;因此,这在结肠炎的治疗中起着积极的作用。
此外,肠道中的分段丝状细菌 (SFB) 可以产生 AtRA,以抵消感染对肠道的损害。
益生菌对维生素D及其受体活性有积极作用,如鼠李糖乳杆菌GG(LGG)和植物乳杆菌(LP);同样在沙门氏菌结肠炎模型中,使用 VDR (-/-) 小鼠验证 LGG 对 IBD 的缓解作用是通过 VDR 信号通路。
此外,胆汁盐水解酶 (BSH)活性罗伊氏乳杆菌NCIMB 30,242 可调节血浆中的活性维生素 D 水平。磷虾油 (KO)、益生菌罗伊氏乳杆菌和维生素 D 的混合物显着降低病理评分和炎症因子的释放,促进黏膜愈合并减少机会性感染的发生。
经益生菌 VSL#3 预处理后,VDR 水平显着提高,共同保护肠黏膜,防止损伤;这对预防CRC的发展起到一定的作用。
用从韩国泡菜中分离的乳酸菌条件培养基处理 HCT116 细胞或肠类器官后,其分泌的蛋白质 P40 和 P75 与 VDR 的表达增加有关;它们还增强自噬反应,共同具有抗炎作用。肠道微生物合成的石胆酸 (LCA) 充当连接 VDR 与微生物的桥梁,从而提高维生素 D 水平。
益生菌配方有助于抑郁症患者维生素水平的增加
一项随机对照试验中,重度抑郁症患者接受了多种益生菌配方,其中含有双歧杆菌W23、乳双歧杆菌W51、乳双歧杆菌W52、嗜酸乳杆菌W22、干酪乳杆菌W56、副干酪乳杆菌W20、植物乳杆菌W62、唾液乳杆菌W24、乳酸乳杆菌W19。
此外,益生菌组和安慰剂组的患者接受了相同剂量的维生素 B7。在两组中,抑郁症的临床参数都有所改善,然而,益生菌干预组与安慰剂组相比,仅在微生物 β 多样性方面存在差异,临床结果指标没有差异。有趣的是,尽管两组都接受了相同剂量的生物素,但接受益生菌的那组维生素 B6 和 B7 的合成上调。
多种益生菌相结合通过增加叶酸和维生素 B12血浆水平,改善精神疾病
八周的个性化饮食与含有多种益生菌的菌株相结合:婴儿双歧杆菌DSM 24737、长双歧杆菌DSM 24736、短双歧杆菌DSM 24732、嗜酸乳杆菌DSM 24735 、德氏乳杆菌、保加利亚乳杆菌DSM 24734、副干酪乳杆菌DSM 24733、植物乳杆菌DSM 24730 、嗜热链球菌DSM 24731 (VSL#3),在健康老年人中增加了叶酸和维生素 B12 血浆水平并降低了 Hcy 血浆水平。
此外,益生菌的添加导致粪便双歧杆菌浓度增加,这种变化与叶酸和维生素 B12 水平呈正相关。
在精神病患者中引入高同型半胱氨酸的评估和治疗可能非常有价值,益生菌可能成为治疗工具之一。
维生素是相互关联的、具有协同作用的微量营养素,当它们处于适当的平衡状态时,它们的全部潜力就会得到充分发挥。
因此,在食用益生菌和发酵食品时,应考虑维生素生产者与代谢者之间复杂的相互作用。
除了以上方式干预菌群之外,也可以通过良好的生活方式调理菌群,从而使维生素达到一个相对健康稳定的水平,减少各类疾病风险。
▸在服用维生素的同时可以服用益生菌吗?
可以。在大多数情况下,服用益生菌不会影响其他补充剂的效果。
一项 2021 年对临床试验的系统评价发现,益生菌可以改善健康人群的微量营养素水平,特别是维生素 B12、叶酸(维生素 B9)、钙、铁和锌。
2017 年的一项非随机临床试验发现,服用益生菌和铁补充剂的参与者比不服用益生菌的铁吸收明显更多。
有研究表明,维生素 D 和益生菌之间存在协同关系。
随机对照试验发现,维生素 D 补充剂与益生菌一起可以改善多囊卵巢综合征患者和同时患有冠心病的糖尿病患者的各种心理健康参数、一般健康状况、代谢和炎症标志物。
2019 年对随机对照试验的系统评价和荟萃分析发现,维生素 D 强化酸奶(富含益生菌嗜酸乳杆菌)有助于改善维生素 D 和胆固醇水平、代谢功能和身体测量值。
然而以上研究都没有单独研究维生素 D 和益生菌的作用,因此尚不清楚结果是否与两者的综合影响有关。
研究人员认为,无论有没有维生素,服用益生菌的时间很重要。作为一般规则,服用益生菌的最佳时间是空腹,大约在进食前 30 分钟。
研究人员担心胃酸的存在会影响益生菌的生存能力。在餐前或餐后几个小时服用时,当胃酸自然降低时,益生菌可以进入肠道,从而提高其生存几率。
何时服用维生素取决于维生素的种类。复合维生素通常最好在早上第一时间服用,非常适合搭配早餐前的益生菌。脂溶性维生素,如 A、D、E 和 K 以及一些矿物质,包括铁和镁,最好与食物一起服用。否则可能会导致胃部不适。
▸应该从食物中补充维生素还是通过维生素补充剂?
2020 年的一篇文献综述发现,与浓缩补充剂相比,许多微量营养素在其全食物形式中的生物利用度更高。因此提倡补充方式以食物为先。
一般认为,对于健康人来说,营养均衡的饮食可以提供身体需要的维生素,不需要额外补充,但对于可能存在免疫功能、肠道健康、吸收不良等问题的人群,可以考虑维生素补充剂进行补充,具体补充剂量请遵医嘱。
下表是维生素易缺乏的高风险人群:

▸可以长期服用维生素补充剂吗?补充过量会带来副作用吗?
一般健康人不需要长期服用维生素补充剂。
对于服用复合维生素片,多余的维生素会被排出体外,因此不用过于担心会带来危害。但是如果长期十倍以上的用量,对身体是有危害的。

doi: 10.7717/peerj.11940
在发现维生素缺乏的症状的时候,我们可能希望通过补充相应的维生素补充剂来改善健康。然而服用任何补充剂之前,我们应该寻找其根本原因而不是直接根据症状盲目补充。
通过肠道菌群健康检测可以了解维生素缺乏状况,且可以根据各类菌群丰度来推断维生素的菌群代谢状况。如果是由于菌群的代谢异常,可能直接补充并没有太大效果,这时候优先调节菌群或许是更好的选择。
如果维生素指标都显示正常没有缺乏(如下图),保持常规饮食不需要刻意补充。还想要更健康,指标更接近70的话,可以在数值略小的指标上,针对性地通过饮食进行补充调理。
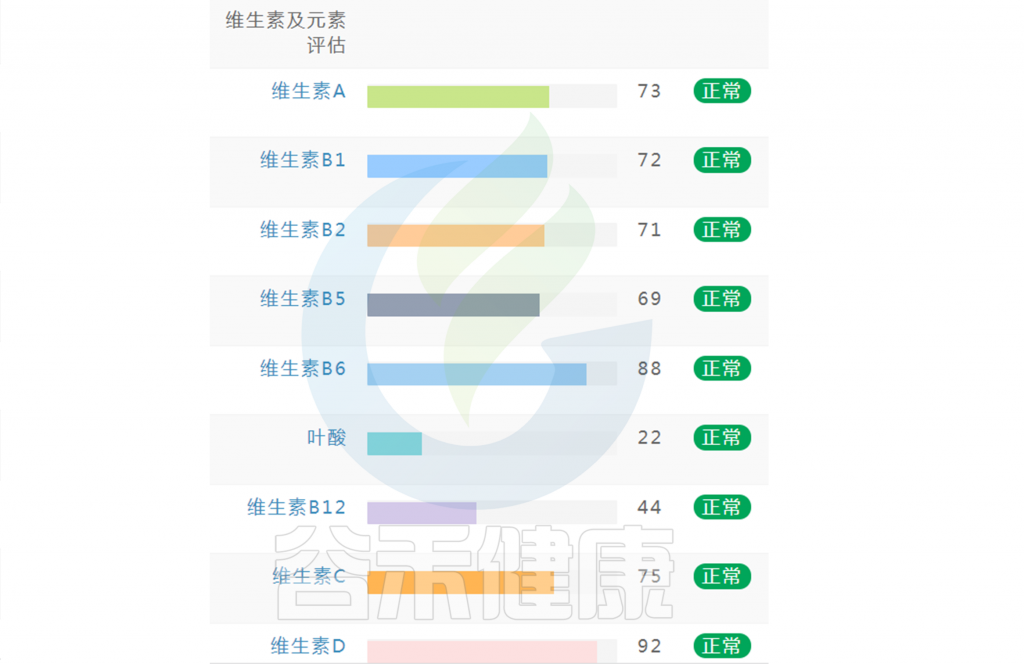

如果维生素指标中出现个别指标缺乏或偏低(如下图),可以通过饮食针对性地进行改善调整,如果已经出现对应症状,例如缺乏维生素A,同时出现干眼症或者夜盲症等相应的症状,可以使用相应的维生素补充剂进行干预,或者根据菌群代谢通路判别,通过菌群调理进行相应干预。
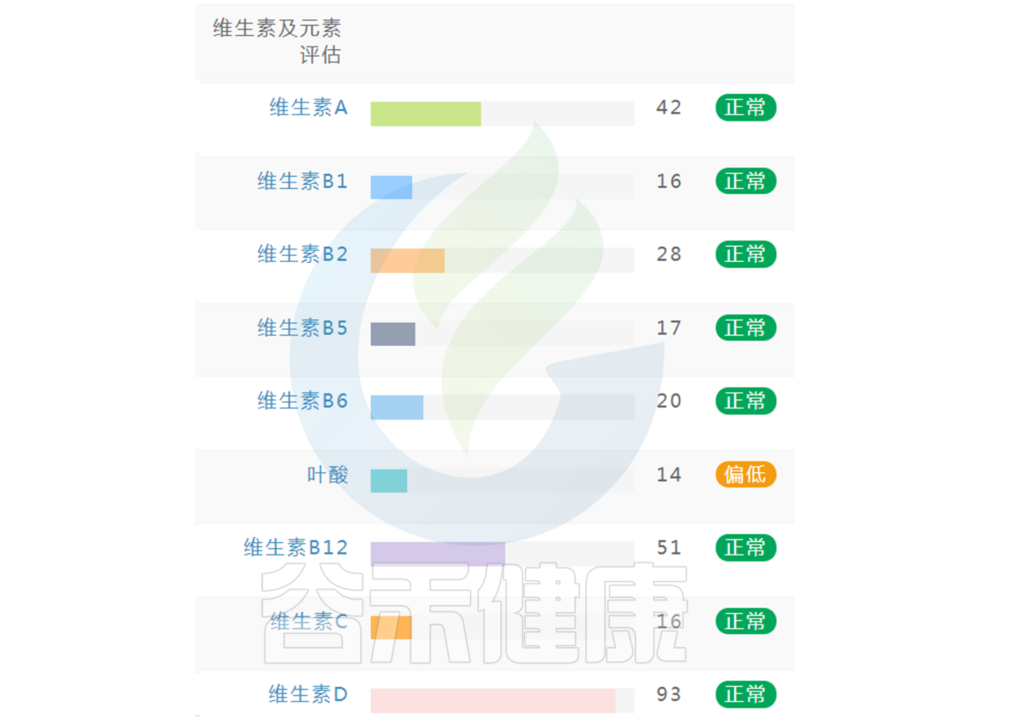
如果维生素指标中出现缺乏或偏低的指标较多,则需要选用复合维生素,各类维生素之间可能存在协作关系,同时配合饮食、菌群进行干预。
选择补充剂,应优先考虑生产规范良好的产品,比如说可以查看是否有“OTC”标志。
注:本账号内容仅作交流参考,不作为诊断及医疗依据。
主要参考文献:
Zhai Z, Dong W, Sun Y, Gu Y, Ma J, Wang B, Cao H. Vitamin-Microbiota Crosstalk in Intestinal Inflammation and Carcinogenesis. Nutrients. 2022 Aug 17;14(16):3383. doi: 10.3390/nu14163383. PMID: 36014889; PMCID: PMC9414212.Zhai Z, Dong W, Sun Y, Gu Y, Ma J, Wang B, Cao H. Vitamin-Microbiota Crosstalk in Intestinal Inflammation and Carcinogenesis. Nutrients. 2022 Aug 17;14(16):3383. doi: 10.3390/nu14163383. PMID: 36014889; PMCID: PMC9414212.
Bellerba F, Muzio V, Gnagnarella P, Facciotti F, Chiocca S, Bossi P, Cortinovis D, Chiaradonna F, Serrano D, Raimondi S, Zerbato B, Palorini R, Canova S, Gaeta A, Gandini S. The Association between Vitamin D and Gut Microbiota: A Systematic Review of Human Studies. Nutrients. 2021 Sep 26;13(10):3378. doi: 10.3390/nu13103378. PMID: 34684379; PMCID: PMC8540279.
Ofoedu CE, Iwouno JO, Ofoedu EO, Ogueke CC, Igwe VS, Agunwah IM, Ofoedum AF, Chacha JS, Muobike OP, Agunbiade AO, Njoku NE, Nwakaudu AA, Odimegwu NE, Ndukauba OE, Ogbonna CU, Naibaho J, Korus M, Okpala COR. Revisiting food-sourced vitamins for consumer diet and health needs: a perspective review, from vitamin classification, metabolic functions, absorption, utilization, to balancing nutritional requirements. PeerJ. 2021 Sep 1;9:e11940. doi: 10.7717/peerj.11940. PMID: 34557342; PMCID: PMC8418216.
Steinert RE, Lee YK, Sybesma W. Vitamins for the Gut Microbiome. Trends Mol Med. 2020 Feb;26(2):137-140. doi: 10.1016/j.molmed.2019.11.005. Epub 2019 Dec 17. PMID: 31862244.
Pham VT, Dold S, Rehman A, Bird JK, Steinert RE. Vitamins, the gut microbiome and gastrointestinal health in humans. Nutr Res. 2021 Nov;95:35-53. doi: 10.1016/j.nutres.2021.09.001. Epub 2021 Oct 21. PMID: 34798467.
Hossain KS, Amarasena S, Mayengbam S. B Vitamins and Their Roles in Gut Health. Microorganisms. 2022 Jun 7;10(6):1168. doi: 10.3390/microorganisms10061168. PMID: 35744686; PMCID: PMC9227236.
Rudzki L, Stone TW, Maes M, Misiak B, Samochowiec J, Szulc A. Gut microbiota-derived vitamins – underrated powers of a multipotent ally in psychiatric health and disease. Prog Neuropsychopharmacol Biol Psychiatry. 2021 Apr 20;107:110240. doi: 10.1016/j.pnpbp.2020.110240. Epub 2021 Jan 9. PMID: 33428888.
Barone M, D’Amico F, Brigidi P, Turroni S. Gut microbiome-micronutrient interaction: The key to controlling the bioavailability of minerals and vitamins? Biofactors. 2022 Mar;48(2):307-314. doi: 10.1002/biof.1835. Epub 2022 Mar 16. PMID: 35294077; PMCID: PMC9311823.