-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


肥胖和营养不良是普遍面临的健康问题,而肠道菌群在其中扮演的什么样的角色?最近一项研究通过交叉过量、过低饮食干预以及随机双盲万古霉素抗生素实验,揭示了不同热量摄入和抗生素会破坏肠道菌群特定代谢产物(如:丁酸和其他短链脂肪酸)影响肠道屏障,并改变特定微生物群落(如阿克曼菌),这种变化是粪便热量流失的原因,表明肠道菌群在饮食能量吸收中起着因果的作用。

单位:美国国家卫生所
期刊: Nature Medicine 《自然医学》
摘要
文章揭示了营养不良和口服万古霉素对人体肠道菌群和营养吸收的影响。以往的研究发现,营养不良显著增加粪便热量损失,且降低了拟杆菌门和厚壁菌门的相对丰度,这是人类肠道中的两个主要门。还有各种证据表明,早期使用抗生素与儿童体重增加有关,在营养不良中,抗生素促进生长的证据好坏参半。在本文中,研究人员进行了一项长期的住院研究,使用了两种干预措施。在每个实验中,研究人员都测量了过量饮食和饮食不足期间的粪便卡路里流失,这是营养吸收的直接表征,第一阶段是随机交叉饮食干预,所有受试者按随机顺序接受3天的过量和不足饮食喂养。第二阶段是随机、双盲、安慰剂对照的药物干预,使用万古霉素或安慰剂(NCT02037295)。研究人员观察到,肠道菌群结构在营养不良和饮食过量的情况下有轻微的变化,但口服万古霉素后群落结构伴随着多样性降低发生了更显著的变化。两种干预措施中嗜粘蛋白艾克曼菌的丰度都增加了,这导致了更多的粪便热量流失。这些结果表明,营养吸收对环境扰动敏感,并与临床前模型相关,表明肠道菌群在饮食能量吸收中可能起因果作用。
背景
全球肥胖症的流行促使人们努力确定影响能量平衡的环境和宿主因素,能量平衡的定义是能量摄入和消耗之间的平衡。虽然卡路里消耗是能量摄入量的关键决定因素,但个体消化和吸收所消耗的饮食底物的能力的不同程度也可能影响能量平衡。在过去的十年中,利用啮齿动物模型得到的研究成果,支持了数以万亿计的微生物在人类胃肠道(肠道菌群)的因果作用,由于它们对能量摄入和消耗的广泛影响,形成了能量平衡的个体间变化。但可惜的是,尚无直接证据表明微生物群对营养吸收有影响.
实验设计
实验对象:
选取了除葡萄糖耐受和肥胖症以外的27名健康志愿者(男17名,女10名,年龄35.1±7.3,BMI 32.3±8.0),其中25名完成了整个实验。在整个研究过程中,参与者都是住院患者,每天都接受监测,没有被报告过副作用,特别是腹泻或腹部症状。
设计方案:
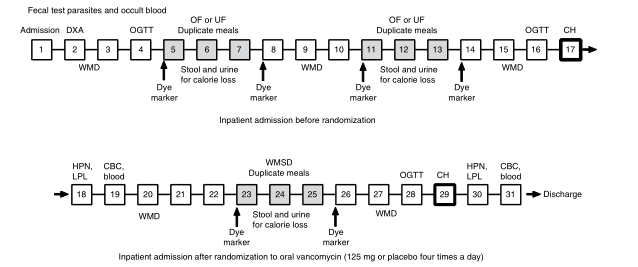
第一阶段:随机的交叉饮食干预
所有受试者均以过量(OF)和节食(UF)三天的随机顺序进行饮食,期间会有3天的洗脱期。OF为WMD的150%的饮食,UF为WMD的50%的饮食。
第二阶段:药物干预
同样的受试者被随机分为安慰剂组和口服万古霉素组
注:
(WMD)体重维持饮食【20%大卡蛋白质;30%大卡脂肪;50%大卡碳水化合物】;(DXA)双能X线吸收法,用于骨密度测定;(OGTT) 口服葡萄糖耐量试验;(Dye marker)表示粪便收集所使用的染料标记物;(CH) 间接量热法,用于评估24小时能量消耗;(HPN,LPL) 肝素诱导的LPL测定;(CBC) 全血细胞计数
主要结果
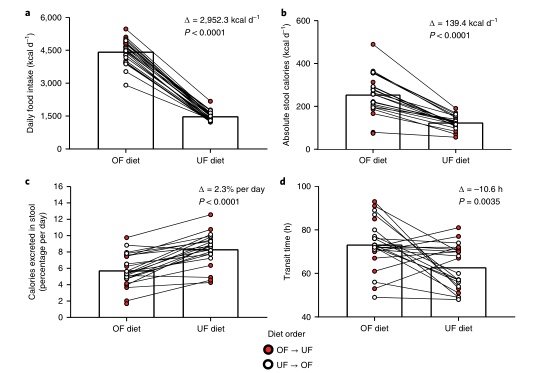
“ Δ ”表示组间的平均差异;“ P ”表示双边配对学生t检验; 红点表示开始饮食阶段为OF的受试者,白点表示开始饮食阶段为UF的受试者
a):过量饮食组(4,446.5 ± 547.8 kcal d−1)的每日摄入热量显著高于营养不良组(1,494.2 ± 211.0 kcal d−1),
b):与营养不良的人相比,过量饮食的人每天消耗的卡路里绝对数量明显更高。
c):当以每天摄入的卡路里的百分比来表示时,UF期间的粪便热量流失相对于OF明显更大,且有很强且显著的体内相关性(Pearson’s r = 0.70, P = 0.004)
d):UF比OF转运时间快,转运时间被定义为每次干预期间染料标记第一次出现和最后一次出现之间的时间(以h为单位)。
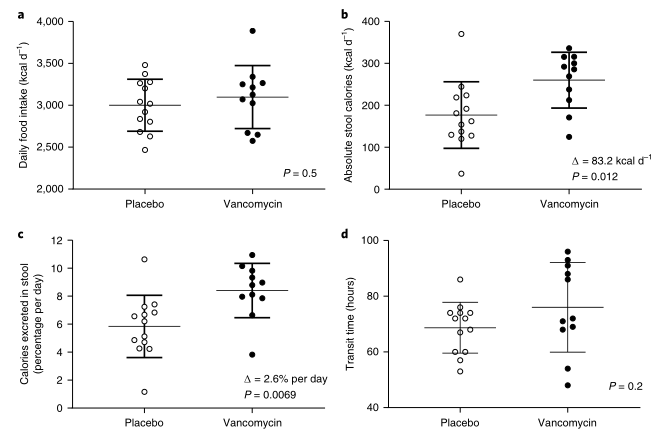
Δ ”表示组间的平均差异;“ P ”表示双边非配对学生t检验;误差条表示95%置信区间的均值
a):3天的平均摄入热量。安慰剂组(Placebo)和万古霉素组(Vancomycin)每天摄入的热量是相当的。
b):万古霉素导致粪便热量流失显著增加。
c):粪便平均热量流失百分比。
d):万古霉素组和安慰剂组的转运时间没有差异(P=0.2)
2.使用扩增子和宏基因组测序相结合的方法,评估了饮食干预和药物干预对肠道微生物群落结构的影响。在饮食干预组间分析中发现了几种对饮食敏感的细菌物种。在药物干预组间分析中也发现了几种显著富集的物种。且扩增子和宏基因组测序结果具有一致性。尽管存在这些差异,但在这两种干扰下,有两种细菌的种类都发生了一致的变化。嗜粘蛋白艾克曼菌和一种隶属于Lachnospiraceae NK4A136群的一个未确认的种。
饮食干预:
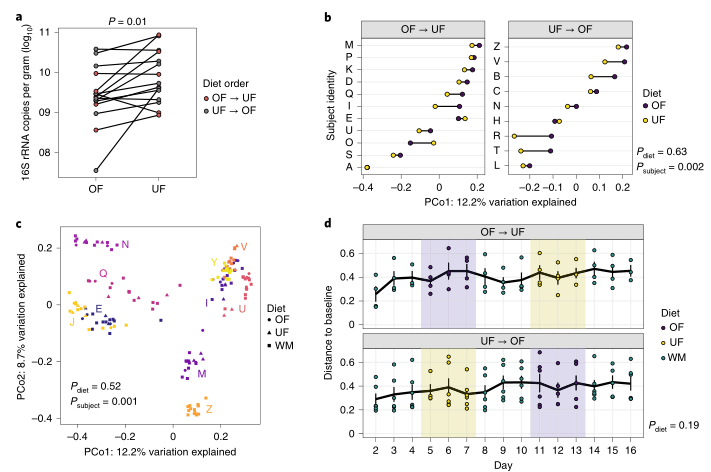
a):整体肠道菌群在OF和UF期间的定植。在UF期间,肠道菌群由于相对地缺乏营养,这可能导致细菌定殖的减少。但是在UF期间与OF相比,总的定殖水平显著增加(P=0.01,双边配对的Wilcoxon检验)。
b):两种饮食措施的Bray-Curtis距离的PCoA第一主坐标的差异。受试者按饮食顺序分开;c):在两种饮食措施期间每天从10个受试者中取样,其PcoA分析结果。每个点代表一个样本,其中颜色表示受试者身份,形状表示饮食方式(WM,保持体重);d):随着时间的推移,微生物群落到基线样本(第一天)的距离。颜色代表饮食,每个点代表一个样本字母表示受试者身份。发现在整个3天的UF和OF干预过程中,总体微生物群落结构保持不变,在基线上保持显著的个体间差异。
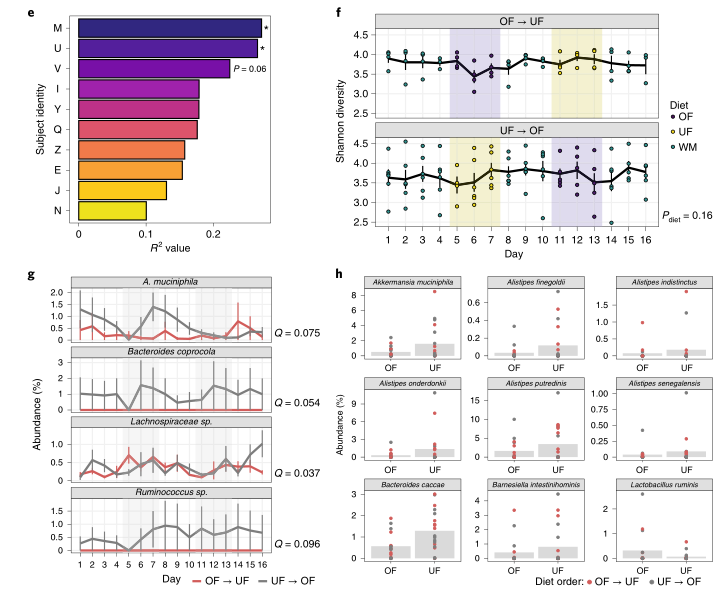
e):在被评估的10个个体中,有2个个体被发现在UF组中的微生物群落总体结构上有显著差异,这可能表明肠道菌群的基线关系到其对饮食干预的敏感性。(对每个受试者进行Adonis分析,R2值量化不同饮食上的方差,“*”表示P<0.05,纵坐标的字母表示受试者身份)
f):在整个第一阶段的16天内,微生物的总体Shannon多样性相对稳定。
g):通过16SrRNA鉴定出的4个与饮食显著相关的物种:嗜粘蛋白艾克曼菌、Bacteroides coprocola、毛螺旋菌、瘤胃球菌。纵坐标为相对丰度,横坐标为时间(d)。
(经FDR调整后的P值,Q < 0.1,双侧Wald检验的DESeq2)。线代表mean ± s.e.m.
h):基于宏基因组测序的物种分类,发现了9种细菌在不同饮食组间的显著差异(FDR < 0.05, 配对的Wilcoxon检验),每个点代表一个样本,纵坐标表示相对丰度。这与16S rRNA基因测序的分析一致。
药物干预:
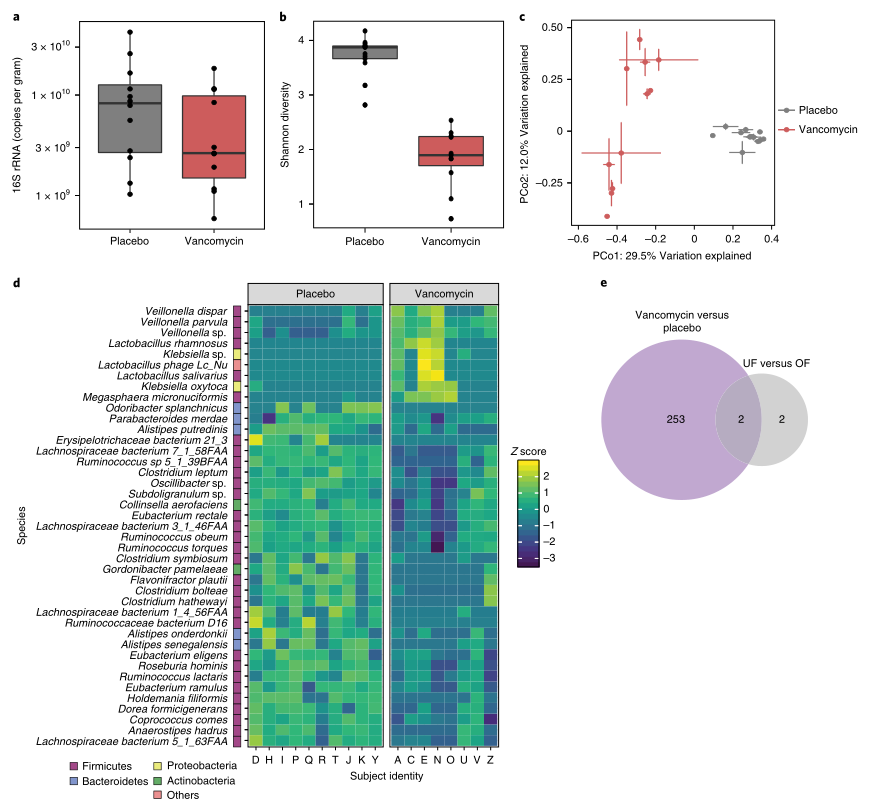
a):不同治疗组的肠道菌群的定植水平无明显差异(P = 0.26,双侧非配对Wilcoxon检验)。每个点代表每个受试者样本的平均值。
b):不同治疗组的微生物群落Shannon多样性。(P <0.0001,双侧非配对Wilcoxon检验)。每个点代表每个受试者样本的平均值。
c):不同治疗组间的基于Bray-Curtis距离的PCoA分析。发现万古霉素对肠道微生物群落结构也有显著影响,超过了先前存在的个体间差异。(每个数据点都显示了每个受试者样本的平均值和标准差)
d):通过宏基因组测序得到的不同治疗组间差异丰富物种的热图。横坐标代表受试者样本,纵坐标代表物种(FDR<0.05,双侧非配对Wilcoxon检验)。其中万古霉素组的物种相对丰度有下降的趋势,31种下降,10种增加。与16SrRNA基因测序数据一致,在万古霉素处理的个体中,有3个Veillonella菌属显著富集,还检测到多种乳杆菌和克雷伯氏菌以及感染乳杆菌的强毒噬菌体(LcNu)的富集。
e):万古霉素和安慰剂与UF和OF之间的16S rRNA序列变异的Venn图。
3. 对UF和OF组、万古霉素组和安慰剂组与代谢疾病相关的宿主-微生物相互作用的机制研究。丁酸盐是肠道细菌代谢的主要终产物。脱氧胆酸,一种次级胆酸,较低的浓度可能意味着肠道屏障的保护和较低的营养吸收。
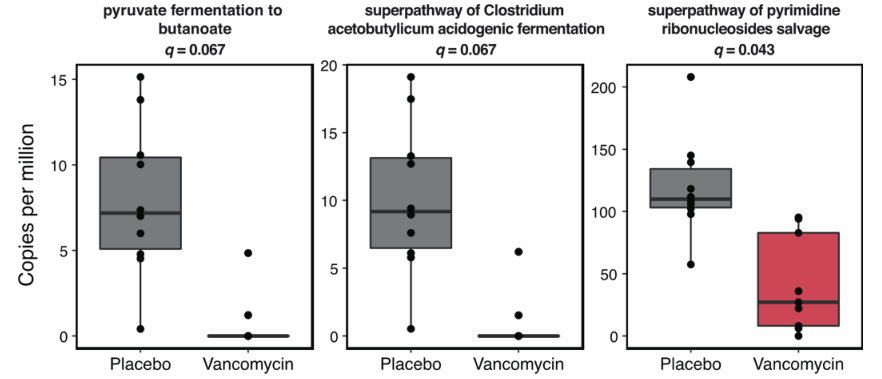
通过分析KEGG代谢途径,发现了三条在万古霉素和安慰剂之间差异丰富的代谢途径。其中的两条(丙酮酸发酵为丁酸和乙酰丁酸梭菌产酸发酵超途径)与糖发酵为主要短链脂肪酸丁酸盐(又名丁酸)有关。说明万古霉素治疗期间肠道菌群可能会减少丁酸的产生或细菌代谢。
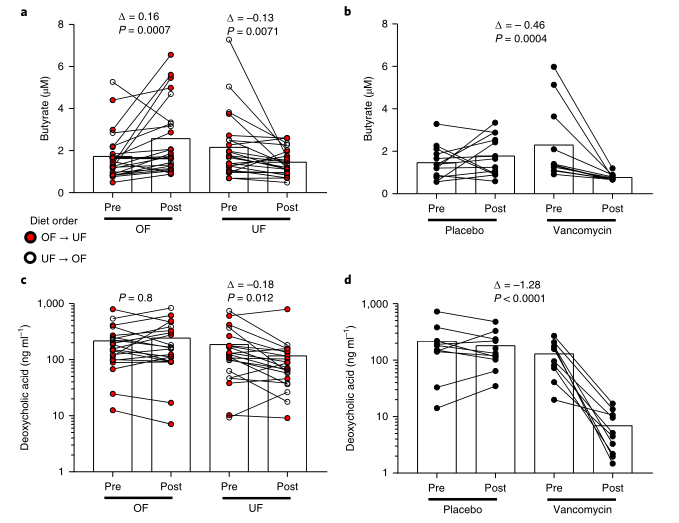
“ Δ ”表示组内干预措施前后的差异
a):OF和UF期间丁酸盐的平均浓度;b):万古霉素组和安慰剂组的丁酸盐的平均浓度。UF和万古霉素处理组的丁酸盐平均浓度均显著下降,这支持肠道菌群在这些干预过程中获取营养的能力下降的说法。
c):OF和UF期间脱氧胆酸的平均浓度;d):万古霉素组和安慰剂组的脱氧胆酸的平均浓度。脱氧胆酸的平均浓度在UF和万古霉素处理组也显著降低了。
结论
在这项分两个阶段的研究中,研究人员直接测量了摄入的和粪便的卡路里,证明了限制热量摄入和口服万古霉素都会导致粪便热量流失增加,血浆丁酸水平降低。这种影响的幅度约为摄入卡路里的2.5%,这将转化为100公斤受试者在1年内体重减轻约1.2公斤。另一方面,研究人员观察到UF和OF对肠道微生物群落结构的轻微干扰,而口服万古霉素引起了广泛的变化,降低了肠道细菌的多样性,并使肠道细菌的相对丰度发生了显著变化。这两种扰动都导致了嗜粘蛋白艾克曼菌的相对丰度增加。而在人一项基于人体的随机、双盲、安慰剂对照的先导研究显示,补充嗜粘蛋白艾克曼菌有降低体重和脂肪量的趋势。此外,体外研究表明,丁酸和其他短链脂肪酸可以刺激肠道屏障的形成,从而保护肠道免受LPSs的破坏。根据研究人员的观察表明,热量摄入和抗生素可能会破坏这些代谢产物和其他调节屏障功能的微生物代谢产物之间的平衡,导致营养吸收的改变。研究中也有一些局限性,比如尽管肠道微生物群落结构和代谢物浓度发生广泛变化,但未发现口服万古霉素对粪便热量的影响、不知道其他抗生素是否会对粪便卡路里产生影响、任何关于营养吸收的机制都是推测出来的,因为没能直接评估营养在肠道中的传输等。