-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com

谷禾健康
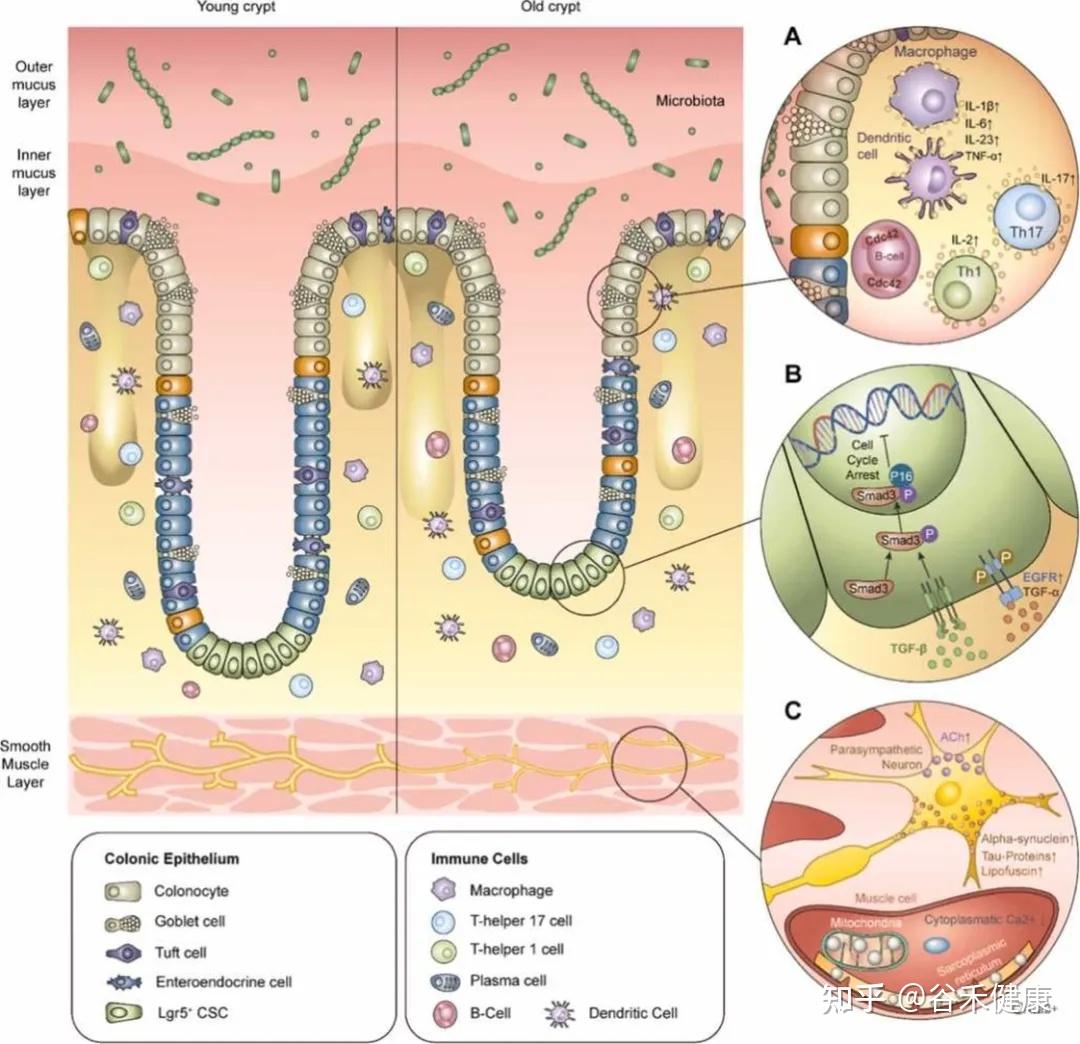
结肠,作为我们消化系统中的关键一环,却是最容易受到衰老影响的器官之一。随着年龄的增长,结肠的结构和功能发生了显著变化,这些变化会导致肠道屏障变得脆弱,进而影响我们的健康。
研究表明,衰老导致结肠黏膜上皮更新速度减缓,隐窝干细胞活性降低,紧密连接蛋白(如occludin、claudin、ZO-1)的表达异常。这些变化使得细胞通透性增加,黏液层变薄,黏液屏障的完整性下降。同时,免疫系统也出现了免疫衰老现象,降低了对有害菌的防御能力。
这一切都可能导致低度炎症状态,表现为内毒素易位和系统性炎症标志物的升高。而在微生态方面,老年人的肠道菌群多样性下降,产短链脂肪酸菌减少,潜在的促炎菌却相对增加,形成了一个恶性循环。
近年来,益生菌作为调节微生态和修复肠道屏障的干预策略,在老年相关便秘、抗生素相关腹泻、感染性腹泻、炎症性肠病辅助治疗和肠易激综合征等多个领域积累了丰富的临床证据。然而,益生菌的效果并非一概而论,它们的保护作用高度依赖于特定菌株,并受到个体差异的影响。
注:不同实验体系中的挑战因素(如大肠杆菌、TNF-α、LPS、氧化应激)、观测指标(如TEER、FITC-dextran通透性、紧密连接蛋白定位、炎症因子谱)和给药形式(活菌、热灭活菌、上清、菌体裂解物)都可能导致不同结论。因此,实际应用中仍需逐株验证其作用机制和可重复性,并明确其“预防型”、“抗炎型”或“修复型”的屏障支持作用。
本文将探讨衰老对结肠的影响,重点围绕益生菌是否能够改善肠屏障功能的临床证据,从结局指标和证据强度等方面进行梳理,尤其关注现有的随机对照试验,并总结不同菌株的具体功效及适应证,提出应用建议和研究展望。
01
衰老和结肠老化
随着年龄增长,身体各个器官以不同的速度衰老。这些变化跨度极大,可能只是轻微的外貌改变,也可能是严重的功能障碍,进而导致疾病、生活质量降低和死亡率增加。
脆弱的消化道:对衰老尤为敏感
在全球范围内,65岁及以上人群(本文定义的“老年人”)中消化系统疾病发病率显著上升。衰老波及整个消化系统,程度不一,其中结肠似乎最容易受累。常见的相关疾病包括憩室病、结直肠癌、显微镜下结肠炎及慢性便秘,都是老年人常见的问题。
结肠不同部位老化不一样,研究有挑战
虽然这些疾病发病率很高,但科学界直到最近才开始重视人类结肠衰老的分子机制研究。研究老化的结肠特别具有挑战性。因为结肠像一个复杂的工厂,不同区段(升结肠、降结肠等)的结构和功能差异巨大,导致它们老化的方式也不尽相同。
此外,结肠包含多种细胞,每种细胞的老化路径都不同,再加上肠道菌群和局部免疫系统等外部因素的干扰,这让研究变得更加困难。
下面我们将从微观层面详细拆解:
上皮:脆弱的第一道防线
结肠的腔面面积约为2平方米,由结肠黏膜覆盖,黏膜由单层柱状上皮和结缔组织构成,上皮层向结缔组织内凹陷形成隐窝(Lieberkühn 腺)。
结肠的隐窝中有多能干细胞,负责快速更新肠细胞。这些细胞在3~4天内完成生命周期,最终脱落到腔内。(读过我们文章的可能了解,这个干细胞的更新需要短链脂肪酸,尤其丁酸,所以缺乏膳食纤维以及产丁酸菌会影响结肠隐窝底部的干细胞更新)
隐窝结构的老化
研究发现,老年人的隐窝可能会缩短,但是否这是结肠老化的普遍特征仍需进一步验证。
结肠上皮必须提供强大的屏障功能,允许选择性吸收水分、电解质和短链脂肪酸。屏障功能由紧密连接和粘附连接维持,任何功能障碍都可能导致与年龄相关的疾病加重,例如炎症性肠病(前面谷禾的文章也讲了很多关于肠道屏障的文章,其中上皮的构成紧密连接起到关键作用,相关阅读:什么是肠道屏障,影响因素,监测评估以及如何治疗干预 )。
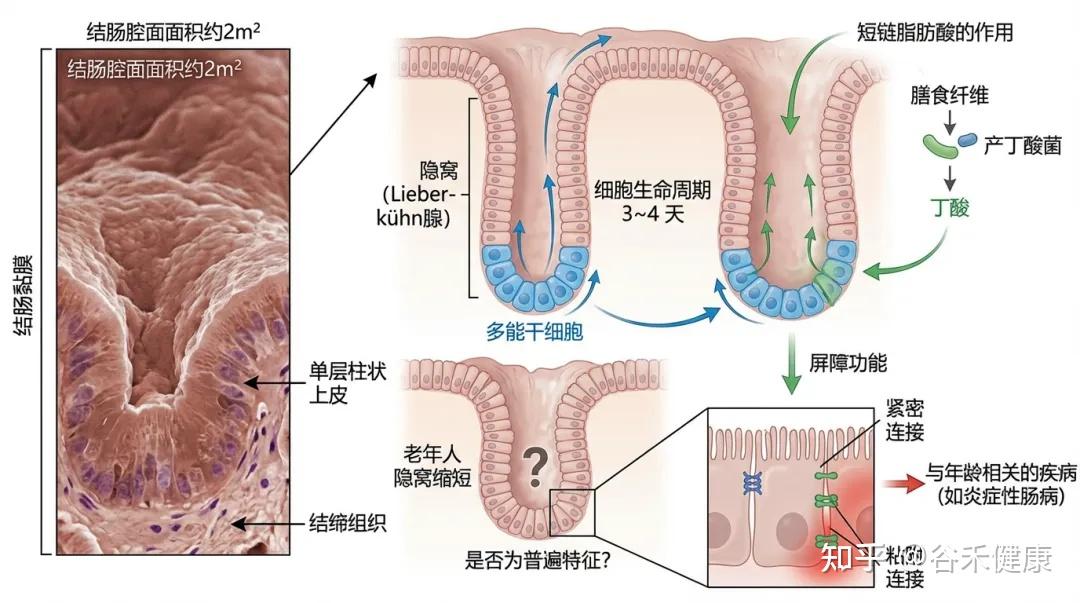
研究显示,老年灵长类动物(非人)的结肠中,紧密连接蛋白显著减少,而在不同解剖区域的变化也存在差异。这表明,结肠的老化特征可能因部位而异。
杯状细胞的变化:为何重要?
衰老还影响结肠上皮的分泌成分。研究发现,老年小鼠的杯状细胞数量显著下降,伴随分泌功能受损。这些变化与慢性低度炎症及氧化应激有关,导致结肠屏障功能减弱(有兴趣可以翻翻以前关于肠道屏障的文章,影响因素以及干预等)。
在像结肠上皮这样的高复制组织中,组织的老化与结肠干细胞的老化密切相关,因为干细胞对于维持上皮的稳态至关重要。
干细胞老化的内外因素是什么?
影响结肠干细胞老化的因素可分为内因和外因。内因包括干细胞的基本特性和突变率,外因则涉及复杂的信号通路。例如,老年大鼠表现出表皮生长因子受体(EGFR)的基础活化增加,这可能与对TGF-α的敏感性增加有关。
Wnt信号在衰老中的作用:如何影响干细胞功能?
Wnt信号通路在维持干细胞功能中起着关键作用。研究发现,衰老小鼠的肠道干细胞中Wnt3水平降低,添加Wnt3可以恢复其形成类器官的能力。这表明Wnt信号在肠道衰老中扮演着重要角色。
内分泌细胞的功能:为何不可忽视?
尽管内分泌细胞在结肠上皮中所占比例不到1%,但它们在调节结肠运动和分泌中发挥着重要作用。老年小鼠的研究显示,肠内分泌细胞的数量显著增加,可能是对年龄相关受体抗性的补偿。
老年小鼠与人类的比较:有什么不同?
在人类乙状结肠中,尽管感觉神经密度降低,肠嗜铬细胞的数量却保持稳定。这表明老年结肠可能存在代偿性神经免疫适应。
表观遗传重塑与衰老:如何影响癌症风险?
衰老是结直肠癌的主要风险因素,结肠粘膜的表观遗传重塑可能是生理衰老与肿瘤发生之间的重要联系。研究发现,正常结肠粘膜中存在年龄相关的甲基化变化,这些变化可能导致癌症的发生。
表观遗传时钟的研究:如何评估衰老?
通过分析334份结肠粘膜样本,研究发现不同的表观遗传时钟与实际年龄之间存在强烈相关性。这些发现表明,功能失调而非加速的表观遗传衰老可能促进肿瘤易感性。
衰老结肠中的表观遗传漂移不仅反映了被动的分子磨损,更是一个塑造组织脆弱性的主动过程。受区域和环境因素影响的表观遗传衰老失调,可能是生理衰老与结直肠肿瘤发生之间的关键机制。
小 结
随着年龄的增长,身体各个器官就像老旧的机器,以不同的速度磨损,消化系统尤其敏感。65岁以上的人群中,结肠问题频繁出现,比如憩室病和结直肠癌,成为老年人常见的健康隐患。研究发现,结肠的不同部分衰老方式各异,内部细胞和微生物的互动让问题更加复杂。结肠上皮的脆弱性与干细胞老化和慢性炎症有关,这不仅影响消化,还可能增加癌症风险。了解这些变化,有助于减缓衰老带来的影响,提升生活质量。
在我们身体的消化系统中,结肠扮演着至关重要的角色。它的推进运动依赖于神经元与平滑肌细胞的精密协调。然而,随着年龄的增长,这种协调性逐渐受到影响,结肠的功能也随之下降。这一过程涉及复杂的生物机制,值得我们深入探讨。
神经网络的角色
结肠的神经网络是自主神经系统的重要组成部分,主要分布在以下两个区域:
这些神经元通过信号传递来调节肠道的运动和分泌,确保消化过程的顺利进行。
衰老对神经元的影响
研究发现,结肠中的神经元随着年龄的增长表现出不同的退行性变化:
-数量减少
胆碱能神经元(兴奋性)数量显著下降,而氮氧化酶神经元(抑制性)数量变化较小。
-形态变化
肠神经元的形态变化高度异质,且结肠周径的增加可能导致神经元密度的稀释效应。
这些变化意味着,尽管神经元的数量在减少,但观察到的密度下降可能并不完全反映真实的细胞损失。
在对13名成人尸检样本的分析中(<35岁 n=6;>65岁 n=7),研究者发现老年人肌间神经元总体减少。此外,另一项对16名患者(33-99岁)降结肠和乙状结肠的研究显示,Hu阳性和ChAT阳性神经元选择性丧失,而nNOS阳性神经元保持相对稳定。
有趣的是,最大规模的研究发现,肌间神经丛中的神经元总数随衰老并无显著变化。但在老年个体的升结肠中,ACh阳性神经细胞体数量却增加,这可能是由于轴突功能障碍导致神经递质在细胞体中积累。
神经支配的变化
结肠不仅受到内在神经元的支配,还受到来自交感神经和副交感神经的广泛外在神经支配:
随着年龄的增长,迷走神经和盆腔副交感神经的结构也经历了退化,影响了肠道的正常功能。
神经营养信号与细胞衰老
衰老过程还显著影响神经营养信号通路。研究表明,GDNF、RET和NOS1的表达在衰老过程中发生变化,提示营养支持的减少可能导致神经元维持能力的下降。此外,慢性衰老标志物p16的表达在老年患者的升结肠中增加,而在降结肠中未见类似变化。
胶质细胞的变化
肠道胶质细胞(EGCs)同样随着年龄的增长经历了结构重塑。尽管SOX10阳性肠道胶质细胞体的数量保持稳定,但S100阳性胶质细胞突起的密度显著下降。这种变化可能影响神经与胶质细胞之间的交流,从而损害神经肌肉协调能力。
小 结
随着年龄的增长,结肠的神经元和平滑肌细胞发生了明显变化。研究发现,兴奋性神经元数量减少,而抑制性神经元相对保留。神经元密度的下降可能是因为结肠周围的组织变大了。此外,衰老还影响了神经营养信号,导致神经元的维持能力下降。肠道胶质细胞也经历了结构变化,虽然数量保持不变,但功能可能受到影响。这些变化共同导致结肠的运动能力和整体健康下降。
结肠平滑肌细胞的作用是什么?
结肠中的平滑肌细胞(SMC)负责产生推进运动,并通过基线张力维持器官的结构完整性。收缩可以通过神经递质(乙酰胆碱,ACh)的化学方式或通过机电耦合来启动。在这两种情况下,收缩最终由钙离子从细胞外间隙和肌浆网流入细胞质来介导。这种钙内流激活肌球蛋白轻链激酶(MLC 激酶),它磷酸化肌球蛋白轻链(MLC),从而触发肌肉收缩。
年龄增长如何影响ACh的反应?
随着年龄的增长,ACh的作用似乎发生了变化。对老年大鼠和狒狒的多项研究表明,来自老年动物的结肠平滑肌细胞对ACh的收缩反应减少,或在接触ACh拮抗剂时放松受损。
在老年个体中,从升结肠分离的肌肉条对电场刺激表现出增强的放松反应,而降结肠的肌肉条则没有表现出类似的变化。
这些发现表明,衰老可能在结肠内引发区域特异性的神经肌肉功能改变,其中抑制通路在近端部分似乎被选择性增强。由于抑制性肠神经元的数量和功能能力在衰老过程中保持稳定,因此推测局部的胆碱能功能障碍可能是观察到的放松增强的根源,且这种障碍仅限于老化的升结肠。
钙稳态变化与胆碱能功能障碍:有什么联系?
关于结肠平滑肌细胞中钙稳态的年龄相关变化也有证据。在从老年大鼠的远端结肠提取的细胞中,细胞质钙水平减少,而钙则在线粒体和肌浆网中积累。
总体而言,观察到的结肠中的年龄相关变化似乎与其他器官中的平滑肌细胞变化相呼应。结肠平滑肌细胞是否存在特定于结肠的与衰老相关的变化仍需进一步研究。
小 结
结肠平滑肌细胞的主要功能是帮助推动食物并保持结肠的形状。随着年龄的增长,这些细胞对一种叫乙酰胆碱的神经递质的反应变得不如以前强,尤其是在升结肠部分,它们更容易放松。这种变化与细胞内钙的平衡失调有关,表明衰老可能导致结肠的神经和肌肉功能发生特定区域的变化。
结肠里的免疫细胞有哪些?
结肠里的免疫细胞很多,主要集中在肠壁表面上皮细胞的下方(称为固有层),包括:
在上皮层内部还有一类“上皮内淋巴细胞”(IEL),以T细胞为主。结肠里“浆细胞”也很多,它们主要分泌IgA抗体(对肠道微生物的选择性定植非常关键),用来在肠道表面“温和地管住细菌”。其中大约90%是IgA2这一类型。
老年人的免疫系统:更易出现慢性炎症
老年人更容易出现“低度、长期”的炎症状态。衰老常见的特征之一是全身长期的低水平炎症,被称为“炎症衰老”。在结肠里也能看到类似现象:免疫系统更容易处在被激活状态,例如一些促炎信号分子增加(如IL-1β、IL-6、IL-17、TNF-α等),B细胞和T细胞也更活跃。
一种可能机制:黏液“隔离层”变弱,细菌更靠近肠壁,引发炎症。
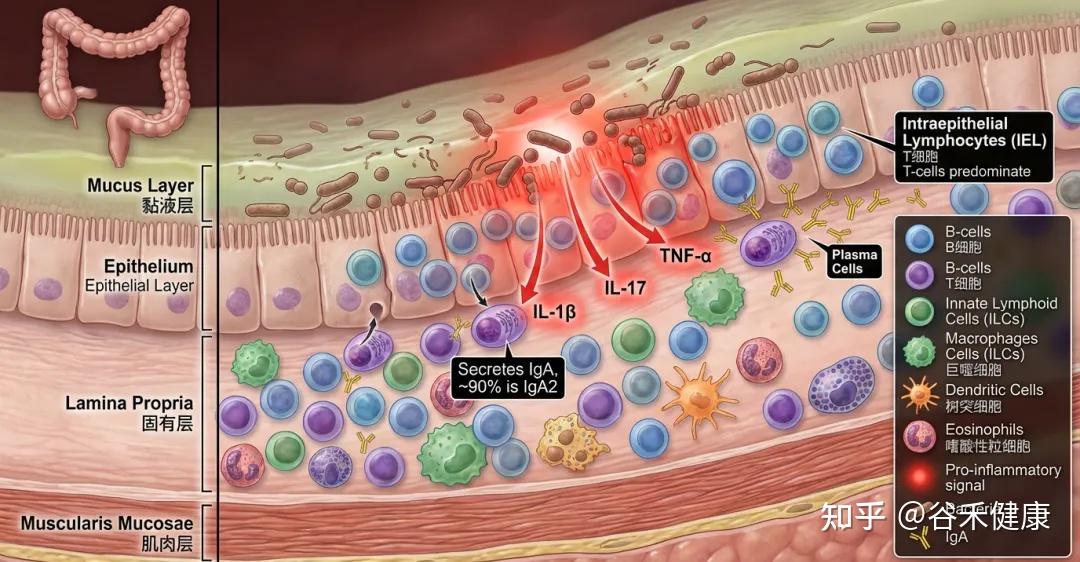
黏液层的保护作用:为什么会变弱?
在衰老小鼠中,细菌更容易钻进这层本该相对干净的内层黏液,从而触发免疫反应和炎症。
进一步的链条可能是:衰老相关地出现一种小RNA(miR-124–3p)表达升高,它会抑制一种关键酶(T合成酶),这会影响MUC2这种黏液主要成分的“糖基化”(可以理解为:黏液蛋白需要正确“挂糖”才能形成坚固有效的保护层)。
免疫细胞的局部差异:老年小鼠的观察结果
研究人员用单细胞技术,对比了年轻和老年小鼠的结肠免疫细胞发现:老年小鼠结肠里“免疫细胞大类的比例”整体看起来变化不大。但如果把结肠按不同部位拆开看,就会发现明显的“局部差异”。
具体来说:
在盲肠和结肠远端(更靠近直肠的一段),老年小鼠的 T 细胞更容易处于被激活的状态,提示局部免疫反应更“紧绷”。
在结肠近端(更靠近小肠的一段),老年小鼠的 B 细胞和浆细胞更多。浆细胞是负责大量分泌抗体的细胞。
Cdc42基因的变化:与衰老有什么关系?
还有一个值得注意的发现:老年小鼠的 B 细胞里,Cdc42 这种基因/蛋白的表达更高。Cdc42 与干细胞衰老有关(包括造血干细胞和肠道干细胞),在人类老年人的血细胞中也发现会升高。这提示结肠局部免疫系统的老化变化,至少有一部分和血液中观察到的免疫老化现象是同方向的。
免疫系统衰老通常表现为免疫能力下降:更容易感染、肿瘤风险上升,也更可能出现免疫紊乱(包括自身免疫问题)。
研究结果显示,老年小鼠结肠免疫系统存在局部差异,反映出免疫功能的复杂变化及其对健康的影响。免疫能力下降导致肠道屏障脆弱,可能引发健康问题。因此,探索益生菌等干预手段以调节肠道功能、改善免疫状态和增强屏障功能显得尤为重要。接下来,我们将深入探讨益生菌对肠道健康的调节作用。
益生菌指的是“在适当剂量和适当组合下,能为所给生物体(如人类)带来健康益处的活微生物”。这些细菌长期被证明通过促进粘液层的形成、分泌抗菌因子、竞争性地粘附肠道上皮细胞以及增加紧密连接形成来调控肠道上皮功能。
益生菌通过多种机制调节肠道屏障功能,主要包括以下几个方面:
增强紧密连接结构
益生菌可通过上调紧密连接蛋白的表达来增强机械屏障功能。例如,研究发现某些乳杆菌和双歧杆菌菌株可增加occludin、claudins和ZO-1的表达,从而加固紧密连接结构,降低肠道通透性。
抑制炎症反应
慢性炎症是导致肠道屏障功能障碍的主要原因之一,而益生菌可通过多种途径抑制炎症反应:
特别值得一提的是,益生菌还可通过激活过氧化物酶体增殖物激活受体γ(PPARγ)来发挥抗炎作用。PPARγ是一种核受体,可调节炎症反应和细胞分化,某些益生菌菌株可通过激活PPARγ来保护肠道屏障功能。
调节肌球蛋白轻链激酶(MLCK)通路
肌球蛋白轻链激酶(MLCK)是调节紧密连接通透性的关键酶。炎症因子可通过激活MLCK,导致肌球蛋白轻链磷酸化,进而破坏紧密连接结构。益生菌可通过抑制MLCK表达或活性来保护肠道屏障。
例如,罗伊氏乳杆菌可通过下调MLCK表达,减轻肠毒素诱导的肠道屏障功能障碍。这一机制在预防和治疗感染性腹泻中具有重要意义。
激活模式识别受体
益生菌可通过与肠道上皮细胞表面的模式识别受体(PRRs)相互作用来调节肠道屏障功能。其中,Toll样受体2(TLR-2)是研究较多的受体之一。
研究发现,某些益生菌菌株可通过激活TLR-2,触发下游信号通路,促进紧密连接蛋白表达和抗炎因子产生。例如,双歧双歧杆菌BB1可通过TLR-2/p38 MAPK通路增强肠道屏障功能,同时抑制NF-κB激活,发挥双重保护作用。
调节肠道菌群平衡
益生菌作为肠道生物屏障的重要组成部分,可通过以下方式调节肠道菌群平衡:
肠道菌群平衡的恢复可减少有害菌对肠道屏障的破坏,同时增加有益菌的保护作用,形成良性循环。
改善消化功能
益生菌可促进食物消化和营养吸收,缓解多种消化问题:
调节免疫功能
肠道是人体最大的免疫器官,益生菌可通过调节肠道免疫细胞活性来增强全身免疫功能:
这些作用使益生菌在预防感染、过敏和自身免疫性疾病方面具有潜力。
影响代谢和体重管理
近年来研究发现,益生菌还可能通过”肠-脑轴”和代谢调节影响体重和代谢健康:
虽然这一领域的研究仍在深入,但已有证据表明某些益生菌菌株可能有助于预防肥胖和代谢综合征。接下来,我们将具体探讨哪些益生菌对肠道健康和代谢调节具有积极影响,以及它们如何在改善整体健康方面发挥作用。
乳杆菌属是发酵食品生产中最广泛使用的益生菌之一,这些食品来源包括动物(例如牛奶和肉类)和植物(例如蔬菜和谷物)。
乳杆菌属包括一大类异质的革兰氏阳性兼性厌氧菌,包括嗜酸乳杆菌(L.acidophilus) 、鼠李糖乳杆菌(L.rhamnosus)、发酵酵母菌(L.fermentum)、干酪乳杆菌(L.casei)、植物乳杆菌(L. plantarum)、瑞士乳杆菌(L. helveticus)、罗伊氏乳杆菌(L. reuteri)
除了在食物发酵中的作用外,乳杆菌属还因物种、宿主年龄或肠道位置不同而异,是人类和动物消化系统中健康的组成部分。
动物研究和临床前结果表明 ,乳杆菌可能有助于预防和治疗多种胃肠道疾病。这些疾病包括肠道感染、抗生素相关腹泻、早产儿 NEC、炎症性肠病、结直肠癌和肠易激综合征。
多项研究证实 ,乳杆菌在消化系统疾病管理中发挥重要作用,通过体外和体内维持上皮屏障完整性。该功能的多种机制包括调节细胞骨架、诱导粘液生成以及紧密连接蛋白的磷酸化,这些都会增强紧密连接功能和免疫反应,同时预防上皮细胞凋亡。
以下总结了乳杆菌的不同菌株及其在肠道健康中的作用。
✧ Lactobacillus amylophilus D14
研究发现,把Lactobacillus amylophilus D14 加到健康状态的肠道细胞(Caco-2)上时,细胞之间的紧密连接通透性不会发生变化,也就是不会让屏障变得更松或更紧。
但如果这些细胞先被致病菌(肠源性大肠杆菌 K88 或鼠伤寒沙门氏菌 SL1344)弄伤,D14 就能起到保护作用,它可以减少关键连接蛋白(ZO-1、claudin-1、E-cadherin)的受损,从而帮助维持紧密连接和屏障功能。其原因可能是 D14 抑制了细胞内的 ERK 信号通路活化(ERK 的磷酸化降低),并减少炎症因子 IL-8 的释放,进而减轻炎症和屏障破坏。
✧ 嗜酸乳杆菌 (Lactobacillus acidophilus)
嗜酸乳杆菌 (Lactobacillus acidophilus) 表面有一种特殊的“外衣蛋白”,叫表面层蛋白(Slp)。
嗜酸乳杆菌的外衣蛋白有什么作用?
研究发现,这种蛋白对肠道有多方面的保护作用,比如:
抢先占住肠道黏膜上的“附着位点”,让有害菌不容易黏上去,帮助肠道细胞减少不必要的凋亡(细胞过早死亡),降低脂多糖(LPS,常见于某些细菌成分)引发的炎症反应。
Slp如何增强肠道屏障?
在细胞实验中,研究人员把Slp作用在Caco-2细胞(常用来模拟肠道上皮的细胞模型)上,发现它能让肠道屏障更牢固,表现为:
注:TER可以理解为用电学方法测试上皮细胞层“漏不漏”。TER越高,说明细胞之间的连接越紧密、屏障越强;TER越低,说明屏障受损、变漏了。
不同菌株的效果差异明显
一项研究比较了20多种益生菌(不同物种和不同“菌株”)对肠道屏障的影响,重点看它们能不能把肠道上皮细胞之间的紧密连接变得更牢。
结果发现嗜酸乳杆菌整体上能明显增强这种封口功能,但同一种细菌的不同菌株效果差很多。
LA1:效果最好,增强幅度接近翻倍
LA2:只有大约一半的提升
LA3:几乎没有影响
这说明:益生菌不能只看“是什么菌”,还要看“是哪一株”。
LA1的保护机制是什么?
进一步研究显示,LA1之所以有效,是因为它能被肠道免疫系统表面的识别开关(TLR2与TLR1/6组成的受体组合)识别并触发信号,从而加强屏障。用小鼠实验也看到:在正常小鼠中,LA1可以减轻一种用DSS诱导的结肠炎;但在缺少TLR2的敲除小鼠里,这种保护作用就消失了,说明LA1的效果离不开TLR2这条通路。
注:TLR-2 指 Toll 样受体 2(Toll-like receptor 2),是一种先天免疫的模式识别受体(PRR),常表达在肠上皮细胞和免疫细胞表面,用来识别微生物成分并触发信号通路。
不同细胞中的信号通路有何不同?
最近的研究发现,同一种乳酸菌成分(LA1)在不同细胞里“走的通路”不一样,所以产生的效果也不一样。
在免疫细胞里LA1会通过TLR-2这类警报器启动经典的炎症信号通路(依赖MyD88),进而激活NF‑κB,让免疫细胞更容易进入应战状态。这属于比较符合预期的免疫激活反应。
在肠道上皮细胞里LA1同样需要TLR‑2,但不走MyD88这条路,而是改走PI3K通路。结果不是“点火”,而是“刹车”——它能抵消TNF‑α这种炎症因子造成的肠道紧密连接变松、通透性升高的问题,从而降低NF‑κB和MLCK等会破坏屏障的分子活性,帮助肠道屏障更稳。
其他乳杆菌的表现如何?
L. acidophilus W37:让TER提高约15%,说明屏障更“紧”。
L. brevis、L. casei:对TER没明显影响。
注:Caco‑2 是来源于人结肠腺癌的上皮细胞系。它常被用来在体外建立“肠上皮屏障模型”,因为在 Transwell 等培养条件下会分化成类似小肠吸收上皮的单层细胞,形成紧密连接,能模拟肠屏障的通透性变化。
常用指标:TER/TEER(跨上皮电阻)和 TER/TEER,以及分子通量(如葡聚糖/荧光葡聚糖)。
有研究发现,嗜酸乳杆菌分泌的一些代谢产物,能让肠道细胞之间的“缝隙”变得更紧:细胞屏障的紧密度指标(TER)会小幅上升(约25%),而一些大分子(比如葡聚糖)从细胞间漏过去的量会减少。进一步看机制,这种乳杆菌的“培养上清液”(相当于它在培养液里释放的各种物质)能抑制炎症信号通路NF-κB的激活,并把紧密连接相关蛋白(如occludin、claudin-1)的状态恢复到更正常,从而防止炎症因子IL‑1β导致的肠道屏障“变漏”。
热灭活的嗜酸乳杆菌还有用吗?
有报告指出,即使把嗜酸乳杆菌加热杀死(热灭活),它本身以及它的上清液也能在另一种肠道细胞模型(HT‑29)里减轻阿司匹林造成的屏障损伤,主要和调节紧密连接蛋白ZO‑1的表达与位置有关。
Lcr35对肠道屏障的保护作用如何?
为了研究另一株乳杆菌Lcr35对肠道屏障的保护作用,研究人员用Caco‑2细胞在体外搭了一个“肠道屏障模型”,并在细胞下方放入免疫细胞(PBMC)模拟免疫环境。然后用沙门氏菌的LPS(会引发炎症的细菌成分)去刺激细胞,模拟感染带来的炎症损伤。结果是:只用LPS会让屏障变差;但在LPS刺激后再加入Lcr35,并培养到48小时,屏障紧密度(TER)明显回升,比仅LPS组高了87%。这提示Lcr35可能帮助修复被LPS破坏的肠道屏障、减少“肠漏”。
Lcr35如何影响炎症反应?
此外,Lcr35 还能明显减少一种炎症信号分子 IL-8 在“肠上皮细胞 + 免疫细胞(PBMC)”共培养体系中向基底侧(相当于体内朝向血液的一侧)释放,说明它有助于降低炎症反应。
干酪乳杆菌(Lactobacillus casei)
最近有研究专门看了干酪乳杆菌(Lactobacillus casei,简称 L. casei)对“肠道屏障受损”的保护作用,并探讨是否和肥大细胞有关。
结果发现:和对照相比,干酪乳杆菌能让猪肠上皮细胞的“电阻值(TER)”提高约 60%(电阻越高通常表示屏障越紧密),同时让大分子(葡聚糖)的渗漏减少 80% 以上。面对会引发腹泻的致病菌产肠毒素性大肠杆菌 K88(ETEC K88)时,干酪乳杆菌能减轻肠屏障变漏的情况,关键在于它能阻止紧密连接相关蛋白(occludin、claudin-1、ZO-1)以及免疫识别相关受体(TLR-2、TLR-4)的表达被病原体“压低”。
L. casei DN-114 001
更早的研究也发现,L. casei DN-114 001 的“菌体裂解物”(把菌体打碎后的成分)可以在小鼠 DSS 诱导的肠炎模型中起到保护作用,带来健康收益。L. casei 能抑制 DSS 导致的肠道渗漏增加,这与它降低炎症因子 TNF-α 和 IFN-γ、并改变肠道菌群组成有关。
还有研究发现,L. casei DN-114 001 在 T84 肠上皮细胞中也能对抗肠致病性大肠杆菌(EPEC)感染带来的类似屏障损伤。
L. casei CRL 431:减少感染损伤
比较了不同乳杆菌对抗沙门氏菌感染的效果,发现:
在他们测试的菌株里,只有 L. casei CRL 431 能明显起到保护作用:表现为肠屏障功能更好、局部炎症更低,从而减少感染损伤。
有研究认为,起保护作用的是活菌,不是培养上清液
活的 L. casei 可以防止 TNF-α 和 IFN-γ 导致的 TER 下降。机制上,它可能通过激活 MAPK/PI3K/Akt 这类细胞信号通路、提高 TLR-2 表达,并保护 Caco-2 细胞中 ZO-1 蛋白的水平,从而避免炎症因子引起的通透性升高。
✧ 植物乳杆菌(Lactobacillus plantarum)
有研究发现,植物乳杆菌(Lactobacillus plantarum)以及它产生的一些成分,可能通过修补肠道屏障来减轻肠道炎症(比如溃疡性结肠炎模型中的结肠炎)。如果肠道屏障损伤,肠道通透性升高,细菌或毒素更容易“漏过去”,炎症就会加重。
下面是这些研究想说明的要点:
研究提示这种保护作用和 STAT3 这个细胞信号“开关”有关:如果在细胞实验里把 STAT3 敲低,再用 EPS116 处理,ZO-1 和 occludin 就上不去,肠道通透性反而变高。说明 EPS116 需要通过 STAT3 才能更好地“加固屏障”。
植物乳杆菌可在感染情况下保护肠道屏障
在人正常结肠上皮细胞模型(NCM460)中,植物乳杆菌能减轻 ETEC(产肠毒素大肠杆菌)感染对屏障的破坏。还有研究显示它能增强 NK 细胞产生 IL-22(一种有助于黏膜修复和屏障保护的免疫因子),即使在 ETEC 感染时也能帮助维持紧密连接屏障。
不同菌株对屏障电阻提升明显
屏障电阻(TER)可以粗略理解为细胞单层的密封程度指标:TER 越高,说明屏障越紧密、渗漏越少。
L. plantarum DSM 2648:让 Caco-2 细胞 TER 比对照提高约 235%;还能显著抵消致病性大肠杆菌(EPEC)对 TER 的破坏,并减少 EPEC 黏附。
L. rhamnosus HN001:也能提高 TER(约 148%)。
L. plantarum MB452:在 10 小时内让 TER 随剂量增加,最高比对照高约 60%;同时提高 ZO-1 和 occludin 的表达。
植物乳杆菌 HY7714 可能通过关掉炎症通路,保护紧密连接
在TNF-α(强促炎因子)处理的 Caco-2 单层模型里,HY7714 能保护 ZO-1、claudin-1、occludin 不被破坏。它还抑制一些与炎症和屏障破坏相关的信号(如 NF-κB、MLCK 等)被 TNF-α 诱导升高,提示其可能通过降低炎症信号来维持屏障完整。
植物乳杆菌 LR002 改善小鼠溃疡性结肠炎
修屏障 + 抗炎 + 调菌群。在 DSS 结肠炎/UC 模型中,LR002 能恢复紧密连接蛋白(ZO-1、Occludin、Claudin-3)的水平。同时降低促炎因子、减少氧化应激;调节肠道菌群,并让短链脂肪酸(SCFA,肠道有益代谢物)水平回升。
机制上可能与激活PPARγ信号、抑制 MAPK/NF-κB 炎症通路有关。
这些研究总体指向同一件事——某些植物乳杆菌菌株或其代谢产物,可能通过增强紧密连接蛋白、降低炎症信号、改善菌群与代谢物,来减少“肠漏”和肠道炎症;不同菌株差别很大;人体研究里未必能直接看到“阻止肠漏”的效果,但在组织/细胞与动物模型中,某些植物乳杆菌确实能增强紧密连接、减轻炎症、提高屏障相关指标。
扩展阅读:
客观认识植物乳杆菌 (L. plantarum) 及其健康益处
✧ 鼠李糖乳杆菌(Lactobacillus rhamnosus)
鼠李糖乳杆菌 LGG 在儿童克罗恩病中的初步研究
较早的研究把一种常见益生菌——鼠李糖乳杆菌 LGG——用于儿童克罗恩病(CD)。结果发现:肠漏明显改善(用尿液中的双糖通透性试验来测),疾病活动度也下降了。但可惜的是,这种改善在随访到 24 周时没有持续下去。
特定菌株 CNCM I-3690 的保护机制
后来又有研究指出:鼠李糖乳杆菌的某个特定菌株 CNCM I-3690,在小鼠炎症模型里能保护肠道屏障。它可以阻止炎症因子 TNF-α 让肠上皮细胞“缝隙变大”(表现为电阻下降),还会影响杯状细胞和黏液层(相当于让肠道表面的保护胶层更稳)。
小鼠的结肠基因表达分析还显示,这个菌株可能通过抑制某些体内蛋白酶,来增强一批与健康肠道屏障相关的基因活动,比如与营养吸收、细胞更新和防护功能有关的基因。
体外实验支持 LGG 的保护作用
很多体外实验(细胞/类器官实验)也支持:活的 LGG 对紧密连接有保护作用,能让屏障在炎症或病原体攻击时更不容易被破坏。
用 TNF-α 和 IFN-γ 模拟炎症攻击 Caco-2 细胞时,活 LGG 可以减轻屏障受损,可能与抑制 NF-κB、ERK1/2 等炎症通路有关;而一些其他乳杆菌即使用更高浓度,也未必能达到同样效果。
在人肠道类器官实验中,活 LGG 能防止 IFN-γ 把关键的紧密连接蛋白压下去。
在“麦醇溶蛋白”(与小麦相关蛋白)诱导屏障变漏的模型中,LGG 能把屏障功能拉回去;不仅活菌有效,热杀死的菌体和它的培养上清(菌分泌/代谢产物的混合物)在某些实验里也显示出一定恢复效果。
在细菌感染中的保护作用
细胞先用活 LGG 处理后,再感染肠出血性大肠杆菌(EHEC O157:H),可以减轻屏障电阻下降、通透性升高,并阻止紧密连接蛋白(如 claudin-1、ZO-1)被“挪位/打散”。但热灭活 LGG 在这类实验里往往效果不明显,提示“活菌状态”可能很关键。
其他不同的 L. rhamnosus 菌株也各有差异
有的本身对屏障指标影响不大,但在大肠杆菌攻击时能起到保护;有的能抑制 TNF-α 造成的损伤并减少 IL‑8(炎症信号)上升,但它的培养上清却未必有效。
总结来说,不少实验提示某些鼠李糖乳杆菌(尤其是 LGG 及特定菌株)可能通过稳定紧密连接、维持黏液层、调节炎症信号等方式,帮助肠道不那么容易漏。但不同菌株、活菌/灭活、以及人体长期效果差异很大;早期儿童克罗恩病研究里也出现了短期改善、长期不一定维持的情况。
✧ 发酵乳杆菌(Lactobacillus fermentum)
发酵乳杆菌 AGR1487
和其他益生菌菌株不一样,发酵乳杆菌 L. fermentum 的 AGR1487 这一株在肠上皮细胞模型(Caco-2)里会削弱屏障:给得越多,细胞层的电阻(TER,常用来衡量屏障是否紧密)下降得越明显,说明细胞之间的封条变松了。
但有趣的是,如果不把细菌本身加进去,而是加入它培养后留下的上清液(可以理解为细菌分泌物/代谢产物的混合液),反而会让TER比对照培养基提高约34%,也就是屏障变得更紧。
AGR1485的不同表现
相比之下,同一物种的另一株 AGR1485(无论是细菌本体还是上清液)对TER基本没影响。
另外,AGR1487 还会让甘露醇更容易穿过细胞单层(甘露醇通量增加),这通常意味着屏障通透性变高、漏得更多;而 AGR1485 不会造成这种变化。
这意味着即使是同一种乳杆菌,不同菌株也可能作用完全不同。AGR1487 会以不利于紧密连接屏障的方式改变细胞内相关基因和蛋白(包括微管蛋白及其相关蛋白)的水平,最终导致肠道屏障功能变差。
✧ 罗伊氏乳杆菌(Limosilactobacillus reuteri)
最近一些研究发现,某些罗伊氏乳杆菌(Limosilactobacillus reuteri)可能有助于加固肠道屏障、降低肠漏风险。
高脂饮食小鼠模型中的积极效果
在高脂饮食小鼠中的发现,研究人员从人类母乳中分离到一株罗伊氏乳杆菌(L. reuteri FN041)。把它给高脂饮食(HFD)的小鼠后,发现小鼠原本因高脂饮食而更漏的肠道(肠通透性升高)得到了缓解。
与此同时,一些与炎症相关的物质(如LPS、TNF-α、IL-16)水平下降。肠道屏障的关键“封条蛋白”(紧密连接蛋白,如occludin、ZO-1、claudin-6、claudin-7)在高脂饮食下通常会减少,而FN041能阻止这种下降。研究者认为,这种益处与肠道菌群产生的短链脂肪酸变化有关(研究中提示与短链脂肪酸减少相关)。
对细胞层渗漏的抑制作用
在仔猪肠道细胞+致病菌模型中的发现,使用从健康断奶仔猪粪便中分离的罗伊氏乳杆菌,先用它“预处理”肠上皮细胞(IPEC-1),再让细胞感染致病性大肠杆菌ETEC K88。
结果发现:预处理能减少细胞屏障被破坏、降低大分子(如葡聚糖)穿过细胞层的渗漏。但如果只用罗伊氏乳杆菌而不感染细菌,效果不明显或较弱。机制上,这种保护与维持紧密连接蛋白(尤其ZO-1、occludin)有关,并且可能通过MLCK相关通路来实现。也有研究观察到:单独用罗伊氏乳杆菌处理时,细胞层的渗漏指标甚至可降低约25%。
不同菌株的效果略有差异
处理IPEC-J2细胞10小时后,细胞层的电阻(TER,数值越高通常代表屏障越紧)只小幅上升约8%,并伴随claudin-1、occludin、ZO-1轻度增加。更重要的是,在LPS(内毒素)刺激下,这株菌的活菌或培养上清都能阻止紧密连接蛋白被下调,同时抑制炎症因子(TNF-α、IL-6)过度升高。
它也能让TER上升约10%,并减少ETEC导致的屏障变漏。
研究者还发现另一种益生菌詹氏乳杆菌(Lactobacillus jensenii)也能在ETEC攻击时起保护作用,但在没有感染压力时,单独使用对屏障影响不明显。它们的保护效应可能与提升热休克蛋白HSP-27以及增加ZO-1有关,意味着这个菌株是发挥感染压力下的保护作用,而不是预防或维持作用。
扩展阅读:
认识罗伊氏乳杆菌(Lactobacillus reuteri)
✧ 唾液乳杆菌 (Lactobacillus salivarius)
L. salivarius SMXD51处理Caco-2细胞24小时后,可使跨上皮电阻(TER)提高约20%;同时还能对抗铜绿假单胞菌PAO1引起的TER下降,起到保护肠道屏障的作用。这种益生与保护效果被认为与上调F-肌动蛋白细胞骨架有关。
进一步比较了不同L. salivarius菌株对过氧化氢(H₂O₂)造成的屏障损伤的保护能力。在检测的33株菌中,UCC118和CCUG38008能通过依赖ERK1/2磷酸化的途径,减轻H₂O₂导致的紧密连接(TJ)蛋白(ZO-1、occludin、claudin-1和JAM)的降解与错位;而无效菌株AH43324则没有这种作用。
在迄今为止报道的各种益生菌细菌中,Bifidobacterium spp.是研究最广泛和使用最广泛的益生菌细菌之一。双歧杆菌属属于放线菌门,目前包括80个(亚)种,它们分布在不同的生态位,包括人类的胃肠道,口腔等。
双歧杆菌属是最早定植人类肠道的细菌,与母乳衍生的低聚糖有关。因此,它们占母乳喂养婴儿肠道中微生物占比很高。B. breve、B. bifidum、B. longum、Bifidobacterium infantis是婴儿阶段常见的检测到的细菌,其中B. bifidum是最突出的物种,其次是B. breve、B. longum、B. infantis。
随着年龄的增长,双歧杆菌的总体下降,但在整个成年期保持相对稳定,并在老年时再次下降。成人肠道中常见的物种包括B. adolescentis和B. catenulatum,其次是B. longum 和 B. bifidum。
需要注意的是,并不存在绝对的“婴儿专属种”和“成人专属种”,只是不同年龄段更常见的种类不同。
为什么双歧杆菌被当作益生菌?
双歧杆菌因为被认为较安全(很多菌株具有GRAS地位,意思是通常被认为是安全的),而且与多种健康益处相关,所以被广泛做成益生菌产品。研究中常提到的潜在作用包括:
因为双歧杆菌本来就是人体肠道的常住居民,不少研究认为它对于维持肠道上皮屏障完整性很关键。
一些研究用16S rRNA(常见的菌群测序方法)分析溃疡性结肠炎患者的肠道菌群时发现:双歧杆菌明显减少,尤其是B. bifidum减少更突出。这提示双歧杆菌(特别是B. bifidum)可能与溃疡性结肠炎的发生发展有关,也可能成为一种有参考价值的微生物标志物。
双歧杆菌怎么加固肠道屏障?
在细胞实验中(如Caco-2、HT-29、T-84等肠上皮细胞模型),用某些双歧杆菌先处理细胞,能够减轻多种因素造成的紧密连接损伤。
机制上常见的解释包括:
一个具体例子:B. bifidum BB1菌株
研究发现,B. bifidum 的某个特定菌株(BB1)能以菌株特异性的方式把肠上皮细胞单层的屏障变得更紧(用TER指标衡量,最高可增加50%–80%,TER越高通常表示屏障越紧)。
保护肠道的机制
有研究用DSS(一种常用来在小鼠体内制造结肠炎/肠损伤的化学物质)做肠道损伤模型,发现一株双歧杆菌 B. bifidum FL-228.1 的预防效果最明显。它之所以能保护肠道,主要做了几件事:
不同双歧杆菌的保护效果
其他动物研究也发现,不同双歧杆菌在多种胃肠道疾病模型中都可能对肠屏障有帮助,例如:
NEC(新生儿坏死性小肠结肠炎)模型:B. infantis能减轻肠通透性升高(不那么漏),并更好地维持 occludin、claudin-4 等紧密连接蛋白在细胞连接处的正常分布,从而降低 NEC 发生率。
另一种 NEC 大鼠模型:B. bifidum 也被证明能改善肠道完整性。
DNBS 诱导的轻度肠炎模型:B. animalissubsp. lactis 能把肠道通透性拉回正常水平,机制包括让多种紧密连接蛋白(尤其 claudin-4)恢复正常,同时帮助结肠局部免疫细胞(Th1/Th2)维持更平衡的状态。
DSS 结肠炎模型:不同菌株效果不一样。有研究显示 双歧杆菌的某个菌株(CCM 7952)能维持紧密连接蛋白表达、降低血液中“肠漏”指标(如 FITC-葡聚糖),疾病严重度也更低;但同物种的另一个菌株(Bl 372)却做不到,说明“菌株差异”很关键。
酒精相关肝病与双歧杆菌的菌株特异性
在酒精相关肝病(长期饮酒)方面,很多研究认为:长期饮酒会导致肠道菌群和代谢物失衡,使肠屏障受损、通透性上升;这样细菌内毒素 LPS 更容易进入门静脉循环,激活 TLR4-NF-κB 通路,引发更多炎症因子。
体外实验也发现,双歧杆菌可以在 LPS 处理的肠上皮细胞模型中降低炎症因子(如 IL-6、TNF-α),并上调/稳定紧密连接蛋白(occludin、claudin-3、ZO-1),从而减少细胞间渗漏。
特别需要强调的是:双歧杆菌的作用高度菌株特异性。同属甚至同种的不同菌株,效果可能完全不同,甚至在免疫反应上方向相反。因此,不能因为某一株有效,就推断所有双歧杆菌都有效。
一些更间接的保护方式
B. infantis 的“无菌条件培养上清”(可以理解为它产生的可溶性代谢物混合物)能抑制 NF-κB 炎症通路,减少 TNF-α 等炎症因子,并阻止炎症因子诱导的肠通透性升高。
B. bifidum 通过酶作用产生成分(如半乳寡糖)后,可能减少沙门氏菌对肠道的黏附和侵袭(相当于降低致病菌“粘上去、钻进去”的机会)。
最后,虽然证据很多,说明双歧杆菌对维持肠屏障有益,但分子机制为什么会这样、到底哪条通路最关键,仍然没有完全弄清。
未来研究的挑战与方向
目前有以下主要难点:
1)菌株差异太大,很难用一套机制解释所有双歧杆菌;
2)它们和人体细胞、以及肠道里其他微生物之间相互作用非常复杂;
3)双歧杆菌不太容易做遗传改造,导致研究工具受限。
未来如果有更好的分子生物学工具、更聚焦的研究,才更有希望把双歧杆菌如何与人体互作并发挥作用的关键机制讲清楚。
扩展阅读:
其他益生菌
✧ 布拉氏酵母菌 (Saccharomyces boulardii)
对肠道屏障的保护作用
较早的研究表明,布拉氏酵母菌(S. boulardii)保护T84单层中EPEC诱导的TER降低和甘露醇通量增加;然而,布拉氏酵母菌不改变健康T84细胞中的TJ屏障功能。
布拉氏酵母菌的保护作用是通过ZO-1的保存和ERK1/2信号通路的抑制介导的。
临床效果
布拉氏酵母菌在第三个月末与未接受益生菌治疗的患者相比,CD患者的肠通透性降低33%。
此外,S. boulardii CNCM I-745已显示出保护免受病原体诱导的TJ屏障功能障碍。
影响上皮屏障完整性的作用
布拉氏酵母菌共孵育有助于维持上皮屏障完整性,而预孵育是显著减少IL-8分泌所必需的。布拉氏酵母菌通过阻断MLC磷酸化并抑制T84感染细胞中的NF-κB和MAPK信号通路来保护屏障功能并抑制EHEC诱导的炎症。
对 Shigella flexneri 感染的影响
另一项研究使用人肠上皮的体外和体内模型检查了布拉氏酵母菌对Shigella flexneri感染的影响。在感染期间,布拉氏酵母菌通过上调TJ蛋白ZO-2并减少ERK、Jun N-末端激酶(JNK)和NF-κB信号通路的激活来增强屏障完整性。
抗炎作用的验证
无细胞布拉氏酵母菌上清液重现了这些抗炎作用。布拉氏酵母菌的抗炎作用在人胎儿肠异种移植模型中得到证实,其中酵母菌株减轻S. flexneri造成的损伤和炎症,但不能预防感染。
✧ E. coli Nissle 1917 (EcN)
只有活的 EcN 益生菌(以及它培养后的上清液,也就是细菌分泌物所在的液体)才能明显增强肠道上皮细胞的“紧密连接”屏障;把细菌热杀死后就几乎没效果。
细胞模型中的屏障增强
在 HT-29 和 Caco-2 细胞模型里,活菌或上清液能让细胞层的电阻(TER,代表屏障紧密程度)提高约 40%–75%,同时让甘露醇这种小分子“漏过去”的程度降低约 40%。
TcpC蛋白的作用机制
研究认为关键原因是 EcN 产生的一种蛋白 TcpC,它会启动细胞内的一些信号通路(如 PKCζ 和 ERK1/2 的磷酸化),并促进紧密连接相关蛋白(如 claudin-14)增加,从而把细胞之间的“缝”收紧。
EcN上清液对肠道屏障的保护作用
EcN 的上清液能防止化疗药 5-FU 导致的肠上皮细胞(IEC-6)屏障变差,表现为 TER 不那么容易下降。
在脓毒症相关的炎症条件下,EcN 上清液可以在体内和体外保护紧密连接屏障:它通过抑制 NF-κB 相关通路,减少会“拉开细胞缝隙”的 MLCK-P-MLC 信号被激活。并且在 TNF-α 和 IFN-γ 这类炎症因子一起存在时,EcN 上清液仍能提高 TER,从而减轻屏障功能障碍。
外膜囊泡的保护机制
EcN 释放的外膜囊泡(OMV,可理解为细菌分泌的“微小包裹”)和可溶性因子,能在 EPEC 致病菌感染时保护 T-84 和 Caco-2 细胞的紧密连接屏障,这种保护与 occludin 和 claudin-14 等紧密连接蛋白不被破坏有关。
在 DSS 诱导的结肠炎小鼠模型中,EcN 还能防止 DSS 造成的肠道通透性升高(减少“肠漏”),这与紧密连接支架蛋白 ZO-1 的表达得以维持有关。
✧ 枯草芽孢杆菌 (Bacillus subtilis)
比较了三种不同的枯草芽孢杆菌(B. subtilis)菌株对肠道上皮细胞模型(Caco-2)屏障的影响。结果发现:只有其中一株(B. subtilis 29784)能让细胞屏障更“紧”(电阻TER提高约50%),另外两株要么没效果,要么反而让屏障变差。
同时,B. subtilis 29784之所以能增强屏障,和细胞里几种“把细胞缝起来”的关键紧密连接蛋白增加有关,包括ZO-1、occludin和claudin-1。
在抗炎方面,不同菌株的效果也不一样(有明显“菌株差异”):某些B. subtilis菌株能抑制IL‑1β引发的NF‑κB信号通路激活,从而显著减少炎症相关物质IL‑8的产生,并降低IL‑1β刺激下iNOS蛋白水平的上升。
在坏死性小肠结肠炎(NEC)的细胞和动物模型中研究了两种益生菌(L. plantarum 和 L. rhamnosus)对肠道紧密连接的影响。
细胞实验结果显示屏障增强
在细胞实验里:他们把这两种菌加到 Caco-2 肠上皮细胞表面 5 小时。
结果显示:两种菌都能让细胞层更不漏(TER 升高、葡聚糖更不容易穿过去),说明屏障更紧。
当用 LPS 或 EGTA 这类物质去破坏屏障时,提前用这两种菌处理能减轻损伤,可能与调节 ZO-1(一种关键紧密连接蛋白)有关。
其中 L. rhamnosus 的保护效果看起来比 L. plantarum 更强。
动物模型中益生菌效果不一致
但在大鼠 NEC 模型里(用阪崎克罗诺杆菌感染诱导):直接给乳杆菌组合反而观察到肠道通透性增加(更漏),这与细胞实验相反。
不过如果在感染前先用这组益生菌预处理,通透性并不会增加,而且还能减少肠道损伤。
作者因此提醒:益生菌并不一定永远是“有益无害”,在某些条件下可能也会刺激或伤害肠上皮,所以临床使用特定菌株需要谨慎。
BWI多菌株益生菌的保护作用
有研究发现,一个叫 BWI 的多菌株益生菌混合物(含 8 种活菌 + 1 种热处理菌株成分)对肠屏障更稳:在 Caco-2 与免疫细胞(THP-1)的共培养模型中,它能维持 occludin(紧密连接蛋白)水平,并激活 AMPK 通路(有助于紧密连接组装),从而保护屏障完整性。
在 LPS 引发的炎症环境下,它还能抑制 NFκB 通路,降低促炎因子相关基因表达。
TER 测量也支持:BWI 能随剂量增加而更有效地防止通透性升高(减少“渗漏”)。
B. bifidum + 嗜热链球菌
一项双盲研究显示:含 B. bifidum 和嗜热链球菌(S. thermophilus) 的商业益生菌配方,能显著减少婴儿的抗生素相关性腹泻。
L. rhamnosus + L. acidophilus + L. helveticus
有研究把L. rhamnosus、L. acidophilus、L. helveticus混合给健康志愿者:当用吲哚美辛(NSAID)人为造成胃肠屏障受损时,活菌能明显减轻“胃”的通透性升高,但对“肠”的通透性影响不明显,说明作用可能因部位不同而不同。
L. helveticus R0052 + B. longum R0175
动物实验中,L. helveticus R0052 与 B. longum R0175联用,能保护心肌梗死后大鼠出现的肠道紧密连接通透性升高;但对健康对照大鼠的屏障并没有明显提升。研究者推测机制可能与抑制NF-κB炎症信号、激活抗凋亡通路以及TLR-2相关调节有关。
很多实验提示改善肠上皮屏障往往需要“活的菌”,因为它们要通过黏附、与上皮细胞直接互动等方式来触发紧密连接的调整;但在个别情况下,细菌产生的特定产物(如胞外多糖)也可能提供类似保护。不同菌株、不同部位、以及是否处在炎症/损伤状态下,都会影响效果。
肠道内壁的上皮细胞之间有一套紧密连接蛋白,像拉链/密封条一样把细胞缝隙关紧,防止细菌、毒素和未消化的大分子随意穿过去,同时又让营养正常吸收。这道屏障一旦变漏,就很容易引发或加重多种胃肠道问题,比如炎症性肠病、肠易激综合征、坏死性小肠结肠炎以及一些病原体导致的肠炎。
越来越多的细胞实验、动物研究和部分临床研究提示:某些益生菌可以帮助维持或修复这道封口带,它们可能通过以下方式保护肠屏障:
而且这些效果往往非常看菌株——同一种类的益生菌,不同菌株效果可能差很多;有时还取决于益生菌是不是活的、它分泌的代谢物、或它表面的成分。另外,它在上皮细胞和免疫细胞里起作用的方式也可能不一样。
不过,我们目前对“益生菌到底是怎样在分子层面修好TJ屏障”的理解还不够完整。
研究结果之所以经常不一致,常见原因包括:
未来更需要做的是:明确哪个菌株通过哪条通路,对哪类人群最有效,并结合肠道菌群检测的结果,分析不同菌群的组成和功能,以指导益生菌的选择。同时,应将剂量、给药方式、疗程标准化,再用设计良好的临床试验去验证这些策略的有效性。
总体来说,益生菌作为一种思路合理的干预手段,确实有潜力帮助加强肠道屏障、缓解与肠漏相关的胃肠疾病,但要实现可靠应用,还需要更扎实的机制研究和更严格的临床证据,免疫功能低下人群使用活菌也应更谨慎。
注:本账号发表的内容仅是用于信息的分享,在采取任何预防、治疗措施之前,请先咨询临床医生。
主要参考文献
Hofmann C, Geiger H. Aging of the Colon – A Mechanistic View. Mech Ageing Dev. 2025 Dec 11:112143.
Baidoo N, Rasis E, Tahiri D, Sanger GJ. The impact of ageing on the structural compositions of the mucosa of human colon. Tissue Cell. 2025 Dec;97:103090.
Abahussin HM, Alotaibi MS, Alhazzaa OA, Alotaibi AG, Alsaab SM, Aljawini NA, Alawad AO. Exploring the intricate link between gut microbiota dysbiosis and the aging process: implications for age-related diseases. Gut Pathog. 2025 Dec 14.
Elfers K, Sehnert AS, Wagner A, Zwirner U, Linge H, Kulik U, Poehnert D, Winny M, Gundert B, Aselmann H, Mazzuoli-Weber G. Functional and Structural Investigation of Myenteric Neurons in the Human Colon. Gastro Hep Adv. 2024 Aug 24;4(1):100537.