-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康
维生素
B族维生素和维生素K是微生物和人类生理学中多种细胞过程所必需的微量营养素。传统上,这些维生素被认为主要来自饮食,但近年来的研究显示,人类肠道微生物群具备合成这些维生素的能力,提供了重要的内源性来源,这一贡献过去常被低估。
值得注意的是,微生物对宿主维生素储备的贡献正逐渐被视为维生素稳态的重要功能。在结肠中,微生物合成的维生素能够通过特定的运输机制被吸收,以发挥其生物学作用。
什么是维生素?
维生素是一类化学结构各异的有机化合物,人体只需要很少的量,但它们对维持细胞和全身的生理功能至关重要。
与提供结构或能量的宏量营养素(如碳水化合物、蛋白质和脂肪)不同,维生素主要通过作为辅因子或辅酶前体的形式发挥作用,帮助酶完成各种反应,这些反应涉及能量代谢、物质合成、氧化还原调节和细胞信号传导。
即使是轻微的维生素缺乏,也可能损害代谢的完整性,并增加患贫血、神经退行性疾病和免疫缺陷等多种疾病的风险。
分类
根据溶解性和生理特性,维生素通常分为水溶性和脂溶性两类。
• 水溶性维生素
水溶性维生素包括B族维生素(维生素B1、B2、B3、B5、B6、B7、B9和B12)和维生素C。它们通常作为辅基或辅酶参与酶促反应,尤其是在能量代谢、核苷酸合成和一碳单位转移反应中。由于其亲水性,水溶性维生素不易在体内储存。
• 脂溶性维生素
脂溶性维生素(维生素A、D、E和K)通过脂类介导的途径被吸收,并储存在脂肪组织和肝脏中,形成一个相对稳定的储备。
脂溶性维生素的功能更偏向于调节而非催化,但对于维持正常的视力、免疫调节、抗氧化防御以及钙磷平衡至关重要。比如,维生素K是凝血因子中谷氨酸残基γ-羧化反应的辅因子。
来源
• 大部分维生素依赖饮食获取或微生物产生
值得注意的是,由于人体无法合成大多数维生素,因此它们是必需的营养素。只有少数例外,如维生素D,它可以在紫外线照射下由皮肤中的7-脱氢胆固醇合成。对于其他所有维生素,人体主要依赖饮食和微生物的产生来获取。
• 肠道菌群合成维生素的能力对人体代谢非常重要
与高等真核生物不同,许多细菌物种具备从头合成必需辅因子的遗传机制,包括维生素B1、B2、B3、B5、B6、B7、叶酸(B9)、B12和甲萘醌(K2)。
其中,6种B族维生素(B1、B2、B3、B5、B6和B9)是关键的辅酶前体,这些辅酶在细菌和哺乳动物中发挥作用,如硫胺素焦磷酸(TPP)、黄素单核苷酸/黄素腺嘌呤二核苷酸(FMN/FAD)、烟酰胺腺嘌呤二核苷酸(NAD/NADP)、辅酶A(CoA)、磷酸吡哆醛(PLP)和四氢叶酸(THF)。
生物素则是一种重要的羧化/脱羧辅因子,在脂肪生成、碳水化合物和氨基酸代谢中发挥重要作用。钴胺素是B12辅酶家族(包括氰钴胺素、甲基钴胺素和腺苷钴胺素)的前体,对所有动物和许多(但并非所有)细菌物种都是必需的。
因此,人们越来越关注人体肠道菌群的合成能力,将其视为B族维生素和维生素K的潜在内源性来源,并逐渐认识到它对宿主维生素稳态的功能性贡献。
这种观念的转变得益于肠道菌群检测方法学的改进和多样化,使得谷禾能够以更高更大规模的分辨率检测和功能性地解释微生物维生素的生物合成。
本文主要关注和讨论目前对人体肠道相关细菌合成B族维生素和维生素K的理解。重点关注用于研究肠道菌群产生维生素潜力的各种方法,包括基因组学、宏基因组学等,以更好地了解微生物与宿主之间的维生素相互作用,从而改善人类健康。
人类肠道菌群是一个庞大且代谢活跃的微生物生态系统,包含丰富的基因功能库。随着新物种和功能的不断发现,我们对它的认识也在不断加深。
哪些证据说明肠道菌群合成维生素
(1)无菌大鼠 vs. 普通大鼠的对比实验
为了证明细菌生产的维生素,我们以一个关于维生素K的经典例子:
实验对象A(无菌大鼠): 肠道里没有任何细菌。
给它们吃不含维生素K的食物,它们就会生病(凝血酶原水平降低,容易出血),因为它们既没从食物中吃到维生素K,肠道里也没有细菌帮忙制造。
实验对象B(普通大鼠): 肠道里有正常的细菌。
结果: 即使吃完全一样的不含维生素K的食物,它们却很健康,凝血功能正常。
结论: 这说明普通大鼠肠道里的细菌“生产”了足够的维生素K,弥补了食物的缺失。进一步推测细菌的产量足甚至以满足生理需求。
因此以上实验表明细菌不仅仅是“产生”了维生素,而且产生的量很大,可能足够达到维持宿主健康(如正常凝血)的生理标准。
(2)人体研究
同样,在人类研究中,即使低维生素K饮食持续3-4周,也不会导致明显的维生素缺乏,除非同时使用广谱抗生素抑制肠道菌群。在这种情况下,会观察到血浆凝血酶原的明显下降,这清楚地表明了肠道菌群在维持维生素K稳态方面的重要作用。
(3)体外研究
一些计算机模拟研究也探讨了肠道菌群对宿主相关微量营养素摄入的潜在贡献,特别是关于B族维生素的膳食参考摄入量(DRI)。这些计算方法发现了能够产生多种B族维生素的微生物生物合成途径,表明肠道菌群可能对宿主的微量营养素摄入产生影响。
具体来说,尽管这仍然是推测性的,但有目前研究普遍认为肠道微生物合成的维生素B3、B6、B9和B12可能占人类相应DRI的约27%-86%。
(4)结肠转运系统
此外,在人类结肠中检测到B族维生素转运系统,进一步加强了微生物和膳食维生素可能协同作用,维持全身维生素稳态的观点。然而,由于微生物产生的维生素在结肠环境中的实际生物利用度仍未得到充分表征,需要进一步明确的研究。
!
注意局部和全身
与小肠中吸收效率明确的膳食维生素不同,微生物合成的维生素吸收取决于其化学形式和宿主转运蛋白的能力。例如,结肠中存在大量微生物合成的类咕啉素(包括维生素B12的变体),其结构常与具有生物活性的钴胺素不同,导致人类宿主的生物利用度降低。
此外,微生物合成的B族维生素主要满足自身的代谢需求,因此,与膳食来源相比,剩余部分(无论是主动分泌还是通过细菌细胞自发裂解释放)所占比例可能较小。
同时,微生物产生的维生素在塑造局部肠道环境(特别是在肠腔内和黏膜界面)中具有重要的生物学意义。已知这些维生素可以支持结肠上皮细胞的代谢需求,影响屏障完整性,调节局部免疫反应,并发挥抗氧化和保护作用。
谷禾数据库整理了大样本人群微生物基因组参考集合的基因组学研究,初步细致地刻画了肠道微生物群中各个成员合成维生素的潜力。
▸ 谁能自己造维生素?
把这些信息汇总到“门”(phylum)这一分类层级时,拟杆菌门(Bacteroidota)和假单胞菌门(Pseudomonadota)中“维生素原养型”(prototrophic,能从头合成某种化合物)的物种比例更高。
这两个门里包含能够合成几乎所有B族维生素的物种,但维生素B12(钴胺素)是个例外:大约只有30%的拟杆菌门基因组和约42%的变形菌门基因组显示出合成B12的潜力。
• 拟杆菌属和大肠杆菌是重要的B族维生素生产者
Bacteroides(拟杆菌属): 一些拟杆菌属的成员可以合成全部八种B族维生素。
E.coli(大肠杆菌), Phocaeicola dorei, Bifidobacterium(双歧杆菌属), Segatella copri(以前叫Prevotella copri): 这些也是肠道中B族维生素的重要生产者。
• 放线菌和芽孢杆菌中能产生维生素的较少
相对地,放线菌门(Actinomycetota)和芽孢杆菌门(Bacillota)中维生素“营养缺陷型/需外源型”(依赖外部来源满足维生素需求)的成员比例更高。
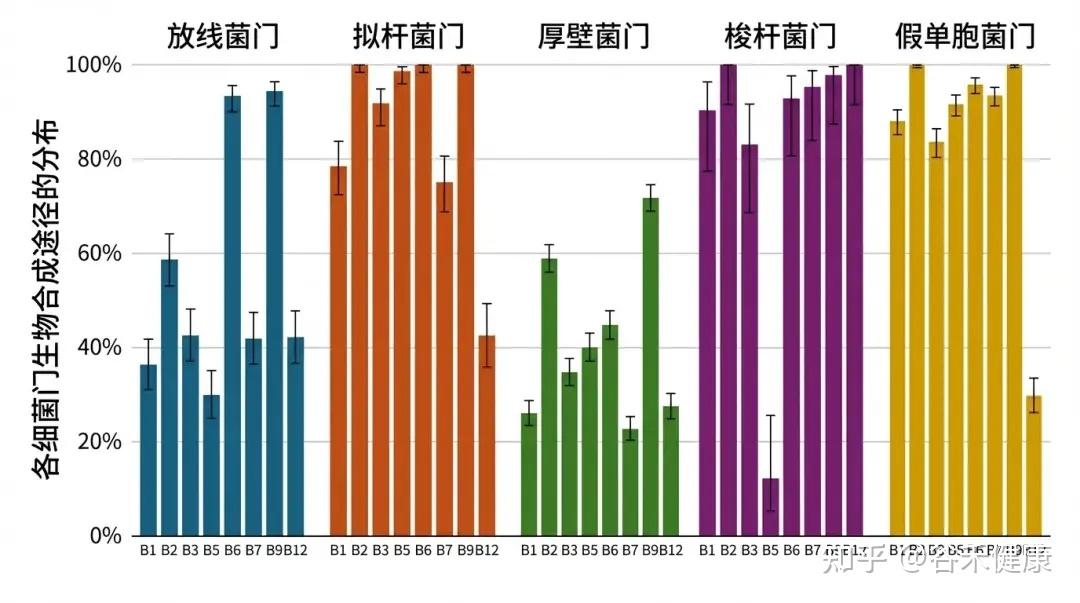
注:研究数量有限,仅供参考
▸ 肠型可能影响维生素的合成能力
• 不同肠型擅长合成的维生素不同(仅供参考)
肠道菌群的组成(肠型)会影响维生素的合成能力。
肠型1(以Bacteroides为主): 更擅长合成生物素、核黄素和泛酸。
肠型2(以Prevotella copri为主): 更擅长合成硫胺素和叶酸。
• 谁是维生素“消费者”?
Faecalibacterium prausnitzii(普拉梭菌): 它会消耗多种B族维生素,尤其是核黄素,核黄素能帮助它在肠道内抵抗氧化。
尽管基因组研究已阐明单个菌株或基因组的生物合成能力,现有方法仍较少将这一视角扩展至整个微生物群落,因此尚难在人群层面绘制维生素生物合成潜力图谱。
现有研究和谷禾的研发表明,特定微生物类群通过其生物合成能力模式和维生素利用策略,在塑造肠道维生素“生态”中起着关键作用。深入理解不同类群对维生素代谢的特异性贡献对于阐明微生物群与宿主营养状态的功能性相互作用至关重要,这些认识还可能指导基于微生物组的干预策略设计,以优化维生素可获得性并解决营养缺乏问题。
在此背景下,比如用能分泌叶酸的乳酸菌做发酵剂,生产叶酸强化乳制品;也在筛选肠道来源的产叶酸菌作为潜在益生菌,用于改善维生素供应。这些例子说明:关于微生物维生素代谢的知识可以转化为食品和治疗策略,最终为利用肠道微生物群有益代谢潜力的营养学方法铺平道路。
尽管人们越来越认识到人类肠道菌群具备合成维生素的能力,但最近的研究强调,肠道菌群中维生素的可用性并非仅仅由生物合成能力决定,还受到微生物群落内部以及宿主处复杂的代谢相互作用的影响。
这些动态过程包括微生物之间的交叉代谢、维生素摄取的竞争以及宿主介导的吸收,所有这些因素共同塑造了最终的营养产出。
▸ 微生物—微生物互作
在微生物层面,维生素的交叉喂养代谢源于不同分类群之间生物合成能力的不均匀分布,且这种差异不仅存在于亲缘关系较远的类群间,也体现在同一属内的不同物种之间。
最近的研究中,研究人员利用 SEED 平台分析了一个包含2000多个经过人工校对的人类肠道细菌基因组的参考数据集。该平台整合了所有已知和推断的生物合成及补救途径组件,包括酶和转运蛋白。这一方法通过预测不同分类等级中原养型(可自身合成)和营养缺陷型(需外部获取)菌株的比例,实现了对维生素生物合成潜力变异性的定量评估。这些跨越不同维生素和分类级别的保守性与变异性模式,为微生物群落中的潜在代谢相互作用奠定了基础。
• 原养型微生物的产物可能支持缺陷型的生长
当原养型和营养缺陷型微生物共存于同一生态位时,这种差异可能导致代谢相互依赖,即原养型微生物释放的代谢产物或中间体能够支持营养缺陷型微生物的生长和代谢功能。
一个明显的例子是维生素B12,这一结构复杂且代谢成本高昂的辅助因子。由于完整生物合成途径需高昂的代谢成本和遗传负担,只有少数厌氧肠道细菌(主要属于厚壁菌门和放线菌门)能够自主生产维生素B12。
然而,这种辅助因子对许多群落成员至关重要,众多成员已进化出高亲和力的转运系统以从环境中获取。例如,Anaerobutyricum hallii(以前称E.hallii)是一种特征明确的丁酸产生菌,能够合成维生素B12,而嗜黏蛋白阿克曼氏菌(Akkermansia)则通过共生利用该维生素进行丙酸的合成。
同样,在肠道微生物群落模型中,缺乏叶酸合成能力的Roseburia intestinalis M50/1生长受到经体外验证的叶酸原养型菌株双歧杆菌Bifidobacterium bifidum CNCM I-3650的益处。这些发现表明,原养型细菌可以通过主动交换代谢物和微量营养素,或通过被动机制(如细胞裂解并释放胞内维生素),来缓解共存菌株的营养缺陷。
这些以维生素为媒介的相互作用不仅是合作性的,竞争也在塑造人类肠道维生素可用性方面起着关键作用。
维生素的可用性受微生物间相互作用等的影响
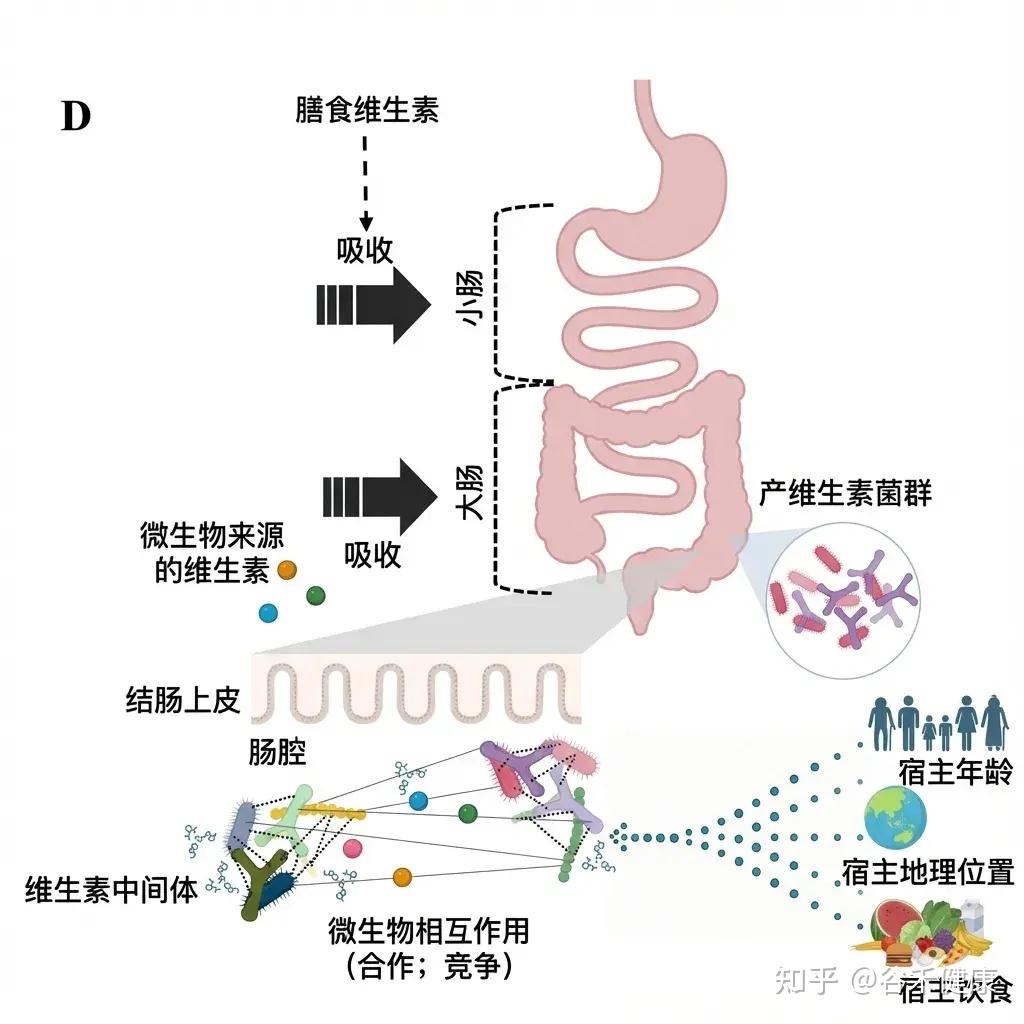
• 肠道微生物群会竞争有限的维生素资源
微生物通过产生维生素结合蛋白和利用特定转运蛋白,与其他群落成员竞争有限的维生素资源。因此,肠道环境可视为一个严格调控的微量营养素市场,其可用性由生物合成能力和摄取效率共同决定。
例如,多形拟杆菌(Bacteroides thetaiotaomicron)表达三种功能性、同源的维生素B12转运系统以获取钴胺素。这些转运蛋白对不同类咕啉类似物表现出独特的特异性,这可能为其在竞争激烈的人类肠道环境中提供选择性优势,同时也体现了肠道微生物为确保获得必需辅助因子所采用的复杂策略和巨大努力。
▸ 微生物—人体互作
宿主与微生物之间的相互作用使这一网络愈加复杂。实际上,宿主通过免疫调节、结肠吸收、粘液分泌和饮食等方式,间接影响维生素的动态变化,从而影响微生物的组成和功能。
• 不同年龄的肠道菌群组成影响维生素合成能力
最近的研究显示,年龄和地理起源等宿主因素显著影响人类肠道菌群的维生素生物合成潜力。具体而言,肠道菌群的测序分析表明,婴儿期维生素B9(叶酸)和K2的生物合成途径非常普遍,这与能合成叶酸的双歧杆菌属(Bifidobacterium spp.)的主导地位以及能够产生维生素K2的大肠杆菌(E.coli)的存在相一致,这些都是早期肠道微生物组的特征。
另一项研究将人群按年龄分组(从几个月大到80岁以上),并将微生物特征与年龄进行关联分析。结果显示,新生儿组(0-4岁)的微生物与参与硫胺素(维生素B1)和烟酸(维生素B3)生物合成的酶呈正相关,表明这些维生素路径与生命早期相关,这与老年组形成对比。
成人的肠道菌群则富含Bacteroides和Prevotella copri,展现出更广泛的代谢能力,因为这些类群通常是维生素B的原养型生物,具备多种B族维生素的完整生物合成途径。
• 不同地区的饮食和生活方式导致维生素合成能力差异
此外,新兴证据表明,地理起源导致全球不同人群肠道菌群在B族维生素生物合成能力上的差异,可能与饮食和生活方式相关因素影响肠道菌群的组成和功能有关。
在这个复杂的生态和代谢网络中,结合本地大数据库明确哪些微生物类群在结肠中参与维生素生物合成、这些维生素是否被宿主吸收以及哪些因素影响其产生,对于理解微生物群对宿主的营养贡献至关重要。这也有助于设计针对微生物群的策略(如益生元、益生菌或工程菌群),以改善维生素状况。
1
维生素B1(硫胺素)
▸ 生物学功能与重要性
硫胺素(维生素B1)是一种水溶性维生素,作为辅酶参与多个核心代谢过程。在活性磷酸化形式TPP(焦磷酸硫胺素)下,维生素B1是碳水化合物代谢中多种酶的关键辅因子,包括丙酮酸脱氢酶、α-酮戊二酸脱氢酶和转酮醇酶,这些酶是三羧酸循环(TCA)和磷酸戊糖途径的关键参与者。
通过这些途径,硫胺素有助于能量生成、氧化还原平衡、核苷酸和脂质的生物合成,并间接参与神经递质的代谢。
▸ 微生物合成与已知微生物贡献者
细菌中的硫胺素生物合成遵循模块化途径,涉及两个部分的分别合成:4-氨基-5-羟甲基-2-甲基嘧啶磷酸(HMP-P)和4-甲基-5-(β-羟乙基)噻唑磷酸 (THZ-P)。随后,这些部分由 ThiE 酶偶联生成磷酸硫胺素,最后转化为活性的 TPP 形式。基因组调查显示,相当大比例的肠道相关细菌基因组,包括拟杆菌属(Bacteroides)、普雷沃氏菌属(Prevotella)、肠球菌属(Enterococcus)和双歧杆菌属(Bifidobacterium)等主要菌属的代表,都拥有从头合成磷酸硫胺素所需的完整基因库。
然而,许多肠道共生菌对硫胺素是营养缺陷型的,依赖于外源性硫胺素或诸如 HMP-P 之类的中间体,这些物质可以从环境中回收或在微生物之间交换。在这些维生素B1营养缺陷型细菌中,已鉴定出不同的补救策略:有些菌株可以回收两种硫胺素中间体,而另一些则缺乏其中一条生物合成支路,依赖外部来源提供相应的缺失化合物,还有一部分完全依赖于摄取预先形成的硫胺素。
值得注意的是,所有营养缺陷型变体都保留了一定的补救能力,反映了对不完整生物合成潜力的多样化进化适应。
有趣的是,普拉梭菌(F. prausnitzii)在将丙酮酸转化为乙酰辅酶A的代谢过程中需要这种维生素,这是丁酸生物合成途径的一部分,突显了维生素B1在肠道菌群成员生产短链脂肪酸(SCFA)中的关键作用。
// 小结
总结来说,维生素B1(硫胺素)不仅是你身体的“能量充电宝”,也是将食物(碳水化合物)转化为能量所必需的“点火器”。没有它,我们的细胞无法有效产生能量,也无法制造DNA和脂肪,甚至会影响神经系统的信号传递。
肠道里住着很多细菌,其中一些是“生产者”。比如拟杆菌和双歧杆菌等常见菌,可以自己从头制造维生素B1,不仅满足自己,可能还能分给别人。还有很多细菌是“消费者”(营养缺陷型),它们自己造不出维生素B1,或者只能造出一半。
有的细菌完全依赖别人,必须从环境里捡现成的维生素 B1 吃。有的细菌只能造一半零件,需要从邻居那里借另一半零件来组装。说明为了生存,细菌逐步进化出复杂的“借用”和“互助”关系。
2
维生素B2(核黄素)
▸ 生物学功能与重要性
核黄素(维生素B2)是两种主要黄素辅酶——黄素单核苷酸(FMN)和黄素腺嘌呤二核苷酸(FAD)的前体。这两种辅酶在核心代谢中广泛参与氧化还原反应,包括电子传递链、脂肪酸氧化、氨基酸分解代谢,以及维生素B6和B9的激活反应。
此外,核黄素通过支持谷胱甘肽还原酶的活性和调节氧化应激,有助于维持抗氧化防御系统。
▸ 微生物合成与已知贡献者
细菌中的核黄素生物合成涉及一组保守基因(ribA、ribB、ribC、ribD和ribE),这些基因将三磷酸鸟苷(GTP)和5-磷酸核酮糖转化为核黄素,随后核黄素被磷酸化为FMN,再腺苷酸化为FAD。
最近的基因组重构研究显示,完整的操纵子在肠道共生细菌中广泛存在,包括拟杆菌属(Bacteroides)、肠球菌属(Enterococcus)和多种乳杆菌。尤为重要的是,乳酸乳球菌(Lactococcus lactis)、植物乳杆菌(Lactiplantibacillus plantarum)和罗伊氏乳杆菌(Limosilactobacillus reuteri)已被提议作为天然生物强化剂,用于提高酸奶、奶酪和发酵乳制品中的核黄素浓度。
然而,基因组分析显示,芽孢杆菌门(Bacillota)和放线菌门(Actinomycetota)中的一些成员缺乏完整的核黄素生物合成操纵子。有趣的是,许多这些核黄素缺乏型细菌编码高亲和力的核黄素转运系统,如RibU(ECF家族)和RibXY(ABC超家族),显示出它们对核黄素衍生辅助因子(如FMN和FAD)的强烈需求。
除了营养作用外,微生物生成的核黄素还参与调节宿主粘膜表面的免疫反应,其关键机制涉及粘膜相关恒定T(MAIT)细胞,这些细胞在识别由非多态性MHC I类相关分子MR1呈递的核黄素生物合成中间体后被激活。该途径建立了微生物维生素B2代谢与粘膜免疫监视之间的直接联系,强调了微生物核黄素生成在宿主-微生物相互作用中的更广泛生理相关性。
// 小结
维生素B2(核黄素)不仅是身体必需的营养素,也是肠道细菌与免疫系统之间的沟通桥梁。进入体内后,维生素B2转化为两种“超级助手”(FMN和FAD),参与无数化学反应,尤其是在将脂肪和蛋白质转化为能量,以及协助产生其他维生素(如B6和叶酸)。它还能帮助抵抗“氧化压力”,保护身体免受损伤。
肠道细菌也能合成B2,许多细菌(如某些拟杆菌和乳酸菌)具备特定基因,能够自己生产维生素B2。然而,并非所有细菌都能合成B2;一些细菌缺乏这种能力,但进化出强大的“抢夺”能力(高亲和力转运系统),能够从环境中获取B2以维持生存,显示出B2对细菌生存的重要性。
意外发现是,细菌制造B2的过程中还会产生一些中间产物,这些产物能够激活免疫系统中的特殊巡逻兵“MAIT细胞”。当MAIT细胞探测到细菌生成B2时,这些细胞会被激活,像是细菌发送的信号,通知免疫系统“我在这里”。这不仅帮助身体识别细菌,还启动免疫监视,保护肠道粘膜的健康。
3
维生素B3(烟酸)
▸ 生物学功能与重要性
维生素B3,即烟酸,包含两种生物活性形式:烟酸(NA)和烟酰胺(NAM)。这两者都是烟酰胺腺嘌呤二核苷酸(NAD+)和烟酰胺腺嘌呤二核苷酸磷酸(NADP+)的前体。这两种二核苷酸是参与氧化还原反应、能量代谢、DNA 修复和细胞信号传导的重要辅助因子。
NAD+是糖酵解、三羧酸循环和氧化磷酸化中的关键辅酶,而NADP+对合成代谢途径和抗氧化防御至关重要。
▸ 微生物生物合成与已知贡献者
与大多数其他B族维生素不同,烟酸可以在体内(主要在肝脏)内源性合成,通过犬尿氨酸途径将色氨酸转化为喹啉酸,后者是NAD+生物合成的关键中间体。然而,这一途径通常不足以满足日常需求,因此饮食摄入或微生物的贡献显得尤为重要。
在肠道中,许多共生细菌拥有一条替代的烟酸从头合成途径,从天冬氨酸开始生成喹啉酸,再转化为烟酸单核苷酸,最终合成NAD+。这一生物合成途径广泛分布于假单胞菌门(Pseudomonadota)和拟杆菌门(Bacteroidota)中,尽管在属和种的水平上存在显著差异。大肠杆菌(E. coli)、脆弱拟杆菌(B.fragilis)和多种双歧杆菌(Bifidobacterium)被确认是肠道环境中的烟酸生成者。
然而,并非所有菌种都编码完整的生物合成基因,许多细菌依赖烟酸补救途径,利用宿主或微生物衍生的前体。最新证据强调了宿主与其肠道菌群之间维生素B3前体的双向交换,支持共享的NAD+代谢。
尽管饮食中的烟酸前体大多在上消化道/小肠中被吸收,但结肠中的微生物可以利用可发酵纤维(如菊粉)或宿主细胞代谢释放的NAM来合成NAD+。微生物来源的NAD+随后转化为NAM和NA,这些物质能够被宿主肠道组织吸收,并在宿主细胞内用于再生NAD+。这突显了一个动态循环,即微生物活动与宿主来源底物共同维持循环中NA水平,即使在缺乏直接饮食摄入的情况下。
// 小结
维生素B3是身体细胞正常运转不可或缺的成分。你可以把它想象成制造“电池”的原料。它主要有两种形式(烟酸和烟酰胺),在体内会变成两种超级重要的物质(NAD+和NADP+)。这两种物质负责帮我们把食物变成能量、修复受损的 DNA,以及保护细胞不“生锈”(抗氧化)。我们的肝脏可以利用蛋白质中的某种成分(色氨酸)自己合成一点维生素 B3,但这通常不够用,大部分需要通过食物摄入。如果你吃不够,你肚子里的细菌能帮大忙。
在你肠道里的许多细菌(比如大肠杆菌和双歧杆菌)拥有特殊的“生产线”,可以用完全不同的原料(天冬氨酸)制造出维生素 B3。
细菌还可以利用我们吃下去的膳食纤维(比如菊粉)或者我们身体代谢剩下的废料,制造出 NAD+。然后它们把这些成品分解成我们可以吸收的形式(烟酸或烟酰胺),这就相当于细菌在结肠里给我们“供货”。我们身体产生的某些前体物质也能被细菌利用。
4
维生素B5(泛酸)
▸ 生物学功能与重要性
维生素B5(泛酸)是辅酶A(CoA)的生化前体,辅酶A作为核心代谢辅助因子,参与广泛的生物过程,包括三羧酸循环(TCA)、脂肪酸合成与β-氧化以及氨基酸代谢,主要在能量生成和合成代谢中充当酰基载体。此外,胆固醇、类固醇激素、血红素和乙酰胆碱的生物合成也需要辅酶A。
维生素B5对于维持细胞能量平衡和代谢功能至关重要。
▸ 微生物生物合成与已知贡献者
细菌可以通过一条从头合成途径来制造泛酸,该途径将泛解酸与β-丙氨酸结合在一起。这条途径由一组高度保守的基因簇(panB、panC、panD、panE)编码,合成出的维生素随后会被转化为辅酶 A。
在人类肠道菌群中,基因组分析显示,几乎所有的假单胞菌门(Pseudomonadota)和拟杆菌门(Bacteroidota)都具备合成泛酸的遗传能力,而受评估的厚壁菌门(Bacillota)和放线菌门(Actinomycetota)成员中,只有不到一半编码了完整的泛酸合成途径。不过,许多无法自身合成泛酸的菌株(营养缺陷型)仍然保留了将外源性泛酸转化为辅酶A的酶机制,这使它们即使无法从头合成,也能完成基本的代谢功能。
正因为假单胞菌门和拟杆菌门普遍具备这种合成能力,所以在成年人的肠道菌群中,尤其是典型的以拟杆菌为主的肠型中,维生素B5的生物合成途径是最常见的代谢途径之一。
// 小结
维生素 B5 之所以重要,是因为它是我们体内一种叫“辅酶 A”的关键物质的原材料。你可以把辅酶 A 想象成细胞工厂里的“搬运工”和“点火器”。 它是身体燃烧脂肪、分解蛋白质和碳水化合物产生能量的过程中不可或缺的一环。身体制造胆固醇、性激素、血红蛋白(血液中携带氧气的成分)以及神经传导物质时,都离不开它。
5
维生素B6(吡哆醇)
▸ 生物学功能与重要性
维生素B6是由六种可相互转化的形式组成,包括吡哆醇(PN)、吡哆醛(PL)、吡哆胺(PM)及其磷酸化形式,其中5′-磷酸吡哆醛(PLP)是最活跃的形式。PLP作为辅酶参与了约140种酶促反应,使维生素B6成为功能多样且复杂的微量营养素之一。除了糖原磷酸化酶外,几乎所有依赖PLP的酶都涉及氨基化合物的生化过程,尤其是氨基酸代谢。
▸ 微生物生物合成与已知贡献者
在人类肠道中,PLP通过两条截然不同的途径合成:较长的依赖脱氧木酮糖5-磷酸(DXP)的途径,这在拟杆菌门(Bacteroidota)和假单胞菌门(Pseudomonadota)中普遍存在;以及较短的不依赖DXP的途径,这在放线菌门(Actinomycetota)中更为常见。
基因组分析表明,PLP的产生在肠道细菌中分布不均。尽管预测双歧杆菌属(Bifidobacterium)、拟杆菌属(Bacteroides)和普雷沃氏菌属(Prevotella)能合成PLP,但许多著名的肠道共生菌,如韦荣氏球菌(Veillonella spp.)、粪肠球菌(Enterococcus faecalis)、普拉梭菌(F.prausnitzii)和Roseburia inulinivorans则被认为是营养缺陷型(无法自行合成)。这些生物体通常携带补救途径的遗传特征,使它们能够将环境中的B6维生素形式转化为可用的PLP。
6
维生素B7(生物素)
▸ 生物学功能与重要性
生物素,也被称为维生素B7,是一种含硫的水溶性维生素。它作为羧化酶的辅酶,参与关键的代谢途径,包括脂肪酸代谢、氨基酸代谢、碳水化合物代谢、聚酮化合物生物合成以及尿素利用。生物素通过赖氨酸残基与靶酶共价结合,促进二氧化碳转移反应,这对维持能量稳态和脂质代谢至关重要。
▸ 微生物生物合成与已知贡献者
细菌中的生物素合成通过两条截然不同的途径进行。在大肠杆菌(Escherichia coli)中,生物素是通过一种改良的脂肪酸合成途径合成的,该途径依赖于bioC和bioH基因,这是一条规范的且在生物素合成的肠道细菌中广泛存在的路径。相比之下,枯草芽孢杆菌(Bacillus subtilis)则利用以bioW基因为中心的独立途径,这条依赖bioW的路线在Bacillota成员中更为常见。
根据最近的基因组调查,所有分析的放线菌门(Actinomycetota)基因组均缺乏从头合成生物素所需的必需基因,这种特征在厚壁菌门也很少见。与其营养缺陷特征相符,大多数放线菌门细菌编码高亲和力的生物素摄取系统,强调了它们对环境生物素来源的依赖,并表明存在选择性机制以确保高效清除这种必需辅因子。
7
维生素B9(叶酸)
▸ 生物学功能与重要性
维生素B9包括一类与四氢叶酸(THF)结构相关的水溶性化合物,THF在“一碳代谢”中作为辅酶发挥作用。THF及其衍生物对于许多反应中转移一碳单位至关重要,这些反应涉及嘌呤、胸苷酸和多种氨基酸的合成,以及核苷酸的合成、DNA的复制、修复和甲基化。
因此,叶酸在核苷酸合成、表观遗传调控和细胞分裂中发挥关键作用,尤其在妊娠和婴儿期等快速生长阶段更为重要。
▸ 微生物生物合成与已知贡献者
细菌从头合成叶酸需要先生成并缩合两种关键中间体:二氢蝶呤三磷酸(DHPPP)和对氨基苯甲酸(pABA)。这些前体通过不同的代谢途径生成,最终汇合形成二氢叶酸(DHF),随后被还原为具有生物活性的四氢叶酸(THF)。
在肠道微生物中,适应婴儿肠道的物种(如B.bifidum、B.longum和B.breve)被认为是重要的叶酸生产者。这些菌株已能在培养基中积累叶酸,表明它们可能为婴儿肠道的叶酸库作出贡献。然而,双歧杆菌通常需要外源补充pABA才能合成叶酸,表明它们在该前体上存在一定程度的“营养缺陷”。
乳杆菌也是能产叶酸的细菌。例如,德氏乳杆菌(Lactobacillus delbrueckii)、瑞士乳杆菌(Lactobacillus helveticus)、罗伊氏乳杆菌(Limosilactobacillus reuteri)、清酒乳杆菌(Latilactobacillus sakei)和植物乳杆菌(Lactiplantibacillus plantarum)的菌株在pABA存在的生长环境中能合成叶酸。
值得注意的是,植物乳杆菌表现出无需补充pABA就能稳定产生叶酸的能力。许多研究评估了肠道微生物对动物宿主叶酸摄入的贡献,已证实肠道细菌合成的叶酸可以在结肠被吸收并被宿主利用。基于这一发现,研究人员探讨了来自各种发酵食品的乳杆菌作为发酵剂生产叶酸强化乳制品,同时也探索将人体肠道来源的乳杆菌作为产叶酸益生菌。
8
维生素B12(钴胺素)
▸ 生物学功能与重要性
维生素B12(钴胺素)是一种含钴的辅因子,也是自然界中体积最大、结构最复杂的非聚合生物分子之一。在人体内,它作为辅酶参与两项关键的线粒体反应:
1)甲基丙二酰辅酶A变位酶(methylmalonyl‑CoA mutase):参与丙酸代谢与能量产生;
2)蛋氨酸合成酶(methionine synthase):在叶酸循环中把同型半胱氨酸再生为蛋氨酸,起关键作用。
在B12的多种形式中,氰钴胺(cyanocobalamin)化学性质最稳定;它被吸收后会经过酶促加工,转化为具有活性的辅因子形式:甲基钴胺(Me‑Cbl)和腺苷钴胺(Ado‑Cbl)。
▸ 微生物生物合成与已知贡献者
钴胺素的生物合成过程非常复杂且耗能,涉及30多个基因,可走需氧或厌氧两条途径,最终都汇合到咕啉环(corrin ring)形成以及钴离子螯合的步骤。
该合成能力主要局限于某些细菌类群,许多肠道微生物并不具备。大规模基因组分析显示,约60%–80%的人类肠道共生菌缺乏合成B12所需的完整基因组合,例如双歧杆菌属(Bifidobacterium)、普雷沃菌属(Prevotella)以及Bacteroides thetaiotaomicron等。
相反,Propionibacterium freudenreichii、梭菌属(Clostridium)、脆弱拟杆菌(Bacteroides fragilis)、阿克曼菌(Akkermansia muciniphila)以及部分Bacillota和放线菌门(Actinomycetota)细菌,编码了完整或近乎完整的B12合成操纵子。
但由于合成B12非常耗能,很多细菌进化出了替代策略来获得这种辅因子及其类似物(咕啉类/钴胺素类似物,corrinoids):例如回收前体或直接从环境/其他菌那里摄取完整分子,从而在肠道微生物群中形成合作与资源共享。
不过在人类体内,结肠产生的B12吸收效率很低,因此微生物来源B12对全身B12水平的直接贡献仍不明确。
// 小结
B12对人体很关键:它参与能量代谢的一条关键反应,以及“叶酸循环/同型半胱氨酸→蛋氨酸”的关键步骤。补剂里常见的氰钴胺只是稳定形态:进入人体后会被转换成真正起作用的两种活性形式(甲基钴胺、腺苷钴胺)。
肠道菌并非都能制造B12:多数常见肠道共生菌缺乏完整“生产线”,只有部分细菌具备较完整的合成基因。很多细菌选择“省钱模式”:不自己合成,而是从环境或其他细菌那里“捡现成/回收零件”。未来还需要继续加强研究。
9
维生素K2(甲萘醌,Menaquinones)
▸ 生物学功能与重要性
维生素K主要有两种形式:一种是叶绿醌(K1),存在于绿色叶菜中;另一种是甲萘醌(K2),它是一类多样的异戊二烯衍生物,主要由细菌产生。甲萘醌(MK-n)的差异在于其异戊二烯侧链长度不同,这会影响其生物利用度和在组织中的分布。
在细菌细胞中,MK-n在细胞质膜的电子传递中起核心作用,支持形成芽孢的过程,并与致病菌的毒力有关。在人类中,维生素K2不足与骨质疏松、心血管疾病以及胰岛素敏感性下降有关。
▸ 微生物生物合成与已知贡献者
细菌中的甲萘醌合成途径涉及两个关键部分的汇合:萘醌环结构与异戊二烯侧链。这两部分首先通过不同代谢途径分别生成,随后再结合形成醌的核心结构。之后,异戊二烯侧链通过逐步添加异戊二烯单位而延长,产生侧链长度不同的甲萘醌变体。这种结构多样性带来功能上的分工,也可能有助于不同细菌适应环境。
目前,若干能产生甲萘醌的细菌菌株已作为工业食品发酵的发酵剂使用,并显示出可提高培养基中维生素K含量的能力。例如,将乳酸乳球菌(Lactococcus cremoris、L.lactis)和乳明串珠菌(Leuconostoc lactis)在复原奶粉或豆奶中培养时,可产生长链MK,并且水平几乎接近成人每日适宜摄入量。这些发现支持:发酵食品可以成为维生素K2的重要膳食来源。
// 小结
总结来说,维生素K有两大类:K1主要来自绿叶菜;K2主要由细菌合成。K2不是单一物质,而是一系列“MK-n”家族成员,侧链长短不同,会影响人体吸收与在体内去向。
对细菌来说,K2是能量代谢(电子传递链)的关键分子,还与芽孢形成和致病性相关。对人来说,K2不足可能与骨质疏松、心血管问题以及胰岛素敏感性变差有关。有些用于发酵的乳酸菌在牛奶或豆奶里能产出一定量的K2,说明发酵食品可能是补充K2的一个重要来源。
▸ 分子测序方法
近一二十年来,高通量测序、多组学与计算建模的重大进展,极大提升了我们对人类肠道微生物组的理解,包括其参与维生素生物合成的作用。
通过测序的基因组与生物信息学绘制“群落层面”的维生素合成潜力。
分享一些有趣关联:高纤维饮食人群的肠道微生物组更富集叶酸与核黄素“潜在生产者”,而西式饮食与更高的“维生素合成缺失”(更依赖外源获取)相关。不同年龄也有差异:成人整体合成潜力更强;婴儿相对更富集维生素K2相关的甲萘醌与叶酸合成潜力。
在临床队列中,2型糖尿病患者的维生素K2及多种B族维生素合成基因丰度下降,提示微生物维生素代谢可能与健康状态相关。
有研究发现炎症性肠病(IBD)患者的钴胺素(维生素B12)与硫胺素(维生素B1)合成相关基因表达显著降低,说明疾病本身会影响微生物维生素代谢的“实际运行”。
!
不足之处
但需要强调的是:无论是16S rRNA 测序还是宏基因组测序,目前主要评估的是菌群的潜在功能能力”——其推断结果高度依赖检测机构所采用的整合菌群基因与代谢通路数据库。现有数据库仍可能存在注释不全或偏倚:替代通路、新发现酶及非模式菌的功能注释缺口更为常见,从而带来功能推断的不确定性。
现阶段,基因组学层面的“检出”并不能直接证明相关基因已在体内表达、对应酶活性确实发生并产生了可观的生理效应;这类问题往往需要结合转录组、蛋白组(必要时包括代谢组)等证据链来支撑。
因而,更理想的路径是将菌群组学结果与人群膳食摄入、临床指标与其他组学数据联合分析,才能更清晰地反映人体维生素“合成—转化—吸收—利用”的真实状态;这也与谷禾健康正在持续研发与构建的综合模型思路一致。
基于上述限制,在谨慎选择菌群检测机构的同时,也应对菌群评估报告中的营养相关指标保持审慎解读:建议结合受试者的症状体征、既往史与用药/补充剂使用、饮食结构及实验室检查结果,进行综合判断与个体化干预,避免将“功能预测”直接等同于“临床结论”。
总体而言,基因组与生物信息学为绘制肠道微生物合成、改造或获取维生素的遗传潜力提供了强有力的入口。它们无法单独给出真实产量与功能输出,但能指导饮食和了解评估肠道菌群代谢维生素的合成和利用潜力,并在群落尺度上建模预测代谢。
▸ 培养方法
测序等基于序列的方法极大拓展了我们对微生物代谢的认识,但要在实验上“坐实”某个微生物是否真的能合成维生素,培养(culture-based)方法仍然不可或缺。通过培养,我们可以直接测试代谢能力、分离出能产维生素的菌或需要外源维生素才能生长的菌(营养缺陷/依赖型),并在营养成分严格可控的条件下设计实验来研究微生物之间的相互作用。
在实验室条件下评估微生物维生素生物合成潜力的一种经典且至今仍广泛使用的方法,是利用“营养缺陷指示菌株”(auxotrophic indicator strains)。这类菌的生长依赖某一种特定B族维生素的外源供给,因此可以通过其生长反应来定量推断样品中该维生素的可用量。这种测定已大量用于研究乳酸菌和双歧杆菌产生叶酸、硫胺素(维生素B1)和钴胺素(维生素B12)的能力。
研究者也会用体外体系直接观察微生物之间的“维生素互喂/交叉供养”(cross-feeding):把一种需要维生素的菌和一种能合成维生素的菌配对共培养。比如在缺乏叶酸的培养基中,R. intestinalis 与 B. bifidum 共培养时能够生长,因为后者会被动向环境释放叶酸合成的中间产物。类似地,在没有外源硫胺素的情况下,Roseburia faecis 能维持对硫胺素依赖的F.prausnitzii 的生长,说明物种间确实发生了有效的营养共享。
为了更接近肠道微生物生态系统的复杂性并延长观察时间,更复杂的体外培养平台(如基于生物反应器的发酵系统)也被用于相关研究。这类封闭、动态系统可以精确调控环境参数(如pH、滞留时间、底物输入),并能长期维持稳定、可重复的“合成”微生物群落。尽管它们已被广泛用于模拟结肠条件下的微生物生态与代谢产物研究,但直接用于研究肠道菌B族维生素的合成与交换目前仍相对有限。不过,这些系统为未来在更接近生理条件的环境中捕捉微生物营养互作提供了很有前景的框架。
!
局限性
但培养方法也有先天局限:相当一部分肠道微生物在标准实验室条件下仍难以培养,限制了我们对一些关键群落成员维生素代谢能力的评估。尽管如此,培养仍是功能微生物学的基石,因为它能对维生素的合成、转运以及物种间交换进行直接的实验验证。
▸ 分析化学方法与代谢组学
代谢组学在阐明微生物代谢方面居于补充重要地位:它通过检测和定量代谢产物,直接提供“微生物实际产生了什么”的证据,因此适合用来研究宿主—微生物以及微生物—微生物之间的代谢互作,包括微量营养素(如维生素)的动态变化。
代谢组学方法大体分为靶向和非靶向两类。靶向代谢组学使用已知标准品,对特定代谢物进行精确定量,例如B族维生素及其衍生物/不同活性形式(vitamers)。
非靶向代谢组学则试图给出更全面的代谢物“全景图”,用于发现意料之外或新的代谢变化。
目前,对代谢物的检测、鉴定与定量能力依赖于分析化学平台的快速发展,包括:
-气相色谱(GC)
-液相色谱(LC)
-高/超高效液相色谱(HPLC、UPLC)。
其中,LC尤其是与质谱联用(LC‑MS)已成为最通用、应用最广的代谢组学工具之一。LC‑MS通常配合电喷雾电离(ESI),可以在食品、牛奶、药物制剂、婴儿配方奶粉、血液和人类粪便等复杂样品中,同时分析多种B族维生素和甲萘醌(维生素K2的一类化合物)。
LC‑MS的一种更高级形式是液相色谱‑串联质谱(LC‑MS/MS)。它通过两级连续的质量分析显著提高灵敏度和特异性,不仅能检测痕量化合物,还能区分结构非常相近的分子,比如同一种维生素的不同同分异构体/不同活性形式。例子是:近期已有研究用LC‑MS/MS实现了维生素B12三种活性形式的同时精准定量,体现了该技术在解析微量营养素“精细多样性”方面的价值。
!
注意
尽管这些方法已成功用于从复杂食物和生物样品中区分并定量多种B族维生素的活性形式,但它们用于研究人体肠道中“微生物自身合成维生素”的工作仍相对有限。不过,由于其高特异性和高灵敏度,这类技术很有潜力成为未来研究的重要工具。
▸ 临床前模型
要真正理解肠道菌群的维生素代谢是否真的有功能意义、能否影响维生素稳态,并为调控菌群来改善健康提供依据。因此,需要把“微生物活动”和“宿主反应”放在同一个整体里研究的宿主相关模型。
▸ 为什么常用鼠类模型?
研究肠道菌群与宿主互作最常用的是动物模型,尤其是小鼠和大鼠。它们的优势是环境和变量可控,能系统地观察“菌群—维生素—宿主”的因果关系。
例如:在叶酸缺乏的大鼠中,给予能大量产叶酸的双歧杆菌(如 Bifidobacterium adolescentis、B.pseudocatenulatum)可以帮助恢复叶酸水平。这类实验说明:微生物合成的维生素有可能在体内发挥营养补充作用。
此外,由于B族维生素与多种人类疾病相关,鼠类也常用来模拟疾病状态,以研究菌群维生素代谢对病理过程的影响。
▸ 维生素合成益生菌:对炎症性疾病的潜力
能合成B族维生素的益生菌在治疗炎症性疾病(尤其是肠道炎症)方面显示出潜力:产核黄素(维生素B2)的 Lactiplantibacillus plantarum CRL2130:在小鼠溃疡性结肠炎和肠黏膜炎模型中,可降低炎症细胞因子、改善症状。
产叶酸的 Streptococcus thermophilus(CRL808、CRL415):在化学诱导的小鼠模型中,可减轻肠黏膜炎症。
若联合使用“产叶酸 + 产核黄素”菌株:在乳腺癌化疗动物模型中,既能提高化疗效果,又能降低如黏膜炎等副作用。
▸ 对神经系统也可能有帮助(动物证据)
一些产B族维生素的菌株在神经保护方面也有动物实验支持:
在帕金森病小鼠模型中,口服产核黄素的L.plantarum CRL2130 或产硫胺素(维生素B1)的 L. plantarum CRL1905,可改善运动协调能力,并减少多巴胺能神经元损失。
这些效果与直接补充商业维生素相当,提示“微生物在体内合成的维生素”确实影响人体维生素的浓度和利用,并能在功能上支持宿主的营养与生理过程。
!
局限性
鼠类模型很有价值,但也要谨慎外推到人:小鼠/大鼠在人类的解剖结构、免疫系统、代谢方式上都有差异,所以动物结果未必等同于人体效果。即便如此,它们仍然是连接体外机制研究与人体真实生理的重要桥梁,用于在“整体生物体”层面验证假设。
人类肠道中微生物维生素生物合成形成的复杂网络,正在成为理解“微生物组—宿主”相互作用的核心内容之一。肠道微生物合成、共享并调节维生素可获得性的能力,并不只是简单的代谢功能,而是一条涉及生态协作、支持宿主以及进化适应的关键轴线。
在过去十年里,高通量测序、功能基因组学以及整合组学的发展显示:许多肠道细菌并不具备合成必需维生素的完整生物合成途径。相反,它们通过代谢交叉喂养形成合作网络,在群落成员之间交换代谢中间体或完整维生素。这些网络有力地说明:肠道微生物群并非一群彼此独立的个体,而更像一个协同运作的“代谢共同体”,并且与宿主健康紧密相关。
要在生态系统层面全面理解这种代谢,需要多学科的方法组合,用于绘制维生素合成的潜力,培养与实验验证能够提供因果证据与机制洞见;动物模型则用于在生理环境中验证微生物贡献。
只有整合这些方法,我们才能把握微生物维生素代谢的全部深度与细微差别。
首先,需要提升组学数据的分辨率与功能解读能力,尤其是针对非模式微生物类群以及非典型维生素变体。这要求建立更完整、更高质量的数据库,并使用更高分辨率,更大人群的组学技术来完善预测,揭示维生素代谢的调控与生态动态。
同样重要的是,将基础发现转化为可行干预手段的需求正在增长。通过使用具有明确维生素产能谱的益生菌、调整饮食以促进微生物合成,或开发个性化的微生物组营养治疗,用于营养支持、疾病预防与个体化健康管理。