-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com

谷禾健康
肠道微生物组作为人体“第二基因组”,在癌症的发生、发展及治疗反应中扮演着日益重要的角色。这些微生物不仅在局部和全身层面调节免疫应答,还深刻影响着炎症、免疫监视和耐受性。
平衡良好的微生物群是有效免疫功能的基石,但由饮食,环境因素,生活方式,感染或药物驱动的干扰可能会促进慢性炎症并损害抗肿瘤免疫力。越来越多的证据表明,这些干扰不仅有助于肿瘤的发生和发展,而且还对治疗产生耐药性。
微生物及其代谢产物能够通过局部及全身性机制,直接影响药物代谢、塑造免疫微环境,并改变肠道、全身乃至肿瘤微环境(TME)中的转录和表观遗传程序。
大量新兴数据支持,微生物组作为预后和预测性生物标志物、癌症防治中可调控因素以及治疗靶点的巨大潜力。以微生物组为靶点的干预措施(如粪菌移植、饮食调整、益生元和益生菌)可作为传统癌症疗法的辅助手段,增强疗效并降低毒性。
本文探讨了微生物组驱动癌症发生发展的多维机制,包括基因毒性、慢性炎症和表观遗传调控。详细分析微生物组如何调节化疗、放疗及免疫治疗的疗效与不良反应,还系统梳理了当前基于微生物组的癌症治疗策略,如粪菌移植、饮食干预、益生菌和后生元等,并总结了相关临床试验的进展。
历史上,微生物与癌症的关联常采用科赫假设(Koch’s postulates)等框架,将疾病归因于具有确定潜伏期的单一病原体。然而,现在人们认识到,微生物作为复杂的群落发挥作用,对宿主产生集体效应,而不仅仅是孤立的病原体。这些效应包括调节炎症、免疫、代谢和表观遗传,从而深刻影响致癌过程。
微生物驱动的致癌机制
微生物群通过多种复杂的机制促进肿瘤的启动和进展,主要包括直接的基因毒性效应、诱导慢性炎症和肠道屏障功能障碍,以及对宿主细胞的表观遗传调控。这些机制相互交织,共同构成了一个促癌的微环境。
肠道微生物组可通过诱导基因组损伤、表观遗传调控或破坏肠道屏障功能参与癌症的启动和/或进展。这些机制共同作用,促进了从正常上皮到恶性肿瘤的转化。
病原菌的致癌策略:信号传导与毒素的双重威胁
定植于上皮表面的病原菌或机会性细菌可通过直接的宿主细胞信号传导、微生物间通讯或分泌毒素发挥致癌作用。其中,细菌基因毒素是研究最为深入的直接致癌因素之一。这些毒素包括tilimycin、indolimines、tilivalline、colibactin和脆弱拟杆菌毒素(Bacteroides fragilis toxin, BFT)等。
编辑
-Colibactin
在这些毒素中,Colibactin的机制研究最为透彻。Colibactin由存在于变形菌门(如特定大肠杆菌菌株)中的聚酮合酶(pks)基因岛编码。这种基因毒素能够诱导DNA双链断裂和烷基化,从而引发基因组不稳定性,促进癌症的发生。
编辑
图源:doi.org/10.1038/s41579-025-01268-6
例如,一项研究发现,在结直肠癌中,由产colibactin的大肠杆菌(pks+ E. coli)引起的突变特征与早发性CRC相关。此外,产BFT的脆弱拟杆菌(ETBF)能够协同pks+ E. coli,其产生的BFT和黏液溶解活性使得colibactin能够穿透黏液层,到达上皮细胞,从而加剧DNA损伤。
微生物代谢物:潜在的DNA损伤元凶?
除了直接的基因毒素,微生物代谢物也可能具有DNA损伤效应。例如,有研究指出微生物将初级胆汁酸转化为次级胆汁酸,后者过量可通过诱导DNA损伤、调节炎症通路和抑制抗肿瘤免疫反应(包括抑制在癌症免疫监视中至关重要的细胞毒性CD8+ T细胞)来促进结直肠肿瘤的发生。
同样,肠道微生物将管腔中的乙醇转化为乙醛,或将某些亚硝胺类致癌物(如N-丁基-N-(4-羟丁基)亚硝胺)转化为更具活性的形式,这些过程均可导致基因组损伤。
雌激素与微生物:远程影响
此外,微生物的β-葡萄糖醛酸酶(GUS)能够重新激活在肝脏中被结合失活的雌激素,提高循环雌激素水平,这可能对乳腺癌等雌激素敏感性肿瘤的发生构成远距离影响。
慢性炎症与肠道屏障功能障碍
慢性微生物感染是癌症发生的重要驱动力
例如,幽门螺杆菌(Helicobacter pylori)感染通过诱导持续性胃部炎症,促进胃癌的发生,而根除幽门螺杆菌已被证实可以预防胃癌。同样,伤寒沙门氏菌(Salmonella typhi)与胆囊癌的发生相关。
编辑
图源:doi.org/10.1038/s41579-025-01268-6
微生物组失衡促癌变
即使在没有明显感染的情况下,微生物组失衡也能通过调节局部炎症反应促进癌变。
例如,通常存在于口腔的具核梭杆菌(Fusobacterium nucleatum)在特定条件下可定植于肠道,并在CRC肿瘤中诱导肿瘤微环境的炎症。
炎症与癌症之间的复杂信号网络
微生物诱导的炎症部分通过模式识别受体(如Toll样受体,TLRs)信号和炎症小体激活介导,导致细胞因子和活性氧(ROS)的产生,这些分子刺激上皮增殖、免疫逃逸以及癌细胞在远端部位的播散和植入。
肠道炎症与肠道屏障功能障碍密切相关
屏障功能受损,即黏液层和上皮细胞无法在管腔微生物群落与宿主上皮之间提供足够的空间,增加了促癌微生物和分泌性基因毒素造成损害的易感性。受损的屏障完整性促进了微生物产物(如脂多糖,LPS)和代谢物(如胆汁酸)的易位,进入体循环。这些因素可驱动远端组织的全身性炎症或免疫抑制,可能导致远端上皮和非上皮癌症及转移的发生。
编辑
保护性微生物代谢物的作用
一些微生物代谢物,如膳食纤维在结肠中发酵产生的短链脂肪酸(SCFAs),通过促进紧密连接形成和刺激黏液产生,对肠道屏障具有保护作用。
表观遗传调控
肠道微生物组是一个强大的表观遗传调节器,能够通过代谢、炎症和饮食-微生物相互作用的组合来塑造基因表达和肿瘤行为。
图源:doi.org/10.1038/s41579-025-01268-6
丁酸盐的双重角色:从能量源到表观遗传调控
最典型的微生物驱动的表观遗传调控机制是SCFA中的丁酸盐对组蛋白去乙酰化酶(HDAC)的抑制。在健康的上皮细胞中,丁酸盐是支持增殖和分化的能量来源。然而,随着肿瘤细胞代谢转向有氧糖酵解(瓦博格效应),丁酸盐不再被有效消耗。其积累导致过度HDAC抑制,改变染色质构象,促进抑癌基因的转录激活,从而抑制癌变。
膳食成分与微生物的影响
其他微生物或膳食成分也能影响表观基因组。例如,叶酸、亚硝胺和致肥胖饮食在小鼠模型中影响DNA甲基化和组蛋白乙酰化,促进肠道肿瘤发生。
产毒脆弱拟杆菌的致癌机制
有趣的是,在小鼠模型中,产肠毒素的脆弱拟杆菌(ETBF)定植通过破坏DNA修复机制促进结直肠肿瘤发生,并诱导广泛的CpG岛高甲基化,这是肿瘤组织中表观遗传变化的标志。
不同类型的癌症与特定的微生物组特征相关联,这些特征不仅存在于胃肠道肿瘤中,也见于乳腺癌、前列腺癌等远端肿瘤,揭示了微生物组在肿瘤生态系统中的广泛影响。
结 直 肠 癌
结直肠癌(CRC)的发展与多种微生物、其代谢物和结肠上皮之间的相互作用密切相关。在动物模型和细胞培养研究中,特定微生物如ETBF(产肠毒素的脆弱拟杆菌)、具核梭杆菌(F. nucleatum)和携带pks基因岛的大肠杆菌(pks+ E. coli)被证明有助于肿瘤发生。
将结直肠癌患者的粪便微生物群移植到无菌小鼠体内,会导致细胞增殖增加、息肉数量增多、异型增生更严重以及炎症标志物水平升高,这强烈表明肠道微生物组失衡可能是结直肠癌发展的致病因素。
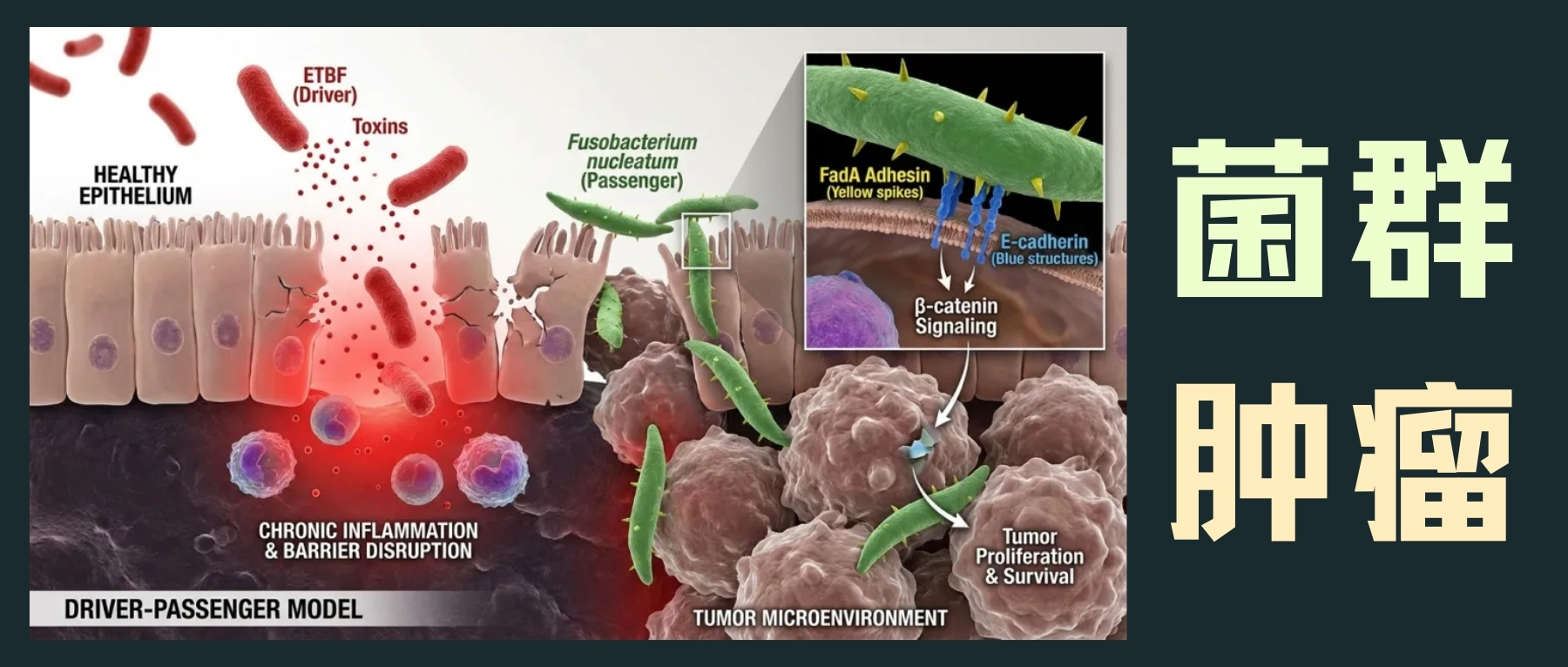
驱动-乘客模型:微生物的协同作用
“驱动-乘客”模型提出,像ETBF这样的驱动菌通过引发慢性炎症和破坏上皮屏障,创造一个允许性环境,让像具核梭杆菌这样的共生乘客菌得以定植并加剧肿瘤进展。具核梭杆菌通过其细胞表面的FadA黏附素与上皮E-钙黏蛋白直接相互作用,激活β-连环蛋白信号通路,促进肿瘤细胞增殖和存活。
编辑
具核梭杆菌与化疗耐药性
此外,具核梭杆菌还通过刺激肿瘤细胞中的自噬相关蛋白,与化疗药物的细胞毒性作用相抗衡,从而与化疗耐药性相关。临床上,结直肠癌肿瘤组织中的具核梭杆菌DNA水平较高与结直肠癌特异性死亡率增加相关,表明其可作为潜在的预后生物标志物。
胃 癌
在胃癌中,幽门螺杆菌(H. pylori)感染是公认的关键致病因素。它通过其毒力因子(如CagA和VacA,在谷禾16S Plus检测实践中,也会检出个别受检者携带 CagA和VacA毒力基因)引发炎症和免疫反应,进而可能有诱发癌症风险。然而,随着胃癌进展,胃内环境发生萎缩,幽门螺杆菌数量反而减少,而其他非幽门螺杆菌物种(如乳酸杆菌属、链球菌属)开始增多。
肝 细 胞 癌
在肝细胞癌(HCC)中,肠-肝轴起着关键作用。肠道屏障功能受损导致细菌及其产物(如LPS)易位至肝脏,诱发炎症、纤维化和肝细胞损伤,最终促进癌变。
肝细胞癌患者的肠道微生物组通常表现为产SCFA的细菌多形拟杆菌(Bacteroides thetaiotaomicron)减少,而促炎细菌(如大肠杆菌)增多。
胰 腺 导 管 腺 癌
胰腺导管腺癌(PDAC)同样与肠道微生物组失调相关。肠道屏障受损允许某些肠道微生物(如变形菌门)易位至胰腺,在局部创造一个免疫抑制的微环境,促进肿瘤进展。此外,微生物对胆汁酸的代谢异常也被认为是PDAC的风险因素之一。
激素依赖性癌症
肠道微生物组在激素代谢中发挥着重要作用,从而影响激素依赖性肿瘤的进展。所谓的雌激素菌基因组(estrobolome)是指能够代谢雌激素的细菌基因集合。肠道中的细菌β-葡萄糖醛酸酶可以解偶联在肝脏中结合的雌激素,使其重新被吸收入血,提高循环中活性雌激素的水平,从而促进乳腺癌等雌激素驱动肿瘤的生长。
在乳腺癌患者中,具有β-葡萄糖醛酸酶活性的菌种(如梭菌属)丰度增加可能与更严重的临床分期有关。同样,在前列腺癌中,肠道菌群能够从头合成雄激素或将皮质醇代谢物转化为雄激素,促进对内分泌治疗的抵抗。
癌症的多步发生模型认为,遗传和表观遗传的序贯改变是恶性转化的驱动力。新兴证据表明,微生物组的失调可能是这一模型中一个额外的、相互关联的因素。
生命早期的微生物组发育
微生物组的发育始于生命早期,受分娩方式、喂养习惯和饮食转变的影响。在这一关键窗口期的干扰可能导致微生物多样性永久性降低和对免疫与代谢稳态至关重要的关键菌种的缺失。
生活方式对微生物组的影响
在整个生命周期中,累积的损害(包括抗生素滥用、慢性压力和低纤维、超加工饮食)会进一步侵蚀微生物的多样性和功能。这种微生物恢复力的逐步丧失可能会损害上皮完整性、增加炎症、削弱代谢信号和免疫监视。
多个研究和科学家提出,微生物组的这种纵向退化可能会降低癌症启动和进展的阈值,与经典致癌过程中的逐步遗传事件相平行。
微生物组健康随生命周期的逐步退化可能促进癌症发展
编辑
图源:doi.org/10.1038/s41579-025-01268-6
图中显示了肠道微生物组健康和恢复力的两种对比轨迹
每次急性干扰后恢复不完全,导致微生物组健康和恢复力逐步退化。
持续的压力源可能将个体推向恶化轨迹,直至达到癌症发展概率更高的阈值。
癌症治疗反应的变异性受到多种宿主和肿瘤相关因素的影响,而肠道微生物组是导致这种变异性的一个重要贡献者。
微生物组主要通过两大机制调节癌症治疗结果:
一是通过微生物对治疗药物的生物转化以及药物对微生物组的反作用;
二是通过微生物介导的宿主免疫反应调节。
微生物组与化疗、放疗及靶向治疗
肠道微生物组编码着庞大的基因库,能够代谢多种肿瘤学和非肿瘤学药物,从而影响药物的生物利用度、疗效和毒性。
微生物介导的影响癌症治疗结果的机制
编辑
图源:doi.org/10.1038/s41579-025-01268-6
药物的微生物生物转化
一个典型的例子是化疗药物5-氟尿嘧啶(5-FU)及其口服前药卡培他滨。某些大肠杆菌和厌氧棒状菌属(Anaerostipes)表达细菌二氢嘧啶脱氢酶(DPD),能将5-FU转化为其非活性形式,从而可能降低其疗效。
类似地,用于治疗胰腺癌的吉西他滨可被某些肿瘤相关γ-变形菌纲细菌表达的胞苷脱氨酶(CDA)脱氨而失活,导致耐药。
微生物也能激活药物
拓扑异构酶I抑制剂伊立替康在肝脏中被代谢为活性形式SN-38,随后经葡萄糖醛酸化为无活性的SN-38G,通过胆汁排入肠道。肠道中的细菌β-葡萄糖醛酸酶(GUS)能将SN-38G重新激活为SN-38,后者会引起严重的上皮损伤、黏膜炎和腹泻等剂量限制性毒性。虽然理论上肿瘤内的再激活可能增强疗效,但肠道内的再激活主要导致毒性增加。
微生物影响疗效与毒性
除了直接代谢药物,微生物组还能通过调节免疫系统间接影响化疗效果。例如,化疗药物环磷酰胺能促进特定肠道细菌(如Enterococcus hirae)易位至次级淋巴器官,诱导产生有助于其治疗效果的TH17细胞(T辅助17细胞)反应。
同样,奥沙利铂的疗效被发现依赖于肠道微生物组,肠道菌群通过激活免疫系统来增强抗肿瘤效果。
放疗与微生物组之间的双向互动
一方面,放疗(尤其是盆腔放疗)会显著改变肠道微生物组的组成,导致多样性下降,并可能增加机会性病原菌。
另一方面,微生物组的组成可以预测患者对放疗的反应和毒性。例如,放疗前肠道菌群多样性较低与晚期放射性肠病相关。在小鼠模型中,粪菌移植(FMT)被证明可以保护机体免受辐射引起的毒性。
靶向治疗
对于靶向治疗,研究尚处早期。一项针对转移性CRC的研究发现,对抗EGFR(西妥昔单抗)和抗VEGF(贝伐珠单抗)治疗的疾病进展组患者,其肠道微生物组中具核梭杆菌的丰度显著高于部分缓解组。
在HER2阳性乳腺癌中,抗生素使用或移植来自抗生素处理供体的小鼠粪菌会削弱曲妥珠单抗的抗肿瘤效果。
微生物组与免疫治疗
免疫检查点抑制剂(ICIs)通过阻断T细胞上的抑制性信号(如PD-1、CTLA-4),重新激活细胞毒性CD8+ T细胞以攻击肿瘤,彻底改变了癌症治疗。然而,只有部分患者对ICIs有反应,而肠道微生物组是决定疗效的关键因素之一。
►▷ 微生物组如何调节免疫反应与治疗效果
多项早期研究独立证实,肠道微生物组的组成与抗PD-1/PD-L1治疗的反应相关。
尽管与疗效相关的具体菌种在不同研究中有所差异(如Akkermansia、Bifidobacterium、Ruminococcus),但其免疫调节机制常常趋同于增强CD8+ T细胞的数量或活性。
例如,在临床前模型中,口服双歧杆菌可增强树突状细胞(DC)的激活和CD8+ T细胞的启动,从而增强对PD-L1阻断的反应。同样,Akkermansia muciniphila通过促进CD8+ T细胞招募至肿瘤,来增强对PD-1抑制的反应。
这些发现表明,与ICI疗效相关的菌种可能共享一种能力,即在肠系膜淋巴结或肠黏膜中诱导依赖于DC的CD8+ T细胞启动,随后通过趋化因子介导浸润至TME。
肠道菌群的影响:U型效应
值得注意的是,微生物组对ICI疗效的影响可能具有“U型”或“倒U型”特征。
编辑
例如,一项针对晚期非小细胞肺癌(NSCLC)患者的研究发现,肠道中A. muciniphila的相对丰度处于中等水平(而非低或高水平)的患者,其临床反应最佳。这提示微生物的影响并非简单的“越多越好”,而是需要一个平衡的生态系统。
►▷ 微生物代谢物:抗肿瘤免疫的关键因素
微生物的功能冗余性可能比分类学组成更为关键,即不同的微生物群落可能产生相似的代谢或免疫输出。多种微生物代谢物被证明在调节免疫治疗反应中发挥核心作用。
肠道微生物代谢物与免疫
编辑
图源:doi.org/10.1038/s41579-025-01268-6
该图描绘了肠道微生物组与免疫系统之间的相互作用,说明了膳食成分(如纤维)如何影响SCFAs、胆汁酸和色氨酸衍生物的产生。这些代谢物调节多种免疫细胞,并通过调节炎症细胞因子和增强癌细胞凋亡来促进抗肿瘤免疫和ICI治疗效果。
编辑
图源:doi.org/10.1038/s42255-025-01287-w
代谢物的作用是情境依赖的
例如,丁酸盐在某些情况下能增强细胞毒性CD8+ T细胞功能,支持抗肿瘤免疫,但在其他条件下也可能促进免疫抑制性的Treg细胞扩增。
同样,具核梭杆菌在不同研究中显示出截然相反的作用:一项研究表明其产生的丁酸能敏化MSS型CRC对ICIs的反应,而另一项研究则发现其产生的琥珀酸会抑制免疫信号通路,导致耐药。
这凸显了菌株、肿瘤微环境和代谢产物背景的复杂性。
►▷ 肠道菌群预测免疫相关不良事件
ICIs激活的免疫系统也可能攻击正常组织,导致免疫相关不良事件(irAEs)。多项报告将基线肠道微生物组组成与irAEs的发生风险联系起来。
然而,由于患者群体异质性、队列规模小以及irAEs定义不一致等原因,目前尚未发现一致的预测性微生物标志物。一些研究提示,特定的菌群(如拟杆菌门丰度较高)可能与结肠炎风险增加有关,但仍需更多机制性研究来阐明因果关系。
鉴于微生物组与癌症疗效和毒性的密切联系,操纵微生物组成员为增强治疗效果提供了新的契机。一系列策略正在研究中,包括饮食干预、益生菌/益生元、粪菌移植(FMT)以及更前沿的工程菌和后生元等。
这些干预措施旨在通过重塑微生物组生态系统,来调节药物代谢、增强抗肿瘤免疫或减轻治疗毒性。
编辑
图源:doi.org/10.1038/s42255-025-01287-w
粪菌移植 (FMT)
粪菌移植是目前研究最深入的微生物组干预手段之一。两项开创性的I期临床试验表明,将来自对ICI有反应的黑色素瘤患者的粪便微生物群移植给耐药患者,可以使一部分患者转为应答者,并伴随着CD8+ T细胞活化增强或TME中免疫细胞浸润的有利变化。
最近,一项在晚期黑色素瘤患者中进行的 I期试验进一步证实,接受健康供体FMT后,患者对一线抗PD-1治疗的反应得到改善,其粪便样本能够在小鼠模型中恢复抗PD-1疗效。
此外,FMT也被用于治疗难治性ICI相关性结肠炎,初步研究显示其能有效缓解症状,并伴随免疫细胞谱的改变。目前,大量临床试验正在探索FMT联合ICI在不同癌种(如肾细胞癌、NSCLC)中的应用。
饮食、益生元与益生菌
饮食干预是一种极具性价比的策略
一项观察性研究发现,高纤维饮食(不使用益生菌)与改善的ICI结局相关。
BE GONE试验(NCT02843425)等临床研究正在评估高纤维食物(如豆类)对微生物组和临床结局的影响,初步结果显示其能增加有益菌(如Faecalibacterium)并改善炎症标志物。
注:zhuBE GONE试验(NCT02843425)是一项由MD安德森癌症中心开展的临床研究,旨在探索食用 canned navy beans对肠道微生物组的影响,以及这种饮食干预是否能减轻肥胖对结直肠癌风险的负面影响。
传统益生菌
益生菌的应用也备受关注。一些传统益生菌(如某些乳杆菌和双歧杆菌)被发现能通过产生特定的代谢物(如I3A、吲哚-3-羧酸)或直接作用来增强抗肿瘤免疫。
下一代益生菌 和 工程菌
例如,A. muciniphila被多项研究证实与ICI的良好反应相关,其巴氏杀菌形式(一种后生元)或其膜蛋白Amuc_1100在临床前模型中显示出抗肿瘤效果。
工程化的大肠杆菌Nissle 1917菌株被改造用于在肿瘤局部递送免疫刺激分子(如将氨转化为L-精氨酸)或免疫检查点抑制剂纳米抗体,从而在不产生全身毒性的情况下增强抗肿瘤免疫。
微生物组干预策略面临的挑战
– 机制不确定性
许多干预措施(如高纤维饮食、传统益生菌)缺乏对特定菌种或功能如何调节疗效的深入机制理解,导致策略普适化,而非个体化。
– 情境依赖性和个体差异
微生物组的效果受宿主遗传、肿瘤类型、治疗方案和生活方式等多种因素影响,使得干预效果难以一概而论。
– 缺乏个体化生物标志物
目前缺少可靠的生物标志物来指导患者分层,或确定应靶向微生物的哪个方面(如药物代谢、屏障功能或免疫调节)。
– 临床试验设计的局限性
癌症患者常伴有免疫抑制、恶病质或胃肠道毒性,难以依从严格的饮食方案或口服疗法。此外,抗生素的普遍使用也干扰了微生物组的评估和干预。
除了作为治疗靶点,微生物组在癌症的早期检测和风险分层方面也展现出巨大潜力。
早期检测与风险分层
肠道微生物组已被探索作为早期癌症检测的工具,尤其是在结直肠癌领域。多项研究通过比较癌症患者与健康对照的微生物组谱,试图识别可用于诊断的微生物标志物。
谷禾健康通过上万例的结直肠癌和结直肠息肉患者及健康对照构建的肠癌识别模型,在样本量、病例类型覆盖与真实世界差异性方面显著优于多数以“数十到数百例”为主的研究型队列。更大的队列意味着模型能够学习到更稳定、可重复的微生物特征组合,降低因地域、饮食、年龄结构、用药史等因素带来的偶然偏差,从而在实际应用中具备更强的泛化能力与可识别性。
同时,许多研究仅做“癌症 vs 健康”的二分类;谷禾模型纳入“结直肠息肉”等癌前人群,更贴合早筛需求,能在症状出现前识别风险,并捕捉从健康到息肉/腺瘤再到癌变的连续变化信号,从而支持早期风险分层与更有针对性的随访与干预。
谷禾结直肠癌模型示意图
编辑
<来源:谷禾肠道菌群检测数据库>
但是不管是谷禾的模型还是科学研究的结果直接引用于临床诊断还需要有一段路走。
首先,横断面研究难以区分因果关系和相关性,且易受混杂因素(如并存病、用药)的干扰。
其次,与现有筛查手段(如 FIT/粪便免疫化学、结肠镜、影像与血液指标)进行对照评估,确定其增益价值与适用场景;并建立标准化的采样、测序/检测、质控与解读体系,控制抗生素、饮食、肠道准备等混杂因素影响。
伴 随 诊 断
微生物组作为伴随诊断工具的前景可能更为广阔,可用于指导治疗决策、预测疗效或毒性风险。例如,通过检测治疗前的肠道或肿瘤微生物组,可以识别出对特定疗法(如ICI)反应可能性较高的患者,或发生irAEs风险较高的患者。
基于对瘤胃球菌(Ruminococcus)等丰度的检测,可以对接受ICI治疗的患者进行分层。理想的伴随诊断应植根于机制理解,而不仅仅是关联数据,从而指导个性化干预,例如决定是否需要将FMT作为一线辅助治疗,或是否需要先通过菌群移植恢复患者对膳食纤维的降解能力再进行饮食干预,而不是盲目的粪菌移植。
人工智能(AI)有望通过实现高级数据整合、模式识别和预测建模,彻底改变微生物组研究。
编辑
图源:doi.org/10.1038/s41579-025-01268-6
面对微生物组多组学数据维度灾难(即特征数量远超样本数量)的挑战,AI提供了解决方案。例如,通过降维、合成数据增强或迁移学习等策略,可以提高模型的稳定性和泛化能力。
新兴的AI方法,如变分贝叶斯神经网络和卷积神经网络,能够整合配对的微生物组和代谢组数据,或将多组学数据转换为图像格式进行分析,从而发掘深层生物学关联。
编辑
数字孪生是另一个令人兴奋的方向。这是一个动态的、虚拟的患者复制品,整合了静态数据(如基因信息)和实时数据(如临床记录、组学数据),以模拟、监测和预测健康结果。将微生物组数据纳入数字孪生模型,可以模拟其与宿主和治疗的复杂相互作用,支持假设驱动的干预措施和个性化治疗调整。
为不同生命阶段(如婴儿期和成年期)开发量身定制的数字孪生模型,将为整个生命周期的微生物组靶向干预提供宝贵的指导。
当前临床试验概览
近年来,旨在利用微生物组改善癌症治疗的临床试验数量激增。
FMT试验主要集中于免疫治疗效果良好的癌种(如黑色素瘤、RCC、NSCLC),旨在逆转或改善对ICIs的耐药性(如NCT05286294, NCT04988841)。其他试验则探索FMT在肝癌(NCT05690048)、胰腺癌(NCT06393400)等其他癌种中的应用,或用于减轻治疗相关的毒副反应,如免疫相关性结肠炎(NCT04038619)。
关于益生元、益生菌和后生元的临床试验同样蓬勃发展,多数旨在增强抗癌免疫治疗的效果(如NCT05303493, NCT06250335)。
A.muciniphila(NCT05865730)和C.butyricum等下一代益生菌的专项试验正在进行中。
这些研究不仅关注疗效,也探索其在围手术期管理、预防癌前病变复发以及减轻治疗副作用方面的潜力。
越来越多的证据表明,肠道微生物组是癌症治疗结果的关键调节器,其通过免疫调节、药物代谢和维持上皮屏障完整性等多种机制发挥作用。这一认知推动了新型诊断和治疗策略的开发,但临床转化仍受制于机制不确定性、缺乏个性化生物标志物以及在癌症人群中实施的挑战。
微生物组研究揭示,宿主与微生物群作为一个整合系统运作,治疗结果源于宿主-微生物-药物三者间的动态相互作用。
功能冗余、微生物可塑性和强烈的情境依赖性使得因果推断变得困难,也可能解释了为何微生物标志物在不同研究中难以重复。当前的许多干预措施基于普适性策略而非深刻的机制理解,而个体差异进一步加大了个性化治疗的复杂性。
为了推动该领域的发展,未来的研究必须转向由AI赋能、以机制为导向的精准干预,这需要以可靠的伴随生物标志物为支撑,并通过大规模、纵向的实用性临床试验证实。至关重要的是,临床试验必须考虑癌症患者的特殊限制,并在真实世界环境中关注有临床意义的功能性终点。随着微生物组科学日益融入肿瘤学,它有望通过将机制精度与临床相关性相结合,重新定义癌症治疗,实现更有效、更耐受的疗法。
注:本账号内容仅供参考和学术探讨,不构成医疗诊断或治疗建议。任何健康问题,请务必咨询专业医生。
主要参考文献
Hajjar R, Mars RAT, Kashyap PC. Harnessing the microbiome for cancer therapy. Nat Rev Microbiol. 2026 Jan 5.
Nobels A, van Marcke C, Jordan BF, Van Hul M, Cani PD. The gut microbiome and cancer: from tumorigenesis to therapy. Nat Metab. 2025 May;7(5):895-917.
de Vos, W. M., Tilg, H., Van Hul, M. & Cani, P. D. Gut microbiome and health: mechanistic insights. Gut 71, 1020–1032 (2022).
Domzaridou, E. et al. The impact of oral antibiotics prior to cancer diagnosis on overall patient survival: findings from an English population-based cohort study. Curr. Oncol. 30, 8434–8443 (2023).
Yuan, L. et al. The influence of gut microbiota dysbiosis to the efficacy of 5-fluorouracil treatment on colorectal cancer. Biomed. Pharmacother. 108, 184–193 (2018).
Routy, B. et al. Gut microbiome influences efficacy of PD-1-based immunotherapy against epithelial tumors. Science 359, 91–97 (2018).
Elkrief, A. et al. Antibiotics are associated with worse outcomes in lung cancer patients treated with chemotherapy and immunotherapy. NPJ Precis. Oncol. 8, 143 (2024).
Ransohoff, J. D. et al. Antimicrobial exposure is associated with decreased survival in triple-negative breast cancer. Nat. Commun. 14, 2053 (2023).
Cong, J. et al. Bile acids modified by the intestinal microbiota promote colorectal cancer growth by suppressing CD8+ T cell effector functions. Immunity 57, 876–889.e11 (2024).
Tintelnot, J. et al. Microbiota-derived 3-IAA influences chemotherapy efficacy in pancreatic cancer. Nature 615, 168–174 (2023).
Bender, M. J. et al. Dietary tryptophan metabolite released by intratumoral Lactobacillus reuteri facilitates immune checkpoint inhibitor treatment. Cell 186, 1846–1862.e26 (2023).
Salminen, S. et al. The International Scientific Association of Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of postbiotics. Nat. Rev. Gastroenterol. Hepatol. 18, 649–667 (2021).