-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康
健康的肠道菌群呈现出物种多样性高、结构稳定、功能良好等的特征,有益菌、中性菌和有害菌之间维持着动态平衡。然而,当这种平衡被打破,即发生菌群失衡,便可能成为多种急、慢性疾病的诱因或加剧因素。
目前谷禾积累了大量样本数据,通过对这些数据的深度分析,我们观察到多种多样的菌群状态,其中不乏一些表现出极端特征的案例。这些案例为我们理解菌群失衡的具体模式及其对健康的潜在影响提供了宝贵的窗口。
本文我们选取谷禾数据库中的一些检测报告,深入探讨几种典型的肠道菌群极端失衡状态,包括:菌群多样性严重低下、特定菌门/菌属的极端优势、益生菌缺乏、益生菌补充过量引发的新失衡等。
通过对这些案例的具体数据进行解读,我们希望能为相关研究人员和临床工作者及后端干预方提供更直观的参考,从而共同推动肠道微生态健康管理的发展。
编辑
( – 衡量微生态稳定的指标 – )
菌群多样性是评估肠道微生态健康状况的首要指标。它包含两个维度:一是物种丰富度,即菌种的数量;二是物种均匀度,即各种菌在群落中数量分布的均衡性。
一般情况下,一个高多样性的菌群生态系统更具弹性和稳定性,能够有效抵御外界干扰(如短期饮食改变、药物影响、病原体入侵),并维持正常的生理功能。相反,多样性低的菌群则显得脆弱,更容易在外界压力下崩溃,导致功能紊乱和疾病风险的增加。
案例一:
多样性荒漠化与病原菌疯长的恶性循环
这份报告显示,菌群多样性评分仅为3分(满分100),属非常低的水平。
编辑
<来源:谷禾健康肠道菌群检测数据库>
香农多样性指数仅为2.29(正常中位数约4,5左右)。
注:香农多样性(Shannon Diversity Index)是生态学中用于衡量生物群落多样性的一种常用指标。H′=−∑(pi⋅lnpi).
香浓多样性指数一个是反映了物种丰富度,一个是反映物种均匀度,综合考虑上述两者,数值越高越复杂。
这表明其肠道微生态环境极其单一,稳定性极差。这种荒漠化的肠道环境,为条件致病菌的过度繁殖提供了绝佳条件。
1)菌属构成分析
编辑
<来源:谷禾健康肠道菌群检测数据库>
可以看到,肠道内沙门氏菌属(Salmonella)的丰度非常高,达到了的68.365%,这其中主要是肠炎鼠伤寒沙门氏菌。
这是一种典型的致病菌,由于它的超高丰度,直接导致了变形菌门(Proteobacteria)的占比飙升至71.436%(正常人群中位数一般不超过10%,甚至低于5%)。
变形菌门被广泛认为是促炎菌门,其成员多为条件致病菌。沙门氏菌的肆虐,如同一场生态灾难,严重挤压了其他共生菌的生存空间,直接导致了有益菌(如双歧杆菌、乳杆菌)和大量核心功能菌属的缺失,这是其菌群多样性低下的直接原因。
编辑
<来源:谷禾健康肠道菌群检测数据库>
可以看到有益菌、核心菌属严重缺乏。
2)生理后果与炎症水平
这种极端失衡带来了严重的生理后果。报告显示,其肠道炎症水平高达95(重度炎症),肠道产气严重。这与沙门氏菌感染的典型症状(腹痛、消化不良、炎症反应)相吻合。
编辑
<来源:谷禾健康肠道菌群检测数据库>
同时,丁酸盐(1分,缺乏)、吲哚(2分,缺乏)等关键抗炎和维持肠道屏障功能的代谢物严重不足,进一步加剧了肠道损伤。
3)恶性循环的形成
这是一个典型的“病原菌疯长 → 多样性锐减 → 肠道功能崩溃 → 炎症加剧”的恶性循环。
此案例中我们看到了菌群多样性的重要性。当多样性降至冰点,肠道微生态的防御体系形同虚设,单一病原菌便可一家独大,主导整个群落,并引发严重的健康问题。
对于此类情况,干预策略不仅要考虑补充益生菌,更关键的是要针对性地清除优势病原菌,并创造条件帮助多样性恢复,当然这种较为复杂的情况是需要一个专业干预指导的过程。
上述是多样性很低,大量被病原菌占据的情况下,那么同样是多样性低的时候,有没有可能有一些相对“好”的菌群在竞争中脱颖而出呢?如果有的话,会发生什么呢?我们来看下一个案例。
案例二:
多样性低,大量普雷沃氏菌占据
接下来我们要看的这份报告是多样性低的另一种典型代表。其肠道菌群被普雷沃氏菌属(Prevotella)以61.025%的绝对优势所统治。
编辑
<来源:谷禾健康肠道菌群检测数据库>
普雷沃氏菌属通常与富含碳水化合物和植物纤维的饮食模式相关,常见于素食或以植物性饮食为主的人群。虽然在某些情况下,普雷沃氏菌属被认为是健康植物性饮食的标志,但当其丰度过高,形成单一优势时,问题便随之而来。
1)菌群多样性降低带来的影响
首先,普雷沃氏菌属的过度增殖同样挤压了其他核心菌属的生存空间,导致了菌群多样性的降低。
编辑
<来源:谷禾健康肠道菌群检测数据库>
报告显示,多个产丁酸的关键菌属如瘤胃球菌属(Ruminococcus)、罗氏菌属(Roseburia)、经黏液真杆菌属(Blautia)均处于缺乏状态。
丁酸是结肠上皮细胞的主要能量来源,具有强大的抗炎作用。这些菌的缺失意味着肠道抗炎能力的下降。
编辑
<来源:谷禾健康肠道菌群检测数据库>
2)促炎反应的风险
其次,高丰度的普雷沃氏菌属本身也与促炎反应相关。部分普雷沃氏菌菌株能够产生脂多糖(LPS),这是一种强烈的免疫刺激物,可引发炎症。
更值得警惕的是,该案例中同时伴随着变形菌门中病原菌埃希氏菌属(25.553%)严重超标,影响肠道菌群平衡,同时诱发高炎症风险。
其II型糖尿病风险评估为0.83(高风险),这与菌群的长期失衡和促炎状态可能存在关联,因为慢性低度炎症是胰岛素抵抗和II型糖尿病的重要病理生理基础。
编辑
<来源:谷禾健康肠道菌群检测数据库>
3)生态平衡的重要性
此案例说明,即使是与健康饮食模式相关的菌属,其过度增殖也可能打破生态平衡,导致核心功能性菌群的缺失和炎症风险的升高。肠道健康的关键在于平衡而非某种超级细菌的绝对优势。
普雷沃氏菌属(Prevotella)和拟杆菌属(Bacteroides)的相对丰度则与长期饮食模式(植物性饮食vs.动物蛋白/脂肪饮食)紧密关联。当某一菌群异常增殖,打破了原有的平衡,就会导致一系列代谢和免疫问题。
这提示我们,饮食干预需要精细化,在保证膳食纤维摄入的同时,也需关注蛋白质、脂肪的均衡配比,避免长期单一的饮食结构导致菌群结构的极化。
#########################################
关于 多样性过低 的分析思路:
谷禾报告中,多样性分值<15 提示 “单一菌群”(菌群数量极少,功能单一);15-30 提示 “多样性较低”(需结合临床症状干预) 。
◆ 核心判断
若多样性低伴随核心菌属缺失、 有害菌比例升高,则提示菌群结构失衡,需重点干预。
◆ 原因分析
——外部因素
饮食单一化:长期高糖 / 高脂 / 精粮饮食(如仅吃精制米面),缺乏膳食纤维(<15g / 日),导致菌群可利用底物不足。
药物滥用:广谱抗生素(如头孢类)、化疗药物直接杀灭有益菌,破坏菌群平衡。
生活方式:久坐少动(肠道蠕动减慢,菌群代谢产物不足)、熬夜(皮质醇升高抑制厌氧菌生长)。
——内部因素
慢性疾病:溃疡性结肠炎、糖尿病、肥胖等疾病直接损伤肠道黏膜,或通过代谢紊乱抑制菌群增殖。
衰老:70 岁后肠道菌群多样性自然下降,核心菌丰度都会有所降低。
◆ 潜在危害与关联疾病
肠道功能异常
腹泻 / 便秘交替、腹胀、肠易激综合征(IBS)风险升高(核心菌减少导致肠道屏障功能下降)。
代谢与免疫风险
短链脂肪酸合成不足,增加肥胖、胰岛素抵抗、心血管疾病风险。
免疫细胞(如T细胞)活化不足,易引发反复感染(如呼吸道 / 肠道感染)。
疾病恶性循环
菌群失衡→消化吸收差→营养缺乏→免疫力进一步下降,形成 “菌群 – 疾病” 循环。
多样性过低的本质是菌群结构失衡,需结合数值、阈值、核心菌 / 有害菌比例及代谢功能综合判断,重点关注核心菌缺失和功能受损,而非单纯追求菌群数量。
#########################################
上述我们看到了多样性低引发的单一菌群大量占据的现象,这是不利的情况,那么,是否意味着多样性越高就越好呢?接下来,我们将通过一个数据库中的高多样性例子来探讨这个问题。
案例三:
多样性很高,是否是更健康的菌群结构?
通常情况下,我们认为多样性越高,肠道菌群结构就越趋向于稳定。然而,当多样性超出一定范围时,情况是否仍然如此呢?
这份报告,在数据库中属于多样性高的情况。
编辑
<来源:谷禾健康肠道菌群检测数据库>
从表面指标看,本案例的菌群呈现“高度多样”的特征:α多样性水平高。
一般成年人能测到的在500-1800种菌之间,平均香浓多样性指数就4-5的样子,这个多样性是显著超过平均值,这类结构通常意味着菌种丰富、生态位充足,理论上更具稳定性与抗干扰能力。
1)菌多但不够好的结构
然而,进一步结合平衡指数、有益菌、有害菌水平、核心菌属占比等指标,会发现这并不是一个典型的“稳态高多样性”,而更像一种“菌多但不够好”的结构。
我们来看一下菌群结构:
编辑
<来源:谷禾健康肠道菌群检测数据库>
结合整个报告来看,虽然多样性高但结构质量一般:核心/有益菌偏少 + 有害菌略偏多 + 还有几项机会型/胆汁相关菌偏高。可以说是一种看起来很热闹,但关键功能菌没站稳的生态结构。
2)核心菌属的缺乏
首先核心菌属占比水平 46(参考80–100):核心菌属不足是最核心的结构信号,报告也明确提示可能存在不常见菌增多或生态紊乱。
编辑
核心菌属累积占比不足,常被解读为常见稳定菌群缺乏,而由更多非核心菌或波动性菌群填充生态位,导致群落看似丰富,却可能更容易在饮食、压力、作息或抗生素等扰动下发生漂移。
3)有益菌与有害菌的失衡
有益菌水平 11(偏低,建议≥50) + 有害菌水平 52(略超参考上限50):说明功能性倾向不理想,“平衡指数29”也与此一致。
编辑
<来源:谷禾健康肠道菌群检测数据库>
在具体菌属层面:
关键产丁酸/抗炎相关核心属,粪杆菌属(Faecalibacterium)、罗氏菌属(Roseburia) 偏低的情况。这些菌常与丁酸盐生成、肠道屏障支持和抗炎稳态相关,缺乏时往往意味着肠道自我修复与抗炎能力的底盘不足。
4)机会致病菌的增多
机会型/胆汁相关菌脱硫弧菌属(Desulfovibrio)、嗜胆菌属(Bilophila) 偏高,且检出的沃氏嗜胆菌(Bilophila wadsworthia) 超过人群90%。这类菌群多常见于饮食结构(高脂/胆汁酸压力)、或近期扰动后的生态位变化。
综上,这是一个典型的多样性高≠更健康的案例:与案例一“病原菌极端优势导致崩盘”、案例二“单一优势菌占据生态位”不同,本案例更像“群落过于分散、关键功能菌不稳”的隐性失衡——需要把关注点从多不多转向核心功能菌是否到位、结构是否稳态。
#########################################
关于 “多样性是否过高” 的分析思路:
多样性过高的情况数据库中并不常见,且相对来说缺乏明确的关于过高的定义及统一的临床问题描述。但从菌群生态平衡的一般原理及现有知识推断,若假设存在 “多样性过高”(如菌种数量异常庞大、均匀性严重失衡),可能存在以下潜在问题:
1. 菌群结构稳定性下降
菌群多样性高通常伴随菌群间竞争激烈,若某类菌种因环境波动(如饮食、药物)出现适应性下降,可能导致整体结构趋于失衡,反而降低稳定性。
如同生态系统中物种过多但缺乏优势种,易因单一物种消失引发连锁反应,例如 “过度分散的菌群” 可能无法有效抵御外界致病菌入侵。
2. 有益菌丰度被稀释
若多样性过高伴随大量非优势菌种(如潜在致病菌、条件致病菌)过度繁殖,可能导致核心有益菌(如双歧杆菌、乳杆菌)的相对丰度被稀释,削弱其生理功能(如短链脂肪酸合成、免疫调节)。
3. 与特定疾病的潜在关联
现有研究多关注多样性低与疾病的关联(如炎症性肠病、代谢综合征),而多样性过高的临床数据较少。但部分罕见病或特殊生理状态下,可能出现菌群异常丰富伴随功能紊乱,例如:自身免疫病、慢性炎症等。
建议:若报告中多样性评分异常偏高,需关注是否存在检测误差或特殊生理状态(如长期摄入广谱益生菌导致菌群过度分散),并结合临床症状(如频繁腹泻、过敏)综合判断。
#########################################
多样性高并不天然等于更健康。当菌群看起来很丰富,但核心菌属占比不足、有益菌被稀释、机会型菌群趁势上升时,这种热闹但不稳的结构同样可能带来功能层面的隐患。
那么,较好的菌群结构应该长什么样?接下来,我们将通过案例四展示一份多样性相对较好的报告,看看多样性恰到好处时,菌群结构在平衡性、核心菌群与功能表现上会有哪些共同特征。
案例四:
多样性较好,核心菌群到位的相对稳态结构
在大多数情况下,它并不追求极端的高或低,而是呈现适度且稳定的多样性:核心菌属占比高、有益菌占优势、有害菌受控,整体更接近一种可持续的稳态。
1)多样性水平稳定
首先从整体生态稳定性来看,多样性水平稳定,说明菌群并未出现荒漠化的低多样性,也没有走向极端的异常发散,多样性在合理区间内往往意味着菌群具备更好的弹性,能更从容地应对饮食波动、作息变化等外界扰动。
编辑
编辑
<来源:谷禾健康肠道菌群检测数据库>
2)核心菌属充足:健康结构的标志
其次,本案例的菌群结构质量也较为理想。核心菌属85,达到报告建议的核心菌属累积占比最好超过80。核心菌属相对充足通常提示群落中以常见、稳定的共生菌为主体,生态位更稳,不容易被少数波动性菌群或机会型菌群抢位,因此也更接近健康人群的结构特征。
编辑
3)有益菌占优:功能性倾向良好
从功能倾向来看,本案例呈现出更符合健康菌群原则的比例:有益菌水平整体已处在建议线以上,既有足够的有益菌群支撑稳定性,也没有出现有害菌明显失控的信号。
最后看综合平衡指标,菌群平衡54。该值位于“中等”区间的偏高段,提示整体已较接近良好状态,但仍存在进一步优化空间。
编辑
<来源:谷禾健康肠道菌群检测数据库>
4)产丁酸菌正常:核心功能菌的支撑
具体菌属层面来看:
重要的核心菌属,包括产丁酸菌等,都处于正常范围(未标红)。
编辑
<来源:谷禾健康肠道菌群检测数据库>
拟杆菌属(Bacteroides)(处于人群79%):典型“基石菌/主导菌属”,在此报告里占比高且仍在报告正常范围内。一般代表复杂多糖降解与交叉喂养能力较强,是核心菌属占比的重要支撑点。
粪杆菌属(Faecalibacterium) (处于人群83%):关键产丁酸、抗炎相关核心菌,在参考范围内,属于加分项。
瘤胃球菌属(Ruminococcus)(人群80%):参与抗性淀粉/纤维素利用,处于正常范围。
总的来说,本案例展示了一个多样性良好且核心菌群充足的稳态结构,反映了肠道相对健康的特征。适度的多样性增强了菌群对外界变化的适应能力,而有益菌的优势地位则支持了整体稳定性。
案例五:
厚壁菌门过度占优势的结构
健康的肠道菌群中,各大菌门、菌属之间维持着相对稳定的比例。厚壁菌门(Firmicutes)和拟杆菌门(Bacteroidetes)是成年人肠道中最主要的两个菌门,它们的比例(F/B ratio)与能量代谢和体重密切相关。
接下来我们要看的是一个典型的门水平比例明显偏移的菌群失衡案例,其最突出的结构特征是——厚壁菌门显著过多,拟杆菌门被严重压缩。
1)门水平的异常信号:厚壁菌门一家独大
报告显示,该个体:F/B 比值 = 12.98(在谷禾数据库中,大多数人群参考范围:0.3–1.0)
这已经不属于轻微偏移,而是一个明确的门层面的生态极化结构。
编辑
<来源:谷禾健康肠道菌群检测数据库>
需要强调的是,厚壁菌门本身并非坏菌门,其中也包含多种产丁酸、支持肠道屏障的有益菌;但当其整体比例被放大到压倒性优势时,往往意味着特定饮食或代谢环境长期偏向,使菌群结构失去弹性。
2)结构层面的真实情况:不是厚壁菌多=结构好
如果继续看整体健康评估,会发现厚壁菌门水平的强大优势,并没有转化为结构质量优势:
编辑
<来源:谷禾健康肠道菌群检测数据库>
可以看到菌群平衡指数、菌群多样性、有益菌水平都偏低,有害菌较多,核心菌属严重缺乏。
这说明一个关键事实:
👉 厚壁菌门虽然数量巨大,但该个体并不是由高质量核心功能菌主导,而更像是由部分机会型或代谢偏向特定方向的菌反复扩增,形成的伪优势。
3)菌属层面:韦荣菌属异常升高
进一步看关键菌属,问题更加清晰:
厚壁菌优势并非由典型肠道核心功能菌主导,而是被高度富集的口腔 / 上呼吸道来源菌属明显拉高,其中以韦荣菌属(Veillonella)异常增多最为突出。
编辑
<来源:谷禾健康肠道菌群检测数据库>
韦荣菌属经典生态位在口腔、咽部、上呼吸道,常与牙菌斑、龋齿、口腔炎症、呼吸道感染高度相关,属于乳酸利用菌,常与链球菌属形成稳定的共生复合体。
该样本中并非单一菌属异常,而是出现了口腔—上呼吸道菌群组合特征:
链球菌属、嗜血杆菌属都偏高,这些菌群通常在口腔、鼻咽部常见的条件致病或共居菌,这些菌属理论上在肠道中正常情况下应是低丰度。
编辑
编辑
<来源:谷禾健康肠道菌群检测数据库>
它们的同步扩增,提示很可能存在:
换句话说,这是一个上消化道菌群下行 + 肠道生态位防御能力不足共同作用的结果。
4)为何这些上消化道菌群下行还能定植?核心菌、有益菌让位
多个产丁酸、抗炎核心菌属显著偏低或未检出:
编辑
<来源:谷禾健康肠道菌群检测数据库>
也就是说,厚壁菌门虽然多,但是真正负责肠道屏障修复、免疫调节的高价值成员并没有站稳生态位。
当这些核心菌群不足时,肠道就会变成一个空位过多、防御薄弱的生态系统,使原本不应成为优势菌的口腔 / 呼吸道菌有机会向下迁移并异常扩增。
5)功能与代谢结果:炎症与内毒素压力升高
这种结构性失衡,在功能指标中已经有所体现:
编辑
<来源:谷禾健康肠道菌群检测数据库>
当菌群结构过于偏移时,内毒素压力、慢性低度炎症和代谢负担往往同步上升。
###################################################
关于厚壁菌偏高属于哪种类型,判断思路:
厚壁菌门/拟杆菌门(F/B)比值是一个简单但粗糙的门水平线索,这在我们之前的文章有写过,详见:
当报告出现厚壁菌门明显占优时,可能需要追问:
这种偏高是短期饮食塑形造成的可逆偏移,还是已经与宿主代谢环境绑定,形成更稳定的结构性失衡? 实践中可按以下路径判断。
首先,先看结构是否还完整
我们上述展示的是一个相对极端的案例,若厚壁菌门只是偏高,但菌群多样性、平衡指数相对尚可,核心菌属并未明显减少,说明生态位仍然多元,系统并未被单一菌群占死。这种情况更常见于饮食诱导型厚壁菌偏高,即在长期高能量、高精制或膳食结构单一的环境中,厚壁菌因能量获取效率较高而被动扩增,但其优势具有一定可逆性。
进一步,拆解厚壁菌门内部的组成质量
厚壁菌门中既包含大量产丁酸、维护肠道屏障与免疫稳态的关键菌属,也可能包含机会型扩增、功能贡献有限甚至与炎症相关的成员。
若厚壁菌门偏高同时,经典产丁酸核心菌(如粪杆菌属、罗氏菌属、部分Blautia 等)仍有存在,提示结构功能尚未完全崩塌;
若厚壁菌门明显占优,但上述核心功能菌反而显著偏低或未检出,则说明这种数量优势并未转化为功能优势,更接近一种生态失衡型扩张。
还需要警惕另一种情况:
若厚壁菌门内部主要由韦荣菌属、链球菌属等非典型肠源菌占据(例如案例五报告中),而典型肠道核心菌普遍缺位,则这一厚壁菌优势更可能是一种来源错位导致的假性结构优势,而非真正的肠道功能性强化。
功能与代谢指标进行交叉验证
饮食诱导型厚壁菌偏高,往往仅伴随轻度产气、能量吸收效率升高等变化,炎症与内毒素状态未必明显异常。
而代谢型厚壁菌偏高,则更常见于炎症水平升高、胆汁酸代谢异常及肠道屏障薄弱等背景之下,提示菌群结构已与宿主的代谢环境形成相互强化的状态。
###################################################
案例六:
拟杆菌过多 ≠ 结构更健康
接下来我们来看一份非常典型的拟杆菌优势型的肠道菌群报告:
拟杆菌的丰度高达 85.613%,菌群整体倾向拟杆菌型。
编辑
<来源:谷禾健康肠道菌群检测数据库>
F/B 比值 0.08(显著低于谷禾数据库中的人群常见范围 0.3–1.0)
编辑
<来源:谷禾健康肠道菌群检测数据库>
仅从这个结果看,容易给人一种偏向植物性、有利代谢的直觉印象。但和厚壁菌偏高一样,拟杆菌偏高本身也只是结构线索,而非结论,同样需要进一步拆解其结构质量与功能背景。
1)整体生态:并非严重失衡型
菌群多样性自然是低的,有害菌也较多,但核心菌属处于正常水平。
编辑
<来源:谷禾健康肠道菌群检测数据库>
进一步看属水平,就会发现问题的关键并不在于有没有拟杆菌,而在于谁在过度主导生态位。
2)拟杆菌属极度集中,占据绝对生态位
其中多株典型拟杆菌(如 B. fragilis、B. vulgatus、B. uniformis 等)同时出现高丰度。
这意味着:碳源利用、蛋白/脂类代谢路径高度集中,其他功能型菌群(尤其是厚壁菌中的发酵—丁酸路径)参与度极低。
编辑
<来源:谷禾健康肠道菌群检测数据库>
图中可以看到,尤其是脆弱拟杆菌(Bacteroides fragilis)特别多,脆弱拟杆菌是人类肠道中的一种重要共生菌,具有复杂的双重角色。它分为两种亚型:不产肠毒素脆弱拟杆菌(NTBF)和产肠毒素脆弱拟杆菌(ETBF)。NTBF通常被认为是有益的,能够增强肠道屏障、调节免疫系统并抑制病原菌感染;而ETBF则通过分泌脆弱拟杆菌毒素(BFT)导致肠道上皮损伤,促进炎症和慢病发展,包括结肠炎、阿尔兹海默病、结直肠癌等。
3)厚壁菌门过低,丁酸通路成为结构短板
与拟杆菌高度集中相对应的是:
这类结构通常意味着:
功能指标很好地解释了这种结构的真实状态。
编辑
<来源:谷禾健康肠道菌群检测数据库>
这类组合非常符合拟杆菌垄断型结构的典型表现:
于是就形成了:
👉 虽不至于严重炎症,但长期胀气、消化负担偏重、肠腔压力较大 的状态。
4)拟杆菌过多,通常出于什么原因?
综合结构与功能特征,可能是以下背景之一或叠加:
此外也有其他非饮食因素的可能:
因此,这种时候,如果强行引入新菌、猛加益生菌或突然大幅调整底物结构,结果有可能不是很理想,拟杆菌可能会再次快速适应,继续占住生态位,新来者被挤走。
总的来说,需谨慎评估拟杆菌过高的情况,避免简单地将其丰度与健康状态等同。
益生菌补充是改善肠道健康的常用手段,能够有效促进消化、增强免疫力和维持微生态平衡。我们的数据库中也显示出两种极端情况的风险:一方面,益生菌的严重缺乏可能导致肠道菌群失衡,增加消化不良和感染的风险;另一方面,过量补充益生菌则可能引发肠道不适,甚至导致菌群的进一步失调。
案例七:
益生菌严重缺乏
接下来我们要看的这份报告最突出的特征,在于典型益生菌的系统性缺失。
从整体结构看,菌群尚未完全崩盘,但支持肠道屏障、免疫调节和代谢稳态的关键益生菌未能有效定植,是该案例的核心问题。
1)核心表现:双歧杆菌、乳杆菌几乎全部检不出
在益生菌模块中,几乎所有常见且功能明确的益生菌,比如双歧杆菌、乳杆菌等均显示为 ND.(ND为未检出)
编辑
<来源:谷禾健康肠道菌群检测数据库>
单个益生菌未检出其实在成年人中并不少见,但当整个双歧杆菌、乳杆菌体系几乎集体缺位时,已不太能用正常个体差异来解释,而更像是一个明确的益生菌底盘不足的结构。
2)指标层面的对应信号:有益菌偏低、核心菌属不足
这一菌属层面的缺失,也体现在综合指标上:
编辑
<来源:谷禾健康肠道菌群检测数据库>
这种组合特征十分典型,不是单一病原菌爆表,而是益生菌长期缺席后,被其他机会型或功能偏向不利的菌群逐步填补生态位,使结构看似还能运转,但稳定性和健康收益明显下降。
3)功能后果:屏障与代谢压力开始显现
在功能与代谢相关指标中,也能看到益生菌缺乏可能带来的连锁反应。
炎症信号偏高,如 LPS、肠道炎症水平超标;肠道屏障不足。
编辑
<来源:谷禾健康肠道菌群检测数据库>
蛋白腐败代谢相关产物(如对甲酚、苯酚)偏高。
编辑
<来源:谷禾健康肠道菌群检测数据库>
这些情况往往与双歧杆菌、乳杆菌不足导致的短链脂肪酸合成下降、屏障支持能力减弱有关。
总的来说,这类情况的干预重点,通常不在单纯追求多样性,而在于重建益生菌生态位,并为其提供长期可持续的生存环境。
如果说这个案例的问题在于——益生菌缺位,生态位长期空置,那么接下来这个案例呈现的,则是另一个方向的偏移——益生菌占位过强,反而挤压了其他核心菌群的生存空间。
案例八:
益生菌补充过犹不及
此案例的报告中,乳杆菌属丰度达到了19.076%,远超正常人群平均水平。
编辑
<来源:谷禾健康肠道菌群检测数据库>
这很有可能是长期或大剂量补充特定乳杆菌制剂的结果。虽然其有益菌高达57,看似健康,但细究之下却隐藏着新的失衡。
首先,单一菌种的极高丰度本身就是一种多样性失衡的表现。尽管其整体多样性评分为39(中等),但这种由外源补充菌株主导的伪多样性可能并不稳定。一旦停止补充,菌群结构可能迅速改变。
编辑
其次,功能上的失衡已经显现。报告显示其肠道产气严重(91,超标)。乳杆菌是主要的产乳酸菌,在发酵碳水化合物时会产生气体。当其数量过多时,过量的气体产生会导致腹胀、消化不良等症状,这与报告中的评估结果相符。
编辑
<来源:谷禾健康肠道菌群检测数据库>
此外,其对甲酚(p-Cresol)水平过高(95,过多)。对甲酚是蛋白质发酵产生的有害代谢物,被认为是尿毒症毒素之一,与慢性肾病、结直肠癌等风险相关。虽然乳杆菌不直接产生对甲酚,但其过度增殖可能改变了整个肠道环境的pH值和代谢网络,为其他能够产生对甲酚的菌群(如部分梭菌)创造了更有利的生长条件。
总的来说,益生菌并非多多益善。盲目、过量地补充单一或少数几种益生菌,可能会人为地制造出新的菌群失衡,导致产气过多、有害代谢物积累等问题。益生菌的补充应更具针对性,最好在检测评估的基础上,根据自身缺乏的菌种进行精准补充,并注意适时调整剂量,同时配合益生元和多样化饮食,以支持整个微生态系统的健康与平衡。
通过对以上极端案例的分析,我们可以清晰地看到,肠道菌群的健康远不止有益菌与有害菌的简单二元对立。它是一个关乎多样性、平衡性、功能性的复杂多维系统。无论是病原菌入侵导致的多样性崩溃,还是长期单一饮食或不当补充导致的比例失衡,亦或是关键功能菌群的缺失,最终都会导向肠道功能的紊乱和疾病风险的升高。
这些案例也为我们提供了重要的启示:
肠道菌群检测的意义在于评估微生态健康。菌群多样性是关键指标,关注物种丰富度和均匀度可及时识别失衡状态。此外,结合关键代谢物(如丁酸盐、短链脂肪酸)的检测,能够全面评估肠道健康。
在临床和机构干预中,针对性策略至关重要。干预不仅应补充益生菌,还需清除优势病原菌,并创造条件以恢复菌群多样性,避免一刀切的方法。饮食干预应精细化,关注膳食纤维、蛋白质和脂肪的均衡,以防止长期单一饮食导致的菌群极化。此外,干预后需进行长期监测与评估,以确保肠道菌群的稳定性和健康,及时调整干预措施,确保最佳效果。
在研究与发展方向上,深入探索微生物与宿主之间的相互作用机制,将有助于更好地利用这些微生物促进健康。
随着研究的深入,我们对肠道菌群的认识仍在不断拓展。未来,结合宏基因组学、代谢组学等多组学技术,我们将能更全面、更深入地描绘个体的肠道健康图景。作为行业的先行者,我们的使命是持续优化检测技术和模型,提升准确度。同时利用大样本数据库将这些复杂的生物信息转化为更加清晰、可执行的健康指导,帮助更多人通过管理好自己的内在肠道微生态,构筑起坚实的健康防线。
注:本文所引用的案例均为谷禾肠道菌群检测数据库中的真实检测数据,但为保护用户隐私,个人信息已做脱敏处理。所有分析和结论仅供参考和学术探讨,不构成医疗诊断或治疗建议。任何健康问题,请务必咨询专业医生。
谷禾健康
肠道微生物组作为人体“第二基因组”,在癌症的发生、发展及治疗反应中扮演着日益重要的角色。这些微生物不仅在局部和全身层面调节免疫应答,还深刻影响着炎症、免疫监视和耐受性。
平衡良好的微生物群是有效免疫功能的基石,但由饮食,环境因素,生活方式,感染或药物驱动的干扰可能会促进慢性炎症并损害抗肿瘤免疫力。越来越多的证据表明,这些干扰不仅有助于肿瘤的发生和发展,而且还对治疗产生耐药性。
微生物及其代谢产物能够通过局部及全身性机制,直接影响药物代谢、塑造免疫微环境,并改变肠道、全身乃至肿瘤微环境(TME)中的转录和表观遗传程序。
大量新兴数据支持,微生物组作为预后和预测性生物标志物、癌症防治中可调控因素以及治疗靶点的巨大潜力。以微生物组为靶点的干预措施(如粪菌移植、饮食调整、益生元和益生菌)可作为传统癌症疗法的辅助手段,增强疗效并降低毒性。
本文探讨了微生物组驱动癌症发生发展的多维机制,包括基因毒性、慢性炎症和表观遗传调控。详细分析微生物组如何调节化疗、放疗及免疫治疗的疗效与不良反应,还系统梳理了当前基于微生物组的癌症治疗策略,如粪菌移植、饮食干预、益生菌和后生元等,并总结了相关临床试验的进展。
历史上,微生物与癌症的关联常采用科赫假设(Koch’s postulates)等框架,将疾病归因于具有确定潜伏期的单一病原体。然而,现在人们认识到,微生物作为复杂的群落发挥作用,对宿主产生集体效应,而不仅仅是孤立的病原体。这些效应包括调节炎症、免疫、代谢和表观遗传,从而深刻影响致癌过程。
微生物驱动的致癌机制
微生物群通过多种复杂的机制促进肿瘤的启动和进展,主要包括直接的基因毒性效应、诱导慢性炎症和肠道屏障功能障碍,以及对宿主细胞的表观遗传调控。这些机制相互交织,共同构成了一个促癌的微环境。
肠道微生物组可通过诱导基因组损伤、表观遗传调控或破坏肠道屏障功能参与癌症的启动和/或进展。这些机制共同作用,促进了从正常上皮到恶性肿瘤的转化。
病原菌的致癌策略:信号传导与毒素的双重威胁
定植于上皮表面的病原菌或机会性细菌可通过直接的宿主细胞信号传导、微生物间通讯或分泌毒素发挥致癌作用。其中,细菌基因毒素是研究最为深入的直接致癌因素之一。这些毒素包括tilimycin、indolimines、tilivalline、colibactin和脆弱拟杆菌毒素(Bacteroides fragilis toxin, BFT)等。
编辑
-Colibactin
在这些毒素中,Colibactin的机制研究最为透彻。Colibactin由存在于变形菌门(如特定大肠杆菌菌株)中的聚酮合酶(pks)基因岛编码。这种基因毒素能够诱导DNA双链断裂和烷基化,从而引发基因组不稳定性,促进癌症的发生。
编辑
图源:doi.org/10.1038/s41579-025-01268-6
例如,一项研究发现,在结直肠癌中,由产colibactin的大肠杆菌(pks+ E. coli)引起的突变特征与早发性CRC相关。此外,产BFT的脆弱拟杆菌(ETBF)能够协同pks+ E. coli,其产生的BFT和黏液溶解活性使得colibactin能够穿透黏液层,到达上皮细胞,从而加剧DNA损伤。
微生物代谢物:潜在的DNA损伤元凶?
除了直接的基因毒素,微生物代谢物也可能具有DNA损伤效应。例如,有研究指出微生物将初级胆汁酸转化为次级胆汁酸,后者过量可通过诱导DNA损伤、调节炎症通路和抑制抗肿瘤免疫反应(包括抑制在癌症免疫监视中至关重要的细胞毒性CD8+ T细胞)来促进结直肠肿瘤的发生。
同样,肠道微生物将管腔中的乙醇转化为乙醛,或将某些亚硝胺类致癌物(如N-丁基-N-(4-羟丁基)亚硝胺)转化为更具活性的形式,这些过程均可导致基因组损伤。
雌激素与微生物:远程影响
此外,微生物的β-葡萄糖醛酸酶(GUS)能够重新激活在肝脏中被结合失活的雌激素,提高循环雌激素水平,这可能对乳腺癌等雌激素敏感性肿瘤的发生构成远距离影响。
慢性炎症与肠道屏障功能障碍
慢性微生物感染是癌症发生的重要驱动力
例如,幽门螺杆菌(Helicobacter pylori)感染通过诱导持续性胃部炎症,促进胃癌的发生,而根除幽门螺杆菌已被证实可以预防胃癌。同样,伤寒沙门氏菌(Salmonella typhi)与胆囊癌的发生相关。
编辑
图源:doi.org/10.1038/s41579-025-01268-6
微生物组失衡促癌变
即使在没有明显感染的情况下,微生物组失衡也能通过调节局部炎症反应促进癌变。
例如,通常存在于口腔的具核梭杆菌(Fusobacterium nucleatum)在特定条件下可定植于肠道,并在CRC肿瘤中诱导肿瘤微环境的炎症。
炎症与癌症之间的复杂信号网络
微生物诱导的炎症部分通过模式识别受体(如Toll样受体,TLRs)信号和炎症小体激活介导,导致细胞因子和活性氧(ROS)的产生,这些分子刺激上皮增殖、免疫逃逸以及癌细胞在远端部位的播散和植入。
肠道炎症与肠道屏障功能障碍密切相关
屏障功能受损,即黏液层和上皮细胞无法在管腔微生物群落与宿主上皮之间提供足够的空间,增加了促癌微生物和分泌性基因毒素造成损害的易感性。受损的屏障完整性促进了微生物产物(如脂多糖,LPS)和代谢物(如胆汁酸)的易位,进入体循环。这些因素可驱动远端组织的全身性炎症或免疫抑制,可能导致远端上皮和非上皮癌症及转移的发生。
编辑
保护性微生物代谢物的作用
一些微生物代谢物,如膳食纤维在结肠中发酵产生的短链脂肪酸(SCFAs),通过促进紧密连接形成和刺激黏液产生,对肠道屏障具有保护作用。
表观遗传调控
肠道微生物组是一个强大的表观遗传调节器,能够通过代谢、炎症和饮食-微生物相互作用的组合来塑造基因表达和肿瘤行为。
图源:doi.org/10.1038/s41579-025-01268-6
丁酸盐的双重角色:从能量源到表观遗传调控
最典型的微生物驱动的表观遗传调控机制是SCFA中的丁酸盐对组蛋白去乙酰化酶(HDAC)的抑制。在健康的上皮细胞中,丁酸盐是支持增殖和分化的能量来源。然而,随着肿瘤细胞代谢转向有氧糖酵解(瓦博格效应),丁酸盐不再被有效消耗。其积累导致过度HDAC抑制,改变染色质构象,促进抑癌基因的转录激活,从而抑制癌变。
膳食成分与微生物的影响
其他微生物或膳食成分也能影响表观基因组。例如,叶酸、亚硝胺和致肥胖饮食在小鼠模型中影响DNA甲基化和组蛋白乙酰化,促进肠道肿瘤发生。
产毒脆弱拟杆菌的致癌机制
有趣的是,在小鼠模型中,产肠毒素的脆弱拟杆菌(ETBF)定植通过破坏DNA修复机制促进结直肠肿瘤发生,并诱导广泛的CpG岛高甲基化,这是肿瘤组织中表观遗传变化的标志。
不同类型的癌症与特定的微生物组特征相关联,这些特征不仅存在于胃肠道肿瘤中,也见于乳腺癌、前列腺癌等远端肿瘤,揭示了微生物组在肿瘤生态系统中的广泛影响。
结 直 肠 癌
结直肠癌(CRC)的发展与多种微生物、其代谢物和结肠上皮之间的相互作用密切相关。在动物模型和细胞培养研究中,特定微生物如ETBF(产肠毒素的脆弱拟杆菌)、具核梭杆菌(F. nucleatum)和携带pks基因岛的大肠杆菌(pks+ E. coli)被证明有助于肿瘤发生。
将结直肠癌患者的粪便微生物群移植到无菌小鼠体内,会导致细胞增殖增加、息肉数量增多、异型增生更严重以及炎症标志物水平升高,这强烈表明肠道微生物组失衡可能是结直肠癌发展的致病因素。
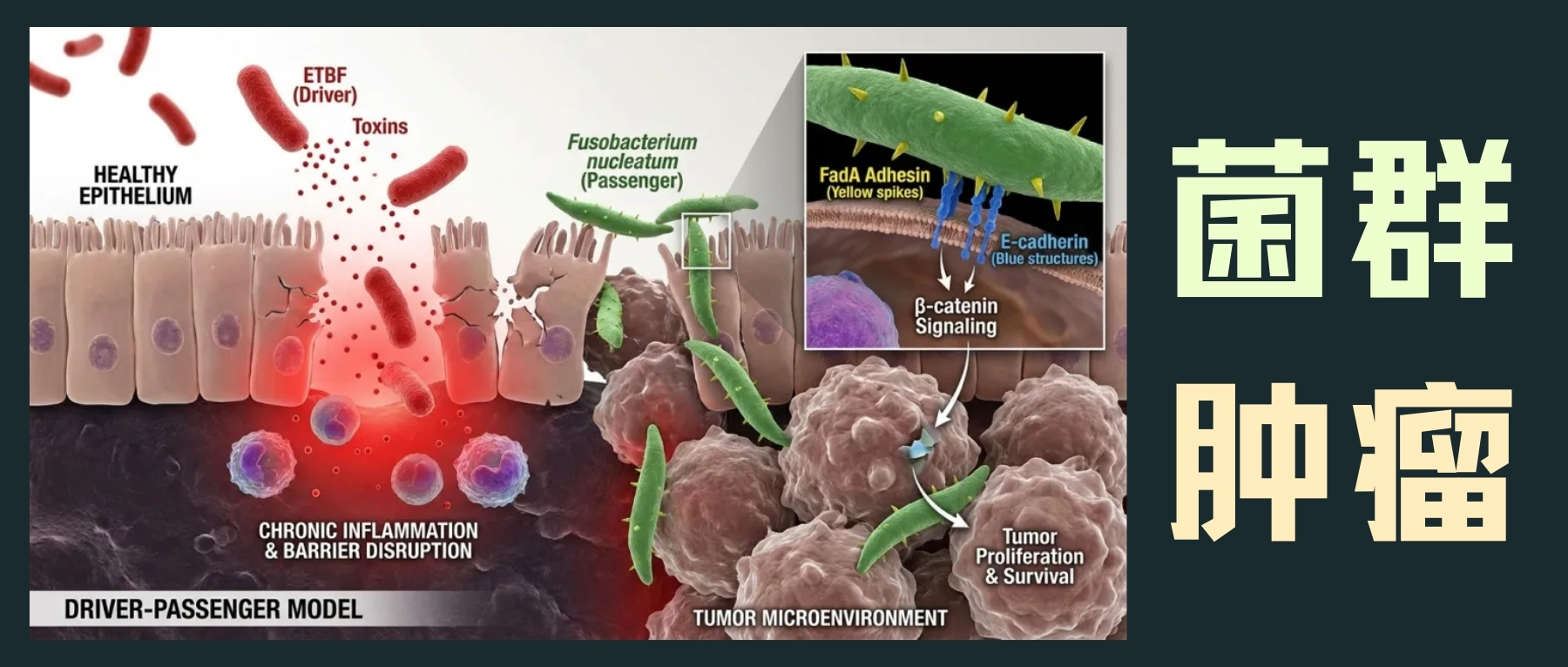
驱动-乘客模型:微生物的协同作用
“驱动-乘客”模型提出,像ETBF这样的驱动菌通过引发慢性炎症和破坏上皮屏障,创造一个允许性环境,让像具核梭杆菌这样的共生乘客菌得以定植并加剧肿瘤进展。具核梭杆菌通过其细胞表面的FadA黏附素与上皮E-钙黏蛋白直接相互作用,激活β-连环蛋白信号通路,促进肿瘤细胞增殖和存活。
编辑
具核梭杆菌与化疗耐药性
此外,具核梭杆菌还通过刺激肿瘤细胞中的自噬相关蛋白,与化疗药物的细胞毒性作用相抗衡,从而与化疗耐药性相关。临床上,结直肠癌肿瘤组织中的具核梭杆菌DNA水平较高与结直肠癌特异性死亡率增加相关,表明其可作为潜在的预后生物标志物。
胃 癌
在胃癌中,幽门螺杆菌(H. pylori)感染是公认的关键致病因素。它通过其毒力因子(如CagA和VacA,在谷禾16S Plus检测实践中,也会检出个别受检者携带 CagA和VacA毒力基因)引发炎症和免疫反应,进而可能有诱发癌症风险。然而,随着胃癌进展,胃内环境发生萎缩,幽门螺杆菌数量反而减少,而其他非幽门螺杆菌物种(如乳酸杆菌属、链球菌属)开始增多。
肝 细 胞 癌
在肝细胞癌(HCC)中,肠-肝轴起着关键作用。肠道屏障功能受损导致细菌及其产物(如LPS)易位至肝脏,诱发炎症、纤维化和肝细胞损伤,最终促进癌变。
肝细胞癌患者的肠道微生物组通常表现为产SCFA的细菌多形拟杆菌(Bacteroides thetaiotaomicron)减少,而促炎细菌(如大肠杆菌)增多。
胰 腺 导 管 腺 癌
胰腺导管腺癌(PDAC)同样与肠道微生物组失调相关。肠道屏障受损允许某些肠道微生物(如变形菌门)易位至胰腺,在局部创造一个免疫抑制的微环境,促进肿瘤进展。此外,微生物对胆汁酸的代谢异常也被认为是PDAC的风险因素之一。
激素依赖性癌症
肠道微生物组在激素代谢中发挥着重要作用,从而影响激素依赖性肿瘤的进展。所谓的雌激素菌基因组(estrobolome)是指能够代谢雌激素的细菌基因集合。肠道中的细菌β-葡萄糖醛酸酶可以解偶联在肝脏中结合的雌激素,使其重新被吸收入血,提高循环中活性雌激素的水平,从而促进乳腺癌等雌激素驱动肿瘤的生长。
在乳腺癌患者中,具有β-葡萄糖醛酸酶活性的菌种(如梭菌属)丰度增加可能与更严重的临床分期有关。同样,在前列腺癌中,肠道菌群能够从头合成雄激素或将皮质醇代谢物转化为雄激素,促进对内分泌治疗的抵抗。
癌症的多步发生模型认为,遗传和表观遗传的序贯改变是恶性转化的驱动力。新兴证据表明,微生物组的失调可能是这一模型中一个额外的、相互关联的因素。
生命早期的微生物组发育
微生物组的发育始于生命早期,受分娩方式、喂养习惯和饮食转变的影响。在这一关键窗口期的干扰可能导致微生物多样性永久性降低和对免疫与代谢稳态至关重要的关键菌种的缺失。
生活方式对微生物组的影响
在整个生命周期中,累积的损害(包括抗生素滥用、慢性压力和低纤维、超加工饮食)会进一步侵蚀微生物的多样性和功能。这种微生物恢复力的逐步丧失可能会损害上皮完整性、增加炎症、削弱代谢信号和免疫监视。
多个研究和科学家提出,微生物组的这种纵向退化可能会降低癌症启动和进展的阈值,与经典致癌过程中的逐步遗传事件相平行。
微生物组健康随生命周期的逐步退化可能促进癌症发展
编辑
图源:doi.org/10.1038/s41579-025-01268-6
图中显示了肠道微生物组健康和恢复力的两种对比轨迹
每次急性干扰后恢复不完全,导致微生物组健康和恢复力逐步退化。
持续的压力源可能将个体推向恶化轨迹,直至达到癌症发展概率更高的阈值。
癌症治疗反应的变异性受到多种宿主和肿瘤相关因素的影响,而肠道微生物组是导致这种变异性的一个重要贡献者。
微生物组主要通过两大机制调节癌症治疗结果:
一是通过微生物对治疗药物的生物转化以及药物对微生物组的反作用;
二是通过微生物介导的宿主免疫反应调节。
微生物组与化疗、放疗及靶向治疗
肠道微生物组编码着庞大的基因库,能够代谢多种肿瘤学和非肿瘤学药物,从而影响药物的生物利用度、疗效和毒性。
微生物介导的影响癌症治疗结果的机制
编辑
图源:doi.org/10.1038/s41579-025-01268-6
药物的微生物生物转化
一个典型的例子是化疗药物5-氟尿嘧啶(5-FU)及其口服前药卡培他滨。某些大肠杆菌和厌氧棒状菌属(Anaerostipes)表达细菌二氢嘧啶脱氢酶(DPD),能将5-FU转化为其非活性形式,从而可能降低其疗效。
类似地,用于治疗胰腺癌的吉西他滨可被某些肿瘤相关γ-变形菌纲细菌表达的胞苷脱氨酶(CDA)脱氨而失活,导致耐药。
微生物也能激活药物
拓扑异构酶I抑制剂伊立替康在肝脏中被代谢为活性形式SN-38,随后经葡萄糖醛酸化为无活性的SN-38G,通过胆汁排入肠道。肠道中的细菌β-葡萄糖醛酸酶(GUS)能将SN-38G重新激活为SN-38,后者会引起严重的上皮损伤、黏膜炎和腹泻等剂量限制性毒性。虽然理论上肿瘤内的再激活可能增强疗效,但肠道内的再激活主要导致毒性增加。
微生物影响疗效与毒性
除了直接代谢药物,微生物组还能通过调节免疫系统间接影响化疗效果。例如,化疗药物环磷酰胺能促进特定肠道细菌(如Enterococcus hirae)易位至次级淋巴器官,诱导产生有助于其治疗效果的TH17细胞(T辅助17细胞)反应。
同样,奥沙利铂的疗效被发现依赖于肠道微生物组,肠道菌群通过激活免疫系统来增强抗肿瘤效果。
放疗与微生物组之间的双向互动
一方面,放疗(尤其是盆腔放疗)会显著改变肠道微生物组的组成,导致多样性下降,并可能增加机会性病原菌。
另一方面,微生物组的组成可以预测患者对放疗的反应和毒性。例如,放疗前肠道菌群多样性较低与晚期放射性肠病相关。在小鼠模型中,粪菌移植(FMT)被证明可以保护机体免受辐射引起的毒性。
靶向治疗
对于靶向治疗,研究尚处早期。一项针对转移性CRC的研究发现,对抗EGFR(西妥昔单抗)和抗VEGF(贝伐珠单抗)治疗的疾病进展组患者,其肠道微生物组中具核梭杆菌的丰度显著高于部分缓解组。
在HER2阳性乳腺癌中,抗生素使用或移植来自抗生素处理供体的小鼠粪菌会削弱曲妥珠单抗的抗肿瘤效果。
微生物组与免疫治疗
免疫检查点抑制剂(ICIs)通过阻断T细胞上的抑制性信号(如PD-1、CTLA-4),重新激活细胞毒性CD8+ T细胞以攻击肿瘤,彻底改变了癌症治疗。然而,只有部分患者对ICIs有反应,而肠道微生物组是决定疗效的关键因素之一。
►▷ 微生物组如何调节免疫反应与治疗效果
多项早期研究独立证实,肠道微生物组的组成与抗PD-1/PD-L1治疗的反应相关。
尽管与疗效相关的具体菌种在不同研究中有所差异(如Akkermansia、Bifidobacterium、Ruminococcus),但其免疫调节机制常常趋同于增强CD8+ T细胞的数量或活性。
例如,在临床前模型中,口服双歧杆菌可增强树突状细胞(DC)的激活和CD8+ T细胞的启动,从而增强对PD-L1阻断的反应。同样,Akkermansia muciniphila通过促进CD8+ T细胞招募至肿瘤,来增强对PD-1抑制的反应。
这些发现表明,与ICI疗效相关的菌种可能共享一种能力,即在肠系膜淋巴结或肠黏膜中诱导依赖于DC的CD8+ T细胞启动,随后通过趋化因子介导浸润至TME。
肠道菌群的影响:U型效应
值得注意的是,微生物组对ICI疗效的影响可能具有“U型”或“倒U型”特征。
编辑
例如,一项针对晚期非小细胞肺癌(NSCLC)患者的研究发现,肠道中A. muciniphila的相对丰度处于中等水平(而非低或高水平)的患者,其临床反应最佳。这提示微生物的影响并非简单的“越多越好”,而是需要一个平衡的生态系统。
►▷ 微生物代谢物:抗肿瘤免疫的关键因素
微生物的功能冗余性可能比分类学组成更为关键,即不同的微生物群落可能产生相似的代谢或免疫输出。多种微生物代谢物被证明在调节免疫治疗反应中发挥核心作用。
肠道微生物代谢物与免疫
编辑
图源:doi.org/10.1038/s41579-025-01268-6
该图描绘了肠道微生物组与免疫系统之间的相互作用,说明了膳食成分(如纤维)如何影响SCFAs、胆汁酸和色氨酸衍生物的产生。这些代谢物调节多种免疫细胞,并通过调节炎症细胞因子和增强癌细胞凋亡来促进抗肿瘤免疫和ICI治疗效果。
编辑
图源:doi.org/10.1038/s42255-025-01287-w
代谢物的作用是情境依赖的
例如,丁酸盐在某些情况下能增强细胞毒性CD8+ T细胞功能,支持抗肿瘤免疫,但在其他条件下也可能促进免疫抑制性的Treg细胞扩增。
同样,具核梭杆菌在不同研究中显示出截然相反的作用:一项研究表明其产生的丁酸能敏化MSS型CRC对ICIs的反应,而另一项研究则发现其产生的琥珀酸会抑制免疫信号通路,导致耐药。
这凸显了菌株、肿瘤微环境和代谢产物背景的复杂性。
►▷ 肠道菌群预测免疫相关不良事件
ICIs激活的免疫系统也可能攻击正常组织,导致免疫相关不良事件(irAEs)。多项报告将基线肠道微生物组组成与irAEs的发生风险联系起来。
然而,由于患者群体异质性、队列规模小以及irAEs定义不一致等原因,目前尚未发现一致的预测性微生物标志物。一些研究提示,特定的菌群(如拟杆菌门丰度较高)可能与结肠炎风险增加有关,但仍需更多机制性研究来阐明因果关系。
鉴于微生物组与癌症疗效和毒性的密切联系,操纵微生物组成员为增强治疗效果提供了新的契机。一系列策略正在研究中,包括饮食干预、益生菌/益生元、粪菌移植(FMT)以及更前沿的工程菌和后生元等。
这些干预措施旨在通过重塑微生物组生态系统,来调节药物代谢、增强抗肿瘤免疫或减轻治疗毒性。
编辑
图源:doi.org/10.1038/s42255-025-01287-w
粪菌移植 (FMT)
粪菌移植是目前研究最深入的微生物组干预手段之一。两项开创性的I期临床试验表明,将来自对ICI有反应的黑色素瘤患者的粪便微生物群移植给耐药患者,可以使一部分患者转为应答者,并伴随着CD8+ T细胞活化增强或TME中免疫细胞浸润的有利变化。
最近,一项在晚期黑色素瘤患者中进行的 I期试验进一步证实,接受健康供体FMT后,患者对一线抗PD-1治疗的反应得到改善,其粪便样本能够在小鼠模型中恢复抗PD-1疗效。
此外,FMT也被用于治疗难治性ICI相关性结肠炎,初步研究显示其能有效缓解症状,并伴随免疫细胞谱的改变。目前,大量临床试验正在探索FMT联合ICI在不同癌种(如肾细胞癌、NSCLC)中的应用。
饮食、益生元与益生菌
饮食干预是一种极具性价比的策略
一项观察性研究发现,高纤维饮食(不使用益生菌)与改善的ICI结局相关。
BE GONE试验(NCT02843425)等临床研究正在评估高纤维食物(如豆类)对微生物组和临床结局的影响,初步结果显示其能增加有益菌(如Faecalibacterium)并改善炎症标志物。
注:zhuBE GONE试验(NCT02843425)是一项由MD安德森癌症中心开展的临床研究,旨在探索食用 canned navy beans对肠道微生物组的影响,以及这种饮食干预是否能减轻肥胖对结直肠癌风险的负面影响。
传统益生菌
益生菌的应用也备受关注。一些传统益生菌(如某些乳杆菌和双歧杆菌)被发现能通过产生特定的代谢物(如I3A、吲哚-3-羧酸)或直接作用来增强抗肿瘤免疫。
下一代益生菌 和 工程菌
例如,A. muciniphila被多项研究证实与ICI的良好反应相关,其巴氏杀菌形式(一种后生元)或其膜蛋白Amuc_1100在临床前模型中显示出抗肿瘤效果。
工程化的大肠杆菌Nissle 1917菌株被改造用于在肿瘤局部递送免疫刺激分子(如将氨转化为L-精氨酸)或免疫检查点抑制剂纳米抗体,从而在不产生全身毒性的情况下增强抗肿瘤免疫。
微生物组干预策略面临的挑战
– 机制不确定性
许多干预措施(如高纤维饮食、传统益生菌)缺乏对特定菌种或功能如何调节疗效的深入机制理解,导致策略普适化,而非个体化。
– 情境依赖性和个体差异
微生物组的效果受宿主遗传、肿瘤类型、治疗方案和生活方式等多种因素影响,使得干预效果难以一概而论。
– 缺乏个体化生物标志物
目前缺少可靠的生物标志物来指导患者分层,或确定应靶向微生物的哪个方面(如药物代谢、屏障功能或免疫调节)。
– 临床试验设计的局限性
癌症患者常伴有免疫抑制、恶病质或胃肠道毒性,难以依从严格的饮食方案或口服疗法。此外,抗生素的普遍使用也干扰了微生物组的评估和干预。
除了作为治疗靶点,微生物组在癌症的早期检测和风险分层方面也展现出巨大潜力。
早期检测与风险分层
肠道微生物组已被探索作为早期癌症检测的工具,尤其是在结直肠癌领域。多项研究通过比较癌症患者与健康对照的微生物组谱,试图识别可用于诊断的微生物标志物。
谷禾健康通过上万例的结直肠癌和结直肠息肉患者及健康对照构建的肠癌识别模型,在样本量、病例类型覆盖与真实世界差异性方面显著优于多数以“数十到数百例”为主的研究型队列。更大的队列意味着模型能够学习到更稳定、可重复的微生物特征组合,降低因地域、饮食、年龄结构、用药史等因素带来的偶然偏差,从而在实际应用中具备更强的泛化能力与可识别性。
同时,许多研究仅做“癌症 vs 健康”的二分类;谷禾模型纳入“结直肠息肉”等癌前人群,更贴合早筛需求,能在症状出现前识别风险,并捕捉从健康到息肉/腺瘤再到癌变的连续变化信号,从而支持早期风险分层与更有针对性的随访与干预。
谷禾结直肠癌模型示意图
编辑
<来源:谷禾肠道菌群检测数据库>
但是不管是谷禾的模型还是科学研究的结果直接引用于临床诊断还需要有一段路走。
首先,横断面研究难以区分因果关系和相关性,且易受混杂因素(如并存病、用药)的干扰。
其次,与现有筛查手段(如 FIT/粪便免疫化学、结肠镜、影像与血液指标)进行对照评估,确定其增益价值与适用场景;并建立标准化的采样、测序/检测、质控与解读体系,控制抗生素、饮食、肠道准备等混杂因素影响。
伴 随 诊 断
微生物组作为伴随诊断工具的前景可能更为广阔,可用于指导治疗决策、预测疗效或毒性风险。例如,通过检测治疗前的肠道或肿瘤微生物组,可以识别出对特定疗法(如ICI)反应可能性较高的患者,或发生irAEs风险较高的患者。
基于对瘤胃球菌(Ruminococcus)等丰度的检测,可以对接受ICI治疗的患者进行分层。理想的伴随诊断应植根于机制理解,而不仅仅是关联数据,从而指导个性化干预,例如决定是否需要将FMT作为一线辅助治疗,或是否需要先通过菌群移植恢复患者对膳食纤维的降解能力再进行饮食干预,而不是盲目的粪菌移植。
人工智能(AI)有望通过实现高级数据整合、模式识别和预测建模,彻底改变微生物组研究。
编辑
图源:doi.org/10.1038/s41579-025-01268-6
面对微生物组多组学数据维度灾难(即特征数量远超样本数量)的挑战,AI提供了解决方案。例如,通过降维、合成数据增强或迁移学习等策略,可以提高模型的稳定性和泛化能力。
新兴的AI方法,如变分贝叶斯神经网络和卷积神经网络,能够整合配对的微生物组和代谢组数据,或将多组学数据转换为图像格式进行分析,从而发掘深层生物学关联。
编辑
数字孪生是另一个令人兴奋的方向。这是一个动态的、虚拟的患者复制品,整合了静态数据(如基因信息)和实时数据(如临床记录、组学数据),以模拟、监测和预测健康结果。将微生物组数据纳入数字孪生模型,可以模拟其与宿主和治疗的复杂相互作用,支持假设驱动的干预措施和个性化治疗调整。
为不同生命阶段(如婴儿期和成年期)开发量身定制的数字孪生模型,将为整个生命周期的微生物组靶向干预提供宝贵的指导。
当前临床试验概览
近年来,旨在利用微生物组改善癌症治疗的临床试验数量激增。
FMT试验主要集中于免疫治疗效果良好的癌种(如黑色素瘤、RCC、NSCLC),旨在逆转或改善对ICIs的耐药性(如NCT05286294, NCT04988841)。其他试验则探索FMT在肝癌(NCT05690048)、胰腺癌(NCT06393400)等其他癌种中的应用,或用于减轻治疗相关的毒副反应,如免疫相关性结肠炎(NCT04038619)。
关于益生元、益生菌和后生元的临床试验同样蓬勃发展,多数旨在增强抗癌免疫治疗的效果(如NCT05303493, NCT06250335)。
A.muciniphila(NCT05865730)和C.butyricum等下一代益生菌的专项试验正在进行中。
这些研究不仅关注疗效,也探索其在围手术期管理、预防癌前病变复发以及减轻治疗副作用方面的潜力。
越来越多的证据表明,肠道微生物组是癌症治疗结果的关键调节器,其通过免疫调节、药物代谢和维持上皮屏障完整性等多种机制发挥作用。这一认知推动了新型诊断和治疗策略的开发,但临床转化仍受制于机制不确定性、缺乏个性化生物标志物以及在癌症人群中实施的挑战。
微生物组研究揭示,宿主与微生物群作为一个整合系统运作,治疗结果源于宿主-微生物-药物三者间的动态相互作用。
功能冗余、微生物可塑性和强烈的情境依赖性使得因果推断变得困难,也可能解释了为何微生物标志物在不同研究中难以重复。当前的许多干预措施基于普适性策略而非深刻的机制理解,而个体差异进一步加大了个性化治疗的复杂性。
为了推动该领域的发展,未来的研究必须转向由AI赋能、以机制为导向的精准干预,这需要以可靠的伴随生物标志物为支撑,并通过大规模、纵向的实用性临床试验证实。至关重要的是,临床试验必须考虑癌症患者的特殊限制,并在真实世界环境中关注有临床意义的功能性终点。随着微生物组科学日益融入肿瘤学,它有望通过将机制精度与临床相关性相结合,重新定义癌症治疗,实现更有效、更耐受的疗法。
注:本账号内容仅供参考和学术探讨,不构成医疗诊断或治疗建议。任何健康问题,请务必咨询专业医生。
主要参考文献
Hajjar R, Mars RAT, Kashyap PC. Harnessing the microbiome for cancer therapy. Nat Rev Microbiol. 2026 Jan 5.
Nobels A, van Marcke C, Jordan BF, Van Hul M, Cani PD. The gut microbiome and cancer: from tumorigenesis to therapy. Nat Metab. 2025 May;7(5):895-917.
de Vos, W. M., Tilg, H., Van Hul, M. & Cani, P. D. Gut microbiome and health: mechanistic insights. Gut 71, 1020–1032 (2022).
Domzaridou, E. et al. The impact of oral antibiotics prior to cancer diagnosis on overall patient survival: findings from an English population-based cohort study. Curr. Oncol. 30, 8434–8443 (2023).
Yuan, L. et al. The influence of gut microbiota dysbiosis to the efficacy of 5-fluorouracil treatment on colorectal cancer. Biomed. Pharmacother. 108, 184–193 (2018).
Routy, B. et al. Gut microbiome influences efficacy of PD-1-based immunotherapy against epithelial tumors. Science 359, 91–97 (2018).
Elkrief, A. et al. Antibiotics are associated with worse outcomes in lung cancer patients treated with chemotherapy and immunotherapy. NPJ Precis. Oncol. 8, 143 (2024).
Ransohoff, J. D. et al. Antimicrobial exposure is associated with decreased survival in triple-negative breast cancer. Nat. Commun. 14, 2053 (2023).
Cong, J. et al. Bile acids modified by the intestinal microbiota promote colorectal cancer growth by suppressing CD8+ T cell effector functions. Immunity 57, 876–889.e11 (2024).
Tintelnot, J. et al. Microbiota-derived 3-IAA influences chemotherapy efficacy in pancreatic cancer. Nature 615, 168–174 (2023).
Bender, M. J. et al. Dietary tryptophan metabolite released by intratumoral Lactobacillus reuteri facilitates immune checkpoint inhibitor treatment. Cell 186, 1846–1862.e26 (2023).
Salminen, S. et al. The International Scientific Association of Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of postbiotics. Nat. Rev. Gastroenterol. Hepatol. 18, 649–667 (2021).
谷禾健康
普通拟杆菌(Bacteroides vulgatus/Phocaeicola vulgatus)是人类结肠中最常见的革兰阴性厌氧杆菌之一,在超过90%的人群中都能够检出。其属于拟杆菌属(Bacteroides),是肠道“核心菌”,既有益生潜力,也在某些条件下与疾病相关。
它具有大量多糖利用位点(PULs),能降解膳食多糖和黏液糖蛋白,产生短链脂肪酸(如乙酸、丙酸、丁酸)和琥珀酸等有机酸。基因组学显示其具有丰富的碳水化合物转运与代谢系统。研究发现,其会产生一种叫做泛酸盐(维生素B5)的物质,影响肠道中的GLP-1和肝脏的FGF21的释放,这两种激素会影响葡萄糖代谢并具有神经保护特性。
B.vulgatus产生的代谢物(如N-乙酰氨基葡萄糖)可以促进另一个肠道有益细菌Akkermansia muciniphila(简称Akk菌)的生长。在高脂饮食导致Akk菌数量减少的情况下,B.vulgatus的施用可以恢复其丰度。
研究发现,普通拟杆菌(B.vulgatus)在肥胖、心血管疾病、2型糖尿病、肠道炎症、内皮功能障碍患者中丰度降低;而在自闭症和甲状腺炎患者中发现其丰度升高。
总的来说,普通拟杆菌(Bacteroides vulgatus) 算是一种有益的肠道共生菌,但其效果依赖于特定菌株的水平特异性。其在心血管代谢病、糖尿病、骨质疏松、结肠炎及感染防御等领域中显示出显著的保护潜力,同时在特定菌株或蛋白酶过度表达、黏膜屏障破坏时又可参与炎症和严重感染。临床应用需基于明确的安全性和作用机制的精准菌株,而不是泛指“B.vulgatus”补充。
普通拟杆菌(Bacteroides vulgatus/Phocaeicola vulgatus)是一种厌氧、革兰氏阴性杆菌。它是人类肠道微生物组中最常见的细菌之一,该菌不仅对维持肠道健康至关重要,还具备多种益生潜力,并与多种疾病(如炎症性肠病和心血管疾病)相关。
分类信息
门:拟杆菌门
纲:拟杆菌纲
目:拟杆菌目
科:拟杆菌科
属:拟杆菌属
物种:普通拟杆菌(Bacteroides vulgatus)
普通拟杆菌(Bacteroides vulgatus)属于拟杆菌门(Bacteroidota)、是Bacteroides/Phocaeicola 属的重要种。
普通拟杆菌(Bacteroides vulgatus)又称Phocaeicola vulgatus,2019年起基于全基因组系统发育分析的研究将若干原属 Bacteroides 的物种重划入新属或其它属,Phocaeicola 作为新属或被恢复的属用于容纳包括 Bacteroides vulgatus 在内的若干物种。
形态与生理
细胞形态:Bacteroides vulgatus为杆状菌,专性厌氧,且不具芽胞形成能力。
抗原性:该菌有多个抗原类型,可能影响其致病性和免疫应答。
• 重要结构与分子特征
脂多糖(LPS):其LPS为低酰化、低磷酸化结构,以四、五酰型为主,与大肠杆菌六酰型脂多糖相比,引发更弱的TLR4促炎反应,具有明显免疫调节/低炎性特征。
蛋白酶与其他酶:具多种蛋白酶和糖苷水解酶,如 GH123 家族的 N-乙酰-β-半乳糖胺苷酶,参与黏膜糖链利用;部分菌株分泌的蛋白酶与溃疡性结肠炎严重度相关。
生态位
Bacteroides vulgatus是人类肠道的常驻共生菌,主要栖息在结肠中,谷禾数据库中显示其人群检出率高达98%。并能通过分解复杂的植物碳水化合物和膳食纤维来产生短链脂肪酸等代谢物。
编辑
代谢能力
Bacteroides vulgatus具有大量多糖利用位点(PULs),能降解膳食多糖和黏液糖蛋白,产生短链脂肪酸(如乙酸、丙酸、丁酸)和琥珀酸等有机酸。基因组学显示其具有丰富的碳水化合物转运与代谢系统。
研究还发现,它会产生一种叫做泛酸盐(维生素B5)的物质,帮助身体释放两种重要的激素。肠道中的GLP-1和肝脏的FGF21,这些激素会调节对糖分的渴望。
耐药性
Bacteroides vulgatus通常对广泛使用的抗生素(如青霉素、头孢菌素和氨基糖苷类)耐药,但对甲硝唑、碳青霉烯类以及某些β-内酰胺和β-内酰胺酶抑制剂仍然敏感。其耐药性可能因感染部位而异。
与其他菌的相互作用
• 促进Akk菌的生长
韩国一项双胞胎队列(n=582)研究表明,B.vulgatus可以促进另一个肠道有益细菌Akkermansia muciniphila(简称Akk菌)的生长。
编辑
研究发现,B.vulgatus通过代谢物的产生,尤其是在黏蛋白降解过程中,促进了Akkermansia muciniphila的丰度。B.vulgatus产生的代谢物(如N-乙酰氨基葡萄糖)对Akk菌的生长至关重要。在高脂饮食导致Akk菌数量减少的情况下,B.vulgatus的施用可以恢复其丰度。
噬菌体互作:被温和噬菌体感染后,可通过抑制感受蛋白 TspO 改变转录组并抑制胆汁酸脱缀合,进而影响宿主胆汁酸信号与表型。
与其他菌的互作:
增强:
Akkermansia muciniphila;
Bacteroidales;
Bacteroides;
Odoribacter;
Peptococcaceae.
抑制:
Bifidobacterium
Coriobacteriales
Adlercreutzia
Collinsella
Porphyromonas
Prevotella
Clostridium
Clostridiales incertae sedis
Clostridiales Family XIII. Incertae Sedis
Blautia
Coprococcus
Dorea
Lachnospiraceae
Ruminococcaceae
Ruminococcus
Dialister
Campylobacteraceae
Erysipelotrichaceae
普通拟杆菌(Bacteroides vulgatus)是人类肠道微生物组中一种重要的厌氧细菌,对维持整体健康至关重要。作为常驻菌群的成员,它参与多种关键生理功能,包括营养物质的代谢、维持肠道微环境的平衡,以及通过产生短链脂肪酸来支持肠道黏膜的完整性。
此外,B.vulgatus还能调节免疫反应,有助于抗炎效应,从而帮助防止各种疾病的发生。这种细菌的健康益处不仅限于肠道,研究表明它与心血管健康、代谢平衡及免疫系统的良好运作密切相关。
1
改善血糖控制并减少糖分渴望
2025年1月,江南大学研究团队在《Nature Microbiology》(IF:20.5)发表重要研究成果:游离脂肪酸受体4(Ffar4)通过肠道菌群调控糖类偏好的分子机制。
编辑
• B.vulgatus丰度下降减少GLP-1的分泌
研究表明,Ffar4表达下调与高糖饮食行为相关,其缺失会导致肠道普通拟杆菌(Bacteroides vulgatus)丰度降低及代谢产物泛酸盐(维生素B5)减少。泛酸盐通过促进GLP-1分泌,激活肝脏FGF21释放,进而作用于下丘脑神经环路,抑制糖类摄入欲望并调节能量代谢平衡。该发现揭示了全新的肠-肝-脑轴调控网络,为代谢性疾病的干预提供了潜在治疗靶点。
GLP-1通过让身体在需要时释放胰岛素,减缓食物离开胃的速度,帮助身体。这能保持血糖稳定,帮助控制食欲。FGF21是另一种激素,能增强身体对胰岛素的敏感度,帮助你燃烧更多能量,并减少对含糖食物的渴望。它们共同创造了一个强大的系统,帮助保持新陈代谢和大脑的正常运作。
2
帮助恢复Akk菌,减轻肥胖
刚才前文就有提到,B.vulgatus通过产生的代谢物(如N-乙酰氨基葡萄糖),促进了Akkermansia muciniphila的丰度。
编辑
You HJ,et al.Gastroenterology.2023
• 改善了Akk菌的耗竭,减轻了肥胖体重
研究发现,Bacteroides vulgatus 与 Akkermansia muciniphila 在瘦受试者(BMI<25)中存在互作关系,但在肥胖群体(BMI≥25)中这种互作消失。补充普通拟杆菌(Bacteroides vulgatus SNUG 40005)显著改善了高脂饮食小鼠的肥胖、胰岛素抵抗和肠道通透性,并通过产生代谢物N-乙酰葡萄糖胺提升了肥胖小鼠中Akkermansia的丰度。
研究者从健康成年人肠道中分离出 Bacteroides vulgatus SNUG40005,并将其灌胃给高脂饮食的肥胖小鼠,结果发现该菌株能显著降低小鼠体重、改善糖耐量并减少血液中脂多糖水平。
// 结论
综合以上结果,Bacteroides vulgatus 通过调节肠道微生物的相互作用,特别是促进Akkermansia muciniphila 的生长,可能对肥胖和代谢健康产生积极影响。这些发现为发展新型治疗方法提供了依据,尤其在管理肥胖和相关代谢疾病方面。
3
抑制动脉粥样硬化
冠状动脉疾病(CAD)患者的肠道微生物谱分析显示,与无冠状动脉风险因素的对照组相比,Bacteroides vulgatus和Bacteroides dorei的丰度显著降低。证实Bacteroides vulgatus和Bacteroides dorei通过降低血液内毒素水平改善动脉粥样硬化小鼠体的症状。
• B.vulgatus与脂多糖水平负相关,影响心血管健康
并且在CAD患者中,B.vulgatus和B.dorei的丰度与粪便脂多糖水平呈负相关,暗示这两种细菌可能通过调控脂多糖的产生来影响动脉粥样硬化的进展。
总之,Bacteroides vulgatus 在调节肠道微生物群、抑制炎症反应及维护心血管健康方面发挥着重要作用。进一步的研究可能帮助开发基于微生物群的策略,用于防治心血管疾病。
4
改善脂质代谢并调节高血脂
Bacteroides vulgatus Bv46 是一种常见的肠道细菌,其在高脂血症(高血脂)中的潜在健康效益受到研究。该研究通过高脂饮食诱导大鼠模型,评估了B.vulgatus Bv46 的补充对体重、脂质代谢、炎症标志物及肝脏病理的影响。
编辑
• 关键发现:
改善脂质代谢:补充B.vulgatus Bv46 显著降低了高脂饮食大鼠的体重增加、食物效率以及肝脏指数,改善了血清脂质状况,包括降低总胆固醇(TC)、甘油三酯(TG)和低密度脂蛋白胆固醇(LDL-C),并提高了高密度脂蛋白胆固醇(HDL-C)的水平。
调节炎症反应:补充后,血清中的促炎细胞因子(如 IL-1β、IL-6 和 TNF-α)显著降低,表明B.vulgatus Bv46 能够减轻全身炎症反应。
肠道微生物的改变:该菌株的补充导致肠道微生物群落组成的显著变化,主要表现为Firmicutes与Bacteroidetes 的比率降低,Bacteroides 和 Parabacteroides 属的丰度增加,这种变化与健康个体的微生物群落特征相似。
短链脂肪酸的产生:补充B.vulgatus Bv46促进了肠道内短链脂肪酸(SCFAs),特别是丙酸和丁酸的产生,这些代谢产物对抗炎和代谢健康具有重要作用。
胆汁酸代谢:研究发现,B.vulgatus Bv46 产生的胆盐水解酶(BSH)有助于胆汁酸的去结合,促进了胆汁酸的转化和排出,从而改善了胆固醇代谢。
代谢组学影响:血清代谢物分析显示,补充B.vulgatus Bv46 能够增强氨基酸、甘油磷脂的代谢,并对脂质代谢产生正面影响。
// 结论
Bacteroides vulgatus Bv46 通过多种机制(包括改善血脂谱、减轻全身性炎症、调节肠道微生物群、增强短链脂肪酸产生和胆汁酸代谢)证明了其在高脂血症干预中的潜力。这些发现不仅支持了B.vulgatus在宿主代谢调节中的作用,也为高脂血症的治疗提供了新的潜在策略。
5
减轻肠道炎症
• B.vulgatus有助于减轻结肠炎症状和病理损伤
有研究探讨了B.vulgatus在小鼠模型中对结肠炎的保护作用及其通过调节肠道微生物群和免疫反应的机制。
编辑
研究发现,B.vulgatus的补充显著减轻了小鼠的结肠炎症状,包括减轻体重下降、改善粪便形态以及减少结肠病理损伤。这表明该菌株在缓解肠道炎症方面具有效果。
此外,B.vulgatus的使用还导致结肠中促炎细胞因子TNF-α、IL-1β和IL-6的表达下降,并可能通过短链脂肪酸(SCFAs)释放实现抗炎效果。
• B.vulgatus可能作为治疗溃疡性结肠炎的靶点
编辑
另一项溃疡性结肠炎(UC)患者的多组学分析研究发表于《Nature Microbiology》,研究发现Bacteroides vulgatus来源的蛋白酶是破坏UC患者肠道屏障的一个原因,体外和体内实验均证实抑制该蛋白酶可降低小鼠结肠炎的发生。Bacteroides vulgatus分泌的蛋白酶可做为治疗UC的潜在靶点。
• 保护急性肠道损伤
还有研究探讨了不同Bacteroides vulgatus菌株对脂多糖(LPS)诱导的急性肠道损伤的保护作用。
从健康的人类粪便样本中分离出七个B.vulgatus菌株,分别命名为FTJS7K1、FTJS5K1、FSDTA11B14、FJSWX62K35、FSDLZ51K1、FBJS10K3和FGSZY37K4。
编辑
研究发现,B.vulgatus FTJS7K1的施药能保护肠道上皮的完整性。B.vulgatus FTJS7K1还抵消了LPS诱导的结肠组织细胞因子mRNA表达变化,以及肠系膜淋巴结中调节T细胞比例的变化。
与LPS组相比,FTJS7K1 组的B.vulgatus增加了乳杆菌、阿克曼氏菌和双歧杆菌的丰度,而 Faecalibaculum 的丰度则下降。此外,B.vulgatus FTJS7K1 组的粪便样本中短链脂肪酸(SCFAs)浓度显著增加。基因组分析表明,FTJS7K1 的保护作用可能通过与防御机制和代谢相关的特定基因介导(例如 SCFA 的分泌)。
6
在骨骼健康中存在矛盾作用
有研究探讨了Bacteroides vulgatus在骨骼健康中的作用,但结果存在矛盾。例如一项研究分析了该菌株在去除卵巢小鼠模型中改善结肠微生物群失调和减轻骨质流失的潜力。
• B.vulgatus在去除卵巢小鼠中减轻骨质流失
研究发现补充B.vulgatus显著减轻了去卵巢小鼠的椎体骨质流失。这一发现表明,该菌株可能在雌激素缺乏引起的骨量减少中发挥保护作用。
B.vulgatus的施用还改善了去卵巢小鼠的结肠微生物群组成,增加了有益菌的丰度,特别是 Lactobacillus 和 Bifidobacterium 属;这些变化与骨质改善的效果相吻合。
• 下调血清戊酸、骨吸收增加
然而,在另外一项研究中发现:B.vulgatus的丰度增加会影响血清戊酸(VA)的水平,而这与骨密度呈正相关。喂食B.vulgatus的卵巢切除小鼠骨吸收增加,骨微结构变差,而喂食VA的小鼠则骨吸收减少,骨微结构改善。
总体而言,Bacteroides vulgatus对骨骼健康的影响并不是简单的有益或有害,而是取决于宿主的生理状态(如激素水平)。在雌激素缺乏的情况下,B.vulgatus的增多可能导致骨密度降低,而在改善肠道健康及抑制炎症的情况下,可能展现出一定的保护作用。因此,针对不同人群或临床情况,应谨慎评估B.vulgatus的治疗潜力。
B.vulgatus丰度过低与疾病
结合上文内容,总体来看,现有研究表明,B.vulgatus的丰度在这些疾病中普遍偏低,且这种低丰度可能与具体的健康问题存在潜在的联系。我们在下方的表格中进行了总结:
编辑
B.vulgatus丰度过高与疾病
尽管研究发现 Bacteroides vulgatus 具有多种代谢或健康方面的益处,但同时也观察到其在某些疾病状态下,其丰度异常增高。
①自闭症患者中丰度较高
编辑
研究发现,Bacteroides vulgatus在自闭症儿童中的丰度显著高于健康对照组,暗示其可能与自闭症症状的发展相关。这种细菌可以产生像丙酸这样的SCFA,在高浓度下可能具有神经毒性并影响行为。
②甲状腺炎患者中增加
编辑
在 Hashimoto 甲状腺炎 (HT) 的患者群体中,B.vulgatus 的丰度显著增加,这与肠道微生物群的失衡及免疫反应激活可能相关。
与其他细菌的对比:HT 患者的肠道微生物组相比于健康对照组,显示出整体的细菌多样性和丰度改变,且B.vulgatus在特定条件下的增多可能与其他有害菌(如Escherichia-Shigella)的共存有关。
③可能是婴儿乳糜泻的风险因素
过高水平的 B. vulgatus 还被认为是婴儿乳糜泻的重要风险因素,这意味着当这种细菌在婴儿的肠道中丰度较高时,患上乳糜泻的可能性会增加。
饮食因素
B.vulgatus的种群规模对所摄入的食物高度敏感,因此饮食是影响其丰度的最重要外部因素。
•高纤维饮食:富含植物纤维和抗性淀粉的饮食能够促进B.vulgatus的生长。全谷物、豆类、蔬菜及坚果等食物能够为这种细菌提供营养,帮助其发酵并产生有益的短链脂肪酸(SCFAs),这些代谢产物对维持肠道健康和代谢调节至关重要。洋葱、大蒜、香蕉和芦笋等食物也被发现能够促进B.vulgatus丰度增加。
•发酵食品:酸奶、开菲尔、酸菜、泡菜等发酵食品也有助于支持B.vulgatus的健康生长。
•富含多酚的食物:食用富含多酚的食物,如浆果、绿茶、黑巧克力和红酒。
•减少加工食品摄入:高加工食品通常纤维含量低,会对有益细菌产生负面影响,导致肠道菌群不平衡,进而抑制 B. vulgatus 的生长。
生活方式因素
•日常锻炼:规律的身体活动有助于增强肠道微生物的多样性,从而支持B.vulgatus的丰度。
•压力管理:持续的心理压力可能对肠道健康产生负面影响。采用减压措施(如冥想、瑜伽和正念练习)有利于维护肠道微生物的平衡。
•健康的睡眠模式:保持规律的睡眠,以支持肠道微生物群的平衡。
药物与补充剂
•益生菌:考虑直接补充益生菌以增加肠道中的B.vulgatus。
•避免不必要的抗生素:仅在必要时使用抗生素,以避免破坏肠道微生物群。
主要参考文献:
quez-Baeza Y, Sauceda C, Daniel N, Gerner RR, Batachari LE, Malfavon M, Zhu Q, Weldon K, Humphrey G, Carrillo-Terrazas M, Goldasich LD, Bryant M, Raffatellu M, Quinn RA, Gewirtz AT, Chassaing B, Chu H, Sandborn WJ, Dorrestein PC, Knight R, Gonzalez DJ. Multi-omics analyses of the ulcerative colitis gut microbiome link Bacteroides vulgatus proteases with disease severity. Nat Microbiol. 2022 Feb;7(2):262-276.
Yoshida N, Emoto T, Yamashita T, Watanabe H, Hayashi T, Tabata T, Hoshi N, Hatano N, Ozawa G, Sasaki N, Mizoguchi T, Amin HZ, Hirota Y, Ogawa W, Yamada T, Hirata KI. Bacteroides vulgatus and Bacteroides dorei Reduce Gut Microbial Lipopolysaccharide Production and Inhibit Atherosclerosis. Circulation. 2018 Nov 27;138(22):2486-2498.
Wang C, Xiao Y, Yu L, Tian F, Zhao J, Zhang H, Chen W, Zhai Q. Protective effects of different Bacteroides vulgatus strains against lipopolysaccharide-induced acute intestinal injury, and their underlying functional genes. J Adv Res. 2021 Jun 15;36:27-37.
Xu M, Lan R, Qiao L, Lin X, Hu D, Zhang S, Yang J, Zhou J, Ren Z, Li X, Liu G, Liu L, Xu J. Bacteroides vulgatus Ameliorates Lipid Metabolic Disorders and Modulates Gut Microbial Composition in Hyperlipidemic Rats. Microbiol Spectr. 2023 Feb 14;11(1):e0251722.
Liu L, Xu M, Lan R, Hu D, Li X, Qiao L, Zhang S, Lin X, Yang J, Ren Z, Xu J. Bacteroides vulgatus attenuates experimental mice colitis through modulating gut microbiota and immune responses. Front Immunol. 2022 Nov 30;13:1036196.
Yuan S, Shen J. Bacteroides vulgatus diminishes colonic microbiota dysbiosis ameliorating lumbar bone loss in ovariectomized mice. Bone. 2021 Jan;142:115710.
Li S, Wang C, Zhang C, Luo Y, Cheng Q, Yu L, Sun Z. Evaluation of the Effects of Different Bacteroides vulgatus Strains against DSS-Induced Colitis. J Immunol Res. 2021 May 29;2021:9117805.
Lin X, Xiao HM, Liu HM, Lv WQ, Greenbaum J, Gong R, Zhang Q, Chen YC, Peng C, Xu XJ, Pan DY, Chen Z, Li ZF, Zhou R, Wang XF, Lu JM, Ao ZX, Song YQ, Zhang YH, Su KJ, Meng XH, Ge CL, Lv FY, Luo Z, Shi XM, Zhao Q, Guo BY, Yi NJ, Shen H, Papasian CJ, Shen J, Deng HW. Gut microbiota impacts bone via Bacteroides vulgatus-valeric acid-related pathways. Nat Commun. 2023 Oct 27;14(1):6853.

谷禾健康
精神分裂症(SCZ)是一种严重的持续性精神障碍,表现为阳性症状(如妄想和幻觉)、负性症状(如动力丧失和社交退缩)以及认知症状(包括工作记忆和认知灵活性缺失)。此外,大多数精神分裂症患者伴有显著的睡眠障碍(SD),常出现入睡困难、睡眠维持问题、睡眠结构紊乱和昼夜节律失调。
睡眠障碍这种共病会加重精神症状,导致更频繁的偏执意念、幻觉和思维紊乱,以及更高程度的抑郁和焦虑。还显著影响治疗依从性和长期预后。
精神分裂症的发病机制涉及遗传、环境、免疫和神经发育等多种因素的相互作用。与此同时,现有研究表明,肠道微生物群通过微生物群-肠道-大脑轴调节大脑功能,影响神经递质的代谢和免疫炎症反应,因此可能在精神分裂症和睡眠障碍的发生和发展中发挥重要作用。
精神分裂症患者常表现出产丁酸细菌减少、产乳酸菌增加,以及与谷氨酸和γ-氨基丁酸(GABA)代谢相关的细菌增加。特别是,在精神分裂症患者中,这种肠道微生物群破坏可能通过影响神经递质平衡、促进神经炎症和干扰昼夜节律等机制,促成精神症状和睡眠问题的发展。
本文整合了现有研究,首先介绍了精神分裂症(SCZ)和睡眠障碍(SD)患者的肠道微生物群特征。探讨了SCZ和SD中关键微生物群及其代谢物的共同影响,以及肠道微生物群通过神经免疫、内分泌和神经递质通路的作用机制。最后,提出了针对肠道微生物群的干预策略在改善精神分裂症伴随SD中的潜在应用。
精神分裂症(SCZ)是一种严重的精神障碍,表现为阳性症状(超出正常范围的行为和思维)如妄想和幻觉;负性症状(缺乏正常的情感和行为)如动力丧失和社交退缩;以及认知症状,包括工作记忆和认知灵活性的缺失。
★ 许多精神分裂症患者伴有睡眠障碍
除了典型的精神症状外,睡眠障碍(SD)是精神分裂症最常见的共病之一,表现为失眠、睡眠片段化、慢波睡眠减少和昼夜节律紊乱。
研究显示,约80%的精神病患者至少患有一种类型的SD。睡眠质量的恶化会加重精神症状,导致更频繁的偏执意念、幻觉和思维紊乱,以及更高程度的抑郁和焦虑。研究发现,睡眠质量受损和昼夜节律紊乱的精神分裂症(SCZ)患者在负性症状评估上得分更高,认知功能障碍更为明显。
此外,SD不仅加重精神分裂症的精神病症状,精神分裂症的核心症状也会破坏睡眠生理。多导睡眠图研究表明,更严重的阳性症状与短的快速眼动(REM)潜伏期、长的入睡潜伏期和低睡眠效率相关,而明显的负性症状与非快速眼动(NREM)睡眠中的慢波振幅降低和REM起始潜伏期缩短有关。
这些发现表明精神分裂症与睡眠障碍之间存在双向病理循环,睡眠障碍不仅是精神分裂症的常见共病,也是影响其症状表达和疾病进展的关键因素。
1
流行病学特征
研究表明,精神分裂症(SCZ)患者的睡眠障碍(SD)患病率显著高于普通人群,影响其生活质量和疾病预后。
精神分裂症患者快速眼动睡眠时间缩短
通过睡眠脑电图(EEG)观察精神分裂症患者与健康对照组的睡眠结构差异发现,精神分裂症患者的快速眼动(REM)潜伏期缩短,REM密度增加,并且REM睡眠比例与症状严重程度密切相关。在非快速眼动(NREM)睡眠期间,精神分裂症患者呈现慢波睡眠减少、纺锤体波密度和振幅下降,以及持续时间缩短。
不同精神分裂症患者睡眠障碍也表现出差异
同时,不同精神分裂症患者组间的睡眠障碍表现也存在显著差异,例如,住院患者在睡眠时间、活动水平和生物钟稳定性方面较门诊患者表现更加严重。这表明精神分裂症临床症状的严重程度不仅取决于病理机制,还受到患者生活环境和治疗状态等多种因素的影响。
2
睡眠障碍对精神分裂症的影响
夜间睡眠不足会进一步导致白天功能障碍和生活质量下降。大量临床研究证实,睡眠障碍与精神分裂症患者核心症状组之间存在显著且特异的关联模式。
睡眠障碍会加重精神分裂症症状并影响治疗效果
睡眠障碍不仅加重精神分裂症的阳性症状(如幻觉和妄想),还会加重负性症状(如情感冷漠和社交退缩),进而影响患者的认知功能。此外,患有睡眠障碍的精神分裂症患者表现出治疗依从性差、静坐不能和攻击性言语。
睡眠障碍的精神分裂症患者自杀行为风险增加
在一项为期八年的纵向研究中,结合Kaplan–Meier生存分析和对数秩检验,发现患有精神分裂症谱系障碍且频繁失眠的患者,其累计自杀行为风险显著增加,证实睡眠障碍会增加这些患者的自杀风险。这些结果显示睡眠问题对精神分裂症患者产生负面影响,强调了加强临床关注精神分裂症患者睡眠的必要性。
3
现有治疗的局限性
目前,治疗合并睡眠障碍(SD)的精神分裂症(SCZ)患者主要依赖传统抗精神病药物,特别是非典型抗精神病药物如氯氮平、奥氮平、喹硫平、利培酮、齐拉西酮和帕利立酮。
这些药物有助于提高精神分裂症患者的总睡眠时间和睡眠效率。然而,它们在改善SD方面的疗效有限,并伴有如体重增加和代谢综合征等副作用,部分患者在接受治疗后仍出现睡眠质量差和睡眠结构障碍。
药物疗法存在副作用,生物行为疗法逐渐兴起
尽管药物治疗是主要干预手段,但患者对药物依赖和副作用的担忧使得部分人不愿长期使用。此外,认知行为疗法(CBT)在改善持续妄想或幻觉患者的睡眠上已显示一定效果,但其临床应用仍需更多研究支持。这表明当前治疗精神分裂症合并睡眠障碍的方法面临显著局限,需探索新的治疗靶点和方法。
近年来,褪黑素的研究显示其在调节睡眠-觉醒节律、改善睡眠质量和缓解精神分裂症症状方面有效。同时,生物反馈疗法及其他非药物干预(如光疗和睡眠卫生教育)也被认为是有效的辅助治疗方式,可以改善患者睡眠质量。
总体而言,现有精神分裂症与睡眠障碍的联合治疗方法在疗效和耐受性上存在明显局限,迫切需要通过进一步研究和临床试验来探索新的治疗方案,以为患者提供更有效和安全的治疗选择。
近年来,研究发现肠道微生物群在调节精神健康和睡眠质量方面扮演着重要角色。数据显示,精神分裂症患者的肠道微生物群与健康个体存在显著差异,表现为多样性降低和特定微生物群落的失衡。与此同时,睡眠障碍的发生也与肠道微生物群的组成变化密切相关,这种相互作用可能通过微生物群-肠道-大脑轴影响患者的情绪、认知功能和睡眠模式。
1
精神分裂症患者的肠道菌群失调
多项研究发现,肠道微生物群与精神分裂症(SCZ)的病理机制、症状和认知功能密切相关。
关于精神分裂症患者肠道微生物群变化的研究
编辑
编辑
变形菌增加,拟杆菌减少,这会影响代谢健康
高通量测序结果表明,与健康对照组相比,精神分裂症患者的肠道微生物群丰富度指数(Chao)和多样性指数(Shannon)均较低,且特定微生物群的组成和丰度存在显著差异。曼-惠特尼U检验显示,精神分裂症患者的拟杆菌门(Bacteroidetes)显著减少,而变形菌显著增加。
Faecalibacterium等产生丁酸盐的抗炎菌减少
在属层面,与抗炎和神经保护作用相关的丁酸产生菌Faecalibacterium、Coprococcus和Bacteroides的丰度下降,而Prevotella和Collinsella丰度增加。短链脂肪酸(SCFAs)产生菌减少和促炎细菌增加可能与精神分裂症(SCZ)患者的病情严重程度有关。
微生物群的差异可能有助于判断疾病不同阶段
在不同疾病阶段的研究中,急性精神分裂症患者的嗜血杆菌属(Haemophilus)和Faecalibacterium数量减少,而缓解期患者则表现出巨单胞菌属(Megamonas)和Megasphaera的增加。
注:在这里小编推测嗜血杆菌属(Haemophilus)在肠道里变少可能更像“口源菌/黏膜相关菌”的信号,急性期患者的黏膜生态位与免疫/炎症微环境发生了系统性改变,而不是单纯少了一种好菌或坏菌,也可能是研究存在饮食,治疗等的混杂因素。
此外,口腔常驻细菌如Veillonella atypica、唾液链球菌(Streptococcus salivarius)和Bifidobacterium dentium在精神分裂症患者肠道微生物群中显著富集,这种病理状态可能削弱肠道屏障和免疫功能,为口腔细菌的肠道定殖提供有利条件。
一项涵盖细菌、真菌、古菌和病毒的综合多界微生物组分析发现,精神分裂症患者肠道中链球菌、脱硫弧菌(利用氨基酸或脂肪酸作为碳源)和Methanobrevibacter smithii等微生物数量增加,而丁酸盐产生菌的数量减少。
精神分裂症人群中吸烟率、牙周状况差异常见;如果口腔来源菌输入或口腔生态改变,使得口腔菌更容易通过吞咽等进入肠道并在那里存活、甚至黏附定殖肠道菌群组成更像“口腔来源的组合”,常见于炎症、屏障受损或环境改变的肠道。可以推测病源菌增加 + 产丁酸菌(如 Faecalibacterium)下降+ 屏障/炎症指标异常(如 LPS/DAO/zonulin、粪便钙卫蛋白、炎症因子),可能是未来辅助判别急性精神分裂症的重要标志组合。
2
与睡眠障碍相关的微生物群变化
在具有睡眠障碍(SD)的人类和动物模型中也观察到了微生物群变化。
关于睡眠障碍患者肠道微生物群变化的研究
编辑
微生物群的多样性与睡眠效率和睡眠时间正相关
对健康成年人睡眠的研究发现,微生物群的多样性与睡眠效率和总睡眠时间呈正相关,而与睡眠碎片化呈负相关。简而言之,肠道微生物群的多样性促进了更健康的睡眠。
此外,针对学龄前儿童的研究表明,夜间睡眠时间较长的孩子肠道微生物群结构与睡眠时间较短的孩子不同,且微生物群中的双歧杆菌和拟杆菌与睡眠时间延长、睡眠效率提高和夜间清醒时间缩短相关。
睡眠紊乱导致肠道菌群失调,普雷沃氏菌等增加
研究还表明,睡眠和昼夜节律紊乱会导致人类和动物模型中的肠道微生物群失调,表现为致病菌增加和有益菌减少。在人类中,睡眠不足和质量差常与普雷沃氏菌科(Prevotellaceae)和丹毒丝菌科(Erysipelotrichaceae)的增加及瘤胃球菌属(Ruminococcus)的减少有关。
在动物模型中,睡眠剥夺和破碎会导致毛螺菌科(Lachnospiraceae)和丹毒丝菌科(Erysipelotrichaceae)增加,而乳杆菌科(Lactobacillaceae)和双歧杆菌科(Bifidobacteriaceae)减少。
人类和小鼠的平行实验显示,不同物种的肠道微生物群存在昼夜节律振荡。此外,将人类在经历时差反应前后的肠道微生物群移植到无菌小鼠中,会导致微生物群结构改变,并出现代谢异常,如体重增加、血糖升高和体脂肪堆积。
不同类型的睡眠障碍患者显示出微生物群的特征差异
不同类型的睡眠障碍(SD)患者似乎表现出不同的肠道微生物群特征。慢性失眠患者主要表现为放线菌门数量增加,抗炎菌属Faecalibacterium含量减少,这一变化可能与长期低度炎症状态相关。
相比之下,急性失眠患者的肠道微生物群中,厚壁菌门增加而拟杆菌门减少,这一模式与急性24小时睡眠剥夺实验的发现高度相似,表明这种短期微生物失衡可能是对睡眠模式突然变化的压力反应。
此外,厚壁菌门数量增加,而拟杆菌门减少,导致(F/B)比例升高。关于急性睡眠时间表延迟的研究进一步证实,睡眠与觉醒周期的改变会增加F/B比。研究还报告指出,急性昼夜节律紊乱促进疾病相关的嘌呤代谢和丁酸生成乙酰辅酶A发酵途径,这些通路与宿主能量代谢和炎症反应相关。
注:这些代谢变化在恢复期内往往会逆转。
3
精神分裂症与睡眠障碍的微生物共性
基于研究发现,精神分裂症(SCZ)患者和睡眠障碍(SD)患者的肠道微生物多样性均降低,且特定微生物群组成发生类似变化。这种多样性的缺乏可能削弱肠道微生态系统的稳定性,增加疾病风险。
能代谢膳食纤维的菌种减少,而促炎菌增加
在微生物群组成方面,抗炎菌减少、促炎菌增加,这与疾病易感性密切相关。此外,结肠中的微生物如拟核菌、双歧杆菌和Faecalibacterium能发酵不易消化的碳水化合物和寡糖,从而合成短链脂肪酸(SCFAs)。这些属的减少显著影响丁酸盐、丙酸酯和乙酸盐的生产。
微生物群通过肠脑轴影响精神分裂症和睡眠障碍
与睡眠密切相关的特定微生物群在精神分裂症患者中数量减少。例如,双歧杆菌的减少与睡眠效率降低和睡眠碎片化有关,而Prevotella的增加可能干扰睡眠结构。
在关于睡眠与肠道微生物组组成的研究中,曼-惠特尼U测试显示,Ellagibacter isourolithinifaciens和Senegalimassilia faecalis在睡眠质量良好的患者中显著富集。在属层面,Senegalimassilia与患者的较好睡眠质量呈正相关。
这些微生物改变的特征表明,精神分裂症和睡眠障碍通过微生物群-肠道-大脑轴(MGBA)相互作用。这一过程涉及短链脂肪酸生成减少、全身炎症加剧和昼夜节律紊乱等机制,这些因素共同促进并加重两种疾病的共存和进展。
在肠道微生物群影响精神疾病的复杂病理网络中,宿主的遗传背景和环境因素共同构成了疾病易感性的基础。全基因组多效性分析揭示了胃肠疾病与精神疾病之间的广泛遗传相关性、共同的致病基因和通路,以及它们与肠道微生物群的遗传关联,证实了微生物群-肠道-大脑轴(MGBA)在这两类疾病的共同遗传基础中的关键作用。
多种环境因素,如地理位置、饮食和生活方式,动态调节肠道微生物群的丰富性和多样性,同时影响MGBA的功能稳态。MGBA作为宿主与微生物相互作用的调控枢纽,通过神经、内分泌和免疫系统之间的多层次双向通信网络,整合肠道微生态系统与中枢神经系统的功能耦合。
具体而言,肠道微生物群通过迷走神经直接调节中枢神经系统的活动,影响血脑屏障的通透性、神经炎症及通过细胞因子介导的免疫调节通路促进神经递质的合成和代谢。MGBA功能障碍可能导致病理变化,如下丘脑-垂体-肾上腺(HPA)轴异常激活及小胶质细胞持续激活,这些与精神疾病如精神分裂症(SCZ)和睡眠障碍(SD)的共病机制密切相关。
肠道微生物群及其代谢物通过肠-脑轴相互作用
编辑
1
神经递质调控
肠道菌群通过神经递质影响精神状态和睡眠
在精神分裂症(SCZ)和睡眠障碍(SD)研究中,神经递质的异常代谢被认为是影响症状的重要因素,而肠道微生物群及其代谢物在神经递质的产生和功能调控中发挥关键作用。如血清素(5-HT)、GABA和多巴胺(DA)的代谢异常可能妨碍SCZ的神经传导及SD的睡眠调节。
研究显示,肠道微生物群通过调控色氨酸代谢直接影响5-HT的生物合成。在松果体中,5-HT经历一系列酶转换,通过N-乙酰化转化为N-乙酰丝氨酸,并进一步O-甲基化合成褪黑素。该生物合成途径的完整性直接影响内源性褪黑素的生成,进而影响睡眠的开始和维持。
因此,肠道微生物群可以通过影响色氨酸的可用性来调控该代谢途径,从而通过特定微生物群增加色氨酸转化为5-HT而非犬尿氨酸途径,从而提高5-HT和褪黑素的水平。
乳杆菌和双歧杆菌通过GABA影响精神分裂症
研究表明,特定微生物群如乳杆菌和双歧杆菌不仅能促进色氨酸转化为血清素(5-HT),还可以直接合成GABA。作为中枢神经系统的主要抑制性神经递质,GABA与精神分裂症(SCZ)患者的焦虑和抑郁症状密切相关,其代谢异常对症状产生影响。通过与GABA受体结合,它有效降低神经兴奋性,延长慢波睡眠时间。
总之,神经递质的代谢在精神分裂症和睡眠障碍的病理机制中扮演重要角色。肠道微生物群通过影响神经递质的水平,不仅影响精神症状,还通过改变睡眠加重病情。因此,针对神经递质代谢的干预措施为治疗SCZ合并SD患者提供了新的思路与策略。
2
免疫炎症通路
肠道微生物群组成的变化会促进神经炎症,而这种炎症被认为是多种精神疾病(包括精神分裂症(SCZ)和睡眠障碍(SD))的重要病理机制。
IL-6和TNF-α等促炎细胞因子增加易导致精神分裂症恶化
肠道微生物群及其代谢物是调控小胶质细胞的成熟、形态和功能的关键分子。微生物群的变化可激活胶质细胞,促使IL-6和TNF-α等促炎细胞因子的释放,这影响神经元的存活与功能,破坏血-脑屏障的完整性,使外周炎症细胞因子和神经活性代谢物渗透中枢神经系统,最终诱发神经炎症反应。
针对SCZ患者的纵向研究显示,IL-6和TNF-α水平较高与脑源性神经营养因子(BDNF)水平下降及认知障碍相关。这些炎症标志物水平较高的SCZ患者更可能出现症状恶化。免疫系统在特定症状中也发挥作用,炎症刺激能改变健康个体腹侧纹状体区域的神经活动,导致动机减弱和奖赏处理缺陷,表明炎症与负性和认知症状之间的病理生理关系。
急性炎症升高也影响睡眠时间和深度
此外,睡眠障碍(SD)与炎症标志物如C反应蛋白(CRP)和IL-6的增加有关,急性炎症升高可改变睡眠的时间和深度。使用曼-惠特尼大学测试的统计分析发现,与对照组相比,接受72小时快速眼动(REM)睡眠剥夺的小鼠血浆内脂多糖浓度升高和TNF-α显著上调。
限制大鼠睡眠后,血-脑屏障的选择性过滤功能减弱,降低了阻断有害物质的能力,增加了神经炎症的风险。
通过调节肠道菌群的抗炎治疗有助于改善精神分裂症合并睡眠障碍
在临床干预中指出,使用认知行为疗法(CBT)治疗慢性和原发性失眠的老年患者后,炎症风险标志物减少,显示免疫炎症通路与睡眠障碍存在显著关联。
抗炎治疗可能是改善SCZ合并SD患者的重要策略。通过降低炎症通路则可减少小胶质细胞的激活和促炎细胞因子的产生,从而改善患者的整体症状和生活质量。
未来的研究应集中于探索特定的抗炎干预方法(如细胞因子拮抗剂或微生物组调控)对精神分裂症(SCZ)合并睡眠障碍(SD)患者的治疗效果及潜在神经保护机制。
3
神经内分泌调节
下丘脑-垂体-肾上腺轴(HPA)是神经内分泌系统的核心部分,在调节应激反应中发挥关键作用,其功能障碍已成为肠道微生物群介导睡眠障碍(SD)的重要机制之一。
压力下的高糖皮质激素导致认知障碍和焦虑增加
在压力条件下,下丘脑分泌的促肾上腺皮质激素释放因子(CRF)激活垂体前叶,释放促肾上腺皮质激素(ACTH),随后刺激肾上腺皮层合成糖皮质激素,如皮质醇。
长期过度暴露于糖皮质激素会影响大脑不同区域的神经元可塑性。这些结构重塑与认知功能障碍和动物实验中焦虑类行为增加密切相关,表明糖皮质激素介导的异常神经回路可能是慢性压力和精神障碍中认知缺陷和情感症状的重要病理基础。大量临床证据表明,HPA轴功能障碍在精神分裂症中普遍存在。
具体而言,精神分裂症患者的皮质醇觉醒反应(CAR)呈现明显异常模式,包括过度多动或钝化。这些患者的晨间基础皮质醇水平显著高于健康人群,而这种HPA轴功能障碍的模式具有疾病特异性,在高风险精神病人群中未观察到类似变化。
精神分裂症患者松果体受损影响褪黑素合成分泌
神经影像学研究显示精神分裂症(SCZ)患者的松果体体积减少、钙化加重,导致褪黑素合成和分泌功能受损。这种多层次内分泌障碍与SCZ临床症状的严重程度相关,并扰乱睡眠与觉醒周期,增加睡眠起始潜伏期和睡眠连续性受损情况。
可见,神经内分泌异常与睡眠障碍(SD)在SCZ中形成复杂的双向调控网络。睡眠不足激活下丘脑CRF神经元,导致HPA轴过度激活和皮质醇增加,而高皮质醇水平则抑制褪黑素合成,干扰睡眠调节,进一步加重SD。这一过程形成“内分泌障碍-睡眠问题-疾病恶化”的病理闭环,促进SCZ的进展和症状维持。
4
代谢物介导的调控
肠道微生物群生成的代谢物,如短链脂肪酸(SCFA)、色氨酸衍生物和胆汁酸,直接或间接参与中枢神经系统的调控,影响神经递质的平衡、维持免疫稳态,并调节昼夜节律。
丁酸盐有助于改善精神分裂症状和睡眠质量
菌群失调可破坏肠道屏障的完整性,增加肠道通透性,损害血-脑屏障的功能。这些双重屏障的破坏使得细菌代谢产物和促炎细胞因子等有害物质更易进入中枢神经系统,引发神经炎症反应。
丁酸盐作为关键代谢物,不仅对维持肠道黏膜的完整性至关重要,还能穿越血-脑屏障,通过激活迷走神经调节睡眠和清醒周期。动物研究发现,静脉注射丁酸盐显著延长了大鼠的非快速眼动睡眠(NREMS)时间。
此外,血清丁酸盐水平的升高与精神分裂症(SCZ)患者阳性和阴性综合征量表(PANSS)的阳性症状分数下降相关,暗示其潜在的神经保护作用。
血清素和胆汁酸水平下降可能是影响精神分裂症和睡眠障碍的重要机制
精神分裂症(SCZ)患者还表现出显著的色氨酸代谢障碍,研究发现其血浆色氨酸水平通常较低,这可能由于色氨酸向犬尿氨酸的转化增强和5-羟色胺(5-HT)合成途径的减少。这种转变导致神经递质5-HT和褪黑素的合成减少,由于这些物质在睡眠调节中起关键作用,其缺乏会加重精神分裂症患者的睡眠障碍(SD)。
代谢物分析显示,精神分裂症患者胆酸通路中的代谢物如糖果酸、牛磺酸脱氧胆酸和牛磺鹅脱氧胆酸的浓度显著降低,胆汁酸水平的下降通过影响抗炎信号通路,促进慢性低度炎症微环境的形成,从而增加神经退行性疾病和精神障碍的风险。研究还发现慢性失眠与特定胆酸结构和组成之间存在关联。
因此,代谢轴的异常不仅是精神分裂症的典型生物标志物,也是精神分裂症中睡眠障碍发病的关键机制之一。针对肠道微生物群及其代谢物的干预措施可为改善精神分裂症合并睡眠障碍患者提供新的治疗靶点。
5
昼夜节律紊乱
肠道微生物群与昼夜节律密切相关,其组成会随宿主生物钟的变化而波动,反之肠道微生物群的紊乱也会影响生物钟、肠道免疫功能和营养代谢。
肠道微生物群影响人体生物钟在精神疾病中发挥重要作用
肠道微生物群的组成和代谢物对宿主时钟基因(如CLOCK和Bmal1)的表达具有独特的调控作用。研究发现,微生物代谢物可以调节中枢神经系统和肝脏的生物节律,比如,短链脂肪酸(SCFAs)直接调控肝细胞中的时钟基因表达,影响宿主生物节律的稳定性。
肠道微生物群失衡在精神分裂症(SCZ)患者中较常见,这种失衡可能通过肠道-大脑轴影响宿主时钟基因的表达。分析首次发作SCZ患者的单核血细胞发现,与健康对照相比,患者的CLOCK、PER2和CRY1基因表达显著降低。而在慢性SCZ患者的成纤维细胞中,时钟基因CRY1和PER2的节律表达丧失。这些研究揭示了肠道微生物群通过代谢物与时钟基因的相互作用,对SCZ患者昼夜节律的稳定性至关重要。
时钟基因表达的变化不仅影响肠道微生物群的结构,还进一步影响核心昼夜节律输出通路的效率。研究表明,昼夜节律紊乱与肠道-大脑轴(MGBA)之间存在显著相互作用,MGBA在精神疾病的整个过程中持续影响患者的健康状况和临床症状。
昼夜节律调节神经内分泌活动影响精神分裂患者临床症状
结合本文前面的内容,昼夜节律通过调节神经内分泌活动和自主神经系统活动,调节睡眠、新陈代谢和免疫等生理过程。该输出通路的失效可能导致睡眠结构紊乱、压力激素节律失调,以及代谢和免疫反应的周期性紊乱,这些共同构成了精神分裂症患者常见的临床症状基础。与此同时,时钟基因表达的变化反过来会影响肠道微生物群的组成,显示出丰富度和多样性的减少,形成复杂的相互作用网络。
例如,研究显示宿主昼夜节律的核心激活基因(Bmal1)和抑制基因(Per1, Per2)共同调节肠道微生物群组成的昼夜振荡。这些时钟成分的基因敲除消除了这些节律波动,改变了小鼠的微生物群落结构。
深入研究肠道微生物群与其代谢物及时钟基因之间的关系,不仅有助于理解精神分裂症的发病机制,还将为基于肠道微生物群干预的未来治疗策略提供新思路。例如,通过调整饮食或补充益生菌以改善肠道微生物群的组成,调控时钟基因的表达以优化昼夜节律信号的传递效率,改善精神分裂症患者的临床症状。
小编总结
这组证据总体在说明:睡眠/昼夜节律紊乱本身就是一个能“驱动”肠道微生态改变的上游因素,而这种改变不仅是“相关”,还可能通过菌群把代谢风险传递出去。菌群不是静态的,它会随进食时间、胆汁酸分泌、肠蠕动、激素(如皮质醇/褪黑素)等出现日内波动,群落结构不稳定和功能(例如短链脂肪酸、胆汁酸转化、内毒素负荷)也会随之波动。
如果精神分裂症患者同时存在常见的睡眠/昼夜节律紊乱,那么观察到的某些肠道菌群特征(如特定门、科/属的增减,口源菌富集,以及产丁酸菌减少等)可能并非完全由疾病本身导致,而是共同受到多条路径的影响,包括:疾病相关应激、药物与生活方式,以及睡眠—生物钟失调这一通路。
与此同时,膳食纤维代谢菌减少提示菌群功能发生改变:尤其是短链脂肪酸(SCFAs)生成能力下降,可能削弱其对肠道屏障维护与免疫调节的作用;而促炎菌增加、抗炎菌减少则意味着机体更偏向促炎状态与肠道高通透,进而可能通过“肠—免疫—脑”轴影响中枢免疫激活与神经炎症。
在监测精神分裂症菌群时,睡眠状态可能是重要的混杂因素,也可能是可干预的上游靶点(改善睡眠可能间接改善菌群与代谢/炎症表型)。
尽管睡眠障碍与多种精神疾病的发生和发展密切相关,但针对精神分裂症(SCZ)合并发病的干预研究仍然不足。目前大多数治疗策略集中于症状控制,如通过抗精神病药物改善核心精神症状,而较少关注肠道微生物群失调机制。
因此,以下讨论提出针对肠道微生物生态的新治疗策略,包括特定益生菌、益生元、饮食干预、粪便微生物移植(FMT)和靶向代谢物治疗,旨在调节肠道-脑轴功能,以改善精神分裂症患者的睡眠问题及相关精神症状。
针对精神分裂症患者的微生物群干预方法
编辑
1
个性化补充益生菌
个体间肠道微生物群的差异会影响药物的疗效和毒性,因此个性化的肠道微生物群调控有助于改善药物反应。
通过检测精神分裂症(SCZ)患者的肠道微生物群,可以制定个性化益生菌方案,有效调节肠道微生物组成,从而改善症状。
长双歧杆菌等益生菌能改善精神状态
益生菌的疗效因菌株而异,不同菌株在调节炎症和压力方面表现出不同作用机制。例如,婴儿双歧杆菌(Bifidobacterium infantis 35624)已被证明能逆转HPA轴功能障碍,并与抗炎和促炎细胞因子比例的正常化相关,具有临床意义。
鼠李糖乳杆菌(Lactobacillus rhamnosus,JB-1)能降低压力诱发的皮质酮水平,缓解焦虑和抑郁行为。长双歧杆菌(Bifidobacterium longum NCC3001)通过MGBA内的迷走神经通路传递信号,使低度肠道炎症小鼠的焦虑行为和海马BDNF水平恢复正常。该菌株在人类试验中也显示抗抑郁效果,与多个情绪处理脑区活动变化相关。
益生菌有助于改善炎症相关、情绪状态及睡眠
在一项针对失眠患者的双盲研究中,参与者接受了植物乳杆菌(Lactobacillus plantarum PS128)或安慰剂。结果显示,PS128组在疲劳水平、脑电波活动和深度睡眠期间醒来次数方面有所改善,同时也缓解了焦虑和抑郁症状。这表明特定益生菌菌株可能通过微生物群-肠道-脑轴的机制(如GABA能系统调控)影响睡眠结构和情绪状态。
一项针对双相情感障碍和精神分裂症谱系障碍患者的双盲随机安慰剂对照试验表明,补充多株益生菌配方能改善与肠道通透性和炎症相关的生物标志物,并对认知功能产生积极影响。
这些研究结果揭示了益生菌补充剂在调节神经功能方面的潜在治疗价值,为进一步探索益生菌的干预机制提供了重要理论基础。
2
膳食益生元补充
益生元是一类能够抵抗宿主消化酶的功能性膳食成分,能选择性促进有益肠道微生物群的代谢活动,从而发挥生理调节功能。
菊粉等益生元改善精神分裂症的精神和行为症状
多项研究发现,半乳糖、菊糖型果聚糖及其合成制剂能够降低促炎因子(如高敏感性CRP、IL-6和TNF-α)的水平,表明特定的益生元干预可以调控炎症相关生物标志物的表达。菊粉作为可溶性膳食纤维,已被证实改善精神分裂症(SCZ)模型小鼠的精神和行为症状,同时增加有益菌数量并改善肠道通透性。
服用低聚果糖和低聚半乳糖的复合制剂也改善了SCZ模型小鼠的肠道功能。这些变化可能通过重塑肠道微生物群、降低促炎细胞因子水平以及增强肠道通透性,从而减少病原体与肠道黏液层的接触,为改善多种精神疾病的核心症状提供重要的病理生理基础。
益生元调节神经递质平衡改善精神状态及睡眠
另一项研究表明,短链半乳糖与长链果糖的联合干预显著促进了短链脂肪酸中乙酸和丁酸的生成。这些益生元成分还有效调控下丘脑和海马体中核心时钟基因BMAL1和CLOCK的表达。
这表明益生元通过多重靶点的协同效应发挥神经调节功能。特别是,益生元对时钟基因的调节可能通过恢复昼夜节律改善睡眠问题,并通过调节神经递质平衡潜在改善精神分裂症核心症状。
为促进益生元疗法在精神疾病临床实践中的应用,后续研究应明确不同益生元的应用价值、个体化剂量策略以及治疗的安全性和有效性评估。
3
饮食调整干预
特定饮食成分通过与肠道菌群互作影响睡眠质量
饮食调整是个性化治疗的重要部分,已有大量科学证据证明饮食与睡眠之间存在关系。健康饮食有助于改善睡眠质量,而加工食品和高糖食物则与睡眠质量较差相关。
特定饮食成分(如脂肪和蛋白质)及习惯(如牛肉、咖啡和干果摄入)通过与肠道微生物群相互作用影响睡眠。
生酮和高纤维饮食有助于改善睡眠质量和免疫
近年来,生酮饮食受到广泛关注,已被证明是改善伴有代谢异常的精神疾病患者心理和代谢健康的一种可行辅助治疗方法。根据匹兹堡睡眠质量指数(PSQI)评估,接受生酮饮食干预后,双相情感障碍和精神分裂症(SCZ)患者的主观睡眠质量有所改善。这表明,生酮饮食可以纳入精神疾病患者的综合治疗策略,有望在控制精神症状、调节代谢和改善睡眠方面带来多重益处。
此外,从高纤维饮食的角度来看,短链脂肪酸(SCFAs)是通过肠道共生细菌发酵膳食纤维产生的。当膳食纤维摄入不足时,SCFAs的生成水平会降低,这将对宿主的各种生理功能产生不利影响。增加膳食纤维摄入以促进SCFA的产生,不仅能增强血液和脑屏障的保护功能,维持肠道黏膜的完整,还能调节肠道微生物群的组成,从而协同促进免疫稳态的建立。
基于这一机制,这种饮食干预策略为改善精神障碍患者的睡眠提供了新思路。通过缓解肠道炎症状态并调节神经递质水平,它可以改善患者的精神症状和睡眠质量。
4
粪菌移植
粪菌移植(FMT)是一种以重建微生物群落为核心的生物治疗策略,通过将健康供体的粪便移植到患者的胃肠道,直接重组受体的肠道微生物群,促进微生物生态系统的平衡,从而实现临床治疗目标。
粪菌移植有助于调节情绪、行为和睡眠质量
作为一种突破性干预方法,粪菌移植(FMT)在动物模型和初步临床研究中展现出独特优势。研究发现,通过移植精神分裂症(SCZ)患者的肠道微生物群,被移植小鼠出现了类似SCZ的行为,包括多动、焦虑增加、社交互动受损和记忆缺陷。
注:这些小鼠还显示出周围和中枢神经系统中色氨酸代谢犬尿氨酸-犬尿酸通路的显著激活,前额叶皮层基底细胞的多巴胺能神经递质释放增强,以及海马体5-HT水平升高,同时谷氨酸能神经递质浓度下降,谷氨酰胺和GABA水平上调。
FMT在人体临床研究中展现出重要价值。比较接受健康供体FMT前后的粪便样本显示,α多样性显著增加,柯林斯氏菌属(Collinsella)和双歧杆菌的丰度也有所上升。FMT治疗还显著降低了患者的血液皮质醇水平,同时改善了睡眠和情绪相关评估指标。
作为潜在治疗干预,FMT通过调节肠道微生物群的组成和功能,促进神经递质及其前体物质的合成,从而发挥治疗作用。这些研究表明,FMT能够有效调节情绪和行为,促进多种精神疾病患者的症状缓解。
!
注意事项
尽管粪菌移植(FMT)展现了广泛的治疗前景,但其临床应用面临标准化不足、疗效不一及长期安全性验证的挑战。高通量测序技术可帮助识别健康稳定的供体。口服FMT胶囊相比传统灌肠方法更方便,患者依从性更高。多样化的给药途径,如结肠镜输注、鼻肠管插管或口服胶囊,有助于平衡疗效与患者依从性。建立安全监测系统可预防和控制感染风险,加强安全监管。
此外,在进行FMT治疗时,必须密切关注精神障碍患者的知情同意能力,确保他们能够在充分了解潜在风险和益处的基础上做出自主决策,并通过伦理审查委员会的批准进行标准化申请。尽管仍需更多研究验证FMT在精神分裂症(SCZ)和睡眠障碍(SD)治疗中的长期效果,但作为个性化治疗的一部分,FMT显示出广泛的应用前景。
5
靶向代谢物药物治疗
在精准医疗领域,靶向代谢物药物治疗正成为新研究方向。尽管传统微生物群移植在临床应用中取得了一定成效,但个体肠道微生物群的差异严重限制了其治疗效果的稳定性和重复性。因此,直接补充微生物代谢物或前体物质为解决这一问题提供了新思路。
靶向代谢物能够避免个体菌群差异,更精准治疗
这种策略能够绕过微生物群移植中的个体差异,直接作用于人体代谢网络,实现更精确的调控。短链脂肪酸(SCFAs)和色氨酸代谢在生理和病理过程中起着关键作用。
以吲哚胺2,3-二氧加氧酶(IDO)抑制剂为例,IDO是色氨酸代谢中的限速酶,其过度活化可导致色氨酸耗竭和一系列神经毒性代谢物的产生,进而引发异常免疫反应和神经功能障碍。IDO抑制剂通过抑制其活性,可以有效调节免疫反应,减少神经毒性代谢物的产生,展现出治疗多种疾病的潜力。
SCFAs和色氨酸代谢物与精神分裂症(SCZ)发病机制及睡眠调节密切相关。未来研究应进一步探讨代谢物的具体作用机制,推动其临床应用的发展,为合并睡眠障碍的SCZ患者提供更安全、更有效的治疗选择。
治疗策略总结
并非所有精神分裂症(SCZ)患者都适合微生物组靶向干预。潜在候选者的识别应基于具体特征,例如明显的胃肠道症状、抗精神病药物反应不良或显著副作用、异常睡眠结构与疾病活动的强相关性,以及肠道微生物组分析结果显示与健康对照有显著偏差。
根据临床表型和微生物特征进行对应治疗选择
目标群体应根据临床表型和微生物特征的组合进行选择。在推进微生态干预时,应明确不同策略的优先级,优先考虑低风险、非侵入性的方法。例如,补充特定益生菌和益生元可作为基础干预,而饮食模式调整可作为长期管理策略。
相比之下,高风险且难以预测的治疗如粪便微生物移植(FMT)应仅考虑用于难治症状、对传统疗法反应不足及严重肠道菌群失调的患者,并在充分知情同意和严格伦理监督下使用。
此外,实施时需认真考虑个体差异和潜在风险。益生菌和益生元干预应考虑菌株特异性效应和个体耐受性,饮食干预需关注患者的依从性和营养平衡。对于FMT,严格的供体筛查至关重要,并需密切监测感染、免疫和代谢不良反应,以及长期精神病学结局,同时建立动态的疗效-安全性评估体系。
本文分析了精神分裂症(SCZ)及其相关睡眠障碍患者的典型肠道微生物群特征。研究发现,这两种状况均表现出肠道微生物群α多样性下降、短链脂肪酸产生细菌减少以及促炎微生物群比例增加。由此可以推测,SCZ患者的肠道菌群失调可能是导致睡眠质量下降的重要因素,而睡眠质量恶化又通过反馈机制加重精神症状,形成恶性循环。
肠道菌群失调、中枢神经系统功能障碍和睡眠稳态紊乱在宿主体内形成自我延续的动态循环,导致精神病理表现和生理节律紊乱的周期性恶化。这些发现为理解精神分裂症患者共病睡眠障碍的机制提供了重要的理论框架。针对肠道微生物群以打破这一恶性循环,为这类患者提供了有前景的新颖治疗视角。
现有研究表明,治疗应采取综合策略。虽然非典型抗精神病药物能改善精神病症状,但对睡眠结构的复杂影响仍需深入评估。认知行为疗法同样对失眠有效,但需根据精神病症状进行调整。因此,针对肠道微生物群的干预策略正在向多层次和精准化方向发展,具体包括补充特定益生菌和益生元,结合饮食调整,通过多途径共同改善精神症状和睡眠质量。尽管粪便微生物移植(FMT)作为高级干预措施展现出潜力,但其效果仍需通过标准化研究来验证。实施时应重点关注胃肠道症状、药物反应不足、精神症状严重程度与睡眠节律紊乱以及肠道微生物群特征显著偏离健康标准的患者。整合临床表型与微生物特征的模型将为精准应用干预策略提供基础,最终推动微生物群靶向治疗的系统化及个性化发展。
我们每个人都在不断追求身心健康的道路上前行,理解肠道微生物群在我们的心理与生理健康中所扮演的角色,不仅能增进我们对自身健康的认识,更能激励我们在日常生活中关注饮食、生活方式等易被忽视的细节。希望未来的研究能够持续启发我们,推动科学领域的进步,为那些受到精神障碍困扰的人们带来新的希望和解决方案。通过这样的努力,我们将共同迈向一个更加健康和明亮的未来。
注:本账号发表的内容仅是用于信息的分享,在采取任何预防、治疗措施之前,请先咨询临床医生。
主要参考文献:
Huang, Z., Huang, Z., Du, Z., Gao, X., Jiang, Y., Zhou, Z., & Zhu, H. (2026). Role and mechanism of gut microbiota and metabolites in schizophrenia complicated with sleep disorder. Gut Microbes, 18(1). https://doi.org/10.1080/19490976.2025.2607817.
McCutcheon RA, Reis Marques T, Howes OD. Schizophrenia-An Overview. JAMA Psychiatry. 2020 Feb 1;77(2):201-210.
Meyer N, Faulkner SM, McCutcheon RA, Pillinger T, Dijk DJ, MacCabe JH. Sleep and Circadian Rhythm Disturbance in Remitted Schizophrenia and Bipolar Disorder: A Systematic Review and Meta-analysis. Schizophr Bull. 2020 Sep 21;46(5):1126-1143.
Reeve S, Sheaves B, Freeman D. Sleep Disorders in Early Psychosis: Incidence, Severity, and Association With Clinical Symptoms. Schizophr Bull. 2019 Mar 7;45(2):287-295.
McGuinness AJ, Davis JA, Dawson SL, Loughman A, Collier F, O’Hely M, Simpson CA, Green J, Marx W, Hair C, Guest G, Mohebbi M, Berk M, Stupart D, Watters D, Jacka FN. A systematic review of gut microbiota composition in observational studies of major depressive disorder, bipolar disorder and schizophrenia. Mol Psychiatry. 2022 Apr;27(4):1920-1935.
Mayeli A, LaGoy AD, Smagula SF, Wilson JD, Zarbo C, Rocchetti M, Starace F, Zamparini M, Casiraghi L, Calza S, Rota M, D’Agostino A, de Girolamo G; DiAPAson Consortium; Ferrarelli F. Shared and distinct abnormalities in sleep-wake patterns and their relationship with the negative symptoms of Schizophrenia Spectrum Disorder patients. Mol Psychiatry. 2023 May;28(5):2049-2057.
Penninx BWJH, Lange SMM. Metabolic syndrome in psychiatric patients: overview, mechanisms, and implications. Dialogues Clin Neurosci. 2018 Mar;20(1):63-73.
Zhu C, Zheng M, Ali U, Xia Q, Wang Z, Chenlong, Yao L, Chen Y, Yan J, Wang K, Chen J, Zhang X. Association Between Abundance of Haemophilus in the Gut Microbiota and Negative Symptoms of Schizophrenia. Front Psychiatry. 2021 Jul 30;12:685910