-

 CNAS L23010
CNAS L23010

 国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业
国家高新企业 | ISO9001认证 | 肠道健康精准检测高新技术研发中心 | 专精特新企业 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康
厌氧棒状菌属(Anaerostipes)隶属于厚壁菌门下的毛螺菌科,是一类革兰氏阳性厌氧产丁酸菌,在维持宿主肠道稳态与代谢平衡中具有关键作用。
该菌属的显著特征是能够产生丁酸,并且其中的A.caccae与A.hadrus还能利用体内的乳酸与乙酸,将其转化为丁酸。一些菌株还拥有维生素B₁₂和E生物合成通路基因,或是将肌醇转化为丙酸与乙酸的代谢途径。
Anaerostipes与其他肠道内重要菌属还存在密切的相互作用。例如A.caccae可发酵由粘蛋白降解菌A.muciniphila生成的葡萄糖、甘露糖、半乳糖等粘蛋白衍生糖,产生丁酸盐、乙酸盐和乳酸盐。此外,A.hadrus通过分解低聚果糖生成的水解产物能够有效促进包括 Lactobacillus 在内的多种益生菌生长和繁殖,表现出其特有的“互利共代谢”特征。
厌氧棒状菌属中的A.hadrus被发现可代谢抗癌药5‑氟尿嘧啶(5‑FU),参与其降解或转化,这一代谢活动可能改变5‑FU在肠道中的稳定性与吸收效率,从而进一步影响其在体内的生物利用度及临床治疗效果。
Anaerostipes具有作为肠道健康和疾病生物标志物的重要潜力,其在儿童克罗恩病、胆汁淤积、结直肠癌、重度抑郁症、强迫症、食物过敏患者中丰度普遍下降,且与疾病进展、炎症及免疫调控密切相关。
深入研究Anaerostipes的生态特征及其在疾病中变化,不仅有助于揭示肠道菌群与宿主互作机制,还为微生态干预与疾病防治提供潜在的新靶点。
1
分类地位与主要菌种
厌氧棒状菌属(Anaerostipes)隶属于厚壁菌门(Firmicutes)、Clostridiales(梭菌目)下的毛螺菌科(Lachnospiraceae)。
毛螺菌科是人体肠道中重要的核心菌群,在碳水化合物代谢、短链脂肪酸(SCFAs)生成及宿主健康调控中发挥关键作用。
模式种为 :Anaerostipes caccae,其丰度受饮食膳食纤维与碳水组成显著影响;
–A. hadrus为主要优势种,呈泛基因组开放性,适应性强;
–A. rhamnosivorans:新从婴儿粪便中分离出来;
–A. butyraticus在禽类肠道中较为丰富。
DNA G+C 含量(mol%):45.5–46
Anaerostipes属的系统发育树
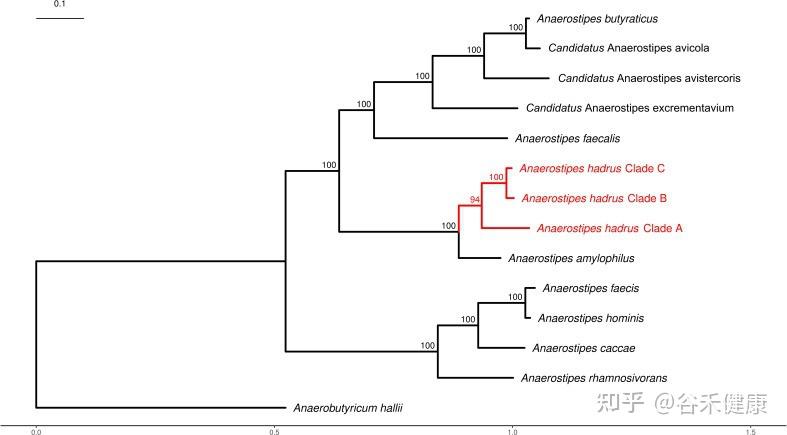
2
细胞及形态特征
细胞形态
–革兰氏阳性,杆状或略弯曲杆形,无运动性。
-多数为严格厌氧菌,部分可形成芽孢。
-尾端圆钝,长度约2–5μm。
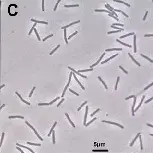
芽孢形成能力
-厌氧棒状菌属(Anaerostipes)中的A. caccae、A. hominis、A. rhamnosivorans能形成芽孢,观察到内生孢子结构。
-虽然A. hadrus、A. butyraticus、A. amylophilus 在实验所用条件下未形成可见孢子,但其基因组保留主要的孢子形成核心基因(spo0A 等)。
-芽孢具有较强的耐氧和耐热能力,部分菌株可在常温下存活数。
3
生长条件
-厌氧棒状菌属(Anaerostipes)为严格厌氧菌,最适生长温度约37°C,适宜pH为6.8–7.2。
– 代谢途径显示该属具极高适应能力,属于肠道生态系统中的“代谢枢纽”。
4
重要的代谢能力
关键丁酸生成菌
-厌氧棒状菌属(Anaerostipes)的一个显著特征是其能够产生丁酸(butyrate),这是一种短链脂肪酸(SCFA),对肠道健康至关重要。丁酸不仅为结肠细胞提供能量,还能促进肠道免疫稳态,并刺激有益菌群的生长。
-同时可生成少量乙酸(acetate)和丙酸(propionate)。
–A.caccae可利用乳酸与乙酸共生成丁酸,是肠道“乳酸清除者”。
–A.hadrus具有细胞外GH32类水解酶,可降解果寡糖(FOS)及菊粉,这种能力使其能与非 FOS 利用菌共代谢。
–A.rhamnosivorans和A.caccae具有独特的肌醇(inositol)转化途径,可将膳食肌醇厌氧代谢为丙酸和乙酸,其代谢活性与宿主血糖、胰岛素水平呈负相关。
–非溶血性,过氧化氢酶和氧化酶均为阴性。
维生素与胆汁酸代谢能力
-厌氧棒状菌属拥有胆汁盐水解酶(bsh)基因,能够去结合胆汁酸,影响宿主胆汁酸稳态。
-厌氧棒状菌属还具有维生素B₁₂和E生物合成通路基因。
5
生态学分布
-广泛存在于全球人群粪便样本中,也出现在部分哺乳动物及禽类(A.butyraticus在鸡盲肠中富集)。
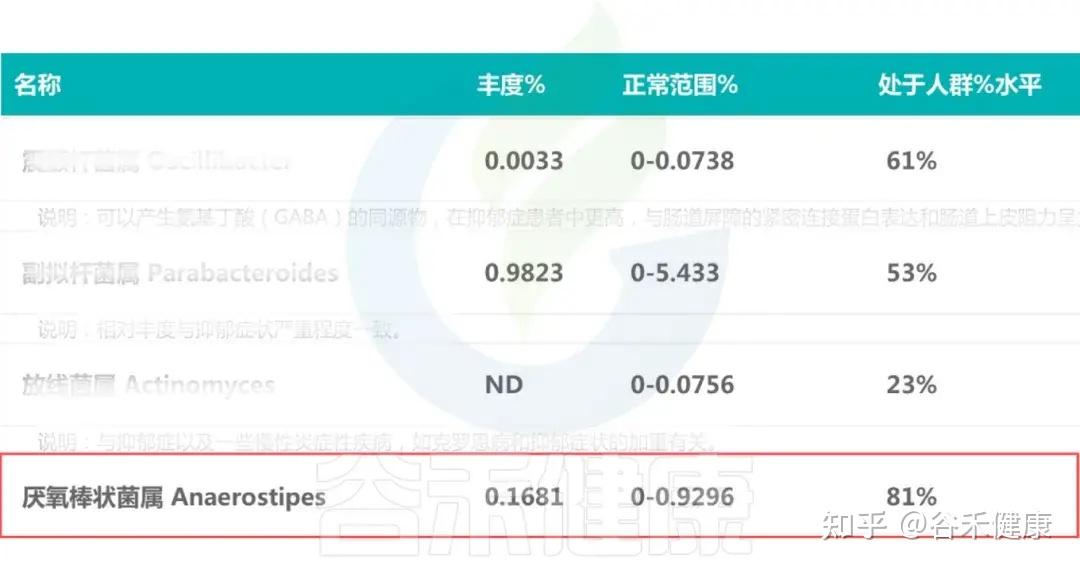
-A.hadrus为人群中优势种,具有开放泛基因组特征,表明其具较高的生态可塑性。
-A.caccae丰度与饮食成分(膳食纤维、寡糖)密切相关。
6
与其他细菌和宿主的互作
厌氧棒状菌属(Anaerostipes)通过代谢共生在肠道生态系统中发挥“碳转接”和“代谢桥梁”的重要作用。
利用乳酸菌产生的乳酸生成丁酸盐
A. caccae已被证明可利用双歧杆菌和乳杆菌等共生菌产生的乳酸盐和乙酸盐发酵产物生成丁酸盐,并能分别转化双歧杆菌的l-乳酸和乳酸杆菌的d-乳酸,从而在减少乳酸积累和维持肠道菌群平衡中发挥重要作用。
利用AKK菌的粘蛋白衍生产物
另一项实验研究发现,A.caccae 可发酵由粘蛋白降解菌 A.muciniphila 生成的葡萄糖、甘露糖、半乳糖和 N-乙酰半乳糖胺等粘蛋白衍生糖,产生丁酸盐、乙酸盐和乳酸盐。A.caccae 和 A.muciniphila 之间的肠粘液层似乎存在共生交叉摄养。
此外,A.hadrus通过分解低聚果糖(FOS)生成的水解产物能够有效促进包括 Lactobacillus 在内的多种益生菌生长和繁殖,表现出其特有的“互利共代谢”特征。
Anaerostipes还与其他细菌存在相互作用,如下所示:
增强
Bacteroidales
Bacteroides
Odoribacter
Peptococcaceae
抑制
Coriobacteriales
Adlercreutzia
Collinsella
Porphyromonas
Prevotella
Clostridium
Clostridiales incertae sedis
Clostridiales Family XIII. Incertae Sedis
Blautia
Coprococcus
Dorea
Lachnospiraceae
Ruminococcaceae
Ruminococcus
Dialister
Campylobacteraceae
Erysipelotrichaceae
此外,Anaerostipes的丁酸盐与丙酸盐产物不仅为结肠上皮提供能量来源,还可:
–促进调节性 T 细胞(Treg)分化;
–抑制 NF‑κB 介导的炎症通路,
–加强肠屏障紧密连接蛋白表达。
7
耐药性
对大多数抗生素都敏感
目前关于 Anaerostipes 的耐药性研究较少,但由于其严格的厌氧特性和对特定环境的依赖,它通常不会对抗生素产生广泛的耐药性。
A. hominis 和一些 A. hadrus 菌株仅表现出编码 β-内酰胺类和多粘菌素抗性的基因,而这些基因在所有 A.caccae 基因组中都不存在。在3个物种中零星观察到与其他抗生素(如四环素、氨基糖苷类和杆菌肽)耐药性相关的基因。
整体而言,A.caccae 与 A.hadrus 均未携带主要的抗生素耐药、毒性或耐胆酸基因。其耐受性主要源于对氧化应激和低pH的内源性适应,与抗生素无关。
厌氧棒状菌属(Anaerostipes)是典型的产丁酸厌氧菌,在人类肠道生态系统中扮演了“代谢枢纽”的角色。它通过能量代谢、基质转化、宿主营养协同、免疫调节和药物代谢等多层机制,对维持肠道与全身健康具有重要意义。
产丁酸、乙酸与丙酸——肠屏障修复、抗炎与能量供应核心驱动力
厌氧棒状菌属(Anaerostipes)的代表菌如A.caccae、A. hadrus、利用乳酸、乙酸及多糖降解产物,通过乙酰辅酶A途径生成丁酸和丙酸。
√ 主要生理作用
–肠上皮能量供给:丁酸是结肠上皮细胞主要能量来源(可达 70% )。
–肠道屏障修复与增强:丁酸刺激紧密连接蛋白(ZO‑1、occludin、claudin)的表达,修复屏障结构,减少肠漏。
-抗炎与免疫调节:丁酸通过抑制 NF‑κB 信号,促进调节性 T 细胞(Treg)分化,减少促炎细胞因子(IL‑6、TNF‑α)释放。
-能量代谢优化:丙酸参与肝糖异生、乙酸供其他益菌利用,共同维持肠内碳流平衡。
这一发酵体系在维持低炎症水平、促进黏膜修复与调节全身能量代谢方面具有核心作用。
分解乳酸、肌醇等底物——维持菌群生态平衡
A. caccae与A. hadrus能使用由双歧杆菌和乳酸杆菌等生成的乳酸与乙酸共代谢,转化为丁酸。这可以避免乳酸过度积累,防止肠腔过酸化,维持pH稳定。

利用低聚果糖和肌醇:A.hadrus可水解低聚果糖,产物反过来促进乳酸菌增殖;并具备将肌醇转化为丙酸与乙酸的代谢途径,有助于调节宿主能量与脂质代谢。
对微生态的意义:通过分解中间代谢物和益生元,Anaerostipes属增强了肠道代谢网络的互补性,是稳定微生态平衡的关键成员。
维生素B12合成——宿主营养代谢支持因子
除了短链脂肪酸的产生外,某些厌氧棒状菌属还可能有助于其他重要的次级代谢物,例如维生素B12。
√ 作用意义
-肠道维生素B12供应源:为需B12菌群如甲烷菌、部分脱硫弧菌提供前体;
–宿主营养参与:B12参与脂肪酸与氨基酸代谢,与能量稳态及神经系统功能密切相关;
–互利生态效应:在共生系统中,Anaerostipes的B12产能增强了菌群代谢互补性。
药物代谢——调节宿主药物应答
√ 可代谢影响抗癌药5‑氟尿嘧啶
A.hadrus被发现可代谢抗癌药5‑氟尿嘧啶(5‑FU),参与其降解或转化,可能影响药物的生物利用度与疗效。

其机制可能涉及脱氨酶或还原酶通路对5‑FU的结构修饰,从而调节肠腔中药物浓度和毒副作用。这表明Anaerostipes在肠道药物代谢群中具有潜在作用,为利用菌株优化药效、降低毒性、实现个体化药物治疗提供新方向。
产生丁酸盐的A.hadrus可能会干扰氟嘧啶药物的疗效或减少结直肠癌患者的不良反应,这可能取决于人类宿主二氢嘧啶脱氢酶(DPD)的水平。
在人体肠道微生态中,厌氧棒状菌属(Anaerostipes)是重要的丁酸生成菌之一,其丰度常被视为肠道健康与代谢稳态的重要指标。
近年来的多项研究发现,不同疾病状态——包括克罗恩病、胆汁淤积、结直肠癌、强迫症、抑郁症、食物过敏等——均伴随着 Anaerostipes 丰度的显著变化。这些波动不仅反映了宿主代谢和免疫环境的改变,也提示该菌属可能在多种疾病的发生与缓解过程中发挥关键调节作用。
1
儿童克罗恩病中Anaerostipes下降

研究显示,克罗恩病患者(尤其是活动期或有高应激水平者)粪便中Anaerostipes的丰度显著下降,与健康儿童对照相比差异明显。
同时,患者中促炎或条件致病菌(如Escherichia-Shigella、Enterococcus、Ruminococcus gnavus等)增加。
2
胆汁淤积患者中Anaerostipes减少

临床与动物模型研究显示,无论是肝胆疾病(如原发性胆汁性胆管炎、药物性胆汁淤积)还是肝外胆汁阻滞,Anaerostipes的相对丰度均呈下降趋势。
这可能是由于Anaerostipes拥有胆汁盐水解酶(bsh)基因,能够去结合胆汁酸,影响宿主胆汁酸稳态。
因此,Anerostipes丰度下降不仅是胆汁淤积相关肠道菌群失衡的标志之一:一方面反映宿主胆汁酸代谢环境的毒性压力;另一方面通过丁酸减少和屏障损伤途径,放大肝‑肠轴炎症与代谢紊乱。
3
Anaerostipes在结直肠癌中减少
√ Anaerostipes随着结直肠癌的发展逐渐减少

有研究显示,从健康个体 → 结直肠腺瘤(CRA) → 结直肠癌(CRC),Anaerostipes的丰度逐渐并显著下降。
在早期腺瘤阶段,该菌种相对丰度已明显低于健康对照;在癌症阶段,其丰度降至最低水平,几乎完全缺失于部分患者样本中。
Anerostipes是主要的丁酸盐生成菌之一。其减少会导致丁酸水平下降,损害上皮细胞线粒体功能,使能量代谢从稳态转向糖酵解。同时,丁酸缺乏削弱了免疫调控和细胞凋亡诱导,使异常增殖细胞逃避免疫清除。
丁酸还能通过抑制组蛋白去乙酰化酶(HDAC)调节基因表达,当产丁酸菌减少时,HDAC 活性增强,促进癌变相关基因(如 c‑Myc、Cyclin‑D1)上调。
综上所述,Anaerostipes既是结直肠肿瘤发生的重要微生态标志,也是肠道微生物干预与癌症预防的潜在靶点。
4
强迫症患者中Anaerostipes减少

有研究收集了21名非抑郁、无药物的强迫症患者和22名年龄和性别匹配的非精神病对照者的晨间粪便和血液样本。
√ 强迫症患者中Anaerostipes等丁酸盐生产菌减少
与对照组相比,强迫症组的物种丰富度/均匀度较低(α多样性,逆辛普森)和三个丁酸盐生产属(Oscillospira、Odoribacter和Anaerostipes)的相对丰度较低。同时,患者的平均CRP水平升高(而IL‑6和TNF‑α无显著变化),且CRP与精神症状呈中至强相关。
5
肾移植受者中Anaerostipes减少

多项肾移植后微生物组研究显示,Anaerostipes丰度在移植早期明显下降,并持续低于健康对照组。
√ 肾移植受者中Anaerostipes减少,并可能导致腹泻
在肾移植受者(KTRs)中,Anaerostipes丰度显著下降,尤其在伴有肠道菌群失调及抗生素或免疫抑制剂相关腹泻的患者中更为明显。
Anaerostipes丰度下降,导致丁酸缺乏削弱上皮细胞能量供应,降低紧密连接蛋白(ZO‑1、occludin)表达,使黏膜屏障完整性受损,从而诱发腹泻。
Anaerostipes缺失与丁酸水平下降呈正相关,提示代谢失衡可能是腹泻的重要机制。
6
重度抑郁症患者中Anaerostipes减少

一项研究探讨了肠道微生物群与重度抑郁症(MDD)的关系,共招募46名活动性MDD患者(a-MDD)及45名健康对照(HC)。
√ Anaerostipes在重度抑郁症患者中丰度较低
研究发现,与健康对照相比,重度抑郁症(MDD)患者中存在相对丰度改变的细菌属:Bilophila(2 倍)和Alistipes(1.5 倍)更高,而Anaerostipes和Dialister在 MDD 患者中较低。
在重度抑郁障碍患者中,Anaerostipes显著减少,伴随丁酸合成能力下降和免疫炎症失衡。这种改变可能通过破坏肠‑脑屏障、增强神经炎症及损害神经营养调控,参与抑郁症的发生与维持。
7
食品过敏婴儿中Anaerostipes减少

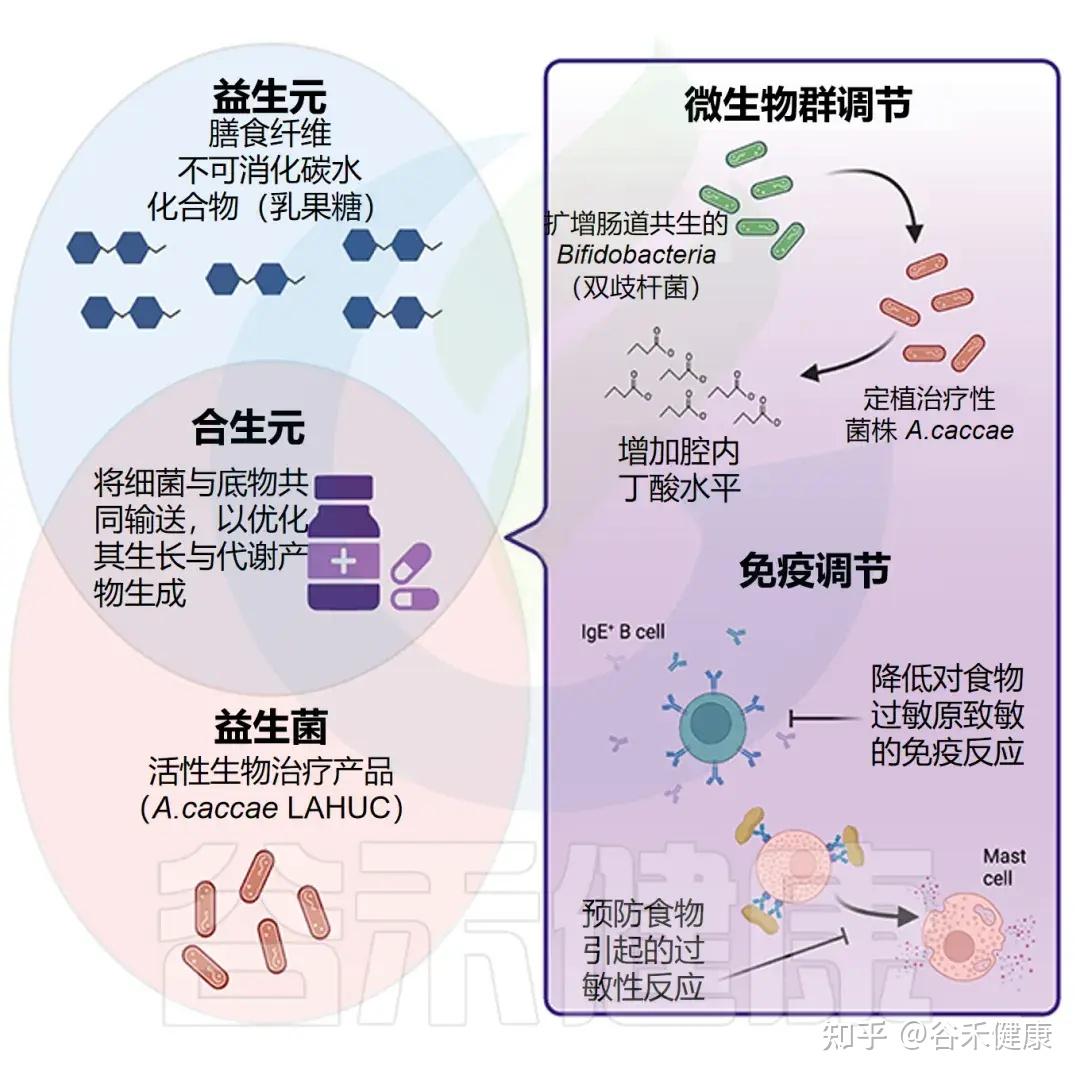
在食物过敏婴儿,尤其是牛奶过敏患者中,研究显示 Anaerostipes(特别是 Anaerostipes caccae)丰度显著下降。相反,在健康婴儿中,这一菌种丰富且与免疫耐受密切相关。
√ Anaerostipes减少可能作为食物过敏发生潜在指标
我们大胆推测Anerostipes的减少可作为婴幼儿食物过敏风险和肠道失衡的潜在标志;恢复A.caccae或其丁酸代谢活性(如补充丁酸菌、乳酸底物或膳食纤维)有望通过微生态干预促进免疫耐受并减轻过敏反应。
8
Anaerostipes在其他疾病中的丰度变化
√ 阿尔茨海默病患者中减少
研究结果显示,与健康对照相比,阿尔茨海默病患者(尤其是APOE‑ε4携带者)肠道中Anaerostipes的相对丰度显著下降。
注:APOE-ε4是载脂蛋白E(APOE)基因的一个等位基因,与阿尔茨海默病(老年痴呆症)风险显著相关。
√ 焦虑、创伤后应激人群中减少
具有焦虑、抑郁或创伤后应激特征(PTSD样表现)的人群中,Anaerostipes丰度显著下降。而在心理状态健康的对照组中,Anaerostipes 丰度明显较高,且与积极情绪和心理韧性评分呈正相关。
√ 儿童局灶性癫痫患者中减少
研究发现,儿童局灶性癫痫患者发病时肠道中Anaerostipes的丰度显著下降,与健康对照组相比明显减少。
在接受抗癫痫治疗后(尤其是病情稳定、发作频率下降者),Anaerostipes丰度明显回升,丁酸代谢通路相关活性亦随之增强。
这提示Anaerostipes的丰度与癫痫活动状态呈负相关,可能反映肠‑脑功能恢复与神经代谢平衡的改善。
√ 慢性疲劳综合征中减少
研究发现,慢性疲劳综合征(CFS)患者肠道中Anaerostipes相对丰度显著下降,与健康对照相比变化明显。
该菌的降低与患者的疲劳严重程度和认知功能障碍评分呈负相关,即Anaerostipes越少,临床症状越重。
与此同时,CFS患者中促炎或条件致病菌(如Enterobacteriaceae、Alistipes的某些菌株)相对增加,提示肠道生态由抗炎平衡型转向炎症型。
编者的话
厌氧棒状菌属(Anaerostipes)在多种疾病(尤其是慢性炎症、代谢疾病、心理疾病及肿瘤相关疾病)中丰度普遍下降,且与疾病进展、炎症及免疫调控密切相关。
其作为肠道健康和疾病生物标志物具有重要潜力,未来可通过饮食或微生态干预提升其丰度以改善健康。
多种方法可有效调节厌氧棒状菌属(Anaerostipes)丰度,主要包括膳食纤维、益生元、益生菌和生活方式干预。
1
膳食纤维补充
多项研究表明,高纤维饮食——包括菊粉、抗性淀粉及阿拉伯木聚糖等——能够显著提高厌氧棒状菌属(Anaerostipes)的丰度,并增强肠道丁酸盐的生成能力。
这些膳食纤维可作为产丁酸菌的发酵底物,为它们的生长提供能量来源,从而改善肠道微生态结构。该方法在健康成人及动物模型中均显示出良好的效果。
2
益生元与合生元干预
特定类型的益生元(如菊粉型果寡糖)以及合生元组合(如 Lactobacillus fermentum K73 联合高油酸棕榈油与乳清)对Anaerostipes的增殖具有促进作用。这些干预方式通过改变肠道内短链脂肪酸代谢路径与底物利用率,进而提升丁酸生成效率。该策略适用于儿童及成人人群。
3
益生菌联合干预
部分益生菌(如 Bifidobacterium animalis、Lactobacillus rhamnosus)在配合膳食纤维应用后,能间接提升 Anaerostipes的丰度。这种组合干预有助于改善肠道代谢环境和菌群多样性,常用于功能性便秘患者及儿童群体中。
4
饮食结构调整
研究指出,增加全谷物、蔬菜(大蒜、洋葱等)与水果的摄入,减少精制碳水化合物比例,可有效改善肠道微生态组成,并促进 Anaerostipes 的生长。这一健康饮食结构可长期维持肠道菌群稳定,对中国成年人及一般健康人群均有益。
5
运动干预
规律的有氧运动与抗阻训练被证实能够显著提升老年人肠道中 Anaerostipes 的丰度,同时增加粪便中丁酸盐的浓度。这一发现表明,运动干预不仅对维护机体代谢健康具有积极作用,还能通过改善肠道菌群结构,促进产丁酸菌的增长,从而增强能量代谢效率和抗炎能力。
此外,该研究结果进一步说明,长期坚持科学的运动方式能够在多层面维持肠道生态平衡,降低慢性炎症水平,对老年人整体健康状况的改善与代谢功能的恢复具有重要意义,体现了运动与肠道微生态之间的密切关联。
6
减少高盐饮食
研究发现,高盐饮食可显著降低Anaerostipes 丰度,从而削弱丁酸生成与肠道免疫平衡。降低盐摄入对维持肠道微生态多样性与代谢稳态具有重要意义,动物模型结果为该机制提供了有力证据。
主要参考文献
Bhattacharjee D, Millman LC, Seesengood ML, Seekatz AM. Diversity and prevalence of Anaerostipes in the human gut microbiota. bioRxiv [Preprint]. 2025 May 1:2025.05.01.651700.
Liu D, Xie L-S, Lian S, Li K, Yang Y, Wang W-Z, Hu S, Liu S-J, Liu C, He Z. Anaerostipes hadrus, a butyrate-producing bacterium capable of metabolizing 5-fluorouracil. mSphere. 2024 Apr 23;9(4):e0081623.
Hesser LA, Puente AA, Arnold J, Ionescu E, Mirmira A, Talasani N, Lopez J, Maccio-Maretto L, Mimee M, Nagler CR. A synbiotic of Anaerostipes caccae and lactulose prevents and treats food allergy in mice. Cell Host Microbe. 2024 Jul 10;32(7):1163-1176.e6.
Bui TPN, Mannerås-Holm L, Puschmann R, Wu H, Troise AD, Nijsse B, Boeren S, Bäckhed F, Fiedler D, deVos WM. Conversion of dietary inositol into propionate and acetate by commensal Anaerostipes associates with host health. Nat Commun. 2021 Aug 10;12(1):4798.
Caso JR, MacDowell KS, González-Pinto A, García S, de Diego-Adeliño J, Carceller-Sindreu M, Sarramea F, Caballero-Villarraso J, Gracia-García P, De la Cámara C, Agüera L, Gómez-Lus ML, Alba C, Rodríguez JM, Leza JC. Gut microbiota, innate immune pathways, and inflammatory control mechanisms in patients with major depressive disorder. Transl Psychiatry. 2021 Dec 21;11(1):645.
Endo A, Tanno H, Kadowaki R, Fujii T, Tochio T. Extracellular fructooligosaccharide degradation in Anaerostipes hadrus for co-metabolism with non-fructooligosaccharide utilizers. Biochem Biophys Res Commun. 2022 Jul 12;613:81-86.
Guo C, Li Y, Wang P, Li Y, Qiu C, Li M, Wang D, Zhao R, Li D, Wang Y, Li S, Dai W, Zhang L. Alterations of Gut Microbiota in Cholestatic Infants and Their Correlation With Hepatic Function. Front Microbiol. 2018 Nov 13;9:2682.
Turna J, Grosman Kaplan K, Anglin R, Patterson B, Soreni N, Bercik P, Surette MG, Van Ameringen M. The gut microbiome and inflammation in obsessive-compulsive disorder patients compared to age- and sex-matched controls: a pilot study. Acta Psychiatr Scand. 2020 Oct;142(4):337-347.
Singh V, Lee G, Son H, Koh H, Kim ES, Unno T, Shin JH. Butyrate producers, “The Sentinel of Gut”: Their intestinal significance with and beyond butyrate, and prospective use as microbial therapeutics. Front Microbiol. 2023 Jan 12;13:1103836.
Low A, Sheludchenko M, Cheng HE, Koh XQ, Lee JWJ. Complete genome sequences of butyrate producing Anaerostipes hadrus strains BA1 and GIF7 isolated from the terminal ileum of a healthy lean male. Microbiol Resour Announc. 2023 Oct 19;12(10):e0070123.
Modica V, Glávits R, Clewell A, Endres JR, Hirka G, Vértesi A, Béres E, Szakonyiné IP. A Comprehensive Toxicological Safety Evaluation of Anaerostipes caccae. Int J Toxicol. 2025 Nov-Dec;44(6):471-487.
Morinaga K, Kusada H, Watanabe M, Tamaki H. Complete Genome Sequence of Anaerostipes caccae Strain L1-92T, a Butyrate-Producing Bacterium Isolated from Human Feces. Microbiol Resour Announc. 2021 Apr 22;10(16):e00056-21.

谷禾健康
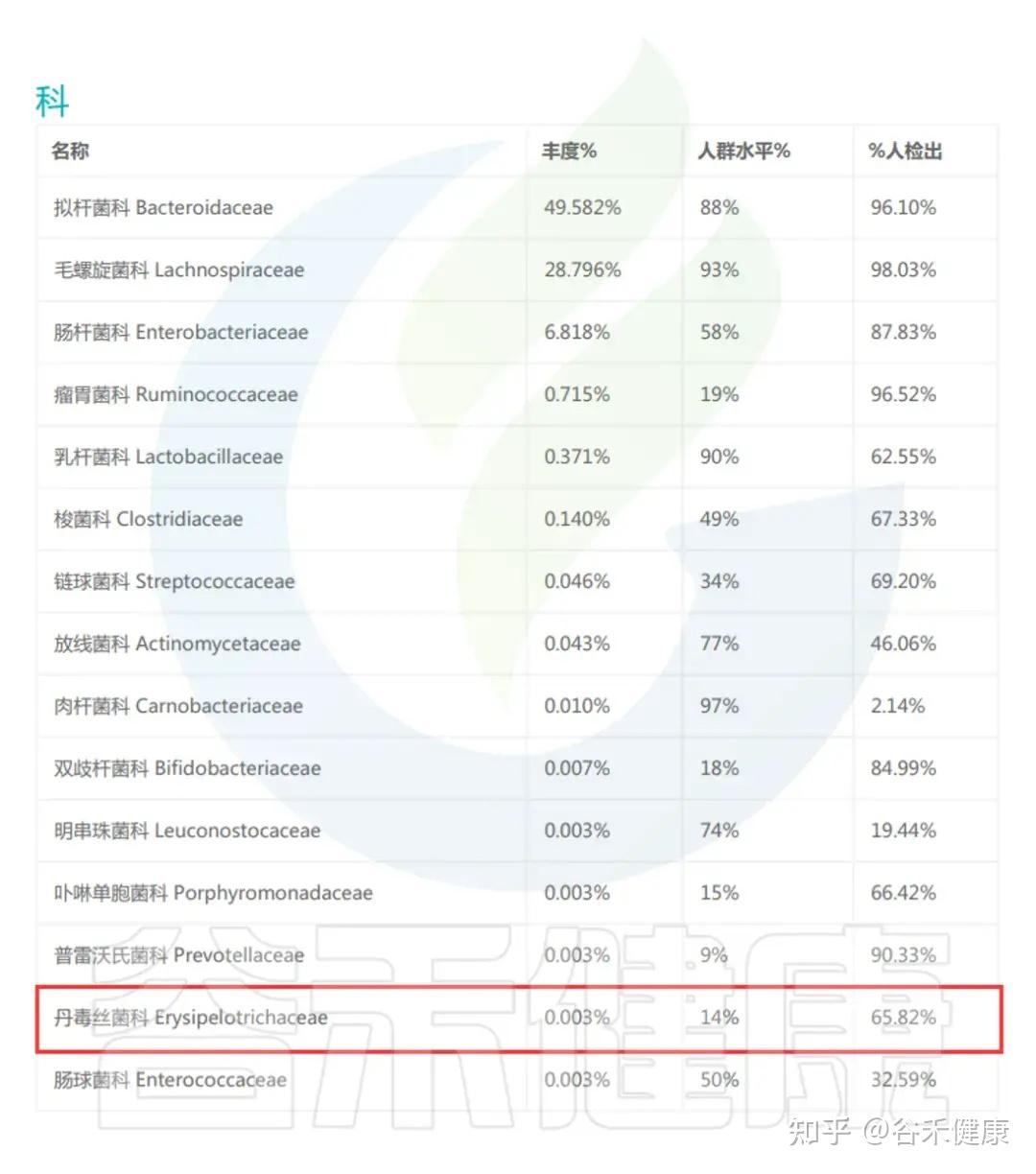
丹毒丝菌科(Erysipelotrichaceae)是厚壁菌门(Firmicutes)中的一类重要细菌,广泛存在于人体肠道中,因其在健康与疾病调控中的重要作用而备受关注。
丹毒丝菌科参与食物分解与能量代谢,并在脂质代谢、胆汁酸循环和免疫调控中发挥关键作用,对维持机体代谢稳态至关重要。
并且该家族的细菌具有较高的免疫原性,丹毒丝菌科的某些成员相比其他肠道菌群更易被IgA包被。研究表明,其相对丰度与肿瘤坏死因子α(TNF)水平呈正相关,并与多种免疫相关疾病密切相关。在炎症性肠病及其他免疫介导疾病(如多发性硬化、特应性皮炎和食物过敏)中,丹毒丝菌科的异常增减可能影响宿主免疫稳态,从而调节炎症反应。
丹毒丝菌科的一个显著特点是功能异质性与环境敏感性。在健康状态下,丹毒丝菌科可以促进短链脂肪酸生成、维持上皮屏障功能及调节免疫应答,有助于肠道稳态。然而,在高脂饮食、代谢紊乱或免疫异常等条件下,其丰度和代谢模式往往出现明显波动,可能促发低度炎症或代谢失衡。大量研究显示,丹毒丝菌科的丰度变化与肥胖、糖代谢异常、炎症性肠病、自闭症谱系障碍及神经退行性疾病等多种疾病密切相关。
深入探索丹毒丝菌科在宿主代谢中的作用机制,不仅有助于揭示肥胖与代谢疾病的微生态基础,也为通过微生物干预改善人体健康提供了潜在的新策略。
注:在生物分类学中,“科”(Family)是界、门、纲、目、科、属、种层级中的一级,科并不属于精细的分类层面,但是在人类健康、科学研究和生态系统中有些是公认且非常重要的细菌科,例如肠杆菌科(Enterobacteriaceae):这是医学上最重要的科之一,包含了非常常见的大肠杆菌(Escherichia coli)和沙门氏菌(Salmonella)。
葡萄球菌科(Staphylococcaceae):主要包括葡萄球菌属 (Staphylococcus),特别是金黄色葡萄球菌(Staphylococcus aureus),普遍存在于皮肤和黏膜上的机会性病原体等。
而丹毒丝菌科成员在脂质代谢、胆汁酸转化和炎症调节等方面具有相似生态功能,其丰度在疾病状态下往往整体升降,呈现更一致的变化趋势。
丹毒丝菌科(Erysipelotrichaceae)是一种革兰氏阳性菌,广泛分布于人体、哺乳动物、鸟类、鱼类和昆虫肠道中的细菌家族,属于厚壁菌门(Firmicutes),Erysipelotrichia纲、Erysipelotrichales目。在肠道微生态、宿主代谢和炎症反应中具有重要作用。
1
形态特征与分类
丹毒丝菌科成员多为革兰氏阳性、直的或稍微弯曲的细长杆状或丝状细胞,既有严格厌氧菌,也有兼性厌氧菌和微需氧菌。不运动,不产生内生孢子。
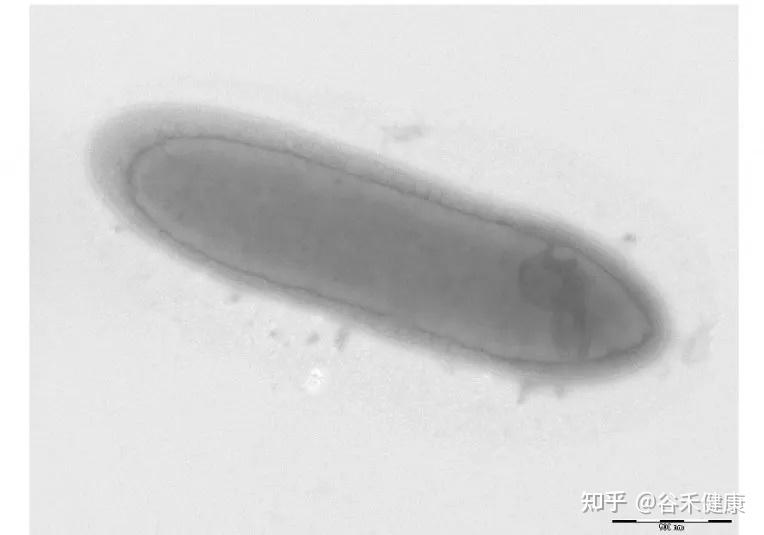
该家族的 G+C 含量较低(约36-40mol%),细胞壁结构独特。目前已鉴定出二十多个属,包括 Erysipelothrix、Allobaculum、Bulleidia、Faecalibaculum、Holdemania、Catenibacterium、Dubosiella等。
其模式菌属为丹毒丝菌属(Erysipelothrix)。
2
生态分布与功能
生长条件:温度范围5–42°C,最适30–37°C;不耐热(60°C 15分钟即可灭活)。
pH范围6.7–9.2,最适7.2–7.6。
丹毒丝菌科(Erysipelotrichaceae)广泛存在于人类和动物肠道,是常见的共生菌群之一。它们与宿主的脂质代谢密切相关,研究显示高脂饮食、肥胖、代谢紊乱等状态下该家族丰度常常升高。此外,丹毒丝菌科也与炎症性肠病、免疫反应、某些代谢疾病(如高胆固醇血症)相关。
3
代谢特性
该家族的细菌具备较强的代谢多样性,能够发酵多种类型的碳水化合物,在这一过程中产生多种短链脂肪酸,例如乙酸、丙酸和丁酸等。部分菌株还具有利用植物多糖以及 N-乙酰半乳糖胺(GalNAc)的能力,这种代谢特性使它们在复杂碳源环境中能够持续生长和维持能量供应。
与此同时,这类细菌在宿主的蛋白质分解、脂肪代谢以及能量吸收过程中也发挥着一定的辅助作用,有助于食物成分的进一步消化与转化,从而在营养物质的利用中占据重要地位。
4
抗生素敏感性
目前关于整体的耐药性特征仍缺乏系统研究,因此其抗药机制和范围尚未完全明确。
然而,根据现有资料可知,该科下属的丹毒丝菌属(Erysipelothrix)在抗生素敏感性方面具有一定的特征表现。研究显示,这一属的细菌通常对磺胺类药物、多黏菌素、庆大霉素以及卡那霉素等抗生素具有明显的耐药性,表现出对这些药物的较强抵抗能力;而在另一方面,它们对青霉素、氯霉素和四环素等抗菌药物则较为敏感。
5
与其他细菌的相互作用
丹毒丝菌科与其他细菌之间存在一定程度的相互作用,能够与多种不同类型的细菌发生协同或竞争关系,包括:
增强:
Bacteroidales
Bacteroides
Odoribacter
Peptococcaceae
抑制:
Bifidobacterium
Coriobacteriales
Adlercreutzia
Collinsella
Porphyromonas
Prevotella
Clostridium
Clostridiales incertae sedis
Clostridiales Family XIII. Incertae Sedis
Blautia
Coprococcus
Dorea
Lachnospiraceae
Ruminococcaceae
Ruminococcus
Dialister
Campylobacteraceae
被抑制:
Bifidobacterium
Coriobacteriales
Adlercreutzia
Collinsella
Bacteroidales
Bacteroides
Porphyromonadaceae
Odoribacter
Parabacteroides
Porphyromonas
Prevotella
Rikenellaceae
Alistipes
Turicibacter
Streptococcus
Clostridiales
Catabacteriaceae
Clostridium
Clostridiales incertae sedis
Peptoniphilus
Clostridiales Family XIII. Incertae Sedis
Blautia
Lachnospiraceae
Coprococcus
Dorea
Eubacterium
Lachnobacterium
Lachnospira
Roseburia
Peptococcaceae
Ruminococcaceae
Ruminiclostridium
Acetivibrio
Faecalibacterium
Oscillospira
Ruminococcus
Acidaminococcus
Dialister
Phascolarctobacterium
Veillonella
Rubrivivax
Alcaligenaceae
Oxalobacter
Bilophila
Desulfovibrio
Campylobacteraceae
Enterobacteriaceae
Escherichia
Holdemania
Akkermansia
6
健康与疾病相关性
•代谢疾病方面:研究结果显示,丹毒丝菌科(Erysipelotrichaceae)的相对丰度与多种代谢性紊乱密切相关,包括肥胖、高脂血症以及肝脂肪变性等。其数量变化常被视为代谢异常的一种微生态特征,提示该菌群可能在宿主脂肪代谢、胆汁酸循环以及能量平衡调控中发挥一定作用。
•炎症与免疫方面:该家族的细菌具有较高的免疫原性,其丰度波动与多种免疫相关疾病密切联系。在炎症性肠病及其他免疫介导疾病(例如多发性硬化、特应性皮炎和食物过敏)中,丹毒丝菌科(Erysipelotrichaceae)的异常增减被认为可能影响宿主免疫反应的稳定性,从而参与炎症反应的调节过程。
丹毒丝菌科在宿主炎症中的潜在作用
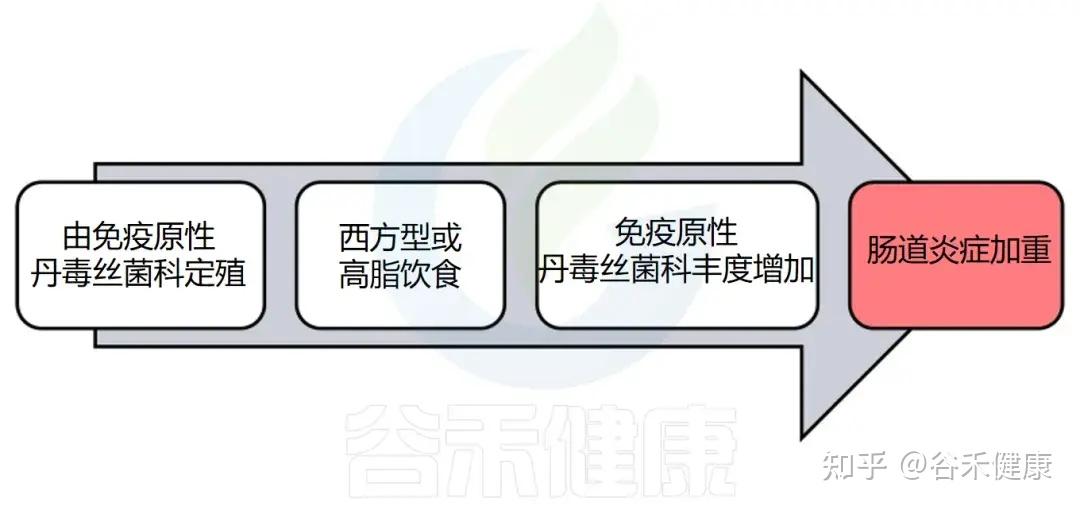
有研究人员开发了一种基于免疫球蛋白 A(IgA)包被细菌进行分类和测序的技术——IgA-SEQ,发现丹毒丝菌科的某些成员相比其他肠道菌群被 IgA 高度包被。随后,在研究慢性 HIV 感染且接受抑制性抗逆转录病毒治疗的患者时发现,丹毒丝菌科的相对丰度与肿瘤坏死因子 α(TNF)水平呈正相关。
•其他疾病方面:部分研究还提示,该菌群的丰度变化与多种神经系统及精神类疾病有关。例如,在帕金森病和阿尔茨海默病等神经退行性疾病患者中,其比例与病情进展存在一定相关性;而在抑郁症与精神分裂症等精神障碍人群中也观察到类似现象。
这些发现表明,丹毒丝菌科(Erysipelotrichaceae)在多系统疾病中的潜在作用值得进一步深入探讨,后文将对此内容进行更为详细的阐述。
1
结直肠癌中水平增加
丹毒丝菌科在胃肠道相关疾病中的重要性,已经被多项研究证实。其在结直肠癌患者体内的富集现象凸显了该菌群与肿瘤发生之间的联系。
具体而言,与健康个体相比,结直肠癌患者肠腔中丹毒丝菌科的丰度显著升高,这种差异性被认为可能与肠道炎症环境的变化密切相关。
此外,在以1,2-二甲基肼诱导的结肠癌动物模型中,肿瘤组中该菌科的丰度水平也明显高于对照组,进一步支持了其在结肠肿瘤形成过程中的潜在作用。这些发现共同表明,丹毒丝菌科的变化可能是肠道微生态失衡与结直肠癌发病机制之间的重要连接环节。

2
炎症性肠病中丰度发生变化
在炎症性肠病(IBD)患者及动物模型中,丹毒丝菌科的丰度发生变化,但相关证据并不一致。
•小鼠肠道炎症中丹毒丝菌科增加
有研究发现,在感染弓形虫或贾第鞭毛虫的小鼠中,回肠处的菌群向丹毒丝菌科转变;另一项研究发现,丹毒菌科丰度显著增加时,小鼠发生了肿瘤坏死因子(TNF)驱动的克罗恩病 (CD) 样透壁炎症。
•也有研究发现克罗恩病中丹毒丝菌科丰度减少
相反,也有研究发现克罗恩病(CD)复发患者的丹毒丝菌科显著减少,另一项研究同样观察到新发 CD 患者中该菌科的丰度下降。他们分析了 IBD 患者和胆汁代谢基因对照的公开宏基因组数据集,发现源自厚壁菌门类群(包括丹毒科)的胆汁盐水解酶基因的丰度在 IBD 中与健康对照相比显著减少。

这些结果表明不同宿主间存在差异,炎症小鼠模型的丹毒科水平较高,而 IBD 患者的水平较低。对此的两种可能的解释包括小鼠和人类肠道微生物群的固有差异或它们在感知细菌配体时先天免疫反应的差异。
注:当以高IgA包被菌群(含丹毒丝菌科)定植无菌小鼠后,发现这些小鼠在葡聚糖硫酸钠处理后发生更严重的结肠炎。
3
丹毒丝菌科有望作为肠道疾病生物标志物
在对克罗恩病(CD)、溃疡性结肠炎(UC)、结直肠癌(CRC)及艰难梭菌感染(CDI)总计3048份肠道菌群 16S rRNA 数据的荟萃分析中,研究发现:

•肠道疾病患者普遍存在丹毒丝菌科的升高
与健康对照组相比,肠道疾病患者(包括CD、UC、CRC和CDI)普遍表现出丹毒丝菌科(Erysipelotrichaceae)丰度的升高。
该科群体的增加与肠道炎症和免疫反应异常密切相关,提示其可能参与肠道菌群失调(dysbiosis)的形成与维持。
在克罗恩病(CD)和艰难梭菌感染(CDI)中,丹毒丝菌科(Erysipelotrichaceae)尤其突出,其中的Erysipelatoclostridium属被鉴定为两种疾病的潜在微生物标志物。
关于丹毒丝菌科在人类疾病中作用的最有力证据来自其与代谢紊乱的关联研究。
1
肥胖个体中丰度升高
早期研究发现,在饮食诱导的肥胖动物中,丹毒丝菌科物种大量繁殖;肥胖个体也表现出该菌科丰度升高。

•参与脂质代谢,与肝脏脂肪含量正相关
后续研究进一步证实,该菌群与宿主体内脂质代谢密切相关。研究还发现丹毒丝菌科的四个谱系,对饮食及宿主健康表型的反应不同。观察到高脂饮食或西方饮食小鼠中该菌科的增加;并有研究发现其丰度与女性受试者肝脏脂肪含量呈正相关,且这一效应在控制胆碱摄入的条件下表现明显。
2
丹毒丝菌科与较高的代谢紊乱相关
对20名年龄在 58 至 71 岁之间、糖耐量正常、糖尿病前期或 2 型糖尿病的个体中,从粪便样本中扩增的 16S rRNA 基因的条形码测序,比较了肠道细菌群落发现:

•丹毒丝菌科丰度过高增加代谢紊乱风险
特定的微生物群在不同的代谢状态下相对富集或减少。例如,丹毒丝菌科(Erysipelotrichaceae)的丰度较高与代谢紊乱有关,而霍尔德曼氏菌属(Holdemania)与脂质和葡萄糖代谢受损的临床指标相关。与代谢性疾病临床表现的相关表明,这些微生物可能有助于代谢损伤或健康。
一项针对奥地利男女肠道菌群与糖代谢紊乱的研究也发现,丹毒丝菌科(Erysipelotrichaceae)和毛螺菌科(Lachnospiraceae)部分菌群与代谢异常相关。Lachnospiraceae科和瘤胃球菌科成员可将复杂多糖分解为短链脂肪酸,如丁酸、丙酸和乙酸。而丹毒丝菌科在肥胖患者接受胃旁路手术后,其丰度明显下降。
3
高脂肪摄入和抽烟会增加丹毒丝菌科丰度
营养学研究进一步表明,膳食脂肪对丹毒丝菌科的丰度具有显著影响。在肠外营养相关肝损伤的小鼠中发现,丹毒丝菌科中特定分类单元积累明显,而肝损伤的减轻则伴随着抗生素治疗后该菌群的下降。
研究还显示,丹毒丝菌科的变化与肠外营养液中大豆油基脂质乳剂的使用密切相关。
此外在进行多重比较校正后还发现,与从不吸烟者相比,丹毒丝菌科的细菌类群在吸烟者中显著富集。
•低脂饮食降低丹毒丝菌科水平及血脂或胆固醇
在接受低脂(约13.5g/1000 Kcal)排他性肠内营养(EEN)治疗的患者中观察到类似现象。结合关于 EEN 治疗可显著减少克罗恩病(CD)患者内脏脂肪面积的结果,进一步暗示脂肪摄入类型可能影响治疗效果。还有研究人员提出,膳食脂肪的组成对 CD 肠内营养疗法的疗效至关重要。
与健康人相比,炎症性肠病(IBD)患者常表现出不同的胆固醇水平,而针对 TNF 的英夫利昔单抗维持治疗则会导致血胆固醇升高及腹部脂肪显著增加。
综上所述,IBD患者丹毒丝菌科丰度的波动可能与血脂或胆固醇表型,以及饮食组成密切相关,并可能对疾病表现和活动程度产生重要影响。
1
自闭症儿童中丰度较高
研究发现,与健康对照组相比,自闭症谱系障碍(ASD)儿童的肠道菌群生物量、丰富度和多样性均显著增加,且微生物群落结构发生明显改变。在属水平上,未鉴定的 Lachnospiraceae、Clostridiales、Erysipelotrichaceae、Dorea、Collinsella 和 Lachnoclostridium 的相对丰度升高。未鉴定的丹毒丝菌科、粪杆菌及毛螺菌科的存在与 ASD 症状严重程度正相关。

•丹毒丝菌科可能有助于判断自闭症严重程度
进一步分析显示,重度 ASD 儿童中未鉴定的丹毒丝菌科丰度最高,而粪杆菌数量最低;其丹毒丝菌科水平也明显高于轻度ASD儿童,粪杆菌则相对更低。因此我们推测肠道微生物群落的结构与自闭症症状的严重程度相关,肠道微生物群分析可能有助于症状学,肠道菌群的调节可能是未来ASD治疗的新策略。
2
阿尔兹海默病中丹毒丝菌科UCG-003减少
在阿尔茨海默病(AD)患者中,肠道微生物群呈现出明显的紊乱特征。具体而言,与健康对照组相比,AD 患者体内的双歧杆菌、梭状芽孢杆菌、Castellaniella、丹毒丝菌科 UCG-003、罗氏菌属、Tuzzerella、乳杆菌科以及Monoglobus的丰度均显著减少。
这些细菌通常与维持肠道生态平衡、促进短链脂肪酸生成及调节免疫反应等功能密切相关,因此它们的减少可能反映出宿主体内代谢与炎症状态的异常。

丹毒丝菌科(Erysipelotrichaceae)是一类肠道常见菌群,广泛参与宿主的代谢、炎症及多种疾病过程。高脂饮食、抽烟等不良习惯会增加丹毒丝菌科水平。多项研究及谷禾数据库均显示,在肥胖和代谢紊乱人群中该菌科显著富集。
由于具备较高免疫原性,丹毒丝菌科在肠道疾病(克罗恩病、溃疡性结肠炎、结直肠癌及艰难梭菌感染)中丰度上升,未来有望成为反映肠道健康状况的潜在生物标志物。
富含膳食纤维或特定益生元(如阿拉伯木聚糖低聚糖、黄酮类槲皮素、菊粉、薏米)的饮食可调节丹毒丝菌科(Erysipelotrichaceae)丰度,说明饮食可以通过菌群进而影响人体代谢健康。
此外,太极拳和运动等生活方式干预也可影响丹毒丝菌科的丰度,提示其在心理与生理健康调节中的潜在作用。研究发现,肠道中未鉴定的丹毒丝菌科物种丰度越高,自闭症症状越严重,进一步证实该菌科在神经系统疾病中的参与,可能有助于辅助判断自闭症严重程度。
未来,应通过多组学分析和功能实验进一步揭示丹毒丝菌科不同成员的代谢特性及其与其他肠道菌群的互作机制。随着肠道菌群检测技术的发展,丹毒丝菌科有望成为评估代谢健康、监测炎症状态及指导微生态干预的重要生物标志物,为精准营养和疾病预防提供新的思路与工具。
主要参考文献
Kaakoush NO. Insights into the Role of Erysipelotrichaceae in the Human Host. Front Cell Infect Microbiol. 2015 Nov 20;5:84.
Ding X, Xu Y, Zhang X, Zhang L, Duan G, Song C, Li Z, Yang Y, Wang Y, Wang X, Zhu C. Gut microbiota changes in patients with autism spectrum disorders. J Psychiatr Res. 2020 Oct;129:149-159.
Lippert K, Kedenko L, Antonielli L, Kedenko I, Gemeier C, Leitner M, Kautzky-Willer A, Paulweber B, Hackl E. Gut microbiota dysbiosis associated with glucose metabolism disorders and the metabolic syndrome in older adults. Benef Microbes. 2017 Aug 24;8(4):545-556.
Teng D, Jia W, Wang W, Liao L, Xu B, Gong L, Dong H, Zhong L, Yang J. Causality of the gut microbiome and atherosclerosis-related lipids: a bidirectional Mendelian Randomization study. BMC Cardiovasc Disord. 2024 Mar 2;24(1):138.
Cox LM, Sohn J, Tyrrell KL, Citron DM, Lawson PA, Patel NB, Iizumi T, Perez-Perez GI, Goldstein EJC, Blaser MJ. Description of two novel members of the family Erysipelotrichaceae: Ileibacterium valens gen. nov., sp. nov. and Dubosiella newyorkensis, gen. nov., sp. nov., from the murine intestine, and emendation to the description of Faecalibaculum rodentium. Int J Syst Evol Microbiol. 2017 May;67(5):1247-1254.
Mancabelli L, Milani C, Lugli GA, Turroni F, Cocconi D, van Sinderen D, Ventura M. Identification of universal gut microbial biomarkers of common human intestinal diseases by meta-analysis. FEMS Microbiol Ecol. 2017 Dec 1;93(12).
Zhang H, DiBaise JK, Zuccolo A, Kudrna D, Braidotti M, Yu Y, Parameswaran P, Crowell MD, Wing R, Rittmann BE, Krajmalnik-Brown R. Human gut microbiota in obesity and after gastric bypass. Proc Natl Acad Sci U S A. 2009 Feb 17;106(7):2365-70.

谷禾健康
胆碱(2-羟基‑N,N,N‑三甲基乙铵),是我们身体正常运转不可或缺的一种必需营养素。它的角色至关重要:一方面,它是构成细胞膜的重要原料,参与合成磷脂酰胆碱等物质来维持细胞的完整结构;另一方面,它也是神经递质“乙酰胆碱”的前体物质,在大脑与神经功能中扮演着关键角色。
正因如此,乙酰胆碱的水平失衡已成为临床上监测阿尔茨海默病、帕金森病及重症肌无力等疾病的关键指标。在日常生活中,我们可以通过食用鸡蛋黄、动物内脏以及大豆等来获取较为丰富的胆碱。
然而,对于这样一种重要的营养素,并非多多益善,需要维持一个平衡,过高或过低都可能对健康构成威胁。
当胆碱摄入不足时,与婴儿大脑发育,中老年神经退行性疾病,代谢综合征以及癌症风险都密切相关。研究报道胆碱缺乏造成基因甲基化失衡,可能促发肝癌、乳腺癌及结直肠癌等的发生。
与此同时最近研究发现,一些肠道细菌例如拟杆菌和梭菌细菌能将胆碱转化三甲胺(TMA),然后再经由肝脏FMO3酶氧化生成氧化三甲胺(TMAO),而TMAO与动脉粥样硬化和血栓形成等心血管疾病密切相关,被视为心脑血管的潜在风险指标。
因此,本文带大家一起了解什么是胆碱,及其与肉碱区别,胆碱在人体的转化代谢和对健康的影响,胆碱不平衡引发的疾病以及饮食调整与健康防控的科学策略。
什么是胆碱?
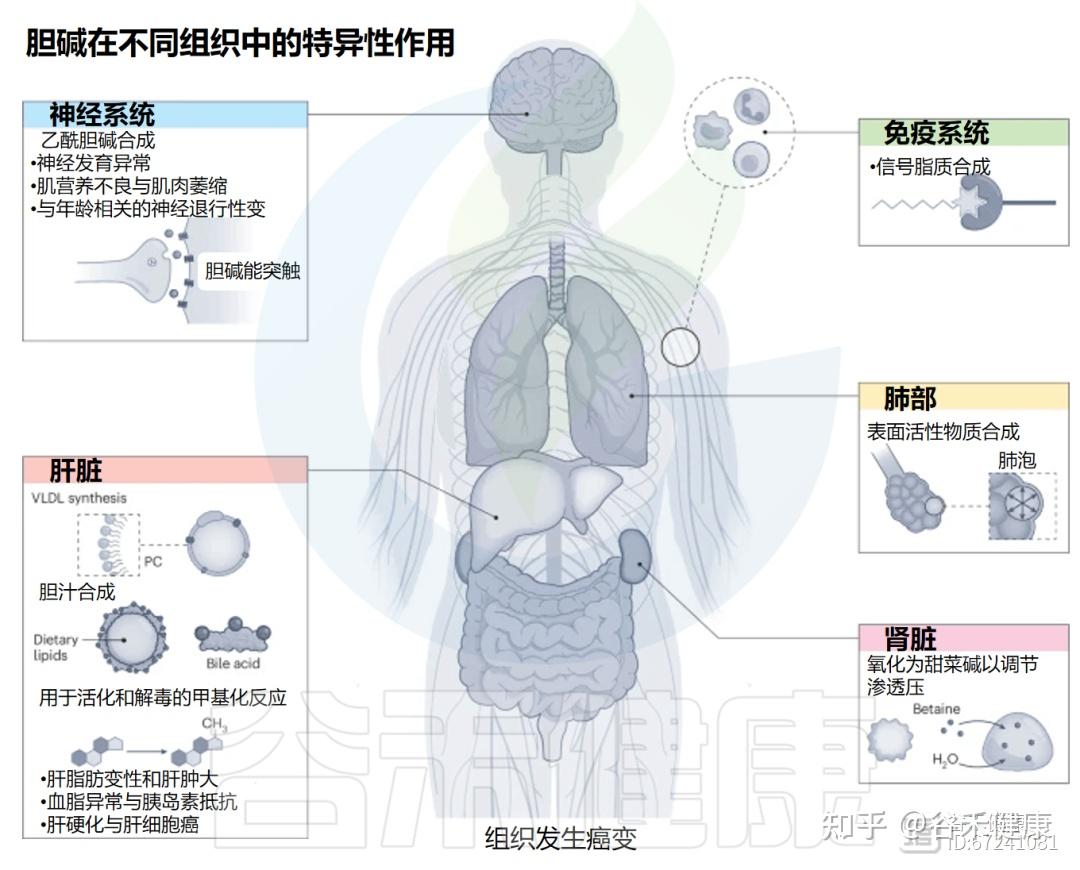
胆碱(2-羟基-N,N,N-三甲基乙铵),是人类必需的营养素,对大脑、肝脏和全身代谢等都非常重要。它既是细胞膜的组成原料(主要参与合成磷脂,如磷脂酰胆碱),又是神经递质乙酰胆碱的前体,帮助大脑传递信号、维持记忆和注意力。同时,胆碱还能转化为甜菜碱(betaine),在体内甲基化反应中提供“甲基”,参与DNA和蛋白质的调控,是表观遗传调节的重要环节。
▸ 胆碱的生物学功能
★ 关键生理角色
结构作用:是细胞膜主要磷脂(PC、磷脂酰乙醇胺PE)的前体,维持膜的完整性与流动性。
神经递质合成:为乙酰胆碱(acetylcholine)合成提供原料,参与记忆、注意和肌肉控制。
甲基供体来源:通过转化为甜菜碱供给 S-腺苷甲硫氨酸(SAM)的甲基,参与DNA、蛋白和磷脂的甲基化,对基因表达和表观遗传调控至关重要。
脂质代谢与肝功能:促进脂肪从肝脏输出,预防脂肪肝。
▸ 影响神经系统发育与功能维持
·胎儿期及早期生命阶段高胆碱摄入可增强大脑海马区的神经发生、突触可塑性与学习记忆能力。
·唐氏综合征模型(Ts65Dn小鼠)中改善注意与空间学习障碍,恢复海马神经发生。
·Rett综合征、小鼠精神分裂症模型(DBA/2小鼠):改善运动协调与感觉信息处理。
·阿尔茨海默病(AD)模型:减少Aβ斑块沉积、缓解胶质细胞活化、维持胆碱乙酰转移酶(CHAT)水平,保护胆碱能系统功能。
▸ 认知维护与老化防护
·成人摄入胆碱量与语言记忆、视觉记忆表现呈正相关。
·胆碱充足可降低白质高信号体积,后者是认知衰退与阿尔茨海默病的影像学标志。
·胆碱与omega-3脂肪酸共同维持脑内磷脂酰胆碱-DHA(PC-DHA)的正常水平。
·充足胆碱可促进血浆及红细胞PC-DHA含量,提高脑内DHA供给,从而改善或延缓认知衰退。
要充分发挥胆碱的这些健康益处,我们就必须确保它的稳定供给。那么,哪些食物才是胆碱的宝库呢?
尽管人体可以通过内源性途径合成一定量的胆碱,但这种合成能力十分有限,通常不足以满足身体需求。因此,还需要通过日常饮食获得,以弥补内源性合成的不足。
▸ 食物中的胆碱
▸ 母乳是婴幼儿重要的胆碱来源
母乳是纯母乳喂养婴儿在出生后6个月内唯一的胆碱来源,被世界卫生组织公认为婴儿的最佳营养来源。
新生儿和婴儿在快速生长阶段对胆碱需求量较高。研究显示,母乳中总胆碱含量从初乳到出生后两周明显上升,随后在6个月后趋于稳定,成熟母乳中总胆碱浓度约为125–166mg/L(1198–1600μmol/L)。
注:部分研究认为母亲的膳食胆碱摄入量可能影响乳汁中胆碱的浓度。补充胆碱可使成熟乳中游离胆碱、磷酸胆碱、甘油磷酸胆碱及总胆碱水平提高约20%–38%。
▸ 不同配方奶粉间胆碱含量差异显著
当无法母乳喂养时,婴儿配方奶粉是主要替代选择。目前建议婴儿配方奶中胆碱含量为7–50mg/100kcal,相当于每日37–265mg,总摄入量取决于婴儿每日约0.78L的奶量。
不同配方和品牌之间的胆碱形式与含量差异较大,大多以氯化胆碱为主要添加形式,部分含有少量大豆卵磷脂。分析显示,不同产品胆碱含量可相差两倍(52–104mg/L),各国市售配方平均在82–209mg/L之间。
研究表明,与大豆配方相比,牛奶配方中游离胆碱和磷脂酰胆碱含量较低,但磷酸胆碱、甘油磷酸胆碱及总胆碱水平更高;与母乳相比,牛奶配方中磷酸胆碱和鞘磷脂水平较低,而甘油磷酸胆碱较高,总胆碱接近。
▸ 鸡蛋、鱼、肝脏、牛奶是优质的胆碱来源
大量证据表明,动物性食物的总胆碱含量普遍高于植物性食物。肝脏、鸡蛋、牛肉、鱼类及海鲜、猪肉和鸡肉是最富含胆碱的代表,其中大部分以脂溶性的磷脂酰胆碱形式存在,是细胞膜的重要组成部分。牛奶因日常摄入频繁,也是良好的胆碱来源。
此外,豆类和坚果、谷物以及各类种子中也含有一定量的胆碱,这些植物性食物虽然胆碱含量较动物性食物低,但仍对日常摄入具有补充作用。同时,十字花科蔬菜如西兰花、花椰菜等也提供一定水平的胆碱,可作为均衡饮食中重要的植物来源。
下面列出了一些常见食物中胆碱和甜菜碱的含量:
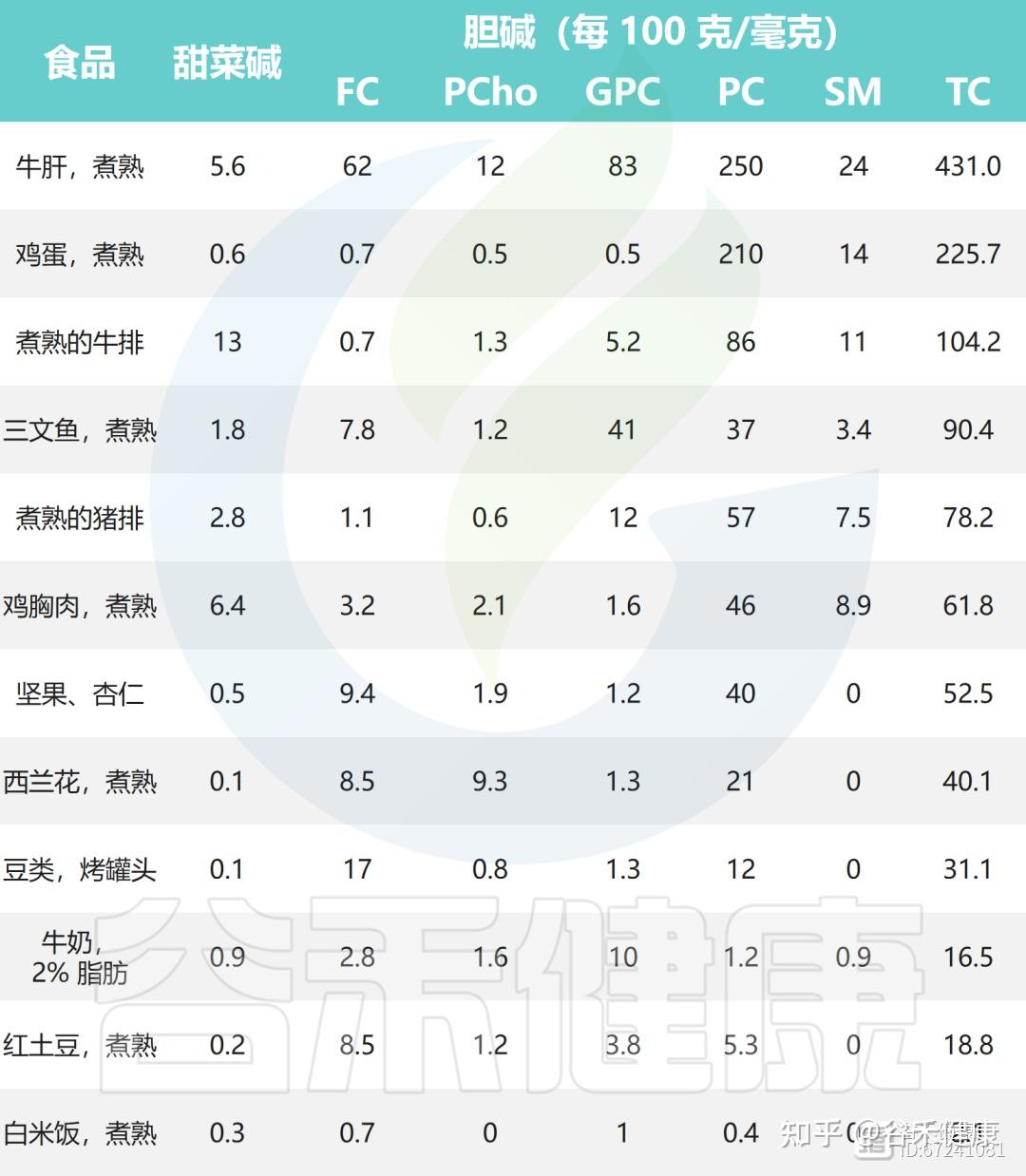
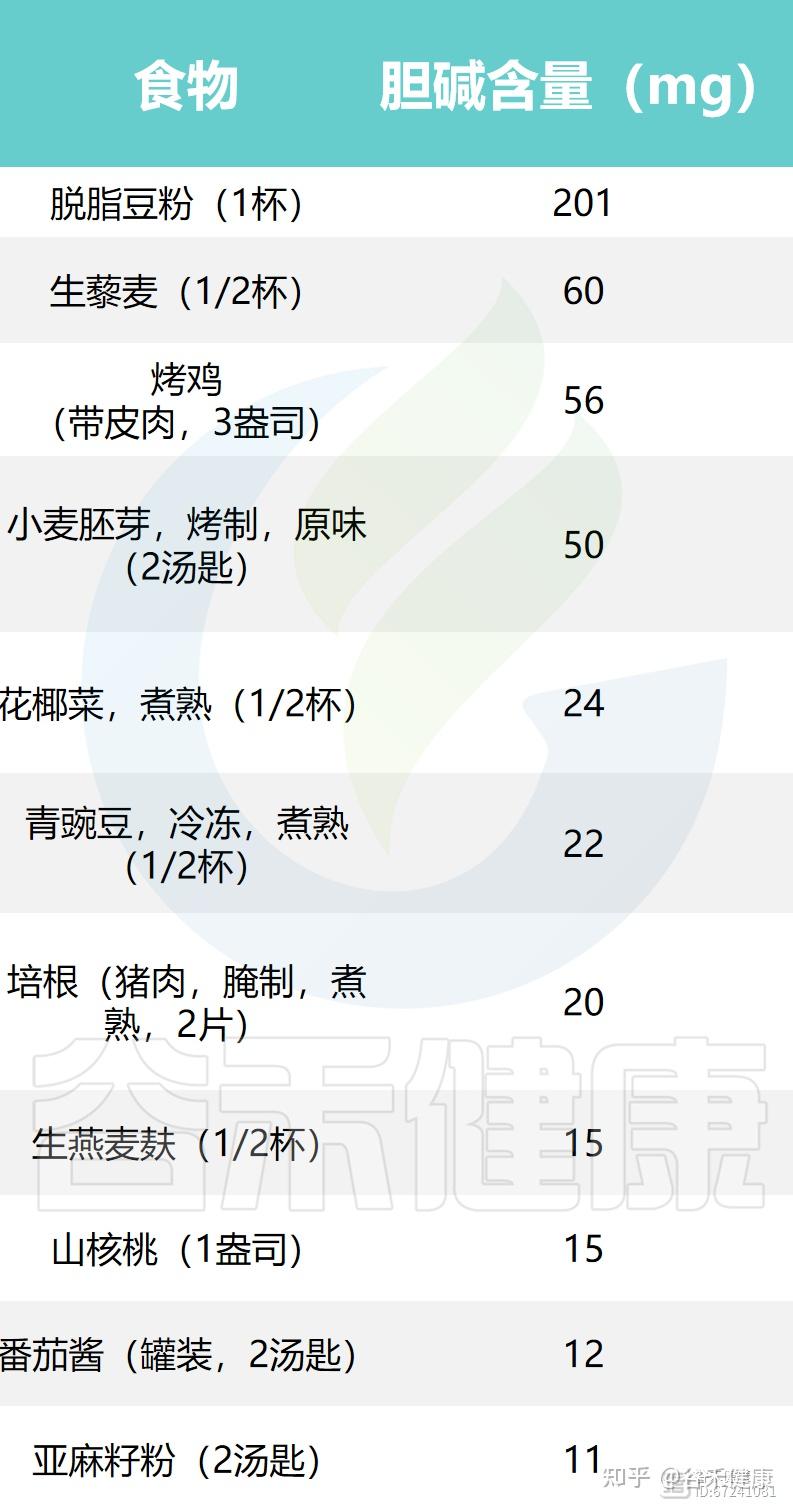
▸ 胆碱与肉碱的区别
虽然名称相似,但胆碱和肉碱是两种功能完全不同的物质,不可混淆。
胆碱是细胞膜,神经递质乙酰胆碱的前体,主要参与结构和信号;绝大部分必须从食物中获取,鸡蛋含量比较高。
肉碱是赖氨酸和蛋氨酸合成的氨基酸衍生物,脂肪代谢的关键物质;人体可以利用赖氨酸和蛋氨酸(两种氨基酸)在肝脏和肾脏中自行合成大部分所需的肉碱,同时也可以从食物中补充,主要来源是红肉(尤其是牛肉和羊肉)。

简单来说,胆碱负责搭建基础设施——细胞膜,又参与信号传导(神经),还参与到复杂的基因表达调控。而肉碱,代谢路径较专一,专门负责将燃料(脂肪酸)高效地运送到线粒体去燃烧供能。
以上我们可以看到,胆碱和肉碱虽然名称相似,但在生理功能上却截然不同,不可混淆。那么下一个更实际的问题是:我们吃下去的胆碱,身体是如何处理它的?这背后又隐藏着哪些与健康息息相关的秘密呢?
胆碱进入人体后,会经历一系列复杂的吸收和代谢过程。这一过程不仅涉及小肠和肝脏,还与我们肠道中的微生物群密切相关,最终决定了胆碱的生物利用度和其代谢产物对健康的影响。
▸ 胆碱的形式与吸收路径
在食品中,胆碱有水溶性(游离胆碱、磷酸胆碱和甘油磷酸胆碱)和脂溶性(磷脂酰胆碱和鞘磷脂)两种形式。
不同胆碱形式的结构
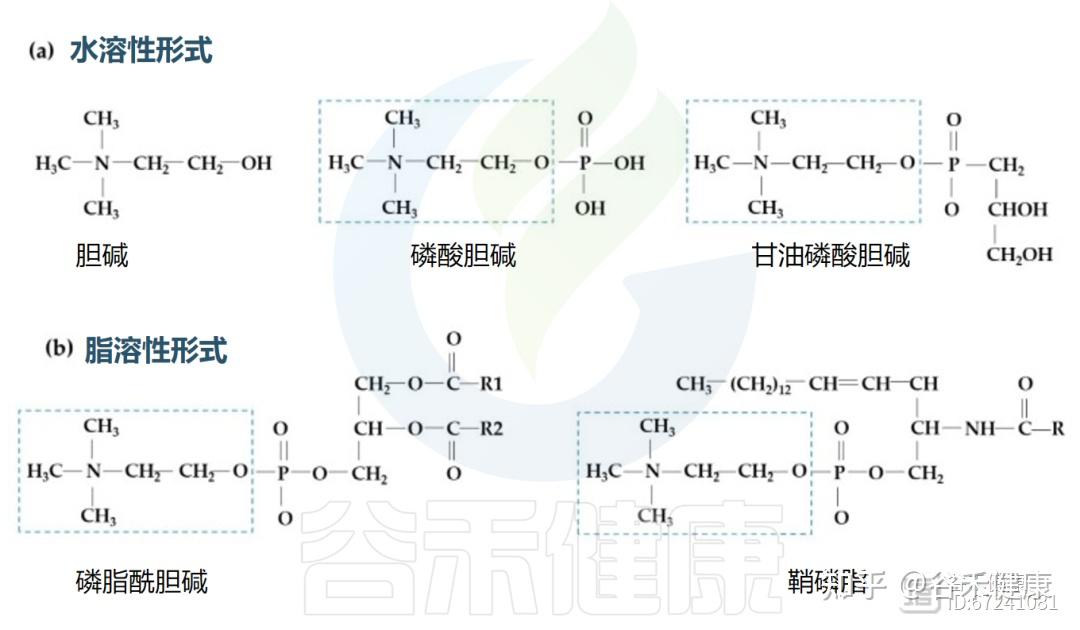
▸ 不同形式的胆碱吸收路径不同
不同形式的胆碱在吸收和代谢途径上存在差异。水溶性胆碱经门静脉输送至肝脏,而脂溶性胆碱在吸收后被封装成乳糜微粒,通过淋巴系统运输。
值得注意的是,婴儿期与成年期摄入的胆碱形式不同,这与食物来源有关。母乳中的胆碱主要为水溶性形式,而随着成长,膳食来源逐渐转向脂溶性胆碱。
▸ 不同形式胆碱在利用度和吸收效率等存在差异
有研究表明,不同形式膳食胆碱在生物利用度、吸收效率和组织分布方面存在差异,并可影响幼儿发育。与游离胆碱相比,膳食磷脂酰胆碱会改变乳汁中胆碱的组成形式,但不影响其总含量。
在人类中,乳汁中不同胆碱形式与婴儿发育的关系仍不清楚。仅有一项土耳其研究指出,纯母乳喂养婴儿的游离胆碱浓度高于配方奶喂养者。
动物研究的证据表明,牛奶中不同形式的胆碱会以不同的方式利用,母体和后代免疫系统对摄入各种形式的胆碱的反应不同就证明了这一点。因此,不同形式的胆碱的摄入应被认为与特定发育阶段相关。
▸ 胆碱在体内的四大代谢途径
进入体内的胆碱主要有四条代谢通路,分别参与不同的生理功能。包括乙酰胆碱、三甲胺(TMA)、甜菜碱、磷脂的合成。
①转化成重要的神经递质—乙酰胆碱
在突触前胆碱能神经元中,胆碱经胆碱乙酰转移酶转化为乙酰胆碱,并以囊泡形式释放至突触间隙,与中枢和外周神经系统的突触后受体结合。
也就是说,乙酰胆碱作为一种关键的神经递质,参与中枢和外周神经系统的信号传递,对记忆、学习和肌肉控制至关重要。
除神经系统外,乙酰胆碱的合成也存在于胎盘、肌肉、肠道及淋巴细胞中。
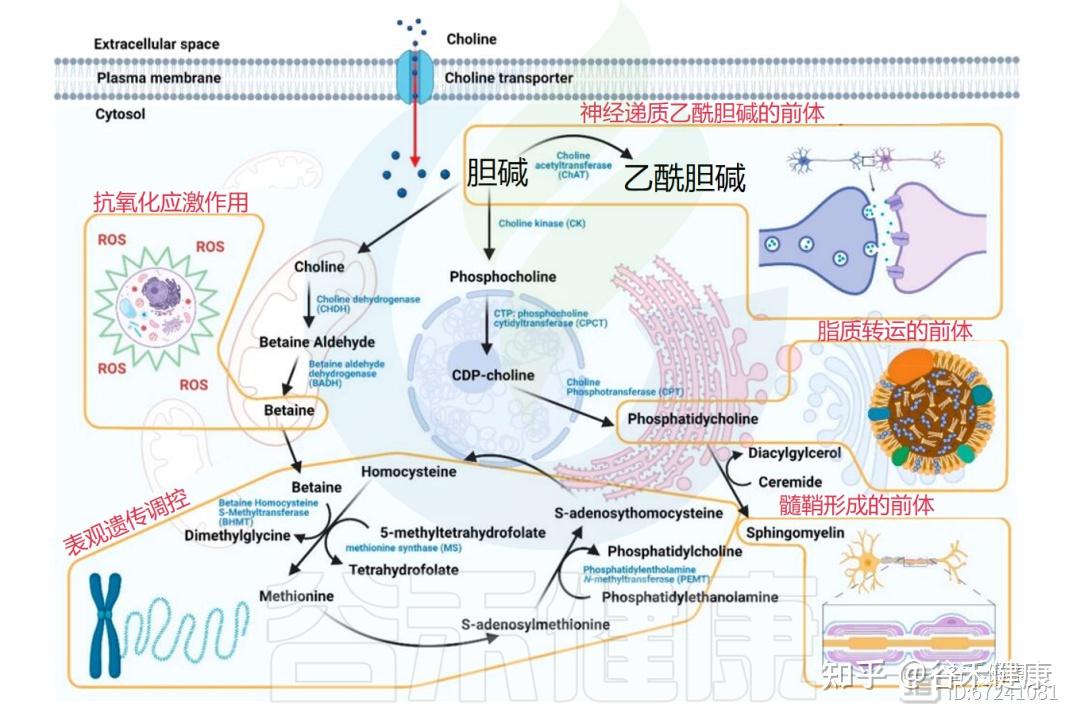
②经肠道菌群代谢为三甲胺及其氧化物
在大肠中,未被吸收的胆碱可被肠道菌群代谢为三甲胺(TMA),随后在肝脏中经黄素单加氧酶氧化为三甲胺氧化物(TMAO)。
饮食中胆碱代谢
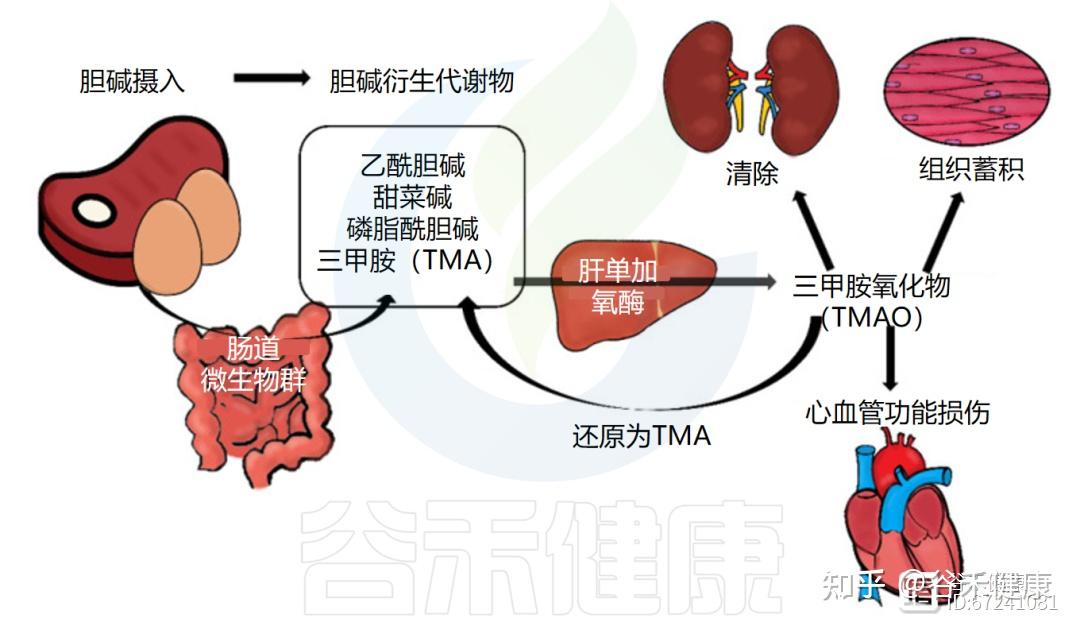
③生成重要的渗透调节剂—甜菜碱
胆碱还可在肝脏和肾脏中经两步氧化反应(胆碱脱氢酶和甜菜碱醛脱氢酶),不可逆氧化生成甜菜碱。甜菜碱既是重要的渗透调节剂,又是关键的甲基供体,可通过甜菜碱-同型半胱氨酸S-甲基转移酶(BHMT)将同型半胱氨酸再甲基化为蛋氨酸,同时生成二甲基甘氨酸。该途径与维生素B12/叶酸依赖型再甲基化途径平行,约占肝脏同型半胱氨酸再甲基化活性的一半。
④形成磷脂的前体—磷脂酰胆碱
胆碱是合成磷脂酰胆碱的前体,后者是机体最主要的磷脂形式。其合成主要通过胞苷二磷酸(CDP)-胆碱途径完成,存在于所有有核细胞中,约占肝脏中总磷脂酰胆碱的70%。
另一途径为磷脂酰乙醇胺N-甲基转移酶(PEMT)催化磷脂酰乙醇胺的三步甲基化反应,需消耗3分子SAM并生成3分子S-腺苷同型半胱氨酸(SAH),后者是同型半胱氨酸的前体。据估计,约50%的同型半胱氨酸来源于此反应,且肝脏为主要发生部位。
注:在人类中,PEMT路径是唯一已知的胆碱从头合成机制。近年研究表明,PEMT途径生成的磷脂酰胆碱在脂肪酸组成上不同于CDP-胆碱途径产物,前者富含长链多不饱和脂肪酸,如二十二碳六烯酸(DHA)。
▸ 肠道菌群:胆碱代谢的关键加工厂
摄入含胆碱的食物后,人体肠道微生物群一小部分微生物(不到1%)携带TMA产生所需的基因,可以将胆碱用于生成三甲胺(TMA)。三甲胺在宿主体内进一步氧化生成三甲氧化物(TMAO),与心血管疾病、肝脏疾病及代谢综合征等健康风险密切相关。
因此,肠道微生态组成与功能的差异,不仅影响胆碱及其衍生物的生物利用度,也决定了其代谢产物对宿主健康的双向调控效应。是连接膳食摄入与宿主生理反应的重要桥梁。
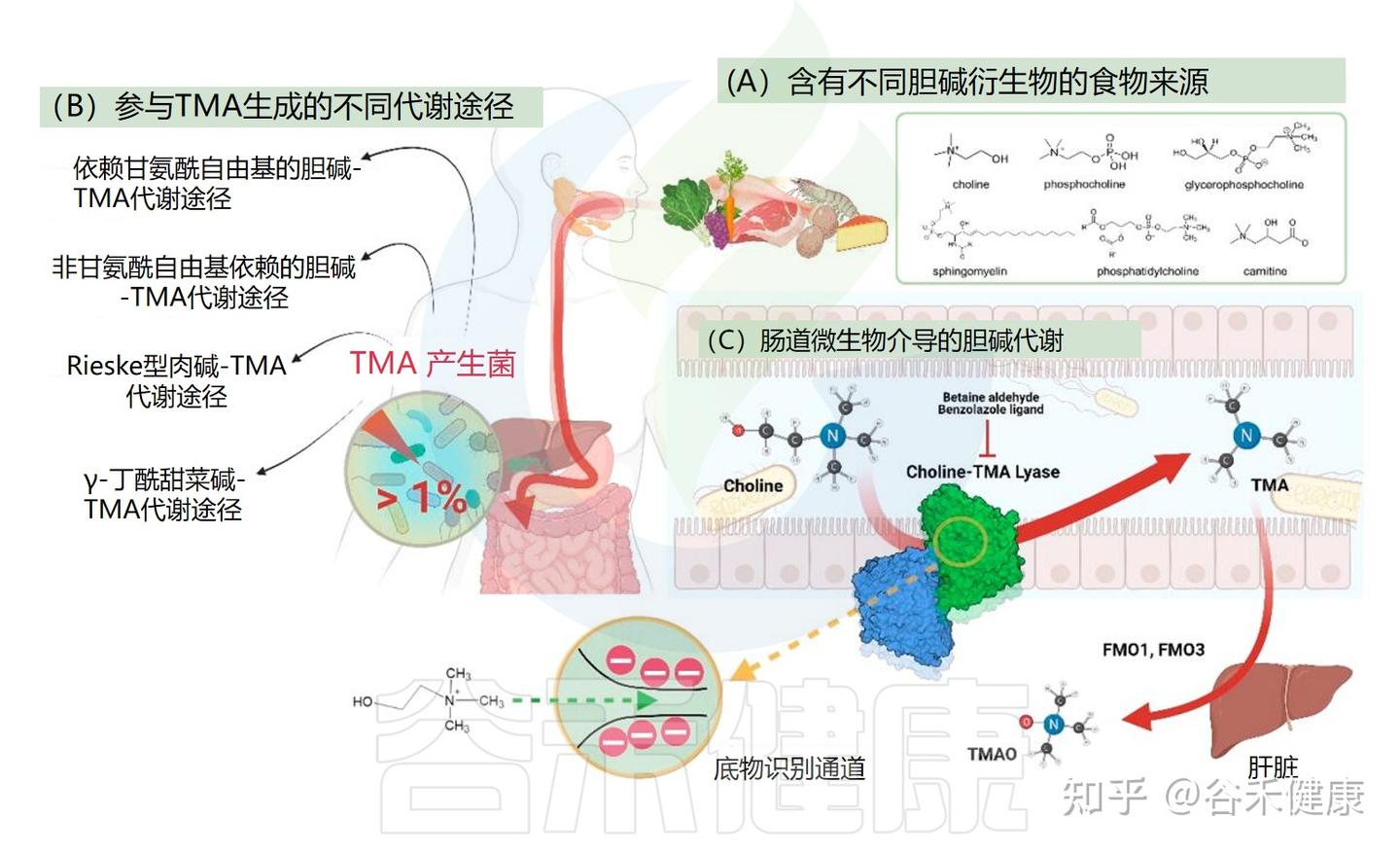
揭秘产TMA的关键菌群与基因
并非所有肠道细菌都能将胆碱转化为TMA。这一过程需要特定的酶系统。过去十年的研究已经鉴定出一些负责TMA生成的细菌基因簇:
研究发现,负责将胆碱转化为TMA的肠道细菌种类繁多,包括:Anaerococcus hydrogenalis、Clostridium asparagiformis、Clostridium hathewayi、Clostridium sporogenes、Desulfovibrio desulfuricans、Escherichia fergusonii、Klebsiella pneumoniae、Proteus penneri、Providencia rettgeri 等。
这些菌主要隶属于厚壁菌门和变形菌门。因此,血浆TMA和TMAO水平的升高,通常与这两类菌门的丰度增加以及厚壁菌门/拟杆菌门比值的增加有关。
可将胆碱降解为三甲胺的细菌菌株


▸ 三甲胺生产细菌与胆碱
▸ 三甲胺产生菌会降低胆碱的生物利用度
研究发现,即使仅有极少量三甲胺(TMA)产生菌(约占总菌群的0.15%),也能显著降低宿主的胆碱生物利用度,且丰度越高影响越显著。这表明肠道TMA生成菌的丰度与组成对胆碱代谢及相关疾病密切相关。
利用定量PCR和Illumina测序分析人类粪便样本发现,TMA产生菌占总菌群不足1%,所有样本均检测到CutC基因,而仅26%含有CntA基因。类似的模式也出现在不同饮食类型动物中:杂食和肉食动物CutC基因丰度较高,而草食动物几乎缺乏CntA基因。
▸ 梭状芽孢杆菌可能是胆碱转化的关键菌
在不同哺乳动物的肠道微生物组中,CutC基因主要分布于放线菌门、变形菌门和厚壁菌门,尤其与厚壁菌门中多个分类群相关,典型代表为梭状芽孢杆菌目成员。三甲氧化物(TMAO)水平与这些菌群丰度之间的一致性进一步支持这一关系。相比之下,CntA基因多样性较低,主要存在于变形菌中。
▸ 不同形式的胆碱与肠道菌群的相互作用
食物中的胆碱衍生物包括水溶性形式(如游离胆碱、磷酸胆碱、甘油磷酸胆碱)和脂溶性形式(如磷脂酰胆碱、鞘磷脂)。由于其化学性质和吸收效率不同,肠道微生物对这些形式的可利用性存在差异。
▸ 不同底物会影响胆碱的酶促转化效率
研究表明,与磷脂酰胆碱相比,酒石酸氢胆碱可使血浆TMAO水平提高约三倍,可能因其非酯结构更易被微生物利用,而磷脂酰胆碱需经额外水解步骤释放胆碱,延缓TMA生成。
另一项膳食干预研究发现,摄入富含磷脂酰胆碱的鸡蛋虽能提高血浆胆碱水平,但TMAO水平与补充游离胆碱者相似,进一步提示底物结构影响其酶促转化效率。近期研究也证实,食用鸡蛋不会像补充酒石酸氢胆碱那样显著升高TMAO水平。
胞苷二磷胆碱(CDP-胆碱)是一种新获欧盟批准的新型食品成分,主要用于中老年人以改善胆碱摄入。其焦磷酸基团可避免在肠腔中被水解,使其具有较高宿主生物利用度,但难以被富含CutC的菌群利用。并且其吸收、水解和去磷酸化机制尚未完全明确。
▸ 抑制胆碱向三甲胺的转化,提高胆碱利用率
对胆碱-TMA裂解酶(CutC)的结构研究揭示了底物识别的分子基础,为开发抑制TMA生成的微生物靶向分子提供了依据。X射线晶体学显示,CutC具有一个埋藏的催化位点,通过带负电残基构成的通道与带正电的胆碱结合,并在底物结合时发生贝壳式闭合反应。
基于这些结构特征,苯并恶唑配体和甜菜碱醛等已被鉴定为CutC的非竞争性抑制剂,可不可逆地抑制胆碱向TMA的转化,从而提高高危人群的胆碱利用率,并降低循环TMAO水平及其相关健康风险。
▸ 关于胆碱、三甲胺和氧化三甲胺
▸ 一些肠道细菌能将TMAO转化为TMA或甲烷
在胆碱代谢中,三甲胺(TMA)在肝脏中经FMO3酶氧化生成氧化三甲胺(TMAO)。值得注意的是,部分变形菌门细菌可利用TMAO还原酶将膳食TMAO逆向代谢为TMA。
此外,近期研究发现,某些肠道古细菌(如Methanomassiliicoccales)能够将TMAO还原为甲烷。当前研究正探索利用这些微生物作为潜在益生菌,以降低与心血管疾病风险相关的循环TMAO水平。
▸ 饮食会通过肠道菌群代谢影响氧化三甲胺含量
氧化三甲胺(TMAO)(由微生物生成的TMA氧化而来)与动脉粥样硬化和血栓形成等心血管疾病密切相关,因此常被视为预测主要不良心脏事件(MACE)的潜在风险指标。
一项关于短期高脂饮食对健康男性的研究发现,空腹血浆TMAO水平保持稳定,而餐后TMAO会随时间显著升高。由于TMAO低分子量和高溶解性,其可被肾脏快速滤过和排泄,使血浆TMAO升高仅为暂时现象。
此外,不同研究中膳食或血清胆碱水平与TMA/TMAO浓度的相关性不一致,也暗示肠—肝轴调控机制尚未明晰。这种差异可能源于肠道微生物群对胆碱生物利用度及TMA/TMAO生成平衡的调节作用。
这种复杂的调控机制,恰恰凸显了维持体内胆碱水平平衡的极端重要性。那么,当身体的胆碱天平发生倾斜时,具体会表现出哪些疾病信号或临床症状呢?下一章,我们将分别探讨胆碱“缺乏”与“过量”这两种失衡状态所引发的一系列身体信号。
胆碱作为一种必需营养素,其在体内的水平需要维持在一个动态平衡的范围内。无论是摄入不足导致的缺乏,还是因肠道菌群代谢异常导致的代谢物(如TMAO)过高,都可能通过一系列身体信号或临床指标发出警报。识别这些信号对于早期干预和预防相关疾病至关重要。
▸ 胆碱缺乏的信号与表现
当膳食胆碱摄入长期无法满足身体需求时,机体多个系统会受到影响,并表现出一系列症状和体征,这些可被视为胆碱缺乏的“信号”。由于胆碱是维持机体正常代谢功能和生理平衡的必需营养素,长期摄入不足不仅会干扰肝脂代谢过程,还可能导致肠道微生物群结构的显著改变,从而引发一系列健康问题。
▸肝脏功能受损与脂肪肝
这是最典型、最直接也是最早出现的表现。由于胆碱是合成磷脂酰胆碱(PC)的必需原料,而PC是肝脏输出脂肪(以VLDL形式)的关键组分,胆碱缺乏会直接导致肝脏脂肪堆积,形成非酒精性脂肪肝(NAFLD)。
临床上可能表现为肝功能检查中的转氨酶(ALT, AST)水平升高。在严格控制胆碱摄入的人体实验中,受试者很快就会出现肝脏脂肪变性的迹象。
事实上,一项严格控制胆碱摄入量的人体干预实验表明,肠道微生物群的组成会明显随膳食胆碱水平的变化而调整,其中包括γ变形菌门(Gammaproteobacteria)相关的特异性改变。此外,实验还发现,丹毒丝菌等群落成员与胆碱耗竭期间肝脏脂肪积聚变化密切相关,提示胆碱缺乏可通过微生物介导的机制影响肝脏脂质代谢。
▸认知功能障碍
虽然这一信号较为隐蔽,不易在短期内察觉,但长期胆碱不足会影响大脑中乙酰胆碱的合成,可能导致记忆力减退、注意力不集中、思维迟缓和学习能力下降。在孕期或婴幼儿期这一大脑发育的关键窗口期,胆碱缺乏的后果更为严重,可能导致成年后永久性的海马区结构改变和认知功能受损。
▸ 阿尔茨海默
一项于2023年发表的重要研究,为胆碱与阿尔茨海默病之间的关联提供了强有力的证据。该研究明确指出,较低的循环(血清)胆碱水平与阿尔茨海默病的病理进展显著相关。
在轻度认知障碍和阿尔茨海默病患者中,胆碱水平较低者脑内的神经炎性斑块密度更高,Braak分期更晚,并伴有更强的炎症反应。该关联在动物实验中得到进一步证实:饮食性胆碱缺乏会加剧阿尔茨海默病模型小鼠的神经病理变化,反之,补充胆碱则能有效减轻这些损伤。
然而,与循环胆碱水平降低的发现形成鲜明对比的是,一些研究(特别是较早期的研究)观察到,在神经退行性疾病患者的脑部,胆碱水平反而呈系统性升高趋势。
这种看似矛盾的现象,其根源并非胆碱的“供应过剩”,而恰恰是神经元膜加速降解,导致胆碱分解产物(如GPC)被释放出来。
这些看似矛盾的结果凸显了阿尔茨海默中胆碱代谢的极端复杂性,其检测水平高度依赖于疾病分期、脑区以及所测量的具体胆碱化合物。
▸ 肌肉损伤与功能下降
胆碱缺乏同样会影响肌肉健康。临床表现为血液中肌酸激酶(CK)水平的升高,这是肌肉细胞受损的标志物。长期来看,由于肌细胞内甘油三酯的积累以及作为甲基供体的胆碱缺乏导致肌肉蛋白合成减少、分解加速,可能引发肌肉无力、疲劳,甚至肌肉萎缩和功能下降。
▸ 代谢紊乱
胆碱缺乏会干扰全身的脂质和碳水化合物代谢。由于脂肪酸在肝脏的氧化能力下降,可能导致血浆中甘油三酯水平升高。同时,胆碱缺乏也与胰岛素抵抗的加重有关,增加了患2型糖尿病的风险。
▸ 遗传性胆碱代谢缺陷
一些罕见的遗传性疾病源于胆碱代谢通路中关键蛋白的功能缺陷。例如,胆碱转运蛋白、胆碱酯酶或磷脂合成相关酶的基因突变,可导致多种临床表型,包括先天性肌无力综合征、肌肉萎缩、癫痫、以及其他复杂的代谢异常。
▸ 发育异常
在胚胎发育过程中,胆碱扮演着至关重要的角色。研究表明,孕期胆碱缺乏与新生儿神经管缺陷的风险增加有关,这凸显了孕期充足胆碱供应对于胎儿正常神经系统发育的重要。
▸ 胆碱过量的信号与表现
胆碱是必需营养素,人体对其有较强的吸收控制与代谢平衡机制。当膳食胆碱摄入增加时,身体通常会通过减少内源合成或加快代谢(例如经氧化为甜菜碱)来维持稳态。因此,在健康人群中,即使日摄入量高于推荐量,也不会立刻造成毒性反应。
▸ 胆碱过量一般不会引起明显不良反应
胆碱过量的不良反应较为罕见,仅早期少数研究(1977年)报道,七名阿尔茨海默症患者服用后,会出现降压作用,并伴有恶心和腹泻。出现不良反应的情况(如血压下降、出汗、胃肠不适)往往是在极端剂量(比如每日7克以上的胆碱盐补充)。
▸ 胆碱代谢产物TMAO过量的隐形风险
胆碱真正应警惕的是代谢通路过载,而非营养素本身,尤其是当肠道菌群过度活跃或肝脏代谢调节失衡时,形成的代谢产物(如TMA 与 TMAO)才是隐藏的风险源。
胆碱的肠道菌群代谢产物TMA/TMAO的水平过高,本身通常不会引起明显的身体不适感。它的“信号”更多是通过体检发现的异常指标,以及一种特殊的体征,也预示着多种慢性疾病的风险正在悄然增加。
▸ 鱼腥体味综合征
这是TMA过高最直接、最尴尬的信号。当摄入极高剂量的胆碱(如每天超过7.5克)或肉碱时,或者在一些存在FMO3酶功能缺陷的遗传病患者中,肝脏无法将肠道菌群产生的大量TMA完全氧化为无味的TMAO。过量的TMA会进入血液循环,并通过汗液、尿液和呼吸排出体外,散发出类似腐烂鱼类的腥臭味。虽然这种情况在普通人群中是罕见的,但它明确地指向了TMA代谢通路的超负荷或障碍。
三项研究指出,当患者每天服用 8−20 克胆碱时,会出现胃肠道影响和鱼腥体味。基于约7.5 g/天的最低观察不良反应水平(LOAEL)并采用安全系数,将19岁及以上成人的可耐受最高摄入量(UL)设定为3.5 g/天。
▸ 心血管事件风险
大量的临床研究已证实,血浆TMAO水平升高是预测未来发生主要不良心血管事件的独立风险指标。对于心血管疾病患者来说,TMAO水平可以作为评估预后的重要参考。
▸ 肝脏疾病
TMAO不仅在非酒精性脂肪肝(NAFLD)患者中水平升高,它本身也能反过来加剧肝脏损伤。研究表明,TMAO能加剧肝脏的脂肪堆积、氧化应激和炎症反应,从而促进NAFLD向更严重的NASH阶段发展。
▸ 慢性肾病
TMAO主要通过肾脏滤过和排泄。TMAO与慢性肾病之间存在恶性循环。一方面,肾功能不全导致TMAO清除障碍,使其在体内大量蓄积;另一方面,高水平的TMAO本身就是一种尿毒症毒素,它能诱导肾小管间质纤维化,进一步损害肾功能,加速慢性肾病的进展。
▸ 代谢紊乱
高TMAO水平也常见于代谢综合征、肥胖和2型糖尿病患者,并与胰岛素抵抗的严重程度相关。
至此,从肝脏、心血管到神经系统,胆碱代谢失衡所引发的系统性风险已清晰可见。无论是胆碱缺乏导致的器官功能受损,还是其代谢产物TMAO过量所驱动的慢病进程,都凸显了维持胆碱稳态的极端重要性。
那么究竟是什么因素在幕后调控着我们每个人的胆碱水平,并决定了其代谢通路的效率与风险?下一章,我们将深入剖析这些决定胆碱“命运”的关键内外因素。
在前文我们已经看到,胆碱的缺乏与其代谢产物过高,都与多种慢性疾病的发生密切相关。但还有问题在于,不同个体对胆碱的需求与代谢反应并不一致,这种差异源于多种宿主和环境因素的综合作用,包括个体的遗传背景、性别与生理阶段、激素水平、饮食结构以及肠道微生物组成等。理解这些影响因素,是建立个体化胆碱营养策略、避免代谢失衡的关键前提。
胆碱摄入需求的个体差异
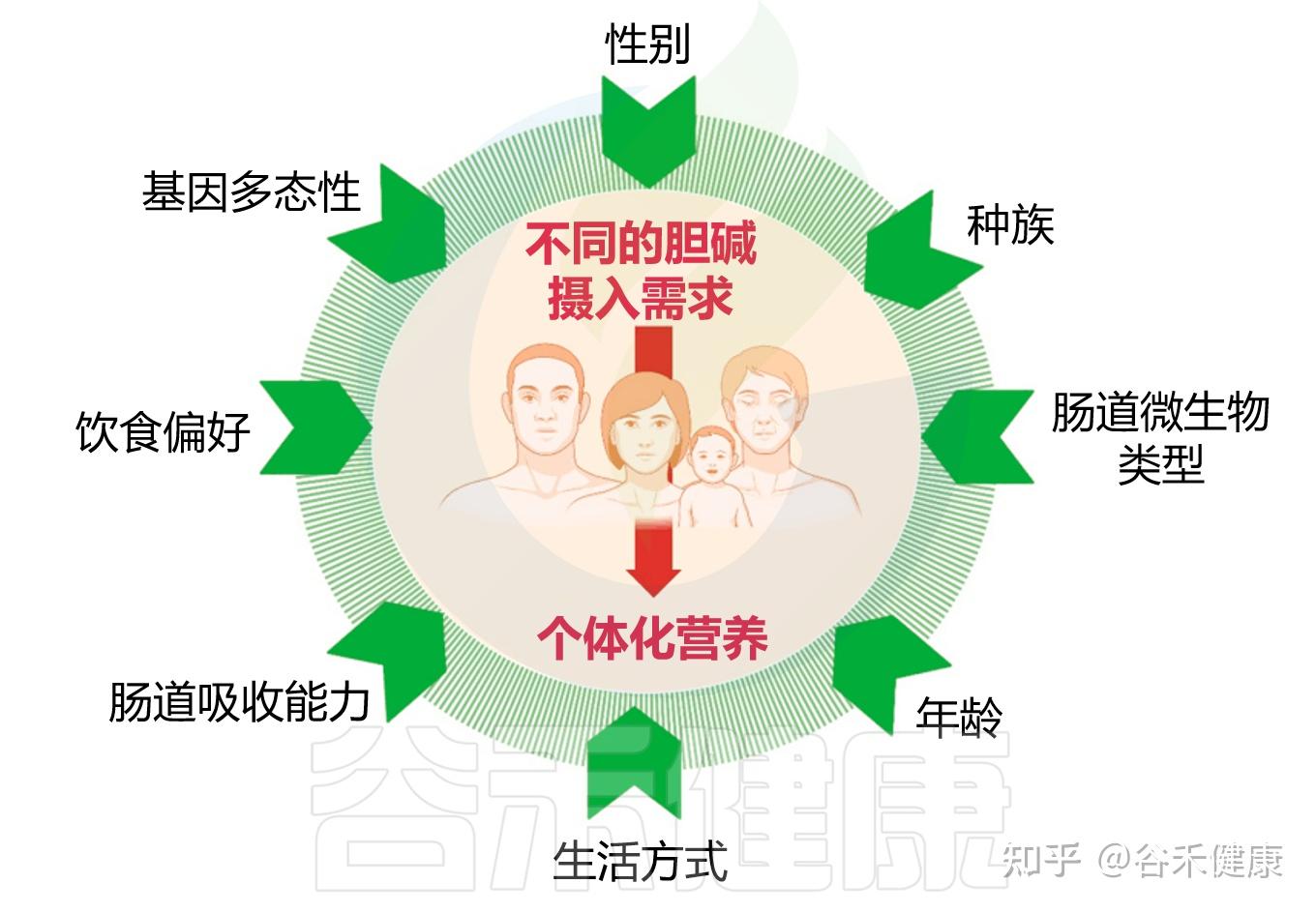
接下来,我们将逐一了解这些因素如何共同塑造个体胆碱代谢特征。
▸ 性别与激素水平
雌激素与PEMT活性:雌激素上调肝脏磷脂酰乙醇胺N-甲基转移酶(PEMT)基因的表达,促进磷脂酰胆碱的内源合成,从而减少对膳食胆碱的依赖。
因此,绝经前女性通常较为耐受低胆碱膳食,而绝经后女性因雌激素水平下降,PEMT活性降低,胆碱需求显著上升。
注:研究显示,在低胆碱膳食条件下,77%的男性和80%的绝经后女性出现缺乏症状,而绝经前女性仅为44%。
性别差异与酶活性:女性肝脏中黄素单加氧酶(FMO3)活性通常高于男性,会影响TMA→TMAO的转化速率及胆碱代谢终产物水平。
▸ 遗传与基因多态性
PEMT(rs12325817, G→C):该多态性位于雌激素反应元件附近,会削弱雌激素对PEMT的调控作用,使女性更易发生胆碱缺乏综合征(CDS)。携带者中约78%在低胆碱摄入下出现CDS症状。
MTHFD1(G1958A)突变:该突变影响叶酸介导的一碳代谢通路,降低甲基供体合成效率,从而增加对胆碱(作为甲基供体)的依赖。该突变与神经管缺陷风险增加相关。
CHDH与BHMT等基因变异:影响胆碱氧化及甜菜碱-同型半胱氨酸甲基转移过程,调节体内胆碱的利用率与甲基化能力。不同种族中相关等位基因分布差异显著,导致胆碱需求的群体差异性。
▸ 年龄与生命周期阶段
婴幼儿:婴儿阶段主要通过母乳摄入胆碱,母乳中胆碱以水溶性形式(磷酸胆碱、甘油磷酸胆碱)为主,易于吸收。早期胆碱摄入对神经发育和认知形成至关重要。早产儿胆碱需求更高,因为其肝脏合成能力尚未完善。
孕期与哺乳期:妊娠期母体需为胎儿及胎盘提供额外胆碱,用于细胞分裂、DNA甲基化及神经发育。哺乳期胆碱需求也升高,用以补充乳汁输出。
老年期:随年龄增长,内源性合成能力和饮食吸收效率下降,同时肝功能减退可能加重需求。老年人胆碱摄入不足已被关联至认知下降和非酒精性脂肪肝(NAFLD)风险。
▸ 饮食
饮食类型:动物性食物(如鸡蛋、肝、肉类、鱼、乳制品)是胆碱的主要来源。素食者或纯素饮食者胆碱摄入普遍低于标准需求。
烹饪与食物形式:高温烹饪会使游离胆碱减少。食物中胆碱的化学形式影响吸收效率——水溶性胆碱(如磷酸胆碱)易经门静脉吸收,而脂溶性形式(如磷脂酰胆碱)经乳糜微粒运输,更受脂质代谢状态影响。
营养互作:叶酸、维生素B12、B6、甜菜碱与胆碱共享甲基供体代谢通路,缺乏任一成分都会增加对胆碱的生理需求。
▸ 过量使用抗生素
长期或不当使用抗生素会对肠道微生物生态系统造成深远影响。广谱抗生素可同时抑制病原菌与共生菌的生长,引发菌群失调,削弱正常微生物竞争力,从而促使艰难梭菌等病原体过度繁殖。
总体而言,抗生素使用所引起的肠道微生物群结构变化,可能与机体代谢失衡以及糖尿病发病率的增加密切相关。这种由抗生素干扰导致的菌群改变会破坏肠道生态系统的稳定性,使益生菌数量减少、代谢功能受扰,从而使肠道逐渐倾向于形成促进TMA生成的代谢表型,进一步影响宿主的代谢健康和能量稳态。
▸ 肠道微生物组影响
微生物代谢胆碱为TMA/TMAO:特定菌群(如CutC/D阳性菌属——Desulfovibrio、Clostridium、Enterococcus等)可将胆碱降解为三甲胺(TMA),后被肝脏FMO3氧化为TMAO。
这一过程不仅影响胆碱的生物利用度,还与心血管疾病(CVD)、慢性肾病(CKD)、NASH等疾病风险相关。
个体间菌群差异:不同人群(年龄、饮食习惯、抗生素使用史)菌群组成各异,导致胆碱代谢途径及利用效率不同。这种差异在宿主遗传背景(如FMO3多态性)影响下进一步放大。
▸ 生理与病理状态
肝功能障碍:肝脏是胆碱代谢的核心器官。肝病患者(尤其是NAFLD/NASH)因磷脂合成与脂质输出受阻,其胆碱需求量显著增加。
代谢状态:胰岛素抵抗、高脂饮食、慢性炎症状态均影响胆碱的代谢与分配,使机体对胆碱的依赖度提升。
▸ 种族与地理差异
膳食习惯与基因共同决定胆碱供给与需求差异。研究显示,在相同叶酸摄入下,非裔美国女性血浆胆碱水平低于白人或墨西哥裔女性,提示胆碱代谢相关基因在不同种群中的分布不均。
以上我们了解到个体的胆碱需求受到遗传、性别、激素水平、生理状态以及肠道菌群等多重因素的综合影响。正因如此,找到一个既能满足身体需要,又不会造成代谢负担的摄入平衡,就成为维持健康胆碱状态的关键。
虽然胆碱的最佳摄入量因人而异,但权威机构仍基于大量流行病学与生化研究,制定了适宜的参考标准,以帮助公众更好地评估日常摄入量是否充足。
美国医学研究所(IOM)早年制定了不同人群的胆碱适宜摄入量(AI):女性425 mg/天,孕妇450 mg/天,哺乳期妇女和男性均为550 mg/天。
欧洲食品安全局(EFSA)在2016年更新建议值:成人400 mg/天,7–11个月婴儿160 mg/天,儿童140–400 mg/天(随年龄和体重变化),孕妇480 mg/天,哺乳期妇女520 mg/天。
目前对胆碱的摄入量建议
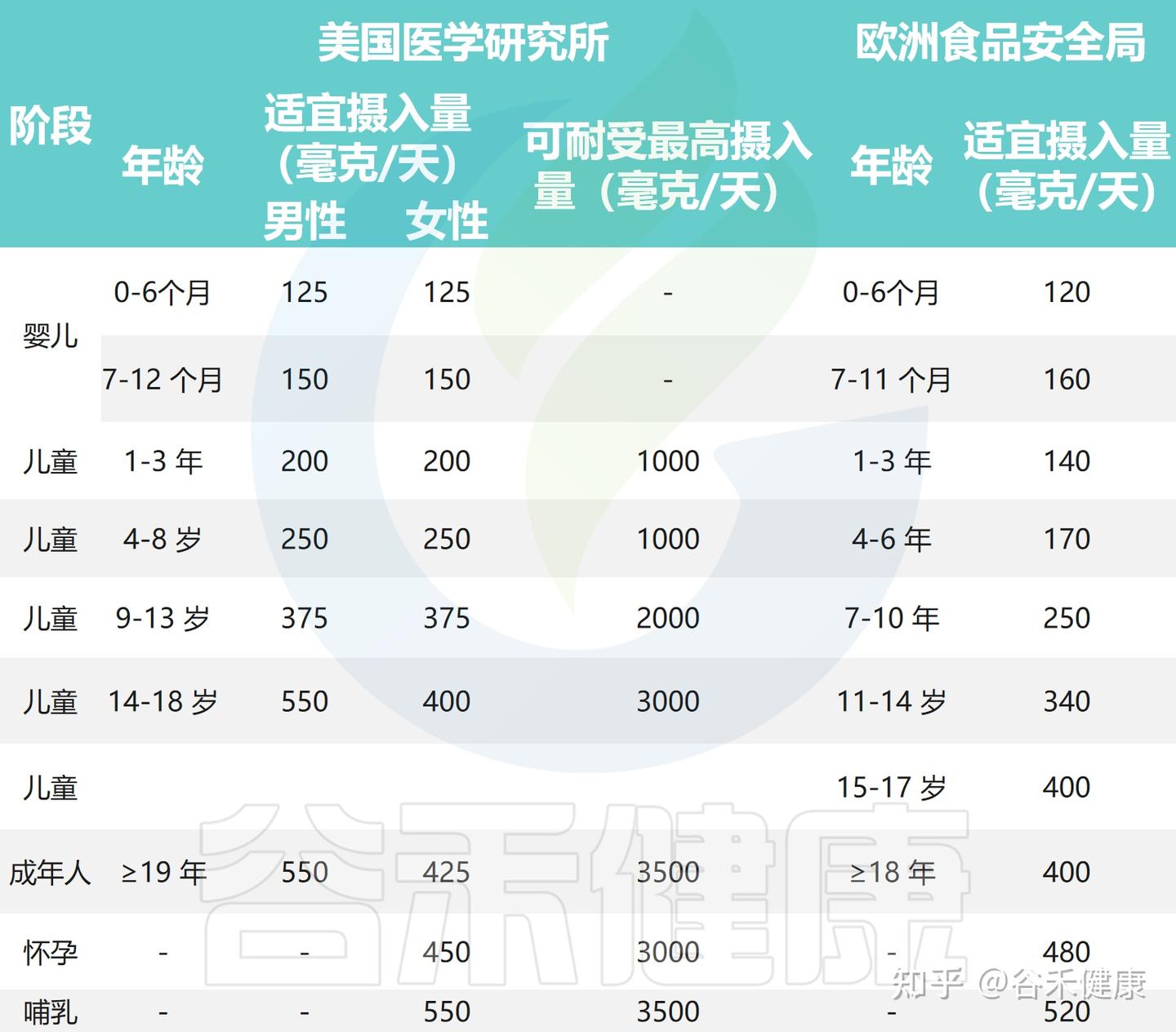
注意:这些推荐值反映的是“维持正常生理功能”的适宜摄入量(AI),并非“最低需求量(RDA)”。也就是说这是用来指导日常膳食的安全范围,而不是严格的个体化目标。
鉴于胆碱代谢的复杂性及其对健康的双重影响,我们的核心目标应该是:在确保摄入充足胆碱以满足机体生理需求的同时,最大限度地减少其在肠道内向有害代谢物TMAO的转化。这并非一个简单的“多吃”或“少吃”的问题,而是一个需要综合性的饮食调整、生活方式干预乃至个体化营养策略的系统工程。
▸ 饮食调整
饮食是影响肠道健康的关键因素,因此饮食调整成为控制三甲胺氧化物(TMAO)相关疾病风险的简便且安全的方式。
动物性来源:这类食物通常被认为是胆碱的最佳来源,含量尤为突出。
植物性来源:对于素食者或希望通过植物性饮食增加胆碱摄入的人群,以下食物是重要选择 。
地中海饮食富含多酚和膳食纤维,具有多重健康益处。流行病学数据表明,长期遵循地中海饮食与尿液、血浆TMAO水平呈负相关。
动物实验也发现,膳食影响肉食诱导的TMAO上升——高纤维饮食可显著减轻其增幅。
植物性或纯素饮食:抑制胆碱向TMA的转化
近年来,植物性或纯素饮食以其健康优势受到关注,这些优势与较低的厚壁菌门/拟杆菌门比例及短链脂肪酸的增加有关。素食和杂食性饮食在微生物群和TMAO水平方面存在差异。
有研究发现,纯素食者在左旋肉碱摄入后TMAO生成能力低于杂食者。膳食纤维可抵抗胃肠道消化并在结肠中被特定细菌发酵为短链脂肪酸(SCFA),进而影响肠道微生态平衡。
研究表明,膳食纤维可抑制胆碱向TMA的转化,从而提高高需求人群的胆碱生物利用度。其机制包括抑制糖酵解副产物甲基乙二醛的积累,减少甘氨酸代谢反馈,从而降低CutC依赖的TMA裂解酶表达;同时,纤维可激活AMPK信号通路以抑制ATP消耗过程,如TMA裂解酶合成。
尽管如此,纤维的效果存在个体差异,受基线微生物基因丰富度及普雷沃氏菌丰度等因素影响。这些发现表明,合理利用膳食纤维及其他饮食成分,有望促进功能性食品的开发,在满足胆碱需求的同时降低TMAO产生。
总体来看,膳食纤维在地中海饮食中的充足供应,以及其在西式饮食中的缺乏,是不同个体间肠道菌群组成和TMAO水平差异的关键因素。
西式饮食增加三甲胺生产者
西式饮食以高动物蛋白、饱和脂肪和低膳食纤维为特征,常摄入家禽、猪肉、牛肉和鸡蛋等动物性食品。这些食物中含有大量磷脂酰胆碱(PC)和左旋肉碱等可被微生物转化为三甲胺(TMA)的前体,随后在肝脏中进一步氧化生成三甲胺氧化物(TMAO)。
西式饮食通常与拟杆菌肠型相关。研究发现,某些微生物进化枝(如奈瑟氏菌科和脱硫弧菌属)与血浆TMAO水平呈正相关,并在冠心病患者及长期摄入动物性饮食者中观察到TMAO显著升高。进一步研究表明,摄入鸡蛋后TMAO水平升高的男性往往具有较高的厚壁菌门丰度,而TMAO水平较低者则表现出较高的拟杆菌门比例。
大部分PC在小肠上部被胰酶水解为1-lyso-PC并迅速吸收,其酶活性受胆盐与PC比例影响,而在空肠下段和回肠中逐渐失活,使部分未水解的PC进入结肠被肠道菌群利用。换言之,高肉食摄入为TMA合成菌提供了充足底物。肠道转运时间和消化酶活性等因素亦会影响未水解PC到达下消化道的量。
PC在小肠下部的积聚为表达CutC酶的细菌(如Proteus mirabilis)提供了有利生态位,使其能以胆碱为碳源进行生长和定植。此外,西方饮食脂肪和乳化剂含量高,易引起菌群失衡,并促进产TMA菌株(如梭状芽孢杆菌、埃希氏菌)的扩张。
研究不同人群中西式饮食的普及程度、肠道转运时间差异及胆汁盐水平,有助于揭示各人群间胆碱代谢差异的潜在机制。
▸ 补充益生菌
益生菌作为另一种干预手段,在动物模型中可有效重塑肠道菌群并降低TMAO水平。
▸ 副干酪乳杆菌F198
例如,膳食补充副干酪乳杆菌F198可恢复肠屏障功能,减少氧化应激性肝损伤;M. smithii定植可降低TMAO并减轻动脉粥样硬化;Enterobacter aerogenes通过调节菌群平衡显著降低血浆和盲肠TMAO。
然而,与人类相比,啮齿动物微生物组差异巨大,个体饮食和基因背景也会影响效果,因此应谨慎外推动物结果。
▸ 植物乳杆菌
植物乳杆菌,尤其是Lactobacillus plantarum ZDY04 菌株,在小鼠模型中被反复证明能显著降低因高胆碱饮食引起的血清TMAO和结肠TMA水平 。其机制可能涉及抑制肠道中TMA的生成菌群 。
▸ 双歧杆菌属
双歧杆菌Bifidobacterium breve 、Bifidobacterium longum的一些菌株在动物研究中也显示出降低血浆TMAO和TMA浓度的能力。
▸ 其他菌株
Akkermansia muciniphila、Enterobacter aerogenes ZDY01 以及一些 Lactobacillus reuteri 菌株在降低TMAO方面的潜力 。一项包含 Lactobacillus rhamnosus GG 的混合益生菌干预,在人体试验中也观察到能减弱胆碱负荷后TMAO的升高程度。
▸ 补充益生元
▸ 补充阿拉伯木聚糖等
“功能性食品”可超越基础营养调节健康。以益生元为例,这类可被特定肠菌利用的不可消化碳水化合物能促进有益菌生长并改善菌群多样性。
在人类研究中,超重者摄入富含阿拉伯木聚糖的益生元提取物后,普雷沃氏菌丰度和短链脂肪酸水平上升,血浆磷脂酰胆碱下降,提示TMA合成底物可用性降低并有助于代谢健康。
▸ 摄入多酚类化合物—如白藜芦醇
多酚类化合物作为另一类植物源膳食成分,具有重要的微生物群调节功能。补充白藜芦醇可增加乳酸杆菌、降低TMAO并缓解高胆碱饮食小鼠的动脉粥样硬化;乌龙茶提取物和柑橘类黄酮表现出相似效应。
临床试验表明,富含多酚的果渣提取物Taurisolo在4周内可显著降低TMAO水平(63.6% vs. 0.54%)。尽管结果积极,但仍需更多机制研究以阐明多酚与TMAO及人类疾病间的关系。
▸ 粪菌移植
粪菌移植(FMT)作为一种新兴手段,通过健康供体的菌群替换受体的失调微生物组,在临床前研究中展现疗效,但实际应用有限。
针对其他疾病的研究显示虽然可部分恢复菌群平衡,但并未显著降低TMAO或改善动脉粥样硬化。未来,结合精准医学的FMT策略或可实现个体化微生物重建,但仍依赖对细菌与疾病因果关系的深入理解。
▸ 针对TMAO生物合成的药物
针对TMAO生物合成的药物干预包括胆碱类似物3,3-二甲基-1-丁醇(DMB)和抗缺血药米屈肼。DMB通过非致死性抑制TMA裂解酶减少TMAO生成并减轻动脉粥样硬化,但尚未在人类中验证;米屈肼较安全,但其作用仅限于肉碱途径。
胆碱相关疾病的治疗方法


▸ 中医药
传统中医药(TCM)通过其独特的理论体系和复方用药,为调节与胆碱相关的功能紊乱提供了不同的视角,尤其是在神经系统和认知功能方面。
中医药研究更多关注的是胆碱的下游产物——神经递质乙酰胆碱(ACh)的功能。乙酰胆碱水平下降与阿尔茨海默病等认知障碍密切相关。一些中药或其活性成分被发现具有胆碱酯酶(AChE)抑制作用,能够减少乙酰胆碱的分解,从而提升其在突触间隙的浓度和作用。
具有乙酰胆碱酯酶抑制活性的中药及成分
研究发现,人参、五味子、远志、麦冬等传统补益药材,以及从石杉科植物中提取的石杉碱甲,均显示出显著的AChE抑制活性,被认为是改善认知功能的潜力药物。
也有研究认为,半夏、川芎、当归、人参等药材本身也含有胆碱成分,但其在复方煎煮后对人体系统性胆碱水平的实际贡献尚需进一步量化研究。
补肾益智汤(方)
一项针对记忆障碍模型的动物研究显示,中药复方“补肾益智汤”能够显著改善小鼠的学习记忆能力。其机制研究发现,该方剂能上调海马和皮层中胆碱乙酰转移酶(ChAT,合成乙酰胆碱的关键酶)的表达,并逆转乙酰胆碱(ACh)水平的下降和胆碱酯酶(ChE)活性的紊乱 。这表明该复方并非简单地补充胆碱,而是通过多靶点调节胆碱能神经系统的稳态。
目前中医药领域的研究主要集中在改善与胆碱能系统相关的病理状态(如认知障碍),而非直接“提高”或“降低”血浆胆碱水平本身。
▸ 运动
规律体育锻炼稳大脑胆碱水平,有益神经健康
研究表明,规律的体育锻炼(如每周三次的骑行训练,持续12周)可以防止大脑中胆碱浓度的异常升高。在阿尔茨海默病等神经退行性疾病中,神经元细胞的减少会导致胆碱浓度上升。规律运动组的大脑胆碱浓度保持稳定,而缺乏运动的对照组则出现升高。这表明规律运动可能通过保护神经元,有助于预防认知障碍和痴呆。
运动对胆碱能系统有积极调节作用
除了直接影响胆碱水平,运动还能对整个胆碱能神经系统功能产生积极影响:
小结
总体而言,饮食调整、益生元/益生菌补充、粪菌移植及药物治疗共同构成调控肠道微生态和降低TMAO水平的潜在策略。
然而,要实现临床转化,需要更系统的机制研究和设计完善的长期随机对照试验。同时,维持良好饮食习惯和健康生活方式仍是改善肠道生态与促进代谢健康的关键。
胆碱,曾经被简单地视为一种神经保护因子、细胞膜的核心组件,如今却被发现,它的命运在进入肠道那一刻便被改写。它的吸收效率、代谢方式、甚至健康效应,皆取决于你的肠道菌群。
未来,这条从认知到干预的路径将变得清晰,随着肠道菌群检测技术日益成熟,我们可以逐渐了解到自己肠道里,哪些菌群在控制胆碱的去向,哪些代谢通路可能与慢病风险相关…
基于这份独一无二的“身体地图”,我们便能采取更具针对性的行动,无论是调整饮食结构,补充特定的益生菌、益生元,还是接受个性化营养规划,最终目标都是主动引导胆碱走向有益的代谢路径,从源头上减少TMAO等风险分子的生成,修复与优化内环境。
主要参考文献
Kenny TC, Scharenberg S, Abu-Remaileh M, Birsoy K. Cellular and organismal function of choline metabolism. Nat Metab. 2025 Jan;7(1):35-52.
Goh YQ, Cheam G, Wang Y. Understanding Choline Bioavailability and Utilization: First Step Toward Personalizing Choline Nutrition. J Agric Food Chem. 2021 Sep 22;69(37):10774-10789.
Arias N, Arboleya S, Allison J, Kaliszewska A, Higarza SG, Gueimonde M, Arias JL. The Relationship between Choline Bioavailability from Diet, Intestinal Microbiota Composition, and Its Modulation of Human Diseases. Nutrients. 2020 Aug 5;12(8):2340.
Wiedeman AM, Barr SI, Green TJ, Xu Z, Innis SM, Kitts DD. Dietary Choline Intake: Current State of Knowledge Across the Life Cycle. Nutrients. 2018 Oct 16;10(10):1513.
Blusztajn JK, Slack BE, Mellott TJ. Neuroprotective Actions of Dietary Choline. Nutrients. 2017 Jul 28;9(8):815.
Dalla Via A., Gargari G., Taverniti V., Rondini G., Velardi I., Gambaro V., Visconti G.L., De Vitis V., Gardana C., Ragg E., et al. Urinary TMAO levels are associated with the taxonomic composition of the gut microbiota and with the choline TMA-lyase gene (cutC) harbored by enterobacteriaceae. Nutrients. 2020;12:62.
Bernhard W., Poets C.F., Franz A.R. Choline and choline-related nutrients in regular and preterm infant growth. Eur. J. Nutr. 2019;58:931–945.
Chan M.M., Yang X., Wang H., Saaoud F., Sun Y., Fong D. The microbial metabolite trimethylamine N-oxide links vascular dysfunctions and the autoimmune disease rheumatoid arthritis. Nutrients. 2019;11:1821.

谷禾健康
刚过去的九九重阳节,唤起了我们对“长长久久”的生命期盼,这是根植于我们文化深处的向往。而今我们期盼的,不再只是生命时钟的不断前行,更是那份长长久久的能够自由行走、清晰思考、感受生活美好的“生命质量”。
衰老,正是稀释生命质量、为晚年带来挑战的关键因素。因此,理解衰老、干预衰老,让每一段生命都充满活力,成为了比单纯追求“长久”更重要的时代课题。

为何同龄人中,有些人看起来精力充沛、容光焕发,而另一些人却似乎被岁月过早地刻上了痕迹?
当看到市面上琳琅满目的NMN、NAD+补充剂,或是主打“肠道健康”的益生菌时,是否也曾好奇:这些宣称能“逆转时光”的产品,其背后真正的科学逻辑是什么?
…
衰老是一个每个人都无法回避的自然的生物学过程,包括基本生理功能的逐渐衰退和进行性衰老。随着年龄的增长,衰老加速,导致细胞内损伤积累,增加年龄相关疾病的易感性。衰老影响每个人,但对每个人影响的程度不同。
近年来,科学界已经逐步确定了一系列导致细胞、组织和整个生物体衰老的生物学过程,这些被扩展到包括衰老的十四个关键标志。它们包括基因组不稳定性、端粒磨损、表观遗传改变、蛋白质稳态丧失、细胞自噬失能、营养感应失调、线粒体功能障碍、细胞衰老、细胞外基质变化、干细胞耗竭、细胞间通讯改变、慢性炎症、菌群失调、心理-社会隔离。
这些特征为理解衰老过程提供了一个基本框架,并且相互之间有着深刻的联系。其中,免疫力下降、肠道菌群失衡和慢性炎症这三个因素相互影响,形成了一个加速衰老的恶性循环。简单来说,肠道不健康会削弱免疫功能,免疫力差又会让肠道问题更严重,最终导致全身慢性炎症,而这种炎症正是心脏病、糖尿病、老年痴呆和癌症等多种年龄相关疾病的共同土壤。
在这个复杂系统中,饮食营养扮演了连接环境、肠道与宿主免疫的中心枢纽角色。因此,我们的餐盘实质上成为了调控自身衰老速度和健康轨迹的“遥控器”。饮食中的每一个选择,都在向这个复杂的“微生物-免疫-炎症”网络发送信号,或促进平衡与修复,或加剧失调与衰败。
传统的营养学常常聚焦于维生素、矿物质等已知营养素。然而,前沿科学发现,食物中还存在大量曾被忽视的“营养暗物质”,如植物化学物质、多酚等。它们虽非传统必需营养素,却在调节健康、对抗衰老中扮演着至关重要的角色。
例如,石榴中的鞣花单宁,需要经过特定肠道微生物的代谢,才能转化为近来在抗衰老市场备受追捧的尿石素A(Urolithin A),后者已被证明能有效清除衰老线粒体,恢复细胞活力。这完美诠释了饮食、微生物和抗衰老之间的精妙联系。
在这些复杂联系之外,现代AI技术正为我们提供了系统化解决方案。目前,人工智能驱动的精准饮食干预将海量的多组学数据转化为可操作的饮食建议,通过分析生物年龄较高或较低人群的数据,机器学习模型能够识别出哪些特定的饮食模式、食物来源的信号分子或肠道菌群特征是“减速”或“加速”衰老的关键驱动因素。最终,可以为个体量身定制饮食方案。
本文将带您深入这一前沿领域,探讨肠道菌群失调与免疫衰老之间如何形成恶性循环,并共同催生“炎症衰老”,我们将了解各种干预方式,是如何成为打破这一循环、调控我们衰老速度的强大工具。
随着年龄增长,我们常常感觉身体变得更脆弱了:更容易感冒,伤口愈合得更慢,恢复得也更吃力。这背后一个很重要的原因,就是我们身体内部的免疫系统发生了变化。免疫力的衰退,即免疫衰老,是衰老过程中的一个核心环节。
这种变化主要体现在两个方面:
衰老过程中先天与适应性免疫系统的变化共同导向炎症性衰老状态
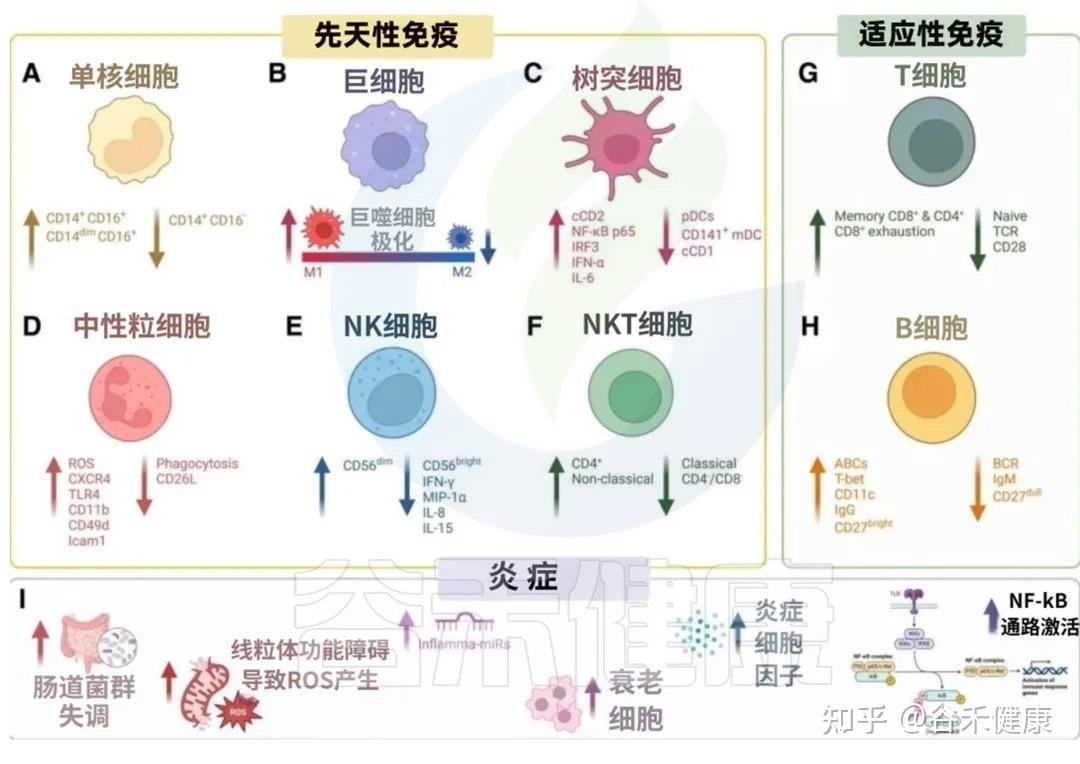
我们来看看衰老是如何影响我们免疫军队的两大核心分支的:先天免疫系统和后天免疫系统。
先天免疫是我们与生俱来的、快速反应的防御系统,是抵御病原体的第一道防线。但随着衰老,这支部队的效率和精确性都大打折扣。
这种功能失调的背后,涉及多种免疫细胞的变化。以下,我们将首先探讨先天免疫系统在衰老过程中的具体改变。
单核细胞:平衡 ➜ 促炎(经典型↓ 中间型、非经典型↑)
从单核细胞看炎症体质的形成:为什么你会感觉身体总在发炎?
在年轻健康时,单核细胞在血液中循环,一旦机体出现感染或损伤,便会迅速赶往炎症部位,并在此分化为巨噬细胞或树突状细胞。单核细胞还能吞噬病原体,并分泌信号分子,精细调控炎症反应。
根据细胞表面的蛋白标志物,人类单核细胞大致可分为三种主要表型:
▸ 衰老带来的失衡
研究表明,衰老导致:
值得注意的是,血液中单核细胞的总数通常保持稳定,这说明衰老的影响主要体现在细胞亚群的功能重塑上,而非数量变化。
▸ 这会带来什么后果?
这种细胞亚型的转变,意味着体内能高效分泌促炎因子的细胞群体增多,这直接助长了“炎症衰老”的慢性炎症状态,并削弱了机体有效修复损伤的能力。
你可能在体检报告上看到高敏C反应蛋白(hs-CRP)的指标,该指标升高往往与体内促炎单核细胞数量或活性增加、持续释放炎症因子有关。hs‑CRP 被视为心血管疾病等多种慢性病的风险预警信号。
巨噬细胞:平衡 ➜ 促炎( M1型↑ M2型↓ )
如果说单核细胞是血液中的巡逻兵,那么巨噬细胞就是驻扎在身体各组织(如皮肤、肝脏、大脑)里的多功能兵。巨噬细胞源自血液中的单核细胞,是处理局部问题的专家。
巨噬细胞的核心在于其“按需切换”的能力,主要有两种工作模式:
注:这里只是为了便于理解简化了,实际上巨噬细胞的极化是一个连续光谱(受多种细胞因子、代谢状态和组织微环境共同调控),往往呈现混合或中间表型,而非仅在两极之间来回切换。
在年轻健康的身体里,这两种模式的切换是及时且高效的。
▸ 衰老带来的失衡
衰老使巨噬细胞的平衡向促炎的M1型偏移。
▸ 这会带来什么后果?
伤口愈合变慢,组织修复能力下降
因为负责修复重建的M2型模式减少,所以在出现损伤(如割伤、手术后)时,组织的愈合过程会变得缓慢且不充分,更容易形成疤痕。
体内垃圾堆积,加速衰老进程
巨噬细胞的一个关键职责是吞噬并清除体内的“垃圾”,比如衰老的细胞和细胞碎片。尽管炎症信号增强,但吞噬与清理能力下降,功能失衡加剧。这导致衰老细胞无法被及时清除,它们在组织中不断累积,并释放更多炎症物质,形成一个“促炎-衰老细胞累积-更促炎”的恶性循环。
可能带来动脉粥样硬化
在血管壁中,功能失调的M1型巨噬细胞会疯狂吞噬胆固醇,但又无法有效代谢,最终变成充满脂质的泡沫细胞。这些泡沫细胞大量堆积,正是形成动脉粥样硬化斑块、导致血管堵塞的核心原因。
这削弱了它们有效召集其他免疫援军,并启动高效免疫反应的能力,进一步维持了体内的炎症状态。
树突状细胞:免疫反应启动效率下降
这些问题的答案,均指向了免疫系统中一个关键角色——树突状细胞(DCs) 的功能衰退。
树突状细胞是功能最强的抗原呈递细胞,重要职责是:
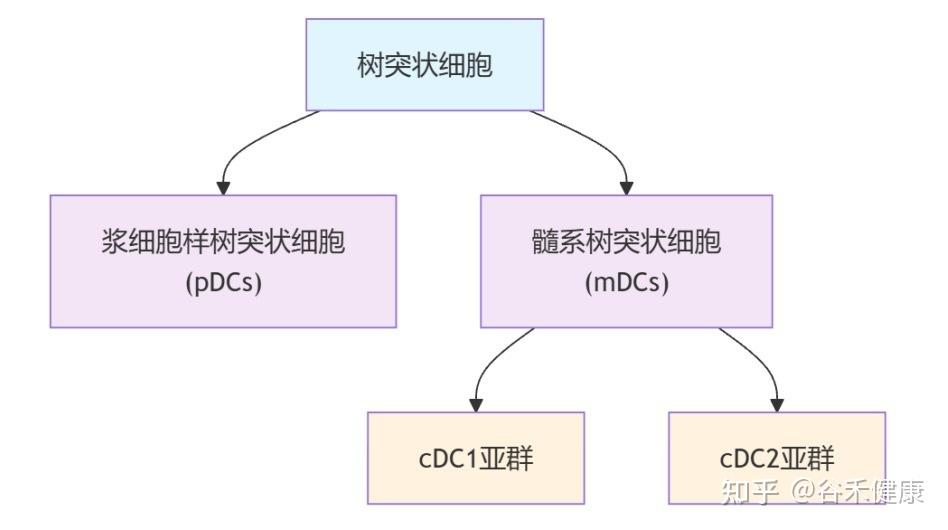
这其中,有一类名为 cDC1 的树突状细胞亚群,是专门负责激活T细胞的,T细胞是消灭病毒和肿瘤细胞的主力。
▸ 衰老影响这些DC亚群的组成和功能
关键指挥官cDC1 数量锐减:研究证实,体内负责激活抗病毒和抗肿瘤反应的 cDC1 细胞数量会显著减少。
剩余部队反应迟钝:剩下的树突状细胞,其呈报敌情的效率也大打折扣,激活T细胞的能力下降。
▸ 这会带来什么后果?
肿瘤和病毒的可乘之机
cDC1的减少,直接导致免疫系统的日常“巡逻监控”能力下降。体内的癌变细胞或潜伏的病毒(如导致带状疱疹的水痘-带状疱疹病毒)更不容易被及时发现和清除,从而大大增加了患癌和机会性感染的风险。
现代肿瘤治疗中的免疫疗法,其核心策略之一,就是想方设法重新激活这条“树突状细胞-T细胞”的攻击轴线。
加剧慢性炎症
这些功能失调的树突状细胞,在“消极怠工”的同时,还会错误地释放更多促炎信号,为身体的“炎症衰老”状态火上浇油。
树突状细胞功能的衰退,让我们在面对病毒和肿瘤时,免疫系统的启动速度和反应强度都打了折扣。
中性粒细胞:低效杀敌 + 高效自伤
中性粒细胞是免疫系统中的“快速反应部队”,一旦有病菌入侵,它们最先到达现场,通过吞噬、释放杀菌物质(如ROS,活性氧)等方式消灭病原体。
年轻时,它们是高效的杀手。但衰老后,它们的功能变得非常矛盾和具有破坏性。
▸ 衰老带来的变化
杀敌能力下降:它们吞噬病菌的效率变低了,用来捕捉病菌的“网”(NETs)也造得又少又差。这直接导致它们无法有效清除病原体,让小的感染迟迟不好,甚至恶化。
无差别攻击增强:虽然杀菌效率变差,但它们释放的化学武器——活性氧(ROS),却不减反增。ROS过度释放导致旁观细胞损伤和组织炎症,这正是“氧化应激”加剧的核心原因之一。
▸ 这对你的健康意味着什么?
这种“低效杀敌 + 高效自伤”的模式,让人在年老后,更容易发生组织损伤和慢性炎症,关节炎、血管损伤等都与这种失控的氧化应激有关。
这就是为什么“抗氧化”是抗衰老领域永恒的热点。市面上流行的维生素C、维生素E、富含多酚的食物等,其核心作用之一就是帮助身体中和这些过量的、由衰老免疫细胞产生ROS,从而减少对自身的伤害。
NK细胞:癌症巡逻减少
NK细胞,即“自然杀伤细胞”,是体内最警惕的“巡逻兵”,它们不需要预警,就能不停地识别并清除癌变细胞和病毒感染细胞。
▸ 衰老带来的变化
随着年龄增长,NK细胞的数量和组成都在变化:
“精锐”减少:NK细胞中功能最强、反应最迅速的“精锐亚群”(CD56亮细胞)数量下降。
“普通”功能下降:虽然细胞总数可能没变少,但整体战斗力和沟通能力都大幅下滑。它们在发现敌人后,释放的求援信号(如干扰素IFN-γ)显著减少,无法有效召集其他免疫细胞协同作战。
“后勤补给”被切断:维持NK细胞生长和活力的关键因子IL-15水平下降,相当于断了粮草,使其功能进一步衰退。
▸ 这对健康意味着什么?
是老年人健康最大的隐患之一。
癌症风险显著增加
免疫系统对早期癌细胞的监控和“清除”能力下降,给了癌细胞潜伏和发展的可乘之机。
病毒感染更易发生
对潜伏病毒(如引起带状疱疹的病毒)的压制力减弱,更容易导致病毒再激活和发病。
NK细胞因其在癌症预防和抗衰老中的巨大潜力,已成为再生医学和细胞治疗领域的绝对明星。
近年来,NK细胞疗法备受追捧,无论是通过体外扩增回输自体NK细胞,还是异体NK细胞产品,都旨在补充和激活这支重要的免疫力量。
据市场分析,全球NK细胞疗法市场预计在未来十年将以超过40%的年复合增长率高速发展,显示出巨大的市场潜力和消费者关注度。
我们的免疫系统分为两支主要部队:一支是反应迅速、指哪打哪的“特种部队”(后天免疫系统),另一支是冲锋在前、快速反应的“先锋部队”(先天免疫系统)。随着年龄增长,这两支部队都会出现不同程度的老化。
T细胞:精英特种兵 ➜ 疲惫老兵
T细胞是免疫系统中负责精准打击和长期记忆的核心战斗力。其中,
针对T细胞的免疫疗法是现代医学的重大突破,尤其是在癌症治疗领域(如CAR-T疗法)。在抗衰老领域,如何清除衰老的T细胞、恢复T细胞“新兵”的多样性,是前沿研究的核心。
▸ 新兵来源枯竭:免疫系统的“兵工厂”关闭了
T细胞的“训练营”是我们的胸腺。胸腺在年轻时非常活跃,源源不断地培养出充满活力、能识别各种新敌人的“新兵”(幼稚T细胞)。
但随着年龄增长,胸腺会严重萎缩,被脂肪取代。结果就是,“新兵”补充几乎断绝,我们识别和对抗全新病毒(比如新型流感病毒)的能力大幅下降。
▸ 老兵开始消极怠工
由于没有新兵补充,军队里只剩下了身经百战的老兵(记忆T细胞)。更糟糕的是,其中一部分老兵因常年作战而变得衰老和耗竭。它们不仅战斗力锐减,无法有效增殖去打仗,还会在体内释放大量“煽风点火”的炎症信号,成为慢性炎症的主要推手。
因此,“胸腺再生”已成为抗衰老领域的前沿探索方向之一。
再生思路:利用 iPSC(诱导多能干细胞)或胸腺组织工程技术,在体外或体内重建功能性胸腺,恢复或提升 T 细胞生成能力。
前沿:已有公司(如 Tolerance Bio)获得数千万美元融资,开展胸腺再生的临床前/临床研究;早期临床试验报告显示参与者的表观遗传年龄出现显著下降,提示胸腺再生可能对抗免疫衰老具有潜在价值。
B细胞:产能不足、武器型号单一
B细胞,是免疫系统的“抗体军工厂”,负责生产能够精准锁定并中和病原体的“导弹”——抗体,是我们获得长期免疫力的核心。
市场上的“抗体水平检测”服务,无论是针对新冠病毒还是其他病原体,其本质就是检测B细胞“军工厂”的工作成果。
随着年龄增长,这家军工厂不仅生产效率下降,更可怕的是,它开始生产出一批危险的“叛乱分子”。
▸ 衰老带来的变化
出现“叛乱分子”:危险的“年龄相关B细胞”(ABCs)崛起,具有极强的破坏性:
▸ 这对你的健康意味着什么?
自身免疫病风险剧增
许多自身免疫病,如类风湿性关节炎、干燥综合征、红斑狼疮,都在中老年时期高发或加重?这背后的一个关键推手,就是不断增多的ABCs细胞。它们产生的“错误抗体”攻击我们自身的关节、腺体乃至全身器官,导致了持续的疼痛和炎症。
抗体生产线僵化,难以应对新威胁
健康的免疫反应,在遇到新敌人时,会先迅速生产一批“通用型”的先锋抗体(IgM)来应急,然后再生产更精准、更持久的“定制型”主力抗体(IgG)。
衰老的B细胞系统彻底打乱了这个节奏:
这就是为何老年人接种流感或新冠疫苗后,产生的保护效果往往不如年轻人。他们的“抗体军工厂”已经失去了快速创新和应对新挑战的能力。
鉴于ABCs在自身免疫病和免疫衰老中的核心破坏作用,它们已成为药物研发的重点靶标。科学家们正在全力研究如何能精准地清除这些叛乱细胞,或抑制它们的活性,从而恢复免疫系统的正常秩序。
抗衰老前沿:研究者正探索通过 JAK‑STAT 抑制剂、代谢调控(如二甲双胍)或靶向 T‑bet/CD11c 等方式降低 ABCs 的频率或功能,以恢复更健康的 B 细胞谱系,提升老年免疫应答和疫苗效果。
如果说免疫系统是身体的“军队”,那么肠道菌群就是栖息在我们体内的、数量庞大的“盟友”与“潜在敌人”的复杂的生态系统,这对我们的健康至关重要,而它的构成也并非一成不变。随着年龄的增长,我们内在的微生物世界正在经历一场深刻的演替。
肠道菌群:随生命历程动态变化的生态系统
我们的肠道菌群从出生那一刻起就开始构建,并在3-4岁时基本成型,这个早期阶段的“地基”对一生影响深远。
婴儿期(奠定基础)
肠道菌群的“地基”搭建。新生儿的肠道以有益的双歧杆菌为主导,这对早期免疫系统的建立至关重要。
成年期(成熟稳定)
随着饮食日益多样化,细菌的种类和复杂性不断增加,而真菌的多样性则趋于减少。到成年时,菌群结构基本成型并进入一个相对稳定的阶段,主要由厚壁菌门和拟杆菌门两大类细菌主导。尽管宏观结构相似,但每个成年人的菌群构成都是独一无二的,如同指纹一般。
从婴儿到百岁老人,肠道微生物的组成和多样性在不同生命阶段呈现动态变化
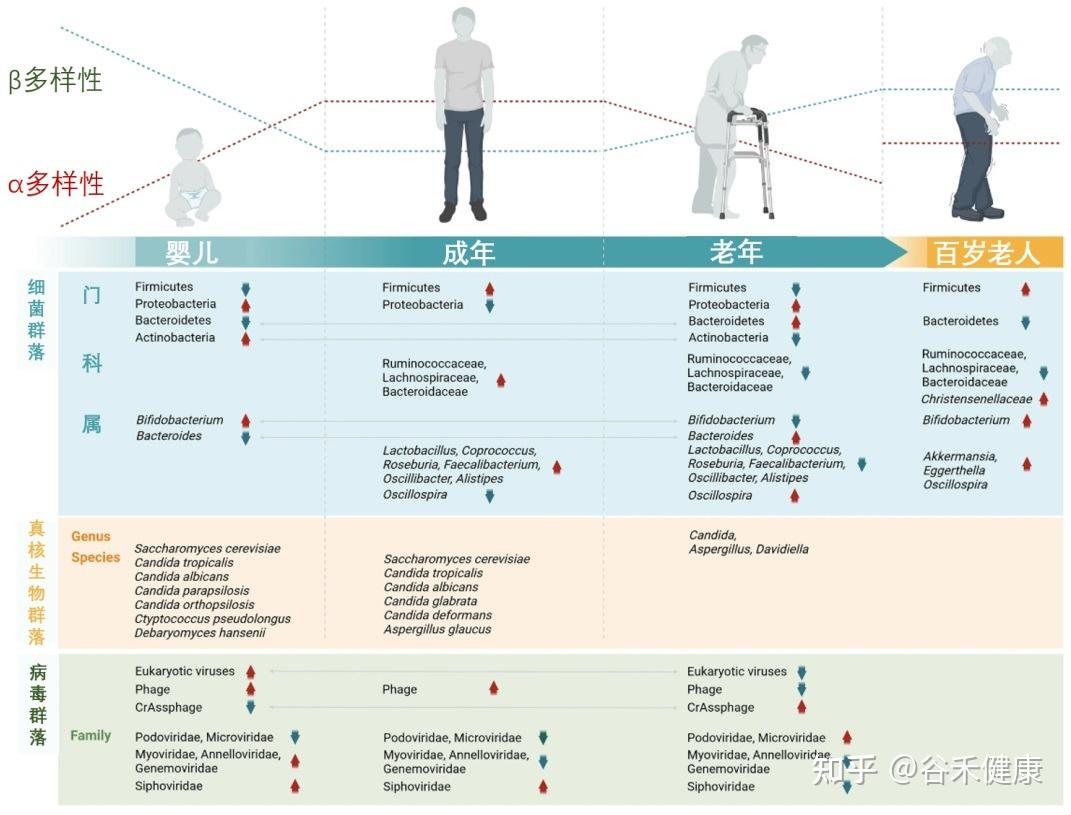
衰老带来的关键转变:生态系统的失衡
随着年龄增长,这个稳定的生态系统开始出现显著的、通常是负面的变化,这一过程被称为“微生物群落老化”。
有益菌的流失,有害菌的增多
多样性降低:如同一个健康的森林退化成单一树种的林场,肠道菌群的总多样性下降,使其变得更加脆弱。
有益菌减少:对我们有益的细菌,如双歧杆菌 和乳杆菌属,数量显著下降。
有害菌增多:与此同时,一些具有促炎特性的“机会致病菌”开始占据优势,如变形菌门等,它们会持续地刺激免疫系统,导致全身性的低度炎症。
从青壮年(22-48岁)到准超级百岁老人(105-109岁)的进程中,一个显著的标志是:
关键功能的丧失:短链脂肪酸的减产
衰老菌群最核心的变化之一,是能够发酵膳食纤维并产短链脂肪酸的细菌大幅减少。
短链脂肪酸(如丁酸盐)是维持肠道健康和调节免疫的基石:它们为肠道壁细胞提供能量,维持肠道屏障的完整性,并能直接向免疫细胞发送“保持冷静”的信号。它们的减少,是肠道功能衰退的关键标志。
长寿的线索:从百岁老人的菌群中学习
随着全球老龄化的加速,研究越来越集中于理解生命晚期的微生物演替,以预测与衰老相关的疾病特征并促进健康老龄化。
有趣的是,研究发现健康长寿的老人(如百岁老人)的肠道菌群并未完全遵循上述的衰退轨迹。相反,它们展现出一些独特的“年轻化”特征:
与老年人(66-85岁)相比,他们的肠道菌群保留了更高的多样性,生态依然丰富。
在他们的肠道中富含长寿菌群,几种被认为与健康和长寿相关的细菌丰度更高,例如:
这些传统的有益菌在他们体内依然维持着高水平。

解密|肠道菌群与健康长寿7 赞同 · 0 评论 文章
“生物群落老化”:衰弱与菌群失调的关联
身体衰弱表现为精力差、活动少、体重减轻、肌肉流失的老年人,与特定的菌群失调模式相关。
研究发现,高衰弱评分的老年人,其肠道中特定的共生菌群,如Coprococcus eutactus、Prevotella copri等耗尽,而一些潜在有害菌,如Clostridium hathewayi,脆弱拟杆菌Bacteroides fragilis等则占据优势。
以下肠道菌群数量增加与衰老相关,并被认为是高衰弱评分的特征,包括:
这些微生物的转变与代谢改变密切相关,包括短链脂肪酸和色氨酸减少,以及苏氨酸、疏水性次级胆汁酸(石胆酸和脱氧胆酸)、三甲胺氧化物(TMAO)、对甲酚、乙醇和氨的增加。同时,依赖于果糖和木寡糖的关键纤维发酵菌群趋于减少。
总之,这些发现支持了“生物群落老化”机制,即微生物多样性减少,其特征是机会性/促炎微生物的增加和共生/有益成员的减少,与加速衰老和增加的衰弱有关。
肠道-免疫轴:菌群如何影响全身衰老
肠道菌群并非孤立地影响健康,它通过“肠道-免疫轴”与我们的免疫系统进行着持续而复杂的对话,直接影响着全身的衰老进程。
衰老的一个核心特征是炎症性衰老(Inflammaging)——一种长期、低度的全身性炎症状态。而肠道菌群失调,是点燃和助推炎症的关键因素之一,从而加剧炎症性衰老。
短链脂肪酸
众所周知,肠道菌群产生的短链脂肪酸(SCFAs)是重要的信号分子,能调节免疫细胞的分化和功能。
饮食中纤维缺乏会导致SCFA合成减少,进而导致黏蛋白降解菌增多,肠道黏液层变薄,屏障功能受损,促炎细胞因子(IL-33和IL-25)增多,最终引发更强的炎症反应。
色氨酸
另一个例子是色氨酸,它是一种由微生物衍生的代谢物,也是一种必需氨基酸。它的代谢产物对于维持肠道稳态至关重要。
在临床前的老年小鼠模型中,缺乏色氨酸的饮食会诱发肠道菌群失调并促进炎症性衰老。
这些机制表明,一个“健康”或“年轻”的微生物组,能够通过抑制慢性炎症和维持肠道屏障,在抵抗细胞衰老和炎症性衰老中发挥关键的抗衰老作用。
我们已经知道,衰老的肠道菌群呈现出多样性降低和功能失调的特征。但一个关键问题是:这种菌群失调究竟是衰老过程的果,还是驱动衰老的因?
越来越多的证据表明,这很可能是一个双向的恶性循环,而多种与年龄相关的因素共同推动了这个循环的加速。
以炎症性衰老为核心,这种系统性的低度慢性炎症状态,通过与宿主免疫系统的紧密互动,导致肠道微生物组的失调。反之,失调的菌群又会加剧炎症。而多种外部和内部因素,则像催化剂一样,不断加剧这个循环。

外部:生活方式与医疗因素的冲击
多种药物的使用
老年人常因多种慢性病而服用多种药物。许多非抗生素药物,如质子泵抑制剂、二甲双胍、非甾体抗炎药等,都会严重影响肠道菌群的组成和多样性。
它们可能引起食欲变化、口干(导致唾液酶分泌减少)和特定营养素吸收不良,共同塑造了一个不利于有益菌生长的环境。
营养不良与饮食改变
随着年龄增长,味觉和嗅觉减退、牙口问题、食欲下降等因素,常导致老年人饮食结构单一,特别是膳食纤维摄入量锐减。
纤维是许多有益肠道细菌(尤其是产短链脂肪酸的细菌)的主要“食粮”。纤维摄入不足,直接导致这些有益菌“挨饿”甚至消失,从而削弱了肠道屏障功能和抗炎能力。
缺乏体育锻炼与社交孤立
这些因素也被证明与肠道菌群多样性降低和不良健康状况相关,它们通过影响激素水平、应激反应和整体代谢,间接塑造了肠道微生态。
内部:消化系统自身的生理性衰退
随着年龄增长,我们消化系统本身的衰老,也在悄然改变着肠道菌群的生存环境。
胃肠道动力减弱
随着年龄增长,肠道蠕动和结肠转运功能减慢,容易导致便秘、腹胀等问题。食物残渣在肠道内停留时间过长,会改变发酵模式,可能有利于腐败菌的生长。
此外,肠神经系统(ENS)中神经元的退化也加剧了这一问题。
消化液分泌减少
注:胆囊逐渐对介导饱腹感的肽类激素——胆囊收缩素变得不敏感,导致其在血浆中的水平升高。这种被抑制的胆囊收缩素功能会逐渐导致食欲/饥饿感下降和食物摄入量减少,并促进老年人的营养不良,所有这些都会逐渐减少对维生素合成、能量代谢和免疫功能至关重要的有益肠道微生物。
有趣的是,百岁老人能产生独特的具有抗菌特性的次级胆汁酸(例如,石胆酸的独特异构体),是一种正向适应,这可能是他们维持肠道稳态的秘诀之一。
而在普通老年人中,失调的次级胆汁酸(如脱氧胆酸及其甘氨酸或牛磺酸结合形式)则与阿尔茨海默病等衰老相关疾病有关。

什么是胆汁酸,其与肠道微生物互作如何影响人体健康18 赞同 · 0 评论 文章

肠道微生物群对胆汁酸代谢和信号传导影响的最新研究成果20 赞同 · 1 评论 文章
肠道自身的衰老
肠上皮细胞(IECs)的更新能力随着年龄增长而下降。肠道干细胞耗竭,导致组织再生和愈合能力减弱。
衰老的肠上皮细胞和杯状细胞(负责分泌黏液)功能下降,导致保护性的黏液层变薄,肠道通透性增加(即“肠漏”),使得细菌及其产物(如LPS)更容易进入血液,引发全身性炎症。
最终后果:“肠道-器官轴”通讯中断
肠道并非一个孤岛,它通过免疫、神经、内分泌和代谢等多种途径,与我们全身所有器官(包括大脑、心脏、肝脏等)构成了一个复杂的双向通信网络。
肠道菌群正是这个网络中的关键,它们合成和调节着无数的信号分子,如:
当肠道菌群失调时,这个通信网络便会中断或充满错误信号。有益减少,有害增多,这种混乱的沟通状态,最终会体现在全身性的功能障碍上,包括免疫失调、心血管问题和认知能力下降等。
总结来说,肠道菌群的健康与否,直接关系到整个身体的衰老轨迹。它既是衰老过程的反映,也是一个可以主动干预、用以延缓衰老和促进老年健康的潜在靶点。
既然我们已经认识到肠道菌群在衰老过程中的重要地位,那么我们能否通过主动干预肠道菌群,来延缓衰老、促进健康长寿?答案是肯定的。
靶向肠道微生态的治疗干预措施,从生态失调中恢复生态平衡(稳态),不仅有望改善肠道健康,而且有望通过减轻年龄相关疾病促进整体健康和健康衰老和长寿。
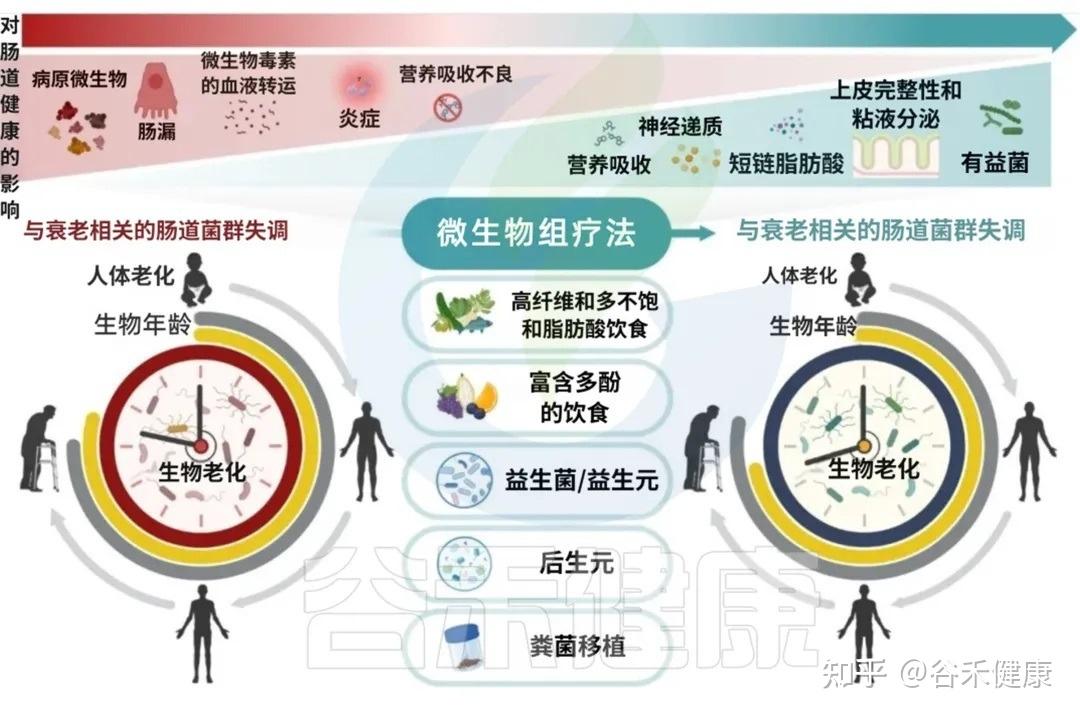
在所有影响肠道菌群的因素中,饮食是核心角色之一。尽管生理性的衰老不可避免,但大量短期、长期的饮食干预研究已证明,通过调整饮食,我们拥有巨大的潜力来延缓衰老的进程。
饮食如何塑造我们的衰老轨迹?
工业革命以来,人类的饮食结构发生了剧变,这种变化的速度远远超过了我们基因的适应速度。然而,我们的肠道微生物凭借其极短的代际时间迅速适应,从而演化出了由饮食、年龄、地理和健康状况共同塑造的高度个体化菌群。
下图清晰地展示了饮食对衰老轨迹的深远影响
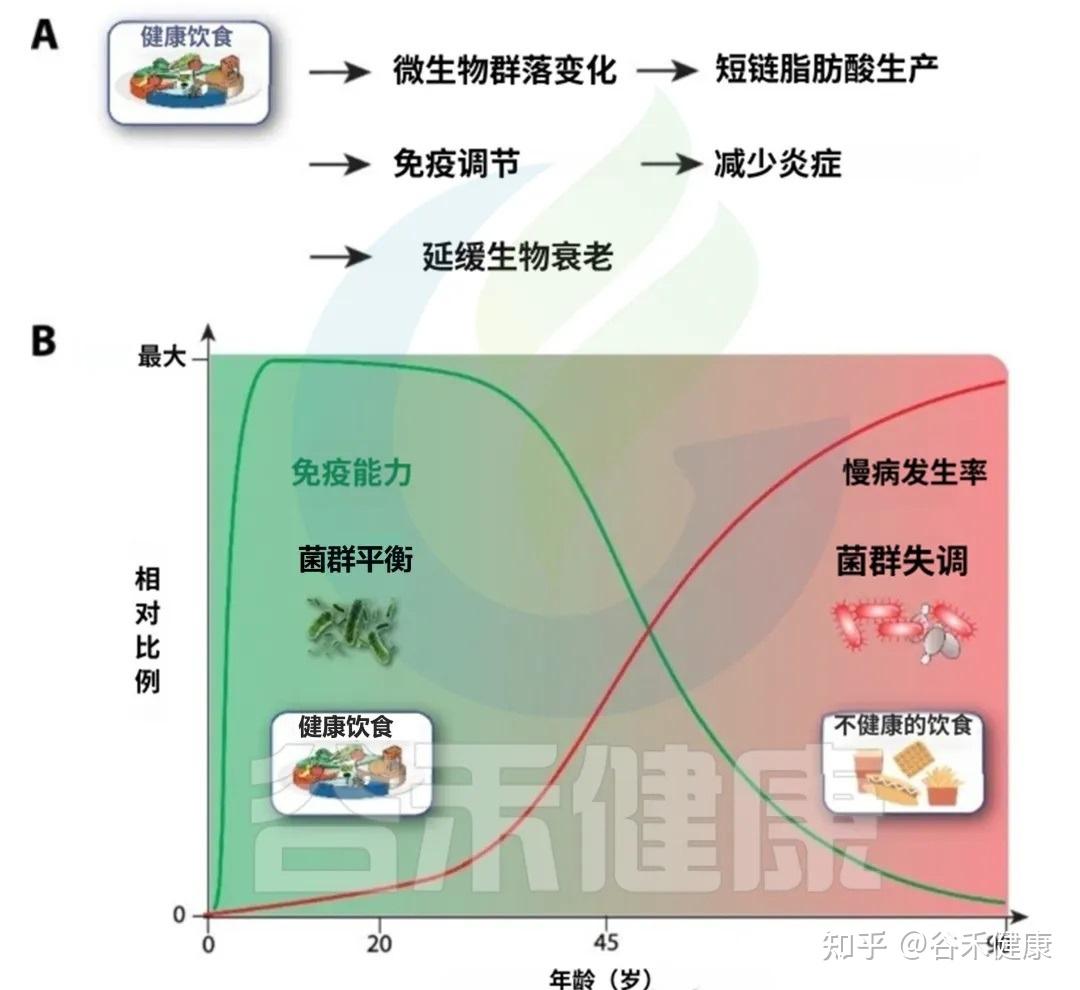
A健康的饮食促进有益的微生物群转变,增强短链脂肪酸的产生,调节免疫反应,并减少慢性低度炎症。这些效应共同导致生物衰老的延迟。
B免疫能力和非传染性疾病发病率与饮食质量的年龄相关轨迹示意图。早期坚持健康的饮食支持生态良好和强大的免疫功能(绿色曲线),而不健康的饮食与生态失调,炎症增加、随着时间的推移慢性病(NCD)负担增加有关(红色曲线)。
中年时期是一个关键的“十字路口”,此时的饮食选择将在很大程度上决定你未来,是走向健康的A路径,还是加速衰老的B路径。
地中海饮食:经过验证的减轻老年衰弱
一项长期、大规模的长期临床研究发现(注册号 NCT01754012),遵循地中海饮食模式与显著降低老年人的衰弱风险密切相关。
其背后的机制正是通过调节肠道菌群:这种饮食模式能有效增加有益菌的丰度,例如:
同时抑制与2型糖尿病、结直肠癌等疾病相关的潜在有害菌,例如:
改良地中海-生酮饮食(MkD):保护大脑功能
在针对轻度认知障碍老年人的研究中,改良的地中海-生酮饮食展现出显著的神经保护效果。其作用路径同样是通过肠道菌群:
高脂饮食:警惕坏脂肪,加剧炎症与菌群失调
近年来,老年人的饮食模式趋向于减少纤维、增加脂肪摄入。这会对衰老产生显著的负面影响。
促炎效应
高脂饮食会显著增加脂肪组织中的促炎因子(如TNF-α)和单核细胞趋化蛋白-1(MCP-1)的水平,并促使免疫细胞(巨噬细胞)向更具攻击性的M1型极化,加剧肝脏等器官的炎症。
破坏肠道菌群
高脂饮食会增加厚壁菌门的丰度(与炎症正相关),同时减少产丁酸菌,如瘤胃球菌科等。这会削弱肠道屏障的紧密连接,增加“肠漏”风险。
关键区别:并非所有脂肪都是有害的。
Omega-6多不饱和脂肪酸:通常具有促炎作用。
Omega-3多不饱和脂肪酸:如鱼油、亚麻籽油中的ALA,则具有明确的抗炎作用。
Omega-3能增加菌群多样性,促进双歧杆菌等有益菌的生长,减少肠杆菌,帮助改善肠道屏障功能,并增加有益的SCFA(富集产短链脂肪酸的毛螺菌科Lachnospiraceae)、减少有害的TMAO的产生。
控制总脂肪摄入并优化脂肪酸来源(尤其是增加Omega-3的比例),对于维护老年人的免疫健康和肠道稳态具有重要意义。
高蛋白饮食:复杂且需谨慎对待
高蛋白饮食对衰老的影响是复杂的,其效果因蛋白质的来源、数量以及个体的健康状况而异。
潜在益处:特定情境下的抗炎
在某些特定条件下,增加蛋白质摄入可能有助于抑制炎症。
例如,一项针对进行阻力训练的百名老年女性(60-90 岁)的研究发现,通过增加瘦红肉消费来提高蛋白质摄入的群体,其血浆中由运动引发的炎症标志物IL-6水平有所降低。这表明,在高蛋白饮食与规律运动相结合时,可能对控制炎症有积极作用。
潜在风险:促炎、免疫失衡、肠道菌群紊乱
——引发促炎反应与免疫失衡
多项研究将高蛋白饮食与促炎因子的升高联系起来。
在老年小鼠中,摄入全蛋白的高蛋白饮食会提高血浆中LPS、IL-6和IL-10的水平,而摄入水解蛋白则会额外增加TNF-α。表明高蛋白饮食,特别是当蛋白质未水解时,可能会在老年小鼠中引发更强烈的促炎反应。
此外,高蛋白、低碳水化合物的组合在老年大鼠中甚至表现出免疫抑制作用。
更为复杂的是,在一项结合了运动干预的研究中,富含Omega-3的高蛋白饮食反而导致了老年人体內具有抗炎作用的IL-10和IL-1Ra水平下降,这可能暗示着免疫调节机制的潜在紊乱。
——破坏肠道微生态与屏障功能
在老年女性中,高蛋白饮食与产丁酸菌的减少相关,而丁酸盐是维持肠道屏障功能和抑制炎症的关键短链脂肪酸,其减少可能导致肠道屏障受损。
动物实验也证实,摄入全蛋白的高蛋白饮食会破坏小鼠小肠的组织结构,减少保护性的杯状细胞数量,并导致链球菌(Streptococcus)等潜在有害菌增多,同时减少有益的双歧杆菌。
——产生有害代谢物
当蛋白质摄入过高(>1.6 g/kg体重/天)时,可能会导致肠道菌群发酵未被消化的蛋白质,产生有害代谢物。
例如,在老年男性中观察到,这种饮食模式与心血管疾病风险标志物——三甲胺氧化物(TMAO)的水平升高有关。虽然在大鼠中也观察到粪便乙酸盐水平的增加,但这同样可能源于蛋白质的异常发酵。
关键调节因素:蛋白质的“质”与“量”
蛋白质的类型(质)是决定其效果的关键。在上述破坏肠道结构的小鼠研究中,水解蛋白相较于全蛋白,显示出了截然不同的保护作用:它改善了小肠结构,增加了杯状细胞和有益的双歧杆菌,并减少了致病菌。这提示我们,蛋白质的消化吸收效率可能直接影响其对肠道健康的作用。
►▷
虽然高蛋白饮食近年来越发流行,但现有数据提示我们需谨慎对待,尤其是在老年群体中。当前的饮食指南建议将蛋白质摄入量限制在1.0-1.2 g/kg体重/天,并保证充足的碳水化合物摄入,这或许是避免潜在风险、维持免疫和肠道稳态的更为稳妥的策略。未来的研究需进一步阐明这些复杂的相互作用,以制定更精准的老年营养建议。
高纤维饮食:抗衰老,滋养有益菌,抑制炎症
高纤维饮食对免疫系统和肠道菌群的有益影响是明确且显著的。然而,大多数老年人的纤维摄入量远低于推荐标准(女性 21 g/天;男性 30 g/天)。
抗炎作用
膳食纤维(特别是可溶性纤维,如菊粉)是肠道益生菌的“首选食物”。它们通过发酵纤维产生大量丁酸盐等短链脂肪酸,这些物质能有效抑制全身和大脑中的炎症反应。
减轻神经炎症
高纤维饮食带来的丁酸盐水平增加,已被证明能有效减少中枢神经系统中“小胶质细胞”的促炎细胞因子表达,从而改善与衰老相关的神经炎症。
在人类研究中,食用富含纤维的谷物与多种炎症标志物水平降低相关,特别是C反应蛋白(CRP)和IL-1Ra。然而,有趣的是,来自水果和蔬菜的纤维并未显示出同样的效果。这提示我们,纤维的来源(如可溶性 vs. 不溶性)、是否存在其他生物活性化合物、以及加工方式都可能影响其最终的生物学效应,亟需进一步研究。
改善肠道菌群
高纤维饮食对肠道菌群的组成有着显著的积极影响,能够促进有益菌群的生长。
一项针对中国老年群体的研究显示,高纤维饮食者的肠道中瘤胃球菌科的丰度更高,而拟杆菌目和毛螺菌科的丰度较低。该变化可能与地理或膳食差异有关,并非绝对不良。
另一项针对55-80岁人群的研究,增加菊粉摄入量与更高的微生物多样性相关,显著提升了以下菌群的丰度:双歧杆菌、Alistipes shahii、Anaerostipes hadrus、Parabacteroides distasonis。
影响的复杂性:纤维类型、宿主年龄与性别的交互作用
尽管高纤维饮食益处明确,但其具体效果并非一成不变,而是受到多种因素的复杂调节。
效果的非普遍性
一项老龄小鼠研究发现,虽然含2.5%菊粉的饮食通过增加双歧杆菌和粪杆菌属(Faecalibacterium),并增强丁酸盐产量来改变了肠道微生物组,但它并未减少不同年龄组间的菌群总体差异,也未能改善全身性炎症或肠道生理指标。这表明纤维的干预效果是特定的,而非全局性的。
年龄特异性
在另一项小鼠研究中,菊粉能够有效降低厚壁菌门与拟杆菌门的比例,但其对特定菌属的影响具有年龄特异性——在老年小鼠中,菊粉显著增加了双歧杆菌和拟杆菌属 的数量。
性别依赖性
近期一项利用人源化小鼠模型的研究,更清晰地揭示了菊粉作用的性别差异。
对两性的共同影响:
对雌性小鼠的更强影响:
对雄性小鼠的特定影响:
高纤维饮食是维持老年健康的关键策略,它能有效抑制炎症并优化肠道菌群。然而,其效果并非“一刀切”。纤维的来源、类型(如菊粉)、宿主的年龄乃至性别,都会影响其最终的生物学功能。在制定未来营养策略时,需考虑个体化因素,以便实现更精准、高效的健康干预。
这提示我们,餐桌或许是最日常却最深远的抗衰老实验场。
色氨酸
讲究最佳剂量
色氨酸,一种必需氨基酸,在人体的应激反应、心理健康及炎症调节中扮演着核心角色。
色氨酸有几种饮食来源,包括:燕麦,香蕉,干梅子,牛奶,金枪鱼,奶酪,面包,鸡肉,花生等。
在衰老背景下,色氨酸对免疫系统和肠道微生物组的影响尤为复杂,呈现出显著的“剂量依赖性”,即适量摄入是关键。
核心机制:犬尿氨酸途径与免疫衰老
色氨酸的免疫调节功能主要通过犬尿氨酸途径实现。在衰老过程中,体内的慢性炎症会激活此通路中的关键酶(IDO),导致一系列的连锁反应,最终可能加速免疫系统的衰老。
具体而言,在该途径中,超过95%的游离色氨酸被关键的限速酶——吲哚胺-2,3-双加氧酶(IDO)所降解,产生犬尿氨酸及其下游代谢物。这些代谢物不仅参与调节免疫功能,还是合成烟酰胺腺嘌呤二核苷酸(NAD+)的前体。
衰老过程本身伴随着慢性低度炎症,这会提高IDO酶的活性。IDO活性增强导致犬尿氨酸/色氨酸比率升高,进而激活芳烃受体(AhR)信号通路。该通路通过上调Foxp3,增加Treg的活化,最终促进胸腺退化和细胞衰老,这一过程被称为免疫衰老。
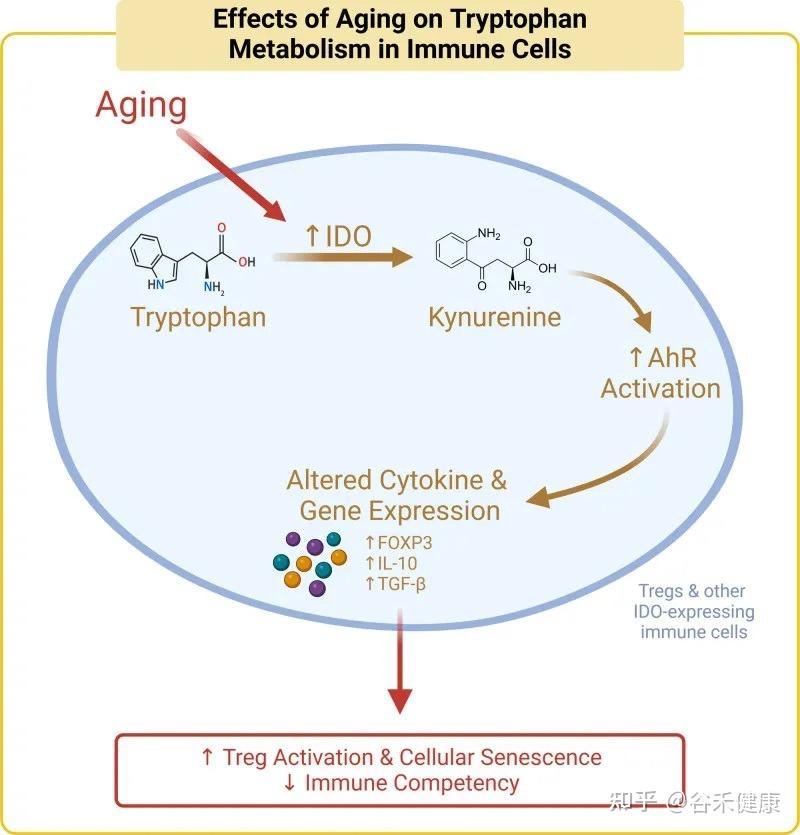
剂量决定效果:色氨酸摄入量的三重效应
关于色氨酸的摄入,研究揭示了一个非常关键的原则:并非越多越好,而是存在一个最佳窗口。
➦ 摄入过少(缺乏):加剧炎症与菌群失调
衰老本身就与小鼠体内色氨酸及其关键代谢物——吲哚的水平下降有关。在此基础上,色氨酸缺乏会进一步恶化健康状况。
一项针对老年小鼠的研究显示,与正常补充(0.2%)相比,缺乏色氨酸的饮食会导致促炎细胞因子IL-6、IL-17A和IL-1α显著增加,同时抗炎因子IL-27水平降低。
肠道微生物组也发生剧烈变化,包括下列菌群丰度均发生改变:
➦ 摄入适中,带来显著益处(最佳窗口)
一项老年小鼠研究中,摄入中等水平的色氨酸(占饮食的0.4%)显示出多重益处。这种饮食模式显著降低了潜在有害菌群的相对丰度,如丹毒丝菌属 (Erysipelatoclostridium)、肠球菌属(Enterococcus) 、Dubosiella菌属。
与此同时,它促进了有益菌的生长:
➦ 摄入过量,产生毒性,弊大于利
“越多越好”的原则在这里并不适用。摄入更高水平的色氨酸(占饮食的0.8%)则会加剧肠道黏膜屏障的损伤、氧化应激、炎症反应、严重的肠道菌群失调。
►▷
综上所述,色氨酸在衰老中的作用极为精准,呈现“剂量依赖性”。它不仅通过犬尿氨酸途径调控免疫,其摄入量还深刻影响肠道菌群与全身炎症。研究表明,存在一个有益的“最佳窗口”(如0.4%的补充),而缺乏或过量摄入均可能损害老年机体。这凸显了对色氨酸等营养素采取精准营养策略的必要性,未来的研究也应扩展至蛋氨酸、支链氨基酸等,以构建更全面的老年营养支持体系。

色氨酸代谢与肠内外健康稳态37 赞同 · 2 评论 文章
Omega-3 脂肪酸:强大的抗炎剂
Omega-3脂肪酸作为一类重要的多不饱和脂肪酸(PUFA),主要来源于鱼类、海鲜、坚果、种子和某些植物油。然而老年人群的Omega-3摄入量却常常低于最佳水平。大量研究证实,Omega-3脂肪酸具有强大的抗炎潜力,是维持衰老过程中免疫稳态的关键。
调节炎症介质产生
Omega-3脂肪酸(包括其前体α-亚麻酸ALA,以及EPA和DHA)能够显著减少促炎性类二十烷酸(如前列腺素E2、白三烯B4和LTC4)的合成。
在一项针对老年大鼠的研究中,补充Omega-3同时降低了IL-1β、MCP-1和TNF-α等多种细胞因子的浓度。
平衡脂肪酸比例
炎症状态不仅取决于Omega-3的绝对量,也取决于其与Omega-6脂肪酸的比例。体内Omega-6与Omega-3的比例过高,会直接导致TNF-α和IL-6等促炎细胞因子水平升高。
影响细胞功能与信号通路
Omega-3能直接影响免疫细胞的功能,包括调节白细胞活性和T细胞的发育。
在老年人的骨骼肌中,富含Omega-3的饮食被证明可以减少促炎细胞因子IL-1β的表达,并抑制mTOR(哺乳动物雷帕霉素靶蛋白)信号通路,从而减轻局部炎症和调节细胞代谢。
通过肠道微生物组介导
在人类中,Omega-3摄入被证实能通过改善肠道微生物组来抵消由肥胖引起的炎症和代谢紊乱。这种菌群改变有助于减少促炎性的循环脂多糖(LPS)水平,并抑制下游的NF-κB炎症信号通路。
协同效应:与生活方式干预结合效果更佳
Omega-3的抗炎效果可以与其他健康干预措施产生协同效应。
研究表明,在肥胖的绝经后女性中,虽然单独补充Omega-3或进行减肥都能降低体内的促炎因子水平,但当Omega-3补充剂与超过10%的体重减轻相结合时,其抗炎效果最为显著。
►▷
提高老年人Omega-3的摄入量,并将其与健康的生活方式(如体重管理)相结合,是抑制慢性低度炎症、维持免疫稳态的有效策略。

探索Omega-3脂肪酸:健康益处与营养补充12 赞同 · 0 评论 文章
膳食多酚:与菌群合作
膳食多酚:与菌群合作
多酚广泛存在于植物性食物中,如蓝莓、葡萄、可可、绿茶、苹果等。它们以强大的抗氧化和抗炎能力而闻名。在预防多种慢性疾病中显示出巨大潜力。
然而,其真正的抗衰老潜力并非通过直接吸收,而是通过与肠道菌群的复杂互动来“解锁”的。
核心机制:肠道菌群是多酚发挥作用的关键中介
由于其化学结构复杂且常常被糖基化,它们在小肠中的直接吸收率非常有限。但这恰恰成为了它们发挥更深远作用的起点。
大量未被吸收的多酚会到达大肠,成为肠道菌群的理想底物,并在此引发双重有益效应。
——直接作为养料,促进有益菌的生长
例如,研究证实,富含花青素和原花青素B2的饮食能够在衰老啮齿动物模型中,显著增加对肠道健康至关重要的产丁酸菌的丰度。
——代谢活化与菌群重塑
肠道菌群在享用多酚的同时,会将其分解代谢为一系列生物活性更强、更易被人体吸收的小分子代谢物。这个过程不仅激活了多酚的抗炎和抗氧化潜力,同时代谢过程本身及其产物还能温和地抑制有害菌,从而优化整个肠道菌群的结构。
多酚与益生菌的协同抗衰老效应
多项研究为肠道介导这一机制提供了有力证据,并揭示了多酚与益生菌之间的协同作用。
——减轻炎症性衰老
一项针对50岁及以上成年人的研究发现,在富含多酚的饮食基础上额外补充特定的益生菌,能够有效减轻慢性低度炎症,同时受试者肠道中的有益菌和短链脂肪酸水平也得到显著提升。
——传统补品的现代诠释
富含抗氧化物的传统草药——红参,其抗衰老效果同样与肠道菌群密切相关。它不仅能直接对抗氧化应激,还能促进有益菌的生长,并通过菌群代谢活动来强化肠道屏障功能。
更值得注意的是,当红参经过特定益生菌发酵后,其抗衰老特性得到显著增强。这归因于抗氧化相关基因的上调和对肠道菌群更有效的积极调节。
我们吃的食物不仅仅是在填饱肚子,更是在喂养体内的亿万微生物。通过多吃富含多酚的彩色果蔬和选择红参等天然补品,我们就能和肠道菌群打好配合,让它们帮我们把食物中的营养变成抗衰老的利器,实现从肠道到全身的健康。

肠道微生物群与膳食多酚互作对人体健康的影响30 赞同 · 3 评论 文章

多酚等膳食成分与肠道菌群协同作用可以更好地改善骨质疏松症3 赞同 · 1 评论 文章
益生菌干预的核心是直接向肠道输送特定的有益微生物,以实现靶向健康效益。
——改善大脑健康与情绪(调节肠-脑轴)
临床研究也证实,通过益生菌干预提高肠道中普拉梭菌(Faecalibacterium prausnitzii) 的水平,与焦虑、抑郁等神经精神症状的改善密切相关。
——强化肠道屏障,抑制全身性炎症
下一代益生菌:巨大潜力
研究的焦点正从传统的乳杆菌属和双歧杆菌属,扩展到一些新发现的、潜力巨大的肠道共生菌,它们被称为“下一代益生菌”。
其他潜力菌株也备受关注:

AKK菌——下一代有益菌21 赞同 · 0 评论 文章
通过精准干预肠道,我们可以恢复其稳态,进而增强免疫、改善代谢,并有效对抗衰老。益生元和合生元构成了这一策略的核心工具箱,它们在衰老的肠道环境中展现出显著的积极作用。
益生元:喂养有益菌
益生元是为有益肠道菌群提供营养的“食物”(如膳食纤维、低聚半乳糖GOS),为整个生态系统的健康奠定基础。
低聚半乳糖 (GOS) 是其中的典型代表,它来源于豆类、乳制品等。研究证实,补充GOS能够:
研究发现,补充GOS可以通过增强食糖细菌及其相关酶(β-半乳糖苷酶)的丰度,来改善肠道上皮完整性和粘液产生,从而调节衰老肠道的稳态。
合生元:益生菌与益生元的“强强联合”
一项临床研究报告称,老年女性在摄入名为MPRO3的合生元产品(由多种益生菌和膳食纤维组成)后,其血液代谢物谱、肠道菌群和整体肠道健康均得到积极调节。
后生元:更安全、更精准的有益物质
后生元是一个新兴且极具潜力的领域。它指的是“源自微生物的有益物质”,包括无活性的菌体、菌体碎片(如细胞壁)或细菌的代谢产物。
后生元的优势在于更稳定、更安全,因为它不涉及活菌的定植问题,而是直接提供发挥功效的“最终产物”。
——菌体成分
热灭活的益生菌(如副干酪乳杆菌)的细胞壁成分脂磷壁酸 (LTA),被证实能直接抑制炎症信号(NF-κB),同时促进黏液分泌,修复肠漏。
——代谢产物
这是指由微生物产生或将膳食成分转化而来的、具有健康效益的小分子物质。
在衰老模型中,它能通过下调 HMGB1-TLR4-NF-κB 炎症通路、减轻氧化应激并积极调节肠道菌群,来全面改善肠道功能。
——无活性的菌体
即便是完整但无活性的微生物,也能通过其细胞结构与人体免疫系统等发生互作,产生健康效益,这种方式被称为“幽灵效应”。
经过间歇灭菌(也称为廷德尔灭菌法)(一种温和加热灭活法)处理的长双歧杆菌(B.longum) 和嗜酸乳杆菌 (L. acidophilus) 菌株,在与运动干预相结合时,展现出改善阿尔茨海默病(AD)病理的潜力。其机制包括:
最终效果:减少大脑中淀粉样蛋白-β的聚集。
►▷
微生物的健康效应,并非完全依赖于其活性。
后生元绕开了活菌在储存、运输和定植中的不确定性,为开发更安全、更稳定、靶点更明确的新型疗法或辅助保健品铺平了道路。未来,后生元也将成为防治衰老疾病的重要途径。
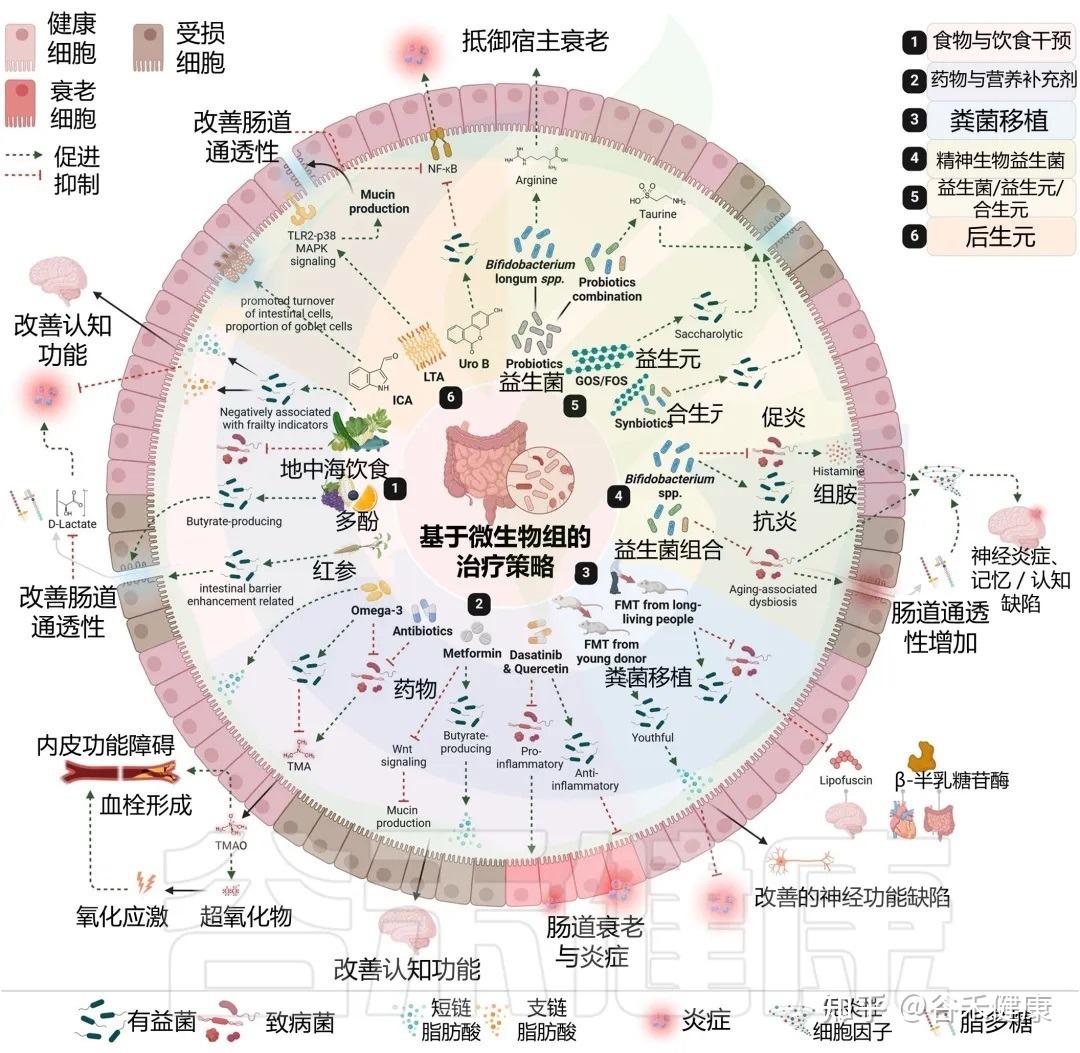
许多我们熟知的药物和膳食补充剂,其作用并非仅仅是简单的化学分子与人体细胞的直接互动。它们的抗衰老等多效性作用,在很大程度上是通过与肠道菌群的复杂“对话”和“合作”来实现的。
药物干预:从直接靶点到微生物介导
案例一:二甲双胍—— 经典的生物转化
作为一线降糖药,二甲双胍的益处远超血糖控制。最近的研究证明,肠道微生物组对其进行了关键的生物转化。
在老年小鼠中,二甲双胍治疗通过抑制Wnt信号通路,增强了肠道粘蛋白的产生,这一由菌群介导的过程最终对神经认知功能产生了积极影响。这表明,没有微生物组的参与,二甲双胍的某些重要功效可能无法完全发挥。
案例二:衰老细胞清除药物—— 协同调节
特定的“衰老细胞清除”药物(如达沙替尼和槲皮素),其作用也不再是单一的。研究表明,它们在清除体内衰老细胞的同时,还能主动调节肠道菌群——即促进抗炎微生物的生长,并抑制促炎微生物。
这一发现强烈暗示,这些前沿抗衰老药物的整体效果,至少部分是通过与肠道菌群的协同作用介导的,共同减少了肠道乃至全身的衰老和炎症。
膳食补充剂:菌群是关键中介
案例一:α-亚麻酸 (ALA) —— 清晰的微生物依赖途径
植物来源的ALA(一种Omega-3脂肪酸)的抗血栓效应,就是一个完美的例证。其作用并非直接,而是遵循一个清晰的微生物依赖路径:
案例二:NAD+抗衰老:肠道菌群的关键一环
补充烟酰胺单核苷酸(NMN)或烟酸(维生素B3)是目前流行的抗衰老策略,其核心机制是提升细胞内的NAD+水平。
研究发现,NMN也能通过调节肠道菌群来维持肠道稳态。鉴于肠道菌群拥有独特的酶来参与NAD+代谢,有理由推测,这类补充剂的抗衰老效果可能直接或间接地与肠道菌群的变化有关。

关于长寿因子(NAD+)你了解多少?——健康益处及如何提高补充效果6 赞同 · 1 评论 文章
粪便微生物群移植(FMT)不再是补充单一菌株或代谢物,而是通过移植一个完整的、健康的微生物生态系统,来彻底重置和改造宿主的肠道环境。
这一新兴策略正从治疗特定肠道疾病(如复发性艰难梭菌感染、IBS、克罗恩病等)的成功案例中,迈向一个更宏大的目标:促进健康衰老与延长寿命。
核心证据:从肠道到大脑的系统性年轻化
大量的临床前和临床研究表明,FMT的益处远不止于肠道本身,它能沿着“肠-脑轴”向上影响,实现系统性的抗衰老效果。
未来展望:建立“长寿菌群”生物样本库
FMT的潜力上限,取决于捐赠者菌群的质量。
关键发现:研究已证实,将长寿老年捐赠者(如百岁老人)的粪菌移植到小鼠体内,可以通过引入有益的细菌及其代谢物,有效改善受体的各项衰老相关指标。
基于这些证据,系统性地探索使用健康、长寿的捐赠者来建立一个特征明确的FMT生物样本库,可能为减轻与衰老相关的健康损害,提供一条有效的治疗途径。

粪菌移植——一种治疗人体疾病的新型疗法7 赞同 · 2 评论 文章
力量训练
中到高强度的抗阻训练,建议每周2-3次。训练强度通常设定在个人最大重复次数(1-RM)的60-85%之间,每个动作进行1-3组,每组重复8-12次。
例如,使用壶铃(一种具有特殊形状握把的重量,配有专门的训练方案)进行 8 周训练,可以改善与肌肉减少症和低度炎症相关的指标。
这种训练能够有效调节体内的微小核糖核酸(miRNAs)。它能抑制促进肌肉萎缩的miRNA,同时激活促进肌肉合成与生长的miRNA,从而打破肌肉流失的恶性循环,实现肌肉质量和力量的维持与增长,有效延缓衰老过程中的身体功能衰退。
高强度间歇训练 (HIIT) vs. 中等强度持续训练(MICT)
研究发现:两者对老年人的肠道菌群和肌肉功能有不同的调节效果。微生物组分析显示,HIIT组α多样性增加,并富集了产短链脂肪酸菌(如 Faecalibacterium prausnitzii),MICT组与多样性稳定和双歧杆菌适度增加相关。
HIIT在提升心肺功能和认知控制能力方面更优;而MICT则对改善情绪(心理健康)和帮助坚持运动更有利。
注:HIIT-涉及短时间高强度运动和短暂休息或低强度运动交替进行。MICT-中等强度持续一段时间的运动(如慢跑、骑行)。
瑜伽
一个为期12周的瑜伽项目,结合了体式、呼吸技巧和冥想,证实了其对阿尔茨海默病患者和其照护者的双重益处。
瑜伽是一种实用、经济的辅助方法,其成功也暗示了其他身心活动在延缓衰老相关疾病方面的潜力。
太极、有氧运动、八段锦
对于膝骨关节炎患者,这几种运动在减轻疼痛和改善身体功能方面的效果相当。
研究发现,太极能在12周内显著改善患者的疼痛管理(依据WOMAC量表评估)、姿势稳定性及功能性活动能力。
►▷
总的来说,老年人保持规律的活动总量(不一定要某种特定类型的运动或强度),能有效改善血管健康。 核心在于“动起来”,任何形式的规律运动都有益于心血管健康,不必过分纠结于某一种特定的运动方式。
要真正运用好肠道菌群来调节或延缓衰者,我们需要更强大、更智能的工具来指引方向。
从海量数据到精准洞察:AI与多组学的力量
我们的身体是一个极其复杂的系统。基因(基因组学)、代谢产物(代谢组学)、肠道菌群(微生物组学)……这些“多组学”数据共同交织,决定了我们的健康轨迹。在过去,我们很难看清这背后的规律。
而现在通过大数据可以整合分析这些不同维度的数据,帮助我们回答那个最核心的问题:在衰老过程中,究竟是哪些菌群、哪些营养分子,起到关键作用。
精准干预的前提:找到一把好的“衰老标尺”
要想知道我们的干预措施是否有效,首先需要一把能够精确测量“生物学年龄”的标尺。这个“标尺”就是衰老生物标志物。
根据国际性的衰老生物标志物联盟提出的全面框架,一把理想的“衰老标尺”必须满足六个关键维度:
可行性、有效性、懂机制、
适用广、反应灵敏、成本可控
换言之,一把好的“衰老标尺”,必须用得起、测得准、看得懂机制、适用广…幸运的是,最新的技术进展,特别是肠道菌群和免疫衰老的生物标志物,正为我们提供了构建这把“标尺”的强大工具。
精准营养时代:告别“一刀切”的健康建议
“精准营养”的最终目标,是根据每个人的独特性,提供量身定制的健康方案。
这意味着,通过对你个人的基因、代谢和肠道菌群进行综合检测,我们能知道,为什么对你有效的维生素D₃,对他来说可能Omega-3脂肪酸更重要。
一句话总结:我们已经推开了“通过调节菌群来抗衰老”这扇大门,但门后的世界依然充满未知。未来的研究方向很明确:通过更大规模的全球合作和更长时间的跟踪研究,全面揭示不同肠道菌群模式与健康衰老之间的内在联系,从而找到最精准、最个性化的方法,让每个人都能通过管理好自己的肠道菌群,实现更长久、更健康的生命。
抗衰老不应被视为与自然规律的对抗
而是一种与生命节奏的和谐共舞。
人间万事,生命最为宝贵;
生命长短,质量至关重要。
掌握科学的抗衰老智慧,
倾听肠道菌群等身体信号,
活出自己生命的最佳状态。
注:本账号内容仅作交流参考,不作为诊断及医疗依据。