 国家高新企业 | ISO9001认证
国家高新企业 | ISO9001认证 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康

一听到高脂饮食,很多人就会想到会增加患心脏病和其他慢性疾病的风险。然而,低碳水化合物、高脂肪的生酮饮食却在各个方面越来越受欢迎,从减肥到自身免疫疾病等。
生酮饮食的支持者认为,通过减少碳水化合物的摄入,可以帮助控制血糖和胰岛素水平,从而降低患糖尿病和肥胖的风险。甚至有人选择生酮饮食是为了提高生产力、精力和思维清晰度。
一些研究表明,生酮饮食可能会对肠道健康产生积极影响,如减少肠道炎症、改善肠道通透性和促进有益菌群的生长。然而,也有研究认为生酮饮食会减少肠道菌群多样性,可能引发代谢紊乱等情况,这是为什么呢?
这些研究之间是否相互矛盾?
许多人对这种饮食方法可能对肠道及肠道微生物组健康产生的影响有担忧。
有一种普遍的观念认为,唯一能为有益肠道微生物提供营养的物质是复合碳水化合物,如果我们没有膳食纤维,我们的肠道屏障也会受到影响。
但事实真的如此吗?
生酮饮食真的会给肠道带来很大危害吗?
生酮饮食对肠道菌群的影响是快速的吗?
生酮饮食中的高脂肪不会增加LPS吸收吗?
为什么说生酮饮食对一些疾病具有保护作用?
生酮饮食到底是促炎多还是抗炎多?
什么人群更适合生酮饮食呢?
……
在本文中,我们将深入探讨生酮饮食对肠道健康的影响,并对证据进行完整的讨论,包括目前知道什么和不知道什么,更全面地了解这种饮食方法,可以更好地选择适合自己的饮食方式。

我们与肠道微生物的关系是数千代共同进化的产物。数百万年来,进化不仅作用于我们 23,000 个人类基因,还作用于我们体内和体表的近 400 万个基因(包括人类和微生物)。之所以成为今天的我们,是因为我们是与微生物一起进化的。
什么是代谢灵活性?
我们进化的环境需要定期适应不断变化的条件。我们的祖先并不能总是稳定地获得食物,当食物匮乏时,他们会偶尔禁食。因此,当食物充足时,我们的身体有能力燃烧和使用碳水化合物,而当食物或碳水化合物稀缺时,我们的身体有能力将膳食脂肪或储存的身体脂肪转化为酮以获取能量。这种根据饮食摄入量变化而改变新陈代谢的能力称为代谢灵活性。
那么问题来了:为什么我们的身体具有代谢灵活性来应对食物供应的变化,而我们的肠道微生物群却没有同样的代谢灵活性?
当淀粉类碳水化合物变得稀缺时,我们的祖先真的会产生“患病”的微生物组吗?
不一定。
我们可以考虑一下因纽特人等传统文化。
因此,所谓“健康”微生物组,就是你个人健康时所拥有的微生物组,对你来说健康的东西可能对其他人来说并不健康。
打个比方,选择任意两个人,平均而言,他们只会分享大约三分之一的肠道微生物群。另外三分之二的肠道菌群将因遗传、地理位置、抗生素和药物使用史、出生方式、饮食以及其他未知的因素而存在显著差异。没有足够的信息来证明一个人的“三分之二”比另一个人的“三分之二”更好。
我们在肠道菌群检测的时候,并不能以单一的指标去武断地认为这个人就是不健康,而是要结合他自身其他指标来综合判断是否需要采取某些干预措施。
我们继续来看研究数据。
很多项研究表明,给动物喂养“高脂肪饮食”会导致严重的肠道菌群失调、肠道通透性增加和全身炎症,表明高脂肪饮食可能对人类肠道微生物群不利。
不过仔细观察会发现,大多数动物研究中使用的“高脂肪饮食”,更准确地说是富含精炼大豆油、猪油和精制糖且纤维含量极低的饮食。
加州大学戴维斯分校教授 Craig Warden 博士称其为“相当于小鼠吃猪皮、排骨、可乐”。换句话说,经典的动物“高脂肪饮食”比任何精心设计的生酮饮食更能反映标准美国饮食换句话说,典型的动物“高脂肪饮食”其实更多地反映了标准西方饮食,而不是精心设计的生酮饮食。
进化来说:人易适应高脂饮食,小鼠适应低脂
低碳饮食下,经过基因筛选的小鼠容易代谢紊乱
最常用于此类研究的小鼠品系 C57Bl/6 小鼠经过基因筛选,因其能够响应“高脂肪饮食”而增加体重和升高血糖。
Richard Feinman 等人写道:
“结果表明,肥胖的啮齿动物模型,在理解代谢机制如何以与人类效应不同的方式工作方面可能最有价值。”
因此,我们不能简单地将针对经过选择性育种、喂食高度精炼“高脂肪饮食”的小鼠的研究结果,直接应用到具有健康意识的人类身上,这是对基础科学的严重误解。
那么,我们来看看人类研究。
2014 年在《自然》杂志上发表了一项研究,研究人员让健康的人类志愿者短期接受植物性饮食或动物性饮食。他们发现独特的肠道微生物群在短短三天内就出现了。
这是微生物组研究领域的一项开创性研究,自 2014 年以来已被引用超过 2700 次。其实这篇文章里面说的动物性饮食是生酮饮食。
– 植物性饮食每天包含 300 克来自谷物、蔬菜、大米、扁豆和水果的碳水化合物;
– 动物性饮食每天包含的碳水化合物少于 3 克,其中 30% 的热量来自蛋白质,70% 的热量来自蛋白质来自鸡蛋、肉和奶酪的脂肪。这种常量营养素比例与生酮饮食一致。研究人员甚至通过尿酮测量证实受试者在动物性饮食的第二天就处于酮症状态。
那么他们发现了什么?
动物性生酮饮食的参与者微生物α多样性没有变化。他们发现耐胆汁微生物相对丰度有所增加,如Bilophila、Alistipes、Bacteroides。已知代谢复杂膳食植物纤维的微生物的相对丰度减少,如Roseburia、Eubacterium rectale、 Ruminococcus bromii。
该文作者写道:
研究结果表明,人类肠道微生物组可以在草食性和肉食性功能特征之间快速切换,这可能反映了人类进化过程中过去的选择压力。
我们的祖先吃动物食品可能是不稳定的,依赖于季节和随机的觅食成功;
而现成的植物性食物提供了热量和营养的后备来源。微生物群落能够迅速、适当地改变其功能,以应对饮食变化,从而增强人类的饮食灵活性。
换句话说,我们的肠道微生物群只是在适应当前不同食物来源的可用性,它不一定会因饮食中碳水化合物或脂肪的数量而变得或多或少具有致病性。
注意:生酮饮食可能会加剧一些菌过度生长——稍后会详细介绍。
那么,更长期的研究呢?
2017 年《微生物学前沿》杂志上发表的一项研究检查了生酮饮食对 25 名多发性硬化症患者粪便微生物群的长期影响。
多发性硬化症 (MS) 是一种影响神经系统的自身免疫性疾病,与肠道病变有关。事实上,一些研究人员怀疑肠道菌群失调和肠道通透性可能先于自身免疫的发展。因此,如果生酮饮食可以显著改善多发性硬化症的症状,它可能不太会损害肠道,甚至可能改善肠道健康。
与健康个体相比,多发性硬化症患者在基线时的Roseburia、拟杆菌属和普拉梭菌属数量往往减少。然后他们进行了六个月的生酮饮食。
作者写道:
生酮饮食的影响是双向的。短期内,细菌浓度和多样性进一步降低。他们在第 12 周开始恢复,并在生酮饮食 23-24 周后显著超过基线值。
这表明,虽然短期饮食变化可以迅速改变肠道微生物群的组成,但我们可能需要关注长期饮食变化,并在多个时间点收集样本,以确定生酮饮食干预的真正效果。
最近发表的一项研究证实,生酮饮食可以改变肠道微生物群的结构和功能。

该小组招募了 17 名超重和肥胖男性参与研究的第一部分。让他们吃基线控制饮食四个星期,然后再吃四个星期规定的生酮饮食。生酮饮食最显着的变化是,几种双歧杆菌物种丰度的显著减少。
研究人员接下来对小鼠进行了控制喂养研究。相对于传统的高脂肪饮食,生酮小鼠饮食对肠道微生物组具有独特的影响,随着碳水化合物限制的增加,双歧杆菌的丰度减少。进一步的实验发现,生酮饮食或酮酯补充剂都会导致肠腔和结肠组织中β-羟基丁酸的增加。
酮体直接抑制双歧杆菌的生长
有趣的是,这与小肠 Th17 细胞的减少有关。Th17 细胞是T辅助细胞的一个亚群,可产生促炎细胞因子 IL-17,作为适应性免疫反应的一部分。这些细胞在维持肠粘膜屏障方面发挥着重要作用,并有助于清除粘膜表面的病原体。然而,Th17 细胞也与自身免疫和炎症性疾病有关,包括类风湿性关节炎、多发性硬化症和牛皮癣。
为了完善这个发现,他们将在基线饮食或生酮饮食期间收集的人类捐赠者的粪便,移植到无菌小鼠体内,以确定 Th17 细胞的变化是否依赖于酮诱导的微生物群变化。接受酮类微生物群的小鼠肠道 Th17 细胞显著降低。
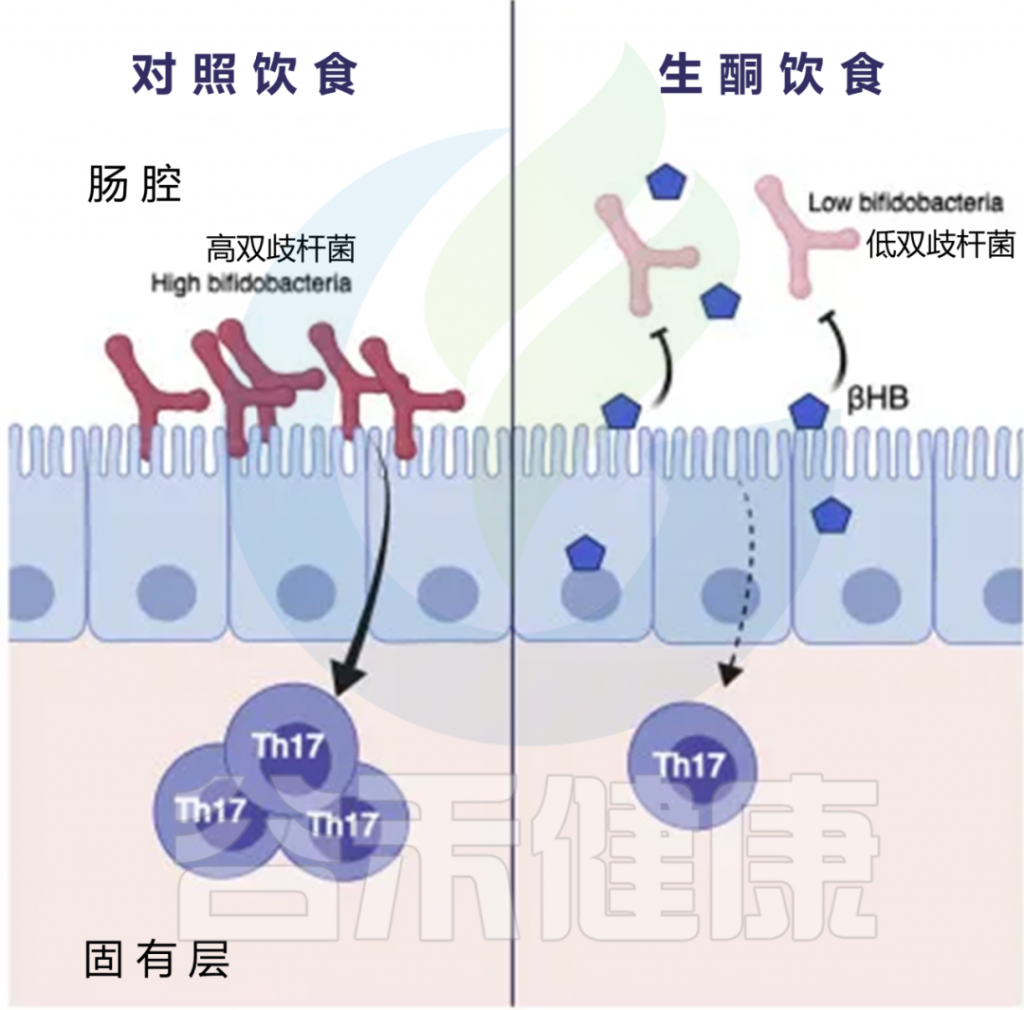
doi.org/10.1016/j.cell.2020.04.027
有趣的是,与生酮饮食相比,基线饮食的总体胆汁酸池没有变化。
生酮饮食不会破坏肠道粘液层
之前的研究表明,喂食无纤维饮食的小鼠结肠粘液层有显著破坏。然而,在生酮饮食中却没有看到这一点。
作者写道:
尽管缺乏可发酵碳水化合物,生酮饮食仍能保持强健的粘液层。
这是一个关键发现。低碳水化合物者可以放心,如果处于酮症状态,肠道粘液层可能不会破坏。生酮饮食不仅维持了粘液宽度,还维持了肠道粘液主要成分 Muc2 的表达。
我们现在已经在人类身上看到了大量关于生酮饮食引起肠道微生物组变化的证据,并且看到了生酮饮食如何影响小鼠的肠道微生物群和粘液层。
让我们看看其他一些设计良好的动物研究。
生酮饮食经常用于治疗对药物治疗无反应的癫痫症。虽然生酮饮食非常有效,但几十年来,生酮饮食到底如何给大脑活动带来好处仍然难以捉摸。
然而,Elaine Hsiao 团队于 2018 年 5 月在《细胞》杂志上发表的一项研究表明,生酮饮食对癫痫的有益作用是通过肠道微生物组介导的。换句话说,如果生酮饮食不能改变微生物群,它就不能有效预防癫痫发作。
这项研究是在小鼠癫痫模型中进行的。与之前的研究一样,他们能够证明给小鼠喂食生酮饮食可以保护它们免受癫痫发作。
然而,他们进一步证明,用广谱抗生素治疗小鼠会消除对癫痫发作的保护作用。同样,在无菌培养箱中饲养且没有肠道微生物组的无菌小鼠,即使在食用生酮饮食时也无法预防癫痫发作。
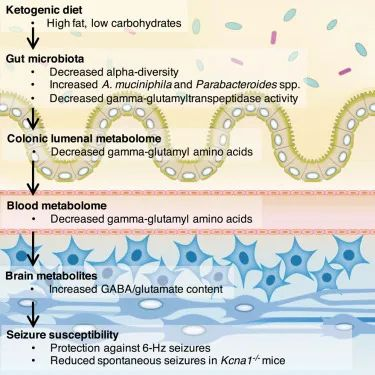
doi.org/10.1016/j.cell.2018.04.027
有趣的是,本研究中的生酮饮食降低了微生物多样性,但增加了Akkermansia muciniphila(简称AKK菌)和副拟杆菌(Parabacteroides)丰度。
扩展阅读:
研究人员想知道这两种微生物是否负责癫痫发作保护,并尝试用阿克曼氏菌和副杆菌来治疗喂食正常高碳水化合物食物的小鼠。令人惊讶的是,这可以防止癫痫发作。
进一步的机制实验发现了一条细菌途径,该途径提高了大脑中抑制性神经递质GABA与兴奋性神经递质谷氨酸的比例。GABA 可以镇静大脑的活动,因此这可以解释癫痫发作的减少,也可以解释为什么许多人发现生酮饮食有助于减少焦虑。
扩展阅读:
癫痫中的微生物群-肠-脑轴
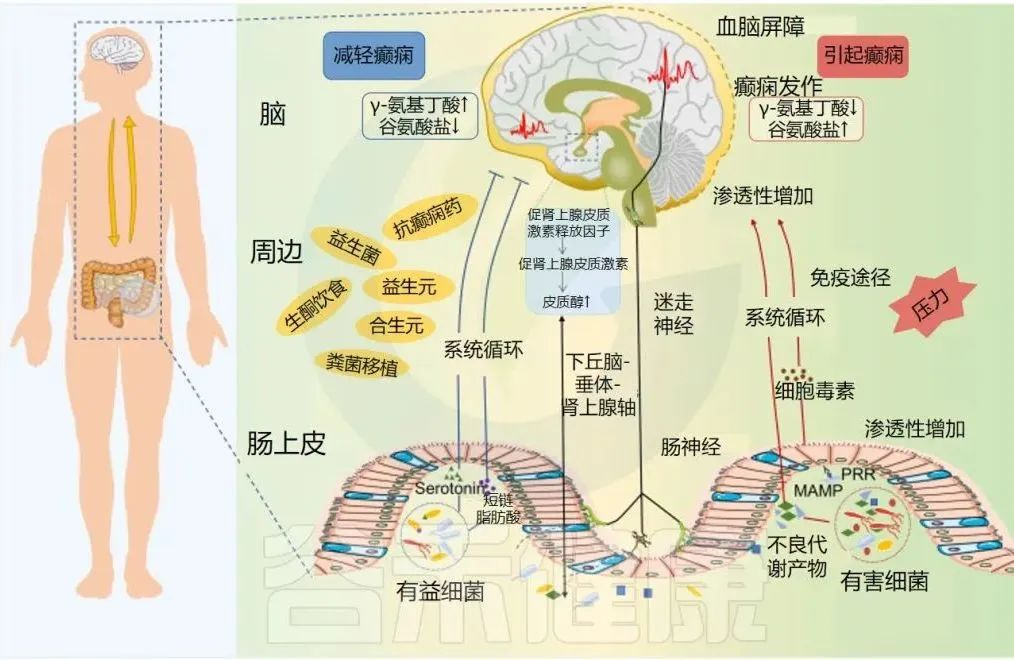
Ding M,et al.Front Immunol.2021
基于相关的人类和动物实验数据,我们深入探讨生酮饮食引起的肠道生理学变化的一些机制。
你可能会问,如果没有任何可发酵碳水化合物,肠道如何生存?
我们知道肠道细菌代谢复杂的碳水化合物,产生短链脂肪酸(SCFA),如乙酸盐、丙酸盐和丁酸盐。丁酸盐在肠道中具有重要的信号传导功能,并且是肠上皮细胞的首选燃料来源。已发表的研究表明,丁酸盐提供了结肠上皮细胞约 70% 的能量需求。
丁酸盐对免疫功能的调节作用
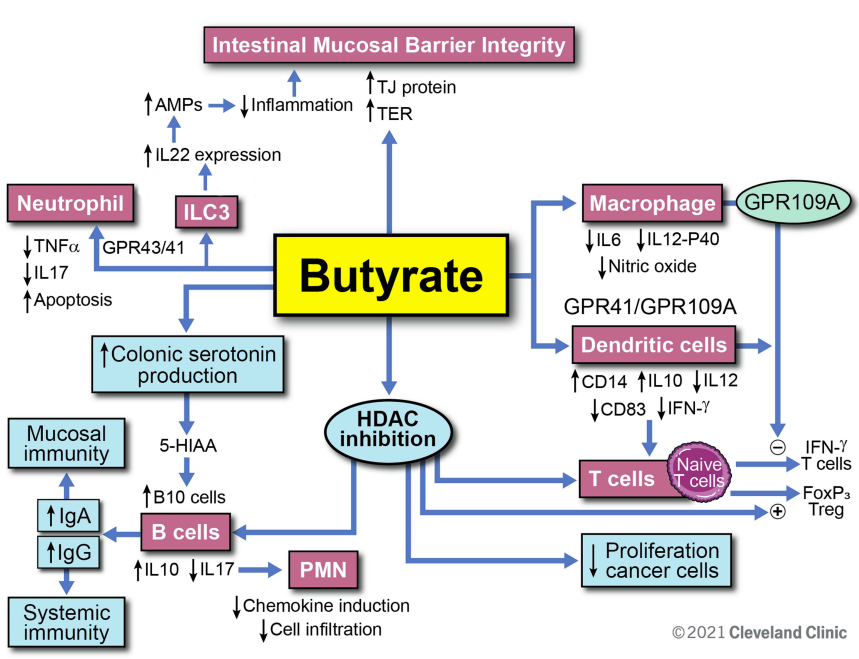
我们需要定期供应丁酸盐来维持肠道屏障功能吗?
不。事实证明,还有其他几种分子可以执行丁酸盐的许多信号传导功能,并作为肠上皮细胞的燃料来源。事实上,这种“首选”燃料来源的想法可能偏离了对食用大量碳水化合物的人(和啮齿动物)的研究。换句话说,生酮饮食中丁酸盐的产生可能会减少,但其他分子可以代替它来帮助维持肠道屏障功能。
扩展阅读:
有三种分子可以替代丁酸:异丁酸、乙酰乙酸、β-羟基丁酸。
异丁酸替代丁酸,刺激肠道受体
异丁酸是蛋白质发酵的代谢产物,其产生量通常低于丁酸。当丁酸较少时,异丁酸可以被肠上皮细胞从肠腔吸收并代谢为能量。前面提到的 2014 年研究发现,食用动物性生酮饮食的人类粪便异丁酸含量升高。
此外,异丁酸可以刺激肠道中与丁酸相同的受体(GPR41、GPR43和GPR109a),从而刺激粘液分泌、抗菌肽释放和免疫调节。
异丁酸浓度不足,效力来补
虽然中等高蛋白饮食中产生的异丁酸水平可能低于高碳水化合物饮食中产生的丁酸水平,但异丁酸已被证明是GPR41(FFAR3)的更强效刺激剂,这是丁酸的主要受体之一。换句话说,异丁酸在浓度上的不足,但在效力上可能弥补了这一不足。
乙酰乙酸 和 β-羟基丁酸 (βHB)
是肝脏产生的两种主要酮体。与丁酸盐一样,βHB 也可以刺激 GPR109a,减少肠道炎症。然而,最值得注意的是,βHB 和乙酰乙酸都是丁酸代谢途径中的中间体。
换句话说,当丁酸盐被肠道上皮细胞吸收时,它实际上首先转化为βHB,然后转化为乙酰乙酸,然后进一步分解为能量。参考下图:
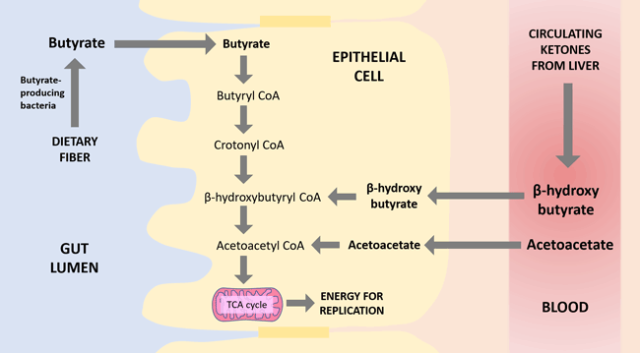
编辑
已知肠道上皮细胞在基底外侧表面(最靠近血流的细胞一侧)表达单羧酸转运蛋白 MCT1 。MCT1 可以转运酮,并且特别在使用酮体获取能量的细胞中表达。几篇论文表明,肠道上皮细胞确实能够利用血管床中的酮体。
酮体与丁酸盐在肠道健康中的角色
使用酮代替丁酸盐的能力可能看起来没有优势,但考虑到许多肠道发炎的人都存在粘膜损伤,丁酸盐的吸收受损。
那么这意味着什么呢?如果你有一个健康的微生物群和肠黏膜,丁酸可能足以应对你肠道的所有需求,不需要酮体。
但是,如果你:
尝试治疗性营养生酮来支持肠道上皮细胞代谢,至少在治疗潜在的肠道病理和治愈肠道粘膜之前是这样。
生酮饮食在治疗肠道疾病中的应用
可惜,很少有研究是针对克罗恩病、溃疡性结肠炎或肠易激综合症的生酮饮食。
一份病例报告发现,旧石器时代的生酮饮食使一名患有严重克罗恩病的小男孩完全缓解。
第二份病例报告发现,补充酮酯的低碳水化合物饮食可显著减少克罗恩病患者的炎症并提高生活质量。
另一项针对 13 名腹泻型肠易激综合征 (IBS-D) 患者的研究发现,10 名患者在 4 周生酮饮食期间症状得到缓解。

有趣的是,许多溃疡性结肠炎的患者发现生酮饮食可以缓解症状。
目前极少有研究评估酮或生酮饮食对肠道屏障功能的影响,在这方面可进一步研究。
鉴于生酮饮食相当严格,许多人开始使用酮酯或盐来实现酮症。其他人可能会在生酮饮食的基础上使用酮酯或盐来达到更深层次的酮症状态。
酮酯或酮盐对肠道微生物和丁酸盐水平的潜在影响
有趣的是,一些体外数据表明,至少在某些个体中,酮酯或酮盐可能会增加肠道丁酸盐水平。《科学报告》 2020 年发表的一项研究调查了体外发酵室中 12 种人类粪便微生物群样本的 β-羟基丁酸盐的动态。
编辑
在 7 个样本(βHB 利用者)中,超过 54% 的 βHB在发酵 30 小时后被代谢,这与已知的丁酸盐生产者粪球菌属丰度的增加有关,而粪球菌属又与丁酸盐产量的增加相关。
在其他五个粪便样本(βHB 非利用者)中,只有不到 19% 的 BHB 被代谢,并且粪便丁酸盐没有变化。
作者推测:
微生物正在将 βHB 转化为丁酸盐
这一观点得到了 2018 年发表在《细胞代谢》杂志上的一项研究的支持,该研究发现啮齿动物的间歇性禁食,导致与酮体合成和降解相关的微生物途径丰富。
另一种可能的机制是通过激活 PPAR-γ 并维持肠道低氧状态,这反过来又会支持肠道中的产丁酸菌。
一项由麻省理工学院的一组研究人员在2019年末发表在《细胞》杂志上的研究发现:
酮体信号调节了肠干细胞的正常功能及其对伤害的响应能力
肠道上皮广泛折叠,上皮表面有峰(绒毛)和谷(隐窝)。肠道干细胞(ISC)位于每个隐窝的底部,负责每隔几天更新整个肠道上皮或修复损伤。
肠道干细胞受到许多影响其发育的不同生长因子的严格控制。之前的研究表明,膳食营养素在决定肠道干细胞功能方面发挥着重要作用,但尚未有人研究酮体及其潜在作用。
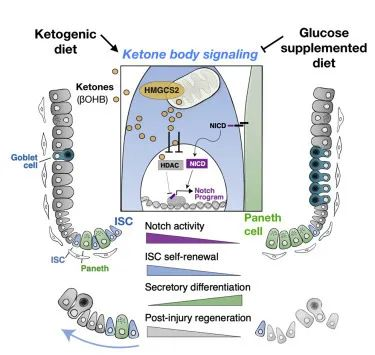
Cheng C W et al., cell,2019
酮体生产酶HMGCS2对肠道健康的影响
研究小组首先发现,生成酮体的酶HMG-CoA合成酶2(HMGCS2)在小肠干细胞中富集。HMGCS2 存在于许多不同的组织中,已知可以限制酮的形成速率。
消除肠道中的Hmgcs2基因会降低隐窝中的 β-羟基丁酸水平,并损害干细胞功能以及后肠道上皮的再生。给予外源性(补充)βHB 可挽救干细胞功能并部分恢复肠道再生。
生酮饮食对肠道干细胞和上皮再生的影响
他们接下来研究了生酮饮食的影响,发现它增加了 HMGCS2 表达、ISC 数量、功能和损伤后再生。相比之下,补充葡萄糖的饮食抑制了肠道干细胞的生酮作用,并使干细胞向杯状细胞和潘氏细胞倾斜分化。
值得注意的是,一旦干细胞分化为成熟的上皮细胞并迁移出隐窝,它们就表达很少的 HMGCS2。这表明成熟的上皮细胞不具备通过经典生酮途径(通过两个乙酰辅酶A分子的缩合)产生大量酮的能力,尽管我们了解到它们确实有能力利用酮。
因此,如果我们在生酮饮食中看到成熟肠上皮细胞中存在高水平的酮,并且这些酮不是在成熟的上皮细胞中产生的,那么酮几乎肯定来自循环。
沿着这些思路,作者写道:
因为外源性酮在体外和体内都能纠正 Hmgcs2 的缺失,肝脏或其他非肠道来源的酮体可能会替代或补充肠道干细胞生成的酮体,在生酮饮食介导的再生过程中,其中循环酮水平高度升高。
避免高脂肪饮食的另一个常见论点是,它们会增加肠道对脂多糖 (LPS) 的吸收。LPS 是一种存在于革兰氏阴性细菌细胞壁中的分子。如果它进入循环,可能会引起低度的全身炎症。
要真正理解这一机制,我们需要了解一下:
脂肪是如何消化和吸收的?
当我们吃脂肪时,小肠中的特殊细胞会释放一种叫胆囊收缩素(CCK)的激素。胆囊收缩素刺激胆囊分泌胆汁进入小肠。在这里,胆汁酸包围脂肪分子,帮助它们变成水溶性的(就像洗洁精有助于乳化油一样)。
人体胆汁酸的肠肝循环
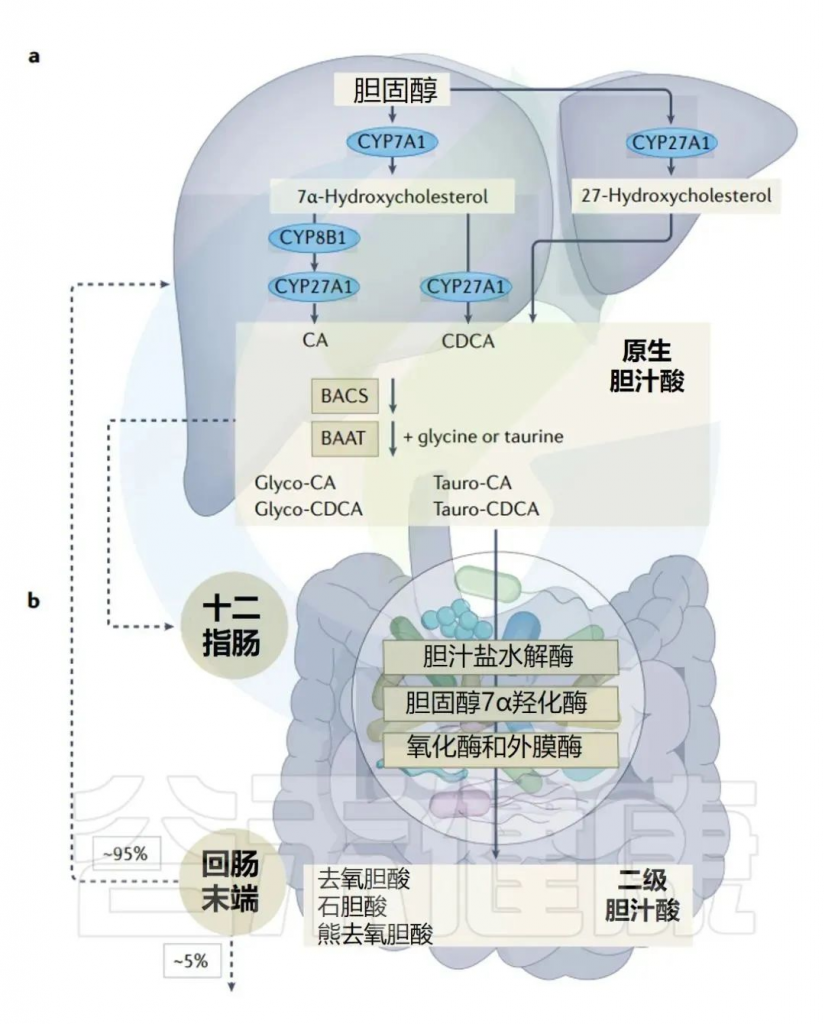
Collins SL,et al.Nat Rev Microbiol.2023
LPS的肠道吸收与运输
事实证明,LPS 对这些称为胶束的水溶性包裹具有很高的亲和力。胶束最终扩散到肠上皮,在那里它们的内容物(包括 LPS)被肠上皮细胞吸收。上皮细胞将脂质和脂多糖重新包装成乳糜微粒,然后乳糜微粒可以通过淋巴管(携带免疫系统淋巴的血管)输送到肝脏。
关于高脂饮食增加LPS吸收的思考
当我们摄入更多的长链脂肪酸时,我们的身体就会产生更多的乳糜微粒,因此更多的脂多糖可以以这种方式搭便车。事实上,富含脂肪的膳食已被证明可以适度增加小鼠和人类的血清 LPS 水平。
虽然这绝对是一个真实的现象并且值得考虑,但其实这个问题不大,原因如下:
LPS 吸收的增加可以减少肠道粘膜的炎症
首先,一些研究表明,乳糜微粒运输 LPS 可能具有优势,因为它有利于肝脏清除 LPS,从而降低 LPS 的毒性。此外,乳糜微粒还具有灭活 LPS 的先天能力。总而言之,LPS 吸收的增加可以减少肠道粘膜的炎症。
乳糜微粒诱导的 LPS 吸收与肠漏相比——小巫见大巫
这一点尤其重要,因为全身接触 LPS 的主要方式不是通过脂肪吸收,而是通过肠漏。当肠道具有渗透性时,大量脂多糖会渗漏到粘膜下层和血液中,引起局部肠道免疫反应和全身炎症。
换句话说,与完全的肠道通透性相比,乳糜微粒诱导的 LPS 吸收可能只是杯水车薪。事实上,对于那些患有严重肠道渗透性的人来说,乳糜微粒诱导的 LPS 解毒甚至可以减少炎症,足以促进肠道上皮的愈合。
生酮饮食的受试者全身炎症减轻
反过来说,如果脂肪诱导的 LPS 吸收是一个问题,那些食用高脂肪生酮饮食的人会出现全身炎症增加?
实际上相反,接受生酮饮食的受试者几乎普遍出现全身炎症减轻的情况。
不必担心高脂肪饮食缺乏丁酸盐或增加 LPS 的吸收。在下一节中,我们将了解胆汁酸如何促进肠道健康。
一些人还认为,高脂肪饮食可能对肠道微生物群和肠道屏障有害,因为它会刺激胆汁酸分泌增加。一般来说,吃的脂肪越多,释放到小肠的胆汁就越多。
事实上,一些研究表明,肠道屏障持续暴露于高浓度胆汁酸会导致肠道通透性增加。然而,生理剂量的胆汁酸已被证明可以支持屏障功能,诱导杯状细胞分泌粘液,促进上皮细胞迁移,并增强肠道先天免疫防御。
胆汁酸介导的肠道屏障功能调节
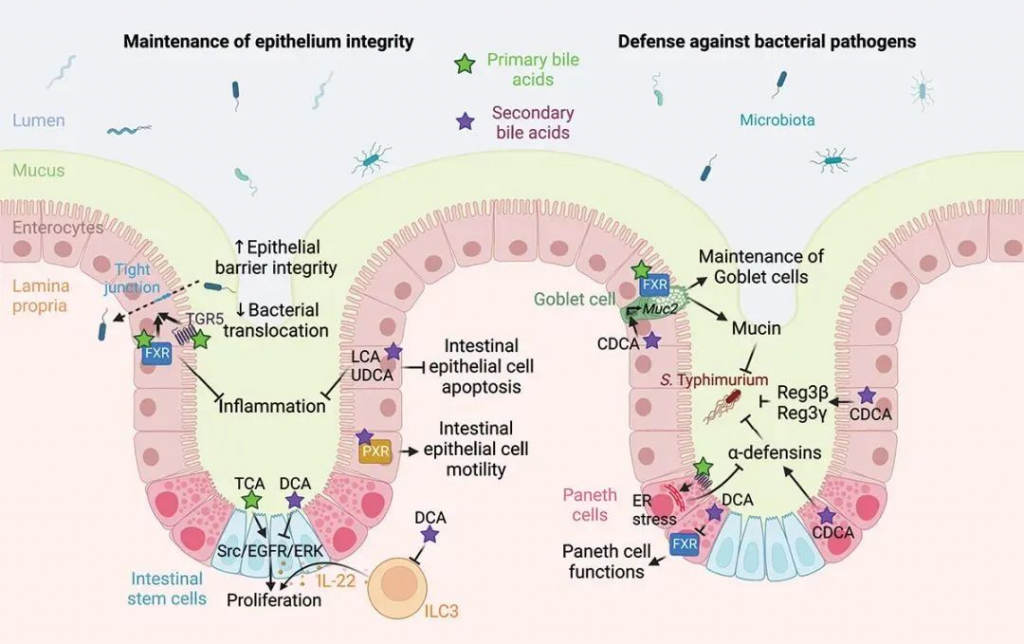
Larabi AB,et al.Gut Microbes.2023
胆汁酸还具有抗菌特性,有助于调节肠道微生物群,尤其可以防止小肠菌群失调。多项研究还表明,胆汁酸可激活肠内分泌细胞释放血清素,从而有助于促进肠道蠕动。
篇幅有限,每种类型的结合和解结合胆汁酸的来龙去脉就不详细阐述了,总的来说,没有足够的证据表明,生酮饮食中胆汁酸的生理增加对肠道微生物群或肠道屏障功能有害。
肉食动物饮食有时候被吹捧为治疗多种疾病的灵丹妙药。虽然全肉饮食作为短期治疗饮食可能是有益的,而且许多人的症状得到改善,但有关这种饮食方法的长期安全性的数据有限。
理论上,假设你从鼻子到尾巴吃遍动物的所有部分,从动物性饮食中获取所有营养素是可能的。有趣的是,上面提到的研究中的短期动物性饮食与维生素生物合成细菌基因表达的增加有关。作为低残渣饮食,肠道炎症的减少也可能在短期内改善营养状况。然而,我们对肉食动物饮食如何长期影响营养状况、激素、生育能力和甲状腺功能知之甚少。
此外,没有证据表明任何祖先只吃肉类或植物为生。即使是因纽特人和生活在极北纬度地区的其他人群,也会不遗余力地采集植物,或以其他方式提高他们的生育能力。
韦斯顿·普莱斯 (Weston A. Price) 在他的著作《营养与身体退化,原始与现代饮食及其影响的比较》中写道:
在北极圈附近驼鹿国家的印第安人中,六月份出生的孩子比例最高。
这是通过父母双方在雄性驼鹿从高山地区下来进入交配季节时,大量食用雄性驼鹿的甲状腺来实现的,此时喉咙下方携带甲状腺的大突起大大增大。
换句话说,这些文化有传统智慧,可以用其他动物的甲状腺进行自我用药,以弥补由于缺乏植物性食物而导致的生育能力下降。大多数现代“肉食动物”并没有这样做,许多人只吃肌肉。
话虽如此,相信在大多数情况下,治疗性生酮饮食可能同样有效,并且需要完全食肉来缓解症状,这是潜在肠道感染的一个迹象。一旦解决了这个问题,理想的饮食可能包括某种形式的植物性食物。
看到这里,希望你已经感觉到生酮饮食对于肠道健康来说一般没有什么可担心的。但这里确实有一个潜在的警告要聊,那就是硫化氢过度生长的个体。
硫化氢 (H2S) 是一种无色气体,通常在体内产生,在低浓度下可作为重要的信号分子。
哺乳动物细胞硫化氢的生物合成
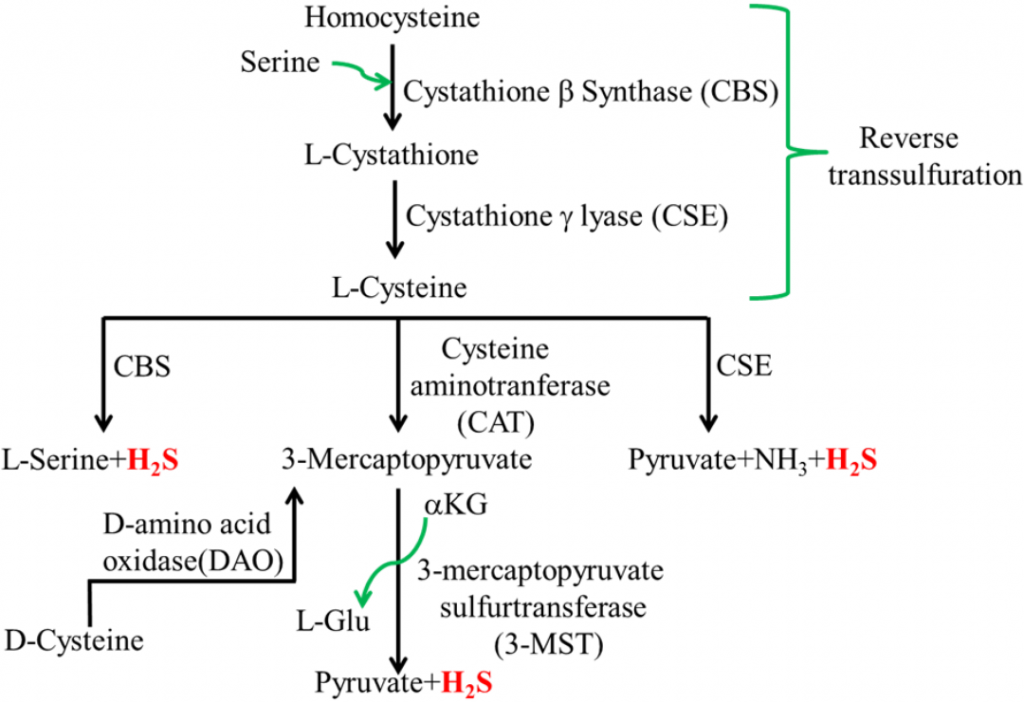
doi.org/10.3390/microorganisms3040866
然而,某些肠道细菌也会产生硫化氢,这些细菌的过度生长会导致硫化氢过量。H2S与腹泻、肠道过敏、IBS、IBD 和结直肠癌有关。
人类肠道中最常见的H2S产生者是Desulfovibrio、Bilophila wadsworthia和Fusobacter nucleatum。这些细菌往往在富含动物蛋白和脂肪的饮食中大量繁殖。
因此,如果有H2S过度生长,最好避免食用生酮饮食,解决了这个问题肠道重新平衡之后再尝试。
注:营养食品多酚(浆果提取物)可将H2S氧化为有效的抗氧化多硫化物,从而引发细胞保护作用。该机制表明,多酚会自动氧化为相应的半醌类物质,然后与H2S反应生成巯基,最终形成多硫化物和硫代硫酸盐。
那H2S过度生长的人适合什么饮食呢?一般来说,高纤维、以植物为主的地中海饮食实际上可能最适合。
扩展阅读:
总而言之, 没有明确的证据表明精心设计的高脂肪或生酮饮食对肠道微生物群或肠道屏障功能有害。事实上,生酮饮食带来的肠道微生物群和肠道屏障的变化甚至可能是我们从生酮饮食中看到如此多益处的原因。
此外,我们并不真正知道健康的肠道微生物群是由什么构成的,而酮和异丁酸酯可以取代丁酸。一些病例报告表明,生酮饮食可以减少 IBS 和 IBD 患者的炎症并改善生活质量。
这里强调的是,并不是说生酮饮食适合每个人。本文的目的并不是建议每个有肠道问题的人都去生酮饮食。只是对生酮饮食与肠道健康相关的证据进行更完整的讨论,让大家有个正确全面的认识。
就肠道健康而言,生酮饮食也有正确和错误的方法。下面两种饮食为肠道带来的治疗效果不同:
就此而言,以下是在食用高脂肪或生酮饮食时遵循肠道健康的一些建议:
1) 关注优质脂肪
如牛油果、牛油果油、橄榄油、多脂鱼、椰子油、放牧酥油、黄油、牛脂等。尽量摄入单不饱和脂肪、多不饱和脂肪和饱和脂肪的混合物。避免高度脂肪加工和精炼油,如菜籽油、玉米油和大豆油。

如果计划长期保持生酮饮食,建议在采用生酮饮食 1-2 个月后检查一下完整的心血管概况。一小部分人的低密度脂蛋白LDL数量会增加,可能需要调整脂肪摄入量或考虑改良生酮饮食,以确保他们不会增加心血管风险。
2)吃非淀粉类蔬菜
不一定需要丁酸盐并不意味着应该减少蔬菜的摄入量。尝试购买各种类型和颜色的生蔬菜和熟蔬菜。
3)多吃浆果
浆果是一种很好的低碳水化合物来源,提供益生元纤维,有助于促进有益细菌的生长。

4)喝咖啡,吃可可
多酚可促进有益细菌的生长,可以适量饮用咖啡和可可。具有严重肠漏或自身免疫性疾病的患者最初可能需要避免这些食物。
5)考虑营养密度,从头到尾吃
食用内脏、贝类、海鲜,并确保富含蛋氨酸的肌肉与富含甘氨酸的动物食品(如胶原蛋白和骨头汤)之间的平衡。
6)亲自实践找到最佳方案
了解生酮是否适合自己的最佳方法是尝试几周,看看感觉如何。特别注意自身能量、皮肤、情绪、生产力、消化、排便等方面。
7)灵活选择生酮饮食
没有必要无限期地处于生酮饮食状态。通过保持 20-120 克的碳水化合物摄入量(取决于自身活动水平),可以轻松地进入和退出生酮状态。实际上,这可能有助于肠道和微生物组保持最高的代谢灵活性。
全面的粪便测试是指除了标准粪便培养之外还可以提供有关肠道健康的更详细信息的任何测试。通常提供以下信息:
而肠道菌群检测使用更彻底的 DNA 测序来更细微地了解到菌属层面的肠道细菌的整体平衡。
谷禾肠道菌群检测还通过复杂的模型构建及大数据分析等方式解读人体健康状况,除了菌群详情之外,还包括疾病风险,营养构成,药物代谢等综合信息。
全面的粪便测试和肠道菌群检测都很有用,它们通常可以相互补充。
哪些人需要全面的粪便或肠道菌群检测?
如果感觉自己有以下症状或一些健康小问题,可能会需要肠道菌群检测:
消化问题、胃酸反流、胀气或腹胀、腹痛、便秘、腹泻、肠易激综合症、炎症性肠病、憩室炎、体重快速增加或减轻等。
患有肠道外其他症状的人也可以进行粪便和/或微生物组检测,例如:
食物不耐受、湿疹或荨麻疹、粉刺、情绪紊乱、抑郁或焦虑、疲劳、失眠、脑雾、关节疼痛、慢性鼻窦问题或过敏、哮喘、痛风等。
这些检测可以帮助自己了解肠道菌群的状况,为制定个性化的治疗方案提供重要参考。
主要参考文献
Singh SB, Lin HC. Hydrogen Sulfide in Physiology and Diseases of the Digestive Tract. Microorganisms. 2015 Nov 12;3(4):866-89.
Austin GL, Dalton CB, Hu Y, Morris CB, Hankins J, Weinland SR, Westman EC, Yancy WS Jr, Drossman DA. A very low-carbohydrate diet improves symptoms and quality of life in diarrhea-predominant irritable bowel syndrome. Clin Gastroenterol Hepatol. 2009 Jun;7(6):706-708.e1.
Cignarella F, Cantoni C, Ghezzi L, Salter A, Dorsett Y, Chen L, Phillips D, Weinstock GM, Fontana L, Cross AH, Zhou Y, Piccio L. Intermittent Fasting Confers Protection in CNS Autoimmunity by Altering the Gut Microbiota. Cell Metab. 2018 Jun 5;27(6):1222-1235.e6.
Zambrano-Zaragoza JF, Romo-Martínez EJ, Durán-Avelar Mde J, García-Magallanes N, Vibanco-Pérez N. Th17 cells in autoimmune and infectious diseases. Int J Inflam. 2014;2014:651503.
Olson CA, Vuong HE, Yano JM, Liang QY, Nusbaum DJ, Hsiao EY. The Gut Microbiota Mediates the Anti-Seizure Effects of the Ketogenic Diet. Cell. 2018 Jun 14;173(7):1728-1741.e13.
David LA, Maurice CF, Carmody RN, Gootenberg DB, Button JE, Wolfe BE, Ling AV, Devlin AS, Varma Y, Fischbach MA, Biddinger SB, Dutton RJ, Turnbaugh PJ. Diet rapidly and reproducibly alters the human gut microbiome. Nature. 2014 Jan 23;505(7484):559-63.
Jiang W, Chen J, Gong L, Liu F, Zhao H, Yan Z, Li Y, Zhang J, Xiao M, Mu J. Microbiota-derived short-chain fatty acids may participate in post-stroke depression by regulating host’s lipid metabolism. J Psychiatr Res. 2023 May;161:426-434.
Clemens Z, Kelemen A, Fogarasi A, Tóth C. Childhood absence epilepsy successfully treated with the paleolithic ketogenic diet. Neurol Ther. 2013 Sep 21;2(1-2):71-6.
Sasaki K, Sasaki D, Hannya A, Tsubota J, Kondo A. In vitro human colonic microbiota utilises D-β-hydroxybutyrate to increase butyrogenesis. Sci Rep. 2020 May 22;10(1):8516.