 国家高新企业 | ISO9001认证
国家高新企业 | ISO9001认证 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康

拟杆菌是革兰氏阴性、专性厌氧菌,在人类肠道微生物群中含量丰富,构成了肠道菌群中大部分比例。
Bacteroides uniformis (一般简称为 B.uniformis),翻译为单形拟杆菌或普通拟杆菌,是拟杆菌属的主要成员,在肠道中起着重要的作用。也被鉴定为阴道微生物组的组成部分。
Bacteroides uniformis是与人类粪便中异黄酮染料木黄酮降解相关的特定细菌物种,可以产生纤维素酶和淀粉酶,降解复杂多糖。
Bacteroides uniformis与肠炎、厌食、肥胖、糖尿病、腹胀、认知发育与情绪运动、多动症、慢性肾病、骨质疏松等相关,是可引起人类或动物疾病的物种,不太可能在人群中传播,并且存在足够的预防或治疗方法。
对单形拟杆菌进行深入研究,有助于我们更好地理解其在人体肠道中的功能,并为相关疾病的预防和治疗提供新的思路。
Bacteroides uniformis是一种革兰阴性细菌,呈杆状。它们通常具有弯曲或弯钩形态,并且没有芽胞。

图源:Microbe Canvas
生理特性
Bacteroides uniformis是一种厌氧菌,不能在氧气存在的环境中生长。它们通常能够利用多糖类物质作为碳源,如淀粉、纤维素和其他复杂碳水化合物。还可以产生一些酶,如纤维素酶和淀粉酶,用于降解消化这些复杂碳水化合物。
分布和生存环境
Bacteroides uniformis是人体肠道,阴道中常见的细菌之一,也可以在其他动物的肠道中找到。它们在肠道中扮演重要的生态角色,参与食物消化、营养吸收和免疫调节等过程。Bacteroides uniformis能够适应肠道的微生态环境,与其他肠道细菌相互作用。
功能和代谢
Bacteroides uniformis在肠道中具有多种功能和代谢活性。它们参与葡萄糖和其他碳水化合物的代谢,并产生短链脂肪酸(如丙酸和乙酸),这些酸有益于肠道健康。此外,Bacteroides uniformis还参与胆固醇代谢、氨基酸代谢和维生素合成等生物化学过程。
肥胖和肥胖相关疾病构成了世界范围内的重大公共卫生问题。除了传统的减肥药物外,下一代益生菌(NGP)似乎非常有希望作为潜在的肥胖预防和治疗药物。
主要的候选NGP已在肥胖和肥胖相关疾病的临床前模型中显示出前景,例如:
B.uniformis已被证明具有对抗肥胖和代谢紊乱的有益特性。在动物模型中, B. uniformis与减肥、降低血清胆固醇和甘油三酯水平以及改善肝脂肪变性有关。此外,它还与血清瘦素水平降低、空腹血糖浓度降低和糖耐量改善有关。
推测的机制包括调节肠道菌群和改善肠道菌群失调、改善肠道屏障功能、减少慢性低度炎症和调节肠道肽分泌。
一项对41名体重指数(BMI)正常的个体肠道菌群和内脏脂肪面积 (VFA)的研究显示,内脏脂肪面积高/低(VFA)两组的肠道菌群存在显著差异,在 L-VFA 组中,B. plebeius 和B.uniformis含量很高。此外,B.uniformis与血清 LDL-胆固醇水平呈负相关。
另一项对32名肥胖成年人(14 名接受了腹腔镜袖状胃切除术 (LSG))和30名基线健康对照者的肠道菌群以及身体指标的研究,并在术后 6 个月进行了随访。通过磁共振成像测量腹部内脏脂肪面积(VFA)和皮下脂肪面积(SFA)。腰围、臀围、腰臀比(WHR)和体重指数(BMI)被列为简单的肥胖参数。通过宏基因组测序分析肠道微生物组。在与腹部内脏脂肪面积(VFA)负相关的物种中,Eubacteria eligens相关性最强,其次是Clostridium citroniae、C. symbiosum、Bacteroides Uniformis、E. ventriosum、C. hathewayi等。
一项涉及 45 名儿童(6 至 12 岁)的横断面研究调查了肠道微生物群与儿童肥胖之间的关系。发现两个BMI组之间的多样性存在差异。这种差异包括真杆菌属(Eubacterium)、普拉梭菌(Faecalibacterium prausnitzii)、Dialister、Monoglobus pectinilyticus、Bifidobacterium pseudocatenulatum、Intestinibacter bartlettii、 Bacteroides intestinalis、Bacteroides uniformis (单形拟杆菌)和 史密斯甲烷杆菌(Methanobrevibacter smithii)。
一项针对减肥手术是否显著改善体重的研究显示单形拟杆菌的丰度可能影响手术后的效果。
术前属于拟杆菌门和厚壁菌门的成员丰度存在差异无应答组:
富含拟杆菌科、拟杆菌属、单形拟杆菌、Alistipes Finegoldii、Alistipes alistipes、Dorea formicigenerans 、瘤胃球菌。
应答组:
富含消化链球菌科、 Gemmiger、Gemiger formicilis、Barnesiella、Prevotellaceae 、 Prevotella。
线性判别分析 >2;p < 0.05。与有反应组相比,无反应组中普氏菌与拟杆菌的比率显着较低 (p = 0.048)。
神经性厌食症(Anorexia nervosa, AN)的特点是一种神秘的食物回避模式,导致严重的营养不良,这种疾病在青春期早期发展。近期,在《Nature Microbiology》上发表的文章研究了77名患有神经性厌食症的成年女性和70名被认为是健康体重的对照组。
利用宏基因组学,作者对微生物组的细菌和病毒成分进行了深入分析。细菌基因组中的结构变异,特别是Bacteroides uniformis(单形拟杆菌)中的结构变异,可能造成了硫胺素生产的破坏。
硫胺素(或称维生素B1)缺乏会影响人体健康,包括记忆丧失、焦虑、抑郁、易怒、失眠、食欲减退和胃肠道不适。这也可以解释在神经性厌食症患者中普遍观察到的硫胺素缺乏的现象。
认知发展
一项针对健康以色列阿拉伯儿童的横断面研究显示一些菌群分类学差异与儿童智商测试FSIQ评分显着正相关,包括Prevotella(普雷沃氏菌属)、Dialister属、Sutterella(萨特氏菌属)、Ruminococcus callidus和Bacteroides uniformis(单形拟杆菌)。
情绪相关
一项针对长期封闭环境中心理变化和肠道菌群的研究,鉴定出四种潜在的“精神抗生素”(单形拟杆菌Bacteroides Uniformis、Roseburia inulinivorans、Faecalibacter prausnitzii、Eubacterectale )。
根据宏基因组、宏蛋白质组和代谢组学分析,四种潜在的精神抗生素主要通过与神经系统功能相关的三种途径改善情绪:
首先,通过发酵膳食纤维,它们可能产生短链脂肪酸,例如丁酸和丙酸;
其次,它们可能调节天冬氨酸、谷氨酸、色氨酸等氨基酸代谢途径(例如,将谷氨酸转化为γ-氨基丁酸;将色氨酸转化为血清素、犬尿酸或色胺);
第三,它们可能调节其他途径,例如牛磺酸和皮质醇代谢。此外,动物实验的结果证实了这些潜在的精神抗生素对情绪的积极调节作用和机制。
运动相关
肠道微生物群可能有助于改善运动表现。日本庆应义塾大学先进生命科学研究所通过分析25名男性长跑运动员的比赛成绩后发现,运动员粪便中单形拟杆菌(Bacteroides uniformis)的丰度与其3000米比赛成绩间存在相关性。
在随后的一项随机、双盲、安慰剂对照研究中,研究人员让健康男性志愿者服用α-环糊精,以增加肠道中的单形拟杆菌总量。结果表明,补充α-环糊精可以提高人体的耐力运动能力。
此外,在小鼠实验中,食用单形拟杆菌显著延长了动物游泳的持续时间;动物盲肠短链脂肪酸浓度以及肝脏中与糖异生相关酶的基因表达均上升,肝糖原含量降低。该研究表明,单形拟杆菌可能通过促进肝脏内源性葡萄糖生成,增强个体的耐力运动能力。
妊娠糖尿病
妊娠合并糖尿病包括孕前糖尿病(PGDM)和妊娠期糖尿病(GDM)。 一项针对234份孕妇粪便样本的16S rRNA测序数据显示,随着妊娠的进展,妊娠糖尿病PGDM 组的肠道细菌种类数量有所减少。巨单胞菌、拟杆菌和 Roseburia Enteris 在 PGDM 组中富集,而 Bacteroides vulgatus、Faecalibacter prausnitzii、Eubacterectale、Bacteroides uniformis(单形拟杆菌)、Eubacteria eligens、Subdolilegum在对照组中比例更高,这些菌血糖与血糖特征呈负相关。
二型糖尿病
一项针对亚洲人的包括36个不同二型糖尿病T2DM研究(健康,n = 3378;T2DM,n = 551)的meta分析显示,T2DM 组中普通杆菌菌、单形拟杆菌和普氏粪杆菌较低。
另一项包括29名T2DM患者和28名健康对照者研究显示,Megamonas funiformis 和 Escherichia 的丰度在T2DM患者的肠道中显着增加。相反,Bacteroides stercoris、单形拟杆菌和Phascolarctobacterium faecium的丰度降低。
单形拟杆菌 (Bacteroides uniformis) 还可能调节动物肠道稳态,减轻小鼠结肠炎。一项研究使用B.uninis JCM5828 及其代谢物对患有葡聚糖硫酸钠盐 (DSS) 诱导的结肠炎的雌性 C57BL/6J小鼠进行治疗。
Bacteroides uniformis治疗显著减轻了结肠炎的进展并恢复了机械和免疫屏障蛋白的表达。此外,Bacteroides uniformis还增加了共生菌双歧杆菌和阴道乳杆菌的丰度,同时减少了致病性埃希氏菌、志贺氏菌的丰度,并调节了肠道胆汁酸代谢。
Bacteroides uniformis在很大程度上调节结肠组织中NF-κB和丝裂原激活蛋白激酶(MAPK)信号通路关键调节蛋白的表达以及TH17细胞的分化。然而,Bacteroides uniformis在体外不能直接抑制TH17细胞分化;它应该是通过参与胆汁酸代谢和调节关键代谢物(α-鼠胆酸、猪去氧胆酸和异石胆酸)来调节固有层的过程,从而调节肠道免疫反应。
此外在一项溃疡性结肠炎(UC)患者的菌群研究中,六种拟杆菌属表现出显着较低的相对丰度,十二种拟杆菌属被发现与至少一项疾病活动指标显着相关。五个物种( Alistipes putredinis、Bacteroides stercoris、Bacteroides Uniformis、Bacteroides rodentium、Parabacteroides merdae )的相对丰度与溃疡性结肠炎活性的四个指标中的三个相关。
12 个关键物种表达了与 UC 发病机制相关的5 个基因(TARP、C10ORF54、ITGAE、TNFSF9和LCN2 )。作为潜在生物标志物的关键物种的丧失可能会加剧 UC 活动。
比较功能性腹胀和膨胀(FABD)患者和12健康个体粪便微生物群的多样性和组成,并评估小肠细菌过度生长 (SIBO) 。结果显示FABD 组的微生物多样性显着低于对照组。与健康对照相比,FABD 患者中变形菌的比例显着升高,放线菌的比例显着降低。与健康对照相比,FABD患者中粪杆菌的比例显着升高,而SIBO(+)FABD患者中普氏菌和粪杆菌的比例也显着升高。与健康对照相比,FABD 患者的普氏粪杆菌 (Faecalibacter prausnitzii) 的丰度显着增加,但单形拟杆菌 (Bacteroides uniformis)和青春双歧杆菌数量明显减少。
乳糜泻患者肠道中的 Bacteroides distasonis、Bacteroides fragilis / Bacteroides thetaiotaomicron、Bacteroides Uniformis、Bacteroides ovatus比对照组更少(p<0.05)。
骨质疏松
一项研究中,与对照组相比,几个物种的丰度发生了变化,在骨质疏松组中发现了特定的功能途径,骨质疏松组中下列菌群的水平下降:
类风湿性关节炎
一项研究包括 76 名类风湿关节炎患者的粪便宏基因组和血浆代谢组的分期概况。
骨关节炎
骨关节炎是一种病因不明的慢性退行性疾病。一项研究针对骨关节炎患者(n = 32)和正常对照组(n = 57)肠道菌群检测,宏基因组测序显示,骨关节炎患者中Bacteroides stercoris、Bacteroides vulgatus、Bacteroides uniformis在物种水平上的丰度显著降低,大肠杆菌、肺炎克雷伯菌、Shigella flexneri、唾液链球菌在骨关节炎中显著增加。
特应性皮炎AD
使用 16S rRNA 测序分析了 93 名志愿者的粪便样本,其中包括 44 名 AD 患者和 49 名健康对照受试者,年龄为 6-22 岁。
卟啉单胞菌科、Blautia、Parabacteroides、Bacteroides ovatus、Bacteroides uniformis 和 Prevotella stercorea 的相对丰度显著较高(P < 0. 05) AD 患者高于健康对照者。与 AD 患者相比,健康对照受试者中梭状芽胞杆菌和粪疟原虫含量较高 (P < 0.05)。
儿童多动症
对11项儿童多动症研究的meta分析显示,拟杆菌属与多动和冲动水平相关。在物种水平上,多动症儿童Faecalibacterium丰度较低,但Bacteroides uniformis、肠球菌、双歧杆菌和Odoribacter增加,可能导致中枢神经系统多巴胺相关功能受损。
此外,多动症儿童肠道中Faecalibacterium丰度的降低可能导致炎症细胞因子的渗透性和交叉性更高。
一项调查多动症儿童及其饮食模式和肠道菌群的研究显示,在注意缺多动障碍(ADHD)组中,粪肠拟杆菌(B. coprocola)的相对丰度降低,而单形拟杆菌(B.uniformis)、卵形拟杆菌(B.ovatus)和粪类杆菌(S. stercoricanis)的相对丰度升高。
结直肠癌转移组
转移性结直肠癌组和非转移性结直肠癌组患者的肠道菌群存在差异。在属水平上,拟杆菌属菌种脆弱拟杆菌和单形拟杆菌组成在转移组中显着高于非转移组。
PD-1免疫疗法反应
肠道微生物群被认为是调节免疫检查点抑制剂治疗功效的关键因素。一项波兰黑色素瘤患者队列中PD-1疗法反应与基线肠道微生物组的研究显示,普氏菌和单形拟杆菌的丰度与反应有关,而无反应者的肠道微生物群富含普氏粪杆菌和脱硫弧菌以及一些未分类的厚壁菌门。
慢性肾病
一项台湾地区人群肠道菌群研究显示,在慢性肾病 (CKD)患者中发现的最丰富的属是拟杆菌属,在物种水平上,血液透析患者中的B. ovatus、B. caccae 、 B.uniformis表现出显著丰度,而腹膜透析患者中的Blautia表现出较高的丰度。
白塞病
在活动性白塞病BD患者其单形拟杆菌丰度显著高于其匹配的健康对照和处于非活动状态的疾病患者 ( p = 0.038)。
单形拟杆菌可以消化多种膳食纤维,作为一种代谢膳食纤维产生乙酸的肠道菌已有大量研究表明日常膳食纤维摄入会影响单形拟杆菌的丰度。
一项横断面研究中检查了全谷物和精制谷物、纤维和麸质的习惯摄入是否与肠道微生物群相关。对779 名参与者137 项食物频率的调查问卷和肠道菌群的分析显示。最高全谷物摄入量四分位与较高丰度的普通拟杆菌、普氏粪杆菌、Blautiaproducta和Rikenellaceae以及较低丰度的单形拟杆菌有关。
一项对不同特异性(低-低聚果糖、低至中-2 型抗性淀粉、中-果胶和高-不溶性 β-1,3-葡聚糖特异性)纤维的微生物发酵研究显示,高特异性不溶性β-葡聚糖促进目标细菌大量增加,Anaerostipes sp. 平均从0.3%增加到16.5%,单形拟杆菌平均为 2.5% 至 17.9%,这与这些细菌所在的每个微生物群落中相关代谢物(分别为丁酸盐和丙酸盐)比例的增加有关。
水溶性醋酸纤维素 (WSCA) 是一种合成纤维来源,可以导致拟杆菌属成员的丰度增加,尤其是单形拟杆菌。在四种具有代表性的人类肠道拟杆菌属中,只有单形拟杆菌在WSCA上的纯培养物中生长并活跃地产生乙酸。
一项对健康志愿者进行了为期 4周的营养干预分析天然单宁提取物混合物对肠道微生物变化的研究显示。从前两周起就可以观察到微生物群的组成和功能的变化,测序显示以下菌相对丰度增加,例如:
利用同位素标记发,发现食用菊粉富集的前三种细菌为单形拟杆菌(Bacteroides uniformis)、产酸拟杆菌(Bacteroides acidifaciens)和狄氏副拟杆菌(Parabacteroides distasonis)。
一项研究评估富含黄酮类化合物的蔓越莓多酚(CP)和龙舌兰(AG)(一种高支链龙舌兰衍生的新果聚糖)对C57BL6雄性小鼠的心脏代谢反应、肠道微生物群组成、代谢内毒素血症和粘膜免疫调节的影响,该雄性小鼠喂食致肥胖高脂肪高糖(HFHS)饮食9周。AG,单独或与CP(CP+AG)联合,主要刺激聚糖降解细菌:
与未经治疗的小鼠相比,接受AG的肥胖小鼠中聚糖降解细菌的增加与丁酸水平的显著增加一致。
总的来说,研究发现高特异性不溶性β-葡聚糖、天然单宁提取物混合物、菊粉、蔓越莓多酚和龙舌兰能增加Bacteroides uniformis的丰度。
主要参考文献:
Vallianou NG, Kounatidis D, Tsilingiris D, Panagopoulos F, Christodoulatos GS, Evangelopoulos A, Karampela I, Dalamaga M. The Role of Next-Generation Probiotics in Obesity and Obesity-Associated Disorders: Current Knowledge and Future Perspectives. Int J Mol Sci. 2023 Apr 4;24(7):6755.
Nie X, Chen J, Ma X, Ni Y, Shen Y, Yu H, Panagiotou G, Bao Y. A metagenome-wide association study of gut microbiome and visceral fat accumulation. Comput Struct Biotechnol J. 2020 Sep 20;18:2596-2609.
Murga-Garrido SM, Ulloa-Pérez EJ, Díaz-Benítez CE, Orbe-Orihuela YC, Cornejo-Granados F, Ochoa-Leyva A, Sanchez-Flores A, Cruz M, Castañeda-Márquez AC, Plett-Torres T, Burguete García AI, Lagunas-Martínez A. Virulence Factors of the Gut Microbiome Are Associated with BMI and Metabolic Blood Parameters in Children with Obesity. Microbiol Spectr. 2023 Feb 14;11(2):e0338222.
Lapidot Y, Maya M, Reshef L, Cohen D, Ornoy A, Gophna U, Muhsen K. Relationships of the gut microbiome with cognitive development among healthy school-age children. Front Pediatr. 2023 May 19;11:1198792.
Cheng M, Zhao Y, Cui Y, Zhong C, Zha Y, Li S, Cao G, Li M, Zhang L, Ning K, Han J. Stage-specific roles of microbial dysbiosis and metabolic disorders in rheumatoid arthritis. Ann Rheum Dis. 2022 Aug 19;81(12):1669–77.
Shirvani-Rad S, Ejtahed HS, Ettehad Marvasti F, Taghavi M, Sharifi F, Arzaghi SM, Larijani B. The Role of Gut Microbiota-Brain Axis in Pathophysiology of ADHD: A Systematic Review. J Atten Disord. 2022 Nov;26(13):1698-1710.
Wang LJ, Yang CY, Chou WJ, Lee MJ, Chou MC, Kuo HC, Yeh YM, Lee SY, Huang LH, Li SC. Gut microbiota and dietary patterns in children with attention-deficit/hyperactivity disorder. Eur Child Adolesc Psychiatry. 2020 Mar;29(3):287-297.
Hao Z, Meng C, Li L, Feng S, Zhu Y, Yang J, Han L, Sun L, Lv W, Figeys D, Liu H. Positive mood-related gut microbiota in a long-term closed environment: a multiomics study based on the “Lunar Palace 365” experiment. Microbiome. 2023 Apr 24;11(1):88.
Ren Y, Hao L, Liu J, Wang P, Ding Q, Chen C, Song Y. Alterations in the Gut Microbiota in Pregnant Women with Pregestational Type 2 Diabetes Mellitus. mSystems. 2023 Apr 27;8(2):e0114622.
Wu X, Park S. Fecal Bacterial Community and Metagenome Function in Asians with Type 2 Diabetes, According to Enterotypes. Biomedicines. 2022 Nov 21;10(11):2998.
Lv M, Li L, Li W, Yang F, Hu Q, Xiong D. Mechanism research on the interaction regulation of Escherichia and IFN-γ for the occurrence of T2DM. Ann Palliat Med. 2021 Oct;10(10):10391-10400.
Yan Y, Lei Y, Qu Y, Fan Z, Zhang T, Xu Y, Du Q, Brugger D, Chen Y, Zhang K, Zhang E. Bacteroides uniformis-induced perturbations in colonic microbiota and bile acid levels inhibit TH17 differentiation and ameliorate colitis developments. NPJ Biofilms Microbiomes. 2023 Aug 14;9(1):56.
Nomura K, Ishikawa D, Okahara K, Ito S, Haga K, Takahashi M, Arakawa A, Shibuya T, Osada T, Kuwahara-Arai K, Kirikae T, Nagahara A. Bacteroidetes Species Are Correlated with Disease Activity in Ulcerative Colitis. J Clin Med. 2021 Apr 17;10(8):1749.
Noh CK, Lee KJ. Fecal Microbiota Alterations and Small Intestinal Bacterial Overgrowth in Functional Abdominal Bloating/Distention. J Neurogastroenterol Motil. 2020 Sep 30;26(4):539-549.
Wang H, Zhang K, Wu L, Qin Q, He Y. Prediction of Pathogenic Factors in Dysbiotic Gut Microbiomes of Colorectal Cancer Patients Using Reverse Microbiomics. Front Oncol. 2022 Apr 27;12:882874.
Ye S, Yan F, Wang H, Mo X, Liu J, Zhang Y, Li H, Chen D. Diversity analysis of gut microbiota between healthy controls and those with atopic dermatitis in a Chinese population. J Dermatol. 2021 Feb;48(2):158-167.
Zhou P, Dai Z, Xie Y, Li T, Xu Z, Huang Y, Sun D, Zhou Y. Differences in tissue-associated bacteria between metastatic and non-metastatic colorectal cancer. Front Microbiol. 2023 Jun 9;14:1133607.
Shivani S, Kao CY, Chattopadhyay A, Chen JW, Lai LC, Lin WH, Lu TP, Huang IH, Tsai MH, Teng CH, Wu JJ, Hsieh YH, Wang MC, Chuang EY. Uremic Toxin-Producing Bacteroides Species Prevail in the Gut Microbiota of Taiwanese CKD Patients: An Analysis Using the New Taiwan Microbiome Baseline. Front Cell Infect Microbiol. 2022 Apr 26;12:726256.
Kim JC, Park MJ, Park S, Lee ES. Alteration of the Fecal but Not Salivary Microbiome in Patients with Behçet’s Disease According to Disease Activity Shift. Microorganisms. 2021 Jul 6;9(7):1449.
Um CY, Peters BA, Choi HS, Oberstein P, Beggs DB, Usyk M, Wu F, Hayes RB, Gapstur SM, McCullough ML, Ahn J. Grain, Gluten, and Dietary Fiber Intake Influence Gut Microbial Diversity: Data from the Food and Microbiome Longitudinal Investigation. Cancer Res Commun. 2023 Jan 11;3(1):43-53.
Cantu-Jungles TM, Bulut N, Chambry E, Ruthes A, Iacomini M, Keshavarzian A, Johnson TA, Hamaker BR. Dietary Fiber Hierarchical Specificity: the Missing Link for Predictable and Strong Shifts in Gut Bacterial Communities. mBio. 2021 Jun 29;12(3):e0102821.
Molino S, Lerma-Aguilera A, Jiménez-Hernández N, Rufián Henares JÁ, Francino MP. Evaluation of the Effects of a Short Supplementation With Tannins on the Gut Microbiota of Healthy Subjects. Front Microbiol. 2022 Apr 27;13:848611.

谷禾健康
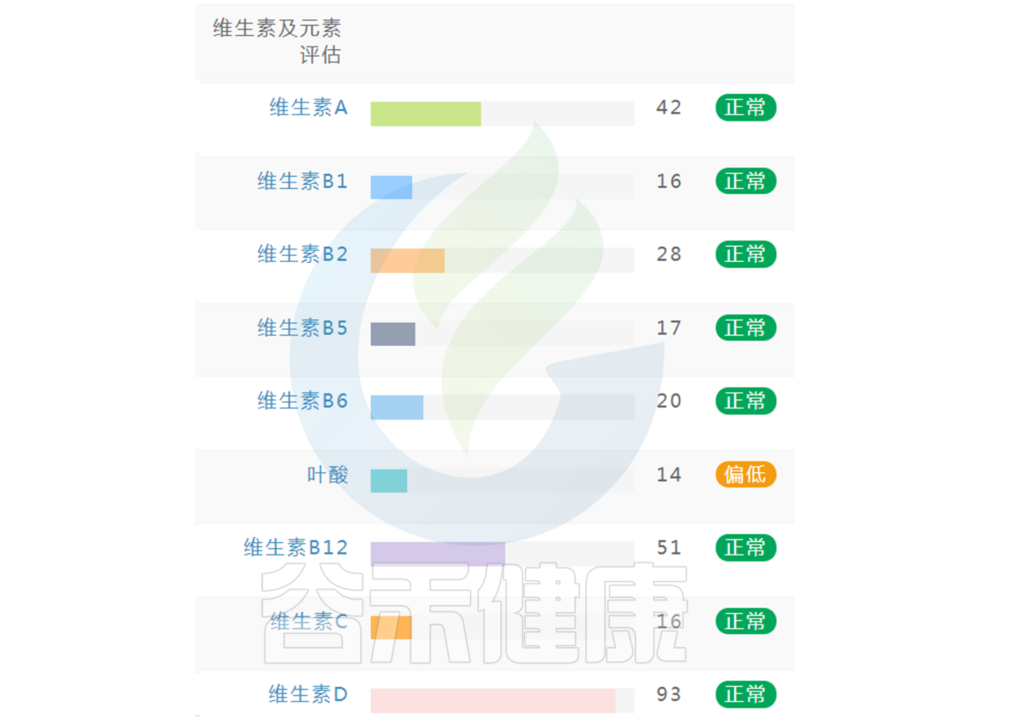
在谷禾肠道菌群健康检测中,我们会看到结果报告中关于维生素的评估如下:

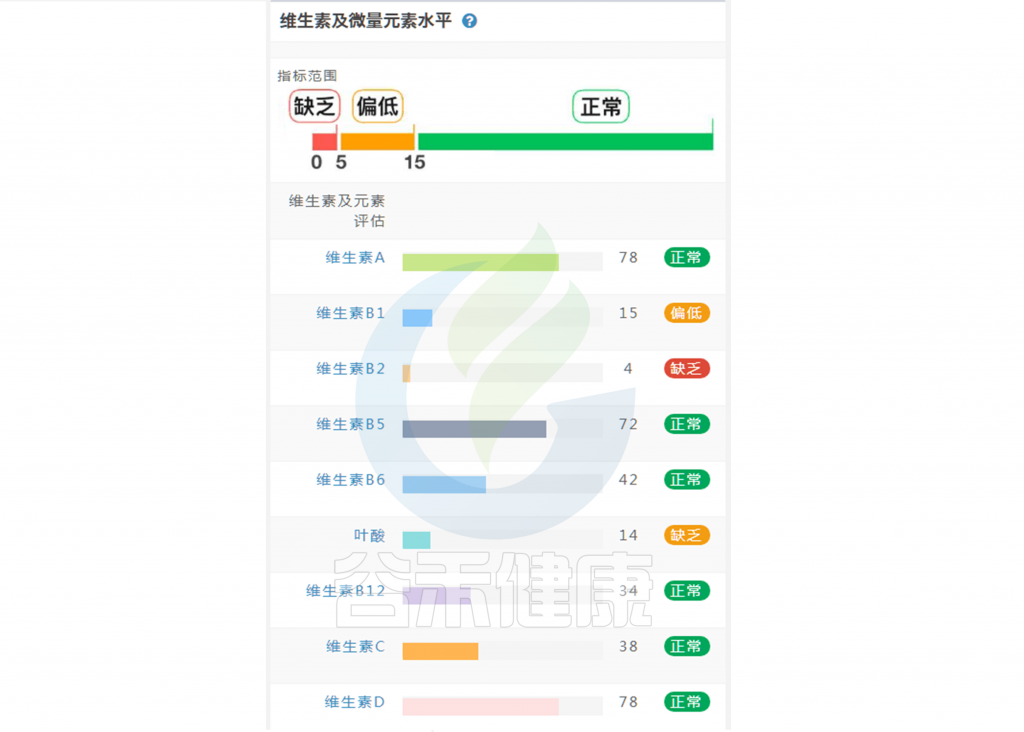
摄入水平建议保持在70-80分之间最佳,如果单项指标低于5表明摄入比例在人群中属于最低的5%,评估为缺乏,如上图中维生素B2;低于15评估为偏低,如上图中叶酸;达到或超过95则表明该项指标可能摄入比例偏高,可适当减少摄入;其余则为正常范围。
上图可以看到,像维生素C这项指标分值在38,虽然正常但相对于最佳来说是偏低的。
一些小伙伴可能会存在这样的疑惑:
为什么肠道菌群检测可以评估维生素?
这些维生素指标的分值代表着什么含义?
肠道菌群和维生素之间有什么样的关联?
它们如何影响人体健康/疾病?
如何判断维生素是否缺乏?
该如何补充?
…
本文就以上问题进行详细解答,同时也包括维生素-微生物群之间的相互作用,维生素维持肠道菌群稳态和减少肠道炎症以预防癌症的机制,产生维生素的益生菌,补充调节维生素的方式包括饮食、益生菌等。
在阅读本文之前,可以先了解一下各类常见的维生素功能,缺乏导致的症状。


每个维生素的详细介绍可以点开以下查看(请在谷禾健康微信公众号找到这篇文章查看)。
维生素B1(硫胺素)
维生素B2(核黄素)
维生素B3(烟酸)
维生素B5(泛酸)
维生素B6(吡哆醇)
维生素B7(生物素)
维生素B9(叶酸)
维生素B12(钴胺素)
以上每个都有关于该维生素的详细介绍,包括:
—正文—
维生素是一种微量营养素,在人体的生长、新陈代谢和发育中起着至关重要的作用。
在谷禾肠道菌群健康检测报告中,维生素分值即代表该维生素的膳食摄入水平和菌群代谢能力(报告中显示的分值是经过一系列计算得到的一个相对值)。
其中B族维生素很多需要通过肠道菌群对初始原料进行代谢之后才会产生,因此肠道菌群相应的基因和代谢途径的丰度水平也会直接反映这些维生素的摄入水平。
我们知道维生素的缺乏可能引起一些不良后果,导致维生素缺乏的原因有很多,摄入不足,吸收不良等都会导致维生素缺乏。
我们日常主要从饮食中获取维生素,肠道是主要吸收部位。例如,维生素 A 主要在近端空肠吸收,维生素 D 在远端空肠吸收最佳,维生素 E 和 K 主要在回肠吸收。因此,肠道功能受损可能会影响维生素的吸收。当然,影响维生素吸收的其他原因还包括年龄,某些疾病,药物等因素。
那么肠道菌群和维生素之间有什么关联?
肠道菌群是人体生理和健康的重要决定因素。肠道菌群帮助吸收营养,并参与维生素代谢。
肠道有益菌:乳酸菌和双歧杆菌,可以重新合成B族和K族维生素,为宿主提供约30%的每日摄入量。与从食物中获得的维生素不同,微生物产生的维生素主要在结肠中吸收。接下来了解一下具体哪些菌群,如何产生维生素。
前一章节我们知道,除了通过饮食提供维生素外,人体肠道中的细菌也可以产生一些维生素,如果吸收得当,可以部分满足人体的需要。
可以把这些细菌微生物想象成小小的维生素工厂。细菌确保为自己和与他们共生的微生物朋友提供维生素,同时也会为人体提供维生素。
合成的B族维生素的菌群较多
研究人员估计了人体肠道细菌可以提供维生素每日参考摄入量的百分比,得出的结论是可以提供:
40-65% 的人体肠道菌群具有合成 B 族维生素的能力。两种最常见的合成维生素是维生素B2和B3,预测分别有 166 和 162 个生产者。
可以合成 B 族维生素的细菌以及B 族维生素缺乏对肠道健康的影响
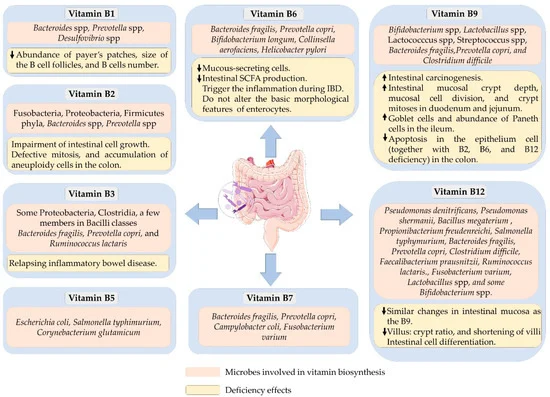
doi.org/10.3390/microorganisms10061168
大部分肠道菌群都参与维生素的合成
随着基因组注释方法的不断完善,研究人员可以预测维生素代谢途径并评估维生素生物合成潜力。通过检索 UniProt 数据库,研究人员发现:
厚壁菌门是维生素的主要代谢相关菌,其次是变形菌门,再然后是拟杆菌和放线菌。这四种菌群是人体肠道菌群的主要组成部分,占总菌群的60%-90%.
下表列出了参与合成B族维生素的肠道菌群,以及相应的代谢机制。


以上是肠道菌群对维生素产生的影响,而维生素和肠道菌群之间的作用是双向的,维生素也会影响肠道菌群,下一章节我们详细了解维生素对肠道菌群的影响。
维生素通过调节免疫力、细菌生长和新陈代谢来改变肠道微生物群的组成。
例如,膳食补充剂中的维生素 B、C、D 和 E 通过有利于双歧杆菌、乳酸杆菌和罗斯氏菌等有益菌属的肠道黏膜扩张和定植,在很大程度上有助于微生物组的组成。
肠道微生物组和宿主之间的微量营养素交换
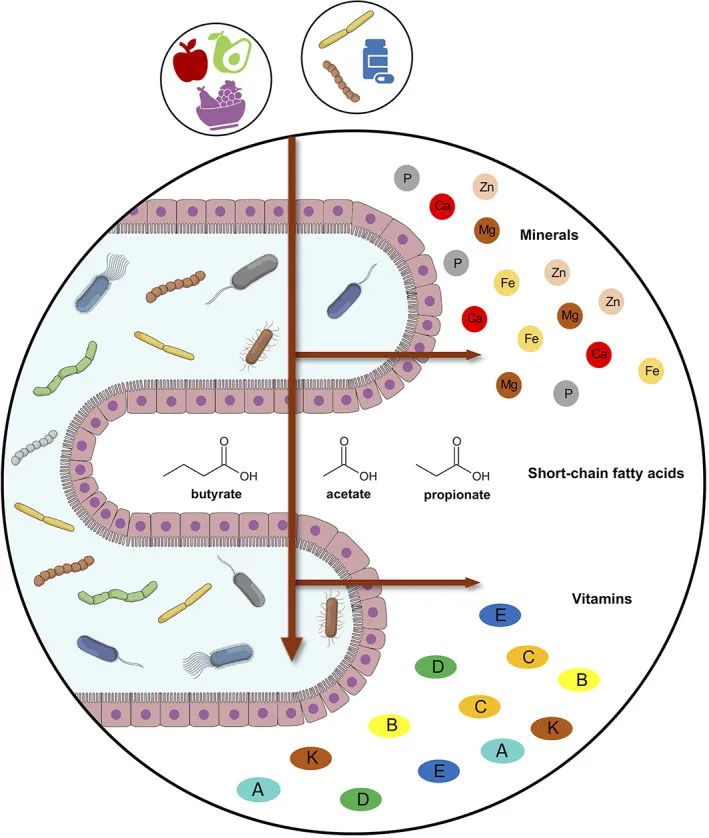
doi: 10.1002/biof.1835
一项研究调查了 96 名健康志愿者,结果表明:
补充维生素 B2 后肠道微生物的种类数量显着增加;联合补充维生素 B2 和 C 导致Sutterella显着减少,但Coprococcus数量增加;
维生素C显着提高肠道微生物的α多样性;
服用维生素D后,促进放线菌的生长和抑制拟杆菌的生长。
补充维生素对人体肠道菌群的影响

doi.org/10.3390/nu14163383
/ 维生素A /
维生素 A 的充足状态可能与微生物多样性增加有关。在小鼠实验中,普通拟杆菌(Bacteroides vulgatus )在维生素 A 缺乏期显着增加。维生素 A 缺乏导致的粘膜反应受损,粘蛋白和防御素 6 表达减少,可能使病原菌更容易穿透肠道屏障。
维生素A缺乏使厚壁菌门中毛螺菌_NK4A136_群、厌氧菌、颤杆菌的数量减少,毛螺菌的含量也降低;然而,Parasutterella呈上升趋势。TLR4 可能参与了维生素 A 调节微生物群的过程。
/ B族维生素 /
研究人员在一个小的成年志愿者群体中进行了一项试点研究,该群体补充了过量核黄素(100mg),持续14天。他们发现,在补充期间,每克粪便中的Faecalibacterium prausnitzii数量增加。作者还注意到厌氧菌Roseburia 增加,大肠杆菌减少。
其他关于B族维生素对肠道菌群的影响详见:
/ 维生素C /
补充维生素 C 可减少肠杆菌科细菌的数量,增加乳酸杆菌的丰度,抑制有害菌的生长,促进有益菌的增加。
也有研究表明,维生素 C 服用4周导致 α 多样性增加,短链脂肪酸浓度增加。

/ 维生素D /
维生素 D 和肠道微生物群的相互作用对免疫稳态至关重要。补充高水平的维生素 D 增加了普氏菌,减少了韦荣氏菌和嗜血杆菌。
婴儿饮食中补充维生素 D 对早期微生物组成的变化有重要影响,而儿童缺乏维生素 D 会导致细菌多样性降低。
最近的一项研究表明,维生素D的活性代谢物1,25-二羟基胆钙化醇,维生素D受体的配体(VDR),影响美国不同地区老年人肠道菌群的α -和β -多样性。
研究人员报告了通过食物频率问卷评估的微量营养素摄入量与孕妇微生物群组成之间的相关性。他们观察到,高脂溶性维生素,特别是维生素D的膳食摄入量与微生物α多样性降低有关(P值<0.001),维生素D和视黄醇与变形菌相对增加有关,变形菌门是一个已知包含多种病原体并具有促炎特性的门。
/ 维生素E /
维生素E对变形菌有抑制作用,而维生素E(和纤维)的摄入量较低与Sutterella水平较高相关,据报道,自闭症和某些胃肠道疾病婴儿的Sutterella水平大量增加。
体外维生素E 可以防止几种人类病原体的生物膜形成,特别是金黄色葡萄球菌和表皮葡萄球菌。
/ 维生素K /
一项动物实验表明,缺乏维生素 K 的小鼠的肠道中,瘤胃球菌、毛螺菌科、Muribaculaceae的含量较多。
关于维生素对人体肠道微生物组直接影响的研究
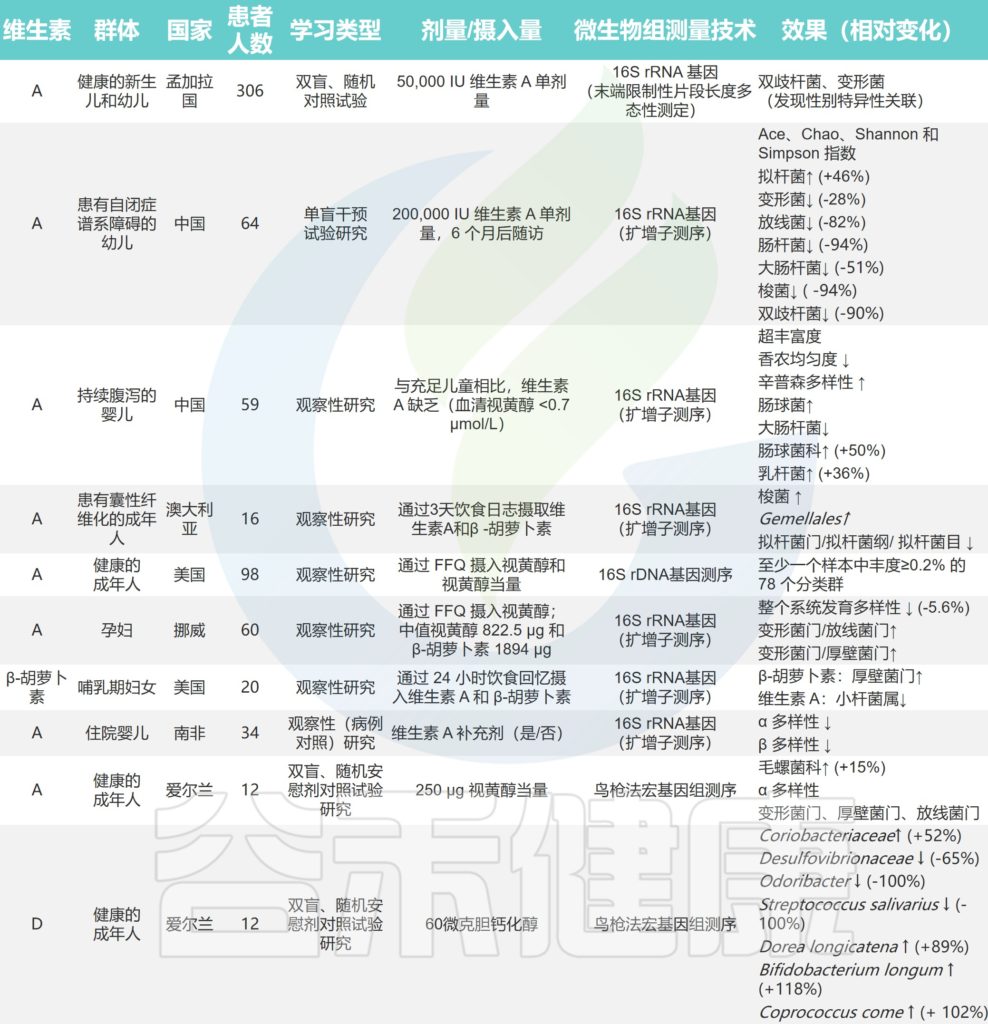
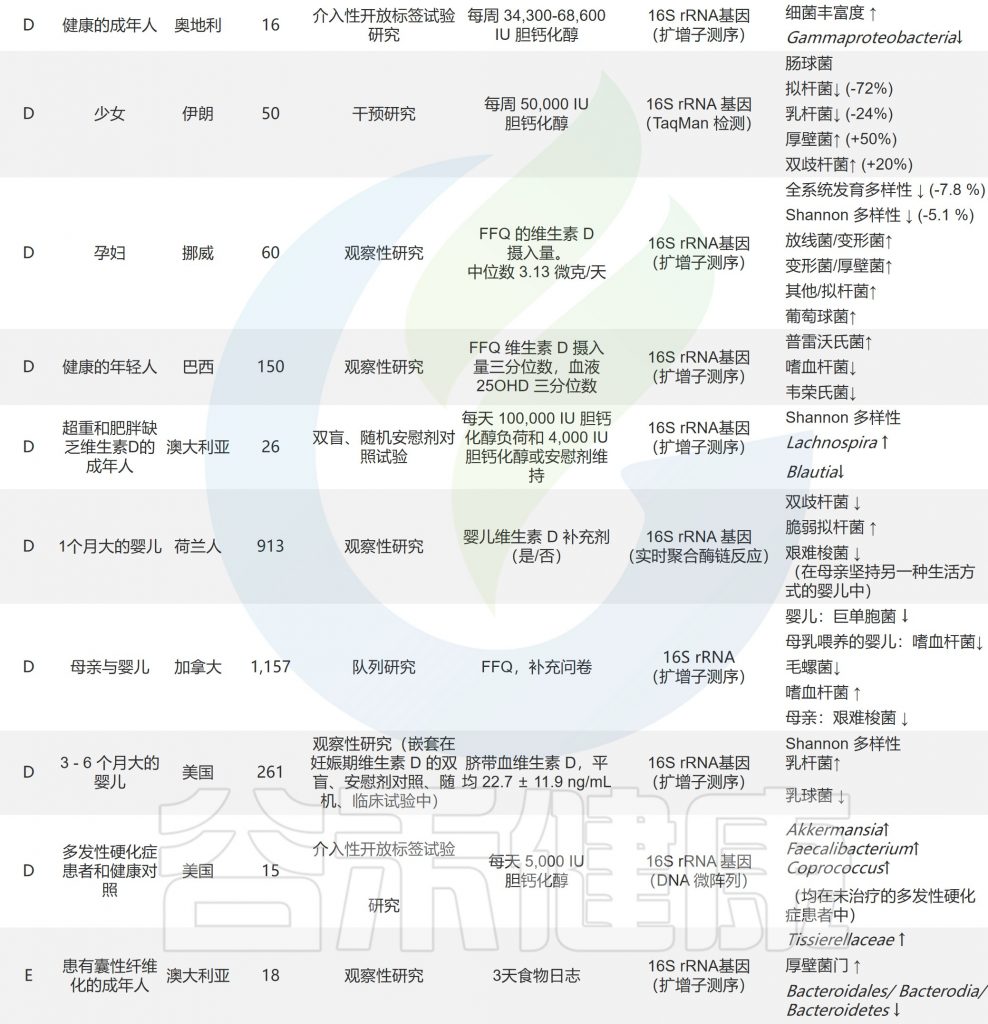
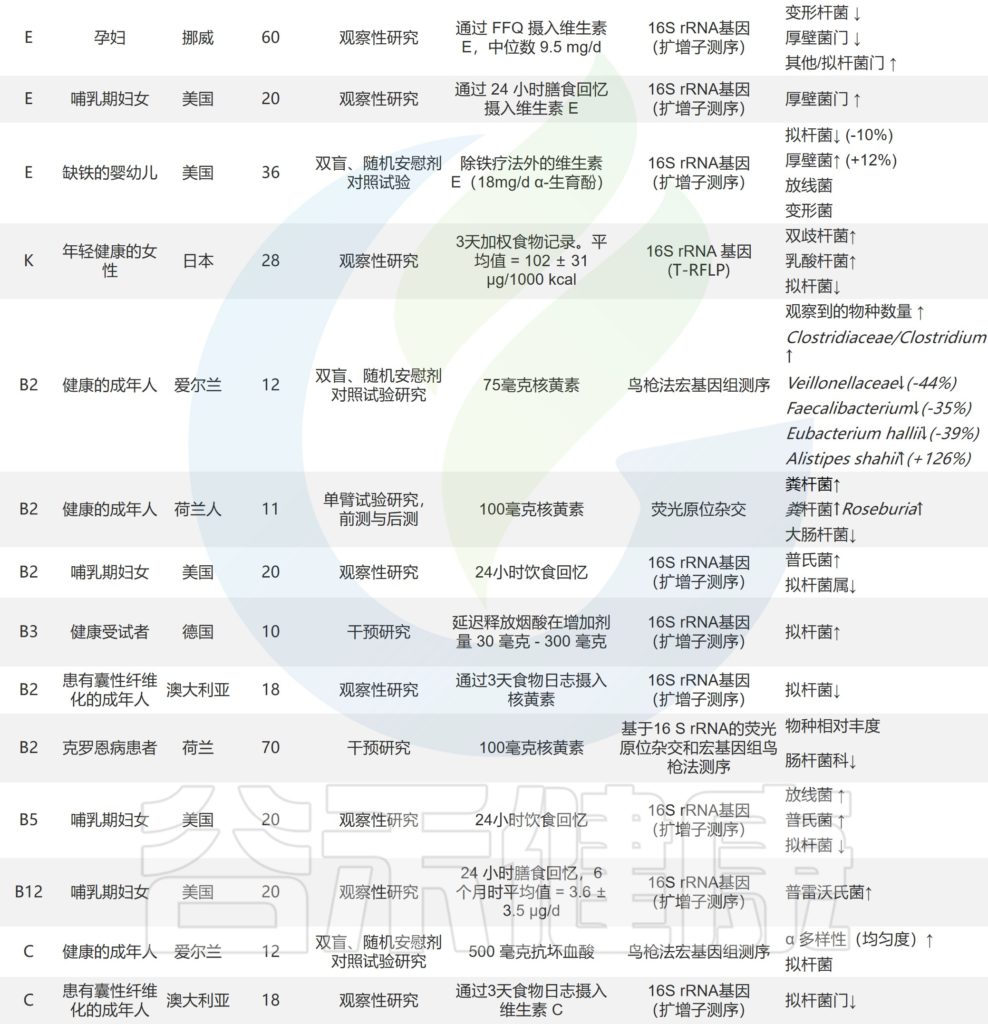
doi.org/10.1016/j.nutres.2021.09.001
饮食是维生素的主要来源,通过饮食补充维生素也会影响菌群。
注:由于测试饮食干预效果所需的随机试验的样本量和持续时间,相关发病率的研究具有挑战性。此外,由于特定的营养素不是孤立地消耗的,而是作为饮食模式的一部分,并且饮食成分之间相互作用,因此饮食带来的实际影响可能只有作为一个整体考虑时才会变得明显。
因此这里我们主要考虑饮食模式,例如地中海饮食等饮食方式。
地中海饮食是营养均衡饮食的典型代表,其特点是大量且频繁地摄入重要的纤维来源(谷物、蔬菜、豆类、水果和坚果)和具有抗氧化特性的化学成分(维生素、类黄酮、植物甾醇、矿物质、萜烯和酚类)。

同时地中海饮食还富含复杂和不溶性纤维含量。我们知道,大量摄入膳食纤维可促进肠道中有益菌群的生长,例如增加拟杆菌、普雷沃氏菌属、罗斯氏菌属、瘤胃球菌属、普拉梭菌等菌属的丰度,从而在肠道中产生高水平的短链脂肪酸,包括丁酸盐。
响应地中海饮食而增殖的细菌可以充当“基石”物种,也就是说它们对于稳定的“肠道生态系统”至关重要。这些变化主要是由于膳食纤维和相关维生素和矿物质的增加,特别是维生素C、B6、B9、铜、钾、铁、锰和镁。
总之,维生素似乎是微生物-宿主间代谢相互作用的重要媒介。
越来越多证据表明,维生素缺乏会导致肠道菌群紊乱,进而引发肠道疾病,甚至促进炎症和肿瘤的发展。下一章节详细讨论,维生素-微生物群相互作用对健康/疾病的影响。
最近的几项观察表明,微生物群失调和维生素缺乏是相互关联的。
维生素对宿主健康的影响

doi.org/10.1016/j.nutres.2021.09.001
这种关系可能直接影响宿主健康:例如,克罗恩病恶化与参与抗炎介质核黄素、硫胺和叶酸生物合成的微生物基因减少有关。
此外,2型糖尿病受试者在与微生物介导的维生素代谢相关的基因丰度谱中显示出显著变化。
营养不良儿童的微生物群显示,参与B族维生素代谢的多种途径(包括烟酸/NADP生物合成)显著减少。
在经历饮食振荡以诱导急性短期维生素A缺乏的灵长类小鼠模型中,Hibberd等人观察到细菌群落结构和宏转录组的调节,其中Bacteroides vulgatus是显著的应答者,在缺乏维生素A的情况下其丰度增加。有趣的是,B.vulgatus是在人类肠道微生物群的灵长类小鼠模型中鉴定的一种生长差异物种。
所有这些观察结果表明,维生素缺乏可能会改变肠道微生物群,从而影响人体健康。
下面我们以肠道疾病和精神类疾病两大类疾病为例,来具体了解维生素-微生物相互作用及其在疾病中的影响。
维生素 A 和 D 分别在近端和远端空肠吸收。维生素E和K主要在回肠吸收;微生物产生的维生素主要在结肠中吸收。维生素缺乏会加重肠道炎症,甚至通过多种机制促进癌症。
肠道菌群->维生素->肠道疾病中的作用
慢性 IBD 发生和发病机制中的关键作用是微生物(尤其是共生菌群)对宿主黏膜免疫功能的影响。同时,肠道微生物群和慢性炎症已被证明与肿瘤发生密切相关。
维生素具有调节肠道菌群和保护肠道的功能。因此,维生素和微生物群的相互作用可能在 IBD 和结直肠癌的治疗中具有巨大的潜力。
维生素A通过促进黏膜愈合、促进产生ASCFA的相关菌增加、降低UC相关菌的水平来达到治疗UC的效果。
费氏丙酸杆菌ET-3 产生维生素 K2 的前体,即 1,4-二羟基-2-萘甲酸 (DHNA),可激活芳烃受体 (AhR) 以改善结肠炎并调节肠道微生物群。
维生素 D 的缺乏会增加拟杆菌门、变形杆菌门和螺杆菌科的丰度,降低厚壁菌门和去铁细菌的丰度门,并且还影响 E-钙粘蛋白表达并减少耐受树突状细胞的数量。
然而,在治疗 IBD 时,维生素 D 与利福昔明的共同给药会影响肠道菌群和利福昔明的疗效。维生素 D 促进A. muciniphila的生长以保护肠粘膜屏障,这些作用对于对抗结直肠癌的发展尤为重要。
研究表明,维生素 E 及其代谢物在调节肠道菌群、减少炎症和抑制癌变方面具有巨大潜力。此外,维生素 Eδ-生育三烯酚 (δTE) 及其代谢物δTE-13′-羧基色原酚 (δTE-13′) 增加了肠道中的乳球菌和拟杆菌,并抑制炎症因子的产生。
维生素->肠道菌群->肠道疾病中的作用
▸维生素在IBD和结直肠癌中的作用不容忽视
大量临床研究表明,缺乏维生素 B 和维生素 D 的人群中结直肠癌的患病率较高。同时,IBD 的长期不愈合使患者面临更高的结直肠癌风险。维生素 D 水平低的 IBD 患者疾病严重程度和预后较差。
▸为什么肠道炎症容易导致癌症高风险?
在炎症背景下,敲除 IKKbetaβ(炎症与癌症之间的联系)可减少由于上皮细胞凋亡增加而导致的癌症发生。在一项关于结肠炎相关癌前癌 (CApC) 的研究中,IL-6 反式信号转导的存在增加了炎症性致癌的风险。如果不及时治疗,由肠道菌群紊乱和维生素缺乏引起的肠道炎症最终可能发展为癌症。
维生素 A 在肠道炎症和癌症中的作用
维生素 A 及其活性代谢物视黄酸 (RA) 在人体免疫系统中发挥着关键作用,并可能对辅助 T 细胞的分化产生影响。
炎症下:视黄酸从保护转变为破坏作用
在非炎症条件下,视黄酸能够抑制 IL-6 受体的表达和 Th1/Th17 的产生。
在炎症条件下,视黄酸从对粘膜的保护作用转变为破坏作用;这反映在活动期 IBD 患者黏膜中视黄酸水平显着升高,伴随着 CD4 和 CD8 分泌的 IL-17 和 IFN-γ 的上调。
维生素A及其代谢物:发挥抗炎作用
维生素 A 及其代谢物通过阻断 Th1 和 Th17 的激活,抑制 IL-17、INF-γ 和 TNF-α 的产生而显示出抗炎作用。同时,它们可以通过与TGF-β协同作用,提高Foxp3的水平,发挥免疫功能,从而促进抗炎因子的发挥。
一项数据显示,低水平的维生素 A 会激活核 NF-kB 并促进胶原蛋白的形成,从而加剧结肠炎的炎症。补充维生素后,肠道炎症明显缓解。
全反式维甲酸 (AtRA) 可降低 UC 和结直肠癌患者结肠黏膜分泌的 TNF-α 和一氧化氮合酶 2 (NOS2) 蛋白的表达。

维生素A保护肠黏膜屏障,其潜在机制是拮抗LPS的肠道破坏作用
在一项关于维生素 A 缺乏对结肠炎和结直肠癌发展的影响的检查中,研究人员使用葡聚糖硫酸钠 (DSS) 诱导小鼠结肠炎;此外,偶氮甲烷 (AOM) 预注射和 DSS 结肠炎的组合诱导了结直肠癌。缺乏维生素的小鼠肠道炎症水平较高,黏膜愈合较慢,免疫反应增强,更容易发生结直肠癌。
AtRA具有抗癌作用,结直肠癌中AtRA 水平降低
在结直肠癌小鼠模型中,肠道细菌引起的炎症影响 AtRA 代谢;这导致其水平下降。在 UC 及其相关结直肠癌的临床样本中发现 AtRA 代谢酶活性降低和 AtRA 水平降低。同时,AtRA通过激活CD8 + T细胞发挥抗癌作用;这为 CAC 的治疗提供了新的见解。
视黄醇和视黄醇结合蛋白(RBP)的结合激活致癌基因STRA6,促进结直肠癌的发生;Holo-RBP/STRA6 通路可通过促进成纤维细胞的致癌作用进一步发挥致癌作用。
在一项关于维生素 A 缺乏对结肠炎和结直肠癌发展影响的动物实验中,当维生素 A 处于低水平时,小鼠体内的维生素 A 脂滴会被降解,免疫反应会增强,结肠炎症会加重,癌变进程将加快。
维生素 B12 和叶酸在肠道炎症和癌症中的作用
IBD 患者缺乏维生素 B12 和叶酸的原因有很多,包括回肠和空肠微生物过度生长、维生素 B12 摄入不足或身体需求增加、维生素肠道破坏增加或吸收能力降低、某些药物(如甲氨蝶呤或柳氮磺胺吡啶)的不良反应、一些病理原因例如蛋白丢失性肠病、肝功能异常、回肠相关病变或手术切除、肠瘘等。
维生素 B12 缺乏不会影响健康的肠道微生物群组成;然而,它会导致实验性结肠炎中肠道菌群失调,并促进条件致病菌的生长。出乎意料的是,维生素 B12 缺乏减少了结肠组织的损伤;这可能与抗炎细胞因子 IL-10 的增加有关。

对甲基缺乏饮食 (MDD) 的潜在作用进行了一项研究,该饮食可降低维生素 B12 和叶酸的血浆浓度,并提高同型半胱氨酸水平,对 DSS 诱导的小鼠结肠炎的影响。喂食 MDD 的 DSS 治疗小鼠比其他治疗组患有更严重的结肠炎。
尽管超氧化物歧化酶和谷胱甘肽过氧化物酶活性保持稳定,但 caspase-3 和 Bax 的水平受到影响。除Bcl-2表达增加外,炎症相关标志物如胞质磷脂酶A2和环氧合酶2的表达也有明显增加趋势;这伴随着金属蛋白酶组织抑制剂(TIMP)3蛋白的表达降低。因此,维生素 B12 缺乏可能会加重实验性 IBD 的炎症程度。
高维生素 B12 水平可通过减少 DNA 甲基化来降低结直肠癌的风险
在结直肠癌患者中,与低血清维生素 B12 组相比,高维生素 B12 组的肿瘤区域和外周血单个核细胞 (PBMC) 中长散布的核元素 1 (LINE1) 甲基化被证明是降低的;肿瘤区域的LINE1甲基化水平也低于周围的非肿瘤区域。
氧化应激是结直肠癌发病机制之一;此外,叶酸和维生素 B12 的水平与体内抗氧化剂谷胱甘肽的水平呈正相关。提高 AOM 诱导的结直肠癌中的叶酸和维生素 B12 水平显示出显着的抗凋亡、抗氧化应激和抗 AOM 细胞毒性。
在对 4517 名 IBD 患者的系统评价和荟萃分析中,补充叶酸被证明可以降低 IBD 患者的结直肠癌风险并防止结直肠癌发展。
有趣的是,有证据表明缺乏甲基供体营养素叶酸、胆碱、蛋氨酸和维生素 B12 会抑制 Apc 突变小鼠的肿瘤发展。总而言之,维生素B12和叶酸在肠道疾病中的作用需要更深入的研究。
维生素 D 在肠道炎症和癌症中的作用
流行病学和动物实验表明,维生素 D 缺乏是 IBD 和 结直肠癌的高危因素。维生素 D 补充剂有助于降低疾病严重程度,可能通过多种机制,包括调节免疫细胞运输和分化,以及抗菌肽合成。
维生素D可以维持肠黏膜屏障的正常功能,提高机体的先天性和适应性免疫
1α,25-二羟基维生素 D3(骨化三醇)是维生素 D 的活性形式,可与 TGF-β 结合,提高 IL-2 水平,调节 T 细胞抑制炎性细胞因子的产生,增强 Foxp3 + Treg 细胞的存活和功能。

维生素D受体(VDR)是维生素D调节免疫和发挥抗炎作用的重要途径
相关资料显示,VDR对肠道有保护作用;它可以通过调节 JAK/STAT 通路来维持肠道稳态并预防癌症。
在 IBD 患者 中,结肠上皮中VDR的含量明显低于正常人。在实验性结肠炎模型中,与缺乏 VDR 的小鼠相比,表达 hVDR 的转基因小鼠的结肠炎症较少。用 hVDR 转基因恢复上皮 VDR 表达可减轻严重结肠炎并降低死亡率。内在机制是 VDR 通过抑制 NF-κB 活化发挥抗凋亡作用,以保护肠道屏障缓解结肠炎。
肠道菌群通过犬尿氨酸通路(合成维生素),在精神健康方面发挥作用
关于肠道细菌在心理健康方面的作用的关键方面,是它们通过犬尿氨酸通路参与调节色氨酸代谢。微生物群能够合成犬尿氨酸途径 (KP) 的酶促辅助因子,如维生素 B2 和 B6。

犬尿氨酸是主要的色氨酸代谢途径,其中 95% 的这种氨基酸被代谢为各种免疫和神经调节犬尿氨酸/色氨酸分解代谢物 (TRYCAT),在大脑中,犬尿氨酸途径主要在神经胶质细胞中分隔。
犬尿氨酸通路在精神、神经退行性和神经系统疾病中的作用是至关重要的,包括重度抑郁症,双相情感障碍,精神分裂症,阿尔茨海默病,亨廷顿病和帕金森病,与 HIV 感染相关的痴呆,手术后认知能力下降,肌萎缩侧索硬化(ALS) 等。
精神病理学和炎症中维生素缺乏与高同型半胱氨酸血症有关
精神病理学和炎症中维生素缺乏的另一个关键机制与高同型半胱氨酸血症(hHcy)有关,这可能是由叶酸、维生素 B6 和 B12 缺乏引起的。
高同型半胱氨酸血症和维生素 B 缺乏在重度抑郁症、精神分裂症、双相情感障碍、自闭症、焦虑症和痴呆症(包括阿尔茨海默病和帕金森病)中起关键作用。
同型半胱氨酸(Hcy)是在蛋白质消化过程中获得的另一种氨基酸蛋氨酸代谢过程中形成的氨基酸和中间体。该反应需要维生素 B12 作为酶促辅因子和叶酸衍生物(5-甲基四氢叶酸)作为甲基供体。
注:Hcy-同型半胱氨酸,是人体内含硫氨基酸的一个重要的代谢中间产物,可能是动脉粥样硬化等心血管疾病发病的一个独立危险因子。
此外,Hcy 可以在需要维生素 B6 作为酶辅因子参与的途径中转化为半胱氨酸。
因此,Hcy 被认为是叶酸和维生素 B12 缺乏的敏感标志物。
高同型半胱氨酸血症导致神经和精神病理学的机制包括:
促进免疫炎症反应、增加肠道和血脑屏障通透性、NMDA受体激动和神经毒性、诱导神经元凋亡、氧化应激、线粒体功能障碍和由于甲基化受损导致的单胺能神经递质合成失调。
目前对体内维生素水平的检测例如:
抽取血液检测其中维生素的含量水平,可以判断是否存在维生素的缺乏情况。
其他,例如通过肠道菌群健康检测,也可以查看近期体内维生素状况。
与通过血液进行维生素检测不同,肠道菌群的评估更加反映一段时间 ( 一般2周左右 ) 的长期状态,如部分B族维生素无法在体内留存,需要每日补充,血液检测波动较大。
注:菌群会受检测前一天饮食的影响,造成15~30%的菌群改变,同样也会反映在营养状况的评估上,因此建议检测前一天尽量保持近期正常饮食 ,这样能更好的反映真实的营养饮食状态。
在了解补充维生素的干预措施之前,我们先从肠道菌群的角度,来了解一下影响维生素合成吸收的因素。
人类基因的变异与肠道结构和微生物组组成有关。人类肠道微生物群中存在不同的维生素 B 生物合成途径支持人类遗传变异影响维生素 B 合成的观点。
维生素的合成吸收不仅需要靠饮食补充,还与吸收相关。而维生素的吸收涉及到相关基因,例如:
MTHFR 基因的突变会影响我们产生加工维生素 B9的酶——亚甲基四氢叶酸还原酶。
亚甲基四氢叶酸还原酶是叶酸代谢通路中的一种重要的辅酶,亚甲基四氢叶酸还原酶基因缺陷,容易造成叶酸在体内的代谢障碍,MTHFR基因最主要的两种突变为C677T、A1298C基因多态性。该两种位点同时突变可显著降低MTHFR活性进而降低叶酸水平。
VDR基因(维生素 D 受体):维生素 D(来自阳光、食物或补充剂)经过转化步骤后,活性形式骨化三醇 (1,25(OH)2D3 ) 可以通过VDR在细胞内发挥作用,是打开或关闭基因的转录因子。该基因突变可能导致维生素D缺乏引起的佝偻病。
维生素缺乏是一个严重的问题,尤其是在老年人中。随着年龄的增长,营养需求会随之变化。
由于食物中的维生素B12 需要胃酸及胃蛋白酶的作用才能释放出来被吸收,而老年人胃酸及胃蛋白酶分泌减少,就会影响维生素B12 的吸收。
患有维生素B12缺乏症的老年人可能出现神经精神或代谢缺陷。
一些药物会改变营养物质的吸收或代谢方式。例如,抗惊厥药也会减少叶酸的吸收。
肠道菌群通过各种代谢途径影响维生素的合成,例如拟杆菌属、肠球菌属和双歧杆菌属等人类肠道共生菌可以从头合成维生素 K 和大多数水溶性 B 族维生素,这在前面第二章节的表已经详细阐述。
在 B 族维生素合成中暴露于抗生素的反应因使用的抗生素类型而异。例如,在饮食中添加青霉素和金霉素会增加雄性大鼠的肝脏维生素 B2 浓度,以及 B2 和 B3 在尿液中的排泄。然而,链霉素和放线菌酮的施用降低了肝脏中维生素 B9 和 B12 的浓度。维生素合成对抗生素暴露的混合反应尚不清楚,但它们可能是由肠道微生物群的选择性改变引起的。
自由基是含有不成对电子的化学物质,可以诱导氧化应激。一个这样的例子是一氧化氮,它与金属离子形成复合物,包括钴,维生素 B12 的一种结构成分,因此使其无法用于细菌维生素 B12 的生物合成。此外,维生素生产者(如脆弱拟杆菌)暴露于过氧化氢等自由基会抑制其生长 ,从而降低维生素的生物合成能力。
维生素主要在小肠中吸收,其生物利用度取决于食物成分,相关相互作用等。
饮食和膳食的组成会通过影响肠道转运时间和/或混合胶束的肠道形成来影响某些维生素的吸收。
饮食中足量的水和膳食脂肪对于分别吸收水溶性和脂溶性维生素至关重要。
*水溶性维生素包括:B族维生素,维生素C;
脂溶性维生素包括:维生素 A、D、E 、K.
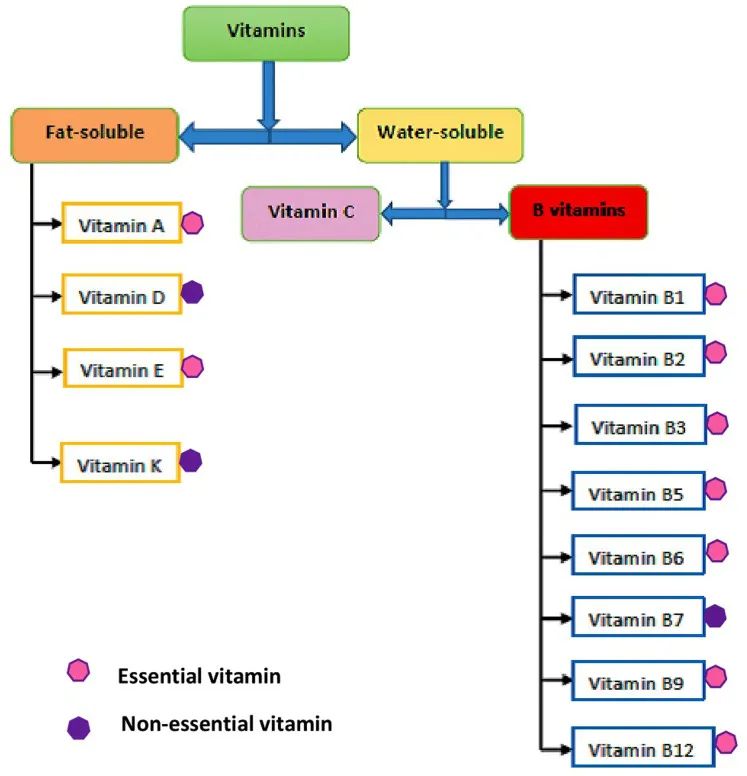
doi: 10.7717/peerj.11940
由于脂溶性维生素可以溶解在脂肪中,因此与膳食脂肪一起食用时最容易被吸收。例如,一种富含维生素 A 的小胡萝卜,如果单独食用,将在食物中获取维生素 A,但如果它是在含有一些膳食脂肪的食物成分中(比如说,橄榄油),将增加体内维生素 A 的吸收。
食物的性质(物理状态)也会影响维生素的吸收效率。例如,存在于可消化性较差的纤维植物材料中的类胡萝卜素已被证明相对于维生素A表现出较低的生物利用度。
当我们看到维生素缺乏的时候,可能希望通过饮食来补充相应缺乏的维生素,下表列出了常见的维生素的食物来源,可供参考。
此外,宿主饮食作为肠道中细菌的底物,其对肠道微生物分布的影响已被广泛研究。含有益生元和其他膳食营养素(如微量营养素和多酚)的饮食可以显着影响有益细菌的生长,包括维生素生产菌。
一些维生素,如核黄素,可作为氧化还原介质并刺激营养缺陷菌(如Faecaibacterium prauznitsii)的生长。
在即将形成共生关系的环境中,限制这些基质会增加微生物和微生物与宿主之间的竞争。
除了通过饮食直接补充之外,我们还可以通过补充益生菌来调节维生素水平,从而改善疾病。
双歧杆菌
在健康成人中补充益生菌菌株青春双歧杆菌DSM 18350、青春双歧杆菌DSM 18352 和假链双歧杆菌DSM 18353,导致粪便中叶酸浓度显着增加。
乳酸菌
乳酸菌通过不同的机制抑制炎症过程,包括调节IBD患者肠道菌群紊乱、保护肠道屏障和黏膜的正常功能、调节人体免疫反应等。乳酸菌通过产生核黄素(维生素 B2)和叶酸发挥抗炎和抗氧化作用。
产维生素的乳酸菌不仅对急性肠炎有抗炎作用,还能有效缓解复发性结肠炎。此外,在与美沙拉秦合用过程中,可有效降低不良反应,提高疗效。
研究人员发现注射产生叶酸的乳酸菌会缓解 5-FU 引起的肠炎小鼠的腹泻,改善结肠组织的结构和功能。这一发现降低了癌症化疗期间发生的肠黏膜炎症的严重程度,并提高了药物有效性;因此,这提高了患者的生活质量。
此外,乳酸菌 和 5-FU 的联合使用可减少 5-FU 引起的血细胞计数减少,并使患者获得完整的治疗周期。
产维生素的益生菌在肠道疾病中的作用

doi.org/10.3390/nu14163383
研究人员从 150 个收集的人类粪便样本中分离出三种产生核黄素和叶酸的益生菌;他们用它们来治疗乙酸引起的大鼠结肠炎。他们发现这些益生菌可以保护结肠黏膜,促进溃疡性病变的愈合;此外,它们具有抗炎和抗氧化应激作用。
一种新分离的具有产生叶酸能力的细菌——清酒乳杆菌LZ217,具有促进丁酸产生和改善肠道菌群组成的作用。
Akkermansia muciniphila 是肠道中的一种常见细菌,可调节 CLT 以保护肠道免受炎症和肿瘤侵袭;它还产生维生素 B12 以缓解 IBD 患者的维生素缺乏症。
研究发现,丙酸杆菌菌株 P. UF1 合成维生素 B12;这对肠道免疫和肠道健康有积极的调节作用。
大肠杆菌通过产生维生素来缓解 IBD. 使用大肠杆菌生产两种产生β-胡萝卜素的菌株来治疗维生素A缺乏症。这些结果显示出巨大的临床潜力。
维生素 A 及其代谢物与短乳杆菌KB290 的组合提高了 CD11c + MP/CD103-DC 比率;因此,这在结肠炎的治疗中起着积极的作用。
此外,肠道中的分段丝状细菌 (SFB) 可以产生 AtRA,以抵消感染对肠道的损害。
益生菌对维生素D及其受体活性有积极作用,如鼠李糖乳杆菌GG(LGG)和植物乳杆菌(LP);同样在沙门氏菌结肠炎模型中,使用 VDR (-/-) 小鼠验证 LGG 对 IBD 的缓解作用是通过 VDR 信号通路。
此外,胆汁盐水解酶 (BSH)活性罗伊氏乳杆菌NCIMB 30,242 可调节血浆中的活性维生素 D 水平。磷虾油 (KO)、益生菌罗伊氏乳杆菌和维生素 D 的混合物显着降低病理评分和炎症因子的释放,促进黏膜愈合并减少机会性感染的发生。
经益生菌 VSL#3 预处理后,VDR 水平显着提高,共同保护肠黏膜,防止损伤;这对预防CRC的发展起到一定的作用。
用从韩国泡菜中分离的乳酸菌条件培养基处理 HCT116 细胞或肠类器官后,其分泌的蛋白质 P40 和 P75 与 VDR 的表达增加有关;它们还增强自噬反应,共同具有抗炎作用。肠道微生物合成的石胆酸 (LCA) 充当连接 VDR 与微生物的桥梁,从而提高维生素 D 水平。
益生菌配方有助于抑郁症患者维生素水平的增加
一项随机对照试验中,重度抑郁症患者接受了多种益生菌配方,其中含有双歧杆菌W23、乳双歧杆菌W51、乳双歧杆菌W52、嗜酸乳杆菌W22、干酪乳杆菌W56、副干酪乳杆菌W20、植物乳杆菌W62、唾液乳杆菌W24、乳酸乳杆菌W19。
此外,益生菌组和安慰剂组的患者接受了相同剂量的维生素 B7。在两组中,抑郁症的临床参数都有所改善,然而,益生菌干预组与安慰剂组相比,仅在微生物 β 多样性方面存在差异,临床结果指标没有差异。有趣的是,尽管两组都接受了相同剂量的生物素,但接受益生菌的那组维生素 B6 和 B7 的合成上调。
多种益生菌相结合通过增加叶酸和维生素 B12血浆水平,改善精神疾病
八周的个性化饮食与含有多种益生菌的菌株相结合:婴儿双歧杆菌DSM 24737、长双歧杆菌DSM 24736、短双歧杆菌DSM 24732、嗜酸乳杆菌DSM 24735 、德氏乳杆菌、保加利亚乳杆菌DSM 24734、副干酪乳杆菌DSM 24733、植物乳杆菌DSM 24730 、嗜热链球菌DSM 24731 (VSL#3),在健康老年人中增加了叶酸和维生素 B12 血浆水平并降低了 Hcy 血浆水平。
此外,益生菌的添加导致粪便双歧杆菌浓度增加,这种变化与叶酸和维生素 B12 水平呈正相关。
在精神病患者中引入高同型半胱氨酸的评估和治疗可能非常有价值,益生菌可能成为治疗工具之一。
维生素是相互关联的、具有协同作用的微量营养素,当它们处于适当的平衡状态时,它们的全部潜力就会得到充分发挥。
因此,在食用益生菌和发酵食品时,应考虑维生素生产者与代谢者之间复杂的相互作用。
除了以上方式干预菌群之外,也可以通过良好的生活方式调理菌群,从而使维生素达到一个相对健康稳定的水平,减少各类疾病风险。
▸在服用维生素的同时可以服用益生菌吗?
可以。在大多数情况下,服用益生菌不会影响其他补充剂的效果。
一项 2021 年对临床试验的系统评价发现,益生菌可以改善健康人群的微量营养素水平,特别是维生素 B12、叶酸(维生素 B9)、钙、铁和锌。
2017 年的一项非随机临床试验发现,服用益生菌和铁补充剂的参与者比不服用益生菌的铁吸收明显更多。
有研究表明,维生素 D 和益生菌之间存在协同关系。
随机对照试验发现,维生素 D 补充剂与益生菌一起可以改善多囊卵巢综合征患者和同时患有冠心病的糖尿病患者的各种心理健康参数、一般健康状况、代谢和炎症标志物。
2019 年对随机对照试验的系统评价和荟萃分析发现,维生素 D 强化酸奶(富含益生菌嗜酸乳杆菌)有助于改善维生素 D 和胆固醇水平、代谢功能和身体测量值。
然而以上研究都没有单独研究维生素 D 和益生菌的作用,因此尚不清楚结果是否与两者的综合影响有关。
研究人员认为,无论有没有维生素,服用益生菌的时间很重要。作为一般规则,服用益生菌的最佳时间是空腹,大约在进食前 30 分钟。
研究人员担心胃酸的存在会影响益生菌的生存能力。在餐前或餐后几个小时服用时,当胃酸自然降低时,益生菌可以进入肠道,从而提高其生存几率。
何时服用维生素取决于维生素的种类。复合维生素通常最好在早上第一时间服用,非常适合搭配早餐前的益生菌。脂溶性维生素,如 A、D、E 和 K 以及一些矿物质,包括铁和镁,最好与食物一起服用。否则可能会导致胃部不适。
▸应该从食物中补充维生素还是通过维生素补充剂?
2020 年的一篇文献综述发现,与浓缩补充剂相比,许多微量营养素在其全食物形式中的生物利用度更高。因此提倡补充方式以食物为先。
一般认为,对于健康人来说,营养均衡的饮食可以提供身体需要的维生素,不需要额外补充,但对于可能存在免疫功能、肠道健康、吸收不良等问题的人群,可以考虑维生素补充剂进行补充,具体补充剂量请遵医嘱。
下表是维生素易缺乏的高风险人群:

▸可以长期服用维生素补充剂吗?补充过量会带来副作用吗?
一般健康人不需要长期服用维生素补充剂。
对于服用复合维生素片,多余的维生素会被排出体外,因此不用过于担心会带来危害。但是如果长期十倍以上的用量,对身体是有危害的。

doi: 10.7717/peerj.11940
在发现维生素缺乏的症状的时候,我们可能希望通过补充相应的维生素补充剂来改善健康。然而服用任何补充剂之前,我们应该寻找其根本原因而不是直接根据症状盲目补充。
通过肠道菌群健康检测可以了解维生素缺乏状况,且可以根据各类菌群丰度来推断维生素的菌群代谢状况。如果是由于菌群的代谢异常,可能直接补充并没有太大效果,这时候优先调节菌群或许是更好的选择。
如果维生素指标都显示正常没有缺乏(如下图),保持常规饮食不需要刻意补充。还想要更健康,指标更接近70的话,可以在数值略小的指标上,针对性地通过饮食进行补充调理。
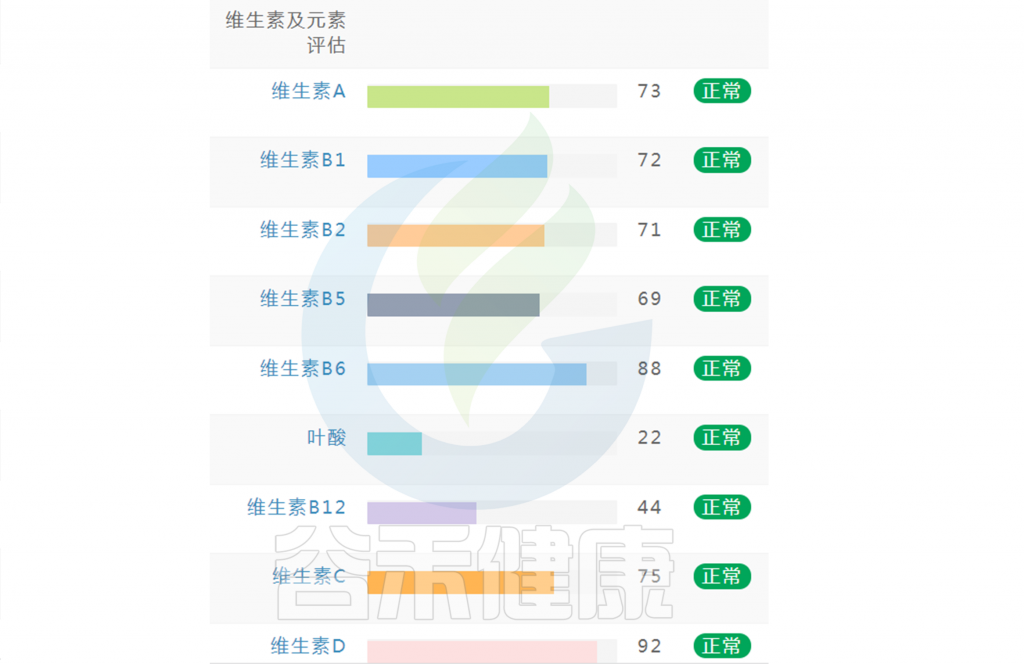

如果维生素指标中出现个别指标缺乏或偏低(如下图),可以通过饮食针对性地进行改善调整,如果已经出现对应症状,例如缺乏维生素A,同时出现干眼症或者夜盲症等相应的症状,可以使用相应的维生素补充剂进行干预,或者根据菌群代谢通路判别,通过菌群调理进行相应干预。
如果维生素指标中出现缺乏或偏低的指标较多,则需要选用复合维生素,各类维生素之间可能存在协作关系,同时配合饮食、菌群进行干预。
选择补充剂,应优先考虑生产规范良好的产品,比如说可以查看是否有“OTC”标志。
注:本账号内容仅作交流参考,不作为诊断及医疗依据。
主要参考文献:
Zhai Z, Dong W, Sun Y, Gu Y, Ma J, Wang B, Cao H. Vitamin-Microbiota Crosstalk in Intestinal Inflammation and Carcinogenesis. Nutrients. 2022 Aug 17;14(16):3383. doi: 10.3390/nu14163383. PMID: 36014889; PMCID: PMC9414212.Zhai Z, Dong W, Sun Y, Gu Y, Ma J, Wang B, Cao H. Vitamin-Microbiota Crosstalk in Intestinal Inflammation and Carcinogenesis. Nutrients. 2022 Aug 17;14(16):3383. doi: 10.3390/nu14163383. PMID: 36014889; PMCID: PMC9414212.
Bellerba F, Muzio V, Gnagnarella P, Facciotti F, Chiocca S, Bossi P, Cortinovis D, Chiaradonna F, Serrano D, Raimondi S, Zerbato B, Palorini R, Canova S, Gaeta A, Gandini S. The Association between Vitamin D and Gut Microbiota: A Systematic Review of Human Studies. Nutrients. 2021 Sep 26;13(10):3378. doi: 10.3390/nu13103378. PMID: 34684379; PMCID: PMC8540279.
Ofoedu CE, Iwouno JO, Ofoedu EO, Ogueke CC, Igwe VS, Agunwah IM, Ofoedum AF, Chacha JS, Muobike OP, Agunbiade AO, Njoku NE, Nwakaudu AA, Odimegwu NE, Ndukauba OE, Ogbonna CU, Naibaho J, Korus M, Okpala COR. Revisiting food-sourced vitamins for consumer diet and health needs: a perspective review, from vitamin classification, metabolic functions, absorption, utilization, to balancing nutritional requirements. PeerJ. 2021 Sep 1;9:e11940. doi: 10.7717/peerj.11940. PMID: 34557342; PMCID: PMC8418216.
Steinert RE, Lee YK, Sybesma W. Vitamins for the Gut Microbiome. Trends Mol Med. 2020 Feb;26(2):137-140. doi: 10.1016/j.molmed.2019.11.005. Epub 2019 Dec 17. PMID: 31862244.
Pham VT, Dold S, Rehman A, Bird JK, Steinert RE. Vitamins, the gut microbiome and gastrointestinal health in humans. Nutr Res. 2021 Nov;95:35-53. doi: 10.1016/j.nutres.2021.09.001. Epub 2021 Oct 21. PMID: 34798467.
Hossain KS, Amarasena S, Mayengbam S. B Vitamins and Their Roles in Gut Health. Microorganisms. 2022 Jun 7;10(6):1168. doi: 10.3390/microorganisms10061168. PMID: 35744686; PMCID: PMC9227236.
Rudzki L, Stone TW, Maes M, Misiak B, Samochowiec J, Szulc A. Gut microbiota-derived vitamins – underrated powers of a multipotent ally in psychiatric health and disease. Prog Neuropsychopharmacol Biol Psychiatry. 2021 Apr 20;107:110240. doi: 10.1016/j.pnpbp.2020.110240. Epub 2021 Jan 9. PMID: 33428888.
Barone M, D’Amico F, Brigidi P, Turroni S. Gut microbiome-micronutrient interaction: The key to controlling the bioavailability of minerals and vitamins? Biofactors. 2022 Mar;48(2):307-314. doi: 10.1002/biof.1835. Epub 2022 Mar 16. PMID: 35294077; PMCID: PMC9311823.