 国家高新企业 | ISO9001认证
国家高新企业 | ISO9001认证 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


谷禾健康

随着国家卫生健康委发布2024版食养指南,以及前几天在上海举办的临床医学与营养食品论坛,越来越多的人开始重视日常膳食的营养与健康。
而说到脂肪,很多人都会“谈脂色变”,想要避免脂肪的摄入,这其实是不正确的。脂肪作为人体必需的基本营养素之一,是不可缺少的。缺乏脂肪会导致人体营养不良、激素失衡,皮肤受损、免疫力下降等一系列问题。
需要明确的是,并非所有脂肪都对健康产生相同的影响,它们之间存在着显著的差异。饱和脂肪和反式脂肪,常见于高加工食品、烘焙食品、油炸食品和一些红肉中,过量摄入这些脂肪可能会导致肥胖、增加心血管疾病和其他健康问题的风险。
而相对优质的不饱和脂肪,对人体健康有着多方面的益处。例如Omega-3脂肪酸能降低血液中的低密度脂蛋白,同时提高高密度脂蛋白水平,从而减少心血管疾病的风险。
2022年底,国家心血管病中心专家委员会心血管代谢医学专业委员会发布了《Omega-3脂肪酸在心血管疾病防治中的作用中国专家共识》,该共识全面、科学地呈现omega-3脂肪酸(高纯度鱼油)在心力衰竭、心肌病、高血压和猝死等多个方面的详细知识,为中国人群的omega-3脂肪酸在预防和治疗心血管疾病中的临床应用提供参考。
此外还具有支持大脑和神经发育、产生抗炎作用、改善认知、抗忧郁、使皮肤更显年轻、调节视网膜健康等作用。
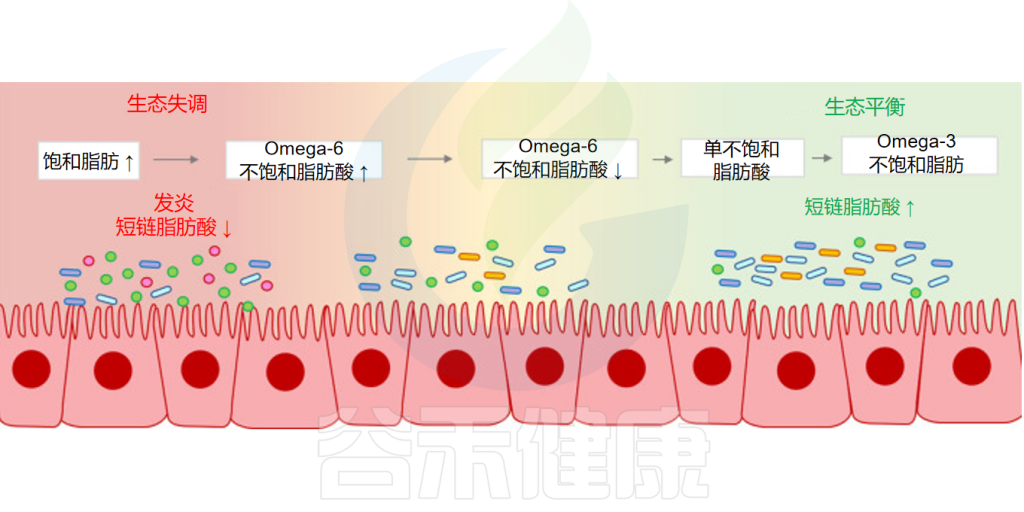
目前的研究认为功效范围从最不健康到最健康:饱和脂肪(SFA)<Omega-6不饱和脂肪酸<单不饱和脂肪酸 (MUFA)<Omega-3不饱和脂肪酸。
特别需要注意的是,人体不饱和脂肪酸Omega-6与Omega-3的比率可能是心血管疾病风险的重要标志。尽管都是人体所必需的重要不饱和脂肪酸,但是在对待炎症方面却展现出了截然不同的作用。Omega-6不饱和脂肪酸促进炎症的发生,引起身体的“失火”;Omega-3不饱和脂肪酸则恰恰相反,缓解并抑制炎症,从而预防重大疾病的发生。
可见他们两者的平衡是非常重要的。这种不平衡可能导致多种疾病,包括血栓形成、炎症、哮喘和炎症性肠病等。
肠道微生物群是我们消化系统中不可或缺的一部分,而不饱和脂肪酸作为一种重要的营养物质,其在消化和吸收的过程中必定有微生物的参与作用。
已经有一些研究发现摄入Omega-3不饱和脂肪酸有助于恢复抗炎肠道微生物群,而健康和多样化的微生物群可以在一定程度上增加Omega-3不饱和脂肪酸的体内转化和代谢。
鉴于不饱和脂肪酸对人体的重要性,以及其作为当前人们关心的重要营养素。本文将以Omega-3脂肪酸为例来讲述这类不饱和脂肪酸对人体的健康益处,可能存在的一些安全隐患。以及主要的饮食来源,日常生活中该如何补充Omega-3不饱和脂肪酸。希望能够在人们日常饮食和临床补充中提供一定的帮助,以此来更好地针对自身情况调节膳食。
我们经常在一些食品或添加剂中听到富含不饱和脂肪酸,那么究竟什么是脂肪酸?什么又是不饱和脂肪酸呢?
脂肪酸是一类含有羧基的脂肪族化合物,通常存在于动植物的脂肪和油中。脂肪酸是构成脂肪分子的基本单元,你可以简单理解为脂肪是由许许多多的脂肪酸分子构成的。
脂肪酸在人体中起着重要作用,包括提供能量、构建细胞膜、合成激素、帮助脂溶性维生素的吸收和保护身体脏器等。
▸ 脂肪酸可分为饱和脂肪酸和不饱和脂肪酸
脂肪酸根据碳氢链饱和与不饱和可分成两类:一类是分子内不带碳碳双键的饱和脂肪酸,如硬脂酸、软脂酸等;另一类是分子内带有一个或几个碳碳双键的不饱和脂肪酸,如亚麻酸、亚油酸、油酸。
饱和脂肪酸通常是固态的,而不饱和脂肪酸则通常是液态的。
饱和脂肪酸(Saturated fatty acid),指不含不饱和双键的脂肪酸。一般来说,动物性脂肪如牛油、猪油比植物性脂肪含饱和脂肪酸多。但也不是绝对的,如椰子油、可可油、棕榈油中也含有丰富的饱和脂肪酸。奶制品(如奶油、奶酪和全脂牛奶)中也有较多的饱和脂肪酸。
一般较常见的饱和脂肪酸有辛酸、癸酸、月桂酸、豆蔻酸、软脂酸、硬脂酸、花生酸等。
▸ 过量食用饱和脂肪酸会增加心血管疾病风险
饱和脂肪酸摄入过多是导致血胆固醇、三酰甘油、低密度脂蛋白胆固醇(LDL-C)升高的主要原因,继发引起动脉管腔狭窄,形成动脉粥样硬化,增加患心血管疾病的风险。
根据世界卫生组织和其他健康机构的建议,应该适度摄入饱和脂肪酸,并将其与不饱和脂肪酸(如单不饱和脂肪酸和多不饱和脂肪酸)相结合,以维持健康的饮食平衡。
不饱和脂肪酸就是指含有不饱和键的脂肪酸,是构成体内脂肪的另一种不可缺少的脂肪酸。根据双键个数的不同,分为单不饱和脂肪酸和多不饱和脂肪酸二种。
▸ 单不饱和脂肪酸
单不饱和脂肪酸(MUFA)是一类含有一个不饱和键的脂肪酸,它们在橄榄油、芥花籽油、花生油等植物油中含量丰富。单不饱和脂肪酸的主要代表是油酸(ω-9脂肪酸),它在橄榄油中的含量可达84%以上。
油酸具有多种健康益处,包括降低低密度脂蛋白(LDL)胆固醇水平,提高高密度脂蛋白(HDL)胆固醇比例,从而有助于预防动脉硬化。此外,单不饱和脂肪酸还具有抗氧化功能、降血糖功能、调节血脂功能和降低胆固醇功能。
▸ 多不饱和脂肪酸
多不饱和脂肪酸(PUFA)指含有两个或两个以上不饱和键的脂肪酸,根据双键的位置及功能又将多不饱和脂肪酸分为Omega-3系列和Omega-6系列。
Omega-3脂肪酸(Ω3)
需要注意的是,Omega-3脂肪酸并不单指一种物质,而是一组多不饱和脂肪酸。因其第一个不饱和键位于甲基一端的第3个碳原子上,故名Omega-3。
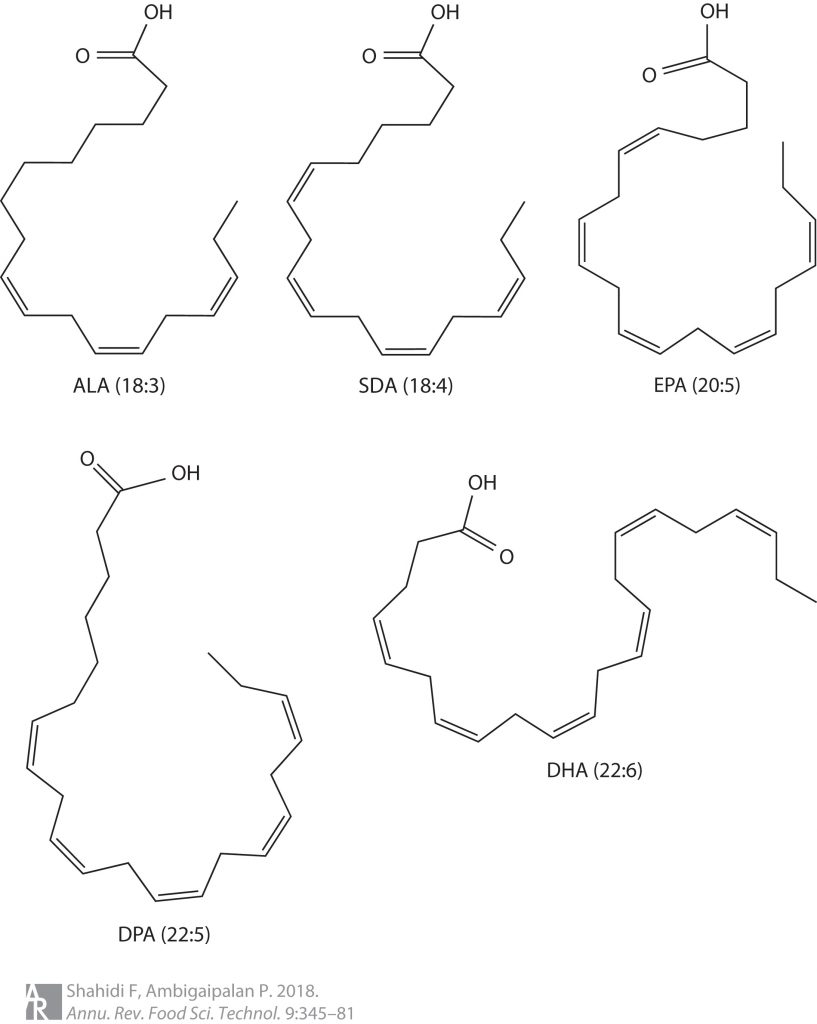
Omega-3脂肪酸主要有α-亚麻酸(ALA)、十八碳四烯酸(SDA)、二十碳五烯酸(EPA)、二十二碳五烯酸(DPA)和二十二碳六烯酸(DHA)。
注:ALA是Omega-3脂肪酸的母体,可去饱和并延伸形成其他Omega-3脂肪酸。
omega-3多不饱和脂肪酸的化学结构
Omega-3必须靠食物来获取
Omega-3是一种对人体健康非常重要的不饱和脂肪酸,它对心脏健康、大脑发育和炎症反应有着重要作用。
Omega-3不饱和脂肪酸同时也是人体合成各种激素及内生性物质必要的营养素,但人体无法自行合成,因此必须通过饮食来获取。Omega-3主要存在于深海油性鱼类(如三文鱼、鲭鱼、沙丁鱼)和一些植物性食物(如亚麻籽、奇亚籽、核桃)中。
Omega-6脂肪酸(Ω6)
同理,不饱和键位于第六个碳原子上的脂肪酸,则称为Omega-6脂肪酸。Omega-6脂肪酸在人体内也至关重要,胆固醇必须与Omega-6的亚油酸(LA)相结合,才能正常运转和代谢;人脑中的不饱和脂肪酸Omega-6和Omega-3各占一半。
Omega-6不饱和脂肪酸的食物来源非常丰富,玉米、大豆等植物及其加工产品如炒菜离不开的玉米油、大豆油等植物油以及我们常吃的猪肉、牛肉、羊肉里,Omega-6不饱和脂肪酸的含量都不少。
Ω3与Ω6的平衡对于炎症至关重要!
尽管都是人体所必需的重要不饱和脂肪酸,但是在对待炎症方面却展现出了截然不同的作用。Omega-6不饱和脂肪酸促进炎症的发生,引起身体的“失火”;Omega-3不饱和脂肪酸则恰恰相反,缓解并抑制炎症,从而预防重大疾病的发生。可见他们两者的平衡是非常重要的。
▸ 拓展:反式脂肪酸又是什么?
在生活中我们还能听到一些食品因含有反式脂肪酸而被认为是不健康的产品,反式脂肪酸(trans fatty acid,TFA)是含有反式非共轭双键结构不饱和脂肪酸的总称。
如果与双键上2个碳原子结合的2个氢原子在碳链的同侧,空间构象呈弯曲状,则称为顺式不饱和脂肪酸,这也是自然界绝大多数不饱和脂肪酸的存在形式。反之, 双键上两个碳原子结合的两个氢原子分别在碳链的两侧,其空间构象呈线性,则称为反式不饱和脂肪酸。
与不饱和脂肪酸不同,反式脂肪酸往往对身体有许多危害。研究发现,反式脂肪酸与心血管疾病发生风险之间存在正相关关系。除此之外还会影响生育和胎儿发育、降低记忆、促进肥胖和血栓的形成、影响神经行为。
鉴于对人体的重要性,以及其作为当前人们关心的重要营养素。本文将具体讲述Omega-3不饱和脂肪酸对人体的健康益处,以及可能存在的一些隐患。
首先我们需要清楚的是,Omega-3脂肪酸包括了一类多不饱和脂肪酸,并不单单指一个物质。主要有α-亚麻酸(ALA)、十八碳四烯酸(SDA)、二十碳五烯酸(EPA)、二十二碳五烯酸(DPA)和二十二碳六烯酸(DHA)。而ALA是Omega-3脂肪酸的母体,可去饱和并延伸形成其他Omega-3脂肪酸。
▸ α-亚麻酸主要来自植物
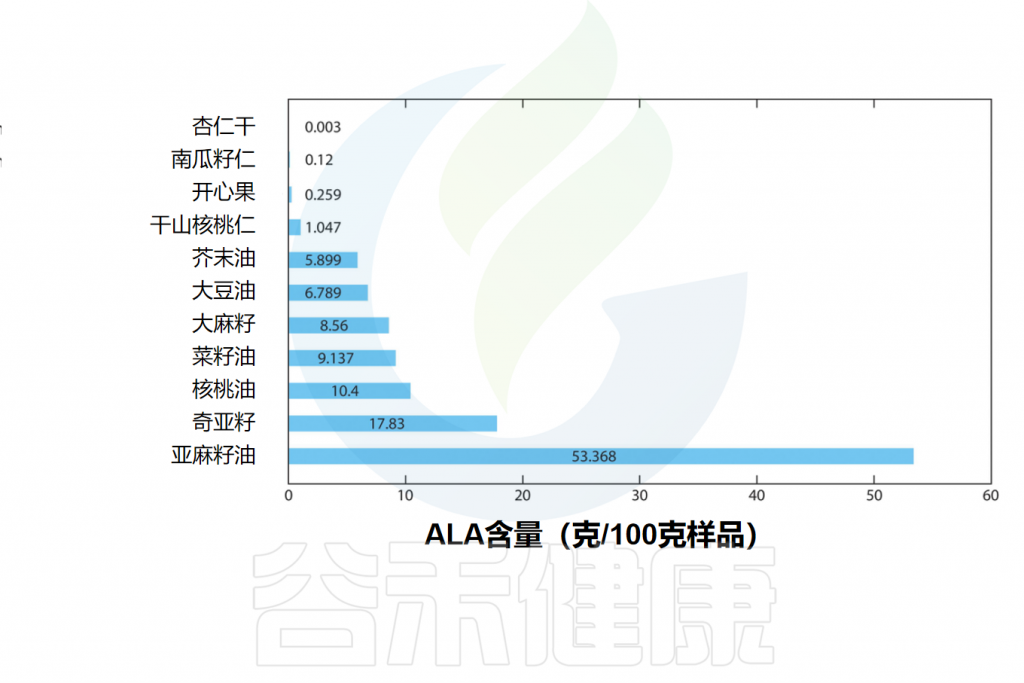
α-亚麻酸(ALA)的主要来源是植物,主要集中在一些种子和坚果以及植物油中。亚麻籽、奇亚籽、核桃和蓝蓟籽油是ALA的良好来源,而红花油、向日葵油、玉米油和大豆油则富含亚油酸(18:2 ω-6)。
亚麻籽及其油通常含有45-55%ALA形式的不饱和脂肪酸。大豆油、菜籽油和核桃含有5-10%ALA形式的不饱和脂肪酸。
一些含有α-亚麻酸(ALA)的食物
▸ 深海鱼中含有较多的EPA和DHA
尽管人体能以ALA为前体合成EPA和DHA。然而,ALA生物转化为EPA和DHA的能力有限;因此,我们需要从饮食中摄取。
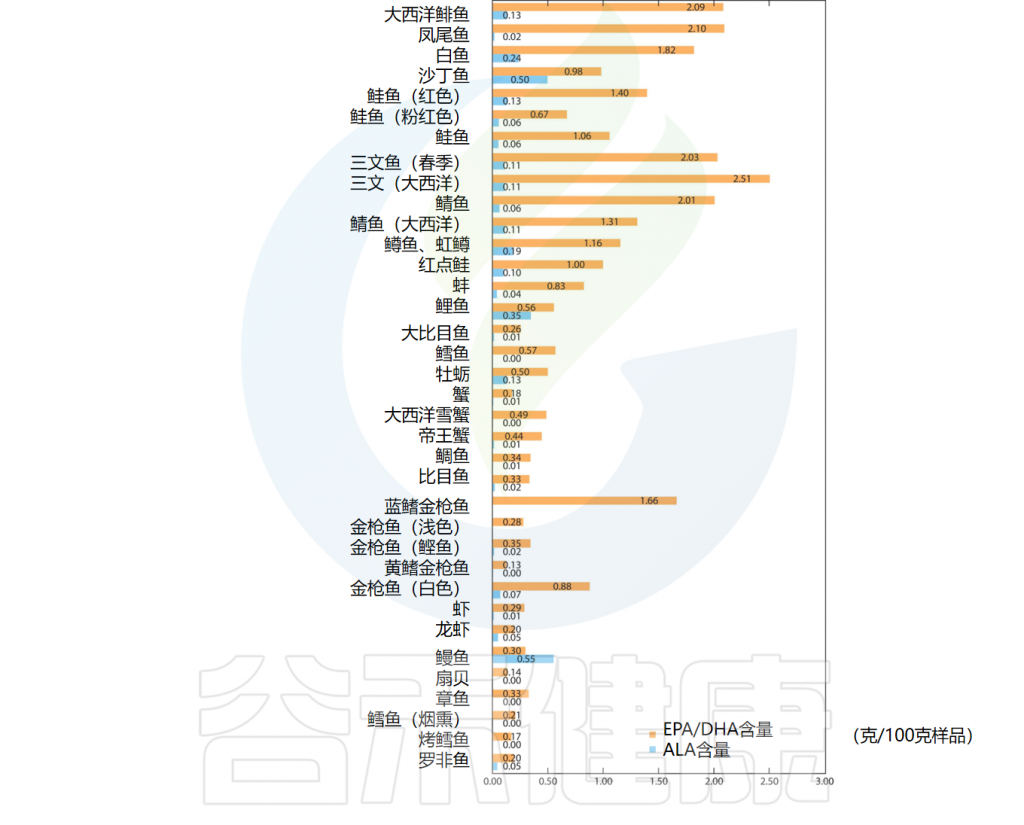
EPA和DHA最重要的饮食来源是油性深海鱼类(例如鲑鱼、金枪鱼、鲱鱼、沙丁鱼、鲭鱼)和海豹、鲸鱼等海洋哺乳动物的脂肪。除此之外,龙虾、雪蟹、扇贝、章鱼等动物也含有一定量的Omega-3脂肪酸。
一些含有DHA/EPA、ALA的食物
▸ 一些藻类和真菌也可以合成Omega-3
微藻和一些微生物(真菌)也含有Omega-3脂肪酸。据报道,海藻是生物圈中Omega-3脂肪酸(DHA)的主要生产者,许多藻类已被确定为DHA的来源。
寇氏隐甲藻(Crypthecodinium cohnii)和裂殖壶菌(Schizochytriumsp)是DHA的两个主要藻类来源,其含量分别占总脂肪酸的55%和40%。
Omega-3脂肪酸,特别是EPA和DHA,其实是由浮游植物合成,最终通过食物网转移并沉积到鱼类和海洋哺乳动物的脂质中。
注:最近,十八碳四烯酸(SDA)受到了关注,在饮食中补充SDA比补充ALA更能提高EPA水平。紫草科的植物,如玻璃苣、Echium vulgare和Buglossoides arvensis、大麻油和鱼类,都是SDA的良好来源。然而,SDA并不是人类饮食的主要成分。
Omega-3可以以乙酯(EE)、三酰甘油(TAG)、游离脂肪酸(FFA)或磷脂(PL)形式存在。研究人员表明,各种形式的Omega-3的消化和吸收高度依赖于膳食中的脂肪含量,这会增强胰酶的活性。
膳食脂肪消化
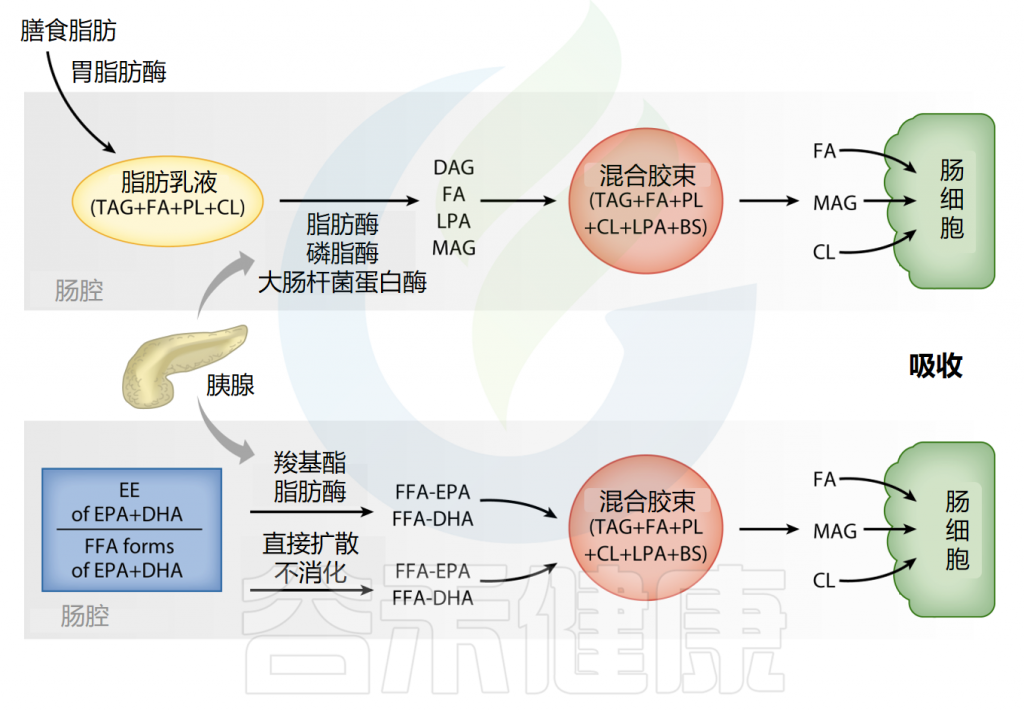
Shahidi F,et al.Annu Rev Food Sci Technol.2018
α-亚麻酸(ALA)被称为必需脂肪酸,因为人类不能从头合成ALA,植物性食品是ALA的主要膳食来源。尽管不能合成ALA,但人体可以通过进一步的去饱和和延伸过程来代谢它,这些过程被认为主要发生在肝脏中。
▸ ALA在人体可代谢转化成EPA、DHA
从膳食ALA合成其他Omega-3脂肪酸的代谢途径如图所示。SDA是从ALA合成的第一个代谢物,随后导致EPA、DPA和DHA的合成。
从ALA合成Omega-3不饱和脂肪酸的代谢途径
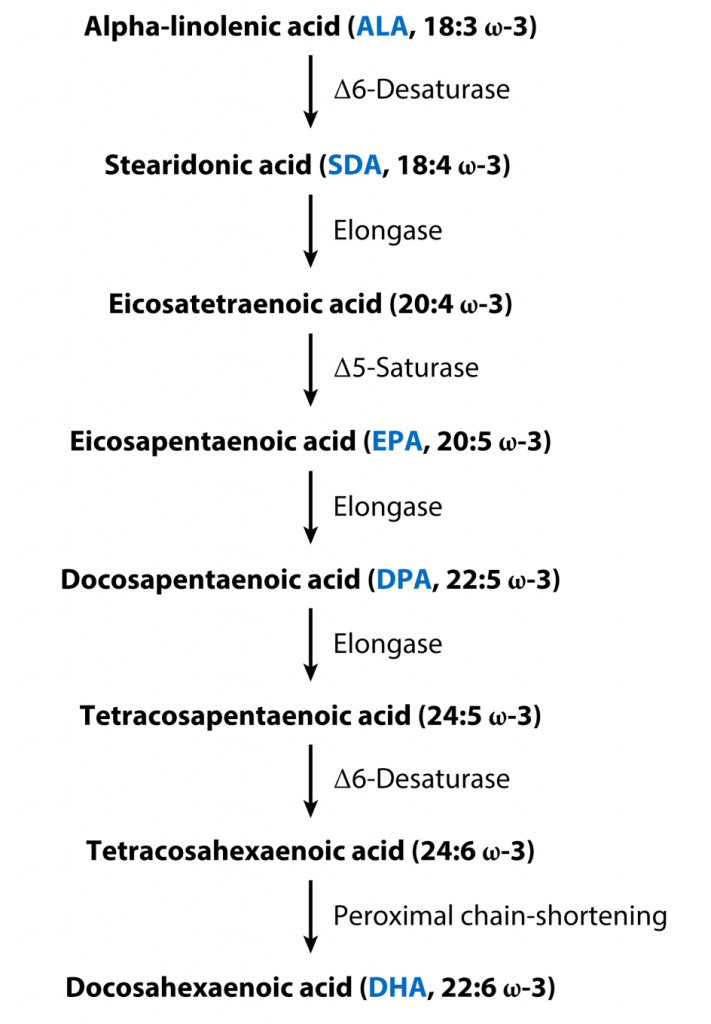
Shahidi F,et al.Annu Rev Food Sci Technol.2018
另一个主要途径涉及从亚油酸合成Omega-6不饱和脂肪酸,其中花生四烯酸是主要的最终产物。
▸ 胰岛素和矿物质水平会影响转化率
由于人类饮食中的α-亚麻酸(ALA)水平通常低于亚油酸,因此Omega-6脂肪酸的血浆和细胞水平往往高于Omega-3脂肪酸。
观察到,摄入ALA显著增加血浆和母乳中的EPA和DPA水平,而仅观察到DHA的轻微增加。另一项使用稳定同位素的研究表明,从ALA转化为EPA、DPA和DHA的效率分别为0.2%、0.13%和0.05%。
该转化需要去饱和酶(Δ5和Δ6)、微粒体系统的延长酶以及过氧化物酶体中的氧化以缩短链。一份报告显示,胰岛素水平低以及蛋白质和矿物质(铁、锌、铜和镁)缺乏可能会降低Δ6去饱和酶活性,从而抑制亚油酸和ALA转化为Omega-6和Omega-3。
▸ Ω6和Ω3对于许多激素的合成至关重要
Omega-6和Omega-3不饱和脂肪酸对于一些激素的合成至关重要,例如前列腺素(PG)、前列环素(PGI)、血栓素(TX)、白三烯、氢过氧四烯酸、羟基二十碳四烯酸等。
这些物质参与多种生理作用,包括促/抗炎、促/抗血小板聚集、血管舒张、血管收缩、免疫反应以及细胞生长和增殖。
不同脂肪酸衍生的物质其功能有时相反
例如,源自花生四烯酸的前列腺素的功能与源自 EPA的前列腺素不同。由花生四烯酸形成的PGE2和TXA2在血小板中产生,并通过有效的化学活性和血小板聚集促进炎症,并充当血管收缩剂。
然而,EPA衍生的PGE和TXA仅起到血管扩张剂和抗聚集剂的作用。因此,Omega-6和Omega-3不饱和脂肪酸在生理功能中起着重要作用,这种不平衡可能导致多种疾病,包括血栓形成、炎症、哮喘和炎症性肠病。
此外DHA已被证明是大脑灰质的主要成分,其磷脂形式已被证明是视网膜、睾丸和精子的主要成分。
作为一种重要的不饱和脂肪酸,Omega-3脂肪酸对我们的健康产生着深远的影响。它被认为是一种必需的营养物质,能够帮助维持心血管健康、影响大脑和视力功能、改善炎症、睡眠等。
了解Omega-3脂肪酸对人体健康的积极影响至关重要,跟着谷禾一起探索Omega-3脂肪酸如何成为我们健康生活的重要组成部分。
• 维护心血管健康
Omega-3可以帮助降低心脏疾病风险。它们通过降低血液中的甘油三酯水平、低密度脂蛋白(LDL)中不良胆固醇,减少血小板聚集(降低血栓形成风险)、降低血压同时提高高密度脂蛋白(HDL)中良性胆固醇量来实现这一点。这些作用共同帮助维护心血管系统的健康。
• 抗炎作用
Omega-3脂肪酸可以通过影响炎症介质的产生来调节炎症反应。具体来说,它们能够减少前列腺素E2(PGE2)和白三烯B4(LTB4)等促炎因子的生成。
Omega-3脂肪酸还通过影响多种信号通路来发挥抗炎作用,包括抑制核因子κB(NF-κB)信号通路。
• 调节大脑健康
Omega-3脂肪酸,特别是DHA,是大脑和神经系统正常发育和功能所必需的,是构成脑细胞膜的成分,也是维护脑部健康的重要功臣。它对儿童大脑发育至关重要,有助于提高学习能力和注意力。在成人中,足够的Omega-3摄入量与降低认知衰退和阿尔茨海默病的风险有关。
• 眼部健康
DHA是视网膜的主要成分,对维持视力至关重要。Omega-3的摄入与降低年龄相关的黄斑变性风险有关,这是老年人失明的一个主要原因。
黄斑变性是指由于年龄、遗传、不良环境、慢性光损伤等各种因素的影响,使眼部视网膜处的黄斑发生萎缩,或代谢异常,导致患者出现视力异常的疾病。
• 抗抑郁和焦虑、消除偏头痛
研究表明,Omega-3可以帮助改善抑郁和焦虑症状。尤其是EPA,被认为在调节情绪和抗抑郁中起着重要作用。
Omega-3还能帮助抑制导致疼痛和发炎的“不良”前列腺素的分泌。它也能减少血液的粘度,以促进脑部的血液循环。这将会减少偏头痛的发作次数,亦能减低其严重程度和待续时间。
• 使皮肤更显年轻
Omega-3能令皮肤均衡保湿及保持健康。它能强化围绕于每一个细胞周围的纤柔细胞膜,使细胞获得充足滋养,同时能有效地把细胞内的废物予以排除。它能使真皮层分泌出更强力的胶原和弹性纤维,帮助消除皱纹和细纹,并挺实渐呈松弛的皮肤。
• 改善睡眠质量
一些研究表明,Omega-3的摄入与改善睡眠质量有关,可能通过影响睡眠调节的神经传递物质和激素实现。例如DHA,被认为可以调节褪黑素的产生。褪黑素是一种重要的睡眠调节激素,它帮助调整人体的生物钟和睡眠周期。
此外,Omega-3脂肪酸还可能带来其他潜在健康益处。为了提供更有力的证据,谷禾综合了大量研究资料,探讨了Omega-3不饱和脂肪酸对各种疾病的影响,旨在帮助大家更深入了解Omega-3不饱和脂肪酸。
1
心血管疾病
由于高脂肪饮食,世界范围内的心血管疾病和相关死亡率越来越高。已经对Omega-3不饱和脂肪酸对主要心血管疾病的影响进行了大量研究,如心肌梗死、中风、先天性心脏病、心律失常、心房颤动、亚临床动脉粥样硬化、冠心病、心力衰竭、心源性猝死、瓣膜病和外周动脉疾病。
• 大量人群数据显示较高的Omega-3摄入量的心血管疾病风险较低
格陵兰岛、加拿大北部和阿拉斯加食用传统饮食的原住民,尽管膳食脂肪摄入量较高,但心血管疾病(特别是冠心病)死亡率远低于预期。饮食中的保护成分被认为是由于定期摄入鲸鱼和海豹肉、鲸脂和多脂鱼而含有大量的Omega-3不饱和脂肪酸。
日本人的传统饮食也具有较低的心血管死亡率,这种饮食富含海鲜,包括富含脂肪的鱼类,有时还包括海洋哺乳动物,其中含有大量的EPA和DHA。从前瞻性和病例对照研究中积累的大量证据表明,西方人群中较高的EPA和DHA摄入量与较低的心血管疾病风险相关。
• Omega-3降低心血管疾病风险的具体作用
Omega-3不饱和脂肪酸,尤其是DHA和EPA,通过改变脂质和止血因素(例如血小板聚集和出血时间)来降低心血管疾病的临床风险。
DHA已被证明具有抗血小板聚集、降低三酰甘油作用和抗心律失常作用。在控制高脂饮食的多变量男性模型中,饱和脂肪酸的血清水平较高与冠心病风险增加相关,而Omega-3不饱和脂肪酸中DHA和DPA与冠心病风险呈负相关。
据报道,Omega-3不饱和脂肪酸还可以降低心脏对室性心律失常的敏感性,延缓动脉粥样硬化斑块的生长(通过减少粘附分子表达和血小板衍生生长因子并具有抗炎作用)。降血压,并发挥抗血栓形成和低甘油三酯(空腹和餐后)作用,因此具有心脏保护作用。
Omega-3对心率和血压的影响归因于一氧化氮生成率的增加,减轻对去甲肾上腺素和血管紧张素II的血管收缩反应,增强血管舒张反应,改善动脉顺应性。
Ω3脂肪酸减少心血管疾病风险的机制
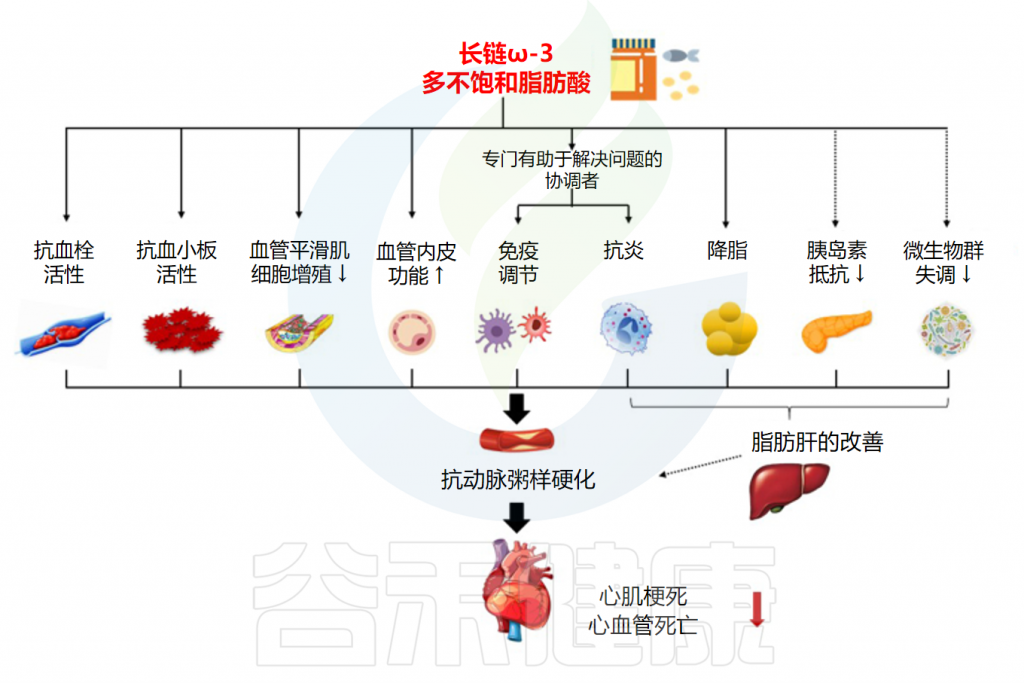
Bae JH,et al.Adv Nutr.2023
下图总结了Omega-3对心血管健康的生理影响:

编辑
Shahidi F,et al.Annu Rev Food Sci Technol.2018
• Ω6与Ω3的比率可能是心血管疾病风险的重要标志
此外,Ω6(亚油酸和花生四烯酸)与Ω3(EPA、DHA和亚麻酸)的比率被认为是分析心血管疾病风险的重要生物标志物。然而据报道,组织中的Ω3水平在心血管风险评估中可能比Ω6或AA/EPA比率具有更好的预后和诊断效用。
对之前发表的文章进行了系统综述分析,了解Omega-3不饱和脂肪酸对心血管健康的影响。谷禾将其整理在下图中。


Shahidi F,et al.Annu Rev Food Sci Technol.2018
2
糖尿病
多项研究表明,补充Omega-3不饱和脂肪酸或鱼油对2型糖尿病具有有益作用。研究发现,食用Omega-3不饱和脂肪酸饮食八周后可增加老年人的胰岛素敏感性,并显著降低血清C反应蛋白。
• Omega-3对糖尿病的影响还存在争议
回顾了以前的一些研究,发现Omega-3不饱和脂肪酸对2型糖尿病或代谢综合征患者的血浆三酰甘油(TAG)水平有有利影响,但对总胆固醇、高密度脂蛋白 (HDL)、低密度脂蛋白(LDL)、空腹血糖或糖化血红蛋白水平没有直接影响。
关于Omega-3不饱和脂肪酸在糖尿病和胰岛素抵抗中的作用仍然存在争议。因此,需要进一步的临床研究来确定Omega-3是否影响人类糖尿病和胰岛素抵抗。
omega-3与糖尿病的研究结果总结

Shahidi F,et al.Annu Rev Food Sci Technol.2018
3
癌症
在过去的十年中,多项实验和流行病学研究表明,Omega-3不饱和脂肪酸可以降低患癌症的风险。
据报道,Ω3不饱和脂肪酸具有抗癌作用,而饱和脂肪酸和Ω6不饱和脂肪酸可能会促进癌症的发展。Ω3不饱和脂肪酸已被证明可以影响多种类型的癌症,包括前列腺癌、结肠癌、乳腺癌、肺癌、结直肠癌、卵巢癌、胰腺癌、皮肤癌和胃癌。此外,Ω3被证明可以提高化疗的疗效和耐受性。
• Omega-3可能的抗癌机制
提出了一些关于Omega-3抗癌作用的分子机制:
(a)减少花生四烯酸衍生的类二十烷酸的生物合成,这导致对癌细胞的免疫反应、炎症调节、细胞增殖、细胞凋亡、转移和血管生成改变;
(b)影响导致新陈代谢、细胞生长和分化变化的转录因子的活性;
(c)改变雌激素的代谢活性,随后雌激素刺激的细胞生长减少;
(d)自由基和活性氧产生的改变;
(e)调节胰岛素敏感性和膜流动性。
据报道,Omega-3不饱和脂肪酸通过降低环加氧酶 COX-2和PGE2水平侵入并抑制肿瘤细胞生长,因此可以作为天然COX抑制剂。
此外,Ω6与Ω3的比率低于5被认为可减缓癌症进展。同时,增加Ω6的摄入量被证明会促进动物和人类患乳腺癌、前列腺癌和结肠癌。
Ω6促肿瘤作用背后的机制包括脂质过氧化、17-β-雌二醇(E2)环氧化后产生致癌物,以及通过增强其他化合物(例如染色质)的基因毒性作用而产生致癌作用。
• 每天适当补充Ω3对癌症患者有积极作用
最近的一项研究表明,将Ω3与1α,25-二羟基维生素D3结合可显著增加乳腺癌细胞系的细胞凋亡。膳食补充Ω3不饱和脂肪酸、α-生育酚、亚麻酸、纤维和植物雌激素对乳腺癌患者具有积极作用。研究表明亚麻籽对乳腺癌患者具有抗增殖活性,并建议绝经前妇女每天摄入25克亚麻籽。
还有研究发现,使用Ω3作为接受放射治疗的头颈癌患者的营养补充剂,有助于他们通过增加蛋白质热量摄入来维持体重并耐受抗癌治疗,从而提高他们的生活质量。
!
一些因素会影响Ω3对癌症的效果
某些因素可能会影响Ω3不饱和脂肪酸对癌症的不一致结果:Ω3不饱和脂肪酸的来源、类型(ALA、DHA或EPA)、形式和含量的差异以及Ω6与Ω3的比率和遗传因素,例如COX和脂氧合酶修饰基因的多态性。
需要更多的临床试验来找出针对特定癌症病理的Ω3有效剂量和配方。
4
阿尔茨海默病和认知能力
多项流行病学研究表明,较低的Ω3不饱和脂肪酸摄入量会增加认知能力下降或痴呆的风险,尤其是阿尔茨海默病。
有足够的临床证据表明Ω3不饱和脂肪酸可以预防阿尔茨海默病。DHA是大脑中膜磷脂的主要成分,特别是在大脑皮层、线粒体、突触体和突触小泡中。
• 不饱和脂肪酸影响脑功能的机制
不饱和脂肪酸对脑功能的作用机制包括改变:
(a)膜流动性;
(b)膜结合酶的活性;
(c)受体的数量和亲和力;
(d)离子通道的功能;
(e)神经递质的产生和活动,以及信号转导,控制神经递质和神经元生长因子的活动。
Omega-3不饱和脂肪酸可导致人体淋巴细胞增殖、TNFα产生、自然杀伤细胞活性以及白细胞介素IL-1 和白细胞介素IL-2产生减少。
• 不饱和脂肪酸的缺乏会影响儿童神经系统
研究人员调查了317名足月婴儿的脐动脉和脐静脉 脂肪酸组成以及早期新生儿神经系统状况,并报告说,较低的胎儿DHA、花生四烯酸(AA)和必需脂肪酸水平会对早期产后神经系统状况产生负面影响。此外,早期新生儿缺乏不饱和脂肪酸可能导致亨廷顿舞蹈症、精神分裂症、高血压和成年后食欲信号增强。
多项研究表明,必需脂肪酸,尤其是Omega-3不饱和脂肪酸的缺乏会导致注意力缺陷多动障碍 (ADHD)。而服用Omega-3不饱和脂肪酸可显著改善缺陷多动障碍儿童的生活质量、注意力集中能力、睡眠质量和血红蛋白水平。
• Ω3脂肪酸的摄入对老年人的认知有益
摄入鱼类和Ω3不饱和脂肪酸已被证明对健康老年人具有积极的认知健康作用,而在考虑阿尔茨海默病患者时,补充Ω3还可以使患有记忆障碍或轻度认知障碍和阿尔茨海默病的老年人受益。
5
抑郁症
据世界卫生组织称,抑郁症可能成为全球第二大疾病。多项流行病学研究表明,食用鱼类与降低抑郁症风险相关。
• 早期发育时缺乏DHA会增加成年后患抑郁症风险
研究发现补充Ω3(EPA+DHA的混合物)对精神分裂症孕妇有积极作用。EPA已被证明可以作为一种抗抑郁剂,引起大脑结构变化,包括大脑侧脑室容量减少和神经元周转减少。
基于28项临床试验的荟萃分析研究提供的证据表明,EPA在治疗抑郁症方面可能比DHA更有效。此外,早期发育过程中DHA的缺乏可能会影响中枢神经系统,并增加成年后患抑郁症的可能性。摄入或补充鱼油/Ω3不饱和脂肪酸已被证明可以保护青少年(15-25 岁)免受重度抑郁症。
• Ω3脂肪酸作为抗抑郁药的机制
使用Ω3脂肪酸作为抗抑郁药的可能作用机制包括:
(a)调节炎症细胞因子的分泌,因为其可能会引发重度抑郁症的体征和症状;
(b)膜流动性增加,导致内皮细胞转运血清素(5-HT)增加;
(c)额叶皮质中DHA浓度增加,这可以增加多巴胺浓度和(多巴胺)D2受体结合;
(d)与神经元细胞膜受体和第二信使相互作用,导致情绪改变。
然而,关于Ω3不饱和脂肪酸潜在抗抑郁能力的一些发现存在矛盾;因此,需要进一步的随机对照试验来研究使用EPA占主导地位的Ω3不饱和脂肪酸制剂的诊断或临床显著抑郁症患者。
6
大脑、视觉发育、妇幼保健
• Omega-3不饱和脂肪酸对大脑发育至关重要
多项研究报告了膳食Omega-3不饱和脂肪酸对大脑发育的重要作用。膳食Ω3摄入量低会增加产前或产后发育期间大脑花生四烯酸 (AA)/DHA的比例。
该比率的变化减少了神经元迁移、神经发生、胚胎皮质板扩张、突触修剪、脑葡萄糖摄取和代谢的延迟,并导致谷氨酸和单胺突触功能受损。
• Omega-3脂肪酸与孕妇及儿童健康相关
DHA是视觉系统中视网膜感光器和皮质灰质的重要结构成分;怀孕期间补充DHA有助于视觉系统的成熟。在妊娠后半期,DHA在神经皮质组织和视网膜膜突触中迅速积累。
大量流行病学研究表明Omega-3脂肪酸与孕期孕产妇健康和儿童健康相关。Omega-3脂肪酸影响妊娠时长、出生体重、围产期抑郁、妊娠高血压/先兆子痫、产后神经发育、认知发育、自闭症谱系障碍、多动症、学习障碍、特应性皮炎、过敏和呼吸系统疾病等。
怀孕期间补充Omega-3脂肪酸已被证明与高等级立体敏锐度、词汇理解力、接受性词汇、言语智商以及从婴儿期到9岁的较高认知分数呈正相关。
Omega-3脂肪酸作为一种重要的营养物质,被广泛认为对人体健康有益,而肠道微生物群则是我们消化系统中不可或缺的一部分。它们之间是否存在某种联系?让我们一起来了解下。
一项使用来自876名同时测得16S微生物组和Ω3不饱和脂肪酸的数据研究表明,在调整混杂因素后,总Ω3不饱和脂肪酸和DHA的血清浓度与微生物组α多样性(香农指数)显著相关。
在调整膳食纤维摄入量后,这些关联仍然显著。对2型糖尿病患者进行的一项随机对照试验显示,与沙丁鱼饮食相比,2型糖尿病患者的厚壁菌门与拟杆菌门的比率显著下降。
补充Ω3脂肪酸可以增加产短链脂肪酸细菌的丰度
健康志愿者补充8周的Ω3不饱和脂肪酸导致产生短链脂肪酸的肠道微生物群持续且可逆地增加。然而,发现微生物多样性缺乏显著变化,这与小鼠研究一致,其中α-多样性没有变化或只有微小变化。
值得注意的是,短期饮食干预无法改变肠道微生物组的主要个体差异。
总而言之,Omega-3不饱和脂肪酸可能通过影响肠道微生物组和连接肠道与脂肪组织、肝脏和胰腺的代谢物来减轻高血糖和胰岛素抵抗。因此,补充Omega-3不饱和脂肪酸可能有助于通过肠道器官轴的有利变化恢复葡萄糖稳态。
膳食中摄入Ω3不饱和脂肪酸(例如DHA和EPA)可以改变肠道微生物群,但膳食补充剂的持续时间或改变肠道微生物群的剂量尚不清楚。多项人类和动物研究表明,DHA和其他Ω3不饱和脂肪酸摄入量的增加与有益肠道细菌的增加相关。
然而,这些研究不仅物种组成的变化不同,而且对生物体的功能益处也不一致。尽管如此,大多数研究表明,虽然参与者和DHA来源存在异质性,但更多的DHA摄入量会增加细菌α多样性以及双歧杆菌等抗炎细菌的丰度,而促炎细菌的丰度则会减少。
Ω3脂肪酸摄入量对肠道微生物群影响的研究
编辑
编辑
Kerman BE,et al.Curr Opin Clin Nutr Metab Care.2024
有助于抑制炎症因子
此外,补充DHA可恢复肠道屏障。在患有炎症性肠病的小鼠中,摄入DHA会特异性抑制促炎细胞因子,促进血液中的抗炎细胞因子,并减少大脑中小胶质细胞的激活。
编辑
来自喂食DHA的小鼠的粪菌移植表示,微生物群赋予移植小鼠抗炎作用。在一项针对HIV感染认知障碍参与者的研究中,摄入DHA24周并没有改善认知能力,尽管它对肠道微生物群有积极作用并降低了血清炎症标志物水平。
总之,一些证据表明增加Ω3不饱和脂肪酸摄入量对人类和动物有恢复作用。
一项针对不吃海鲜的素食主义者和纯素食者的队列研究显示,尽管Ω3不饱和脂肪酸血液水平较低,但痴呆或认知能力下降的风险较低。
居住在加利福尼亚州洛马琳达的人群,食用不含红肉、鸡肉或海鲜的植物性饮食与较低的心血管疾病和神经退行性疾病有关。
与吃肉的人相比,素食主义者的黄嘌呤、组氨酸、支链脂肪酸、乙酰化肽、神经酰胺和长链酰基肉碱等代谢物的水平较低。而这些代谢物许多与胰岛素抵抗、心血管风险增加和炎症有关。
• 更稳定的肠道微生物有利于将ALA转化为其他Ω3脂肪酸
英国的一项前瞻性研究(196名杂食者、231名素食者和232名纯素食者)报告称,随着时间的推移,素食者和纯素食者中的Ω3不饱和脂肪酸水平保持稳定,这表明ALA的内源性转化为EPA和DHA可能足以在多年内保持Ω3不饱和脂肪酸水平的稳定。
植物性饮食产生这些有益效果的方法之一是促进肠道微生物组更加多样化和稳定。例如,与杂食动物相比,素食主义者和素食者的某些拟杆菌门数量明显更高。纤维可以增加乳酸菌的丰度。植物性食物中富含的多酚可以增加肠道中双歧杆菌和乳酸菌的丰度,并具有抗炎特性。高植物纤维摄入量还支持纤维发酵成短链脂肪酸。
我们推测,在海鲜摄入有限且DHA与EPA水平较低的群体中,对Omega-3脂肪酸的缺乏反应可能受到饮食习惯和肠道微生物组成的影响。
• 多样而稳定的微生物群有助于缓解Omega-3摄入不足带来的负面影响
在摄入高纤维植物性饮食的人群中,多样而稳定的微生物组有助于促进抗炎状态,其丰富的短链脂肪酸、抗氧化剂和长链脂肪酸(如Ω6)可能补偿DHA或EPA水平低下的负面效应。
相反,在缺乏Omega-3脂肪酸、偏好加工肉类、低纤维植物饮食和不健康生活方式的西方饮食背景下,较低的微生物多样性和菌群失衡可能促进炎症性疾病,如阿尔兹海默病(AD)的慢性炎症途径激活。
编辑
Kerman BE,et al.Curr Opin Clin Nutr Metab Care.2024
开展了PreventE4(NCT03613844)研究,这是一项针对365名根据APOE4基因型分层、认知正常个体进行的为期两年的2克DHA与安慰剂对照的随机双盲试验。
PreventE4的主要目标是补充DHA六个月后,根据APOE4基因型,脑脊液(CSF)DHA水平的变化。次要目标包括脑成像结果的变化,而探索性目标则包括在基线、干预后6个月和24个月时评估的肠道微生物组及脑脊液和血浆的代谢组指标。研究人员预期,DHA补充将通过肠道微生物组成和代谢组的变化,部分解释对脑脊液DHA水平、成像和认知结果的影响。
• 补充Ω3脂肪酸有助于微生物群更健康、多样化
DHA补充将把西方饮食诱导的微生物表型转变为更健康、多样化的微生物群,这将与脑脊液DHA水平的显著提升、血浆和脑脊液中炎症标志物的降低以及成像和认知测量的改善相关联。
相比之下,DHA补充后未发生变化的西方饮食微生物表型可能不会对DHA补充产生有益反应。
最后,尽管Ω3/Ω6水平在血液和脑脊液中有所提高,但在基线时就拥有多样化和健康微生物群的个体可能只会显示较小的临床结果变化。
Ω3脂肪酸,作为一种对人体至关重要的脂肪酸,它在维持人体健康方面扮演着极其重要的角色。这种脂肪酸不仅对心血管健康有益,还能在许多其他方面促进身体健康,如改善大脑功能、降低炎症等。
然而,任何物质的摄入都应当遵循一个基本原则,那就是“过犹不及”。正如所有营养素一样,Ω3脂肪酸也需要适量摄入。既不应该摄入过少,以免身体无法获得必要的营养支持,也不应该过量摄入,因为这可能会导致一些不良的健康影响。
Omega-3脂肪酸可能会影响血小板功能,减少血小板计数和反应性,延长出血时间,并增加抗凝剂与促凝代谢物(分别为前列环素和血栓素)的比例。
除了融入血小板膜外,Omega-3脂肪酸(EPA和DHA)还与花生四烯酸竞争代谢转化的环氧合酶和脂氧合酶途径,从而降低血栓素A2的产生。
血小板功能的调节取决于 EPA 和 DHA 的剂量,主要发生在剂量大于 2 克/天时。这些影响似乎主要是由 EPA 的作用介导的。由于这些影响,有人担心长链 omega-3 PUFA,尤其是高剂量使用时,会不利地促进出血并延长出血时间。
• 当前的研究还没有发现Omega-3和失血过多存在相关性
关于Omega-3脂肪酸可能导致出血过多的可能性,一项研究汇总了来自19项精心设计的临床试验的证据,这些患者接受了重大手术(冠状动脉搭桥术、颈动脉内膜切除术和股动脉插管术)。
根据这些数据,得出的结论是,无论是单独使用EPA/DHA还是使用抗血栓/抗血小板药物治疗的患者,长链Omega-3脂肪酸都不会增加临床上显著出血的风险。
2018年的出版物报告了之前未发表的8项肠内营养临床试验数据,其中包括鱼油作为Omega-3脂肪酸的来源;这些试验针对不同的患者组(N=600名患者)提供了不同剂量的 EPA+DHA(1.5-10.2 克/天),持续时间不同(8天至52周)。Omega-3不饱和脂肪酸对凝血参数没有影响,并且Omega-3不饱和脂肪酸组和安慰剂组在出血事件方面没有差异。
Omega-3不饱和脂肪酸增加出血是理论上的考虑;然而,可能还需要更多的人体临床试验来证明其安全性,以打消人们的顾虑。
一些临床试验表明,Omega-3脂肪酸可能与患房颤(AF)的可能性增加有关,特别是对于心血管风险高或血脂升高的人群。
一些试验提供了不同剂量和不同配方中Omega-3脂肪酸对房颤的影响,较高的Omega-3脂肪酸补充可能会增加房颤的风险。
基线时没有心血管疾病、癌症或心房纤颤的参与者被随机分配接受840毫克/天Omega-3 不饱和脂肪酸(460毫克EPA和380毫克DHA)或橄榄油作为安慰剂。5.3年后,两组之间的房颤事件发生率没有较大差异(3.7%与3.4%)。
然而,使用较高剂量的Omega-3不饱和脂肪酸的试验发现,房颤风险增加。例如,每天3.2克EPA+DHA作为游离脂肪酸的治疗导致3.5年后发生心房纤颤的可能性更高(2.2%对比1.3%)。
在REDUCE-IT实验中,与对照组相比,随机接受每天近4克纯化EPA乙酯的患者在中位4.9年后发生房颤的风险显著增加。OMEMI 试验中约1.6克/天的Omega-3脂肪酸(930 毫克EPA和660毫克DHA)中间剂量也导致治疗组与安慰剂相比发生更多房颤。
包括2012年至2020年间发表的7项随机对照试验。在81210名患者中,72.6%参加了每天测试≤1g Omega-3不饱和脂肪酸的试验,27.4%参加了每天测试>1g Omega-3不饱和脂肪酸的试验。随访时间为4.9年。使用较高剂量的Omega-3脂肪酸与房颤风险增加相关。
因此,大多数最近试验的荟萃分析表明,Omega-3不饱和脂肪酸可能会增加房颤的风险,特别是在高剂量使用时。
最近的研究认为,Omega-3不饱和脂肪酸对房颤的影响是U形的:中等剂量时它们会降低房颤风险,但高剂量时会增加风险。
鉴于Omega-3不饱和脂肪酸改善心血管的能力,2019年,美国心脏协会更新了之前的建议,即每天使用2-4克EPA+DHA来降低甘油三酯。
作为单一疗法或作为其他降甘油三酯疗法的辅助疗法。欧洲心脏病学会和欧洲动脉粥样硬化学会发布了《血脂异常管理临床实践指南》的更新版,特别建议“在患有甘油三酯的高危患者中尽管使用他汀类药物治疗,但其水平在1.5至5.6mmol/L(135–499 mg/dl)之间,Omega-3不饱和脂肪酸应考虑与他汀类药物一起使用。”
美国脂质协会声明称,“对于年龄≥45岁患有临床动脉粥样硬化性心血管疾病(ASCVD)的患者,或年龄≥50岁患有糖尿病且需要药物治疗且有≥1个额外危险因素的患者,空腹甘油三酯为135至499 mg/dl高强度或最大耐受他汀类药物治疗,建议使用Omega-3不饱和脂肪酸以降低ASCVD风险”。
美国心脏协会重申了之前对心血管疾病患者使用EPA+DHA的支持并扩展它,指出对于患有流行性冠心病(例如近期发生心肌梗死)的患者的建议基本保持不变:对于这些患者来说,补充Omega-3不饱和脂肪酸治疗是合理的。即使该临床人群的冠心病死亡率可能略有下降(10%),也可以证明采用相对安全的疗法进行治疗是合理的。
Omega-3可以通过饮食和补充剂获得。饮食来源主要包括富含Omega-3的鱼类,如三文鱼、鲭鱼、鲑鱼和金枪鱼。对于不常吃鱼或希望通过补充剂摄入Omega-3的人,可以考虑鱼油补充剂、藻油补充剂(适合素食者)或亚麻籽油补充剂。
定期检查健康状况,特别是心血管健康指标和血脂水平,可以帮助评估Omega-3补充的效果,并根据需要调整摄入量。
Omega-3脂肪酸,作为一类不饱和脂肪酸,主要包括α-亚麻酸(ALA)、二十碳五烯酸(EPA)和二十二碳六烯酸(DHA),对人体健康具有重要影响。
许多研究已经证明,Omega-3脂肪酸对心血管健康具有显著益处,能有效降低心血管疾病的风险,包括降低血压、减少甘油三酯水平及抑制炎症。
此外,Omega-3脂肪酸对大脑健康也至关重要,特别是DHA,它是大脑结构的重要组成部分,对维持认知功能、预防认知衰退有重要作用,还能在一定程度抗抑郁。
在孕妇和婴儿的营养中,Omega-3脂肪酸对神经系统的发育同样不可或缺,还有助于提高视力和认知能力的发展。
尽管Omega-3脂肪酸的健康益处众多,但它们在人体内不能自主合成,必须通过饮食来获取。这就需要通过富含Omega-3的食物如三文鱼、鲭鱼、鲑鱼和沙丁鱼等深海鱼类;此外,亚麻籽、奇亚籽、核桃以及高品质的亚麻籽油和藻类油也是优质的植物性Omega-3来源,或是通过补充剂来确保足够的摄入量。
Omega-3不饱和脂肪酸与肠道微生物群的多样性相关,足量的Omega-3有助于抑制炎症因子修复肠道屏障,同时更稳定健康的肠道微生物有利于将α-亚麻酸转化为Ω3脂肪酸,维持Omega-3的稳定水平,增加健康益处。
需要注意的是,补充Omega3脂肪酸时也应适度适量,无论是饱和脂肪酸还是不饱和脂肪酸,如果摄入量超过了人体的能量需求,多余的脂肪酸就会在体内转化为脂肪储存起来,导致人体肥胖,以及可能存在的一些未被发现的隐患,重要的是根据每个人自身的需求来制定精准的日常膳食。
主要参考文献
Kerman BE, Self W, Yassine HN. Can the gut microbiome inform the effects of omega-3 fatty acid supplementation trials on cognition? Curr Opin Clin Nutr Metab Care. 2024 Mar 1;27(2):116-124.
Djuricic I, Calder PC. Pros and Cons of Long-Chain Omega-3 Polyunsaturated Fatty Acids in Cardiovascular Health. Annu Rev Pharmacol Toxicol. 2023 Jan 20;63:383-406.
Shahidi F, Ambigaipalan P. Omega-3 Polyunsaturated Fatty Acids and Their Health Benefits. Annu Rev Food Sci Technol. 2018 Mar 25;9:345-381.
Li JJ, Dou KF, Zhou ZG, Zhao D, Ye P, Zhao JJ, Guo LX. Role of omega-3 fatty acids in the prevention and treatment of cardiovascular Diseases: A consensus statement from the Experts’ Committee Of National Society Of Cardiometabolic Medicine. Front Pharmacol. 2022 Dec 12;13:1069992.
Patel D, Evanchuk J, Wang R, Dunbar CL, Munhoz J, Field CJ. Regulation of immune function in healthy adults: one-stop guide on the role of dietary fatty acids, gut microbiota-derived short chain fatty acids, and select micronutrients in combination with physical activity. Appl Physiol Nutr Metab. 2023 Aug 1;48(8):554-568.
Yan Y, Jiang W, Spinetti T, Tardivel A, Castillo R, Bourquin C, Guarda G, Tian Z, Tschopp J, Zhou R. Omega-3 fatty acids prevent inflammation and metabolic disorder through inhibition of NLRP3 inflammasome activation. Immunity. 2013 Jun 27;38(6):1154-63.
Bae JH, Lim H, Lim S. The Potential Cardiometabolic Effects of Long-Chain ω-3 Polyunsaturated Fatty Acids: Recent Updates and Controversies. Adv Nutr. 2023 Jul;14(4):612-628.
Samrit T, Osotprasit S, Chaiwichien A, Suksomboon P, Chansap S, Athipornchai A, Changklungmoa N, Kueakhai P. Cold-Pressed Sacha Inchi Oil: High in Omega-3 and Prevents Fat Accumulation in the Liver. Pharmaceuticals (Basel). 2024 Feb 7;17(2):220.
Rinninella E, Costantini L. Editorial: Polyunsaturated fatty acids and gut microbiota. Front Nutr. 2023 Jul 28;10:1256817.

谷禾健康

运动对心肺健康、肌肉力量、葡萄糖代谢、免疫系统和心理健康有影响。新的横断面研究证据表明,运动锻炼与肠道微生物群组成之间可能存在密切关联。

干预研究支持锻炼对肠道微生物群的有益影响。纵向研究表明,经常中等强度的耐力运动对肠道微生物产生最有益的影响,但是不同类型的运动训练方案(例如,阻力、间歇、伸展/柔韧性、耐力/有氧等)对肠道微生物群的影响存在差异。其他如饮食摄入,结肠运送时间,训练状态,共享训练环境,自愿性,健康或疾病状况,年龄,性别等因素也是评估运动和肠道菌群的混杂因素。

反过来,肠道微生物群对运动表现、恢复和疾病模式的各种指标都有间接影响,例如通过肌细胞因子,激素,神经肽和其他代谢物发出信号,调节下丘脑-垂体-肾上腺轴的激活,以及影响与表现相关的代谢途径。
了解肠道微生物群在运动表现中的各种作用,对于寻求改善锻炼结果以及减少训练恢复时间的普通人和运动员来说都非常重要。
本文就以下方面进行详细阐述:

最近的研究表明,运动对肠道微生物群有很多好处。它与有益微生物物种数量的增加和微生物多样性的丰富以及短链脂肪酸合成和碳水化合物代谢的增强有关。
适度运动的频率会导致厚壁菌门的多样性更大。包括Faecalibacterium prausnitzii(产生丁酸,抗炎共生菌),颤螺菌属(Oscillospira) ,有助于更健康肠道环境的Lachnospira和Coprococcus属的成员。
体脂百分比、肌肉质量和身体活动与几种细菌种群显著相关
研究发现,锻炼与女性中具有促进健康功能的细菌的比例更高有关。包括以产生丁酸盐的能力而闻名的F. prausnitzii(普拉梭菌)和Roseburia hominis,以及运动员体内丰富的Akkermansia muciniphila,低水平与肥胖和糖尿病等代谢状况有关。
一项研究调查了 40 名国际职业橄榄球联盟球员的微生物组,并将其与 BMI 高或低的相似年龄的对照组进行比较。结果表明,运动员肠道微生物多样性显著著增加。
与对照组相比,许多其他参数也显示出显著改善的结果。其中包括短链脂肪酸 (SCFA),该研究发现与对照组相比,运动员体内的乙酸盐、丙酸盐、丁酸盐和戊酸盐水平明显更高。”
简而言之,运动已被证明可以显著改善与身体表现和健康相关的几个指标,特别是在有益细菌类型及其功能方面。
然而,这些观察性研究的结果只能确认训练状态和微生物群之间的关联,而不能确定因果关系。
运动与肠道微生物群组成之间的关联似乎是双向的。来自动物研究的越来越多的证据也表明肠道微生物群在宿主的身体机能中起着重要作用。肠道微生物群的组成和代谢活动可能有助于消化膳食化合物并改善运动期间的能量收集,这可以为运动员在高强度运动和恢复期间提供代谢益处。
观察性研究表明,与久坐的受试者相比,运动员微生物组中与氨基酸和碳水化合物代谢相关的代谢活动和途径增加。
在肠道中,细菌将不易消化的碳水化合物发酵成短链脂肪酸乙酸盐、丙酸盐和丁酸盐。训练和定期锻炼与人类粪便短链脂肪酸含量增加有关,并且在动物研究中,特定短链脂肪酸与改善身体机能有关。
大多数短链脂肪酸从肠道吸收并有助于宿主的能量代谢。
丁酸盐主要被结肠中的上皮细胞用作能量来源。
乙酸盐在肌肉组织中代谢,但也可以穿过血脑屏障。
丙酸盐可用作肝脏中葡萄糖合成的前体。
此外,短链脂肪酸可改善肠道屏障完整性,降低局部和全身炎症风险。临床前研究强烈表明短链脂肪酸可能是身体机能的关键调节剂。
值得注意的是,宿主可能不是唯一受益于运动期间与微生物群的共生关系的一方。
目前关于肠道微生物群与身体机能之间相互作用如下:
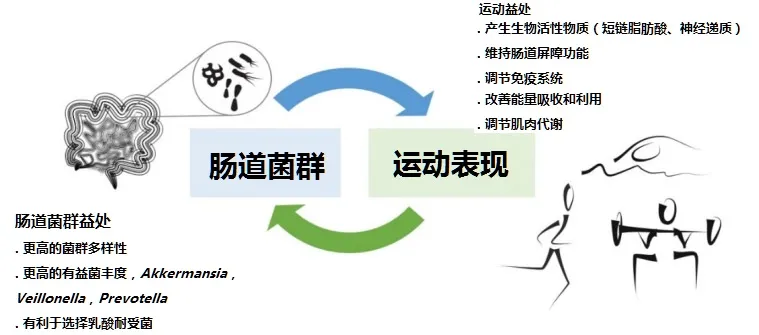
Maija Marttinen et al., Nutrients.2020

你可能想知道运动是否会改变微生物群,或者拥有健康的微生物群是否会让你更加活跃想运动。其实这用一句俗话讲就是“先有鸡还是先有蛋”的情景。
例如,肠道菌群失调会引起炎症,从而导致负面情绪,抑郁等症状,而抑郁不利于外出和积极运动锻炼。
多项研究表明,运动实际上可以改变你的肠道微生物群。
女性:运动与久坐女性菌群有差异
2017 年一项针对女性的研究表明,积极活动方式的女性和久坐女性之间肠道微生物群特征的差异。
积极参与者被选为在试验期间在 7 天内进行至少 10 小时运动的组。久坐组参加安静的活动,并从日常生活中不是经常运动的女性中挑选出来,每周进行 3 次不超过 30 分钟的适度运动。
11 个属(细菌的分类等级)在运动女性和久坐女性之间存在显著差异。重要的是,运动的女性群体拥有更丰富的促进健康的细菌,包括Faecalibacterium prausnitzii、Roseburia hominis和Akkermansia muciniphila.
他们还发现“体脂百分比、肌肉质量和身体活动与几种细菌种群显著相关。”
换句话说就是,过着积极的生活方式更能取悦某些细菌,这是一种正向反馈。
橄榄球运动员比久坐者具有更高的α多样性
一项对爱尔兰男性职业橄榄球运动员的研究表明,与久坐的对照组相比,运动员肠道微生物群的 α 多样性(细菌丰富度,例如在粪便样本中鉴定了多少细菌种类)更高。
肠道微生物群多样性与蛋白质消耗和血浆肌酸激酶水平呈正相关,血浆肌酸激酶水平是运动引起的肌肉损伤的生物标志物。
与高 BMI 对照组的比例相比,在橄榄球运动员和低体重指数 (BMI) 对照组中检测到的Akkermansia细菌比例更高。与低 BMI 的对照组相比,运动员中拟杆菌属的含量显著减少。
从大人群水平上看,Akkermansia和拟杆菌属与肥胖呈负相关。
在微生物代谢水平上也检测到橄榄球运动员和久坐对照组之间的差异,在运动员中检测到的氨基酸和碳水化合物代谢途径活性增加。此外,与久坐的对照组相比,橄榄球运动员的粪便 SCFA(乙酸盐、丙酸盐和丁酸盐)水平更高。
竞技自行车运动员中:经常训练者普氏菌高
在竞技自行车运动员中,每周训练超过 11 小时的自行车手比那些不经常训练的人的普氏菌相对丰度更高。
此外,元转录组学分析表明,普氏菌的转录与微生物组中的支链氨基酸 (BCAA) 代谢途径呈正相关。支链氨基酸,尤其是亮氨酸,是促进肌肉蛋白质合成的必需氨基酸,可以促进运动后的恢复。(详见本文09章节——蛋白质小节)
与业余自行车手相比,在职业自行车手中发现了更多的粪便Methanobrevibacter smithii。该菌与上调的甲烷代谢相关,这与肠道微生物组中短链脂肪酸代谢途径的上调呈正相关。
遗憾的是,该研究没有饮食控制和非运动员对照组。与在骑自行车的人中观察到的结果一致,在一小群精英竞走者中,粪便微生物群被分为普氏菌或拟杆菌为主的肠型。
马拉松运动员:韦荣球菌增加
马拉松运动员中的韦荣球菌丰度在马拉松后显著增加。此外,同一研究小组使用来自超级马拉松运动员和奥运会级别赛艇运动员的粪便样本进行宏基因组分析,结果显示与运动前样本相比,运动后与乳酸和丙酸代谢相关的基因富集。
在小鼠中进行的一项后续研究表明,研究人员从跑步者的粪便中分离培养出Veillonella atypica菌株,给小鼠灌注,结果发现,小鼠开始跑得更多,在跑步机上的跑步时间增加了 13% 。
中强度锻炼的人:促进健康和抗炎细菌增加
除了由专业或竞技运动员进行的高强度训练外,根据世界卫生组织 (WHO) 每周进行 150 分钟中等强度运动的指导方针,以推荐的最低水平进行运动 ,似乎足以改变肠道微生物群的组成。
与久坐不动的女性相比,以低强度进行连续运动的绝经前女性的嗜粘蛋白阿克曼菌、普拉梭菌等的丰度增加。这些都是与促进健康和抗炎作用相关的细菌种类。
此外,运动组和久坐组之间不同的饮食模式可能影响了肠道微生物群的组成,与久坐的女性相比,运动女性的膳食纤维摄入量明显更高,久坐组加工肉类的摄入量比例明显更高。
长期运动的人:菌群多样性更高
在迄今为止最长的运动干预中,研究了在 6 个月内,具有相似运动能耗的不同强度和方式的定期有氧训练对肠道微生物群的影响。
总共 88 名久坐的超重/肥胖受试者被随机分为四个组,包括习惯性生活(对照组)、非机动自行车积极通勤、休闲时间中等强度的运动或剧烈运动。
与对照组相比,所有运动组的 β多样性(样本间差异)都发生了变化,剧烈运动组的参与者组内菌群差异度变小,换句话说就是构成趋向一致。
此外,与对照组相比,剧烈运动组在3个月时的 α多样性增加更多。这表明可能需要更剧烈的运动来诱导久坐、超重/肥胖受试者的肠道微生物群发生变化。
在一项关于剧烈运动的研究中,拟杆菌门增加,厚壁菌门/拟杆菌门比率下降。这一结果与运动员有关,因为拟杆菌的增加在复杂糖聚合物的代谢转化和蛋白质降解中起着至关重要的作用。
梭菌属和Blautia属也减少了。梭菌在全身免疫反应中起着重要作用,而Blautia会增加促炎细胞因子的释放。有趣的是,结肠葡萄糖浓度与拟杆菌呈正相关,并与厚壁菌门、厚壁菌门/拟杆菌门比率和Blautia属相反。此外,Blautia属的丰度较低与更好的全身胰岛素敏感性相关。
这些结果强调了肠道底物摄取对全身的重要性,尤其是葡萄糖和蛋白质摄取,可能对肠道微生物群产生积极影响。
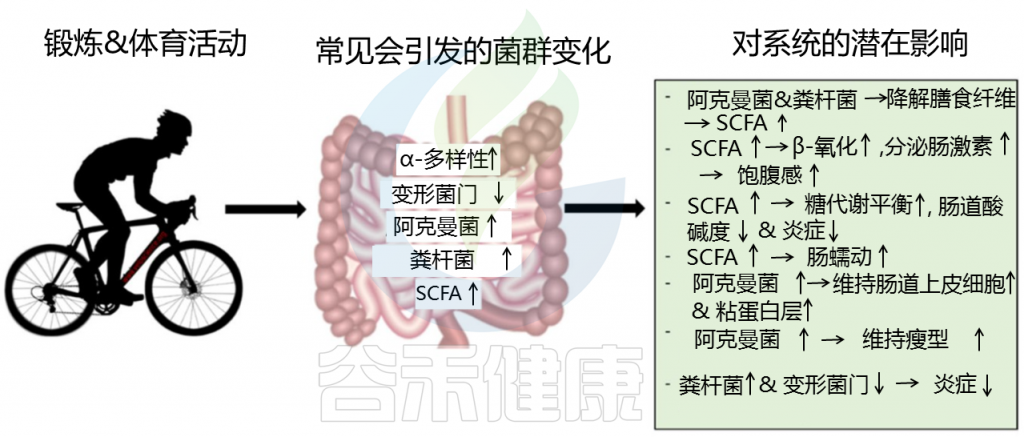

Lensu, S. et al., Metabolites, 2021
在儿童和老年人中也证明了身体活动水平与肠道微生物群组成之间的关联。
儿童:运动者菌群中梭菌目、毛螺菌科增加
来自美国肠道项目的 7-18 岁儿童研究队列中,在控制协变量(年龄、性别和使用抗生素和益生菌)。运动频率与富含厚壁菌门的肠道微生物群有关。此外,每天锻炼的儿童在梭菌目、毛螺菌科中的属增加了。
老年男性:与粪杆菌和Lachnospira菌有关
在老年男性中,根据步数和自我报告的活动测量的体力活动与微生物 α 多样性无关,但体力活动水平与粪杆菌属和Lachnospira属之间存在适度关联。
这些研究表明,运动员或经常运动人群与久坐人群之间的肠道微生物群组成存在差异。
运动者菌群特征可能与饮食有关
然而,运动员和身体活跃的人体内微生物群组成的一些特征可能是通过饮食来解释的,而不是运动的影响。
运动员经常遵循支持训练和表现的严格饮食,而极端运动通常与极端饮食有关。与正常人群相比,运动员的蛋白质摄入量可能要高得多。蛋白质补充剂通常用于满足训练者对蛋白质的更高需求,尽管蛋白质补充剂的流行也可能受到有关增加肌肉质量和改善性能和恢复的说法的影响。
摄入大量蛋白质后,未被吸收的蛋白质会进入结肠并促进特定细菌的生长和选择。
持续 10 周的蛋白质补充剂(乳清分离物和牛肉水解物)增加了跑步者拟杆菌的丰度,并减少了与健康相关的分类群,包括Roseburia spp、Blautia spp 和长双歧杆菌。然而,肠道微生物群组成的这种改变对宿主健康的长期影响仍不清楚。
动物研究:运动产生的变化与年龄、饮食、是否自愿、个体生理状态等因素都有关
很少有研究关注自愿运动对肠道微生物群的影响,迄今为止,除了七项实验研究外,所有研究都使用了小鼠模型。这些初步研究表明,运动会影响肠道微生物群的组成。
大鼠定期跑步运动与产丁酸菌的增加以及丁酸盐浓度的增加有关。其他动物研究表明,通过影响小鼠肠道微生物组成,每日轮式跑步运动可能会改善不健康状态的某些方面,例如饮食引起的肥胖、糖尿病和毒性。这些影响包括改变优势门厚壁菌门和拟杆菌门之间的比例。然而,这在研究之间并不总是相同。
在对动物进行的运动研究中,对于哪些种群受慢性运动的影响几乎没有达成一致。除了运动和乳酸杆菌之间的正相关关系之外,没有其他分类群在经常锻炼的小鼠或大鼠中相对丰度持续增加。
运动所产生的变化似乎取决于个人的生理状态。例如,无论是肥胖-高血压大鼠还是正常大鼠,有规律的强迫运动对微生物群的丰度都有不同的影响。高脂饮食的大鼠运动对微生物群的改变与正常饮食的大鼠不同,并且糖尿病小鼠产生的改变与其对照小鼠不同。
总的来说,这些发现表明,长期运动对微生物群的调节不仅取决于个体的生理状态,还取决于饮食。此外,动物强制运动与自愿运动之间的另一个显著差异是运动量。这在人类骑自行车的数据中得到了概括,需要在动物模型中进一步研究。
此外,年龄,性别也会呈现不同效果。据观察,与成年大鼠相比,运动对幼年大鼠的微生物群产生更有效的改变。在这些检查运动训练对肠道微生物群的影响的小鼠研究中,一个共同的发现是增加了α多样性。

在研究人类肠道微生物群时,很难分别研究运动和饮食。这种关系因饮食摄入变化而变得更加复杂(例如,抗阻力训练运动员的蛋白质摄入量增加或耐力运动员的碳水化合物摄入量增加,以及总体能量和营养摄入量的增加)。
为什么部分运动人群和久坐人群的菌群无显著差异?
高蛋白 + 膳食纤维少 = 运动改变菌群无效
韩国的一项研究表明,高蛋白/限制性膳食纤维与健康久坐人群之间的肠道微生物多样性或有益细菌没有显著差异。然而,当蛋白质或膳食纤维摄入量符合 KRDA(韩国推荐膳食允许量)时,肠道微生物多样性和有益细菌的相对丰度与健康久坐的受试者相比有显著差异。这些结果表明,运动对肠道微生物群的积极影响取决于蛋白质和膳食纤维的摄入量。结果还表明,在补充益生菌之前,应解决营养充足的问题。
研究人群之间膳食摄入量的差异,可能解释了不同研究结果之间观察到的一些不一致之处。
在韩国的一项临床研究中,总蛋白质摄入量与微生物多样性呈负相关 ,而爱尔兰职业橄榄球运动员的高蛋白质摄入量与微生物多样性增加有关。韩国运动员不符合膳食纤维摄入量的膳食建议(建议≥ 25 g/天;健美运动员的中位摄入量 19 g/天,耐力运动员 17 g/天),而爱尔兰橄榄球运动员的纤维摄入量处于推荐水平(中位摄入量 39 克/天)。
未消化的膳食纤维是肠道微生物群的重要能量和碳源,是短链脂肪酸合成的底物,是微生物多样性的关键贡献者。高蛋白饮食与低膳食纤维饮食相结合,可能对肠道微生物群组成有害,而不是单独摄入高蛋白。
营养补充剂介入运动和微生物关联
此外,主要来自动物研究的有限数据表明,流行的运动营养补充剂,如咖啡因、支链氨基酸、碳酸氢钠和肉碱,可以改变肠道微生物群的组成。大型研究队列的结果表明,运动与梭菌和毛螺菌科中的属增加有关。
其他小样本人群研究
尽管有几项研究调查了可能缺乏足够统计功效的小样本群,但有趣的是,通常诸如Akkermansia 和Prevotella等属在运动员和身体活跃的受试者中含量更高。然而,由于临床研究的数量仍然有限,参与者的人口统计学和膳食摄入量(特别是膳食纤维摄入量)差异很大,因此应谨慎得出结论。
运动前后营养变化不大,但是菌群有变化
运动对肠道菌群的影响需要考虑运动期间的饮食因素,那么运动前后对营养元素是否会显著变化?
一个研究小组表明,运动训练干预改变了久坐、未受过训练的芬兰女性的肠道微生物群组成,而饮食习惯、体重或身体成分没有改变。
作者证明,耐力运动改变了超重、久坐女性的肠道微生物群,这些女性参加了一项运动干预,包括每周 3 次、持续六周的自行车训练。研究表明,在训练干预后,总摄入量或常量营养素或膳食纤维的摄入量没有差异。
然而,耐力运动增加了Verrucomicrobia和Akkermansia相对丰度并减少肠道中与炎症相关的变形菌数量。此外,变形菌门和疣微菌门属对运动有反应,并且与年龄、体重、体脂百分比和食物摄入量无关。另一项研究为期 12 周的有氧运动训练计划显著增加了拟杆菌属的相对丰度,但是在年长、久坐的女性中,营养摄入没有变化。
下表总结了关于运动和/或运动饮食对肠道微生物群影响的研究



Mohr AE, et al., J Int Soc Sports Nutr. 2020

除了影响肠道微生物群,运动还会影响胃肠道生理机能。尽管运动通常是一种有益的或“刺激性”压力,但如果持续时间和强度的增加得不到足够的训练、休息、营养和抗氧化状态的支持,它就会变得有害。
运动后的生理效应
运动会激活自主神经系统,增加外周组织和胃肠道中皮质醇和儿茶酚胺、肾上腺素和去甲肾上腺素的循环浓度。这会导致流向胃肠道的血流量减少,导致缺氧、ATP 耗竭和氧化应激。这些作用会破坏肠道屏障,增加肠道通透性、内毒素血症、营养消耗和炎症。胃肠道通过释放与胃肠道紊乱相关的神经递质,如 γ-氨基丁酸 (GABA)、神经肽 Y 和多巴胺来应对压力激活。这些生理效应与运动的强度、持续时间和频率成正比。
长时间运动可能造成胃肠道紊乱
虽然低至中等强度的运动促进胃肠蠕动和转运时间,但剧烈的 [ >60%最大摄氧量(VO2max) ] 或长时间 (≥2 小时) 运动可能会产生相反的效果,并会造成急性胃肠道紊乱。定期运动可促进适应以维持肠道血流并减少炎症,当然恢复也必须足够。
为什么耐力运动员中常出现胃肠道问题?
胃肠道问题很常见,特别是在耐力运动员中,30-50% 的运动员出现胃肠道不适症状。这些症状可以通过生理,机械,心理,营养因子,包括血流量减少,增加的肠通透性引起的,产量增加应激激素和炎症细胞因子,胃排空不足。
然而,在耐力跑之外,很少评估胃肠道症状。例如,一项对参加 4 天严格越野滑雪行军的士兵的研究显示肠道通透性增加,但没有报告胃肠道症状,这使得对主观体验的影响和对运动表现的影响尚不清楚。
肠道上皮具有高周转率(3-5 天),需要大量的能量和营养。在没有足够燃料的情况下长时间高强度训练的运动员有可能出现肠道完整性和功能紊乱以及胃肠道症状。特别是,习惯性碳水化合物摄入量不足会增加对长时间、持续剧烈运动的促炎应激反应。

★
根据运动类型、强度、年龄和其他因素,20-50% 的运动员会出现胃肠道症状,并且随着运动强度的增加而增加。
高强度运动带来的负面影响
在对 29 名训练有素的男性铁人三项运动员的研究中,在比赛中,93% 的人报告消化功能紊乱,两名参与者因严重呕吐和腹泻而不得不放弃比赛。这些在运动员中很常见,因为在剧烈运动期间体温升高,血液从胃肠道流向周边肌肉和器官,如心脏和肺。远离肠道的血流重新分布以及对肠黏膜的热损伤可导致肠道屏障破坏,继而引发炎症反应。
在每周进行 4-10 小时耐力运动的健康年轻成年男性骑自行车者中,仅以 70% 的最大工作负荷进行 1 小时的运动就会产生内脏灌注不足,这会导致胃肠道循环减少、肠道通透性增加和小器官受损。
另一项研究表明,在 70% VO2max 下运动的人会导致内脏血流量减少 60-70%,当血流量减少 50% 时,运动引起的缺血会导致肠道通透性增加 。
加一句题外话,例如明星,网红为了美,限制碳水摄入,同时大量高强度锻炼来达到快速瘦身的效果,其实损害了肠道健康,可能会引起全身炎症反应,不要盲目效仿。
然而,研究主要集中在运动期间急性摄入(之前和期间)对胃肠道症状的影响,而不是习惯性饮食,尽管越来越多的运动员和研究人员关注避免食物的策略,例如低发酵低聚糖,二糖、单糖 、FODMAP 饮食或无麸质饮食。
剧烈运动 -> 胃肠道紊乱 -> 影响肠道微生物群
导致胃肠道症状的氧化应激增加和肠道屏障功能紊乱也会影响肠道微生物群。LPS(由肠道通透性增加引起的革兰氏阴性菌的成分)的易位会导致内毒素血症并触发促炎细胞因子分泌到胃肠道中,这可能会影响肠道微生物群并进一步加剧病情。
反过来:肠道微生物群失调 -> 胃肠道紊乱
相反,微生物代谢物丁酸盐和丙酸盐可作为结肠细胞的能量来源,减少粘膜降解、胃肠道通透性和炎性细胞因子。
肠道微生物群可作为生物标志物
由于微生物组成和多样性的改变与运动员胃肠道不适的流行有关,因此肠道微生物群组成可用作运动后代谢和全身压力的生物标志物。
例如,一项研究运动对血清和粪便代谢组以及肠道微生物群的急性影响的研究表明,一次运动上调骨骼肌底物利用和血清中碳水化合物代谢物的代谢途径,增加粪便氨和氨基酸代谢物,并增加梭菌的丰度。因此,微生物和代谢物谱的急剧变化可以提供有关运动对胃肠道和代谢影响的信息。
此外,考虑到运动对肠道微生物群的影响以及对以肠道为中心的饮食策略的需求,胃肠道症状评估可以补充有关肠道微生物群组成的信息。

一般运动员在运动训练中摄入大量单糖,以最大限度地储存糖原和维持血糖,同时尽量减少膳食纤维和抗性淀粉的摄入,以防止胃肠道紊乱。膳食纤维和抗性淀粉摄入不足可能会导致排便减少,从而导致肠道功能下降,也会降低肠道微生物群的多样性。
此外,运动员比非运动员消耗更多的动物蛋白来满足肌肉增生的需要。蛋白质摄入过多会导致肠道微生物中氮底物过量,产生腐败的发酵产物,如氨、硫化氢、胺、酚、硫醇和吲哚。随着食糜通过肠道,碳水化合物含量减少,腐烂的发酵变得更加有害。
实际上,蛋白质摄入过量,同时结肠中可发酵的膳食底物较低,会导致结肠黏膜DNA损伤。
高强度运动通过血液影响肠道微生物群
此外,高强度运动刺激血液从肠道器官重新分配到肌肉,同时它们积极进行细胞呼吸。血液的频繁重新分布可能会通过内脏低灌注和缺血以及随后的再灌注来扰乱肠道微生物群。因此,需要研究特定运动类型和运动员饮食对肠道微生物群的长期影响。
肠道微生物群在胃肠道功能、肠道免疫、内分泌以及调节氧化应激和水合水平等方面扮演多种角色,对肠道微生物群改善运动员肠道屏障功能的机制的研究也就越来越多。
微生物群产生的 SCFA 影响一系列宿主过程
在结肠和盲肠中,复杂的植物来源的多糖被消化,随后被肠道微生物(如乳杆菌、双歧杆菌、梭状芽孢杆菌、拟杆菌)发酵成短链脂肪酸和气体,这些气体也被专门的细菌(如还原性产乙酸菌)用作碳和能源、硫酸盐还原菌和产甲烷菌。肠道中乙酸盐、丙酸盐和丁酸盐在结肠和粪便中的摩尔比约为 60:20:20。肠道微生物群的组成,微生物群之间的代谢相互作用,及主要膳食宏量和微量营养素的数量和类型,决定了肠道微生物群产生的短链脂肪酸的类型和数量。
一个人吃的植物来源的多糖、寡糖、抗性淀粉和膳食纤维越多,这些细菌就越能将这些难以消化的食物来源发酵成有益的短链脂肪酸。微生物群产生的短链脂肪酸影响一系列宿主过程,包括控制结肠 pH 值,进而影响微生物群组成、肠道运动、肠道通透性和上皮细胞增殖。
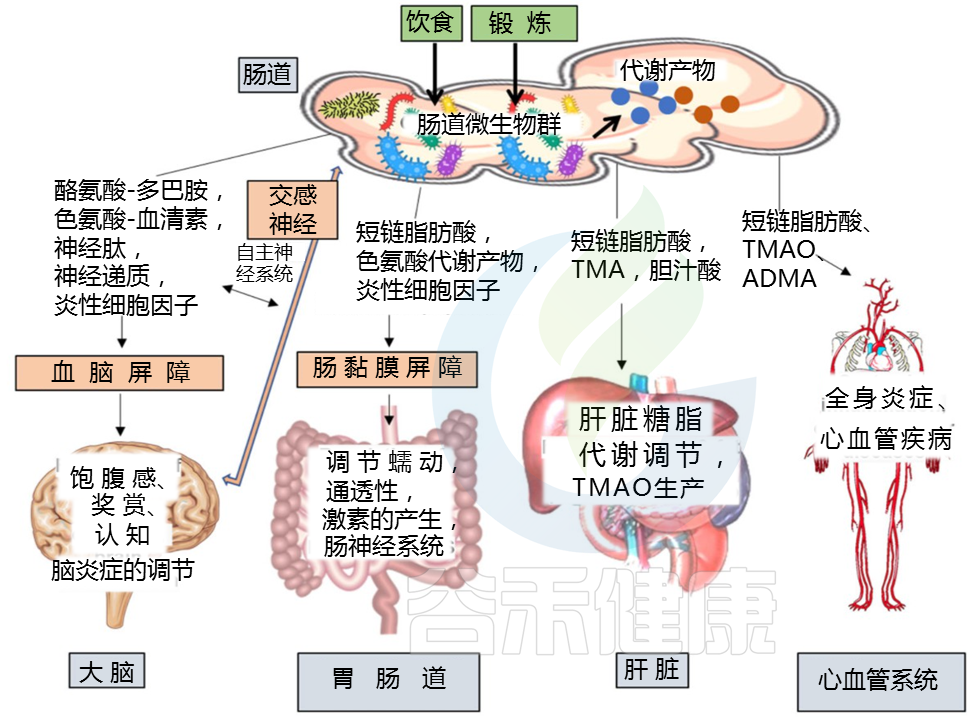
Lensu, S. et al., Metabolites, 2021

运动引起的压力会改变分解代谢激素、细胞因子和肠道微生物群,这可能会导致胃肠道紊乱、焦虑、抑郁和表现不佳。肠道微生物群在人类生物学的许多方面都具有基础性作用,包括新陈代谢、内分泌、神经元和免疫功能。
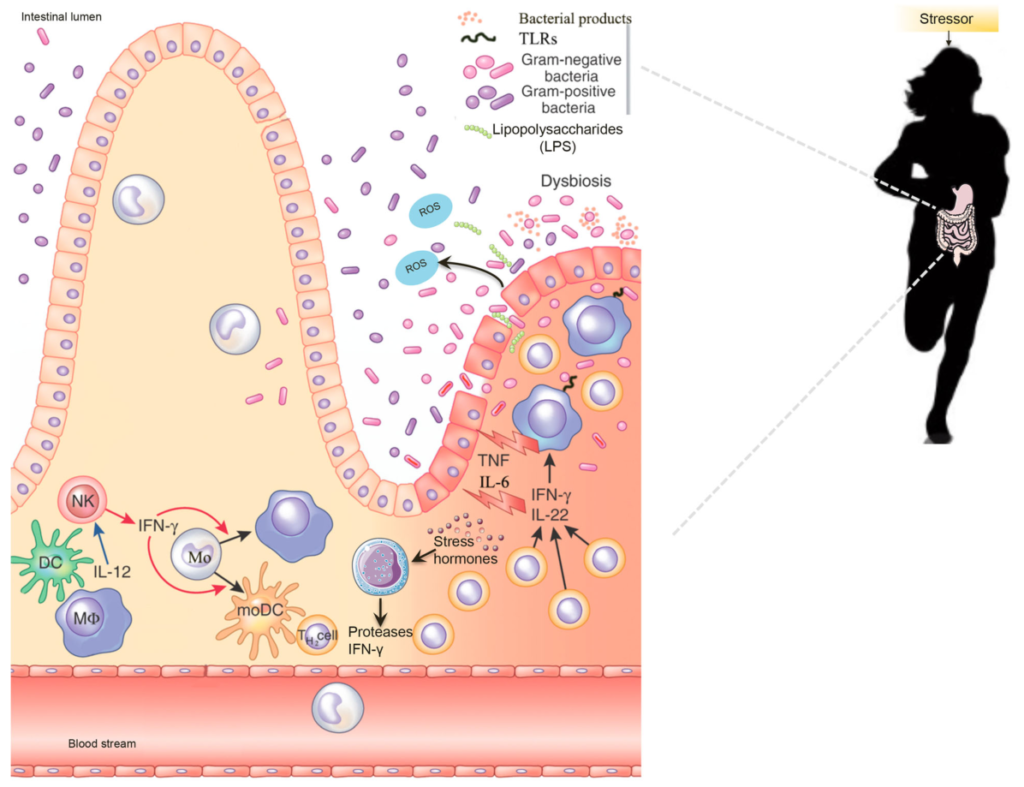
Allison Clark & Núria Mach,J Int Soc Sports Nutr. 2016
适当的肠道屏障功能对于维持健康和免疫力至关重要。但是训练和比赛数小时的精英运动员会经历身体和情绪压力,导致生理稳态发生变化,刺激SAM(交感神经-肾上腺髓质轴)和 HPA轴(下丘脑-垂体-肾上腺轴)高强度运动期间的胃肠道紊乱。
在剧烈运动期间,运动员的体温会升高,血液会在剧烈运动时从胃肠道流向周围肌肉和器官,例如心脏和肺。远离肠道的血流重新分布以及对肠黏膜的热损伤可导致肠道屏障破坏,继而引发炎症反应。长时间的剧烈运动会增加胃肠道中的应激激素和脂多糖 (LPS) 易位,从而引发免疫反应,这通常会导致促炎细胞因子和肠道通透性增加。
由于活性氧 (ROS) 的产生增加以及肠道微生物群组成和活性的改变(所谓的生态失调),肠道通透性可能会变得更糟。
胃肠道通过释放 GABA、神经肽 Y (NPY) 和多巴胺等激素来应对压力,这些激素会导致胃肠道紊乱、焦虑、抑郁、食物摄入减少和压力应对能力降低。相反,微生物群产生的丁酸盐和丙酸盐可以增加跨上皮抵抗,从而改善肠道屏障功能并减少炎症。
胃肠道通过释放 GABA、NPY和多巴胺等激素来应对压力
GABA,这是身体的主要抑制中枢神经系统的神经递质,调节血压和心率和在各种胃肠道功能中起着重要作用,如运动性,胃排空和瞬态下食道括约肌放松,以及焦虑、抑郁,疼痛感和免疫反应。
适度运动可以增加下丘脑中的 GABA 水平,从而降低静息血压、心率和交感神经张力。在 25 °C 水中强迫游泳时,发现大鼠海马 GABA 水平下降(基线的 70%)。
神经肽 Y(NPY)也会在胃肠道中响应各种压力刺激(例如剧烈运动)而释放,并在减弱 HPA 轴方面发挥作用。
注:神经肽Y是一种36个氨基酸的肽,位于整个肠脑轴,是大脑中最普遍的神经肽,在压力恢复和炎症过程中发挥作用。
检测了 12 名训练有素的赛艇运动员的神经肽 Y血清水平,发现运动后神经肽Y的浓度显著增加。虽然很少有研究研究了血清和海马 NPY 水平对运动的反应,但这些结果表明它在减少剧烈运动时的压力反应方面发挥作用。
多巴胺(去甲肾上腺素和肾上腺素的前体)也可以在胃肠道压力期间合成。
多巴胺的产生取决于几个因素:
整个肠道中有多种多巴胺受体,表明它在肠-脑轴中发挥作用。胃肠道、脾脏和胰腺会产生大量的多巴胺。在人胃上皮细胞中发现了多巴胺合成的限速酶酪氨酸羟化酶,表明其功能存在于大脑中的神经传递之外。每天大约 1-2 小时的习惯性运动已被证明会增加大脑中的多巴胺水平。
肠道微生物群如何与周围组织(如胃肠道粘膜层)的应激激素直接相互作用?
去甲肾上腺素(NE)已显示对肠道嗜水气单胞菌(Aeromonas hydrophila)、博德特氏菌属(Bordetella)、空肠弯曲杆菌(Campylobacter jejuni)、幽门螺杆菌(Helicobacter pylori)、李斯特菌(Listeria)和沙门氏菌(Salmonella enterica)有直接影响。
其中去甲肾上腺素促进致病细菌生长的一些方法是,通过增加其毒力因子 K99 菌毛粘附素的表达以及激活鼠伤寒沙门氏菌中毒力相关因子的表达来促进大肠杆菌粘附在肠壁上,然后使这些细菌更容易感染。
此外,去甲肾上腺素还会增加非致病性大肠杆菌和其他革兰氏阴性菌的水平。
微生物组如何调节运动引起的压力反应?
最近发表了一项研究,揭示了对胃肠道和全身健康很重要的,独特微生物群—宿主相互作用。
在结肠炎小鼠模型中,自愿跑步 6 周会减轻症状,而强制跑步机跑步会加剧肠道炎症和临床结果。粪便和盲肠水平与 6 周强制跑步机跑步组相比,与免疫功能和肠道疾病密切相关的在自愿跑步者中显著降低。
此外,与久坐组相比,强制组中的瘤胃球菌(Ruminococcus gnavus)在肠道粘液降解中具有明确的作用,以及增加了丁弧菌属、Oscillospira属和粪球菌属。
这项针对运动和压力动物的初步研究表明,运动可以改变微生物群的组成以及代谢功能,这可能根据运动强度和自愿性等对菌群产生积极或消极的影响。

由于营养、遗传和环境因素,在人类临床研究中剖析肠道微生物群对运动表现的确切作用可能很困难。无菌动物模型克服了其中的许多挑战,并已被用于证明肠道微生物群对身体表现结果所起的作用。
失去肠道微生物群的小鼠,运动表现下降
研究了无特定病原体 (SPF)、无菌 (GF) 和脆弱拟杆菌(Bacteroides fragilis)无菌小鼠的游泳能力。GF 小鼠从游泳到精疲力竭的时间最短,SPF小鼠最长,表明在没有肠道微生物群的情况下表现会下降。观察到与SPF小鼠相比,GF 小鼠表现降低的类似发现。
其他研究:失去肠道微生物群的小鼠运动表现无影响,但肌肉功能下降
与上述相反,另外的研究,GF 小鼠和 SPF 小鼠在运动至精疲力竭时的身体表现没有差异。然而,与 SPF 小鼠相比,GF 小鼠表现出肌肉质量减少、肌纤维减少和肌肉力量降低。GF 小鼠的肌肉萎缩与线粒体生物合成失调和氧化能力降低有关。SPF 小鼠肠道微生物群的移植恢复了 GF 小鼠的肌肉质量,与未治疗的 GF 小鼠相比,用短链脂肪酸混合治疗增加了 GF 小鼠的骨骼肌质量和肌肉力量。
抗生素治疗极大地改变了肠道微生物群的组成
研究证明肠道微生物群在光谱抗生素治疗后耗竭,同时减少了小鼠的耐力运行时间,通过重新接种微生物群恢复后,耐力能力恢复正常。耐力能力的变化与肌肉质量、肌纤维类型或线粒体功能的变化无关,但与肌糖原水平的变化有关,在重新接种后恢复。
多项研究报告了类似的发现,其中与未治疗的对照组相比,使用多种抗生素治疗的小鼠的跑步机运行时间更短。
SCFA 产生的影响及其对运动表现的作用
通过用具有不同底物可用性的纤维喂养小鼠,以在肠道中产生微生物 SCFA。与喂食高度可发酵纤维的小鼠相比,喂食可发酵纤维减少的小鼠的跑步时间显著缩短,这表明微生物群及其底物都与身体机能有关。
为了进一步探索 SCFAs 在表现能力中的假定作用,对抗生素治疗的小鼠进行皮下注射乙酸盐或丁酸盐。乙酸盐而非丁酸盐的输注改善了抗生素引起的剧烈运动带来的不良反应。
无菌动物当然是一种极端模型,可能无法解释在人类微生物群中观察到的更细微的差异。不过,无菌动物模型的研究已经建立了肠道微生物群与身体机能之间的因果关系。
总体而言,恢复肠道微生物群失调似乎可以有效恢复啮齿动物的运动能力和骨骼肌参数。
此外,肠道微生物群组成的差异或肠道微生物群的缺乏可以调节与肌肉结构、肌肉力量和/或能量利用相关的运动能力。
身体活动分为力量和耐力两大类,这取决于你的身体如何产生能量来维持你的运动表现。
无氧运动
力量运动通常高强度,如举重、短跑和拳击。这些运动通过锻炼细胞的无氧途径来增强肌肉质量。这就是说你的肌肉利用其有限的糖原储备来制造 ATP(肌肉的燃料),而无需使用氧气。
最近的一项研究表明,宿主骨骼肌在无氧运动期间产生的乳酸通过循环进入肠腔,为结肠中利用乳酸的物种提供了选择性优势。这项开创性工作的结果表明,在高强度运动期间,宿主以乳酸的形式为特定细菌提供燃料,这些细菌又会产生代谢物,例如丙酸盐,对运动宿主有益。
有氧运动
这与耐力运动不同,有氧运动允许身体以较低的强度进行运动,但运动时间要长得多,例如长跑、骑自行车和滑雪,此类运动肌肉使用氧气将脂肪和糖类转化为 ATP 作为燃料。
测量心血管健康最流行的方法是 V02最大值,它可以查看你的身体在剧烈运动期间可以使用的最大氧气量。用于评估耐力表现,并且可以通过高强度运动得到显著改善。
几项研究表明,微生物群组成与心肺健康之间的关系可以解释“分类丰富度”(微生物组中鉴定的细菌多样性)的 20% 以上的变化。注意到这些变化与其他因素无关,包括年龄、脂肪摄入量和碳水化合物摄入量。
有氧运动对微生物群及身体的益处
研究表明,有氧运动对你的微生物群有好处,包括有益菌和整体多样性丰度增加。
重复进行有氧运动可以增加健康个体和患有慢性便秘的中年患者的胃肠道转运时间。
有氧运动还会增加粪便 SCFA 浓度,从而降低结肠腔的 pH 值。
此外,作为运动副产物并在全身循环的代谢物(例如乳酸),可能会通过肠道过滤并作为某些细菌分类群(例如韦永氏菌)的能量来源。
有氧运动类型及建议
有氧运动是长期而稳定的,确保为你的肌肉提供氧气,以便它们可以产生燃料 (ATP)。这包括任何可以提高心率并长时间保持心率的运动。
比如:步行、慢跑、跳舞、慢骑自行车、椭圆机和健身房的划船机、登山、游泳等都是有氧运动。但是,锻炼的强度和持续时间还是根据身体的总体健康水平而异。
有氧运动是长期的。放轻松,坚持下去,你的身体会适应的。
NHS 已经发布了成人的运动建议:
至少150分钟中等的有氧运动,如骑自行车或快走
每周进行 2 天或更多天的力量锻炼,可以锻炼所有主要肌肉(腿部、臀部、背部、腹部、胸部、肩部和手臂)
或者
每周进行中等强度和剧烈有氧运动的组合——例如,两次 30 分钟的跑步加上 30 分钟的快走相当于 150 分钟的中等有氧运动
每周进行 2 天或更多天的力量锻炼,可以锻炼所有主要肌肉(腿部、臀部、背部、腹部、胸部、肩部和手臂)
适当的训练计划旨在平衡精英运动员所经历的全身压力因素以及个性化的饮食计划,以提高表现并减少运动引起的压力症状。
某种营养素对应激反应的调节程度取决于其持续时间、运动员的整体营养状况、运动的类型和强度、生理状况以及肠道微生物群的组成和功能。由于精英运动员的压力反应相当复杂(从肠漏到分解代谢和抑郁症),定义标准的饮食计划很困难。
一般来说,许多精英运动员被鼓励摄入大量的简单碳水化合物和蛋白质以及少量的脂肪和纤维,以提供快速的能量来源,同时避免潜在的消化问题,例如高纤维饮食有时会出现的胀气和腹胀。精英运动员的饮食计划也基于某些微量营养素的消耗,如铁、钙、氨基酸、必需脂肪酸和抗氧化剂。
饮食设计应考虑肠道微生物群
由于饮食强烈影响微生物群的组成和功能,通过营养治疗调节肠道微生物群可以改善运动员的压力反应并提高表现。可以假设,每个饮食计划可能都伴随着微生物群的同步调整。为运动员设计个性化饮食时的另一个重要考虑因素是了解微生物组如何随时间变化。
目前和未来运动员或经常的锻炼计划应根据其对肠道微生物群的潜在影响来考虑饮食策略,包括以运动为中心的饮食策略(例如,蛋白质补充剂、碳水化合物负荷)对肠道微生物群的影响以及以肠道为中心的饮食策略的影响。

对性能的饮食策略,除了摄入益生元、益生菌和合生元外,摄入足够的膳食纤维、多种蛋白质来源,并强调不饱和脂肪,尤其是 omega-3脂肪酸,在优化运动员的健康和表现。
蛋白质
蛋白质是骨骼肌的主要成分。然而,特定氨基酸在肝脏和骨骼肌的吸收和分解代谢以及它们调节肌肉蛋白质合成反应的能力方面有所不同。
必需氨基酸,尤其是支链氨基酸 (BCAA),对于肌肉蛋白质合成至关重要,并且比非必需氨基酸产生更大的肌肉蛋白质合成反应。因此,膳食蛋白质会影响蛋白质利用和骨骼肌对运动的合成代谢反应。
补充亮氨酸导致血浆亮氨酸和总支链氨基酸浓度显著增加,并改善耐力表现和上肢力量,影响血浆色氨酸:支链氨基酸比率。BCAA 的补充也被用于通过改变大脑神经递质的产生(如 5-HTP、多巴胺和去甲肾上腺素)来调节运动期间疲劳的影响。由于缺乏证据,无法对运动员应服用的 BCAA 类型或数量提出建议。
运动员可能需要的蛋白质是一般人群的两倍
用以维持蛋白质合成、能量产生、免疫功能和肠道完整性和运动引起的压力的结果。
这对于耐力和阻力训练的运动员来说比较重要。耐力运动员可能需要在运动后恢复期摄入更多的蛋白质,尤其是在禁食状态下进行耐力运动时,因为这可能会增加肌丝蛋白水解。
虽然根据饮食和生理因素而变化,例如消化率、氨基酸的数量和组成、食物基质以及其他营养素的存在,但约 10% 的蛋白质未被消化,可能会到达结肠被肠道细菌分泌的蛋白酶进行蛋白水解。
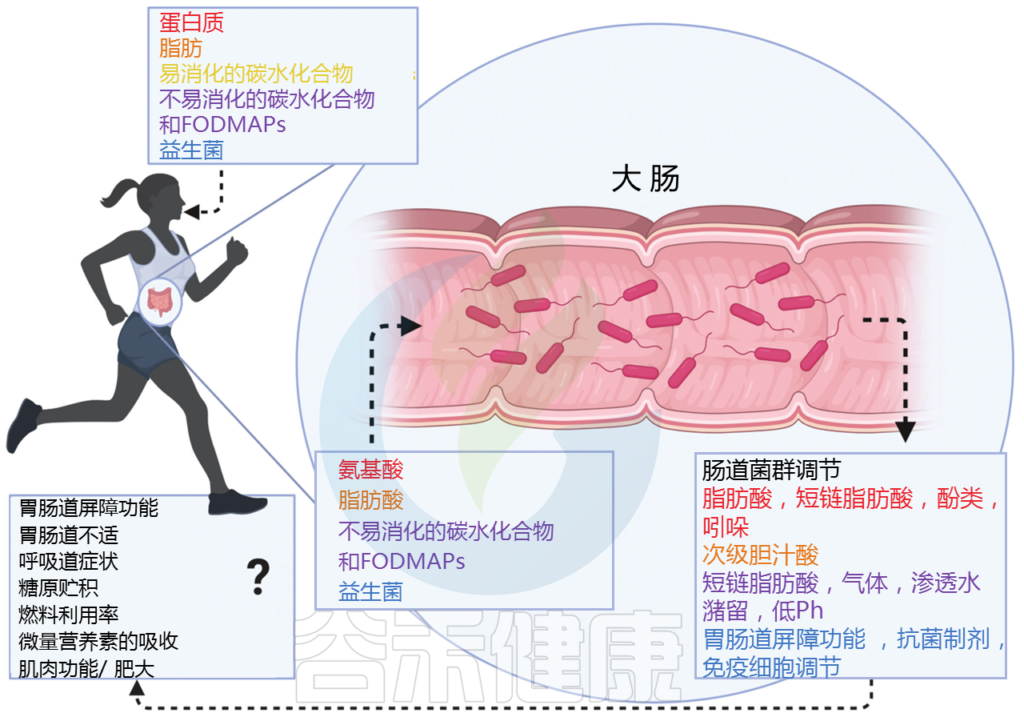
Hughes RL, et al., Adv Nutr. 2021
关于肠道微生物群代谢,氨基酸可以根据其发酵代谢产物进行分类:含硫氨基酸、芳香族氨基酸和色氨酸。
过量蛋白质摄入的不利影响
这些代谢物包括支链脂肪酸和短链脂肪酸、氨、硫化物、吲哚和酚类化合物。虽然其中一些代谢物(例如 SCFA 和吲哚)可能具有改善肠道完整性等有益效果,但其他代谢物(例如氨和对甲酚)会降低肠道上皮完整性。过量的蛋白质摄入可能会导致蛋白水解代谢物的产生水平超过宿主吸收、转化或解毒有害代谢物的能力,导致对肠道屏障功能、炎症和结肠健康的不利影响。
非蛋白质成分有助于运动后的蛋白质合成反应
另一个领域是全食物蛋白质与蛋白质补充剂的影响,因为全食物具有相同或更好的增效作用。例如,摄入全鸡蛋与蛋清相比,摄入全脂牛奶与脱脂牛奶相比,会导致更多的氨基酸摄入和运动后肌原蛋白合成,表明非蛋白质成分(例如,脂质、碳水化合物、微量营养素和其他生物活性化合物)有助于运动后的蛋白质合成反应。
过量蛋白质补充剂增加结直肠癌风险
蛋白质补充剂,包括添加到能量饮料中的支链氨基酸和牛磺酸,通常被运动员用来增强运动对骨骼肌的合成代谢和适应性作用,并促进恢复。过量的牛磺酸会导致牛磺胆酸(TCA)、脱氧胆酸(DCA) 和硫化氢 (H2S) 浓度升高,这与结直肠癌风险增加有关;然而,这些补充剂对运动肠道微生物群的影响尚不清楚。
谷氨酰胺
运动前几天食用高蛋白、低碳水化合物的饮食会导致运动后血浆谷氨酰胺浓度降低。然而,谷氨酰胺补充剂几乎没有得到对健康、营养良好的运动员的严格控制的科学研究的支持。此外,研究者指出谷氨酰胺补充剂应取决于症状(即血浆谷氨酰胺水平低、肠漏)。
酪氨酸
新的中央疲劳假说指出,当血清素水平升高而多巴胺水平降低时,疲劳就会开始,这可能是许多运动员服用酪氨酸补充剂以防止其消耗的原因,尽管尚未确定推荐的补充剂量。酪氨酸或 4-羟基苯丙氨酸可在体内由苯丙氨酸合成,存在于许多高蛋白食物中,如豆制品、鸡肉、火鸡、鱼、花生、杏仁、鳄梨、牛奶、奶酪、酸奶和芝麻。
肠道微生物群通过增加膳食蛋白质的生物利用度和吸收以及增加肌肉蛋白质合成影响肌肉功能
有证据表明,肠道微生物有助于蛋白质的吸收和利用。例如,益生菌补充剂(副干酪乳杆菌)增强了植物蛋白的生物利用度,将必需氨基酸和支链氨基酸的浓度提高到与动物蛋白相当的浓度。此外,当与蛋白质共同给药时,益生菌凝结芽孢杆菌(GBI-30,6086) 减少了上皮细胞炎症,改善了营养吸收,并产生了增加人类氨基酸吸收的蛋白酶。这些作用可以减少肌肉损伤并促进肌肉恢复,从而提高适应能力和表现。
需要注意的是,细菌虽发酵氨基酸,但它们代谢动物和植物蛋白的方式不同。每个饮食计划都伴随着微生物群组成和功能的同步调整。因此,纯素食者、素食者、杂食者和红肉摄入量高的饮食的微生物群组成差异很大。
多项研究表明在高蛋白饮食中添加抗性淀粉可以抵消高蛋白摄入的负面影响,进一步说明摄入足够的膳食纤维对肠道和整体健康的重要性。
碳水化合物
毫无疑问,充足的碳水化合物消耗对于繁重的训练计划和成功的运动表现至关重要。
碳水化合物怎么补充?
对于每天训练超过 2 小时的运动员,膳食碳水化合物的摄入量为每天 7 至 12 克/千克,脂肪摄入量通常小于每天体重的 1 克/千克(消耗总卡路里的 20%)。

碳水化合物在长时间的剧烈运动中恢复肌肉和肝脏糖原储存,减轻压力激素水平升高,如皮质醇,并可以限制与高强度运动相关的免疫抑制。高碳水化合物饮食(8.5 g/Kg/d;总能量摄入的 65%)和随意食用碳水化合物在高强度训练期间可以减少疲劳并改善身体机能和情绪。
运动前和运动中摄入大量简单碳水化合物
针对运动员的饮食建议在运动前摄入大量简单碳水化合物以维持葡萄糖稳态,并在运动前摄入低纤维以减少胃肠道不适,同时补充说,以植物为基础的高纤维饮食可能会降低能量供应。在运动前和运动期间摄入简单碳水化合物(例如,葡萄糖、果糖、蔗糖、右旋糖)可以减轻疲劳、提高运动表现、促进水重吸收和维持水分充足。
摄入等量的果糖和葡萄糖,优化果糖吸收减轻不适
然而,葡萄糖和果糖负荷以及果糖与葡萄糖的比例会影响肠道微生物发酵和胃肠道应激。葡萄糖和果糖的组合导致比摄入单一碳水化合物更高的碳水化合物氧化率,减少运动期间内源性能量储存的消耗。摄入等量的果糖和葡萄糖可优化果糖吸收,减少微生物发酵,从而减轻胃肠道不适症状。
乳糖提高运动表现和恢复能力
乳糖还可以作为运动前、运动中和运动后的良好燃料来源,以提高运动表现和恢复能力,同时还可能促进对肠道微生物群的有益影响,例如双歧杆菌和乳酸杆菌的增加。
注意:
高碳水化合物饮食不会改善免疫功能,也不会防止经过大量训练后血浆谷氨酰胺浓度降低。
富含简单和精制碳水化合物的饮食不会促进健康的肠道微生物群组成,也不会产生有益的短链脂肪酸。
需要更多的研究来了解微生物群从饮食中提取营养的能力,并包括宿主的代谢变化。
膳食纤维
一般每 1,000 卡路里摄入足够的纤维总量为 14 克,即成年女性为 25 克,成年男性为 38 克。
低膳食纤维供应与较低的微生物群多样性、较少的短链脂肪酸产生和较少的抗病原菌相关,所有这些都可能对宿主产生有害的长期后果。
运动员或运动锻炼期间可以通过增加植物性食物的摄入量(例如全谷类、豆类、蔬菜、水果和坚果),同时在恢复期和训练期减少来自高添加糖、精制碳水化合物和脂肪的加工食品的能量,从而获得足够的膳食纤维摄入量,因为在激烈的训练或比赛之前吃高纤维饮食可能会导致胃肠道不适,如腹胀、胀气。
腹胀详见:“肚子像气球?”“好像怀孕?”——可能是腹胀惹的祸
此外,膳食纤维和大量食用植物性食物似乎会抑制细菌从蛋白质中产生有害代谢物,这强调了摄入足够的复合碳水化合物以维持肠道微生物组碳水化合物发酵的重要性。
脂肪和多不饱和脂肪酸
运动员的脂肪消耗量往往很低,占膳食能量的 15-30% 。长时间运动期间脂肪代谢的增加(30-50% 的膳食能量)可能具有糖原节约作用,并可能改善耐力表现和健康。
高脂肠内营养可以减轻肠道灌注不足导致消化功能紊乱后的肠道炎症、细菌易位和肠道损伤。
高脂饮食的危害
另一方面,高脂饮食会导致类似焦虑的行为增加,选择性破坏探索性、认知性和刻板行为,神经炎症破坏肠道屏障功能的标志物,以及与高脂肪饮食的小鼠相比增加循环内毒素和淋巴细胞表达。
在人类中,与高碳水化合物饮食(65% 的饮食能量)相比,富含脂肪的饮食(62% 的饮食能量)可能对免疫功能有害。
这些作者比较了 10 名未经训练的年轻男性在每周 3-4 次持续 7 周的耐力训练期间食用富含碳水化合物的饮食,和10 名高脂饮食的受试者。高脂饮食的运动员的 NK 细胞活性较低。
注:NK 细胞溶解一定数量肿瘤靶细胞的能力
Omega-6 多不饱和脂肪酸
它可以改变细胞膜流动性并间接影响免疫功能,包括减少 IL-2 的产生和抑制有丝分裂原诱导的淋巴细胞增殖,从而在运动期间和运动后产生潜在的不良免疫功能。
omega-3 多不饱和脂肪酸
它的最佳剂量约为 1–2 g/d,二十碳五烯酸与二十二碳六烯酸的比例为 2:1,可能会减少运动过程中 ROS 的产生。

高脂饮食对运动的影响不明确
到目前为止,由于结果相互矛盾,很难就补充 omega-3 的数量和持续时间向运动员提出任何明确的建议。目前,高脂肪饮食对后续运动表现的影响是模棱两可的,并且缺乏关于压力个体的信息。
最重要的是,摄入高脂肪和卡路里的饮食与慢性“低度”全身炎症、肠道通透性和血浆LPS增加以及总细菌多样性降低以及拟杆菌和梭菌的相对比例增加有关。因此,似乎食用高脂肪饮食也可能导致肠道微生物群发生不利变化。
维生素和抗氧化剂
运动员通常不会补充维生素和其他抗氧化剂,但建议运动员应考虑增加抗氧化剂的摄入量,如维生素 C、E、β-胡萝卜素和多酚,以减少 ROS 的形成和脂质过氧化。

用蓝莓和绿茶提取物(作为布洛芬替代品)补充多酚并没有改变既定的炎症和氧化应激,但增加了肠道细菌多酚代谢特征的代谢物(例如马尿酸盐、4-羟基马尿酸、4-甲基儿茶酚硫酸盐)和跑步者在3天剧烈运动后恢复期间的生酮。
不推荐补充个别微量营养素或食用大剂量的简单抗氧化剂混合物
尽管没有任何负面影响的报道,但富含多酚提取物(蓝莓和绿茶)的运动员饮食并没有减轻剧烈运动带来的生理压力,也没有提高恢复速度。
摄入大剂量的个别维生素(在运动员中并不少见)可能弊大于利,因为大多数维生素在体内主要作为辅酶发挥作用。一旦这些酶系统饱和,游离形式的维生素就会产生毒性作用。因此,运动锻炼期间应该通过增加水果和蔬菜的摄入量来获得复杂的抗氧化化合物混合物。
益生菌
常规益生菌包括双歧杆菌属和乳酸杆菌,尽管在运动员中研究的其他细菌包括芽孢杆菌属、肠球菌属、链球菌属、韦永氏菌或酵母布拉氏酵母菌。
益生菌带来的健康益处及对运动效果的影响
益生菌可减少感染、炎症、肌肉酸痛和胃肠道通透性或不适。迄今为止,益生菌益处的最实质性证据是改善上呼吸道感染的发生率、持续时间和严重程度,这可能会间接提高运动成绩。
呼吸道症状改善的研究包括来自乳酸杆菌家族的有机体。L.salivarius也可能通过增加产生丁酸盐的类群Roseburia和Lachnospiraceae 来降低胃肠道通透性,并减少疣微菌。虽然有证据表明益生菌功能的共享机制,但益生菌的益处通常取决于益生菌的菌株和剂量。
益生菌可以通过改善肠道通透性和抗氧化状态以及减少炎症来减轻剧烈运动对运动员胃肠道不适和肌肉酸痛的影响。布拉氏酵母菌和嗜酸乳杆菌和双歧双歧杆菌的组合有助于预防旅行者腹泻。
益生菌还可以通过生物活性代谢物的产生(例如短链脂肪酸、神经递质)、肠道 pH 的调节和肠道的改变等机制改善营养吸收和利用、糖原储存、身体成分、能量收集、激素产生以及认知和情绪微生物群的活动。例如,植物乳杆菌增加了铁人三项运动员的耐力表现,同时增加了粪便短链脂肪酸。
一项对小鼠的研究表明,从一名奥林匹克举重运动员身上分离出的细菌菌株 [ L. salivarius亚种 salicinius (SA-03)] 通过增加肝脏和肌肉糖原并降低乳酸、血尿素氮、氨和肌酸激酶在运动后提高耐力表现和肌肉力量。
然而,更多的研究表明,多菌株益生菌比单菌株益生菌具有更强的增效作用,这表明多种菌株可能以互补的方式发挥作用以提供性能优势。
益生菌可能因此有利于通过直接和间接的机制,提高运动成绩,虽然增补效应的证据仍然稀少。
益生菌如何补充?
益生菌菌株和剂量的差异以及个人的基线饮食、免疫状态和微生物群组成可能会导致研究之间的结果存在差异,从而使比较和得出结论变得困难。
大多数针对运动员的益生菌补充研究并未评估肠道微生物群,因此很难确定疗效是否取决于基线或参与者肠道微生物群组成的变化。同时饮食摄入,尤其是纤维和益生元底物的摄入,也可能影响益生菌的作用,因此应在分析中加以考虑。因为消费者应该意识到,如果没有足够营养的饮食支持,单独补充益生菌可能不会产生预期的效果。
此外,针对运动的益生菌补充研究通常样本量较小(即 10 至 30 名参与者),并且通常仅包括或主要包括男性参与者,这是有问题的,因为存在可能是性别特定的影响。
发酵食品对运动的影响
人们越来越关注发酵食品中活培养物的影响 ,以及它们的影响或与肠道微生物群的关联。然而,很少有研究调查发酵食品(包括酸奶、开菲尔、酸菜)对运动的影响。
三项使用开菲尔或发酵乳的研究报告称,运动诱发的 CRP 或肌酸磷酸激酶和肌肉酸痛降低,表明这些发酵食品对减少炎症有积极作用。一项小鼠研究报告了开菲尔对力量和耐力的增效作用。因此,含有活微生物的发酵食品可能对炎症和运动表现有益。
合生元
合生元是“包含活微生物和宿主微生物选择性利用的底物的混合物,它赋予宿主健康益处”。合生元可能是益生菌和益生元的组合(互补合生元),尽管单个成分不一定需要满足益生菌和益生元的标准,只要它们在共同给药时协同作用(协同合生元)。因此,益生元成分可以增强益生菌(协同合生元)的功能,或者这两种成分在引入肠道及其常驻微生物(互补合生元)后可以提供独立的有益功能。
这种微生物和选择性利用底物的组合可能比单独补充益生元或益生菌具有不同的效果。然而,只有 1 项研究调查了这些成分对身体活跃的人类的协同和独立影响。合生元补充剂(副干酪乳杆菌431、动物双歧杆菌乳酸亚种BB-12、嗜酸乳杆菌LA-5、鼠李糖乳杆菌)与单独补充益生元(阿拉伯胶)相比,LGG、raftiline、raftilose、乳铁蛋白、免疫球蛋白、阿拉伯胶)与血清 IL-16 浓度的增加较小相关,但合生元补充剂和阿拉伯胶单独都不影响 SCFA 浓度、免疫或胃肠通透性。因此,与单独补充益生元或益生菌相比,合生元可能对运动员的健康和表现产生不同或额外的影响。
微量营养素
微量营养素有助于免疫功能、炎症、能量代谢和骨骼健康,影响运动表现。充足的铁、锌和维生素 A、E、C、B-6 和 B-12 的摄入量对于适当的免疫功能至关重要,在运动员的高强度训练和比赛条件下可能会受到影响。
此外,由于汗液和尿液的流失以及氧化应激的增加,运动员对某些微量营养素的饮食需求可能会增加。此外,女运动员或女性增加锻炼缺铁的风险更高,影响健康和表现。
微量营养素与肠道微生物群
缺乏抗氧化微量营养素(例如,维生素 C 和 E 以及硒)会减少共生肠道细菌的数量,同时促进大肠杆菌的增加。
在压力增加的动物中,维生素 C、维生素 E、多酚、硫辛酸和微生物抗氧化剂的抗氧化剂混合物可恢复肠道氧化还原状态,这与双歧杆菌和乳杆菌增加以及大肠杆菌减少有关。然而,过量摄入某些微量营养素也可能增加感染易感性。例如,婴儿过量补铁会增加病原微生物,包括大肠杆菌,并导致肠道炎症。
因此,在压力增加或微量营养素缺乏的情况下补充微量营养素可能对免疫和炎症具有微生物群介导的益处。
钙和维生素D
钙和维生素D支持骨骼健康。此外,维生素 D 可能通过调节钙依赖性收缩、蛋白质依赖性骨骼肌合成代谢、线粒体功能和胰岛素敏感性来影响骨骼肌质量和强度。纤维摄入后双歧杆菌、毛螺菌科和拟杆菌的增加与钙吸收的增加呈正相关。这可能是由于短链脂肪酸的产生,它通过降低结肠 pH 值或调节信号通路或基因表达来增加钙吸收。维生素 D 的摄入也会影响肠道微生物群,尽管结果的可变性排除了确定补充剂对特定分类群的影响的能力。摄入钙和维生素 D 与肠道微生物群之间的双向关系对所有年龄段运动员的骨骼健康都有重要意义,无论是生长还是维持骨密度,以降低骨折风险。
需避免的食物
胃肠道问题在运动员和长期运动锻炼人群中比较常见。为了缓解症状,运动员可能会避免或限制某些会引发症状的食物。运动员还可以采用营养策略来增加胃排空并改善水和营养物质的吸收,包括避免高 FODMAP食物和含麸质食物。
FODMAP 是不易消化的短链碳水化合物,可增加胃肠道内的渗透负荷。肠道微生物可以将这些膳食成分发酵形成气体,从而导致有些人出现腹胀和胃肠道不适。

最近一项调查耐力运动员 FODMAP 摄入量的研究报告称,高摄入量都会导致胃肠道症状。初步结果表明,低FODMAP饮食减轻了运动员胃肠道症状。然而,FODMAP也充当肠道微生物群的燃料,它们的限制可能会影响群落的组成和功能。
有一种推测,无麸质饮食之所以能改善胃肠道症状,并不是其本身,而是其中 FODMAP 食物的减少。
只有一项研究调查了无麸质饮食对非腹腔耐力运动员的影响,其中报告无麸质饮食对表现、胃肠道症状、健康、肠道损伤或炎症没有影响。

运动可能是改变肠道菌群组成和恢复肠道共生的重要干预措施
目前的研究支持运动作为一种重要的行为因素的作用,它可以影响肠道微生物组成和功能的定性和定量变化,并对宿主有益。运动可以丰富微生物群的多样性,刺激可以调节粘膜免疫、改善屏障功能的细菌的增殖,并刺激能够产生防止胃肠道疾病和提高性能的物质的细菌和功能通路。
尽管这些变化可能不会以类似的方式在个体间发生,也可能取决于微生物群和宿主的基线特征。
值得注意的是,某些菌群可能在运动员中富集,例如与瘦表型相关的A. muciniphila和产生丙酸盐的Veillonella(通过乳酸代谢)。精英运动员身上丰富多样的、有利于代谢的肠道微生物群,很可能是在整个青春期和成年期参加高水平运动期间,多年高营养摄入和高强度运动和训练的累积表现。
运动带来的益处涉及内在和外在因素的结合
常运动的人更有可能接触到他们的环境生物圈,并遵循整体健康的生活方式,因此拥有更健康的微生物群。
同时,耐力训练的内在适应性,例如血流量减少、组织缺氧以及转运和吸收能力增加,可导致胃肠道发生变化。胃肠道转运时间的变化又会影响结肠腔内的 pH 值,这可能导致肠道微生物群的组成发生变化。而较长的结肠转运时间与肠道微生物群多样性的减少有关,同时伴随着从近端结肠到远端结肠的转运过程中 pH 值的增加。
长时间过度运动对肠道功能产生不利影响
尽管运动通常有益健康,但如果持续时间和强度的增加,且得不到足够的休息、营养的支持,它就会变得有害。
剧烈运动将血液从内脏循环重新分配到活跃的呼吸组织。长时间的肠道低灌注会损害黏膜稳态并导致肠细胞损伤,可能会导致肠道缺血,特别是在脱水的情况下,表现为腹部绞痛、腹泻或偶尔血性腹泻,也会使肠道通透性增加,产生炎症。这种不利影响在耐力运动中尤其如此。
目前对人体肠道微生物群与运动之间相互作用的研究仍然缺乏
尤其是与控制饮食相结合的研究,这是一个重要的混杂因素。准确测量营养成分和饮食质量,将有助于把运动对肠道微生物群的影响与其他混杂因素区分开来。
研究还应记录液体摄入量或测量水合生物标志物(如和肽素),以确定水合状态是否影响肠道微生物群,反之亦然。
此外,饮食和运动对肠道微生物群的影响通常是短暂的,并且在干预完成后不会持续。这表明长期的生活习惯对于诱导肠道微生物群的稳定变化是必要的。在关键发育窗口期间的干预措施可能对肠道微生物群产生更持久的影响,当然这需要进一步研究。
未来与运动相关的肠道微生物群的研究领域

Mohr AE, et al., J Int Soc Sports Nutr. 2020
未来的研究应侧重于使用分层方法,使用人体临床试验来识别可能有益于运动表现的目标细菌,并使用动物和体外研究来确定因果关系和机制。
然后可以再次使用人体试验来确定是否补充已鉴定的细菌或实施饮食习惯(例如,益生元/不易消化的碳水化合物、ɷ-3 脂肪酸补充剂、蛋白质摄入量的类型/数量),以提高细菌丰度和/或功能有利于运动表现。
需要在控制饮食的情况下调查高蛋白饮食、全食物蛋白质来源和蛋白质补充剂的影响的临床研究,以确定这些饮食模式和成分对运动员肠道微生物群的影响。
此外,需要更多的研究来阐明膳食脂肪的数量和类型对肠道微生物群的影响以及随后微生物群介导的(例如,通过胆汁酸)对运动表现的影响。
总之,人们越来越意识到,微生物群的个体差异会导致运动反应和健康结果的差异性。
未来的研究还应该整合其他“组学”数据
整合其他“组学”数据,以确定可能导致、促成、介导或调节饮食和运动对肠道微生物群的影响的潜在代谢物、基因和表观遗传修饰。
“组学”数据的使用与机器学习方法相结合,有可能揭示肠道微生物群与其代谢物、饮食和运动表现之间的新关联,并预测对饮食策略的个性化反应。这些发现的影响包括提高运动员成绩和改善健康,尤其是胃肠道和呼吸系统健康的潜力。
此外,研究应对肠道微生物群、饮食和人类健康之间的相互作用有更深入的了解,这些相互作用可能具有超越运动人群的影响和应用,以造福所有人的健康。
声明:本账号发表的内容仅是用于信息的分享,仅供学习参考使用。在采取任何预防、治疗或治愈的措施之前,请先咨询临床医生。
主要参考文献:
Clark A, Mach N. Exercise-induced stress behavior, gut-microbiota-brain axis and diet: a systematic review for athletes. J Int Soc Sports Nutr. 2016;13:43. Published 2016 Nov 24. doi:10.1186/s12970-016-0155-6
Lensu, S.; Pekkala, S. Gut Microbiota, Microbial Metabolites and Human Physical Performance. Metabolites 2021, 11, 716.
Mohr AE, Jäger R, Carpenter KC, et al. The athletic gut microbiota. J Int Soc Sports Nutr. 2020;17(1):24. Published 2020 May 12. doi:10.1186/s12970-020-00353-w
Jang LG, Choi G, Kim SW, Kim BY, Lee S, Park H. The combination of sport and sport-specific diet is associated with characteristics of gut microbiota: an observational study. J Int Soc Sports Nutr. 2019;16(1):21. Published 2019 May 3. doi:10.1186/s12970-019-0290-yHughes RL,
Holscher HD. Fueling Gut Microbes: A Review of the Interaction between Diet, Exercise, and the Gut Microbiota in Athletes. Adv Nutr. 2021;12(6):2190-2215. doi:10.1093/advances/nmab077
Jollet M, Nay K, Chopard A, et al. Does Physical Inactivity Induce Significant Changes in Human Gut Microbiota? New Answers Using the Dry Immersion Hypoactivity Model. Nutrients. 2021;13(11):3865. Published 2021 Oct 29. doi:10.3390/nu13113865
Marttinen M, Ala-Jaakkola R, Laitila A, Lehtinen MJ. Gut Microbiota, Probiotics and Physical Performance in Athletes and Physically Active Individuals. Nutrients. 2020;12(10):2936. Published 2020 Sep 25. doi:10.3390/nu12102936
Sohail MU, Yassine HM, Sohail A, Thani AAA. Impact of Physical Exercise on Gut Microbiome, Inflammation, and the Pathobiology of Metabolic Disorders. Rev Diabet Stud. 2019;15:35-48. doi:10.1900/RDS.2019.15.35
Monda V, Villano I, Messina A, et al. Exercise Modifies the Gut Microbiota with Positive Health Effects. Oxid Med Cell Longev. 2017;2017:3831972. doi:10.1155/2017/3831972
Clauss M, Gérard P, Mosca A, Leclerc M. Interplay Between Exercise and Gut Microbiome in the Context of Human Health and Performance. Front Nutr. 2021;8:637010. Published 2021 Jun 10. doi:10.3389/fnut.2021.637010
Okamoto T, Morino K, Ugi S, Nakagawa F, Lemecha M, Ida S, Ohashi N, Sato D, Fujita Y, Maegawa H. Microbiome potentiates endurance exercise through intestinal acetate production. Am J Physiol Endocrinol Metab. 2019 May 1;316(5):E956-E966. doi: 10.1152/ajpendo.00510.2018. Epub 2019 Mar 12. PMID: 30860879.
Ticinesi A, Nouvenne A, Cerundolo N, et al. Gut Microbiota, Muscle Mass and Function in Aging: A Focus on Physical Frailty and Sarcopenia. Nutrients. 2019;11(7):1633. Published 2019 Jul 17. doi:10.3390/nu11071633
Hughes RL, Holscher HD. Fueling Gut Microbes: A Review of the Interaction between Diet, Exercise, and the Gut Microbiota in Athletes. Adv Nutr. 2021 Dec 1;12(6):2190-2215. doi: 10.1093/advances/nmab077. PMID: 34229348; PMCID: PMC8634498.
Zhao J, Zhang X, Liu H, Brown MA, Qiao S. Dietary Protein and Gut Microbiota Composition and Function. Curr Protein Pept Sci. 2019;20(2):145-154. doi: 10.2174/1389203719666180514145437. PMID: 29756574.