 国家高新企业 | ISO9001认证
国家高新企业 | ISO9001认证 二级病原微生物安全实验室
二级病原微生物安全实验室- 联系电话:+13336028502
- +400-161-1580
- service@guheinfo.com


宏基因组测序方案是针对16s分辨率和宏基因组高成本之间的一个折中方案,通过降低测序深度,每个样本100万reads左右,但是物种的分辨率并没有一般宏基因组(普遍5~10G数据量)差很多。 不通过拼接组装,直接基于kraken2等kmer,或MetaPhlAn2等标记基因的参考基因组方法进行种属丰度分类。结合其到菌株的物种分类和丰度数据可较16s方案下的PICRUST更加准确的预测基因构成。


比较适合想要获得更全和更精细分类精度而同时不需要获得完整基因组序列和重建菌群基因的,浅宏基因组测序就可以成为很好的选择,其成本低,分析简便快速,同样能获得宏基因组的基本丰度数据。
不过浅宏基因组也有其适用范围,根据样品类型的不同,一些样品可能包含 >99%的人类宿主DNA,这不仅增加了序列成本,而且给测量带来了不确定性。
在许多研究中也会采取在进行宏基因组测序文库的准备之前去除宿主DNA的方法。但是,在去除宿主DNA后,可能没有足够的微生物基因组DNA用于宏基因组测序,这通常需要最少50ng的输入。
浅宏基因组较适合于宿主DNA含量较低的样本如:人类粪便、水体、土壤等;
不太适合:口腔唾液、肺泡灌洗液、血液等人体体液类样本。
我们可以免费提供针对粪便及环境样本助力临床/科研取样。
人体口腔、痰液、腹水、脑脊液、尿液、皮肤、阴道分泌物等高寄主细胞含量样本可根据我们的处理方案简单处理后大幅降低宿主DNA比例。
测序平台:Illumina Novaseq,PE150,默认:100万reads/样
2-3周左右出报告


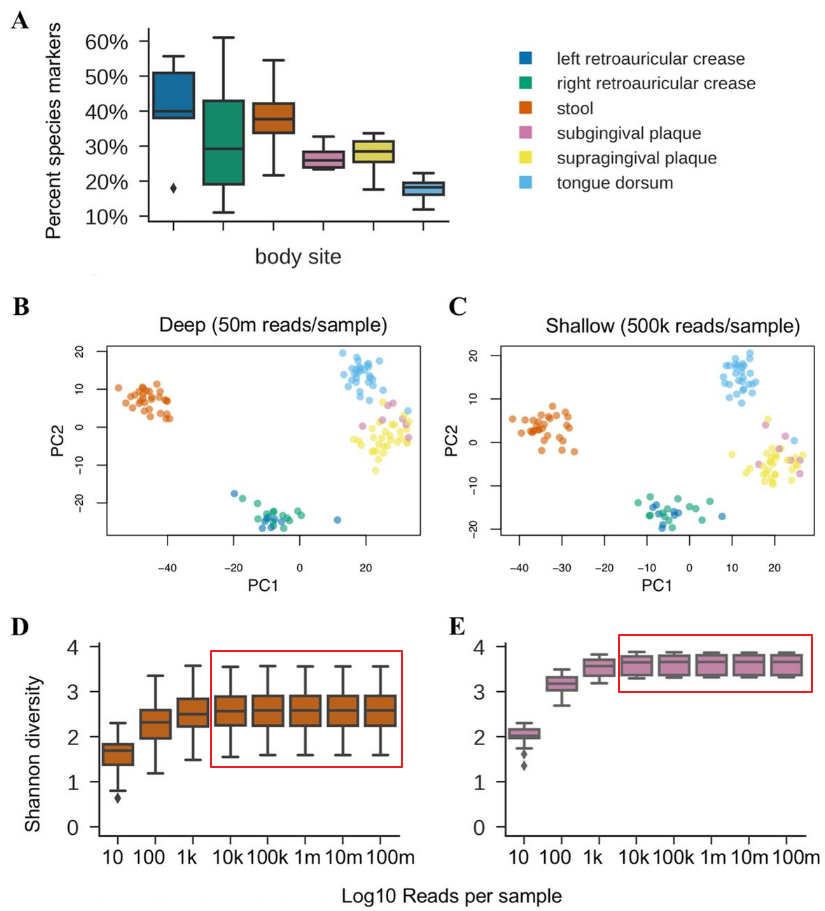
当测序深度达到50万reads以上,浅宏基因组与深度测序宏基因组在主要物种构成的丰度已经基本一致。如下图所示:

样本需求量低:公司研发实现了低当量微生物样本提取和建库,保证提取丰度以及片段完整性同时,样本量需求低于同行其他公司要求;对于样本获取困难的样本,也可以选择微量建库,样本量可低至10ng。
免费取样盒和针对性取样建议:粪便及环境样本提供取样盒助力临床/科研取样,人体口腔、痰液、腹水、脑脊液、尿液、皮肤等高寄主细胞含量样本可根据我们的处理方案简单处理后大幅降低宿主DNA比例。
严格标准的实验流程:自动化样品处理平台辅助,每轮设置阳性对照,上轮检测样本对照,阴性对照。评估污染,轮次比对,最大化减少误差,保证样本重复性和稳定性
Illumina测序平台:宏基因组测序(PE150)采用先进的Illumina Novaseq测序平台,快速、高效地读取高质量的测序数据、结合样品特点和数据的产出,充分挖掘环境样品中的微生物菌群和功能基因
大数据分析流程质量流程控制严格:优化的数据质量控制,包括过滤比对质量低、非特异性扩增、覆盖度低、低复杂度的序列,从而快速准确获得样本中微生物信息及其丰度信息,最大化提高质量数据
分析内容丰富全面:物种分析,基因预测与分析,多样性和相似性分析,功能分析,网路互作分析,代谢网络,关联分析等
完整详细的报告:提供质检实验报告,分析统计报告,分析报告解读,原始数据
高效个性化服务:在线项目系统方便您及时查看项目动态和下载报告以及与分析人员高效交流,免费支持个性化图表修改以及重新分组出报告。
价格低,周期快:包括提取,测序到分析,最快2周出报告。
大数据分析团队和多中心大项目分析经验(团队主要源自浙江大学,包括生物信息学,计算机,微生物以及统计分析等专业,积累了多年的大健康项目多中心项目分析经验,有助于多样本,多表型,多组学联合分析
若需要进一步了解咨询,可以致电联系我们

谷禾健康


假设你能看到人体内所有的基因,你应该会感到震惊。他们中只有1%是人类。另外99%属于细菌、酵母、病毒和微小的原生动物。这些微生物被称为微生物群,它覆盖着你的全身内外。
可以说,潮湿温暖的肠道环境是地球上最拥挤的空间之一。它容纳了大约上千种不同的微生物物种,其所含基因远超过我们的人类基因。

神奇的是,这些微生物及其基因会影响我们的爱情生活,帮助我们像应用程序一样挑选相配的伴侣。取决于你的微生物群状态,这可能是好事,也可能是坏事。
人类可能需要花费数千年的时间才能改变基因,但是微生物可以在20分钟左右的时间内产生新一代的基因泵送的同胞细胞。然后微生物围绕着我们发展进化圈,古老的防御体系,我们的身体要不断为这些变化的微生物创造环境。
因此,在原始时代的某个时候,我们募集了有益的细菌来保护我们免受致病菌的侵害。在潮湿和温暖的环境中,微生物通过抵抗病原体来保护我们,这种关系使我们在充满病原体的世界中成长[1]。
这种共生有多重要?所有的动物都不遗余力地将选定的微生物传给它们的孩子,例如小马会去吃马妈妈的便便,因为它需要摄取母亲粪便中的微生物。
在人类中,产道为早期微生物的形成提供了的途径。母乳中含有的细菌会进一步建立婴儿的初始肠道微生物群。母乳甚至含有专门为喂养这些微生物而生产的益生元。

然而,我们的肠道微生物(统称为微生物群)也有自己的需求-并且他们知道如何满足。
令人惊讶的是,微生物可以产生人类神经递质,包括多巴胺和5-羟色胺,这是目前抗抑郁药物最流行的两个目标。微生物也会产生激素和脂肪酸,所有这些都是有效的情绪操纵器。
再加上细菌毒素和微生物,对他们的宿主有着强大的控制能力。你是不是认为自己有意识地决定爱吃甜食?不,很可能你的微生物才是真正的甜食渴望者,并且你的欲望已经被塑造成可以满足它们的欲望。
事实是,肠道微生物并不是我们的“朋友”,它们是我们共同用餐的伙伴,但随时都可以帮助我们。
它们都有自己的食欲:酵母渴望糖;拟杆菌属(Bacteroidetes)会喜欢脂肪;普雷沃特菌属则比较喜欢碳水化合物;双歧杆菌是纤维爱好者。
它们都有自己的方法来讨好自己喜欢的,使用两种基本技术的变化来影响我们的食物选择[3]。
如果我们不给它们想要的东西,微生物就会产生毒素,使我们感到不舒服,因为他们知道如何使我们痛苦。
微生物通过改变我们的味蕾,增加阿片和大麻素受体以及产生神经递质(如多巴胺和5-羟色胺)来增加我们对食物的渴望。也是因此他们也知道如何使我们快乐[4]。

如果微生物能够指导我们的行为,那么他们还能做什么?从微生物的角度考虑,为了扩大其领土,它们可能会驱使我们更多地社交。从微生物的角度来看,有什么比亲吻,握手或拥抱更好的传播途径呢?
以色列2010年的一项研究将一批果蝇分成了两组。他们给一组喂以糖蜜为食的饮食,另一组为淀粉。每组都建立了合适的微生物群,经过精心调整以消化各自的饮食。
然后,他们在交配室中把这四个混合在一起(每组取一对)。一个交配室实际上只是一个很小的塑料碗,上面有透明的盖子,这样研究人员就可以算出性行为。
具有相同微生物群的果蝇更有交配意向
尽管所有果蝇之间都可以完全通行,但他们还是希望与具有相同微生物群的果蝇交配[5] 。
从几十代来看,果蝇一直生活在自己的群体中,基本上是两个独立的物种。那么有人问,怎么知道这是由于微生物引起的,而不仅仅是呼吸中有糖蜜的气味?答案很简单:当研究人员给果蝇使用抗生素杀死其微生物群时,他们的偏好就消失了。
细菌不会产生性信息素,但会调节其信息素
首席科学家 尤金·罗森伯格(Eugene Rosenberg)说:“共生细菌可通过改变性信息素(sex pheromones,在哺乳类动物中通过唾液,汗液和尿液释放)水平来影响果蝇交配偏好。细菌不会产生性信息素,但会调节其信息素。”
信息素是一种神秘的化学物质,可以起性吸引剂的作用。昆虫会嗅到其中的单个分子而飞走数英里。它显示了微生物群对于交配选择的重要性。
罗森伯格在后续论文中提到,蝇类并不是唯一被微生物操纵配偶选择的动物:“细菌对人类和其他动物的嗅觉有影响,而嗅觉是选择性伴侣的重要输入。”
可以这样理解,你的细菌将皮肤油脂转化为属于你自己的脂肪酸混合物,从而决定了你的气味。这是你的“特定味道”。
罗森伯格及其小组进一步推测,婴儿的抗生素治疗可能会影响这种情况,并可能导致菌群的流失和产生不同的气味[6] 。
早期使用抗生素会影响未来的爱情生活?这种猜测令人担忧,但罗森伯格认为,通过谨慎地在抗生素使用后重新繁殖微生物群,这种情况可能会逆转。
从客观上看,性有时让人满头大汗,但我们还是设法克服了这一点。细菌也可能通过操纵我们的激素发挥作用。
就像动物一样,微生物利用激素彼此交流[7] 。这些化学物质可以帮助我们改善性生活。例如催产素,参与保持身体健康,也和快速愈合有关,但它也在社会关系中发挥作用。催产素是“荷尔蒙激素”,它可以帮助我们忽略性的不便,得以繁衍后代。
这对微生物来说,也是一个巨大的胜利,因为性可以帮助它们找到新的人类领土。接吻可以使它们的生活更美好:亲密接吻每秒可在参与者之间转移800万细菌[8]。

摄入益生菌如罗伊氏乳杆菌可提高体内催产素的水平[9]。看到这,你是不是想赶紧去买益生菌补充剂了?别急,高纤维食物也可以提高自己的罗伊氏乳杆菌水平。
伴侣的选择还受微生物自身免疫系统的影响。主要的组织相容性复合体(MHC)由免疫蛋白组成,这些免疫蛋白为我们每个人提供了独特的气味特征。MHC蛋白是通过与微生物接触而产生的,代表了与病原体战斗的浓缩版本。
从理论上讲,我们无意识地选择了拥有完全不同的MHC的伴侣。这意味着将补充我们自身,有效地使我们对病原体的抵抗力加倍。
当你选择一个具有兼容的MHC特性的伴侣时,它们会让你闻起来很友好。如果你有孩子,他们就会在健康的微生物群上有一个良好的开端。
已婚或同居伴侣可以在很大程度上影响彼此的压力水平,情绪和健康行为方式。这意味着配偶不快乐或不健康,或敌对婚姻会让你更不健康。
当然另一方面,你的伴侣可以起到积极的作用,让你更活跃,减轻体重或减少饮酒,从而有可能改善您的身体健康。
一个最近的评论文章俄亥俄州立大学的Janice Kiecolt-Glaser及其同事的研究表明,婚姻互动,配偶情绪和生活方式习惯对健康的影响可能是通过肠道来介导的[10]。
最近,研究人员已更加意识到人体中,肠道是与大脑,免疫系统和心血管系统(通过迷走神经)进行通讯的中心枢纽。

研究表明,抑郁,饮食,睡眠,压力和敌对的婚姻相互作用会减少肠细菌的生物多样性,或使肠屏障更具渗透性,并更有可能使炎性因子渗入血液(称为“渗漏性肠”)。
肠道菌群多样性较低或肠道泄漏较多,会增加您对慢性炎症,肥胖症和糖尿病或心脏病等慢性疾病的抵抗力。因此,与伴侣生活在一起可能会以更多的你想象不到的方式影响肠道和整体健康[11]。
在一起生活为什么会影响这些因素?事实证明,身体互动,触摸,亲吻和性行为促进了微生物群的共享。肠道菌群与心血管疾病或糖尿病的许多危险因素有关,包括葡萄糖代谢,体重指数,腰围和高密度脂蛋白。
共享的压力源,情绪和健康习惯
促进已婚夫妇健康风险相似性的另一个因素是,他们可能共享共同的压力源,或者受到彼此情绪和压力水平的影响。无论是面对共同的压力源(例如经济压力或生病的孩子),还是伴侣将工作压力带回家,压力都具有传染性。
婚姻中的冲突,压力或敌意也可能影响您的情绪并增加皮质醇水平。伴侣也容易受到彼此健康或不健康行为和睡眠方式的影响。

研究表明:
拥有沮丧的伴侣会使你患抑郁的风险加倍。
不幸福的夫妻比幸福的夫妻更难消除负面情绪和压力。
伴侣有慢性睡眠问题的人有的炎症水平更高。如果你的伴侣在晚上醒着,可能会打扰你的睡眠。
肠道菌群,肠道渗漏和慢性炎症
一个健康的肠道具有多种细菌或病毒,它们分布均匀,没有一个物种能占主导地位。研究表明,菌群多样性低的人比菌群多样性高的人更容易发生慢性炎症。一些研究表明,饮食习惯也会影响微生物群的多样性。
与西方饮食相比,传统西方饮食富含红肉,精制糖和饱和脂肪,而微生物多样性较低,而地中海饮食则更多地依赖植物和健康脂肪。高饱和脂肪饮食还可以增加肠道的通透性,使毒素和炎性物质更有可能渗入您的血液中。
从婚姻敌意到全身性炎症的途径
一项研究表明,对婚姻的看法更加敌对的夫妇减少了肠道微生物的多样性,并增加了不健康的饮食习惯。在这项研究中,研究人员通过对脂多糖结合蛋白(LBP)进行评估,对婚姻状况进行了录像和编码,并测量了微生物的多样性。具有更多敌对性的夫妻的LBP较高,这又与C-反应蛋白(炎症的标志物)的水平较高有关。
因此,这项研究显示了通过减少肠道生物多样性,从婚姻敌意到全身性炎症的途径。此外,较敌对的夫妇的饮食中饱和脂肪含量较高,这可能会影响肠道微生物并增加炎症[11]。
配偶比兄弟姐妹具有更相似的微生物群
一项美国的研究,针对威斯康星州人群的研究,对配偶(N = 94)和兄弟姐妹对(N = 83)的分析进一步表明,配偶比兄弟姐妹具有更相似的微生物群和更多共同的细菌类群,在兄弟姐妹和不相关配偶之间没有观察到差异。即使考虑到饮食因素,这些差异仍然存在。
结果表明,人与人之间的互动,特别是持续的密切婚姻关系,会影响肠道菌群。已婚个体所拥有的微生物群落相对于独居者具有更大的多样性和丰富性,具有亲密关系的夫妻具有最大的菌群多样性,鉴于数十年来的研究记录了婚姻对健康的益处,这点值得注意[12]。
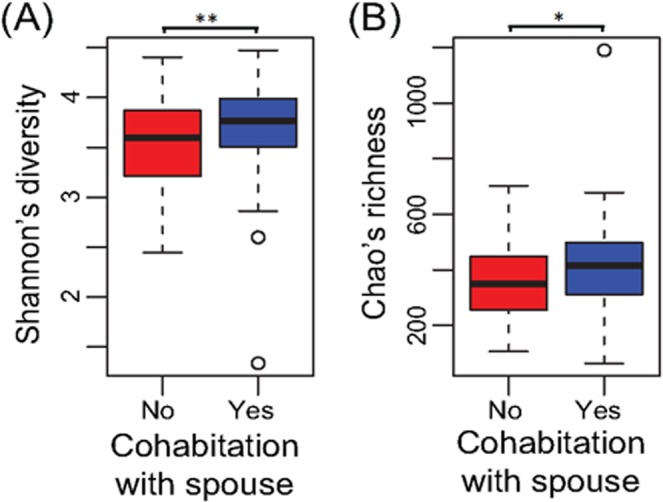
可以看到,具有亲密关系的夫妻其菌群多样性更高,而且存在显著差异。
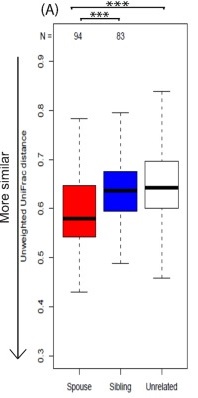
夫妻之间的肠道菌群相似度也超过兄弟姐妹和不相关人群。
虽然饮食通常与胃肠道微生物群相关,但亲密关系表明人类互动和共同行为的影响较少得到理解。紧靠和频繁的身体接触与促进相似个人之间直接微生物共享灵长类动物中微生物的相似性是相关的。
在这项研究中,亲密关系可能代表了在一起度过的时间,身体情感以及其他可能导致微生物共享的人类互动的总和。事实上,有证据表明唾液微生物群影响肠道微生物群,而唾液微生物群可能受接吻的影响。
高质量婚姻可能有助于微生物
通过进一步分析共享的菌发现,有趣的是,这些潜在共享的OTU中的大多数都来自严格厌氧的分类单元,这表明在宿主之间的富氧环境中持续存在可能不是密切人际关系的传播限制因素。
我们进一步发现,不仅已婚夫妇具有更多相似的肠道菌群,而且已婚个体所拥有的微生物群落相对于独居者更具多样性和丰富性。亲密的婚姻关系比兄弟姐妹之间共享的遗传因素和早期生活环境影响更大。
这一发现之所以有趣,部分是因为它与大量证据相吻合,证明了高质量婚姻与发病率和死亡率之间的牢固联系。未来可能会试图弄清将密切关系与微生物成分联系起来的机制。例如,尽管我们没有发现证据表明饮食共享是造成这些发现的主要原因,但我们无法测试精确的身体接触和亲密关系频率作为替代性解释机制。
菌群预测家庭关系
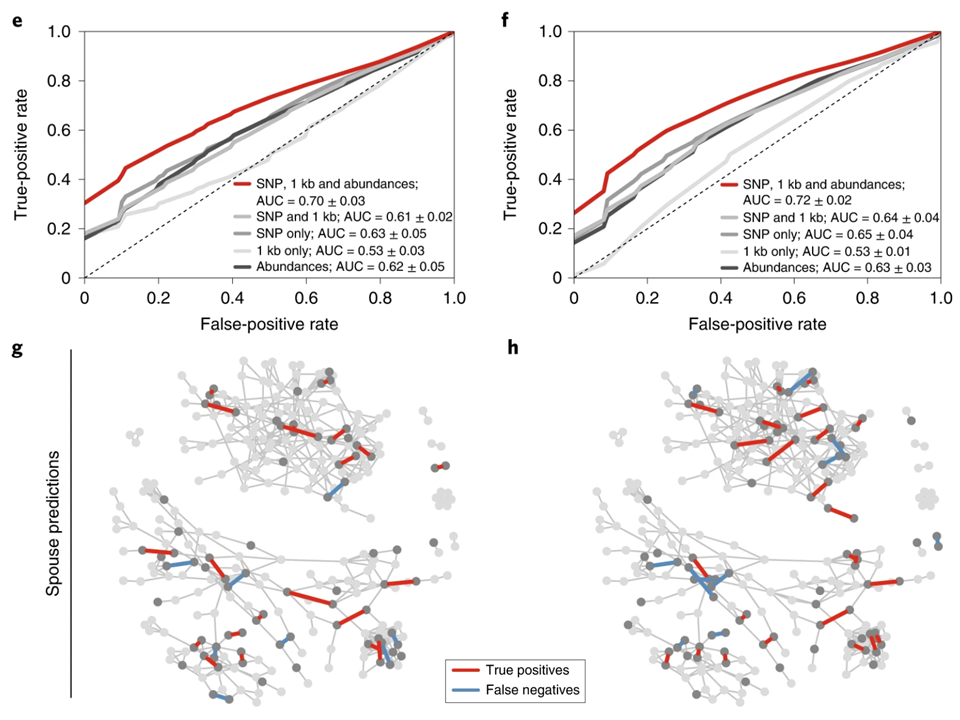
通过评估共有菌群来预测区分家庭和夫妻配偶,预测家庭模型的整体性能较差,但这些预测似乎仍依赖于网络结构,因为在肠道和口腔样本中,某些家庭内部的所有关系都得到了准确的预测。
值得注意的是,模型表明,近25%的配偶非常容易以高置信度进行预测。为什么某些夫妻比其他夫妻更容易预测,这可能反映出共同的敏感性,特定行为或婚姻关系的相对重要性[13]。

1. 共同努力,让生活更健康
当你和伴侣同时工作以减轻体重,多睡,多运动,少喝酒时,更有可能互助成长。看到伴侣变得更健康可以激励你去做同样的事情。
2. 更加富有同情心和相互尊重,而不是敌对地进行沟通
记住,你们是站在同一边的。请注意,对话如果朝消极方向进行,请稍作休息。尝试降低防御力,保持耐心,减少批评。
3. 如果你的伴侣在工作,家庭或育儿方面有压力,请尝试提供帮助并给予支持
最终,压力较小的配偶对你们俩来说都意味着更好的健康。如果尽管您尝试帮助您的伴侣仍然感到压力,则应集中精力分散自己,锻炼,冥想或进行愉快的活动,以减轻压力。
4. 另外,请确保了解您的肠道菌群和拥有良好的菌群
这样可以帮助你拥有美丽的皮肤,光亮的头发,毕竟健康的人自带魅力。

要调整您的微生物群,以下简单步骤供参考:
有了健康的微生物群,你会处于健康状态,并选择了与微生物相容的伴侣,它们可能会比任何约会应用程序更能帮助你找到良好合适的伴侣。
相关阅读:
肠道微生物组如何影响运动能力,所谓的“精英肠道微生物组”真的存在吗?
欢迎关注:谷禾健康
——让你和你的家人更健康
参考文献
1. Scott C. Anderson,Microbes and the Mind. Psychologytoday., 2019,07
2. Scott C. Anderson,The Shocking Source of Your Cravings. Psychologytoday, 2019, 07
3. Alcock, Joe, Carlo C Maley, and C Athena Aktipis. “Is Eating Behavior Manipulated by the Gastrointestinal Microbiota? Evolutionary Pressures and Potential Mechanisms.” Bioessays 36, no. 10 (October 2014): 940–49.
4. Temko, Jamie E., Sofia Bouhlal, Mehdi Farokhnia, Mary R. Lee, John F. Cryan, and Lorenzo Leggio. “The Microbiota, the Gut and the Brain in Eating and Alcohol Use Disorders: A ‘Ménage à Trois’?” Alcohol and Alcoholism 52, no. 4 (July 1, 2017): 403–13.
5. Sharon, Gil, Daniel Segal, John M. Ringo, Abraham Hefetz, Ilana Zilber-Rosenberg, and Eugene Rosenberg. “Commensal Bacteria Play a Role in Mating Preference of Drosophila Melanogaster.” Proceedings of the National Academy of Sciences of the United States of America 107, no. 46 (November 16, 2010): 20051–56.
6. Sharon, Gil, Daniel Segal, Ilana Zilber-Rosenberg, and Eugene Rosenberg. “Symbiotic Bacteria Are Responsible for Diet-Induced Mating Preference in Drosophila Melanogaster, Providing Support for the Hologenome Concept of Evolution.” Gut Microbes 2, no. 3 (June 2011): 190–92.
7. Stabb, Eric V. “Could Positive Feedback Enable Bacterial Pheromone Signaling To Coordinate Behaviors in Response to Heterogeneous Environmental Cues?” MBio 9, no. 3 (July 5, 2018): e00098-18.
8. Kort, Remco, Martien P. M. Caspers, Astrid van de Graaf, Wim van Egmond, Bart J. F. Keijser, and Guus Roeselers. “Shaping the Oral Microbiota through Intimate Kissing.” In Microbiome, 2014.
9. Varian, Bernard J., Theofilos Poutahidis, Brett T. DiBenedictis, Tatiana Levkovich, Yassin Ibrahim, Eliska Didyk, Lana Shikhman, et al. “Microbial Lysate Upregulates Host Oxytocin.” Brain, Behavior, and Immunity 61 (March 2017): 36–49.
10. Kiecolt-Glaser JK, Gouin JP, & Hantsoo LV (2010). Close relationships, inflammation, and health. Neuroscience and Biobehavioral Reviews. Close relationships, inflammation, and health. Neuroscience and Biobehavioral Reviews. 35, 33-38. PMC2891342
11. Melanie Greenberg Ph.D. How Married Couples Influence Each Other’s Physical Health. psychologytoday. 2019.10
12. Dill-McFarland KA, Tang ZZ, Kemis JH, et al. Close social relationships correlate with human gut microbiota composition. Sci Rep. 2019;9(1):703. Published 2019 Jan 24. doi:10.1038/s41598-018-37298-9
13. Brito IL, Gurry T, Zhao S, et al. Transmission of human-associated microbiota along family and social networks. Nat Microbiol. 2019;4(6):964-971. doi:10.1038/s41564-019-0409-6

每个人都想长生不老,但没有人想变老。我们渴望长寿,但是对衰老又非常恐惧。研究发现长寿者和体弱者的微生物群之间存在着深刻的差异,与年龄相关的微生物失调会导致肠道通透性、全身炎症和过早死亡,但这些差异在多大程度上促进或阻止了晚年的健康尚不清楚。肠道微生物群随着年龄的增长而变化,但目前尚不清楚这些变化在多大程度上是由于生理变化、年龄相关性炎症或免疫衰老、饮食、药物或慢性健康状况引起的。
近日,加拿大麦克马斯特大学(McMaster University)的研究团队发表在《细胞》子刊《Cell Host & Microbe》究肠道微生物群与不健康衰老进行了回顾讨论分析。

与年龄相关的肠道生理变化可能会改变微生物群
生命早期微生物群的动态特性是众所周知的,但更多细微的多样性变化一直持续到中年(大约40岁),此时存在相对稳定期。这种稳定性丧失和年龄相关性失调开始的时间点可能因个体而异,如果部分是由衰老生理学变化引起的,则可能与生物年龄(即生理年龄)比时间年龄(即寿命数)的相关性更大。弄清年龄、药物、饮食和共病性对微生物失调的相对贡献是一项挑战性的工作(图1);然而,在像老鼠、鱼、线虫和果蝇这样的模型生物,表明至少某种程度的生物失调是衰老的一个特征。
同样,对老年人的饮食、生活方式和药物进行的大量仔细调查表明,某些微生物物种的增加和减少是随着年龄的增长而变化的。肠道生理学随着年龄的增长而变化,由于微生物群在很大程度上是由生理学形成的,这些变化可能有助于某些微生物的持续或生长。在模型生物体中,预防肠道生理学中的年龄相关变化可缓解微生物失调并延长寿命。例如,老鼠的粘液分泌随着年龄的增长而减少,形成一个更薄且不连续的粘液层。粘蛋白在胃肠道内提供一层保护膜,防止微生物直接与上皮细胞相互作用,当这一层丧失时,通常不会与上皮层相互作用的微生物会引起炎症反应。它也是梭状科、阿克曼菌科、双歧杆菌科和拟杆菌科中许多菌株的营养来源,所有这些菌株都显示出随着年龄的变化而变化。
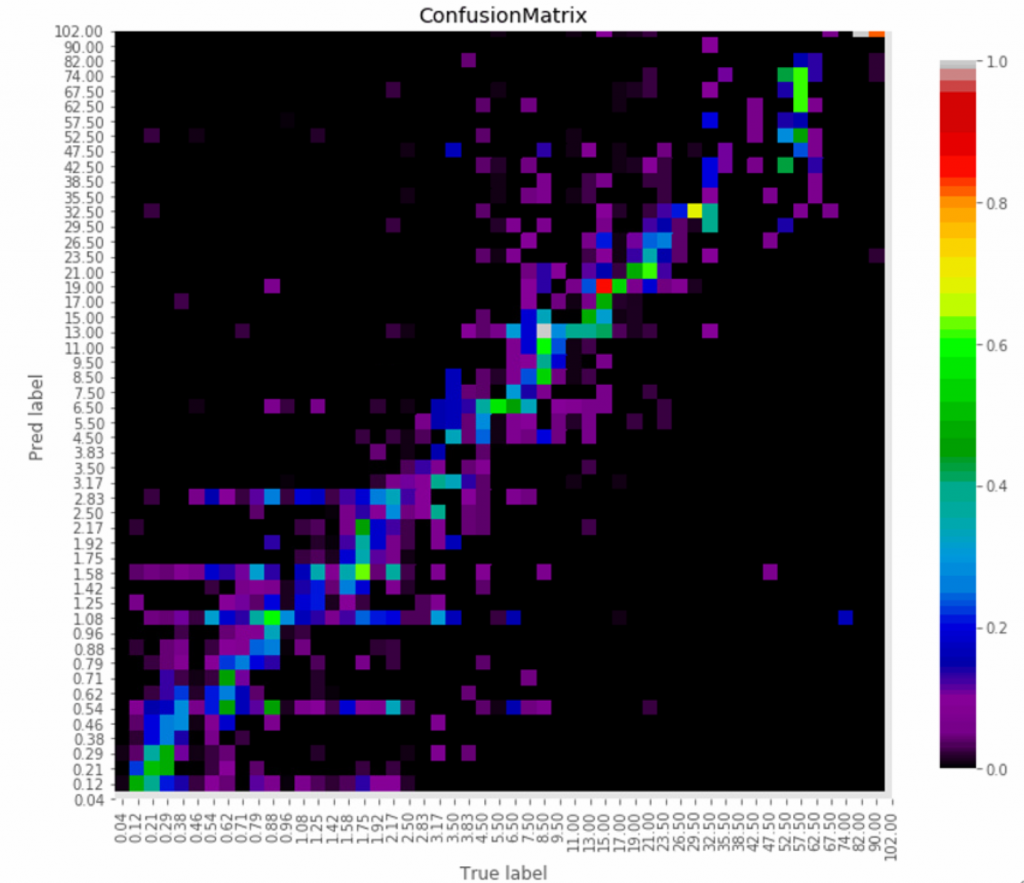

谷禾健康-肠道年龄预测模型图
从上图看出肠道年龄和生理年龄基本是符合的,说明人体真实年龄与肠道菌群的年龄特征是相符合的。
健康相关的行为也有助于健康的微生物群,如果微生物群随着年龄的增长而变化,不同老年人之间的肠道微生物差异比不同年轻人之间更大。
早期年龄段的菌群变化更加迅速,基本上出生第一年每个月都有其对应的年龄菌群特征,之后到菌群的年龄特征范围变宽,在30~50岁左右以5年为一个年龄段。50岁以后基本以10年为一个年龄段,而且肠道菌群由于疾病状态和菌群紊乱等情况导致的年龄偏差会变大。
与通常认为的越健康的人肠道菌群越年轻,或者越健康的宝宝肠道年龄更早熟的认知不同,健康人的肠道菌群年龄恰恰是最符合真实年龄的,与真实年龄差异越大,无论是年轻还是年老,都意味着肠道菌群出现问题。
粘液代谢微生物如Akkermansia muciniphila, Bacteriodes fragilis, Bacterioides vulgatus, Bifidobacterium和 Prevotella 等是否对粘液层的降解起作用尚不清楚,尤其是因为粘液代谢物种,如类杆菌属和嗜粘杆菌在百岁老人中增多,因此被认为是有益的。嗜粘液单胞菌代谢粘蛋白的能力与其刺激粘蛋白产生的能力相结合。因此,补充一些菌株已被证明可以改善年龄相关的粘蛋白损失,并具有积极的健康和免疫益处,包括延长类幼鼠的寿命。
肠功能是否存在老年性变化存在相当大的争议。然而,合理一致的报告支持细胞旁通透性增加和结肠运输减少。一般的共识是结肠运输减少可能是由于老化肠道的生理变化,而通透性增加是由于年龄或健康状况相关的炎症。局部炎症可以通过微生物群的变化直接或间接调节。
炎症是肠道通透性和微生物失调的驱动因素
衰老,以及伴随衰老而来的慢性健康和代谢状况,其特征是轻度慢性炎症的增加。炎症细胞因子水平高于年龄平均水平的个体,其中最常测量的是白细胞介素(IL)-6和肿瘤坏死因子(TNF),更容易发展成慢性健康状况或虚弱者,活动较少,面临过早死亡。“炎症老化”影响肠道完整性,并可能与微生物群的变化有因果关系(如下图)。
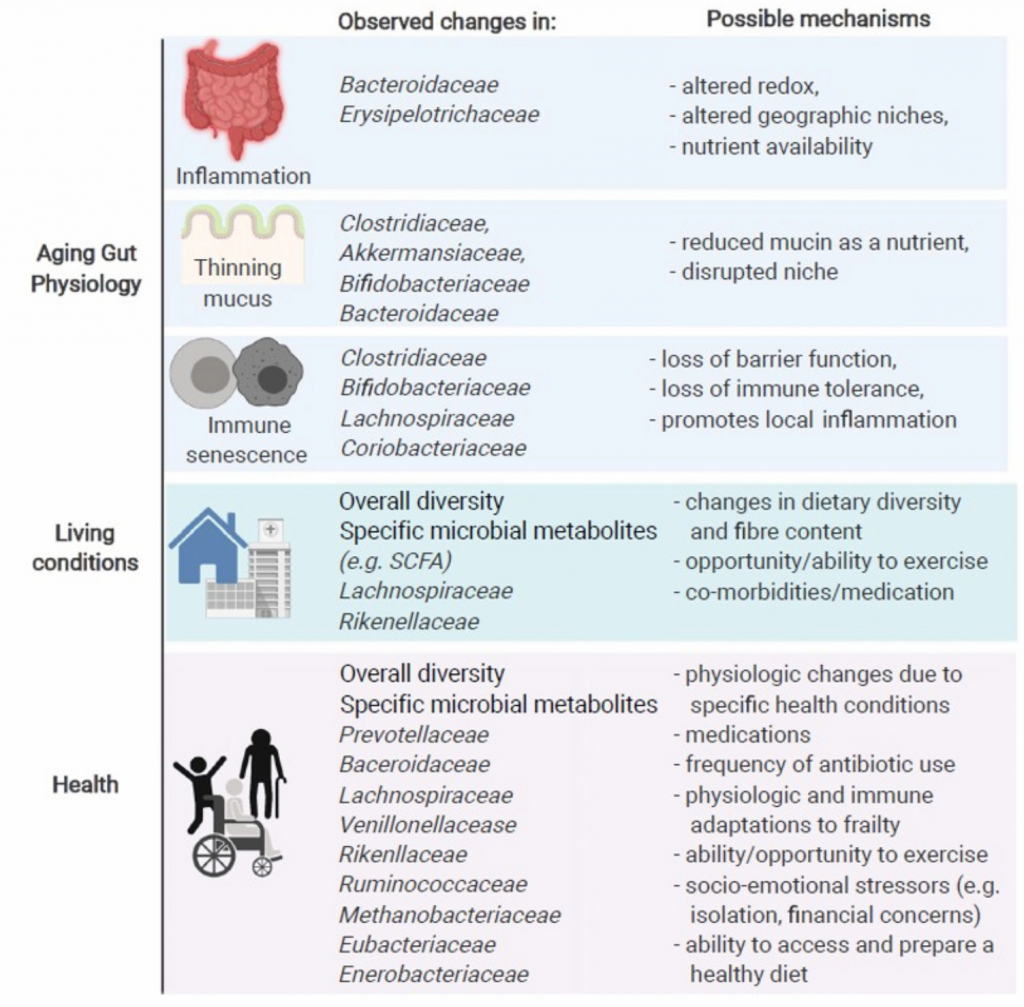

图1 老化微生物区系的变化
微生物群中与年龄相关的变化归因于生理,生活方式和健康状况。这些因素中的每一个都与微生物群某些成员的相对丰度变化有关。列出了一些可能解释观察到的增加或减少的行为,代谢和生理机制
老的TNF基因敲除小鼠(18个月以上)与野生型(WT)小鼠不同,老年小鼠(但不是年轻小鼠)的微生物群落在抗TNF治疗后发生变化。同样,在缺乏炎症信号负性调节因子NLRP12的小鼠中,保护的结肠炎Lachnospiraceae菌减少,而促进结肠炎的Erysipelotrichaceae以TNF-和IL-6-依赖的方式增加。这两项研究都发现这些物种相对丰度的变化依赖于肿瘤坏死因子,这表明这些物种的变化更可能依赖于炎症而不是年龄。这些微生物能够更好地适应当地氧化还原和营养环境的变化,这将使它们在发炎的肠道中获得竞争优势。这可以解释为什么几乎所有慢性炎症性疾病(如心血管疾病、痴呆症和炎症性疾病)都与微生物失调有关。一个补充的解释可能是在炎症反应过程中,特定的微生物生态位丢失或受到干扰。炎性细胞因子的表达增加会降低紧密连接蛋白(例如,zonulin和claudins)的表达,这会增加通透性,并可能导致炎症持续。
肠道驻留和招募的髓样细胞对于维持肠道完整性以应对微生物群的扰动至关重要。髓系对年龄相关性炎症的影响特别敏感。慢性炎症损害单核细胞和中性粒细胞的发育和组织巨噬细胞功能。这些细胞吞噬能力下降,调节失调或过度炎症反应导致病理学改变。髓系免疫衰老在多大程度上导致屏障功能受损或微生物组功能障碍尚未完全阐明,但减少慢性炎症可改善髓系功能障碍并减少失调。
虽然年龄相关的变化在肠道内的淋巴细胞中的作用尚未完全确定,但淋巴细胞群体中似乎存在微生物群依赖性和年龄依赖性变化。衰老肠道的变化与艾滋病毒携带者的变化有着强烈的相似性。在这两种情况下,驻留T细胞(尤其是CD4+T细胞)的数量或功能降低,这被认为是导致微生物失调、肠道通透性和全身炎症的原因。尽管淋巴组织年龄相关的变化与微生物失调之间的因果关系尚未被证实,但在猿猴免疫缺陷病毒(SIV)感染的灵长类动物中的研究表明,当CD4+数量因抗病毒治疗而增加时,微生物失调至少部分被逆转。有趣的是,在发炎的肠道中,无论是在衰老、艾滋病病毒或炎症性肠道疾病的情况下,微生物的分布都相当保守,这意味着这些微生物对炎症肠道的适应能力更强,与特定的健康状况无关。
长寿者与虚弱者的区别
对长寿老人(即百岁老人和超级百岁老人)的研究发现,他们的微生物群落往往更为多样,与健康状况较差的个体相比,微生物类群数量更多(图1)。事实上,α多样性似乎是长寿的合理预测因素,这意味着,但并非证明,维持或促进多样性的饮食和其他干预措施可能值得老年人采用。
即使在地理位置不同的百岁老人中(即中国人与意大利人),毛螺菌科、疣微菌科和艾克曼菌的成员也很丰富,这意味着这些可能是长寿和健康微生物群的普遍特征。这一发现尤其引人注目,因为特定微生物和疾病之间的许多联系因地理位置而异。对长寿者的微生物组进行的宏基因组分析发现,一些与获取营养有关的基因得到了丰富;然而,在所有与长寿和健康相关的生活方式因素中,饮食,特别是高纤维饮食是最常被采用的。微生物组组成的差异是造成这些个体异常年龄的原因,还是谨慎生活方式的结果,这将是一个挑战性的解剖。相比之下,动物模型的数据表明,老化相关的微生物失调会导致过早死亡。
当中年杀手鱼补充了年轻的微生物群时,它们的寿命延长了,而果蝇的老化微生物群促进了肠道通透性和过早死亡。
体弱者的研究说明了不健康衰老的极端情况。
体弱被定义为“由于多种生理系统的衰老相关的储备和功能下降,从而构成应对日常或急性应激源的能力,而导致衰老的临床可识别状态”。 体弱并非健康状况不佳的必然状态,健康状况相对较年轻的个人可能会体弱。 尽管我们经常在衰弱的个体中发现许多与衰老相关的疾病(例如,肌肉减少症,行动不便,慢性健康状况),但这些疾病中的任何一种的存在并不一定意味着一个人处于衰弱状态。 量化体弱性很复杂,但很关键,因为与年代年龄相比,体弱性可以更好地预测寿命和风险。 因此,体弱者的微生物组的组成与老化的微生物组不同,并且它们是不可互换的。 虚弱者的研究补充但不替代疾病相关的营养不良的研究。
体弱者的微生物群最一致的特征是多样性的丧失。 丧失多样性的原因很复杂,其范围包括饮食变化,运动能力或机会降低,长期护理设施中的居住,抗生素暴露量的增加以及药物的改变。 居住社区的老年人在服用抗生素时多样性急剧下降,但他们的微生物群最终会“反弹”,类似于他们的抗生素前微生物群。 虚弱者的老年人服用抗生素后多样性的丧失就不那么明显了,因为他们一开始就没有那么多的多样性。除了降低的α多样性外,虚弱者的微生物群中某些类群或种类也增加了,包括梭菌和肠杆菌科的成员。但是Lachnospiraceae, Ruminococcaceae,Erysipelotrichaceae,Prevotella却减少了,包括潜在的“益生菌”物种,如Faecalibacterium prausnitzii。 虚弱者的微生物群的组成与虚弱者程度,精神健康,肌肉减少症,全身性炎症和其他健康状况相关,但尚不清楚这些因素是因果还是相关的。
全身性衰老在衰弱方面有充分的文献记载,但没有数据表明虚弱者的肠道具有更高的渗透性或粘液消耗性,或者它是否具有与微生物营养不良有关的其他特征 老肠。 相比之下,饮食是导致虚弱者的微生物群特征的原因的证据令人信服。 饮食,特别是低纤维/蔬菜和高饱和脂肪/糖饮食会导致虚弱者的微生物组。 不幸的是,缺乏纤维的饮食似乎是导致长期居住在长期护理机构中的微生物群死亡的主要原因。
体弱者和长寿者的一个共同特征是与营养获取相关的特定微生物代谢产物的变化,炎症调节和肠道完整性。 一直有报道说短链脂肪酸(SCFA)的产生减少, 但是由于富含纤维的食物的减少似乎与虚弱者密切相关,因此很难确定原因和结果。 SCFA包括丁酸酯,丙酸酯,乙酸酯,乳酸和乙酸,其中丁酸酯是屏障功能的重要介体,因为它促进上皮细胞增殖并增加紧密连接蛋白的表达。 其他SCFA是肠道常驻微生物的能源,从而支持多样性。 观察到的与年龄和体弱相关的SCFA产生物种(如Lachnospiraceae和Ruminococcus)的下降。 是否直接导致屏障功能障碍或晚年健康尚待确定。 在一项衰老小鼠研究中,饮食不随年龄而变化,粪便丁酸增加,这表明观察到的人的SCFA与年龄和体弱相关的下降可能是由于饮食的改变而不是按年龄或健康状况。 有趣的是,来自老年小鼠的富含丁酸盐的微生物群对神经发生有有益作用,但并未改变肠的完整性,这表明丁酸盐的有益作用并不局限于其在肠道完整性中的作用。
微生物和肠道生理的性别差异
生命早期微生物群的动态特性众所周知,但多样性的细微变化一直持续到中年,此时存在一段相对稳定的时期。
这种稳定性丧失和与年龄相关的生物失调开始的时间点可能因人而异,并且如果部分是由于衰老生理学的改变引起的,则与生物学年龄(即生理年龄)的相关性要比按时间顺序(即 年)。 区分年龄,药物,饮食和合并症对微生物营养不良的相对贡献具有挑战性(图1); 但是,据报道,模型生物如小鼠,鱼类,线虫和果蝇与年龄有关的变化,提示至少某种程度的营养不良是细菌的特征。在C57BL/6小鼠中,雌性小鼠的乳杆菌科相对丰度更高,而雄性小鼠则有更多的瘤胃球菌科和Rikenellaceae菌科。
这些差异对易感性或对健康状况的保护作用的程度尚不清楚,但是当用雌性小鼠的菌群定植无病菌小鼠时,与雄性微生物菌落定殖的无病菌小鼠相比,细胞炎症减少了。 重要的是,这些变化与受体小鼠的性别无关。 在人类中,性别差异并未得到很好的研究,尽管年轻(<40岁)女性的α多样性更高,而且细菌和拟杆菌科的相对丰度因性别而异。 在小鼠中,由于雌激素介导的紧密连接蛋白增加,已证明与年龄相关的性激素变化会影响通透性。
性激素对人体肠道生理的影响以及最终对人体微生物失衡的贡献尚待确定。 在人类中,饮食,地理和健康状况对微生物群的影响可能大于生物学性别。
老龄化干预
由于肠道生理的改变而导致的老化微生物组的改变将不容易被修改。 然而,那些可归因于饮食或与年龄有关的炎症的疾病是干预的目标,饮食和运动可改善疾病本身。 尽管涉及饮食调整和/或益生菌使用的干预措施已在健康的年轻人中显示出适度和短暂的影响,但衰老微生物组多样性的降低可能使其更易于操作。 确实,在小鼠模型中,干预中年会改善某些晚年结局。
正如讨论的那样,肠道微生物组中许多与年龄和体弱相关的变化是不良饮食的特征。
与此相一致,已发现老年人采用富含纤维的“地中海”饮食的干预措施可改善健康状况,并将全因死亡率降低多达50%。 此外,这些饮食干预措施已显示可增加微生物多样性和SCFA,并减少全身性炎症。 尽管通过采用健康饮食也可以改善或预防与全身性炎症相关的晚年健康状况(例如心血管疾病,虚弱),但要确定人与人之间是否存在因果关系仍是一项挑战。 益生元和益生菌也已用于改善免疫功能,通过改善疫苗接种反应和减少感染,虚弱者和其他后期健康状况(例如,心血管疾病)。 当前的益生菌方法基于通常不是人类肠道固有的菌株,不会占据永久居所,并且可能通过非特异性机制(例如定植抗性)发挥其有益作用。鉴定具有促进健康作用且随年龄或年龄相关健康状况而降低的共生微生物可以在改善晚年健康状况方面更为成功,而在衰老过程中重新引入微生物代谢物ost可能与引入活菌一样有效和安全。
未来方向
模式生物已经并将继续领导对肠道通透性和早期死亡率的特定微生物-宿主相互作用的研究。最初的临床试验证明了使用人类共栖体的价值。随着我们发现更多与健康衰老相关的菌株和特定的微生物基因途径和代谢物,我们将能够针对特定的健康状况量身定制治疗方法,或对抗微生物群危害药物或条件的影响。在我们了解单个微生物或微生物基因改变衰老轨迹的机制之前,我们需要使用更广泛的干预措施。一些微生物类群随着年龄、慢性病和其他炎症条件的变化而不断变化,这意味着减少全身性和局部性炎症可能会带来立竿见影的健康益处。用饮食中的钨酸盐或铁来改变发炎肠道的氧化还原状态已被证明可以防止大肠杆菌科细菌的生长。同样,一些常见的廉价药物,如二甲双胍,除了具有预期的代谢作用外,还可以降低微生物失调的发生率。这些疗法可能是非特异性的,但它们也有便宜的优势,因此很容易融入健康的老龄化计划。
结论
高龄是一个独特的发展阶段,老年人不仅仅是慢性健康状况的总和。衰老的微生物群,就像衰老本身一样,似乎承受着韧性下降的痛苦。接触抗生素、饮食、药物和生活方式的改变对老年人肠道菌群的组成有很大的影响(如果不是灾难性的)。尽管缺乏弹性是个问题,但它也可能提供一个机会之窗。虽然饮食和益生菌干预措施对健康的年轻人的影响通常很小且持续时间很短,但在老年人和体弱的成年人中,它们似乎有更明显和更持久的影响。
采用“保护微生物”饮食的障碍与遵守任何饮食建议是一样的。流动性、独立性和经济自主性的老年人已经遵守公共卫生建议,以实现健康和均衡的饮食,而经济、行动能力和自主性受到限制的老年人愿意但无法遵守。具有讽刺意味的是,开发益生菌或益生元预防性“药物”来改善与年龄相关的健康状况,可能比饮食干预更容易纳入常规护理,因为获得药物的社会经济障碍在获得普遍医疗保健的老年人中不那么严重。
在人口水平上,老龄化是一个不平衡和不公平的过程,我们中的一些人衰老的速度比其他人要快;然而,虚弱或亚健康人群肠道微生物事最容易被控制的。这一事实,再加上公众对微生物组学知识的热情,可以为改善老年人的健康状况提供一个独特的干预点。
参考文献:
DeJongEN, Surette MG, Bowdish DME. The Gut Microbiota and Unhealthy Aging:Disentangling Cause from Consequence. Cell Host Microbe. 2020;28(2):180-189.doi:10.1016/j.chom.2020.07.013

谷禾健康
呼吸道感染(RTIs)是全世界儿童发病和死亡的主要来源。在过去的十年中,已经清楚的是,呼吸道和肠道菌群与呼吸道感染的发病机理有关。宿主和环境因素可以促使呼吸微生物群在早期生活中走向成熟,这又与对呼吸道感染的持续易感性有关。近日,荷兰研究团队发表在《Cell host microbe》的一篇综述论文,详细阐述了微生物群在儿童呼吸道感染易感性中的作用,并回顾了呼吸道微生物群组成与呼吸道感染易感性联系起来的流行病学和机制证据,讨论了微生物在呼吸道感染急性期驱动感染和炎症中的作用机理。

背景:
呼吸道感染是全世界儿童发病和死亡的主要来源。 这些感染的范围从轻度的上呼吸道感染(U呼吸道感染)或普通感冒,到威胁生命的疾病,包括下呼吸道感染(L呼吸道感染)或肺炎。尽管全球死亡率总体上正在下降,但它仍然是5岁以下儿童死亡的主要原因,占该年龄组总死亡人数的15%(联合国儿童基金会和世界银行,2019年)。
重要的是,肺炎是导致肺功能下降和慢性后遗症的驱动因素,包括成年后哮喘和慢性阻塞性肺病(COPD)的发展。考虑到呼吸道感染在生命早期可能产生长期影响,因此越来越需要了解调节这些感染易感性和严重性的因素。
尽管揭露了许多这些因素,包括出生方式,进食类型,吸烟,早产,托儿所的出勤率和兄弟姐妹的存在,但潜在的生物学机制仍然难以捉摸。传统上,呼吸道感染被认为是由病毒或细菌引起的,由诸如流感嗜血杆菌和肺炎链球菌等“病原体”以及呼吸道合胞病毒(RSV)引起。但是,考虑到这些相同细菌和病毒的无症状“定殖”是普遍现象,这种关于呼吸道感染病因的以病原体为中心的观点似乎已经过时了。相反,最近对呼吸微生物群(即,由细菌,病毒,古细菌和位于粘膜表面上和表面的单细胞真核生物组成的群落)的研究表明,更广泛的微生物群落参与了呼吸道感染的病因。 除了局部微生物群的影响外,肠道微生物群还似乎通过其免疫调节特性促进了呼吸道感染的发病机理和严重程度。总之,这些新证据强调了我们对呼吸道感染病因学机制复杂性的历史性认识不足。
呼吸道微生物的早期来源和组装
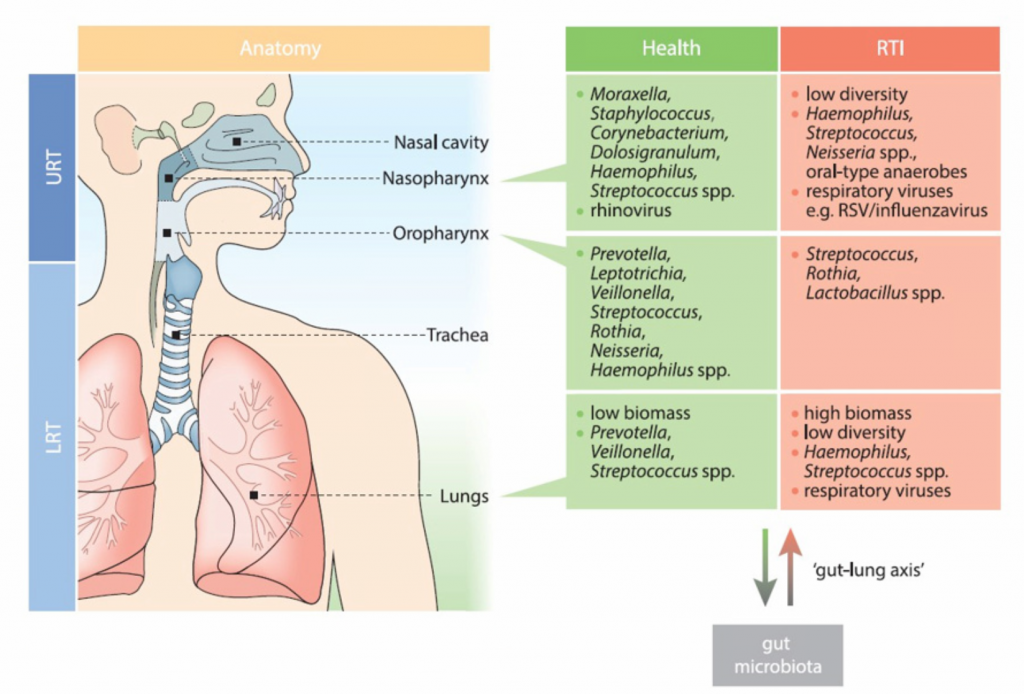
在健康方面,如图1所示,整个解剖龛的呼吸道细菌群落组成均不同。
尽管现在有几项研究表明,在怀孕期间胎儿会暴露于母体微生物产物中,而且甚至可能稀疏地存在活的微球菌属某些种。新生儿的大部分微生物组是在出生期间均匀混合微生物后获得的,因此主要来自母亲。一般来说,这种母体“初始试剂盒”通常由阴道、肛肠和皮肤微生物组成,尽管这与分娩方式不同。这种最初同质的微生物群在局部选择性压力下迅速在身体部位多样化。例如,鼻咽微生物群在生命的最初几周发展最为迅速,最初的金黄色葡萄球菌作为核心微生物出现,随后是革兰氏阳性共生菌棒状杆菌和Dolosigranulum菌(Dolosigranulum菌是1993年Aguirre等提议设立的一个菌属,该菌属细菌为兼性厌氧、触酶阴性或弱阳性的革兰阳性球菌,仅1个菌种)的定植和生长。从6周龄开始,莫拉菌属某些种迅速开始繁殖,并最终在3个月龄时超过该生态位。
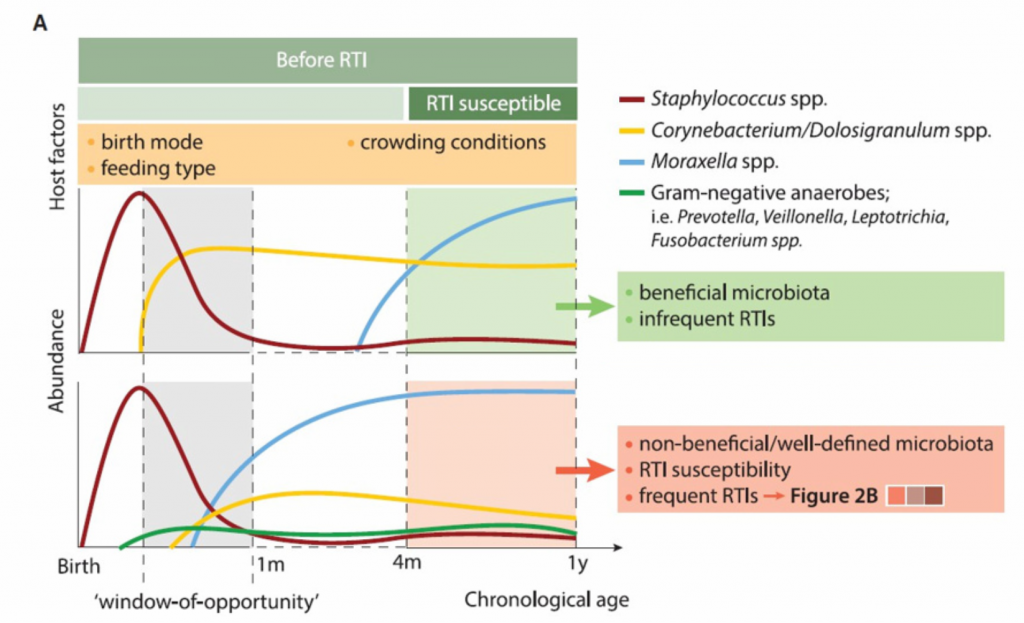

图1:健康和呼吸道感染期间各呼吸生态位的关键微生物群落成员健康和疾病期间上呼吸道(URT;鼻咽、口咽)和下呼吸道(LRT;肺)微生物群落组成概述。
至关重要的是,在围产期和新生儿期,这些微生物的成熟方式受到宿主和环境因素的严重影响。 与肠道相似,早期上呼吸道(URT)菌群的发育因出生方式而异,通常早期和长期的棒状杆菌/Dolosigranulum spp数量丰富。 在阴道分娩的婴儿中,金黄色葡萄球菌的持续存在和厌氧菌的出现,包括普雷沃氏菌,韦荣氏菌和卟啉单胞菌。在剖腹产(剖腹产)出生的孩子中。 喂养的方式类似地影响定居模式,除了金黄色葡萄球菌富集外,这表现出阴道分娩和母乳驱动的群落之间的相似性,这主要与皮肤-皮肤接触有关(即都是通过母乳和剖腹产获得的)。 与阴道分娩和母乳有关的微生物群组成的相似性可能是由母乳相关的免疫学因素驱动的,例如免疫球蛋白(Ig)A和生长因子,很可能自然地支持源自母亲的共生微生物。
最近的证据表明,母乳还含有自己的微生物,可能直接填充呼吸道粘膜。URT中微生物群结构和发育的其他重要决定因素包括暴露于拥挤条件下,例如托儿所的出勤和年幼的兄弟姐妹的存在。 这些因素也是呼吸道感染发生的众所周知的危险因素,可以通过观察到的相关微生物变化来解释,例如,普雷沃氏菌的早期富集和嗜血杆菌属的较高丰度。
解开影响微生物群组成的不同新生儿因素具有挑战性,因为许多因素之间有着千丝万缕的联系。例如,通过剖腹产分娩的母亲更可能早日停止母乳喂养。 此外,母乳菌群的组成似乎也受到分娩方式的高度影响,突显了研究其独立作用的难度。很少有研究调查下呼吸道(LRT)微生物群的驱动因素,这是一项极富挑战性的工作,因为这种利基的可获得性有限且细菌密度低,尤其是在健康婴儿中。但是,一项研究评估了健康早产儿和足月儿的气管抽吸物,结果表明,LRT菌群组成的差异最大,其胎龄不同,早产儿有葡萄球菌或脲原体,足月儿出现混合的成人型厌氧菌群,包括静脉内拉菌、普雷沃特菌和梭杆菌。与其他生态位类似,影响早期LRT微生物群的因素包括出生方式(仅早产儿)和产后年龄(仅足月儿)。
早期呼吸道微生物和儿童呼吸道感染
在呼吸道感染发展的各个阶段,有人提出了呼吸菌群组成的重要性(图2)。 多项纵向(出生)队列研究已证明了早期呼吸道微生物群发育与呼吸道感染敏感性和晚年呼吸道健康之间的关联。值得注意的是,在出生后的第一个月内,URT中过早从葡萄球菌过渡到以莫拉氏菌为主的分布,省略了棒状杆菌和Dolosigranulum占主导地位的早期阶段,这与出生后第一年发生呼吸道感染的频率更高有关。 尽管仍然需要证明其因果关系,但微生物群发育的第一个偏差和呼吸道感染发生之间的时间差异(通常从4个月开始)表明,早期微生物群暴露可能有助于先天和全身免疫,从而调节连续的呼吸道感染敏感性 。
或者,呼吸道感染敏感性增加至少可以部分归因于与微生物群落定殖事件的发生时间一致的其他事件,特别是由于母体IgG水平下降导致被动免疫的逐步下降。 值得注意的是,这些不是孤立的事件,也不是相互排斥的事件,可能会发生母体免疫力下降与婴儿特异性微生物和免疫介导作用之间的相互作用。
微生物群发育与呼吸道感染敏感性之间关系的关键似乎是定植事件的发生时间。
尽管到3-6个月时,几乎所有儿童都过渡到了以莫拉氏菌为主导的菌群,但莫拉氏菌的早期出现。 与气道粘膜的炎性免疫反应有关,以及第一次呼吸道感染和喘息的早期发作。 同时,链球菌早期富集(约9周)与早期L呼吸道感染的较高风险相关。 应当指出的是,除了定居的时间外,这些相关性可能是由物种或什至菌株水平的变化所驱动的,这可以通过卡他莫拉氏菌或林肯莫拉氏菌在早期定殖的婴儿的呼吸道感染风险差异来说明。
尽管奖赏可能引起免疫调节作用,但研究还暗示携带特定病原体(如肺炎链球菌)是呼吸道感染发生的直接危险因素。
传统上,特别是肺炎链球菌和流感嗜血杆菌是直接引起严重感染如细菌性肺炎的病原体。然而,尽管这些病原体在明显的细菌性呼吸道感染中已经确立并发挥了重要作用,但最近的证据表明,它们与更广泛的疾病表型有关,例如传统上认为是病毒起源的细支气管炎和并发性喘息。结合在一起,发现三种病原体(RSV,肺炎链球菌和流感嗜血杆菌)的存在和丰富程度可指示幼儿的疾病状况,而与感染表型(即肺炎,细支气管炎和混合感染)无关(Man 等,2019a)。 这与先前的研究一致,URR中以链球菌和嗜血杆菌为主的微生物群谱与RSV疾病的严重程度相关,而以葡萄球菌为主的谱菌似乎具有保护性。棒状杆菌和Dolosigranulum spp的丰度同时下降。 与更严重的预后相关,包括入住重症监护室。 因此,我们假设这些生态力量的总和最终将支撑呼吸道感染结果。
流感嗜血杆菌与肺炎链球菌和RSV之间的相互作用是有关病毒-细菌相互作用如何影响疾病严重程度的临床相关实例。重要的是要注意,尽管呼吸菌群领域取得了进步,但仍需要阐明支持这些关联数据的机制。 结果,越来越需要研究“混合感染”中的因果途径,重点研究共生微生物群可调节临床呼吸道感染结果的机制。
微生物群介导的呼吸道感染易感性调控机制
生命早期的微生物群落可能直接通过微生物与微生物的相互作用或通过宿主免疫系统间接预防呼吸道感染。 尽管现有的实验模型无法在真实,复杂的人类微生物群落中重建这些相互作用,但有关流行病学研究中突出的特定呼吸道法则已有相关证据。例如,尽管金黄色葡萄球菌因其致病潜力而广为人知,但由于其免疫调节特性,似乎是重要的早期鼻咽共鸣。 小鼠研究表明,URT中的金黄色葡萄球菌定植可通过诱导抗炎性M2肺泡巨噬细胞来抑制流感诱导的免疫介导的肺损伤。 这种共鸣的行为可能进一步取决于共同定殖的微生物物种,例如纹状棒状杆菌,抑制金黄色葡萄球菌的毒力基因的表达。葡萄球菌进化枝的其他成员,包括沙门氏菌和表皮葡萄球菌,也通过其抗菌肽诱导能力和生物膜形成能力在塑造鼻腔微生物群落中起着至关重要的作用。Dolosigranulum与棒状杆菌属共存的流行病学关联。 健康的部分原因可能是直接抑制了潜在的病原体。 实验性人类挑战研究支持了这一点,研究表明,直接挑战后,Dolosigranulum的高丰度与肺炎球菌的低丰度有关,并且与微生物群稳定性提高和黏膜细胞因子生成低有关。 体外研究已经证实,Dolosigranulum本身或与棒状杆菌属菌种协同作用可分别抑制金黄色葡萄球菌和肺炎链球菌的生长,这很可能是一系列抗菌肽产生的结果。棒状杆菌同时也是已证明通过Toll样受体(TLR)3介导的保护作用和体外直接代谢活性抑制潜在的病毒和细菌病原体。
早期微生物群发育与健康结果之间关联的潜在机制可能涉及其他免疫介导途径。 在早产儿和足月儿的早期气管样本中,宿主IgA基因表达被证明与预测的微生物IgA蛋白酶功能相关,这意味着微生物与宿主的串扰。此外,在小鼠身上,局部微生物群和树突状细胞之间的特定早期相互作用会在肺部产生调节性T(Treg)细胞亚群,防止气道高反应性。
当这些相互作用在以后的生活中发生时,这种保护就被取消了,再次强调了及时暴露于微生物对呼吸道粘膜免疫稳态发展的重要性。 除了对自然感染的免疫反应外,还建议肠道和鼻微生物会影响宿主对呼吸道疫苗的免疫反应,潜在地调节疫苗效力并影响宿主对后续呼吸道感染的防御。相反,肺炎球菌疫苗与呼吸道微生物群组成的变化有关,活减毒流感病毒疫苗的接种导致其他呼吸道病原体(如肺炎链球菌)的获得和密度的瞬时增加。 这些发现强调,应该做更多的工作来理解这些双边互动,并将其用于未来的量身定制的预防策略。
呼吸道感染中微生物介导的机制
除了在改变呼吸道感染敏感性中可能发挥作用外,呼吸道微生物群还与呼吸道感染发作的开始以及症状的严重程度有关。 尽管已知细菌在明显的细菌感染中具有致病作用,但特定的细菌群落成员,尤其是链球菌和嗜血杆菌属菌种,已牵涉到更广泛的疾病实体中,包括被认为是病毒起源的L呼吸道感染。 入侵这些病态生物可能会引起生态不稳定,并因此引起某种程度的炎症,尽管这本身可能尚未导致症状。 这种情况可能会促使包括环境刺激物(如香烟烟雾暴露)在内的触发因素进一步升级为有症状的感染(图2)。 确实,在小鼠中发现只有在也存在肺炎链球菌的情况下,烟雾暴露才可以改善微生物群落的平衡。 在这种情况下,并发病毒感染也可能成为“第二击”。 支持这一想法的是,在检测到病毒存在之前,患有富含莫拉氏菌的微生物群的儿童没有症状,从而导致L呼吸道感染。 在L呼吸道感染的细菌-病毒组合诊断模型中,病毒的存在最能将健康儿童与患有呼吸道感染的儿童区分开,无论其表型如何,其中包括推测的(细菌性)肺炎病例。这表明病毒感染可能会进一步扰乱已经受到挑战的宿主-微生物界面,从而导致疾病的表型和严重程度。 符合条件的是,同时感染了链球菌/嗜血杆菌为主的微生物群的RSV感染婴儿更有可能住院治疗,并显示出与TLR信号相关的基因表达更高以及嗜中性粒细胞和单核细胞募集。
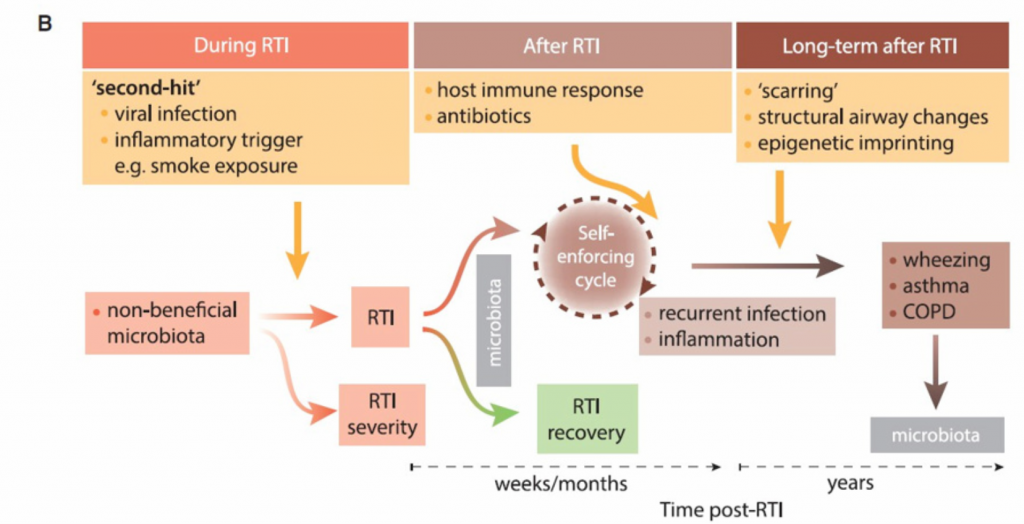


图2 呼吸道感染前、中、后呼吸道微生物区系的影响。
A.在4个月大的第一次RTI发作之前,呼吸菌群已经显示出与连续RTI敏感性相关的独特的微生物成熟模式。 这些早期的发育模式转化为有益的,平衡的微生物群,或转化为定义不明确和失衡的微生物群,后者通常与RTI的风险有关。
B. 一旦非有益的呼吸道微生物群建立起来,可能需要“第二次打击”来打破平衡,导致严重程度不同的感染。在RTIs之后,我们认为微生物群可以通过促进恢复状态而恢复到以前的状态,或者保持在扰动状态,这可能引发一个促炎症途径的自我强化循环。这种炎症状态反过来又使个体易受复发性rti的影响。长期来看,这种状态可能通过气道结构的改变永久改变呼吸道微环境,甚至可能导致长期后遗症,包括哮喘和慢性阻塞性肺病。
相反,对于以葡萄球菌为主的微生物群定殖的儿童,情况恰恰相反。 体外研究进一步证明了这一点,表明用不可分型的流感嗜血杆菌引发初级支气管上皮细胞可导致ICAM-1上调,并促进促炎性细胞因子(包括IL-6和IL- 8在受到额外的RSV攻击后。 除了这些通过宿主炎症引起的间接相互作用外,直接病毒细菌相互作用还可能影响L呼吸道感染发病的早期阶段,这项研究表明,预先与流感病毒一起孵育的肺炎球菌证明了在其他幼稚小鼠中细菌粘附的增加。
一旦达到平衡,感染和炎症就会并存,相互促进。该理论在L呼吸道感染的背景下得到了很好的描述。 在这些感染期间,正常的低密度和高多样性微生物区系会被一种推定的病原菌过度繁殖。随后的病原体诱导的宿主炎症可能作为炎症和微生物变化的自我强化循环的起点,从而促进了进一步的病原体生长。
呼吸道生态环境中的微生物与宿主的相互作用
尽管宿主-微生物相互作用对呼吸系统健康的重要性显而易见,但这些相互作用可能会因解剖位置而异。在健康的URT中,自然存在于鼻咽和口咽生态位的微生物群落之间存在明显的区别。 但是,这种地形上的区别在呼吸道感染发作之前和期间开始逐渐消失,尤其是口型细菌包括Prevotella,Neisseria,Veillonella,Fusobacterium和Porphyromonas出现在鼻咽中。
同样,在L呼吸道感染的背景下,微生物群落之间的区别在解剖边界变得模糊。 在患有这些感染的儿童中,在成对的鼻咽和气管样本中检测到的病毒和细菌群落组成大部分重叠,这表明URT微生物群(例如通过微生物过度生长和微量抽吸)可能是LRT微生物群的来源,从而导致了症状。急性L呼吸道感染。 或者,可以在不同的呼吸生态位中发挥类似的控制力(例如炎症),选择相似的微生物群落。 尽管本研究中URT和LRT微生物群落之间存在大量重叠,但仍选择了一个分类单元,包括葡萄球菌,棒状杆菌和Dolosigranulum spp。 在鼻咽以外很少发现,这说明这些物种具有生态位特异性的生态作用。
与不同生态位的微生物组成不同,某些物种确实在整个呼吸道中发生,但是它们的免疫调节功能可能会随它们所嵌入的生态位和特定生态位社区而变化。 例如,厌氧菌(如厌氧杆菌和Veillonella)被认为是口腔和口咽的正常标志,它们的丰度似乎表明呼吸系统健康。 然而,当在肺中鉴定出相同的微生物物种时,它们与IL17 + CD4 + T细胞和中性粒细胞的水平升高以及TLR4反应减弱有关(Segal等,2016)。这些发现都强调了呼吸微生物物种和健康状况之间的联系只能在其完整的生态环境中进行评估,而生态环境可能因生态位而异。
呼吸道感染术后微生物扰动的影响
如上所述,证据支持早期呼吸微生物群在呼吸道感染发展中的作用,并强调呼吸道感染期间发现的微生物群组成的扰动。我们假设,这种受干扰的微生物群组成不仅导致微生物群的定殖抵抗力和恢复力降低,并且在呼吸道感染期间增强症状,而且导致症状持续存在和未来复发的风险。最近的数据表明,婴儿呼吸道感染后三周内链球菌科的富集与随后一段时间内的持续症状有关。此外,抗生素治疗,通常为生殖道感染,可能会进一步扰乱已经受到挑战的微生物群落,有可能降低感染后对新获得病原体的抵抗力。
事实上,在抗生素治疗后,居住在呼吸道的促进健康的共栖体,包括棒状杆菌和白云雀属,以及肠道共生体,如双歧杆菌属,在抗生素治疗后被消除,从而可能增加感染复发的风险。这也许可以解释为什么抗生素治疗后急性中耳炎复发率更高,尽管这还没有在随机对照环境中进行研究。
尽管可能涉及一个自我执行的循环,在该机制中特定的微生物群落可以促进或维持促炎环境,从而促进病原体大量繁殖,但尚未阐明这种现象的确切机制。 当这些病原体引发进一步的促炎性级联反应时,恶性循环迫在眉睫(图2)。
据推测,当不能恢复到稳定状态时,这些变化可能会持续并转化为疾病的长期后遗症。对易患哮喘儿童的研究证据表明,下咽部微生物群的组成特征为Veillonella,Prevotella和Gemella spp。 出生1个月时,患者气道炎症与6岁时哮喘的诊断有关。 这项最新研究增加了先前的研究,将卡他莫拉菌和流感嗜血杆菌的早期存在与1个月大的哮喘多发新生儿气道中的促炎性免疫特征联系起来。此外,婴儿期急性感染期间莫拉菌属,嗜血杆菌和链球菌的富集与变态反应致敏或细支气管炎后嗜血杆菌和链球菌的富集有关。 或3至5岁时反复喘息,进一步支持了这一理论。 无论如何,需要进一步研究支持这些关联的机制,以了解确切的因果关系。
通过表观遗传的印记,早期生命中的微生物和免疫扰动可能在晚些时候改变气道的生理功能的一种可行方式是。
体外模型和分子流行病学研究表明,年轻时的RSV感染确实会在生活中涉及哮喘的各种免疫改变基因中诱导组蛋白和DNA甲基化修饰。
同样,有益的微生物可以通过产生短链脂肪酸(SCFA)来调节宿主表观基因组,如肠道营养证明的那样。 这些SCFA与呼吸道的生物学相关性已通过一项体外研究得到证明,该研究表明暴露于acc.accolens后从鼻上皮表面释放的SCFA抑制了肺炎链球菌的生长。
肠肺轴
除了呼吸道中局部微生物介导的作用外,越来越多的证据表明,肠道菌群在调节呼吸道免疫力中起着重要作用。这两个粘膜部位之间的连接通常称为肠肺轴。
除了肠道和肺微生物群之间的一般联系外,人们还发现,肠道微生物定植似乎与早期生命特别相关。 在小鼠中进行的一项研究表明,肠道定居,尤其是在新生儿窗口内,可以防止卵白蛋白诱导不变的自然杀伤性T(iNKT)细胞积聚到肺中,这一过程与过敏性哮喘的发展有关,并通过降低Cxcl16基因的甲基化程度来介导 。 肠道菌群似乎也促进了第3组先天性淋巴样细胞(ILC3s)向肺的动员,有助于防御肺炎。 新生儿时期肠道菌群的耗竭严重损害了这种防御,而成年小鼠的相同程序显示出对肺炎易感性的作用有限,强调了微生物菌群与宿主相互作用的时机很重要。一项最近的出生队列研究支持了这一点,该研究表明阴道分娩支持的双歧杆菌属早期丰度与生命的第一年间的呼吸道感染之间存在时间上的联系。 该研究表明肠道微生物组可以充当介体,将已知的危险因素(例如分娩方式与呼吸道感染易感性)联系起来。
此外,在呼吸道感染期间,肠道微生物群落可能会影响疾病的严重程度,这已经通过鼠类研究调查了细菌和病毒性呼吸道病原体。 符合条件的是,已提出了益生菌给药(主要是乳酸杆菌和双歧杆菌属)对U呼吸道感染的发生率和持续时间的影响,尽管这些研究的质量有限阻碍了结论,这主要是由于研究规模不足或随机方法不清楚以及盲目性。
此外,在呼吸道感染期间,肠道微生物群落可能会影响疾病的严重程度,这已经通过鼠类研究调查了细菌和病毒性呼吸道病原体。 符合条件的是,已提出了益生菌给药(主要是乳酸杆菌和双歧杆菌属)对U呼吸道感染的发生率和持续时间的影响,尽管这些研究的质量有限阻碍了结论,这主要是由于研究规模不足或随机方法不清楚以及盲目性。如前所述,肠道微生物群影响呼吸道感染的机制大概是免疫介导的,或者涉及微生物衍生产物向血流的释放。例如,微生物代谢物去氨基酪氨酸通过增强I型干扰素信号传导,消除肺部免疫病理学来保护小鼠免受流感的侵害。有趣的是,这些微生物群驱动的有益影响不仅限于细菌,因为共生真菌在这方面也被证明是重要的。
般而言,这些常驻社区成员似乎可以校准免疫语调并教育免疫系统如何控制病原体以预防症状性感染。 后者似乎与病毒感染最相关,但也与细菌感染有关,已经揭示了特定的机制。例如,已显示通过特定细菌群的Nod样受体(NLR)-可通过肺泡巨噬细胞中IL-17A依赖性的粒细胞-巨噬细胞集落刺激因子(GM-CSF)信号传导增强保护免受细菌感染。
肠道菌群可能影响呼吸道感染的一种不太直接的免疫介导途径可能是与针对呼吸道病原体的疫苗相互作用。 小鼠模型揭示了潜在的机制,肠道共生可能通过细胞或代谢物介导的与巨噬细胞或B或T细胞之间的相互作用来增强免疫记忆的形成,Lynn和Pulendran(2018)综述。例如,微生物鞭毛蛋白已显示以TLR5介导的方式诱导更高水平的浆细胞和三价流感疫苗(TIV)特异性IgG。 肠道菌群对人类疫苗接种反应的影响可能涉及复杂的途径,正如对抗生素改变的菌群患者进行的TIV应答的多组学分析所表明的那样。 尽管抗生素的耗竭仅对免疫力低的患者显示了对TIV特异性抗体的影响,但微生物菌群的畸变与TIV后转录组和代谢组学模式的变化相关,包括炎性体信号转导增加。
尽管仅是关联性的,但该证据表明肠道菌群可通过局部和全身相互作用介导疫苗效力。
肠与肺之间的相互影响是相互的。 研究表明,小鼠的RSV和流感感染都会影响肠道菌群的组,使这些小鼠更容易受到随后的肠感染的影响。流感引起的肠道微生物变化和SCFA产量减少也显示出增加了对继发性肺炎球菌感染的易感性,强调了肠道与肺之间的强烈串扰。
未来的展望
在过去的几年中,一般的“一种病原体,一种疾病”的范例已经开始向整个生态系统的呼吸道感染发病机制理论转移。 该理论既包括微生物相互作用,也包括微生物-宿主介导的免疫调节,它们是呼吸道感染的适应性和敏感性的基础。
最近的知识不仅加深了我们对呼吸道感染发病机理的了解,而且还有助于重新定义预防,诊断或治疗方式。例如,Langelier等结果表明,他们可以通过使用集成的微生物组和宿主转录组分析,将重症患者的肺炎与其他急性呼吸衰竭的其他原因准确区分(Langelier等,2018)。 此外,实时宏基因组测序已被用于诊断细菌性肺炎的微生物起源,同时能够检测微生物抗性基因,从而可以在感染的早期阶段进行量身定制的抗生素治疗。这种知识还可以导致新的生物治疗方法。
尽管这些实例很有前途,但我们应该加大对生物学机制的认识,以支持宿主,微生物和外界之间的健康平衡。 为此,作者建议并行使用模型系统和系统生物学方法。
尽管揭示微生物群组成和功能与呼吸道感染发病机理各个阶段的健康结果之间的关联非常重要,但重要的警告仍然是已证实的因果关系的稀疏性。微生物组研究的一个主要挑战是在模型系统中捕获代表人类有机体的整个生态系统范围的宿主-微生物相互作用的复杂性。 结合基因和组织工程学等其他领域的最新进展(例如人类微生物菌落定殖的[人源化]鼠模型),可以为这些问题提供一些解决方案。
通过对这些模型生物进行遗传操作获得的功能丧失或丧失功能的实验,再结合下一代测序技术,可用于评估微生物宿主相互作用或微生物基因组介导的表观遗传改。此外,先进的体外模型,包括芯片上气道模型或气道类器官可用于研究可控环境下的宿主-微生物相互作用,其中后者已被证明可用于对RSV或流感病毒感染进行建模。
体内动物模型和类器官系统都可以与基因编辑技术相结合,以调节宿主或组织侧(基因表达和代谢产物/蛋白质的产生)或改造微生物的基因组。
尽管取得了这些进展,但由于每个定义的体内和体外模型都缺乏人类生理学和环境变化的复杂性,因此人类研究具有希望。与观察性研究相反,这些研究使我们能够深入了解病原体获取周围的微生物群落动态,并允许对单个变量进行操作,例如共同定殖细菌或病毒,或测试疫苗相互作用。 与疫苗学领域类似,近年来,疫苗学领域采取了“系统科学”的方向,类似的多组学方法也可能有助于了解呼吸道感染的病因。 包括病毒,噬菌体和真菌在内的目前尚未深入研究的非细菌微生物群落,将使我们能够更详细地捕获整个生态系统范围内微生物群落的真实变化。这将使我们能够更广泛地研究环境,微生物和宿主之间与呼吸系统疾病的病因和表型之间的相互作用。
儿童呼吸道感染的长期后果以及微生物群在呼吸道感染发病机理中各个阶段的全面作用要求采取早期预防和治疗干预措施以促进呼吸系统健康。

谷禾健康


日常生活中,我们更多地认为心情是由思想控制的。这虽然是常识,但并非完全正确。
荷尔蒙也十分影响我们的情绪,同时我们的情绪也受到免疫系统和肠道微生物的影响。更复杂的是,在这个纠结的生物网络中,我们的生活承受着巨大的压力。
精神压力是身体对生活压力的反应。它设法使身体恢复平衡,正常发挥免疫力,激素和神经的作用。来自工作上的压力或生活的压力都可能会导致抑郁和焦虑。无论哪种情况,都可以从免疫系统开始。
抑郁症是全世界致残的主要原因之一。据估计,五分之一的人在一生中都会经历抑郁症。大约85%的人在经历第一次抑郁症发作后的10年内会复发。

今年,COVID-19大流行,更给全球人类造成了极大的焦虑和不安全感,持续的危机将导致很多心理和精神健康问题。
肠道是人体最大的器官,肠道中微生物包括细菌,病毒,真菌等。微生物的平衡对于身心健康至关重要。
而现代生活中的各个方面,例如压力大,加工食品饮食,抗生素,杀虫剂以及经过消毒的城市环境,都减少了健康肠道菌群的数量和丰富度,同时增加了有害菌群的数量。最新的抑郁理论表明,肠道菌群失衡可能在这种疾病中起主要作用。
一项2019年的研究将来自精神分裂症患者的粪便微生物移植物引入无菌小鼠中,发现这些小鼠随后表现出与精神分裂症有关的行为。
同样,另一项研究指出对患有抑郁样特征的啮齿动物施用益生菌可以减少这些特征,从而使啮齿动物恢复正常行为。所有这些表明,肠道菌群的外部操纵具有进行新的心理健康治疗的潜力。
抑郁症患者的肠道菌群与健康人不同。与健康个体相比,它们的肠道菌群多样性和丰富性较少。《自然》杂志上的一项新研究发现,肠道微生物对于消除小鼠的恐惧反应至关重要。
众多研究表明肠道微生物连接大脑至少有三种途径:免疫、神经系统,激素和代谢物。
病原体发作后,免疫系统就会立即按下紧急按钮。但是免疫系统也可以对心理压力做出反应,即所谓的“无菌压力”。与侵略者作斗争是一回事,但是让我们抵抗精神压力似乎是对免疫系统的一大要求。
有一种简单的方法来证明压力和免疫力之间的密切联系:每天将普通小鼠引入恶霸小鼠中几分钟。结果很神奇,受欺负的小鼠仅需一到两周即可产生炎症,这是通过其血液中的促炎化学物质测得的。其中,他们的淋巴细胞——白细胞发生了变化。
另外,有一种特别培育出来的淋巴细胞水平较低的老鼠比普通老鼠更焦虑,更不善于交际。但是,当您向这些害羞小鼠注入来自受欺负小鼠的淋巴细胞时,会发生一些有趣的事情:可能与你期望的相反,它们变得不那么焦虑,开始更多地社交。
在应激小鼠中,这些淋巴细胞正疯狂地试图减少恶霸引起的炎症。这是自然界最持久的回路之一:负反馈回路,可防止反应失控。威胁带来的心理压力会引发这些淋巴细胞抑制炎症。一旦转移,它们对宿主小鼠产生有益的“减轻压力”作用,导致促炎性化学物质减少并赋予其新宿主弹性。
这个有趣的实验表明,纯粹的心理压力可以改变免疫系统。这表明,通过简单地重新平衡免疫系统可以治疗抑郁症。
美国阿尔伯特·爱因斯坦医学院Paul S. Frenette小组发现,肠道微生物组可以调节心理压力引起的炎症。这一研究成果在线发表于2020年7月30日的 《免疫》。利用镰状细胞病的血管闭塞性发作(简称VOE)作为血管疾病模型,研究人员发现压力可通过引起糖皮质激素的激素反应增强VOE,这些激素反应可增强肠道壁的通透性,导致微生物依赖的IL-17A固有层辅助性T细胞17的分泌,随后引发VOE中性粒细胞循环池扩大。
我们已经看到反复的压力如何导致免疫反应,以及由此产生的炎症导致抑郁和恐惧。但是微生物扮演什么角色?
虽然认知疗法和增加5-羟色胺的抗抑郁药可以有效地治疗抑郁症,但这些治疗方法对超过三分之一的抑郁症患者无效。最近的抑郁理论表明,肠道微生物群的失衡和连接肠道和大脑的轴的功能障碍可能参与其中。
这个世界上布满了细菌,其中许多细菌都比吃我们的早餐更好。为了应对这种恶劣的现实,动物们很早就招募了自己的一组友好微生物来保护自己。这些有益细菌并没有真正站在我们这边,只是他们很乐意在温暖和潮湿的肠子中发酵,不断地吃自助餐。这些细菌被称为共生细菌,拉丁语是“共享餐桌”。
当病原体试图侵入这一长期建立的伙伴关系时,共生菌会手撕它们。从本质上讲,我们的微生物群是免疫的先锋。为了与人类宿主建立如此重要的关系,共栖者需要教会免疫系统容忍它们。这是在生命的早期,出生后一千天之内发生的,如果这个过程受到干扰,那么可能会终身受疾病困扰。
就像牧羊犬引导羊群一样,免疫细胞监视着共生菌,使它们在肠道内和血液循环外被包围。而细菌则分泌脂肪酸来安抚免疫细胞,保护它们免受攻击。通过这些分泌物,肠道细菌可以在远离肠道的地方发挥作用,甚至可以改变大脑的形状和功能。
这意味着微生物会改善情绪。
那些可以改善情绪的菌群,包括某些乳酸菌和双歧杆菌,甚至可以降低皮质醇水平。这些被称为精神药物,它们代表了另一种可能的抑郁症治疗方法。尽管这些都属于该领域的早期研究,但已证明它们可以减少负面想法,改善认知并降低IBS症状。
微生物可以影响你的海马体或杏仁核的大小,这些大脑中心与情绪、食欲和恐惧有关。海马体试图阻止下丘脑-垂体-肾上腺轴(HPA轴)偏离轨道,如果它的生长发育迟缓,就会影响应激反应。

如果说免疫细胞和微生物是生物乐队的主要参与者,那么HPA轴就是指挥。HPA轴是下丘脑-垂体-肾上腺的缩写,它协调着逐渐增加的激素释放与皮质醇的释放,皮质醇是战斗或逃避反应的药物。压力通路会通过交感神经系统(SNS)和/或下丘脑-垂体-肾上腺(HPA)轴从大脑传递信号。SNS的激活导致肾上腺素(从肾上腺髓质)和神经递质去甲肾上腺素(从各个器官的神经末梢)释放激素。
HPA轴激活最终导致肾上腺皮质分泌糖皮质激素。 糖皮质激素通常具有免疫抑制功能。 例如,在压力下升高的糖皮质激素浓度显示可通过B和T淋巴细胞的凋亡引起适应性免疫缺陷,并且糖皮质激素已在药理学上用作有效的抗炎药。 炎症被认为是导致与压力有关的疾病的常见途径。 考虑到糖皮质激素作为免疫抑制剂的作用,应激诱导炎症的机制仍然不清楚。
迷走神经是肠道和大脑之间的主要传输通路。
迷走神经也被称为“徘徊神经”,因为它是人体中最长的神经,并且有无数分支从脑干一直延伸到肠的最下部,并一路接触大部分主要器官。
迷走神经是副交感神经系统的主要组成部分,它调节“休息和消化”或“趋于友好”的反应。另一方面,为维持体内平衡,交感神经系统驱动“战斗或躲避”反应。
迷走神经通过引起所谓的“放松反应” 来抵消战斗或躲避中的应激反应。
迷走神经的早期解剖图
来源:Wellcome Library/Public Domain
炎症反应在许多疾病的发展和持续中起着核心作用,并可能导致慢性疼痛衰弱。在许多情况下,炎症是您身体对压力的反应。因此,减少神经系统中的“战斗或逃跑”反应并降低应激的生物标志物也可以减轻炎症。

瑜伽和冥想等日常习惯或可以对抗炎症
越来越多的证据表明,对抗炎症的另一种方法是通过接合迷走神经并改善“迷走神经张力”。这可以通过使用瑜伽和冥想等日常习惯来实现。
植入迷走神经刺激装置,改善类风湿关节炎
在更极端的炎症情况下,例如类风湿关节炎(RA),可以使用植入的迷走神经刺激装置(VNS)来实现。
最近,来自阿姆斯特丹和美国的国际研究人员团队进行了一项临床试验,该试验表明,使用小型植入装置刺激迷走神经可通过抑制细胞因子的产生显着减少炎症并改善类风湿关节炎患者的预后。
学会呼吸,缓解焦虑,辅助降压
健康的迷走神经表现为吸气时心率略有上升,呼气时心率略下降。
每次呼气时,迷走神经都会向心脏喷射一些乙酰胆碱。
横膈膜深呼吸(长时间缓慢呼气)是刺激迷走神经并减慢心率和血压的关键,特别是在表现焦虑时。
迷走神经张力指数与健康状况相关
较高的迷走神经张力指数与身心健康息息相关。相反,迷走神经张力指数低与发炎,抑郁,情绪低落,孤独,心脏病发作和中风有关。
2010年的一项研究发表在《心理学》杂志上:积极情绪如何建立身体健康:感知到的积极社会关系解释了积极情绪和迷走神经张力之间的螺旋上升。
在这项研究中,北卡罗来纳大学教堂山分校的Barbara Fredrickson和Bethany Kok研究了迷走神经,发现高迷走神经张力指数是积极情绪、身体健康和积极社会关系之间反馈回路的一部分。
慢性压力与胃溃疡有关
相信大家可能有过对公开演讲感到恐惧的经历,这种站在人前的演讲会导致消化不良。由于沿着肠脑轴的迷走神经通路是双向的,因此当人真正感到压力时,这些脑-肠连接创造了一条来回交流的高速公路,可能会失去控制。
脑岛接收来自肠道的压力信号,从而使大脑在胃部发出更多与压力有关的警钟。
注:脑岛为大脑的岛叶,控制很多感觉和情绪的产生。
Levinthal和Strick(2020)的最新研究表明,大脑会立即将压力信号从脑岛发送到肠道。随着时间的推移,慢性压力以一种可能导致胃溃疡的方式劫持了这些脑肠连接。
有趣的是,他们推测,促进“战斗或逃跑”反应的交感神经系统会沿着迷走神经通路发送大脑到肠道的信息,这些信息与大脑皮层的运动区域更紧密地联系在一起。
更好地理解脑-肠连接如何控制胃,将为肠胃科医生治疗肠道问题和胃肠道疾病带来新的更好的方法。
HPA轴通过几种不同的化学物质与微生物群和大脑进行通讯
细菌分泌物:代谢物如短链脂肪酸。
免疫化学物质:细胞因子,如干扰素,白介素和肿瘤坏死因子。
腺分泌物:肾上腺素和皮质醇等激素。
神经传递化学物质:神经递质,例如5-羟色胺,多巴胺和GABA。
更多关于肠道菌群与神经系统这部分内容详见之前的文章:肠道微生物(菌群)与脑神经(中枢神经)到底如何联系?
微生物代谢产物是细菌在进食和代谢食物时分泌的化学物质。
不同的细菌在不同的情况下会产生独特的代谢产物。其中一些代谢物是短链脂肪酸,例如丁酸,可以使其进入大脑,从而影响大脑的生长和功能。
从肠道内的微生物和细胞释放的化学物质可直接导致迷走神经和迷走神经支配的大脑区域的电活动变化。迷走神经的活动众所周知会影响人类行为。实际上,植入刺激该神经的电子设备(迷走神经刺激器)可以有效地治疗患有严重的,对治疗有抵抗力的抑郁症和癫痫症的患者。
越来越多的研究表明,与健康对照组相比,患有多种精神疾病的人倾向于具有不同的肠道菌群模式。例如,两项研究发现与健康对照组相比,精神分裂症患者的肠道菌群多样性要低得多。
其他研究表明,抑郁症患者和自闭症患者与健康对照组相比,肠道菌群的模式也不同。这与相关研究有关提示特定的肠道菌群在涉及精神疾病的神经递质和代谢产物的产生和调节中起重要作用。这包括5-羟色胺,多巴胺和γ-氨基丁酸(GABA)。
肠道微生物影响大脑和行为的其中一种方法是通过这些微生物或是受这些微生物影响的胃肠系统细胞释放化学物质。这些化学物质释放到血液中,然后穿过血脑屏障并影响神经细胞的生长,功能和连通性。
这些化学物质中的一部分也会影响大脑免疫系统的细胞。此外,人们早就知道,肠道中合成的某些化学物质也是由大脑细胞产生的(例如生长抑素和胆囊收缩素等),这些由大脑合成的肠道化学物质可有效调节大脑功能。
发现的第一种神经递质——乙酰胆碱
1921年,一位名叫奥托·洛维的德国生理学家发现,刺激迷走神经会触发释放Vagusstoff物质(德语为“ Vagus物质”),从而导致心率降低,“迷走神经物质”后来被识别为乙酰胆碱。并成为科学家发现的第一个神经递质。
乙酰胆碱就像一种镇静剂
Vagusstoff就像镇静剂一样,可以减缓心跳间隔并改善心率变异性(HRV)。稳健的迷走神经张力和更高的HRV齐头并进,是整体心理和身体健康的标志。
你可以通过做深呼吸并长时间呼气来简单地自我管理。有意识地利用迷走神经的力量可以在抑制炎症反射的同时建立一种内心平静的状态。
皮质醇
皮质醇是人体通过增加血压,心率和呼吸来增强压力反应的方式,以便逃脱或者逃离烦扰。 在此过程中,它还会降低免疫反应:首先,你逃脱烦扰,然后才处理流感或食物中毒。这是一个合理的回应方式,只是片刻的恐慌。 但是随着时间的流逝,防御能力下降可能导致肠漏,从而将心理压力转化为微生物压力。
5-羟色胺
在肠道中也发现了与抑郁和幸福有关的化学物质,例如血清素(5-羟色胺)。90%的5-羟色胺是在消化道而非大脑中产生的。许多抗抑郁药通过增加5-羟色胺发挥作用。
科学家发现肠道菌群会产生许多其他神经递质,例如多巴胺,去甲肾上腺素,GABA等,它们对情绪,焦虑,专注等至关重要。肠道微生物群会导致大脑反应方式发生变化。
我们知道,抑郁症不仅是精神疾病。抑郁症患者可能同时患有多种疾病,包括脑功能障碍,免疫系统失调和应激激素紊乱等。
研究表明,肠道菌群在免疫,激素平衡和神经系统功能中起着至关重要的作用。
新的理论和研究表明,肠道菌群失衡可能导致许多与抑郁症有关的疾病。前面我们知道,肠道菌群会影响HPA轴的发育,该轴调节压力反应并参与皮质醇的释放。在抑郁和长期处于压力下的人中,HPA轴可能失调,导致过量的皮质醇(一种压力激素)被循环。
肠道菌群也在免疫系统功能中发挥作用,并调节称为细胞因子的化学信使的产生。促炎性细胞因子的失衡可导致慢性炎症和自身免疫性疾病,通常与抑郁症同时发生。
肠道菌群也参与神经系统的功能。肠道菌群失衡可能会影响神经递质(例如血清素)的水平,已知这些物质与抑郁症有关。
其他研究将肠道菌群失衡与降低γ-氨基丁酸(GABA)的水平联系在一起,GABA是一种可以缓解焦虑的大脑化学物质。大脑和肠道可能通过迷走神经进行交流,迷走神经是一条遍及全身的大神经。
肠道微生物群和神经系统疾病详见之前的文章:最新研究速递 | 柳叶刀:肠道微生物群在神经系统疾病中的作用
2019年发表在《自然》杂志的一项新研究:肠道微生物对于消除小鼠的恐惧反应至关重要。该研究是对肠脑轴力学的不断探索中的最新成果。
他们发现了一组代谢产物,这些代谢产物影响大脑处理恐惧的方式。特别是,科学家们正在研究小鼠用了多长时间才能克服习得的恐惧反应。
在发出信号后,立即对这些小鼠进行小小的足部电击。学会了这种联想之后,每当听到信号时,他们都会陷入恐惧中。它们的大脑已经将听到信号的神经元与那些预期电击的神经元联系起来。这种硬连线的神经联系就是巩固大脑记忆的方式。
正常和无菌小鼠都能学会恐惧关联,但Artis和同事发现,无菌小鼠不能忘记恐惧。只要它们保持无菌,在听到信号时总是会冻僵。
如果研究人员再给无菌老鼠一些健康的微生物,他们就可以忘记这种关联,恐惧反应很快消失了。并且直到小鼠达到一定年龄才起作用。此后,即使肠道菌群好,他们也总是对这种音调做出反应。
研究人员排除了迷走神经和免疫系统的作用。相反,他们发现这种作用与四种特定的代谢产物密切相关。在正常生殖的小鼠中,这些代谢物从肠道到达大脑,并促进记忆形成和随后的遗忘。如果没有那些细菌来提供代谢产物,无菌小鼠似乎注定会永远对的音调做出反应。
研究人员已经知道,精神分裂症和肠道生物群系之间已有数年的联系。可惜他们一直无法完全理解两者之间为什么或如何相关。
一项新研究由多名中国研究人员与位于锡拉丘兹的纽约州立大学医学院研究团队共同发表的论文可能提供了一些答案。
该小组招募了63名严重程度不同的精神分裂症患者和69名健康对照者。两组的性别组成,平均年龄和平均体重指数相似。
然后,研究人员从这些组中收集了样本,并通过测序评估了每个受试者肠道微生物群。他们测试了两组之间的差异,以及可能将患者精神分裂症症状的严重程度与肠道生物群系内特定失衡联系起来的差异。
研究小组在2019年2月版的《科学进展》上撰文称,“发现两组动物肠道微生物组成存在明显差异”,两组细菌群落在门或类水平上存在差异。
此外,他们发现“全球微生物表型并没有受到性别或药物状况的很大影响。” 换句话说,与健康对照的肠道生物群系相比,精神分裂症受试者的肠道生物群具有一些特定菌群丰度增加,而其他特定菌群缺乏。
研究人员还发现,精神分裂症患者的肠道菌群失调与重度抑郁症患者不同,并且存在明显的微生物标志物,与症状严重程度密切相关。他们甚至可以非常准确地确定生物群样本是否来自精神分裂症受试者或对照受试者。
为了进一步证明肠道生物群对受试者的精神状态的影响,研究人员随后将精神分裂症受试者的肠道微生物样本转移到一组健康对照小鼠的肠道生物群中。然后,他们将这些先前健康的对照小鼠的行为与一组一直健康的对照小鼠的行为进行了比较。
令人惊讶的是,研究人员发现,将精神分裂症患者的肠道细菌移植到健康对照小鼠中会诱发某些鼠类精神分裂症的症状。这意味着研究人员仅使用精神分裂症受试者的肠道细菌就能将精神分裂症的症状转移至小鼠。
正如论文作者所写,这项研究提供了开创性的证据,表明精神分裂症与肠道菌群组成的变化有关,这种变化既与精神分裂症有关,又与其症状严重程度相关。
该研究不仅在精神分裂症和肠道生物群之间建立了明确的联系,还进一步证明了许多精神障碍是系统性问题,如果没有更全面的视野,就无法正确治疗。
压 力
一些研究表明慢性和暂时性压力均可影响肠道菌群的分布。同样,啮齿动物的研究表明子宫内的压力和母体分离会破坏肠道菌群的平衡,对心理健康产生连锁反应。
自然分娩和母乳喂养
其他研究表明暴露于母体微生物对后代健康多样的肠道发育很重要。这可以通过阴道分娩,皮肤接触和母乳喂养来实现。
漏 肠
有人提出,不健康饮食,酒精和其他因素引起的微生物群变化可使肠道内膜或上皮更易渗透。肠道上皮是一种壁或屏障,旨在防止有害菌产生的有害物质循环进入体内。当肠道变得“渗漏”时,由于炎症细胞因子的产生增加,可能会发生慢性炎症。在许多抑郁症患者中也发现了慢性炎症,这可能部分解释了抑郁症和心脏病之间的联系。
纤 维
为了使食物的口感更符合现代人的需求,很多食物在加工过程中被剥去了纤维,然而对人体有用的许多微生物都依赖纤维。
所谓垃圾食品的真正问题在于,它会使你体内的有益菌饥饿。纤维存在于洋葱,朝鲜蓟,芦笋和许多绿叶蔬菜中。地中海饮食强调这些食物,是值得效仿的典范。

抗 生 素
避免使用抗生素。这些虽然是挽救生命的药物,但是它们带来的副作用是杀死肠道微生物。请谨慎使用。
关于肠脑轴的新兴研究已经产生了关于精神疾病可能病因的新见解。而且,这一研究领域在诊断和治疗方面都具有很大的希望和潜力。如果炎症是与压力相关的抑郁症的核心,那么疗法如何起作用?
神奇的是,诸如认知行为疗法之类的治疗实际上可以降低促炎化学物质的水平。
抗抑郁药的发展引发了精神病学的巨大革命,它们是如何发挥作用呢?
最早的理论之一是它们“填补”了大脑中的神经递质。据认为,5-羟色胺在患有抑郁症的人中很少,因此任何可以增加其在大脑中水平的药物都是有益的。
选择性5-羟色胺再摄取抑制剂(SSRIs)可以使5-羟色胺在大脑中循环,因此可以做到这一点。但是,鉴于SSRI还可以减轻大脑炎症,因此可能需要对该机制进行一些重新解释。
免疫系统异常复杂,我们对此了解甚少,但最近的研究表明,它与抑郁症紧密相关,减轻炎症可以减轻抑郁症。
例如,益生菌可以提供健康的肠道细菌,而抗生素可以破坏有害的肠道细菌。同样,粪便微生物移植可用于将健康和多样的肠道细菌转移给缺乏的细菌。人们开始推测这些可以用于治疗精神疾病。
01
益 生 菌
益生菌已在动物研究中显示出减少炎症细胞因子的作用。发表在《英国营养杂志》上的一项研究描述了一项针对30名患有抑郁症志愿者的试验。
每天给这些沮丧的志愿者补充益生菌补充剂,其中包括乳酸杆菌和双歧杆菌细菌。在试验结束时,他们“显着”减轻了心理困扰的症状,包括抑郁和焦虑。
除补充剂外,酸奶和咸菜等发酵食品还含有益生菌。
02
Omega-3 补充剂
一些研究表明,omega-3补充剂可以有益地影响肠道菌群的组成并增加抗炎化合物(包括脂肪酸)的产生。
肠道微生物,脂肪酸和免疫力可以共同发挥作用,以维持肠道壁的完整性并减少肠道渗漏。
omega-3补充剂可以帮助某些类型的抑郁症。
Omega-3的天然来源包括鱼类,尤其是高脂肪鱼类,例如鲑鱼,沙丁鱼和鲭鱼。
03
益 生 元
如果饮食中不能摄取足够的纤维,那么益生元也会起到类似的作用。这些是人体无法消化的复杂糖,但是肠道微生物可以消化。
04
运 动
要知道久坐对肠和肠道微生物并不友好。如果运动是一种药物,那将价值数百万。目前尚不清楚具体作用机制,但是运动可以提高微生物群的质量。

05
规 律 饮 食
古人云:日出而作,日落而息。
这句话同样适用于你的微生物群,它也具有昼夜节律。如果这两个节奏相互同步,那么生活就是美好的事物。跟着大自然的昼夜节律,对于微生物而言也是非常舒适的节奏。
总而言之,沮丧可能源于悲伤,失落或糟糕的生活。但是它也可能是您的微生物群引起或加剧的,这意味着我们每个人都有机会摆脱困境。善待肠道微生物,你会发现自己的心情可以有所改善。
应当指出,关于精神疾病和肠脑轴的大多数研究都是在啮齿动物上进行的,加利福尼亚大学专家克莱尔·马丁及其同事正确地指出“因果关系的证据仍然很少”。
的确,缺乏双盲随机纵向研究来研究益生菌,抗生素或粪便微生物移植对精神疾病康复的影响。同样,反向因果关系的问题也没有得到充分解决。
例如,与精神疾病相关的生活方式因素和药物的副作用可能导致肠道菌群紊乱和失衡。换句话说,微生物群分布的变化可能是精神疾病的结果,不一定是原因。
但是不管是结果还是原因,精准的了解特定的肠道微生物及其特征与特定的精神疾病之间的关系可能有助于精神病患者的诊断和靶向治疗和个性化治疗有帮助。
相关阅读:
肠道微生物组如何影响运动能力,所谓的“精英肠道微生物组”真的存在吗?
参考文献
Brachman, Rebecca A., Michael L. Lehmann, Dragan Maric, and Miles Herkenham. “Lymphocytes from Chronically Stressed Mice Confer Antidepressant-Like Effects to Naive Mice.” The Journal of Neuroscience 35, no. 4 (January 28, 2015): 1530–38.
Pereira, Joana da Cruz, Kieran Rea, Yvonne M. Nolan, Olivia F. O’Leary, Timothy G. Dinan, and John F. Cryan. “Depression’s Unholy Trinity: Dysregulated Stress, Immunity, and the Microbiome.” Annual Review of Psychology 71, no. 1 (2020)
The Gut-Brain Axis: The Missing Link in Depression. Evrensel A, Ceylan ME.Clin Psychopharmacol Neurosci. 2015 Dec 31;13(3):239-44. doi: 10.9758/cpn.2015.13.3.239.
Fulling, C., Dinan, T.G., & Cryan, J.F. (2019 Mar 20). Gut microbe to brain signaling: what happens in vagus… Neuron. 101(6): 998-1002.
Scott C. Anderson, Stress, Inflammation, and Microbes: A Moody Trinity,2019, Nov, 30
Del Grande da Silva, Giovanna, Carolina David Wiener, Luana Porto Barbosa, Jaciana Marlova Gonçalves Araujo, Mariane Lopez Molina, Pedro San Martin, Jean Pierre Oses, Karen Jansen, Luciano Dias de Mattos Souza, and Ricardo Azevedo da Silva. “Pro-Inflammatory Cytokines and Psychotherapy in Depression: Results from a Randomized Clinical Trial.” Journal of Psychiatric Research 75 (April 2016): 57–64.
Martina Sgritta, Sean W. Dooling, Shelly A. Buffington, Eric N. Momin, Michael B. Francis, Robert A. Britton, Mauro Costa-Mattioli. “Mechanisms Underlying Microbial-Mediated Changes in Social Behavior in Mouse Models of Autism Spectrum Disorder.” Neuron (First published online: December 3, 2018) DOI: 10.1016/j.neuron.2018.11.018
Pan, Ying, Xu-Yang Chen, Qing-Yu Zhang, and Ling-Dong Kong. “Microglial NLRP3 Inflammasome Activation Mediates IL-1β-Related Inflammation in Prefrontal Cortex of Depressive Rats.” Brain, Behavior, and Immunity 41 (October 2014): 90–100.
Jacka, Felice N., Adrienne O’Neil, Rachelle Opie, Catherine Itsiopoulos, Sue Cotton, Mohammedreza Mohebbi, David Castle, et al. “A Randomised Controlled Trial of Dietary Improvement for Adults with Major Depression (the ‘SMILES’ Trial).” BMC Medicine 15, no. 1 (January 30, 2017): 23.
Melanie Greenberg. Feeling Depressed? Gut-Brain Dysfunction May Be to Blame, 2018, Dec 30,
Karen-Anne McVey Neufeld, John Bienenstock, Aadil Bharwani, Kevin Champagne-Jorgensen, YuKang Mao, Christine West, Yunpeng Liu, Michael G. Surette, Wolfgang Kunze & Paul Forsythe. “Oral Selective Serotonin Reuptake Inhibitors Activate Vagus Nerve Dependent Gut-Brain Signalling.” Scientific Reports (First published: October 3, 2019) DOI: 10.1038/s41598-019-50807-8
Christopher Bergland. The Vagus Nerve May Carry Serotonin Along the Gut-Brain Axis, 2019, Oct 06
Christopher Bergland. Vagus Nerve Stimulation Dramatically Reduces Inflammation. 2016, Jul 06,
Sudo, Nobuyuki, Yoichi Chida, Yuji Aiba, Junko Sonoda, Naomi Oyama, Xiao-Nian Yu, Chiharu Kubo, and Yasuhiro Koga. “Postnatal Microbial Colonization Programs the Hypothalamic-Pituitary-Adrenal System for Stress Response in Mice.” The Journal of Physiology 558, no. Pt 1 (July 1, 2004): 263–75.
Dinan, Timothy G., Catherine Stanton, and John F. Cryan. “Psychobiotics: A Novel Class of Psychotropic.” Biological Psychiatry 74, no. 10 (November 15, 2013): 720–26.
Bravo, Javier A., Paul Forsythe, Marianne V. Chew, Emily Escaravage, Hélène M. Savignac, Timothy G. Dinan, John Bienenstock, and John F. Cryan. “Ingestion of Lactobacillus Strain Regulates Emotional Behavior and Central GABA Receptor Expression in a Mouse via the Vagus Nerve.” Proceedings of the National Academy of Sciences 108, no. 38 (September 20, 2011): 16050–55.
Chu, Coco, Mitchell H. Murdock, Deqiang Jing, Tae Hyung Won, Hattie Chung, Adam M. Kressel, Tea Tsaava, et al. “The Microbiota Regulate Neuronal Function and Fear Extinction Learning.” Nature 574, no. 7779 (October 2019): 543–48.
Samoon Ahmad. Schizophrenia and the Gut. 2019, Mar 05,
Xu C, Lee SK, Zhang D, Frenette PS. The Gut Microbiome Regulates Psychological-Stress-Induced Inflammation [published online ahead of print, 2020 Jul 24]. Immunity. 2020;S1074-7613(20)30280-6. doi:10.1016/j.immuni.2020.06.025
VanElzakker, Michael B., M. Kathryn Dahlgren, F. Caroline Davis, Stacey Dubois, and Lisa M. Shin. “From Pavlov to PTSD: The Extinction of Conditioned Fear in Rodents, Humans, and Anxiety Disorders.” Neurobiology of Learning and Memory 113 (September 2014): 3–18.
Scott C. Anderson,Unending Fear and the Gut-Brain Axis,2019,Oct 24
欢迎关注: 谷禾健康
——让你和你的家人更健康


本文由谷禾健康整理编译自:VIOME TEAM, 2020 Gut Microbiome Health and Cellular Health are the Keys to Optimizing Physical Performance AND How Athletic Performance is affected by your Gut Microbiome, Cellular, and Mitochondrial Health.
想象一下如果有一天,您可以模仿最优秀的运动员的微生物组和细胞健康状况,从而可以跑得更快,跳得更高,也就是说可以提高自己的运动能力。是不是感觉很神奇?

每个人身上都充满了微生物,而运动员身上的微生物可以为他们的比赛提供优势。
这要从肠道微生物组开始说起。我们都知道,每个人都有数万亿种细菌,病毒和真菌,它们生活在人体的多个微生物生态系统中,称为微生物组。
对于运动员来说,肠道微生物在他们的表现和恢复速度方面起着更加重要的作用。

肠道微生物负责帮助我们的身体分解碳水化合物,纤维,蛋白质,调节能量[1]。这些微生物影响身体的炎症反应,压力适应力,神经功能,甚至影响精神力量,所有这些对于运动都很重要[2]。
设想如果你的细胞健康状况不佳或不佳,这可能意味着您的细胞功能无法有效发挥,能量产生低下或细胞由于氧化应激,炎症或环境毒素而处于应激状态。

基因组和转录组测序技术的发展以及人工智能处理围绕能量调节和运动恢复的大量数据的能力使研究人员探索了以下问题:
“微生物组分析可以帮助我们预测下一位伟大的运动员吗?”
“将来,我们能否从精英运动员身上收获微生物,并将高性能的微生物能力传递给其他人?”
“食物和营养会通过在细胞乃至线粒体水平上积极影响他们的身体,从而影响运动员的恢复能力,增强免疫力以帮助他们训练和比赛吗?”
“基于性能的益生菌和益生菌会被广泛使用吗?”
尽管没有人能预测未来,但探索这些问题的过程会带来许多可能性。
哈佛大学的研究人员发现“精英肠道菌群”
运动表现,恢复能力,甚至运动员从事的运动类型都与特定的微生物有关。现在,这些发现促使研究人员寻找增加肠道中有益细菌的多样性和丰富度的方法,以获得更好的运动能力和更快的恢复能力。
在一项研究中,哈佛大学的研究人员从波士顿马拉松比赛训练的运动员的肠道微生物样本中取样。研究人员在马拉松比赛后再次对参与者进行了测试,发现人体分解乳酸所需的一种细菌数量激增。这些科学家认为,这种特定细菌的增加是对体内乳酸水平升高的一种反应,因为它是它们的主要食物来源[3]。
他们的发现引出了一个问题:这种细菌将来是否可以用于降低体内乳酸水平并可能加快恢复时间?

在另一项研究中,哈佛大学的科学家将赛艇运动员的肠道微生物组与超级马拉松运动员进行了比较,发现其组成存在明显差异,这表明特定的运动可能会促进特定的微生物生态系统[2]。
这些研究的发现,不仅使公司寻求创造基于性能的益生菌和益生菌,更是促使一些科学家们相信,将来他们将能够挖掘精英运动员的微生物组来帮助他人。
看到这里,或许你会有这样的疑问,微生物组是如何准确地影响运动能力?以下是微生物组影响运动表现的九种方式:
01 减 少 炎 症
肠道微生物组在炎症中起着重要作用:升高或降低炎症水平。炎症会干扰运动表现,减慢恢复速度,并且是许多慢性疾病的根本原因。
肠道微生物组失衡或营养不良与炎性疾病相关(我们前面的文章有阐述过:炎症性肠病中宿主与微生物群的相互作用),因此保持健康的微生物组有助于减少全身炎症至关重要[6]。
此外,现在可以更容易地看到人体细胞的炎症水平,这可能是由肠道微生物群和环境因素(病原体、压力、运动等)共同触发的。
02 提 高 能 量 水 平
当肠道微生物组保持平衡和健康时,它可以帮助提高能量水平,并且线粒体可以调节和产生细胞能量,因此,对人体和微生物健康都至关重要。通过以下方式,可以转化为更好的性能:
通过更好的乳酸分解来减轻疲劳[7]
控制氧化还原功能,可以延迟疲劳症状[8]
增加ATP水平,你的分子能量[9]
调节新陈代谢[4]
向线粒体提供必需的代谢产物–细胞的动力源[9]
调节能量的收集,存储和消耗[4]
03 增 强 精 神 力 量
这个听起来有点不可思议,其实我们的肠道微生物会沿着迷走神经与大脑对话。肠道微生物在心理健康状况中起着重要作用。
肠道微生物失衡,则可能导致精神疾病。肠道失衡或营养不良甚至与焦虑和抑郁有关(我们前面的文章有阐述过:深度解读 | 肠道菌群和中枢神经系统的关系)。肠脑轴是塑造精神力量中看不见的手,对于那些承受不起压力的职业运动员来说,这是必不可少的。
04 塑 造 理 想 的 身 体 成 分
肠道微生物组有助于身体更有效地运转。平衡的肠道会影响以下方面,因此通常更容易健康:
身体成分
白色与棕色脂肪
膳食对血糖的反应
05 强 健 骨 骼
微生物组通过激素和免疫系统调节帮助建立骨骼质量和强度。均衡的肠道菌群也可以增加钙和镁的矿物质吸收。在运动相关的创伤中,功能正常的微生物组可以加速骨骼愈合[11]。

06 帮 助 营 养 吸 收 和 使 用
平衡的微生物组对于更好地吸收和使用营养至关重要。如果您的肠道微生物组有炎症且不平衡,则微生物是为了努力存活下来,而不是提取必需的维生素,蛋白质和酶。
此外,肠道菌群还通过将消化道无法加工的食物转化为生存所需的营养来提供营养[12]。为了使运动员在巅峰时期表现出色,他们需要拥有蓬勃发展的肠道微生物群。
07 提 升 水 合 状 态
肠道微生物组与运动过程中适当的水分调节有关,这意味着人体可以更有效地利用水。另外,肠内膜的完整性是适当水合作用的关键因素,健康的肠道微生物组也有助于维持水分[13]。
08 改 善 睡 眠
肠道微生物组失衡(功能失调)与睡眠质量差和认知灵活性降低有关,因为肠道微生物组控制着各种激素(例如皮质醇,5-羟色胺和GABA)的水平,所有这些激素都会影响睡眠质量[14]。微生物群还影响褪黑素的产生,这对于适当的睡眠-觉醒周期是必不可少的[15]。

高质量的睡眠、良好的肠道健康、能量水平和表现都存在于一个强化循环中,这些循环既可以相互促进,也可以拖累你。运动员知道他们需要适当的睡眠才能表现良好。但是,许多人可能没有意识到,有一种促进睡眠神经递质的药是在自己的肠道内产生的。
09 抗 氧 化 防 御 系 统
人体内有一个强大的系统,称为抗氧化防御系统,即氧化还原信号,它使用抗氧化酶使您保持健康。运动员需要这套系统处于良好的工作状态,才能始终保持出色的表现并保持比赛的最高水准。

健康的氧化还原状态与均衡的肠道微生物组有关。这个肠道微生物组调节的抗氧化酶系统[8,16]:
防止运动引起的组织损伤
防止剧烈运动引起的氧化损伤
与运动员的身体状况有关
减轻身体疲劳
改善运动表现
通常,密集和持续的运动训练以及高水平的竞争会产生大量的自由基,这些自由基可能超过典型人体的能力。这使运动员容易受到氧化应激的影响,并更有可能累积有害的炎症。
肠道微生物组学和人类细胞科学的未来是性能科学的未来
健康饮食(多样性饮食)是一个很好的开始。你可以通过饮食把你的运动表现提升到一个新的水平,特别是支持属于你独特的微生物群和身体的饮食。
谷禾健康肠道菌群健康检测服务结合了高通量测序技术,大数据和人工智能,可以帮助您了解健康的独特需求以及独特的食物并补充建议。帮助您微调肠道微生物组的功能,以最大程度地减少有害代谢物的产生并最大化有益代谢物的产生。
参考文献
1. Blaser MJ. The microbiome revolution. J Clin Invest. 2014;124(10):4162-4165. doi:10.1172/JCI78366
2. Christopher Bergland Does Gut Microbiome Influence Mindset and Mental Toughness?Harvard researchers link specific gut microbiota with peak athletic performance. 2017
3. Torrice M. A Conversation with Jonathan Scheiman. ACS Cent Sci. 2017;3(10):1057-1058. doi:10.1021/acscentsci.7b00470
4. Monda V, Villano I, Messina A, et al. Exercise Modifies the Gut Microbiota with Positive Health Effects. Oxid Med Cell Longev. 2017;2017:3831972. doi:10.1155/2017/3831972
5. Endurance exercise and gut microbiota: A review.Author links open overlay panelNúriaMachabDolorsFuster-Botellaa June 2017, Pages 179-197
6. Clemente JC, Manasson J, Scher JU. The role of the gut microbiome in systemic inflammatory disease. 2018 BMJ ;360:j5145
7. Pessione E. Lactic acid bacteria contribution to gut microbiota complexity: lights and shadows. Front Cell Infect Microbiol. 2012;2:86. Published 2012 Jun 22. doi:10.3389/fcimb.2012.00086
8. Neish AS. Redox signaling mediated by the gut microbiota. Free Radic Res. 2013;47(11):950-957. doi:10.3109/10715762.2013.833331
9. Clark A, Mach N. The Crosstalk between the Gut Microbiota and Mitochondria during Exercise. Front Physiol. 2017;8:319. Published 2017 May 19. doi:10.3389/fphys.2017.00319
10. Davis CD. The Gut Microbiome and Its Role in Obesity. Nutr Today. 2016;51(4):167-174. doi:10.1097/NT.0000000000000167
11. Xu X, Jia X, Mo L, et al. Intestinal microbiota: a potential target for the treatment of postmenopausal osteoporosis. Bone Res. 2017;5:17046. Published 2017 Oct 4. doi:10.1038/boneres.2017.46
12. Krajmalnik-Brown R, Ilhan ZE, Kang DW, DiBaise JK. Effects of gut microbes on nutrient absorption and energy regulation. Nutr Clin Pract. 2012;27(2):201-214. doi:10.1177/0884533611436116
13. Colgan SP. Swimming through the gut: implications of fluid transport on the microbiome. Dig Dis Sci. 2013;58(3):602-603. doi:10.1007/s10620-013-2575-3
14. Galland L. The gut microbiome and the brain. J Med Food. 2014;17(12):1261-1272. doi:10.1089/jmf.2014.7000
15. Anderson JR, Carroll I, Azcarate-Peril MA, et al. A preliminary examination of gut microbiota, sleep, and cognitive flexibility in healthy older adults. Sleep Med. 2017;38:104-107. doi:10.1016/j.sleep.2017.07.018
16. Neish AS. Redox signaling mediated by the gut microbiota. Free Radic Res. 2013;47(11):950-957. doi:10.3109/10715762.2013.833331

谷禾健康
高脂饮食会诱发肥胖、胰岛素抵抗、葡萄糖耐受不良和脂肪变性,而脂肪性肝炎向纤维化和肝细胞癌(HCC)的进展主要与高膳食胆固醇有关。非酒精性脂肪性肝病(NAFLD)是一类代谢疾病,可从脂肪肝进展至脂肪性肝炎,进一步导致肝硬化甚至肝细胞癌(HCC),胆固醇被认为是疾病发展过程中主要的脂毒性分子。
近日,香港中文大学于君团队及其团队研究人员在《Gut》上发表了题为“Dietary cholesterol drives fatty liver- associated liver cancer by modulating gut microbiota and metabolites(膳食胆固醇通过调节肠道微生物群和代谢产物驱动脂肪肝相关的肝癌,DOI:10.1136/gutjnl-2019-319664)”的研究论文,阐述了膳食胆固醇在NAFLD–HCC发生中的作用及其相关的分子机制。这项研究证明了长时间的高胆固醇饮食可以引起小鼠自发性NAFLD-HCC(非酒精性脂肪肝肝细胞癌)。抑制胆固醇可以恢复肠道微生物群,完全阻止NAFLD-HCC的发展。

背景
非酒精性脂肪性肝病(NAFLD)是代谢综合征的肝脏表现,包括从单纯性脂肪变性到非酒精性脂肪性肝炎(NASH)的一系列肝脏病理。NASH可进展为肝硬化、终末期肝功能衰竭和肝细胞癌(HCC)。目前,非酒精性脂肪肝是世界范围内发病率和医疗负担的主要原因。脂肪毒性会导致NASH、纤维化/肝硬化,甚至HCC。在肝脏脂质种类中,胆固醇被认为是NASH发生过程中的主要脂毒分子。肝脏是调节全身胆固醇稳态的中心。膳食胆固醇对血浆和肝脏胆固醇稳态有重要影响。虽然膳食胆固醇在NASH进展中的作用已被论述,但长期胆固醇治疗在自发性和进行性NAFLD-HCC发展的作用和致病基础尚不清楚。一些研究表明,肠道菌群是一个有助于NAFLD发生和其发展为NAFLD-HCC的环境因素。微生物衍生的代谢物,如胆汁酸、短链脂肪酸和三甲胺和它们影响的信号通路可能有助于NAFLD的发展。特别是肠道菌群代谢产物3 -(4 -羟苯基)乳酸,对肝脏脂肪变性和肝纤维化具有共同的基因效应。
实验设计
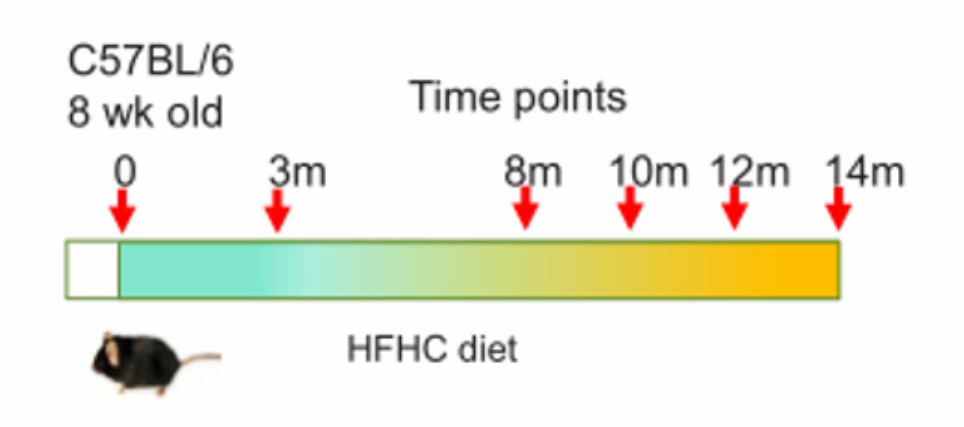
普通饲料(NC,18%脂肪,58%碳水化合物,24%蛋白质,0%胆固醇);高脂/低胆固醇饲料(HFLC,43.7%脂肪,36.6%碳水化合物,19.7%蛋白质,0.013%胆固醇);高脂/高胆固醇饲料(HFHC,43.7%脂肪,36.6%碳水化合物,19.7%蛋白质,0.203%胆固醇)
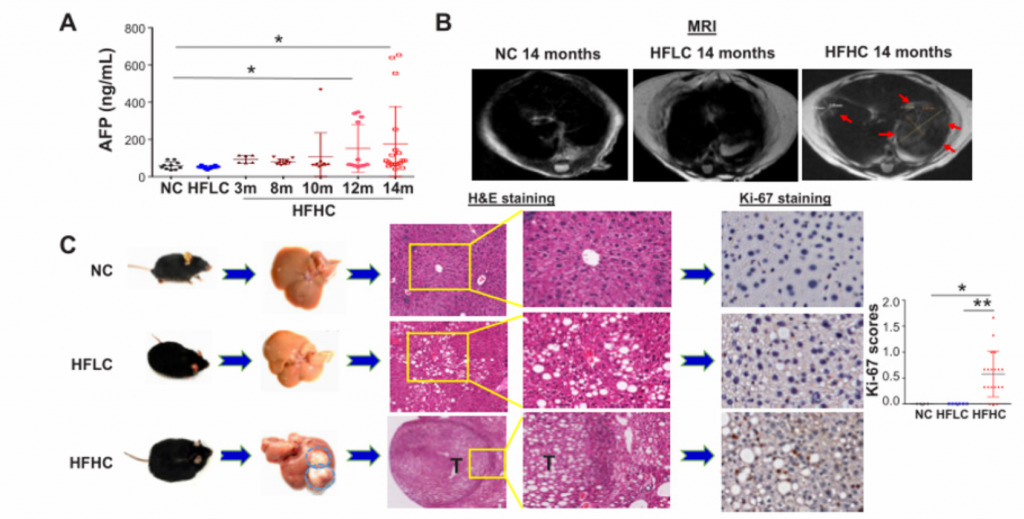

如图所示,以上饲料用于随机喂养8周龄雄性C57BL/6野生型同窝出生幼鼠14个月。阿托伐他汀(降胆固醇药)药物被用于喂食HFHC膳食7个月后的小鼠,持续7个月。然后分别在3、8、10和12个月龄处死。
粪移植实验:
取被喂养不同饲料的小鼠的1 g粪便样品用5ml磷酸盐缓冲生理盐水(PBS)混匀,然后将该混悬液2 0 0μL灌胃移植给无菌小鼠。于移植后8、10、14个月各组中随机抽取小鼠处死。
实验结束时,小鼠被禁食,取血清/组织。记录体重和内脏脂肪重量。肝脏被迅速切除并称重,评估表面结节的存在和大小。分离肝肿瘤,在液氮中快速冷冻,并将其保存在−80°C进行进一步实验。肠道菌群分析采用16SrRNA测序,血清代谢物分析采用液相色谱-质谱(LC-MS)代谢组学分析。
主要结果
1. 膳食胆固醇可自发驱动NAFLD-HCC的发生。


A)[endif]喂养HFHC饲料的小鼠在第3、8、10、12、14个月检测的血清AFP水平以及喂养NC和HFLC饲料的小鼠在第14个月检测的血清AFP水平。在第10个月观察到AFP水平升高,在第12个月和14个月,与HFLC或NC饲料喂养的小鼠相比,HFHC饲料喂养的小鼠的AFP水平逐渐升高。
B) [endif]肝脏MRI影像。在第14个月时,喂养HFHC饲料的小鼠出现肝肿瘤,而其余两个没有
C) [endif]依次为小鼠肝脏的大体形态、镜下结构以及Ki67染色的免疫组化图像。HFHC小鼠肝脏切片组织学检查均为肝细胞癌,平均每只小鼠肝细胞癌细胞数为2.7±2.6,最大直径为4.1±5.0 mm。与HFLC喂养的小鼠相比,HFHC喂养的小鼠肝脏切片中Ki-67阳性细胞明显增多,表明HFHC喂养的小鼠细胞增殖增加。
D) [endif]依次为体重,内脏脂肪,肝脏重量,肝脏与体重的比率。随着肝癌的形成,喂养HFHC饲料的小鼠的这些指标的水平显著高于喂养NC饲料的小鼠。同时,喂养HFLC饲料的小鼠也表现出这些指标水平的上升。
E) [endif]依次为血清胆固醇、肝游离胆固醇、肝胆固醇酯含量、糖耐量试验及空腹胰岛素水平。与HFLC和NC相比,HFHC小鼠的这些指标的水平都有所上升。与NC相比,HFLC小鼠的葡萄糖耐量和空腹胰岛素也有所增加。
2. 高胆固醇膳食喂养的小鼠的非肝癌肝组织形成了NASH和纤维化。


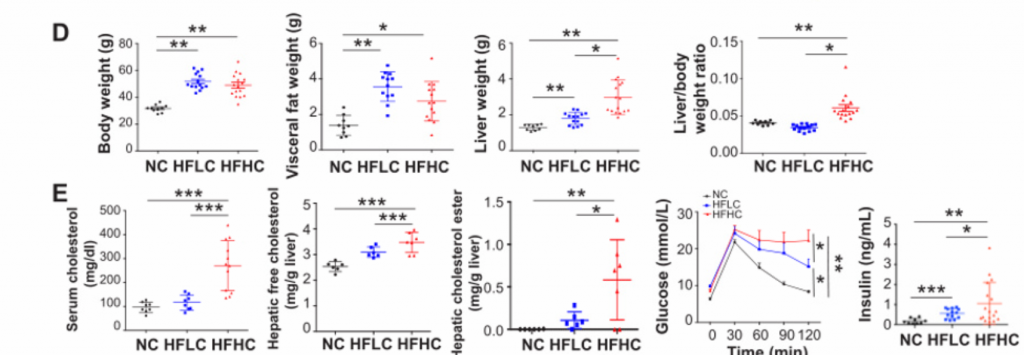
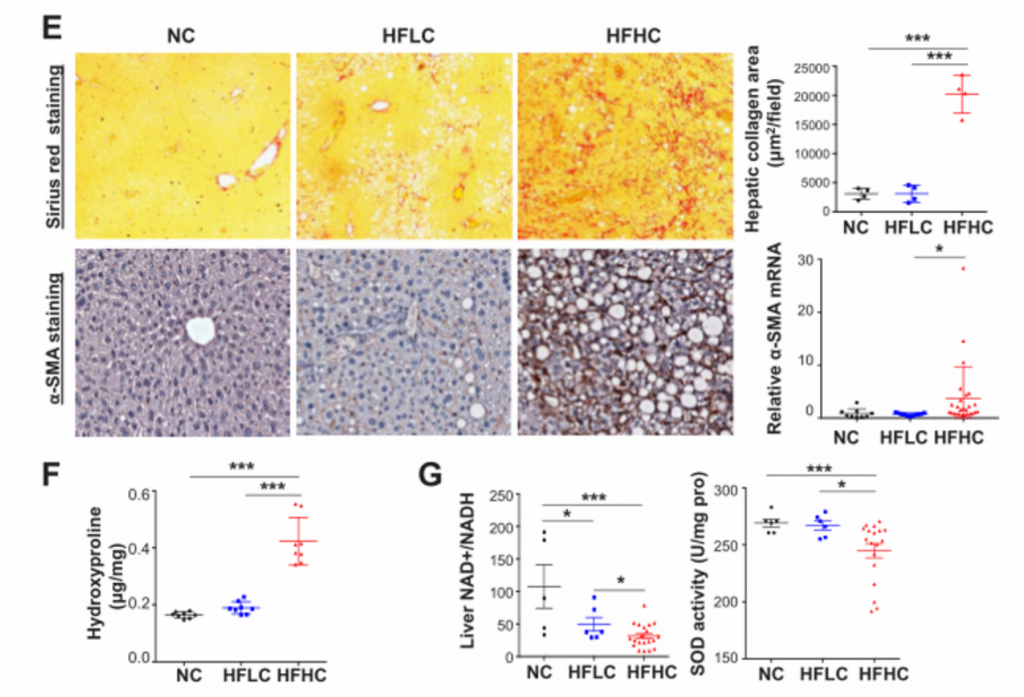
A)HE染色后的肝脏切片组织检查。HFHC小鼠出现以脂肪变性和小叶炎症为特征的脂肪性肝炎,而在HFLC小鼠中只观察到脂肪变性。
B)血清ALT和AST水平。HFHC小鼠ALT水平和AST水平显著高于HFLC和NC小鼠。
C) 细胞因子谱法测定喂养NC、HFLC和HFHC饲料的小鼠第14个月的血清IL-6、IL-1抑制因子和IL-1蛋白水平。这些指标的水平均有所上升。
D)在喂养NC、HFLC和HFHC饲料的小鼠第14个月时用ELISA法测定小鼠肝脏促炎细胞因子IL-6、IL-1α和IL-1β蛋白水平,RNA测序测定Cx3cl1、Mcp1、Cxcl10、Mip1β、Mip1α、CCL5、Cxcl16、TNFαmRNA水平。与NASH相关的促炎细胞因子Cx3cl1等在HFLC小鼠肝组织中显著上调。
E) 从上至下依次为天狼星红染色和免疫组化染色。分别观察胶原沉积和α-SmA蛋白。RT-PCR法测定mRNA表达水平。HFHC小鼠的肝组织表现出严重的纤维化损伤,胶原分布面积明显增加。肝星状细胞活化表现为α-平滑肌肌动蛋白(α-SMA)的基因和蛋白水平升高。
F) 肝羟脯氨酸含量。其在HFHC小鼠中含量明显升高。
G) 肝脏的氧化应激检测。喂养HFHC饲料的小鼠的肝脏NAD+/NADH比值和SOD活性显著降低,提示膳食胆固醇可诱导肝脏的氧化应激。
3. 高胆固醇膳食引起小鼠肝脏依次发展为脂肪肝、脂肪性肝炎、纤维化和NAFLD-HCC。
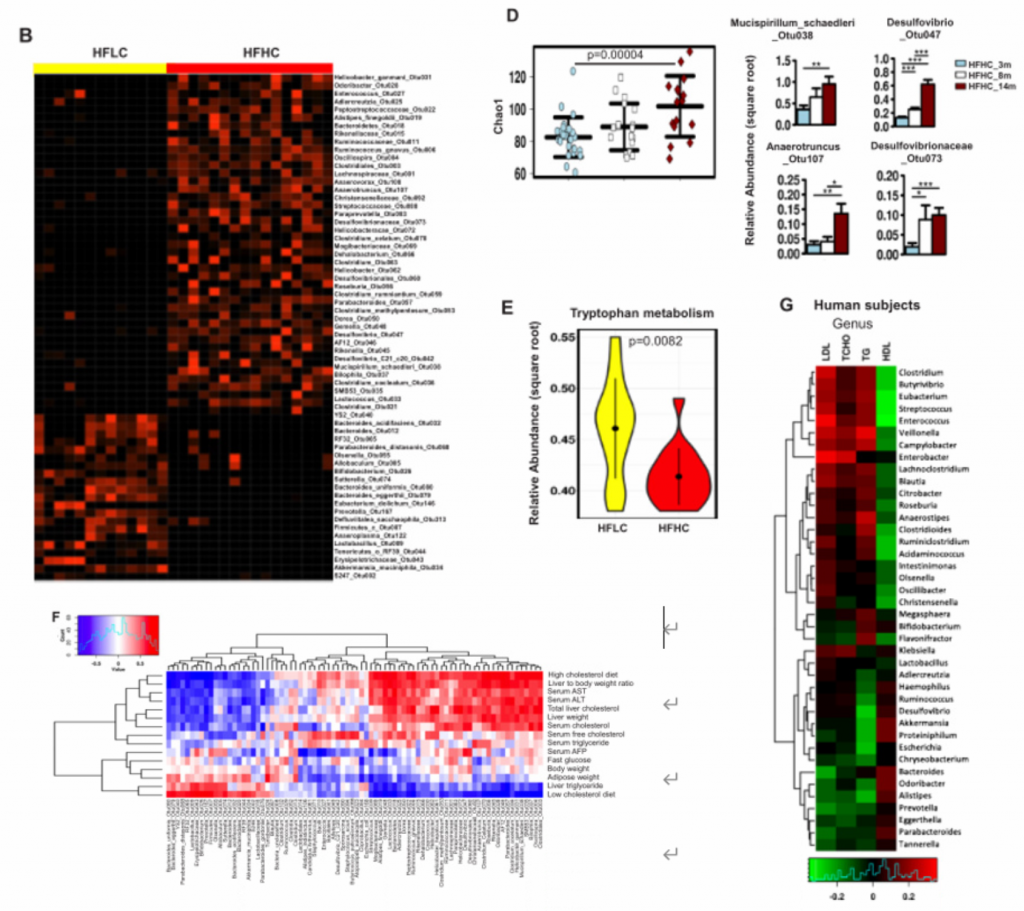


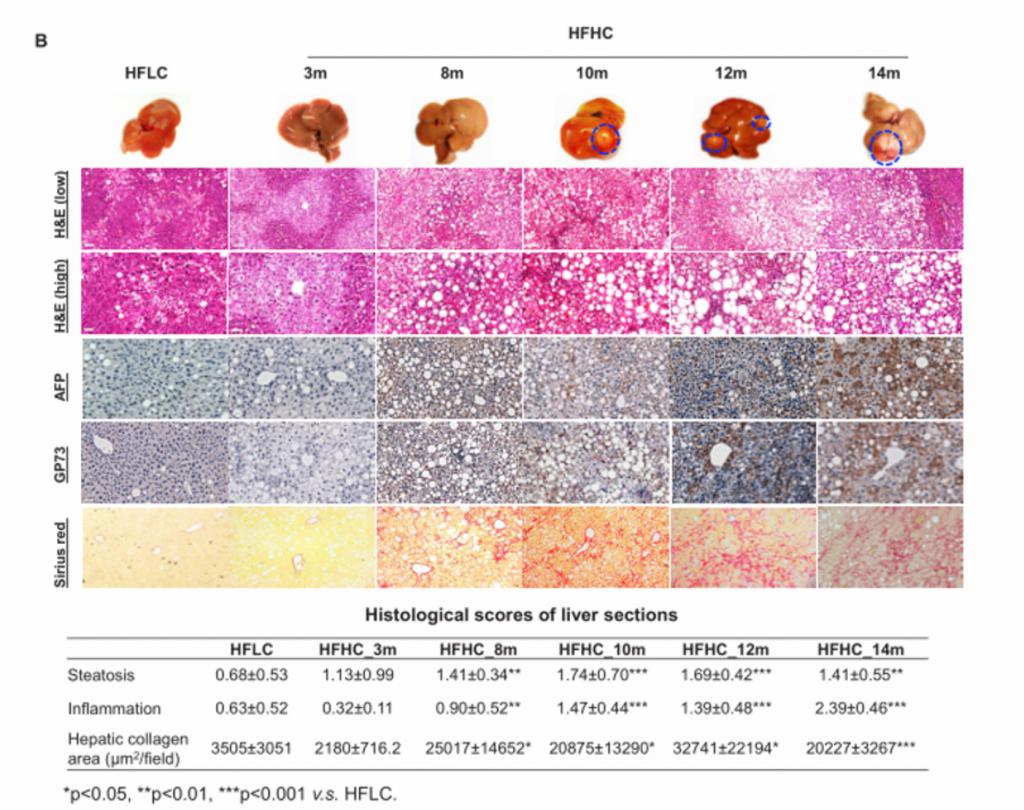
B)从上至下依次为HFLC喂养14个月和HFHC喂养3、8、10、12和14个月小鼠肝脏大体、肝脏肿瘤标志物AFP和GP73的H&E染色和免疫组化染色、天狼星红染色,脂肪变性和炎症的组织学评分以及天狼星红染色定量的肝胶原面积。HFHC小鼠肝脏组织学在3个月时表现为轻度炎症性脂肪变性,8个月时脂肪性肝炎伴纤维化,10、12、14个月时肝癌形成,而HFLC小鼠在3、8、10、14个月时仅表现为脂肪变性而没有进一步发展成肝癌。HFHC小鼠的肿瘤标志物免疫组化染色观察到阳性染色,HFLC小鼠没有。
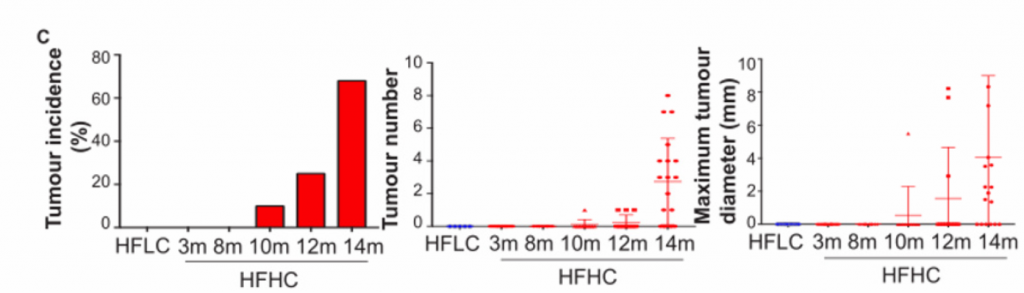
C)在HFHC膳食控制下的不同时间点的小鼠的最大肝肿瘤的肿瘤发病率、肿瘤数量和最大肿瘤直径。
4. NAFLD-HCC的肠道菌群失调与胆固醇水平相关。
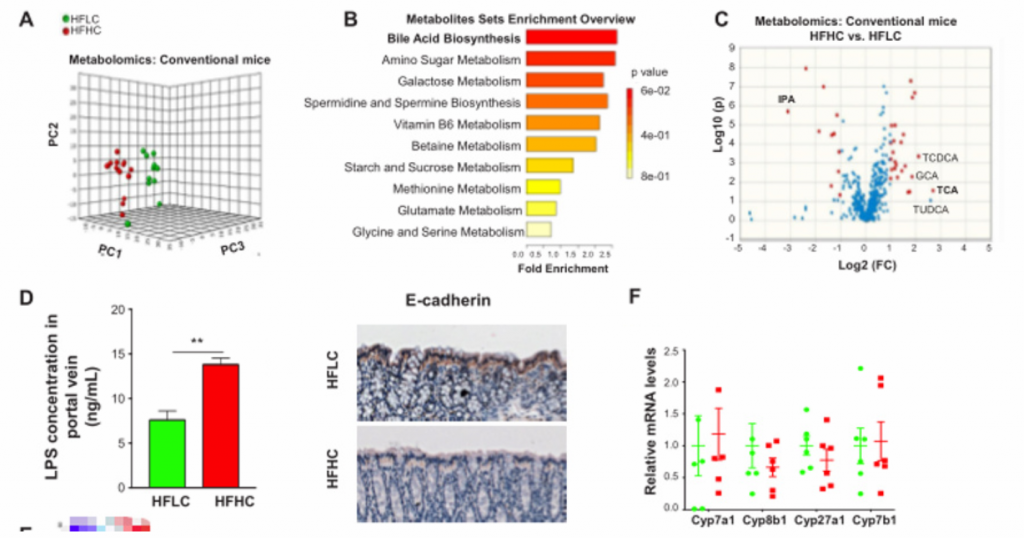
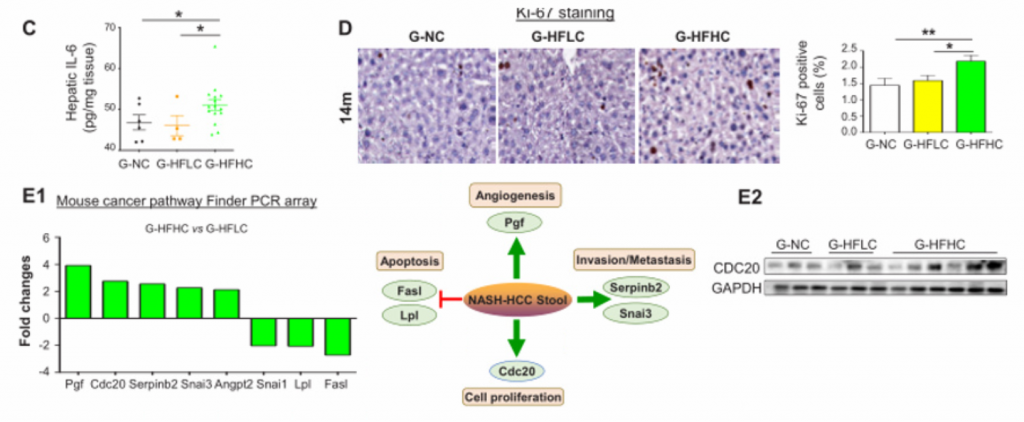






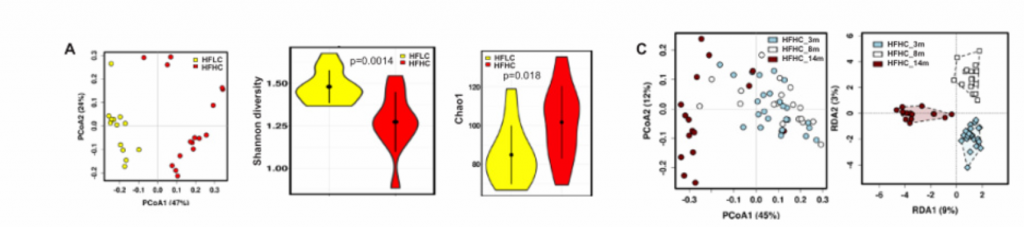
A)14月龄的HFLC和HFHC小鼠之间的肠道微生物的PCoA分析、香浓多样性和丰富度分析,PCoA分析中P<0.001. HFHC小鼠的微生物多样性更低,丰富度更高。
B)14月龄的HFLC和HFHC小鼠的粪便细菌热图。
C)HFHC膳食控制3、8和14个月后的肠道微生物的PCoA和冗余分析。发现HFHC_3m、HFHC_8m和HFHC_14m的小鼠的肠道微生物群落明显聚类,这表明肠道微生物组成随NAFLD-HCC进展阶段的变化而变化。
D)在HFHC饲养3、8 ~ 14个月,用Chao1指数测定微生物群落丰富度,发现其逐渐升高。随着NAFLD-HCC进展,细菌丰富度依次增加。
E)喂养HFLC和HFHC的小鼠肠道菌群的色氨酸代谢能力。HFHC小鼠肠道菌群的色氨酸代谢能力降低。综上,高胆固醇膳食导致肠道菌群失调和微生物色氨酸代谢受损。
F)细菌丰度与小鼠表型的相关性。
G)在59例高胆固醇血症患者和39例健康人的研究中,人血清总胆固醇、甘油三酯、低密度脂蛋白胆固醇和高密度脂蛋白胆固醇(横轴)与细菌(纵轴)基因组测序的相关性。双歧杆菌和类杆菌与血清总胆固醇、低密度脂蛋白胆固醇呈负相关,与高密度脂蛋白胆固醇呈正相关。
5. 膳食中的胆固醇通过诱导代谢产物的改变而促进NASH-HCC的进展。胆固醇通过调节宿主血清代谢物,以及至少部分通过增加TCA和降低IPA,促进了NASH-HCC的进展。

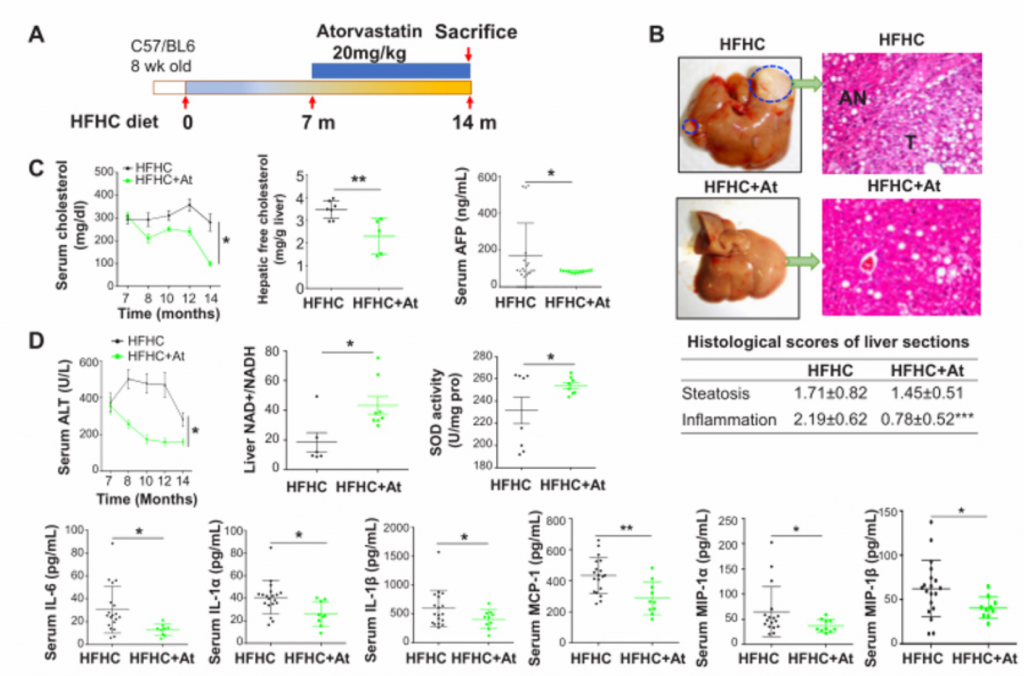
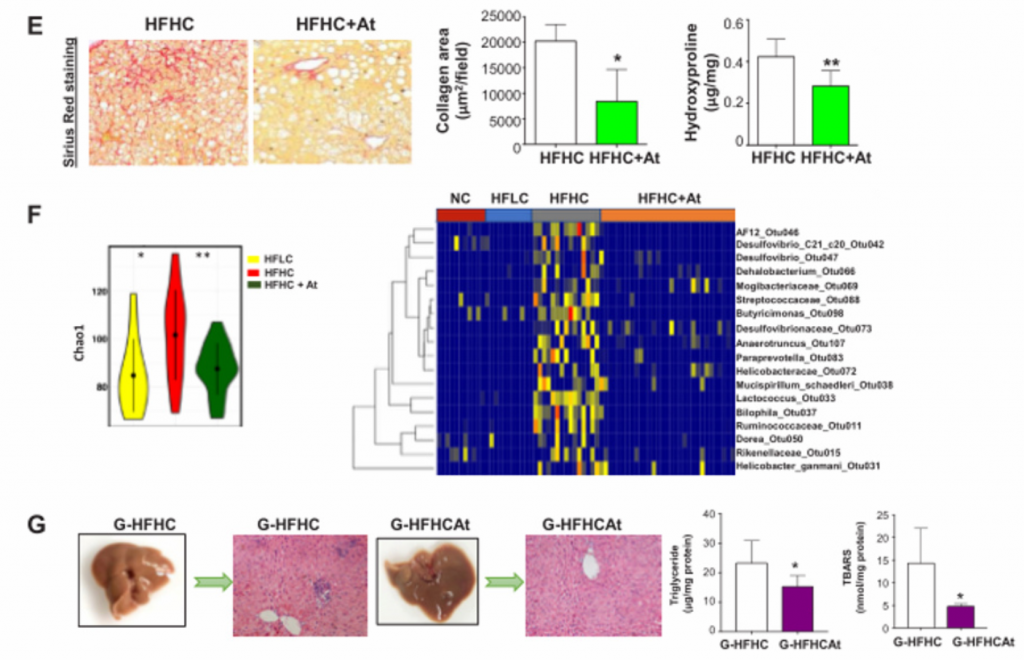

A) 主成分排序分析表明,膳食胆固醇含量对血清代谢产物有显著影响
B)HFHC小鼠的具有差异的富集代谢物的通路分析。胆汁酸合成是关键。
C) [endif]血清代谢组学火山图,指示了HFLC和HFHC小鼠的代谢产物的异常值。初级胆汁酸包括牛磺胆酸(TCA)、TUDCA、甘胆酸(GCA)和TCDCA,这些也是HFHC小鼠中异常上调的代谢物。IPA是微生物色氨酸代谢的产物,也是HFHC小鼠中异常下调的代谢物。
D) [endif]HFLC和HFHC饲料喂养3个月的小鼠门静脉LPS浓度和14个月的小鼠结肠组织E- cadherin表达。两者相比,HFHC小鼠门静脉血清脂多糖(LPS)浓度升高,结肠E-钙粘蛋白丢失。提示膳食胆固醇可损害肠道屏障功能
E) [endif]微生物与代谢物的相关性分析。红色呈正相关,蓝色呈负相关。
F) [endif]HFLC和HFHC饲料喂养小鼠肝脏组织中Cyp7a1、Cyp8b1、Cyp27a1和Cyp7b1 mRNA水平。高胆固醇膳食不能改变肝脏中细胞色素P450 (Cyp)7a1、Cyp8b1、Cyp27a1、Cyp7b1等胆汁酸合成酶的mRNA表达。
G) [endif]油红O染色显示,TCA加重胆固醇诱导的人LO2细胞甘油三酯的积累,IPA抑制胆固醇诱导的肝癌细胞、HKCI-2和HKCI-10细胞甘油三酯的积累。
H) [endif]IPA抑制NASH-HCC细胞系的细胞增殖。
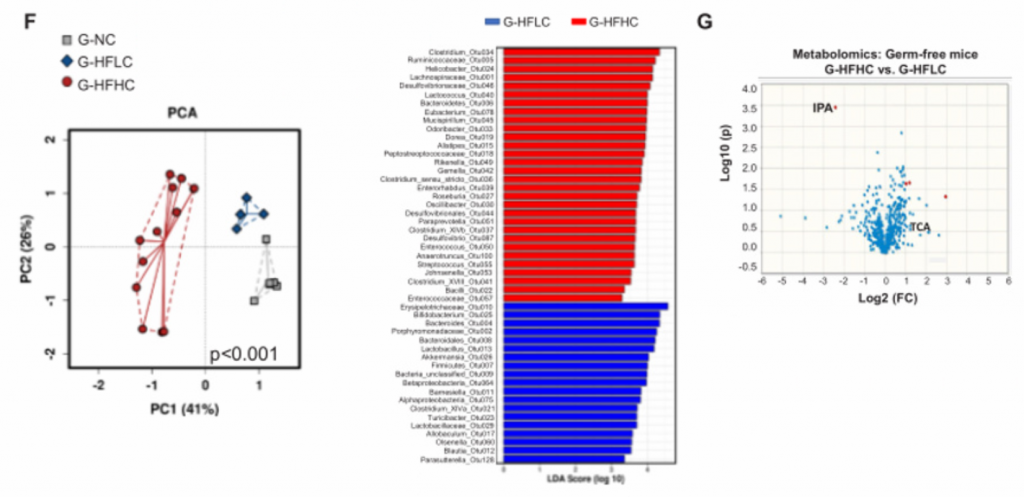
6. 膳食胆固醇调节的肠道菌群通过诱导代谢产物的改变,促进NAFLD和肝细胞的增殖,从而促进胆固醇诱导的NAFLD-HCC的形成。
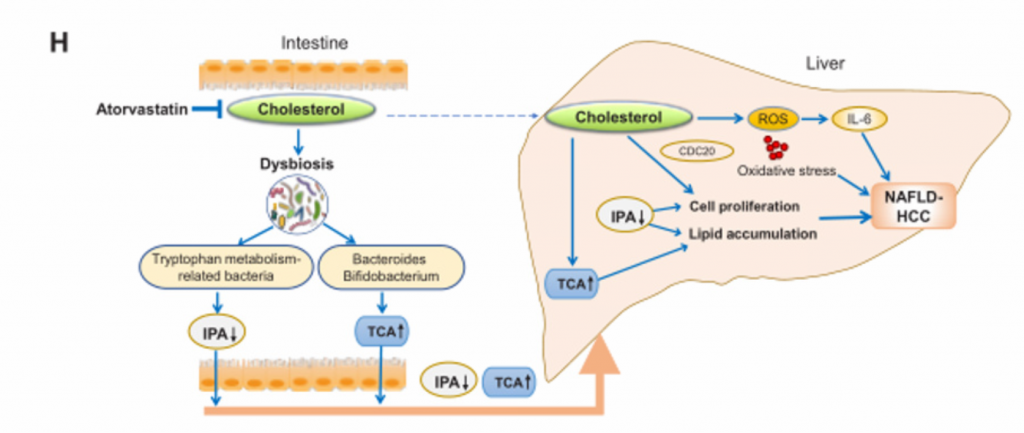



A)将喂养NC、HFLC和HFHC饲料的小鼠(14个月)的粪便移植到NC条件下的无菌小鼠(G- NC、G-
HFLC和G- HFHC)中。图中为G- NC组、G- HFLC组和GHFHC组灌胃无菌小鼠肝脏的大体形态和组织学检查。G- HFHC小鼠在14月龄时出现一个肝结节,而在8月龄和10月龄时未出现肝结节。组织学检查证实该结节发育不全,有小球状增生,细胞增殖增强。
B) [endif]8、10、14月龄时,G-NC、G-
HFLC和G-HFHC组无菌受体小鼠的肝脏甘油三酯含量、脂质过氧化反应和肝组织学改变。FMT后8、10、14个月,G-HFHC小鼠肝脏脂质积累明显增加,并伴有肝组织损害
C) [endif]G-NC、G- HFLC、G-HFHC组小鼠14月龄时的肝脏IL-6蛋白水平。
D) [endif]肝切片Ki-67染色。可见在14月龄时,G-HFHC小鼠中肝细胞增殖增加。但在FMT后8个月和10个月时肝细胞增殖并未见增加。
E) [endif]肿瘤通路检测。图中直方图向上表示基因表达上调,向下为下调。免疫印迹法验证CDC20(细胞增殖)表达上调。
F) [endif]G-NC、G- HFLC、G-HFHC小鼠肠道微生物群的PCA分析和LDA直方图。在不同的膳食控制下,肠道菌群的差异很大。
G) [endif]G- HFLC和G- HFHC小鼠血清代谢组学分析。G- HFHC小鼠的IPA较G-HFLC小鼠降低,与喂养HFHC饲料的常规小鼠一致。
7. 降胆固醇治疗完全抑制了高脂血症小鼠NAFLD-HCC的形成。



A)阿托伐他汀治疗喂养HFHC饲料的C57BL/6小鼠的示意图。给小鼠喂食HFHC 饲料7个月,并继续喂食HFHC饲料和阿托伐他汀7个月。(HFHCAt)
B)HFHC小鼠的肝组织HE染色及肝脏大体形态,分别计算了其脂肪变性和炎症的组织学评分。在实验结束时(14个月),阿托伐他汀完全抑制了HFHC饮食诱导的NAFLD-HCC的形成,并改善了NASH的严重程度。
C)从左至右分别为血清胆固醇水平、肝脏游离胆固醇水平、血清甲胎蛋白水平,显著降低。
D) 丙氨酸氨基转移酶(ALT)、血清促炎细胞因子(IL-6、IL-1α、IL-1β、单核细胞趋化蛋白-1、巨噬细胞炎性蛋白-1α和巨噬细胞趋化蛋白-1β)显著降低。
E)阿托伐他汀通过显著减少肝脏胶原沉积和羟脯氨酸含量来改善肝纤维化
F)用NC、HFLC和HFHC饲料喂养的小鼠,在阿托伐他汀治疗或不治疗的情况下,粪便中细菌的Chao1指数和热图。经阿托伐他汀治疗后,HFHC喂养的小鼠肠道菌群丰富度显著恢复。
G)被灌服HFHCAt(阿托伐他汀治疗的HFHC喂养小鼠)粪便的无菌小鼠的肝脏大体形态、组织学检查、甘油三酯和脂质过氧化含量。与G-HFHC组相比,G-HFHCAt组小鼠肝脏组织学有所改善,肝脏甘油三酯和脂质过氧化水平降低。
H)胆固醇诱导的NAFLD-HCC发生机制示意图。胆固醇破坏胆汁酸代谢和微生物色氨酸代谢,导致血清TCA增强,IPA降低,从而促进NAFLD-HCC的发展。
结论
长时间的高胆固醇饮食通过调节肠道微生物群,诱导雄性小鼠NAFLD-HCC自发和进行性发展。胆固醇破坏胆汁酸代谢和微生物色氨酸代谢,导致血清TCA增强,IPA降低,从而促进NAFLD-HCC的发展。降胆固醇治疗完全抑制了膳食胆固醇诱导的NAFLD-HCC的形成。这项研究强调,抑制胆固醇和调控肠道菌群及其相关代谢产物可能是预防NAFLD-HCC的有效策略。
尊敬的客户和合作伙伴:
根据国家税务总局浙江省税务局关于全面推广使用电子普通发票的公告,国家税务总局浙江省税务局公告2020年第1号文件,规定全省推广使用的电子普通发票包括增值税电子普通发票和通用电子发票。我公司从2020年7月20日起正式启用增值税电子普通发票,全部增值税普通发票均采取电子发票方式进行开具,不再提供纸质增值税普通发票。现公告如下:
一、增值税电子普通发票的法律效力、基本用途、基本使用规定等与税务机关监制的增值税普通发票相同;
二、电子发票启用后,同时停开原通用机打发票,使用任何打印机将pdf版本电子发票打印出来(黑白发票即可);
三、 电子发票的传送方式为手机短信或PDF的邮件,请务必预留有效的手机号及电子邮箱,登陆邮箱后可进行发票下载、查看和打印。并请同时预留邮寄地址,以便转为纸制发票后邮寄;
四、电子发票会在开具后直接向作者发送,如需查询发票副件,请联系我们。
上述开票调整给您带来的不便,敬请谅解。
详询400-161-1580。
杭州谷禾信息技术有限公司

谷禾健康
发育迟缓的原因有很多,牵涉到比如母体子宫内生长迟缓、神经内分泌和激素因素、儿童早期腹泻和其他感染频繁、环境肠道功能障碍、环境毒素和遗传因素等。 环境肠道功能障碍(EED)是一种以绒毛萎缩和隐窝增生为特征的获得性小肠亚临床疾病,病因不明,可能占所有发育迟缓病例的40%以上。

近日,美国华盛顿大学医学院Jeffrey I. Gordon团队的发表在《新英格兰医学杂志》研究分析了营养不良伴肠病儿童的十二指肠微生物群(DOI:10.1056 / NEJMoa1916004 ),研究结果研支持生长发育迟缓与小肠微生物群组成和肠病之间存在因果关系,并为开发针对这些微生物对EED的作用的疗法提供了理论依据。
环境性肠功能障碍(EED)是一种神秘的小肠疾病,被认为与儿童营养不良(一个紧迫的全球健康问题)有关。由于对小肠黏膜和微生物群落直接取样较为困难,因此,难以确定这种疾病的发病率、病理生理特征及其对生长发育迟缓的影响。
该研究研究组在孟加拉国达卡市贫民窟中招募了110名没有营养干预的生长发育迟缓的儿童,平均年龄为18个月,对80例行活检的儿童进行了内镜检查, 确认的EED以及可用的血浆和十二指肠样品。
研究组对80例活检证实EED,且血浆和十二指肠样本可用的儿童进行了内窥镜检查。
研究组量化了从这些儿童获得的十二指肠活检样本中的4077个血浆蛋白和2619个蛋白的水平,确定了从每个儿童的十二指肠抽吸物中回收的微生物群中细菌菌株的水平,还从居住在同一地区的年龄匹配的健康儿童中获得了21个血浆样本和27个粪便样本。用从十二指肠抽吸物中培养出的细菌菌株定殖给孟加拉饮食的年轻无菌小鼠。

*加减值是±SD。 要将α-1抗胰蛋白酶的值转换为每升克,请乘以0.01。
由于四舍五入的关系,百分比总数可能不等于100。 IQR表示四分位距,NA不适用。
†环境肠道功能障碍(EED)的生物标志物得分是从0开始的连续测量,得分越高表明一组粪便炎症生物标志物(α-1抗胰蛋白酶,髓过氧化物酶和新蝶呤)的水平越高。
在从孩子那里获得的细菌菌株中,一组共有14个分类单元(通常不归类为肠病原体)的绝对水平与线性增长呈负相关(年龄z评分,r = -0.49; P = 0.003),并且与参与免疫炎症反应的十二指肠蛋白呈正相关。 粪便微生物群中这14个十二指肠分类群的代表与健康儿童的样本显着不同(通过方差的排列多变量分析,P <0.001)。 小肠的肠病在已被从EED儿童获得的培养的十二指肠菌株定殖的gnotobiotic小鼠中发展。
在从儿童获得的细菌菌株中,共有14个类群(通常不被归类为肠道病原体)的绝对水平与线性生长发育呈负相关,与参与免疫炎症反应的十二指肠蛋白呈正相关。
十二指肠蛋白质组成分、十二指肠细菌分类绝对水平与发育迟缓的相关性,粪便微生物群中这14个十二指肠分类群的代表与健康儿童的样本亦存在显著差异。

在从儿童获得的细菌菌株中,共有14个类群(通常不被归类为肠道病原体)的绝对水平与线性生长发育呈负相关,与参与免疫炎症反应的十二指肠蛋白呈正相关。
(EED)的研究儿童中获得的十二指肠细菌将肠病传播到致敏小鼠上。 接受EDD患儿十二指肠培养菌定殖的小鼠进展为小肠病。
